
김원사 서울대학교 지질학과 졸업(이학사) 캐나다칼톤 대학교 대학원 지질학과졸업(이학석사, 이학박사) 독일하이델베르크대학교객원교수 캐나다광물연구소 객원교수 현재 충남대학교 지질학과교수 저서 『 보석학』 『 지구환경과학』 둥다수
조암광물학 
 조암광물학
조암광물학
책머리에 우리가 살고 있는 지구의 표면은 고체 상태인 여러 종류의 암석 으로 구성되어 있고, 이들 암석은 다시 여러 종류의 광물로 되어 있는데, 이 를 조암광물이라고 한다. 조암광물은 인류의 역사가 시 작되면서 생활의 터전이 되는 대지와 불가분의 관계를 이어 왔으 며, 최근까지도 각종 화학원소 및 산업 재료가 되는 물질을 대부 분 광물로부터 얻고 있다. 이 책에서는 암석을 이루고 있는 수천 종의 광물 중에서 비교적 산출 빈도나 중요성이 많은 100 여 총의 광물을 선별하여 이들에 대한 주요한 광물학적 성질에 대해 기술하였다. 또한 이들을 편광 현미경을 비롯하여 주사전자현미경, 전자현미분석, X 선 형광분 석, 원자흡수분광분석, 적외선흡수분광분석, 시차열분석, X 선 회 절분석 등을 이용하여 연구하는 과정에 대해서도 기술하였다. 마 지막으로 상평형 이론을 도입하여 조암광물이 천연에서 어떠한 과 정을 통해 만들어지며, 또 이들의 지질학적, 광물학적 의미는 어
떠한지에 대해서도 간략하게 다루었다. 이 책을 저술할 수 있도록 재정 지원을 하여준 대우재단에 감사 드리며, 이 책의 원고를 읽어 주시고 조언을 해 주신 서울대학교 김수진 교수님께도 감사드린다. 또한 원고 정리에 도움을 준 충남대 학교 지질학과 광물학 연구실의 신현숙 박사와 집필에 전념할 수 있 도록 도와준 가족에게도 감사한다. 아무쪼록 이 책이 조암광물에 대해 한 단계 높은 공부 릅 하 는 데 도움이 되었으면 한다. 1998 년 9 월 김원사
차례
책머리에 5제 1 장 조암광물1.1 조암광물 의 정의 131.2 조암광물 의 생 성 141.2.1 화성환경 • 141.2.2 퇴적환경 • 201.2.3 변성환경 • 25제 2 장 조암광물의 물리 • 화학적 성질2.1 색 312.1.1 광물의 발색 원인 • 332.1.2 홉수 • 332.1.3 고체 불순물 • 382.2 결정구조 382.2.1 결정의 3 요소 • 382.2.2 대칭의 3 요소 • 392.2.3 결정축과 축각 • 462.2.4 결정축과 대칭축과의 관계 • 462.2.5 7정계 • 492.2.6 결정형 • 522.2.7 결정면 밀러지수법 • 59
2.2.8 결정 투영 • 632.2.9 32정족 • 672.3 화학성분 722.3.1 화학분석 자료 처리 • 722.3.2 고용체 • 742.3.3 정량 화학분석 자료의 처리법 • 802.4 벽개 · 열개 · 단구 872.4.1 벽개 • 872.4.2 열개 • 892.4.3 단구 • 892.5 경도 912.5.1 경도의 정의 • 912.5.2 모스 경도계 • 912.6 비중 942.6.1 비중의 정의 • 942.6.2 비중 측정법 • 95제 3 장 조암광물의 광학적 성질과 편광현미경 관찰3.1 조암광물의 광학적 특성 1033.1.1 등방성 • 1043.1.2 이방성 • 1053.2 색과 다색성 1103.3 소광 및 소광 특징 1123.3.1 항상 검게 보이는 경우 • 112
3.3.2 4번 규칙적으로 검게 보이는 경우 • 1133.3.3 정계에 따른 소광 특징 • 1163.4 장축 부호 1193.4.1 일축성 광물 • 1203.4.2 이 축 성 광물 • 1213.5 간섭상 1233.5.1 일축성 간섭상 • 1253.5.2 이축성 간섭상 • 1293.6 이방성 광물의 광학 부호 1343.6.1 일축성 광물 • 1343.6.2 이축성 광물 • 1383.7 광축각 (2V) 1413.7.1 광축각 • 1413.7.2 광축각 측정법 • 142제 4 장 조암광물 각론4.1 조암광물의 분류 1514.2 광물의 분류 1524.2.1 규산염 광물 • 1524.2.2 산화 광물 • 1564.2.3 탄산염 광물 • 1574.2.4 황산염 광물 • 1574.2.5 수산화염 광물 • 1584.2.6 인산염 광물 • 1584.2.7 할로겐 광물 • 158
4.3 광물 각론 1594.3.1 규산염 광물 • 1594.3.2 산화염 광물 • 2924.3.3 탄산염 광물 • 3084.3.4 황산염 광물 • 3254.3.5 수산화 광물 • 3354.3.6 인산염 광물 • 3404.3.7 할로겐 광물 • 344제 5 장 조암광물 기기 연구5.1 주사전자현미경 분석 3475.1.1 원리 및 구조 • 3475.1.2 지질학적 용도 • 3485.2 전자현미분석 3505.2.1 원리 및 구조 • 3505.2.2 정성분석 • 3515.2.3 정량분석 • 3535.2.4 광물 시료 준비 • 3535.2.5 분석 자료 검토시 유의사항 • 3555.2.6 전자현미분석법의 장점과 단점 • 3555.3 X선 형광분석 3565.3.1 원리 및 구조 • 3565.3.2 시료 준비 • 3525.3.3 X선 형광분석의 장점과 단점 • 3595.4 원자흡수분광분석 360
5.4.1 원리 및 구조 • 3605.4.2 시료 준비 • 3645.4.3 원자흡수분광분석법의 장점과 단점 • 3645.5 적외선 흡수분광분석 3655.5.1 원리 및 구조 • 3655.5.2 시료 준비 • 3665.5.3 적외선 흡수스펙트럼의 해석 • 3675.5.4 조암광물의 적외선 흡수스펙트럼의 예 • 3685.6 시차열분석 3695.6.1 원리 및 구조 • 3695.6.2 시료 준바 • 3705.6.3 시차열분석 자료 해석 • 3715.6.4 주요 조암광물의 시차열분석 자료 • 3725.7 X선 회절분석 3755.7.1 원리 및 구조 • 3755.7.2 시료 준비 • 3775.7.3 X선 기록지 해석 • 3785.7.4 JCPDS 카드 • 3845.7.5 X선 회절분석의 응용 • 384제 6 장 상평형 및 지질학적 의미6.1 상평형과 상률 3876.2 1성분계 상다이어그램 3906.3 2성분계 상다이어그램 3926.3.1 고용체를 형성하지 않는 경우 • 392
6.3.2 완전고용체를 형성하는 경우 • 3986.3.3 용리현상이 일어나는 경우 • 4026.4 3성분계 상다이어그램 408참고문헌 • 419찾아보기 • 423제 1 장 조암광물 1.1 조암광물의 정의 지구의 표면인 지각은 고체 덩어리로 되어 있고, 이 고체 덩어 리인 암석( 岩石 , rock) 은 다시 광물( 鑛 物, mi neral) 이라는 작은 구성 입자로 되어 있다. 광물은 〈하나 또는 여러 종류의 원소가 화학적 으로 결합하여 내부적으로 규칙적인 원자배열을 하고 있는 고체 물질로서, 천연에서 무기적 과정으로 생성된 것〉을 의미한다. 암 석은 성인(成因)에 따라 화성암, 퇴적암, 변성암으로 분류하며 이 들 암석을 구성하는 광물 역시 서로 다론 지질 환경의 영향을 받 는다. 암석을 구성하는 광물을 조암광물(造岩 鑛 物, rock-fo rming mi neral) 이라고 하는데, 그 수효는 약 3000 종이 된다. 조암광물을 연구하면 광물의 물리 • 화학적인 자료뿐만 아니라 광물을 산업적 으로 활용할 수 있게 되고, 또 이들 광물로 구성되어 있는 암석의 생성 환경 및 시기, 지질학적 변천과정 동에 대해서도 알 수 있게
된다. 1.2 조암광물의 생성 1.2.l 화성환경 1.2.1. 1 화성암의 생성 지각의 대부분은 화성암으로 되어 있다 . 그 러나 상당 부분 의 화 성암이 지표를 따라 얇게 분포하고 있는 퇴 적 압이나 변성암으 로 가려져 있다. 화성암은 맨틀 상부 또는 지 각 의 하 부 물질 이 녹아 만들어진 액체 상태의 마그마가 냉각되면서 형 성된 암석이다. 마 그마는 약 900~l600°C 정도인 고온의 물질인데, 100 여 가지의 화 학원소로 구성되어 있다 . 그 중에서 존재량이 약 1% 이상되는 성 분은 0(46.7 % ), Si (2 7.7% ) , Al(8.1 % ) , Fe(5.1% ) , Ca(3.6 % ) , Na(2.7%), K(2.6%), Mg (2 .1 % ) 등 8 가지이고, 이들이 전체의 99% 를 차지한다. Ti (0.86%) 을 비롯한 나머지 90 여 가지의 성분은 1% 정도를 차지할 뿐이다. 그래서 위에 기술한 8 가지의 원소 를 〈 지 각 구성의 8 대 원소〉라고 부른다. 마그마에는 H20, CO 2 뿐만 아니라 HzS, HCI, CH 』, CO 등의 기체 성분도 상당량 들어있다 . 그러나 기체 형태의 02 는 거의 포함되어 있지 않다 . 지구 중심부로부터 마그마로 전달되던 열이 어떤 이유로 인해 차단되는 경우에는 마 그마가 서서히 식게 되는데 이때 용융점이 높은 광물부터 정출( 晶 出)이 시작된다. 마그마가 냉각될 때 정출되는 광물의 종류와 순서 를 실험적으로 알아 낸 암석학자는 미국의 Bowen 교수로서, 그는 감람석 [(Mg , Fe )z S i 04] 이 제일 먼저 정출되며, 특히 Mg 성분이 많은 감람석 (fors te r i te, Mg zS i 04 ) 부터 정 출되 다가 점 점 Fe 성 분이
많은 감람석(fay al it e, FezS i O~ )으로 변하는 사실을 발견하였다 . 이와 거의 동시에 정출되는 또 하나의 광물은 사장석인데 높은 온도에서 처음 만들어지는 사장석에는 Ca 성분이 많고, 온도가 점점 내려감 에 따라 Na 성분이 증가한다. 사방정계인 감람석이 정출된 후에는 Mg 성분이 높은 사방정계 또는 단사정계의 휘석이 정출되기 시작 하고, 이어서 Fe 성분이 많은 사방휘석이 정출한다. 역시 이 단계 에서도 사장석은 계속 정출하게 되며, 이 전단계에서 만들어 진 사 장석에 비해 Ca 성분은 감소하고 Na 성분은 증가한다. 휘석의 정 출 이 마쳐지면 이어서 각섬석이 정출하게 되며, 나중에 혹운모가 계속 정 출 한다. 특히 감람석 一 휘석~ 이어지 는 계열의 광물 들 은 결정구조가 모두 다른데 이를 불연속계열(不 連 紹 系列, dis c onti nu ous seri es ) 이 라고 부른다. 그러 나 사장석 은 Ca 와 Na 성분에 차이가 있을 뿐 삼사정계의 결정구조는 변하지 않는다. 이 때문에 Ca-사 장석 ~ (Ca, Na) - 사장석 ~ (Na, Ca) - 사장석 _> Na-사 장석 계열을 연속계열(連 領 系列, conti nu ous se ri es) 이라고 부 른 다 . 아직 마그마에는 액체 성분이 남아 있기 때문에 계속해서 칼리 장석, 백운모, 석영 등이 정출되며 이 과정은 액체 성분이 완전히 소비될 때까지 계속된다. 이렇게 마그마가 냉각될 때 일어 나는 광물의 연속적인 정출과정을 〈 Bowen 의 반응계열〉 (Bowen's reacti on se ri es) 이라고 한다(그림 1.1). 초기에 만들어진 감람석이나 휘석이 마그마 내에 그대로 존재하면서 마그마와 계속 반응을 하 여 새로운 광물을 정출시키는 경우도 있지만, 때로는 초기에 만들 어진 광물이 높은 비중으로 인해 마그마 챔버 아래에 가라앉아 잔 류 마그마 용액과 충분한 반응을 하지 않게 되는 불평형 상태가 만들어질 수도 있다. 후자(後者)의 경우를 분별정출작용(fra c ti onal c ry s t al li za ti on) 이라고 한다. 이러한 증거로는 휘석 결정의 바깥 부 분이 각섬석으로 둘러쌓여 있거나, 사장석의 중심부가 바깥 부분
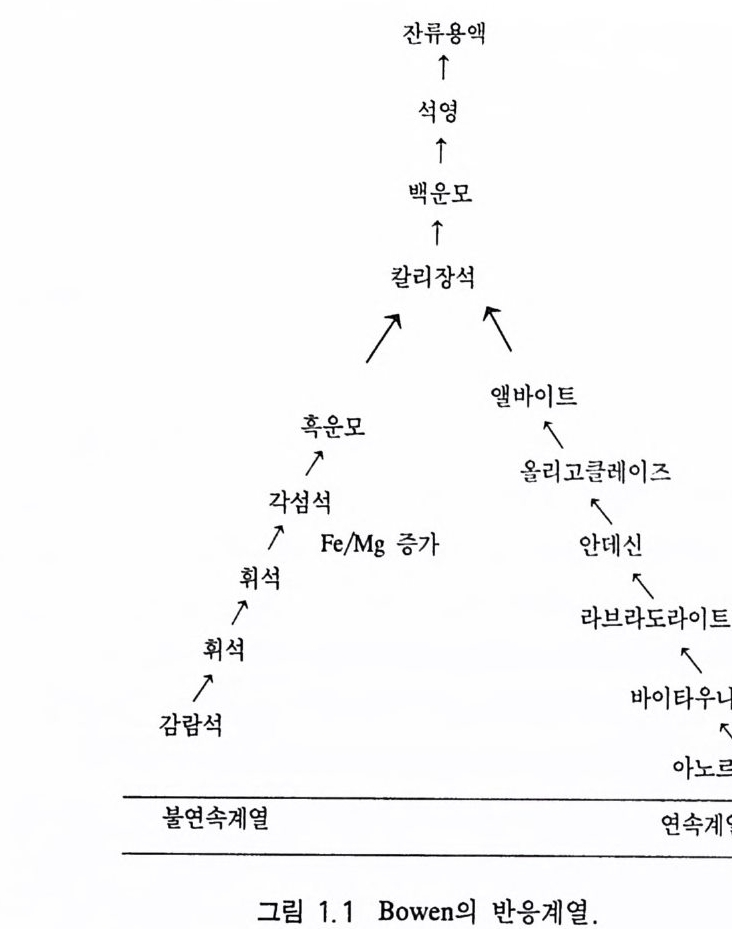 잔류용액
잔류용액
보다 Ca 성분이 높아 편광현미경 관찰시 대상구조가 나타나는 현 상 등이 있다(그림 1.2) . 1.2. 1. 2 화성 암의 분류 ®형성 깊이에 따른분류 화성암은 마그마가 냉각될 때 정출되는 여러 광물로 이루어진 암석으로서, 그 화성암울 구성하고 있는 광물의 종류와 조직에 따
 그림 1.2 불평형상태에서 형성된 사장석. 중심부분이 외곽보다 Ca 성분이
그림 1.2 불평형상태에서 형성된 사장석. 중심부분이 외곽보다 Ca 성분이
라 화성암의 명칭이 주어진다. 화성암을 구성하는 광물의 종류는 마그마의 성분과 마그마의 냉각 정도에 따라 결정되며, 광물의 조 직은 마그마의 냉각 속도에 의한 광물 결정의 크기에 의해 주로 좌우된다. 한편 마그마의 냉각 속도는 마그마의 고결 위치와 직접 적인 관련이 있다. 마그마가 지하 깊은 곳에서 천천히 고결될 경 우 광물 결정은 눈으로 식별이 가능할 정도로 크게 된다. 그러나 마그마가 지각에 생긴 어떤 틈을 따라 지표로 나와 급격히 식게 되면 광물 결정의 크기가 매우 작아 육안으로의 광물 식별이 거의 불가능해 진다. 지하 심부에서 마그마가 고결되어 만들어진 화성 암을 심성암(深成岩)이라 하며 이런 암석은 구성 광물의 입자가 크 기 때문에 눈으로도 식별이 가능하게 된다. 이런 암석 조직을 현 정질(顯晶質)이라 하며, 광물 입자들의 평균 크기가 5mm 이상이
면 조립질 (組粒 質 ), l ~5mm 이면 중립질(中粒/t'(), Imm 이하 이면 세립질(細粒 質) 이라고 한다. 마그마가 지각에 생긴 균열을 따라 솟아나오면 화산 폭발이 되 는데 이때 지표로 흐르는 마그마 물질을 특별히 용암( 炤岩 , lava) 이라고 한다. 용암이 굳어져 만들어진 암석을 화산암(火山岩)이라 고 하며, 이 암석은 지표에서 급히 냉각되어 만들어진 것이므로 이를 구성하고 있는 광물의 입자 크기는 매우 작게 된다. 대부분 세립질이지만(그림 1.3) 경우에 따라서는 더욱 미세한 유리질 조직 일 수도 있다. 마그마가 지하 심부에서 정출되기 시작하다가 지표 가까운 위치까 지 상승하는 경우도 있다. 이러한 환경에서 만 둘 어진 암석을 반심성 암(半深成岩)이라 한다. 반심성암에는 큰 광물 결정이 세립질의 광물 과 함께 공존하는데, 이 를 반상조직 (IkI 狀組籠t por p h yr it i c tex tu r e) 이 라고 한다(그림 1.4 ). 큰 광물 결정을 반정 (Iki 晶 phe nocrys t ) , 세립 질의 주위 부분을 석 기 (石基, matr i x ) 라고 한다. 따라서 암석의 조직만 관찰하여도 그 화성암의 생성 환경을 추 측할 수 있게 된다. ® 화성암을 구성하는 조암광물 화성암울 이루는 조암광물중 그 암석의 특징을 나타내는 중요한 광물들을 주요 조암광물이라 하고, 그 외 광물을 보조 조암광물이 라고 한다(표1.1) . 화성암의 주요 조암광물과 보조 조암광물의 예 는 표 1. 2 와 같다.
 그림 1.3 화산암 에서 관 찰 되는 세립질 조직 .
그림 1.3 화산암 에서 관 찰 되는 세립질 조직 .
 그림 1.4 반 심 성암에서 관찰되는 반정과 석기로 구성됨.
그림 1.4 반 심 성암에서 관찰되는 반정과 석기로 구성됨.
 표 1.1 화성암의 조암광물
표 1.1 화성암의 조암광물
1.2.2 퇴적환경 1.2.2.l 퇴적암의 생성 지표에 노출되어 있는 암석은 의부의 환경 요인에 의해 파괴되어 작게 부스러지게 되고 이런 암석 부스러기들은 비나 바람, 빙하 등에
 표 1. 2 주요 화성 암의 주요 조암광물과 보조 조암광물
표 1. 2 주요 화성 암의 주요 조암광물과 보조 조암광물
의해 이동되어 결국 바다나 호수 또는 강 바닥에 쌓이게 된다. 기존에 있던 화성암이나 변성암 또는 퇴적암이 서서히 부서지면서 파괴되는 현상을 풍화작용(風化作用, wea th e ri n g)이라고 하며, 풍화작용을 일으 키는 요인에 따라 기계적 풍화작용(機械的風化作用 , mechanic a l wea th e ri n g)과 화학적 풍화작용(化學的風化作用, chem ica l weath e rin g) 으로 나눈다. 전자(前者)에 해당하는 요인으로는 바람, 급격한 온도 변화, 지압력 변화 등이 있고, 후자(後者)에 속하는 요인으로는 강
수에 의한 물 등이 있다. 풍화산물인 암석 또는 광물 부스러기들은 바다나 호수로 이동된 후 오랜 기간 고결되지 않은 상태로 존재하게 되는데, 이 느슨한 상태의 물질을 퇴적물(:tftfti物 sed i men t s) 이라고 한다. 퇴적물은 그 위에 쌓인 퇴적물이 누르는 압력에 의해 입자 사이에 있던 수분이 추출되게 되고(탈수 작용, dehy dr ati on ), 그 결과 입자 간격이 좁 아 진다(다져짐 작용, comp ac ti on ). 그 후 물에 용해되어 있던 실리카 성 분이나 탄산칼슘 성분이 입자 틈새에 침전하게 되면 퇴적물이 서로 단 단하게 결합되어(교결 작용, cementa t io n ), 그 결과 퇴적물은 비 로소 굳은 암석이 되며 이를 퇴적암(사 t柏株 sedim enta r y rock) 이라고 한 다. 퇴적물이 퇴적암으로 변하는 일련의 물 리 • 화학적 과정을 속 성작용( 領成作用 , d i a g enes i s) 이라고 한다. 암석이나 광물의 부스러 기가 쌓여 만들어진 퇴적암을 쇄설성 퇴적암([i 십骨性推積岩 , elasti c sedim e nta ry rock) 이 라 한다. 때로는 바다나 호수에 녹아 있던 성분이 화학적으로 침전하여 퇴적물을 만들기도 한다. 깊은 바다에서 침전하는 탄산칼슘 성분 의 방해석으로 되어 있는 석회암, 사해(死海)처럼 증발량이 많고 고 립된 환경에 있는 해수로부터 침전한 소금으로 이루어진 암염, 호수 에서 침전하는 석고층, 선캠브리아기의 환원 환경에서 침전했던 퇴적기원 철광상 등은 화학적 퇴적암(化學的推積 岩 , chemi ca l sed i men tary rock) 의 예이다. 이처럼 쇄설성 퇴적암과 화학적 퇴적암 은 모두 퇴적물의 기원에 따른 명칭이다. 1.2.2.2 퇴적암을 이루는 주요 조암광물 퇴적암울 구성하는 광물은 첫째, 기계적인 풍화작용과 화학적인 풍화작용에 강하여 잘 견디어 낸 광물과 둘째, 기존에 있던 광물 이 화학적인 풍화작용으로 파괴되고 다시 새롭게 만들어진 광물로
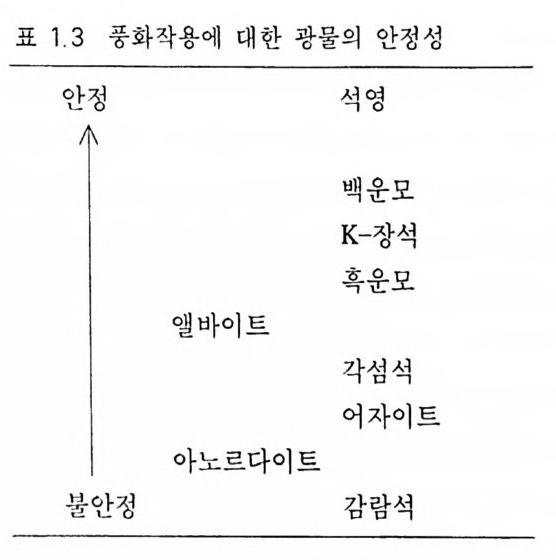 표 1 3 풍화작용에 대한 광물의 안정성
표 1 3 풍화작용에 대한 광물의 안정성
나눌 수가 있다 . 풍화작용에 안정한 광물의 순서에 따르면 (표 1.3 ), 마그마 고결 말기에 만들어진 광물일수록 안정하며, 초기에 정 출 된 광물일수록 불안정함을 알 수 있다 . 즉, 감람석이나 휘석 처럼 고온·고압에서 안정하던 광물은 상온·상압에서 일어나는 풍 화작용 에 매우 불안정한 반면, 석영처럼 비교적 저온 • 저압의 환경 에서 만들어진 광물은 풍화작용에 안정함을 의미한다 . 퇴적암에서 흔히 관찰되는 광물로는 석영, 칼리장석, 운모, 사장석, 저어콘, 석 류석, 자 철석 등이 있다. 이 밖에도 캐올리나이트, 일라이트, 스멕타 이트 등과 같은 점토광물(*占土 鑛 物, clay mi neral) 도 있는데, 이들은 풍화작용에 약한 감람석, 휘석, 일부 사장석 등이 파괴되면서 새 로 만들어진 것들이다 . 1.2.2.3 퇴적암의 종류와 주요 조암광물 역암( 礎岩 , cong lo merate ) 자갈과 모래, 점토 등의 입자가 한데 엉켜 있는 암석이다. 자갈이란 직경이 2mm 이상 되는 암석 파편
또는 광물 입자를 말한다. 광물 입자는 침식작용에 강한 석영이 대부분이다. 자갈의 형태는 운반 거리에 따라 다른데, 일반적으로 이동 거리가 클수록 둥글게 된다. 따라서 자갈의 형태를 관찰하면 기원암의 위치 등을 추측할 수 있게 된다. 부정합면 위에 있는 기 저역암(基底礎岩, basal cong lomera t e) 을 구성하는 자갈은 대부분 주 변에 있는 암체으로부터 운반되어 온 것들이어서 모가 나 있다. 사암(砂岩, sandsto n e) 모래 크기의 광물 또는 암석 파편으로 된 퇴적암이다. 모래란 직경이 2~ 点 mm 범위 입자이다. 구성 광물 은 석영과 장석이 대부분이고, 혹운모, 녹니석과 같은 점토광물도 상당량 있다. 사암에는 수평층리와 사층리 같은 퇴적구조가 관찰 될 수가 있는데 퇴적구조는 퇴적 당시의 환경을 추측할 수 있게 한다. 사암의 색은 구성 입자들의 종류뿐 만 아니라 입자를 결합 시키는 고결 물질에 따라 주로 좌우되는데, 고결 물질이 석영이나 방해석일 경우 옅은 회색, 노란색 등 밝은 담색 계통의 사암이 되 고, 적철석이나 침철석인 경우는 적색 내지 갈색의 사암이 된다. 고결 물질이 녹니석인 경우에는 녹색 사암이 된다. 셰일 (shale) 점토 크기의 광물들이 쌓여 만들어진 암석으로서, 얇 고 미세한 퇴적층리가 발달한다. 점토라 함은 点 mm 이하의 입자를 가리킨다. 주요 구성 광물은 운모류를 포함한 점토광물이며, 석영 도 다수 존재한다. 석회암(石灰岩, lime sto n e) 석회암은 주로 방해석 (CaCO J)으로 구 성되어 있는 암석이다. 방해석은 해수에 용해되어 있던 칼슘과 탄 산 이온들이 화학적으로 결합하여 침전한 것이며, 그 밖에 조개껍 질이나 생물체의 각질부분이 발견되는 경우가 많다.
증발암( 蒸發岩 , evapo r ite ) 바닷물이 방파제에 의해 고립될 경우 수분이 증발하면 그 결과 물 속에 녹아 있던 성분들이 화학결합을 하면서 침전하게 된다. 침전하는 광물의 순서는 일반적으로 방해 석 一 석고 / 경석고 一 소금 一 칼리소금이다. 따라서 해수에서 형성 된 증발암인 경우 석고나 경석고로 이루어진 암층 위에 소금층이 형성되어 있는 경우가 많다 . 만약 300m 두께의 바닷물 속에 용해 되어 있는 성분이 모두 침전할 경우 0 . 15m 의 석고층과 3.6m 의 소 금 층, 0.8m 의 칼리소금 (KC!) 층이 만들어지는 것으로 알려져 있다. 1.2 .3 변성환경 l,2,3 .l 변성암의 생성 기존에 있던 화성암이나 퇴적암이 열이나 압력의 영향으로 원래 지니고 있던 암석의 조직 또는 광물의 조성에 변화가 생긴 경우 이 를 변성암( 幾 成岩, meta m orp hic rock) 이라 하며, 변성암이 만들어 지는 일련의 과정을 변성작용( 變 成作用, me t amo rphi sm) 이라고 한 다. 원래의 암석이 열에 의해 변성작용을 받을 경우 이를 열변성 작용( 熱發 成作用, heat me ta mo rp h i sm) 이라 하며, 열변성작용은 기존 의 암석과 지하 심부로부터 이동해 온 고온의 마그마의 접촉부에 서 일어나므로 이를 접촉변성작용(接觸 變 成作用, conta c t meta m orp h is m ) 이 라고도 한다. 변성 작용을 일으키 는 또 하나의 요인 인 압력에는 지표로부터 가해지는 지압력 (地壓力, confi nin g pre ssure) 과 지각변동에 따른 편압력 (偏 壓 力, dif fere nti al pre ssure) 등이 있는 데 이러한 요인으로 일어나는 변성작용을 동력변성작용(動力 變 成作 用, dyn a m ic me t amo rphi sm) 이라고 한다. 동력변성작용은 그 영향이 미치는 범위가 매우 넓기 때문에 광역변성작용(廣域 變 成作用, reg ion al meta m orp hism ) 이 라고도 한다.
변성작용을 받으면 광물의 입자 크기가 원래의 암석일 때보다 더 커진다. 이러한 현상은 원래 암석에 있던 다수의 미세한 광물 결정들이 모여서 소수의 큰 결정을 만들기 때문인데 이러한 현상 을 재결정작용(再結晶作用, recr y s t all i za ti on) 이라고 한다. 따라서 단 위면적에 들어 있는 광물의 총 수효는 이전보다 감소한다. 한편 원래의 암석에 운모나 각섬석처럼 납작하거나 또는 길쑥한 광물이 포함되어 있을 경우, 압력이 가해지는 방향에 수직되게 재배열을 하여 일종의 결이 만들어지는데 이를 엽리(j당뿐, fo l i a ti on) 라고 한 다 엽리는 동력변성작용을 받아 생긴 변성암의 특징 이다 . 1.2.3 .2 변성암을 구성하는 주요 조암광물 변성작용이 일어나면 암석의 전체적인 화학성분은 변하지 않은 채 새로운 온도와 압력 조건에 안정한 광물군(鑛物群, mi ne ral assembla g e) 으로 변하는 것이 일반적이다. 이 를 등화학 변성작용 (等化學變成作用, iso chem ica l meta m orp h is m ) 이 라고 한다. 그러나 석회암에 화성암체가 관입하여 석회규산염 광물을 만들 경우에는 석회암의 전체적인 화학성분이 변하게 된다. CaCOJ + Si0 2 ~ CaSiO J + C02 방해 석 이 산화규소 규희 석 탄산가스 위 방정식은 석회암의 주구성 광물인 방해석이 화성암 관입체로 부터 공급된 이산화규소 물질과 화학반응하여 규회석과 탄산가스 를 형성하는 과정을 나타낸 방정식으로서, 원래의 석회암에 없었던 이산화규소 성분이 추가되었을 뿐만 아니라 탄산가스 성분은 소실 된다 이러한 경우를 이화학 변성작용(異化學 變成作用, allochem ica l meta mo rp h is m ) 이 라고 한다.
변성작용이 일어나는 동안 새로 만들어진 광물을 변성광물( 變 成 鑛 物, meta m orp h ic mi ne ral ) 이 라고 하며 , 대 표적 인 예 로 투각섬 석 , 양 기석, 투휘석, 제이다이트, 규회석, 석류석, 홍주석, 규선석, 남 정석, 녹염석, 십자석, 사문석, 활석 등이 있다. ® 접촉 변성암 규암 (珪岩 , qua r tzit e) 사암이 열변성작용을 받아 만들어진 암석으 로서 , 구성 광 물은 대부분 석영이며, 그 밖에 백운모, 혹운모, 장 석 등이 소량 합유되어 있다. 암석의 색은 사암일 때보다 밝다 . 석재나 유리 원료로 사용된다. 대리암( 大理岩 , marble) 석희암이 열변성작용을 받아 만들어진 암석으로서, 재결정작용을 받아 커진 방해석 입자들이 모자이크 형태로 접해 있는 것이 특징이다. 햇빛에서 관찰하면 방해석 결정 의 표면에서 빛이 반사되어 반짝거린다. 건축재나 공예품 제조에 사 용된다. 호른펠즈 (hom fe ls) 셰일이 열변성작용을 받아 만들어진 암석으로 서, 세립질 조직과 검은색을 띤다. 이 암석의 이름은 세립질 조직 으로 인해 〈양의 뿔 (horn) 처럼 예민한 각을 가진 꺼칠꺼칠한 조각 으로 깨지는 덩어리(fe ls) 〉라는 의미에서 유래하였다. ®광역 변성암 판암(板岩, slate ) 셰일이 압력을 받게 되면 판상 형태의 운모 광 물들이 한 방향으로 평행하게 배열하게 된다. 이 때문에 엽리가 생겨 망치로 때릴 경우 얇은 판상체로 분리가 된다. 판암의 색은 검은 것이 대부분이지만 회색, 갈색, 녹색 등도 있다. 판암을 점
판암(*胡反岩)이라고도 한다. 오래전에는 지붕이나 온돌을 만드는 데 많이 사용하였다. 천매암(千枚岩, phy llite) 판암이 될 때보다 더 큰 압력을 받을 때 만들어지는 변성암으로서, 주로 견운모와 녹니석으로 구성되어 있 다. 녹색과 소규모의 파랑상(波浪狀) 표면구조를 나타내는 것이 특 징이다 녹색은 변성광물로 녹니석이 다수 생겼기 때문인데, 햇빛 아래에서 관찰하면 이 광물의 표면으로부터 빛이 반사하여 마치 비단 옷감에서 처럼 반짝인다. 소규모의 파랑상 엽리구조 를 천매 구조라고 한다 . 견운모, 녹니석, 혹운모 등 운모류 광물이 주구성 물질이다. 편암(片岩, schis t) 천매암이 만들어질 때보다 더 높은 압력을 받 게 되면 뚜렷한 엽리구조를 나타내면서 광물 입자도 육안으로 식 별이 가능할 정도로 커진다. 편암에서의 엽리 특징은 구불구불하 며 파랑상 형태보다는 규모가 더 크다. 이를 특히 편리(片理, schi- s t os ity)라고 한다. 편암을 구성하는 주요 광물로는 석영, 백운 모, 혹운모, 각섬석, 십자석, 규선석, 남정석, 석류석, 녹니석 등 이 있다. 편마암(片麻岩) 매우 높은 압력이 가해질 때 만들어지는 암석으 로서, 암색층과 담색층이 교호하고 있는 특징적인 구조를 나타낸 다. 이러한 특이한 구조를 편마구조(片麻構造, gn e i ssos ity)라고 한 다. 편마구조가 만들어지는 과정에 대해서 확실히 밝혀진 것은 없 으나, 암석 속에 있던 광물들이 상하 이동을 한 결과인 것으로 추 정하고 있다. 죽 백색을 띠는 석영과 장석이 한데 모이고, 어두운 색을 지니는 각섬석, 혹운모 등이 따로 모여 각각 담색충과 암색
층을 형성한다. 석류석, 휘석, 각섬석, 근청석 등의 변성광물이 생성될 수 있다.
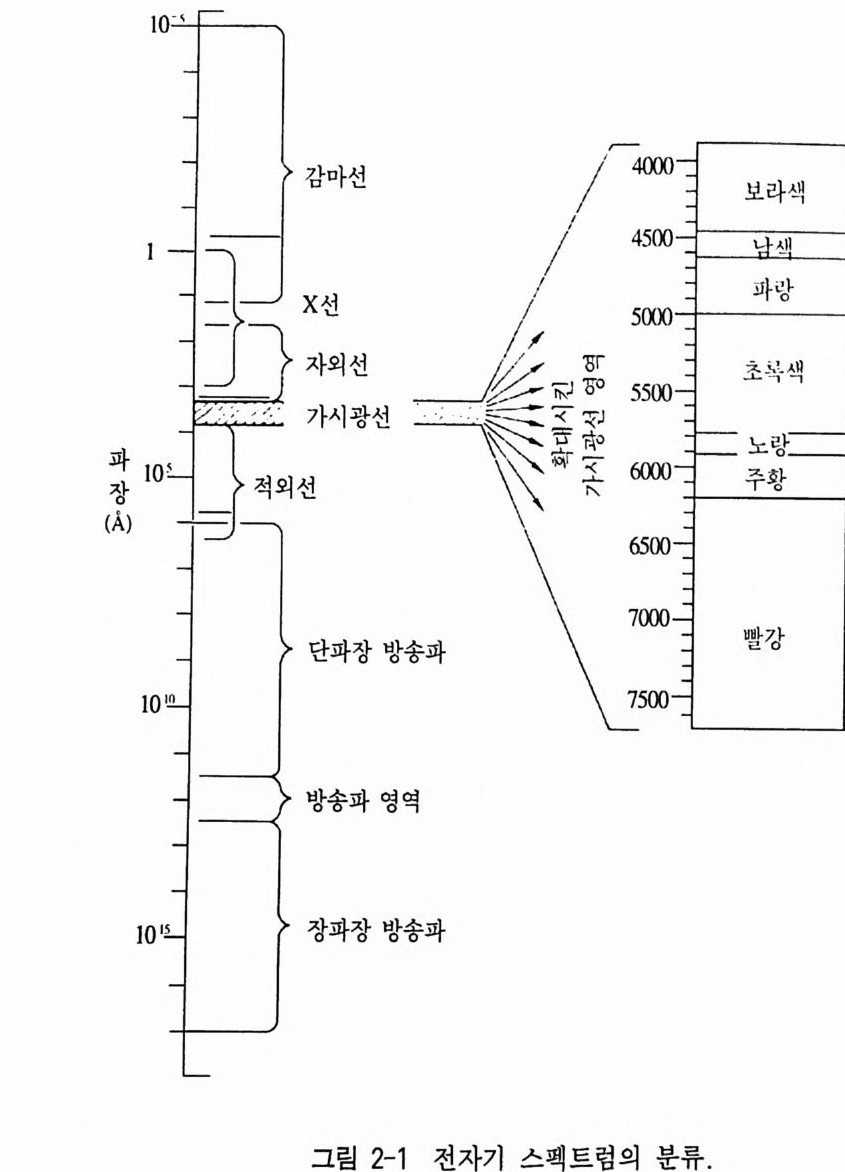
제 2 장 조암광물의 물리 • 화학적 성질 2.1 색 광 물 이 지니는 색을 몸색 (bod y color ) 이라고 하며, 흔히 색(色, color) 이라고 간략하게 표현한다. 색은 광물의 고유한 성질로서, 광 물 에 의해 반사되거나 통과된 빛이 우리 눈을 통해 뇌에 전달됨으 로써 느끼게 되는 것인데, 광물의 색을 느끼기 위해서는 반드시 빛 이 존재해야 한다 . 태양으로부터 나오는 빛은 파장이 다른 연속적인 에너지로 구성되어 있는데, 이를 전자기파( 電 磁 氣 波, electr om agn e tic wave) 또는 전자기 스펙트럼 (electr om agn e ti c s p ec tru m) 이라고 한다 (그림 2.1 ). 이 중 우리의 눈으로 느낄 수 있는 전자기파를 가시광 선(可視光線, v i s i ble lig h t)이라고 하며, 그 파장의 범위는 대략 3800 ~7800A 이다 . 가시광선에 속하는 모든 파장의 광선이 한데 모이 면 무색인 광선이 되는데 이를 백색광(白色光, wh ite light)이라고 한다. 뉴턴 (New t on) 은 백색광을 프리즘에 통과시켜 봄으로써 백색
 감마선 / ’ 400} 3900A
감마선 / ’ 400} 3900A
광은 여러 가지의 색으로 구성되어 있음을 발견하였으며, 각 색의 대 략적 인 파장의 범 위 는 다음과 같다 . 빨강 (7800~6300 A), 주황 (6300~5900 A), 노랑 (5900~5700 A), 연두 (5700~5500 A), 초록 (5500~5100 A), 청 록 (5100~4800 A), 파랑 (4800~4500 A), 보라 (4500~3800 A) 등이 다. 2.1.l 광물의 발색 원인 광물이 색을 띠는 가장 대표적인 원인은 가시광선에 속하는 파 장의 일부를 광물이 선택적으로 흡수하거나 또는 모든 색의 파장 울 고르게 홉수하기 때문이며, 그 밖에도 고체 불순물, 분산, 간 섭, 형광, 인광 등에 의해서도 색을 떨 수 있다. 한 가지 유념해 야 할 점은 동일한 광물인 경우, 화학적 • 결정구조적으로 순수하 고 완전할 경우에는 같은 색을 띠게 되지만 천연에서 산출되는 광 물처럼 주구성 성분 원소가 아닌 다론 원소를 함유하고 또 결정구 조의 완벽성이 유지되지 않는 경우에는 동일 광물일지라도 산출지 나 생성 환경에 따라 색깔이 다른 경우가 일반적이다. 여기서는 조암광물의 가장 일반적인 발색 원인인 홉수와 고체 불순물에 대 해서만 기술하기로 한다. 2.1.2 홉수 광물에는 가시광선의 일부 파장 또는 전부를 흡수할 수 있는 능 력이 있다 . 광물이 빛의 일부 파장만 흡수하는 것을 선택흡수(選擇 吸收, selecti ve abso rpti on) 라고 하며, 이때 느껴지는 색은 광물에 의 해 흡수되지 않은 파장들로 이루어진 잔류색(殘留色, resid u alcolor) 인 셈이며, 따라서 특정한 색을 띠게 된다. 가시광선에 속하는 파
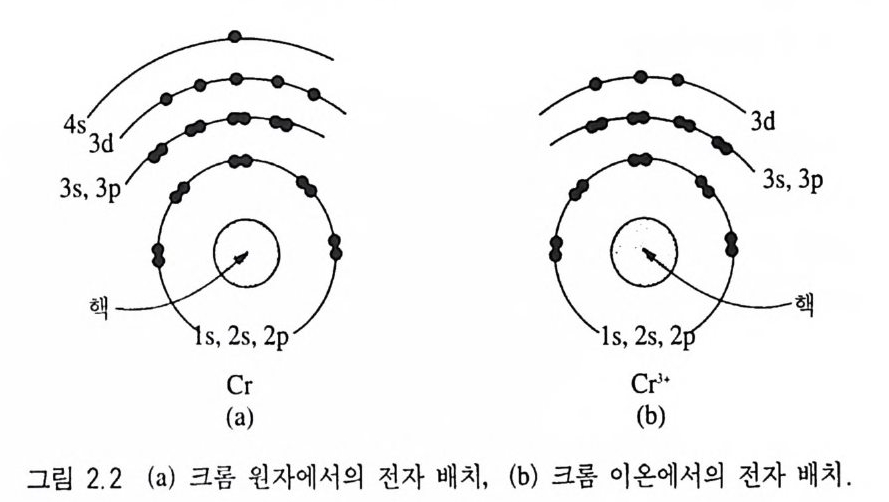
장을 모두 고르게 홉수하면 그 정도에 따라 무색, 회색, 검은색 등이 되는데 이 를 일반흡수( 一般 吸收, gen eral abso rpti on) 라고 한다. 광물에서 선택흡수가 일어나는 대표적인 원인에는 이른바 발색원소 (정社色元素, colori ng elemen t)라고 부르는 전이원소(轉 移元素, tran sit ion elemen t)가 존재하기 때문이다(표 2.1). 전이원소가 광물을 구성하 는 주요 화학원소일 경우 자색(自色, idio c hromatic color) 이라고 하 며(표 2.2), 이들 원소가 주구성 원소가 아닌 미량으로 포함되어 있는 경우 타색 (他色, allochromatic color) 이 라고 한다(표 2.3 ) . 강옥의 변종인 루비를 예로 들어 어떠한 과정으로 선택흡수가 일어나 적색을 띠는지에 대해 알아보자 . 강옥 (Ah0 3) 은 순수한 경 우 무색인데 소량의 크롬 원소를 불순물로 함유하여 적색을 띤다 . Cr3 .은 Al3. 을 치환하게 되는데 , 크롬 원자에는 원래 24 개의 전자가 원자핵 주위를 돌고 있고, 그 중 6 개가 쌍을 이루지 않은 상태로 있다(그림 2.2 a ). 그러나 Cr3 ♦ 이온에는 쌍을 이루지 않은 6 개의 전 자 중 3 개는 화학결합에 사용되고, 나머지 3 개만 쌍을 이루지 않 은 상태로 있게 된다(그림 2.2b). 루비가 빛을 받게 되면 이 3 개 의 전자가 빛에 있는 2.2e.V. (연두색)와 3.0e . V. (보라색)의 에너지 를 흡수하여 높은 궤도로 옮겨진다. 결국 루비에 닿은 가시광선 중 연두색과 보라색 파장의 에너지는 전자 이동에 소모되어 없어지고 그 나머지 파장들만 반사 또는 통과되어 아름다운 적색을 띤다. 루비의 적색을 구성하고 있는 실제 빛의 파장을 확인하기 위해 분 광기 (分光器, s p ec tr osco p e) 로 관찰한 결과는 그림 2 .3과 같으며, 연 두색과 보라색 영역의 파장이 흡수되어 검게 나타남을 알 수 있다. 동일한 발색원소라도 광물에 따라 색이 달라질 수 있다. 예를 뇰어 크롬이 녹주석에 존재하면 녹색을 띠게 하는데, 이것은 강옥 은 삼방정계이고, 녹주석은 육방정계의 결정구조를 하고 있어 크 롬의 최외각에 위치한 전자에 미치는 힘이 각각 다르기 때문이다 .
 표 2.1 발색 원소
표 2.1 발색 원소
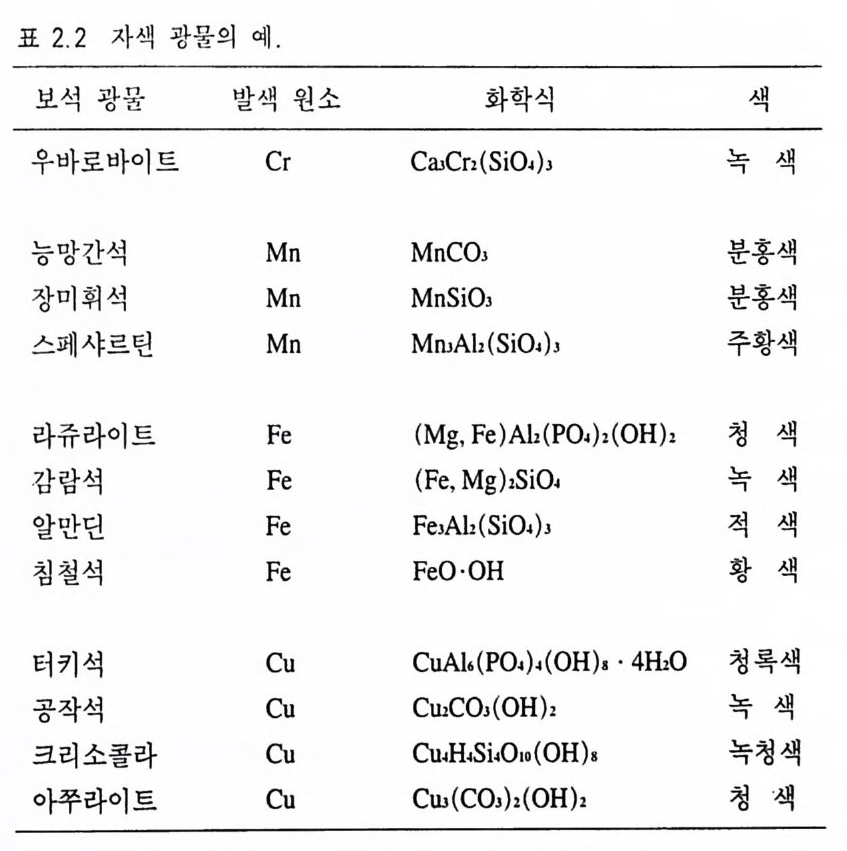 표 2.2 자색 광 물 의 예 .
표 2.2 자색 광 물 의 예 .
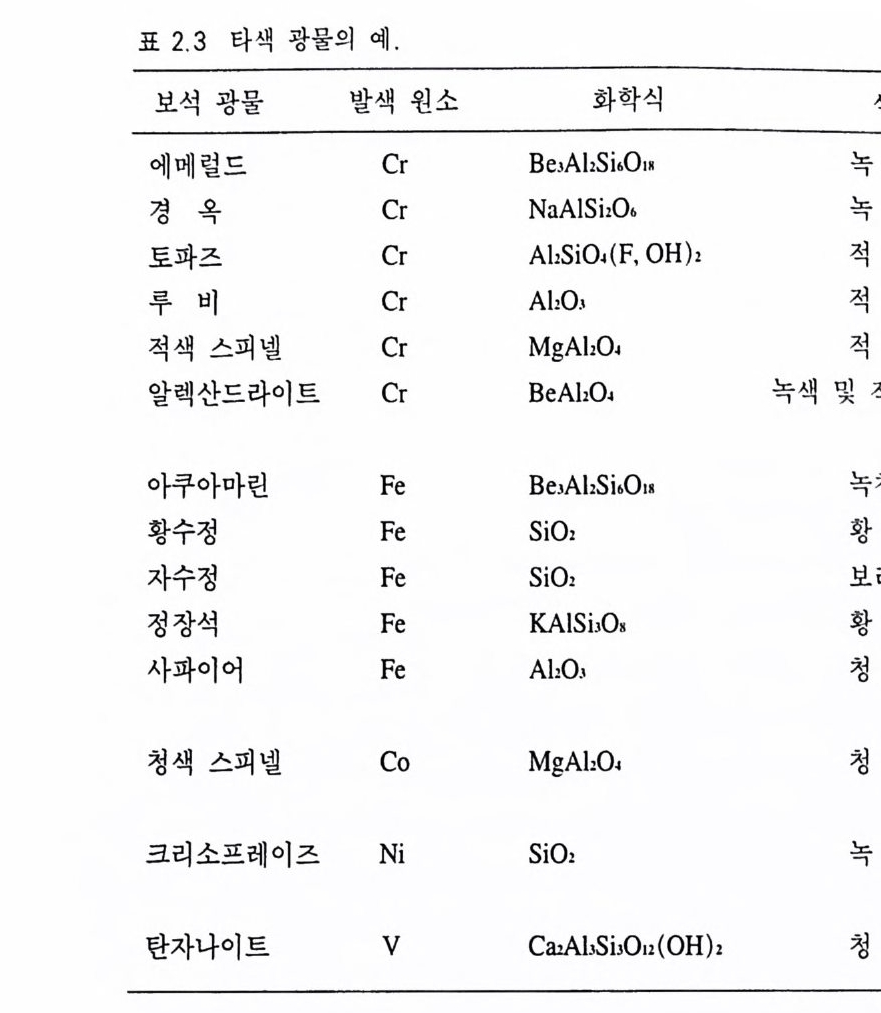 표 2.3 타색 광물의 예 .
표 2.3 타색 광물의 예 .
빛의 흡수를 일으키는 기타 요인으로는 착색 중심(着色中心)이라고 일컫는 컬러센터 (color cente r ), 분자궤도전이 (分子軌道轉移 molecular orbit al tr ans iti on) 에 따른 전하 이동(電荷移動, charge tran sfe r ), 외 래 원소(外來元素) 존재 등이 있다. 착색 중심은 전자의 결함구조(缺 格構造, defe c t s tru c tur e) 에 기인하는 것으로서, 형석인 경우 음전하
 d3
d3
의 전자가 불소이온의 자리에 자리잡기 때문에 발색이 되는 전자 컬러센터 (electr o n color cen t er) 의 경우이며, 연수정의 경우에는 S i 4 ♦ 대 신 Al3 ♦ 이 치 환하여 생 기 는 구멍 컬 러 센터 (hole color cente r ) 때 문에 발색이 된다. 전하 이동에 의한 발색은 서로 다른 산화수를 가지 는 2 개 또는 그 이상의 발색원소 이온이 궤도를 돌고 있을 때 일 어나며 근청석과 청색 강옥의 발색 원인이 된다. 황색 또는 청색 다이아몬드는 탄소와 전자수가 다른 질소나 붕소가 불순물로 들어 있기 때문에 발색이 되는데 이것은 외래 원소가 존재하기 때문에 생기는 빛의 홉수의 예이다 .
 그림 2.3 루비의 홉수 스펙트럼. 연두색과 보라색 영역에 넓은 흡수띠가 있음.
그림 2.3 루비의 홉수 스펙트럼. 연두색과 보라색 영역에 넓은 흡수띠가 있음.
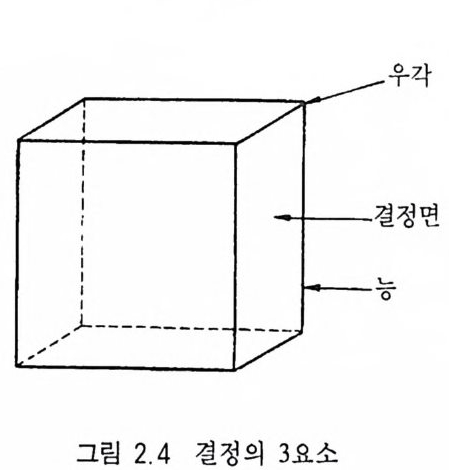
2.1.3 고체 불순물 칼세도니는 순수할 경우 회색 계통의 색을 띠고, 수정은 무색을 띠게 된다. 만약 칼세도니 속에 적철석 입자가 미세하게 분산되어 있으면 적색을 띠는데 이런 변종을 재스퍼 Uas pe r) 라고 한다. 석영의 경우는 미세한 녹니석이 함유되어 있으면 녹색을 띤다. 2.2 결정구조 광물은 〈구성 원자들이 3 차원적으로 규칙적인 배열을 하고 있는 천연 고체〉라고 표현할 수 있는데, 원자들이 공간적으로 배열할 수 있을 가능성은 230 가지이다. 이를 230 공간군(空間群, spa c e grou p ) 이라고 한다. 공간군을 대칭축, 대칭면, 대칭심 등 대칭의 3 요소의 조합으로만 분류하면 32 가지가 되는데 이를 32 정족(晶族, class) 또 는 점군(點群 poi n t gr ou p)이라고 한다. 결정구조를 대칭축만의 특 징으로 분류하면 7 가지 로 분류할 수 있는데 이 를 7 정 계 (晶系, cry st a l s y s t em) 라고 한다. 조암광물을 연구할 때 결정구조적인 내용을 잘 알고 있어야 광물의 결정형 및 광학적인 특징을 이해할 수 있게 된다. 2.2.1 결정 의 3 요소 결정질 고체가 결정면(結晶面)이라 불리우는 평탄한 면으로 둘 러싸여 있을 때 이를 결정(結晶)이라 한다. 결정에는 결정면뿐만 아니라 서로 나란하지 않은 두 개의 결정면이 만나는 능(稷, edg e)
 우각
우각
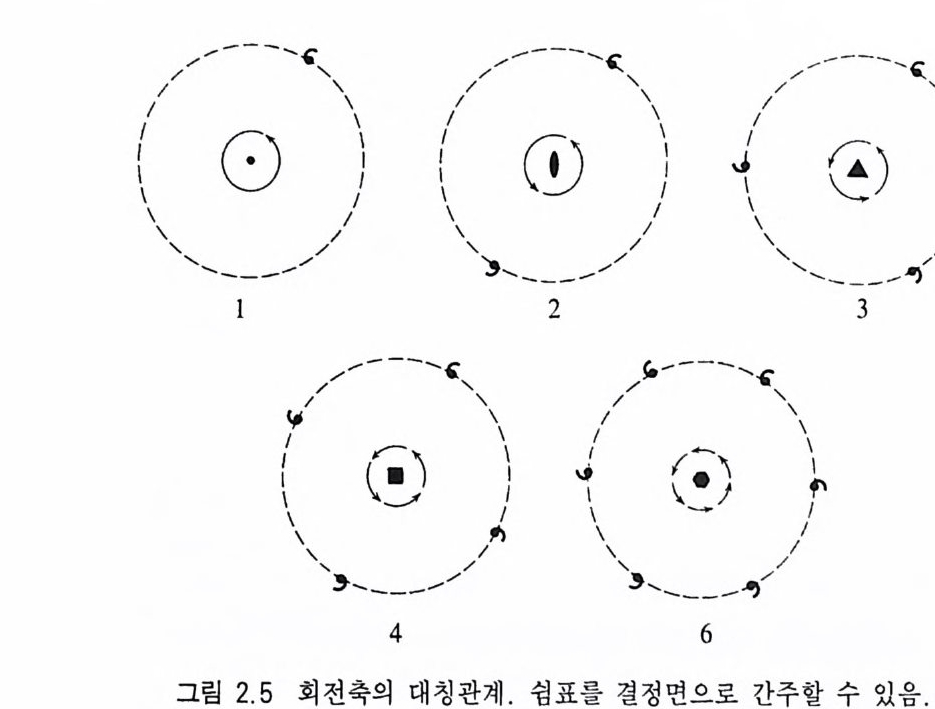
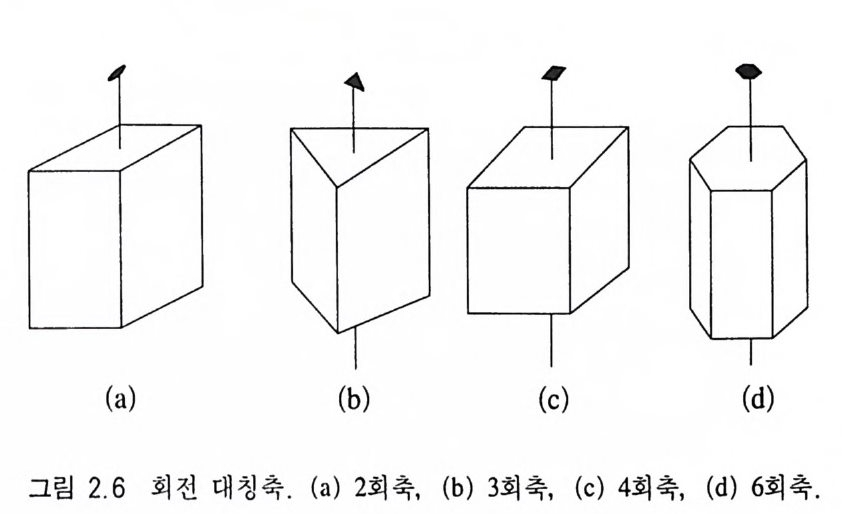
과 3 개 이상의 결정면이 만나는 우각(隅角, comer) 이 있다(그림 2.4 ). 이 3 요소를 〈결 정의 3 요소〉라고 하며 결정면 (F), 능 (E), 우 각 (C) 사이에는 F+C=E+2 인 관계식이 성립하는데 이를 〈오일러 의 방정 식 >(E uler' s equ a ti on ) 아 라고 한다. 2.2 .2 대 칭 의 3 요소 결정을 회전하거나 양분할 때, 또는 반전시킬 경우 결정의 외 부 특징이 동일한 형태로 규칙적으로 반복될 수가 있는데 이를 대칭 (對稱 s y mme try)이라 하고, 이러한 과정을 대칭조작(對稱操 作, sym metr y op era ti on) 이라고 한다. 결정의 중심을 통과하는 직선 울 기준으로 3(j() ° 회전했을 때 크기와 모양이 같은 동일한 형태가 규 칙적으로 반복될 때 이 회전시킨 축을 회전대칭축(回轉對稱軸 rota tion axis o f s ymm e try)이 라 하며 간단히 회전축(回轉軸 rota t io n ax i s) 이라 고도 한다. 결정을 한 바퀴 회전시킬 때 동일한 형태가 1 회, 꼬], 3 회, 4 회, 6 회 반복될 수가 있는데(그림 2.5 ) 이때 회전시킨 직선 방 향을 각각 1 회, 2 회, 3 회, 4 회, 6 회 회전축이라 하며, 1 회 회전축
 {/\/ \/ \ /\ / (\Oll‘\\ \\I/ I/)/l/// 1 \/ / \ D /\ /`- -_一_ _ 一_- -`/
{/\/ \/ \ /\ / (\Oll‘\\ \\I/ I/)/l/// 1 \/ / \ D /\ /`- -_一_ _ 一_- -`/
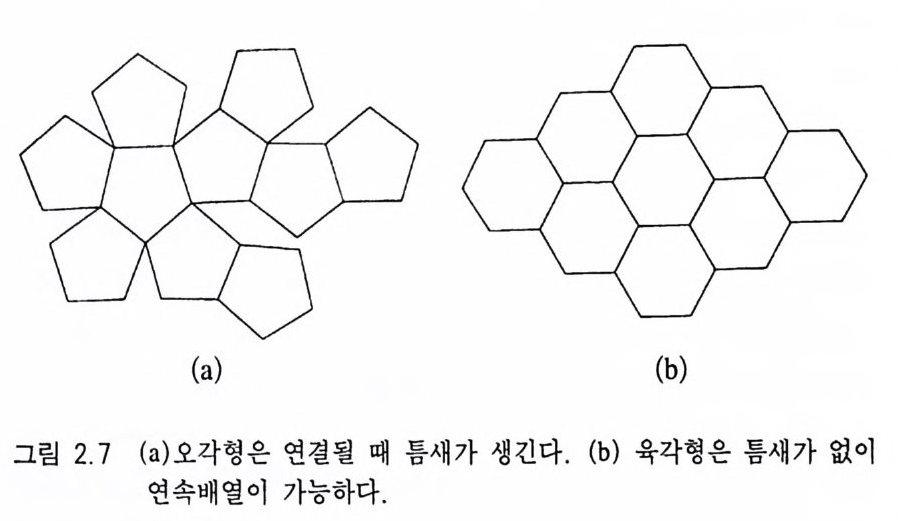
은 어떤 결정에서도 나타날 수 있으므로 대칭축으로 간주하지는 않는다. 따라서 회전대칭축에는 2 회, 3 회, 4 회, 6 회 등 4 가지가 있다(그림 2.6). 5 회 대칭축이 없는 이유는 원자들이 5 회 대칭을 유 지한 채로 3 차원적인 배열을 연속적으로 할 수 없기 때문이다(그림 2.7 a ). 대칭축에는 회전축(回轉對稱軸)뿐만 아니라 회반축, 회영축 등이 있으며 대칭축이라 할 때는 일반적으로 회전대칭축을 의미한 다. 회전대칭축의 특징과 표시법은 표 2 .4와 같다. 결정을 양분시킬 경우 결정의 특징(크기, 모양, 결정면, 능, 우 각)이 그 면을 기준으로 거울에 비친 것같이 대칭적으로 존재할 때 이 양분시킨 면을 대칭면(對稱面, p laneo f s y mme try)이라 한다 (그림 2.8). 대칭면은 m 또는 P 로 표시한다. 또한 결정의 한 쪽에 있는 모든 특징들이 결정 내에 있는 한 점 울 기준으로 같은 거리의 반대쪽에 투영시킨 것처럼 존재할 때 이
 (a) (b) (c) (d)
(a) (b) (c) (d)
 (a) (b)
(a) (b)
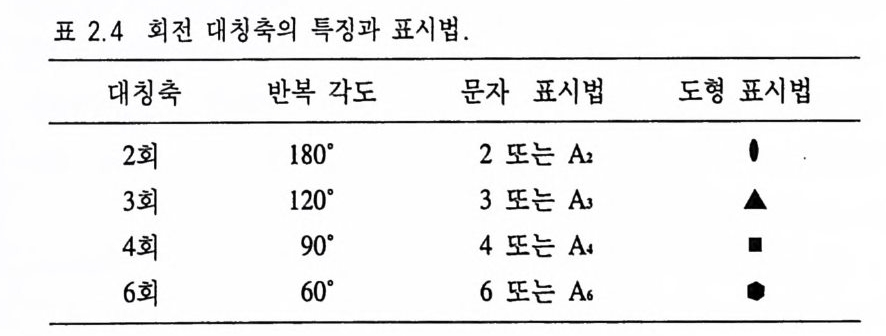 표 2.4 회전 대칭축의 특징과 표시법 .
표 2.4 회전 대칭축의 특징과 표시법 .
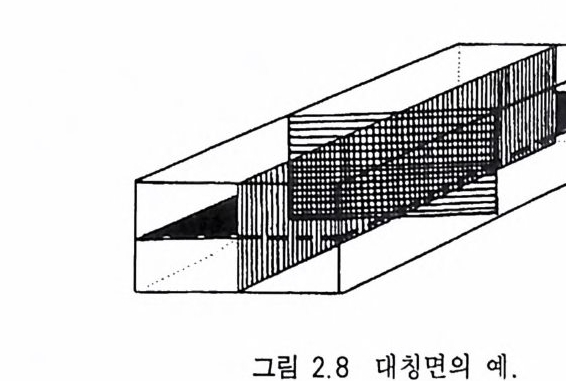 그림 2.8 대칭면의 예 .
그림 2.8 대칭면의 예 .
 A
A
점을 대칭심 (對稱心, cen t ero f s y mme try)이라 한다(그림 2.9). 대칭심 은 C 또는 i로 표시한다. 결정에 대칭심이 있는지를 쉽게 알 수 있는 방법은 그 결정에 있는 모든 결정면에 대해 한 결정면을 평 면 위에 놓아 밀에 있는 결정면과 동일한 모양과 크기를 가지는 결정면이 위에 수평으로 존재하고 동시에 그 방향이 반대일 경우 라면 그 결정에는 대칭심이 있다는 결론을 내릴 수가 있다. 대칭 축, 대칭면, 대칭심을 〈대칭의 3 요소〉라고 한다. 회반축(廻反軸 ro t o in vers i on axi s) 은 회전의 개념에 반전(反轉 in- vers i on) 이 결합된 것이라 할 수 있으며 숫자 위에 -(bar) 를 사용하
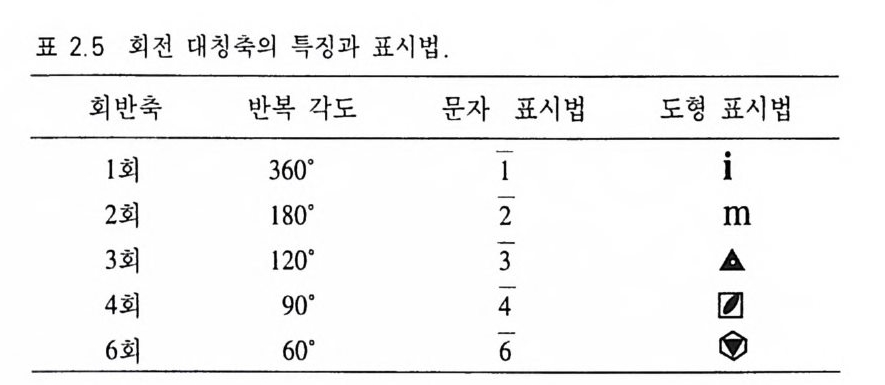 표 2.5 회전 대칭축의 특징과 표시법 .
표 2.5 회전 대칭축의 특징과 표시법 .
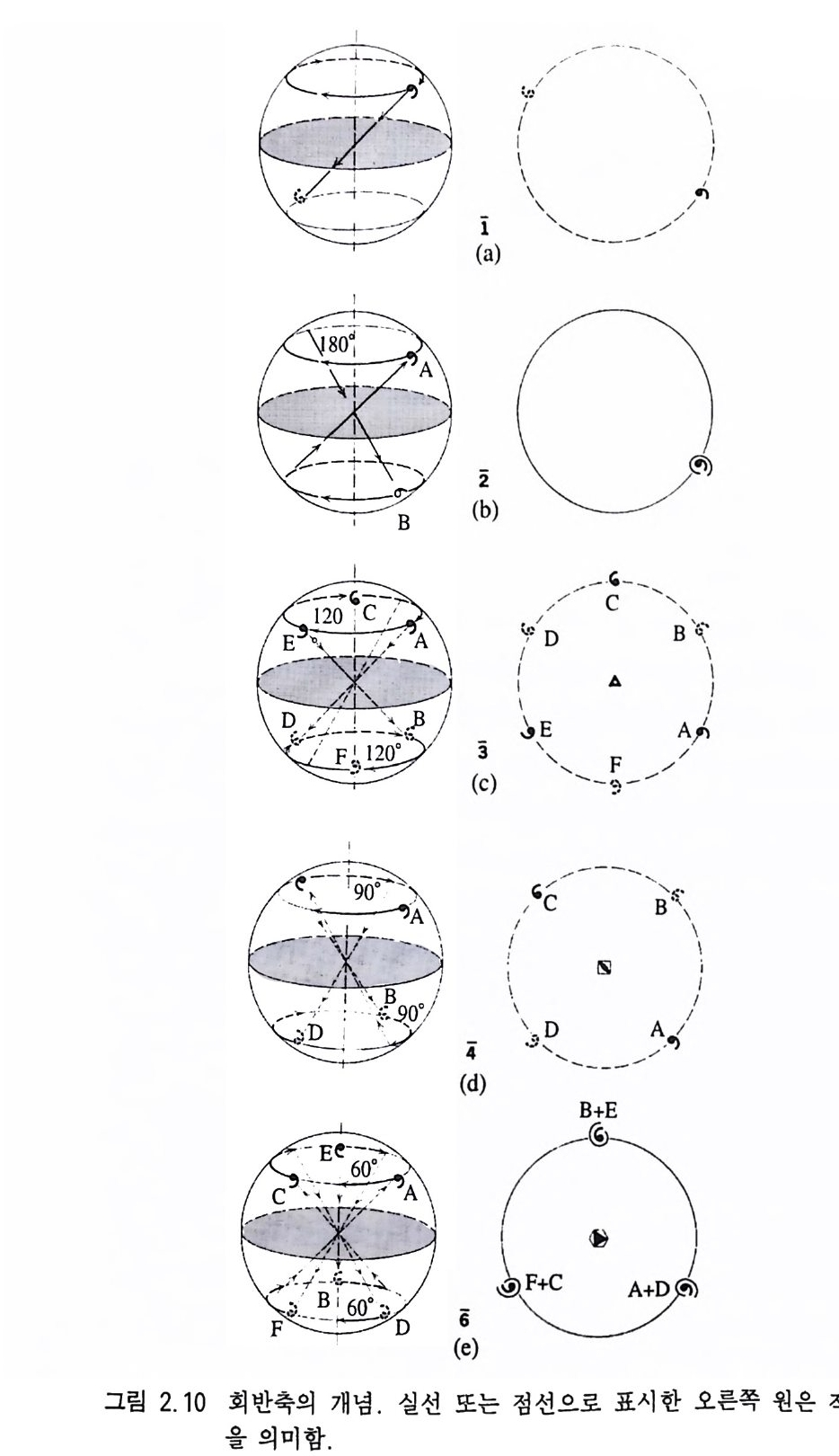
여 나타내고(ii), 기호법은 표 2.5 와 같다. 회전축은 그림 2 .5처럼 같은 형태가 동일한 위치에 규칙적으로 반복되는 경우이지만 회반 축은 일단 회전을 시킨 다음 계속하여 반전을 시켜야 한다. 예를 들어 지구의 북반구에 한 점이 있을 때(그림 2.1 0 ) 1 회 회반축 (I) 은 북극과 남극점을 연결한 축을 따라 360° 를 회전시키고, 이어서 지 구 중심을 통해 아래로 반전을 시키면 된다. 그리고 적도 아래의 남반구에 있는 이 점을 다시 360° 회전한 후 지구 중심을 기준으 로 반전시키면 북반구에 있던 원래의 점에 되돌아 오게 된다 (a). 적도면 위에 있는 점은 실선으로, 그리고 그 아래 있는 점은 점선 으로 표시하였다. 완성된 회반축의 결과를 얻기 위해서는 같은 그 림이 반복될 때까지 계속 시행하여야 한다. 2 회 회반축 (2) 은 북반 구의 점을 180° 회전시킨 다음 계속하여 지구 중심을 통해 반전시 킨다. 그리고 같은 그림이 계속 반복될 때까지 과정을 되풀이한다 (b) . 3 회 회반축 (3) 은 북반구에 있는 점을 120° 회전시킨 후 지구 중심을 통해 남반구로 반전을 시키고, 계속 이를 120° 회전시켜 다시 북반구로 반전시키는 과정을 되풀이한다 (c). ~ 회반축 (4) 은 900 의 간격으로, 6 회 회반축 (6) 은 600 의 간격으로 동일한 과정을 반복하면 된다 (d,e). 홍미로운 사실은 1 회 회반축은 대칭심 (C), 2 회 회반축은 대칭면 (m), 3 회 회반축은 3 회 회전축과 대칭심이 결
 ,. /一 _.—\ \
,. /一 _.—\ \
 (a)o: 三) CJ 웅
(a)o: 三) CJ 웅
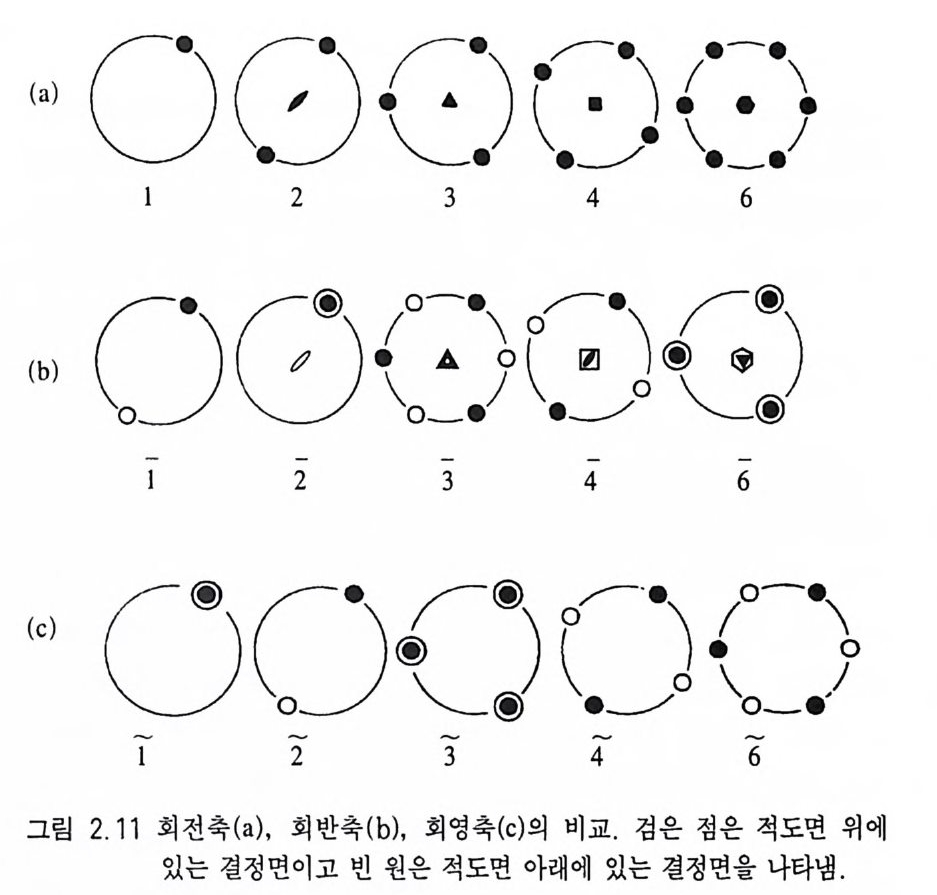
합되어 있는 것 (3+C), 그리고 6 회 회반축은 3 회 회전축에 대칭면이 결합되어 있는 것 (3/m) 과 동일하다는 점이다. 회영축(廻映軸 roto r efl ec ti on ax i s) 은 회전과 반사가 결합된 것이 다 즉, 주어진 각도만큼 회전시킨 다음 계속하여 적도면을 기준으 로 반사시킨다. 회영축의 표시법은 숫자 위에 . ~를 사용한다(ii). 1 회 회영축은 대칭면 (m), 2 회 회영축은 대칭심 (C), 3 회 회영축은 3 회 회전축에 대칭면이 결합된 것 (3/m), 6 회 회영축은 3 회 회전축 에 대칭심이 결합되어 있는 것 (3+C) 과 동일한 기능이 있다. 회영 축을 나타내는 기호법은 따로 없다. 회반축과 회영축의 관계는 1=2, 2=1, 3=6, 4=4, 6=3 이 다. 결정면에 대한 회전축, 회반죽 회영축의 상호관계는 그림
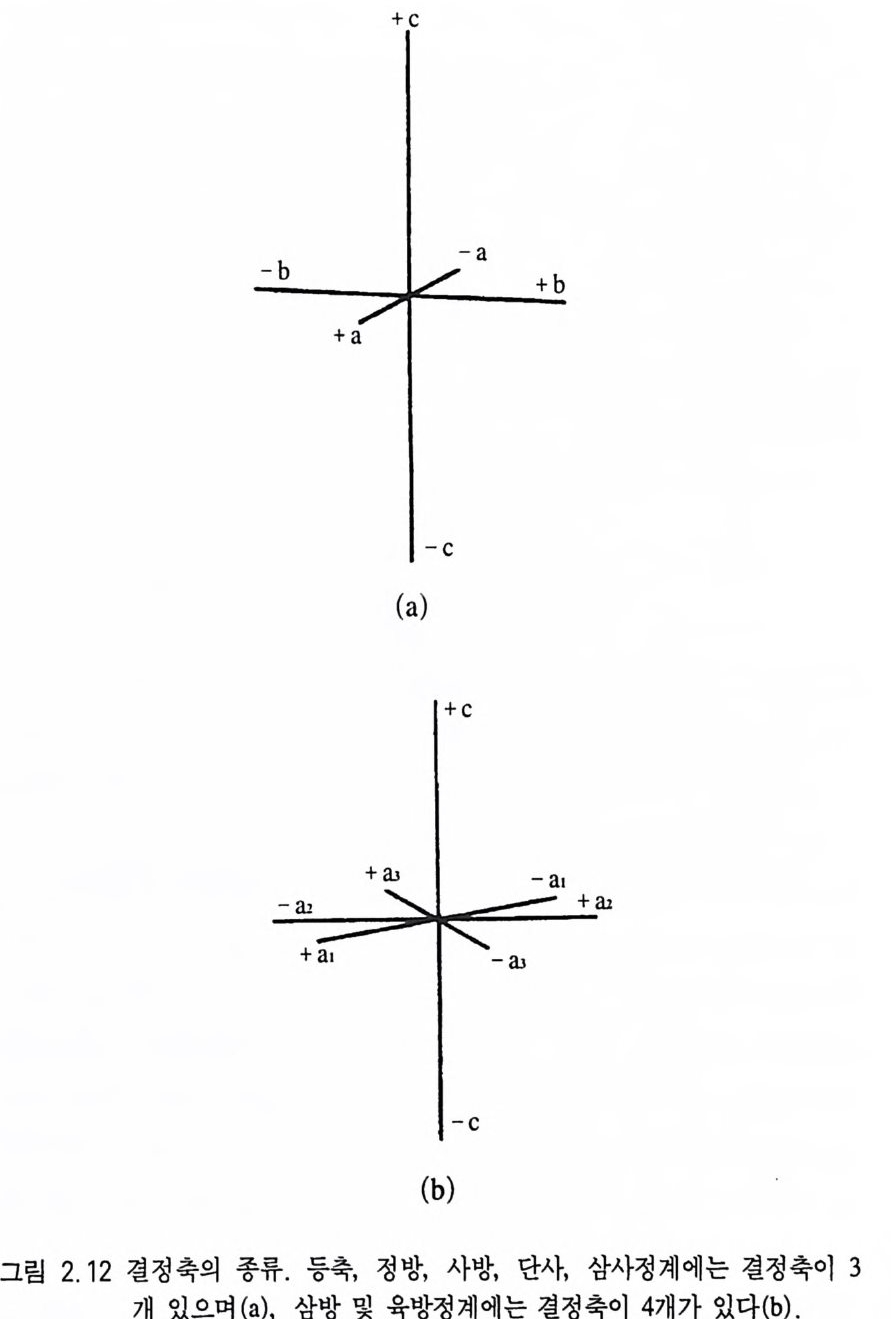
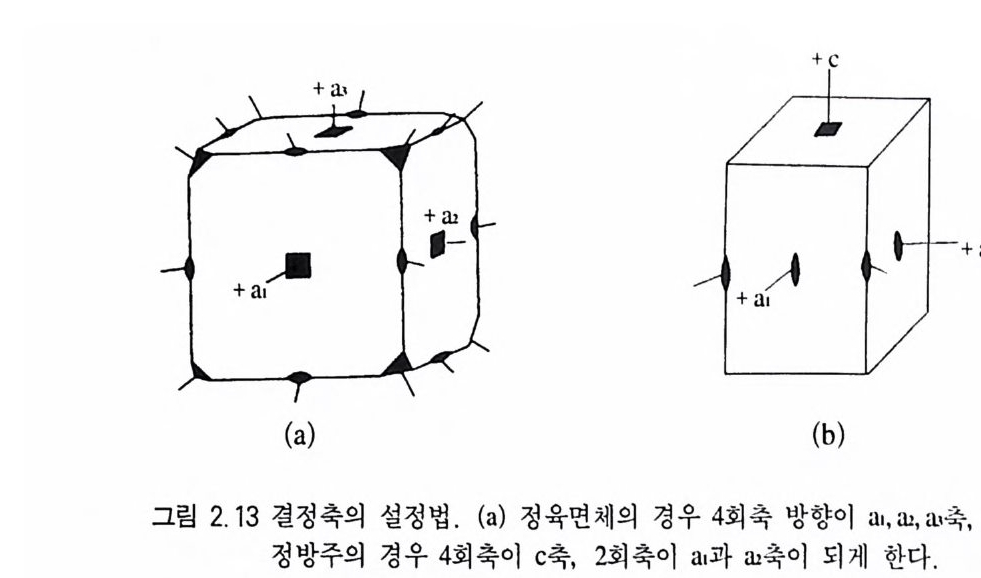
2.11 과 같다. 결정의 대칭을 나타낼 때 회반축이나 회영축을 사용 하지 않고 회전축을 사용하는 이유는 회반축과 회영축의 기능을 회전축에 대칭면 또는 대칭심을 결합시켜 표현할 수 있기 때문이 다, 2.2,3 결정축과 축각 결정축(結晶軸 cryst al log r aphic axi s) 이 란 결정의 특징 (결정면, 능, 우 각)을 공간적으로 나타내는 데 필요한 최소한의 기준 방향을 말하 는데, 결정계에 따라 3 개 또는 4 개가 있다. 결정축은 a, b,C 로 표시 하며 a 는 전후축(前後軸), b 는 좌우측(左右軸), c 는 수직 축(垂直軸)을 나타낸다. 이들 결정축이 교차하는 점을 근원점(根源點 o rigi n) 이라 고 한다. 근원점을 기준으로 a 축은 앞쪽이 (+), b 축은 오른쪽이 (+), C 축은 위쪽이 (+) 방향이며, 이와 반대 방향들은 (-)가 된 다. 결정축과 결정축이 교차하여 이루는 사잇각을 축각(軸角, axia l ang le) 이라고 하는데, b 축과 c 축이 이루는 각 (b/\c) 을 a, a 축과 c 축 이 이루는 각 (a/\c) 을 /3, a 축과 b 축의 각 (a/\b) 을 y로 표시 한다. 삼방정계와 육방정계에는 수평 방향의 동일한 축이 3 개 (a,, a2, &), 이들에 수직인 c 결정축 등 모두 4 개의 결정축이 있다(그림 2.1 2 ) . 2.2.4 결정축과 대칭축과의 관계 결정축을 설정할 때에는 그 결정에 존재하는 대칭축과 관련하여 정한다. 만약 대칭축이 있는 결정인 경우 대칭축과 결정축을 일치 시킨다. 대칭도가 다른 대칭축이 다수 존재할 경우에는 대칭도가 높은 대칭축과 결정축을 일치시킨다• 예를 들어 그림 2 .1 3 와 같이
 +c
+c
 +c
+c
 +b
+b
 +c
+c
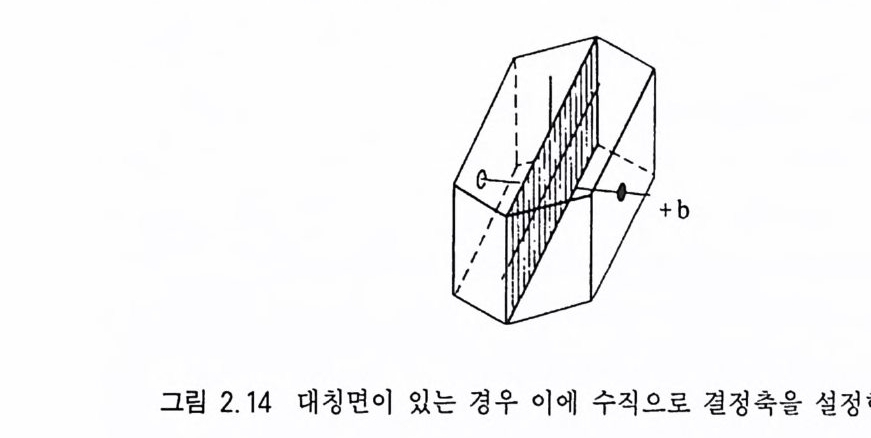
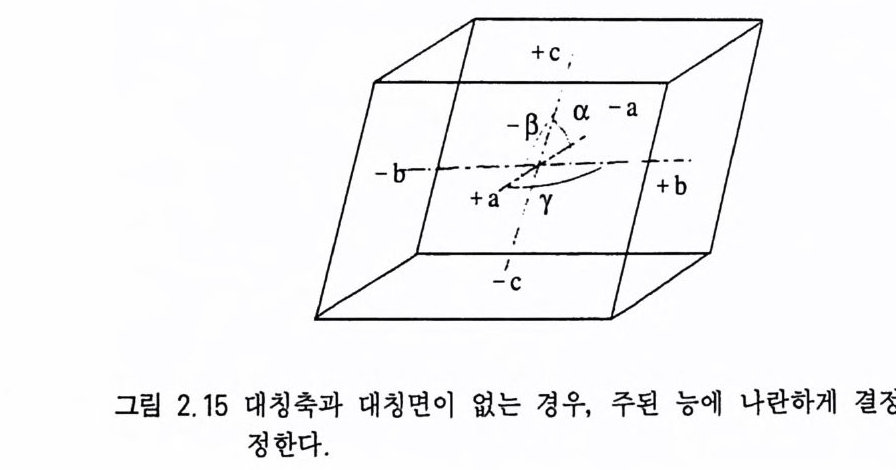
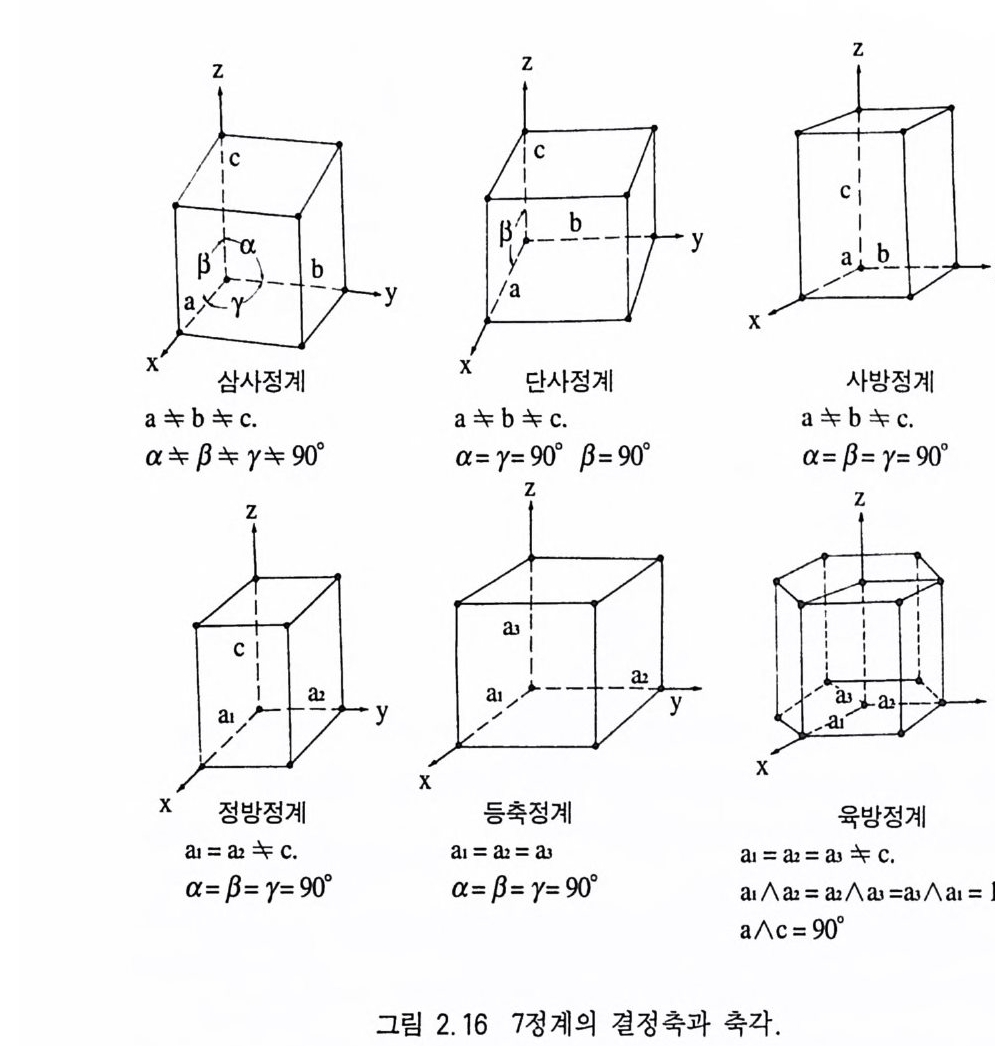
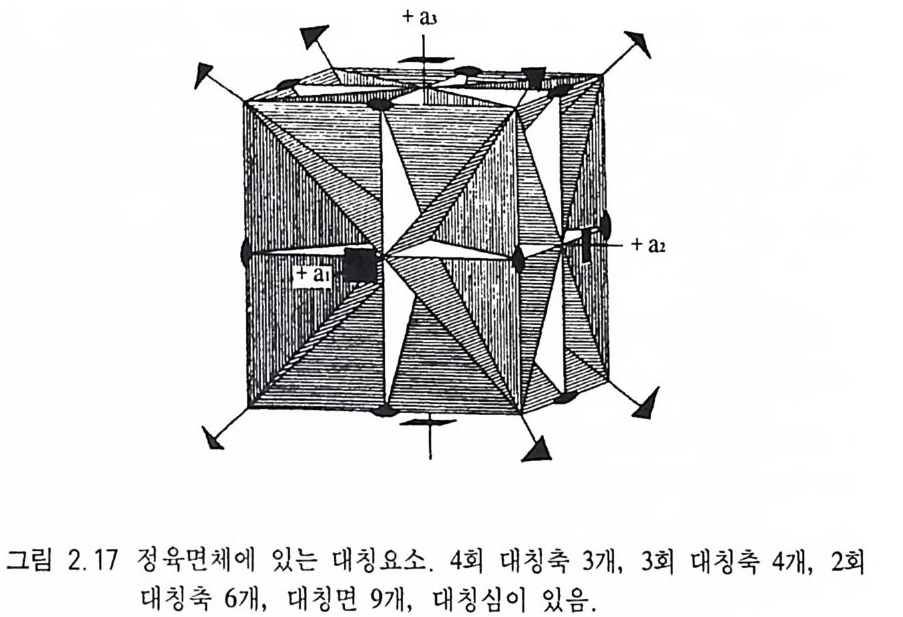
정육면체에는 4 회 대칭축이 3 개, 3 회 대칭축이 4 개, 2 회 대칭축이 6 개가 존재한다 . 따라서 결정축은 최대 대칭도를 나타내는 4 회 대 칭축과 일치시키고 각각 a,b,c 로 표시하면 되는데, 등측정계인 정 육면체의 경우, 세 결정축 (a,b,c) 이 모두 성질이 동일하므로 a1,a i, 印로 표시 한다. 이 때 1, 2, 3 은 전후축, 좌우측, 수직 축을 각각 의 미한다 대칭축은 없고 대칭면만 있는 경우에는 대칭면에 수직인 방향으로 결정축을 위치시킨다(그림 2.1 4 ). 대칭축과 대칭면이 모 두 없는 경우에는 그 결정에 있는 가장 큰 결정면들이 교차하여 만 들 어지는 능에 나란하게 결정축을 설정한다(그림 2.1 5 ). 이때 결 정축은 결정면에 직각이 아니고 바스듬히 통과하는 상태가 된다. 2.2.5 7 정계 모든 광물 결정은 대칭축의 대칭도 특징에 따라 7 가지로 분류되 는데 이 를 7 정계라고 한다(그림 2.1 6 ). 과거에는 결정축과 축각의 특징에 따라 6 정계로 분류하였다. 등축정계 이 정계에 속하는 결정에는 반드시 3 회 대칭축이 4 개 있다 . 이러한 특징을 가지는 등축정계(等軸晶系, cub i cs y s t em) 의 결 정을 공간적으로 나타낼 때 서로 직각인 3 개의 동일한 결정축이 필요한데, 결정축은 3 개의 4 회 대칭축 방향과 일치시킨다. 따라서 a=b=c 가 되어 이를 a,=&=& 로 표시하며, 축각은 a=f3 =r= 90° 이다. 등측정계에 속하는 결정들이 가질수 있는 최대 대칭요소 는 3A4, 4AJ , 6A i, 9m, C 이 다(그림 2.1 7 ) . 정방정계 이 정계에 속하는 결정은 반드시 4 회 대칭축을 하나 가 진댜 이러한 특징을 지니는 정방정계(正方晶系, tetr a g o n alsys te m )
 z z z
z z z
의 결정을 공간적으로 표시하기 위해서는 서로 직각인 결정축이 3 개가 필요한데, 그 중 전후(前後), 좌우(左右) 방향의 결정축은 성 질이 동일하다 (a=b). 따라서 수직방향의 4 회 대칭축과 c 결정축을 일치시키고, 2 개의 2 회 대칭축에 a 와 b 결정축을 일치시킨다. 결국 a[=&:: !i;:c , a= /3=y= 90° 인 관계가 성립한다. 정방정계에 속하는 결정이 가질 수 있는 최대 대칭요소는 1A4, 4&, 5m , C 이다.
 +a2
+a2
사방정계 서로 직각으로 교차하는 2 회 대칭축이 3 개 있는 결정계 로서, 이 3 개의 2 회 대칭축과 결정축을 일치시킨다. 2 회 대칭축의 성질이 모두 다르고 직각이므로 a~b~c, a= f3=y= 90° 가된다. 사 방정계( 斜方晶系 , o rt horhomb i cs y s t em) 에 속하는 결정이 가질 수 있 는 최대 대칭요소는 3A2, 3m, C 이다 단사정계 2 회 대칭축이 하나 있다. 수평 방향의 꼬 1 대칭축을 b 결 정축과 일치시키고, 앞쪽으로 기울어진 능의 방향과나란하게 a 축 울, 수직방향의 능에 나란하게 c 결정축을 위치시킨다. a 와 c 결정축 의 축각(p)은 직각이 아니며, +a 방향 쪽이 90° 보다 크다. 따라 서 a~b~c, a=y =9 0°, f3픽 900 이다. 이때 a 와 c 결정축은 결정면 에 수직 이 아닌 상태 로 교차한다. 단사정 계 (單斜晶系, monoclin ic s y s t em) 의 결정이 가질 수 있는 최대 대칭요소는 lA i, lm, C 이다.
삼사정계 대칭축이 없는 정계로서, 크게 발달한 결정면 들 이 교 차하여 만들어지는 능에 나란하게 3 개의 결정축을 잡는다. 축각은 모두 직 각이 아니 다. 따라서 a=s; :b =s ;:c , a= i;:f3=s;=,o] 다. 삼사정 계 ( 三 斜晶系, tricl in i c s y s t em) 의 결정이 가질 수 있는 최대 대칭요소는 C 이댜 삼방정계 3 회 대칭축이 하나 있는 정계이다 . 결정축은 4 개로서 수직축 (c) 은 3 회 대칭축과 일치시키고, 나머지 결정축 3 개는 2 회 대칭축과 일치시킨다 . 3 개의 수평축은 한 평면 내에 있고 모두 동 일한 특징을 가지므로 a1, ai, aJ로 표시한다. 결정축과 축각의 관 계는 a1=a2=a J=s;:c , +a1/\ 十&= +ail \ +aJ= +aJ/ \ +a1= 120°, a/\ c=90° 이다. 삼방정계(三方晶系 trig onals y s t em) 에 존재할 수 있는 최대 대칭요소는 lAJ , 3Az, 3m, C 이다. 육방정계 6 회 대칭축이 하나 존재하는 정계이다. 결정축의 수효 와 축각의 관계는 육방정계와 동일하지만 c 결정축이 6 회 대칭축이 되며, 나머지 3 개의 수평 방향의 결정축 (a1, ai, &)은 2 회 대칭축과 일치시킨다. 육방정계(六方晶系 hexa g onals y s t em) 에 존재할 수 있 는 최대 대칭요소는 lA6, 6k, 7m, C 이다. 7 정계에서의 결정축과 축각의 특징, 최대 대칭도는 표 2.6 과 같다. 2.2.6 결정형 결정에 발달한 결정면들 중에서 동일한 결정면이 하나 이상 있 고 또 이들이 그 결정에 존재하는 어느 대칭요소에 의해서 서로
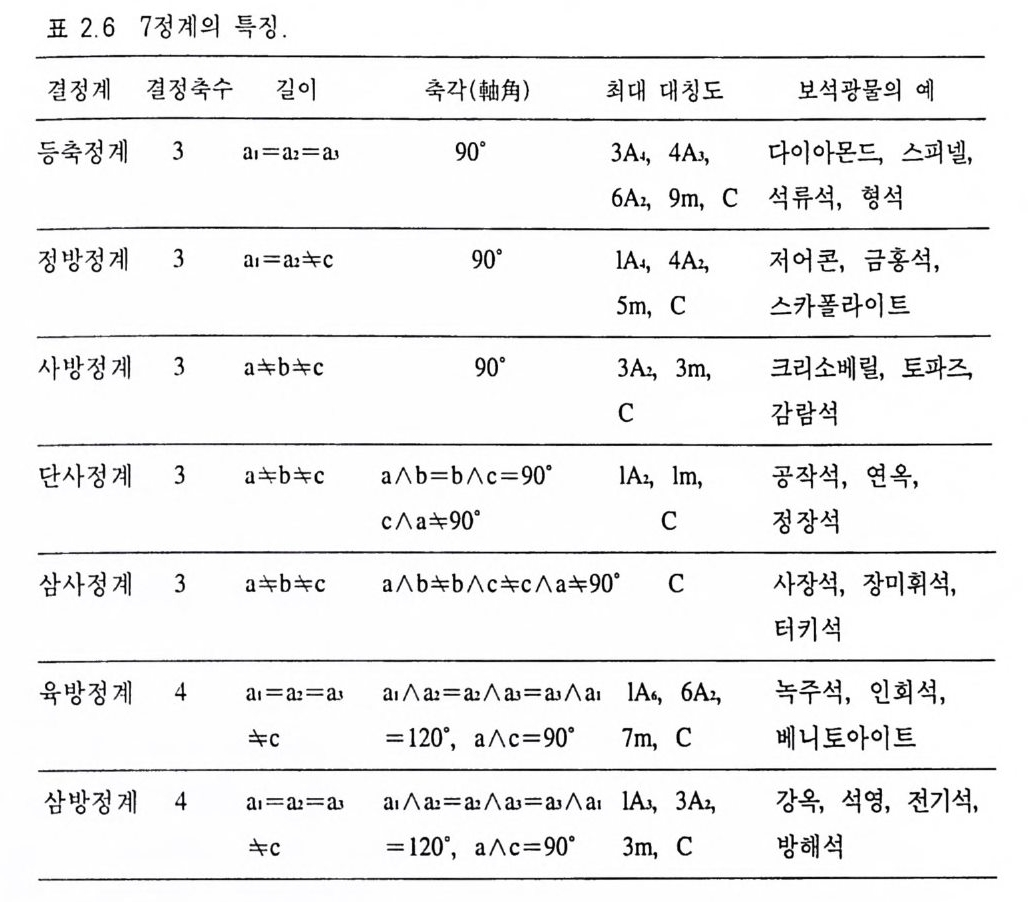 표 2.6 7 정계의 특징.
표 2.6 7 정계의 특징.
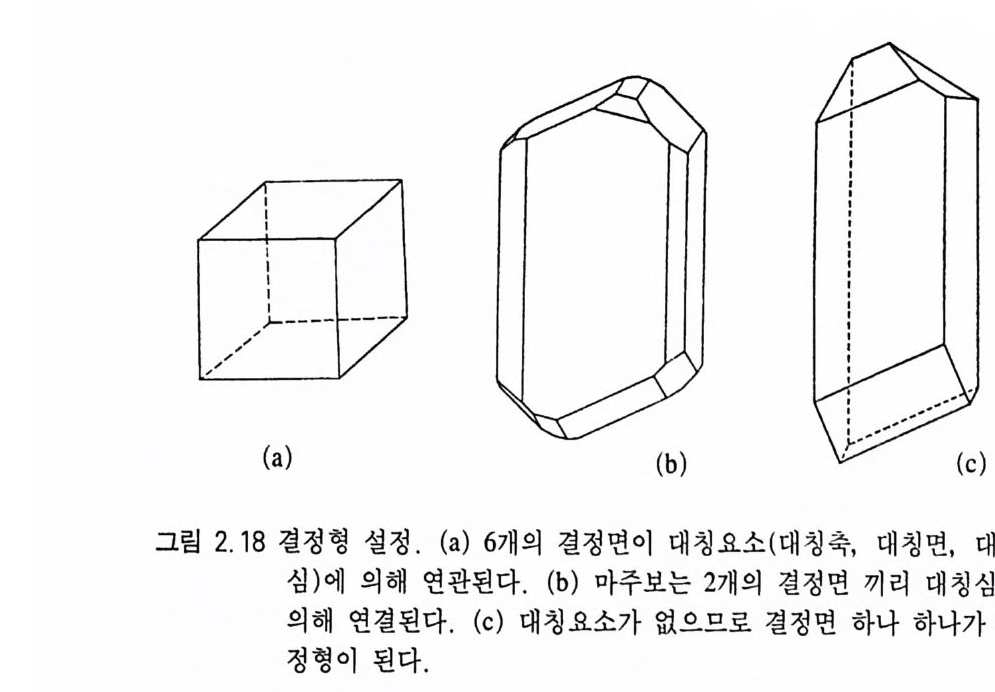
연관될 경우 이 결정면들은 하나의 결정형(結晶形, Fonn) 을 이루 게 된다. 즉, 결정형이란 〈대칭요소에 의해 연관되는 하나 이상의 동일한 결정면들의 집합체〉라고 정의할 수 있다. 여기서 〈동일한 결정면〉이라는 의미는 모양과 크기가 같아야 한다는 뜻이다. 〈대칭 요소〉라 함은 그 결정에 존재하는 대칭축, 대칭면, 대칭심을 말하 며, 이 중 어느 하나 이상의 요소에 의해서 서로 연관되어야 한다. 예를 들어 등축정계에 속하는 정육면체(그림 2 .1 8a) 에는 정사각형 모양의 결정면이 6 개가 있고 이들은 이 결정에 존재하는 4 회 대칭축 이나 3 회 대칭축, 또는 대칭면, 대칭심에 의해 서로 연관된다. 따라
 (a) (b)
(a) (b)
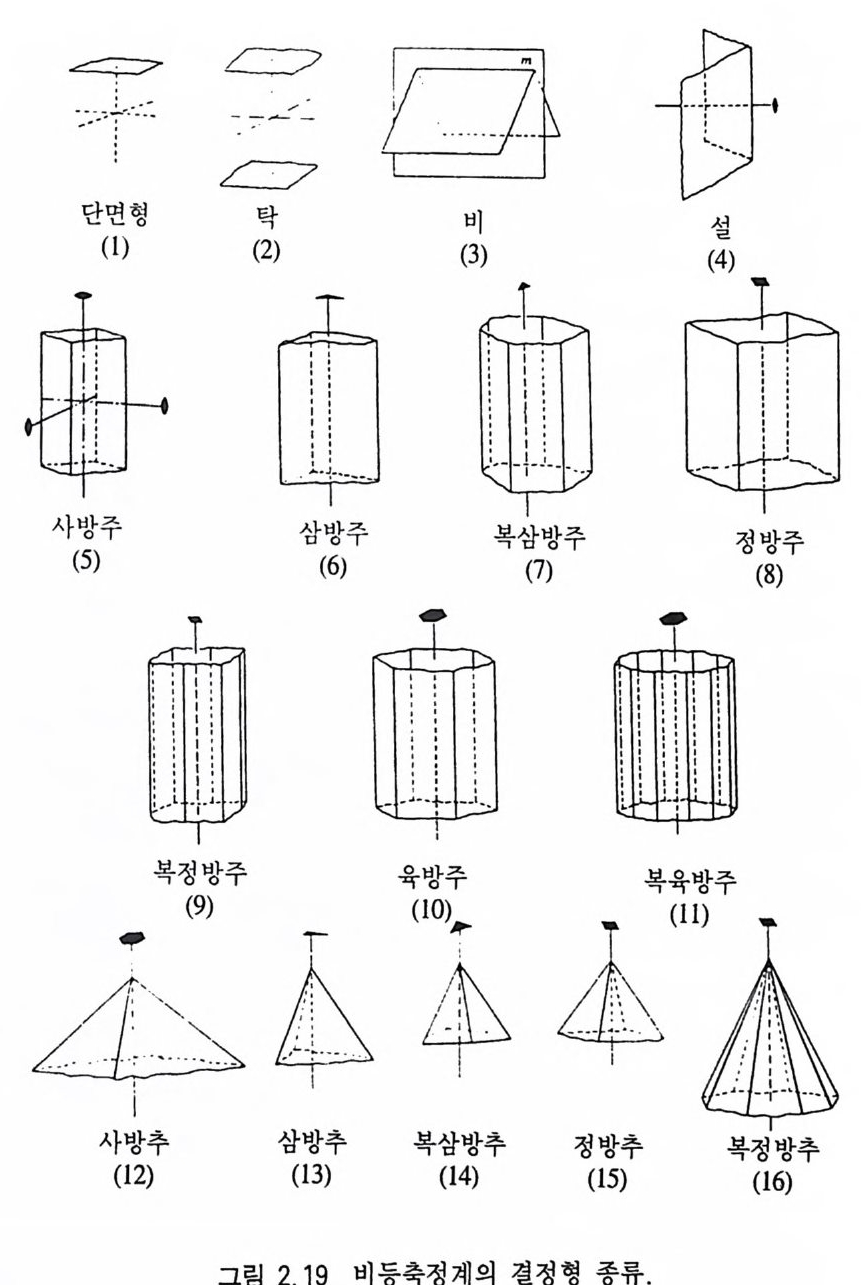
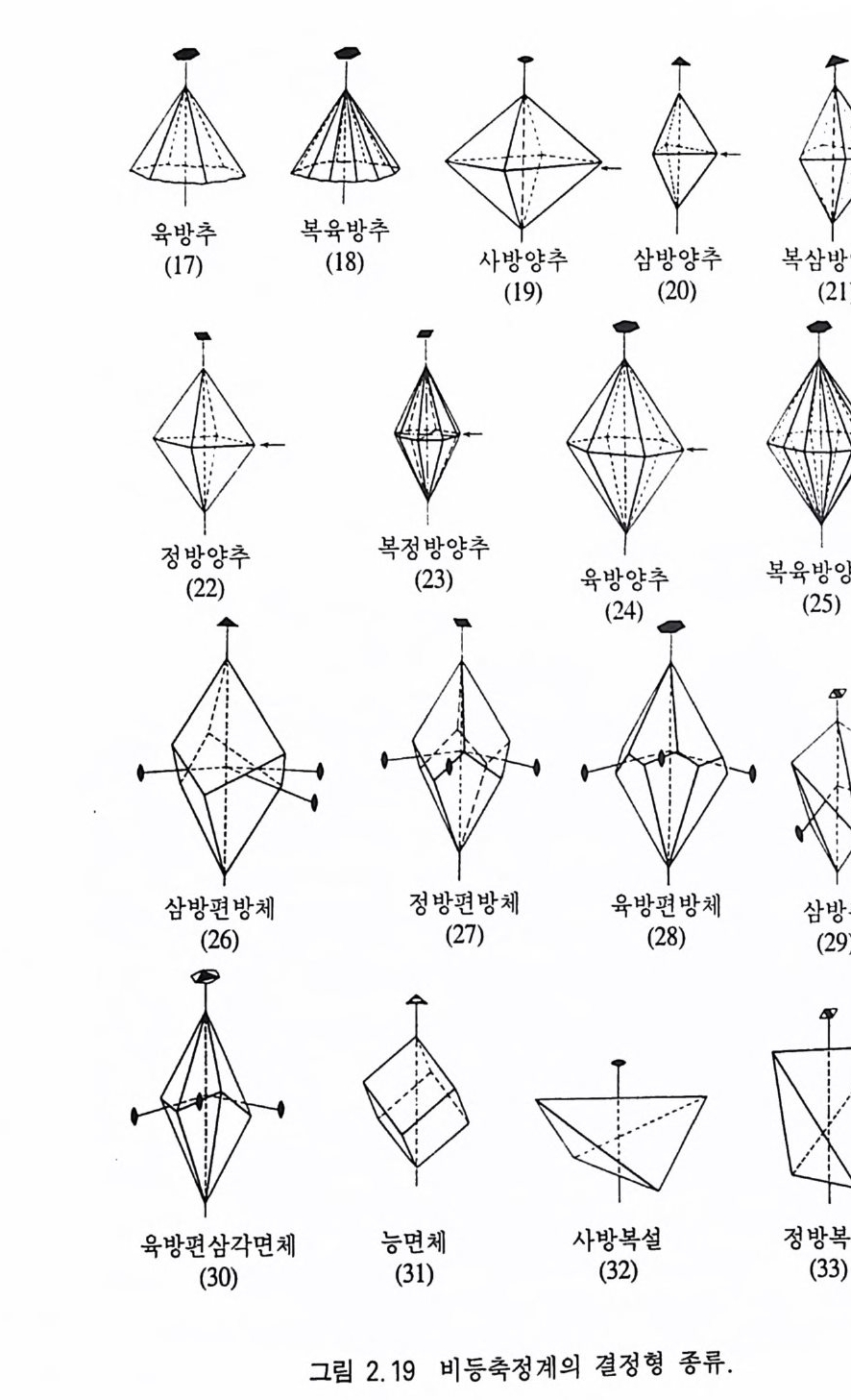
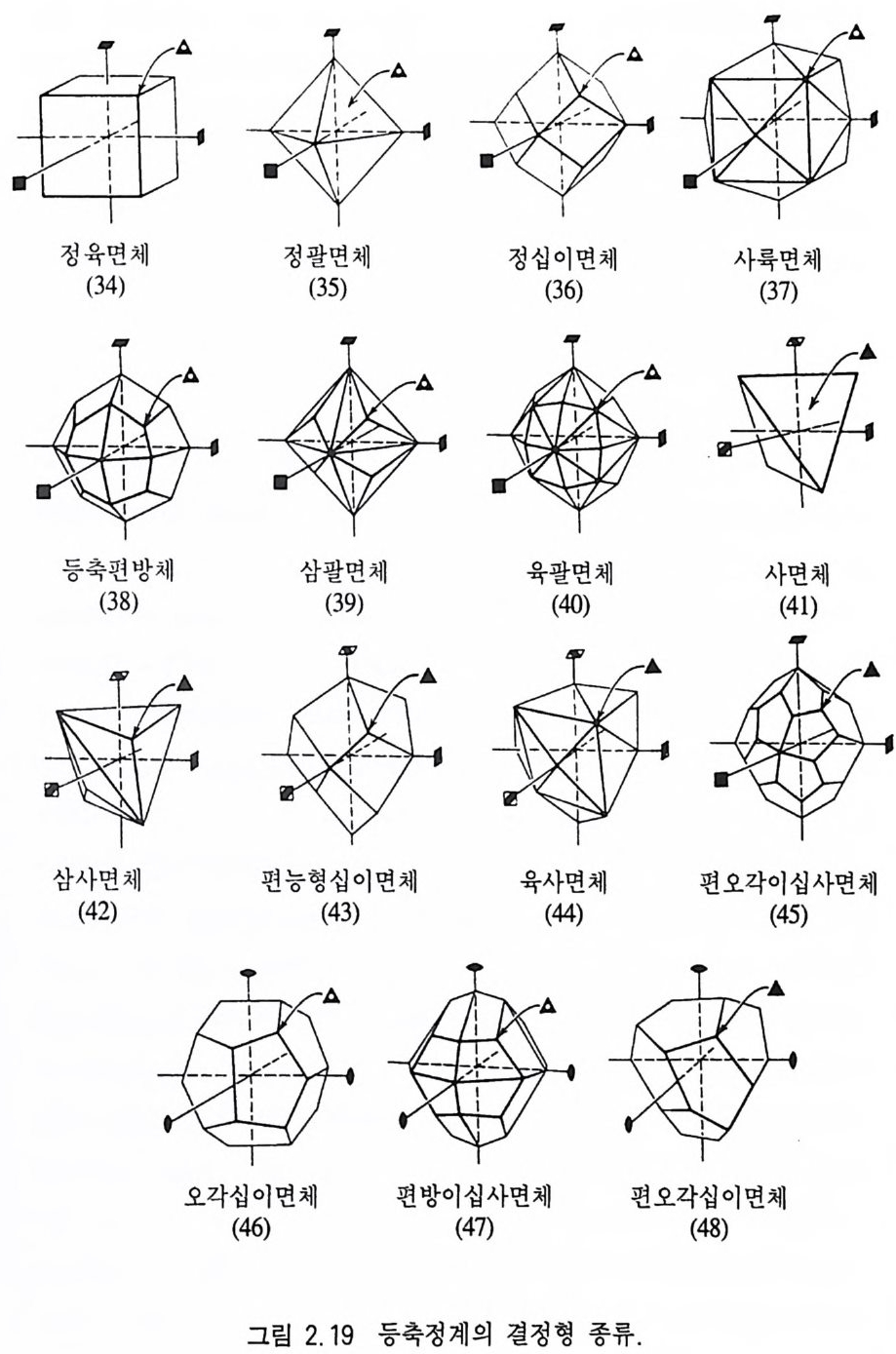
서 6 개의 결정면온 하나의 결정형을 이루고, 이 결정형의 이름은 정 육면체(正六面體, cube) 이다. 대칭심만 있는 삼사정계 결정인 경우 (그림 2.1 8 b), 동일하고 나란한 2 개의 결정면은 탁(卓, pi naco i d) 이 라는 결정형을 이루지만 대칭심도 없는 삼사정계 결정의 경우에는 (그림 2.1 8 c) 결정면들을 연관시켜 줄 수 있는 대칭요소가 존재하 지 않으므로 각 결정면 하나 하나가 독립된 결정형을 이루는데 이 를 단면형(單面形, pedi on) 이라고 한다. 광물 결정에서 발견될 수 있는 결정형의 예는 그림 2 .1 9 와 같으며, 이둘중 조암광물에서 빈 번히 관찰될 수 있는 주요 결정형에 대해 간략히 설명하기로 한다. 단면형 (單面形, p e di on) 은 하나의 결정면으로 이루어 진 결정형 이다. 탁(卓 pin aco i d) 은 서로 나란한 두 개의 동일한 결정면으로 구성
 <단(면I)=형 乙乙(탁2) 二(비3) 广'설S
<단(면I)=형 乙乙(탁2) 二(비3) 广'설S
 雷°〕〈: 멸王〈iY 추 言g入복정( 2방-_I 3' ) 양 I추 사 방(19양 ) 추 .O.. , u(02L 4o0k) 삼 기소-- g 〉〈g수추 l 복 복 검 Y0 \广:問)양 -주 추
雷°〕〈: 멸王〈iY 추 言g入복정( 2방-_I 3' ) 양 I추 사 방(19양 ) 추 .O.. , u(02L 4o0k) 삼 기소-- g 〉〈g수추 l 복 복 검 Y0 \广:問)양 -주 추
 “
“
되어 있는 결정형이다 . 비 (廊 dome) 는 서로 기울어진 두 개의 동일한 결정면으로 구성 된 결정형으로서, 이 두 결정면은 대칭면에 의해 연관된다. 주(柱, pri sm) 는 3, 4, 6 개의 면이 한 방향으로 나란하게 발달한 결정형으로서, 이 결정면들이 3 회 대칭축에 의해 연관되면 삼방주 (三方柱), 4 회 대 칭 축이 면 정 방주(正方柱), 6 회 대 칭 축이 면 육방주 (六方柱)가 된다. 녹주석, 인회석, 전기석 등이 있다 . 추(銀 py r ami d) 는 서로 기울어져 있는 3, 4, 또는 6 개의 결정면 이 한 점에서 만나고 동시에 각각 3 회, 4 회, 6 회 대칭축에 의해 서로 연관되어 있을 경우를 말하며 이때 이 결정형의 이름은 각각 삼방추(三方雜), 정 방추(正方維), 육방추(六方雜)가 된다. 방해 석, 석영 등이 있다. 양추(兩銀 bip yra m id) 수평면을 기준으로 위 아래에 추가 발달 하며, 이들이 서로 대칭면에 의해 연관될 때의 결정형을 말한다 . 수평면이 대칭면 구실을 한다. 양추에 속하는 결정면들이 3,4,6 회 대칭축에 의해 연관될 때 각각 삼방양추, 정방양추, 육방양추가 된다. 강옥, 저어콘이 있다. 정육면체(正六面體, cube) 는 6 개의 정사각형 결정면으로 이루어 진 결정형으로서, 간단히 육면체라고도 한다. 황철석, 형석 등이 속한다. 정팔면체(正八面體, octa he dron): 8 개의 정삼각형 결정면들로 이 루어진 결정형이다. 다이아몬드, 형석, 스피넬 등이 속한다. 정 십 이 면체 (正十二面體, dodecahedron) 는 평 행사변 형 인 12 개 의 결 정면으로 구성된 결정형이다. 석류석이 있다. 어느 한 종류의 결정형에 의해 공간이 완전히 폐쇄될 수 있을 경 우, 이 결정 형 을 폐 형 (閉形, closed form ) 이 라고 하고, 그렇지 않을
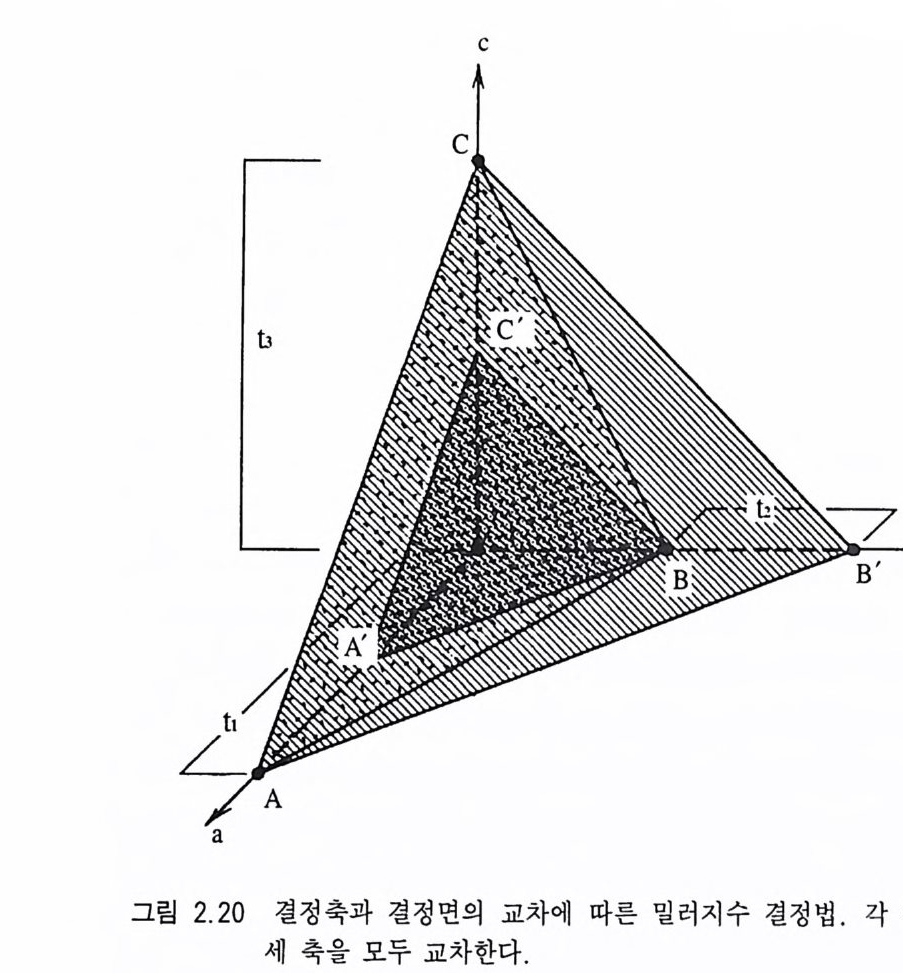
경우 개형(開 該 ope n fo nn) 이라고 한다 . 정육면체, 정팔면체, 정십 이면체, 양추 등은 폐형의 예이며, 단면형, 탁, 주 등은 개형의 예이다. 또한 어떤 광물 결정이 하나의 결정형으로만 이루어져 있 으면 이 를 단형(單該 s i m p le fo nn) 이라 하고, 두 개 이상의 결정형 으로 구성되어 있으면 취형( fr~形 , comb i na ti on) 이라고 한다. 폐형일 경우 단형이나 취형으로 결정이 존재할 수 있으나, 개형인 경우에 는 반드시 다른 결정형과 결합된 취형으로만 존재할 수 있다. 2,2,7 결정면 밀러지수법 결정에 발달하는 결정면이 결정축과 어떤 기하학적인 배열 상태 를 하고 있는지를 간단한 지수(指數 i nd ic es) 를 써서 나타내면 편리 할 경우가 많다. 그동안 여러 표현법이 제안된 바가 있었으나 밀 러가 고안해 낸 밀러지수 (M i ller i nd i ces) 가 가장 널리 사용된다 . 밀 러지 수는 결정 축을 단위 거 리 (單位距離, uni t len gth)로 교차하는 단 위면( 單位面 un itp lane) 을 기준으로 어떤 결정면이 각 결정축을 절 단하는 거리를 단위거리의 배수로 나타낸 다음 이들의 역수(逆數) 의 비(比)로서 표현하는 방법이다. 결정면의 밀러지수는 반드시 (h k I) 처 럼 소괄호를 사용하여 나타내며, h 는 a 축과, k 는 b 축, l 은 c 축과의 관계를 의미한다. 밀러지수 사이에는 쉼표 등을 사용하지 않는다. b. ABC 가 a, b, c 결정 축의 단위 거 리 인 h, t2, h 을 교차하는 단위면일 때(그림 2.20) 세 결정축 a,b,c 를 교차하는 길이는 lt1 : lt2 : l tJ이 되며 이 배수의 역수의 비는 1 : 1 : 1 이 된다. 따라서 단위면의 밀러지수는 (1 11) 이다. b. AB'C 는 단위면을 기준으로 a 축은 같은 거리(lt 1), b 축은 2 배 (2 t z), C 축은 1 배{ltJ)의 거리로 교 차하므로 길 이 의 비 는 1 : 2 : 1 이 고 그 역 수의 비 는 1/1 : 1/2 : 1/1 이어서 여기에 2 를 곱해 정수비로 계산하면 2 : I : 2 가 된다.
 c
c
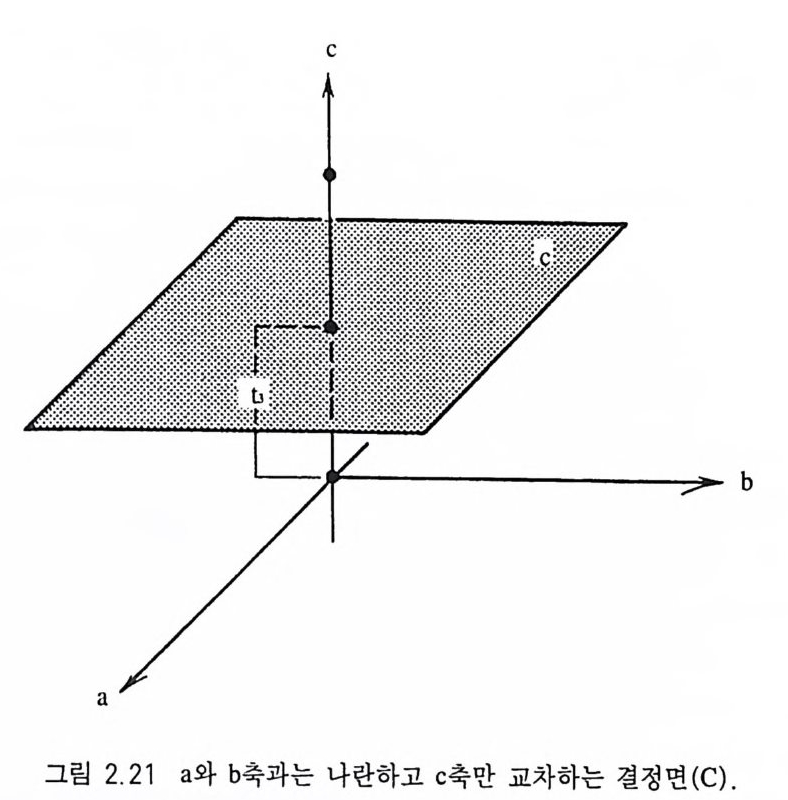
따라서 t::,, AB'C 의 밀러지수는 (212) 이다. 결정면 t::,, A'BC ' 인 경 우 결정축을 교차하는 거리의 비는 1/2 : 1: 1/2 가 되고 이들의 역수비는 2 : 1 : 2 이어서 밀러지수는 (212) 이 된다 . 중요한 것은 단위면과 나란한 결정면은 결정축과 교차하는 길이 배수에 관계없 이 단위면의 밀러지수와 같은 지수를 가지는 점이다. c 측만 교차하고 a 와 b 축과는 나란한 결정면일 경우(그림 2.21 ) a, b 축과의 교차거리는 OO 로 나타낼 수 있고 c 축은 단위 길이만큼 절 단하므로 이들의 역수 비는 0 : 0 : 1 이 된다. 따라서 C 결정면
 cA
cA
 f
f
t\: (+) (-) (-) ai(+ ) B >· A J•홉요卜르<〈 ) a1(+) | \ 그림 2.2 3 육방정계 및 삼방정계에서 4 개의 결정축을 모두 교차하는 결정면 .
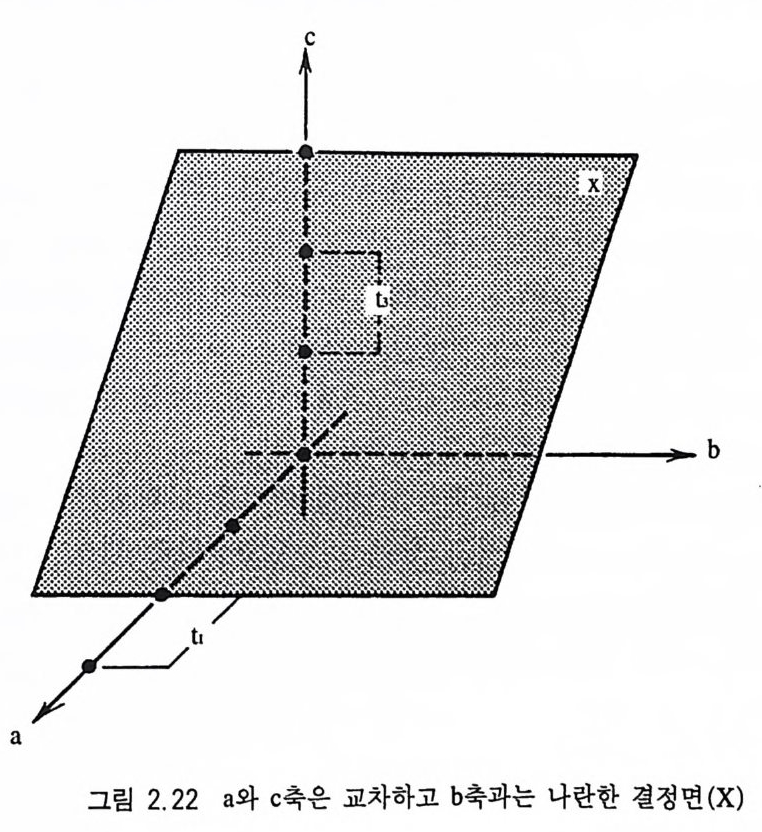
의 밀러지수는 (001) 이다. X 면처럼(그림 2.2 2 ) a 축과 c 축을 절단하 고 b 축과는 나란할 경우, 교차하는 길이의 비는 2 : 00 : 3 이고 이들의 역수의 비인 밀러지수는 (302) 가 된다. 육방정계나 삼방정 계는 결정축이 4 개가 있기 때문에 밀러지수는 (hk i I) 이 된다. h,k, i는 결정면이 a1, ai, &축과, 그리고 l 은 c 축과의 관계를 의미한다. 예를 들어 +a1, +往 국 b, +c 를 교차하는 결정면 !::::.ABC( 그림 2.23) 의 밀러지수는 (1 121) 이 된다. h, k, i의 사이에는 항상 h+k+ i=O 관계가 성립한다. 단위포가 각 결정축을 교차하는 실제 거리를 단위포 상수(單位 胞常數, uni t cell p arame t er) 라고 한다. 이 단위길이를 비로 나타낸 것을 축률(軸率 axial rati o) 또는 표축비 (標軸比, par amete r ra ti o) 라 고 한다. 예를 들어 원소광물인 황의 단위포 상수는 a=l0.4 5
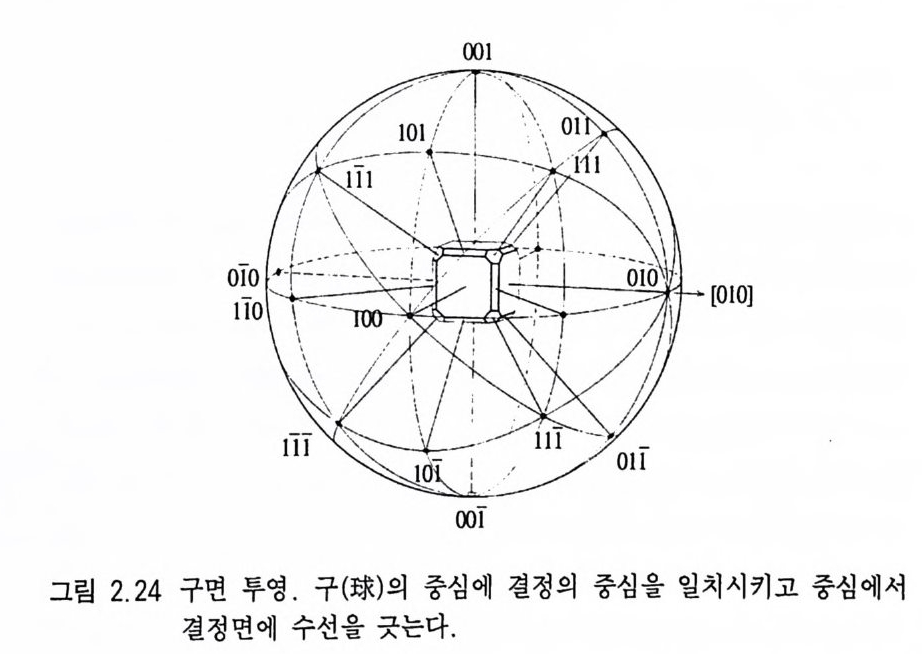
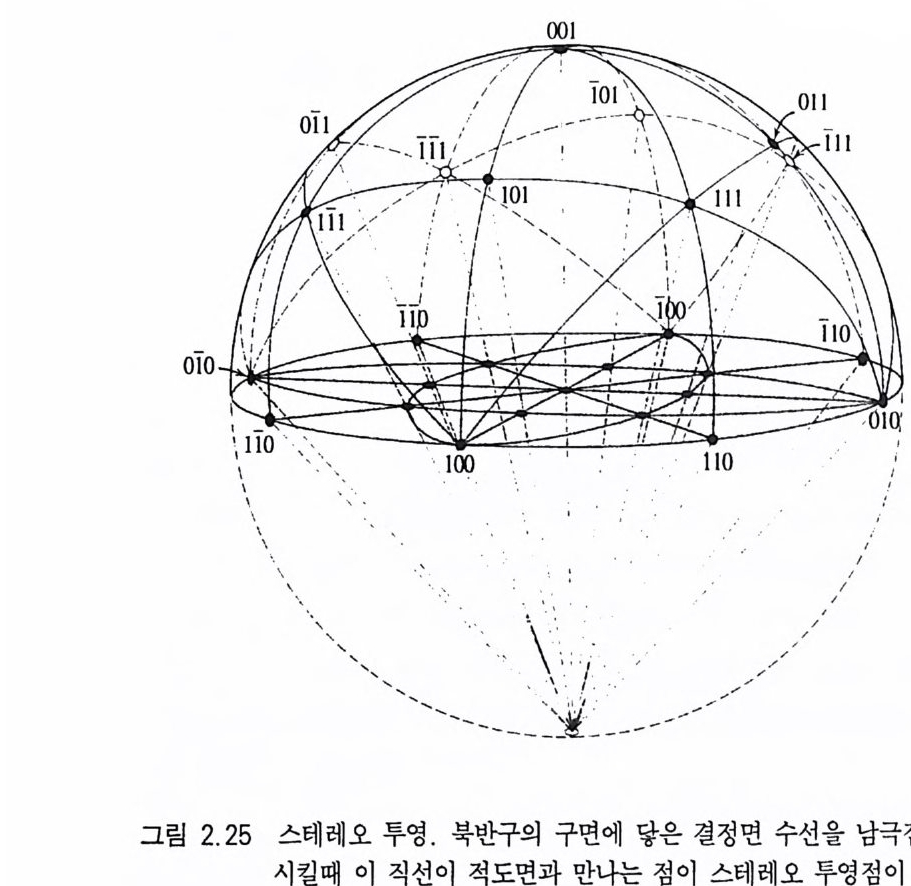
A, b= 12.84A, c=24 .4 6A 이 며 축률 또는 표축바 는 a : b : c= 0.8139: 1 : 1. 9049 가 된다. 석영의 단위포상수는 a=4.913A, c=5.405 A 이며, 축률은 a : c=l : 1.1 00 이다. 2.2.8 결정 투영 결정 면과 결정 축과의 관계를 3 차원적 인 구면 투영 (sp he ric a l p ro j ec ti on) 으로 묘사하기가 그리 쉽지 않다. 따라서 이들의 관계를 2 차원의 평면에 도시하여 나타내는 것을, 스테레오 투영 (s t ereo g ra p h i c p roj ec ti on) 이라고 한다 . 이 투영법은 구(球, s p here) 의 중심에 결정의 중심을 일치시키고 중심으로부터 투영하려는 각 결 정면에 수선을 그어 이 직선이 구의 표면에 만나는 점(그림 2.2 4 ) 을 북극점 또는 남극점에 연결시킬 때 이 직선이 적도면과 만나는 점(그림 2.25) 을 사용하는 것으로서, 적도와의 교점을 그 결정면의
 입: \三
입: \三
 _001 \
_001 \
스테레오 투영점(投 影點 )이라고 한다. 스테레오 투영을 할 때 적도 면으로 사용하는 도면이 있는데 이를 스테레오 망면 (s t ereo gra ph ic net) 또는 울프 망면 (Wul ff ne t)이라고 한다(그림 2.2 6 ). 결정면을 스 테레오 망면에 투영하기 위해서는 북극과 남극점을 연결하는 축 (N-S 축)과 결정면에 그은 수선이 이루는 각(p)을 측각기로 xl 고, 결정면에 그은 수선이 (010) 면에 그은 수선 (o=0°) 과 이루는 각(¢)을 잰다. 예를 들면, 그림 2.25 의 정팔면체에 있는 (1 11) 면 에 그은 수선이 N-S 축과 이루는 각(p)은 54.4 4 °, 동서방향의 직 선 (E-W 축)과 이루는 각(¢)은 +45° 이다 . 스테레오 망면에 투명지
 그림 2. 2 6 스테 레 오 망면 (ste re ogr a p hic n et) .
그림 2. 2 6 스테 레 오 망면 (ste re ogr a p hic n et) .
롤 올려 놓고 E-W 선(가로선)상의 오른쪽을 기준점(硏 =0°) 으로 하 고 원주를 따라 시계도는 방향으로 +45° 가 되는 위치를 정한 다 음 스테레오 망면의 중심으로부터 직선을 긋는다. 그리고 이 직선 이 ~=00 인 직선과 일치되도록 투명지를 회전시킨다. 그 다음 스 테레오 망면의 중심으로부터 바깥쪽으로 54.44°( p)만큼 이동하여 점을 찍으면 (1 11) 면의 스테레오 투영점이 된다. 그런 다음 투명 지를 원래의 위치로 돌려 놓는다. 적도면 아래에 있어 남반구에 투영되는 결정면은 p값을 (기값으로 표시한다. o 를 (-)로 표시할 때는 ¢=0° 를 기준으로 반시계 방향으로 회전하는 것을 의미한다.
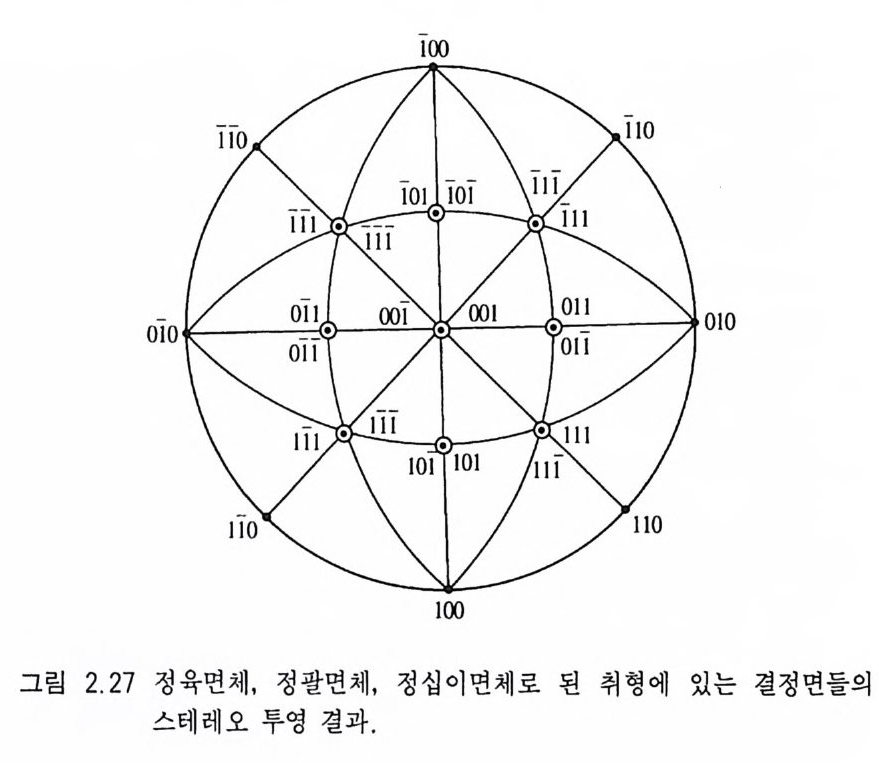
정육면체와 정팔면체, 그리고 정십이면체가 결합된 취형 결정 (그림 2.24) 에 대해 각 결정면의 스테레오 투영점을 표시하기 위해 서는 결정면의 좌표(p, ~)를 측정하면 다음과 같다. 정육면체 결정면 (1 00)=(90°, 90°), (010)=(90°, 0°), (001 )= (0°, 0°), (foO )=(90°, 270°), (OTO)=(90°, 180°), (Oof )= (-0°, 00 ) 정팔면체 결정면 (1 1 I)= (54.4 4 °, 45°), (11 1)=(54.44°' 135°), (f f I) = (54.44° , 225° ) , (1 「 1) = (54.44° , 315° ) , (1 l l) = (-5 4.44° , 45°), (TT l)= (-54.44°, 135°), (TT 0=(-54.44°, 225°), (T 1 T)= (-54.44° , 315° ) 정십이면체 결정면 (O 11 )= (45° , 0° ), (10 1 )= (45° , 90° ), (O 「 l)= (45° , 180° ), (「 0 I) = (45° , 270° ), (I 1 O) =(90° , 45° ), (1 1 O) = (90°, 135°), (11O)=(90°, 225°), (「 10)=(90°' 315°)' (01 「)= (-45°, 0°), (10 1)=(-45°, 90°), (O1「) =(-45°, 180°), (10 1)= (-45 ° , 270° ) 정육면체의 (001) 면, 정팔면체 중 (1 11 ), (1 11 ), (1 11 ), (1 1 f)면, 그리고 정십이면체중 (011), (10 1), (011), (I OI) 은 적도 면 아래인 남반구에 투영되므로 •으로 표시하는 북반구의 결정면 과 구별하기 위하여 0 으로 표시한다(그림 2.27). 참고로 c 결정축에 수직이고 a 와 b 결정축에 평행인 (OO I) 결정면 온 스테레오 망면의 중앙에 투영이 되며, c 결정축과 평행인 (h0 0), (OkO), (hkO) 결정면은 스테레오 망면의 원주상에 투영이 된 다. 그리고 세 결정축을 모두 교차하는 (hkl) 결정면은 스테레오 망면의 내부에 투영이 된다. c 결정축을 교차하고 동시에 a 또는 b 결정축 중 하나와 교차하는 (hOI), (0kI ) 결정면들은 스테레오 망 면의 가로 및 세로선상에 투영된다.
 100
100
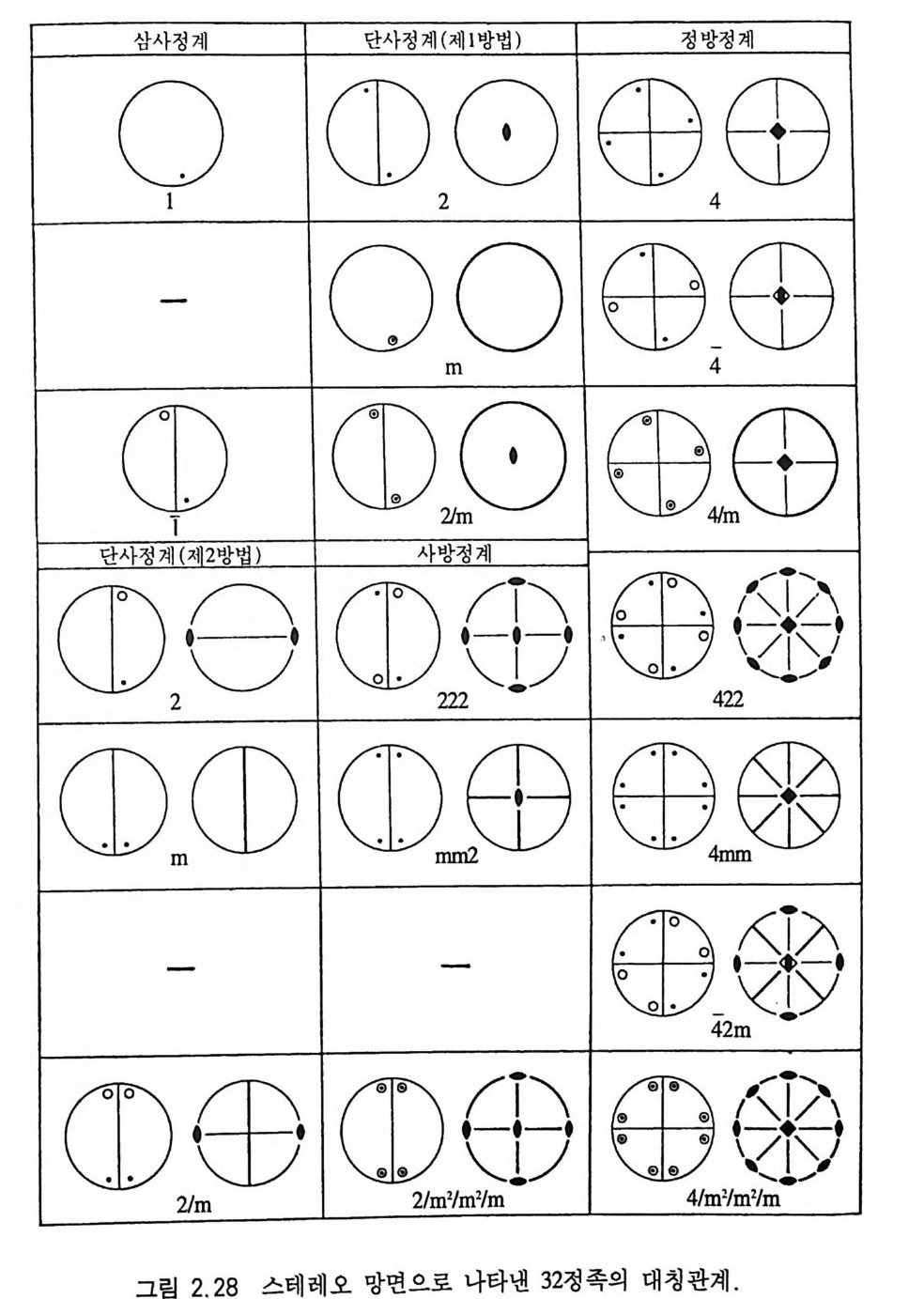
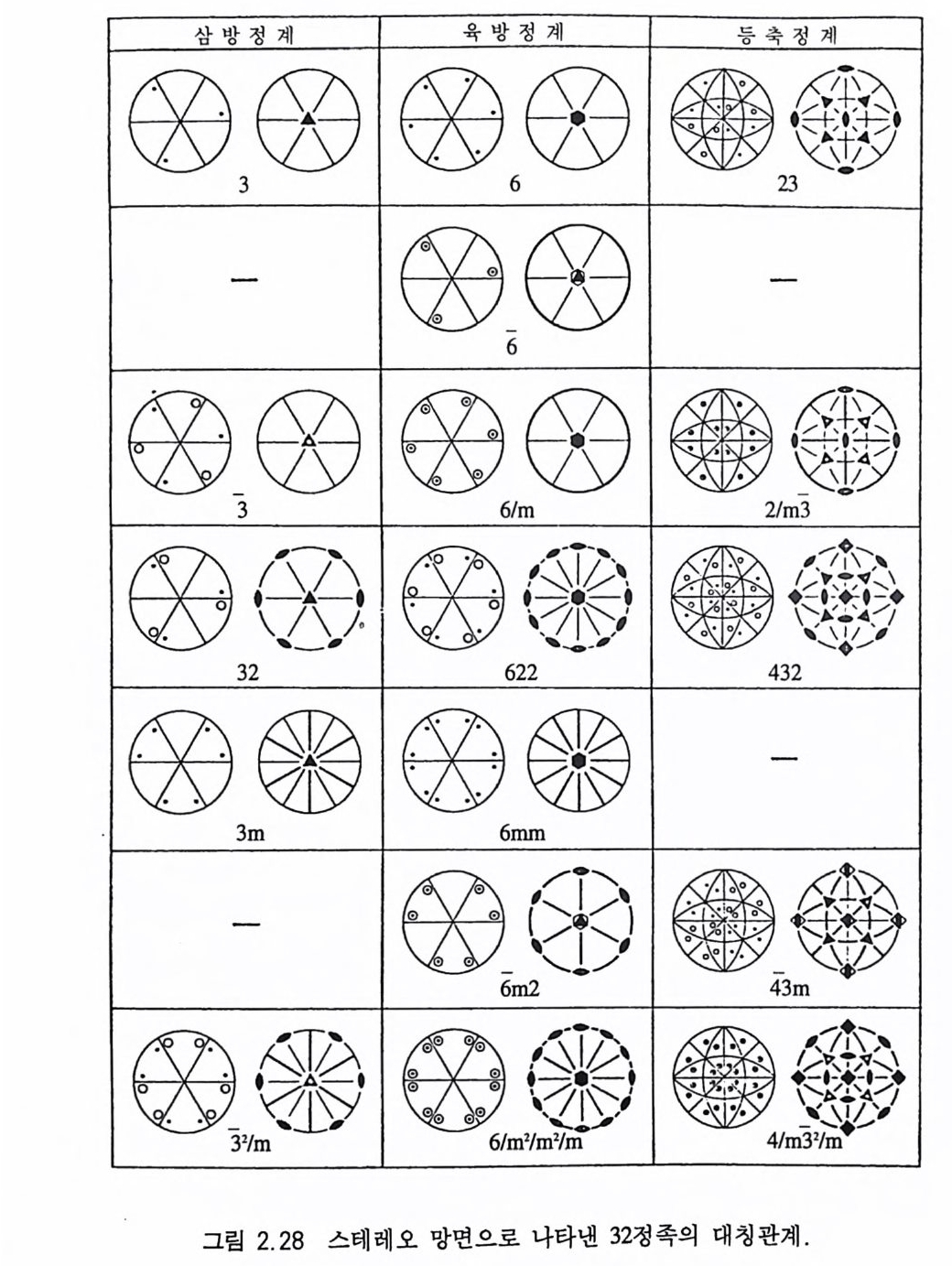
2.2 .9 32 정족 32 정족(晶族, class) 은 회전축뿐만 아니라 대칭면, 대칭심 모두를 기준하여 구분한 것이다. 7 정계에 속하는 32 정족과 각 정족에 있 는 대칭요소의 내용은 표 2 .7과 같다. 32 정족에서 일반 (hkl) 결정면으로부터 유도되는 결정면의 공간 적인 배치 및 대칭요소, 그리고 결정형 등에 대한 정보는 스테레 오 투영을 한 자료를 이해하면 된다(그림 2.28). 각 정족의 특징을 알기 위해서는 정족을 표시하는 기호의 의미를 알아야 한다. 삼사 정계에서 정족을 가리키는 숫자는 1 차 방향(一次方向, prim ary d i rec ti on) 대칭을 의미하며, 수직축인 c 결정축 방향이 된다. 즉 N-
 표 2.7 32 정족과 대칭요소 .
표 2.7 32 정족과 대칭요소 .
 삼 사 정계 단 사정계(제 I 방 법) 정방 정계
삼 사 정계 단 사정계(제 I 방 법) 정방 정계
 〈:〉군33@@33@삼방 y 정 2계 m 육방정교 2I`m,mI`2'mI, 계 @沿@@ 훌8毋를틀를를 홀412 뼈 m.'3/22&_32/乙:、〉`ij강4\l`?:; ,t,:\;\,/,8Im / 多?-'♦. ,- '&&‘^1一 `’望습-円jt- 多 합장I`'\:\??/\ ,',♦\1?
〈:〉군33@@33@삼방 y 정 2계 m 육방정교 2I`m,mI`2'mI, 계 @沿@@ 훌8毋를틀를를 홀412 뼈 m.'3/22&_32/乙:、〉`ij강4\l`?:; ,t,:\;\,/,8Im / 多?-'♦. ,- '&&‘^1一 `’望습-円jt- 多 합장I`'\:\??/\ ,',♦\1?
S 축이 1 회 대칭축(I 정족) 또는 1 회 회반죽 (T 정족)이 된다는 것이 다 단사정계에 속하는 정족도 하나의 기호로 표시하는데, 1 차 방 향인 b 결정축의 대칭울 의미한다. 즉 2 정족에서는 가로방향인 b 결정축이 2 회 대칭축이 된다. m 정족은 1 차 방향인 b 결정축에 수 직으로 대칭면이 있다는 의미이다. 숫자가 없이 m 만 있으면 그 방 향에 수직으로 대칭면이 존재한다는 것을 의미한다. 2/m 정족은 1 차 방향인 b 축이 2 회 회전축이고 동시에 이에 수직인 대칭면이 존 재한다는 의미이다. 사방정계의 정족인 경우 세 숫자 또는 문자 (m) 가 있는데 각각 1 차 방향 (a 축), 2 차 방향 (b 축), 3 차 방향 (c 축) 의 특징을 의미한다. 따라서 222 정족은 a, b, c 결정축 모두가 2 회 회전축이 된다. mm2 정족은 a 와 b 결정축에 수직으로 대칭면 이 있고, c 결정축은 2 회 회전축이 된다는 의미이다. mmm 정족은 3 개의 결정축에 각각 수직인 대칭면이 존재한다. 정방정계는 첫번 째 숫자가 1 차 방향인 c 결정축의 대칭을 의미하며, 두번째 숫자나 문자는 2 차방향인 a1 과 a2 방향의 대칭을, 그리고 세번째의 숫자나 문자는 3 차 방향인 a1 과 &축 사이 방향의 대칭을 가리킨다. 따라 서 4 와 4 정족에서는 c 결정축이 4 회 희전축 또는 4 회 회반축인 정 족이다. 4/m 정족은 c 결정축이 4 회 회전축이고 이에 수직인 대칭 면이 존재하는 정족이다. 422 정족은 c 결정축이 4 회 회전축이고 a, 과 &결정축에 각각 2 회 회전축, 그리고 a1 과 &결정축의 사이 방 향에 추가로 2 개의 2 회 회전축이 있다. 삼방정계와 육방정계인 경 우 첫번째의 숫자는 1 차 방향인 c 축의 대칭을, 두번째 숫자나 문 자는 2 차 방향인 a1, ai, & 결정축 방향, 그리고 세번째는 a1, 年, & 결정축 사이 방향의 대칭을 의미한다. 등축정계인 경우 처음의 숫 자나 문자는 1 차 방향인 a1, ai, 83 결정축 방향, 두번째는 2 차 방향 인 한쪽 우각과 반대편의 우각을 연결하는 사선 방향, 세번째는 한쪽 능과 반대쪽에 있는 능의 중심을 잇는 사선 방향의 대칭을
의미한다 그림 2.29 는 스테레오 망면 내에 (hkI) 로 표시되는 일반 결정면을 투영한 관계를 나타낸 것으로, 일부 결정축만 교차하는 결정면들은 윗그림과 다른 결정면 배열을 나타낸다. 어떤 결정이 어느 정계와 정족에 속하는지 알아보기 위해서는 먼저 그 결정에 존재하는 모든 대칭요소 를 정확하게 찾아낸 다음 대칭축의 특징에 의해 정계를 구분하고, 그밖에 존재하는 대칭 축, 대칭면, 대칭심 자료가 32 정족 중 어느 정족에 해당하는가 를 찾으면 된다. 2,3 화학성분 광물의 화학성분은 광물의 성질을 좌우하는 가장 기본적이면서 도 중요한 요소이다. 광물의 화학성분은 오랜 과거의 광물 생성 환경 및 연령을 지시해 줄 수 있을 뿐만 아니라 지각변천 역사까 지도 알려줄 수가 있으므로 그 의미는 매우 크다. 2.3.l 화학분석 자료 처 리 화학성분을 분석하는 기기분석 방법에 대해서는 제 5 장에서 다루 기로 하고, 여기서는 기기분석법을 통해 얻은 자료로 광물의 화학 식을 계산하는 과정에 대해 설명하고자 한다. 자연금 (Au) 이나 자 연동 (Cu) 처 럼 단일 원소광물 (na ti ve element m i neral) 은 분석자료가 원소 형태로 나타나며, 규산염이나 산화염 광물처럼 산소가 포함 되어 있는 경우는 각 원소의 산화물 형태로 분석자료가 마련된다. 황화물이나 테루르 광물 등은 각 원소 형태로 분석자료가 마련된 다. 원소나 산화물의 양은 중량 %(we ightp ercen t)로 표시된다.
광물의 실제 화학분석 자료 를 보면 광물 화학식에 나타나 있지 않은 원소들이 다수 포함되어 있는 사실을 알 수 있게 된다. 이러 한 사실을 단순히 화학분석에 사용한 기기의 사용 오류나 그 광물 내에 또는 광물 분석을 위한 준비과정에서 어떤 불순물이 첨가되 어서 생긴 결과라고 성급하게 단정할 수는 없다 . 오히려 광물에는 화학식에 포함되어 있지 않은 다수의 기타 원소들이 함께 공존하 고 있는 것이 일반적이다 . 그 이유는 무엇일까? 우리가 기억하고 있는 대부분의 광물 화학식은 필수 구성원소로만 이루어진 순수한 상태 를 나타낸 것이며, 이 를 이상화학식 (理想化 學 式, ide al fon nula) 이라고 한다. S i Oz 로 표현되는 석영의 화학식은 이상화학식이다. 그러나 석영을 실제로 화학분석하면, 극소량의 Fe,Ca,Mg 등이 거 의 항상 포함되어 있음을 알 수 있다. 그러나 이들 미량 성분들을 (Si, F e,Ca,Mg )O z 처럼 화학식에 포함시키지 않는 이유는 S i를 치 환한 상태로 존재하는 이들 원소가 석영의 산출지에 따라 그 종류 가 달라질 수 있고 또 그 함유량도 매우 적기 때문이다. 이에 비 하여 섬아연석은 이상화학식이 ZnS 이지만, 천연에서 산출되는 섬 아연석에는 Fe,Mn,Cd 등의 금속원소가 Zn 을 치환하는 상태로 항 상 존재하는데, 이 중에서도 가장 많이 함유되어 있는 원소가 Fe 이다 . 따라서 섬아연석의 화학식을 (Zn, Fe)S 로 표현하기도 하는 데, 이것은 산출지에 관계없이 거의 모든 섬아연석에 Fe 가 들어 있고 그 함유량도 상당하기 때문이다. 이와 같이 거의 항상 수반 되는 주요 화학원소까지 함께 기재하는 방식을 일반화학식(一般化 學式, gen eral fon nula) 이 라고 한다. 감람석 의 경 우는 원소간의 치 환 이 연속적이면서 현저하여 (Mg , Fe)z S i0 4 처럼 두 단종(端種) 광물 (포르스테라이트, 페이알라이트)의 대표적인 원소를 포함시켜 일반화 학식으로 나타낸다 . 여기서도 유념할 점은 감람석에 금속원소로서 Fe, Mg , S i만 존재 하는 것 이 아니 고 Mn, Al 등의 다른 원소도 존재
하는데, 그 함유량이 극히 작고 또 원소 종류가 산출지에 따라 상 이할 수 있으므로 일반화학식에 포함시키지 않는 것이다 . 2.3.2 고용체 자연에서 산출되는 광물은 이상화학식에 표시되는 화학성분만을 지니는 경우는 거의 없고 모든 경우 항상 다른 원소를 불순물의 형태로 포함하게 된다. 그 이유는 광물을 정출시키는 마그마나 열 수용액 등 모용액(母溶液)이 화학적으로 순수하거나 또는 단순한 화학조성을 가지는 물질이 아니라 거의 100 여 종에 가까운 화학원 소를 함유하고 있기 때문이다. 모용액으로부터 원소들이 결합하여 화합물을 형성할 때, 광물 구조 내에 마련되어 있는 양이온과 음 이온의 위치가 매우 한정되어 있기 때문에 비슷한 성질을 띠는 원 소들은 동일한 위치에 함께 자리잡게 된다. 이와 같이 비슷한 성 질의 이온들이 치환작용으로 광물 내에 존재하게 되는 경우 그 광 물의 화학조성은 어떤 범위 내에서 변한다. 이러한 광물을 고용체 (固溶體, soli d s olu ti on) 라고 한다. 모든 광물은 이상화학식에 포함 되어 있지 않은 원소를 불순물 형태로 함유하고 있기 때문에 고용 체이다. 따라서 엄밀한 의미에서는 〈광물은 모두 고용체이다〉라는 표현이 옳다. 광물에는 불순물로 취급될 수 있는 다른 원소를 비 교적 적게 함유하여 거의 순수하게 산출되는 광물도 있고(예: 석 영) 섬아연석처럼 항상 다른 원소를 상당량 함유하여 뚜렷한 고용 체로 산출되는 경우도 있다. 한편, 자황철석은 철 (Fe) 이 있어야 할 원소 자리에 간혹 철 원소가 비어 있는데, 이 경우는 다른 원 소가 추가로 존재하는 경우와 반대인 현상으로서 역시 고용체에 포함시킨다. 고용체 광물은 이상화학식에 나타나 있는 것과 같은 원소간의 정 확한 일정 비 례의 법 칙 (一定比例法ffJJ, sto i c h iom etr y) 이
성립되지 않는 것이 보통이다. 고용체를 형성하는 원인에는 다음 3 가지가 있다. ® 치환고용체 광물을 구성하는 양이온 또는 음이온이 다른 양이 온이나 음이온에 의해 치환되어 있는 경우로서, 이를 치환고용체 ( 四換 固 溶體 substit ut i on al solid soluti on ) 라고 한다 . M g 2S i O 』 ( 포르스 테라이트)와 Fe2S i O 』(페이알라이트)의 경우 양이온인 M g”와 Fe” 가 서로 자유롭게 치환하여 감람석 [(M g, Fe)2S i 04] 이라는 고용체의 전 형적인 예를 보여 준다. 고용체를 현저하게 나타내는 광물의 경우 불순물로 취급될 수 있는 다른 원소를 전혀 포함하지 않은 순수한 상태(이상화학식으로 표현될 수 있는 광물)로부터 원소간의 치환이 최 대로 일어난 한계상태까지의 범위를 고용체 범위 (固溶體範園), soli d soluti on ran g e) 라고 하고 이 양 극단의 성분을 가지는 광물을 단종 (端種 end member) 이 라고 한다. 감람석 의 경 우 포르스테 라이 트와 페이알라이트는 단종이다. 섬아연석의 경우는 Fe 가 Zn 을 최대로 약 32 ato m i c %까지 치환하므로 고용체 범위는 ZnS- (Zno.6 8F e0. J2 )S 이며, 이때 ZnS 와 (Zno.68Feo .J 2)S 는 단종이다. 감람석의 경우처럼 두 광물 사이에 화학성분이 어떤 비율로도 끊임없이 연속적으로 변 하는 고용체 를 완전고용체 (完全固溶體, comp le te soli d s oluti on ) 또는 연속고용체 (連積固溶體, conti nu ous solid solu ti on) 라고 하고, 섬아연 석처럼 FeS 성분까지 이르지 않고 일정한 고용한계를 나타내는 경 우를 부분고용체 (部分固溶體, partial solid soluti on ) 또는 불연속고용 체 (不連領固溶體, dis c onti nu ous solid soluti on ) 라고 한다. 치환에 미치는 요소 원자들의 치환에 영향을 미치는 주요 요소에는 @ 원소 또는 이 온의 크기, © 결정구조, © 산화수 차이, ® 온도가 있다.
슝 원소 또는 이온의 크기 치환이 일어날 수 있는 환경은 두 원소 의 크기가 거의 유사할 경우이다. 치환은 두 원소 또는 이온의 반 지름(반경, radiu s ) 차이에 따라 좌우된다 . 만일 두 원소 또는 이온 간의 반지름 차이에 따른 비율을 Ar 이라고 할 때 Ar 은 다음과 같 이 정의할 수 있다. Ar= 큰 원소(이온)의 반경 -작은 원소(이온)의 반경 X 100 작은 원소(이온)의 반경 만약 Ar 이 15% 이하일 때는 치환이 자유롭게 이루어진다. 그러 나 Ar 이 15%~40% 사이일 때는 원소간의 치환은 가능하지만 약간 의 제약이 수반된다 . 그리고 Ar 이 40% 이상일 경우에는 치환이 매 우어렵다 . 감람석 의 경 우 M g와 Fe” 의 이 온 반경 은 각각 o.66A, o . 76A 으 로서, t)J- =15% 가 되고 또 산화수도 동일하여서 두 이온간의 치환 이 매우 자유롭게 된다 . 이와 같은 광물의 예는 투각섬석 [C 터vfg sS i s022(0H )i] -양 기 석 [Cc12(Mg , Fe)sS i s 아 (OH )i], 마그네 사이 트 (M g CO J)-능철석 (FeCO J)이 있다. 한편, 방해석 (CaCO J)과 능철 석 (FeCO J)은 모두 삼방정계의 구조로 되어 있지만 두 이온 Ca2·=0.9 9 A, Fe2·=0.76A 의 반경 차이에 따른 비율이 30.2% 로 크기 때문에 치환의 정도가 미미하다. © 결정구조 원소의 크기가 유사하여 치환이 가능한 경우에도 원 소간의 치환이 일어남에 상관없이 동일한 결정구조가 그대로 유지 되는 경우는 치환이 순조롭지만, 치환이 진행됨에 따라 원자들의 구조적 재배치가 일어나야 하는 경우에는 치환에 많은 제약이 있게 된다 예를 들어 섬아연석의 경우 ZnS( 섬아연석 )-FeS( 자황철석)로
나타낼 수 있는 완전고용체가 실제로 형성되지 않는다. 그 이유는 Zn2· = 0.74A, Fe2 · =0.76A 으로 이온반경의 차이에 따른 비율 (Ar) 은 2 % 로 원소 치환이 매우 자유로울 수 있지만 섬아연석은 등측정 계, 자황철석은 육방정계 또는 단사정계의 결정구조를 하고 있기 때문에 Fe 이 Zn 을 어느 한계이상으로 많이 치환하게 되면 새로운 구조 로 재구성되어야 하는데 고체인 경우 원자들의 구조적 재배열 이 매우 어 렵 기 때문에 부분고용체만 있게 된다 . @ 산화수 차이 이온간의 산화수 차이가 1 보다 같거나 작을 경우 원소간의 치 환 이 비교적 자유롭다. 마그마 고결 말기에 정출되는 저어콘 (ZrS i 04) 에는 우라늄이나 토륨 이온이 많이 함유되어 있다. 이 것 은 zr· 룰 같은 산화수를 가진 u4• 과 Th 가 치환하기 때문이 다 . 따라서 저어콘을 많이 함유하고 있는 화강암이나 페그마타이트는 방사성을 띠게 되고, 이 광물을 내포물로 함유하고 있는 혹운모에 서는 저어콘 주변부를 따라 결정구조가 파괴되어 있어 편광현미경 의 교차니콜하에서 검게 관찰된다. 이러한 현상은 저어콘에 들어 있 는 U 이나 Th 으로부터 a- 방사선이 나와 혹운모의 결정구조를 파 괴하면서 바정질화를 시키기 때문인데 이를 메타믹트상태 (me tami c t sta t e ) 또는 후비정질화( 後 非晶 質 化)라고 한다 . 마그마의 고결 초기에 정출되는 감람석이나 휘석은 양이온이 주로 Fe”, Mg ”, Ca” 로 되어 있기 때 문에 산화수 차이 가 2 이 상이 되 는 U 4 ♦ , U6•, Th4 ♦, T 硏 등이 이들 원소를 치환할 수 없으므로 결국 마그마 용액중에 계속 잔류 하게 되어 결국 마그마 고결 후기의 잔류용액에는 이들 원소가 크 게 농집하게 된다. 사장석의 경우 단종인 앨바이트 (NaAIS iJ Os) 와 아노르다이트 (CaAhS i2 아) 사이에는 완전고용체가 형성된다. 이 경우 Na1• 과 Ca2· 의 치환에 따르는 산화수의 결손을 보완해 주기 위해 Na1• • Si4 •. ...._.
Ca2' • AP' 형태의 치환이 일어난다. 이러한 특이한 치환을 쌍쌍치 환( 雙雙置 換 , coup le d substit ution ) 이 라고 한다 . @ 온도 일반적으로 광물이 생성되는 온도가 고온일수 록 원자나 이온의 크기에 따른 치환 제약이 감소하게 된다 . 따라서 고온의 열수용액에서 생성된 섬아연석의 경우 온도가 상승함에 따라 Fe 의 함량이 많아지는데, 800°C 에서 약 32% 로 최대가 되며, 온도가 더 이상 높아져도 Fe 의 치환량은 증가하지 않는다. 이러한 특 성을 이 용하여 섬아연석 내의 Fe 함량을 분석함으로써 섬아연석이 생성 된 온도를 추측할 수 있는데, 이러한 역할을 지질온도계(地 質溫 度 計 , g eo th ennome t er) 라 한다. 지질온도계로 사용될 수 있는 또 다 른 광물로는 자철석이 있는데, 자철석 내의 티타늄 함량이 온도에 영향을 받기 때문이다. 알칼리 장석 인 아노르도클레 이 즈 (anorth oclase) 는 고온에 서 Nal+(1.10A) 와 K1 . ( l. 68A) 을 모두 함유한 고용체로 정출하지만 660°C 로 점차 냉각되면 앨바이트 (NaAlSb 아)와 정장석 (KAlS i 3 아)으 로 분리가 일어나 두 광물이 공존하는 조직을 나타낸다. 이것은 아노르도 클레이즈가 고온에서 형성될 때는 이온 크기의 차이에 따른 제 약 요소가 상당히 감소하여 고용체를 이 루지 만, 온도가 하 강함에 따라 이 제약 요소가 점점 활성화되기 때문인데 이처럼 원 래는 한 고용체로서의 광물이었지만 낮은 온도에서 서로 다른 성분 의 광물로 분리 되 는 현상을 용리 (溶離, exsoluti on ) 라고 한다. 만약 원래의 아노르도클레이즈 내에 칼리성분이 많았다면 용리후의 구 조는 칼리장석의 바탕에 앨바이트가 소량 분포되어 있느 조직을 나타내 게 되 는데 이 를 퍼 다이 트 조직 (pe rt hitic tex tu re) 이 라고 한다 (그림 2.2 9 ) . 그와 반대 인 경 우는 역 (逆) 퍼 다이 트 조직 (anti pe rt hitic te x tu re) 이 된다.
 그림 2.2 9 퍼다이트 조직. 겁은색은 정장석이고 흰색은 앨바이트이다 .
그림 2.2 9 퍼다이트 조직. 겁은색은 정장석이고 흰색은 앨바이트이다 .
® 간극고용체 원소나 이온으로 이루어진 광물 결정구조 내에는 틈새가 존재할 수 있다 . 이런 공간을 원자나 이온이 추가로 채울 수가 있는데 이 를 간극고용체 (間陳固溶體 int e r stit ial soli d solu ti on) 라고 한다. 녹주 석 (BeJA lzSi6 0 1s) 의 경 우 6 각 환형 구조의 터 널 속을 K, Rb, Cs, HzO 등이 채우는 경우가 많다. 간극고용체의 또 다른 예인 우라니나이 트 (uo2) 는 등축정계의 면심격자 구조에 생긴 톰 사이에 산소가 추 가로 존재하기 때문에 일반적으로 UOz+ x 의 화학식을 가진다. 간극 고용체임에서는 추가로 존재하는 원소의 양이 증가할수록 순수할 때보다 비중이 증가한다 . 따라서 비중을 측정하면 간극고용체임을 알 수 있게 된다.
®결손고용체 원자나 이온이 있어야 할 격자 위치가 때로는 비어 있는 경우가 있다. 이러한 현상은 자황철석에서 대표적으로 관찰되는데 원자나 이온의 결손으로 인해 이상화학식으로부터 성분 변화가 나타나는 경 우를 결손고용체 (缺 損 固溶 體 , ommi ss io n al solid soluti on ) 라고 한다 . 운석에서 발견되는 트로이라이트(t ro il it e) 는 Fe:S 가 1 : l 인 FeHS H 이지 만, 지각에서는 Fe,S s 의 비율 등 항상 Fe 의 함량이 적다. 철 (Fe) 원자가 비어 있는 정도에 따라 자황철석의 화학식은 Fe,-,S (x=O ~0.2) 로 표시된다 . 결손고용체로 산출되는 광물은 순수할 때 보다 비중이 항상 작다. 자황철석의 경우 x=O 이면 FeS 가 되고, x=0.2 면 F eo. 8S 가 된다. 그러 나 화학분석 자료만으로는 간극고용체 인지 결손고용체인지를 알 수 없다. 따라서 바중을 정확하게 측정하여 결정하여야 한다. 2,3,3 정량 화학분석 자료의 처리법 정량 화학분석 자료로 광물의 화학식을 계산하는 과정에 대해 알아 보자 . 정량 화학분석치의 합계가 100% 가 되면 이상적이지만 100% 보다 士 l~2% 정도 범위의 값인 경우에도 신뢰할 만한 분석 자료로 인정할 수 있다. ®황화광물 화학분석자료는 원소의 중량% 형태로 표시된다. 중량% 수치를 원자량(原子量 ato m i c we ig h t)으로 나누어 원자몰비 (ato m i c pro - p o rti on) 를 구하여 사용한다. 황동석 (표 2.8) Cuo .54 Feo .54 sI . 08 이 되며 이를 다시 자연수의 비로 환 산하면 Cu:Fe:S=l : 1 : 2 가 되어 화학식은 CuFeSz 가 된다.
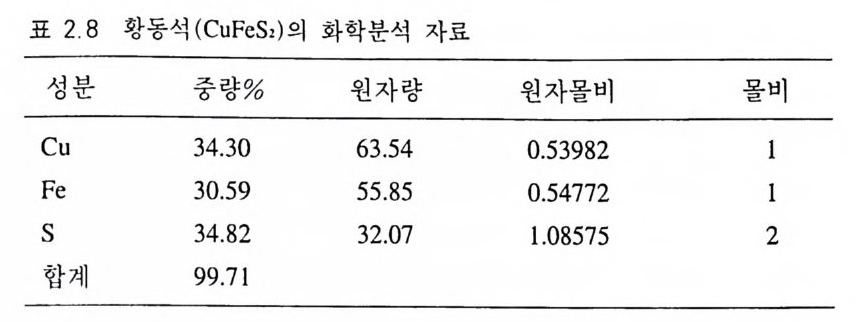 표 2 8 황동석 ( CuFeS ,) 의 화 학 분석 자료
표 2 8 황동석 ( CuFeS ,) 의 화 학 분석 자료
 표 2.9 황철석 ( FcS, )의 화학분석 자 료
표 2.9 황철석 ( FcS, )의 화학분석 자 료
황철석 ( 표 2.9 ) 원자몰비가 Fe : S=0.834 : 1. 654 이므로 이는 다 시 l : l.98 8 또는 1. 008 : 2 로 나타낼 수 있다. 따라서 화학식은 FeS1 . 9 때 또는 Fe1 .oos S 2 가 가능하게 된다 . 음이온을 자연수로 만드는 것이 상례이므로 화학식은 Fe, 寧 &가 된다 . 이를 더 간략하게 표시 하면 FeS2 가 된다. 섬아연석 (표 2.1 0 ) Zn, S 외 에 Fe, Mn, Cd 등이 공존하는 고용체 로서 이들 원소는 Zn 을 치환한다. 따라서 음이온과의 비를 계산할 때 (Zn, F e,Mn, C d) 형태로 한데 묶어 처리한다. 양이온과 음이온 원자비의 총합은 (Zn, Fe, Mn, Cd) :S= l. 061 : 1. 047 가 되고 음이온인 S 를 1 로 환산하여 다시 정리하면 1. 01 : 1 이 되어 간략히 1 : 1 로 표현 할 수 있게 된다. 특히 Cd 의 양은 매우 적어 일반화학식에 포함시
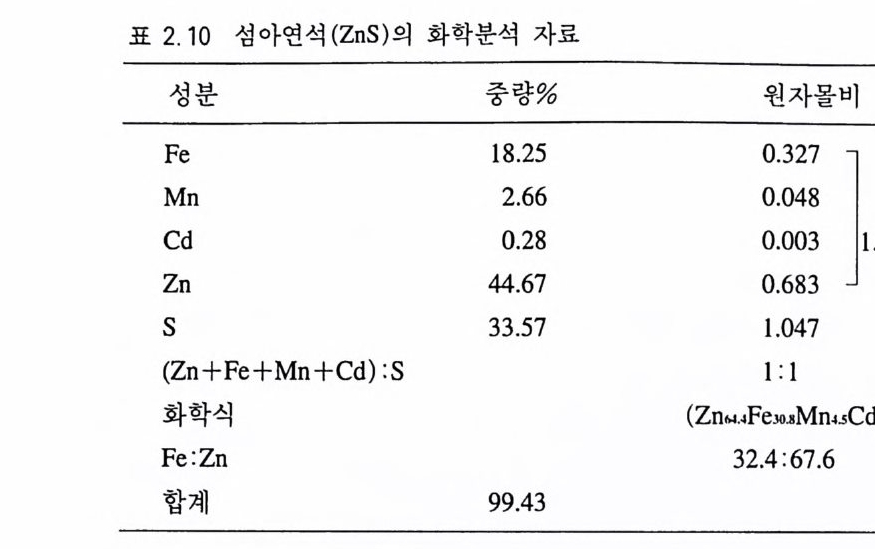 표 2.1 0 섬아연석 (Z nS ) 의 화학분석 자료
표 2.1 0 섬아연석 (Z nS ) 의 화학분석 자료
키기가 어려워 생략하면, 결국 화학식은 (Zno . 65Feo .3 1Mno . os) r 1. 01S 가 된 다. 이룰 더욱 간략하게 (Zno . 65Feo .3 1Mno . os)S 로 나타낼 수가 있다. 이 섬아연석은 Fe 가 Zn 을 32 mol% 치환하고 있는 경우이므로 섬아연 석 고용체의 단종에 해당하고 생성온도는 800°C 이상임을 알 수 있 게 된다. ®규산염광물 금속원소 산화염 형태의 중량%로 표시되며, 이룰 분자량으로 나누어 분자몰비롤 구한 다음, 양이온과 산소의 원소몰비를 따로 분리하여 계산한다 . 음이온인 산소원자의 수를 알고 있을 경우 산 소 원소몰수를 기준으로 금속원자의 원소몰비를 계산한다. 감람석 (표 2.1 1) 감람석에는 양이온 구실을 하는 원소가 2 가지가 있고, 이들이 결정구조 내에서 자리잡을 수 있는 위치는 고정되어 있다. 죽 Fe, Mg 및 이들울 치환하는 Mn 등은 팔면체 배위를 하
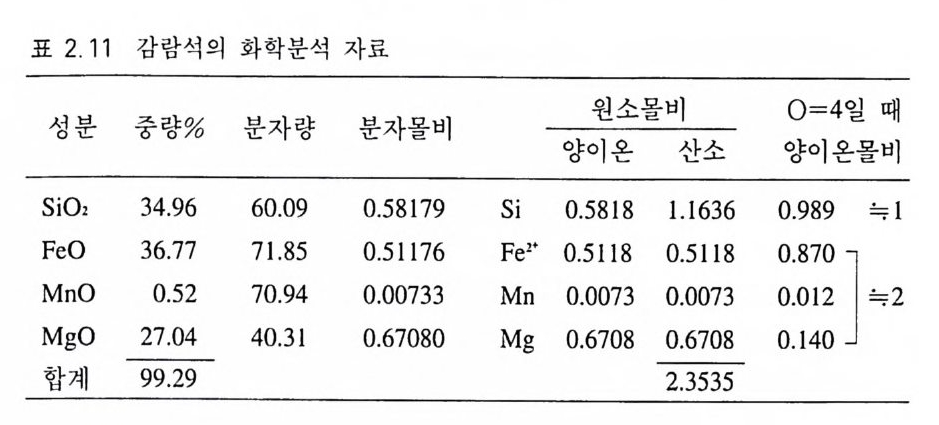 표 2.1 1 감람석 의 화학분석 자료
표 2.1 1 감람석 의 화학분석 자료
고 있는 자리에 있게 되며, S i는 사면체 중심에 위치하게 된다. 계 산 순서는 산화염 중량 %를 분자량으로 각각 나누어 분자몰비를 구 하고 이 수치로부터 각 양이온의 원소몰비를 따로 계산한다 . Si0 2 인 경우 산소 원소몰비는 2 X 0.5818= l.1 636 이 된다. 산소 원소몰비 의 총합 은 2 .3 535 인데, 우리는 이미 감람석에서 산소의 개수가 4 라 는 사 실 을 알고 있으므로 양이온의 원소몰비를 4 를 기준으로 하여 다시 계 산한다. 죽 양이 온의 원소몰비 수치 에 다가 4/2 .3 535 를 각각 곱한다 . 화학식은 (M g wFeo JJ1 M il o.01) u o2S io . 990 까 되며, 이것을 간략하 게 표현하기 위해 금속이온의 합을 2 를 기준으로 하여 다시 계산 하고 또 S i의 수를 대략 1 로 볼 수가 있으므로 대략의 화학식은 (M g1.1 2Feo . s 6Mno . 01)S i O 까 된다. 감람석은 포르스테라이트 (Fo) 와 페이 알라이트 (Fa) 의 고용체이므로 Fo=1 .14 /(1.1 4 +0.87)=0.567, Fa= 0.87/( 1.14 +0.8 7 ) =0 .4 33 이 되 어 Fo+Fa= l. 00 인 관계 가 성 립 한다 . 따라서 이 감람석을 F0o .56 7F 述 m 으로 표현할 수도 있고, F0o.56 1 또는 Fan . 꼬으로만 표시 할 수 있다. 이 를 백 분율로 나타내 어 Fo56 .1 Fa4J. J, Fos6.1 , Fll .lJ.J 등으로 표현해도 된다. 투휘석-헤덴버가이트 휘석 (표 2.1 2 ) 휘석에는 양이온이 들어가는 위치가 여러 개 있고 각 위치에 들어가는 양이온의 종류도 한정되어
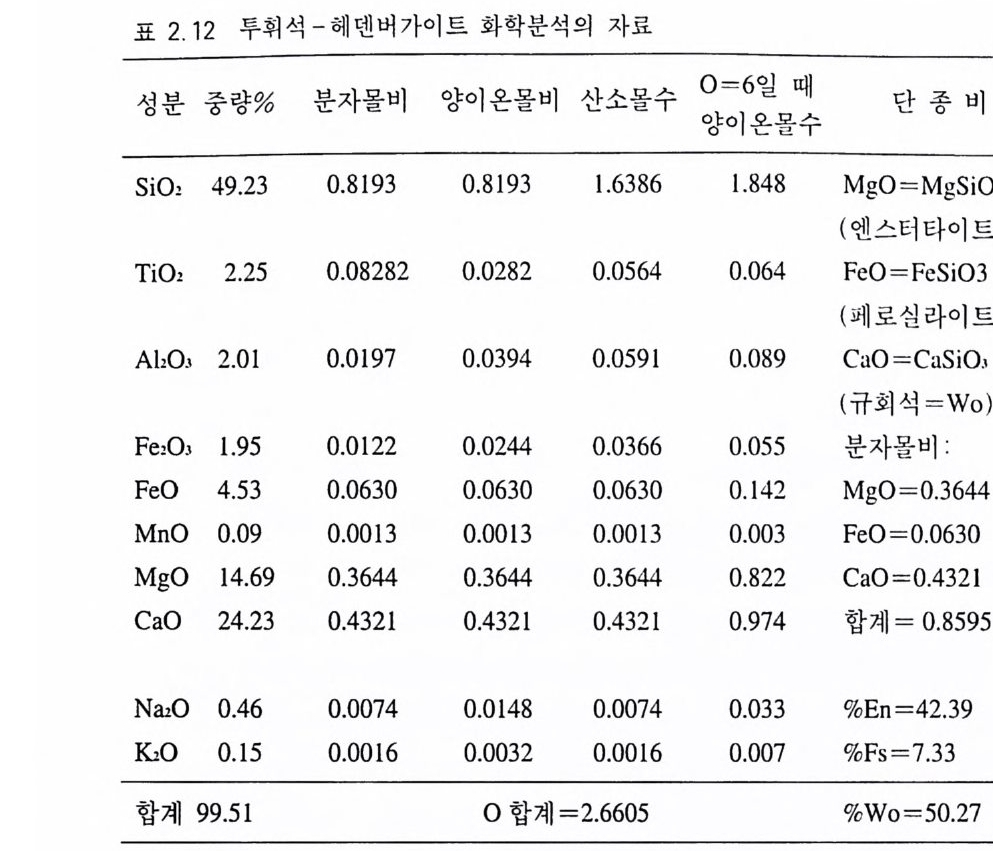 표 2.12 투휘석-헤덴버가이트 화학분석의 자료
표 2.12 투휘석-헤덴버가이트 화학분석의 자료
있다. 우선 중량%를 분자량으로 나누어 분자몰비를 구하고, 이로부 터 양이온몰비를 계산한다. 그리고 각 산화염 분자 형태로부터 산소 원자몰비를 구한다 . 우리는 투휘석과 헤덴버가이트의 화학식을 이미 알고 있기 때문에 산소 원자수가 6 개인 것을 기준으로 하여 양이온 수를 다시 계산한다. 이 룰 위해 양이 온몰비 수치 에 다 6/2.6605 를 곱 해 주면 된다. 이제는 각 양이온의 배치가 이루어져야 하는 단계 가 되었는데, 배위수가 4 인 위치에는 S i4 + 를 비롯하여 T i 4 ♦, Al” 가 자리잡게 한다. (Si, Ti, A I) 의 합이 2.0 이 되어야 하고 Si4 •+ Ti4 • = 1. 912 가 되므로 0.089 인 Al” 에서 2.0 이 되는데 부족한 0.088 만 떼어
내고 나머지 AP'(0.001) 은 Fe1•, Fe2', Mn2•, M g”와 한데 묶는다. 또 Ca2•, Na1•, K1 를 한데 묶는다 이렇게 하여 얻어지는 화학식은 (Cao.m N ao.O JJK o.o o, ) no1~ ( Fe3•o.ossFe2•o.1~iM n o.0 03 M go.m ) no 끄 ( S i1.S-1 HT io . 따 Alo . oss) D.o06 이 된다 . 이 화학식은 휘석의 일반화학식인 Cai( Mg ,F e)1(Si, A l) 20 6 와 잘 일치함을 알 수 있다. 휘석의 분석치를 휘석군의 단종 광물성분으로 표현하기도 한다. 위 휘석의 분석치 내에 CaO, Mg O , FeO 성분이 포함되어 있으므 로 규희석 (Wo: CaSiO J ), 엔스터타이트 (En : Mg Si 0 1 ), 페로실라이트 (Fs: FeS i 03) 의 mo!% 로 나타낼 수 있다. 즉, M g O 의 분자몰비가 0.3644, FeO 가 0.0630, CaO 가 0 .4 321 이고 이들의 합이 0.8595 이므 로, %En =0.3644x100/0.8 5 95 =42.39, %Fs =0.0630x100/0.8595 = 7.3 3 , %Wo=0 .4 321xl00/0.8595=50.27 이 된다. 양기석 (표 2.13) 양기석을 포함한 각섬석군에 속하는 광물의 화학 분석 자료에는 물 (H20) 이 포함된다. 이것은 광물 내에 (OH) 상태 로 존재하는 성분에서 기인된 것이다. 여기서 Hi O(+) 란 105°C 이 상의 온도예서 방출되는 수분이고, H20(-) 는 105°C 이하에서 방 출되 는 수분을 가리 킨다. 전자(前者)를 구조수(構造水, stru c tu ra l wa t er) 라고 하며, 화학식의 계산 과정에 포함시킨다. 그러나 후자 (後者)는 광물의 표면이나 작은 툼 사이에 있는 수분으로서 흡착수 (吸着水, adsorp tion wa t er) 라고 하며, 화학식 계산 과정에서는 제외 시킨다. 이 화학분석 자료를 처리해 나갈 때 이미 우리가 양기석임을 알고 있다고 가정 하면 그 일반화학식 이 Ca i(M g , Fe)sS i a022(0H)2 임 을 알게 된다. 그래서 앞으로 취급될 원소들의 배치에도 참고할 수가 있다. 다른 규산염 광물에서처럼 중량%로부터 분자몰비를 계 산한 후 양이온의 몰비를 계산해 낸다. 한편 음이온인 0 및 (OH)
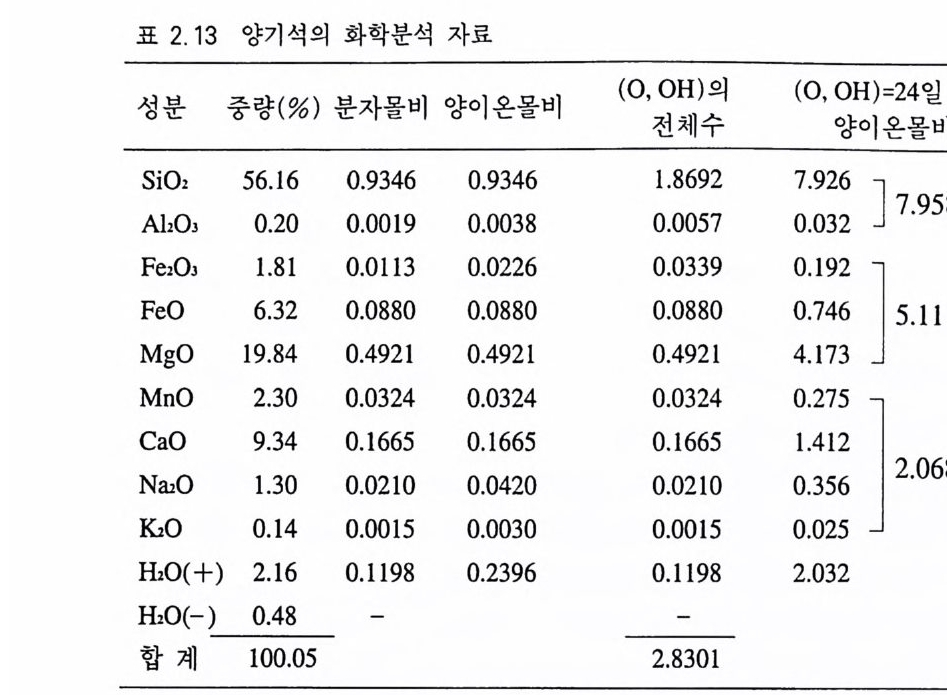 표 2.1 3 양기석의 화학분석 자료
표 2.1 3 양기석의 화학분석 자료
의 합은 2.8301 이 된다. 그런데 일반화학식으로부터 O 와 (OH) 의 총수가 24 임을 알 수 있으므로 모든 양이온을 24 개의 음이온을 기준으로 계산하기 위해 24/2.8301 을 각각 곱한다. S i는 8 이 되어 야 하는데 7.926 밖에 되 지 않으므로 Al 의 0.032 를 한데 묶어 7.958( 늑 8) 이 되게 한다. 그리고 Fe,M g을 한데 묶으면 5.111 이 되 며 이 수치는 5 에 근접하게 된다. Ca, Na, K, Mn 도 한데 묶으면 2.068 이 되어 역시 2 에 근접하게 된다 . 결국 이 양기석의 화학조 성 은 (Ca1A1Naa.36 M no.2, K o.02) 파 (Fe0 .1 9F8o.7 5M g 4.17 )rs .11 (Si7 .93A lo.0 3) Z7% 어 (OH)2 로 표현할 수 있다. ® 황산염 광물 석고 (표 2.1 4 ) 각 산화염의 중량%를 분자량으로 나누어 분자비
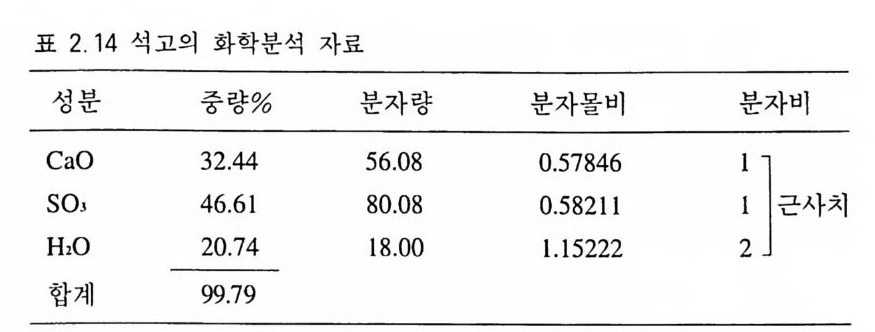 표 2.1 4 석고의 화학분석 자료
표 2.1 4 석고의 화학분석 자료
를 구한다 . 이 경우 분자몰비가 CaO : SO J : H i 0=0 .5 8 : 0.58:1.15 이어 서 대략의 분자몰비는 l : l : 2 라고 할 수 있다. 따라서 화학식은 산 화염의 형태 그대로인 Cao • sol • 2H i0 또는 양이온과 음이온을 한데 모아 CaSO 』 • 2H i0 로 쑬 수도 있다. 후자가 더 바람직 한 표 현이다. 2.4 벽개 • 열개 • 단구 2.4.l 벽개 어떤 광물이 외부로부터 물리적인 힘을 받을 때 어느 특정한 방 향을 따라 매끈한 면을 만들면서 쪼개지는 경우가 있는데 이러한 현상을 벽개(男開 cleava g e) 라 하고, 이때 생긴 평탄한 면을 벽개 면(勞開面, cleava g e p lane) 이라고 한다. 벽개가 발달하는 것은 광물 내부의 원자 배열 상태와 직접 연관이 있다. 즉, 3 차원적으로 배 열되어 있는 원자들 사이에서 어떤 방향을 따라 원자들의 결합력 이 약할 경우 외부로부터 충격을 받으면 우선 원자들의 결합력이 약한 방향을 따라 분리가 일어나게 되는데 이러한 원인으로 벽개
 (a) (b) (c)
(a) (b) (c)
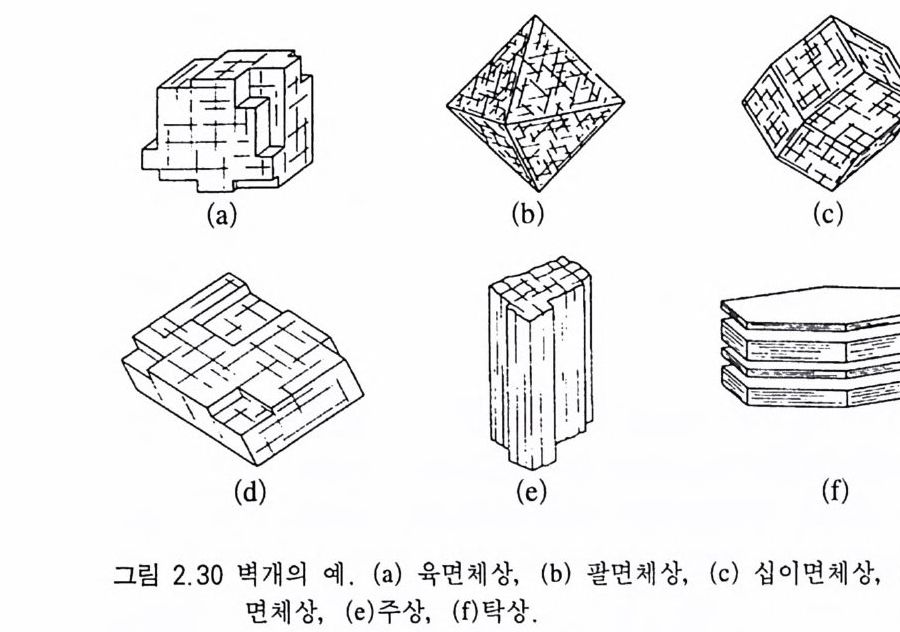
가 생기게 된다. 일반적으로 벽개는 결정면에 나란하게 발달한다 . 원자들의 결합력에 영향을 미치는 요소로는 원자간의 거리, 인력 및 반발력 등이 있다. 벽개가 발달하는 방향과 수효도 광물의 특징이다(그림 2.3 0 ). 운 모류 광물은 6 각형의 판상결정 형태에 나란하도록 얇게 분리된다. 이러한 벽개를 탁상(卓狀) 벽개라고 한다. 혹운모나 황옥처럼 수직 방향인 c 결정축에 직각인 한 방향으로 발달하는 벽개를 특히 저면 (底面)벽개라고 한다. 소금이나 방연석은 정육면체의 결정면에 나 란한 3 방향으로 쪼개지며 동시에 서로 직각이다. 이런 특징의 벽 개를 육면체상(六面體狀) 벽개라고 한다 . 방해석에는 3 방향의 벽 개가 있지만 그 방향이 직각이 아니고 비스듬하다. 이룰 능면체 상(菱面體狀) 벽개라고 한다. 각섬석은 두 방향으로 쪼개지는 특 징이 있어 이를 주상(柱狀) 벽개라 하고, 섬아연석의 경우는 6 방향
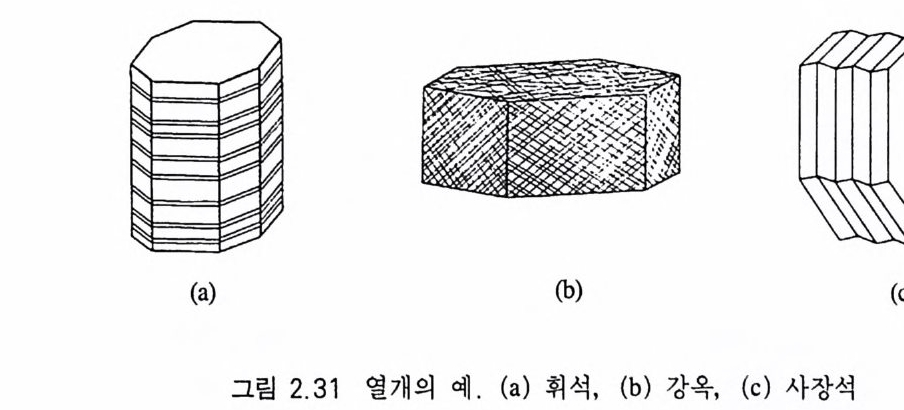
으로 쪼개지는데 이를 12 면체상(十二面體狀) 벽개라고 한다 . 작은 힘을 주어도 선명한 벽개면이 만들어지는 광물이 있는가 하면, 어떤 광물은 센 힘을 주어야 쪼개지고 또 그 면도 매끈하지 않은 경우가 있다 . 이처럼 벽개 발달의 정도와 질(質)에 따라 다음 과 같은 용어로 구분하여 표현한다. 완전(完全, per f ec t) : 벽개면이 쉽고 명확하게 만들어 지는 경 우. 방해석, 운모, 다이아몬드, 형석. 우수 (1 及 秀, go od): 양질의 벽개면이 비교적 쉽게 만들어지는 경우 . 장석. 양호(良好, fair) : 우수와 불량의 중간 정도로 벽개면이 만들어 지는 경우. 크리소베릴. 불량(不良 po or): 평탄한 면이 잘 만들어지지 않는 경우. 저 어콘, 인회석. 2.4.2 열개 쌍정(雙晶)이 발달한 사장석이나 휘석, 강옥에 충격이 가해지면 쌍정면을 따라 분리되는 경우가 있다. 이처럼 쌍정면을 따라 분리 가 일어나는 현상을 열개 (裂開 parti n g)라고 한다. 열개가 일어난 면은 벽개면처럼 평탄하다. 휘석은 탁상 열개, 강옥은 능면체상 열개, 사장석은 탁상 열개가 발달한다(그림 2.3 1). 2.4.3 단구 어떤 광물은 충격을 받을 때 매끈한 면으로 쪼개지지 않고 불규 칙한 면을 만들면서 깨진다. 이를 단구(斷口, fr ac tur e) 라 하고, 이
 (a) (b) (c)
(a) (b) (c)
때 생긴 면을 단구면(斷口面)이라고 한다 . 단구는 광물 내의 원자 간 결합력이 사방으로 같거나 거의 동일할 때 생긴다. 유리나 혹 요석같이 일정한 결정구조가 없는 비정질 물질에서도 단구가 만들 어진다. 단구면의 특징에 따라 용어를 달리 사용한다. 패각상(貝穀狀 conchoid a l) 단구: 조개껍데기의 내부처럼 둥근 줄무늬가 생기는 경우. 석 영, 혹요석 . 침상(鍊狀 hackly) 단구 : 까끌까끌한 나뭇결 같은 표면이 만 들어지는 경우, 연옥, 자연동. 섬유상(織維狀 fibr ous): 마치 솜처럼 떨어지는 경우 . 사문석 . 불평탄(不平坦 uneven): 불규칙한 표면이 생기는 경우 . 처 트, 강옥.
2.5 경도 2.5.l 경도의 정의 광 물 의 경도 (硬度 , hardness) 는 광물의 단단함을 나타내는 용어로 서, 굵힘이나 마모작용에 저항하는 정도를 의미한다. 경도는 광물 을 구성하고 있는 원자나 이온의 배열상태 및 특징에 따라 크게 좌우된다. 흑 연과 다이아몬드의 경우, 두 광물이 모두 탄소 (C) 로 구성되어 있으나 등축정계로 촘촘히 배열되어 있는 다이아몬드는 광물 중에서 경도가 제일 높은 반면, 육방정계의 층상구조를 지니 고 있는 흑연은 제일 작다. 또한 원자들의 점밀도가 높은 방향은 경도가 높고, 그렇지 않은 방향은 작다. 이와같이 한 광물 내에서 도 원자들의 점밀도가 방향에 따라 차이가 있기 때문에 엄밀히 말 하면 광물의 경도는 위치에 따라 모두 다르다. 그러나 대부분 그 차이가 현저하지 않으므로 무시하지만, 남정석(藍晶石, kyanit e) 에 서는 뚜렷한 차이를 나타낸다. 남정석은 장축 방향으로는 모스 경 도가 5 정도이지만 이와 직각인 방향은 7 로서 매우 높다. 일반적으 로 광물을 구성하고 있는 원자나 이온들의 반경이 작고 가까울수 록 , 또 산화수가 클수록 경도가 높은 경향이 있다. 2.5.2 모스 경도계 독일의 광물학자인 모스 (Mohs) 는 광물마다 마모에 견디는 능력 이 다름을 깨닫고 대표적인 광물을 10 개 선택하여 긁힘에 저항하 는 능력이 높아지는 순서로 이들을 배열하였다(표 2.1 5 ). 이룰 모 스 경 도계 (硬度 計 , hardness scale) 라고 한다. 경 도 등급은 단순히 순서적인 배열일 뿐, 절대적인 수치의 배수(倍數) 개념이 아니다.
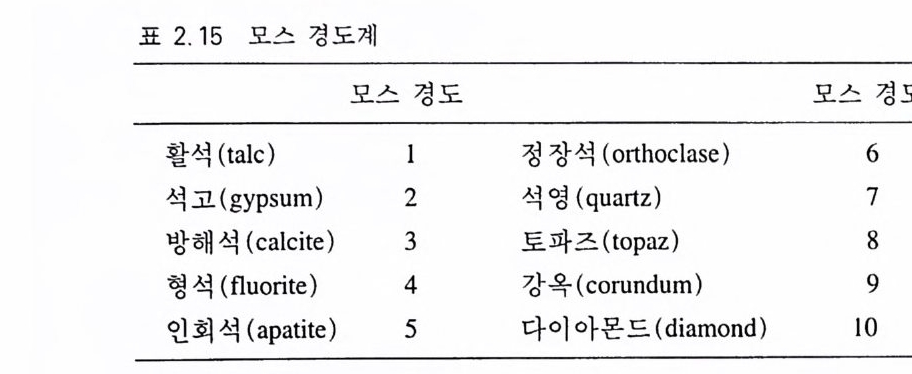 표 2.1 5 모스 경도계
표 2.1 5 모스 경도계
 400 I- -
400 I- -
 = >
= >
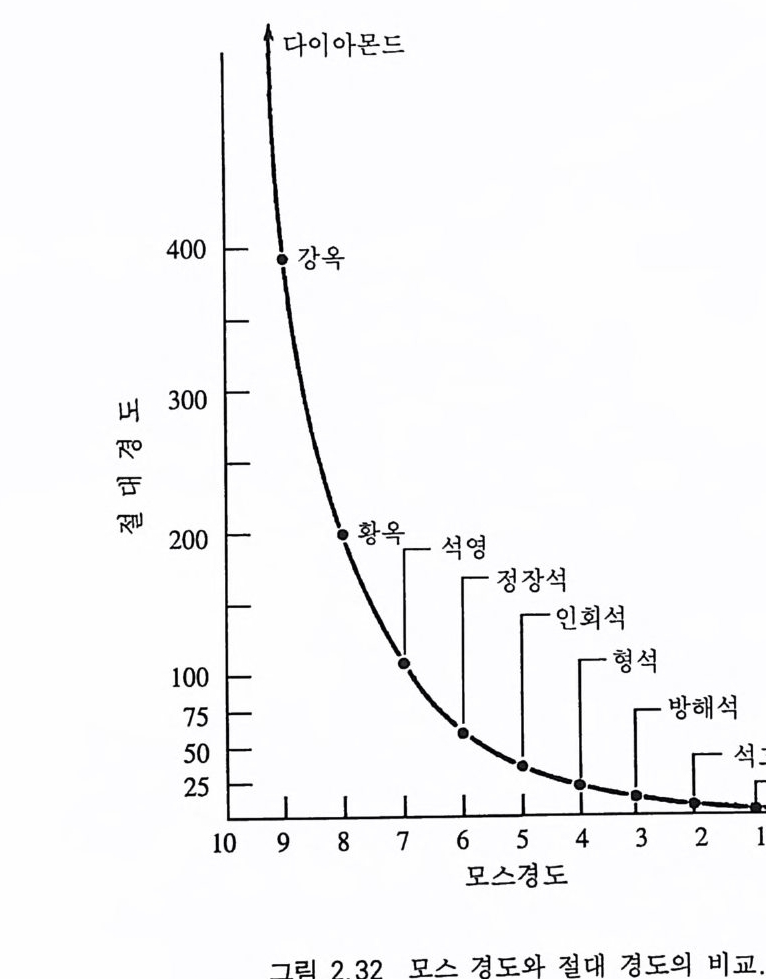
다시 말하면 모스 경도가 2 인 석고가 경도가 1 인 활석보다 2 배 강 하다는 의미가 아니라는 점이다. 실제로 경도가 9 인 강옥과 이보 다 한 등급 높은 다이아몬드의 실제 경도 차이는 경도 l( 활석)로부터 9( 강옥)까지의 경도 차이보다도 훨 씬 크다(그림 2.3 2 ). 경도를 측정할 때는 연필형으로 되어 있는 경도심 (硬度志, hardness pen cil , 그림 2 .3 3) 이나 판상체의 경도판(硬度板, hardness p la t e) 을 사용한다 . 만약 어떤 광물에 경도심 5( 인회석)를 사용하여 표면을 가볍게 긁었을 때 굵히지 않았고, 또 경도심 7( 석영)에는 긁힌 자국이 남 고, 경도심 6( 정장석)으로는 서로 굵히지 않는다면, 이 광물의 경도 는 6 이 된다. 한편 어떤 광물이 경도심 7 에는 굵히지만 경도심 6 에 는 긁히지 않았다면 이 광물의 경도는 6 과 7 사이인 6 .5로 정한다.
 二二二二二二二
二二二二二二二
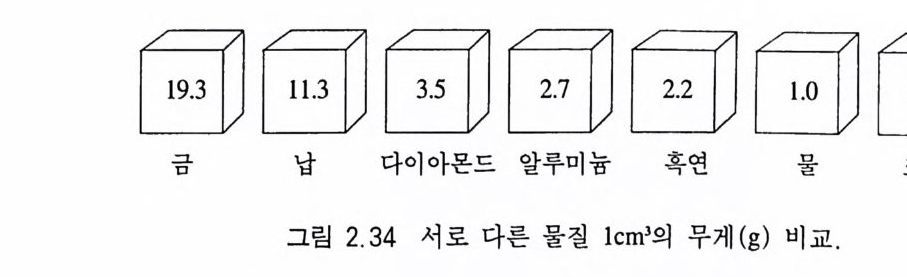
2.6 비중 2.6.l 비중의 정의 어떤 물체의 단위체적이 지니는 무게를 밀도(密度, dens ity)라고 한다. 그리고 어떤 물체의 밀도와 4°C, 1 기압 상태의 물의 밀도와 의 비(比, ra ti o) 를 비중(比重, s p ec ifi c gr av ity)이라고 한다. 그런데 4°C, 1 기 압 상태의 물 lcm3 의 무게는 l g이다. 따라서 어떤 물체의 비중은 그 물체의 밀도를 물의 밀도로 나눈 것과 같은데, 물의 밀도 는 l g /cm3 이므로 어떤 물체의 비중은 그 물체의 밀도와 일치하게 된다 . 어떤 광물의 비중은 〈그 광물의 무게와 이 광물과 같은 부 피를 가지는 물의 무게와의 비〉라고 정의할 수 있다. 밀도는 단위 (g /cm3) 가 있는데 비하여 비중은 단위가 없다. 광물과 기타 물질의 비중을 동일한 체적을 기준으로 하여 비교하면 그림 2 .3 4 와 같다. 광물의 비중은 그 광물을 구성하고 있는 원소들의 원자량, 촘촘 히 배열되어 있는 정도에 좌우된다. 원자량이 큰 원소로 되어 있 을수록, 또 원자들이 밀집 배열되어 있을수록 비중이 크다.
2.6.2 비중 측정법 비중을 측정을 하기 위해서는 밀도를 구하는 방법을 사용한다. 즉 , 광물의 공기중에서의 무게와 부피를 알아야 한다. 그러나 불 규 칙 한 형태의 광물 부피를 정확하게 계산하기란 거의 불가능하 다 아르키메데스 (Arch i medes) 는 어떤 물체를 물속에 넣으면 물체 에 미치는 부력 때문에 공기중에서보다 더 가벼워지는데 이 가벼 워진 무게는 그 물체 를 치환한 물의 무게와 일치한다는 사실을 알 아 냈다 . 이 를 아르키 메 데 스의 원 리 (Archim edes' Pri nc ip le ) 라고 한 다. 물 l g은 물 1cc 의 무게이므로, 광물의 체적을 알기 위해서는 공기중에서 측정한 광물의 무게와 물 속에서 측정한 광물의 무게 를 빼면 그 무게의 차이가 바로 그 광물의 부피가 된다 . 공기중에서의 광물 무게 비중= 공기중에서의 광물 무게-물 속에서의 광물 무게 이 아르키메데스의 원리를 사용하면 광물의 비중울 간단히 측정 할 수 있다 . 비중값은 소수점 이하 둘째자리까지 계산한다. ® 비중저울을 사용한 측정법 광물의 비중을 정확하게 측정할 수 있는 방법으로서, 과거에는 비중 측정용 저울이 별도로 제작되었으나 이제는 생산이 중단된 상태이고, 최근에는 전자 화학저울에 비중 측정용 부품을 간단히 설치하여 비중을 측정한다(그림 2.3 5 ). 물 속에서의 무게를 측정하 기 위해서 증류수나 수돗물을 사용한다 . 수돗물인 경우 기포가 많 이 존재하여 이들이 광물 표면에 많이 붙게 되면 무게 측정에 오 류가 생길 수가 있다. 이런 경우에는 가는 붓울 사용하여 기포를

그림 2.35 비중 측정용 전자저울 . 제거시킨다. 이 측정법은 0.6g 이상인 광물의 비중을 측정하는 데 적당하다 물 대신 유기용매를 사용하는 경우도 있는데, 유기용매 는 표면장력을 감소시키는 효과와 함께 용액 내에서의 무게 감소 가 상대적으로 증가하기 때문에 작은 광물의 비중을 측정할 때 사 용된다. 물 대신 유기용매를 사용한 경우에는 측정한 온도에서의 용액의
 광물을 집게로
광물을 집게로
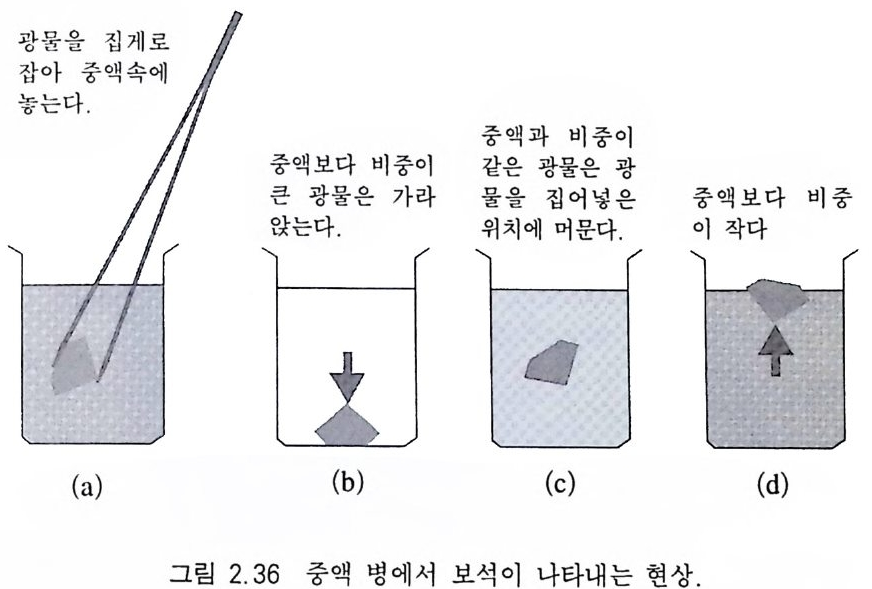
비중값을 위 공식에 곱해 주어야 한다 . 비중을 측정할 때 유의해야 할 점은, 광물인 경우 표면이나 내 부에 균열이 있는 경우가 많으므로 여러 번 측정하여 평균값을 사 용하도록 한다 . ® 중액 사용법 비중을 알고 있는 유기용매 속에 광물을 넣어 그 거동을 관찰하 는 방법 이 다(그림 2.3 6 ) . 집 게 를 사용하여 광물을 중액 속에 넣고 가만히 놓았을 때 (a) 만약 그 광물이 이 놓여진 위치에서 수평운 동을 한다면 중액과 광물의 비중이 일치하고 (c), 광물이 위로 떠 오르면 중액보다 광물의 비중이 작으며 (d), 만약 광물이 아래로 가라앉으면 광물의 비중이 더 크다는 것을 의미한다 (b). 이러한 현상 역시 아르키메데스의 원리를 이용한 것이다. 그러나 중액을
 JI2 .1 6 ~ '2lJ E.. £. At% !rJi:-' 2lJ~ 19.l !'i;;rJ . .
JI2 .1 6 ~ '2lJ E.. £. At% !rJi:-' 2lJ~ 19.l !'i;;rJ . .
A}%611 1:I1-Fg, ~~5}~ ~~~ 1:I1-F.!i!.q~ t:llEf9.l 1:I1-Fg, ~ 'T ~ ~ 7il4-7} \iq. - F~~ ~ 1:I1-F°1 q~ %%°1 4~a:l ~ g, tIJl °1 ~g, ~4f5}711 ~Cl5}-c t~l tJ~4- K:i1}~olq. ojl~ ~e>1 ~~(1'l1 -F=2.6 5)..Q...£ olf-OJ~ .£.~ 4fol] A}i?(?i'.Pi:)°1 ~ :~-£1e>1 ~ g, tIJl, 1:I1-F°1 3.33~ P1l~rJIo}01.£.q01s %~ 4fol] °1 -!-~%g, ~ 71] £1~, ~~ ~ ~.£ lIi.£.g~ J.}i?(1'l1'F=19.3)~ %71 1'l}~..Q...£ ~i1 7}c}?J-°l-1 171] ~Cl¥lq.
 ?조
?조
비중을 측정하는 데 사용되는 용액을 표 2 .1 6 에 나타내었다. 중 액은 매우 고가(高價)의 액체이므로 절약해 사용하여야 한다 . 이 때문에 여러 번 사용한 중액은 여과지에 통과시켜 이물질을 제거 한 다음 재사용하면 된다. 또 대부분 휘발성이 강한 물질들이므로 환기가 잘 되는 실내에서 사용하도록 해야 한다. 중액을 섞어 만 든 혼합 용액을 사용할 경우에는 용액의 일부가 휘발하여 비중이 변할 수가 있다 . 따라서 중액을 사용하기 전에 지시석 (그림 2.3 7 ) 을 넣어 비중을 미리 확인할 필요가 있다. ® 비중병 사용법 크기가 매우 작은 광물은 비중 저울을 이용하여 측정하더라도 그 오차가 커서 정확한 수치를 얻기가 힘들다. 이런 경우에 비중
 it
it
병을 사용하면 해결된다. 비중병(그림 2 .3 8) 은 투명한 유리로 만든 작은 용기로서 일정한 부피의 용액만을 담을 수 있고 초과되는 양 은 밖으로 흘러나가도록 되어 있다. 비중병 속에 담겨 있는 용액 의 부피는 용기 밖에 표시되어 있다 . 비중병을 사용해 비중을 측 정하기 위해서는 먼저 빈 비중병과 마개의 무게를 측정해 두어야 한다. 작은 비커에 중액을 봇고 광물이 중액속에서 수평운동을 할 때까지 비중이 다른 용액을 추가하여 중액과 광물의 바중이 일치 되게 한다. 그런 다음 이 중액을 비중병 속에 가득 옮겨 붓고 마 개를 닫는다. 흘러나온 중액은 휴지로 닦아 낸다. 그리고 중액이 들어 있는 비중병의 무게를 저울로 측정한다. 이 무게에다 빈 비 중병과 마개의 무게를 빼면 중액만의 무게가 계산된다. 용액의 부 피는 이미 알고 있으므로 다음 식으로 광물의 비중을 측정할 수 있다.
광물의 비중=중액의 비중=중액의 밀도 = 중액의 무게 중액의 부피 예 를 들어 용량이 50cc 인 비중병과 마개의 무게가 10.00 g이고, 닌닌.. 중병에 중액을 가득 넣고 잰 무게가 210.00 g이었을 때, 광물의 중은 중엑의 비중과 동일하므로 . 광물의 비중=중액의 바중= 2105g0 -c1 c 0g = 4.00 이 되어 이 광물이 강옥임을 알 수 있게 된다. 비중병의 요o랴o T0 10cc, 20cc, 25cc, 50cc, 100cc 등 다양하다 .
제 3 장 조암광물의 광학적 성질과 편광현미경 관찰 3,1 조암광물의 광학적 특성 하얀 종이에 십자선을 그린 다음, 두꺼운 유리판을 올려 놓고 들여다보면 직선이 원래 대로 보이고, 이러한 현상은 유리를 회전 하여도 변하지 않는다. 그러나 투명한 방해석 결정을 올려 놓고 그 속을 들여다 보면, 직선이 두 개로 겹쳐서 보이며(그림 3.1 ), 방해석 결정을 돌리면 이중으로 겹쳐 보이던 십자선이 좁아지다가 다시 넓어지는 것을 볼 수 있다. 이와 같은 현상으로부터 물질에 따라 그 속에 입사한 빛이 서로 다른 행동을 한다는 사실을 알 수 있게 된다 . 빛이 투명한 물체 속을 통과할 때, 그 광선의 경로는 스넬의 굴 절법칙(屈折法ff l J, lawo f re fr ac ti on) 에 의해 예측될 수 있다 . 죽 광학 밀도가 다른 두 매질의 경계를 직각으로 입사하는 빛은 광선의 경 로가 변하지 않고 그대로 직진하는데 비해, 비스듬히 입사하는 빛
 그림 3.1 투명한 방해석을 통해 관찰되는 복굴절현상 .
그림 3.1 투명한 방해석을 통해 관찰되는 복굴절현상 .
은 광선의 경로가 변하는 굴절현상을 일으키게 된다. 이 법칙에 의하면 종이에 그린 십자선 위에 투명한 물체를 놓고 들여다 볼 경우 유리판을 통해 관찰된 것처럼 빛이 직진하므로 굴절없이 원 래의 모양대로 보여야 한다. 그러나 방해석을 통해서는 두 줄로 겹쳐 보이므로 빛의 굴절이 일어났음울 알 수 있고 이런 현상은 스넬의 굴절법칙에 위배가 된다. 이러한 사실을 깨닫게 된 광물학 자들은 빛과 광물 사이에 일어나는 반응에 대해 연구하기 시작하 게 되었고 이제는 그 비밀이 많이 벗겨지게 되었다. 조암광물을 연구할 때 편광현미경을 사용하는데, 편광을 사용하면 광물의 결 정구조에 따라 광학현상이 달리 관찰되기 때문이다. 3.1.1 등방성 광물이 모든 방향에 대해 동일한 광학적 성질을 나타내는 것을
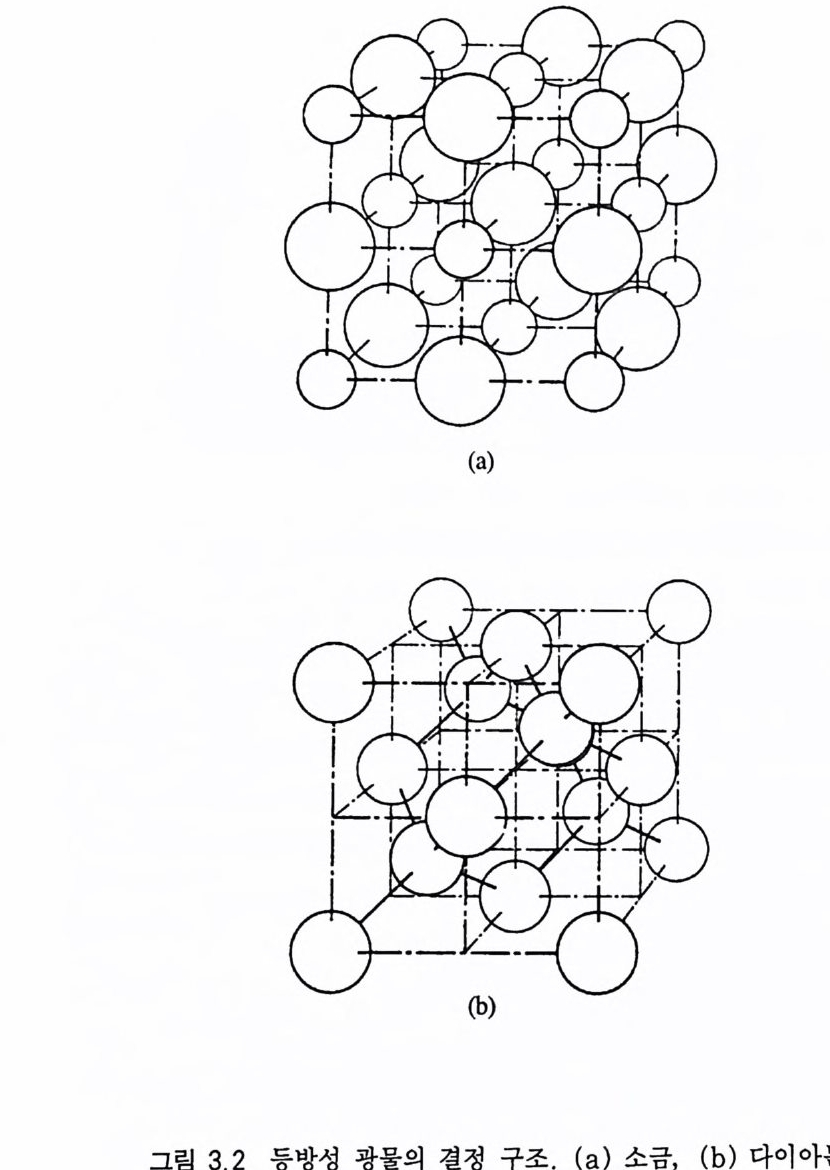
등방성( 等方 株 i so t ro pi c) 이라 하며, 이것은 그 광물의 결정학적 방 향을 따라 원자 배열방식이 동일하기 때문에 생기는 현상이다. 따 라서 등방성 광물에 빛이 입사하면 모든 방향에 대해 항상 일정한 속도로 빛이 진행하게 된다. 등측정계에 속하는 광물에서는 세 결 정학적 방향으로 원자 배열이 동일하다. 즉 이온 결합을 하고 있 는 광물(예 : 소금, 그림 3.2 a) 인 경우 원자핵 주위에 있는 8 개의 전자가 모든 방향에 대해 대칭적으로 분포하고 있으며, 공유결합 울 하는 광물(예 : 다이아몬드, 그림 3 . 2b) 인 경우는 원자간의 결합 력이 대칭을 이루고 있기 때문이다. 이런 특징이 있는 광물에 빛 이 입사하면 모든 방향으로 흡수나 굴절이 동일하게 일어나게 된 다 따라서 등방성 광물에서는 모든 방향에 대해 빛이 같은 속도 로 진행하기 때문에 굴절률이 동일하여 결과적으로 하나의 굴절률 만 가지게 된다 . 또한 빛의 진행 방향에 수직인 모든 방향으로 진 동하는 일반광과 광선의 진행 방향에 수직인 한 면 내에서만 진동 하는 편광이 등방성 광물을 통과할 경우 빛의 진동방향은 변하지 않게 된다. 유리, 호박, 단백석, 혹요석 같은 비정질(非晶質, amorp h ous) 물 질도 등방성을 띤다. 이들에는 구성원자들이 불규칙하게 배열되어 있다. 3.1.2 이방성 7 정계 중 등축정계 이외에 속하는 광물에 빛이 입사하면 그 입사방향에 따라 서로 다른 속도로 진행하는 두 개의 편광이 만들 어진다. 이것은 진동하는 전자장 상태인 빛이 광물을 통과하는 동 안 원자들에 의해 서로 다른 전기적 인력 (電氣的引力, electr ica l a ttr ac ti on) 을 받기 때문이다. 원자밀도가 최대인 면을 따라 최대의
 (a)
(a)
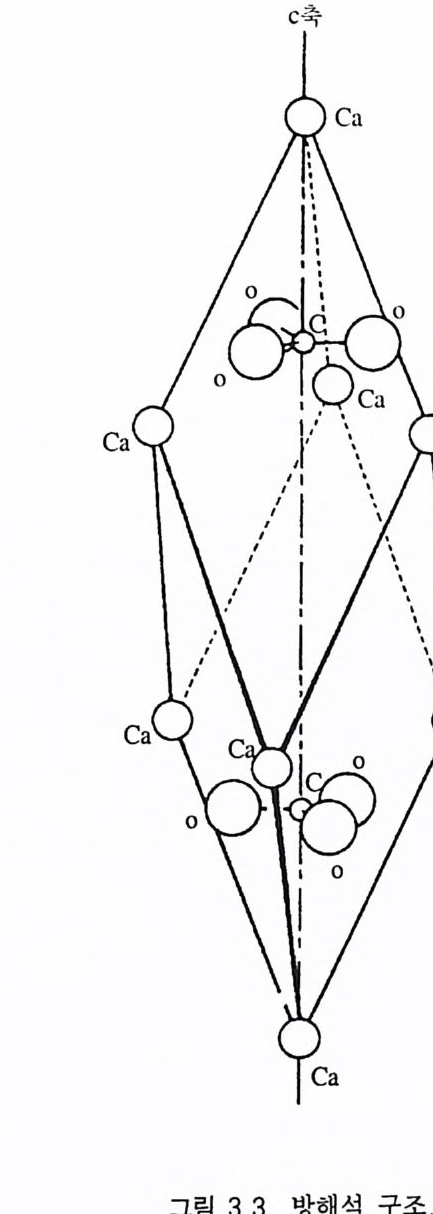
편극현상이 일어나며, 원자밀도가 최소인 방향은 그에 수직이다. 편극현상이 크면 클수록 빛의 진행속도가 감소하게 되는데 이 때 문에 굴절률은 커진다 . 이와 같이 이온결합이나 공유결합을 하고 있는 광물에서 방향에 따라 편극현상을 일으키는 힘이 차이가 있 을 때 그 광물은 이방성( 異方性 , an i so t ro pi c) 을 띠게 된다 . 삼방정 계인 방해석의 경우(그림 3.3), 탄산염 (COF) 착이온은 c 결정축에 수직인 평면으로 배열되어 있고 또 강한 공유결합을 하고 있어서 c 결정축을 따라 통과하는 빛은 이 착이온의 면과 나란하게 편극이 된다. 따라서 이 방향으로 굴절률이 크게 되고 그 결과 빛의 속도 도 느려 진다. 한편 c 결정축에 수직인 방향으로 입사한 빛은 진동 방향에 따라 서로 다른 속도로 진행하게 된다. c 결정축에 수직으 로 진동하는 빛은 탄산염 착이온의 배열방향과 나란하게 진동하므 로 편극이 최대가 되어 속도가 느리지만, c 결정축과 나란하게 진 동하는 빛은 편극효과가 최소로 되어 가장 빠른 속도로 진행하게 된다. 이 때문에 굴절률은 각각 최대 및 최소가 된다 . 이방성 광물에 광축(光軸 o pti cax i s) 이 아닌 방향으로 빛이 입사 하면 반드시 광축과 수직되게 진동하는 광선과 이에 수직인 방향 으로 진동하는 또 하나의 광선으로 나뉘게 되는데, 이렇게 하나의 광선 이 두 개 의 광선 으로 나뉘 는 것 을 복굴절 (複屈折, double re fr a ti on) 이라고 한다 . 두 편광 중에서 스넬의 굴절법칙을 따르는 광선을 상광선(常光線, ord i n ary ra y)이라 하고, 이에 적용되지 않는 광선을 이상광선(異常光線, extr ao rdin ary ra y)이라고 한다. 두 광선 은 모두 편광(偏光, p lane p ol ari zed lig h t)이며 두 편광의 진동면은 서 로 수직이다. 죽 이상광선은 광선이 진행하는 방향과 광축을 포함 하는 면내에서 진동하고, 상광선은 이에 수직되게 진동한다. 이방 성 광물 내에서도 어떤 특정한 방향을 따라 입사한 빛은 등방성의 경우와 동일한 굴절현상을 나타내는데, 이 방향을 광축(光軸)이라
 c 축
c 축
 표 3. 1 광 물 의 광학적 특 성 분류
표 3. 1 광 물 의 광학적 특 성 분류
고 한다 이 방성 광물은 광축의 수효에 따라 일축성 (一軸性, unia xial ) 과 이축성( 二 軸住 b i ax i al) 으로 다시 나뉜다. 일축성 광물은 정방 정계, 삼방정계, 육방정계에 속하는 광물들이고, 이축성 광물은 사방정계, 단사정계, 삼사정계에 속하는 광물들이다. 일축성 광물 인 경우 광축은 항상 c 결정축과 일치한다. 그러나 이축성 광물에 서는 광축이 a,b,c 결정축과 일치하는 것이 아니라 주진동축(主振動 軸, princ ip a l vabratio n ax i s) 인 X, Y, Z 와 관련이 있다. 등방성 및 이방성 광물의 광학적 특징을 표 3 .1에 요약하였다. 조암광물의 광학적 특징은 결정구조와 직접적인 연관이 있으므로 편광현미경으로 다른 어떤 최신 분석기기로도 알 수 없는 많은 광 물학적(굴절률, 결정형태, 벽개, 다색성, 광축각 등), 암석학적(조 직, 암석명, 정출 환경, 지구조 변천사, 변성환경 등) 정보를 얻을 수 있게 된다.
 ‘K
‘K
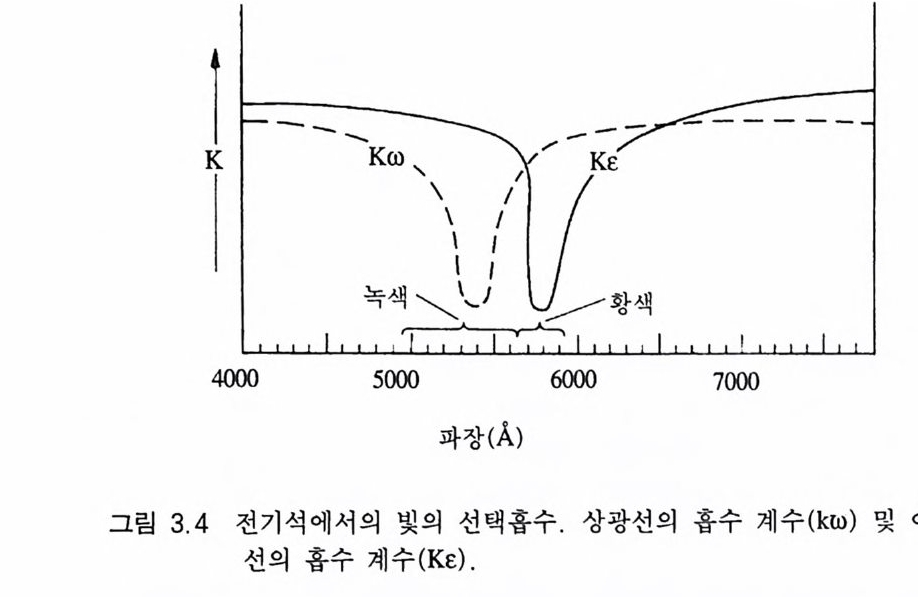
3.2 색과 다색성 편광현미경으로 관찰되는 광물의 색은 0.03mm 의 매우 얇은 두 께로 만들어 관찰하는 것이므로 일반적으로 광물일 때보다 색이 훨씬 옅다. 등방성 광물인 경우에는 일반 흡수나 선택 흡수에 관 계없이 광물 전체를 통해 흡수 및 통과가 동일하게 일어나며, 광 물을 회전시켜도 색의 변화가 없다. 그러나 이방성 광물인 경우는 빛의 진동방향에 따라 빛을 홉수하는 파장영역과 정도가 다른 것 이 보통이다 . 즉, 굴절률 크기에 따라 빛의 파장을 흡수하는 영역 과 정도가 다를 수 있다는 의미이다. 예를 들어 전기석은 광축방 향을 따라 입사하는 편광에 대해서는 5650~5900A 영역의 파장을 통과시키고 그 외 파장은 거의 흡수하여(그림 3.4 ) 결국 노란색을 띠며(그림 3.5a), 광물을 90° 회전시켜 상광선의 진동방향과 광물
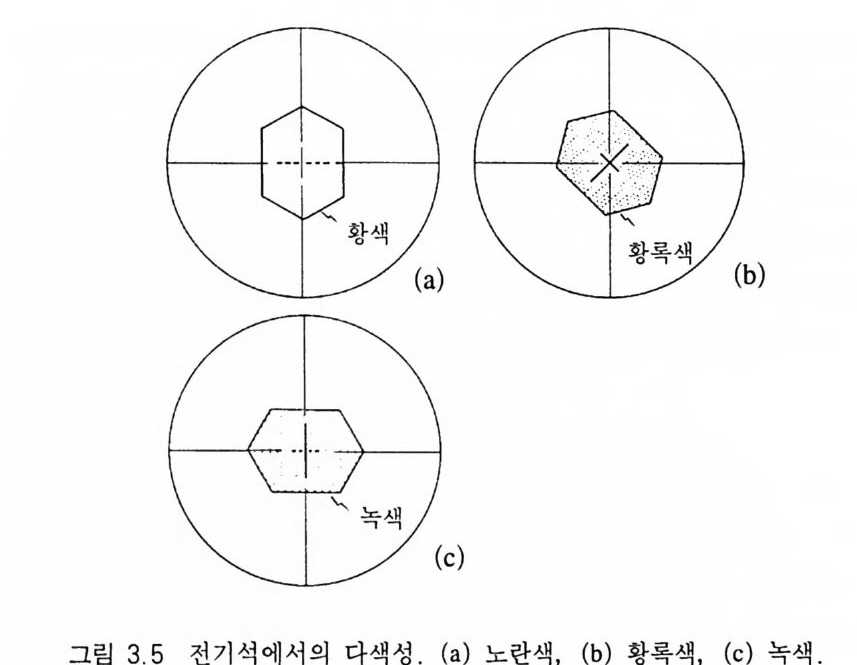 그림 3.5 전기석에서의 다색성. (a) 노란색, (b) 황록색, (c) 녹색 .
그림 3.5 전기석에서의 다색성. (a) 노란색, (b) 황록색, (c) 녹색 .
에 입사한 편광의 진동방향이 일치되면(그림 3.5 c) 5000~5650A 영 역 의 파장을 통과시 키 고 그 의 파장은 흡수하여 (그림 3.4 ) 결국 녹색으로 된다. 그 중간되는 위치에서는 두 파장 영역을 모두 통 과시키기 때문에 녹황색을 띤다(그림 3.5 b ). 이와 같이 광물 내에 있는 주진동방향과 광물에 입사하는 편광의 진동방향의 일치여부 에 따라 서로 다른 영역의 파장이 흡수 또는 통과되어 색이 변하 는데 이 현상을 다색성( 多 色性, p leochro i sm) 이라 한다. 다색성은 색이 있는 유색(有色) 이방성 광물에서만 나타날 수 있는데 이를 관찰하기 위해서는 광물을 회전시키면서 관찰하여야 한다. 일축성 광물에는 광물 내에 주진동방향이 2 개(E, 0))가 있으므로 두가지 색 만 나타날 수 있고, 이축성 광물에는 주진동축이 3 개(X, Y, Z) 가 있어서 3 가지의 서로 다른 색이 나타날 수 있다. 전자의 경우를 이 색성 ( 二 色性, dic h rois m ), 후자의 경우를 삼색성 (三色性, trich rois m )
이라고 한다 . 이색성과 삼색성을 함께 다색성이라 한다 . 이색성을 나타내는 전기석의 다색성은 〈 C= 노랑, o = 초록〉 이라 표 현하며 이를 다색성 공식( 多 色 性公式 , p leochro i c fo rmula) 이라고 한다 . 이 축 성 광물인 녹색 각섬석인 경우는 삼색성 을 띠며, 다 색 성 공 식 이 〈 X= 황록색, Y= 녹색, z = 암 록 색 〉 이 된다 . 다색성은 그 뚜렷한 정도에 따라 강함 (s t ron g), 명료 (d i s ti nc t ) , 약함 ( we a k ) , 매우 약 합 (very weak) 등으로 표시 한다 . 3,3 소광 및 소광 특징 광물 박편을 교차니콜 (crossed nic o ls) 상태에서 희전시키면, 특정 위치에서 광물 입자의 전체가 검게 변하는 현상을 관 찰할 수 있게 된다 . 이렇게 광물 입자가 검게 되는 것을 소광( i肖 光, e x ti nc ti on ) 이 라고 한다. 광물 입자의 소광은 ® 전체가 항상 검게 보이는 경우 와 ® 전체가 4 번 규칙적으로 검게 변하는 경우가 있다 . 4 번 소광 하는 광물의 경우 소광하는 위치에서 그 광물에 발달하는 어떤 결 정학적인 방향(예 : 결정면, 벽개)이 하부 또는 상부 니 콜 의 주진동 방향과 이루는 각(角, an g le) 을 소광각(消光 角 , exti nc ti on ang le) 이라 고한다 . 3.3.1 항상 검게 보이는 경우 광물을 통과해 나온 광선이 상부 니콜인 어낼라이저 (anal y ser) 를 통과하지 못하기 때문에 일어나는 소광현상으로서, 등방성 광물 모두에서 나타난다. 또한 광축에 수직으로 절단된 이방성 광물의 박편에서도 동일한 현상이 관찰된다. 등방성 광물은 물론이거니와
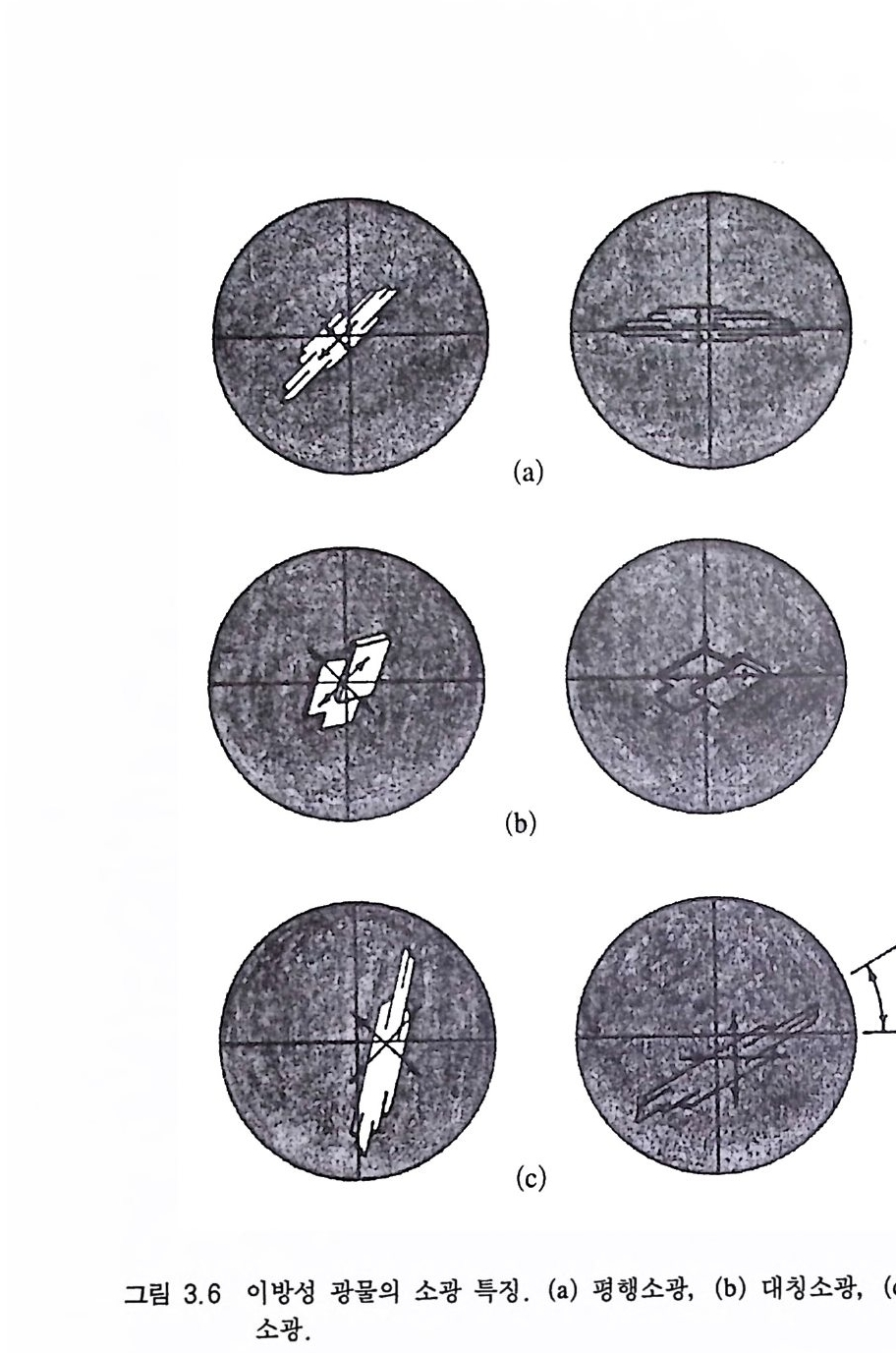
이방성 광물도 광축을 따라서는 등방성을 나타내므로, 편광현미경 의 폴랄라이저를 통과해 광물로 입사하는 남북 방향으로 진동하는 편광은 광물을 통과해 나올 때에도 진동방향이 변하지 않은 상태 로 있게 된다. 따라서 이 빛은 동서 방향으로 진동하는 빛의 성분 만을 통과시키는 어낼라이저에 의해 모두 차단되어 결국 검게 보이 게 된다. 등방성 광물의 입자 전체가 항상 검게 보이는 것을 〈항상 소광 〉 이라고 표현한다. 3.3.2 4 번 규칙적으로 검게 변하는 경우 이방성 광물에서 관찰되는 소광현상으로서, 가장 어두워 지는 경우가 90° 간격으로 4 번 반복된다. 이러한 현상을 〈 4 회 소광〉이 라고 표현한다 . 그리고 이 소광위치(i肖光位置, ex ti nc ti on p os iti on) 로 부터 45° 회전시키면 제일 밝게 된다. 소광이 일어나는 위치에서는 이방성 광물 내에 있는 2 개의 주진동방향이 상부 및 하부 니콜의 진동방향과 일치하는데, 이런 위치에서는 남북 방향으로 진동하는 편광이 광물 속을 진동방향에 변화없이 그대로 통과되어 결국 어낼 라이저에 의해 차단되므로 소광이 된다. 소광 위치에서 광물의 결정면이나, 벽개 또는 쌍정면이 상부 또 는 하부 니콜의 진동방향과 이루는 각도에 따라 평행소광(平行消 光, par allel exti nc ti on ), 대 칭 소광(對稱消光, sym metr ica l exti nc ti on ), 경 사소광 ({頃斜消光, inc lin e d exti nc ti on ) 으로 구분한다. 평행소광은 광물에 있는 직선구조가 하부 또는 상부 니콜의 진 동방향과 일치 하는 경 우로서 (그림 3.6 a), 정 방정 계, 삼방정 계, 육 방정계 둥 일축성 광물과 이축성 광물 중 사방정계인 광물에서 관 찰된다. 대칭소광은 두 방향으로 어긋난 결정면 또는 벽개를 지니고 있
 •
•
 C
C
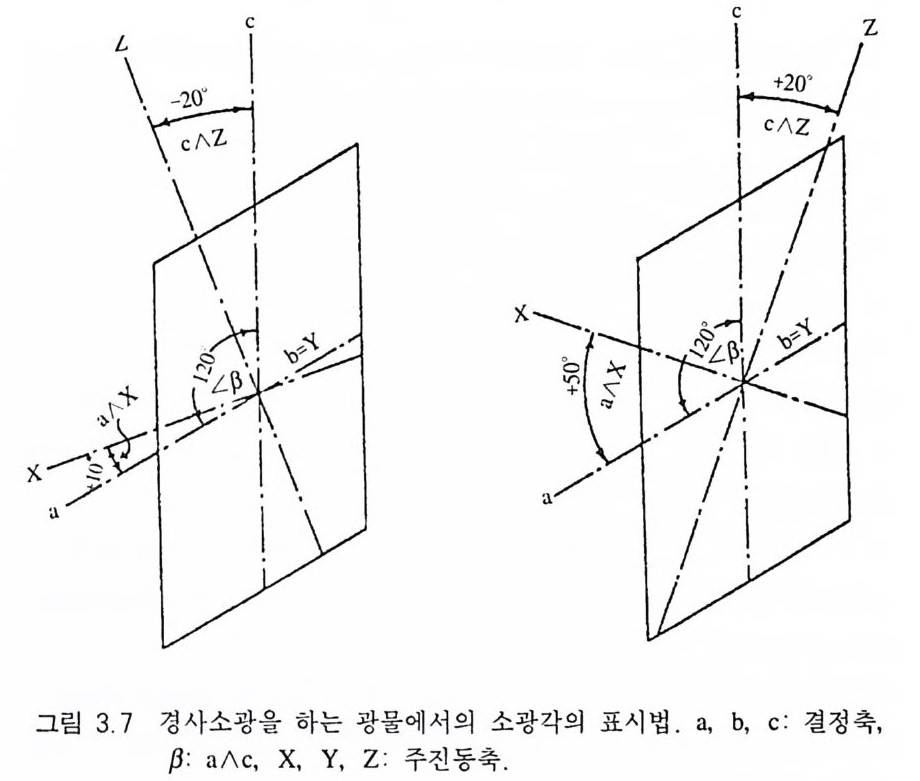
는향의 삼 방벽정개계가 및이 루육는방 정사계잇의각 이광 물하에부서 또관는찰 상되부는 니현상콜으의로 서진,동 방두향 에방 의해 2 등분되는 경우이다 ( 그림 3.6b). 경사소광은 광물 내의 직선구조가 하부 또는 상부 니콜의 진동 방향과 0° 또는 90 까 아닌 각도 를 이루고 있는 경우로서, 단사정 계, 삼사정 계의 광물에서 관찰된다(그림 3.6 c). 특히 단사정 계의 광물에서는 c 결정축과 그 주진동축이 이루는 각도 (cAZ) 가 소광각 이 된다. 단사정계의 광물에서는 항상 b 결정축과 Y 주진동축이 일 치하며, + a 와 +c 결정축의 사잇각인 住큰 90° 보다 크다 이때 Z 주 진동축이 c 결정축의 뒤쪽에 위치하면 소광각을 (+)의 각도로, 그 앞쪽에 위치하게 되면 (내의 각으로 표시한다(그림 3.7 ) .
3.3.3 정계에 따른 소광 특징 자형의 광물 박편에서 관찰될 수 있는 소광 특징을 각 정계별로 요약하면 다음과 같다. • 동축정계는 등방성을 띠므로 항상 소광한다. • 정방정계는 광축이 항상 c 결정축과 일치하고, 이에 수직인 방 향으로 두 결정축이 존재한다. c 결정축에 수직으로 절단된 (001) 면 의 광물 박편은 항상 소광하지만, 그 외 방향으로 절단된 박편은 평행소광한다. • 삼방정계 및 육방정계는 평행소광을 하며, 두 방향의 벽개나 결정면이 발달할 경우 대칭소광을 한다 . 광축에 수직인 (0001 ) 박 편은 항상 소광한다. • 사방정계는 세 결정축과 주진동축이 항상 일치하므로 평행소 광을 한다. 두 방향의 벽개나 결정면이 발달할 경우 대칭소광을 한다. • 단사정계는 b 결정축과 Y 주진동축이 항상 일치하고, a 와 c 결 정축을 포함하는 면내에 X 와 Z 이 놓이게 되므로 일반적으로 경사 소광을 한다 . (010) 면에 나란한 광물 박편에서 최대 소광각을 얻을 수 있다. (1 00) 면에 나란한 광물 박편은 평행소광을 하고, (001) 면 을 나타내는 광물 박편은 두 방향의 벽개가 있는 경우 대칭소광을 한다. • 삼사정계는 축각이 90° 가 아닌 세 결정축 a, b, c 가 주진동축 X,Y,Z 와 일치하는 경우가 없으므로 항상 경사소광을 한다 . 때로는 등방성 및 이방성 광물 모두에서 한 광물 입자의 전체가 동시에 소광이 되지 않고 일부분만 소광이 되는 경우가 있는데 이
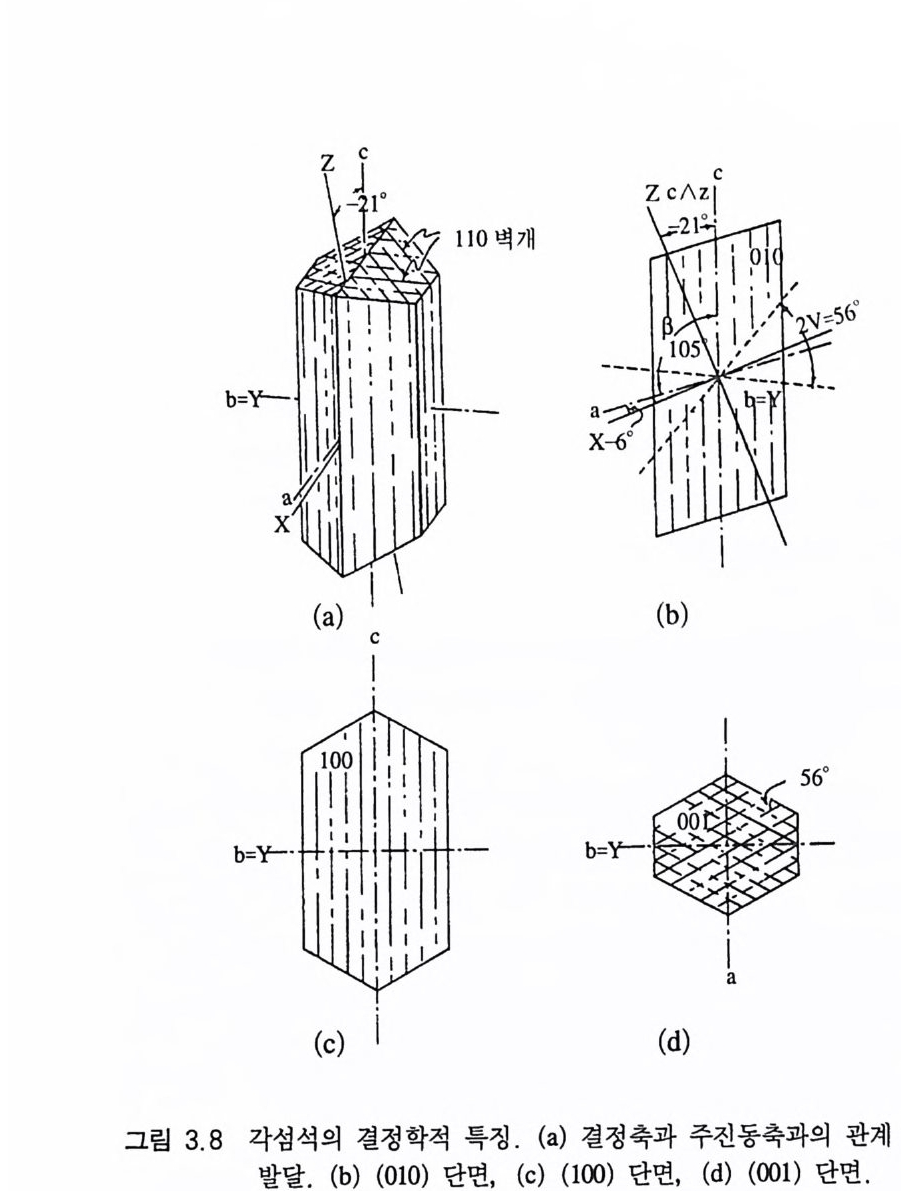
를 파동소광(波動消光, wavy ex ti nc ti on) 이라고 한다. 이런 현상은 광물이 정출된 후 광물의 결정구조가 부분적으로 변형되었기 때문 에 생기는 것인데, 화성암이나 변성암 내에 있는 석영, 석류석 등 에서 흔히 관찰된다. 화성암에 있는 광물인 경우는 고온에서 정출 된 후 상온으로 냉각되는 과정에서 고온에서 안정했던 결정구조가 일부 변형을 일으키기 때문이다. 높은 압력을 받아 만들어진 변성 암에서는 압력에 의해 결정구조의 변형이 있을 수 있다. 따라서 이러한 비정상적인 소광현상으로부터 그 광물을 포함하고 있는 암 석의 성인 환경을 추측할 수도 있다. 동일한 광물이라도 결정면 및 벽개 발달의 유무, 광물의 절단 방향 등에 따라 소광현상이 달리 나타날 수 있다. 예1. 석영의 경우, 정동(晶洞)같은 개방 환경에서 성장한 결정 은 6 방주 결정형으로 산출되므로 이런 자형(自形, euhedral) 의 결정 이 c 결정축과 나란하게 절단되어 있는 박편의 경우는 주상 결정면 이 하부 또는 상부 니콜의 주진동방향과 나란한 위치에서 소광하 므로 평행소광을 한다. 그러나 c 결정축에 수직으로 절단된 6 각형의 입자는 광축을 따라 빛이 진행하는 경우이므로 항상소광을 한다. 한 편 화강암에서의 석영은 항상 타형(他形, anhedral) 으로 산출되는 데, 벽개의 발달도 전혀 없는 이런 석영 입자로는 소광각을 측정 할 수 없다. 따라서 소광 명칭을 사용할 수 없게 된다. 예 2. 각섬석은 단사정계의 광물로서, {110} 방향의 벽개가 완전 하게 발달할 뿐만 아니 라 결정 축 (a, b, c) 과 주진동축 (X, Y, Z) 과의 특수한 상호 관계 때문에 박편 관찰시 매우 홍미로운 소광 특징을 나타낸다 죽, a/\c=l05°, b=Y, c/\Z=-21° 이며, 벽개의 사잇각
 \ c [
\ c [
은 56° 이다(그림 3.8a). 따라서 a/\X=-6° 이다(그림 3.8b). Y 에 수직으로 절단되어 (010) 방향에 나란하게 연마된 광물 박 편에서는 소광각이 -21· 로 최대가 된다(그림 3.8b). 그러나 a 결정 축에 수직으로 절단되어 결국 (1 00) 면에 평행한 광물 박편인 경우
는 마치 Z 과 c 가 일직선상에 있는 것처럼 보이는 위치이고, 동시 에 Y=b 이므로 평행소광을 나타낸다(그림 3.8 c). 한편 c 결정축에 거의 수직으로 절단되어 (001) 면에 나란하게 만들어진 광물 박편인 경우에는 b=Y 이고, 또 a 와 X 가 일치하는 위치이므로(그림 3.8d) 소광된다 . 이 경우 하부 또는 상부 니콜의 진동방향인 a 또는 b 방향이 두 방향의 벽개가 이루는 각을 이등분하게 되므로 결국 대 칭소광 을 나타낸다. 그러나 (010), (10 0), (001) 면과 나란하게 만 들 어지지 않은 광 물 박편의 경우에는 0~21° 범위의 소광각을 가지 게 되는데 이런 경우가 실제로 더 많다 . 3.4 장축 부호 장축 부호( 長 軸符 號 , sig n o f elon g a ti on) 는 주상(柱狀)의 결정형태 를 가지는 이방성 광물에 대해 장축을 따라 진동하는 편광이 빠른 광선인지 아니면 느린 광선인지를 결정하여 부호로 나타내는 것으 로서, 신축부호(伸 軸 符 號 )라고도 한다 . 만약 장축을 따라 느린 광 선이 진동하고 있다면 이를 〈 장축 느림(l en gth slow) 〉 또는 (+) 부 호로 간단히 나타낸다. 광물 입자의 장축방향을 따라 빠른 광선이 진동하고 있다면 〈장축 빠름(l en gthfa st)〉 또는 (一)로 표현한다. 광 물의 장축방향을 따라 느린 광선이 진동한다는 것은 그 방향으로 의 굴절률이 크다는 의미이고, 반대로 빠른 광선이 진동하면 굴절 률이 작음을 의미한다. 이방성 광물 내에서 빠른 광선과 느린 광 선의 진동방향은 서로 직각이다. 장축 부호를 정할 때에는 광물 박편에 있는 입자 중에서 장축을 뚜렷이 나타내는 입자를 선택하여 소광 위치로 옮긴 다음, 이 위치 로부터 시계 또는 반시계 방향으로 45° 만큼 회전하여 고정시킨다.
이 위치에서는 그 광물의 간섭색이 제일 밝게 보이게 되는데 이런 상태를 명광(明光, d i s ti nc ti on) 이라고 한다. 편광현미경에 있는 보 조판(補助板 accessar y p la t e) 용 구멍에 석고판(石背*瓦 gyps um pla te ) 을 넣어 광물의 간섭색 등급이 원래보다 증가하는지 아니면 감소 하는지를 결정한다. 만약 간섭색이 원래보다 석고판에 의한 위상차 (550111µ) 만큼 증가 하면 이것은 광물 내의 느린 광선의 진동방향과 석고판의 느린 광 선의 진동방향과 일치하는 경우이다. 이런 조건에서는 광물과 석 고판의 빠른 광선의 진동방향도 자연히 일치하게 된다 . 이러한 경 우를 첨가보정 (追加補烽 addit ive com pensa ti on) 이라고 한다. 석고판 의 금속 부분에는 느린 광선의 진동방향이 표시되어 있으며, 일반 적으로 s 또는 l 로 표시되어 있다. 전자는 slow, 후자는 독일어인 lan g sam 의 약자로서 느린 광선을 의미한다 . 석고판의 빠른 광선의 진동방향은 느린 광선에 직각이다. 이러한 사실을 이용하여 광물 내 에 있는 두 광선의 속도를 결정할 수 있게 된다. 이와 반대로 석고판을 넣었을 때 간섭색의 등급이 원래보다 550mµ 만큼 감소하면, 광물 내에 있는 빠른 광선과 석고판의 느린 광선의 진동방향이 일치하고, 동시에 광물의 느린 광선과 석고판 의 빠른 광선의 진동방향과 일치하고 있음을 알 수 있게 된다. 이 런 조건에서는 간섭색의 등급이 감소하게 되며, 이를 감소 보정 (滅小補懿 subtr ac ti ve comp en satio n ) 이 라고 한다. 장축 부호와 광학 부호(光學符號, o pti cs ign)는 별개의 개념으로서 그 부호가 항상 일 치하는 것은 아니다 . 3.4.l 일축성 광물 주상 형태의 석영 결정이 들어 있는 광물 박편을 교차 니콜하에
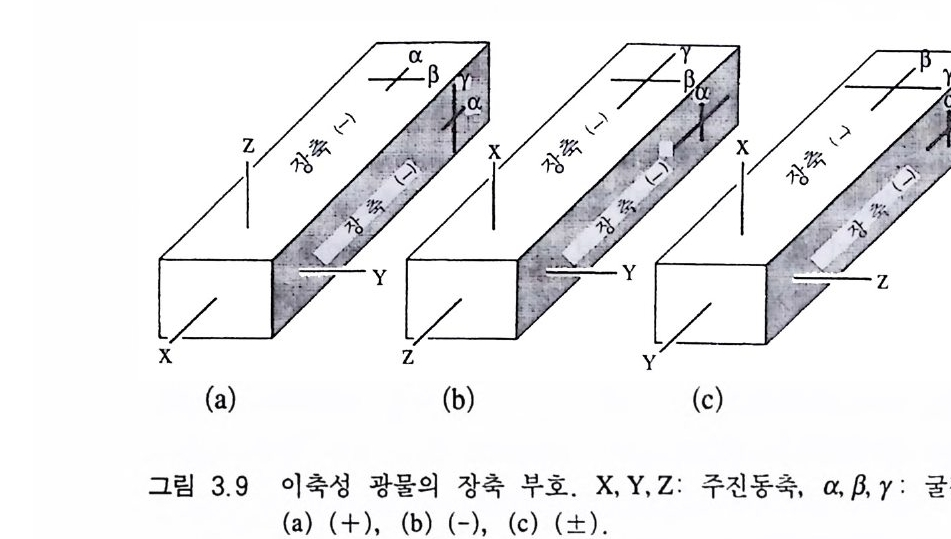
서 관찰하면 장축 방향이 남북 방향이 될 때 소광이 일어난다. 이 위치에서 반시계 방향으로 45° 회전시키면 백색을 띠는 1° 간섭색 이 관찰된다. 이때 석고판을 넣으면 간섭색은 1· 황색으로 변한다. 이러한 현상은 석고판의 느린 광선과 광물의 빠른 광선의 진동방 향이 일치했기 때문이며, 감소 보정이 일어난 경우이다. 간섭색이 l. 황색 (350mµ) 으로 변한 것은 원래의 I. 백색 (200mµ) 이 석고판의 위상차만큼 감소 |200mµ- 550mµ |=350mµ) 되었기 때문이다. 따라서 석영의 장축 부호는 〈 장축 느림〉 또는 (+)이다. 장축을 나타내는 일축성 광물에서는 일반적으로 c 결정축을 따라 장축 방향과 일치 하고, 동시에 c 결정축과 광축이 일치하므로 장축 부호와 광학 부 호는 일치하게 된다 . 인회석은 장축을 따라 빠른 광선이 진동하고 있다. 따라서 소광 위치로부터 반시계 방향으로 45° 회전시킨 후 석고판을 넣으면 간섭 색이 원래의 l° 백색 (200mµ) 으로부터 석고판에 의한 위상차 (55 0, nµ) 만큼 증가하는 첨가보정이 일어나 2· 청색 (750 ,nµ)으로 바뀐다. 이 러한 현상은 광물과 석고판의 빠른 광선과 느린 광선의 진동방향이 각각 일치하기 때문인데, 이로부터 장축을 따라 빠른 광선이 진동 함을 알 수 있고 장축 부호는 〈장축 빠름〉 또는 (-)가 된다. 3.4.2 이축성 광물 길쭉한 형태의 사방정계 광물인 경우 주진동축인 X,Y,Z 중 하 나가 반드시 장축과 일치하게 되며, 나머지 두 진동축은 이에 직 각인 위치로 배열한다(그림 3.9). 참고로 주진동축 X, Y, Z 을 따라 굴절률 a, {3, )까 각각 있게 되고, 또 Y > {3 > a 인 관계가 있으므 로 X 축을 따라 가장 빠른 광선이, Y 축을 따라 중간 속도의 광선 이, 그리고 Z 축으로는 가장 느린 광선이 있게 된다. 따라서 만약
 z
z
X 축이 장축과 일치 하고 있으면 (그림 3.9 a) Y 또는 Z 축 중 어 느 축이 그에 수직으로 배열하든지 상관없이 〈장축 빠름〉 또는 ( - )가 된다. 또한 장축을 따라 Z 축이 배열된 경우는(그림 3.9 b) 그에 수 직으로 어떤 주진동축이 있든 관계없이 항상 〈 장축 느림〉 또는 (+)가 된다. 그러나 장축을 따라 Y 축이 있게 되면(그림 3.9 c) 광 물의 절단된 위치에 따라 장축 부호가 변할 수 있다. 따라서 장축 부호는 (土)가 된다 . 이축성 광물의 장축 부호를 결정할 때에도 석고판을 사용하면 되며, 첨가 또는 감소보정이 일어날 때의 간섭색 변화는 일축성 광물일 때와 동일하다. 다만 단사정계와 삼사정계의 광물인 경우 는 엄밀히 말해 장축 방향과 주진동축이 완전히 일치하지는 않는 다. 따라서 일반적으로 경사소광을 나타내는 이 두 정계의 광물은 소광각이 45• 보다 훨씬 작을 경우, 소광 위치로부터 45° 만큼 반시 계 방향으로 회전시킨 다음 석고판을 사용하여 일축성의 경우처럼 간섭색의 증감으로 결정하면 되고, 소광각이 45• 에 근접하는 광물 인 경우는 장축 부호의 의미가 없어진다. 이축성 광물의 장축 부
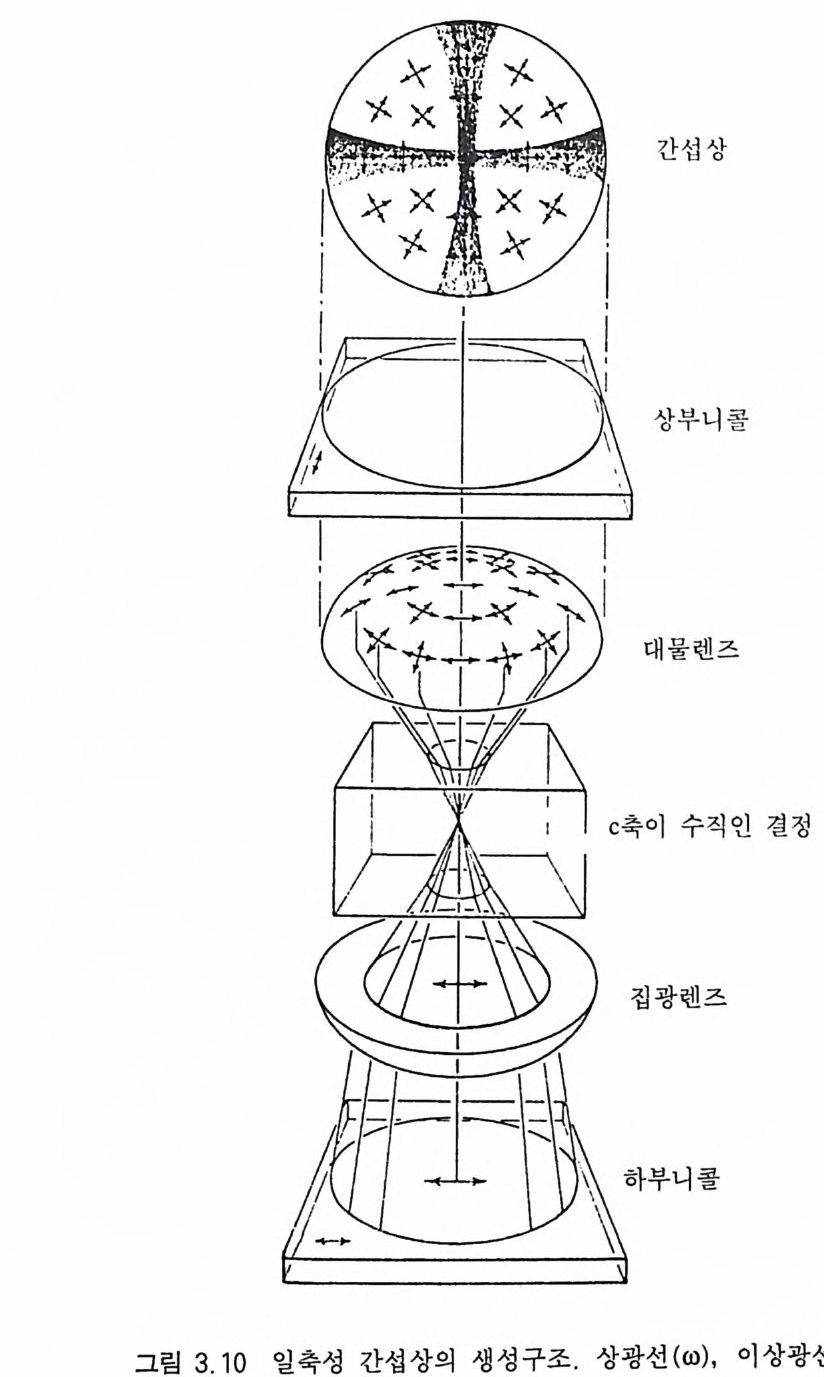
호는 광학 부호와 전혀 무관하다. 3.5 간섭상 이방성 광물에 수렴광(收敵光)이 입사하면 특이한 광학 효과 가 나타난다. 즉 , 폴랄 라이저를 통과해 나온 편광이 집광렌즈를 통 과하면 수렴광이 만 들 어지고, 이 수렴광이 광물에 입사하여 광물을 통과해 나올 때는 서로 간섭을 일으켜 간섭상(干涉像, int e r f er ence fig ure) 이라는 특 이한 형상을 만든다. 간섭상을 얻기 위해서는 재물 대위에 광물 박편을 올려 놓고 소광 위치에 고정시킨 다음, 편광 현미경의 부품인 집광렌즈 (condens i n g lens) 와 고배율의 대물렌즈 그 리고 벌트랜드렌즈 (Be rtr and lens) 를 사용한다. 간섭상은 기본적으 로 십자(十 字) 형태의 검은 막대와 그 주위에 생기는 동심원(同心 llil) 모양의 색 띠로 구성되어 있다. 전자를 아이소자(i so gyre ), 후 자 를 아이소크롬(i sochrome) 이라고 한다. 아이소자는 폴랄라이저의 진동방향과 일치하는 광선 성분만 있는 부분으로서 이 곳을 통과 해 나오는 편광은 모두 어낼라이저에 의해 차단되므로 소광되어 검게 보이는 것이다. 아이소크롬은 동일한 위상차를 나타내는 점이 연결되어 만들어지는 동심원 구조인데, 복굴절률이 큰 광물일수 록, 고배율의 대물렌즈일수록 아이소크롬의 수효가 증가한다. 화 강암에 있는 석영과 정장석은 광학현상이 매우 비슷하여 쉽게 구 별할 수 없을 때가 종종 있다. 이런 경우 일축성(석영)과 이축성 (정장석) 광물의 간섭상의 형태와 거동에 차이가 있기 때문에 간섭 상을 만들어 보면 쉽게 구별할 수 있게 된다.
 간섭상
간섭상
 pi
pi
 %훑
%훑
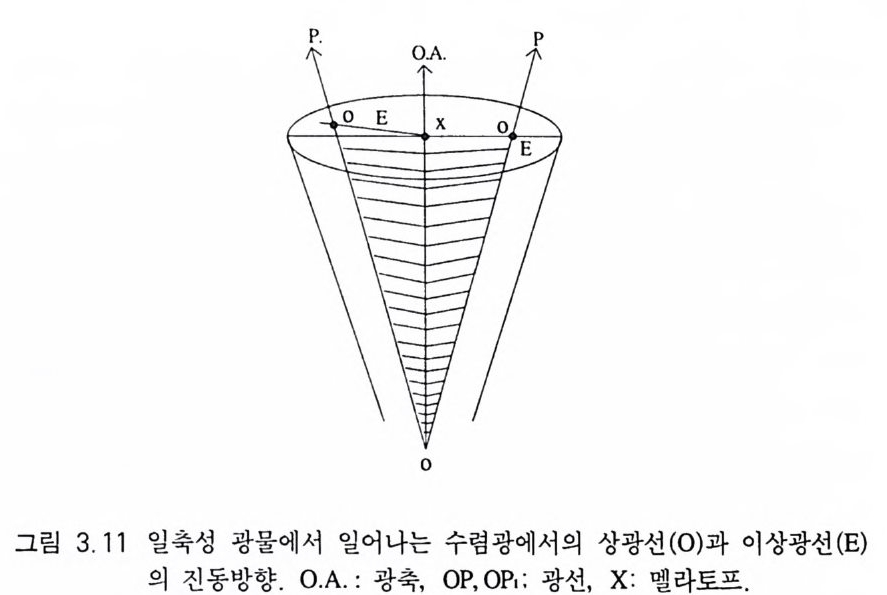
3.5.1 일축성 간섭상 일축성 광물의 광축 방향에 수직으로 절단된 광물 박편인 경우 (그림 3.10), 광물을 통과해 나오는 수렴광의 상광선과 이상광선의 진동방향의 특징은, 이상광선은 항상 원의 중심을 향해 진동하는
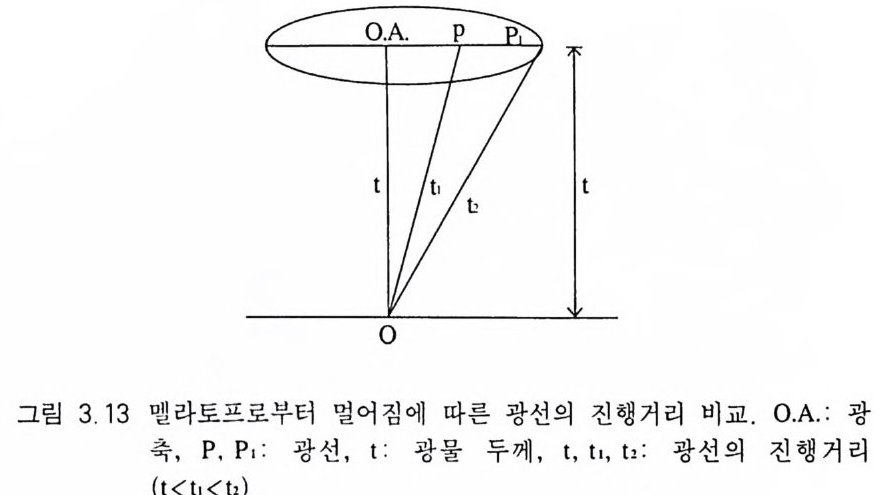
반면에, 상광선은 그에 수직인 접선 방향으로 진동한다 . 그것은 이상광선은 광축과 광선의 진행방향을 포함하는 면내에서 진동하 고, 상광선은 그에 수직되게 진동하기 때문이다(그림 3.11 ). 이런 경우 얻어지는 일축성 간섭상의 형태는 그림 3.12 와 같으며, 검은 막대가 있는 부분은 수렴광하에서도 진동방향이 변하지 않은 부분 으로서 소광이 일어난 영역인데, 가로 막대는 이상광선이, 그리고 세로 막대는 상광선이 진동하고 있는 부분이다 . 그리고 두 막대 사이 부분은 상광선과 이상광선이 함께 공존하는 영역으로서 이상 광선은 원의 중심을 향해, 상광선은 접선방향으로 진동하고 있다 . 따라서 이들은 어낼라이저의 진동방향 성분을 가지고 있으므로 밝 게 된다. 어낼라이저의 진동방향 성분을 최대로 가지는 위치는 두 아이소자의 중간 부분이다. 서로 직각인 두 개의 검은 막대가 교 차하는 부분은 광축이 솟아 오르는 위치로서 이 를 멜라토프 (mela t o p e) 라고 한다 . 아이소크롬은 멜라토프가 중심인 동심원이 다. 일축성 간섭상의 특징은 ® 멜라토프에서 아이소자의 폭이 가 장 좁고, 이로부터 멀어질수록 넓어지며, ® 아이소크롬이 있을 경우 멜라토프에서 멀어질수록 위상차가 커져 간섭색의 동급이 높 아지고, @) 광물 박편을 회전하여도 아이소자의 분리가 일어나지 않고 전체의 모양이 변하지 않는 것이다 . 멜라토프로부터 멀리 떨 어 진 아이 소크롬의 간섭 색 등급이 높은 이 유는 위 상차(位相差, reta r- dati on : ti)를 결정하는 요인[!::.=t X(N-n)] 중 빛이 진행하는 거리 (t)가 멜라토프로부터 멀어질수록 증가하기 때문이다(그림 3.13). 일축성 간섭상도 광물의 절단 방향에 따라 그 형태와 특징이 다 르다. 광축중심 간섭상(光軸中心干涉像, cente r ed opt ic- ax is figu re) 광축에
 。
。
수직으로 절단된 광물 박편에서 관찰되는 간섭상으로서(그림 3.1 4 a), 멜라토프가 현미경 시야의 중심에 위치한다. 간섭상이 좌우 대칭을 이루고 있다. 박편을 회전시켜도 간섭상의 형태에는 변화 가 없다. 광축비중심 간섭상(光軸非中心干涉像, of f-ce nte r ed op tic -axis figu re) 광축에 비스듬히 절단된 광물 박편에서 관찰되는 간섭상으 로서 (그림 3.1 4 b), 멜라토프가 시야의 중심과 일치하지 않는다. 광 물이 광축과 어느 정도의 각도로 절단되었는가에 따라 현미경 시야 에 두 아이 소자가 동시 에 (그림 3.1 4 b) 또는 하나만 보일 수가 있다 (그림 3.1 4 c) . 멜라토프는 항상 아이 소자가 좁아지는 쪽에 위 치한다. 섭광 간섭상(閃光干涉像 flas hf igu re) 광축과 나란하게 절단된 광 물 박편에서 관찰되는 간섭상으로서(그림 3.1 4 d), 이 위치로부터 박편을 조금만 회전하여도 순식간에 간섭상이 사라진다. 섬광 간 섭상의 경우 가장자리 일부를 제외하면 시야의 거의 모든 부분이
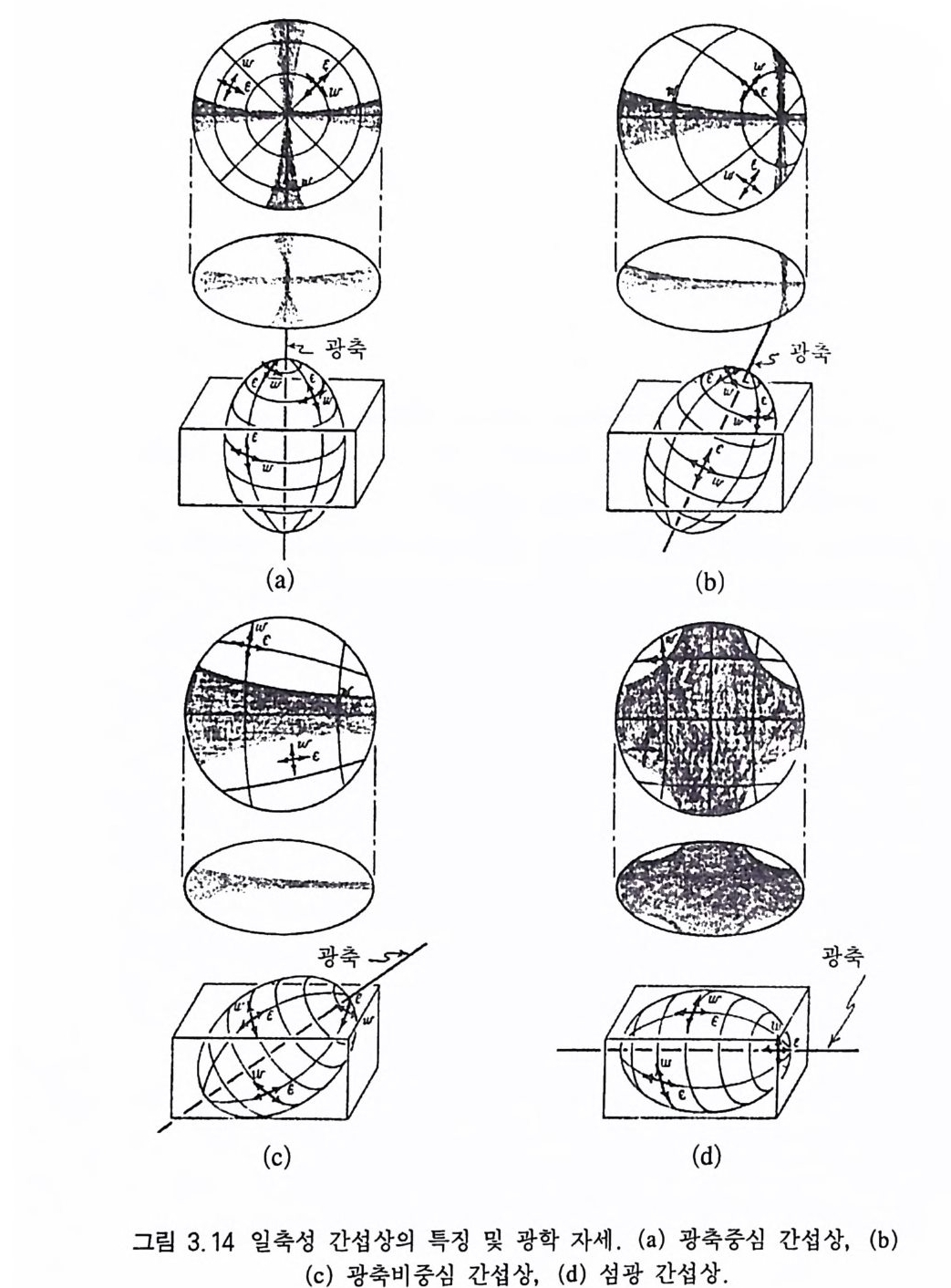 :
:
 900 4'5 '
900 4'5 '
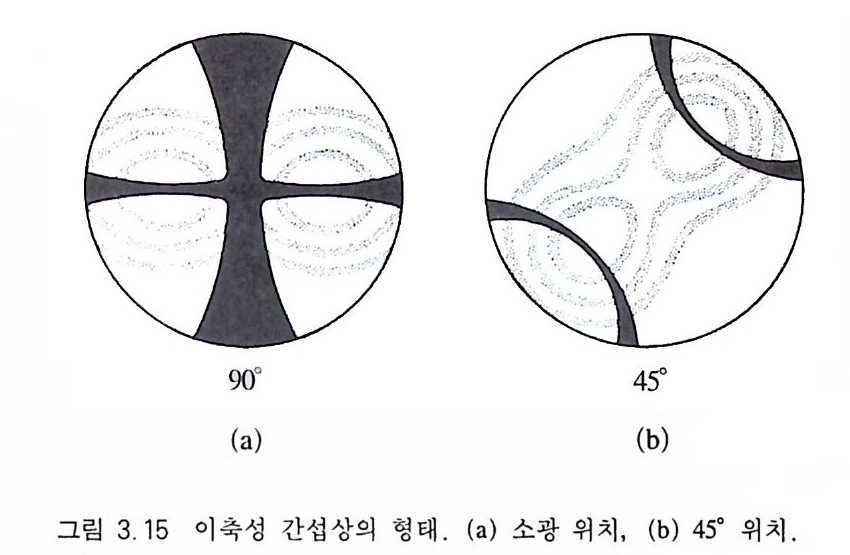
검게 보이는데, 그 이유는 상광선과 이상광선의 진동방향이 두 편광판의 진동방향과 일치하여 소광하기 때문이다. 다만 시야의 가장자리 부분에서는 진동방향의 변형으로 인해 약간의 광선이 어 낼라이저를 통과하므로 밝다. 3.5.2 이 축성 간섭 상 이축성 광물에는 광축이 2 개 있으며, 이들은 이축성 광물에 있 는 3 개의 주진동축 (X, Y, Z) 중에서 xz 축을 포함하는 면에 놓여 있다. 이면을 광측면(光軸面 o pti c p lane) 이라고 한다. Y 축은 이 면 에 수직 으로 위 치 하며 이 를 광축면 수선 (光軸面垂線, op tic normal) 이라 한다. 소광 위치에서 만들어지는 이축성 광물의 간섭상 역시 십자 형태의 검은 아이소자와 두 광축이 솟는 멜라토프 주위에 생 기는 아이소크롬으로 구성되어 있다(그림 3.15a). 일축성 간섭상과
 ZI
ZI
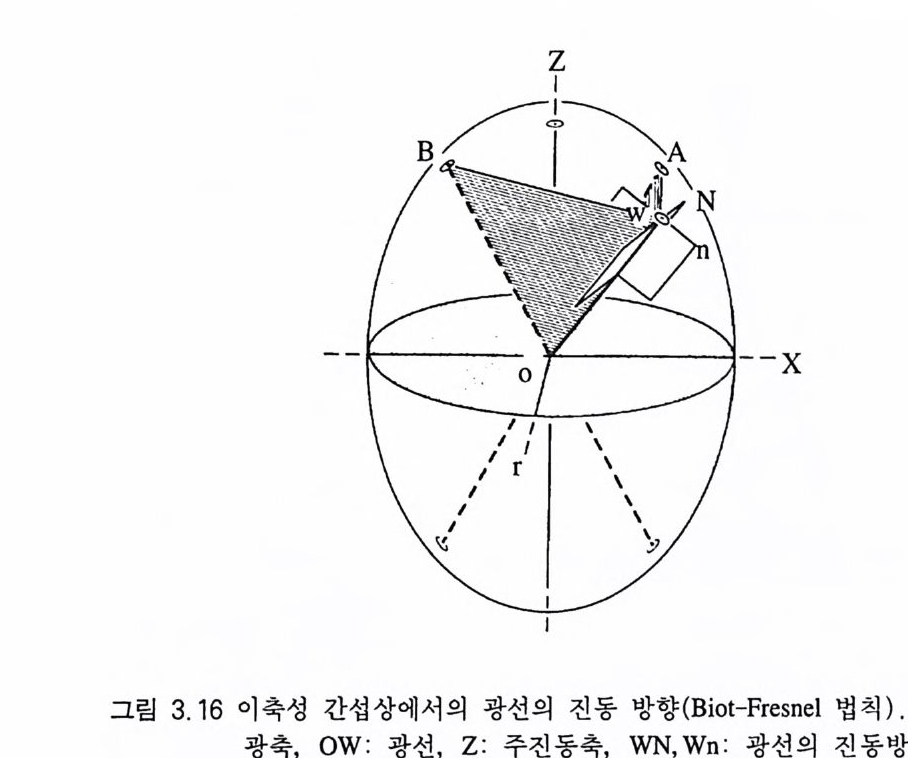
다른 점은 ® 두 광축을 포함하는 방향 (XZ 면)의 아이소자는 두께 가 얇은 대신, 광축면 수선 (Y) 이 있는 방향의 아이소자는 두껍 고, ® 멜라토프가 2 개 있으며 광측면 수선을 기준으로 대칭적으 로 있고, ® 광물 박편을 회전하면 십자 형태의 아이소자가 쌍곡 선 형태로 분리된다(그림 3.1 5 b). 이축성 간섭상 내의 각 부분에서 진동하는 두 광선의 진동방향은 Bio t - Fresnel Rule 에 의해 알 수 있다. 죽, 〈광선이 진행하는 어떤 지점에서의 광선의 진동방향은 두 광축에서 그 지점을 연결하여 만들어지는 각을 이등분하는 방 향으로 빛이 진동한다〉는 것이다(그림 3.1 6 ). 이러한 사실로부터 아이소자는 광선이 어낼라이저에 의하여 차단되어 소광이 되는 부 분임을 알 수 있게 된다.
 o.
o.
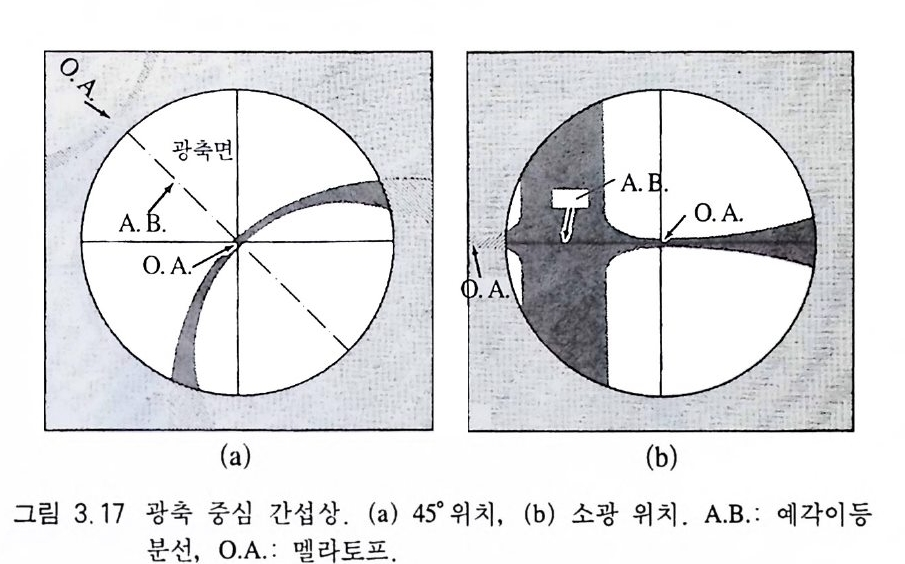
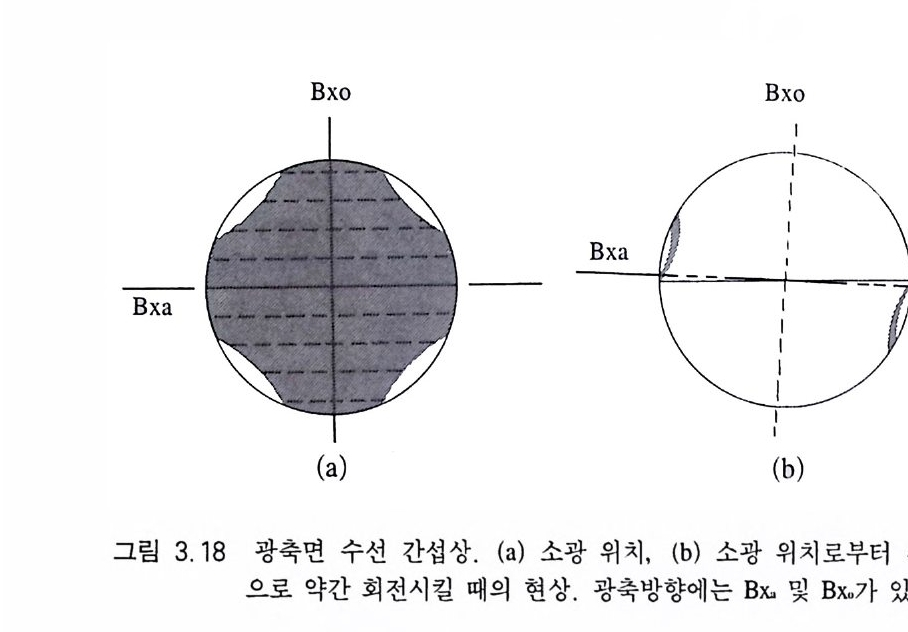
이축성 간섭상도 광물의 주진동축에 대해 어떤 방향으로 절단되 었는가에 따라 형태가 다르다. 예각이등분선중십 간섭상(銃角二等分線中心干涉像, acute bis e ctr ix - cente r ed figu re) 두 광축이 이루는 각(角)이 90° 보다 작을 경우 그 각을 이등분하는 수선이 시야의 중심에 있도록 절단된 광물에서 볼 수 있다(그림 3.1 5 ). 광물을 회전하면 십자 형태의 아이소자는 사라지고 그 대신 쌍곡선 형태의 아이소자가 대칭적인 위치에 만 들어지는데, 45• 회전했을 때 최대의 분리가 일어난다(그림 3.15 b). 아이소크롬이 존재하는 광물 박편인 경우는 이동한 멜라토프 를 중심으로 동심원이 형성된다. Bx. 간섭상이라고도 한다. 광축중심 간섭상(光軸中心干涉像, op tic ax.is- cente r ed figu re) 두 개 의 광축 중 한 광축에 수직되게 절단된 광물 박편에서 관찰되는 간섭상으로서(그림 3.1 7 b), 광축이 솟는 지점이 시야의 기준에 위
 Bxo B xOI1
Bxo B xOI1
치한다. 이 위치로부터 45° 회전시키면 하나의 쌍곡선이 시야의 중 심에 생기는데(그림 3.1 7 a) 예각 이등분선은 쌍곡선이 볼록한 쪽 방 향에 존재하며, 또 다른 쌍곡선은 예각 이등분선을 기준으로 대칭 적인 위치에 존재하게 되는데 현미경 시야 밖에 있으므로 관찰할 수는 없다. 광축면수선 간섭상(光軸面垂線干涉像, opt ic nonnal figu re) 광축면 에 나란하게 절단된 광물 박편에서 관찰되는 간섭상으로서(그림 3.1 8 ), 두 광축이 모두 재물대 위에 나란하게 놓여 있고 광축면 수 선 (Y) 이 이에 수직으로 향하고 있는 경우이다. 일축성 간섭상 중 섬광 간섭상과 매우 홉사하다 . 45• 를 회전하면 현미경 시야에는 아무런 형태도 남아 있지 않게 된다. 둔각이등분선중심 간섭상(純角二等分線中心干涉像, obtu s e bis e ctr ix - cente r ed figu re) 두 광축이 이 루는 둔각을 이 등분하는 선 에 수직 으
 乙r , ,,, ___ z Y 폰x z
乙r , ,,, ___ z Y 폰x z
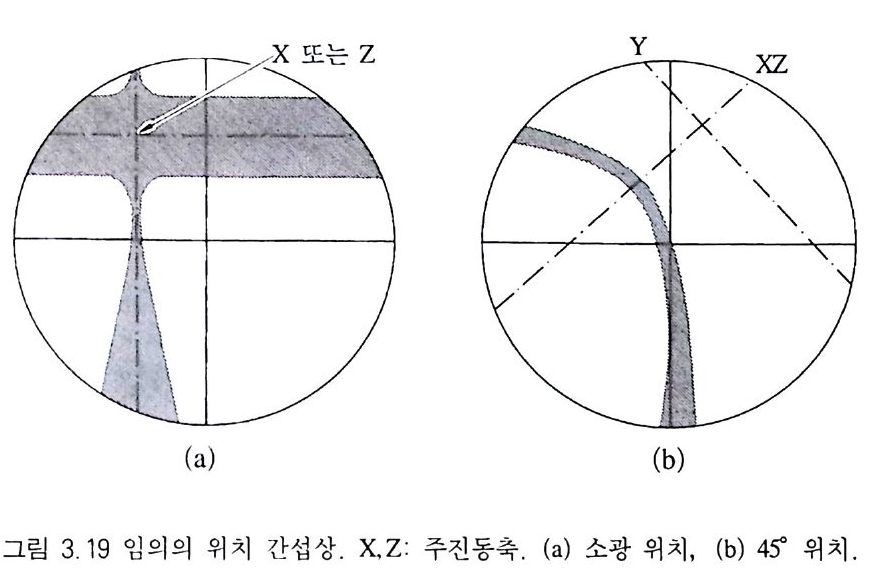
로 절 단된 광물 박편에서 관찰할 수 있는 간섭상으로서, 소광위치 에서의 예 각 이등분선중심 간섭상과 형태가 유사하다. 그러나 광물 박편을 회전할 때 매우 신속하게 아이소자가 사라지는 점과, 또 45° 희전시킨 위치에서 아이소자를 전혀 볼 수 없는 점이 다르다. Bx,, 간섭상이라고도 한다. 임의위치 간섭상(任 意位置 干涉像, random figu re) 광축에 비스듬히 절단된 광물 박편에서 관찰되는 간섭상으로서, 2 개의 주진동축을 포함하는 기본면(基本面, pri nc ip al p lane) 이 시야의 중심선과 일치하 지 않는다(그림 3.1 9 ) . 때로는 현재 관찰하고 있는 이축성 간섭상이 어떤 경우의 간섭상 인지를 명확하게 구별하기 어려운 때가 있다. 이들을 구별하는 한 방법으로서, 우선 소광 위치에서 간섭상을 만든 다음, 이 위치로부
 표 3.2 간섭상의 종류 식별법
표 3.2 간섭상의 종류 식별법
터 어느 각도 (8) 만큼 회전시켰을 때 아이소자가 사라지는지를 알아 보아 결정한다 (표 3.2). 3.6 이방성 광물의 광학 부호 어떤 광물들은 현미경에서의 광학 현상이 비슷하여 식별하기가 쉽지 않은 경우가 있다. 특히 이들이 일축성 또는 이축성으로 동 일할 떄는 간섭상 형태만으로 구별할 수가 없게 된다. 이러한 경 우 광학 부호(光學符號, op tic s ign)를 측정하면 구별이 가능해 질 수가 있다. 광학 부호를 결정할 때에는 우선 간섭상을 만든 다움 보조판(補助板, accessar y p la t e) 을 사용한다. 3.6.l 일축성 광물 일축성 광물의 광학 부호는 이상광선에 의한 굴절률 (e) 과 상광 선에 의한 굴절률 (co) 의 대소(大小) 관계에 따라 결정되는데, 만약 e> (l)이면 (+), (l)> e 이면 (-)라고 정하였다. 일축성 간섭상으로
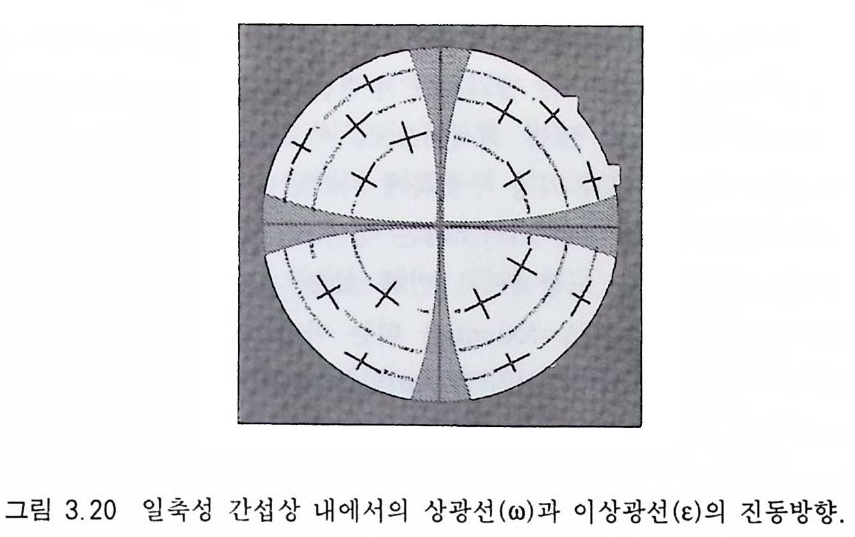 그림 3.2 0 일축성 간섭상 내에서의 상광선((J))과 이상광선 (c) 의 진동방향.
그림 3.2 0 일축성 간섭상 내에서의 상광선((J))과 이상광선 (c) 의 진동방향.
광학 부호를 결정하는 과정을 설명하기 위해 우선 광축중심 간섭 상을 예로 들어 설명하면 편리하다. 십자 형태의 아이소자 사이 부분을 각각 1,2, 3, 4 상한으로 나누고 각 상한에서 상광선과 이상 광선이 진동하는 방향을 먼저 파악한다 . 앞에서도 언급한 것처럼 이상광선 (c) 은 멜라토프가 있는 중심 방향으로, 상광선((J})은 그에 수직인 접선 방향으로 진동한다(그림 3.20). 석고판에는 느린 광선 의 진동방향이 표시되어 있으므로 이에 직각 방향으로는 빠른 광 선의 진동하는 것을 알고 있는 셈이 된다. 일반적으로 석고판의 입사 방향은 북서 방향이므로 이와 나란한 2, 4 상한울 선택하여 간섭색의 변화 양상을 분석하면 편리하다. 2,4 상한에서는 광물의 상광선이 석고판의 느린 광선과 진동방향이 일치하고 있음을 알 수있고 동시에 이상광선이 석고판의 빠른 광선의 진동방향과 일치 하고 있음도 알고 있는 셈이 된다. 석영을 예로 들면, 석영의 간섭상은 아이소자만 있을 뿐 아이소 크롬은 나타나지 않는다 . 이것은 석영의 복굴절률이 0.009 로 매우
작기 때문이다. 아이소자와 멜라토프가 있는 부분은 위상차의 개 념으로 Omµ 인 부분이며, 멜라토프 주변은 약 150111µ 정도의 간섭 색을 나타내는 백색 또는 회색이므로, 석고판을 삽입할 경우 이 부분에서 색의 변화가 가장 뚜렷하게 나타난다. 이제 석고판을 넣 고 간섭상을 보면, 검은 아이소자는 적색으로 변하였고, 멜라토프 주변의 2,4 상한은 노란색으로 변해 있고, I,3 상한은 청색으로 변해있다. 우선 적색(l:! =550111µ) 을 띠는 아이소자는 원래 Omµ 였던 부분이 석고판에 의한 위상차 (550111µ) 만큼 증가했기 때문이며, 노란 색(l:! =400111µ) 은 1° 에 속하는 간섭색으로서 원래의 위상차 (150mµ) 와 석고판의 위상차의 감소보정에 의한 현상이다. 감소보정이 일 어나는 경우는 광물의 빠른 광선이 석고판의 느린 광선과 중첩되 어 있는 경우이므로, 석고판의 느린 광선과 나란하게 진동하고 있 는 〈상광선이 빠르다〉는 사실을 알 수 있게 되며 동시에 〈 이상광 선은 느리다〉라는 사실도 알 수 있게 된다. 이러한 결과로부터 굴 절률은 광선의 속도와 반비례하므로 상광선이 나타내는 굴절률 (ro) 이 이상광선이 나타내는 굴절률 (e) 보다 작은 (.l)< c 이 되어 석영의 광학 부호는 (+)가 된다. 만약 1,3 상한을 선택하여 분석할 경우에는 멜라토프 주변이 2° 청색 (700mµ) 으로 변했으므로 첨가보정이 일어난 경우이다. 이로 부터 석고판의 느린 광선과 1,3 상한의 이상광선의 진동방향이 일 치하고 있음을 알게 되므로 〈이상광선이 느리다〉는 것을 알 수 있 게 된다. 이러한 사실은 〈상광선은 빠르다〉를 지시한다. 결국 이 상광선의 굴절률 (e) 이 상광선의 굴절률 (ro) 보다 큰 경우가 되므 로, 광학 부호는 역시 (+)가 된다. 따라서 2,4 상한 또는 1,3 상 한 중 어느 부분을 선택하더라도 광학 부호는 동일하게 된다. 멜라토프 주위에 아이소크롬이 많이 존재하는 광물인 경우는 석 고판 대신 운모판(雲母板 mica p la t e) 을 사용하는 것이 편리하다.
운모판은 약 140111µ 정도의 위상차를 나타내는데, 특별히 감소보정 이 일어나는 멜라토프의 주변에 검은 점 (!),,=150mµ-140mµ= 10111µ) 이 생기기 때문에 식별이 용이한 경우이다. 석영의 경우 2, 4 상한에서 검은 점이 생기며 이로부터 감소보정이 일어났음을 알 수 있게 된다. 따라서 운모판의 느린 광선의 진동방향과 일치하는 상광선의 진행 속도가 빠름을 알 수 있게 된다. 결국 0)
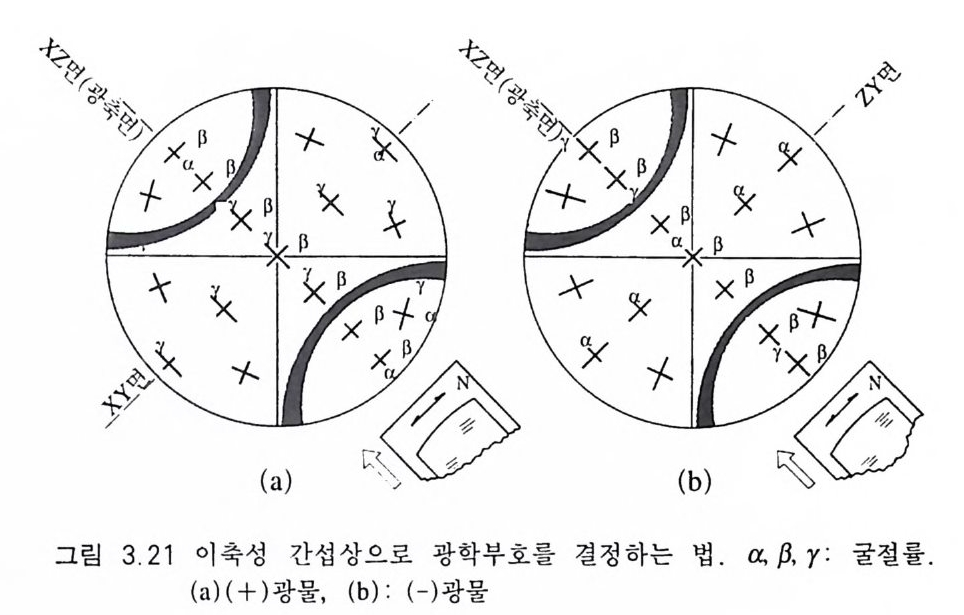
3.6.2 이축성 광물 이축성 광물의 광학 부호는 일축성 광물의 경우와 달리 두 광축 의 예각 이등분선이 Z 또는 X 축인지에 따라 결정된다 . 만약 예각 이등분선 (Bx.) 이 Z 축이면 (+), X 축이면 (-)이다 . 두 광축은 광 축면인 XZ 면에 놓여 있으므로 둔각 이등분선 (Bxo) 은 자연히 그 반 대가 되어, Bx . =Z 이면 Bxo=X 가 되고, Bxo=Z 이면 Bx.= X 가 된 다. 광학 부호를 정할 때 석고판 또는 운모판을 넣어 간섭색이 증 가 또는 감소 하는지를 관찰하는 것은 일축성 광물과 마찬가지이 지만, 소광 위치로부터 45° 만큼 회전시켜 아이소자가 쌍곡선 형태 로 최대 분리가 된 위치에서 실행하는 점이 다르다 . 이축성 간섭상으로부터 광학 부호를 결정하는 과정을 예각이등 분선중심 간섭상을 예로 들어 설명하면 편리하다. 우선 쌍곡선 형 태의 아이소자가 2,4 상한에 위치하도록 광물 박편을 45° 회전시키 고 두 쌍곡선의 중앙 위치에 예각이등분선이 있다고 가정한다(그 림 3.21). 그리고 예각이등분선 (B x.)이 Z 인지 또는 X 인지를 결정해 야 한다. 이를 위해 석고판을 넣고 쌍곡선의 바깥 부분과 안쪽 부 분의 간섭색 변화를 관찰하면 된다 . 여기서 이미 알고 있어야 할 사항은 쌍곡선의 중앙부에는 멜라토프가 있고 또 두 쌍곡선에 있 는 멜라토프롤 연결한 직선이 광측면 (XZ) 이라는 점, 그리고 광축 면에 수직으로 광축면 수선 (Y) 이 존재한다는 점이다. 첨가 또는 감소보정이 일어나는 영역의 경계는 쌍곡선 아이소자가 된다. 이 때 예각이등분선이 있는 볼록한 형태를 나타내는 두 쌍곡선의 사 이 영역을 선택하면 좋고, 특히 쌍곡선에 가까운 부분을 관찰하는 것이 좋다. 만약 어떤 광물의 간섭상이 그림 3.21 과 같고, 석고판을 넣었을 때 4 상한에 있는 쌍곡선의 바로 위 부분이 청색이 되었다면 이것
 {t8
{t8
는 BXu 가 있는 부분을 포함한 영역에서 첨가보정이 일어난 경우이 다 앞에서 언급하였듯이 광축면에 직각인 방향으로 광축 수선 (Y) 이 있고 또 Y 방향으로는 굴절률 f3가 있게 되는데 Y 방향으로 진동 하는 광선의 속도가 느림을 알 수 있다. 즉, 굴절률 f3가 이와 직 각인 다른 것보다 커야 하므로 결국 광축면 방향으로는 빠른 광선 이 있게 된다. 따라서 그 방향으로 굴절률이 작은 a 가 있다. 결국 시야의 중심부에는 f3와 a 가 직각으로 있게 되어 Z 축이 수직방향으 로 있음을 알게 된다. 이로부터 Bx.=Z 이 되므로 광학 부호는 (+)이다. 광학 부호가 (기인 광물인 경우에는 Bx. 가 있는 쌍곡선 사이 부분이 황색이 되어 감소보정이 일어났음을 알 수 있다. 이 영역 에서는 광축면 수선 (Y) 이 놓여 있고, 감소보정이 일어났으므로 Y 방향으로 진동하는 광선이 빠른 광선이 되어야 한다. 따라서 Y 방 향과 수반되는 굴절률 f3보다 느린 광선이 광축면에 놓여 있어야
 (a) (b) /\\
(a) (b) /\\
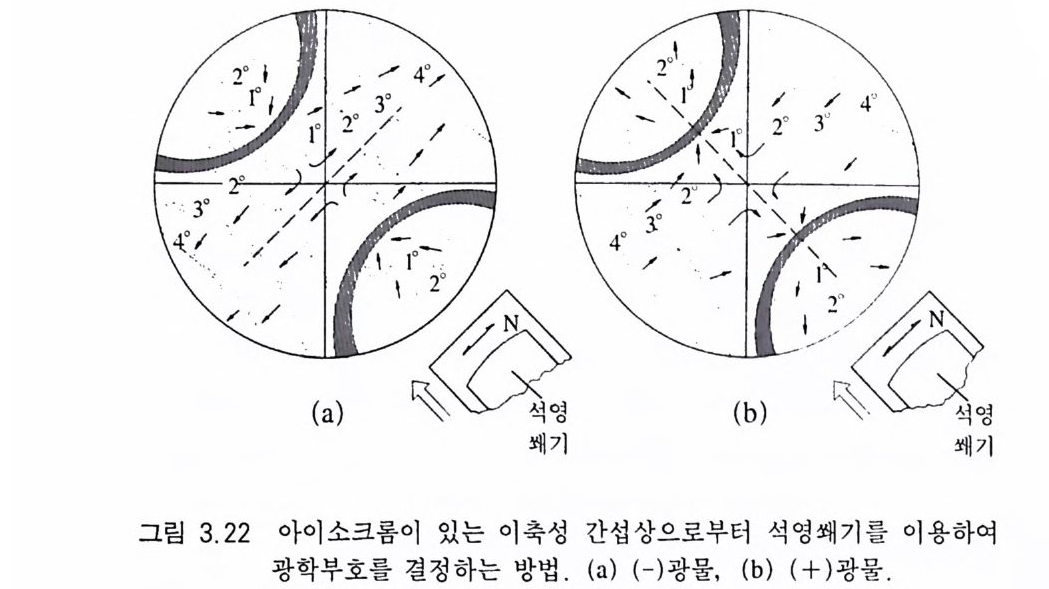
하므로 T} 됨을 알 수 있다. 결국 나머지 주진동축인 X 가 상하로 향하고 있음을 알 수 있으므로 BX a =X인 (-) 광물임을 알 수 있 게 된다. 45• 인 위치에서 하나의 쌍곡선 아이소자만 나타나는 경우는 쌍 곡선의 휘어진 모양을 관찰하면 Bx. 가 어느 쪽에 있는지를 예측할 수 있게 되므로 위의 경우와 마찬가지로 분석을 하면 된다. 아이소크롬이 있는 간섭상인 경우에는 운모판이나 석영쐐기를 넣어 아이소크롬의 이동 방향을 관찰함으로서 첨가 또는 감소 보 정임을 결정하면 된다 . 첨가보정이 일어나는 영역에서는 바깥쪽 에 있던 아이소자가 안쪽으로 이동하게 되고, 감소보정이 일어나 는 영역에서는 아이소크롬이 바깥쪽으로 이동하게 된다(그림 3.22).
 ?v,_ V` <\/ \2V x 2V`
?v,_ V` <\/ \2V x 2V`
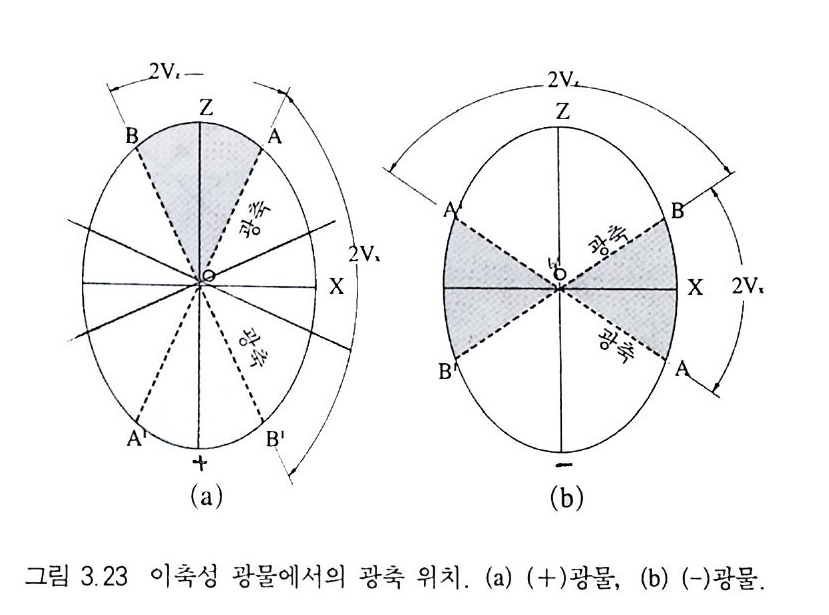
3.7 광축각 (2V) 3.7.1 광축각 이축성 광물에는 등방성을 띠는 방향인 광축이 2 개 있다. 이들 은 주진동축인 X 와 Z 축을 포함하는 광축면 내에 있으며, Z 나 X 축을 기준으로 X 자 형태로 대칭적으로 존재한다(그림 3.23). 두 광축의 사잇각을 광축각(光軸角)이라 하는데, Z 축을 기준으로 한 광축각을 2Vz, X 축에 대한 광축각을 2Vx 라 하며, 2Vz +2Vx= l80° 인 관계가 성립한다. 광축각은 일반적으로 2V 로 표현하며 예각 인 광축각을 의미한다. 만약 예각의 광축각을 2 등분하는 이등분선이 Z 축이면, 즉 Bx.=Z 이면 이 광물의 광학 부호는 (+)가 되고, 예 각의 광축각을 2 등분하는 이등분선이 X 축이면, 즉 Bx.=X 이면 이 광물의 광학 부호는 (-)가 된다. 이축성 광물 중에는 현미경에서
 2E
2E
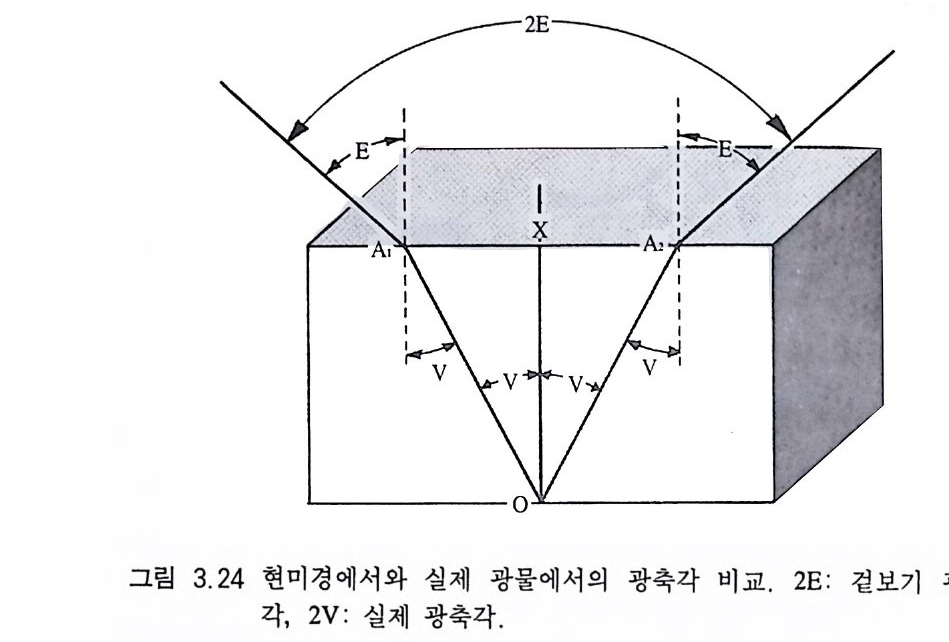
관찰되는 일반적인 광학 현상은 물론 광학 부호까지 같아서 식별 하기 어려운 경우가 있는데 이 때 광축각 (2V) 을 측정하면 더욱 신 빙성이 있는 감정을 할 수 있게 된다. 3.7.2 광축각 측정 법 맬러드법 (Mallard's meth o d) 편광현미경을 통해 관찰되는 시야내 에 두 개의 멜라토프가 모두 있는 경우에 사용되는 방법이다. 현 미경을 통해 나타나는 광축각은 광물 내에서의 실제 광축각 (2V) 보 다 더 크게 보이게 된다(그림 3.24). 그 이유는 광물을 통과해 나 온 광선이 공기 중에서 굴절하기 때문이다. 이처럼 우리 눈에 나 타나는 광축각을 2E 로 표시하며, 스넬의 굴절의 법칙에 따라 2V 와는 다음 관계식이 성립한다.
 ,·· ,
,·· ,
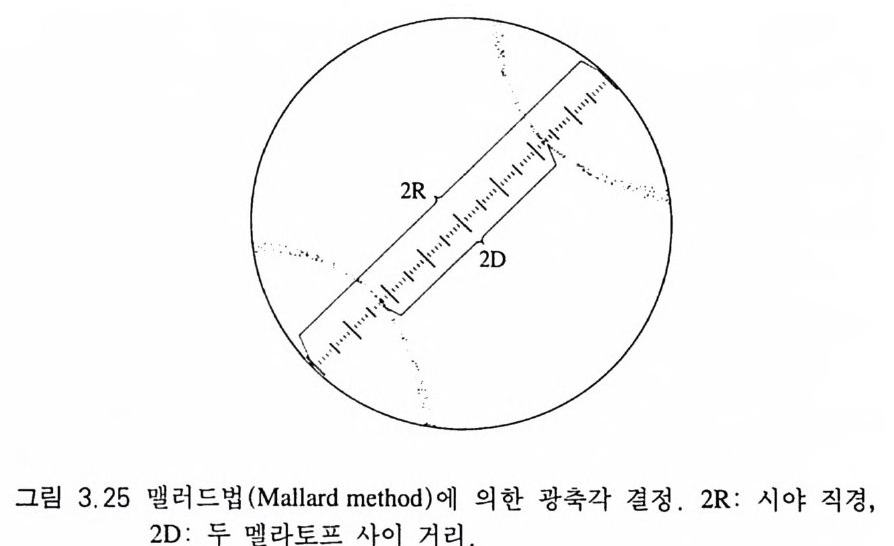
Sin— p— smV = l 따라서 sin E=/3 sin V 이고, f3는 광축을 따라 진행하는 광선이 나타내는 굴절률이다 . 현미경 시야에서 관찰되는 두 멜라토프 사 잇거리의 절반을 D 라 하면(그림 3.25), D=Ksin E=K/3 s in V 가 성립된다. D 는 현미경의 시야 중심으로부터 한 멜라토프까지의 거리로서 대안렌즈에 있는 미눈금자로 읽으면 된다. K는 맬러드 상수 (Mallard' s cons tant)라고 하는데, 맬러드 상수는 E 값과 p값을 알고 있는 광물을 선택하여 현재 사용하고 있는 현미경에서의 정 확한 값울 계산하면 된다 . 예를 들어 중정석은 2E=63°12', /3= 1. 636 이므로 E=31°36' 이다. 그러므로 맬러드 상수는
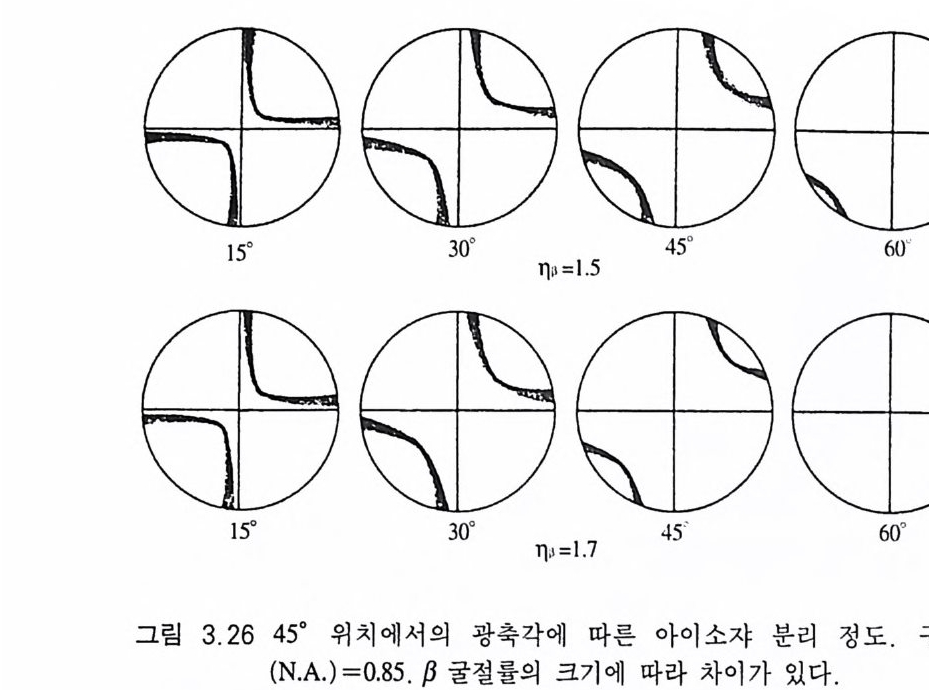 15° 30° ntI= l.5 45° 60 ''
15° 30° ntI= l.5 45° 60 ''
K= -sinD E = -s-in-2 -321.-5 ° -36:' -= 42.9 가 된다 따라서 正와 2V 는 다음 방정식으로부터 계산이 가능하다. sin E = DK 4D2. 9 sin V = 42.D9 f3 구경치 (N.A. )가 0.85 이고, 굴절률 {3가 각각 1. 5 와 1. 7 인 광물에서 관찰되는 쌍곡선 아이소자의 위치는 그림 3.26 과 같다.
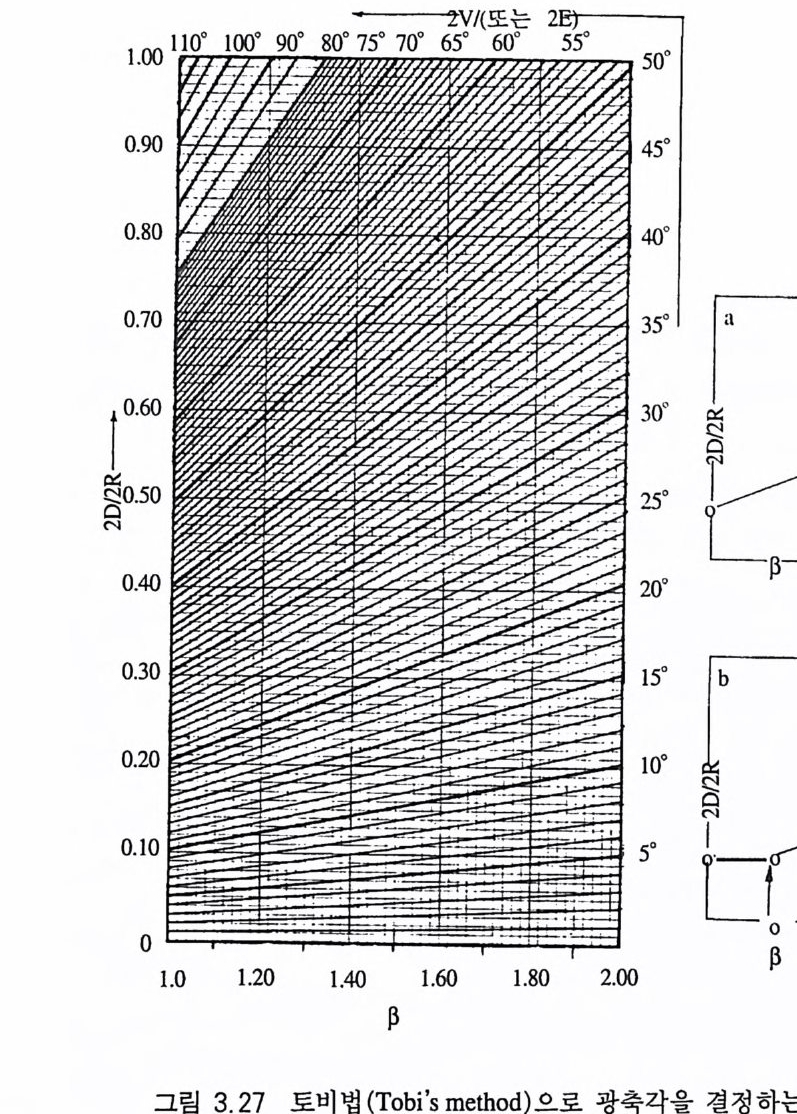
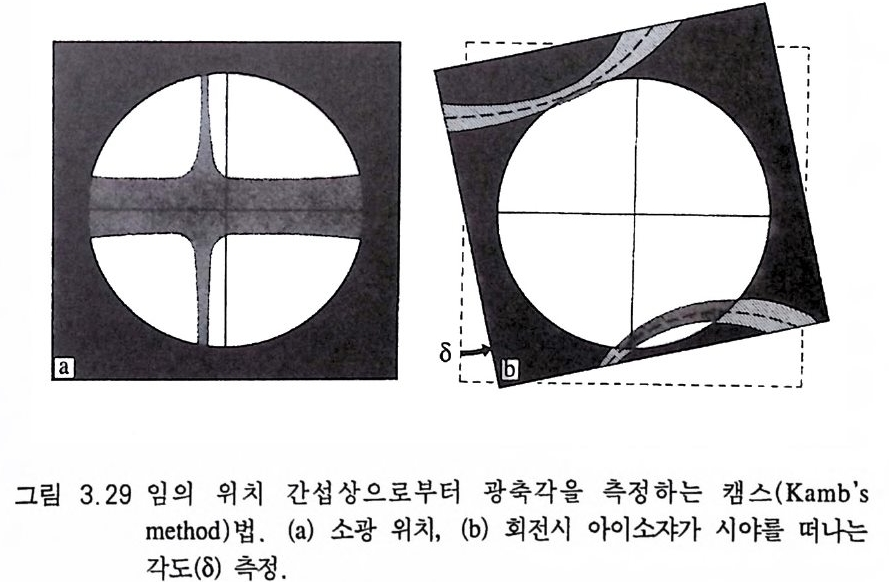
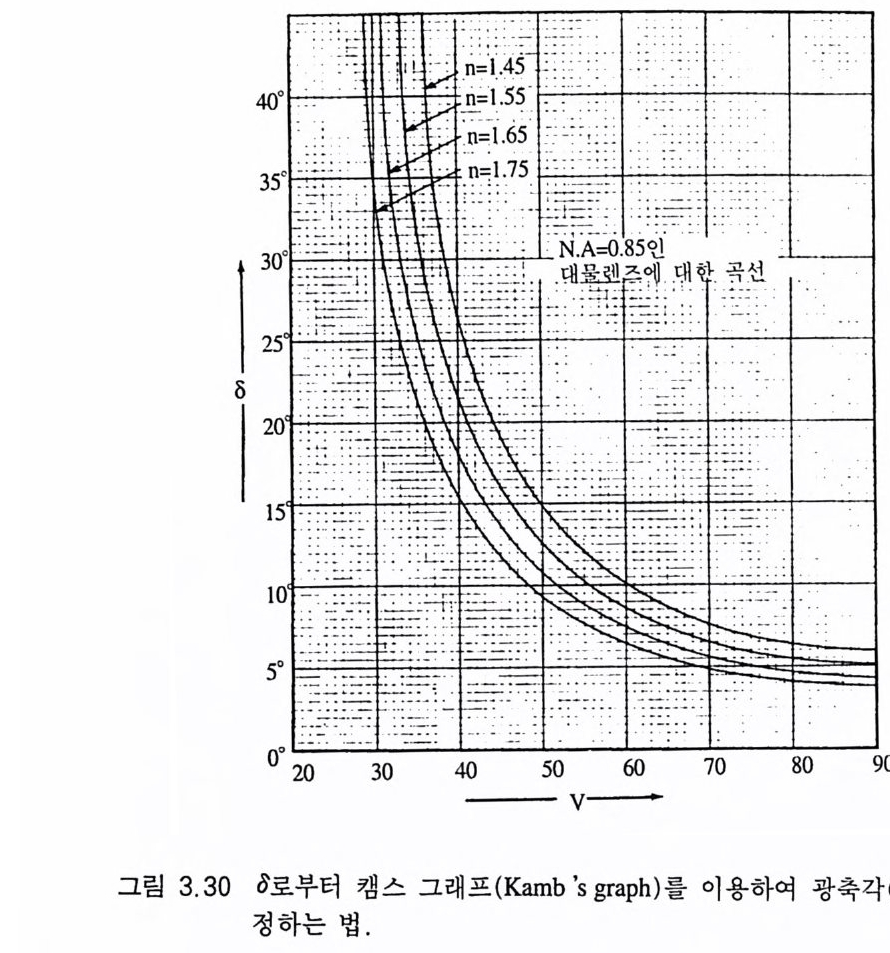
토비법 (Tob i 'sme t hod) 이 방법은 현미경 시야 내에 두 멜라토프가 대칭적으로 존재하는 광물 박편의 경우에 적용되며, 맬러드 상수를 계산할 필요가 없기 때문에 편리하다. 이 방법을 적용하기 위해서 는 현미경 시야의 직경 (2R) 울 측정하고, 두 멜라토프 사잇거리 (2D) 를 측정 하여 그 비 (2 D/2R) 를 계산한 다음(그림 3.2 5 ) 토비에 의해 제시된 그래프 를 이용하면 된다(그림 3.2 7). 이 그래프는 대 물 렌즈의 구경치 (N .A.)가 0.85 인 경우, 죽 45 배 렌즈를 사용했을 때 적용되는 것이며, 기타 배율의 대물렌즈를 사용했을 때에는 각 각의 새로운 구경치 (A' )를 적용하여 (2D/2R) X (A '/ 0.85) 를 사용하 면 된다. 2D/2R 값을 왼쪽의 세로 축에서 찾아 그 위치에서의 사선(斜 線)을 따라 가면 2E 값이 얻어지며(그림 3.27a), /3굴절률을 알고 있는 경우에는 2D/2R 에서 가로 축에 있는 /3값에서 수선을 올려 만나는 교점까지 수평선을 그은 다음 이 위치에서 사선을 따라 올 라가면 2V 값을 얻게 된다(그림 3.2 7 b). 라이트법(Wrig h t' s meth o d) 이 측정 법 은 광축 하나가 시 야의 중심 에 있는 광축중심 간섭상인 경우에 적합하다(그림 3.28). 현미경에서 관찰되는 쌍곡선의 휘어진 정도를 보고 판단하는 방법으로서, 2V 가 90° 인 경우에는 거의 직선에 가까우며, 0° 일 때는 직각 형태를 나 타낸다 . 캠스법 (Kamb' s meth o d) 두 광축에 약간 어 긋나게 절단된 광물 박 편에서 관찰되는 간섭상에 대해 적용하는 2V 측정법으로서, 소광 위치에서 얻어진 간섭상(그림 3.29a) 을 반시계 방향으로 재물대를 회전하면서 아이소자가 시야의 가장자리를 스치며 사라지는 각도를 측정한다. 두 쌍곡선 아이소자 중 하나는 먼저 그리고 다른 하나는 나중에 사라진다(그림 3.29b). 그때의 회전 각도를 각각 &, & 라
 』 2V/ (또는 2
』 2V/ (또는 2
 2V=l5°
2V=l5°
 ----------_J
----------_J
 3
3
고 하자. 광물 박편을 다시 원 위치로 돌린 다음, 이번에는 시계 방향으로 회전하면서 쌍곡선 아이소자가 시야의 가장자리에 닿는 회전 각도를 읽어 각각 &, & 라고 적는다. 이제 이 네 수치의 평 균값 [o=(o,+82+03+84)/4] 을 계산하여 그래프(그림 3 .3 0) 에 적용시 킨다. 이 그래프도 구경치가 0.85 인 대물렌즈를 사용했울 때에 적 용되며, 대략의 f3 굴절률(그래프에는 正녁: 표시되어 있음)을 알고 있 어야 한다 사용하는 방법은 8 값을 세로 축에서 찾고, f3값에 근접한
 22 VV ,니 \ ° 1 에 ' I l 5 0 ' I4W II1W II'n ’
22 VV ,니 \ ° 1 에 ' I l 5 0 ' I4W II1W II'n ’
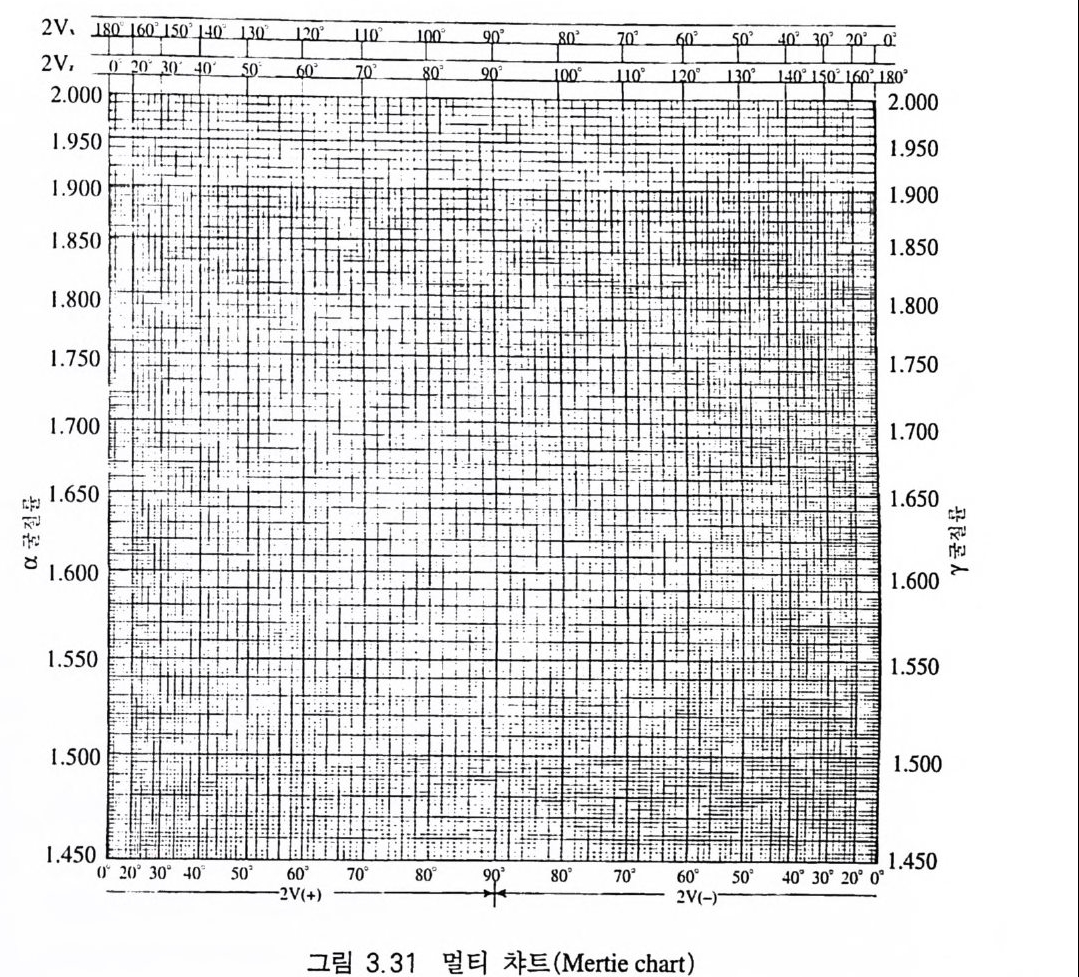
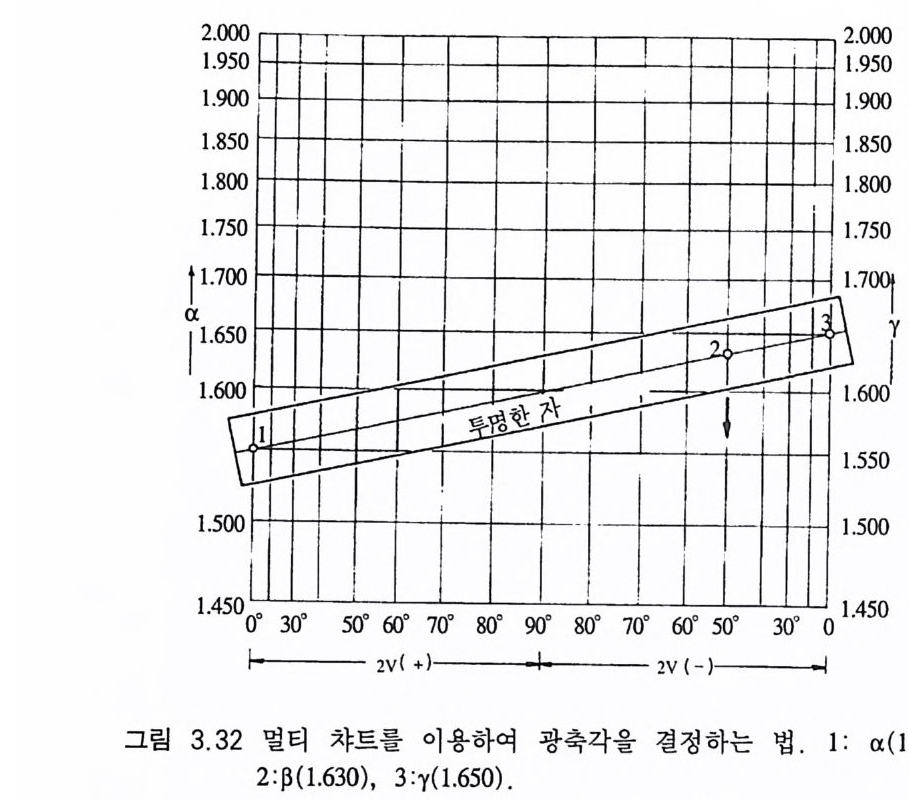
곡선까지 수평선을 그어 만나는 교점에서 아래로 수직선을 그으면 광축각의 절반인 V 가 얻어진다. 멀 티 법 (Mert ie' s meth o d) 이 축성 광물의 굴절률 3 개를 모두 알고 있는 경우에 적용되는 방법으로서, 먼저 a 굴절률을 그래프(그림 3. 31) 의 왼쪽 세로 축에서 찾고, r 굴절률을 오른쪽 세로 축에서 찾아
 2.000
2.000
직선으로 연결한 후, f3 굴절률값에 해당하는 점을 찾아 수선을 내리면 2V 값이 가로 축에 나타나게 되고, 동시에 광학 부호까지 얻을 수 있 게 된다. 예를 들어 굴절률이 각각 a=I.55 0, {3=1.63 0, y=1.65 0 인 광물인 경우, 이를 멀티그래프(그림 3 .3 1) 에 적용하면 그림 3.3 2 와 같이 되어 2V 가 50° 이며 동시에 광학 부호는 (-)임을 알 수 있게 된다 . 이 그래프를 이용할 경우, 세 굴절률 중 2 개와 2V 및 광학 부호를 알면 나머지 굴절률을 알아낼 수가 있다 .
제 4 장 조암광물 각론 4,1 조암광물의 분류 광 물 을 분류할 때 목적에 따라 분류 기준이 달라질 수 있으나, 광 물 학적으로는 화학성분에 근거하여 분류하는 것이 일반적인 관례 이다. 이 분류법은 광물을 구성하고 있는 음이온을 기준으로 하고 있는데, 여러 가지 측면에서 다른 분류법보다 타당성이 있어 19 세 기 중반부터 활용되고 있다. 음이온을 기준으로 한 분류법의 장점 은 다음과 같다. 첫째는, 같은 음이온으로 되어 있는 광물들인 경우 양이온에 따 라 분류했을 때보다 더 밀집한 유사성이 있다는 점, 둘째는 동일 한 음이온을 지니는 광물들은 대개 동일하거나 유사한 지질학적 환경에서 함께 산출된다는 점, 셋째는 음이온에 따라 분류하는 것 이 무기물을 분류하고 또 그 화합물을 명명하는 최근의 화학계의 경향과도 부합한다는 점이다 .
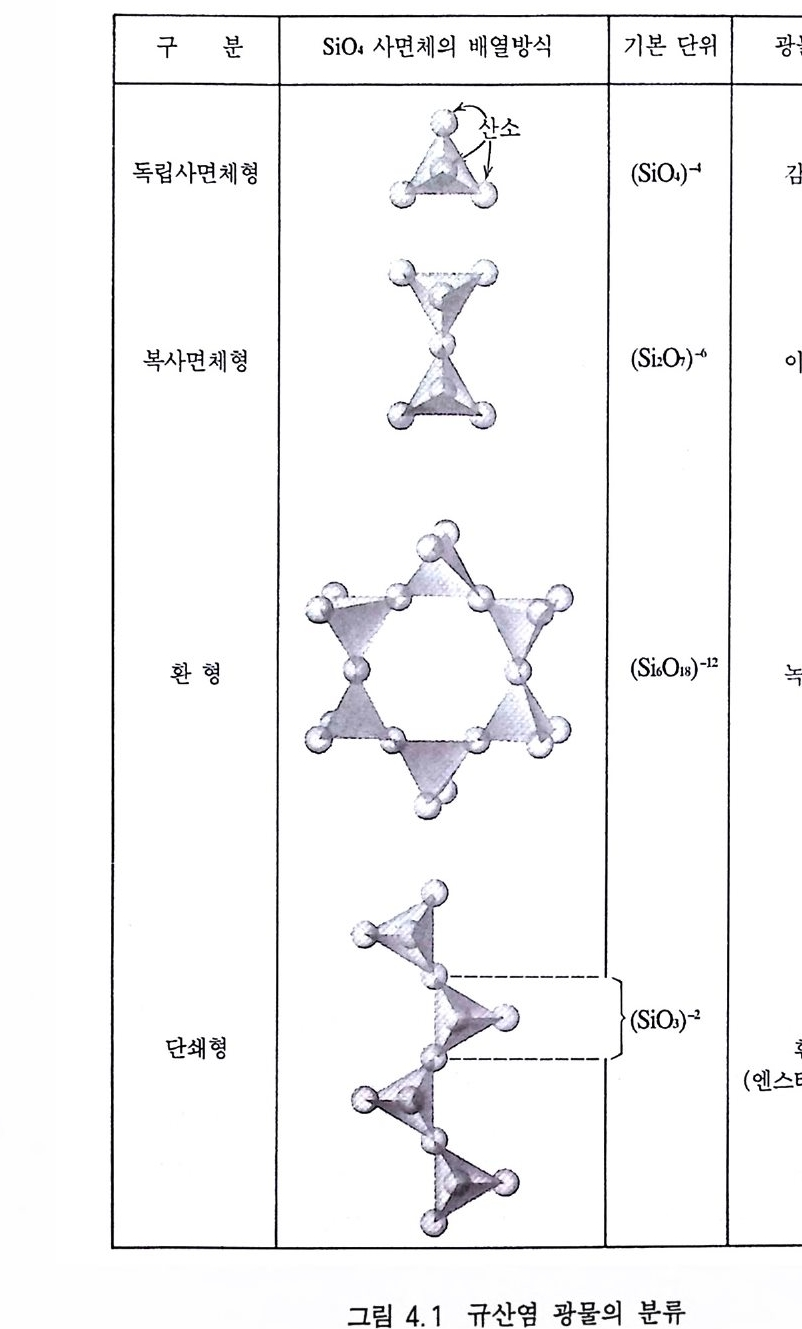
한편, 음이온에 의해 분류된 경우에서도 결정구조적으로 상이한 부류가 나중에 발견되어 화학적인 측면뿐만 아니라 결정구조적인 측면까지 고려하여 광물을 다시 세분할 필요성이 생기게 되었다. 이에 따라 광물은 우선 족(族, class) 으로 대별하고, 족은 다시 화 학적 특징에 의해 아족(亞族, fa m il y)으로 세분되며, 족 또는 아족 은 결정구조적인 유사성에 따라 군(群, g rou p)으로 나뉜다. 군은 종(種, s p ec i es) 과 종으로 이루어진 계열(系列, ser i es) 로 구성되어 있다. 일부 종은 다수의 변종( 襄 種, v ari e ty)을 가진다 . 규산염 광물, 산화 광물, 탄산염 광물, 황화 광물, 황산염 광 물, 할로겐 광물 등은 족에 해당하는 분류 등급이며, 규산염 광물 내의 독립사면체형 구조, 단쇄형 구조, 망상형 구조, 환형 구조 광물 등의 분류는 아족의 예이다 . 휘석군, 각섬석군, 석류석군, 장 석군 등은 군의 예이며, 휘석군의 투휘석 -헤덴버가이트계열, 각섬 석군의 투각섬석-양기석 계열, 석류석군의 파이로프-알만딘-스 페샤르틴 계열, 장석군의 사장석 계열 등은 계열의 예이다. 석영 은 종이며, 이는 다시 색깔에 따라 자수정, 황수정, 백수정, 연수 정 등의 변종으로 더욱 세분된다. 사장석 계열에는 앨바이트, 올 리고클레이즈, 안데신, 라브라도라이트, 바이타우나이트, 아노르 다이트 동의 여러 종이 있다. 4.2 광물의 분류 4.2.1 규산염 광물 Si0 4 사면체가 음이온 구실을 하고 있는 광물을 말한다. 규산염 광물은 Si0 4 사면체의 결합방식에 따라 여러 개의 아족으로 나뉘
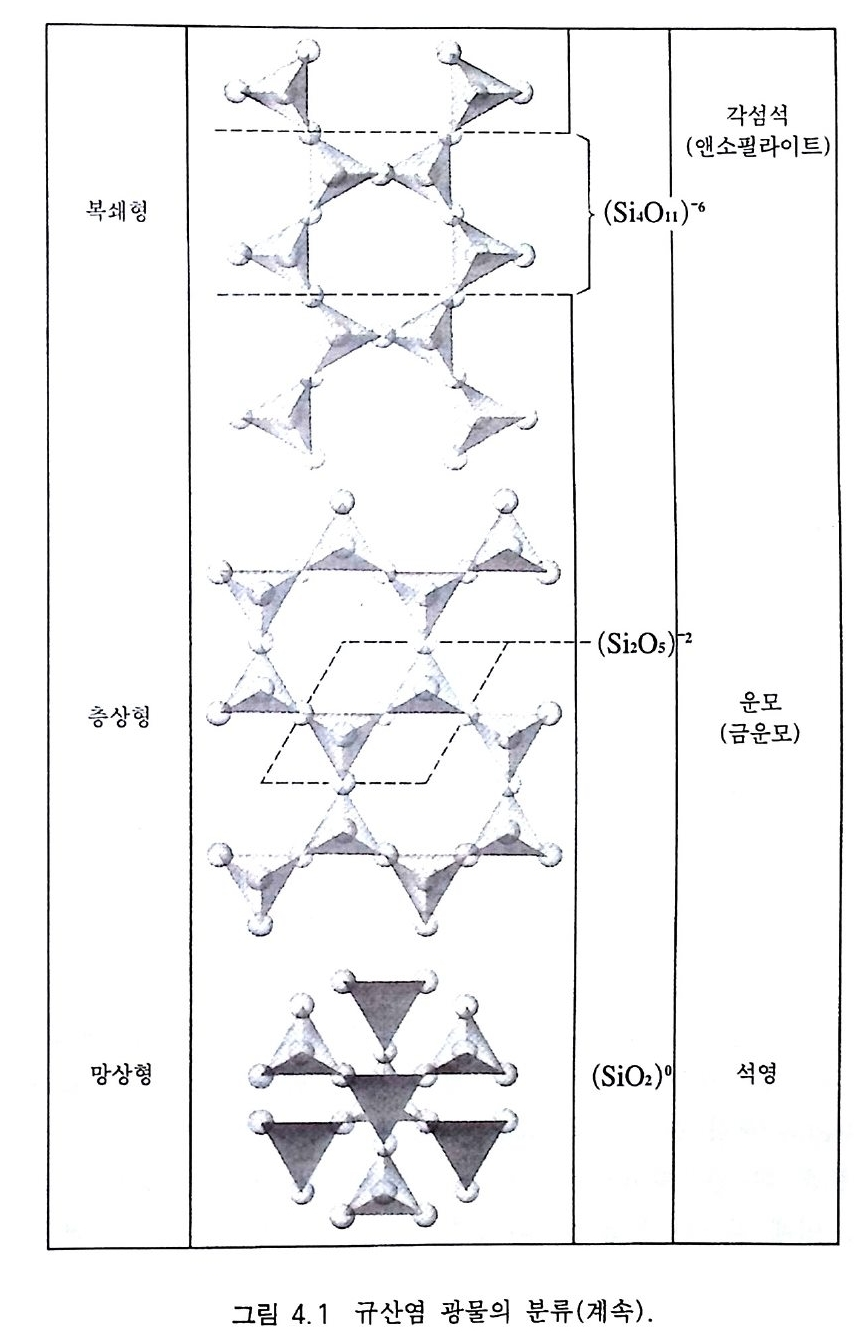
며, 각 아족의 음이온 기본단위 특징이 다르다(그림 4.1 ) . 독립사면체형(蜀立四面體型) 구조를 지니는 경우는 S i O 』 사면체 가 독립적으로 존재하고 있다. 그리고 금속 양이온이 이들 사면체 사이에 위치하면서 전기적 중성을 이룬다. 음이온의 기본 형태가 (S i 04)+ 가 되고 Si : O=l :4 가 된다. 감람석 [(Fe, Mg )iSi 0 4 ], 저어콘 (ZrS i O 』)이 그 예이다. 복사면체형(復四面體型) 구조를 하고 있는 광물에서는 Si0 4 사면 체 두 개가 사면체의 한 꼭지점에 있는 산소를 공유하며 쌍을 이루 어 음이온 구실을 하는 경우이다 . 이 경우 S i :0=2:7 이며, (ShO i)6- 가 음이온 구실을 한다. 아커마나이트 (Ca2M gS i 201), 이극석 [Zn4Si2 0 , (0H) • H2 이이 그 예 이 다. 환형 (環 型 )구조는 3 개, 4 개, 6 개의 Si0 4 사면체가 고리모양으로 연결되어 있는 구조로서, 3 개의 사면체가 연결된 경우는 (SiJ 0 9)6- , 4 개가 연결되어 있는 경우는 (Si4 0 12)S.. , 6 개가 연결되어 있는 경 우는 (S i.아 )12 가 기본 단위가 된다. 3 각 환형구조인 경우는 베니 오아이트 (BaT i Sb09), 4 각 환형구조의 예는 액시나이트 [(Ca, Mn, Fe)J A 12(B0J) Si4 0 12(0H)], 6 각 환형 구조는 녹주석 (Be J AuS i ,O 미 이 그 대표적인 예이다. 단쇄형(單鎖型) 구조를 하고 있는 광물의 경우는 Si0 4 사면체가 일직선상으로 산소를 공유하면서 연결되어 있는 형태로서, 기본 단위는 (SiO J )2- 또는 (S i 20,)4 가 된다. 광물 예로는 엔스터타이트 (Mg Si O J ), 장미 휘 석 (MnSiO J ), 규회 석 (CaSiO J ) 등이 있다. 복쇄형(復鎖型) 구조를 하고 있는 광물의 경우는 Si0 4 사면체로 구성되어 있는 직선상의 사슬이 2 개가 나란하게 배열되어 있고 이들 사이에 마주 보는 사면체가 산소를 공유하고 있는 형태로 서, (S i BOll)' 2,.가 기본 단위가 된다. 광물 예로는 투각섬석 -양 기석 계 열 [C ai (M g, Fe)sS i s022(0H )i]이 있다.
 구 분 SiO , 사면체의 배열방식 기본 단위 1 광 물 예
구 분 SiO , 사면체의 배열방식 기본 단위 1 광 물 예
 복 쇄잉 --l 一 一尺 - ~f广 一一 广\ {- l一 ’,、' r i 나갑식戶 `’^ >\PJ 一 7J l ( Sh0 마기(앤 소각필섬라석이 트)
복 쇄잉 --l 一 一尺 - ~f广 一一 广\ {- l一 ’,、' r i 나갑식戶 `’^ >\PJ 一 7J l ( Sh0 마기(앤 소각필섬라석이 트)
층상형( 層 狀型) 구조는 단쇄상 구조 3 개가 결합하여 하나의 층을 이 룬 형태로 생각할 수 있다. 이 경우 S i O 』 사면체 4 개가 한 기본 단 위를 이루어 결국 (S i ,O,o)4 · 가 기본 단위가 된다. 활석 [ M g JS i 40 10 ( 0 H ) 2), 사 문 석 [ M g ~S i 40 10 ( 0 H ) 나 , 금 운 모 [KMg J( AISbO,o)(OH) i] 등이 그 예에 해당한다. 이 중 금운모의 경 우는 (Al, Si) : 0 = 4: 10 이며, Alk 가 S i#를 치환하는 경우이므로 전기적으로 균형을 이루기 위하여 Kh 가 추가로 참여한다. 망상형 (網狀型) 구조는 Si0 4 사면체의 각 꼭지점에 있는 산소가 모두 다른 사면체와 공유되어 있는 구조로서, 결국 Si : 0 = I : 2 가 된다. (S i 02) 가 기 본 단위 이 다. 석 영 (Si0 2 ), 칼리 장석 (KAISiJ O H) 등 이 광물 예인데, 장석인 경우 (Al, Si) : 0 = I : 2 이다. K+ 는 Al» 가 S i다릅 치환하여 생긴 결손을 막는 역할을 하고 있다. 규산염 광물은 현재 알려진 약 3000 여 종의 광물 중 25% 정도를 차지하고 있고, 광물이나 암석을 연구할 때는 가장 자주 접하게 되는 광물이기 때문에 매우 중요하게 다루어진다. 이 책에서는 조암광물로서의 중요성이 비교적 높은 광물인 석 영, 장석, 준장석, 감람석, 휘석, 각섬석, 석류석, 녹렴석, 사문 석, 규선석, 운모, 저어콘, 황옥, 전기석, 근청석에 대해 다루었다. 4.2.2 산화 광물 산화 광물은 산소가 음이온인 경우이며, 하나 또는 몇 개의 금 속 원소와 결합하고 있다. 산화 광물은 단순 산화 광물 (s i m p le o xi de) 과 복합 산화 광물 (com p lex ox i de) 로 다시 나뉜다. 단순 산화 광물은 한 종류의 금속 원자와 산소가 결합되어 있는 형태를 말하 며, 이때 금속과 산소 원자의 결합 비율은 상관이 없다. 일반적으로 Xi O 형 (예 : Ct1 20 ), XO 형 (예 : ZnO, Mg O ), XO 형 (예 : Ti0 2 , Mn02)
으로 표시한다 . 복합 산화 광물은 XY2G 로 표시하며, 이때 금속 원자 X 와 Y 의 위치가 구별되어 있다 X 는 心] 배위수를 가지는 사면체 구 조 내에 있게 되며, Y 는 6 의 배위수를 가지는 팔면체상 배위다면체 중심 에 위 치 한다 . X 는 +2 가의 양이온으로서 Mg , Fe, Zn, Mn 등이 며, Y 는 +3 가의 양이온으로서 Al, Fe, Mn, Cr 등이다. X 2+에 해 당하는 이온끼리는 폭넓은 고용체를 형성하지만, y;.이온끼리는 매 우 재한적인 고용체를 형성한다. 산화 광물로는 강옥, 금홍석, 첨정석, 자철석, 적철석, 티탄철 석, 크롬철석에 대해 기술하였다. 4.2 .3 탄산염 광물 탄산염 광물은 (CO J)2-가 움이온 구실을 하고 동시에 결정구조의 기본이 되므로 탄산염 광물들은 성질이 매우 유사하다 . 특히 탄산 염 광물을 식별할 때 시행하는 염산반응 테스트는 수소 이온이 있 을 때 탄산염 광물이 매우 불안정해지면서 탄산가스와 물로 분해 되는 현상을 이용한 것이다. 이 반응식은 2H-+co J2- =ILO+C02 로 나타낼 수 있다. 방해석, 마그네사이트, 능망간석, 능철석, 백운석, 아라고나이 트에 대해 기술하였다. 4.2.4 황산염 광물 (S04)2- 착이온이 움이온 구실을 하는 광물을 가리키며, 이 때 S” 는 4 개의 산소 원자로 되어 있는 사면체 구조의 중심에 위치하 게 된다. 중정석, 석고, 경석고에 대해 기술하였다 .
4.2.5 수산화염 광물 수산기인 (OHr 가 음이온 역할을 하고 있는 광물로서, 물 (H20) 분자를 가지기도 한다. 이러한 구조의 광물은 원자간의 결합력이 약하기 때문에 산화 광물에 비하여 물리적인 힘이 약한 것이 일반 적인다. 수활석, 깁사이트, 다이아스포, 보에마이트 , 침철석에 대해 기 술하였다. 4.2.6 인산염 광물 (P04)~ 착이 온을 포함하고 있는 광물로서 , P 5+이 온의 반경 이 S 보다 약간 크기 때문에 (S04) 2 - 경우처럼 4 개의 산소로 둘러싸여 있 는 배위상태를 나타낸다 . 인회석 , 모나자이트에 대해 기술하였다 . 4.2.7 할로겐 광물 할로겐족 원소에 속하는 Cl~, Br-, F, r 등의 원소를 함유하고 있는 광물이다 . 이러한 음이온으로 구성되어 있는 광물들은 산화 수가 작은 양이온과 결합할 경우 대칭도가 매우 높은 결정구조를 하게 되는데, 그 예로서 등축 면심격자 형태의 소금 (NaCl) 이 있 다. 죽, N 값과 er 은 각각 6 개의 상대방 이온으로 둘러싸여 있는 팔면체상 배위를 하고 있다. 실바이트 (KC I), 형석 (CaF2) 둥이 있 으나, 암석에서 산출되는 빈도수가 비교적 큰 형석에 대해서만 다 루었다.
4.3 광물 각론 4.3.l 규산염 광물 4. 3 . 1.1 석영군(Q UARTZ GROUP) 석영군(石英群)에 속하는 광물들은 석영(q ua rt z), 트리디마이트 (tri d y m it e) , 크리 스토발라이 트 (cr i s t obal it e), 코에 사이 트 (coes it e), 스 티쇼바이트 (s ti shov it e) 등으로 모두 화학식이 S i 02 이다. 단백석 (o p al) 도 동일한 화학성분을 지니고 있으나 규칙적인 원자배열을 지니고 있지 않으므로 준광물에 해당한다. 동질이상체(p ol y mo rp h) 관계에 있는 이들은 온도와 압력에 있어 그 안정영역이 다르다. 석영-트리디마이트-크리스토발라이트계(系, se ri es) 는 특히 온도에 따라 결정구조가 변하는데 573°C 이하에서는 저온 석영 (low qu ar tz) 으로, 573• 에서 870°C 범위에서는 고온 석영 (h ig hq u art z), 870° 에서 l470°C 범위에서는 트리디마이트, 1470° 에서 l710°C 사이에서는 크 리스토발라이트로 안정하게 존재하고, 그 이상의 온도에서는 용융 된다(그림 4.2). 마그마가 고결되어 만들어지는 화성암 내에 있는 석영은 처음에는 고온 석영 형태로 존재하다가 점차 냉각되면서 저온 석영으로 변하는 경우가 대부분이다. 코에사이트와 스티쇼바 이트는 매우 높은 압력에서만 안정한 광물로 각각 38,000 기압과 130,000 기압에서 합성된 바가 있다. 칼세도니 (chalcedon y)는 석영의 은미정질 변종이다. 【저 온 석 영 (Low Qu ar tz)> 화학성분 Si0 2 결정계 삼방정 계 . P3,. a=4.913, c=5.4 0 5A 색 투명한 경우가 대부분이며 간혹 반투명하다. 순수할 때는 무
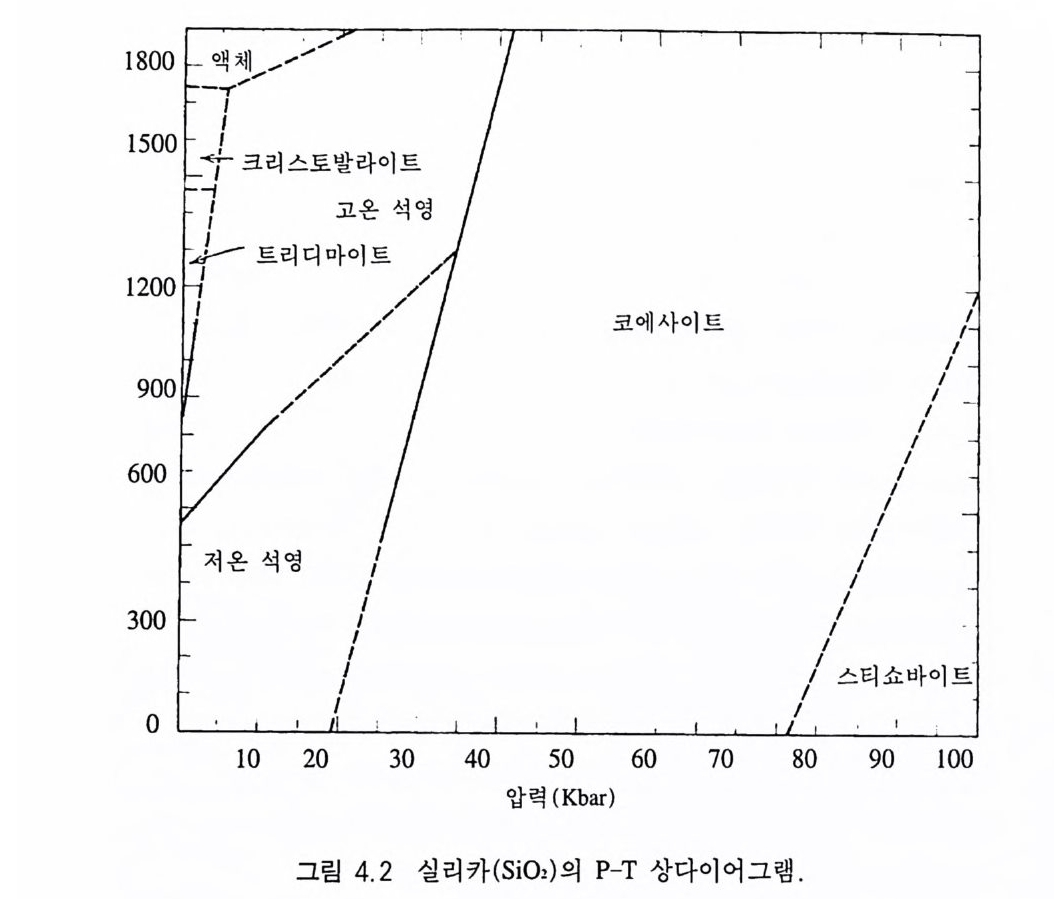 .,,,
.,,,
색이지만, 불순물을 소량 함유하면 색을 띤다(표 4.1 ). 철 (Fe) 이 있을 경우 보라색(자수정), 망간 (Mn) 인 경우 황색(황수정), 티타 늄 (T i)인 경우 분홍색(장미석영)이 되며, 녹색의 퓨사이트(fu chs it e) 입자가 미세하게 포함되어 있을 경우에는 녹수정이 된다 . 또한다 수의 액체 내포물이 들어 있으면 우유빛의 유백수정이 되고, 방사 성 입자에 의해 결정구조의 일부가 파손되면 어두운 회색을 띠는 연수정이 된다. 박편에서는 모두 무색이다. 결정형태 자형 결정은 3 방주와 3 방추 또는 양추가 결합되어 있
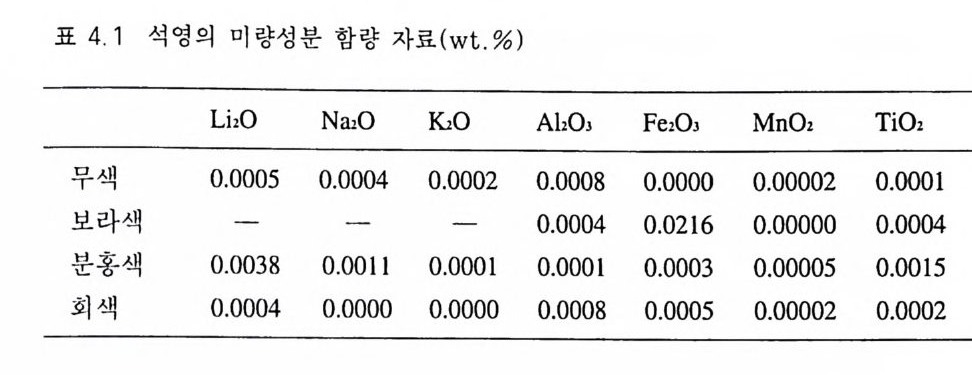 표 4 1 석영의 미량성분 함량 자료 (w t . %)
표 4 1 석영의 미량성분 함량 자료 (w t . %)
어 마치 6 각주 모양을 지닌다 . 그러나 화성암 내에서 조암광물로 존재할 경우는 불규칙한 타형의 입자 형태를 지닌다. 간혹 정장석 이 나 미 사장석 과 혼정 하여 문상조직 (gr ap hi c tex tu r e) 을, 사장석 과 혼정 하여 미 르메 카이 트 조직 (my rm ek ite tex tu r e) 을 나타낸다. 벽개 없음 경도 7 비중 2.6 5 양각 매우 낮음 굴절률 (J)=1.54 4, E=1 .55 3. 복굴절률 =0 . 009. 표준 박편인 경우 1° 백색 또는 황색의 간섭색을 나타낸다 . 광학부호 일축성, (+) 소광특징 4 번 소광하며, 입자가 타형일 경우 소광각을 측정할 수 없다. 자형 결정이고 또 주상 결정면의 일부가 존재하면 평행 소광을 나타낸다. 화성암에 존재하는 석영은 혼히 파동소광을 한 다. 이것은 고온에서 형성된 석영의 결정구조가 냉각되면서 일부 변형되었기 때문이다. 동력변성암 내에 존재하는 석영도 파동소 광을 나타내는데 이것은 압력에 의해 결정구조가 변형되었기 때 문이다. 장축부호 결정의 장축 방향으로 느린 광선이 진동하고 있으므로
(+)이다 . 간섭상 일축성 간섭상의 전부 또는 일부가 관찰된다. 복굴절률 이 작으므로 아이소크롬은 나타나지 않는다. X 선회절선 4.26(3), 3.34(1 0 ), 2.4 5 ( 1), 1.8 18(6), 1.5 41 (1 ), l.08 1( l)A. [고온 석 영 (High Qu ar tz)> 화학성분 Si0 2 결정형태 육방양추인 형태를 취한다. 유문암이나 석영반암 내에 서 발견될 수가 있다. 기타사항 고온 석영은 정출된 후 573°C 이하로 냉각이 되면 자 연히 저온 석영으로 변한다. 따라서 현재 관찰하는 석영은 모두 저온 석영이다. 【트리 디 마이 트 (T ri dymit e) 】 화학성분 Si0 2 결정계 사방정계(가육방정계). a=l0.04, b=l7.28, c=8.20A 색 박편하에서 무색이다. 결정형태 얇은 육각형태를 취하며 매우 미세한 크기로 산출된다. 벽개 불량한 주상 결정이 발달한다. 경도 7 비중 2.26 양각보통 굴절률 a=l. 46 9, /3=1.46 9, ,-1.47 3. 복굴절률 =0.004 광학부호 이축성, (+) 2V 35° 간섭상 결정입자들이 미세하므로 간섭상을 만들기가 매우 어렵다.
X 선 회절선 4.3 ( 10), 4.1 0 000), 3.86(2), 3.82(s)A 기타사항 트리디마이트는 고온의 기체에서 정출되며, 유문암, 안산암 등과 같은 화산암 내에 발달한 공동에서 산출된다. 【크리 스토발라이 트 (Cr i s t obal it e) 】 화학성분 Si0 2 결정계 정방정계(가등축정계) . P4,212,, a=4.97, c=6.93A. Z=3 색 박편하에서 무색이다. 결정형태 육면체의 미세한 결정으로 산출되며, 화산암 내의 공 동에서 발견된다.
벽개 없음. 휘어진 형태의 단구가 발달한다. 경도 6~7 비중 2.3 3 양각보통 굴절률 (J)= 1.48 4, e= 1.48 7. 복굴절률 =0 . 003 X 선 회절선 4.osoo), 3.1 4 0), 2.840), 2.4 8 (2), 2.4 6 0)A 기타사항 크리스토발라이트는 유문암, 안산암, 현무암과 같은 화산암 내에 있는 공동에서 산출하는데 트리디마이트와 매우 유사 하다. 이들을 구별하기 위해서는 굴절률 측정과 X 선 회절분석을 실시하여야 한다. 【코에 사이 트 (Coes it e) 】 화학성분 Si0 2 결정계 단사정계. C2 /c. a=7.1 7 , b=l2.3 8 , c=7.17A 색 무색, 투명 결정형태 미세하고 납작한 육각형태를 취한다. X 선 회절선 6.2(0, 4.3 8 (0, 3.43(3), 3.@(to), 2.7 6 (1 ), 2.690)A기타사항 미국 애리조나주의 운석이 떨어진 곳에서 발견된다 . [스티 쇼바이 트 (S ti shov it e) 】 화학성분 Si0 2 결정계 정방정계. a=4.1 7 , c=2.6 6 A A-H1 E기_..-A, ll X 선 회절선 2.96(1 0 ), 2.24(2), l.98 (3), l.87 (2), t.53 (5), L47(2)A 기타사항 미국 애리조나주의 운석이 떨어진 곳에서 코에사이트 와 함께 발견되는데, 현재까지로는 운석의 떨어짐에 따른 압력이 미친 곳 외에서는 만들어지지 않는 것으로 알려져 있다. 석영군에 속하는 광물 중 비 중이 가장 크다 (4 . 28) . 【칼세 도니 (Chalcedony )> 화학성분 Si0 2 결정계 삼방정계 색 순수할 경우는 무색 또는 옅은 회색울 띠지만, 불순물을 함 유하면 다양한 색을 띤다. 발색소로 니켈 (N i)을 함유하면 선명한 녹색(크리소프레이즈, ch ryso p ra se), 철 (Fe) 을 함유할 경우 적색(코 넬리언, cornelia n ), 미립의 갈철석이 포함되어 있는 경우 황색(사아 드, sard), 녹니석이나 액티놀라이트의 미립자들이 들어 있는 경우 녹색(프레이즈, pra se), 적철석의 미립자들이 있는 경우 거의 불투 명한 적색(재스퍼, j as p er) 이 된다. 칼세도니 가운데 동심원상의 무 늬가 발달한 것이 있는데 이를 아게이트 (a g a t e) 라 하고, 직선상의 무늬가 있는 것을 오닉스 (on y x) 라고 한다. 결정형태 괴상(城狀) 형태를 지니며 표면은 둥근 포도상 조직을 가진다. 굴절률 1.5 3~1 .54 . 복굴절률은 측정이 불가능하다.
경도 6.5 ~ 7 비중 약 2.6 0 소광특징 은미정질 상태의 집합체이므로 편광현미경에서 항상 밝게 보인다 . 기타사항 광학 부호, 간섭상, 장축 부호 등은 결정할 수 없다. 칼 세도니에는 미세한 다공질 조직이 있어 진한 설탕물에 담근 후 산성용액으로 씻으면 여러 색깔로 착색이 된다. 유색 변종들은 보 석 가공용으로 사용된다. 칼세도니는 실리카 (S i 02) 성분을 지나치 게 많이 용해하고 있는 열수용액으로부터 만들어진다 . 4. 3. 1. 2 장석군 (FELDSPAR GROUP) 장석군( 長 石群)에는 칼리장석류와 사장석류(斜長石類)가 있다. 장석의 화학식은 AB 』아로 표시될 수가 있는데, 전자는 A 위치에 K 원소가, 후자는 Ca 와 Na 원소가 있다 . 칼리장석류에는 정장석 (正 長石 , orth oclase), 새 니 딘 (sanid i n e), 미 사장석 (微斜長石, mi cr oclin e ), 아노르도클레이즈 (ano rth oclase) 등이 있으며, 사장석류 에는 Ca 의 함량이 증가함에 따라 앨바이트, 올리고클레이즈, 안데 신, 라브라도라이트, 바이타우나이트, 아노르다이트로 세분한다. 장석군에 속하는 광물은 거의 모든 화성암의 주요 조암광물로 존 재하며, 이들의 풍화물로 형성된 퇴적암이나 변성암에도 폭넓게 존재한다. 장석군에 속하는 주요 광물의 상호관계는 정장석 (ort ho clase), 앨바이트 (alb it e), 아노르다이트 (ano rthit e) 로 표시되는 상평형 다이어그램으로 나타낼 수 있다(그림 4.3 ). 일반적으로 정 장석은 Or, 앨바이트는 Ab, 아노르다이트는 An 으로 나타낸다 . 정 장석 (Or) -앨바이트 (Ab) 사이의 관계는 고온에서는 완전고용체(完 全 固 溶體, conti nu ous soli d soluti on ) 를 형 성 하여 새 니 딘 [ (K, Na)AlShOs] 과 아노르도클레이즈 [(Na, K)AlSh 아]가 되지만, 냉각되
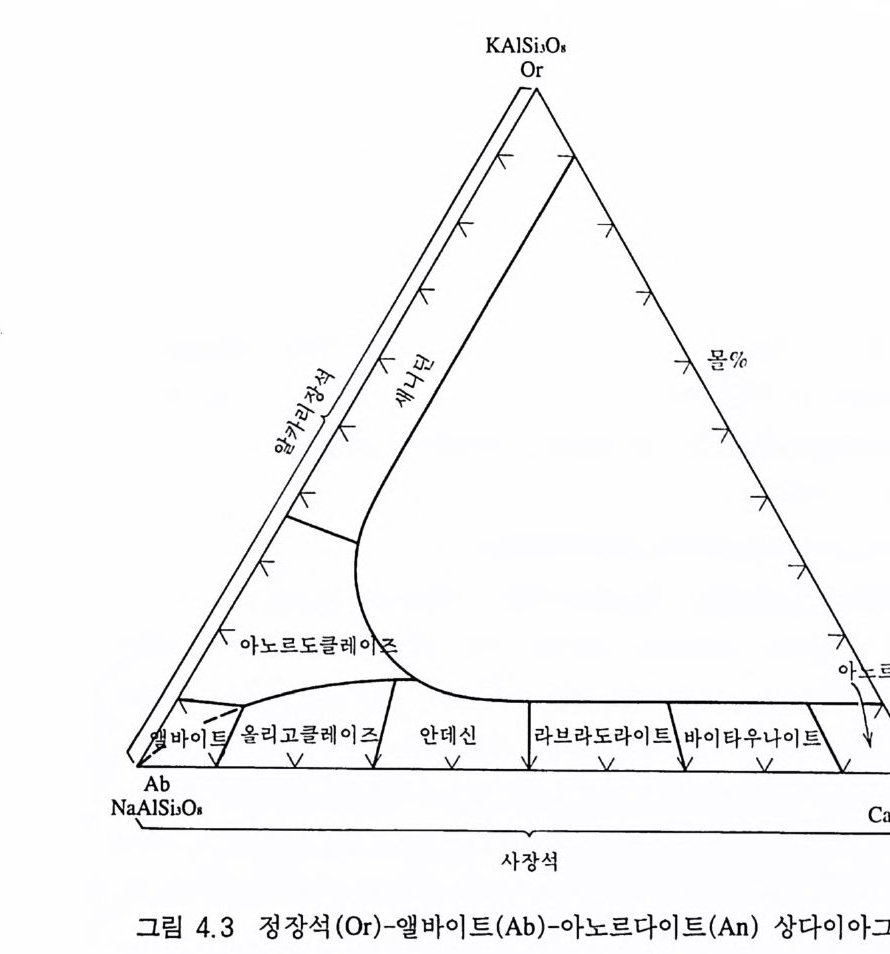 KAlSiJ O I
KAlSiJ O I
면 정장석과 앨바이트로 용리가 일어나 혼정하게 된다. 이 때 정 장석이 앨바이트보다 더 많으면 퍼다이트(p e rthit e), 그 반대이면 역퍼다이트 (an tip e rthit e) 라고 한다. 현미경을 통해 본 퍼다이트의 조직은 특징적이다(그림 4.4 ). 정장석, 미사장석, 새니딘, 앨바이 트 등은 K, Na 등 화학 주기율표상의 알칼리금속에 속하는 원소가 주요 성 분으로 함유되 어 있으므로, 이 를 알칼리 장석 (alkali f eld spa r ) 이라고도 한댜 알칼리장석도 아노르다이트 성분 (CaAhShO s ) 을 정
 仁
仁
장석의 경우 5% 정도 고용체로 함유하고 있으며 그 양온 앨바이트 쪽으로 갈수록 다소 증가한다. 사장석인 앨바이트 (Ab) _아노르다이트 (An) 사이는 Na 와 Ca 가 자유롭게 치환하여 고온에서 뿐만 아니라 저온에서도 완전고용체 를 형성한다. 사장석의 경우도 (Si , A I) -0 로 되어 있는 사면체가 망상구조를 이루고 있는데 사면체의 중심에 있는 S i다를 A1 3+가 치 환하면 사면체의 톰 사이에 있던 Na1• 룰 Ca2+ 가 일부 치환하게 된 댜 따라서 Na1•Si-1 + +--4 Ca2•AI3+ 사이 의 치 환이 일어 난다고 생 각할 수 있다. 이 러 한 치 환을 쌍쌍치 환(雙雙置煥, coupl e d substit ut i on ) 이 라고 한다 . An 성분의 함량(%)에 따라 앨바이트 (0~10), 올리고클레이 즈(I O~30), 안데신 (30~50), 라브라도라이트 (50~70), 바이타우나
이트 (70~90), 아노르다이트 (90 ~ 100) 로 구분한다 . 사장석도 칼리 장석 (KAlSiJ O 8) 성분을 최대 약 5% 정도 고용체로 함유한다 . • 칼리 장석 (Pota s siu m Feldspa r ) 【새 니 딘 (Sanid i n e )> 화학성분 (K, Na)AlSiJ O s 결정계 단사정계. c')jm . a=8.6 , b=l3.0, c=7.2 A , {3= 1 16° 색 박편하에서 무색이며, 매우 깨끗하게 보인다 . 결정형태 화산암 내에서 주상 형태의 결정으로 산 출 된다. 벽개 {001 } 방향의 완전한 벽개와 {010} 방향의 불량한 벽개가 발 달한다 . {10 0} 방향의 열개가 발달하기도 한다 . 경도 6 비중 2.5 6 ~2.62 양각낮다. 굴절 률 a= 1.51 8 ~ 1.52 0, /3= 1.52 3 ~ 1.525, y= 1.524 ~ 1.526 . 복굴 절률 =0.007 . 간섭색은 1· 회색 내지 회백색이다 . 광학부호 이축성, (-) 2V O~12· 소광특징 (001) 면은 평행소광, (010) 면은 5°, 광축에 수직인 면 은 항상소광을 나타낸다. 쌍정 칼스바드 쌍정 (Carlsbad twi nn i n g)이 관찰되는 경우가 많다. 간섭상 이축성 간섭상을 가지지만, 광축각이 작으므로 일축성 간섭상과 거의 유사하다. X 선 회절선 6.65( 1), 4.24(5), 3.95( 1), 3.79(5), 3.33( 10 ), 3.28(6), 3.23(5), 2.99(3)A 기타사항 현미경에서 새니딘을 정장석과 구별할 때는 광축각이
작고 광물 내부가 깨끗한 점을 이용한다. 새니딘은 유문암이나 조 면암에 존재한다. 새니딘은 (Si , Al)04 사면체가 산소 (0) 를 공유하 며 연결된 망상구조로 되어 있다. 【 정 장석 (Orth o clase)> 화학성분 (K, Na)AISbOs 결정계 단사정계 . C2 /m . a=8.5 6 , b=13.0, c=7.1 9 A, /3=1 16° 색 순수한 경우 백색이며 불투명하다 . 미립의 적철석을 함유하 면 분홍색 내지 적색을 띤다 . 박편하에서는 무색이며, 변질된 부 분이 있을 경우 뿌떻게 보이는 것이 특징이다. 결정형태 주상 형태를 취하며, 페그마타이트에서는 자형 결정으 로 산 출 된다 . 벽개 {001} 에 나란한 완전한 벽개가 발달하고, {010} 을 따라 양 호한 벽개가, {110} 을 따라서 다소 불량한 벽개가 발달한다. 경도 6~6.5 비중 2.5 5 ~2.63 양각낮다 . 굴절률 a= 1.51 8, /3= 1.52 4, r= 1.5 26. 복굴절률 =0.008 . 1° 회 색 또는 백색의 간섭색을 나타낸다. 광학부호 이축성, (-) 소광특징 {001} 방향은 평행소광, {010} 방향은 5°~12° 범위를 나 타낸다 장축부호 장축 방향을 따라 빠른 광선이 배열하며, 부호는 (-) 이다. 쌍정 칼스바드 쌍정이 빈번히 관찰된다. 간섭상 이축성 간섭상이며, 광학부호는 (-)이다. 광축각이 크다. 2V 69~72°
X 선 회절선 6.4 8 (1 ), 5.86( 1), 4.22(7), 3.94(2), 3.77(8), 3.61 (2), 3.4 7 (4), 3.3 1 (10 ), 3.29(6), 3.24(6), 2.99(5), 2.901 (3)A 기타사항 칼리장석의 동질이상체 중 새니딘과 결정구조가 매우 유 사하다. 정 장석 의 경 우 S i와 Al 의 부분적 인 질서 (秩序, orderi ng ) 현 상이 나타낸다 . 새니딘과는 광축각이 크기 때문에 구별된다. 정 장석은 화강암, 섬장암 등의 조암광물로 산출되며, 고령토로 변 질된다. 【미 사장석 (Mi cr ocli ne )> 화학성분 K 시 Sh08 결정계 삼사정계, Cl. a=8.5 7 84, b=12.9600, c=7.2112A . a= 90°18' , /3= l15°58' , r=8 9°75' 색 백색 또는 회색이며, 박편하에서는 무색이다. 변질된 부분은 뿌영게 보인다. 결정형태 주상결정 형태를 취할 수 있으나 일반적으로 반자형 또는 타형으로 존재하는 경우가 많다. 벽개 {110} 을 따라 완전한 벽개가, {010} 을 따라 양호한 벽개 가, {110} 을 따라 불량한 벽개가 발달한다. 경도 6~6.5 비중 2.5 6 ~2.63 양각낮음 굴절률 a=l.518~1 .52 2, /3=1.52 2~1 .52 6, y=1.52 5~1 .53 0. 복굴 절률 =0.007. 간섭색은 1· 회색 내지 백색이다. 광학부호 이축성, (-) 소광특징 (001) 면은 소광각이 15°, (010) 면은 5• 이다. 쌍정이 발 달하는 경우는 파동소광을 나타낸다. 장축부호 벽개가 발달하는 (010) 방향을 따라 빠른 광선이 배열
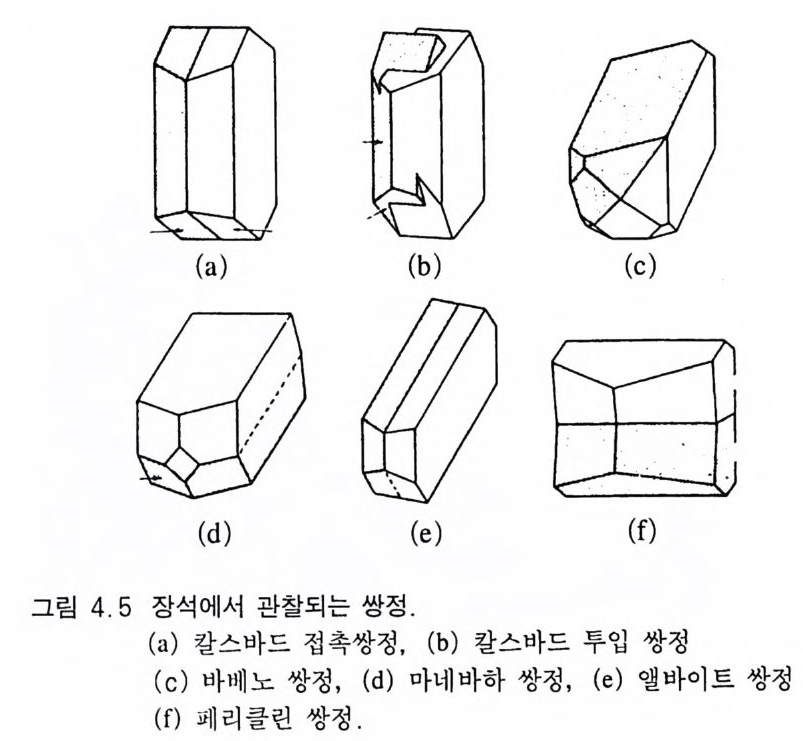 (a) (b) (c)
(a) (b) (c)
한다. (-) 쌍정 {01 이면이 쌍정면 구실을 하는 앨바이트 쌍정 (albit e t w in)과 [010] 이 쌍정축 구실을 하는 페리클라인 쌍정 (pe ri cli n e twi n) 이 동시 에 발달하는 경우가 많다(그림 4.5). 박편에서는 이 격자상의 쌍정 이 잘 나타나는데 이 를 그리 디 론 구조(gridi ron stru c tu re) 라 하며 (그 림 4.6 ) , 미사장석을 식별하는 증거로 활용된다 . 간섭상 쌍정을 이루고 있는 경우가 대부분이므로 간섭상을 만들 기가 거의 불가능하다. X 선 회절선 6.4 8 (1 ), 4.22(5), 3.80(2), 3.29(5), 3.24(1 0 ), 3.0 1 ( 1), 2.970)A 기타특징 미사장석과 앨바이트가 혼정을 이루어 퍼다이트가 되
 그림 4.6 그리디론 조직을 나타내는 미사장석.
그림 4.6 그리디론 조직을 나타내는 미사장석.
기도 한다. 미사장석은 삼사정계로서 대칭축과 대칭면이 없기 때 문에 S i와 Al 의 고정된 위치가 4 개가 되어 질서의 정도가 더 증가 한다. 미사장석은 화강암, 섬장암, 편마암에서 혼히 관찰된다. 미 사장석은 칼리장석중 가장 낮은 온도에서 안정한 동질이상체(同 質 異像體)이다. • 사장석 (Plagi oc lase Feldspa r s) 사장석은 모두 삼사정계의 결정구조를 지니고 있으며, 화학성분 이 연속적으로 변하기 때문에 굴절률, 비중도 점이적으로 변한다. 굴절률은 그림 4.7 과 같이 An 성분이 증가할수록 커지며, 비중 역 시 An 성분의 증가에 따라 커진다. 사장석은 모두 백색 또는 회백 색이며, 일부 라브라도라이트는 청색 또는 녹색을 띤다. 그러나, 박
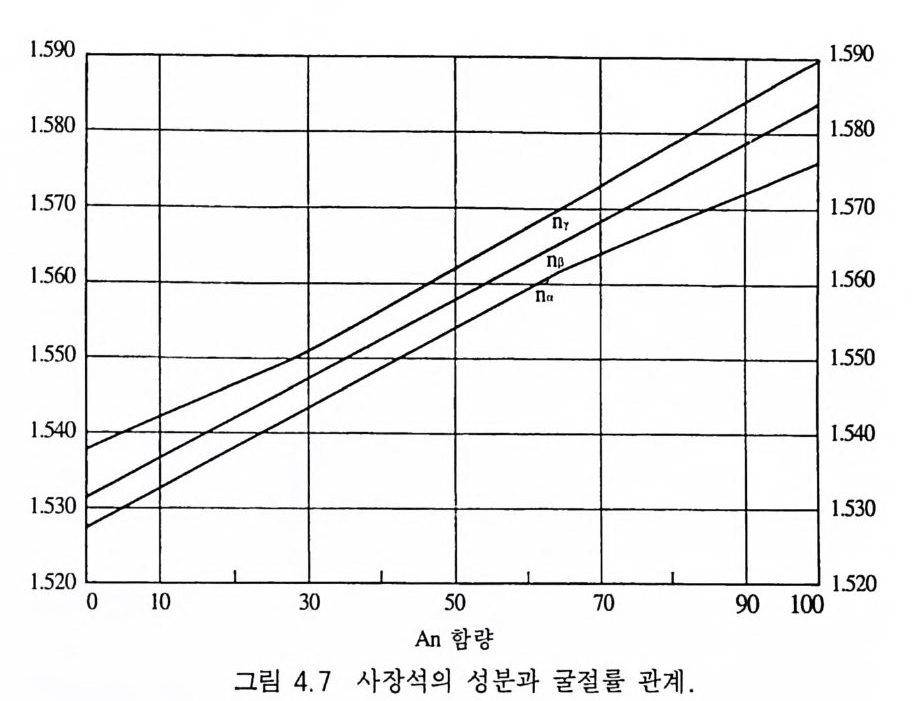 1.59 0 1590
1.59 0 1590
편하에서는 모두 무색이다 . 자형 결정형태는 주상이며, {00 마면과 나 란한 완전한 벽개가 발달한다. 이와 함께 {010}, {110} 방향의 양호 또는 불량한 벽개도 발달한다. 화성암에서 산출될 때 결정의 중심 과 외곽부의 성분이 달라 누대구조를 나타내는 경우가 많다. 일반 적으로 중심부에 An 성분이 높고, 바깥으로 갈수록 An 성분이 적 어진다. 만약 사장석 결정이 성분 차이없이 거의 균질한 경우는 이 결정이 마그마로부터 평형상태에서 매우 서서히 만들어졌음을 의미한다. 【앨바이 트 (Alb it e) 】 화학성분 Ano-10 결정계 삼사정 계 . Cl. a=8.138, b=l2.79, c=7.161A, a=
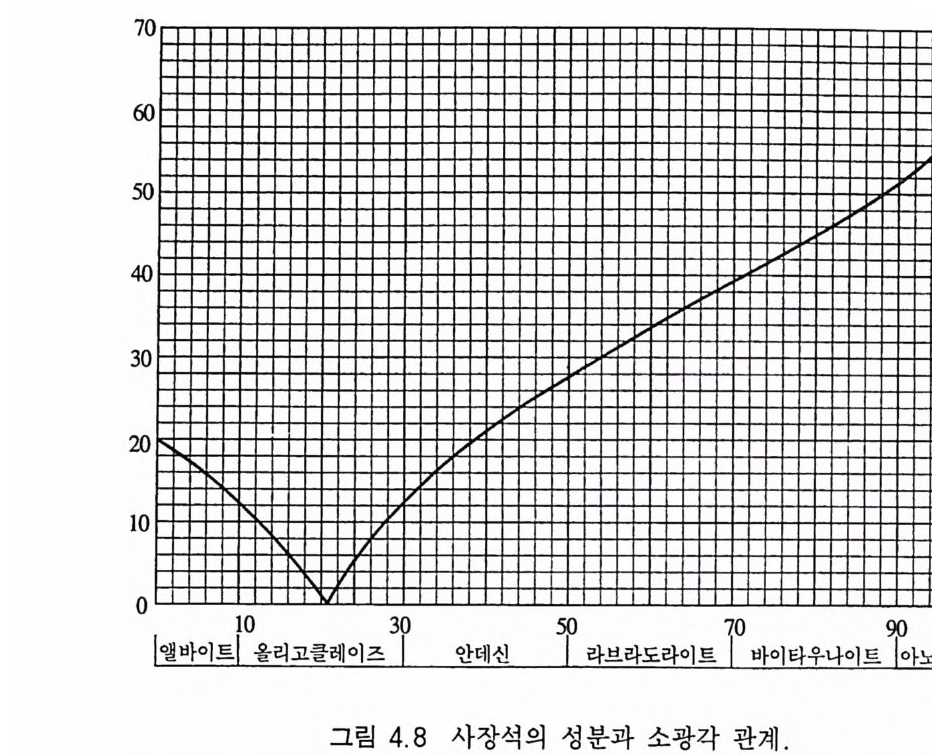 70
70
94.27, {3=1 16.61, y=8 7.69° 비중 2.617 양각낮음 굴절률 a=l. 52 7~1 .53 3, {3=1.53 1~1 .53 7, y=1.53 8~1 .54 2. 복굴 절률 =0.009~0.011. 간섭색은 1· 백색 내지 황색이다 광학부호 이축성, (+) 소광특징 앨바이트 쌍정을 지니는 입자는 최대 12~19° 의 소광각을 나타내며(그림 4.8), (001 ) 벽개를 따라 깨진 입자는 3~5°, (010) 에 나란한 입자는 15~20· 의 소광각을 가진다. 쌍정 {01 이면이 쌍정면 구실을 하는 앨바이트 쌍정이 거의 항상 발달한다(그림 4.9). 칼스바드 쌍정 ([001] =쌍정축)과 페리클라인 쌍
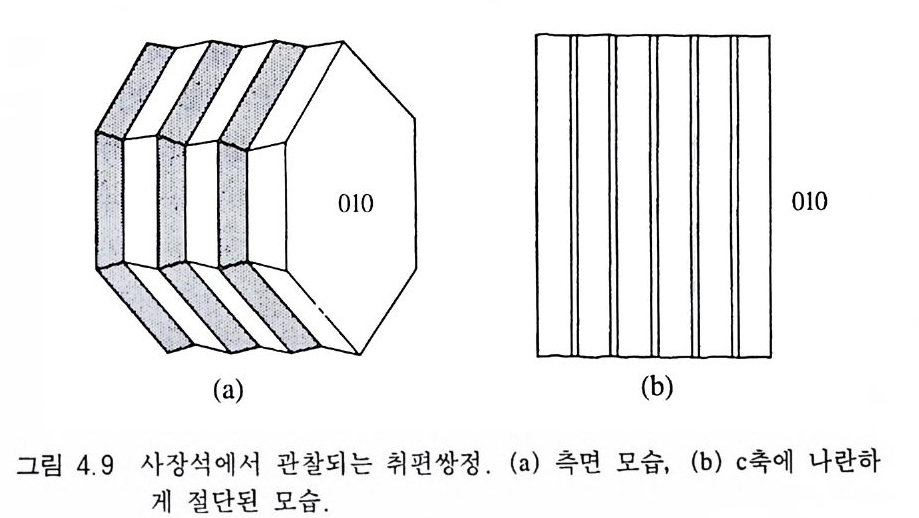 010
010
정 ([01 이=쌍정축) 또는 앨바이트 쌍정이 함께 존재할 수도 있다(그 립 4.5 ) . 간섭상 이축성, (+). 2V 77~82° X 선 회절선 6.3 7 ( 1), 4.03(1 0 ), 3.66(6), 3.50( 1), 3.22(6), 3.2 0 (5), 3.1 9 (5), 3.1 7 (2), 3.1 5 (5), 2.964(2)A 기타사항 앨바이트는 화강암, 화강암질 페그마타이트, 사장석 맥, 변성암 등에서 발견된다. 【올리 고클레 이 즈 (Ol ig oclase) 】 화학성분 An10- JO 결정계 삼사정계. cI 비중 2.62~2.65 양각낮음 굴절률 a=l. 53 3~1 .54 3, /3=1.53 7~1 .54 8, r=1.54 2~1 .55 1. 복굴 절률 =0.008~0.009. 간섭색이 1· 회색 내지 백색이다.
소광특징 앨바이트 쌍정을 나타내는 입자는 최대 0~12° 의 소광 각을 가지며 (그림 4.8 ) , (001) 방향의 벽개를 나타내는 입자는 0~3°, {010} 방향의 벽 개 를 지 니 는 입 자는 0~ 15 ° 의 소광각을 가 진다. 쌍정 앨바이트의 경우와 동일함 광학부호 이축성, (+) 또는 (-) 2V 82~90° 기타사항 화강암, 유문암, 섬장암, 조면암 등에서 산출된다. 화 강암질 페그마타이트와 일부 변성암에도 있다 . 【안데 신 (Andesin e )> 화학성분 An .lO냉 양각낮음 굴절률 a= l.543 ~ 1.554, /3= 1.5 48 ~ 1.55 8, y= 1.55 1 ~ 1.56 2 . 복굴 절률 =0 . 008. 간섭색은 1· 회색 또는 백색임. 소광특징 앨바이트 쌍정을 가지는 입자는 최대 소광각 13~27.5° 를 나타내며, (001 ) 벽개면을 따라서는 0~7°, (Ol0) 벽개면을 따 라서는 0~16° 의 소광각을 나타낸다. 광학부호 이축성, (+) 또는 (-) 2V 76~90° 기타특징 화성암 중 특히 섬록암과 안산암에 많이 포함되어 있다. 【라브라도라이 트 (Labradori te) > 화학성분 Allso-10 양각낮음 비중 약 2.70 굴절률 a=l. 55 4~1 .56 4, {3=1.5 58~1 .56 9, r=1.56 2~1 .57 3. 복굴
절 률 =0.008 ~0.009 소광특징 앨바이트 쌍정을 가지는 입자의 경우 최대 소광각이 27.5~39 ° 이다 . (001) 벽개를 지니고 있는 경우 7~16°, (010) 벽개 인 경우 16~29° 이다 . 광학부호 이축성, (+) 2V 76~90° 쌍정 앨바이트의 경우와 동일하다. 기타사항 반려암, 현무암 등의 주요 조암광물이다 . 산청군 일대 의 회장암 내에서 많이 산출하고 있다. 쌍정면 또는 벽개에서 일 어나는 빛의 간섭 또는 회절현상에 의해 청색 또는 녹색을 띠는 변종이 있는데, 이들은 보석 원석으로 쓰이며, 핀란드가 대표적인 생산국이다 . 【바이 타우나이 트 (B yt ow nit e) 】 화학성분 An,0-9 0 양각낮음 굴절률 a=l. 56 4~1.573, /3= 1.5 6 9~1 .57 9, r=1.57 3~1 .58 5. 복굴절 률 =0.009~0.012. 간섭색은 1· 회색, 백색, 또는 옅은 황색이다. 소광특징 앨바이트 쌍정을 나타내는 결정은 최대 소광각이 39~51° 이며, (001 ) 벽개를 지니는 입자에서는 16~32°, (010) 벽개 를 나타내는 입자는 29~36° 이다. 쌍정 앨바이트의 경우와 동일 광학부호 이축성, (-) 2V 79~88° 기타사항 반려암, 회장암, 현무암 등에서 산출된다.
【아노르다이 트 (Ano rthit e) 】 화학성 분 An90-100 결정계 삼사정계. Pl. a=8.1 8 , b=12.88, c=14.17A, a=93°l0, /3=l 15°5l, r=9 1°13 양각보통 굴절률 a=l. 57 3~1 .57 7, /3=1.5 79~1 .58 5, y=1.5 85~1 .5 90. 복굴 절률 =0.012~0.013. 간섭색은 1° 회색, 백색 또는 황색이다. 소광특징 앨바이트 쌍정을 하는 결정은 최대 소광각이 51~70° 이 며 , (001 ) 벽 개 를 나타내 는 입 자는 32~40°, (010) 벽 개 를 나타내 는 입자는 37° 이다 쌍정 앨바이트와 동일함 광학부호 이축성, (-) 2V 77~79° 기타사항 아노르다이트는 다른 사장석 광물에 비해 산출 빈도가 매우 드문 편이다 . 일부 접촉 변성암이나 화산암에서 발견된다 . 각 섬석을 함유하고 있는 암석이 열변성작용을 받게 되면 다음 방정식 과 같이 앨바이트와 아노르다이트, 그리고 휘석이 만들어진다. NaC 파 v1 g 3Fe•2ALS i 60 끄 (OH)z + 4 Si0 2 ~ NaAIS iJ이 + caAhSh08 각섭석 앨바이트 아노르다이트 + CaMg Sh 06 + Mg zF eSiJ O , + ILO 투휘석 휘석 4. 3 . 1. 3 준장석군 (FELDSPATHOID GROUP) 준장석군(準長石群)에 속하는 광물에는 네펠린 (ne p be li ne), 칼시 라이트 (kals ilit e), 류사이트(l eu cit e), 소달라이트 (sod alit e), 멜리라이 트 (mel i l it e), 칸크리나이트 (canc ri n it e) 등이 있다. 이들은 S i 04 와 Al04 사면체로 연결된 망상구조(綱狀構造, fr amework) 를 하고 있으
며, 이산화규소 성분이 적은 마그마로부터 만들어진다. 네펠린과 칼시라이트는 동일한 결정구조로 되어 있지는 않지만, 모두 육각 환형구조로 되어 있으며 사면체의 중심에 있는 S i의 절반이 Al 으 로 치환되어 있다. 사면체들 사이에 알칼리족 원소가 위치하여 전 체적으로 전하가 균형을 이룬다 . 그런데 이 위치에 있게 되는 K+ 와 N 硏 이온은 크기가 다르므로 이로 인해 전체적인 결정구조는 다소 변형되어 있다. 류사이트는 사면체(四面 體 , t e t r a hedron) 로 이루어진 사각 또는 육각 환형구조( 六角還型 構造)가 서로 교차 연결된 결정구 조 를 하고 있으며, 사면체의 중심 l/3 이 AI 이온으로, 2/3 가 Si 이 온으로 채워져 있다. Al·. . 이 S i-I+를 치환함에 따른 전하 결손을 K+ 이 온이 사면체 틈 사이에 위치하여 전기적 중성을 유지해 준다. 【네 펠 린 (Nep he li ne )> 화학성분 (Na, K) (AI, Si) zO ~ 결정구조 육방정 계 . Pfo . a=9.957, c=8.353A( 그림 4.10) 색 백색 또는 옅은 황색 . 박편하에서는 무색이다. 결정형태 짧은 육방주 형태를 취한다. 박편 관찰시에는 직사각 형 또는 육각형 형태로 나타난다 . 벽개 {1 010} 을 따라 양호한 벽개가, {0001} 을 따라 불량한 벽개 가 발달한다. 경도 5.5~6 비중 2.55~2.66 양각 매우 낮음 굴절률 e=l. 52 7~1 .54 3, (J)=1.53 0~1 .54 7. 복굴절률 =0.003~0.004. 간섭색은 1° 회색이다. 소광특징 직사각형 형태인 결정에서는 평행소광, 기저면을 따라 절단된 경우는 항상 소광한다.
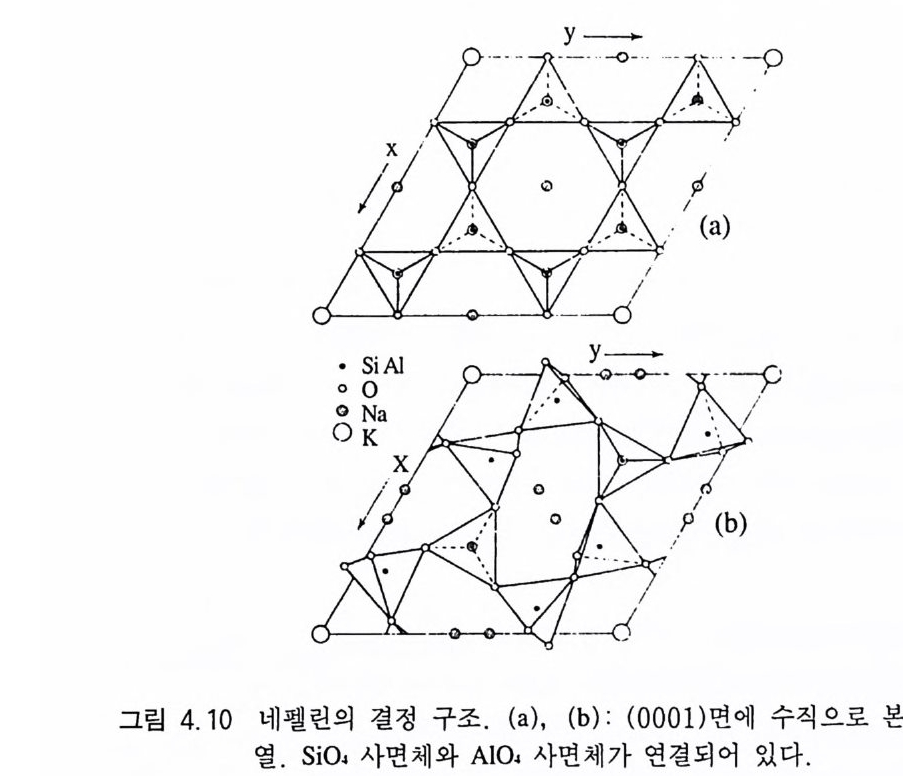 y ,
y ,
광학부호 일축성, (-) 장축부호 직사각형 입자의 긴 쪽을 따라 빠른 광선이 위치한다. (-) . 간섭상 기저면을 따라 절단된 경우는 일축성 간섭상을 나타내 며, 아이소크롬은 없다. X 선 회절선 4.33( 1), 4.19(4), 3.83(6), 3.26(5), 3.00(1 0 ), 2.88(4), 2.33(4), 2.3 0 (2)A 기타사항 네펠린은 Na 성분이 많은 섬장암, 포놀라이트에 많이 산출하며, 일부 현무암에서도 관찰된다. 네펠린은 불석, 소달라이 트, 백운모, 칸크리나이트 등으로 변질된다.
【칼시 라이 트 (Kals il it e) 】 화학성분 KA!Si0 4 . Na iO 성 분이 2~5% 함유되 어 있다. 결정구조 육방정 계 . P6J 2 2. a=S.1 6 , c=8.7 0 A 색 백색 경도 6 비중 2.60~2.63 양각 매우 낮음 굴절률 £=1.5 3 2~1 .53 7, (J)=1.53 8~1 .54 3. 복굴절률 =0.005~0.006 . 벽개 {1010}, {0001} 방향의 불량한 벽개가 있음 . X 선 회절선 4.35( 1), 3.97(4), 3.12(1 0 ), 2.58(5), 2.4 7 ( 1), 2.4 3 (1 ), 2.2 l (l )A 기타사항 네펠린과는 X 선 회절분석으로 구별될 수 있다. 칼시라 이트는 규산염 성분은 적고 칼리 성분이 많은 화산암의 주요 조암 광물로 발견된다 . 【류사이트 (Leuc it e) 】 화학성분 KA!Sh06 결정계 정방정계 (l4 J a), a=l3.0, c=l3.7A. 625°C 이상에서는 등 축정계 (Ia3d) 이며 a=l3.4A 이다. 사각 환형구조와 육각 환형구조 (그림 4 .1 1) 의 결합으로 되어 있다 . 색 백색 또는 회색. 박편하에서는 무색이다 . 결정형태 {211 } 편방체 모양의 자형 결정으로 산출되는 경우가 많다. 박편하에서는 8 각형 모양을 나타낸다. 양각보통 굴절률 E=1 .50 8, co=1 .50 9. 복굴절률 =0.001 . 벽개 {110} 방향의 불량한 벽개가 발달한다. 소광특징 파동소광을 나타내는 경우가 빈번하다 .
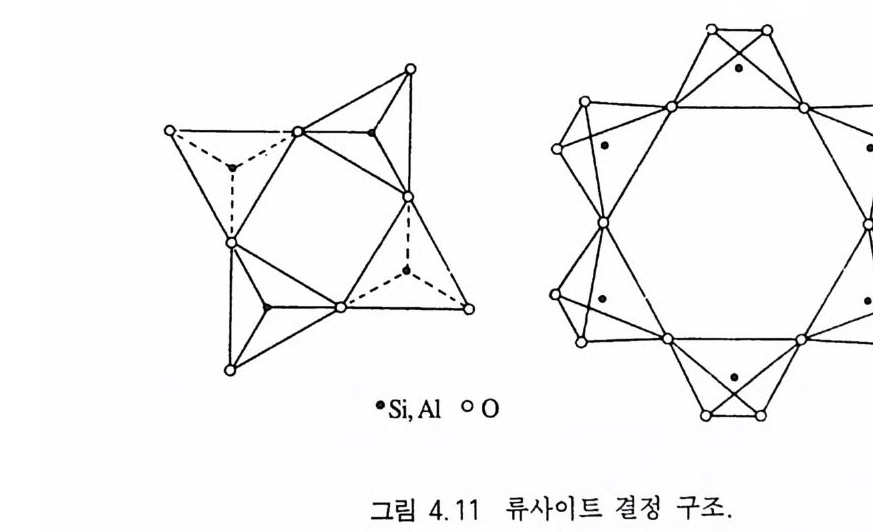 •Si, A l O 0
•Si, A l O 0
쌍정 여러 방향으로 반복적인 취편쌍정을 나타내어 미사장석과 홉사한 경우가 있다. X 선 회절선 9.5 ( 4), 5.54(4), 5.3 9 (5), 4.75(4), 4.3 4 (2), 3.78(3), 3.60(4), 3.60(4), 3.52(3), 3.44(8), 3.27(1 0 ), 3.0 9 (3), 3.04(3), 2.9 1 8(7), 2.842(7)A 기타사항 류사이트는 칼리 성분이 많은 화산암(바사나이트, 현무 암, 테프라이트)에서 반정으로 발견된다. 간혹 류사이트가 칼리 장 석과 네펠린으로 완전히 교대되거나 류사이트의 가장자리가 칼리 장석과 네펠린의 혼정물질로 싸여 있는 경우가 있는데 이를 슈도 류사이트(p seudoleuc it e) 라고 한다. 【소달라이 트 (Sod alit e) 】 화학성분 NacAL(S i O ◄ )z CI 결정계 등축정계, P43n. a=8.91A. 거의 같은 수의 S i 04 와 Al04 사면체가 연결되어 있는 망상구조를 지니고 있다(그림 4.1 2 ). 모
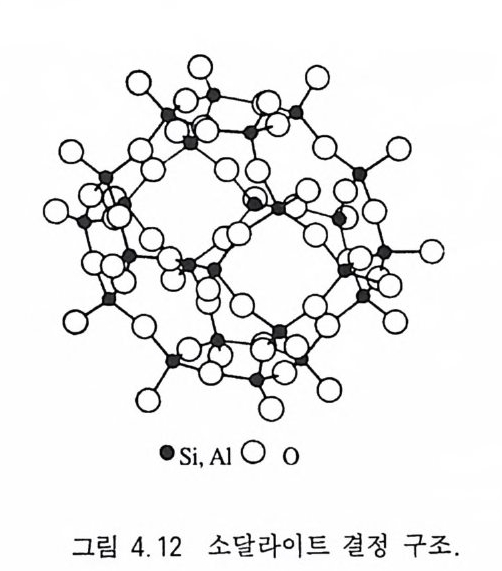 •si,A I O 0
•si,A I O 0
서리에 있는 산소 원자는 각각 두 개의 사면체와 공유(共有)하고 있다. 결정형태 육면체 색 청색, 회색, 녹색, 분홍색, 백색 . 박편하에서는 무색 또는 회색이다 . 벽개 {110} 방향의 불완전한 벽개가 발달함 양각보통 경도 5.5 ~ 6 비증 2.27~2.3 3 굴절률 1.4 83~1.4 8 7 소광특징 교차니콜하에서 항상 소광이다. X 선 회절선 6.3 0 (8), 4.45(4), 3.63(1 0 ), 2.81(5), 2.5 7 (7), 2.3 8 (7), 2.10(8), t.99 (3), t.89 (3), t.81 4(3), t.56 9(6), t.52 3(4)A 기타특징 네펠린 섬장암, 조면암처럼 Na 성분이 많은 화성암에 서 주로 산출되며, 네펠린뿐만 아니라 칸크리나이트, 멜리나이
트, 형석 등과 공존하는 경우가 많다. 【멜리 라이 트 (Mel ilit e) 】 화학성분 (Ca, Na)2[Mg , Fe+2, Al, Si]J 0 1 결정계 정 방정 계, P421m. a=7.8 , c=5.0A 결정형태 짧은 정방주 색 옅은 황색, 갈색, 녹갈색 . 박편하에서는 무색이다 . 경도 5~6 비중 2.95~3.05 벽개 {001 } 양호, {110} 불량 양각 다소 높음 굴절률 £=1.61 6~1 .66 1, (J)=1.62 4~1 .6 66. 복굴절률 =0.001~0.013 소광특징 평행소광 장축부호 길쭉한 방향을 따라 느린 광선이 진동함. (+) 광학부호 화학 성분에 따라 일축성, (+) 또는 (-) 기타사항 멜리라이트는 게레나이트(g ehlen it e) [C ai AhS i O 기와 아커 마나이트 (akerm anit e) [C 파 M gS ii O 기의 고용체이다 . Al 대신 M g의 치환 양이 많아질수록 굴절률과 비중이 감소한다 . 광학부호도 (-) 에서 (+)로 변한다. Ca 대신 Na 의 치환 양이 증가하면 굴절률이 낮아진다. 네펠린 현무암의 주요 조암광물이다. 멜리라이트는 시 멘트의 클링커 슬래그에서도 발견된다. 【칸크리 나이 트 (Canc ri n it e) 】 화학성분 (Na , Ca) 여 (Al6S i 60 미 (COJ , S04, Cl) ]1 s .2.o · 1~5 H20 결정계 육방정계. Pfo . a=12.9 7 , c=5.3 0 A 색 무색, 백색, 옅은 청색, 옅은 황색, 옅은 적색. 박편하에서 는무색
벽개 {1010} 을 따라 양호한 벽개가 발달한다 . 양각보통 굴절률 c= l.49 6~ 1.5 00, (J)= l.5m~ 1.52 4, 복굴절률 =0.007~0.028. 간섭색은 1° 황색에서 2· 색까지 올라간다 . 소광특징 결정면이나 벽개면에 나란한 평행소광을 나타낸다. 장축부호 벽개 방향을 따라 빠른 광선이 진동한다. (-) 광학부호 일축성, (-) X 선회절선 6.5(7), 4.85( 10 ), 4.20(6), 3.7 2 (1 0 ), 3.255(1 0 ), 2.779(9), 2.631 (8), 2.446(1 0 ), 2.280(4), 2.1 9 1(3), 2.1 2 4(1 o )A 기타사항 네펠린 섬장암에서 발견된다 . 네펠린뿐만 아니라 사장 석, 미사장석, 소달라이트 등의 광물과도 공생한다. 4. 3. 1. 4 감람석군(O LIVINE GROUP) 감람석군(橫藍石群)에 속하는 광물로는 포르스테라이트 (for ste r ite ) , 페이알라이트(fay al it e), 테프로아이트(t e p hro it e), 크네 벨라이트 (knebel it e), 그로코크로아이트(g laucochro it e), 몬티셀라이 트 (mon ti cell it e), 키르크스타이나이트(kir chs t e init e) 등이 있는데, 구 조화학식인 (A, B)2S i 04 에 어떤 금속원소가 A 와 B 에 자리잡는지에 따라 결정된다(표 4.2). 감람석군에 속하는 광물들은 모두 사방정계의 결정구조를 지니 고 있으며, [SiO s ]-1 - 다면체둘이 6 개의 산소원자로 둘러싸인 M~, felt 에 의해 연결되어 있는 독립사면체 구조를 하고 있다(그림 4.1 3 ). 기타 가능한 양이온으로는 Ca , Mn, Ni 등이 있으나 실제 이들의 존재량은 매우 제한적이다. 가장 일반적으로 산출되는 감람석 광 물은 포르스테라이트와 페이알라이트의 고용체(固溶體, soli d solu ti on) 인데 이를 감람석이라고 한다. 감람석은 염기성 마그마가 서 서 히 냉 각되 면서 정 출되 기 때문에 마그마 내 에 있던 Mg 1+( 0.66A)
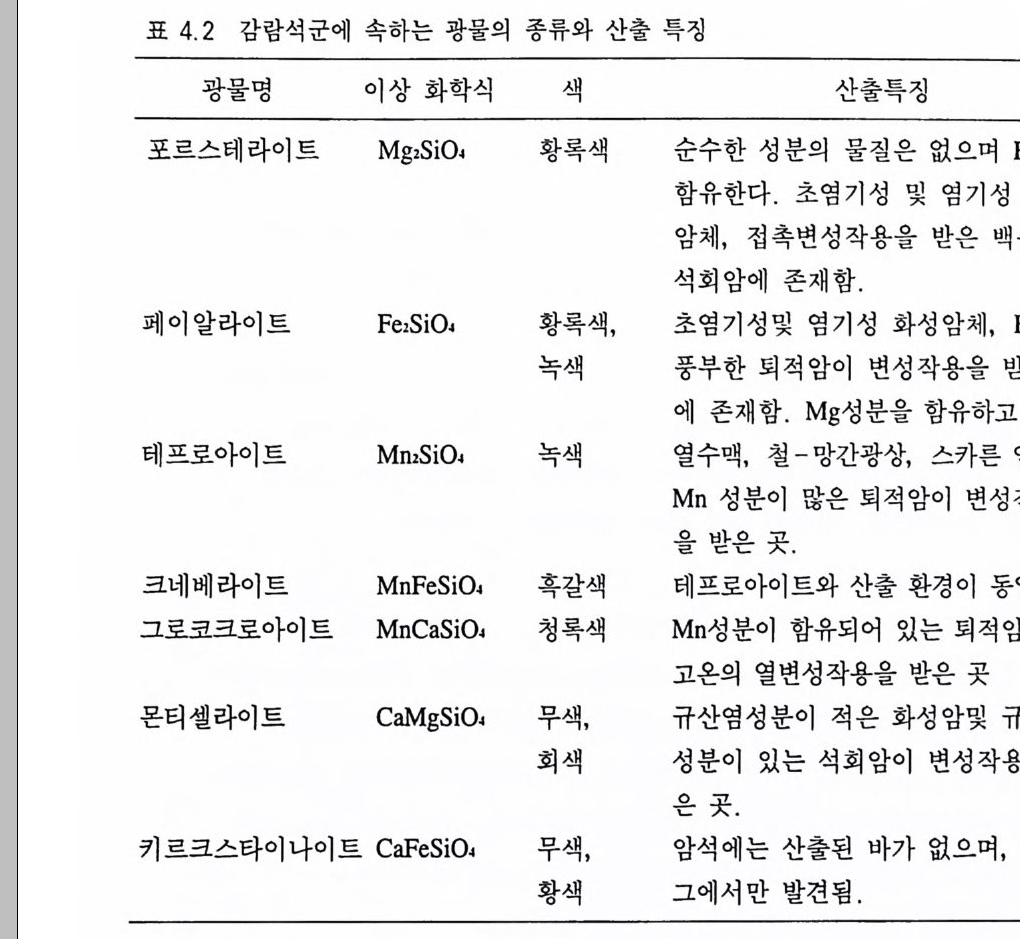 표 4. 2 감람석 군에 속하는 광물의 종류와 산출 특징
표 4. 2 감람석 군에 속하는 광물의 종류와 산출 특징
와 Fe i. (o.76A) 가 거의 자유롭게 서로 치 환한다. 따라서 그 화학성 분은 (Mg , Fe)2S i O 로 표현된댜 즉 감람석은 포르스테라이트 (Po) 와 페이알라이트 (Fa) 를 단종(端種, endmember) 으로 하고 있는 고 용체로서 그 성분비를 간단히 Fo 또는 Fa 로 나타낸다. 예를 들 면, Fo80( 또는 Fa20) 은 그 감람석 내 에 포르스테 라이 트 성 분을 80mol% 함유하고 있다는 의미이다. 이는 페이알라이트 성분을 20mol% 함유하고 있다는 뜻을 동시에 내포하고 있다. 감람석이
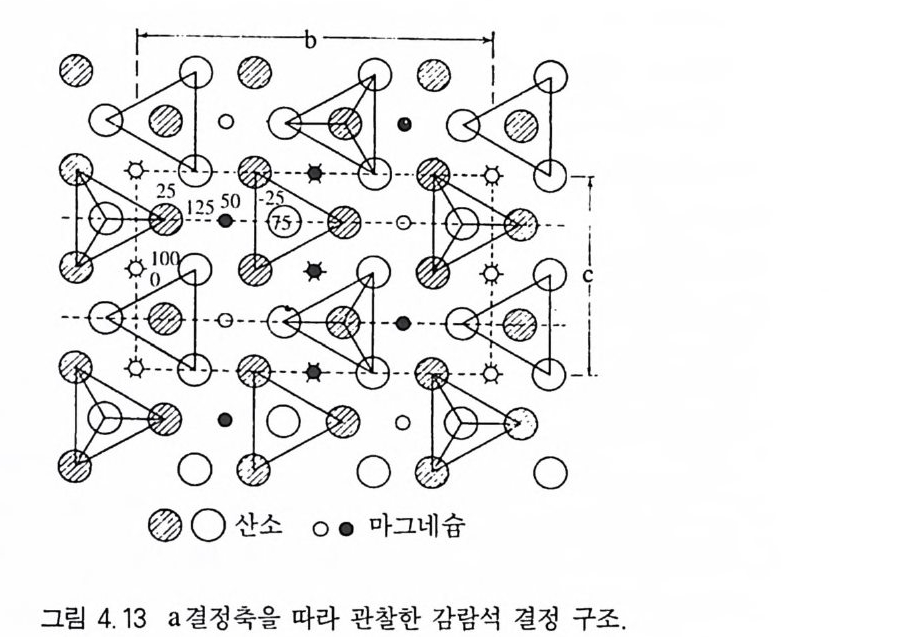 _1 -
_1 -
정 출 되는 환경에서의 Ca 함량은 지하 심부의 거대한 마그마 내에서 는 1000p pm 이하이며, 암맥(岩脈 d y ke) 이나 암상(岩床 sill ), 용암 ( 瑢器 la v a) 처럼 지표에 가까워져 냉각되는 마그마 환경에서는 그 함량이 5000 pp m 까지로 증가한다. Ca 성분은 마그마 내에서 규산 염 성분의 활동 능력을 좌우하며, 감람석이 정출하는 동안 사장석 도 함께 정출하는지의 여부에도 영향을 미친다. 감람석 내의 Fe 함량이 많아질수록 Mn 함량도 증가하나 Ni 성분은 감소한다. 이 것은 M g와 N i은 마그마 정출 초기에 만들어지는 감람석에 들어가 며, Fe 와 Mn 은 비교적 나중에 만들어지는 감람석 내에 들어가는 경향이 있기 때문이다. Co 의 함량은 일반적으로 매우 적다 . 한편 Pel>, Cr-3 +, All+, T i-I+와 같은 원소의 함량도 매우 적은데, 그것은 이들 이온이 M g 2+ 와 Fe 2+ 를 다수 치환할 경우 전체적인 산화수의 불균형 울 초래하기 때문이다. 그러나 다수의 감람석 화학분석 자료를 보
면 소량의 C 戶 ,Fek 가 항상 포함되어 있는데 그 이유는 감람석이 정출된 후 서서히 냉각되는 과정에서 이들 원소가 산화물의 형태 로 용리된 채 감람석 내에 포함되어 있기 때문이다 . 실제로 감람 석의 (001) 과 (1 00) 면을 따라 이들의 미세한 팔면체 결정들이 관 찰 되고 있다 . 순수한 성분의 포르스테라이트는 1890 ° C 에서, 페이알라이트는 l205°C 에서 정출된다. 이온 반경이 작은 양이온이 산소와 결합할 때의 원자결합력(原子結合力)이 이온 반경이 큰 원자의 경우보다 세기 때문에 정출온도(晶出溫度)가 높다(즉, 녹는점이 높다). 감람 석의 경우, M g”가 Fe 2+에 의해 점이적으로 치환되기 때문에 페이 알라이트 성분에 가까워 질수록 정출 온도가 낮아진다 . 이 때문에 염기성 마그마로부터 처음 정출되는 감람석에는 Mg 성분이 많으 며, 그 결과 잔류용액에는 Fe 성분이 많아지게 된다 . Mg 2 ~Fe2• 간의 교대(交代, subs tituti on) 가 일어날 때는 완전한 열역학적 평형 상태가 유지된다 . 간혹 현무암과 같은 화산암 내에 대상구조(帶狀 構造, zonal s tru c tu re) 를 나타내는 감람석이 발견되는 경우가 있는 데, 이때 중심부가 가장자리보다 항상 Mg 성분이 높다. 감람석은 열수(熱水, hy dr oth e rmal solu ti on) 에 의해 쉽게 변질되 며 , 저 변성 작용 (低變成作用, low -g rad e meta m orp h is m ) 에 도 쉽 게 영 향을 받는다. 또한 풍화작용(風化作用)에도 매우 약하다. 감람석 이 변질되면 사문석, 이딩사이트(i dd i ng s it e), 볼링가이트 (bowli ngite) , 녹니석 (chlori te) , 각섬석군 광물, 활석, 마그네사이트 등이 만들어 진다. 감람석에 미치는 외부 요소(온도, 압력)에 따라 앤티고라이트, 크리소타일, 라이자다이트 등의 사문석 동질이상체 (同質異像體, pol ym orp h ) 중 어떤 광물이 형성되는지가 결정된다. 이와 함께 활석(滑石)이나 탄산염 광물(炭酸鹽鑛物)이 수반되는 경 우가 일반적이며, 그 생성 반응식은 아래와 같다.
3 Mg 2S i O~ + H20 + Si0 2 -)2 Mg JS hOs(OH)~ 감람석 사문석 2 Mg JS iz O s(OH)4 + 3 CO 己 Mg JS i4 0 1o(OH) z + 3 Mg C OJ + 3 ILO 사문석 활석 마그네사이트 순수한 포르스테라이트 성분을 지니는 감람석은 아직 발견된 바 가 없다. 듀나이트 (dun it e) 를 구성하는 감람석은 대략 Fo92 의 성분 을 지니고 있으며, 페리도타이트의 감람석은 Fo88 이다. 반려암이나 현무암에서 산출되는 감람석의 성분은 Foss-Fo° 정도이다. 페이알 라이트 성분을 지니는 감람석은 석영을 함유하는 섬장암에서 주요 조암광물로 산출된다. 포르스테라이트에 가장 근접한 성분을 가지 는 감람석은 열변성작용(熱變成作用, hea t me tam o rphi sm) 을 받은 석 회암(石灰岩, li mes t one) 이나 백운암(白雲岩, dolo mit e) 에서 산출되 며, 이때의 생성 방정식은 다음과 같다. 2 CaM g (CO J)i +S i 02 크 M g 2S i 04+2 CaCOJ + 2 CO2 백운석 포르스테라이트 감람석은 성분에 따라 물리적 성질(굴절률, 광축각, 벽개, 비 중, 색깔, 단위포 상수 등)이 연속적으로 변하는 특징을 나타낸다. 굴절률은 그림 4 .1 4 와 같이 Fe 성분이 중가함에 따라 커진다. 즉 Fe2S iQ 4 의 단위 mol% 당 따斗 #f절률이 0.002 정 도 증가한다. 광축 각 (2V) 역시 82° 에서 134° 로 증가하며, Fau 을 기준으로 광학부호가 (+)에서 (-)로 바뀐다. 벽개의 경우, Mg 성분이 많을 때는 불량 한 {010} 벽 개 가 발달하지 만, Fe 성 분이 많아지 면 {010} 벽 개 뿐만 아니라 {100} 벽개도 훨씬 더 양호하게 발달한다. 비중도 Fe 성분 의 증가에 따라 3.2~4 .3으로 커지며, 감람석의 색깔 역시 Fe 성분
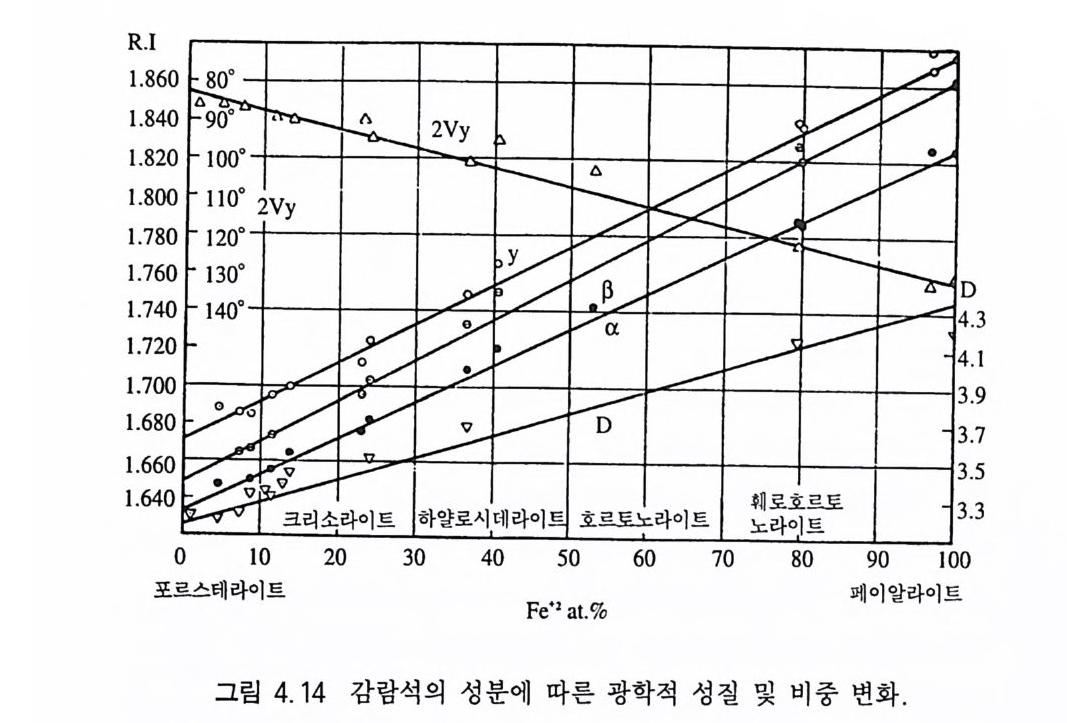 R.I
R.I
이 많아질수록 녹색이 짙어진다. 녹색의 투명한 감람석 변종을 페 리도트(p e ri do t)라 하며 보석 원석으로 사용된다 . 【포르스테 라이 트 (Fors t e rit e) 】 화학성분 Mg 2S i 04 결정계 사방정계. Pbnm. a=4.75, b=l0.20, c=5.98A 색 녹황색, 황록색. 박편하에서는 무색 결정형태 자형 결정은 짧은 주상(柱狀) 형태이지만 매우 드물다. 대부분 타형 결정으로 산출된다. 암석 내에서 조암광물로 산출될 때는 자형, 반자형으로 존재하는 경우가 많다. 벽개 불완전한 {010} 벽개가 발달한다. 경도 6.5
비중 3.2 7 양각 비교적 높다. 굴절 률 a= l.635 ~ l.64 0, /3= l.65 l ~ 1.6 6 0, y= 1.6 7 0~ 1.6 8 0 . 복굴 절률 =0.035~0.040. 최대 간섭색은 2· 등급의 분홍색이다. 광학부호 이축성, (+) 소광특징 결정면이나 벽개에 나란한 평행소광을 나타낸다. 장축부호 벽개가 있는 경우 그 방향을 따라 느린 광선이 진동한 다 (+) 광축각 85~90° 간섭상 이축성 간섭상을 나타내며, 광죽면온 (001) 면이다. X 선 회절선 5.1 0 (5), 3.88(7), 3.4 7 (2), 2.76(6), 2.512(7), 2.4 5 800), 2.3 4 7(2), 2.2 6 9(4)A 기타사항 순수한 성분의 포르스테라이트는 발견되지 않으며 Fa 성 분을 18mol% 정도 함유하고 있다. 금운모(金 雲母 , p holog o pit e) 가 함께 공존하는 경우가 많다. 【페 이 알라이 트 (Fa y al it e) 】 화학성분 Fe2SiO ~ 결정계 사방정계. Pbnm. a=4.82, b=l0.4 8 , c=6.09A 색 연녹색 또는 녹색 . 박편하에서는 무색 내지 옅은 황색을 띤 다. 미약한 다색성이 있다. 결정형태 포르스테라이트와 동일하나, 자형(自形) 결정으로 산출 되는 경우가 거의 없다. 벽개 {010} 와 {10 0} 방향의 양호 또는 불량한 벽개가 발달한다. 경도 6.5 비중 4.3 7 양각 매우 높다.
13。100} j0윤1 - 페사,0라'엔브A로 방o’9 이'페0트 로 二二二/7 실00트 석 라엔변 신 匡 이 환트 _ I,一 l클」 단匡 사`리` 엔노 《C、의 어_ 하 스止자 해이요터`o결 Mn一匡떄 한핍泊卵 트에臼닷呼 \100트亨 5 파 90이휘로트석 사어50|,Ill Li스·1트 포트 변듀t 종민어/단알사칼 경휘리에 옥석A휘l지4 석 ]문 란 _,.합 。 유I匡 。 } 。· 트 .._ 스터타0 LK`0 Or} K` r。 트
l0 그림 4.1 5 휘석군의 분류. 굴절률 a=l. 80 5~1 .83 5, {3=1 .838~1 .87 7, y=1.84 7~1.886. 복굴 절 률 =0.042~0.051 소광특징 벽개에 나란한 평행소광을 한다. 광학부호 이축성, (내 장축부호 벽개 또는 결정면을 따라 느린 광선이 진동한다. (+) 광축각 47~54° X 선 회절선 5.23(4), 4.38(2), 3.98(5), 3.78(2), 3.55(8), 3.05(4), 2.828(9), 2.630(5), 2.5 6 5(7), 2.so1 (10 ), 2.410(s)A 4. 3. 1. 5 휘석군 (PYROXENE GROUP) 휘석군(輝石群)에 속하는 광물은 사방정계 또는 단사정계의 결정구조를 지니는데 이 때문에 사방휘석류(斜方輝石 갖Ji , o rt hopy roxene) 와 단사휘석류( 單斜輝石갖頁, cl i nopy roxene) 로 구분한다 . 휘석군에 속하 는 광물은 규소와 산소 원자로 이루어진 사면체가 산소 원자를 공유 하면서 마치 줄 (cha i n) 처럼 일직선 형태로 연결되어 있는데, 이를 단쇄상 구조( 單鎖狀構造 , sin g l e -chain s t ruc t ure) 라 한다. 휘석군에 속하는 광물에 대하여 결정구조 및 화학성분에 따라 분류한 도표 가 그림 4 .1 5 에 있다. 휘석군에 속하는 광물의 일반화학식은 XYZ206 로 표현될 수 있 다 (X=Na , Ca, Mg , Fe2+, Mn2+, Ni, Li; Y=AI, Fe2+, Mn2+, Mg , FeJ+ , C~. Ti . .. ; Z=Si, AI ). X 는 배위수가 6 또는 8 인 M2 위치이며, Y 는 배위수가 6 인 8 면체 중심에 위치한 M1 자리이다. Z 은 배위수가 4 인 사면체 의 중심에 위치한다 . 휘석의 화학식은 산소의 원자수 6 을 기준으 로 계산한다 . Z 위치는 일단 S i와 Al 으로 완전히 채워지며 FeJ+도 사면체 속에 들어갈 수 있다 . Al 의 존재량과 위치는 휘석의 생성 환경 조건에 따라 좌우된다. Al 은 일반적으로 8 면체 배위를 하는 Y 에 들어가지만, 규산염의 활동농도 (s ili ca ac ti v ity)가 낮은 마그마 내에서는 배위수가 4 인 Z 에 위치한다 . 압력도 영향을 미치는데, 압 력이 높을 경우 Al 은 배위수가 6 인 8 면체의 배위다면체 중심에 위 치하려고 한다 . M g와 Fe 원소간의 치환은 매우 용이하지만, Na 과 Ca, 혹은 (Mg , Fe”) 와 (Fel+ , Al) 사이의 치환인 경우는 Ca(Mg , Fe) +--+Na(Fe J+ ,Al) 처럼 쌍쌍치환이 일어나게 된다 . 휘석은 M2 위치에 있는 원소에 의해 분류되는 것이 일반적이며 (표 4.3), 광물명 뒤에 공간군(空間群, s p ace gr ou p)이 하나 이상 표 기되어 있는 것은 동질이상체가 있음을 의미한다. 사방휘석과 단 사휘석 결정구조의 예가 그림 4 .1 6 과 그림 4 .1 7 에 있다. 이들은 2 회 회전축인 b 축을 따라 투영한 것이다. 사방휘석의 a 단위포 상 수는 단사휘석의 경우보다 약 2 배가 된다.
 표 4.3 휘석의 화학성분과 결정 구조 .
표 4.3 휘석의 화학성분과 결정 구조 .
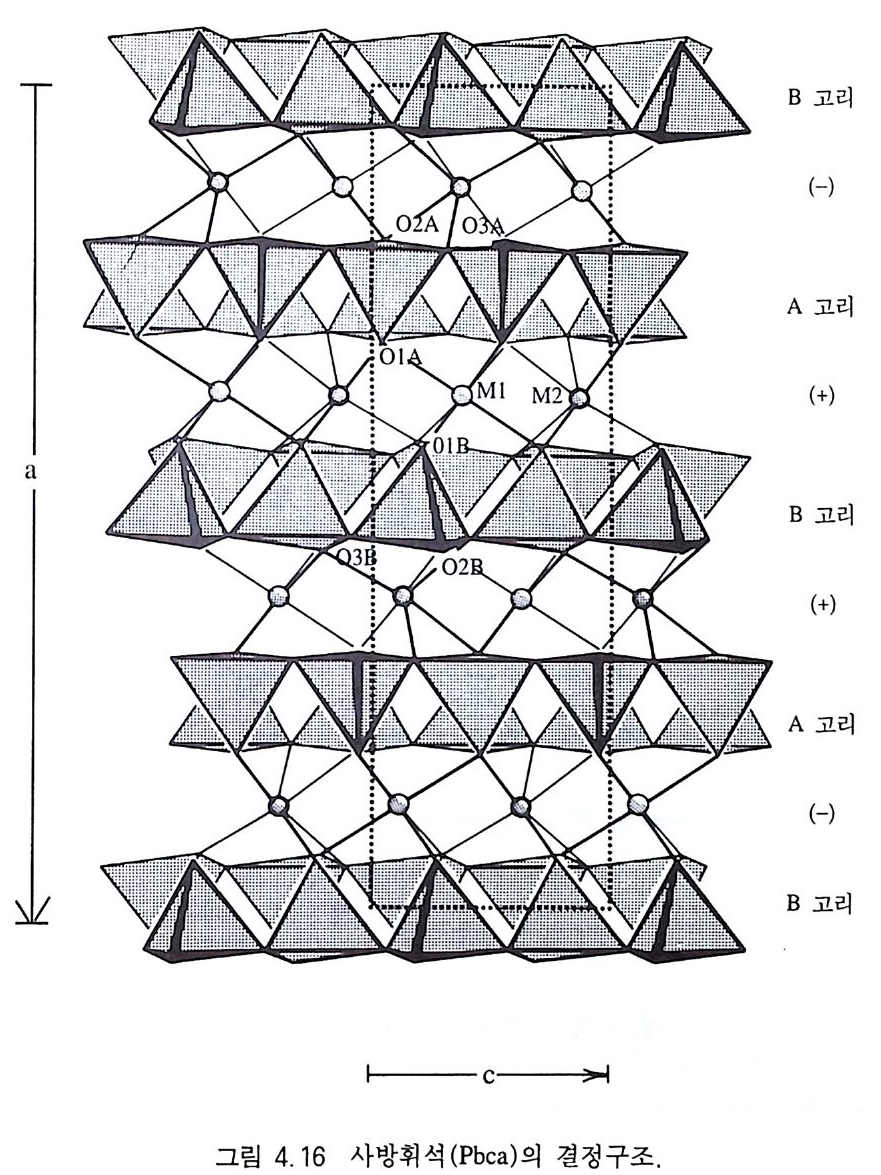 B 고리
B 고리
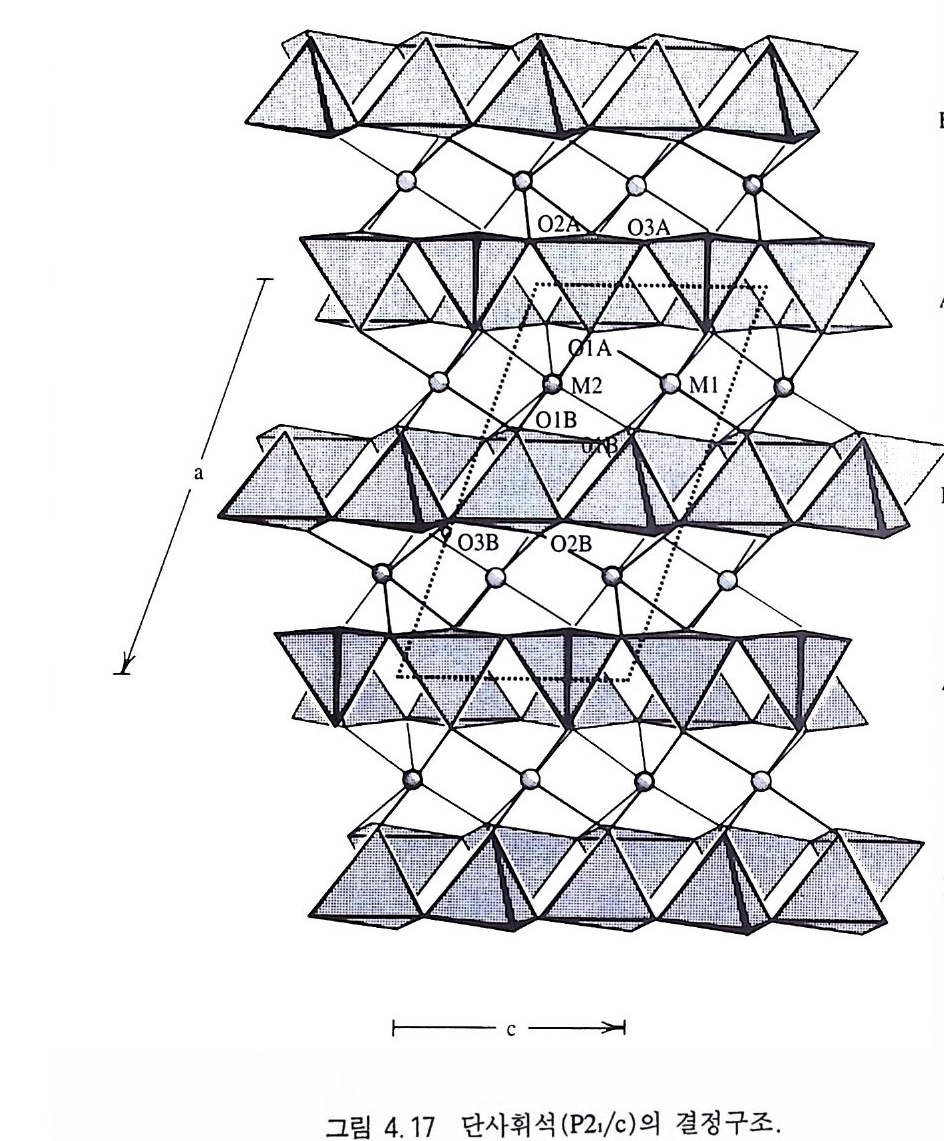 B 고리
B 고리
사방휘석의 경우, 광학적 특징이 화학성분의 변화와 밀접한 관 계가 있다(그림 4.18). 굴절률이 직선에서 다소 벗어나는 경우가 있는 것은 Al 성분이 들어있기 때문이다. 사방휘석을 분쇄하면 {210) 벽개를 따라 깨지므로 굴절률 감마(y)를 용이하게 측정할 수 있다. 따라서 굴절률 측정을 통해 M g/F e 의 성분바를 결정할 수 있 다 . 광축각 (2V) 은 M g과 Fe 의 중간 성분을 기준으로 대칭이 된다. 엔 스터 타이 트와 올소페 로실 라이 트 (orth o fe r rosil it e ) 는 광학부호가 (+ ) 이지만, 중앙 부분에 있는 광물들은 (-)이다. 브론자이트와 하이퍼신은 다색성 ( 多 色性, p leochro i sm) 이 뚜렷한데, 이는 Fe 타과 Al 이 치환되어 있기 때문이다. 사방휘석은 복굴절률이 작고, 평행 소광을 하는 점이 단사휘석과 다르다. 마그마로부터 정 출되 는 대 부분의 휘 석 은 투휘 석 (dio p si d e , Di ) CaMg S i2 0 6, 헤덴버가이트 (hedenber git e, Hed) CaFeSii 06 , 엔스터타 이 트 (ens t a tit e, En) M g2S i 20 6, 페 로실 라이 트(fe rros i l it e, Fs) Fe2Sh06 로 표현되는 그림으로 나타낼 수 있다(그림 4.1 9 ). 톨레아이트질 마그마(t hole iti cma g ma) 로부터 휘석이 정출될 때, 마그마 내의 규산 염 활동농도 (s i l i ca ac ti v ity)에 따라 아래의 반응식 에 의해 감람석 대 신 더 안정한 사방휘석(單斜輝石)이 생성된다. Mg 2S i O ~+Si0 2 =2 Mg S iO J 감람석 용액 엔스터타이트 톨레아이트질 마그마는 단사휘석 (C 2/ c) 인 어자이트 (au git e) 와 함 께 사방휘석 (Pbca) 인 브론자이트 (bronz it e) 가 함께 정출되어 두 가 지의 휘석이 만들어진다 . 한편, 이 두 가지 휘석의 정출이 계속되 면 잔류용액에 Fe 가 점점 풍부하게 되고, 마침내 사방휘석 대신 단사정 계 (P2i/ c) 인 피 지 오나이 트(pig eo nit e) 가 어 자이 트와 공존하다
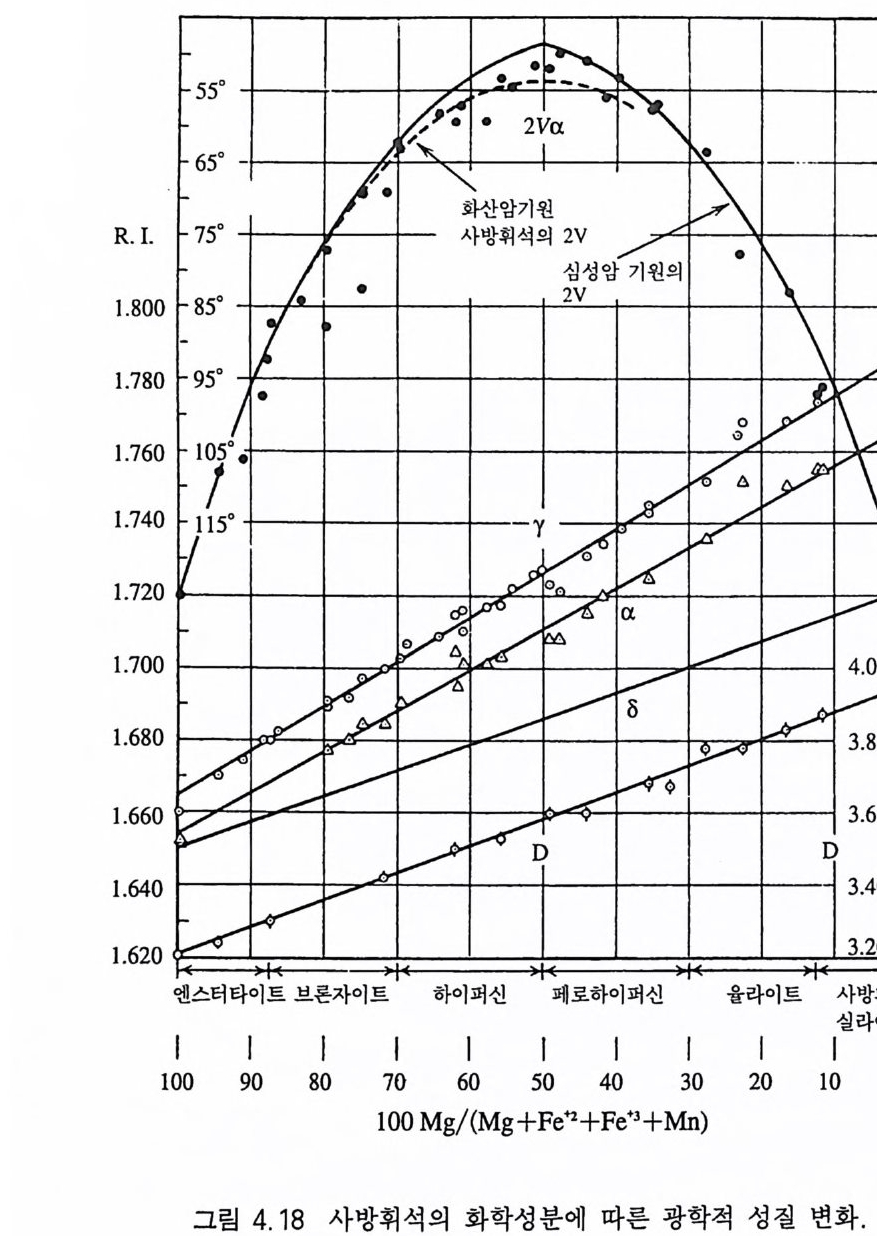 55°
55°
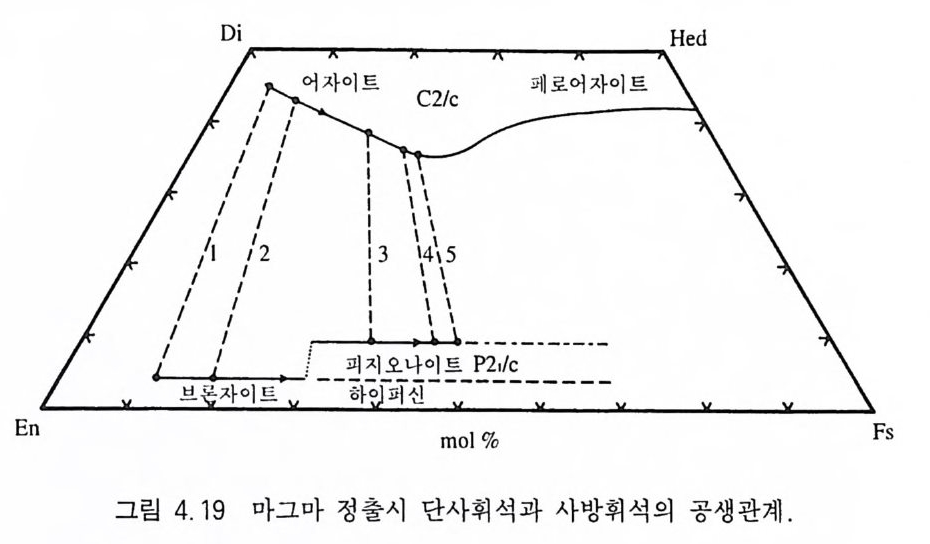 D1
D1
가, 마침내 철 (Fe) 성분이 많은 페로어자이트(fe rroau git e) 가 정출되 게 된다(그림 4.1 9 ). 이러한 예는 유명한 스케어가드 관입암체 (Skaerga a rd i n t rus i on) 에서 관찰된다. 즉, 이 관입암체( 貫入岩體) 중 초 기에 정출된 부분에는 CaHMg 4sF e ,o 성분의 단사휘석(어자이트)과 Ca4Mg ,sF e,s 성 분의 사방휘 석 (브론자이 트) 이 공존하고, 이 보다 후기 에 형성된 암체에는 CaJs M g 31 F e2s 성분의 단사휘석(어자이트)과 Ca9M g 4sF e46 성분의 피지오나이트(단사휘석)가 공존하고 있음이 확 인되 었다. 마그마의 분화작용(分月 1 j晶出作用, mag m a dif fere nti at io n ) 이 더 진행되면 페로어자이트 하나만 정출되다가 결국 헤덴버가이 트가 정출되게 된다. 이와는 대조적으로, 알칼리 현무암질 마그마 (alkali b asalt m ag m a) 가 냉 각될 때 는 투휘 석 (diop s i d e ) 같은 단사휘 석 만이 정출될 뿐, 사방휘석이나 피지오나이트와는 절대로 공생하지 않는다. 여기서는 사방휘석 중 엔스터타이트와 하이퍼신, 단사휘석은 투 휘석, 어자이트, 피지오나이트, 헤덴버가이트, 에지린, 제이다이
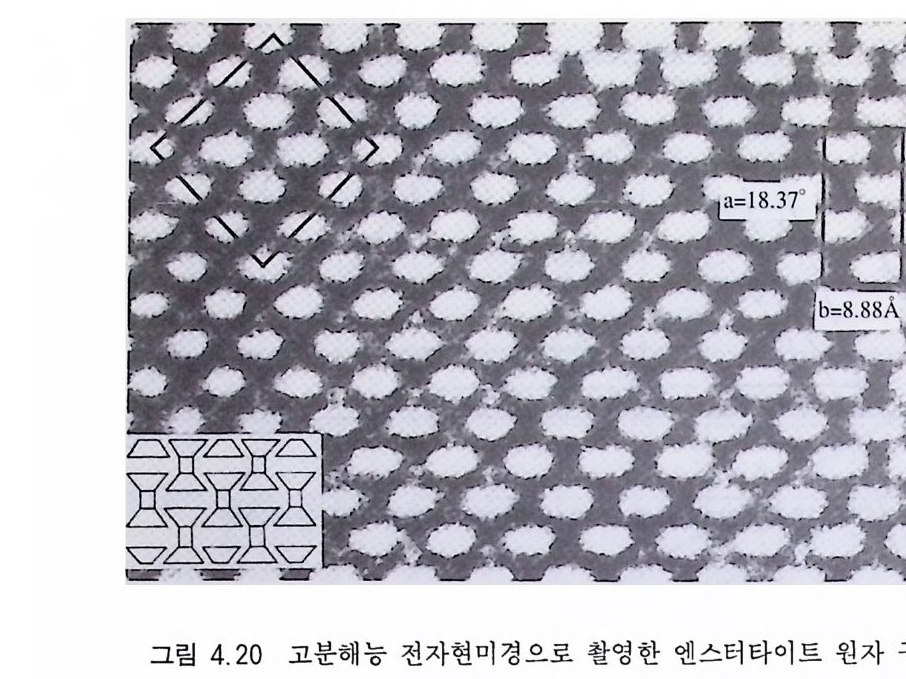 ,. . : . ,
,. . : . ,
트, 스포듀민 등 암석 중에서 주요 조암광물로 산출하고 있는 광 물에 대해 기술하기로 한다 . 【엔스터 타이 트 (Ens t a tit e) 】 화학성분 (M g I 마 90Fe().,o)S i O J 결정계 사방정 계 . Pbca, a= 18.2, b=8.8, c=5.2A( 그림 4.2 0 ) 색 회색, 황색, 녹색 등 다양하지만, 박편하에서는 무색이다. 결정형태 자형은 주상(柱狀) 형태이지만 이런 결정 형태로 산출 되는 경우는 매우 드물다 . 괴상이나 엽상 형태가 일반적이다 . 그러 나 박편하에서는 주상 결정의 한 단면이 관찰되는 경우가 많다. 벽개 {111 } 방향을 따른 두 방향의 벽개가 거의 직각 (88°, 92°) 을 이룬다 . {010} 방향에 나란한 한 방향의 벽개가 발달하기도 한다.
주상형태의 결정에서는 벽개가 항상 장축 방향에 나란하다 . 경도 5.5 바중 3.2 양각 높다. 굴절률 a=1.6 5 0~1.665, /3=1 .6 5 3~1 .67 0, y=1.6 58~1 .67 4. 복굴 절률 = 0 . 008~0.009 . 최대 간섭색은 1° 황색이다. 소광특징 대부분 평행 소광을 나타내며, c 축에 수직으로 절단되 어 두 벽개를 나타내는 경우는 대칭소광을 한다 . 장축부호 벽개나 장축의 결정면을 따라 느린 광선이 진동한다. (十) 광학부호 2V=58~80°. 이축성, (+). 광축면은 (010) 이다. X 선 회절선 4.4 1 (2), 3.30( 1), 3.17(7), 3.1 5 (5), 2.8 7 0(1 0 ), 2.530(2), 2.4 6 8( 1) A 기타사항 엔스터타이트는 다색성이 거의 없는 점이 하이퍼신과 다르며, 단사휘석과는 평행소광하는 점이 다르다 . 엔스터타이트는 앤티고라이트로 변질되는데, 원래의 엔스터타이트 결정 형태가 보 존되어 있을 때는 이를 배스타이트 (bas tit e) 라고 부른다. 【하이 퍼 신 (Hy pe rsth e ne)> 화학성분 (Mg 111 - s oFe.JO .SO )SiO J 결정계 사방정계. Pbca. a=18.3 2 5, b=8.918, c=5.216A 색 황색, 녹색 . 박편하에서는 무색 내지 옅은 녹색, 또는 옅은 적 색을 띤다. 다색성이 있으며, 옅은 녹색에서 적색으로 변한다. 결정형태 엔스터타이트와 동일하다 . c 축에 수직인 단면온 정방 형에 가깝다. 벽개 엔스터타이트와 동일함 경도 6
비중 3.6 양각높다 . 굴절 률 a= l.67 3 ~ 1.71 5, {3= 1.6 7 8 ~ 1.72 8, y= 1.68 3 ~ 1.73 1 . 복굴 절률 =0.010~0.016. 최대 간섭색은 1° 황색 또는 적색이다 . 소광특징 장축 방향을 나타내는 결정은 평행소광을, c 축에 수직 인 입자는 대칭소광을 나타낸다. 장축부호 장축 방향을 따라 느린 광선이 진동한다 . 광학부호 이 축성, (-) . 2V=63~90° X 선 회절선 4.57( 1), 4.03(2), 3.18(1 0 ), 2.960(3), 2.883(5), 2.835(2), 2.121 (2) , 2.555(4), 2.510(3), 2.4 8 4(3)A 기타사항 다색성이 있는 점이 특징이다. 염기성 화성암인 노라 이트 (no rite ) 와 반려암의 주요 조암광물이며, 안산암이나 화강암에 서도 간혹 발견된다 . 【투휘 석 (Di op s id e )> 화학성분 Ca(Mg , Fe) (SiO J )i. CaO 25.9%, Mg O 18.5%, Si0 2 55.6% 결정계 단사정계. c'21c . a=9.76, b=8.92, c=5.25A, {3=1 05.79° 색 백색, 연록색. 박편하에서는 무색, 옅은 녹색 동으로 보인다 . 결정형태 자형은 주상 결정이 대부분이며, c 축 방향으로는 정방 형 또는 8 각형 형태롤 취한다. 괴상 형태로도 산출되며, {001} 방 향의 취편쌍정도 발달한다. 쌍정면이 (1 00) 인 접촉쌍정도 빈번히 관찰된다. (110) /\ (110) =92°50' , (001) /\ (111 ) =33°50' , (111 ) /\ (111)=59°11', (001 )/\(10 0)=74°lff . 박편하에서는 짧은 주상 형 태로 존재하는 경우가 가장 많고, c 축에 수직으로 절단된 경우는 4 각형 또는 8 각형 모양을 한다. 경도 5~6
비중 3.2 벽개 {110} 에 나란한 벽개가 발달하며, 교차하는 두 벽개의 각 도는 8T 와 93 ° 이다 . 양각 높 은 편이다 . 굴절률 a= l.6 5 0~ 1.69 8, /3= 1.6 57~ 1.70 6, y= 1.68 1~ 1 .72 7. 복굴 절률 =0 . 029 ~ 0 . 03 1. 최대 간섭색은 2° 에 속한다. 소광특징 c 축 에 나란하게 절단된 입 자는 최 대 소광각인 37~440 경 사소광 을 하며, c 축 에 수직인 입자는 두 벽개가 대칭을 이루는 경 사소광을 한다 . 장축부호 벽개와 작은 각을 이루는 소광 위치에서, 장축 방향을 따라 느린 광선이 진 동한다 . (+ ) 광학부호 이축성, (+ ). 2V=58~60°. 광측면이 (010) 이다. {001} 에 나란한 입자는 양호한 광축중심 간섭상 (o pti c- ax.i s figu re) 을 나타낸다. X 선 회절선 3.3 5 ( 1), 3.2 3 (2), 2.9 9 (1 0 ), 2.9 5 2(2), 2.893(3), 2.566(2), 2.528(4), 2.5 1 8(3), 2.3 0 4(2)A 기타사항 투휘석은 헤덴버가이트와 완전고용체를 이루고 있으 며, M g와 Fe 의 치환정도에 따라 물리적, 광학적 성질이 연속적으 로 변한다 . 투휘석은 투각섬석( 透 角閃石, trem oli te) 또는 양기석(陽 起石, ac ti no lit e) 으로 변질된다. 투휘석은 석회질 암석이 열변성(熱 變 成)을 받은 접촉 변성암(接觸 變 成岩)에서 주로 발견되며, 광역 변성암에서도 발견된다 . 석류석, 규회석, 아이도크레이즈와 같은 광물과 공생하는 경우가 많다. 【어자이트 (Au git e) 】 화학성분 (Ca, Na) (Mg , Fe, Al) (Si, Al )20 6. 화학성분이 다소 변함.
 그림 4.21 어자이트 결 정 .
그림 4.21 어자이트 결 정 .
결정계 단사정계 . C2/c. a=9.783, b=8.9 6 5, c=5.272A, /3= l05.7 ° 색 짙은 녹색, 검은색 . 박편하에서는 무색, 옅은 녹색 , 옅은 청 갈색 등으로 보인다 . 누대구조( 累帶構造 )가 가끔 관찰된다. 다색성 은 없거나 매우 약한데, (100) 면을 나타내는 입자의 경우 다색성 이 가장 뚜렷하다 . 결정형태 주상 형태를 가지며 (그림 4.2 1 ) , 종단면은 4 각 또는 8 각 형태이다 . 박편하에서도 짧은 주상 형태나 8 각형의 입자로 관찰되는 경우가 많다 . 쌍정면이 {100} 인 접촉쌍정이 있으며, {001} 면이 쌍정 면 구실을 하는 취편쌍정도 발달할 수가 있는데 이를 특히 헤링본 구조 (herr ing b o ne stru c tu re) 라고 한다 . 경도 5~6 비중 3.2 ~ 3.4 벽개 {110} 의 두 방향 벽개가 발달한다. 교차각은 8T 와 93° 이다. 양각높다. 굴절률 a=l. 68 8~1 .71 2, /3=1.70 1~1 .71 7, y=l.71 3~1 .73 7. 복굴
절률 =0.021~0 . 025. 최대 간섭색은 2° 의 중간색이다. 그러나 {10 0} 에 나란한 면은 1° 의 낮은 간섭색을 나타낸다. 소광득징 장축 방향을 나타내는 입자에서는 최대 소광각이 36~45 ° 이다. 4 각 또는 8 각형의 입자는 두 벽개에 대한 대칭소광을 나타낸다 . 일부 입자에서는 모래시계 (hour g lass) 와 닮은 파동소광을 나타내기도 한다. 장축부호 작은 각으로 소광되는 위치에서의 벽개 방향을 따라 빠 른 광선이 진동한다. (+) 광학부호 이축성, (+). 2V=58~62°. 광축면은 (010) 이다 . X 선 회절선 3.21 (8) , 3.0 2 00), 2.908(8), 2.9 0 4(1 0 ), 2.578(6)A 기타사항 투휘석과 어자이트는 현미경에서의 특징이 유사하여 구별하기가 쉽지 않다. 어자이트는 반려암, 현무암, 페리도타이트 와 같은 화성암의 주요 조암광물이며, 편마암과 그래눌라이트 (gra nulite ) 같은 변성암에서도 발견된다. 투휘석은 마그마 고결 말 기(固結末期)에 각섬석으로 변하거나, 열수변질(熱水 變質 )을 받아 투각섬석이나 양기석으로 변한다. 【피 지 오나이 트 (Pig e on ite) > 화학성분 (Mg , Fe, Ca)(Mg , Fe)Sii 06 . CaSiO J 성분이 약 10% 함유 되어 있으며, 이는 일반화학식당 약 0.2% 의 Ca 원자에 해당한다. Al 의 함량이 다른 금속 원소의 2% 도 안되기 때문에 Al+S i의 합 (合)이 화학식에 있는 2 원자에 미달한다. 이 때문에 Fe 과 Ti 원자 가 4 면체의 배위다면체 내에 추가로 들어가게 된다. 화학성분은 M g과 Fe 의 치환에 의해 주로 변하는데, 현무암질 마그마로부터 처음 정출하는 피지오나이트는 M g :Fe=70:30 이지만, 분별정출작 용이 진행되어 감에 따라 그 비율이 35:65 로 변한다. 피지오나이 트의 정출은 이 단계에서 멈추게 되고, 그 대신 Ca 성분이 많은
페 로어 자이 트 (ferr oaug ite) 나 페 로헤 덴 버 가이 트 (fe r rohedenbergi te) 가 정출한다 . 결정계 단사정계 . P2J c. a=9.71, b=8.96, c= 5 .25A, /3=1 08.3 3 ° 색 녹갈색, 갈색, 검은색 . 박편하에서는 무색으로 보이며 , 약한 다색성이 나타난다. 결정형태 짧은 주상 결정형태를 지니지만, 타형으로 산 출 되는 경우가 많다 . 박편하에서도 타형의 입자로 흔히 관찰된다. 쌍정면 이 (1 00) 인 취편쌍정이 발달하는 경우가 많다. 경도 6 비중 3.3 ~ 3.4 벽개 {110} 에 나란한 두 방향의 벽개가 발달하며, 교차 각 은 87° 와 93• 이다. 양각 비교적 높다. 굴절률 a= l.68 0~ 1.71 8, /3= 1.69 8 ~ 1.72 5, y= 1.7 19~ 1.74 4. 복굴 절률 =0.021~0.033. 최대 간섭색은 2° 등급이다. 소광특징 최대 소광각은 22~45° 범위이다. 두 방향의 벽개가 있 는 경우 대칭소광을 나타낸다. 장축부호 벽개 방향의 장축을 따라 느린 광선이 진동한다 . (+) 광학부호 이축성, (+). 2V=O~40°. 광축면은 (010) 이다. X 선 회절선 4.62(2), 4.4 6 ( 1), 3.2 1 (8), 3.02(1 0 ), 2.908(8), 2.904(1 0 ), 2.578(6), 2.4 8 8(2), 2.4 5 9(2)A 기타사항 높은 온도에서만 안정하기 때문에 급냉한 현무암, 돌러 라이트 (dole rite), 휘록암(di abase) 등에서 발견된다 . 반정으로 존재 하는 경우는 매우 드물고, 석기에 나타난다. 만약 서서히 냉각하 는 마그마에서 피지오나이트가 만들어진 경우에는 {001 } 방향으로 어자이트가 용리되어 있는 현상이 관찰될 수 있으며, 결국 사방정 계의 결정구조로 변하게 된다 .
【헤 덴버 가이 트 (Hedenber git e) 】 화학성분 CaFeSiz 0 6. 투휘 석 (CaM gS iz 0 6 ) 과는 Fe 과 M g의 치 환에 의한 완전고용체를 형성한다 . 결정계 단사정 계 . C2/c. a=9.851, b=9.010, c=5.255A, /3= 104.82° 색 녹색, 갈록색, 암록색 . 박편하에서는 무색 또는 옅은 녹색으 로 보인다 . 결정형태 나무 그루터기 모양의 긴 주상 결정으로 산출된다 . 경도 6 비중 3.5 0 ~3.56 벽개 {110} 방향의 두 벽개가 발달함. 교차각은 8T 와 93• 이다. 양각 매우 높음 . 굴절률 a=l. 73 2~1 .73 9, /3=1.73 7~1 .74 5, y=l.75 1~1 .75 7. 복굴 절률 =O.Ol8~0.019. 최대 간섭색은 1· 보라색이다. 소광특징 장축 방향의 결정은 최대 소광각이 약 42• 에 이른다. 장축부호 벽개가 발달한 장죽의 입자의 경우 빠른 광선이 진동 한다. (- ) 광학부호 이축성, (+). 2V=60° X 선 회절선 6.55( 1), 3.27(2), 3.00(1 0 ), 2.9 0 7( 1), 2.583(2), 2.5 4 4(4), 2.238(1 ) A 기타사항 석회질 암석이 열변성작용을 받은 스카른 (skarn) 등의 접촉 변성암에서 주로 산출되며, 화성암의 경우 심장암이나 화강 암에서 간혹 관찰된다. 【에지 린 (Ae girin e) 】 화학성분 NaFe(SiO J ) z. Na i.O 13.4 %, FeO 34.6%, Si0 2 52.0% 결정계 단사정계 C'2 Jc . a=9.851, b=9.010, c=5.255A, /3= 104.82°
색 녹색, 암록색, 갈색. 박편하에서는 녹색으로 보이며, 다색성 이 매우 강하다. 결정형태 긴 주상 결정으로 주로 산출되며 끝이 좁아진다. 섬유 상 결정의 집합체로도 산출된다 . 얇은 도변상(刀邊狀) 형태로도 존 재한다 박편하에서도 긴 주상 결정 형태로 나타나는 것이 일반적 이며, c 축에 수직인 경우 4 각형 또는 8 각형의 입자로 나타난다. 경도 6~6.5 비중 3.4 0 ~3.44 벽개 {11 아 방향의 두 벽개가 발달하며 교차각은 8T 와 93° 이다 . 양각높다. 굴절률 a= l.74 5~ 1.7 77, {3= 1.7 70~ 1.82 3, y= 1.78 2~ 1.8 36. 복굴 절률 =0.037~0.059. 3° 또는 4• 의 최대 간섭색을 나타내지만, 짙은 녹색 때문에 간섭색이 잘 관찰되지 않는다. 소광특징 최대 소광각은 2~10° 범위에 있다. 장축부호 장축 방향을 따라 빠른 광선이 진동한다. (-) 광학부호 이축성, (-). 2V=60~66°. 광축면은 (010) 이다 . X 선 회절선 6.55(2), 3.0 0 (1 0 ), 2.583(3), 2.544(4), 2,238( 1), 2.1 4 9(2)A 기타사항 아크마이트 (ac mit e) 라고도 부른다 . 네펠린 섬장암과 같 이 나트륨 성분이 많은 화성암에서 산출되며, 비교적 드문 광물이 다. 정장석, 준장석류, 어자이트 등과 공생한다 . 【제 이 다이 트(Ja de it e) 】 화학성분 NaAI(SiO J ) 2. NazO 15.4 %, AhOJ 25.2%, Si0 2 59.4 % . Al 과 S i는 다른 원소에 의해 교대가 거의 일어나지 않기 때문에 대부 분의 제이다이트는 이상화학식에 가까운 화학성분을 지닌다. 결정계 단사정 계 . c'}jc . a=9.50, b=8.61, c=5.24A, /3= l07°26'
색 녹색, 백색, 갈색, 분홍색. 백색 바탕에 녹색 점이 있는 형 태가 일반적이다. 녹색이 짙은 경우는 다색성이 관찰된다. 결정형태 주로 입상질 조직의 괴상 형태로 나타난다. 주상 또는 섬유상 결정 형태로도 산출된다. 박편하에서도 입상, 주상, 또는 섬유상 형태로 관찰된다. 쌍정면이 (1 00) 인 접촉쌍정이 간혹 발견 된다. 경도 6.5 ~ 7. 다결정질 상태이므로 인성(忍性, t oug hness) 이 매우 강하다. 비중 3.3 ~ 3.5 벽개 {110) 의 두 방향 벽개가 발달하며, 교차각은 8T 와 93° 이 다. 주상 결정에서는 장축에 나란한 한 방향의 벽개가 발달한다. 양각높음 굴절 률 a= l.65 5 ~ 1.666, {3= 1.6 5 9 ~ 1.67 4, y= 1.66 7 ~ 1.688. 복굴 절률 =0.012~0.023. 2° 에 속하는 간섭색을 나타낸다. 소광특징 주상 결정의 경우 최대 소광각은 30~44° 이다. 장축에 수직으로 절단된 입자는 대칭소광을 한다. 장축부호 소광각이 작은 위치에서의 장축 방향을 따라 느린 광 선이 진동한다. (十) 광학부호 이축성, (+). 2V=70~75°. 광축면은 {010} 이다. X 선 회절선 6.22(2), 4.29(5), 3.10(3), 2.922(7), 2.831( 10 ), 2.4 9 0(2), 2.4 1 7(3)A 기타사항 경옥(硬玉)이라고 하며 일명 비취(器菜)라고도 한다 . 제이다이트는 저온 • 고압(低溫高壓) 변성환경에서 만들어진 변성암 에서만 발견된다. 앨바이트 사장석으로부터 제이다이트가 만들어 지는 환경은 그림 4.22 와 같으며, 그 생성방정식은 다음과 같다.
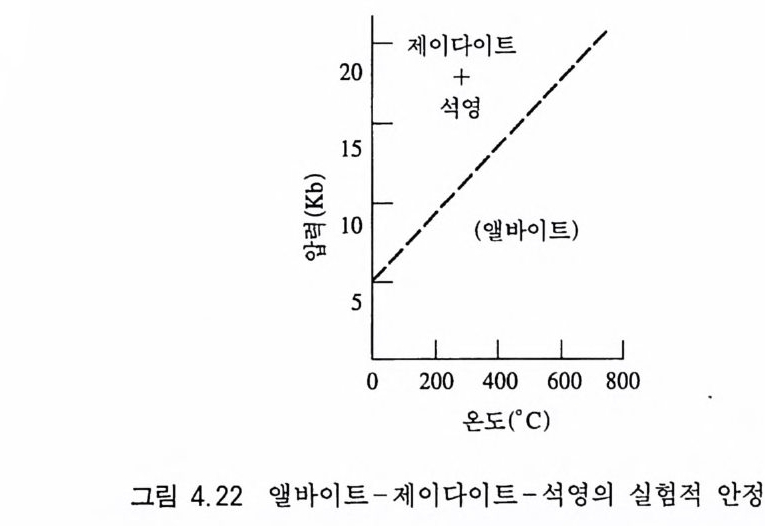 제이다이트 //
제이다이트 //
NaAIShOs ~ NaAISi2 0 6+Si0 2 사장석 제이다이트 석영 제이다이트는 알프스산맥, 미국 캘리포니아, 미얀마 복부지 방, 일본 등 대륙 지각의 연변부 근처를 따라 주로 분포한다 . 균 질한 녹색과 양호한 투명도를 지니는 제이다이트는 보석으로 가공 된다. 【스포듀민 (Sp o dum ine )> 화학성분 LiA I(S iO J )2, LhO 8.0%, A120J 27.4 %, Si0 2 64.6%. 소 량의 Na 이 L i을 치환할 뿐, 기타 성분 사이의 원소 치환은 거의 없어 이상화학식에 가까운 화학성분을 가진다. 결정계 단사정 계 . C2/c. a=9.52, b=8.32, c=5.25A, {3= 111°28' Z=4 색 백색, 회색, 분홍색, 황색, 녹색. 특히 투명하고 분홍색인 경우 쿤자이트 (kunz it e), 녹색인 경우 히데나이트 (h i dde nit e) 라고 하
는데, 이들의 색은 각각 Mn 과 Cr 에 의해 발색된다 . 박편하에서는 무색으로 관찰되지만, 두꺼운 박편인 경우는 다색성을 나타낸다 . 결정형태 주상 형태이지만, {10 0) 방향으로 납작한 문패상 형태 일 경우가 많다 . 결정 표면에는 수직 조선이 발달하는 점이 특징 이다 . (J OO) 면이 쌍정면 구실을 하는 쌍정이 발달한다. 경도 6.5 ~ 7 비중 3.03~3.20 벽개 {100} 에 나란한 두 방향의 완전한 벽개가 발달하며, 교차 각은 93 ° 이다 한편, {J OO) 방향의 열개(裂開 parti n g)가 벽개보다 더 현저하게 발달하기도 한다. 양각 비교적 높다. 굴절률 a=1 .6 51~1 .6 68, /3=1.66 5~1 .67 5, y=1.67 7~1 .68 1 . 복굴 절률 =0.013~0.027. 최대 간섭색은 1° 상위색 또는 2° 중위색이다 . 소광특징 주상 형태인 결정은 최대 소광각이 23~27° 이다 . 장축 에 수직인 단면은 두 방향의 벽개를 나타내는데, 이들은 대칭소광 을 보인다 . 장축부호 결정의 장축 방향을 따라 느린 광선이 진동한다 . (+) 광학부호 이축성, (+). 2V=54~69° X 선 회절선 6.12(3), 4.38(5), 4.21(6), 3.4 5 (4), 3.19(4), 2.93(1 0 ), 2.8 0 (8), 2.4 5 (6)A 기타사항 스포듀민은 Li 성분이 풍부하게 함유되어 있는 화강암질 페그마타이트에서 주로 산출되며, 앨바이트, 레피돌라이트, 전기석 과 같은 광물들과 공생한다 . 피탈라이트(p e t al it e), 레피돌라이트 (Iep ido lite ) , 앰블리고나이트 (ambl ygon it e) 등과 함께 L i의 광석 광 물로 사용되어 왔다. 특히 양질의 쿤자이트와 히데나이트는 귀한 보석광물로 취급되고 있다 .
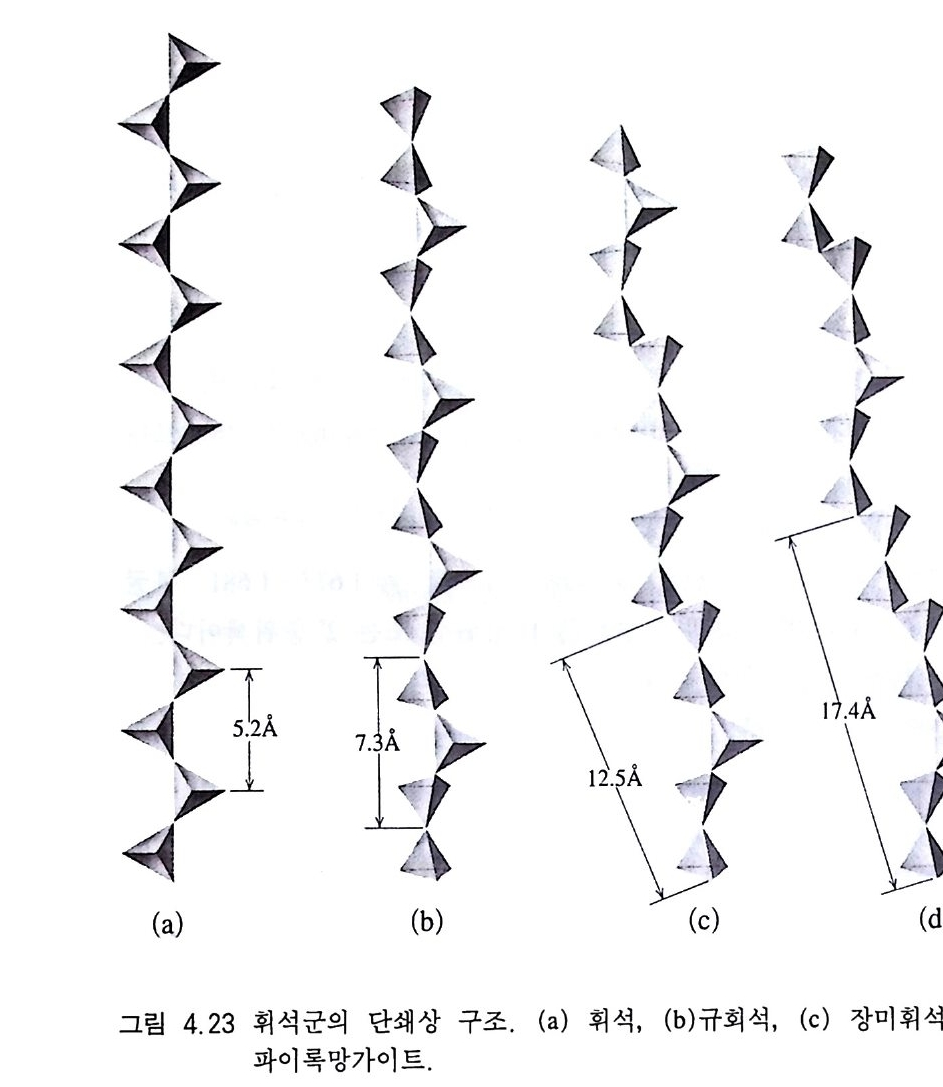 지지>i>/ ` :4군4 :’, 一} `r\ > :4}\~,\\ 4— ~~ ’자 4· 、 ~ rL\
지지>i>/ ` :4군4 :’, 一} `r\ > :4}\~,\\ 4— ~~ ’자 4· 、 ~ rL\
4. 3. 1. 6 준휘석군 (PYROXENOID GROUP) 휘석군 광물과 마찬가지로 S i :0=3:1 의 단쇄상 구조를 하고 있 으면서도 휘석군 광물의 구조와 다른 규산염 광물들이 있는데 이 를 준휘석군 광물( 準輝 石群 鑛 物)이라고 부른다. 준휘석군 광물에는
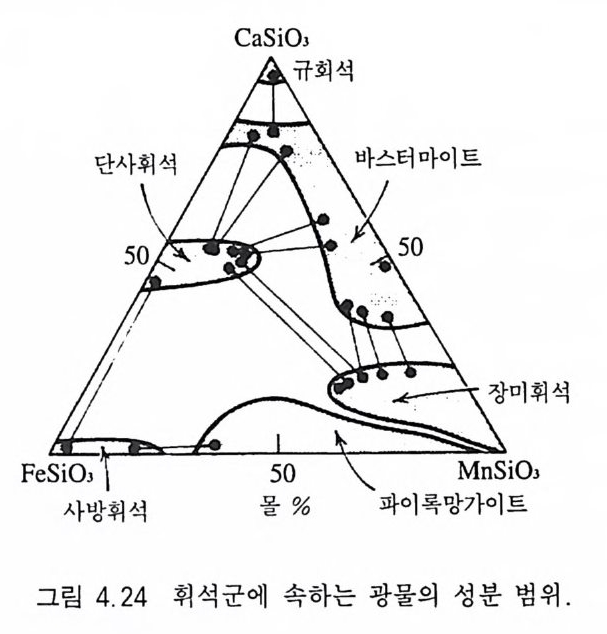 사방 휘석 몰 %
사방 휘석 몰 %
규회 석 (wollasto n it e, CaSiO J ), 장미 휘 석 (rhodonit e, MnSiO J ), 바스터 마이 트 [bus t am it e, (Mn, Ca, Fe) Si O J ], 펙 토라이 트[p ec t ol it e, Ca2NaH(SiO J )i ], 파이록망가이트[py roxman git e, (Mn, Fe)S i O 나, 세 란다이트 [serand it e, Na i(M n, Ca)4Si6 0 11 • ILO] 등이 있다 . 휘석군과 준휘석군 광물은 단쇄상 구조 사이에 배위수가 6 인 양이온이 있는 점은 공통이나, 휘석군의 광물에서는 c 축을 따라 Si0 4 사면체가 연 결되어 있고 그 반복 최소거리가 약 5.2A 이지만, 준휘석군 광물에 서는 Si0 4 사면체가 b 축을 따라 연속되는데 그 형상이 휘석에서처 럼 단순하지 않고 꼬여 있는 모습을 하고 있다(그림 4.2 3 ). 또한 b 축을 따른 반복 거리도 7.3A( 규회석), l2.5A( 장미휘석), 17 .4 A( 파이 록망가이트) 등으로 증가한다 . 준휘석군에 속하는 광물은 폭넓은 고용체를 형성한다(그림 4.24). 여기서는 조암광물로 산출 빈도가 높은 규회석, 장미휘석에
대해서만 기술하기로 한다. 【규회 석 (Wollasto n ite) > 화학성분 CaSiO J. CaO 48.3 % , Si0 2 51. 7% . Fe, Mn, Mg 등이 Ca 을 치 환할 수 있다. 특히 규회 석 은 CaSiO J - FeS i O J 의 고용체 를 형 성하는데 이 때문에 FeSiO J 성분을 76% 까지 함유할 수 있다. 결정계 삼사정 계 . Pl. a=7.934, b=7.3 3 4, c=7.0 7 5A, a= s9•55' , /3=9 5°22 ' , y= 103°26' . 규회 석 ( 珪灰石 ) 은 결 정 구조상 휘 석 군 광물들과는 상이하며, b 축을 따라 3 개의 사면체가 연결되어 있 는 단쇄상 구조를 하고 있다 ( 그림 4.23). 그러나 연결되어 있는 사 면체들의 배열방식이 휘석류 광물들과는 달리 변형되어 있어서, 반 복되는 최소 거리가 휘석류에서처럼 약 5.2A 이 아니고 7 .3 A 정도이 다. Ca 은 8 면체상 배위의 위치에 있으면서 단쇄상 구조 를 연결해 주고 있는데 이 점은 휘석군의 광물과 동일하다 . Z=6 색 무색, 백색, 회색, 박편하에서는 무색이다. 결정형태 납작한 주상 또는 섬유상 형태를 취한다. 괴상으로도 산출한다 . 경도 5~5.5 비중 2.8~2.9 벽개 완전한 {100} 벽개와 우수한 {10 1} 벽개가 발달한다 . 두 방 향의 벽개의 교차각은 840 이다 . 양각 비교적 높다 . 굴절률 a=l. 62 0, /3=1.63 2, y=1.63 4. 복굴절률 =0.014. 최대 간섭 색은 1· 주황색이다 . 소광특징 장축 방향을 나타내는 입자는 평행소광 또는 이에 거의 가까운 소광을 한다. 이에 수직인 단면은 경사소광을 나타낸다. 장축부호 장축 방향이 b 축이며, 이 방향을 따라 느린 광선 또는
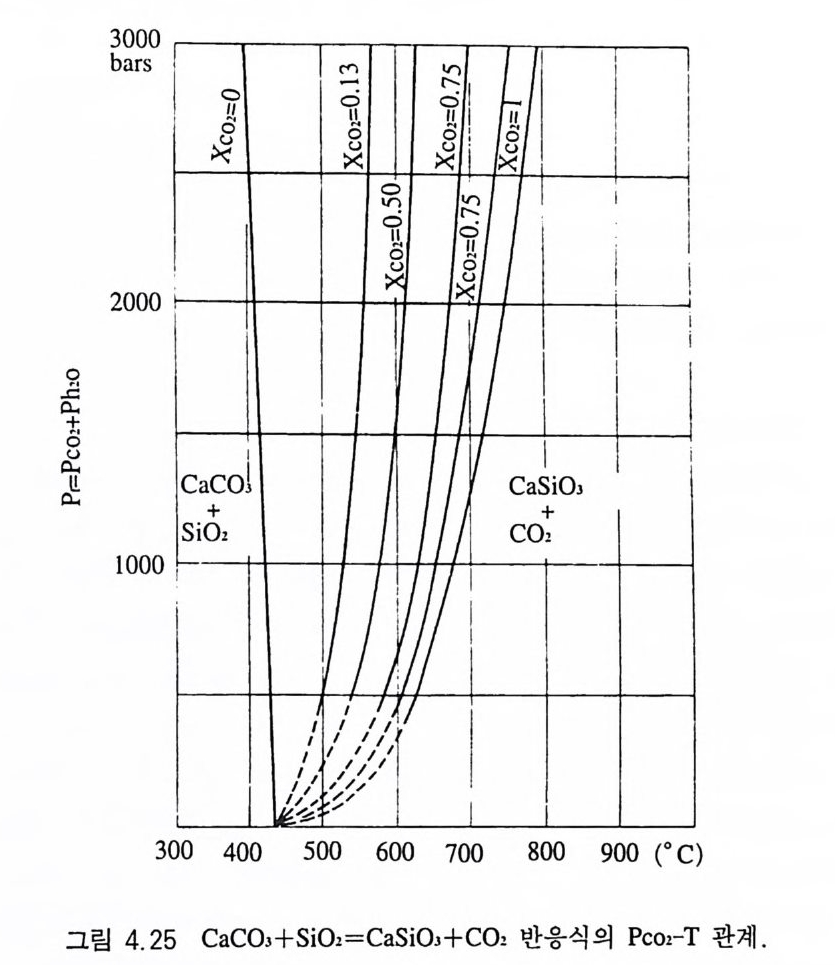 3b0ar0s0
3b0ar0s0
빠른 광선이 진동한다. 광학부호 이축성, (-). 2V=39°. 광축면은 (010) 이다. X 선 회절선 7.67(2), 3.83(8), 3.5 1 (7), 3.314(1 0 ), 3.086(6), 2.977(3), 2.721 (3), 2.5 5 6(4), 2.4 7 7(2), 2.3 4 0(3), 2.3 0 2(5)A 기타사항 규회석은 결정질 석회암인 대리암에서 주로 산출되 며, 방해석과 석영이 열변성작용을 받을 때 다음의 방정식으로 만 들어지며, 그 생성환경은 그림 4.25 와 같다.
CaCOJ + Si0 2 ― ➔ CaS i O J +C02 방해석 석영 규희석 또한, 석회질 성분을 함유하고 있는 퇴적암 내에 열수용액이 관 입하여 변성교대작용이 일으킬 때에도 생성된다. 공생하는 광물로 는 투휘석, 석류석, 투각섬석, 사장석, 녹렴석 등이다. 규희석은 요업원료, 비료원료로 쓰인다. 【장미 휘 석 (Rhodonit e) > 화학성분 MnSiO J . Ca 성 분을 약 20 mol% CaS i O ., 까지 함유할 수 있고, Fe 도 약 14% FeO 만큼 치 환으로 함유할 수가 있다 . 결정계 삼사정 계 . Pl. a=7.699, b= 12.4 7 , c=6.702A, a= 93°58' , /3=9 3°04' , y=6 8° 12' . Z= 10. 장미 휘 석 ( 薔 薇輝石) 은 b 축의 단위길이 내에 5 개의 S i O 』 다면체가 약간 꼬인 형태로 계속 연결되 어 있다(그림 4.23) 색 분홍색, 갈색, 산화망간 물질이 내포물로 들어 있을 경우 검 은 반점이나 수지상(樹枝狀) 조직을 나타낸다. 박편하에서는 무색 이다. 다색성을 매우 미약하게 나타낼 수 있다. 결정형태 자형은 c 축을 따라 길쭉한 주상 결정 형태를 취하지 만, 치밀한 세립질 괴상 형태로 산출되는 것이 더 일반적이다. 경도 5.5~6 비중 3.4 ~ 3.7 벽개 {110} 방향의 완전한 주상 벽개가 발달한다. 양호한 {001} 방향의 벽개가 있다. 양각높다. 굴절률 a= l.71 6~ 1.73 3, /3= 1.7 20~ 1.73 7, y= 1.7 28~ 1.74 7. 복굴 절률 =0.012~0.014. 최대 간섭색은 lo 주황색이다.
소광특징 주상 입자인 경우 최대 소광각이 25° 정도이다 . 광학부호 이축성, (+). 2V=60~75• X 선 회절선 3.57( 1), 3.34(3), 3.26( 1), 3.14(3), 3.10(2), 2.9 8 0(7), 2.9 2 4(7), 2.112(1 o )A 기타사항 변성교대작용을 받은 망간광상에서 주로 산출된다. 색 깔과 투명성이 좋은 광물은 보석 원석으로 사용된다 . 4. 3 . 1. 7 각섬석군 (AMPHIBOLE GROUP) 각섬석군(角松]石郡)에 속하는 광물들의 화학식은 Ao. 1 B2CsTs022(OH, F, Cl )i로 표현될 수 있으며, 이때 A=Na , K, B=Na , Li, Ca , Mn, Fe 터 Mg , C=Mg , Fe 터 Mn, Al, Fe3+ , Ti, T=Si, Al 이다 . 각섬석군에 속하는 광물들은 (S i 4011)6- 의 기본단위가 c 축 방향을 따 라 약 5 .3 A 의 거 리 로 반복하는 복쇄 상 구조 (復鎖狀構造, double- chain str uc tu r e) 로 되 어 있다. 양이 온 자리 인 A 위 치 는 0 또는 OH 로 둘 러싸인 배위수가 10~12 인 위치이며, B 는 배위수가 6~8 인 M4 위치이다 . C 는 M,, M2, MJ , M 』 등 배위수가 6 인 위치이며, 특히 M 과 M 는 산소 4 개와 (OH, F) 2 개로 둘러싸여 있다. T 는 4 개의 산소로 되어 있는 사면체의 중심 위치이다 . Al 3+이 S i”를 치환하게 되면 양의 산화수가 부족하게 되어 이를 보충하기 위해 A 자리에 Na , K 등이 오게 된다. 에데나이트 (ede nit e), 파가사이트(p ar g as it e) 등은 이러한 방식으로 형성된다. 각섬석군을 의미하는 앰피볼 (am phi bole) 이란 용어가 〈모호하다 (amb ig uous) 〉는 뜻을 지닌 그리스어 〈 am ph i bolos 〉에서 유래되었듯 이 각섬석군에 속하는 광물들은 그 화학성분이 너무 복잡하고 다 양하다. 이 때문에 체계적인 분류에 근거한 여러 광물 명명법(命名 法, nomencla tu re) 이 오래전부터 제안되었었으나 실현되지 못하다 가, 1978 년 국제 광물학연 맹 (Inte r natio n al Mine ralog ica l Associa t i on ) 에
의해 이들을 분류할 새 기준이 마련되었다. 이 기준에 의하면, 각 섬석군에 속하는 광물의 화학성분은 (0, OH, F, Cl) 가 24 가 되도 록 해 정립된 각섬석군의 광물명울 우선 선택해 정하고, 구성원 소는 아니지만 치환상태로 존재하는 화학성분을 나타낼 수 있도 록 접 두어 (pre fi x) 또는 수식 어 (adje c ti ve ) 를 추가로 광물명 앞에 표 시한다. 영문으로 표기할 경우는 접두어와 광물명 사이에 alum ino -, fer r i-, fluo r-처 럼 하이 픈 (h yp hen) 을 사용한다. 각섬석군이 속하는 광물들은 B 위치에 있는 양이온에 의해 4 가지 로 분류한다. (Ca+Na)s< 1.34 Fe-Mg -M n 각섬 석 류 (iro n -m ag n esiu m -mang an ese amp hi b o les, 표 4.4 ) (Ca+Na) 오 1.34 Ca-각 섬 석 류 (calcic amp hi b o les, 표 4.5) Nas<0.67 (Ca+Na)B~1 .34 Na . Ca- 각섬석류 (sod i c-calc i c amp hi b o les, 표 4.6) 0.67::;Nas< 1.34 Naa2 ::l.34 알칼리 각섬석류 (alkal i amp hi b o les, 표 4.7) 각 부류에 속하는 광물들의 종류와 화학식은 이들 표에 나타나 있다. 알칼리 각섬석류 (alk ali -am phi bole) 가 만들어지기 위해서는 M4 위치에 있는 Ca 을 Na 이 치환하게 되는데, 이 때 생기는 양의 산화수 부족은 (Al, Fe”)2 이 (Mg , Fe) 를 치 환함으로써 상쇄 된다. 그 결과 글로코페인(g lauco p hane) 과 리베카이트(ri ebec kit e) 가 만들어 진다. 특히 Fe-Mg - Mn 각섬석류에는 단사정계 (C ')j m, P2 J m) 와 사방정계 (Pnma) 의 두 가지 광물이 있고, 기타 각섬석류에 속하는 광 물들은 단사정계의 결정구조를 하고 있다. 단사정계의 C') jm , P2J m
 표 4.4 Fe-Mg -M n 각섬석군 광물의 일반화학식 및 단종 화학식 .
표 4.4 Fe-Mg -M n 각섬석군 광물의 일반화학식 및 단종 화학식 .
 표 4.5 Ca- 각섬석군 광물 및 단종의 일반 화 학식 .
표 4.5 Ca- 각섬석군 광물 및 단종의 일반 화 학식 .
 표 4.6 Na-Ca 각섬석군 광물 및 단종의 일반화학식 .
표 4.6 Na-Ca 각섬석군 광물 및 단종의 일반화학식 .
 표 4.7 알칼 리 각섬석군 광 물 및 단종 의 일 반 화 학 식 .
표 4.7 알칼 리 각섬석군 광 물 및 단종 의 일 반 화 학 식 .
구조, 사방정계의 Pnma 의 결정구조가 각 각 그 림 4.2 6 , 4.27, 4.2 8 에 있다 각섬석군에서 관찰되는 두드러진 치 환 현상은 Fe 이 M g옹 치환하는 것이다. 사방정계의 결정구조에서는 M1, M2 , M.1 , M~ 위 치 모두가 M i와 F&-+ 에 의해 채워질 수 있지만, 단사정계인 경 우 는 M, MA M 판 M i나 F&-+ 로 채 워지 고, M 는 주로 N a 과 C a.9..로 채워진다. 그러나 M gi.과 Fei. 이온의 전자배치 (electr o nic con- figur a ti on) 가 다르기 때문에 M g거를 치환하여 들어가는 Fe i.의 우선 적 위치는 결정장의 영향 (c ry s tal-fi elde ff ec t)을 받는다. 참고로, 양 기석 (ac tin o lite)의 경우, Fe” 는 M1, MJ , M 려 순서로 채워진다 그 외 Zn, Co, Ni, Cu, Cr 등이 미량 존재할 수 있는데 이들은 이온 의 크기나 산화수에 있어 주구성원소와 비슷하다. 각섬석군의 광
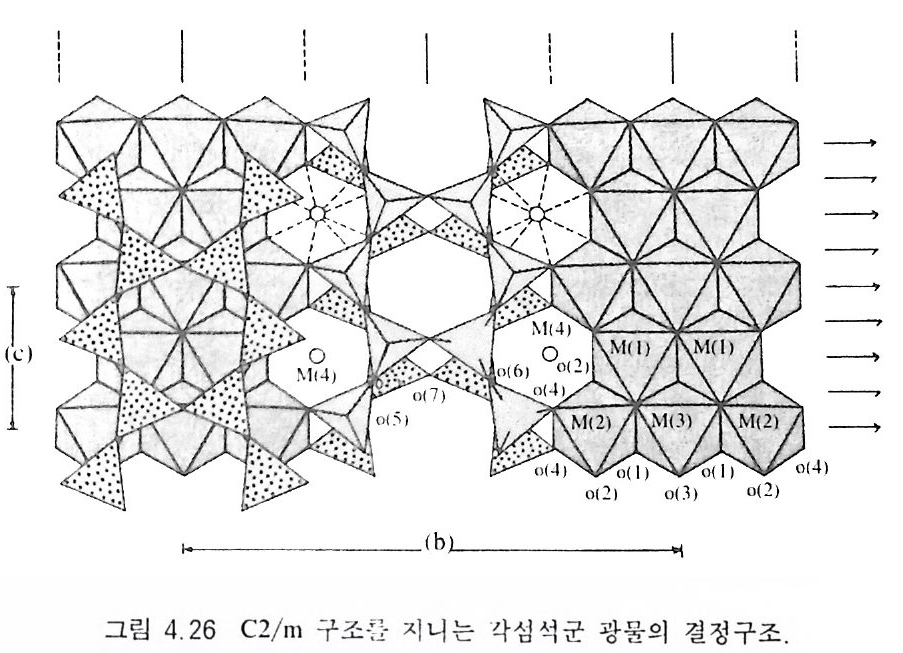 )
)
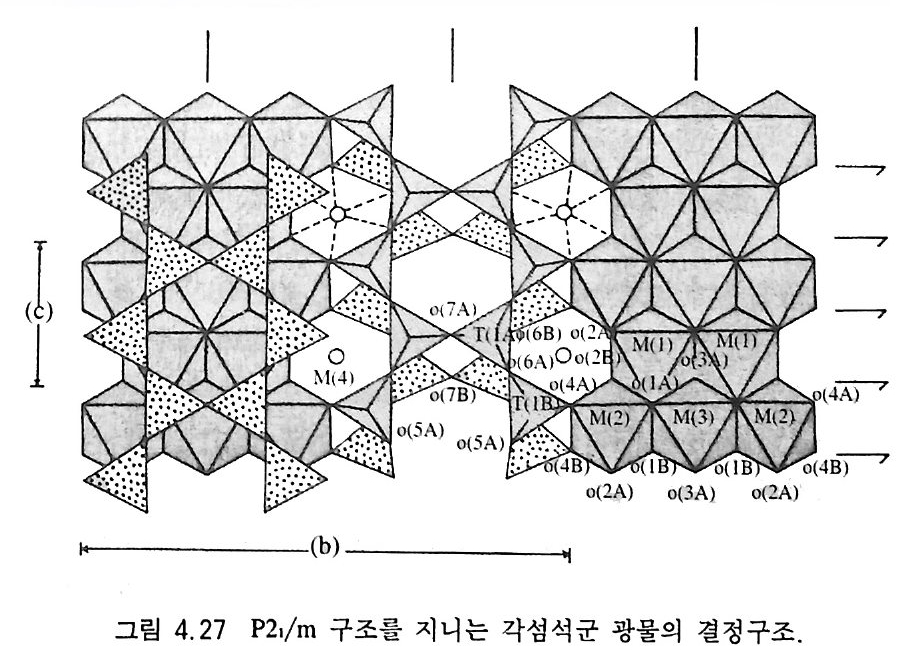 Il 77
Il 77
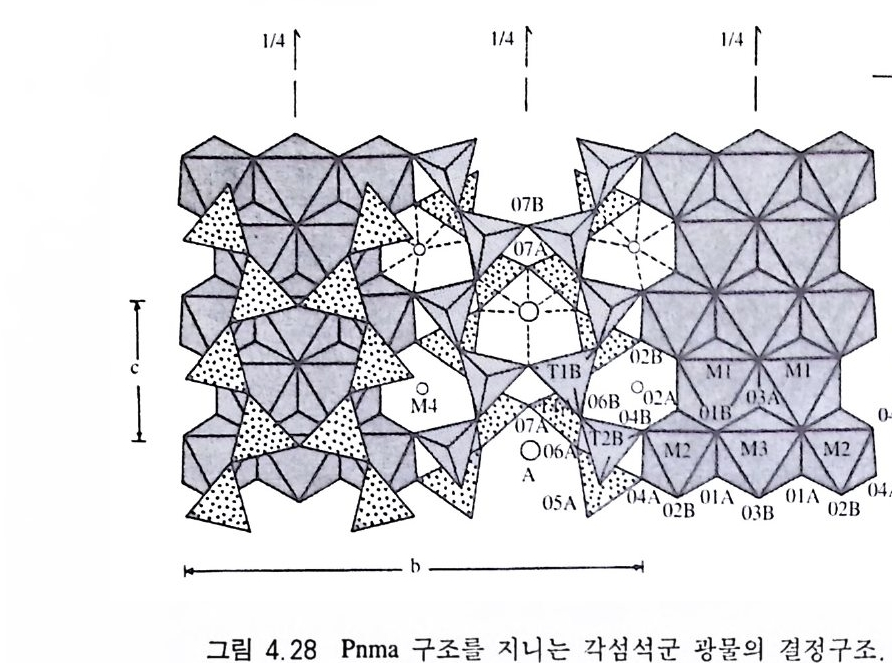 I 'T f I’ f I 'T f
I 'T f I’ f I 'T f
물에는 교차각이 56~5T 와 123~124 ° 인 두 방향의 벽개가 발달하 며, 각섬석의 고분해능 투과전자현미경 사진은 그림 4.29 와 같다. 이 사진은 c 축을 따라 촬영한 것으로서, 흰색 부분은 A 위치에 해 당한다. 각섬석군 광물에는 ( OH ) 가 들어 있어서 휘석군 광물보다 고온 에서 덜 안정하다 . 이 때문에 각섬석군 광물을 가열하면 휘석 등 의 무수 광물(無水 鑛 物, anhy dr ous m i neral) 로 변질된다 . 각섬석군에 속하는 광물은 거의 모든 화성암에 널리 산출되고 있으며, 일부 변성암에서도 주요 조암광물로 존재한다 . 각섬석군 의 광물은 고온에서 휘석으로 쉽게 바뀌기 때문에 이룰 이용하여 생성 당시의 온도와 압력을 추정한다. 글로코페인(g lauco p hane) 은 저온·고압에서 생성되었음을 나타내고, 수산기 (OH) 가 부족한 일 부 파가사이트(p ar g as it e), 해스팅사이트 (has ti n g s it e) 는 수분의 함량
 그림 4.2 9 고분해능 전자현마경으로 안영한 각섬석의 원자구조 .
그림 4.2 9 고분해능 전자현마경으로 안영한 각섬석의 원자구조 .
이 직은 고온의 상태에서 만들어졌음을 의미한다. 녹색편암 변성 상(g reensch i s t fa c i es) 에 안정 했 던 양기석은 이보다 높은 앰피볼라이 트 변성상 (h ig h- g rade amp hi b o lite fac i es) 에서는 각섬석으로 변한다. 온도 와 압 력 에 변화가 생기면 Ca 과 Na , M g과 Fe, S i와 Fe, 0 와 OH 사이의 치환이 일어난다 . 【앤소필 라이 트 (An th op h y ll it e) 】 화학성분 (Mg , Fe)1(S i,어 )2(0Hh. Mg O 29.2 5 %, FeO 8.43%, SiO : 58.4 8 %, AhOJ 0.5 7 % , MnO 0.27% , CaO 0.1 4 %, ILO 2.80% 결정계 사방정계 . Pnma. a=18.56, b=18.08, c=5.2 8 A. Z=4 색 회색, 옅은 갈색, 다양한 녹색. 박편하에서는 거의 무색이 다. 색깔이 짙은 입자는 다색성을 약하게 나타낸다. 결정형태 긴 주상, 섬유상 결정 형태를 취하며, 주상 결정인 경우 수직 조선이 뚜렷하게 발달한다. 타형으로 산출되는경우도 많다.
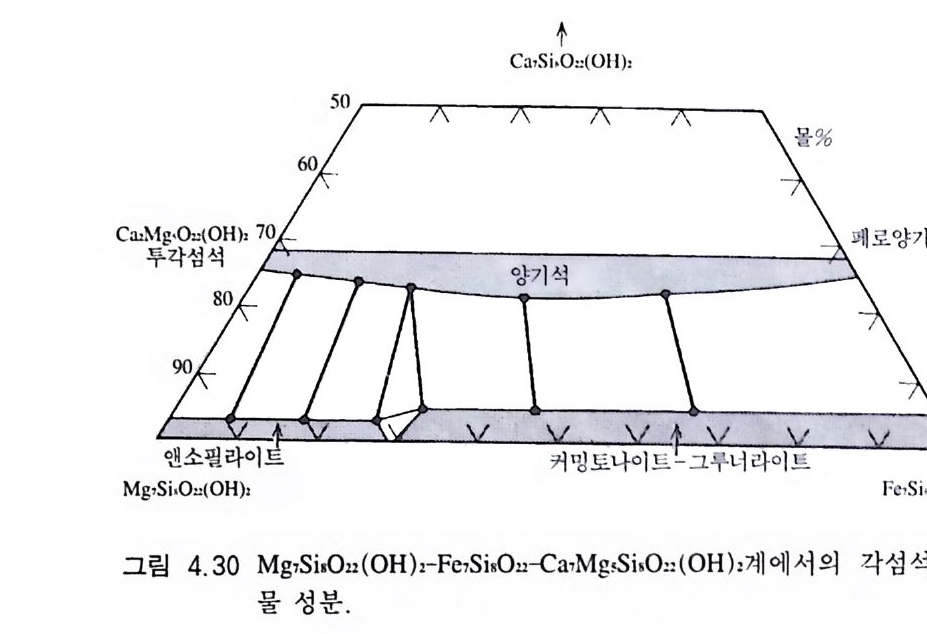 Ca,Si ,^ O : : (0 1- 1 ):
Ca,Si ,^ O : : (0 1- 1 ):
경도 5.5 ~ 6 비중 2.85~3.2 벽개 {110} 과 나란한 두 방향의 벽개가 54° 또는 126 ° 로 교차하 며 발달한다 . 양각높음 굴절률 a=l. 59 8~1.652, {3=1.61 5~1.662, y=1 .6 2 3~ 1 .676. 복굴 절률 =0.016~0.025. 최대 간섭색은 2 · 의 낮은 색깔이다. 소광특징 주상 형태의 입자는 평행소광, c 축에 수직으로 절 단 된 입자는 벽개를 기준으로 대칭소광을 나타낸다. 장축부호 장축 방향을 따라 느린 광선이 진동한다. (+) 광학부호 이 축성 , ( + ) . 2V =70~90· X 선 회절선 s.26(6), 3.65(4), 3.2 4 (6), 3.0 5 (1 0 ), 2.84(4)A 기타사항 앤소필라이트는 M g의 일부가 Fe 에 의해 치환되어 고 용체를 형성하지만 Fe1S i 10 파 OH)z 인 그루너라이트(gru ne rit e) 와는 완 전고용체를 형성하지 않는다(그림 4.3 0 ). 그 이유는 그루너라이트
가 단사정계의 결 정구조 를 하고 있기 때문이다. 기드라이트 (g edr it c) 는 앤소 필 라이트의 변 종 으로서 Na 와 Al 을 함유하고 있으 며 , 화 학 식 은 Na,,5 ( M g, Fe 바 ( M g , Fei. )J s (AI, Fe .I 令) , s S i 6Ah0 l 2 ( OH)l 이 다. 기 드 라이 트 의 광학부호는 앤소필라이트와는 달리 (-)이다. 앤 소판 라이 트는 감람석을 함유한 초염기성 화성암 또는 백운암질 쉐 인 이 빈성작용을 받아 만 들 어 진 다. 근청석 (cord i e rit e) 을 함유하는 선암 또는 선 마 암 에서도 발 견된다. 앤소필라이트는 활 석으로 변질 한 다. 【커 밍 토 나이 트 -그 루 너 라이 트 ( Cumm i n gt on it e -Grunerite ) > 화학성분 (M g , Fe b(O H)!(S i 4 0 11)!-Fe1( 0 H) i(S i , 01 1) z 고용체 . Mg O 20.8 4 ~ 0.04% , FeO 17.73~ 4 7.96% , Si 0 2 51 .5 3~47.54%, H20 2.79~ 1.5 5% , MnO 0.2 2 ~ 2.14% , Al iOJ 5.02~0.20%, CaO 1.34 ~0 .00% , Na20 0.6 5 ~0.29% 결 정계 단사정계. C 김m . 커밍토나이트 a=9.5 3 4, b=18.231, c= 5.3 2 3A, /3= 101 .9 7° , 그루너라이트 a=9.652, b=18.380, c= 5.3 3 8A, /3= 101 .8 6°. Z=2 색 회색, 녹색, 갈색. 박편하에서는 거의 무색 또는 옅은 녹색 울 띤다. 미약한 다색성을 나타내는 경우도 있다. 결정형태 주상 또는 석면과 유사한 섬유상 형태, 방사상 형태를 지닌다. 경도 5.5 ~ 6 비중 3.10~3 . 60( 그림 4.3 1 ) 벽개 {110} 에 나란한 두 방향의 벽개를 가지며 교차각은 56°, 124° 이다. 양각 높은 편이다 . 굴절률 a= l.635~ 1.69 6, {3= 1.6 44~ 1.70 9, y= 1.6 55~ 1. 729( 그림
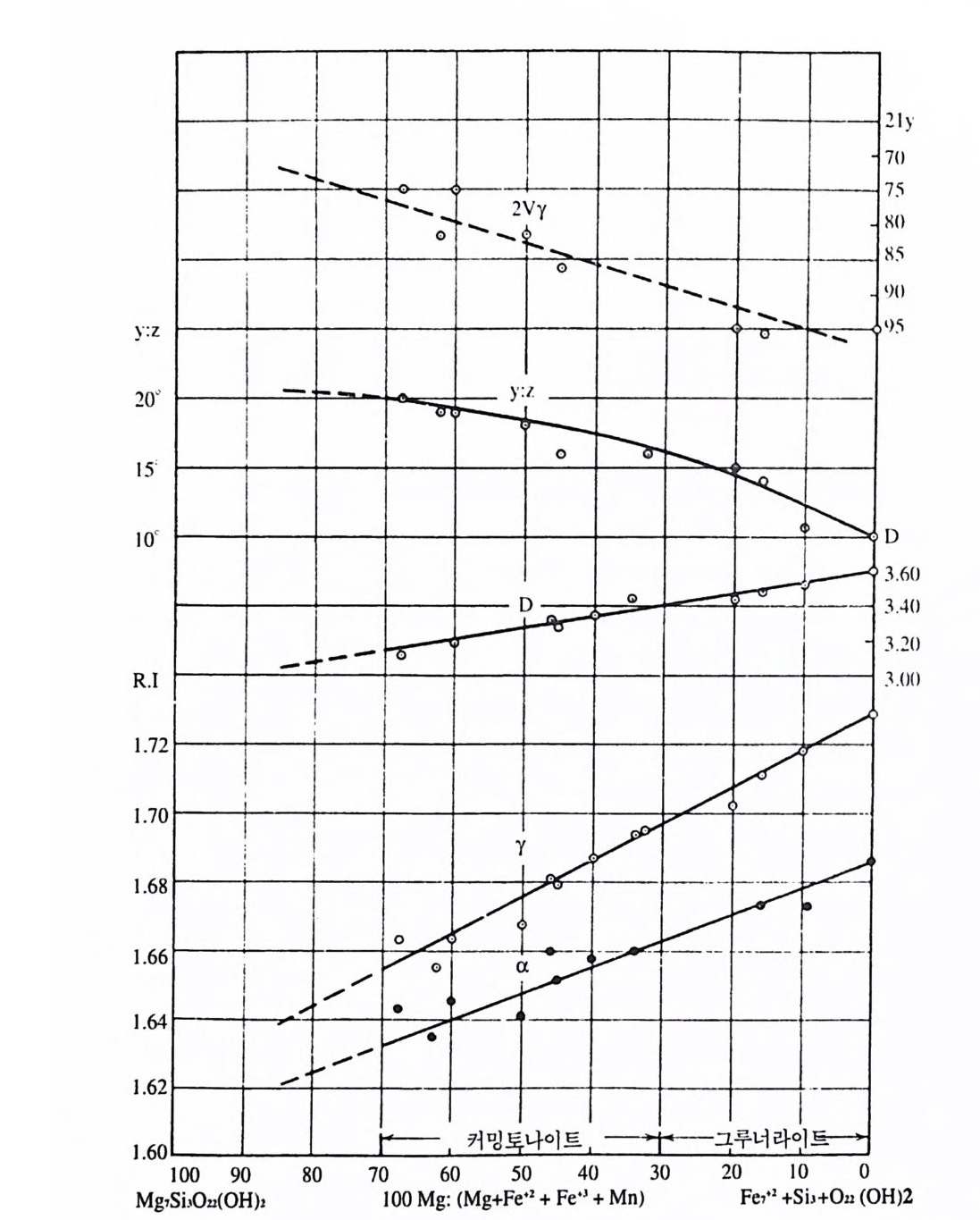 ~F, 'J`
~F, 'J`
그림 4.3 1 커밍토나아트—그루너라이트계의 성분에 따 른 광학적 성 질 과 비 중 변화 .
4.31). 복굴절률 = 0.020 ~ 0 . 045. 장축 방향으로는 1°, 기타 방향으로 는 2 ~ 3 ° 의 간섭색이 나타난다. 소광특징 장축 방향을 따라 15~20 ° ( 커밍토나이트), IO~15° ( 그루 나라이트)의 최대 소광각을 나타낸다 . M g의 함유량이 많을수록 소 강사이 증가한다 . 장 축 부호 장죽음 따라 느린 광선이 진동한다. (+) 광학부호 키밍토 나이 트는 이 축성 (+), 2V=68~87°; 그루너라이 토는 이 `숙 성, 仁 ) . 2V= 7 9~ 86° X 선 회절선 커밍토나이트 9.12(5), 8.3 0 (1 0 ), 5.09(2), 4.83(2), 4.5 5 (4), 4.14(4), 3.87(3), 3.4 5 (4), 3.26(8), 3.06(9), 2.75(7), 2.623(5)A : 그루너 라이 트 9.21 (5), 8.33(1 0 ), 4.84(3), 4.68(3), 4.58(3), 4.5 8 (3), 3.88(5), 3.4 7 (5), 3.28(5), 3.07(8), 2.99(4), 2.766(9), 2.639(7J , 2.s o 7<6lA 기타사항 70mol% Fe , S i ~ O 끄 ( OH ) 를 기준으로 커밍토나이트와 그 무너라 이 트로 구분된다. 광학 부호도 이를 기준으로 바뀐다 . 불산 (HF), 탄산나트륨 (Na i CO J)에만 녹는다. 커밍토나이트는 Ca 성분이 적고 Fe 성분은 많은 동력변성암에서 산출되며, 변성 각섬암 (a m ph i bol it c) 에서도 발견된다. 커밍토나이트는 양기석과 공존하는 경우가 많 으며, 화산암인 석영 안산암에서는 반정으로 산출된다. 그루너라이트는 퇴적 기원인 층상철광(i ron- fo rma ti on) 이 변성작용 을 받은 곳에서 발견된다. 커밍토나이트와 그루너라이트는 높은 변성환경에서 휘석 또는 감람석으로 바뀐다. 이 두 광물은 석면으 로 활용된다. 【투각섬 석 -양 기 석 (Tremolite - A cti no lite ) > 화학성분 Ca i(M g , Fe)s(Sia 0 22) (OH)?. 투각섬석과 양기석, 그리고 페로양기석은 M g과 Fe 의 치환에 의해 완전고용체를 형성한다. 투각
섬석과 양기석의 성분은 FeO 18.8 1 % , Mg O 11. 2 2% , CaO 10.17% , Ah03 3.88%, Na iO 1.67 % , KiO 0.09% , HiO 1.94 % , Ti02 0.7 4 % . 투각섬 석은 M g을 치환하는 R 의 양이 50mol % 미 만이며, 그 이 상일 때는 페로양기석(f erro-ac ti nol it e) 이라고 한다. 결정계 단사정계. C2Jm 투각섬석 a=9.84, b= 1 8.0 2, c= 5 .2 7 A. . /3= 1 야 0 57' : 양기석 a=9.884, b=18.1 4 5, c=5.294A, /3= 1044 2' . Z= 2 색 투각섬석은 백색 또는 회색, 양기석은 녹색운 띤다. 일반직 으로 M g을 치환하는 Fe 의 성분이 많을수록 녹색 이 진 어 진다. 박 편하에서는 전자는 무색이며 다색성이 없으나` 후자는 옅은 녹색 을 띠며 다색성이 있다. 결정형태 얇고 긴 도변상(刀 邊狀) 또는 방사상 형태의 결정형태 를 취하며, 특히 섬유상 형태의 양기석 변종을 비 솔 라이트 (b y ssol it e) 라고 한다 . 경도 5~6 비중 2.9~3.4 4 . M g을 치환하는 Fe 의 함량이 많아질수 록 비 중 이 커진다(그림 4.3 2 ). 벽개 {110} 에 나란한 두 방향의 완전한 벽개가 발달하며 교차각 은 56° 와 124° 이다. 장축 방향으로 절단된 입자는 이에 나란한 한 방향의 벽개가 발달한다. 양각 비교적 높다 . 굴절률 a=l. 60 ~1 .68 , /3=1.6 1~l. 69 , r=1. 63~ 1. 70( 그림 4.32). 복굴절률 =0.022~0.027. 굴절률도 Fe 의 양이 많아질수록 증가한다. 간섭색은 최대 2· 의 중간색을 가진다. c 축에 수직으로 절단된 단면 은 1· 의 백색 또는 노란색의 간섭색을 나타낸다. 소광특징 장축 방향이 있는 입자에서는 최대 소광각이 10~20· 이 고, 거의 평행에 가까운 소광을 나타내는 경우도 있다. c 축에 수 직인 단면은 대칭소광을 나타낸다.
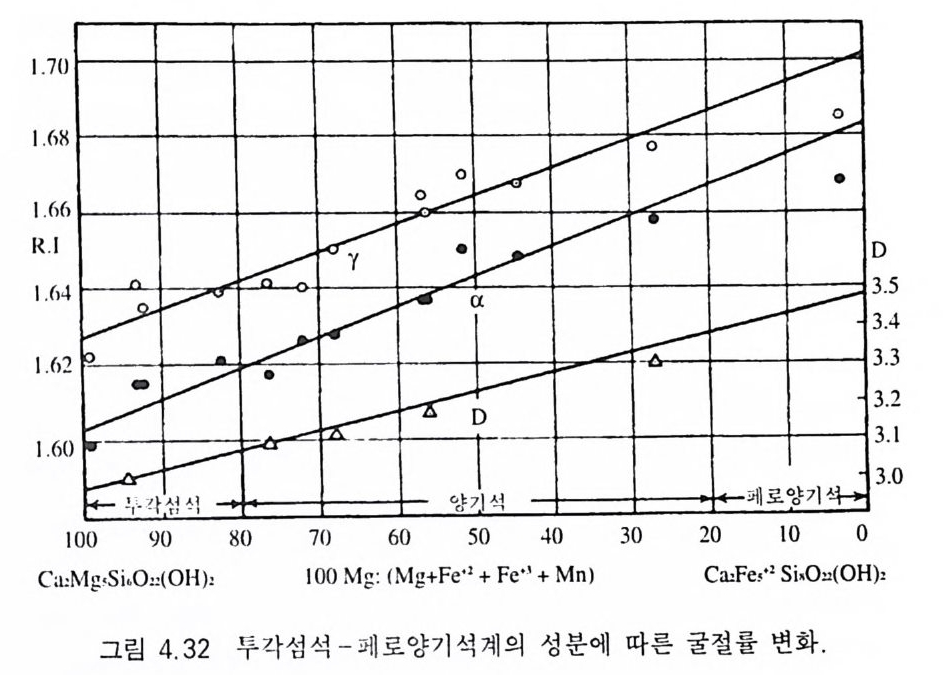 1.7 0
1.7 0
장 축 부호 장축 방향 을 따라 느 린 광선이 진동한다 . (+) 광학부호 이 축 성, ( 키 . 2V= l0~20· X 선 회절선 투 각섬석 8.9 8 ( 1) , 8.38(1 0 ), 5.07( 1), 4.5 1 ( 2) , 4.20(3), 3.3 8 (4), 3.27(7), 3.12(1 0 ), 2.9 3 8(4), 2.805(4), 2.705(9), 2.529(4), 2.3 8 0(3l, 2.3 3 5( 3> A : 양기석 9.12(6), 8.4 7 (7), 5.13(4), 4.91 (7), 4.54(6), 4.23(3), 3.8 9 2(6 ) , 3.4 0 1 (8 ), 3.290(5), 3.1 4 3(7), 2.9 5 9(7), 2.8 2 3(3), 2.744(4) , 2.719(1 0 ), 2.644(6), 2.543(1 0 ), 2.3 4 4(5)A 기타사항 투각섬석과 양기석의 중간 성분인 연옥(軟玉) 변종은 섬유상 미결정들이 임의의 방향으로 엉겨 있는 다결정질 물질이 며, 인성이 매우 강하여 보석 원석으로 사용된다 . 한편, 섬유상 입자가 치밀하게 엉겨 있는 투각섬석 변종도 있는데 이룰 마운틴
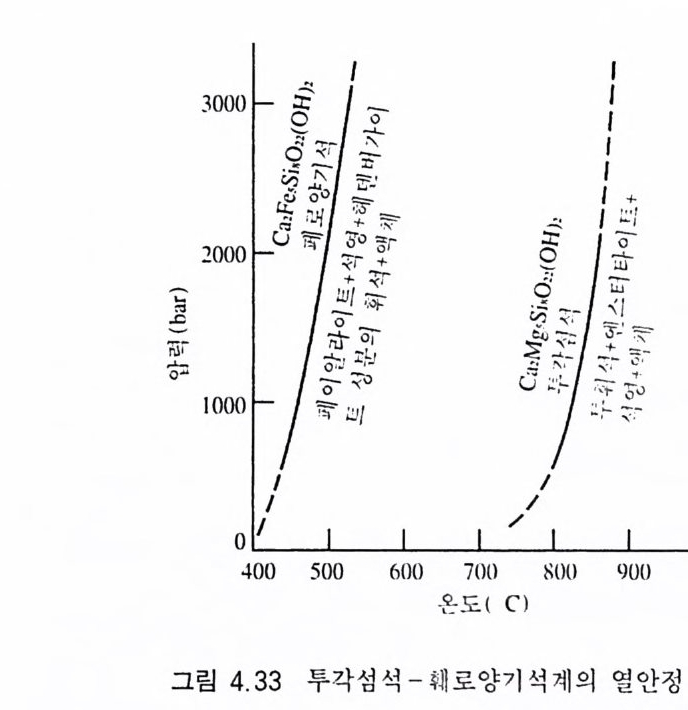 II
II
레더 (mounta in leath e r) 또는 마운틴 콜 크 ( moun ti an cork) 라고 한 다 . 투각섬석과 양기석은 변성광물로서, 접 촉 변성암과 광역 변성암 모두에서 발견된다. 접촉 변성암인 경우는 백운석이 석 영과 반웅 하여 만들어지는데, 그 생성방정식은 다음과 같 다. 5 CaMg (C OJ ) 2+8 Si0 2 +H2 0 ~ C 따 M g s S i s 아 (OH )i +3 CaCOJ + 7 CO2 백운석 석영 투각섬석 방해 석 투각섭석은 고온에 불안정하여 투휘석으로 변한다(그림 4.3 3 ). 양기석은 녹색편암 변성상(gr eensch i s tfaci es) 에 속하는 광역 변성암 에서 특징적으로 산출되며, 글로코페인 편암(g lauco p hane sch i s t)에 서도 석영, 녹렴석, 글로코페인, 로소나이트, 품펠라이트 둥과 함
خ ����\
��. 0�,� � (Hornbelnde)>T�Y�1�� �(a N ,K)o . 1 Ca 2 M(g, Fe , Als)(HO F,b(iS,Al )s022 S.i 0 2 42.50 %, gMO 14.19% , CaO 128.3 %, bAOJ 14.69%, F e .O 951 %, Ni aO 2 01. % , 1<01 0.6 5%, H20 .612%, T0 2i 1.8%4 ��� Ĭ 責��Ĭ. C2/m. a9.=8 7, b=8.10 1, c=5.33A, /3 = 15�04 4' . =Z2 �� ��@� y���<�\���0� p�X� ��@���L��� 䲑�X��. ���X������ �@� y��� ��� ���D� `�p�. ���1�t� 买� �X��. ������ ���� ���� |��� t�p�, ,� ���x� ����ij �9� ��� .���t�@� �6 ��� Ǭ� \� � �� |� ���и��. ��t�t� (1 00 ) t�x� � � t� � 9� ��\��. ��ij 5~ 6 D�� 3. 0~3.4 ��� {110} �� ���\�� �P ��)�X� ��� 5�6� ,14�2 X� �ij� | t�� � p� �8�XՌ� ��X��, {100}, {001} D� 0�|� ���� ��`� �ij ���. ��� D�P�� ���. t��`� a=l.614~l.675, /3=l.618~l.691, y=l. 633~l.701. ��t� �`� =0.019~0.026. t��`�@� M g|� X�XXՔ�� Fe X� ��t� ιD��]� ����\� . \�� �-���@� 2 � X �����t�� . �������2.610(5 ) , 2.565( 3) , 2.3 6 0(3), 2.180(4)A 기타사항 각섬석은 화성암과 변성암 모두에서 매우 주 요한 조암광 물로 존재한다 . 섬록암과 섬장암, 편암, 편마암, 변성 각 섬암 등에 서 많이 산출된다 . 각섬석은 초염기성암이나 염기성암으 로부 터 중 성 암, 산성암인 화강암에 이르기까지 폭넓게 산 출 된다 . 이 때 문 에 각 섬석의 화학성분이 매우 다양하다. 마그마의 고 결 초기 에 만 들 어 지 는 각섬석에는 Mg 성분이 많고, 후 기에 만 들 어 지는 각심석 에 는 Fe 성분이 증가한다 . 화성암에 있는 각 섬석에 누 대 구조가 관찰 되는 경우가 있는데, 이 경우 일반적으로 중 심에 는 Mg 성분 이 많 고 가 장자리에는 Fe 성분이 많다 . 마그마 고 결 말 기 또 는 변성작용을 받을 때 휘석이 각섬석으로 변 질 되거도 한다 . 각 섬 석 계열 광 물 은 화학성분과 광학적, 물리적 성 질 이 다양하기 때문에, 명명 (命名) 에 관한 제안이 많이 있었다 . 화학성분에 따라 보편적으로 쓰 이는 광물명예는 에데나이트 (eden it e ), 팔가사이트 ( p ar g as it e ), 해스팅사이 트 (has ti ng s it e), 체르마카이트(ts cherm akit e) 둥이 있다. 【글로코페 인 -리 베 카이 트 (Glauco p hane -R ieb eck ite) > 화학성분 N 티 M g 3 AlzS i s022(0H )i -N 파 Fe i •Fe i3 • S i s022(0H )i. Mg - Fei+ , Al-Fe 3+의 치환이 현저하고, 이 때문에 굴절 률 , 광 축 각이 변한다. 결정계 단사정계. C2/m. 글로코페인 a=9.595, b=17.798, c= 5.3 IT TA , /3= 103°()( 5' 리 베 카이 트 a=9.769, b= 18.048, c=5.3 3 5A , /3= 103°59' 색 회색, 청색, 연보라빛 청색(글로코페인), 암청색, 검은색(리 베카이트). Fe 성분이 많을수록 검은색을 띤다. 박편하에서는 연보 라빛 청색 내지 무색(글로코페인), 암청색 또는 황록색(리베카이 트)을 나타낸다. 다색성온 뚜렷한 편이다.
결정형태 좁고 긴 주상 형태 또는 침상 형태를 가진다. 섬유상 형태 를 취하는 리베카이트 변종을 크로시돌라이트 (croc i dol it e) 라고 한다. 경도 6 비중 3.1~ 3 .4 벽개 {ll 이 방향의 양호한 두 벽개가 발달하며, 교차각은 56°, 124 ° 이다. 양각 높음 굴절 률 a= 1.62 1 ~ 1.6 9 3, {3= 1.6 3 8 ~ 1.695, y= 1.639 ~ 1.6 97, 복굴 절 률 =0.004~0.018. 리베카이트와 글로코페인은 최대 간섭색이 1° 의 색이지만, 광물 자신의 색이 진하기 때문에 간섭색을 거의 감 지 할 수 없는 경우가 많다 . 소광특징 주상의 입자는 최대 소광각이 5° 내외이며, c 축에 수직 인 입자는 벽개를 기준으로 대칭소광을 나타낸다. 크로시돌라이트 는 거의 평행소광을 한다. 장축부호 글로코페인은 장축 방향을 따라 느린 광선이 진동하 며, 리배카이트는 빠른 광선이 진동한다. 광학부호 이축성, (-). 글로코페인은 2V=O~68°, 리베카이트는 2V=40~90° 이다. X 선 회절선 글로코페 인 8.26(1 0 ), 4.4 5 (3), 3.22(2), 3.06(6), 2.693 (6)A : 리 베 카이 트 8.40(1 0 ), 4.51 (2), 3.27(2), 3.12(6), 2.726(4)A 기타사항 글로코페인은 편암, 편마암, 에콜로자이트, 대리암 같 은 변성암에서만 산출되며, 저온 • 고압의 생성환경을 반영한다. 백운모, 석영, 석류석, 스핀, 로소나이트, 클리노조이사이트 등과 공생한다. 리베카이트는 화강암, 섬장암, 조면암, 일부 페그마타이 트에서 산출된다. 크로시돌라이트는 석면으로 사용된다.
4. 3. 1. 8 석류석군 (GARNET GROUP) 석류석군(石 權石群 )은 정벽 (1 \h 째 8 ) 과 화학성분이 유사한 여러 광 물로 구성되어 있으며 모두 등축정계의 Ia3d 공간군의 결정구조 률 지닌다. 단위포 함량 (Z) 은 8 이다. 석류석군에 속하는 광불의 일반 화학식은 A J B2(S i O~) •1으로 나타낼 수 있으며, A 는 배위수 가 8, B 는 배위수가 6 인 양이온의 위치이다. A 자리에는 이 온 반경이 비 교석 븐 +2 가의 양이온이 오고, B 자리에는 이보다 작은 + 3 가의 양이온 이 자 리잡는다. A 에는 Ca2\ Mg 2\ Fe2\ Mn2\ B 에 는 Al·`\ Cr\\ Fc·`· 등 의 원소가 위치한다 . 특히 A 또는 B 에 고정적으로 위치하는 원 소에 따라 아류(亞 類) 인 두 계열 (se ri es) 로 구분된다 . 즉, 파이랄스 파이 트 계 열 (pyra lspi te se ri e s) 과 우그란다이 트 계 열 (ug ra ndit e seri e s ) 인데, 전자에는 B 가 Al 으로 고정되어 있고 A 에는 Mg , Fe, Mn 등이 위치한다. 파이로프(py ro p e ), 알만딘 (almand i ne), 스페샤르틴 (s p ess arti ne) 이 이에 속한다 . 후자에는 A 가 Ca 으로 고정되어 있고 B 에는 Cr, Al, Fe 이 위치한다. 우바로바이트 (uvarov it e), 그로슐라 (gros sular), 안드라다이트 (andrad it e) 가 이에 속한다. 중요한 목징으 로는, 각 계열 내에서는 원소간의 치환이 다양하게 일어나지만, 두 계열간의 광물들 사이에서는 원소간의 치환이 거의 일어나지 않는 다는 점이다 . 예를 들어, 파이랄스파이트 계열에서는 A 에 자리하 는 Mg , Fe, Mn 끼리 어떤 비율로도 자유롭게 치환이 이루어져 세 광물의 성분을 동시에 소유하는 완전고용체로 산출된다. 그러 나 B 자리에 있는 Al 은 Cr, Fe 과 같은 +3 가 이온에 의한 치환이 거의 없다. 이와 마찬가지로, 우그란다이트 계열에서도 A 위치의 Ca 은 Mg , Fe, Mn 등으로 치환이 거의 되지 않는 반면에 B 위치에 있는 원소인 Cr, Al, Fe 은 서로 자유롭게 치환한다. A 와 B 위치에 있는 원소에 따른 각 계열의 구성 광물명과 이상화학성분은 다음 과 같다(표 4.8).
 표 4.8 석류석군의 두 광물계와 구성 광물의 이상화 학식.
표 4.8 석류석군의 두 광물계와 구성 광물의 이상화 학식.
때 로는 B 자리에 있는 이온에 따라 Al- 석류석(파이로프, 알만딘, 스페샤르틴 , 그로슐라), Fe- 석류석(안드라다이트), Cr- 석류석(우 바로바이 트) 등으로 분류하기 도 한다. 간혹 (OH)4 가 S i 04 를 일부 치환하기도 하는데 이런 현상은 그로슐라에서 관찰되며 최대 약 8.5 % 의 IuO 를 포함한다. 그로슐라에 있는 S i 04 의 일부가 (OH)4 로 치 환되 어 있는 것을 하이드로그로슐라 (h y dro gr assular, Ca iA bSh(OH)4Q s ) 라고 한다. 석류석군에 속하는 광물은 모두 동일한 정벽을 나타내는데, 가 장 전형적인 결정형은 12 면체(그림 4 .3 4a) 이다. 그 밖에도 편방체 (그림 4.34b), 12 면체와 편방체가 결합된 취형(그림 4.3 4 c), 12 면 체, 편방체, 육팔면체가 결합된 취형(그림 4.34e) 이 있다. 석류석 에는 벽개의 발달이 없으며, 패각상 또는 불평탄한 단구가 발달한 다. 광학적으로는 모두 등방성이지만, 때로는 미약한 이방성을 나 타내기도 한다. 죽 거의 모든 알만딘과 파이로프가 등방성을 띠는 반면, 스페샤르틴과 우그란다이트 계열의 석류석은 빈번히 이방성 울 띤다 . 광택은 유리광택 또는 수지광택을 나타낸다. 경도는 약 7.5 정도로서 분말로 만들어 연마제로 사용한다. 석류석은 활석, 사 문석, 녹니석 등으로 변질된다. 석류석군에 속하는 광물은 화학성분의 차이에 의해 색, 비중, 굴 절률 등의 물리적 성질이 변한다. 석류석을 박편으로 제작하여 편
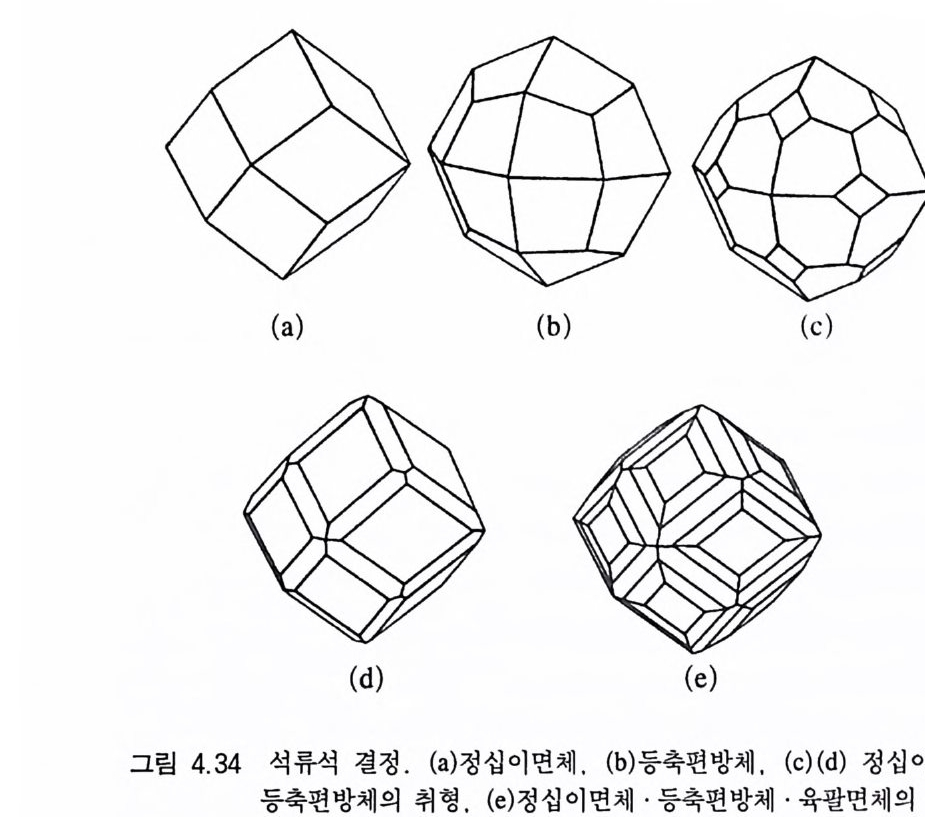 (a) (b) (c)
(a) (b) (c)
광현미경으로 관찰하면, 항상 소광하는 경우와, 결정구조의 미약한 변형에 의해 입자 전체가 동시에 소광되지 않는 경우도 있다. 간혹 화학성 분의 차이 에 의 해 육각형 태 의 누대 구조 ( 累帶構造, ~onal s tru c tur e) 를 나타내기 도 한다. 【파이 로프(Pyr o p e) 】 색 순수한 경우는 무색이지만, 철과 크롬울 미량 함유하여 짙은 적색 또는 거의 검은색을 띤다. 박편하에서는 무색 또는 매우 옅 은 적색을 띤다. 비중 3.7~3.8
굴절률 1.7 3~ l.75 X 선 회절선 2.8 6 (6), 2.5 6 2(1 0 ), 2.4 4 3(4), 2.3 3 9(2), 1.53 1 (5)A . a= ll.4 5 5A 기타사항 이 광 물 명은 〈불 꽃 〉 을 의미하는 그리스어에서 유래하 다 . 투 명하고 짙 은 적색인 경우 보석으로 활용된다 . 간혹 옅은 장 미 빛 적색 또 는 보라빛 적색을 띠는 변종이 있는데 이를 로돌라이 트 (rhodol it e) 라고 한 다 . 로 돌 라이트의 화학성분은 파이로프 : 알만 딘 = 2: I 정 도이다. 파이로프는 페리도타이트와 킴벌라이트 같은 초 염기성암 또 는 이 들 이 변질되어 만들어진 사문암 내에서 주로 산 출 되며 , 남아프리카공화국, 러시아, 호주, 체코 등에서 양질의 결 정 들 이 산 출 된다. 【알만딘 (A lmandin e ) > 색 암적색, 적자색, 적색, 적갈색. 반투명한 경우가 많다 . 박편 하에서는 무색 또는 매우 옅은 적색을 띤다. 비중 3.80~4.25 굴절 률 1.76 ~1 .81 X 선 회절선 4.04(3), 2.8 7 (4), 2.569(1 0 ), 2.3 4 8(2), 1.59 9(4), l.540(5), l.257(3)A. a= ll.53 A 기타사항 광물명은 오래전 석류석을 가공하였던 소아시아의 지 명인 알라반다 (alabanda) 에서 유래되었다. 알만다이트 (alman dit e) 라 고도 한다. 편암처럼 이질 퇴적암이 변한 광역 변성암 내에서 주 로 발견되며, 화산암 내에서 반정으로도 산출된다. 인도, 스리랑 카, 마다가스카르 , 탄자니아, 잠비아, 브라질, 미국 등의 국가에 서 양질의 결정들이 산출된다.
【스페 샤르틴 ( Sp es sart ine ) > 색 황색, 주황색, 적갈색. 박편하에서는 무색이다 . 비중 4.12~4.20 굴절률 1.7 9~ 1.82 X 선 회절선 4.76( 1) , 2.91 (2), 2.60( 10 ), 1.8 86(2), 1.6 81 (2), 1.6 14(3), I.55 7(4)A . a=t I.63 A 기타사항 스페샤르타이트 (s p essa rtit e) 라고도 한다. 망간 성분이 있는 장미휘석, 테프로아이트(t e p hro it c) 등과 공생하는 겅우가 많 으며, 화강암질 페그마타이트나 스카론 광상 (skarn de p o s it)에서도 산출된다 . 스리랑카, 미얀마, 브라질, 미국 등의 국가에서 양질의 결정이 산출된다 . 【우바로바이 트 (Uvarov it e) 】 색 암록색 또는 에메랄드 녹색 . 박편하에서는 무색 또는 매우 옅은 녹색을 띤다. 비중 3.77 굴절률 1.87 X 선 회절선 4.24(2), 2.999(7), 2.684( 10 ), 2.557(2), 2.449(6), 2.3 5 2(3), l.60 3(6)A .. a= 11. 99 9A . 기타사항 처음 발견되었던 지명인 우바로프 (Uvarov) 에서 광물명 이 유래되었다. 크롬철석이 있는 사문암 내에서 주로 산출된다 . 우랄산맥, 히말라야산맥에서 양질의 결정이 산출되고 있다. 【그로슐라 (Grossular) > 색 백색, 녹색, 황색, 옅은 적색. 색에 따라 헤소나이트(황갈 색, 주황색, 적색)와 차보라이트(에메랄드 녹색)로 세분된다. 박편 하에서는 무색을 띤다.
비중 약 3.65( 해소나이트), 3.62( 차보라이트) 굴절률 1. 742~ 1.7 48( 해소나이트), 1.742( 차보라이트) X 선 회절선 2.959(3), 2.6 4 7(1 0 ), 2.417(2), 1.92 1 (3), 1.6 43(3), 1.58 1 (S)A . a= 11. 8 50A 기타사항 그로슐라라이트(g rossul arit e) 라고도 한다. 석회질 암석 이 광역 또는 접 촉 변성작용을 받을 때 주로 생성된다. 변성작용을 받 은 현무암의 공동속이나 열수변질과정을 거친 화강암질 페그마타 이트에서 발 견된다 . 투명하고 색이 선명한 해소나이트와 차보라이 트 는 보석으로 가공된다 . 양질의 해소나이트 결정은 스리랑카, 브 라질, 미국에서, 그리고 차보라이트는 파키스탄, 케냐 등에서 산 출 되고 있다. 특히 충남 부여군 지선리일대에는 초염기성암을 관 입한 약 10cm 정도 두께의 그로슐라맥이 발달하고 있는데 이는 세계적으로도 매우 희귀한 경우이다. 【안드라다이 트 (Andrad it e) 】 색 황색, 녹색, 갈색, 혹갈색. 특히 크롬에 의해 녹색을 띠는 변 종을 디 만토이 드 (deman t o i d) 라고 하며 석 류석 중 가장 귀 한 보석 원석으로 사용된다. 거의 불투명한 검은색 변종을 멜라나이트 (melan it e) 라고 한다 박편하에서는 무색 또는 매우 옅은 황색, 갈 색, 회색 등을 띤다. 비중 3.86 굴절률 1.73 4 X 선 회절선색 4.26(2), 3.015(6), 2.696(1 0 ), 2.462(5), 1.95 6(3), 1.67 3(3), 1.6 11(6)A . a=12.0 5 9A 기타사항 안드라다이트는 불순물을 많이 함유하고 있는 석회암 이 열 또는 동력 변성작용, 기타 변성교대작용을 받을 때 다음 반 옹식에 따라 생성되는 것으로 알려지고 있다.
3 CaCOJ + 3 Si0 2 + Fe20J - ---t Ca JF e2Sb012 + 3 CO2 방해석 석영 적철석 안드라다이트 이 반응이 일어날 때, FeO 가 추가로 유입이 되면 헤덴버가이트 가 만들어지며 , Si0 2 성분의 공급이 거의 없는 경우에는 다음의 반응식에서처럼 안드라다이트-헤덴버가이트 - 자 철석 의 공생 광물 군이 만들어진다. 4 CaCOJ + 2 Fe20J + 2 FeO + 5 Si0 2 ~ Ca .iF e2Sb012 十 CaFeSii 06 + 방해석 적철석 석영 안드라다이트 헤던버가 이트 FeJ0 4 +4 CO2 자철석 디만토이드는 사문암이나 편암에서 주로 산출되며, 우 랄산맥 이 대표적인 산지이다. 이곳에서 산출되는 결정 내에는 섬유상의 비 솔라이트 (b y ssol it e) 결정이 내포물로 존재하는 것이 특징이다. 멜 라나이트는 네펠린 섬장암과 같이 알칼리 성분이 많은 화성암에서 주로 산출된다. 【하이 드로그로슐라 (H y dro gr ossular) 】 색 녹색, · 분홍색, 청색, 회색. 녹색은 크롬에 의해, 분홍색은 망간에 의해 발색된다. 박편하에서는 거의 무색으로 관찰된다. 비중 3.35~3.5 5 굴절률 1.7 0~ 1.73 X 선 회절선 5.13(9), 4.4 4 (4), 3.35(5), 3.14(5), 2.8 1 0(8), 2.465(3), 2.295(1 0 ), 2.039(9), t.74 4(4), t.68 0(5)A. a=12.572A 기타사항 Ca 이 유입되면서 변성교대작용이 일어난 곳, 또는 물
과 Al 성분이 첨가 되면서 변질된 반려암 등에서 산출된다 . 남아프 리카공화국, 미국, 캐나다, 뉴 질랜드 에서 양질의 결정이 산출된다. 4. 3 . 1. 9 녹럼석군 ( EPIDOTE GROUP) 녹럽석군( 유 .' k ift 1 i群) 에는 클 리노조이사이트, 녹렴석, 피몬타이 트, 간립석, 조 이사이트 등 5 개의 광물이 속해 있다 . 이들은 규산 염 광불의 구조 중 복사면체 (1 及四面體, double tet r a hedra stru ctu r e) 구 조 를 하고 있다. 이 들 광물의 구조에는 S i 201 의 복사면체뿐만 아니 라, SiO ~ 사면체도 있다. 또한 b 축 방향을 따라 AIOS} AIO 』 ( OH)! 로 구성된 8 면체상 다면체가 연결된 쇄상( ift ~k) 구조도 있다(그림 4.35). 이들 쇄상 구조는 S i O~ 와 Sh07 다면체에 의해 연결되어 있 다. 이와는 별도로 팔면체 구조가 있어 클리노조이사이트의 경우 팔 면체 중심 에 Al 이, 녹렴 석에서는 F e-와 A1 이 자리잡는다 . 녹렴석군 에 속하는 광물의 일반화학식은 AzBJ C (O, OH, F) IJ으로 표현될 수 있으며, A= C a, CeJ+ , La· , Y J ♦, Th, Fe!•, Mn2•, Mn3' , Na, B= Al, Fe·, Mn -, Fe2', Mn2', Ti, C=Si 등의 원소가 위치한다. 녹 렴석군 에 속하는 광물 중 클리노조이사이트, 녹렵석, 홍렴석, 갈 렵석은 모두 단사정계의 2/m 정족, P2J m 공간군의 결정구조를 지 니고 있으며, 클리노조이사이트의 동질이상체인 조이사이트는 사 방정계로 정출된다. 클리노조이사이트와 조이사이트의 경우 조이 사이트의 a 축 길이가 클리노조이사이트의 2 배인 결정학적인 관계 가 있다 . 【클리 노조이 사이 트 (C li nozo i s it e) 】 화학성분 Ca2Ah(Si0 ~)J( OH) . CaO 14.3%, AhOJ 25.1%, SiO i 59.1 %, H20 1.5% . 녹렴석과 클리노조이사이트는 완전고용체를 형 성한다 .
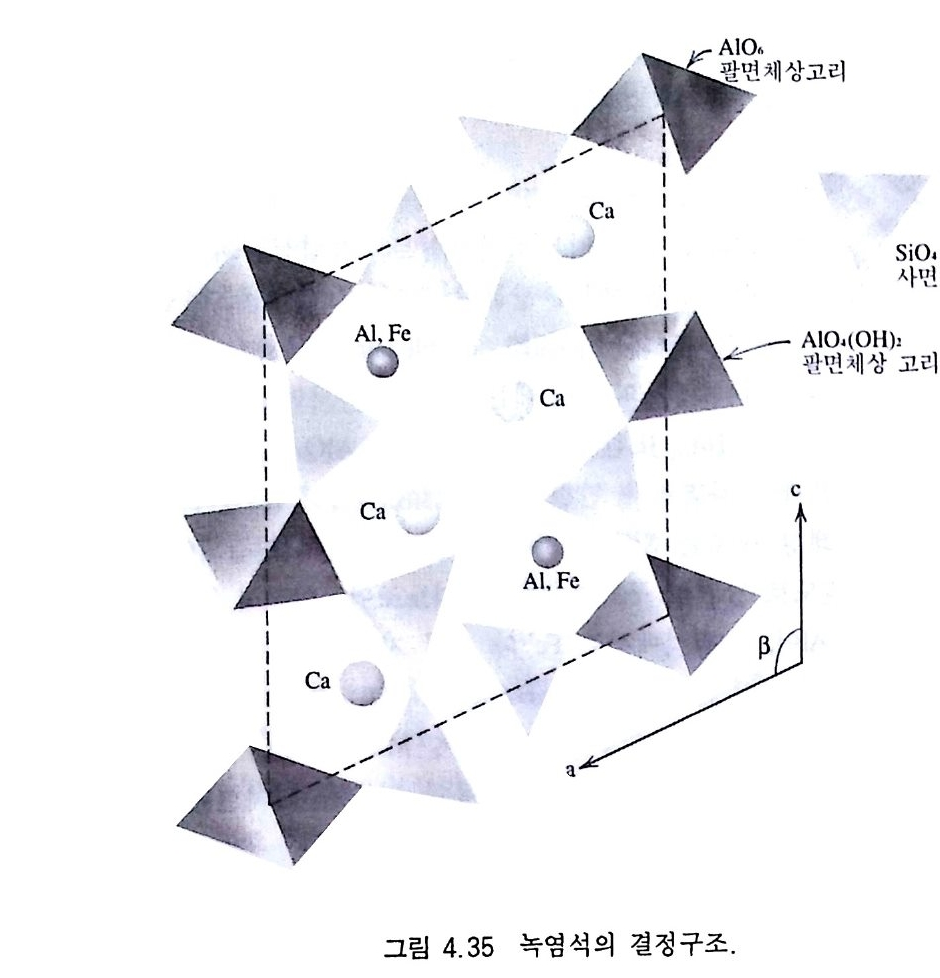 /
/
결정계 단사정계. a=B.86, b=5.59, c=1 0.12 A , /3=1 15°23' . 2=2. 색 옅은 녹색, 분홍색, 회색. 투명 또는 반투명하다. 박편하에 서는 거의 무색이다. 다색성은 거의 없다 . 결정형태 b 축 방향을 따라 길쭉한 주상 형태의 결정을 나타내 며, 장축 방향에 나란하게 조선이 발달한다. 입상질 또는 괴상으 로도 산출된다. 간혹 섬유상 형태로 존재한다. 벽개 {001 } 방향의 완전한 벽 개, {10 0} 방향의 불량한 벽 개 가
발달한다. 경도 6~7 바중 3.25~3.4 5 광택 유리 광택 굴절률 a=1 .7 10~1 .72 3, /3=1.71 5~1 .72 9, y=1.71 9~1 .73 4. 복굴 절률 = 0.005~0.Oll. 간섭색은 l° 의 중간색이다. 소광 특 징 결정 의 장축 방향을 따라 평행소광, 그에 수직인 방향 (b 축에 수직인 방향)으로 절단된 입자는 최대 소광각이 약 12· 에 이 른 다 . 광학부호 이 축 성, (+). 2V=66~90°. 광축면이 (010) 이다. 장축부호 b 축을 따라 /3가 있으므로, 장축을 따라 빠른 광선 또 는 느린 광선이 진동할 수 있다. X 선 회절선 8.01(8), 5.03(5), 4.77(3), 4.58(2), 4.00(4), 3.9 8 (4), 3.75(3), 3.4 7 (5), 3.4 0 (3), 3.1 9 (3), 2.9 2 (4), 2.89(1 0 ), 2.79(8)A 기타사항 각섬암, 각섬석 편암, 글로코페인 편암 내에서 동력 변성작용의 산물로 발견된다. 클리노조이사이트의 생성과정은 다 음의 반응식으로 나타낼 수가 있다. 3 (Mg , Fe)sAhSb01o(OH) 다 10 CaCOJ + 21 SiO z +-+ C 직J S iJ Ou(OH) 녹니석 방해석 클리노조이사이트 + 3 Ca i(M g , Fe)sS i sO 끄 (OH)2 + 10 CO2 + 8 HiO 양기석 화성암에서도 사장석이 열수 변질되어 산출되는 경우가 있다. 광물명은 발견자인 BaronvonZo i s 의 이름에서 유래되었다 . 청색의 투명한 변종을 탄자나이트(t anzan it e) 라 하고, 분홍색인 변종을 툴
라이트(th ul it e) 라고 하는데 이 두 가지 물질 모두 보석으로 쓰인 다 . 최근 충남 부여군 지선리의 그로슐라 석류석맥 내에서 툴라이 트가 발견된 바가 있다. 【녹렴 석 (Ep ido te ) > 화학성분 Ca i(A l, Fe)J ( Si0 4 )3 ( 0H) . 만약 Fe J+가 (Fe+Al) 합계 의 15% 미만이면 클리노조이사이트가 된다. 결정계 단사정계 . a=8.90, b=5.63, c=10.20A, /3=1 15°24' . Z=2. 색 황록색, 녹색, 검정색. 반투명하다. 박편하에서는 무색 내지 옅은 황록색을 띤다 . 약한 다색성을 띤다. 결정형태 b 축을 따라 길쭉한 주상 결정으로 산출되며 (그림 4.36) 입상, 섬유상, 또는 괴상 형태로도 산출된다. 벽개 {001} 방향의 완전한 벽개가 발달한다 . 경도 6~7 비중 3.3 5 ~3.4 5 . Al 을 치 환하는 Fe 의 양이 증가할수록 비 중이 커 진다. 광택 유리 광택 양각높음 굴절률 a= l.72 0~ 1.73 4, {3= 1.7 24~ 1.76 3, r= 1.7 34~ 1.77 9. 복굴
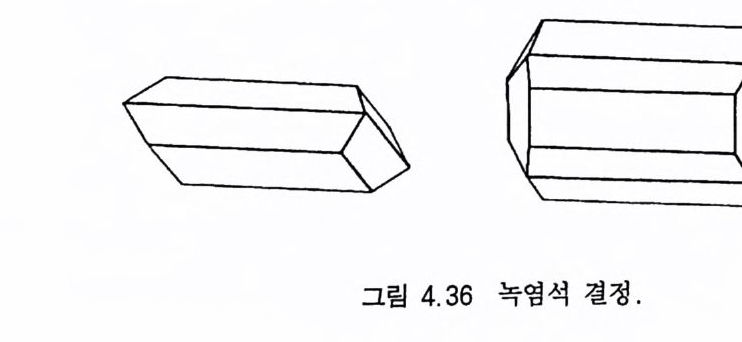 二
二
절률 =0.014~0.045. Al 을 치환하는 Fe 의 양이 많을수록 복굴절률 도 커진다. 소광특징 장축 방향을 나타내는 결정 입자는 평행소광을 한다. 간섭색 최대 간섭색이 약 2~3· 의 간섭색에 해당한다. 장축부호 입자의 장축 방향을 따라 빠르거나 느린 광선이 진동 한다 . 광학부호 이 축성, (-) . 2V=69~89°. X 선 회절선 5.0 5 ( 3), 4.02(5), 3.4 9 (3), 3.4 0 (4), 2.900(10), 2.817(4), 2.688(7), 2.679( 10), 2.656(3 ), 2.599(5), 2.460(s)A 기타사항 녹렴석(섬k i盜石)이란 광물명은 〈 커진다〉라는 의미의 그 리스어에서 유래하였는데, 그 이유는 주상 결정의 한쪽 바닥면의 길이가 다 른 쪽보다 더 길기 때문이었다 . 클리노조이사이트와 생 성과정이 거의 동일하다. 변성광물로 산출하는 경우가 가장 많은 데, 장석, 휘석, 각섬석, 혹 운모 등이 광역 변성작용을 받아 생성 된다 공생하는 광물로는 녹니석, 양기석, 회중석, 석류석 등이 있다 주로 편암, 편마암, 대리암, 각섬암에서 산출된다. 화성암 에서도 열수변질의 산물로 생성된다 . 염기성 화성암이 동력 변성작용 을 받을 때에도 생성된다. 양질의 결정은 오스트리아의 운터슐츠바하 탈 (un t ersulzbach t al), 미국의 알래스카 등지에서 산출된다. 【홍렴 석 (Pie m onti te) > 화학성분 Ca i(A l, Fe, Mn )J( S i O 』)J (OH) . 결정계 단사정계. a=8.843, b=5.665, c=10.1 5 0A, /3=1 15.25° 색 황색, 주황색, 적색, 보라색. 박편하에서는 결정의 몸색보다 매우 옅은 색을 띤다. 다색성이 강하다. 결정형태 자형은 주상 결정 형태이지만, 주로 입상 또는 괴상으 로 존재한다.
경도 6.5 비중 3.4 5 벽개 {001} 방향의 기저 벽개가 발달한다. 양각높음 굴절률 a= 1.74 5 ~ 1.7 58, /3= 1.7 64~ 1.78 9, y= 1.8 06 ~ 1.832. 복굴 절률 =0.061 ~0.082. 소광특징 평행소광 간섭색 몸색에 의해 가려져서 관찰하기 어렵다 . 장축부호 측정이 매우 어렵다. 광학부호 이축성, (+). 2V=56~86° X 선 회절선 8.00(2), 5.02(4), 4.00(5), 3.5 0 (4), 3.20(3), 2.903(1 0 ), 2.831 (4), 2.690(4), 2.670(4), 2.598(5), 2.5 2 8(4), 2.4 0 7(5), 2.3 0 2(3), 2.l 59 0)A 기타사항 피드몬타이트(pi edmon tit e) 라고도 한다. 편암 또는 편마 암에서 주로 산출된다. 광물명은 1853 년 광물학자인 Kenn go tt에 의 해 처음 발견된 이탈리아의 피몽 (P i emon te)지방의 이름에서 유래되 었다. 【갈렴 석 (Allanit e) > 화학성분 (Ca,F ff+ ,C e,La ,N a)i (AI,F e,M n,B e,Mg )J( Si0 4 ) (Si2 0 1) (OH) 결정계 단사정계 . a=8.93, b=5.7 7 , c=10.157A . /3=1 14.69°. z=2 색 갈색, 암갈색, 검은색. 조혼색은 녹회색 또는 갈회색 . 지방 광택 박편하에서는 갈색을 띠며, 다색성은 명료한 편으로서 옅은 갈색으로부터 짙은 갈색으로 변한다. 결정의 표면은 대개 황갈색 의 풍화물질로 덮혀 있다. 결정형태 괴상 또는 입상질 형태로 산출된다.
벽개 {001} 방향의 불완전한 벽개가 발달한다 . 경도 5.5~6 비중 3.5 ~ 4.2 양각 높 다. 굴 절 률 a= l.690 ~ 1.79 1, {3= 1.70 0 ~ 1.81 5, r= I.70 6 ~ 1.828. 복굴 절률 = 0.01 ~0 .03 소광특징 주로 평행소광을 한다. 간섭색 광물 몸색에 의해 가려져 관찰이 어렵다. 장축부호 측정하기가 어려움 광학부호 이 축성 , ( -) . 2V =60~90° X 선 회절선 3.53(4), 2.92(1 0 ), 2.886(3), 2.714(7), 2.627(4), 2.561 (2), 2.1 8 2(4), 2.158(3), 2.135(2)A 기타사항 갈렴석은 U, Th 과 같은 방사성 원소에서 방출되는 알 파(a.)선에 의해 결정구조가 파괴되어, 메타믹트 상태로 변해있는 경우가 많다. 이러한 경우 X 선 회절실험을 하면, 회절선의 양상이 뚜렷하지 않고, 회절선의 수효도 매우 적게 된다. 갈렴석이 변질 되거나 매타믹트 상태로 되면 부피가 팽창되어 결정 내에 균열이 생기게 된다. 메타믹트 상태인 결정을 600°c 에서 수시간 동안 가 열하면, 파괴되었던 결정구조가 상당히 복원되어 X 선 회절실험을 할 경우, 회절선의 형태와 수효가 크게 향상된다. 비중 값도 가열 시킨 후에 다소 증가한다 . 이것은 가열 과정을 통해 결정구조가 복원되면서 부피가 감소하기 때문이다. 갈렴석은 화강암, 섬장 암, 섬록암, 페그마타이트와 같은 화성암 및 접촉 변성작용을 받은 대리암에서 발견된다 . 러시아의 우랄산맥, 그린란드, 스웨덴 등이 대표적인 산지이며, 우리나라에서는 경남 하동군 옥종면에서 회장 암의 진화 말기에 형성된 페그마타이트에서 괴상 형태로 산출되고 있음이 수년전 처음 발견된 바가 있으며, 충북 어래산 일대에서도
산출된다. 갈렴석은 1808 년 그린랜드에서 이 광물을 처음 발견한 Thomas Allan 의 이름을 기념하여 명명되었다. 오르다이트 (o rthit e) 라고도 불린다. 【조이 사이 트 (Zo i s it e) 】 화학성분 Ca2(Al, Fe)J( Si 0 4 )J ( OH) . CaO 25~ 2 5% , Al iO, 32~35%, Si0 2 37~39%, H20 l~2%. 클리노조이사이트와는 동질 이상체인 관계이다. 결정계 사방정계 . Pnmc. a=16.1 9 , b=5.4 5 , c= 1 0.1 3 A 색 회색, 녹색, 갈색, 분홍색( 툴 라이트) . 박편하에서는 무색이 며, 망간 성분에 의해 분홍색을 띠는 툴라이트 변종은 박편하에서 도 약한 분홍색과 함께 다색성을 나타낸다. 유리광택을 띤다. 조 혼색은 백색이다. 결정형태 b 축을 따라 길쭉한 침상 형태를 나타낸다. 괴상 형 태 로 산출되는 경우가 일반적이다. 벽개 {10 0} 방향의 완전한 벽개 및 {001} 방향의 불완전한 벽개 가 발달한다. 경도 6 비중 3.2~3.4 양각높음 굴절률 a=l. 68 5~1 .70 5, /3=1.68 8~i .71 0, r=1 .697~1 .72 5. 복굴 절률 =0.004~0.008. 결정축과 주진동축의 배열방식에 두 가지가 있 다 . 죽, a=Z, b=Y, c=Z 인 경우와, a=Z, b=X, c=Y 인 경우 이다(그림 4.3 7 ). 전자인 경우는 철 (Fe) 을 함유하지 않은 결정에서 발견되며, 비정상적인 짙은 청색의 간섭색을 나타낸다. 후자는 철 울 함유하고 있는 결정에서 관찰되며, 정상적인 간섭색을 나타낸다. 소광특징 평행소광을 한다.
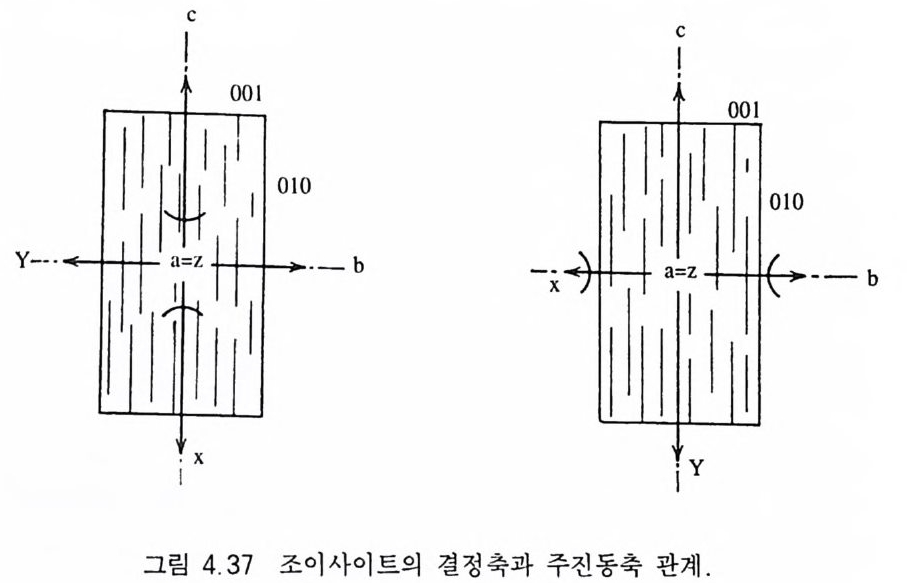 II‘ C 001 CI
II‘ C 001 CI
장축부호 장 축 방향을 따라 빠른 광선 또는 '느린 광선이 진동한다. 광학부호 이 축 성, (+ ). 2V=30~60• . 기타사항 Ca 을 Mn 이 치환하면 분홍색 변종이 되는데 이룰 특히 툴 라이트(t hul it e) 라고 하며, 보석으로 가공한다. 우리나라에서는 충남 부여군 외산면 일대에서 산출된다. 점토질 또는 석회질 성분 을 함유하고 있는 사암 또는 쉐일이 광역변성작용을 받을 때 주로 생성되며, 불순물을 함유한 석회암이 열변성작용을 받을 때, 염기성 화성암이 광역변성작용을 받을 때에도 만들어진다 . Ca 성분이 높은 사장석이 열수변질을 받아 서수리티제이션 (sauss uriti za ti on) 현상이 일어날 때에도 만들어진다. 광물명은 이 광물 표품을 광물학자인 Werner 에게 연구하도록 처음 제공했던 Baron von Zo i s 의 이름에서 유래되었다 .
4. 3. 1. 1 0 사문석군 (SERPENTINE GROUP) 사문석군(蛇紋石群)은 M g J SbO;(OH) 』의 이상화학식으로 표현되는 크리소타일, 앤티고라이트, 라이자다이트 등 3 개의 동질이상체로 구성된다. 이들 광물은 층상구조로 되어 있는 규산염 광물로서, S i O 』 다면 체 가 수평 방향인 a 축 방향으로는 5.3 A , b 축 방향으 로는 9 . 2A 의 간격으로 육각형태로 연결되어 있고, 수직인 c 축 방향으 로 는 7.3 A 정도의 간격으로 층들이 반복된다. 사면체로 연결된 층과 팔면체로 연결된 층이 하나씩 결합되어 만 들 어진 구조가 c 축을 따 라 반복되는데 이를 I:I 층상구조라고 한다. 배위수가 6 인 자리의 2/3 인 4 자리가 +3 가 이온이 채워지기 때문에 다이 -옥타헤드랄 (di -o cta h edral) 광물이라고 한다. 원소간의 치환은 그리 활발하지 않은 편이며, S i를 Al 이, M g을 Al 과 Fe 등의 원소가 교대한다. 그러나, 실제로 M g을 치환하는 Fe 의 양은 매우 적은 편이다. 사 문석은 초염기성암의 일종인 페리도타이트가 변질되어 만 들 어진 경우가 많은데, 이때 원암의 감람석이나 휘석 내에 있던 철성분은 사문석 내로 결정화가 되는 것이 아니고, 자철석이나 적철석과 같 은 별도의 광물을 만들면서 분리된다. 실험적인 연구결과에 의하 면, N i도 M g을 상당량 치환할 수 있음이 확인되었지만, 실제 천 연산 사문석 광물에서는 N i의 함량이 0.25% 정도로 매우 낮다 . 사 문석을 공기중에서 600°c 로 가열하면, 다음 과정을 통해 감람석이 만들어진다. 2 M gJ S iz Os(OH) 己 3 M g zS i O 』 + Si0 2 + 4 H20 사문석 감람석 석영 사문석의 시차열분석 (D.T.A.) 결과에 따르면 700°~800°C 에서 구 조수 (stru c tu ra l wate r ) 의 팽 창에 의 한 홉열 피 크 (endoth e rm ic pea k) 가
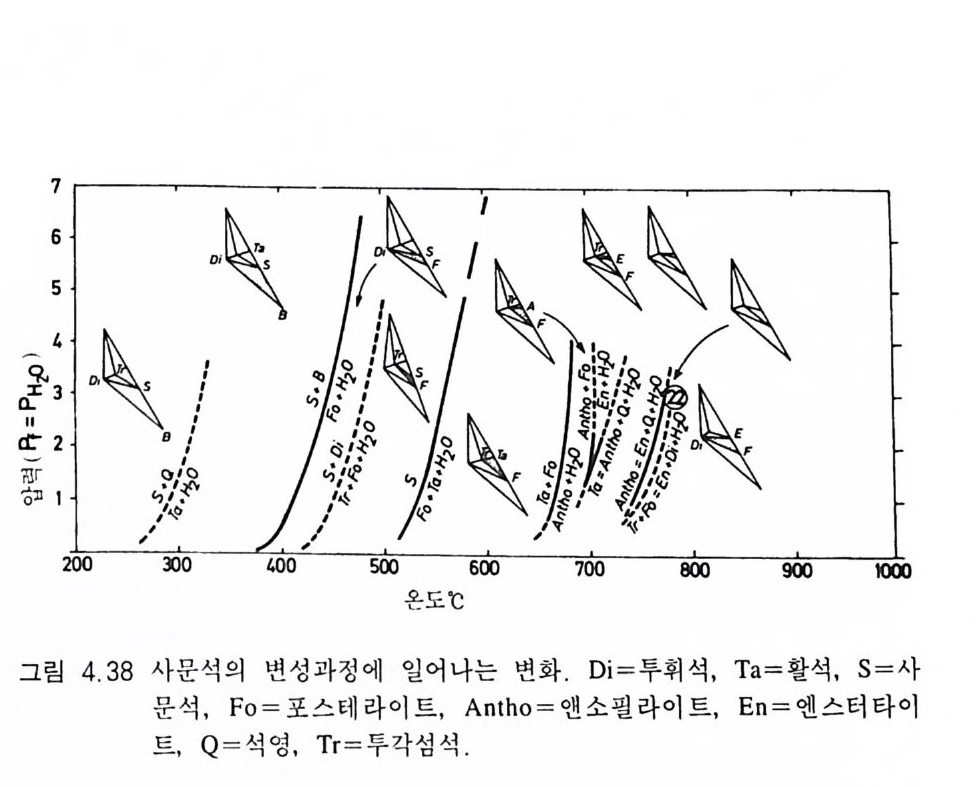 76543`21
76543`21
나타나고, 800 °~ 820 ° C 에서는 감람석 생성에 의한 발열 피크 (exoth e nnal p eak) 가 나타난다. 그 밖에도 llo·c 등의 낮은 온도에 서 넓고 희미한 홉열 피크가 나타날 수 있는데, 이것은 사문석 입 자 표면에 묻어 있는 수분의 추출에 의해 생긴 것이다. 실험적 연 구 결과에 의하면, 열수가 포함되는 환경에서 사문석은 500°C 이 상이 되면 감람석과 활석으로 변한다(그림 4.3 8 ). 물 이의의 다른 성분이 개입되지 않는 환경에서는, 400•c 이하의 온도에서 감람석 이 사문석으로 변하며, 철 성분을 함유되어 있는 감람석인 경우는 이보다 더 낮은 온도에서 사문석으로 변하며 자철석이나 적철석도 함께 만들어진다. 【크리 소타일 (Chry so ti le )> 결정계 단사정계(2/ m) 및 사방정계 등 두 동질이상체가 있다. 단
사정계 a=5.34, b=9.2 5 , c=14.65A, /3= 9 3•16' , 사방정계 a= 5.3 4 , b=9.25, c= 14.20A. Z=4 색 옅은 녹색. 박편하에서는 거의 무색이다. 견사광택을 띤다 . 반투명하다 . 결정형태 섬유상 결정으로 산출된다 . 특히 a 결정 축 방향 을 따라 길쭉하게 성장되어 있는 동시에 휘어져 있는 것이 특 징이다 . 또한 머리카락처럼 원통 형태를 하고 있거나 속이 비어 있는 경우도 있다. 경도 2~3 비중 2.55 이하 양각낮다 . 굴절률 (0=1.5 32~1 .54 9, E=1 .54 5~ 1 .55 6. 복굴절률 =0.013~0 . 017 . 최대 간섭색은 1° 의 밝은 황색이다 . 소광특징 거의 평행소광을 나타낸다. 장축부호 장축 방향을 따라 느린 광선이 진동한다. 광학부호 이축성, (+) X 선 회절선 단사정 계 7.2 8 (6), 4.54(1 0 ), 3.6 4 (4), 2.62( 4) , 2.5 3 (4), 2.4 5 (4), 2.28(1 ), 2.090), 1.53 1 (5), 1.50 1 (5)A, 사방정 계 7.10(1 0 ), 4.63(2), 4.4 0 (4), 3.88(3), 3.55(7), 3.31 (2), 2.624(3), 2.4 9 9(5), 2.3 2 6(8), 2.1 3 4(2), I.94 5(0A 기타사항 크리소타일은 사문암 내에서 맥상의 형태로 산출되는 것이 특징이다. 크리소타일의 생성에 대해서는 대략 두 가지의 학 설이 있다 . 즉, 원암으로부터 사문석이 만들어지는 과정중에 직접 만들어졌다는 학설과, 원암의 균열속에 있던 광화용액으로부터 크 리소타일이 성장하면서 기존의 광물을 교대했다는 학설이 있다(그 림 4.3 9 ). 크리소타일은 섬유상 조직과 요곡성에 의해 그 가치가 좌우되는데, 이들 성질이 우수할 경우 방열복, 방열 건축재료 또 는 공업 재료, 브레이크 라이닝 제조 둥에 사용된다. 백색 석면
 그림 4.3 9 사문석내에 발달하는 크리소타일 맥(백색) .
그림 4.3 9 사문석내에 발달하는 크리소타일 맥(백색) .
(whit e a sbesto s ) 이 라고도 불린다. 그러 나 이 광물이 호흡기 관에 다량 홉수되었을 경우에는 체의로 배설되지 않는 관계로 발암의 원인이 될 수 있기 때문에 주의하여야 한다. 석면물질의 95% 가 크리소타 일이며, 러시아의 우랄산맥과 캐나다의 노바스코시아주에서 전세 계 생산량의 대부분을 채광하고 있다. 광물명은 그리스어인 chrusos( 황금색)와 ti los( 섬유)에서 유래하였다. 【앤티 고라이 트 (An tig o rit e) 】 결정계 단사정계 및 사방정계의 동질이상체가 있다. 단사정계 a=43.53, b=9.259, c=7.263A, /3= 91° 8 ' . Z= 16 색 황록색, 녹색. 박편하에서는 무색 또는 옅은 녹색이다. 지방 광택 또는 견사광택을 띤다. 결정형태 짧은 주상 또는 섬유상 형태를 취한다. 휘석 또는 감 람석의 주변부를 따라 존재하는 경우도 많다. 경도 2.5 비중 2.6 양각낮음 굴절률 a=l.555~1 .5 64, /3=1.56 2~1 .57 3, r=1.56 2~1 .57 3. 복굴 절률 =0.007~0.009. 최대 간섭색은 1· 의 황색이다.
소광특징 일반적으로 평행소광을 한다. 장축부호 장축 방향을 따라 느린 광선이 진동한다. 광학부호 이축성, (-). 2V=20~90° X 선 회절선 7.29( 10 ), 6.4 3 (4), 5.82(4), 5.1 5 (4), 4.6 4 (4), 4.26(2), 3.61(8), 2.794(2), 2.525(10), 2.4 5 8(6), 2.4 2 9(2), 2.3 8 6(2)A 기타사항 앤티고라이트는 사문암의 주구성 광물이며, 다 결 정 집 합체로 산출되는 것이 보통이며, 우리나라에서는 충남 부여군 일 대에 분포하고 있다. 특히 앤티고라이트중 녹황색을 띠면서 투명 또는 아투명한 변종이 있는 데, 이를 보위나이트 (bowen it e) 라 하며 보석으로 가공되고 있다. 보위나이트는 함남 단천군에서 산출되었다 는 기록이 있다. 한편 부여군 외산면에서는 사문암을 관입하고 있는 석류석맥의 양측 접촉부를 따라 짙은 녹색을 띠면서 투명 내지 아투 명한 앤티고라이트 변종이 산출되고 있음이 최근 발견되었는데 이 를 귀 사문석 (pre cio u s serp e nti ne ) 이 라고도 칭 한다. 이 변 종은 경 도가 약 5~6 이고 색깔과 투명도가 우수하여 귀한 보석으로 알려져 있으며 〈조선 비취〉 또는 〈한국 비취〉라고 부른다 . 굴절률은 약 1.56 , 비중 은 2.67, 지방광택을 띤다. 화학성분은 Si 02 42.4 9 %, M gO 39.08%, Fe20J 3.85%, H20 1 1. 87% 이다. 그외 미 량 성분으로는 Cr(2188p pm ), Ni (lllO p pm ), Co(58p pm ), Ta(1 0 8p pm ) 등이 있다 . X 선 회 절자료는 7.4 0 (1 0 ), 4.64(3), 3.68(7), 2.76(7), 2.53(5), 2.5 0 (3), 2.1 1 (3), 1. 11(2)A 이다. 광물명은 이 광물이 처음 발견된 지명인 이달리아의 An tig o ri o 에서 유래되었다. 【라이 자다이 트(Li zard it e) 】 결정계 단사정계, 육방정계, 삼사정계, 사방정계 둥의 변종이 있다 단사정계 a=5.3 l , b=9.20, c=7.31A (사방정계로 격자지수화
 그림 4.4 0 방사상 형 태의 라이자다이트 광 물 집합체 .
그림 4.4 0 방사상 형 태의 라이자다이트 광 물 집합체 .
함 ), 육방정 계 a=S.340, c=7.100A, 삼사정 계 a=S.3 2 2, b= 9.219, c= 43.s9A( 사방정계로 격자 지수화함) 색 백색, 연록색, 황색, 녹색. 박편하에서는 무색 또는 옅은 녹 색으로 관찰된다 . 결정형태 미립 결정인 경우가 대부분이며, 전자현미경으로 관찰 하면 판상체로 되어 있음을 알 수 있다 . 방사상 형태의 광물 집합 체 로도 산출된다(그림 4.4 0 ) . 경도 2.5 비중 2.55 벽개 {001 } 방향의 완전한 벽개가 발달한다. 양각낮음 굴절률 a=l. 53 8~1 .55 4, r=1.54 6~1 .56 0. 복굴절률 =0.006~0.008 .
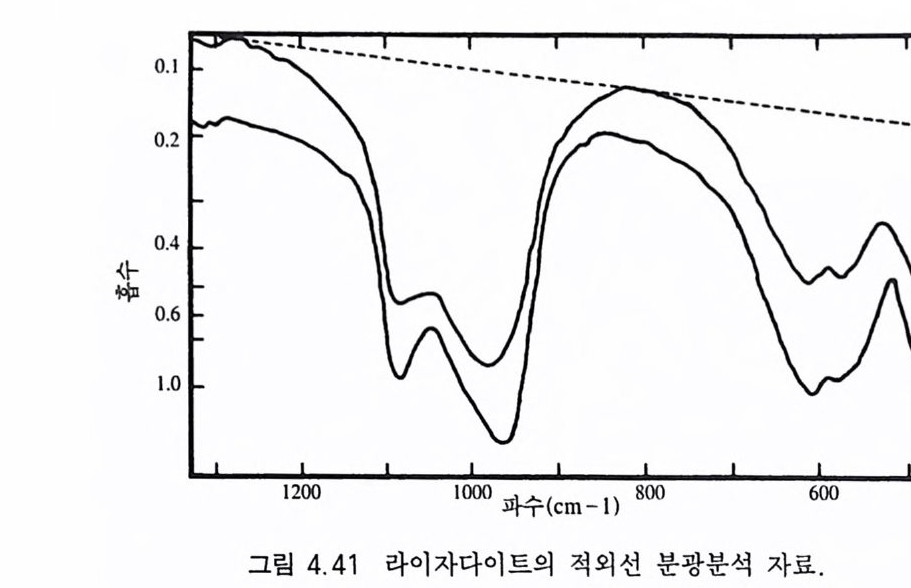 0.1
0.1
최대 간섭색은 1· 의 밝은 황색이다 . 소광특징 길쭉한 결정 입자는 평행소광을 나타낸다 . 장축부호 장축 방항을 따라 느린 광선이 진동한다 . 광학부호 이축성, (-) X 선 회절선 단사정 계 7.4 (10 ), 4.6 ( 8), 3.9(5), 3.67(8), 2.875( 1), 2.663(4), 2.505(1 0 ), 2.156(8), l.79 9(s)A, 육방정 계 7.10(8), 4.63(4), 3.88(4), 3.5 5 (6), 2.4 9 9(1 0 ), 2.133(5), 1.771 (3)A, 삼사정 계 7.33(1 0 ), 4.60(6), 3.66(1 0 ), 2.6 2 3(3), 2.502(1 0 ), 2.335(7), 2.1 4 9(6), 1.96 3(7), 1.5 35(8), 1.50 1 (7)A, 사방 정 계 7.25(6), 4.61 (2) , 3.62(6), 2.503(1 0 ), 2.148(4), 1.78 8(2), 1.54 1 (3) , L507 (2)A 기타사항 경남 울산 일대에 분포하는 사문암의 주구성 광물이 다. 라이자다이트에 대한 적외선 분광분석 실험자료에 의하면(그 림 4.4 1), S i -0 의 팽창에 의한 흡수 피크와 0H 의 진동에 의한 홉 수 피크가 각각 975cm·' 와 610cm · 1 에 기록됨을 알 수 있다 .
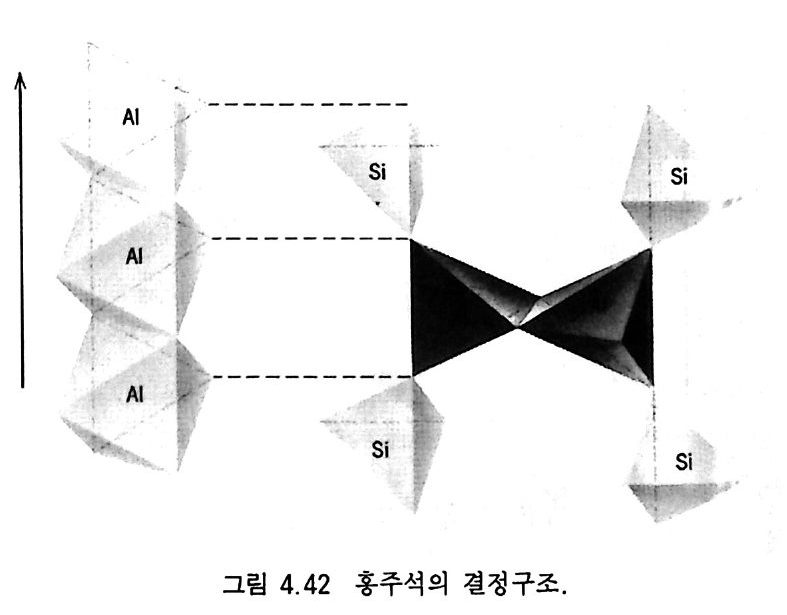 Al .r
Al .r
4. 3. 1. 1 1 규선석군 (SILLIMANITE GROUP) 규선석군(珪線石群)에는 홍주석(紅柱石), 규선석(珪線石), 남정 석(藍晶石) 등 3 개의 광물이 있으며, 이들은 결정구조는 상이하지 만 모두 AhS i Os 의 화학식으로 표시되는 동질이상체들이다. 이들 세 광물들은 독립사면체 구조를 지니고 있으며, 팔면체의 능을 공 유하면서 만드는 쇄상구조가 c 축을 따라 존재한다. 결정구조 내의 Al 의 위 치 에 따라 AllIAll61S i 05 로 표현할 수 있으며, 괄호 속의 숫 자는 배위수를 의미한다. 홍주석은 Al 원자의 절반이 팔면체로 연 결되어 있는 쇄상 배위다면체(배위수 6) 내에 있고, 나머지 절반은 SiO , 다면체로 연결되어 있는 배위수가 4 인 구조 내에 있게 된다 (그림 4.4 2 ). 규선석에서는 Al 이 S i O, 와 AIO, 다면체가 교대로 연결 된 배위수 4 인 위치와, 배위수가 6 인 팔면체로 연결된 쇄상구조 내에 각각 존재한다(그림 4.43). 남정석의 경우에는 Al 모두가 배 위수가 6 인 팔면체상 배위다면체 내에 존재한다(그림 4.44). 따라
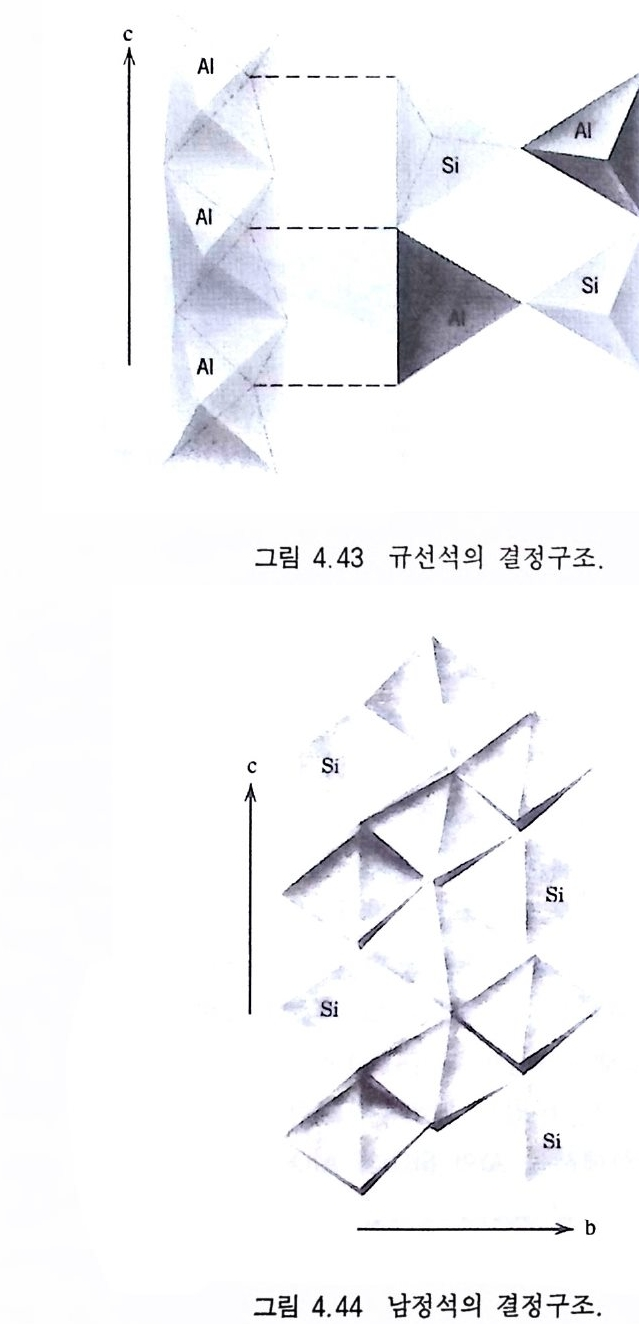 c
c
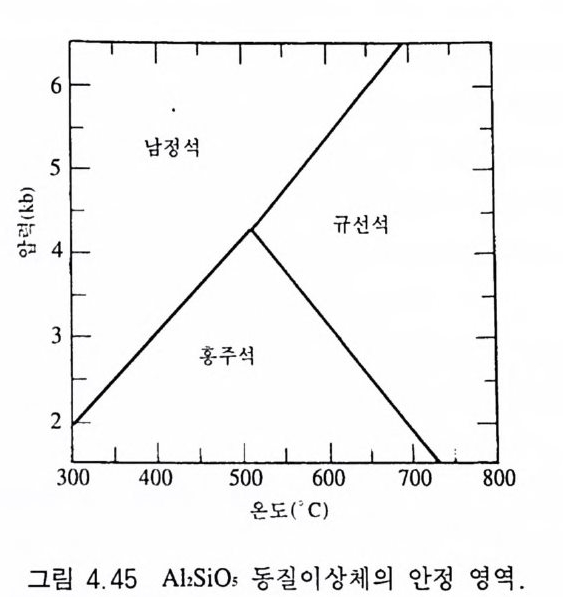 6
6
서 , 홍 주석 은 Al151Al '61S i 0s , 규선 석 은 All41Al '61S i 0s , 남정 석 은 Al1 6 1Al1 6 1S i 0 s 로 각각 표시할 수 있다 . 규선석군에 속하는 광물들은 모두 알루미늄 성분이 풍부한 이질 (泥 質 ) 퇴적암이 변성작용을 받을 때 AhO J +S i 02=AhS i Os 의 과정 울 통해 만들어진다. 변성환경에 따라 생성되는 광물이 달라지는 데 이에 관한 상다이어그램이 그림 4 .4 5 에 있다. 규선석은 고온에 서 동력변성작용이 일어날 때 만들어지고, 홍주석은 압력보다는 고온의 열변성작용이 우세한 접촉변성 환경에서 만들어진다. 남정 석은 온도보다는 압력이 크게 우세하게 작용한 변성환경에서 만들 어진다 . 이로부터 어떤 변성암 지역에 있는 편암 내에서 규선석이 변성광물로 존재한다면, 이것은 이 암석이 적어도 500°C 이상인 고온에서 변성작용을 받았음을 시사해 준다. 만약 편암 내에 위의 두 광물 또는 세 광물이 공존한다면 이것은 이 변성암이 만들어진
온도-압력의 환경을 보다 구체적으로 나타내 준다. 즉, 홍주석, 규 선석, 남정석이 함께 공존하는 편암이 있다면, 이 암석은 500°C 의 온도와 4000 기압 정도의 압력인 환경에서 변성작용을 받았음을 알 수 있게 된다. 세 광물의 비중 크기는 남정석 (3.5 5 ~3.66) > 규선석 (3 . 23)> 홍주석 (3 .1 6~3.20) 의 순서인데, 이것은 가장 고압인 환경에 서 안정한 남정석의 원자배열 밀도가 제일 크기 때문이다. 【홍주석 (Andalusit e) > 결정계 사방정 계 . 2/m 2/m 2/m, Pnnm. a=7.78, b=7.92, c= 5.57A 색 적색, 적갈색, 녹갈색. 투명 내지 반투명. 유리광택 . 박편하에 서는 거의 무색이며 간혹 적색을 띠기도 한다. 다색성이 뚜렷하다. 결정형태 주상 결정으로 산출되며, c 축에 직각으로 절단된 입자 는 거의 정사각형 모양이다. 어떤 결정에서는 검은 탄소물질이 십 자 모양으로 배 열되 어 있는데 이 러 한 변종을 공정 석 (chia s to l ite ) 이 라고 한다(그림 4.4 6 ). 경도 7.5 비중 3.1 6 ~3.20 벽개 {110} 에 나란한 벽개가 잘 발달하며, 이 때문에 c 축에 수직 인 방향에서는 거의 직각으로 교차하는 두 방향의 벽개가 관찰된다 .
 …만만 O 心心心
…만만 O 心心心
양각 높은 편이다. 굴절률 a=l.632, /3=1 .638, y=1 .643. 복굴절률 =0.007~0.011. 간 섭색은 I . 의 황색이다. 소광특징 장축을 지니는 결정은 평행소광을, 이에 수직으로 절 단된 입자는 대칭소광을 나타낸다 .. 장축부호 결정의 긴 방향을 따라 빠른 광선이 진동한다 . 광학부호 이축성, (- ) . 2V=84° X 선 회 절선 5.54( 10), 4.5 3 (9), 3.92(7), 3.52(6), 3.4 9 (4), 2.78(2), 2.77(9), 2.4 8 6(2), 2.4 8 2(2), 2.4 6 6(5), 2.273(4), 2.255(4), 2.170(9lA 기타사항 이질 성분이 많은 쉐일이 접촉변성작용을 받을 때 주 로 생성이 되며, 흔히 근청석 (cord i e rit e) 과 공존한다. 투명한 적색 결 정이 브라질과 스리랑카에서 산출되는데 이들은 보석으로 가공 된다 공정석은 얇은 두께로 잘라 공예품 장식용으로 사용된다. 스페인의 안달루시아 (Andalus i a) 가 대표적인 산지이며, 브라질, 오 스트리아, 호주에서도 산출된다. 홍주석은 분말로 만들어 자동차 점화 플러그나 내열성 요업제품을 만드는데 사용된다. 광물명은 처음 발견된 지명 (Andalus i a) 에서 유래되었다. 【규선석 (Sil lim anit e) > 결정계 사방정 계 . 2/m 2/m 2/m, Pbnm. a=7.44, b=7.60, c= 5.75A. Z=4 색 갈색, 옅은 녹색, 백색. 박편하에서는 무색이다 . 유리광택 . 투명 또는 반투명하다. 결정형태 가늘고 긴 주상 결정으로 산출된다. 약간 휘어진 형태 를 나타내는 경우도 많다. 섬유상 형태로 산출되기도 하는데 이 변종을 파이브롤라이트(fi brol it e) 라고 한다.
경도 6~7 비중 3.23 벽개 {010) 방향의 완전한 벽개가 발달한다. 박편하에서는 주상 결정에 직각인 방향으로 균열이 발달하여 마치 대나무 마디처럼 보이는 것이 특징이다 . 양각 높은 편이다. 굴절률 a= 1.65 7, {3= 1.6 58, r= 1.67 7. 복굴절률 =O.020~0.023. 최 대 간섭색은 주상 입자는 2· 청색을 나타내고, c 축에 수직으로 절 단된 입자에서는 복굴절률이 0.001~0 . 009 로 매우 작기 때문에 l ° 의 간섭색을 나타낸다 . 소광특징 길쭉한 결정은 평행소광, 이에 수직으로 만들어진 입 자는 대칭소광을 나타낸다 . 장축부호 장축 방향을 따라 느린 광선이 진동한다. 광학부호 이축성, (+). 2V=20~30° X 선 회절선 5.3 6 (2), 3.42(1 0 ), 3.37(7), 2.896( 1), 2.679(3), 2.541(4), 2.4 2 10), 2.204(6), 2.111(2)A 기타사항 규선석은 이질 성분이 많은 암석이 고온에서 동력변성 작용을 받을 때 만들어지는 변성광물이다 . 편암, 호른펠즈, 편마 암에서 주로 산출되며, 공생하는 광물로는 석영, 혹운모, 백운 모, 사장석, 석류석, 근청석 등이 있다. 규소 성분이 적은 암석에 서는 강옥과 공생하기도 한다. 광물명은 예일대학교 화학과 교수 였던 Benja min S illi man 의 이름에서 유래되었다. 【남정석 (Ky anite) > 결정계 삼사정 계 . i Pi a=7.I O, b=7.74, c=5.57A. Z=4. 색 청색, 백색, 회색, 녹색. 박편하에서는 무색 또는 매우 옅은 청색을 띤다 다색성이 관찰될 수 있다 . 유리광택 또는 진주광택.
결정형태 납작하고 긴 주상 결정으로 산출된다. 경도 방향에 따라 경도 차이가 현저하게 나타나는 대표적인 광 물로 서, 장축 방향으로 5, 이에 수직인 방향으로는 7 이다. 비중 3.55 ~ 3 .6 6 벽개 1100) 방향의 완전한 벽개가 발달하며, {010} 와 {001} 방향 으로는 덜 명료한 벽개가 발달한다. 양각 높 다 . 굴절률 a= 1.1 72, /3= 1.72 0, y=1.72 8. 복굴절률 =0.016. 간섭색은 1° 적색이다. 소광특징 최대 소광각은 주상 결정인 경우 약 30° 이고, c 축에 수 직인 입자는 거의 평행소광을 나타낸다 . 장축부호 장축 방향을 따라 느린 광선이 진동한다. 광학부호 이 축성, (-) . 2V=82° X 선 회절선 430(3 ), 3.7 7 (2), 3.35(7), 3.1 8 ( 10 ), 3.0 2 ( 1), 2.947(2), 2.727( 1), 2.699(3), 2.694(3), 2.520(3), 2.509(2), 2.3 5 5 0), 2.3 5 0(3), 2.3 3 1 (2)A 기타사항 남정석은 이질암이 광역변성작용을 받을 때 주로 만들 어지며, 석류석, 십자석, 강옥 등과 공생하는 경우가 많다. 페그 마타이트와 같은 일부 화성암에서, 또 에콜로자이트나 킴벌라이트 와 같은 초고압 변성암에서도 간혹 발견된다. 투명한 청색 결정이 스위스에서 산출되는데, 이들온 보석으로 가공된다 . 그 밖의 주요 산출국으로서는 프랑스, 인도, 케냐, 미국 등이 있다 . 남정석의 산업적 용도는 안달루사이트와 동일하다. 광물명은 〈청색〉을 의미 하는 그리스어에서 유래되었다. 4. 3. 1. 12 운모군 (MICA GROUP) 운모군에 속하는 광물들은 규소와 산소가 만들어진 사면체 또는
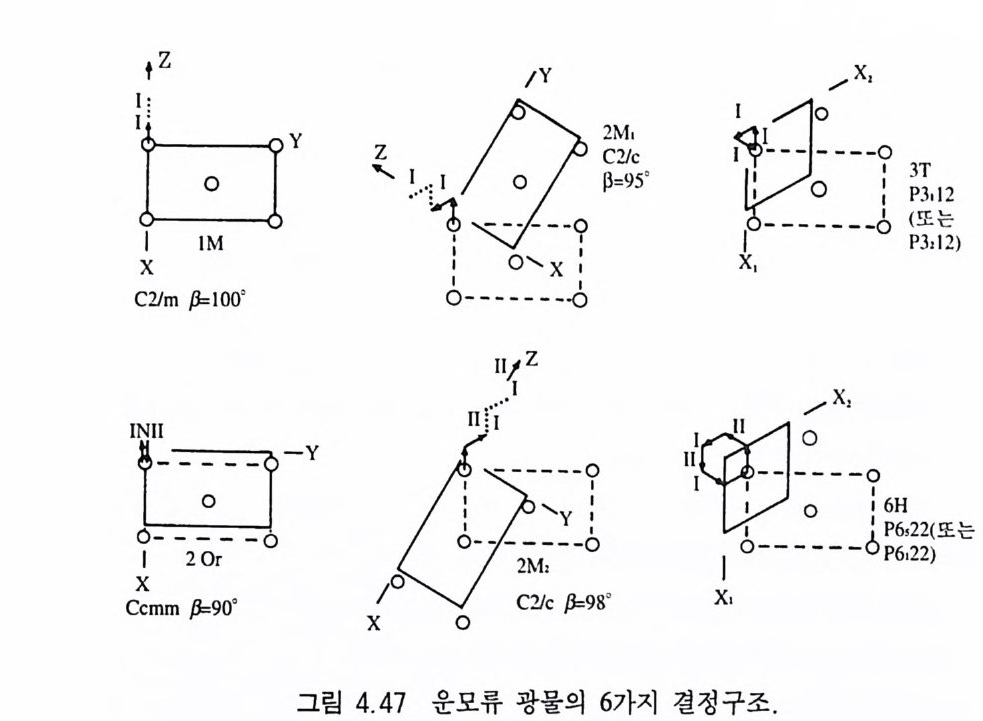 C:二:It2 z/m /}=IM 10 0' Y Y xz/ 。\ I·: ... .l4 o:II':》yf「0 -作 8。2- C귁 M깁 cO 5 。 x|:』 ’凡戶 i 0/oO x/-`.ii凡 O- O-6-H&P-I-I JPo잭功 IPT--'J 0끈 g 晶또 P 는 J
C:二:It2 z/m /}=IM 10 0' Y Y xz/ 。\ I·: ... .l4 o:II':》yf「0 -作 8。2- C귁 M깁 cO 5 。 x|:』 ’凡戶 i 0/oO x/-`.ii凡 O- O-6-H&P-I-I JPo잭功 IPT--'J 0끈 g 晶또 P 는 J
층상구조( 層 狀 構造층,상 구조( 層 狀층 構상造구,조 ( 層 狀 構造층,상 구조( 層 狀 構造, sheet s tru c tur e) 를 하고 있다. 사면체충(t e tr ahedral la y er) 은 [S i 0 4 ] 의 사면체 가 꼭지점에 있는 산소원자를 공유하면서 6 각형의 모양으로 연결 되어 있으며, 팔면체층 (oc tah edral la y er) 은 팔면체상 배위다면체가 능을 공유하면서 연결되어 있다. 운모 광물에는 사면체층 2 개가 팔면체층 한 개를 위 아래에서 결합하는 기본 단위가 c 축에 수직되 게 일정한 간격으로 반복하는 구조를 하고 있는데, 이를 2:1 구조 라고 한다. 혹운모나 백운모에서는 이 반복 거리가 약 10A 이다 . 운 모 내에서 층들이 규칙적으로 배열하는 방법에는 6 가지가 있으며 (그림 4.4 7 ), 이 때문에 동질이상체가 많다. M 은 단사정계, T 는 삼 방정계, O 는 사방정계, H 는 육방정계를 의미한다. lM, 2M1, 2M i 의 결정학적인 상호관계는, 우선 lM 은 기본형으로 생각하면 되
고, 2M, 은 lM 에 비하여, a 와 b 축의 단위포 길이는 동일하나 c 축으 로 반복되는 층 들 의 거리가 lM 의 경우보다 약 2 배가 된다는 것을 의미한다. 2M 2 는 lM 과 비교할 때, c 축의 반복거리가 약 2 배가 되 는 점 외에도 a 축과 b 축 의 값이 서로 바뀌게 된다. 백운모의 경 우, lM 인 광 물 에서는 a=5.208, b=8.995, c=10.275 A 인데 비하 여, 2M 인 동 질 이상체에서는 a=5.201, b=8.967, c=20 . 058A( 약 2 x 10.275 A ) 이고, 2M 2 에서는 a=9.0 1 7, b=5.210, c=20.4 3 7 A 이 된 다 . IM, 2M,, 2M2 , 0, 3T, 6H 의 공간군은 각각 C2/m, C2/c, C2/c, Ccm2,, P3,12 또는 P321 2 , P6,22 또는 P6 s 22 이다 . 운모군에 속하는 광 물 들의 화학성 분은 X2Y - 1- 6 Zs0 2 o (O H, F) 』 또는 XY2 .., Z 』 O w (OH , F )z의 이상화학식으로 나타낼 수 있다. 이때 X 는 사면 체 또는 팔면체가 연결된 층 사이에 존재하는 양이온으로서, Na, K, Ca , Ba, Rb, Cs 등의 원소가 해당된다. 이를 층간원소( 層 間元 素 , i n t erla y e rca ti on) 라고 하며, 배위수는 12 이다 . Y 는 팔면체 속에 자리 잡 는 양이 온으로서 , All+, M g 2 ♦ , Fe2 ♦, Fe3+ 이 고, 간혹 Mn, Cr, Ti, Li 등의 원소도 올 수 있다. Y 원소는 배위수가 6 인 팔면 체 중 심에 있게 되며, +3 가의 양이온이 올 경우에는 6 개의 팔면 체상 배위다면체 중 4 개만 채워지고, +2 가의 양이온이 올 경우에 는 팔면체상 배위다면체 6 개 모두가 채워진다 . Z 은 배위수가 4 인 사면체상 배위다면체 내에 자리하는 원소로서 S i와 Al 이며, 간혹 Fel+ , T i*가 올 수도 있다 . 운모군 광물은 Y 에 자리하는 양이온의 수에 따라 세분되는데, Y 자리에 오는 이온이 4 개면 다이 _옥타헤 드랄 (d i -oc t ahedral) 운모, 6 개면 트라이 -옥 타헤드랄(tri -oc t ahedral) 운모라고 한다. 또 X 에 있는 이온의 특징에 따라서도 분류하는 데, K 나 Na 처럼 +1 가인 이온일 경우는 보통 운모 (common mica ) 또는 진짜 운모(t rue mica ) 라 하고, Ca 과 같은 +2 가 이 온이 올 때 는 이쇄성 운모(易碑性 雲 母, bri ttle m i ca) 라고 한다. 보통 운모는
요곡성이 있으나, 이쇄성 운모는 요곡성 대신 이쇄성이 있다. K1•, Na1• 이온은 Al .l+이 사면체 속에 있는 S i거 를 치환할 때 생기는 산화수의 부족을 채우기 위해 있게 되며, Ca2+ 이온은 Al.l+ 이온 2 개 가 사면체상 배위다면체의 Si .. . 이온 2 개를 치환할 때 생기는 산화 수의 결손을 보완하는 역할을 한다 . 위의 분류 기준에 따 른 운모 광물의 분류 예는 표 4.9 에 있다. 【백 운모 (Muscov it e) 】 화학성분 KAlz(AISiJ 0 10) (OH) z. K 대신 Na, Rb, Cs 가, Al 대신 Mg , Fe2•, Fel>, Li, Mn, Ti, Cr 등이, 그리고 OH 대신 F 가 치환 할수있다. 결정계 단사정계. '2/m . 공간군 C'2 Ic 외에도 여러 동질이상체가 존재하지만 C '2I c 인 것이 가장 빈번하게 산출된다. a=S.21, b= 8.9 9 5, c=10.21sA, [3=1 01° 35 ' . Z=4. 내부 결정구조는 그림 4.4 8 과같다 . 색 무색 투명함 . 유리광택 내지 견사 또는 진주광택 . 박편하에 서도 무색이다. 결정형태 판상체 또는 비늘 모양의 결정 집합체로 산출된다 . 미 세한 섬유상 결정들이 비늘같은 집합체를 이루면서 진주광택을 떨 때 이를 견운모(組雲母, se ri c it e) 라고 한다. 요곡성( 燒 曲性)이 있고 탄성도 있다. 경도 2~2.5 비중 2.76~2.88 벽개 {0001} 방향의 벽개가 완전하게 발달하므로 종이처럼 한겹 한겹 분리된다. 양각낮다. 굴절률 a= l.56 0~ 1.57 2, /3= 1.59 3 ~ 1.61 1, r= 1.5 99~ 1.61 5. 복굴
 표 4. 9 운모류 광물의 분류.
표 4. 9 운모류 광물의 분류.
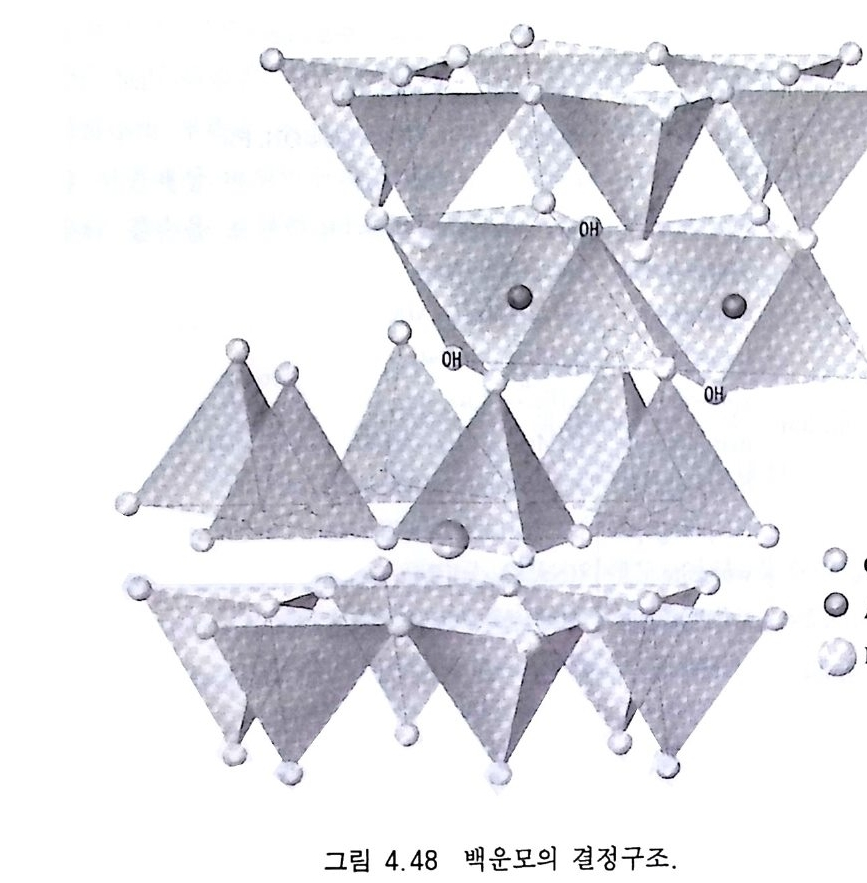 그림 4.4 8 백운모의 결정구조 .
그림 4.4 8 백운모의 결정구조 .
절률 =0.037~0.04 1. 최대 간섭색은 2° 의 상급에 해당하는 색이지 만, 벽개와 나란한 입자는 복굴절률이 0.004~0.006 정도이므로 1° 에 속하는 간섭색을 나타낸다 . 소광특징 벽개 방향에 나란한 평행소광을 한다. 장축부호 벽개 방향을 따라 느린 광선이 진동한다 . 광학부호 이축성, (기. 2V=30~40° X 선 회절선 lM 10.08(1 0 ), 5.04(4), 4.4 9 (9) 4.3 5 (3), 4.1 1 (2), 3.6 6 (6), 3.36(1 0 ), 3.07(5), 2.582(5), 2.565(9), 2.550(2),
2.156(2), 2.013(3)A 기타사항 금운모는 황산에서 분해가 되지 않는 점, 레피도라이 트는 적색 불꽃을 내는 점이 다르다. 백운모는 대부분의 화성암과 변성암에서 발견되는 조암광물이며 페그마타이트에서는 석영, 장석 등과 함께 공생하며 거대한 결정을 이루기도 한다 . 섬유상의 미세 한 변종인 견운모는 장석이 열수에 의해 변질될 때, 또 장석과 토 파즈, 남정석 등이 후퇴 변성작용을 받을 때 만들어진다 . 내열성 이 높아 전열기의 단열재로 많이 사용되었다. 분말화 시킨 금운모 를 벽지에 섞으면 반짝거리는 효과가 나며, 윤활유를 제조할 때에 도 첨가한다 . 충전제나 방화물질 제조에도 사용된다. 광물명은 구 러시아에서 유리대신 사용하였던 〈 머스코비 -글라스〉라는 이름의 광물에서 유래되었다. 운모를 의미하는 m i ca 라는 용어는 〈빛나는〉 울 뜻하는 라틴어 m i care 에서 유래되었다. 【금운모 (Phlo go pit e) 】 화학성분 KMg J( AISb010) (OH, F)2. K 대신 Na , Rb, Cs, Ba 가 치 환하며, Mg 대신 Fe2• 가 치환할 수 있다. 결 정 계 단사정 계 . 2/m . C'2 Jm . a =S.3 3 , b=9.23, c= 10.26A , /3= 99°l2' . C2}m 의에도 2M 과 3T 의 동질이상체가 있으나 그 산출 빈도 는적다 . 색 황갈색, 녹색, 백색. 유리광택 내지 진주광택. 얇은 결정은 투명하다 금홍석 침상 결정들이 내포물로 존재하면, 성채(星彩) 를 나타낸다. 박편하에서는 무색 또는 옅은 갈색으로 관찰된다. 다색성이 매우 희미하게 관찰될 수가 있다 . 결정형태 육각형의 얇은 판상체로 산출된다. 요곡성과 탄성이 있다. 경도 2.5~3
비중 2.86 벽개 {0001 } 방향의 완전한 벽개가 발달한다. 양각보통 굴절률 a= l.5 5 1 ~ 1.562, /3= 1.5 9 8~ 1.60 6, y= 1.5 98~ 1.60 6. 복굴 절률 =0.044~0 . 047. 최대 간섭색은 30 의 중간색에 속한다 . 그러 나, 벽개면인 {0001} 방향으로 만들어진 박편에서는 복 굴절률 이 0 에 가깝기 때문에 lo 의 매우 낮은 간섭색을 나타낸다. 소광특징 벽개 방향과 나란한 평행소광 을 나타낸다. 장축부호 벽개 방향을 따라 느린 광선이 진동한다 . 광학부호 이축성, (-). 2V=O~100. 광 축 각이 매우 작기 때문에 거의 일축성과 유사한 간섭상을 나타낸다. 광축의 최대 분리는 소 광위치로부터 45° 회전한 위치에서 일어나는데, 이 위치에서는 두 광축이 분리하고 있음을 관찰할 수가 있다. X 선 회절선 lM 9.94(1 0 ), 3.39(2), 3.348( 10 ), 3.144(I), 2.614(3), 2.5 1 30), 2.4 2 9(2), 2.1 6 90), 2.011 (3), I.53 4(2)A 기타사항 백운모와는 황산에서 분해가 되는 점으로, 또 혹 운모 와는 색깔이 옅고 광축각이 작은 점과 다색성이 거의 나타나지 않 는 점 등으로 구별될 수 있다. 금운모는 백운암질 석회암이 변성 작용을 받을 때 이미 존재해 있던 칼리장석과 반응하거나(I), 또 는 백운모와 반응하여 (2) 만들어진다. 3 CaM g (CO J )2+KAIS iJ O 다표 0 --'7 KMg JA 1Sh01o(OHh+3 CaCOJ 백운석 칼리 장석 금운모 방해석 +3 C02 …………………… (1) 3 CaMg (COJ h +KALSb01o(OH) 2--'7 KMg JA ISh01o(OHh+3 CaCOJ 백운석 백운모 금운모 방해석 +3 C02+AhOJ …………… (2)
두번째 반응식에 있는 여분의 산화알루미늄은 다시 첨정석을 만 드는 데 사용될 수 있다 (M g O+AhO J ~ M g AhO 』) . 킴벌라이트에서도 금운모가 주요 조암광물로 산출되는데, 그 양 은 약 6~8% 정도이다 . 금운모의 산업적 용도는 백운모와 동일하 댜 금운모의 색깔에서 마치 타오르는 불꽃을 연상할 수 있기 때 문에 이런 의미 를 지니는 그리스어에서 광물명이 유래되었다. 【 혹 운모 (B i o tit e) 】 화학성분 K(M g, Fe)J( AISbO,o) (OH) z. 금운모와는 완전고용체를 형 성하며, 금운모에 비해 M g을 치환하는 F~ 의 양이 많고, Fe 와 Al 도 M g을 치 환한다 Al 이 S i를 치 환한다 K 가 Na, Ca , Ba , Rb, Cs 등에 의해 치환될 수 있다 . 결정계 단사정계. 2/m . lM , 2M1, 3T 인 세 동질이상체 중 공간군 이 C2/m 인 lM 의 산출빈도가 가장 높다. a=S.30, b=9.21, c= 10.1 6 A, /3= 99°3' 색 암갈색, 검은색, 암록색. 박편하에서는 갈색, 황갈색, 적갈 색, 녹갈색 등을 띠고, 다색성이 매우 뚜렷하다 . 결정형태 육각 판상체의 결정으로 산출되며, 요곡성과 탄성이 있다. 경도 2.5 ~ 3 비중 2.8~3.2 벽개 {0001} 방향의 완전한 벽개가 발달한다. 양각보통 굴절률 a= l.54 1 ~ 1.57 9, /3= 1.5 74~ 1.63 8, r= 1.5 74~ 1.63 8. 복굴 절률 =0 . 033~0.059. 최대 간섭색은 2· 적색이지만, 광물의 짙은 색 에 가려져 정확하게 관찰하기는 어렵다. 소광특징 벽개에 거의 나란한 평행소광을 나타낸다.
장축부호 벽개 방향을 따라 느린 광선이 진동한다. 광학부호 이축성, (-). 2 V=O~25• X 선 회절선 IM 10.1 (10 ), 4.59(5), 3.37(1 0 ), 3.1 6 (2), 2.92(2), 2.66(8), 2.52(4), 2.4 5 (8), 2.28(2), 2.18(8), 2.00(8), 1.91 (2), 1.7 5(2), 1.6 7(8), 1.5 4(8), 1.4 7(2), 1.4 3(2), l.36 (6), l.33 (4), 1.31 (4)A 기타사항 현미경에서 각섬석과 구별하는 방법으로는 각섬석은 두 방향의 벽개가 있고 또 그러한 입자는 대칭소광을 한다. 각섬 석도 한 방향의 벽개를 나타낼 수 있는데 이 경우 대부분 경사소 광을 하는 것이 특징이다. 흑운모를 끓는 황산에 넣으면 분해되면 서 우유 빛깔의 용액이 된다. 흑운모가 산출되는 지질학적 환경은 매우 다양하다. 화강암, 페그마타이트, 반려암, 페리도타이트 등 의 심성암뿐만 아니라, 현무암, 안산암, 유문암과 같은 화산암에 서도 산출된다 . 화성암에 산출되는 혹운모의 성분은 규산염 성분 이 많은 암석일수록 Fe2+ 성분은 증가하고 Mg 성분은 감소한다(그 림 4.4 9 ) . 동시 에 Al, Fe 만도 증가하며 , Si, T i은 감소하는 경 향이 있다. 미 량원소에 있어서도 Ga : Al, Li : Mg , Mn : fe2+, Rb : K 의 비는 증가하며, Ni :M g , Co:Fe2+ , Ba:K 의 비는 감소한다 . 혹운 모는 화산암보다 심성암에 훨씬 많이 존재한다. 이것은 실험적 결 과와도 부합하는 데, 혹운모와 성분적으로 연속성이 있는 금운모 의 경우, 금운모의 안정곡선이 압력이 매우 낮은 조건 이외의 영 역에서는 항상 화강암의 용융곡선보다 위에 존재하며, 현무암의 용 융곡선과는 교차하고 있다. 이 사실은 금운모와 흑운모가 압력이 높 은 상태에 있는 염기성의 심성암에서는 안정하지만 압력이 낮은 분 출환경에서는 불안정해진다는 의미를 지니고 있다 . 이질암이 변성작용을 받을 때에도 생성된다 . 이질암이 접촉변성 작용을 받으면 이 암석에 있던 녹니석, 백운모, 금홍석 등이 소비
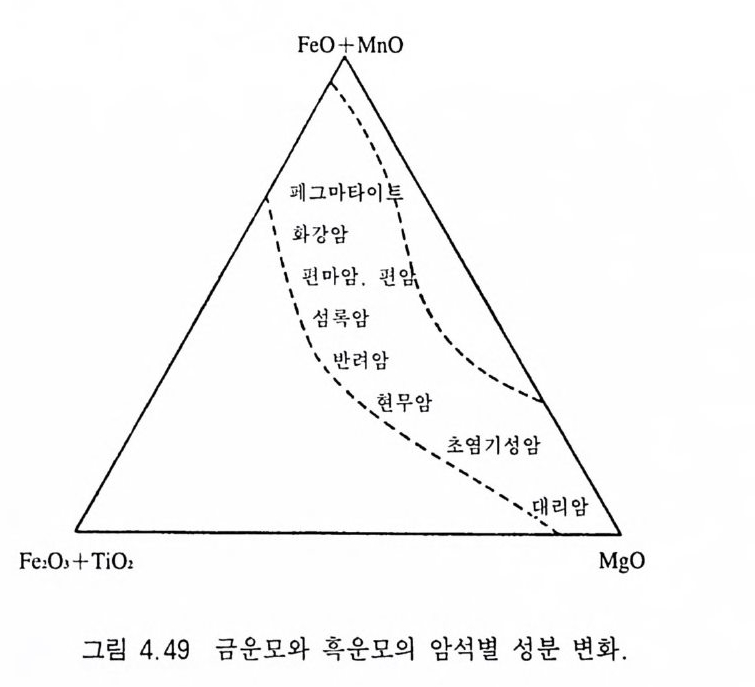 FeO+ M nO
FeO+ M nO
 그림 4.5 0 다색성훈을 나타내는 혹운모 . 저어콘 입자 주변에 검은 부분이
그림 4.5 0 다색성훈을 나타내는 혹운모 . 저어콘 입자 주변에 검은 부분이
되면서 혹운모를 변성광물로 만들게 되고, 그 결과 호른펠즈에서 는 홍주석이나 근청석 등과 공생하기도 한다. 그러나 고온의 열변 성작용이 계속 진행될 때에는 혹운모가 칼리 장석, 사방휘석, 규 선석, 또는 근청석에 의해 교대된다. 동력변성작용이 일어날 때 기존의 어떤 광물이 변성 반응을 통해 혹운모로 변하는지에 대해 서는 아직 암석학적 증거가 없다 . 다만 흑운모의 양이 증가하는 암석에서는 녹니석의 양이 감소하는것으로 알려져 있다. 압력이 높아지는 환경에서도 흑운모는 계속 안정하게 존재하는데, 변성 등급에 따라 혹운모의 성분에 변화가 있음을 알 수 있다. 즉, 압 력 이 높아짐 에 따라 흑운모 내 에 Fe2+, Mn, Fe J+의 양이 감소하 고, Ti, Mg 성분은 증가한다. 화강암에서 발견되는 흑운모 내에는 둥근 다색성훈(p leochro i c halo) 이 발달하는 경우가 많은데(그림 4.50), 이것은 흑운모 결정 내에 방사성 원소를 함유하고 있는 저어콘과 같은 광물 내포물에 서 방출되는 방사성 입자에 의해 결정구조가 부분적으로 파괴되었 기 때문에 나타나는 현상이다. 광물명은 프랑스의 물리학자 J. B. B i o t의 이름에서 유래되었다 . 【레 피 돌라이 트 (Le pi dol it e) 】 화학성분 K(L i, A1)2-J ( AlSh010) (0, OH, F) i. 화학성 분의 변화는 주로 Li과 Al 의 치환에 의해 나타난다. 일반적으로 L i 20 는 3.3 ~ 7 wt. % 정도 함유되어 있다. 팔면체상 배위다면체의 중심위치인 이 자리 에 Fe, Mg , Mn 동이 오기도 한다. K 대신 Na, Rb, Cs 등이 치 환할 수 있다. 결정계 단사정 계 . 입 m. lM , 2M i, 3T 동의 세 동질이상체가 있 다. lM a=5.3, b=9.2, c=l0.2A , /3= 100°, Z=l. 2M i a=9.2, b= 5.3 , c=20A, /3=9 8°, Z=2. 3T a=5.3 , c=30.0A, Z=3
색 분홍색, 연보라색, 회백색. 반투명. 진주광택. 박편하에서는 무색으로 보인다. 결정형태 두꺼운 판상체 또는 육각형의 짧은 주상 결정으로 산 출된 다. 벽개 {0001} 방향의 완전한 벽개가 발달한다. 경도 2.5 ~ 4 비중 2.8~2.9 양각보통 굴절률 a=1.525~1 .54 8, {3=1.55 1~1.585, y=1 .554~1 .58 7. 복굴 절률 =0.018~0.038. 최대 간섭색은 3• 중간 등급이다 . 벽개에 나란 한 입자는 복굴절률이 매우 작기 때문에 낮은 간섭색을 나타낸다. 소광특징 벽개 방향을 기준으로 소광각이 7° 까지 이르지만 대부 분 평행소광을 한다. 장축부호 벽개 방향을 따라 느린 광선이 진동한다. 광학부호 이축성, (-). 2V=40° X 선 회절선 lM 10.0(8), 4.99(8), 4.53(4), 4.3 5 (2), 4.1 3 (2), 3.87(2), 3.62(8), 3.34(1 0 ), 3.08(7), 2.90(4), 2.680(5), 2.5 7 8(8), 2.4 7 3(4), 2.3 9 1 (5) , 2.257(2)A 기타사항 백운모와 구별할 때에는 화염반응을 관찰하는 것이 가 장 좋다. 레피돌라이트는 적색 연기를 낸다. 레피돌라이트는 리튬 (Li)을 함유하고 있는 광물 중에서 산출 빈도가 제일 높은 광물로 서, 화강암질 페그마타이트에서 주로 산출되며, 앰블리고나이트 [LiA I (F, OH)P04], 스포듀민, 전기석, 토파즈, 녹주석, 석영 등과 공생한다 페그마타이트에서는 혹운모나 백운모를 교대한 광물로 산출된다 . 리튬을 공급하는 대표적인 광석 광물이며, 내열성 유리 를 제조할 때에도 사용된다. 〈비늘〉을 뜻하는 그리스어에서 광물 명이 유래되었다.
4. 3.1. 13 녹니석군 (CHLORITE GROUP) 녹니석군(綠泥石群)에는 클리노클로, 페니나이트, 차모사이트, 프 로클로라이트, 수도아이트 등의 광물이 있으며, 이들 광물의 특징은 층상구조로 되어 있다. 특히 규산염 광물 중 활 석과 수 활 석 (bru cit e) 구조가 혼합되어 있는 결정구조의 특징을 지니고 있다. 즉 규소, 산 소로 이루어진 사면체층(t) 2 개와 팔면체층 (o) l 개로 결합되어 있는 활 석 구조와, 팔면체층 하나로 된 수활석 구조가 결 합된 듯 한 기본 단위를 가지고 있다(그림 4.51). 이것을 2: l : l(=t :o : o) 구조라고 표현한다. 따라서, 녹니석군 광물의 화학성분은 [Mg J( S i~ 0 10)(OH)2 (활석) + Mg J( OH)6 (수활석)]의 형태로 나타낼 수 있으며 M g을 치 환하는 Fe2+ , Fe 3+의 양과 Al 과 S i를 치 환하는 Al 의 양에 따라 위 의 화학식과 많은 차이를 나타낸다 . 따라서 녹니석군의 광물은 다시 일반화학식 &교 40n(OH)8 로 표현될 수 있다. 이때, A=Al, Fe2+, fe3+, Li, Mg , Mn, N i이고 Z=Al, Si, fe 3+ 이다 . 녹니석군에 속하 는 광물들은 화학성분, 결정학적 특징, 물리적 성질이 매우 유사하 기 때문에, 정량화학분석과 X 선 회절분석, 정밀한 광학적 관찰이 수행되어야만 구별이 될 수 있다. 녹니석군의 광물은 녹색편암 변 성상예 속하는 변성암의 주요 구성광물이며, 양기석이나 녹렴석과 공생하는 경우가 많다. 일부 편암이나 판암이 녹색을 띠는 것은 녹니석이 많이 함유되어 있기 때문이다. 심성암에서도^ 산출되는 데, 이때는 휘석이나 각섬석, 흑운모, 석류석 등의 변질 산물로 존재한다. 【클리 노클로 (C lin ochlore) 】 화학성분 Mg sA l (Sb1JA 111J ) 01o(OH)s 결정계 단사정계 a=S.3 2 , b=9.21, c=14.29A 색 녹색 박편하에서는 무색 또는 녹색을 띤다. 다색성이 있다.
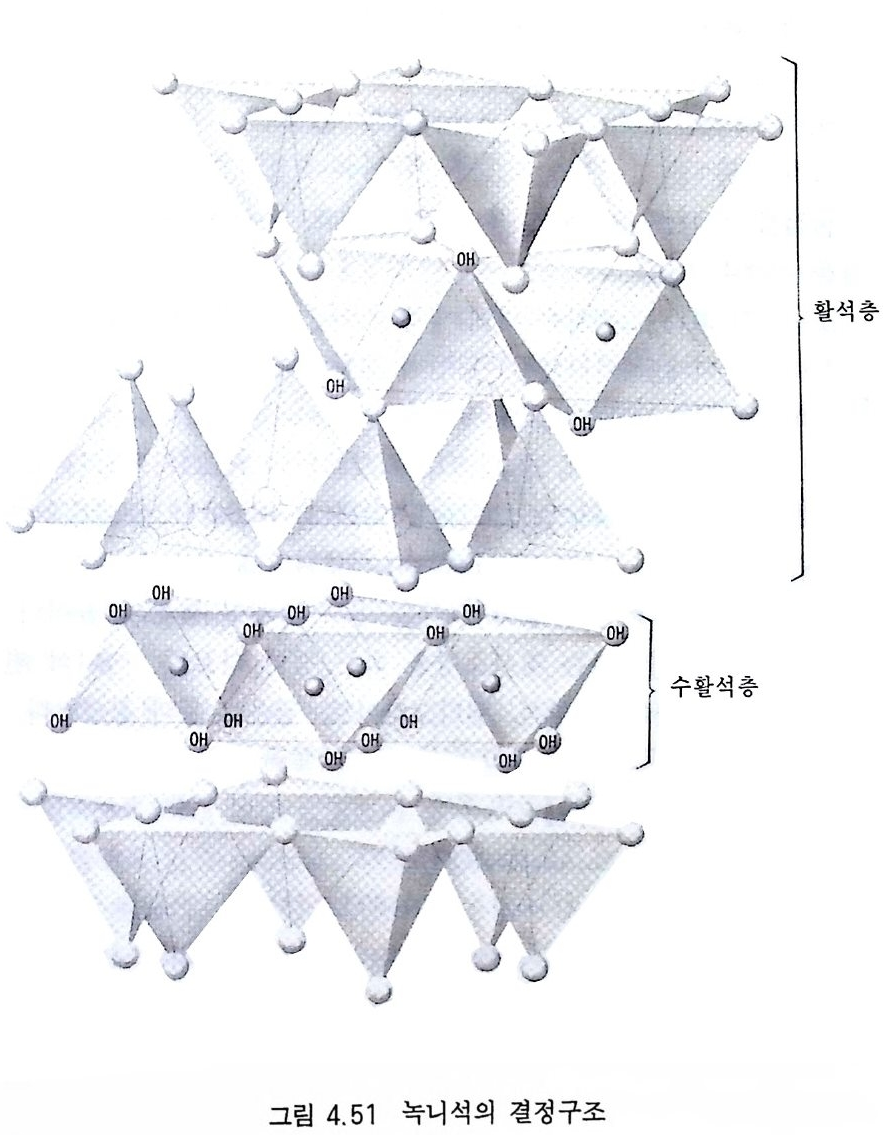 활석충
활석충
유리광택 내지 진주광택을 띤다 . 투명 또는 반투명하다 . 결정형태 자형 결정은 육각 판상체로 산출된다. 얇은 비늘처럼 산출되며 굽은 형태도 발견된다 . 벽개 {0001} 방향의 완전한 벽개가 발달한다. 경도 2~2.5 비중 2.6~3.3 양각보통 굴절률 a= 1.57 1 ~ 1.588, /3= 1.571 ~ 1.5 8 8, y= 1.5 7 6 ~ 1.5 79. 복굴 절률 =0.004~0 . 011 소광특징 최대 소광각은 벽개 방향을 기준으로 2~9 ° 이다. 장축부호 벽개를 따라 빠른 광선이 진동한다. 광학부호 이축성, (+). 2V=O~50° X 선 회절선 14.1 ( 7), 7.0 7 (9), 4.72(8), 4.59( 1), 3.5 4 (1 0 ), 2.84(5), 2.58(3), 2.4 3 (5), 2.37(4), 2.25(3), 2.06( 1), 2.026(2), 2.000(6), 1.8 83(3), 1.8 25(3), 1.5 62(4), 1.5 34(7)A 기타사항 녹니석 광물 중에서 산출 빈도가 제일 높은 광물이다. 다른 녹니석군 광물과는 경사소광을 하는 점이 다르다. 녹니석 편 암의 주구성 광물이며, 활석, 앤티고라이트, 금운모 등과 공생한다. 【페 니 나이 트 (Pen ni n it e) 】 화학성분 Mg uA l(Si.i .lAl o.8 )0 1o(OH)s 결정계 단사정계 색 녹색. 박편하에서도 녹색을 띤다. 다색성이 있다. 결정형태 다른 녹니석군 광물과 같다. 벽개 {0001} 방향으로 완전한 벽 개가 발달한다. 양각보통 굴절 률 a= l.57 5 ~ 1.58 2, /3= 1.57 6 ~ 1.58 2, r= 1.5 76~ 1.583 . 복굴
절률 =0.001~0.004. 간섭색 표에 없는 독특한 청색 간섭색을 나타 낸다 . 소광특징 벽개에 거의 나란한 평행소광을 한다. 장축부호 벽개 방향을 따라 느린 광선 또는 빠른 광선이 진동한다. 광학부호 이축성 , (+) 또는 (-). 2V=O~20· 기타사항 페니나이트는 특이한 청색 간섭색을 나타내고, 광축각 이 작은 점 , 평행소광을 하는 점 등이 특징이다. 【차모사이 트 (Chamos it e) 】 화학성분 FeJA bSii O, o • 3H2 0 결정계 단사정계. a=S.4 0 7, b=9.365, c=l3.997A 색 녹색, 녹회색, 갈색. 박편에서는 옅은 녹색, 회색 또는 갈색 을 띠며, 다색성이 약하게 나타난다 . 결정형태 어란상의 동심원상 구조로 존재하는 경우가 일반적이 댜 섬유상 또는 판상체로도 산출된다 . 벽개 다른 녹니석군 광물과는 달리 벽개의 발달이 완전하지 못 하다. 양각보통 굴절률 약 1.63 5. 복굴절률은 최대 0.008 에 이른다 . 장축부호 벽개 또는 동심원의 충을 따라 느린 광선이 진동한다. 광학부호 이축성, (-). 2V 는 매우 작다. X 선 회절선 14.0 ( 6), 7.08(1 0 ), 4.681(3), 3.5 2 3(5), 2.821(1 ), 2.619(3), 2.574(2), 2.469(1 ), 2.4 0 5(2), 2.279( 1), 2.014(2), 1.56 0(2), l.52 3(1 ) A 기타사항 철석(ir ons t one) 의 주구성 광물이며, 능철석, 방해석, 황 철석 등과 공생하는 경우가 많다. 광물명은 스위스의 Chamson 지방 의 이름에서 유래되었다.
【프로클로라이 트 (Prochlori te) > 화학성분 Mg s.1 A l(Si2 .6A J 1 .4 )01o(OH)s 결정계 단사정계 색 녹색 박편하에서도 녹색을 띠며 다색성은 약한 편이다 . 결정형태 비늘상으로 산출된다 . 벽개 {0001 } 방향의 벽개가 잘 발달한다. 양각보통 굴절률 a=l.588~1 .65 8, /3=1.58 9~1.667, y=1 .599~1.667. 복굴 절률 =0.001~0.011 소광특징 평행소광 또는 이에 가까운 소광을 한다. 장축부호 벽개 방향을 따라 빠른 광선이 진동한다. 광학부호 이축성, (+). 2V=O~30° 기타사항 일부 녹니석 편암에서 산출되며, 자철석과 공생하는 경우가 있다. 일부 Mg -F e 규산염 광물의 변질산물로 존재하는 경우도 있다 . 4. 3.1. 14 저어콘 (ZIRCON) 화학성분 ZrSi0 4 . Zr02 67.2% Si0 2 32.8%. 예외없이 l~4% 정도의 하프늄 (H f)을 함유한다. 노르웨이산 저어콘에서는 22~24% Hf 02 가 함유된 적도 있었다. 메타믹트 상태인 일부 결정에서는 S i 02 와 ZrO 까 혼합되어 있는 것으로 알려졌다. Th, P, Fe, Al 등도 거의 항상 미량으로 존재한다. Sn, Nb, Ta 과 같은 원소도 간혹 발견되 는데, 이들은 내포물로 존재하는 다른 광물 때문인 것으로 해석 된다. 결정계 정 방정 계 . 4/m 2/m 2/m. 14J am d. a=6.60, c=5.98A. Zr 은 8 개의 산소원자에 의해 둘러싸여 있고, S i는 4 개의 산소원자로 되 어 있는 배위다면체 속에 있다. 저어콘에 들어 있는 방사성 원소
인 U, Th 으로부터 알파입자가 방출되어 저어콘 결정구조의 일부 또는 전부가 비정질화된다 . 비정질화가 많이 진행될 수록 비중이 최 대 16% 정도 감 소하고, 굴절률도 작아진다. 결정구조가 거의 완전 한 경우를 고온형 저어콘 (h ig hz i rcon), 거의 비정질화된 입자를 저 온형 저어 콘 ( low z i rcon) 이 라고 한다 . 비정 질화가 된 결정을 1000 ~ 14oo • c 에서 수시간 가열하면 원래의 결정구조로 복원된다. 색 무색, 갈색 , 회색, 녹색, 적색. 청색은 거의 무색 또는 갈색 인 결정을 가열시켜 변색시킨 것이다. 이들을 햇빛 아래 오래 두 면, 퇴색된다. 유리광택 또는 아금강광택, 투명 내지 아투명하다. 박편하에서는 거의 무색을 띠며, 유색인 입자에서는 다색성이 희 미하게 나타난다. 결정형태 주상 결정에 양추가 결합된 취형이 일반적이다. 경도 7.5. 이쇄성이 매우 높기 때문에 모서리가 쉽게 마모되거나 부서진다. 비중 4.68. 비정질화가 될수록 비중이 3.9 정도로 감소한다. 벽개 {010) 방향의 불량한 벽개가 발달한다. 양각 매우 높다 . 굴절률 고온형 E= 1.9 70~ 1.9 77, w= 1.9 24~1 .93 4. 복굴절률= 0.036~0.0 5 3. 저온형 E=1 .8 27~1 .8 72, w=1 .7 82~1 .86 4. 복굴절률= 0~0.0 0 8. 최대 간섭색은 4° 의 높은 색이지만 입자가 미세할 경우에 는 이보다 낮은 간섭색을 띤다. 소광특징 평행소광 장축부호 장축을 따라 느린 광선이 진동한다. 광학부호 일축성, (+) X 선 회절선 4.4 3 (5), 3.3 0 2(1 0 ), 2.650(1 ), 2.518(5), 2.3 3 6(1) , 2.217(1), 2.066(2), l.908(l), l.751(l), l.712(4), l.651(l)A 기타사항 저어콘은 거의 모든 종류의 화성암에서 산출되지만 특
히 화강암, 페그마타이트, 섬록암과 같은 산성암 및 중성암에서 주로 산출된다. 또한 사암, 충적층과 같은 쇄설성 퇴적암에도 널 리 존재한다. 특히 이들 암석에 존재하는 저어콘은 퇴적물의 근원 지를 추정하는 데 이용된다. 대리암, 편마암, 편암 등의 변성암에 도 안정하게 존재한다. 호주나 브라질에서는 해변의 모래에서 다 량의 저어콘이 회수된다. 투명한 결정은 보석으로 가공되며, 특 히 무색인 결정은 다이아몬드의 모조품으로 사용되었는데 이 들을 자 르곤 Uar g on) 이라고도 부른다. 저어코늄의 녹는점은 백금의 용융점 (1775°C) 보다도 더 높기 때문에 내화물이나 도가니 를 만드는 데 사 용된다. 금속 저어코늄을 추출하여 원자로 제조 원료로 사용하는 데 이것은 저어코늄이 고온에서 잘 견디며, 내식성이 우수하기 때 문이다. 광물명은 페르시아어인 〈금〉과 〈색〉을 뜻하는 zar 와 g un 에 서 유래했다는 설과 광물의 주성분인 저어코늄 (z i rcon i um) 에서 하 였다는 설이 있다. 4.3 . 1 .15 황옥 (TOPAZ) 화학성분 AhSi0 4 (F, OH)2. AhOJ 56.6%, Si0 2 33.4 %, H20 10.0%. OH-대 부분이 F 로 치환되어 있으며, F 의 함량은 최대 약 20.7% 이다. 결 정 계 사방정 계 . 2/m 2/m 2/m. Pbnm. a = 8.3 9 , b = 8.80, c = 4.65A . Z=4. 규산염 광물 중 독립사면체 구조를 하고 있다 . 황옥 온 Al04F2 로 되어 있는 팔면체상 다면체가 c 축을 따라 연결되어 있 으며, S i 04 의 독립사면체가 이룰 교차하면서 연결되어 있다. 이러 한 구조 때문에 주상 형태의 결정이 만들어진다. 색 무색, 황색, 분홍색, 청색, 녹색. 투명 내지 아투명. 유리광 텍 박편하에서는 무색이다 . 결정형태 사방주에 양추 또는 추가 결합된 취형으로 산출된다.
주면(p r i sm fa ce) 에 수직 방향의 조선이 발달하는 경우가 있다 . 벽개 (001) 방향의 완전한 기저상 벽개가 발달한다. 이때 Si- 0 결 합은 깨어지지 않으나, Al-0 와 Al-F 결합은 파괴된다 . 경도 8 비중 3.4 ~ 3 .6 양각 비교적 높다. 굴절률 a= 1.6 07~ 1.629, /3= 1.6 10~1 .63 1, y= 1.6 17~1.638. 복굴 절률 =0.009~0.010. 간섭색은 l ° 의 회색, 백색, 연황색으로서 석영 과 유사하다 . 소광특징 주상 결정은 평행소광, 이에 수직인 입자는 대칭소광 울 나타낸다.
장축부호 벽개 방향을 따라 빠른 광선이 진동한다. 광학부호 이 축성 , ( + ) . 2Y =48~65° X 선 회절선 4.3 9 5( 1), 4.111( 1), 3.693(6), 3.1 9 5(7), 3.037(4), 2.986(2), 2.937(10), 2.4 8 0(2), 2.3 9 6(1 ), 2.378(3), 2.361(5), 2.105(4)A 기타사항 (OHr 를 치환하는 F 의 양이 많아질수록 비중과 광축 각이 커진다. 그러나 굴절률은 이와 반대의 현상을 나타낸다(그림 4.5 2 ). 황옥은 보석으로 많이 사용된다 . 최근에는 무색 또는 황색 결정을 가열 및 방사선으로 처리하여 청색으로 변색시켜 보석으로 가공한다. 황색인 결정을 가열시키면 적색으로 변하기도 하는데 이 룰 〈브라질 루비 (Brazil ian ruby ) 〉라고 한다. 황옥은 F 성 분이 많 이 농집된 마그마 고결 말기에 정출되며, 전기석, 인회석, 형석, 석영, 녹주석, 장석 등과 밀접하게 공생한다 . 주로 화강암과 페그 마타이트에서 산출된다. 대표적인 산지로는 러시아의 네르친스크 (무색, 황색), 무르진스크와 우랄산맥(청색), 브라질의 미나스 제 라이스(황색)가 있다. 광물명은 홍해의 섬 이름인 To p az i on 에서 유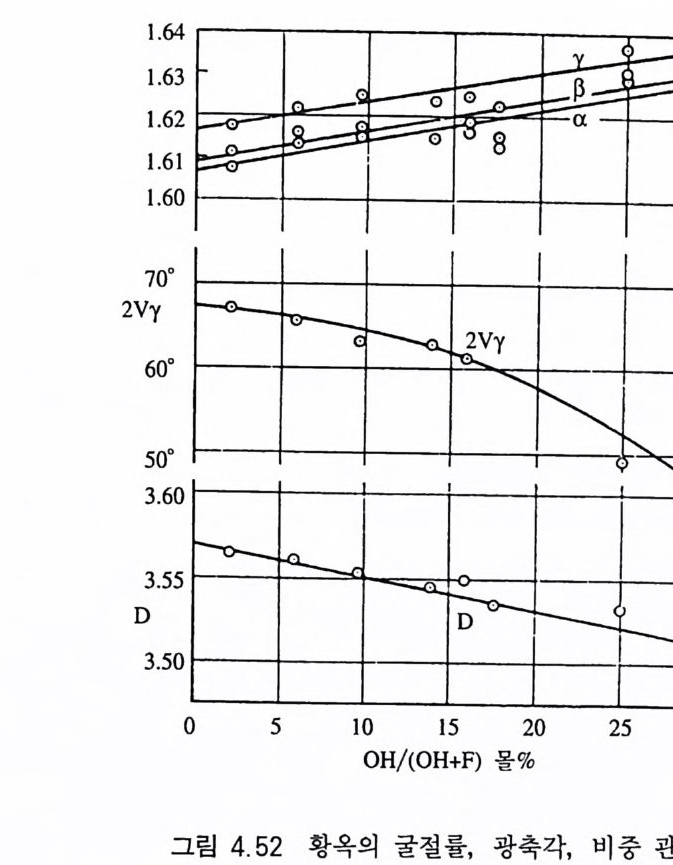 1.64
1.64
래되었다. 4.3. 1. 16 전기석 (TOURMALINE) 화학성분 전기석의 화학성분은 매우 복잡하며 일반화학식 XYJ Z 6(BOJ )JS i6 0 11(0H, F)4 로 나타낼 수 있다. X=Na, Ca, K, Mg , Y=Mg u, Feu, Fe3+ , Li, Al, Z=Al, Fe 3+이다 . 전기석의 변 종과 그들의 화학성분은 다음과 같다. 드라바이 트 NaM g 3 Ai 6(BO J )3S i6 아 (OH, F)4
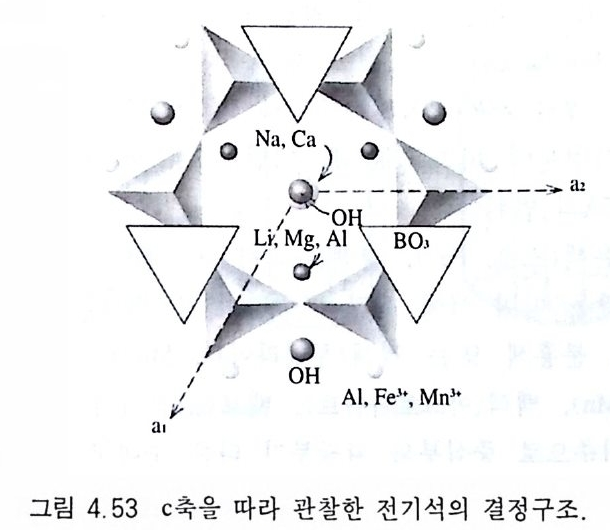 냐 근..I
냐 근..I
페 리 드라바이 트 NaM gJ Fe6(80 J hS i 6 아 (OH, F) 』 스콜 NaFe ., Al6(BO J)J S i6 어 (OH, F)4 칠라이사이트 NaMnJA 16(BOJ )JS i6 0 1s(OH, F) 』 엘바이트 Na(Li, AlhA16(80J) JS i6 0 1s(OH, F)4 우바이 트 CaMg J( Mg Ais ) (B0J) JS i6 0 1s(OH, F) 』 부거 라이 트 NaFeJA l6(80J) JS i6 0 1sOJ ( OH, F) 리 디 코우타이 트 Ca(Li, AlhA16(B0J) JS i6 0 1sOJ ( OH, F) 특히, 스콜-드라바이트, 스콜-엘바이트는 완전고용체를 이룬 댜 그러나 드라바이트-엘바이트의 성분을 가지는 광물은 아직 발견되지 않았다. 결정계 삼방정계. 3m.R3m. 6 각 환형구조를 지니고 있는 규산 염 광물이다. S i 601s 로 된 6 각 고리가 있고 그 중심에는 N 안와 OH- 가 반복된다(그림 4.53) . 삼각형 모양의 B03 로 되 어 있는 층이 환 형구조충과 교호하고 있고, 팔면체상 (Li, Mg , Al)O4(0H)2 가 Si6 0 1a
고리 와 BOJ 삼각형 구조를 연결해 주고 있다. Si6 0 JH 고리 는 (Al, Fe, Mn)Os(OH) 구조에 의해 수직방향으로 연결되어 터널을 형성한다 . Y 와 Z 에 위치하는 원소는 배위수가 6 이다. 단위포 상 수는 화학성분에 따라 다른데, 일반적으로 a=15.8 4 ~ 1 6.03, c= 7 .1 0~7.25A 의 범 위 이 다. 색 검은색(스콜, Fe2•) , 갈색(드라바이트, Fe3 ·). 엘바이 트 는 다 양한 색깔을 띠며 색에 따라 변종명이 주어 진 다 . 녹 색 (벌드 라이 트, Fe2•), 분홍색 또는 적색(루벨라이트, Mn2·) , 청색 ( 인디 콜 라이 트, Fe, Mn), 백색(아크로아이트) . 때로는 전기석 결정의 색이 수 직축을 기준으로 중심부와 외곽부가 다른 누대구조 를 나타내기도 하고, 결정의 상하 위치에 따라 색이 다른 경우도 있다 . 특히 전 자인 경우 중심이 붉고 바깥쪽이 녹색인 경우가 많은데 이 를 수박 석 (wate n nelon sto n e) 이 라고 하며 , 후자의 경 우처 럼 여 러 가지 색 이 수직적으로 분포하는 것을 파티컬러(parti -color) 라고 한다. 박편하 에서는 무색으로부터 광물색에 가까운 옅은 황색, 녹색 등으로 보 이며, 다색성이 뚜렷하게 관찰된다. 유리광택을 나타내며, 스 콜 의에는 거의 투명 내지 반투명하다. 광축인 수직방향으로는 빛의 흡수가 매우 현저하게 일어나며 이에 수직인 방향으로는 그 정도 가덜하다. 결정형태 삼방주 또는 이에 육방주가 추가로 결합된 긴 주상 결 정으로 산출되며, 한쪽 끝에 추가 발달하는 경우가 많다(그림 4.54). C 축에 수직인 면은 둥근 삼각형 단면을 나타낸다. 주상 결정 면에는 수직 조선이 발달한다 . 벽개 벽개 대신 패각상 단구가 발달한다. 경도 7~7.5 비중 3.0~3.25 양각높다.
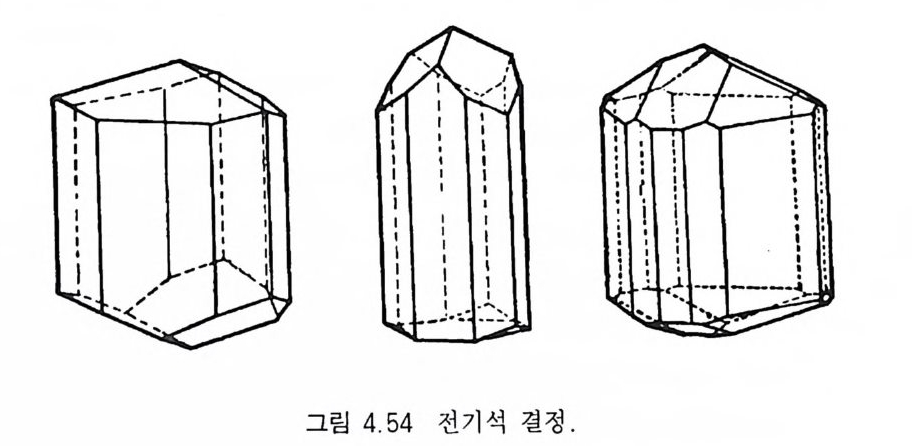 ,. .,.,,I''',1 ,',',. .,. ’,
,. .,.,,I''',1 ,',',. .,. ’,
굴절률 스콜 £ = 1.6 28 ~ 1.6 5 8, (.\) = 1.652 ~ 1.6 9 8, 드라바이트 c= 1.6 1 3~ 1.6 2 8, ro = 1.6 32 ~ 1.6 5 5, 엘바이트 £=1.61 5, (0 = 1.63 5 ~ 1.655 . 복굴 절률 =0.022~0 . 040( 스 콜 ), 0.019~0.025( 드라바이트) , 0.015~ 0 . 023( 엘 바이트) . 간섭색은 광물 자신의 짙은 색 때문에 명확하게 관찰되지 않는다. 소광특징 평행소광을 한다 . 장축부호 장축 방향을 따라 빠른 광선이 진동한다. 광학부호 일축성, (-) X 선 회절선 스콜 6.3 5 (2), 5.00(2), 4.62( 1), 4.2 2 (4), 4.00(6), 32은대이적콜..44 인트칭기이98 결4( 에타으댜(56산정서사)로) ,,구지 항 검22로산조되 .은.4출9가 는 어65색 내되4열 2(을며(에2엘있하5),바 ,서)기 거,제섬 2나,산.외2S3때 . 4i 9출한 08 문1압브4 ( 2 2이력라빈유)(사1 A다을질도색 .0면 )의. 가 ,체 가전 전 로2가하미기.기5 장면나8석석연1 스 은결은(높전7 되 은)기게보,주 어 적라석것로2 이 .으5은 있성스1 화로 9,는질검강( 2을은가암)환러, 공색 질형시띠되2을 구아.는며5페 0의,조데띠1그 가(는 5마이대우 ) ,것타표비스랄
산맥, 미국의 메인주 등이 있다. 전기석의 압전기 효과 때문에 압 력계 부품 제조에 사용된다. 광물명은 스리랑카에서 산출되던 보 석 원석을 칭하던 tur amal i에서 유래되었다 . 4. 3.1 . 17 근청석 (CORDIERITE) 화학성분 (Mg , Fe)iA .14 Sis 01s ·n l-LO . Mg O 13.8 % , Al20J 34.9%, Si0 2 51. 3% . Fe 이 M g을 다소 치환하지만, 50% 이상 치환하는 경우는 거의 없다. Mn 도 M g을 치환하나 그 양이 매우 적다. Al 의 양은 거의 일정하다. 6 각 환형구조에 있는 Al 과 S i의 바는 1 : 5 로 거의 일정하다 . H20 분자도 존재하는데 이들은 c 축을 따라 발달하는 터 널구조 내에 위치한다 . Na 과 K 도 항상 존재하는데, 이들도 이 터 널구조 속에 위치하는 것으로 알려져 있다. 결정계 두 동질이상체가 있다. 상온에서 안정한 결정은 사방정 계이다. 2/m 2/m 2/m. Cccm. a=9.80, b=l7.1 3 , c=9.35A. Z=4. 고온에서 안정한 6 각 환형구조를 가지는 동질이상체는 육방정계의 6/m6/m6/m 정족, P6/mcc 공간군으로 녹주석과 동일한 결정구조 룰 하고 있다. 고온에서 안정한 동질이상체를 인디아라이트 (indialit e) 라고 하며, a=9.8, c=9.3A 이다 . 두 동질이상체는 모두 (Si, A l)04 사면체 6 개가 연결된 6 각 환형구조로 되어 있으며, 이때 의 (S i sAIO 미 고리는 c 축을 따라 층층이 쌓여 있다. M g과 Fe 은 배 위수가 6 인 위치에 있다. 저온에서 안정한 근청석(董靑石)에는 6 각 환형구조가 약간 변형되어 있다. 색 청색, 청회색, 무색. 투명하다. Fe 성분이 많을 경우 청색을 짙게 띠는데 이러한 결정은 보석으로 가공되며, 보석학에서는 아이 올라이트(i o lit e) 라고 부른다. 유리광택을 띤다. 박편하에서는 거의 무색이다. 두꺼운 결정에서는 뚜렷한 다색성(삼색성)이 관찰된다. 결정형태 짧은 주상 결정형태가 일반적이며, 투입쌍정으로도 산
출된다. 경도 7~7.5 비중 2.60~2.66 벽개 {010} 에 나란한 불량한 벽개가 나타나는 수 있으나, 보통 패각상 단구가 발달한다 . 양각 낮음 굴절률 a=l.53 2~l.552, /3=l .536~l.562, y=1 .539~1 .57 0. 복굴 절률 =0.007~0.01 l. 최대 간섭색은 l° 의 황색이다 . 소광특징 결정면에 나란한 평행소광을 한다. 광학부호 이축성, (-) 또는 (+). 2V=40~80° X 선 회절선 8.5 4 (8), 8.4 5 (8), 4.9 1 (3), 4.86(1 ), 4.67(1), 4.09(7), 3.39(7), 3.37(6), 3.15(5), 3.1 3 ( 10 ), 3.046(6), 3.033(5), 3.0 1 4(6), 2.6 5 3(3), 2.645(2)A 기타사항 석영과 매우 유사하며, 이축성을 띠는 점이 다르다 . 청색인 경우는 뚜렷한 삼색성을 띠는 점이 약한 이색성을 띠는 자 수정과 다르다. 근청석은 녹니석, 활석, 견운모 등으로 변질된다. 이암이 열변성작용을 받을 때 변성광물로 생성된다 . 호른펠즈에서 는 규선석, 첨정석, 사장석, 휘석 등과 공생하며, 편마암에서는 규선석, 석류석, 앤소필라이트 등과 공생한다 . 화강암이나 페그마 타이트에서도 발견되지만 매우 드물다 . 광물명은 프랑스의 광물학 자 P. L. A. Cord i er 의 이름에서 유래되었으며, 보석명으로 사용되고 있는 아이올라이트는 〈청색〉을 의미하는 그리스어에서 유래되었다 .
4.3.2 산화염 광물 4. 3. 2.1 적철석군 (HEMATITE GROUP) 【강옥 (Corundum) 】 화학성분 AhOJ . Al 52.9%, 0 47.1 %. Cr, Fe2•, Fe3•, Ti가 미 량 존 재할 수 있다. 결정계 삼방정계. 32/m. R3c. a=4.76, c=12.98A. Z=6. 산소 는 촘촘히 6 각형의 배열을 하고 있으며, 6 개의 산소로 만들어진 팔면체상 배위다면체의 2/3 만 Al 로 채워져 있고 나머지는 비어 있 다(그림 4.55) . 색 순수할 때는 무색이지만, 전이원소를 불순물로 함유하게 되 면 다양한 색을 띤다. Cr 을 함유하면 적색이 되며, Fe .i+와 T i도을
 /\
/\
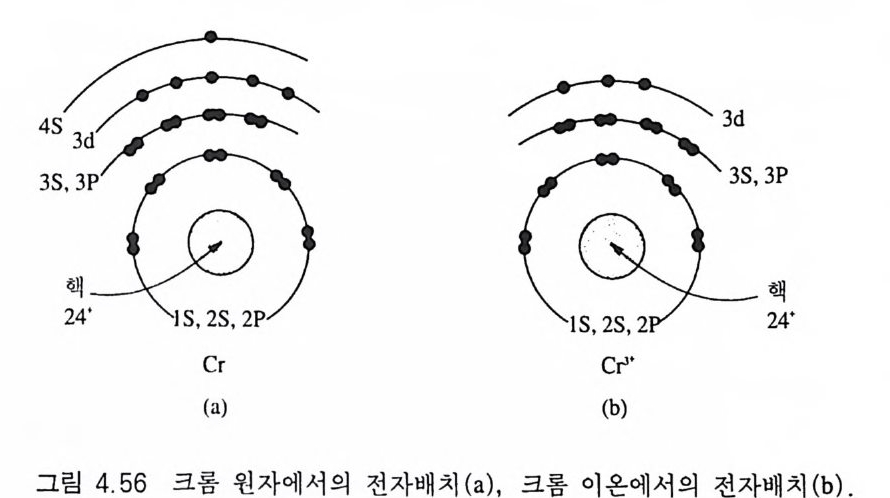 43 3d
43 3d
함유하면 청색이 된다. Fe” 가 존재하면 녹색이 된다. 적색인 강옥 (鋼玉)을 루비 (rub y)라고 하며, 무색, 청색을 포함한 기타 모든 색 의 강옥을 사파이 어 (sapp h ir e ) 라고 한다. 루비 에 함유되 어 있는 Cr20 J의 함량은 일반적으로 최대 2% 정도이다. 청색 사파이어에는 Fe20 파 T i 02 가 각각 0 .1 4% 와 0.3 2 % 정 도 함유되 어 있다. 크롬을 함유하고 있는 루비에서 적색이 발색되는 원인은, 크롬원자의 핵 주위를 돌고 있는 쌍을 이루지 않고 있는 6 개의 전자 중에서(그림 4.5 6 a), 원자결합에 사용되지 않은 3 개의 전자가(그림 4 .5 6 b) 빛에 너지를 받게 되면 높은 에너지 준위로 올라가게 된다. 이 과정에 서 전자들은 그림 4 .5 7 에서와 같이 기저상태 (A) 로부터 C 와 D 준 위로 올라가기 위해 빛에 있는 황록색 (2.2 e.V. )과 보라색 (3.0 e.V.) 파장을 흡수하는데, 그 결과 흡수되지 않고 통과 또는 반사되는 잔류광선이 합해져서 루비에서의 독특한 적색을 띠게 한다. 이러 한 현상온 분광기로 관찰하면 확인할 수 있다. 투명 또는 반투명 하다. 유리광택을 띤다. 광물의 몸색 질기에 따라 박편하에서 무 색 또는 옅은 색깔로 관찰된다. 두꺼운 박편일 경우 이색성을 관
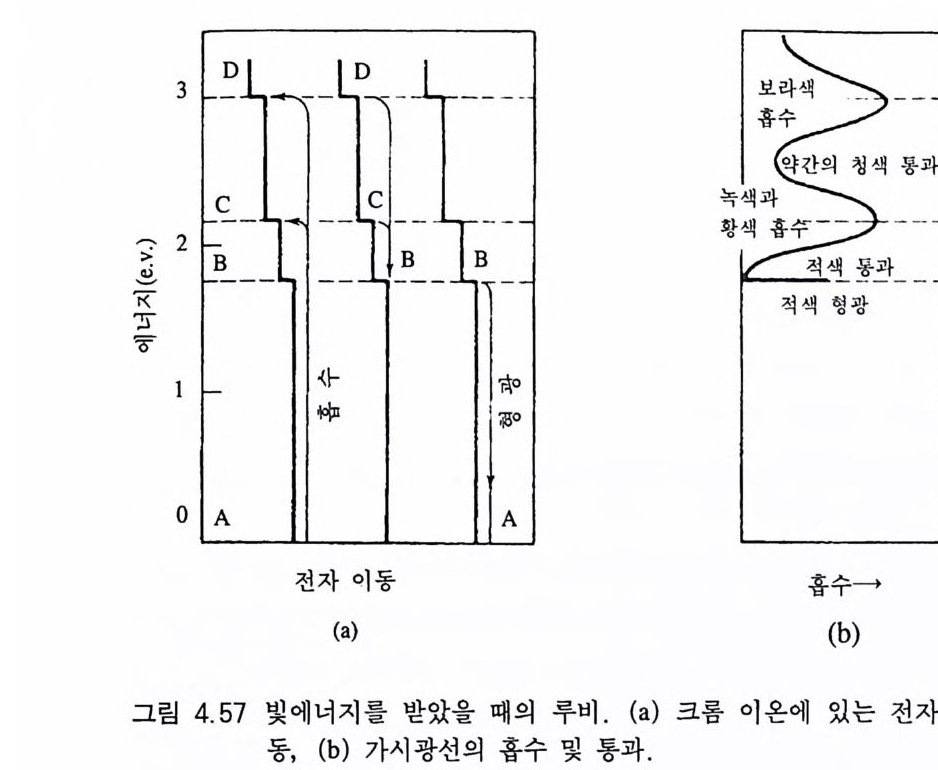 3 L D-
3 L D-
찰할 수 있다. 결정형태 6 각 판상 또는 주상 형태로 산출된다. 색깔에 따라 결 정 형태가 다를 수 있는데, 루비는 주로 육방주 형태로, 사파이어 는 육방양추 형태를 취한다. 사파이어에는 결정표면에 수평 조선 이 발달할 수 있다 . 취편쌍정이 발달하는 경우도 많다 . 경도 9. 일반적으로 사파이어가 루비보다 경도가 다소 높다. 인 성이 매우 강하다 . 비중 3.9 9 ~4.02 벽개 벽개는 없으며, {0001} 또는 {10 11} 방향을 따른 열개가 발 달할 수 있다. 심한 충격을 받으면 패각상 단구를 만들 수 있다.
양각 매우 높음 굴절률 E= 1.7 59~1 .76 3, co= 1.7 67~1 .77 2. 복굴절률 =0 . 008~0.009. 박편을 제작할 때 경도가 높기 때문에 다른 광물보다 다소 두껍게 만들어진다. 이 때문에 최대 간섭색이 2° 까지 증가할 수 있다. 소광특징 결정면에 나란한 평행소광을 나타낸다. 장축부호 장축 방향을 따라 빠른 광선이 진동한다. 광학부호 일축성, (-) X 선 회절선 3.4 7 9(8), 2.552(9), 2.3 7 9(4), 2.085(10), 1.74 0(4), 1.6 01(8), 1.4 04(3), 1.3 7 4(5), 1.2 39(2), l.04 2(1 )A. 기타사항 대리암, 편암, 편마암 등의 변성암에서 주로 산출된 댜 섬장암과 같이 실리카 성분이 적은 마그마로부터 정출된 화성 암에서도 발견된다. 투명하고 색이 진한 결정은 보석으로 가공된 다. 최고 양질의 루비 결정은 미얀마의 모곡지방에서 산출되고 있 으며, 그 밖에 케냐, 베트남 등에서도 비교적 양질의 원석이 산출 된다 . 태국, 스리랑카에서는 비교적 낮은 품질의 루비 결정이 산출 된다. 사파이어는 색이 다양하기 때문에, 청색인 경우는 그냥 〈사파 이어〉라고 하고, 그 밖의 색은 〈황색 사파이어〉, 〈녹색 사파이어〉 처럼 색깔을 포함시킨다. 천연 결정의 색깔이 너무 짙거나 옅울 때, 또 불필요한 색깔이 가미되어 있을 때에는 산화 또는 환원 환 경에서 가열 처리시켜 보다 나은 색으로 변색시킨다 . 금홍석 내포 물이 다수 있는 보석에서는 가열 후 서냉시킴으로 성채를 만들기 도 하며, 소수의 금홍석이 내포되어 있어 이를 제거해야할 경우에 는 가열 후 급랭시킨다. 보석 가공에 적합하지 않은 낮은 품질의 강옥은 분말로 만들어 연마제로 사용한다. 천연에서 산출되는 보석원석용 고품질 강옥의 생산량은 수요에 비해 크게 부족하였기 때문에, 1902 년 프랑스의 베르누이 교수는 인공적으로 강옥을 제조할 수 있는 합성장치를 개발하였다. 이 방
법은 수소와 산소를 태워 만들어지는 고온 (21oo · c) 의 불꽃을 사용 하여 원료물질을 일단 녹인 후 결정화시키는 방법인데 이를 화염 용융법 (flam e fus io n meth o d) 또는 발명 자의 이 름을 따서 베 르누이 법 (Verneuil m eth o d) 이 라고 한다. 현재 에 도 이 방법 으로 대 량의 합성 석을 제조하여 보석이나 시계부품, 기타 전자부품 제조에 널리 사 용하고 있다 . 강옥의 원료안 알루미나 분말에 발색원소 를 첨가시 켜 황색 (N i), 녹색 (Co), 보라색 (Cr , Ti, Fe), 옅은 자주색 (V) 을 띠 는 합성 강옥을 만든다. 양질의 합성 루비나 사파이어 를 제조하는 방법에는 이밖에도 융제법 (flux meth od), 열수법 (hy dr oth ermal meth o d), 초크랄스키법 (Czochralski meth o d), 스컬법 (Skull meth o d) 등이 있는데, 생산 원가 측면에서는 화염용융법이 가장 경제적이 다. 그러나 레이저용부품처럼 양질의 결정이 필요한 경우에는 초 크랄스키법으로 합성한다 . 보석으로 가공된 강옥이 천연석인지 아 니면 합성석인지를 구별하기 위해서는 내포물과 홉수 스펙트럼을 관찰하면 된다. 천연 강옥 내에는 금홍석, 운모 등과 같이 산출지 의 모암과 관련된 천연 광물 결정이 내포물로 존재하는 반면, 합성 석에는 기포, 융제, 백금조각 등 합성제조술과 관련된 내부 특징이 관찰된다. 광물명은 강옥을 의미하는 인도어 Kaurun t aka 에서 유래 하였으며, 변종명인 루비는 〈적색〉을 의미하는 라틴어 ruber, 사파 이어는 〈청색〉을 의미하는 그리스어 sa pphi rus 에서 유래하였다 . 【적 철석 (Hemati te) > 화학성분 Fe203. Fe 70%, 0 30% . 미 량의 FeO 와 MnO 가 함유될 수 있다 . 실험적 결과에 의하면, 800°C 에서 Ti 02 가 약 5% 정도 적 철석 (赤鐵石) 내에 함유될 수 있으며, l050°C 이상에서는 티타늄철 석과 완전고용체를 형성한다. 적철석은 자철석 성분 (Fo0 』)을 1% 미만 고용체로 함유할 수 있다(그림 4.5 8 ).
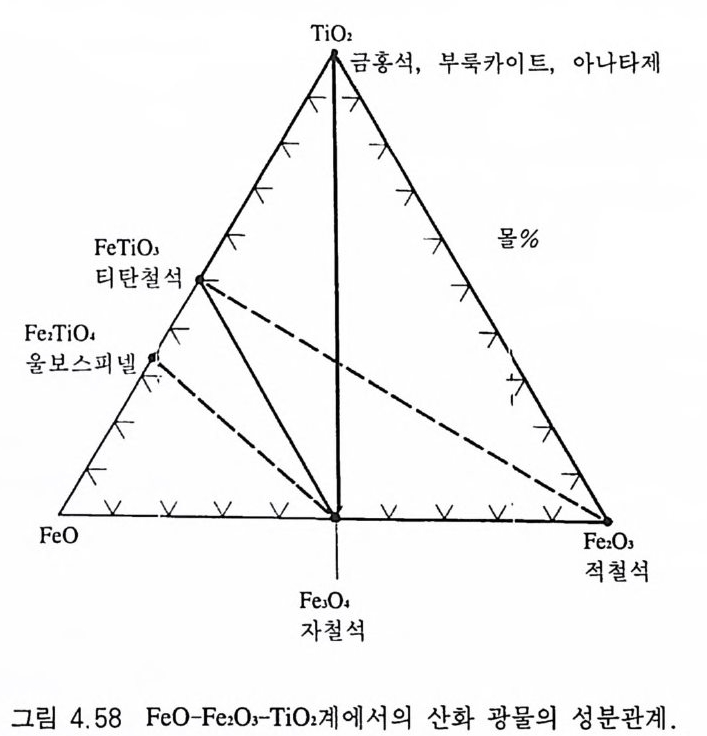 TiO ,
TiO ,
결정계 삼방정 계 . 32/m. R3c. a=5.04, c=l3.76A. Z=6. 색 적갈색, 검은색, 암회색. 금속광택을 띠며, 조혼색은 적색이 다. 두꺼운 결정은 불투명하지만, 박편인 경우는 반투명하고 적색 울 띤다. 반사광하에서는 회색에서 청색으로 변하는 뚜렷한 다색성 을 나타낸다. 반사광하에서 짙은 적색의 내부반사를 나타낸다. 결정형태 얇은 판상체로 산출되며, 능면체의 결정형 또는 괴상 체로 산출된다(그림 4.5 9 ). 기저면 (0001) 에는 삼각형 무늬가 발달 할 수가 있다. 얇은 판상 결정들이 집합체룰 이루어 장미송이 모양 을 만들기도 한다. 때로는 둥근 포도상 표면 조직을 나타낸다. 얇은 판상체인 변종을 스펙큘라라이트 (s pec ul arite)라 하고, 8 면체의 자철 석 가상을 지닌 것을 말타이트 (m artit e) 라고 한다. {0001} 과 {10 11}
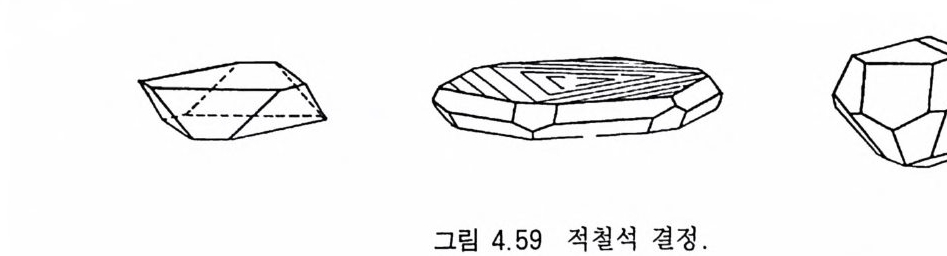 < <
< <
면에 취편쌍정이 발달할 수 있다. 경도 5.5~6.5 비중 5.26 벽개 벽개의 발달은 없으며, {0001 } 또는 {l0Il} 방향을 따라 열 개가 발달할 수 있다. 굴절률 £=2.94, (I)=3 .22 광학부호 일축성, (-) X 선 회절선 3.66(3), 2.69(1 0 ), 2.51 (5), 2.2 0 1 (2), 1.8 38(4), 1.69 0(6), 1.5 96(2), 1.4 84(3), 1.4 52(4), 1.3 10(2), 1.25 8( 1), 1.16 2(1 ), 1.14 1 (1), 1.10 20), 1.05 5(2)A 기타사항 화성암에서 산출되는 경우는 비교적 드물지만 화강암 에서 소량 산출된다. 퇴적암이나 변성암에서 주로 산출된다 . 현무 암 내의 감람석이 변질되어 적철석과 녹니석으로 변하기도 한다. 자철석 또는 티탄철석과 용리에 의한 혼정을 나타내는 경우가 많 다. 기존의 갈철석, 자철석, 능철석 등이 동력변성작용에 수반되 는 산화과정을 통해 대규모의 층상철광 (banded iron ores) 을 형성하 는 경우가 있는데, 미국 미시간주의 메사비 철광이 대표적인 예이 댜 적철석은 철강업의 원료인 철을 생산하는 광석으로 대부분 사 용되고 있으며, 회흑색을 띠는 결정은 보석으로 가공된다. 광물명 은 〈피〉를 의미하는 그리스어에서 유래되었다.
[~ ~~ 6i( Ilmenite)'] ~2f~~ FeTiOJ .F e3 6.8, Ti31 .6, 031.6%. Mg3!} Mno]Fe~ ±2J= ~]¥l-~ ~ 9).2..E...£ ~lfr:§}~-6J::' (Fe,Mg,M n)TiOJ.£ .R~~ ~ 9)et .F e20J7 } ~ ~ 6wt.% 7}2J= Jl% ~ ].£ ~% ~ e>i 9)et . 950· -lOSO· e o]AJoJ].Ai~ Fe20J.2} ~~Jl%~~] ~ 8J.AJ~et . ~~7:H ~l:lJ~ lll.3 .R 3.a =5.09, c=1 4.06.!..Z =6. :Q~o]et. lfr.A}:;g-ii}oJ].Ai~ ~~~~ n:j~, et~.AJ~ y.e.hRet. ~~ ~ EH AitB .0 ]9 ]~ !f-~ {t-~ AJ ~~] 8JE l1 ~ ~ ii}7-]lfr. :i!]A J.2...£ '8-~~ ~ 7cl4-7}[ :1 ~lfr~o]et. ~J~o] ~tgii}~ 7cl4-£9)et. ~£ 5.5-6 tll% 4.7 .F e~ ~l¥!-ii}~ ~±oJ] n:}c} l:l]%-°1 et± ~~et. ~, Mn9.J OJ:01 ~7}ii}tB. l:l]%-O] ~7}ii}Jl, Mgo1 ~7}ii}tB. l:l1%- 0]{ }±~et. ~7H ~7H9.J ~tg::' ~.2..~, {OOO1}3!} non)oj] y.~~ ~.7H7} ~tg~ ~ 9)et. X~ ~I~~ 3.737(3),2.754(10),2.544(7),2.237(3), 1.868(4),
1.726(6),1.635(1),1.505(3), 1.468(3), 1.342(l)A 7IE~A~~ ~~6i3!}~ ~~~.2...£, 7-}~6i3!}~ 7-}.AJo] Cll=~ ~3!} lfrA}:;g-ii}oJ]Ai et~.AJo] 7J~ ~ ';.2...£ £Ill] T~~ ~ 9)et. ~ ~~6i::' :§}.Acl~oJl Jf-.AJ~ :;g-%.£ ~81 {}~!8.et. ~iil ~AJ~, lfr~ ~3!} :Q::': §}.AJ~ oJl~ t:l1i T.2.9.J :;g-~17} llH Ell~ e>i 9)~ 7cl4-7} tlfet. ~ ~ 4-c.ly.c }9.J 7cl\ tii }%iC ~ t:l1o Jl ~.¥.ii} ~ ~ AJ~oJ1Ai ~illl] ~t:l1 iT.2.9.J ~~~6i :;g-AJo1 ~~~~et . 01 ~~~6i :;g-AJ ::. ~l..lloJ1Ai ~ %~ii}lll ~JHii}~ ~2..£, :;g-~19.J -&-°1 ~t:l1 Cll= 100moJl tgii}~, ~lI}Q{~~et.lI}Q{~~et.lI}Q{~~et.lI}Q{~~et.lI}Q{~~et.lI}Q{l~I~}eQt{.~~et.
x.2~~]01. {!~£, 2.1 A]O},7Hy-q';oj] ~ .£. nj '1=-.£ ~AJ ~ ~oj] ?:§).a~e>i ~q. ~'1=-, 'ttO}~~ 7}-tl-~~ , 'd.£, . !:!.c} ~o11~ 8H 't! .91 £2jJ01] ~tCl-~~ AH p ·Jo ]- e ~H8'}a:j ..2. ~%~ jH~~ 1:l} 7} ~ q. ~ tCl-~ ~ ~ ;g- %~:il} ~7}j] ~ El--E-~ -tl-1t 8'}~ rI]lE ~ 'd :;g.~ :ioIlc-¥.-;'::Jr-A '.Il, rL:.l.--cJ 'l1~oO ] r''lI.\.s - .:o:I.-±- , ;7~1 c l5l:-.:::I.JdO ~1;r:~'l .0::I.,± O] C~~ ~C ~ 8 l ] A2.l \ U!:I Ilo. .:~. o}yc} 7}~~~A].:ll, g:- ¥--6 J01] 7J ~ ~).a O ] ),~ Z! q. rr}c}A i, ~ El--E-~ ~'1=-~, c5J--tl-71, ~~~, A}% ~} '; ~ ~ £~ ~7J -tl- 'fl oj], g:? :§AJ7]~~;g-, ~7clE1], 'd-tl-{ !-1i~ ~ ] O } A~ ] 2i: , ltl]'dEgj ~li..£ Zl.B..8'}71] A}%~q. :;g.%~~ C1A]0}gj ( ~ ~{!- ~) o1 ]A i it- Cl1~~q . 4.3 .2.2 ~~~-2 (SP INELG ROUP) ~~~~(~ dt{J M )oj] 4;'-8'}~ ~%.91 ~§:Pd~ ~ ~~-6J XY 20~ .£ Y-El-~ ~ ~.£.~, ~~TI~ ~] ~ o ] ~~8'}11] ~ e>i Y- E..£ .:ll% ~~] ~ c5,Pa~ q. X=Mg2. ,F e2. , Zn2., Mn2+, Y= FeJ· , AP+, Cr ·o] ~ , B-.5ll± ~oj] 327H~ {!-~~A }7} ~ ~ ~q . o] ~ ~ % T-2i:~ oj]~ llH.5ll~ 7} 4g :~ 6'd llH.5llq 1?! ~]7} ~.:ll J 4;'-01] ;g-4;'-0]. g-o] A}~1f~q. ~ B-.5ll± ~oj]~ llH.5ll4-7} 6'd A}~7} 327H, llH.!fl4- 7}4 7H'd A}~7} 647H ~~ 4-7} ~~t~], J % llH.!fl4-7} 6'd A} ~~ 167H7}, 4'd A}~ ~ 87H7} oJ:o].g-.£..£ j H ~~ A] l1 ] .'{lq. ~~~ ~.91 ~%~ Zfl lH.5llq1?!j~]oj] ~~7}~ 0J:o].g-~ ~;;tJoj] rr}c} (~AJ ~ 7S~ (normals pinel):il} (~~ ~ ~ (inverses pinel).£..£ Y-~ q . ~ AJ ~~~oj]Ai ~ llH.5ll4-7} 4'd A}~ 87H7} X.£, J~.:ll llH.5ll4- 6 'd A}~ 167H7} Y.£ jH~~A:l XsY.6 ZJ2 g:~ XY20~~ ~~~.£..£ Y- E}~ 4-~ q. J2.1Y-, ~~~~ T-2i:oj]Ai~ llH.5ll4-7} 4'd 87H A}리 모두가 Y 이온 8 개로 모두 채워지고, 배위수가 6 인 자리 16 개는 Y 양이온 8 개와 X 양이온 8 개로 채워져 결국 Y8(Y8x8) O 3l 또는 Y(YX)O~ 의 화학식을 가지게 된다 . 스피넬과 크롬철석은 정상 첨 정석이며, 자철석은 역첨정석의 예이다. 첨정석군 광물의 단위포 상수 (a) 의 크기는 Xl· 와 T+ 이온의 반지름에 좌우되며, 그 관계식 은 a(A) =5.7 9 0 + 0.9 5 R2+ + 2.7 9 R.l+ 이다 . 【첨 정 석 (Sp ine !)> 화학성분 Mg A h04. Mg O 28.2, AbOJ 71. 8 %. M g의 일부를 Fe2•, Zn, Mn2+ 등이 치환한다 . Al 은 Fe 3+과 C f+에 의해 일부 치환될 수 있다. 결정계 등축정 계 . 4/m 3 2/m. Fd3m. a=8.1 0 A. Z=8 색 백색, 적색, 분홍색, 청색, 녹색, 갈색, 검은색. 투명, 아투 명, 또는 반투명하다. 유리광택을 띤다 . 조혼색은 백색이다. 박편 하에서는 무색, 옅은 갈색 , 연두색 등으로 관찰된다 . 결정형태 전형적인 결정형태는 8 면체이며, 8 면체와 12 면체가 결 합된 취형으로도 산출한다(그림 4.60). 매클 형태의 쌍정도 발견된
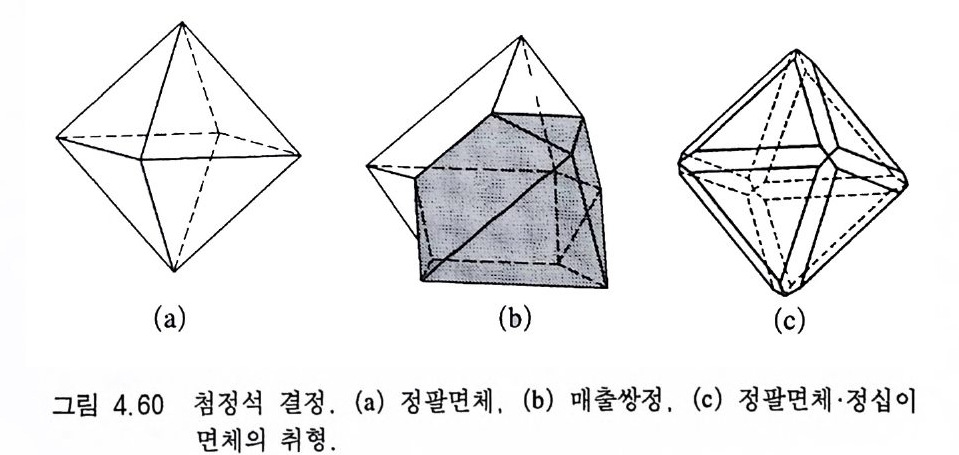 (a) (b) (c)
(a) (b) (c)
다. 괴상 또는 불규칙한 입상질 형태로도 산출된다. 벽개 불완전한 팔면체상 벽개가 발달할 수 있다 . 패각상 단구가 발달한다 . 경도 8 비중 3.5 ~ 3.6 양각높다 . 굴절률 1.71 8 X 선 회절선 4.7 3 (2), 2.90(4), 2.4 7 (1 0 ), 2.05(5), 1.6 72( 1), 1.57 6(4), 1.44 8(6), 1.24 9( 1), I.06 6(2)A 기타사항 화성암 내에서 부성분 광물로서 산출되며, 석회암이나 이암이 고온에서 접촉변성작용을 받을 때에도 만들어진다. 변성암 에서는 금운모, 자황철석, 흑연 등과 공생하는 경우가 많다. 투명 하고 색이 짙은 결정은 보석으로 가공된다. 최근에는 합성 첨정석이 보석 가공용으로 다량 제조되고 있는데, 주요 제조법은 화염용융법 이며 , 원료로는 M g O 와 AhO 를 사용하고 있다 . 착색을 시키기 위 해서는 Cr( 적색), Co( 청색), Cu( 분홍색), Mn( 갈색), Cr+Mn( 녹 색) 등을 원료물질에 첨가시킨다. 천연 첨정석은 Mg O : AbOJ = 1 : 1 이지만, 합성석은 Ah03 의 함량이 M g O 보다 1~3 배 정도 더 많 다 . 이러한 화학성분의 차이 때문에 나타나는 여러 물리적 성질에 의해 천연석과 합성석을 쉽게 구별할 수 있다 . 죽, 합성석은 비중 이 약 3.63 으로 천연석 (3 . 60) 보다 높으며, 굴절률도 1. 728 로 천연석 (1. 718) 보다 높다. 또한 편광기로 관찰하면 천연석은 항상 어두운 데 비하여, 합성석은 이상복굴절 현상으로 인해 완전소광을 일으키 지 않는다. 흡수스펙트럼도 유용한데, 적색의 천연석에서는 밝은 형광선 여러 개가 적색 영역에 존재하는데 비해, 합성석에서는 685run 의 형광선 하나만 나타난다. 청색인 경우 자외선을 쬐면 합 성석에서는 적색 형광이 난다. 천연 첨정석에서는 천연 광물이 내
포물로 존재하지만, 합성석에서는 기포가 관찰된다. 【자 철 석 (Mag ne ti te) > 화학성분 FeJ0 4. Fe3• (F e2+, Fe3') 0 4. Fe 72.4 , 0 27.6%. Fe2• 를 치환 하는 Mg , Mn2 까, 또 Fe 3 를 치 환하는 Al, Cr, Mnl+ , T i”가 상당 량 있을 수 있다 . 역첨정석 구조를 가진다 . 800°C 이상에서는 울 보 스 피넬 (Fe2T i O 』)과 완전고용체를 형성한다(그림 4.61 ). 결 정 계 동축정 계 . 4/m 32/m. Fd3m. a = 8.4 0 A . Z = 8 색 검은색 . 금속광택 . 조혼색도 검다. 불투명하다. 반사광하에 서 회색을 띠며, 다색성은 없다. 결정형태 팔면체 또는 십이면체의 결정형태를 지니며, 조선이 발달할 수 있다(그림 4.62) .
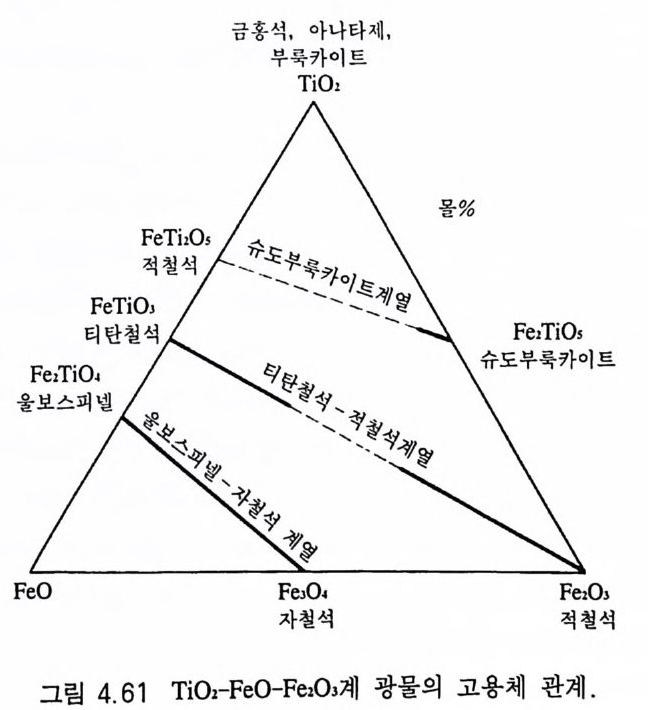 금홍석 , 아나타재,
금홍석 , 아나타재,
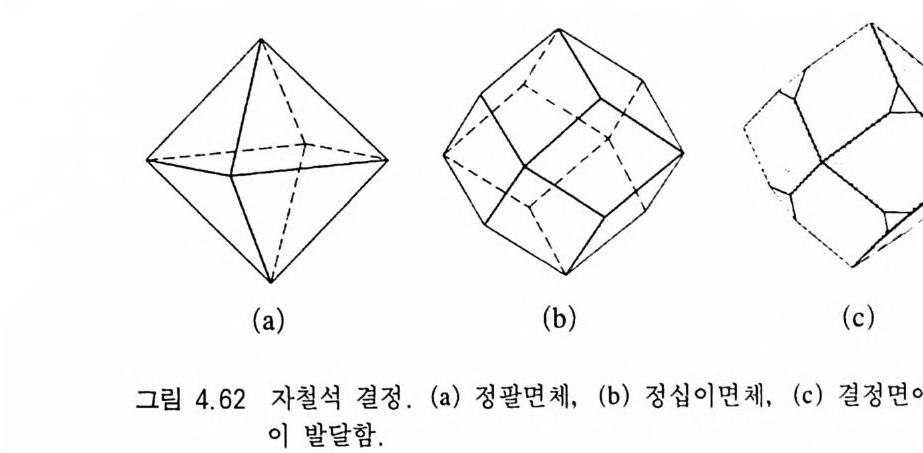 ,/, .
,/, .
경도 6 비중 5.2 굴절률 2.4 2 X 선 회절선 4.852(1 ), 2.967(3), 2.532(1 0 ), 2.4 2 4(1 ), 2.099(2), 1.71 5( 1), 1.61 5(3), 1.48 4(4), 1.28 0(1 ), I.09 3( l)A 기타사항 자철석(磁鐵石)은 대표적인 철광석 광물이다 . 대부분의 화성암에 부성분 광물로 산재되어 있다 . 특히 변성작용을 받은 선 캠브리아기의 퇴적기원 암석 내에 대규모의 층상광체가 발달하는 예가 있는데 이를 층상철광(ir on fo rma ti on) 이라고 한다. 미국의 슈 피리어호 일대와 캐나다의 래브라도 협곡 일대에 있다. 화성광상 은 스웨덴의 키루나를 비롯하여 노르웨이, 루마니아, 러시아 등에 분포되어 있다 . 자력을 강하게 띠는 변종은 시베리아, 엘바섬, 남 아프리카공화국에서 산출된다. 염산에 천천히 녹는다. 광물명은 마케도니아의 마그네시아 (ma gn es i a) 지방의 이름에서 유래되었다는 설과, 자력을 띠는 물리적 성질로부터 유래되었다는 설이 있다. 우리나라에는 충북 신예미 광산에 자철석 광상이 있다.
【크롬철석 (Chromi te) > 화학성분 FeCr20 ~ . FeO 32.0, Cr20J 68.0%. Fe2• 대신 M g이, Cr 대 신 Al, Fe3 까 치환하며, 마그네시오크로마이트 (ma g nes i o chromi te, Mg C rzO~) 와는 폭넓 은 고용체 를 형 성 한다 . 결정계 등축정계. 4/m32/m. Fd3m. a=8.36A .. Z=8 색 검은색 불투명. 금속광택 . 조혼색은 암갈색임 . 반사광하에 서 연마편은 회흑색을 띠고 다색성은 없다 . 결정형태 자형은 팔 면체이지만 주로 입상질 또는 괴상으로 산출 된다 . 경도 5.5 비중 4.6 굴절률 2.16 X 선 회절선 4.82(5), 2.95(6), 2.5 2 (1 0 ), 2.4 0 ( 1), 2. 0 7(7), l.69 (4) , 1.60 (9) , 1.46 (9) , l.40 (1 ) , 1.31 (2) , 1.2 6(5) , 1.20 (3 ) , 1.16 (2), 1.ll ( 3)A 기타사항 페리도타이트와 같은 초염기성 암석에서 혼히 산출되 는 광물이다 . 마그마의 고결 초기 단계에서 정출된다 . 남아프리카 공화국의 Bushveld Comp le x, 짐바브웨의 Great D i ke 에서 분별정출 작용으로 형성된 휘록암 부분에 층상으로 산출된다 . 크롬을 공급하 는 유일한 광석광물이다. 크롬을 혼합하면 강철의 강도와 인성이 매 우 향상되고, 내구성도 뛰어나게 된다 . N i과 Cr 의 합금인 니크롬 (N i chrome) 은 열선을 제조하는데 사용된다 . 크롬철석은 그 자체로 내열성이 있기 때문에 용광로 시설을 마감처리하는 벽돌 제조에 사용된다 . 크롬은 녹색, 황색, 주황색, 적색을 내는 안료로도 사 용된다. 광물명은 광물 속에 들어있는 주구성원소(크롬)에서 유래 되었다.
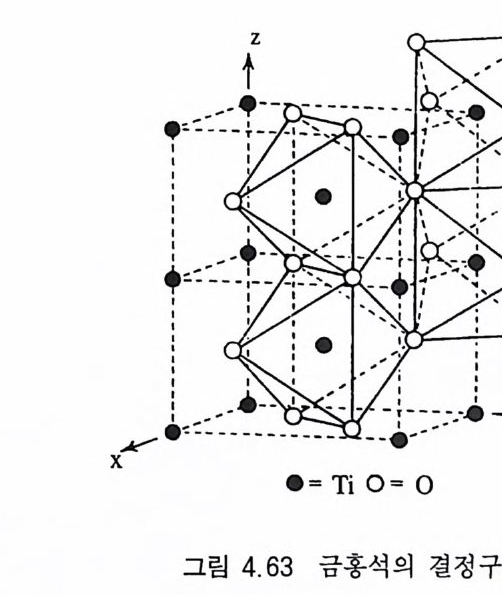 ?갑- --_iz
?갑- --_iz
【금홍석 (Ruti le )> 화학성분 Ti0 2 . Ti 60, 0 40%. 금홍석 (金紅石) 을 화학분석 하면 Fe2+ , Fel+, Nb, Ta 등의 성분이 상당량 검출된다. Fe” 가 T i4+를 치 환하면 Nb S+와 Ta S+가 산화수의 부족을 채워 준다. 따라서 금홍석 의 일반화학식은 Fe,(Nb, Ta )i ,T i 1- J ,02 로 나타낼 수 있다. 결정계 정 방정 계 . 4/m 4/m 4/m. P42/mnm. a=4.59, c=2.96A. Z=2. 금홍석의 결정구조는 그림 4.63 과 같으며, T i O, 로 되어 있는 팔면체상 다면체가 2 개의 능을 공유하고 있다. 금홍석은 아나타제 (anata se , !4./amd) 와 부룩카이트 (broo kit e, Pbca) 등 두 동질이상체 를 가지고 있다. 이 중 금홍석은 넓은 범위의 온도와 압력 조건에 서 안정한 것으로 알려져 있는데, 이것은 결정구조 내에서 팔면체 상 다면체의 능 4 개(아나타제)와 3 개(부룩카이트)를 공유하는 다른 동질이상체와 달리 2 개의 능만 공유하기 때문에 더 안정한 것으로
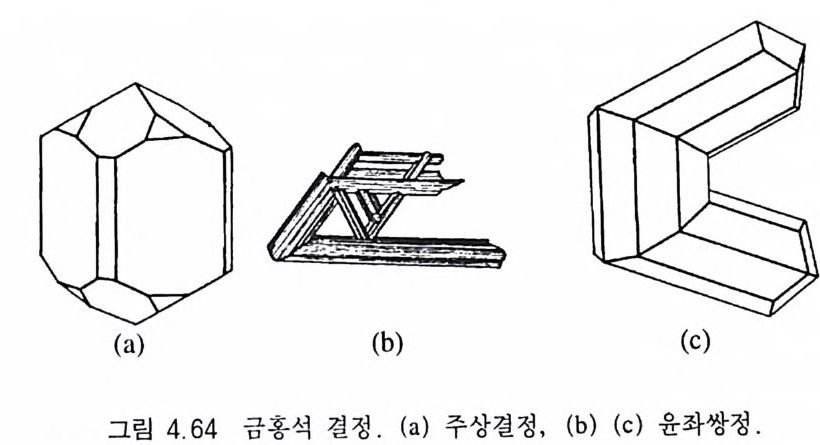 {a) (b) (c)
{a) (b) (c)
해석된다. 색 적색, 적갈색 , 검은색. 투명, 반투명 또는 아반투명 . 금강광 텍 박편하에서는 황색 또는 황갈색 . 다색성이 잘 관찰된다. 결정형태 전형 적 인 결정 형태는 양끝이 양추로 마감되는 주상 결 정형태이다(그림 4.6 4 ). 침 상 결정으로도 산출된다 . 결정면에 수 직 조선이 발달할 수 있다. 팔꿈치 모양의 반복쌍정을 나타내기도 한다. 경도 6~ 6 .5 비중 4.1 8 ~4.25 양각 매우 높음 굴절률 ro=2.603~2.616, £=2.889~2.9 0 3. 복굴절률 =0.286~0 . 287 . 간섭색은 매우 높은 등급에 속하지만, 전반사 현상 때문에 잘 관 찰되지는 않는다. 소광특징 평행소광 광학부호 일축성, (+) X 선 회절선 3.247(1 0 ), 2.487(5), 2.2 9 7(1 ), 2.1 8 8(3), 2.054(1) , 1.68 7(6), 1.62 3(2), 1.4 790), t.45 2(1 ), 1.35 9(2), L346(2)A
기타사항 화강암, 화강암질 페그마타이트, 편마암 , 운모 편암, 대리암, 백운암 등에서 산출한다 . 강옥이나 석영 결정 내에 침상 내포물로 산출되는 경우가 있다. 노르웨이, 스웨덴, 스위스에서는 암석 내에서 산출되며, 호주의 해변에는 대규모의 사광상이 형성 되어 있다. 금홍석은 용접봉에 피막을 입히거나 요업공업의 황 색 안료, 백색 안료, 인공치아 제조 등에 쓰이고 있다 . 과거에는 인 조 금홍석을 화염용융법으로 제조하여 다이아몬드 모조석으로 사 용하였다 . TiC 1 4 용액을 가열하여도 금홍석이 만 들 어진다 . 금홍석 의 용융점은 l825°C 이다. 광물명은 〈 적색 〉 을 의미하는 라틴어 ru ti lus 에서 유래하였다 . 4.3.3 탄산염 광물 4. 3 . 3 . 1 방해석군 (CALCITE GROUP) 【방해석 (Calcit e) > 화학성분 CaCOJ . 순수할 경우 CaO 56.0, CO2 44.0% 이다 . Mg , Fe, Mn, Sr 등의 원소가 Ca 을 치환할 수 있지만 그 양이 매우 미 미하므로 대부분의 방해석(方解石)은 거의 순수한 화학조성을 가진 다 . 백운석과 공생하는 방해석은 최대 약 9mol% 정도의 M g을 함 유하는 경우가 있다 . 실험결과에 의하면, 방해석은 M g CO J를 500°C 에서 5 mol.% , 900°C 에서 27 mol% 정도 함유할 수 있다. 이 러한 현상으로 인해 방해석 내에 백운석의 용리체가 존재하는 경우 가 있다. MnCO J도 방해석 내에 최대 42mol% 까지, 그리고 FeCOJ 는 5~10mol% 정도 함유될 수 있는 것으로 밝혀졌다. 결정계 삼방정계. 32/m, R3c. a=6.3 7 , c=17.06A. 방해석의 구
조는 암염( 岩鹽) 의 결정구조와 비교하여 생각하면 이해가 쉽다. 즉, Na 과 Cl 를 Ca 과 CO J로 각각 교체 하고, 3 회 축인 c 축을 누르면 면심격자 형태인 능면체상 단위포가 만들어지며(그림 4.6 5 a), 이때 단위포의 길이는 a=6.37A, aR=10 1° 55' 가 된다(그림 4.65b). 이 형 태의 단위포에는 CaCO J 가 4 개 포함되어 있어 Z=4 이지만, 능면체 의 모서리에 있는 C0 3 가 서로 반대 방향을 향하고 있기 때문에 진 짜 단위포(t rue cell) 라고 할 수 없다 . 따라서, 진짜 단위포는 한 변 (a) 이 2x6 .3 7A 이고, 야 =l01°55' 이며 따라서 32 개의 CaCO J를 포함 하게 된다 . 이 경우 Z=32 가 된다. 더 작은 능면체상 단위포도 가능 한데, 이 경우 a=6.3 7 A , aR=46°0 7 ’ 이며, Z=2 가 된다(그림 4.65b). 색 무색 또는 백색이 대부분이다. 간혹 회색, 황색, 분홍색, 녹 색, 청색을 띠는 경우도 있다 . 투명 또는 반투명하다. 유리광택으로 부터 토상광택까지 다양하다 . 박편하에서는 무색으로 관찰된다. 결정형태 방해석은 약 300 가지 이상의 결정 형태로 산출되며, 그 중에서도 능면체가 일반적이다(그림 4.66). 주상 및 편방체 형태로 도 산출된다. {0112} 방향의 엽상형 쌍정도 흔히 발달한다. 벽개 {1011} 방향의 완전한 능면체상 벽개가 발달한다. 경도 3. 측정 방향에 따라 다소 차이를 나타내는데, {0001} 면은 2.5, {0001} 면은 3.5 이다 . 비중 2.71. 방해석의 결정구조 속에 치환으로 존재하는 원소에 따라 비중이 변할 수 있다. 양각 방해석 입자의 배열 방향에 따라 높거나 낮아짐 . 굴절률 E=l. 48 6, (l)=1.65 8. 복굴절률 =0 .1 72. 복굴절률이 매우 크 기 때문에 투명한 방해석 결정을 통해 보면 반대편의 물체가 이중으 로 보인다. 최대 간섭색은 매우 높은 등급의 백색, 회색이 된다. 소광특징 결정면이나 쌍정면을 기준으로 대칭소광을 나타낸다. 광학부호 일축성, (一). 간섭상을 만들어 보면 아이소자 주위에
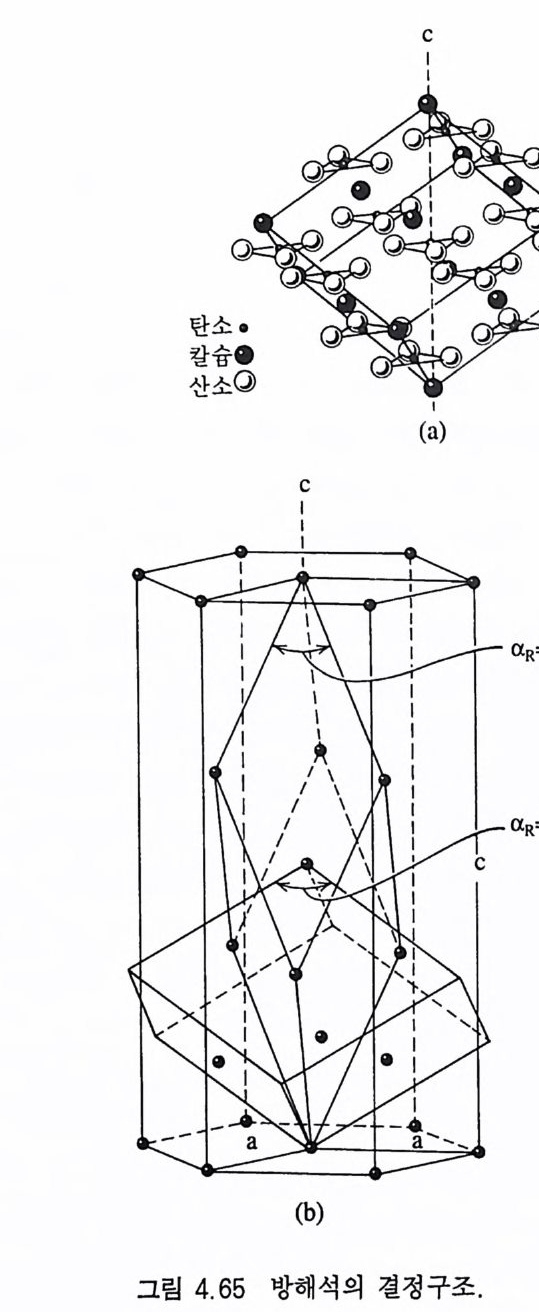 CII
CII
 :
:
아이소크롬이 많이 존재한다 . X 선 회절선 3.86(1 ), 3.035(1 0 ), 2.4 9 5( 1), 2.285( 1), 2.095( 1), 1.92 7(1 ), 1.91 3(2), t.87 5(2), t.62 6(0A 기타사항 현미경하에서 방해석에 보이는 대각선 방향의 줄무늬 가 쌍정인지 또는 벽개인지를 구별할 때는 교차니콜하에서 관찰하 면 된댜 즉, 교차니콜하에서 검게 보이면 벽개이고, 간섭색을 나 타내는 줄무늬로 보이면서 재물대를 회전할 때 간섭색이 변하면 쌍정이다. 방해석은 붉은 염산에 탄산가스를 내면서 쉽게 분해된 다. 이러한 분해 정도의 차이를 이용해 야외에서 방해석과 백운석
을 구별한다. 방해석의 분해 온도는 1 기압에서 894.4 ° C 이다 . 방해 석은 퇴적암과 변성암에서 주요 조암광물로 산 출 되며, 화성암에서 도 불석과 함께 정동 내에서 산출된다 . 열수환경에서도 정출되는데 이 경우는 거의 마지막 단계에서 맥상형태로 침전한다 . 방해석은 석 회암, 대리암의 주구성광물이다. 시멘트를 제조하는 데 주로 사용되 며, 비료, 화장품, 치약, 종이, 철강공업에도 활 용된다 . 투 명한 방 해석을 아이슬란드 스파 (Iceland S p ar) 라고 하는데, 이 들 은 과거 편 광현미경이나 안경의 광학 부품을 제조하는 데 사용되었다. 광물명 은 〈 타버린 석회〉라는 의미의 그리스어에서 유래되었다 . 【마그네사이트 (Mg C OJ )] 화학성분 Mg C OJ . Mg O 47.8, CO2 52.2%. M g과 Fe 의 치환에 의 해 능철석(菱 鐵 石)과 완전고용체를 형성한다(그림 4.67). M g을 치 환하는 Mn 과 Ca 의 양은 매우 적다. 결정계 삼방정 계 . 32/m, R칭 c. a=4.63, c= l5.02A . Z=6. 색 백색, 회색, 황색, 갈색 . 투명 내지 반투명 . 유리광택. 박편 하에서는 무색이다. 결정형태 능면체가 전형적인 결정형태이지만 결정으로 산출되는 경우는 매우 드물다 . 입상질 형태로도 산출된다. 벽개 {10 11} 방향의 완전한 벽개가 발달한다. 경도 3.5~5 비중 3.0 ~ 3.2 양각 비교적 높음 굴절률 (l)=1.70 0, E=1 .50 9. 복굴절률 =0 .1 9 1. 간섭색은 높은 등급 의 백색 계통으로서, 회백색을 띤다. 소광특징 대칭소광을 한다. 광학부호 일축성, (-)
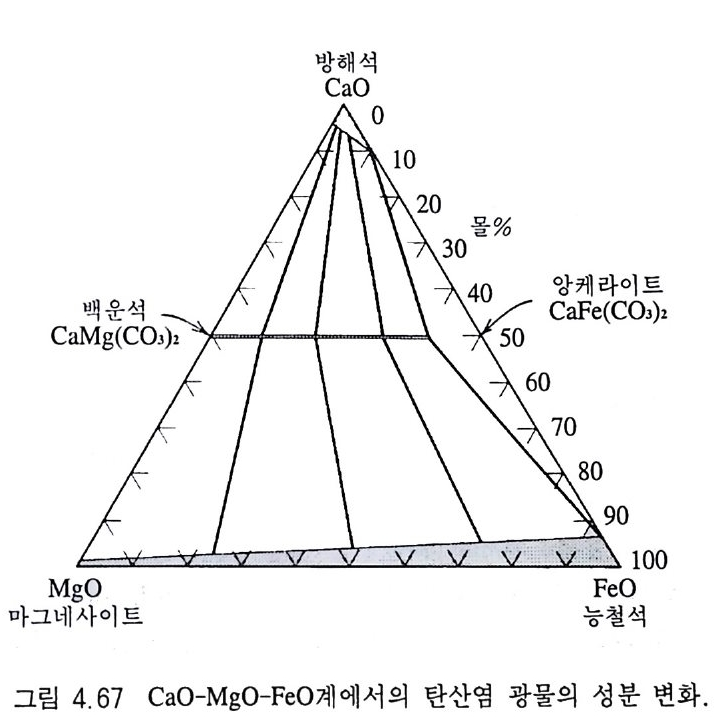 앙케라이트
앙케라이트
X 선 회절선 2.742(1 0 ), 2.5 0 3(2), 2.3 1 8( 1), 2.1 0 2(4), 1.93 9(1 ), 1.7 690), l.70 0(3)A 기타사항 마그네사이트는 페리도타이트나 사문암과 같이 Mg 성 분이 많은 화성암이나 변성암이 변질될 때 만들어진다. 이 경우 탄산이온을 함유하고 있는 물의 역할이 결정적으로 필요하다. 이 런 과정으로 만들어지는 마그네사이트는 미결정질이며 매우 치밀 한 조직을 가진다. 이와는 대조적으로, 벽개가 발달할 정도로 큰 마그네사이트 결정은 활석이나 녹니석, 운모 등을 함유하는 편암 이 변성작용을 받을 때 만들어진다. Mg 성분을 함유하고 있는 열 수로부터 직접 정출되거나 , 또는 이러한 성분을 함유하고 있는 열 수에 의해 석회암이 교대작용을 받을 때에도 만들어진다. 이때 백 운석이 중간 단계의 물질로 존재한다. 대표적인 광상은 중국의 만
추리아, 우랄산맥의 사트카, 오스트리아의 스티리아 등지에 있다. 마그네사이트를 고온으로 가열하여 Mg O 형태로 만들어 내화제용 벽돌을 만드는데 사용한다. 그 밖에도 마그네슘을 정제하는 원료물 질로 사용되고 있다. 최근에는 바닷물을 증류하여 마그네슘을 추출 한다 . 광물명은 이 광물의 주구성 성분인 M g에서 유래되었다 . 【능철석 (Sid e ri te) > 화학성분 FeCOJ . FeO 62.1 , CO2 37.9%. Mn 과 M g이 Fe 을 치 환 하며, 마그네사이트와 능망간석은 완전고용체를 형성한다. Ca 과는 이온의 차이가 크기 때문에 치환이 매우 제한적이다. 결정계 삼방정 계 . 32/m, R3c. 색 갈색으로서 짙기는 다양하다. 유리광택. 투명 내지 반투명하 다. 박편하에서는 무색 또는 회색이다. 간혹 황색 또는 갈색 반점 이 있을 수 있다. 결정형태 주로 능면체로 산출되며, 간혹 결정면이 휘어진 경우 도 있다. 입상질 형태로도 산출된다. 벽개 {10 11} 방향의 완전한 벽개가 발달한다 . 경도 3.5 ~ 4 비중 3.96. Fe 을 치환하는 M g이나 Mn 의 양에 따라 비중이 감 소한다. 양각 결정의 배열 방향에 따라 높거나 보통 정도이다 . 굴절률 E=l. 59 6~1 .63 3, (I)=1.83 0~1 .87 5. 복굴절률 =0.234~0.242. 간섭색은 높은 등급의 백색 계통이다. 소광특징 벽개 방향을 기준으로 대칭소광을 한다. 광학부호 일축성, (내 X 선 회절선 3.59(2), 2.795(1 0 ), 2.3 4 6(2), 2.1 3 4(2), 1.9 65(2), 1.79 6(1 ), 1.73 8(3), 1.73 1 (3), t.50 6(1 ), t.42 60)A
기타사항 가열하면 강한 자성을 띤다 . 염산을 떨구면 거품을 내 며 반응한다. 능철석은 점토광물과 함께 산출되는 경우가 많다. 셰일 내에서 석탄과 같은 탄소물질과 함께 혹철광 (black-band ore) 을 형성하기도 한다. 석회암이 Fe 성분을 다량 함유하는 열수용액 에 의해 교대될 때에 만들어지기도 하는데, 이렇게 만들어진 광상 이 오스트리아의 스티리아 (S tyri a) 에 있다. 철광의 원료로 사용되 며, 광 물 명은 철 (Fe) 을 의미하는 그리스어에서 유래되었다. 【능망간석 (Rhodochrosit e) > 화학성분 MnCOJ . MnO 61. 7, CO2 38.3%. Mn 과 Fe 사이의 치환 으로 능칠석과는 완전고용체를 형성한다. Ca 은 Mn 을 일부 치환한 다. Mg 역시 Mn 을 소량 치환한다. Zn 도 Mn 을 일부 치환할 수 있다. 결정계 삼방정계 . 32/m. R3c. a=4.78, c=15.6 7 A. 방해석과 동일 한 결정구조를 하고 있음. 색 분홍색 계통의 적색 또는 황갈색을 띤다. 투명 내지 반투명 하다. 유리 광택. 박편하에서는 거의 무색이며, 두꺼운 박편일 경 우 약간의 분홍빛이 감지될 수 있고 다색성도 관찰될 수 있다. 투 명 또는 반투명하다. 유리광택을 띤다. 둥근 무늬 또는 층상구조 가 보이기도 하는데, 특히 투명하거나 띠구조가 잘 발달한 것은 보석으로 가공한다. 결정형태 능면체가 전형적인 결정 형태이긴 하지만 매우 드물 고, 대부분 괴상 형태로 산출된다. 때로는 포도상 조직으로 산출 되기도 한다. 벽개 {1011} 방향의 완전한 벽개가 발달한다. 경도 3.5 ~ 4 비중 3.5~3.7
굴절률 E=1 .59 7, (J)=1.81 6. 복굴절률 =0.219 . 투명한 결정에서는 복굴절 현상에 의해 이중상 (doubl i n gi ma g e) 이 관찰된다. 소광특징 벽개 방향을 기준으로 대칭소광을 한다. 광학특성 일축성, (-) X 선 회절선 3.66(3), 2.84(1 0 ), 2.3 9 (1 ), 2.1 7 2(2), 2.0 0 0(2) , I.82 90), I.77 0(3), I.53 30)A 기타사항 염산에 거품을 내면서 반응한다 . 610~635 ° C 에서 분해 되면서 MnO 를 만들며, 700°C 에서는 산화되어 하우스마나이트 (Mn3 Q 4) 가 된다. 능망간석은 고온의 변성교대작용으로 형성된 광 상에서 장미휘석, 스페샤르틴, 브라우나이트, 테프로아이트와 같 은 Mn 광물과 함께 산출된다. 열수맥으로부터 직접 침전하기도 한다. 일부 페그마타이트에서도 발견된다. 능망간석은 망가나이 트 (MnO • OH) 또는 연망간석 (Mn02) 으로 변질된다. 광물명은 〈 장 미〉와 〈색〉을 나타내는 2 개의 그리스어에서 유래되었다 . 4. 3. 3. 2 아라고나이트군 (ARAGONITE GROUP) 【아라고나이 트 (Arago n it e) > 화학성분 CaCOJ . 비교적 순수한 성분을 지닌 채로 산출되며, 약간 의 Sr 이나 Pb 이 Ca 울 치환할 수 있다. 결정계 사방정 계 . 2/m 2/m 2/m. Pmcn. a=4.9 5 , b=?.96, c= 5.73A _ Z=4 색 무색, 백색, 옅은 황색. 투명 내지 반투명 . 유리광택. 박편 하에서는 무색을 띤다. 결정형태 주로 4 가지 형태로 산출되는데(그림 4.68), (1) 가는 주 상 결정의 양끝에 추가 결합된 취형 (a), (2) {010} 의 탁(pi naco i d) 과 {110} 과 {011} 의 사방주가 결합된 판상체 (b), (3) 접촉쌍정
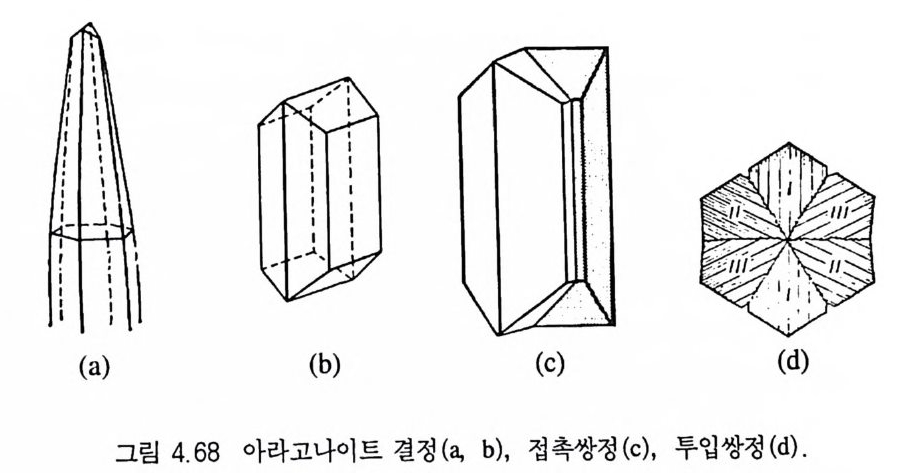 (a) (b) (c) (d)
(a) (b) (c) (d)
(c), (4) 윤좌쌍정 (d) 등이다. 그 외 신장상 또는 종유상 형태로도 산출된다 . 벽개 {01 이 방향의 명료한 벽개와, {110} 방향의 불량한 벽개가 발달한다 . 경도 3.5~4 비중 2.95 굴절률 a=l. 53 0, /3=1.68 0, r=1.68 5. 복굴절률 =0 .1 55 소광특징 평행소광을 한다. 광학부호 이축성, (-) . 2V=18° X 선 회절선 3.3 9 6(1 0 ), 3.273(5), 2.871( 1), 2.730(1 ), 2.700(5), 2.4 8 1(3), 2.4 0 9( 1), 2.3 7 2(4), 2.341(3), 2.328( 1), 2.188( 1), 2.1 0 6(2), 1.9 77(7), I.88 2(3), I.87 7(2), I.81 4(2)A 기타사항 아라고나이트는 방해석과 동질이상체 관계이며, 방해 석에 바해 더 높은 압력과 낮은 온도 조건에서 안정하다(그림 4.69). 또한 아라고나이트는 대기압에서 방해석보다 덜 안정하기 때 문에, 아라고나이트의 외형을 지닌 방해석 가상(假像, pse udomorp h )
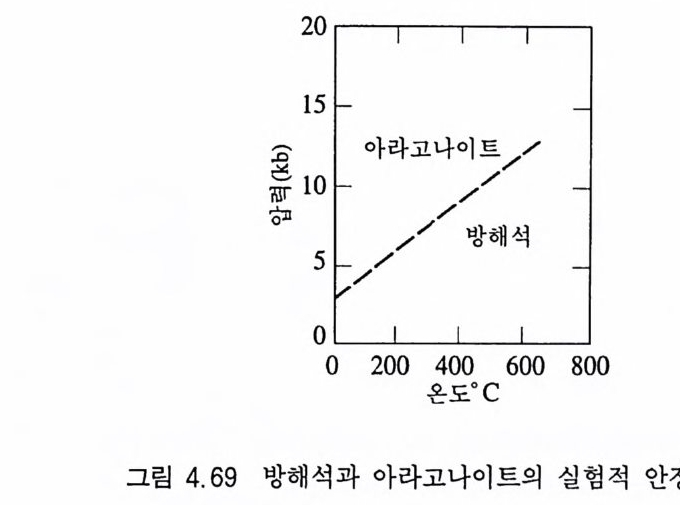 20
20
이 빈번하게 발견된다. 실험적 연구 결과에 의하면 탄산칼슘 성분 울 함유한 용액이 따뜻할 경우 아라고나이트가, 찰 경우 방해석이 침전하는 것으로 알려져 있다. 조개껍질이나 진주는 따뜻한 해수 에서 침전된 것이므로 처음에는 모두 아라고나이트 구조이다가 후 에 방해석 구조로 바뀐다. 아라고나이트는 온천이 솟는 곳에서 석 고와 함께 침전되는 경우가 있다. 사문석의 표면에 섬유상 형태의 물질로 막이 씌워 진 듯이 발달하는 경우도 있으며, 현무암의 정동 내에서는 행인상 구조를 이루며 산출되는 경우도 있다. 광물명은 윤좌쌍정을 하는 아라고나이트가 처음 발견된 스페인의 아라곤 (Ara g on) 의 지명에서 유래되었다. 【위 더 라이 트 (Wi ther it e)> 화학성분 BaCOJ . BaO 77.7, CO2 22.3%. Ca 과 Sr 등이 Ba 을 소량 치환할 수 있다. 결정계 사방정 계 . 2/m 2/m 2/m. Pmcn. a=5.26, b=8.85, c= 6.55A. Z=4.
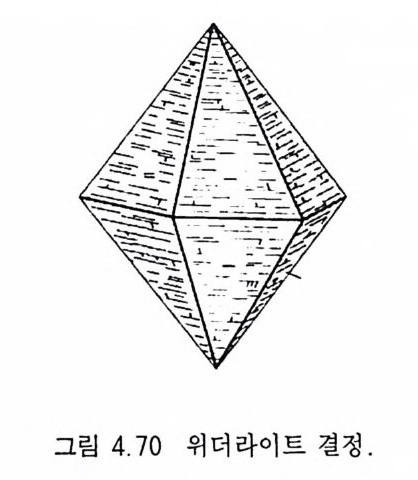 그림 4.7 0 위더라이트 결정 .
그림 4.7 0 위더라이트 결정 .
색 무색, 백색, 회색. 반투명하다 . 유리광택. 결정형태 전형적인 결정 형태는 3 개의 결정이 6 방 양추형태를 이루는 쌍정이며(그림 4.70), 결정면상에 수평 조선이 뚜렷하게 발 달하는 점도 특징이다. 그 외 신장상, 주상, 입상 형태의 결정도 산출된다. 벽개 {010} 방향의 명료한 벽개와, {110} 방향의 불량한 벽개가 발달한다. 경도 3.5 비중 4.3 굴절률 a=l. 52 9, /3=1.67 6, r=1.67 7. 복굴절률 =0 .1 48 소광특징 평행소광을 한다. 광학부호 이축성, (-). 2V=l6° X 선 회절선 4.56( 1), 4.4 5 (1 ), 3.7 2 (1 0 ), 3.67(5), 3.2 1 5( 1), 2.656( 1), 2.628(2), 2.590(2), 2.1 5 0(3), 2.1 0 4(1 ), 2.048( 1), 2.019(2)A 기타사항 Ba 성분 때문에 황록색의 불꽃을 내며 탄다. 염산을 떨구면 거품을 내면서 반응한다. 황산을 떨구면 반응하여 BaS04 를
침전시킨다. 비교적 드문 광물로서, 방연석을 함유하고 있는 맥에 서 발견된다 . 영국의 핵스헨 오스트리아의 짤츠부르크 등지에서 산출된다. 【스트론티 아나이 트 (Str on ti an it e) > 화학성분 SrCOJ . SrO 70.2, CO2 29.8%. Ca 이 Sr 을 최 대 25 a t.%까 지 치환할 수 있다 . 결정계 사방정 계 . 2/m 2/m 2/m. Pmcn. a=S.1 3 , b=S.4 2 , c= 6.09A. Z=4. 색 백색, 회색, 황색, 녹색 . 유리광택 . 투명 내지 반투명하다. 결정형태 침상형태의 결정들이 방사상 구조를 이루며 산출하는 경우가 대부분이다. 벽개 {110} 방향의 양호한 벽개가 발달한다. 경도 3.5~4 비중 3.7 굴절률 a=l. 52 0, /3=1.66 7, r=1.66 9. 복굴절률 =0 .1 49 소광특징 평행소광을 한다. 광학부호 이축성, (-). 2V=7 °. X=c, Y=b X 선 회절선 4.367(1 ), 4.207(1 ), 3.535(1 0 ), 3.4 5 0(7), 3.014(2), 2.838(2), 2.597(0, 2.554(2), 2.481 (3), 2.4 5 8(4), 2.4 5 1 (3)A 기타사항 고온의 센 불꽃을 대면 붉은 Sr 연기를 낸다. 염산과 반 응하며, 황산을 떨구면 반응하여 SrSO~ 를 침전시킨다 . 중정석, 셀레 스타이트, 방해석 등과 함께 석회암에서 맥상 형태로 산출된다. 화성암에서도 간혹 발견된다. 황화광물과도 공생하는 경우가 있 다. 스트론튬의 원료 광물로 사용되고 있으며, 폭죽 제조나 적색 연기를 내는 제품을 만드는 데 사용되고 있다. 강원도 홍천 철광 상에서 자철석 둥과 함께 산출한다. 광물명은 처음 발견되었던 스
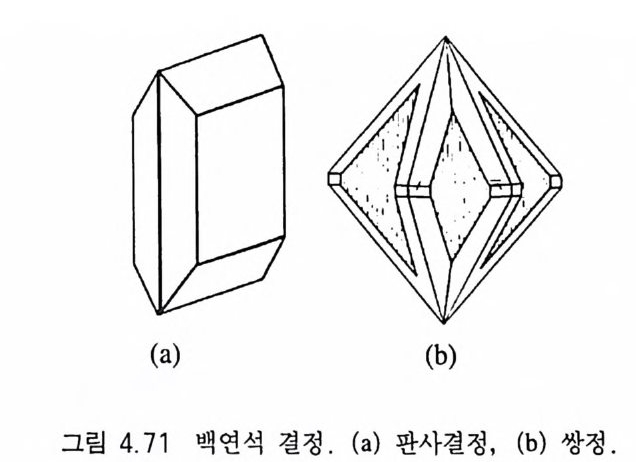 (a) (b)
(a) (b)
코틀랜드의 지명 (S t ron ti an) 에서 유래되었다 . 【백 연석 (Cerussit e) > 화학성분 PbCOJ . PbO 83.5, CO2 16.5 %. 결정계 사방정 계 . 2/m 2/m 2/m. Pmcn. a=S.1 5 , b=8.47, c= 6.l l A. Z=4. 색 무색, 백색, 회색. 투명 내지 아투명. 아금강광택. 결정형태 다양한 형태로 산출된다. 간혹 판상(그림 4.71 a) 또는 쌍정(그림 4.7 1 b) 으로 산출된다 . 입상 또는 섬유상으로 산출되는 경우도 있다. 벽개 {110} 방향의 우수한 벽개와 {021} 방향의 양호한 벽개가 발 달한다. 경도 3~3.5 비중 6.55 굴절률 a= 1.804, {3= 2.077, y=2 .079. 복굴절률 =0.275 소광특징 평행소광을 한다.
광학부호 이축성, (一). 2V=9°. X=c, Y=b X 선 회절선 4.427(2), 4.255(1 ), 3.5 9 3(1 0 ), 3.498(4), 3.074(2), 2.589( 1), 2.522(2), 2.487(3), 2.081(3), 2.009( 1), 1.9 33(2), L859(2)A 기타사항 따뜻한 붉은 염산에 거품을 내며 녹는다 . 방연석 광상 이 있는 곳에 탄산 이온을 함유하는 용액이 작용하여 2 차적으로 만들어진다. 이때 앙글레사이트, 능아연석 (smi thso nit e) , 갈철석 등 과 같은 2 차 광물이 함께 공생하는 경우가 많다. 방연석과 함께 연(鉛)의 주요 광석광물이다. 광물명은 백철(白 鐵 )을 의미하는 라 틴어에서 유래하였다. 4. 3 . 3 . 3 백운석군 (DO LOMITE GROUP) 【백 운석 (Dolom ite) > 화학성분 CaMg (C OJ ) 2. cao 30.4 , Mg O 21. 1, CO2 47.9%. 1oo·c 이상의 고온에서는 성분의 변화가 다소 있다. 자연에서 산출되는 백운석의 성분은 Ca:M g의 비가 58:42~47.5 : 52.5 범위에 있다. 앙 케라이트 [CaFe(CO J h] 와 완전고용체를 형성한다. 백운석은 고온에 서 마그네사이트와 완전고용체를 형성하지 않지만(그림 4.72), 방 해석과는 완전고용체를 형성한다. 이러한 현상을 이용하면, 공생 하고 있는 방해석과 백운석의 화학성분을 통해 두 광물이 함유되 어 있는 암석의 생성 온도를 추측할 수가 있다. 결정계 삼방정계. 3. R3. a=4.84, c=15.95A. Z=3. Ca 과 Mg 이 온의 반경 차이가 매우 크므로 (33%) 치환이 자유롭지 않고, 각 원 자는 질서있게 채워진다. 색 백색, 분홍색이 도는 회색, 녹색, 갈색. 투명 내지 반투명하 다. 유리광택. 박편하에서는 무색이다.
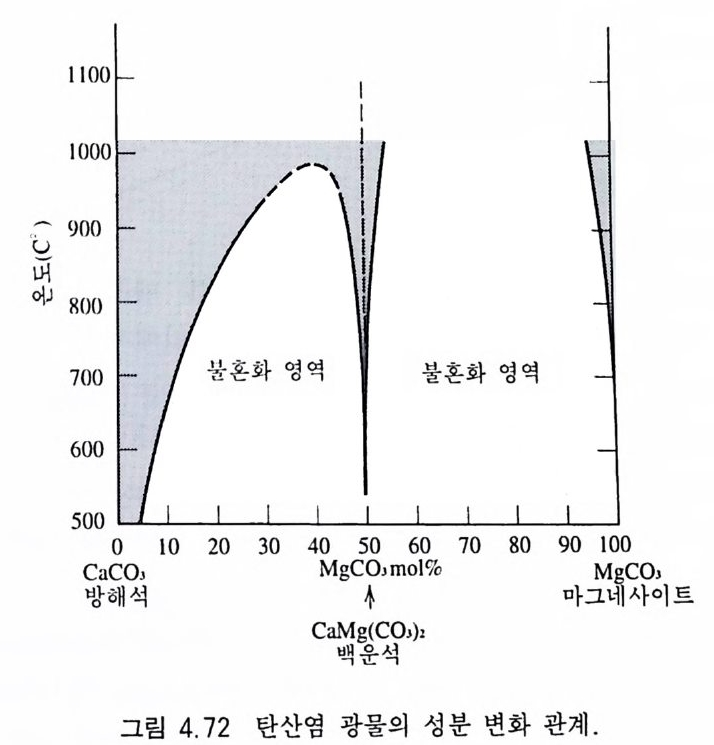 1100,
1100,
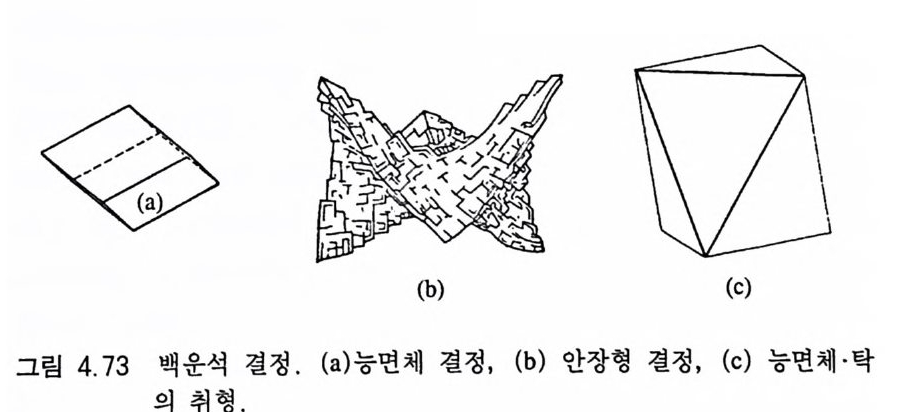 <
<
결정형태 능면체(그림 4.7 3 a), 휘어진 결정면 을 지닌 상태 ( b ) , 경사 가 급한 능면체 (c) 등으로 산 출 된다 . {0001} 에 따 른 접촉 쌍정과 {022 마방향의 취편쌍정이 발달한다. 벽개 {1011} 방향의 능면체상 벽개가 완전하게 발 달 하여 두 방향 의 교차하는 선구조 를 나타낸다 . 경도 3.5~4 비중 2.85 굴절률 CO=l .68 1, E=l .50 0. 복굴절률 =0 .1 8 1. 매우 높 은 등 급의 백색 계통 간섭색을 나타내며, 입자의 가장자리에서 는 4 ~ 5 ° 의 밝 은 간섭색을 보이기도 한다 . 소광특징 벽개 방향을 기준으로 대칭소광을 한다 . 광학부호 일축성, (-) X 선 회절선 3.6 9 (1 ), 2.886(1 0 ), 2.6 7 0( 1), 2.540(1 ), 2.4 0 5(1 ) , 2.1 9 2(3), 2.015o), 1.8 04(2), I.78 6(3), I.56 7o)A 기타사항 박편하에서는 방해석이나 마그네사이트와 매우 비 슷 하 다. 정확하게 구별하기 위해서는 화학분석이나 X 선 회 절 분석 , 착 색실험 등을 실시해야 한다. 품고 찬 염산에는 반응이 매우 느리 며, 따뜻한 염산에만 거품을 내면서 신속히 반응한다 . 이러한 현 상은 석회암과 백운암 (dolos t one) 을 야외에서 구별하는데 사용된다. 백운석은 석회암이 M g의 교대작용에 의해 2 차적으로 만 들 어진 것 으로 알려져 있으며, Ca 과 M g의 치환이 매우 제한적이기 때문에 실제 백운암에는 백운석과 방해석이 공존하고 있다. 석회암이 백 운암으로 변할 때 체적 감소가 일어나기 때문에 공동이 생길 수가 있 다 . 미 국 미 시 시 피 밸 리 형 광상 (Mi ss is s ip pi Valley type ore dep os it s ) 은 이렇게 만들어진 공동 속에 대규모의 연, 아연 광상이 형성되 어 있는 것을 지칭한다. 마그네슘울 추출하는 광석광물로 사용되 며, 내화벽돌, 건축자재 등으로 쓰이고 있다.
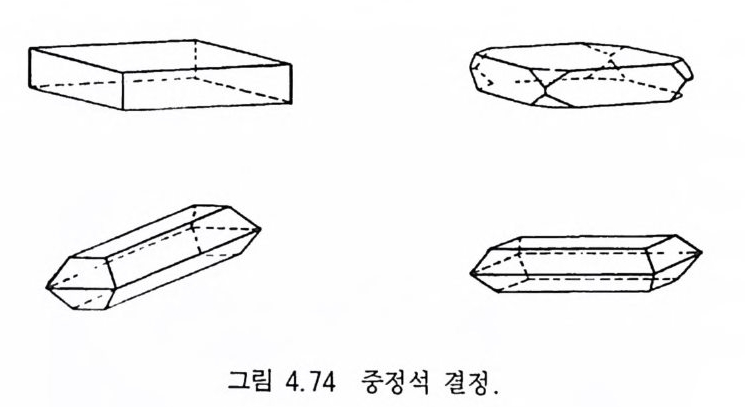 三 三
三 三
4.3.4 황산염 광물 4. 3. 4 . 1 중정석군(B ARITE GROUP) 【중정 석 (Bari le )> 화학성분 BaSO 』 . Bao 65.7, sol3 4.3%. Ba 과 Sr 과의 치환에 의하 여 셀레스타이트 (celes tit e, SrSO,) 와 완전고용체를 형성한다. Pb 도 Ba 을 소량 치환한다 . 결정계 사방정 계 . 2/m 2/m 2/m. Pnma. a=8.87, b=5.4 5 , c= 7.1 4 A . Z=4 색 무색, 백색, 옅은 청색 또는 황색. 투명 내지 반투명. 유리 광택. 박편하에서는 무색이다. 결정형태 a 또는 b 축을 따라 길쭉한 판상 형태로 나타난다(그림 4.7 4 ) . 간혹 매 우 얇은 엽 상 결정 들로 이 루어 진 장미 꽃송이 (ba rite rose) 형태를 나타내기도 한다(그림 4.75). {11 이 면이 쌍정면 구실 울 하는 취편쌍정도 발견된다. 벽개 {001}, {01 아 방향의 완전한 벽개가 90• 로 발달하며, {210} 방 향의 양호한 벽개도 발달한다.
 그림 4.7 5 장미 꽃송이 형태의 중정석 결정 집합체.
그림 4.7 5 장미 꽃송이 형태의 중정석 결정 집합체.
경도 3~3.5 비중 4.5 로 매우 높은데, 이는 중정석의 매우 중요한 성질이다. 중정석(重晶石)이란 이름도 이로부터 유래되었다. 양각 높은 편이다. 굴절률 a=1 .63 6, {3=1.63 7, r=1.64 8. 복굴절률 =0.012 . 최대 간 섭색은 석영보다 다소 높으며 1· 의 황색을 넘지 않는다. 소광특징 {001} 방향의 벽개에 나란한 평행소광을 하며, {001} 에 나란하게 절단된 박편에서는 대칭소광을 한다. 장축부호 {001 } 방향의 벽개를 따라 느린 광선이 진동한다. X 선 회절선 4.44(2), 4.33(3), 3.899(5), 3.773( 1), 3.577(3), 3.445(1 0 ), 3.3 1 9(7), 3.103(9), 2.836(5), 2.735( 1), 2.729(4), 2.4820), 2.325(1 ), 2.211 (2)A 기타사항 중정석은 열수맥에서 연, 아연, 동, 코발트 등의 광물 들과 함께 산출되는 경우가 많고, 일본의 쿠로코 광상에서는 화산
암 내에서 다량 산출된다. 석회암이나 사암에도 존재한다. 온천이 솟는 곳에서도 침전된다. 중정석은 유전이나 천연가스를 찾기 위 한 시추작업을 할 때 보조물질로 사용하며 바륨 (Ba) 을 추출하는 데에도 사용된다 . 바륨은 페인트나 양탄자, 직물을 제조할 때 원 료물질로 사용된다 . 바륨은 황산바륨으로 재침전시켜 종이의 충진 세 로, 화장품의 원료로, 페인트의 색소로, 방사선 촬영을 위한 조 영제( 造影'제) 등으 로 사용된다. 광물명은 비중이 높아 무겁기 때문 에 〈무 겁다 〉 라는 의미의 그리스어에서 유래되었다 . 【셀 레 스타이 트 (Celesti te) > 화학성분 SrSO~. SrO 56.4 , S01 43.6%. Ba 과 Sr 의 치 환에 의 해 중 정석과는 완전고용체를 형성한다. 경석고 (Caso~) 와는 매우 제한적 인 고용체 관계가 성립한다 . 결정계 사방정 계 . 2/m 2/m 2/m. Pnma. a=8.3 8 , b=S.37, c= 6.85A. Z=4. 색 무색, 백색, 옅은 청색 또는 적색을 띠는 경우도 있다. 유리 광택 또는 진주광택. 투명 내지 반투명하다. 결정형태 중정석 결정과 유사하다 . {001 } 방향에 따른 납작한 판 상 또는 주상 형태로 산출된다(그림 4.76). a 축을 따라 길쭉하게 발달한 결정에서는 결정면 d{IOI} 과 m{210} 이 비슷한 크기로 발
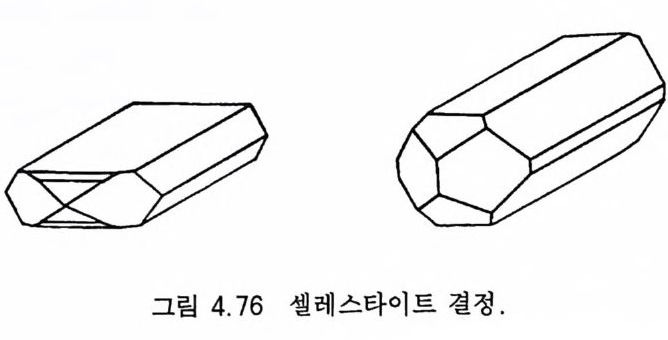 그림 4.7 6 셀레스타이트 결정.
그림 4.7 6 셀레스타이트 결정.
달한다. 벽개 {001} 방향의 완전한 벽개와 {21 이 방향의 우수한 벽개가 발 달한다 . 경도 3~3.5 비중 3.95~3.97 굴절률 a=1. 62 2, /3=1.62 4, r=1.63 1 . 복굴절 률 = 0.009 소광특징 평행소광 광학부호 이축성, (+). 2V=50°. X=c, Y=b X 선 회 절선 4.23 (1 ), 3.77 (3), 3.4 3 3 (3), 3.295 (10 ), 3.177 (6), 2.9 7 2(1 0 ), 2.731(6), 2.6 7 4(5), 2.377(2), 2.253(2), 2.141(2), 2.045 (5), 2.041 (6), 2.006(4)A 기타사항 석회암이나 사암에서 산점상으로 또는 이들 암석에 발 달한 공동의 내벽에서 산출한다. 이때 방해석, 석고, 암염, 유 황, 형석 등과 공존하는 경우가 많다. 폭죽이나 조명탄을 제조하 는데 사용되는 질산스트론튬 [Sr(NO J )2] 을 만드는 원료로 사용된다 . 광물명은 처음 발견된 광물이 연한 청색을 띠었으므로 이 색을 의 미하는 coeles ti s 에서 유래하였다. 【앙글레사이트 (Ang le site ) > 화학성분 PbS04. PbO 73.6, SOJ 26.4%. 결정계 사방정계. 2/m2/m2/m.Pnma. a=8.4 7 , b=5.39, c=6.94 A. Z=4. 색 무색, 백색, 회색, 옅은 황색. 투명 내지 반투명. 아금강광택 . 결정형태 납작한 판상체 형태가 전형적이다(그림 4.77). 둥근 층 상구조를 하고 있는 집합체로도 산출된다. 벽개 {001} 방향의 우수한 벽개와 {210} 방향의 불완전한 벽개가 발달한다.
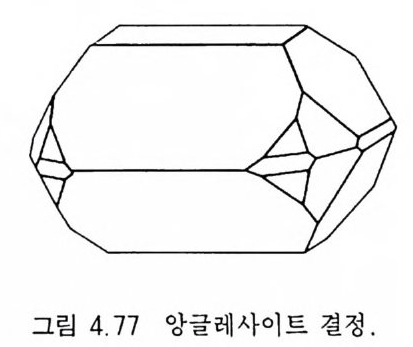 그림 4.7 7 앙글레사이트 결정 .
그림 4.7 7 앙글레사이트 결정 .
굴절률 a= l.877, /3= 1.8 83, y= 1.8 94. 복굴절률 =0.017 소광특징 평 행 소광을 한다. 광학부호 이축성, (+). 2V=75°.X =c, Y=b X 선 회절선 4.26(9), 3.813(6), 3.622(2), 3.4 7 9(3), 3.333(9), 3.220(7), 3.001 ( 10), 2.773(3), 2.6 9 9(5), 2.618( 1) 2.4 0 6( 1), 2.2 7 6(2)A 기타사항 앙글레사이트는 연( 鉛 )광상 표면이 산화될 때 만들어 지는 2 차 광물이다. 대부분의 경우 방연석의 핵을 중심으로 동심 원상의 층상구조를 하고 있다 . 방연석, 섬아연석, 능아연석 등의 광물과 공생하는 경우가 많다. 연을 추출하는 광석으로 사용되 며, 처음 발견된 An g lese y섬의 이름에서 광물명이 유래되었다. 4. 3. 4. 2 석고 (GYPSUM) 화학성 분 CaS04 • 2H20. CaO 32.6, SOJ 46.5, H20 20.9%. 석 고 (石 音 )를 가열하면 처음 0~65°C 에서 물 분자가 일부 소실되어 CaS04 • 송 H20 가 된다(그림 4.78). 이 과정에서 석고의 결정구조는 약간 변형되는 것으로 추정하고 있다. 계속 가열하면 95°C 에서 물 분자가 완전히 소실되어 경석고 (CaS04) 가 된다. 이러한 현상은 시 차열분석시 2 개의 홉열 피크가 나타남을 통해 확인할 수 있다.
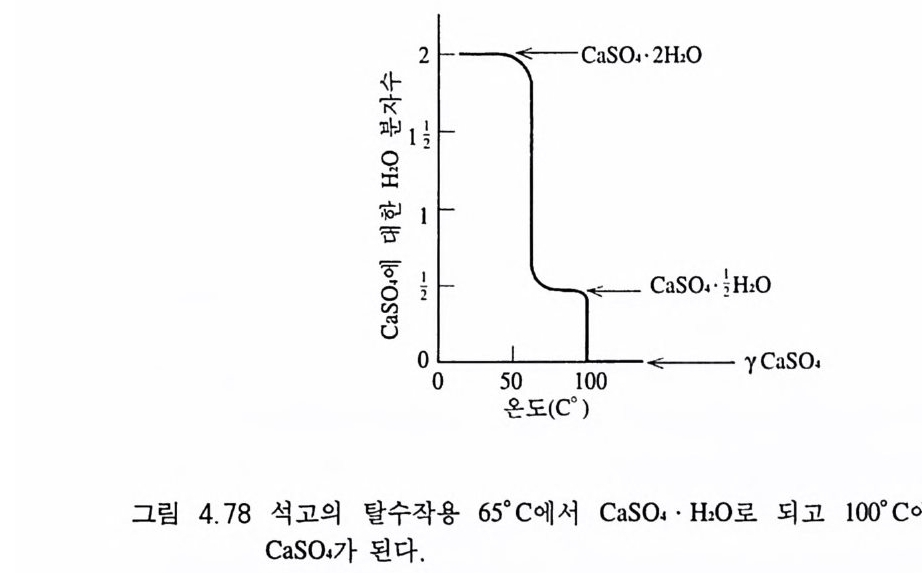 2
2
결정계 단사정계. 2/m. C2/c. a=6.2 8 , b=15.1 5 , c=5.67A. Z=4. 색 무색, 백색, 옅은 회색, 갈색, 황색, 적색. 유리광택 내지 진주광택을 띤다 . 섬유상 조직을 가지는 변종에서는 견사광택을 띤다 투명 내지 반투명하다. 박편하에서는 무색이다. 결정형태 {01 이 방향의 납작한 판상체나, {1 20} 과 {111} 면이 결 합된 형태를 하고 있다(그림 4.79a). 접촉면이 (1 00) 인 접촉쌍정도 자주 발견된다(그림 4.79b). 벽개 {01 이 방향의 완전한 벽개가 발달하여 비늘처럼 분리되며, 섬 유상 조직을 나타내는 변종에서는 {011} 방향의 벽개가 발달한다. 패각상 단구도 발달한다. (1 00) 과 (1 01) 의 각은 66°10’ 이다. 경도 2 비중 2.3 2 양각낮음 굴절률 a=l. 52 0, /3=1.52 2, ,-1.52 9. 복굴절률 =0.009. 간섭색은
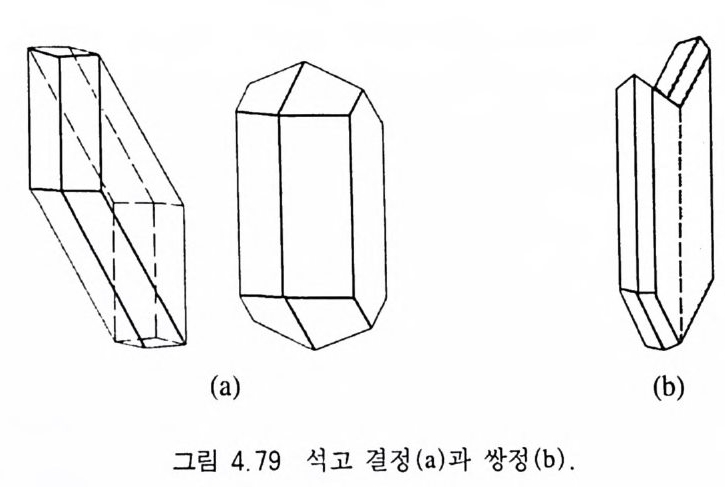 (a) (b)
(a) (b)
r 의 백색 또는 옅은 노란색을 띤다. 소광특징 (010) 에 수직으로 절단된 입자인 경우 벽개에 나란한 위치에서 소광한다. 최대 소광각은 약 37° 이다 . 장축부호 Y=b 이므로 벽개를 따라 빠르고 느린 두 광선이 동시 에 각각 진동한다. 광학부호 이축성 (+). 2V=58°.Y =b X 선 회절선 7.61(4), 4.74( 1), 4.28(9), 3.80( 1), 3.07(3), 2.871 (lo) , 2.788(2), 2.684(5), 2.4 8 6(2), 2.0870), 2.073(2)A 기타사항 석고중 섬유상 조직을 가지며 견사광택을 띠는 변종을 새 틴 스파 (sati n spa r) 라 하고, 세 립 의 괴 상체 를 앨 라바스터 (alabaste r ), 투명하면서 비늘처럼 분리되는 변종을 셀레나이트 (selen it e) 라고 한다. 퇴적암이 분포하는 곳에서 주로 발견되며, 담 수나 염수가 증발하여 만들어진다. 새틴 스파는 맥상으로도 산출 된다. 경석고가 석고로 변할 수도 있는데 이 경우 부피 증가에 의 해 휘어짐이 생기기도 한다 . 석회암이 분포하는 지역에 화산활동 이 있을 경우 화산물질 중 유황이 석회암과 작용하여 석고를 형성
하기도 한다. 경석고, 암염, 유황, 방해석, 황철석, 백운석, 석영 등의 광물과 함께 산출된다. 대규모의 석고 광상은 미국의 캘리포 니아주, 애리조나주, 아이오와주, 텍사스주, 캐나다, 프랑 스, 일 본, 이란 등지에 분포되어 있다. 석고는 주로 건축자재로 사용된 댜 죽, 석고를 분말로 만든 후 가열해 75 % 정도 의 수분이 증발하 도록 만든 다음, 물과 혼합시키면 서서히 물을 홉수하여 결정화되 면서 굳어진다 . 이룰 원료로 하여 석고보드 를 제작한다 . 석 고보 드 는 임시 건축물을 단기간 만들어 둘 때, 건축물의 실 내 천장이나 벽을 만들 때 주로 사용된다 . 토양 중화제, 시멘트의 원료물질로 도 사용된다. 새틴 스파나 알라바스터는 장신구나 공예품으로 가 공하는데, 경도가 매우 낮기 때문에 관상용 진열품 제조에만 쓰인 댜 석회 성분이 있는 광물을 의미하는 그리스어에서 광물명이 유 래되었다 . 4. 3. 4. 3 경석고 (ANHYDRITE) 화학성 분 CaS04. CaO 41 .2, SOJ 58.8%. 미 량의 Sr 과 Ba 이 Ca 을 치 환할 수 있다. 화학분석시 수분이 검출되는 수가 있는데, 이것은 석고가 불순물로 공존하기 때문이다. 결정계 사방정계 . 2/m 2/m 2/m. Amma. a=6.95, b=6.96, c= 6.21A. Z=4. Ca 의 배위수는 8 이다. 색 무색, 옅은 청색, 보라색, 갈색, 적색. 유리광택 내지 진주 광택. 박편에서는 무색이다. 결정형태 탁상 형태인 경우가 대부분이며(그림 4.8 0 ), b 축을 따라 길죽한 주상 형태로 산출되기도 한다 . 암염과 유사한 결정 형태와 벽개 양상을 나타낸다. {101} 면이 쌍정면 구실을 하는 취편쌍정이 발달할 수 있다. 벽개 {010} 방향의 완전한 벽개, {10 0} 방향의 거의 완전한 벽
 그림 4.8 0 경석고 결정.
그림 4.8 0 경석고 결정.
개, {001) 방향의 우수한 벽개가 발달한다. 경도 3~ 3 .5 비중 2.8 9 ~2.98 양각보통 굴절률 a=l.570, {3=1.57 6, y=1.61 4. 복굴절률 =0.044. 최대 간 섭색은 3· 의 녹색까지 이른다. 소광특징 벽개에 나란한 평행소광을 한다 . 광학부호 이축성, (+). 2V=42°. X=c, Y=b, Z=a. X 선 회절선 3.8 7 ( 1), 3.4 9 8(1 0 ), 2.849(3), 2.4 7 3(1 ), 2.3 2 8(2), 2.208(2), 2.1 8 30), 2.086(1 ), 1.8 69(2), 1.7 49(0, L7480)A 기타사항 경석고는 가수반응을 하여 석고로 변할 수 있으며 이 과 정에서 부피가 증가한다. 석고와 비슷한 환경에서 만들어지며, 암염 이 발달하고 있는 지역에서도 산출된다 . 현무암의 기공에서도 행 인상 조직인 상태로 발견된다. 경석고를 분말로 만들어 토양 중화 제 또는 시멘트 제조에 많이 사용한다 . 황산 제조를 위한 유황을 추출하는 데에도 사용된다 . 물이 없다는 의미를 지닌 그리스어에 서 광물명이 유래되었다.
4. 3 . 4 . 4 알루나이트 (ALUNITE) 화학성분 KAb(SO 』 )2(0H)6. KiO 11. 4, AhOJ 37.0, SOJ 38.6, H20 13.0%. Na 이 K 를 상당량 치 환할 수 있다. 만약 Na 이 K 보다 많이 존재하면 나트로알루나이트 [na tr oalun it e, (Na , K)AL(SO, )i (OH )6]라고 부른다. 결정계 삼방정계. 3m. R3m. a=6.97, c=l7.3 8 A. Z=3. 색 백색, 회색, 적색, 분홍색. 유리광택 내지 진주광택. 투명 내지 반투명. 박편하에서는 무색이다. 결정형태 판상체 또는 거의 등축정계의 결정에 가까운 능면체로 산출된다. 괴 상으로 주로 산출된다. 벽개 {0001 } 방향의 불량한 벽개가 발달한다. 경도 4 비중 2.6~2.8 양각보통 굴절률 ro=1 .57 2, E=1 .59 2. 복굴절률 =0.020. 최대 간섭색은 2° 청색이다. 소광특징 평행 또는 대칭소광을 한다. 장축부호 벽개 또는 결정면의 방향을 따라 빠른 광선이 진동한다. 광학부호 일축성, (+) X 선 회절선 5.77(3), 5.72( 1), 4.96(5), 3.4 9 (2), 2.99( 10 ), 2.293(8), 1.92 6(7), 1.90 3(3), 1.74 6(2), 1.50 3(3), l.49 4(1 ) A 기타사항 유문암, 조면암, 안산암과 같은 화산암이 열수에 의해 변질되어 생성된다. 특히 칼리장석이 있는 부분이 황화염 성분을 지니고 있는 용액으로 영향을 받을 때 만들어진다. 칼리와 알루미 늄을 추출하는데 주로 사용된다. 광물명은 주구성 성분인 알루미 늄을 의미하는 라틴어에서 유래하였다.
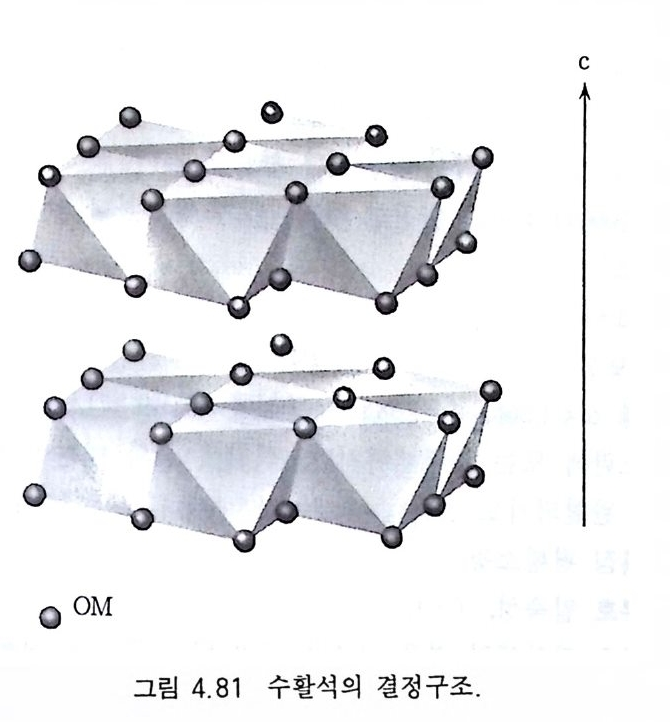 c
c
4.3 .5 수산화 광물 4. 3. 5 .1 수활석 (BRUCITE) 화학성분 Mg (O H)2. Mg O 69.0, H20 31. 0% . 소량의 Mn 2+와 Fe2 까 M g을 치환한다. 결정계 삼방정계 . 32/m. C3m. a=3.1 3 , c=4.74A, Z=l. 층상구 조를 하고 있으며(그림 4.8 1 ), M 팝는 6 개의 수산기 (0H) 에 의해 팔면체상 배위상태에 있다. 따라서 정전결합력 (e.V.) 은 +2/6=1 /3 이 된다. 색 백색, 회색, 옅은 녹색. 투명 내지 아투명하다. 표면온 유리 광택 내지 수지광택을 띠며, 바닥은 진주광택을 띤다. 박편하에서 는 무색이다.
결정형태 {0001} 과 나란한 판상 형태를 지니며, 비늘처럼 생긴 엽상 형태의 작은 결정들 집합체로 산출되는 것이 보통이다. 괴상 인 경우도 있다. 요곡성이 있으나 전성은 없다. 벽개 {0001 } 방향의 완전한 기 저 벽 개 가 발달한다. 경도 2.5 바중 2.3 9 양각보통 굴절률 (l)=1.56 6, E=1 .58 5. 복굴절률 =0.019. 간섭색은 일반적으 로 1· 노란색 또는 주황색이지만, 적갈색 등의 비정상적인 간섭색 이 간혹 관찰되기도 한다. 소광특징 평행소광 광학부호 일축성, (+). 장축부호 판상체일 경우 장축을 따라 빠른 광선이 진동한다. X 선 회절선 4.7 4 (8), 2.3 7 (1 0 ), I.79 3(1 0 ), 1.37 2(7), l.18 9(9)A 기타사항 수활석은 열변성작용을 받은 백운암에서 페리클레이즈 (M g O) 의 변질물로 산출되는 경우가 가장 많고, 사문암이나 녹니 석 편암에서 저온의 열수광물로 산출되는 경우도 있다. 사문석의 변질물로 산출되기도 한다. 내화재 원료물질로 사용되며, 마그네 슘울 추출하는 데에도 사용된다. 광물명은 미국의 광물학자 Arch iba ld Bruce 의 이름에서 유래하였다 . 활석과는 높은 경도와 지 방광택을 잘 나타내지 않음으로써 구별이 가능하고, 백운모와는 전성이 없는 점으로 구별이 가능하다. 한편 활석과 백운모는 광학부 호가 (-)인 점이 수활석과 다르다. 염산에 넣으면 쉽게 용해된다. 4. 3. 5. 2 기브사이트 (GIBBSITE) 화학성분 Al(OH)3. 소량의 Fe2037l- 거의 항상 함유되어 있으며 Fel+ 7 } Al” 를 치환하는 것으로 여겨진다.
결정계 단사정 계 . 2/m. P21/n. a=8.641, b=5.(J7 0 , c=9.719A , /3= 94°34'. Z=8. 기브사이트의 결정구조는 Al 이온이 수산기 (0H) 로 구성되어 있는 2 개의 층 사이에 위치하고 있다 . Al 이온은 팔면체 상 배위 를 하며, 이러한 배위를 나타내는 자리의 2/3 에만 Al 이온 이 있게 된다 . 색 백색, 회색, 녹백색, 적백색 . 박편하에서는 무색 또는 옅은 갈 색 을 띤다 . 결정형태 얇은 판상체로 산출되는 것이 일반적이다 . 주상 결정 또는 방사상 형태의 결정 집합체로도 산출된다. 벽개 {001 } 방향의 완전한 벽개가 발달한다. 경도 2.5 ~ 3 .5 비중 2.4 양각보통 굴절률 a=l.56 , {3=1.56 , y=1.58 . 복굴절률 =0.02. 최대 간섭색 은 1 ° 의 상급 또는 2 · 의 낮은 간섭색이다 . 소광특징 최대 소광각이 약 26° 정도이다 . 장축부호 판상체 결정인 경우 장축 방향을 따라 느린 광선이 진 동한다 . 광학부호 이축성, (+). 2V=O~40· X 선 회절선 4.85( IO) , 4.3 7 (5), 4.3 2 (2), 2.4 5 (2), 2.3 8 (2)A _ 기타사항 보에마이트나 다이아스포와 함께 산출되는 경우가 많 고, 이들은 보크사이트의 주요 구성물질이 된다 . 보크사이트는 강 수량이 많은 열대지방에서 Al 성분을 많이 함유하고 있는 화성암 이 풍화될 때 만들어지는 것이 보통이다 . 또한, Al 성분을 많이 함유하고 있는 화성암에 발달한 정동이나 열수맥 내에서 저온성 열수광물로 산출되기도 한다.
4. 3. 5. 3 다이아스포 (DI ASPORE) 화학성분 a-AIO(OH). 소량의 Fe 과 Mn 이온이 Al 을 치환할 수 있다. 결정구조 사방정 계 . 2/m 2/m 2/m. a=4.396, b=9.4 2 6, c= 2.844A. Z=4. 보에마이트와는 동질이상체인 관계가 있다 . 색 백색, 회백색, 무색. 불순물이 함유되어 있는 경우 갈 색, 적 색, 분홍색 등을 띤다. 박편하에서는 무색 또는 옅은 청색 을 띤다 . 결정형태 {010} 에 나란한 납작한 형태의 결정으로 산 출 되는 것이 일반적이며, 다수의 광물 집합체로도 산출된다. 벽개 {01 이 방향의 완전한 벽개가, {llO} 방향의 양호한 벽개가 발달한다. 경도 6.5~7 비중 3.3~3.5 양각높음 굴절률 a=I.68~1 .70 , {3=1.70 ~1 .72 , r=1.73 ~1 .75 . 복굴절률= 0.048. 3° 에 속하는 간섭 색 을 나타낸다. 소광특징 평행소광을 한다. 광학부호 이축성, (+). 2V=84° 장축부호 장축 방향으로 빠른 광선이 진동한다. X 선 회절선 3.98(1 0 ), 2.3 1 (8), 2.1 2 (1), 2.07(7), I.62 9(8)A 기타사항 편암 등 변성암에서 주로 산출되며, 알루나이트를 함 유하고 있는 화성암이 변질될 때 만들어지기도 한다. 보에마이 트, 기브사이트와 함께 보크사이트를 구성하는 주요 광물이다. 기 브사이트를 가열하면 다이아스포가 만들어지며, 이룰 더욱 가열하 면 강옥으로 변한다. 내화재의 원료로 사용된다.
4. 3. 5 . 4 보에마이트 (BOEMITE) 화학성분 y-A IO(OH). 결정구조 사방정계 . 2/m 2/m 2/m. a=2.8 6 8, b=12.227, c= 3.7 0 0A .. Z=4. 색 백색 결정형태 {001) 방향에 나란한 판상체의 결정 형태를 취하지만, 다수의 결 정 들 이 모여 포도상 형태의 덩어리로 산출되는 경우가 많 다. 벽개 {IOI} 에 나 란 한 벽개가 발달한다 . 경도 3.5 ~ 4 비중 3.0 양각 높 음 굴절률 a= 1.68 3, {3= 1.64 5, y= 1.65 1 . 복굴절률 =0 . 013 X 선 회절선 6.ll(I O ), 3.1 6 (6) , 2.34(5), 1.8 6(3), 1.8 5(2), l.66( l ), l.45(1 ), l.4 3 ( l )A 기타사항 보크사이트의 주요 구성광물이며, 다이아스포와는 동 질이상체 관계이다 . 4. 3. 5 . 5 침철석 (GOETHITE) 화학성분 a- F eO • OH. Fe 62.9, 0 27.0, H20 10.1 % . Mn 이 최대 약 5% 정도 치환상태로 존재한다. 결 정구조 사방정 계 . 2/m 2/m 2/m. Pbnm. a=4.65, b= 10.02 , c= 3.04A . Z=4. 다이아스포와 동일한 구조를 지니고 있다. 색 황갈색, 적갈색, 암갈색. 조혼색은 황갈색이다. 결정형태 주상 결정 형태를 가지며, 수직 조선이 발달하기도 한 댜 침상체 또는 신장상의 결합체로서도 산출된다. 방사상 구조를 지니는 집합체로도 산출된다.
벽개 {010} 방향의 완전한 벽개와 {100) 방향의 양호한 벽개가 발 달한다. 경도 5~5.5 비중 3.3 ~ 4.3 X 선 회절선 4.2100), 2.69(8), 2.44(7), 2.1 8 (4), l.71 9(5)A 기타사항 철을 함유하는 광물인 황철석, 능철석, 자철석, 그로 코나이트 동이 산화 환경에서 풍화될 때 만들어진다. 철을 함유하 고 있는 황화물 광체가 지표에서 변질된 고산(g ossan) 내에서 주로 산출된다. 철광으로 사용되며, 독일의 시인 괴테 (Goe t he) 의 이름에 서 광물명이 유래되었다. 4.3.6 안산염 광물 4. 3. 6. 1 인회석 (APATITE) 화학성분 Cas(P04)3 ( F, Cl, OH) . Cas(PO 』)J F 인 불소인회 석 (fluo ra- pat i te) , Cas(P04)3 C l 인 염 소인회 석 (chlorap at i te) , Cas(P04 )3 (0H) 인 수산인회석 (h y drox y la p a tit e) 으로 구분한다. 그러나 F, Cl, OH 가 함께 공존하는 경우가 대부분이다. (P04) 가 (S04), (Si0 4 ) 등에 의 해 일부 치환될 수 있다. 尸가 S” 로 치환될 때는 Ca2+ 가 N 안에 의 해 동시에 치환되는 쌍쌍치환을 한다. Mn 과 Sr 도 Ca 울 치환할 수 있다. 결정계 육방정 계 . 6/m. Pfo /m . a=9.3 9 , c=6.89A. Z=2. 색 녹색, 갈색, 청색, 보라색, 무색 등이 있다. 녹색은 Fe 에 의해 생기며, Mn 의 산화수 상태에 따라서도 색이 좌우된다. 즉, Mn 3+인 경우는 청색, Mn 안 경우는 보라색이 된다. Mn 의 함유량에 따라 서도 색의 짙기가 변하는데, 일반적으로 그 양이 많아질수록 짙어 진다. 투명 내지 아투명하다. 박편하에서는 무색이다.
 그림 4.8 2 현미경하에서의 인회석 결정 . 육각형의 단면 또는 주상형태를 하
그림 4.8 2 현미경하에서의 인회석 결정 . 육각형의 단면 또는 주상형태를 하
결정형태 길쭉한 주상 형태의 결정으로 산출되는 경우가 가장 많고, 단면은 6 각형을 나타낸다. 이런 결정 형태는 박편하에서 자 주 관찰된다(그림 4.82) . 벽개 {0001} 방향의 불량한 벽개가 있다. 경도 5 비중 3.1 5 ~3.20 양각보통 굴절률 £=1.63 0~1 .65 1, (l)=1.63 3~1 .66 7. 복굴절률 =0.003~0.004. 간섭색은 1° 회색 내지 백색이다. 화학성분의 차이에 따라 굴절률 도 다르다 . 즉, 염소인회석인 경우가 굴절률 (ro) 이 제일 높으며 (1.66 7), 수산기의 양이 증가함에 따라 굴절률이 감소하다가 불소 인회 석 인 경 우에 가장 작아진다(1. 633) . 소광특징 평행소광을 한다. 6 각형을 나타내는 단면인 경우는 항
상 소광한다. 광학부호 일축성, (-) 장축부호 장축을 따라 빠른 광선이 진동한다. X 선 회절선 2.80(1 0 ), 2.7 7 (4), 2.70(6), 1.8 4(6), I.74 5(3)A 기타사항 마그마의 분화 말기에 형성된 화성암 내에서 주로 산 출된다 . 열수맥에서 산출되기도 하며 열변성 또는 동력변성작용을 받은 변성암에서도 발견된다 . 인산 비료의 원료광물로 사용된다 . 투명한 결정은 보석으로 가공된다. 4. 3 . 6. 2 모나자이트 (MONAZITE) 화학성분 (Ce, La, Th, Pr)PO~. Th027} 4~ 2 0% 정도 함유되어 있는 경우가 일반적이다 . S i 02 도 소량 함유되어 있을 수 있다. 결정계 단사정 계 . 2/m. P21/n. a=6.79, b=7.0l, c=6.4 6 A. /3= 103°38'. Z=4. 색 황색 또는 황갈색 . 박편하에서는 옅은 황색 또는 무색이다 . 결정형태 주상 형태(그림 4.83) 를 취하나 결정으로 산출되는 경우 는 매우 드물다 . 입상질 형태의 괴상 형태로 산출되는 경우가 대 부분이다 . 벽개 {0001 } 방향의 명료한 벽개가 발달한다. 경도 5~5.5 비중 4.6~5.4 양각 매우 높음 굴절률 a=l. 78 6~1 .80 0, /3=1.78 8~1 .80 1, r=1.83 7~1 .84 9. 복굴 절률 =0.049~0.05 1. 최대 간섭색은 3~5• 의 높은 색에 해당한다. 소광특징 장축을 지니는 결정은 2~10· 정도의 소광각을 나타낸 다 . 광학부호 이축성, (+)
 .. ' •.• . •
.. ' •.• . •
장축부호 장축을 따라 느린 광선이 진동한다. X 선 회절선 4.1 7 (3), 3.3 0 (5), 3.09(1 0 ), 2.99(2), 2.8 7 (7)A 기타사항 모나자이트는 페그마타이트, 화강암 같은 화성암에 주 로 산출되며, 이들 암석의 풍화물로 형성된 퇴적물 내에서도 산출 된다. 모나자이트는 희유원소를 많이 함유하고 있는 대표적인 광 물이며, 특히 Th, U 같은 방사성 원소를 함유하고 있기 때문에 방 사성을 띤다. 진한 황산에 넣고 가열하면 분해된다. 브라질과 인 도, 호주의 해변에서 다량 회수되고 있다 . 주로 Th 울 추출하는 원 광석으로 사용된다 . U 울 함유하고 있기 때문에 u23s/Pb206, u/ Pb ur ,, PbUTI/P b l06, Thm /P b 惡에 따른 방사성 동위 원 소법 에 의 해 절대연령을 측정하는데 사용된다.
4.3.7 할로겐 광물 4. 3. 7 .1 형석 (FLUORITE) 화학성분 CaF2. Ca 51. 3, F 48.7%. Y, Ce, Sr 등의 희토류 원소 가 Ca 을 치환할 수 있다. 결정계 등측정 계 . 4/m 3 2/m. Fm3m. a=5.4 6 A. 2=4. Ca 이 온 은 등축면심격자를 이루며, 불소 이온은 단위포 를 8 개로 나눈 작 은 육면체의 중심에 위치하고 있다(그림 4.84). Ca 이온은 8 개의 F 이온에 의해, 그리고 F 이온은 4 개의 Ca 에 의해 둘러싸여 있다. 색 옅은 녹색, 황색, 청록색, 보라색, 무색, 갈색, 분홍색 등 매우 다양하다. 색이 다른 층상구조를 나타내는 경우도 있다 . 결정형태 정육면체로 산출되는 경우가 가장 많고, 투입쌍정으로 존재하는 경우도 있다 . 벽개 {111 } 방향으로 완전한 벽개가 발달한다. 경도 4 비중 3.1 8
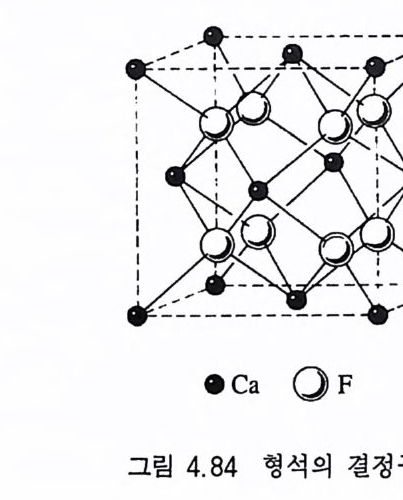 E:: /2...... ----- - --
E:: /2...... ----- - --
양각 비교적 높다. 굴절률 1.4 34 소광특징 항상 소광한다 . X 선 회절선 3.15( 9) , t.93 1 <10), t.64 7(4), I.36 6( 1), 1.11 s(2)A 기타사항 황화광물이 주로 있는 열수맥에서 맥석광물로 산출되 며, 화강암과 접촉하고 있는 석회암 내에도 산출된다. 마그마 고 결 말 기에 형성된 화성암 내에서도 산출된다 . 일부 페그마타이트 에 있는 형석을 대상으로 한 유체포유물 연구 결과 450~550°C 정 도에서 형석이 정 출 되었음을 알 수 있다 . 투명한 결정은 보석으로 가공되기도 한다 . 형석은 철을 제련할 때 융재로 사용되며, 우유 빛 유리 를 만 들 때에도 사용된다 . 불산울 제조하는 데에도 쓰인 다 . 오래전에는 광학제품을 만드는 데에 많이 사용되었으나, 최근 에는 인공 형석을 합성하여 사용한다.
제 5 장 조암광물의 기기 연구 5.1 주사전자현미경 분석 5.1.l 원리 및 구조 주사전자현미 경 (走 査電子顯微鏡 , sca nning electr on micr oscop e, 그림 5 .1)은 광학현미경으로는 관찰하기 불가능한 아주 미세한 물질의 형태를 빛이 아닌 전자를 이용하여 확대 관찰하는 고성능 확대경 이라고 할 수 있다. 주사전자현미경의 원리는 가는 전자선(電子 線, elec tr onbeam) 을 시료 위에 주사(走査)시키고, 이때 발생되는 2 차 전자(二次 電子, seconda ry elec tr on) 를 검출기로 받아 영상 신호로 서 브라운관 (CRT) 에 보내 상(像, i ma g e) 으로 전환시키는 것이다 (그림 5.2). 시료로부터 발생되는 2 차 전자는 주로 시료의 표면으 로부터 발생되며 그 에너지가 50e.V. 이하로 매우 작다. 시료에 도전성( 導電 性)을 부여하기 위하여 시료를 받침대나 유
 ::7•7 를 . 0. 0: :• . •: i`; • ` J ,\ .‘, I
::7•7 를 . 0. 0: :• . •: i`; • ` J ,\ .‘, I
리 슬라이드 위에 올려 놓은 후 표면에 금속을 얇게 입힌다. 확 대 배율이 수만 배 정도일 경우에는 금 (Au) 을 , 10 만 배 이상일 경우 에는 백금 (P t)을 사용한다. 시료 표면에 금속막을 입히면 2 차 전자 의 발생을 증가시킬 뿐만 아니라 시료의 손상을 방지할 수 있는 효과가 있다. 광물 표면에 금속을 고루 피복시키기 위하여 먼저 탄소를 얇게 증착시킨다. 5.1 .2 지질학적 용도 주사전자현미경은 극히 미세한 광물을 확대해 연구하는데 특히
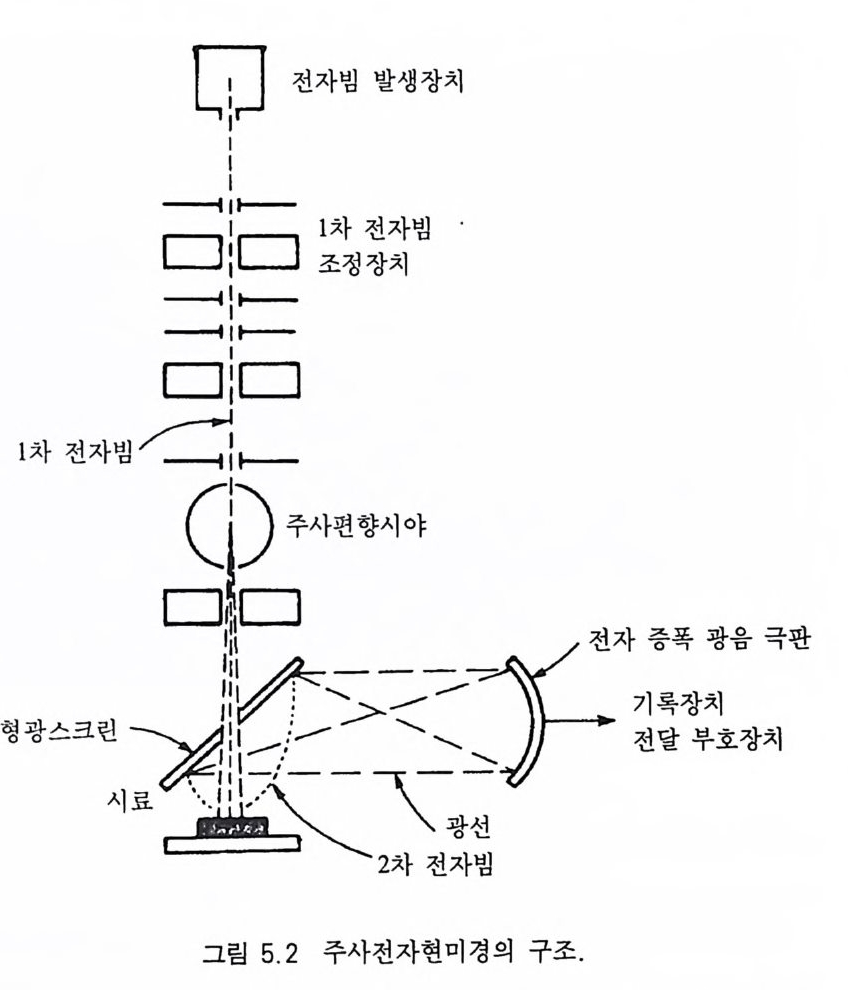 l 차 전 K L] 빔「三급「之1I111曰_11II1' _l u二llA l\白广二전 〔〔g》三―-vr치생J자ot 헝_빔 /二l 『기전 록달 紅묘 장 극치 판
l 차 전 K L] 빔「三급「之1I111曰_11II1' _l u二llA l\白广二전 〔〔g》三―-vr치생J자ot 헝_빔 /二l 『기전 록달 紅묘 장 극치 판
유용하다. 연옥이나 석면과 같은 광물의 미세 조직과 점토광물의 미세 결정의 외형을 관찰하는 데 많이 활용된다(그림 5.3).
 그림 5.3 젠세나이트 Uensen it e, C\l JT eo. • 2 Hi 0) 결정의 전자현미경 사진.
그림 5.3 젠세나이트 Uensen it e, C\l JT eo. • 2 Hi 0) 결정의 전자현미경 사진.
5,2 전자현미분석 5.2.1 원리 및 구조 전자현미분석은 광물을 용해하지 않고 그 화학성분을 정량 분석 할 수 있기 때문에 최근에 가장 보편화된 화학분석법이다. 전자현 미분석기 (電子顯微分析器, electr on pro be mi cr o analys e r, 그림 5 .4)는 전자총, 집광렌즈, 대물렌즈, 광학현미경 장치, X 선 검출기 (WDS, EDS), 영상 및 신호처리 장치 등으로 구성되어 있으며(그림 5.5 ), 최 근에는 주사전자현미경에 광물의 화학성분을 분석할 수 있는 WDS 또는 EDS 장치를 부착시켜 두 기능을 겸하는 경우도 많다. 전자 현미분석은 전자선이 시료에 충돌할 때 발생되는 특성 X 선을 검출 하는 것인데, 특성 X 선온 시료를 구성하는 원소에 따라 특정한 에
 그림 5.4 전자현미분석기 .
그림 5.4 전자현미분석기 .
너지(파장)를 가지므로, 이 에너지(파장)를 알면 그 시료를 구성하 고 있는 화학원소를 알아낼 수 있게 된다. 일반적으로 Ka 과 La 선 을 이용한다. 5.2 .2 정성분석 파장분산 스펙트럼법 광물 시료에서 발생하는 특성 X 선의 파장 을 측정하여 그 광물을 구성하고 있는 화학원소를 알아 내는 방법 으로서 , WDS 법 (Waveleng th Di sp e r siv e Sp ec tr os cop y meth o d) 이 라고도 한다. 이 분석법은 시료에서 발생되는 여러 특성 X 선을 결정구조 를 이미 알고 있는 결정 (c ry s t al) 에 회절시켜 원소를 분리해 내는 방
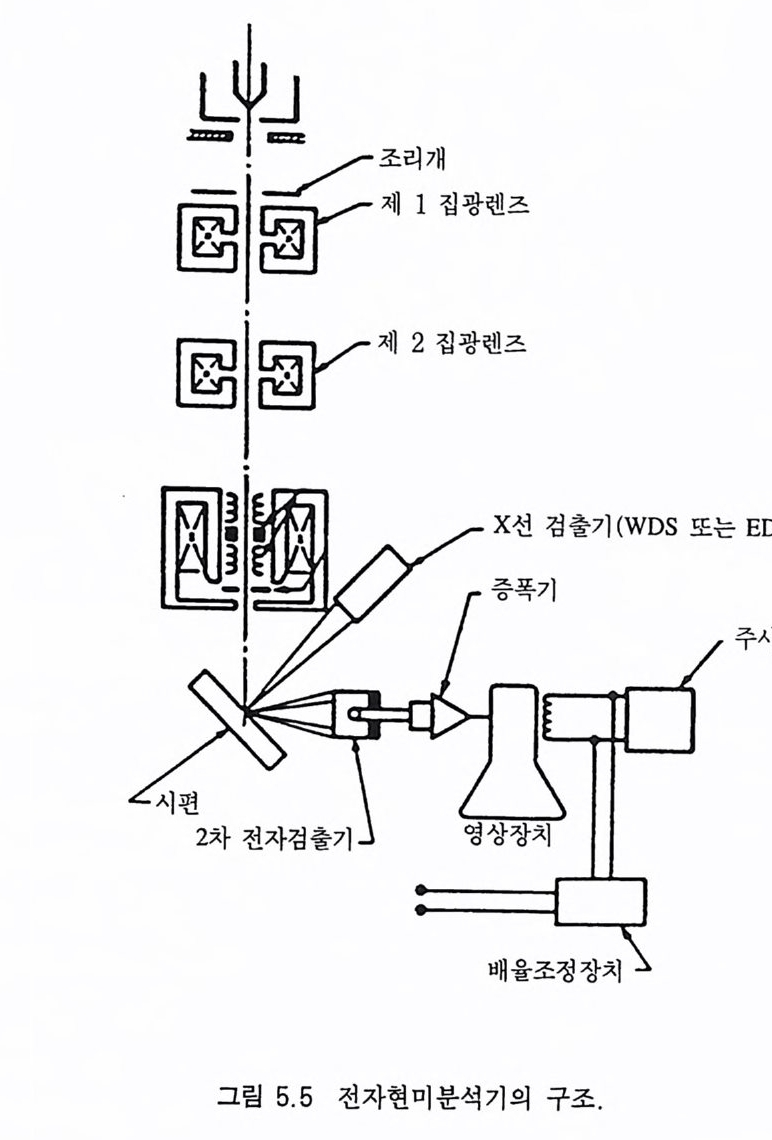 I 窟:門
I 窟:門
 표 5.1 파장분산 스펙트럼법과 에너지분산 스펙트럼법 비교
표 5.1 파장분산 스펙트럼법과 에너지분산 스펙트럼법 비교
법이다. 회절을 일으키는 데 사용되는 결정은 분석하려는 원소의 원 자량에 좌우되며 KAP( 질량이 작은 원소), APD( 중간 원소), L iF(질 량이 큰 원소) 등의 결정을 사용한다. 에너지분산 스펙트럼법 광물 시료에서 발생되는 특성 X 선과 연속 X 선을 검출기로 받아 각각의 특성 X 선을 에너지에 따라 구별하여 스펙트럼으로 나타내는 방법으로서, EDS 법 (Energy Di sp er siv e Sp ec tr os cop y me th od) 이라고도 한다. WDS 법에 비하여 간편하고 신 속하게 구성 원소의 특성 X 선을 알아 낼 수 있다. 파장분석 스펙 트럼법과 에너지분산 스펙트럼법의 특징은 표 5 .1와 같다. 5.2 .3 정량분석 광물 시료를 구성하는 원소의 양 (C) 은 시료에서 발생하는 그 원
소의 특성 X 선의 강도(I)에 비례하며 C=K • / 인 관계가 성립한 다. 이때 K 는 비례상수이다 비례상수는 원소의 종류에 따라 다 른데 원자번호 (Z), 홉수계수 (A), 형광 (F) 등의 요소에 의해 영 향을 받는다. 그러나 광물 시료 를 구성하고 있는 원소의 함량을 미리 알 수가 없으므로 정확한 비례상수 를 계산할 수가 없다. 따 라서 구성 원소의 종류와 함량을 정확하게 알고 있 는 표 준 시료 (標準試科 s t andard) 에서 얻어지는 특성 X 선의 양웅 기 준 으 로 비데 상수를 계산할 수 있게 된다. 실제의 경우 시료와 표준 시 료 와의 분 석 조건이 동일하여 비례상수는 같게 되므로 견국 각 원소의 정량적 함량은 특성 X 선의 강도와 비교하여 측 정할 수 있다. 5,2,4 광물 시 료 준비 전자현미분석은 고체 시료만 분석이 가능하다. 분석할 수 있는 원소는 원자번호가 11 인 Na 보다 원자번호가 더 큰 원소이지만 최 근에는 이보다 원자번호가 작은 원소도 측정이 가능할 정도로 기 술이 향상되었다. 분석할 시료는 유리 슬라이드에 붙이거나 수지 로 고정시킨 후 윤이 나도록 표면을 연마해야 하며, 표면은 반드 시 수평이 되어야 한다. 시료의 크기는 적어도 5~10mµ 이상이어 야 하며, 분석을 실시하기 전에 탄소 코팅을 해야 한다. 만약 광 물의 입자가 5mµ 이하 정도로 너무 작을 경우에는 분석 결과의 신뢰도가 감소할 수 있다. 한편 이 분석법은 검출 오차범위가 존 재량의 0.01% 로 비교적 높기 때문에 광물을 구성하는 원소 중에서 그 함량이 0.1 % 이상되는 원소인 경우에만 비교적 신뢰할 수 있는 분석치를 기대할 수 있다. 표준 시료는 분석하려는 광물 시료와 화학조성이 유사할수록 분석 오차가 적어지므로, 가능하면 시료와 화학조성이 비슷한 표준 시료를 선택하도록 하는 것이 좋다. 분석
할 광 물 시료의 구성 성분이 다양할 경우에는 여러 개의 표준시료 를 동시에 사용하여야 한다 . 5.2 .5 분석 자료 검 토시 유의 사항 산화선- 이나 규산 염 광 물 인 경 우 시료의 분석 결과는 구성원소의 산화 염 잉 태 로 나 열 되고 그 함량은 중량 % 로 제시된다 . 황화광물 등 은 원소 의 중량 % 로 표 시된다. 기기에 공급되는 전압과 전류가 변 하 면 화학분석 결과도 약 간 달 라질 수가 있다 . 전압이나 전류가 같은 상태에서 전 자 현 미 분 석 을 실 시할 경우에도 매번 화학분석치 가 일정 하 지 는 않는데 이 것 은 분석기기에 흐르는 전류의 세기가 미세하게 변하기 때 문 이다 . 분석치 의 총합 계 는 100 % 가 되어야 이상적이지만 이런 경우는 극히 드물 다 . 일반 적 으 로 100 士 2 % 이내의 수치이면 분석상의 명백 한 오류가 없는 한 양호한 분석치로 인정한다 . 물을 함유하고 있 는 수 산 화 광 물 이나 분석이 불 가능한 원소가 들어있는 광물인 경 우 에 는 그 합계가 100 % 로부터 상당히 멀어지게 되므로 그 분석결 과 를 취 급 할 때 조심하여야 한다. 시료의 표면상태가 불평탄한 경 우에도 오차가 많이 생길 수 있다 . 5.2 .6 전자현미분석법의 장점과 단점 전자현미분석의 장점은 크기가 작은 시료라도 측정이 가능하고 시료의 준비 과정도 비교적 간단하며, 시료를 비파괴적으로 분석 할 수 있다는 것이다 . 또한 광물이 미세하게 혼정이 되어 있을 경 우에도 각 구성물질의 화학성분을 정확하게 알아 낼 수 있는 장점 이 있다. 다양한 원소로 구성되어 있는 광물을 분석하기 위해서
표준시료도 다양하게 갖추어 두어야 한다 . 한편, 미량으로 함유되 어 있는 원소는 정확하게 정량분석하기 어렵고, 전이원소의 원자 가(原子衍)가 구별되지 않는 점, 물의 분석이 되지 않는 점, 원자 번호가 작은 원소의 분석이 어려운 등의 단점도 있다. 5.3 X 선 형광분석 5.3.l 원리 및 구조 광물 시료에 X 선을 쬐면 시료 를 구성하고 있는 원소는 여기( 勘 起 exc it a ti on) 되어 각각의 특성 X 선을 발생시킨다. 이 특성 X 선을 분광결정(分光結晶)에 통과시켜 일어나는 분광 각도의 차이 를 검출 기로 파장을 계산하여 원소의 종류를 알아 낸다. 또 특성 X 선의 강도는 그 광물 시료에 있는 원소의 함량에 비례하므로 특성 X 선 의 강도를 측정하여 정량분석한다. X 선 형광분석기 (X 線 益 光分析 器, X-ray fluo rescence spe c tr om ete r , 그림 5.6) 는 X 선 발생 장치 , 시 료실, 분광 장치, 측정 및 기록장치로 되어 있다(그림 5.7). 5.3.2 시료 준비 분말가압 성형법(粉末加壓成型法) 암석이나 광물 표품은 전체적으 로 균질하지 않을 뿐만 아니라 내부에 미세한 틈이 존재할 수가 있으므로, 원형대로 사용하지 않고 분말로 만든 후 정제(p elle t)를 제작하여 사용한다(그림 5.8,5.9). 시료만으로 정제로의 성형이 어 려 울 경 우에 는 H3BO3, LhB401 과 같은 결 합제 (結合劑 bin d er) 을 혼 합시킨다. 입도(粒度)가 다르거나 균질하지 않은 경우에는 X 선 형
 --
--
광의 강도가 달리 나타날 수 있으므로 분쇄기로 분말을 만든 후 채 (sie v e) 를 사용하여 입 도 를 고르게 해 야 한다. 용융법 ( '瑢 融法) 고체 시 료를 융제 와 함께 녹여 유리 디 스크(g lass d i sc) 를 만 들 어 사용하는 방법이다. 일반적으로 사용되는 융제로는 Liz C OJ , LiB 0 2, Liz 8 401, N따 8407 등이 있다 . 유리 디스크는 떨어 져도 쉽게 깨어지지 않아야 하고 내열성도 높아야 하며 반복해서 사용할 수 있어야 좋다. 시료를 용융시킬 때 너무 높은 온도로 가 열 하면 휘 발성 분이 증발될 수가 있으므로 1050~ 1100° c 가 적 당하 다. 용융시킬 때에는 백금 또는 백금과 금으로된 합금 도가니를 사용한다(그림 5.1 0 ) . 시료의 성분에 따라 융제의 양도 달라진다. 예를 들어 화강암과 같은 산성암은 시료와 융제 (L 표 M4G) 의 비율이 I : I 이 되게 하고, 현 무암처럼 Fe 와 Mg 성분이 많이 들어 있는 암석 시료는 I: 4~5 정도가 되게 한다. 시료의 양은 100mg 정도이면 충분하다.
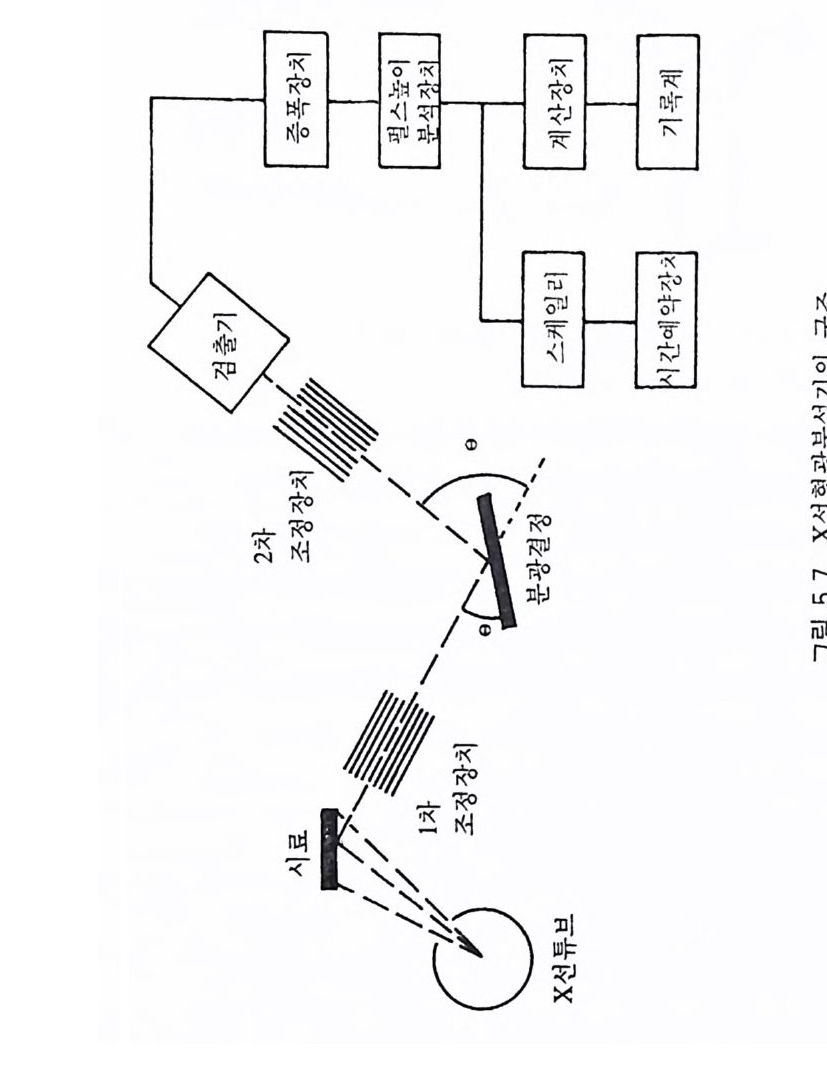
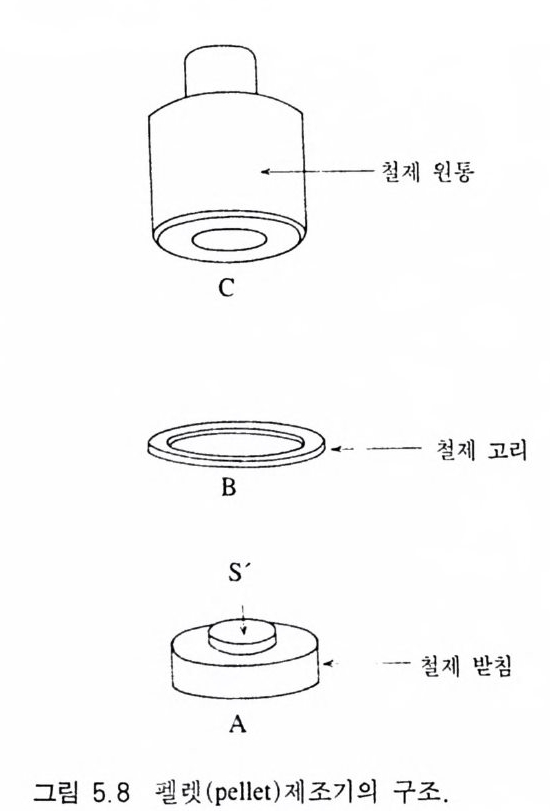 一철 제원몽
一철 제원몽
5.3.3 X 선 형 광분석 의 장점 과 단점 X 선 스펙트럼이 비교적 단순하고 원소간의 간섭효과가 적기 때 문에 분석자료의 신뢰도가 높다. 또 여러 성분을 동시에 분석할 수 있기 떄문에 분석에 소요되는 시간이 적다. 분석치의 신뢰도는 0.01% 정도로 매우 높고, ppm 단위의 양도 측정이 가능하다 . 원자 번호가 작은 원소(예 : 불소 이하)는 측정이 어렵다. 암석의 전체 화학성분(全岩分析)을 규명하는 데 적합하다. 이 분석법은 시료를 파괴하지 않고서도 측정이 가능하므로 고고학적인 유물, 보석, 금 속 등의 성분을 규명하는 데에도 사용되고 있다.
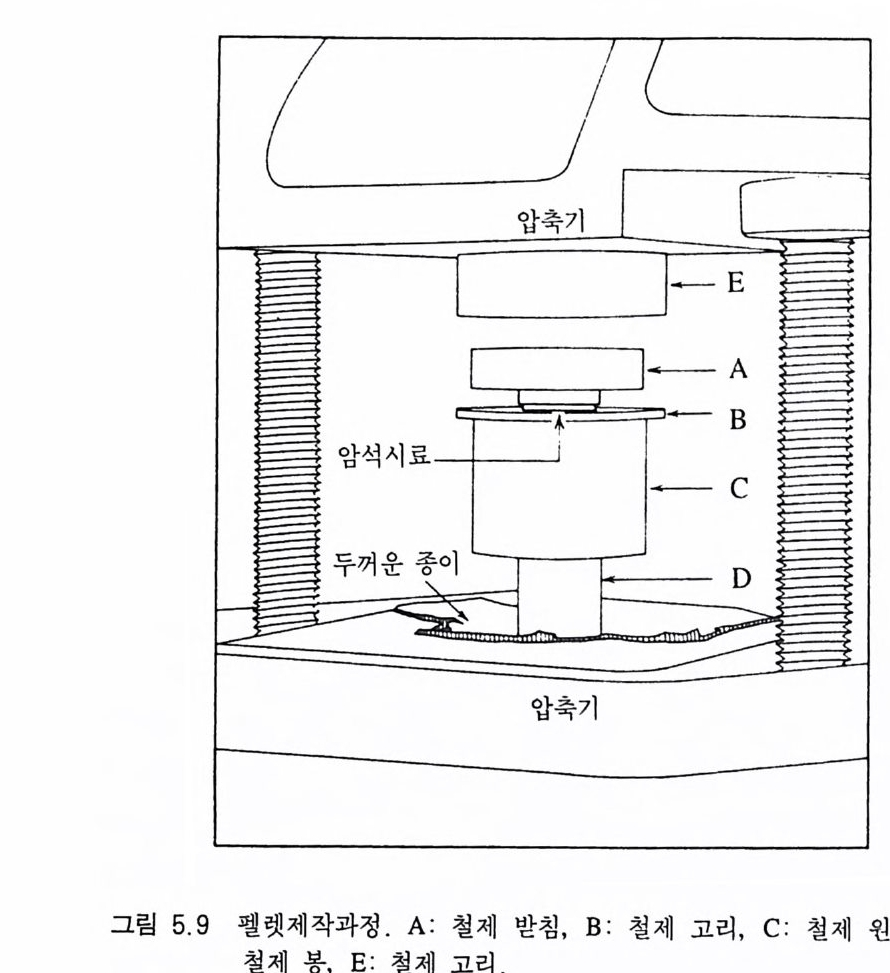 /|/ __j/
/|/ __j/
5.4 원자홉수분광분석 5.4.l 원리 및 구조 원자흡수분광분석은 원자의 증기층이 있는 공간으로 광선을 통 과시킬 때 기저상태에 있던 원자가 빛의 특정한 파장(에너지)을 홉
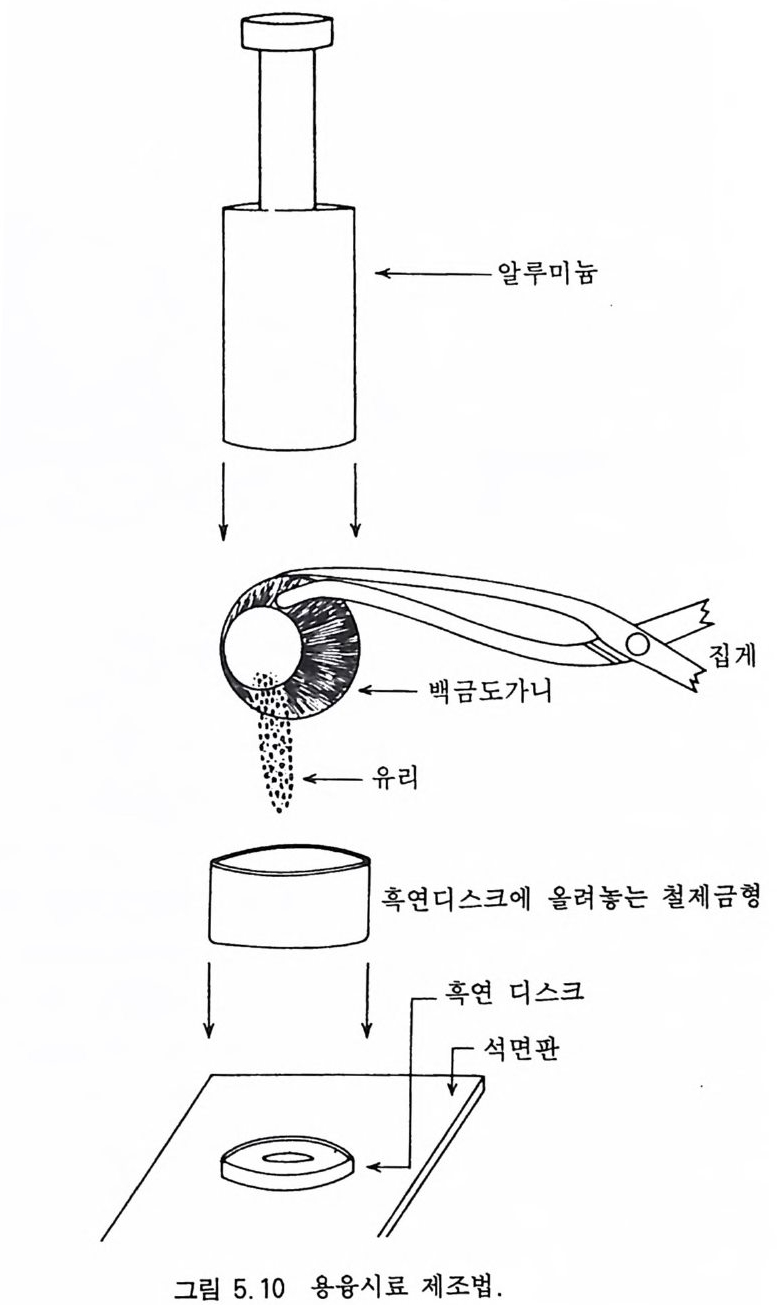 < 알루미늄
< 알루미늄
 그림 5. 1 1 원자흡수분광기 .
그림 5. 1 1 원자흡수분광기 .
수하는 원리를 이용한다. 원자흡수분광분석기(原子吸收分光分析 器, ato m ic a bsorp tion spe c tr om ete r , 그림 5 .1 1) 는 광원장치, 시료 를 원 자로 바꾸어 주는 장치, 분광장치, 측정장치로 구성되어 있다(그 림 5.1 2 ). 용액 상태인 시료를 분무기를 사용하여 안개 형태로 화 염 (약 2500~3000°K) 속으로 주입시키면 시료는 가열되어 분자나 이 온상태로 있던 원소가 중성인 원자화(原子化)로 되면서 광선의 고 유한 파장(에너지)을 홉수하게 된다. 이를 분광장치에서 스펙트럼 형태로 전환시킬 떄 생기는 검은 흡수선의 강도를 이용하여 정량 분석한다. 원소마다 최외각에 있는 전자의 에너지 준위가 다르므 로 원소마다 고유한 파장을 흡수한다 . 나트륨 (Na) 원자의 경우 3s 준위에 있는 최의각 전자가 에너지 준위가 높은 3p 또는 4p 준위 로 옮겨 가기 위 해 589 run 와 330 run 의 파장을 흡수한다. 그 결과 Na 원자의 흡수스펙 트럼 에 는 589 run 과 330 run 의 검 은 이 중선 이 선명하게 나타난다.
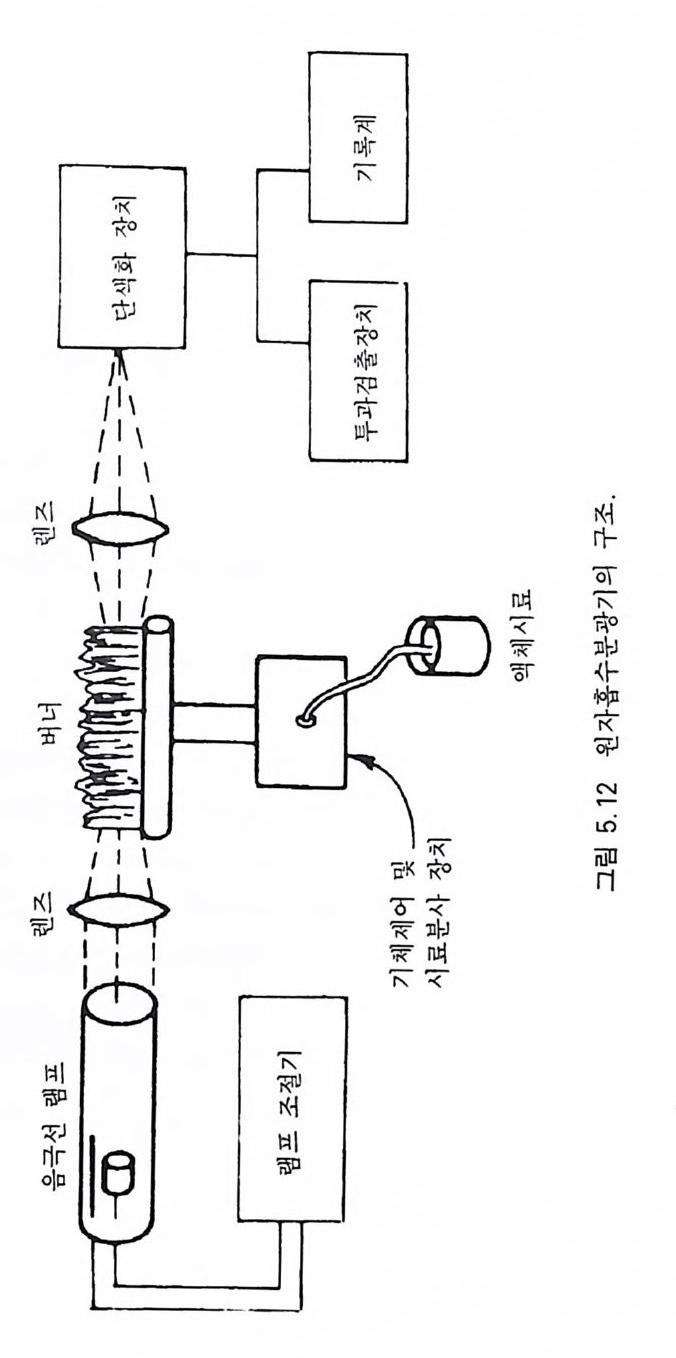 계
계
5.4.2 시료 준비 시료는 수용액이나 유기용액처럼 액체 상태이어야 한다 . 용액의 수소이온 농도지수나 색은 상관이 없다. 물에 녹는 물 질은 수용액 으로 만들어 사용하면 되지만, 물에 녹지 않는 대부분의 광 물 인 경우에는 황산, 질산, 염산, 불산 , 과염소산, 탄산나 트륨을 사용 하여 용해시킨다 . 유기용매인 경우 분무기의 효율이 증 대되고 표 면장력도 작게 되어 시료를 미세한 안개 형태 로 만 들 어 화염과의 반응을 촉진시키는 효과가 있다. 그러나 이 들 용액은 스 펙트럼에 영향을 미칠 수 있고 또 용액 중에 분석 할 원소가 함유되어 있 을 경우 분석할 원소의 농도에 영향을 줄 수가 있다. 정확한 분석을 위해서는 농도를 알고 있는 표준 시료용액을 마련해 두어야 한다. 5.4.3 원자흡수분광분석법의 장점과 단점 검 출 한계 가 0.001 ~0.020 pp m정 도로 매 우 높고, 공 존 하는 다 론 원소로부터의 영향도 비교적 적다. 고체 시료 를 용액상태로 처리 해야 하는 다른 기기 분석법에 비하면 처리과정이 비교적 간단하 다. 그러나 광원이 있는 원소만 분석이 가능하기 때문에 붕소 (B), 인 (P) 등을 제외한 대부분의 비금속원소는 분석이 불가능한 단점이 있다. 또한 분석하려는 원소가 바뀔 때마다 광원을 바꾸어 야 하는 불편함도 있다 . 최근에는 미량원소의 측정 능력이 더욱 향상 된 유도쌍플라즈마 원자방출분광분석기의 보급이 늘어나고 있다.
5.5 적외선 홉수분광분석 5.5.l 원리 및 구조 분자 를 이루고 있는 원자는 어떠한 온도 조건에서도 신축 진동 (str e tc h in g v i bra ti on) 이나 굽힘 진동 (bend i ng v i bra ti on) 을 한다. 진동운 동이 있기 위해서는 결합의 종류 및 세기, 결합을 이루는 원자의 종 류에 따라 고유한 진동 주파수(振動周波數, vib r ati on al fr e quenc y)에 해당하는 빛 에너지 를 흡수해야 한다. 따라서 분자의 운동에너지와 비슷한 에너지를 가지는 적외선을 비추면 이들이 진동을 일으키는 데 필요한 특정 주파수의 파장이 홉수되며, 이 홉수된 에너지가 적 외선 홉수스펙트럼 (IRs p ec t rum) 을 나타낸다. 이러한 현상을 이용하 여 분자의 결합 상태를 알아 내는 방법을 적외선 홉수분광분석(赤 外 線 II 及 收 分 光分析, inf r ar ed absorp tion spe c tr os cop y) 이 라 한다 . 적외선은 파장이 0.78~lOOO Jll n 인 에너지로서, 파장의 크기에 따 라 근적외선(近赤外線), 중적외선(中赤外線), 원적외선(遠赤外線)으 로 분류한다. 적외선의 영역별 파장 크기, 파동수 및 진동수는 표 5.2 와 같다 . 적 외 선 홉수분광분석 기 (infrar ed absorp tion spe c tr om ete r , 그림 5.1 3 ) 는 기본적으로 광원, 시료장치, 단색화 장치(單色化裝置), 검출
 표 5.2 적외선 파장영역
표 5.2 적외선 파장영역
 그림 5.13 적 외 선흡수분광분석 기 .
그림 5.13 적 외 선흡수분광분석 기 .
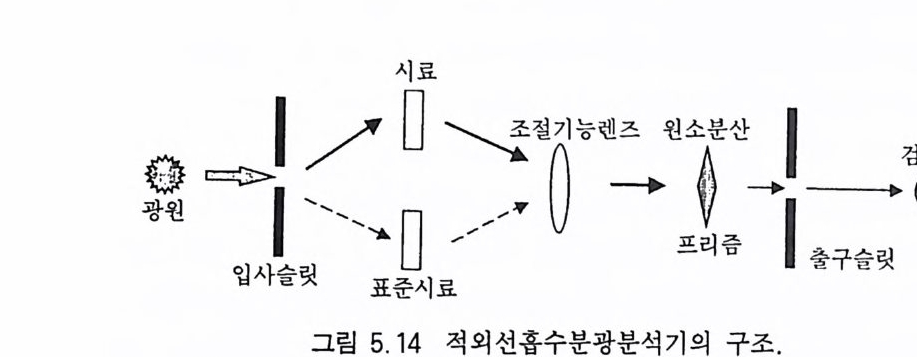 __ __
__ __
기, 기록장치로 되어 있다(그림 5.1 4 ). 이 분석 자료로부터 분자구 조에 대한 정보를 얻을 수 있게 되며, 대략의 정성 및 정량 자료 도 얻을 수가 있다 . 최근에는 분석의 신뢰성도 높고 여러 원소를 동시에 분석할 수 있는 푸리에변환 적외선분광분석기 (FT-IR s p ec tr ome t er) 가 널리 보급되고 있다. 5,5,2 시료 준비 유동 파라핀법 고체 시료인 경우 분말을 만들어 유동(流動) 파라
핀(p ara ffi n) 과 잘 개어서 죽처럼 만든 다음 시료판에 발라 사용하 는 방법으로서, 누졸법 (nu j ol me t hod) 이라고도 한다. 그러나 이 방 법을 사용하면 유동 파라핀의 홉수띠가 함께 나타나므로 경우에 따라서는 어떤 홉수띠가 시료에 속한 것인지를 판별하기가 어려울 수가 있다 . KBr 정제법 광물의 분말 시료 를 KBr 분말과 혼합시킨 후 정제 ( p ell e t ) 를 만 들 어 사용하는 방법이다 . 이를 위해 약 1mg 정도의 광 물 분 말을 고순도의 KBr 분말 100~200 m g과 잘 혼합한다 . KBr 은 적외선 영역에서 홉 수현상을 거의 일으키지 않으므로, 광물 시료 만의 흡 수선을 얻 을 수가 있다. 한편 KBr 은 공기 중의 수분을 홉 수하는 성 질 이 있으므로 이 를 방지하기 위해 진공 속에서 만들어 야 한다 . 수분이 함유될 경우 바탕값 (back g round) 이 커져 바람직하 지 않다. 5.5 .3 적 외선 홉수스펙트럼의 해석 광 물 은 그 원자결합 방식에 따라 여러 가지의 신축 및 굽힘 진 동운동을 하므로 매우 복잡한 스펙트럼을 나타낸다 . 따라서 이들 의 각 흡수대를 모두 해석해 내는 것은 그리 쉽지 않다 . 따라서 숙련된 경험이 필요하다. 특정한 결합을 하고 있는 분자가 운동하 는데 필요한 적외선 에너지의 양은 이론적으로 계산할 수가 있기 때문에 이를 토대로 분석자료에 그려진 홉수선을 해석할 수 있게 된다 . 예를 들어 CO 결합의 신축운동에 필요한 이론적 에너지는 1600 cm ~ 1 인데, 적외선 분석실험에서는 1500~1900cm-, 범위내에서 홉수선이 기록된다.
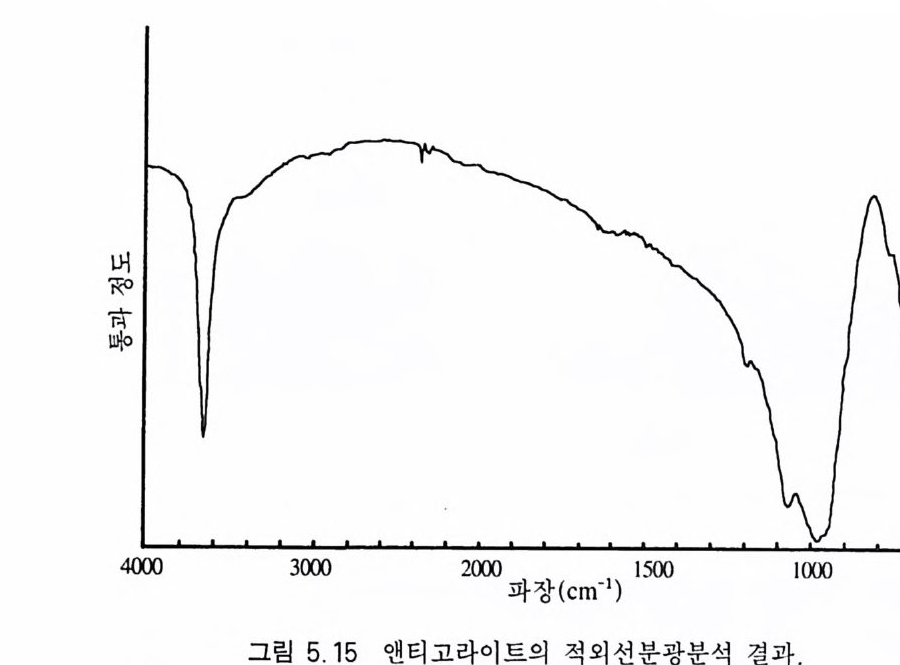 버
버
5.5.4 조암 광물의 적외선 흡수스펙트럼의 예 앤티고라이트의 적외선 흡수분광분석 자료(그림 5 .1 5) 에 따르면 3670, 1190, 1070, 980, 610 cm-• 에서 피크가 나타나며, 이 중 3670 cm-1 의 피크는 OH 결합의 신축 진동, 1190,1070,980cm-' 피크들은 SiO 결합의 신축 진동, 그리고 610cm 기 피크는 OH 결합의 굽힘 진 동에 의한 것으로 해석된다.
 一— ―· 를‘'
一— ―· 를‘'
5.6 시차열분석 5.6 .1 원리 및 구조 시 차열 분석 법 (時差熱分析法, dif fere nti al the rmal analys i s ) 은 광물 시 료를 일정한 속도로 가열시키면서 광물 시료가 흡수 또는 방출하 는 열을 비활성 표준시료와 비교하여 이들 사이의 온도 격차를 측 정하는 분석법이다. 표준시료는 주로 알루미나 (Ah01) 분말을 사용 한다. 시차열분석기(그림 5.16) 의 기본구조는 가열장치, 시료장 치, 기록장치로 구성되어 있다(그림 5.1 7 ). 시료를 장착시키는 공 간은 진공상태로 유지시키거나 또는 아르곤 (Ar) 가스룰 주입시킬 수 있도록 설계되어 있다. 광물과 표준 시료의 온도는 백금과 로
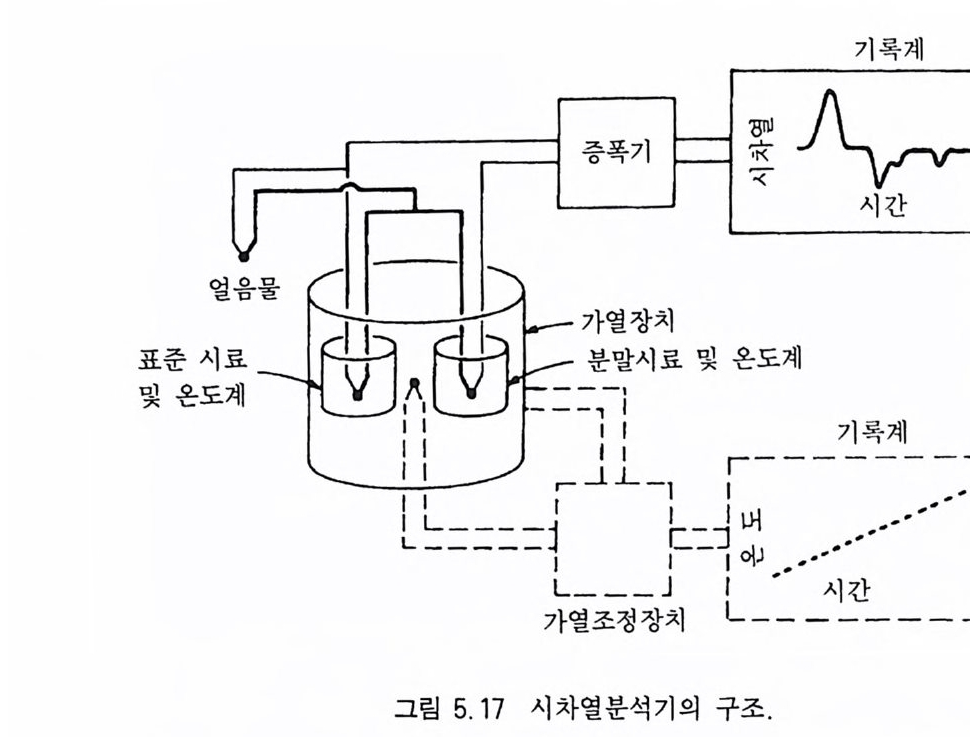 기 록 계
기 록 계
듐으로 만든 가는 합금 선으로 측정한다. 광물 시료와 표준시료의 온도 차이 (AT) 가 매우 작기 때문에 증폭장치를 사용하여 확대시 킨다. 5.6.2 시료 준비 시료는 분말로 만들어 사용하며, 한번 측정할 때 수십 내지 수 백 m g을 사용한다. 시료는 석영 유리관이나 금속 도가니에 넣고 측정하는데, 가열하는 동안 도가니와 시료와의 화학반응을 막기 위해 비금속 광물을 분석할 때는 금속 도가니를, 금속 물질을 분 석할 때에는 석영 도가니를 사용한다. 일부 시차열분석기는 온도 측정용 철심을 시료 속에 묻고 측정하도록 설계되어 있는데, 이런
경우 가열중 광물 시료와 철심이 반응하지 않도록 해야 한다. 이 를 위해 석영 유리관을 얇게 성형시켜 철심을 피복한다 . 5.6.3 시차열분석 자료 해석 시차열분석 자료에는 기준선을 중심으로 위 또는 아래로 향하는 곡선이 그려지는데, 위로 향한 것은 발열반응이고, 아래로 향한 것은 홉열반응을 나타낸다. 앤티고라이트의 시차열분석 자료(그림 5 . 18) 에 따르면 343.0°C 와 830 .1 °C 에서 발열반응을, 755.0°C 에서 홉 열반응을 일으킨다. 755.0°C 에서의 홉열반응은 결정 내에 있는 구 조수의 추출에 따른 현상인 것으로, 또 830 .1 °C 의 발열반응은 단 사정계의 앤티고라이트가 사방정계인 감람석으로 변하는 구조적
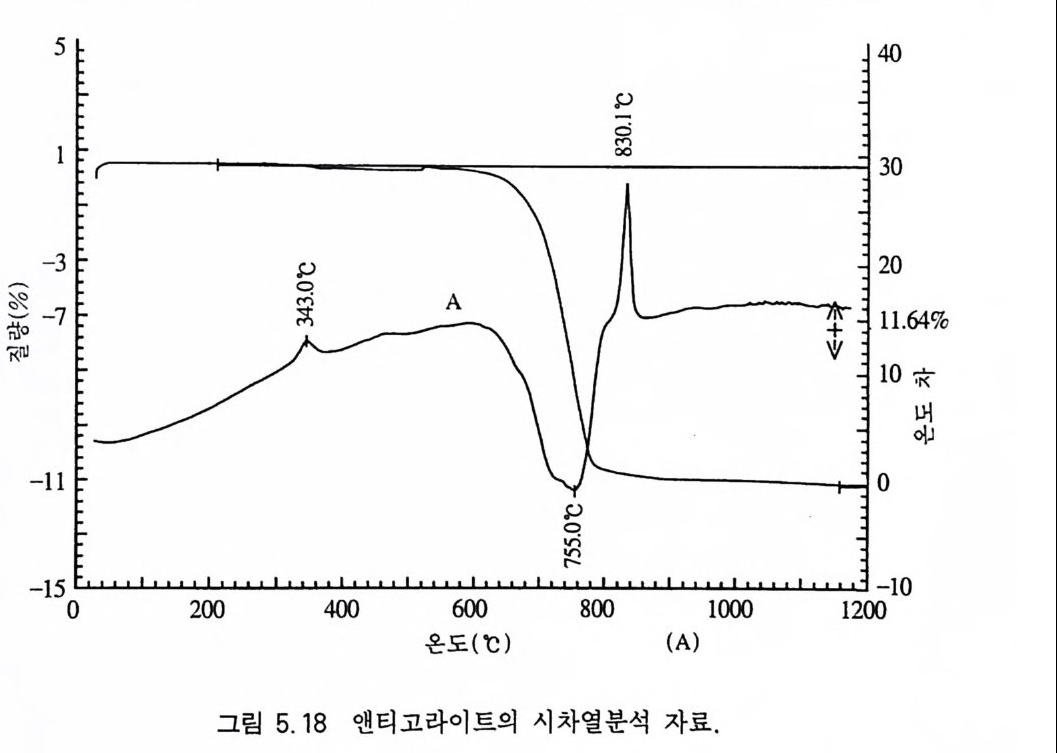 5
5
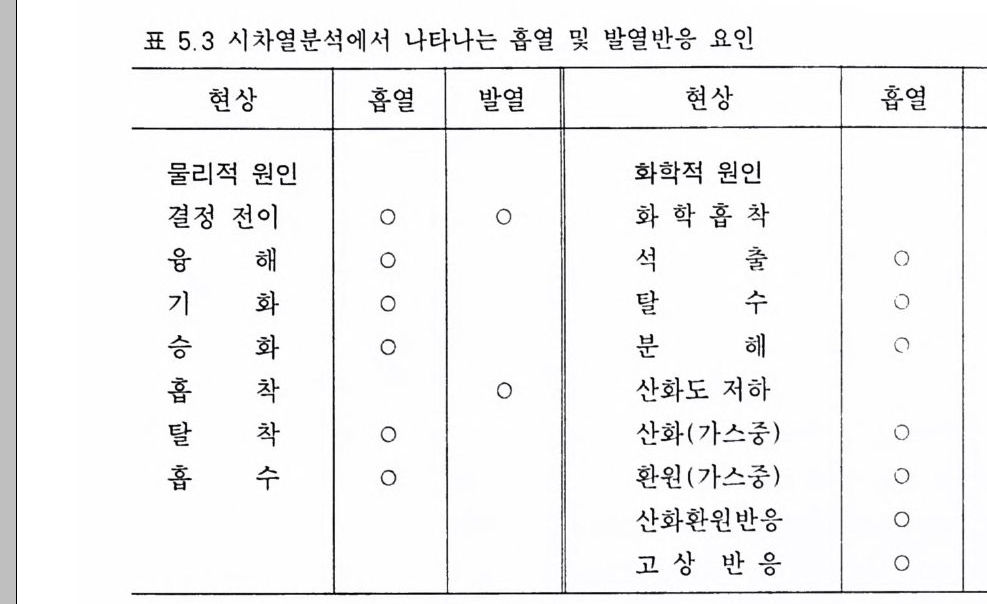 표 5.3 시차열분석에서 나타나는 홉열 및 발열반응 요인
표 5.3 시차열분석에서 나타나는 홉열 및 발열반응 요인
전이에 따른 현상인 것으로 해석된다. 그리고 343.0°C 에서의 발열 반응은 앤티고라이트가 고온에서 안정한 동질이상체로 변하는 현 상에 기인된 것으로 해석된다. 시차열분석에서 발열반응과 홉열반응을 일으키는 요인은 표 5.3 과 같다. 열반응 곡선에 영향을 미치는 요소로는 시료량, 열전도 도, 비열, 시료의 입도(粒度), 가열장치 내의 분위기, 온도의 상 승속도 등이 있다. 5.6.4 주요 조암 광물의 시차열분석 자료 주요 광물의 열반응 자료는 표 5 .4에 수록되어 있다.
 표 5.4 주료 광물의 시차열분석 자료
표 5.4 주료 광물의 시차열분석 자료
 표 5.4 주료 광물의 시차열분석 자료
표 5.4 주료 광물의 시차열분석 자료
 그림 5.1 9 X 선 회절 분 석기
그림 5.1 9 X 선 회절 분 석기
5.7 X 선 회절분석 5.7.l 원리 및 구조 원자 들 이 3 차원적으로 규칙적인 배열을 하고 있는 광물에 X 선이 입사하면 X 선이 진행하는 경로에 있는 원자 내의 전자들은 X 선의 진동수와 동일하게 진동하게 된다 . 이들 전자들은 X 선의 일부 에 너지를 흡수하여 입사한 X 선과 같은 진동수와 파장을 가지는 새로 운 X 선을 발생시킨다. 이때 발생하는 파동은 간섭현상에 의해 대 부분 상쇄되어 없어지고, 2 • chusin 0=nl (Bragg 방정식)의 조건이 만족되는 특정한 방향의 파동만 서로 부추겨서 증가하게 된다 . 이 러한 현상을 회절(回折, d iffr ac ti on) 이라고 한다. X 선 회절분석기 (X 線回折分析器, 그림 5 .1 9) 의 기본 구조는 X 선
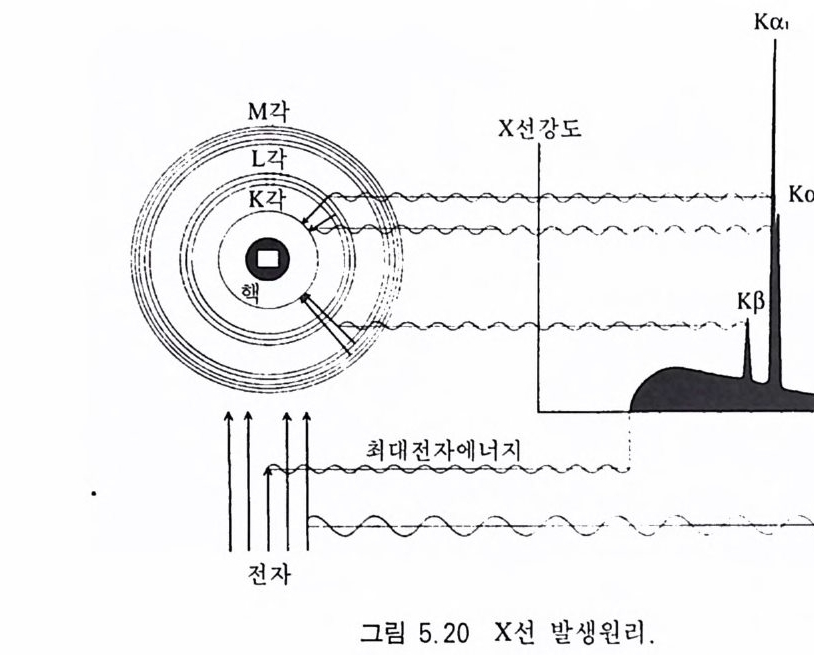 Ka,
Ka,
발생장치, 시료장치, 감응장치, 기록장치로 되어 있다. X 선 발생 장치는 진공관 형태로 제작되어 있으며 전류와 전압이 공급되면 넓은 범위의 파장을 고르게 지니고 있는 X 선과 양극(t ar g e t)으로 사용하는 금속 물질에 의한 특정한 파장의 X 선이 발생하게 되는데 전자(前者)를 연속(連 緖 ) X 선, 후자(後者)를 특성 (特性) X 선 또는 고유(固有) X 선이라고 한다(그림 5.20). 특성 X 선은 Ku , K~ 선으로 구성되어 있는데, 강도가 작은 K p선을 제거하기 위해 필터를 사용 한다. 필터는 두께가 약 0.02mm 이며 타겟 물질보다 원자번호가 하나 작은 금속 물질로 제작한다. 그 예로서 원자번호가 29 인 구 리 (Cu) 를 타겟 물질로 사용할 경우 필터는 원자번호는 28 인 니켈 (N i)로 제작한다.
 '
'
5,7,2 시료 준비 조암 광물을 식별하고자 할 때 가장 많이 쓰이는 방법이 분말법 ( 粉末法 , pow der me th od) 이다 . 분말 시료의 처리법은 사용하는 장 비가 분말회절분석기( 粉 末回折分析 器 , 그림 5.21) 인지 또는 디바이 셔 카메 라 (Deb y e-Scherrer camera , 그림 5.22) 인지 에 따라 달라진다. 전자인 경우는 약 200mesh 크기로 만든 광물 분말을 유리로 된 시료판 (sam p le holder) 에 넣어 사용하고, 후자인 경우는 시료를 유 리 대롱에 부어 넣거나 접착제를 첨가해 가는 원통 모양으로 만들 어 사용한다. 광물의 구조에 따라서도 시료 처리가 달라 질 수가 있 댜 예를 들어 층상구조를 지니는 운모 또는 점토광물인 경우 c 결 정축에 수직인 격자의 특징을 관찰하기 위해서는 유리 슬라이드 위 에 시료를 놓고 아세톤을 이용하여 유리면에 붙도록 처리하며, 그
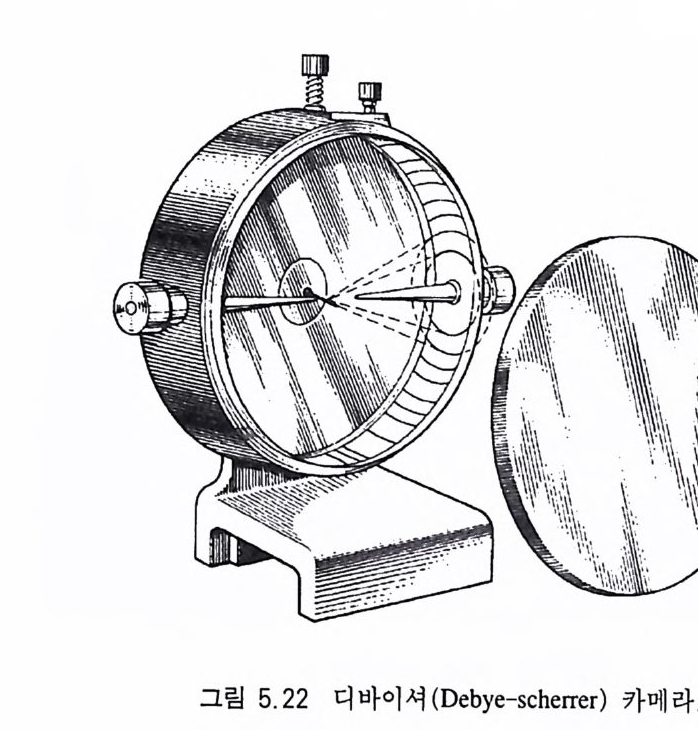 그립 5.2 2 디바이셔 (Deby e- scherrer) 카메라 .
그립 5.2 2 디바이셔 (Deby e- scherrer) 카메라 .
외 방향의 격자들의 특징을 알아 보고자 할 때에는 유리 시료판에 시료를 넣고 다져서 고정시킨다. 전자 형태의 시료를 방향성 시료 (ori en te d samp le ), 후자인 경우를 임의성 시료 (random sam p le) 라고 한다. 5.7.3 X 선 기록지 해석 분말회절분석기의 경우는 피크가 기록지에 그려지는데(그림 5.23), 기록지의 가로축은 20 의 값이고, 세로축은 강도(int ens ity)이 다. 각 피크의 높이를 강도(强度, i n t ens ity)라 하고, 피크의 2/3 위 치의 중앙에서 수선을 내려 가로축과 만나는 곳이 28 값이 된다. 이로부터 피크의 강도와 회절각 (8) 을 알 수 있게 된다. 이 0 값을
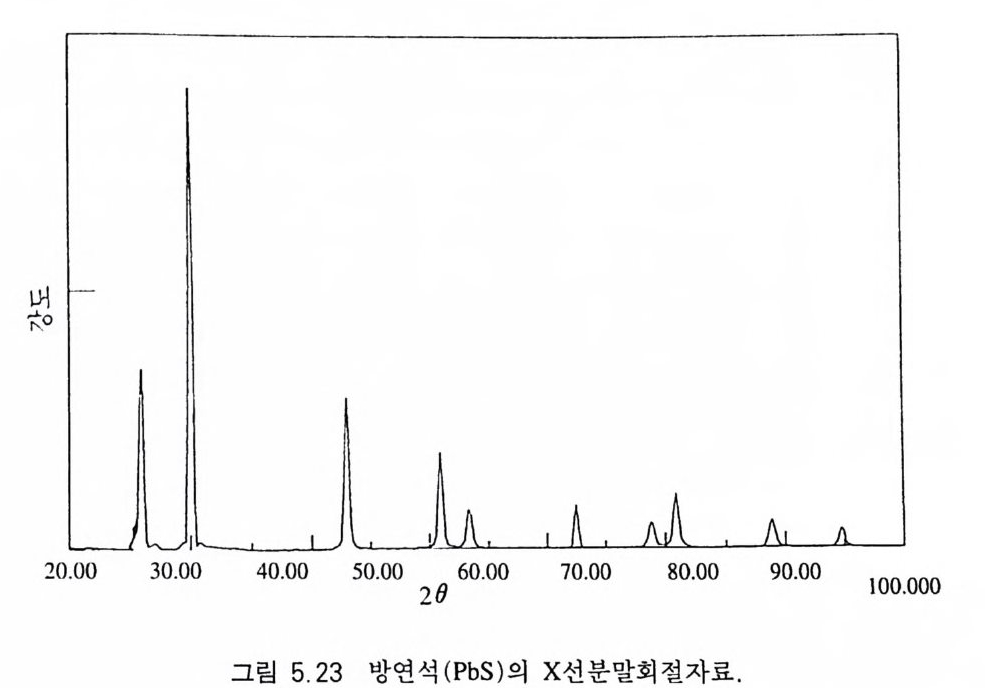 버
버
Bragg 방정식인 d,,u = 2 ns.i:nl 0 에 대입하면, 각 피크를 발생시킨 hkl 방향의 격자거리 (du,) 를 계 산할 수 있다. 예를 들어 은회색을 띠는 어떤 금속광물을 분말로 만들어 X 선 분말회절 실험한 결과가 그림 5.23 과 같을 때 각 피크에 해당하는 강도 (I/ I o) 와 20 값을 그래프로부터 읽은 후, 20 의 절반인 0 값을 Bragg 방정식에 대입하면 각 피크에 대한
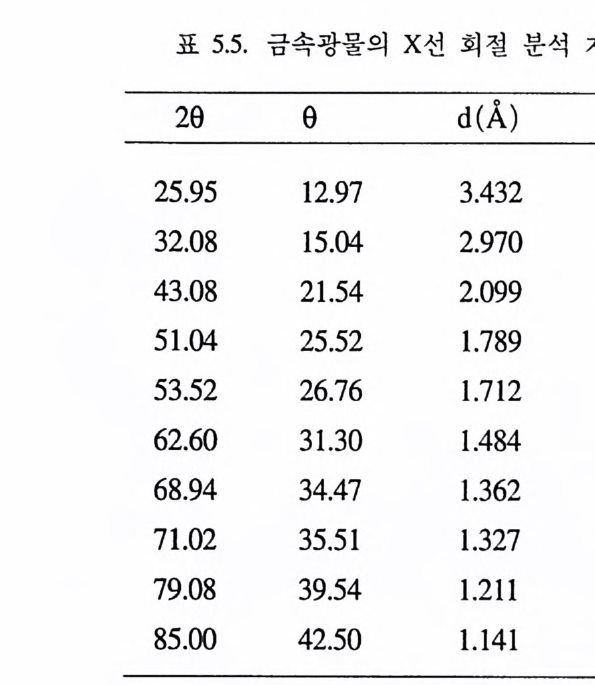 표 5.5. 금속광물의 X 선 회 절 분석 자료
표 5.5. 금속광물의 X 선 회 절 분석 자료
이 광물의 이름을 알아보고자 할 때에는 먼저 피크의 강도가 가 장 높은 것부터 낮아지는 순서로 나열한다 . 즉, 2.970A, 3.4 3 2A 2.0 9 9A, 1.78 9A, 1.32 9A, 1.48 8A, 1.11 1A, 1.36 5A, 1.21 4A 1.14 1A 이 된다. 다음 차례는 ‘Powder Dif frac tio n Fil e S earch Manual’ 이 란 자료책에서 강도가 제일 큰 d 값 (2.970A) 이 속해 있는 부분을 찾아 (표 5.6) 앞에서 순서적으로 정리한 d(A) 값과 일치하는 것이 있는 지를 찾는다. 이때 분석에서 얻어진 d(A) 값이 자료책의 d(A) 값과 완전하게 일치할 필요는 없으며, 약간의 차이가 있을 수 있다. 그 이유는 동일한 광물이라고 하더라도 화학성분이 결정마다 약간씩 다를 수가 있으며 그 결과 격자의 거리가 약간 달라지기 때문이다. 이런 점을 감안하고서 자료책을 찾아보면 이 물질명은 방연석(方鉛 石, gal ena) 이 며 그 화학식 은 PbS, 그 밖의 구체 적 인 자료는 파일
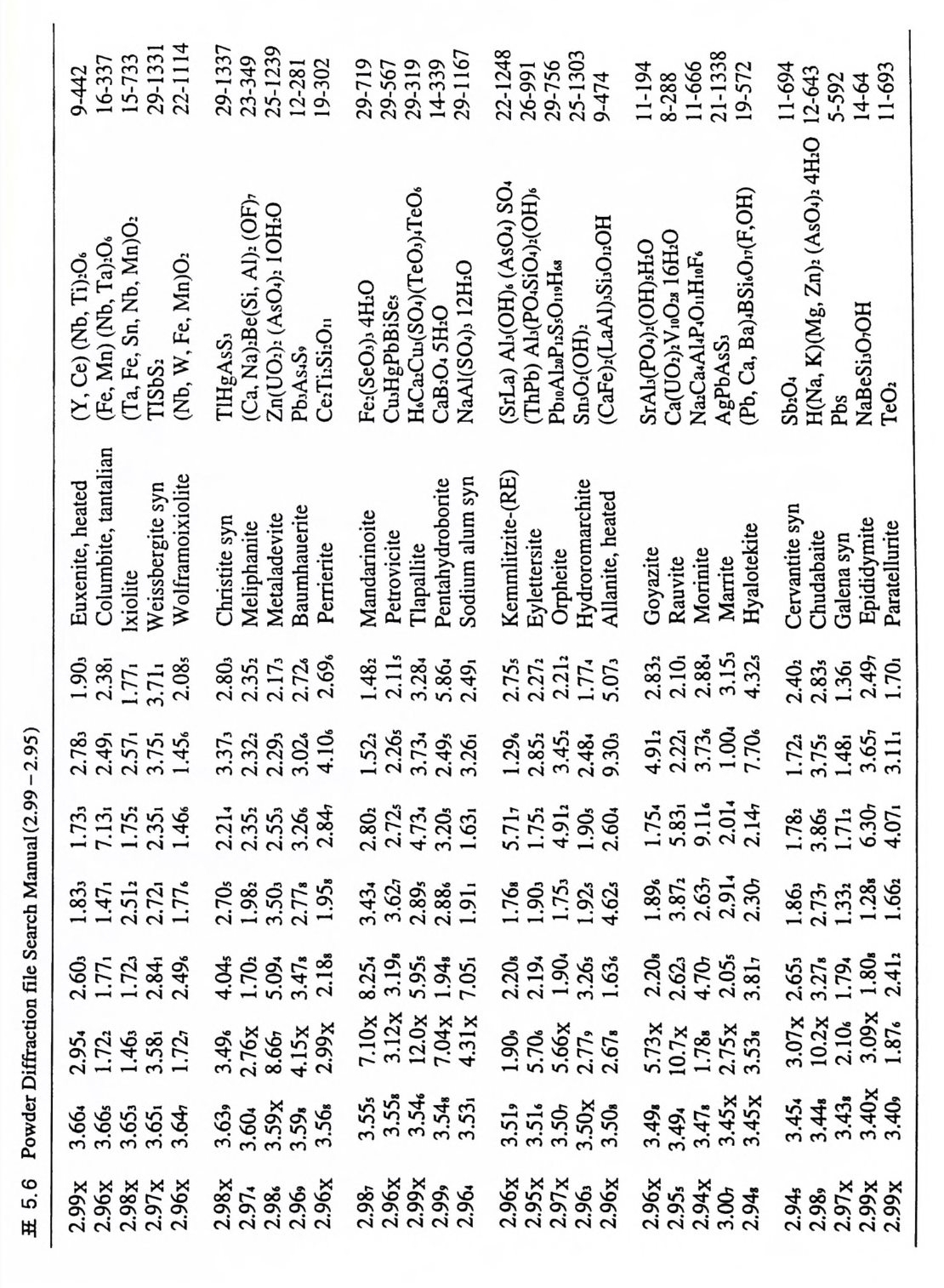 29-44 37-3 1613573 - 913231-2- 4111293137-2 9-233 4532291 --11228 -910329-9172 -56927 -99123 19334- 7 -96112- 22842169- 9129 2756-- 332501 749-4-1 194128-88 -11 666- 218313-91 75241-19 63-6214 5-529 4-146 631-19
29-44 37-3 1613573 - 913231-2- 4111293137-2 9-233 4532291 --11228 -910329-9172 -56927 -99123 19334- 7 -96112- 22842169- 9129 2756-- 332501 749-4-1 194128-88 -11 666- 218313-91 75241-19 63-6214 5-529 4-146 631-19
번호가 5_592 인 카드에 수록되어 있음이 표시되어 있다. 파일 (file) 이 란 Joint Com mittee on Powder Di ffrac ti on S t andards 의 자료를 말하는데 흔히 JC PDS 카드라고 부른다 . JC PDS 카드중에서 번호 가 5_592 인 것을 찾아 보면(그림 5.24) 이 광물에 대한 X 선 회절 자료뿐만 아니라 결정구조, 단위포 상수, 화학성분, 비중 등이 구 체적으로 기록되어 있다 . 때로는 광물로부터 얻어진 X 선 회절분석 자료와 일치하는 JC PDS 카드가 없는 수가 있다. 이런 경우는 X 선 회절분석 자료로 부터 계산된 d(A) 값의 강도 순서를 달리해 가면서 Pow d erDi ffrac ti on Fil eS earchManual 자료와 일치하는 것이 있는지 를 찾아 보아야 한 댜 그래도 일치하는 것이 전혀 없는 경우에는 신종(新 種 ) 광물일 가능성이 있으므로 보다 체계적인 연구가 필요하게 된다. 5.7.4 JC PDS 카드 수록 자료 형석 (CaF 2 ) 의 JC PDS 4-0864 카드(그림 5.25) 를 예로 들어 각 부분의 의미를 알아보면 다음과 같다. A,B,C: 형석의 X 선 분말회절 자료 중 강도가 가장 높은 것 3 개의 d(A) 값과 강도를 순서적으로 나열 D: 형석의 X 선 회절분석 자료 중에서 제일 처음 나타나는 피크 의 d(A) 값과 강도 E: 형석의 화학식 및 광물명 F: 자료의 신뢰도. *: 양호, i : 불량, 표시가 없는 자료는 보 통정도. G: X 선 회절자료를 피크의 287} 커지는 순서로, 즉 d(A) 이 작 아지는 순서로 나열 H: 각 피크의 강도
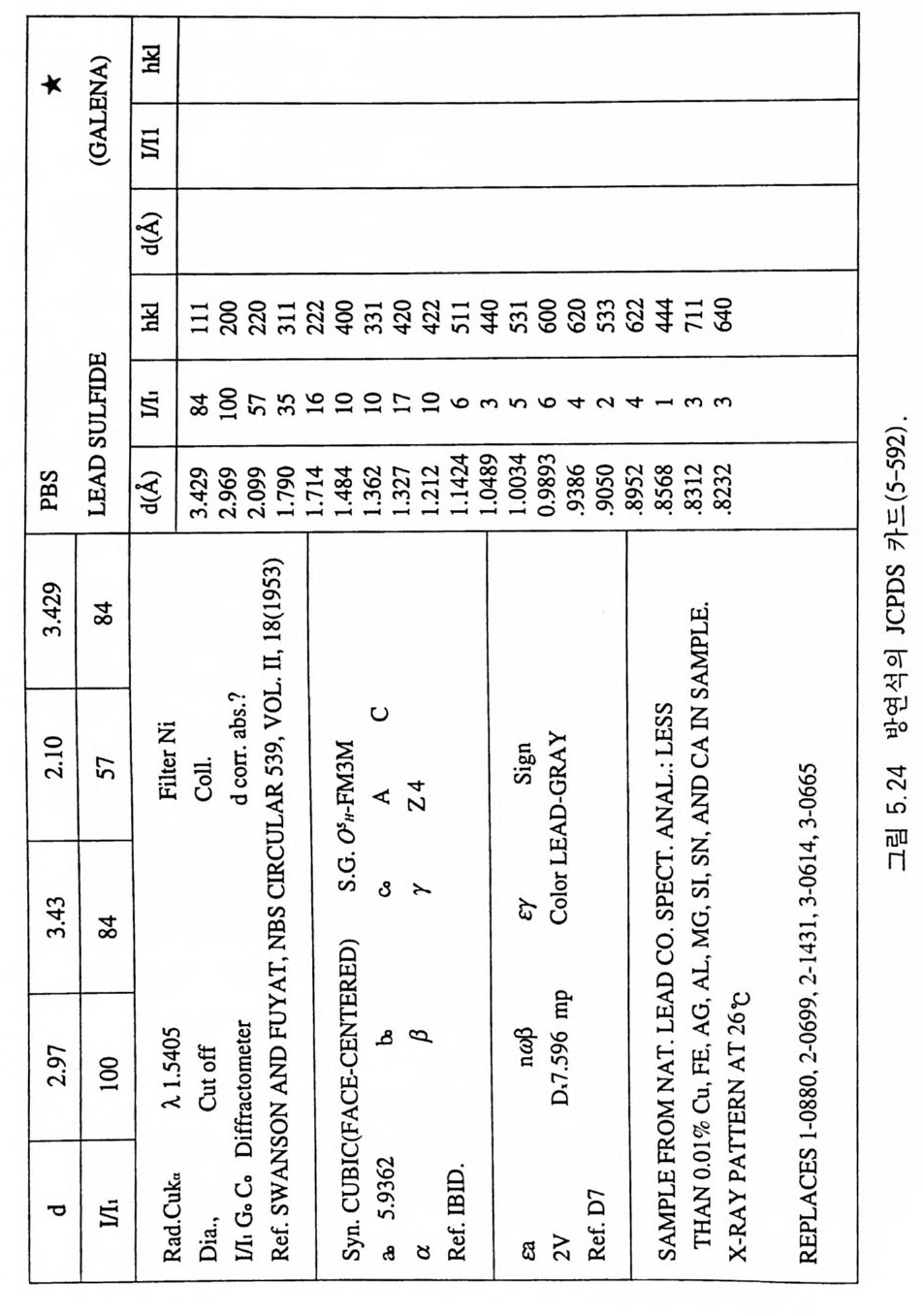 그림2 45방 석연 . 의D카SJC P ARPECLE8,90 069-21-S 80 36,14413-2-01 ,36 6-05 , X-RTRA ENI YAPA 6'C 2T A0H.NT0, 1ECu A %,FGN,, MS S,AIL G, N NCI ,AAD SA.LEM P RAOMPMLESF LD ECO NAT A..NC ETS. AALPE . SLS: RD7 fe. 2 V5,Dlo 7.6Cm9AAp orLED -RYG '하 £ n어Sg in eR.f I.BI D /3R aZ 4 a5,93.6b 2C o A C n.CSU yB(ECEFANTC-ICERED) SG. O.'HM-FM3 .efRNA SON AWSND FUYAT, NSB CVICULAR 539,R 1. II ,(81953)LO /G, C。. 11ter iDrffactmoe corr.a dbs?. D., ai fCut ofCol. l .Rad uk.504. 5 Ct..1i FilterN 100 /1814 157 84 d .2973.43 0 2.13.429
그림2 45방 석연 . 의D카SJC P ARPECLE8,90 069-21-S 80 36,14413-2-01 ,36 6-05 , X-RTRA ENI YAPA 6'C 2T A0H.NT0, 1ECu A %,FGN,, MS S,AIL G, N NCI ,AAD SA.LEM P RAOMPMLESF LD ECO NAT A..NC ETS. AALPE . SLS: RD7 fe. 2 V5,Dlo 7.6Cm9AAp orLED -RYG '하 £ n어Sg in eR.f I.BI D /3R aZ 4 a5,93.6b 2C o A C n.CSU yB(ECEFANTC-ICERED) SG. O.'HM-FM3 .efRNA SON AWSND FUYAT, NSB CVICULAR 539,R 1. II ,(81953)LO /G, C。. 11ter iDrffactmoe corr.a dbs?. D., ai fCut ofCol. l .Rad uk.504. 5 Ct..1i FilterN 100 /1814 157 84 d .2973.43 0 2.13.429
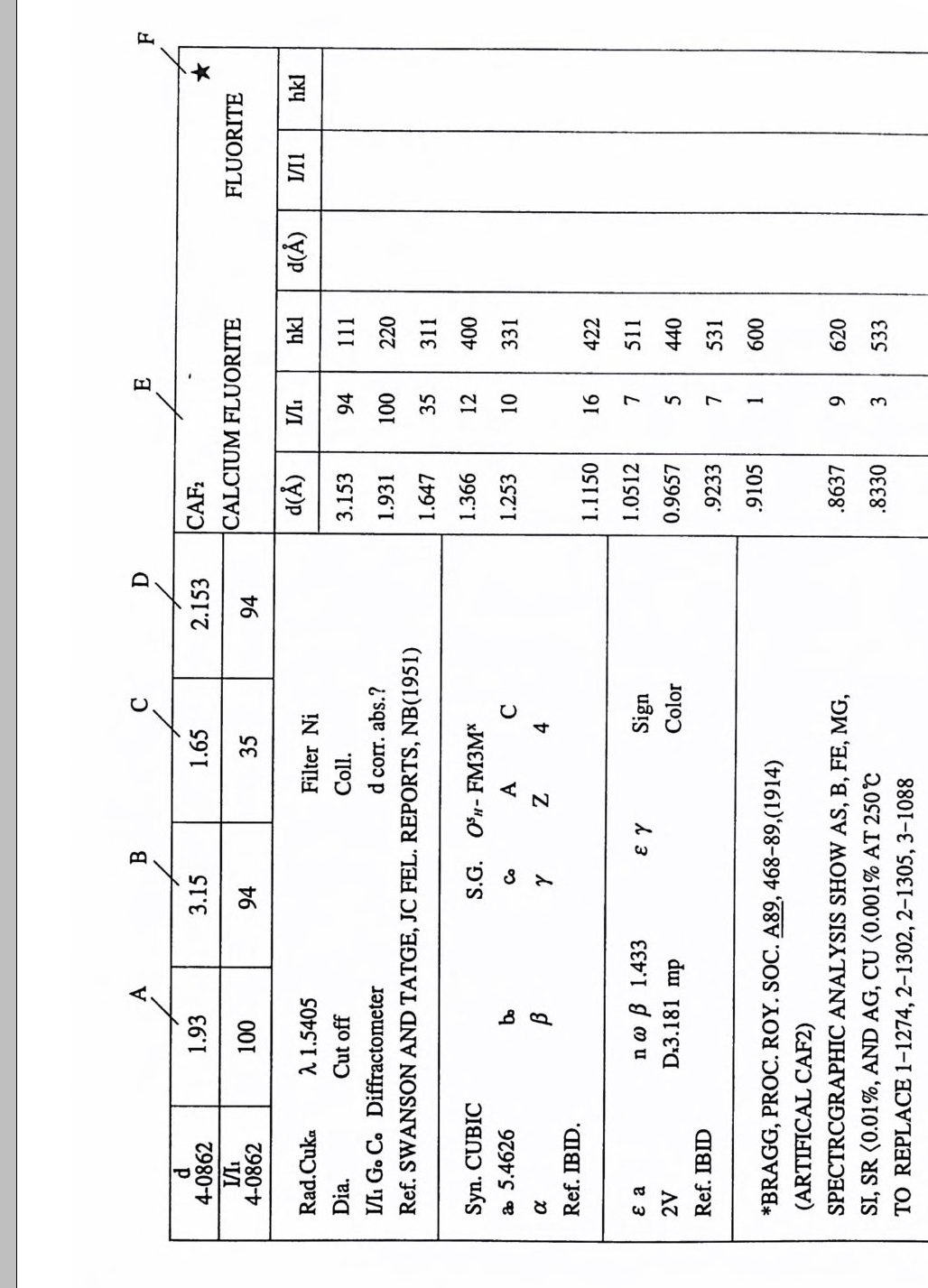
I : 각 피크의 격자지수 이 외에도 카드의 왼쪽 부분에는 X 선 회절분석에 사용한 방사 선 (C uK. . ), 필터 (Ni ), 결정 계 (등축정 계 ), 단위 포 상수 (5 . 4626 A.), 단 위포 함량 (Z=4), 굴절률(1. 433), 비중 (3 .1 81), 문헌자료 등이 수록 되어 있다. 5.7 .5 X 선 회 절 분석의 응용 X 선 회 절 분말분석의 주요 기능은 우선 광물명을 정확하게 판별 을 하는 것이며 , 그 밖에도 결정구조 해석, 결정도 파악, 상전이 (相轉移 ), 혼합 물질 내에서의 각 광물의 대략적인 정량분석, 고용 체 를 이루는 광 물 의 대략적인 정량분석, 동질이상체, 질서-무질서 상태 등을 밝힐 수 있다.
제 6 장 상평형 및 지질학적 눙° 요o 지질학적인 환경에서 광물이 어떻게 생성되고 또 다론 광물과는 어떠한 안정적 공생(共生, p ara g enes i s) 관계를 유지하는지, 그리고 새로운 환경에서 이들의 변화는 어떠할 것인지를 알아보기 위해 자연에서 광물이 생성될 때 영향을 미치는 화학 성분, 압력, 온도 등의 대표적인 요소를 단순화시켜 실험적인 합성연구를 한다. 이 장에서는 상평형 이론에 대한 기초적인 내용과 상평형 연구 자료 가 어떻게 조암광물을 연구하는 데 이용이 되는지에 대해 다루기 로한다. 6.1 상평형과 상률 상평형 (相平衡, ph ase e qu i l i b ri um) 이라 함은 현재 존재하는 상 (相, p hase) 이 현재의 조건에서 가장 안정하기 때문에 조건이 변하
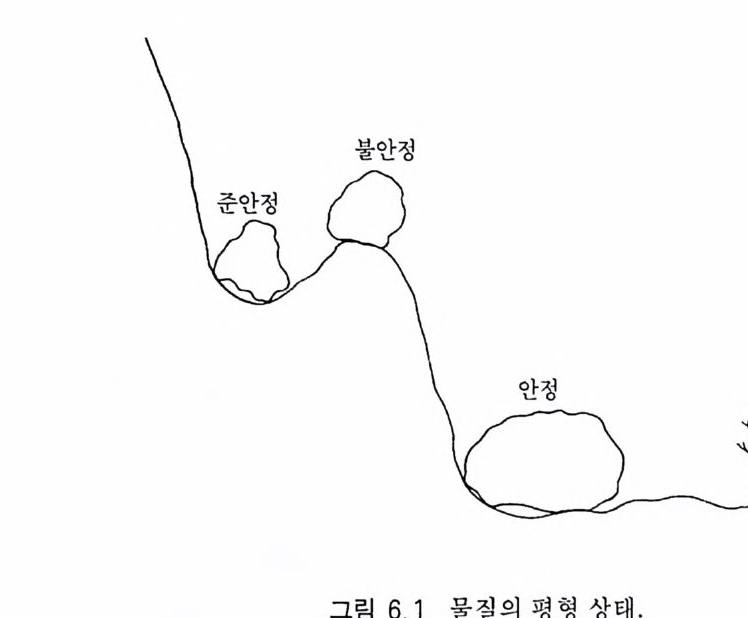 그립 6.1 물질의 평형 상태.
그립 6.1 물질의 평형 상태.
지 않는 한 자발적으로는 다른 상으로 변하지 않는 상태 를 말한 다. 고온 또는 고압 상태에서 안정한 다이아몬드나 남정석 등은 상온·상압인 환경에서 오히려 불안정해져 외부로부터 어떤 자극이 있을 경우 새로운 환경에 적합한 광물로 변하려고 한다 . 이런 광 물 들은 표면상으로는 안정한 것처럼 보이나 실제로는 그렇지 않은데 이런 상태를 준안정(準安定, me tast able) 이라고 한다(그림 6.1) . 불안 정(不安定, uns ta ble) 은 광물이 현재의 환경에 알맞는 형태로 변화 하는 과정 중에 있는 경우를 의미한다 . 1875 년 J. W. G i bbs 는 어떤 특정한 공간과 조건에서 평형상태로 존재할 수 있는 상(相, p hase) 의 수효에 대한 법칙을 발견하였는데 이를 G i bbs 의 상률(相律 PhaseRule) 이라고 한다. F+P=C+2
F 는 자유도(自由度, deg re e of free dom), P 는 상(相, p hase) 의 수, C 는 그 계(系, s y s t em) 에 존재하는 최소의 성분(成分, com p onen t)의 수이다. 자유도 (F) 란 주어진 계에서 평형상태에 있 는 상의 수를 변화시키지 않은 상태에서 독립적으로 변할 수 있는 변수( 度 手, va ri able) 의 수효를 가리키며, 상률에 있는 2 는 변수가 온도와 압력 등 두 가지 요소만 있다는 의미이다. 만약 온도와 일 반적인 압력 외에 수증기 압력이 추가로 있는 조건이면 상률은 F+P=C+3 이 되고, 온도는 변하지 않고 압력만이 변할 수 있는 조건이라면 F+P=C+l 로 된다 . 상 (P) 이란 물리적으로 뚜렷하여 다른 물질과 구분이 가능한 것을 의미한다. 성분의 수 (C) 는 그 계 에 존재하는 상을 표현하는데 필요한 최소 성분 수를 의미한다. 만약 석영 (S i 02) 과 크리스토발라이트 (S i 02), 트리디마이트 (S i 02) 로 이루어진 계라면, 상의 수 (C) 는 3 이며, 성분의 수 (C) 는 l 이 된다. 한편 석영 (S i Oz) 과 엔스터타이트 (M g S i O J), 포르스테라이트 (M g 2S i O 』)로 이루어져 있는 공간이 있다면, 상의 수 (P) 는 3 이 되 고, 엔스터타이트는 석영과 포르스테라이트의 화학성분으로 나타 낼 수 있으므로 (S i 02+M g 2S i O 』 =2M g S i 0 J), 성분의 수 (C) 는 2 가 된다. 성분의 수가 l 이면 1 성분계(一成分系, onecomp o nent sys t e m ), 2 이면 2 성분계(二成分系 two comp on ent sys t e m ), 3 이면 3 성 분계 (三成分系, three comp on ent sys t e m ) 이 다. Goldschm i d t는 거의 모든 암석이 실제의 지질학적인 환경에서 어 느 범위의 온도와 압력의 영향을 받고 있으므로 자유도 (F) 는 2 가 되 어 G i bbs 의 상률이 P=C 가 됨을 알 수 있고, 따라서 〈암석을 구성 하는 조암광물의 수 (P) 는 그 계에 존재하는 성분의 수 (C) 와 같거 나 또는 적다〉라고 하였는데 이를 Goldsc hmi d t의 광물학적 상률 (Goldschm idt ' s mine ralog ica l pha se rule) 이 라고 한다.
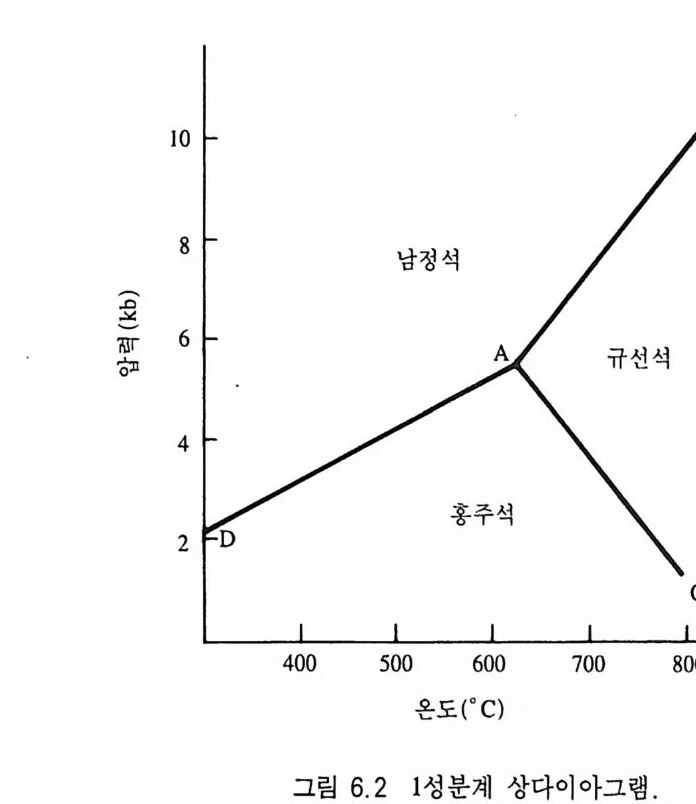 B
B
6. 2. 1 성분계 상다이어그램 동질이상체(同質異像 體 , p ol y mo rphs) 인 남정석 , 규선석, 홍주석 울 포함하고 있는 광물계는 AhS i Os 인 성분 하나로 모든 광물을 나 타낼 수 있으므로 1 성분계의 대표적인 예이다 . 이들의 안정 영역 과 공생 관계 롤 나타내 는 상다이 어 그램 (ph ase diag r am , 그림 6.2) 에 의하면 온도와 압력이 변수임을 알 수 있기 때문에 이 계에 적용 되는 Gi bbs 의 상률은 P+F=C+2 이며 C=l 이다. 1 성분계 상다이 어그램은 성분이 동일하므로 압력 (P) 과 온도 (T) 를 변수로 하는 P- T 상다이어그램이 된다. A 는 세 광물이 함께 공존하는 조건으로
서, P=3 이 되고 C=l 이므로 자유도 (F) 는 0 이 된다. 죽, 세 광물이 공생되도록 유지시키면서 독립적으로 변화시킬 수 있는 변수는 〈없 다 〉 라는 의미이다. 이러한 조건을 무변수 상태(無 要 數狀態, inv aria n t condi tion ) 라고 한다. 한편 두 광물이 공존할 수 있는 조건은 AB, AC, AD 의 직선으로 표시된다. 이런 경우는 P=2 이므로 F= l 이 된다 즉, 두 광물이 평형상태에서 공존하도록 유지시킨 상태 에서 독립적으로 변할 수 있는 변수는 〈 온도나 압력 중 하나이다〉라 는 의미이며, 이런 상태를 단일변수 상태(單 一變 數狀態, univ a rian t cond iti on) 라고 한다. 예 를 들어 남정석과 규선석이 공존하는 조건 은 AB 선 상인데, 8kb 의 압력과 725°C 의 온도에서 두 광물은 공존 한다 . 만약 온도가 825 ° C 로 증가할 경우 압력이 10kb 로 종속적으 로 변하면 두 광물은 계속 공존할 수 있다. 즉, AB 선 상의 온도 나 압력 중 어느 한 요소가 변할때 다른 요소가 종속적으로 변할 경우 두 광물은 안정하게 유지된다. 마지막으로, 한 광물만 안정 적으로 존재하는 영역은 비교적 넓은 온도와 압력 범위로 표시된 다 . 이런 조건에서는 P=l 이 되어 F=2 가 된다. 즉, 이변수 상태 ( 二맞 數度狀態, diva rian t cond iti on) 가 된다. 예를 들어 홍주석이 안 정한 영역은 AD 와 AC 사이인데, 이 영역에서는 온도와 압력 등 두 요소가 안정 영역 내에서 서로 독립적으로 변하여도 홍주석은 스스로 안정할 수 있다 . 이 상다이어그램으로부터 얻을 수 있는 지질학적인 의미로는 어 떤 변성암 내에 세 광물이 동시에 함유되어 있는 변성암이 있을 경우 그 암석은 약 5 .5 kb 의 압력과 620°c 의 온도에서 생성되었음 울 알 수 있게 되어 과거의 변성환경을 추정할 수 있다. 그러나 자 연에서는 이 세 광물이 모두 공존하는 경우보다 두 광물 또는 한 광 물만 함유하는 변성암이 더 일반적이다. 이것은 각 광물의 안정 영 역이 비교적 넓은 온도와 압력 범위에 걸쳐 있기 때문이다. 만약 남
정석과 홍주석이 공생하는 변성암 지대라면 온도는 최대 620 · c 이고 압력은 약 2~5.5kb 정도인 변성작용이 있었음을 추정할 수 있게 된 댜 단일 광물인 경우는 안정영역의 온도 및 압력 범위가 더욱 넓 다 공생 광물군(共生鑛物群 mi ne ral assembla g e) 은 지 질온도계 (地質 溫度計, geo th e nnomete r ) 또는 지 질압력 계 (地 質壓 力 3 -1-, geo baromete r ) 의 역할을 할 수 있으므로 매우 중요한 의미를 가진다 . 6, 3 2 성분계 상다이어그램 2 성분계 상다이어그램은 일정한 압력에서 이루어지는 상평형관 계를 나타내며, 일반적으로 세로축은 온도 (T), 가로축은 성분 (X) 을 나타낸다. 따라서 등압(等 堅 )조건에서의 T-X 상다이어그램이 된다 . 이러한 조건에서는 G i bbs 의 상률이 F+P=C+l 이 된다. 6. 3. l 고용체를 형성하지 않는 경우 2 성분계의 가장 대표적인 상다이어그램은 스핀 (CaS i T i Os) 과 아노 르다이트 (CaAhS iz 이) 사이의 상관계를 나타내는 것으로서 (그림 6.3 ), 두 광물은 상대방의 성분을 전혀 함유하지 않는 순수한 화학 조성을 지니는 것으로 간주한다. 그림 6 . 3 에 의하면 스핀은 가열할 때 1382°C 에서 액체로 변하며, 아노르다이트는 l550°C 에서 액체로 변한다. 이러한 사실은 〈 CaS i T i Os 의 성분을 지니는 고온의 액체가 서 서 히 냉 각될 때 1382°C 에 서 스핀을 정 출시 키 고, 또 CaAhSi2 0 8 성분의 액체는 1550°C 로 냉각될 때 아노르다이트롤 정출시킨다〉라 고 바꾸어 말할 수 있다. 위 두 광물의 경우처럼 광물을 가열하였 을 때 그 광물의 화학성분과 동일한 성분의 액체로 변하는 현상을
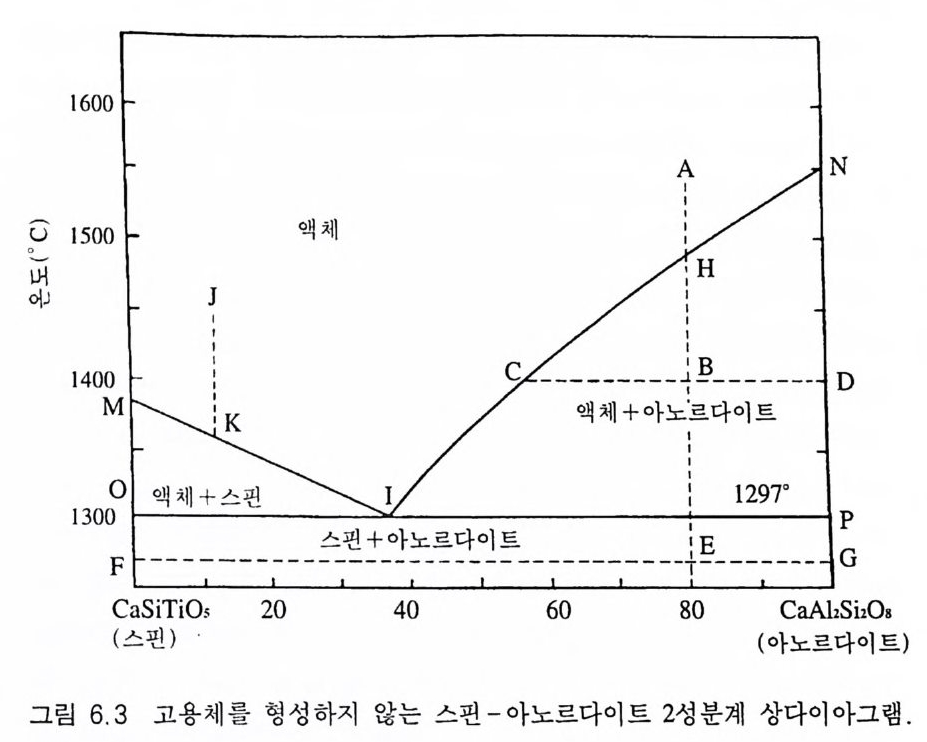 1600
1600
조 화용융( 調 和 瑢融 cong rue nt meltin g ) 이 라고 한다 . 두 개의 곡선 MI 와 NI 의 윗부분은 액체만이 안정하게 존재하는 영역이고 (P= l) , 두 곡선과 직선 OP 사이의 부분은 액체와 광물이 공존하는 영역이다 (P=2). 그리고 직선 OP 아래 부분은 두 광물이 공존하고 있는 영역이 된다 (P=2) . 곡선 MI 와 NI 는 액체만이 존재 할 수 있는 영역과 액체와 광물이 함께 공존하는 영역의 경계선으 로서 액상선( 液 相 線 , liq u id u s curve) 이라 한다. 직선 OP 는 액체와 광물이 공존하는 영역과 고체인 두 광물만 존재할 수 있는 영역의 경계선으로서 이를 고상선(固相 線 , soli du s curve) 라고 한다. 액상선 은 액체만으로 존재할 수 있는 최저 온도 경계를 나타내는 것이 고, 고상선은 액체가 존재할 수 있는 최저 온도 경계를 나타낸다.
A 성분 (80% CaAbSii Os +20% CaS i T i Os) 을 지니는 액체가 1550°C 이 하로 서서히 냉각되면서 고체로 변하는 과정은 점 A 에서 수직선을 그어봄으로서 예측할 수 있는데, 이 수선을 등성분 수선( 等 成分垂 線 , iso p le th ) 이 라고 한다 . 즉, A 성 분의 액 체 는 1550°C 와 1490°C 사 이에서 액체만으로 존재하며, 149o•c 와 l297° 사이에서는 액체와 아노르다이트, 1297° C 이하에서는 스핀과 아노르다이트로 안정하 게 공존한다. 이를 자세히 설명하면, A 성분의 액체가 149o·c ( H) 로 냉각되면, 아노르다이트를 정출하기 시작한다 . A 성분의 액체로 부터 아노르다이트가 정출하게 되면, 액체 내에는 아노르다이트 성분이 감소하게 되어 잔류 액체의 전체 성분은 마치 스핀의 성분 이 증가한 양상을 나타낸다. 어떤 온도에서 공존하고 있는 상 (p hase) 을 알아 보고자 할 때에는 수평 선을 그으면 된다. 예를 들 어 1400·c 에서 공존하는 상을 알아보려 면 수평 선 CD 를 그으면 된 댜 죽, 1400·c 에서는 C 의 성분 (55% CaAhSii 0, +45% CaS i T i Os) 을 가지는 액체와 D 의 성분을 가지는 광물(아노르다이트)이 공존하고 있음을 알 수 있다. 수평선 CD 처럼 주어진 온도에서 공존하고 있 는 상을 이어 주는 선을 이음선(ti e li ne) 이라고 한다 . 한편 각 온도 에서 공존하고 있는 두 상의 양적 비율은 이음선 (CD) 과 등성분 수 선 (AE) 이 만나는 교점 (B) 을 기준으로 나누어진 이음선의 길이의 비 와 같게 되 는데 이 를 Lever 법 칙 (Lever Rule) 이 라고 한다. 만약 CB 의 길 이 가 2.25 cm 이 고 BD 의 길 이 가 1.90 cm 라면, 아노르다이 트 와 액체의 양은 각각 아노르다이트= 42..12 55 ccmm X100=57.2%
액 체 = 41..91 0 5 ccmm X 100=42.8% 가된다 . 온도가 하강함에 따라 아노르다이트도 계속 정출되어, 잔류 액 체의 성분은 H ~ C ~ I 로 변하게 된다. 점 I 에서는 잔류 액체로 부터 아노르다이트만 정출하는 것이 아니라 스핀도 함께 정출되기 시작하는데, 이처럼 액체와 두 고체 광물이 함께 공존하는 점을 공융점(共融點 eu t ec ti c p o i n t)이라 한다. 공융점에서 정출되는 아노 르다이트와 스핀의 양적 비율은 Lever 법칙을 적용하면 37% (아노르 다이트)와 63 %( 스핀)가 됨을 알 수 있다. 공융점에서는 잔류 용액 이 완전히 소비될 때까지 두 광물이 정출되고, 1297 °C 이하에서는 고체인 두 광물만이 존재하게 되는데 A 성분을 가지는 액체가 완전 히 고체로 변했을 때의 두 광물의 구성 비율은 Lever 법칙을 이용 하면 80% 의 아노르다이트 (FE) 와 20% 의 스핀 (EG) 이 됨을 알 수 있다. 액체만 존재할 수 있는 액상선 위의 영역에서는 자유도인 F=2 가 되며, 액체와 광물이 공존하고 있는 영역에서는 F=l, 공융점 (I)에서는 F=O 가 된다 . J성분의 액체는 K 에 해당하는 온도로 냉각되면 스핀을 정출시키 기 시작하며 잔류용액의 성분은 점점 CaAhS i 2 아 쪽으로 향하게 된 다. I 에 도달하게 되면 잔류 용액으로부터 스핀과 함께 아노르다이 트도 정출하게 되며 액체가 다 소모될 때까지 온도 (l297°C) 는 변하 지 않게 된다. 결국 스핀과 아노르다이트가 각각 88% 와 12% 만큼 구성되어 있는 암석이 된다. 이 상다이어그램을 지질학적인 개념으로 활용하면, A 성분을 가 지는 마그마가 1400°C 로 냉각된 상태에서 갑자기 지각에 발달한
균열을 따라 화산의 형태로 분출하였다면 그 화산암의 특징은 유 리질 석기에 아노르다이트 반정이 약 55% 들어 있는 반상조직이 됨을 예측할 수 있게 된다. 또한 80% 의 아노르다이트와 20% 의 A 핀으로 구성된 지각 하부 물질은 지하 심부로부터 전달되는 열의 축적으로 인해 A 성분의 마그마가 됨을 알 수 있다. 이처럼 마그마 에 어떤 성분이 유입되거나 유출되는 경우가 아니고서는 마그마의 처음 성분은 마그마가 완전히 고결되어 만들어진 암석의 전체 성 분과 항상 일치하게 된다. 그림 6 .4는 류사이트 (KAIS ii O.) 와 크리스토발라이트 (S i 02) 그리고
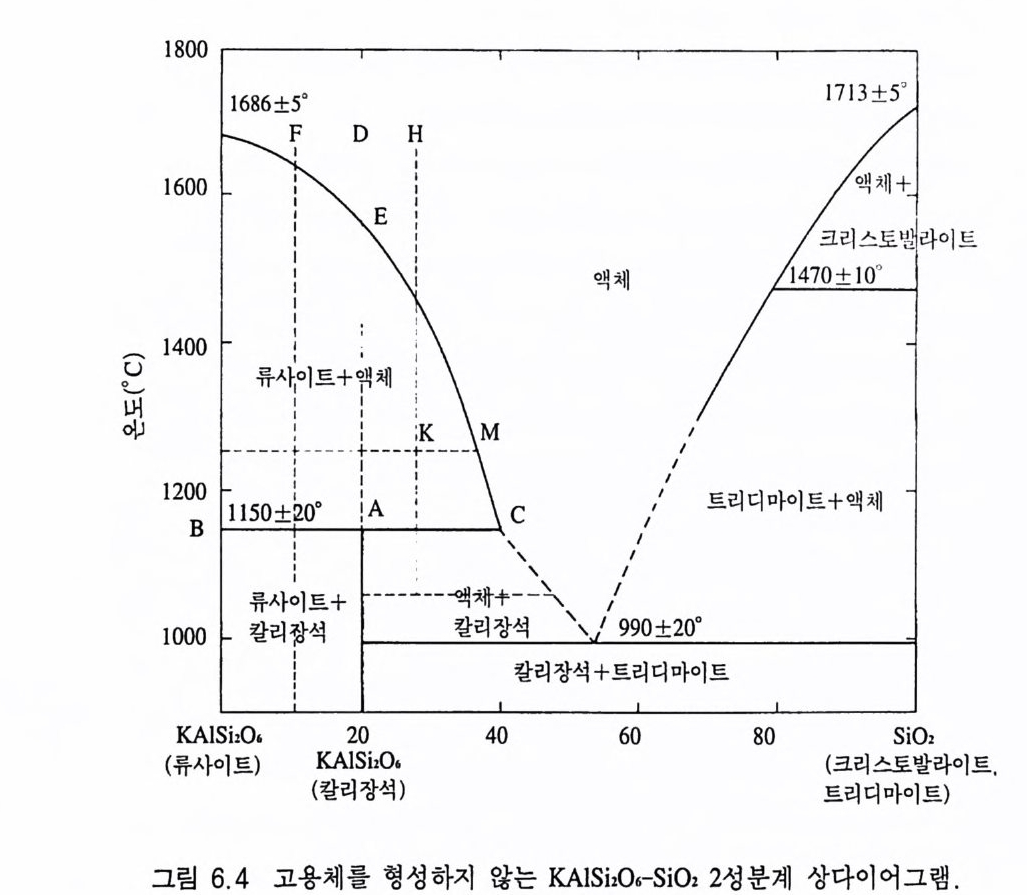 1800
1800
이들 성분으로 나타낼 수 있는 칼리장석 (KAIS ii 06 · S i 02) 을 포함하 고 있는 2 성분계 상다이어그램으로서, 칼리장석을 1150 土 2o·c 로 가열하면 칼리장석과는 전혀 다른 성분의 액체 (C) 와 류사이트 (B) 를 만들면서 녹게 된다 . 칼리장석이 완전히 녹아 없는 상태가 될 때까지 계의 온도는 l150°C 로 유지가 되며, 계속 가열하면 류사이 트와 액체가 공존하다가 마침내는 원래의 칼리장석 성분과 일치하 는 성분의 액체 (D) 로 변한다. 칼리장석의 경우와 같이 어떤 광물을 가열했을 때 원래 광물의 성분과는 전혀 다른 액체와 고체로 녹는 현상을 비조화용융(非 調 和瑢融 inc ong ru ent mel ti n g)이 라고 한다. 만약 칼리장석과 동일한 성분을 가지는 액체(마그마) D 가 서서 히 냉각되어 E 온도에 도달하게 되면 류사이트를 정출하기 시작하 며 액체의 성분은 서서히 액상선 EC 를 따라 변하게 된다. 온도가 ll50 ° C 로 하강하면 이 미 정 출했던 류사이 트와 잔류 액 체 (C) 가 반 응하여 칼리장석을 만들며, 그때의 반응식은 다음과 같다. 액 체 (60% KAISi 20 6 + 40% S i0 2 ) + 류사이 트 (KAIS i 206) ~ 칼리 장석 (KA!Sb 이) C 점에서는 3 개의 상이 공존하므로 (P=3), F=O 이 된다. 따라서 액체가 완전히 소모되어 모두 칼리장석으로 변할 때까지 온도는 변 하지 않고 그대로 유지하게 되며, 결국 원래의 액체 성분과 동일한 성분의 칼리장석으로 변하게 된다. C 점을 반응점(反應點, reacti on poi n t 또는 per it ec ti c p oi n t ) 이 라고 한다. H 성분을 가지는 액체가 서서히 냉각되면, 류사이트를 정출하게 되고 용액의 성분은 점점 S i 02 가 많은 쪽으로 변하게 된다. 1150°C 가 되면, 아래식과 같이 류사이트와 액체가 반응하여 칼리장석을 형성하게 되는데 액체의 양이 훨씬 많으므로 류사이트가 다 소비 되어도 액체는 남게 된다.
액체+류사이트~칼리장석+액체 류사이트가 완전히 소비되면 온도는 다시 하강하게 되며, 액체 로부터 칼리장석이 계속 정출하면서 결국 공융점인 I 에 도달하게 된다 . I 에서는 액체로부터 칼리장석 외에 트리디마이트가 함께 정 출되며 액체가 완전히 소모될 때까지 온도 (990°c) 는 변하지 않는 다. 액체가 완전히 사라지면 온도는 내려가 결국 칼리장석과 트리 디마이트의 혼합물을 형성한다. F 성분의 액체는 냉각될 때 처음 류사이트롤 정출하고 ll50°C 에서는 액체와 류사이트가 반응하여 류사이트와 칼리장석으로 변하는 반응이 일어난다. 액체가 다 소 비되면 결국 류사이트 (50% )와 칼리장석 (50 % )이 공존하는 화성암이 만들어 지게 된다. 6.3.2 완전고용체를 형성하는 경우 완전고용체를 형성하는 대표적인 광물로는 사장석과 감람석이 있다 . 완전고용체를 형성하는 경우에는 두 단종을 잇는 액상선 뿐 만 아니라 고상선도 곡선의 형태를 나타낸다. 우선 사장석의 경우 롤 예로 들면(그림 6.5), 액상선 위는 모두 액체만 안정하게 존재 하는 영역이며, 고상선 아래 부분에서는 고체(사장석)만 안정하다. 그리고 액상선과 고상선의 사잇부분은 액체와 고체(사장석)가 공존 하는 영역이다 . 완전 고용체를 형성하는 광물인 경우도 주어진 성 분의 액체가 냉각될 때 변화하는 과정온 등성분 수선을 그려 예측 할 수 있다. 또한 특정한 온도에서 공존하는 두 상은 이음선을 그 어 봄으로서 알 수 있으며, 각 상의 성분은 액상선 또는 고상선 위의 점에서 수선을 그어 가로축에 있는 성분을 읽으면 된다. 순 수한 아노르다이트 성분의 액체는 1553°C 에서 아노르다이트로 정
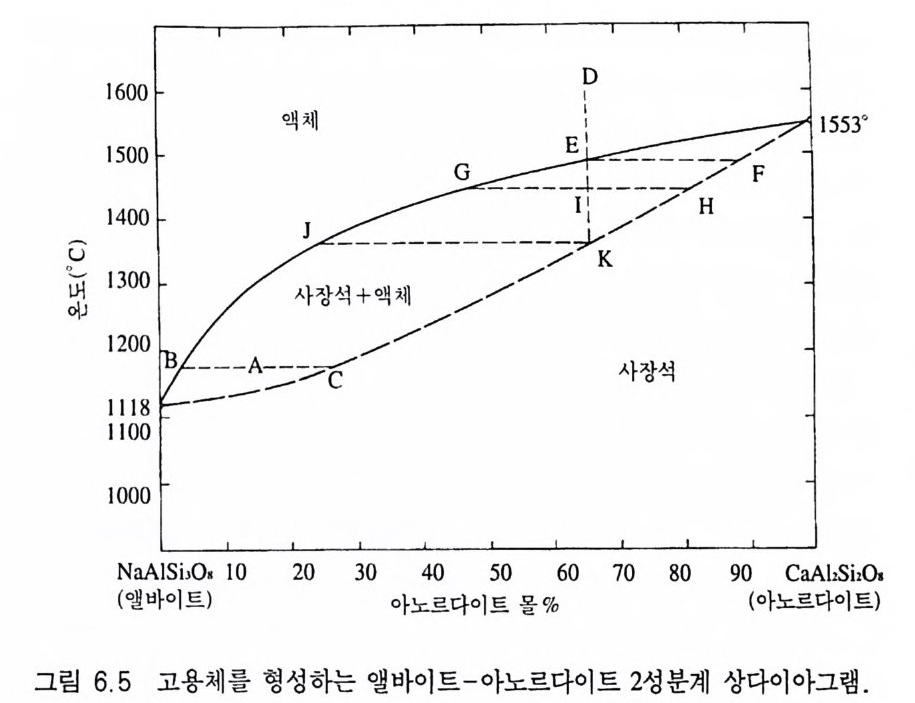 1600 G~D 三 /--,,;
1600 G~D 三 /--,,;
출 하고, 또 앨바이트 성분의 액체는 l1l8°C 에서 앨바이트로 정출 한다. 그러나 두 단종의 중간 성분을 지니는 액체의 정출 과정은 다소 차이가 있다 . 예를 들어 D 성분 (An65) 을 가지는 액체가 냉각하 기 시작하여 E 의 온도(약 1490•c) 에 이르면 사장석이 막 정출하기 시작하며, 이 사장석 (F) 의 화학성분은 F 에서 등성분 수선을 그어 가로축과 만나는 점(약 An88) 이 된다 . 사장석이 정출됨에 따라 액 체의 성분은 액상선을 따라 E~G~ J로 변하게 되며 이와 공존하 는 사장석 성분 역시 F~H~K 로 변하게 된다. 처음 만들어진 사장석(바이타우나이트)이 평형상태에서 액체와 끊임없이 반응하면 서 1450°C 로 되 면 사장석 (H) 은 An88 로부터 An81 으로 성 분이 변 한 다. An81 과 공존하는 액체 (G) 의 성분은 An .11이다 그리고 이 온도에 서 공존하고 있는 액체와 사장석의 양적 비율은 1.2 cm(HI ) :1.4
cm (I G) 가 되어 46 . 2% 의 액체와 53.8% 의 사장석으로 구성되어 있음 을 알 수 있다. 온도가 계속 하강하여 1360'C 로 되면 액체의 성분 은 J로 변하고 이와 공존하는 사장석 (K) 의 성분은 An 짜라브라도라 이트)이 된다. 그러나 이 온도에서는 실제로 액체가 하나도 없는 상황이므로 더 이상 사장석이 정출할 수 없게 되어 정출작용은 완 료된다. 결국 마지막에 만들어지는 사장석의 성분은 액체의 원래 성분과 일치함을 알 수 있다 . 만약 액체와 이로부터 정출된 사장석 사이에 완전한 화학반응이 일어나지 않는 비평형상태가 유지되면 먼저 만 들 어진 사장석 표면 에 후기에 만들어지는 사장석이 계속 피복하게 되므로 사장석의 성분은 내부의 바이타우나이트 성분으로부터 표면의 라브라도라이 트까지로 앨바이트 (Ab) 성분이 연속적으로 증가하게 된다 . 이런 사장석을 박편으로 관찰하면 누대구조 (zonal s t ruc t ure ) 가 선명하게 나타난다. 이러한 실험적 결과는 어떤 심성암에 누대구조 를 나타 내는 사장석이 존재할 때, 이 광물은 비평형 상태에서 만들어 졌 음 을 제시해 줄 수 있다 . 때로는 사장석의 내부보다 외곽 부분이 아 노르다이트 (An) 성분이 높은 경우가 있다. 이러한 현상은 사장석 이 정출할 때 온도가 일정하게 하강했던 것이 아니라 오히려 상승 하였었거나 또는 주변 암석의 첨가가 일어나 Ca 성분이 증가한 환 경이 있었음을 추정할 수 있게 한다. 또한 사장석 이 정 출할 때 분별 정 출작용(fr ac ti onal cry st a l liza ti on ) 이 일어났다고 가정하면, 바이타우나이트가 처음 정출되어 가라 앉은 후 잔류 용액과 더 이상 반응을 하지 않는다. 그리고 계속 An 성분이 적은 사장석이 연속적으로 정출면서 차례로 가라앉게 된다. 이러한 현상은 현무암질 마그마가 분별 정출 작용을 하면서 광물을 정출시킬 때 사장석 계열 중 An 성분이 많은 사장석으로부 터 An 성분이 적은 사장석을 차례로 정출시키는 사실과, 반려암에
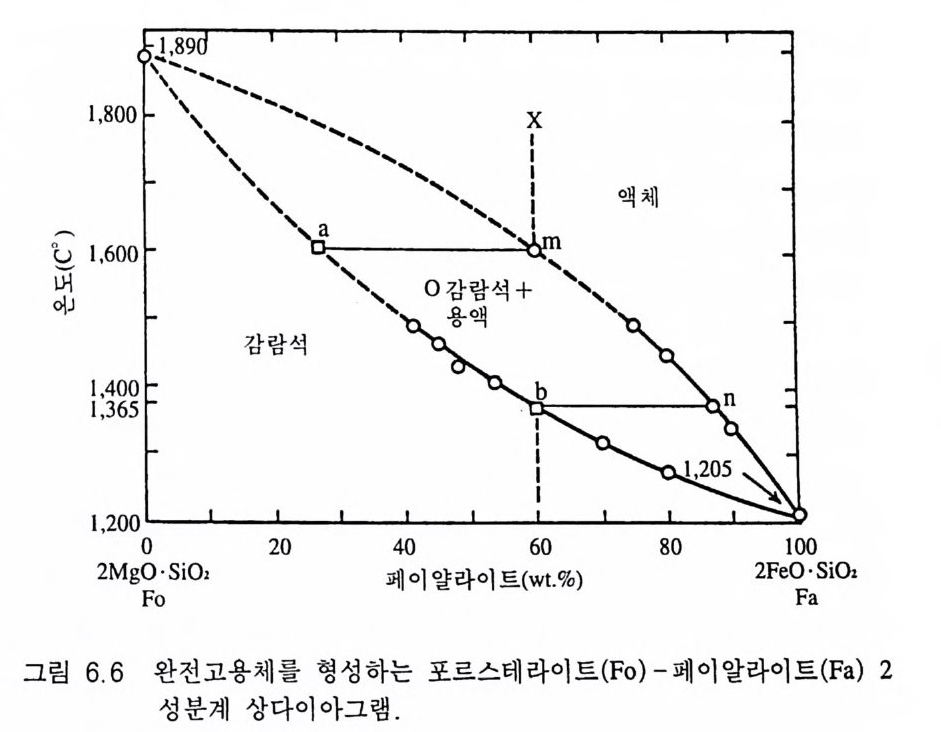 C l버oU)( l,860 。0。 I-, `、i'` , 8 \`9 `\` ` `\` `、``\ ... `. `\` ```소 `O ` `감용`액람 ` 석`+`?:i 눅 `` `
C l버oU)( l,860 。0。 I-, `、i'` , 8 \`9 `\` ` `\` `、``\ ... `. `\` ```소 `O ` `감용`액람 ` 석`+`?:i 눅 `` `
있는 사장석은 An 성분이 높은 반면에 화강암에 있는 사장석은 An 성분이 낮은 현상을 잘 설명할 수 있게 한다. 감람석의 경우(그림 6.6) 고온인 1s9o•c 에서 순수한 M g-감람석 (포르스테라이트, Fo) 이 정출하며, Fe- 감람석(페이알라이트, Fa) 은 1210·c 에서 정출한다. 만약 X 성분(60wt.% Fa) 을 가지는 고온의 액 체가 16oo·c 로 냉각되면 감람석 (a) 을 정출시키기 시작하고, 이때 의 감람석 성분은 a 에서 수선을 내려 26w t. %Fa 가 됨을 알 수 있 다 액체의 온도가 서서히 내려감에 따라 액체의 성분은 m~n 으 로 변하며, 감람석의 성분도 a 크 b 로 변한다. 1365°c 가 되면 이음 선에 의해 감람석 (b) 과 액체 (n) 가 공존하는 것을 알 수 있게 되는 데, X 에서 등성분 수선을 긋고 Lever 법칙을 적용하면 실제로는
액체가 없음을 알 수 있다. 다시 말하면 X 성분의 액체는 결국 동 일한 성분을 가지는 감람석을 정출시키면서 완전히 소비되고 만다. 온도가 계속 내려간다고 해도 60wt .% Fa 성분의 감람석은 성분의 변화없이 그대로 존속하게 된다. 감람석은 (Mg , Fe )z S i O 의 화학성 분을 가지는데 일반적으로 M g >Fe 이면 포르스테라이트, Mg < Fe 이면 페이알라이트라고 구분한다. 6.3.3 용리현상이 일어나는 경우 고온에서는 원소간의 치환에 의해 고용체로서 안정하게 존재하 던 광물도 온도가 낮아지면 타 원소를 고용할 수 있는 능력이 감 소하여 일정량 이상의 타 원소를 더 이상 포용할 수 없게 된다 . 따라서 초과되는 타 원소는 새로운 광물의 형태로 분리가 되는데 이 러 한 현상을 용리 (溶離 exsolu ti on) 라고 한다 . 용리현상을 나타내는 대표적인 주요 조암광물의 예는 칼리장석 앨바이트 사장석이다. 그림 6.7(a) 는 마그마 내의 수증기압이 1 기압 정도로 지표 아주 가까운 환경에서 일어나는 반응으로서 화산암이 형성될 수 있는 조건이라고 말할 수 있다. X 성분(약 Or58Ab42) 을 가 지는 용액(마그마)이 서서히 냉각하게 되면 12oo·c 에서 류사이트를 정출하게 되고, Y 에 도달하면 류사이트와 액체가 반응하여 W 성 분울 가지는 장석을 만들게 된다. 공융점 (Z) 온도인 1078°C 에서는 장석이 계속 정출하면서 결국 액체는 없어지게 된다. 1078°C 이하 에서는 액체의 원래 성분과 동일한 아노르도클레이즈 [(K, Na)AlShOs] 란 균질한 장석 고용체로 존재하다가 660°C 이하가 되 면 2 개의 장석으로 분리되는 영역으로 진입하게 된다. 예를 들어 600°C 에서는 N 성분을 가지는 앨바이트 장석과 M 성분의 정장석으 로 분리되며, 500°C 에서는 0 성분 (Or75Ab 비의 칼리장석과 P 성분
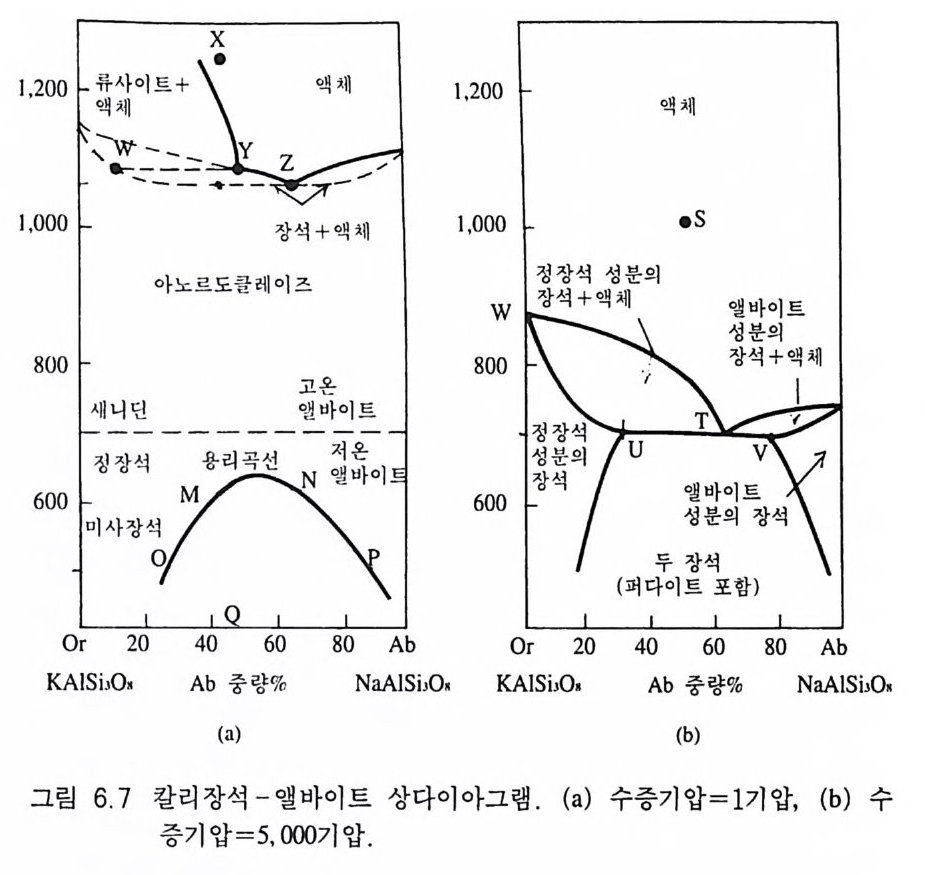 1,2 0 0 I- 류 사이 트+ \ 액체 1,2 0 0
1,2 0 0 I- 류 사이 트+ \ 액체 1,2 0 0
(OrrnAb9o) 의 앨바이트가 혼정 ( 混 晶)하게 되는데, 그들의 양은 Lever 법칙에 따라 칼리 장석이 더 많다. 즉 칼리장석(정장석 또는 미사장석) 내에 앨바이트 사장석이 용리되어 있는 퍼다이트 구조 (p e rt h it e) 가 만들어진다. 이때에도 칼리장석과 앨바이트 사장석은 타 원소를 소량 함유하고 있는 고용체이다 . 칼리 장석 은 Al 과 Si 원자의 질서 -무 질서 (order-d iso rder) 현상이 일어나 온도에 따라 동질이상체를 형성하는데, 700°C 이상에서는 무질서 상태인 새니딘으로, 700~600°C 범위에서는 정장석, 그리고
600°C 이하에서는 질서상태가 완전한 미사장석으로 존재한다 . 앨 바이트 역시 700°C 이상에서는 고온 앨바이트로, 그 이하에서는 저 온 앨바이트로 존재한다 . 따라서 퍼다이트 구조는 다량의 미사장석 또는 정장석과 저온 앨바이트가 소량 혼정되어 있는 조직이다 . 마그마 내의 수증기압이 높아지면 광물의 초기 정출 온도가 크 게 낮아 지고, 용리곡선의 위치는 오히려 상승하는 현상이 일어 난다. 예를 들어 수증기압이 1000 기압 정도이면 공융점 온도가 850°C 로 낮아지고, 또 2000 기압이면 750°C 로 낮아진다. 그리고 수 증기압이 5000 기압으로 증가하면 그림 6 . 7(b) 와 같은 상평형 관계 가 성립된다. S 성분의 마그마가 서서히 냉각되어 800 ° C 가 되면 칼리 장석 이 정 출하기 시 작하고, 703 · c 가 되 면 공융점 인 T 에 도달 하게 되며 액체가 다 소비될 때까지 U 성분의 칼리장석과 V 성분 의 앨바이트가 정출하게 된다 . 온도가 더 하강하면 칼리장석과 앨 바이트 모두 용리현상을 각각 일으키게 되는데, U 성분을 지녔던 칼리장석은 약간의 앨바이트를 분리시켜 퍼다이트 조직을 가지게 되고, V 성분의 앨바이트는 약간의 칼리 장석을 용리시켜 역퍼다 이트 (an tip e rthit e) 조직을 나타내게 된다. 따라서 어떤 화강암에 퍼 다이트와 역퍼다이트 구조를 가지는 장석이 공생하고 있으면 이 암석은 수증기압이 5000 기압 정도인 지하 약 20km 의 깊이에서 형 성되었음을 추측할 수 있게 한다. 그림 6.8 은 팔라듐과 텔루륨의 2 성분계 상다이어그램으로서 Pd11Te i, Pd,Te J은 저자에 의해 처음 발견한 신종 화합물이다. 이 상다이어그램에 나타나 있듯이 ko tu ls kit e(PdTe) 와 merens kyit e(PdTe2) 는 680~@·c 범 위에서 PdTe-PdTez 고용체로서 존재하다가 @·c 이하에서는 용리를 일으켜 퍼다이트 조직을 나타냄울 발견하였으며(그림 6.9), 이런 조직은 남아프리카공화국의 Merensky Reef, 미국 몬태나주의 Sti llwa te r Com p lex 에 있는 백금 광상의 광석 광물에서도 발견되었다(그림 6.10 ).
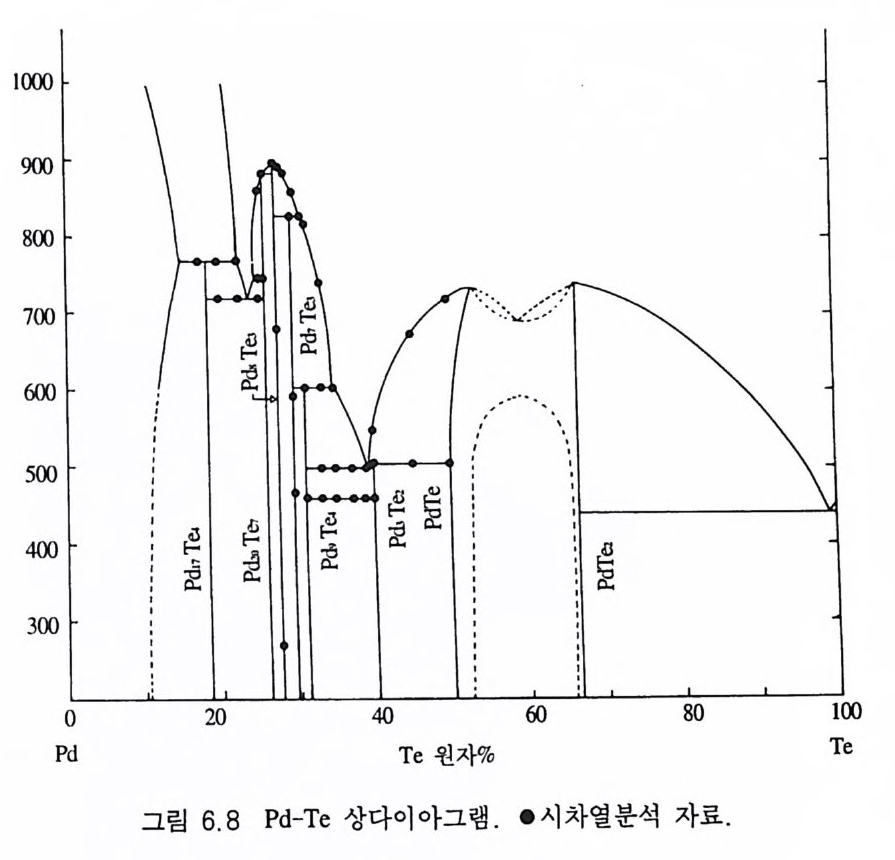 ICXXl
ICXXl
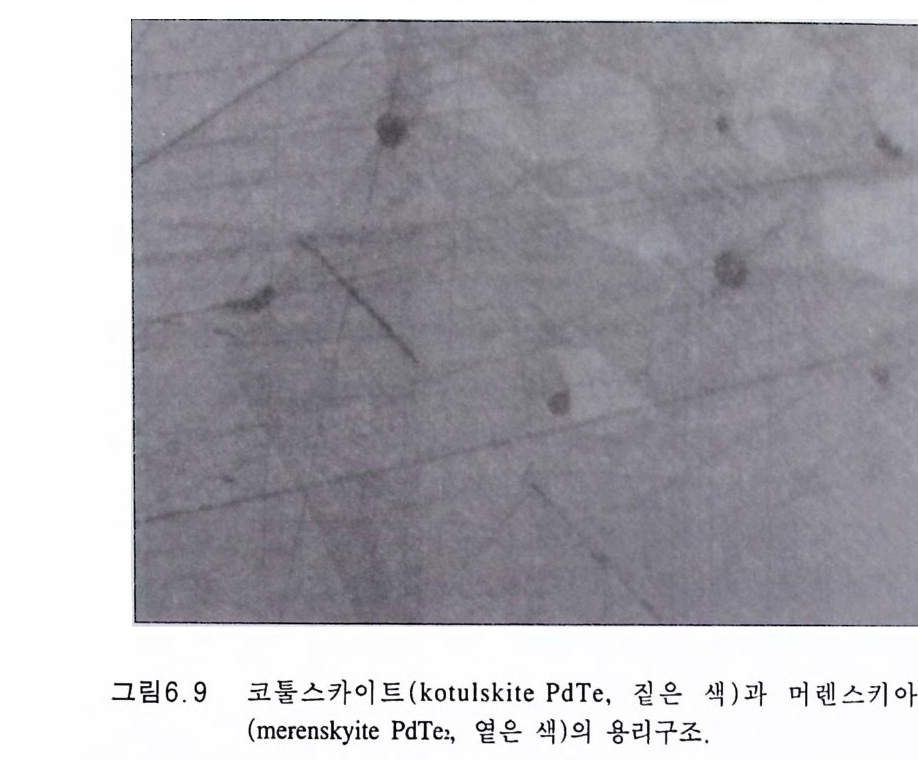 그림 6.9 코툴스카이트 (ko t ulsk it e PdTe, 짙은 색)과 머렌스키아이트
그림 6.9 코툴스카이트 (ko t ulsk it e PdTe, 짙은 색)과 머렌스키아이트
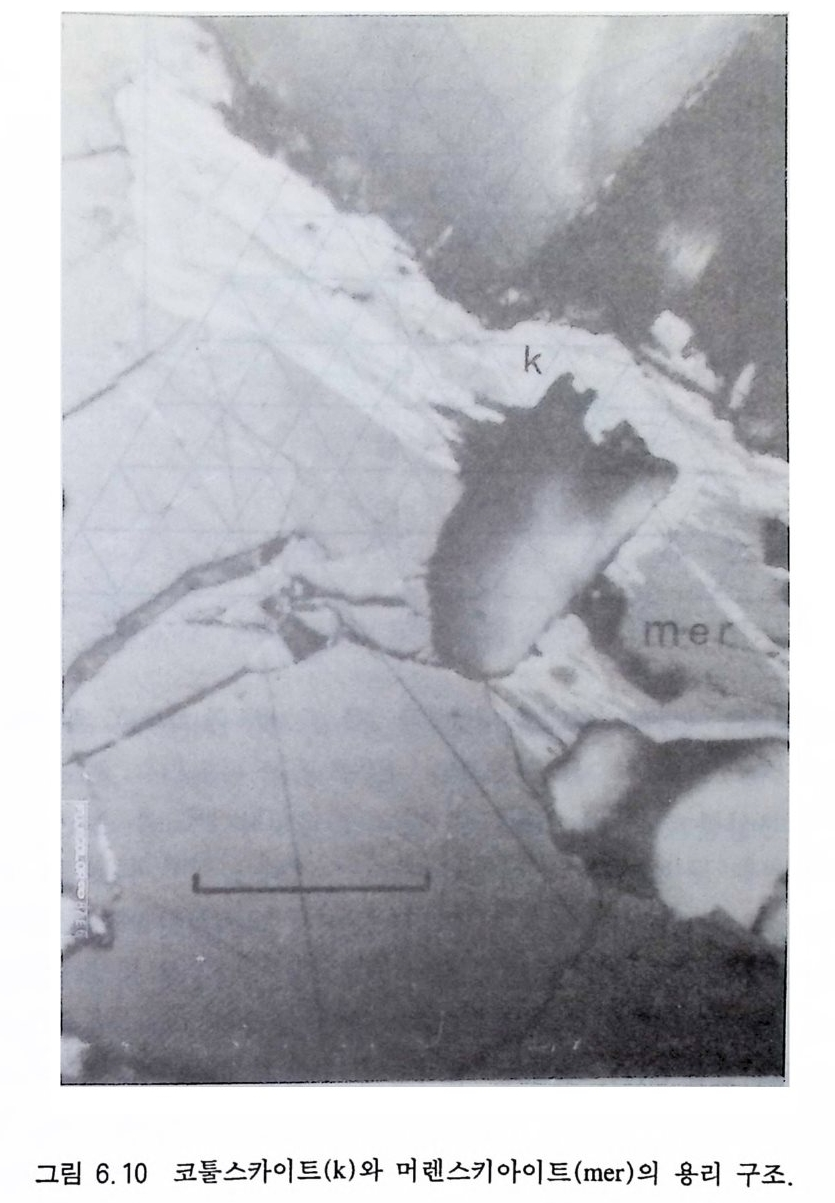 그림 6. 10 코툴스카이트 (k) 와 머렌스키아이트 (mer) 의 용리 구조.
그림 6. 10 코툴스카이트 (k) 와 머렌스키아이트 (mer) 의 용리 구조.
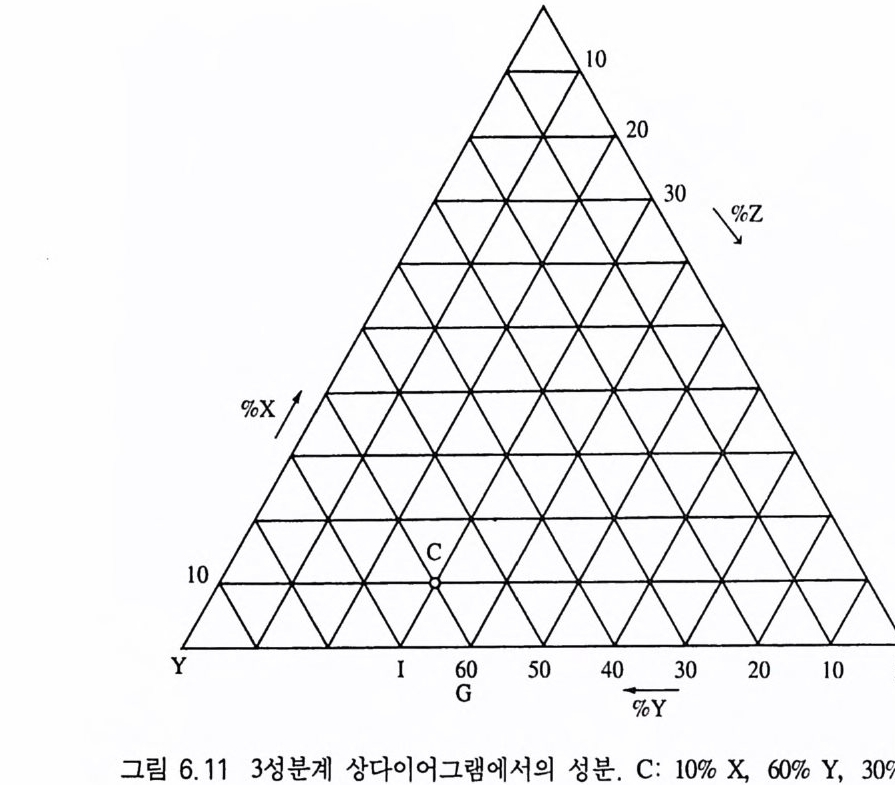 Y 60G 50 40 30 20 10 z
Y 60G 50 40 30 20 10 z
6.4 3 성분계 상다이어그램 3 성분계 상다이어그램은 정삼각형 도면에 나타내며 세 꼭지점에 각 성분을 표시한다. 3 성분계 상다이어그램은 일정한 압력 조건에 서의 상평형 관계를 나타내는데, 성분은 삼각형 내의 한 점으로 표시한다(그림 6.1 1). 온도는 삼각형에 수선을 그어 나타내는데(그 림 6.1 2 ) 이를 평면도로 나타낼 때에는 등고선과 비슷한 등온곡선 (그림 6 .1 3) 으로 표시한다. 3 성분계 상다이어그램의 세 변은 2 성분 계 상다이어그램을 기초로 작성되는 것인데(그림 6.1 4 ), 삼각형 내 의 굵은 곡선인 경계곡선 (bound ary curve) 은 2 성분계의 공융점을 3
 A_'|
A_'|
성분계로 표현시킨 것으로서, 두 개의 광물과 액체가 공존하는 최 소 온도를 나타내는 골짜기라고 이해하면 된다. 3 개의 경계곡선은 가장 낮은 온도에 해 당하는 3 성 분 공융점 (ter na ry eute c ti c poi n t) 에 서 만나게 된다 . 이 점에서는 F=O 이며 액체가 다 소비될 때까지 3 개 의 광물이 동시에 정출하게 된다. 만약 그림 6 .1 3 처럼 광물끼리 고용체를 전혀 형성하지 않는 계에 서 온도 하강에 따라 일어나는 변화에 대하여 알아보자. 그림 6.1 5 에서와 같이 A 성분을 가지는 액체의 온도가 내려 가면 규회석이 정출되고 액체의 성분은 규회석을 나타내는 꼭지점으로 부터 멀어 지는 방향으로 변하게 된다. 규회석이 정출함에 따라 액체의 성분 은 B 를 거쳐 D 로 옮겨 가게 된다 . 만약 액체의 성분이 A 로부터 B 로 변하였을 경우 규회석과 액체의 양적 비율은 각각
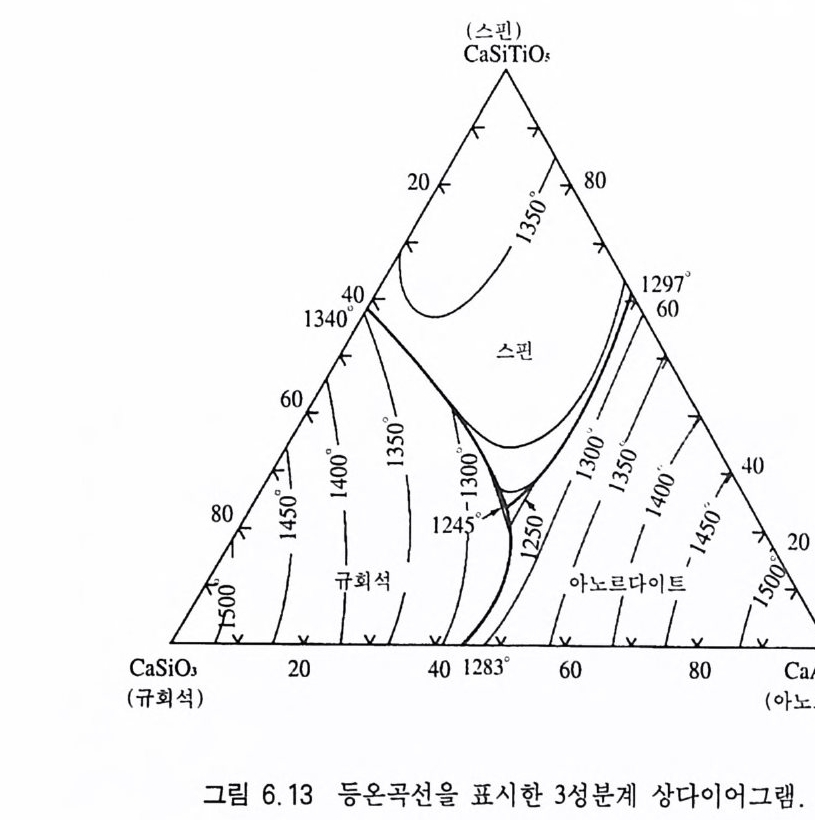 (스핀)
(스핀)
규회석 = CABB X l()()=34% 액 체 = CCBA X l()()=66% 가된다. D 에서는 규회석 뿐만 아니라 스핀도 액체로부터 정출하기 시작 하며, 액체의 성분은 3 성분 공융점 (E) 으로 이동하게 되고 여기서 는 아노르다이트까지 정출하면서 액체가 완전히 소비된다.
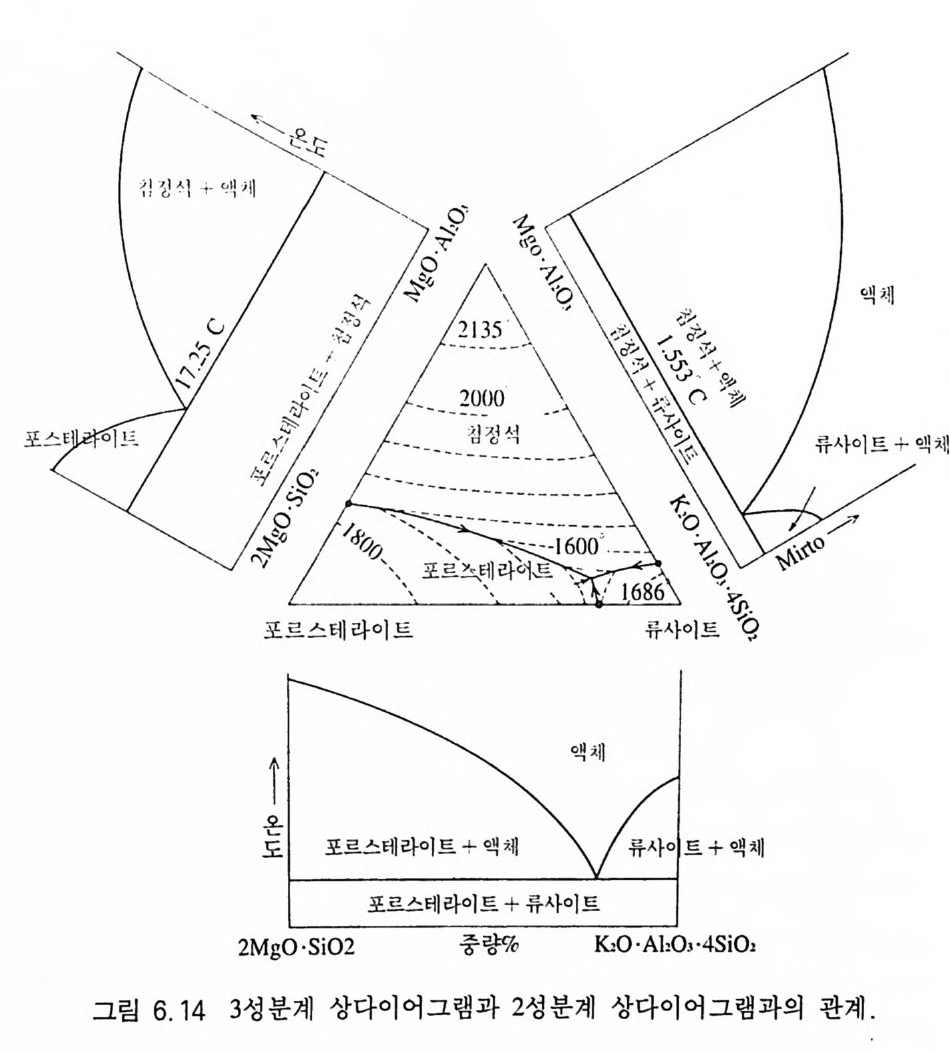 \``\
\``\
 스핀
스핀
만약 계에 존재하는 세 광물 중 2 개가 완전고용체 를 형성하는 경우는 다소 복잡해 진다 . 투휘석-앨바이트-아노르다이트 사장 석을 함유하는 3 성분계를 예로 들면(그림 6.1 6 ), 앨바이트와 아노 르다이트는 완전 고용체를 형성하고 있다. 경계곡선 (e - e ' ) 은 투휘 석과 아노르다이트의 공융점 (e) 온도 (l275 ° C) 에서 최대가 되고, 투 휘석과 앨바이트의 공융점 (e' ) 온도 (11oo·c) 에서 최소가 된다 . 이 상다이 어 그램 을 Boo·c 와 12oo·c 로 분리 시 켜 그리 면 각각 그림 6.1 7 , 그림 6 .1 8 과 같다. 그림 6 .1 7 에서 X 의 성분을 갖는 액체는 13oo • c 에서 s 성분의 액체와 j 성분의 사장석과 공존하게 되며, w 성분의 사장석은 a 성분의 액체와 공존한다 . 온도가 더 내려가
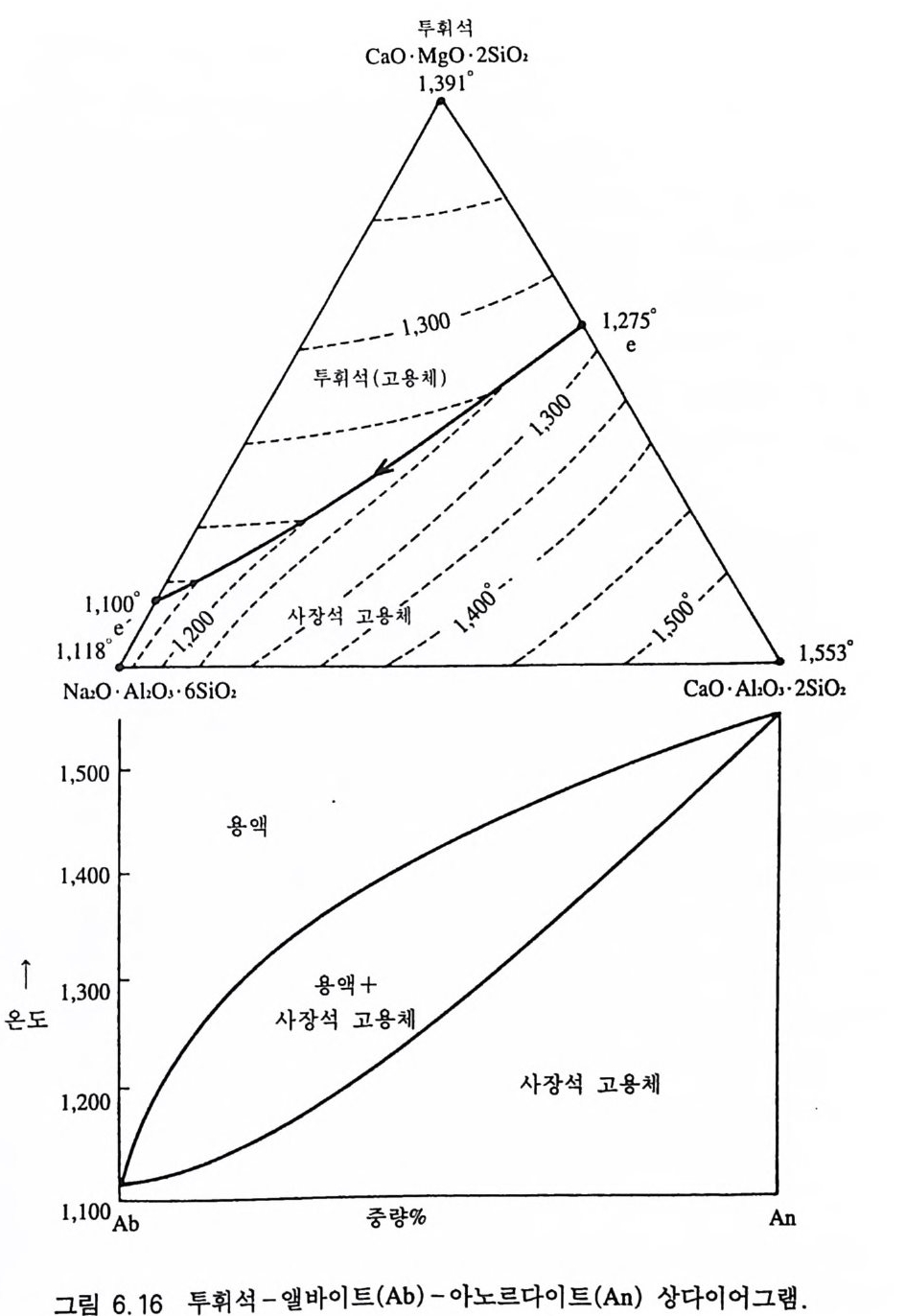 투휘석
투휘석
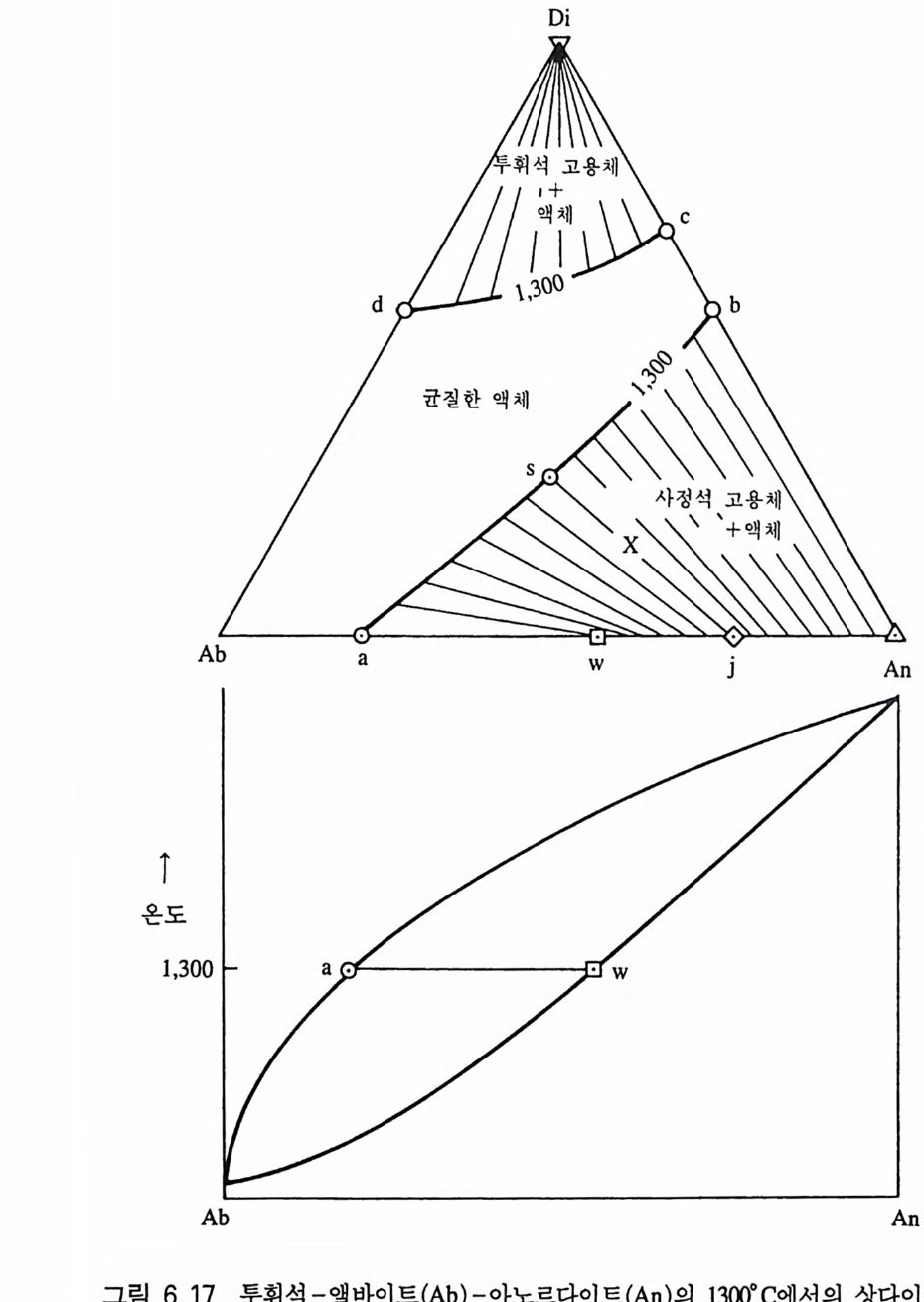 Di
Di
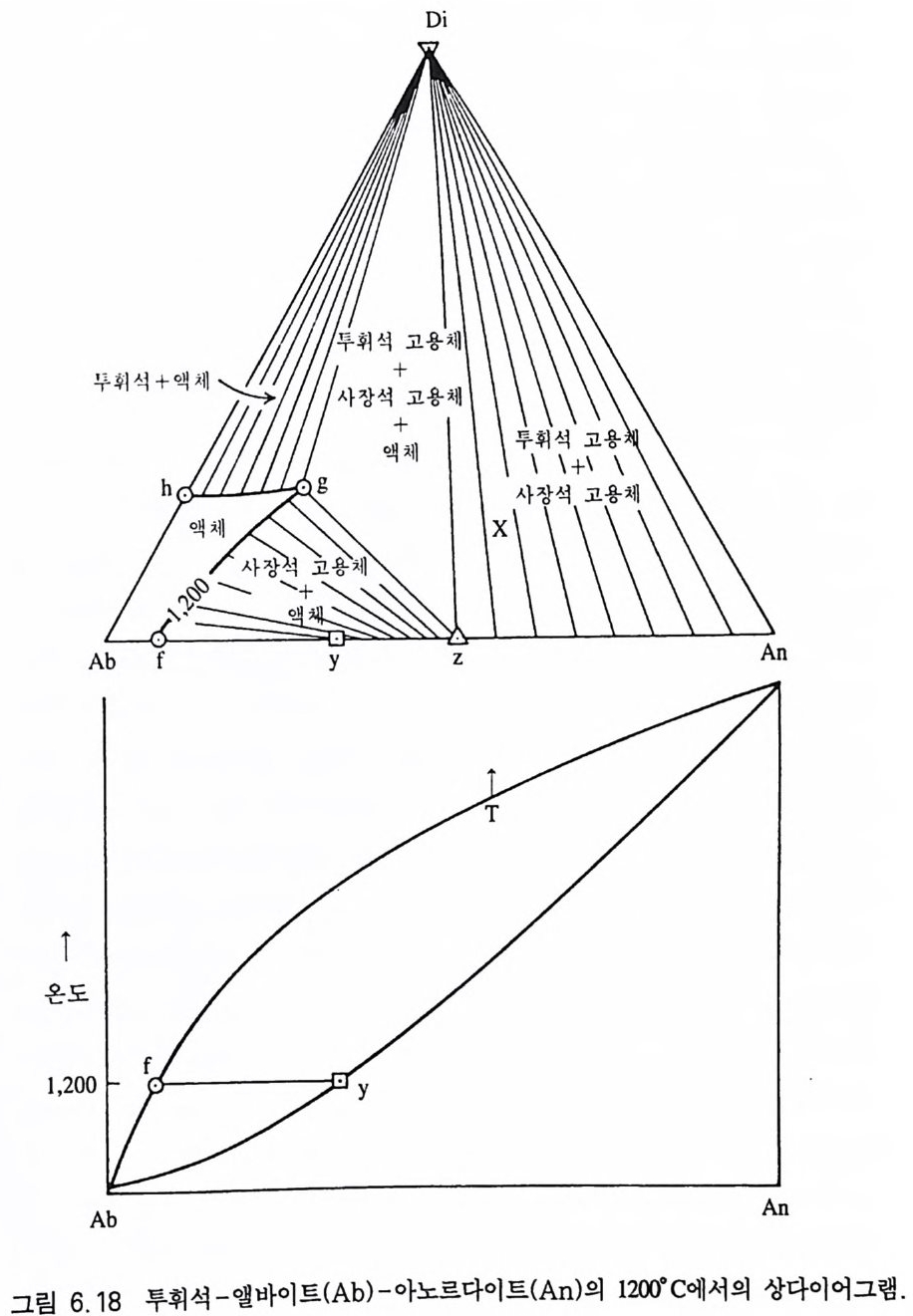 Di
Di
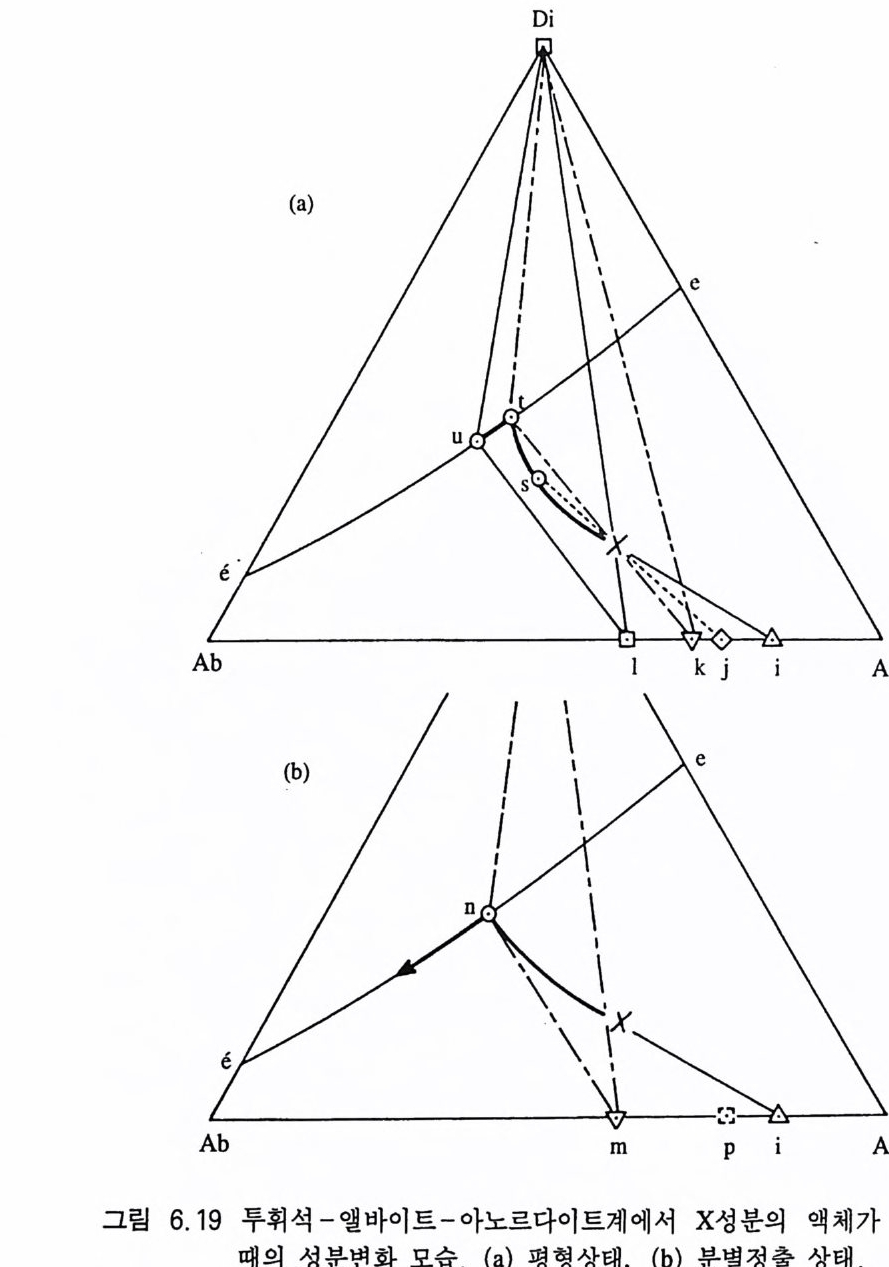 Di
Di
12oo·c 가 되면 투휘석과 사장석만이 공존하고 액체는 없어 지게 된다. 이러한 현상을 그림 6.19 를 통해 알아보자. 우선 X 성분의 액체가 14oo·c 로 냉각되면(그림 6.1 6 ) i 성분의 사장석을 정출하기 시작하며, 따라서 액체의 성분은 X t로 표시되는 곡선을 따라 변화 하게 된다. 액체의 온도가 계속 13oo·c 로 떨어지면 s 성분의 액체 와 j 성분의 사장석이 공존하게 된다(이음선 sj) . 온도가 계속 하강 하면 액체의 성분은 t로 이동하고 이때 공존하는 사장석의 성분은 k 이다 이 온도에서는 액체 내의 투휘석 성분이 포화되어 비로소 투휘석이 동시에 정출된다. 액체는 u 의 성분에 도달하여 l 성분의 사장석을 정출시키면서 완전히 소멸하게 된다. 다른 예 로서 투휘 석 (CaMg S ii 06 ) - 포르스테 라이 트 (M g 2S i 04) -석 영 (S i 02) 으로 구성되어 있는 계의 경우(그림 6.2 0 ), X 성분을 가지 는 액체(마그마)가 냉각될 때 일어나는 변화에 대해 알아보자. X 성분의 엑체는 먼저 포르스테라이트를 정출하게 되고 그 결과 액 체의 성분은 포르스테라이트 성분으로부터 멀어지는 방향으로 변 하며, 결국 경계곡선 AB 에 도달하여 휘석을 함께 정출시킨다 . 평 형상태에서는 포르스테라이트가 불안정하기 때문에 이미 정출된 포르스테라이트는 액체와 계속 반응하여 상당수의 포르스테라이트 가 재용융되고 그 대신 휘석을 정출시키게 된다. 휘석이 정출됨에 따라 액체의 성분은 경계곡선을 따라 변화하게 되는데 휘석 내의 M g성분을 치환할 수 있는 Ca 성분은 한계가 있으므로 어느 단계 에서는 두 종류의 휘석이 생기게 된다. 결국 최종 단계에서는 포 르스테라이트와 두 종류의 휘석이 공존하는 암석이 만들어지게 된 다. 이러한 현상은 Mg 2S i 0 4-A-B 영역 내에 속하는 성분을 지닌 액체에서는 동일하게 일어난다. 한편, Y 성분의 액체는 처음 포르스테라이트를 정출시키고 그에 따라 액체의 성분은 CD 에 도달하게 되고 Ca- 휘석이 함께 정출하
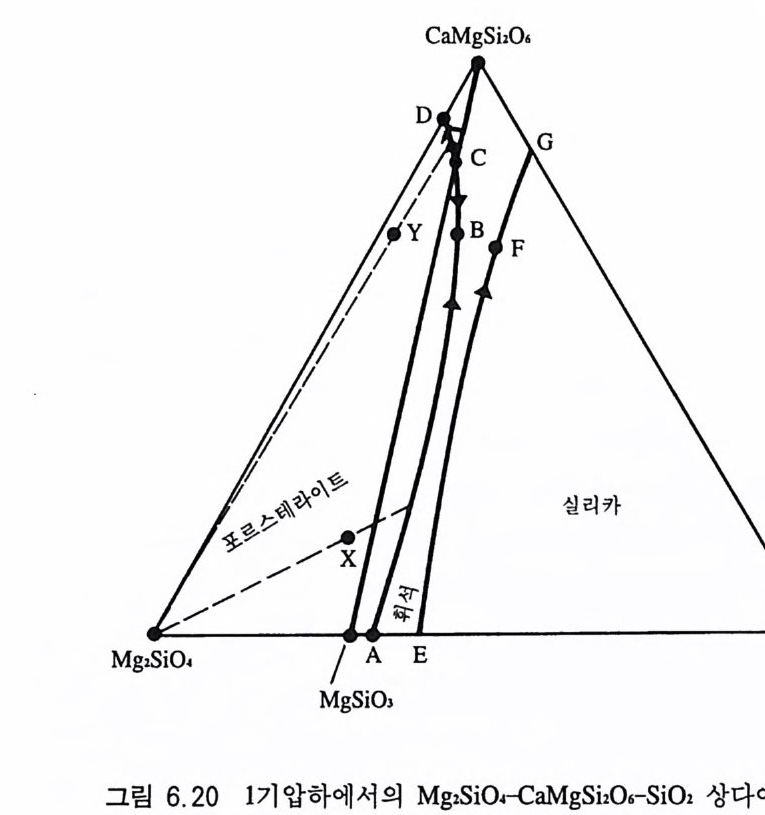 CaMg Si , O ,
CaMg Si , O ,
게 된다. 그러나 포르스테라이트는 안정하기 때문에 액체로 재용융 되지는 않는다. 결국 액체의 성분은 D 로 이동하게 되고 포르스테라 이트와 ca-휘 석이 안정하게 공존하는 암석이 만들어진다. 실제로 X 성분은 톨레아이트질 마그마(th ole iti c ma gm a) 를 나타내 는 것으로서 톨레아이트질 현무암에는 포르스테라이트와 두 종류 의 휘석이 공존하고 있음을 알 수 있다. 그리고 다수의 포르스테라 이트 결정의 외곽 부분에 용해된 혼적이 남아 있다. Y 성분의 액체 는 알칼리 감람석질 마그마를 대표하고 있는데, 알칼리 감람석질 현무암에는 감람석과 휘석이 공존하고 있으며 감람석 결정에 용식 된 현상이 없다.
참고문헌 기초과학지원연구소(1 995), EPMA 분석의 원리와 응용, 74p . 김수진(1 996), 광물과학. 우성문화사, 593p . 김 원사(1 992), 보석 학. 우성 문화사, SSlp. 정지곤, 김원사, Watk ins on, D.H.(1 9 89), 하동지역에 분포한 회장 암질암의 구조와 티타늄광체의 산출상태, 지질학화지 , 98-111. 박기채 (19 91 ), 기기분석의 원리, 탐구당, 851p . 유병설, 박만기 (19 85), 기기분석, 동명사, 483p . 이대운, 이항, 김영상, 김택제(1 985), 기기분석, 549 p. 이 민성 (19 88), 화성 암 성 인론, 민음사, 240 p. 채명준, 이후성, 김하석 (1989), 기기분석, 830 p. 최규원, 박기채, 이길상(1 963), 기기분석, 탐구당, 389 p. Bail ey , S. W. (1984), An int r o ducti on to the meth o d of op tica l cry st a llog rap h y , Holt, Rine ha rt and Wmsto n , 294p . Ba ile y, S. W. (1984), Mica s, Miner alog ica l Soci et y of Ameri ca , 584p .
Bloss, F. D. (19 61), An int r o ducti on to the meth o d of op tica l cry st a llo g ra ph y , Holt R ine ha rt and Wi ns to n , 294p . Bloss, F. D. (19 71), Cry s ta ll og rap h y and cry s ta l chemi str y , Holt, R ine ha rt and Wins to n , Inc., 545p . Brownlow, A. H. (19 79), G eochem istr y , P rentic e -Hall, I nc., 498p . Cull ity, B. D. (19 78), Elements of X -ra y dif frac ti on , Addis o n-Wesley Publish i ng Co., 553p . Deer, W., Howi e, R . and Zussman, J. (19 80), An int r od ucti on to the rock forming mine rals, Long m an Ltd . , 528p . Doe, B. (19 73), Lead iso to p e , Sp ring e r , 137p . Ehlers, E. G. (1972), The int e r p re ta t io n of geo log ica l ph ase dia g r a ms, W. H. Freedom and Comp an y, 280 p . Ernst, W. G. (1976), Petr o log ic pha se equ i l ibr i a, W.H. Freedom and Comp an y, 333p . Evans, R. C. (1966), An introd ucti on to cry st a l chem istr y , Cambrid g e , 410 p. Faure, G. and Powell, J. (1973), Str on ti um iso to p e geo log y, Sp ri n g e r , 188p . Ferr y, J. M. (1982), Characte r i za tio n of meta mo rp hism thr oug h mi ne ral equ i l ibri a , 397p . Goresy, A (1976 ), Ox ide mine rals, South e rn Printing Co., 5 6lp. Hutc h i so n, C. S. (1974), Laborato r y handbook of pet ro g r ap h ic t ec hniq u es, Joh n Wi ley & Sons, 527p . Goresy, A., Hagg e rty , S. E., Lin d sley, D. H. and Rumble, D. (1976), Ox ide miner als, Miner alog ica l Soci ety of Ameri ca , 30lp. Gribb le, C and Hall, A. J. (1992), O p tica l mine ralog y: Pri nc i ple s and pra ctic e , UCL, 280 p .
Kerr, F (19 59), Op tica l mi ne ralog y, McGraw —H i ll Book Co., 442p . Ki m, W. S., Chao, G. Y. and Cabri , L. J. ( 19 90), Phase relati on s in the Pd - Te sys te m , J. of Less -C ommon Meta l s, 162, 61 -74. Klein , C. and Hurburt , C . S. (19 71), Manual of mine ralog y, Joh n W iley & Sons, 596p . Morse (1980), Basalts a nd ph ase dia g ram s, Sp ring e r-Verlag. Phil lips , F . C. (19 71), An int r o ducti on to cry s ta ll og rap h y, Long m an, 351p . Prewi tt, C. T. ( 1982), Py ro xenes, Mi ne ralog ica l Socie ty of Ameri ca , 525p . Reeder, R . J. (19 83), Carbonate s : mi ne ralog y and chem istr y , Mi ne ralog ica l Socie ty of Ameri ca , 394p . Ri bb e, P. H. (1982), Or tho sil ic a te s , Mi ne ralog ica l Socie t y of Ameri ca , 450 p. Ri bb e, P. H. (19 83), Feldsp a r mi ne ralog y, Mi ne ralog ica l Socie t y of Ameri ca , 362p . Smy k atz -K loss, W. (19 74), Di ffere nti al the rmal analys i s , Sp ring e r - Verlag , 185p . Veblen, D. R. (19 81 ), Amp h ib o les and oth e r hy d rous pyri b o les - mine ralog y, Mi ne ralog ica l Soc iet y of Ameri ca , 372p .
찾아보기
-l 가시광선 31 각섬 석 16, 20, 233 각섬 석 군 195, 217 간극 고용체 79 간섭상 123 간섭색 120 갈렴석 248 감람석 14, 20, 35, 188 감람암 21,82 강옥 20,92 개형 58 견운모 268 결손 고용체 79 결정 투영 63 결정의 3 요소 38 결정축 46 결정형 52 경도 91 경사소광 113 경석고 332 경옥 36,209 고상선 393 고온석 영 159, 162 고용체 74 고체 불순물 38 공융점 395 공작석 35 광물 13 광물각론 159 광물학적 상률 389 광역 변성작용 26
광축 lITT 광축각 141 광학부호 134 교결작용 22 구루너라이트 227 구면투영 63 구조수 85 규산염 광물 82, 152, 159 규선석 263 규선석군 259 규암 27 규회석 214 그로슐라 210 그로코크로아이 트 186 그리디론 구조 171 근청석 190 글루코페인 234 금운모 20,271 금홍석 20, 309, 319 기계적 풍화작용 21 기브사이트 348 Gi bbs 의 상률 288 기저 역암 24 L 남정 석 91, 261, 264 네펠린 20, 179 녹니석 188 녹니석군 278 녹렴석 246 녹렴석군 243 누대구조 400
능망간석 35,3 1 5 능철석 314 E: 다색성 110 다색성 훈 276 다이아몬드 10 다이아스포 338 다져짐 작용 22 단구 90 단면형 54 단백석 159 단사정계 51,68, 109 단사휘석 192 단쇄형 구조 153 단위포 상수 62 단종 75 단형 59 대리암 27 대상구조 16 대칭 39 대칭면 39 대칭소광 113 대칭심 39 대칭조작 39 독립사면체형구조 153 동력 변성작용 25 동질 이 상체 159, 188, 390 듀나이트 189 드라바이트 288 동방성 104 둥측정 계 49, 68, 109
등화 학 변성작용 26 근 라브라도라이 트 16, 165, 176 라이 자다이 트 188, 2 56 라이트법 145 라쥬라이트 35 레피 돌 라이트 276 루 벨 라이트 288 루비 36, 2 9 3 류사이트 20, 181, 39 6,4 1 1 리베카이트 234 □ 마그네사이트 312 말타이트 297 망상형구조 156 맬러드법 142 머렌스카이트 406 멀티법 149 멜리라이트 184 모나자이트 342 모스경도계 91 몬조나이트 21 몬티셀라이트 186 미사장석 20, 170 밀러지수 59 1::1 바스터마이트 213
바이 타우나이 트 16, 165, 177, 399 반려암 21 반상조직 18 반정 18 방해 석 92, 103, 308 백색광 31 백연석 321 백 운모 16, 20, 268 백운석 322 백운암 189 벽개 87 변성암 25 변성작용 25 변종 288 보에마이트 339 복굴절 107 복사면체형구조 153 복쇄형구조 153 볼링가이트 188 부룩카이트 296 부분 고용체 75 분광기 34 분말가압 성형법 356 분별정출작용 400 불연속 고용체 75 브론자이 트 192, 197 비 58 비정질 105 비조화용융 397 비중 87 비취 209
人 사문석 188, 252 사방정 계 50, 68, 109 사방훼 로실 라이 트 192 사방휘석 192, 197 사아드 164 사암 24 사장석 20, 165, 172 사파이어 36,293 산화염 광물 156 삼방정 계 52, 68, 109 32 정족 67 삼사정 계 51, 68, 109 삼색성 111 상광선 107 상률 388 상평형 387 새니딘 20, 168 색 31, 33, 110 석고 92,329 석고층 22 석기 18 석류석군 20,236 석 영 16, 20, 9 2, 159 석회암 22,24, 189 선택흡수 34 섭록암 21 섬아연석 81 섬장암 21 세란다이트 213 세루사이트(백연석) 321 세립질 19
셀레스타이트 327 셰일 24 소광 112 소광각 112 소달라이 트 20, 182 수박석 288 수산화염 광물 157, 335 스넬의 법칙 103 스콜 288 스테레오 망면 65 스트론티아나이트 320 스티 쇼바이 트 159, 164 스페르샤르틴 35, 240 스펙큘라이트 207 스포듀민 210 스피넬 36 스핀 20 시차열분석 369 심성암 17 쌍쌍치환 167 。 아게이트 164 아나타제 3CJ 7 아노르다이 트 165, 178 아노르도클레 이 즈 165 아노르타이트 16 아라고나이트 316 아이소자 123 아이소크롬 123 아쭈라이트 35 아쿠아마린 36
아크로아이트 288 안데신 16, 165, 176 안드라다이트 241 알렉산드라이트 36 알루나이트 334 알만딘 35,239 알바이트쌍정 171 알칼리장석 166 알칼리휘석 192 암염 22 앙글레사이트 328 액상선 393 앤소필라이트 225 앤티고라이트 188, 25 5 앨바이트 16, 165, 173,4 1 3 양기석 85,229 양추 58 어 자이 트 20, 192, 2 03 에너지분산 스펙트럼법 353 에데나이트 217 에머랄드 36 에지 린 20, 202, 199, 2Cf7 Gi bbs 의 상률 388 X 선 형광분석 356 X 선 회절분석 375 엔스터 타이 트 197, 200 역암 23 역퍼다이트 166 연속고용체 75 열개 89 엽리 26 오닉스 164 올리 고클레 이 즈 16, 165, 175
올소페로실 라이 트 197 음파사이트 192 완전고용체 398 요곡성 268 용리 402 용암 19 용융법 357 우바로바이 트 35, 240 운모군 265 운모류 20 울보스피넬 303 원소광물 72 원자흡수분광분석 360 위더라이트 318 육방정 계 52, 69, 109 율라이트 198 이딩사이트 188 이방성 106 이상광선 107 이상화학식 73 이색성 111 이축성 109, 121 이화학 변성작용 27 인디콜라이트 288 인산염 광물 158, 340 인회석 20,92,340 일반화학식 73 일반흡수 34 일축성 109, 120 x 자수정 36
자철석 20,303 잔류색 33 장미휘석 35,213,216 장석군 165 장축부호 119 재결정작용 26 재스퍼 164 저어콘 20,282 저온석영 159 적색스피넬 36 적외선흡수분광분석 365 적철석 20,293 적철석군 292 전기석 286 전자기스펙트럼 32 전자기파 31 전자현미분석기 350 접 촉변성 작용 25, 27 정 방정 계 49, 68, I()I) 정십이면체 58 정육면체 58 정 장석 20, 36, 92, 169 정팔면체 58 제이다이트 199,208 조립질 18 조암광물 13,103 조암광물의 분류 151 조이사이트 250 조화용융 393 주 58 주사전자현미경 347 준장석군 178 준휘석군 212
중립질 16 중정석 325 증발암 25 天 차모사이트 281 천매암 29 철광상 22 첨정석 301,4ll 첨정석군 300 추 58 축률 62 취형 59 층상형구조 156 치환고용체 75 침철석 35,339 7 정계 49 구' 칸크리나이트 184 칼리장석 66,165 칼세 도니 159, 164 칼시라이트 181 캠스법 145 커밍토나이트 227 코넬리언 164 코에사이트 159, 163 코툴스카이트 406 쿤자이트 210 크네베라이트 186 크롬칠석 305
크리소콜라 35 크리소타일 188,253 크리소프레이즈 36, 164 크리스토발라이트 159, 163 클리 노조이 사이 트 243 클리노클로 278 E 탁 54 탄산염 광물 157, 309 탄자나이 트 36, 245 탈수작용 22 터키석 35 테프로아이트 186 토비법 145 토파즈 36,92 톨레 아이 트질 마그마 197 퇴적암 20,22 투각섬석 229 투휘석 197,202,413 툴라이트 245,251 트리디마이트 159, 162 티 탄철석 20, 297, 299 工 파가사이트 217 파동소광 117 파사마이트 192 파이로프 238 파이록망가이트 213 파장분산스펙트럼법
파티컬러 288 판암 27 퍼다이트 166 페니나이트 280 페로실라이트 197 페로하이퍼신 192 페리도트 190 페리클라인쌍정 l71 페 이 알라이 트 186, 191 펙토라이트 213 편마암 29 편암 28 평행소광 113 폐형 58 포르스테라이트 186, 190,411 표축비 62 풍화작용 21 프레이즈 164 프로클로라이트 282 피드몬타이트 248 피 지 오나이 트 192, 197, 205 궁 하이 드로그로슐라 242 하이퍼신 20, 192,201 할로겐광물 344
헤 덴버 가이 트 197, 2fJ7 현정질 14 형석 92,344 호른펠즈 27 홍렴석 247 홍주석 262 화강섬록암 21 화강암 21 화산암 18 화성암 14 화학적 풍화작용 21 환형구조 153 활석 92, 188 황동석 81 황산염 광물 87, 157 황수정 36 황옥 284 황철석 20,81 황화광물 80 회반측 42 회영축 45 회장암 21 회전축 39 휘석 15, 84 휘석군 15,20, 192 혹운모 15,223 흡수 33 흡착수 85 히데나이트 210
김원사 서울대학교 지질학과 졸업(이학사) 캐나다 칼톤 대학교 대학원 지질학과 졸업(이학석사, 이학박사) 독일 하이델베르크 대학교 객원교수 캐나다 광물연구소 객원교수 현재 충남대학교 지질학과 교수 저서 『 보석학 .!l 『 지구환경과학 』 등 다수 조암광물학 대우학술총서 • 자연과학 132 1 판 1 쇄 펴냄 -1998 년 12 월 30 일 지은이 ~~김원사 펴낸이 -박맹호 펴낸곳 - (주)민음사 출판등록 1966. 5.19. 제 1 6-4 90 호 135-120 서 울시 강남구 신사동 506 대표전화 515-2000 팩시밀리 515-2007 값 25,500 원 ® 김원사, 1999 자연과학, 광물학 KD0460 Prin t e d in Seoul, Korea ISBN 89-374 -36 32-9 94460 89-374 -30 0 0-2 (세트)
1 대우학술총서 1 자연과야 IO I
1 소립자와 게이지 상호작용 김진의 2 동력학특론 이병호 3 질소고정 송승달 4 상전이와 임계현상 김두철 5 촉매작용 진종식 6 뫼스바우어 분광학 옥항남 7 극미량원소의 영양 숭정자 8 수소화봉소와 유기붕소 화합물 윤능민 9 항 생물질의 전합성 강석구 10 국소적 형태의 Ati ya h-sin g e r 지표 이 론 지동표 11 Muc op ol y s accha r i des 의 생화학 및 생물리학 박준우 12 천체물리학 홍승수 13 프로스타글라딘 합성 김성각 14 천연물화학연구법 우원식 15 지방영양 김숙희 16 결정화유리 김병호 17 고분자에 의한 화학반응 조의환 18 과학혁명 김영식 19 한국지질론 장기홍 20 정보이론 한영열 21 원자핵반응론 정운혁 22 파괴역학 김상철 23 분자궤도 이론 이익춘 24 반응속도론 정경훈 25 미분위상수학 이현구 26 자기공명방법 조성호 27 풀라스마 물리학과 핵융합 최덕인 28 천문관측과 분석 이시우 29 석탄에너지변환기술 김상돈 30 해양미고생물학 백광호 31 편마분방정식론 김종식 32 대통일 이론 소광섭 33 금속전자계의 다체이론 김덕주 34 액정중합체 진정일 35 복합재료권 숙인 36 단백질 생합성 박인원 37 한국의 광물종 김수진 38 일반상대론 이철훈 39 레이저 광산란 분광학 김종진 40 복소다양체론 김상문 41 역학적 연구방법 김일순 42 핵구조물리학 민동필 43 후리에 해석과 의미분 작용소 김도한 44 한국의 고생물 이하영
45 질량분석학 김명수 46 급변론 박대현 47 생체에너지 주충노 48 리이만 기하학 박을룡 49 군표현론 박승안 50 비선형 편미분 방정식론 하기식 51 생체막 김형만 52 수 리분류학 고철환 53 찰스 다윈 정용재 54 금속부 식 박용수 55 양자광학 이상수 56 효소반응 속도론 서정현 57 화성암 성인론 이민성 58 확률론 구자홍 59 분자분광학 소현수 60 벡터속 이론 양재현 61 곤충신경 생리학 부경생 62 에너지띠 이론 모혜정 63 수학기초론 김상문 64 신 경 과학 김승업 박찬웅 65 BCH 부호와 Reed- So l omon 부호 이 만영 66 양자 전기역학 김영덕 67 군환론 박재걸 68 대수기하학조영현 69 양자장이론 이재형 70 해양오염과 생태계 심재형 71 비기체 연소합성 ( SHS ) 여철현 72 크로마토그래피 이대운 73 곤충의 사회행동 추종길 74 동위원소 지질학 김규한 75 X- 선 결정학 김양 77 통계역학조순탁 78 고분자의 구조와 형태학 이석현 79 LC 에 의한 광학 이성질체의 분리현명호 80 신경전달물질 서유헌 81 발생과 유전자 발현 이양립 82 스테로이드 화학 김완주김득준 83 다체계론엄정 인 84 중핵반응론 김병택 85 비가역 열역학 이철수 86 등각장론임 채호 87 방사선생물학 남상열 88 석유지질학이용일 89 베르누이 시행의 통계적 분석 배도선·김성인 90 신경세포생리학 강만식
91 생리활성을 가진 C-P 화합물의 화학 김용준 강익중 92 생물유가화학 서정헌 93 조직배양 김승업 94 유기전이금속화합물 조남숙 외 95 실내환경 과학 김윤신 96 유한요소법 정상권 97 대수적 위상수학 우무하 김재룡 98 파인만 적분론 장건수 99 응용 미생물학 박무영 100 리보플라빈 이상선 101 노화 김숙희 김화영 102 매트릭스 격리분광학 정기호 103 신경계 조직배양 김승업 104 지구화학 김규한 105 은하계의 형성과 화학적 진화 이시우외 107 액체의 미립화 이상용 108 접토광물학 문희수 109 중국수학사 김용운 김용국 110 퇴적암석학 유강민 우경식 111 로렌츠기하학 김종철 112 몬테카를로 방법의 물리학적 -응 용 김재삼 113 천체역학 최규홍 114 확미분방정식 김재회 115 전자현미경의 원리와 응용 이정용 116 미세구조유체 흐름의 원리 양승만·박오옥 117 고분해능 분자분광학 이상국 118 생명체의 신호전이 채쾌 의 119 고체추진제 노만균 120 군과 조화해석 계승혁 121 인공수정과수정란이식 입경순의 122 인산이노시를 정성기 • 장영테 123 탄화수소의 산화반응 이규완 124 매듭론 고기형 • 진교택 125 빛의 양자이론 이해웅 126 양자유체 4He 엄정인 127 Li e 군의 표현론 양 재현 128 작용소론 노재철 129 조화적분론 박진석 130 위너적분른 장건수 131 유변학문탁진