 인산이노시톨
인산이노시톨 정성기 연세대학교 화학과 졸업 일리노이 대학 화학과 박사 예일 대학 연구원, 연구 교수, 텍사스 A&M 대학 조교수, 스미스 클라인 프렌치 연구소 수석 연구원, 포항공대 응용 생유기 연구소장 현재 포항공대 화학과 교수, 포항공대 기초과학 연구소장 장영태 포항공 대 화학과 졸업 포항공대 화학과 석사 포항공대 화학과 박사 번역서 『 페니실린을 찾아서 』
 인산이노시톨
인산이노시톨
 인산이노시톨
인산이노시톨
 부모님과 가족들에게 고마움을 전합니다 .
부모님과 가족들에게 고마움을 전합니다 .
머리말 미오이노시톨 (my o-Inos it ol) 은 포도당과 같은 분자식 (C6H1206) 을 가 지는 구조 이성질체로서, 1850 년 Scherer 에 의해 심장 근육으로부터 처 음 추출되 었고 1914 년 W iel and 등에 의 하여 최초로 합성되 었다 . 현대 유기 화학의 기준에서 본다면 이노시톨 자체는 분자의 크기나 모양에 서 빈약한 느낌을 줄 정도로 간단한 분자이다. 1930-1 %0년대에는 당 시 관심사였던 입체 화학 (s t ereoche mi s try)과 형태 (co nfo rma ti on) 연구의 대상으로 이노시톨에 대한 연구가 활발하게 수행되었고, 이에 대한 대 부분의 화학적 문제는 해결된 것으로 보였다 . 이노시톨 자체뿐만 아니라 1872 년 Pfe ff er 에 의해 처음 분리된 육인 산이노시톨 (my o-Inos it ol hexa kisp h osph ate , ph y tic ac i d) 은 식물의 씨앗 등에 높은 농도로 함유되 어 있으며, 인지 질 이 노시 톨(p hos p ho in os iti de) 온 모든 세포막의 구성 성분이기도 하다. 따라서 생물학자들과 식품 과학자들은 이노시톨의 유도체들을 인의 저장소, 성장 인자 또는 비타 민의 일종으로 생각해 왔다. 그러나 1980 년대 중반 인산이노시톨이 생 체내 신호 전달에 중요한 역할을 하는 2 차 전달 물질 (second messeng er ) 임이 밝혀지면서, 이노시톨의 화학적 생화학적 연구는 다시 활기를 띠 게 되었고 현재 분야를 넓혀가며 르네상스를 구가하고 있다. 사회를 구성하는 개체와 마찬가지로 세포들은 이웃 세포들과 끊임없
는 대화를 유지하고 있다. 세포 수준의 대화에서는 호르몬, 신경 전달 물질 및 분화 인자 (d iff eren ti a ti on fa c t or) 와 같은 화학적 신호들이 주로 이용된다 . 그런데, 대부분의 화학 신호들은 친수성 물질로 지질성의 세포막을 통과하지 못하기 때문에 외부 신호를 세포 내로 전해 주는 신 호 전달 (s ig nal tran sducti on ) 과정이 세포간 대화의 핵심 문제가 된다. 지 금까지 연구된 신호 전달 현상을 크게 보면 이온 통로(i on channel) , 단 백 질 티 로신 키 나제 (pro te in tyro sin e kina se, PTK) 및 GTP 결 합 단백 질 (G- 단백질)을 경유하는 방법 등 3 가지의 신호 전달 체계로 구분할 수 있다 1950 년대에 Rall 과 Su th erland(1971 년 노벨 의학상 수상)는 아드레날 린의 효과가 세포내의 고리인산아데노신 (cAMP) 생성과 연계되어 있음 울 발견하였고, 1970-1980 년대에는 Rodbell 과 G il man(1994 년 노벨 의 학상 공동 수상)이 세포 밖의 수용체와 세포내에서 cAMP 를 형성하는 아데닐레이트 시클라제 사이에 G- 단백질이 연결 고리 역할을 수행함 울 밝혀내어, cAMP 의 2 차 전달 물질로서의 역할이 정립되었다. Berr idg e 등은 1983 년 세로토닌 (5-h y drox ytryptarni ne, sero t on i n) 에 의 하여 곤충의 침샘 내의 칼슘 농도가 증가하는 현상에서 1,4,5- 삼인산 이노시톨〔 m y o-Inos it ol 1,4,5-tri sp h osp h ate , I (l ,4,5)P 니의 2 차 전달 물 질 역할을 밝혔다. 즉, 수용체에 접수된 신호는 G- 단백질을 통하여 포스포리 파제 C (ph osph o lip a se C, PLC) 활성 화로 이 어 지 고, 그 결과로 세포내에서는 IP3 과 디아실글리세롤 (d i ac y l gly c e rol, DAG) 이 형성된다. 생성된 IP3 은 칼슘 농도를 증가시키고, DAG 는 단백질 키나제 C(PKC) 룰 활성화시키는 2 차 전달 물질의 역할을 수행한다 . 세포내에서 생성 된 IP 려 동적 평형은 각종 키나제(kin ase) 와 포스파타제(p hos p ha ta se) 에 의하여 유지되는 것으로 보이나, 이 부분에 대한 정확한 이해는 아직 도 미흡하다. 특히 I(l , 4, 5)P3 이외의 다른 IPn 들의 생리 활성은 아직 분명히 규명되지 않은 상태이고, 일부 IP4 는 세포 외로부터의 칼슘 유
입 에 관여 한다는 제 안이 유력 시 되 고 있다 . IP4 수용체 가 GTPase acti va ti ng p ro t e i n ( GAP) 의 일종이라는 보고와 PLC-P 는 G_ 단백질에 의하여, PLC - y는 수용체 단백질 티로신 키나제에 의하여 각각 활성 화된다는 사실은 세 가지의 신흐 전달 체계 즉, 이온 통로, PTK 및 G - 단백질 경로 간에 상당한 신호 교차가 있음을 시사하고 있다. 다른 한편, 매우 빠른 속도로 진행되고 있는 세포의 신호 전달 현상 연구는 인체의 질병에 대한 이해와 치료제 개발에도 중요한 공헌을 할 것으로 보인다 . GTPase 효과를 가지는 ras 단백질(p 21) 의 돌연변이가 전체 암의 약 25 % 에서 발견되고 있으며, 수용체를 통하여 약리 효과 룰 나타내는 약 50% 의 약물들이 G- 단백질 경로에 관여하는 것으로 추정되고 있다. 따라서 신호 전달 체계의 이상에 기인하는 것으로 보 이는 각종 질병(암, 염증, 신경 질환)에 대한 새로운 치료법의 개발은 이 분야의 화학, 생화학적 연구와 더불어 보다 밝은 전망을 보이고 있다. 본 저서는 새로운 분야인 세포내 신호 전달 현상과 이에 관련된 생 유기화학에 관심을 가진 독자를 위하여 집필되었다. 이 책의 제 1 장에 서는 일반적인 신호 전달 현상과 2 차 전달 물질로서의 IP J의 역할 및 대사에 대해 기술하였다. 2 장에서는 이노시톨의 화학적 구조와 형태 해석을 다루었고, 3 장에서는 이노시톨을 화학적으로 다루는 방법과 특 성들을 기술하였다 . 4 장에서는 최근까지 보고된 인산이노시톨의 합성 경로를 정리하고, 새로운 합성 전략 등을 소개하였다. 5 장에서는 인산 이노시 톨 의 유도체와 유사체의 설계 및 합성을 기술하였다 . 6 장에서는 인산이노시톨과 생체내 수용체 간의 구조 활성 관계와 대표적인 대사 효소들의 억제제 연구에 관한 동향과 전망을 다루었다. 본 저서에서는 1996 년 중반까지의 주요 논문을 포함하도록 노력하였 댜 대학원생이나 이 분야 연구자들에게 새로운 연구 방향을 제시하는 데 도움이 된다면 필자들의 노력이 헛되지 않을 것으로 생각하며, 이 책의 발간을 도와준 대우재단에 감사드린다.
차례
머리말 7제1장 서론1-1 신호 전달 151-2 I(1, 4, 5)P₃ 221-3 이노시톨의 생합성 241-4 이노시톨 인지질 261-5 IP₃ 대사 271-6 IP₃ 수용체 31제2장 이노시톨의 구조 및 형태2-1 이노시톨의 구조 372-2 형태 해석 40제3장 이노시톨의 화학3-1 Diol 보호 483-2 Triol 보호 563-5 인산화 743-6 분광학 813-7 광학 활성의 이노시톨 유도체 823-8 위치 선택성 83제4장 인산이노시톨(IPn) 합성
4-1 합성상의 일반적인 문제점 1074-2 일인산이노시톨 1104-3 이인산이노시톨 127 4-4 삼인산이노시톨 1374-5 사인산이노시톨 1644-6 오인산이노시톨 1734-7 발산적 방법에 의한 인산이노시톨 합성 174제5장 이노시톨 유사체 및 유도체5-1 이노시톨 유사체1855-2 일인산이노시톨 유사체 및 유도체 1895-3 이인산이노시톨 유사체 및 유도체 1905-4 삼인산이노시톨 유사체 및 유도체 1915-5 사인산이노시톨 유사체 및 유도체 201제6장 구조 활성 관계 및 대사 효소 억제제6-1 PI-synthetase 2096-2 Inositol monophosphatase 2136-3 IP₃ 수용체 2176-4 IP₃ 3-kinase 2276-5 IP₃ 5-phosphatase 2326-6 IP₄ 수용체 235부록:이노시톨 유도체들의 물리 및 분광학적 성질•245약어표 1H: 1H-NMR 13C : 13C-NMR JI P : 31p _ NMR Ace : aceto n id e (iso p ro p ylide ne) Anal : elementa l analys i s BOM : benzy lo xy m eth yl Ben : benzy lide ne Bs : benzenesulfo n yl Bt : buty ryl Camp : camp ha nate . CAN : eeri e a mmoniu m nitrat e Carb : 1 -ph eny le th yl earbamate Crot : eroty l DAG : diae yl g l y e e rol DCC : I, 3-die y c l ohexy lc arbodii rnide DDQ : 2, 3 -die h loro -5 , 6 -dic ya no -1 , 4 -benzoq ui n o ne DMF : N, N -d ime th ylf o rm a mide • DMP : 2, 2 -d ime th o xy pro p an e DMSO : dim eth yls ulf ox id e DPPC : diph eny l p ho sph o ehlori da te EA : eth yl aeeta te EE : eth yl eth e r EI : electr on impa et mass spe e tr om etr y FAB : fas t - a to m bombardment mass spe e tr om etr y HRMS : high resouti on mass spe e tr om etr y Hex : eyc l ohex ylide ne I(l, 4, 5)P3 : ino sit ol (1, 4, 5) -trisph o sph a te
MC : meth y le ne chlori de MS : mass spe c tr om etr y Man : acety lm andelate Mnc : menth yl carbonate Mnt : menth o xy ac ety l Mp : meltin g po in t Or th : ort ho fo n nate PE : pet r ol eum eth e r PI : ph osph ati dy l ino sito l Pl(4, 5)P2 : pho sph ati dy l ino sit ol (4, 5)bis p h osph ate Piv : piva loy l (trim eth y la cety l) PLC : ph osph oli pa se C PMB : p -m eth o xy be nzyl Pro : pro p -1 -eny l SEM : (trim eth yls il y l ) eth o xy m eth yl Tar : tartrat e TBDMS : t -b uty ld im eth y ls il yl TBDPS : t -b uty ld i ph eny ls il yl TBPP : tet r ab enzy l pyro p h osph ate TEA : trieth yla m ine Tf : trifluo rometh a nesulf ony l TFA : trifluo roaceti c aci d THP : tet r ah y d rop yra ny l TIPS : 1, 1, 3, 3 -tetr a iso p ro p yld i sil o x anedi - 1 , 3 -yl Tr : trityl Ts :· p 一 tol uenesulph o ny I TSA : p -to l uenesulph o n ic a ci d XP : o -xy le ned i0x yp h osph ory l [a] : op tica l rota t i on
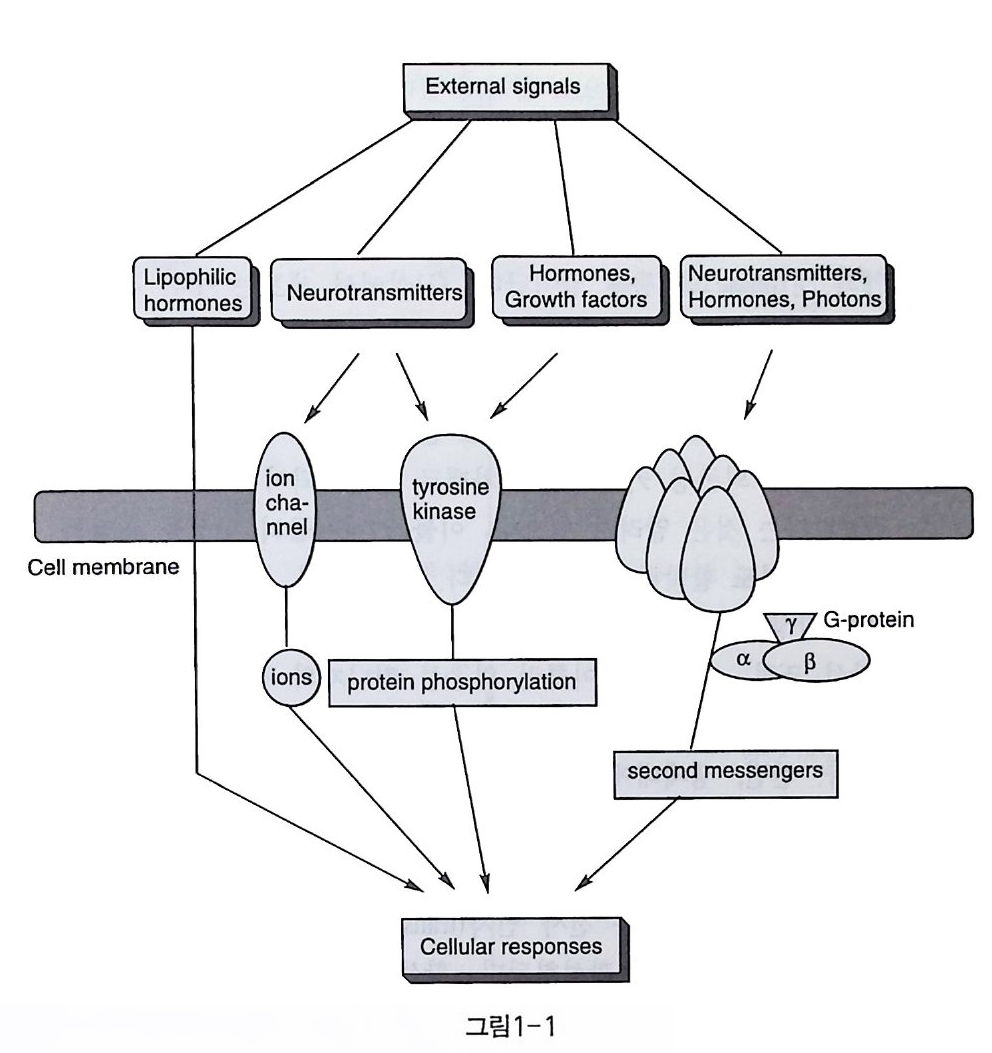
제 1 장 서론 1-l 신호 전달 살아 있는 모든 세포는 단세포 생물이건 인체의 세포건 상관없이 주 변 환경을 감지하고 변화에 대응할 필요가 있다. 세균과 같은 단세포 생물은 영양분이 존재하는 쪽으로 이동하며, 위험한 환경으로부터는 멀어지는 방향으로 비교적 단순하게 운동한다 . 고등 생물의 경우 주위 의 환경에 따라 근육 세포는 수축하고, 신경 세포는 전기적 자극을 전 달하며, 일부 세포들은 다른 세포에 대한 신호로서 단백질 분자를 분 비하기도 한다. 또 적절한 환경이 조성되거나 필요성이 있을 때는 급 속도의 세포 분열과 번식도 일어난다. 정상적인 생물체에서는 문자 그 대로 수천 가지의 화학적 신호들이 매우 복잡한 방법으로 교환되고 있 다. 만약 이러한 신호 전달 기능이 잘못 수행되면 개체 전체에 치명적 인 결과가 초래되기도 한다. 인체에 있어서의 암, 염증, 자가 면역 질 환 및 정신 질환 등을 그 예로 들 수 있다. 세포간의 정보 교환은 호르몬, 성장 인자(gr o wth fac to r ), 신경 전달 물질 (neuro tr ans mitt er) 둥의 화학적 신호나 신경 세포에서와 같이 주로
전기적 신호를 통하여 일어남이 알려져 있다(그림 1-1) 〔1). 친지질성의 스테로이드와 같은 호르몬 등은 인지질 이중막으로 구성된 세포막을 직접 통과해 세포 내의 수용체에 결합하여 활성을 나타낸다 . 한편 전 기적인 신호들은 세포막의 이온 통로(i on channel) 등의 개폐를 통해 신호를 전달한다 . 그러나 세포막을 통과할 수 없는 많은 친수성 신호 전달 물질들은 세포막에 자리잡고 있는 세포의 안테나격인 수용체를 통하여 받아들여진 후 세포 내로 신호를 간접적으로 전달하는 기작을 활성화시키는데 이것을 신호 전달(tr ansrnernbrane sig n allin g 또는 sig n al tran sducti on ) 이 라고 한다. 신호 전달계에 관여하는 수용체들은 기작에 따라 몇 가지로 분류될 수 있는데, 우선 수용체 자체가 이온의 흐름을 제어하는 이온 통로로 작용하는 경우가 있다 . 이 경우에는 세포질 내의 이온 농도를 변화시 킴으로써 효소 등의 활성을 조절하게 된다. 니코틴성 아세틸 콜린 수 용체는 리간드를 통한 이온 통로의 중요한 예이다. 이 수용체는 전기 뱀장어와 전기가오리의 발전 기관 부위에 많이 존재하며 가장 찰 연구 된 수용체 중 하나이다. 이 발전 부위의 세포막을 아세틸 콜린으로 처 리하면, 이온 통로가 열리면서 양이온의 유입으로 인한 탈분극 (de p o lar iza ti on ) 현상을 전기생리학적 방법으로 쉽게 측정할 수 있다. 이러 한 기작을 통하여, 화학적 신호인 아세틸 콜린은 전기적 신호로 바뀌 게 되며, 동시에 세포 내의 양이온 농도는 급격하게 증가한다. 탈분극 의 결과는 표적 세포가 신경 세포라면 연속적으로 전기 신호가 전달되 지만, 부신의 크로마핀 (chrom affi n) 세포인 경우에는 칼슘 유입을 통해 크로마핀 과립을 세포 외로 분비하거나 아드레날린을 방출하게 한다. 또 표적 세포가 근육 세포인 경우에는 각종의 근육 단백질을 활성화시 켜 근육의 수축을 유도한다. 두번째 형태는 수용체 스스로가 티로신 키나제의 활성을 가진 효소 로 작용하는 경우이다. 이러한 수용체는 세포막 속에 묻혀 있으면서
 Hormones, I| N eurotr a nsmi tter s,
Hormones, I| N eurotr a nsmi tter s,
세포 밖으로는 1 차 신호 물질을 인지하고 결합하는 부위를 가지고, 세 포 안쪽에 효소의 활 성을 나타내는 활성 부위가 존재한다 . 효능약 (a go ni s t)이 세포 밖의 수용체 부분에 결합되면, 세포 내의 목표 단백질의 특정 티로신기에 인산화가 일어나는 것이다 . 이 신호 전달 기작은 많 은 성장 호르몬과 인슐린 등의 작용에 관여하는데@〕, 여기에는 크게 사이클린 (c y c li n) 의존성 키나제 경로와 M 사>(mit o g en-ac ti va t ed p ro t e in)
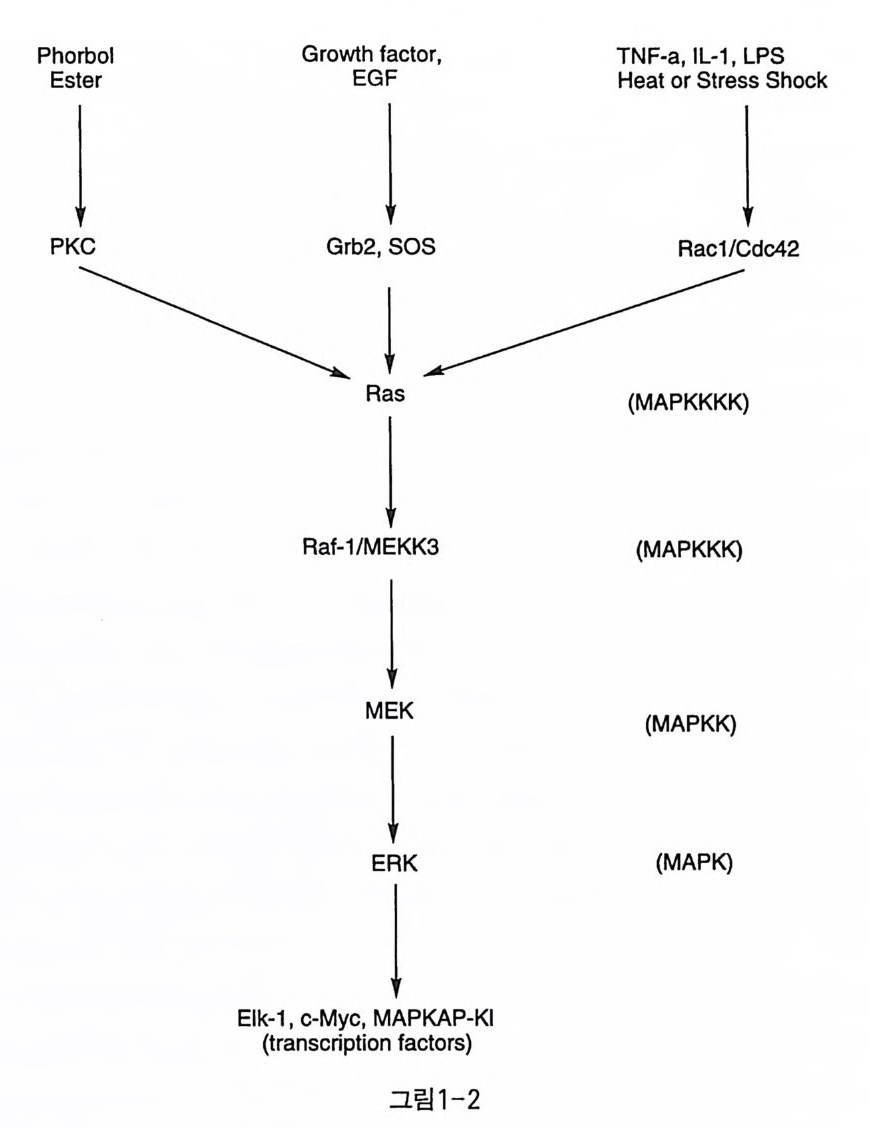
키나제 경로가 존재하는 것으로 알려져 있다. 외부 신호 전달에 의한 중요한 세포 내 반응 중 하나는 세포 분열안 데, 진핵 세포의 세포 분열 주기는 매우 정교하게 조절되고 있다 . 세 포 분열 주기는 Gl(ga p l), S(DNA 합성), G2(ga p 2 ), M( 유사분열) 등 의 4 개의 상(p hase) 을 통해 일어난다. Gl 상에서 세포는 주위 환경이 분열에 적합한 지를 판단하고 S 상에서 DNA 를 합성하며, G2 상에서는 세포 분열에 필요한 준비가 완료되었는지를 확인한 후 M 상에서 세포 가 두 개의 딸세포로 나누어진다. 세포 분열 주기가 진행되는 동안 각 종의 사이클린 의존성 키나제들이 차례로 활성화되어 4 개의 상에 개 입, 조절한다는 것은 알려져 있으나, 이들 키나제들의 활성을 조절하 는 기작은 아직도 활발히 연구되고 있다. 예를 들어, 사이클린의 조절 소단위의 합성과 파괴를 통한 조절, 키나제의 인산화 및 탈인산화를 통한 활성 조절, 그리고 사이클린 의존성 키나제와 직접적인 결합을 통해 분열을 억제하는 p21 , p2 7, p5 7 등의 억제 단백질들이 계속 발견 되고 있다. 한편, 생체내에는 세포 분열 주기가 정상적으로 진행되고 있는지를 점검하는 되먹이기(fe edback) 조절도 존재한다. 그중에서 핵 심 적 역 할을 수행 하는 것 이 종양 억 제 단백 질 (tumo r sup pre ssor pro te in ) 인 p 53 이댜 p53 단백질은 전사 인자(tr ansc ripti on fa c t or) 의 일종으로 DNA 가 상처를 입었을 때 활성화된다. 활성화된 p 53 은 사이클린 의존 성 키나제의 억제제인 p 21 의 생성을 촉진하여 세포 분열 주기를 중지 시키거나, 아폼토시스 (a p o pt os i s, 세포 예정사)를 유발한다. 인간 암의 약 Q% 정도에서 p 53 의 돌연변이, 파괴, 또는 p53 결합 단백질을 통 한 불활성화 동이 발견되고 있다. 한편, tamo x ifen 등의 항암제는 p5 3 을 활성화시켜 암세포의 아폼토시스를 유도하여 항암 효과를 나타내는 것으로 알려져 있다〔 3 〕. 성장 인자에 의한 세포 분열을 촉진하는 신호는 사이클린 의존성 키 나제 경로뿐만 아니라 M 사》 키나제 경로를 통해서도 전달된다(그림
 Phorbol G 『o wt h fac to r , TNF-a, IL-1, LPS
Phorbol G 『o wt h fac to r , TNF-a, IL-1, LPS
1-2). EGF(ep ide rmal grow th fa c t or) 는 수용체 티로신 키나제를 활성화 하여 중간체 단백질인 She 단백질을 인산화하며, 인산화된 She 는 Grb2(gr ow t h fac to r recep tor bin ding p ro t e in)의 SH2 영 역과 결합하게 된다 Shc/Grb2 복합체는 SOS 를 통해 Ras 로부터 GDP 를 유리시킨다.
자유 형태의 Ras 는 GTP 와 빠른 속도로 강한 결합을 이루어 활성화된 다 Ras/GTP 복합체는 Ra f - I 을 활성화시키고, 그 정보가 MAP 키나 제 경로를 따라 전달되며, 최종적으로 전사 인자인 c-My c, Jun , E1k_l 등을 활성화하여 DNA 생성을 촉진한다. 또한 Ras 는 대부분의 성장 인자로부터의 신호가 모이는 교차점 또는 스위치로서의 역할을 수행한다 인체 암의 약 30% 에서 돌연변이된 Ras 단백질이 관찰되고 있다〔 4,5,6). 세번째로는 많은 친수성 신호 전달 물질들이 수용체를 통하여 세포 내에 새로운 2 차 전달 물질을 만들어내는 세포 내 효과 인자 단백질 (eff ec to r ) 효소와 연결되는 방식으로 작용한다. 우선 의부의 신호가 수 용체 에 결합하면, GTP 결 합단백 질 (GTP bin d ing pro te i n , G-단 백 질 ) 이 수용체에 의해 활성화된다 . G_ 단백질은 세 개의 다른 소단위체인 a., p, Y 로 이루어져 있는데, 일단 활성화가 되면 a 에 붙어 있던 GDP 가 GTP 로 치환되면서, pY 단위체가 활성화된 a. -GTP 로부터 분리된 댜 유리된 이 a_GTP 는 효과 안자 단백질로 작용하는 아데닐레이트 시클라제, 구아닐레이트 시클라제, 포스포리파제 등을 활성화하여 이 른바 2 차 전달 물질을 생성시킨다. 대사 분비, 세포의 성장 및 근육의 수축, 이완 등의 많은 세포 활동이 이러한 2 차 전달 물질에 의해 조절 된다. 현재까지 알려진 2 차 전달 물질로는 adenosin e 3', 5' -cyc l i c monop ho sp ha te ( cAMP), gu anosin e 3', 5' -c y cl i c monop ho sp h ate (cGMP), diac y lg l y c e rol (DAG), my o -inos it ol (l, 4, 5) -tr isp h o sph a te ( I(l , 4,5)P3 〕와 Caz+ 등이 있다 . 신경 전달 물질인 아드레날린이 간이나 근육에 저장된 글리코겐의 분해를 촉진시킨다는 것은 Su th erland 에 의해 밝혀졌다〔 7). 일단 아드 레날린에 의해서 수용체가 활성화되면 G_ 단백질울 거쳐 아데닐레이트 시클라제가 활성화되어 2 차 전달 물질인 cAMP 를 세포 내에 생성시킨 댜 cAMP 는 cAMP 의존성 단백질 키나제 (PKA) 를 활성화하여 연속적
표 1 cAMP 를 경유하여 신호 를 전달하는 1 차 전달 물질들 1 차 전달 물질 표적 세포 생리 효과 글루카곤 간 글리코겐 분해, 당 생성 아드레날린 지방 (~1 수용체) 지방 분해, 지방산 생성 억제 아드레날린 심장 (~1 수용체) 심장 박동, 수축력 증가 바소프레신 신장 (V2 수용체) 나트륨/물 재흡수 루트로핀 (Lutr op in) 난소 프로게스테론 합성 ACTH 부신 피질 당코르티코이드 합성 갑상선 자극 호르몬 갑상선 갑상선 호르몬 합성 부갑상선 호르몬 뼈 뼈 재흡수
으로 포스포릴라제 키나제의 활성화를 통해 포스포릴라제 a( 활성 형태) 를 생성한다. 포스포릴라제 a 는 글리코겐을 1 ―인산포도당(g lucose-1- p hos p ha t e) 으로 변환시킨다. P K.A는 칼슘 이온에 의해서도 활성이 높 아지며, Ra f -1 을 인산화하여 Ras 신호 경로를 차단하는 작용도 나타 낸다 따라서 Ras 를 통한 MAP 키나제 경로와 cAMP 경로 사이의 접 합은 R af -1 을 통해 일어나는 것이다 . 호르몬이나 신경 전달 물질 등 의 다양한 1 차 전달 물질들이 cAMP 를 2 차 전달 물질로 활용하고 있음 이 밝혀져 있다(1). 그러 나, cAMP 의 2 차 전달 물질 역 할을 발견한 Su th erland 가 아드레 날린에 의한 글리코겐 분해 실험을 개의 간 대신에 쥐의 간을 이용하여 수행하였더라면, cAMP 의 역할을 알아내지 못하였을 것이다. 왜냐하 면, 쥐의 간세포에는 B 一수용체는 존재하지 않고, a! _수용체만이 존 재하는데도 아드레날린이 글리코겐의 분해롤 촉진하기 때문이다. 그 기 작은 cAMP 와는 무관하게 인산이노시톨이 2 차 전달 물질로 작용하여 세포 내 칼슘 농도를 증가시켜 글리코겐 분해에 필요한 효소들을 활성 화시키는 것으로 밝혀졌다. 현재 많은 수의 1 차 전달 물질들이 인산이
표 2 이노시톨 인지질 가수 분해를 통하여 신호를 전달하는 1 차 전달 물질들 1 차 전달 물질 표적 세포 생리 효과 아드레날린 간 (al 수용체) 글리코겐 분해바소프레신 간 (Vl 수용체) 글리코겐 분해 ATP 간 (P2 수용체) 글리코겐 분해 아세틸콜린 외분비 췌장 (Ml /M 3 수용체) 분비 아세틸콜린 평활근 (M3 수용체) 수축 트롬빈 혈소판 응집 PDGF 섬유아세포 세포증식
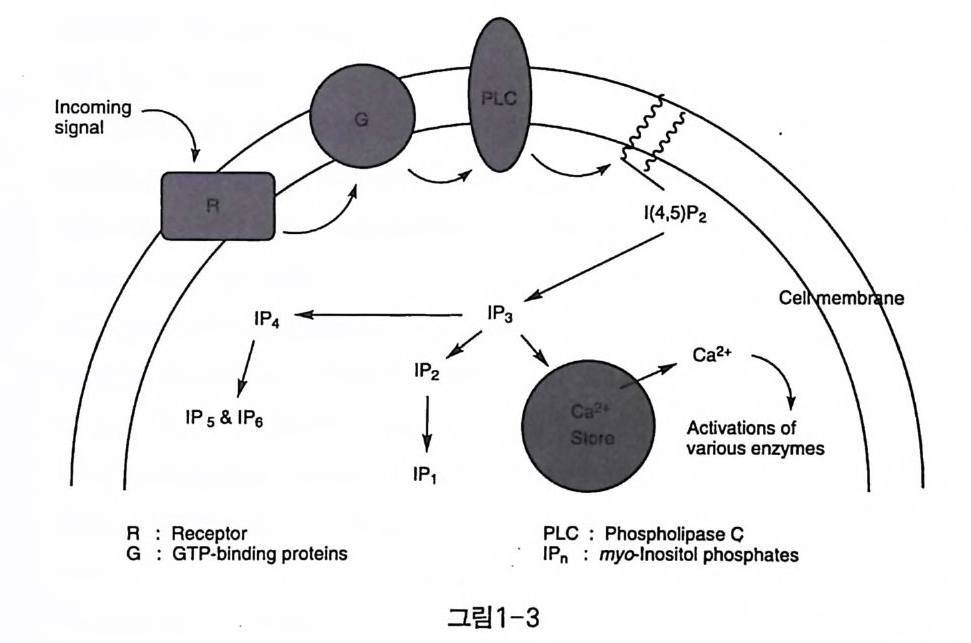
노시톨울 2 차 전달 물질로 활용하고 있는 것으로 나타나고 있다〔1). 최근에 들어서는 인지질 이노시톨인 포스파티딜 3,4,5- 삼인산이노 시톨〔P I(3, 4, 5)P 니 역시 가능한 2 차 전달 물질로 주목받고 있으며 [8] , NAD 적 대 사 물질 인 cyc l i c adenosin e dip h osp h ate rib o se (cADP - ribo se) 역시 Ca” 에 관여하는 2 차 전달 물질일 가능성이 거론되고 있 다〔이 또 s phing o lipi d 의 대사 물질인 sph ingo sin e 1- p hos p ha t e 는 특정 mit og en 의 2 차 전달 물질일 것으로 추측되고 있다 (10). 1- 2 1( 1, 4, 5)P3 [m y o - In 函 m 口, 4, 5 -tr i s p hos ph 떠이 미오이노시톨은 포도당과 같은 분자식을 가진 당의 일종으로서 1850 년 경 Scherer 에 의 해 처 음으로 천연물로부터 분리 되 었다 (11) . 1975 년 Mi chell 은 수용체 조절에 의한 이노시톨 인지질의 가수 분해가 세포 내 칼슘 이온 농도 변화와 직접적인 연관이 있음을 보여주었다(1 2 〕. 1983 년 Berr idg e 등은 포스파티딜 4, 5- 이인산이노시톨〔 PI(4, 5)P2) 이 G- 단백질의 조절을 받는 포스포리파제 C(PLC) 에 의해 가수 분해되
어 두 종류의 2 차 전달 물질인 디아실글리세롤과 1 (1 ,4,5)P J을 생성하 며, 이때 생성된 1 (1 ,4,5)P 떠 세포 내의 칼슘 농도를 증가시키는 것으 로 보고하였다(그림 1-3) 〔 l 이 . 한편, Nis h iz u ka 등은 디아실글리세롤이 당시 관심의 초점이 모아지고 있던 단백질 키나제 C 를 활성화시키는 별도의 2 차 전달 물질임을 밝혔다 [14 〕 · 칼슘은 근육 세포의 경우 근수축에 중요한 역할을 한다는 것이 오래 전부터 알려져 있었다. 최근에 와서는 세포 내의 많은 단백질의 인산 화가 칼슘 농도 변화에 의해 유도되며, 칼슘의 분비는 많은 효능약의 일차적인 반응임이 밝혀졌다. 세포질 내의 칼슘 농도는 크게 두 가지 다른 기작에 의해 조절된다. 첫째는 효능약의 작용에 의해 세포막의 전위가 달라져서 세포막에 존재하는 전위의존성 칼슘 통로가 열리는 것이다 . 세포 내의 칼슘은 대부분 막이나 단백질에 결합되어 있어서, 자 유로운 이온 농도는 매우 낮은 상태를 유지한다. 그래서 이온 통로가
 IP5&.II P6 IiP 2/ \/ 1(4,5)PAC2c ti vaa ti on2 s o\f
IP5&.II P6 IiP 2/ \/ 1(4,5)PAC2c ti vaa ti on2 s o\f
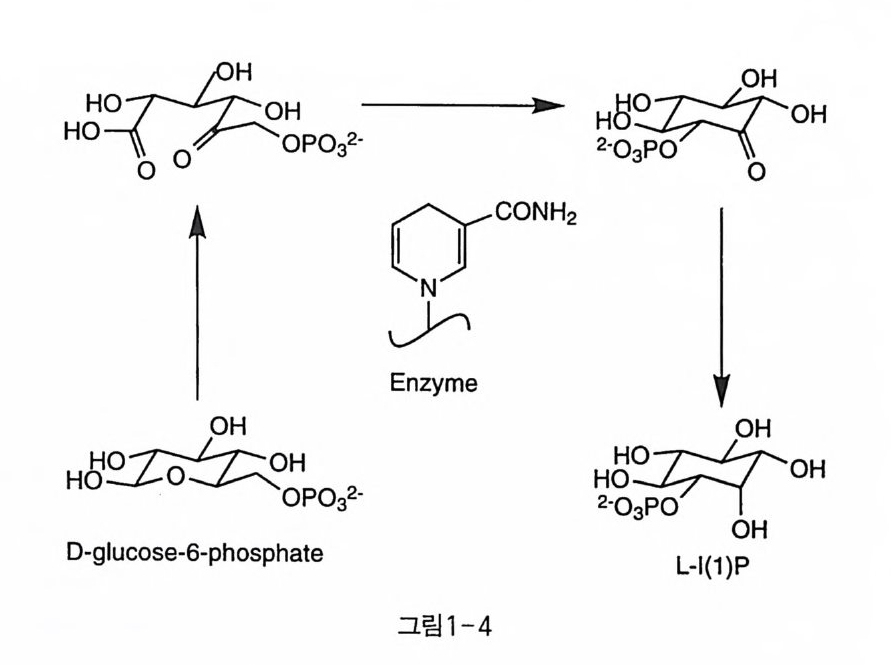
열렸을 때 세포 안팎의 농도 기울기에 의해 칼슘 이온이 유입되어 세 포질내의 칼슘 이온 농도가 증가하는 것이다 . 둘째로는 다른 종류의 효능약에 의해 세포질 내의 칼슘 저장소로부터 칼슘이 분비되어 칼슘 의존성 효소들을 활성화하는 것이다. 칼슘에 의한 세포 내 반응은 효 능약의 종류뿐만 아니라 세포의 종류에 따라서도 차이룰 나타낸다. I (l ,4,5)P J이 외부의 신호에 의해 세포 내의 칼슘을 분비하는 2 차 전 달 물질로 작용한다는 발견은 신호 전달계의 새로운 장을 열었다고 할 만하다 이로 인해 이노시톨 화학과 생화학은 르네상스를 맞이하였 고, 현재까지도 생화학 분야에서 인산이노시톨 분야는 가장 많은 논문 인용수를 자랑하는 뜨거운 연구 분야가 되었다. 그러나 아직도 IP3 의 복잡한 대사 경로들은 연구중에 있으며, 그 대사 물질 중에서 새로운 활성을 가진 구조들이 속속 밝혀지고 있다. 1 -3 이노시톨의 생합성 사람의 경우 필요한 이노시톨의 대부분은 음식물을 통해서 섭취된 다 그래서 한동안은 이노시톨이 비타민의 일종으로 간주되기도 하였 댜 소량의 이노시톨만이 생체내에서 합성되는데 식물이나 다른 동물 에서도 이러한 기작이 존재하는 것으로 알려져 있다. D-gl u cose-6- p hos ph a t e 에 L -m y o -inos it ol -1 -ph osph a te s y n th ase 가 작용하여 이 성 질체화 반응을 통해 L-l (l )P(D-1(3)P) 를 만든다. 이 효소는 효모 및 포유 동물의 고환 및 뇌에서 분리 정제되었고, 이 반응의 경로는 그림 1-4 에 나타내었다[1 5 〕. 재미있게도, D- g lucose-6- p hos p ha t e 의 티오 인산 유사체는 이 효소의 기질로 사용되지 못하여 이노시톨로 전환되 지 않았다 [16 〕· 이렇게 생성된 L- I( l)P 에 이노시톨 모노포스파타제가 작용하여 이
 H~v~PO 운 O。H
H~v~PO 운 O。H
노시톨이 만들어지는 것이다. 이 모노포스파타제는 인지질 이노시톨의 순환에서 중요한 역할을 담당하는데 그것은 이 효소가 I (l )P 의 두 이 성질체, 죽 생합성으로 생성된 L-l (l )P 뿐만 아니라 PIP 려 가수 분해 로 생긴 IP 려 대사 물질인 D-l (l )P 도 기질로 사용하기 때문이다. 이 효소는 또한 D 와 L- I( 4)P 와 I(5) P 등도 탈인산화시킨다는 것이 밝혀 졌다 이노시톨 모노포스파타제는 뇌에서 분리 정제되었고, X 선 결정 구조도 밝혀졌다(1 7) . 한편 리튬 이온은 이 효소를 저해한다. 리튬이 투여된 쥐의 뇌에서 유리된 이노시톨의 함량이 저하됨이 알려져 있으며 리튬 약이 조울증 치료에 효과를 나타내고 있으므로, 이 치료 기작은 이노시톨의 모노포 스파타제의 작용 저하에 의한 것으로 유추되고 있다. 음식물로 섭취한 이노시톨은 혈액 -뇌 장벽 (Blood Brai n Ba rrier , BBB) 을 통과해서 뇌로 들어갈 수가 없기 때문에 D- g lucose-6- p hos p ha t e 를 거치는 생합성 과정이 중요한 역할을 담당할 것으로 생각된다. 이 경우 생성된 L-
I(l) P 의 탈인산화 반응에 촉매해야 할 모노포스파타제의 작용이 저해 되면 자유 이노시톨이 생성될 수가 없어서 이노시톨 인지질의 합성이 중단된다. 한편 리튬에 의한 방해 작용은 드물게도 무경쟁 방해 (uncom p e titi ve i nh i b iti on) 의 기작에 의한 것으로 알려졌다(1 8). 죽, 리튬 이온은 인산 화된 효소의 분해에 해당하는 두번째 반응 단계를 방해하는 것으로 생 각된다. 결정 구조와 함께 광범위한 의약화학적 연구로 보다 나은 저 해제의 합리적인 구상이 이루어지고 있으므로 머지않아 새로운 항조울 제가 개발될 가능성이 높다 . 현재까지 합성된 모노포스타제 저해제들 의 합성은 뒤에서 다시 다룬다 (6-2 참조). 1-4 이노시톨 인지질 동물 세포에서 이노시톨을 포함한 인지질은 전체 인지질의 10% 에도 미치지 않는다 . 그중에서도 PI 가 가장 많으며 (90% 이상), 대부분은 소 포체 (endop la sm ic r eti cu lum) 에 위 치 하고 있다. P I( 4)P 와 PI( 4, 5 )P 2 는 PI 에 비해 적은 양만을 차지하고 있으며 세포막의 안쪽 부분에 위치한다 . PI 는 특정 효소 (PI-4--: kin ase) 에 의해 인산화되어 P I( 4)P 가 되고, 다 시 다른 효소 PIP-5- kin ase 에 의해 신호 전달에 중요한 지질인 PI( 4, 5)P 카 생성된다. 수용체의 활성화에 수반된 G- 단백질의 변화는 포스 포리파제 C 를 활성화하여, 그 기질인 PIP2 의 가수 분해를 통해 IP J와 DAG 를 생성시킨댜 이 두 분자는 별도의 2 차 전달 물질로서 작용하 는데, 친수성인 IP J는 세포질로 확산되어 소포체의 칼슘 통로 수용체 를 활성화시키고, 세포 내 저장소로부터 칼슘을 방출시킨다. 신호 전달 경로가 잘 알려진 IPJ 경로와는 별도로, 3 번 위치가 인산 화된 새로운 인지질에 관한 분야가 최근 밝혀지고 있다. PI( 3) P, PI(3,
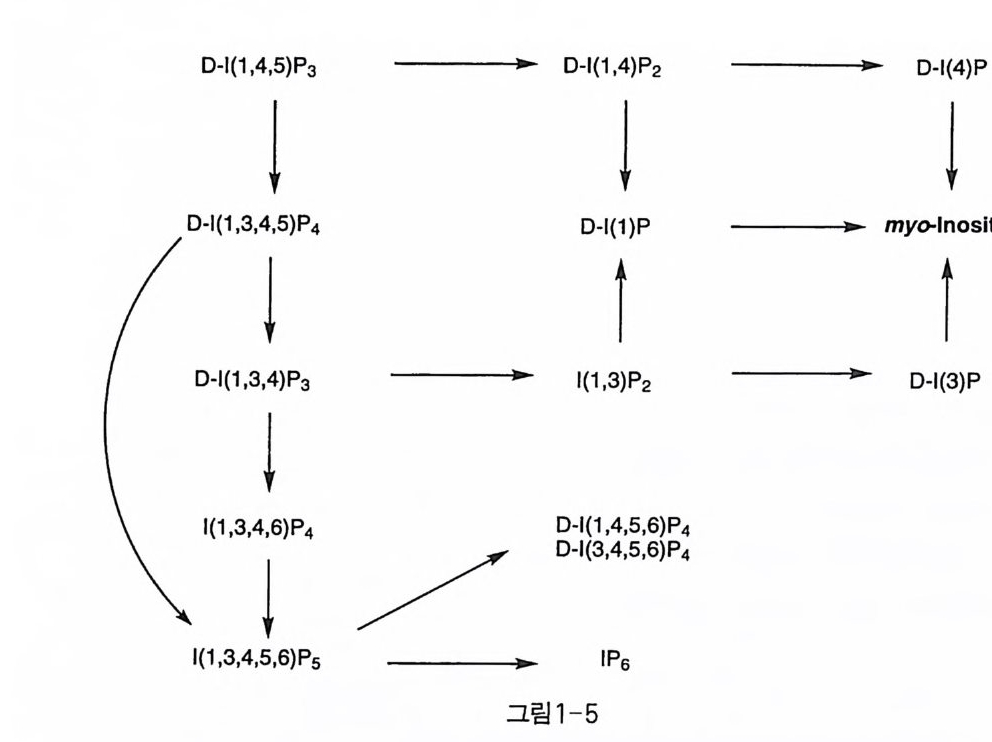
4)Pi., PI( 3, 4,S)PJ 등이 여기에 해당하는데, 한동안 그 생성 원천이 무 엇인가에 대해 논란이 있었지만(1 9), 지금은 활성화된 세포에서 PI( 4, 5)P2 에 특정 3- 키나제가 작용하여 P I( 3,4,5)P J가 형성되는 기작이 받아 들여지고 있다〔 20) . P I( 3)P 와 P I( 3,4)P2 는 앞에서 만들어진 PI(3,4,5)P4 에 포스파타제가 작용하여 생성된 것으로 추정된다 . 이러한 3- 인산기 를 가진 인지 질들은 PI(4, 5)P2 와는 달리 PLC 의 기 질로 작용하지 않 아, 인산이노시톨울 신호 전달 물질로 생성하지는 않는다. 최근에는 PI-3- ki nase 에 의해 생성된 인지질들이 PH(pl e ckstr in homolog y) 영역 과 결합하여 ARF 또는 Akt(pro te i n kina se B, PKB) 의 활성화에 중요한 역할을 담당한다는 사실이 밝혀져, 이들 3 번 인산 인지질들이 각종 성 장 호르몬이나 인슐린 동의 신호 전달에 핵심적인 역할을 담당한다는 증거들이 속속 나오고 있다 @1). 1-5 IP3 대사 2 차 전달 물질이 일단 세포 내에서 분비되어 신호를 전달하고 세포 를 활성화시킨 후에는 효율적으로 비활성화되어야 수용체가 정상 상 태로 되돌아가서 다음 신호에 대비할 수 있게 된다. 그러나 어떤 경우 에는 변화된 대사 물질이 또다른 경로의 신호 물질로 작용할 수도 있 댜 IP 려 대사 경로에 대한 대략적인 요약을 그림 1-5 에 나타내었다 [22 ,23, 24] • PLC 에 의한 PIP 려 가수 분해는 단순하지만은 않다. PIP2 에 물 분자 가 친핵체로 공격하면 IP3 와 DAG 가 생성되지만, 트롬빈으로 활성화된 혈소판의 경우에는 이노시톨의 2 번 수산기가 가수 분해 자리를 공격하 여 cl (l ,2)P(4,5)P2 가 형성된다〔 25). 그래서 초기 연구에서는 이 고리형 인산이노시톨 자체가 ~} 전달 물질일 것으로 추정되기도 하였으나, 칼
 D-1(1, 4,5- )P3 D-1(1,l 4)P 2 D-1l(4) P
D-1(1, 4,5- )P3 D-1(1,l 4)P 2 D-1l(4) P
슘 분비 와의 관련성을 조사해 본 결과 1( 1, 4, 5)P3 의 활성 이 중요함이 증명되었다〔 26 〕. 2 차 전달 물질로서 1 (1 ,4,5)P3 의 역할은 현재로서는 잘 정립되어 있 다고 할 수 있다. IP 려 대사에는 크게 두 가지 주요 경로가 발견되었 댜 첫번째는 IP 폐 5- 포스파타제가 작용하여, 1 (1 ,4)P2 로 바뀜으로서 진행되는 경로이다 . 이 효소는 가용성인 세포질형과 막결합형이 모두 존재하는데, 사람의 혈소판인 경우 두 가지 형태가 모두 존재한다. 그 생성물인 1 (1 , 4)P2 가 DNA 중합 효소의 활성화〔力〕와 6- p ho sp ho fr uc to - 1- kinase 의 활성 조절〔 28 〕, 그리고 c yt oskele t al-ac ti n 의 증가〔 29 〕 등에 관여한다는 보고가 있기는 하지만, 5_ 포스파타제의 가장 중요한 역할 은 칼슘 분비 작용의 종결인 것으로 생각된다. 1( 1,4)P2 는 계속 대사되 어 I( l) P 나 l( 4)P 를 거쳐 이노시톨로 돌아가서 다시 인지질의 순환 경
로에 이용된다 . IPJ 대사의 또다른 경로는 3- 키나제에 의한 인산화를 통해 I{l ,3 ,4, 5)P 가 형성되는 것이다 . 이 효소는 1986 년에 처음 발견되어 〔 3 이 분리 정제되었고〔 31,32 〕 유전자의 배열 결정과 클론화도 이루어졌다〔 33,34). I {l ,3,4,5)P 가 !PJ의 대사 물질일 뿐만 아니라 그 자체가 2 차 전달 물 질일 가능성에 대해서 오랫공안 논쟁이 있어왔다 . 이러한 논쟁은 IP4 분자가 세포 밖의 칼슘울 세포막을 통해 세포 내로 유입하는 데 관여 한다는 주장〔 3 회과 IP4 가 IPJ 수용체에 작용한다는 주장으로 대별되는 데〔 36), 아직도 명확한 결론은 내려져 있지 않다. IP 려 기능이 무엇이건 간에, IP4 는 !PJ에 작용하는 것과 같은 포스파 타제에 의해 탈인산화되는 것으로 보인다. 그러나, 이 효소에도 가용 성형과 막결합형이 있으며, 전자에는 다시 하나 이상의 아종류가 존재 하여 상황이 복잡하다〔 37 〕. 막결합형과 가용성형 중 제 1 형인 효소는 따와 IP4 모두에 작용하나 IP 예 친화성이 더 큰 반면, 제 2 형 효소는 IP폐 는 거의 작용하지 않는댜 여기서 만들어지는 생성물인 I(l,3 ,4)PJ 역시 세포 내의 칼슘 농도를 조절하는 데 관여하는 것으로 제안되었으 나〔 3 이, 아직 명확하지는 않다〔 39). I{ l,3,4)P J의 대사는 조직의 종류에 따라 차이를 보이는데, 포스파타제가 작용하여 I(l , 3)P2 와(또는) !{3, 4)P2 가 만들어졌다가 각각 I (l )P 와 I(3)P 를 거쳐 이노시톨로 되돌아 간다 . 한편, I(1, 3, 4, 5)P4 는 어떤 세포에서는 5_ 포스파타제에 의해 다시 I {l ,4,5)P J로 되돌아갈 수도 있다〔 40 〕. 그러나 이 효소는 IPs 나 IP6 에 대 해 I {l ,3,4,5)P4 보다 더 큰 친화성을 가지므로, 그 자연상의 기질은 IPs 나 IP6 일 것으로 추정된다〔 41). I (l ,3,4)P 는 5/6 국기나제에 의해 인산화되어 I {l ,3,4,5)P4 나 I{l,3 ,4, 6)P 를 형성하기도 하는데〔 4 2, 43), I (l ,3,4,6)P4 는 I {l ,4,5)P J보다 약하 기는 하지만 뚜렷한 칼슘 분비 효과를 가지고 있다〔 44, 45). 동물 세포
에서 1 (1 ,3,4,5)P4 는 5/6- 키나제에 의해 인산화되어 1 (1 ,3,4,5,6)Ps 를 만들기도 하는데, 생성된 IPs 는 IP6 와 광학 이성질체 관계의 1(1 , 4,5, 6)P4 과 1( 3,4,5,6)P4 로 대사된다. 이러한 다인산이노시톨들은 식물이나 조류의 적혈구에서 다량 존재하고, 그 작용은 인산 저장소 또는 헤모 글로빈에 대한 산소의 친화도를 조절하는 것으로 알려져 있었다〔 46 〕. 이들 다인산이노시톨들이 동물 세포에 존재한다는 것과, 이 분자들이 세포 내 또는 세포 외의 신호 물질로 작용한다는 사실은, 비록 이들이 직접적으로 신호 전달계에 관여하는 것이 아닐지는 모르지만, 새로운 연구 분야로서의 가능성을 가지고 있다고 할 수 있겠다. 포유 동물에서와는 달리 효모에서는 1(1 ,4,5)P3 에 대해 포스파타제가 작용하지는 않고, 키나제에 의해 인산화되어 IP4 를 거쳐 IPs 나 IP6 로 진 행됨이 관찰되었다. 그런데, 이때 일차적으로 생성되는 IP4 는 1(1 , 3,4, 5)P 가 아닌 I(1,4,5,6)P4 로서 효모에서는 IP 려 대사에 I(1 , 4,5)P3 6- 키 나제가 주로 작용한다는 사실이 밝혀졌다〔 47 〕 . IPs 나 IP6 등의 다인산이노시톨의 역할이 아직 분명하게 규명되어 있 는 것은 아니지만, 식물의 씨앗 등에 다량 함유되어 있다는 사실로부터 이들 다인산이노시톨들이 생체의 안정성을 유지하는 데 관여하리라는 가설은 오래 전부터 제기되어 왔다. 이러한 기작의 한 가지 설명은 생 체에 해로운 라디칼 반응을 억제하는 효과를 나타낸다는 것인데, 실제 로 IP6(ph y t ic ac i d) 는 3 가 철 이온을 촉매로 하여 일어나는 히드록시 라 디칼의 생성을 억제한다〔 48 〕. 이것은 촉매로 작용하는 3 가 철 이온과 IP 려 강한 결합에 기인하는 것으로 생각된다. 이러한 결합에는 IP6 의 6 개의 인산기 중 1, 2, 3 번 인산기 주머니가 중요한 역할을 담당한다는 증거가 있다 (4-4-2 참조)〔 49 〕. 최근에 알려진 또다른 재미있는 사실 은 IP6 가 인산화의 마지막 생성물이 아니라 피로인산 형태를 가지는 IP 려나 IP, 도 존재한다는 간접적인 증거가 보고된 것이다〔 50 〕. 그 정확 한 구조나 활성에 대해서는 아직도 밝혀야 할 부분이 많이 남아 있다.
l-6 IP3 수용체 JP3 수용체는 리 간드인 IP3 와 결합하면 칼슘의 출입 을 활성 화하는 이 온 통로로서, 세포 내 소포체에 위치하고 있음이 많은 연구 결과 정립 되었다 !PJ 수용체는 JP3 작용의 중요성이 밝혀지기 이전인 1979 년 생 쥐 (mouse) 의 소뇌로부터 처음 분리되었다 (51) . 당시에는 P400 이라고 불리었던 이 단백질은 푸르키니에 (Pur ki nj e) 세포가 결여된 변종 생쥐 의 뇌에서는 거의 나타나지 않았고 정상적인 생쥐에서만 관찰되었다 . 1988 년에 Sny de r 등은 쥐 (ra t)의 소뇌에서 정제한 !PJ 결합 단백질이 %0 kD 의 분자량을 가지며, IP 폐 대한 강한 결합 (~=lOOnM) 을 나타 냄을 보고하였다〔 52). 같은 해 Miko sh iba 등은 생쥐의 소뇌에서 푸르 키니에 세포에 풍부한 P400(Purki nj e cell en rich ed pro te in ) 단백질을 정 제하였고〔 5 미, 분자량 250kD 인 이 단백질이 앞서 분리된 !PJ 결합 단 백질과 면역학적으로 동일한 단백질임을 증명하였다〔 54). 또 전자 현 미경 사진을 통한 관찰 결과 수용체는 4 개의 동일한 소단위체의 사량 체를 이루고 있으며, 사각형 모양을 이룬 수용체 단면의 한 변 길이는 약 25nm 에 달했다. 한편 같은 생쥐의 소뇌로부터 수용체의 cDNA 클 론을 통해서 얻은 단백질은 2, 749 개의 아미노산으로 이루어져 있으며, 여 기서 유추된 분자량은 313kD 에 이르렀다〔 55). 이후 쥐 , 초파리, 사람으로부터도 cDNA 클론이 이루어졌는데 이전 에 알려진 생쥐의 배열과 상당한 유사성을 가짐으로써, JP3 수용체는 종에 관계 없이 상당 부분 보존되어 왔음을 알 수 있다. 동종 사량체 인 수용체의 각 소단위에 IP3 가 한 분자씩 결합하며, 결합 부위는 N_ 말단에 위치한다 IP 려 결합 부위에는 (+)전하를 띠는 Arg, Ly s 이 풍부하고, C- 말단에는 6 개 내지 8 개의 막 통과 부위가 존재하는 것 같다 수용체는 뇌에서 많이 발견되었지만, 정소, 동맥의 평활근, 자 궁, 난소 및 소장의 평활근에도 존재한다 . 세포 내의 위치로는 주로
활면 소포체 (smooth endop la sm ic reti cu lum) 에 존재 하지 만, 조면 소포체 (roug h endop la sm ic re ti culum) 나 핵막 외부에도 존재한다. 골격근이나 심장 근육의 근소포체에 존재하는 리아노딘 (r y anod i ne) 수용체와는 1 차 구조가 부분적으로 유사하지만, 세포막의 칼슘 통로와는 구조적 유사 점이 없다 . ATP 결합 자리도 당량만큼 가지고 있으며, ATP 의 존재 하에서 칼슘 분비는 증가된다. 또, cAMP 의존성 단백질 키나제에 의 해서 수용체 특정 위치에 있는 두 개의 세린 자리에 인산화가 일어나 서 칼슘 이온 방출을 조절한다. 한편 칼슘 이온 자체도 이 수용체에 결합할 수 있고 칼슘 방출에 영향을 미치지만 정확한 기작은 아직 알 려 져 있지 않다〔 56). mRNA 의 alte r nati ve s pli c i n g에 의해 수용체의 여러 가지 변이체들이 존재하는데, 처음에 알려졌던 쥐 뇌에서 분리된 것은 제 1 형에 해당한 다 제 2 형도 쥐의 뇌에서 분리되었는데, 1 형과 68-69% 정도 동일한 배열을 가지면서, IP 폐 대한 친화성은 1 형보다 크고 아미노산 잔기는 48 개가 짧다. 제 3 형은 1 형, 2 형과 각각 62% 와 65% 의 동일률을 가지고 신장과 소화관, 뇌 등에서 발현되 며 IP3 뿐만 아니 라 I(l , 3, 4, 5)P4 와 IP6 에도 결합한다. 쥐의 태반에서 얻어진 제 4 형은 부분적인 배열만이 보 고되어 있다. 현재까지는 모두 4 형까지 알려져 있는데, 이것은 단지 발견의 시작에 불과할지도 모른다〔 5 기 . 참고문헌 印 Hardi e, D. G., Bio c hemi ca l Messeng er . Hormones, neurotr an smi tter s and gro wth f ac to r s, Champ m an & Hall, London, 1991. 띠 Takemoto , D. J.; Cun nick , J. M. Cell Sig n all ing 1990, 2, 99 -104. [3] D raetta , G.; Paga n o, M. Ann. Rep . M ed. Chem. 1996, 3 1, 241-248.
印 Ay ra l-Kalousti an , S.; S kotn i c k i, J . S. Ann. Rep. M ed. Chem. 1996, 31, 171 -180. (5) Ste i n , B.; A nderson, D. Ann. Rep. Med. Chem. 19%, 31, 289-298. [6) Avruch, J.; Zhang , X. F.; Ky riakis, J. M. Trends Bio c hem. Sci . 19'J4, 19, 279-283. (7) Suth e rland, E. W . Sc ien ce 1972, 177, 401 -4 08. (8) Hemmung s, B. A. Sc ien ce 1997, 275, 628-630. (9] B err idg e, M. J. Natu r e 函, 365, 388 -3 89. U 이 Ol ive ra, A.; Sp ieg e l , S. Natu r e tm, 365, 557-560. ( 11 ) Scherer, J. Ju stu s Lieb ig s Ann. Chem. 1850, 73, 322-32 8. (1익 Mich ell, R. H. Bio c him . Bio p h ys . Acta 1975, 425, 81 -1 47. (13 ) Str eb , H.; I rvin e , R. F.; B err idg e, M. J.; S chulz, I. Natu r e 1983, 306, 67 - 69. [H ] N i sh i zu ka, Y. Natu r e 1984, 308, 693-698. 問 Wong , Y. H. ; Sherman, W. R. J. Bio l . Chem. 1985, 260, 11083 -11()C J(). [16) Baker, G. R.; Bil lington , D. C.; G a ni, D. Bio o rg. Med. Chem. Lett . 19'Jl, ], 17- 2 0. U 기 Bone, R.; Sp ring er , J. P.; At ac k, J. R. Proc. Natl. Acad. Sc i., USA tm, 89, 10031-1 0035. [18] Shute , J. K.; Bak 따 R.; B il li n 앙叫 D. C.; G 타 D. J. Chem. Soc., 먀 m Commun. 1988, 626-6 28. U 이 Irvin e , R. F. Curr. Op in. Cell. B io l . 國 , 4, 212 -2 19. @]P arker, P. J. ; Wate r f ield , M. D. Cell Growt h Di ffer. 函, 3, 747 -752. (21) Hemmung s, B. A. Sc ien ce 1997, 275, 1899. [22 )Shears, S. B. Bio c hem. J. 1989, 260, 313 -3 24. [23 )Shears, S. B., Advances in Second Messeng er and Phosph op r ote i n Research (Ed. Putn e y, Jr. , J. W. ) . Raven, New York, tm, pp 63 -9 2. [24 )M aje r us, P. W. Annu. Rev. Bio c hem. tm, 61, 225 -2 50.
〔칙 Ishi i, H.; Connolly, T. M.; Bross, T. E.; Maje r us, P. W. Proc. N atl. Acad. Sc i., USA 1986, 83, 63CJ 7- 6401. [26 ) Wi lc ocks, A. L.; Str upish , J.; Irvin e , R. F.; Nahorski , S. R. Bio c hem. J. 1989, 257, 2CJ 7 -3 00. [27 ) Sy lv ia , V.; Curtin, G.; Norman, J.; Ste c , J.; Busbee, D. Cell 1988, 54, 651-658. (28) Mayr , G. W. Bio c hem J. 1989, 259, 463 -4 70. (29] H uang , C. ; Lia n g, N. C. Cell Bio l . Int. 파, 18, 7CJ 7 -8 04. 圓 Irvin e, R. F.; Letc h er, A. J.; Heslop , J. P.; Berr idg e, M. J. Natu r e 1986, 320, 631 -634. [31 )J oh anson, R. A.; Hansen, C. A.; Wi lliam son, J. R. J. Bio l . Chem. 1988, 263, 7465 -7 471. 〔 3 익 Lee, S. Y.; Sim , S. S.; Kim, J. W.; Moon, K. H.; Kim, J. H.; Rhee, S. G. J. Bio l . Chem. 19 책 265, 9434-9440. 固 Choi, K. Y.; Kim, H. K.; Lee, S. Y.; Moon, K. H.; Sim , S. S.; Kim, J. W.; Chung, H. K.; Rhee, S. G. Scie n ce mo, 248, 64-66. @]T akazawa, K.; Vandekerck, J.; Dumont, J. E.; Erneux, C. Bio c hem. J. mo, 272, lITT-1 12. 固 Irvin e , R. F., Advances in Second Messeng e r and Phosph op r ote i n Research(Ed. Putn e y, Jr., J. W .). Raven, New York, 1992, pp 161-185. 〔 3 이 Wi lc ox, R. A.; Cha lliss, R. A. J.; Baud in, G.; Vasella, A.; Pott er , B. V. L.; Nahorski , S. R. Bio c hem J. 函, 294, 191 -1 94. 詞 Erneux, C.; Lemos, M.; Verj an s, B.; Vanderhaeg he n, P.; Delvaux, A.; Dumont, J. E. Eur. J. Bio c hem. 1989, 181, 317-322. 璃〕 Irvin e, R. F.; Letc h er, A. J.; Lander, D. J.; Berr idg e, M. J. Bio c hem. J. 1986, 240, 301-30 4. [39 ] S tru한 sh, J.; C 。 oke, A. M.; Pott er , B. V. L.; Gig g, R.; Nabors 뵤 s. R.
Bio c hem. J. 1988, 253, 901 -9 05. (40) Hoer, A.; Hoer, D.; O berdis s e, E. Bio c hem. J. 1990, 270, 715- 7 19. 回 Nog imo ri , K.; Hug he s, P. J .; G lennon, M. C.; Hodg so n, M. E.; Putn e y, Jr., J. W.; Shears, S. B. J. Bio l . Chem. J.9CJ1 , 266, 16499-16506. [42 ] Shears, S. B.; Pa rry, J. 止 Tang , E. K. Y.; Irvin e , R. F.; M i야 ell, R. H.; Kirk, C. J. Bio c hem. J. 1987, 246, 139 -1 47. [43 )B alla, T.; G u illem ett e, G.; Baukal, A. J.; Catt, K. J. J. Bio l . Chem. 1987, 262, 9952-9955. [44 ) Gawler, D. J.; Pott er , B. V. L.; Gig g, R.; Nahorski , S. R. Bio c hem. J. J.9CJ1 , 276, 163 -1 67. 〔 4회 Ivorra, I.; Gig g, R.; Irvin e , R. F.; Parker, I. Bio c hem . J. J.9CJ1 , 273, 317- 321. (46) Cosgr ov e, D. J., Inosito l Phosph ate s , the ir Chemi str y , Bio c hemi st r y and Phys i o l ogy , Elsevie r , Amste r dam, 1980. 〔 4 기 Este v ez, F.; Pulfo rd , D.; Sta r k, M. J. R.; Ca rter , A. N.; Downes, C. P Bio c hem. J. 19'J4, 302, 7()<)-716. [48 ] H awk ins , P. T.; Poy ne r, D. R.; Jac kson, T. R.; Letc h er, A. J.; Landerm D. J.; Irvin e , R. F. Bio c hem. J. 19')3, 294, 929 一 934. [49 )S p ier s, I. D. ; B arker, C . J.; Chung , S. K.; Chang , Y. T.; Freeman, S.; Gar- din e r, J. M.; Hirs t, P. H.; Lambert , P. A.; Mich ell, R. H.; Poy ne r, D. R.; Schwalbe, C. H.; Sm ith, A. W.; Solomons, K. R. H. Carbohyd r . Res. 19%, 282, 81- 9 9. [50 )M ayr , G . W.; Radenberg, T.; Thiel, U.; Vog el , G.; Ste p h e ns, L. R. Carbo-hyd r . Res. 1992, 234, 247 -262. [51 )M iko shi ba , K.; Hutc h et, M.; Changu e x, J. P. Dev. Neurosci. 'J!J79 , 2, 254- 275. @]S up at t ap o n e, S.; Worley, P. F.; Baraban, J. M.; Sny de r, S. H. J. Bio l .
Chem. 1988, 263, 1530 -1 534. [53 ] Maeda, N.; N 向 be , M.; Nakahir a , K. ; 畢 坤i ba, K. J. Neuro 야血 1988, 51, 1724-1 730. [54 )Maeda, N . ; N i ino be, M.; M i ko sh iba , K . EMBO J. 1990, 9 , 61-67. 〔 5 회 Furuic h i, T.; Yoshik a wa, S.; Mi ya waki, A.; Wada, K. ; M aeda, N.; Mi kos hi ba , K. Natu r e 1989, 342, 32 -3 8. (56) Miko sh iba , K. Trends Phannacol. Sc i. J.9CJ3, 14, 86-89 . 詞 Furuic hi, T.; M ilco shi ba , K . J. Neurochem. J.9CJ5 , 64, 953 -960.
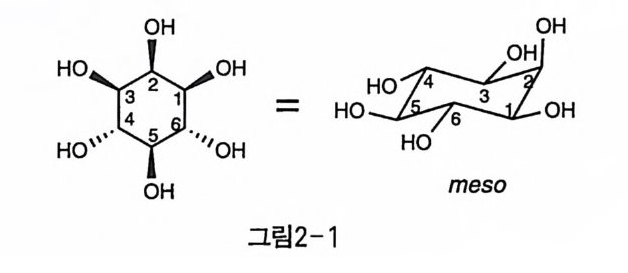
제 2 장 이노시톨의 구조 및 형태 2-1 이노시톨의 구조 이노시톨온 포도당과 같은 분자식 (C 버 u06) 을 가진 탄수화물의 일종 이다. 화학적인 면으로 보면, 탄소로만 이루어진 육각형 고리에 수산 기가 각 자리에 치환된 cyc l ohexane hexol 의 구조를 가진다(그림 2- 1). 1850 년 Scherer 에 의해 처음 발견되었는데 [1] , 심장의 근육으로부터 분 리되었다고 해서 근육을 뜻하는 그리스어 어간인 〈in os it〉라고 명명되 었다가, 후에 알코올을 뜻하는 접미사 〈 ol 〉이 붙어 in os it ol 이라는 이름 울 갖게 되었다. 처음 발견된 이노시톨은 광학 활성이 없었으므로 mesa- i nos it ol 이라고 불렸는데, 이후에 발견된 다른 6 개의 이노시톨
 HO OH OH - HO~亨 ’oHH
HO OH OH - HO~亨 ’oHH
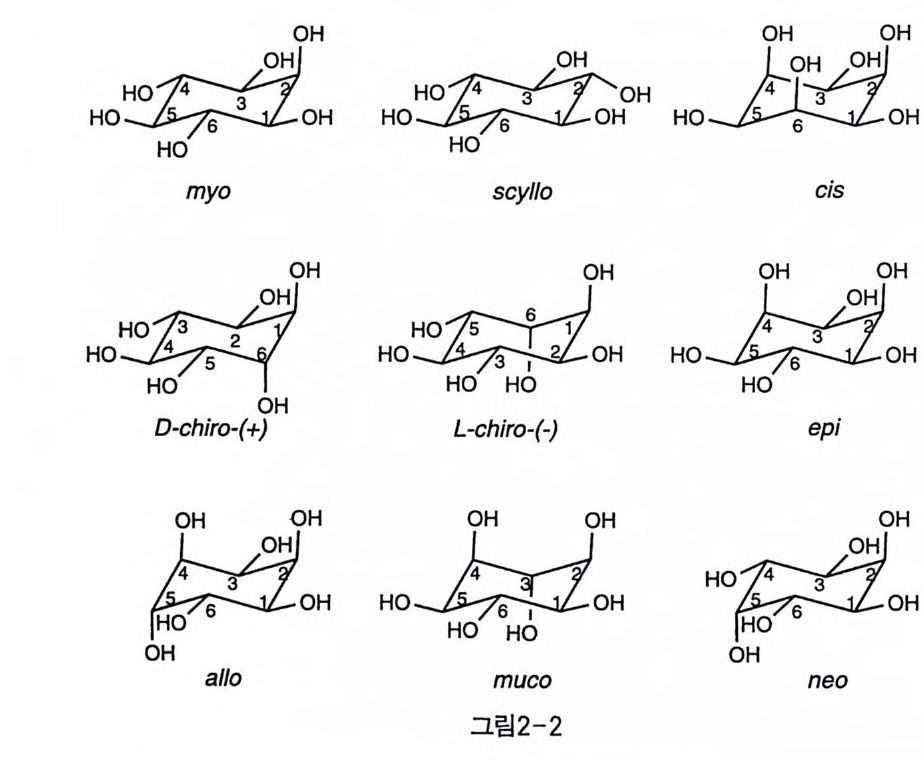
입체 이성질체들이 모두 광학 활성이 없는 메조 형태임이 밝혀진 뒤에 도 오랫동안 이 첫 이노시톨은 mesa- i nos it ol 이라는 이름으로 불렀다. 1894 년 Bouveaul t는 이노시톨에 모두 9 개의 입체 이성질체가 가능함 울 예측하였고(익, 각각이 발견 또는 합성됨에 따라 고유의 이름을 붙 였다(그림 2 一 2)(3) . 9 개의 이성질체 중 이전에 meso 로 불리던 m y o 를 포함하여 7 개 (allo, cis , epi , muco, my o, neo, scyl lo ) 는 분자 내 부에 대칭면이나 대칭축이 존재하여 광학 활성이 없는 meso 화합물이고, 나 머지 두 개는 거울상 이성질체의 쌍인 (+)와 (-)ch i ro- i nos it ol 이다 . 이노시톨들은 일반 탄수화물과는 달리 고리 안에 산소가 포함되어 있지 않고 탄소만으로 이루어 진 고리를 뼈 대로 가지므로, c y c lit ol 이 라 고도 불리 는 carbocyc l ic carboh y dra t e 의 일종이 기 도 하다〔미 .
 HO~긴 。H H HOH:HOH HO::
HO~긴 。H H HOH:HOH HO::
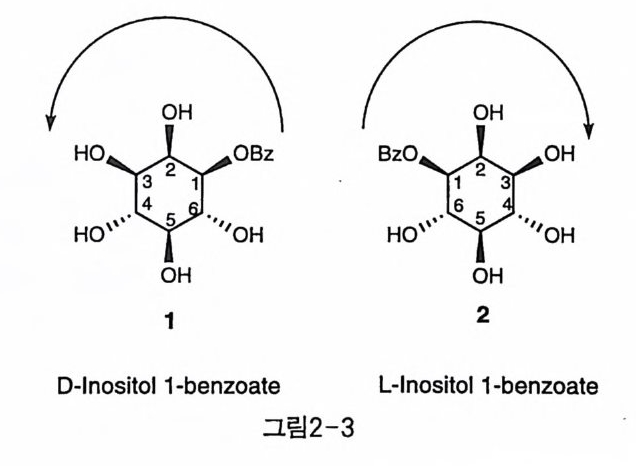
일반적으로 이노시톨울 포함한 c y cl it ol 에 이름을 붙이는 것과 각 탄 소에 번호를 매기는 일은 기준에 따라 대단히 복잡한 문제들을 야기한 댜 이 분야에 익숙한 연구자들조차도 제각기 다른 명명법을 고안, 사 용함으로써 심각한 혼란이 있었다. 거기다가 이노시톨 분자 자체의 구 조적 복잡성 때문에 가장 잘 고안된 명명법조차 많은 문제점을 가지고 있었다 그래서 비교적 최근까지도 이노시톨의 명명법은 IUPAC(lnte m a- tion al Un ion of P ure and Ap pli e d Che mi s try)의 연구 대상이었다 (4). 각 입체 이성질체 이노시톨들의 번호매김은 그림 1-2 에 나타내었으 며, 여기서 복잡한 설명은 피하고 자연에서 가장 풍부한 미오이노시톨 의 예를 들어보도록 한다. 그림 2-1 에서 보는 것처럼 미오이노시톨은 C - 2 와 C-5 를 가로지르는 대칭면이 존재한다. 이것은 탄소의 번호를 매기는 데 두 가지 방법이 가능함을 의미한다. 만약 이 C - 2 와 C-5 에 치환체가 도입된다면 광학적 비활성이 계속 유지되겠지만, 다른 위치 에 치환체가 붙을 경우 대칭이 깨어지고 두 개의 거울상 이성질체 쌍 이 생겨날 것이다. 예를 들어 C-1( 또는 C-3) 에 벤조일기가 도입된 Inos it ol-1-benzoa t e 을 살펴보자(그림 2-3). 이 경우 치환체에 가장 작 은 숫자가 할당되도록 한다면 1, 2 모두 벤조일기의 위치가 1 번이 되어
 HO OBz BzO
HO OBz BzO
야 한다. 이때 관습상 반시계방향으로 번호매긴 것을 D- 로 하고, 시 계방향으로 매긴 것울 L- 로 명명한다. 그리고 가능하면 표현의 일치 를 위해 D- 형태로 나타내는 것이 추천되고 있다. 2— 2 형태 해석 시클로핵산 고리가 처음 알려졌을 때에는 평면 구조를 가지고 있으 리라고 추측되었는데, 탄소 원자의 사면체 구조를 고려해 보면 평면 구조가 심한 변형을 겪게 될 것이라는 반론이 만만치 않았다. 이에 따 라 두 가지 안정한 비평면형 구조로서 〈의자〉 모형과 〈배〉 모형 (그림 2-4) 이 제안되었고, 이를 뒷받침할 만한 전자 회절, X 선 회절, 분광 학 및 열역학적 특성 연구들에 의해 대부분의 고리는 〈의자〉형을 이루 고 있음이 밝혀졌다〔 3 〕 .
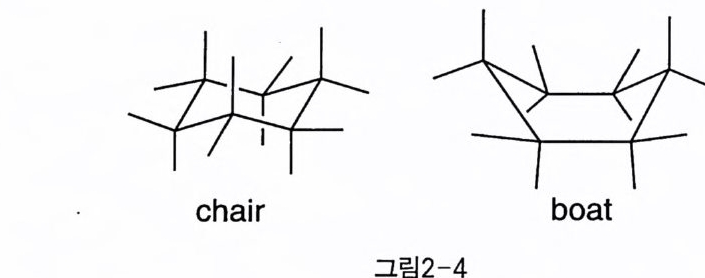 chair boat
chair boat
의자 형태의 시클로헥산은 두 가지 형태 즉, 수직 방향(axi al) 과 수 평 방향 (e q ua t o ri al) 의 치환기를 가질 수 있다. 치환기가 붙어 있지 않 은 시클로헥산인 경우 이 의자 구조는 그다지 단단하지 못하여 또다른 의자 형태로 쉽게 전환될 수가 있다. 그 결과 원래 수직 방향이었던 치환기들은 모두 수평 방향으로 바뀌고, 그 역도 성립한다(그림 2-5). 이러한 같은 분자의 다른 배열 방식을 형태 (co nfo rma ti on) 라고 한다.
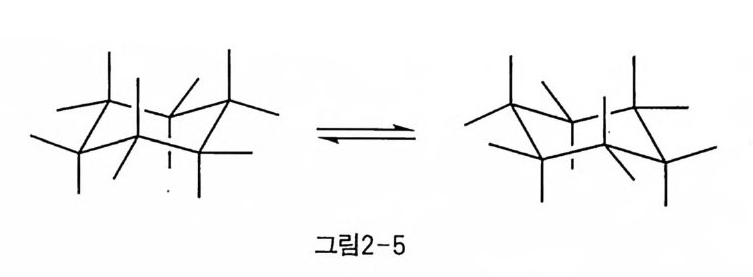 그림 2-5
그림 2-5
여기에 부피가 큰 치환기가 붙게 되면, 수평 방향인 경우에 수직 방 향보다 공간적 배경에 충분한 공간을 확보할 수 있어서 의자 형태의 변형이 어렵게 된다. 죽, 1, 3 수직 치환체 간의 입체 장애를 줄여서 에너지 면에서 더 안정하게 되는 것이다. 미오이노시톨의 X 선 회절 구조는 위에서 예측한 대로 5 개의 OH 기 가 수평 방향이며, 1 개가 수직 방향인 의자 형태를 가지고 있음울 보 여주었다〔회 . IR 〔이과 NMR(7) 등의 물리적 측정값들 역시 이 구조를 뒷받침하였다 . 나머지 이노시톨들도 기본적으로 의자 구조를 가지며, 가 능한 한 수직 방향의 OH 기가 적은 형태를 가질 것으로 추측할 수 있 다(그림 1-2). 수직 방향의 OH 가 세 개인 이노시톨들은 가능한 두 가 지 의자형이 동등하게 안정할 것인데, ci s- 와 muco- 의 경우는 두 형 태가 겹쳐질 수 있어서 구분이 되지 않는 반면에 a /l o- 는 각 형태가 거울상을 가지고 있어서 상온에서는 분리할 수 없는 라세미 혼합물로 존재한다(그림 2-6) . An gy al 은 이노시톨의 형태를 이용하여, 비결합 상호 작용의 정량적
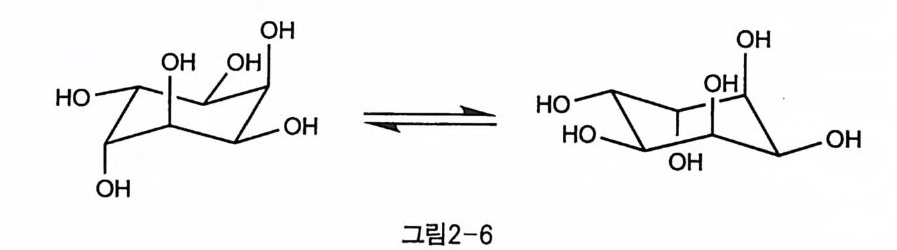 HO 广H OH 근 HOH~OOH H
HO 广H OH 근 HOH~OOH H
기초를 마련하였다. 그는 비결합 상호 작용이 전혀 없는 가상의 이노 시톨에 대한 상대값으로 모든 이노시톨의 자유에너지를 계산하였다 . my o 3.0, scyl lo 3. 2, chir o 3. 55 , D —ch ir o 4.0, neo 4. 3, ep i 4.9, allo 5.05, muco 5.1, cis 8 . 05 〔인 이 수치들은 산 촉매 하에서의 이 노시톨 에피머화 반응의 평형 상수와도 잘 일치한다〔 9 〕 . 이 결과에 의하 면 , 수직 방향의 수산기를 전혀 갖지 않는 scy llo 보다 m y o- i nos it ol 이 더 안정함을 나타낸다. 이것이 자연에서 m y o- i nos it ol 이 가장 풍부하 게 존재하는 이유일지도 모른다. 2-2-1 인산화의 영향 이노시톨 고리의 수산기에 인산화가 되는 경우에도 인산기가 포화 상태, 즉 IP6 가 아닌 경우에는 의자 형태에 큰 영향을 미치지 않는 것 으로 보인다. 한편 m y o-lP 려 경우, 나트륨 염의 X 선 구조가 예상과 는 달리 의자 형태가 역전된 5- 수직 /1- 수평의 구조를 나타낸다는 것 이 밝혀졌다 n 이 . 일반적으로 불안정한 역전 구조를 이루는 추진력은 두 가지로 나누어 생각해 볼 수 있다 . 첫째는 분자 내 정전기적 및 입 체 상호 작용이다. 이웃한 수평 방향의 인산기가 해리되어 음전하를 띠게 되면 서로 밀치는 힘이 작용하게 되어, 상호 수직 방향으로 배향 될수록 이러한 정전기적 반발력을 줄일 수 있다는 것이다. 물론 이 경 우 1, 3 번 위치의 수직 방향 치환기 간의 비결합 상호 작용은 불리한 쪽으로 작용할 것이다. 그러나 여기에 두번째 요소인 이온 및 수소 결 합이 중요한 역할을 담당한다. 1, 3 번 위치의 수직 방향으로 배향된 인 산기들 간에는 수소 결합이 가능한데, 여기에 나트륨이 치환되어 이 결합이 더욱 단단해지는 것이다(그림 2-7). p H 가 점점 낮아지게 되 면, 나트륨들이 수소 이온으로 치환되어 이 이온 결합들이 상대적으로 약한 수소 결합으로 대체됨으로서 의자 형태는 다시 역전될 것으로 생
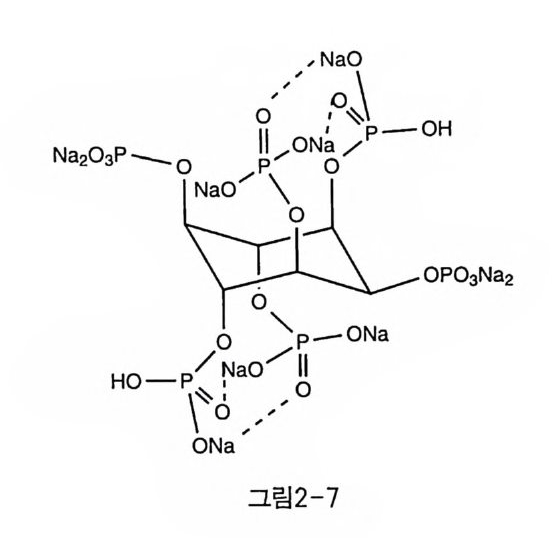 Na2°3P-o 2 『\ /'’ ,ONNa:〉 o P -0H
Na2°3P-o 2 『\ /'’ ,ONNa:〉 o P -0H
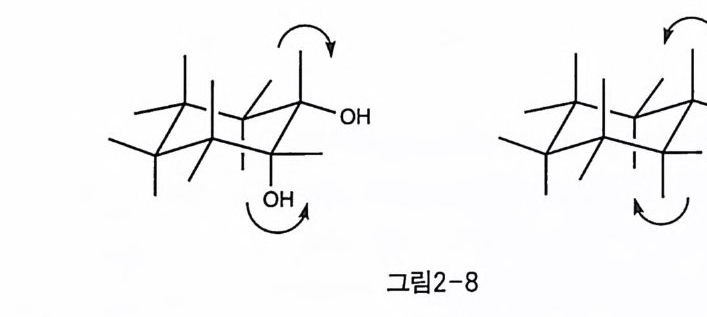
각할 수 있다 . 이러한 사실은 훨씬 이전에 전위차 적정(p o t en ti ome tri c titr a ti on) 에 의해 제안된 바 있었는데 (11), 31P -NMR 연구를 통해 다시 확인되었다(1 2). 2-2-2 아세탈의 영향 이노시톨 고리가 변형이 되지 않은 완전한 의자 형태라면, 이웃한 수평 방향의 수산기 간의 거리는 시스 관계에 있는 수직-수평 방향 수산기 간의 거리와 동일하다. 그러므로, 시스 혹은 트란스 간의 고리 형 아세탈의 형성은 두 경우에 동등하게 일어날 것으로 기대할 수 있 다 . 이때 형성되는 고리형 아세탈은 오각형으로서 탄소 원자간 결합각 의 변형을 최소화하기 위하여, 동일 평면성을 유지하려는 경향을 가진 다 . 결과적으로 고리 아세탈에 참여하는 두 이웃한 수산기는 준평면 울 이루고자 하는 방향으로 변형을 일으킬 것이다. 시스의 경우(그림 2-8), 수직 방향의 수산기는 고리의 바깥쪽으로 향하는 변형을, 수평 방향의 수산기는 고리의 안쪽으로 향하는 변형을 일으키는데, 이노시
톨 고리의 입장에서는 두 변형이 모두 이노시톨 고리를 더 평평하게 만들어서 결합각을 크게 할 것으로 예측된다. 한편 트란스의 경우(그 림 2-8) 에는 두 수산기가 모두 이노시톨 고리의 바깥으로 향하는 변형 울 일으켜, 이노시톨 고리는 변형이 더욱 접혀서 탄소간 결합각은 작 아지고, 에너지 면에서 불리하게 된다. 이러한 이유로 고리화 반옹이 열역학적인 조건에서 진행된다면, 먼저 시스 아세탈이 형성되고 트란 스 아세탈은 더 격렬한 조건에서 형성될 것이다. 이러한 예측은 실제 로 이노시톨의 고리 아세탈화 반응으로 확인되었다 (13 〕 .
 f
f
최근에는 I(1,4)Bz2 의 시스 및 트란스 아세탈 유도체(그림 2 - 9) 가 단 결정으로 얻어졌고, X 선 결정 구조 연구로 위 가설들의 옳음이 직접 적으로 증명되었다(1 4).
 >OH <
>OH <
이노시톨 고리를 이루는 6 개 탄소의 내면각의 합이 클수록, 그 이면 각의 합이 작을수록 이노시톨 고리는 평평하다고 볼 수 있다. 미오이 노시톨의 결정 구조〔회에서는 내면각의 평균값은 110., 이고, 이면각 의 평균값은 56 . 8° 였다. ab ini t o 계산에 의한 결과도 결정 구조와 거 의 일치하는 값을 나타내었다(내면각 111 .2 °' 이면각 55.3°)[1 5 ] .그 림 2-9 의 시스 아세탈인 경우 내면각이 112.8° 이고 이면각이 49.o 로서 고리 전체가 평평하게 펼쳐진 것을 알 수 있다. 한편, 트란스 아세탈 인 경우 내면각이 110.0 ° 이고, 이면각이 58 . 50° 로서 그 효과가 시스인 경우보다는 작지만, 이노시톨 고리의 접힘이 자유 이노시톨에 비해 더 심해진 경향성을 나타낸 것이다(1 4) . 참고문헌 ( 1) Scherer, J. Ju stu s Lie b ig s Ann. Chem. 1850, 73, 322-32 8. 띠 Bouveault, L. Bull. Chim . Soc. F r. 1 894, 11, 144. [3) Poste m alc, T., The Cy cl ito l s, 1965, Holdenday, San Fransis c o. (4) IUPAC, Bio c hem. J. 1989, 258, 1. [5] R abin o wi tz, I. N.; Kraut, J. Acta Cry st . 1964, 17, 159 -168. (이 Barker, S. A.; Bourne, E. J.; Ste p h e ns, R.; Whiffen , D. H. J. Chem. Soc. 1954, 3468 -3 473. (7) Lem ieu x, R.; Kulli ng, B.; Bernste in , H.; Schneid e r, W. J. Am. Chem. Soc. 1957, 79, 1005 -1006. (8) Eli el, E. L.; Alling er , N. L.; Ang ya l, S. J.; Morr iso n, G. A., Confo n nati on al Analys i s , Joh n Wi ley, New York, 1965, p 357. (9) Ang ya l, S.; Gori n, P.; Pit ma n, M. Proc. Chem. Soc. 1962, 337. (10) Blank, G. E.; Pletc h er, J.; Sax, M. Ac ;ta Cry st . 1975, B31, 2584-2592.
(I I) Barre, R.; Cou rtoi s , J. E.; Wonnser, G. Bull. Soc. Chim . Bio l. 1954, 36, 455. (12) Coste l lo, A. J. R.; Glonek, T.; My er s, T. C. Carbohyd r . Res. 1916, 46, 159-171. (13) Ang yal , S.; Tate , M.; Gero, S. J. Chem . Soc. 1961, 4116-4122. (14 ) Chung , S. K.; Chang , Y. T., Whang , D.; Kim, K. Carbohyd r . Res., 1996, 295, 1-6. U 회 Lia n g , C.; Ewig , C. S.; Sto u ch, T. R.; Hag le r, A. T. J. Am. Chem. Soc. 1994, 116, 3904 -3 911 .
제 3 장 이노시톨의 화학 이노시톨울 포함한 탄수화물들은 아미노산처럼 다양한 작용기를 분 자 내에 가지고 있지는 않지만, 다수의 수산기(아민기를 포함하는 탄수 화물도 있지만)를 함유하고 있다. 따라서 탄수화물의 화학에서는 이들 수산기들 간의 반응성 차이를 이용하는 선택적인 ·보호 및 탈보호 등 위치 선택성이 중요한 연구 대상이 되어왔다. 일반적인 탄수화물에서 는 고리에 산소 원자가 끼여 있음으로 인해 발생하는 아노머 효과, a 와 p 이성질체의 존재를 포함하는 고리의 동력학적인 여닫힘 등으로 인해 일반적으로 반응 결과가 복잡하게 나타난다. 반응 생성물이 단일 하게 나타나는 경우도 그 반응 조건이 입체 구조가 다양한 탄수화물 전반에 일반적으로 적용되지 않고, 시행 착오에 의해 얻어진 특이한 조건인 경우가 많다. 이에 비해 이노시톨은 탄소로만 고리가 형성되어 있어 고리 열림 반응이 일어나는 경우가 드물고, 입체 전자적 효과 (O- 탄수화물에서의 아노머 효과와 같은)도 그다지 두드러지지 않아 서, 탄수화물의 형태 분석을 위한 안정한 모델로 사용되기도 하였다. 이 장에서는 탄수화물의 일종으로서의 이노시톨에 대한 반응들과 특정 한 유도체를 형성하기 위해 사용된 이노시톨의 독특한 반응성들, 그리
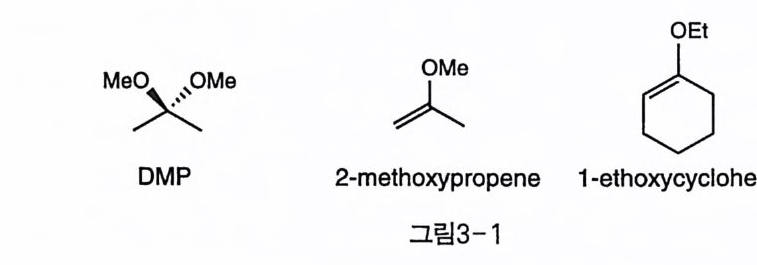
고 다양한 물리 화학적 성질을 다루기로 한다. 3-1 Diol 보호 이웃한 수산기를 다수 가진 탄수화물이나 이노시톨의 경우 선택적인 보호기의 도입을 위해 이웃한 두 수산기를 하나로 묶는 전략을 우선 생각해 볼 수 있겠다. 이런 목적으로 가장 많이 사용된 것은 아세탈 (acetal)이다. 아세탈은 카르보닐기를 가진 화합물과 디올 간에 물 한 분자가 빠지는 축합 반응을 통해서 일어나는데, 엄밀하게 말하면 알데 히드인 경우에만 아세탈이라고 불러야 하고 케톤과 이노시톨이 결합한 다면 케탈(ketal)이라고 불러야 하겠지만, 탄수화물에서는 관습적으로 통칭하여 아세탈이라고 부른다. 많이 사용되는 아세탈은 isopropylidene(acetonide, Ace), cyclo-hexylidene(Hex), cyclopentylidene이 있고 benzylidene이 사용된 예도 있다. 초기 에 는 cyclohexanone을 사용하고, 산 촉매 하에서 Dean -Stark 장치로 물을 제거하면서 cyclohexylidene을 만들었다〔1). 차차 아세탈 생성은 2, 2-dimethoxypropane(DMP)을 사용하여 아세탈의 알 코올 치환 반응을 이용하는 것이 일반화되었고, 보다 더 반응성이 큰 2-methoxypropene이나, 1-ethoxycyclohexene이 반응의 속도론적 조 절에서 사용되기도 하였다(그림3-1).
 MeX0 、OMe
MeX0 、OMe
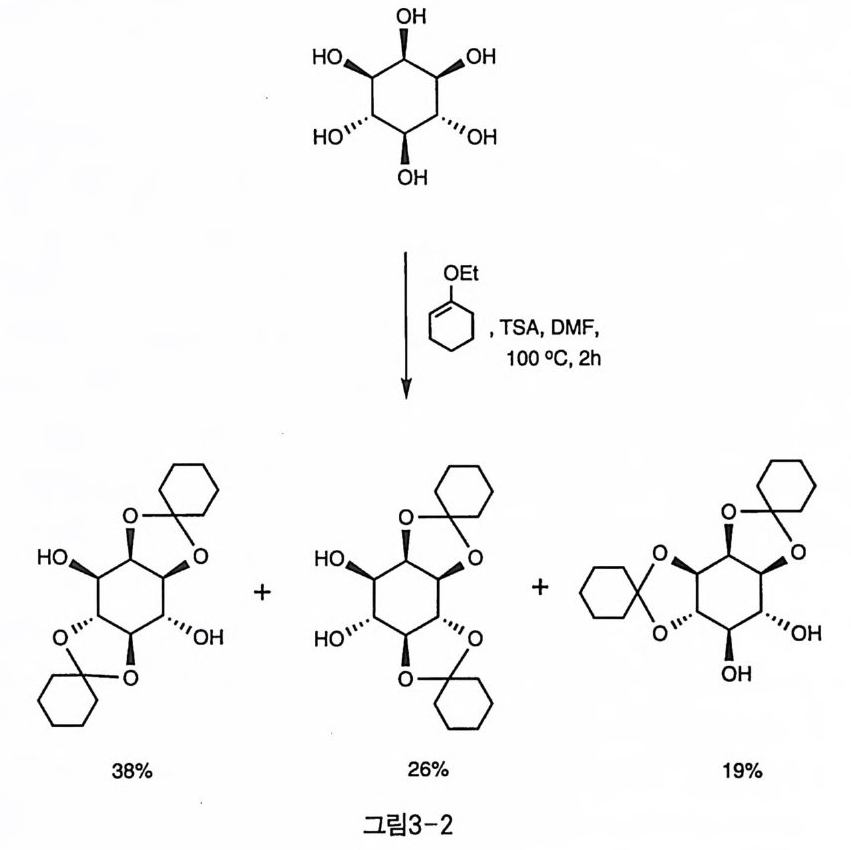
myo-inositol에서는 1, 2번(또는 2, 3번) 수산기가 시스 관계에 있으 며, 3,4와 4,5번(또는 1,6번과 5,6번) 수산기는 트란스 관계에 있다. 2장에서 살펴본 바와 같이 열역학적인 면에서 시스 아세탈이 트란스 아세탈에 비해서 더 안정하다. 그래서 평형 조건을 유지하면서 1당량 의 아세탈을 이노시톨에 도입하면, 시스 아세탈(1, 2번 또는 2, 3번)이 주로 형성된다. 2당량의 아세탈이 도입되면 세 개의 유도체가 형성되 는데, cyclohexylidene인 경우 여러 연구팀에서 시행한 실험 방법에 따 라 생성되는 이성질체들의 상대적인 양은 약간씩 차이가 있지만 비슷 한 경향을 나타내었다(그림3-2)〔2〕•
 曺占〉EOI로01g E如
曺占〉EOI로01g E如
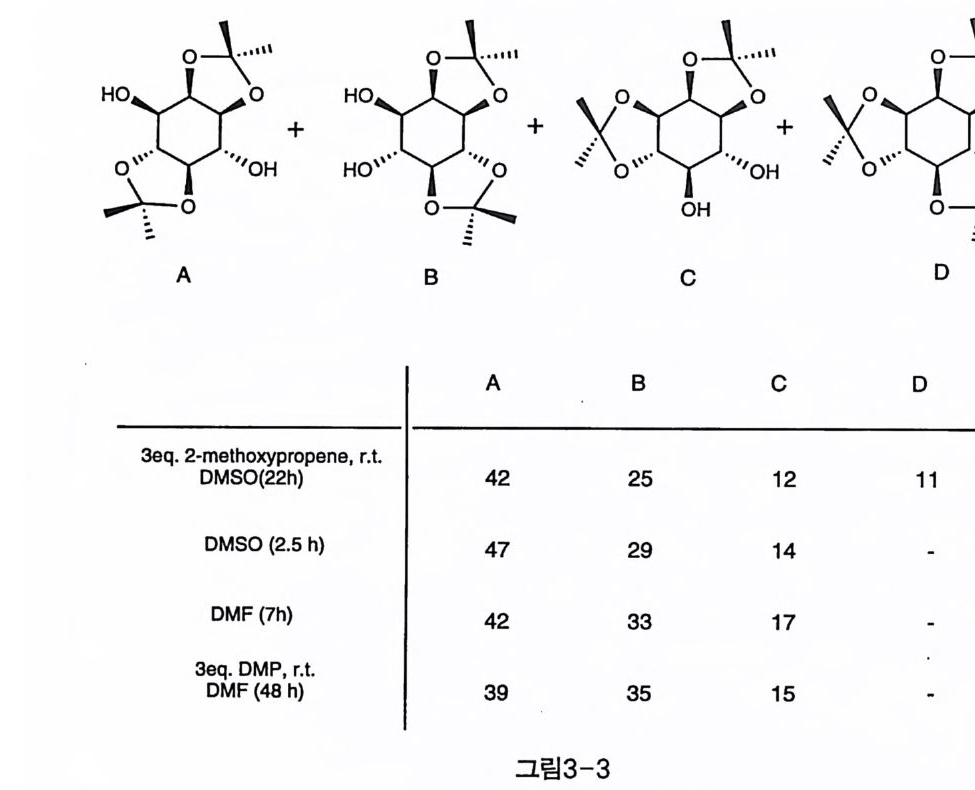
Iso p ro pyli dene 에 대해서도 반응 조건에 따라 달라지는 각 이성질체 의 생성비를 NMR 로 추적한 연구 결과가 보고되었다(그림 3-3)(3). 용 매의 극성도 생성비에 영향을 주는데, DMF 보다 DMSO 를 이용했을 경우, I (l ,2:4,5)Acez 가 조금 더 우세하게 생성되며, 이 경우도 반응이 진행되면서 다른 이성질체로 변해 가는 경향을 보였다. I(l , 2)Acez 가 먼저 생성된 후, 속도론적으로 I( !;2:4,5)Ace 2 가 빨리 생성되고, 평형 으로 이동하는 경향을 보이는 것이다. 가열 조건에서 반응하여 평형을 이룬 경우(1 ,2:4,5): (1 , 2 : 5,6):(1 , 2:3,4) 의 비는 대개 2:2 : 1 정도이다 . 생성되는 이성질체들은 부분적인 재결정과 실리카젤 칼럼 크로마토그 래피를 통해 분리되었다. 여기서 얻어진 각 이성질체들은 다양하고 유
 : 축 ~ 5
: 축 ~ 5
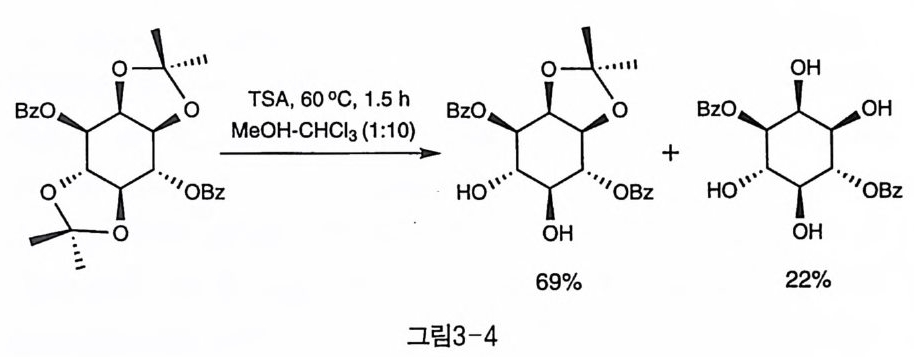
용한 이노시톨의 유도체 합성에 널리 이용되고 있다 . 시스와 트란스 아세탈의 안정성 차이는 선택적인 가수 분해 반응에 서 잘 나타난다. 1 (1 ,4)Bzz 의 d i ace t al 을 산 조건에서 선택적으로 탈아 세탈화하면 트란스 아세탈이 떨어진 생성물이 주로 얻어진다. 이때 시 스 아세탈만이 떨어진 생성물은 전혀 얻어지지 않는 것으로 보아, 두 아세탈이 모두 가수 분해된 화합물은 트란스 아세탈이 먼저 떨어지고 시스 아세탈이 떨어진 것으로 생각된다(그림 3-4) 〔 4 〕 ,
 TSA, 60 °C, 1.5 h 。~,... ' \,... BzO O■ H
TSA, 60 °C, 1.5 h 。~,... ' \,... BzO O■ H
한편, I(l , 4)Bru 에 반응 속도론적 조건으로 아세탈기를 도입하면, 트 란스 아세탈이 먼저 생성된다. 이때 트란스 대 시스 아세탈의 비는 3:1 정도로 나타났다(그림 3-5) 〔 5). I (l ,4)Bz2 의 경우에도 비슷한 결과 롤 얻었으나, 벤질기인 경우보다 아세탈화 또는 탈아세탈화 반응이 모 두 상당히 느리게 일어남이 관찰되었다 . 그리고 반응 시간이 길어지거 나 온도를 올리게 되면 반응은 열역학적인 평형으로 이동하여 시스 아 세탈의 · 양이 점차 증가하거나 di ace t al 이 생성됨이 관찰되었다〔선 . 트 란스 아세탈이 먼저 생성되는 것은 이노시톨 고리의 수평 방향으로 뻗 어 있는 두 개의 수산기가 수직 방향의 수산기를 하나 포함하는 시스 디올에 비해 입체적 장애를 덜 받기 때문으로 생각된다 . 트란스에 대한 시스 아세탈의 열역학적 안정성에 대해서는 2 장에서 자세히 다루었다.
 ·::*::, B<:0\>OH<
·::*::, B<:0\>OH<
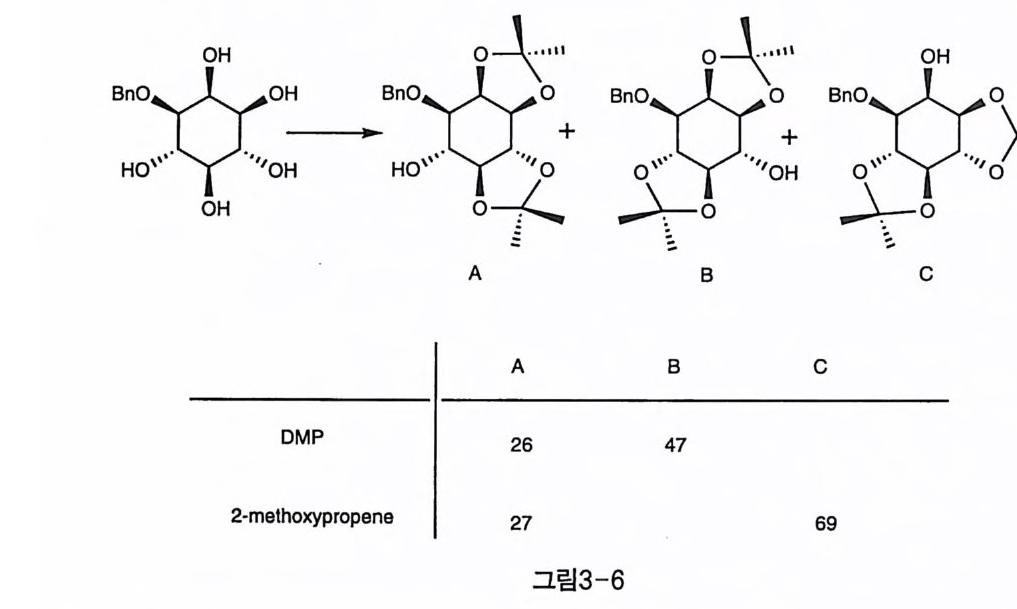
그 밖에도 보고된 선택적인 아세탈 반응들의 예를 그림3-6에 나타 내었댜 온도를 올리거나 케톤 자체 혹은 DMP를 사용하면 열역학적 조절을 받아 시스 아세탈이 우세하게 형성되는 경향이 있으며, 온도를 낮추고 보다 반응성 이 큰 2-methoxypropene이 나 1 -ethoxycyclohexene 을 사용하여 반응 속도론적 조건에서 반응하면 트란스 아세탈을 우세 하게 얻을 수 있다(그림3-6)〔3).
 HH一A B B一n:亨一Oc :Y,I
HH一A B B一n:亨一Oc :Y,I
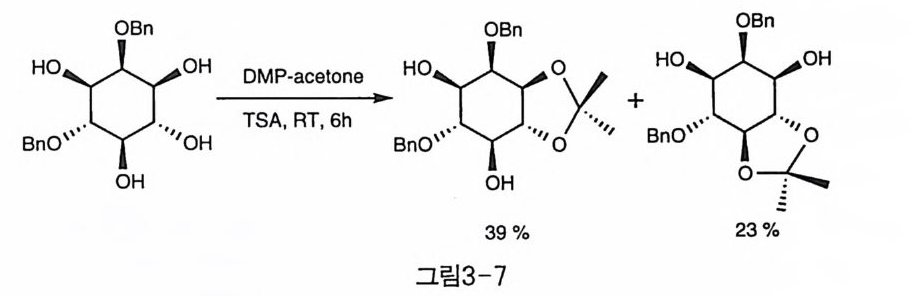
같은 트란스 아세탈인 경우에도, 3,4_아세탈보다 4,5-아세탈이 다 소 불안정한 것을 알 수 있는데, 이것은 시스 관계에 5번 수산기와 수 직 방향의 2번 수산기와의 입체 장애 때문으로 생각된다. 이러한 효과 는 2번에 보다 덩치 큰 작용기가 붙어 있거나, 아세탈 자체가 입체 장 애를 가진 경우 두드러질 것으로 예상된다(그림3-7)(6) .
 BH 二亨OBn °0Y,'+B9Bn: \
BH 二亨OBn °0Y,'+B9Bn: \
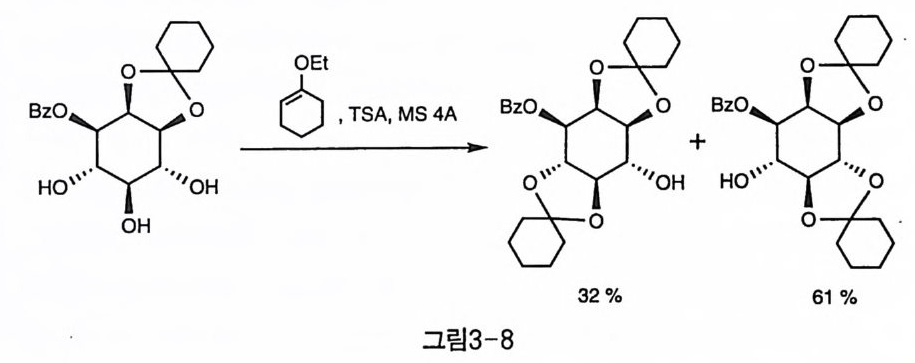
열역학적 조건인 평형 반응을 억제하기 위해서 반응성이 큰 1-ethoxycyclohexene를 산 조건 에 서 작용시 키 면서 , 분자체 (molecular sieve)를 함께 사용하여 어느 정도의 선택적 아세탈화 반응을 유도한 예도 있다(그림3-8)〔2). 그러나, 이런 예와 같이 선택성에 있어서의 분자적 수준에서의 설명이 가능할 만한 체계적인 연구는 아직 이루어 져 있지 않다.
 6OEI ,TSA,MS4A
6OEI ,TSA,MS4A
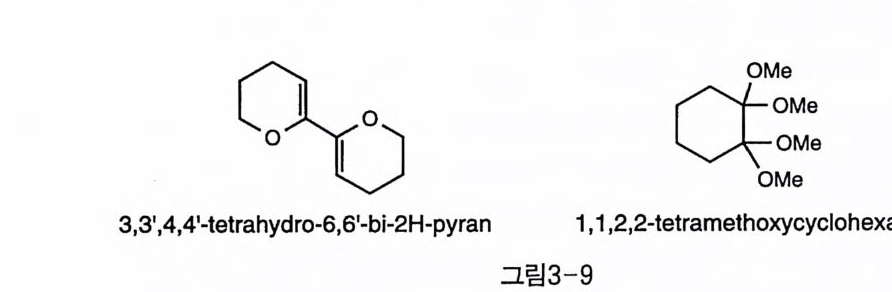
반응 속도론적인 조절을 하지 않고도 트란스 디올을 선택적으로 보 호하는 방법이 별도의 작용기를 이용해 개발되었다. 이노시톨에 적용 된 예는 아직 없지만, 탄수화물에서 시스와 트란스의 이웃한 수산기가 존재하는 경우 트란스만을 선택적으로 보호하기 위해 개발된 시약으로 는 3, 3', 4, 4' -tetr ah y dr o-6, 6' -bi- 2H-py ra n(bis - DHP) 〔까와 1, 1, 2, 2- t e tr ame th ox y c y clohexane(8) 의 예가 있다(그림 3-9) . 이들은 앞에서 예를 든 다른 아세탈들이 오각형의 고리를 형성하는 데 비해 육각형의 고리를 만듦으로써 트란스 디올에 태한 선택성을 높인 것이 특징으 로, 이노시톨에 응용된다면 유용한 보호기로 활용될 가능성이 높다.
 \ 二0M o。eMM :ee
\ 二0M o。eMM :ee
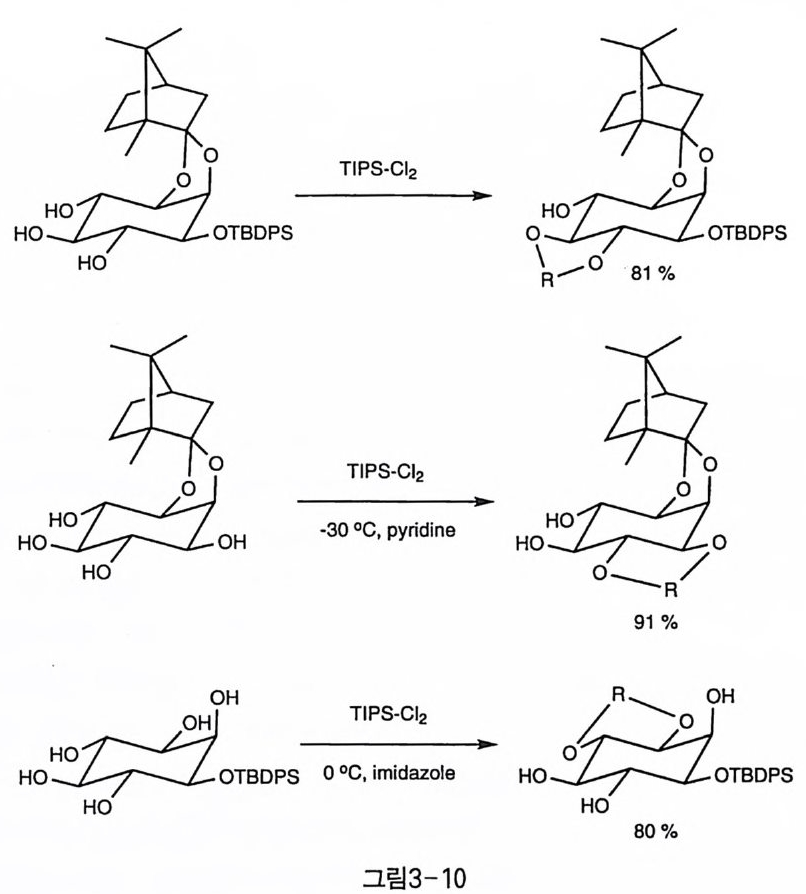
그리 고 아세 탈은 아니 지 만 이 노시 톨울 1, 3 -dic h loro -1 , 1, 3, 3 - t e trai so p ro py l di s il oxane(TIPS-Ch) 로 처리하여, 고리형 실릴기로서 트 란스 디올만을 선택적으로 보호한 예가 1989 년에 처음 보고되어 1(1 , 3, 4, 6)P4 의 합성 에 응용되 었다〔 9 〕 . TIPS 는 칠각형 의 고리 로 형 성 되 며 (그 림 4-20) 입체 장애가 큰 i so p ro py l 기를 가지고 있어서, 트란스 디올 중 에서도 4,5- 디올보다 3,4- 디올에 뚜렷이 더 큰 선택성을 보였다(그림 3-10) [10 ] . 아세탈의 제거에는 산 조건에서의 가수 분해 반응이 가장 일반적인 방법이다. 그러나, 분자 내의 다른 작용기가 산에 약한 경우에 선택적 으로 아세달만을 제거하기 위해서는 특별한 주의가 필요하다. 벤조일 과 토실기가 함께 존재하는 경우, HCl-EtO H 조건에서 환류시키면 벤
 TIPS- Cl 2
TIPS- Cl 2
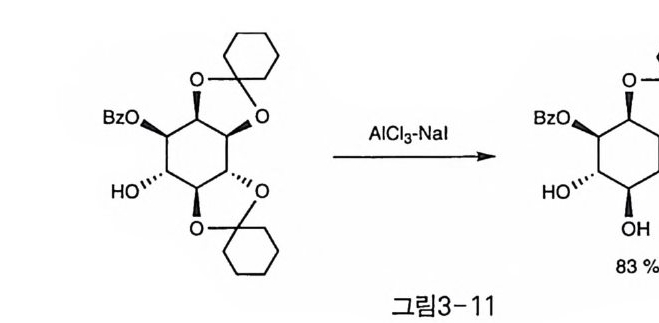
조일과 아세탈은 가수 분해되고 토실기만 유지되나, 보다 부드러운 산 인 아세트산 수용액에서는 벤조일도 유지되면서 아세탈만이 가수 분해 된다(1). 시스와 트란스 아세탈의 안정성 차이를 이용하여 트란스 아 세탈만을 부드러운 산 조건에서 선택적으로 가수 분해하는 방법은 그 림 3 一 4 에서도 그 예를 보였지만, 1 당량의 에틸렌 글리콜을 산과 함께 반응하여, 아세탈의 치환 반응을 유도하는 방법도 알려져 있다(1, 11). AlCb-NaI 조건도 시스 아세탈을 유지하면서 트란스 아세탈만을 선택 적으로 가수 분해하는 조건임이 알려졌다(그림 3 기 1) 〔 12). 실릴기가 존
 AICl3- N al
AICl3- N al
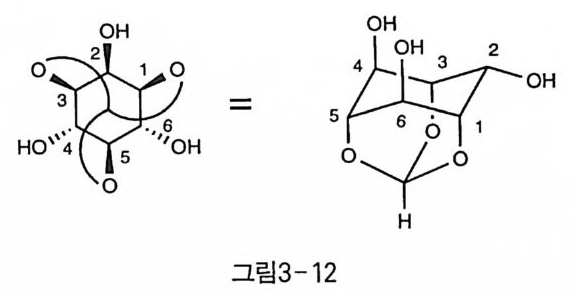
재하는 경우, HCI/M e OH, AcOH/Zn, TFA 등의 산 조건에서의 반응 은 탈실릴화 또는 실릴기의 이동 등이 부반응으로 발생하였으나, BF3- e th era t e 와 merca pt oe th anol 울 이 용하여 TBDPS 에 는 손상을 주지 않고 camph or 아세탈만을 선택적으로 제거한 반응 예도 보고되었다(1 0) . 3-2 Tri ol 보호 이노시톨에 있어 tri ol 을 한꺼번에 보호한 것으로 현재까지는 ort ho - fo rma t e 가 유일한 예이다. 이 재미있는 보호기는 1975 년 Kish i 등에 의 해 처음 소개되었고[1 3), 이후에 비슷한 방법의 합성 [14 , 15) 과 대규모 의 반응에 쓸 수 있는 개량된 방법도 보고되었다 [16 〕 . 。띠 1o fo rma t e 가 도입되면 보통 5 개의 수산기가 수평 방향이고 1 개의 수산기만이 수직 방향인 이노시톨의 의자형 구조가 반전되어, 수평이던 5 개의 수산기가 수직으로 배향된 구조를 갖는다(그림 3-12) 〔 13 〕. O rth o fo rma t e 의 경우, 형태가 보통의 이노시톨과 다른 만큼 물리적 성질이나 각 수산기들의 반응성도 상당히 달라진 양상을 보인다. 우선 1H-NMR 에서 보면 보통의 이노시톨에서는 잘 나타나지 않는, w- cou pling이라고도 알려진 원거리 짝지음(l on g-rang e cou pli n g)이 관찰 되어 상당히 복잡한 양상을 나타낸다 [14).
 OH
OH
반응성에 있어서 우선 각각 1 당량의 강한 염기 (NaH 또는 KH) 와 할 로겐화 알킬 등의 친전자체를 가하여 Sr?- 반응을 하면 먼저 4 번(또는 6 번) 수산기에 먼저 반응이 일어나고, 그 다음으로 남은 다른 수직 방 향의 6 번(또는 4 번)의 수산기가 반응한다. 결국 입체 장애가 가장 적 울 것으로 생각되는 수평 방향의 2 번 수산기가 가장 반응성이 낮은 것 이다(그림 3-13) 〔 15, 1 기. 이러한 반응성은 1,3-di axial 관계에 있는 4, 6 번 수산기 사이에 염 기의 금속 양이온이 강하게 배위되어 수산기에 생성된 음이온이 안정 화되는 것으로 설명된다. 이러한 안정화 효과를 갖지 못하는 2 번 수산 기가 반응성이 가장 낮게 되는 것이다(그림 3-14). 한편, 입체 장애가 큰 TBDPS 등의 실릴기를 도입할 때 (13, 1 선, 효 소를 이용한 아세틸화 반응(1 6), 피린딘 등의 약염기 하에서의 벤조일 화(1 8) 등에서는 2 번 수산기가 먼저 반응하는 경향을 보였다(그림 3 一 15). 또, 같은 벤질화 반응이라도 강염기 조건에서는 수직 방향의 수산기 가 벤질화되지만(1 5), 산 조건에서 반응하거나 상이동 촉매 하에서는 수평 방향의 2 번 수산기가 더 선호되는 경향을 보였다(그림 3-16) 〔 14 〕. O rth o fo rma t e 의 제거는 산 조건에서의 가수 분해 반응으로 이루어지 는데, 일반적으로 아세탈보다도 산에 강하여 아세트산 수용액에서는 비교적 장시간의 반응에도 안정하므로 HCI/M e OH 조건에서 가열하여 제거한다〔 19).
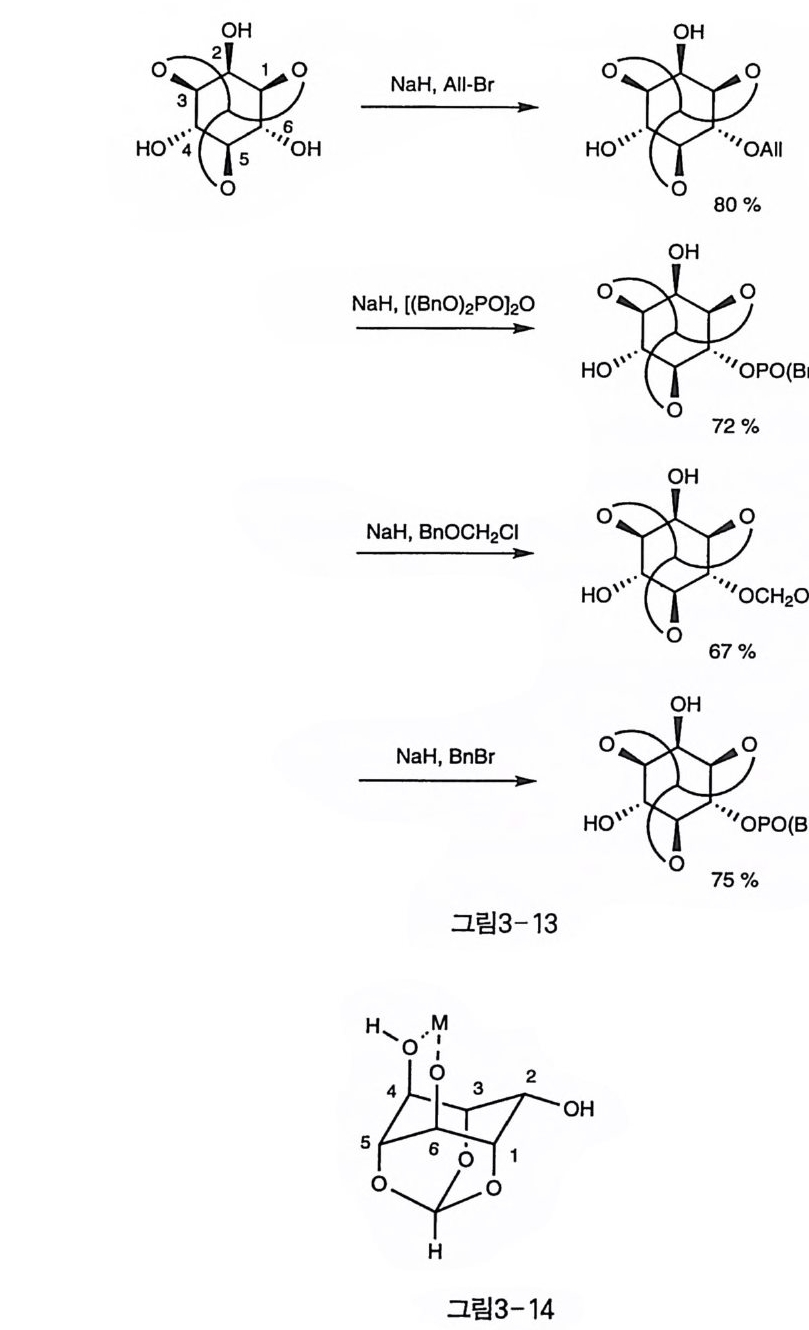 。 字OH RO %A ll
。 字OH RO %A ll
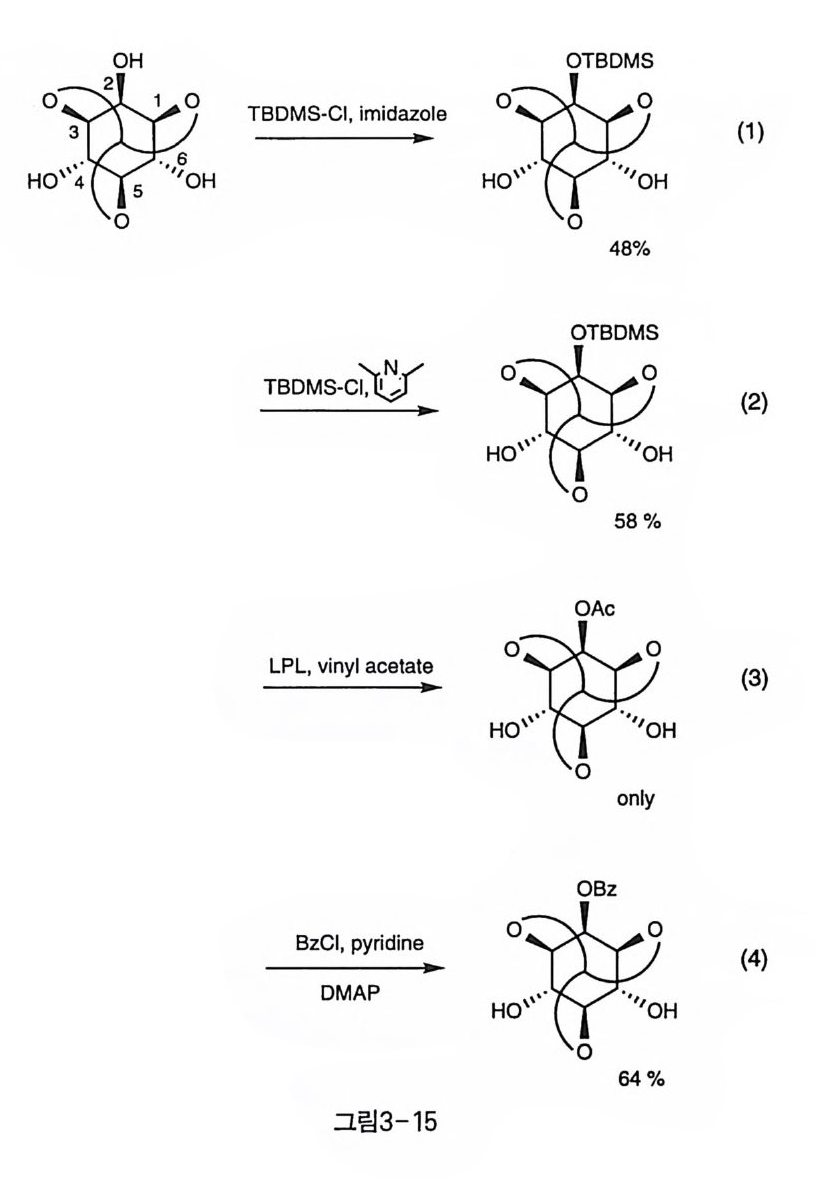 OTBDMS
OTBDMS
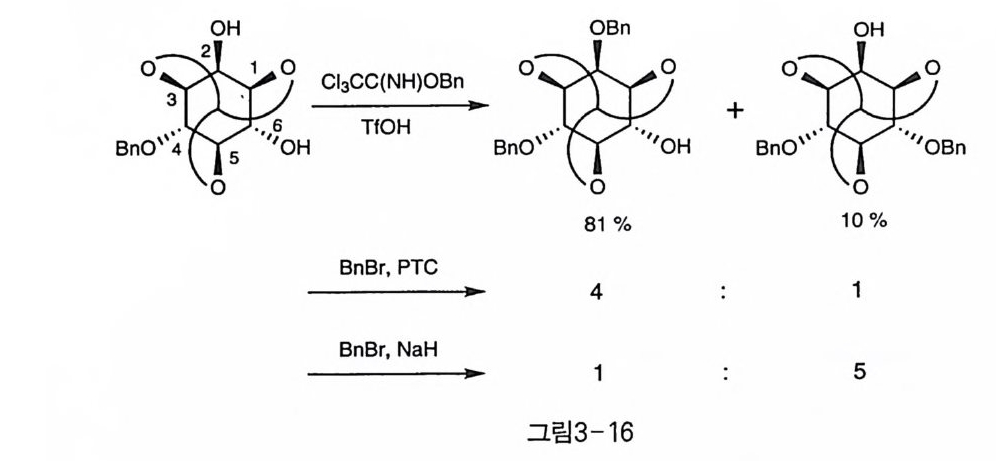 OBn OH
OBn OH
3-3 에데르 대개의 경우 에테르 (E th er) 결합으로 연결된 알킬(allcy l) 들은 산, 염기 에 안정하여, 적당한 탈알킬 반응이 존재한다면 합성에 유용한 보호기로 쓰일 수가 있다 . 이노시톨에서도 많은 알킬기가 보호기로 사용되었는 데, 대표적인 예가 벤질, 메틸, 알릴, 파라메톡시벤질, 실릴기 등이다. 3- 3 -1 벤질화 벤질기는 산과 염기에서 안정하며, 가수소 분해로 쉽게 제거될 수 있어서 매우 유용한 보호기이다 . 일반적인 벤질화 반응은 염기 조건 하 (NaOH, Nall 등)에서 BnCl 또는 BnBr 등과 반응하여 얻는다. 염기 조건에서 반응이 일어나므로 염기에 약한 에스테르기 등은 될수록 벤 질화 반응 후에 도입하는 것이 일반적인 전략이 된다. 그러나, 에스테 르기 존재 하에서의 벤질화 반응이 불가피할 경우에는 중성 또는 산성 조건에서의 반응이 요구된다. •
Oza ki 동은 산에 불안정한 아세탈과 염기에 불안정한 벤조일기를 함 께 가진 기질에 통상적인 염기 조건에서 반응했을 경우, 아실기의 이 동이 일어난 후 벤질화된 생성물이 생성됨을 관찰하였다. 이 경우 CbCC(NH)OBn 을 TfOH 조건에서 반응하여 다른 작용기들에 영향을 주지 않고 벤질기를 도입할 수 있었다(그림 3-17)(20 〕.
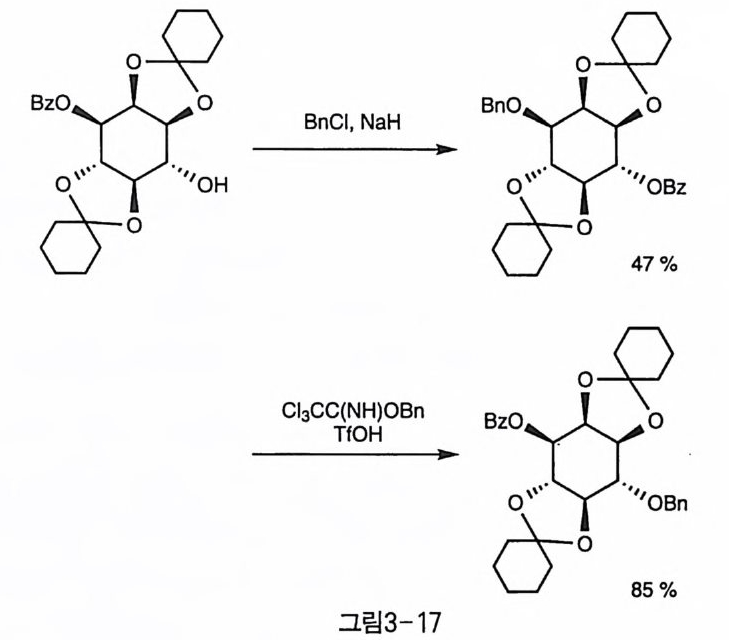 BnCI, N aH
BnCI, N aH
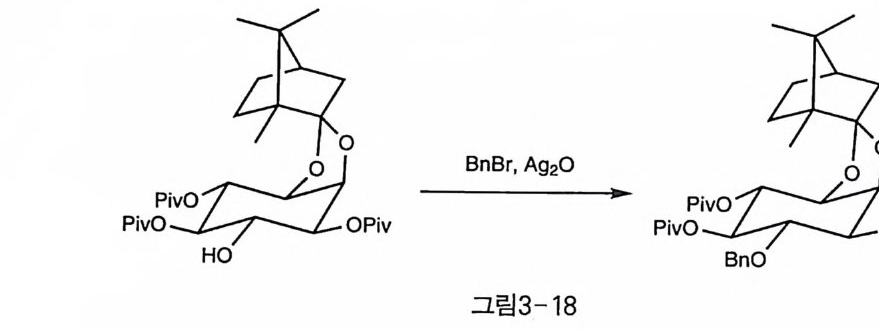
또, 주위에 pi valo y l( trim e thy lace ty l) 기와 같은 에스테르가 존재할 때 강염기 대신 BnBr 와 A g 20 를 이용하면 벤질화가 가능하였다(그림 3- 18)[2 1 ). 그러나, A g 20 를 사용하는 방법은 이웃에 시스 관계의 아세 틸기가 존재하는 경우에는 아실 이동 반응을 유도할 수도 있다 (3-4-3 참조). Sn 중간체를 이용한 방법도 있는데, 이것은 이웃한 수산기가 존재 할 경우, B lli SnO 로 먼저 물을 제거하면서 고리형 중간체를 형성하
 BnBr, Ag 2 0
BnBr, Ag 2 0
고, 중강된 수산기의 친핵성을 이용하여 천전자체를 공격하는 전략이 댜 1, 2 번의 수산기가 열려 있는 1( 3,4,5,6)BZ4 가 기질로 사용되었을 때, 수직 방향에 비해 수평 방향으로 배향된 1 번 위치에 선택적으로 벤질화된 화합물이 주생성물로 얻어지기는 하였으나, 아실 이동 또는 탈아실화된 부생성물들도 함께 얻어졌다(그림 3-19)(22 〕 . 탈벤질화 반응은 Pd-C 촉매 하에서 가수소 분해하는 방법이 중성
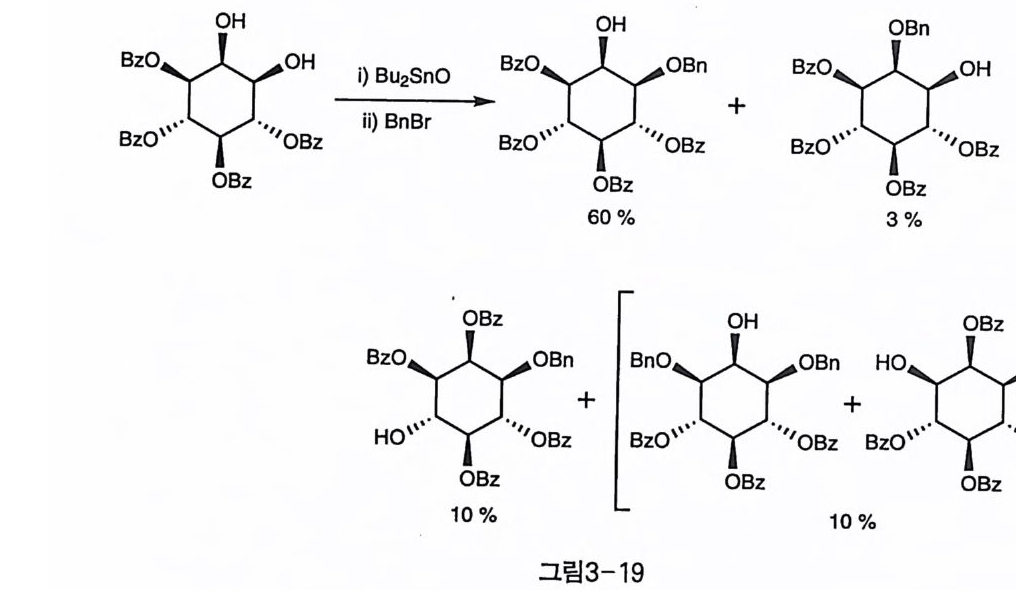 ::亨OBz 。0: Z 二·::::::¢1O0\B%:z: :::¢+:6O 0:B%z: :::: +* :Bz:o1B0z:%o + 〉巧zOBnOB ~:Hz: B仁
::亨OBz 。0: Z 二·::::::¢1O0\B%:z: :::¢+:6O 0:B%z: :::: +* :Bz:o1B0z:%o + 〉巧zOBnOB ~:Hz: B仁
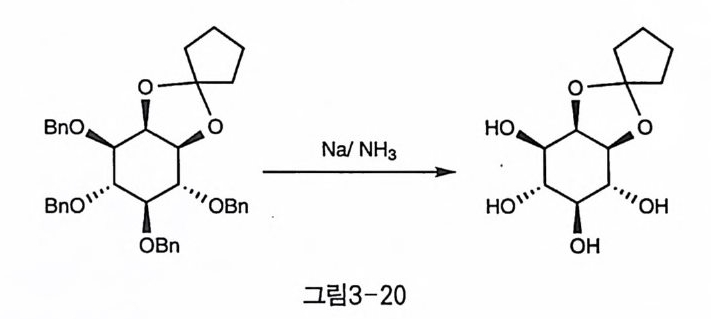
조건에서 진행할 수 있고 온도를 높이지 않아도 되므로 간편하여 널리 사용된다 . 그러나 인산에스테르의 벤질기와 함께 탈보호해야 할 경우 반응 중에 인산이 생성되므로, 산성 조건을 피해야 하는 경우에는 반응 진행 중에 염기를 첨가시키면서 산성도를 조절해야 하는 번거로움이 있 댜 도 기질의 다른 위치에 산에 약한 작용기가 있는 경우, 염기 조건 인 Na /NH를 탈벤질화 반응에 이용하는 경우도 있다(그림 3-20)(23 〕 •
 Na /N H3
Na /N H3
그러나 위의 반응들은 대량 반응 조건에는 적합하지 않아서 일반적 으로 쓰이 는 방법은 아니지 만 aceto l ys i s 방법 이 대 량 규모의 반응으로 이노시톨에 시도되었다〔 24 〕 . 벤질화되어 있는 이노시톨에 AczO/cat. ClO ◄ - 롤 가하면, 벤질기가 아세틸기로 치환되는데, 여기에 상당한 선 택성이 관측되었다. I(l,4,5,6)Bn ◄ 와 I (l ,3,4,5,6)Bns 를 기질로 사용했 을 때, 1 번과 3 번의 벤질이 다른 위치의 벤질에 비해 저항성을 가진 댜 이에 비해 IBn6 를 기질로 사용하면, 짧은 반응 시간 동안에는 어느 정도의 선택성을 보여서 2 번의 벤질기도 보존된 생성물을 낮은 수율이 지만 결정으로 얻을 수 있었는데, 반응 시간이 길어지면 여러 가지 다 양한 화합물이 생성되어 선택성이 떨어짐을 보여주었다(그림 3-21)(24). 직접 이노시톨에 적용된 것은 아니지만, Oza ki 등은 Bn 과 All 을 모 두 제거할 수 있는 시약으로 AlCb-PhNMez 를 개발하였다〔 25 〕 .
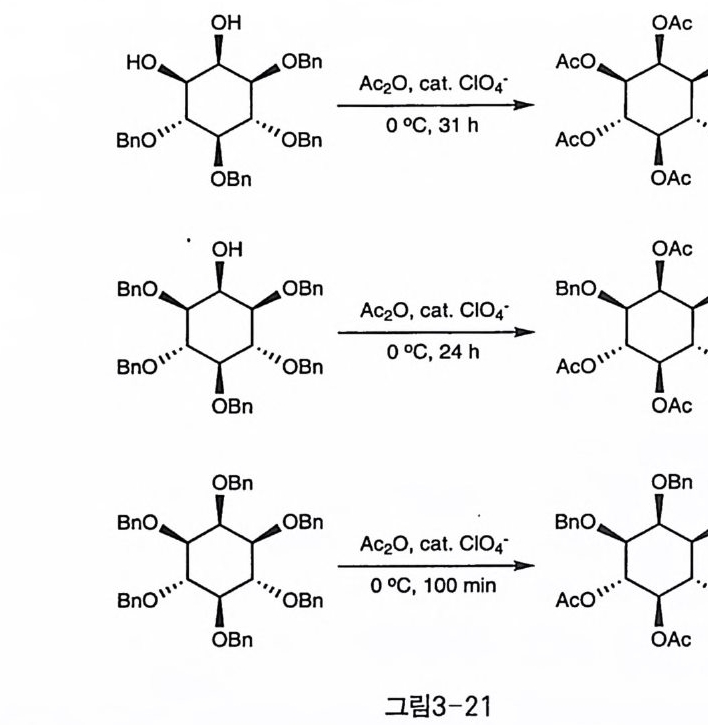 OH OAc
OH OAc
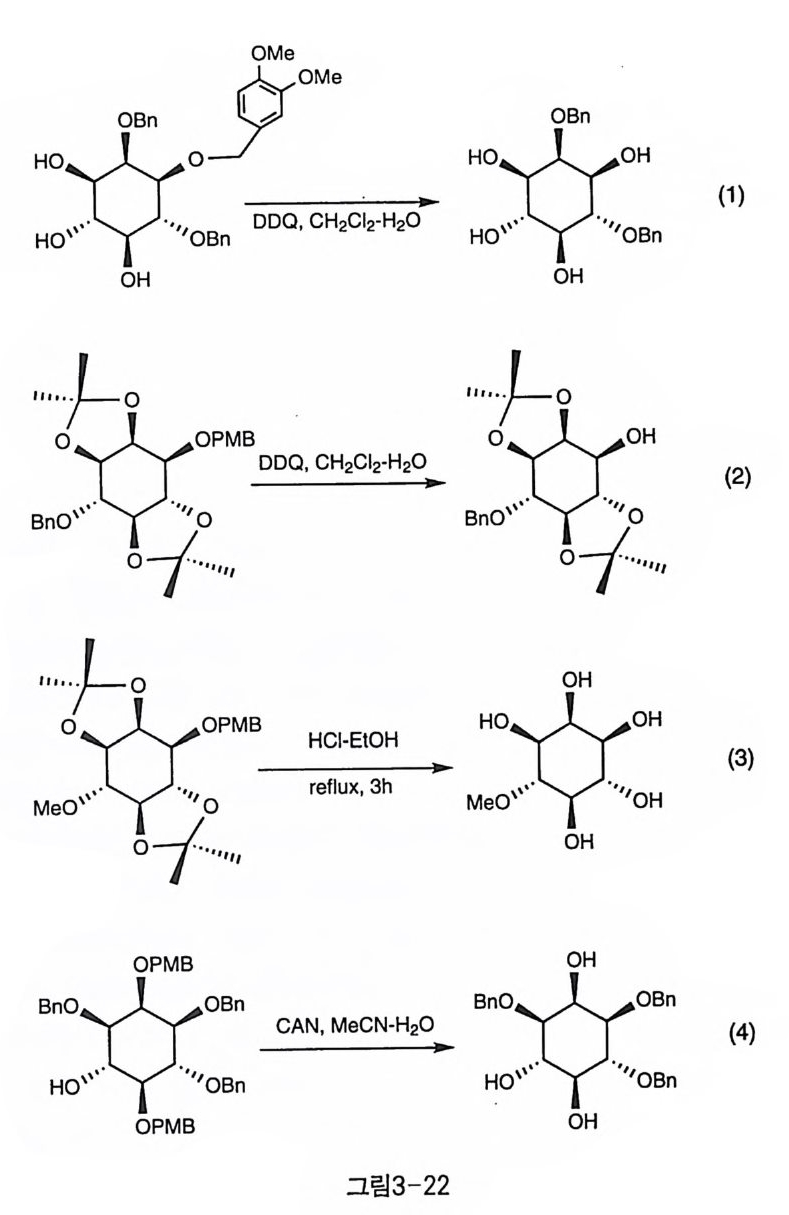
3-3-2 메톡시벤질화 p-M eth o xy be nzyl ( PMB) 또는 3,4-dim eth o xy be nzyl 등은 벤질과 비 슷한 성질을 가져서 염기 조건 하에서 도입할 수 있고 산, 염기에 비 교적 안정하며 가수소 분해 반응으로 제거할 수도 있다 . 그러나 주로 이 보호기들은 벤질기와의 선택적 탈보호를 위해 사용되는데, DDQ ( 2, 3 -dic h loro -5, 6-di c y a n o -1 , 4-be nzoq ui n o ne) 나 CAN (ceri c ammoniu m nitrate) 등의 시약으로 산화적 분해 방법을 쓰면 벤질기에는 영향을 주 지 않으면서 이들 메톡시벤질기들만을 제거할 수 있기 때문이다. Falck 동은 벤질 존재 하에서 DD Q룰 사용하여, 3,4-di me th o xy be n- z y l 기를 제거하는 반응을 수행하였다(그림 3-22-1)(26). 일반적으로 3,
 H亨O ,。 ?OMe H亨O :H (1 )
H亨O ,。 ?OMe H亨O :H (1 )
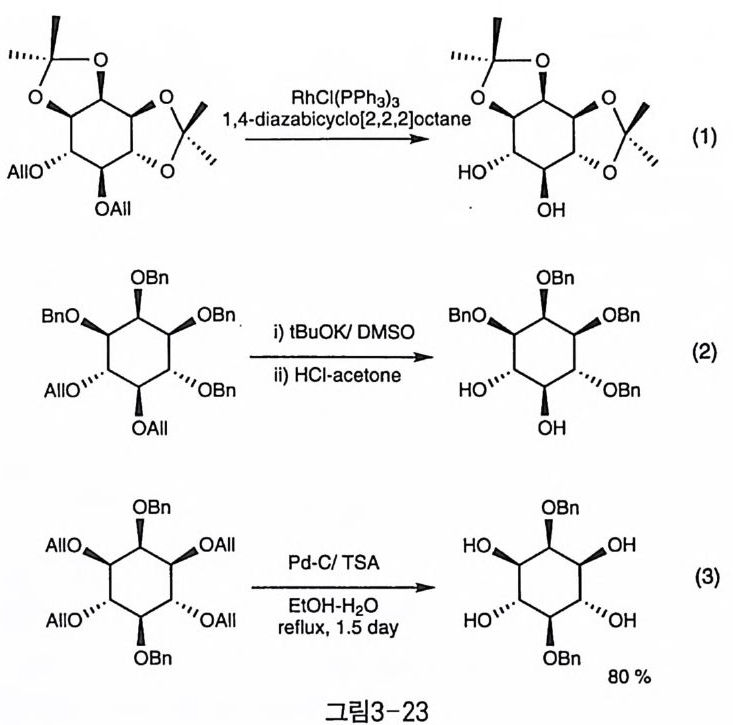
4- dirn e th ox y benz y l 기가 PMB 보다 반응성이 커서 부드러운 조건에서도 분해할 수 있는 것으로 알려져 있다. 산에 약한 아세탈이 포함되어 있 는 기질에서도 선택적으로 PMB 만을 제거할 수도 있다(그림 3-22- 2)[2 7 ).P MB 가 비교적 산 조건에서 강하기는 하지만, 강산에서 격렬 하게 반응하면 분해가 되는 경우도 있다(그림 3-22-3)(2기 . CAN 역시 DD Q와 비슷한 조건에서 선택적으로 PMB 를 제거하는 시약으로 사용 될 수 있다(그림 3-22-4) (28] ' 3-3_3 알릴화 알릴 (all yl) 역시 다양한 반응 조건에서 비교적 안정하여 선호되는 작용기인데 NaH 등의 염기 조건이나, Sn 중간체를 거쳐 All-X 친전 자체를 이용하여 도입할 수 있다. 벤질기 동과 함께 존재할 때 선택적 으로 알릴만을 제거하는 반응 조건들이 여러 가지 방법으로 연구되었 댜 알릴기의 이중 결합을 이동시켜 p ro p -1-en y l 을 중간체로 만든 다 음 산 조건에서 가수 분해하는 것이 일반적인 알릴 제거의 기작인데, 첫 번째 단계인 이중 결합의 이동 방법과 두번째 단계의 가수 분해 방법 의 조합에 따라 다양한 조건이 시험되었다. 산에 약한 아세탈이 함께 존재하는 기질에 전이 금속이 포함된 trist - ripb enyl p b osph ine rbod ium (I) chlo ri函 RhCl (PPb 詞 울 이 용하여 이 중 결 합을 이동시키고, H g (II)CL-H g(11) 0 를 이용하여 아세탈은 그대로 유 지한 채 pro p - 1-enyl 중간체를 제거하는 방법이 Gig g 등에 의해 개발 되었다(그림 3-23-1) 〔 29). 첫 단계의 이중 결합 이동은 염기인 tBu OK 조건에서 수행하고, 산으로 가수 분해하는 방법도 같은 연구자들에 의 해 벤질 존재 하에서의 알릴 제거에 이용되었다(그림 3-23-2) 〔 2 이. 두 단계의 반응을 보다 간단하게 개량한 조건도 개발되었는데, Pd-C 촉 매 하에 이중 결합의 이동을 유도하면서, 동시에 산울 함께 가해서 알
 A” 亭.O0 YJ, 1 , 4·d i-四Rb h i Ccrl。(lPoP[2h,32),J “2 ]O 백 ' :°'亨0)-’ 。 :f,,, (1)
A” 亭.O0 YJ, 1 , 4·d i-四Rb h i Ccrl。(lPoP[2h,32),J “2 ]O 백 ' :°'亨0)-’ 。 :f,,, (1)
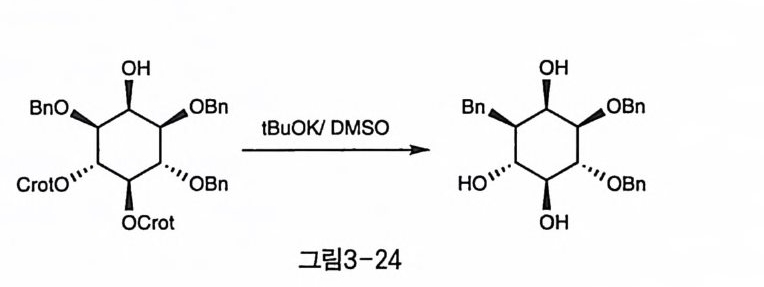
릴을 제거하는 방법이다(그림 3-23-3) 〔 30). 탈알릴화 반응의 단계를 보다 간단하게 하기 위해 알릴 대신 크로틸 (croty l) 을 사용하는 반응도 연구되었다. 크로틸은 도입 방법과 성질이 알릴과 거의 유사하지만, 염기만을 사용하여 한 단계로 분해할 수 있 는 간편함이 있다(그림 3 - 24)[28).
 C:::i ::: tBu O그K 림/D 3M-S2O4 ::*::
C:::i ::: tBu O그K 림/D 3M-S2O4 ::*::
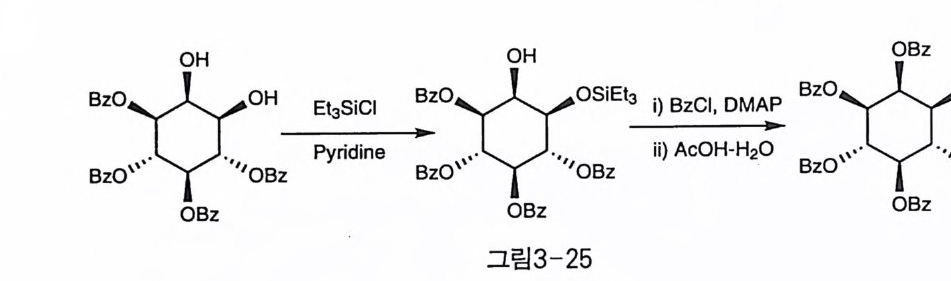
3-3_4 실릴화 다양한 실릴기들이 이노시톨에도 적용되었는데, 실릴기는 중성이나 염기 조건에서 비교적 안정하며, 수산기를 가진 분자의 휘발성을 증가 시키므로, GC(ga s chromato g ra ph y ) 분석을 위한 유도체로도 이용되었 댜 일반적으로 실릴기의 제거에는 산가수 분해 또는 R4N F 시약이 주 로 사용되고, 이노시톨의 경우 수직 방향인 2 번 수산기보다는 수평 방 향의 1 번 수산기에 대한 선택성이 크다(그림 3-25) 〔 12 〕 •
 :::〈::三〈::三二 ::<::Z
:::〈::三〈::三二 ::<::Z
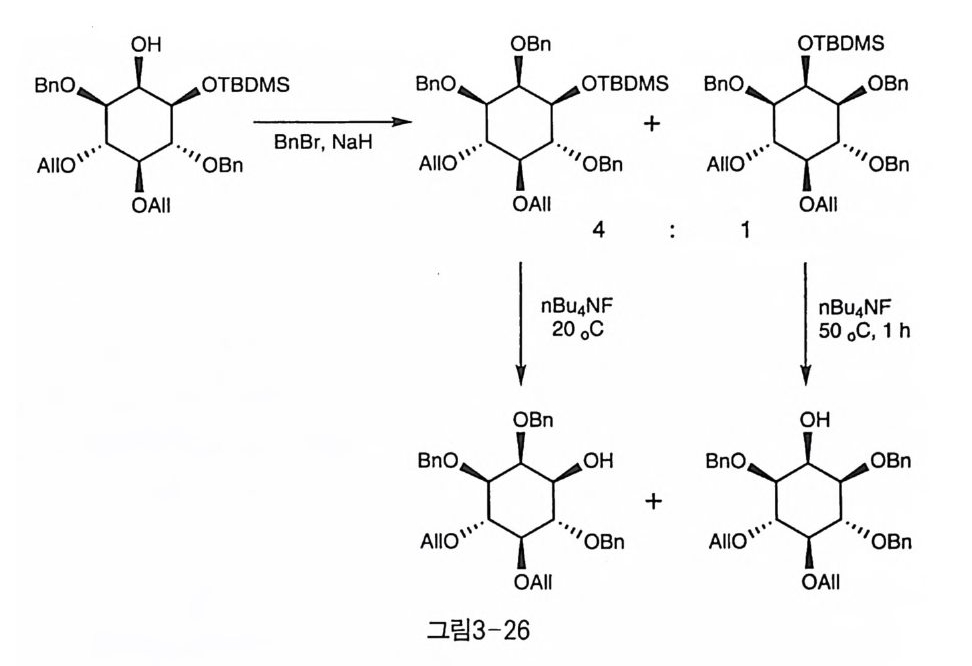
한편 강한 염기 조건에서는 이웃한 수산기로의 실릴기 이동도 일어 날 수 있다. 이때, 탈실릴화 반응은 수평 방향인 경우가 수직 방향보 다 더 빠르게 일어나는 경향을 보였다(그림 3-26) 〔 31) 염기 조건에서의 실릴기 이동을 피하기 위하여, 실릴 존재 하에서 친핵성인 Gr ign ard 시약을 이용하여 선택적으로 벤조일기만을 제거한 반응도 연구되었다 (그림 4-42) [32 ] . 3-3-5 메틸화 수산기의 보호에 메틸기는 오래전부터 사용되어 왔다. 가장 일반적 인 도입 방법은 염기 조건에서 MeX 와 반응하는 것인데, 필요한 조건 에 따라 C 比 N2 〔회나 Na-me thy ls 미血y lme thani de 와 Mel 을 사용하는
 Bn00 AII 따丁 AOI二Bn。AI BnOg仁loC荷ToB4BD Mns+ Bn。AII 曺g三nB5O5 QN ° F h1
Bn00 AII 따丁 AOI二Bn。AI BnOg仁loC荷ToB4BD Mns+ Bn。AII 曺g三nB5O5 QN ° F h1
방법띠 등이 이노시톨에 응용되었다. 이노시톨에서의 탈메틸화 반응은 BFJ-etherate[34)또는 Nal-AlCh(l익의 예가 보고되었다. 3-4 에스데르 에스테르(Ester) 결합으로 연결되는 아실기 (acyl)도 알킬기와 함께 이노시톨의 보호기로 널리 사용되었다. 아세틸과 벤조일기가 보편적으 로 널리 사용되는 아실기이며, 이들은 피리딘 등의 약한 염기와 낮은 온도에서도 쉽게 이노시톨에 도입할 수 있고, 염기 조건에서 가수 분 해로 제거하는 것이 보통이다.
3 - 4 기 아세틸 천연물에서도 널리 발견되는 작용기로서, 수산기에 산 또는 염기 조 건에서 무수 아세트산으로 반응하든지, 피리딘 등의 약염기에서 AcCl 와 반응하여 도입한다 . 일반적으로 결정성이 좋아서 탄수화물과 같이 수산기가 많은 화합물의 구조 결정을 위한 유도체로 만들 때 많이 사 용된댜 아세트산 둥의 유기산에서는 어느 정도 안정하지만, HCl 등 의 무기산에서 가열하면 평형 반응을 통해 가수 분해될 수도 있다 . 보 통은 염기인 NaOH 나 NaOMe 를 써서 가수 분해하여 제거하는데, 알 코올과 하이드라진을 이용한 제거 방법도 있다〔 35 〕 • 3-4-2 벤조일기 Bz20 나 BzCl 등을 이용하여 수산기에 도입하는 것은 아세틸과 거의 동일하다 . 아세틸에 비해 산에 대한 안정도가 매우 커서 유용한 중간 체로 이용될 수 있는데, 아세트산 조건에서는 끓여도 안정하다. 제거 는 주로 염기 조건에서 가수 분해하는 방법이 사용되지만, 이웃한 실 릴기의 보존을 위해 염기 조건을 피하고 Gr ign ard 시약을 사용하는 방 법도 보고되었다(그림 4 一 42) 〔 32 〕' 3-4-3 아실 이동 반응 아실기의 이동은 글리세롤에서 일어난 예가 1920 년에 F i scher 에 의해 처 음 보고되 었다〔 3 이 . 탄수화물에 서 는 1, 2-iso p ro p ylide ne -e x-D -glu - co fur anose 의 3 - 벤조일기가 6 번 수산기로 이동한 것이 처음 보고되었 으며〔 37 〕' 이후에 보고된 예들은 주로 g luco py ranose 에서 4 7 6 으로의 아실 이동이 대부분이었다〔 38 〕. 그리고 이때 사용된 조건들은 염기 조
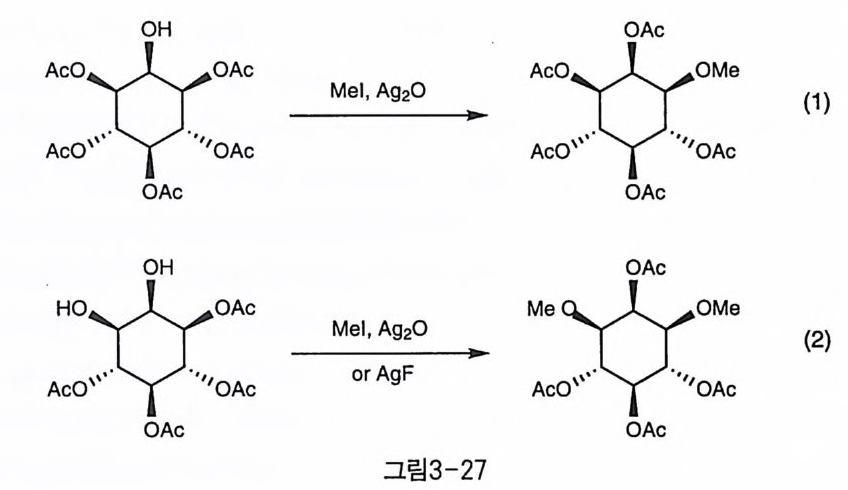
건이거나, 또는 실릴기를 제거하기 위한 불화 암모늄 조건도 있었고 Ag 20 하에서 Mel 를 써서 메틸화를 시도하던 과정에서 의도하지 않았 던 아실 이동을 관찰한 예들도 있었다. 이노시톨에서의 아실 이동에 관한 첫 보고 역시 아세틸기로 보호된 이노시톨의 메틸화 반응을 시도하던 중에 우연히 발견되었다. 1(1 , 3,4, 5,6)Acs 의 2 번 수산기에 메틸기를 도입하기 위해 A g 20 와 Mel 를 반응 시킨 결과 주생성물로는 l 또는 3 번의 아세틸기가 2 번으로 이동한 후 메틸화가 일어난 화합물이 얻어졌다(그림 3-27-1) 〔 39). 1(1 , 4,5,6)Ae i 에 비슷한 조건에서 메틸화를 시도한 경우에도, 1 번의 아세틸기가 2 번 으로 이동한 생성물이 주로 얻어졌다(그림 3 一 27-2)(40) .
 OH OAc
OH OAc
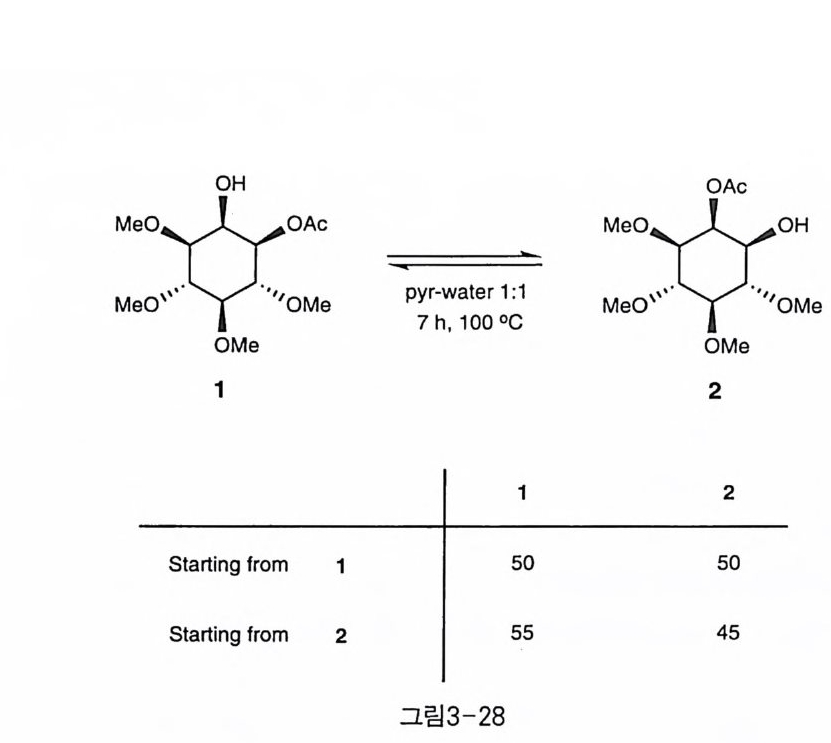
수직 방향과 수평 방향에 대한 아실기의 안정화 정도를 측정하기 위 해 평형 조건에서 아실 이동 반응을 출발 물질을 달리하며 추적한 결 과 수평 방향의 아실기가 약간 더 우세한 경향을 보였으나 그 차이가 그다지 크지는 않았다(그림 3-28) 〔 41). 시스와 트란스간의 아실 이동 속도를 피리딘과 물의 배합 비율을 조절하면서 추적한 결과 물의 양이
 Me0 Me O>H AcMe Me0 Me >OAc HM
Me0 Me O>H AcMe Me0 Me >OAc HM
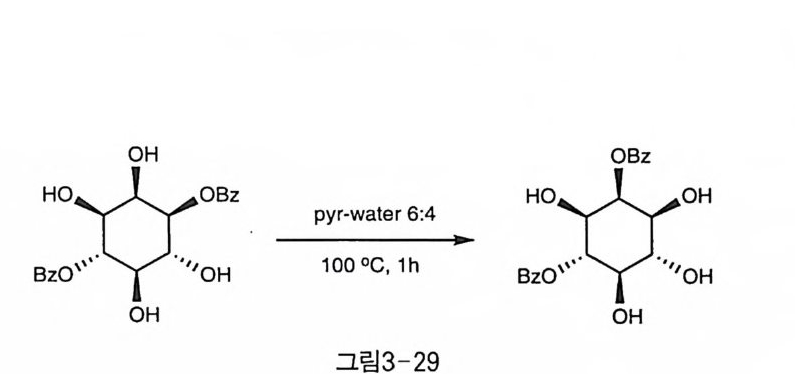
많아질수록 시스뿐만 아니라 트란스 방향 이동도 용이하게 일어났고, 물 의 양이 줄어들면 트란스에 비해 시스 방향의 이동이 빠르게 일어남을 관찰할 수 있었다. 그러나 어느 조건에서도 트란스 이동을 완전히 억 제한 채로 시스 방향으로만 선택적으로 이동시킬 수는 없었다. 한편 보트형의 중간체를 거쳐야만 일어날 수 있는 5 번 수산기로부터 2 번 수 산기로의 아실 이동은 피리딘一물 조건에서는 일어나지 않았다〔 4 1). Meek 등은 l (1 ,4)Bz2 에서 출발하여 트란스 방향의 벤조일 이동은 억 제하고 시스 방향으로 선택적인 벤조일 이동 반응을 하여 1( 2,4)Bz2 를 얻었다고 보고하였으나 분리된 수율이 10% 에 불과하였고(그림 3- 29)[4 2 ), 같은 조건에서 아실 이동을 추적해 본 결과 시스와 트란스 간의 아실 이동 속도 차이가 통제할 수 있을 정도로 크지는 않음을 알 았다〔 43 〕• Chung 등은 1(1 , 4)BZ2 와 1(1 , 6)Bz2 및 그 아세 탈 유도체를 이 용하 여, 다양한 염기와 용매, 반옹 온도 하에서 벤조일 이동 반응의 반응
 >OOHH pyr- w ate r 6:4 OH王
>OOHH pyr- w ate r 6:4 OH王
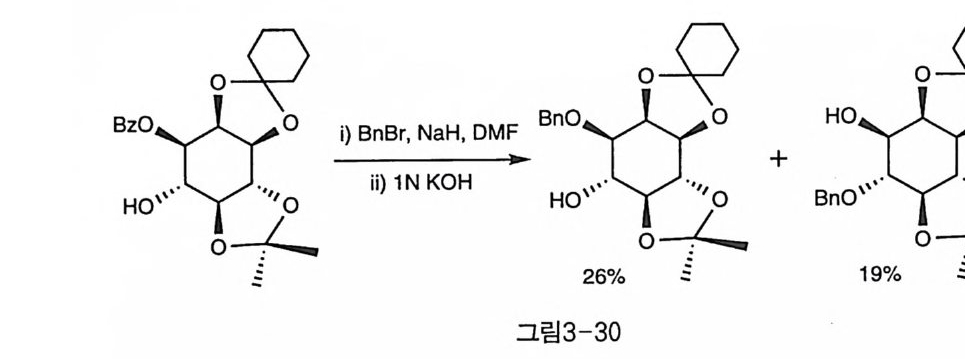
속도론적인 특징을 연구하였다. 열역학적인 평형 조건에서는 어떤 출 발 물질을 사용하여도 가능한 이성질체들이 고루 분포됨을 확인할 수 있었다. 이것은 벤조일의 위치가 수직 방향 또는 수평 방향에 관계 없 이 열역학적인 안정성에는 큰 차이가 없음을 나타낸다. 반응 속도론적 인 조건 하에서는 어느 정도의 선택성이 관찰되었는데, 우선 일반적으 로 시스 방향의 이동이 트란스 방향으로의 이동보다는 빨랐다. 이웃한 수산기로의 벤조일기 이동은 사면체 구조의 반응 중간체를 거칠 것으 로 생각되는데, 시스 수산기 간의 중간체가 트란스 경우보다 안정한 것으로 보인다. 이러한 시스/트란스 간의 안정성의 차이는 오각형 고 리 구조인 아세탈에서도 관찰되었다〔 4). 또, 이러한 시스/트란스 간의 선택성은 이노시톨 고리 구조가 단단하게 고정되어 있는 경우에 두드 러지게 나타났으며, 온도를 낮추는 경우에도 선택성이 향상되었다. 또 이동 속도는 용매의 극성이 클수록 빨라지는 특성을 보였다. 극성 용 매가 음전하를 띤 고리형 중간체를 안정화시켜 활성화 에너지를 낮추 는 것으로 해석된다〔 43 〕 . 벤조일기에 이웃한 수산기가 존재하는 경우, 무수 조건이라도 강염 기 하에서 벤질화 반응을 하면 빠르게 아실 이동이 일어나서 혼합물 상태의 벤질 화합물을 생성하게 된다(그림 3-30)(44 〕•
 HO` To- 효- '!0- - ii) 1N KOH HOV26 % I。 --흐 !.'-0- BnO 19% oI ---E:
HO` To- 효- '!0- - ii) 1N KOH HOV26 % I。 --흐 !.'-0- BnO 19% oI ---E:
3_5 인산화 인산이노시톨이 다양한 생리 활성을 가진 것이 알려진 이후, 이노시 톨 고리의 특정한 위치의 수산기에 인산기를 도입하는 많은 반응들이 연구되었다. 원래 인산화 반응은 핵산의 합성에서 많이 사용되어 왔 고, 실제로 그 분야에서 개발된 방법들이 이노시톨에도 대부분 적용되 었댜 인산기는 산화수가 +5 인데, 인산화 반응은 처음부터 산화수가 +5 인 P(V) 시약을 사용하는 방법과 +3 인 아인산기를 먼저 도입하 고, 산화시키는 P(m) 시약 방법이 있다 . 널리 사용되지는 않았지만 두 가지 방법의 중간 정도 반응성을 나타내는 P(N) 시약도 소개되었다 . 3-5-1 P(V) 시약을 이용한 방법 P(V) 시약의 장점은 시약이 비교적 안정하다는 점이다. 그러나 2 차 수산기에 대한 반응성이 낮은데 특히 이웃한 두 개의 수산기에 동시에 인산화시키는 것은 특히 어렵다는 것이 알려졌다. 이웃한 수산기의 경 우 먼저 하나의 수산기에 인산기가 도입되고 나면 입체 장애에 의해 두번째 인산기가 도입되는 것은 저해되면서, 이웃한 나머지 수산기가
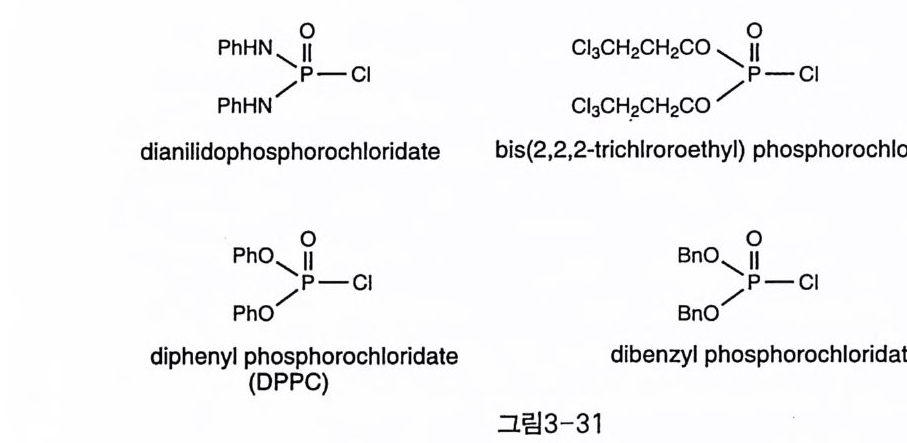
인산기를 공격하여 오각형의 고리 인산을 만드는 쪽이 우세한 경우가 많다. 고전적인 방법으로는 인산, 피로인산, 폴리인산 등으로 존재하 는 수산기들을 한꺼번에 인산화하는 방법이 사용되었지만, 고리 인산 화를 비롯한 부반응들이 수반되는 등 문제점이 많아서 보다 세련된 형 태의 인산화 시약의 개발이 요구되어 왔다. 가장 먼저 사용된 P(V) 시약은 POCb 로서 최초의 사용은 1857 년까 지 거슬러 올라간다 (45) . 이노시톨에 적용된 것으로는 I (l )P 의 합성에 성공적으로 사용된 예가 있었다(그림 4-8)(46 〕 . Phosp ho rochlorid a te ( Ru >O CI) 시 약도 많이 사용되 었는데 (그림 3- 31), 최초의 1 (1 ,4,S)P J의 합성에 이용된 d i an ili do p hos p horochlo ri da t e 는 인산기 도입에서의 부반응과 i soar' 11y ln itrit e 를 이용한 보호기 제거 반응 들이 만족스럽지 못하여 개량된 방법이 요구되었다(그림 4-40) 〔 47). Bis ( 2, 2, 2 -tr ich loroeth yl) p hos p horochlo ri da t e 도 1(1 , 4, 5)P J와 그 5- 티 오인산기 유도체의 합성에 이용되었는데, 인산기의 보호기 제거에는 Li -NH3 와 Na-NHJ 방법이 사용될 수 있는데, L i -N 比의 경우 티오인 산기에서는 탈황 작용을 일으킨다는 부적절한 점이 관찰되었다. 이때 보호기 제거는 전자가 공급되어 er 하나가 먼저 떨어지고 연속적으로 일어나는 ~-el imi na ti on 에 의한 것으로 설명되었다〔 48). Di ph eny l p hos p horochlo ri da t e(DPPC) 은 성공적인 인산화 시약으로서 이웃한 수 산기에는 적용할 수 없지만, 그 밖의 경우에는 초기 인산이노시톨 합 성에서 널리 사용되었다. 이 시약은 1949 년에 이미 l( 2)P 의 합성에 이 용되었으나, 수직 방향의 2 번 수산기에 대한 반응성이 좋지는 않았고 (그림 4-13) 〔 49), L-l (l )P 를 합성하는 데는 성공적으로 사용되었으며 (그림 4-3) 〔 50), 이웃하지 않은 두 수산기를 인산화하여 1 (1 ,4)P2 의 합 성에도 이용된 예가 있다 (5 1) . 인산의 보호기인 페닐기는 Pt02 촉매 하에서 가수소 분해하여 제거할 수 있다. Di be nzyl p hos p horochlo ri da t e 은 그다지 사용례 가 많지 는 않지 만, (2,
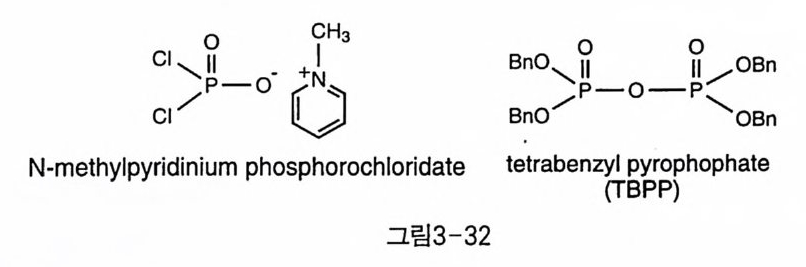
3)camp ho r 아세탈에서 선택적으로 1 번 위치만을 인산화하는 반응에서 적용되었다(그림 4-12) 〔 52 〕. 인산기의 벤질기는 Pd-C 촉매 하에서 가 수소 분해하면 쉽게 제거된다. 인산의 보호기가 페닐이고 인산 이외의 보호기가 벤질인 경우에는 두 단계의 탈보호 (Pd 一 C /IL, Pt O z-H2) 반 옹을 하든지 (그림 4-6) [53 ), 인산의 페닐기를 벤질로 바꾸는 tran seste r i - fica ti on 반응 후 Pd-C 촉매로 한번에 보호기를 제거할 수도 있다(그 림 4-7)(54 〕 • Phos p horo di chlo ri da t e(P(0)ChO-) 는 알코올과 반응할 작용기를 두 개 가지고 있으므로 다른 두 분자를 연결하는 데 사용될 수 있어 인지 질의 합성에 응용된 예가 있는데, 이노시톨에서는 분자 내의 이웃한 두 수산기 간에 고리형 인산기를 형성하는 데 활용되었다(그림 4-22) [55 ). 이때는 N-me thy l pyri d i ne 의 염 형태로 사용되었다(그림 3-32).
 PPhhHHNN /\P 荷 -CI CCll33CCHH22CCHH22CCOO '/- -. 。P~ — Cl
PPhhHHNN /\P 荷 -CI CCll33CCHH22CCHH22CCOO '/- -. 。P~ — Cl
P(V) 시약 중에는 tet r ab enzy l p y ro phos p ha t e(TBPP) 가 이웃한 수산기 의 인산화에 일반적으로 적용할 수 있는 유일한 시약이다. TBPP 는 디 벤질인산을 DCC 조건에서 축합하여 만들며, 결정성 고체로 얻어진다. 인산화 반옹은 먼저 수산기들을 강염기로 탈수소화하여 수산기 음이온
으로 만든 후 TBPP 를 가해 주는 것이다. 많은 예가 인산이노시톨에서 보고되었는데, 강염기를 사용해야 하므로 염기에 약한 다른 보호기가 포함되어 있는 경우에는 사용이 제한되는 단점이 있어 주로 벤질기 등 으로 보호된 이노시톨 유도체의 인산화에 사용되었다(그림 4-14) 〔 15).
 CCll\/。 P -o-巳+ NC| H 3 BBnnO_0,,,\,.0P — o-— 0•P / '-O-oBs nn
CCll\/。 P -o-巳+ NC| H 3 BBnnO_0,,,\,.0P — o-— 0•P / '-O-oBs nn
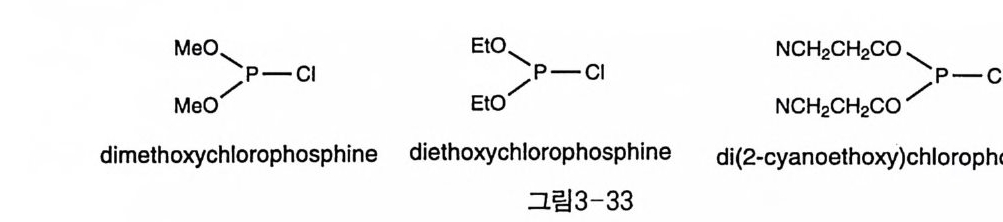
3-5- 2 P( III ) 시약을 이용한 방법 P(il l) 시약들은 습기에 민감하여 취급에 주의해야 하는 점이 있지만 P(V) 시약보다 일반적으로 반응성이 커서, 이웃한 수산기 둥과 같이 P(V) 시약으로 인산화가 어려운 때에 먼저 아인산 형태로 도입한 후 산화시키면 쉽게 인산화할 수 있는 경우가 많다. 이렇게 하면 부반응 으로 자주 나타나는 고리 인산화 반응이 거의 없고, 또한 산화를 황으 로 시행하면 티오인산기를 도입할 수도 있는 장점도 있다. 이 시약의 초기 형태로는 PCb 가 I( l) P 의 합성에 사용되었는데, 이 노시톨에 PCl3 을 가한 후 벤질알코올울 계속 가하여 치환 반응을 유도 한 것이다(그림 4-5) 〔 56). 보다 세련된 시약으로 dime th o xy ch lorop ho s- phine (그림 4-46) 〔 42 〕과 dieth o xy ch lorop h osp hine (4-7 참조)〔 4, 1 이이 염 기 조건에서 성공적으로 이노시톨 중간체를 인산화하였다(그림 3-33) . 이때 사용된 보호기인 에틸이나 메틸기는 HBr 또는 TMSBr 로 제거할 수 있다. 또, di (2-c y anoe th oxy )chloro p hos phin e 도 비슷한 방법으로 I (l ,3,4)P3 의 합성에 이용되었다〔 57) . 이때의 보호기는 Na-NIL 조건에
 MMeeOo ` / P -CI EEttOO >P— Cl NNCCHH2C2HC2HC2Oc /o , P— Cl
MMeeOo ` / P -CI EEttOO >P— Cl NNCCHH2C2HC2HC2Oc /o , P— Cl
서 ~-e limi na ti on 으로 제거할 수 있다. 보다 안정 한 시 약으로 p hos p hora mi d it e 들이 개 발되 었는데 (그림 3 — 34), 이들은 약산인 lH-te t r az ole 존재 하에서 아인산기를 수산기에 도입할 수 있는 특징을 갖는다. Di(b enzy lo xy )diet h yla mino p n osp hine 보다는 diiso p ro p yla mino p h osp hine 쪽이 더 안정 하여 시 약을 만들 때 Si0 2 크로마토그래피로 정제가 가능하므로 보다 편리하다〔 58]. 이 시 약은 거의 모든 보호기의 존재 하에서도 사용할 수 있으므로 인산이노 시톨의 합성에 널리 이용되었다〔 51]. 한편, 두 개의 벤질기 대신 크실 렌 이 치 환된 0 -x y le ne -a , a '-di y l N, N -die t h y lp h osp h orami di t e (XEPA) 역시 비슷한 조건에서 반응할 수 있는 시약으로 최근에 와서 많이 사용되고 있으며〔 59), 특히 보호기의 입체 장애가 작아서 다수의 인산기를 도입하는 반응에 편리하다(그림 4_88) 〔 18 〕. 에틸기가 메틸기 로 치환된 유도체인 XMPA 도 사용되었다(그림 4...:.19) 〔 52 〕 •
di( b en-z yClo xBB ynn)dCOO i `e/ t h Py —>l am Ni n-Eot N2 p h :o sp h i n e di( b enz yclo x yBB)dnnc OOii s `/o pP: r o— p> yPNla im P-r 2 i n {o :p ho s p hi n e XEPA XMPA 그림 3-34
두 개의 작용기를 가진 2-cya n oeth o xy (d ii so p ro p yla m ino )chlorop ho s- phin e 과 meth o xy 유사체들은 다른 반응 조건 하에 서 상이 한 작용기 를 도입할 수 있는 특징을 가진다(그림 3-35). 실제로 이 시약들은 인산이노시톨의 합성에 사용되었고(그림 4-44) (60), benzyl o xy di ( d ii so - pro y la m ino ) p hos phi ne 도 마찬가지로 이노시톨의 인지질 합성에 이용 된 예가 있었다〔 31 〕 .
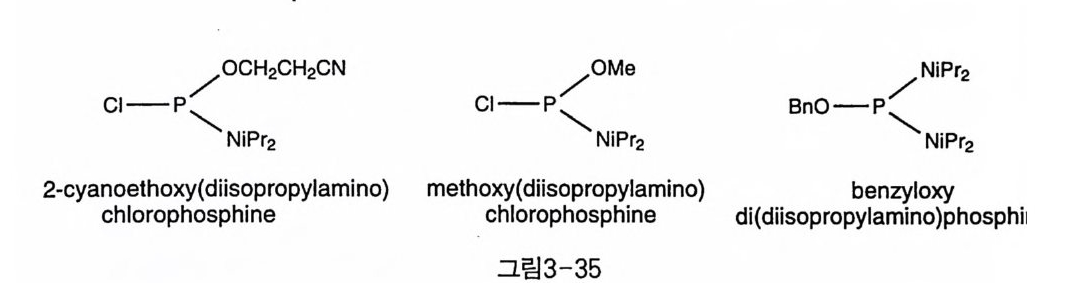 CI-P< ONCiP H r 22 CH2CN Cl— P\ / O NMiP er 2 BnO— P /\ NN iiPP rr 2 2
CI-P< ONCiP H r 22 CH2CN Cl— P\ / O NMiP er 2 BnO— P /\ NN iiPP rr 2 2
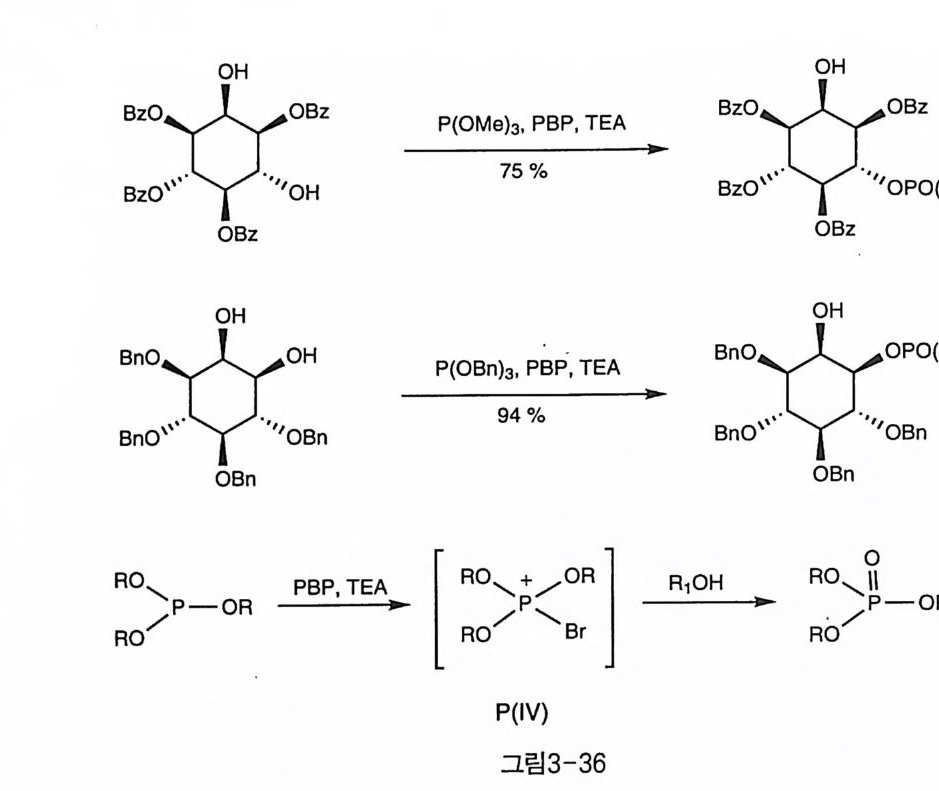
3-5-3 P(IV) 시약을 이용한 방법 Phosph o n ium salt( I V) 시 약은 P( ill)과 P(V)의 중간 정도의 반응성을 가지므로 선택적 반응에 유용하게 쓰일 수 있다. XEPA 를 사용한 die s te r 합성에 이용되었던〔 6 1) 이 P(IV) 시약은 이노시톨 수산기 간의 선택적 인산화에 이용되었다(그림 3-36)(62). 반응은 P(OMeh 나 P(OBn)3 에 pyridinium brom ide p erbro mi de(PBP) 와 반응 기질인 알코올 을 TEA 와 함께 저온에서 섞어서 수행하는데 P(OMe)3 쪽이 좀더 반응 성이 큰 것으로 나타났다. 3-5-4 인산기 이동 산이나 염기 조건 하에서 인산기는 떨어지기도 하고 이웃 수산기로 이동하기도 한다. IPs 로 실험한 결과 시스 방향의 이동은 비보호 상태
 ::*>OH 。o: Z P(OMe9b4 ,% P BP, TEA :::::y<::::(:(OOB Mna) 2),
::*>OH 。o: Z P(OMe9b4 ,% P BP, TEA :::::y<::::(:(OOB Mna) 2),
의 인산에스테르에서 110°c, 20 분 정도 가열하면 일어나며, IM HCl 울 가하고, 110°c 에서 80 분 가량 가열하면 트란스 방향의 이동도 일어 난다〔 63 〕 . 또 1(1 , 6)P2 를 80% AcOH 수용액 조건에서 환류 가열하면 1(2, 6)P2 가 얻어진다. 죽 이 조건에서는 트란스 이동은 억제되며, 시스 수산기 간의 인산기 이동이 일어나는 것이다〔 1). 보호기가 붙어 있는 경우에 인산기 이동은 더 빠르게 일어나는데, 메틸기로 보호된 IPI 의 나머지 다섯 개의 수산기를 Mel, Ag O 조건에서 메틸화를 시도하면 메틸화 반응보다 인산 이동이 더욱 빨리 일어나는 것이 관찰되었다 . 이때 인산기의 이동은 이웃한 수산기의 공격에 의해 오각형 고리가 만 들어졌다가 다시 고리가 열리면서 이동하는 것으로 생각할 수 있는 데, 보통은 중성 조건으로 알려진 Ag O 조건에서 시스뿐만 아니라 트
란스 방향의 이동도 빠르게 일어남이 관찰되었다 . 단지 이 경우에도 시스 수산기 간의 고리 인산기가 트란스 고리 인산보다는 더 안정한 경향을 나타내었다〔 33 〕 • 3-6 분광학 이노시톨 고리에 직접 연결되어 있는 meth ine 수소들은 1H-NMR 에 서 구조를 규명하는 데 중요한 역할을 한다. 이노시톨 고리 구조가 의 자형을 유지하는 동안에는 Hl-H2( 또는 H2-H3) 간에는 수평-수직간 60 도 정도의 이면각을 가져서 짝지음 상수가 2-3Hz 정도의 값을 가지 는 반면, 그 밖의 수소 간에는 수직-수직간에 거의 180 도에 가까운 이면각을 가져서 9-llHz 정도의 짝지음 상수값을 갖는다. 또, 이노시톨 고리에 직접 연결되어 있는 meth ine 수소들은 수산기 가 치환되지 않은 경우, 대개 03-5 ppm 정도의 화학이동 값을 갖는 댜 수산기에 알킬기가 치환된 경우에는 화학 이동값이 크게 달라지지 않지만, 아실기가 치환되면, 아래 영역 (down fi eld) 으로 1p pm 정도의 이동이 관찰된다. 따라서, 인산이노시톨의 중간체로 널리 사용되는 벤 질이노시톨은 벤질의 CHz 에 의한 신호들도 meth ine 신호와 겹쳐서 IH_NMR 만으로는 정확한 구조를 규명하기가 어려운 경우가 많다. 반 면에, 아세틸이나 벤조일의 유도체인 경우에는 쉽게 화학 이동값과 짝 지음 상수를 조합하여 구조를 밝혀낼 수가 있다. 이노시톨에 도입된 아세틸기의 CIL 의 1H-NMR 신호들에 대한 체계 적인 연구 결과, CDCL 용매에서 수평 방향의 Ac 기가 o2.0p pm 정도 인 데 비해 수직 방향은 o2.2 p pm 정도로 구분이 된다는 사실이 관찰 되었다. 한편, 이노시톨 고리에 0 대신 N이 치환된 경우에는 Ac 의 신호가 ol. 9 ppm 정 도로 나타났다〔 64 〕 .
몇 종류의 이노시톨과 그 메틸 유도체들에 있어 “C-NMR 에 대한 화학 이동값들 조사와 새로운 구조 예측 가능성을 다룬 연구도 이루어 졌다〔 65) . 또, 이노시톨의 보호기로 많이 사용되는 i so p ro pyli dene 의 1H-NMR 화학 이동값들도 체계적으로 정리되어 보고되었다〔 66). 3— 7 광학 활성의 이노시톨 유도체 3-7-1 광학 활성을 가진 천연물에서의 유도 천연물을 이용해서 광학 분할 과정 없이 광학 활성을 가진 이노시톨 유도체를 만드는 과정이 다수 알려져 있다. 구체적으로 사용된 천연물 에 는 L -q ue brach itol , D -I (3)Me, ( -) -q uini c aci d, D -g lu curono -6, 3-lacto n e, gal acti no l 동과 생 체 내 에서 의 이 노시 톨 생 합성 과정 을 모 방한 Ferr ier 반응으로 gal acto s e, mannose, glu cose 등을 사용하는 방 법이 있다. 4 강에 실제 활용 예들의 구체적인 과정이 나타나 있다(그 림 4-2) . 3-7-2 광학 분할 이노시톨을 출발 물질로 사용하여 광학 활성의 유도체를 얻고자 한다 면, 적당한 단계에서 광학 분할이 필요하다 . 이러한 광학 분할은 라세 미상의 이노시톨 유도체를 부분 입체 이성질체 쌍으로 만들어 재결정이 나 크로마토그래피로 분리하는 방법이 대부분을 차지한다. D-mannose 의 오르소에스테르를 비롯하여 (S)-(+)-acety lm andelic a ci d, (S)-( -)- 및 (R) -( + ) -camp ho r dime th yl aceta l , L -m enth yl chlorofo r mate , L - menth o xy ac ety l chlori de , (R) -( + ) -1-ph eny le th yl iso cya n ate 동이 광
학 분할제로서 사용되었다(그림 4 기). 현재까지는 (S)- (一)- 및 (R)- ( + ) -cam p hana t e 가 이 노시 톨 유도체 의 광학 분할에 가장 효율적 인 분 할제로 보인다. 한편, 키랄 HPLC 를 이용한 중간체 분리도 시도되었 으며, 에스테라제, 리파제, 프로테아제 등의 효소를 이용한 아실 도입 및 가수 분해 반응도 수행되었다. 3— 8 위치 선택성 수산기 이외의 작용기가 따로 없는 이노시톨의 경우 작용 기간의 선 택적 반응은 고려의 대상이 되지 않지만 수산기 간의 위치 선택적 반 응은 대단히 중요한 주제이다. 같은 수산기 간의 반응성 차이를 구별 해야 하므로 미오이노시톨인 경우, 다른 다섯 개의 수산기가 수평 방 향인 데 비해 수직 방향인 2 번 수산기를 실마리로 활용하는 것이 우선 고려해 볼 만하다 . 그러나, 수평 방향의 수산기 사이의 선택성이 요구 되는 상황도 자주 발생하여, 많은 선택적 반응이 연구되었음에도 현재 까지는 선택성의 기원을 밝히는 문제뿐만 아니라 실용적인 응용도 확 립되어 있지는 않다. 3-8-1 ( 1, 2) 선택성 수평 방향의 1 번 수산기와 수직 방향의 2 번 수산기 간의 선택성은 비교적 쉽게 얻어진다. 이노시톨 고리가 의자형을 유지하는 경우, 수 평 방향의 수산기들이 고리의 바깥쪽으로 배향되는 데 비해 수직 방향 의 2 번 수산기는 고리면과 수직으로 배향되므로, 이노시톨과 반응하는 시약이 접근하는 데 입체적 장애를 많이 받게 된다. 그리하여 친핵 반 옹의 경우 1 당량의 친전자체와 반응시키면 대부분 1 번 수산기가 먼저
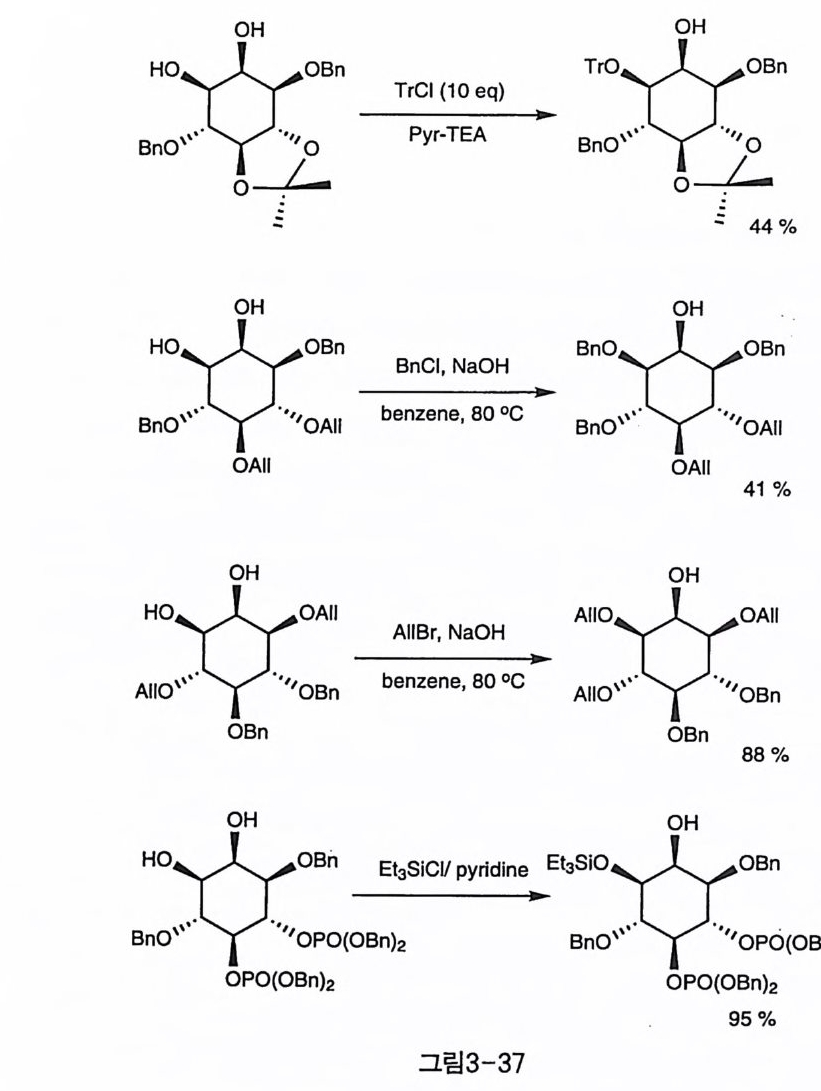
반응에 참여 한다. 입 체 장애 가 큰 trityl기 를 도입 하면 1 -trityl만이 얻 어지기는 하지만, 1차 알코올과 높은 수율로 반응하는 데 비하면 2차 알코올인 이노시톨의 수산기에서는 수율이 낮게 얻어진다(그림3-37-l) [5). 염기 조건에서 직접적 인 벤질화, 알릴화(그림3_37_2, 3) [17]
 OH OH
OH OH
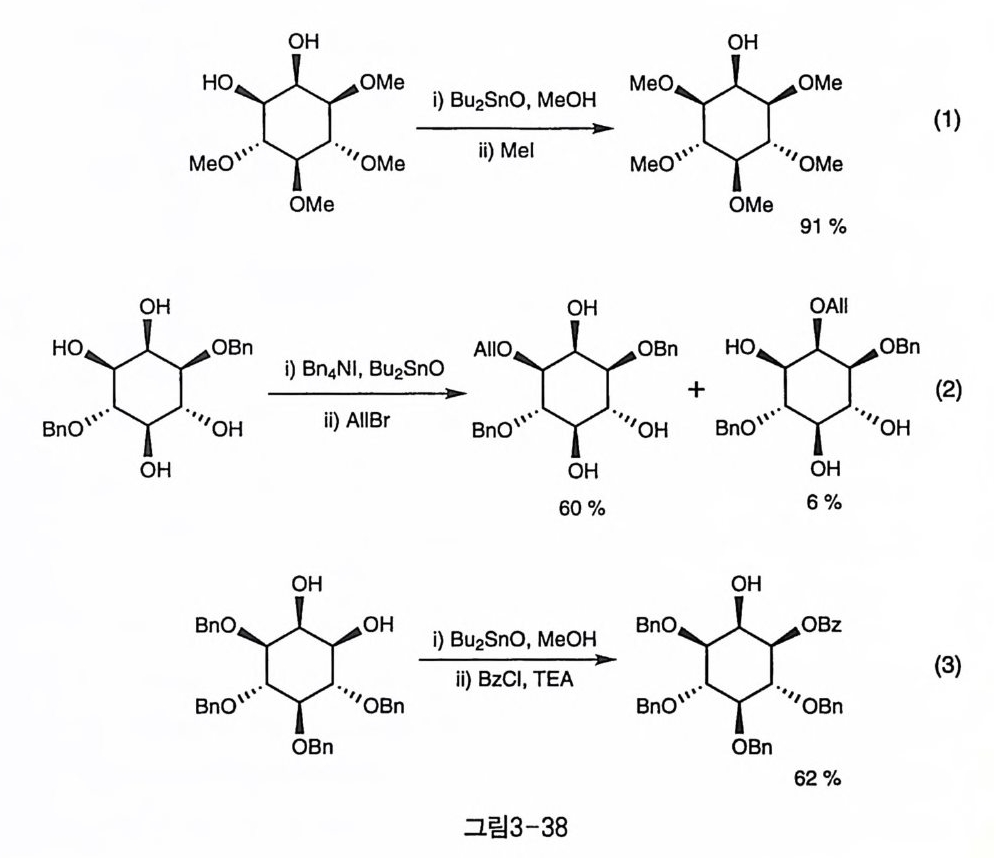
또는 실릴화 반응(그림3-37-4) 〔5회울 시도하여도 역시 1번 수산기가 먼저 반응함을 알 수 있는데 이 반응들은 적정량의 친전자체를 사용해 야 하고 반응 속도 및 반응 시간 동의 최적화 과정이 필요하다. 두 개의 수산기 모두에 작용기가 도입되는 부반응을 억제하면서도 선택성은 더 향상시키려는 시도로서, 고리 주석의 중간체를 거쳐 반응 하는 방법도 많이 사용되었다. 이러한 고리 주석 중간체를 통하면, 수 산기의 친핵 반응성이 커져서 별도의 염기를 사용하지 않고도 반응을 진행시킬 수 있어서 메틸화(그림3-38-1)(2), 벤질화(그림3-38-2)〔회, 아실화(그림3一38-3)〔67〕 반응이 모두 가능하다.
 H
H
트란스 디올 간에는 보고된 바가 없지만, 시스 관계인 1,2- 디올 간 에는 benzy lide ne 아세탈을 형성시킬 수 있다 . benzy lide ne 아세탈은 exo 와 endo 의 두 가지 이성질체가 가능한데, 이노시톨에 직접 a, a- di me th ox yt oluene 을 처리하면 exo 와 endo 가 거의 같은 양으로 얻어진 댜 나머지 수산기들을 벤질이나 벤조일로 보호한 뒤 재결정으로 exo 와 endo 를 분리해서 환원시키면 선택적으로 각각 1-Bn 과 2-Bn 이 만들 어진다(그림 3-39)(22 〕. 비슷한 위치 선택성이 다른 오각형 benz yli dene 에 서도 관찰된 바가 있었고, 이는 입체 전자 효과로 설명할 수 있다〔 68).
 二亨。OH。 : R = IB) zP hiio)CRr H BX(On Me)2 ::*:lRO/_:〉广HR e9O +Hnac w R.tot0h i IRooN0亡J`hp亨nlOBR loR R00 H R
二亨。OH。 : R = IB) zP hiio)CRr H BX(On Me)2 ::*:lRO/_:〉广HR e9O +Hnac w R.tot0h i IRooN0亡J`hp亨nlOBR loR R00 H R
 한편 아세탈 대신 오르소에스테르를 중간체로 하여, 산 조건에서 가
한편 아세탈 대신 오르소에스테르를 중간체로 하여, 산 조건에서 가
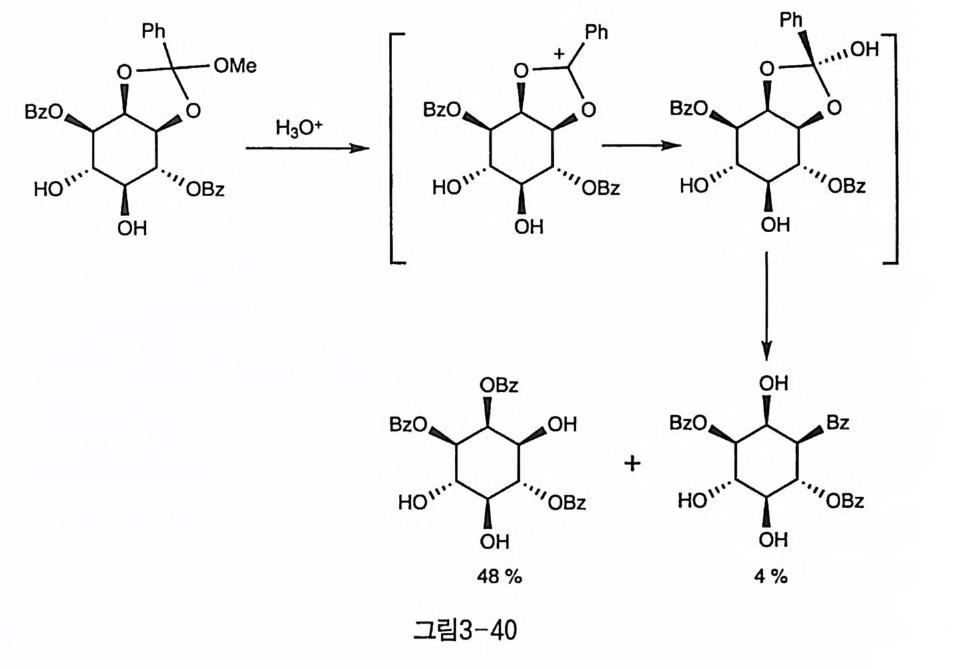
르소에스테르가 형성되는데, 이때 물 분자는 입체 장애가 작은 바깥쪽 에서 접근하는 것이 우세할 것으로 생각된다〔 69). 결과적으로 알킬 부 위는 endo 쪽으로 배위하게 되어 고리 열림은 그림 3-39 의 환원 반응 과 같은 입체 전자 효과로 2 번 Bz 가 우세하게 얻어진다(그림 3 - 40) 〔 70) . 오각형 benzy lide ne 아세 탈을 ozonol y s i s 하면 비 슷한 중간체를 거 쳐 수 직 방향에 Bz 기가 생성될 것임이 암시되었으나〔 69), 이노시톨에 적용 된 예는 아직 보고되지 않았다.
 Ph
Ph
3_&2 (1, 4) 선택성 두 개의 오각형 아세탈로 형태가 고정된 1,4- 디올인 경우 두 수산 기가 모두 수평 방향임에도 어느 정도의 선택성을 부여할 수가 있다 . 두 개의 c y clohex yli dene 으로 보호된 1,4 의 두 수산기는 벤조일화 반응
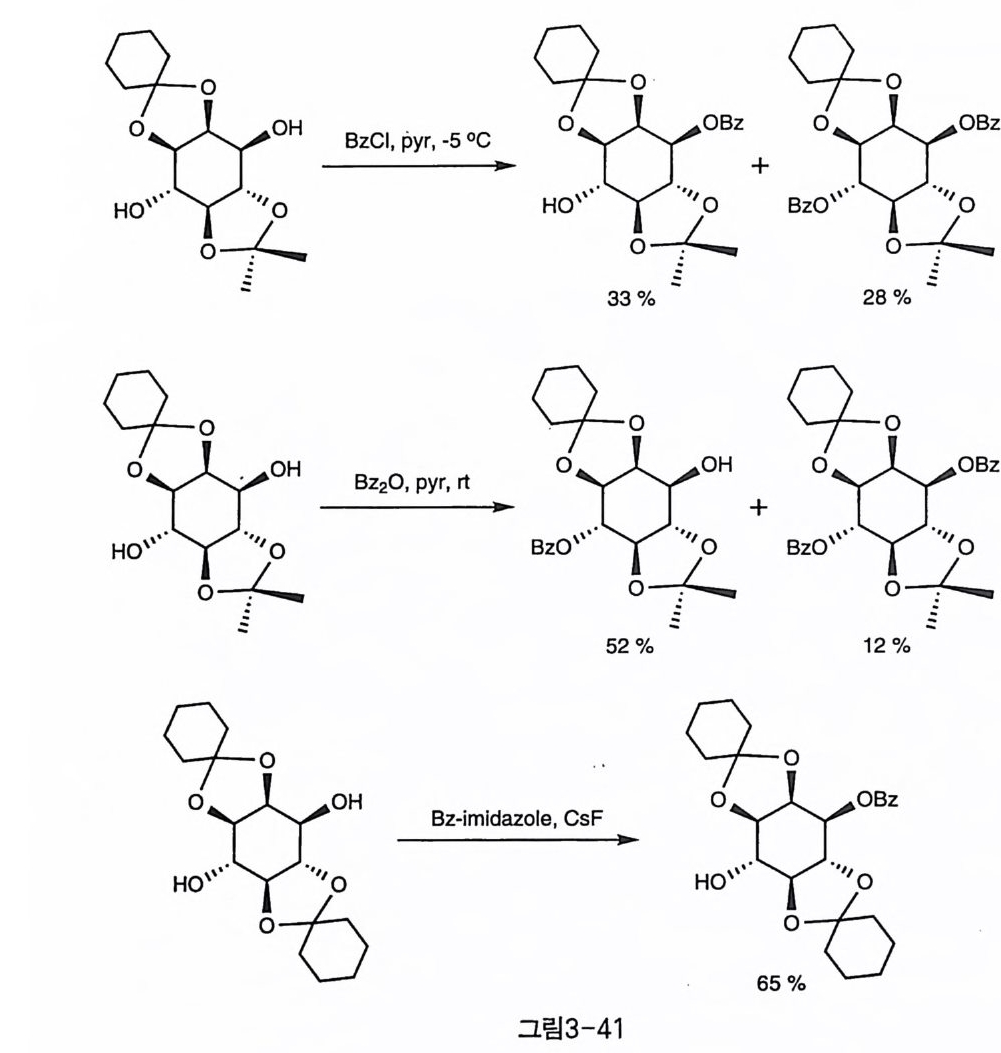
의 경우 1 번이 우세함이 비교적 일찍부터 알려져 있었다〔 71) . 그 후 여러 조건에서 벤조일화 반응이 시험되었는데, 일반적인 반응 조건인 피리딘 용매 하에서 BzCl 로 반응하면 1 번 수산기가 우세하게 벤조일화 되기는 하지만 두 개의 벤조일이 도입된 부생성물이 상당량 함께 얻어 졌다(그림 3-41-1) 〔 72 〕 . 이 경우 BzCl 대신 반응에서의 입체 장애가
 BzCI, pyr, -5 °c
BzCI, pyr, -5 °c
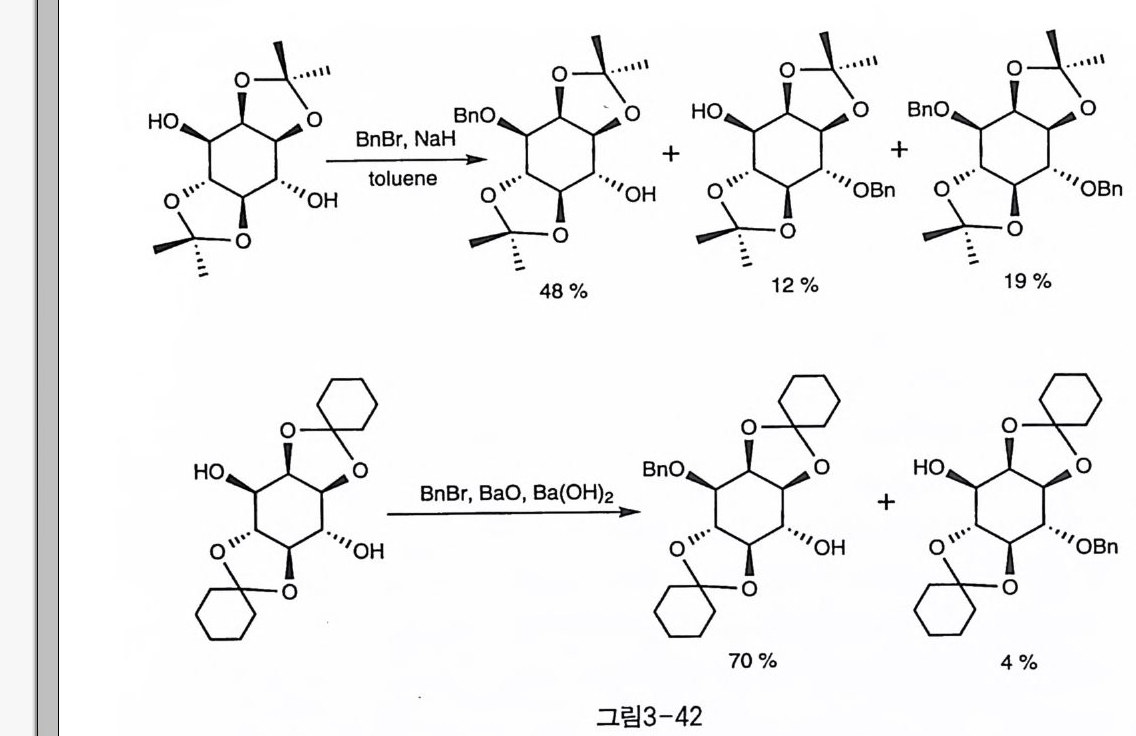
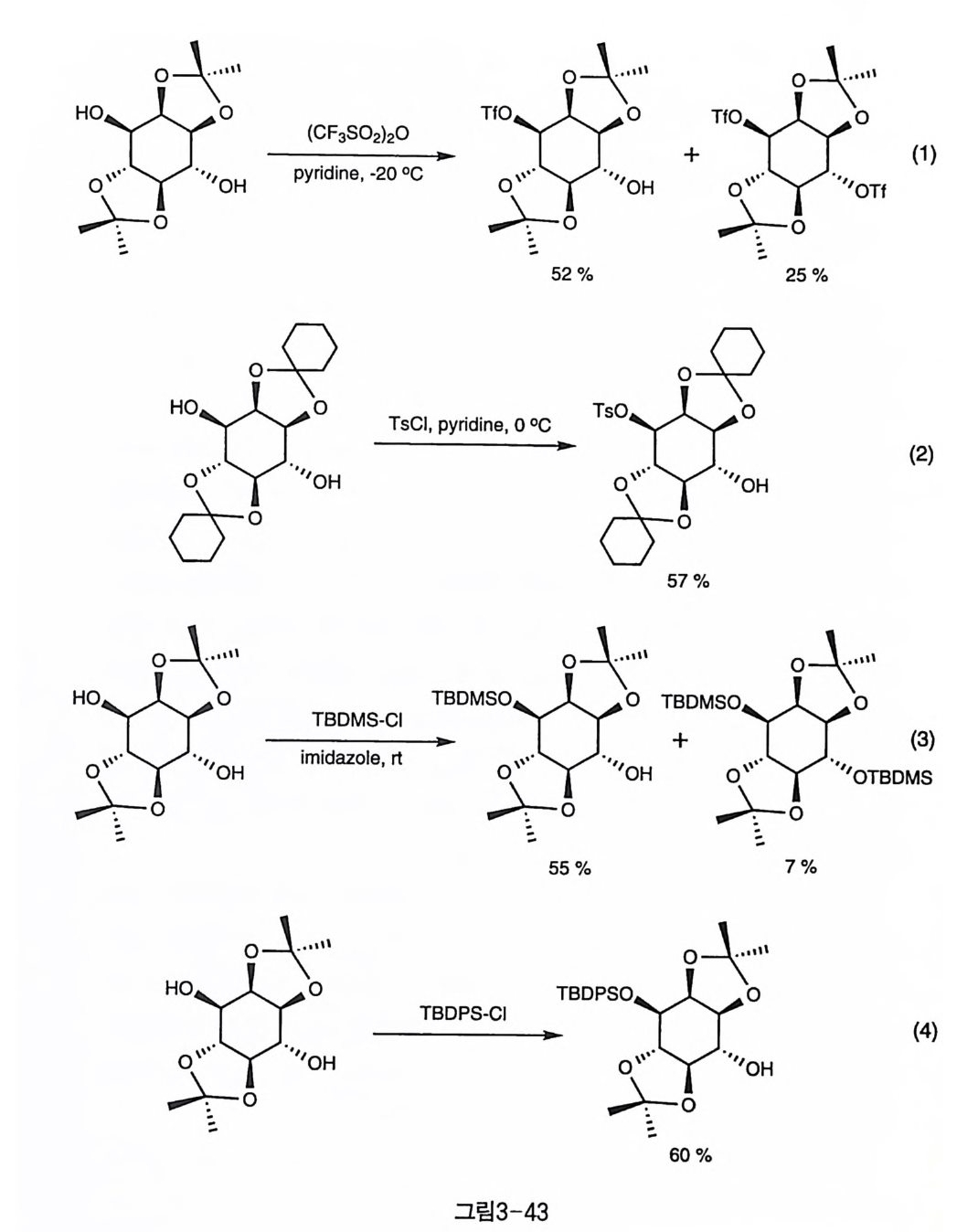
보다 클 것으로 예상되는 Bz 2 0 와 반응하면 반대로 4 번 수산기에 벤조 일화된 생성물이 훨씬 우세하게 나타났다(그림 3-41-2). 1,4 번 수산기 의 반응성 차이에 대하여 알려진 반응 중에 4 번이 우세하게 나타난 것 은 이것이 거의 유일한 예인데 이는 1 번 수산기가 시스 관계의 이웃한 2 번 수산기에 의해 입체 장애를 받기 때문에 주위가 모두 트란스 관계 인 4 번 수산기에 비해 반응성이 낮아진 것이라고 해석되었다〔 72). 한 편 Oza ki 등도 벤조일화 반응에서 일반적인 경향성대로 1 번 수산기의 반응성이 우세한 결과를 얻었는데, 이들은 BzCl 대신에 벤조일-이미 다졸울 CsF 와 함께 사용하여 , 1 번 수산기에 대한 반응성을 향상시켰 다(그림 3-41-3) [20 ] ’ 강염기 하에서의 벤질화 반응도 일반적으로 1 번 수산기가 우세함이 여 러 연구팀에 의해서 보고되었다. 그러나 대개는 주생성물인 1-Bn 만을 재결정 등으로 분리했을 뿐 1,4 선택성에 대하여 정량적으로 측정한 예 는 많지 않았다. 톨루엔 용매와 NaH 염기 하에서 BnBr 를 작용시켜 1- Bn 생성물을 60% 정도의 수율로 얻은 예가 보고되어 있었지만 (73), 같은 조건에서 재현한 실험 결과는 선택성이 그다지 높지 않음을 보여 주었다(그림 3-42-1) 〔 74). 벤질화 반응 중 선택성이 가장 좋은 조건은 BaO 와 Ba(OH )i를 BnBr 과 함께 반응시킨 경우였다(그림 3-42-2) 〔 75). 술폰화 반응도 1 번 수산기에 선택적으로 일어나는데, T f (74 〕와 T范 2 〕 등의 예가 보고되었다(그림 3 - 43-1,2). 입체 장애가 큰 실릴화 반응도 비슷한 경향을 나타냈는데, TBDMS 〔刀)와 TBDPS(76] 동이 연구되었다(그림 3-43-3,4). 1 번 수산기의 경우 이웃한 시스 관계의 2 번 수산기에 의해 입체 장 애가 큰데도 불구하고 일반적으로 친핵 반응성이 크다. 이에는 여러 가지 설명이 있을 수 있다. 우선 생각할 수 있는 것은 두 수산기 간의 산성도 차이로서 산성도가 큰 쪽이 더 쉽게 음이온을 형성하여 친핵 반응성이 클 것으로 생각할 수 있다. 두 수산기에 대한 열역학적인 산
 i 느 ::. ::.
i 느 ::. ::.
성도는 ab ini t io 계산에 의해 각각 1 번과 4 번의 수산기 이온의 안정성 을 통해 검정되었으나, 4 번 수산기 이온 쪽이 더 안정한 것으로 나타 나 열역학적 산성도는 반응성을 결정하는 요인이 아님이 밝혀졌다 [m . 한 편, 반응 속도론적 산성도는 두 수산기의 수소 이온이 수소성 용매를 첨가했을 때의 치환 속도로서 측정하였는데, 이 경우에도 4 번 수산기 쪽이 더 산성임이 확인되었다〔 78) . 이러한 산성도의 차이는 1 번 수산기의 경우 시스 관계인 2 번 수산기의 산소 원자와 분자 내 수소 결합을 이루는 것이 용이하여 발생하는 것으로 생각할 수 있다. 위의 두 실험 결과는 모두 반응성 차이에 있어서 1 번 수산기의 우세는 수산 기의 산성도로는 설명되지 않음을 나타내었다. 그래서, 1 번 수산기의 높은 친핵 반응성온 2 번 수산기의 산소 원자에 의한 throu g h -spa c e
 (CF3S02l20 (1 )
(CF3S02l20 (1 )
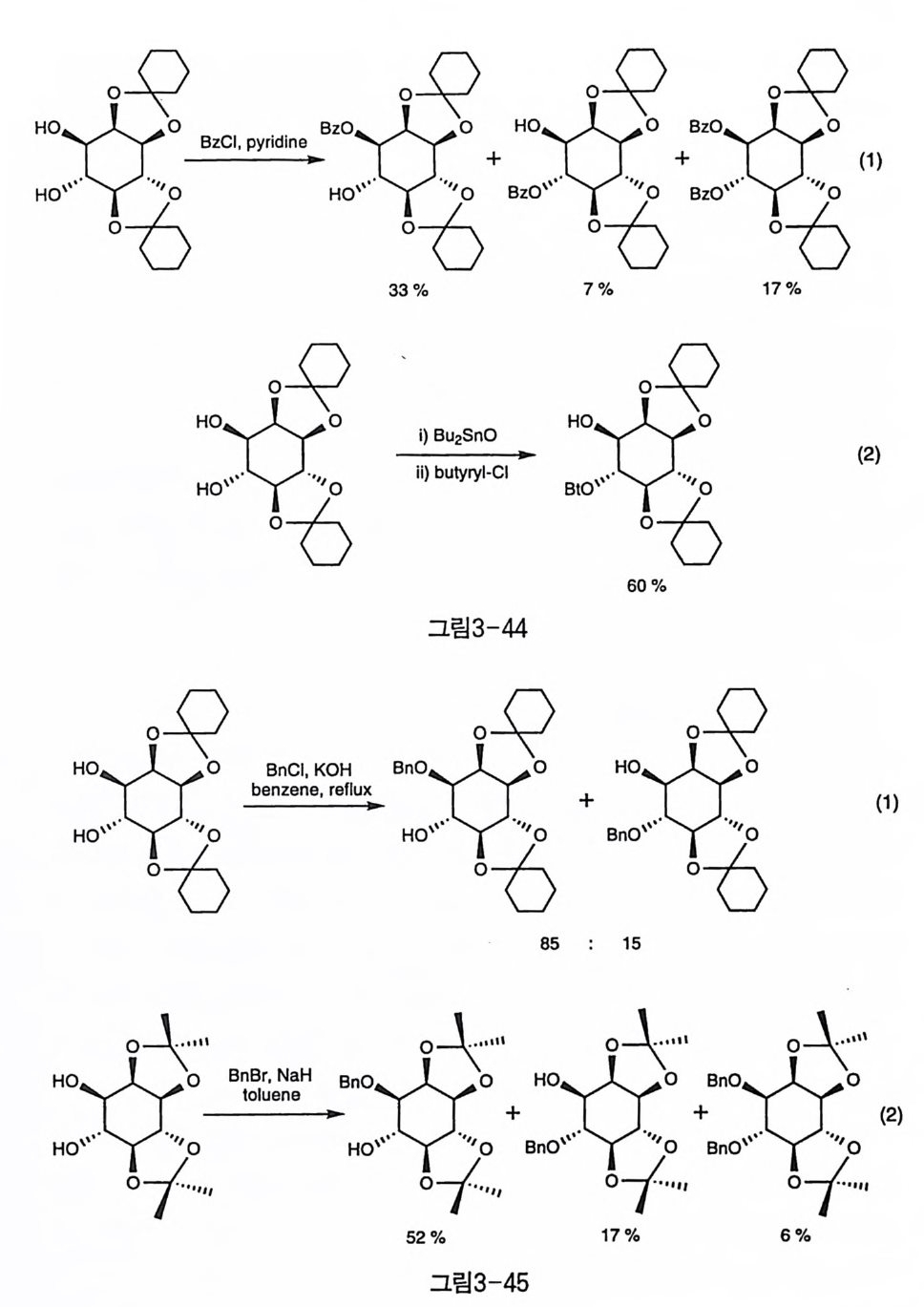
a-e ffe c t에 의한 것이라는 설명이 제안되었으나〔 74), 1 번 수산기 이온 울m ]안• 정 화시키는 용매 효과 역시 중요한 역할을 하는 것으로 보인다 3-8-3 (1, 6) 선택성 D i ace t al 로 보호된 1,6_ 디올의 X 선 결정 구조는 비틀린 배 모양이다 〔 7 이 . 그러나, MM 계산과 NMR 연구 결과는 기체상과 용매 속에서는 의자형을 이루고 있음을 보여주었다 (74). 1, 6 수산기 간의 선택성 역 시 형태가 상당히 고정된 di ace t al 에서 많이 연구되었다. 일찍이 dic y- clohexy lide ne 아세탈의 벤조일화 반응의 경우 6 번 수산기에 비해 1 번 수산기에 대한 반응성이 크다는 사실이 알려져 있기는 했으나, 주생성 물조차도 수율이 33% 에 불과하여 반응의 개선이 요구되었다(그림 3_ 44-1)[1 ).비 교적 최근에는 1-Bz 만을 70% 정도의 수율로 얻은 결과 도 보고되었으나, 이전의 반응과 뚜렷한 반응 조건의 차이는 없었다 [67 ). 1 ,6 수산기는 이웃한 수산기이기 때문에 1,2 반응성에서 사용되 었던 Sn 중간체를 이용한 아실화 반응도 시도되었다. 고리 주석 중간 체를 이용하여 부티릴기를 도입할 경우에는 6-B t가 60% 수율로 얻어 졌다(그림 3-44-2) 〔 8 이 . 벤질화 반응에 있어서도 일반적인 염기 조건에서 1 번 수산기의 반응 성이 우월함을 나타내는 결과가 보고되어 있었다 . 이때 상대적인 생성 물의 양은 GLC 로 정량되었고 반응 용매로는 벤젠이 사용되었는데, 생 성된 1-Bn 와 6-Bn 의 비는 85:15 정도였다(그림 3_45_1) 〔 81). 비슷한 반응을 톨루엔에서 시행했을 때에도 1 번 수산기에 대한 반응성이 크게 나타남을 보여주었다(그림 3-45-2) 〔 74 〕 ' 그러나 반응 용매로 극성인 DMF 를 사용한 경우에는 반응 시간에 관계 없이 두 수산기 간의 반응성에 거의 차이가 없었고 W 선, Sn 중간
 33% 7% 17%
33% 7% 17%
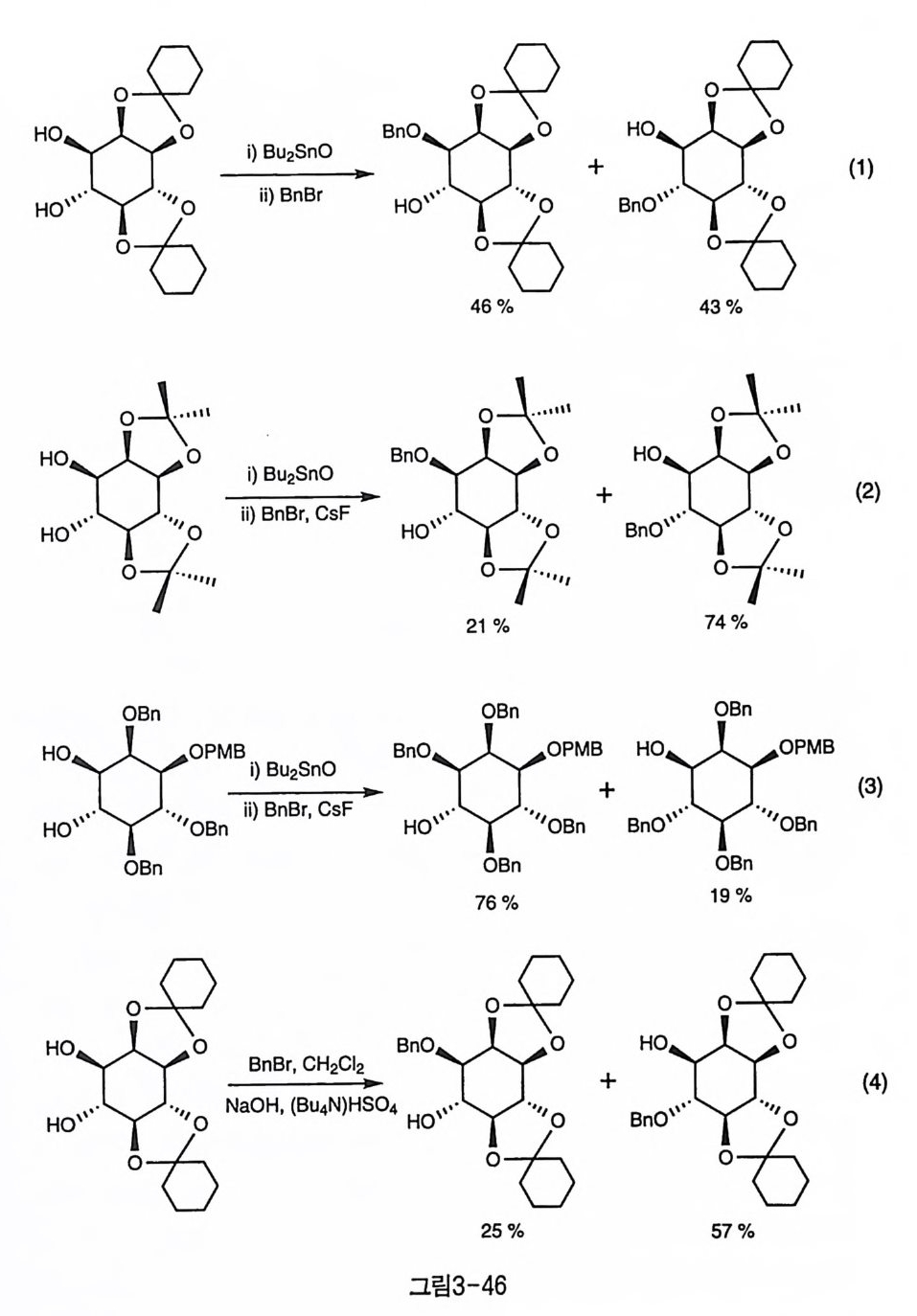
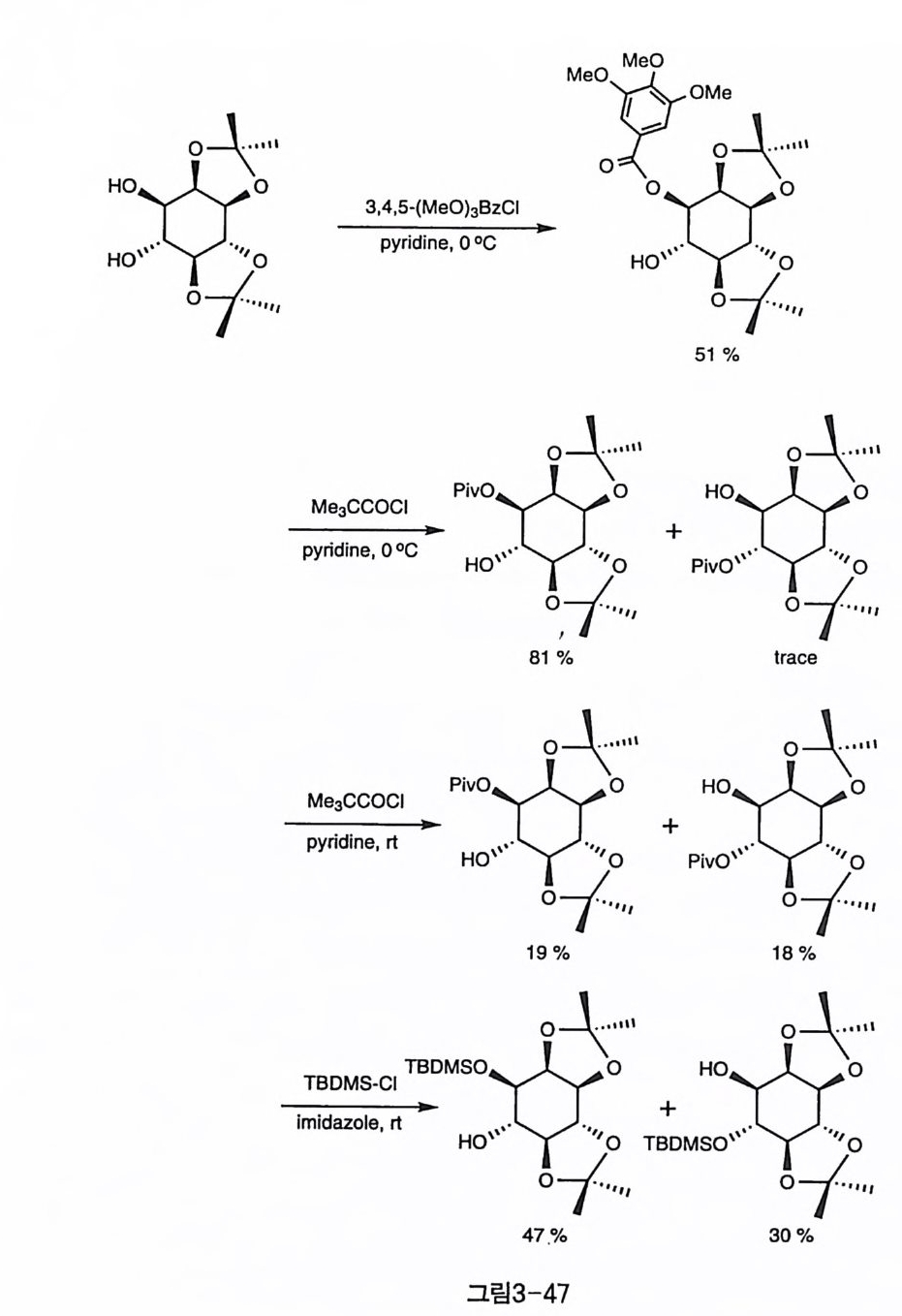
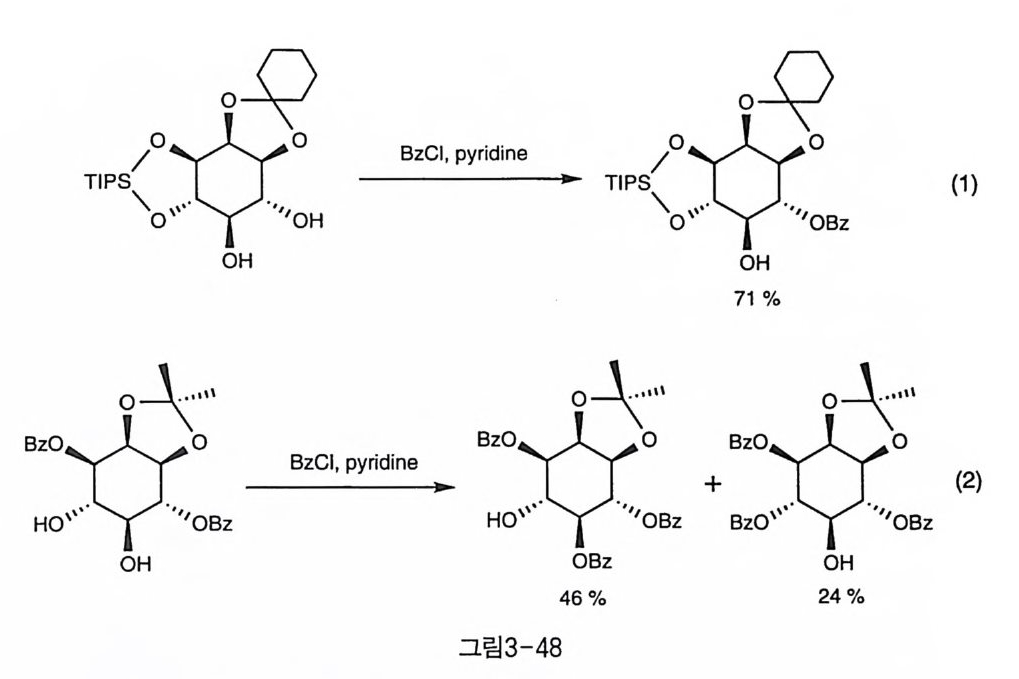
체를 사용한 경우에도 생성비는 비슷하게 나타났다(그림 3-46-1)(22 〕· 재미있게도 이 경우 친전자체와 함께 CsF 를 가해 주면 4 번에 대한 반 응성이 월등하게 커진다는 사실이 알려졌고〔 82), 이에 대한 정량적 실 험 결과도 이러한 경향성을 뒷받침하였다(그림 3-46-2 ) (74 〕. 또 재미있 는 것은 아세탈로 보호되지 않아서 비교적 이노시톨 고리의 형태 변화 가 자유로울 것으로 기대되는 출발 물질에 주석 중간체를 이용해서 벤 질화하면, 1 번 수산기에 대한 반응성이 크게 나타난다(그림 3-46- 3)[8 3 ).한 편 상전이 촉매를 사용할 경우에는 반대로 4 번 수산기에 대 한 반응성이 큰 것으로 나타났다(그림 3 一 46-4) 〔 2 〕. 입체 장애가 큰 아실 주게와의 반응에서는 온도가 낮은 경우 1 번에 대한 선호도가 큰데, 온도가 증가하면 선택성이 없어진다. 입체 장애 가 큰 실릴기인 TBDMS 를 도입하는 경우에도 어느 정도 1 번 수산기에 대한 선택성이 관찰되었다(그림 3-47)(74). 3-8-4 (4, 5) 선택성 4,5 번 수산기 역시 1,6 번 수산기와 마찬가지로 둘 다 수평 방향이 며, 이웃한 관계에 있다. 단 1,6 인 경우에는 1 번 수산기가 시스 관계의 2 번 수산기 산소와 분자 내 수소 결합을 더 용이하게 할 수 있다는 차 별성이 있는 데 비해 4,5 번 수산기들은 이웃한 수산기들 역시 모두 트 란스 관계에 있어 반응의 선택성을 일으킬 단서가 그다지 눈에 띄지 않 는다. 단지 수직 방향인 2 번에 입체 장애가 큰 치환기가 도입되면, 시 스 관계인 5 번 수산기의 반응성이 낮아질 것으로 기대되는 정도이다. 피리딘 동의 략한 염기 조건에서 아실화한 반응의 예를 보면 오각형 아세탈과 칠각형의 TIPS 기를 가진 기질에서 뚜렷한 4 번 수산기에 대한 선택성이 관찰된다(그림 3-48-1) 〔 9). 이 경우에는 입체 장애가 큰 TIPS 기의 영향으로 바로 이웃한 5 번 수산기에 천전자체의 접근이 어
 HO.. A .... 0 i) Bu2SnO BnO.. A .... 0 H (1)
HO.. A .... 0 i) Bu2SnO BnO.. A .... 0 H (1)
 II
II
 BzCI, pyridine TIPS<«Bz
BzCI, pyridine TIPS<«Bz
려웠던 것으로 생각할 수 있다. 그러나 보기 드물게 5번 수산기에 대 한 아실화 반응이 보다 선택적인 예도 있는데, 선택성에 대한 정확한 설명은 아직 알려져 있지 않다. 다만 (1,2) 아세탈에 의한 이노시톨 고 리의 변형이 두 수산기의 환경을 변화시켰을 것으로 보인다(그림3-
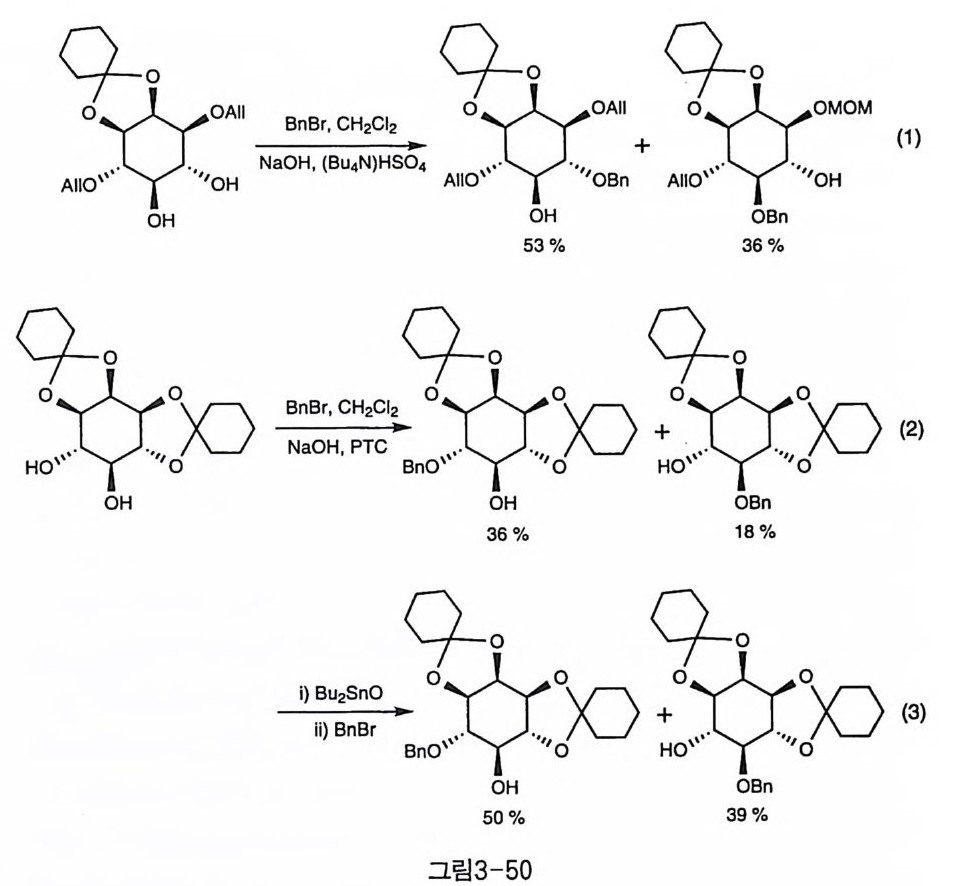
48-2) [19). 강염기 하에서 직접적인 알킬화 반응을 하면, 두 수산기 간에 큰 차 이는 없지만, 4번 수산기가 약간 더 우세한 경향을 보인다(그림3-49-1,2[44),그림3-49짓(27〕). 상전이 촉매를 사용한 알킬화에서는 4번 수산기에 대한 선호도가 좀 더 커지는 경향이 나타난다(그림3-50기)〔84〕. Diacetal인 경우에는 상 전이 촉매를 사용한 경우(그림3-50-2)〔2〕가 고리 주석 중간체를 사용 한 경우(그림3-50-3)〔2익보다 나은 선택성을 보인다. 이는 위에서 언 급한 대로 2번의 치환기에 의한 입체 장애가 중요한 요소로 작용하기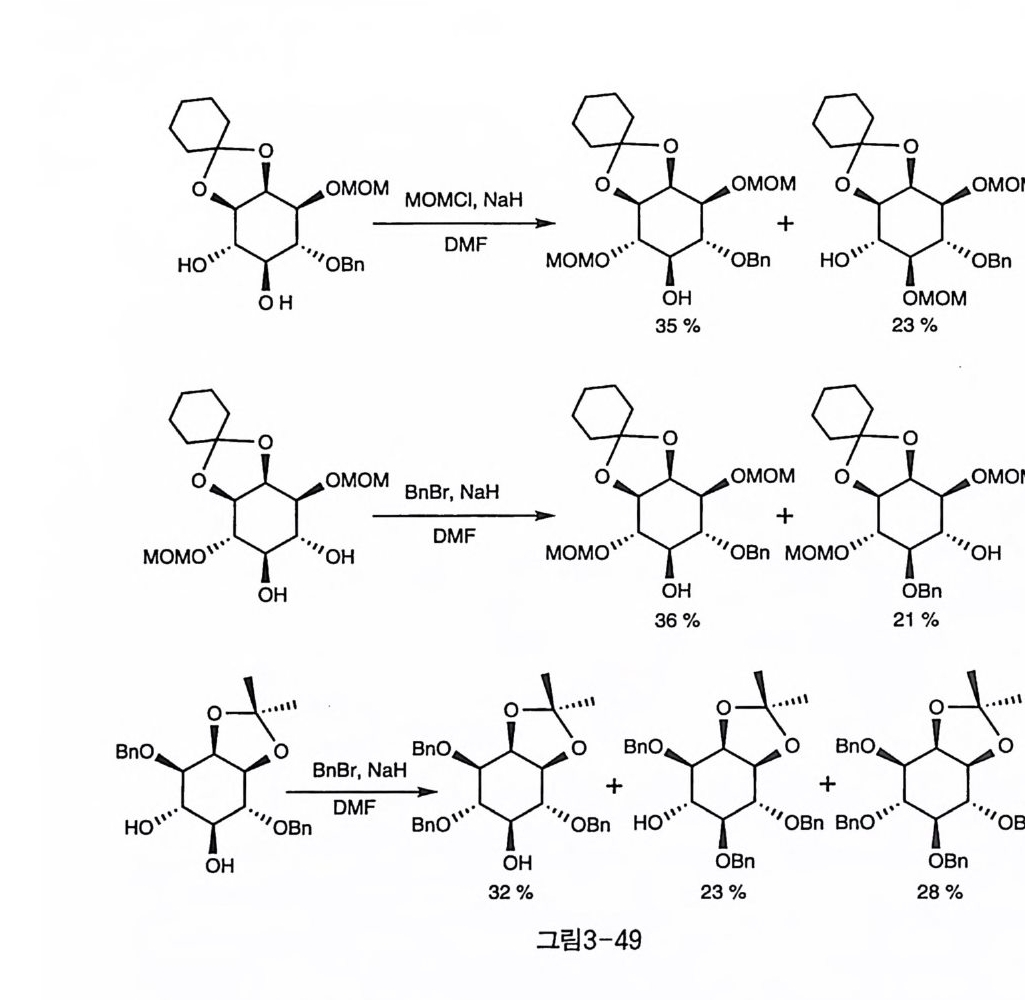 <0> 。' F M0도no: \::OM (1)
<0> 。' F M0도no: \::OM (1)
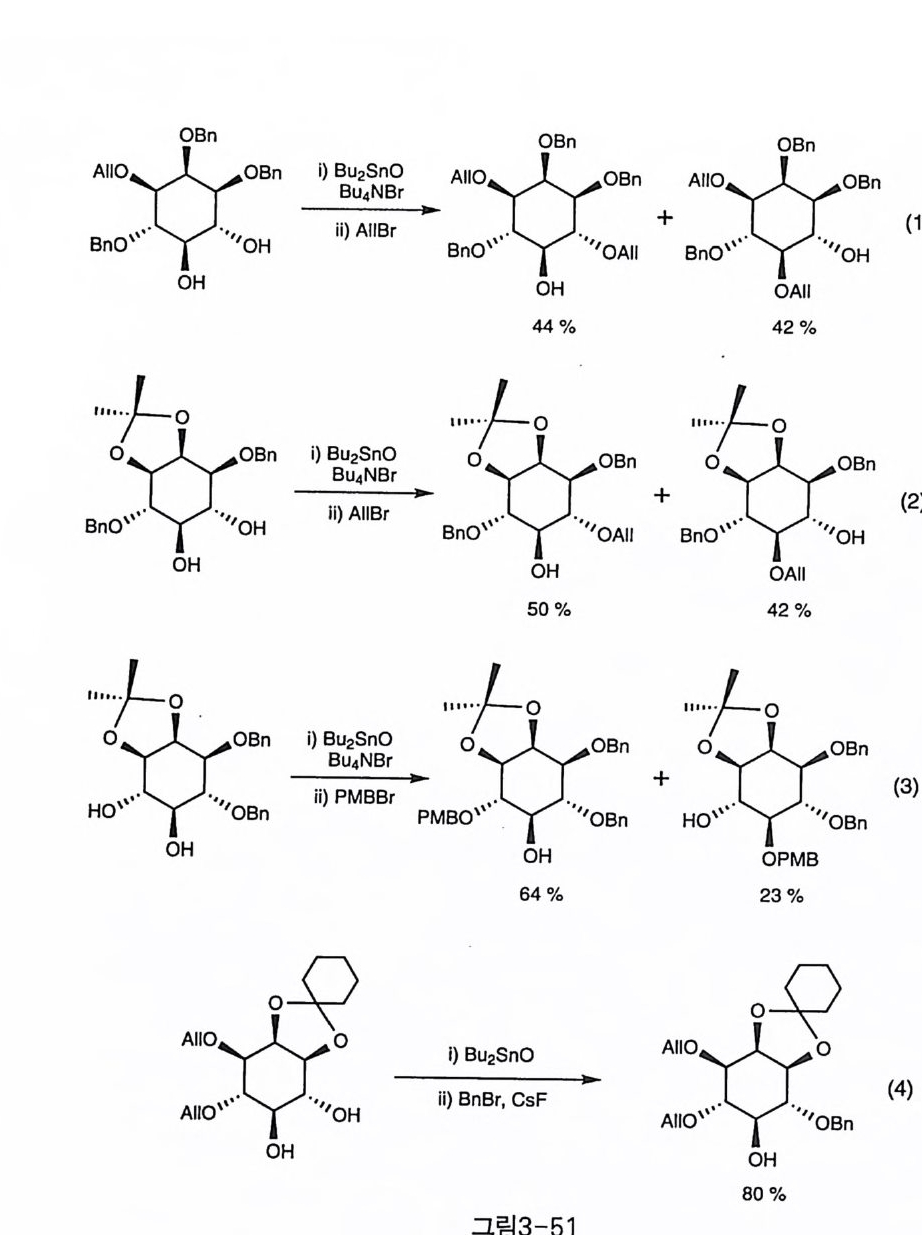
때문인 것으로 생각된다. 고리 주석 중간체를 거치는 경우에는 기질에 따라 상당한 차이가 드 러나, 아세탈로 고정되어 있지 않은 경우에는 거의 선택성이 없음이 나타나고(그림3-51-1)(85), 아세탈로 고정되어 있는 경우에도 아세탈 의 위치에 따라 차이가 있다. (1,2)아세탈인 경우 선택성이 그다지 높 지 않은 반면에(그림3-51-2), (2,3)아세탈인 경우는 4번 수산기에 대 한 선택성이 현저하게 높아진다(그림3-51-3)(28). (2,3)아세탈이 존재 하는 경우에 CsF를 천전자체와 함께 사용했을 때 가장 높은 선택성을
 \AH N�N\:ABn+ \o:OM (1
\AH N�N\:ABn+ \o:OM (1
% ���� 3-50 ���д����(���� 3 N 51-4) 0 86). 0�|�� 4, 5 �� °�0��� �\� ���1
 ::*:: 三 Ao`B no OnB仁O 00 Bn+A A I 00I Bn >5OBn Bn H,'' 1 ,’1
::*:: 三 Ao`B no OnB仁O 00 Bn+A A I 00I Bn >5OBn Bn H,'' 1 ,’1
참고문헌 (1) Ang yal , S . J.; Tate , M. E.; G ero, S. D. J. Chem. Soc. 1961, 4116 -4122. 떠 Gareg g, P. J.; Iversen, T.; Joh ansson, R. ; L in d berg, B. Carbohy dr . Res. 1984, 130, 322 -326. (미 Fernandez de la Pradil la; Jara mi llo , C.; Jim enez- B arbero, J.; Ma rtin -Lomas, M.; Penades, S .; Z apa t a , A. Carbohy dr . R es. 1 990, 207, 249-257. 띠 Chung , S. K.; Chang , Y. T. J. Chem. Soc., Chem. Commun. 1995, 11-12. (회 Gig g, J.; Gig g, R.; Payn e , S.; Conant, R. J. Chem. Soc., P erkin Trans. 1 1987, 1757-1762. 〔이 Desai , T.; Gig g, J.; Gig g, R.; Pay ne , S. Carbohy dr . Res. 1992, 228, 65-79. (7) Ley, S . V. ; L eslie , R.; Tif fin, P. D.; Woods, M. Tetr a hedron Lett. 1992, 33, 4767-4770. (8) Ley, S. V. ; P ri ep k e , H. W. M.; W arrine r, S. L. Ang ew . Chem. Int. Ed. Eng l. 1994, 33, 2290 -2292. [9) Wata n abe, Y. ; M i tan i, M.; Mori ta, T.; O za ki, S. J. Chem. Soc., Chem. Commun. 1989, 482 -483. (10) Bruzik , K. S.; T sai , M. -D. J. Am. Chem. Soc. 1992, 114, 6361-6374. (11) Oza ki, S.; Kondo, Y.; Shio t a ni, N.; Og as awara, T.; Wata na be, Y. J. Chem. Soc. , Perkin Trans. 1 1992, 729 -737. (1미 Akiya ma, T.; Takechi, N.; Oza ki, S.; Sh iot a , K. Bull. Chem. Soc. Jpn . 1992, 65, 366 -372. (1회 Lee, H. W.; Kish i , Y. J. Org. Chem. 1985, 50, 4402 -4404. (14 ) Baud in, G.; Glanzer, B. I.; Swa mina th a n, K. S.; Vasella, A. Helv. Chim . Acta 1988, 71, 1367 -1378. (15 ) Bi lling ton , D. C. ; B aker, R.; Kulag ow ski , J. J.; Mawer, I.; Vacca, J. P.; deSolms, S. J.; Huff , J. R. J. Chem. Soc., Perki n Trans. 11989, 1423 -1429. (16] A 띠 ersch, P.; Schn 백 er, M. P. Tetr a hedron: Assy m metr y 1993, 4, 2135-
2138. (17 ) Bil ling t on , D. C.; Balcer, R. J. Chem. Soc., C hem. Commun. 1987, 1011- 1013; deSolms, S . J.; Vacca, J. P.; Huff , J . R. Tetr ah edron Lett. 1987, 4503 -4506. (18 ) Oza ki, S.; K og a, Y.; Lin g , L.; W ata n abe, Y.; Kim ura, Y.; Hirat a , M. Bull. Chem. Soc. J pn. 1994, 6 7, 1058-1063. [19 ] 야 un g, S. K.; Chang , Y. T.; Sohn, K. H. J. Chem. Soc., Che m . Commun. 1996, 163 -1 64. [20 )Ozak i, S.; Kondo, Y.; Nalca hira, H.; Yamaoka, S.; W ata na be, Y. Tetr a he-dron Lett . 1 987, 28, 4691-4694. [21 ) Salamori cz yk , G. M. ; P ie t r us ie w i cz, K. M. Tetr a hedron Lett . 1991, 32, 6167-6170. (22) Garegg , P. J.; Lin d berg, B . Carbohyd r . Res. 1988, 173, 205-216. (23) Reese, C. B.; Ward, J. G. Tetr a hedron Lett. 1987, 28, 2309-2312. (2A) Ang ya l, S. J.; Randall, M. H.; Tate , M . E. J. Chem. Soc. 1967, 919-922. 固 Akiya ma, T.; H irof u ji, H .; O za ki, S. Tetr a hedron Lett . 1991, 32, 1321- 1324. [26 ] F alck, J. R .; Abda li, A. Bio o rg. Med. Chem. Lett . 1 993, 3, 717 -720. [”]G igg, J.; Gigg, R.; Payn e , S.; Conant, R. J. Chem. Soc., P erkin Trans. 1 1987, 423 -429. [28 ] Desai , T.; Gig g, J.; Gig g, R.; Ma rtin- Zamora, E. Carbohyd r . Res. 1994, 262, 59-77. [29 ) Gigg, J.; Gig g, R.; Payn e , S.; C onant, R. J. Chem. Soc., P erki n Trans. 1 1987, 2411-2414. (3 이 Massy, D. J. R.; Wy ss , P. Helv. Chim . Acta 1990, 73, 1037 -1 057. [31 ) Dreef, C. E.; E li e, C. J. J.; Hoog er hout, P.; van der Marel, G. A. ; v an Boom, J. H. Tetr ah edron Lett . 1 988, 29, 6513 -6516. @]W ata na be, Y.; Fusim oto , T.; S h ino hara, T.; Oza ki, S. J. Chem. Soc.,
Chem. Commun. 1991, 428-429. 〔회 Ang ya l, S. J.; Russell, A. F. Aust. J. Chem. 1969, 22, 383-390. [34 )L ey, S . V. ; Ste m f eld , F. Tetr a hedron 1989, 45, 3463 -3 476. 〔 3 회 Ly ut i k, A. I.; Kryl o va, V. N.; Kozlova, S. P.; K lya s hchit sk i i, B. A.; Shvets , V . I.; Evstig n eeva, R. P.; Zhdanovic h , E. S. Zh. Obshch. Khim . 1971, 41, 2747 -2753. 〔 3 이 Fis c her, E., Ber., 1920, 53B, 1621 -1633. 〔 3 까 Ohle, H., Ber., 1924, 57B, 403 -409. [38 )B onner, W. A. J. Org. Chem. 1959, 24, 1388 -1390. 〔 3 이 Anderson, L.; Lande!, A. M. J. Am. Chem. Soc. 1954, 76, 6130-6132. 〔삐 Ang yal , S. J.; Gi lh am, P. T.; McDonald, C. G. J. Chem. Soc. 1957, 1417 -1422. [41 )Ang ya l, S. J.; Melrose, G. J. H. J. Chem. Soc. 1965, 6494-6500. (42) Meek, J. L.; David s on, F.; Hobbs, F. W. J. Am. Chem. Soc. 1988, 110, 2317 -2318; Hobbs, F. W.; Meek, J. L. US Pate n t, 4, 873, 355. 1989. [43 )Chung , S. K.; Chang , Y. T. J. Chem. Soc., Chem. Commun.1995, 13-14. (44) Okada, K. ; H ashiz u me, K.; Tanin o , H.; Kakoi, H.; Inoue, S. Chem. Phann. Bull. 1989, 37, 791-793. 固 Sch iff, H. Ju stu s Lie b ig s Ann. Chem. 1857, 102, 334 -339. [46 )Mets c h ies , T.; Schultz, C.; Jas to r f f, B. Tetr a hedron Lett. 1988, 29, 3921- 3922. [47 ) Ozal ci, S.; Wata n abe, Y.; Og as awara, T.; Kondo, Y.; Sh iot a ni, N.; Ni sh i i, H.; Mats u k i, T. Tetr a hedron Lett .1 986, 27, 3157-3160. 團 Cooke, A. M.; Noble, N. J.; Payn e , S.; G ig g, R.; Pott er , B. V. L. J. Chem. Soc., Chem. Commun. 1989, 269-271; Noble, N. J.; Cooke, A. M.; Pott er , B. V. L. Carbohy dr . Res. 1 992, 234, 177-187. [49 )I seli n, B. M. J. Am. Chem. Soc, 1949, 71, 3822-3825. 〔 5 이 Ballou, C. E.; Piz e r, L. I. J. Am. Chem. Soc. 1960, 82, 3333-3335.
詞 Chung , S. K.; Ry u, Y.; Chang , Y. T.; Moon, S. H. Kor. J. Med. Chem. 1992, 2, 33 -4 4. g끽 Pie t r us ie w i cz , K. M.; Salamori cz y k, G. M. ; B ruzk, K. S. Tetr a hedron 1992, 48, 5523 -5542; ide m, ibi d . 1994, 50, 573. 〔 5 미 Shvets , V. I.; Klya s hchit sk i i, B . A.; Ste p s nov, A. E.; Evsti gn eeva, R. P. Tetr a hedron 1973, 29, 331 -3 40. [54 ) Bil ling ton , D. C.; Balcer, R.; Kulag o wski , J. J.; Mawer, I . J. Chem. Soc., Chem. Commun. 1987, 314 -3 16. [55 )W ata n abe, Y.; Og a sawara, T.; Nalca hira , H. ; M ats u k i, T .; Oza ki, S. Tetr a - hedron Lett . 1 988, 29, 5259 -5 262. g이 Molotk o vsky , J. G. ; Berge l son, L. D. Tetr a hedron Lett . 1 971; 12, 4791- 4794; Molotk o vsky , J. G. ; Berge lson, L. D. Chem. Phys . Lipid 1973, 135 - 147. (57) D1-ef, C. E.; van der Marel, G. A.; van Boom, J. H. Reel. Trav. Chim . Pays - Bas 1987, 106, 161 -162. [58 )Y u, K. L.; Fraser-Reid , B. Tetr a hedron Lett . 1988, 29, 979 -9 82. [59 ] 짜t anabe, Y.; Komoda, Y.; Ebis u y a, K.; Oza ki, S. Tetr a hedron Lett. 1990, 31, 255 -2 56. @]C ooke, A. M.; Pott er , B. V. L.; Gi gg, R. Tetr a hedron Lett . 1987, 28, 2305-2308. 圓 W tana be, Y.; Komoda, Y.; Oza ki, S. Tetr a hedron Lett. 1992, 33, 1313- 1316. (62) Wata n abe, Y.; Inada, E.; Jinn o, M.; Oza ki, S. Tetr a hedron Lett. 1993, 34, 497-500. [63 )T ate , M. E. Anal. Bio c hem. , 1 968, 23, 141-149. [64 ] L ic h te n th a ler, F. W.; Em ig, P. Carbohy dr . R es. 1968, 7, 121 -137. [65 )D onnan, D. E.; Ang ya l, S. J.; Robert s, J. D. J. Am. Chem. Soc. 1970, 92, 1351-1354.
[66 ] D esai, T.; F emandez-Mayo r alas, A.; Gig g, J.; Gig g, R.; Pay ne , S. Carbo- hyd r . R es. 1990, 205, 105-123. 〔 6 까 Balcer, R.; Kulag ow ski , J. J.; Bi lling ton , D. C.; L eeson, P. D. ; L iv e rt on , N. J. Chem. Soc., Chem. Commun. 1989, 1383-1385. [68 ) Gareg g, P. J.; H ultb e rg, H.; Wall in, S. Carbohyd r . Res. 1982, 108, 97 - 101 . 〔 6 이 Deslong ch amp s, P., S te r eoelectr o nic E f fects in Orga n ic C hemi str y, Perga - mon Press, 1983, pp 80 -8 5. [70 )C hung , S. K.; Chang , Y. T.; Sohn, K. H. Kor. J. Med. Chem. 1994, 4, 57 -65. [71 )T arusova, N. B.; Grosheva, V. S.; Kozlova, S. P.; Tep lins kay a, R. B.; Pre-obrazhenski i, N. A. Zh. Org. K him . 1968, 4, 967-971 . [72 ) Og aw a, S.; Ok i, S.; Kunit om o, H.; Sua mi, T. Bull. C hem. Soc. Jpn . 1977, 50, 1867 -1871 . 〔 7 이 Vacca, J. P.; d eSolms, S. J.; Huff , J. R. ; B i lli n g ton , D. C.; Balcer, R.; Kulag ow ski , J. J.; Mawer, I. Tetr a hedron 1989, 45, 5679-5702. [74 )C hung , S. K. ; R y u, Y. Carbohyd r . Res. 1994, 258, 145-167. 〔 7 회 Dreef, C. E.; Tuin m an, R. J.; Lefe b er, A. W. M.; Eli e, C. J. J.; van der Mare!, G. A.; van Boom, J. H . Tetr a hedron 1991, 47, 4709-4722. (76) Ward, J. G.; Young , R. C. Tetr a hedron Lett . 1988, 29, 6013-6016. (77) Kim , K. S.; Cho, S. J.; Oh, K. S.; Son, J. S.; K im , J.; Lee, J. Y.; Lee, S. J.; Lee, S.; C hang , Y. T.; Chung , S. K.; Ha, T. K.; Lee, B. S.; Lee, I. J. Phys . Chem. A, 1997, 101, 3776. [78 )C hung , S. K.; Chang , Y. T. Kor. J. Med. Chem. 1997, 7, 15. [79 ) Chung , S. K.; Ry u, Y.; Chang , Y. T.; Whang , D.; Kim, K. Carbohy d r. Res. 1994, 253, 13-18. 〔 8 이 Gou, D. M.; Liu , Y. C.; Chen, C. S. Carbohy dr . Res. 1992, 234, 51-64. [81 ) A ng yal , S. J.; Russell, A. F. Aust. J. Chem. 1968, 21, 391 -404.
〔 8 익 Liu, Y. C.; Chen, C. S. Tetr a hedron Lett. 1989, 30, 1617 -1620. 園 Desai , T .; G ig g, J.; Gig g, R.; Payn e , S. Carbohyd r . Res. 1992, 225, 209- 228. [84 ] D reef, C. E.; S chie b ler, W.; van der Marel, G. A.; van Boom, J. H. Tetr a -hedron Lett. 1991, 32, 6021 -fJ 024. [85 )D esai , T.; F ernandez-Mayo r alas, A.; Gig g, J.; Gig g, R.; P ayn e , S. Carbo- hyd r . Res. 1 992, 234, 157 -175. [86 ] G 叫 D. M.; C hen, C. S. Te t rahe& 야 Lett. 1992, 33, 721 구 24.
제牛상 인산이노시톨 (IPn) 합성 D-1 (1 ,4,5)P 파 중요한 2 차 전달 물질이라는 사실이 밝혀지기 전부 터 상당수의 IP 려 고전적 합성이 이루어져 왔다(1, 2, 미 . 그러나 많은 개선점들이 요구되기도 하였다. 특히 이웃한 수산기가 존재하는 경우 오각형의 고리형 인산기가 부반응으로 생성되는 것을 억제하는 것이 중요한 문제 중의 하나였다. 인산이노시톨의 생물학적 활성이 속속 밝 혀지면서 IP 려 합성은 르네상스를 맞이했다고 할 만큼 활발하게 이루 어졌다. 이후 개선된 전략에 의한 IPn 합성에 대한 새로운 단행본〔 4, 5] 과 총설들〔 6-9 〕도 발표되었다. 그러나 최근에도 새로운 IPn 또는 그 유사체들을 합성하는 개선된 방법들이 계속 보고되고 있다. 4-1 합성상의 일반적 인 문제점 특정 인산이노시톨울 합성하는 데는 크게 네 가지 해결해야 할 문제 점들이 있다 . (1)인산기가 목표하는 위치에 도입되기 위해서는 적절히 보호된 이노시톨의 유도체가 필요하다. (2) 효율적인 인산기 도입 방법
이 필요하다. 특히 이웃한 두 수산기에 인산기를 도입할 때에는 고리 인산의 형성을 억제할 수 있어야 한다 . ( 3) 인산기 도입 후 보호기를 제거하는 과정에서 인산기가 이웃한 수산기로 이동하거나 고리 인산을 형성하는 것을 막아야 한다 . (4) 광학 활성을 가진 인산이노시톨을 만 들기 위해서는 광학 활성의 출발 물질을 선택하거나 적절한 단계에서 광학 분할을 실시해야 한다 . 4-1-1 보호기 도입 이노시톨에 보호기를 도입하는 전략은 오래전부터 연구되어 왔다〔 1 〕 . 가장 일반적으로 사용되어 온 보호기들은 아세틸, 벤질, 벤조일, p- 메톡시 벤질, 알릴, iso p ro p yli d e ne, cy cl ohexy lid e ne, ort ho fo rm ate , 실 릴기 등이다 . 각 보호기의 도입 및 제거, 그 밖의 성질에 대해서는 3 장에서 자세하게 다루었다 . 4-1-2 인산기 도입 효율적인 인산기 도입을 위해 다양한 인산화 시약들이 개발되었으 며, 각각의 특성에 대해서는 3 장에서 자세히 다루었다 (3-5 참조). 4-1-3 보호기 제거 일반적으로 인산기의 보호기 제거 과정에서 이웃한 자유 수산기가 존재한다면, 인산기 이동 반응이나 고리 인산의 형성이 부반응으로 일 어난다 그러므로, 인산기의 보호기가 먼저 제거되는 반응 조건이 바 람직하다 촉매 하에서의 가수소 분해 반응이나 산, 염기 등의 반응이 사용되며, 반응 후 소량의 불순물을 제거하기 위해서는 이온 크로마토
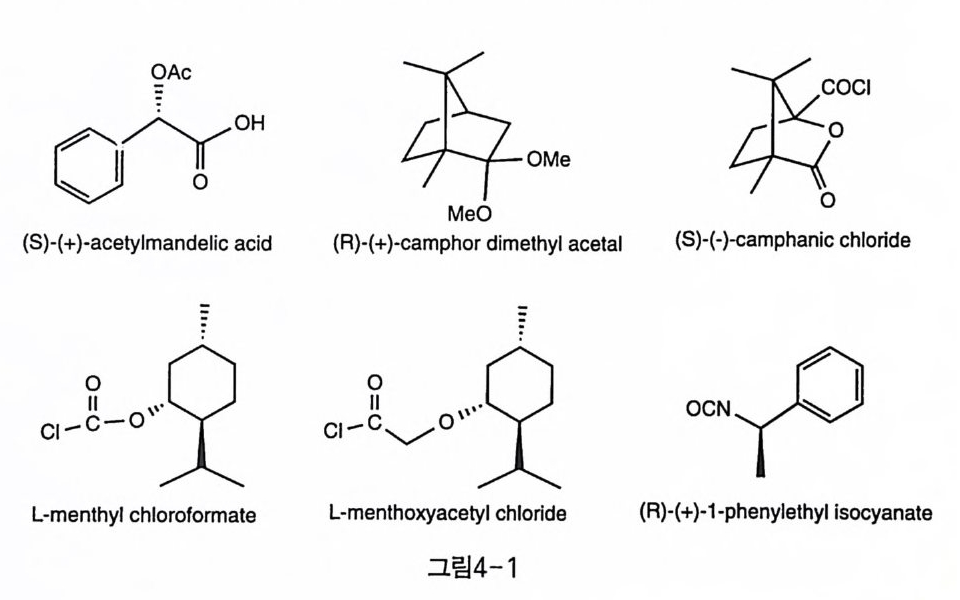
그래피를 실시하기도 한다. 4-1 -4 광학 활성을 가진 이노시톨 유도체 합성 메조 화합물인 벤젠이나 이노시톨울 출발 물질로 사용하는 경우, 적 당한 단계에서 광학 분할이 필요하다 . lPn 의 합성에서는 대부분의 광 학 분할이 라세미 상의 이노시톨 유도체를 부분 입체 이성질체 쌍으로 만들어 재결정이나 크로마토그래피로 분리하는 방법이었다 . 얼마 전까 지만 하더라도 D-mannose 의 오르소에스테르 (10) 를 이용하는 것이 유 일한 방법이었지만 최근 들어 다양한 분할제들이 개발되었다(그림 4- 1). (S)-( +)-acety lm andeli c a c id, (S)-(-) ~ 및 (R)-(+)-camp ho r dim e th yl aceta l , L -m enth y l chlorofo rm ate , L -m enth o xy a cety l chlor ide , (R) - (+) -1-ph e ny le th yl iso cy a nate 등이 있는데, 현재까지로는 (S)-(-)- 및 (R) -( + ) -cam p hana t e 가 이 노시 톨 유도체로서 가장 효율적 인 분할 제로 보인다. 한편, 키랄 HPLC 를 이용한 중간체 분리도 시도되었으
 ogOAc O H >OMe 訂
ogOAc O H >OMe 訂
며 에스테라제, 리파제, 프로테아제 등의 효소를 이용한 아실 도입 및 가수 분해 반응도 수행되었다. 출발 물질 자체를 자연에서 쉽게 구할 수 있는 광학 활성 물질을 사 용함으로써 이러한 광학 분할의 문제를 원천적으로 해결한 연구도 보 고되 었다 여 기 에 사용된 주요 출발 물질에 는 1-quebrachitol, D -3 -methyl -chiro -inositol, ( -) -quinic acid, D -glucurono -6, 3 -lactone, galactinol, D-mannitol 동이 있다 또, 생체 내 반응을 흉내 낸 Ferrier 반응을 이 용하여, D -galactose, D -glucose, D -mannose로 부터 이노시톨을 만드는 방법도 보고되었다(그림4-2).
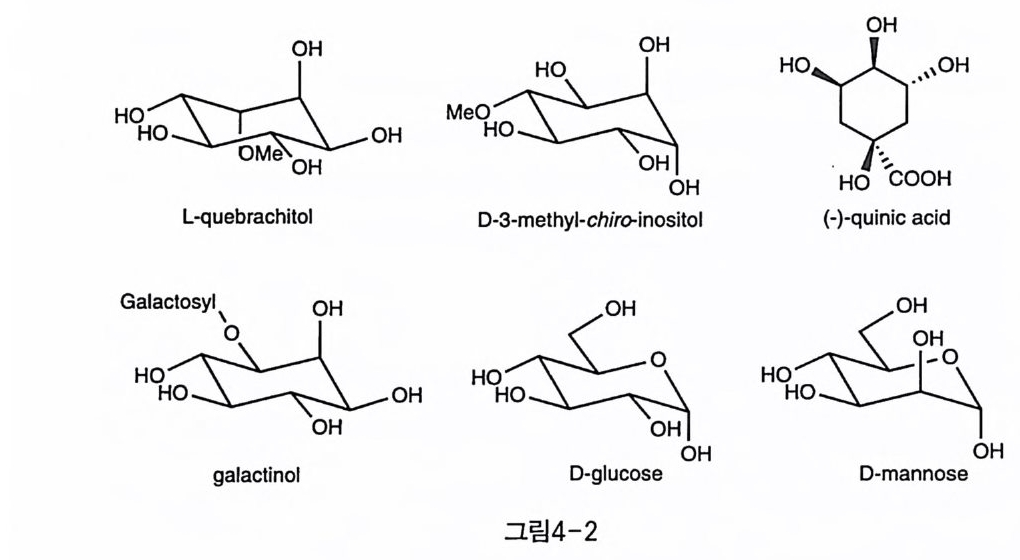 H O0H OH
H O0H OH
4-2 일인산이노시톨 일인산이노시톨에는 모두 4개의 가능한 위치 이성질체가 존재하는 데, 대칭 평면을 갖는 두 개의 I(2)P, 1(5)P와 두 광학 이성질체 짝인
1(1 or 3)P, 1(4 or 6)P가 있다. 현재까지 존재 가능한 메조 및 광학 활 성의 IPl은 모두 합성되었고, 라세미 형태로도 합성이 보고되어 있다. 4-2-1 1(1)P 이노시톨 인지질의 가수 분해 산물이 우회전성이며, 그 입체 구조가 D-l(l)P임(11)이 알려진 전후로 이들 일인산이노시톨의 라세미 및 각 광학 활성 I(l)P의 합성은 활발하게 이루어졌다. D-와 L-l(l)P의 입 체적 구조는 절대 배열이 알려져 있던 galactinol로부터 L-l(l)P울 만 들어서 밝힐 수가 있었다(그림4-3, Ballou 등)〔12). Galactinol은 이노 시톨의 D-3 위치에 galactose가 결합된 화합물인데, 모든 수산기를 벤 질로 보호한 후 가수 분해하여 D-1(1,2,4,5,6)Bns를 얻어 DPPC로 인 산화한 후 두 단계에 걸쳐 가수소 분해하여, L-l(l)P를 얻었다. 그 이후 anhydroconduritol을 이용하여, l(l)P와 l(4)P의 혼합물을 얻는 방법 (Kurihara 동) [1회 과 ( 士) -I (3, 4, 5, 6)Bn4에 직 접 인산화하
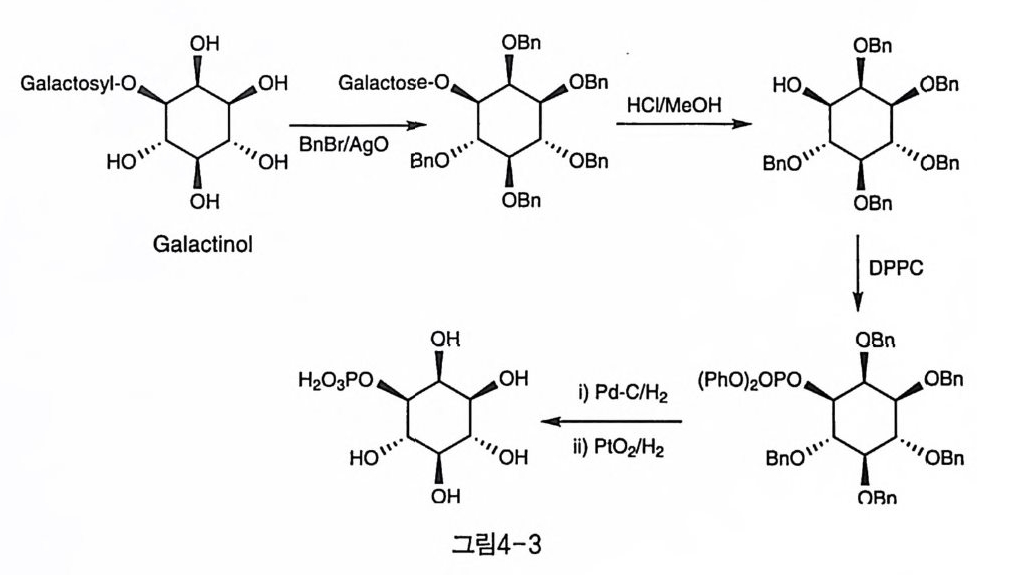 Ga ac tos Galactinol H2°3POH〔一Ho0亨:OQH :二_一一(Ph0)20:nH字0 :!ODBP:nP C:
Ga ac tos Galactinol H2°3POH〔一Ho0亨:OQH :二_一一(Ph0)20:nH字0 :!ODBP:nP C:
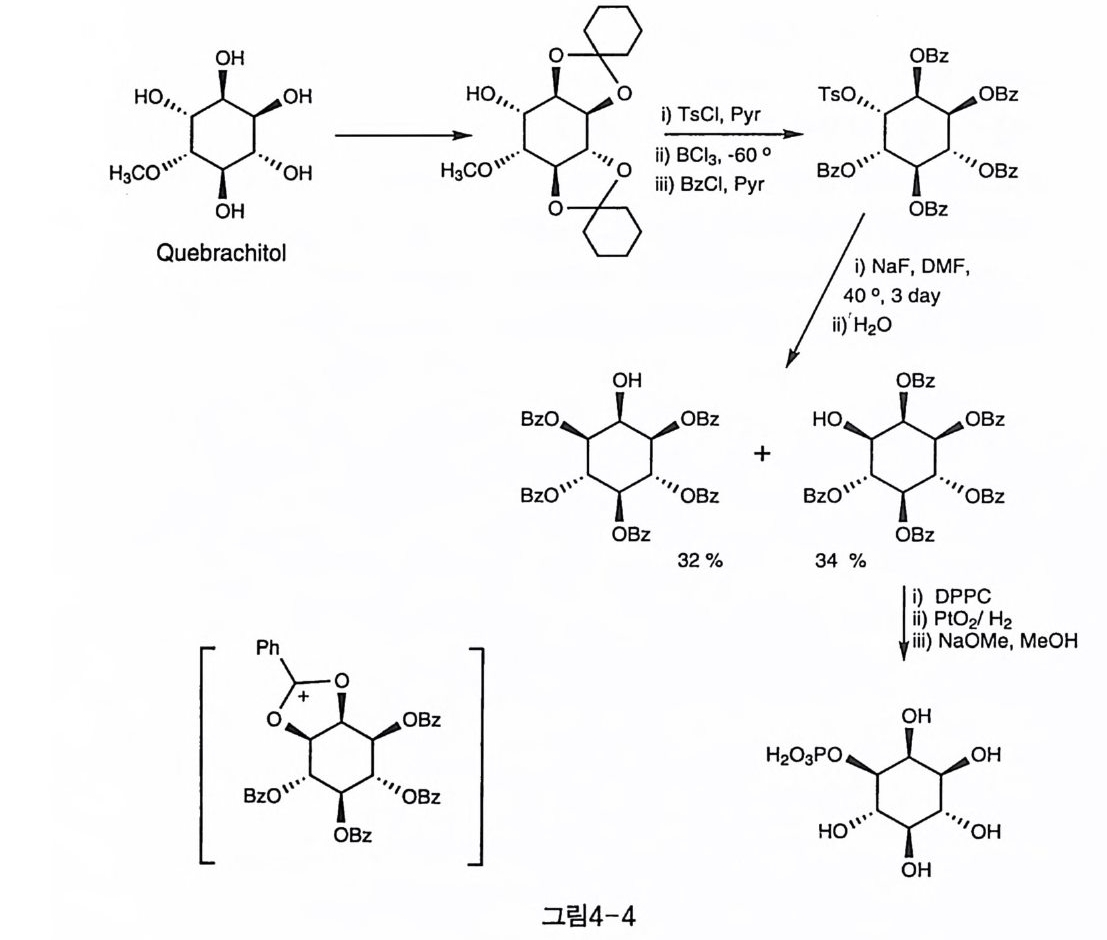
여, I (l )P 와 1(2)P 를 7: 꾸기 비로 얻은 결과(Ki el y 등)〔 14 〕가 보고된 바 있으나 수율이 낮고 개선해야 할 문제점들을 가지고 있었다. 천연물인 q uebrach it ol 을 출발 물질로 이용한 L - l (l )P 의 합성도 비슷 한 무렵 에 보고되 었다(그림 4-4, Gero 등) 〔1 회 . Q uebrach it ol 은 (-) - 2-m eth o xy -ch ir o -i nos it ol 이 며 , 고무나무에 서 추출되 는 천 연물이 다. Q uebrac hit ol 을 c y clohex yli dene 으로 보호한 뒤 Ts 기 를 도입 하고, BCl3 로 처리하면 아세탈과 메틸기가 모두 제거된다 . 생겨난 수산기들을 모
 H3C仁O``` 一H O::.: cX\: 특::::: : ~: ~OB,
H3C仁O``` 一H O::.: cX\: 특::::: : ~: ~OB,
두 벤조일기로 보호한 후, 약한 친핵체인 NaF 를 넣고 가열하면, 벤조 일의 이중 결합 산소가 Ts 기를 밀어내고 고리형 탄소 양이온 중간체를 생성시킨다. 물로 반응을 마무리하면 고리가 열리는데, 이때 열리는 방향에는 별다른 선택성을 보이지 않았다. 얻어진 중간체를 인산화하 고 보호기를 제거하여 L-I (l )P 를 합성하였다. 이노시톨 라세미 혼합물의 첫 광학 분할 시도로는 고전적인 산-염 기 염을 통한 방법이 시도되었다(그림 4-5, Molotk o vsky 등)〔 16). 라세 미 상태의 I(2,3,4,5,6)Acs 의 수산기에 옥살릴기를 도입하여 물로 반응 을 마무리하면 카르복실산이 생성된다. 여기에 여러 가지 천연 염기를
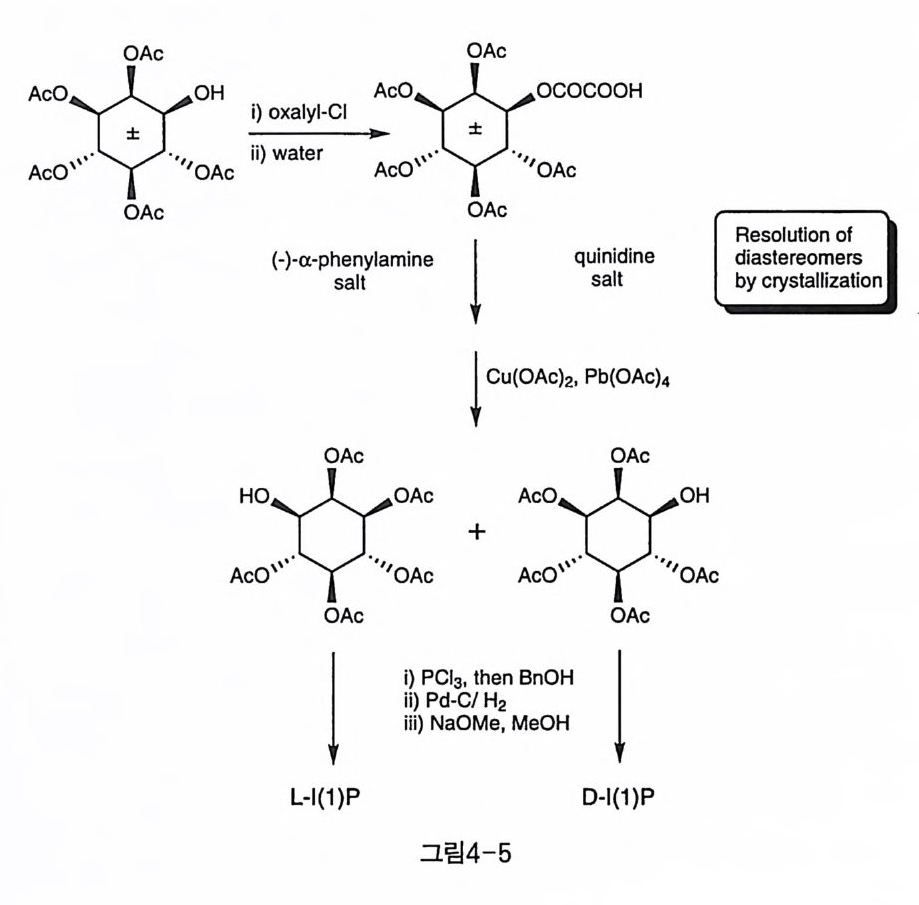 二亨 三亨 ::C0COOH
二亨 三亨 ::C0COOH
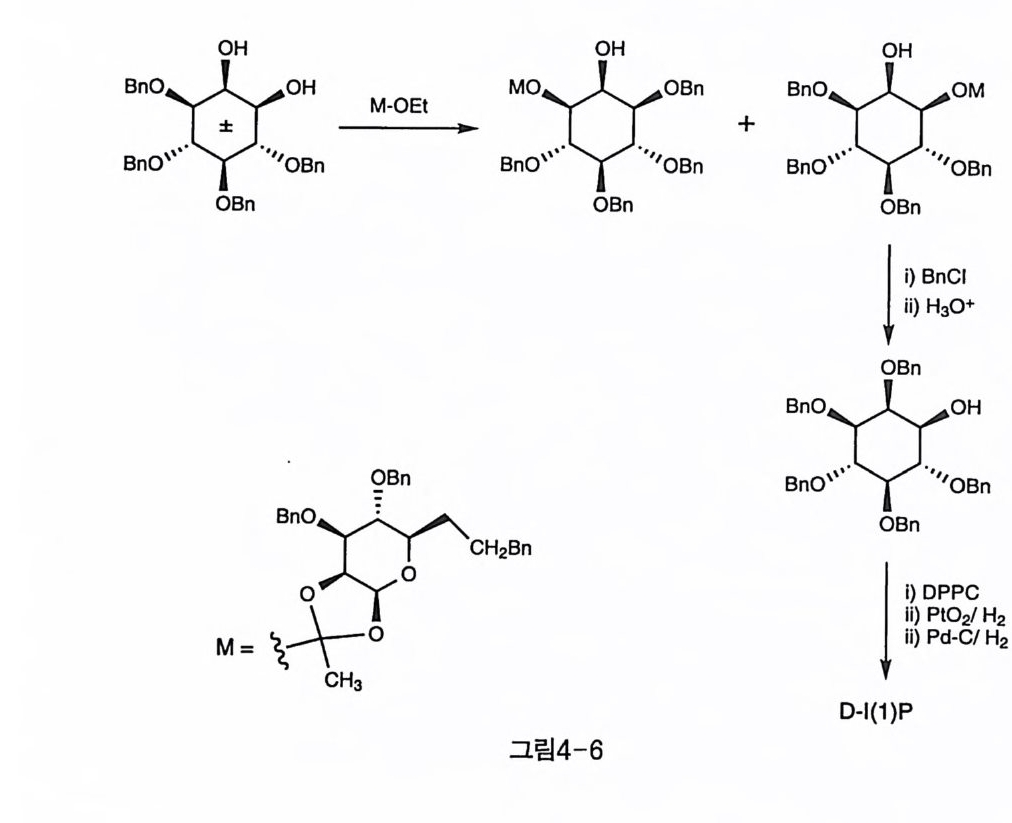
이용하여 선택적 결정화를 위한 최적 조건을 찾았다. 높은 수율을 얻 기 위해서는 각 거울상 이성질체에 대해 다른 염기를 사용해야만 했는 데, qu ini d i ne 을 사용했을 때 D-1-oxal y l-I(2,3,4,5,6)Acs 가 결정으로 얻어졌고, (-)-a- p hen y l arni ne 을 사용하면 L-1-oxalyl - I( 2, 3, 4, 5, 6)Acs 가 결정으로 얻어졌다. 사에틸납으로 옥살릴기를 제거하면 각각 순수한 광학 활성의 IAcs 가 얻어지고, 벤질인산기를 통해 D_, L- I(l) P 가 합성되었다. 다른 재미있는 예로서 mannose 의 오르소에스테르를 만들어 이노시 톨 유도체의 광학 분할을 시도한 연구가 러시아 과학자들에 의해 보고 된 바 있다(그림 4-6, Shvets 등) [17 ).라 세미 혼합물 상태의 (土) _I( 3, 4,5,6)Bn• 에 벤질화된 mannose 를 오르소에스테르 형태로 결합시켜 부
 :::三 字M + :::*::,
:::三 字M + :::*::,
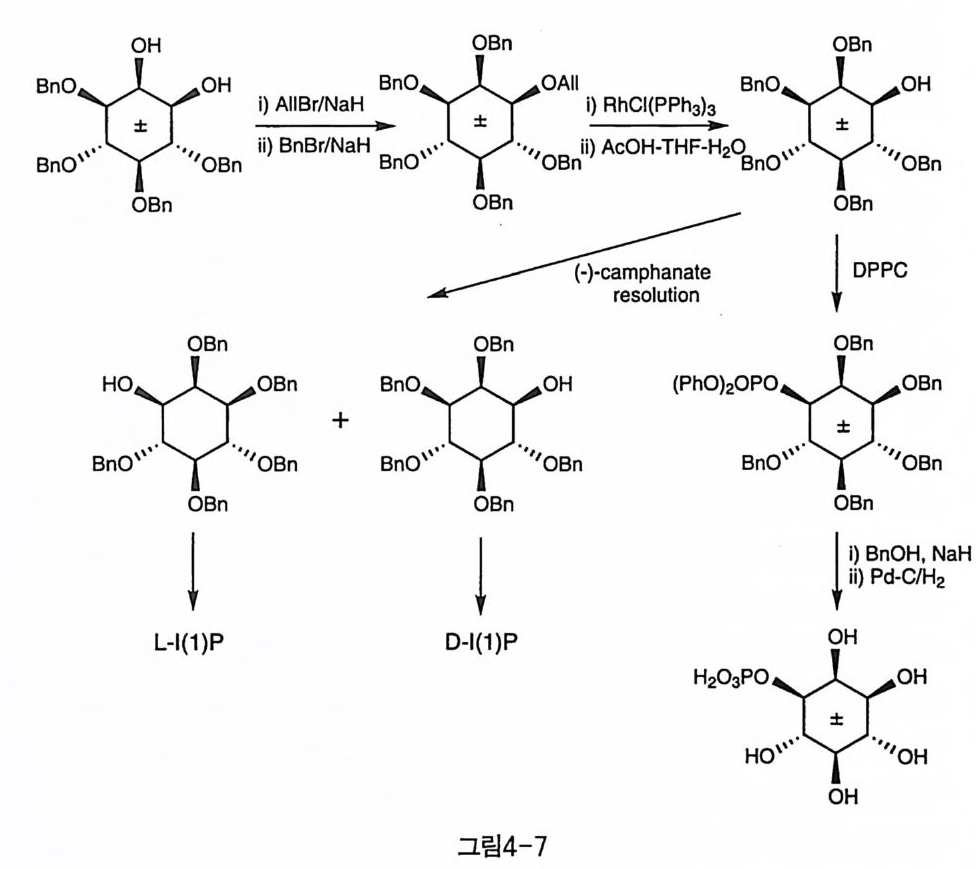
분 입체 이성질체를 크로마토그래피로 분리하였다 . 오르소에스테르는 염기에 안정하므로 염기 조건에서 남은 2 번 수산기를 벤질화시킨 후 산 조건에서 가수 분해하여 D-(2 , 3,4,5,6)Bns 를 얻을 수 있었다. 보고 된 방법으로 인산화하고 , 보호기를 제거하여 D-l (l )P 를 합성하였다. 보다 선택적인 방법으로, (士 )-1(3,4,5,6)Bn4 의 1 번 수산기를 알릴 기로 보호한 후 나머지 수산기를 벤질화하고 다시 알릴기를 제거하여 (土 )-1(2,3,4,5,6)Bns 가 합성되었다(그림 4-7). 이전에 보고된 바와 같 이 DPPC 로 인산화한 후 두 단계에 걸친 가수소 분해를 시도한 결과, I(l) P 뿐만 아니라 1(2)P 가 2.5% 정도 불순물로 생겨남이 확인되었다.
 :::OH亨 ::n 二::亨OBn :::I: 巴2 0:: 亨OBn °0:n
:::OH亨 ::n 二::亨OBn :::I: 巴2 0:: 亨OBn °0:n
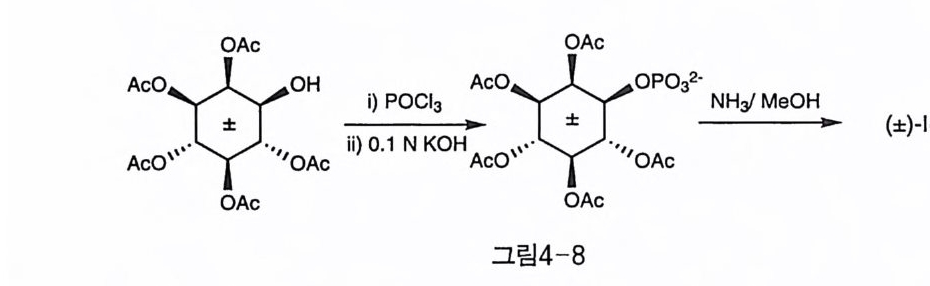
이것은 이웃한 수산기가 존재하는 경우, 인산에스테르가 고리형 중간 체를 형성하여 일어난 것으로 해석할 수 있다 . 이 부반응은 페닐에스 테르를 벤질에스테르로 tr anses t e rifi ca ti on 한 후 Pd_C 촉매 하에서 한 단계만으로 가수소 분해함으로써 억제할 수 있었다. 이 경우에는 인산 기의 벤질에스테르가 수산기의 벤질에테르보다 훨씬 빨리 분해되기 때 문이 다 . ( 士 ) -I (2, 3, 4, 5, 6)Bns 는 (-) - camp ha nate 유도체 를 통해 광학 분할하여 각각 D-, L-l (l )P 도 합성되었다(1 8 〕. 일인산이노시톨의 인산기가 티오인산으로 치환된 유도체는 IP1 의 가 수 분해 저항성의 IP1 유사체로 활용될 수 있다 . 이러한 점에 착안하 여, 티오인산이노시톨울 합성하는 방법으로도 적용될 수 있는 새로운 반응이 개발되었다(그림 4-8, Jas to r f f 등)(1이. (士)-1( 2,3,4,5,6)Acs 에 POCb 를 가한 후 남은 염소기를 가수 분해하여 인산기를 도입하였다 . 이 경우 POCh 대신 PSCb 로 반응하면 티오인산기를 도입할 수도 있었 댜 남은 아세틸기를 약염기 조건에서 가수 분해하면 (土 )-l (l )P 가 성 공적으로 생성되었다.
 ::O:Ac \::三。0 O:Ac 三
::O:Ac \::三。0 O:Ac 三
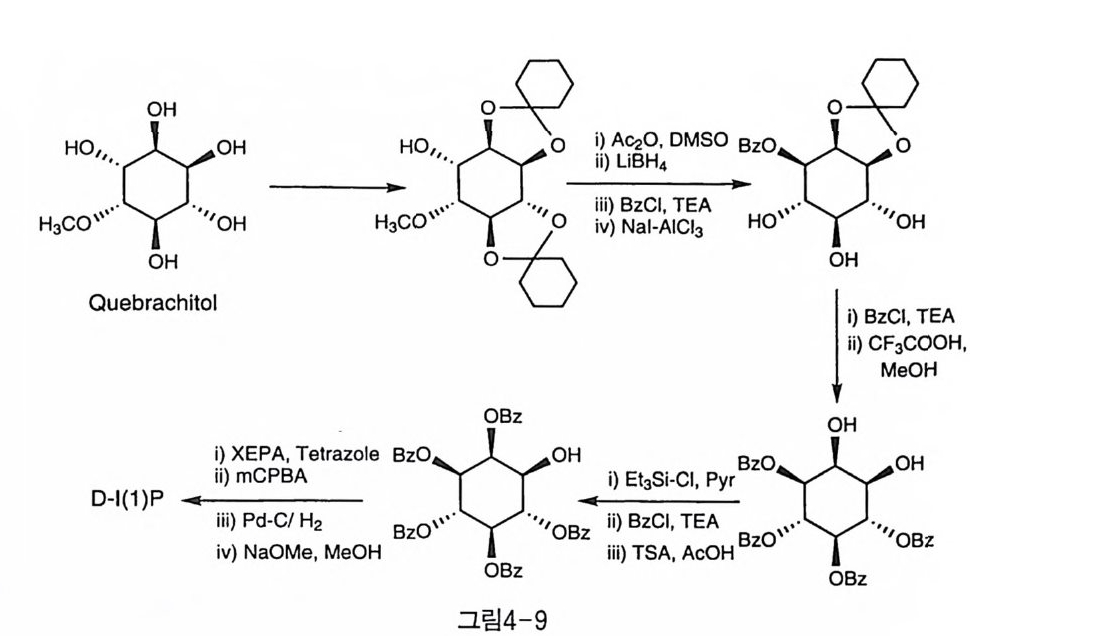
앞서 q uebrac hit ol 을 이용하여 L-l (l )P 을 합성한 예를 보였는데, 약 20 년 후 Oza ki 등은 같은 출발 물질로부터 D-l (l )P 의 합성을 선보였 다(그림 4-9)(20 〕 ' 처음 cyc l ohexy lide ne 아세탈을 형성하는 단계까지는 동일하고, 남은 수산기를 산화시켜 카르보닐기로 만들었다가 환원시키 면 90% 이상이 미오이노시톨 형태로 얻어졌다. 고전적인 탈메틸 방법
 H3 H00Q u,.ec sbra HOH oc亨hitol 00il iHxilimHEl Hivl 二一BHOO, B` :>OzBzz 0益TE凡OAo0HHB
H3 H00Q u,.ec sbra HOH oc亨hitol 00il iHxilimHEl Hivl 二一BHOO, B` :>OzBzz 0益TE凡OAo0HHB
인 HI나 BCh을 사용하면, 벤조일기와 아세탈도 함께 영향을 받는다는 것이 관찰되었고, Nal-AlCL 조건에서 벤조일과 시스 아세탈은 영향 을 받지 않은 데 비하여, 메틸과 트란스 아세탈만이 효율적으로 제거 되었다. 남은 수산기를 벤조일로 보호하고, 시스 아세탈을 제거하여 D-I(3,4,5,6)BZ4를 얻었다. 수평 방향의 1번 수산기를 실릴로 먼저 보 호한 후, 남은 2번 수직 방향 수산기에 벤조일을 도입하였다. 다시 실 릴을 제거한 후, 새로운 인산화 시약인 XEPA를 1H-tetrazole과 함께 반응하면 아인산기가 도입되고, 계속된 산화 반응으로 인산기를 도입 할 수 있었다. 이 렇게 도입 된 o -xylene -a, a'-diyldioxy phosphoryl (XP)기는 벤질인산과 같이 촉매 하에서 가수소 분해로 제거될 수 있 었고, 염기로 남은 벤조일기를 가수 분해하여 D-l(l)P를 합성하였다. 벤젠을 출발 물질로 한 IP의 합성도 연구되 었다. 벤젠을 Pseudo-monas putida라는 미생물로 산화시키면, cis-3, 5-cyclohexadiene-1, 2-diol이 생성된다. 이 디올은 cyclitol 합성의 중요한 중간체로 활용될
수 있는 유용한 물질이다 . 여기에 몇 단계의 에폭시화 및 위치 선택적 고리 열림 반응을 거쳐 다양한 IPn 을 합성할 수 있었는데, 그 한 예로 서 (土)-I(l) P 의 합성을 기술하였다(그림 4-10, Ley 등 )(21) .
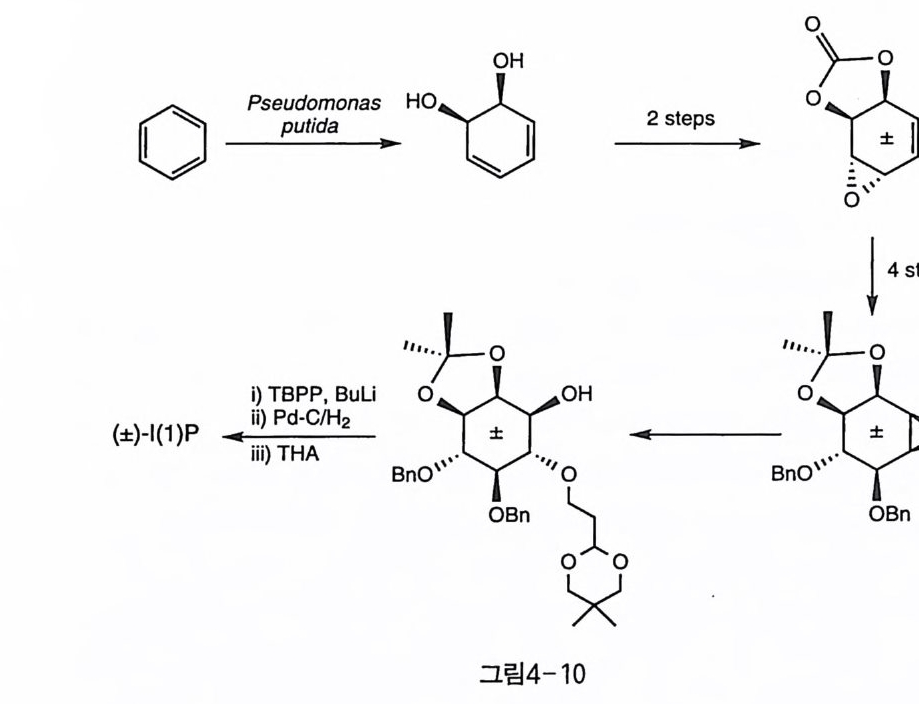 。P sepuud oti dma o nas H 。 占HO 二亡。》 0
。P sepuud oti dma o nas H 。 占HO 二亡。》 0
Shen 둥은 (1, 2;4, 5)cyc l ohexy lide ne i nos it ol 의 1 번 수산기를 선택적 으로 벤질화한 후 남은 4 번 수산기 에 ( 기 -cam phana t e 를 붙여서 광학 분할을 하였다. 얻어진 각 이성질체는 탈벤질화한 후 인산기를 도입하 여, D-및 L-l (l )P 를 합성하였다(그림 4-11) 〔 22). 새로운 광학 분할제로서 cam p hor 를 이노시톨에 적용한 결과도 보고 되었다(그림 4-1 2, Bruz ik 둥 )(23, 24). 이노시톨울 직접 D-cam p hor 의 메틸 아세탈로 처리한 후, 생성되는 4 가지 가능한 이성질체를 평형 상 태에서 결정화하면 한 가지 이성질체만이 비교적 높은 수율 (65% )로 얻
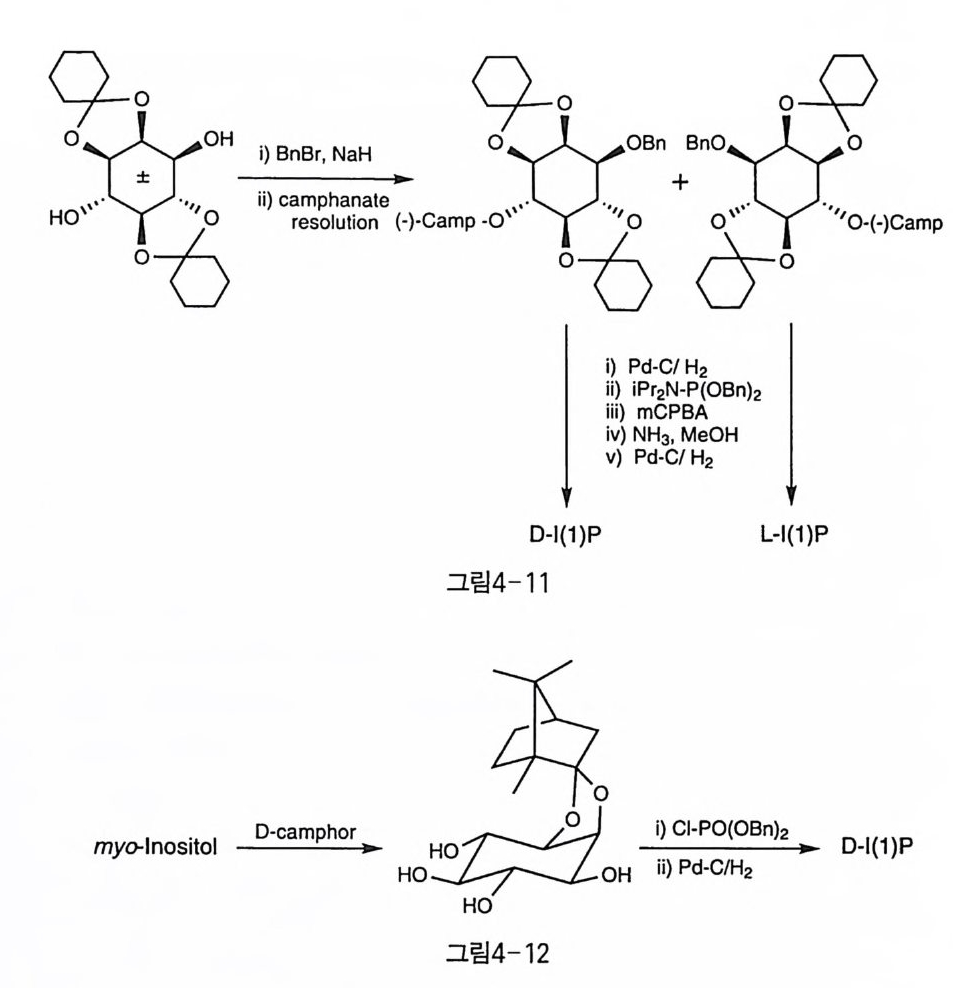 i) BnBr, N aH ~ ~ ^ 소 ~un
i) BnBr, N aH ~ ~ ^ 소 ~un
어졌다. 이 중간체는 다양한 1P 의 합성에 이용되었는데, 여기에 직접 인산화하면 D-I (l )P 가 주요 생성물로 얻어졌다. 한편, L-cam p hor 를 사용하여 같은 과정을 반복하여 L- I(l) P 도 합성하였다〔 24]. 4-2-2 1(2)P 광학적 활성을 가지지 않은 IP 려 1912 년 밀겨의 산 가수 분해물에서
발견되어 그 구조가 제안되었으며〔25〕, 제안된 구조의 확인과 함께 최초 의 합성 이 보고되 었다(그림4-13, Iselin 등) [26]. Acetobacter suboxydans 가 이노시톨의 2번 수산기만을 선택적으로 산화시킨다는 것을 이용하 여 myo -inositol을 scyllo -inosose로 만들었다. 수산기 들을 아세 틸로 보호하고, 촉매 하에서 환원시 켜 다시 myo -inositol로 만들었는데 이 때 용매를 아세트산을 쓸 경우에는 25% 정도의 scyllo-inositol이 함께 생성되었지만, 메탄올을 사용한 경우는 myo-inositol만 얻어졌다. 수 직 방향의 2번 수산기는 DPPC와 반응시킬 때 낮은 온도에서는 쉽게 인산화되지 않아, 80°C까지 가열하고 과량의 DPPC를 사용했을 때에 만 64% 수율로 생성물을 얻을 수 있었다. 가수소 분해 반응과 탈아세 틸 반응을 거쳐 l(2)P가 합성되었다. 최근에는 inositol orthoformate를 이용한 보다 현대적인 합성 방법이 보고되 었다(그림4-14, Billington 등) [27). Inositol orthoformate에 강염 기 조건에서 벤질화 반응을 시도하면 4,6-과 2,4-디벤질이노시톨이
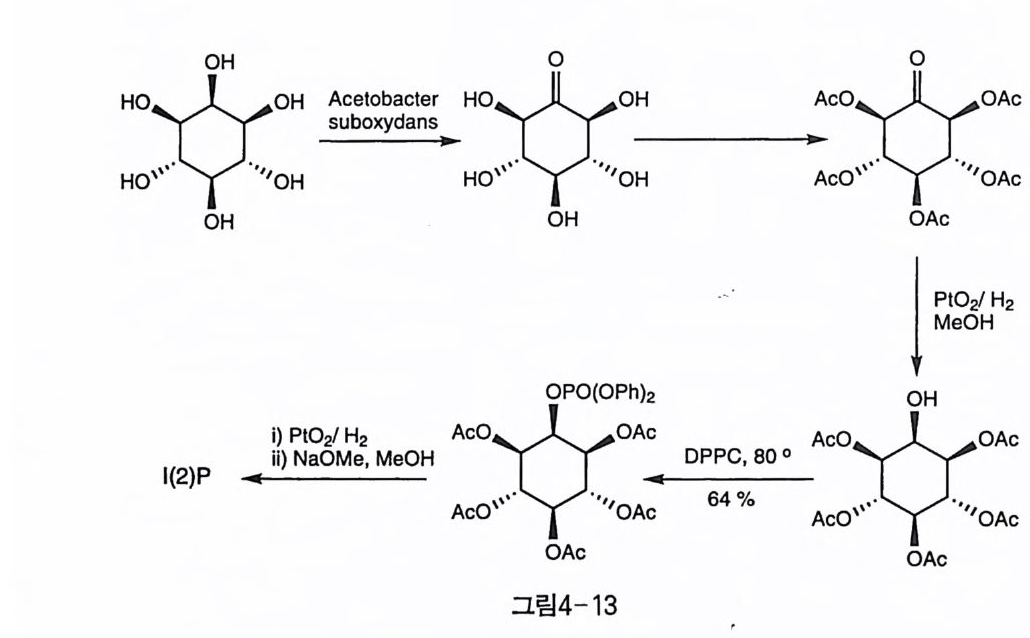 字:ACSU =H :::::::
字:ACSU =H :::::::
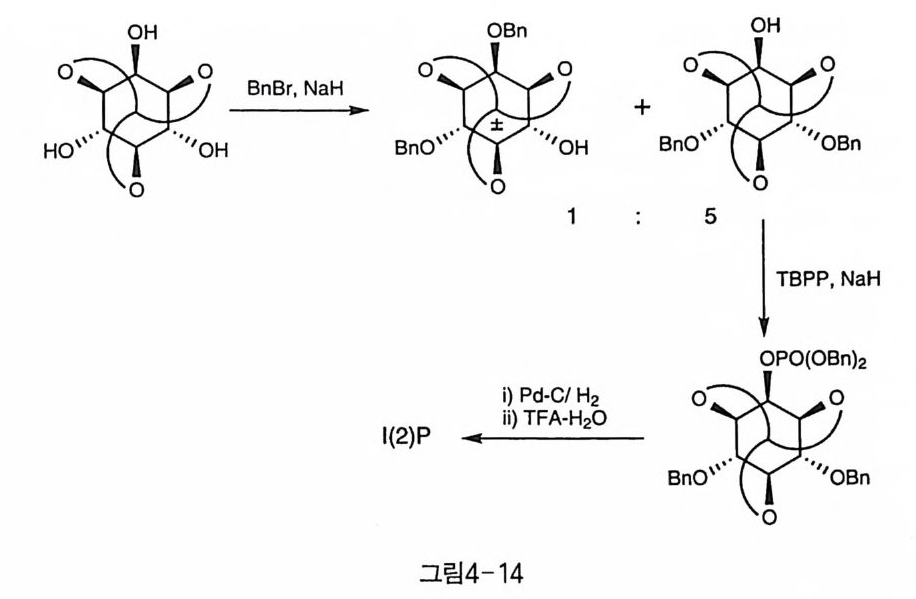 亨三° 0 亨亨 Bn
亨三° 0 亨亨 Bn
5 : 1 의 비로 얻어진다 . 주 생성물인 4,6- 디벤질이노시톨의 남은 2 번 수 산기를 TBPP 로 인산화한 후 보호기를 제거하여, 쉽게 I(2)P 를 얻을 수 있었다. 4-2-3 1(4)P 1961 년에 뇌의 인지질 성분을 염기 조건에서 가수 분해했을 때 이전 에 알려졌던 I (l )P 와는 다른 두번째 광학 활성을 가진 lP 떠 소량이긴 하지만 존재함이 알려졌고, 당연히 이것은 I( 4)P 의 한 광학 이질체일 것으로 생각되었다〔 28). 이와 비슷한 시기에 Ang ya l 등은 I(1,2;5, 6)Hex2 을 부분적으로 보호하여 라세미 형태의 I( 4)P 의 합성을 보고하 였다(그림 4-15) [29 ] . 1979 년에는 러시아 과학자들이 그림 4-6 에서 D-mannose 의 오르소 에스테르를 이용하여 만들었던 D-I (l ,4,5,6)Bn4 를 이용하여, 몇 단계
의 보호와 탈보호를 거쳐 D-1(4)P 를 합성하였다(그림 4-16, Shvets 등) [10 ]. 그림 4-11 에서 D-, L-l (l )P 의 합성에 사용되었던 중간체들은 각각 D-, L- l( 4)P 에의 합성에도 활용되었다(그림 4-17, Bil ling ton 등)(1 8,
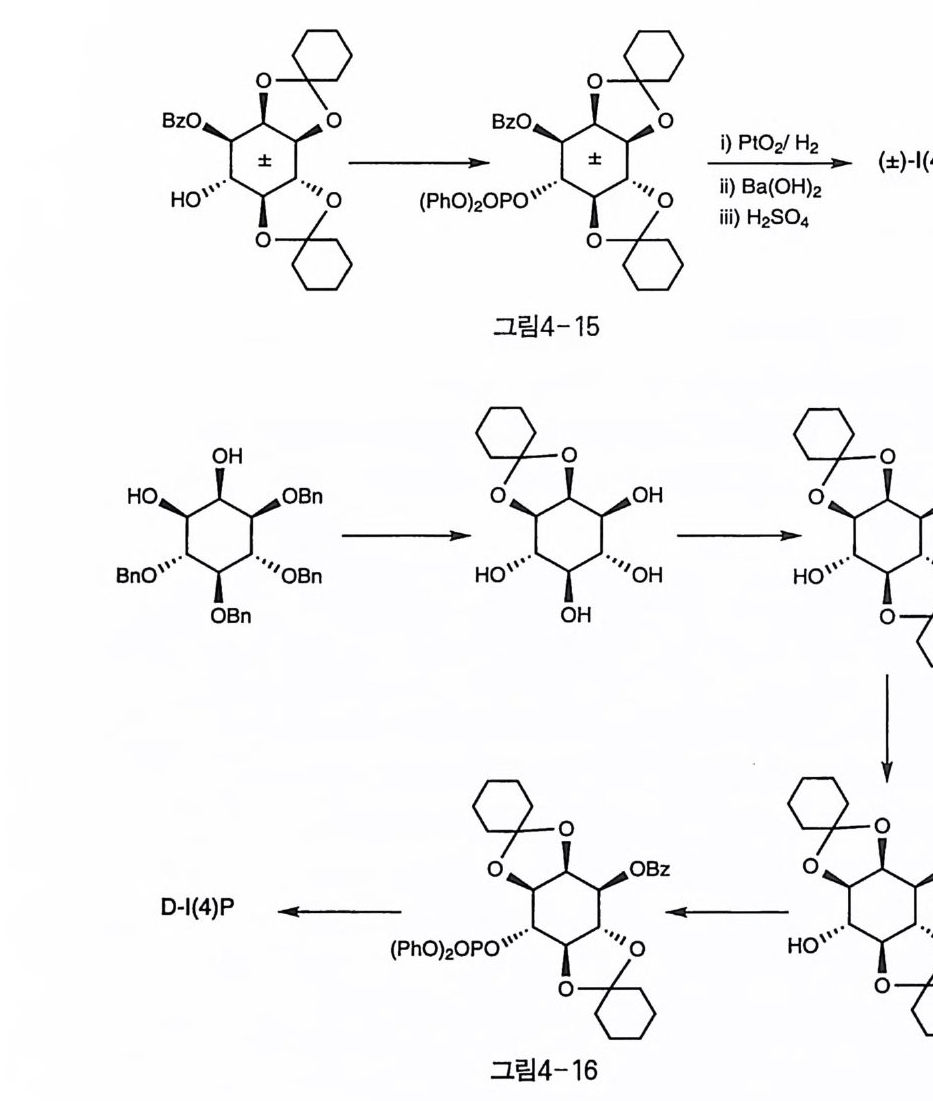 i) PI02/ H2 .. (士 )-1(4)P
i) PI02/ H2 .. (士 )-1(4)P
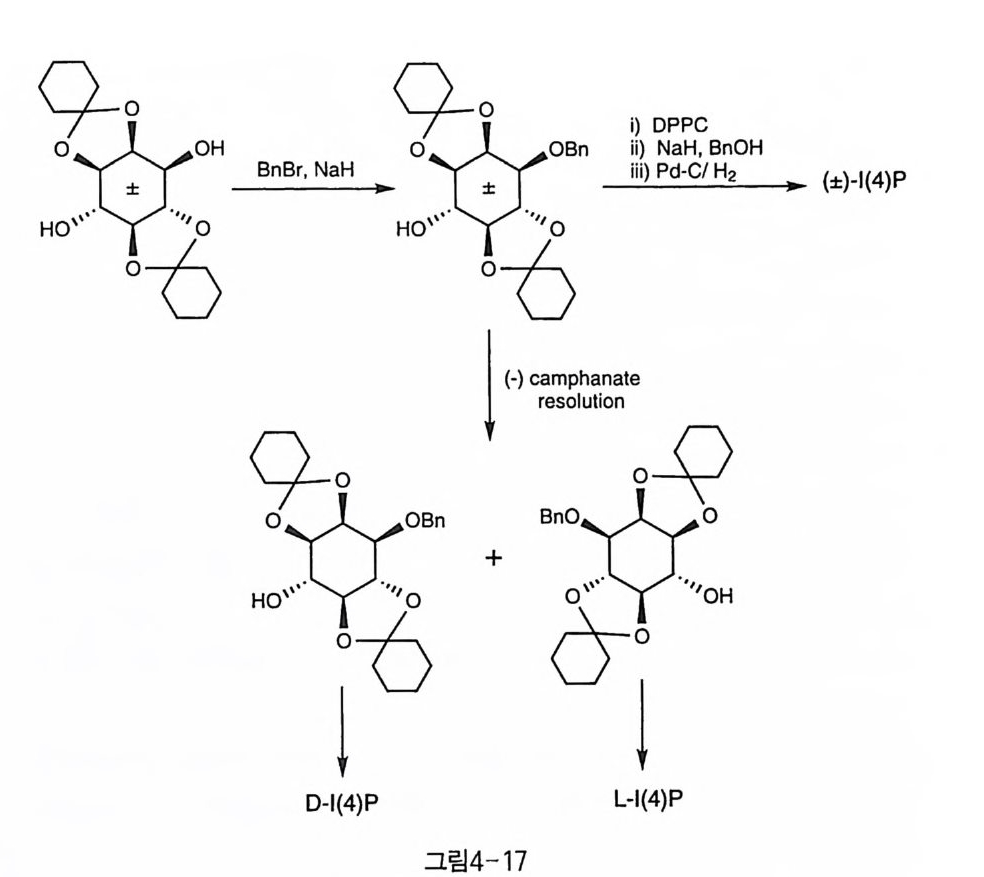 H(o IIiI`’li나 DPIN 凡PCaPCl d He 2 (土 )-1(4)P
H(o IIiI`’li나 DPIN 凡PCaPCl d He 2 (土 )-1(4)P
3 이 . 그림 4-11 에서와는 달리 벤질 대신 키랄 보조기인 cam p hana t e 를 먼저 가수 분해하고, 남은 4 번 수산기에 페닐인산기를 도입했다가, 페 닐에스테르를 벤질에스테르로 tr anses t e rifi ca ti on 한 후 Pd-C 촉매 하에 서 보호기를 제거하였다 . 이노시톨의 o rth o fo rma t e 를 1 당량의 강염기와 TBPP 로 처리하면, 라 세미 상태로 4 번 수산기에 인산화된 생성물이 주로 얻어진다(그림 4- 18, Bil ling ton 등)〔 27, 31 ). 이것은 벤질화 반응에서와 같은 경향으로, 사용된 1 당량의 염기에 의해 생성된 4 번 수산기의 음이온이 6 번 수산 기와 수소 결합을 이루어 안정화되는 것으로 설명할 수 있다. 인산기
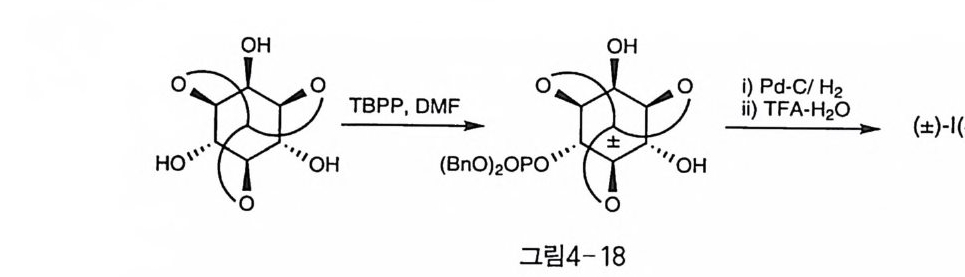 亨三0) 20PO0亨 0H 루 (土 )·1(4)P
亨三0) 20PO0亨 0H 루 (土 )·1(4)P
의 벤질에스테르는 가수소 분해하여 제거하고 오르소에스테르는 TFA 로 제거하여 (士) -I(4)P 를 얻었다. 그림 4-129l D-camp ho r 유도체를 TBDMS-Cl 로 처리하면 1, 4 번 수산기만을 보호할 수 있고, 남은 5, 6 번 수산기를 아세탈화한 후 TBDMS 를 불소 시약으로 제거하면 1, 4 번 수산기가 열린 중간체를 얻 을 수 있다. 여기에 강염기 하에 벤질기를 도입하면 1 번 수산기가 선 택적으로 벤질화되고, 남은 4 번을 인산화하여 D- I( 4)P 를 얻을 수 있 었다(그림 4-19, Bruzik 동) (24) . 일반적으로 아세탈기는 이노시톨의 경우 시스형이 트란스보다 더 안 정한데, 트란스에 선택적인 새로운 방법이 동장하였다. 1, 2-cyc l o-
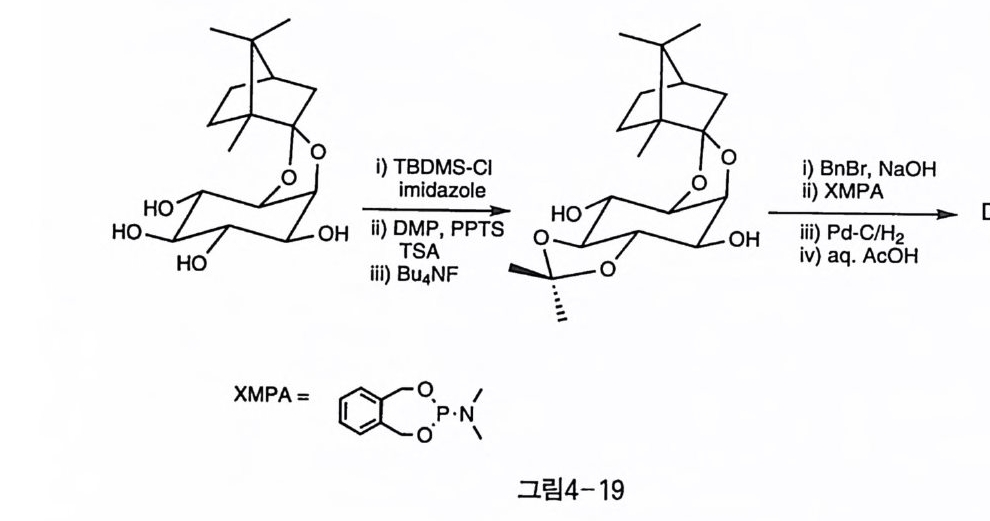 i) BnBr, NaOH
i) BnBr, NaOH
hexylidene inositol에 TIPS -Ch(I, 3-dichloro-I, I, 3, 3 -tetraisopropyldis-iloxane)로 반응하면 3,4-TIPS가 만들어진다. 이 중간체를 BzCI로 처 리하면 6번 수산기가 벤조일화되는데, 여기에 강염기와 TBPP로 처리 하면 벤조일기가 이동하면서 원래 벤조일이 붙어 있던 자리에 인산기 가 도입된 생성물이 47% 수율로 얻어진다. 이 화합물의 여러 보호기 를 차례로 제거하면, (士)-l(4)P가 얻어졌다(그림4-20, Ozaki 등)〔32〕•
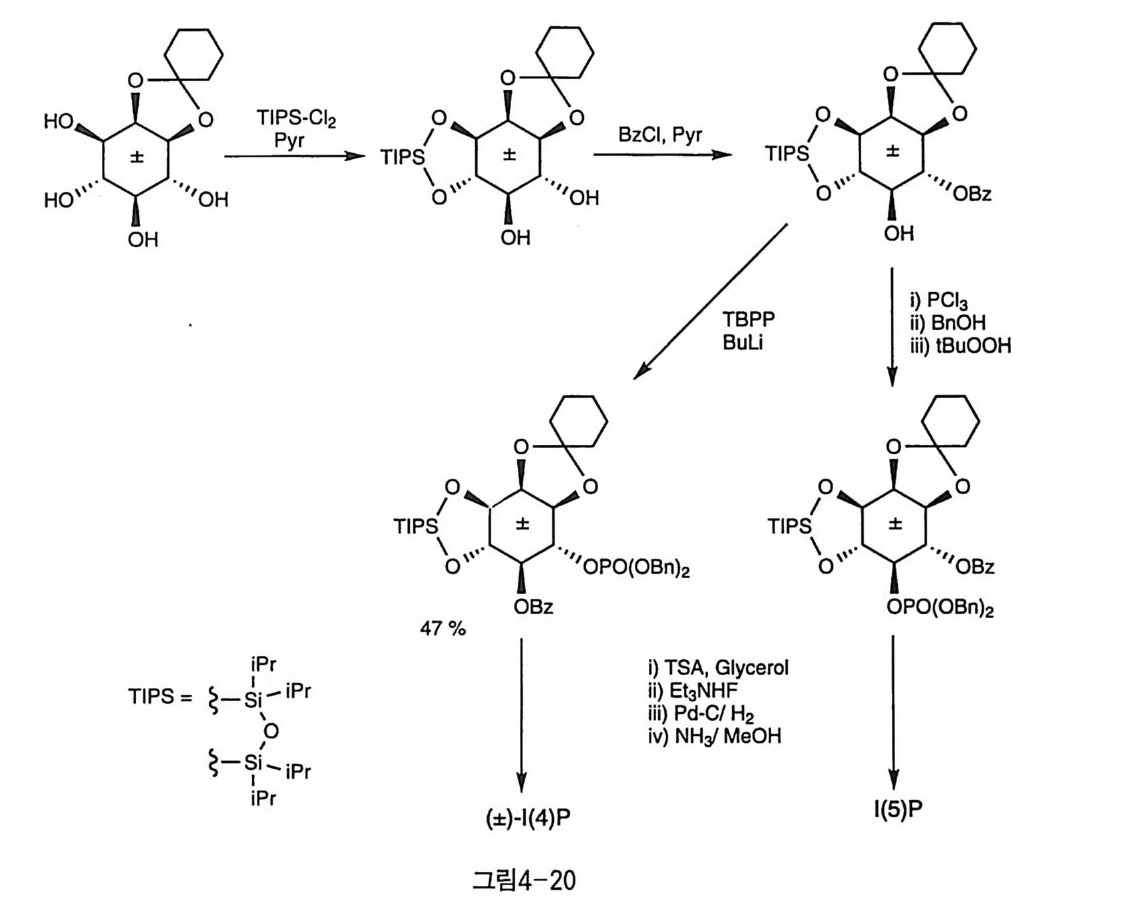 H0 H iPr 二47% H/〔i) 一iTSA, GlyBciuTUe rolI Ps 0///\O 」:IlOHIi-—_
H0 H iPr 二47% H/〔i) 一iTSA, GlyBciuTUe rolI Ps 0///\O 」:IlOHIi-—_
4-2-4 1(5)P 그림 4-20 에서 TBPP 대신 부드러운 조건 하에서 PCh 로 인산기를 도입한 후 보호기를 제거하면 1(5)P 가 얻어진다. 이 이전에는 이노시 톨울 출발 물질로 한 합성은 보고된 바가 없었으며, 유일한 예로는 2- ami no-2-deox y -neo- i nos it ol 을 아세틸화한 후 아질산으로 처리하여 SN2 반응으로 아민기를 수산기로 바꾸는 간접적인 방법이 있었다(그림 4-21, Ang ya l 등 )(29) . 이렇게 얻어진 1(1 , 2, 3, 4, 6)Acs 를 인산화하여 1(5)P 를 얻었다.
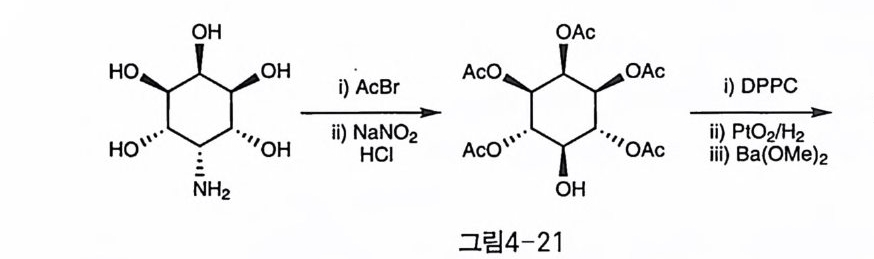 ::NH2틀 ::훌 :::O:H :: i)D PPC » l(5)P
::NH2틀 ::훌 :::O:H :: i)D PPC » l(5)P
4-2-5 lcP 1(1, 2)cP 역시 다른 IP1 들과 함께 자연에서 인지질의 가수 분해 과정 에서 생성되어 존재할 것으로 제안되었다〔 33 〕 • D-1(3, 4, 5, 6)Bn4 률 p hos p hod i chlo ri da t e 로 인산화하면 5 각 고리 형 인산기 가 도입 된다(그림 4-22 , Oza ki 동)〔 34). 생성된 화합물의 벤질 보호기들을 가수소 분해 하여 D-l (1 ,2)cP 가 얻어졌다. 이런 고리형 인산기는 아세탈과 마찬가지로 시스형이 더 안정한 데, 상대적으로 불안정한 트란스 인산도 합성이 시도되었다. 라세미 상태의 1 (1,2, 3,4)Bn ◄ 를 시스 디올에 사용된 p hos p ho di chlo ri dat e 로 인산 화하고 보호기를 제거하여 (土) -1(4, 5)cP 을 얻었다(그림 4-23, van
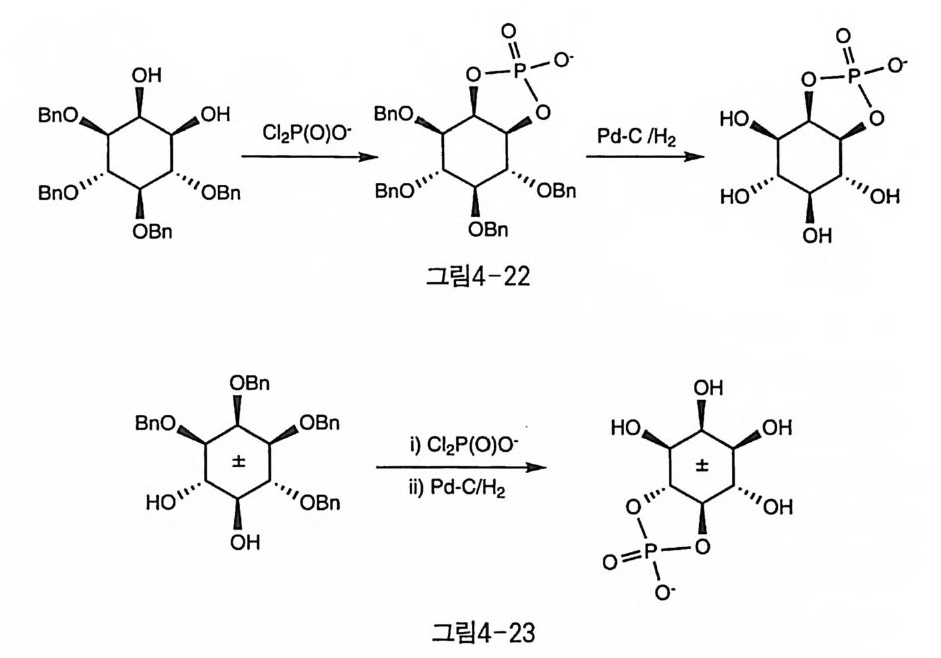 :::仁三 °0〈 〈0 OO Bon 二 ::<
:::仁三 °0〈 〈0 OO Bon 二 ::<
Boeckel 등 )(35) . 합성된 화합물은 31P-NMR 에서 고리형 인산기의 특 징에 해당하는 017 .4pp m 의 신호를 나타내었다. 4_3 이인산이노시톨 I(l,4,5)P3 의 중요성에 비해 이인산이노시톨들은 그 대사 물질 정도 로 인식되어 그다지 큰 주목을 받지 못하였다. 그러나 최근 들어서는 이안산이노시톨의 생물학적 활성에 대한 연구도 여러 시스템에서 보고 되고 있다. 라세미 형태의 1,4-, 1,6-, 4,5- 이인산이노시톨은 디시클 로헥실리딘 중간체에 DPPC 로 인산화하여 얻는 방법이 이미 오래 전에 보고되 어 있었다(그림 4- 깍 Ang yal 둥) [29 ] • 앞서 mannose 오르소에스테르를 활용한 광학 분할을 통해 IP1 을 합
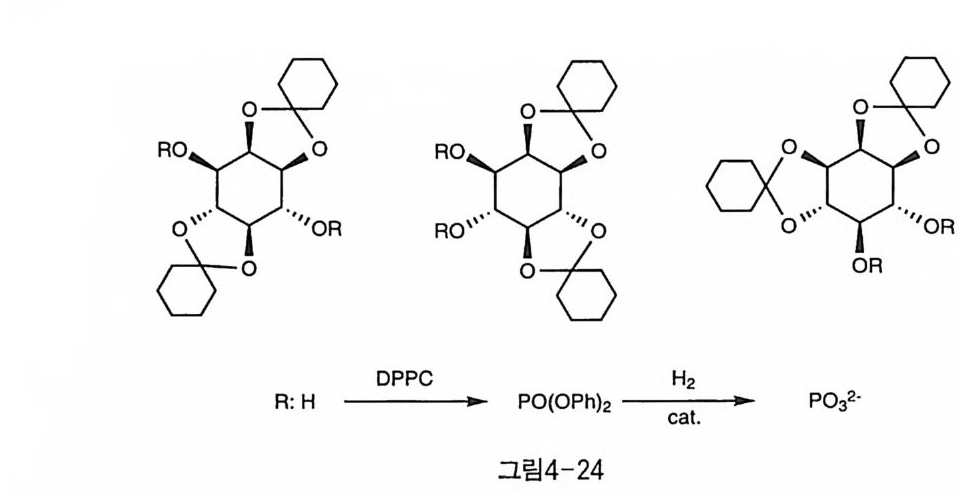 DPPC H2
DPPC H2
성한 것과 비슷한 전략으로 Shvets 등은 위 이인산이노시톨들의 광학 이성질체의 합성도 보고하였다〔 36 〕. 4-3-1 1(1,2)P2 최근에 생체 내 존재가 알려진 1 (1 ,2)Pz 는 여전히 그 광학적 입체 구 조가 규명되지 않았으나, Fe J+과 결합함으로써 항산화제의 활성을 가진 것으로 생각되는 I (l ,2,3)P3 의 유사체로 관심을 모았다. 비교적 잘 알 려진 방법들을 활용하여 라세미 형태로의 합성이 보고되었고, 항산화 제로서의 활성도 검사되었으나 항산화작용은 미약하며 오히려 라디칼 생성을 촉진한다는 것이 밝혀졌다(그림 4-25, Mi ch ell 등)〔 37). 벤질 대신 벤조일 보호기가 도입된 I(3,4,5,6)BZ4 를 중간체로 이용한 합성도 보고되었다(그림 4_26) 〔 38). 여기에서는 에틸 아인산기를 수산 기에 먼저 도입한 후 산화시키는 방법으로 인산화하였으며, 에틸 보호 기는 TMSBr 조건에서 제거할 수 있었다. 벤조일기를 제거하기 위한 염기 가수 분해 조건(l M LiO H, 80°C, 3h) 에서 인산기는 자리 이동이 나 가수 분해가 되지 않고 안정함이 확인되었다.
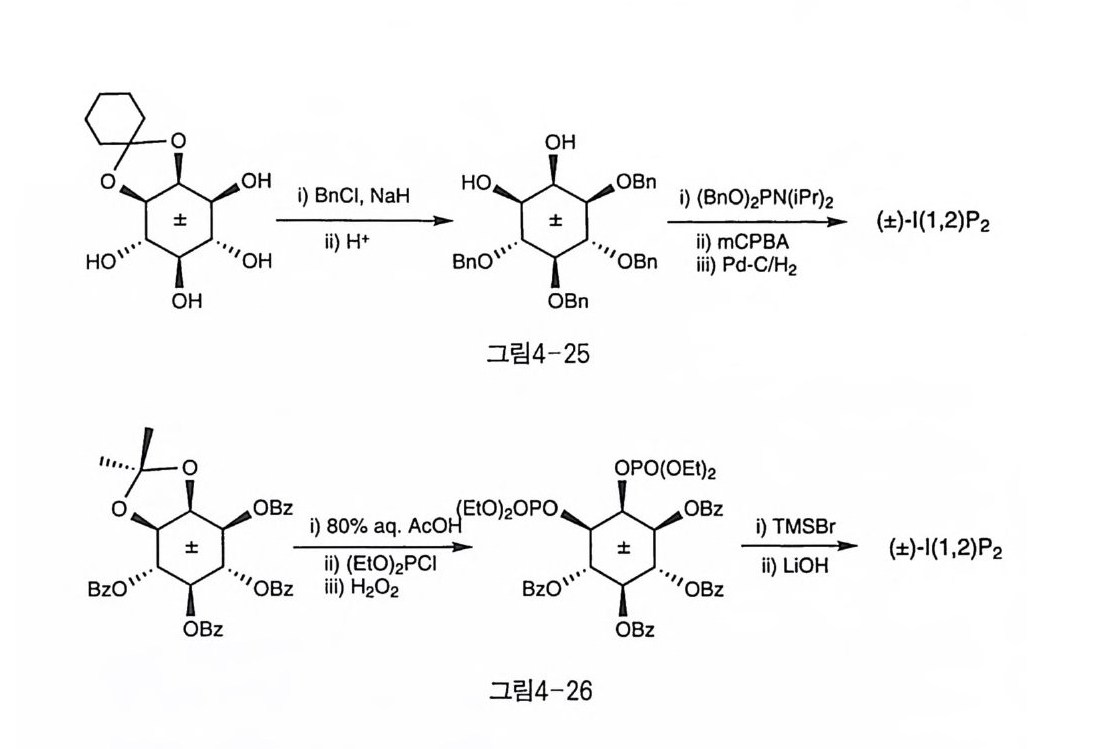 >o
>o
4-3-2 1(1,3)P2 I(l,4,5)P3로부터 생성된 I(l,3,4,5)P4는 I(l,3,4)P3를 거쳐 대사 물질 로 I(l, 3)P를 형성하는 것으로 추측된다. Billington 등은 이노시톨 orthoformate로부터 쉽 게 만들어 지 는 I (2, 4, 6)BnJ에 DPPC를 이 용한 선 택적인 인산화 반응을 통하여 I(l,3)P2와 I(l,5)P2를 82:18의 바율로 얻 울 수 있었다. 재결정을 통하여 38% 수율로 I(l, 3)P2를 얻었는데, 얻 어진 페닐인산기를 벤질인산기로 바꾸는 transesterification 반응은 화합 물의 분해만을 일으켜 성공하지 못했다. 그리하여, Li-암모니아 조건 에서 페닐 보호기를 제거하여 I(1, 3)P2의 합성이 완료되었다(그림4-27, Billington 등) [27,31 ) . I(4, 5, 6)BZJ 중간체를 3당량의 (EtO)꾼Cl로 처리한 후 산화시키면 1, 3번이 인산화된 화합물이 주요 생성물로 얻어진다. 이것은 수평 방
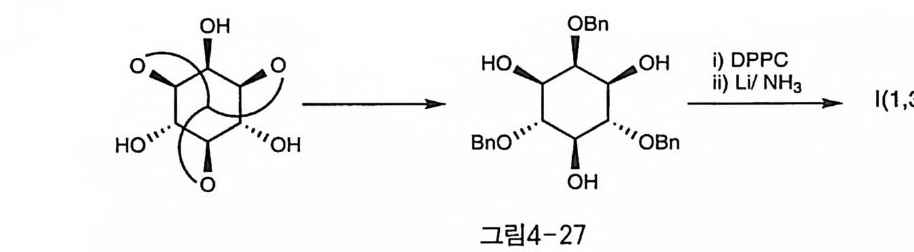 字一 B그:림 4:-2*7 ::n 二 1(1,3)P2
字一 B그:림 4:-2*7 ::n 二 1(1,3)P2
향의 수산기에 비해 수직 방향의 수산기가 입체 장애가 큰 환경에 둘 러싸여 있어 반응성이 낮아진 것으로 설명된다. 보호기는 TMSBr 과 L i OH 를 차례로 사용하여 제거하여 1 (1 ,3)P2 를 얻었다(그림 4-28) 〔 38 〕 .
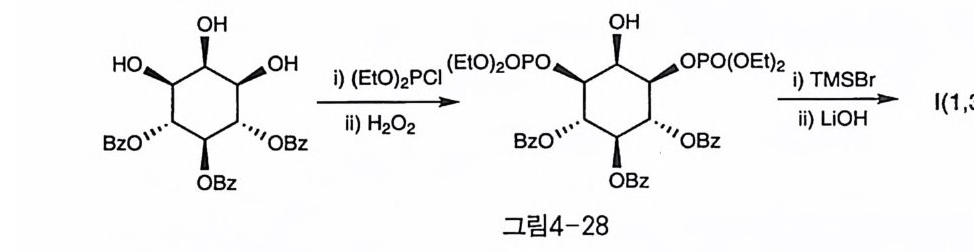 B:: 亨::三E t O)20B:::(OE t)눅 I(13)P2
B:: 亨::三E t O)20B:::(OE t)눅 I(13)P2
4-3-3 1(1,4)P2 1 (1 ,4,5)P J에 5- 포스파타제가 작용하여 생성되는 것으로 알려진 1(1 , 4)P2 는 일찍부터 합성의 대상이 되었다. Pott er 등은 아세탈로 보호된 1,4- 디올에 포스파이트기를 도입한 후 산화시켜 1( 1,4)P2 를 합성하였 다. 이 경우 일반적인 산화제 대신 황과 피리딘 조건에서 포스파이트 기를 산화하면 티오인산 유도체를 얻을 수 있었다(그림 4-29, Pott er 등)〔 39 〕 · Bi lling ton 등은 An gy al 이 사용한 cy cl ohexy lide ne 아세탈을 cam- p hana t e 로 광학 분할하여 각각의 광학 이성질체를 합성하였다〔 30). D-Camp ho r 아세탈을 이용한 D- (1 ,4)P2 의 합성도 보고되었다(그림
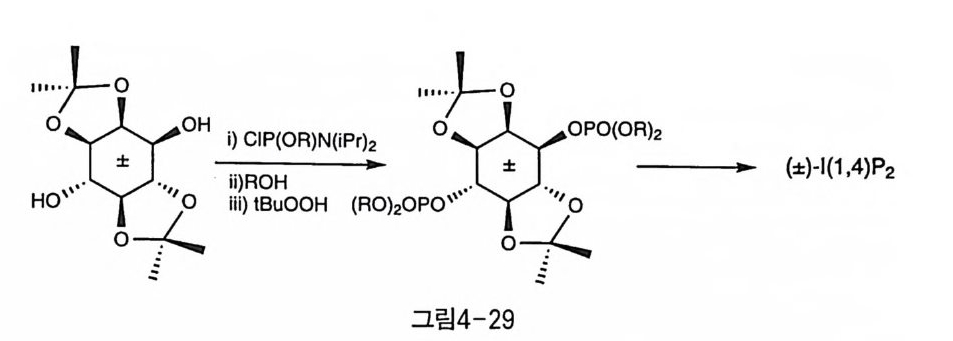 \二O )20PO0\PO(OR二 (±)·1 ( 1,4)P2
\二O )20PO0\PO(OR二 (±)·1 ( 1,4)P2
4- 3 0, Pie t r u sie w i cz 등 )(24, 40). D -C am p hor 로 보호된 이 노시 톨울 TBDMS-Cl 로 처리하면, 선택적으로 1,4- 수산기만이 실릴화되어 몇 단계의 보호/탈보호 후에 인산기를 도입하여 D-(1 , 4)Pz 를 얻을 수 있 었다. IPJ 합성 에 사용된 1(2, 3 , 6)BZ J 중간체를 3 당량의 (E t O) 꾼 Cl 로 처 리 한 후 산화시키면 1, 4 번이 인산화된 화합물이 주요 생성물로 얻어진다. 이것은 이웃한 수산기가 존재하는 경우 한쪽이 먼저 아인산화되면, 아 인산기의 에틸 보호기에 의한 입체 장애로 두번째 인산기 도입이 저해 되는 것으로 해석된다. 그리하여 이웃한 수산기가 존재하지 않는 1 번
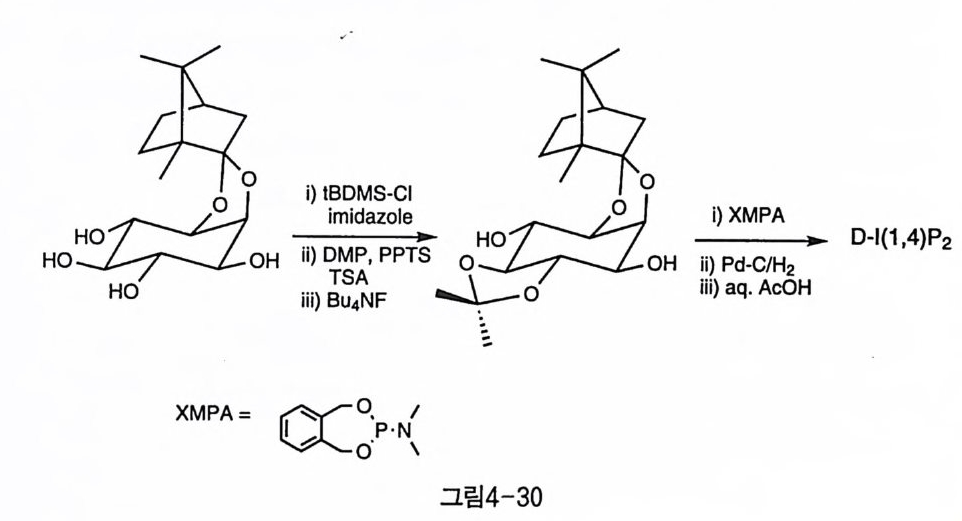 '
'
수산기가 먼저 반응한 뒤 4, 5번 수산기가 경쟁 반응을 하게 되는데, 2-Bz과 시스 관계에 있는 5번 수산기가 입체 장애로 인해 반응성이 낮아져 4번 수산기가 인산화된 것으로 생각된다. TMSBr과 LiOH를 차 례로 사용하여 보호기를 제거해서 l(1,4)P2를 얻었다(그림4-31)〔38).
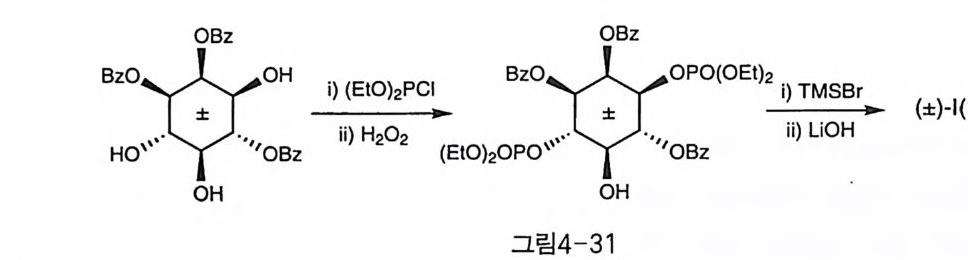 B::仁三20B:〈::ZO(OEI)2틀 (士)-1(1,4)P2
B::仁三20B:〈::ZO(OEI)2틀 (士)-1(1,4)P2
4-3-4 I ( 1, 5)P2 I(l,4,5)PJ에서 4번 인산기가 제거된 I(l,5)P2는 칼슘 분비의 생물 활 성을 가질 것이라는 제안이 있었다〔41). 이에 van Boeckel 등은 이노 시톨의 orthoformate로부터 출발하여 그림4-27과 같은 방법으로 I(2,4, 6)BnJ를 만들고, 상전이 촉매를 사용하여 선택적으로 1번 위치에 벤질 기를 도입하여 I(l, 2, 4, 6)Bn4를 만들었다. 이 중간체를 (-) cam-phanate로 광학 분할한 후 인산화하여, 각각 D-, L-l(l,5)P2를 합성 하였다(그림4-32, van Boeckel 등)〔42). 같은 중간체로 인산기 대신 sulfate와 sulfonamide가 도입 된 유사체 도 함께 합성 되 었다.
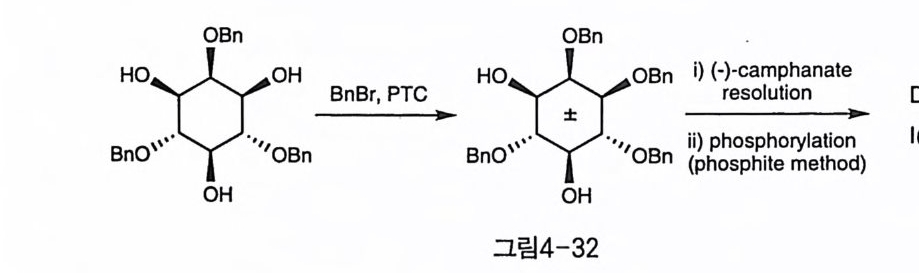 字川b麟0pS·shp pm血ohirmy lhtjo on 이 D1(1 a,5n)dP 2L
字川b麟0pS·shp pm血ohirmy lhtjo on 이 D1(1 a,5n)dP 2L
벤조일기와 isopropylidene 아세탈로 보호된 중간체를 이용하여 1(1, 5)P를 합성하는 경로도 개발되었다(그림4-33)(38〕 . 그림4-26에서 사 용된 것과 같은 방법으로 인산화 반응을 수행하였고, TMSBr로 인산 기의 보호기인 에틸기를 제거하였다. 염기 조건에서 벤조일기를 가수 분해하고 이온 교환 수지(H+)를 통해 아세탈기를 제거하여 I(l,5)P2를 얻을 수 있었다.
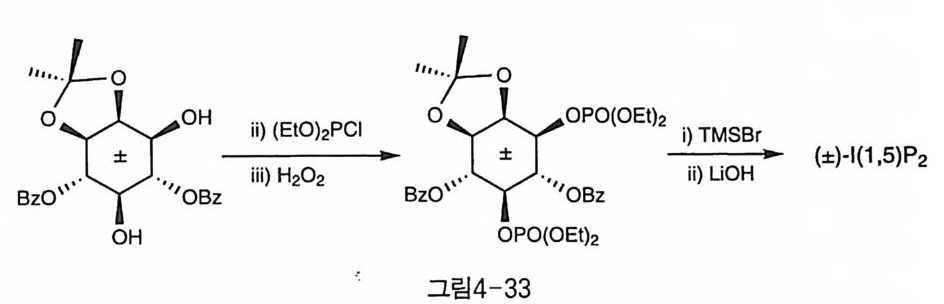 BIz:l亨-o ::Ziii) H202 Bz」00'亨_。OPO(OE::th: (OEI)2틀 (土)-1(1,5)P2
BIz:l亨-o ::Ziii) H202 Bz」00'亨_。OPO(OE::th: (OEI)2틀 (土)-1(1,5)P2
4-3-5 1(1, 6)P2 아세탈기로만 보호된 1,6-디올을 에틸인산기로 인산화하고, TMSBr 로 보호기를 제거하여 1(1, 6)P2를 합성한 경로도 보고되었다(그림4-
34)[38).아세탈기의 제거는 TMSBr 반응 후 물을 가해 생성된 산으로 가수 분해하여 수행되었다.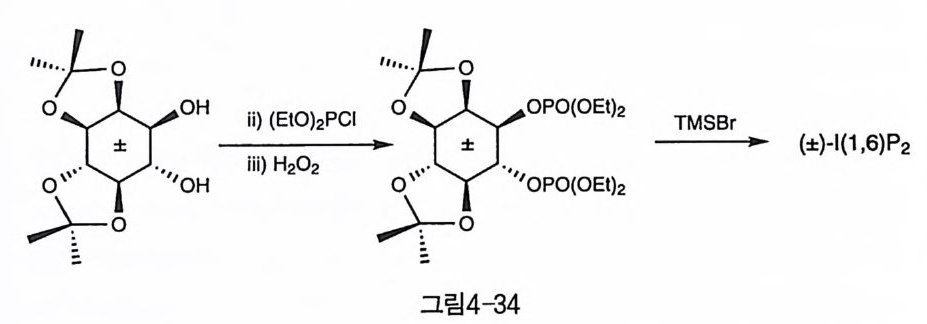 OH 二OpOpEh與tp TMSBr ,. (士)-1(1,6)P2
OH 二OpOpEh與tp TMSBr ,. (士)-1(1,6)P2
4-3-6 I (2, 4)P2 1(1 , 5, 6)BZ3 중간체를 3 당량의 (E t O)zPCI 로 처리한 후 산화시키면 2, 4 번이 인산화된 화합물이 주요 생성물로 얻어진다 . 재미있는 것은 수평 방향의 3 번 수산기 보다 수직 방향의 2 번 수산기 가 더 큰 반응성 을 나타내어 인산화되었다는 것이다 . 일반적인 경우, 수직 방향의 수 산기는 입체 장애가 심한 주위 환경 때문에 수평 방향의 수산기보다 반응성이 낮다. 이 경우에는 수평 방향의 4 번 수산기가 먼저 인산화된 다음 이웃한 3 번 수산기에 입체 장애를 유발시켜, 2 번 수산기에 먼저 인산화 반응이 일어난 것으로 생각할 수 있다. 즉, 인산기의 에틸 보 호기에 의한 입체 장애가 수직-수평 방향의 차이에 의한 입체 장애 효과를 누르고 주요하게 작용한 예라고 설명할 수 있다. 결정화에 의 해 주생성물을 분리하고, 보호기는 TMSBr 과 Li OH 를 차례로 사용하 여 제거하여 1( 2, 4)P2 를 얻었다(그림 4-35) 〔 38 〕 ·
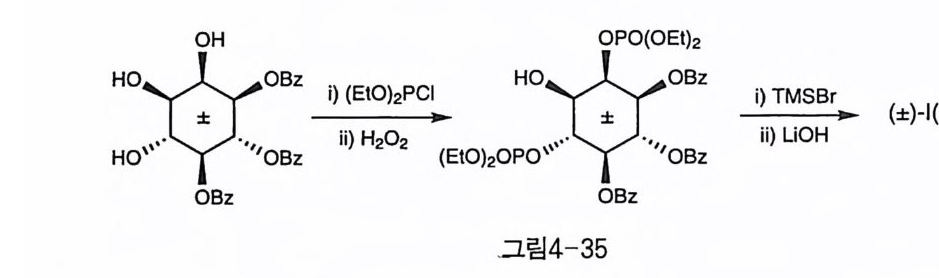 字O。OBHz 0 :: 三 :EIO)20PH0\亨 :OOBPz:O (OE:l)2 틀 (士 )-1(2,4)P,
字O。OBHz 0 :: 三 :EIO)20PH0\亨 :OOBPz:O (OE:l)2 틀 (士 )-1(2,4)P,
4-3-7 I (2, 5)P2 Inosito l o rth o fo rma t e 를 피리딘 염키 조건에서 1 당량의 BzCl 와 반응 시키면, 2 번 위치에 먼저 벤조일기가 도입된다(그림 3-15-4) . Or tho - fo rma t e 를 산 조건에서 제거하여 I( 2)Bz 울 얻어, 산 조건에서 아세탈 도입 반응을 하여 두 개의 위치 이성질체를 얻었다. I (l , 6 : 3,4)Ace2 보
다는 1(1 , 6:4 , 5)Acez 쪽이 2 - Bz 에 의한 입체 장애를 받아 열역학적으 로 불안정할 것으로 기대되었으나, 반응에 사용된 시약의 종류 (DMP 또는 2-me th ox yp ro p ene) 나 반응 온도에 관계 없이 거의 동일한 양이 생성됨이 확인되었다. 크로마토그래피로 두 이성질체를 분리한 후 1(1 , 6:3, 4)Acez 이성질체의 벤조일기를 제거하여 2, 5_ 디올을 생성시키 고, 인산화하여 1(2, 5)P 2 를 합성 하였다(그림 4_36) [38 ). 인산화와 보호 기 제거 조건은 그림 4 - 34 와 동일하였다.
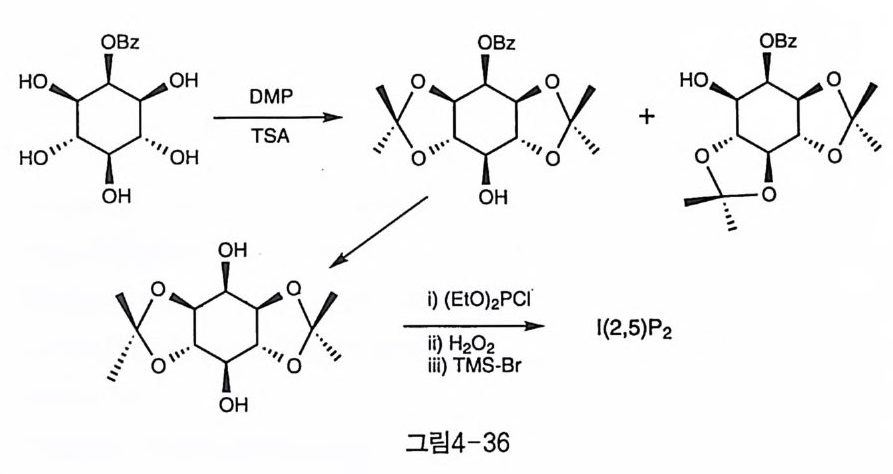 ::\\〈:\「 :v
::\\〈:\「 :v
4-3-8 I (4, 5)P2 I( l,4,5)P3 의 칼슘 분비 효과는 4, 5 번의 인접한 인산기에 의한 것이 라는 추측을 가능케 하였다. 이에 Pott er 등은 Gig g 등이 합성을 보고한 I(l , 2, 3, 4)Bn ◄ 를 중간체로〔 43 〕' p hos p hor amidit e 를 이용하여 성공적으로 이웃한 수산기를 인산화하여 라세미 형태의 I(4,5)P2 를 합성하였다〔 44 〕. 이노시톨의 고리 구조를 만들기 위해 cond urit ol 에서 출발하여 합성 하는 방법도 연구되었는데, 그중 라세미 형태의 !(4,5)P2 를 합성한 예 가 보고되 었다(그림 4-37, Carless 등) [45 ] ·
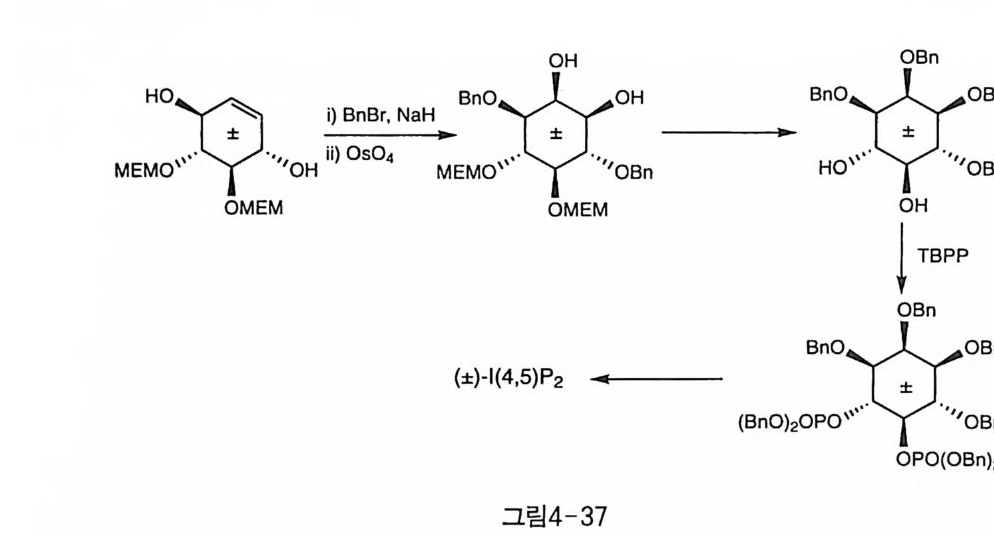 ME::~:'OH도근::\O:H :n一
ME::~:'OH도근::\O:H :n一
또다른 합성 경로로는 I(l,4)Bz2를 출발 물질로 하여, 몇 단계의 반 옹을 통해 아세탈과 벤조일로 적절히 보호하여 I(1,2,3,6)BZ4를 만들어 이용하는 예가 있다. 그림4-26과 동일한 방법으로 I(l,2,3,6)BZ4울 인 산화하고, 보호기를 제거하여 !(4,5)P2를 합성하였다(그림4-38)〔38).
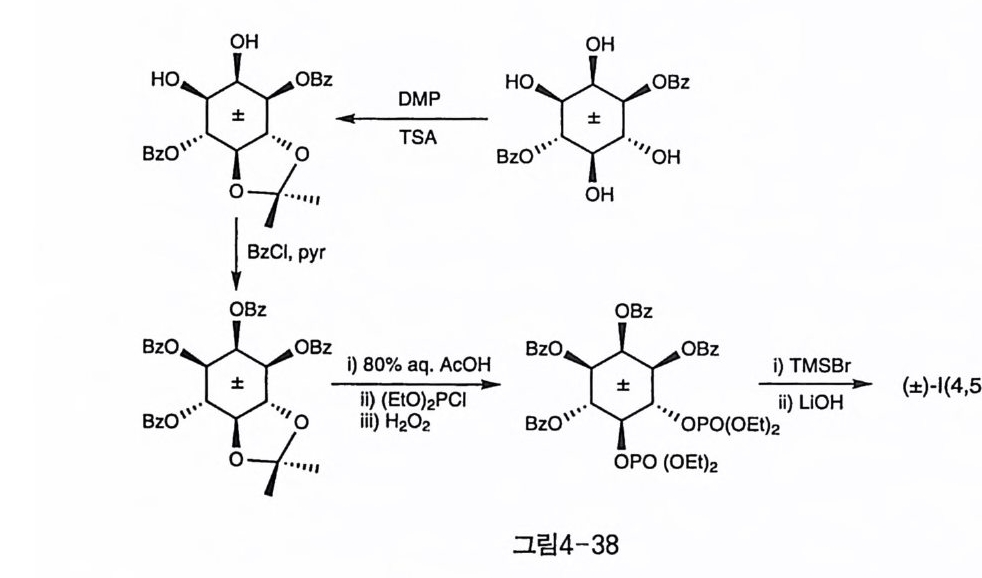 OH DMP HO~ 1OH
OH DMP HO~ 1OH
4-3-9 I (4, 6)P2 그림4-33에서 사용된 것과 같은 조건의 중간체를 이용하여 1(4,6)P2 를 합성하는 경로가 함께 보고되었다(그림4-39)〔38). 그림4-33에서와 같은 조건으로 인산화 반응을 수행하였고, TMSBr로 에틸기를 제거한 후, 염기 조건에서 제거되는 벤조일기와 산 조건에서 제거되는 아세탈 기를 차례로 제거하여 1(4,6)P2를 얻을 수 있었다.
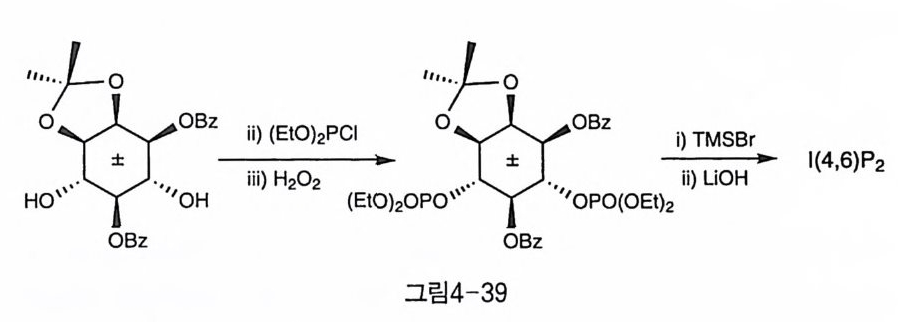 oBz oH二 20PO亨f。°0:ZO(OEt를
oBz oH二 20PO亨f。°0:ZO(OEt를
4-4 삼인산이노시톨 4-4-1 1(1,4.5)P3 1,4,5-삼인산이노시톨이 세포 내의 2차 전달 물질로서 외부의 신호 를 받아 세포 내의 칼슘 농도를 증가시킨다는 사실이 알려진 후, 많은 화학적 합성 연구가 진행되었다. 최초의 합성은 1986년 일본 연구팀에 의해 발표되었다(그림4-40, Ozaki 등)(46). 벤질과 알릴기로 보호된 이 노시 톨에 L-menthyloxyacetyl기 를 광학 활성 보조기 로 이 용, 1번과 2번의 수산기 중 선택적으로 1번 수산기에만 도입하여 성공적으로 광 학 분할하였다. 일반적으로 수평 방향인 1번과 수직 방향인 2번 수산
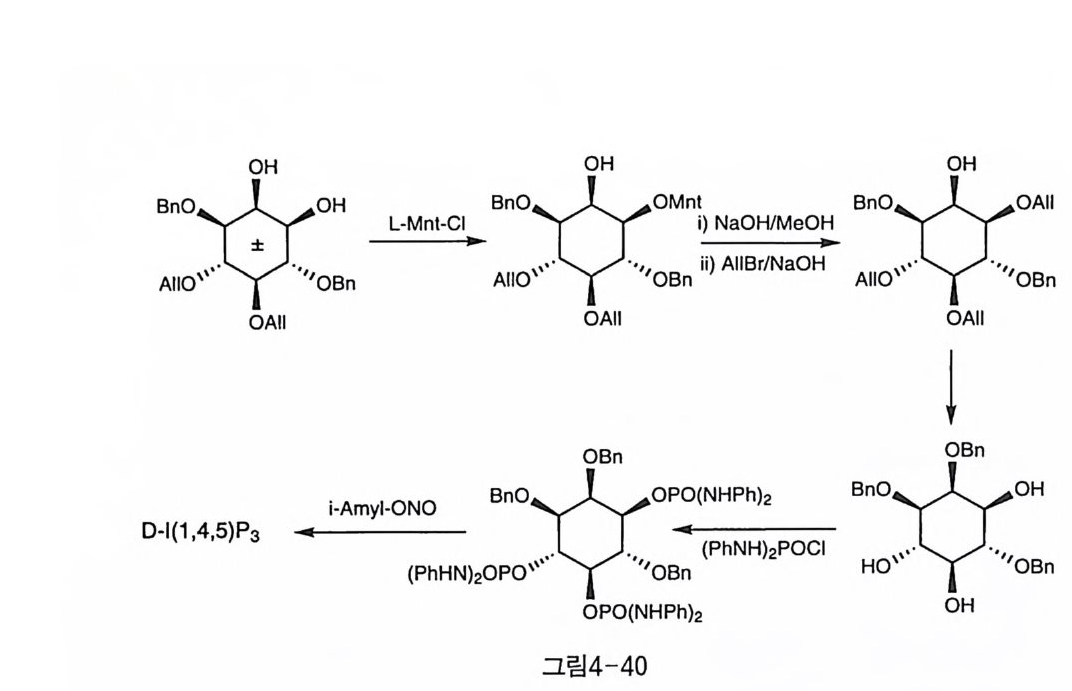 0 O>H n 三: :亨:OH :言三근 :::\亨OH。 :::
0 O>H n 三: :亨:OH :言三근 :::\亨OH。 :::
기에 대한 알킬화나 아실화 반응은 입체 장애가 적은 1 번에 더 잘 일 어나는 경향이 있다. 광학 활성의 중간체는 키랄 보조기를 제거한 후, 다시 한번 선택적 알릴화 반응을 거쳐 D- 1( 2,3,6)Bru 를 생성시켰 댜 이 중간체에 d ianili dop hosp horochlo ri da t e 를 이용해 인산화하여 1(1 , 4,5)P 를 얻기는 하였으나, 이웃한 4, 5 번 수산기에서는 부반응으로 고 리 인산이 형성되는 둥 개선되어야 할 문제점들이 남아 있었다. 이러 한 문제점들은 후에 같은 연구자들에 의해 TBPP 를 이용한 인산화 방 법이 개발됨으로써 극복되었다〔 47). 같은 연구자들은 또, 4, 5 번의 수산기를 먼저 TBPP 를 이용하여 인 산화한 다음, 남은 1 번과 2 번의 수산기를 여러 가지 방법으로 처리하 여 D-1 (1 ,4,S)P J뿐만 아니라 고리 인산기를 포함한 D-1(1,2)cP(4,S)Pz 와 D- 1( 2,4,S)P J까지 합성할 수 있는 경로를 개발하였다(그림 4-41, Ozak i 등 )(34 〕 . 한편 여러 단계의 보호 및 탈보호 반응을 줄이기 위해 이노시톨에 직접 여러 개의 벤조일기를 도입하는 반응이 시험되었다. 여러 조건
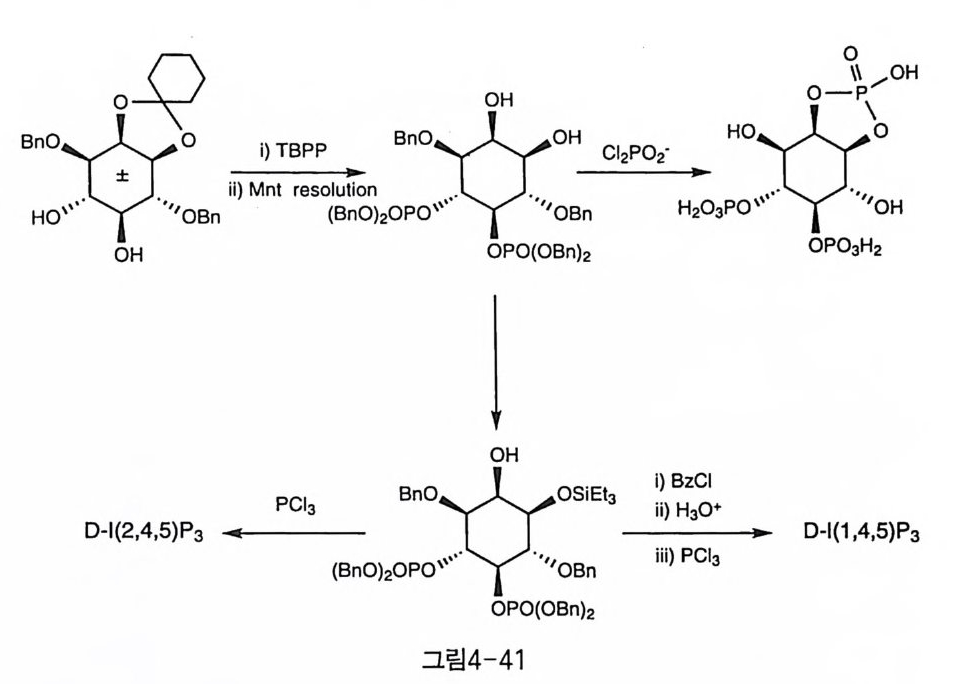 B: :0亨: 三。BP noo iI o::三 3:i ?\\,,o,OH H
B: :0亨: 三。BP noo iI o::三 3:i ?\\,,o,OH H
중 피리딘 하에서 3.3 당량의 BzCl 를 사용하였을 때 15% 의 수율로 메조 형태의 I(l,3,5)B ZJ가 크로마토그래피를 통하여 얻어졌다. 이 중간체는 D- tart ara t e 를 키랄 보조기로 사용했을 때, 높은 순도로 D-4 번 수산기 에만 에스테르를 형성함이 밝혀졌다. 남은 두 개의 수산기를 실릴화하 고, 4 개의 아실기를 제거하기 위해 실릴기의 이동을 일으키는 일반 염 기 조건 가수 분해 대신에 Gri gna rd 시약이 사용되었다. 실험 결과, E tMg Br 을 사용했을 때는 모든 아실기가 제거되었으나, MeM g Br 인 경 우에는 E tMg Br 에 비해 반응성이 낮아서 D-3 번 위치의 벤조일기만 선 택적으로 보존할 수가 있었다. 얻어진 각 중간체들은 D-I(l ,4 ,5)PJ 및 D-I (l ,3,4,5)P ◄ 의 합성에 이용되었다(그림 4-42 , Ozak i 동 )(48) . Cy cl op en ty lide ne 아세탈이 사용된 예도 비 교적 초창기 합성 에 나타 났댜 2, 3 번 수산기를 아세탈로 보호하고 덩치가 큰 실릴기를 도입하 면 1, 4 번이 선택적으로 보호된다. 여기에 2, 7-di br omo-9-ph e nyl -
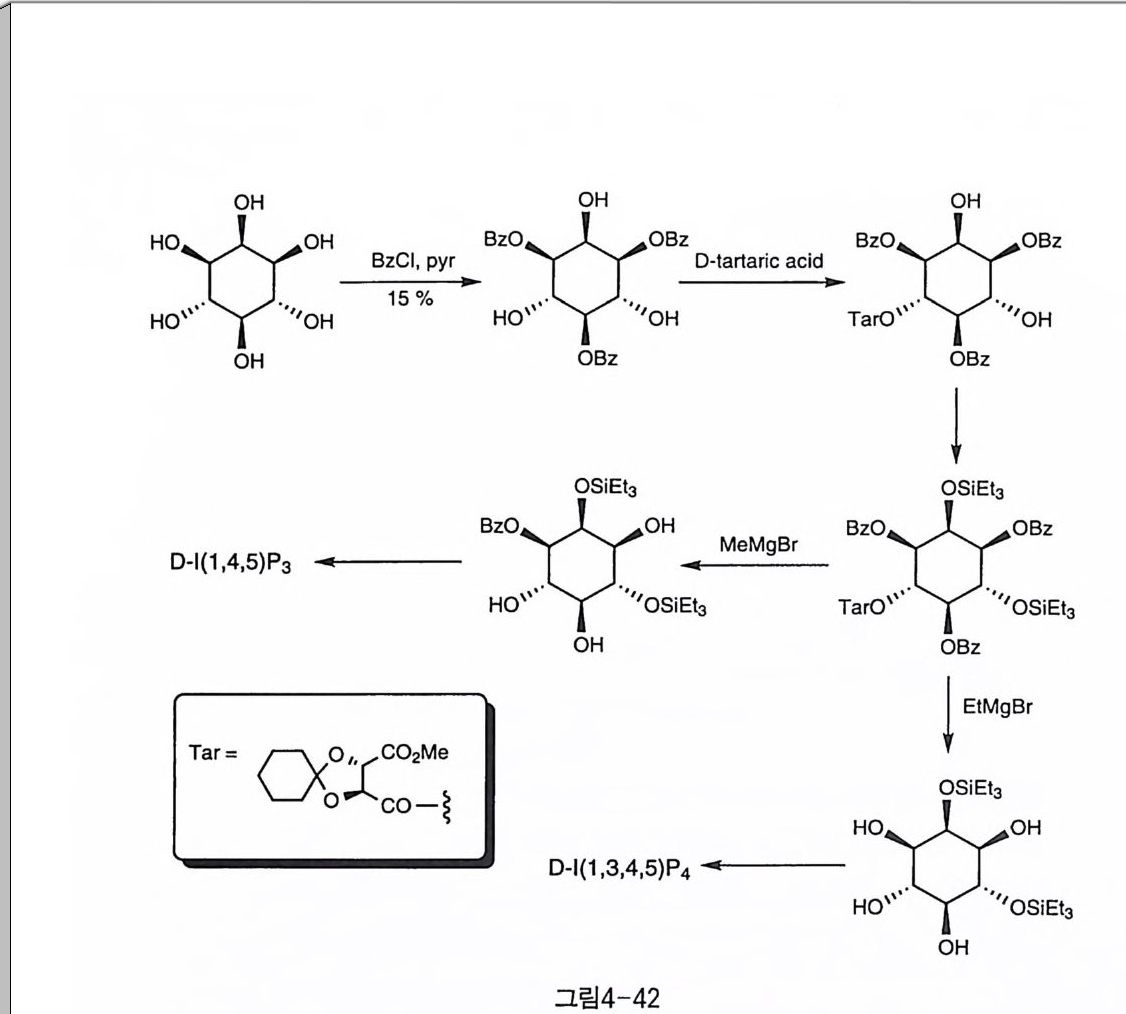 HD00 -T1Ha(1r,=4 ,亨 5oHO 0)P°3 XCO 02 HOc—三Mo — e: BZB 0Z0 OHDH그-O1림g亨 ( oH1O> O ,4HB3z - ,4 4, 25 )H O P B, ~H二一 z[T :B zO :`ar O*O S O>i:HEzlOB:l尸 ! 3 : B,ez 匡,, s r
HD00 -T1Ha(1r,=4 ,亨 5oHO 0)P°3 XCO 02 HOc—三Mo — e: BZB 0Z0 OHDH그-O1림g亨 ( oH1O> O ,4HB3z - ,4 4, 25 )H O P B, ~H二一 z[T :B zO :`ar O*O S O>i:HEzlOB:l尸 ! 3 : B,ez 匡,, s r
9-xanth e ny l c hlo ri de 를 반응시키면 6 번 수산기를 보호할 수 있다 . 실 릴기를 제거하고 열린 1,4,5_ 수산기를 E 타-.J -P(OC Hi CH 2 CN) 2 로 인산 화하여 라세미 1 (1 ,4,5)P J를 합성하였다 . 이때, 보호기 제거에는 aq . ML 가 사용되었다. 한편 광학 활성 이성질체를 만들기 위해서는 glu - cop yra nosyl 유도체 를 이 용하여 I (1, 4, 5, 6)Bn4 의 광학 분할이 시 도되 었 다. 이후, 라세미인 경우와 같은 방법으로 D-1 (1 ,4,5)P J가 성공적으로 합성되었다(그림 4-43, Reese 등)〔 49 〕· 1( 3,6)Bru 에 속도론적 지배 조건에서 아세탈을 도입하면, 열역학적 으로는 더 불안정하지만 입체 장애를 덜 받는 트란스 아세탈이 먼저
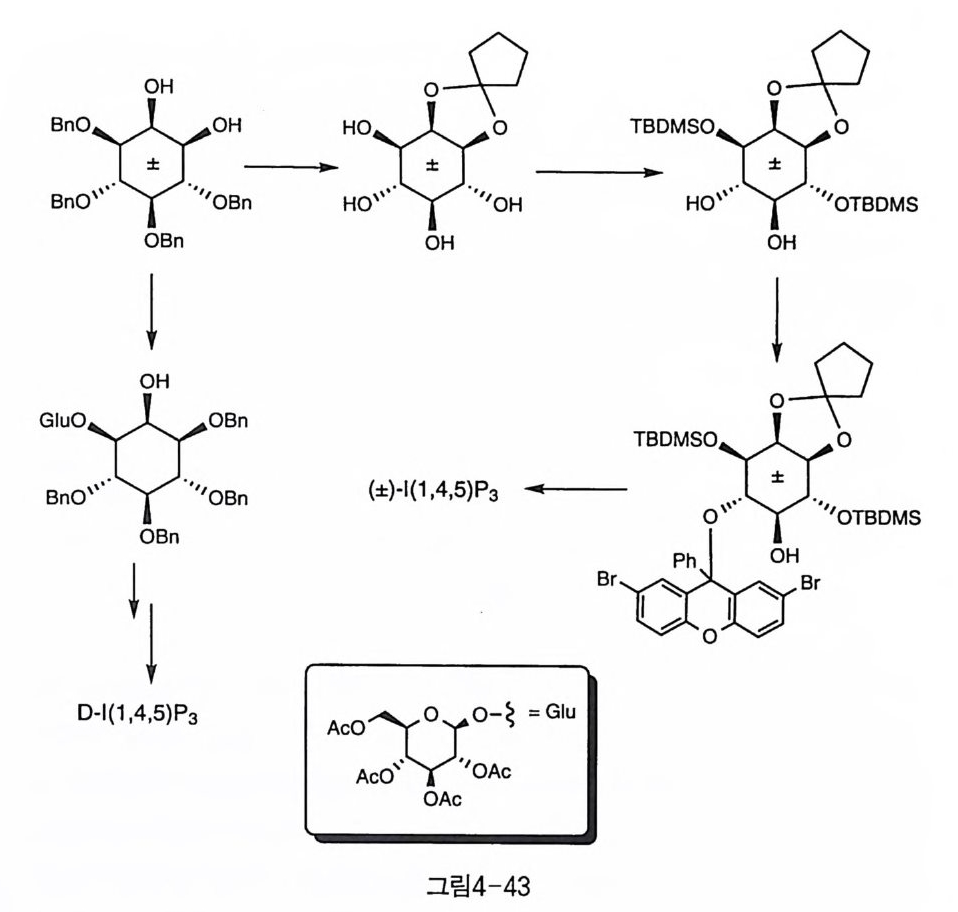 !OBn OH OH
!OBn OH OH
형성된다 . 이 중간체를 활용하여 몇 단계를 거친 후 1(2, 3,6)BD J를 얻 어 i PrzN 一 P(OC Hi C Hi CNh 로 인산화하여 라세미 형태의 1 (1 ,4,5)P J을 합성하였다(그림 4-44, Pott er 등)〔 50). 이때 인산기의 보호기 제거 반 응은 Na /NIL 조건으로 수행되었다 . 한편, 같은 방법으로 얻은 1(2, 3, 6)Bn J를 이 용하여 인산기 뿐만 아니 라 su lfa t e 와 su lfo n ami de 를 도입 해 전하가 다른 등입체성 분자를 만드는 방법도 보고되었다〔 51 〕· I(2, 3;4, 5)HeX2 의 6 번 수산기를 선택적으로 벤질화한 후, 남은 수산 기를 carn p hana t e 로 아실화하고 광학 분할하여 두 광학 이성 질체가 모
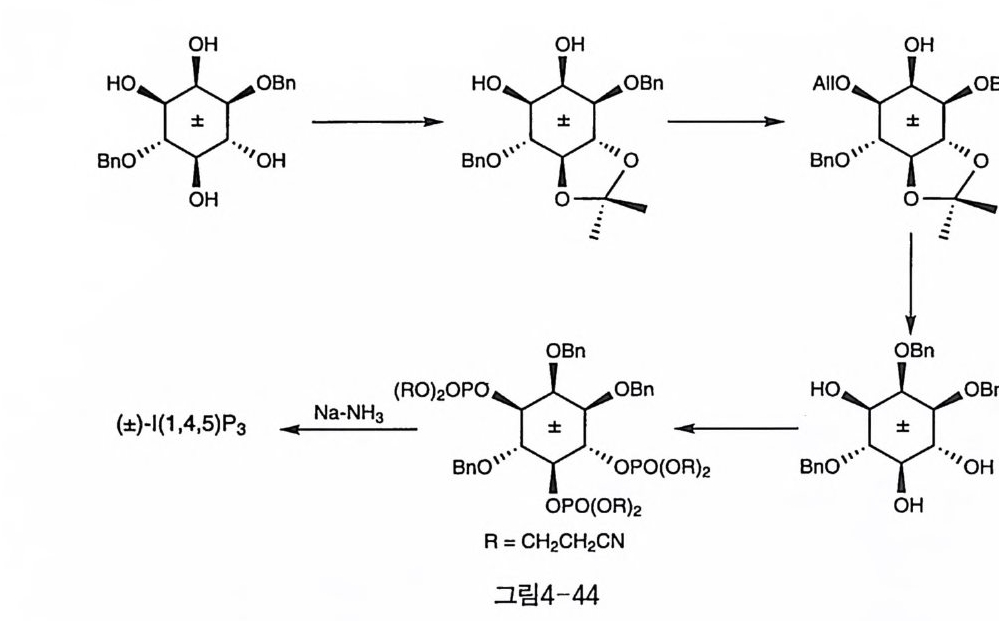 B:::一B::〔OH Bn一:::。rOH
B:::一B::〔OH Bn一:::。rOH
두 얻어졌다. 두 개의 아세탈을 부분 가수 분해하면 열역학적으로 더 불안정한 트란스 아세탈만을 선택적으로 제거할 수 있고, 남은 수산기 들을 인산화하고 보호기를 제거하여 D와 L-1(1,4,5)P3를 합성할 수 있 었다(그림4-45, Vacca 동) [30,52]’ 이노시톨로부터 쉽게 얻을 수 있는 1(3, 6)Bz2의 네 수산기 중 세 개 만을 선택적으로 인산화하는 대단히 짧은 단계의 합성도 보고되었다.
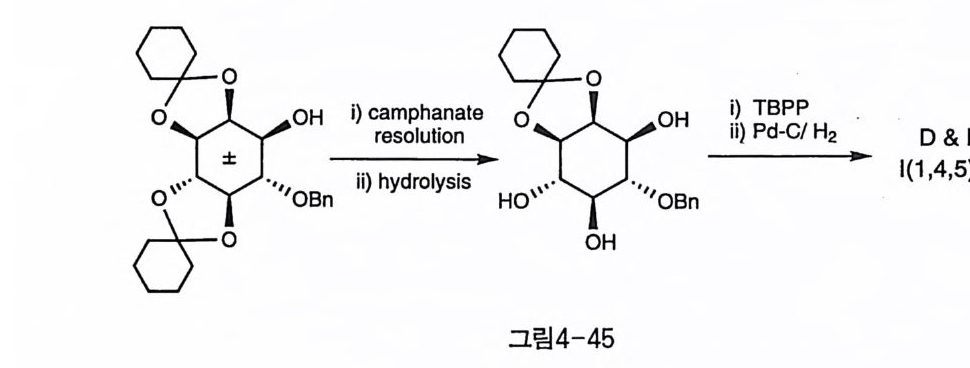 OH ’) eampnanate o소 J.. i0H iii)) TPBdP-CP/ H2 D& L-
OH ’) eampnanate o소 J.. i0H iii)) TPBdP-CP/ H2 D& L-
이 경 우 3.3 당량의 (MeO) 꾼 Cl 을 염 기 와 함께 사용하면 반응성 이 낮은 수직 방향의 2번 수산기만이 인산화가 되지 않고 나머지 세 개의 수산 기가 인산화되어, I(l , 4, 5)P3 가 간단하게 합성되었다(그림 4 켜 o, Meek 등)〔 5 이 . 이때 아인산기를 산화하기 전에, 남은 2 번 수산기는 아세틸 기를 도입하여 인산기의 이동 반응을 막았다. 한편, 인산기의 보호기 제거에는 HBr 을 사용하였다. 이 합성 경로는 알려진 I(l ,4 ,5)P3 합성 중 가장 효율적인 경로 중의 하나이다.
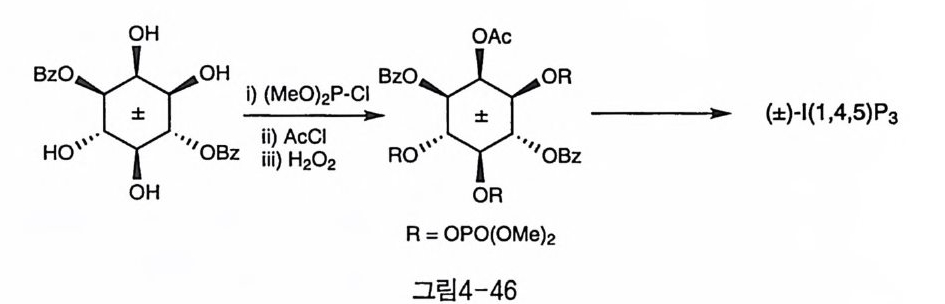 B:: 亨OH ::Z 二::OR ?- (士 )-1(1,4,S)Pa
B:: 亨OH ::Z 二::OR ?- (士 )-1(1,4,S)Pa
그림 4 一 19 에서 소개한 바대로, 벤젠을 Pseudomonas p u ti da 라는 미생 물로 산화시켜 이노시톨 구조를 만드는 방법은 다양한 인산이노시톨의 합성에 이용되었다. I(l) P 의 합성에 이용되었던 에폭시드 중간체를 활 용하여 1 (1 ,4,5)P3 가 합성되었고, 이 에폭시드를 광학 활성의 (R)-sec- ph eny le th yl alcohol 로 고리 열기 반응을 하여, 각각의 광학 이성질체를 분리하였다. 이 중간체들로부터 각각 D 와 L 의 I (l ,4,5)P3 가 합성되었다 (그림 4-47, Ley 등) [21 ,5 4) . 화학적인 방법으로 벤젠을 산화하여 얻어진 cond urit ol 을 중간체로 하여 1(4,5)P2 를 합성한 예를 그림 4_37 에서 소개한 바 있다. 이 중간체 는 그 밖에도 다양한 인산이노시톨의 합성에 이용되었는데, 이 방법으 로 라세미 형태의 I(1 , 4,5)P:i, 1(2, 4,5)P3 및 1 (1,2, 4,5)P4 가 만들어졌다 (그림 4-48, Carless 동) [45 ] '
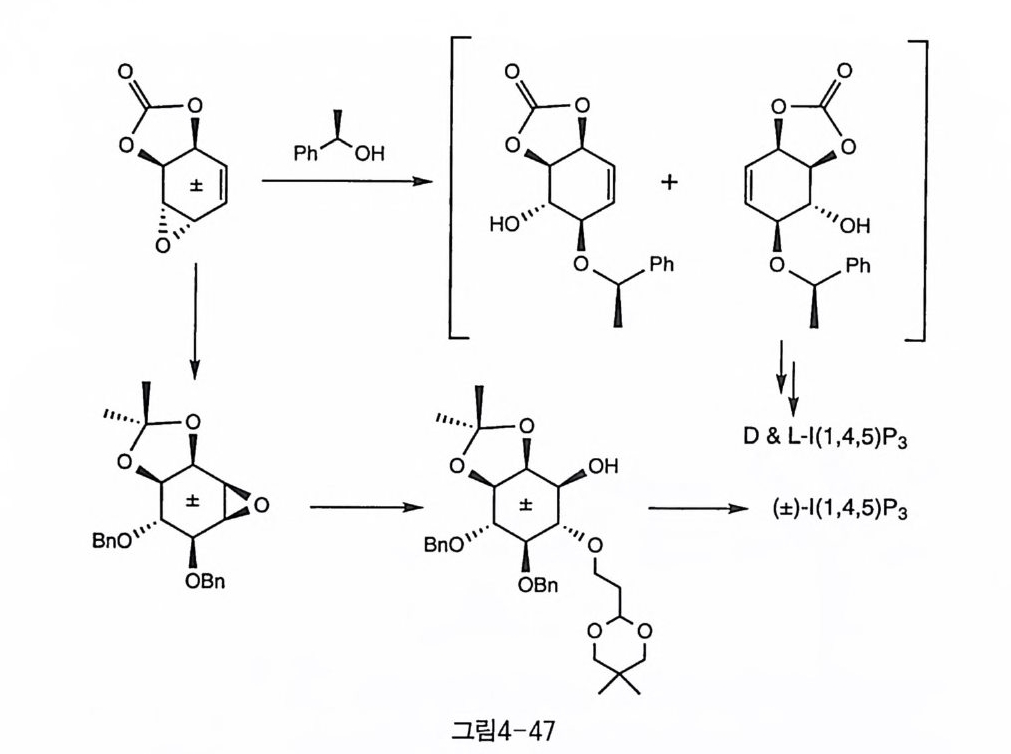 。0 0
。0 0
그림4-6에서 소개했던 D -mannose의 오르소에스테르를 이 용하는 광학 분할이 l(1,4,5)PJ 합성에도 적용되었다. 먼저, 4, 5번의 수산기를 인산화한 후, 1번 수산기를 오르소에스테르화하는 경로로 광학 분할하 여 D와 L-l(1,4,5)P과 합성되었다(그림4-49, Shvets 등)[55〕. ` Menthoxyacetyl기로 광학 분할을 하고 여 러 단계의 보호/탈보호를 거쳐 D-1(1,4,5)PJ 및 D-1(1,3,4,5)P4을 합성하는 예가 네덜란드의 과 학자들에 의해서도 보고되었다(그림4-50, van Boom 등)〔56〕. chiro-Inositol을 출발 물질로 이용하여 IP3를 합성하는 경로도 개발 되 었댜 천연물인 D -pinitol (3-methyl D -chiro -inositol)과 L -quebra-chitol(2-methyl L-chiro-inositol)로부터 메틸기를 제거하면, 각각 D 와 L -chiro -inositol을 얻을 수 있다. D -chiro -inositol로부터 출발하
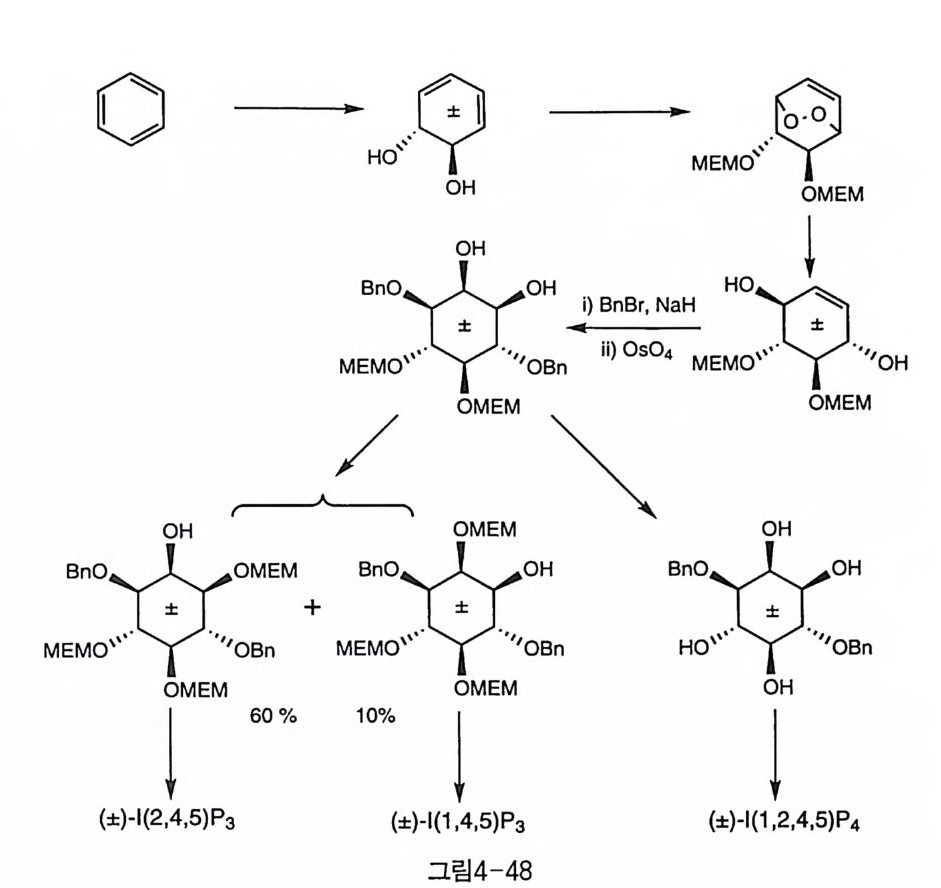 O 一 HO: ? 一 MEM0```
O 一 HO: ? 一 MEM0```
여 시스 관계에 있는 두 쌍의 이웃한 수산기를 선택적으로 아세탈기로 보호할 수 있고, 몇 단계에 걸쳐 1 번 수산기에 T f기를 도입하였다. 트 란스 관계에 있는 이웃한 벤조일기의 참여로 고리형 중간체를 거쳐 1 번의 입체 구조가 반전되어 미오이노시톨 유도체가 얻어진다. 이때 2-Bz 와 1-Bz 가 3:1 의 바율로 얻어지고, 주생성물의 벤질기를 제거하 여 I(2, 3, 6)BZ J 중간체를 얻고, 벤질인산기로 인산화한 후 가수소 분해 반응과 염기 가수 분해로 보호기를 제거하여 D-1 (1 ,4,5)P J를 얻었다. L -chir o -i nos it ol 을 출발 물질로 사용하여 같은 반응을 진행하여 L- I(l, 4, 5)P J도 합성 되 었다(그림 4-51, Ballou 등) [57 ).
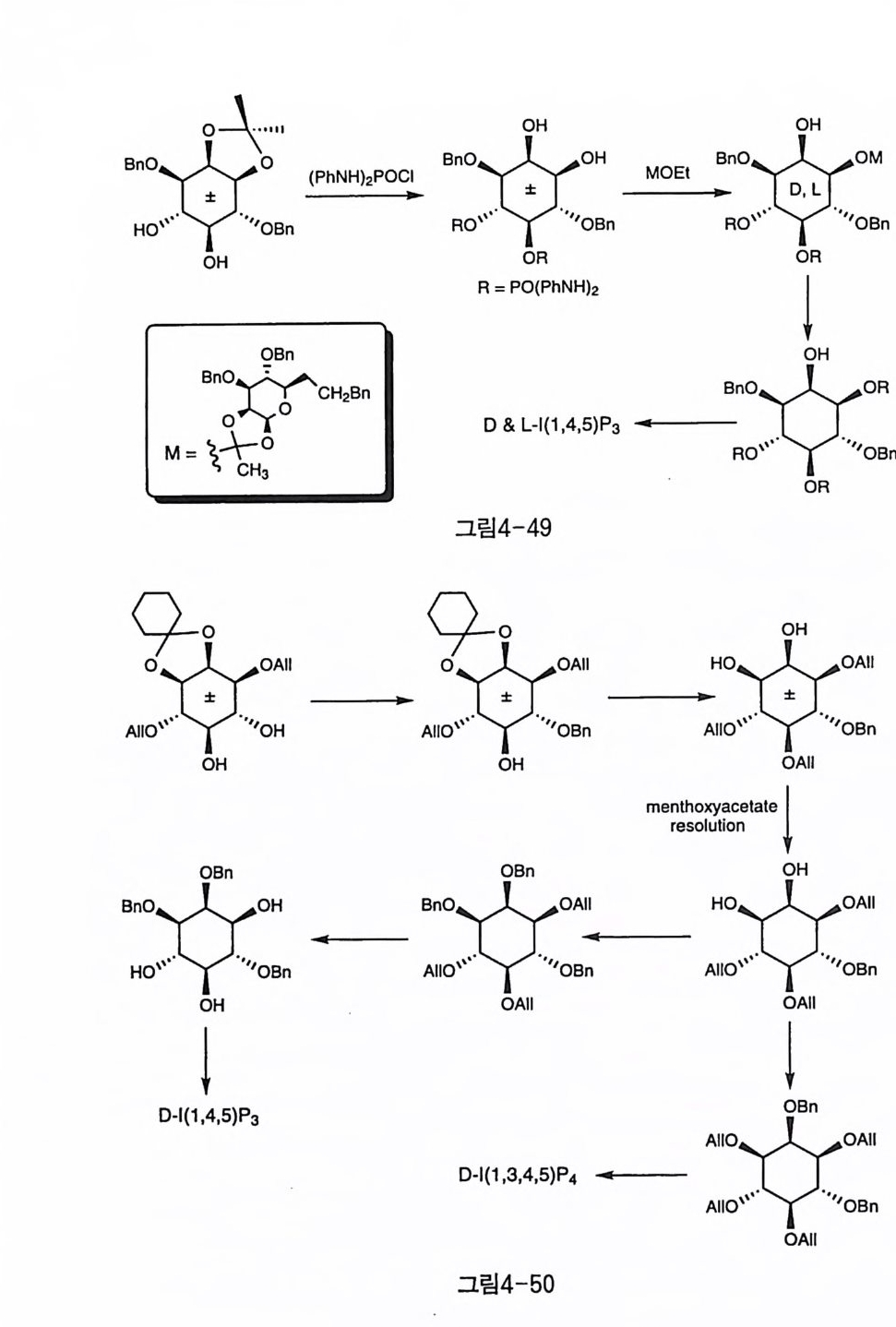 ::OH
::OH
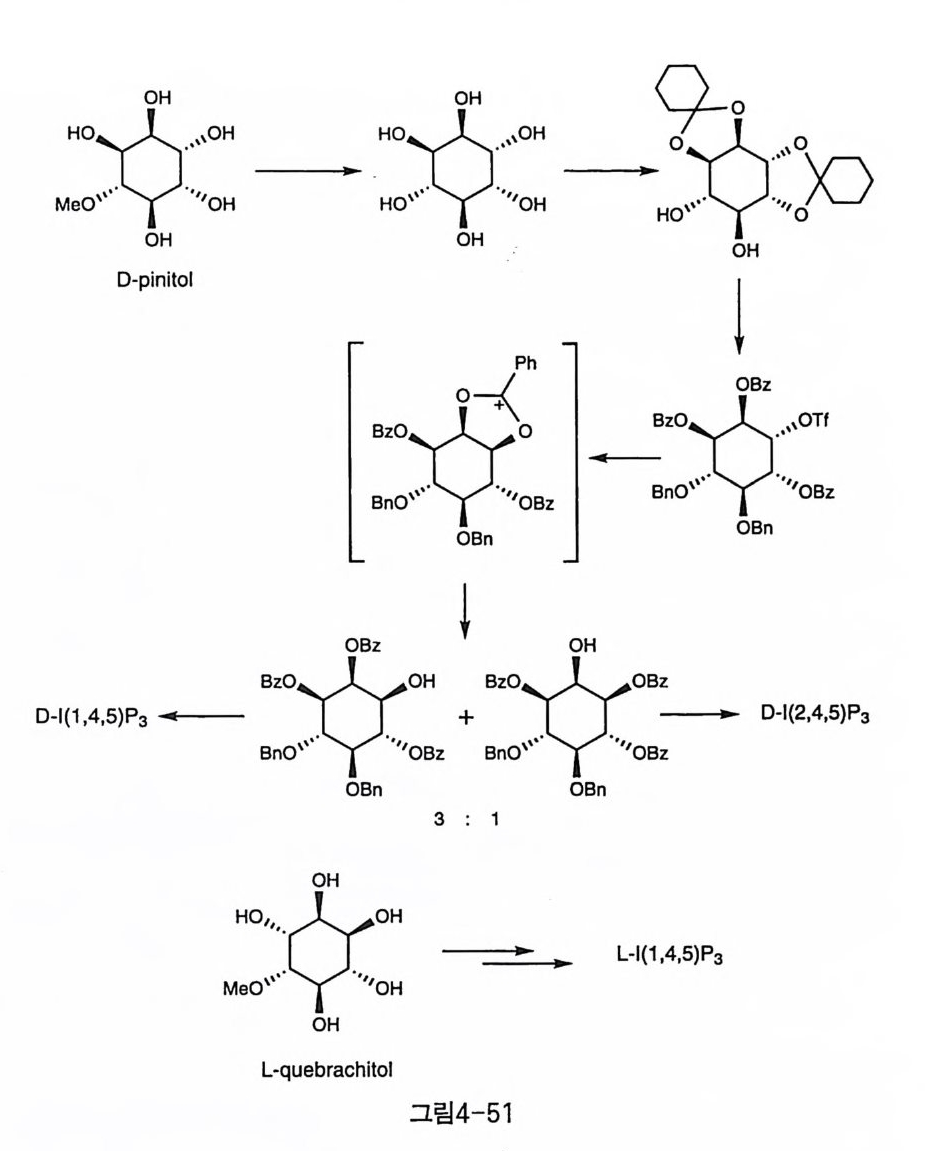 ?HO
?HO
Falck 등은 천연물인 (-)-quinic a ci d 를 출발 물질로 하여 여러 단 계의 반응을 거쳐 D 一 I(l , 4, 5)P J을 합성하였다(그림 4-52, Falck 등)〔 58). 출발 물질 자체롤 광학 활성 분자를 사용하여 별도의 광학 분 할 과정이 필요하지 않다는 장점이 있기는 하지만, 합성의 경로가 길
 H C02Me
H C02Me
어서 그다지 효율적인 방법은 아니다. 1( 2,3 :4 ,5)HeXl 에 Sn 복합체를 만들어 CsF 존재 하에서 벤질화 반응 울 하면, 높은 선택성을 가지고 6 번 수산기가 벤질화된다. 이것은 1(1, 4,5)P 의 합성에 중요한 중간체가 됨을 그림 4-45 에서 보인 바 있다. Men thy lcarbon y l 기 를 이 용한 화학적 광학 분할과 choleste r ol es t erase 를 이용한 효소 화학적 방법을 사용하여 성공적으로 광학 활성을 가진 이 성질체를 얻을 수 있었고, pho sph o ram idite 방법으로 인산화하여 D-
1 (1 ,4,S)P 를 합성하였다(그림 4-53, Chen 동)〔 59, 60] . Inosit ol bora t e 를 통하여 ( -) -m enth y l carbona t e 를 중간체 로 합성 하 고 이를 광학 분할하는 재미있는 반응이 보고되었다. 이때 선택적으로 1 번 위치에 광학 보조기가 도입될 수 있었고: 몇 단계의 반응을 거쳐 D-I (1 ,4,S)P 까 성공적으로 합성되었다(그림 4-54, Penades 등)〔 61).
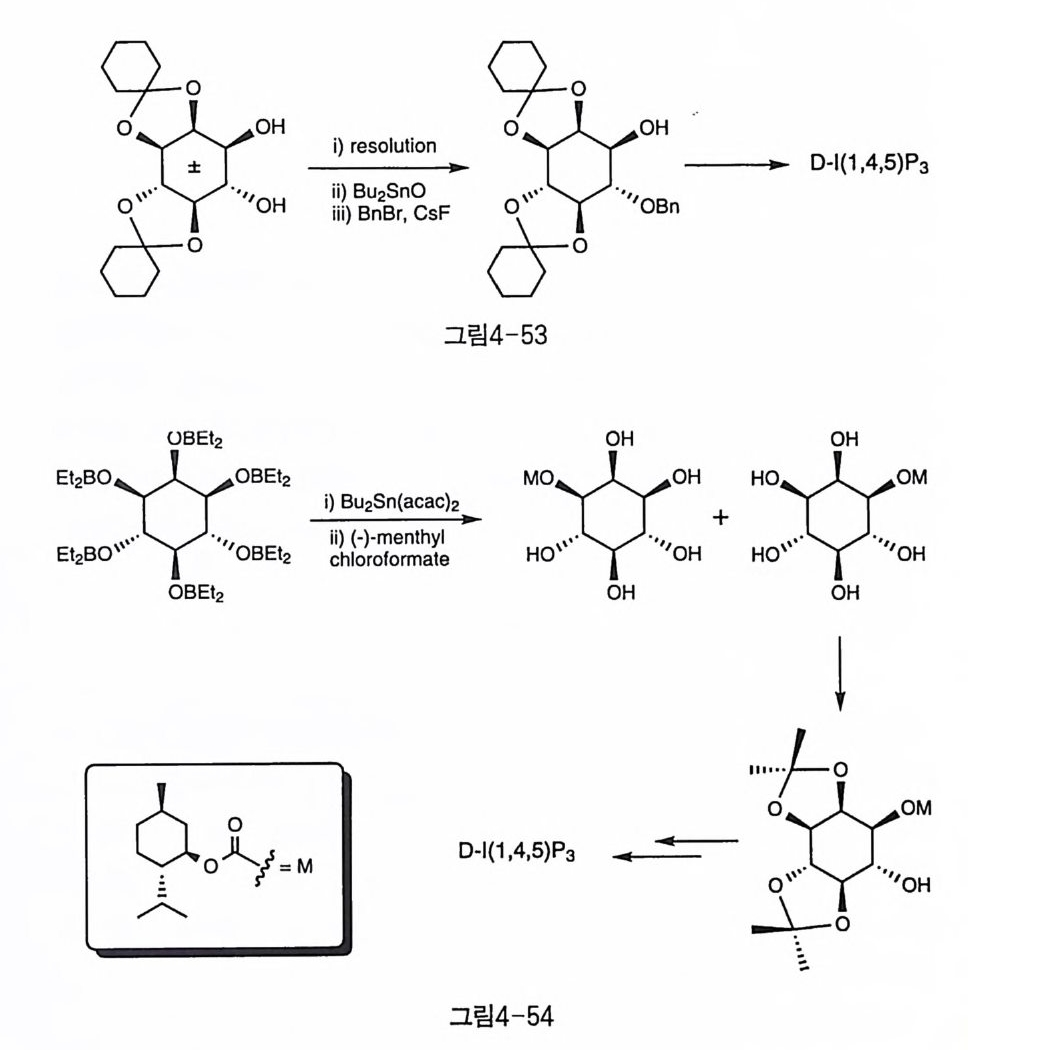 i) 『 esolu t i on J:: _ Y \ OH 一 D-1(1,4,5)P3
i) 『 esolu t i on J:: _ Y \ OH 一 D-1(1,4,5)P3
Mandelic acid의 유도체도 이노시톨의 광학 분할에 활용되었다. 1(2, 3)Hex에 Mandelic acid의 에스테르를 도입하면, 선택적으로 1번 위치 에 도입되어 광학 분할이 성공적으로 수행되었다. TIPS로 4, 5번 수산 기를 선택적으로 보호하고 몇 단계의 반응을 거침으로써 D-1(1,4,5)P3 가 성공적으로 합성되었다(그림4-55, Bruzik 등)〔62〕·
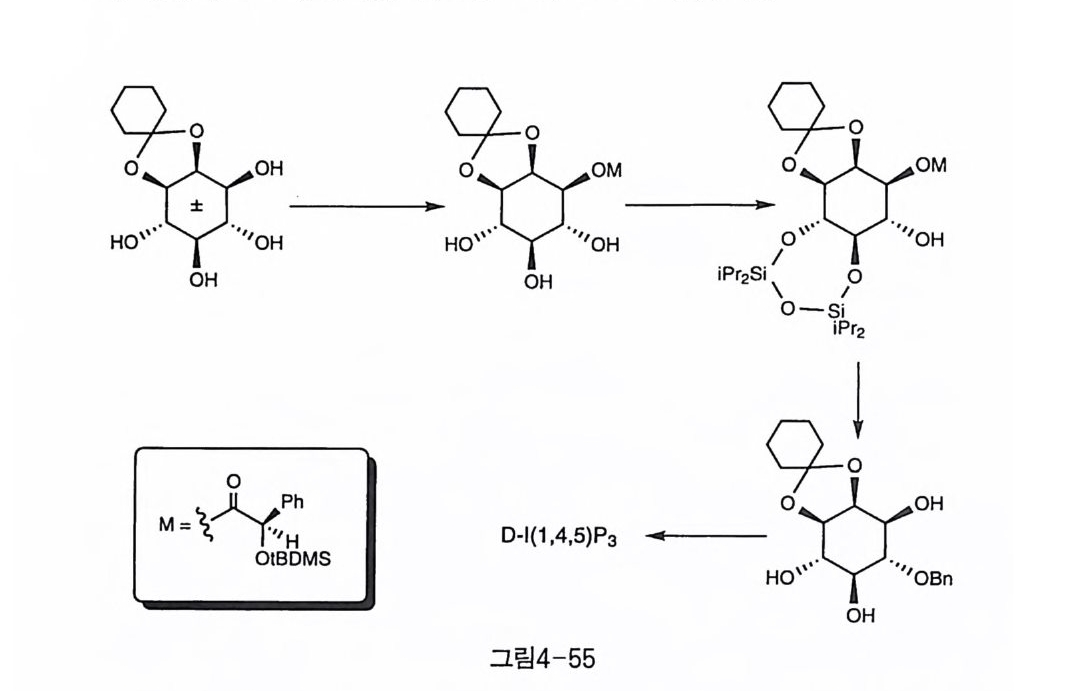 >
>
그림4-19에서 선보였던 D-camphor를 이용한 합성 경로가 D-1(1,4, 5)P3에도 적용되 었다(그림4-56, Bruzik 동) (24, 63]. 이노시톨의 (2, 3) -D-camphor 아세탈 유도체에 다양한 조건에서 알킬화 또는 아실화 시 험을 해본 결과, 4당량의 pivaloyl-Cl을 사용한 경우 1, 4, 5 위치를 선택적으로 보호할 수 있었다. 몇 단계의 보호/탈보호 반응을 거쳐 성 공적으로 D-l(1,4,5)P3이 합성되었다. 1(3,6)Bz2를 산 조건에서 orthobenzoate로 처리하면 (1,2)-고리형 오
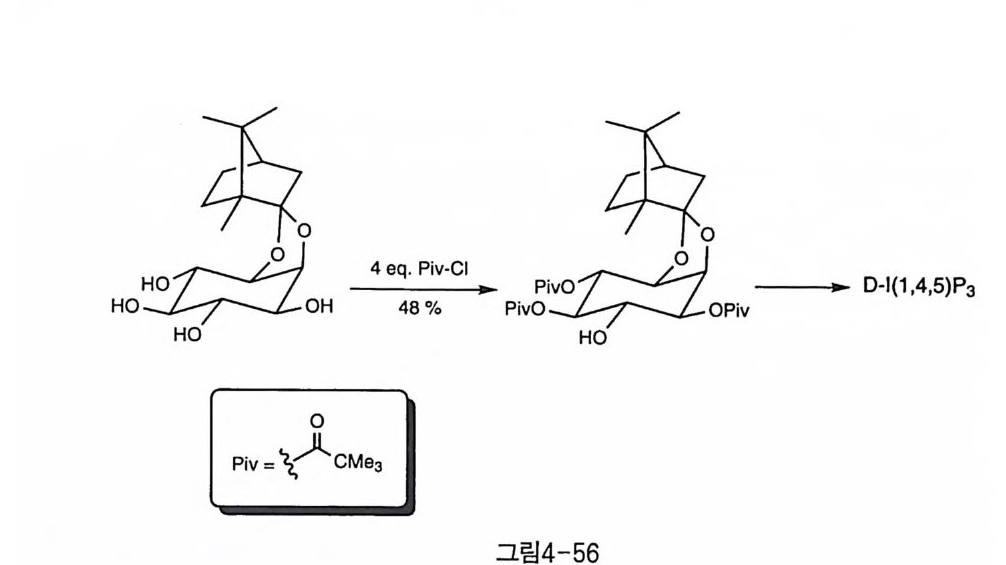 HO~OH 48% P i vO~ 적 P i v
HO~OH 48% P i vO~ 적 P i v
르소에스테르 중간체가 형성되고, 물을 가하여 가수 분해하면 수직 방 향의 2 번에 Bz 이 도입된 화합물이 주생성물로 얻어진다. 이때의 위치 선택성은 입체 전자 효과로 설명할 수 있고, 그림 4-40 에 추정되는 중 간체의 구조를 나타내었다. 생성된 !(2,3,6)B ZJ를 인산화하고 보호기를 제거하여 라세미 형태의 I (l ,4,5)P3 를 높은 수율로 합성할 수 있었다 (그림 4-57, Chung 등) [63 ] •
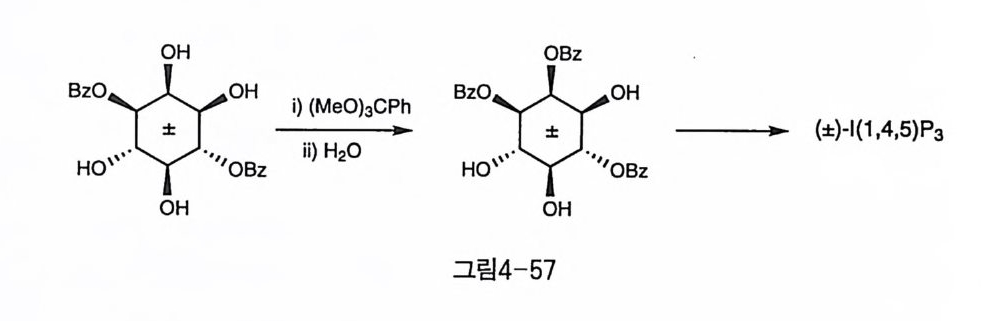 B:: 亨OH ::Z 亡 B:: 亨:O:Bz :, 一 (•)-1(1,4,S)P,
B:: 亨OH ::Z 亡 B:: 亨:O:Bz :, 一 (•)-1(1,4,S)P,
4-4-2 I ( 1, 2, 3)P3 IP가 생체 내의 라디칼 반응을 촉매하는 Fe려를 강하게 억제한다는 사실로부터, 어느 위치의 인산기가 철이온과의 결합에 중요한 역할을 담당하는지에 대한 연구가 진행되어 왔다. 그 결과, 이노시톨의 1, 2, 3 번 인산기가 Fel>와의 결합에 중요한 역할을 담당한다는 사실이 합성을 통해 증명되었다. 1(1,2)Hex에 덩치가 큰 실릴기를 도입하면 3번 수산 기에 선택적으로 실릴화되고, 남은 4, 5, 6번 수산기를 벤조일로 보호 한 후 실릴과 아세탈을 제거하여 1, 2, 3번 수산기를 개방하였다. 이 수산기들을 phosphoramidite 방법으로 인산화하여 메조형 인 1(1, 2, 3)P3 를 얻었다(그림4-58, Poyner 등)〔64〕 . 합성된 1(1,2,3)P3와 가능한 모든 IP들이 Fel>가 촉매하는 라디칼 생성 반응에 미치는 영향을 조사한 결 과, 철이온의 결합에 관여하는 1, 2, 3 인산기 주머니의 존재를 뒷받침 하였다〔37).
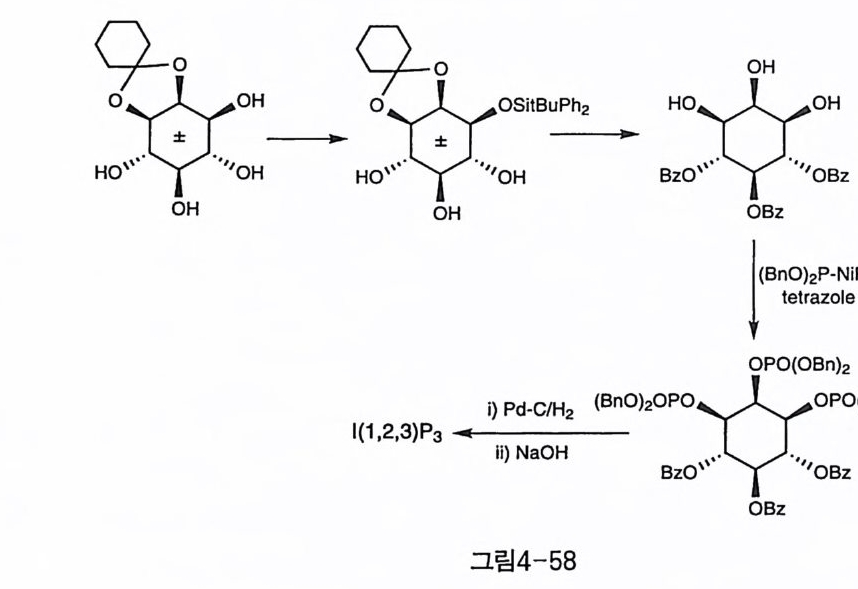 BH 00 z HOO仁OHO
BH 00 z HOO仁OHO
한편, 선택적 알킬화 반응과 산가수 분해 반응을 이용한 경로도 개 발되 었다(그림 4-59, Chung 둥) (6 회 . 1(1 , 2:4, 5)Ace2 에 1 당량의 BnBr 로 처리하면, 선택적으로 1-Bn 이 주생성물로 얻어진다. 산 조건에서 트 란스 아세탈만을 선택적으로 제거한 후, 벤조일기를 도입하여 그림 4 一 58 과 동일한 1( 4,5,6)BZ J를 합성하였다. 이 중간체를 에틸인산기로 인 산화한 후 보호기를 제거하여 I (l ,2,3)P J를 합성하였다.
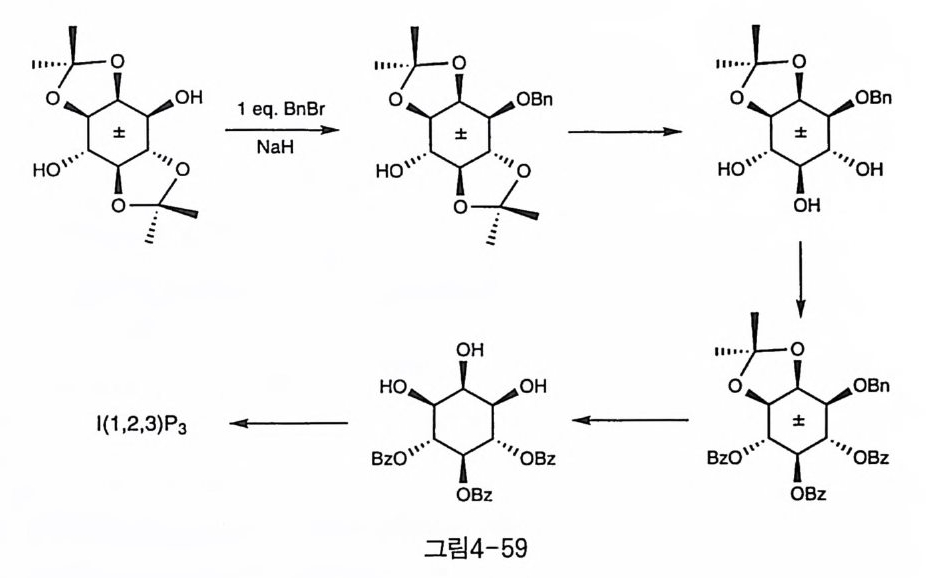 효 효
효 효
4-4-3 I ( 1, 2, 6)P3 IP 려 화학적 또는 효소 반응을 통한 가수 분해 산물로 알려진 1(1 ,2, 6)P J는 1(1 , 4, 5)P J와는 달리 세포 내 신호 전달계에는 관여하지 않지 만, 항염증 작용 및 당뇨병 치료의 가능성 등 새로운 특성을 나타내는 재미있는 화합물이다. IP, 로부터의 가수 분해 방법 외에는 화학적 합성 이 그다지 많이 알려져 있지는 않다. 선택적 벤질화를 주요 단계로 하
고 cam p hana t e 로 광학 분할하여 D-1(2,3,4)Bn J를 만들어 인산화함으로 써 1 (1,2, 6)P J를 합성하는 경로가 심포지엄 발표 형식으로 보고된 예가 있었다(그림 4-60, Gig g 등 )(66).
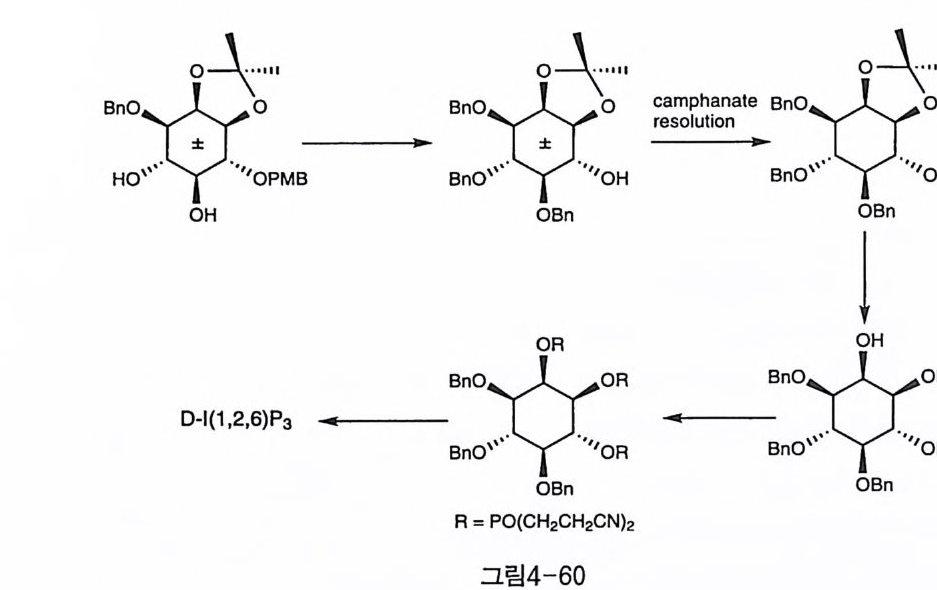 B: 〈D1 (1,2 , 6: ):PM, B一 ~: :::*:\::<: 三ca re 一一一 B字B w三O'n
B: 〈D1 (1,2 , 6: ):PM, B一 ~: :::*:\::<: 三ca re 一一一 B字B w三O'n
최근에 와서 효소를 이 용한 광학 분할을 통한 D -I(l, 2, 6)P3 의 합성 이 보고되 었다(그림 4-61, Schneid e r 등) . Inosit ol o rt ho fo rma t e 로부터 두 단계 반응으로 I(4, 6)BZ2 을 먼저 만들어 효소인 LPL 을 이용해서 vin yl bu tyr a t e 와 반응하면, D-1 번 위치에 선택적으로 B t기가 도입되 었다. 오르소에스테르 중간체를 이용해서 2 번 수산기를 아세틸로 보호 하고 나머지 수산기들을 산 조건에서 벤질화하였다. 에스테르들을 염 7, 조건에서 가수 분해하였는데, Bn 사이의 Bz 은 입체 장애에 의해 가수 분해되지 않고 유지되었다. Phosph o ram idite 방법으로 인산화하 고, 보호기를 제거하여 D-l (l ,2,6)P3 를 합성하였다〔 67). 한편, 자연에서 풍부하게 존재하는 phy tic ac i d(IP6) 를 baker's yea st
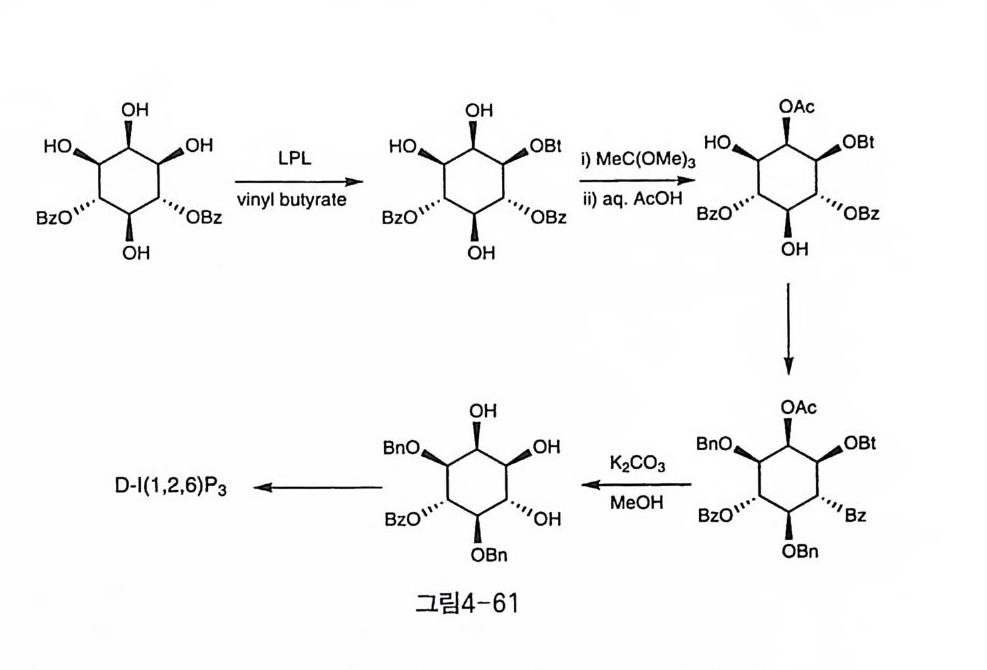 B: :틀 ::Z 三::: 三:*:::
B: :틀 ::Z 三::: 三:*:::
로 가수 분해하여 D-1 (1 ,2,6)P J를 얻는 방법도 보고되었다〔 68) . 4-4-4 I ( 1, 3, 4)P3 인산이노시톨 합성 초창기의 연구로, 알릴과 벤질을 이용한 다단계 의 보호/탈보호를 거쳐, 라세미 형태의 1Bm 중간체를 만들어 1(1 , 3, 4)P3 를 합성하는 경로가 알려져 있었다(그림 4-6 2, van Boom 등)〔 69 〕. 이때, 1( 2,5,6)B1b 의 인산화는 Cl-P(OCILCH1CN)1 를 이용한 아인산기 도입과 tB uOOH 를 사용한 산화 반응으로 진행되었다. 마지막 단계에 서는 먼저 NaOH 로 인산기의 보호기들을 제거하고, 가수소 분해 반응 으로 Bn 들을 제거하였다. 비슷한 시 7 . 1 에 Vacca 등은 앞의 과정과 거의 동일한 방법으로 1(2,5, 6)Bn3 를 만들었는데, 인산화 방법에 있어서 보다 진보된 TBPP 를 이용 하여 I (l ,3,4)P3 도 합성하였다(그림 4-63, Vacca 둥)〔 30, 70). 1(1 , 4, 5)P3 의 합성에서 알려져 있던 menth o xy ace ty l 기를 이용하는
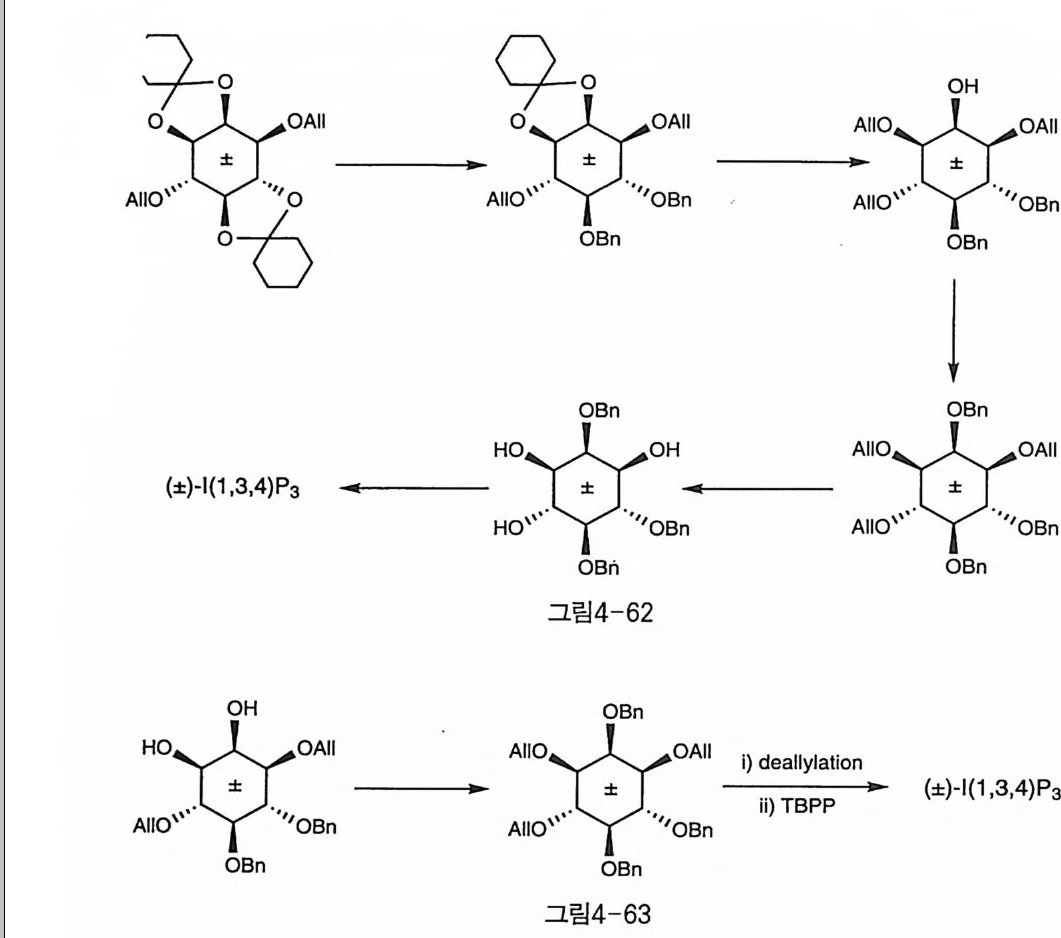 AIIO`. T >O AIIO' TOB n 'OBn 三::::::
AIIO`. T >O AIIO' TOB n 'OBn 三::::::
방법과 함께, 1, 2 번 수산기를 가진 이노시톨 유도체룰 chir alc el OD 라 는 광학 활성 HPLC 칼럼을 통해 광학 분할하는 방법으로 D-1(1 , 3, 4)P3 의 합성이 보고되었다(그림 4-64, Oza ki 등)〔 71). 라세미 형태의 1(2,5,6)Bll3 를 얻어서 아세탈 유도체룰 만든 후, cam- p hana t e 로 광학 분할하여 각각 D 와 L-1 (1 ,3,4)P3 를 합성하는 방법도 보고되 었다(그림 4-65, Prestw ich 동) [72 ). 그림 4-53 에서와 같이 men thy lcarbon y l 기를 이용한 화학적 광학 분할
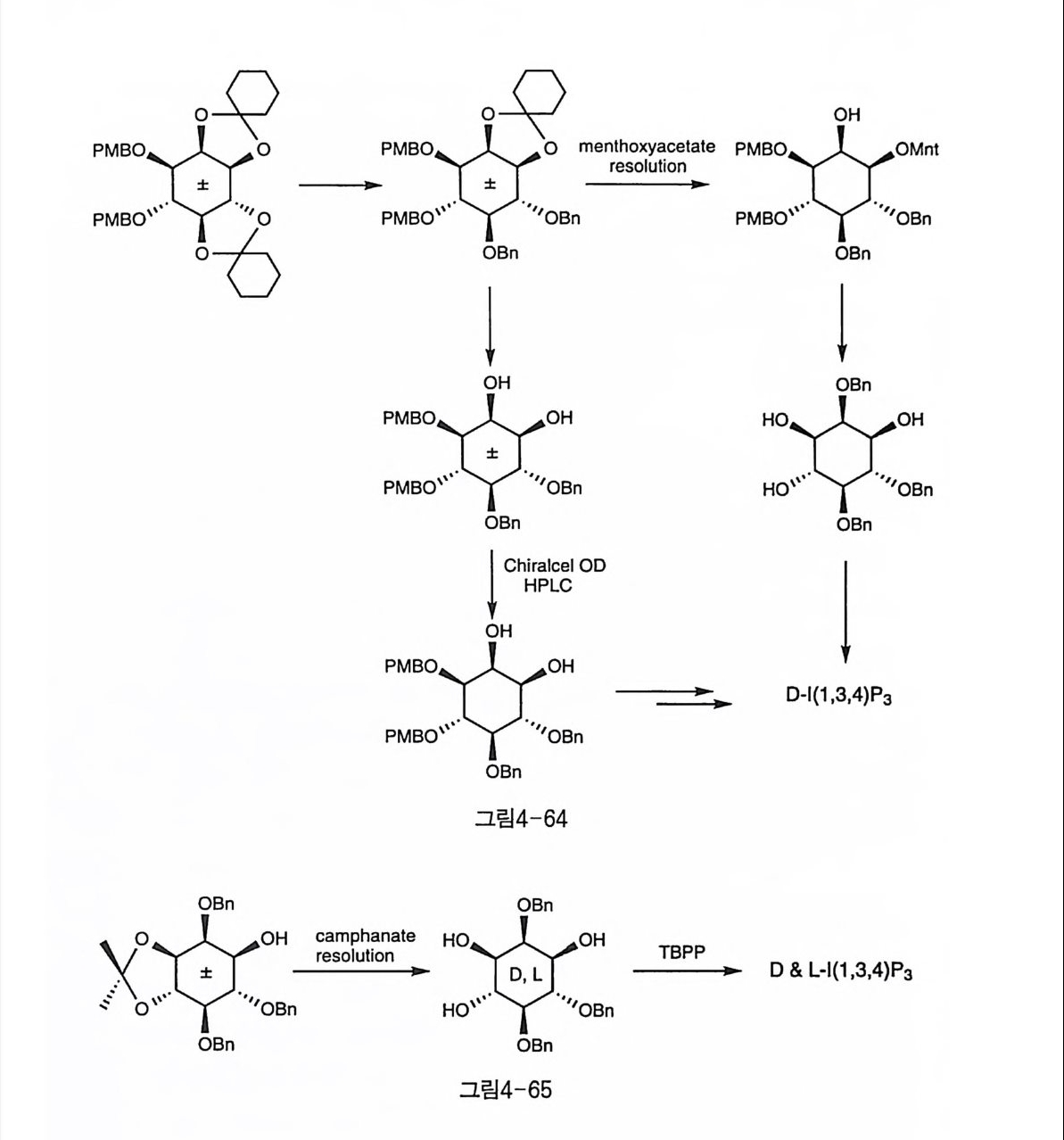 PMB 一P 三n e mg一xyaceota I e PPMM::\l]o,0B0:nntn¢oB
PMB 一P 三n e mg一xyaceota I e PPMM::\l]o,0B0:nntn¢oB
과 choleste r ol es t erase 를 이용한 효소 화학적 방법으로 광학 이성질체 를 얻어 D-1(1 , 3, 4)P37} 합성된 예도 보고되었다(그림 4-66, Chen 등)〔(i(), 7 기 광학 분할된 1,6- 디올은 알릴과 벤질을 이용한 다단계 보호/탈보호를 거쳐 D-1( 2, 5,6)Bn3 로 전환되었고, 인산화를 통해 D- I (l ,3,4)P 파 합성되었다.
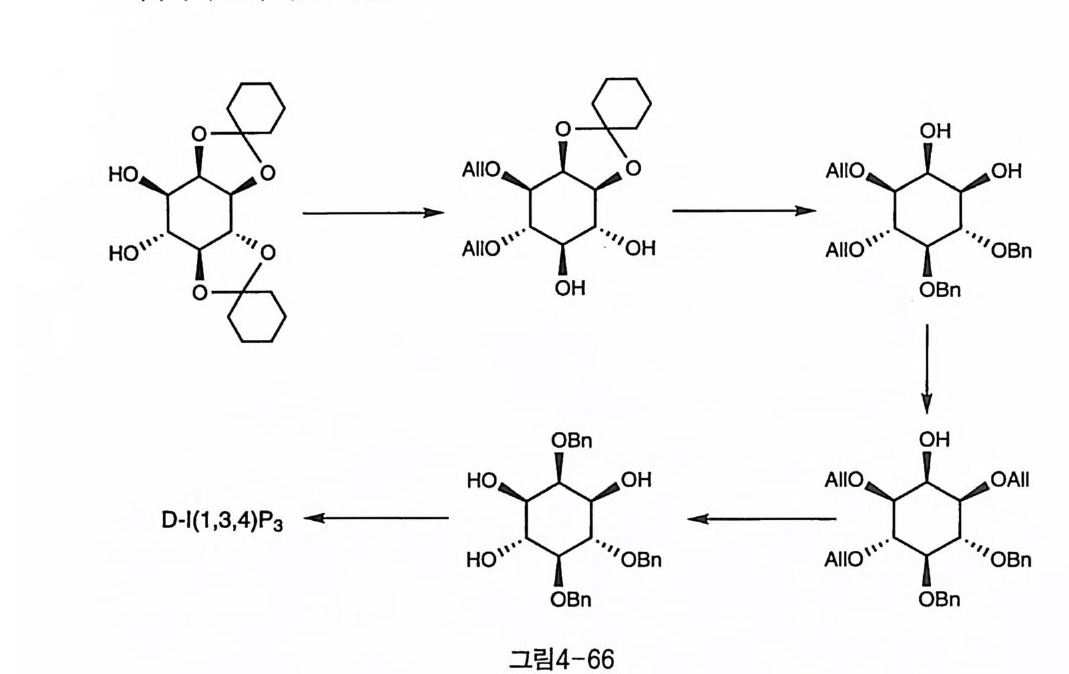 A 。 4 ’ 스\ 。 願寧 OH갤OH ¢OBn
A 。 4 ’ 스\ 。 願寧 OH갤OH ¢OBn
그런데, 그림 4-64 에서 보고된 D -1(1 , 3, 4)P J는 [a ] D 값이 -6 인 데 비해 그림 4-66 에서 만들어진 D-1 (1 ,3,4)P J는 〔 CX)D 가 +14 를 나타내었 으며, 각 D 및 L-1 (1 ,3,4)P J의 칼슘 이온 방출력에 대해서도 불확실한 점이 남아 있었다. 이에 camp ha nate 광학 분할을 통해 알려진 입체 구 조와 비교하여, 명확하게 규명된 D 와 L-1(1,3,4)P3 의 합성이 새로 시 도되었다(그림 4-67, Pott er 등)〔 74). 이렇게 합성된 두 광학 이성질체 중 D- 형태가 L- 형태보다 칼슘 분비 능력이 떨어짐이 확인되었다.
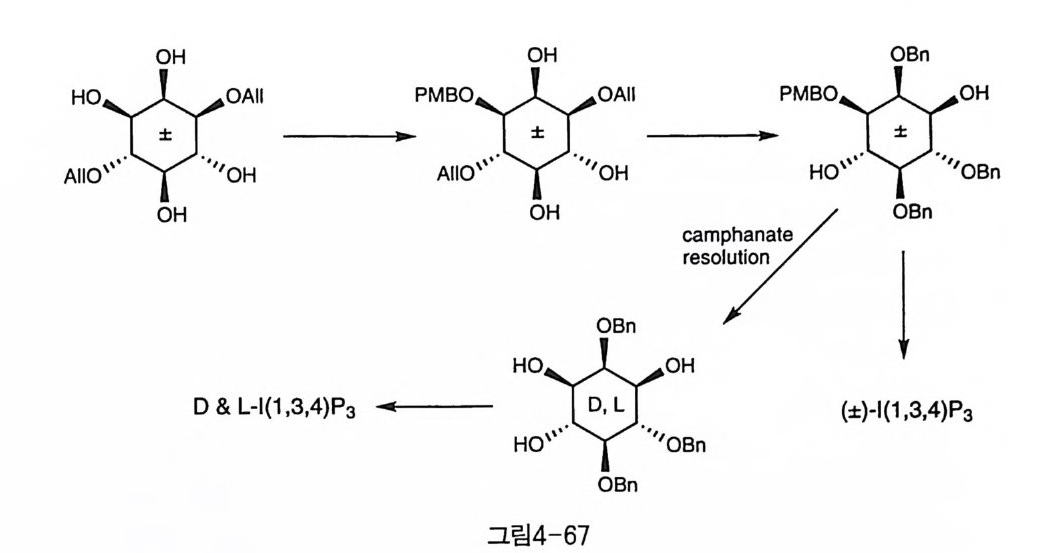 AH 。 II 亨H 一 PM:l00 亨:OH: ' 一 PM::字 OBn °0:n
AH 。 II 亨H 一 PM:l00 亨:OH: ' 一 PM::字 OBn °0:n
4-4- 4 1(1,3,5)P3 천연에서 발견되지 않은 IP) 중 하나인 1 (1 ,3,5)P) 는 이노시톨 ort ho - fo nna t e 를 중간체로 손쉽게 합성되었다 . 우선 o rth o fo nna t e 로 1, 3, 5 번 수산기를 보호한 다음 남은 세 개의 수산기를 벤질화하고, 산 조건에 서 가수 분해한 후, 인산화하여 메조 화합물인 1(1 , 3, 5)Pl 를 합성하였 다(그림 4 一 68, Vacca 등) [75 ).
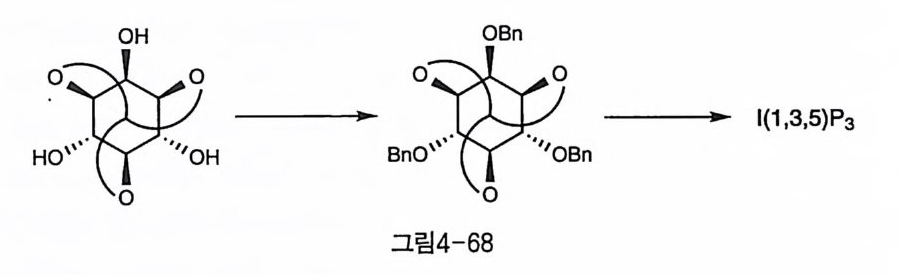 亨H 一 그Bn 림 4-68 亨n 一 ,_1` 요G,터
亨H 一 그Bn 림 4-68 亨n 一 ,_1` 요G,터
4-4—5 1( 1, 4 6)P3 I(l,4,6)P3는 1(1,4,5)P3와 유사한 모양을 가진 1P3로서, 1(1,3,4,6)P4 가 칼슘 분비 효과를 나타낸다는 것이 알려진 후 합성이 추진되어 왔 댜 첫 합성은 라세미 형태의 1(2,3,5)BnJ를 거쳐 만드는 방법으로 이 루어졌다(그림4-69, Potter 등) [76).
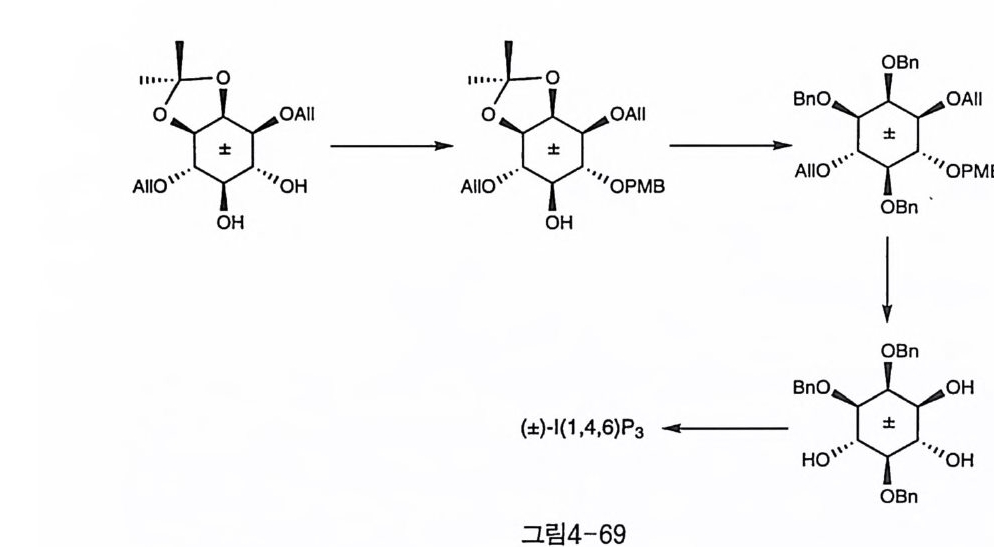 上字oAoH 一’ 00 AIIBP M 一AB0 11 AIIPM
上字oAoH 一’ 00 AIIBP M 一AB0 11 AIIPM
효소 화학적 방법으로 I(2,3)Hex을 광학 분할해서 얻고 여기에 선택 적으로 아세틸화하면, 일반적으로 1번 위치가 빠르게 아세틸화되는 것 에 비해 5번과 6번에 아세틸화된 생성물이 1:1 정도의 비율로 얻어진 다. 이 경우 일반적인 염기 대신에 4A 분자체를 사용하고, 흔히 사용 하는 DMF 대신에 DMA(dimethylacetamide)를 용매로 사용한 것이 주 목할 만하다. 이때 5번에 아세틸화된 중간체를 분별 결정으로 분리해 내 바로 인산화하여, 각각 라세미, D, L-l(l,4,6)P3를 합성할 수 있었 다(그림4-70, Ozaki 등) [77]•
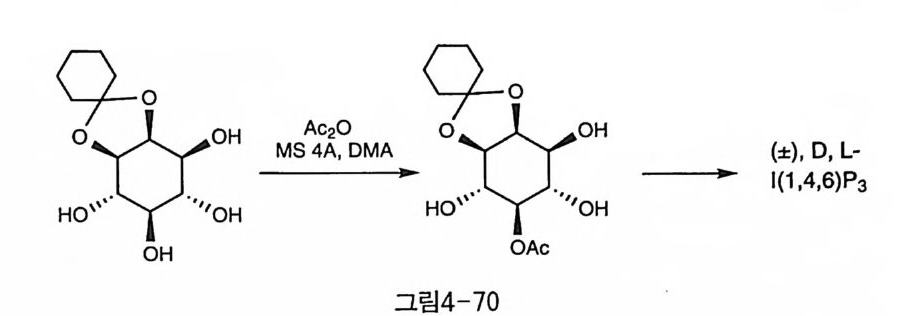 9H: 亨-:0O H : 三 9:0`-亨 。:O A:c :
9H: 亨-:0O H : 三 9:0`-亨 。:O A:c :
4-4-6 1(1,5,6)P3 PI(3,4,5)P J가 세포 내에서 발견되면서, 그 생리 활성을 밝히는 연구 와 함께 그 합성도 시도되고 있다. 이 과정에서 D-1( 3, 4,5)P3(L-I(1 ,5 , 6)P3) 가 함께 합성되었다. 그림 4-52 에서 qui n ic a ci d 로부터 출발하여 만들어진 중간체를 활용하여, D-PI(3,4,5)P3 및 D - 1(3,4,5)P의 합성 울 나타내었다. DDQ 등의 산화제를 이용하여 쉽게 제거할 수 있는 3, 4-d i me th ox y benz y l 기가 1 번 수산기를 보호하는 데 사용되었다(그림 4- 71, Falck 등) [78 ). 4-4-7 1(2, 4, 5)P3 1 (1 ,4,5)P 라 유사한 구조를 가지며, 약하지만 칼슘 분비에 관여하는 것으로 알려진 이 분자의 합성도 일찍부터 시도되어 왔다. 라세미 형 태의 합성은 이미 1987 년에 처음 보고되었는데, 몇 단계의 알려진 반 응을 거쳐 만들어진 I (l ,3,6)B1b · 를 인산화하는 방법이 사용되었다(그림 4-72, Vacca 등) [30 ,7 0] • 광학 활성을 가진 D- 1(2, 4,5)P J의 합성은 Oza ki 등에 의해 이루어졌 는데, D-1(1 , 4, 5)P3 와 함께 그림 4-41 에 그 합성 과정을 나타내었다 [34 ] . 벤젠으로부터 유래된 cond urit ol 을 이용한 라세미 I(2, 4 ,5)P~ 합
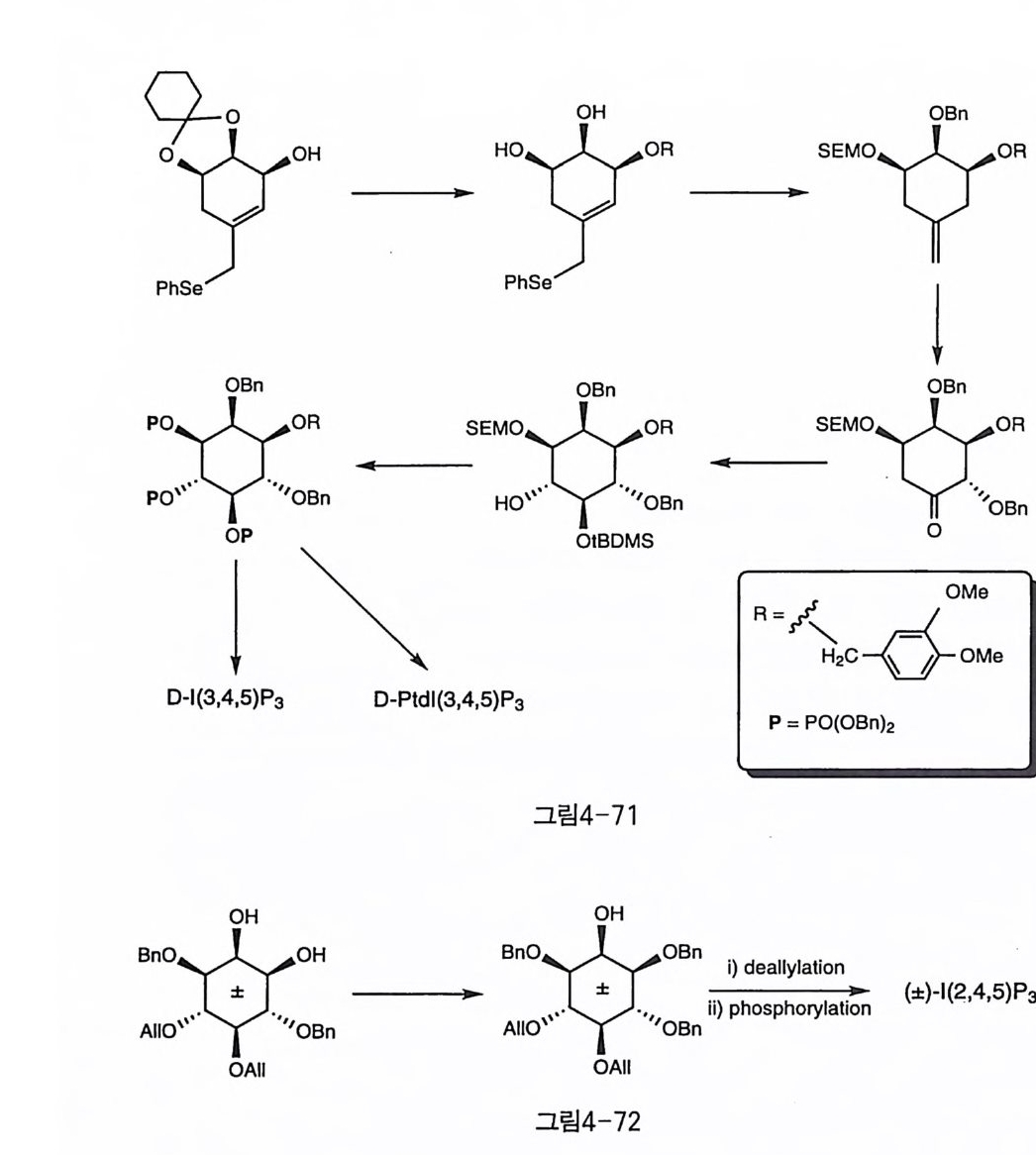 p 0 OOBnp¢j- S E::i s::n R =二二/~C- 0-j OBnOB仁OVn 0MMe e
p 0 OOBnp¢j- S E::i s::n R =二二/~C- 0-j OBnOB仁OVn 0MMe e
성도 그림 4-48 에 나타내었다〔 45 〕 . 한편, 그림 4_51 에 표기한 대로 D 및 L-ch i ro- in os it ol 로부터 출발하여 각 광학 이성질체인 1( 2,4,5)P3 를 합성하는 예도 보고되었다〔 79).
4-4一8I (2, 4, 6)P3 Chung 동은 이 노시 톨 orthofonnate 중간체 를 직 접 인산화 반응시 켜 쉽게 1(2,4,6)P3를 합성하였다. 단지 이 경우 흔히 사용되는 DPPC를 사용했을 경우에는 인산화 반응이 제대로 진행되지 않았고, phosphite 방법을 사용했을 때 높은 수율로 생성물을 얻었다(그림4-73, Chung 등)〔63〕.
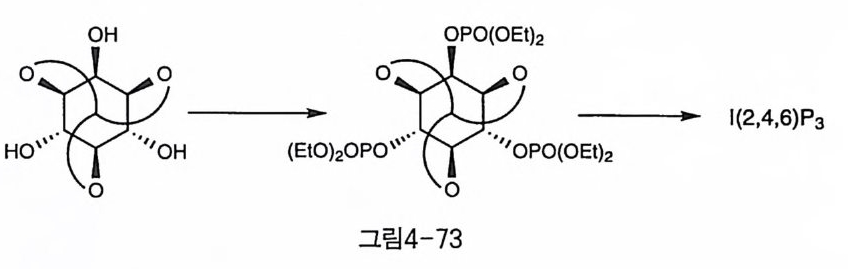 亨H 一g 。L 。그P 림00 4-73
亨H 一g 。L 。그P 림00 4-73
4-4-9 I (4, 5, 6)P3 천 연 에 서 알려 지 지 않은 메 조상의 1(4, 5, 6)P3가 1(1, 4, 5)P3와 함께 합성되었으며, 금속과의 결합 및 이온화 특성이 연구되었다(그림4-74, Spiess 등) 〔8이 . 4-4-10 I(1,2)cP(4,5)P2 유일하게 보고된 D-l(l,2)cP(4,5)P2의 합성을 그림4-41에 나타내었 다〔34). 이 화합물은 PLC 효소에 의한 1차 생성물이며, D-l(l,4,5)P3 및 D-1(2,4,5)P3의 전구체일 것으로 추측되어 관심을 끌었던 분자이 댜 실제로 이 분자롤 염기 조건에서 가수 분해했을 때 D-I(l,4,5)P3 나 D-1(2,4,5)P3가 얻어지는 것이 확인되기도 하였다.
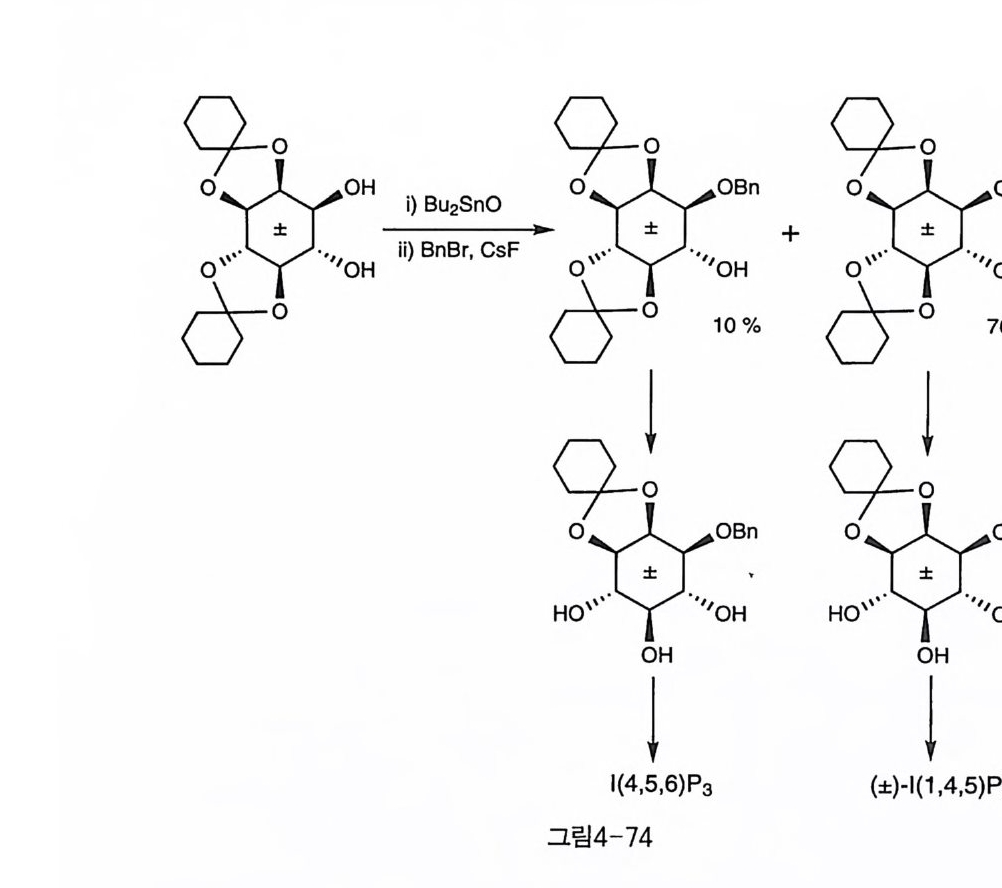 i) Bu2Sn0
i) Bu2Sn0
4-5 사인산이노시톨 4-5 기 | ( 1, 3, 4, 5)P4 1(1 , 4,5)P3 대사의 중요한 경로 중 하나로서, 3 급기나제에 의해 3 번 수산기가 인산화되면 1(1 , 3, 4, 5)P4 가 형성된다. 이 JP 4 는 단순한 대사 물질일 뿐만 아니라 세포 외의 칼슘을 세포 내로 유입하는 데 관여하 는 새로운 2 차 전달 물질일 것임이 제안되어 다양한 경로의 합성이 보 고되었다.
초기 의 합성 에 이 노시 톨 orthoformate를 활용한 예 들이 있었다. 이 노 시톨 orthoformate에 강염기 조건에서 알킬화 반응을 시도하면, 오르소 에스테르에 의해 의자 형태가 반전된 이노시톨 고리에 의해 수직 방향 으로 배향된 4 또는 6번의 수산기가 먼저 알킬화된다는 것이 밝혀졌 댜 이러한 성질을 이용하여, 4번 수산기를 알릴〔31) 또는 benzy-loxymethyl기로(70) 먼저 보호하고 남은 두 개의 수산기를 벤질화한 후 다른 보호기들을 제거하면 1(2, 6)Bn2가 얻어진다. 이 중간체에 TBPP를 이용하여 인산화하여 라세미 형태의 1(1,3,4,5)P4가 합성되었 다(그림4-75, Vacca 등) [27].
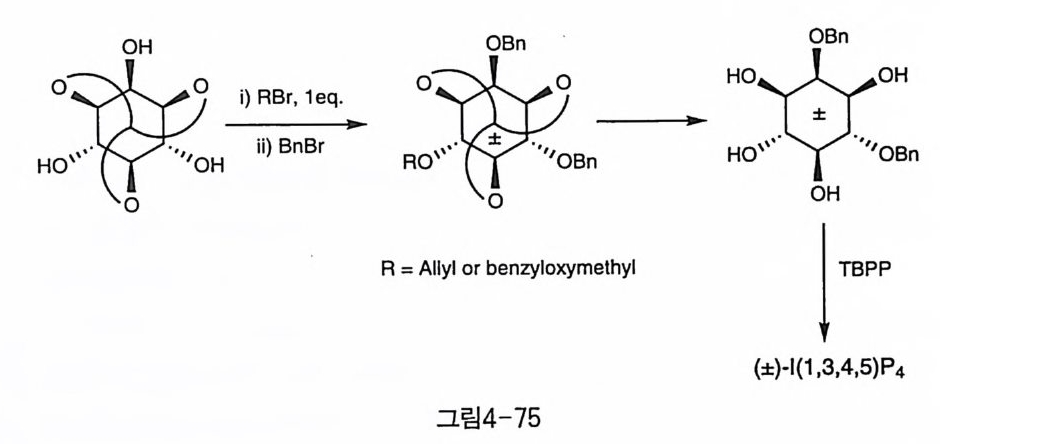 R 亨B n 一0 OjB nn: OH
R 亨B n 一0 OjB nn: OH
Orthofonnate를 이 용한 광학 활성 합성도 보고되 었다. 덩치 가 큰 실 릴기로 먼저 2번 수산기를 보호한 후 남은 두 개의 수산기를 butyrate 로 보호하고, 효소 PLE(porcine liver esterase)를 이용한 선택적 가수 분 해 반응을 이 용하거 나 1-phenylethyl carbamate를 이 용하는 방법 이 모 두 시도되었다. 두 경우 모두 몇 단계를 거쳐 D, L-1(2,6)B11z·를 생성 시켰고, phosphoramidite 방법으로 인산화하여 I(l,3,4,5)P4의 두 광학 이성질체가 합성되었다(그림4一76, Vasella 등)〔81).
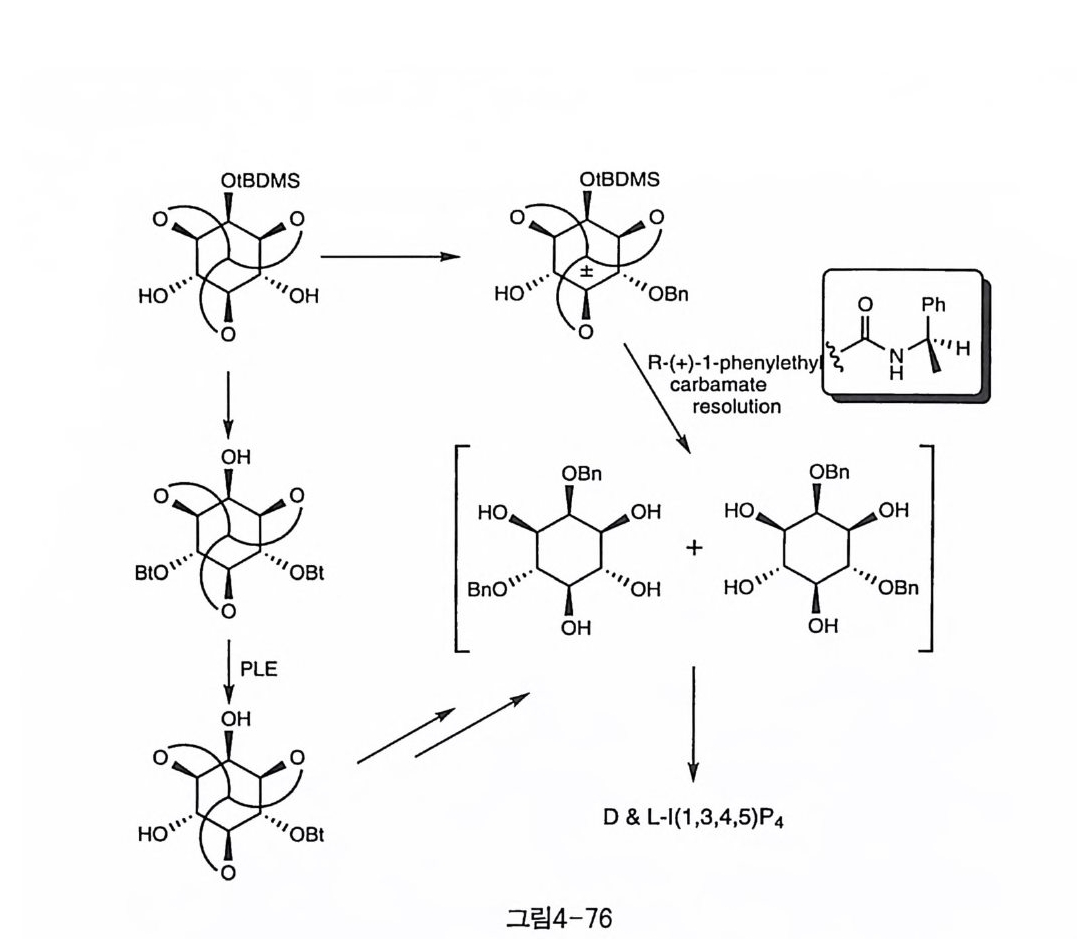 HO字H-OO> EtBL> OH/l 一 / _B H H그00 림n 4- 亨oHOBn7O 亨g6o ' OH0M〉露 \oH 입 `n曺o res+ 土g P hte向e玉 maoOHOBn 〉 lU」HOHO4p h ’ H `n
HO字H-OO> EtBL> OH/l 一 / _B H H그00 림n 4- 亨oHOBn7O 亨g6o ' OH0M〉露 \oH 입 `n曺o res+ 土g P hte向e玉 maoOHOBn 〉 lU」HOHO4p h ’ H `n
Men th ox y ace ty l 기를 활용하는 광학 분할로 D-I (l ,3,4,5)P 를 합성한 경 로도 보고되 었다. I (l, 2 :4, 5)Hex 2 의 3 번 수산기 를 benzoy l imida zole 울 사용하여 선택적으로 벤조일화하고, 산 조건에서 6 번 위치를 벤질 화하였다. 트란스 아세탈을 선택적으로 가수 분해한 다음 벤조일화하 고 열려진 1, 2 번 수산기 중 1 번에 선택적으로 men th ox y ace ty l 기를 도 입함으로써 광학 분할하였다. 다시 산 조건에서 2 번 위치를 벤질화한 다음 아실기들을 제거하여 D-!( 2, 6)Bn2 를 만들 수 있었다. 탄수화물 화학에서 중요한 위치 선택적 반응을 잘 활용한 전형적인 예라 할 수 있다• mm 를 TBPP 로 인산화하여 D-I(l , 3, 4, 5)P4 를 얻었다(그림 4- 77, Ozak i 등) [82 ).
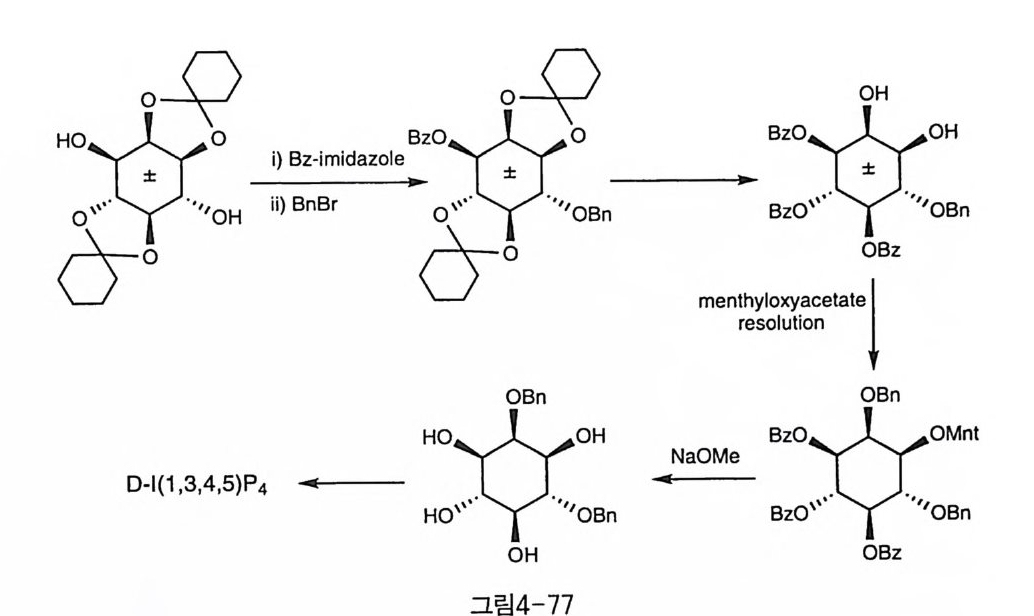 ii) BnBr ,....,. ...._,,, ''no~ Bzo'· T ''OBn
ii) BnBr ,....,. ...._,,, ''no~ Bzo'· T ''OBn
곧이어 네덜란드 연구자들도 rnenthoxyacetyl기를 이용한 또다른 합 성 경로를 보고하였다(그림4-50). 이때는 D-1(2,6)B112 중간체를 phos-phoramidite 방법으로 인산화가 수행되었다〔56〕. 라세미 1(1, 4)Bz2를 만들어 인산화하면 I(l, 2, 4, 5)P4가 얻어지고, 염 기 조건에서 아실 이동 반응을 유도하면 트란스 방향보다 시스 방향의 벤조일 이동이 우세하여 1(2,4)Bz2가 얻어진다. 이렇게 얻어진 IB21.를 메틸인산기로 인산화한 후, HBr과 염기를 써서 차례로 보호기를 제거 하여 I(1,3,4,5)P4를 합성하였다(그림4-78, Meek 등)〔53). 이노시톨에 직접 다수의 벤조일기를 도입하는 방법이 시험되었는 데, 3.5당량의 BzCl를 피리딘 조건 하에서 반응시켰을 때 1(1,3,4, 5)B瓦가 34%의 수율로 얻어졌다. 남은 두 개의 수산기를 벤질화하고 벤조일을 제거한 후 인산화하여 짧은 경로로 라세미 I(l,3,4,5)P4를 합 성 할 수 있었다(그림4-79, Ozaki 등) [83).
그림4-42에서 나타낸 것처럼 I(1,3,5)BZ3를 이용한 D-I(l,3,4,5)P4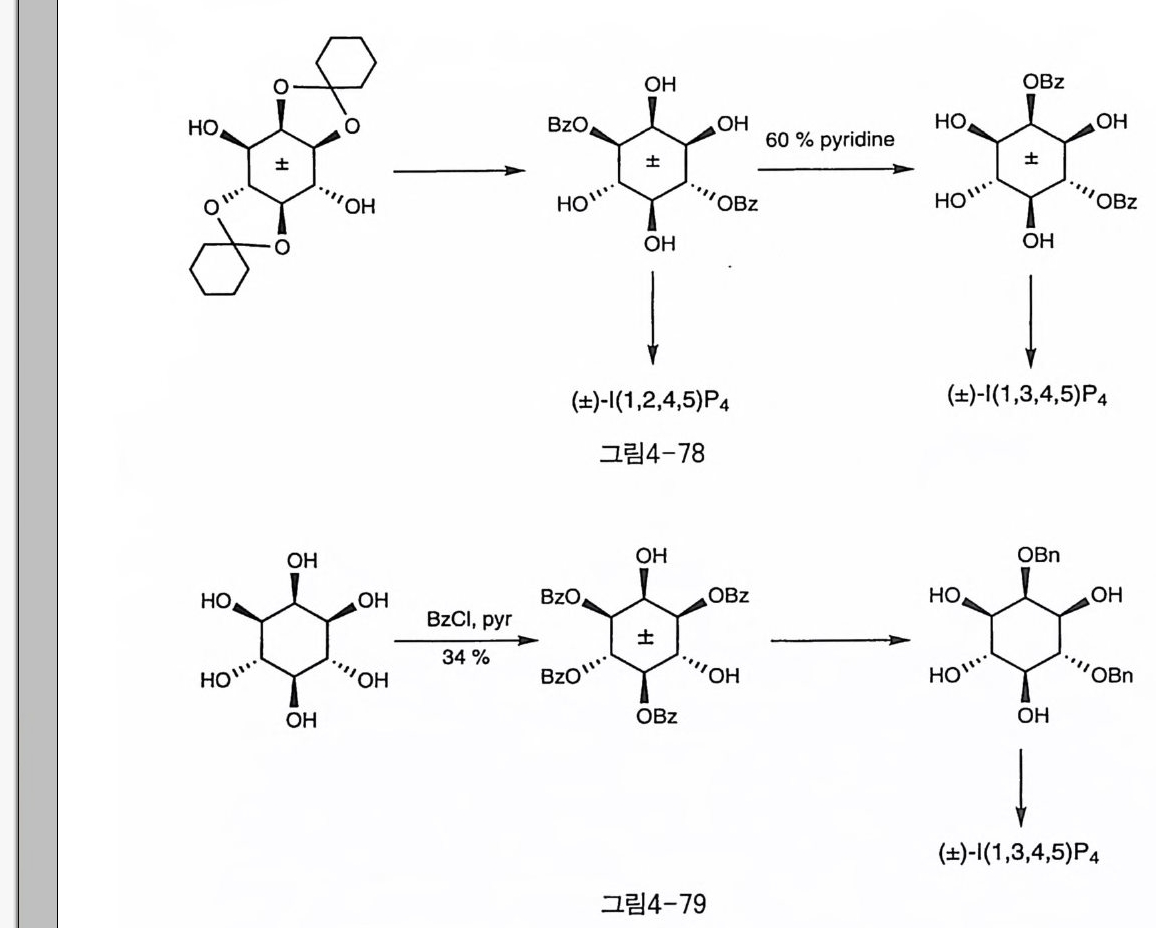 B:: 亨OH ::Z二 ::<::Z
B:: 亨OH ::Z二 ::<::Z
의 합성도 이루어졌다〔 48 〕 . 같은 연구자들은 tartr a t e 가 도입된 중간체 에 실릴기 대신에 벤질기를 도입하여, D-I(2,6)Bn2 를 거쳐 D-1(1 , 3,4, 5)P 를 만드는 방법도 보고하였다〔 84 〕. 그림 4-53 과 그림 4-66 에서 얻어진 광학 이성질체 역시 D-1(1 , 3,4, 5)P, 의 합성 에 이 용되 었다(그림 4-80, Chen 등) [ro ,7 3] ·
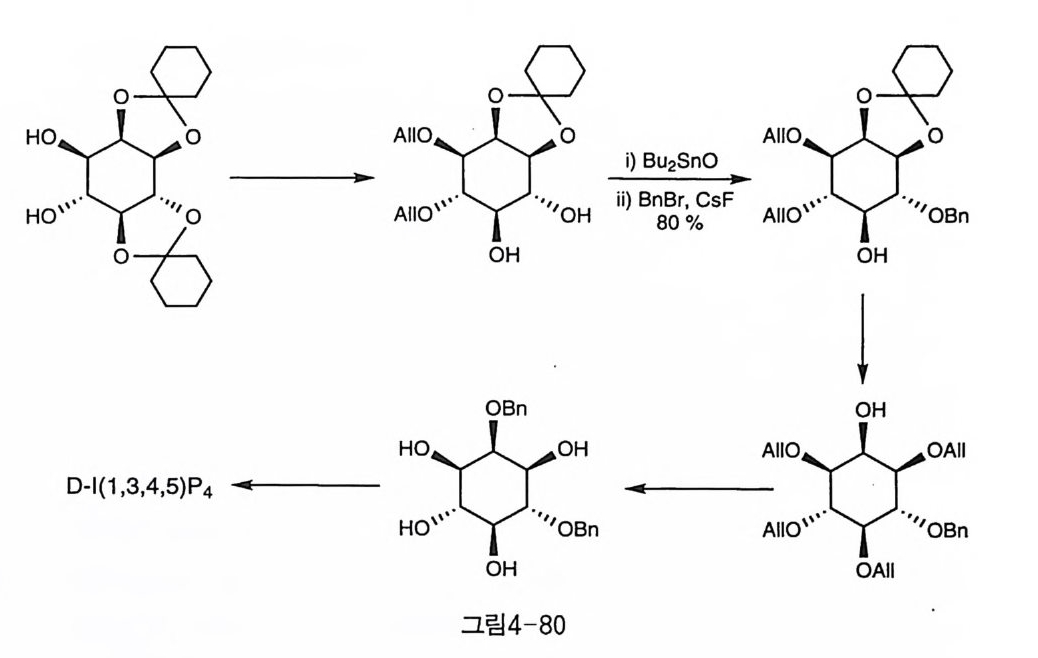 HO..,. .,J..._ _.O -.. AIIO`No ~.. A110
HO..,. .,J..._ _.O -.. AIIO`No ~.. A110
4-5-2 I ( 1. 2, 4, 5)P4 I(I,4,5)P3의 2번 위치가 인산화된 I(l,2,4,5)P4는 I(I,4,5)P3와의 구조 적 유사성으로 인해 칼슘 분비 등의 생리 활성을 가질 것으로 기대되 었댜 최초의 합성은 1(3,6)Bzz를 중간체로 하여 라세미 형태로 이루어 졌다(그림4-78, Meek 등) [53).
그림4-48에서 벤젠을 산화하여 얻어진 conduritol을 중간체로 라세 미 I(I,2,4,5)P4가 합성된 경로가 보고된 바 있었다〔45〕• I(I,2,4,5)P4의 생리 활성이 I(l,4,5)P3와 유사함이 알려지면서, 그림 4-78와 바슷한 경로이긴 하지만 isopropylidene 중간체를 이용한 합성 과 그 생리 활성에 대한 결과가 보고되기도 하였다(그림4-81, Potter 둥)〔85).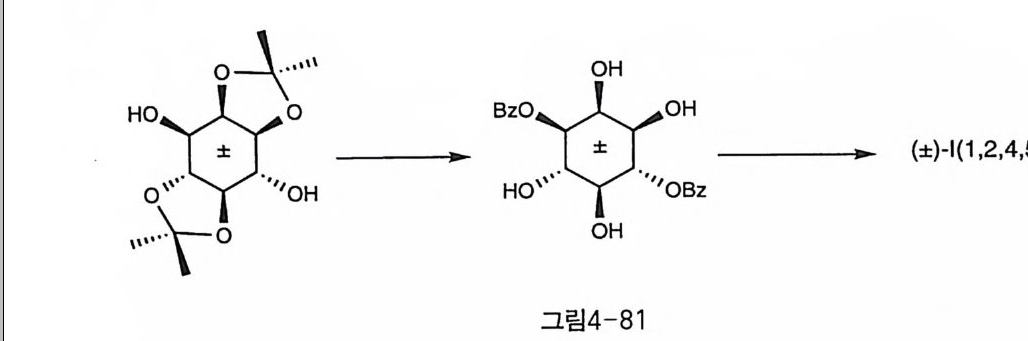 (士 )-1(1,2 ,4 ,S)P4
(士 )-1(1,2 ,4 ,S)P4
4-5-3 I ( 1, 3, 4, 6)P4 이노시톨을 트란스 관계의 이웃한 디올을 보호할 수 있는 TIPS 와 반응시키면 I (1 ,6 ; 3,4)TIPS2 가 얻어진다. 남은 두 수산기를 벤조일화하 고 TIPS 를 제거한 후 인산화하여 메조 형태의 1 (1 ,3 , 4,6)P4 가 합성되었 다(그림 4-8 2, Ozak i 동)〔 32).
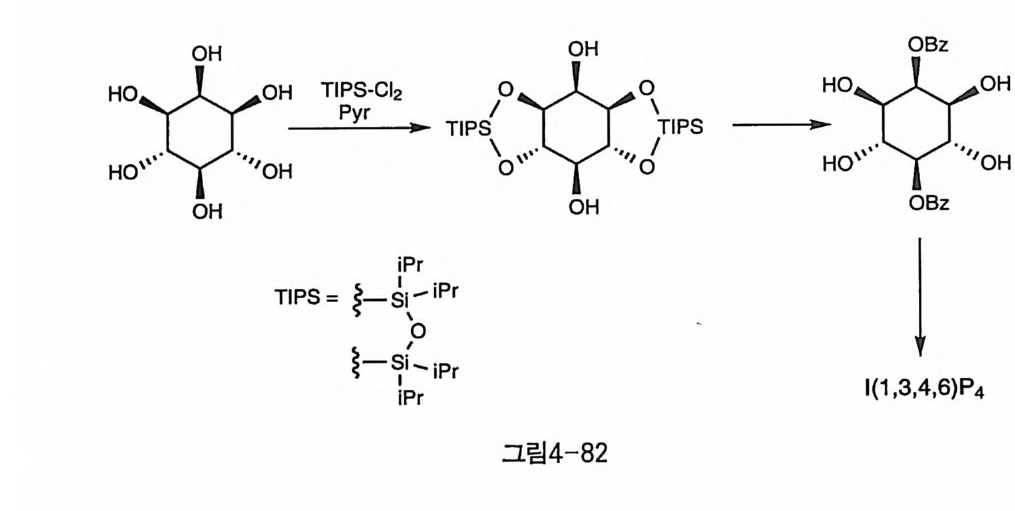 따YOHgTI P S = t~二--s한iIPPt: oir-r i PPrT r P s 따了oH T IPs 一 g 1(1,3,o4j ,B6 )Pz4: O守H Bz
따YOHgTI P S = t~二--s한iIPPt: oir-r i PPrT r P s 따了oH T IPs 一 g 1(1,3,o4j ,B6 )Pz4: O守H Bz
4-5-4 I ( 1, 4, 5, 6)P4 최초의 합성은 1( 2,3)Ace 를 직접 인산화하여 라세미 형태로 이루어 졌다(그림 4-83, Meek 등 )(53) .
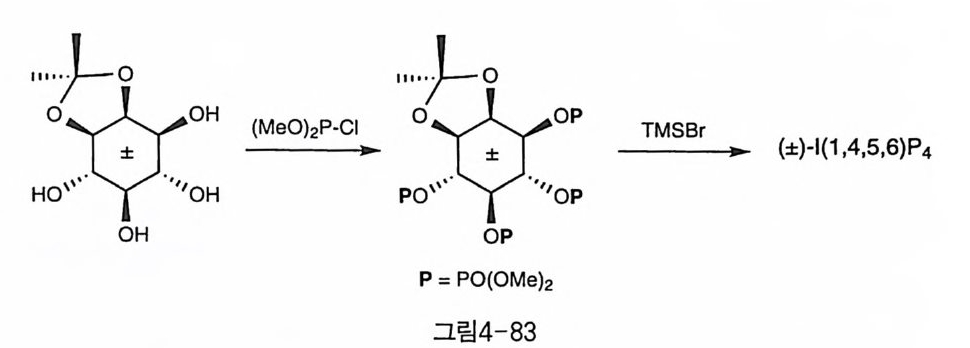 上〉H 00 H三H ” °P') 그=- 림P0O。 4(O- 8M3e:) 2
上〉H 00 H三H ” °P') 그=- 림P0O。 4(O- 8M3e:) 2
광학 활성을 가진 D-1 (1 ,4,5,6)P4 의 합성은 D-camp ho r 아세탈을 이 용하여 이루어졌다. 같은 방법으로 L-cam p hor 를 사용했을 경우 L- 1(1,4,5,6)P4 도 합성되었다(그림 4-84, Bruzik 등 )(24 〕 •
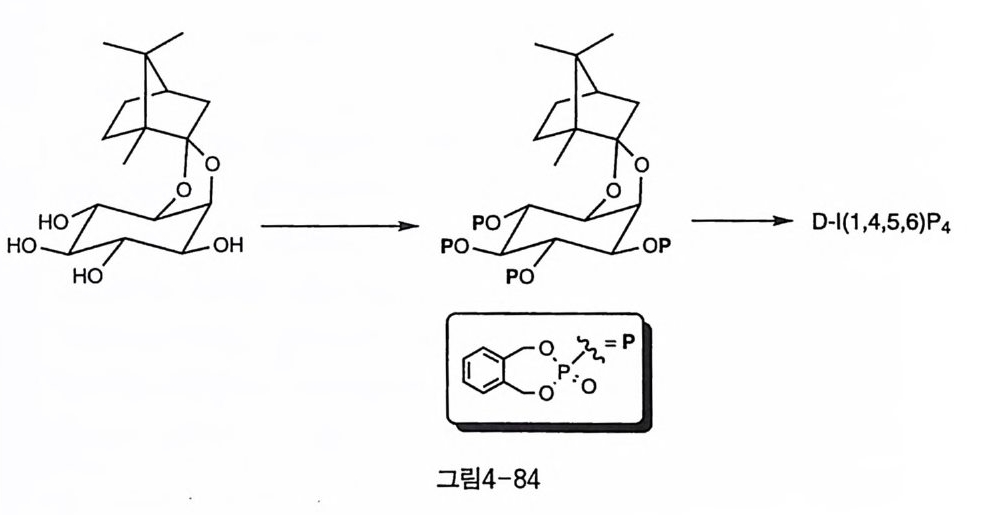 PO- J.---r--1-0P
PO- J.---r--1-0P
효소를 이용한 광학 분할을 통하여 각각 D와 L-I(l,4,5,6)P4를 합성 하는 경로도 개발되었다(그림4-85, Ozaki 등)〔86). 이 광학 분할 생성 물은 그림4-70에서 활용된 바 있다.
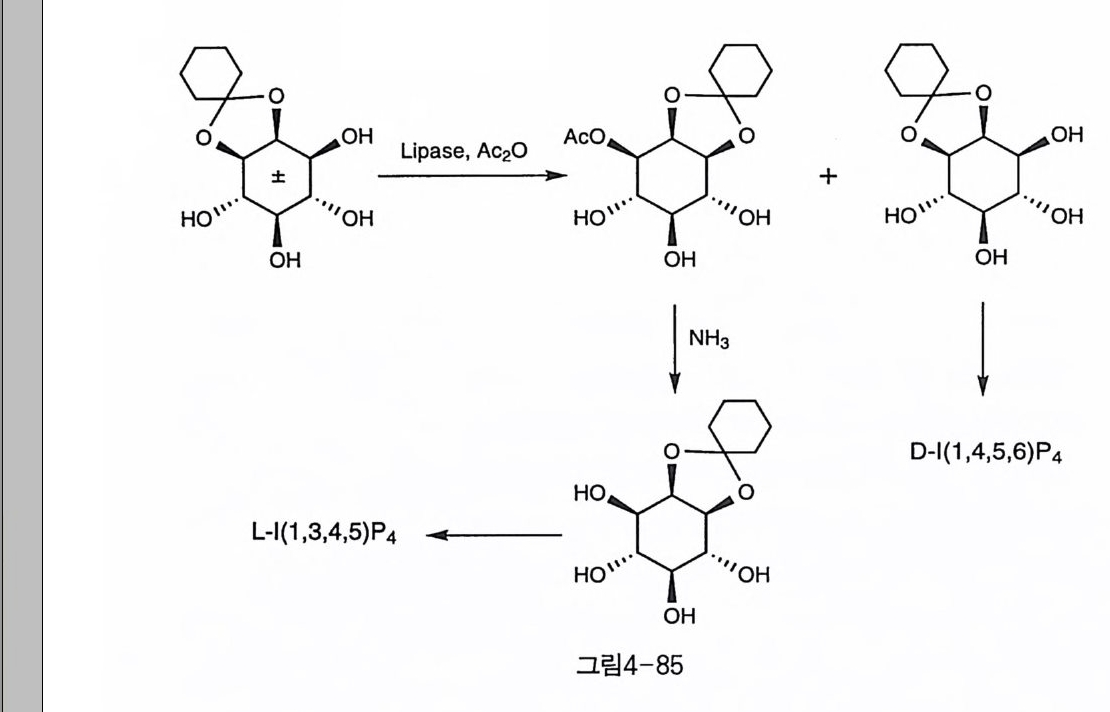 oHoH- 一_A00三C H OH二〉曺00 HH
oHoH- 一_A00三C H OH二〉曺00 HH
IO,4,5,6)P4의 생체내 활성이 연구되면서 세포막을 통과할 수 있는 친지질성 유도체도 만들어졌다. 수산기들은 부티릴기로 보호되고 인산 기들은 acetoxymethyl기로 보호된 유도체는 세포막을 쉽 게 투과할 수 있을 것으로 예상되고, 세포 내에서 여러 가수 분해 효소에 의해 아실 기가 제거되면 이온 상태의 1(1,4,5,6)P4를 유리할 수 있도록 설계되었 댜 광학 분할은 camphanate를 통해 이루어졌으며, 각각의 광학 이성 질체가 이온형 및 세포막 투과형으로 만들어졌다(그림4-86, Schultz 등)〔얽〕.
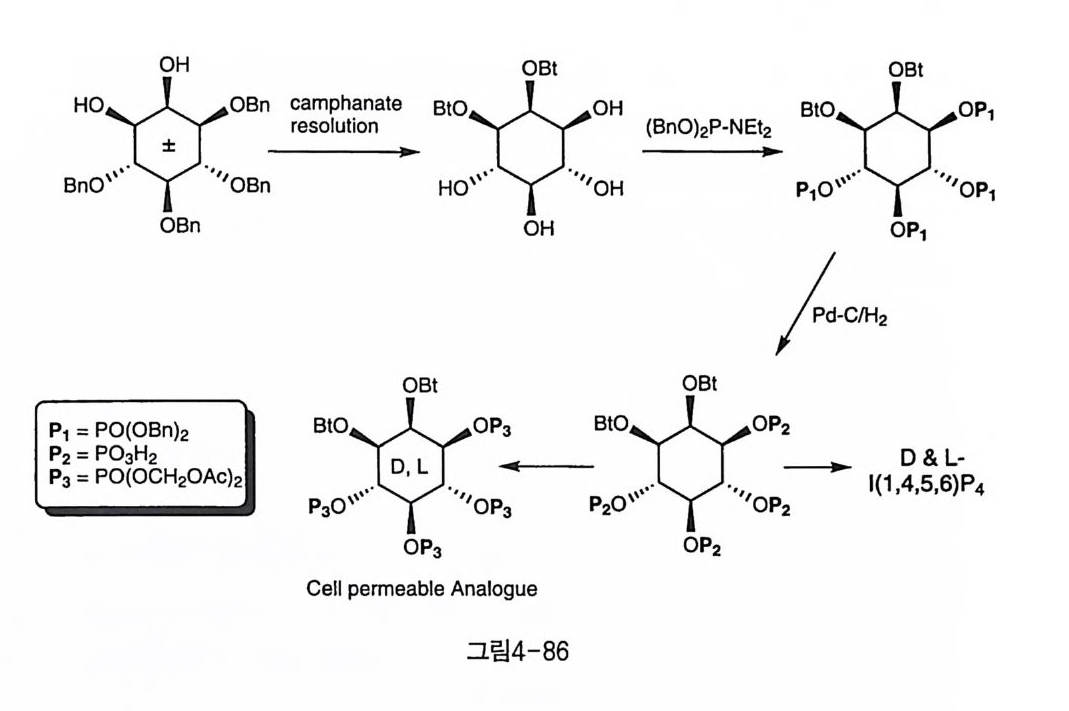 B:O:Bn :三 ::OH :三 :::¢O:P1 :::
B:O:Bn :三 ::OH :三 :::¢O:P1 :::
4-6 오인산이노시톨 IP 나 IP 예 비해 IP5 는 오랫동안 그다지 주목을 받지 못하였으나, 최 근 들어 그 생리 활성에 대한 연구가 점차 활기를 띠고 있다. IP 는 다른 인산이노실에 비해 보고된 합성의 예도 그다지 많지 않 은데, 오래된 예로서 라세미 상태의 IBn 에 N-benzoy lp h o sph o ram idic a ci d 로 인산화하여 1 (1 , 2,4,5,6)Ps 와 1 (1 ,2,3,4,5)Ps 가 합성된 바 있었다 (그림 4-87, Ang yal 등) [88 ] . 최근 이노시톨 오르소에스테르의 2 번 위치를 선택적으로 벤조일화한 중간체를 통하여 1 (1 ,3,4,5,6)Ps 가 합성된 예가 보고되었다(그림 4-88, Ozak i 등) [89 ] ·
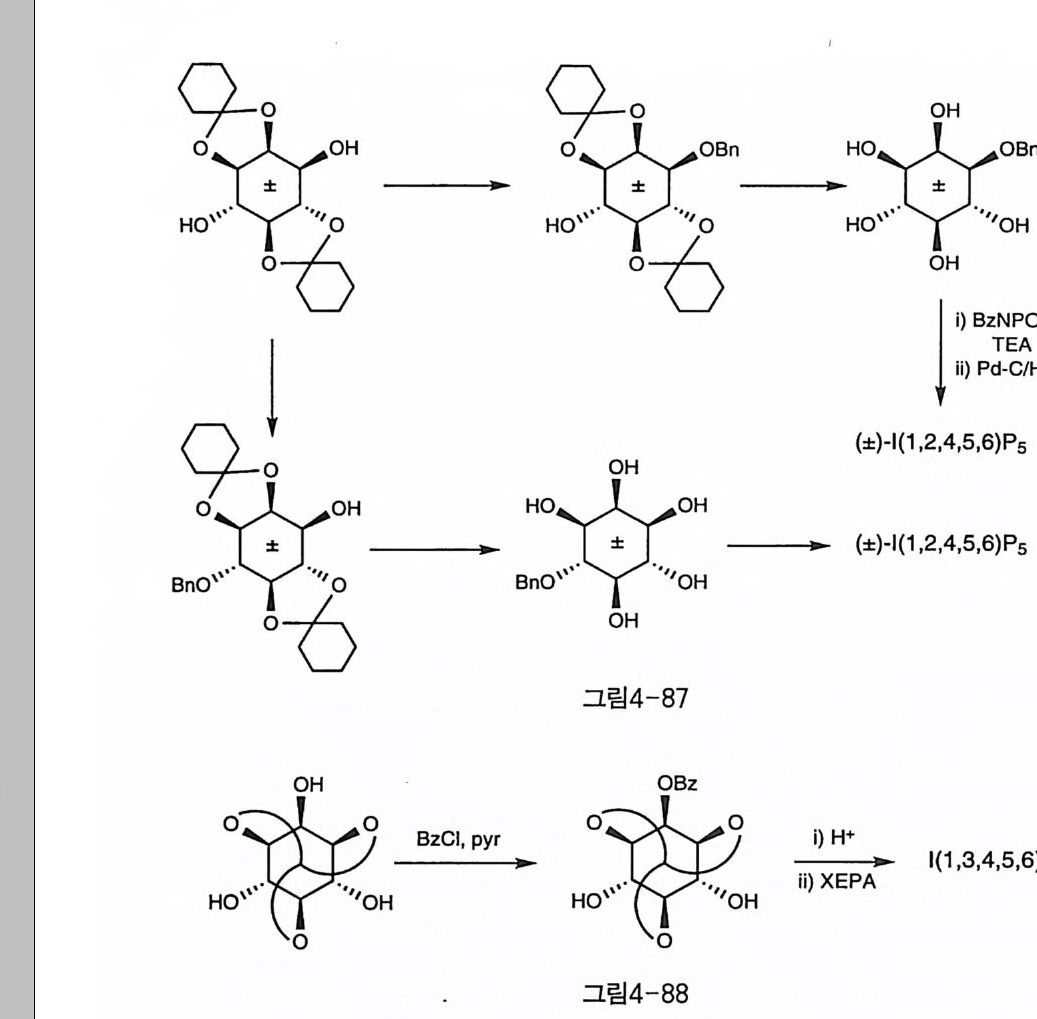 » H0` T .'0 H
» H0` T .'0 H
4-7 발산적 방법에 의한 인산이노시톨 합성 지금까지 牛J에서 살펴 본 인산이노시톨의 합성은, 각각의 화합물을 합성하는 데 별개의 합성 경로를 거쳐 개발하는 전통적인 유기 합성 방법이었다. 합성의 목표가 되는 화합물의 숫자가 적은 경우에는 선택
적인 단일 합성 경로를 개발하는 것이 매우 효율적인 방법일 수 있다. 그러나, 자연에서 존재하거나 생리 활성이 있다고 보고된 인산이노 시톨의 숫자는 점점 늘어가는 추세이며, 따라서 합성의 목표가 되는 화합물의 숫자도 늘어나고 있다. IP1 에서 IP6 까지 존재 가능한 인산이 노시톨의 숫자는 모두 63 개이며 라세미 형태로는, 39 개(그림 4-89) 인 데, 현재까지 자연에서 존재가 확인된 것은 그 절반에 약간 못미치고 있으며, 합성은 절반올 조금 웃돌고 있다. 한편 각각의 합성은 별개의 화학 연구진에 의해 수행되었기에 통합된 생리 활성의 연구에는 제한 이 따를 수밖에 없었다. 뿐만 아니라 각종의 인산이노시톨과 반응하는 수용체나 효소를 대상으로 길항제나 억제제를 개발하기 위해서는 기하 적 구조가 잘 정의된 인산이노시톨 이성체와 이들 단백질간의 결합 친 화도를 이해하는 것이 필요하다. 그리하여, 가능한 모든 인산이노시톨 을 합성할 수 있는 체계적인 합성 경로의 연구가 요구된다.
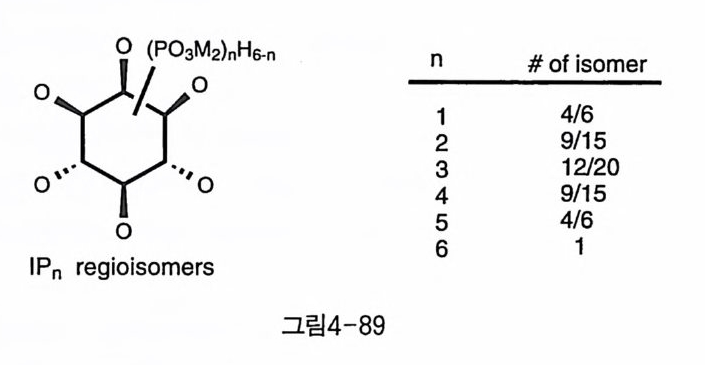 n #of iso mer
n #of iso mer
인산이노시톨 합성에 있어서의 중요한 문제점 중 하나는 인산기 도 입을 위한 적절한 중간체를 만들 수 있어야 한다는 것이다. 죽, 인산 기가 도입될 자리에는 자유 수산기가 남아 있어야 하며, 나머지 자리 는 적절하게 보호되어야 한다. 이러한 보호기들은 인산기 도입 반응 중에는 안정해야 할 뿐만 아니라, 마지막 、 단계의 탈보호 반옹에서는
쉽게 제거되는 특성이 요구된다. 이러한 조건을 만족하는 보호기로서 가수소 반응으로 쉽게 제거되는 벤질기나 가수소 반응중에 생성되는 인산에 의해 제거될 수 있는 아세탈 등의 보호기가 선호되었다. 한편 으로는, 염기 조건에서 제거될 수 있는 아세틸이나 벤조일기도 널리 사용되었다. Meek 등은 l (1 ,4)Bzz 가 염기 조건에서 벤조일기 이동 반응을 일으켜 1(2, 4)Bzz 를 선택적으로 생성시킨다는 결과를 보고하였다〔 53) . Chung 등은 이 반응을 재현하는 과정에서 이러한 벤조일 이동 반응이 보고된 조건 하에서는 그다지 선택 적성이 없음을 발견하였다 . 다양한 반응 조건 하에서 생성되는 이성질체들의 양을 HPLC 나 NMR 로 체계적으로 추적해 본 결과, 평형 상태에 도달하면 존재 가능한 9 개의 mz2 이성 질체들이 거의 고론 분포로 생성된다는 것이 밝혀졌다〔 90). 죽 이 중 간체의 이성질체들을 분리할 수 있는 조건만 찾는다면, 가능한 모든 인산이노시톨의 합성이 손쉽게 이루어질 가능성을 보여주는 것이었다. 반응 혼합물 속에 존재하는 9 개의 구성 성분을 분리하는 작업이 쉽 지는 않았지만, 벤조일기 이동을 일부 영역에서만 일어나도록 제한하 는 기법을 병행하여 IP4 합성의 중간체인 mz2 를 모두 얻을 수 있었다. mz2 를 에틸포스파이트로 처리한 후, 산화시켜 인산기를 도입하고, 보 호기들을 TMSBr 과 KOH 를 차례로 사용하여 제거하여 9 개의 IP4 를 모 두 합성하였다(그림 4-90) [91 ] . IP 의 경우 모두 12 개의 위치 이성질체가 존재하며, 합성의 중간체 로는 인산기와 상보적인 위치에 벤조일기가 도입된 IB ZJ가 필요하다. Chung 등은 IP4 합성에서 이용되었던 부분적 벤조일 이동 반응을 이용 하여 가능한 12 개의 IB ZJ룰 모두 만들었고, 인산화/탈보호 반응을 거 쳐 성공적으로 IP J를 합성하였다(그림 4-9 1) (92] . 각각 4 개의 위치 이성질체가 존재하는 IP! 〔 9 이과 IPs 〔엇〕도 위와 같 이 벤조일 이동 전략을 이용하여 모두 합성되었다. IP 려 경우 IP4 의
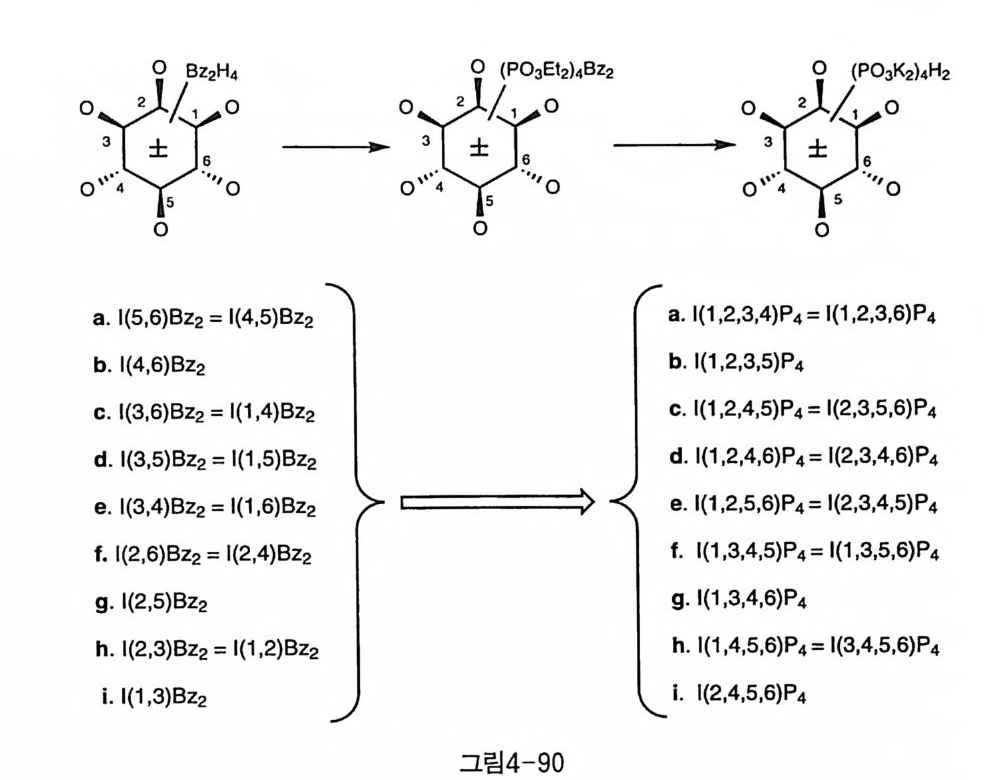 .. 3
.. 3
합성에 사용된 IBz2 를 벤질화하고, 벤조일기를 가수 분해한 다음 인산 화함으로써 합성하는 경로가 예로 보고되었다〔 38). 한편, 같은 연구원 들은 발산적 방법 외에 별도의 효율적인 합성 경로를 개발하여 보고하 였다 (4-3) [38 ). 죽, 벤조일 이동 반응을 기본 전략으로 하는 합성법을 활용하여 가 능한 인산이노시톨의 위치 이성질체는 모두 합성되었고, 합성된 인산 이노시톨들은 1(1 , 4,5)P3 수용체〔 38, 9 외와 I (l ,3,4,5)P ◄ 수용체〔 96, 97] 에 대한 활성과, 1(1 , 4,5)P3-3-ki na se 억제 효과〔 38 〕 및 철 이온을 촉 매로 하는 생체 내 라디칼 생성 반응 억제 연구〔 3 기 등에 이용된 바가 있다.
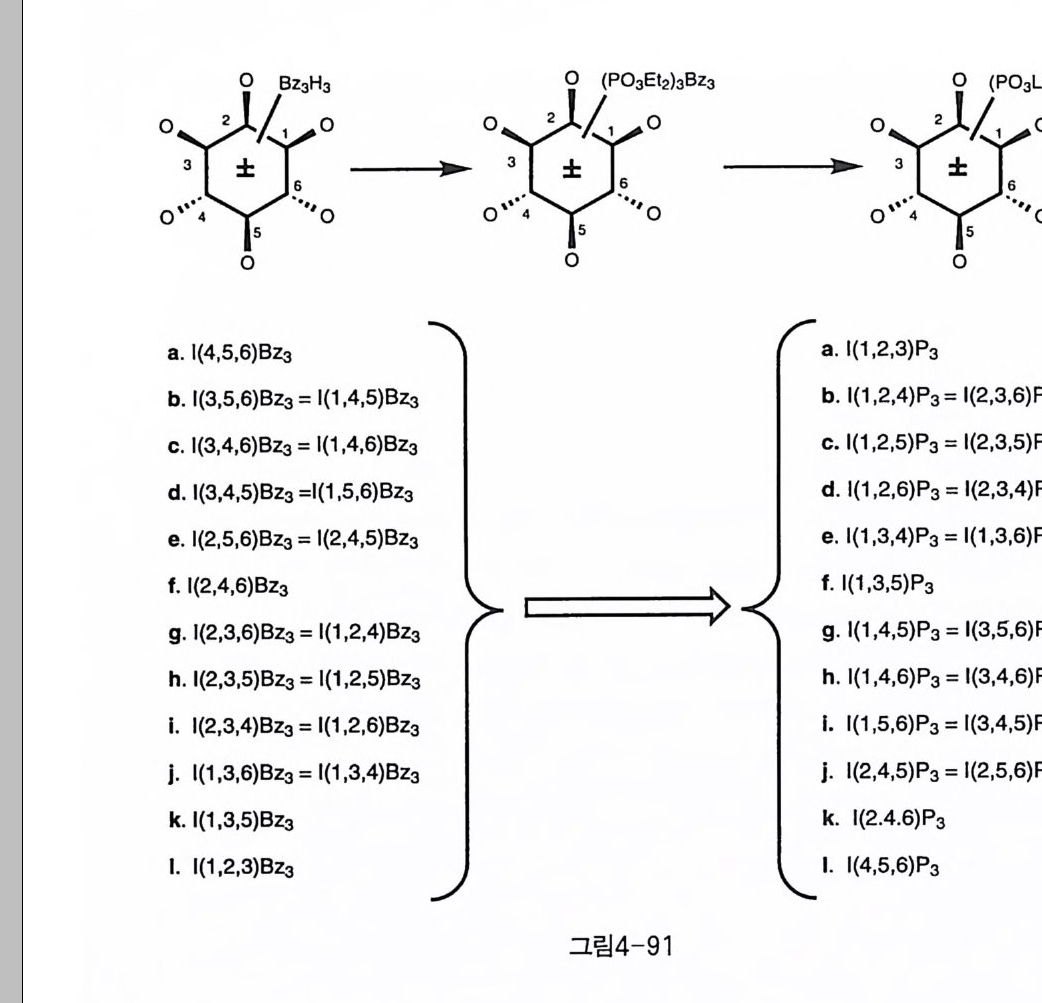 。 。 。
。 。 。
참고문헌 印 Poste m ak, T. The Cyc li tols , Holden -Day, San Francis c o, 1965. [2] Cosgr ov e, D. J. Inosito l Phosph ate s , the ir Chemi st r y, Bio c hemi st r y and Phys i o l og y, Elsevie r , Amste r dam, 1980. (3) Shvets , V. I. Usp ek hi Khim i i 1974, 43, 1074 -1101; Russ. Chem. Rev.
1974, 43, 488 -5 02. 印 Inosito l Phosph ate s and Deriv a ti ve s -Syn th e sis , Bio c hemi st r y and Thera- pe uti c Pote c ti al (ACS Sy m p . Ser. 463, Ed. Reit z, A. B. ) , Ameri ca ! Chem i- cal Socie t y , Washin g ton , DC, 19'Jl. [5] B il ling ton D. C. The Inosit ol Phosph ate s : Chemi ca l Sy n th e sis and Bio l og i- cal Sig n if ican ce, VCH, Wein h eim , 1993. [6) Pott er , B. V. L.; Lamp e, D. Ang ew . Chem. Int. Ed. Eng l. 1995, 34, 1933- 1972. (7) Ozak i, S. ; Wata n abe, Y. Yuki Gosei Ky o kai Shi 1989, 47, 363 -3 73. (8) Bi lling ton , D. C. Chem. Soc. Rev. 1989, 18, 83 -1 22. 〔이 Pott er , B. V. L. Nat. Prod. Rep. 1990, 7, 1-24. U 이 Ste p s nov, A. E.; S hvets , V. I. Chem. Phys . Lip ids 1979, 25, 247-263. (11) Piz e r, F. L.; Ballou, C. E. J. Am. Chem. Soc. 1959, 81, 915-921. (12 ) Ballou, C. E.; Piz e r, L . I. J. Am. Chem. Soc.1960, 82, 3333-3335. U 미 Kuri ha ra, N.; Sh iba ta , H.; Saek i, H.; Nakaji ma , M. Jus tu s Lie b ig s Ann. Chem. 1967, 701, 225-232. (14 ) Kiel y, D. E.; Abruscato , G. J.; Baburap, V. Carbohyd r . Res. 1974, 34, 300-313. (15 ] M 函 er, D 갭 arn 叫 J. E. G. 간 ero, S. D. Ti라 rahedron 1969 효홉江 5687. (16 ) Molotk o vsky , J. G.; Berge l son, L. D. Tetr a hedron Lett. 1971, 12, 4791- 4794; Molotk o vsky , J. G.; Berge lson, L. D. Chem . Phys . Lip ids 1973, 19, 135-147. U 기 Shvets , V. I.; Klya shchit sk i i, B. A.; Ste p s nov, A. E.; Evstig ne eva, R. P. Tetr a hedron 1973, 29, 331 -3 40. (18] Bi lli n gton , D. C.; Baker, R .; K 띠 a g。 WS 뵤 J. J.; Mawer, I. J. Chem. Soc., Chem. Commun. 1987, 314-316. (19] M 述辛 s, T.; S 야띠tz, C.; J禪屯 B. Te t rahe& 야 Lett. 1988, 29, 3921-
3922. (2 이 Akiya ma, T.; Takech i, N.; Oza ki, S. Tetr a hedron Lett. 1990, 31, 1433- 1434; Akiya ma, T.; Takech i, N.; Oza ki, S.; Sh iot a , K. Bull. Chem. Soc. Jpn . 1992, 65, 366 -3 72. (21 ) Ley, S. V.; Parra, M.; Redg rav e, A. J.; Ste m f el d, F. Tetr a hedron 1990, 46, 4995 一 5026. [22 )B erlin , W. K.; Zhang. W. S.; Shen, T. Y. Tetr a hedron 1991, 47, 1-20. [23 ] Salamori cz yk , G. M.; Pie t r us ie w i cz , K. M. Tetr a hedron Lett . 1991, 32, 4031-4032. (24) Pie t r us ie w i cz , K. M.; Salamori cz y k, G. M.; Bruzik , K. S. Tetr a hedron 1992, 48, 5523 -5 542; ide m, ibi d 1994, 50, 573. 固 Poste m ak, T. Helv. Chim . Acta 1941, 24, 1045 -1 058. [26 )I seli n, B. M. J. Am. Chem. Soc. 1949, 71, 3822-3825. @기 Bil ling ton , D. C.; Baker, R.; Kulag ow ski , J. J.; Mawer, I.; Vacca, J. P.; deSolms, S. J.; Huff , J. R. J. Chem. Soc., P erkin Trans. 1 1989, 1423 -1429. [28 ] G rado, C.; Ballou, C. E. J. Bio l . Chem. 1961, 236, 54-60. [29 ] 샤 1 gy al, S. J.; Tate , M. E. J. Chem. Soc. 1961, 4122-4128. 〔 3 이 Vacca, J. P.; deSolms, S. J.; Huff , J. R.; Bi lling ton , D. C.; Baker, R.; Kulago w ski , J. J: ; Mawer, I. Tetr a hedron 1989, 45, 5679 -5 702. 印 Bil ling ton , D. C.; Baker, R. J. Chem. Soc., Chem. Commun. 1987, 1011- 1013. @]W ata n abe, Y.; Mitani, M.; Mori ta, T.; Ozaki , S. J. Chem. Soc., Chem. Commun. 1989, 482-483. 固 Dowson, R. M. C.; Frein k el, N. ; J un g al wala, F. B.; Clarke, N. Bio c hem. J. 1972, 127, 113 -118. [34 ] W ata na be, Y.; Og as awara, T.; Naka hira, H.; Mats u k i, T.; Oza ki, S. Tetr a -hedron Lett. 1988, 29, 5259 -5 262. [35 ] w 寧떠uin, P; van Boeckel, C. A. 凡 펴먀 pp 11 曰꼬
〔 3 이 Krylo va, V. N.; Kobelkova, N. I.; Olein i k , G. F.; Shvets , V. I. Zhur. Org. Khim . 1980, 16, 315 -322. 詞 Sp ier s, I. D.; Barker, C. J.; Chung , S. K.; Chang , Y. T.; F reeman, S.; Gar-din e r, J. M.; Hi rst, P. H.; Lambert , P. A.; Mi ch ell, R. H. ; P oy ne r, D. R.; Schwalbe, C. H.; Sm ith, A. W.; Solomons, K. R. H. , C arbohyd r . Res. 1996, 282, 81-99. [38 )Chang , Y. T., Ph. D. Di ss ert at i on , POSTECH, 1997. [39 )Hamblin , M. R.; F lora, J. S.; P ott er , B. V. L. Bio c hem. J. 1987, 246, 771- 774. 〔仰 Salamonczyk , G. M.; Pie t r us ie w i cz , K. M. Tetr a hedron Lett. 1991, 32, 6167-6170. [41 )Schultz , C.; Gebauer, G.; Mets c h ies , T.; Rensin g , L.; Jas to r f f, B. Bio c hem. Bio p hy s . Res. Commun. 1990, 166, 1319-1327. 〔 4익 Weste r duin , P.; W i llem s, H. A.; van Boeckel, C. A. A. Tetr a hedron Lett. 1990, 31, 6915 -6918. 〔 4 회 Gig g, J.; Gig g, R.; Payn e , S.; Conant, R. J. Chem . Soc., Perki n Trans. 1 1987, 423 -429. 〔띠 Hamblin , M. R.; Pott er , B. V. L.; Gig g, R. J. Chem. Soc., Chem. Commun. 1987, 626 -6 27. 〔 4회 Carless, H. A. J.; Busia , K. Tetr a hedron Lett. 1990, 31, 3449-3452. 圈 Oza ki, S.; Wata n abe, Y.; Og as awara, T.; Kondo, Y.; Sh iota ni, N.; Ni sh i i, H.; Mats u k i, T. Tetr a hedron Lett. 1986, 27, 3157-31(,(), 〔 4기 Oza ki, S.; Kondo, Y.; Sh iot a ni, N.; Og as awara, T.; Wata na be, Y. J. Chem . Soc., Perkin Trans. 1 1992, 729-737. 圈〕 Wata n abe, Y.; Fusim oto , T.; Shin o hara, T.; Oza ki, S. J. Chem. Soc., Chem. Commun. 1991, 428 -429. [49 ] R 函 ”E 챗 ard, J. G. Te t rahed 向 Lett. 1987, 28, 2309 꿉끄 [50 )Cooke, A. M.; Pott er , B. V. L.; Gig g, R. Tetr a hedron Lett. 1987, 28,
2305- 2 308. [51 ) Weste r duin , P.; W illem s, H. A. M. ; van Boeckel, C. A. A. Tetr a hedron Lett . 1990, 31, 6919-69 22. [52 )Vacca, J. P.; deSolms, S. J.; H uff , J. R. J. Am. Chem. Soc. 1987, 109, 3478-3479. [53 )Meek, J. L.; David s on, F.; H obbs, F. W. J. Am. Chem. Soc. 1988, 110, 2317-2318. [54 ] L ey, S. V.; Ste r n feld , F. Tetr a hedron Lett . 1988, 29, 5305 -5 308. [55 ) Ste p s n ov, A. E.; Runova, 0. B.; Schlewer, G.; Sp ies s, B.; Shvets , V. I. Tetr a hedron Lett . 1989, 30, 5125 -5128. (5 이 Dreef, C. E.; Tuir u nan, R. J.; Eli e, C. J. J.; van der Marel, G. A.; van Boom, J. H. Reel. T rav. Chim . Pays -Bas 1988, 1 07, 395 -3 97. 〔 5 기 Tegg e , W. ; B allou, C. E. Proc. Natl. Acad. Sc i. USA 1989,8 6 ,94-98. 園 Falck, J. R. ; Y adag ari, P. J. Org. Chem. 1989, 54, 5851-5852. 園 Liu , Y. C. ; C hen, C. S. Tetr a hedron Lett. 198i 3o, 1617 -1620. (ffi) Gou, D. M. ; L iu , Y. C.; Chen, C. S. Carbohy d r. R es. 1992, 234, 51-64. 圓 Ag uilo, A.; Ma rtin- Lomas M. ; P enades, S. Tetr a hedron Lett . 1992, 3 3, 401-404. 園 Bruzik , K. S.; My er s, J.; Tsai , M. -D. Tetr a hedron Lett. 1992, 33, 1()( )C)- 1012. 園 Chung, S. K.; Chang , Y. T.; Sohn, K. H. Kor. J. Med. Chem. 19'J4,4 ,5 7- 65. (64) Sp ier s, I. D.; Freeman, S.; Poy ne r, D. R.; Schwalbe, C. H. Tetr a hedron Lett. 1995, 36, 2125 -2 128. [65 )C hung , S. K.; Chang , Y. T. Kor. J. Med. Chem., 19%, 6, 253 -2 58. [66 ] Desai , T.; Fernandez -Mayo r alas, A.; Gig g, J.; Gig g, R.; Jar am illo , C.; Payn e , S.; Penades, S.; Schnets , N., re 也), pp8 6-102. 〔 6까 Andersch, P.; Schneid e r, M. P. Tetr ah edron: As ym metr y 寧, 7,-3 4 9-35 2.
(部〕 Blum, C.; Karlsson, S.; Schlewer, G.; Sp ies s, B.; Rehnberg, N. Tetr a he-dron Lett . 1995, 36, 7239 -7 242. [69 )Dreef, C. E.; van der Marel, G . A.; van Boom, J. H. Reel. Trav. Chim . Pays -B as 19'if l, 106, 161 -1 62. 〔 7 이 deSolms, S. J.; Vacca, J. P.; Huff , J. R. Tetr a h~dron Lett . 1981, 4503 - 4506. (71) Oza ki, S.; Kohno, M. ; Nakahir a , H.; Buny a, M.; Wata n abe, Y. Chem. Lett . 1988, 7 7 -8 0. 〔 7 익 Boehm, M. F.; Prestw ic h , G. D. Tetr a hedron Lett . 1 988, 29, 5 217-5220. [73 )Gou, D. M .; Chen, C. S. Tetr a hedron Lett. 寧, 33, 721-724. ?]R ile y, A. M.; Payn e , R.; Pott er , B. V. L. J. Med. Chem. 1994, 37, 3918- 3927. 〔히 Vacca, J. P.; d e Solms, S. J.; Young , S . D.; H uff , J. R .; Bil ling ton , D. C.; Baker, R.; Kulag ow ski , J. J.; Mawer, I. M.,re f印,pp 66-85. (7 이 Mi lls, S. J.; Al-Ha fidh , J.; Westw ic k , J.; Pott er , B. V. L.; B io o rg. Med. Chem. Lett . 19'J3, 3, 2599 -2 604. [77 ) Wata n abe, Y.; Og as awara, T.; Ozaki, S.; Hira ta , M. Carbohy d r. R es. 1994, 258, 87 -9 2. (78) Falck, J. R.; Abdali, A., ref( 4 ), pp 145-154. (79] Tegg e , W.; Den is, G. V.; Ballou, C. E. Carbohyd r . Res. 19'J1 , 217, IC fl- 116. (8 이 Schlewer, G.; Sp ies s, B. Bio o rg. Med. Chem. Lett . 1995, 5, 1 225 -1230. [81 )Baudin , G. ; G l nzer, B. I.; Swa mina th a n, K. S.; Vasella, A. Helv. Chim . Acta 1988, 71, 1367 -1 378. @]O zak i, S.; Kondo, Y.; Naka hira, H. ; Yamaoka, S.; W ata n abe, Y. Tetr a he-dron Lett . 1981, 28, 4691-46 94. 〔 8 기 Wata n abe, Y.; Sh ino hara, T.; Fusim oto , T.; Ozak i, S. Chem. Phann. Bull. 1990, 38, 562 -5 63.
[84 ] Wata n abe, Y.; Oka, A.; Shim i zu , Y.; Oza ki, S. Tetr a hedron Lett. 1990, 31, 2613-2616. 〔 8 회 Mi lls, S. J.; Sa fran y, S. T.; Wi lc ox, R. A.; Nahorski , S. R.; Pott er , B. V. L. Bio o rg. Med. Chem. Lett. 1993, 3, 1505-1510. 圈 Oza ki, S.; Lin g , L.; Og as awara, T.; Wata n abe, Y.; Hirat a , M. Carbohyd r . Res. 1994, 259, 307 -3 10. 〔 8 기 Roemer, S.; Rudolf, M. T.; Sta d ler, C.; Schultz , C. J. Chem. Soc., Chem. Commun. 1995, 411-412. 〔 8 이 Ang ya l, S. J.; R ussell, A. F. Aust. J. Chem. 1968, 21, 391-404. [89 )O zak i, S.; Kog a, Y.; Lin g, L.; Wata n abe, Y.; Kim ura, Y. ; H irat a , M . Bull. Chem. Soc. Jpn . 1994, 67, 1058-1063. [90 )Chung , S. K.; Chang , Y. T. J. Chem. Soc., Chem. Commun. 1995, 13 -14. (91) Chung , S. K.; Chang , Y. T. J. Chem. Soc., Chem. Commun. 1995, 11 -12. (92) Chung , S. K.; Chang , Y. T.; Sohn, K. H. J. Chem. Soc., Chem. Commun. 1996, 163-164. 固 Chung, S. K.; Chang , Y. T. Kor. J. Med. Chem., 1996, 6, 162-165. [94 )Chung , S. K.; Chang , Y. T. Bio o rg. Med. Chem. Lett ., 1 996, 6, 2039- 2042. 〔芳〕 Marchant, J. S.; Chang , Y. T.; Chung , S. K.; Irvin e , R. F.; Tayl o r, C. W. Bio c hem. J., 1997, 321, 573-576. [96 ) Cullen, P. J.; Chung , S. K.; Chang , Y. T.; Dawson, A. P.; Irvin e , R. F. FEBSLett. , 1995, 358, 240-242. [“]S tr ick er, R.; Chang , Y. T.; Chung , S. K.; Reis e r, G., Bio c hem. Bio p hy s . Res. Commun., 1996, 228, 596-604.
제 5 장 이노시톨 유사체 및 유도체 5-1 이노시톨 유사체 이노시톨은 세포 내로 유입되어 PI-s y n t he t ase 에 의해 이노시톨 인 지질로 변환된다. 그러므로 이노시톨의 유도체나 유사체가 이 인지질 의 합성 경로에 이노시톨 대신 들어갈 수 있다면, 인산이노시톨울 거 치는 신호 전달계에 대한 다양한 약리 효과를 유도할 수 있을 것이다. 특히, 인지질의 가수 분해 산물인 인산이노시톨의 유사체인 경우에는 분자 내에 여러 개의 전하를 가지고 있어 세포막을 통해 전달되기가 어려운 문제가 있으나, 이노시톨 유사체인 경우에는 전하를 띠지 않으 므로 세포막 통과가 상대적으로 유리하다. 우선 수산기의 치환체로서 흔히 사용되는 불소가 이노시톨에도 응용 되었다. Kozik o wski 등은 my o- i nos it ol 에서 출발하여 DAST 로 F 를 도 입하고, cam p hana t e 를 이용한 광학 분할을 거쳐 D 와 L-l-deoxy - 1- fl uoro-m y o- in os it o l( I (l )F) 을 합성하였다(1). 같은 연구자들은 보다 짧은 반응 경 로를 개 발하여 , D -3 -meth y l - chir o -i nos it ol 로부터 DAST (dieth yla m ino sulf ur trifluo ri de ) 를 이 용한 불소화 반응으로 D -l (l )F
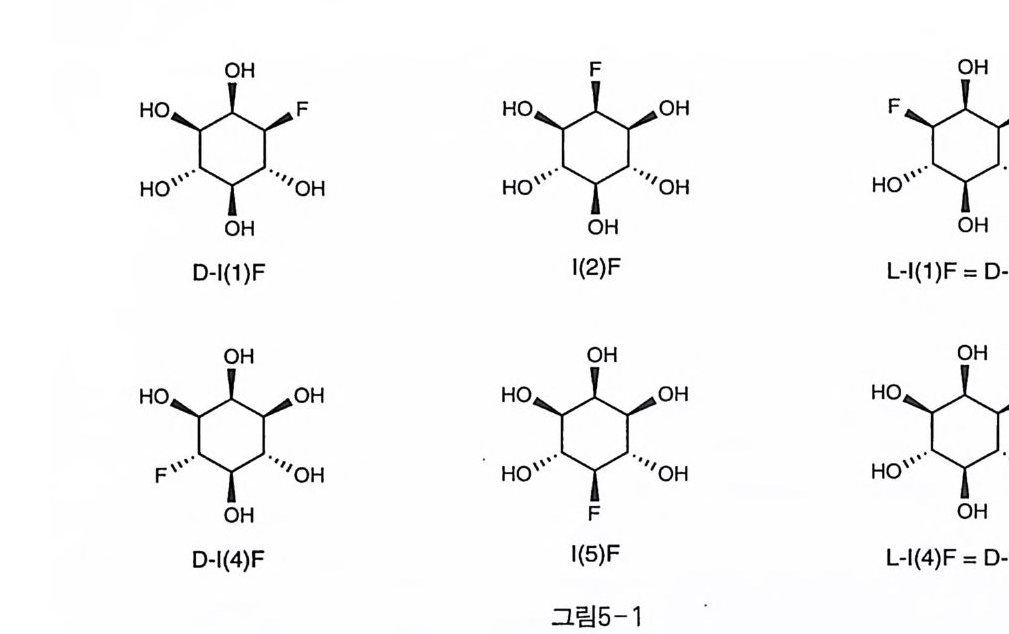 OH F OH
OH F OH
를 만들었다〔 2 〕. Of fer 동은 my o -i nos it ol 로부터 출발하고 , DAST 와 cesiu m cam p hana t e 를 이용하여 D 와 L _ -I (l )F 를 합성하였는데〔 3 〕, 또한 이들은 2 번 수산기를 산화하고 재환원 과정에서 NaB 전 4 로 J H 를 도입한 후, 소 량 생성 되 는 scyl lo 중간체룰 분리 하여 불소화 반응함으로써 2 번 위 치 에 방사성 표지된 l(2) F 유도체도 만들었다. 이때, 화학적인 방법 대 신 ino sit ol deh y dro g enase 를 이 용해서 방사성 표지 를 하는 방법 도 함께 개발되었다. 또한 다양한 중간체를 활용하여 광학 활성 및 메조 상태 인 6 개의 가능한 불소 치환된 이노시톨 (IF1) 을 모두 합성하였다〔 4). 수산기를 DAST 로 처리하면 주로 수산기의 입체 구조예 반전이 일 어나면서 F 가 도입된다. 그러므로 이노시톨의 2 번 수산기를 DAST 와 반응시켜, 2 번의 입체 구조가 m y o 와 달라진 sc y llo-IF 의 합성이 비교 적 오래전에 보고된 바 있다〔 5) . 같은 화합물은 Po tt er 〔이와 Lowe 등 m 에 의해서도 합성이 보고되었다. Lowe 둥은 s cy llo 와 my o 형태의
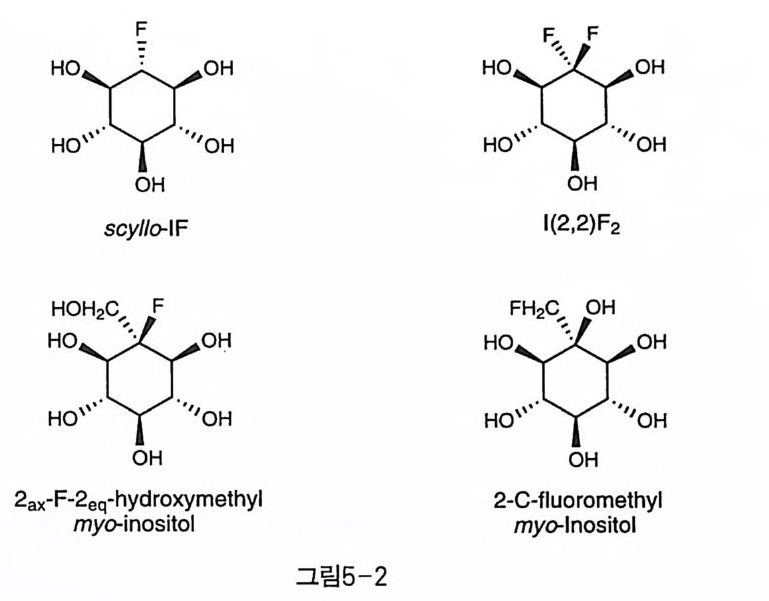 F
F
1(2)F 와 불소와 같은 탄소에 띤가 표지된 화합물들을 함께 합성하였 다. I (1 ,3,4,5,6)Bns 를 산화하여 케톤을 얻고 이를 NaBH4 로 환원 반응 하면, m y o 가 주생성물로 얻어지고 s cy llo 가 소량 얻어진다〔 4, 7) . 수산기 대신 카르보닐기가 존재할 경우 DAST 로 반응하면, 수율은 일반적으로 낮지만 같은 탄소에 두 개의 불소가 도입된다 . Pott er 동은 이노시톨의 2 번 수산기를 산화시켜 케톤울 만든 후, DAST 로 반응하 여 2-deoxy -2, 2-dif luo ro -my o -i nos it ol 을 합성 하는 경 로를 보고하였 고 [6] , Yang 등은 역 시 DAST 를 사용하여 2-deoxy -2..-fluo ro -2,q - hy d roxy m eth y l -m y o -i no sit ol (8 댜 2 -C -f luo rometh y l -my o - i nos it ol(9 〕올 합성하였다. 한편, Guid o t 등은 2 번 수산기를 SH 로 치환 한 2-mercapt o 유도체 합성을 보고하였는데, 2 번 수산기를 입체 반전 시키면서 I 를 도입하였다가 다시 S 친핵체로 공격하여 my o 형태의 유 도체를 만들었다(1 0 〕 .
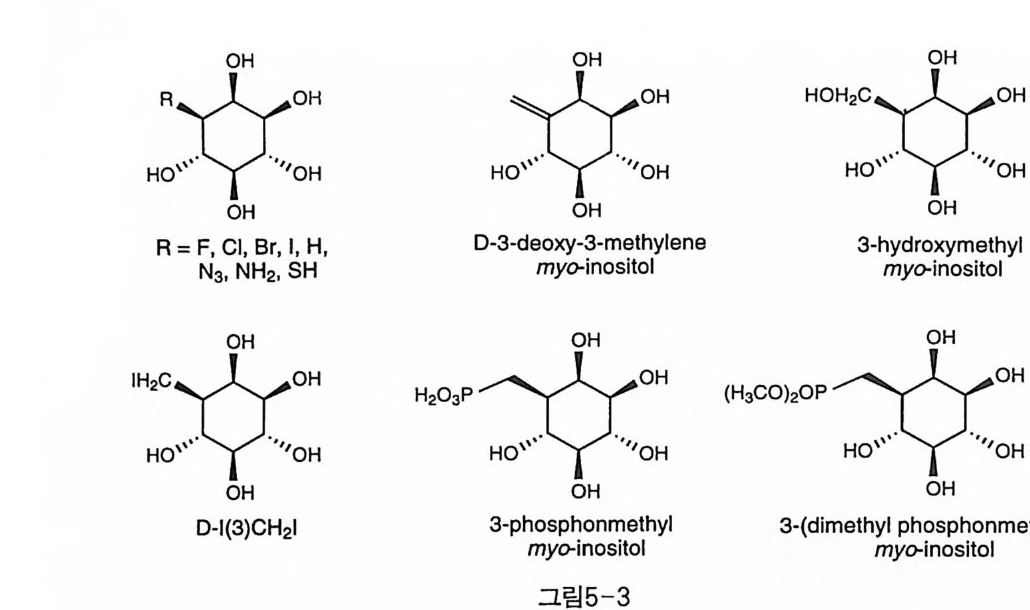 OH OH OH
OH OH OH
Kozik ow ski 동은 3 번 수산기가 치환된 다양한 이노시톨 유사체들을 합성하였다 . 이들은 L- q uebrac hit ol 에서 출발하여, D-l(3)F[ll) 을 비 롯한 Cl, Br, I 등의 할로겐 치환체들 [12) 과 D-3-deoxy -inos ito l [13] 울 합성하였다. 또 N3, NIL, SH 치환체들[1 3 〕도 비슷한 경로로 합성 되 었고 3-C-meth yl 유도체도 3-수 산기 를 산화시 킨 후, Gr ign ard 반 응으로 수직 방향의 친핵성 반응으로 만들어졌다 [12) . 3 번 위치에 meth y le ne, hy d roxy m eth y l, CH2I, ph osp h onometh y l, dim eth y l pho sph o nometh yl 등을 도입한 유사체들도 합성되었고, 이들이 세포 성 장에 미치는 영향이 연구되었다[1 4 〕, 한편, 4 번(또는 6 번) 수산기 대신 deoxy, F, meth yl 등이 붙은 이 노시톨 유도체들이 Ley 등에 의해 라세미 형태로 합성된 것이 보고되 었다[1 5 〕 · m y o-I(S)F 를 합성하기 위한 노력으로, Baker 등이 5 번 수산기만 열 려 있는 중간체에 DAST 를 반응시킨 결과 입체 구조가 반전된 neo 이
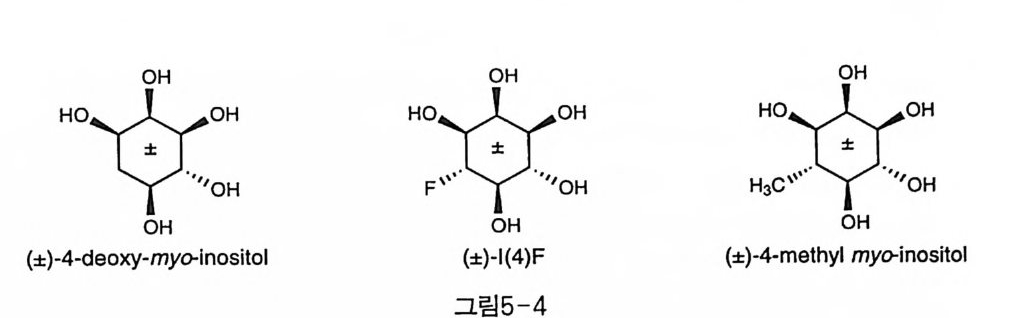 (士 )-H4 - deoO xy -Ym y er i :no:s i t ol H(±)·:1(4:)F : (士 ) - 4-m:e t h* y l my: o-in:o s ito l
(士 )-H4 - deoO xy -Ym y er i :no:s i t ol H(±)·:1(4:)F : (士 ) - 4-m:e t h* y l my: o-in:o s ito l
노시톨 생성물이 주로 얻어졌다(1 6) . 같은 연구자들은 5 번 수산기를 trifl a t e 로 치환한 후 친핵성 반응으로 입체 구조를 반전시켜서 DAST 반응을 통해 1(5)F 를 얻었다 U 기 . 5 번 위치를 산화시켜 케톤으로 만든 후 DAST 와 반응시켜 1(5, 5)F2 도 합성하였다. 이때 1(5)F 는 deute r i um 치환 실험 결과 2 번의 수소의 치환이 가장 빠르다는 것이 밝혀졌고, ino sit ol deh y dro g enase 를 이 용하여 방사성 인 면가 치 환된 유도체도 함 께 만들어졌다 . 또한 이들은 m y o 나 neo 형태를 가진 5-Cl, Br, I 치 환체들과 라세미 형태의 l( 4)F 도 합성하였다 U 이 . 5-2 일인산이노시톨 유사체 및 유도체 Jas to r f f 등은 I(2, 3, 4, 5 , 6)Acs 를 thiop ho sph o ry l chlo ri de(PSCb) 로 반 응하여 라세미 형태의 I(l)PS 를 합성하였다(1 8) . Bi lling ton 등은 IBns 에 phos p hor ami d it e 로 아인산기 를 먼저 도입 한 다음 S 를 도입 하는, 보 다 세련된 방법을 활용하여 라세미와 각각의 광학 이성질체 형태의 I(l) PS 를 합성 하였다〔 19 〕 · 고리형 화합물인 cl (l , 2)PS 도 라세미 형태로 합성되었는데, Jas to r f f 등은 PSCh 를 이용한 직접적인 인산화 방법으로 I( l,4,5,6)AC4 에 티오 인산기를 도입하여 endo 와 exo 의 혼합물을 1:1 정도의 비율로 얻고 역 상크로마토그래피로 분리하였다〔 20) . Tsa i 등은 라세미 상태의 I(l ,4, 5,
6)Bn4에 phosphoramidite 방법으로 고리 아인산기를 도입한 후 S를 가 하여, endo와 exo를 각각 얻을 수가 있었고, 이 경우 얻어진 화합물들 은 Pl-PLC의 반응 특이성 연구에 표준 물질로 이용되었다(21) . 한 편, 같은 연구자들은 PLC를 촉매로 이용하여 cl(l,2)P의 고리를 ROH 로 여는 transesterification 반응도 보고하였다〔22〕 . 포스폰산 유도체 로는 D _ I ( l )P의 methylphosphonate 유도체 가 van Boom 등에 합성되었다〔23〕. 이노시톨 고리의 수산기를 제거한 deoxy 유도체들도 여러 연구자들 에 의해 합성되었다. Billington 동은 I(l)P의 유도체로서 라세미 형태 의 2-deoxy 와 6-deoxy 유도체를 먼저 합성하였는데〔24〕, 없애고자 하는 수산기를 I로 먼저 치환한 후 라디칼 반응을 이용하여 수산기를 제거하였다. Bruzik 동은 광학 활성을 가진 D-2-deoxy-l(l)P를 합성 하였다〔25〕 5-3 이인산이노시톨 유사체 및 유도체 IP려 티오인산 유도체인 I(l, 4)PS2〔%)와 1(4, 5)PS2@기의 합성이 Potter 동에 의해 각각 보고되었다. 또, 포스폰산 유도체로는 I(3,4)P2의 3-methylphosphonate 유도체 가 van Boom 등에 의 해 보고되 었다〔28) .
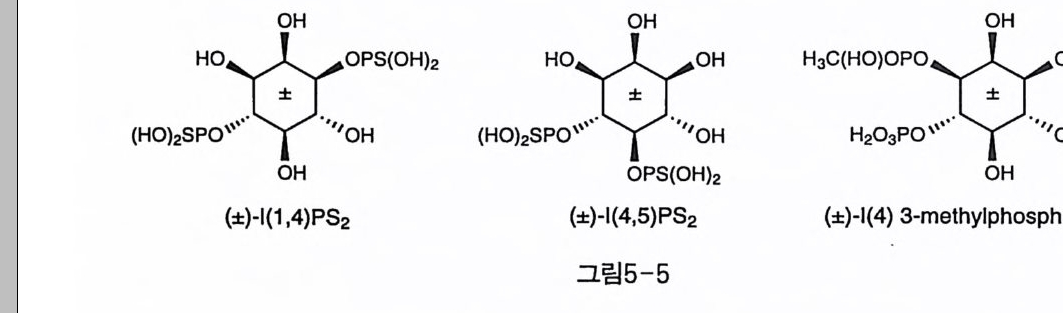 (HOOS:*::S(OH), (HO),S::仁
(HOOS:*::S(OH), (HO),S::仁
5 구 1 삼인산이노시톨 유사체 및 유도체 5-4-1 티오인산 유도체 인산기를 티오인산기로 치환한 유도체는 핵산 화학에서 그 유용성이 널리 알려져 있었다. 또한 지금까지 합성된 수백 개의 cAMP 유사체 중에서 선택적 길항제는 cAMP 의 티오인산 유도체뿐이었다. 티오인산 기는 인산기의 0 한 개가 S 로 치환된 유도체로서 일반적으로 포스파 타제에 의한 인산 가수 분해 반응에 저항성을 가지며, 인산기에 비해 지질막 투과성도 나은 편이다. 한편, 방사성 표지인 35S 를 도입할 수 있는 방법으로 활용되기도 한다. 또, 0 보다는 S 가 더 좋은 친핵체이 기 때문에 형광 표지와 같은 선택적인 작용기의 도입에 활용될 수도 있다. 티오인산 유도체로는 I (l ,4,5)P3 의 유사체인 I (l ,4,5)PS J가 Pott er 등 에 의해 최초로 보고되었다〔 29). 합성에서는 I(2, 3, 6)Bn J가 중간체로 이용되었으며, 아인산기를 도입한 후 원소 S 를 이용하여 티오인산기를 만들었다. van Boom 등에 의한 두번째 합성에서도 역시 아인산기를 이 용했으나, S 를 도입하는 단계에서 p henace ty l di s ulfi de 를 이용하였다〔 30 〕. 세 개의 인산기가 모두 티오인산기로 치환된 화합물뿐만 아니라 특 정 위치만이 치환된 화합물들도 합성되었다. Pott er 등은 I(l ,4 ,5)P3- 5S 떠)와 I(l , 4, 5)PJ- 4 , 5& 〔 32 〕를 합성하였고, 이중 1(1 , 4, 5)Pr4, 5Sz 는 N-bromosucc inimi de 에 의해 탈황 작용이 일어나 (4,5) _고리형 피 로인산기 를 만드는 중간체로 활용되 었다〔 32) . 1(1 , 4, 5)P~ 대사에 관 여하는 5- 포스파타제에 대한 저해제로 쓰일 수 있을 것으로 예상되는 I (l ,4,5)Pr5S 는 van Boom 등에 의해서도 합성되었다〔 30). Pott er 등은 1(1 , 4, 5)PJ -1S 도 합성 하여 [33 ] l 번 인산기 에 형 광 작용 기를 붙이는 데 활용하였다〔 34). 라세미 형태의 I (l ,4,5)P J -1S 온 van
Boom 등에 의해서도 합성이 보고되었다〔 30 〕. D-1 (1 ,4,5)PS3 의 6-deoxy 유도체〔 3 회 와 m y o-1 (1 ,4,5)PS J의 3 번 수 산기의 입체 구조가 반전된 chir o -1(2,3,5)P&[ 35 ,3 이 도 Pott er 등에 의해 합성되어, 1(1 , 4,5)P3 수용체에 대한 결합 정도와 칼슘 방출 효과 가 측정되었다. 또, 같은 연구자들은 L -I (1, 4, 5)PS:i, I (1, 3, 5)PS:i, chir o -I (1, 4, 6)PSJ 도 각각 합성하여, 3- 키나제와 5- 포스파타제에 대한 활성을 검사하 였다. 이들은 칼슘 방출에는 관여하지 않으면서 대사 효소 저해제의 가능성을 보여주었다〔 37). 5-4-2 포스폰산 유도체 포스폰산은 인산기에 비해 포스파타제에 대해 안정할 뿐만 아니라, 알 킬기의 위치에 따라 전하가 적어지기도 하고 친지질성이 커져서 지질 이중막을 통과하기가 용이한 경향이 있다. 최초로 합성된 포스폰산 유도체는 van Boom 등에 의해 보고된 라 세미 형태의 1,4,5- 수소포스폰산(1 -H- p hos p hona t e) 이었다〔 38 〕 · 5- 포스파타제에 대한 안정성을 고려한 5- 포스폰산 유도체도 합성 이 시도되었다. (-)-Qu in ic ac i d 를 출발 물질로 다양한 이노시톨 유 도체를 합성하였던 Falck 등이 1(1, 4, 5)P3 의 5-meth yle neph o sph o nate 합성을 처음 보고하였다〔 39). van Boom 등은 1 (1 ,4,5)P3 의 유도체인 5-meth ylp h o sph o nate 및 5-(d ifl uorome thy l) p hos phona t e 와〔 40, 41) I(l , 3,4)P3 의 유도체인 3-me thy l p hos p hona t e 를 합성하였다〔 28) . I(l , 4, 5)P3 의 1-meth ylp h o sph o nate 유도체 는 라세미 형 태로 Sp ies s 동에 의 해 합 성 이 보고되 었다〔 42). 또, Weste r duin 등은 I(l , 4, 5)P3 의 5-meth y lp h osp h onate , 4, 5- bis (m eth ylp h o sph o nate ) , 1, 4, 5-tri s( meth ylp h o sph o nate ) 둥을 라세미
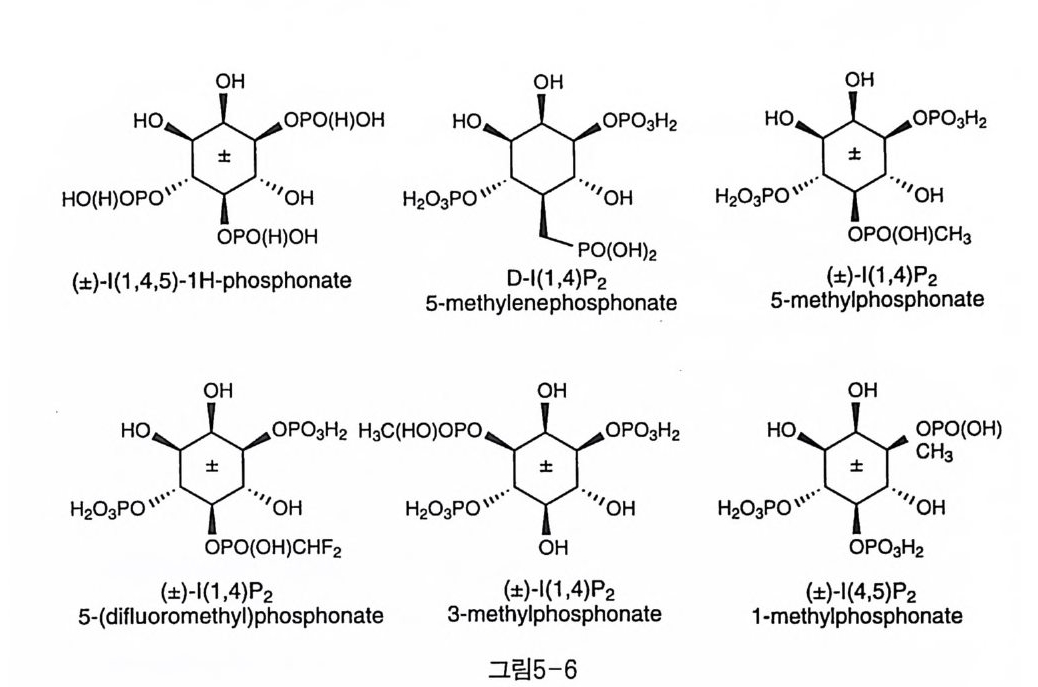 HO(H)OHP:HHO(H)OH H2°3P\<\ 0\\\\2° 3PH0\< OIo:)PHCOH33H2
HO(H)OHP:HHO(H)OH H2°3P\<\ 0\\\\2° 3PH0\< OIo:)PHCOH33H2
형태로 합성하였다〔 43, 44). 같은 연구자들은 포스폰산 이외에도 인산 기 를 대 체 하는 작용기 로서 sulfo n am ide , sulfa te, carboxy m eth yl 등의 1(1 , 4,5)PJ 유사체들을 라세미 형태로 합성하였으나, 칼슘 분비와 관계 된 생 리 효과는 나타내지 않았다〔 44, 45] . 또’ Kozik o wsk i 등은 D- 1 (1, 4, 5)P J의 유도체 로서 hexadeoxy -1, 4, 5 -tris ( meth yle nesulf on ic acid ) 를 합성하여 IPJ 수용체와의 결합성을 검사하였다〔 46). 5-4-3 2 번 위치 변환 유사체 I(l ,4,5)P3 의 2 번 수산기의 중요성을 연구하기 위해 다양한 변형이 2 번 위치에 가해졌다 . Oza ki 둥은 라세미 형태의 2-deoxy - I(l, 4, 5)P3 의 합성을 보고하였다〔 47 〕 . 적절히 보호된 중간체의 2 번 수산기를 먼 저 산화하여 케톤기를 형성한 다음 h y drazone 으로 변형했다가 환원하
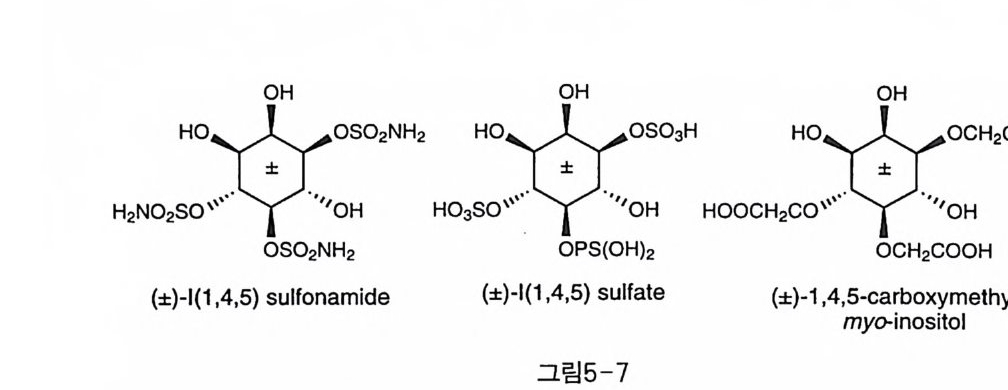 H2N02s:2: 아 NH2 HO3s\0 广° 3H HOOCH2:< ::2CO OH
H2N02s:2: 아 NH2 HO3s\0 广° 3H HOOCH2:< ::2CO OH
는 방법으로 수산기를 제거하고, TBPP 로 인산화하여 2-deoxy - 1(1 , 4, 5)P 를 만들 수 있었다. 수산기와 비슷한 전기 음성도를 가지지만 수소 결합의 받게 역할만 할 수 있고 주게 역할을 할 수 없는 F 의 치환체도 합성이 시도되었 다. 라세미 상태의 두 화합물, scyl l o-I( 2) F( I, 4, 5)P3 와 1(2, 2)F2(1 , 4, 5)Pl 의 합성이 Prestw ich 등〔 48 〕과 Pott er 등〔이에 의해 각각 보고되었 댜 또 광학 활성의 D, L- 1( 2,2)F2(4,5)P3 의 합성도 Po tt er 에 의해 보 고되었고, 각각 대사 효소 저해제로서의 활성이 검색되었다〔 49 〕. my o 형태의 입체 구조를 가진 l( 2)F (l ,4,5)P3 는 scyl l o-in o sit ol 구조 로부터 DAST 반응으로 얻고자 시도되었으나, 기대와는 달리 입체 구 조의 반전이 일어나지 않아서 sc y llo-I(2)F (l ,4,5)P3 만이 얻어진 경우 가 보고되었다〔 48 〕. Pott er 등은 scyl lo 형태 중간체의 수산기 하나를 Tf 기로 치환한 후 Bu 4N°F로 반응하여 my o 형 태의 입 체 구조를 가진 l( 2)F (l ,4,5)P 를 성공적으로 합성할 수 있었다〔 5 이. 또, 합성에 사용 된 중간체를 이용하여 I (l ,4,5)P3 의 2 번 수산기의 입체 구조가 반전된 라세미 s cy llo-I (I ,2,4)P3 도 합성하였다〔 50). 1( 1,3,4)P3 의 2 번 변환 유도체도 합성되었는데, Prestw ich 등은 2 번 수산기에 DAST 로 반응하여 입체 구조가 반전된 scy ll o-I( 2) F( I,3 ,4)PJ 와 1(2, 2)F (l ,3,4)P3 을 합성하였다〔 51 〕 ·
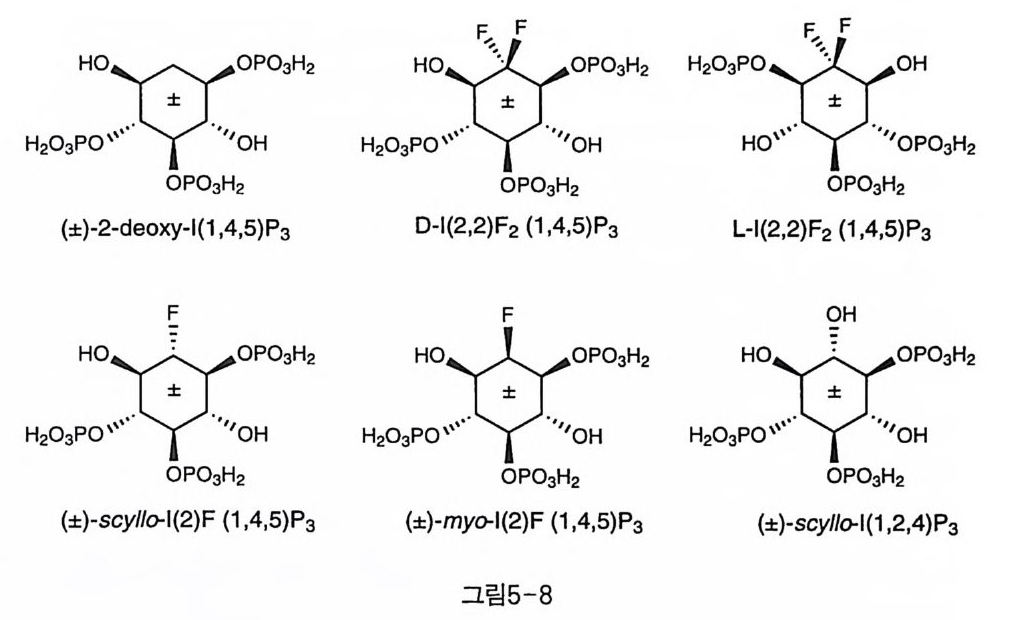 H20 3p H 0。 `亨 OOPH0 3H 2 H203 PH °。 ’亨OOPH0 3H2 H203 pH 。 。F F亨,:H PO 3H2
H20 3p H 0。 `亨 OOPH0 3H 2 H203 PH °。 ’亨OOPH0 3H2 H203 pH 。 。F F亨,:H PO 3H2
5一 4-4 3 번 위치 변환 유사체 Kozik o wsk i 등은 L -q uebrac hit ol 로부터 3 -d eoxy -m y o -in os it ol 을 얻어 광학 활성의 1 (1 ,4,5)P3 와 1( 1,5,6)P3 의 deoxy 유도체를 합성하였 다〔 52). 여기서 사용된 3-deox y -m y o- in os it ol 은 차례로 2 번과 6 번 위 치도 탈수산화 반응을 하여 다양한 1 (1 ,4,5)P3 의 유도체를 만드는 데 사용되었다〔 53). 같은 연구자들은 l (1 ,4,5)P3 의 3 번 수산기의 역할을 규명하기 위하여 다양한 치환기를 3 번 위치에 도입하였는데, D-3- 虹 54), 3-C- C 固 5 회, 3-Cl, 3-Br, 3-Me[5 6 ), 3- N'Hi -l” 璃向 駒 합성 되어 생리 활성과 구조의 관계가 연구되었다. Carless 등은 1 (1, 4, 5)P3 의 3 번 수산기 의 입 체 구조가 반전된 chi ro - 1( 2,3,5)P3 도 합성하였는데, condur itol F 에서 출발하여 라세미 형태로
합성을 보고하였고〔58), Potter 등은 L-chiro-inositol로부터 출발하여 L-chiro-I(2, 3, 5)PJ를 합성 하였다〔59, 60) . 5-4-5 6번 위치 변환 유사체 Ley 둥은 벤젠으로부터 출발하여 이노시톨 유도체를 만들었는데(그 림4-10, 4-47), 에폭시드를 중간체로 하여 다양한 친핵체를 이용한 고리 열림 반응으로 6번 수산기가 치환된 유도체들을 합성하여 라세미 형태로 6-deoxy, 6-methoxy, 6一methyl,6-F인 1(1,4,5)PJ가 만들어 졌다(15, 61) . 라세미 상태의 6-methoxy-I(1, 4, 5)PJ은 Vacca 등에 의 해서도 합성되었다〔요〕. 또, Galactose로부터 Ferrier 반응을 통해 D-6-deoxy-1(1,4,5)PJ가 만들어져서 IPJ 수용체와 대사 효소들에 대한 활성이 검색되기도 하였다〔63〕•
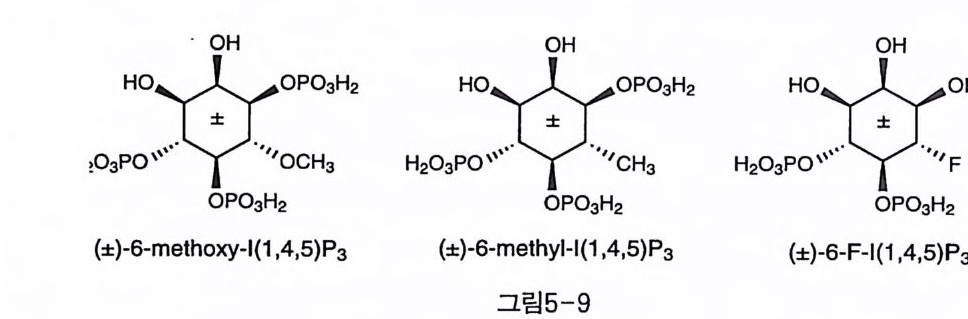 Q3H.( P. OP0O뱌3c2HH542a야 PP Ho::3야H2
Q3H.( P. OP0O뱌3c2HH542a야 PP Ho::3야H2
5-4-6 복수 위치 변환 유사체 라세미 상태의 2,3,6-trideoxy-I(1,4,5)PJ의 합성은 초기에 Vacca 동 에 보고되 었다〔62〕 • Kozikowski 등은 L -quebrachitol로 부터 3 -deoxy -myo -inositol을 얻은 후 계속해서 2번과 6번 위치도 탈수산화 반응으로 광학 활성의
3-deoxy, 2, 3 -did e oxy , 2,3,6- t r i deox y -1 (1 , 4 , S ) P J를 합성하여 fP3 수 용체에 대한 결합 친화도와 칼슘 방출 효과를 연구하였다〔 53). Carless 등은 m y o-1(2)F (I ,4,S)P J 의 3 번 수산기의 입체 구조가 반전 된 라세미 ch i ro-1(6)F(2,3,S)P J를 합성하였다 . 여기서는 수직 방향의 수산기에 DAST 로 반응하였을 때, 입체 구조의 반전이 일어나지 않고 그대로 유지되는 결과가 나타났다〔 64 〕 . Pott er 등은 L- q uebrac hit ol 로부터 L-ch i ro-I (1 , 4 , 6)P J와 그 티오인 산 유도체를 합성하여 5- 포스파타제에 대한 저해제로서의 활성을 검 색하였다〔 65 〕 •
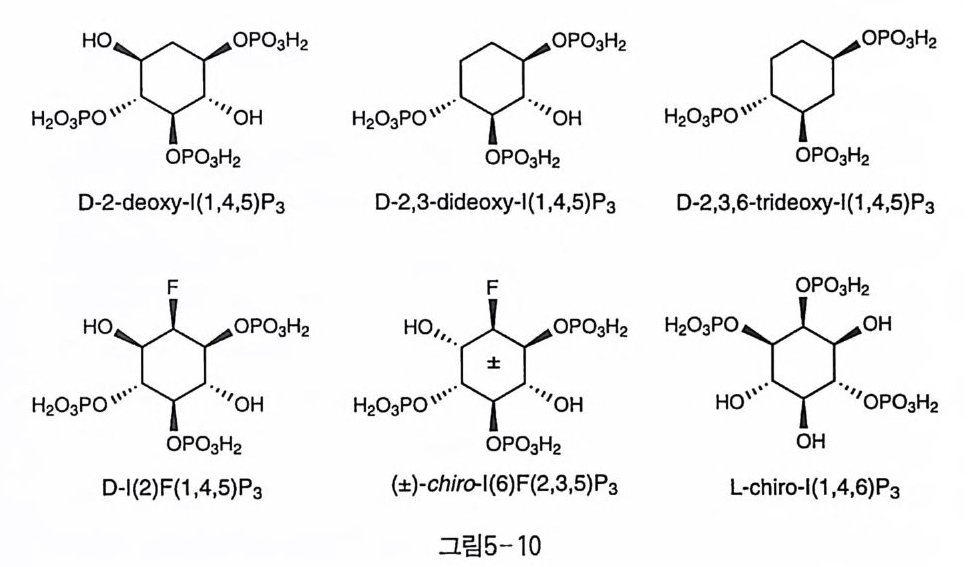 H203 PHO O亨 。O HP0 3H2 H2 야 PO `\` ••亨 OoHP0 3H2 H203PO `\`’ : OP03H2
H203 PHO O亨 。O HP0 3H2 H2 야 PO `\` ••亨 OoHP0 3H2 H203PO `\`’ : OP03H2
5-4-7 이노시톨 고리 변환 유사체 이노시톨 고리 자체에 0 가 개입된 0-su g ar 의 유사체와 육각형 고 리 대신 고리의 탄소 수를 변화시킨 유사체가 보고된 바 있다. Chung 등은 L- 1( 1,4,5)P J의 0-sug ar 유사체로서 mannose-P J〔{i6〕과
그 포스폰산 유사체 (67) 를 합성하여 생리 활성을 검색하였는데, L- 1 (1 ,4,5)P3 와 같이 칼슘 분비에는 효과가 없었고 포스폰산 유사체가 3- 키나제의 저해제 활성을 가지는 것으로 나타났다〔 68). D-l (1 ,4,5)P3 의 0-suga r 유사체로는 아노머 자리에 C-P 결합을 가 진 gal acto s e -P J 가 Vasella 등에 의 해 처 음 합성 되 었으나, 생 리 활성 에 관한 실험 결과는 보고되지 않았다〔 69 〕 . Pott er 동은 포도당에서 출발하여 이노시톨의 육각형 고리 대신 오각 형 고리를 모체로 하는 D-1(1 , 4,5)P3 유사체를 합성하고, 칼슘 분비 효과가 있음을 보였다 (70 〕 ·
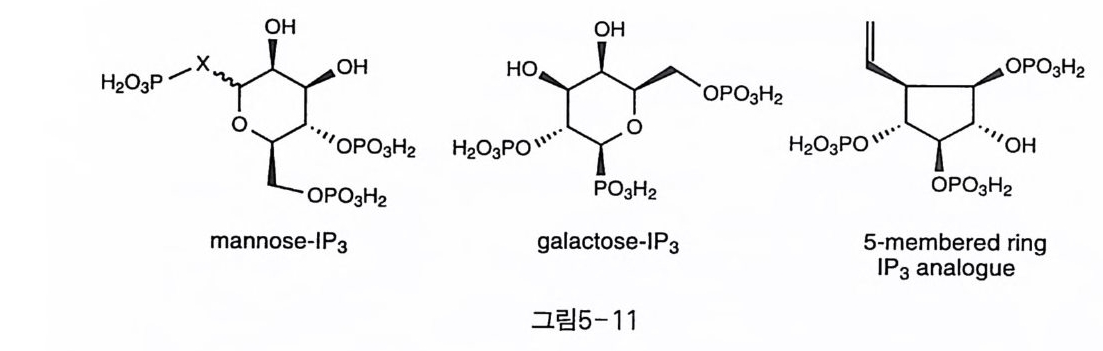 H2 。 3P/x 仁 2 >OH >P 03H 2 >[뱌
H2 。 3P/x 仁 2 >OH >P 03H 2 >[뱌
5-4-8 방사성 동위원소 치환 유도체 생리 활성을 가진 분자에 방사성 동위원소로 표지를 붙이면, 수용체 에 대한 결합이나 대사 과정을 추적할 수 있는 좋은 도구가 된다. 그 래서 인산이노시톨에도 여러 가지 동위원소를 도입하려는 노력이 시도 되었다. 가장 많이 시도된 방법은 특정 수산기를 산화시켜 케톤을 형성시킨 다음 띤 시약으로 환원하여 이노시톨 고리에 전를 도입하는 방법이다. 이 경우에는 방사성 표지가 이노시톨 고리 자체에 붙어 있어서 이노시
톨의 대사 과정까지 추적할 수 있고 턴의 반감기가 길다는 장점이 있 지만, 상대적으로 방사능이 낮은 편이서 민감도가 떨어지는 단점이 있다. 인산이노시톨인 경우에는 31P 대신 32 p로 치환하는 방법도 사용되었 댜 이 경우에는 비교적 반감기가 짧은 대신 방사능 감도가 좋고, 인 산기의 변화를 추적할 수 있다는 장점이 있다. 이노시톨의 티오인산 유도체에서는 뻥 대신 35S 를 표지로 붙이는 예 도 보고되었다. 그리하여 D- 〔 35S)l (1 ,4,5)PS 겁} NEN Du Pon t에서 합 성되어 IP3 수용체 결합 연구〔 71) 에 활용되었다. 5一 4-9 친지질성 유도체 인산이노시톨 자체는 인산기의 음전하와 수산기의 친수성으로 세포 막을 투과하기가 어렵다. 그래서 인산이노시톨의 세포막 통과를 용이 하게 하기 위하여 수산기나 인산기에 에스테르 작용기를 도입하면, 세 포 내의 포스파타제에 의해 에스테르기들이 제거되어 활성을 띤 인산 이노시톨이 생성되리라고 기대할 수 있다. 원래 친지질성의 cAMP 유 도체를 만드는 데 사용된 이 기법〔 72 〕이 인산이노시톨에도 적용되어 I (l ,4,5)P 와 I (1 ,3,4,5)P4 의 친지질 유도체가 합성되었으나, 예비적인 실험 결과만이 보고되었다〔 73). 대개는 ace t ox y me thy l 기가 인산기의 음 이 온을 보호하는 데 쓰이 고, 수산기는 bu tyry l 기 등으로 보호하는 방법 이 시도되었는데, 성공적인 합성과 세포 내의 활성이 보고된 것은 광 학 활성의 D 와 L 의 I (1 ,4,5,6)P4 가 첫 예이다〔 74). 5-4-10 광친화성 유도체 활성이 없는 전구체 형태로 세포 내에 주입되었다가 빛을 조사하였을
때 활성 분자로 바뀌는 화합물을 광불안정 전구체 (ph o to l abil e pre cursor) 이라고 한다 . 이러한 유도체들은 특히 반응 속도론적인 실험에서 분산 속도가 문제를 야기할 때 편리하여 반응 개시로부터의 시간에 따른 변 화를 추적할 수 있다는 장점을 가진다 . Trenth a m 동은 1(1 , 4, 5)P J의 인산기를 (2- nitr op hen yl) d i azoe th ane 으 로 예스테르화하여 하나 또는 여러 자리에 에스테르가 도입된 광친화 성 화합물을 합성하여 칼슘 분비 실험에 이용하였다〔 75 〕· 이와는 달리 광친화성 유도체(p ho t oa ffinity label) 는 빛을 조사하였을 때, 분자 내의 특정 작용기가 활성을 나타내어 주위의 다론 작용기들 과 반응을 일으키도록 만들어진 화합물이다 . 특정 인산이노시톨 수용 체가 존재하는 위치의 규명이나 정제를 위해서는 광친화성 유도체를 만드는 것이 큰 도움이 된다 . 1(1 , 4, 5)P J의 aryla zid e 유도체가 최초로 보고된 광천화성 유도체로 서 , Kog a 등은 1( 1, 4, 5)P 를 p -a zid o benzoic ac i d 와 반응하여 혼합물 상태로 광친화성 유도체를 얻었는데 합성 수율은 9 기 1% 로 그다지 좋 지 않았다 . 그렇지만, 이 화합물은 대식 세포에서 I (l ,4 , 5)P J 의 작용을 비가역적으로 억제할 수 있음을 보여주었고 [76), 같은 연구자들은 방 사성 표지를 단 화합물을 비슷한 방법으로 합성하여 대식 세포에서 3 개의 단백질에 결합한다는 결과를 얻었다〔 77). Ozak i 둥은 D-1(1 , 4, 5)P J의 2 번 수산기 에 p-ami nobenzo y l 을 연결 고리로 하는 다양한 에스테르기를 도입하여 광친화성 유도체를 만들었 다 [78) . 이중 일부는 친화성 지지체 (affini t y ma tri x) 를 만들기 위해 Se p harose 에 결합시킬 수 있었고 [79), 비방사성 표지로서 b i o ti n 을 결 합시킨 유도체는 적혈구 g hos t의 5- 포스파타제를 성공적으로 표지할 수 있었다〔 80). 같은 방법으로 라세미 상태의 1(1 ,3,4,5)P4 와 1(1,3,4,5, 6)Ps 의 2 번 수산기가 치환된 유도체를 만들었으며, 1(1 ,3 ,4,5)P4 친화성 지지체는 소의 심장에서 추출한 막 성분으로부터 IP4 결합 단백질을 분
리하는 데 이용되었다〔81). Ballou 등은 deoxy IPJ의 유사체 로 광천화성 유도체 를 만들었으나, 구체적인 응용은 아직 보고되지 않았다〔8익. 같은 연구자들은 1(1,4, 5)PJ의 1번 인산기에 빛에 의해 활성을 띠는 작용기를 연결한 유사체도 만들었는데, 호염기성 백혈구 세포의 소포체에서 칼슘 분비 능력을 상 당 부분 유지하고 있음울 보였다〔83). Prestwich 등은 1번 인산기에 ro-aminoalkyl로 연결된 친화성 지지 체를 각각 1(1, 4, 5)PJ(84]'I(1, 3, 4, 5)P4(8乳IP6〔8이에 대해 만둘어 각 각 결합 단백질의 분리에 이용하였다. Chen 등은 1(1,4,S)PJ의 6번 수산기에 치환기를 도입한 친화성 지지 체를 이용하여 1(1,4,S)PJ에 대한 항체의 정제에 이용하였다〔8기. 5-5 사인산이노시톨 유사체 및 유도체 1(1,3,4,5)P4의 티오인산 유도체들이 여러 연구자들에 의해 합성되었 댜 van Boom 등은 라세미 형태의 1(1, 3, 4, 5)P4-5S를 합성하였고 (3이, Potter 등은 1(1,3,4,5)P4-3S를 라세미 형태로 합성하여〔88), 5-포스파타제의 저해제 활성을 나타냄을 밝혔다〔89). Kozikowski 등은
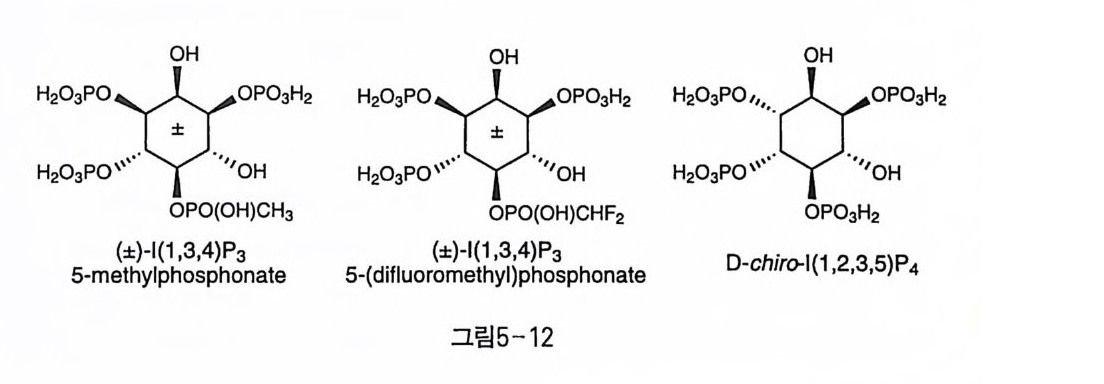 뱌均003 P3P5- OOP成n03H 2 3 H也뱌뱌o 꾼ofH2o3HP20o3 P 0 D二仁 0H2 3m
뱌均003 P3P5- OOP成n03H 2 3 H也뱌뱌o 꾼ofH2o3HP20o3 P 0 D二仁 0H2 3m
L- q uebrach it ol 로부터 출발하여 D-I (l ,3,4,5)P4-3S 도 합성하였다〔 90 〕· I (l, 3, 4, 5)P4 의 포스폰산 유도체 로 5 -m e t h y l p hos p hona t e 와 5 - (d ifl uorome thy l) p hos p hona t e 의 합성 이 van Boom 등에 의 해 보고되 었 는데, 이 유도체들은 IP 의 유도체로도 함께 합성이 보고된 바 있었다 [40 ,4 1] . I (1 ,3,4,5)P4 의 3 번 인산기의 입체 구조가 반전된 D-chir o -I(1 , 2,3, 5)P4 의 합성이 L- q uebrach it ol 로부터 출발한 경로와〔 5 회 D-mannose 로 부터 Ferr ier 반응을 통해 얻어진 경로 (91) 가 각각 보고되었다. 참고문헌 印 Kozik ow ski , A. P.; Xi a, Y.; Rusnak, J. M. J. Chem. Soc., Chem. Commun. 1988, 1301 -1 303. @] Kozik o wski , A. P.; Fauq , A. H. ; P owi s, G.; Melder, D. C. J. Am. Chem. Soc. 1990, 112, 4528 -4 531 . 띠 Of fer, J. L.; Metc a lfe , J. C.; Sm ith, G. A. J. Chem. Soc., Chem. Commun. 1990, 1312-1313. [4) Of fer, J. L.; Voorheis , H. P.; Metc a lfe , J. C.; Sm ith, G. A. J. Chem. Soc., Perkin Trans. I 1992, 953 -9 60. [5] Yang , S. S.; Beatt ie, T. R.; Shen, T. Y. Tetr a hedron Lett. 1982, 23, 5517- 5520. (6) Sawy er , D. A.; Pott er , B. V. L. J. Chem. Soc., Perkin Trans. I 1992, 923- 932. (7) Lowe, G.; McPhee, F. J. Chem. Soc., Perkin Trans. I 1991, 1249-1 253. (8) Yang , S. S.; Beatt ie, T. R.; Shen, T. Y. Syn th . Commun. 1986, 16, 131-138. [9] Y ang , S. S.; Min, J. M.; Beatt ie, T. R. Syn t h . Commun. 1988, 18, 899-905. (10 ) Guid o t, J. P.; Le Gall, T. Tetr a hedron Lett. 1993, 34, 4647 -4650.
(11) Kozik o wsk i, A. P.; Fauq , A. H.; Rusnak, J. M. Tetr a hedron Lett . 1989,30, 3365-3368. U 익 Kozik o wski , A. P.; Fauq , A. H.; Powi s, G.; Melder, D. C. Med. Chem. Res. 19'Jl, 1, 277 -2 82. (13) Powi s, G.; Aksoy , I. A.; Melder, D. C. ; A ksoy , S.; Eic h ing er , H.; Fauq , A. H. ; K ozik ow ski , A. P. Cancer Chemoth e r. Pharmacol. 19'Jl, 29, 95 -104. 〔印 Kozik ow ski , A. P.; Powi s, G.; Galleg os , A.; T ckmante l , W. Bio o rg. Med. Chem. Lett . 1993, 3, 1323 -1 326. (15 ) Ley, S. V.; Parra, M.; Redg rav e, A. J.; Ste r n feld , F. Tetr a hedron 函, 46, 4995-5026. (16 ) Jian g , C.; Moy er , J. D. ; B aker, D. C. J. Carbohyd r . Chem. 1987, 6, 319- 355. 따 Jian g , C.; Schedler, D. J. A.; Morr is, Jr., P E.; Zaye d , A. A.; Baker, D. C. Carbohyd r . Res. 1990, 207, 277 -2 85. (18 ] M 函血` t澤야 ul tz, C 汀血屯 B. ~印야려 ron 뇨 1988, 29 갱副 3922. U 이 Baker, G. R.; Bi lling ton , D. C.; Ga ni, D. Bio o rg. Med. Chem. Lett . 19'Jl, 1, 17 -2 0; ide m, Tetr a hedron 19'Jl, 47, 3895 -3 908. 〔 2 이 Schultz , C.; Jas to r f f, B.; Mets c h ies , T. Tetr a hedron Lett. 1988, 29, 3919- 3920. [21 )L in , G.; Tsa i, M. D. J. Am. Chem. Soc. 1989, 111, 3()( )9- 3101. (22) Bruzik , K. S.; Guan, Z.; Ridd le, S.; T sai , M. D. J. Am. Chem. Soc. 19%, 118, 7679 -7 688. [23 )Dreef, C. E.; Douwes, M.; Elie , C. J. J.; van der Mare!, G. A.; van Boom, J. H. Sy nt h e sis 19')1, 443-447. [24 ] Baker, R.; Kulag ow ski , J. J.; Bi lling ton , D. C.; Leeson, P. D.; Live rt on , N. J. Chem. Soc., Chem. Commun. 1989, 1383 -1385. @]P ie t r us ie w i cz , K. M.; Salamori cz y k, G. M.; Bruzk, K. S. Tetr a hedron
1992, 48, 5523 -5 542; ide m, ibi d . 191J4, 50, 573. 〔 2 이 Hambli n, M. R.; Flora, J. S.; Pott er , B. V. L. Bio c hem. J. 1987, 246, 771- 774. (2 기 Hamblin , M. R.; Pott er , B. V. L.; Gig g, R. Bio c hem. Soc. Trans. 1987, 15, 415-416. [28 ] Dreef, C. E.; Tuin m an, R. J.; Lefe b er, A. W. M.; Eli e, C. J. J.; van der Mare!, G. A.; van Boom, J. H. Tetr a hedron 1991,47,47()C J_ 4722. @]C ooke, A. M.; Gig g, R.; Pott er , B. V. L.; J. Chem. Soc., C hem. Commun. 1987, 1525 -1 526. [30 ) Dreef, C. E.; Mayr , G. W.; Jan sze, J. P.; Roelen, H. C. P. F.; van der Mare!, G. A.; van Boom, J. H. Bio o rg. Med. Chem. Lett . 1 991, J, 239 -2 42. [31 )C ooke, A. M.; Noble, N. J.; Pay ne , S.; Gig g, R.; Pott er , B. V. L. J. Chem. Soc., Chem. Commun. 1989, 269-271; Noble, N. J.; C ooke, A. M.; Pott er , B. V. L. Carbohy dr . Res. 1992, 234, 177 -187. [32 )Noble, N. J.; Dubreuil , D.; Pott er , B. V. L. Bio o rg. Med. Chem. Lett . 1992, 2, 471 -476. [33 ) Lamp e, D.; Pott er , B. V. L. J. Chem. Soc., Chem. Commun. 1990, 1500- 1501. @]L amp e, D.; Mills, S. J.; Pott er , B. V. L. J. Chem. Soc., Perki n Trans. 1 1992, 2899-29 06. 固 Safr an y , S. T.; W ilc ox, R. A.; Liu , C.; Dubreuil , D.; Pott er , B. V. L.; Nahorski , S. R. Mol. Phannacol. 1993, 43, 499 -5 03. [36 ) Liu, C.; Al -Hafi dh , J.; W estw i ck , J.; Pott er , B. V. L. Bi oo rg. Med. Chem. 191J4, 2, 253 -2 57. 詞 Lamp e, D.; Liu, C.; Pott er , B. V. L. J. Med. Chem. 1994,37,9 ff/-9 12. [38 ) Dreef, C. E.; van der Marel, G. A.; van Born, J. H. Reel. Trav. Chim . Pays - Bas 1987, 106, 512-513. [39 ] Falck, J. R.; Abdali, A.; W 血曲따야 S. J. J. Chem. Soc., Chem.
Commun. 1.9'JO, 953 -9 55. 〔삐 Dreef, C. E.; Schie b ler, W. ; van der Mare!, G. A.; van Boom, J. H. Tetr a hedron Lett. 19C J1 , 32, 6021 -6 024. 〔띠 Dreef , C. E.; J an sze, J. P.; Elie , C. J. J.; van der Mare!, G. A.; van Boom, J. H. Carbohyd r . Res. tm, 234, 37 -5 0. (4익 Sch mitt, L.; Sp ies s, B.; Schlewer, G. Tetr a hedron Lett . J.9'J3, 34, 7059- 7060. 困〕 Wi llem s, H. A. M. ; V eeneman, G. H.; Weste r duin , P. Tetr a hedron Lett . 函, 33, 2ff75 -'N IB. [44 )Weste r duin , P.; Wi llem s, H. A. M.; van Boeckel, C. A. A. Carbohyd r . Res. 函, 234, 131 -1 40. 〔 4 회 Weste r duin , P.; Wi llem s, H. A. M. ; v an Boeckel, C. A. A. Tetr a hedron Lett. 1.9'J0, 31, 69I9 -6 922. [46 ] Kozik ow ski , A. P.; Og nya nov, V. I.; Chen, C.; Ku rian , P.; Crews, F. T. Tetr a hedron Lett. J.9CJ3 , 34, 219 -2 22. (47) Inosit ol Phosp ha te s and Deriv a ti ve s -Sy n th e sis , Bi oc hem ist r y and Therap eu ti c Pote n ti al (Ed. Reit z, A. B . ) , Americ a ! Chemi ca l Socie t y , Washi ng ton , DC 血, pp 43 -6 5. 慮〕 Marecek, J. F.; Prestw ich , G. D. Tetr a hedron Lett. 1989, 30, 5401-5404. (49) Saw ye r, D. A.; Pott er , B. V. L. Bio o rg. Med. Chem. Lett. J.9CJ1 , 1, 705- 710. (50) Lamp e, D. ; Pott er , B. V. L. Tetr a hedron Lett . J.9'J3, 34, 2365 -2 368. [51 )B oehm, M. F.; Prestw ich , G. D. Tetr a hedron Lett . 1988, 29, 5217-5220. [52 )Seewald, M. J.; Aksoy, I. A.; Powi s, G.; Fauq , A. H.; Kozik ow ski , A. P. J. Chem. Soc., Chem. Commun. 1.9'JO, 1638 -1639. [53 )Kozik o wski , A. P.; Og ny an ov, V. I.; Fauq , A. H.; Nahorski , S. R.; Wi lc ox, R. A. J. Am. Chem. Soc. 19'J3, JJ5, 4429-4434. [54 )Kozik ow ski , A. P.; Fauq, A. H.; Aksoy, I. A.; Seewald, M. J.; Powi s, G. J.
Am. Chern. Soc. 191JO, 112, 7403 -7 404. [55 )Kozik o wski, A. P.; Og ny an ov, V. I.; Fauq , A. H.; W ilc ox, R. A.; Nahorski , S. R. J. Chem. Soc., Chem. Commun. 1994, 599 -6 00. (5 이 Fauq , A. H.; Kozik o wski, A. P.; Og uy an ov, V. I.; W ilc ox, R. A.; Nahorski , S. R. J. Chem. Soc., Chem. Commun. 1994, 1301 -1 302. [57 ) Kozik o wski, A. P.; Fauq , A. H.; W ilc ox, R. A.; Chall is, R. A. J.; Nahorski , S. R. J. M~d. Chem. 1994, 37, 868 -8 72. 園 Carless, H. A. J.; Busia , K. Tetr a hedron Lett. 函, 31, 1617 -1620. 〔 5 이 Liu , C.; Nahorski , S. R.; Pott er , B. V. L. J. Chem. Soc., C hem. Commun. 1991, 1014-1 016. @]L iu , C.; Nahorski , S. R.; Pott er , B. V. L. Carbohyd r . R es. 19'J2, 234, l
3300-3301. [71 )Challiss , R. A.; Sm ith, S. M.; Pott er , B. V. L.; Nahorski , S. R. FEBS Lett . J.9()1, 281, 101 -1 04. (72) Schult z, C. ; V aja n ap ha nic h , M.; Harootu n ia n , A. T.; Sammak, P. J.; Barrett, K. E.; Tsie n , R. Y. J. Bio l . Chem. 199.3,2 68,6316-6322. 〔히 Schultz , C . ; T sie n , R. Y. FASEB J. 19'J2,6 ,Al924. [74 ) Roemer, S.; R udolf , M. T.; S ta d ler, C .; S chultz, C. J. Chem. Soc., Chem. Commun. J.9CJS , 411 -4 12. 얽회 Walker, J. W.; Somlyo , A. V.; Goldman, Y. E.; Somlyo , A. P; Trenth a m, D. R. Natu r e 1987, 327, 249 -252; Walker, J. W.; Reid , G. P.; McCray, J. A.; Trenth a m, D. R. J. Am. Chem. Soc. 1988, 110, 7170-7177; Walker, J. W.; Feeney, J .; Trenth a m, D. R. Bio c hemi st r y 1989, 28, 3272-3280; Blatt, M. R.; Thie l, G.; Trenth a m, D. R. Natu r e, 1990, 346, 766-769. (76) Hirat a , M.; Sasagu ri, T.; Hamach i, T.; Hashi m oto , T.; K u kita, M.; Kog a, T. Natu r e 1985, 317, 723 구 25. (77) Ish im ats u , T.; Kim ura, Y.; Ikebe, T.; Yamagu c h i, K.; Kog a, T.; Hirata , M. Bio c hem. Bio p h ys . Res. Commun. 1988, 155, 1173 -1 180. 虛〕 Ozaki, S.; Wata n abe, Y. ; O g as awara, T.; Hira ta , M .; Kanemats u , T. Carbohyd r . Res. 19'J2, 2 34, 189 -2 06. 園〕 Hira ta , M. ; Wata n abe, Y. ; I shi m ats u , T.; Yanaga , F.; Kog a, T.; Ozal ci, S. Bio c hem. Bio p h ys . Res. Commun. 1990, 1 68, 379 -3 86. (8 이 Wata n abe, Y. ; H irat a , M.; Og as awara, T.; Kog a, T.; Ozal ci, S. Bio o rg. Med. Chem. Lett. J.9CJ1 , J, 399 -4 02. [81 )O zal ci, S.; Kog a, Y.; Ling , L.; Wata n abe, Y.; Kimu ra, Y.; Hirat a , M. Bull. Chem. Soc. Jpn . 19')4, 67, 1058 -1 063. (82) Jina , A. N.; Ralph , J.; Ballou, C. E. Bio c hemi st r y 1990,29,5203-5'2 ffJ. (83) Tegg e , W. ; B allou, C. E.; Carbohy dr . Res. 函 2, 230, 63-77. [84 ] P restw ich , G. D.; Marecek, J. F.; Mourey, R. J.; Theib e rt , A. B.; Ferr is, C.
D.; Danoff , S. K.; Sny de r, S. H. J. Am. Chem. Soc. 19'Jl, 113, 1822-1825. [85 ] P res 函 ch, G. D.; Este v ez, V. A. Ti印야려 ron Lett . 函 1, 32, 1623 -1 626; Este v ez, V. A.; Prestw ich , G. D. J. Am. Chem. Soc. 19'Jl, 113,9885-9887. 〔 8 이 Marecek, J. F .; Prestw i ch , G. D. Tetr a hedron Lett . 19'Jl, 32, 1863-1866. 〔 8기 Gou, D. M.; Sh ieh , W. R.; Lu, P. J.; Chen, C. S. Bio o rg. Med. Chem. 函 ,2,7-13. (部〕 Liu , C.; Pott er , B. V. L. Tetr a hedron Lett . 19'J4, 35, 1605 -1608. 圈〕 Wi lco x, R. A.; W 血 ham, E. M.; Liu , C.; Pott er , B. V. L.; Nahorski , S. R. FEBS Lett . 19'J3, 336, 267 -2 71. [90 ) Kozik ow ski , A. P.; Fauq , A. H.; Wi lco x, R. A.; Nahorski , S. R. J. Org. Chem. 19')4, 59, 2279 -2 281 . [91 ) C hung, S. K.; Yu, S. H. Bio o rg. Med. Chem. Lett ., 1996, 6, 1461-1464.
제 6 장 구조 활성 관계 및 대사 효소 억제제 6 기 PI -syn t h e ta s e 1(1 , 4, 5)P3 의 전구체인 PI(4, 5)P2 는 이노시톨이 지질과 결합하여 PI 를 형성하는 과정을 거쳐 만들어지는데, 이 과정을 촉매하는 효소가 PI-s y n th e t ase 이댜 PI 는 계속해서 키나제에 의해 인산화되어 PI(4)P 가 되었다가, 다시 다른 키나제 효소에 의해 인산화되어 PI(4, 5)P2 로 바뀌 어 신호 전달의 준비를 갖추게 되는 것이다. 그러므로 이 효소 자체에 대한 억제제뿐만 아니라 기질로 작용하여 PI 의 일부로 만들어지는 이 노시톨 유사체들은 다음 단계중 어딘가에서 신호 전달 과정을 차단할 수 있을 것으로 기대할 수 있다. 최근에는 PI 의 3 번 수산기에 인산화 된 인지질들도 발견되어 1(1 , 4, 5)P3 와는 별도의 신호 전달 과정에 작용 함이 밝혀지고 있다(1 -4 참조). 이들 인지질의 인산화에는 Pl-4- kina se, PI-5- ki nase 뿐만 아니라 PI-3-ki na se 등이 유기적으로 연관 되어 있으며, 각각의 효소에도 다수의 아종류가 존재하여 더욱 복잡한 양상을 나타낸다(1) . 5 장에서 다루었던 인산기를 가지지 않는 이노시 톨의 유도체와 유사체들 중 다수가 PI s yn th e ta se 에 대한 기 질 활성 및
저해 효과가 검색되었다. PI-s y n th e t ase 에 의해 이노시톨 인지질이 생합성되는 경로에 대한 고전적인 연구는 A gr ano ff에 의해 수행되었다@〕. 9 개의 이노시톨 입 체 이성질체 모두를 포함한 다양한 이노시톨 유도체를 이용하여 효소 의 반응성을 연구해 본 결과, PI-s y n th e t ase 가 기질에 대해 까다로운 선택성을 가지고 있음이 밝혀졌다. 이노시톨 이성질체 중에는 my o - i nos it ol 만이 기질로 사용되었고, 이노시톨의 수산기 하나가 산화되어 케톤 형태를 가진 ino sose 중에서는 e pi-i nosose(m y o- i nosose-4) 와 sc y llo- i nosose(my o- in osose-2) 만이 10% 정도의 기질 활성을 나타내 었다. 한편, ep i -inos it ol (15%), cis - inos it ol (40%), scyl l o -i no sit ol (23%), my o -1(2)P(1 7 %), D -m y o -I(l )P (35%), 라세미 my o -1(4)P(1 4 %) 등이 효소 억제제로 작용하였고, 시험된 유사체 중에는 gal actin o l(my o -in o sit ol gal acto s id e , 그림 4-2 참조)이 50% 의 저해 활성 울 나타내어 가장 강력한 억제제로 작용하였는데, 반응 속도론적 연구 결과 비경쟁적 (non-com p e titi ve) 억제제의 특성을 나타내었다〔 3 〕. Baker 등의 연구 결과에서도 PI s yn th e t ase 는 기질 특이성이 엄격하 게 나타났고, 합성된 어떤 유도체들도 이노시톨 자체보다는 기질로서 의 효과가 낮았다. my o- l( 5)F 가 비교적 좋은 기질로 사용되었는데도 이노시톨에 비하면 26% 정도에 불과하였다. 이 유도체는 PI 로 전환된 후에 키나제에 의해 4 번 위치에는 인산화가 되지만, 5 번이 F 로 치환되 어 있어 예상한 대로 더 이상의 인산화는 일어나지 않았다. 5-Deoxy 유도체는 PI s y n th e t ase 에 의해 약하게 기질로 인지(1 5% )되었지만, 다 른 5- 할로겐 치환체들은 기질로 사용되지 않거나 매우 약한 활성만을 나타내었다. 일반적으로 치환기의 입체 장애가 커지면, 기질로서의 활 성이 낮아지는 경향을 보였으며, 좋은 기질일수록 이노시톨 자체에 대 한 효소 저해 효과도 크게 나타났다. 단, 재미있게도 1(5,5)Fz 인 경우 에는 기질로는 작용하지 않으면서도 75% 의 효율적인 효소 억제제로
표 1 (Baker 등) 이노시톨 유도체 및 유사체 기질 활성(%) 저해 효과(%) my o -in o sit ol 100 68 R=H 15 士 4 22 my o -l(S)R FBC lr 256< 土 土5 2 4 <<311000 R=F 16 士 2 15 Cl 10 士 1 <10 neo -1(2)R Br 5 士 2 <10 I <5 <10 NH2 7 士 l <10 my o 一 1(5, 5)F2 <5 75 scyl lo -I(l )R RF =H <<55 <<1100 (土 )-m y o-1(4)R RF =H <<55 <1130 ( 土 ) -l 一 deoxy -m y o -in o sito l 6 士 l 12
작용하였다(기준 : my o -in o sit ol 68%). 각 유사체들의 기질 활성과 저해 효과를 표 1 에 나타내었다 (4). 같은 연구자들은 이노시톨의 3 번 위치 유도체들에도 주목하여, L- q uebrac hit ol 로부터 출발하여 3 겁.mi no, 3-F, 3 -deoxy, 3-keto 등의 유사체들도 합성하여, PI-s yn th e t ase 에 대한 기질 활성과 억제 효과를 연구하였다. 이들 3 번 위치 치환체들은 10% 에 못미치는 약한 기질 활 성을 나타내었지만, 9-47% 정도의 효소 저해 효과를 나타내었다(표 2). 또한 방사성 표지된 이노시톨의 세포 내 유입 저해 실험에서는 3_ deoxy, 3-F, 3-am ino 유사체들이 80- 이% 정도의 저해 효과를 나타 내어, 이들 유사체들이 이노시톨과 경쟁하며 세포 내로 유입되어 PI 로
표 2 (Baker 등) 이노시톨 유도체 및 유사체 기질 활성(%)• 저해 효과 (%)b D-my o- 1(3)deoxy 6 9 D -my o -I (3)deoxy (6)0Me 。 28 D-my o -l(3) NJ 1 17 D-my o -1(3)Nf fi 9 19 D-my o -I(3) NTu(6)0Me 。 10 D-my o- 1(3)CI 1 3 D-my o- 1(3)SH 1.5 40 D-my o- 1(3)F 7 37 D -my o -inos ose -3 7 47 my o -1(5)F 28 22 .,n y o- i nos it ol 이 1 00%일 때 상대적인 값 빈 5 mM my o -(3H)in o sito l and 5mM 유사체 사용.
합성될 것임을 강력하게 암시하였다〔 5 〕 . Lowe 등도 먼로 표지된 이노시톨이 PI 로 만들어지는 반응을 추적하 여 여러 위치에 deoxy, F, Nlh, OMe 등으로 변형이 가해진 이노시톨 유도체들이 나타내는 저해 효과를 측정하였다. 사용된 여러 유도체 중 s cyllo- I(l) F(61%) 와 l( 5)0Me(65%) 이 PI-s y n th e ta se 에 가장 효과적인 억제제임이 밝혀졌다. 또 먼로 표지된 s cy llo-l(l)F 와 my o- l( 2)F 를 이 용한 실험에서 이들 유도체들이 PI-s y n th e tas e 에 약한 기질 활성만을 가지지만, my o- l( 2)F 의 경우 일단 PI 로 합성되면 P I( 4)P 와 PI( 4, 5)Pz 까지 인산화가 진행되는 것으로 보인다〔 6 〕. Of fer 등은 먼로 표지 된 불소화 이 노시 톨들을 이 용하여 이 들 유도체 의 세포 내 유입과 PI 로의 전환 여부〔기를 조사하였다. 사용된 유사체 들 중 D- l( 3)F 와 1(5)F 만이 PI-s y n th e ta se 의 기질로 작용했으며 그중 에서도 D- l( 3)F 만이 세포 내에 유입되고 PI 로 만들어질 수 있었다. 그 러나 세포 내 유입과 PI 로의 전환이라는 두 가지 문제가 동시에 제기
되므로 IF 들은 세포막을 통과할 수 있는 다른 방법을 사용하지 않으 면, 이들 유도체들이 PI(4,5)P2 형성을 막는 억제제로 사용되기는 어려 울 것으로 전망되었다. Kozik ow ski 동은 3 번 위 치 의 변형 에 주목하여, 다양한 유도체를 합 성하여 형질 변환 세포와 정상 세포 (NIB 3T3, Swi ss mouse 의 섬유아세 포)에서 비교 검색하였다 . v- s is - T ransfo rm ed 세포는 PI-3-kin a se 활 성이 증가되어 있는 세포로서, 3 번 수산기가 변형된 유도체가 PI 로 합 성되어 들어가면 PI-3- ki nase 가 더 이상 작용할 수 없어 정상 세포보 다 PI- 3 -ki na se 억제제에 더 민감한 특징을 가진다. 실험 결과 D- 1(3)F 가 강력하고 선택적인 세포 성장 저해 효과를 나타내었고, 배양 액에 이노시톨울 가해 주면 이 저해로부터 어느 정도 회복되었다. 이 불소 치환체는 이노시톨의 세포 내 흡입도 방해하는 것으로 나타나 이 노시톨 인지질 합성의 기질로 작용하는 것으로 생각된다〔 8). 같은 연 구자들에 의 해 q uebrac hit ol 로부터 합성 된 F, a, Br, I, N3, NIL, SH, deoxy 등의 다양한 3 번 위치 변형 이노시톨들은 같은 세포들의 성장 저해 효과를 시험한 결과, I(3) NJ 유도체 (ICso 0.0 4 mM) 가 가장 효능이 뛰어났고 변형 세포에 대해 보다 선택적으로 작용하였다(정상 세포의 1 , 200 배 ) [9, 1 0). 3 번 위 치 에 meth y le ne, hy dr oxy m eth yl, Clhl, pho s- pho nometh yl, dim eth yl pho sph o nometh yl 동이 치 환된 유도체들(그림 5- 3) 은 저해 효과를 나타내지 않았다 (11) . 6-2 Inosito l monop ho sph a ta s e 생리 활성 분자인 IPJ7 l- 만 들어진 후 활성을 나타내고 나면 IP~ 인 산기들이 차례로 가수 분해되어 이노시톨로 되돌아 가는데, ino sito l mono p hos p ha t ase(IM) 는 IP 을 이노시톨과 인산으로 가수 분해하는 효
소이다. 이전에 리튬 이온이 IM 의 무경쟁적 (uncom p e titi ve) 억제제임이 알려져 있었으나, 임상에 사용되는 이 약이 상당한 부작용을 나타냄으 로써 보다 선택적인 억제제의 개발이 요구되었다 . IM 에 대한 억제제 개발은 Merck 연구팀에 의해 광범위하게 시도되어 다수의 이노시톨 유도체 및 유사체들이 합성되었다. I(l )P 유도체에 대한 조사 결과 D-2-deoxy I(l) P 가 IM 의 기질로 받아들여지기는 하지만, 기질 활성이 낮았기 때문에 (Vm .. 78% of I(l )P , Km 1.3 mM), 2 번 수산기가 효소의 기질 인식에 중요한 것으로 유추되었다. 한편, 라세미 6-deoxy I(l )P 유도체는 효소 저해 효과 (ICso 70 µM) 를 가지며, 이와 유사한 L-2-deoxy I (l )P 도 저해 효과 (ICso 50µM) 를 나타내어 6 번 수산기는 기질 인산기의 가수 분해에 관 여하는 것으로 해석되었다(1 2). 그리하여 초창기 연구들은 다양한 위 치의 deoxy 유도체의 합성에 집중되었고, 합성된 화합물 중 라세미 (2, 3, 5) tri deox y -I (l )P 가 약한 효소 저해 효과 (IC20 90 µM) 를 나타내었 다 한편 D-(3 , 5, 6) tri deox y -I(1)P 는 강한 저해 효과 (ICso 3 µM) 를 나 타내었고, L-(3,5,6) tri de9x y -I (l )P 는 약한 기질 활성을 나타내어 3, 5 번의 수산기는 기질 인식에 그다지 중요하지 않음을 시사하였다(그림 6-1) 〔 1 이. 또한, 2 번 위치에 다양한 알킬 치환기가 도입된 라세미 l(l )P 유도체들도 합성되었는데, 2-0Et( Ki 40 µM) 이 가장 저해 활성 이 높았고, -0Me(70 µM), -0Bt (l50 µM), -0Hex(210 µM) 등의 순 으로 나타났다 (14). 이는 IM 의 결합 부위로 생각되는 2- 수산기 결합 자리에 상당한 공간이 자리하고 있음울 유추하게 한다. 일반적으로 IM 은 기질 특이성이 높지 않아서 여러 IP1 이성질체에 작용할 뿐만 아니라 2'-AMP 와 같은 뉴클레오티드의 가수 분해도 촉 매하는 것으로 알려져 있었다. 2'-AMP 와 D-(3, 5, 6)tr ide oxy - I(l) P 룰 겹쳐 보았을 때, 6 번 위치의 치환(푸린 염기에 해당)이 효소에 의해 허용될 것으로 전망되어 Merck Sha rp & Dohrne 의 연구자들에 의해
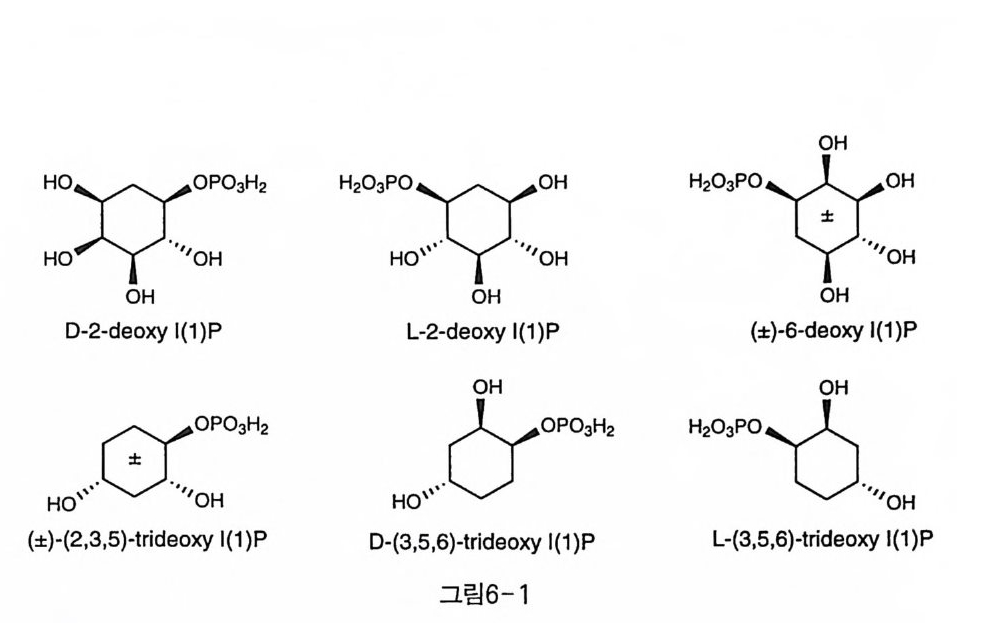 ::亨::야 H2 H2°3PHoo:IOo: H2 。3 P。 O>H
::亨::야 H2 H2°3PHoo:IOo: H2 。3 P。 O>H
3, 5-d i deox y -I (l )P 의 6 번 위치 치환체가 다수 합성되었고, 그중 1- (2-hyd r oxy ph eny l) -buty l 치환체가 현재까지 알려진 화합물 중 가장 강한 억제제로 밝혀졌다 (ICso 0.('fJ µM) 〔 1 회 . 한편으로는 생체 내에서 비교적 비특이성인 포스파타제에 의해 쉽게 가수 분해되는 인산기 대 신 보다 안정한 포스폰산 등으로 치환된 유도체들을 만들고자 하는 시 도도 있었다. 그러나, I(l) P 의 인산기를 포스폰산으로 단순 치환한 I(1)me thy lene p hos phona t e(16) 나 (3, 5, 6) tri deox y -l (l )P 의 포스폰산 유 도체는 아무런 저해 효과를 가지지 못하였다(그림 6-2) 〔 17 〕. 같은 연구자들은 무기 인산기 자체도 IM 의 약한 경쟁적 억제제(Ki 0.5 2 µM) 로 작용한다는 사실에 착안하여 me thy leneb i s p hos p hona t e 룰 이 노시톨 골격에 도입한 화합물들을 합성하여 IM 에 대한 저해 효과를 검색하였다(그림 6-3) 〔 17). 이노시톨 C-1 자리에 산소 원자가 없는 경 우 효소에 대한 친화도가 크게 감소하며, 산소가 존재하는 경우에도 mono p hos p hona t e 보다는 b i s p hos phona t e 가 강한 친화도를 나타내 었다. Me thy leneb i s p hos p hona t e 나 hy dr oxy m eth yle ne p hos p hona t e 가 뛰 어 난 효소 억제 효과를 나타내었으므로, 이를 기본 골격으로 한 다양한 화
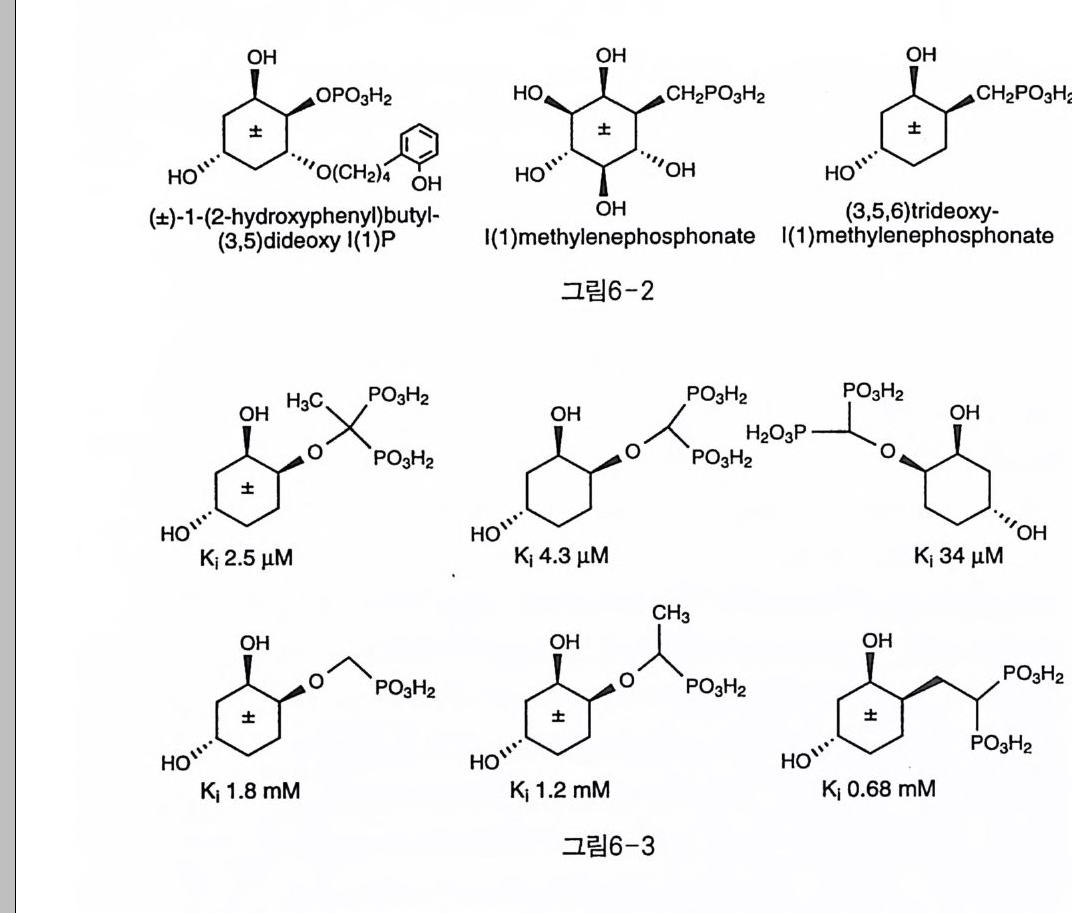 HO`> ::C 0:::H HHo::2PO3H2 HO```.> CH2 PO3H2
HO`> ::C 0:::H HHo::2PO3H2 HO```.> CH2 PO3H2
합물들이 합성되어 활성이 검색되었다(1 8 〕. 이노시톨과 구조적 유사성 이 없는 화합물 가운데에서는 3-(3, 4-di ch lorobenza rnido )benzy l 유도 체가 가수 분해에 저항을 가지는 화합물 중 가장 강한 저해 효과를 나 타내 었다 (ICso 0.08 µM) (그림 6-4) [19 ] · 인산기보다 일반적으로 가수 분해가 어려운 I(l )PS 도 각각 D 와 L 형 태로 합성되었는데, 두 이성질체 모두 1M 의 기질로 작용하여 천천히 가수 분해되었으며 약한 경쟁적 억제제로 작용하였다 (D, L 모두 Ki 1.0 µM) [20 ] . IM 자체의 효소 기작과 기질과의 결합 방식을 밝히기 위한 연구도
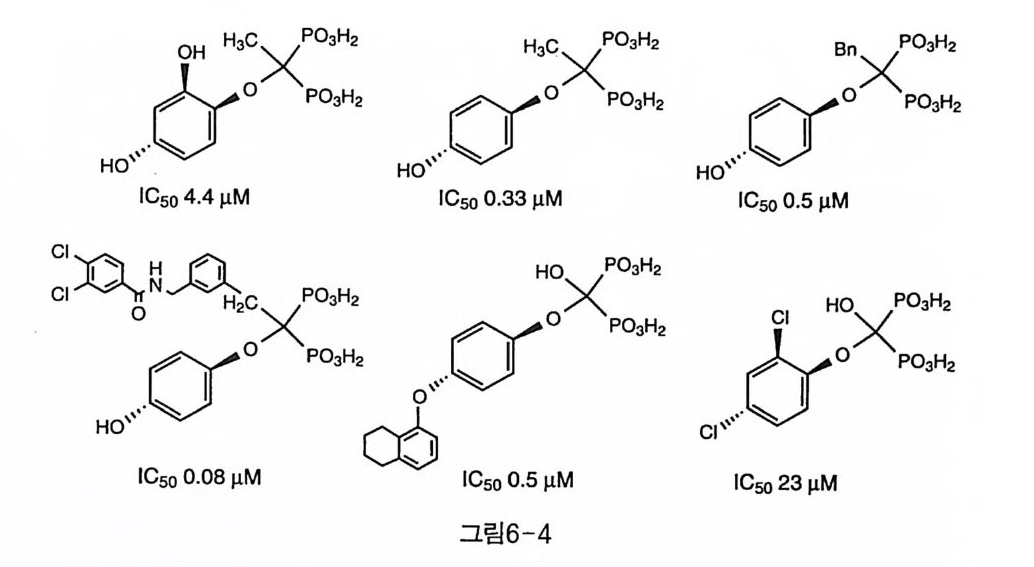 H3c X PO3 H 2 Bn XP O3H2
H3c X PO3 H 2 Bn XP O3H2
수행되었다 . 효소 작용에 필수적인 M g:z..에 대한 Li+의 저해 작용 기작 연구 @U 와 이노시톨울 매개로 한 리간드의 산소-인 간의 치환 반응 〔 22 〕이 먼저 연구되었다. 기질과의 결합 방식은 아데노신 2- 인산〔 23 〕 과 이노시톨 구조 및 유사체들에 대해 상세하게 연구되었다〔 24-26). 6— 3 IP3 수용체 I (l ,4,5)P J 이 수용체에 결합해 칼슘울 분비하여 다양하고 중요한 세 포 내 반응을 유발한다는 사실이 정립되었기에(1-2, 1-6 참조), IP~ 수용체에 대한 결합 방식과 칼슘 분비에 대한 구조적 요건을 밝히기 위한 연구가 광범위하게 이루어졌다. IP3 가 일차적으로 결합하는 주 요 3 가지 단백질 중 I(l, 4, 5)PJ 3- 키나제가 기질 특이성이 가장 높 고, I(1 , 4, 5)PJ 5- 포스파타제가 가장 낮은 데 비해 칼슘 통로인 I(l , 4, 5)PJ 수용체는 기질 특이성에 있어 그 중간 정도인 돗하다.
수용체에 대한 결합에서 1(1 , 4, 5)P3 의 각 인산기 및 수산기가 하는 역할을 규명하기 위하여 각 위치가 변형된 1(1 , 4, 5)PJ 유도체 및 유사 체들이 합성되었고 (5-4 참조), 합성된 화합물들의 수용체 결합력 및 칼슘 분비 능력의 검색을 통해 구조-활성 관계가 정립되고 있다. 먼저 1 번 인산기 에 입 체 장애 가 큰 작용기 (gly c e rol, gly c o aldehy de , allcyla m ino eth a nol 등)를 도입 한 유도체 들을 기 니 피 그의 이 하선 세 포 (pa roti d acin a r cell) 에서 칼슘 분비 효과로 시험해 본 결과, IP3 에 비해 (ECso I.7 µM) 대 부분의 유도체의 ECso 값이 3 _ 8 배 정 도로만 증가하였 으며 칼슘 분비 최대치는 모든 유도체에서 동일하였다〔 2기 . 1 번 인산 기에 3-am ino p ro p yI 에스테르와 아미노기 말단에 광친화성 유도체를 만든 경우 칼슘 분비 능력은 쥐의 뇌에서 분리된 수용체에서 IP3 에 비 해 8 배 정도로만 약해지며 [28 ), 이 광친화성 유도체는 IP3 의 결합 부위 가 수용체의 N 말단 20% 부근에 해당한다는 사실을 밝히는 데 성공적 으로 사용되었다〔 29). I (l ,4,5)P3 의 1_ 티오인산 유도체와 여기에 형광 표지가 붙은 유도체도 합성되어 역시 칼슘 분비의 효능제로 작용할 것 으로 기대되었으나 아직 생화학적인 결과는 보고되지 않았다〔 30). Ozaki 등은 I(l , 4, 5)P3 의 2 번 수산기 위 치 가 변형 된 유도체 들을 합 성하여 쥐의 소뇌 또는 소의 부신 피질에 대한 결합력과 기니피그 대 식 세포에서의 칼슘 분비 효과를 검색하였는데 [31 ), 2-deoxy 유도체 는 2_3 배 정도로만 활성이 줄어든 완전 효능제였다. 한편, 수직 방향 의 2 번 수산기에 에스테르 결합으로 연결된, 입체 장애가 큰 작용기들 이 도입된 유도체들도 1.5-8 배 정도로 약해지긴 했으나, IPJ 수용체에 대한 완전한 효능제로 작용하였다. 칼슘 분비뿐만 아니라 수용체에 대 한 결합 친화도에서도 비슷한 경향을 나타내었다. Pott er 등은 1(1 , 4, 5)P3 의 2 번 수산기의 입체 구조가 반전된 scy ll o-1(1 , 2, 4)P3 와 수산기 가 F 로 치환된 my o -l( 2) F( l, 4, 5)P J도 라세미 형태로 합성하였는데 [32 ),S H-SY5Y human neuroblasto m a 세포에서 1(1 , 4, 5)P J보다 각각
3 배와 2 배 정도만 약해진 완전 효능약으로 작용하였다〔 33). 라세미 상 태의 scyl l o-1(2)F( l, 4, 5)P 와 1(2, 2)2(1 , 4, 5)P3 도 Pott er 등에 의해 합 성되어 〔 3 섞, SH-SY5Y 세포 (35) 와 1321Nl human as tr oc yt oma(36) 에 서 칼슘 분비 효과가 검색되었다. 1( 2,2)F2 (1 ,4,5)P3 에서는 두 세포 모두 에서 IP3 보다 3 배 정도 약해진 효능약으로 작용하였고, scy l lo-1( 2) F( l, 4, 5)P3 은 각각 6 배와 12 배 정도 낮아진 칼슘 분비 효과를 나타내었다. 구조적으로 비교해 보면, sc y llo ―유사체나 2, 2-Fz 유도체에 비해 my o — 1( 2)F( l, 4, 5)P 과 자연상의 IP 폐 더 가깝다고 할 수 있다. F 는 수소 결합의 받게 역할은 할수 있지만, 주게 역할은 할 수가 없는데 l(2) F( l, 4, 5)P3 가 IP3 와 비슷한 효능을 나타내므로 IP3 가 수용체와 작용 할 때 2 번 수산기가 수소 결합 받게의 역할을 담당할 가능성이 있다. 한편, 같은 연구자들이 보고한 lP4 중에는 라세미 상태로 합성된 my o - 1(1 , 2, 4, 5)P 가 壓보다 약 3 배 정도 약한 데 비해〔 33, 37), 2 번 인산기 가 수평 방향으로 배향된 scy l lo-I(1 , 2, 4, 5)P4 〔 38 〕는 lP3 와 거의 동둥한 강한 칼슘 분비 효과를 나타내었다〔 33). 소의 부신 피질을 이용한 수 용체 결합 친화도에서는 이들 유도체들이 IP3 보다 6-12 배 정도 낮은 것으로 나타났다 (33). 라세미 화합물들 중 D 형태만이 수용체 결합과 칼슘 분비에 중요한 역할을 한다고 가정하면 이들 2 번 유도체들은 자 연상의 1(1 , 4, 5)P3 와 거의 동등한 효능약이라고 볼 수 있다. 그러나 아 직 각각의 이성질체들이 모두 합성된 것은 아니어서 추가적인 연구가 필요하다. 한편, scy ll o-1(1 , 2, 4, 5)PS4 는 IP3 보다 30 배 정도 효능이 약 해졌으며, 최대 칼슘 분비 량도 80% 정도인 부분 효능약(p ar ti al a g on i s t)으로 작용하였다〔 3 기. 위의 두 연구팀의 결과를 종합해 보면 1(1 , 4, 5)P3 의 2 번 위치에는 음전하를 띠거나 중성인 치환체가 입체 배 향에 관계 없이 도입되어도 IP3 수용체에 대한 결합 및 칼슘 분비 효과 에는 큰 영향을 미치지 않는다는 것을 알 수 있다. 따라서, 2 번 수산 기는 앞에서 언급한 대로 수소 결합의 받게 역할을 수행하거나 아예
수용체와의 결합에 관여하지 않을 가능성도 있다. 1(1 , 4, 5)P J의 3 번 위치 치환체 중 deoxy 유도체는 NIH 3T3 세포에 서 완전한 효능약으로 작용하였는데, 이 세포에서 I(1 , 3, 4, 5)P4 는 칼슘 분비 효과를 나타내지 않았다〔 39). F 유도체도 합성되어, Swi ss 3T3 세포에서 1(1 , 4, 5)P J와 거 의 동등한 칼슘 분비 효과를 나타내 었고 〔때, SH-SY5Y 세포에서는 1(1 , 4, 5)P J보다 3 배 정도 약한 효능약으 로 작용하였다〔 4 1) . Ozak i 등은 3 번 위치 에 Bz 을 바 롯한 입 체 장애가 큰 치환체가 도입된 1(1 , 4, 5)P J의 유도체를 만들어 쥐 소뇌에서 결합 친화도를 검색했는데, 2 번 치환체들이 높은 친화도를 나타낸 데 비하 면〔 31) 100 배 이상으로 매우 낮아진 활성만을 나타내었다〔 42). 1(1 , 4, 5)P J의 3 번 수산기는 그대로 유지한 채, 수직 방향으로 CFJ가 추가로 도입된 유도체는 수용체 결합도에서 IP3 에 비해 3 배 정도만 약해진 데 비해, 3 번 위치에 수직 방향의 인산기가 도입된 L-chir o -I(1 , 2, 3, 5)P4 는 700 배 이상 친화도가 낮아졌다〔 43 〕 . 칼슘 분비 효과도 비슷한 경향 을 나타내었으며, 이는 수용체 결합에 있어 3 번 수직 방향으로 어느 정도의 입체 장애는 허용되지만 인산기와 같은 음전기를 띤 치환체는 허용되지 않는 것으로 보아 수용체 부분이 음전하로 대전되어 있을 가 능성을 제시하였다〔 43 〕. 3 번 수산기의 입체 구조가 반전된 L-chir o - 1(2, 3, 5)P J〔 44 군i 5 〕도 lP 데 비해 SH 一 SY5Y 세포에서 칼슘 분비예 대 한 ECso 가 5-10 배 정도로서 상당한 칼슘 분비 효능을 가지고 있었다 [41 ). 이 화합물의 인산기가 티오인산으로 치환된 L-chir o- I(2, 3, 5)PS 의 경우에는 ECso 값이 IP 려 14 배 정도이며 최대 칼슘 분비가 33% 정도인 부분 효능약으로 나타났다〔 33) . 1321Nl human astr oc y tom a 에서 칼슘 분비 효과를 측정하였을 때에는 L-chir o -1( 2, 3, 5)P J이 IP3 의 10 배, 3-F 치환체는 IP 려 3 배 정도로만 약해진 효능을 나타내었다 [36 ).한 편, 수평 방향으로 배향된 3 번 위치의 치환기가 H, F 외에도 Cl, Br, OCIL 등으로 입체 장애가 커질수록 수용체에 대한 결합력과
칼슘 분비 효과가 줄어드는 것이 관찰되었다〔 46, 47] . 이는 1(1 , 4, 5)P3 의 3 번 수산기가 3_ 키나제에 의해 인산화된 I(1 , 3, 4, 5)P 4 가 수용체에 대한 친화도가 낮아진다는 관찰과 일치하는 경향이다. 3 번 수산기에 인산화된 생성물인 D- 1 (1 , 3, 4, 5)P4 는 소뇌막에서 1(1 , 4, 5)P J의 결합을 저해하는 효과를 나타내긴 하지만, IP3 에 비하면 380 배 정도로 낮은 결 합력 을 가지 고 있었다〔 48 〕 . 한편 소의 대 동맥 평 활근 (bov i ne aort ic smooth muscle) 에서의 칼슘 분바에도 라세미 1(1 , 3, 4, 5)P 는 1R 에 비해 200 배 정도 낮은 효능을 나타내었다〔 4 이 . D— 3 -am ino - I (1 , 4, 5)P J는 SH-SY5Y 세포에서 1P 폐 비해 14 - 21 배 정도로 약한 효능약으로 작 용하였는데, pH 7.2-7.6 에서는 완전 효능약으로, pH 6.8 에서는 80% 정도의 부분 효능약으로 작용하였다. 한편, 쥐 소뇌막에 대한 결합 친 화도 실험에서는 pH 6.8-7.6 영역에서 완전한 IPJ 치환이 일어나므로 pH 변화에 따른 수용체 형태의 변화 가능성이 제시되었다〔 50 〕• 1(1 , 4,5)P3 중 4, 5 번 인산기는 칼슘 분비에 필수적인 것으로 보이고 [51 ), 4 번 인산기는 수용체의 인식에 중요하게 작용하여 4_P 가 없는 유사체들은 활성을 나타내지 못하였다 . 세 개의 인산기가 모두 티오인 산으로 치환된 I(1 , 4, 5)PS3 은 Swi ss 3T3 세포에서는 1(1 , 4, 5)P J에 비해 3-4 배 정도만 약해진 효능을 나타냈으며〔 5 2, 53), SH- S Y5Y 세포에 서 23 배 정도 약한 칼슘 분비 효능약으로 작용하였는데 (54), 1(1 , 4, 5)PJ - 4 , 5S2 도 이와 비슷한 칼슘 분비 효과를 나타내었다〔 55). 쥐 소 뇌막을 이용한 결합 친화도 실험에서는 1(1 , 4, 5)PS J이 1(1 , 4, 5)P3 에 비 해 2-3 배 정도로만 낮아진 친화도를 나타내었다〔 48 〕 . 그러나 아직 4 번 만 선택적으로 치환된 유도체의 활성은 검색되지 않아서 4 번 인산기의 역할에 대해서는 좀더 연구가 필요하다. Pott er 등에 의해 합성된 라세미 상태의 1(1 , 4, 5)P3-5S 〔%〕는 SH- SY5Y 세포에서 1(1 , 4, 5)P3(ECso 0.1 1 µM) 에 비해 7 배 정도 약한 완전 효능약 (ECso 0.8 µM) 으로 작용하여, 23 배 정도 약한 1(1 , 4, 5)PSJ (E Cso
2.S µ M) 보다는 높은 활성을 나타내었다〔 54). 또 I(1 , 4, 5)P3-SS 로 처 리 했을 때는 분비된 칼슘의 재흡수가 관찰되었으나, I(l, 4, 5)PS3 은 3- 키 나제와 5- 포스파타제에 대해 저항성을 가져서 지속적인 칼슘 분비가 가능하였다. 1(1 , 4, 5)P J -5S 는 5- 포스파타제에 대해서는 저항성을 가 지지만 3- 키나제에는 기질로 작용하여 인산화되는 것으로 보인다 [54 ).티 오인산 유도체뿐만 아니라 1(1, 4, 5)P3 의 5-meth y le nep ho sph o -nate 유도체도 소의 부신 (bov i ne adrenal g land) 에서 지속적인 칼슘 분비 효과를 나타내었다g기 . 5-Me t h y l p hos p hona t e 는 사람의 혈소판에서 IP 려 칼슘 분비에 길항 효과를 나타내었으며 IP3 수용체에 경쟁적으로 결합하였다 . 함께 합성된 5-di fluo rometh ylp h o sph o nate 유도체는 훨씬 약한 길항 효과를 나타내었는데, 이 화합물들은 IP3 의 작용에 선택적 길항 효과를 나타내는 첫 유도체로 기대된다〔 58). I(l , 4, 5)P3 의 D-6-deoxy 유도체는 g alac t ose 로부터 합성되어, SH- SYSY 세포에서 칼슘 분비의 완전한 효능제로 작용하였지만 IP 폐 비 해서는 70 배 정도 낮은 효능을 나타내었다〔 59). 따라서 6 번 수산기가 수용체 결합과 칼슘 분비에 상당히 중요한 역할을 담당하지만, 절대적 으로 필요한 것은 아니라고 볼 수 있다. 다양한 6 번 치환 유도체들이 합성되었으나 생물학적 특성이 검색된 것은 많지 않은데, 라세미 상태 의 6-0Me 유도체는 평활근에서 칼슘 분비에 대한 ECso 가 IP 려 200 배 에 달했다〔 49). D- I( l,4,5)P3 의 6 번 위치에 긴 친지질성 사슬을 달아 친화성 지지체로 활용할 수 있도록 만든 유도체는 돼지 뇌 미립체에서 IP 폐 비해 200 배 정도 낮은 칼슘 분비 효과를 나타내었다〔 60 〕. 6 번에 인산기가 도입된 라세미 I(l , 4, 5, 6)P4 는 칼슘 분비 효과도 없을 뿐만 아니라 고농도에서도 IP 려 작용에 아무런 영향을 나타내지 않았다 [61 ). 6- 수산기는 수용체 결합 또는 수소 결합을 통해 IP3 의 형태를 고정하는 데 필요한 것으로 생각되며, 따라서 6-F 치환체에 대한 생 리 활성 검색이 요구된다고 하겠다.
입체 특이성의 측면에서 보면, L-1 (1 ,4,S)P J는 칼슘 분비 능력이 없 고〔 5 2, 53), 수용체에 대한 결합력은 D-1(1 , 4, 5)P3 에 비해 있 H) 배 이상 낮은 것으로 보인다 (49, 62]. 이 와 같은 입체 특이성은 각각 D, L 의 I(2,2)F 2 (1,4,5)P3 을 사용한 실험에서도 확인되었다 . 즉, SH-SY5Y 세 포를 이용한 칼슘 분비 실험에서 D 형은 1(1 , 4, 5)P3 에 비해 2 배 정도 활 성이 낮아지긴 하지만 완전한 효능제인 반면 L 형은 400 배 이상 활성이 낮아졌다〔 63 〕• 1(1, 4, 5)P 분만 아니라, 고리형 인산기를 가진 1(1 , 2)cP(4, 5)P2 의 중 요성 에 대 한 이 견들이 한동안 다양하게 제기 되 었다. 초기 에 Swi ss 3T3 세포〔 64 〕와 혈소판〔 65 〕울 이용한 칼슘 분비 연구에서는 1(1 , 2)cP(4, S)P27} 1 (1 ,4,5)P 와 대등한 칼슘 분비 효과를 가지고, Lim ulus 광수용 체에서의 전도성 유도에서는 1(1 , 2)cP(4, 5)P27l- 1 (1 , 4, 5)P3 보다 다섯 배 나 강한 효과를 나타내는 것으로 보고되어 [65 ),1(1 , 2)cP(4, 5)P2 자체 가 새로운 2 차 전달 물질일 것으로 제안되었다. 그러나 추가로 쥐의 소뇌막에 대한 결합력과 Swi ss 3T3 세포에서의 체계적인 칼슘 분비 실 험을 해본 결과 1(1 , 2)cP(4, 5)P2 의 효능이 1(1 , 4, 5)P3 에 비해 각각 40 배 와 10 배 이상 약한 것으로 나타났다〔()6) . 이전의 실험에서 나타난 1(1 , 2)cP(4,S)P 의 강한 칼슘 분비 효과는 산 등에 의한 가수 분해로 인해 1(1 , 4, 5)P 파 생성되어 일어난 것으로 추정되었다. 기니피그의 대식 세 포를 이용한 칼슘 분비 실험에서도 1(1 , 2)cP(4, 5)P2 의 활성이 1(1 , 4, 5)P3 에 비해 10 배 이상 낮아진다는 것이 관찰되었다〔 31). 그리하여, 칼 슘 분비 에 작용하는 가장 중요한 2 차 전달 물질은 1(1 , 2)cP(4, 5)Pz 가 아닌 1(1 , 4, 5)P3 이라는 것이 정립되었다. 한편 여러 연구팀들에 의해 1(2, 4, 5)Pl7} D-I( l, 4, 5)P3 에 비해 평활 근 세포에서 (라세미 상태일 때) 29 배 [49 ),Swi ss 3T3 세포에서 13 배 [g], 기니피그 대식 세포에서 49 배〔 31), 쥐의 간세포에서 69 배〔 67), 쥐 의 호염기성 백혈구에서 31 배 [68 ] 정 도 약하기는 하지만 뚜렷한 칼슘
분비 효과가 있음이 밝혀졌다. 1( 2, 4,5)P3 는 1(1 , 4,5)P3 수용체에 결합하 여 칼슘 분비 효과를 가질 뿐만 아니라, 3- 키나제나 5- 포스파타제 동 의 대사 효소에 의해 쉽게 대사되지 않으므로, 안정한 1(1,4,5)P3 유사 체로 다양한 생물학 실험에 이용되었다. 그러나 1( 2, 4,5)P3 의 최대 효능 을 검사하기 위해 쥐의 간세포에서 초기 칼슘 분비 속도를 측정해 본 결과, 1(2, 4, 5)P3 는 1(1 , 4, 5)P3 에 비 해 65% 정도의 부분 효능약임 이 밝혀 졌댜 한편 리 간드의 협 동성 을 나타내 는 Hill 상수도 1(1 , 4, 5)P3 가 3 인 데 비해, 1(2, 4,5)P3 는 1. 9 로서 두 리간드의 작용 방식에 차이가 있음을 나 타내었다. 쥐의 간세포에는 1P3 수용체 제 1 형이 약 19%, 제 2 형이 81% 정도 발현되는 것으로 알려져 있기는 하지만 1( 2, 4,5)P3 가 부분 효능약 으로 작용하는 기작이 수용체 아형의 분포와는 관계가 없는 것으로 보 인다〔 69). D-1( 2, 4,5)P3 의 1 번 수산기의 입체 구조가 반전된 D-chi ro - I (l ,3,4)P3 도 1( 2, 4,5)PJ 와 비슷한 ECso(I (l ,4,5)PJ 보다 30 배 정도 높은 값) 울 가진다는 것이 함께 보고되었다〔 68, 70). 이때, L 형은 D 형보다 800 一 %0 배 약하게 나타나서 입체 선택적임을 나타내었다. D-chir o -1(1 , 3, 4)P 는 D-1 (1 ,4,5)P의 1 번 인산기의 입체 구조가 반전된 것으로도 볼 수 있는데, 이들 수직 방향의 인산기를 가진 유도체들이 1P3 수용체에 비교적 강하게 결합하는 것은 이노시톨 고리가 결합에 용이하도록 변형 되었거나, 1P3 와 수용체 간에 새로운 결합 방식이 존재할 가능성도 있 댜 1(2, 4, 5)P3 의 3 번 위치가 변형된 D-3-azid o -1( 2, 4, 5)P3 는 인간의 결장암 세포인 HT29 에서 매우 낮은 칼슘 활성을 나타내었고, 수용체 에 대한 결합력은 1(1 , 4, 5)P3 보다 2CXX}배나 약하게 나타났다 (71) . Kozik ow ski 등의 연구에 의하면, 1 (1 ,4,5)P3 에서 차례로 3-deoxy, 2, 3-did e oxy 유도체를 만들어 SH-SY5Y 세포에서 칼슘 분비 효과가 검 색되었을 때에는 그다지 효능이 약해지지 않았지만(각각 3 배와 4 배), 2, 3, 6- tri deox y에서는 급속히 효능이 떨어지는 현상 (EC 와 IP 려 200 배)이 관찰되었다〔 72). 이는 이전에 라세미 형태의 tride oxy 유도체로 평활근
에서 실험했을 때와 유사한 결과이다 (ECso IP 려 130 배)〔 49). I(l )P (4, S) py roP 는 칼슘 분비 활성을 나타내지 않았고 (5 회, Jp 3 의 인산기 대신 sulfa te, sulfo n am ide , carboxy m eth y l, meth y lp h o sph o nate 등의 다른 입체 등방성 치환체를 도입한 유도체들은 혈소판 응집이나 리간드 결합 조사에서 아무런 활성을 나타내지 않았다〔 73, 74] • Schultz 동은 cis, cis - cyc l ohexane 1, 3, 5-P3 와 cis- cyc l ohexane 1, 5-I% 가 Neurospo ra crassa 에 서 분리 된 액 포로부터 칼슘울 분비 할 수 있음을 보였다〔 75) . 그러나 I(l, 3, 5)P3 가 평활근에서는 활성을 나타내 지 않았으므로〔 49), Neurospo ra crassa 의 수용체가 포유 동물과는 다 룰 가능성을 보여주었다. 그러나, 현재까지 알려진 IP3 수용체들의 구 조는 종에 따라 상당한 동일성을 유지하고 있는 것으로 알려져 있었기 에 이 가능성은 세심한 주의를 기울인 검증이 필요하다. I(l , 3, 4, 5)P4 의 칼슘 분비에 대한 정확한 역할에 대해서는 논란이 분 분한데, 1(1 , 4, 5)P3 에 3- 키나제가 작용하여 생성되는 이 대사 물질이 세포 외의 칼슘울 세포 내로 유입한다는 · 가설〔 76) 과 IP3 와 같은 수용체 에 작용하여 칼슘울 방출한다는 가설이 있다〔 7 기 . 자연에서 발견되는 lP4 중에서는 I(1 , 3, 4, 6)P4 가 SH_SY5Y 세포에 서 1(1 , 4, 5)P3 에 비해 50 배 정도 약하지만 뚜렷한 칼슘 분비 효과를 나 타낸다는 것이 관찰되었다〔 61). 그러나, 이 경우 최대 칼슘 양은 IP3 의 90% 정도인 부분 효능약으로 작용하였다〔 3 이. 높은 농도에서 I(l ,3 ,4, 6)P 가 I(l , 4, 5)P3 의 작용을 방해하는 것으로 보아 이 lP4 는 1(1 , 4, 5)P3 수용체에 작용하여 칼슘을 분비하는 것으로 추정되었다. 혈소판을 이 용한 실험에서도 IP3 에 비해 약 54 배 정도 약한 활성을 나타내었다 W 이 라세미 상태의 1(1 , 4, 5, 6)P4 는 쥐의 소뇌막에 대한 결합 친화도 에서 IP 폐 비해 630 배 정도 약하게 결합하였다〔 48 〕. 여러 IP3 중에서는 재미있게도 D-I(l , 4, 6)P3 가 IP3 수용체의 완전한 효능제로 작용한다는 사실이 밝혀졌는데, 쥐의 호염기성 백혈수에서의
칼슘 분비는 1(1 , 4, 5)P J 의 125 배 정도 약하였고, 쥐 소뇌에 대한 결합 친화도는 16 배 약한 정도였다〔 79). D-1(1 , 4, 6)P J 을 D-1(1 , 4, 5)P J와 겹 쳐 보면 2, 3 번의 수산기가 반전된 형태임을 알 수 있다. 합성된 라세 미 1(1 , 4, 6)P J을 혈소판에서 시험했을 때는 1(1 , 4, 5)P J에 비해 11 배 정 도 약한 효능약으로 작용하였다〔 78 〕 • 1(1 , 3, 4)PJ 역시 칼슘 분비에 관여한다는 보고가 있었으나, 그 입체 구조에 대해서 한동안 일치되지 않은 논란이 있었다 (4-4-4 참조) . Ozak i 등은 D-1(1 , 3, 6)P J이 쥐의 호염기성 백혈구에서 1(1 , 4, 5)P J에 비해 89 배 정도 약한 칼슘 분비 효과가 있음울 보고하였다〔 79 〕 • P 야t er 등은 정확한 구조 결정과 함께 1(1 , 3, 4)P J의 두 광학 이성질체를 모두 합성하고 Lim ulus 광수용체에서 D- 1 (1 , 3, 6)P J가 D-1(1 , 3, 4)P J에 비해 훨씬 강하게 칼슘을 분비한다는 사실을 증명하였다〔 80). D- I (1 , 3, 6)PJ 울 D-1(1 ; 4, 5)P J와 비교하면 2, 6 번의 수산기가 반전된 형태이다 . 그 러나 라세미 1(1 , 3, 4)P J는 평활근에서 I(l , 4 , 5)P J 보다 400 배나 낮은 칼 슘 분비 효과를 보였기에〔 49), 다른 수용체에서도 마찬가지 효과를 가 지는지는 명확하지 않다. 그밖에 1(4, 5)P2(400-650 배)〔 67, 7 이, GroP I( 4,5)P2(3 - 10 배)〔 27, 66] 등은 IP폐 비해 수용체에 약하게 결합하였으나 l(l )P , 1(1 , 2)cP, 1(1 , 4)P2 〔히〕’ D-1(1 , 3,4)PJ[ 53 ), 1(1 ,3,4,5,6)Ps 固, 8 익, IP6 효) 등 대부분의 IPn 들은 壓 수용체 에 대한 항진 효과가 거의 없었다. 1(4, 5)P2 의 포스폰 산 유도체가 합성되어, 쥐의 호염기성 백혈구에서 칼슘 분비 효과가 검 색되었는데, 1(4, 5)P2 에서는 ECso 70µM 로 약하지만 효능을 나타낸 데 비해〔 7 이 포스폰산 유도체는 5mM 에서도 아무런 효과가 없었다 (83 〕. 이상에서 검색된 활성들을 종합해 보면 4, 5 번의 인산기는 1(1 , 4, 5)PJ 수용체의 인지에 필수적이며, 1 번 인산기가 칼슘 분비 능력을 크 게 향상시킨다고 할 수 있다. 1( 2,4,5)P J가 상당한 활성을 가지므로 1 번 인산기와 2 번 인산기가 수용체의 동일한 부분과 결합할 가능성이
있으며, 1 번 인산기나 2 번 수산기에 입체 장애가 큰 치환체가 도입되 어도 활성이 유지되므로 이 부분은 용매 쪽으로 배향되어 있을 수도 있다. 3 번 수산기 부분은 작은 치환체가 도입되었을 때와 입체 구조가 반전된 경우에도 활성이 상당 부분 유지되므로 크기에 적합한 주머니 부분이 수용체에 존재할 것으로 기대된다 . 6 번 수산기는 수소 결합을 통하여 결합을 도와주므로 상당히 중요한 부분이라고 불 수 있다. 이 상에서 얻어진 정보로 재구성한 IPJ 수용체의 결합 모형을 그림 6-5 에 나타내었다 .
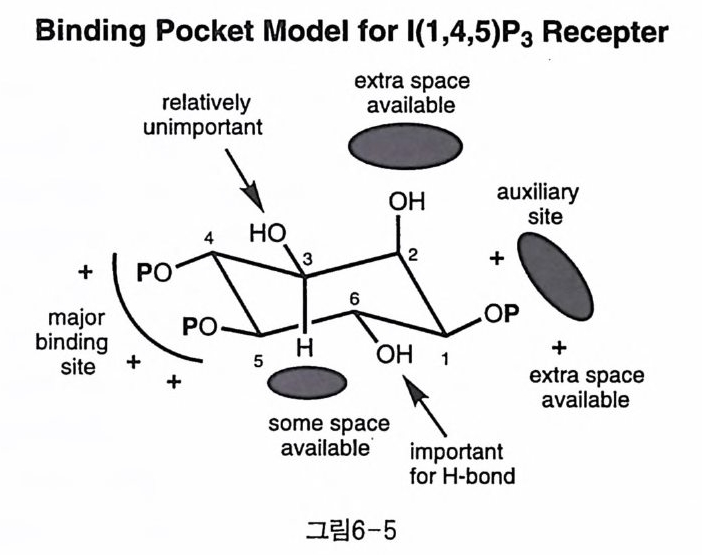 Bi nd in g u nPriem olapc tio kvr\ et e alytn t M odel- fa ov 『Oa i1lH a( b 1le,4 ,5)P3s iRt e e cep ter
Bi nd in g u nPriem olapc tio kvr\ et e alytn t M odel- fa ov 『Oa i1lH a( b 1le,4 ,5)P3s iRt e e cep ter
6-4 IP3 3-ki na se 1(1 , 4, 5)P3 의 주요 두 가지 대사 경로 중 하나는 3_ 키나제에 의한 인산화 반응으로 1(1 , 3, 4, 5)P4 가 생성된다. 3 弓기나제의 기질 특이성온 IPJ 수용체 자체 보다 더 큰 것으로 보인다〔 84 〕 .
1 번 인산기가 없으면 쥐 뇌에서 부분 정제한 3- 키나제에 대한 친화 성은 급격하게 낮아져서 1(2, 4, S)Pl 는 인산화되지 않고, I(4, 5)P2 는 매 우 약하게 기질 활성을 나타내었으며 [85 ),I{l , 2)cP(4, S)Pz 도 같은 3- 키나제에 의해 인산화되지 않았다〔 86) . 또, I(1, 4, 5)P3 굿 ,s 〔 54), I{l , 4, S)PJ -4 , 5S2(87 〕는 1(1 , 4, 5)P3 보다 느리긴 하지만 기질로 작용하여 인 산화되는 반면, I(l, 4, 5)PS3 〔 54 갤이는 인산화가 일어나지 않았다• 한 편 1(1 , 4, 5)P3 에 대한 도키나제의 Km 이 3.2 µM 일 때 I(I, 4, 5)PS3(K 230µM) 과 I{l , 4, 5)Pr5S(Ki 5 µM) 는 친화도에서 상당한 차이룰 보이 며 경쟁적 억제제로 작용하였다〔 54). 이것은 1 번 인산기가 효소의 기 질 인지에 중요한 역할을 담당함을 나타낸다. 라세미 상태의 2- d eoxy - I(1, 4, S)P J는 1(1 , 4, 5)P3 의 인산화를 효과적 으로 저해하였는데, 그 K 값은 IP3 자체와 유사한 정도였다〔 31) . 2 번 수산기에 입체 장애가 큰 치환기가 도입된 경우에도 효소와 강하게 결 합하여 경쟁적 억제제로 작용하였는데, 이들이 기질 활성을 갖는지는 보고되지 않았다〔 31). 라세미 상태의 sc y llo-2-F 와 2, 2-F2_I(l, 4, 5)P3 는 모두 I(1,4,5)P3 보다 느리긴 하지만 3- 키나제의 기질로 허용되 었다〔 35 〕 . 2, 2-F2-I{l , 4, 5)P3 울 각각의 이성질체로 분리하여 확인한 결과 D 형은 기질로 사용되었으나, . L 형은 억제제로 작용하였다〔 6 이 . L 형 의 이성질체가 저해 작용을 나타내는 기작은 명확하지 않으나, 칼슘 분비에 관여하지 않으면서 효소 억제 효과를 나타내므로 선택적인 효 소 억제제 개발에 실마리가 될 것으로 기대된다. 라세미 1(2)F{ l, 4, 5)P3 는 효소의 기질이면서 한편으로는 뛰어난 저해 효과 (K 3.0 µ M, IP3 의 4 배)도 가지고 있었다〔 33). 2 번 수산기가 역전된 scy ll o-1(1 , 2, 4)PJ 도 약한 기질이면서 억제제(Ki 4.0µM , IP 려 5 배)로 작용하였다〔 33 〕. 2 번 위치에 인산기가 도입된 I{l , 2, 4, 5)P4 는 고농도에서도 효소에 의해 인지되지 않았는데, 2 번 인산기가 역전된 s cy llo-I {1 ,2,4,5)P4 와 그 티 오인산 유도체는 I{l , 4, 5)P3 보다 각각 30 배와 67 배 약한 억제제로 작용
하였다〔 33). 이 결과를 종합해 보면 2 번 수평 방향으로는 어느 정도의 여유 공간이 존재하는 것으로 보이는데, 수직 방향으로 입체 장애는 허용하면서도 인산기 도입은 허용되지 않으므로 2 번 수직 방향에 음전 하를 띤 아미노산들이 배치되어 있을 것으로 추정된다 . 예상할 수 있는 바와 같이 D-3-F-my o -l(1, 4, S)PJ 또는 입체 구조 가 반전된 L- c hir o -1( 2, 3, S )PJ 등의 3 번 치환 유도체들은 3 - 키나제에 의해 인산화되지는 않았고, 각각 I(l , 4, S)PJ( Ki 3.2 µM) 보다 3 배 (K 8.6µM) 와 2 배(Ki 7.1 µM) 약한 정도의 억제제 활성을 나타내었다〔 41). L- c hir o -1( 2, 3, S)P J의 티오인산 유도체인 L-chir o -1( 2, 3, S)PS J는 IP3 와 거의 같은 효소 억제 효과를 나타내, 현재까지 알려진 화합물 중 가 장 강력한 3- 키나제 억제제이다〔 8 이. 3 번 위치에 Bz 울 비롯한 입체 장 애가 큰 치환체가 도입된 1 (1 ,4,S)P J의 유도체들은 대부분 활성을 나타 내지 않았는데, 단지 3-m-am ino benzoyl 치환체가 높은 저해 활성을 나타내었다〔 42) . 3-p- amino benzoy l 치환체는 아무런 효과가 없었으 므로, 3 번 수산기의 수평 쪽 특정한 방향에 음전하를 띤 결합 부위가 존재할 가능성을 제시한다. 3 一 키나제의 생성물인 I{l ,3,4,5)P4 는 라세미 상태 로 약한 억 제 제 활성 (ICso 90 µM, !PJ의 35 배 ) 을 나타내 었다〔 49) . 그 러나 효소의 저해에 과량의 I(l , 3, 4, 5)P4 가 요구되므로, I(1 , 3, 4, 5)P4 에 의한 3- 키나제의 음의 되먹이기 기전 (ne g a ti ve fe edback) 이 생체내 에서 존재한다고 보기는 어렵다 . 3- 키나제에 의해 3 번 위치에 인산화가 일어나면 IPJ 수용체로부터 쉽게 떨어져 나가게 되므로, 이 인산화는 IP 려 수용체 결합을 조절하는 것으로 생각할 수 있다. I(l , 3, 4, S)P4 - 5S 도 3- 키나제에 경쟁적인 억제제로 작용한다는 보고가 있었다 (90) . 4 번 인산기만을 선택적으로 변형한 유도체는 아직 3_ 키나제에 대한 활성 이 검사되지 않았고, I(1, 4, 5)P3-4, 5S2 는 I(l, 4, 5)P J -5S 에 비해 10 배 정도 3 ―키나제에 대한 친화도가 낮았다〔 87). 이것은 4 번 인산기 가 효소 인지에 중요함을 암시한다.
앞에서 언급한 대로 1(l, 4, 5)P3-5S 가 3- 키나제의 기질로 사용되기 는 하지만, 1(1 , 4, 5)P3 에 비해서는 매우 느리게 반응이 일어난다〔 54). 그래서 5 번 인산기도 효소 인지에 상당한 영향을 미치는 것으로 생각 할수있다. 6-Deoxy - I(1, 4, 5)P3 는 1(1 , 4, 5)P3 에 비해 절반 정도의 친화도로 3- 키나제에 인지되어 1(1 , 4, 5)P3 의 인산화를 저해하는 효과를 나타내 며, 명확한 증거는 없지만 3- 키나제의 기질로 작용할 것으로 보인다 (59). 그러나 라세미 상의 6-0Me 유도체는 친화성이 120 배나 약화되 었는데〔 49), 마찬가지로 수소 결합의 가능성이 없는 deoxy 유도체는 3- 키나제에 강한 친화도를 보였기 때문에, 6-0Me 기에 대한 효과는 입체 장애에 의한 것으로 판단된다. 1(1 , 4, 5)P3 에서 차례로 수산기가 제거된 3-deoxy, 2, 3-did e oxy , 2, 3, 6-tri de oxy - 1(1 , 4, 5)P3 유도체들은 3- 키나제에 대한 저해 효과를 나타내었는데, IP3 에 바해 각각 29 배, 22 배, 42 배 낮아진 효능을 나타 내었다〔 91 〕. 입체 선택적인 면에서 살펴보면, L-1(1 , 4, 5)P3 는 D-1(1 , 4, 5)P3 에 비해 100 배 이상 3- 키나제 저해 효과가 낮아진다 (ICso 292µM)[4 9 ] . 그 런데 재미있게도 L-1(2, 2)Fz(l , 4, 5)P3 은 효소에 강한 저해 효과를 나 타내었다(Ki 11. 5 µM) [63 ] . 라세미 cyc l ohexane-1, 2, 4-P J는 약한 저해 작용 (ICso 327 µM, IP J의 126 배)만을 나타내었는데〔 49), 놀랍게도 benzene-1, 2, 4 - P J가 3- 키나 제에 높은 친화성 (ICso 6.1 µ M, IP J의 9 배)으로 인지되어 효소 저해 효과 를 나타내었다〔 92). 그러나, 이 화합물의 포스폰산 유도체는 3- 키나 제에 대해 아무런 생리 활성을 나타내지 않았다〔 91). 라세미 또는 메 조 상태로 합성된 1(2, 4, S)P3, 1(1 , 2, 4)PJ, 1(1 , 3, 5)P3 동은 3- 키나제에 거의 저해 효과를 나타내지 않았다〔 49 〕 . 한편 D-1(1 , 4, 5)P3 의 2, 3 번 수산기가 역전된 형태인 D-1(1 , 4, 6)P3 은 3- 키나제에 강력한 억제제로
작용하였으나 2, 6 번 수산기가 역전된 D-1(1 , 3, 6)P J은 거의 저해 효과 를 나타내지 못하였다. 그러나 이 두 IP3 는 모두 3- 키나제의 기질로 작용하지 는 않았다〔 79 〕 , 한편, 발산적 합성으로 얻어진 가능한 모든 인산이노시톨의 이성질 체를 이용하여, IP3 ki nase 에 대한 억제 효과를 측정한 결과 6 번 위치 의 수평 또는 수직 방향이 입체적으로 치환된 이성질체들은 결합이 허 용되지 않았으며 , 3 번 수산기의 수평 방향은 허용되지 않지만, 수직 방향으로는 치환기를 도입할 수 있는 여유 공간이 존재하는 것으로 추 정되었다〔 93 〕 , 이상에서 얻어진 IP3 ki nase 에 대한 구조 활성 관계를 그림 6-6 에 정 리하여 나타내었다.
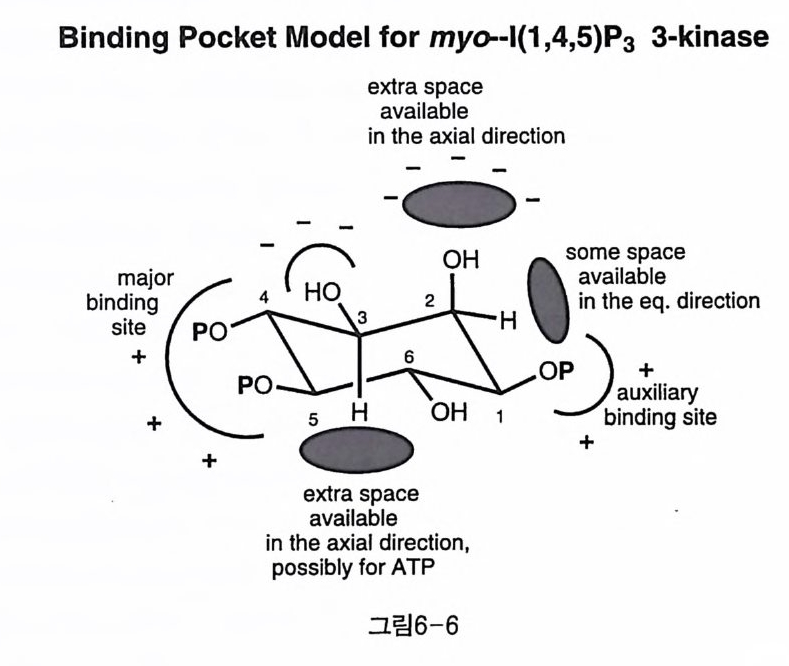 Bin d in g Pocket Model fo r my o--1 (1,4,5)P3 3-kin a se
Bin d in g Pocket Model fo r my o--1 (1,4,5)P3 3-kin a se
6-5 fP3 5 -p ho sph a ta s e 5-Phos p ho t ase 는 IP3 수용체 나 3-키 나제 에 바 해 상대 적 으로 특이 성 이 낮아서 많은 이노시톨 유사체들이 결합할 수 있지만, 기질로 사용 될 수 있는 것은 소수에 불과하다. 우선 1(4, 5)Pz 가 기질 활성이 매우 낮은 것으로 보아 1 번 인산기는 기질 인식에 중요한 역할을 담당하는 것으로 보인다 (87). 2 번 수산기가 변형된 1(1 , 4, 5)P3 유사체들은 대부분 5- 포스파타제의 경쟁적 억제제이면서 동시에 기질로 작용할 수 있었다〔 31). 놀라운 것 은 2-deoxy - 1(1 , 4, 5)P J를 비롯한 대부분의 2 번 변형 유사체들이 1(1 , 4,5)P3 자체보다도 효소에 대한 친화성이 더 크게 나타난 것이다. 라세 미 2-F-my o -I(l, 4, 5)PJ (Ki 14 .4 µM) 과 2 번 수산기가 역전된 scyl l o- 1(1 , 2, 4)P3(Ki 24.2 µM) 은 1(1 , 4, 5)P3(Ki 15 µM) 와 비슷한 정도의 저해 효과를 나타내었으나, 기질로는 작용하지 않았다〔 33). my o - I (I , 2, 4, 5)P,(K i 2.9 µM), scyl l o-I(I , 2, 4, 5)P4(K1 4.3 µM), scyl lo -I(l, 2, 4, 5)PS,(Ki 0.3 µM) 등은 IP3 보다도 5- 포스파타제에 높은 친화도를 나타 내었는데, 이중 scyl l o-I(l , 2, 4, 5)P4 만이 기질 활성을 나타내었다〔 33 〕• 2-F-scy ll o-I(l , 4, 5)P3 은 효소에 의해 인지되어 인산 가수 분해가 일 어나기는 하지만 1(1 , 4,5)P3 보다는 약한 기질로 작용하였다 (35 〕. 라세 미 2, 2-Fz-l(1, 4, 5)P3 은 5- 포스파타제의 억제제로 먼저 보고되었으나 [35 ), 각각의 광학 이성질체가 합성되어 검색된 결과 D 형은 좋은 기 질로 작용하였으며, L 형은 효소 억제제로 작용하였다(Ki 26 µM)[6 3 ). 일반적으로 5- 포스파타제는 D-I(l , 4, 5)P3 에 선택적이며 L 형은 D-1(1 , 4, 5)P3 보다 20 배 이상 저 해 효과가 낮기 때문에 [94 ), 이 결과는 간단하 게 설명하기가 어렵다. 2 번 위치에 입체 장애가 큰 치환기가 도입된 경우, D-I(l , 4, 5)P3 유도체들은 5- 포스파타제의 기질로 작용하였는 데, L-2-am ino benzoy l- 1(1, 4, 5)P3 은 D-1(1 , 4, 5)P3 보다도 4 배나 강한
효소 억제제 활성을 가지고 있음이 보고되었다〔 95 〕. 3-Deoxy 유도체는 좋은 기질로서 1(1 , 4,5)PJ 자체보다도 조금 더 큰 친화성으로 효소에 결합하고〔 87), 3-F 유도체도 1(1 , 4, 5)P3 보다 10 배 나 강한 친화도를 보이며, 경쟁적 억제제 작용을 나타내었으며, 동시 에 5- 포스파타제의 기질로도 작용하였다〔 4 1) . 3 번 위치에 Bz 울 비롯 한 입체 장애가 큰 치환체가 도입된 1(1 , 4, 5)P J의 유도체들은 대부분 IP 와 비슷한 정도의 효소 억제 활성을 나타내었다〔 42). 한편, 3 번 수 산기의 입체 구조가 반전된 L-chir o -I(2, 3, 5)P J는 1(1 , 4, 5)P3 보다 5 배 정도 강한 억제제로만 작용하였다〔 41). L-chir o -1(2, 3, 5)P J의 티오인 산 유도체인 L 국 h i ro-1(2, 3, 5)PS J는 1P3 보다 무려 60 배나 강한 효소 억제제로 밝혀졌으며 이것은 현재까지 알려진 가장 강력한 5- 포스파 타제 억제제이다〔 89 〕 , 3 번에 인산기가 도입된 1(1 , 3, 4, 5)P4 는 소의 대 동맥에서 정제된 5_ 포스파타제에 대해 놀랍게도 1(1 , 4, 5)P3 자체보다 도 9 배나 높은 친화도를 나타내었으며, 효소의 기질로 작용하여 천천 히 가수 분해되었다〔 49 〕. 혈소판에서 분리된 5 一포스파타제에서도 같 은 결과가 얻어졌으며, 이때 생성물로 1(1 , 3, 4)P3 가 만들어졌다〔 86). 5 번 인산기를 티오인산으로 치환한 유사체도 기대한 바와 같이 억제 제로 작용하였는데 (Ki 6.8 µM), I(l , 4, 5)PS3 은 Ki 1.7 µM 로서 I(l , 4, 5)P3-5S 보다 좋은 억제제로 나타났고, 두 유사체 모두 5- 포스파타제에 의해 가수 분해되지 않았다〔 54 〕 . I(1, 4, 5)P3-4, 5S2 도 5- 포스파타제에 대해 저항을 나타내며, 강한 억제제로 작용하였다(Ki 1.3 µM)[5 5 ).한 편 1(1 , 4, 5)PS J은 1(1 , 3, 4, 5)P4 5- p hos pha t ase 에도 저해 효과(Ki 1.33 µM) 를 나타내었다 (54). 5- 포스폰산 유도체는 지속적인 칼슘 분비 효과를 나타내어 5_ 포스파타제에 의한 가수 분해를 저해하는 효과를 가진 것 으로 추측되었지만 정확한 효소 활성은 아직 보고되지 않았다〔 5 기. 6 번 위치 변형체들도 5- 포스파타제에 대해 저해 효과를 가지며, I(l , 4, 5)P3 에 비해 D-6-deoxy -I(l, 4, 5)P3 은 2 배〔 59), 라세미 6-0Me
은 4 배 정도로만 친화도가 감소하였다〔 4 이 . 즉, 6 번 수산기는 기질과 효소의 결합 자체에는 영향이 크지 않은 데 비해 효소의 반응 기작에 관여하는 것으로 해석할 수 있다 . 한편 1(2, 4 , 5)P3 따, 49) 와 I(l , 2 )cP(4, 5)P2[ % ,% )는 효소의 기질로 작용하지만, 라세미 I(l , 4, 5)PS J 는 탈인산화되지 않았다〔 9 기 . L- 1 (1 , 4, 5)PSJ( K 1 0.50 µM), 1(1 , 3, 5)PSJ (K 1 0.4 3 µM), chir o -1(1 , 4, 6)PSJ (K 1 0.3 µ M) 등은 5- 포스파타제에 좋은 억제 효과를 가지며, 이들은 칼슘 분비에 관여하지 않고, 뒤의 두 화합물은 3- 키나제에도 작용하지 않 아서 5- 포스파타제의 선택적인 억제제로 쓰일 수 있다〔 98 〕 . 한편 D- I(l , 4, 6)P3(Ki 9.2 µM) 과 D-1(1 , 3, 6)P3( K i 27.4 µM) 은 5- 포스파타제에 대한 강한 저해 효과를 나타내었으며 D-I(l ,4 ,5)P3(K i 15.9µM) 과 비슷 하거나 오히려 높은 친화도를 나타내었다〔 7 이 . D- 1 (1 , 4, 6)P3 과 D-I(l, 3, 6)P 운 모두 D-1(1 , 4, 5)P3 보다 느리긴 하지만 효소의 기질로 작용하 여 천천히 가수 분해되었다. 입체 선택성 면에서 보면, L-1(1 , 4, 5)P3 는 D 형에 비해 3 배 정도로 만 친화도가 낮아졌을 뿐이다〔 4 이 . 또 4, 5 위치의 이웃한 인산기가 존 재하지 않는 다른 IP 3 도 5- 포스파타제에 시험되었는데, 라세미 상태의 I(l , 3, 4)P 와 I(l, 3, 5)P3 는 L-~(1 , 4, 5)P3 와 비슷한 정도의 효소 저해 효 과를 나타내었다〔 49 〕 • 라세미 cyc l ohexane -1, 2, 4-P J는 5-포 스파타제 에 약한 저 해 작용 (Ki 137 µM, IP 려 11 배 )을 나타내 었는데 [49 ], benzene -1, 2, 4 - I 》는 K 32 µM 로 IP 파 거의 비슷한 값(Ki 38 µM) 을 가진 것으로 나타나 새로 운 종류의 억제제의 가능성을 보여주었다 (92 〕 . 그러나, 이 화합물의 포스폰산 유도체는 IP3 에 비해 10 배 정도 약한 저해 효과를 나타내었다 [91 ).이 노시톨의 술폰산 유사체들이 칼슘 분비에서는 생리 활성을 나타 낸 예 가 거 의 없는데 , cyc l ohexane -1 , 2, 4-tri s ( meth yle nesulfo n ate ) 가 IP3 보다 4배 나 높은 5- 포스파타제 저해 효과를 나타내었다〔 91 〕 •
6-6 IP4 수용체 1(1 , 3, 4, 5)P4 의 작용 기작을 밝히는 시도의 하나로, IP4 가 결합하는 수용체를 찾고자 하는 노력도 활발히 진행되고 있다. 초기 연구로서 쥐의 소뇌막 IP4 결합 자리에 친화도를 조사한 결과 라세미 상태의 1(1 , 3, 4, 5)PS 4 만이 약 12 배 정도 낮은 친화도를 나타내었을 뿐, 1(1 , 4, 5, 6)P4, 1(1 , 3, 4, 6)P4, 1(1 , 3, 4, 5, 6)Ps, IP6 등의 다양한 인산이노시톨들 이 l00 배 이 상 낮은 친화도만을 나타내 었다〔 48 〕 . Sny de r 등은 IP4- pho to a ff inity label 을 이용하여, 쥐의 뇌에서 182, 84, 174 kD 의 결합 단백질들을 분리하였다〔 99 〕 . 분리된 단백질 중 일부는 IP4 뿐만 아니 라, 1P 폐 친화성을 가진 것으로 나타나 생체 내에서의 역할은 계속 규 명 중이다. Irvin e 등은 돼지의 혈소판으로부터 104kD 의 단백질을 분리하였 고, 이것을 말초 조직에서의 IP4 수용체일 것으로 추정하였다(1 00) . 이 단백질은 몇 종류의 IP3 나 IPs, 그리고 가능한 모든 IP4 위치이성질체 9 개 중 1(1 , 3, 4, 5)P4 에만 선택적으로 결합하여, 높은 결합 특이성을 나 타내었다 (10 1) . 구조 활성 관계 분석 결과, 1(1 , 3, 4, 5)P4 중 1, 3, 5 인 산기가 결합에 중요할 것으로 기대되었으나, 1 (1 ,3,5)P3 를 이용한 직접 적인 시험은 아직 이루어지지 않았다 . 한편 이 단백질은 뒤에 GTPase acti va ti ng p ro t e i n(GAP) 의 일종이라는 것이 밝혀져서, 인산이노시톨을 통한 신호 전달계와 단백질 키나제 경로 간에 신호 교차가 존재할 가 능성을 제시하였다 (102). Reis e r 등은 돼지 소뇌로부터 42 kD 의 결합 단백질을 분리하였는 데, 이 단백질은 1(1 , 3, 4, 5)P4 뿐만 아니라 1(1, 3, 4, 5, 6)P s 에 비슷한 정 도의 친화성을 나타내었다 (103 〕 . 이 단백질에 가능한 모든 IP:i, IP4, IPs 위치 이성질체들을 이용하여 결합 정도를 측정한 결과, 2 번 수산기가 결합에 중요한 역할을 수행한다는 것과 3,4,5 번 위치의 인산기가 필수
적임을 나타내었다(1 04). 이 단백질의 구조 활성 관계는 그림 6-7 에 정 리하여 나타내었다 .
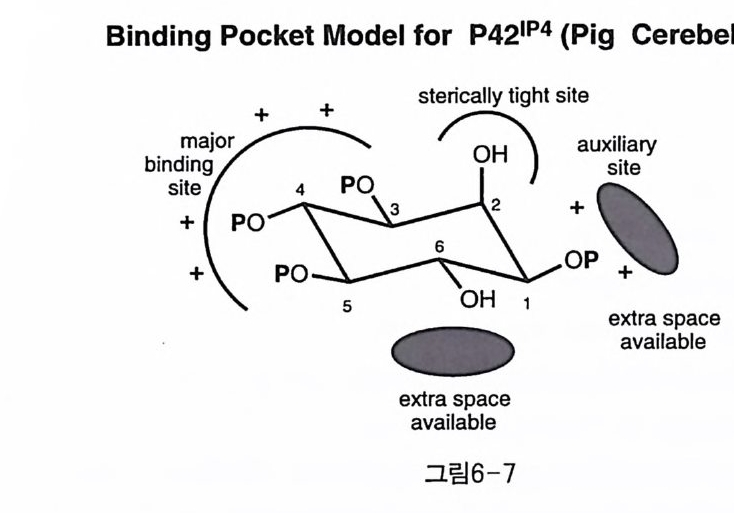 Bi nd in g Pocket Model fo r P421P4 (Pig Ce 『 ebellum)
Bi nd in g Pocket Model fo r P421P4 (Pig Ce 『 ebellum)
참고문헌 (1 ) Ca rpe nte r , C. L. ; Cantl ey , L. C. Bio c hemi st r y 19'JO, 29, 11148 -1 1156. [2) Ag ran off , B. W.; B radley, R. M.; B rady, R. 0. J. Bio l . Chem. 1958, 233, 1007-1083. 떠 Benja mins , J. A.; A g ran off , B. W. J. Neurochem. 1969, 16, 513-527. [4] M oy er , J. D. ; R eiz e s, O.; A hir, S.; J ian g , C.; Ma lino wski , N.; Baker, D. C. Mal. Phannacol. 1988, 3 3, 683 -689. 〔회 Joh nson, S. C.; Dahl, J.; S h ih, T. L.; Schedler, D. J. A.; Anderson, L.; Ben- jamin, T. L.; Baker, D. C. J. M ed. Chem. 1993, 3 6, 3628-36 35. (6) McPhee, F.; Downes, C. P.; Lowe, G. Bio c hem. J. J.9CJ1 , 277, 407- 4 12. (7) Of fer, J. L.; Metc a lfe, J. C.; Sm ith, G. A. Bio c hem. J. 1993, 291, 553 -3 60.
(8) Kozik o wski , A. P.; Fauq, A. H.; Powi s, G. ; M elder, D. C. J. Am. Chem. Soc. 1990, 112, 4528 -4 531 . 朗 Kozik ow ski , A. P.; Fauq , A. H.; Powi s, G.; Melder, D. C. Med. Chem. Res. l?Jl, J, 277-282. [10) Powi s, G.; Aksoy , I. A.; Melder, D. C.; Aksoy , S.; Eic h ing er , H.; Fauq , A. H.; K ozik ow ski , A. P. Cancer Chemoth er. Phannacol. 1 9' )1, 29, 95-104. (11 ) Kozik o wski , A. P.; Powi s, G.; Galleg os , A.; Tii ck mante l , W. Bio o rg. Med. Chem. Lett. 19'J3, 3, 1323 -1 326. [12 ) Baker, R.; Kulago w ski , J. J.; Bil ling ton , D. C.; L eeson, P. D.; Lennon, I. C.; L iv e rt on , N. J. Chem. Soc., C hem. Commun. 1989, 1383-1385. (13) Baker, R.; Leeson, P. D. ; L iv e rt on , N. J.; Kulago w ski , J. J. J. Chem. Soc., Chem. Commun. 1990, 462 -4 64. (14 ) Russel, M. G. N.; Baker, R.; Bi lli n g ton , D. C. Carbohy dr . Res. 1992, 234, 263-268. (15 ) Baker, R.; Ca rrick , C.; L eeson, P. D. ; L ennon, I. C.; Liv e rt on , N. J. J. Chem. Soc., Chem. Commun. l?Jl, 2 98 -3 00. (16 ) Kulag ow ski , J. J. Tetr a hedron Lett. 1989, 30, 3869 -3 泣
回 Kulago w ski , J. J.; Baker, R.; Fletc h er, S. R. J. Chem. Soc., Chem. Com- mun. l?Jl, 1649 —16 50. (18 ) Fletc h er, S. R.; Baker, R.; Leeson, P. D.; Teall, M.; Harley, E. A.; Raga n , C. I. Bio o rg. Med. Chem. Lett. 1992, 2, 627 -630. U 이 Fletc h er, S. R.; Baker, R.; Ladduwahett y, T.; Sha rpe , A.; Teall, M.; Ata c k, J. R. Bio o rg. Med. Chem. Lett . 函, 3, 141 -1 46. @]B aker, G. R.; Bil li n gton , D. C.; Ga ni, D. Bio o rg. Med. Chem. Lett . 1991, 1, 17 -2 0; ide m, Tetr a hedron, l?Jl, 47, 3895 -3 908. (21) Shute , J. K.; Baker, R.; Bil lington , D. C.; Ga ni, D. J. Chem. Soc., Chem. Commun. 1988, 422 -423; ide m, ibi d . 1988, 626-628. [22 ] B aker, G. R.; Ga ni, D. Bio o rg. Med. Chem. Lett . 函 1, J, 193-196.@]C ole, A. G.; G a ni, D . J. Che m . Soc., Chem. Commun. 1994, 1139 -1 141. [24 ] Schulz, J.; Wi lk i e, J.; Lig h tf oo t, P.; R uth e rf or d, T., Gani, D. J. Chem. Soc., C hem. Commun. 1995, 2353 -2 356. [25 ) W ilkie, J.; Cole, A. G.; Gani, D . J. Chem. Soc., P erkin Trans. 1 1995, 2695 -2 7(1 7. [26 ] Cole, A. G.; W ilk ie, J.; Ga ni, D. J. Chem. Soc., Perkin Trans. 1 1995, 2709-2727. 〔 2기 Henne, V.; Mayr , G. W .; G rabowski , B .; Kop pitz, B.; S ling , H. D. Eur. J. Bio c hem. 1988, 174, 95 -1 01. (28) Prestw ich , G. D.; Marecek, J. F.; Mourey , R . J.; T heib e rt , A. B.; Ferr is, C. D.; Danoff , S. K.; Sny de r, S. H. J. Am. Chem. Soc. 1991, 113, 1822-:- 1 825. [29 ) Mourey, R. J.; E ste v ez, V. A.; Marecek, J. F.; Barrow, R. K.; Prestw i ch , G. D.; S ny de r, S. H. Bio c hemi st r y 1993, 32, 1719-1726. 圓 Lamp e, D. ; Mills , S. J.; Pott er , B. V. L. J. Chem. Soc., Perkin Trans. 1 函, 2899-2906. [31 ) Hirat a , M.; Wata n abe, Y.; Ish im ats u , T.; I kebe, T.; Kim ura, Y. ; Y am-agu c hi , K.; Oza ki, S.; K og a, T . J. Bio l . Chem. 1989, 264 -, 20303 -2 0308. [32 )L amp e, D.; Pott er , B. V. L. Tetr a hedron Lett . 1993, 34, 2365-2368. [33 ) Wi lc ox, R. A.; Sa fran y, S. T.; L amp e, D.; Mills , S: J.; Nahorski , S. R.; Pott er , B. V. L. Eur. J. Bio c hem. 1994, 223, 115 -124. @]S awy er , D. A.; Pott er , B . V. L. J. Chem. Soc., P erkin Trans. 1 tm, 923 - 932. [35 )S a fran y , S. T.; Sawy er , D. ; W ojc i k iew i cz , R. J. H. ; N ahorski , S. R.; Pot- ter , B. V. L. FEBS Lett. 1990, 2 76, 91 -9 4. [36 ) Wi lco x, R. A.; Nahorski , S. R.; Saw ye r, D . A.; Liu , C.; P ott er , B. V. L. Carbohyd r . R es. 寧, 234, 237-246. @]M 비 s, S. J.; Sa fran y, S. T.; W ilc ox, R. A.; Nahorski , S. R.; Pott er , B. V. L. Bio o rg. Med. Chem. Lett . 1993, 3, 1505 -1510 .
[38 ] L amp e, D., Ph. D. D 函떠 a ti叫 血恥函ty 아 B 띠 h, tm. 〔朗 Seewald, M. J.; Aksoy , I. A. ; P owi s, G.; Fauq , A. H.; Kozik o wski , A. P. J. Chem. Soc., Chem. Commun . 1990, 1638 -1 639. (40) Kozik ow ski , A. P.; Fauq , A. H.; Aksoy , I. A.; Seewald, M. J.; Powi s, G. J. Am. Chem. Soc. 1990, 112, 7403 -7 404. [41 ) Sa fran y, S. T.; W ilc ox, R. A.; Liu , C. ; P ott er , B. V. L.; Nahorski , S. R. Eur. J. Pharmacol. Im, 226, 265 -2 72. [42 ) Hirat a , M.; Wata n abe, Y.; Kanemats u , T.; Oza ki, S.; Kog a, T. Bio c him . Bio p h ys . Acta ms, 1244, 404-410. 〔 4 미 Kozik o wski , A. P.; Og ny an ov, V. I.; Fauq , A. H.; W ilc ox, R. A.; Nabors- ki, S. R. J. Chem. Soc., C hem. Commun. 19'J4, 599-600. [44 ] L iu , C.; Nahorski , S. R.; Pott er , B. V. L. J. Chem. Soc., Chem. Commun. m1, 1014-1 016. 〔 4회 Liu , C.; Nahorski , S. R.; Pott er , B. V. L. Carbohyd r . Res. Im, 234, 1(J J- 115. 〔 4 이 Kozik o wski, A. P.; Fauq , A. H. ; Malaska, M. J.; Tuckmante l , W.; Og ny an ov, V. I.; P owi s, G. Curr. Med. Chem. 19'J4, 1, 1- 1 2. 〔 4기 Fauq , A. H.; Kozik o wski , A. P.; Og ny an ov, V. I.; W ilc ox, R. A.; Nabors- ki, S. R. ]. Chem. Soc., Chem. Commun. 19')4, 1301-1302. 圈 Challis , R. A. J.; W illco cks, A. L.; Mulloy , B.; Pott er , B. V. L.; Nahorski , S. R. Bio c hem. J. m t, 274, 861-86 7. 〔 4이 Polokoff , M . A.; Bencen, G. H. ; V acca, J. P.; DeSolms, S. J.; Yo 血g, s. D. ; Hu ff, J. R . J. Bio l . Chem. 1988, 263, 11922-11927. 圓 Kozik ow ski , A. P.; Fauq , A. H.; Wi lc ox, R. A.; Cha lliss , R. A. J.; Nabors- ki, S. R. J. Med. Chem. 函, 37, 8 68-872. 詞 Berr idg e, M. J.; Irvin e , R. F. Natu r e 1984, 312, 315-321. @]T ayl o r, C. W.; Berr idg e, M. J.; Brown, K. D.; Cooke, A. M.; Pott er , B. V. L. Bi oc hem. Bio p h y s. Res: Commun. 1988, 150, 626-63 2.
[53 ) Str upish , J.; Cooke, A. M.; Pott er , B. V. L.; Gigg, R.; Nahorski , S. R. Bio c hem. J. 1988, 253, 901 -9 05. [54) Sa fran y , S. T.; Wojc ikiew i cz , R. J. H.; Str upish , J.; McBa in, J.; Cooke, A. M.; Pott er , B. V. L.; Nahorski , S. R. Mol. Pharmocol. 19' Jl , 39, 754-761 . 〔 5 회 Noble, N. J.; Dubreuil , D.; Pott er , B. V. L. Bio o rg. Med. Chem. Lett . 1992, 2, 471 -476. [56 )C ooke, A. M.; N oble, N. J.; Payn e , S.; Gig g, R.; Pott er , B. V. L. J. Chem. Soc., C hem. Commun. 1989, 269-271; Noble, N. J.; Cooke, A. M.; Pott er , B. V. L. Carbohyd r . Res. 1992, 234, 177 -1 87. 〔幻 Falck, J. R.; Abdali , A.; Wi tten berge r , S. J. J. Chem. Soc., Chem. Commun. 1.9'JO, 953 -9 55. [58 ] 恥 e f, C. E.; S ch ieb ler, W .; v an der Marel, G. A.; van Boom, J. H. Tetr a - hedron Lett . 1991, 32, 6021 -6 024. 〔 5 이 Safr an y, S. T.; Wojc i k i e w i cz , R. J. H.; Str u p ish , J.; Nahorski , S. R.; Dubreuil , D.; Cleop ha x, J.; Gero, S. D.; Pott er , B. V. L. FEES Lett . 19' Jl , 278, 252-25 6. @]G ou, D. M.; Sh ieh , W. R.; Lu, P. J.; Chen, C. S. Bio o rg. Med. Chem. 函 ,2,7-13. [61 ) Gawler, D. J.; P ott er , B. V. L.; Gig g, R.; Nahorski , S. R. Bio c hem. J. 1991, 276, 163 一 167. [62 )Wi llco cks, A. L.; Cooke, A. M.; Pott er , B. V. L.; Nahorski, S. R. Bio c hem. Bio p h ys . Res. Commun. 1987, 146, lff ll- lf178 . 園 Sawy er , D. A.; Pott er , B. V. L. Bio o rg. Med. Chem. Lett. 1991, I, 705 - 710. @]I rvin e , R. F.; Letc h er, A. J.; Lander, D. J.; Berr idg e, M. J. Bio c hem. J. 1986, 240, 301-30 4. [65 ] 페 son, D. B.; Connolly, T. M.; Bross, T. E.; Maje r us, P. W.; Sherma1, W. R.; Ty le r, A. N.; Rubin , L. J.; Brown, J. E. J. Bio l . Chem. 1985, 2{x ),
13496-13501. (66) Wi lc ocks, A. L.; Str upish , J.; Irvin e , R. F.; Nahorski , S. R. Bio c hem. J. 1989, 257, 2'F / -3 00. 〔 6 기 Nunn, D. L.; T ayl o r, C . W . Bio c hem. J. 函, 270, 227-232. [68 )D en is, G . V. ; B allou, C. E. Cell Calci um J.9CJ1 , 12, 395-401. [69 ) Marchant, J. S.; Chang , Y. T.; C hung , S. K.; Irvin e , R. F.; T ayl o r, C. W. Bio c hem. J. , 1991, 321, 573 -5 76. [70 )Tegg e , W.; D en is, G . V.; B allou, C. E. Carbohyd r . Res. J.9CJ1 , 217, 1(J J- 116. [71 ) Kozik o wski , A. P.; Fauq , A . H.; Powi s, G. ; K uri an , P.; C rews, F. T. J. Chem. Soc., Chem. Commun.l992, 3 62-364. n띠 Kozik o wski, A. P.; Og ny an ov, V. I.; Fauq , A. H.; Nahorski , S. R.; Wi lco x, R. A. J. Am. Chem. Soc. 1993, 115, 4429 -4 434. 〔 7 미 Wi llem s, H. A. M.; Veeneman, G. H.; Weste r duin , P. Tetr ah edron Lett. l992, 3 3, 2ff75 -2 ff78 . 떠〕 Weste r du in, P.; W illem s, H. A. M.; van Boeckel, C. A. A. Carbohy dr . Res. l992, 234, 131-140. [75 )Schultz , C. ; G ebauer, G.; Mets c h ies , T.; Rensin g , L.; Jas to r f f, B. Bio c hem . Bio p hy s . Res. C ommun. 19 책 166, 1319-1327. [76 )Irvin e , R. F. Advances in Second Messeng e r and Phosp h op r ote i n Research, (Ed. Putn e y, J r. , J . W . ) Raven Press, New York, 1992, 26, 161- 185. 詞 W ilco cks, R. A.; Cha lliss , R. A. J.; Liu , C.; Pott er , B. V. L.; Nahorski , S. R. Mol. Pharmacol. 1993, 44, 8 10-81 7. [78 ] Mi lls, S. J.; Al-Ha fidh , J.; Westw ick , J.; Pott er , B. V. L. Bio o rg. M ed. Chem. Lett . 1993, 3, 2599-2604. 〔 7 아 Hirata , M.; W ata na be, Y.; Y oshi da , M . ; Kog a, T.; Oza ki, S. J. Bio l . Chem. 1993, 268, 19260-19 266.
圓 Rile y, A. M. ; P ayn e , R.; Pott er , B. V. L. J. Med. Chem. J.9CJ4, 37, 3918- 3927. [81) Str eb , H. ; I rvin e , R. F.; B err idg e, M. J.; S chulz, I. Natu r e 1983, 306, 67- 69. [82 )J ose ph , S. K.; Hansen, C. A.; Wi lli a m son, J. R. Mol. Pharmacol. 1989, 36, 391-397. 〔 8 刃 Ly ss ik a to s , J. P.; Bednarski , M. D. Bio o rg. Med. Chem. Lett . 19'J3, 3, 685-688. [84 )Nahorski , S. R.; Pott er , B. V. L. Trends Pharmacol. Sci. 1989, JO, 139- 144. 〔 8 회 Morr is, A. J.; MWTay, K. J.; Eng la nd, P. J.; Downes, C . P.; Mi ch ell, R. H. Bio c hem. J. 1988, 251, 157 -1 63. 〔 8 이 Connolly, T. M.; Bansal, V. S.; Bross, T. E.; Irvin e , R. F.; Maje r us, P . W. J. Bio l . Chem. 1987, 262, 2146-21 49. [87) Sa fran y, S. T., Ph. D. Di ss ert ation , Un ive rsit y of Leic es te r , 19'J3. 〔部〕 Tayl o r, C. W.; Berr idg e, M. J.; Cooke, A. M.; Pott er , B. V. L. Bio c hem. J. 1989, 259, 645 -6 50. [89 ] S a fran y, S. T.; Mills, S. J.; L iu, C.; Lamp e, D. ; N 야 le, N. ; Nabors 뵤 s. R .; Pott er , B. V. L. Bio c hemi st r y J.91)4, 33, 1ITT63-1ITT69. [90 ] Dreef, C. E.; Mayr , G. W .; J an sze, J. P.; Roelen, H. C. P. F.; van der Marel, G. A.; van Boom, J. H. Bio o rg. Med. Chem. Lett . 19'Jl, 1, 2 39 -2 42. [91 ) Kozik ow ski , A. P.; Og nyan ov, V. I.; Chen, C.; Fauq , A . H.; Sa fran y , S. T.; Wi lco x, R. A.; Nahorski , S. R. J. Med. Chem. 19'J3, 36, 3 035-3038. 岡 Poit ras , M.; Bern ier , S.; Boulay, G.; Fou rnier , A.; Gu ille mett e, G. Eur. J. Pharmacol. 函, 244 -, 203 -2 10. [93 )C hang, Y. T., Ph. D. Diss ert ation , POSIBCH, 19'J7. [94 ) Cooke, A. M.; Nahorski , S. R.; Pott er , B. V. L. FEBS Lett. 1989, 242, 373-377.
〔 9 회 Hi rat a , M.; Yanag a, F.; Kog a, T.; Og as awara, T.; W ata n abe, Y. ; O zak i, S. J. Bio l. Chem. 1990, 265, 8404 -8 407. 〔 9 이 Auchus, R. J.; Ka ise r, S. L.; Maje r us, P. W. Proc. Natl. Acad. Sci. USA 19'if l, 84, 1206 -12I fJ. [97 ] w 비 cocks, A. L.; P 。tt er, B. V. L.; C 。 oke, A. M. ; N ab 函뵤 S. R. E叫 L Pharmacol. 1988, 155, 181-183. 〔앳〕 Lamp e, D.; L iu, C.; Pott er , B. V. L. J. Med. Chem. 19'J4, 37, 'Xrl-9 12. [99 )Theib e rt , A. B.; Este v ez, V. A.; Mourey, R. J.; Marecek, J. F.; Barrow, R. K.; Prestw i ch , G. D.; Sny de r, S. H. J. Bio l . Chem. 1992, 267, 'Xrl l- 函. (10 이 Cullen, P. J.; Dawson, A. P.; Irvin e , R. F. Bio c hem J. 1995, 305, 139- 143. (101 ) Cullen, P. J.; C hung , S. K.; Chang , Y. T.; Dawson, A. P.; Irvin e , R. F. FEBS Lett. 19'JS, 358, 240-24 2. 〔血〕 Cullen, P. J.; H.s u an, J. J.; Truong , O.; Letc h er, A. J.; Jac kson, T. R.; Dawson, A. P.; Irvin e , R. F. Natu r e 19'JS, 376, 527-530. U 따〕 Danie , F.; Reis e r, G. Bio c hem. J. 19'Jl, 275, 453-457. U 야〕 Str ick er, R.; Chang, Y. T.; Chung , S. K.; Reis e r, G., Bio c hem. Bio p hy s . Res. C ommun. , 19%, 228, 596 -fi 04.
 부록: 이노시톨 유도체들의 물리 및 분광학적 성질
부록: 이노시톨 유도체들의 물리 및 분광학적 성질
차례 약어 보기 • 248 치환기 순서 • 249 A. my o -I nosit ol • 251 I. Inosit ol • 251 Il. Inosit ol pho sp ha te s • 251 1. Monop ho sph a te 2. Bi sp h o sph a te 3. Tr isp h o sph a te 4. Tetr akisp h o sph a te 5. Penta kisp h o sph a te 6. Hexa kisp h o sph a te 7. Thiop ho sph a te ill. In osit ol wi th ch iral aux iliary • 281 1. Camp ha nate 2. Menth o xy ac ety l 3. Menth yl carbonate 4. Acety lm andelate 5. Ta rtrat e 6. Camp ho r 7. 1 -( ph eny le th yl) acety l IV. Inosit ol Aceta l • 288 1. Monoaceta l 2. Diac eta l 3 . Tr iac eta l 4. Or tho fo n nate V. Allcyl and /or Acy l D eri ve ti ve s • 303 B. chir o -I nosit ol • 327
C. scyl lo -Inosit ol • 332 D. Oth e r ino sit ol s • 333 참고 문헌 • 335
약어 보기 Mp (I-LO ): meltin g poi n t (0C ), cry s ta l liz e d from H20 Rf: based on the sil ica gel pla te (a)o15: op tica l rota tion (sod ium D lin e , at 25 °C) Anal: elementa l analys i s 1H:1H-NMR 13C: 13C -N MR lip (number): lip -N MR (chem ica l sh ift by ppm ) IR: infrar ed spe c tr os cop y UV: ultra v io l et spe c tr os cop y Mass: mass spe c tr om etr y FAB : fas t a to m bombardment mass spe c tr om etr y HRMS: high resoluti on mass spe c tr om etr y EI: electr on im p ac t mass spe c tr om etr y CI: chem ica l ion iza ti on mass spe c tr om etr y X -ray: X -ray cry st a llog rap hy EE: eth yl eth e r MC: meth yle ne chlori de PE: pet r ol eum eth e r EA: eth yl aceta t e
치환기 순서 이노시톨의 치환기는 다음 약어의 알파벳 순으로 배열되어 있다 . Ac: acety l Ace: aceto n ide (iso p ro p yli d e ne) All: a llyl BOM: benzyl o xy m eth yl Ben: benzy lid e ne Bn: benzyl Bs: benzenesulfo n y l Bt : buty ryl Bz: b e nz oy l Camp : c amp ha nate Carb: 1 -p he ny le th yl carbamate Crot: croty l Hex: cyc l ohexy lide ne Man: acety lm andelate Me: meth yl Mnc: menth yl_ c arbonate Mnt: menth o xy ac ety l MOM: meth o xy m eth yl Or th: ort ho fo rm ate Pen: cyc l op en ty lide ne PMB : p -m eth o xy be nzy l Piv : piva loy l (trime th yla cety l) Pro: pro p -1 -e ny l SEM: (trime th yls il yl) eth o xy m eth yl Tar: t artrat e
TBDMS: t -b uty ld im eth yls il y l TBDPS: t ~buty ld ip h eny ls il y l Tf: trifluo rometh a nesulfo n y l THP: tet r ah y dr op yra ny l TIPS : 1, 1,3,3 -te t r aiso p ro p yld i si lo xaned i -1 ,3 -y l Tr: trityl Ts: p -to l uenesulph o ny l XP: o--xy l e ned iox yp h osph o ry l
A . my o -Inosit ol I. Inosit ol Mp 225-227 (EtO H-HzO). Anal. [A 8);Mp 222-224. [A l9);M p 224-225. [Z 16); 13C. [A 17)
II. Inosit ol ph osp ha te s 1. Monop h osph ate 1 -1 .l(l)P 1 -1 -1 . Salt f or m (士)-fo rm ammon ium : 1H. FAB. HRMS. [L E3)ammon ium , 6-CILCILNIL (pH 7): 1H. 13C. 31P (6.67). FAB. HRMS. [Z 19)cy cl ohexy la mmoniu m , 2 -hexy l: Mp 244 -254 (H20 -aceto n e). 1H. FAB. [B 16] K: 31p (4.6 ) . [Z lO] Na: J1p [C H8] D-fo rm bis c yc l ohexyl a mmon ium : 〔야 20+3.55 (c 1, ILO, at p H 9). [B 3); Mp 190.5 -192.5. 〔야포 3.9 (c 3.0, ILO). 1H. IR. [0 23);M p 180-195. 〔이 020+2.25. Anal. [Z l3); Mp 193 -195. 〔야 +3.55 (c 2.0, ILO, pH 9.5). 1H. 31P (4.64, pH 9.5). FAB. [B R18); Mp 191 -192. 〔야 +4.5 (c 1.06 , ILO, pH 9). [Z 26); Mp 194-196 (!LO -aceto n e). [a ] o +3.8( c 3.1, ILO, pH 9). [Z 7); Mp 202-204. [a ]o +3.4 ( c 1, ILO, pH 9). [Sl O)L-fo rm bis c yc l ohexy la mmoniu m : [cx )o20-3.4 5 ( c 1, ILO, at pH 9). [B 3); [ cx)o25-3.2 (H20, pH 9),+ 9 .3 (ILO, pH 2). Anal. [B AS);Mp 194-196. [cx )o-3.4 ( c 1.1, ILO, pH 9). [B R18);Mp 190-191. [cx )o-2.8 ( c 0.39, ILO, pH 9). [Z 26); Mp 190-192. [a.)0 22- 4.9 (c 5.68, ILO, pH 9). Anal. [G E2); Mp 190-192. [a )D- 3.7 (c 3.8, ILO, pH 9). [Z 7)
1 -1 -2 . Prote c te d for m (士)-fo nn 1-PO(OBn)2, 3,4,5,6-Bn4, 2-hexyl : Syr up. 1H. [B l6) 1 -P O(OCH2CH2CN)2, 2,3,6 -BnJ: Mp 122 -124 (EA -P E). 1H. 31P. Anal. [G l4] l-PO(OCHzCHzCN)2, 2,3 , 6-BnJ, 5 -Pro: Mp 109 -110 (PE ). 1H. 31P. Anal. [G 14] l-PO(OCH2CCh)2, (4,5)Ace, 2,3 , 6-BnJ: Mp 114-115 (PE ). 1H. 31P. Anal. [G 14] 1 -P O(OCH2CCb)2, 2,3,6 -BnJ: Mp 141 -143 (EA -PE 1: 3) . 1H. 31P. Anal. [G l4] 1-PO(OPh)z, (2,3;5,6)Ar. ez : Oil . Rf 0.3 (EA -hexane 1:1). 1H. Ile. 31P . FAB. [Bl6] 1-PO(OPh)2, 3,4,5,6-Bn ◄, 2- h exyl : Sy ru p. 1H. [B 16] 1-PO(OPh)z, 6-Bz, (2,3;4,5)Hexz: Mp 153. [A IO] K salt, 2,3,4,5 ,6 - Acs: 31P (4.7 ). [Z lO] triet h yla mmon ium salt, 2,3,4 ,5 ,6 -Acs: 31P (-0 .2 ) . [Z lO] D- f orm 1 -PO(OBn)2, 2,3,4,5,6 -Acs: 〔야 -14.2 ( c 2.8 , diox ane). [Z7 ] 1-PO(OBn)2, 4- ( 기 -Camp , (2,3 ; 5,6)He 쟈: Mp 138-139 (EA-hexane).@D 十 4.17 (c 0.12, CHC13). 1H. Anal. [Z 26)
l -P O(OBn)2, (2,3)D -Camp ho r: Mp 96 -9 8. 〔야 -1 0.7 (c 2, CHCb). 1H. uc. 31P (-0 .60). [B R18)1-PO(OBn)2, (2,3;5,6)Hex2: Mp 141-142. [a.)D+ 10( c 0.1 2 , CHCb). Anal. [Z 26] 1 -PO(OEt) 2, (2,3)D -C amp ho r: Syr up. Rf 0.23 (Me OH -C HCh 1:15). 〔야 -1 4 (c 1.5, CHCb). 1H. 31P (-0 .6). [B R18] 1-PO(OCH2CCb)2, 2,3,6-BnJ, 4-Pro: Mp 119-120 (EA-PE 1:5, tra ce pyridine ). 1 H. 31P. Anal. [G 14] 1 -XP, 2,3,4,5,6-Bzs: Mp 126-127. [a.)D2 6+22.7( c 1.19 , CHCb). 1H. IR. Anal. [0 23] L-fo rm 1-PO(OBn)2, 2,3,4,5,6-Acs: 〔야+ 14.5 (c 3, dio x ane). [Z 7)l -PO(OBn)2, 4-(-)- Camp , (2,3;5,6)HeXz: Mp 156-157. [a.)o +4.7( c 0.19, CHCh). 1H. Anal. [Z 26] 1-PO(OBn)2, (2,3;5,6)Hex2: Mp 140-141 . 〔야 -13 (c 0.13, CHCh). 1H. Anal. [Z 26) 1-PO(OEt) 2, 2,3,4 ,5 ,6-BZs: 꼬 P [C H8)1- P O(OPh)2, 2,3,4,5,6-BZs: Mp 197-199. 〔이 023-13 (c 1.74 , CHCL). Anal. [G E2) 1-2. 1(2)P 1 -2 -1 . Salt f or m cyc l ohexy la mmon ium : Mp 183 -185. 1H. FAB. Anal. [B 13] Na: 31P [C H8] 1 -2 -2. Prote c te d for m2-PO(OBn)2, 4,6-Bn2, (1, 3,5)0rt h: Mp 102-103 (EA-hexane). 1H. FAB. Anal. [B 13) 2-PO(OEt) 2, 1,3,4 ,5 ,6-BZs: 31P [C H8] 1-3.1(4)P 1 -3 -1 . Salt f or m (土)-fo rm cyc l ohexy la mmon ium : Mp 133 -134 (!LO -aceto n e). 1H. FAB. Anal. [B 13); Mp 206 -2 07. [A lO] Na: J1p [C HS) D-fo rm cyc l ohexy la mmon ium : (a)o211-1 .3 (c 5, ILO, pH 9). [B 3);M p 180-200. 1H. HPLC. FAB. Anal. [ B 14) ; Mp 183 -188. [a )o -1.2 (c 2.6, ILO). 1H. 13C. 31P (4.94). FAB. [B R18] L-fo rm cyc l ohexy la mmon ium : [a) o20+1 .1 (c 5, luO, pH 9). [B 3);Mp 180-200. 1H. HPLC. FAB. Anal. [B 14] 1 -3 -2 . Prote c te d for m (土)-fo rm 4-PO(OCH .zC Ch)2, 2,3,6-Bl li, 5 -Pro: Mp 131-133 (EE-PE 1:2). 'H. 31P. Anal. [G 14] 4-P0(0Bn)2, (l,3,5)0rt h: Mp 97-99 (EE ). [B 4);'H . FAB. Anal. [B l3] 4 -PO(OEt) 2, 1,2,3,5,6-BZs: 미 P [C H8] 4-PO(OPh)2, (2,3;5,6)Ace2, 1-Bn: Rf 0.6 (EA -hexane 1:1). 'H. 13C. FAB.
[C Hll) 4-PO(OPh)2, 3-Bz, (l,2;5,6)Hexz: Mp 155. [A lO) D-fo rm 4-PO(OBn)2, 1-Bn. (2,3;5,6)Hex: Sy ru p . [a )o - 27.0 ( c 1, CHCb). 1H. FAB. HPLC. Anal. (B 14] 4 -PO(OPh)2, 1 -Bn. (2,3;5,6)Hex: Sy ru p . [a ] o -24.9 (c 0.69, CHCb). 1H. HPLC . [B 14] 4 -XP, (2,3)D -Camp ho r, (5,6)Ace, 1 -Bn: Rf 0.16 (aceto n e -CC14 l : 10). [a )D +9.2 (c 2.4 , CHCb). 1 H. 31P ( -1 .42 ). [B R18] L-fo rm 4 -P O(OBn)2, 1 -Bn. (2,3;5,6)Hex: S yr띠) . [a ]v +26.5 ( c 1, CHCL). 'H. FAB. HPLC. Anal. [ B 1 4] 4 -PO(OPh)2, 1 -Bn. (2,3;5,6)Hex: Sy ru p . 〔 a 〕 D + 25. 。 (c 0.73, CHCL). 1H. HPLC. [B 14] 1 -4 .l(S)P 1 -4 -1 . Salt f or m cyc l ohexy la mmon ium : Mp 209 -2 11 . [A lO] Na: 3 1P [C H8)
1 -4 -2 . Prote c te d for m 5 -P O 표 1,2,3,4,6 -A cs: Mp 229. [A lO] 5 -PO(OEt) 2 , 1,2,3,4 , 6-B Zs: 31P 〔야 8) 5 -PO(OPh)2, 1,2,3,4,6 -A cs: Mp 168. [A lO]1 -5 . IcP 1 -5 -1 . Salt f or m (士)-fo rm (l,2)cP, 6 -c ac 呼 (pH 7): 1H. 13C. 31P (18 .7). FAB. HRMS. [Z 19] 2. Bis ph osph a te 2 -1 . l(l),)P2 2 -1 -1. Salt f or m (土)-fo rm Na: 1H. 31P. [C H12] 2 -1 -2 . Prote cted for m 1,2-P O(OEt) z , 3,4,5,6 -Bz .i: Mp 186 -1 88. 1H. 13C. 31P. FAB. [C H12] 2 -2 . 1(1,3 )P 2 2 -2 -1. Saltf orm cyc l ohexy la mmon ium : Mp 165 一 166 (ILO -aceto n e). 1H. FAB. Anal. [B 4, B13] Na: 1H. 31P. [C H12] 2 -2 -2 . Prote cted for m 1,3 -P O(OBn)2, 2,4 ,5 ,6 -Bn,: Sy ru p. 31P. Anal. [G 9] 1,3-PO(OBn, ONa), 2,4 ,5 ,6-Bn,: Mp 239-242. 31P. Anal. (G9] 1,3 -PO(OEt) 2, 4,5,6 -B Zl: 1H. 13C. 31P. FAB . [C H12]
1,3 -PO(OPh)2, 2,4 ,6 -B nJ: Mp 109 -1 10 (EE -PE). 1H. FAB. Anal. (B4, B13) 2 -3 .l(1, 4 )P2 2 -3 -1 . Salt for m (士) -for m cyc l ohexy la mmon ium : Mp 186 -1 97. [A IO] Na: 1H. 13C. 31P . [C HI,CH12] D-fo r m cyc l ohexy la mmon ium : Mp 184 -1 94. [a )o + 0.1 2 ( c 4, IhO). 1H. FAB. Anal. (B14) ; Mp 178 一 182. [a )o+1 .8 (c 5.0, H20). 1H. 31P (4.28, 4.92). FAB. [B R18] L-fo r m cyc l ohexy la mmon ium : Mp 184-1 94. 〔야 -0 .12 (c 4, lLO). 1H. FAB. Anal. [B 14] 2 -3 -2 . Prote c te d for m (士) -form 1,4 -P O(OCHzCCb)2, 5 -Ac, 2,3 , 6 -BnJ: Mp 197 -1 98 (EA -PE). 1H. 31P. Anal. [G 14] 1,4 -P O(OCHzCCL)2, 2,3,6 -BI1 J: Mp 152 -154. 1H. 31P. Anal. [G 14] 1,4 -P O(OCHzCCh)2, 2,3,6-B il l, 5 -Pro: Mp 158 -1 59 (MC -PE). 1H. 31P. Anal. [ G 14] 1,4 -P O(OCHzCHzCN)2, 1,2,3,6-Bn4: M p 96 -9 8 (EA -E E). 31P. Anal. [G 9] 1,4 -P O(OEt) 2 , 2,3,6 -BZ J: Mp 156 -158. 1H. 13C. 31P. FAB. [C H12)
1,4 -P O(OPh)2, (2,3;5,6)Ace2: Mp 140 -1 43. Rf 0.65 (EA -h exane 1:1). 'H. 13C . 31P. FAB. [C Hl) 1,4 -P O(OPh)2, (2,3;5,6)Hex2: Mp 183. [A lO] D-fo rm 1,4 -P O(OBn)z, 5 -Ac, 2,3,6 -B nJ: Sy ru p . 1 H. 31P . [G 14)
1,4 -P O(OBn)z, 2,3,6 -BnJ: Mp 80 -8 2. 〔야 +7.9 (c 1, CHCb). 'H. 3'P. Anal. [G 14] 1,4 -P O(OBn)z, 2,3,6 -B nJ, 5 -P MB: Mp 88 -90 (EA -P E). [a.)o2 5+7.9( c 1, CHCL). 1H. 31P. Anal. [G 14] 1,4 -P O(OBn)z, 2,3,5,6 -B n4: Mp 79 -8 1 (EE -P E). @]0 25+4.4 (c 1, CHCh). 31P. Anal. [G 9] 1,4 -P O(OCH iCl liCN )2, 2,3,6 -B ru: Sy ru p . 〔야 -4 .3 (c 1, CHCh). Rf 0.4 (EA ). 31P. Anal. [G 11) 1,4 -P O(OCH2CH2CN)2, 2 ,3,6 -BnJ, 5 -PMB: Mp 118 -119 (EA -PE). [a.)n 25+8.l (c 1, CHCh). 1 H. 31P. Anal. [G 11] 1,4 -PO(OPh), (2,3;5,6)HeX i: Mp 181 -1 82. [a.)n +5.6( c 0.5 2 , CHCL). 1H. FAB. Anal. [B 1 4] 1,4 -X P, (2,3)D -Camp ho r, (5,6 ) Ace: Sy ru p . Rf 0.22 (aceto n e -C HCL 1:4 ) . 〔이터-1.1 (c 2.2, CHCh). 1H. 31P (-2.2 2, -1 .28 ). [B R16, B R18] L-fo r m 1,4 -P O(OPh), (2,3;5,6)HeX i: Mp 181 -1 82. [cx )n- 5 .7 (c 0.5 2 , CHCL). 1H. FAB. Anal. [ B 14)2 -4 .l(l,S)P1 2 -4 -1 . Salt f or m (土)-fo rmNa: 1 H. 31P. [C H12) D-fo rm H: [a ]o +6.0( c 0.5, Hi。). [v 5) L-fo rm H: (a.]D - 5.9 (C 0.5, ffi。) . N 외 2 -4 -2 . Prote c te d for m (士) -f or m 1,5 -P O(OCILCCb)2, 4 -A c, 2,3,6 -B ll3: Sy ru p . 1H. 31P. Anal. [G 14] 1,5 -P O(OCILCCb)2, 2,3,6 -B nJ: Mp 153 -154. 1H. 31P. Anal. [G 14] 1,5 -PO(OCILCCh)2, 2,3,6 -B nJ, 4 -Pro: Mp 148 -1 49 (EA -P E). 1H. 31P. Anal. [ G 14) 1,5 -PO(OEt) 2 , (2,3)Ace, 4,6 -B z3: Oil . Rf 0.1 (EA -M C 1:5). 1H. 13C. 31P. FAB. [C H12] 2 -5. l(l,6)P2 2 -5 -1 . Salt for m (士) -f orm cyc l ohexy la mmon ium : Mp 161 -1 63. [A IO] Na: 1H. 31p _ [C H12)
2 -5 -2. Prote c te d for m (土)-fo rm 1,6 -P O(OCILCILCN)2, (3,4 ) -A ce, 2,5 -B 112: Sy ru p . 1H. [G 8]1,6 -PO(OEt) 2 , (2,3;4,5)Ace2: Oi l. Rf 0.3 (MeOH -Mc 1:20). 1H. 13C. 31P. FAB. [C H12] 2 -6 . 1(2,4)P2 2 -6 -1 . Salt for m (士)-fo rm Na: IH. 31P. [C H12)
2 -6 -2 . Prote c te d for m 2,4 -P O(OEt) 1, 1,5,6 -BZ J: Mp 187 -189. 1H. 13C. 31P. FAB. [C H12] 2 -7. 1(2,S) P z 2 -7 -1 . Salt fo rm Na: 1H. 31P. [C H12] 2 -7 -2. Prote c te d for m 2,5 -PO(OEt) 2, (l,6;3,4 )A ce2: Oil . Rf 0.25 (EA -M C 1:5). 1H. 13C. 31P. FAB. [C H12] 2 -8. 1(4,S)P1 2 -8 -1 . Salt f o rm (士)-fo rm ammon ium : 31P (4.68, 4.86, pH 12). [P l ) cyc l ohexy la mmon ium : Mp 182 一 183. [A IO]Na: 'H. 31P. [C H12)
2 -8 -2 . Prote c te d for m (土) -f orm 4,5 -P(OCH iCH iCN )2, 1,2,3,6 -B n4: 3 1P (14 0.4 5 , 140.75). [P l ) 4,5 -P O(OBn)2, (l,2) Ace, 3,6 -B n2: Oi l. Rf 0.8 (EA-h exane 1:1). 1H. 13C. 31P. FAB. [C Hl] 4,5 -PO(OBn)2, 3,6 -B n2: Mp 128 -1 30. Rf 0.3 (EA -hexane 1:1). 1H. 13C. 31P. FAB. Anal. [ C Hl] 4,5 -PO(OBn)2, 1,2,3,6-B n4: Mp 102 -104 (EA-P E 1:10). 31P. Anal. [G 9] 4,5 -P O(OCH2CH2CN) 2, 2,3,6 -BnJ: Rf 0.2 0 (EA). 1H. 31P ( -2 .88, -2 .99). FAB. [P5 ] 4,5 -P O(OCH2CH2CN)2, 2,3,6 -BI1 J; 1 -PMB: Sy ru p . Rf 0.22 (EA). 1H. 31P (-5 .9 7 , -6.15). F AB. [P5 ] 4,5 -PO(OCH iCH iCN )2, 2,3,6 -BnJ, 1 -P ro: Mp 118 -120 (EtO H ). Rf 0.76 (EtO H -EA 1:9). 1H. 13C . 31P ( -3.57, -3 .70). FAB. HRMS. Anal. [P5 ] 4,5 -P O(OCH1CH2CN)2, 1,2,3,6 -B n4: Mp 103 -105 (EA -PE). 31P. Anal. [G 9)4,5 -PO(OEt) 2, 1,2,3,6 -B u Mp 136-1 39. Rf 0.25 (EA -M C 1:5). 1H. 13C. 31P. FAB. [C H12] 4,5 -P O(ONa)1, 1,2,3,6 -B n4: Mp 250 -255 (EtO H -H iO 4:1). 31P. Anal (for 4H i0) . [G 9] 4,5 -PO( NH Ph)1, (l,2) Ace, 3,6-B ru: Mp 110 -1 11 . [S8 ] D-fo n n 4,5 -PO(OBn)2, 3,6 -B 112: [cx )o21- 21 .4 (c 2.0, CHCh). [0 6] 4,5 -PO(OBn)2, 2,3,6 -B ru: Mp 90 -9 1 (EE -PE). [cx )o25- 15.6 (c 1, CHCh). 31P. Anal. [G 11)4,5 -PO(OBn)2, 2,3 , 6 一 Bn3, I -PMB: Mp 95 -9 7 (EE, trac e EtO H). 〔야 -1 0.2 (c 1, CHCb). R f 0.3 (EE -PE 3: 1). 31P ( -1 .75 , -2.15). A nal. [G I1 ) 4,5 -P O(OCH2CH2CN)2, 2 ,3,6 -B nJ: Sy ru p . [a) o15+8.5 ( c 4.5, CHCb). [P5 ] 4,5 -PO(OCHzCHzCN)z, 2,3,6 -B n4, 1 -P MB: Mp 84 —8 6 (EtO H). [a ] D “ +4.4 (c 1, CHCb). 1H. 31P. Anal. [G l4] 4,5 -P O(OCH2CH2CN)2, 2,3,6 -BnJ, I -P ro: Mp 13I -1 32 (EtO H). [a) o19 + I 1.5 (c 3.5, CHCb). Anal. (PS ) 4,5 -P O(OCH2CH2CN)2, 2,3,6 -B n4: Sy ru p . (a)o25+7.4 (c 1, CHCh). 11-! . . ,.31p _ Anal. [G 14)
4,5 -P O( NHPh )2, 3,6 -B nz: Mp 181 (EtO H). 〔야 +34 (c 2.3 , CHCb). [S8 ] L-fo rm 4,5 -P O(OBn)2, 3,6 -B 血 〔 a 〕 D2 나 2 1. 0 (c 2.0 , CHCh). [0 6] 2 -9. 1(4,6) P2 2 -9 -1 . Salt for m Na: 'H. 31P. [C H12] 2 -9 -2. Prote c te d for m 4,6-PO(OEt) z, (1, 2)Ace, 3,5 -B zz: Mp 155 -158. Rf0. 15 (EA-M C 1:5). 1H. 13C. 31P. FAB. [C H12] 3. Trisp h osp h ate 3 -1. 1(1,2,3)P3 3 -1 -1 . Salt for m Li: IH. 13c. “P. [C Hll]3 -1 -2 . Prote c te d for m 1,2,3 -PO(OEt) 2 , 4,5,6 -Bz .i: Mp 174-1 76. 1H. 13C . 31P. FAB. [C Hll] 3 -2 . 1(1,2,4)PJ 3 -2 -1 . Salt f or m (土) -for m Li: 31p _ [C H5] 3 -2 -2 . Prote c te d for m (士)- form 1,2,4 -P O(OEt) 2 , 3,5,6 - B z3: 31P. [C H5] 3 -3.1(1,2,S)PJ 3 -3 -1 . Salt for m (士) -form Li: JI P. [C H5] 3 -3 -2 . Prote c te d for m (土)-fo rm 1,2,5 -PO(OEt) 2, 3,4 ,6 -Bz .i: 31P. [C H5)
3 -4 . 1(1,2,6)PJ 3 -4 -1 . Salt for m(土) -form Li: 31p _ [C H5] 3 -4 -2 . Prote c te d for m (土) -for m 1,2,6 -PO(OEt) 2, 3,4 ,5 -B Z3: 31P. [C H5] 3 -5. 1(1,3,4)P3 • 3 -5 -1 . Salt for m (士) - fo rm Li: 31P. [C H5] Na: 1H. 31P (3.8 7 , 2.4 4 , 2.5 2 ). Anal. [ B 1 4] triet h yla mmon ium : 1H. 31P (0.13, 0.24, 0.97, pH 7). F AB. HRMS. [P 6) D-fo r m ammon ium : (a) o22 - 6 (c 0.5 , Hz0). 1 H. [0 7] K: [a )o 2 3+1 3.6 (c 2, H20, pH 8.2 ) . 1 H. 31P (3.28, 4.1 6 , 4.87). [C 3, C 4) triet h yla rnmon ium : 〔이 026+37 (c 0.4 2 , pH 7.8). HRMS. [P 6) L-fo r m triet h yla mmon ium : (a.)02 6 -4 0 (c 0.4 2 , pH 7.8). HRMS. [P 6] 3 -5 -2 . Prote c te d for m (士)-fo rm 1,3,4 -P O(OBn)1, 2,5,6 -B ru: 1H. 31P (-1.31 , -1.45 , -1.89 ). FAB. [B 14); 1H. UC. FAB. [P6 ]
1,3,4 -P O(OEt) 2, 2,5 , 6 -BZ J: 31P. [C H5) D-fo rm 1,3,4 - P O(OBn)2, 2,5,6 -B nJ: 〔이군 0 6 (c 1, CHCh). Anal. [P6 ] 1,3,4 -P O(OCH2CH2CN)2, 2,5,6 -B nJ: Sy ru p . 〔야 25 -2.3 (c 1, CHC13). 31P. Anal. [G9) L-fo rm 1,3,4 -P O(OBn)2, 2,5,6 -BnJ: Sy ru p . (a.]02 5 -5.8 (c 1, CHC13). 31P. Anal. 〔 G 이 ; [a.)02 5- 5 .8 (c I, CHCh). (P6] 1,3,4 -P O(OBn, ONa), 2,5,6 -B n3: Mp 268 -2 71 (EtO H -Aceto n 1:5). [0.)D 15 -8 .4 (c 1, M eOH). 3 1P. Anal. [ G 9] 3 -6. 1(1,3 ,5 )P3 3 -6 -1 . Salt for m K: IH. IJC . JI P. [C H3] Li: 31P. [C H5] 3 -6 -2. Prote c te d for m 1,3,5 -P O(OEt) 2 , 2,4,6 -B z3: Mp 142 -1 43. Rf 0.3 1 (EA -hexane 1:1). 1H. 13C. 31P. FAB. [C H3] 3 -7. 1(1,4,S)PJ 3 -7 -1 . Salt for m (士) _ form ammon ium : 1H. FAB. [L e3);31 P (3.3 8 , 5.11, 5.21, pH 12). [P 2]
K: 1H. 31P. [C H3)
Li: 1H. [M E2); 31P. [C H5) Na: 1H, 31P . Anal. [C Hl) D-fo n n ammon ium : [a) o23- 1 0.3 (c 1.8, H20, pH 6.7 3 ). 1 H. 13C. 31P (1.28 , 2.30, 3.2 3 , at pH 6.7 3 , 3.64, 5.4 1 , 5.5 3 at pH 11. 8 2). Anal. [0 1 ,0 26); [a) 025- 9.4 (c 1.30 , HiO, ammoniu m salt). [0 36); 〔이 022 -2 4 (c 0.15, H20, pH 6.9). [L E3); 1H. 31P (3.4 7 , 5.13, 5.26 at pH 10.7). [Z 22);( 야 -2 8 (c 0.37, H20, pH 10). 31P (3.3 7 , 5.09, 5.18). [S8 )cyc l ohexy la mmon ium : (a)o -3 0 (c 0.1, HiO, pH 10). 1H. FAB. Anal. [B 14); @Sl6 -3 5.1. 1H. 31P (3.61(2P), 4.9 1 at pH 8, 5.08, 5.95, 6.17 at pH 12). Anal. [b ll);〔 이 546 - 17 (c 1.1, HiO, pH 7), -46 (c 1.0, HiO, pH 12). [P E3] Na: (a)o20-28 (c 0.16, HiO, pH 9.5 ). FAB. Anal. [B 2);M p > 270. [a) o23- 11. 1 (c 0.9, HiO, pH 6.9). 1H. 13C . Anal. [0 26); Mp > 270 (Me OH -H iO) . 1H. 31P (5.4 2 , 4.52, 3.82). [0 36);M p 200-2 02. (a)o -30 (c 0.8, HiO, pH 9.5). 1H. 13C. 31P (3.63, 5.31, 5.41 ). FAB. [B R18);〔 이 020 -30 (c 0.5, HiO, pH 9.5). [C 2] K: [a) o23- 9 .4 (c 1.27 , HiO, pH 6.9). [a) o23- 25.2 (c 1.03 , H20, pH 10.6). 1 H. Anal. [0 17,0 26) 2,3,6 -B Z J (Na salt): 1H. 31P. [B All); (a)o -24 (c 0.5, HiO, pH 9.3). 1H. 31P (2.86, 4.4 9 , 4.67). [C 4) L-fo r m ammon ium : 〔아타 27 (c 0.15, lliO, pH 6.4 ). [L E3); (a.)o +30 (c 0.29, lliO, pH 10). [S8 ] cyc l ohexy la mmon ium : 〔 a 〕꾼十 39.0. FAB. [B ll) Na: [a ] 0 20+35( c 0.1, lliO, pH 10. 야 F 사 3. An 라 [B 2); Al 떠 (B14)3 -7 -2 . Prote c te d for m (土) -form 1,4,5 -P(OCILCILCN)2, 2,3,6 -B nJ: 31P (139.6, 140.2, 141 .0) . (P2) 1,4 ,5 -P (OCH2CH2CN)2, (2,3) —cy c lop en ty lide ne, 6 -(2,7 -dib r omo -9 - phe ny lx anth e n -9 —y l): Mp 133 -1 35. Anal. [Z 22] 1,4 ,5 -P O(OBn)2, 2 -Ac, 3,6 -B 112: Rf 0.3 (EA -hexane 1: 1). 1H. 31P. [C H1) 1,4 ,5 -P O(OBn)2, (2,3)Ace, 6 -M e: Oil . 1H. 3•p (-1.04 , -1.18 , -1.40 ). IR. FAB . Anal. [L El,LE3) 1,4 ,5 -P O(OBn)2, 3,6 -B 112: Mp 98.l. 1H Anal. [Z 25)
1,4,5 -PO(OEt) 2, 2,3,6 -BZ J: Mp 158 -162 (EE -P E). Rf 0.4 (Me OH -M C 1:10). 1H. 13C. 31P. FAB. [C H3] 1,4,5 -P O(OMe)2, 2 -Ac, 3,6 -B z2: Mp 224 -2 28. 1H. 31P (2.55, 2.11, 1.96 ). [M E2] D-fo rm 1,4,5 -P O(OBn)2, 6 -Bn, (2,3)Hex: Oil . 〔 a 〕급 0 -4.2 (c 0.1, CHCb). [B 2); 1H. 31P(-2.01, -2.22, -2.4 1).F AB. [B 14);( a.)0 20-4.3(c2.4 2 ,CHCb).1H. [C 2, C4] 1,4 ,5 -P O(OBn)2, 2,3,6 -B ru: Mp 112 -1 13 (EA-P E 1:10), 1H. 31P. [G 14); Mp 109 -110 (EA -hexane). [a ] 02 8 -5 .3 (c 1.7, CHCb). 1H. 13C. 31P (-1.32 , - 1.08 , -0.9 3 ). IR. Anal. [02 6); 31P ( -1.15 , -1,27 , -1.36 ). [V 2] 1,4 ,5 -P O(OBn)2, 2,3,6 -BZ J: Syr up. [a.)54 6- 11. 3 (EtOH ). 1H. 31P (-0.9 5, -1 .12 , -1.42 ). Anal. [B All) 1,4,5 -P O(OCH2CH2CN)2, 2,3,6 -B ru: Mp 105 -1 07 (EA -PE). [a) D+4.0 (c 1, CHCb). 1H. 31P. Anal. [G 14] 1,4 ,5 -P O( NHPh )2, 3,6-B n i: Mp 230 -2 31 (EtO H). [a.)D+1 6 (c 3.5, CHCb). [S8 )1,4,5 -PO( NHPh )2, 2,3,6 -B ru: Mp 227 -229 (be nzene). 31P (1.82 , 2.93(2P)).FAB. [026]
1,4,5 -XPJ, 6 -Ac, (2,3) -Hex: Mp 126 -128 (EA). 〔아 -20.0 (c 2.30, CHCb). Rf 0.21 (CHCb-acetone 4:1). 1H. 31P (-1.91, -2.40, -3.48). Anal. [036]1,4,5 -XPJ, (2,3)D -Camphor, 6 -Bn: Syrup. Rf 0.15 (acetone -CHCb 1:30). 31P (-2.06, -1,55, -0.84), [BR16,BR18) 1,4,5 -XPJ, 2,3,6 -Bru: Mp 101 -103 (EA-hexane). [a]n29-7.6 (c 1.05, CHCh). 1H. 13C. 31P (-1.28, -0.30, 0.48). Anal. [026]L-form 1,4,5 -PO(OBn)2, 6 -Bn, (2,3)Hex: Oil. 〔이v+6.5 (c 0.28, CHCb). FAB. [B14)1,4,5 -PO(OBn)2, 2,3,6-BnJ: Mp 113 -115 (EA-PE 1:20), 31P. [G9)1,4,5 -PO(OCH2CH2CN)2, 2,3,6 -BnJ: Mp 105 -107. 〔야 -3.7 (c 1, CHCb). [G14]3 -8. 1(1,4,6)PJ 3 -8 -1. Salt form (士)-formLi: 31P. [CH5]Na: Mp>240 (ILO -MeOH). 1H. 13C. 31P (1.91, 2.06, 3.34 at pH 6.04). Anal. [033]D-form Na: [a]D20-8.9 (C 。.9,Th이. [033]L-form Na: [a)o20+9.4(c 0.85, I-LO). [033]3 -8 -2 . Prote c t ed for m (士) -form 1,4 ,6 -P O(OEt) 2, 2,3,5 -BZJ : 31P. [C H5] 1,4 ,6 -X PJ, 5 -A c, (2,3) -H ex: Mp 139 -1 41 (EE -M C ). 1H. IR. Anal. [0 33] D-fo rm 1,4,6 -X PJ, 5 -A c, (2,3) -H ex: Mp 141 -1 43.5 (EE -M C). 〔야 -2 9.0 (c 0.9 , MC ). 1H. Jtp (0.81, -1 .11 , -3 .04). [03 3,036) L-fo rm 1,4,6-X PJ, 5 -Ac, (2,3)- H ex: Mp 141 .5 -1 45 (EE -MC ). 〔야 20+29.5 (c 1.0 , MC ). [03 3] 3 -9 . 1(1,5,6) P J 3 -9 -1 . Salt form (士)- form Li: 31P. [C H5] L-fo r m Na: 1H. [F3 ] 3 -9 -2 . Prote c te d for m (土)-fo nn 1,5,6 -PO(OEt) 2, 2,3,4 -BZ J: 31P. [C H5]
L-fo rm 1,5,6 -P O(OBn)2, 3 -A c, 2,4 -B n2: [a )o -1 5.7 (c 1, CHCb). 1 H. 31P ( -2.4 0 , -1 .85 , -1 .53 ). [C 5] 1,5,6 -P O(OBn)2, 2,4 -B n2: 〔야 -8 .2 (c 1, CHCb). 1H. 31P ( -2.12, -1 .55 , -1 .43 ). [C 5] 1,5,6 -P O(OBn)2, 2,4 -B OM2, 3 -P MB: 1H. 13C. HRMS. [F 4] 1,5,6 -P O(OBn)2, 2,4 -B OM2: 1H. 13C. 31P ( -0.54, -0 .99, -1 .03 ). HRMS. [F4 ] 3 -10. 1(2,4,S)PJ 3 -10 -1. Salt f or m (土)-fo rm Li: 31P. [C H5] Na: 1H. 31P (5.3 8 , 7.0(2P)). FAB. Anal. [B 14)
ammon ium : 13C. [C l] D-fo rm cyc l ohexy la mmon ium : [a) 546- 8 .0 5 (H20). 1H. 31P (5.08(2P), 5.21 at pH 9). Anal. [B A13) L-fo rm cyc l ohexy la mmon ium : [D _ for m 2,4 ,5 -P O(OBn)2, 1,3,6 -B nJ: Sy ru p . [cx )o26- 9.0 (c 1, CHCh). 31P. Anal. (Gll ) ; 1H. 31P ( -1 .53 , -1 .57 , -1 .76 ). FAB. Anal. (B 14) 2,4 ,5 -P O(OBn)2, 1,3,6-BZ J: Syr up. [CX )S4- 17.l (EtO H ). 1H. 31P (-1. 55 , -1 .92 , -1 .95 ). 〔 BA 印 2,4 ,5 -P O(OBn, ONa), 1,3,6 -B ru: Mp 269 -2 71 . [a ] D2 5 - 5.0 (c 1, CHCh). 31P (-0. 4 0 , -0.61 士 2). [G ll] L-fo r m 2,4 ,5 -P O(OBn)2, 1,3,6 -BZ J: Sy ru p . (이요+ 16.4 (EtO H). 1H. 31P (-1. 55 , - 1.92 , -1 .95 ). [B A13] 3 -11. 1(2,4,6)P3 3 -1 1 -1 . Salt for m K: 1H. 13C. 31P. [C H3] Li: 31p _ [C H5)
3 -1 1 -2. Prote c te d for m 2,4,6 -P O(OEt) 2 , 1,3,5 -B Zl: 31P. [C H5) 2,4 ,6 -P O(OEt) 2, (1, 3,S)Orth : Oi l. Rf 0.5 (MeOH -M C 1:10). 'H. 13C. 31P. FAB. [C H3) 3 -12. I(4,5,6)P3 3 -1 2 -1 . Salt for m Li: 31P. [C H5] 3 -12 -2. Prote c te d for m4,5,6 -PO(OEt) 2, 1,2,3 -BZ J: 31P. (CHS] 3 -13. I(l,2)cP(4,S)P2 D-fo r m ammon ium : (a)o23 -1 1 (c 1.0, ILO). (06) 3 -14. l(l)P(4,5)py roP D-fo rm ammon ium : 1H. 13C. 31P ( -9.02, -8.65, 2.52 at p H 6.73). [0 26] 4. Tetr al dsph o sph ate 4 -1 . 1(1,2 ,3,4 )P4 4 -1 -1 . Salt f or m (士)-fo rm K: 31p _ [C H4] 4 -1 -2 . Prote c te d for m (士)-fo rm 1,2,3,4 -PO(OEt) z, 5,6 -B zz: 31P. [C H4] 4 -2 . 1(1;1 ,,3,S)P4 4 -2 -1 . Salt f or m K: 31P. [C H4]
4 -2 -2 . Prote c te d for m 1,2,3,5 -PO(OEt) 2 , 4,6 -B z2: 31P . [C H4] 4 -3 . 1(1,2,4,S)P ◄ 4 -3 -1 . Salt for m (士) -form ammon ium : 1H. 13C. [C l] K: 31P. [C H4] Li: 1 H. 31P (6.17, 6.29, 6.3 5 , 6.64, pH 10). [M E2] 4 -3 -2 . Prote c te d for m (土) 一 fon n 1,2,4 ,5 - PO(OEt) z, 3,6 -Bz: M p 122 -1 23. [P7) ; 31P. [C H4)
1,2,4,5 -P O(OMe)z, 3,6 -Bz: Mp 211 -213. 1H. 31P (1.68 , 2.03, 2.1 7 , 2.74). [M E2)4 -4 . 1(1 ,2 ,4,6) P4 4 -4 -1. Salt for m (士) - fo rm K: 31p _ [C H4] 4 -4 -2. Prote c te d for m (士)-fo rm 1,2,4,6 -PO(OEt) 2, 3,5 -B Z2: 31P. [C H4]4 -5. 1(1,2,5,6)P4 4 -5 -1 . Salt for m (土)-fo rm K: JI P. [C H4] 4 -5 -2 . Prote c te d for m (土)- for m 1,2,5,6 -PO(OEt) 2, 3,4 -B z2: 31P. [C H4] 4 -6 . 1(1 ,3,4 ,5)P4 4 -6 -1. Salt f or m (土)-fo rm cy cl ohexy la mmon ium : Mp 175 -177 (H20 -aceto n e). 1H. FAB. Anal. [B 4, B13] H, 2 -( pN H2)Bz: Rf 0.17 (nPrOH -N HJ - H20 5:4:1, cellulose TLC ). 1H. Anal. [0 37) H, 2 -( amino cy cl ohexy lC O): Rf 0.24 (nPrOH -NHJ - HzO 5:4:1, cellulose TI..C). 1H. Anal. [0 37] K: 31P. [C H4] Li: 1H. 31P. [M E2] D-fo rm ammon ium : [0.)D 24- }3 (C 1.0, ILO). [0 5] K: (a.)02 0 - 3.83 (c 3.6, ILO, pH 5.4 ). [01 7); [a.)02 3- 3.5 (c 5.5, ILO, pH 8.3 ). 1H. 31P (2.94, 4.58, 4.73, 5.27). [C 3,C4] cyc l ohexy la mmon ium : Mp 173.7 -175.7. Rf 0.31 (H20 -2 5% NIL -PrOH
2:5:5). [a.)02 5- 2.5 (c 1, H20). 1H. 13C. 31P. IR. [Z l ) L-fo rm cyc l ohexy la mrnon ium : Mp 169.8 - 1 71 .8. (야 +2.6 (c 1, !LO ). [Z l ) 4 -6 -2 . Prote c te d for m (士) -f orm 1,3,4,5 -P O(OBn)2, 2,6 -B n: Sy ru p . 1H. FAB. [B 13)
1,3,4,5 -P O(OEt) 2, 2,6 -B z2: 31P. [C H4] 1,3,4 ,5 -P O(OMe)2, 2,6 -B z: 1H. 13C. [M E2] 1,3,4 ,5 -X P4, 6 -B n, 2 -( pN 02)Bz: Rf 0.4 3 (Me OH -M C 1:10). 1H. IR. Anal. [03 7] D-fo rm 1,3,4,5 -P O(OBn)2, 2,6 -B n2: Sy ru p . 〔야 -4 .0 (c 1, CHCL). 3 1P. Anal. [G 8); Sy ru p . [a.Jo - 3 .5 (c 2.9 , CHCb). 1H. [C 4); Rf0. 04 (Me OH-M C 1:50). 'H. 13C. 3'P (-1 .34 , -1 .01 , -0 .83, -0 .60). [Z l ); 3 1P (-0. 76, -1 .06 , -1 .24 , -1.57 ). [V 2] 1,3,4 ,5 -P O(OBn, ONa), 2,6 -B 112: Mp 297 -300 (EtO H -A ceto n e). 〔야라 3.8 (c 1, MeOH). 3 1P. Ana1(3ILO). [G 9] 4 -7 .l(l,3,4,6) P4 4 -7 -1 . Salt f or m K: 31P. [C H4] 4 -7 -2 . Prote c te d for m1,3,4,6 -PO(OBn)z, 2,5 -B nz: Sy ru p . 31P. Anal. [G 9)
1,3,4,6 -P O(OBn, ONa), 2,5 -B n2: Mp 313 -316 (EtO H -H zO 4:1). 31P. Anal (3Hz0). [G 9] 1,3,4,6 -PO(OCILCILCN)z, 2,5 -B nz: Mp 109 -110. 1H. 31P. Anal. [G 8)1,3,4,6 -PO(OEt) z , 2,5 -B zz: 31P. [C H4) 4 -8. 1(1,4,5,6) P4 4 -8 -1 . Salt for m (士)-fo rm K: 31P [C H4] Li: •H. 31p _ [M E2] D-fo rm Na: Mp > 270. 〔야 24 -1 0.2 (c 2.4 6 , !LO , pH 10.7). 1H. 13C. 31P (0.8 3 , 1.75 , l.85(2P)). Anal. [03 5); [a ]n - 6.2 (c 2.15, !LO , pH 9.5). 1H. 31P (4.02, 4. 책 4.4 1 , 4.93). FAB. [B R18) L-fo r m H: [a.)D2 0 -3 .0 (c 1.0, ILO). 1H. 31P (0.82, 0.55(2P), -0.11). FAB. [Z 27)H (3 -Me): 〔아다 2.7 (c 0.5 , ILO). 1H. 31P (1.3, 0.9, 0.4 (2P)). FAB. [Z 27)Na: Mp > 270. 〔이 D24+9.8 (C 1.43 , ILO, pH 11 .1). [0 35] 4 -8 -2 . Prote c te d for m (士)-fo rm 1,4,5,6 -PO(OEt) 1, 2,3 -BZ i: 31P. [C H4] 1,4,5,6-P O(OMe)1, (2,3)Ace: 1H. [M E2] D-fo rm1,4 ,5 ,6 -P O(OBn)2, (2,3) -Hex: Sy ru p . 〔 a 詞 3 -8.7 (c 5.77, MC ). Rf 0.4 (MeOH -M C -E A 1:10:20). 1 H. 31P (-0.62, -0.52, -0.4 6 , 0.06). Anal. [0 35) 1,4 ,5 ,6 -X P4, (1, 2)L -Camp ho r: Rf 0.16 (aceto n e -CHCb 1:30). [
5 -1 -2 . Prote c te d for m (士)-fo rm 1,2,3,4 ,5 -P O(OMe)2, 6 -B n: pre p . [A 26] 1,2,3,4 ,5 -PO(OEt) 2, 6 -B z: 31P 〔 CH 이 5 -2 . I(l,2,3,4,6) Ps 5 -2 -1. Salt f or m Na: 꼬 P [C H9] 5 -2 -2 . Prote c te d for m 1,2,3,4 ,6 -PO(OEt) 2 , 5 -B z: 31P 〔 CH 이 5 -3. l(l,2,4,5,6)Ps 5 -3 -1 . Salt for m (士)-fo rm ba rium : pre p. [A 26] Na: 31p [C H9] 5 -3 -2 . Prote c te d for m (土)-fo rm 1,2,4,5,6 -PO(OEt) 2, 3 -B z: 31P [C H9] 1,2,4,5,6 -P O(OMe)2, 3 -B n: Mp 177 -1 81 . Anal. [A 26] 5 -4 . 1(1,3 ,4 ,S,6} Ps
5 -4 -1 . Salt for m H, 2 -Bz: R f 0.24 (nPrOH -N HJ - H20 22: 1: 16, cellulose TLC ). 1 H. [0 37] H, 2 -( pN H2 )B z: Rf 0.4 1 (nPrOH -N HJ - H20 11: 1: 8, cellulose TLC ). 1H. (037] K: Rf 0 .3 (nPrOH-N IL-H iO 5:4:1, cellulose TLC ). 1H. 13C . Anal. [0 37) Na: 31P 〔 CH 이 5 -4 -2 . Prote c te d for m 1,3,4 ,5 ,6 -PO(OEt) z , 2 -Bz: 3 1P [C H9] 1,3,4 ,5 ,6 一 XPs, 2 -B z: R f 0.5 (Me OH -M C -EA 1: 10:20). ' H. Anal. [0 37) 1,3,4 ,5 ,6 -X Ps, 2 -( pN 02)Bz: Mp 174 -1 75. Rf 0.3 3 (CHCb -a ceto n e 6:4). 1H. Anal. [ 0 37] 6. Hexak isp h o sph a te 6 -1 . Salt f or m 31P (pH titrat i on ). [Z 23] 6 -2 . Prote c te d for m (土)- form 1,2,3 , 4 ,5 ,6 - PO (OMe)2: M p 247 -249. 1H. Anal. [A 18] 7. Inosit ol thiop h osph ate 7 -1 . Free for m (土)-fo rm
1 -PS, cyc l ohexy la mmon ium : Mp 165 -170 (luO -aceto n e). 1H. 13C. FAB. IR. Anal. [ B 15)
1 -PS, Ki salt: 31P (45.2). [ZI O)1 -PS, Ki salt, 2,3,4 ,5 ,6 -A cs: 3 1P (44.1). [Z IO] 1 -PS, 4,5 -P 2, triet h y la mmoniu m : 1H. 31P (42.1 3 , 4.5 8 , 3.50, pH 8). FAB. HRMS. [P5 ] D-fo rm 1 -PS, cyc l ohexy la rnmon ium : [a.Jo +1 .8 {c 2.5 , HzO, pH 6.5). [B 15] 3 -PS, cyc l ohexy la mmoniu m : [a.Jo - 2 .5 (c 2.5 , HzO, pH 6.5). [B 15] 1 -PS, 4,5 -P2, triet h yla mmon ium : @건 -4 2.7 (c 0.19, HzO, pH 9.4 ). [P5 ] 7 -2. Prote c te d (士) -for m 1 -PS(OCILCILCN)2, 2,3,4 ,5 ,6 -B ns: Mp 97 -9 8 (Me OH). 1H. 13C. FAB. IR. Anal. [ B 15] 1 -PS(OCILCILCN )2, 4,5 -PO(OCILCILCN)2, 2,3,6 -BnJ: Sy ru p. 1H. 13C. 31P (66.8 3 , -2.83, -3.10). FAB. HRMS. [P5 ) D-fo r m 1 -PS(OCILCILCN )1, 2,3,4 ,5 ,6 -B ns: Sy rup. (ex) -2.2 (c 1, CHCb). [B 15] 3 -PS(OCILCILCN )1, 1,2,4 ,5 ,6 -Bns: S y ru p . 〔야+ 1.4 (c 1, CHCb). [B 15] 5 -P S(OBn)1, 1,4 -P O(OCILCILCN)2, 2,3,6 -Bib : Sy ru p . (cx)o 25 - 4.7 (c 1.1, CHCL). 31P (68.77, -1 .88 , -2.28). Anal. [G ll] 1 -PS(OCH2CILCN)1, 4,5 -PO(OCILCH2CN)2, 2,3,6 -BnJ: [cx ) o+l 0.5 (c 2.5 , CHCL). [P5 ]Ill. Inosit ol wit h chir al auxil ia r y (Numberin g based on D-fo rm ) 1. Camp h anatc 1 一 (+) -Camp , (4,5)Ace, 2,6 -B n2, 3 -P MB: Mp 150 -1 52 (EE). [CX )D25 - 53 (c 1, CHCb). Anal. (G13] 3 -( -) - Camp , (5,6)Ace, 2,4 一 Bn2, 1 -P MB: Mp 151 -1 53 (EE ). [cx )o25+ 49 (c 1, CHCb). 1H. Anal. [G 13] 1 -( +) -C amp , (4,5)Ace, 2,316 -B n3: Mp 170 -1 71 . [CX )o27 -5 3 (C 1, CHCb). Anal. [G 9)
3 -( -) -Camp , (5,6)Ace, 1,2,4 -B n3: Mp 170 -172. 〔아 +53.1 (c 1, CHCh). [G 3); 1H. [G 9)4 -( -) -Camp , (2,3)Ace, 1,5,6 -B nJ: Mp 190 -1 91 (EA -PE 1 : 1). 〔야다 34 (c 0.8, CHCL). 1 H. Anal. [G 6)6 -( -) -Camp , (1, 2)Ace, 3,4,5 -BI1 .J: Mp 177 -1 79 (EA -P E 1:2). 〔이 D26 -4 7 (c 1, CHCh). 1H. Anal. [G 6] 1 -( -) -Camp , 6 -Bn, (2,3)Hex: Mp 176-1 78. [cx )o20- 3 2 (c 0.1 , CHCL). [B 2); 1H. [B 14) 3 -( -) -Camp , 4 -Bn, (1,2)Hex: Mp 145 -1 49. 〔아 +26 (c 0.1 , CHCL). 1H. FAB. Anal. [B 14] 1 -( -) - Camp , 6 -Bn, (2,3;4,5)HeX2: Mp 152 -1 53. [B 2); (cx)o -3 7 (c 0.1, CHCh). 1H. FAB. Anal. [B 14] 3 -( -) -Camp , 4 -B n, (1, 2;5,6)HeX2: Mp 121 -1 23. [B 2);叫 +23 (c 0.1, CHCL). 1H. FAB. Anal. [B 14)4 -( -) - C amp , 1 -B n, (2,3;5,6)HeX2: Mp 231 -2 33 (EA-P E 1:2). 〔야 -3 0 (c 0.4 5 , CHCL). 1H. FAB. HPLC. Anal. [B 14] 6 -( -) - C amp , 3 -Bn, (1,2;4,5)Hex2: Mp 228 -230. 〔야 +20 .4 (c 1.2, CHCh). 1H. FAB. HPLC. Anal. [B 14] 1 -( -) -Camp , (2,3,4 ,5 ,6)Bns: X -ray. [B 3); Mp 161 -164. [cx )o -17.6 (c0.5, CHCb). 1H. 13C. Anal. [B 15] 3 -( 기 -C amp , (l,2 ,4 ,5 ,6)Bns: Mp 146 -1 48. 〔아+ 12.0 (c 0.5 , CHCb). 'H. 13C. FAB. IR. Anal. [B l5] 4 -( 기 -C amp , (2,3;5,6)Hex: Mp 236 -2 37. [a.)n- 2 5.5 (c 0.11, CHCb). 1H. Anal. [Z 26] 6 -( -) -Camp , (l,2 ;4,5)Hex: Mp 224 -225. 〔야+ 12 (c 0.1, CHCb). 1H. Anal. [Z 26J 4 -( 키 -C amp , (2,3;5,6)Hex, 1 -Tf: Mp 157 -159. [a.)n +4.4 6 ( c 1.42 , CHCb). 1H. [Z 26] 6 -( 기 -C amp , {1, 2;4 , 5)Hex, 3 -Tf: Mp 129 -1 31 . [a.)n +4.4 6 ( c 0.4 6 , CHCb). 1H. [Z 26] 1,5 -( +) -Camp 1, (3,4 ) Ace, 2,6 -Bn1: Mp 216 -217. [a.)n 15 - 36 (c 1, CHCb). A nal. [ G 8)
3,5 -( 키 -C amp 1, (1, 6)Ace, 2,4 -B n1: Mp 221 -223. 〔 a 詞 5+36.5 (c 1, CHCb). 1 H. Anal. [G 8] 4,5 -( +) -Camp 1, (1, 2)Ace, 3,6 -B n1: Mp 148 -1 50 (EA -EE -PE 1:4:1). [a.)n 15+ 10.0 (c 1, CHCb). Anal. [G lO) 5,6 -( 기 -C aml )l, (2,3)Ace, 1,4-B il l: M p 148 -1 50 (EE -PE 2:1). 〔이 D15 -9.1 (c 1, CHCh). 1H. Anal. [G lO] 4,5 -( +) -Camp 1, 1 -All, 2,3 ,6 - BnJ: Mp 142 -1 43 (EA -hexane). [a ]0 1 1 +19.4 (c 5, CHCL). 1H. 13C. FAB. Anal. [P5 ] 5,6 -( -) -C aml) l, 3 -A ll, 1,2,4 -Bll i: Mp 174 -1 77 (EA -h exane). [a ]D 1 8 -2 5.0 (c 4.2, CHCh). 1H. 13C. Anal. [P5 ] 4,5 -( -) - Camp 1, 1,3 -Alb, 2,6 -B n1: Small hard prism . Mp 163 -165. [a.)n 15+ 17.5 (c 1, CHCL). 1H. Anal. [G 8)5,6 -( 기 -C amp 1, 1,3,4 -Alh, 2 -B n: Mp 136 -1 38 (EE ). [a ] D1 5 -2 1 (C 1, CHCb). 1H. Anal. [G 9] 4,5 -( 기 -Camp 1, 1,3,6-Alb, 2-Bn: Mp 209-211 . [a.)n 15+7 (c 1, CHCb). 1H. Anal. [G 9]4,5 -( -) -C amp 2, 2,3,6 -A lh, l -Crot: Mp 118 -1 20. [야 25+2 . 9 (c 1, CHCb). 1 H. Anal. [G l3) 5,6 -( -) — C amp 2, 1,2,4 -A lb, 3 -C rot: Mp 110 -1 11 (EE -PE). [야 25 -2 2 (c 1, CHCb). 1H. Anal. [G l3] 2,4 -( -) - C arnp 2, 1,3,5,6 一 Alk Mp 167 -1 69. (a.)o25 一 13 (c 1, CHCb). 1H. Anal. [G 7] 2,6 -( —) _ Camp 2, 1,3,4 ,5 -A lk Mp 116.5 -1 19 (EA-P E 1:3). 1H. Anal. [m ] 1,6 -( 키 -C amp 2, 2,4 -B n2, 3,5 -P MB: Mp 160 -163. 〔야 25 -1 0 (c 1, CHCb). 1H. Anal. [G 8) 1,6 -( -) -C amp 2, 3,4 -Bil l, 2,5 -P MB: Mp 114 -1 16 (EA -PE ). [a) Dl5一 14.4 (c 1, CHCb). 1H. Anal. [G ll] 3,4 -( -) - Carnp 2, 1,6 -B n2 2,5 -PMB: Mp 176 -1 77 (EA -PE 2:1). [a,)D2 5 -1 .2 (c 1, CHCb). 1H. Anal. [G ll] 3,4 -( -) - C arnp 2, 2,6 -B il l, 1 ,5 -P MB: Mp 196 -1 98. 〔야 0 (c 1, CHCL). 1H. Anal. [G 8] 1,4 -( -) - C amp 2, 2,5,6 -B nJ, 3 -P MB: Mp 186 -1 88 (Me OH ). 〔야 -1 1 (c 1, CHCb). 1H. 13C . FAB. Anal. [P6 )
3,4 -( -- ) -Camp 2, 2,5,6 -BnJ, 1 -P MB: Mp 198 -200 (EA -P E 1:1). 1H. Anal. (G9] 3,6 -( -) -Carnp 2, 2,4,5 -B ns, 1 -P MB: Mp 194 -1 95 (Me OH ). 〔야 +5 (c 1, CHCb). 1H. 13C. FAB. Anal. [P6 ] 4,5 -( -) - C amp 2, 2,3,6 -BnJ, 1 -P MB: Mp 111 -112 (Me OH). [a) D+ 13.1 (c 1, CHCb). 1H. Anal. [ G 13)5,6 -( -) - C amp 야, 1,2,4 -B nJ, 3 -PMB: Mp 172 -175. [cx )o25- 1 9.3 (c 1, CHCb). 1H. Anal. [ G 13] 1,4 -( +) -C amp 2, 2,3,5,6 -B n4: Mp 229 -2 31 (Me OH -EA 8:1). 〔야 25 _ 1.9 (c 1, CHCL). Anal. [G 9] 1,4 -( -) -Camp 2, 2 ,3,5,6 -B n4: Mp 192 -194 (Me OH). 〔야 25 -7 .7 (c 1,CHCb). 1H. Anal. [ G 9)
2,4 -(- ) -Camp •, 1,3,5,6 -B n4: Mp 173 -1 74. 〔야 +2.0 (c 1, CHCb). 1 H. Anal. [ G 6)3,4 - ( -) -Camp 2, 1 ,2 ,5 ,6 -Bn.: M p 200 -202. [a.)02 5- 1 .3 (c 1, CHCb). 1H. Anal. [ G 6] 3,6 -(- ) -Camp 2, 1,2 ,4 ,5 -B n4: Mp 234 -236 (EA -PE). [a.)0 25+1 .1 (c 1, CHCb). 1H. Anal. [G 9] 4,5 -( -) - Camp 2, 1,2,3,6 -B n4: Mp 176 -178 (MeOH). [a.)0 25+1 1 (c 1, CHC13). 1H. Anal. [G 9] 1,4 - ( -) -Camp 2, (2,3;5,6) -H eXl: Mp 280 -320. sub 328 -329. [a) D -31.0 (c 0.2, CHCb). 1H. FAB. Anal. [B 14)3,6 -( -) -Camp 2, (1, 2;4,5 ) -H ex2: Mp 250 -330. sub 338 -339. 〔야 +9.0 (c 0.2, CHCb). 1 H. FAB. Anal. [B 14] 2. Menth o x yac ety l 1 -( L) -M nt, 4,5 -A ll2, 3,6 -B n2: Mp 67.5 -6 8.5 (he xane). Rf 0.5 2 (EA -hexane 3:2 ) . [a.)n3 0- 54.1 (c 2.2, CHCL). 1H. 13C. IR. Anal. [0 26] 3 -( L) _ Mnt, 5,6 -Alh, 1,4 -Bil l: Rf 0.61 (EA -he xane 3:2). [a.)n3 0- 1 4.7 (c 1.9, CHCL). 1H. 13C. IR. [0 26] 1 一 (L) -M nt, 3 ,5 , 6 -A lL, 4 -Bn: (a.) 020 -50.5 (CHCL). [ V 2] 3 -( L) -M nt, 1,4 ,5 -Alb, 6 -B n: [a] n2 0 -18.9 (CHCL). [V 2] 3. Menth y l c arbonate 1 -( L) -M nc: Mp 171 -173. 〔야 -7 1 (c 1.5, MeOH ). [PE 3] 3 -( L) -M nc: Mp 183 -186. 〔야 -1 6 (c 1.7, MeOH). [PE 3] 1 -( L) -M nc, (2,3;4,5)Ace2: Mp 62 -6 4. 〔야 -6 1 (c 1.0, MeOH). [PE 3] 1 -( L) -M nc, (2,3;5,6)Ace2: Mp 184 -186. [a.Jo - 64 (c 0.73, MeOH). [PE 3]1 -( L) -M nc, 6 -B n: Mp 60 -6 5. (a)o -4 7 (c 0.9, CHCb). (PE3) 1,6 -(L) -M nc2, (2,3;4,5 ) Hex2: Rf 0.74 (EE-h exane 1:3). [a) o20- 6 1 .1 (c 1.02, CHCb). [C 2)
3,4 -(L) -M nc2, (1, 2;5,6)HeX2: Rf 0.87 (EE -hexane 1:3). [a) o20- 31 .8 (c 1.0, CHCb). [C 2] 4. Acety lm andelate 5 -( +) -M an, 4 -B n, (1, 6;2,3)Hex: Mp 143 -1 44 (EE -PE ). [a.)0 22+35( c 1, CHCb). Rf0. 66 (EA-CHCh 1:60). A nal. [L 2)5 -( +) -Man, 6 -B n, (1,2 ;3 ,4 )H ex: (야 22+24 (c 1, CHCb). R f 0.7 7 (EA -CHCb 1:60). [L 2)1 -( L) -Man, 3,4 -B n2, 5,6 -P MB2 : R f 0.4 6 (EA -t ol uene 1: 3). [Z 17)3 -( L) -M an, 1,6 -B n2, 4,5 - P MB2: Rf 0.5 7 (EA -t ol uene 1: 3) . [Z 17) S. Tart ra te 4 -( iPr , 2,3 -Bnz -( +) -Tar), 3 -Bn, (1,2;5,6)Hexz: 〔이 o -3 9 (c I.I, CHCb). R f0. 68 (EA-to l uene 1:4). 1 H. 13C. [L 3)6 -( iPr , 2,3 -Bn2 -( +) -Tar), 1 -Bn, (2,3;4,S)Hexz: [a )o- 3 9 (c I.I, CHCh). Rf0 .5 9 (EA -to l uene 1:4). 1H. 13C. [L3 ] 4 -D -Tar, 1,3,5 -B z3, 2,6 -( SiE tJ )z : Mp 139 -1 41 . [a) o24 + 7.55( c 1.0, CHCh). [0 17] 6. Camp h or (2,3) -D -Camp ho r: Mp 231 -232. Rf 0.2 5 (Me OH-C HCh 1:4). 1H. 13C. Anal. [B R18,BR19] (5,6)Ace: Rf 0.18 (aceto n e -CHCb 1:15). 〔이타 ·26.5 (c 2.2, CHCb). 1H. 13C.[B R16,BR18) (5,6)Ace, 1 -B n: Rf0 .2 5 (aceto n e -C C14 1:10). [a ) o-1 1. 4 (c 2.1, CHCL). 1H. 13c . [B R18)
(5,6)Ace, 1,4 -TBDMS2: Sy ru p. Rf 0.21 (EE -hexane 1:40). 〔야 +3 (c 2.0, CHCh). 1 H. 13C. [B R16,BR18) 6-Bn: Mp 44-45. Rf0. 2 (MeOH-CHCh 1:70). 〔야 +16.2 (c 2.5 , CHCh). 1H. 13c. [B R16,BR18] 6 -Bn, 1,4,5 -P iv J : Mp 184 -1 85. Rf 0.1 2 (EE -C C14 1:15). [a) o- 1 4 (c 2.1 , CHCL). 1H. 13C . [B R16,BR18) 1,4,5,6 -Bn4: (a)o 2 0+ 18 (c 3, CHCh). Rf 0.14 (benzene -i Pr 20 100:1 ) . 1H. Anal. (for oth e r iso mers tog et h e r) [B R9,BR19) 6-B z, 1 -TBDPS, (4,5)TIPDS: Rf0 .2 (EE-h exane 1:20). (a)o + 26.2 (c 2.6, CHCh). 1H. 13C . [B R19)4,5 -B z2, (1,6)TIPDS: Rf 0.32 (EE -t ol uene -hexane 1:50:50). 1H. 13C. Anal. [B R19)5 -M OM: [a )o+1 9.1 (c 1.4 , MeOH). 1H. 13C. HRMS. [B R19) 6-M OM: [a )o+1 4.5 (c 4.5, MeOH). 1H. 13C. HRMS. [B R19) 6 -M OM, 4 -Piv , 1 -TBDPS: Rf 0.27 (aceto n e -hexane 1:8). 13C. [B R19] 4 -MOM, 1 -TBDPS: 1H. [B R19)6 -M OM, 1 -T BDPS: [a) o- 39.5 (c 4.2, CHCL). 1H. 13C . HRMS. [B R19] 5,6 -M OM2: Mp 96 -97. Rf 0.15 (aceto n e -hexane 3:10). 1H. C HRMS. [B R19)5,6 -MOM2 , 4 -Piv , 1 -TBDPS: Rf 0.39 (aceto n e -h exane 1:8). 1H. 13C. (BR19] 4,5,6 -MOM J: Rf0. 13 (EE -h exane 2:1). 1H. C HRMS. [B R19] 4,5,6 -MOMJ , 1-TBDPS: Rf0 .4 (EE -he xane 1:1). 1H. 13C. [B R19] 1 -Piv : Foam. Rf 0.2 (Me OH -CHCh 1: 10). 1H. 13C. [B R18 ] 4 -Piv , 1 -TBDPS: Rf 0.27 (aceto n e -h exane 5:20). 1H. 13C . HRMS. [B R19] 1,5 -P iv 2 : Foam. Rf 0.24 (aceto n e -C HCL 1: 10). 1H. [B R18]1,4,5 -Piv J : Mp 110-1 12. 〔야 _ 12 (c 2.1 , CHCb). Rf 0.27 (aceto n e -CCl, 1:SO). 1H. 13C. [B R16,BR18] 1,4,6 -Piv J : Sy ru p . Rf0. 1 0 (aceto n e -C C14 1:20). 1H. [B R18) 1,5, 6 -Piv J : Mp 206 -2 08. Rf 0.2 8 (aceto n e -CCl, 1: 20). 1H. (BR18) 1 -TBDPS: Foam. Rf 0.22 (MeOH -CHCb 1:30). 〔 a 硏 -2 4.7 (c 4.4 , cHCb). 1 H. •ic . Anal. [ B R18,BR19] 1 -TBDPS, (4,S)TIPDS: Rf 0.64 (aceto n e -hexane 1:10). 1H. 13C. FAB. [B R19] 1,4 -TBDPS2: Sy ru p . Rf 0.2 (EE-h exane 1:3). [a.)o-1 0 (c 2.0, CHCL). 1H. IJ C . [B R16,BR18) ; Rf 0.32 (aceto n e -hexane 3:20). [a ] o -30.s. 1H. 13C. [B R19] (1, 6) TIPDS: Rf 0.3 3 (aceto n e -hexane 3:20). [a ]o +9.3( c 2.1, CHCL). 1H. 13C . Anal. [B R19)
7. ( + ) -(R) -1 -( ph eny le th y l) amino carbony l ( Carb) 4 -Carb, 6 -B n: Mp 186 -1 88. Rf 0.3 (Me OH -E A 1:50). [a ] 02 5+48.4 ( C 1, CHCh). 1 H. 13C. IR. Anal. [Z l ) 4 -Carb, 6-B n, 1,3,5 -Or th: Rf 0.4 7 (EA -h exane 1:1 ) . (a.)0 245+25.8 (c 1, CHCh). 1 H. 13C . IR. Anal. [Z l ) 6 -Carb, 4 -Bn, 1,3,5 -Or th: Rf 0.39 (EA -he xane 1:1). [a ]D 245+22.3 (C 1, CHCh). 1H. 13C . IR. Anal. [Z l ) 4 -Carb, 2,6 -B n: Rf 0.65 (EA -hexane 4:1). [a ]0 2 5+21 .9 ( c 1, CHCL). 1H. 13C. IR. Anal. [Z l] 6 一 Carb, 2,4-B ru: Rf0. 62 (EA -hexane 4:1). 〔이 0245+39.8 (c 1, CHCh). 1H. 13C. IR. Anal. [Z l ) 4 -Carb, 2,6 -B ru, 1,3,5 -Or th: Rf 0.295 (EA -hexane 1:2). (a.)0 25+ 14.2 (c 1, CHCh). 1H. 13C. IR. Anal. [Z l] 6 一 Carb, 2,4 -B ru, 1,3,5 -Ort h: Rf 0.28 (EA -he xane 1:2). [a.)0 245+1 3.3 (c1, CHCh). 1H. 13C . IR. Anal. [Z l) IV. Inosit ol Aceta l 1. Monoaceta l 1 -1 . (1,2)Aceta l 1 -1 -1 . (1,2)Ace (士) -form : Mp 182 -1 84. [G l) ; Mp 182 -1 83. [A 26)
5 -A c, 3,4 -B lll, 6 -P MB: Syr up. 1H. Anal. [G 6)6 -A c, 3,4 -B n2, 5 -P MB: Mp 112 -1 13 (EA -P E). 1H. Anal. [G 6)6 -A c, 3 ,4 ,5 -B I1 J: Mp 98 -9 9 (PE ). 1H . Anal. [ G 6] 6 -A c, 5 -M e: Anal. [A 9] 3,5 -A c2, 4,6 -B lll: Mp 110 -1 11 . [G 12] 4,5 - Ac2, 3,6-B lll: Mp 114 -1 16. Anal. [G 3] 5,6 -A c2, 3,4 - B n2: Mp 127 -1 28. [G 6] 3,4,6 -A cJ, 5 -M e: Mp 107 -1 08. Anal. [A 9] 3,4 ,5 -AcJ, 6-Bn: Mp 90- 9 1. 1H .. A nal. [G lO] 3,4,5 ,6 -Ac .: Mp 123 -1 25. 1H. GlO Mp 122 -1 23. [A 13] 4 -A ll, 6 -B n: Mp 82 -8 3 (EE -hexane). 1H.1 c . CI. Anal. [Z 19] 6 -All, 3 -B n: Mp 120-1 21 (EA -PE 1:2). Anal. [ G 6] 6 -A ll, 4 -B n: Mp 75.5 -7 6 (EE -hexane). 1H. 13C. CI. Anal. [Z 19] 4 -A ll, 3,6 -Bil l, 5 -C rot: Sy rup. 1H. [G ll] 5 -A ll, 3,6 -Bil l, 4 -C rot: Sy ru p . 1H . [G ll] 6 -A ll, 3,4 ,5 -BI1 J: Mp 99 -1 01 (EA -PE 1:10). Anal. [G 6); 1H. 13C. Cl. Anal. [Z1 9] 1,5 -A lh: Mp 90 -92 (PE ). 1H. Anal. [ G 7] 3,6 - A lh: Mp 130 -1 32 (EA -P E). Anal. [G 2] 3,6 -A lh, 4 -B n: Oil . Anal. [G 2]3,6 -A lb, 5 -B n: Oil . Anal. [G 2] 3,4 ,6 -Alb: R f 0 .8 (EE- P E 3:1). (Gl2) 3 -Bn, 4,5 ,6 -BZ J: Mp 214 -215. Rf0 .4 (EA-h exane 1:2). 1H. 13C. [C Hll) 3 -Bn, 6 -PMB: Mp 148 -1 49 (EA-P E 1:1) Anal. [G 6] 3,6 -B n2: Mp 161 -1 63. (G2, GlO) ; Rf 0.5 (EE ). [G lO); Mp 152 -1 53. Rf 0.5 (CHCb-E A 1:1). 1 H. Anal. [C Hl] 4,6 -Bn2: M p 97 -98. Rf 0.5 (EE -PE 2: 1). (G12) 3,6 - B n2, 4,5 -B l1: Sy ru p . 1H. HRMS. (P5] 3,6 -B n2, 4 -Crot: 1H. [G 12] 3,6 -B n2, 5 -Crot: 1H. [G 12)
5,6 -B n2, 4-M e: 1H. IR. HRMS. [L E3] 3,4 -B n2, 6 -PMB: Sy ru p . [ G 6] 3,4 ,5 - BnJ: Mp 89 -90. Anal. [ G 6)3,4 ,6 - BnJ: Mp 80 -81 . Rf 0.8 (EE -P E 2: 1). [G 12] 3,5,6 -B nJ: Mp 60-6 1 . Rf0. 7 (EE-P E 2:1). Anal. [G 12] 3,4,5 -BnJ, 6 -C HzCHzOH: Sy rup. 1H. 13C. Cl. Anal. [Z 19] 3,4 ,5 -BnJ, 6 -C H2CHzOTs: S y ru p . 1H. 13C . Cl. Anal. [Z 19] 3,4 ,5 - B ll i, 6 -PMB: Mp 76 -7 7 (EA -PE). A nal. [G 6] 3 -Bz: Mp 196 -197 (MeOH). Rf 0.2 6 (MeOH -MC -EA 1:10:20). 1H. [03 6] 3,6 -Bz2: X -ray [C H10] 3,4,5 ,6 -B u Rf0 .2 5 (EA -he xane 1:3). 1H. 13C. [C H7] 5 -M e: Anal. [A 9)4 -Me: 1H. IR. HRMS. [L E3] 3,6 -P MB2: Mp 129 -130 (EA -P E). A nal. [ G 2) D-fo rm 4,5 -A c2, 3,6 -B n2: Mp 83 -85. 〔야 25+22.l (c 1.5, CHCL). [G IO] 3,6 -B n2: Mp 85 -8 7. [a.)0 25+3.0( c 1.53 , CHCL). [G IO)L -f orm : Obt. by Enzym ati c Resoluti on . [야 20+44 . 8 (c 2.0, MeOH). [Z l1 ) 4 -A c: Mp 159 -1 60 (CHCh -hexane). [야 21+2 1. 9 (c 1.28 , MeOH). Rf 0.3 1 (Me OH-M C -E A 3:10:2 0 ). 1 H. IR. (036) 5 -A c: Mp 171 -173.5 (CHCb). [a )o21+35.4 (c 1.32 , MeOH). Rf 0.3 1 (Me OH -M C -E A 3:1 0 :20). 1H. [0 36] 4,5 -A c2, 3,6 -B nz: Mp 84 -8 6 (PE). 〔야 -2 4.3 (c 1, CHCb). 1H. Anal. [G lO] 3,5,6 -A lb: Rf0. 7 ( EE -P E 3:1). [G 12)
4 -B n: Mp 120 -1 21 . 〔야+ 12 (c 0.6, MeOH). [PE 3] 3,6 -B n2: Mp 80 -8 3 (EA -P E). 〔야 -4 .0 (c 1, C HCh). 1 H. Anal. (GIO) 3,6 -Croll: Mp 108 -1 10 (EA-P E), (야 25 - 21 .7 (c I, CHCh). 1H. Anal. [G lO)1 -1 -2 . (1,2)Hex (士)-fo rm: Mp 176-178. 1H. 13C. [L 3);Mp 181-183 (ph ase tra nsit ion 160 -1 63). I R. 1H. 13C. FAB. [B 15); Mp 174 -1 75 (EtO H). [0 26); Mp 178. [A IO) 3,4,5,6 -A C4: Mp 118 (EtO H). Anal. [A IO) 5 -A c: Mp 171 -1 73.5 (Me OH -E E). 1H. IR. Anal. [ 0 33] (4,5)Ace: Mp 172 (EE ). 1H. Anal. [ 2 18);Mp 180.5 -1 81 .5. Anal. [Z 8] (4,5)Ace, 6 -Ac, 3 -B z: Mp 219. 1H. Anal. [ Z 8) (5,6 ) Ace, 3 -A c, 4 -M e: Mp 140.5 -1 41. 5. Anal. [Z 8)(4,5)Ace, 6 -A c, 3 -T s: Mp 215 -2 16. 1H. Anal. [Z 8] (5,6)Ace, 4 -A c, 3 -T s: Mp 151 -1 53. 1H. Anal. [Z 8] (4,5)Ace, 3,6 -A c2: Mp 175.5 -1 76.5. 1H. Anal. [Z 8] (5,6)Ace, 3 -B n: Mp 135 -1 36 (EE ). 1H. Anal. [Z 18)(5,6)Ace, 4-Bn: Sy ru p. 'H. HRMS. [Z 18] (5,6)Ace, 4 -Bn, 3 -M OM: Sy ru p. 1H. HRMS. [Z 18](4,S)Ace, 3 -B z: Mp 172.5 -1 73. 1H. Anal. [Z 8] (4,S)Ace, 6 -B z: Mp 177 -1 78. 1H. Anal. (ZS) (4,S)Ace, 3 -B z, 6 -M e: Mp 128 -1 29.5. 1H. Anal. [Z 8] (5,6)Ace, 3 -B z, 4 -M e: Mp 129 -1 31 . 1H. Anal. [Z 8)
(5,6)Ace, 4 -Bz, 3 -M e: Mp 150.5 -1 51 .5. 1H. Anal. [Z 8] (4,5)Ace, 3,6 -B z2: Mp 230. Anal. [Z 8] (5,6)Ace, 3,4 -B z2: Mp 199 -2 02. Anal. (ZS) (5,6)Ace, 3 -M e: Mp 169 -1 71 . Anal. [Z 8] (5,6)Ace, 3 -M OM: Mp 76 -7 7 (hexane). 1 H. Anal. [Z 18] (4,5)Ace, 3,6 -M OM2: Mp 102 -1 03 (EtO H). 1H. Anal. [Z 18)(4,5)Ace, 3 -T s: Mp 167 -1 69. 1H. Anal. [Z 8] • (5,6)Ace, 3 -T s: Mp 223 -227. 1H. Anal. [Z 8) (4,5)Ace, 3,6 -T s2: Mp 192 -1 95. 1H. Anal. [Z 8) (5,6)Ace, 3,4 -Ts2: Mp 165 -1 67. 1H. Anal. [Z 8) 6-All, 3 -B n: Mp 125.5 -126.5 (MC -hexane). Rf0 .4 6 (Me OH-M C 1:19). 1H. 13C. [V 3] 3,6 -A lh: Mp 126.5 -1 27 (MC -h exane). Rf 0.3 5 (Me OH -M C 1:19). 1H. IJC . [V 3] 4,5 -A ll2, 3,6 -B 112: Sy rup. Rf 0.6 (EA -h exane 1:3). ~ H. 13C. IR. [02 6] 5,6 -A lh, 3,4 -B 112: 1H. FAB. [B 14) 4-Bn , 3,5 -M OM2: Sy ru p . 1H. HRMS. [Z 18) 4 -B n, 3,6 -M OM2: Mp 80 -8 1 (EE ). 1H. Anal. [Z 18] 5 -B n, 3,6 -M OMl: Sy rup. 1H. HRMS. [Z 18)4 -B n, 3,5,6 -M OM .J: Mp 52 -5 3 (EtO H). 1H. Anal. [Z1 8] 3 -B n, 6 -P MB: Mp 140 -1 42. Rf 0.12 (aceto n e -MC 1:99). 1H. °C. [V 4] 3,4-B n: Mp 114-116. 1H. FAB. Anal. [B 14)3,6 -B n2: Mp 140 -1 41. [0 26); M p 147.5 -1 48.8. IR. UV. Anal. [S 1 ) 4,5 -B 112, 3,6 -M OMl: Mp 67 -6 8 (he xane). 1H. Anal. [Z1 8] 3,4,5 —B n: Mp 103. Rf 0.4 1 (aceto n e -M C 3:97). 1H. 13C. Anal. [V 4]3,4,5 -Bn, 6 -P MB: Oil . Rf0. 53 (EE-h exane 1:1 ) . 1 H. 13C. [V 4)
3,4 ,5 ,6 -B n4: Mp 84 -8 6 (EtO H). 1H. 13C . FAB. IR. Anal. [B l5] 3,6 -M OM2: Mp 114 (EE). 1H. Anal. [Z l8] D -f orm : Mp 188 -1 89 (MeOH). [a ] 02 2 -36.0 (c 1.05 , MeOH, 96% ee). (035] 3 -A c: Mp 150 -1 52 (MC). 〔 a 詞 +28.6 (c 1.75 , MeOH, 98 ee). 1H. IR. Anal. [0 36] 5 -A c: Mp 170 -1 72.5 (Me OH -EE). [a.)0 20 - 2 9.5 (c 1.05 , MeOH). [0 33) 3 -Ac, 4,5,6-B Z J: Mp 190 -1 91 (EA ). [a ]0 2 1-3 .4 (c 2.95, CHCL, 98 ee). Rf 0.2 6 (EA -he xane 1:3). 1H. IR. Anal. [ 0 36) 3,4 -Alh: (야라 1.6 (c 1.9, C HCh). 1 H. [C 3,C 4] 3,4 -A lh, 6 -B n: [a.)0 23+1 3.6 ( c 1.5, CHCh). 1H. [C 3,C 4] 3,4 -A lli, 5,6 -B n2: [a.)02 3- 4 .5 (c 1.2, CHCL). 1H. [C 3,C4] 3,4 ,5 -Alb, 6-Bn : Sy ru p. (a,)o23 -9.2 (c 1.5, CHCh). 1H. [C 3,C 4] 4 -Bn: Mp 138 -139. 〔파 -2 2 (c 0.1 , CHCh). [B 2); 1H. FAB . Anal. [B 14] 3,6-B n: Mp 119. 〔야타 33 . 0 (c 0.5 , CHCL). A nal. [0 26) 3 -B z: Mp 198 -200 (Me OH). 〔야타 -53.3 (c 1.22 , EtO H). 1H. IR. Anal. [01 2,023] 3,4 ,5 ,6 -Bz: Mp 239 -239.5. 〔야 +29.3 (c 3.00, EtO H). 1H. IR. Anal. [02 3] L -f orm : Mp 188 -189 (MeOH). 〔야 22+36.0 (c 0.95, MeOH). Rf 0.1 0 (Me OH -M C-E A 3:10:20). 1H. [03 3,035, 036) 5 -Ac: Mp 172-1 74.5 (Me OH). [a.)0 22+30( c 0.9 , MeOH). [03 3] 4 -B n: Mp 137 -139. 〔야 +21 (c 0.1 , CHCb). [B 2); 1H. Anal. [B 14); 〔야 + 20.8 (c 1, CHCb). 1H. Anal. [C 2,C4) ; Mp 136 -1 37. [F l] 1,4,5,6 -B u Mp 242 -243 (EA). 〔 a 〕곱드 24.7 (c 2.19, CHCb). Rf 0.17(CHCh-h exane 5:1). 1H. IR. (036] 1 -1 -3. (1,2 )Ben (士) -f orm 3,4 ,5 ,6 -Bn(exo): 1H. 13C. (L3] 3,4 ,5 ,6 -Bz(endo): 1 H. 13C. [L 3] 3,4,5,6 -B z(exo): Mp 272 -274 (EE -PE). Rf 0.88 (EA -t ol uene 1:9). 1H. IJC . [L 3) 3,4,5,6 -Bz(endo): Mp 221 -2 23 (MC -MeOH). Rf 0.84 (EA-to l uene 1:9). 1H. 13C.Anal. [ L 3] 1 -1 -4 . (1,2 )Pen (土)- form : Mp 164-1 66. Anal. [A IO);Mp 156 -1 58. [Z2 2] 3,4,5,6 -A c•: Mp 132 (EtO H). Anal. [A IO] 3,4,5,6 -B n4: Mp 72 -7 3. [Z 22] 4 -( 2,7 -d ibr omo -9 -p he ny lx anth e n -9 -y l): Mp 189 -1 94. [Z 22] 1 -2. (1,6)Ace (土)-fo rm 3,4 -A c2, 2,5 -B n2: Mp 125 -1 26 (PE). 1H. Anal. [G 8] 3,5 -Ac2, 2,4 -B n2: Mp 117 -1 18. 1H. Anal. [G 8] 3,4 -A c2, 2,5 -P MB2: Mp 121 -1 22. 1H. Anal. [G 8)
2,4 -B ru: Mp 94 -96 (PE , trac e TEA). 1H. Anal. [G 8)2,5 -B ru: Mp 184 -1 86 (MC -EE 1:1). Anal. [G 8] 2,4 -B ru, 3,5 -P MB2: Mp 112 -1 14 (PE , trac e TEA). 1H. Anal. [G 8)3,4 -B ru, 2,5 -P MB2: Mp 119 -1 21 (PE ). 1H. Anal. (Gl]2,4 ,5 -B nJ, 3 -P MB: Mp 119 -1 20 (EA -PE 1:5). 1H. Anal. [G 9) 2,5 -P MB2: Mp 141 -1 43. Anal. [G 8) D-fo n n 2,3,4,5 -B n4: Mp 108 -1 09. (야 25+ I 1.5 (c I, CHCb). 1 H. Anal. [ G 8] L-fo rm 2,4 - B n2: Mp 13I -1 32.5 (PE , trac e TEA). (a)o25 -1 9 (c 1, CHCb). [G 8) 1 -3. (4,S)Ace (土)-fo rm 2 -Ac, 1 -All, 3,6 -B n2: Mp 62 -6 4 (PE). A nal. [G 3)
2 -Ac, 1 ,6 - AIL, 3 -B n: Sy ru p . 1H . [G 6] 1,2 -A c2, 3,6 -B 112: Mp 99 -1 01 (EA -P E). Anal. [G 3] 1,3 -A c2, 2,6 -B 112: Sy ru p . 1 H. [G 8] 1 -All, 3,6 -B 112: Mp 103 -1 05 (EA - P E 1:1 0 ). Anal. [ G 3) 1 -All, 2,3,6 -B nJ: Mp 82 -8 4 (PE ). Anal. (G4) 1,3 -AIL: Mp 57 -5 8. [G 8)3,6 -A IL: Mp 108 -1 10. [G 4) 1,6 -A IL, 3 -B n: Mp 57 -5 9 (EA - P E 1:1 0 ). Anal. [G 6] 1,3 -Alli, 2,6 -B 112: Mp 106 -1 08. 1H. Anal. [G 8] 1,2,6 -A llJ, 3 -Bn: Mp 123 -124 (EA -P E 1:4 ) . 1H. Anal. [ G 6] 3 -B n, 1 -C rot, 6-PM B: Sy rup. 1H. [G 13] 6 -Bn, 1 -Crot, 3 -P MB: Sy ru p . 1 H. [G 13] 2,6 -B 112: Mp 110 -1 12 (PE, trac e TEA). Anal. [G 8) 3,6 -Bn i: Mp 149-151 (EA -PE ). [G 3] 2,3 -B ru, 1 -C rot, 6 -P MB: Mp 111 -1 13 (EA-P E). 1H. Anal. [G 13)2,6 -B ru, 1 -Crot, 3 -P MB: Mp 69 -7 1 (PE ). 1H. Anal. [G l3]2,6 -B nz, 3 -P MB: Sy ru p . 1H. Anal. [G l3] 3,6 -B nz, 1 -P MB: Sy ru p . 'H. [G13] 3,6 一 Bnz, 2 -P MB: Mp 83 -8 5 (PE). 1H. Anal. [G 13] 3,6 -B nz, 1 -P rr: Mp 107 -1 08 (PE). 1H. 13C. MS. Anal. [P 4] 3,6 一 Bnz, 1 -Tr: Mp 154 -1 56. [G 3] 2,3,6 -B ru: Mp 75 -7 7. Anal. [G 2); Mp 76 -7 7. 1H. [G 13] 2,3,6 -B nJ, 1 -Crot: Mp 59 -60 (PE). 'H. Anal. [G 13] 2,3,6 -B nJ, 1 -P ro: Mp 115 -1 16. Anal. [ G 4] 1,2,3 ,6 -B n4: Mp 92 -9 4 (PE). Anal. [G 2] 1,2 ,3 ,6 -B u Mp 246 -248 (MeOH ). Rf 0.7 (EA -he xane 1:3, 3 time s). 1H. IJC . [C H12)
3,6 一 Bzz: X 一 r 작 [C HlO] D-fo rm 1,2,3,6 -B n4: Mp 82 -8 3 (PE ). [a) D25- 3 4.2 (c 1, CHCb). 1H. Anal. (Gll] 3,6 -TBDPS2: (a]D - 24.1 (c 2.77, CHCb). [PE 4) L-fo n n 1,3,6 一 AllJ: Sy ru p . Anal. [G 7] 2,6 -B 112, 3 -P MB, 1 -A ll: Sy rup. 1H. (G13] 2,3 ,6 -B nJ: [a) o25+36.6( c 1.4 , CHCL). Anal. [G 3] 1,2,3,6 -B n4: Mp 83 -8 4. [a )o 2 5+31( c 1, CHCb). Anal. [G 9] 2. Di ac eta l 2 -1 . (1,2;3,4)Aceta l 2 -1 -1 . (1,2;3,4)Acei (士) -form : Mp 150-1 52 (EA -PE 1:10). Anal. [G 4] 5,6 -A ci: Mp 140 -1 42. Anal. [G 4]2 -1 -2 . (1,2;3,4)Hex2 (土)-fo rm: Mp 157 -1 59 (PE). [L I);M p 157-1 58 (aceto n e -PE). 1H. EI. Anal. [B 1 4) ; Mp 158 (benzene -hexane). [A IO] 5,6 -A cz: Sy ru p . Rf 0.7 3 (EE -C HCb 1: 3). 1H. [0 30] 5 -B n: Sy ru p . [L I) 6 -B n: Mp 125 -1 26 (EE -PE). [L I] 5,6 -B zz: Mp 205. anal. [A IO) D -f orm : Mp 155 -1 57 (EE). 〔아 -5 .0 (c 1.17 , MeOH). [0 30) 5 -A c: amorp h ous solid . (a.) 021+ 1.4 (c 1.44 , MeOH). Rf 0.5 5 (EE -CHCb I :3). 1 H. IR. Anal. [0 30) L-fo rm : Mp 155 -1 57 (EE). [a) n27+5.3 ( c 1.17 , MeOH). 1H. IR. [0 30] 2 -2. (1,2;4,S)Aceta l 2 -2 -1 . (1,2;4,5)Ace2 (士)- for m: X-r 작 [C H2);Mp 171 -173. Anal. [G l);M p 166 -168. [P EI); Mp 166 -1 70 (EA ). 1H. 13C. [PS ); Mp 167 -1 68.5 . Rf 0.5 (EA). 1H. 13C. Anal. (CHI, CH7] 3 -A c, 6 -A ll: Mp 125 -1 26 (PE ). [G 2)
6 -A c, 3 -A ll: Mp 154 -1 56 (PE). [G 7); Mp 153 -1 55 (PE). [G 2] 3 -Ac, 6 -B n: Mp 151 -1 52. 1H. Anal. [G 6] 6-Ac, 3 -B n: Mp 18 도 185. 1H. Anal. [G 6,P El) 3 -A c, 6 -P MB: Mp 148 -1 50. 1H. Anal. [G 6] 6 -A c, 3 -P MB: Mp 189 -1 91 . 1H. Anal. [G 6] 3,6 -A c2: Mp 230 -2 32 (EA -PE). 1H. Anal. [G l) ; Mp 223 -224. [P El] 3 -A ll: Mp 129 -1 31 (PE , trac e TEA). [G 7); Mp 127 -1 29 (PE ). Anal. [G 2]6 -A ll: Mp 130 -1 31 (EA -P E). [G 2)
6 -All, 3 -B n: Mp 118 -1 20. Anal. (G6) 3 -All, 6 -M e: Mp 81 -8 3 (PE). Anal. [G 2)6 -All, 3 -P MB: Mp 98 -9 9 (PE). Anal. (G2] 3,6-Alb: Mp 85 -8 7. Anal. [G 2);Mp 81-82 . [PE I );M p 83 -8 5 (hexane). 1H. 13C. [P 6)3 -B n: Mp 167 -1 69 (EA -PE). [G 2); Mp 167 -1 70. [PE I); Mp 162 -1 63. Rf 0.2 (EE -PE 7:3). 1H. 13C. Anal. [C H7] 6 一 Bn: Mp 135 -1 37 (EA -PE). Anal. [ G 2); Rf 0.2 (EE -PE 7:3). [C H7] 6 -Bn, 3 -P MB: Mp 111 -1 13 (PE). Anal. [G 2); Mp 131 -1 33. 1H. Anal. [G l3) 3 -Bn, 6 —P MB: Mp 132 -1 33. Anal. [G 6) 3,6-B n2: Mp 153 -1 55 (PE). Anal. [G 1);Mp 150-153. 1H. Anal. [C H1, CH7] 3,6 -B z2: Mp 328 -330 (DM F). Anal. [G l ); M p 322 -3 23. [P El) ; Mp 328 -330. 1H. [P6 ); Mp 322 -324. 1H. (CH7) 6 -Me, 3 -PMB: Mp 117 -1 19 (PE). Anal. (G2] 3,6 -Octy h : Mp 84 -8 5 (PE). 1 H. Anal. [G 9] 3 -Piv : Rf 0.3 (EE -PE 7:3 ) . 1 H. 13C. [C H7] 6 -Piv : 1H. 13C. [C H7] 3,6 -Piv 2 : 1H. 13C. [C H7] 3 -PMB: Mp 158 -160. Anal. [G 2); 1H. [G 13); Mp 154 -154.5. Rf 0.5 (EA-C HCL 1:1). 1H. [C H7] 6-PM B: Mp 145 -1 47 (EA-PE 1:5 ) . 1H. Anal. [G 6] 3,6 -P MB2: Mp 130 -1 31 (EA -PE). Anal. [G 2); Mp 123 -125. Rf 0.8 (EA -C HCb 1:1) . 1H. Anal. [ CH 7] 3 -TBDMS: Mp 149 -1 51 . Rf 0.4 3 (EE -PE 7:3). 1H. 13C. FAB. Anal. [ C H7] 3,6-TBDMS2: Rf0. 81 (EE-P E 7:3). 1H. 13C. [C H7] 3 -TBDPS: Mp 142 -1 45. [Z 9)3 -Tf: Mp 107 -1 10. Rf 0.35 (EE -PE 7:3). 1H. 13C. EL Anal. [C H7)
3,6 -T f2: Mp 125 -1 27. Rf 0.8 0 (EE -PE 7:3). 1 H. 13C. IR. [C H7] D -f orm : Mp 176 -1 77. 〔야 -2 1 .7 (c 0.4 6 , CHJ C N). [PE 4] L -f orm : Mp 159 -1 61 . [a,)o25 + 2 2( c 1.08 , CHJ C N). [Z 12); Mp 175 -1 77 (CHCb -P E). 〔야 +23 . 3 (c 1, CHJ C N). 1 H. Anal. [G IO] 3 -A c, 6 -Bn: Mp 150 -1 51 (PE). 〔야 +5 . 2 (c 1, CHCb). 1 H. Anal. [G IO] 3,6 -A c2: Mp 206 -207 (EA -PE). [a ] 02 5 -17.2 (c 1, CHCb). 1H. Anal. [G IO] 6 -Bn: Obt. by par tia l hy dr og en olys i s from 3,6 一 Bn2. Mp 132 -1 34 (EA -PE). 〔이 025+66.5 (c 1, CHCb). A nal. [G lO] 3,6-B n2: Mp 159 -1 61 (PE ). 〔야 +85.0 (c 1, CHCb). 1H. Anal. [G IO] 3 -Crot, 6 -Pro: Mp 87 -8 9 (PE , trac e TEA). 〔야 25+3 1. 9 (c 1, CHCb). 1H. Anal. [ G lO] 3 -T BDPS: Mp 127 -128. 〔야 20 -2 .5 (c 2.02, Cl- LC N). 1H. Anal. [ Z 9)2 -2 -2. (1,2;4,S)HeXl (士) _ form : 172-174. [L 1); M p 171-173 (aceto n e -PE). 1 H. EI. Anal. [B 14); M p 174. Anal. [A lO); Mp 179.5 -1 80.5. H. 13C . [V 3] 3,6 -A c2: M p 179 (EtO H). Anal. [A lO] 6 -All, 3 -B n: Mp 89.5 -90.5 . Rf 0.71 (aceto n e -MC 3:97). 1H. 13C. [V 3] 3,6 -Alh: Mp 63 -64.5 . Rf 0.56 (aceto n e -MC 3:9 7 ). 1H. 13C . [V 3)3 -Bn: Glass. 1H. HPLC. HRMS. [B 14) ; Mp 109 -110 (EE -hexane). Rf 0.3 (aceto n e -MC 3:97). 1H. 13C. 〔回 ; Mp 137 -138. 1H. 13C. [V 4] 6 -B n: Mp 135 -136 (PE). Anal. [A 26); Mp 132 -1 33 (EE -hexane). Rf 0.36 (aceto n e -MC 3:97). 1H. 13C. [V 3] 3 -Bn, 6 -PMB: Mp 137 -139. Rf 0.53 (aceto n e -MC 3:97). 1H. 13C. Anal. [V 4)3,6 -B nz: Mp 148 -1 49 (EtO H). Anal. [A 26); Mp 116 -1 17. IR. UV. Anal. [S1 ] 3,6 - B zz: Mp 262 (benzene). A nal. [A lO] 3 -Tf: 1 H . [Z 26) D -f orm : Foam. (cx)o -16.0 (c 3.1 5 , CHCL). 1H. El. (B14) ; Mp 182 -1 83. (cx)o26 -26.4 (c 1.25 , CHCb). 1H. IR. Anal. [0 23] 3 -B n: 〔야라 25.90 (c 1.1, CHCb). [B 3); Foam. 1H. H 露 S. HPLC. [B 14] 3 -Bz: [cx )o26+49.0( c 1.51 , CHCb). R f 0.3 (EA-h exane 1:3). 1 H. IR. Anal. [0 23] 3,6 -B zz: Mp 258 -260. [cx )o26+28.9( c 1.35 , CHCb). 1 H. IR. [0 23) L -f orm : Foam. [a) o1 5.7 (c 3.65, CHCb). 1H. El. [B 14] 3 -斷 : [a ] 02 0- 26.07 (c 1.1, CHCL). [B 3);Foam. 1H. H 血 S. HPLC. [B 14)
2 -3. (1,2;5,6)Aceta l 2 -3 -1. (1,2;5,6)Ace2 ( 土 ) -f orm : X -r 작 [C H2); Mp 172 -1 75 (EA ). Anal. [G 4); Mp 169 一 170. [P El) ; Mp 166 -167. 1H. 13C . Anal. [C H7) 3,4-Ac2: Mp 165 -1 68. Anal. [ G 4);Mp 160-163. [P El] 4 -Ac, 3 -All: Mp 95 -9 7 (PE ). Anal. [G 7] 4-Ac, 3 -B n: 1H. [P El] 3 -A ll: Mp 118 -1 19 (PE , trac e TEA). Anal. [G 7)3 -Bn: Mp 156 -159. 1H. 13C . Anal. [P El) ; Mp 158 -159. Rf 0.27 (EE -PE 7:3). 1H. 13C. El. Anal. [C H7)4 -Bn: Rf 0.52 (EE -PE 7:3). 1 H. uc. El. [C H7] 3,4 -B ru: Rf 0.6 7 (EE -P E 7:3). 1 H. 13C . El. Anal. [C H7] 3,4-Bz2: Mp 197 -200 (Me OH). Anal. [G 4); M p 187 -1 89. Rf 0.3 (EA -hexane 1:3 ) . 1H. 13C. [C H7] 3 -Piv : Mp 100 —1 02. Rf 0.4 (EE -PE 7:3). 1H. 13C . IR. FAB. [C H7)
4 -Piv : Mp 127 -1 29. Rf 0 .5 (EE -PE 7:3). 1 H. 13C. IR. FAB. [C H7)3 -TBDMS: Rf 0.56 (EE -PE 7:3). 1 H. 13C . EL [C H7)4 -TBDMS: Rf 0.7 1 (EE -PE 7:3). 1H. 13C. EL [C H7)3,4 -T BDMS2: Rf 0.82 (EE -PE 7:3). 1H. EL [C H7] 3 -TMS: Mp 160 -1 61 . 1H. 13C. EL [C H7] 4 -TMS: 1H. 13C. [C H7)3,4 -T MS2: 1H. 13C. FAB. [C H7] L-fo rm 4 -Bn: Mp 89 -91 . 〔야 -1 6 (c 0.9, CHCb). [PE 3] 2 -3 -2 . (1,2;5,6)HeX2 (士)-fo rm: Mp 130-131 (PE ). [L l);M p 134-135 (aceto ne-PE). 1 H. EL Anal. [B l4); M p 133 (be nzene -PE). Anal. [A lO] 3,4 -A c2: Mp 120. Anal. [A lO)3 -Bn: Sy rup. [L l) ; 1H. [B l 4] 4 -Bn: Sy ru p . [L l) ; Mp 87 -89. 1H. FAB. Anal. [B l 4] 3,4-B ru: Sy ru p . 1H. [B l4] 4 -Bt: Sy ru p. 1H. [C 4] 3 -Bz: Mp 173 (EtO H ). Anal. [A lO] 3 -Bz, 4 -Ts: Mp 146 -147 (EtO H ). Anal. [A lO)4 -Bz: Mp 185 (EtO H). Anal. [A lO] 4 -Bz, 3 -Ts: Mp 207 (EtO H). Anal. [A lO)3,4 -B z2: Mp 158. Anal. [A lO] D -f orm : Mp 144 -1 45 (EE ). 〔야 -2 2.3 (c 0.74, CHCh). [03 0); 따 -15.3 (c 1.5, CHCh). [C 2,C4) 3 -A c: Mp 139 -1 11 (EE). (a 問+ 16.6 (c 1.0 5, CHCh). Rf 0.31 (EE -CHCh 1: 3). 1H. IR. Anal. [0 30) 4 -A c: Mp 114 -1 16 (EE). (야 21 -14.0 (c 5.4 , MeOH). R f 0.50 (EE -C HCL 1: 3). 1H. IR. Anal. [0 30] 3,4 -A IL: Sy ru p . 〔이타 -6.5 (c 0.4 , CHCh). 1H. [C 4)
3 -B z: 〔야+ 1.8 (c 2.4 4 , CHCh). Rf 0.35 (EA -hexane 1:3). 1H. IR. Anal. [0 23] 3 -Bz, 4 -M e: Mp 118 -1 19 (EA -hexane). Rf 0.4 (EA -hexane 1:4). 〔 a 〕 D 끄 -7 .21 (c 2.22, CHCh). 1H. IR. Anal. [02 3) 4 -M e: Sy ru p . [a) o29- 1 .99 (c 10.7, CHCh). 1H. IR. Anal. [ 0 23] L -f or m: Mp 144 -1 46 (EE). 〔 a 詞•+ 19.3 (c 0.75, CHCb). Rf 0.11 (EE- CHCh 1:3). 1H. IR. [0 30); (cx)o20+ 18.4 (c 1.0, CHCb). [C 2)4 -A c: (cx)o 20 -8.4 (c 1.2, CHCh). [C 2] 3 -A c, 4 -B n: [a ] 02 0 -1 4 (c 1, CHCb). 1H. [C 2,C4) 4 -斷 : [a ] 02 0- 4.2 (c 1.0, CHCb). 1H. [C 2,C4) 4 -Bt: [cx )o- 1 4 (c 0.4 5 , CHCL). [C 4)2 -4 . (1,6;3,4)Ace2 Mp 212-2 14. Rf0. 2 (EA-h exane 1:1) . 1H. 13C. [C H12] 2,5 -B ru: Mp 173 -1 74. 1H. Anal. [G 8] 2-Bz: Mp 181-183 (EE-hexane). Rf 0 .4 5 (EA-hexane 1:1). 1H. 13C. [C H12] 2,5 -PMB: Mp 143 -1 44. 1H. Anal. [G 8)2 -5. (1,6;4,5)Ace1 2 -Ac, 3 -Bo: Mp 138 -142 (hexane). 1H. Anal. [P El]2 -B z: Mp 188 -1 90. Rf0. 50 (EA -hexane I:1). 1H. '3C . [C H12)
3 -B o: Mp 142 -1 45. 'H. 13C. Anal. [P El] 3. Triac eta l Mp 220 -2 21 (he xane). 1 H. 13C. Anal. [P El] 4. Or tho fo r mate Mp 300 -302. 1H. IR. FAB. Anal. [22 0); Mp 282 -285. Rf 0.23 (aceto n e -hexane 1:1 ) . 1H. Anal. [0 37); 13C . [Z l);R f 0 .3 (MeOH -M C 1:10). 1H. [C H3] ( 土 ) or meso -f orm : 2 -A c, 4,6 -B n2: Mp 116 -1 18 (EA -h exane). 1H. Anal. [Z 20)4,6 -A c2, 2 -TBDMS: Mp 64 -6 5. 1H. Anal. [Z 20] 2,4 ,6 -A cJ: Mp 173 -174. 1H. Anal. [Z 20] 4-All: Sy rup. 1H. HRMS. [B 13] 4 -All, 6 -Bn: Mp 119 -120 (EE -h exane). 1H. 13C. CI. Anal. [Z 19] 4-All, 6-Bn, 2 -TBDMS: Sy ru p . 1 H. 13C . CI. Anal. [ Z 19) 4-All, 2,6-Bru: Sy ru p . 1H. HRMS. [B 13)4 -All, 2 -TBDMS: Sy ru p . 1H. 13C . CI. Anal. [Z 19)4 -Bn: 1H. 13C. IR. Anal. [Z l) 4- B n, 2-TBDMS: Mp 51 -5 3 (hexane). 1 H. 13C. IR. Anal. [ Z l] 4 -Bn, 6 -ClLOBn, 2 -( pN 02)Bz: Rf 0.6 (EA -h exane 1:2 ) . 1H. Anal. [03 7) 4,6 -B ru: Mp 125 (EA -hexane) 1H. FAB. Anal. [B 13) ; Mp 124 -125. 1H. 13C. IR. FAB. Anal. [Z 20] 4,6 -B ru, 2 -TBDMS: Mp 124 -1 25. 1H. IR. FAB. [Z 20]2,4,6 -B n3: Mp 102 -1 04 (PE). ' H. FAB. Anal. [B 13] 4,6 -Bt i: M p 59 -6 0. Rf 0.53 (EA -hexane 1: 1) . 1H. 13C. IR. Anal. [Z l) 4,6 -Bti , 2 -TBDMS: Oil . Rf 0.7 3 (EA -hexane 1:3). 1H. 13C. IR. Anal. [ Z l ) 2 -Bz: Mp 202 -2 04. Rf0. 13 (EA-h exane 1:2). 1H. Anal. [03 7) 2,4,6 -BZ J: Mp 224-2 25. Rf0 .74 (MeOH-M C 1:1 0 ). 1H. 13C. FAB. [C H3) 2-(p N 02)Bz: Mp 236-2 38. Rf0 .3 6 (EA-hexane 1:1). 1H. Anal. [03 7] 4-Cl - LO Bn: Mp 96-97 . Rf0. 4 1 (EA-h exane 10:1). 1 H. IR. Anal. [0 37) 4- C l- LO Bn, 2-(p N 02)Bz: Rf0 .4 5 (EA-hexane 1:1 ) .1H . IR. Anal. (037) 2 -TBDMS: Mp 179 -1 81 . 1H. IR. FAB. Anal. (Z20) ; 13C. (Zl) D-fo rm 6 -Bn: Oi l. Rf 0.24 (EA -hexane 1:1). [a.)02 5- 1 6_-6 (c 1.0, EtO H). Anal. [Z l] 6 -Bn, 2,4 -T HP2: Oi l. Rf 0.36 (EA -hexane 1:3 ) . [a.)02 5- 14.5 (c 1.5, CHCh). 1 H. 13C. IR. Anal. (Zl ) 2,6 -B ru: Oil . Rf 0.54 (EA-h exane 1:1). (a.)02 5 -8.4 (c 1.0, EtO H ). 1H. 13C . IR. Anal. [Z l] 2,4 -B n2, 6 -Bt: Oil . (a.)02 5 -2 2.1 (c 1.1, CHCh). 1H. 13C. IR. Anal. [ Z l) 6 -Bt: Mp 69 -70. (a.)02 5 -5.7 (c 1.5, CHCL). 1H. 13C. IR. Anal. [ Z l] 6 -Bt , 2,4 -T HP2: Oi l. Rf 0.65 (EA -hexane 1:1). [a ]0 2 5 -20.0 (c 1.1, CHCh). 1H. 13C. IR. Anal. [Z l] 2,4 - THP2: Oil . Rf0 .4 3 (EA-h exane 1:1). (a.)02 5 -8.9 (c 1.4, CHCL). 1H. 13C. IR. Anal. [ Z l] V. Alky l a nd/or Acy l Deriv e ti ve s meso or (土) -form 4- A c, 1,3,4 ,5 -All4: Mp 70 -72. 1H. Anal. [G 7] 5 -Ac, 1,3,4 ,6 -All ◄: Mp 103 -1 05 (PE ). 1 H. Anal. [G 7]
4 -A c, 2,3,5,6 -B n4, I -P MB: Mp 122 -1 24 (PE). 1H. Anal. [G 9)
4 -A c, 1,3,4 ,5 -C roti : Mp 91 -9 3. 1H. Anal. [G 7] 1 -A c, 2,3,4 ,5 ,6 -B ns: Mp 85 -8 9 (PE ). Anal. [G 3)1,4 -A c2, 5 -A ll, 2,3,6 -B nJ: Mp 106 -1 07 (EA -PE 1:10). 1H. Anal. [G l4] 1,5 -Ac2, 4 -All, 2,3,6 -B nJ: Mp 92 -9 4 (EA -P E). 1 H. Anal. [G l4] 4,5 -Ac2, 1 -All, 2,3,6 -B nJ: Mp 134 -1 36 (EA-P E 1:10). Anal. [ G 3)1,2-Ac2, 3,4 - Alh, 5,6 - B n2: Sy ru p . 1 H. (G6] 4,5 -A c2, 1,3 -A ll2, 2,6 -B lll: Mp 128 -1 29 (PE ). 1 H. Anal. (G8] 4,5 -A c2, 1,3,6 - Alb, 2 -B n: Mp 122 -1 23 (PE ). 1H. Anal. [G 9] 4,5 - Ac2, 2,3,6 -Alb, 1 -C rot: Mp 117 -1 19. 1H. Anal. [G 13] 2,4 - Ac2, 1,3,5,6-A lk Mp 88 -8 9. 1H. Anal. (G7] 2,5 -A c2, 1 ,3,4,6 -A lk Mp 73 -7 4. 1H. Anal. [G 7] 4,5 -Ac2, 1,2,3,6 -A ll4: Mp 100 -1 01 (PE ). 1 H. Anal. [G 7] 4,5 -Ac2, 2,6 -B n2, 1,3 -P ro: Mp 136-1 38. 1H. Anal. [G 8] l,6-Ac2, 2,4 ,5 -B ru, 3 -PMB: Mp 95 -9 6 (EE -PE ). 1H. Anal. [G 9) 1,4 -A c2, 2,3 ,6 -B ru, 5 -Pro: Mp 110 -1 12 (PE, trac e pyridin e ). 1H. Anal. [G 14] 1,5 -A c2, 2,3,6 -BnJ, 4 -Pro: Mp 108 -110 (PE, tra ce TEA). 1H. Anal. [G 14] 1,3 -Ac2, 2,4,5,6 一 Bn4: S y rup. 1H. [G 9] 1,4-Ac2, 2,3,5,6 -B n4: Mp 128 -1 29 (EA -P E 1:25). 1 H. Anal. [G 9] 1,6 -A c2, 2,3,4 ,5 -B n4: the nnosal ian t. jum p at 70 when heati ng , at 40 when coolin g. [G 6); Mp 106 -1 08 (PE ). [G 4) 2,4 -A c2, 1,3 ,5 ,6 一 Bn,: Mp 105 -1 07 (EA -PE). [G 6) 4,5 -Ac2, 1,2,3,6-B n4: Mp 132-1 34 (EA-P E). [G 4,G 2] 2,4 -A c2, 1,3,5,6 -Croti : Mp 76 -78. 1H. Anal. [G 7] 2,5 -Ac2, 1,3,4 , 6-C roti : Syr up. 1H. [G 7] 2,4,5 -AcJ, 1,6 -Alh, 3 -B n: Mp 113 -1 14. 1H. Anal. [G 6] 2,4,5 -AcJ, 3,6 -Alh, 1 -Crot: Mp 128 -1 29 (PE or EtO H -H20 1:1). 1H.Anal. [G 13] 1,2,4 -A cJ, 3,5,6 -A lb: Mp 90 -9 2 (PE). 1H. Anal. (G7) 2,4,5 一 AcJ, 1,3,6 -A lb: Mp 135 -1 37 (PE). 1H. Anal. [G 7] 2,4 ,6 -AcJ, 1,3,5 -A lb: Mp 124 -1 25 (EA-P E 1:5). 1H . Anal. (G7) 2,4 ,5 -A cJ, 3 -B n, 1 -C rot, 6 -P MB: Mp 125 -1 27 (PE). 1H. Anal. [G 13] 1,4 ,5 -A cJ, 2,6 -B nz, 3 -P MB: Mp 127 -1 28. [G 12] 2,4 ,5 -A cJ, 3,6 -Bil l, 1 -C rot: Mp 103 -1 05 (EA-P E 1:8). 1H. Anal. [G 13] 1,2,4 -A cJ, 3,5,6 -B ru: Mp 112 -1 13. (G12) 1,2,5 -A cJ, 3,4 ,6 -B nJ: Mp 85 -8 6. (G12] 1,2,6 - A cJ, 3,4 ,5 -B nJ: Mp 117 -1 19 (EA 一 PE 1: 5). 1H. Anal. [G 6) 1,4,5 -A cJ, 2,3 ,6 -B nJ: Mp 123 -1 25. Anal. [G 2); Mp 116.5 -1 17 (EtO H ). Rf 0.7 (EA -hexane 1 :3). 1 H. IR. Anal. ( 026) 2,4,5 -A cJ, 1,3 ,6 -B nJ: Mp 148 -1 50 1H . 13C . [PE 2] 2,4 ,6 -A cJ, 1,3,5 -B nJ: Mp 157 -1 60. 1H. IJC, Anal. [ PE 2] 4,5,6 -AcJ, 1,2,3 -B nJ: Mp 155 (EtO H). 1H. Anal. [A 20)
2,4 ,6 -A CJ , 1,3 ,5 -Crou: Mp 72 -7 5. 1H. Anal. [ G 7] 1,2 ,4 -AcJ, 3,5,6 -M eJ: Mp 101 -1 03 (EA -P E 1:9). 1 H. Anal. (G13] 1,4 ,5 -A cJ, 2,3,6 -M eJ: Mp 157 -1 59. [G l2)1,4 ,6 -A cJ, 2,3,5 -M eJ: Mp 161 -1 63. [G 12] 1,4,5 - A cJ, 2,3 ,6 -P roJ: Mp 105 -1 06. 1H. Anal. [G 13)2,4,5 -A cJ, 1,3,6 -P roJ: Mp 113 -1 15 (PE , trac e pyridine) . Anal. [G 7); 1H. [G 13)1,4 ,5 ,6 -Ac4: Mp 142 -1 43. Anal.A 1 3 Mp 138 -1 40. Anal. [A lO] 1,2 ,3 ,5 -Ac4, 4 -All, 6 -B n: Mp 134 -1 36. 1H. CI. [ Z 19) 1,2,4 ,5 -A C -4, 3,6 -Alh: Mp 118.5 -1 19.5 (EA -he xane). 1H. Ile. FAB. Anal. [P6 ] 1,2,4,6 -AC -4, 3,5 -Alh: Mp 142 -1 44. 1H. Anal. [ G 7] 1,2,5,6 -A c4, 3,4 -A lh: Mp 144 -1 46 (EA -PE). 1H. Anal. [G 6] 2,4,5,6 -A C -4, 1,3 -A llz: Mp 141 -1 43. 1H. Anal. [G 7]2,4 ,5 ,6 -A c4, I -Bn, 3 -M e: Mp 197 -1 99 (MeOH). UV. Anal. [A 20] 1,2,3,5 -A c 』, 4,6 - B n2: Mp 189 -1 90. [G 12] 1,2,4 ,5 -Ae i, 3 ,6 -B n2: Mp 131 -1 33 (EtO H). Anal. [G 2); Mp 128 -1 29. IR. UV. Anal. [S l] 1,3,4 ,5 -Ac4, 2,6 -B n2: Mp 163 -1 65 (EA -PE 3:5). 1H. Anal. [G 8] 1,3,4 ,6 -Ae i, 2,5 -B n2: Mp 177 -1 79 (EA -PE 1:2 ) . 1H. Anal. [G 8] 2,4 ,5 ,6 -Ae i, 1,3 - Bil 2: Mp 184 (EtO H). 1 H. Anal. [A 20] 1,3,4,5 - A C4, 2,6 -M e2: Mp 176 -1 78 (EA-P E 1:2 ) . [G 13); Anal. [G 7] 1,3,4,6-Ac4, 2,5 -Me2: Mp 148 -1 50 (MeOH-H 20 1:1). 1H. Anal. [G 7); Mp 151 -1 52. [G 13] 2,4,5,6 -A C4, 1,3 -M e2: Mp 202. Anal. [A l3) 1,3,4 ,6 -A C4, 2,5 -P MB2: Mp 138 -1 40. 1H. Anal. (G8] 1,2,4 ,5 -A c4, 3,6 -T s2: 195 -1 97. [Z8 ] 1,2 ,3 ,4 ,6 -A cs: Mp 178. [A lO)
1,2,4,5,6 -A cs: Mp 161 -1 64 (H20). Anal. [A 20); Mp 163 -1 64. IR. Anal. [S l] 1,3,4 ,5 ,6 -A cs: Mp 177 -1 79. [Z 14,A 2) 1,2,4 ,5 ,6 -A cs, 3 -A ll: Mp 133 -1 35 (EtO H). 1H. Anal. [G 7); Mp 130 -1 31 (EE -hexane). 1H. 13C. Anal. [PE 2) 1,2,3,4 ,5 -Acs, 6 -B n: Mp 162 -164. 1 H. [G lO); Anal. [ G 2] 1,2,4 ,5 ,6 -Acs, 3 -B n: Mp 166 -1 67. Anal. [ G 6); Mp 167 -1 68 (EtO H). 1 H. UV. Anal. [A 20); Mp 166 -1 67. IR. UV. Anal. [S l ] 1,3,4 ,5 ,6 -Acs, 2-Bn : Mp 222. 1H. Anal. 〔 A2 이 1,3,4,5,6 -A cs, 2 -( pN IL)Bz: Mp 201 -2 03. Anal. [Z 14] 1,3,4 ,5 ,6-Acs, 2 -( pN 02)Bz: Mp 233 -2 35. Anal. [Z 14] 1,2,3,4 ,5 -A cs, 6 -M e: Mp 130 -1 32 (EtO H -H zO). [G 2] 1,2,3,4 ,5 -Acs, 4 -M e: M p 131 -1 32. [Z 8)1,2,3,4 , 6 -A cs, 5 -Me: Mp 200 -201 (EtO H). [G 2); Mp 201 -203. 1H. 〔 Gl 선 ; Mp 200 -202.A n al. [A 8)1,2,4 ,5 ,6 -A cs, 3 -M e: Mp 154 -156. [G 2);154 -154.5 (Et O H). Anal. [A 2);Mp 152 -1 53. [A 13);M p 14- 1 54.5 . [Z 8) 1,3,4,5,6 -A cs, 2 -M e: Mp 235 -2 36 (EtO H). (G2, Al3) 1,2,4 ,5 ,6 -A cs, 3 -Ts: Mp 151 -1 52.A20 Mp 149 -1 50. [A lO] Ac6: Mp 213 -2 15. (Zl4) ; 213 -2 14. [Z 16); 210 -212. Anal. [A 8] 1 -All: Mp 122-1 24 (EtO H). Rf0 .1 5 (MeOH-C HCb 1:3): 1 H. [P E2)
5 -A ll: Mp 180 -1 85 (EtO H). 1H. [PE 2] 1 -A ll, 3,6 -B ll2: Mp 108 -1 10. (G3) ; Mp 107 -1 08. [G 4) 2 -A ll, 1,4 -B ll2: Mp 93 -9 4. [G 3] 5 -All, 1,4 -B ll2, 6 -Crot: Mp 88 -: 91 (EE -P E). 1H. Anal. [G ll] 6 -All, 1,4 -B n2, 5 -Crot: Mp 98 -1 00 (EE -P E). 1 H. Anal. [G ll] 4 -A ll, 3,6 -B ll2, 5 -P MB: Mp 110 -1 17 (EA -P E). Anal. [G i l ) 4 -A ll, 1,5,6 -B n: Mp 98 -9 9 (EE-h exane). Rf 0.1 6 (aceto n e -M C 3:97). 1H. 13C. [V 3) 5 -A ll, 1,2,4 -B nJ: Mp 56-58 (EA -P E). Anal. [G 14)4 -A ll, 1,5,6 -Bn, 3 -TBDMS: Mp 62.5 -63.5 (pe nta n e). Rf 0.44 (EE -hexane 1:1). 1H. 13C. [V 3] 1 -A ll, 3,4 , 5,6-B n4: Sy ru p . 1H. 13C. FAB. IR. [B 15] 4 -All, 1,2,3,6 -B n4: Mp 123 -1 25. Anal. [G 2)5 -A ll, 1,2,3,4 -B n4: Mp 78 -8 0 (PE ). Anal. [G 2)4 -A ll, 1 ,2,3,6 -B n4, 5 -M e: Mp 87 -8 9. Anal. [G 2) 4 -A ll, 1,2,3,6 -B n4, 5 -C rot: Sy ru p . R f0. 7 (EE -PE 1:1). 1H. [G ll) 5 -A ll, 1,2,3,4 -B n4, 6 -C rot: Sy ru p. Rf0. 8 (EE -PE 1:1). 1H. [G ll) 1 -A ll, 3,4 ,5 ,6 -B n4, 2 -h exy l: S y rup. 1H. [B 16] 4 -A ll, 1,2,5,6 -B n4, 3 -T BDMS: Oil . Rf 0.5 5 (EE -h exane 1:1). 1H. 13C. [V 3] 4 -All, 1,3,5,6 -B n4, 2 -TBDMS: Oil . Rf 0.50 (EE -hexane 1:1). 1H. 13C. (V3)' 1 -All, 2,3,4 ,5 ,6 -B ns: Mp 60 -6 2 (EtO H ). 1H. 13C. FAB. IR. Anal. [B l5)1 -All, 4 -M e: Mp 170 -1 72 (EtO H). Anal. (G2) 1,3 -Alh: Mp 119 -1 20 (EA). Rf 0.6 (MeOH -CHCb 1:3). 1H. 13C. Anal. [PE 2); Mp 119 -1 21 . Anal. [G 7] 1,6 -A lh: Mp 142 -1 44 (EtO H). Anal. [G 4)
4,5 -Alh: Mp 137 -1 38. Anal. (G4) ; Mp 137 -1 39. [P El] 1,4 - All2: Mp 137 -1 39 (EtO H). Anal. [G 4);Mp 133 -1 36 (EtO H). [P6 )1,4 -A lh, 3 -P MB: Mp 94 -9 6 (EA -hexane). 1 H. 13C. FAB. anal. [P6 ] l,4 -A ll2, 5 -B n: Mp 162 -1 64. Anal. [G 2)1,4 -A lh, 6 -B n: Mp 107 一 109. Anal. (G2] 1,6 -Alh, 3 -B n: Mp 94 -9 6. [G 6)1,4 -Alh, 5,6 -Bil l: Mp 78 -8 0. Anal. (G2) ; Mp 76.5 -7 8 (MC -hexane). Rf0 .4 8 (Me OH-MC 1:19). 1H. 13C. [V 3) 1,6-Alh, 4,5 -Bil l: Mp 68 -6 9 (PE). Anal. [G 6)4,5 -Alh, 1,6-B lll: Mp 88 -9 0 (hexane). 1H. FAB. Anal. [ B 14] 4,5 -A ll2, 3,6 -B ru: Mp 107 -1 08 (EA -PE). Anal. [G 2); Mp 106 -108. @]; M p 104.5 -1 06 (be nzene -hexane). 1H. IR. Anal. [ 02 6) 1,4 -A ll, 5,6 -Bn, 3 -TBDMS: Mp 59 -60.5 (pe nta ne ). Rf 0.4 8 (EE -h exane 1:1). 1H. 13C. [V 3] 4,5 -Alh, 1,3,6 -BI1 J: Sy ru p. 1H. FAB. [B 14] 1,4 -Alh, 2,5,6 -BnJ, 3 -PMB: Mp 72 -74 (hexane). 1H. 13C. FAB. Anal. [P6 ] 1,4 -A lh, 2,5,6 -B nJ, 3 -TBDMS: Oil . Rf 0.67 (EE -hexane 1:1). 1H. 13C. (V3] 1,4 -Alh, 3,5,6 -BI1 J, 2 -TBDMS: Oil . Rf 0.61 (EE -hexane 1:1). 1H. 13C. (V3] 4,5 -Alh, 1,2,3,6-Bn.: Mp 52 -54 (PE ). Anal. [G 2] 1,4 -Alh, 3 -Crot: Mp 91 -9 3 (PE). Anal. [G 13] 5,6 -Alh, 1,4 -P MB2: Mp 109 -1 10. Anal. [G 2] 1,3,4 -A IL: Syr up. [G 7]1,3,5 -Alb: Mp 68 -6 9.5 ( EA -P E 2:5). Anal. (07) 1,4 ,5 -A lb: Mp 131 -1 32 (EA -P E). A nal. [G 7] 1,4 ,6 -A lb: Mp 120 -1 22. [G l2] 1,3 ,4 -A lb, 2 -B n: Mp 53 -5 5 (PE). Anal. (09) 1,3 ,4 -A lb, 5 ,6 -B n2: Mp 60 -6 2. Anal. (02) ; 1H. FAB. Anal. (B 14) 1,3 ,4 -A lL, 2,5 ,6 -BI1 J: Sy ru p . 1H. FAB. Anal. (Bl4) 1,2 ,6 -Alb, 3,4 ,5 - B nJ: Mp 36. Anal. [G 6] 1,4 ,5 -Alb, 2,3 ,6 -BI1 J: Mp 53 -5 5. Anal. [G 2] 1,4,5 - A llJ, 2 -M e, 3 ,6 - P MB2 : M p 78 -7 9. Anal. [G 2) 1,4,5 -A llJ, 3 -P MB: Mp 53 -5 5. (012) 1,4 ,5 -A llJ, 3,6 -P MB2: Mp 76 -7 7 (EA-P E). Anal. [G 2] 1,4 ,5 - Alb, 2 ,3,6 - P MBJ : Mp 73 -7 4 (PE ). Anal. [G 2) 1,2,3 ,4 -A lk Mp 115 -1 17 (PE). A nal. [G 7] 1,3,4 ,6 - A ll4, 2 ,5 -B n2: Sy ru p . 1H. [G 8)
1,3,4,6 - A ll4, 2,5 -P MB2: Sy ru p . 1H. [G 8) 1,3,4 ,5 ,6 -A lls: 1H . 13C . [Z 21] 1 -B n: Mp 207 -2 09 (EtO H). [0 2); Mp 203 -2 05 (EtO H ). [L l,A 26) ; Mp 206 -2 08 (Me OH). A nal. [ A 20); Mp 195 -1 97 (EtO H). 1H. 13C. [PE 2] 4 -B n: Mp 165 -1 68 (EtO H). [0 2); Mp 165 -1 67 (EtO H ). [L l) ; Mp 169 - 170 (EtO H). Anal. [A 26] 5 -B n: Mp 280 -2 83 (EtO H -ILO). [0 2); 281 -2 83 (EtO H -ILO). [L l) ; Mp 279 -282 (EtO H -甲 0). 1H. [PE 2] 6 -Bn, 2 -( pN 02) B z: Rf 0.1 8 (Me OH -M C 1:10). 1H. IR. Anal. [0 37) 1 -B n, 3,4 ,5 ,6 - B u Mp 212 -2 15. Rf0. 55 (EA -to l uene 1:6). A nal. [L 3] 2 -Bn, 3,4,5,6 -B u Mp 205 -2 07. Rf 0.69 (EA -to l uene 1:6). Anal. [L 3] 4 -B n, 1,2,3,5,6 - B z: Mp 182 -1 83. Anal. [L 2] 1 -B n, 3 -Crot, 4 -P MB: Mp 124 -1 25 (EA -P E). 1 H. Anal. [G 13)4 -Bn, 3 -Crot, 1 -P MB: Mp 130 -1 32 (EA -PE 8:5). 1H. Anal. [ G 13] 1 -B n, 2 ,3 ,4 ,5 ,6 -M es: Syr up. [L1 ]4 -Bn, 1,2,3 , 5,6 -M es: Mp 81 -8 2 (PE). Anal. [L1 ] 5 -B n, 1,2,3,4 ,6 -M es: Mp 77 -7 9 (PE). [L l) 1 -Bn, 4 -PMB: Mp 182 -184 (EtO H). Anal. (G13] 4 -Bn, 1 -PMB: Mp 186 -1 88 (EtO H). Anal. [G 13] 1 -Bn, 3,4,5,6 -P MB: Mp 138 -140 (EE -PE). 1H. 13C . Anal. [L3 ] 1,3 -B nz: Mp 150 -1 52. Anal. [A 20);Mp 180 -1 83 (EtO H). 1H. 13C. [P E2)
1,4 -B nz: Mp 205 -207. Anal. [G 1 ); Mp 203 -204. IR. UV. Anal. [S1 ] 1,5 -B nz: Mp 137 -1 40 (MeOH -hexane). 1H. 13C . [P E2] 2,4 -B nz: Mp 125 -126 (EA -PE). Anal. [G 8); Mp 119 -120.5 (CHCb -PE). 1H. FAB. Anal. (B13) 2,5 -Bnz: Mp 270-2 72 (DMF-E tO H). Anal. [ G 8] 4,5 -B 112: 1H. HRMS. [L E3)4,6 -B 112: Mp 138 -140. [G 12)1,4 -B nz, 5,6 -Btz : Mp 78 -79. Rf 0.4 8 (EA-C HCb 1:1). 1H. HRMS. Anal. [P5 ] 1,4 -B nz, 5,6 -Btz , 3 -P MB: Mp 104 -106. 1H. Anal. [P5 ] 1,4 -B 112, 3 -Crot: Mp 109 -1 11. 1H. Anal. [ G 13] 1,4-B1 12, 3,6 -Crotz : Mp 82 -84 (EA-P E 1:10). Anal. [G 13] 1,4 -B1 12, 5,6 -Crotz : Mp 88.7. 1H. Anal. [Z 25] 1,4 -B 112, 3,5,6 -CrotJ , 2 -PMB: 1H. Anal. [ Z 25)4,5 -B 112, 2 -Me: Mp 217 -219 (EtO H). Anal. [G 2] 4,5 -B112, 6-M e: Mp 165. 1H. IR. HRMS. [LE 3] 1,4 -B1 12, 2,5 -M ez: Mp 131 -134 (EA -PE 1:3). Anal. [G 13] 1,4 -B1 12, 2,6-M ez: Mp 153 -1 55 (EA -P E 2:5). Anal. [G 13] 1,4 -B 112, 2 -PMB: Mp 139 -140. 1H. Anal. [G 13); Mp 117.8 (EE -hexane). 1H. Anal. [Z2 5) 2,4 -B 112, 1 -PMB: Mp 124 -125. [G 12)2,4 -B1 12, 1,5 -P MBz: Mp 175 -176. 1H. Anal. [G 8) 1,6-B1 12, 2,5 -P MB2: Mp 155 -1 57 (EtO H). 1H. Anal. [G ll]1,4 -B nz, (2,3 ;5 ,6)sulfit e: Mp 162-1 64. IR. UV. Anal. [S1 ] 1,2,4 -B nJ: Mp 116 -1 18 (EA -P E). Anal. [G 2); Mp 117 -1 19. [G 3] 1,3,4 -B nJ: Mp 102 -1 04 (EE -h exane). 1H. FAB. Anal. [B 1 4) ; Mp 100 - 103. 1H. [P E2] 1,3,5 -B nJ: Mp 163 -1 64. 1H. [PE 2] 1,4,5 -B ib : Obt. by Benzyl a ti on via tin oxid e . Mp 119 -1 20. [G 12)
1,4,6 -B nJ: Obt. by Benzyl a ti on via tin ox ide . Mp 83 -8 4. [G 12)1,5,6 -B nJ: Mp 154 -1 56 (EA -P E). A nal. [ G 6)2,4 ,5 -B nJ: Mp 135 -1 37 (EA -P E). Anal. [G2) ; Mp 126 -1 28. H Anal. [B 14) ; Mp 135 —1 36.5 9EA -h exane). 1H. 13C. FAB. [P6 ] 2,4,6 -B ib : Mp 83 -8 4.5 (EE -PE). FAB. Anal. [B 13] 1,2,4 -B nJ, 5,6 -Btz , 3 -P MB: Mp 88 -90 (PE). 1H. HRMS. Anal. [P5 ] 1,4 ,5 -Bib , 2,3,6 -B z3: Mp 146 -1 47. [G 12] 1,4,6 -B ib , 2,3,5 -BZ J: Mp 129 -1 30. [G 12] 3,4,5 -B nJ, 6 -C H2CH2NJ : Mp 76 -7 7 (EE -h exane). 1H. 13C. CL Anal. [Z 19] 1,2,4 -B il l, 3,5,6 -M e: Mp 115 -1 16 (PE ). 1H. Anal. [G 13] 2,4 ,5 -B nJ, 1 -P MB: Mp 100 -1 02 (EA -h exane). 1H. 13C. FAB. Anal. [P6 )2,4 ,5 -B nJ, 6 -P MB: Mp 172 -1 74 (EtO H ). 1H. Anal. [G 9] 1,2,4 -B ib , 3 -P MB: Mp 93 -94. 1H. HRMS. Anal. [P5 ] 1,2,4 -B ib , 5 -P MB: Mp 103 -1 04. Anal. [G ll] 1,2,4 -B il l, 5 -PMB, 3,6 -Pro: Mp 78 -7 9 (PE ). Anal. [G ll] 2,4 ,5 -BnJ, 1 -PMB, 3,6 -P ro: Mp 110 -112 (EtO H). 1H. 13C. FAB. Anal. [P6 )1,2,4 -B ib , 3 -P ro: Mp 101 -1 03 (EtO H -! LO ). 1H. 13C. FAB. Anal. [P5 ] 1,2,4 -B ib , 5 -Pro: Mp 85 -8 6 (EE -P E 1:3, trac e TEA). Anal. [G 14)1,5,6 -B il l, 4 -Pro: Mp 98 -1 00. Anal. [G 6] 1,2,4 -B ru, 3,5 -P roz: Mp 104 -1 06 (PE , trac e TEA). 1H. Anal. [G 14] 1,2,4 -B ru, 3,6 -P roz: Mp 126 -1 28 (PE , trac e TEA). 1H. Anal. [G 14]2,5,6 -B nJ, 1,4 -P ro2: Mp 62 -6 3 (pe nta n e). Rf 0.61 (EA -hexane 1:1). 1H. 13C. Anal. [V 3] 1,2,3,4 -B n ◄: Mp 87 -8 9. [G 4) 1,2,4 ,5 -B n4: Sy ru p . 1H. [G 9)
1,2,5,6 -B n4: Mp 169 -1 70 (EtO H). Anal. [ G 4] 1,2,5,6 -B n4, 4 -Pro: Mp 84.5 -8 5.5 (pe nta n e). Rf 0.5 7 (EA -hexane 1:1). 1H. 13C. Anal. [V 3)1,3,4,5 -B n4: Mp 116-1 18 (EA-P E 1:10). Anal. [ G 6] 1,4,5,6-Bn4: Mp 114-115 (MeOH). 1H. 13C. FAB. IR. Anal. [B 15);Mp 127.5 -1 28. Rf 0.21 (EA -M C 1:10). [Z 24); Mp 127. [A 27)2,4,5,6 -B n4: Sy rup. 1H. [G 9)2,4,5,6 -B n4, 1,3 -B Zl: Mp 122 -1 23 (Me OH). 1H. Anal. [G 9)1,4,5,6-Bn,, 2 -hexy l: Sy rup. 1H. [B 16)1,2,3,4 -B n ◄, 5 -M e: Mp 86-88 (PE ). Anal. [G 2)1,2,3,4 -B n,, 6 -M e: Mp 142 -1 43 (EE -PE). Anal. [G 2] 1,2,3,4-B n ◄, 5 -Me, 6-Pr o: Mp 99 -1 01 (PE ). Anal. [G 2)1,4 ,5 ,6 -B n4, 3 -P MB: Mp 126 -1 27 (EA 一 hexar,e). 1H. 13C. MS. Anal. [P4 ] 1,2,3,4 -B n ◄, 5 -P ro: Mp 95 -9 6 (PE ). Anal. [G 2); Mp 96 -9 7 (PE ). Rf 0.5 (EE -PE 1:1). 1H. [G ll] 1,2,3,4 -B n4, 6 -P ro: Mp 140 -1 42 (PE ). 1H. [G ll) ; Mp 142 -1 43. [G 2) 1,2,4 ,5 -B n◄ , 3,6 -P ro2: Mp 95 -9 7 (PE , trac e TEA). 1H. Anal. [G 9] 2,4 ,5 ,6 -B n4, 1,3 -P ro2: Mp 80 -8 1 (PE, trac e TEA). 1H. Anal. [G 9)1,2,4 ,5 ,6-Bns: Mp 91-93 (EtOH ). 1H. 13C. FAB. IR. Anal. [B 15);Mp 86- 88 (he xane). 1H. 13C. MS. [Z 24); Mp 92 -9 4. [0 15] 1,3,4 ,5 ,6 -B ns: Mp 127 -1 28. 1H. 13C. [L 3)1 -Bz: Mp 84 -8 7 (MeOH -hexane). 1H. 13C. [P E2); Mp 219 -220. 1H. [C H9] 2-Bz: Rf0: 5 (Me OH-CHCh 1:1). 1H. [0 37); Mp 240-2 42. 1H. [C H9] 4 -B z: Mp 208 -210. 1H. [C H9]5 -B z: Mp 238 -240. 1H. [C H9) 1,2 -B z2: 1 H [C H4] 1,3 -B z2: 1H 〔떠 4) 1,4 -B z2: Mp 243 -246. IH. [M E2); Mp 245 -249. 1H. 13C. FAB. [C H3] 1,5 -B z2: 1H (CH4) 1,6 —B z2: 1 H [C H4] 2,4 -B z2: 1H. 〔 ME 띠 ; IH [C H4] 2,5 -B z2: 1H 〔 CH 산 4,5 -B z2: 1H [C H4)
4,6 - B z2: 1H 〔야 4) 1,2,4 -B Z J: Mp 265 -2 68. Rf0. 4 (EA -M C 1:3 ) . 1H. 13C. [C H3] 1,3,5 -BZ J: Mp 133 -1 35. (017) 2,4 ,6 -B Z J: Mp 200-2 03. Rf0 .6 5 (EA -he xane 1:1). 1H. 13C. FAB. [C H3] 4,5,6 - B Z J: Mp 210-21 1 . 1H. 13C . FAB. [C Hll] 1,2 , 3,4 -B z4: Mp 206 -207 (EA -E E). Rf 0.1 (EA -hexane 1:3). 1H. 13C. [C H12)1,4,5,6 -B ZA: Mp 216 -2 17 (EE -PE). Anal. 1H. 13C. [L 3)1,2,3 ,4 ,5 -B 2s: 1H. (CHS); Mp 127 -1 28. Anal. [L 2] 1,2,3,4,6 -B Zs: 1H. [C H8] 1,2 ,4 ,5 ,6 - B Zs: 1H. [C H8] 1,3,4,5,6 -B 2s: Mp 227 -232. (GEl ) ; Mp 240 -2 45. [G E2); 1H. [C H8] 1,3,4 ,5 ,6 -B 2s, 2 -p yra ny l: Mp 220-2 31 . Anal. [ G E2] 1,3 , 4 ,5 ,6 -B2 s, 2 -THP: Mp 226-2 30. [G El] 2 -( pN Hz)Bz: Mp 249 -254 (ILO). A nal. [Z 14] 2-(p N 02)Bz: Rf0. 4 3 (Me OH-C HCb 1:2 ) . 1H. [0 37] 1,3,4,6- C roti : Mp 50 -52. Anal. [G 7] 1 -Me: Mp 202 -204 (EtO H). [G 2); Mp 200 -201 . [A 2); Mp 199 -200. [A l3); M p 197 -198. [Z8 ] 2 -Me: Mp 213 -214 (EtO H -ILO). [G 2); Mp 212. Anal. [A 13]5 -M e: Mp 238 -2 41 (EtO H -H 20). A nal. [A 8); Mp 239. [A l3] 2 -M e, 1,4 -P MB2: Mp 159 -1 60. Anal. (G2) 1,2 -M e2: 13C. [A 17); Mp 162 -1 63. Anal. [A 13) 1,3 -M e2: 13C . [A l7) 1,4 -M e2: Mp 193 -1 94 (EtO H). A nal. [G 7); 13C . [A 17) 2,5 -M e2: Mp 270 -272 (EtO H). A nal. [ G 7); Mp 271 -272 (EtO H). [G 13] 4,5 -M e2: Mp 130 -1 32 (MC). A nal. [ G 13)
1,2,3,4 ,5 -M es: Sy ru p. [L1 ] 1,2,3,4,6 -M es: Mp 85 -8 7 (PE). Anal. [L1 ] 1,2,4 ,5 ,6 -M es: Mp 89 -9 0 (PE). Anal. [L1 ] 1,3,4 ,5 ,6 ~ Mes: M p 82 -8 3 (EE -PE). Anal. [ L 1] 1,4 -O cty h : Liq u id Cry st a l melt at 141 , clear at 171 . Anal. [G 9] 2,5 - P MB2: Mp 229 -2 31 . Anal. [ G 8] 1,2,4 -P MBJ : Mp 137 -1 39 (EA-P E). Anal. [G 2] 1,4,5 , 6-P MB4: Mp 123 -1 24. Anal. 1H. 13C . [L3 ] 1 -( pM e)Bz: Mp 185 -1 87 (Me OH). 1H. 13C . Anal. [PE 2] 1 -T s: Mp 223 -224 (HiO) . Anal. [ A lO] 4 -Ts: Mp 181 -182 (EtO H). A nal. [A lO) D-fo rm 1 -Ac, 3,4,5 -Alb, 2,6 -B 112: (a)o -34 (c 0.9 , CHCh). 1H. [C 5] 1 -Ac, 2,6 -B1 12: Mp 108 -1 09. 〔야 -4 9 (c 1, CHCh). 1H. Anal. [C 5)3 -Ac, 1,2,4,5,6 -B ns: Mp 91 -92. 〔야라 28 . 2 (c 1, CHCh). Anal. [ G 3] 4 -Ac, 1,3,6 -BnJ, 2,5 -P MB2: Mp 137 -1 38 (EA -PE). [a ] 02 5+6.0( c 1, CHCL). 1H. Anal. [G ll] 4-Ac, 2,3,6-B ru, 1,5 -PMB2: Mp 129-130 (EA-P E 1:10). 〔야타 7 .4 (c 1, CHCh). 1H. Anal. [G 13] 6 -A c, 1,3,4 -B ru, 2,5 -P MB2: Mp 138 -139. 〔야 25 -8.0 (c 1, C HCh). Anal. (Gll]4 -Ac, 2,3,6 -B nJ, 1,5 -P ro2: Mp 114 -1 16. (파 25+20 (c 1, CHCh). 1H. Anal. [G 14] 5 -A c, 2,3,6 -B nJ, 1,4 一 Pro2: Mp 78 -8 0. [a )o 2 5+20( c 1, CHCh). 1 H. Anal. [G 14] 3 -A c, 4,5,6 -B z: Mp 103 -1 04 (EA). 〔야 -2 1 .3 (c 1.69 , CHCh, 98% ee). Rf 0.4 5 (EA -h exane 2: 1). 1H. 13C . Anal. [0 36] 1 -A c, 2,3,4,5,6 -M es: [a )o - 7 (c 0.8, CHCb). 1H. 13C. Anal. [L 3] 3 -A c, 1,2,4,5,6 -M es: 〔야 +7 (c 0.8, CHCb). Anal. [L3 ] 4-Ac, 1,2,3,5,6-Mes: Mp 112一 114 (PE). [a )o + 1( c 0.9, CHCb). 1H. 13C. Anal. [L3 ] 6 -Ac, 1,2,3,4 ,5 -Mes: Mp 112-1 14 (PE). 〔야 -1 (c 1.1, CHCL). Anal. [L 3) 1,5 -A cz, 4 -A ll, 2,3,6 -B nJ: Mp 101 -1 03. (a)o 25 -1 7.5 (c 1, CHCL). Anal. [G 14)
4,5 -A c2, 1 -All, 2,3,6 -BnJ: Mp 132 -1 33. 〔야 +41 (c 1, CHCb). 1H. Anal. [ G 13)5,6 一 Ac2, 3 -All, 1 ,2,4-B nJ: Mp 133 -1 34 (EA - P E 1:10). 〔이 D25 -42 (C 1, CHCb). A nal. [G 13)4,5 -A c2, 1,3 -Alh, 2,6 -Bil i: Mp 123 -1 24 (PE ). [a) o25+39( c 1, CHCL). Anal. [ G 8] 4,5 -A cz, 1,3,6 -AllJ, 2 -B n: Mp 138 -1 39. 〔야타 24 (c 1, CHCL). [G 9] 5,6 -Ac2, 1,3,4 _ 帥, 2 -Bn: Mp 133 -1 35. 〔야 25 -2 4 (c 1, CHCL). [G 9)4,5 -A c2, 2,3,6 -Alb, 1 -Crot: Mp 125 -126. [a) o25+28.6( c 1, CHCb). Anal. [ G 13)5,6 -A cz, 1,2,4 -Alb, 3 -C rot: Mp 126 -127. 〔아 -2 8.3 (c 1, CHCb). Anal. [G 13)4,5 -Acz, 2,6-B il i, 1,3 -Pro: Mp 133 -1 35. [a) o25+35( c 1, CHCL). Anal. [G 8] 1,4 -A c2, 2,3,6 -BnJ, 5 -PMB: Mp 115 -1 17 (EE -PE). 〔야 -1 6 (c 1,CHCb). 1H. Anal. [G 14)
4,5 -Ac2, 2,3,6 -B ru, 1 -P MB: Mp 125 -1 26 (EA-P E 1:10). [a]D 25+34.7 (c 1, CHCb). Anal. [G 13] 5,6 -Ac2, 1,2,4 -B nJ, 3 -P MB: Mp 125 -1 26 (EA -PE 1:4). (a,)o25 -36 (c 1, CHCb). 1 H. Anal. [G 13) 1,4 -A c2, 2,3,6 -B nJ, 5 -Pro: Mp 127 -1 28 (PE ). [a,)o25 -22.9 (c 1, CHCb). 1H. Anal. [G 11] 4,5 -A c2, 2,3,6 - B ru, 1 -Pro: Mp 153 -1 55. [a.)0 25+48.7( c 1, CHCh), 〔이 D25 +41. 7 (c 1, pyridi n e ). [G 11); Mp 154 -1 55. [a.)0 25+49( c 1, CHCb). [G 13] 1,4 -A c2, 2,3,5,6 -B n4: Mp 132 -1 33. [a.)02 5- 2 7 (c 1, C HCh). Anal. [G 9] 3,4 -A c2, 1,2,5,6 -B n4: M p 90 -9 1. [a.)o2 5+5.3 ( c 1, CHCh). 1H. Anal. [G 6] 3,6 -A c2, 1,2,4,5 -B n4: Mp 132 -1 33. 〔야라 23.5 (c 1, CHCh). A nal. [G 9)2,4,5 -AcJ, 1,3,6-B nJ: Mp 155 -1 57 (EE -P E). [a ]0 2 5+52.6 ( c 1, CHCh). 1H. Anal. [G ll] 1,2 ,4 -A cJ, 3,5,6 -Mel: M p 110 -1 12 (PE ). A nal. [ G 13] 1,3,4,5 -A c4, 2,6 -B n2: Mp 117 -118 (EE -PE 2:1). [a.)o26 + 13.5 (c 1, CHCb). Anal. [G 8] 1,2,3,4 -A C4, 5,6 -M e2: Mp 123 -1 25. (a.)o25 -3 (c 1, CHCb). 1H. Anal. [ G 9] 1,2,3,6 -A C4, 4,5 -M e2: Mp 124 -1 25. [G 9] 1,3,5,6 -AC4, 2,4 -M e2: Mp 164 -1 66. [a.)02 6- 6 .5 (c 1, CHCh). [G 7); Mp 166 -1 68. 〔야 -6 .3 (c 1, CHCh). 1H. Anal. [G 6)1,2,4 ,5 ,6 -A cs: Mp 185 -187 (CHCh -EE). 〔야 + 14.0 (c 1.6, dio x ane). [Z7 ] 2,3,4,5,6 -A cs: Mp 185 -187 (CHCh -EE). 〔야 -1 3.9 (c 1.6, dio x ane). [Z7 ] 1,2,3,4 ,5 -Acs, 6 -B n: Mp 131 -132. 〔야 +26 (c 0.4 , CHCh). Anal. [L3 ] 1,2,3,5,6-Acs, 4-Bn: Mp 131- 1 32. 〔야 -2 6 (c 1, CHCL). A nal. [L3 ] 3 -All, 2,4 -B1 12: Mp 108 -110 (EE -PE). 〔이 025 -3.6 (c 1, CHCb). Anal. [G 13]5 -All, 3,6 -B nz, 4 -C rot: Mp 92 -9 4 (PE). [a ] 02 5 -1 0.2 (c 1, CHCb). 1H. Anal. [G ll ] 1 -All, 3,6 -B nz, 4,5 -C rotz : Mp 50 -5 2 (PE). [(X]0 26+0.5 (c 1, CHCL). Rf 0.6 (EE-P E 2:1). 1H. Anal. [G ll) 5 -A ll, 3,6 -Bil l, 1,4 -C rotz : Sy ru p . 1H. [G ll ] 3 -A ll, 2,4 -B nz, 1 -P MB: Mp 121 -1 22 (EA -PE). [ex )025 -2 2 (c 1, CHCb). 1H. Anal. [G 13) 4- A ll, 3,6 -B nz, 5 -P MB: Mp 116-1 17 (EA-P E). [(X]D2 -1-6 .7 (C 1, CHCb). 1H. Anal. [G ll] 1 -All, 2,3,6-B ru: Mp 95 -9 7 (EA-P E 1:25). [ cx )o 2 5+1 9.5 (c 1, CHCb). 1H. [G 13);Mp 97 -9 8. [cx )o 1 8+21 .5 ( c 4, CHCL). 'H. 13C . El. Cl. Anal. [ P5 ) 3 -All, 1,2,4 -B n1: Mp 96-98 (PE). (ex 〕굽 6 -2 0.5 (c 1, CHCh). A nal. [G 3); Mp 96 -9 8. [cx )o19- 2 1 .9 (c 4.3 , CHCL). [P5 ] 4 -A ll, 1,5,6 -B ru: Mp 120 -1 21 . [(X]02 6+3.4 ( c 1, CHCh). Anal. [G 6] 1 -A ll, 2,3,6 -B ru, 4,5 -Crotz : Sy rup. 1H. [G ll) 5 -A ll, 2,3,6 -B n1, 1,4 -C rotz : Sy ru p . Rf 0.8 (EE -PE 1:2). 1H. [G ll) 4-All, 2,3,6 -B n1, 1,5 -P MBz: Mp 92-94 (PE ). [(X]02 5+12( c 1, CHCL). 1H. Anal. [G 14] 4 -A ll, 1,3,5,6 -B n4: Mp 87 -8 8 (PE). ((X]02 6+1 4 (c 1, CHCL). Anal. [G 6] 3 -A ll, 1,2,4 ,5 ,6 -B ns: Mp 71 -7 2 (PE). [(X]02 7 -2 .2 (c 1, CHCh). Anal. [G 3] 5 -A ll, 1,4 -C rotz : Mp 128 -1 29 (EA -P E). [(X]02 5+6.7( c 1, CHCL). 1H. Anal. [G ll] 1,4 -A lh, 3,6 -Bil l, 5 -P MB: Mp 110 -1 12 (PE ). [(X]02 5+ 17.0 (c 1, CHCL). Rf0 .9 ( EE-P E 3:1). 1H. Anal. [G ll] 3,4 -A lh, 5,6 -Bil l: [(X]0 23+0.5( c 1.2, CHCL). 1H. [C 3,C 4] 4,5 -Alh, 3,6 -B nz: Mp 105 -1 06 (be nzene -hexane). Rf 0.2 (EA -hexane 1:6). [(X]01 6 -1 4.3 (c 1.3, CHCL). [0 1,0 26] 5,6 -A lh, 1,4 -B il l: Mp 105 -1 06 (be nzene -h exane). [cx )o'6+1 4.2 (CHCL).
[0 1,0 26] 4,5 -Alh, 3,6 -B n2, I -T BDMS: Mp 58.5 -6 0 (pe nta n e). [ex.詞 0 -7 .7 (c I, CHCL). [V I] 4,5 -Alh, 1,3,6 -B nJ: Mp 73 -7 4. 〔 a 問 +0.3 (c I, CHCb). [V I) 4,5 -A lli, 2,3,6 -B n3: Mp 86.5 -8 8. [cx.)o20 -6 .2 (c I, CHCb). [V I] 1,4 -A lli, 2,3,6 -B n3, 5 -P MB: Mp 56 -5 7. [(X.]0 25+1 2.6 (c I, CHCb). 1H. Anal. [G I i] 4,5 -A lli, 1,3,6 -B n3, 2 -TBDMS: Mp 35.5 -3 6.5 [cx.)0 20 -4.7 (c I, CHCb). [VI ) 4,5 -A lli, 2,3,6 -B n3, 1 -T BDMS: [cx.)o2 0+7.9 (c I, CHCb). (VI ) 1,3,6-Alb, 2-Bn : Sy ru p. [cx.)0 25+23( c I, CHCb). [G 9)
1,4 ,5 -시 L, 6 -B n: [ex.)0 20+20.0 ( CHCb). [V 2] 3,4 ,5 -Alb, 6 -B n: [cx.)0 23- 1 0 (c 2, CHCb). 1H. [C 3,C 4] 3,5,6 -A fl3, 4 -B n: [ex.)02 0 -20.0 (CHCb). [V 2)3,4 ,5 -A ilJ, 2,6 -B n2: [ex.Jo +1 0.5 (c 0.95, CHCh). 1H. [C 5) 1,3,4 -꽈 , 5,6 -B n2: 〔이 023+23.8 (c 3.3 , CHCb). 1H. [C 3,C4) 1,4,5 -Alb, 3,6 -B n2: Sy ru p . Rf 0.3 (EA -h exane 1:3 ) . [cx.)0 30+3.l( c 1.6, CHCL). 1H. IR. 〔 02 이 1,3,4 -A lb, 2,5,6 -B n3: Sy ru p . [CX.)0 23+1 5.5 (C 0.8, CHCh). 1H. [C 3,C 4] 1,4 ,5 -Alb, 2,3,6 -B n3: Syr u p . Rf 0.5 (EA -he xane 1:7 ) . [a ]0 3 0- 2 .5 (C 1.6, CHCh). 1H. 13C . IR. [0 26);M p 50.5 -5 1. 5. 〔야 20 -2 .9 (CHCh). [V 2] 1,2,4 -꽈 , 3 -Crot: Sy ru p . 〔이 025 -1 9.3 (c 1, CHCh). [G 13] 2,3,6 -A IL, 1 -Crot: Sy rup. 〔따라 19.7 (c 1, CHCh). [G 13] 1,3,4,5 、 -Af1 4, 6-B n: [cx.)0 23+1 0.7 (c 3.1 , CHCh). 1 H. [C 3,C4) ; 〔야+ 12.2 (CHCL). [V 2)1,3,4,5 -All4, 2,6 -B lll: 〔이 023+0.8 (c 1.1, CHCL). 1H. [C 3,C4) ; [CX.)D 20+0.6 (CHCL). [V 2] 1 -B n: Mp 210 -2 11 (EtO H -i Pr OH). 〔 a 〕잡도 26 (c 0.7, MeOH). 1H. 13C. Anal. [L 3)3 -Bn: Mp 210 -2 11 (EtO H -i Pr OH). [a ]0 2 2+25( c 0.5, MeOH). [L 3)
4 -Bn: Mp 175 -1 77 (MeOH -i Pr OH). (ex 詞 2+6 (c 1, MeOH). Anal. 13C. [L 2)6 -Bn: Mp 176 -178. [cx )o 22 -6 (c I, MeOH). Anal. [L 2); Mp 175.5 -177.7. Rf0 .0 8 (Me OH -EA 1:9). [cx ) o22 -5.6 (c 1, MeOH). 1H. 13C. IR. Anal. [Z l ) 1 -Bn, 2,3,4 ,5 ,6 -A cs: Mp 187 -188. (야 -3 9 (c 0.8, CHCb). [L3 ] 3 -Bn, 1,2 , 4 ,5 ,6 -Acs: Mp 186-1 88. [cx )o + 39( c 1, CHCh). [L 3)4 -Bn, 1,2,3,5,6 -B zs: Mp 212 -214 (EE -PE). [cx )o22- 1 8 (c 1, CHCb). [L 2] 6 -B n, 1,2,3 ,4 , 5 -B zs: Mp 213 -2 14 (EE -PE). (이 022+ 18 (c 1, CHCb). [L2 ] 2,4 -B il l: M p 146- 1 48. [cx )o25+28( c 1, CHCL). [G 8);Mp 146-147. [a ]D 2 5 +28 (c 1, EtO H). [G 13); Mp 145.8 -146.1 (EE). Rf 0.20 (EA). 〔이 D25 + 29.7 (c 1, EtO H). Anal. [Z l) 2,6 -Bil l: Mp 147 -148. (야 25 -2 8 (c 1, CHCb). Anal. [G 8); M p 146 -147. 〔야 -2 9.2 (c 0.6 5 , EtO H). [01 1 );[ cx )o23- 2 9 (c 0.6 5 , EtO H). 1H. Anal. [C 3, C4); Mp 144.5 - 145.5. (cx)o 20 -2 7 (c 0.32, EtO H). [F 3); Mp 145.2 -146.1 (EE ). Rf0 .20 (EA ). [cx )o25-29.2(c 1, EtO H). 1H. 13C. Anal. [Z l);M p 120- 121 .5. (cx)o20 -22.9 (CHCb). [V 2] 2,6 -B n2, 1 -( 3,4 -( OMe)2) -Bn: Mp 142.5 -143.5. @]D2 D -39.0 (C 0.6, CHJ C N). 1H. [F3 ] 2,6 -B n2, 1 -( 3,4-(O Me)2) -Bn, 3 -SEM, 5 -TBDMS: 〔야 -3 8.3 (c 1.2, Cf fiCN ). 1H. [F3 ] 5,6 -B nz, 1,2,4 -B z3; Mp 140 -1 42. @]s46 -81 .2 (dio x ane). 1H. Anal. [B A11)5,6 -B n2, 1,3,4 -BZ J: Mp 196. (cx)S46 -30.9 (diox ane). 1H. Anal. [ B All] 3,6 -Bil l, 4,5 -Croh: Mp 83 -8 5. 〔야 -8 .8 (c 1, CHCb). 1H. Anal. [G 11] 3,6 -B n2, 4,5 -Croh, 1 -PMB: Mp 85 -8 7. [cx )o25+1 .2 (c 1, CHCb). 1H. Anal. [ G ll)3,6 -B n2, 1,4 ,5 -CrotJ : Mp 56 -5 7. [a) D2 드 2.6 (c 1, CHCb). R f 0.6 (EE -PE 2: J). 1H. Anal. [G 11) 2,4 -B n1, 1 -P MB: Mp 120 -1 22 (EtO H). [a) D25- 1 0.4 (c 1, CHCb). 1H. Anal. [G l3) 2,6 -B il l, 1,5 -P MB2: Mp 166 -1 67 (EtO H). [a ] 02 5- I O (c 1, CHCh). Anal. [G 8] 1,6 -B n2, 4,5 -P MB1: [a.)o2 4+1 6 (c I, CHCh). [Z 17) 3,4 -B n2, 5,6 _ PMBl: [a.)o24 -1 6 (c 1, CHCh). [Z 17] 1,2,4 -B n): Mp 118 -1 20. [a.)02 5- 9.0 (c 1, CHCh). Anal. [G 3); Mp 116 - 118 (EtO H -I LO) [a.)o1 8-I O.I (c 2.5 , CHCh). 1H. [P5 ] 1,3,6 -B nJ: Liq u id cry st a lline pro p er t ies , meltin g at 112 , givi n g a clear liquid at 127 (PE ). [a.)02 5+ 16.2 (c 1, CHCh). R f 0.3 (EE). 1 H. Anal. [G ll] 1,5,6 -B ib : Mp 155 -1 56. [a.)o26 O (c 1, CHCh). Anal. [G 6) 2,3,6 -B ru: Mp 121 -1 23. [a.)o2 5+I O (c 1, CHCh). 1H. [G 9); Mp 120 -1 22. [a.)0 25+7 (c 1, CHCh). [G ll);M p 122-1 23. [G 13);M p 117 -1 19. [a) D16 + 15.5 (c 1, CHCh). 1H. 13C. IR. [0 1,0 26) ; Mp 115 -1 15.5. [a.)0 20+8.9 (CHCh). [V 2)
2,4 ,5 -B il. 3: Mp 104 -1 06 (EA-P E 1:10). [a.)0 25+25( c 1, CHCb). [G 9); Mp 104 -1 06. [a.)o1 1+32( c 1, CHCh). [P 6)2,5,6 -B ]l 3: Mp 104 -1 06 (EA -P E 1:10). [a ] 02 5- 2 7 (c 1, CHCL). lH. Anal. [G 9); [a.)o23 -2 5.4 (c 0.5 , CHCL). 1H. [C 3,C4) ; Mp 104 -1 06. [a.) 023 -3 2 (c 1, CHCL). [P 6)3,4 ,5 -Bil. 3: Mp 115 -1 57. 〔야 0 (c 1, CHCh). Anal. [G 6] 1,3,6-B ]l 3, 4,5 -Crotz : Mp 85 -8 7 (PE). 〔야 +3 .4 (c 1, CHCh). 1H. Anal. [G ll) 2,3,6 -B ru, 4,5 -Crotz , 1 -P MB: Mp 62 -64 (PE). (야 -3 .7 (c 1, CHCL). 1H. Anal. [G ll] 2,3,6 -B]l 3, 1,4 ,5 -C rotJ : Sy ru p . 1H. [G ll] 1,2,4 -B ]l 3, 3 -M e: Mp 109-111 . 〔야 -2 5 (c 1, CHCb). Anal. [G 3] 1,2,4-B ]l 3, 3,5,6 -MeJ: Mp 84 -_8 5 (PE). [a ] 02 5 -1 .7 (c 1, CHCh). Anal.[G 13) 1,2,4 -B nJ, 3 -P MB: Mp 106 -1 07 (EA -P E 1:6). 〔야 -1 5.3 (c 1, CHCh). 1H. Anal. [G 13) 2,3,6 -B nJ, 1 -P MB: Mp 105 -1 06 (EA -PE 1:10). (야+ 15.5 (c l, CHCb). Anal. [G 13); Mp 104 -1 06 (EA -P E 1:10). [야+ 12.8 (c 1, CHCb). 'H. [G ll] 2,3,6 -B ru, 5 -P MB: Mp 100-1 02 (EE-P E). (야 +5.9 (c 1, CHCb). 1H. Anal. ( G14); (a)o25+6.6 (c 1, CHCb). [G ll) 2,4 ,5 -B nJ, 1 -P MB: Mp 95 -9 7 (EA -h exane). 〔이 022 -4 (c 1, CHCb). Anal. (P6) 2,5,6 -B nJ, 1 -P MB: Mp 154 -1 55 (EA -P E 1:3). 〔야 -1 4 (c 1, CHCb). Anal. [G 9) 2,5,6 -B nJ, 3 -P MB: Mp 95 -9 6.5 (EA -h exane). [a ] 02 4+4( c 1, CHCb). Anal. [ P6 ] 1,2,4 -B ru, 5 -P MB, 3,6 -P ro: Mp 76 -7 7 (PE). [a ] 026 -8 .6 (c 1, CHCb). 1H. Anal. [G ll] 1,3,6 -B nJ, 2,5 -P MB2: Mp 77 -7 9 (EtO H). 〔야+ 10.5 (c 1, CHCb). Rf 0.2 5 (EE -P E 1:1). [G ll) 2,3 ,6 -B nJ, 1,5 -P MB2: Mp 78 -7 9 (EtO H). 〔야타 10.7 (c 1, CHCb). 1H. Anal. [G 13) 2,3,6-B I1 J, 1,5 -P MB2, 4 -P ro: Mp 104 -1 06 (PE, trac e TEA). [a) D -1.6 (c 1, CHCb). 1H. Anal. [ G 14) 1,2,4 -BI1 J, 3 -P ro: Mp 117 -1 19 (EA -h exane). (야 -4 1. 1 (c 4.3 , CHCb). Anal. [P 5)
2,3,6 -B ru, 1 -P ro: Mp 114 -1 15 (PE, trac e TEA). [a) o25+33( c 1, CHCb). 1H. Anal. [G 13);Mp 113-115 (EA-PE). 〔이 025 34.5 (c 1, CHCb). [G ll); Mp 116 -1 18 (EtO H -I- LO ). 〔야 +40.6 (c 4, CHCb). Anal. [P5 ] 2,3,6-B nJ, 5 -Pro: Mp 78 -8 0 (PE). [a) o25+14.2( c 1, CHCb). 1 H. Anal. [G ll]2,3,6 -B nJ, 1,4 -P ro: Mp 143 -1 44 (PE, trac e TEA). [a) o25+48( c 1, CHCb). Anal. [G 14] 1,2,3,4 -B n4: Mp 105 -1 06 (PE). (야 -1 5 (c 1, CHCb). 1H. Anal. [G 9)
1,2,3,6 -B n4: Mp 103 -1 04. 〔파타 12 (c 1, CHCb). [G 9) - 1,2,4 ,5 -B n4: Mp 105 -1 07 (EA-P E). [a) o25-4 .3 (c 1, CHCh). Anal. [G 9] 1,2,4,6 -B n4: 〔야 -9 .1 (c 1, CHCb). [V 5] 1,2,5,6 -B n4: Mp 153 -1 54. [a) o25- 1 5.5 (c 1, CHCb). 1 H. Anal. [G 6] 1,3,5,6 -B n4: Mp 97 -9 8. 〔야+ 12 (c 0.93, CHCb). A nal. [G 6)1,4 ,5 ,6 -B n4: Mp 148 -1 49 (EA-P E 3:5). [a) o26+21( c 1, CHCb). [G 6); 1H. (GlO) ; Mp 138 -140. 〔야 +23 . 2 (CHCb). 〔 0 인 ; [a )n 1 '+24.2( c 1.3, CHCb). [0 4); Mp 141 -1 43 (be nzene -hexane). Rf 0.4 2 (CHCh -aceto n e 50:1) . 1H. [B R9); (a)o20+ 18.8 (c 0.99, CHCh). [Z 22] 2,3,4,5 -B n4: Mp 153 -1 54. 〔야라 14 (c 1, CHCh). [G 8) 2,3,4 ,6 -B n4: (a)n + 10.0 (c 1, CHCh). [V 5] 2,3,5,6 -B n4: Mp 105 -1 07. 〔야타 -3 . 9 (c 1, CHCh), +4.6 (c 0.55, CHCL). Anal. [G 9] 3,4 ,5 ,6 -B n4: Mp 148 -1 50. 〔야 -2 0.4 (c 1, CHCh). 〔 G 이 ; [a) o19- 2 2.3 (c 1.3, CHCL). [01 ,0 4); Mp 140-142. 〔 a 〕값도 25 (c 2.7 , CHCh). [B R9] 1,2,3,4 -B n4 5,6 -M e2: Mp 62 -6 3 (PE). [G 9] 1,2,4 ,5 -B n4, 3,6 —O cty l: Mp 44 -46 (MeOH). [a ] 02 5 -9.8 (c 1, CHCb). Anal. [G 9] 2,3,5 , 6-B n4, 1 -P MB: Mp 62 -6 4. (a)n25+8.5 (c 1, CHCL). Anal. [G 9)1,3,5,6 -B n4, 4-Pr o: Mp 96-98 . (야 -2 .7 (c 1, CHCL). Anal. [G 6] 3,4 ,5 ,6 - B n4, 1 -THP: Rf 0.2 (EE -hexane 1:1). 13C. [B R18] 3,4 ,5 ,6 -B n4, 1 -THP, 2 -CS(SMe): Sy ru p . Rf 0.25 (EE -h exane 1:3). 1H. [B R18) 1,2,4 ,5 ,6 -Bll. 5: Mp 64 -6 5. 〔야+ 10.0 (c 1, CHCL). Anal. [G 3); (a)o20+9.l (c0.3,CHCL). [B 3);Mp 6 2-64.Anal.[ B 15] 2,3,4,5,6 -B ns: 〔이 n -9.0 (c 0.3, CHCh). [B 3); Mp 63 -65. Anal. (B15) ;回 022 - 11. 5 (c 2, CHCb). 1H. [P6 ] 1,2,4 ,5 ,6 -B ns, 3 -P ro: Mp 89 -9 0. [a.)o+ 27.0( c 0.9, CHCb). Anal. (G3) 6 -B OM, 1 -P MB, 3,4,5 -T BDMSJ: (야 -4 .09 (c 0.83, CHCb). 1H. 13C. HRMS. [F 4] 2,6 -B OMz, 1 -PMB: Mp 103 -104. [a.)02 4 63.9 (c 0.84, CHCb). 1H. 13C. HRMS. [F 4] 2,6 -B OMz, 1 -PMB, 3,4 ,5 -T BDMSJ: 〔야 22.9 (c 1.22 , CHCb). 1H. 13C. HRMS. [F 4)
4,5 -B zz, (1, 6)TIDPS: Mp 147 -1 48. Rf 0.21 (aceto ne-h exane 1:4). [a.)D - 17.4 (c 5.0, CHCb). 1H. 13C. EI. Anal. [B A19] 5,6 -B zz, (3,4)TIDPS: Mp 148. 〔야+ 17.6 (c 5.0, CHCh). 1H. 13C. EI. Anal. [B A19)4,6 -B zz, 1 -B t: 〔야 20 - 15 (c 2.0, EA). [Z ll) 1,2,4 -B Z J: Mp 186 -1 90 (EtO H). (a.)54 6 -6 .5 (THF). 1H. Anal. [B All] 1,3,6 -B Z J: Mp 184-1 94 (Me OH ). 〔이 546 -38.3 (diox ane). 1H. Anal. [B All] 2,3,6- B Zl: Mp 188 -1 91 (EtO H ). [a.)5 46+5.4 ( THF). 1H. Anal. [B All);R f 0.2 4 (Me OH -C HCh). 〔이 ~+5.9 (c 2.5 , THF). 1H. Anal. [B R19] 2,5,6 -B Z J: Rf 0.35 (Me OH -C HCh 1:9). 〔야 -8 .6 (c 2.5, CHCb). 1H. 13C. HRMS. [B R19] 3,4 ,5 -B z3: Rf 0.31 (MeOH -C HCb). 〔야+ 10.2 (c 2.8, CHCb). 1H. 13C. [B R19] 3,4 ,5 -B Zl, 2,6 -M OM i, 1 -T BDPS: Rf 0.33 (aceto n e -h exane 1:3). 〔이다 41 (c 1.6, CHCb). 1H. 13C. [B R19] 2,3,6 -B z3, 1 -T BDPS: Rf 0.3 (MeOH -CHCb 1:40). 〔야 -1 .5 (c 2, MeOH). 1H. 13C. FAB. [B R19)3,4 ,5 -BZ J, 1 -T BDPS: 1H. 13C. [B R19] 2,3,6 -B Z J, 1 -TBDPS, (4,5)TIPS: Rf 0.2 (aceto n e -h exane 1:20). 1H. FAB. [B R19] 2,5,6 -B Zl, 1 -TBDPS, (3,4)TIPS: Rf0. 44 (EE -h exane 1:6). 1H. [B R19)1,3,4,5 -B u (a)o 22 -5.35 (c 2.4, CHCb). [0 10) 1,3,5,6 -B u [a) o22+5.4 2 ( c 2.5, CHCb). [0 10] 1,4 ,5 ,6-B ZA: Mp 210 -2 12 (EA). 〔야 22 -3 0.6 (c 1.57 , EA, 94% ee). [a) o20- 16.6 (c 1.57 , CHCh, 94% ee). Rf0. 10 (EA-h exane 1:2). 1H. IR. Anal. [03 6] 2,3,4 ,5 -Bz .i: Rf 0.56 (MeOH -C HCh 1:9). [a )o+75( c 1.2, MeOH). 1H. 13C. Anal. [B R19] 3,4 ,5 ,6 -B u Mp 226 -2 27. [a) o18+19.8 (c 1.01 , CHCh). 1H. IR. Anal. [02 3) 3,4,5,6 -Bz .i, 1 -SiE tJ: Mp 162 -1 63. (a)o 2 6+22.4 (c 1.43 , CHCb). 1H. IR. Anal. [0 23) 1,2,3,4,5 -B Zs: Mp 191 -1 94. [a ] 02 2+47( c 1, CHCb). [L 2] 1,2,3,5,6-B Zs: Mp 190 -1 94 (EE -PE). [a ] 02 0 -49 (c 1, CHCb). [L 2] 1,2,4,5,6 -B Zs: Mp 123 -1 25. 〔야 -5 9.5 (c 1.8, CHCh). [G El) ; Mp 125 - 130. 〔야 -5 3 (c 1.6, CHCb). Anal. [G E2] 2,3,4 ,5 ,6 -B zs: Mp 135 -136. [C X)D26+65.2 (c 1.15 , CHCb). 1H. IR. Anal. [0 23);( 야타 60 (c 1.5, CHCb). [Z ll] 2,3,4,5,6 -B Zs, 1 -SiE tJ: Mp 186 -1 88. 〔야 +55.9 (c 1.11 , CHCh). 1 H. IR. Anal. [02 3] 1,2,3,4,5 -B zs, 6 -[ (2 ,3,4)- B nJ, - L -f uc op yra nosy l): 〔 a 〕잡도 13 (c 0.5, CHCh). [L 2)
1,2,3,5,6 -B zs, 4 -[ (2 ,3,4 )- B nJ, - L -f uc op yra nosyl ): @D22 -62 (C 0.7, CHCh). [L2 ] 1,2,4 ,5 ,6-B Zs, 3 -pyra ny l: Mp 172 -175. (a)o25 -20 (c 2.14, CHCh). [G E2)1,2,4 ,5 ,6-B Zs, 3 -THP: Mp 173 -1 75. [a )o 25 -1 9.2 (c 2, CHCh). [G El] 4-(- L -fu c opy ra nosyl ): Mp 241-2 43 (Me OH-iP rOH ). [a) o22- 1 10 (c 0.2, I-LO ). 13C. [L 2) 6-( - L -f uc op yran osyl ): [a ] D2 2 -9 9 (c 0.4 , I-LO ). 13C. [L 2] 1 -M e: Mp 205 -206. [a ] D1 8 -3 2.05 (C 3.5, 血 0). [Z 4); Mp 205 -2 05.5. [a ] D -32.6 (c 1, I-LO ). [25 ); Mp 203 -204. 〔야 -3 2 (c 2, I-LO ). [Z 6); 13C.(A17] 3 -M e: Mp 205 -2 07. (a.)0 25 + 31 .9 (c 1, H20). [G 3); M p 199 -203. 〔 a) 다 31 .16 . (Z2); Mp 201 -2 02. (야 +3 1. 4 . (Z 이; Mp 199-2 00. 〔아 +34 . 따) ; Mp 199 -200 (H2 0) . [cx )o 2 5+34.0 ( c 0.6, H20). Anal. (BAS) ; Mp 202 -204. [cx )o20+32.8 . [ S ll) 1,4 -M e2: Mp 221 -222. (야 -2 5 (c 1.5 , H20). (PE3) 2,4 -M e2: Mp 146 -1 48. 〔야 +3 .4 (c 1, MeOH). Anal. [G 6); (cx)o26+3.2 (c 1, MeOH). [G 7)
5,6 -M e2: Mp 196 -1 98 (EtO H -E A 3:10). 〔이 02 6 -7 (c 1, MeOH). Anal. [G 9); Mp 197 -200 (EtO H -EA). [G 13] 4,5 -M e2: Mp 199 -200. 〔야 25+8 (c 1, MeOH). [G 9] 3,5 ,6 -MeJ: Mp 153 —1 55 (EA). (야라 2.9 (c 1, CHCh), 12.6 (c 1, MeOH ). Anal. (G13) 1,2,3,4,5 -M es: (야 -5 (c 1, CHCb). Anal. [ L 3)1,2,3,5 ,6 -M es: (야 +5 (c 0.8 , CHCb). 1H. 13C . Anal. [L3 ] 1,2 ,4 ,5 ,6 -M es: Mp 116 -1 18 (EE -PE). [a )o + 4(c 0.9 , CHCb). Anal. [L3 ); Mp 117 一 117.5. 〔야 -4 (c 2.5, H20 ) . Anal. (BA2) 2,3 ,4 ,5 ,6 -M es: Mp 116 -1 18 (EE -PE). [cx )o- 4 (c 0.8, CHCb). 1H. 13C. Anal. [L3 ] 2,6 -M OM2, 1 -TBDPS: Rf 0.09 (aceto n e -hexane 1:2). [a.)o +46( c 1.8, MeOH). 1H. 13C. [B R19] 2,5,6 -MOMJ : Mp 75.5 -76.5. Rf 0.1 4 (aceto n e -hexane 1:1 ) . 〔야 -1 5.4 (c 0.6, MeOH). 1H. EI. (BR19] 2,3,4,5 -M OM4: Rf 0.23 (aceto n e -hexane 1:1) . 〔야 +3.6 (c 1.2, CHCh). 1H. 13C. EI. [B R19] 2,3,4,5 一 MOM4, (1,6)TIPDS: Rf 0.26 (aceto n e -hexane 1:5). [ex )o+30.3 ( c 3.5, CHCh). 1H. 13C. EI. [B R19] 3,6 -Octy L : Liq u id Cry st a l melt a t 130 -132 , clear at 168 -1 70. 〔야타 14.1 (c 1, MeOH). A nal. [G 9]I -TBDPS: Rf 0.5 (MeOH -CHCh 1:4 ) . (a)o -6.4 (c 3.5, MeOH). 1H. 13C. [B R19)
I -TBDPS, (3,4 )T IPS: Rf 0.3 3 (aceto n e -h exane 1: 4). 1H. 13C . [B R19)I -TBDPS, (4,5)TIPS: Rf 0.4 (aceto n e -h exane 1: 4) . 1 H. 13C . [B R19) (l,6 )TIPS: Rf 0.22 (MeOH -CHCb I:9 ) . 〔아 +8.5 (c 3.4 , MeOH). 1H. 13C. [B R19]B . chir o - Inosit ol (士) -c hir o : Mp 246 -2 47. [Z 8] Ac6: Mp 110. [A 19] 3 -A c, (4,S)Ace, 6 -Bz, (l,2) Hex: Mp 166.5 -1 67. 1H. Anal. [Z8 ] (4,S)Ace, 6 -B z, (l,2) Hex: Mp 176.5 - 1 77. Anal. (Z8) (4,5)Ace, 6 -Bz, (l,2) Hex, 3 -T s: Mp 165.5 -1 67. 1H. Anal. ( Z8) (4,5)Ace, (l,2) Hex, 3 -T s: Mp 134 -1 36. Anal. [Z8 ] 1,2,6 -BnJ: Mp 147 -1 48. Anal. [G 3] 1,2 -B z2, 4 -M e: 1H. IR. HRMS. [L E2) 1,3 -B z2, 4 -M e: 1H. IR. [LE 2] 2,3 —B z2, 4 -M e: 1H. IR. HRMS. [LE 2) (1, 2)Hex: Mp 182 -1 83. Anal. (Z8] 3 -M e: 1H. HRMS. [LE 2) D - chir o : [a.)o+ 60( c 2.5, H20). [A 8); Mp 235 -237. 〔야 +68 (c 0.55, HzO). [Z2 6)
4 -PO(OH)z, (1, 2;5,6)Ace2, 3 -Me (cy cl ohex. lya mmon ium ): Mp 177 -177.5 (pe nia n e -hept an e). 〔이 025+2.0 (c 1.4 , EtO H). Anal. [B A3] 4 -PO(OH)z, 3 -Me (cy cl ohexy la mmon ium ): Mp > 250 (EtO H -aceto n e). (a.)o2 5+20.5 (c 5, HzO). Anal. (BA3] 1 -PO(OBn)z, (2,3;5,6)Hex: Mp 136 -1 37. (a.)o+ 38.4 (c 0.13, CHCh). 1H. Anal. [Z 26] (1,3 ,4)PO(OH)z (cy cl ohexy la mmon ium ): [a.)m +37.1( pH 1) 1H. 31P. Anal. (BA13] (1,3,4)PO(OBn)z, (2,5,6)BZ J: Syr up. (a.)5 46+ 19 (diox ane). 1H. 31P (-1 .0, -1.08 , -1.45 ). Anal. [B A13] 4-PO(OPh)z, (1,2 ;5,6)Ace2, 3 -M e: Mp 69. 〔야 +45 .3. Anal. [BA 3] 1,2,5,6 -A c4, 3 -Me, 4 -Ts: Mp 153. 〔 a 〕삽 9 - 18.2 (c 4.3, CHCb). Anal.[A 21)
1,2,5,6 -A c4, 3,4 -M e2: Mp 102.5 -103.5. [a )o 24 -1.4 (c 2, CHCh). Anal. [A 6] 1,2,3,5,6-Acs, 4 -M e: Mp 98. [a )o 14 + 4( c 2, EtO H). [A 21] {1, 2)Ace: Mp 152 -1 53. 〔야 +95.7 (c 2, H10). Anal. (BAI] (1, 2;5,6 ) Ace2: M p 145 -150. [a )o 10 + 4.8( c 3, EtO H). Anal. [B AI ) (1, 2;5,6)Ace2, 3,4 -B n1: M p 50-5 3. 〔이5-1 6 +22 . 8 (EtO H). 1H. Anal. [B A11) (l,2 ; 5 , 6 ) Ace2, 3 -Me: Mp 104.5 -106. (a)o 끄 - 45.4 (c 1.9 , CHCb). Anal. [A 6); M p 103 -1 03. [a )o 23 - 22.0 (c 3.4 , H10). [A 26) (1, 2;5,6)Ace2, 3 -M e, 4 -Ts: M p 90. (a)o 2 4+53.4 . Anal. [A 21 ) (1,2 ;5,6)Ace2, 3,4 -M e1: Mp 88 -9 0. 〔이 023 - 44.4 (c 1.9, CHCh). A nal. [A 6] (1,2 ;3,4;5,6 ) AceJ: Mp 213 -214. [a )o 11 -36.5 (c 2, CHCh). A nal. [ B AI] 3,4 -B1 12: Mp 133 -134. @5-16 -9.8 (DM F). Anal. [B All] 3,4 -B n1 2,5 -B z1: Mp 166 -1 68 (EE -hexane). [a) S46+ 120.1 (dio x ane). 1 H. Anal. [B All) 3,4 -B il l, 1,2,5 -B Zl: M p 146 -149. [a ]5 -16 +99(CHCh). 1H. Anal. [B A11] 3,4 -B n2, 1,2,5,6 -B u Mp 112 -114. (이 s46+3 1. 4 (dio x ane). 1H. Anal. [B All] 1,2 - B z2, 4 -Me, 3 -Mnt: Oil . 〔야 +99 . 2 (c 4.5 , CHCL). 1H. IR. HRMS. Anal. [L E2) 1,2,5 -B Zl: Mp 228 -2 30. 〔이 546+6 1. 5 (diox ane). Anal. [B A13)1,2,3,5,6-BZs: Glass. 〔야 +46.2 (c 0.9 , CHCh). 1H. IR. HRMS. [L E2] 1,2,3,5,6 -B 2s, 4-M e: Glass. 〔야 +62.7 (c 0.3 , CHCh). 1H. IR. HRMS. [L E2)3 -( 기 -C amp , (1,2;4,5 )H eX2: Mp 185 -186. [a )o3 1 (c 0.37, CHCh). 1H. Anal. [Z 26] (1,2)Hex, 3, 4-B1 12: Mp 91 -9 2. 1H. 13C. 〔回 (1,2;5,6)HeX2, 3 -Ac, 4 -Me: Mp 80 -82. 〔야 +78 . 5 (c 1.3, CHCL). 1H. Anal. [A 24]3 -Me (pini t ol) : Mp 185 一 186. [a.)0 23+66.8 . [ A 6);u c. [A 17);[( JJD 20+61.5 (c 0.27, H20). 1 H. [L E2] 3 -Me, 4 -Ts: Mp 193. 〔야 25 -I (c 3.7, pyri d i n e ). Anal. [A 21] 3,4 -M e2: Mp 191 -193. [a.)0 2'+73.0( c 2, H20). Anal. [A 6) L-chir o: Mp 242·-243. 〔야 -64 . 5 (c I, HzO). [A 21 );1 3C. [A l?);M p 238 -240. [a )o 22 -6 9 (c 1, HzO). Anal. [B A2); Mp 226 -229. [a) o- 61 .6 (c 0.3 7 , HzO). [Z26] 1 -PO(OBn)z, (2,3;5,6)Hex: Mp 134 -1 35 (EE -hexane). [야 -4 6.3 (c 0.3 3 , CHCb). Anal. [Z 26] 3 -PO(OH)z (cy cl ohexy la mmoniu m ): Mp >250. 〔이 025 -25.6 (c 2, HzO). Anal. [B A3] 3 -PO(OH)z, (1, 2;5,6)Acez (cy cl ohexy la mmoniu m ): Mp > 250. 〔아 -2 .2 (c 1, HzO). Anal. [B A3] 3 -PO(OEt) z , (1, 2;5,6)Acez: Mp 135 (pe nta n e). [a) o25- 49.7 (c 2.3, EtO H). Anal. [B A3)
(3,4)cPO(OH ), (1, 2;5,6)Acez (cy cl ohexy la mmon ium ): Mp > 250. 〔야 +16.7 (c4, HzO). Anal. [B A3] (1,3 ,4 )P O(OH)z (cy cl ohexy la mmon ium ): [a)5-16 - 43.3 (pH 1). Anal. [B A13) (1, 3, 4)P0(0Bn)z, (2,5,6)Bz .i: Sy ru p . @책 - 17.5 (dio x ane). [B A13) (1, 2,3)P0(0L i)z: [a)o26 -19.2 (c 1.25 , HzO, pH 10). 1H. 13C. 31P. [C H6] (1, 2,3,5)P0(0L i)z: [a) o25- 3 3 (c 1, HzO, pH 10). 1H. 13C. 31P. [C H6) (3,4 )c PO(OPh), (1, 2;5,6)Ace2: Mp 150 -200. Anal. [B A3] 3 -Ac, (1, 2;5,6)Ace2, 4 -Ts: Mp 144 (Me OH). [a) o1'-114 (c 2.3, CHCL). Anal. [A 21 ) 3,4 -A cz, (l,2;5,6)Ace2: Mp 129. [a) o22- 116.5 (c 2.1, CHCL). [A 26] 1,2,5,6 -Ac ., 3,4 -T s: Mp 158 (EtO H). 〔야+ 17.4 (c l.3, CHCL). [A 16] 1,2,3,4,5 -A cs, 6 -Bn: 1H. [A 20)1,2,3,4,5 -Acs, 6-Me: Mp 111 . [a) o15- 3 1 (c 3.8, EtO H). Anal. [A 21](1, 2)Ace: Mp 157 -1 58. Anal. (A12, A26] (1, 2) Ace, 3,4 -B n2: Mp 92 -9 3. 〔아 28 - 70.5 (c 1.15 , CHCh). Anal. [A 12) (1, 2)Ace, 5 -M e: Mp 134 -1 35.5 . 〔이 023 -88.8 (c 1.6, H20). [A 26] (1,2 ;5,6)Ace2: Mp 153. [a) o20- 4.7 (c 1.2 , EtO H). [A 26] (1,2 ;3,4)Ace2, 5 -M e: Mp 117 -1 18.5. (a)o29 -1 9.3 (c 0.775, CHCh). Anal. [G E3) (1,2 ;3,4)Ace2, 5 -M e, 6 -Ts: Mp 128.5 -129.5. 〔 a 〕값 9 -1 2 (c 0.733, CHCb). Anal. [G E3] (1, 2;5,6)Ace2, 3 -M e: Mp 102 -1 04. [a) o16+45( c 1.3, CHCh). (A15) (1,2 ;5,6)Ace2, 3,4 -M e2: Mp 88 -8 9. Anal. [A 15] (1, 2;5,6)Ace2, 3,4 -( pN 02)Bs: Mp 171 -1 72. [a )o 17 -62 (c 1.0, CHCb). Anal. [A 16] (1, 2;5,6)Ace2, 3,4 -Ts: Mp 161 -162. (a]0 1 4 -7 9.5 (c 2.6 , CHCb). Anal. [A 21)
(1,2;3,4 ;5 ,6)AceJ: Mp 213 -2 14. [a) o25+38.1( c 1, CHCb). [A 26) (l,2;5,6)Belll: Mp 158 -1 59.5 (iPr OH ). [a) o25+6.0( c 1, CHCb). [B A15)3,4 -B n2: Mp 135 -136. 〔아 -5 8.5 (c 0.6 6 , CHCb). Anal. [A 12); Mp 134 -1 35. (a) 546+ 10.6 (DMF). Anal. [B A11] 3,4 -B n2, 2,5 -B z2: Mp 168 -1 69 (EE -hexane). [1,2,5 -B z3: Mp 228 -2 31. (마 6 -6 7.5 (dio x ane). 1 H. Anal. (BA13) 1,4 ,6 -B z3: Mp 189 -1 90. (cx.)0 20 -36.6 (c 0.99, EtO H). [P3 )
1,2,3 ,4 ,5 -Bz, 6 -Ts: Mp 195 -1 97. Rf 0.52 (EA -benzene 1:19). (cx.)0 25 -41 .8 (c 2.4 6 , CHCb). Anal. [G E2] 1,2,3,4,5,6 -B z6: Mp 251 .5 -252.5. (야 -6 2.l (c 1.9, eth yle ne dic h lori de ). Anal. (BA2] 3 -( -) - Camp , (1,2;4,5)HeXz: Mp 211 -2 13. [ex.Jo -4 3 (c 1.2, CHCb). 1H. [Z 26) (1, 2)Hex, 3,4,6 -B nJ: Mp 72 -74 (benzene). [A 24,A l2) (1, 2;5,6)Hex2, 3,4 -B n2: Mp 91 -92. 〔야 -2 1 .6 (c 1.25 , CHCb). Anal. [A l2); Mp 182 -1 84 (EtO H). [B All] (1, 2;3,4 )H ex2, 5 -Me: Mp 117 -119. 〔야 -1 9.3 (c 0.775, CHCb). Anal. [G E2] (1, 2;3,4 )H eXz, 5 -Me, 5 -T s: M p 128 -1 29. (야 -1 2 (c 0.73, CHCb). A nal. [G E2)1 -M e: Mp 207. [cx.)0 18- 5 8 (c 1.5, fuO ). Anal. [A 21] 2 -M e: 13C .A 17 Mp 193 -1 95. [G E2] 2 -Me, 1 -Ts: Mp 178 -179.5. (cx.)0 24 -6 8 (c 0.5, MeOH). Anal. [G E3] 3 -Me: Mp 185 -186. [cx.)0 24- 6 5.5 (c 2, fuO ). [A l);따 20-6 1. 4 (c 0.21, fuO ). [ L E2] 3,4-M e2: Mp 191 -1 92. 〔야 -7 3.2 (c 2, lliO) . [A l] 3,4 -( pN 02)Bs2: Mp 260. 〔 a 詞 ·-1 20 (c 1.0, CHCh). Anal. [A 16] 1 -T s: Mp 172 -1 74. (cx.)o22 - 37.7 (c 1.82 5, CHCh). Anal. [G E2] 3,4 - Ts2: Mp 185 -1 86. [cx.)0 27- 2 8 (c 4.3 , pyridine ). Anal. [A 21]C . scy ll o -Inosit ol scyl lo : Mp 345 -347. [Z 15); Mp 353 -355. Anal. (Z16) ; Mp 330 -3 40 (EtO H -H 20). [ A 19); 13C . (A17) 6 -Ac, 2,4 -B n2, (1,3,5)0rt h: Mp 102 -1 04 (EA -hexane). 1H. Anal. [Z 20] 2,4,6 -A cJ, (1, 3,5)0rt h: Mp 124 -1 26 (EA -hexane). 1H. Anal. [Z 20] Acs: Mp 211 -2 13. Anal. [Z 14) Acs, Me: Mp 192 -1 94. Anal. [A l] Ac6: Mp 296 -2 98. [Z 14); 299 -300. [Z 16); Mp 293 -295. [A 19] (1,2)Ace, 4 -All, 3,6 -B n2: Mp 105 -1 06 (PE). Anal. [G 3] 2,4 -B n2, (1, 3,5)0rt h: Mp 98 -9 9 (Me OH). 1H. IR. Anal. [Z 20) 1,2,3,4 ,5 ,6 -P O(OMe)2: Mp 275 -278. 1H. Anal. [A 18] (1,3,5)0rt h: Mp 330 (EA ). 1H. IR. Anal. [Z2 0] (1, 3,5)0rt h, (2,4,6)0rt ho aceta t e : Mp 177 -1 78 (EA -hexane). 1H. IR. FAB. Anal. [Z 20) D-fo rm (1,2 )Ace, 3,6 -TBDPS2: [(J.,]o -2 1 .6 (c 1.15 , CHCb). 1H. 13C. [P E4] ino sose Acs: Mp 209 -212. [21 4);Mp 205 -2 09. 1H. [Z 15]
D . Ot h er ino sit ols allo Ac6: Mp 144. [A l9); Mp 143 -144. Anal. [A 16) (l,6) Ace, (3,4 )H ex, 2,6 -B zz: Mp 162 -1 65. 1H. Anal. (Z8] cis: Mp 377 (EtO H -! LO ). [A 19) Ac6: Mp 208. Anal. [A 19] Bz6: Mp 252. Anal. [A 19] ino sose: Mp 179 -180. Anal. [A 19] epi : Mp 285. [Z 16);13 C . [A 17] 5,6 -A c2, (1, 2;3,4)Ace: M p 138. [A 26] 3,6 一 Ac2, (1,2 ;4,5)Ace: Mp 201 -203. [A 26] 1,2,3,4 -A c4, 5,6 -( pN 02)Bs: Mp 190. Anal. [A 16] 1,3,4,5,6 -A cs, 2 -NIL -B z: Mp 198 -2 02 (EtO H). A nal. [Z 14) 1,3,4,5,6 -A cs, 2 -( pN 02)Bz: Mp 156 -1 58. Anal. [Z 14) Ac6: 189 -1 91 . [Z 14); 189 -1 90. Anal. [Z 16); Mp 187. [A 19) (1,2 ;3,4 )A ce: Mp 180 -1 81 (EA). [A 16,A26] (1, 2;4,5)Ace: Mp 181 . [A 26) (1, 2;3,4 )A ce, 5,6 -( pN 02)Bs: Mp 145 (EtO H). Anal. [A 16] (1,2 ;3,4 ;5 ,6)Ace): Mp 127 -1 28. [A 26)
2 -禪 )Bz: Mp 214 -2 23 (ILO). Anal. [Z 14] muco: Mp 285 -290. [Z 8)(4,5)Ace, 2,3 -Bil l, 6 -M e: 1H. IR. HRMS. [L E3] (4,5)Ace, 6 -Me: 1H. IR. HRMS . [L E3] (1,2;4,5)Ace2, 3 -Bn, 6 -C (S) SMe: Mp 138. 1H. Anal. [A 24]1,2,3,6 -B u Mp 256 -257. Anal. [Z8] 1,2,3,6 -B Z4, (4,5)Hex: Mp 177 -179. 1H. Anal. [Z 8] neo: Mp 315. Anal. [A 21 ) Ac,: Mp 253 (EtO H). Anal. [A 21]
참고문헌 [A l) Anderson, L.; Talceda, R.; Ang yal , S. J.; M cHug h, R. Arch. Bio c hem. Bio p h ys . 1958, 78, 518 -5 31 . [A 2)Anderson, L.; Lande}, A. M. J. Am. Chem. Soc.; 1954, 76, 6130- 6132. [A 3] A nderson, L.; Laedy, H. A. J. A m. Chem. Soc. 1950, 72, 3141 -3147. 〔사〕 Anderson, L.; Aronson, J. N . J. Org. Chem. 1959, 24, 1812-1 813. [A 5)Str au be- R iek e, H.; Lardy, H. A.; Anderson, L. J. Am. Chem. Soc. 1953, 75, 694 -697. (A6) Anderson, A. B.; M cDonald, D. L.; Fis c her, H. 0. L. J. Am . Chem. Soc. 1 952, 74, 1479 -1480. [A 7)Anderson, L.; Tomota , K.; Kussi, P.; Kirkw ood, S. J. Bio l . Chem. 1953, 204, 769 一 780. [A 8] B al 回 C. E.; A I 떠函야 , A. B. J. Am. Chem. Soc. 1953, 75, 648 -650. 園 Anderson, L.; DeLuca, E. S.; Bi ed er, A.; Post, G. G. J. Am.Chem. Soc. 1957, 79, 1171 -1174. [A lO)A ng ya l, S. J.; Tate , M. E.; Gero, S. D. J. Chem. Soc. 1961, 4116- 4122. [A ll) Ang yal , S. J.; Gero, S. D. Aust. J. Chem. 1965, 18, 1973 -1976. [A 12)Ang yal , S. J.; Ste w a rt, T. S. Aust. J. Chem. 1966, 19, 1683 -1691 . 〔 Al 회 Ang yal , S. J.; Gi lha m, P. T.; McDonald, C. G. J. Chem. Soc. 1957, 1417-1422. 〔 Al 선 Ang yal , C. L.; Ang yal , S. J. J. Chem. Soc. 1952, 6 95 一 697. 〔 Al 회 Ang ya l, S. J.; M cDonald, C. G. ; M ath e son, N. K. J. Chem. Soc. 1953, 3321 -3323.
〔 Al 이 Ang yal , S. J.; Gi lha m, P. T. J. Chem. Soc. 1 958, 375 -379. [A 17)Dorman, D. E.; A ng yal , S . J.; Robert s, J . D . J. Am. Chem. Soc. 1970, 92, 1351 -1354. [A 18)A ng yal , S . J.; Russell, A. F. Aust. J. Chem. 1969, 22, 383 -390. (Al 이 Ang yal , S. J.; McHug h, D. J. J. Chem. Soc. 1957, 3682 -3691 . [A 20)A ng yal , S. J.; Randall, M. H.; Tate , M. E. J. Chem. Soc. 1967, 919 -
922. [A 21)A ng yal , S. J.; Math e son, N. K. J. Am. Chem. Soc. 1955, 77, 4343 -4346. [A 22)A ng yal , S. J.; Russell, A. F. Aust. J. Chem. 1968, 21, 391 -404. [A 23] M cC 。 nnell, J. F.; Ang ya l, S. J.; Ste v ens, J. D. J. Chem. Soc., P 아 k i n Trans. 2 1972, 2039 -2044. 〔 A2 선 Ang yal , S. J.; O die r , L. Carbohyd r . Res. 1982, 101, 209 -219. [A 25)A ng yal , S. J.; Rang e, D. Carbohyd r . Res. 1979, 76, 121 -130. 〔 A2 이 Ang ya l. S . J.; McDonald, C. G. J. Chem. Soc. 1 952, 686 -695. ”幻 Ang yal . S. J.; Tate , M. E. J. Chem. Soc. 1965, 6949. [B l)d eSolms, S. J.; Vacca, J. P.; Huff , J. R. Tetr a hedron Lett. 1987, 4503 — 4506. 먀띠 Vacca, J. P.; deSolms, S. J.; Huff , J. R. J. Am. Chem. Soc. 1987, 109, 3478-3479. [B 3] B illi n gt叫 D. C.; B aker, R.; K 비 a g ows 뵤 J. J.; Mawer, I. J. Chem. Soc., Chem. Commun.1981, 314-316. 따〕 Bi lling ton , D. C.; Baker, R. J. Chem. Soc., Chem. Commun. 1987, 1011-1013. [B 5] S h 따 e, J. K.; Baker, R.; B 비通血 D. C.; G 백 D. J. Chem. S 。 c., Chem. Commun. 1988, 422 -423.〔郞〕 Shute , J. K.; Baker, R.; Bil ling ton , D. C.; Gani, D. J. Chem. Soc., Chem. Commun. 1988, 626-628. [B 7)Polokoff , M. A.; Bencen, G. H.; Vacca, J. P.; deSolms, S. J.; Young , S. D.; Huff , J. R. J. Bio l . Chem. 1988, 263, 24, 11922 一 11927. 〔郞〕 Raga n , C. I.; Watl ing , K. J.; GEE, N. S.; Asp le y, S.; Jac kson, G.; Reid , G. G.; Baker, R.; Bil ling ton , D. C.; Barnaby, R. J.; Leeson, P. D. Bio c hem. J. 1988, 249, 143 -148. (B9) Vacca, J. P.; deSolms, S. J. U.S.Pate n t 4, 755,612. 1988. [B IO)Bil ling ton , D. C. U.K .P ate n t GB 2,206,581.1989. [B l l ) Baker, R.; Kulag o wski, J. J.; Bi lling ton , D. C.; Leeson, P. D.; Live rt on , N. J. Chem. Soc., Chem. Commun.1989, 1383-1385. 〔 B 切 Bil ling ton , D. C. Chem. Soc. Rev. 1989, 18, 83-122. [B 13] B 曲뻥叫 D. C.; Baker, R.; K 비햄向뵤 J. J.; Mawer, I.; Vacca, J. P.; deSolms, S. J.; Huff , J. R. J. Chem. Soc., Perki n Trans. 11989, 1423 -1429. 〔 B 印 Vacca, J. P.; deSolms, S. J.; Huff , J. R.; Bil lington , D. C.; Baker, R.; Kulago w ski , J. J. ; Mawer, I. Tetr a hedron 1989, 45, 5679 一 5702. (B15) Baker, G. R.; Bi lling ton , D. C.; Gani, D. Tetr a hedron 1991, 47, 3895-3908. 〔 Bl 이 Russell, M. G. N.; Baker, R.; Bil lington , D. C. Carbohyd r . Res. 1992, 234, 263 -268. [B AI) Ballou, C. E.; Fis c her, H. 0. L. J. Am. Chem. Soc. 1953, 75, 3673 -3675. [B A2] K abat, E. A.; McDon 백 D. L.; B 때叫 C. E.; Fis c her, H. 0. L. J. Am. Chem. Soc. 1953, 75, 4507 -4509. [B A3)K ilgo ur, G. L.; Ballou, C. E. J. Am. Chem. Soc. 1958, 80, 3956-
3960. 〔 BA 선 Piz e r, F. L.; Ballou, C. E. J. Am. Chem. Soc. 1959, 81, 915 -921 . (BAS] B allou, C. E.; Piz e r, L. I. J. Am. Chem. Soc. 1960, 82, 3333 -3 3 효 [B A6)T om lins on, R. V.; B allou, C. E. J. Bio l . Chem. 1961, 236, 1902 - 1906. [B A7)Brockerhoff , H.; Ballou, C. E. J. Bio l . Chem. 1961, 236, 1907 - 1911 . (BA8] G rado, C.; Ballou, C. E. J. Bio l . Chem.1961, 236, 54 규i。’ (BA9] T o mli函 n, R. V.; Ball 叫 C. E. B i ochem 泣ry 1962, J, 166 -1 71 . 〔 BAl 이 Nalcaji rna , T.; Ballou, C. E. J. Bio l . Chem. 1974, 249, 7685 -7694. [B AU)T egg e , W.; Ballou, C. E. Proc. N atl. Acad. Sci . USA 1989, 86, 94- 98. [B A12)J ina, A. N.; Ralph , J.;-B allou, C. E. Bio c hemi str y 1990, 29, 5203 -5209. [B A13)T egg e , W.; Den is, G. V.; Ballou, C. E. Carbohyd r . Res. 1991, 217, 107 —11 6. 〔 BAI 서 Tegg e, W.; Ballou, C. E. Carbohyd r . Res. 1 992, 230, 63 -77. 〔 BAI 회 Shneour, E.; Ballou, C. E. J. Am. Chem , Soc. 1958, 80, 3960 -3961 . [B RI)B ruzik , K.; Jian g , R. -T.; Tsa i, M. -D . Bio c hemi st r y 1983, 22, 2478-2486. 〔 B R'.긱 Bruzik , K.; Tsai , M. -D . Bio c hemi st r y 1984, 23, 1656 -1661 . 〔 B R'.사 Jian g, R. -T.; Shyy , Y. -J .; Tsai , M. -D . Bio c hemi st r y 1984, 23, 1661-1667. [B R4] T 타 T. -C.; H 따 J.; Jian g , R. -T .; Bruzik , K.; T 빠 M. -D. Bio c hemi str y 1985, 24, 3180 —31 88. 〔 B~ 기 Bruz ik, K.; Salamonczyk , G.; Ste c , W. J. J. Org. Chem. 1986, 51,
2368-2370. 〔 BR 이 Raetz , C. R. H.; Carman, G. M.; Dowhan, W.; Jian g , R. -T.; Waszkuc, W.; Loff red o, W.; Tsai, M. -D . Bio c hemi str y 1987, 26, 4022- 4027. [B R7] R 函血 _ Ja ns 핵 T.; Jian g , R. -T .; T빠 M. -D . B i o 먀따 m 1988, 27, 4619-4 624. (BR8] S arvis , H. E.; Lo ffr떠 o’ 짜 Dluhy, R. A.; Hernq vi s t, L.; W函 er, D. A.; Tsai , M. -D. Bio c hemi str y 1988, 27, 4625 -4631. [B R9] B ru 팩 K. S.; Salam 寧 z y k, G. M. @幽沖 R 邸 1989, 195, 67 - 73. [B RIO)L in , G.; Tsai , M. -D . J. Am. Chem. Soc. 1989, 111, 3099-3101. [B Rll) Loff red o, W. M. ; Jian g , R. -T . ; Tsa i, M. -D . Bio c hemi str y 1990, 29, 10912 一 10918. [B R12)L in , G.; Bennett, F.; Tsai , M. -D . Bio c hemi str y 1990, 29, 2747 - 2757. (BR13) Rosario -J an sen, T.; Pownal, H.; Jian g , R. -T.; Tsa i, M. -D. Bio o rg. Chem. 1990, 18, 179-1 84. [B R14)Salamori cz yk , G. M.; Bruzil, K. S. Tetr a hedron Lett . 1990, 31, 2015 一 2016. 〔 BRl 회 Salamori cz yk , G. M.; Pie t ru s ie w i cz , K. M. Tetr a hedron Lett. 1991, 32, 4031 -4032. [B R16)Salamori cz yk , G. M.; Pie t ru s ie w i cz , K. M. Tetr ah edron Lett. 1991, 32, 6167 -6170. [B Rl7)Bruzik , K. S.; My er s, J.; Tsa i, M. -D. Tetr a hedron Lett. 1992, 33, 1009-1012. [B R18] P ie t r u sie w i cz , K. M.; Salam 碩띠 k, G. M .; Bruzk, K. S. Tetr a hedron 1992, 48, 5523 -5542.
〔 BRl 이 Bruzik , K. S.; Tsa i, M. -D . J. Am. Chem. Soc. 1992, 114, 6361 - 6374. 〔 BR2 이 Bruzik , K. S.; Tsai , M. -D . Bio o rg. Med. Chem. 1994, 2, 49 -7 2. [B R21) Bruzik , K. S.; Kubia k , R. J. Tetr a hedron Lett . 1995, 36, 2415 -2418. [C l)C arless, H. A. J.; Busia , K. Tetr a hedron Lett. 1990, 31, 3449-3 452. 〔띠 Liu, Y. C.; Chen, C. S. Tetr a hedron Lett. 1989, 30, 1617 -1620. 〔댜 Gou, D. M.; Chen, C. S. Tetr a hedron Lett .1 992, 33, 721-724. @]G ou, D. M.; Liu , Y. C.; Chen, C. S. Carbohyd r . Res. 1992, 234, 51- 64. [C 5)G ou, D. M.; Chen, C. S. J. Chem. Soc., Chem. Commun. 1994, 2125 - 2126. (@]G ou, D. M.; Sh ieh , W. R.; Lu, P. J.; Chen, C. S. Bio o rg. Med. Chem. 1994, 2, 7-13. [C HI) Chung, S. K.; Ry u, Y.; Chang , Y. T.; Moon, S. H. Kor. J. Med. Chem. 1992, 2, 33 -4 4. [C H2] 야 un g, S. K.; Ry u, Y.; Chang , Y. T.; Whang , D.; Ki m , K. Carbohyd r . Res. 1994, 253, 13 -1 8. [C H3] 야 un g, S. K.; Chang, Y. T.; Sohn, K. H. Kor. J. Med. Chem. 1994, 4, 57-65. 〔 CH 선 Chung, S. K.; Chang, Y. T. J. Chem. Soc., Chem. Commun. 1995, 11-12. 〔 CH 회 Chung , S. K.; Chang , Y. T.; Sohn, K. H. J. Chem. Soc., Chem. Commun.1996, 163-164. [C H6] 야 un g, S. K.; Yu, S. H. Kor. J. Med. Chem. 1996, 6, 35 -46.
〔 CH 기 Chung , S. K.; Ry u, Y. Carbohyd r. R es.1994, 258, 145 -167. [C H8)Chung , S. K.; Chang , Y. T. Kor. J. Med. Chem.1996, 6, 162-1 65. [C H9)Chung , S. K.; Chang , Y. T. Bio o rg. Med. Chem. Lett . 1996, 6, 2039-2042. 〔 CHl 이 Chung , S. K.; Chang , Y. T., W hang , D.; Kim , K. Carbohyd r . Res. 1996, 295, 1 -6 . [C Hll)C hung , S . K.; Chang , Y. T. Kor. J. Med. Chem. 1996, 6, 253 一 258. 〔 CHI 익 Chung , S. K.; Chang, Y. T.; Kwon, Y. J. Carbohyd r . Chem. in pre ss (1998). 〔町 Falck, J. R.; Yadag iri, P. J . Org. C hem.1989, 54, 5851-5852. [F 2)R eddy, K. K.; Falck, J. R. Tetr a hedron Lett. 1993, 34, 7869 -7872. 〔回 Falck, J. R.; A bdali, A . Bio o rg. Med. Chem. Lett. 1993, 3, 717 구 20. 〔四〕 Reddy, K . K.; S aady, M.; F alck, J. R. J. Org. Chem. 1995, 60, 3385 -3390. [G l)G ig g, J.; Gig g, R.; Payn e , S.; Conant, R. Carbohyd r . Res. 1985, 142, 132-134. 〔 G 띠 Gig g, J.; Gig g, R.; Payn e , S.; Conant, R. J. Chem. Soc., P erki n Trans. 11987, 423 -4 29. [® ]G ig g, J. ; Gig g, R. ; Payn e , S . ; Conant, R. J. Chem. Soc., Perkin T rans. 11987, 1757 -1762. 〔어〕 Gig g, J.; Gigg, R.; Payn e , S.; C onant, R. J. Chem. Soc., Perki n Trans. 1, 1987, 2411 -2414. [G 5)G igg, J.; Gigg, R.; Payn e , S.; Conant, R. Carbohyd r . Res. 1985, 140, cl -c 3. (G 이 Desai , T.; Femandez-Mayo r alas, A.; Gigg, J.; Gig g, R.; Payn e , S.
Carbohyd r . R es. 1990, 205, 105 -1 23. [m ] D esai , T.; G ig g, J.; Gig g, R.; Payn e , S.; Penades, S.; Rog er s, H. J. Carbohyd r . Res. 1991, 216, 197 -2 09. [G 8)Desai , T.; Gig g, J.; Gigg, R.; Payn e , S. Carbohyd r . Res. 1992, 228, 65-79. [G 9)D esai , T.; Gig g, J.; Gig g, R.; Payn e , S. Carbohyd r . Res. 1992, 225, 209-228. (Gl 이 Desai, T.; Gigg, J.; Gig g, R.; Ma rtin -Zamora, E.; S chnetz , N. Carbohyd r . Res. 1994, 258, 135-144. [Gll ) Desai , T.; G ig g, J.; Gig g, R.; Ma rtin - Zamora, E. Carbohyd r . Res. 1994, 262, 59 -77. [G 12)Gig g, J.; Gig g, R.; Ma rtin -Za mora, E. Tetr a hedron Lett . 1 993, 34, 2827-2830. 〔 G 印 Desai , T.; G ig g, J.; Gig g, R.; Payn e , S.; Penades, S. Carbohyd r . Res. 1992, 234, 1 -21. 〔 Gl 선 Desai , T.; Fernandez -Mayo r alas, A.; Gig g, J.; G ig g, R.; Payn e , S. Carbohyd r . R es. 1992, 234, 157 -1 75. 〔 G 印 Gig g, R.; Warren, C. D. J. Chem. Soc. C . 1969, 2367. [G El) Merci er , D.; Gero, S. D. Tetr a hedron Lett . 1968, 31, 3459 -3462. [G E2] M 函i er, D.; Barn 야’ J. E. G.; Gero, S. D. 7l라 rahedron. 1969, 25, 5681-5687. [G E3] G ero, S. D. Tetr ah edron Lett. 1966, 29, 591-595. [L l)G aregg , P. J.; Iversen, T.; Joh ansson, R.; Lind berg, B. Carbohyd r . Res. 1984, 130, 322 -3 26. 〔끄〕 Garegg , P. J.; Lin d berg, B. Carbohyd r . Res. 1985, 139, 2 09 -215.
[L 3] G ar 행g, P. J.; L i ndb아g, B. Carbohyd r . R 益 1988, 173, 20 도 떠 6 [L EI) Ley, S. V.; Ste r nfe ld , F. Tetr a hedron Lett . 1988, 29, 5305 -5 308. [L E2)Ley, S. V.; Ste r nfe ld , F. Tetr a hedron 1989, 45, 3463 -3476. (L 巴〕 Ley, S. V.; Parra, M.; Redg ra ve, A. J.; Ste r nfe ld , F. Tetr a hedron 1990, 46, 4995 -5 026. [M l) Kulago w ski , J. J . Tetr a hedron Lett . 1 989, 30, 3869 -3872. [M 2)Baker, R.; Leeson, P. D.; Live rt on , N. J.; Kulago w ski , J. J. J. Chem. Soc., Chem. Commun. 1990, 462 -4 64. (M3] 邸 er, R.; Ca rrick , C.; Leeson, P. D.; Lennon, I. C.; Live rt on , N. J. J. Chem. Soc., Chem. Commun. 1991, 298 -300. [M 4] K 미땡 OWS 뵤 J. J.; Baker, R.; Fl 述 her, S. R. J. Chem. Soc., Chem. Commun. 19 91, 1649 一 1650. [M EI) Meek, J. L.; David s on, F.; Hobbs, F. W. J. Am. Chem. Soc. 1988, 110, 2317 -2318. [M E2)Hobbs, F. W.; Meek, J. L. US Pate n t, 4,8 7 3,355. 1989. @ ]O za ki, S.; Wata n abe, Y.; Og as awara, T.; K ondo, Y.; Sh iot a ni, N.; Ni sh i i, H.; Mats u k i, T. Tetr a hedron Lett. 1986, 27, 3157-3 160. [®]W ata n abe, Y.; Mitani, M.; Oza ki, S. Chem. Lett .1 987, 123-126. [®]W ata na be, Y.; Naka hira, H.; Buny a, M.; Oza ki, S. Tetr a hedron Lett. 1987, 28, 4179-4180. 〔。 4 〕 Wata n abe, Y. Og as awara, T.; Sh iot a ni, N.; Oza ki, S. Tetr a hedron Lett . 1987, 28, 2607-2610. 〔。 5 〕 Ozaki, S.; Kondo, Y.; Nakahir a , H.; Yamaoka, S.; Wata n abe, Y.
Tetr a hedron Lett . 1 987, 28, 4691 一 4694. [0 6)W ata n abe, Y.; O g as awara, T.; Nakahir a , H.; Mats u k i, T.; Oza ki, S. Tetr a hedron Lett. 1988, 29, 5259 -5262. 〔。 7 〕 Oza ki, S.; Kohno, M. ; N akahir a , H.; Buny a, M. ; W ata n abe, Y. Chem. Lett. 1988, 77 一 80. 〔。 8 〕 Wata n abe, Y.; Mi tan i , M. ; M ori ta, T.; Oza ki, S. J. Chem. Soc., Chem. Commun. 1989, 482 -4 83. 〔。 9 〕 Hira ta , M.; Wata n abe, Y.; Ishmats u , T.; lkebe, T.; K i m ura, Y.; Yamagu c hi, K.; Oza ki, S. Kog a, T. J. Bio l . Chem. 1989, 264, 20303 -20308. 〔 01 이 Wata n abe, Y.; Sh ino hara, T.; Fusim o to , T.; Oza ki, S. Chem. Phann. Bull. 1990, 38, 562 -563. [0 11)W ata n abe, Y.; Oka, A.; Shim i zu , Y.; Ozak i, S. Tetr a hedron Lett . 1990, 31, 2613 -2616. 〔 01 띠 Akiya ma, T.; Takechi, N.; Oza ki, S. Tetr a hedron Lett . 1990, 31, 1433-1434. [01 3)H irat a , M.; Wata n abe, Y.; l shi ma ts u , T.; Yanag a, F.; Kog a, T.; O za ki, S. Bio c hem. Bio ph ys . es. C ommun. 1990, 168, 379 -386. [0 14)H ira ta , M.; Yanag a, F.; Kog a, T.; Og as awara, T.; Wata n abe, Y.; Oza ki, S. J. Bio l . Chem. 1990, 265, 8404 一 8407. [01 5)A kiyam a, T.; Takechi , N.; Sh ima , H.; Oza ki, S. Chem. Lett. 1990, 1881-1884. (016] W ata na be, Y.; K omoda, Y.; Ebis u y a, K.; Oza ki, S. Tetr a hedron Lett . 1990, 31, 255 -256. [01 7)W ata na be, Y.; Fusim o to , T.; Sh ino hara, T.; Oza ki, S. J. Chem. Soc., Chem. Commun. 1991, 428 -429. [01 8] 사 d y ama, T.; Hirof u ji, H.; Oza ki, S. Tetr a hedron Lett . 1991, 32,
1321 —13 24. [01 9] A k iya ma, T.; Ni sh im oto , H.; Ozak i, S. Tetr a hedron Lett . 1 991, 32, 1335-1338. 〔 02 이 Wata n abe, Y.; H rata , M. ; O g as awara, T.; Kog a, T.; Oza ki, S. Bio o rg. Med. Chem. Lett. 1991, 1, 399 -4 02. (0 끄 ]H ira ta , M.; Ki m ura, Y. ; lshim ats u , T.; Yanag a, F.; Shuto , T.; Sasag ur i, T.; Kog a, T.; Wata n abe, Y. Oza ki, S. Bio c hem. J. 1991, 276, 333- 3 36. 〔 0 끄〕 Wata n abe, Y.; Fuji mo to , T.; Ozaki, S. J. Chem. Soc., Chem. Commun. 1992, 681-683. 〔 02 회 Ak iya ma, T.; Takechi, N .; Oza ki, S.; Sh iot a , K. Bull. Chem. Soc. Jpn . 1992, 65, 366 -3 72. [0 24)W tan abe, Y.; Komoda, Y.; Oza ki, S. Tetr a hedron Lett. 1992, 33, 1313-1316. 〔 02 회 Ling , L .; Wata n abe, Y.; Akiya ma, T.; Oza ki, S. Tetr a hedron Lett. 1992, 33, 1911 -1 914. [0 26)O za ki, S.; K ondo, Y.; Sh iot a ni, N .; Og as awara, T.; W ata na be, Y. J. Chem. Soc., Perkin Trans. 11992, 729 -7 37. [0 幻 Wata n abe, Y. ; lnada, E. ; Jinn o, M. ; Oza ki, S . Tetr a hedron Lett . 1993, 34, 497 -5 00. 〔 0 認〕 Wata n abe, Y.; Nakamoto , C.; Oza ki, S. Sy nl ett . 1993, 115 -1 16. (029] O za ki, S.; Wata n abe, Y.; Hirat a , M.; Og as awara, T.; Kanemats u , T.; Yoshid a , M. Drug Desig n for Neuroscie n ce, Kozik o wsk i, A. P., ed. Raven Press, Ltd . , New York, 1993. [03 0)L ing , L.; Li, X.; Wata na be, Y.; Akiya ma, T.; Oza ki, S. Bio o rg. Med. Chem. 1993, 1, 155 -1 59. [03 1)L ing , L.; Oza ki, S. Tetr a hedron Lett. 1993, 34, 2501-2504.
(032) Wata n abe, Y.; Hi ro fu s i, H.; Oza ki, S. Tetr a hedron Lett. 1994, 35, 123-1 24. [03 3)W ata n abe, Y.; Og as awara, T.; Oza ki, S.; Hira ta , M. Carbih y d r . Res. 1994, 258, 87 -9 2. [0 34)H ashii , M.; Hirat a , M.; Oza ki, S.; Nozawa, Y.; Higa sh ida , H. FEBS Lett. 1994, 340, 276 -2 80. [0 35)O zaki, S.; Ling , L.; Og as awara, T.; Wata n abe, Y.; Hira ta , M. Carbohyd r . Res. 1994, 259, 307 -3 10. [0 36)L ing , L.; Oza ki, S. Carbohyd r . Res. 1994, 256, 49 一 58. 〔 03 기 Ozak i, S.; Kog a, Y.; Ling , L.; Wata n abe, Y.; Kimu ra, Y.; Hirat a , M. Bull. Chem Soc. J pn . 1994, 67, 1058 一 1063. (038] H irat a , M.; Narumoto , N.; Wata n abe, Y.; Kanemats u , T.; kog a, T.; Ozak i, S. Mol. Pharmacol. 1994, 45, 271 一 276. [03 9] 。 z aki, S. DEPate n t 4 ,027,076Al.1991. 〔 04 이 Ozak i, S.; Wata n abe, Y.; PCT, WO 87/05598. 〔印 Hambli n, M. R.; Pott er , B. V. L.; Gig g, R. J. Chem. Soc., Chem. Commun.1981, 626-627. [m ] C ooke, A. M.; Pott er , B. V. L. Tetr a hedron Lett. 1987, 28, 2305- 2308. 〔 P 刃 Liu, C.; Nahorski, S. R.; Pott er , B. V. L. J. Chem. Soc., Chem. Commun.1991, 1014-1016. 떠〕 Sawy er , D. A.; Pott er , B. V. L. J. Chem. Soc., Perki n Trans. 1 1992, 923-932. [P5 ] L amp e, D.; Mills, S. J.; Pott er , B. V. L. J. Chem. Soc., Perki n Trans. 1 1992, 2899 -2906. 〔 P 이 Rile y, A. M.; Payn e , R.; Pott er , B. V. L. J. Med. Chem. 1994, 37,
3918 -3 927. 〔 回 Mi lls, S. J.; Sa fra ny , S . T.; Wi lc ox, R. A.; Nahorski , S. R.; Pott er , B. V. L. BMCL 1993, 3, 1505 -1 510. [P EI) F ernandez de la Pradil la, Jar ami llo, C.; Jim enez -Barbero, J.; Ma rtin -Lo mas, M. ; P enades, S.; Zapa t a , A. Carbohyd r . Res. 1990, 207, 249- 2 57. [P E2] Z a p뿌 & Fernandez de la Pra &恥 Ma rtin -Lomas, M.; Pe 血磁 S. J. Org. Chem. 1991, 56, 444 一 447. [P E3)Ag ui l a , A.; Ma rtin -Lomas M.; Penades, S. Tetr a hedron Lett . 1992, 33, 401 一 404. [P E4)Chia r a, J. L.; Martin -Lomas, M. Tetr a hedron Lett . 1994, 35, 2969- 2 972. [SI) Ly ut i k, A. I.; Krylo va, V. N.; Kozlova, S. P.; Klya s hch itskii, B. A.; Shvets , V. I.; Evstig n eeva, R. P.; Zhdanovic h , E. S. Zh. Obshch. Khim . 1971, 41, 2747 -2753. [S 2)Shvets , V. I.; Klya s hch itsk i i, B. A.; Ste p s n ov, A. E.; Evstig ne eva, R. P. T etr a hedron 1973, 2 9, 331 -340. 函〕 Ste p s n ov, A. E.; E vstig n eeva, R. P.; Shvets , V. I.; Klya s hch itskii, B. A. Bio o rg. K him . 1976, 2, 1618 -1626. 〔 S 산 Ste p s n ov, A. E.; Klya s hch itsk i i, B. A.; Shvets , V. I.; Evstig ne eva, R. P. Bio o rg. K him . 1976, 2, 1627 -1 633. 〔 S 회 Ste p s n ov, A. E.; Shvets , V. I. Chem. Phy s. Lip ids 1979, 25, 247-26 3. [S 6)K rylo va, V. N.; Gornaeva, N. P.; Olein ilc, G. F.; Shvets , V. I. Zh. Org. Khim .1980, 16, 315-322. [S 7] K ryl o va, V. N.; Ly ut i k, A. I.; Gornaeva, N. P.; Shvets , V. I. Zh.
Obshch. Khim . 1981, 51, 210 -214. [S8 ] 없 e p snov, A. E.; R unova, 0. B.; Schlewer, G.; Sp ies s, B .; S hvets , V. I. Tetr a hedron Lett . 1989, 30, 5 125 -5128. [S9 )Bushnev, A. S.; Hendri ck son, E. K.; Shvets , V . I.; Hend rick son, H. S. Bio o rg. Med. Chem. 1994, 2, 147 -1 51 . [S 10)K lya s hchit sk ii , B . A.; Pi m enova, V. V.; Bashkato v a, A. I.; Zhelvakova, E. G.; Sokolov, S. D.; Shvets , Preobrazhenski i, N . A. Zlz. Obshch. Khim . 1970, 4 0, 2482. [S 11)K lya s hchit sk i i, B. A. ; S ta r osti na , A. K.; Lin b erg, L. F.; Shvets , V. I.; Evstig n eeva, R. P. Zh. Org. Khim . 1971, 7, 492. (Vl) Dreef, C. E.; Eli e, C. J. J.; Hoog er hout, P.; V der Mare!, G. A.; V Boom, J. H . Tetr a hedron Lett . 1 988, 29, 6513-6 516. W 익 Dreef, C. E.; Tuin m an, R. J.; Eli e, C. J. J.; V der Mare!, G. A.; V Boom, J. H. Reel. Trav. Chim . Pays -Bas 1988, 107, 395-397. (V3) Dreef, C. E.; Tuin m an, R. J.; Lefe b er, A. W. M.; Eli e, C. J. J.; V der Marel, G. A.; V Boom, J. H. Tetr a hedron 1991, 47, 4709-4722. N 산 Eli e, C. J. J.; Verduy n, R.; Dreef, C. E.; Brounts , D. M.; V der Mare!, G. A.; V Boom, J. H. Tetr a hedron 1990, 4 6, 8243-8254. (V5] W es t따血 P.; W i llem s, H. A.; V Boeckel, C. A. A.; Tc따 야 edron Lett . 1 990, 31, 6915 -6918. [Z l)B audin , G.; Gl nzer, B. I.; Swa mina th a n, K. S.; V asella, A. Helv. Chim . Acta 1988, 71, 1367 -1378. [Z 2] 編 t, E. R.; Tollens, B.; J u stu s Lie b ig s Ann. Chem. 1892, 272, 288. [Z3 ] K .i賜 F. E.; J u 따 L. J. Chem. Soc. 1953, 1192. [ZA )B i en , S.; Gins burg, D. J. Chem. Soc. 1958, 3189.
〔 Z 회 Post, G. G.; Anderson, L. J. Am. Chem. Soc. 1 962, 84, 478. (Z 이 Plouvie r , V. C. R. Hebd. Seances Acad. Sci. 1955, 241, 983. 〔 Z 기 Molotk v sky, J. G.; Berge l son, L. D. Tetr a hedron Lett . 1971, 12, 4791 -4 794.; Molotk v sky, J. G.; Berge l son, L. D. Chem. Phy. Lip ids 1973, 11, 135 -1 47. [Z 8] 액 awa, S.; Ok i, S.; Kunit om o, H.; Sua mi, T. Bull. Chem. Soc. Jpn . 1977, 50, 1867 -1 871 . (Z9) Ward, J. G.; Young , R. C. Tetr a hedron Lett. 1988, 29, 6013 -6016. (Zl 이 Mets c hie s , T.; S chultz , C.; Jas to r f f, B. Tetr a hedron Lett. 1988, 29, 3921-3922. [Zll ) Andersch, P.; Schneid e r, M. P. Tetr a hedron: Assym metr y 1993, 4, 2135-2138. [Z 12)J on es, M.; Rana, K. K. ; W ard, J. G.; Young , R. C. Tetr a hedron Lett. 1989, 30, 5353 -5356. (Z13) Brown, D. M.; Clark, B. F. C.; Lett er s, R. J. Chem. Soc. 1961, 3774 一 3779. 〔 Zl 사 May, E. L. J. Org. Chem. 1952, 17, 286-289. [Z 15)Kohne, B.; Praefc k e, K. Lie b ig s Ann. Chem. 1985, 866-86 8. 〔 Zl 이 Anderson, R. C.; Wa llis, E. S. J. Am. Chem. Soc. 1948, 70, 2931- 2935. [21 7)C hid a , N.; Koiz u m i, K.; Kitad a, Y.; Yokoy am a, C.; Og aw a, S. J. Chem. Soc., chem. Commun.1994, 111-113. (Z18) Okada, K.; Hashi zu me, K.; Ta nino , H.; Kakoi, H.; Inoue, S. Chem. Pharm. Bull. 1989, 37, 791 -793. [Z 19)Cobb, J. E.; Joh nson, M. R. Tetr a hedron 1991, 47, 21 -3 0. 〔 Z2 이 Lee, H. W.; Kish i , Y. J. Org. Chem. 1985, 50, 4402 -4404. [Z 21 )M arecek, J. F.; Prestw ic h , G. D. Tetr ah edron Lett. 1991, 32, 1863 -
1866. 〔 Z 끄〕 Reese, C. B.; Ward, J. G. Tetr a hedron Lett .1 987, 28, 2309-2312. 〔 Z2 미 Coste l lo, A. J. R.; Glonek, T.; My er s, T. Carbohyd r . Res. 1976, 46, 159 -1 71 . [Z 24] M assy, D. J. R.; Wy ss , P. Helv. Chim . Acta 1990, 73, 1037-1057. 〔 Z2 회 Schnetz -B outa u d, N.; Sp ies s, B.; Schlewer, G. Carbohyd r . Res. 1994, 259, 135 -1 40. [Z % ]B erlin , W. K.; Zhang. W. S.; Shen, T. Y. Tetr ah edron 1991, 47, 1 - 20. [Z 27)Roemer, S.; Rudolf, M. T.; Sta d ler, C.; Schultz, C. J. Chem. Soc., Chem. Commun. 1995, 411 -412.
찾 O~ .!i!..7 1
-I 광천화성 (ph oto a ffinity ) 유도체 200, 235 광학 분할 82 GAP 235 드 단백질 키나제 C 23 디아실글리세롤 23 DAST 185 dial koxy ch lorop ho sph ine 77, 79 2, 2-di me th o xyp ro p an e 48 dibu ty lt in oxid e 62, 85, 99 DDQ 64 DPPC 75 E: 리아노딘 32 리튬 효과 25 ras (p2 1 ) 단백 질 9, 19 □ MAP 키나제 17 mandeli c acid 150 2-meth o xyp ro p an e 48, 52
L -m enth oxy a cety l chlorid e 109, 166 L -m enth yl chlorofo rm ate 109 日 BBB (blood brain ba rrier ) 25 benzyl ide ne 86 벤질화 60, 63, 87, 92, 94 人 cAMP 20 cGMP 20 cADP -ribo se 22 cyc l ohexy lide ne 48, 88 cyc l op en ty lide ne 139 sph ingo lip id 22 사이클리톨 38 사이클린 의존성 키나제 17 성장 호르몬 17 세포 분열 18 세포 예정사 (a pn pt os i s) 18 신경 전달 물질 15 실릴화 68 。 iso p ro p ylide ne 48
(S) -( +) -acety lm andeli c acid 109 아세탈 48 aceto b acte r suboxy da ns 120 아실 이동 반응 70 알릴화 66, 100 1 -eth o xy cy c l ohexene 48, 53 ort ho fo r mate 56, 159, 165 2 차 전달 물질 20, '1:7 Inosose 120, 210 이노시톨 명명법 38, 39 이온 통로 16 인슐린 17 1 차 전달 물질 21, 22 입체 이성질체 37 EGF 19 GTPase 9 ' 9 -x anth e ny l chlori de 140 종양 억제 단백질 18 G- 단백질 20 = 키나제 꼬 9 CAN 64 (R) - (+) -camp h or dime th y l aceta l l()C )
(S ) -( -) -c amp ha nic chlori de 109 camp ho r 119, 150, 171 conduri tol 135, 143 ( -) -qui n ic aci d 82, llO, 147 L -q ue brachit ol 82, 110 qui n idi n e l13 E D -t artaric aci d 140 탈분극 현상 (de p ol ari za ti on) 16 1, l, 2, 2 -te t r a meth o xy cy cl ohexane 54 3, 3 ', 4, 4'-te t r ah y dr o -6 , 6'-bi - 2H - pyra n 54 tet r a benzy l pyro p h osp h ate (TBPP) 76, 155 trityl7 l 84 TIPS 54, 170 TMS 105 티로신키나제 16 TBDMS 59 티오인산 유도체 191 프 Ferr ier 반응 82, 1%, 21J2 (R)-( +) -1-ph e ny le th yl iso cya n ate 1()C )
ph osph orami di t e 78, 165 pho sph o rochlorid a te s 75 포스폰산 유도체 192 포스포리파제 C(PLC) 8, 22 PI -3 -k ina se 27, 213 por cin e liv e r este r ase (PLE) 165
pse udomonas put i da 117 ph yt ic acid 30, 154 D -p ini t ol 144 PSCb 189 PMB 64
정성기 연 세 대학교 화학과 졸 업 일리노이 대 학 화학과 박사 예일 대학 연구원, 연구 교수, 텍사스 A&M 대학 조교수, 스미스 클 라인 프렌치 연구소 수석 연구원 포항공대 응용 생유기 연구소장 현재 포항공대 화학과 교수 포항공대 기초과학 연구소장 장영태 포항공대 화학과 졸 업 포항공대 화학과 석사 포항공대 화학과 박사 번역서 『 페니실린을 찾아서』 인산이노시톨 대우학술총서 • 자연과학 122 1 판 1 쇄 찍음 1998 년 6 월 1 일 1 판 1 쇄 펴냄 1998 년 6 월 5 일 지은이 정성기 · 장영태 펴낸이 才卜孟浩 펴낸곳 (후) 민옵^t 출판등록 1966. 5. 19. 제 16-490 호 서울특별시 강남구 신사동 506 대표전화 515-2000/ 팩시밀리 515-2007 값 21,000 원 ® 정성기 • 장영태, 1998 자연과학 화학 KDC/439.1 5 7 Pri nt e d in Seoul, Korea ISBN 89 크 374-3622-1 94430 89-374-3000-2 (세트)
| 대우학술총서자언과학 1 1 소립자와 게이지 상호작용 김진의 43 후리에 해석과 의미분 작용소 86 등각장론 임채호 . 2 동력학특론 이병호 김도한 87 방사선생물학 남상열 3 질소고정 송승달 44 한국의 고생물 이 하영 88 석유지질학 이용일 4 상전이와 임계현상 김두칠 45 질량분석학 김명수 89 베르누이 시행의 통계적 분석 5 촉매작용 진종식 46 급변론 박대현 배도선 김성인 6 뫼스바우어 분광학 옥항납 47 생체에너지 주충노 90 신경세포생리학 강만식 7 극미량원소의 영양 승정자 48 리이만 기하학 박을룡 91 생리활성을 가진 C - P 화합물의 8 수소화붕소와 유기붕소 49 군표현론 박승안 화학 김용준 강익중 화합물 윤능민 50 비선형 편미분 방정식론 하기식 92 생물유기화학 서정헌 9 항생물질의 전합성 강석구 51 생체막 김형만 93 조직배양 김승업 10 국소적 형태의 Ati ya h - si n g e r 52 수리분류학 고철환 94 유기전이금속화합물 조남숙 외 지표이론 지동표 53 찰스 다윈 정용재 95 실내환경 과학 김윤신 11 Mucop ol y saccha ri des 의 54 금속부식 박용수 96 유한요소법 정상권 생화학 및 생물리학 박준우 55 양자광학 이상수 97 대수적 위상수학 우무하 김재룡 12 천체물리학 홍승수 56 효소반응 속도론 서정현 98 파인만 적분론 장건수 13 프로스타글라딘 합성 김성각 57 화성암 성인론 이민성 99 응용 미생물학 박무영 14 천연물화학연구법 우원식 58 확 률 론 구자홍 100 리보플라빈 이상선 15 지방영양 김숙희 59 분자분광학 소현수 101 노화 김숙희 김화영 16 결정화유리 김병호 60 벡터속 이론 양재현 102 매트릭스 격리분광학 정기호 17 고분자에 의한 화학반응 조의환 61 곤충신 경 생리학 부경생 103 신경계 조직배양 김승업 18 과학혁명 김영식 62 에너지띠 이론 모혜정 104 지구화학 김규한 19 한국지질론 장기홍 63 수학가초론 김상문 105 은하계의 형성과 화학적 진화
