 Sig n al Transd u cti on in Liv i n g Orga nis m s
Sig n al Transd u cti on in Liv i n g Orga nis m s 재쾌 서울대학교 화학교육과 ( B .S) 와 서강대학교 화학과 ( M. S) 를 졸업하고 미국 텍사스 주립대학 화학과에서 박사학위를 취득하였으며 캘리포니아 대학 연구원과 연세대학교 조교수, 충북대학교 생화학과 교수를 역임했다. 김학용 충북대 학교 화학과를 졸업 하고 미국 코네 티 컷 주립대학교에서 박사학위를 취득한 후 현재 캘 리 포 니 아 대 학의 연구원으로 있다. 박문환 충북대학교 과학교육과와 한양대학교 화학과 ( M.S ) 졸업, 충북대학교 화학과에서 박사학위를 취득했으며 미국 네브라스카 주립대학에서 연구원을 역임한 후 현재 태산 정밀 부속 연구소에 재직중이다
생명체의 신호전이  Sig n al Transd u cti on in Liv i n g Orga nis m s
Sig n al Transd u cti on in Liv i n g Orga nis m s
이 책을 존경하는 恩師 故 蔡快 님의 磁有 I 에 삼가 바칩니다.
 생명체의 신호전이
생명체의 신호전이
책머리에 생밍 현상 발현 의 근원적 이해 를 위한 수많은 생명 과학자들의 엄청 난 노리에도 불구하고 생명의 신비는 아직도 안개 속에 감추어진 채 드 러나고 있지 않다. 급속도로 발전하는 과학기술도 생명의 신비를 시원스 럽게 밝히기에는 역부족인데, 그 이유는 생명 현상이 너무나 복잡하고 정교한 메커니 즘 에 의해 발현되고 있기 때문에 이 문제롤 완전히 해결 한다는 것은 어떤 의미에서는 영원히 인간 사고의 한계를 벗어난 신의 영역에 속하는 신비 그 자체라는 생각에 미칠 때가 많은 것이다. 그러나 수많은 생명 과학자들에 의한 부단하고 집요한 생명체에 관한 연구는 어떤 경우 상당한 깊 이까지 그 작용 메커니즘을 이해할 수 있는 경지에 와 있기도 하다. 생명 현상 발현의 신비를 이해하려는 노력은 생명 과학 의 모든 분야에서 끈질기게 진행되고 있지만, 그 중에서도 생명체의 신 호 전달 과정을 이해하고자 하는 연구들이 생명 신비의 커튼을 여는 데 큰 공헌을 할 것이라고 저자들은 믿는다. 따라서 최근 생명 과학 분야에 서 가장 많은 홍미와 관심이 집중되고 있는 연구 분야가 이 분야라고 말 해도 과언이 아닐 정도로 많은 연구 결과들이 쏟아져 나오고 있는 것이 다. 1970 년대부터 태동하기 시작한 이 연구 분야는 1980 년대에 들어와서 획기적인 연구 결과들이 출현했으며 2000 년대에는 그 연구의 진행이 과 히 절정에 달할 것으로 예상된다. 본인은 후학들에게 이러한 연구 내용 들을 이해시켜 이 분야 연구의 홍미를 유발시키고 참여시켜야겠다는 사 명감을 느껴, 이번에 생체 신호 전이라는 대학원용 교재를 만들게 되었 다. 생체 신호 전이에 대한 단계적이고 종합적인 내용을 9 개 장에 나누
어 기술하였는데, 가급적이면 신호 전달 분자 들 의 구조와 기능을 연결시 켜 기술함으로써 신호 전달 메커니즘을 분자적 수준에서 이해합 수 있 도록 정리하였다. 이 책을 집필하는 데 저자의 게으른 탓에 상당한 시간 이 소요된 관계로 먼저 집필해 놓았던 장의 내용은 최근 논문 둘 의 인용 이 부족하다는 사실을 부언하는 바이다. 이 책의 원고 릅 컵퓨터 로 정리 하는 데 많은 도움을 준 우리 실험실의 한 봉덕군을 비롯한 대학원생-,: 에 게 깊은 감사의 뜻을 표한다. 1998 년 4 월
차례
책머리에 1제1장 수용체 11-1 G-단백질과 연결되어 있는 수용체 • 11-2 채널과 연결되어 있는 수용체 • 161-3 촉매의 기능을 동시에 가지고 있는 수용체 • 32제2장 G- 단백질 512-1 G-단백질의 구조와 성질 • 522-2 G-단백질 소단위체들의 관계와 기능 • 562-3 Ras 단백질 • 622-4 G-단백질들의 구조적 유사성 • 702-5 G-단백질 a 소단위체들의 구조와 기능 • 73제3장 포스포이노시티드 813-1 포스파티딜 이노시톨 대사 • 843-2 이노시톨 포스페이트 대사 • 96제4장 칼슘 이온 113
4-1 IP3에 의한 Ca²+의 동원 • 1184-2 리아노딘 수용체 채널 • 120 4-3 Ca²+에 의해 유도되는 Ca²+의 방출 • 1254-4 G-단백질에 의해 조절되는 Ca²+채널 • 1264-5 Ca²+유입 채널 • 1284-6 이노시톨 포스페이트에 의한 Ca²+유입 • 1314-7 칼슘 진동 • 1344-8 세포질 내의 진동 • 1364-9 진동과 신호 전이 기작 • 136제5장 단백질 인산화와 단백질 키나제 1475-1 cAMP 의존성 단백질 키나제 • 1485-2 Ca²+/ 칼모듀린 의존성 단백질 키나제 • 1615-3 단백질 키나제 C • 1705-4 수용체 티로신 키나제 • 1805-5 단백질 탈인산화 효소 • 192제6장 이온 채널 2036-1 전기 생리학에 관한 일반적인 개념 • 2046-2 어떻게 채널이 열리고 닫히는가? • 2086-3 이온 채널 • 2166-4 신호 전달 기작 • 229제7장 신호 전이와 유전자 발현 243
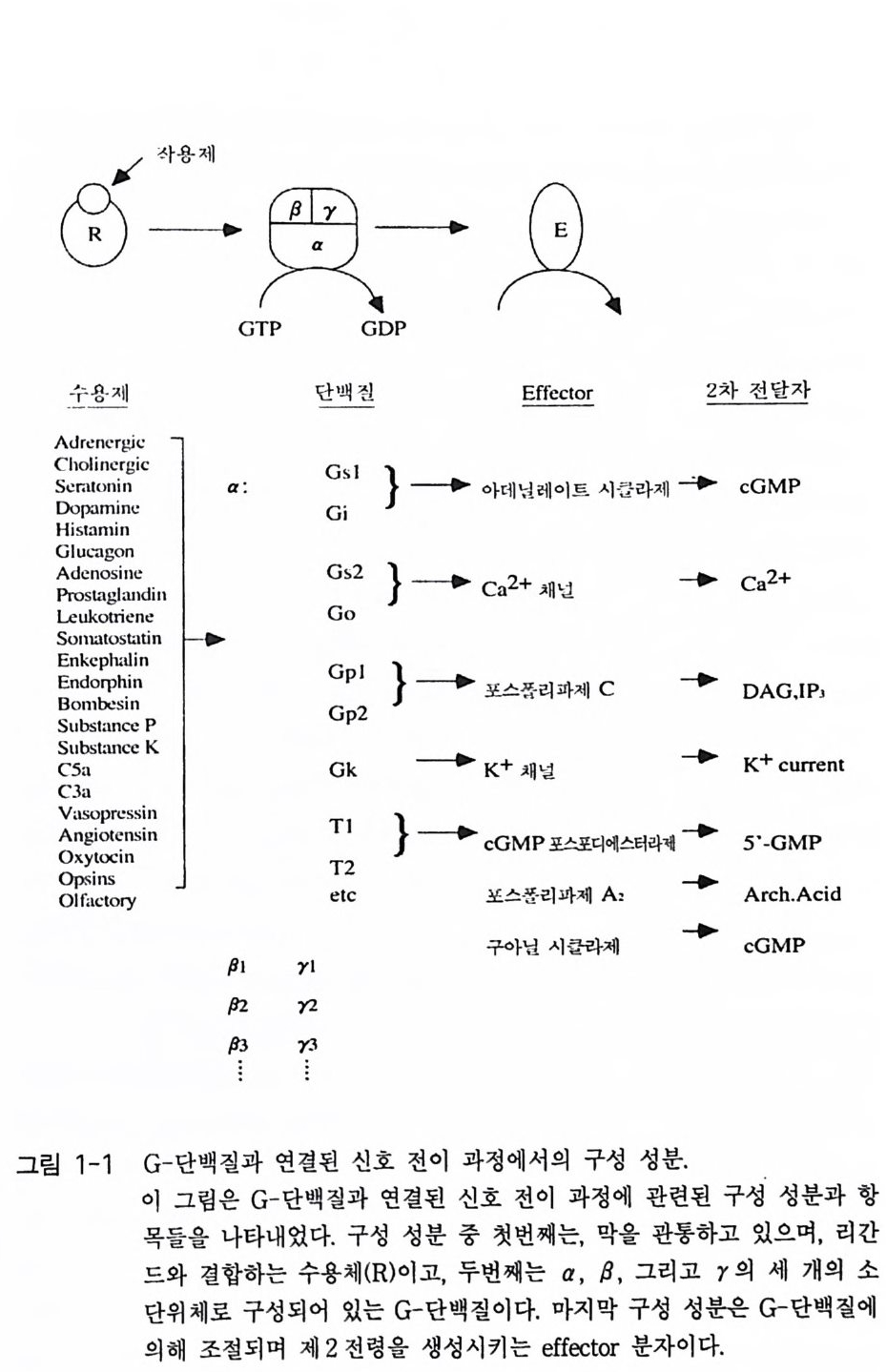
7-1 진핵생물의 신호 전이 및 유전자 발현 • 2477-2 고등 식물의 신호 전이 및 유전자 발현 • 2517-3 암과 유전자 발현 • 2607-4 전사 인자 • 272제8장 박테리아의 신호 전이 2858-1 단백질 인산화와 신호 전달 기작 • 2868-2 고전적인 단백질 키나제와 포스파타제계 • 2898-3 감지와 반응계 • 2988-4 인산 전이 효소계 • 307제9장 식물의 신호 전이 3199-1 신호와 수용체 • 3209-2 G-단백질 • 3219-3 이노시톨 인지질 대사 회로 • 3319-4 신호 전이에서 Ca²+의 역할 • 3389-5 단백질 인산화와 단백질 키나제 • 3429-6 신호와 유전자 발현 • 348약어표 • 357용어해설 • 362찾아보기 • 397제 1 장 수용체 생명체가 주위 환경으로부터 신호 를 받아들여 필요한 세포 반응을 유 발 하 는 단계까지의 일련의 생리 / 생화학 반응 경로 를 신호 전이 (s ign al tr a n s duc ti on) 라고 하 는 데 , 이 신호 전이 과정의 일차적인 단계가 신호수 용이다 신호수용은 신호의 종류에 따라 이들을 받아 들 이는 다양한 수용 체 분 자 들 이 세포의 여러 위치에 존재하는 것으로 알려졌다. 이 장에서 는 대 표 적인 수용체 들 로서 원형질 막에 위치한 세 가지 유형의 수용체 둘 에 관 해서만 기본적인 구조와 기능에 관해서 기술하고자 한다. 이들 세 가지 수용체들을 분류하면 ® G- 단백질과 연결된 수용체 (G- p ro t e in link ed recep tor ), (2) 채널로 연결되어 있는 수용체 (channel - link ed re- cept or ), ® 촉매의 기능을 동시에 가지고 있는 수용체 (ca talyti c- link ed recep tor ) 들이 다. 1-1 G- 단백질과 연결되어 있는 수용체 G - 단백질과 연결된 대표적인 수용체에는 ® 아드레날린 수용체 @
로돕신, ® 무스카린 아세틸콜린 수용체 (mACh recept or ) 등이 있다 . 이 들 수용체들은 신호를 수용한 후 원형질막에 위치하고 있 는 G - 단백질을 활성화시키며, 활성화된 G- 단백질은 그 종류에 따라 eff ec to r 분자둘 [예, 아데닐레이트 시클라제 (aden y la t e cyc l ase), 포스포리파제(p ho sph o lip as e C, pho sph o lip a se A2 등), 포스포디 에 스터 라제 (ph osph o d i- este r ase) 또는 채널 단백질 등]을 활성화시킨다. 이 들 활 성화된 eff ec to r 들은 세포질 내의 제 2 의 전령 (cAMP, Ca2+ , c GMP 등 ) 생성 음 촉 매하게 된다(그림 1-1). 이렇게 생성된 제 2 의 전령 들은 신호 전달옹 위 한 그 다 음 단계의 생화학 반웅들을 조절한다. 신호 전이에 참여하는 생화학 반 옹들 중 가장 대표적이고 중요한 반옹이 단백질의 인산화 반옹인데, 이 인산화 반응을 조절하는 효소는 단백질 키나제(p ro t e i n ki nase) 와 단백질 포스파타제 (pro te in pho sph ata s e) 이 며 이 들 효소의 활성 도가 대 부분 제 2 전령들에 의해 조절되는 것이다 [예, cAMP 의존성 단백질 키나제, Ca2t / calmodul in 의존성 단백질 키나제, Ca2+ I DAG 의존성 단백질 키나제 (PKC)]. 1-1-1 아드레날린 수용체 아드레날린 수용체 (Adren ergi c Rece pto r) 라 함은 신경 전달 물질 중의 하나인 카테콜아민 (ca t.ec hol amin e) 류의 화합물(예, epi ne ph rine , norepi ne - phiine, dop amine 둥)이 리간드로 결합할 수 있는 수용체를 일컫는다. 이 수용체는 아드레날린 수용체 (adren alin e rece pt or) 라고도 부르며 그 종류 는 네 가지 형태 (a1, a2, f31 , f3 2) 가 있으며, 이들은 신경 조직을 비롯하 여 다양한 조직 세포에 존재하는 것으로 알려져 있다.
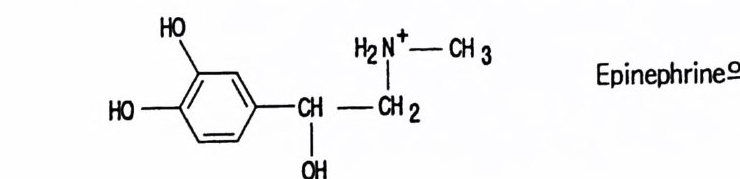 oo \CH —::+: CH 3 E pi ne ph r i ne 의 구조
oo \CH —::+: CH 3 E pi ne ph r i ne 의 구조
 / 4 } 용제 \
/ 4 } 용제 \
a 와 /3형의 수용체는 상호 작용 하 는 G - 단백질의 종류 에 따라 구분 하고 있는데, a - 아 드레날린 수용체의 경우는 주로 저해적 G - 단백질 (G,) 과 상호 작용하여 eff ec to r 분자인 아데닐레이트 시 클 라제의 활성을 억 제 시키며 , /3-아드레날린 수용체는 아데 닐 레이 트 시 클 라제 를 환성화 시 키 는 G - 단백질 (G s ) 과 상호 작용하는 수용체이댜 이 들 두 가지 유형의 수 용체 들 중 /3 형은 지금까지 관심의 대상이 되어 많은 연구 견과 · 간 가 지고 있다. 따라서 이 장에서는 8 - 아 드 레 날린 수용체에 관해서만 좀 더 자세하게 기술하고자 한다. 8 - 아드레 날린 수용체 는 /31 형과 /32 형의 두 가 지로 구분되는데 이들 두 형태의 수용체는 그 구조적인 면에서도 명확한 차 이를 가지고 있으며 약리학적인 측면 에서도 차이가 뚜렷한 것 으 로 보고 되어 있다(1). 이 수용체의 경우 리간드가 결합하면 G - 단백질 (G s ) 과 상 호 작용을 하게 되며 그 결과는 아데닐레이트 시 클라제 의 활성을 높 여 세포 내 cAMP 의 농도를 증가시키게 된다. 사람의 세포로부터 8 - 아 드 레날린 수용체의 유전자가 클로닝되었으며, 이 단백 질 의 아미 노산 서열 올 비롯한 몇 가지 중요한 구조적인 정보들이 보고된 바 있다 (1) . 삼차원 구조는 로돕신과 매우 유사함이 밝혀졌으며 아미노산 서열도 로돕신과 상동성 (homolo gy)이 있다고 알려졌다 (2 , 3, 4, 5). 아미노산 서열의 상동 성은 막속에 묻혀 있는 부분(tran smembrane dom ain)에서 특히 컸으며 친수성 부위에서는 상당한 차이가 있음이 나타났다(그립 1-2). 단백질 접힘(fo l di n g)과 리간드 결합에 필요한 부위 를 알아보기 위하여 B- 아드레날린 수용체 유전자를 결손 돌연변이 (dele ti on mu tati on) 시켜 (6, 7), cos-7 세포에 집어넣고 발현되는 단백질들을 Weste rn blot 방법 으로 확인한 후, 방사성 동위원소가 표지된 리간드의 결합을 분석함으로 써 리간드 결합 부위가 확인되었다. 그 결과 N- 말단과 C- 말단의 친수성 부위가 절단된 경우는 아고니스트인 iso pr o te ren ol 이나 안타고니스트인 ICYP 와 같은 분자가 결합하는 데 전혀 ·영 향을 주지 못했다. 또한 이들
 N..
N..
결손 돌연변이의 경우 수용체 단백 질 들 이 세 포막 에 축적되는 것 에 전혀 영향을 주지 못했댜 이 사실은 친수성 루프 ( loo p)의 부위에 위치한 이 영역들은 단백질의 접합 막 결합 그 리고 리간 드 결합 등에 판수적 영역 이 아님을 말해 주는 것이다. 이와는 대조적으 로 박을 두과 하 는 부위릅 절단하는 돌연변이 를 시켰을 경우 /3 - 아 드 레날린 수용체가 박에 잔 축 적되지 않을 뿐만 아니라 리간드 결합 능력도 저하됨을 반견하였다 . 이 사실은 /3-아드레날린 수용체의 경우 리간 드 결합 부위가 소수상 부위 에 위치하고 있음을 말해 주는 것이다. 쥐 (hams t er) 의 /3-아드레날린 수용체는 15 개의 시 스테 인 잔기 를 가지 고 있는데 이들 중 3 개의 시스테인 잔기는 G- 단백질과의 상호 작용을 위하여 보존되어 있다 (6, 7). 약리학적 연구에 의하면 一 S ― s ― 결합 과 이 결합의 재배치가 리간드 결합에 매우 중요하다. Dix o n 등은 이 들 15 개의 시스테인 잔기를 다 른 아미노산으로 하나씩 치환시킨 후 리간 드 가 결합하는 능력을 조사해 보았다(표 1-1 ) . 그 결과 4 개의 시스테인 잔기 (C y s - 106, Cy s -1 8 4, Cy s -190, Cy s -19 1) 들만이 리간드 결합에 영향을 미쳤다. /3-아드레날린 수용체 는 N - 말단 에 연결된 탄수화물을 상당량 가지고 있는데, 효소의 처리로 탄수화물 부 위를 제거하였을 경우 f3 - 아드레날린 수용체의 기능에는 별다른 영향 을 주지 않음이 밝혀졌다 (8, 9). 글리코실화(g l y cos y la ti on) 되는 부위는 4 군데 인데, 두 곳은 N- 말단 부위이고 다른 두 곳은 C- 말단 부위이다 . N - 말단 부위에서 글리코실화에 참여하는 아미노산 잔기는 아스파르트산 (6 번과 15 번)으로서 이들이 제거된 돌연변이체의 경우 i so p ro t erenol 과 ICYP 의 정상적인 결합에 영향을 미치지 않았다 . 이 결과들은 f3-아드레날린 수 용체의 글리코실화가 세포에서 f3-아드레날린 수용체의 교통정리 등을 위해서 중요성을 가지나 리간드 결합에는 큰 역할을 하지 않는다는 것이 다. 리간드의 양이온성 아민기가 결합하는 아미노산 잔기는 As p -113 으 로 밝혀졌는데, [Glu-113] /3-아드레날린 수용체가 발현되는 세포막에서
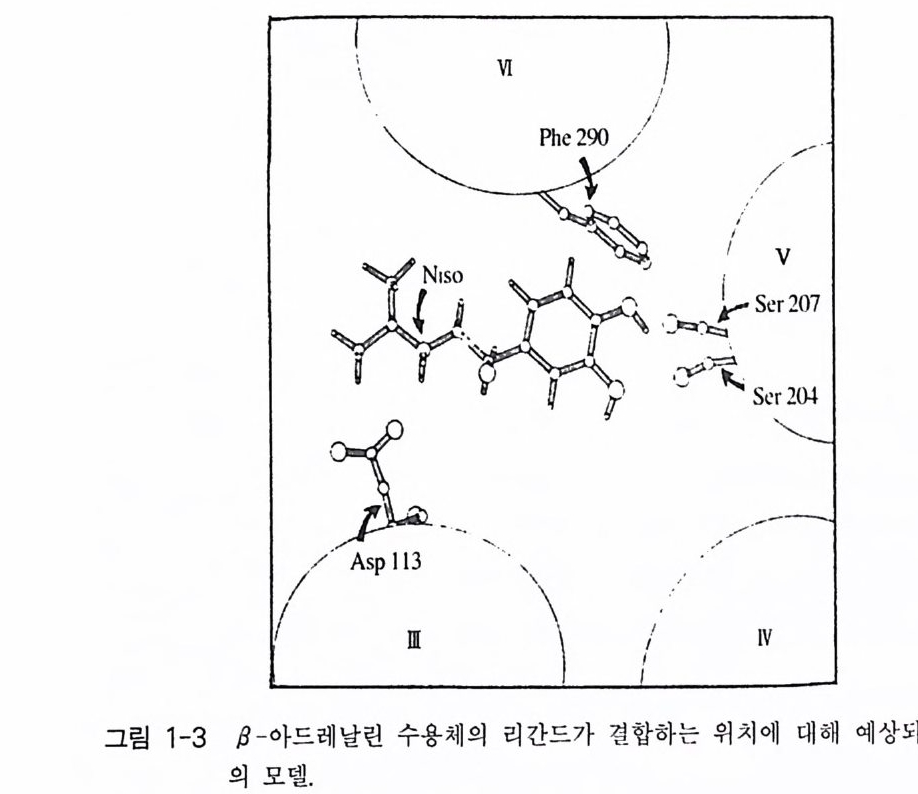
표 1 기 f3 - 아 드 래날린 수용체와 리간드 결합에 시스테인 잔기의 치환 효과 Muta n t KI,Ci(pYMP ) Iso Kp roo (nte Mr e) n o l fjA R 60 200 [Va l 771HAR 135 140 fVo l· l( 沿 l i 3An 100 50:3 0 000 IV al - I l 6] 1 3AR 130 60 [Va l 184 ] MR 70 3:2000 [Val U)() ]1 3A R n.d . 40: 9 000 [Val -19 J ll3A n n.d. 20:10000 D(2 ff il 40 10 [Va l 28.51 H AR n.d . 200 [Va l- 3 2 7]8 AR n.d . 300 [Val341)1 訥 R 120 200 D(371, 383, 395, 411 ) 50 300 는 최 대의 아데 닐 레이 트 시클라제의 활 성도 를 나타내기 위하여 iso p ro - t ere n o l 의 농도가 야생형 ( w i ld_ 유형)의 수용체와 비교하여 100 배 이상의 농도 가 필 요함 을 관찰하였다 . 그림 1 - 3 은 리간드가 결합하는 초보적인 모델을 표시하고 있는데, 아 고니스트인 iso p ro te r enol 주위에 막 투과 헬릭스 몇 개가 감싸고 있음을 볼수 있댜 구조적인 측면에서 한 가지 더 언급해야 되는 점은 B- 아드레날린 수 용체가 그 신호를 G - 단백질을 경유하여 eff ec to r 분자인 아데닐레이트 시클라제에 전달하게 되므로 반드시 8- 아드레날린 수용체의 경우 G- 단백질과 상호 작용하는 부위는 이 분자의 내부 친수성 루프 어딘가에 위치해 있다는 점이다 . 이 부위 를 알아보기 위하여 역시 결손 돌연변이 체를 제조하여 실험을 수행한 결과 N - 말단 부위의 절단으로 만들어진 돌연변이체의 경우는 G- 단백질과 결합하는 데 아무런 영향을 주지 않았
 ,,1' \ VI )
,,1' \ VI )
으며, C_ 말단의 경우 239-272 부위의 절단은 아데닐레이트 시 클 라제 ·읍 자극시키지 못함을 관찰하였댜 G- 단백질에게 신호 를 전달하는 또 다 른 수용체들에서 G- 단백질 접촉 부위는 아미노산 서열의 상동성이 /3-아 드레날린 수용체의 것과 비교할 때 상당히 적음을 보이는데, 이 부위의 홍미로운 성질은 양쪽성 성질의 a 헬릭스를 가지고 있다는 사실이다. /3-아드레날린 수용체의 경우 이 부위는 221-228 부분이다. 여러 가지 결손 돌연변이들이 아데닐레이트 시클라제의 활성도에 미치는 영향이 표 1 —2 에 표시되어 있다.
표 1-2 /3 - 아 드 레날린 수용체와 아데닐래이트 시 클 라재와의 짝지음에 영향을 미치 는 돌 연변이체 Muta n t l
 I 수용제 1
I 수용제 1
결과 Na + 의 세포 내로의 유입(infl ux) 이 금지되어 원형질막을 중심으로 과분극화 (h yperpo l ariz a ti on) 가 일어나게 된다. 막의 과분극화는 이 세포 와 연결되어 있는 신경세포로 빛의 신호를 전달하게 된다(그림 1-4). 로돕신이 광을 홉수하면 11-cis 레티날의 이성질화 반응(i some ri za ti on) 을 일으켜 all-tr an s 레티날로의 전환이 있게 되며 이로 인한 옵신의 3 차원적인 구조 변화가 유도되게 된다. 수용체의 이러한 구조 변화는 G- 단백질의 활성화로 연결된다. 로돕신의 아미노산 서열이 밝혀진 이래 (10) 이 수용체 단백질의 구조적 정보가 풍부해졌으며, 소수성 아미노산
들로 구 성된 7 개의 막 통과 헬 릭스 를 구성하고 그 가운데 부위에 존재 하 는 Ly s -2 9 6 잔기에 11- c i s 레티 날 색소가 pro to n ate d Sc hiff - b a s e 로 공 유 결 합되어 있음이 밝혀졌다(그림 1-5 ) . 34 8 개의 아미 노 산 잔기 들 로 구성되 어 있는 단일 폴리펩티드 인 이 단 백 질은 막 을 7 번 가 로 지 르는 막 결합 단백질로서, N- 말단은 디스크 내 부에 놓 이 게 되며 C - 말단은 세포질 쪽 에 위치한다 . C - 말단 부 위에 는 세 린과 트 래오닌 잔기의 아미노산 들 이 많은데 이 들 은 광선 조사 후 인 산 화가 되며 이 인산화 반응은 로돕신을 비활성화시키는 역할을 한다. 로돕 신이 광 옹 홉-수 한 후 G - 단백질 (Gr) 을 활성화시킬 수 있는 구조적
 트랜스 듀신, 로 놉- 신 키나 제 .
트랜스 듀신, 로 놉- 신 키나 제 .
으로 활성화된 상태까지 도달하기 위해서는 몇 개의 중간체 를 거치게 되는데 그 들 은 다음과 같댜 l0 - 1 2 초의 범위 내에서 ba t horhodop s i n 으로 바뀐 다음 이것은 10 - 9 초 범위에서 lu mi rhodo p s i n 으로 바뀌고, 이것은 10 - ( i초 범 위 에 서 meta r hodop si n I 으로, 10 선 초 범 위 에 서 meta r hodop si n II 로 바뀌며 수 분내에 이 것은 meta r hodop si n III 로 바뀐다. Mcta r hodop si n II 는 Sch iff-b ase 결합에 양성자가 떨어진 상태이며 레티날은 트 렌 스 형 으로 존재한다 Meta r hodop si n III 는 곧 옵신과 트 렌스 래티난 로 가수분 해되며 트랜스 레티날은 레티날 i somerase 에 의해 11 - 시 스 래티난로 바 뀌고 다시 옵신과 결합하여 원상태로 돌아가게 된다. 현재까지의 연구 결과에 의하면 cGMP 가 가수 분해되는 반응은 meta r hodop si n II 상태에 서 일어나는데, 이때 meta rho dop si n II 상태 를 R C 라고 부 르 며 이 상태는 27 kcaVmol 의 에너지를 저장하고 있다 (ll). cGMP 가 가수분해되는 반응은 활성화된 포스포디에스터라제에 의한 것인데, 포스포디에스터라제의 활성화는 활성화된 G1 가 일으키며, Gl 의 활성화는 활성화된 로돕신 (me ta II R) 에 의한 것이댜 로돕신과 meta II R 간의 활성화 에너지는 40 kcaVmol 로 보고되어 있는데, 이 사실은 빛이 없이는 G 를 활성화시킬 수 있는 로돕신이 만들어지기 어렵다는 것을 암 시하는 것이다. R • 가 G 와 상호 작용하게 되면 G1 와 결합되어 있던 GDP 가 떨어지게 되며, 로돕신 키나제가 결합하여 인산화 반응을 일으키게 된다(1 2). R 떠 세번째 세포질 쪽의 루프 부분이 G1 와 결합하는 데 중요 하다는 사실이 펩티드의 절단 실험(1 3) 과 돌연변이 실험(1 3) 을 통해 입 증되었다. R • 에 의한 G1 의 활성화 능력은 두 개의 단백질(로돕신 키나제 ; 68 kDa 의 세포질 단백질, arrestin ; 48 kDa 의 세포질 단백질)에 의해 무력화 되는 것으로 알려져 있다. 빛이 조사된 후 로돕신 키나제는 R • 의 세포질 쪽 부위에 결합하며 R • 의 C- 말단에 있는 세린과 트레오닌의 인산화 반 옹을 촉매화한다. Arres ti n 은 인산화된 R • 에만 결합하여 인산화된 R• 가
G 를 활성화시키는 능력을 현저하게 감소시킨다 (14, 15). Arres ti n 이 없을 경우 R . 가 완전히 바활성화되기 위하여 최소한 10 군데 이상이 인산화 되어야 하는데, 이것이 존재할 경우는 R * 가 2-3 군데만 인산화되어도 완 전히 비 활 성화되는 것으로 알려져 있다. 1-1-3 무스카린 아세틸콜린 수용체 무스카린 아세틸 콜 린 수용체 (Musc arini c Acety lc holi ne Recep tor : mAChR) 는 G 단백질과의 상호작용을 통하여 아데닐레이트 시클라제의 활 성 억제, 이노시 톨 인지질(p hos pho i nos iti de) 의 분해, 그리고 K 채널의 조절 등 다양한 세포 반응 들을 조절하는 것으로 알려져 있다. 이와 같이 다양한 생화학적 / 생리적 효과 를 나타내는 여러 종류의 무스카린 아세틸 콜 린 수용체들이 과연 존재할 것인가 하는 의문이 생기는데, 약리학 적 으로 분명하게 구별되는 무스카린 아세틸콜린 수용체들이 각기 다른 조 직에 존 재한다는 사실이 밝혀졌다. 길항자와의 친화력 차이에 따라 심장 조직에서 Ml(I ) 형과 M2(II) 형 그리고 소선(g landule) 에 존재하는 M3 (III) 형과 같은 것들이 있다. 신경계에 존재하는 대표적인 신경 전달 물 질이 아세틸콜린인데, 이 아세틸콜린의 수용체는 두 가지가 있다. 하나 는 무스카린 아세틸콜린 수용체이고 다른 하나는 니코틴 아세틸콜린 수 용체이며, 이들 수용체들은 분명한 구조적, 기능적 차이점을 가지고 있 다. 이들 수용체들이 존재하는 생체 내 부위도 서로 다르며, 니코틴 아세 틸콜린 수용체의 경우 운동 뉴런과 골격근에서 주로 발견된다. 무스카린 시냅스는 니코틴에 의해서는 영향을 받지 않으나 무스카린에 의해서는 활성화될 수 있댜 뇌 신경세포에는 무스카린 아세틸콜린 수용체가 니코 틴 아세틸콜린 수용체보다 상당량 많이 존재하기 때문에 무스카린 아세 틸콜린 수용체는 주로 뇌 세포에서 클로닝되었다. 무스카린 아세틸콜린 수용체의 DNA 를 cDNA li br ary로부터 찾아내기 위한 olig o nucleoti de
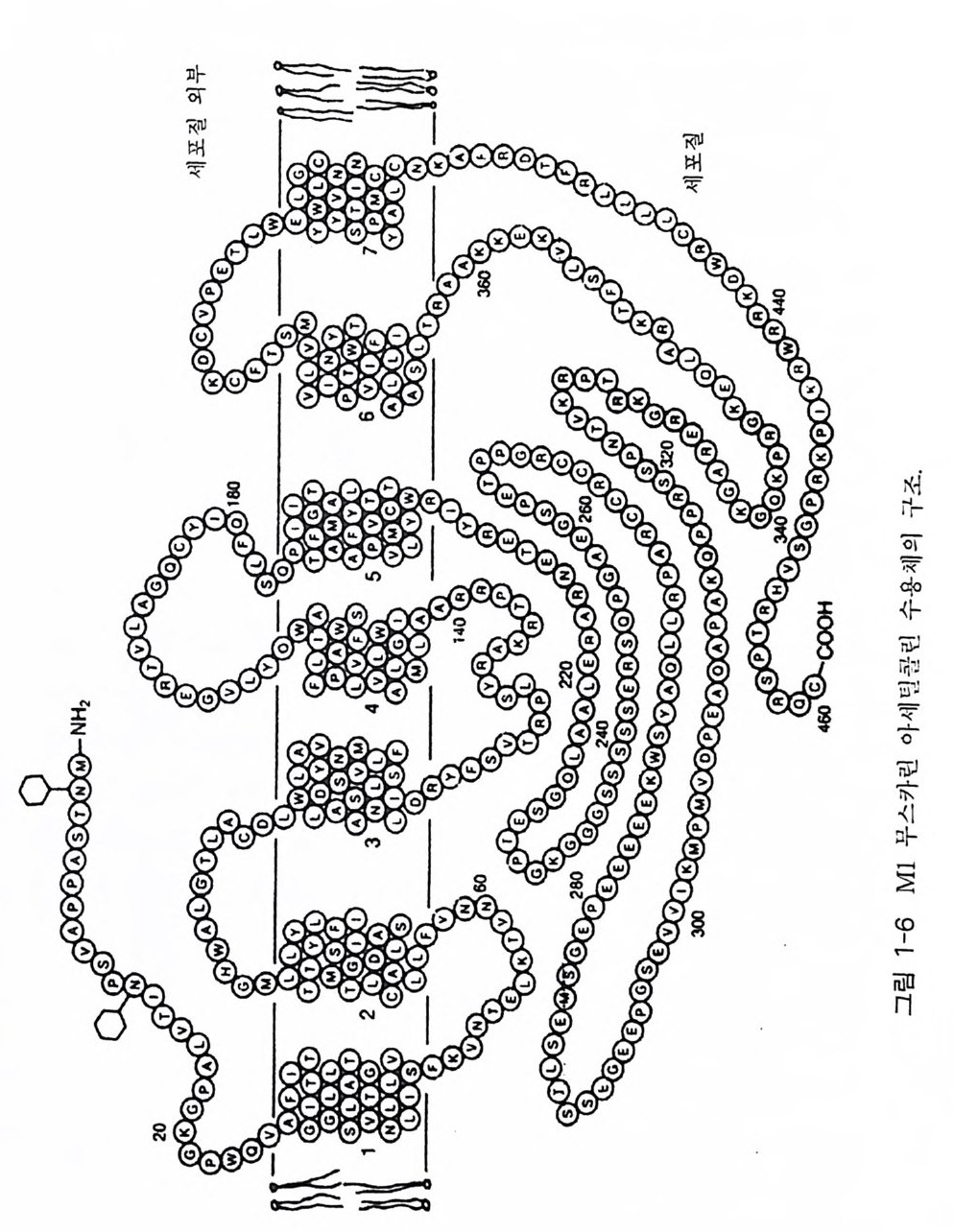
p rob e 을 만든 후 무스카린 아세 틸콜린 수용체의 cDNA 를 클로 닝하 고 이것을 개구리 난세포 (Xenop u s ooc yt e) 에 집 어 넣고 발현시켜 4 가지 유 형의 무스카린 아세틸콜린 수용체 를 얻었다. lVIl, M2, M3, 1\1 4 의 4 가지 유형의 무스카린 아세틸 콜 린 수용체는 항위궤양 약의 한 가지 종류 인 piren zepi ne 및 그 유도체 들 과 각각 다 른 친화력을 갖는다. Ml 무스카 린 아세틸콜린 수용체의 경우 pi renz e pi ne 과 매우 큰 친화력운 갖는 대, 개구리 난세포에서 발현된 무스카린 아세 틸콜린 수 용체의 경우 이 억 제제와 강하게 결합하는 것으로 보아 M1 무스카린 아세 틸안린 수용체 임을 확신할 수 있었다 . Ml 무 스 카린 아세 틸콜린 수용재 는 분 자량이 51. 4 kDa 이었으며 460 개의 아미노산으로 구성되어 있는 것으로 밝혀졌 댜 한 가지 부가할 사항은 전체 분자 질량 의 26% 가 넘는 탄수화물 군이 이 단백질에 결합되어 있다는 것이다. 통상적으로 이용하 는 소수성 분석 방법에 의하면 이 분자는 막을 7 번 통과하는 a - 헬릭스 를 가지고 있으 며, 삼차원적 구조는 f3 _ 아드레날린 수용체의 것과 유사한 점을 가지고 있다. 이 분자의 N- 말단은 막의 외부에 위치하며 두 개의 N - 글 리코실화 부위를 가지고 있다. c- 말단의 경우 세포질 쪽에 위치해 있으며 인산화 반응에 참여할 수 있는 많은 세린과 트레오닌 잔기들이 이 부위에 위치 해 있다(그림 1-6). 무스카린 수용체들은 G 一단백질과 상호 작용을 함에 있어 그 양상이 /3-아드레날린 수용체들과 유사하다. 돼지의 Ml 무스카린 아세틸콜린 수용체의 경우 G - 단백질의 ai( in hibi t ory) 소단위체를 활성화시켜 아데 닐레이트 시클라제의 활성을 억제시키며, 다른 유형의 무스카린 아세틸 콜린 수용체들을 as(sti mu lato r y) 소단위체를 활성화시켜 아데닐레이트 시클라제의 활성도를 올려 주는 것으로 알려져 있다 . 아데닐레이트 시클 라제에 대한 이들의 다양한 효과들은 세포 내 cAMP 의 양을 조절하게 되며 c Mv!P는 세포 내에서 제 2 의 전령으로서 그 역할을 수행하게 되는
것이다. cAMP 를 통한 신호는 단백질 인산화 반응으로 이어지 는 데 , 예 를 들면 K 의 막 투과 정도의 변화 를 수반하며 그 결과는 신경 세포막의 막전위 를 조절하게 되는 것이다. 돼지의 심장 근육에 존재하는 M2 형의 무스카린 아세틸 콜린 수용체 도 클로닝되었고 분석되었다 . 이 분자는 Ml 무스카린 아세 틸콜린 수용체보다 약간 크며 466 개의 아미노산으로 구성되어 있다 . M1 형과 같이 막을 7 번 가로지르는 특 성 을 가지고 있으며 아미노산 서연도 Ml 것과 매우 유사하다 (82 % 의 상동성을 가지고 있 음). M2 무스카린 아세 탄 콜린 수용체도 G — 단백질과 상호작용을 하는데, 그 작용 매커니 즘은 약 간 다른 것으로 알려 져 있다. 전체 복합체 (GTP - G - p ro t e i n - mAChR ACh) 는 K 채널과 상호작용을 하며, 그 후 GTP 는 GDP 로 가수분해되고 무스카린 아세틸콜린 수용체 - G - 단백질 복합체는 분리되며 K 채널은 닫히 게 된다(그림 1-7). 무스카린 아세틸콜린 수용체들의 경우 막 횡단 부위의 아미노산 서열 에 높은 상동성을 가지고 있기 때문에, 이들 cDNA 를 클로 닝하기 위한 olig o nucleoti de p robe 는 아미노산 서열이 보존되어 있는 이 부분에 대하 여 만들어 사용한다. G- 단백질과 상호 작용하는 무스카린 아세 틸콜린 수용체들은 다양한 효과를 나타낼 수 있는데 아직 이 들 효과의 정도는 명확히 설명되고 있지 못하다. 그러나 다양한 수송로의 이온 운송 능력 을 조절할 가능성과 숙주 세포의 대사 작용에 변화 를 야기시 킬 가능성 이 많을 것으로 예상된다. l-2 채널과 연결되어 있는 수용체 채널과 연결된 수용체 (Channel-l i nked Rece pto r) 는 다론 말로 표현하 면 리간드에 의해서 문이 열리고 닫히는 수송로(lig and-g a t ed channel) 라
 Ai C h
Ai C h
고 하 는 데 , 이 부류에 속하는 대표적인 수용체 둘은 니코틴 아세 틸콜린 수용체와 GABA 수용체( r-am ino buty ric acid recep tor ) 그리고 글리 신 수용체가 있댜 이들 채널의 개페는 리간 드 분자에 의해 조절 되 는 데 이 온의 흐름은 농도 구배가 생성되는 방향으로 진행된다. l-2-l 니코틴 아세틸콜린 수용체 (nAChR) 1906 년 Lan g le y는 근육 수축에 미치는 니코틴의 효과 실합 에서 니 코 틴과 결합하는 어떤 수용체가 있는데 그것은 근육 수축 물질은 아 닐 것 이라는 생각을 했었다. 그 후 65 년이 흘 러 신경 전달 물질 인 아세 틸콜린 에 대한 니코틴 수용체가 분리되었고, 오 늘날 이 단백질의 일차 구조가 밝혀졌댜 이 단백질은 막을 관통하는 오량체 ( a2 /3 r o ) 4 개가 모여서 구성된 제어 (allos t e ri c) 단백질이다. 이 단백 질 은 a 소단위체에 두 개의 아세틸콜린 결합 자리가 있으며 이온 채널을 포함하고 있다. 4 개 소단위 체의 아미노산 서열이 밝혀져 있으며 이 단백질의 경우 3 차원적 구조 의 변화를 통하여 이온 채널의 열림이 조절되고 다양한 부류의 약리학적 활성을 갖는 리간드들에 의해 입체 형태가 변화된다. 니코틴 아세틸콜린 수용체가 가장 많이 존재하는 곳은 전기메기 또는 전기뱀장어 등과 같은 전기를 발생시키는 물고기들의 발전판 (elec tro p lax) 이댜 이들 발전판의 pos ts y n a pt ic 막을 전자 현미경으로 관찰해 보면 매우 높은 밀도로 니코틴 아세틸콜린 수용체가 존재하는 것으로 알려져 있다. 따라서 니코틴 아세틸콜린 수용체에 관한 최초의 분자 생 물학적 연구는 이들 발전판들이 많이 이용되었다. 니코틴 아세틸콜린 수 용체의 정제를 위하여 친화성 크로마토그래피에 리간드로 많이 이용했 던 분자들로는 뱀에서 추출되는 신경 독성 펩티드 (na j a t o xi n 과 a -b ung aro toxin)들을 꼽을 수 있다. 이들 신경 독성 물질들은 니코틴 아 세틸콜린 수용체에 특이하게 결합하기 때문에 이들( a-BuTX 또는
 。
。
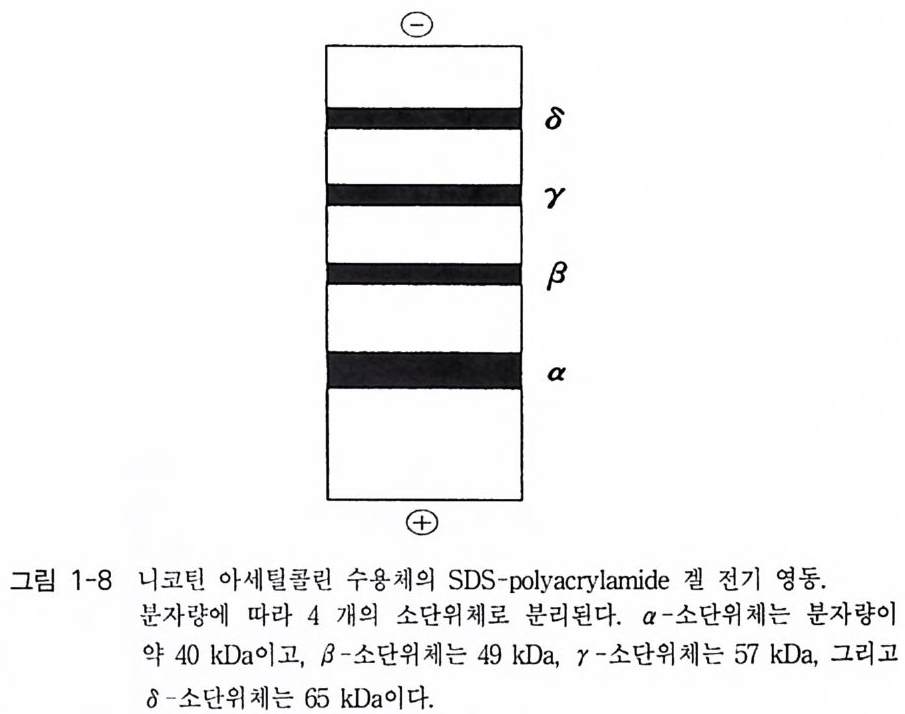
cobra TX) 을 리간 드로 이용한 친화성 컬럼 크로마토그래피 방법으로 니 코틴 아세틸 콜린 수용체를 정제할 수 있게 되는 것이다 . 이러한 방법으 로 발전판의 니코틴 아세틸콜린 수용체를 분리한 후 SDS-PAGE (sod ium dodecy l sulfa te poly a c ry la m ide gel elec tr op hores i s) 를 실시해 보 면 4 개의 띠 (a, /3, r, o) 가 나타난다(그림 1-8 ) . 이렇게 정제된 니코틴 아세틸콜린 수용체로 부터 아미노산 서열을 부 분적으로 밝혀 olig o nucleoti de p robe 을 만들고 그 p robe 을 cDNA 클로닝 에 이용하여 이 단백질의 일차 구조를 밝힌 바 있다. 분리한 cDNA 를 개구리 난세포 (Xenop us ooc yt e) 에 넣고 니코틴 아세틸콜린 수용체를 발 현시키는 데 성공하였다. 니코틴 아세틸콜린 수용체가 제대로 만들어졌 는지 알아보기 위하여 난세포 막을 분리하여 전기 생리적 방법을 이용 하여 아세틸콜린 수용체의 기능을 점검하거나, 전기메기의 발전판으로
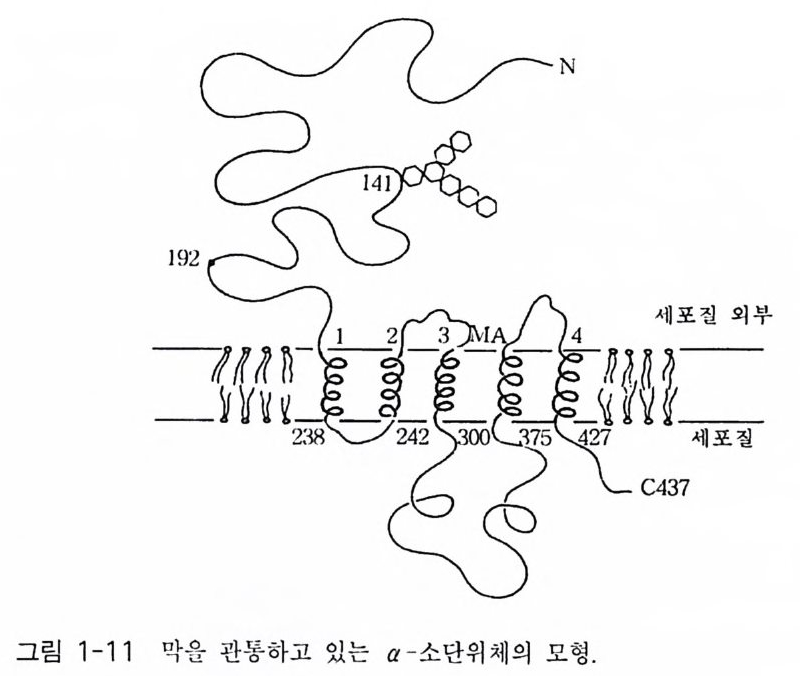
부터 정제한 니코틴 아세틸콜린 수용체와 함께 SDS 一 PAGE (SDS- poly a c 1')'la m ide ge l elec tr o p hores i s) 에 걸어 그 위 치 를 비교합으로써 확인 하였다. 전기메기의 니코틴 아세틸콜린 수용체는 분자량 268 kDa 의 다 량체 단백질이며, 5 개의 소단위체 (a2 /3 r 8) 로 구성되어 있다. 척추 동 물에서 지금까지 발견된 니코틴 아세틸콜린 수용체의 경우 모두 5 개의 소단위체로 구성되어 있는데, 쥐의 뇌에서 발견된 니코틴 아세틸콜린 수 용체의 경우는 5 개의 소단위체가 a3 f32 로 구성되어 있다. 사람, 송아지, 전기메기의 니코틴 아세틸콜린 수용체 a 소단위체의 아미노산 서열이 그림 1-9 에 표시되어 있다. 이들 아미노산 서열을 비교해 보면 상당히 높은 아미노산 서열의 상동성을 가지고 있다. a 소단위체의 경우 소수 성 아미노산 집단의 위치가 모두 비슷하며(그립 1- 10 ), 그 사실은 한 조 상의 유전자로부터 이들이 진화되었을 가능성을 나타내는 것이다 . 소수 성 아미노산 집단의 위치는 각 소단위체들의 어느 부위가 막에 묻혀 있 는지를 말해 주는 것이다. 이 분자의 N- 말단은 세포의 밖에 위치하며, 막을 관통하는 횟수는 5 회이고 주로 소수성 아미노산 집단이 a- 헬릭스를 형성하며 막을 관통 하고 있다(그림 1-11). C- 말단은 세포 내에 존재하고 있으며, 5 개 소단위 체 모두는 유사한 소수성 아미노산 집단을 가지고 있고 그들은 유사한 양상으로 막을 가로지르고 있다. 5 개의 소단위체가 어떻게 배치되어 있 는가 하는 문제가 관심사인데 전자 현미경의 영상 분석 결과에 의하면 G 대칭 구조를 가지고 있는 것으로 나타났다. 1-2-2 니코틴 아세틸콜린 수용체의 기능 막 채널의 기능에 관한 연구를 위하여 최근에 몇 가지 기술들이 개발 되었는데 이들을 이용하여 니코틴 아세틸콜린 · 수용체의 성질에 관한 연 구들이 활발히 진행되어 왔다. 정제된 니코틴 아세틸콜린 수용체를 리포
 L 2 61으 1 .II t ·T·로군TSLGAELCLHREALKVV三vG恒VPVEE구HTvsfOVDVARLaO『A NL LT람V사H OVOIL닐OY l :OLlVVVH I E1O iSL!C오:U!LA_'-L- -G브모IKV ,LR T ELGVI.FE S학ELVSVRH D'I소LVTE EV VI9LNL `GdOVNKOENYITLTORVVOL; V\IQ Q SGViHELE上l군L군t조T효仮k핀 덜 .召m6”v云 느 T의므 TTGV전TT 견덴T」a/lo 고공며3브브cam. ltI'cf L만1 O VCV aNEO RL LIL t g OL ' Og眞LKT맥V TVIOVYLDG/EF1FPH5rK판Gm下늄志 VT I SIPOK HVLUE FYSKCIlI((( I OGT”C 'IVGO D UVLD'“(A0 G 'VLF TSFmTT T(PIGXXTLMLVOHFGClEKPI SCOVEFFTIHWTTISSI V1PODEWTNP G9l(TI(Q .: I!.G0'K五-O노恥TkI§.띠!호.편Y.G .FD0ALVALm G Y9lLa죠TA”다VTI쿄T 5으d죠으밉뜨그브기모Rh품#컬 군프으됴오 ICE! I SXYFs- s zoo m.I •'g .,OLDCTTTl PYPNF LIL I PVI F.YC\ PLVIHRSIfVISTLLGIEGSTVLPLFKFYSV T DIVTLLSVLL FLQ D 전LPYCTTIVI,YHICLFLY 1,LSNT1FG LFVVPSTLLSTGELSPnLYYLHKVIS VL l'l TOPCD mT(T FFSLLC 1v위lV떠~m1,HGLlTLSIEKSGD TV.IPmIT SV _V._lTVL lLlSVL F I 1M •M 2 '’ l mo, nMoo ltiiAHH”杓IIHVfBV(IK1EvhIYdL,VAsI '.It pmmIsFII'P O 1D Kc0S KKID OS IKIHr SIIGPmsTHHsI(VVN門IVIHrF HGSIFII門S P K GIS FmYK I'GST}S . IVITI I IS'AIVITV IF' I PTIIFO ImsDTE1FDKO SEICRD I` PS OI( I( ,3-w, , gI'Lss,T여I S晶kvY며TFL연I(G w HHTH F 띄므EZh* ''mT전SFF뉴&P프고따 도브 흐n브다fIlOgI I iSGq단. I1안SOQ전)I(닌O TIO 1 e n L ...KSVEPHI • M:E 0SXCTI A YIKG3 IES AIvA :CLVIIFV‘U I LHDImIIVL GRVFiATLI G O1GOLAMI EI( KS EPHCV llC.LL'덱VL AASN£00KSNETIAT IICG I NEAV1CE: I HIIDI£IVATL G R.9FATLI G I GOAOLNI Eil 소골IAS(IL.!:효. 'YH”“ 됴_ 곡1토 브 Kn AF四『mEL1GR 루 4M' '9-1 림그 o)deprTo(기메기전소,아 틴코니 의람사 와세린소콜틸-a 체용수 단 위 의체.열서 산노미아
L 2 61으 1 .II t ·T·로군TSLGAELCLHREALKVV三vG恒VPVEE구HTvsfOVDVARLaO『A NL LT람V사H OVOIL닐OY l :OLlVVVH I E1O iSL!C오:U!LA_'-L- -G브모IKV ,LR T ELGVI.FE S학ELVSVRH D'I소LVTE EV VI9LNL `GdOVNKOENYITLTORVVOL; V\IQ Q SGViHELE上l군L군t조T효仮k핀 덜 .召m6”v云 느 T의므 TTGV전TT 견덴T」a/lo 고공며3브브cam. ltI'cf L만1 O VCV aNEO RL LIL t g OL ' Og眞LKT맥V TVIOVYLDG/EF1FPH5rK판Gm下늄志 VT I SIPOK HVLUE FYSKCIlI((( I OGT”C 'IVGO D UVLD'“(A0 G 'VLF TSFmTT T(PIGXXTLMLVOHFGClEKPI SCOVEFFTIHWTTISSI V1PODEWTNP G9l(TI(Q .: I!.G0'K五-O노恥TkI§.띠!호.편Y.G .FD0ALVALm G Y9lLa죠TA”다VTI쿄T 5으d죠으밉뜨그브기모Rh품#컬 군프으됴오 ICE! I SXYFs- s zoo m.I •'g .,OLDCTTTl PYPNF LIL I PVI F.YC\ PLVIHRSIfVISTLLGIEGSTVLPLFKFYSV T DIVTLLSVLL FLQ D 전LPYCTTIVI,YHICLFLY 1,LSNT1FG LFVVPSTLLSTGELSPnLYYLHKVIS VL l'l TOPCD mT(T FFSLLC 1v위lV떠~m1,HGLlTLSIEKSGD TV.IPmIT SV _V._lTVL lLlSVL F I 1M •M 2 '’ l mo, nMoo ltiiAHH”杓IIHVfBV(IK1EvhIYdL,VAsI '.It pmmIsFII'P O 1D Kc0S KKID OS IKIHr SIIGPmsTHHsI(VVN門IVIHrF HGSIFII門S P K GIS FmYK I'GST}S . IVITI I IS'AIVITV IF' I PTIIFO ImsDTE1FDKO SEICRD I` PS OI( I( ,3-w, , gI'Lss,T여I S晶kvY며TFL연I(G w HHTH F 띄므EZh* ''mT전SFF뉴&P프고따 도브 흐n브다fIlOgI I iSGq단. I1안SOQ전)I(닌O TIO 1 e n L ...KSVEPHI • M:E 0SXCTI A YIKG3 IES AIvA :CLVIIFV‘U I LHDImIIVL GRVFiATLI G O1GOLAMI EI( KS EPHCV llC.LL'덱VL AASN£00KSNETIAT IICG I NEAV1CE: I HIIDI£IVATL G R.9FATLI G I GOAOLNI Eil 소골IAS(IL.!:효. 'YH”“ 됴_ 곡1토 브 Kn AF四『mEL1GR 루 4M' '9-1 림그 o)deprTo(기메기전소,아 틴코니 의람사 와세린소콜틸-a 체용수 단 위 의체.열서 산노미아
 A;.‘.,:.,• .•’'g. I V 널 ,'m息쿨 EE『臨 一 ‘L FAmoDA'-l』I.꿀홉 l藍, F ,..i.E* 곳젭 s로'u-gi돈v 舞r**庄4 I, •`l`, •L .'•짬v 썹 · 젭Og·^ •,ID‘l눌4I Yss.F . 麟 DS I.’ 풀五屈csOyL ELC,•E 록. CInL .:g. E iLEl.Q,D ‘S FV ..s V짧 一.‘QD.,: F ...C‘· 昌. 됴홉 V ..‘ S . is 空묘윤 .· 홉A ·릅I s .Vc.l華V l일.;'.E ` 뽑‘l -l .m E툴9.콥 홍 꿉꾼• 똘正•$ v.gm'. .圭^ F 重I ·—.I.•..,.LI..•. ' : 턴 .'민셉F. ..s g . .· ..- .•..-. .· 옹.. .’.- . ·홉 ..먄 O ..E.l.i I'.,v..s』 9i仲 머.'.』v Irkk r ~ VrKI·. T습 crTnI`''』 KD”,S•ssD I 鴻溫L.溫 5유O H sD 널MKR o I VN.^E Vr I.. ...“E v-m,. . ..I”.-V - • 콥 .A • I vr, .. .v ·. I·.l 墨L0 . .E홉 s. 겹 E 훑gi 습·엿 맵V 'K§lsI LC•cC0 뜹..•I 묘 T .붙 '.tD0,vk. 1 s· T,.I,; .t. ;윤ltS덟 S •'l•.E Mt t• T DS째 죠쌉 언 맣 ..,...뺀.... ,겁겁 . ..,...`. .• :••LsL-.. ·—•• -`.•·'0 .L- :.• 0圭 . -·.` -.‘ ;훑 됴 M-.유 '.2.; . ,,,,'.' — 풀中.. 'm‘ g. I ‘ I IS 'm 15
A;.‘.,:.,• .•’'g. I V 널 ,'m息쿨 EE『臨 一 ‘L FAmoDA'-l』I.꿀홉 l藍, F ,..i.E* 곳젭 s로'u-gi돈v 舞r**庄4 I, •`l`, •L .'•짬v 썹 · 젭Og·^ •,ID‘l눌4I Yss.F . 麟 DS I.’ 풀五屈csOyL ELC,•E 록. CInL .:g. E iLEl.Q,D ‘S FV ..s V짧 一.‘QD.,: F ...C‘· 昌. 됴홉 V ..‘ S . is 空묘윤 .· 홉A ·릅I s .Vc.l華V l일.;'.E ` 뽑‘l -l .m E툴9.콥 홍 꿉꾼• 똘正•$ v.gm'. .圭^ F 重I ·—.I.•..,.LI..•. ' : 턴 .'민셉F. ..s g . .· ..- .•..-. .· 옹.. .’.- . ·홉 ..먄 O ..E.l.i I'.,v..s』 9i仲 머.'.』v Irkk r ~ VrKI·. T습 crTnI`''』 KD”,S•ssD I 鴻溫L.溫 5유O H sD 널MKR o I VN.^E Vr I.. ...“E v-m,. . ..I”.-V - • 콥 .A • I vr, .. .v ·. I·.l 墨L0 . .E홉 s. 겹 E 훑gi 습·엿 맵V 'K§lsI LC•cC0 뜹..•I 묘 T .붙 '.tD0,vk. 1 s· T,.I,; .t. ;윤ltS덟 S •'l•.E Mt t• T DS째 죠쌉 언 맣 ..,...뺀.... ,겁겁 . ..,...`. .• :••LsL-.. ·—•• -`.•·'0 .L- :.• 0圭 . -·.` -.‘ ;훑 됴 M-.유 '.2.; . ,,,,'.' — 풀中.. 'm‘ g. I ‘ I IS 'm 15
 N
N
솜 이나 지질 이중층에 끼워 넣고 이것의 생리적 성질들을 용액 상태에 서 접검 하였다. 패치 크램프를 이용하여 난세포 막에 존재하는 니코틴 아세 틸콜린 수용체의 기능에 관한 연구도 진행된 바 있고, 생화학적 방 법이나 전자 현미경을 이용하여 a-bun g aro t ox i n 이 결합하는 소단위체 의 결합 부위를 찾아내기도 하였다. 최근에는 돌연변이 실험 방법을 이 용하여 니코틴 아세틸콜린 수용체의 기능과 구조에 관한 연구도 많이 진행되고 있다. 상기에 기술한 방법들이 채널 단백질을 연구하는데 매우 중요하기 때 문에 다음에 이들에 관하여 간단히 그 내용을 살펴보기로 한다. 리포솜 (l ip osome) 지질은 그 양쪽성 성질 때문에 리포솜을 쉽게 만 들 수 있는데, 단일층의 리포솜을 만들어 니코틴 아세틸콜린 수용체를 결합시키기에는 너무나 약하기 때문에 다중충 리포솜을 만들어 니코틴
 그림 1-12 리포솜과 니코틴 아세 틸콜 린 수용체 들 의 결합
그림 1-12 리포솜과 니코틴 아세 틸콜 린 수용체 들 의 결합
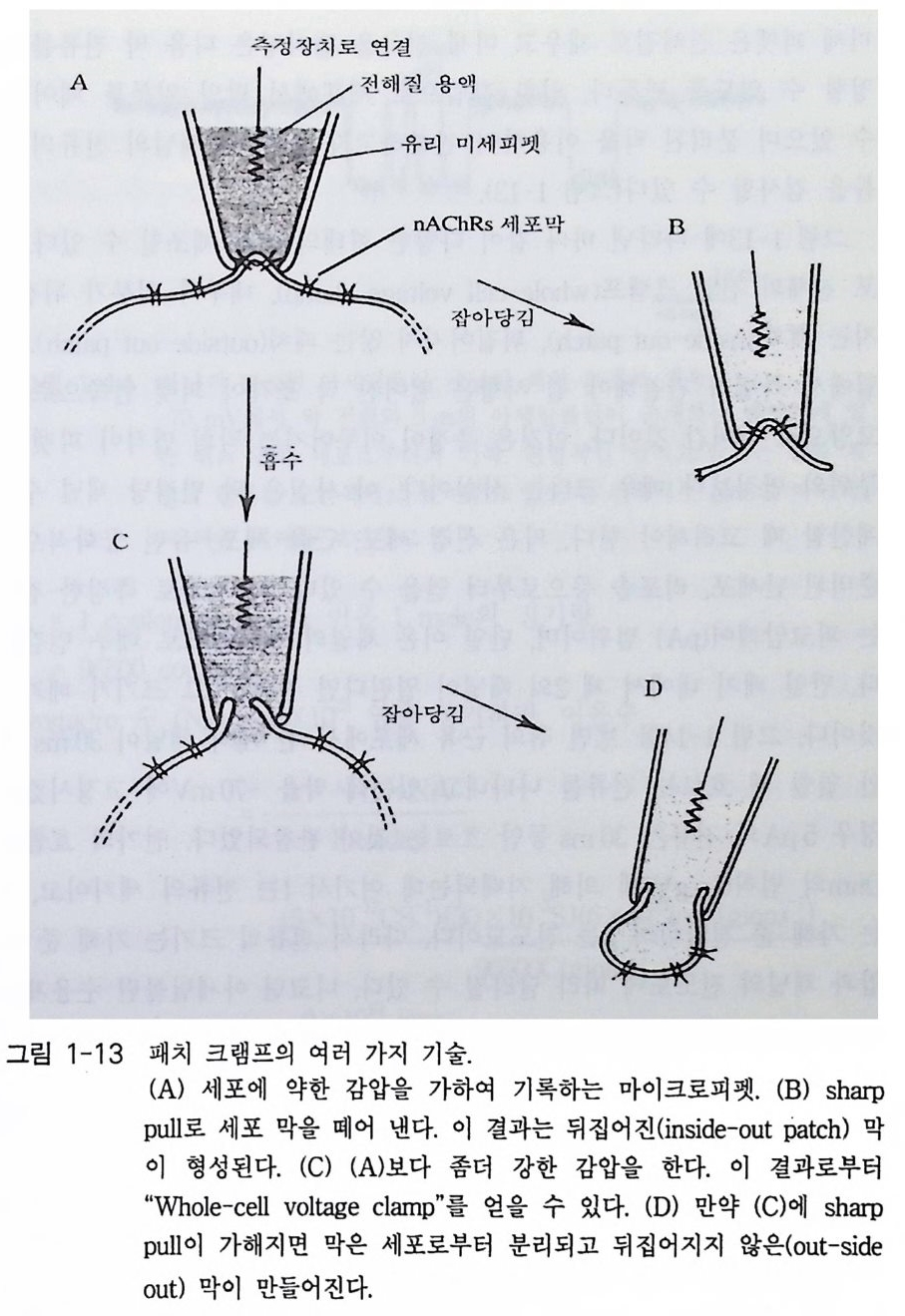
아세틸콜린 수용체를 결합시켜 사용하고 있다(그림 1-12). 대부분의 경우 니코틴 아세틸콜린 수용체들은 a-bung a roto x in 결 합 부위가 밖을 향하도록 리포솜에 결합한다. 아세틸콜린을 리포솜 현탁액 에 첨가하면 Na 떠나 K 져 방출되는데 , 만일 아세틸 콜 린의 길 항자인 tub ocurar ine 같은 화합물을 첨가하면 아세틸콜린에 의해 방 출 되던 이온 들이 더 이상 방출되지 않는다. 물론 리포솜에 결합된 채널 들 은 패치 크 램프로 점검할 수도 있다. 패치 크램프 기술 이 기 술은 1976 년 Erw in Neher 와 Bert Sakmann 에 의해 개발되었으며 이온 채널의 생리적 성질들을 연구하는데 획기적인 공헌을 하였다. 이 기술을 이용하여 생리학자들은 하여금 단일 채널 을 통한 이온의 흐름을 조사할 수 있었다. 이 기술의 핵심은 유리 미세 피펫(끝의 직경이 0.5 µm)을 관심 있는 막에 부착시키는 것이다. 피펫의 끝과 막 사이의 봉합이 매우 높은 저항 (lOG Q)을 갖도록 만들어야 한다.
 측정장 치 로 연 결
측정장 치 로 연 결
미세 피펫은 전해질로 채우고 미세 전극을 집어넣은 다음 막 전류 를 측 정할 수 있도록 만든다. 약한 감압으로 세포에서 막의 일부 를 떼어 낼 수 있으며 분리된 막을 이용하여 관찰하고자 하는 막 체널의 전류의 흐 름을 검사할 수 있다(그림 1-13). 그림 1-13 에 나타낸 바와 같이 다양한 형태의 계 를 제조합 수 있다. 세 포 전체의 전압 크램프 (whole - cell voltage clamp ), 내부와 외부가 뒤 집어 지는 패치(i ns i de-ou t patch ), 뒤집어지지 않는 패치 (ou t s i de - ou t patch ). 그 림에서 특별히 관찰해야 될 사항은 떨어진 막 조각이 피팻 안쪽으로 요 모양으로 들어간 것이댜 이것은 측정이 이루어지는 막의 면적이 피팻 끝 부위의 면적보다 매우 크다는 사실이다. 이 사실은 막 면적당 채널 수를 계산할 때 고려해야 한다 막은 신경 세포, 근육 세포, 유전 공학적으로 준비된 난세포, 리포솜 등으로부터 얻을 수 있다. 이 기술로 측정한 전류 는 피코암페어(p A) 범위이며, 단일 이온 채널의 개폐이므로 매우 민감하 다. 만일 패치 내에서 제 2 의 채널이 열린다면 전류는 그 크기가 배가될 것이다. 그림 1-14 를 보면 쥐의 근육 세포에서 한 개의 채널이 30ms 동 안 열릴 때 흐르는 전류를 나타내고 있는데 막을 -70mV 에 고정시켰을 경우 5 p A의 전류가 30ms 동안 흐르는 것이 관찰되었댜 전기의 흐름은 Ohm 의 법칙 (I= g V) 에 의해 지배되는데 여기서 I 는 전류의 세기 이고, v 는 가해 준 전압이며 g는 전도도이다 따라서 전류의 크기는 가해 준 전 압과 채널의 전도도에 따라 달라질 수 있다. 니코틴 아세틸콜린 수용체의 경우 수송로가 열리는 빈도가 가해 준 아세틸콜린의 양에 의존한다. 그림 1-14 의 경우 채널이 열렸을 때 움직이는 이온의 개수를 계산할 수 있다.
 三
三
lA = 1 coulomb/s ec, 1 가 이온 1 mole 의 전기 량 = 96500 coulomb, Avog a dro 수 (N 사 = 6 X 1023 임 을 상기 하면, 이 온수 AX 시간 X NA 1 Faraday = (5 X 10-12CS-1)(309 X65 1000-C3S(g)( i6o Xn 1r0l 23io n s(gi on f 1) = 9Xl010 ion s 9.6Xl04 = 1 x 106 ion s 이 계산치는 정상적인 신경 세포막에서 단일 니코틴 아세틸콜린 수용 체에 의해 조절되는 채널을 통하여 일어나는 정상적인 이온 수에 비하여 매우 크다. 이온의 흐름은 전압의 크기에 의존성을 나타내는데; 어떤 주
어진 이온에 대하여 전압은 막 전위 (Vm) 와 Nemst 전위 (V, )의 차이이다. 이 차이는 막이 방전됨에 따라 감소하게 되며, 따라서 생리적 조건에서 l 가 이온들의 흐름을 윗식으로 계산한 것보다 몇 배 작게 나타난다. 생화학적, 전자 현미경적 기술 생화학적 기술과 전자 현미경적 기 술들 은 수용체에 아세틸콜린의 결합 부위 를 결정하는 좋은 수단이다. 가장 보편적인 방법은 a-bun g aro t o xi n 을 사용하는 경우인데, 이 아세틸 콜 린 길항자는 수용체 a- 소단위체에서 아미노산 서열이 185- 19 6 번째에 결 합하는 것으로 밝혀졌다. 특히 192- 19 3 번째 위치한 시 스 테인 잔기 들 이 결합에 결정적 역할을 한다고 보고되었다. 전자 현미경적 기술은 아세틸콜린 결합 부위 를 알아볼 수 있게 해주 며, a-bun g aro t o xi n 의 존재 유무에 따른 신경 세포막에서 니코틴 아세 틸콜린 수용체의 전자 현미경 사진을 찍어 컴퓨터 처리를 통하여 독소 의 위치를 알아볼 수 있으며, 아세틸콜린 결합 부위에 독소가 위치한다 는 사실로부터 전자현미경 영상에서 이들 소단위체들의 위치 를 유추 할 수 있다. 니코틴 아세틸콜린 수용체의 채널은 두 개의 아세틸콜린 분자 가 결합해야만 열리는데, 첫번째 아세틸콜린 분자가 a- 소단위체의 결합 부위에 결합하면 두번째 a- 소단위체에 또 다른 아세틸콜린 분자의 결 합 확률을 증가시키기 위한 입체 구조 변화를 유도시킨다고 보고되어 있다. 두 개의 아세틸콜린 분자들이 니코틴 아세틸콜린 수용체에 결합하 게 되면 다시 한 번 이 수용체의 입체 구조 변화를 일으키게 하여 채널 을 순간적으로 열어 주게 되며 이온들이 흐를 수 있게 한다. 1-2-3 GABA 수용체 척추동물의 중추 신경계들에서는 두 개의 중요한 저해 기능적 전달 매체들 [r- ami nobu tyri c aci d (GABA) 와 글리신]이 발견되고 있다. 이들
두 가지 경우 모두 작은 음이온 채널을 조절함으로써 그들의 효과를 나 타낸다. 이들이 er 채널을 열어 줄 경우 막의 과분극화 현상이 유발된 댜 GABA 수용체의 경우 두 개의 뚜렷한 유형이 있는데, 하나는 GABAA 수용체 유형으로서 subsyn a p tic 막에 위치해 있는 것으로 믿어 지 며 , 다 른 하나는 GABAB 유형 으로써 pre syn a pt ic 막에 위 치 해 있다. GABAA 수용체가 직접 다 채널을 조절함으로써 그 기능을 발현시키는 반면, GABAll 수용체의 경우는 G- 단백질을 통한 충돌-결합 메커니즘 (coll i s i on 一 cou p li n g mechan i sm) 을 통하여 그 기능을 발현하는 것으로 알 려져 있댜 이 절에서는 GABAA 수용체 하나만 언급하고자 한다. GABAA 수용체 유형의 약리학적 연구는 많이 진행되어 있는 편이다 이 수용체의 경우 적어도 4 가지 약물의 결합 부위를 가지고 있는데, 그 들 은 GABA, benzodi az epi ne s, picr oto x i n, 그리 고 barb iturat e 이 다. 니 코틴 아세틸콜린 수용체를 a - t o xi n 을 이용한 친화성 칼럼 (a ffinity column) 을 이용하여 정제하는 것과 마찬가지로 GABAA 수용체의 경우 benzo- diaz epi ne 컬럼을 사용하여 정제할 수 있다. 정제된 GABAA 수용체의 경 우 두 개의 a- 소단위체 (48,800 Da) 와 두 개의 /3-소단위체 (51,400 Da) : a 2 f3 2 로 구성 되 어 있다. 이 두 개 의 소단위 체 들은 olig o nucleoti de pro be 을 만드는 데에 사용되었고 소의 대뇌 피질 cDNA li b rari es 를 선별하는 데 사용되었다. 선별된 cDNA 로부터 이들 두 소단위체들의 아미노산 서 열을 분석한 결과, a- 소단위체의 경우 429 개의 아미노산으로 구성되어 있으며, /3-소단위체의 경우 449 개의 아미노산으로 구성되어 있음이 밝 혀졌댜 이들 두 개의 소단위체들의 아미노산 서열을 비교해 보면 아미 노산 잔기의 57% 가 동일하거나 보존되어 있음을 알 수 있었다. 올챙이의 경우, 그들의 세포막에 GABA 수용체를 가지고 있지 않은 데, 이들 세포에 GABAA mRNA 를 집어넣은 후 의부에 GABA 를 첨가할 시 그 세포막을 통하여 Cl- 에 의한 전기 전도도가 크게 증가하는 것을 관찰하였다. 이 사실은 완전한 GABAA 수용체의 유전자가 클로닝되었다
 N
N
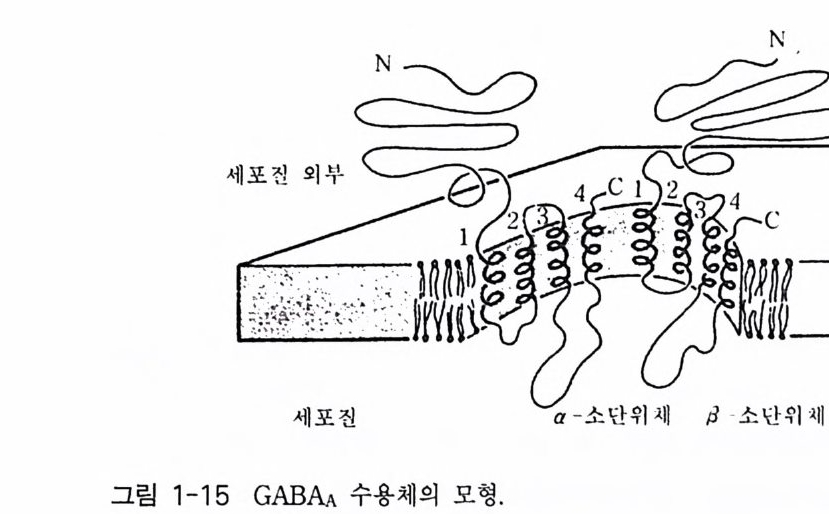
는 사실과 그 유전자에 의해 완전한 채널 단백질이 만 들 어지고 있다는 사실을 입증하는 것이다. 이 수용체 분자의 경우 소수성 부위의 아미노 산 서열을 분석한 결과 4 개의 부위로 구분할 수 있었고, a 一헬 릭스 를 형성하는 부위라는 사실을 알았으며, 이들 막을 가로지르는 헬릭스를 M1, 島,島, 그리고 M 라고 명명하였다. 그러나 GABAA 수용체의 경우 니코틴 아세틸콜린 수용체에서 발견되 는 양쪽성 성질을 갖는 부위는 발견되지 못하고 있다. GABAA 수용체의 구조는 그림 1-15 에 표시되어 있는데, 두 개의 a- 소단위체와 두 개의 B- 소단위체로 구성되어 있기 때문에 16 개의 막을 가로지르는 헬릭스를 갖게 된다. 수송로의 구경은 그 가장 좁은 지점에서 5.6 A 을 초과 하지 않는다. 1-2-4 글리신 수용체 글리신 (Gl y c in e) 수용체도 글리신에 의해 활성화되는 채널 단백질들인 데, 이 들은 포유 동물의 뇌 간과 척 수의 pos ts yn apt ic 막들에 서 주로 발견
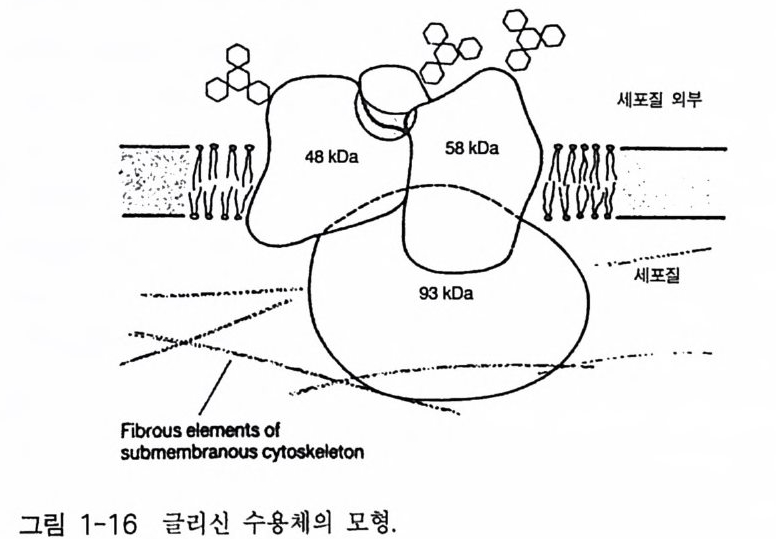
된다. 이 채널 들 의 경우도 그 구경이 매우 좁으며( < 5.2 A) 음이온들에 매우 선택적이다 이 들 역시 C[ 만 통과시킨다 . 스트리키닌(신경홍분제)에 대한 글 리신 수용체 (Gl y R) 의 친화성은 글리신 수용체 연구에 많은 도움 이 되었댜 스 트리키닌은 니코틴 아세틸콜린 수용체의 경우에는 a - t ox i n 과 , GABAA 수용체 의 경 우에 는 benzo di aze pi ne 과 유사한 역 할을 하 는 것 으로 알려져 있다. 따라서 글리신 수용체의 경우 스트리키닌을 이용한 친화성 컬 럼으로 정제할 수 있으며, 이렇게 정제하였을 때 이 분 자 는 세 개 의 po)y p eptide (48 kDa, 58 kDa, 93 kDa) 로 구성 되 어 있음을 알았댜 막에서 이 들 세 개의 소단위체들의 위치는 면역학적 전자현미경 (im munoelectr o n micr oscop y) 방법으로 확인되었다. 정제된 글리신 수용 체 를 이용하여 단일 항체 를 만 들 수 있으며, 이들을 금에 부착시켜 중추 신경과 반응시켰다 . 그림 1-16 에 글리신 수용체의 가상적인 모형을 표시하고 있는데, 이 수용체의 글 리신 결합 부위는 48kDa 와 58kDa 의 일부분으로 구성되어 있으며, 48kDa 단백질이 이온 채널을 형성하는 것으로 알려져 있다. 93
 세포질 외부
세포질 외부
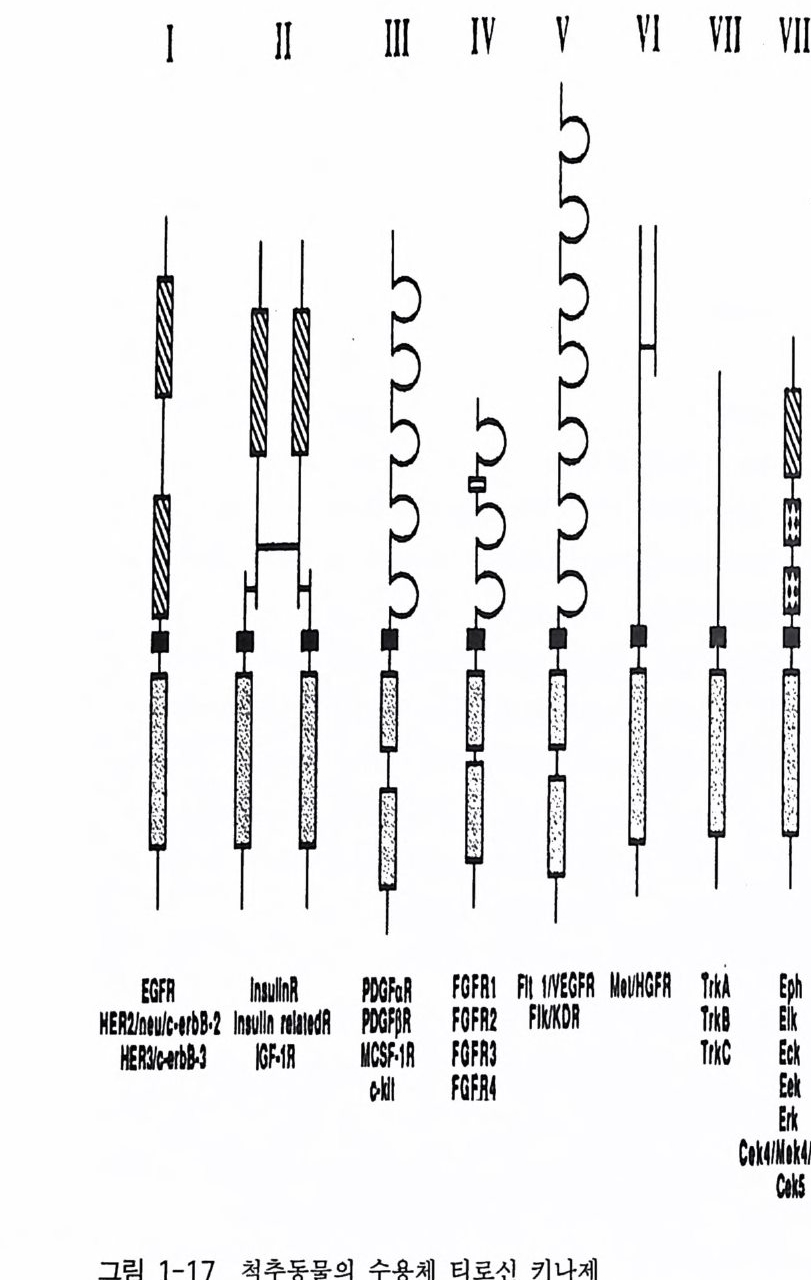
kDa 의 단백질은 막을 가로지르는 이들 두 개의 단백질 들 과 결 합되어 있 는데, 그 위치는 막의 세포질 쪽에 있는 것으로 되어 있고 세포 골 격과 상호작용할 가능성을 시사한다. 쥐의 척수에 있는 글리신 수용체의 스트리키닌 결합 소단위체 (48kDa 소단위체)가 성공적으로 클로닝되었으며 그 아미노산 서열이 결정되었 다. 421 개의 아미노산으로 구성되어 있으며 정확한 분자량은 48,383Da 이다. 통상의 소수성 지수 분석에 의하면 세 곳의 (M1, M~ , Mi ) 막 몽과 부위를 가지고 있으며, C 一말단 근처의 아미노산 서열은 GABA!\ 수용체 나 니코틴 아세틸콜린 수용체의 M4 부위의 아미노산 서열과 유사합을 나타내고 있다. 니코틴 아세틸콜린 수용체와는 달리 글리신 수용체는 양 쪽성을 나타내는 부위를 가지고 있지 않다. 이와 같은 차이점들에도 불 구하고 이들 세 종류의 수용체들 (nAChR, GABAAR , Gl y R) 은 진화적 측 면에서 볼 때 유사한 아종 (subs peci es) 에 속한다고 보고되고 있다 . 이러 한 주장은 주로 아미노산 서열의 높은 상동성에 근거를 두고 있는 것이 다. 이들 세 가지 종류의 수용체들의 아미노산 서열상에서 최대의 상동 성은 막을 가로지르는 헬릭스 부분에서 발견되는데, 특히 M2 헬릭스의 경우 GABAA 수용체와 글리신 수용체에서 그 상동성이 매우 높댜 따라 서 이들 두 수용체가 가지고 있는 M2 헬릭스는 같은 역할을 할 것으로 기대된다. 1-3 촉매의 기능을 동시에 가지고 있는 수용체 (Ca t al yti c link ed recep tor ) 세포의 생존, 분열, 분화 둥에 결정적인 영향을 미치는 신호들 중 성 장 인자들을 대표적으로 제시할 수 있다. 많은 성장 인자들은 수용체 티
로신 키나제 (rece pt or tyro sin e kina se ; RTK) 와의 상호 작용으로 그 신 호가 세포 내로 전달되게 된다. 수용체 티로신 키나제는 외부 신호의 수 용체의 역 할 과 효소(티로신 키나제)의 역할을 동시에 수행하는 혼성 분 자 (ch i me ri c mol e cule) 이다 . 현재까지 알려져 있는 촉매의 기능을 동시에 가지고 있 는 수용체의 대표적인 경우가 바로 수용체 티로신 키나제이다. 지난 10 년 동안 밝혀진 몇 가지 대표적인 수용체 티로신 키나제 아속들 을 그 립 1 - 17 에 나타내었다. 수 용체 티 로 신 키나제의 다양성에도 불구하고 이들 단백질들에 의해 시작되 는 세 포 내 신호 전이 경로들의 유형을 살펴보면 상당히 큰 공통 점 을 발 견 할 수 있댜 포유류의 경우 생화학적, 분자 유전학적 연구 결 과에 의하면 모든 수용체 티로신 키나제들에서 리간드가 세포 외부의 영역에 결 합함으로써 세포질 영역에 위치한 티로신 키나제의 활성을 올 려 주 는 것으로 알려져 있다 . 이 결 과는 신호 전이에 참여하는 그 다음 분자들을 활성화시키게 되 는 것 이다. 활 성화되는 신호 전이 관련 단백질로서는 포스포리파제 Cr (PLC r ), 포스파티딜이노시톨 3- 키나제 (PI-3- ki nase), GTPase-acti va tin g pro te i n ( GAP), pp60c -src, p2 lras, Raf- 1 키나제, ERKl 과 ERK2 키나제, 그리고 S6 리보조멀 키나제들이 있다 . 이들 분자를 포함하는 신호 전이 경로의 활성화는 유전자 발현의 변화를 유도하며, 결국 세포의 표현형 변화를 가져오게 되는 것이다 . 한 가지 홍미 있는 사실은 같은 종류의 수용체 티로신 키나제라도 세포가 다르면 다른 생물학적 반응을 나타낸 다는 것이다 수용체 티로신 키나제에 의한 신호 전이 연구는 최근 5 년 동안에 놀 랄 만한 진전을 보였으며 따라서 그 모든 연구 결과를 기술할 수는 없고 단지 수용체에 관한 연구 결과들만을 간단히 기술하고자 한다. 신호 전이에 참여하는 분자들의 활성화에 관한 연구들이 지렁이 (Cae norlnbdit is ele gans)와 초파리(D rosop hi la melano gast er) 에서 유전학적
 II III IV V VI VII VIII IX
II III IV V VI VII VIII IX
분석을 통하여 독립적 으로 수행되어 왔다. 이 연구 결과들에 의하면 세 포의 유형 발달에 수용체 티로신 키나제 분자가 중요한 역할을 한다는 사실과 이 들 생명체에서의 수용체 티로신 키나제의 신호 전이 경로가 포유류와 매우 유사함이 발견되었다. 예를 들어 지렁이에서 lin - 3, let- 2 3 그리고 let- 6 0 유전자 들 의 산물들은 EGF 수용체 또는 ras 와 구조 적인 상동성을 나타내며, 이들은 음문 발육에 중요하다는 사실이 밝혀졌 댜 유전학적 연구에 의하면 /e t - 60(ras) 는 lin - 3(EGF!T GF-a )나 let- 2 3 (EGFR) 와 e pi s t as i s 합이 밝혀졌으며, 이 사실은 이것이 신호 전이 경로 의 아래 단계에 위치해 있음을 말하는 것이다. 초파리에서는 R7 광수용 체의 발달아 sevenless( 자외선을 감지하는 R7 광수용체를 가진 파리의 돌 연변이체) 유전자 산물인 수용체 티로신 키나제(구조적으로 c- ros 와 인슐 린 수용체둘과 유사함)의 기능에 의존적이다. Sevenless 다음에 위치한 신호 전이 분자들로서는 SOS(son of sevenless) 단백질, Gap! , Rap! 그리 고 ras-1 같은 것둘이 있으며, SOS 단백질은 구아닌뉴클레오티드 교환 안자와 유사하며 ras-1 을 활성화시키는 기능을 가지고 있는 것으로 사 료 된다. Gap !과 Rap !은 아마도 ras-l 신호 전이를 음성적으로 조절하는 것으로 알려져 있다 . 수용체 티로신 키나제에 리간드가 결합하면 수용체 티로신 키나제들 은 그들이 가지고 있는 티로신 잔기가 인산화되는 일이 발생하는데, 이 과정을 자동 인산화 (au t o phosp ho ry la ti on) 라고 부른다. 몇몇 수용체 티로 신 키나제에서는 리간드가 결합하면 수용체의 이량화가 유도된다(1 7, 18). 자동 인산화 이후, 세포질 쪽에 위치한 수용체의 인산화된 티로신 잔기들은 세포질 내에 존재하는 특이한 분자들과 상호 작용할 수 있는 매우 선택적인 부위로 작용하게 된다. 이들 신호 전이 분자들은 성장 인 자들에 대한 세포 반응을 중개하게 되는 것이다. 신호 전이 분자들이 직 접 수용체 티로신 키나제와 결합하며 이 결합은 키나제들의 어떤 특정
 :773日;97 t:;-:tP E:@@ : 巫€) 포-
:773日;97 t:;-:tP E:@@ : 巫€) 포-
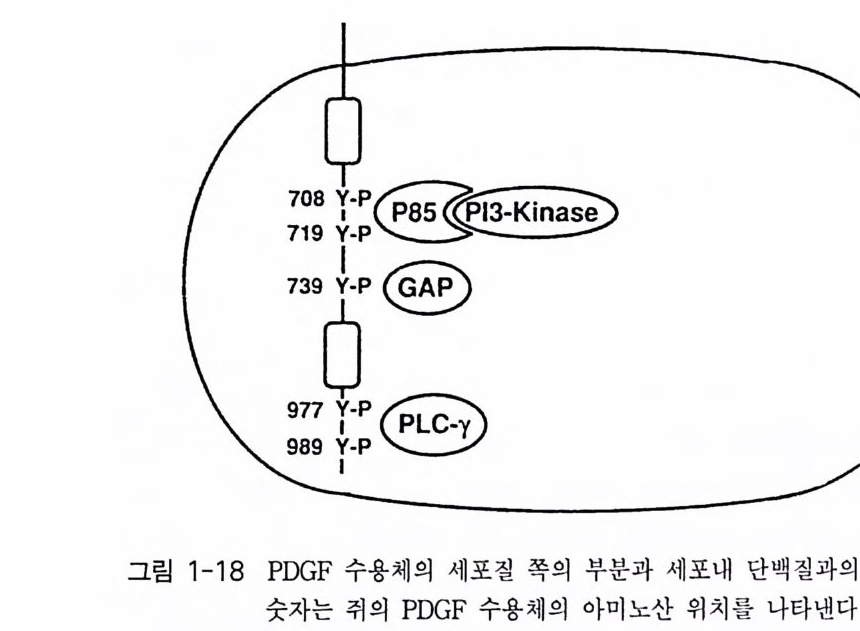
부위와 이루어진다는 사실이 자동 인산화된 PDGF /3 - 수용체가 PI-3- 키 나제와 결합한다는 사실로부터 확인되었다(1 9). 세포질 쪽에 위치한 부위 가 제거된 PDGF /3-수용체의 돌연변이체의 경우 티로신 키나제의 활성 을 가지고 있으며 PLC-r 와 같은 다른 신호 전이 분자를 활성화시킬 수 있는 능력을 가지고 있으나 PI-3- 키나제는 결합을 하지 않음을 발견 하였다. 일련의 돌연변이 연구를 통하여 PI-3- 키나제는 수용체의 티로신 잔기 (708 번째와 719 번째)에 결합할 수 있다는 사실을 발견하였다(그림 1-18). 다른 신호 전이 분자인 GTPase 활성화 단백질 (GTPase Acti va tin g Prote in , GAP) 은 티로신 739 에 결합하며, PLCr 가 붙는 티로신 잔기는 '17 7 번째와 989 번째임이 밝혀졌다(그림 1-18). 수용체 티로신 키나제와 신호 전이 분자들 간의 상호 작용에 관한 구 조적 특이성을 연구하는데 합성 펩티드들을 사용하는 것이 매우 유용하
댜 티로신이 인산화된 펩티드(아미노산 5 개 정도로 구성)들은 수용체를 인지하는 신호 전이 분자들의 결합 부위를 점거함으로써 수용체 티로신 키나제와 신호 전이 분자들 간의 상호 작용을 매우 선택적으로 차단한 다. 신호 전이 분자들과 펩티드의 결합은 매우 선택적이며 펩티드의 매 우 적은 농도(1 ~10 µM) 에서도 일어나는데, 펩티드의 주요 티로신 잔기 가 인산화되어 있을 경우만 결합이 일어난다. 예를 들면, PDGF /3-수용 체의 경우 PI - 3 - 키나제에 대한 두개의 결합 부위의 아미노산 서열은 YV - P - M - L 과 PYM - D - M - S 이 다. 이 들과 같은 아미 노산 서 열로 구성 되 어 있는 합성 펩티드 둘 은 수용체에 PI-3- 키나제가 결합하는 것을 차단 시키나, GAP 이나 PLC y가 결합하는 것은 차단시키지 못한다. 그러나 이들보다 더 짧은 펩티드의 경우는 결합을 차단하지 못한다 . 이 사실은 PI - 3 - 키나제가 수용체에 결합하는 데 요구되는 펩티드의 최소 길이는 5 개의 아미노산 잔기라는 사실이다 (20). PI - 3 국기나제가 결합하는 부위의 중요한 양상으로 YXXMX 의 아미노산 서열이 인산화된 티로신 잔기의 c- 말단 쪽으로 위치한다는 사실이 최근에 보고되었는데, X 위치에는 몇 몇 특 정한 아미노산들만이 위치할 수 있다는 것이다. 인산화된 티로신의 C 말단 쪽에 위치한 아미노산 잔기들이 수용체와 키나제의 상호 작용의 친화도와 특이성을 결정하는데 N- 말단에 위치한 아미노산 잔기들보다 중요하다는 사실이 확인되었다. 수용체 티로신 키나제들과 높은 친화도로 결합하는 많은 신호 전이 분자들의 공통된 점들은 그들이 SH2 영역을 가지고 있다는 사실이다. SH2 영역이란 src 단백질의 비촉매 영역과 상동성을 가지고 있는 아미 노산 100 개로 구성된 부위를 말하는 것이다 (23). Hana fus a 등 (24) 은 1990 년 최초로 erk SH2 영역들이 전이된 세포들에서 ®-T yr-p ro t e in과 직접 결합한다는 사실을 보고하였다. 몇 개의 SH2 영역의 구조는 NMR 과 X-Ray 결정학적 방법으로 확인된 바 있고, 인산화된 티로신에 대한 결합 부위가 확인되었다. 그러나 아직도 인산화된 티로신을 포함하는 부
위와 SH2 영역간의 상호 작 용에 관한 특 이성이 구조적인 측면 에서 밝혀 진 바 없다. 수용체의 인산화된 티 로신 의 C_ 말단 쪽에 위치한 어떤 아미 노산 서열 부위가 ® -T yr 결합 부위 근처에 위치한 특정 /3_ sh e et 부위 (신호 전이 분자)와 상호 작용하는 것으로 생각되고 있다 . SH2 영역 을 포함하고 있는 많은 단백질 들 이 확인되고 있 는 데 , 이 들 단백 질들 이 인지 하고 결합하는 수용체의 특정 부위의 아미 노산 서열이 밝혀진 경우는 PI - 3 견]나제, PLC r 그리고 GAP 등이댜 Corkscrew 라고 부르 는 다른 SH2 단백 질은 티 로신 포스파타제( tyro sin e p hos p ha ta se) 이며 tor so g ene 에 의해 만 둘 어 지 는 초파 리 수용체 티 로신 키나제에 의한 신호 전이에서 중요한 역할 을 하 는 것 으로 알려져 있댜 또 다른 어떤 SH2 함유 단백질 들 은 수용체와 효 소 들 간의 연결자 로서 역할을 하는데, 예 를 들 면 PI - 3 - 키나제의 촉 매 적 기능을 가지고 있 는 소단위체인 p llO 은 PDGF 수용체와 p8.5 소단위체를 연 결 시켜 준 다 . 아직은 수용체 티로신 키나제와 신호 전이 분자간의 결합 으로 인한 정확한 기능에 관하여 이해하고 있지 못한데, 아마도 신호 전이 분자 둘 의 기질 가까이에 그들을 위치시키기 위한 것으로 추측하고 있다. 수용 체 티로신 키나제들의 티로신 키나제 활성도는 두 가지 기능을 가지고 있다 첫째, 신호 전이 분자를 강하게 결합시키는 역 할 과, 둘째 인산화에 의해 신호 전이 분자를 변화시키는 것이다. 1-3-1 p2 1 ras Proto - oncog e ne 중의 하나인 ras 가 발현된 p2 1 단백질이 성장 인자들 의 자극에 의한 세포 분열을 중개하는 데 중요한 역할을 한다는 사실이 많이 보고되 고 있다. p21 ras p ro t o-onco g ene 들은 Ha 와 Ki의 sarcoma viru s 의 형질 전환 유전자들과 유사한 성질을 가지고 있는 것으로 알려 져 있댜 80 %의 상동성을 가지고 있는 세 개의 유사한 Ras 단백질들
(Ha , Ki, N) 은 대부분의 포유 동물의 세포들에서 발견되며, 이들은 Ras_ 유사 단백질의 가족에 속한다고 말한다. 성장 인자의 신호 전이에서 ras 가 중요한 역할을 한다는 실험적 증거 들이 많이 보고되어 있는데, 그 중의 한가지 예를 든다면 다음과 같은 것이 있댜 PC12 세포들의 분화와 인슐린에 의해 유도되는 올챙이의 성 숙 현상이 ras 항체의 투입에 의해 차단된다는 것이다. Ha, Ki 그리고 N ras 유전자 들 에 의해 만들어지는 단백질들은 21 kDa 인데, 이들은 만들어 진 후 C 一 말단이 원형질막의 내부 표면에 잘 붙게 하기 위해 구조적인 변화 를 수반하는 것으로 알려져 있다 . Ras 단백질들은 GTPase 의 기능을 가지고 있으며, GTP 가 결합된 활성형과 GDP 가 결합된 비활성형 사이를 순환하는 성질을 가지고 있다. 성장 인자들이 작용을 하게 되면 GTP 가 결합된 Ras( 활성화됨)와 GDP 가 결합된 Ras( 바활성화됨)의 비율이 증가하게 된다 (23). Ras GTP 는 다음 신호 전달 분자들과 상호 작용을 하여 그 신호를 전달하게 된 다. 활성형 Ras 와 비활성형 Ras 의 비율을 조절하는 두 그룹의 단백질들 이 확인되었다 . 첫번째 그룹의 단백질은 Ras 의 GTPase 활성도를 크게 올려 주는 부류로써 GAP 과 neurofi br orn in 유전자 산물로 구성되어 있 댜 두번째 그룹의 단백질들은 Ras 의 상태에 영향을 미치는 단백질들로 서 뉴클레오티드 교환 인자들 또는 GNRI 짜:i u anin e Nucleoti de Releasin g Pro t e i n) 와 같은 것들이다. GNRP 는 비활성화되어 있는 Ras 로부터 GDP 를 제거함으로써 Ras 를 활성화시키는 능력을 가지고 있다. 따라서 GNRP 는 Ras 의 활성제라고 말할 수 있으며, GAP 은 활성을 낮추는 인자 라고 말할 수 있다. 성장 인자의 수용체들은 구아닌 뉴클레오티드 교환 단백질(guanin e nucleoti de exchang e p ro tein)의 활성화에 의해 Ras 의 뉴클레오티드 상태 를 변화시키는 것으로 사려되고 있다. 신호 전이에서 교환 인자들에 대 한 가장 강력한 증거들은 효모나 초파리의 유전적 연구 결과들로부터
얻어지고 있댜 Ras 에 대한 교환 인자 들로 서 효모에서는 CD C2 5, SDC25 그리고 s t e6 가 확인되고 있다. 빠른 시일 내에 해결해야 될 중요한 문제들은 ® 어떻게 성장 인자 들 이 Ras 의 활성도를 조절하는가를 밝히는 것과, ® 성장 인자 들 에 의해 중재되는 Ras 활성도의 변화에 어떤 종류의 구아닌 뉴클레오티드 교환 단백질이 개입되는지를 알아보는 것이다. 1-3-2 수용체 티로신 키나제 (RTK) 의 종류 표피 성장 인자 수용체 표피 성장 인자 수용체 (E pi dennal Grow th Facto r Rece pt or) 는 다양한 종류의 세포에서 발현되는 170 kDa 의 막 투과 티로신 키나제이다 . 표피 성장 인자 수용체족으로 분류되기는 하지만 다른 형태의 수용체 (Clas s I, 그림 1-17) 들로서는 p18 .5 neu 티로신 키나제 (erbB-2 또는 Her2) 와 erb B- 3 와 같은 것들이 있다. 이들 세 가지 종류의 수용체 들은 세 포 외 부 에 시 스테인이 많은 영역을 두 개 가지고 있으며 세포질 쪽에는 방해받지 않 는 하나의 티로신 키나제 영역을 가지고 있다. 리간드족 들 은 표 피 성장 인자 수용체에 높은 친화력으로 결합하며 표피 성장 인자에 민감한 세 포들의 분화를 촉진시킨다. 여기에 속하는 리간드들로서는 TGF- a , Pox virus grow th fac to r , amp hireg u lin, hepa rin- bin d i ng EGF-lik e gro w th fac to r 등이 있다. 최근에 pl8 .5 neu 에 대한 수용체가 정제되고 클로닝되 었다. 이 리간드가 어떤 세포들에서는 의형적 분화를 유도하는 능력을 가지고 있는 것으로 알려져 이것을 neu differ enti at i on fac to r (NDF) 라 고부른다. 리 간드와 표피 성 장 인자 수용체 또는 pl8 .5 neu 와의 상호 작용은 수 용체의 이량화(dim e riz a ti on) 와 자동 인산화의 결과를 가져온다. 표피 성 장 인자 수용체인 경우 c- 말단에 위치한 992, 1068, 1148, 1173 과 1186 번
째의 티로신 잔기들이 자동 인산화가 된다 (24) . 자동 인산화의 경우 티 로신 키나제 활 성도 를 올려 주는 것으로 보고되어 있다. ATP 가 결합하 는 아미노산 잔기인 리신 -721 을 돌연변이시키면 키나제 활성도가 소멸 되며, 수용체에 의해 중재되는 Ca 2 + 의 흐름, pH 변화, 전사의 활성화, 세 포 분화 등이 소멸된다. 표피 성장 인자 수용체의 키나제 활성도가 리간 드 에 의해 유도되 는 수용체의 다음 단계들의 조절에 관여하는지의 여부 는 아직 확실치 않다. 그러나 표피 성장 인자 수용체의 C- 말단에 위치한 18 개의 아미노산 집단이 수용체의 다음 단계들의 조절과 세포질 내 Ca 2 ♦ 농도 증 가에 요구되는 것으로 보고되고 있다 (25) . 활 성화된 표 피 성장 인자 수용체와 결합하는 몇 종류의 신호 전이 분 자 들 이 있는데, 그 중에 대표적인 것이 PLCr 이다. 세포를 표피 성장 인 자로 처리했을 때 PI 대사가 촉진되는데, 그 이유는 표피 성장 인자 수 용체에 있는 티로신 992 가 PLC r 와 높은 친화력으로 상호 작용을 하여 PLCr 의 활 성도를 높여 주기 때문이다 (26). 이 때 PLCr 효소의 티로신 잔기가 인산화된다. 표피 성장 인자에 의해 중재되는 세포의 성장에서 PI 대사가 정확하게 어떤 역할을 하는지 모르고 있는 상황이다. 그런데 PI 4- 키나제와 PI5- 키나제가 표피 성장 인자 수용체와 결합한다는 사실 이 보고되었고, 분자량 46kDa, 52kDa 그리고 66kDa 의 SHC 단백질들 이 세포 내에서 그들의 SH2 영역을 통하여 활성화된 표피 성장 인자 수 용체와 회합하는 것으로 알려져 있다 . SHC 단백질들도 역시 티로신 잔 기가 인산화되며, 이 단백질은 SH2 영역과 프롤린/글리신이 풍부한 영 역으로 구성되어 있고, 어떤 종류의 촉매적 영역도 가지고 있지 않음이 밝혀져 있다. 따라서 이 단백질들은 PI-3 키나제의 p85 소단위제의 기능 과 유사한 li nke r/ ada pt or 로서 역할을 수행할 가능성을 가지고 있다. 인슐린 수용체 인슐린 수용체는 두 개의 a 소단위체와 두개의 8 소단위체로 구성된
이종사량체 (he t ero t e tr arne ri c) 구조 를 가지고 있 는 수용체 티로신 키나제 족의 대표적인 수용체이다 세포 밖에 위치한 리간 드 결 합 소단위체 는 세포질 쪽에서 티로신 키나제 영역을 가지고 있 는 막 통 과 /3 소단위제에 —s- s— 결 합으로 연결되어 있댜 IR 티로신 키나제 족 에 속하 는 다 른 수용체들로서 ins ulin - lik e gro w th fa c t or - l( IGR - lR) 과 ins ulin - re late d rece pt or(IRR) 이 있는데, 아직까지 이들의 리간드가 발견되지 않고 있다. 인슐린이 그 수용체에 결합하면 다양한 반응 둘 이 일어나 는 데 , 그 반옹 들은 대사적 효과와 성장 촉진 효과들로 대별된다. 대사적 효과 들 로서는 포도당 수송과 글리코겐 합성에 관한 것 들 이다. 최 근 보고 (27) 에 의하면 인슐린에 의해 활성화되는 단백질 키나제가 단백질 포스파타제 유형 l(PPl) 을 인산화시키며, 그 결과 PPl 이 활성화되면 글 리코겐 합성 효소 의 세린 잔기를 탈인산화시켜 이 효소의 활성도 를 증가시키는 것으로 밝혀졌다. 인슐린에 의해 중재되는 다른 대사 효과 들 로서 지방 생성, 지 방 분해 그리고 단백질 합성 등이 있다. 다른 성장 인자들과 마찬가지로 인슐린과 IGF - 1 도 수용체의 세포 외 부에 노출된 부위와 상호 작용한다. 리간드가 수용체에 결합하면 /3 소 단위체의 자동 인산화 반응이 일어나며 키나제의 활성화가 일어나게 된 댜 인슐린 결합시 /3 소단위체의 인산화에 관해서는 분자 내부의 시스 반응과, 분자간의 트랜스 반응 메커니즘 두 가지가 제안되어 있다 (28, 29). 사람의 경우 인슐린 수용체의 /3 소단위체에서 티로신 인산화가 일 어나는 주요 부위가 두 개로서 C- 말단 쪽의 티로신 1316 과 1322 그리고 티로신 1146, 1150, 1151 을 포함하는 영역이다 . 인슐린 수용체의 신호 전 이에서 홍미로운 점은 막을 가로지르는 부위에서 세포질 쪽에 가까운 부위에 위치한 티로신 잔기들이 세포 반응을 중재하는 중요한 역할을 한다는 사실이다 이 부위에 속하는 티로신 960 을 돌연변이시키면 수용 체의 자동 인산화 반응 또는 키나제 활성화에 아무런 효과를 갖지 못한 다. 그러나 이 돌연변이 수용체의 경우 생물학적으로 비활성이며 감소된
생물학적 반응을 야기시 킨다 . 혈소판-유도 성장 인자 수용체 혈소판- 유 도 성장 인자 (Pla t e l e t - de ri ved Grow th Fac t or) 는 평활근 세 포 (smoo t h muscle cell) , 신경 교세포(gli al cell) , olig o dendrocy te pro - ge nit or cells, 섬유 아세 포( fi brobla s t) 그리고 몇 종류 의 내피 세포 (en d판o t-h 유d 도ia l 성ce 장ll ) 에인서자 는강력 A한 사 유슬사과 분B열 사 슬촉이진 —기s능- 을s -가지결 고합 에있 다의 해(32 )구 . 성혈된소 3 개의 이 량체로 존재하는데 , 어떤 경우는 호모이량체(AA/B B) 로 다른 경우는 이 종 이량 체 (AB) 으로 존재한다. 혈소판-유도 성장 인자 수용체는 두 가지 형태가 있는데, 하나는 혈소판-유도 성장 인자 a 수용체이고 다 른 하나는 혈소판 - 유도 성장 인자 8 수용체이다. a 와 f3수용체는 매우 유사한 아미 노산 서열을 가지고 있으며 구조적 영역의 배치도 같음이 확 인되었댜 이 들 두 종류의 혈소판-유도 성장 인자 수용체들에서 중요하 게 다 른 점은 리간드 결합의 특 이성과 조직에 따른 발현 양상의 차이이 다. a 와 8 수용체 모두는 혈소판 _ 유도 성장 인자에 의한 유사 분열을 중재하는데, 8 수용체만이 리간드에 의한 세포 골격의 변화를 중재한다. 그리고 이 들 두 수용체들에 의해 인산화되는 단백질들의 유형은 동일 하지는 않지만 유사하다. 혈소판-유도 성장 인자가 결합하면 수용체는 비공유성 이량체 를 만든다. 다른 종류의 2 가형(di valen t form ) 혈소판-유 도 성장 인자들의 존재 하에서 이량체 형성의 유형은 다음과 같다. A 사 슬 리간드는 혈소판_유도 성장 인자 a 수용체에만 결합하는 반면, B 사 슬 리간드는 혈소판-유도 성장 인자 a 수용체와 혈소판-유도 성장 인자 8 수용체 모두에 결합한다. 따라서 리간드 결합에 따라 형성되는 수용체 이량체 (aa, bb, ab) 형태는 주어진 세포에서 발현되는 수용체의 유형뿐만 아니라 세포를 자극시키는 혈소판-유도 성장 인자 이량체(AA, BB, AB) 의 형태에 따라서도 결정된다. 최근의 연구 결과에 의하면 수용체의 세
포질 쪽 부위와 막투과 영역을 제거한 혈소판_유도 성장 인자 수용체의 돌연변이체를 만들었는데, 이 들 의 경 우 용액 내에서 혈소판-유도 성장 인자 의존성 이량체 를 형성하는 것을 관찰하였다 (31). 따라서 세포질 쪽 또는 막 투과성 부위에 있 는 아미노산 들은 리간 드 에 의해 유도되는 수 용체의 이량화에 요구되지 않는다는 사실을 보여주는 것 이다 . 신호 전달 분자들이 수용체 티로신 키나제들과 직접 결합한다는 사실 이 혈소관-유도 성장 인자 /3수용체와 P13- 키나제와의 상호 작용 연구 로부터 얻어진 것이다 그 후 혈소판_유도 성장 인자 수용체와 PLC-r, GAP, raf 그리고 pp60 c- sr c 티로신 키나제 들 이 결합한다는 사 실도 발견 되었댜 그림 1-18 에 나타난 바와 같이 이 들 신호 전 이 분자들과 혈소판 -유도 성장 인자 수용체간의 결합 부위는 대체적으 로 일정한 부위에 모 여 있댜 뉴로트로핀 수용체들 뉴로트로핀 (neuro tr o phi n) 들은 신경 세포들의 성장, 분화에서 중요한 역할을 하는 리간드족들이다. 비신경계에서도 뉴로트로핀 들은 세포 분열 을 자극하는 능력을 가지고 있다. 최근 5 개의 리간드 들 이 알려져 있는데, 그들은 nerve grow th fac to r (NGF), brai n- deri ve d neurotr op hic fac to r (BD NF), neurotr op h in- 3 (NT-3), neurotr op hin- 4(NT- 4) 그리 고 neurotr o- phi n-5(NT-5) 이다. 세포의 유형에 따라 뉴로트로핀의 결합 부위 를 두 가지 로 나눌 수 있는데, 하나는 높은 친화력 (Kd=l0-1 1 M) 을 갖는 부위 이 고 다른 하나는 낮은 친화력 (Kd=lO -9 M) 을 갖는 부위이다. 친화력이 높 은 부위와 낮은 부위는 상호 교환되는데 이들에 대한 생화학적 이해가 미비한 실정이댜 뉴로트로핀에 대한 수용체로서 확인된 단백질들의 경 우 두 종류가 보고되 어 있다. 하나는 p 75LNGFR(LNGFR) 로 명 명 되 는 단백 질인데, 이것은 종간에 높은 보존성을 보이며 신경 조직과 비신경 조직 모두에서 광범위하게 발현되는 75-80kDa 의 막 결합 당단백질이다.
p 75L NGF R 의 세포 외부 영역은 시스테인 잔기 들 이 풍부하며, TNF 수용체 와 같은 몇 가지 단백질들에서의 시스테인이 풍부한 영역과 매우 유사 한 점을 가지고 있댜 이 수용체의 세포 내부 영역(사람의 단백질 : 1 5.5개 의 아미노산)은 어떤 알려진 단백질과도 상동성을 가지고 있지 않으며, 어떤 알려진 효소의 기능도 가지고 있지 않다. p 75L NGF R 이 섬유아세포에 서 발현될 때 이 수용체는 모든 뉴로트로핀들과 낮은 친화력으로 결합 한다 두번째 의 뉴로트로핀 수용체 종류는 trK A, trK B, trK C 유전자 들 에 의해서 발현되는 단백질들이다. p 75L NGF R 과는 대조적으로 p14 0tr k, pl4 0 t rk !J 그리고 p l40 trk C 의 세포질 영역들은 티로신 키나제의 촉매적 영 역 을 가지고 있댜 포유류 동물에서 발견되는 trk 단백질들의 세포 외부 영역은 어떤 특 이 한 구조적 요소가 없으며 i rnrnuno g lobu li n (Ig)과 유사한 영 역 과 fibr on- ecti n 유형 III(FN III) 영 역 을 가질 수 있다는 가능성 을 시 사할 뿐이 다. 초파리 tr k 의 경우 세포 외부 영역에 6 개의 lg 유사 영역을 가지고 있다 는 사실이 밝혀졌다. tr k 족에 속하는 각각의 단백질들은 적어도 한 개의 뉴로트로핀과 결합할 수 있는데, 리간드가 결합하면 수용체 분자의 티로 신 키나제 활성도를 올려 주게 된다. p 140 trk의 경우 NGF, NT-3, NT-4 그리고 NT-5 가 결합하고 활성화되는 데 반하여 BDNF 의 경우는 결합하 지 않는댜 p14 Q trkB 단백질은 BDNF, NT-3, NT_4 그리고 NT-5 와 결합 하고 활성화되며, NGF 와는 결합하지 않는댜 그러나 pl4 0trk -c 단백질은 NT-3 와 결합하고 활성화되나, NGF 또는 BDNF 와는 결합하지 않는다. p 75LNGFR 와 tr k 족의 수용체들 간의 기능적 관계는 아직 명확하게 밝혀 지지 않고 있는 상황이다. 한 가지 명확한 증거로서는 trk 수용체의 경우 p7 5LNGFR 의 부재시 뉴로트로핀에 대한 생물학적 반응을 중개할 수 있다 는 것이다 . 또 다른 하나의 증거는 p 75LNGFR 이 신호 전이에서 어떤 역할 을 한다는 것이다. 뉴트로핀에 의해 유도되는 신호 전이 경로에 관한 연 구는 PC12 세포들에서 가장 많이 진행되어 왔다 . PC12 세포를 NGF 로
처리하면 PLCr 의 티로신 잔기의 빠른 안산화, PLCr 와 p l40 t.rk와의 회 합은 물론 티로신 키나제의 빠른 활성화와 pl4 0Irk 수용체의 자동인산화 가 일어난다. 어떤 그룹에서는 세포 내 cAMP 의 농도 증가도 관찰한 바 있다 . 그밖에 NGF 의 자극은 세포 내 ca2· 농도를 증가시키고, c-fo s 와 c--jun 유전자들의 전사가 증가하며 몇 가지 세포 내 단백질들의 인산화 룰 증가시킨다는 보고가 있다. 단백질의 인산화는 세린, 트레오 닌 그리 고 티로신 잔기의 인산화이며, 인산화된 단백질 들 의 경우 그 활성도가 증가한다는 것이다 . NGF 처리 후 증가되는 인산화 정도의 결과로 효소 의 활성도가 증가되는 단백질들로서는 티로신 수산화 효소, ERKl, ERK2, S6 리보조멀 키나제 그리고 Raf -1 등이 있다. 몇 가지 실험에 의하면 신경세포의 성장에 필요한 신호 전이에서 ras 가 포함된다는 사실을 확인하였다 . PC12 세포들에서 ras 의 발현은 ERKl 과 ERK2 의 활성화와 Raf -1 의 과인산화를 야기시킨다. anti -m s 항 체를 PC12 세포에 주입시키면 NGF 에 의존성을 나타내는 신경세포의 성 장이 중단된다. Dom ina nt neg a tiv e ras 의 발현은 p l40 trk의 자동 인산화 를 막지 못했으며 수용체와 PLC-r 와 결합을 저해하지 못하였다. 이 사실 은 ras 가 신호 전이 경로에서 상당히 후반부에 위치하고 있다는 것이다. ras 의 이소프레닐화(i so p ren y la ti on) 반응이 신경세포의 성장에서 중요한 역할을 한다는 사실이 밝혀졌다. 섬유 아세포 성장 인자 수용체 섬유 아세포 성장 인자 (F i broblas t Grow 出 Fac t or) 들은 세포의 분열, 분화를 포함한 다양한 생물학적 반응들을 중재한다 (32). 섬유 아세포 성 장 인자들은 여러 생명체들에서 혈관 형성을 유도하는 능력을 가지고 있으며, 개구리 배에서 중배엽 형성을 유도하기도 한다. 최근까지 알려 진 섬유 아세포 성장 인자족에 속하는 것들은 7 가지 종류가 있는데, 산 성 섬유 아세포 성장 인자, 염기성 섬유 아세포 성장 인자, int - 2
onc o g e n e 산 물, hst oncog e ne 산 물, 섬유 아세포 성장 인자 5, 섬유 아세 포 성장 인자 6 그 리고 kenati no cy te gro w th fac to r (KGF) 등이댜 세포 표 면에 존 재하 는 섬 유 아세 포 성장 인자 수용체 들 의 유전자들로서 섬유 아세 포 성 장 인자 수용체 1, 섬유 아세포 성장 인자 수용체 2, 섬유 아세 포 성장 인자 수 용체 3 그리고 섬유 아세포 성장 인자 수용체 4 와 같은 것둘 이 알려 져 있다 . 이 들 유전자 들 의 산물 들 은 구조적으로 상관성을 가 지 고 있 으 며 , 티 로 신 키나 제 의 활 성도 를 가지고 있으며, 쥐의 배 발생 시 조직 에 따 라 다 르 게 발 현된다. 섬 유 아세포 성장 인자들은 세포 표면이 나 세 포 외 ma tri x 에 위치한 hep arin sulfa te 프로테오글리칸(p ro t eo giyc a n ) 분 자에 결 합한다. 기준이 되는 섬유 아세포 성장 인자 수용체는 막 을 가로 지 르는 영역이 한 개 있으며, 수용체의 세포 외 부위는 세 개 의 Ig 유사 영역 을 가지고 있다. Ig 영역 I 과 II 사이에는 acid box 영역 이라고 부 르는 짧은 영역이 존재한다 . 섬유 아세포 성장 인자 수용체 l 단백 질 의 경우 이 영역은 8 개의 연속적인 산성의 아미노산 잔기들이 모 여 있 는 핵심 부위이다. 수용체의 세포질 영역은 티로신 키나제의 촉매 영역이 위치해 있다 . 14 개의 아미노산으로 구성되어 있는 짧은 ins er t s eq uence 가 키나제 영역을 거의 같은 두 부위로 나눈다. 키나제 영역 다 음은 약 55-65 개의 아미노산으로 이루어진 C- 말단 영역이다. 섬유 아세포 성장 인자들이 그들의 수용체에 결합하면 수용체의 티로 신 키나제 활성도를 증가시키며, 티로신 잔기들의 자동 인산화 반응이 촉진되고, 수용체의 이량화가 유도된다 . 그 결과 동종이량체 그리고 이 종이량체 수용체들이 섬유 아세포 성장 인자 수용체 1, 섬유 아세포 성 장 인자 수용체 2 그리고 섬유 아세포 성장 인자 수용체 3 단백질들 사 이에서 생성될 수 있다. 이량화된 수용체들의 인산화는 분자간 인산기 전달 기작으로 일어난다 (33). 섬유 아세포 성장 인자로 세포를 자극하면 세포 내 p H 가 증가하며, Ca 앙 농도가 증가하고, PI 대사가 활발해지며, 세포 내 단백질들의 인산화가 증가한다. 섬유 아세포 성장 인자의 작용
으로 그 인산화가 증가하는 단백질 들 은 PLCr, Raf- I , ERKI 그리고 ERK2 키나제들과 S6 리보조멀(ri bosomal) 키나제 등이다 이 들 단백 질 들의 효소적 활성도가 증가하며 PLCr 의 경우는 리간드 자극 후 섬유 아세포 성장 인자 수용체와 안정한 복합체 를 형성한다. 섬유 아세포 성장 인자 수용체와 PLCr 의 회합은 PLCr 의 SH2 영역 에 의한 수용체 C- 말단 영역에 존재하는 한 개의 인산화된 티 로 신 잔기 (766) 를 인지함으로써 일어난다. 티로신 잔기 766 번째 를 페닐알라닌으 로 치환한 돌연변이체의 경우의 L6 근원 세포와 중국산 쥐의 난소 (CHO) 세포에서 수용체와 PLC - r 가 회합을 하지 않는다. 이 돌 연변이체의 수 용체는 리간드 의존성의 PI 대사 촉진도 하지 않으며, 세포 내 Ca2• 농도 도 증가시키지 않는댜 그러나 이 돌연변이체의 수용체는 자동인산화는 되며 다른 세포 단백질들의 인산화를 중재하며, 세포 분열을 중재한다. 이 결과는 L6 세포와 중국산 쥐의 난소 CHO 세포에서 세포 분열을 촉 진하기 위한 FGF 의 능력은 PI 가수 분해와 Ca2• 동원에 의존하지 않는 다는 사실을 입증하는 것이다. 참고문헌 1) Dixon , R. A, Sig al , I. S. and Str ad er, C. D. (19 88) Molecular Bi ol og y of Sig nal Transducti on , Vol. Lil l, Cold Sp ring Harbor Sy m p os ia , p 487 2) Dixon , R. A F., et al. (1986) Natu r e 321, 75 3) Fin d lay, J. B. C. and Papp in, D. J. C. 0986) Bio c hem J 238, 625 4) Nath a nson, N. M. (19 얽) Annu Rev. Neurosd. 10, 195 5) Yarden, Y., et al. (1986) Proc Natl. Aa :zd Sd . USA . 83, 6795 6) Dixon , R. A F., et al. (1 9 얽 a) EMBO J 6, 3269 7) Dixon , R. A F., et al. (1987b) Na tur e 326, 73
8) George , S. T., Ruoho, A. E. and Malbon, C. C. 0986) ]. Bi ol. Chem. 261, 16559 9) Sti le s, G. L., Benovic , J. L., Caron, M. G. and Lefk o wi tz, R. J. (1984) ]. Bi ol. Chem. 259, 16439 10) Ovchin n ik o v, Y. A. 0982) FEBS Lett . 1 48, 179 11 ) Coope r, A. 0981 ) FEBS Lett . 1 23, 324 12) Kuhn, H. 0984) Inte r actio n s Betw e en Photo e xc it ed Rhodop s in and Lig h t- a c ti va te d En zym es in Rods. In Prog re ss in Reti na l Research (ed. N. Osborne and J. Chader) , p 123, Perga mon, New York. 13) FranJ < e, R. R., Sakmar, T. P., Op rian , D. D. and Khorana, H. G. 0988) ]. Bi ol. Chem 263, 2119 14) Nli lle r, J. L., Fox, D. A. and Lit man , B. J. 0986) Bi oc hemi st r y 25, 4983 15) Wi lde n, U., Hall, S. W. and Kuhn, H. 0986) Proc Natl. Aazd Sd. USA . 83, 1174 16) Lang le y. T. N. (1906) Proc. R. Soc. London. 78, 170 17) Uero, H., Collest, H. A., Escobedo, J. A. and Wi lliam s, L. T. (19 91) Sc ien ce 252, 844 18) Kashles, Q., Yarden, Y., F is h er, R., IBlrich , A and Schlessin ger , J. 0991) Mo!. Cell. Bi ol. 1 1, 1454 19) Coug h lin , S. R., Escobedo, J. A. and Wi lliam s, L. T. 0989) Sdence 243, 1191 20) Fanti, W. J., Escobedo, J. A., Ma rtin, G. A., Turek, C. W. and DelRosar io, M. 0992) Cell 69, 413 21) Anderson, D., e t al. (1990) Sdence 250, 頭 22) Mats u da, M., M aye r , B. J., Fu kui, Y. and Hana fus a, H. (19 90) J Bi ol Chem. 248, 1537
23) Bollag, G., McCorm ick , F. 0991 ) Annu Rev. Cell Bi ol . 7, 610 24) Walto n , G. M., Chen, W. S., Rosenfe ld , M. G. and Gil l, G. N. (19 90) ]. Bio l. Chem. 265, 1750 25) Chen, W. S. (1989) Cell 59, 33 26) Roti n, D., et al. (1992) EMBO ]. 11, 559 27) Dent, P., Lavoin n e, A, et al. (19 90) Natu r e 348, 302 28) Shoelson, S. E., Bon i-S chnetz l er, M., Pil ch , P. E. and Kahn, C. R. (1991) Bi oc hemi st r y 30, 7740 29) Fratt ali, A L., et al. 0992) ]. Bi ol. Chem. 267, 19521 30) Heldi n, C. H. and Weste r mark, B. (19 90) Cell Reg ul. l , 555 31) Duan, D-S. R. and Pazin , M. J., et al. 0991) ]. Bi ol. Chem. 2 鉛 413 32) Burge ss, W. H. and Macia g , T. (1989) Annu Rev. Bi oc hem 58, 575 33) Bellot, F., C rumley, G., et al. (1991) EMBO ]. 10, 2849
제 2 장 G- 단백질 모든 세포들은 그들 주위로부터 정보를 받고 이용하는 능력을 가지고 있다. 광선, 화학 물질과 같은 외부 신호들이 특정한 감각 기관들에 존재 하는 표적 세포들을 자극한다. 순환하거나 국부적으로 방출되는 호르몬 들, 신경 전달 물질들, 성장 안자들이 세포 사이의 화학적 전령으로 작용 한다. 이들 전령들과 세포 표면에 위치한 특정한 수용체들과의 상호 작 용은 막투과성 신호 전이 체계의 최초의 단계이다. 많은 경우에 이들 수 용체의 자극은 다른 eff ec to r 단백질(예, 효소들 또는 이온 채널)을 활성화 시키며 그 결과로 세포 내에서 특이한 작용을 유발시키는 제 2 의 전령들 이 만들어진다 모든 진핵 세포에서 이종 삼량체 구조의 G- 단백질 (hete ro tr irne ri c G-pr o te in ) 족들은 세포막에서 세포 표면에 위치한 ef- fec to r 단백질 분자들과 상호 작용하여 신호 전이의 핵심적 중간자로서 의 역할을 담당하고 있다. 본 장에서는 이종 삼량체의 구조를 가지고 있 는 분자량이 큰 G- 단백질들의 구조와 기능에 관한 내용에 역점을 두어 기술하되 분자량이 작은 G- 단백질들에 관해서도 약간 언급하고자 한다. G- 단백질의 기본 성질 중 중요한 두 가지 내용은 CD GTP 가 결합함으로 써 활성화되는 성질과 @GTPase 의 성질이다. 이들 성질에 관한 자세한
메커니즘도 본 장에서 다루고자 한다. 2-1 G- 단백질의 구조와 성질 이종삼량체인 G- 단백질들의 경우는 세 개의 다른 소단위체 둘 로 구성 되어 있는데, a 소단위체는 분자량이 39-46kDa 이며, /3 소단위체는 37 kDa 이고 r 소단위체는 8kDa 이다. 이들 폴리펩티드 들 의 성질 둘 은 표 2-1 과 2-2 에 표시하였다 B 와 r 소단위체들은 하나의 단위체와 같이 작용하는 매우 강하게 회합되어 있는 복합체로 존재한다. 이종 삼량체를 만드는 데 동일한 /3 r 소단위 복합체가 다른 a 소단위체들과 회합하 게 되며 a 소단위체의 정체가 G- 단백질의 개별적인 구분의 척도가 된 댜 이 a 소단위체들은 여러 뉴클레오티드들 중 구아닌 뉴클레오티드 (GDP 또는 GTP) 에 대한 높은 친화력을 갖는 결합 자리를 가지고 있다. GDP 가 결합된 a 소단위체는 B r 에 강하게 결합하며 비활성이고, GTP 가 결합된 a 는 /3 r 와 분리되며 eff ec to r 단백질 분자들을 조절하는 작 용을 한댜 M g 2+ 과 함께 A1F4 _ 를 첨 가하면 GDP 가 결합되 어 있는 a 소 단위체와 상호 작용을 하고 a 소단위체룰 활성화시킨다. 최근에는 B r 소단위 체 복합체도 a 소단위 체와 마찬가지 로 eff ec to r 단백질들의 활성도를 조절한다는 증거들이 제시되고 있다. 모든 a 소단 위체들은 GTPase 의 기능을 가지고 있어 결합된 GTP 를 가수분해시켜 GDP 와 무기 P를 생성시킨댜 어떤 a 소단위체들은 박테리아의 독소들 에 의해 공유결합적인 변형이 일어날 수 있는 특이한 아미노산 잔기들 을 가지고 있다. 박테리아 독소들 중 콜레라 독소 단백질은 a 소단위체 에 존재하는 특정 아르기닌 잔기에 NAD 로부터 ADP- ri bose 를 옮겨 붙 여 주는 촉매성 기능을 가지고 있으며, 이 현상을 콜레라 독소에 의한 ADP- 리보실레이션 현상이라고 부른다. 백일해 독소에 의한 ADP- 리보
표 2-1 포유류 G - 단백질 a 소단위체들의 성질둘. /fsuamb ui nlyi t (kDMaaX ssI 0 3) ac%id Aidme ninti ot y , Toxi n° Tis s ue dist n b uti on Rep rer ec seep nt ot ar st i ve Eff ec to r/ro le Gaa 、 .`. ,i 、u 1 (( 22XX l'( 4445..27 JOO CCTTXX uL'bb iiqq uu iittoo uu ss TBASHRd, , ogtlhu ec ras g o n , } Tll CNAada2e·' n ccyhh laaa ntne nn eecllyss c l ase aul f M.7 88 CTX Olefap ci ttho ef )l'i u nm e u ro- Odoran t l Adeny la te cyc la se G Oaa iit~lI 444000...355 18읽080 PPPTTTXXX NNUbeeaaiqrr ullyy i t o uuubb s iiqq uuiittoouu ss M2, Ch oot,h e ars z AR, !1! CKA a+d2e ' ncchyha laan tnne ne elcsly sc l ase ( ?) aaooAu
표 2-2 포유류 G - 단백질 B 와 r 소단위체 들 의 성 질 들 . Subunit (kDMa Xas 1s0 -3 ) % Aidme riitn i ot y aa c id Tis s ue dist ri bu ti on Eff ec to r /ro le 8 131 37.3 100 Ubiq uitou s Re qu ir ed for Ga- re cept OJ B2 37.3 90 Nearly ubiq u ito u s int e r acti on 83 37.2 83 Nearly ubiq u ito u s Inl1ib i ti on of G 。 acti va ti on 84 37.2 89 Nearly ubiq u it ou s Modulate acti va ti on of cer~ tain adeny la te cyc l ase~ by G ` 。 or calmodulin Sup port of ago nis t - i n d ucec recept or ph osph ory la ti or and desensiti za ti on r r1 8.4 100 Reti na , oth e r(?) i Phosph olip a se C r2 7.9 38 Bra in, adrenal, oth e r(?} i K' channels(?) r3 8.5 8.5 Bra in, tes tis r4 (?partial) (34) [Kidn ey, reti na (?)] l Phosph o li pa se A,.(?) 75 7.3 7.3 Liv e r, oth e r(?) 76 7.5 7.5 Bra in, oth e r(?) h% Amino acid ide nti ty: comp ariso n is with the first-li s te d member of each family . 실레이션도 유사한 메커니즘으로 일어나는데 이 경우는 C- 말단 근처에 있는 시스테인 잔기에 ADP- ri bose 가 붙는다. 콜레라 독소에 의해 a 소 단위체가 변형되면 G- 단백질의 GTPase 작용이 억제됨으로써 이 단백질 울 계속해서 활성화시키게 되며, 백일해 독소에 의한 변형은 수용체에 의한 G- 단백질의 활성을 막아 주는 억제 작용을 하는 것으로 알려져 있 다. G- 단백질의 어느 소단위체도 세포막의 지질 이중충과 회합할 수 있
 바닥 상태 수용체 환성
바닥 상태 수용체 환성
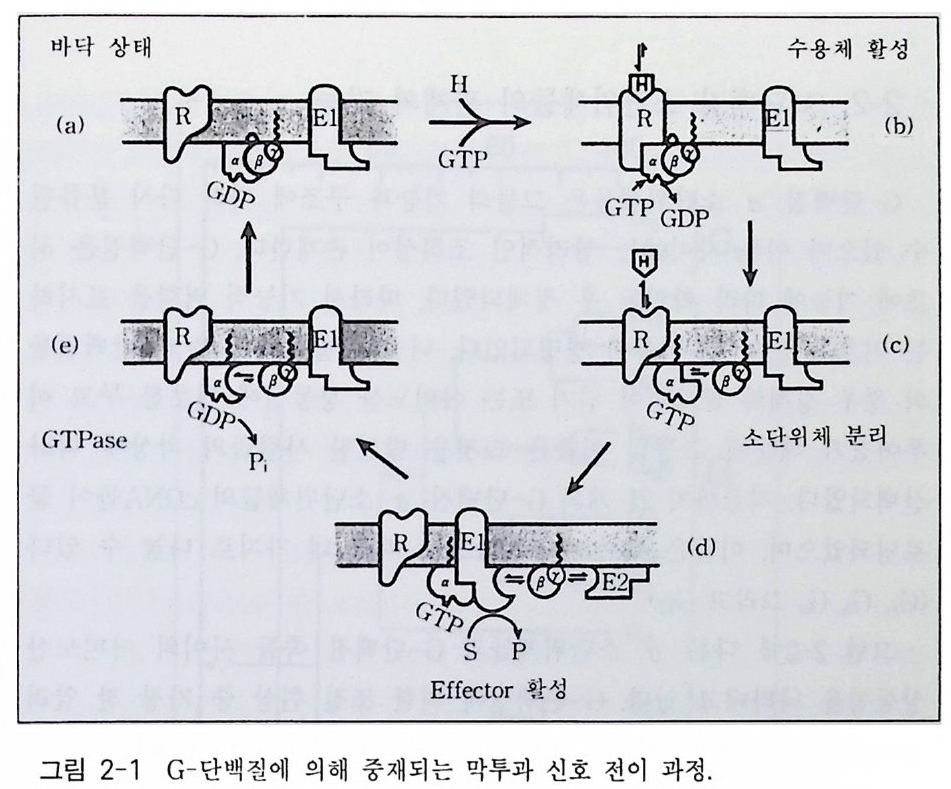
는 부분을 가지고 있지 않는데, 이종삼량체의 G- 단백질은 원형질막에 결합되어 있다 이 사실은 Y 소단위체가 p ren y la ti on 되어 있고 몇몇 a 소단위체들이 m yris t o y la ti on 되어 있기 때문이다. G- 단백질의 지질에 의한 변형이 이 들 소단위체들로 하여금 막에 결합할 수 있는 능력을 부여하게 되며 a 와 /3 r 의 친화력도 증진시키게 된다 (l) . 그림 2-1 에 수용체, G- 단백질 그리고 eff ec to r 분자들 간의 상호작용을 표시하고 있으며 G- 단백질의 활성과 비활성 순환 과정에 대한 자세한 내용도 설명하고 있다.-
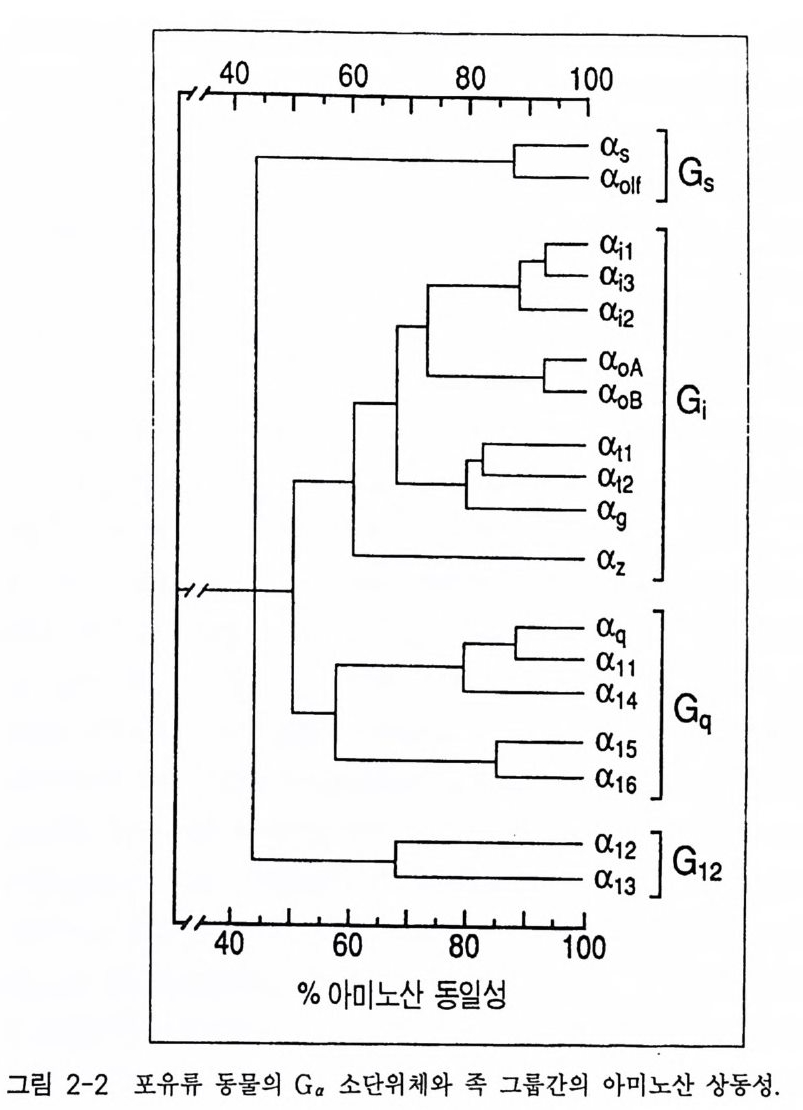
2-2 G- 단백질 소단위체들의 관계와 기능 G 단백질 a 소단위체들은 그들의 기능과 구조에 따라 다시 분류될 수 있으며 이들 사이에는 합리적인 조화성이 존재한다 . G- 단백질은 최 초에 기능에 따라 확인된 후 정제되었다. 따라서 기능적 역할을 표시하 는 기호롤 붙여 그 이름이 명명되었다. 나중에 발견된 많은 G- 단백질 들 의 경우 정제와 클로닝이 염기 또는 아미노산 상동성에 기초 를 두고 이 루어졌기 때문에 그들의 이름은 그것을 발견한 사람 들 의 착상에 따라 선택되었다. 지금까지 21 개의 G- 단백질 a 소단위체 들 의 cDNA 들이 클 로닝되었으며, 이들은 아미노산 상동성에 따라 네 가지로 나눌 수 있다 (Gs, G;, Gg 그리 고 G12). 그림 2-2 에 다른 a 소단위체들과 G- 단백질 족들 사이의 아미노산 상동성을 나타내고 있다. G- 단백질에 의한 조절 현상 중 가장 잘 알려 진 두 가지 예가 호르몬의 자극에 의해 활성화되는 아데닐레이트 시클 라제계 (2) 와 광선에 의해 활성화되는 cGMP 포스포디에스터라제계 (3) 인 데, G- 단백질과 수용체 그리고 eff ec to r 분자와의 상호작용을 이해하기 위한 가장 대표적인 모델로 이용하고 있다. 두 경우 특정한 G - 단백질이 참여한다는 결정적인 증거는 정제한 성분 (a 소단위체와 eff ec to r 분자)을 재구성하는 실험으로 확인되었다. 이와 같은 연구들은 특정한 신호 전이 경로에서 G- 단백질이 참여한다는 사실을 가장 강력하게 입증해 주는 것 이다. 호르몬이나 냄새의 수용체들은 Gs 족의 G- 단백질과 상호작용을 하 여 아데닐레이트 시클라제를 활성화시키며 그 결과 cAMP 의 합성을 촉 진한다. 단일 모체인 mRNA 로부터 alte r nativ e s pli c i n g에 의해 Gs 의 경우 4 개의 구별되는 폴리펩티드로 발현된다(분자량 44,200~45,700). 이들 단 백질들은 SDS 겔 상에서 분자량 45,000(Gsa-s) 과 52,000(Gsa-L) 을 갖는 두 개의 명확한 밴드로 분리된다. 그러나 이들 단백질들의 기능상 차이 점은 아직 명확히 알려지지 못한 상황이다. 지금까지 알려진 아데닐레이
 , 4I0 ' • 6I0 • I 8I0 I 10I 0
, 4I0 ' • 6I0 • I 8I0 I 10I 0
트 시클라제의 이성질체들은 5 개가 있으며 이들 모두는 G sa 에 의해서 활성화된다. Folf 단백질 소단위체는 후각 신경 내피 세포에서 전적으로 발현되며, 냄새 수용체와 냄새 특이성 아데닐레이트 시클라제를 연결시 키는 작용을 할 것으로 생각된다. G sa 의 경우 아데닐레이트 시클라제의
활성 이외에 적어도 두 개의 이온 채널을 조 절 하 는 것 으 로 알려져 있다. G sa 에 의해 조절되는 두 개의 이온 채널 들 은 골격 근 육 세 포 에 존 재하 는 디히드로피리딘 (deh y dro pyridi ne) 에 민감한 전압 의 존성 Ca2’ 채널과 심장 세포에 존재하는 N 집 채널이다 . 눈 세포에 존 재하 는 광수용체인 로 돕신은 tr ansduc i n(G t)을 자극하여 cGMP 특 이성 포스포디 에 스 터라제 를 활성화시켜 세포질 내에 존재하는 cGMP 의 농도 를 감소시킨다. G t1의 경 우 망막의 간상 세포에서 거의 다 발현이 되 는 데 비하여, 트 렌 스 ;구신의 두번째형인 Ge 의 경우는 원추 세포에서 발현되며 원 추 세 포 에 존 재하는 옵신과 포스포디에스터라제의 활성화를 연 결 시키 는 작용을 하 는 것으로 관찰되고 있다 최근에 g usduc i n 이라고 부 르는 새 로운 G - 단백질 (G 서이 혀의 미각기관에서 발견 (4) 되었는데, G g 와 G1 의 경우 아미 노산 서열이 매우 유사 (80 %)하였고, 특히 수용체와 eff ec to r 분자들이 상호 작 용하는 a 소단위체 부위는 더욱 유사하였다. 야의 작용에 관해서는 아직 정확 한 정보가 없는 상태이댜 광범위한 부류의 호르몬, 신경 전달 물질 , 성 장 인자들의 생리적 작용이 PLC 의 활성화 능력으로 설 명되고 있다. PLC 는 PIP 2 라는 인지질의 한 종류를 가수분해시켜 IP :i 와 DAG 를 생성시 키는 효소라는 사실은 잘 알려져 있다. 수용체에 의한 PLC 의 활 성화 과 정에서 백일해 독소나 콜레라 독소에 민감하지 않은 G - 단백 질들도 관여 하고 있다는 증거가 여러 곳에서 얻어지고 있다 . 적어도 8 개의 a 소단 위체들이 이들 박테리아의 독소에 의해 변형되지 않는다는 사실이 밝혀 졌다. 최근 보고들에 의하면 이 경로의 조절자로서 역할을 수행하는 G- 단백질들이 존재한다는 것이다. 소의 뇌와 쥐의 간에서 G IJ와 Gu 의 혼합 물음 정제하였는데, 이들과 매우 유사한 단백질을 칠면조의 적혈구에서 도 분리하였다. 이들 단백질들과 정제한 PLC /3 1 을 재구성한 결과 효소 를 특이적이고 현저하게 자극한다는 사실을 발견하였다. 정제된 PLC/ 31 , PLC/ 32 그리고 PLC /3 3 와 정제된 Gq a 또는 Gua 등과의 재구성 실험에 서도 이들 현상을 관찰할 수 있었다. Gq, G11 그리고 G14 온 많은 조직들
에서 발견되나 G q족에 속하는 G1 5 와 G1 6 은 혈액 생성 세포 들 에서만 발현 되 는 것으로 알려져 있댜 G1 5a 와 G1 6a 는 G q a 와 아미노산 상동성은 별로 높 지 않다 (57 % 와 58 % ). 이와 같은 제한된 조직 분포는 이들 단백질들 의 특 이한 신호 전달 역할 을 암시하는 것이다. 그러나 재구성 연구에 의 하면 정제된 G1Ga PLC/ 31 , PLC/ 32 그리고 PLC /3 3 를 활성화한다는 것이 밝혀졌댜 GII 족 에 속하는 G - 단백질들과 PLC 이성질체 들 과의 상호작용 에 관한 득 이성 을 결정 하기 위해서는 더 많은 연구가 진행되어야 한다. 백일해 독소는 제한된 수의 조직들에서 PLC 의 호르몬에 의한 활성을 억 제하 는 데, 이 사실은 G 와 같은 단백질의 참여를 시사하는 것이다. 그러 나 지금까지 G 와 G 。 같은 단백질이 이 경로에 참여한다는 결정적인 증 거는 없 는 상태이댜 GI 아속에 속하는 몇 가지 단백질들과 effe c to r 분자 들 사이의 직접적인 상호작용에 관하여는 아는 바가 적은 편이다. 백일 해 독소 가 많은 세포 반응 들 을 차단시키는데, 이 사실은 다양한 신호 전 달 경로에서 Gj 족의 단백질들이 참여하고 있다는 사실을 암시하는 것이 다. 지금까지의 연구 결과에 의하면 아데닐레이트 시클라제의 저해와 몇 가지 이온 수송로들의 활성화 또는 억제작용 등에 G 족이 관여하는데 이러한 작용들은 세 개의 Gj a 소단위체들과 Goa 의 두 개의 spl i ce v ari an t 들 의 역할에 기인하는 것으로 생각된다. 많은 호르몬 수용체들의 자극이 아데닐레이트 시클라제 활성도를 억제하는데 , 이 반응을 백일해 독소의 처리로 막을 수 있다 G 단백질이 참여하는 많은 반응들이 있음 에도 불구하고 정제된 G i a 를 사용하여 아데닐레이트 시클라제의 활성도 를 억제하는 시도들은 제한적으로 성공했을 뿐이다 (5, 6). 이들 관찰들은 Gi 중합체로부터 유도된 8 r 가 아데닐레이트 시클라제의 활성제인 Gsa 와 이 효소가 간접적인 상호작용에 의해 억제된다는 생각을 하게 되었 다 (7). 또 다른 설명으로 다음의 두 가지를 제시한 바가 있다. B r 는 어 떤 특정한 아데닐레이트 시클라제를 직접 억제할 능력을 가지고 있을 수 있다는 개념과 이 효소의 활성도에 대하여 Gia 단백질의 효과가 간
접적으로 작용할 가능성도 있다는 것이다. 백일해 독소 에 민감한 G- 단 백질들도 근육이나 신경세포 등에서 이온 채널 들을 조절한 다. 예 를 들 면 무스카린 콜리너칙 수용체들이 심장의 수축 세포에서 K 채널 을 활성화 시킨다. 그 경로는 백일해 독소에 의해 차단되며 채널의 활 성 도는 구아닌 뉴클레오티드에 반응성을 나타낸다. 이들 세포로부터 잘라 낸 막의 조각 들에 활성화된 Gia 단백질을 첨가하면 K 채널이 활 성화되 는데 Gia 1, Gi a2 그리고 Gi a 3 모두가 같은 정도로 작용한다 (8). 어떤 신경세포의 K 채 널들도 백일해 독소에 의해 같은 방법으로 활 성화된다. 그러 나 아직도 인지질 층에 위치한 K 채널과 G - 단백질의 a 소단위체들과의 직접적 인 상호작용은 알려지지 않았고, 다만 어떤 사람 들 은 G - 단 백질의 /3 r 소단위체가 중요한 역할을 할 것이라고 믿고 있다. G 와 G- 단백질들의 세포 내 농도가 G s 와 G q의 농도보다 훨씬 더 높다. 뇌에서 G oa 는 막단백 질의 l~2 %를 점하고 있는데, 이 사실은 이 단백 질 이 K ' 과 Ca 앙 채널 만을 조절하는 데 사용될 것이라는 생각이 타당치 않음을 시사하는 것 이댜 그렇다면 왜 Go 가 신경 성장 원추 세포에 농축되어 있을까? 최근 의 연구 결과들은 G 족에 속하는 단백질들이 세포 내 깊숙한 곳에 있 는 경우들도 조절할 수 있다는 사실을 제시하고 있다. 콩팥 세포에서 Gi a 3 는 골지체 복합체에 위치해 있음이 발견되고 있다. 이 들 세포에서 Gi a 3 가 과다하게 발현되면 단백질의 분비와 수송이 둔화되며, 이 효과는 백 일해 독소의 처리에 의해 그 효과가 역전된다 (9) . 곰팡이 독소인 brefe l- din A 라는 물질은 골지체막의 코트 단백질인 f3 一 co p의 방출을 자극하여 골지체막과 소포체막의 병리적 융합을 촉진시킨다. 세포를 GTPrS 와 AlF4- 로 처리하면 brefe ld i n A 의 작용울 역전시킨다. G_ 단백질의 /3 r 소단위체를 cell-fre e s y s te m 에 첨가하면 GTPrS 에 의해 중재되는 f3 -co p의 골지체막에 결합을 막아 준다. 이 발견들은 G 아속에 분류되는 이종삼량체의 G- 단백질이 막의 수송에서 중요한 조절 역할을 한다는 사 실을 시사하는 것이다 . G- 단백질과 짝을 지은 수용체들의 작용을 나타
낼 수 있는 펩 티 드인 mas t op aran 이 골지 체 막에 /3 一 co p의 결합을 자극하 며 brefe ld i n A 의 효과를 차단한댜 이 발견들은 이종삼량체의 G- 단백질 들 의 작용이 세포 표면에서 막투과성 신호 전달에만 국한되지 않는다는 강한 증거를 제시하는 것이다 . 전통적으로 a 소단위체가 G - 단백질의 거의 전부라고 생각해 왔다. 왜 냐하면 이것에 GTP 가 결합하며 가수분해되고 e ff ec t or 와 상호 작용하기 때 문 이다 . 그러나 현재는 /3 y 소단위체 복합체도 조절 인자로서 중요한 역할하는 것으로 알려져 있다. GDP 가 결합된 a 소단위체를 안정화시키 며 G - 단백질 복합체를 막에 고정시키는 일도 /3 r 의 역할이다. 최근에는 /3 y 자신도 eff ec to r 단백질들과 기능적으로 상호 작용할 수 있다는 증 거 들 이 제시되고 있다, 포유류 동물계에서 /3 r 가 eff ec to r 단백질과 상호 작용한다는 직접적인 생화학적 증거가 아데닐레이트 시클라제의 다른 이 성질체 를 연구함으로써 얻어졌다 . 대부분의 조직들에서 발현되는 아데닐 레이트 시클라제들은 /3 r 에 의한 조절에 크게 면역이 되어 있는 것으로 보고되어 있으나, 뇌에서 발견되는 몇 개의 효소들은 유형에 특이적인 양 상으로 /3 r 에 의해 조절된다(1 0). 유형 I( G s a 와 칼모듈린에 의한 활성)의 아데닐레이트 시클라제는 /3 r 에 의해 직접 억제되며, 유형 II 와 유형 IV 에 속하는 효소들은 /3 r 에 의해 조건부로 활성화된다. /3 r 는 G s a 가 있 을 때만 활성을 나타낸다. 이 사실은 신호 전이 경로에서 교차 대화 (cross-ta l k) 에 대 한 가능성 을 나타내 는 것 이 다. 다른 eff ec to r 분자들도 /3 r 에 의해 조절되는 것으로 나타나고 있다. HL-60 의 gran ulocyt e 에 있 는 PLC 가 /3 r 에 의해 크게 활성화된다 (11). /3 r 는 K+ 채널의 활성도에 도 영향을 미치는 것으로 알려지고 있는데 (12), 아직은 이들 효과가 직접 적으로 전달되는 것인지 아니면 간접적으로 전달되는 것인지 확실하지 않은 상태이다. 최근에 /3 r 는 활성제에 의해 유도되는 수용체의 인산화 와 둔화 현상에도 참여하는 것으로 보고되고 있다 (13). 상기의 사실들은 막에서 G- 단백질 소단위체들의 분해는 a 와 /3 r 모두를 통하여 평행적
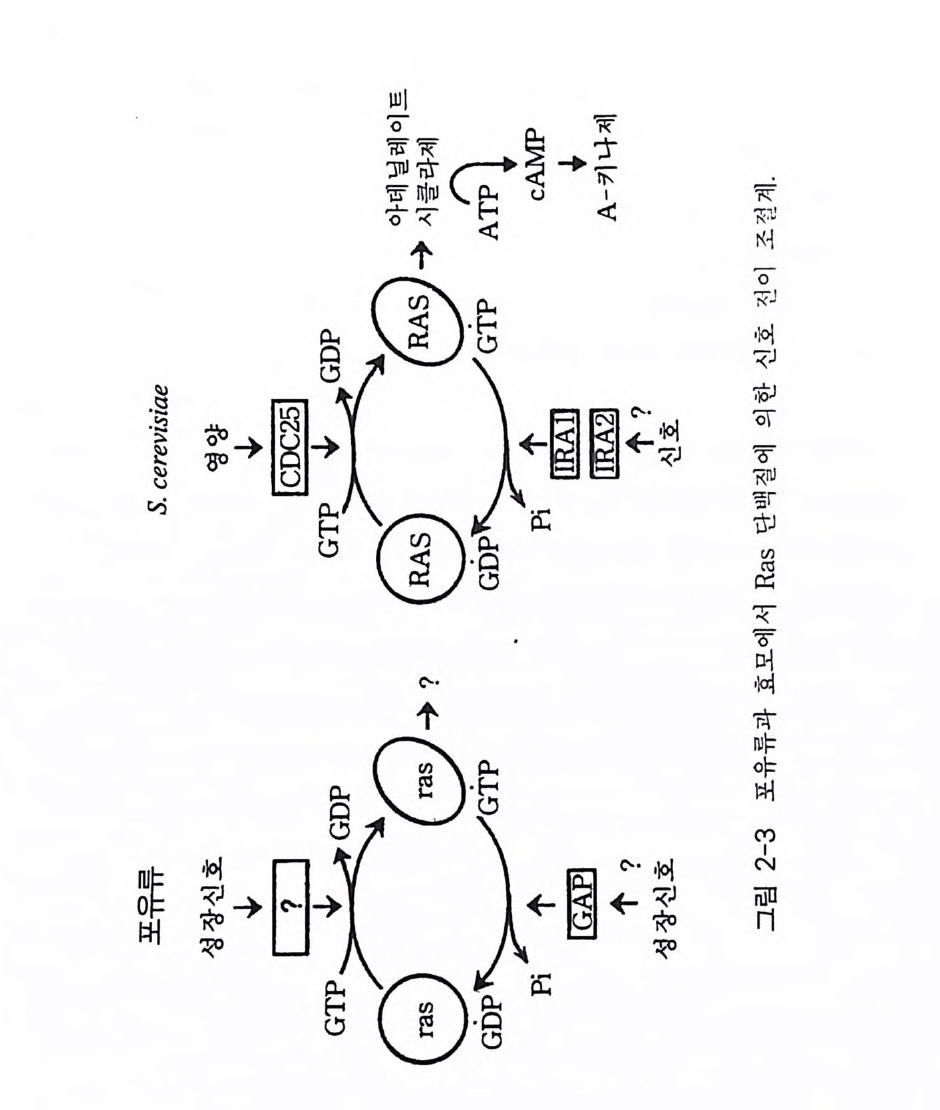
이거나 또는 상호적인 신호 들을 생성시 킬 수 있 는 것 이다 . G- 단백질에 의해 조 절 되는 경 로들 은 보다 많 이 존 재하며 , 분 명히 밝 혀지지 않은 있지 않은 몇 가지 세포 반응 들 이 구아닌 뉴 클 레오티 드 에 의존성을 나타내며, AlF 4- 에 의해 활 성화되고 , 백일해 독소 에 민 감 하게 반응하는 것으로 알려진 바 있다. G - 단백 질 에 의해 조절될 가 능 성이 있 는 eff ec to r 분자들로는 PLA 2 와 PLD 그리 고 수많은 이 온 채 널 등 이 제 시되고 있다. 가능한 세포 반응 들 은 성장 조 절 , 티 로 신 키나제 성장 인자 수용체들의 효과 , 세포 외로의 분비 현상 그리고 단백 질 수송 등을 생 각 할 수 있다. 이들 경로에 참여하는 수용체 들 , G - 단백 질들 그 리고 ef- fec to r 분자들은 아직 알려져 있지 않다. 2-3 Ras 단백질 ras 유전자의 발현에 의해 만들어지는 Ras 단백질은 작 은 분 자량 을 갖는 G - 단백질의 일종이다 . ras 유전자들은 처음에 쥐의 악성 종 양 바이 러스의 종양 유전자 (onco g ene) 로서 발견되었으며, 나중에는 사람의 특 정 종양을 유발시킬 수 있는 세포 내 유전자로 확인되었다. 진핵 세포 들 에 존재하는 Ras 단백질들의 구조는 상호 높은 상동성을 나타내는데, 이 사 실은 세포의 기능에서 그들의 역 할 이 필수적임을 말해 주는 것이다. Ras 단백질들이 GTP 와 결합하고 그것을 가수분해시킨다는 사실과 지질에 의한 변형을 통하여 원형질막과 결합한다는 사실은 Ras 단백질도 G- 단 백질과 같이 막투과성 신호 전이계에서 전달자로서 작용할 수 있음을 시사하는 것이다. 그러나 Ras 단백질과 G- 단백질 간의 성질 면에서는 몇 가지 다른 점들이 있댜 Ras 단백질들은 단량체이며 G- 단백질들은 삼량체이다. GTPase 의 활성도는 Ras 의 경우 G- 단백질보다 매우 낮다. 따라서 교환 반응을 촉진시키기 위해 요구되는 EP 이외에 GAP 에 의한
GTP 가수분해가 Ras 의 경우 꼭 필요하댜 정제된 재조 합 Ras 단백질들 은 결합된 GTP 의 가수분해는 물론 결합된 GDP 의 교환 속도가 매우 느 리댜 Ras 단백질의 기능은 세포의 유형에 의존성을 나타내는데, 섬유 아세 포 들 에서 Ra s - GTP 는 세 포 분열을 자극하며, 쥐의 PC12 세포와 신경돌 기 세 포 에서 는 세포 분화를 자 극한 다 . 더욱 홍미 있는 사실은 효모의 Ras 단백질은 포유류 세 포들 에서의 G ,,(J와 같이 아데닐레이트 시클라제 를 자극한다 (14). 2-3-1 포유류의 Ras 단백질 포 유류의 ras 유전자 족 (H a , Ki, N- ras) 은 가장 잘 연구된 pro to - oncog en e 중의 하나이다(1 5) . 이 유전자들은 21 kDa 크기의 단백질(p 21) 을 암호화하고 있다 E. col i로부터 정제된 재조합 p 21 을 사용하여 연구 한 결과 p 21 에도 GDP/GTP 가 결합하고 가수분해되는 현상이 관찰되었 다( 그림 2-3). Ras p 21 의 GTPase 활성도는 GAP 라고 불리는 세포질 단 백질에 의해 크게 상승된다 . 역유전자 방법 (reverse g ene ti cs) 에 의한 기 능적 영역의 분석 결과는 p 21 의 생물학적 기능에서 결합된 GDP/GTP 의 중요성을 보여주고 있다. 따라서 ras 유전자 산물들은 세포의 분열이나 분화와 같은 오랜 시간대에 일어나는 세포 반응들을 조절하는 신호 전 달 GTP 결합 단백질로 생각된다 . GDP 가 결합된 p 21 과 GTP 가 결합된 p 21 의 생물학적 활성도를 비교해 보면 전자는 비활성이고 후자는 활성 을 나타낸다(1 6). Val-12 돌연변이체나 viral Ras p 21 과 같은 Ras p 21 들 은 효모 (S. cerevis ia e ), 쥐의 세포(pc 12), NIH 3T3 세포들에 존재하는 wil d- 유형의 Ras p 21 보다 GTP 가 결합한 형으로 더 많이 존재한다. Ras p 21 의 GDP 결합형과 GTP 결합형의 삼차원 구조를 분석해 보면 두 군 데에서 입체 구조의 차이를 나타낸다 (17). 첫번째 부위는 아미노산 잔기
 GTP @:麟아이트제시➔ 기 AA McP四A + 조이 전.절계
GTP @:麟아이트제시➔ 기 AA McP四A + 조이 전.절계
30~38 사이에 있으며 eff ec to r 인지 영역이다 . 두번째 부위는 잔기 60~ 76 사이에 존재한다 단일 항체인 Yl3-259 는 두번째 부위에 결합함으로 써 Ras 에 의해 중재되는 신호 전이를 저해한다 . 두 부위 모두가 Ras p21 과 GAP 의 상호작용에 필수적이댜 세포에서 GDP / GTP 가 결합된 Ras p 21 의 측정은 Ras 의 신호 전이 체 계의 전반부 를 이해하는 데 매우 유용하다. 전체 Ras p 21 과 GTP 가 결합 된 Ra s p 21 의 양의 비율이 Ras p 21 의 활 성도를 나타내기 때문에, Ras 의 e ff e c t o r 는 확 인되지 않았더라도 GTP 가 결합된 p 21 의 농도 변화를 측정 합으 로 써 , 신호 전달 체계의 전반부에서 Ras 활성도를 정량할 수 있는 것 이댜 성장 인자로 처리된 세포와 처리하지 않은 세포에서 Ras p 21 의 활 성 도를 비 교함으로써 혈소판-유도 성 장 인자, 표피 성 장 인자, CSF-1 들 이 리간 드 첨가 후 수 분내에 Ras p 21 을 활성화하는 것을 보여준다. 그러 나 bFGF, 인슐린, 봄베신 등은 아무런 효과가 없었다(표 2-3 ) . Ras p 21 과 연결된 성장 인자 수용체들은 원래 티로신 키나제 활성도 를 가지며 , 미지의 표적 분자들의 티로신 인산화가 성장 신호 전이에서 중요하다고 생각되고 있다 . 성장 인자 수용체로부터 Ras p 21 까지 무엇이 신호 를 중재하는지는 아직 밝혀져 있지 않다. GTP 가 결합된 Ras p 21 의 축적은 src/abl 또는 erbB- 2 등을 발현시키는 종양 유전자와 함께 변형 체 들 에서도 관찰되었다(표 2-3). 이 결과들은 Ras 가 어떤 종류의 티로신 키나제 들 의 후반부에서 기능을 한다는 사실과, Ras 의 활성도를 통한 이 들 키나제들의 비조절적 활성화 (unre gul a t ed ac ti va ti on) 가 변형의 원인이 된다는 사실을 보여주는 것이다. NIH 3T3 세포에 anti -R as p21 항체인 Y13-259 를 주사하면 혈소판-유도 성장인자와 표피 성장인자에 의해 유 도되는 DNA 합성이 억제된다 (18). src 또는 frns 티로신 키나제에 의한 세포 분열이나 변형에서 중요한 역할을 한다는 사실을 암시하는 것이다. Ras p 21 이 혈소판-유도 성장인자 또는 표피 성장인자의 신호 전이에 참 여한다는 사실은 정상 세포와 ras 전이 세포들에서 제시된 바 있다.
표 2-3 GAP 의 티 로신 인 산화 와 성장 인자의 자 극 및 종양 유 전자 환성화 에 의 힌 p2 1- G TP 증 가 . Phosp h o 111l at i on Inc re a s e of Ty ros in e kina se of GAP p21 • GT P GrO\ vth fac to r recept or PDGF- R + + EGF- R + + FGF- R IGF- 1- R CSF- 1- R (c • fms) + + Oncog en e pro duct src + +?. fps +++ ab! + erbB- 2 + Ras p 21 의 신속한 활 성 화는 PHA(ph y toh emag glu ti nin) 또 는 anti -C D3 항체로 처리한 T ― 림프구에서도 관찰되었다. 이 경우 PKC 가 T 세 포 의 수 용체 와 Ras p2 1 사이 에 참여 하며, GAP 활성 도의 감소가 PKC 자 극 후 관찰되었다 (19). Ras p 21 의 활성도 조절 메커니즘은 아직 명확하게 밝혀 지지 않고 있다. 아마도 두 유형의 메커니즘에 의해 Ras p 21 이 활 성화되 는 것으로 추측된댜 하나는 GDP/GTP 교환 중가이댜 이종 삼량체로 구성된 G- 단백질의 경우 활성제와 결합된 수용체는 a 로부터 GDP 의 방 출을 시작하며, a 소단위체는 활성형의 GTP 결합 구조로 바뀌게 된다. 몇몇 성장 인자 수용체들의 경우 활성제가 결합하면 Ras p 21 에 결합되 어 있는 GDP/GTP 교환을 자극할 수 있다는 제의가 있다. 표피 성장 인 자와 혈소판-유도 성장 인자는 p 21 에 결합되어 있는 구아닌 뉴클레오티 드의 교환을 자극하는 것으로 보고되었는데 (20), 정확한 속도론적 개념 또는 수용체와 p 21 간의 상호작용 메커니즘 등은 밝혀져 있지 않다. 성장
인자 수용체들과 Ras p21 사이에는 또 다른 어떤 성분이 참여할 가능성 도 있다 최근에 Ras p 21 에 결합된 GDP/GTP 의 방출을 자극하는 단백질 이 몇몇 실험실에서 정제되었다 (21, 22). Ras p 21 의 활성화에 대한 다른 가능성은 GTPase 의 억제이댜 세포에서 Ras p 21 의 GTPase 활성도는 GAP 에 의해 크게 증가한댜 만일 GAP 의 활성도가 전반부의 성장 신호 들 에 의해 감소된다면 GTP 와 결합한 활성을 띤 Ras p2 1 은 축적될 수도 있댜 따라서 GAP 는 Ras p 21 의 가능한 조절자 후보가 되는 것이다. 2-3-2 GTPase 활성화 단백질 Trabey 등(1 6) 은 Ras p 21 의 GTPase 의 활성도를 증가시키는 단백질을 발견하였다. 그러나 성게 난세포의 추출물에 존재하는 활성화되어 있는 돌연변이체에서는 이러한 작용이 없었다. GAP 의 활성도는 많은 종류의 조직과 배양된 세포들에서 확인되었다. E. col i로부터 정제한 재조합된 Ras p 21 의 경우 전이된 돌연변이체의 Ras p 21 의 GTPase 의 활성도에 비 해 10 배나 감소하였다. 그러나 돌연변이된 Ras p 2 1( val-12) 의 GTP 결합 에 따른 삼차원 구조의 반감기는 정상적인 Ras p 21 보다 긴데, 그 이유는 GAP 의 효과로 생각된다. 소의 뇌에서 정제한 GAP 은 125kDa 의 단백질 이며 그 일차 구조는 cDNA 클로닝으로부터 결정되었다. 이 GAP 은 아 미노산 1044 개로 구성되어 있으며 SH2 와 SH3 영역을 가지고 있다. c- 말단 영역의 1/3 정도면 Ras p2 1 의 GTPase 를 자극하는데 충분하다. GAP 를 발현시키는 유전자가 사람의 염색체 5 에서 지도화되었다 (23). Val-12, Thr-59, Leu-61 이 돌연변이된 Ras p2 1 들의 GTPase 는 GAP 에 의해 활성화되지 않았으나 이들 돌연변이체들은 GAP 과 상호 작용하는 데 정상적인 Ras p 21 과 경쟁할 수 있다. 그러나 effe c to r 결합 영역에서 아미노산이 치환되어 돌연변이화된 Ras p 21 의 경우는 정상적인 Ras p2 1 과 GAP 의 상호작용에 영향을 미치지 않으며, GAP 은 이들 돌연변이체
의 GTPase 활성도를 올리지 못한다 (24). Ras 유도성 전이의 억제제로 알려진 Rap lA 단백질 (25) 은 eff ec to r 결합 영역에서 아미노산 서열이 Ras p 21 과 동일하댜 Ras p 21 의 GAP 에 의한 GTPase 의 자극이 정제된 성분들로 재구성한 계에서 Rap lA 단백질에 의해 억제되었다. Rap lA 단 백질의 GTPase 활성도는 GAP 에 의해 활성화되지 않는데, Rap lA 단백 질에 특이성을 가지는 GTPase 활성 단백질이 보고된 바 있댜 GAP 의 효과는 몇 종류의 인지질들에 의해 억제되는데 그 인지질 들 은 포스파티 딕산, 포스파티딜 이노시톨 포스페이트, 아라키돈산 등이며, 이들은 성장 인자의 자극에 의한 반응으로 생성되는 것으로 알려져 있다. 어떤 인지 질과 관계되는 물질들이 Ras 에 의존적으로 유사 분열을 일으킬 수 있 기 때문에 인지질들이 GAP 을 통한 Ras 활성도를 조절할 가능성을 갖 게 된다 최근에는 각종 티로신 키나제들과 GAP 이 생화학적으로 연결되어 있 다는 증거들이 보고되고 있다 . 그 첫번째가 GAP 의 티로신 인산화이고, 두번째가 GAP 과 혈소판-유도 성장 인자 수용체의 물리적인 회합아다. GAP 은 혈소판-유도 성장인자와 표피 성장 인자에 의해 빠르게 티로신 잔기가 인산화되는 데 비하여, 인슐린이나 염기성 섬유 아세포 성장 인 자는 이런 효과를 나타내지 못한다 (26). 인산화되지 않은 GAP 이 대부분 세포질에 위치하는 데 비하여 인산화된 GAP 은 세포막에 위치한다. 돌연 변이체들에서도 GAP 은 티로신 잔기의 인산화가 일어나는데, 그것을 인 산화시키는 키나제는 수용체와 유사한 종양 유전자 티로신 키나제이며 src, fps , fms , abl 등의 생성물이다 (26). 두 개의 단백질들 p6 2 와 p 190 도 티로신이 인산화되며 GAP 에 의해 같이 침전으로 떨어진다. 그러나 이들 두 단백질은 아직 그 특성들이 연구되지 않은 상태이다. 티로신의 인산 화가 GAP 의 기능을 조절할 가능성이 있다. 인산화된 GAP 은 Ras p 21 의 GTPase 활성도 자극을 감소시킬 가능성이 있으며, 또한 GAP 의 인산화 는 GAP 의 위치와 기능을 조절하는 다른 신호 전이 참여 성분들에 대한
친화력을 변화시 킬 가 능 성이 있다 . 그러나 지금까지 이에 대한 증거는 없는 상태이다 . 혈소판 - 유도 성장 인자 수용체는 리간드가 결합하면 PLC- r , PI-3 키나제 , raf pro to - o n cog e ne 산물들과 회합한다 . 이 복합체를 STP(sig n al tra ns fe r parti cle) 라고 부 론 다 ( 27) . 회합된 성분들은 수용체 티로신 키나 제의 직접적 인 기 질 이며 효소의 활성도는 인산화에 의해 증가된다 . 최근 에 GAP 이 PDGF - STP 에 회합되는 것이 발견되었댜 키나제의 삽입 영 역 을 삭제 했을 때 수용 체 가 PI-3 키나제와 GAP 과 결합하는 능력이 상 실 되 는 데 비해, PLC- r 나 Raf 단백질과는 그렇지 않았다. 이 사실은 성 장 신호의 다 른 유형 들 이 이 들 성분 들 을 통하여 전달될 수 있음울 시사 하는 것 이댜 GAP 은 Ra s p 21 과 직접 그리고 특 이하게 상호 작용하는 유일한 단백 질인데 아직도 GAP 의 생리적 역할에 대해서는 아는 바가 거의 없는 상 태이다 아마도 GAP 는 Ras p 21 의 가능한 표적 분자일 수 있다는 것이 다. 이 러 한 사실을 뒷받침 하는 몇 가지 발견들이 있는데, CD Ras p 21 이 GTP 의 존 성으로 GAP 에 결합한다. ® GAP 는 Ras p 21 과 e ff ec t or 의 상 호작용에 꼭 필요한 부위라고 생각되는 effe c to r 영역에 작용한다는 것이 다. @ Ras p 21 의 돌연변이체들도 GAP 와 결합한다. 최근에 artial 세포 에서 Ras p21 - G AP 복합체가 무스카린 수용체가 K 채널과 짝짓는 것 을 방해한다는 결과가 보고되었다. 이 사실 또한 상기의 개념과 일치하 는 것이댜 효모의 ras 에 대해서도 많은 연구 결과들이 보고되어 있으나 본 장에 서는 그 내용의 기술은 생략하기로 하되 필요하면 참고문헌 (28) 을 참조 하면 될 것이다. 효모에서도 GAP 과 같은 성질을 갖는 단백질이 발견되 었으며 그들의 유전자안 IRA1 과 IRA2 에 의 해 이 들이 발현된다는 사실 도 보고되었다.
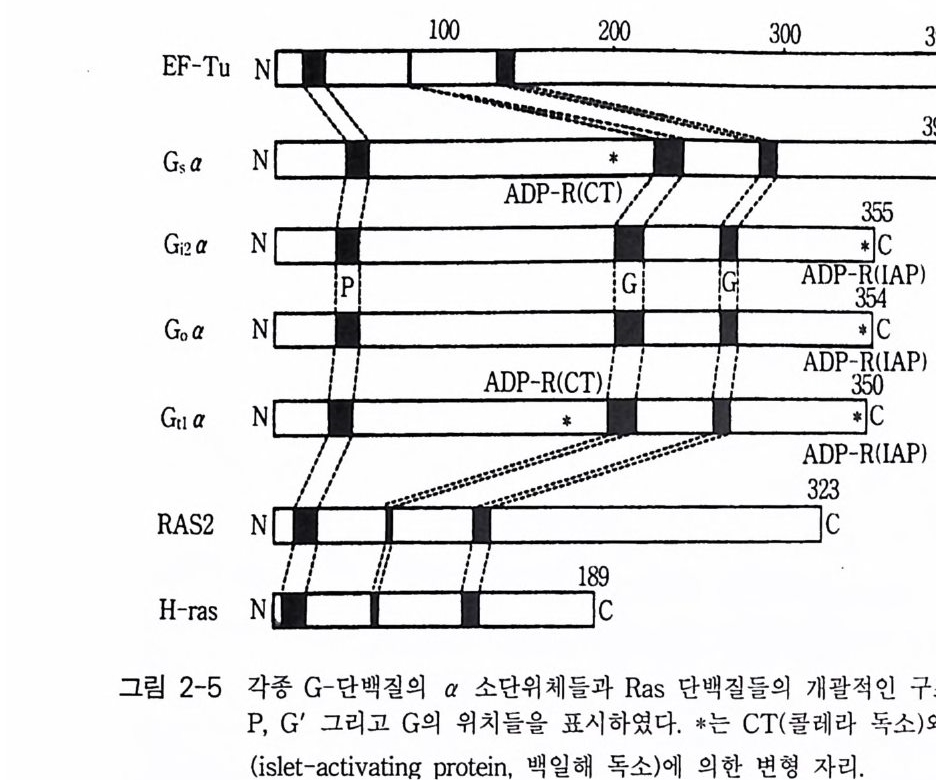
2-4 G- 단백 질들의 구조적 유사성 각종 G ―단백질들의 일차 구조의 유사성을 살펴보면 몇 개의 영 역에서 높은 아미노산 상동성을 보인다(그림 2-4, 2- 5 ). 지금까지 알려진 G- 단백질들에서 높은 상동성을 나타내 는 부분 들 을 P, E, G', G, G'’ 로 나누어 설명하고자 한댜 P 부위 이 부위 는 공통적 인 서 열 양상이 G-X - X - X-X - G - K - S / T 인 데, 이 구 조는 G- 단백질들에서뿐만 아니고 많은 뉴클레오티 드 트리스포스페이트 를 사용하는 효소에서도 공통으로 나타나는 특성아 있다. 이 부위는 아 마도 가수분해 과정에 직접 참여하는 것으로 생각된다. Ha-ms p21 단백 질의 글리신 -12 를 발린이나 다른 아미노산들로 돌연변이시키면 GTPase 의 활성도가 없어지고, 전이 활성도가 증가되는 것이 관찰되었다 . EF-T u 와 Ras 단백질의 x- 선 분석은 이 부위가 결합된 GDP 의 f3와 r 인산기에 가깝 다는 사실을 확인하였다. 또한 리신 -16 의 아미노 그룹은 GTP 의 f3 또는 y 포스페이트와 그리고 루프에 있는 아미노산 10 번과 11 번의 주사슬 산소 들 과 수소결합을 형성하는 것을 발견하였다 (29). Ras 단백질의 Ser- 17 에 있는 히드록시 산소는 M g 2 님 과 상호작용을 한다. E 부위 이 부위는 Ras 의 아미노산 잔기 32~42 를 포함하며 effe c to r 분자와 상호 작용하는 자리로 알려져 있다. ras p21 단백질의 이 부위에서 돌연 변이가 되면 GTP 결합 성질에 영향을 주지 않고 전이 활성도의 상실을 초래하게 된다. 이 부위의 아미노산 서열은 다른 족들 간에는 크게 보존 되지 않는 반면 같은 족간에는 크게 보존된다.
 (A) a X X X X O KS/T
(A) a X X X X O KS/T
 100 200 300 3
100 200 300 3
ctivat
ing protein, 1� |�t� ų��)�� X� \� ��� ��|� G' ��� t� ��ǔ� Ras �1����X� ���� G TPase X� 0���t� ��h���� ��� . �� ���x� ��� ����@� D-X-X-G- Qt�p� �����X� G- �1������� ���� �t���� ���. Ras �1���X� DŤ��t��Ұ� -57 �� �x� G- �1������� ���� ��Q�XՔ� DŤ��t��Ұ� ��0��t� D�ȹij Mg 2+ �� ��i���� �ǔ� �� <�\� ����� ���. Ras �1���X�성도 를 강하게 격감시키는 반면 전이 활성도는 강화시킨다 . 최근 보고 (30) 들 에 의하면 G - 단백질의 이 부위를 돌연변이시키면 어떤 세포들에 서는 종양 유전자 표현형을 나타낸다는 것이다. 상응하는 부위에서 EF- Tu 의 아미노산 서열은 D-C-P-G - H 인데, 이 부위는 리간드 교환 (GDP 로 부터 GTP 로)에 의해 유도되는 삼차원적 구조의 변화를 일으키는 자리로 알려져 있다. G 부위 이 부위는 GTP 의 구아닌 고리와 직접 상호 작용한다 . 공통적인 서열 양상은 N ― K ― X-D 이며 모든 G - 단백질들에서 보존된댜 EF-Tu 의 연구 에서 N-K-C-D 서열의 변형 (C y s-137) 은 GTP 와의 상호작용을 파괴한다 는 결과를 관찰하였다. 그 후 이들 네 개의 아미노산 잔기들이 구아닌 고리와 가깝게 위치해 있다는 사실을 x- 선 분석으로 알아내었다. Ras 단백질에서는 As p -119 의 —CO OH 그룹이 구아닌 고리밖에 있는 아미노 그룹과 고리 내에 있는 질소 1 번과 상호 작용한다. G 부위 이 부위는 Ras 단백질의 3 차원 구조에서 GTP 의 구아닌 고리에 가깝 게 위치하고 있다 . Ras 에서 이 부위의 보존된 아미노산 서열 양상은 E-T-S-A-K 이며, G 단백질들에서는 상응하는 부위의 아미노산 서열이 N_(F/ M )-T-C 一 A-(TN)-D-T 이 다. 2-5 G- 단백질 a 소단위체들의 구조와 기능 신호 전이에서 G_ 단백질의 중요성을 말할 때 역시 이종삼량체 G- 단 백질이 대표성을 가지며, a fJ r 의 세 개 소단위체들 중 GTP 결합 부위
를 가지고 있는 a 소단위체가 중요한 소단위체임을 부정 할 수가 없다. 따라서 전반적인 G - 단백질의 구조 와 기능에 대해서 는 앞 절 에서 언 급 하 였지만 이 절에서는 a 소단위체의 구조와 기 능 에 대하여 좀더 세밀하 게 알아보고자 한다 . 그림 2-6 에 9 개 G- 단백질 들 의 a 소단위체의 1 차 구조 를 비교하여 표 시하였는데 그 구조적 상동성이 전체적으로 매우 높 음 을 발견할 수 있 댜 표 2 -4 에서 보여주는 바와 같이 전체적인 구조의 높은 상 동 성에 부 가하여 아미노산과 뉴클레오티드 서열의 강한 보 존 현상이 나타나고 있 다 . G s a 의 아미노산 서열이 사람과 쥐의 경우 매우 높 게 보존되고 있 는 데 394 개의 아미노산들 중 1 개만이 다 르 다. Gi l a 의 서열은 소와 사람에서 완전히 동일하다 G2 a, Gi3 a, Gn a 그리 고 Gxa 의 경우 다른 표유류들 사이에서 98 % 의 상동성이 유지되었다. G- 단백질 a 소단위체들의 진화 양상은 다양한 포유류들로부터 얻은 예 상되는 아미노산 서열들 간의 차이점들에 기초하여 그릴 수 있다(그림 2-2). 3 개의 G- 단백질 a 소단위체들의 아속은 Gs , GI, 그리고 G t이다. 세 개의 GIa 종들 사이의 상동성이 G s a 와 Gt a 아속들의 상동성보다 높 다 는 사실은 놀랄 만한 일이다 . 그림 2-5 는 E. col i의 EF-Tu, Ga, 효모의 Ras2 단백질 그리고 Ha-Ras p2 1 단백질들의 구조 를 개략적으로 보여주 표 2-4 다른 포유류 종들 간에 G- 단백질 a 소단위체의 아미노산 서열의 보존 spec ies a Amino acid seq u ences Nucleoti de seq u ences rGs a VS hGs a 393/394(99.7 % ) 112 8/11 82(95.4 %) bGit a VS hGit a 3541354( 100%) 998/1062(94.0 % ) rGi 2a VS hGi2 a 350/35 .5( 98.6%) 98.5 /1 065(92.4 %) rGha vs hGha 349/354(98.6%) 981/1062(92.4 %) rGoa VS bGoa 348/354(98.3 % ) 99'2 j10 62(93.4 %) rGxa VS hGxa 349/ 懿 (98.3%) CJ77 /1065(91 .7% ) ah, 사람 ; r, 래트; b, 소
 bk.b'bcC22.t노CCC`t. .iob l I••I 2,`.C~ 2•l•lll., o•'.m·•lb .,1,‘’,’'C ,O.,. .,`,`..2.‘,’82 。,1' . .1...-.--..’l-.1- -- ' 1.. .•-1 ~꾼 •-1•.1... .,,..’,,•..•11, -.. .'• •1 ..,-1• '.•1-•.c,.l •1••'o .•,H. .•'o` .. • o. ..,. c•o. .c•.0.LTToTT凰0GL.c .a. ..X翼重oX翼XMEOE a.o .Oa.`•,.H>o• a.LN....T^•c cy,s•T^·^Lo . .X3., . TL^ 'o`. X >.TVo•X^.翼cX.`•T ' ` ^ ^V·-·.X--T•XT^--^.•VT E IToZ、oQ0Qoq 、o-鼻X • V TE •X VlI•-Tl•xl-•XIl Vl x-E`E鼠-K.K.-•-lX1.Vx-•- 1 . •--•QXxV- •l•xol XlL•l•-•l`xG • ••l ILl ••I- NM•X II• VXVI• I•X-•I•IV••X•II• II •IX•aI•”翼XMIK.•II-I ^o .•I X I••S. ^A를^,^.-^.o •I ' • q•a s •^、^01••Go •••La••Y•`,a ••.• •LA, c홀홀..量. , •o . V.'• • _•C.-o^. L •^.• Aa.>. - ••-.,-A-.-.翼XXXX.XIIX-. •.s- -- . .I--K•.- ·-.--.-z.--.I ---•--I--- .-I---,--•--M I .--- -I.• -·~•KOEAI--•-- I • --•-^QL - u --- •--o..-'-L^.a- -•-I-‘L-- X•·1-`IoQ•、• -- • L H• -- •L·`.·讐-.重• ~ N -3 .L • -o••-.L- - I•••--.-XL-•^.. •-· L-• ^---.•-.-••OIL-- • ·• --•.-- - .-•-••-^重y‘xio•-•. -• .- •- •- -..A.·.-Y .--• ..-T - .z . x·xA. •I•^A^0.t ^ .^.^.0X.^.TT0 ^0I.^.to·rV^v.T蠶tYYY.TY'Y.0I. X` v. .C` 0TAXQIX翼tIXUXXI•V yK·o . Xy^o-VAA1,'쇼 Lo` LI-. V IVL.1V•V tII VI V ·XV VLI.TYXVOZ.TX.GV, T ITIT T
bk.b'bcC22.t노CCC`t. .iob l I••I 2,`.C~ 2•l•lll., o•'.m·•lb .,1,‘’,’'C ,O.,. .,`,`..2.‘,’82 。,1' . .1...-.--..’l-.1- -- ' 1.. .•-1 ~꾼 •-1•.1... .,,..’,,•..•11, -.. .'• •1 ..,-1• '.•1-•.c,.l •1••'o .•,H. .•'o` .. • o. ..,. c•o. .c•.0.LTToTT凰0GL.c .a. ..X翼重oX翼XMEOE a.o .Oa.`•,.H>o• a.LN....T^•c cy,s•T^·^Lo . .X3., . TL^ 'o`. X >.TVo•X^.翼cX.`•T ' ` ^ ^V·-·.X--T•XT^--^.•VT E IToZ、oQ0Qoq 、o-鼻X • V TE •X VlI•-Tl•xl-•XIl Vl x-E`E鼠-K.K.-•-lX1.Vx-•- 1 . •--•QXxV- •l•xol XlL•l•-•l`xG • ••l ILl ••I- NM•X II• VXVI• I•X-•I•IV••X•II• II •IX•aI•”翼XMIK.•II-I ^o .•I X I••S. ^A를^,^.-^.o •I ' • q•a s •^、^01••Go •••La••Y•`,a ••.• •LA, c홀홀..量. , •o . V.'• • _•C.-o^. L •^.• Aa.>. - ••-.,-A-.-.翼XXXX.XIIX-. •.s- -- . .I--K•.- ·-.--.-z.--.I ---•--I--- .-I---,--•--M I .--- -I.• -·~•KOEAI--•-- I • --•-^QL - u --- •--o..-'-L^.a- -•-I-‘L-- X•·1-`IoQ•、• -- • L H• -- •L·`.·讐-.重• ~ N -3 .L • -o••-.L- - I•••--.-XL-•^.. •-· L-• ^---.•-.-••OIL-- • ·• --•.-- - .-•-••-^重y‘xio•-•. -• .- •- •- -..A.·.-Y .--• ..-T - .z . x·xA. •I•^A^0.t ^ .^.^.0X.^.TT0 ^0I.^.to·rV^v.T蠶tYYY.TY'Y.0I. X` v. .C` 0TAXQIX翼tIXUXXI•V yK·o . Xy^o-VAA1,'쇼 Lo` LI-. V IVL.1V•V tII VI V ·XV VLI.TYXVOZ.TX.GV, T ITIT T
고 있댜 요들은 몇 개 부위에서 잘 보존된 아미노산 서열을 가지고 있 댜 이들 보존된 서열들의 작은 부분들이 EF-Tu 와 Ras 단백질들의 구 아닌 뉴클레오티드 결합 영역에 기여되는 서열들의 부위와 상동성을 갖 는댜 이 부위들이 아마도 GTP 결합, GTP 가수분해 그리고 다른 구아 닌 뉴클레오티드들에 의한 삼차원 구조 변화의 핵심적 역할을 하는 구 조를 형성하는 것으로 생각된다. 이들 부위들을 P, E, G, G' 그리고 G 로 표기하였으며, 몇 개의 연구실에서 P, G', G 부위에 위치한 아미노산 들을 치환하는 실험을 수행하였다. Gsa 에서 Gl y - 49 를 발린으로 치환한 결과 GTP 가수분해의 반응 속도 상수 값을 낮추어 주었다. 그림 2-4A 에 표시된 바와 같이 Gxa 의 P 자리에 있는 3 개의 아미노산 잔기 (T S-N) 들은 다른 a 에 있는 아미 노산 잔기들 (A-G-E) 과 다르댜 이 차이 가 다른 a 들과 비교하여 Gxa 의 낮은 GTPase 활성도를 갖게 하는 것이 아닌가 생각된다 (31). Casey 등의 보고 (31) 에 의하면 돌연변이 방법을 이용하여 이 부위에 있는 아미노산 서열을 Gxa 의 것으로 바꾸었을 때, 재조합된 Gs a 돌연변 이체는 wil d- 유형의 Gsa 에 비해서 l
성장 호르몬을 분비하는 뇌하수체의 종양들에서 G s a 의 돌연변이가 나타 났다 (33). 돌연변이 자리 중의 하나는 G , a 의 글루타민 -227 이며, 이것은 Ras 단백질들의 글루타민 -61 에 해당되는 것이다. 돌연변이 연구 결과에 의하면 G s 。 227 번의 글루타민을 류신으로 치환하였을 때 GTPase 의 활 성도가 감소되며 G s a 의 활성도가 유도된다는 것이다. 콜레라 독소는 Gsa 와 G t a 의 ADP- 리보실레이션을 시키며, 그 결과는 GTPase 의 활성을 감 소시킨다. G t a 에서 변형의 자리는 아르기닌 -174 이며 G s a 에서는 아르기 닌 - 201 이다. Gil m an 등 (34) 은 이 아르기닌을 알라닌, 글루타민산, 리신 등으로 치환했을 때 Kca t GTP 가 감소한다는 사실을 발견하였고, 이들 돌연 변이된 단백질들은 GTP 의 존재 하에서 아데닐레이트 시클라제를 계속 적으로 활성화시킨다는 사실을 발견하였다 . 뇌하수체의 종양들에서 발견 되는 G s a 의 돌연변이는 GTP 의 가수분해를 저해하며, 아데닐레이트 시 클라제의 활성도를 상승시킨다. 모든 알려진 G ―단백질들의 a 소단위체 들은 아르기닌 -201 에 해당되는 자리에 아르기닌 잔기를 가지고 있다. 부 신 피질의 종양의 돌연변이체들은 보존된 아르기닌 -179 가 시스테인 또 는 히스티딘으로 치환된 G2a 가 발견된다. Gsa 의 아르기닌 -201 주위에 있는 아미노산 서열은 G t a 뿐만 아니라 Gi a 와 Goa 의 서열과 큰 상동성을 나타낸다. 활성화된 수용체는 HL60 세포들에서 콜레라 독소에 의해 백 일해 독소의 기질을 ADP- 리보실레이션시킨다는 사실이 최근에 보고된 바 있다. 이 결과들은 모든 G- 단백질들의 a 소단위체들의 보존된 아르 기닌 잔기가 활성화된 수용체와 상호 작용함으로써 가면이 벗겨질 수 있으며 GTP 가수분해의 조절에서 중요한 역할을 수행할 수 있다는 것 이다. Gsa 의 C- 말단에 위치하는 것으로 예상되는 a- 헬릭스가 수용체와의 접촉 부위라는 사실이 강하게 입증되고 있다. c- 말단에 위치한 4 개의 아미노산 잔기들 중 백일해 독소에 의한 시스테인의 ADP- 리보실화가 수용체와 G- 단백질의 상호 작용을 방해한다. 망막의 간상체 세포에 존
재하는 arres ti n 의 중간 부위의 아미노산 서열은 G t a 의 C - 말단 서열과 유사하다 (35). Arres ti n 은 G t a 와 경쟁적으로 인산화된 로돕신에 결합한 다. G- 단백질 a 소단위체의 C - 말단에 상응하는 합성한 펩티 드들 도 G- 단백질과 수용체들의 상호 작용을 저해할 수 있다. Chim eri c a 소단위체 의 분석은 G s a 의 C- 말단의 40 % 가 수용체와 상호 작용하는 데 특 이하게 참여한다는 것이다. G s a 의 C - 말단 부위 근처에 있는 서열을 GI a 의 것으 로 치환하더라도 GDP 의 분리와 GTP 가수분해 속도가 변하지 않으며 , G s a 의 돌연변이는 G s a 의 세포막에 재조합 후 GTP 의 촌 재 하에서 아데 닐레이트 시클라제의 활성을 증진시킨다. G , a 의 C - 말단에 있 는 아마노 산 38 개를 G,2a C- 말단 아미노산 36 개로 치환한 chi m eri c a - 단백질이 포유 동물 세포에서 발현되었다. 이 Gs a/G; a ch i mera 가 발현되는 세포 에서 아데닐레이트 시클라제는 활성제없이도 수용체에 의해 계속적으로 활성화되었다. 활성제가 없을 때 GTP 유사체에 의한 cAMP 의 합성의 지체기는 관찰되지 않았다. 이러한 지체기는 a 소단위체로부터 GDP 가 늦게 분리되기 때문인데, 활성화된 수용체가 GDP 의 분리 속도 를 가속화 시키기 때문에 지체기가 없어지는 것으로 추측된다. 이들 자료는 G s a 의 c- 말단의 치환이 GDP 분리 속도를 간접적으로 증가시키는 결과 를 초래 한다는 사실을 시사하는 것이다. 그러나 활성화된 수용체가 a 단위체로 부터 GDP 분리 속도를 가속화시키는 구체적인 메커니즘은 아직 확실하 지 않댜 참고문헌 1) Lin d er, M. E., et al. (1991) J Bio l. Chem. 266, 4654 2) Gih nan, A G. (1987) Annu Rev. Bi oc hem. 56, 615 3) Str yer , L. (1986) Annu Rev. Neurosci. 9, 87
4) McLaug hl in , S. K., McK inn on, P. J. and Margo lskee, R. F. 0992) Natu r e 357, 563 5) Kata d a, T., et al. 0984) ]. Bi ol. Chem . 259, 3586 6) Lin d er, M. E., et al. 0990 ) ]. Bi ol. Chem. 264, 8243 7) Gil m an, A. G. 0984) Cell 36, 577 8) Yata ni, A., et al. 0988) Natu r e 336, 680 9) Sto w , ]. L., et al. 0991) ]. Cell. Bi ol. 114, 1113 10) Tang , W. J. and Gil m an, A. G. (19 91) Scie n ce 254, 1500 11) Camp s, M., et al. 0992) Eur. ] . Bi oc hem. 206, 821 12) Log o th e ti s, D. E., et al. 0988) Natu r e 336, 680 13) Hag a, K. and Hag a , T. 0988) ]. Bi ol. Chem. 267, 2222 14) Gib b s, J. B., Marshall, M. J. 0989) Mi cr obia l. Rev. 53, 171 15) Ba rfac id , M. (1 9 얽) Annu Rev. Bi oc hem. 56, 779 16) Trahey, M. and McCorm ick , F. 0987) Sc ien ce 238, 542 17) Milbu rn, M. V., et al. (19 90) Sc ien ce 247, 939 18) Mulcahy, L. S., et al. ( 198. 5) Natu r e 313, 241 19) Downward, J., et al. (19 90) Natu r e 346, 719 20) Kamata , T., et al. (19 84) Na tur e 310, 147 21) West, M., et al. (19 90) FEES Lett . 2 59, 245 22> W olfm an, A. and Mocara, I. G. (1990) Sc ien ce 248, 67 23) Lemons, R. S., et al. (19 90) Genomi cs 6, 383 24) Cales, C., et al. (1988) Natu r e 332, 548 25) Piz o n, V., et al. (19 88) Oncog e ne 3, 201 26) Ell is, C., et al. (1990) Natu r e 343, 377 '27) Ullr ich , A. and Schlessin g er , J. (1990) Cell 61, 203 28) Kazir o, Y., e t al. (19 91 ) Annu Rev. Bi oc hem. 60, 349 29) Pa i, E. F., et al. (1989) Natu r e 341, 209
30) Ly on s, J., et al. 0990) Sc ien ce 249, 655 31) Casey, P. J., et al. (19 90) J Bio l. Chem. 265, 2383 32) Mi ller, R. T., et al. (19 88) Natu re 334, 712 33) Clementi, E., et al. ( 19 90) Oncog e ne 5, 1059 34) Freis s muth , M. and Gil m an, A. G. 0989) J Bio l. Chem 264, 21907 35) Sh ino hara, T., et al. 0 987) Proc. Natl. Amd Sci . USA . 84, 6975
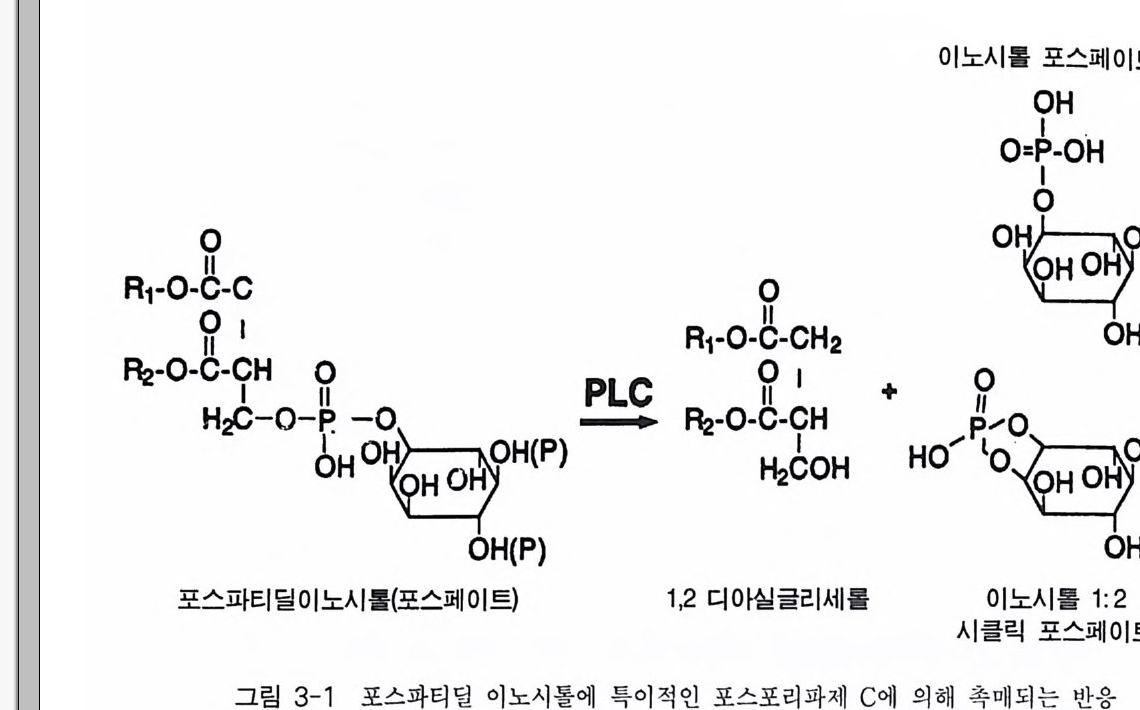
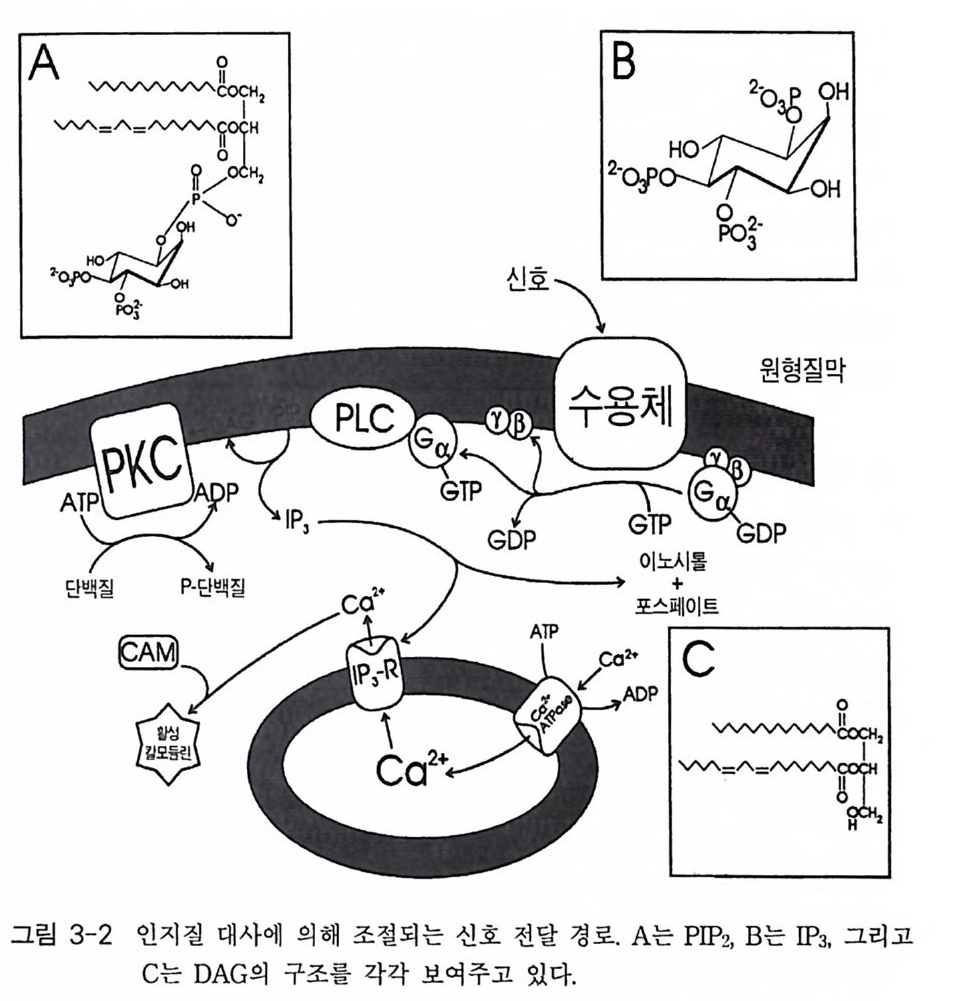
제 3 장 포스포이노시티드 제 1 장에서 언급한 것처럼 적절한 외부 신호에 의해 활성화된 수용체 는 세포 내에서 제 2 의 전령을 생성하게 된다. 이러한 신호 전이 경로 중에서 가장 잘 알려진 예로서 cAMP 계를 들 수 있는데 , 이 경우 호르 몬, 신경 전달 물질, 또는 빛 등에 의해 활성화된 수용체가 세포막에 존 재하는 단백질인 아데닐레이트 시클라제를 활성화시킴으로써 제 2 의 전 령인 cAMP 를 생성한다. 최근에 알려진 신호 전달 경로 중 또 다른 하나가 인지질 대사 과정 (ph osph ati dy l ino sito l me ta bo li sm) 인데, 이는 인지질의 가수분해로 생성된 이노시톨 트리스포스페이트(in os it ol trisp h o sph a te , IP3) 와 디아실글리세롤 (diac y lg ly c e rol, DAG) 이 제 2 의 전령으로 세포 성장 및 분화, 광 전이 반 옹, 수축 작용, 호르몬 분비 그리고 대사 조절에 이르기까지 많은 분야에 서 조절 기능을 수행하고 있다. 이 신호 전달계에서 제 2 의 전령을 생성 하는 데 관여하는 효소가 포스포리파제 C 유형의 포스포디에스터라제 이 다. 죽 의부 신호에 의해 활성화된 포스파티딜이노시톨에 특이적인 포스 포리 파제 C(ph o sph atid y l ino sito l spe cific pho sph o lip a se C, PLC) 는 포스파 티 딜 이 노시 톨 4, 5-비 스포스페 이 트(ph os p ha ti d ylin os it ol 4, 5-bis p h osph a te ,
 oI노/0A
oI노/0A
PIP2) 를 가수분해하여 제 2 의 전령 인 lP3 와 DAG 를 생성 한다(그림 3-1). 생성된 두 종류의 제 2 의 전령들 중 하나인 DAG 는 많은 동질 효소 (i soe nzym e) 를 가지 고 있는 단백 질 키 나제 C 를 활성 화시 키 는 반면 , 다 른 하나인 lP3 는 ER 이나 세포 소기관 막에 존재하는 lP3 수용체에 결합함으 로써 이들 소기관으로부터 Ca2 + 을 동원 (mob ili za ti on) 시킨다(그림 3-2 참 조). DAG 에 의해 활성화된 단백질 키나제 C 가 앞서 언급한 세포 반응, 예 롤 들면, 세포 성장, 분화, 호르몬 분비 등의 반응을 조절한다. 또한 lP3 에 의해서 증가된 세포질 내의 Ca2+ 이 Ca2+ 의촌성 단백질, Ca2+ /칼모듈 린, 또는 Ca2+ 의존성 단백질 키나제의 활성화를 통해서 동물 세포뿐만 아니라 식물 세포에서의 세포 반응을 조절하고 있다(1, 2, 3, 4). lP3 는 lP3 키나제에 의해 인산화되어 lP4 를 생성하게 되며 생성된 lP4 역시 다양한 세포에서 Ca2+ 의 농도를 조절하고 있다. 또한 I(l, 3, 4, 5)P4 는 다른 종류
 A 。
A 。
의 IP 라 lP5, 그리고 IP 려 전구 물질로 작용하기도 하는데, 이들 lP4, lP5, 그리고 IP 려 생리학적 역할은 아직 알려져 있지 않은 상태이다 (5, 6, 7, 8).
3-1 포스파티딜 이노시톨 대사 3-1-1 포스파티딜 이노시돌들 포스포이노시티드(p hos p ho i nos iti de) 는 D-m y o- i nos it ol 이나 인산화 형 태의 D-m y o- i nos it ol 의 1 번 탄소 및 글리세 롤 골격의 3 번째 탄소와 포스 포디에스터 결합에 의해 형성된 포스포글리세라이 드 이다( 그 림 3-2 A). 일반적으로 세포 내에는 3 종류의 포스포이노시티드 들 이 있는데, 전체 포 스포이노시티드의 80% 를 차지하는 포스파티딜 이노시 톨 (PI) , 포스파티 딜 이 노시 톨 -4- 모노포스페 이 토(p hos p ha ti d y 1- i nos it ol- 4 -mono p hos p ha te, PI( 4) P), 그리 고 포스파티 딜 이 노시 톨 - 4 , 5 - 비 스포스페 이 트(p hos pha ti d y l ino sit ol- 4, 5-bis p h o sph a te , PH4, 5)P2) 로 구성 되 어 있다 . 포스포이 노시 티 드의 생합성은 1960 년대 초 소포체에서 밝혀졌는데 (9, 10), P I( 4)P 는 PI 로 부터 PI-4- 키나제에 의해서 생합성되며 다시 PH4, 5)P2 는 P I( 4)P 로 부터 P I( 4)-5- 키나제에 의해서 연쇄적으로 합성된다 (11). 모든 포스포이노시 티 드들의 ` 전구 물질 인 PI 는 CDP-DAG(cyt idine diph osph ate diac y lg ly - cerol) 중의 DAG 가 이노시톨에 결합함으로써 합성된다(1 2). 동물 세포에 있어서 PI(4)P 는 전체 인지질의 약 0.5 %이며 PH4, 5)P2 는 약 0.2% 에 지나지 않는다. 이 양은 종에 따라 약간의 차이가 있는데, 예를 들면 조류 (al g ae) 는 P I( 4)P 가 0.45% 그리고 PI( 4, 5)P 2 가 약 0.2% 이 며 (13), Dunaliel l a sal in a 의 원형질막에는 각각 5.2 % , 그리고 1. 5% 씩 존 재한다 (13). 이 양은 동물 세포나 다른 식물 세포들에 비해 6-7 배 높은 편이다. 그러나 고등 식물의 경우 이들 양은 훨씬 낮은 것으로 알려져 있다. Sarnanea , saman 의 p ul vini의 경우, P I( 4)P 는 약 0 . 2% 인 반면 PI(4, 5)P 놉 훨씬 낮은 0 . 02% 에 지나지 않는다 (14). 각 세포들마다 다른 양의 PIP 나 PIP 률 가지고 있는 것은 그 세포가 갖는 특수한 역할에 기인하는 데 예를 들어 외부 신호에 빠르게 반응해야 하는 S. saman 의 세포들은
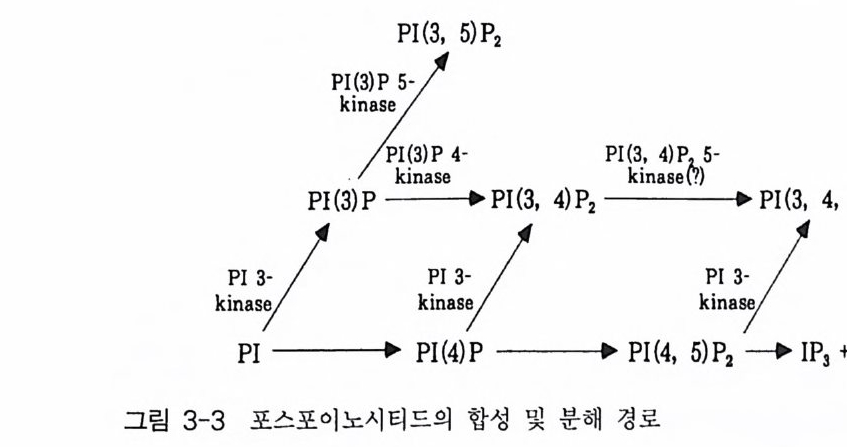
합성된 PI( 4, 5)P 2 가 분해되어 분해 산물인 제 2 의 전령들이 그 역할을 빠른 시간 내에 수행할 수 있도록 하기 위함이다. 어쨌든, 신호 전이에 참여하고 있는 PI( 4, 5)P 2 는 세포 내에서 많은 양을 필요로 하지 않는다. 왜냐하면, 빠른 시간 내에 PI 와 PI(4)P 로부터 합성되고 분해되어 JP 3 와 DAG 를 생성함으로써 대사 조절을 포함한 세포 반응을 조절해야 하기 때문이댜 동물 세포에는 이노시톨의 3 번째 탄소에 인산기를 가지는 PI( 3) P, PI (3, 4)P2 , PI(3, 5)P2 , 그리 고 PI(3, 4, 5)P3 가 있다 (3, 7, 15). P I( 3)P 는 최 근에 Sp iro dela p ol y rh i za 에서 발견되었으며 (16), P I( 3)P 와 PI( 3, 4)P2 또한 Ch-lamy d omonas eu ga ne t os 에서 발견되었다 (17) . 동물 세포에서 이들 지질 들이 성장 인자들에 의해 빠르게 증가하는데 이들 역시 세포 증식에서 제 2 의 전령으로 작용할 것으로 추측된다. 따라서 동물 세포뿐만 아니라 식물 세포에서 이들 3- 포스포이노시티드들은 세포 증식, 세포 성장, 그 리고 배우자 형성(g ame t o g enes i s) 등을 조절할 것으로 여겨진다. 3-1-2 포스파티덜 이노시돌의 생합성 앞에서 잠시 언급한 것처럼, 모든 다른 포스포이노시티드들의 생합성 을 위한 전구 물질인 PI 는 이노시톨링에 CDP-DAG 의 DAG 가 전달됨으 로써 이루어지는데 이때 관여하는 효소가 DAG 전이 효소이다(1 8). 인산 화된 포스포이노시티드들은 특수한 포스포이노시티드 키나제들에 의해 서 인산기가 PI 의 이노시톨링에 결합함으로써 형성된다 (7). 이들의 생합 성 과정은 비교적 간단하다고 할 수 있는데 포스포이노시톨 -4- 키나제에 의해서 PI 가 인산화되어 P I( 4)P 를 생성하며 다시 PI( 4) P-5 키나제에 의 해 PI(4) 가 인산화되어 PIC4,5)P2 가 생성된다(그림 3-3).
 PI( 3, 5)P2
PI( 3, 5)P2
포스포이노시톨 4- 키나제 1969 년 Harwood 와 Haw tho me09) 등이 간의 원형질막과 소포체에서 두 가지 유형의 PI 키나제를 발견한 이후, 최근에 이들 두 유형의 PI 키 나제가 섬유 아세포와 소의 뇌 세포에서 발견되었다 (20, 21, 22). 이 들 두 유형의 PI 키나제는 음이온 교환 컬럼으로부터 분리되는데 유형 1 PI 키 나제가 빨리 용출되며, 세제에 의해 활성도가 억제되지만 아데노신에 의 해서는 억제되지 않는다. 반면 유형 2 PI 키나제는 세제에 의해 활 성화 되며 아데노신에 의해서는 억제를 받는다. 유형 2 PI 키나제는 이노시톨링의 D-4 를 인산화시키며 유형 1 PI 키 나제는 이노시톨링의 D-3 를 인산화시킨다 (21) . 따라서 이들 두 유형의 PI 키나제는 동질 효소가 아니라 각각 PI 3 - 키나제 또는 PI 4- 키나제로 추정된다 Endemann 등 (22) 은 두 종류의 PI 4- 키나제를 소의 뇌로부터 분리하였는데 이들 두 효소의 분자량은 각각 55 와 230kDa 이었다. 이들 중 분자량이 55kDa 인 PI 4- 키나제는 섬유 아세포의 유형 2 PI 4 - 키나제 와 모든 성질 면에서 비슷한 것으로 나타났다. 또한, 이들 섬유 아세포나 소의 뇌에서 분리된 PI 4- 키나제와 비슷한 성질을 갖는 키나제들이 사
람의 적혈구 세포의 원형 질 막 ( 2 2 ) , 돼지의 간 , 소의 자궁 (23), 그리고 A 431 세 포 (24) 등에서도 보고되었다. PI 4- 키나제 활 성도의 조절 기작은 아직까지 잘 알려져 있지 않다. 조 절 기작을 이해하기 위해서는 in viv o 실험 에 의해 이 루 어 져 야 하는데 , PI 4 - P 의 생성은 ATP 와 PI 를 필요로 하며 생성된 PI 4 - P 가 포스 파타제 , 포 스포리파제, 또는 PI-4- P 5- 키나제 에 의해서 이 루 어진 것인지, PI 4 - 키나제에 의해서 생성된 것인지를 구 분하기가 쉽 지 않다 (25) . 그러나 PI 4- 키나제 활 성도가 cAMP, 포볼 에 스 터 (ph orbo l est e r s ) , DAG(di ac y lg l y c er o l) , concanava lin A, calciu m ion oph ore, 그 리 고 G TPr S 에 의해 조절 받는다 는 in vit ro 연구 결과를 통 해서 그 조절 기작을 유추 할 수 있다 (26) . 즉, PI 4- 키나제 활성도 역 시 PI 4 - 키나제와 G - 단백 질 을 포 함하 는 신호 전이 기작을 통해서 조절 된다 는 것 으 로 여겨진다. 포스파티딜이노시톨 3- 키나제 PI 3 - 키나제는 암 세포에서 암을 유발하는 유전자를 생성하는 전달 기작에 관여하는 것 으로 최근 알려졌는데(이 부분에 관해서는 7 장 신호 전이와 유 전 자 발현에서 상세히 다루기로 함), 이 효소는 종양 유전자를 조 절 하 는 데 관여하는 신호 전달계의 중간체들이고 단백질 티로신 키나 제 (tyro sin kina se), pp60v -sr c 그리 고 PDGF 수용체 등과 함께 분리 되 고 있다 (27, 28). 이는 PI 3 - 키나제가 종양 유전자의 생성과 관련되어 있음 을 시사해 준다 . 최근에 단백질 티로신 키나제가 PI 3 - 키나제와 결합되 어 있음이 밝혀졌다 (20) . 분리 정제된 PI 3 - 키나제는 PI 뿐만이 아니라 PI-4-P 와 PI-4, 5-P 2 의 이노시톨링의 D - 3 를 인산화시키고 있다. PI 3- 키나제는 단백질 티로신 키나제의 활성화가 관여하는 다양한 경 로에 의해서 조절되는 것으로 알려져 있다. 앞에서 언급된 PI 3- 키나제 는 pp62 v-ye s (29), v-abl, BCR-abl 종양 단백질, 인슐린 수용체 (30), CSF- 1 수용체 , v-frn s 종양 단백질 (3 1), 그리고 PDGF(32) 들과 상호작용하는
것으로 알려졌다 이러한 연구 결과들을 근거로 제안한 모델을 살펴보 면, 먼저 PDGF 에 의해 활성화된 PDGF 수용체의 활 성화가 일어날 때 PI 3- 키나제는 세포질로부터 PDGF 수용체의 C - 말단인 세 포질 쪽으로 이동하게 되며 , 이 이동은 PI 3 - 키나 제가 세포막에 존재하는 PI, PI-4 -P 또는 PI-4, 5 - P 2 를 기질로서 이용 할 수 있게 도와준다. 많은 단백질 티 로신 키나제와 그들의 기질은 약 70 개의 아미 노산 으 로 구성되 어 있는 SH- 2 영역(또는 src 상동성)을 가지고 있는데, 분리된 PI 3 - 키나제 역 시 SH-2 영역을 가지고 있다 . 포스파티딜이노시톨 -4- 포스페이트 5- 키나제 PI-4-P 5 키나제는 PI -4- P 에 있는 이노시 톨링 의 D- 5 위치를 인산화 시 키 는 데 관여 하는 효소로 PI-4 , 5-P2 를 생 성 한다. PI-4 , 5-P2 의 합성 경로에 관해서는 아직까지 자세히 밝혀져 있지 않지만 이 효소 는 세포 질에 용해된 형태나 세포막에 결합된 형태로 존재함이 밝혀졌다 (33, 34). 뇌에서 분리한 세포질에 있는 PI-4-P 5- 키나제의 분자량은 100~110 kDa 인 것으로 밝혀졌고 (35), Mori tz 등이 소의 뇌로부터 분리 정제한 막 결합 PI-4-P 키나제의 분자량은 110kDa 인 것으로 밝혀졌다. 최근 Sm ith 동은 쥐의 뇌에서 분리 정제한 이 세포막 결합 PI 4- 키나제는 GTPrS 에 의해 활성화되는 데 비해 세포질에 존재하는 효소는 GTPrS 의 영향을 받지 않는다는 사실을 밝혔다 (37) . 이는 효소가 세포질에 존재 하다가 어떤 신호 전이에 의해 세포막으로 이동하는 것이 아니라 세포 질에 용해된 형태나 세포막에 결합된 형태의 PI-4-P 5 - 키나제는 서로 다른 효소임을 시사해 주고 있다. 포스파티딜이노시톨군-포스페이트 4- 키나제 최근에 포스포이노시티드 키나제 활성도가 사람의 혈소판에서 새로이 발견되었는데 (38), PI-3-P 로부터 PI-3, 4-P2 를 생성하는 데 관여하는 효 소는 PI-3-P 4- 키나제이다. 혈소판은 트롬빈에 의해 PI( 3, 4)P2 를 통해서
조절되는데, 이 효소가 혈소판에 존재한다는 사실은 PI-3-P 키나제가 트롬빈에 의해 조절되는 세포 반응의 중간체로서 그 역할을 가지고 있 음을 시사해 준다. 3-1-3 포스파티딜 이노시롤의 생리학적 기능 P I( 4)P 의 가장 잘 알려진 역할은 PI-4-P-5 키나제의 기질로서 그리고 PI( 4, 5)P 2 의 전구 물질로서의 역할인데, PIP2 가 가수 분해되어 제 2 의 전 령인 IP3 와 DAG 를 생성하여 세포 반응을 조절하기 때문에 PIP 가 PI( 4, 5)P 2 의 전구 물질로서 중요하다는 사실이 부각되어 왔었다. Inokuch i 등 은 Jur kat 세포를 [ 3 H] 과 32 Po l 로 동시에 표지시킨 후 인지질 대사 과정 을 추적해 보았다 (39). 그들은 [3H] 의 양을 통해서 인지질의 양을, 그리 고 [ 32 p]의 양을 통해서 포스포이노시티드 키나제들에 의한 인산화 과정 을 알아볼 수 있다. 이들 실험 결과에 의하면 상당히 많은 양의 PIP 중 에서 지극히 일부분만이 PI( 4, 5)P2 의 전구 물질로 작용한다는 사실이다. 이는 PIP 가 PI( 4, 5)P2 의 전구 물질로서의 역할 이외에도 다른 생리학적 기능을 가지고 있음을 시사해 주고 있다. 한 예로서, 몇몇 액틴 결합 단 백질들이 P I( 4)P 나 PI(4, 5)P2 와 결합되어 있는데, 이들 인지질들이 액틴 (ac tin) 결합 단백질 중의 하나인 g elsol i n 을 액틴 필라멘트로부터 유리시 킴으로써 새로운 필라멘트의 형성을 조절하는 것으로 밝혀졌다 (40, 41). PIP 까 IP3 나 DAG 의 전구 물질로서 인지질 대사 과정에서 중요한 역 할을 하고 있음은 이미 밝혀졌다. PIP2 가 신호 전이 전달 과정의 중간체 로서뿐만 아니라 다른 생리학적 기능을 가지고 있는데, 이 PIP2 역시 액 틴 결합 단백질의 하나인 p ro fili n 에 결합함으로서 액틴-p ro :filin 결합체를 분리하는데 관여하는 것으로 알려졌다 (42). 이러한 연구 결과들은 PI( 4) P 나 PI( 4, 5)P 짜 PLC 의 기질로서 작용하는 것 이의에도, 죽 신호 전달 과 정에서 중간체로서의 역할 이외에도 다른 세포 내 기능을 가지고 있음
을 시사해 주는데 앞에서 언급한 세포 골격 의 조절자뿐만 아니라 PI( 4) P 의 경우, DNA 중합효소 a 의 활성도를 조절한다는 연구 결 과도 있다 (43). 그림 3-3 에서 보는 바와 같이 D- 3- p h o sph O D' lat e d p hos p ho i nos iti de 들 은 신호 전이 과정에 참여하고 있는 P I( 4)P 나 PI( 4, 5)P 2 와는 다 른 생성 과정을 가지고 있으며 제 2 의 전령인 lP 3 나 DAG 를 생성하 는 전구 물질 로서의 역할은 가지고 있지 않댜 몇몇 생화학자 들은 이 지질 둘 이 신호 전이의 전구 물질로서의 역할보다는 신호 그 자체 로 서의 역 합 이 있을 것이라는 가능성을 제시하고 있다. 앞에서 언 급 한 것처럼 PI 3 - 키나제가 단백질 티로신 키나제에 결합하고 있다. 이는 PI 3- 키나제의 생성물인 PI( 3, 4)P 라 PI(3, 4, 5)P3 가 이들 종양 단백질을 생성하는 신호 전이 전 달계와 관계가 있음을 암시하고 있다. 예 를 들 어 PI 3 - 키나제와 결합 하 는 부분을 제거한 poly o m a midd le T 돌연변이체 중에서 형질 전환에 영 향을 미치지 않은 돌연변이체의 경우, PI( 3, 4)P 2 나 PI( 3, 4, 5)P 3 가 증가한 것으로 나타났는데 이는 이 지질들이 성장을 위한 신호 그 자체로서의 기능을 가지고 있음을 시사해 준다 (44). 3-1-4 포스포리파제 c 포스포이노시티드에 특이성을 가지는 PLC 들은 포스포이노시티드 를 분해하여 제 2 의 전령인 IP3 와 DAG 를 생성하는데 관여하는 효소이다. 이 PLC 는 여러 이성질체를 가지고 있는데 지금까지 9 개의 이성질체 (a, /3L /32 , /33 , r1, r2, 81, 82 그리고 83) 들이 발견되었으며 이들은 크 게 a, fJ, r 그리고 8 등 네 개의 군으로 나누고 있다 (45). 전기 영동 법에 의해 추정된 이 효소의 분자량은 PLCa 가 57~70kDa, PLC /3가 150~154kDa, 그리고 PLCr 가 145~148kDa 그리고 PLC8 가 8.5~ 88 kDa 으로 밝혀졌다 (46). 이 네 군의 촉매 성질들은 비슷한데 가장 일반적
인 포스포이 노시 티 드들 즉, PI, PI( 4) P, PI( 4, 5)P2, (특히 PI( 4, 5)P 사를 분 해 하여 물 에 잘 녹는 IP, IP2, 또는 IP3 및 물에 녹지 않는 DAG 를 각각 생성한댜 또한 이 들 PLC 들 은 그들의 촉 매력이 Ca 앙 농도와 밀접한 관 계가 있 는 데 , 특 히 PI( 4, 5)P2 를 가수분해할 때 Ca 앙 의존성이 높다 (47) . 그림 3 - 4 는 PLC /3, Y , 그리고 8 군의 아미노산 서열을 보여 주고 있댜 이 들 세 군은 X 와 Y 로 불리는 비슷한 아미노산 염기 서열을 보여 주고 이 들 은 각각 150 개와 1240 개의 아미노산으로 구성되었다 . 이들 두 영역은 각각 60 % 와 40% 의 아미노산 상동성을 가지고 있다. 다시 말해 X 영역은 이 들 세균의 아미노산이 최소한 60% 가 같으며 Y 영역의 경우 세 군 사이의 아미노산이 상동성이 40% 이다. PLC/ 3 PLC f3 는 G - 단백질에 의해 활성화되는데 (45, 48, 49) G- 단백질에 관해 서는 이미 2 장에서 자세히 언급하였다. G - 단백질 p 유형 (G 값이 PLC 를 활성화시킨다고 알려져 있는데, 최근 PLC 을 활 성화시키는 G- 단백질 q 유형 (G십 이 분리 정제되었다 (50). Gq 계 는 적어도 5 개의 G- 단백질들이 있는데, Gq, Gu, G14, G1s, Grn 이 그것이 다 (51). 이들 중 G q와 Gu 의 아미노산 상동성이 88% 인데, PLC· 를 활성화 시키는 능력이 거의 비슷하다 (52, 53). 이들 두 G 一단백질들은 PLC /3 1 을 활성화시키지만 PLCr1 이나 PLC01 은 활성화시키지 못한다 (45). 여러 Gp 계의 G- 단백질 중에서 각각은 PLC/ 3 이성질체들 중에서, 선택적으 로 활성화시키고 있다. 이들 결과는 다른 외부 신호들에 의해 활성화된 수용체가 바록 PLC f3를 활성화시키는 여러 G- 단백질이 존재하지만 그 중에서 필요한 G- 단백질을 활성화시켜 궁극적으로 그 역할에 적절한 PLC/ 3 이성질체를 선택적으로 활성화시킴으로써 좀더 세분화된 신호 전이 체계를 통해서 세포 반응을 조절하고 있음을 시사해 준다.
PLC- r PLC /3가 Gq 유형의 G - 단백질에 의해 환 성화되 는 것과는 단리 PLCr 는 단백질 티로신 키나제에 의해 PLCr 의 티 로 신 잔기가 안산화되면서 활성화된다. PLC r 의 티로신 인산화 는 혈소판 - 유 도 성 장 인자(p lalclcl · deri ve d gro w th fac to r , PDGF) 나 표 피 성 장 인 자 (c pi dcnnaI gro wlh fac to r , EGF) 에 반옹하는 세포에서 일어나는데, 이 튤 세포사 표내 상장 인자 수용체, PLC/ 3, PLC8, 그리고 PLCr 튤 가지고 있지 만 표피 상장 인자의 자극에 의해서 인산화되 는 것은 오직 PLC r 뿐이다 (55). PLC r 는 SH3 영역을 가지고 있 는 데 이 들 영역 윤 src 상 동성 이라 일컫는 다. src 상동성 (SH 영역)은 신호 전이 과정에서 단백전 과 단백질 사이의 상 호 작용을 나타내는 부위 를 의미한다. PLCr 1 과 PLCr 2 의 SH 영역 윤 삭제시킨 후 PLC 활성도를 측 정했 을 때 PLCr 활 성도가 상 실 되었 는 데, 이는 PLCr 들이 이 영역을 통해서 다 른 단백 질 (예 률 들 면, 표피 성장 인 자 수용체)과 상호 작용을 통해서 활성화되고 있음을 시사해 주고 있다 (56). PLCr1 의 티로신이 활성화된 표피 성장 인자나 혈소판 - 유도 성장 인자 수용체들에 의해 인산화되어 PLCr1 이 활성화되지만 티 로 신 키나 제 활성도를 지니고 있는 다른 수용체(예 를 들 어 인슐린 수용제나 CSF- 1 수용체)들은 PLCr1 을 인산화시키지는 못한다 (57, 58). PLCr1 은 티로신 키나제에 의해 티로신 잔기가 인산화되면 활성화되지만 티로신 포스파 타제에 의해 탈인산화가 일어나면 활성도를 상실하게 된다 (59). PLCr1 은 4 개의 티로신 인산화 자리가 존재하는데 분리 정제된 표피 성장 인자 수용체가 티로신 771, 783, 1254, 그리고 472 를 인산화시키는 것으로 밝혀졌다 (60, 61). 티로신 잔기 472 는 PLCr1 의 X 부위에 인접해 있으며, 771 과 783 은 SH- 영역 사이에 죽, 조절 영역 사이에 존재하며, 1254 는 PLCr1 의 C- 말단 부근에 존재한다 (63, 그림 3-4). 티로신 771, 783, 1254 는 PLCr1 의 주요 자리로 알려져 있으며, 472 는 그렇게 중요하 지는 않은 것으로 알려져 있다 (61).
분리 정제된 표 피 성장 인자나 혈소판- 유 도 성장 인자 수용체는 PLC r1 의 771, 7& 1 그 리 고 12 여 를 인산화시칸다 . 이 들 세 자리 중 티로신 7 8:-3옹 메닌안라닌으 로 치환시켰을 때, 혈소판 - 유도 성장 인자에 의한 PL C 의 환성화는 완전히 억제되었으나, 티로신 1254 의 돌연변이체는 약 11() % 시해되었고 터 로 신 771 의 돌연 변이체 는 약 50% 증가하였다 (62). 이 튤 안. IL ·산 과 는 PLCm 이 세 포질 에 촌 재하다가 혈소판-유도 성장 인 자나 표 피 상상 인자에 의해 세포가 자극받으면 PLCr1 은 세포질에서 세포막으로 이 상하게 되 는 대, 이 는 PLCr 1 의 SH ― 영역이 티로신 키나제 환성도읍 지닌 수용체와 전합 하여 인산화되 는 동시에 활성화되면서 세 포막 에 존재하다가 포스포 이 노시티드둘응 분해하여 제 2 의 전령을 생성 하고 있음을 시사해 준다. PLCr :! 환성도는 hae m ato p o iet o r 세포 에서 많이 발견되는데, PLCr2 역 시 SH- 2 및 SH - 3 영 역을 가 지고 있으며 PLC r 1 의 티로신 - 771 이나 783 과 유사한 티로신인 티로신 759 를 가지고 있다 . 그러나 PLC r 1 의 C- 말단 부근에 존 재하는 T y r - l254 와 유사한 티로신을 가지고 있지 않다(그림 3-4 참조). 이 동질 효소의 활 성화 경로는 지금까지 알아본 PLCr 의 경우와 거 의 비 슷 하다 . PLCr 2 를 rat- 2 세포 (64) 나 NIH-3T3 섬유 아세포 (65) 에 과 발현시켰옹 때 혈소판-유도 성장 인자 수용체 또한 PLC r 2 를 인산화시켰 댜 비 록 혈소 관 유도 성장 인자 수용체가 PLCr 2 를 인산화시켰지만 혈소 판-유도 성장 인자 수용체는 일반적으로 haemato p o iet o r 세포에는 존재하 지 않기 때문에 혈소판-유도 성장 인자 수용체가 PLCr2 의 조절자는 아 니댜 이 연구 결과는 PLCr 2 의 활성화 경로가 PLCr1 의 그것과 비슷하 다는 것을 의미하며 또한 PLC 가 haemato p o iet ic 세포에서 특수한 역할을 수행하고 있음을 시사해 준다. 즉, haemato p o iet ic 세포는 IgE 수용체나, T-cell 수용체, 그리고 Fe 수용체 를 가지고 있는데, 이들 수용체 역시 티 로신 키나제의 활성도를 가지고 있다. 이는 PLCr 2 가 이들 수용체에 의 해 활성화되면서 이 들 신호에 의해 조절되는 세포 반응에 신호 전이 과
 a
a
정 의 중 간체 로 서 작 용 할 가 능 성이 있음 을 시사해 준다. PLCa 분 자 당 5 7 ~ 70kDa 를 가지 고 있 는 PLC 가 많은 조 직에서 발견되었는 내, 이 l'L C a 논 다 론 이성 질 체인 PLC/ 31 , PLCr 또 는 PLCo 가 가지는 아미 노 신 성선 상 ( X 와 Y 영역)을 가지고 있지 않댜 M artin 등 (66) 은 간 의 미 寸 1 세 로부터 PLCr 와 아미 노 산 서열이 거의 일치하 는 58kDa 단백 전운 분 리하 였는 데 이 단백 질은 PLC 활 성도 를 가지고 있지 않았다. B e nn e tt와 Crook e (67 ) 은 자 궁 으 로 부터 분리 한 PLC 로부터 RBL 1 l i br 碩 윤 선 별 하여 항 체 물 구했는 데 , 이 항체 를 사용하여 PLCa 클론을 얻었다 . 이 방법은 PLC 보다 는 면역원에 오염된 단백질 들을 항원으로 해 서 생 긴 항체일 가 능 성 을 가 지 고 있기 때문에 PLCa 클 론은 이들 오염 된 단백 질로부 터 왔 을 가 능 성이 있다. 또한 이 들 이 얻은 PLCa 클론은 언 반 적으로 알 려 진 PLC 와 는 아미노산 상동성이 거의 없으며 오히려 thi o r cc l oxan, pro te i n disu lfid e iso m e ra se 그리 고 FRp 72 들 과 아미 노산 동 전 성이 유사하다 . 여러 세포에서 분리되거나 발견된 PLCa 가 PLC 이성 전 체의 하나일 것이라는 연구 결과 들 이 많이 있다 . 그러나 PLCa 가 PLC/ 3, PLCr 또는 PLCo 들 이 단백질 가수분해 효소에 의해 분해된 펩 티 드 잔기일 가능성도 배제할 수 없다. PLCo PLC8 는 PLC 의 아미노산 동질성을 보여주는 X 와 Y 영역을 가지고 있으며 PI, PI( 4) P, 그리고 PI( 4, 5)P2 모두를 가수분해할 수 있다. 그러나 PLC8 가 어떠한 기작에 의해서 활성화되는지는 아직 밝혀져 있지 않은 상태이댜 비록 수용체에 의한 PLC8 의 활성화 기작은 밝혀지지 않았지 만 혈압이 높은 쥐에서 PLC8 의 활성도가 정상적인 쥐의 PLC81 의 활성 도와 비 교해 볼 때 높은 것으로 나타났으며 (6.5), 치 매 환자의 뇌 에 있는
쌍을 이룬 나선형 필라멘토의 형성에 있어서 PLCo 의 비정상 적 인 분포 가 발견되었다 (68). 수용체에 의한 PLC 의 환 성화 기작 및 이 률의 신호 전이 기작은 앞으로 중요한 연구 분야의 하나 로 등장한 것으로 기대된다. 3-2 이노시톨 포스페이트 대사 외부 신호에 의해 신호 전이가 이 루 어지 는 동 안 PLC 는 PI(4, 5)P 2 를 가수분해하여 I(l, 4, 5)P3 를 생성시키고, 또한 PI 와 PH 4) P 로부 터 I(l)P와 Hl, 4)P2 를 각각 생성시키는 것을 우리는 앞에서 알아보았다. 이노시 톨 링의 첫번째와 두번째 탄소가 인산 결합 에 의해 형성된 시 클릭 이 노 시 톨 포스페이트 역시 대사 과정 중에 생성된다. 각 반옹에 관여하는 특수한 키나제나 포스파타제들에 의해 이노시 톨 의 첫번째 탄소에서 여섯 번째 탄소에 이르기까지 인산화나 탈인산화가 이루어짐으로써 여러 가지 다양 한 이노시톨 포스페이트와 그들의 이성질체 들 이 이노시 톨 포스페 이 토 대 사 과정에서 생성되는데 여기서 이들의 대사 과정 및 그들의 제 2 의 전 령들로서의 역할을 알아보기로 한다 . 이노시톨 포스페이트 대사에 관한 최 근 문헌들을 참고하기 바란다 (69, 70, 71). 3-2-1 이노시톨포스페이트 대사 과정 Hl, 4, 5)P3 는 I(l, 4, 5)P3 5- 포스포모노에스터라제[I(l, 4, 5)P3 5- p hos p ho-monoes ter ase] 에 의해 I(1, 4)P 2 를 생성하거나 lP3 양키나제에 의해 Hl, 3, 4, 5)P4 를 생성하기도 한다 특히 이들 중 I(l, 3, 4, 5)P4 는 lP3 와 같이 세포질 Ca2• 농도나 세포 소기관들 사이의 Ca 안을 이동시키는 기능을 가지고 있다 (71). 특히, Hl, 3, 4, 5)P4 를 생성하는 lP3 3- 키나제 활성도는 세포 내의 Hl, 3, 4, 5)P4 의 양에 의해 조절되는데, 이는 lP3 나
IP . 1 는 세포질 내에서 Ca2· 양을 조절하는데 상호 보완적인 관계가 있음 융 시사해 준다 (72). PLC 에 의해 PI( 4, 5)P 2 가 분해될 때 I(I, 4, 5)P3 와 그의 시클릭 유도체 인 I(l, 2, 시 찬 릭, 4, 5)P, i 가 생성되는데 중성 p H 나 생리적인 이온 강도를 지닌 조 건하에서 는 IP 」 가 우세하게 생성되어지며, 일반적으로 시클릭 유 노 재의 대사 속도는 비교직 느린 편이다 (73, 74). 비교적 대사 속도가 느 린 시 칸러 유 도 체 는 항상성 기작에 관여하는 것으로 여겨진다. 이들의 대사 과장 및 가 능한 생체 내에서의 역할에 관해서는 이 절의 r 이노시톨 시 클 릭 포스 페이토j옵 다루 는 부분에서 언급하고자 한다. IP : 나 IP : i 의 탈 인산화 과정의 궁극적인 기능은 결국 세포 내에 이노시 몰을 유지하기 위함인데 , 이 들 은 L i ' 나 M g 2 • 의 영향을 받는 포스포모노 에 스 터라제에 의해 l( 4)P 와 I(3, 4) P 2 로 각각 전환된다. 이때 M g 2 • 은 이들 효소릅 환 성화시키지만 L i . 은 이 들 효소를 억제시킨다. IP(!, 4)P2 나 IP3 는 l(4) P 또는 I(I, 3)P 2 로 전환되기도 하는데 이때 관여하는 효소들은 M g 2’ 이나 L i ’ 의 영향은 받지 않는다 (2). 이 노 시 봅 포스페이트들의 일련의 탈인산화 반응은 결국 세포 내의 이 노 시 몹 및 이노시톨 포스페이트들의 항상성을 유지시키는데, 세포 내에 서의 이노시톨 농도를 유지하는 데는 두 가지 상호 보완 과정이 존재한 댜 첫째로는 포도당으로부터 I(l) P 를 합성하여, 이것으로부터 이노시톨 포스페이토를 생성하는 과정인데 앞에서 언급한 것처럼 이때 관여하는 효소(1-포스포모노에스터라제)는 L f의 영향을 받는다. ·다른 한편으로는 세포 내의 다른 소기관으로부터 이노시톨 포스페이트가 능동 수송이나 수동 수송으로 전달되기도 하는데 이들로부터 이노시톨을 생성하는 데 관여하는 효소 (4- 포스포에스터라제)는 L f의 영향을 받지 않는다(그림 3-5, 8). L i'은 이노시톨 모노포스페이토 포스포에스터라제(in os ito l mo- nop h osph ate ph osph o- es t erase) 와 이노시톨 포스페이트 -l- 포스페이트 포스포에 스터 라제 (ino sito l ph os- ph ate - 1-ph osph ate p hosp hoes t erase) 를
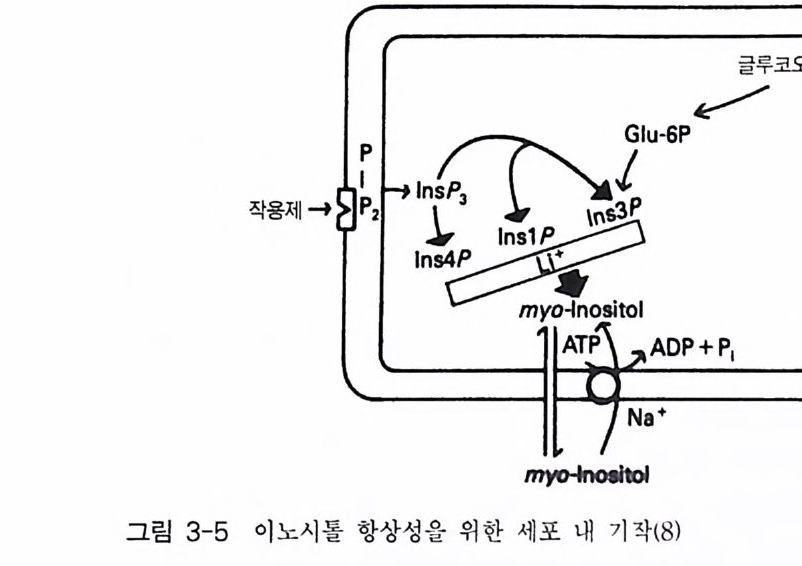 P u-6P c 굴루 코오스
P u-6P c 굴루 코오스
억제하는데 , 이들 L i ’ 에 의한 억제는 비 경 쟁 적 기 작 으 로 이 루 어 진다 . 이 러한 경우가 특이한데 아마도 이 효소 들 사이의 구 조적 또 는 진화적 인 요인에 의 해 기 인된 것으로 여 겨 진다 (75, 76, 77). IP 遷 기질로 하는 효소 중의 하나인 lP3 3 ― 키나제 는 1P :l 로부터 I(I, 3, 4, 5 , )P 4 를 생성한다. 이때 효소는 M g 안 과 ATP 를 필 요 로 한 다 ( 7 8 ). 그러 나 이 lP3 3 - 키나제는 lP 3 는 인산화시키지만 I(1 ; 2 시 클릭, 4, 5) P3 는 인 산화시키지 못한다 (72, 79). 이 효소는 Ca2 t 결합 단백 질 인 칸모듈 린 과 2 개의 촉매 소단위체 (ca talyti c subu nits, 53 kDa) 로 구성되어 있다. 따라서 생 리 적 인 Ca 안 농도에서 lP3 3 - 키나제 활 성도는 증가한다. 이 효소는 인 산화에 의해 조절된다 . 예를 들어 단백질 키나제의 활성제인 포볼 에스 터(p horbol es te r) 에 의해 이 활성도가 2 배로 증가한다는 연구 결과가 보 고되었다 (8) . 또한 간세포 (he p a tocyte)에서 이 효소는 PKA 와 PKC 에 의 해 활성도가 증가함이 밝혀졌다 (81). NIH- 3 T3 세포나 CCL39 쥐 (ham ste r) 섬유 아세포에서 트롬빈, 혈소판-유도 성장 인자 또는 봄베신
(bombesin ) 등 에 의해 이 효소의 활성도가 16 배에서 18 배까지 증가하였 으며 또 한 lP:l 농도는 상당히 낮은 데 반해 IP 4 의 농도는 증가하였다. 이 때 Ca2’ 농도를 측정 해 본 결과 감소하는 것으로 나타났다 (82). 이는 그 동안 밝혀진 IP.i 또한 세포질에서 Ca 2’ 의 농도를 증가시킨다는 연구 결 괴 (8:-l)와는 단리 IP . 1 는 Ca 2· 의 농도 증가에 아무런 영향이 없음을 밝히 고 있다. II)1 의 세 포 내에서의 역할에 관해 연구되어야 할 것이다. IP 라 lP fi는 세 포 내의 여러 소기관들에서 상당히 넓게 분포되어 있는 데 아직까지 이 등 의 역합에 대해서는 밝혀져 있지 않은 상태이다. IP5 는 6 개의 가능한 이성 질체둘 이 있다. 이 들 대부분은 여러 식물과 Di ct y o - s t el i n 에서 밝혀졌다(8.3). 동물 세포에서는 비록 다른 이성질체들이 미량 발견되었지만, IO, 3, 4, 5, 6)P 5 가 주된 IP5 이성질체이다(8.3, 84). 동물 세 포 에서, IP`; 합성의 주요 경로는 1(1, 3, 4, 5)P4 가 이노시톨 포스페이트 - 5 - 포스파타제에 의해 IO, 3, 4)P 3 가 되며 다시 IO, 3, 4,)P3 6- 키나제에 의해 1(1, 3, 4, 6)P . 1 로 이성질화된다. IO, 3, 4, 6)P .i는 5- 키나제에 의해 1(1, 3, 4, 5, 6)P5 로 합성되며 이 I(1, 3, 4, 5, 6)P5 는 다시 IP6 로 합성되거 나 1(3 , 4, 5, 6)P. 1 또는 IO, 4, 5, 6)P .i로 분해되기도 한다 (85, 86, ITT, 88). IP.1, IP5, 그리고 IP6 의 신호 전이에서 그들의 기능은 아직 밝혀져 있지 않다. Hanley (8 9) 등에 의하면 IP5 와 IP6 가 세포 외부의 활성제로서 신경 세포 를 자극하며, 심장 박동이나 혈압을 감소시킨다고 보고하였다. 그러 나 아직까지 그 신호 전이 기작은 밝혀져 있지 않은 상태이다. 비록 I(l, 2, 4, 5)P -i의 Ca2’ 동원 능력 이 IO, 4, 5)P3 에 비 해 3 배 정도 약하지 만, IP4 가 쥐의 호염기성의 백혈병 세포에서 Ca 안을 동원시킨다는 사실 또한 최 근에 밝혀졌다 (90). 지금까지 이노시톨 포스페이트들의 대사 과정을 간략 하게 알아보았다. 그림 3-6 은 이들 대사 과정을 보여주고 있다. 이들 대사 과정의 중간체들인 이노시톨 포스페이트들의 역할에 대해 서는 lP3 를 제외한 나머지는 거의 밝혀져 있지 않은 상태이다. 이들의 기 능에 대한 연구 결과가 곧 밝혀질 것으로 기대된다.
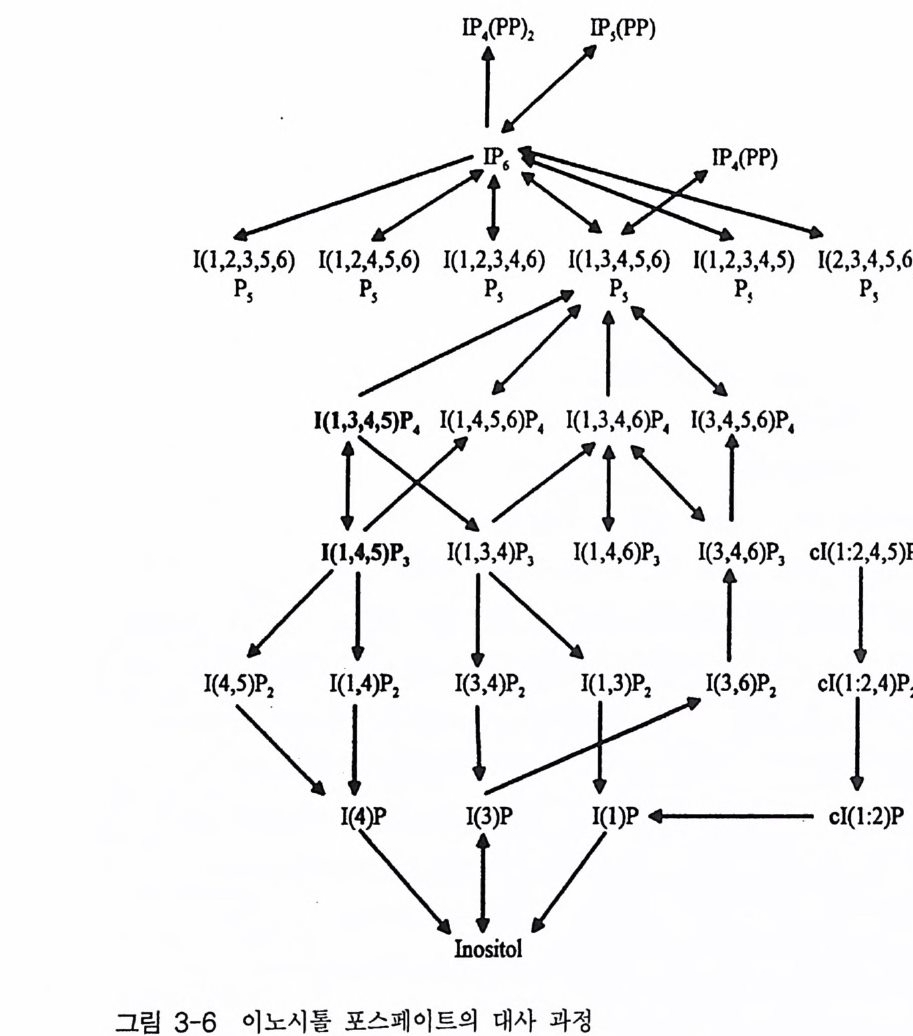 IP,(P P )l IP,(P P )
IP,(P P )l IP,(P P )
3-2-2 이노시톨 시클릭 포스페이트 앞에서 언급한 것처 럼, 시클릭 유도체인 1(1, 2 c y c li c)P3 는 PLC 에 의 해 PI (4, 5)P 가 분해될 때 미량 생성된다 (73, 74 그림 3-7). Majer us 둥 (91) 은 cy cl ic JP3 역시 IP 파 마찬가지로 세포질의 Ca2+ 농도를 중가시키
며 역할 또한 lP 3 의 기능과 거의 비슷한 것으로 발표하였다. 그러나 최 근 연구 결과 들 에 의하면 시클릭 lP 3 는 lP3 수용체와의 친화력에서뿐만 아니라 Ca 2’ 을 동원시키는 능력 에서도 lP 3 와 비교해 볼 때 현저히 떨어 지 는 것 으로 나타났다 (92). 시간릭 포스패 이 트 결합을 가수분해하 는 효소는 시클릭 가수분해 효 소( i nos it o l I, L cy cl ic p ho s p ha t e-2- phos p hoh y drolase) 인데 모든 시클릭 포스페 이 트등 은 궁 극 적으로 시 클릭 가수 분해 효소 (c y cl i c h y drolase) 에 의해 분해되 어 진댜 Majc r us 등 (93, 94) 은 최근에 시클릭 가수 분해 효 소 를 분리하였으며 cDNA 를 얻었 다 . 이 cDNA 로 NIH-3T3 세포를 형질 전환시켰을 때 시 클 릭 I(1, 2)P ·2 의 농도가 2~5 배까지 감소하였다 (95). 이 는 세포 내에서 이 효소의 농도 가 시 클릭 IP 양에 직접 영향을 미치는 것으로 생각된다. 또한 시클릭 가수 분해 효소 활성도를 높여준 세포는 정상적 인 세포보다 성장이 낮은 것 으로 나타났는데, 이는 이노시톨 시클 릭 포스페 이 트가 세포 성장과 밀접 한 관계가 있음을 보여주는 연구 결 과이다 (94). 아 울러 시 클릭 가수분해 효소는 암 세포와 관련이 있는데, 시 큘 릭 가수 분해 효소가 종양 유전자의 생성을 억제하는 항-종양 유전 자의 한 예 로 서 보고되었다 (96). 그러나 Downes 등 (97) 은 이들 시클릭 화합물둘이 Ca 2 ’ 의 농도를 조절하기보다는 아직까지 밝혀지지 않은 어 떤 기능(예 믈 들 어, Maje r us 등이 언급한 세포 성장의 조절자의 역할)을 가질 수도 있지만 다른 한편으로는 대사 사고에 의해 생성된, 이른바 불 량품일 가능성도 있으며, 세포 내에서는 전혀 기능을 가지고 있지 않다 고 언급하였댜 왜냐하면 PLC 에 의 한 PIP 2 의 가수분해시, 오직 l% 만이 시클릭 화합물을 형성하는데 , 이 양이 너무나 미량에 지나지 않기 때문 이댜 이들 이노시톨 시클릭 포스페이트들이 단지 대사 사고에 의한 불 량품인지 암 세포 성장에 관여하는 상당히 중요한 역할을 지닌 조절자 인지는 앞으로의 연구 결과를 통해 계속 지켜볼 만한 홍미로운 연구 과 제일 것으로 생각된다.
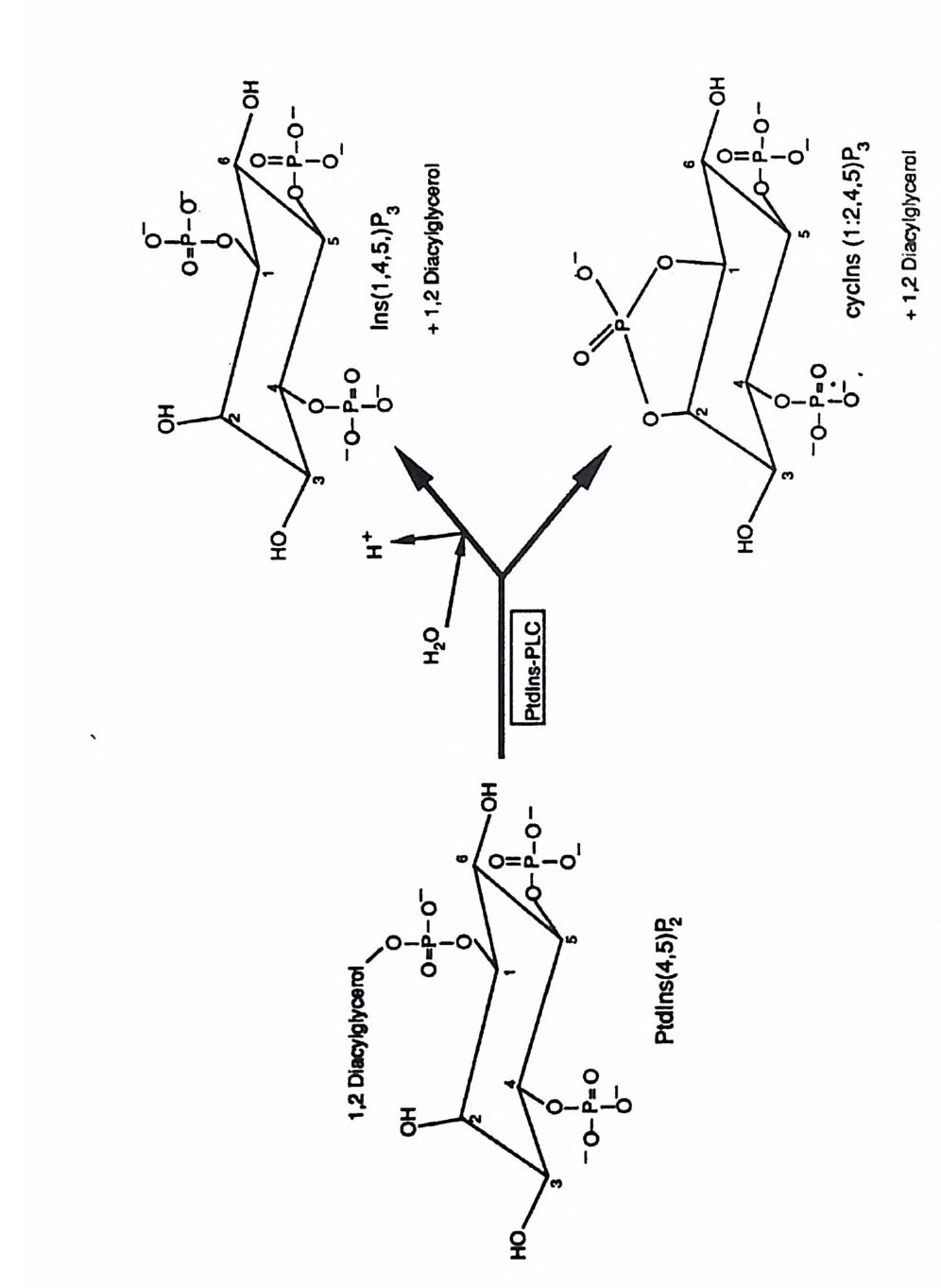 OHHO
OHHO
3-2-3 이노시톨 포스페이트 수용체 앞에서 살펴 본 바와 같이 lP 3 의 가장 중요한 기능은 세포질 내의 Ca2• 의 농도읍 층 가시키 는 것으로, lP 3 가 소포체나 다른 소기관의 막에 존재 하 는 II 십 수용체에 결 합합으 로 써 이 루 어진다 . 다양한 세포에서 lP3 수용 체가 분 리 정재되었 는 데, 이 들 은 lP3 결합 단백질이면서 동시에 Ca2• 채 널로 서의 역 한웅 수행하고 있다 (98, 99). IP.l 수 용체 는 사량체 로 서 각 소단위체 펩티드 체인의 분자량은 250 l
존재 외에는 아직 밝혀지지 않았지만 기능적인 면에서의 차이보다는 다 양한 조직, 또한 다양한 세포 로부 터 합성되는 과정에서 동질성의 상실에 서 기인하는 것으로 생각된댜 lP3 수용체 는 소포체 막에 존 재하며 이 는 血 수용체의 가장 중요한 기능인 Ca24 동원과 밀접한 관계가 있다. 신 제 로 소포체는 세포 내에서의 Ca2· 저장소 ([Ca2 · ] = l0mM) 로서의 기능옹 가 지고 있다. 소포체 이외에도 , 핵막, 골지체 에서 도 IP:i 수 용체의 촌 재가 학 인되었다 (l02) . 이 들 lP3 수용체는 Ca 2 · 이 핵으로부터 세 포진로 이 동합을 의미하는데, 궁극적으로 세 포 성장이나 증식을 포합한 세포 반옹의 조절 기능을 가지고 있을 것으로 여겨진다. 핵막은 거대 분자, 즉 DNA 나 단백질의 수송이 가능한 핵공이 존재 하 며 이온들의 이동은 다른 세포막과 는 달 리 이 들 구멍을 통해 서 자유롭 게 이동이 가능하다. 그럼에도 불구 하고 IP3 수용체 즉 Ca2’ 수송로 들 의 존재 의미가 홍미롭댜 최근에 IP3 수용체가 분리된 핵으로부터 Ca 2 · 을 방출시킨다는 연구 결과가 밝혀졌다 (102, 103). lP3 결합 단백질 이외에 도 다른 이노시톨 포스페이트 결합 단백질의 존재가 확 인되었다 . 그중 하나 가 1(1, 3, 4, 5)P4 결합 단백질인데 이는 돼지와 쥐의 소뇌 막으로부터 부 분적으로 분리 정제되었다 004, 105, 106, 107). Donie 등 이 돼지의 소뇌 로부터 정제한 IP4 결합 단백질의 분자량도 42 kDa 로서 IP4 에 대한 Ki 값은 5mM 인데 IP 께 대한 氐 값은 약 0.5mM 인 것으로 밝혀졌다 007). Snyd e r 등(1 06) 이 최근에 쥐의 뇌로부터 분리한 IP4 결합 단백질은 두 종류로서 앞에서 언급한 Don ie 등이 분리한 것과 성질이 비슷한 것으로 밝혀졌는데, 단지 분자량에서 차이를 보여주고 있다. 즉 이들 두 단백질 의 분자량도 각각 182kDa 와 258kDa 이다. lP4 결합 단백질의 다양성이 특이한 IP 려 이성질체에 기인하는 것인지는 아직 밝혀지지 않았다. IP6 를 위한 결합 단백질의 존재도 확인되었다(1 08 , 109). 분리한 소뇌 막에 대한 1P 려 氐 값은 60nM 인데 비해 lP5 의 氏 값은 1 µM 이었다. IP6 결 합 자리가 미토콘드리아, 미엘린 (m y e lin), 그리고 시냅토솜 (s yn a pt o -
som e ) 등 으 로 부터 분 리한 막에 존 재함이 밝혀 졌는 데 (l09) 특 히 IP6 결합 자 리 는 소 뇌, chlroid ple x is , 그 리고 핵 등 에 많이 존 재한다. 이는 IP6 결 합 자리가 뇌에 많 이 존 재하 는 것 으로서의 기능과 관계가 있을 것으로 생 각된 다. 이 둘 단백질 의 기 능 에 관해서 는 앞으로 연구되어야 할 과제 들 이다 . 지급 까지 우 리 는 포스 파티 딜 이노시 톨 대사 및 이노시톨 포스페이트 대사에 관 하여 그 생합 성 및 생체에서의 기 능 등에 대해서 폭넓게 알아 보았 댜 이 노 시 돕 포스페 이 토 중 의 하나인 IP 3 의 생성 및 그 기능에 대해 서는 비 교적 잘 알려져 있 는 데 반해 , 다 른 포스파티딜 이노시 톨 이나 다 른 이 노 시 몰 포스 페이 트 에 대해서 는 비교적 그 기능이 명확하지 않다 . 포스파 티 딜 이 노 시 톨 중 하나인 PIP 2 가 IP 3 나 DAG 의 전구 물질로서의 기능은 확실 하지만 세 포 골격 의 조 절 자로서의 기능은 부분적으로 이해 되 고 있 는 실 정이며 , 다 른 대사 산 물 인 I(3, 4)P z 나 H3, 4, 5)P3 역시 종양 단 백 전을 생성하 는 신호 전이와 관련이 있을 것으로 여겨지나, 그 기작 은 명 확 하지가 않다 . 이노시 톨 포 스페이트 들 의 기능은 앞서 언급한 IP3 를 제외하고 는 명확하지가 않다 . IP4 가 IP 3 와 마찬가지로 세포 내 저장소 로부 터 Ca 21 을 동원시키 는 것으로 생각되지만 몇몇 세포에서는 Ca2+ 동 원으 로 서의 기능이 명확하지 않다 . 그외 IP 5 나 IP6 둥 다른 이노시톨 포 스 페이 트들 역시 그 기능이 명확하지 않다. 이들 그 기능이 밝혀지지 않 은 포스포이노시티드들의 세포 내에서의 역할의 규명이 밝혀지면 세포 내에서의 생명 활동과 그 조절 기작인 신호 전이 전달 기작을 이해하는 데 기여할 것으로 여겨진다. 참고문헌 1) Berr idge , M. J. (19 93) Natu r e 361, 315
2) lVI aj er us, P. W. (1992) Annu Rev. Bi oc hem 61, 225 3) Ivlaje r t s, P. W., Ross, T. S., Cunn ing h am, T. W. , C aldwell, K. K., Jef f er son, A. B., and Bansa l, V. S. (1990) Cell 63, 459 4) Fen is, C. D., a nd Snyd e r, S. H. (1992) Annu. Re v. Phys o /. 54, 469 5) Irvine , R. F. (19 92) Cur. Op inio n Cell Bio l. 4, 212 6) Downes, C. P. & Macph e e, C. H. (1990) Eur. ] . Bi oc hem Im, 1 7) Ca rpen te r , C. L. & Cantl e y, L. C. (19 90) Bio c h e m 29, 1114 7 8) Downes, C. P. (19 89) Bio c hem Soc. Trm1s. 17, 259 9) Agrano ff, B. W., Bradley, R. M., & Brady, R. 0. ( 1958 ) ]BC 2 葛 1077 10) Agra noff , B. W. (19 83) Lif e S c i. 32, 2 여 7 11) Downes, C. P. & Mich ell, R. H. (1985) In molecular mechanis m s of tran smembrane sig nal in g(C ohen, P. & Houslay, M. D., eels) p 3. Elsevi er , Neth e rlands 12) Brederoo, J., de Wi ld t, P., Popp - Sn igd ers, C., Irvin e , R. F., & Musgr av e, A. (19 91 ) Planta 184, 175 13) Peeler, T. C., Ste ph enson, M. B., Ein s pa h r, K . J., Thomp so n, G. A. Jr. (19 89) Pla nt Ph ysi o l. 89, CJ'70 14) Cote , G. G., DePass, A. L., Qu armby, L. M., Tate , B. f., Morse, M. ]., Cra in, R. C., & Satte r, R. L. (19 89) Plant Ph ysi o l . 9 0, 1422 15) Ste ph ens, L. R., Hu gh es, K T., & Irvine , R. F. (19 91) Natu r e 351, 3-1 16) Brearley, C. A, & Hanke, D. E. (19 92) Bi oc hem ]. 28.3, 25.5 17) Irvine, R. F., Letc h er, A. J., Ste ph ens, L. R., and Musg rav e, A. (1992) Bio c hem ]. 281 18) Weis s , S. B., Sm ith, S. W. , & Kennedy, E. P. (1958) ]BC 231, 5.3 19) Harwo od, J., & Haw tho rne, J. (19 69) Bi oc hi m Bi op h ys. Ac ta 171, 75 20) Whitman, M, Kapl a n, D., Robert s, T., & Cantl e y, L. (19 87) Bio c hem J 247, 165
21 ) Whit m an, M., Downes , C. P., K e ale r , M., Keller , T., and Cantl e y, L. (1988) Natu r e 332, 644 22) Endcmann, G., D unn, S. N., and Cantl e y, L. C. (19 85) Bi oc hemi st r y 26, 68-15 23) Porte r , F. D., Li, Y. S., and Duel, T. F. (1988) ]BC 263, 8989 24) Walke r, D., Doug h ert y, N., and Pik e , L. J. 0988) Bi oc hem . Z'l, 6504 25) Chahwala, S. B., Fleis c hman, L. F., and Cantl e y, L. 09 初 Bi oc hem 26, 612 26) Kato , H., Uno, I., Ish i kw a, T., a nd Takenawa, T. (1989) ]BC 264, 3116 27) Kap la n, D. R., Whitm an, rvI. , Schaffh a usen, B., Pallas, D. C., White, M., Cantl ey , L., and Robert s, T. M. (19 ITT) Cell 50, 1021 28) Sug im oto , Y., Whitm an, M., Cantl e y, L. C., and Eri kso n, R. L. (1984) PNAS 81, 2117 29) Fukui, Y., and Hanafu s a, H. 0989) Mo!. Cell Bi ol. 9, 16.5 1 30) Rude rm an, N. B., Kape ll er, R., White, M. F., and Cantl ey L. C. (1980) PNAS 87, 14111 31 ) Va rtico vski , L., Druker, B., Morr iso n, P., Cantl ey L., and Robert s, T. (19 89) Natu r e 342, 699 32) Aug er , K. R., Seru nian , L. A, Solto f f , S . P., Libb y, P., and Cantl ey , L. C. 0989) Cell 57, 167 33) Ima i, A, Rebecchi , M., and Gersheng o rn, M. 0986) Bi oc hem ]. 240, 341 34) Van Dong en , C., Ew ier s, H., and Gis p e n , W. (1984) Bi oc hem J 223, lg 7 35) Cochet, C., and Chanbaz, E. M. (19 86) Bi oc hem J 盆 25 36) Mori tz, A, DeGraan, P., Ekha rt, P., Gis p e n , W., and Wr rtz, K 0990)
J Neurochem. 책 351 37) Sm ith, C., and Chang, K J. 0989) ]BC 264, 3206 38) Yamamoto , K, Grazia n i , a., Carp en te r , C., Cantl ey , C., and Lap etirn . E. 0990) ]BC 265, 22086 39) Inokuchi , S., and Imboden, J. (19 90) ]BC 2ffi , 59& '3 40) Jam ney, P. A, and Sto s sel, T. P. (19 89) ]BC 264, 4825 41) Jam ney, P. A, and Sto s sel, T. P. 0987) Natu r e :325. 362 42) Lassin g, I., and Lin d berg, U. (19 85) Natu r e 314, 472 43) Sy lv ia , V., Cw tin, G., Nonnan, J., Ste c , J., and Busbee, D. (19 88) Cell 54, 651 44) Seru nian , L. A, Au ge r, K. R., Robert s, T., and Cantl ey , L. C. (19 90) J Viral . 64, 4718 45) Rhee, S. G., Choi, K . D. 0992) ]BC 267, 12393 46) Rhee, S. G., Pann-Gh ill, S., Sung -H o, R., and Lee, S. Y. (1989) Sc ien ce 244, 546 47) Rhee, S. G. 0991) TIES 16, 297 48) Maje r us, P. W. 0992) Annu Rev. Bi oc hem 61, 225 49) Meldr um, E., Parker, P. J., Carozzi, A (1991) EBA 1092, 49 50) Smrcka, A V., Hepl e r, J. R., Brown, K, 0., S te m weis , P, C. 0991) Sc ien ce 251, 804 51) Hepl e r, J. R, and Gilm an, A G. 0992) TIES 17, 383 52) Shenker, A, Goldsm ith, P., Unson, C. G., and Sp ieg e l , A M. (19 91) ]BC 266, 9309 5.3) Blan k, J. L., Ross, A M., and Ex ton , J. H. (1991) ]BC 266, 18206 54) Tayl o r, S. J., Chae, H. Z., R hee, S. G., and Exto n , J. H. (19 91) Natu r e 350, 516 55) Me ise nhelder, J,, Suh, P. G., Rhee, S. G., and Hunte r, T. (1989) Cell
57, 1109 56) Emori , Y., Homma, Y., Sori m ach i, H., Kawasak i, H., Naka nish , 0., Suzuk i, K, and Takenawa, T. (1989) ]BC 264, 21885 57) Downin g , ]. R., Margo lis , B. L., Zil b erste i n , A, Ashmun, R. A, Ullrich , A, Sherr, C. ]., and Schlessin g e r, J. 0989) EMBO J. 8, 3345 58) Nis h ib c , S., Wahl, M. I., Wedg a ert ne r, P. B., 邸 m, J. J., Rhee, S. G., and Carp en te r , G. (1989) PNAS 87, 424 59) Nis h ib e , S.,Wahl, M. I., Hernandez-Soto m ay o r, S. M. , Tonks, N. K, Rhee, S. G., & Ca rpen te r , G. (19 90) Sc ien ce 250, 1253 60) Wahl, M. I., Nis h ib e , S., I
71) ln1in e , R. F. 0992) Cur. Op . Cell. Bio . 4, 212 72) Connolly, T. M., Bansa l. V. S., B ross, T. E., I rvin e , R. F., & Maje r us, P. W. 0987) ]BC 262, 2146 73) Sekar, M. C., Dix o n, ]. F., & Hol<..i n , L. E. 09 87 ) ]BC 262 . :섬 O 74) Harden, T. K., Hawk ins , P. I., Ste p h e ns, L., Boy er , J. L., and Downes, C. P. (1988) Bio c hem J 252, 583 75) Halkher, L. M. , and Shennan, W. R. 0980 ) ]BC 墨 1089 G 76) Maje r us, P. W. , Connolly, T. M., Bansal. V. S., Inhom, R. C., Ro ss, T. S., a nd Lips, D. L. (19 88) ]BC 263, 3051 77) Gee, N. S., Reid , G. G., J ac kson, R. G., Ban1aby, R. T., and Rag a n, C. I. (19 88) Bio c hem J 253, 777 78) Irvin e, R. F., Moor, R. M., Pollock, W. K, Sm ith, P. M. , & Wreg ge tt, K A. (19 88) Phil os . Trans. R. Soc. London Ser. B. 320, 281 79) Moms, A. J., Murray, K. J., En gla nd, P. ]., Downes, C. P., & Mi ch ell, R H. (19 88) Bio c hem ]. 劉 157 80) King , W. G., and Ritten house, S. E. (19 89) ]BC 264, 6070 81) Eid e n, T. J., Altin , J. G., Karajal ai ne n, A., and By gra ve, F. L. (19 88) Bi oc hem ]. 216, 697 82) Balla, T., Sim , S. S., I ida , T., C hoi, K Y., Catt , K ]., and Rhee, S. G. (1991) 266, 24719 83) Ste ph ens, L. R, HaV !kins, P. T., S ta nley , A. F., M oore, T., Polyn e r, D. R (19 91 ) Bi oc hem J T/5, 48.5 84) Pittet, D., Schlege l , W., Lew, D. P., Monod, A., and Mayr , G. W. (1989) ]BC . 264, 18489 8.5) Balla, T., Gu illem ette , G., Baukal, K ]., & Catt , K J. (19 얽) ]BC 262, 9952 86) Ste ph ens, L. R., Hawk ins, P. T., Barker, C. J., Downes, C. P. (19 88)
Bio c hem ]. 253, 721 87) Hanse n, C. A., Dahl, S. V., Huddell, B., Wi lliam son, ]. R. 0988) FEBS Lett . 236, 53 88) Shears, S. B. 0989 ) ]BC 264, 19879 89) Vallejo , M., Jac kso n, P., Lig h tm an, S., & Hanley , M. R. (19 87) Natu r e 330, &% 90) Hir a ta , M., Naru mo to , N., Wata n abe, Y., Kanemats u , T., Kog a, T., & Ozaki , S. 0994) l'do l. P harm. 45, 271 91 ) Wi lso n, D. B., Connolly, T. M. , Borss, T. E., Maje r us, P. W., Sherman, W. R., Ty le r, A. N., Rubin , L. J., & Brown, J. E. (198.5) ]B C 260 , 13496 92) Wi llc ocks, A. L., Str u p ish , J., Irvin e , R. F., & Nahorski , S. K (1989) Bio c hem ]. 257, 297 93) Ross, T. S. & Maje r us, P. W. (19 86) ]BC 261, 11119 94) Ross, T. S. & Maje r us, P. W. (19 91) ]BC 266, 8.51 95) Ross , T. S., Ta it, J. F., & Ma jer us, P. W. (19 90) Sdence, 248, 605 96) Maje r us, P. W. , Ross, T. S., Cu nning h am, T. W., Caldwell, K K., Jef f er s on, A. B., & Bansal, V. S. (19 90) Cell 63, 459 97) Downes, C. P. & Macph ee, C. H. (1990) Eur. ]. Bi oc hem 193, 1 98> S up a tta pon e, S., Worley, P. F., Baraban, J. M., and Sny d er, S. H. (19 88) ]BC 263, 1530 99) Ferr is, C. D., Hu ganir, R L., Sup a tta pore , S., & Sny d er, S. H. (19 89) Na ture 342, 얽 100) Takeshi m a, H., N is h i mu ra, S., H ats u rnoto , T., Ishi da , H., Kangw a, K (1989) Natu r e 339, 439 101) Nakahawa, T., Okano, H., Fu ruish i , T., Aruga , J., & Mikos hi ba , K (19 91 ) PNAS 88, 6244
102) l\fa l viy a, A. N., Rog u e, P. Vin c endon, G. (19 90) PNAS 87, 9270 103) Nic o te r a, P., O reniu s , S, Nil ss on, T., & Dergg re n, P. 0. 0990) PNAS 87, 6858 104) Don ie, F., Hulser, E., & Reis e r, G . 0990) FEES Lett . 2 68, 184 105) Theib e rt , A. B., Sup attapore , S., F en is, C. D., D anoff , S. K, Ev an s, R. K, & Sny d er, S. H. 0990) Bio c hem ]. 267, 441 106) Theib e rt , A. B., Esdevez, V. A., Fen is, C. D., D anoff , S. K., 13ruTow, R. K 0991) PNAS 88, 3165 1(J 7) Don ie, F., Reis e r, G. (19 91 ) Bio c hem ]. 275, 453 108) Hawk ins , P. T., Rey n olds, D. ]., Poy n er, D. R., & Hanley, M. R. 0990) BBRC 167, 819 109) Nic o lett i, F., Bruno, V., Cavallar, S., & Cop a ni , A., Sort ino , M. A., Canono, P. L. 0990) Mo!. Ph :Jrm acol. 37, 689
제 4 장 칼슘 이온 정자의 이동에서 시작되는 생명 현상의 초기 단계부터 심장 박동이 멈 추는 마지막 순간까지 생리 현상에 관여하는 Ca 2+ 의 이동은 끊임없이 계 속 되고 있다 . 세포의 Ca 20 의 이동 (cellular Ca2· movemen t)은 세포질 내 의 Ca2’ 이동(i n tr acellular Ca2' movemen t)과 세포 외부에 존재하고 있는 Ca 2’ 의 이 동 (ex tr acellular Ca2· movemen t)에 의해 이루어지고 있다. 세포 내의 Ca2 ’ 농도의 변화는 여러 가지 다른 종류의 자극에 의해 이루어진 댜 궁극적으로 짧은 시간 안에 이루어지는 세포의 생리 반응(예, 이온 수송의 조절 또는 효소의 활성도 조절)과 비교적 긴 시간에 이루어지는 생리 반응(예 , 유전자 조절 및 단백질 합성)과 같은 다양한 세포의 생리 반응이 세포질의 Ca 양 변화에 의해 조절되고 있다. 다양한 종류의 세포 에서 이루어지는 이러한 생리 현상을 조절하는 제 2 전령으로서의 Ca2 + 의 역할에 관해서 최근 많은 총설들이 나오고 있다(1, 2, 3, 4). Ca2 + -민감성 형광 지시약이나 미세 전극에 의해 측정한 세포질 내의 Ca2+ 농도는 대부분의 진핵 세포에서 100~300nM 범위인 것으로 알려 져 있고 세포 외부의 Ca2+ 농도는 약 lmM 이며, 세포 내 소기관들 중 Ca 안 의 저장소로서 작용하는 소포체의 경우는 약 10 mM, 다른 소기관은
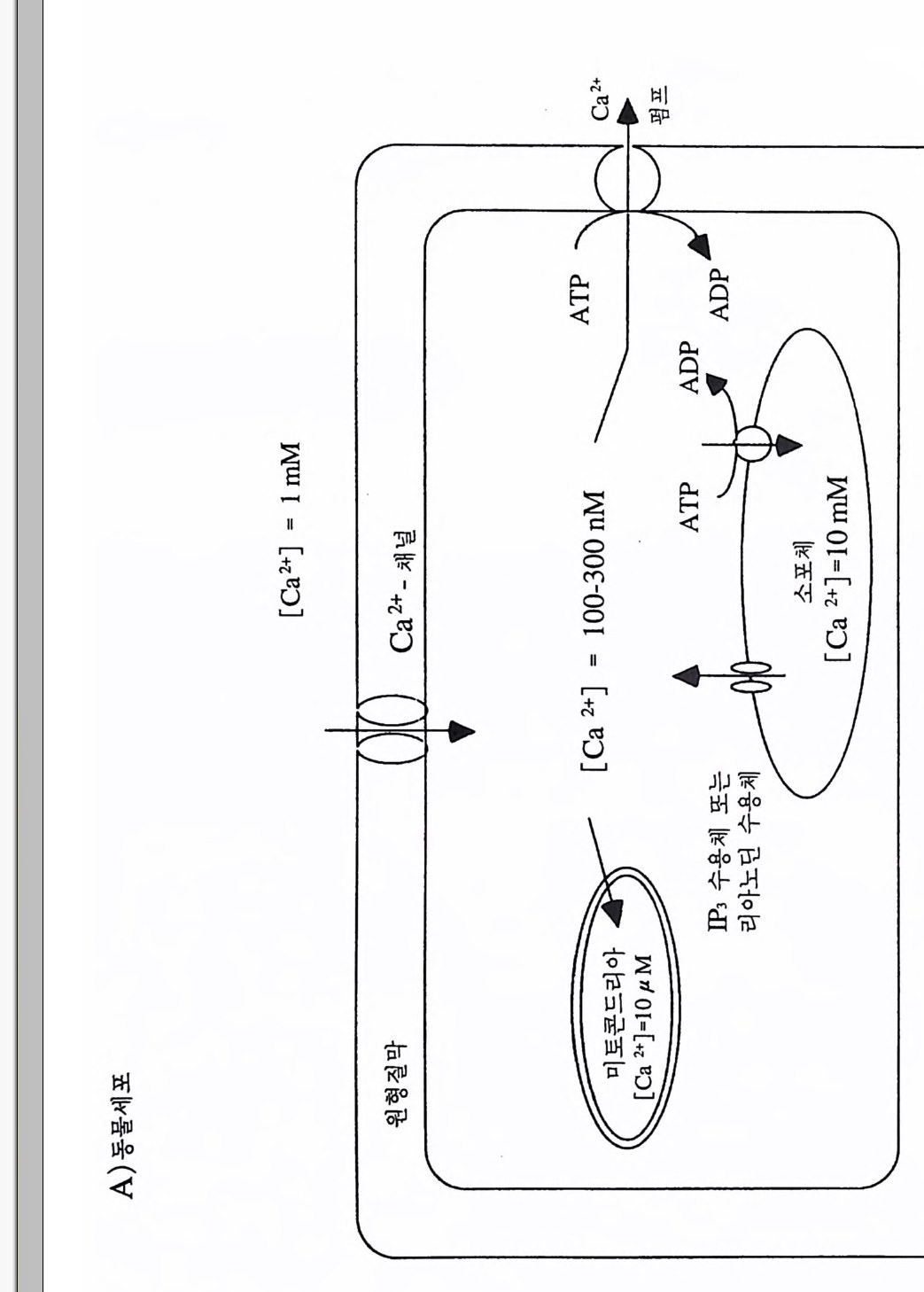
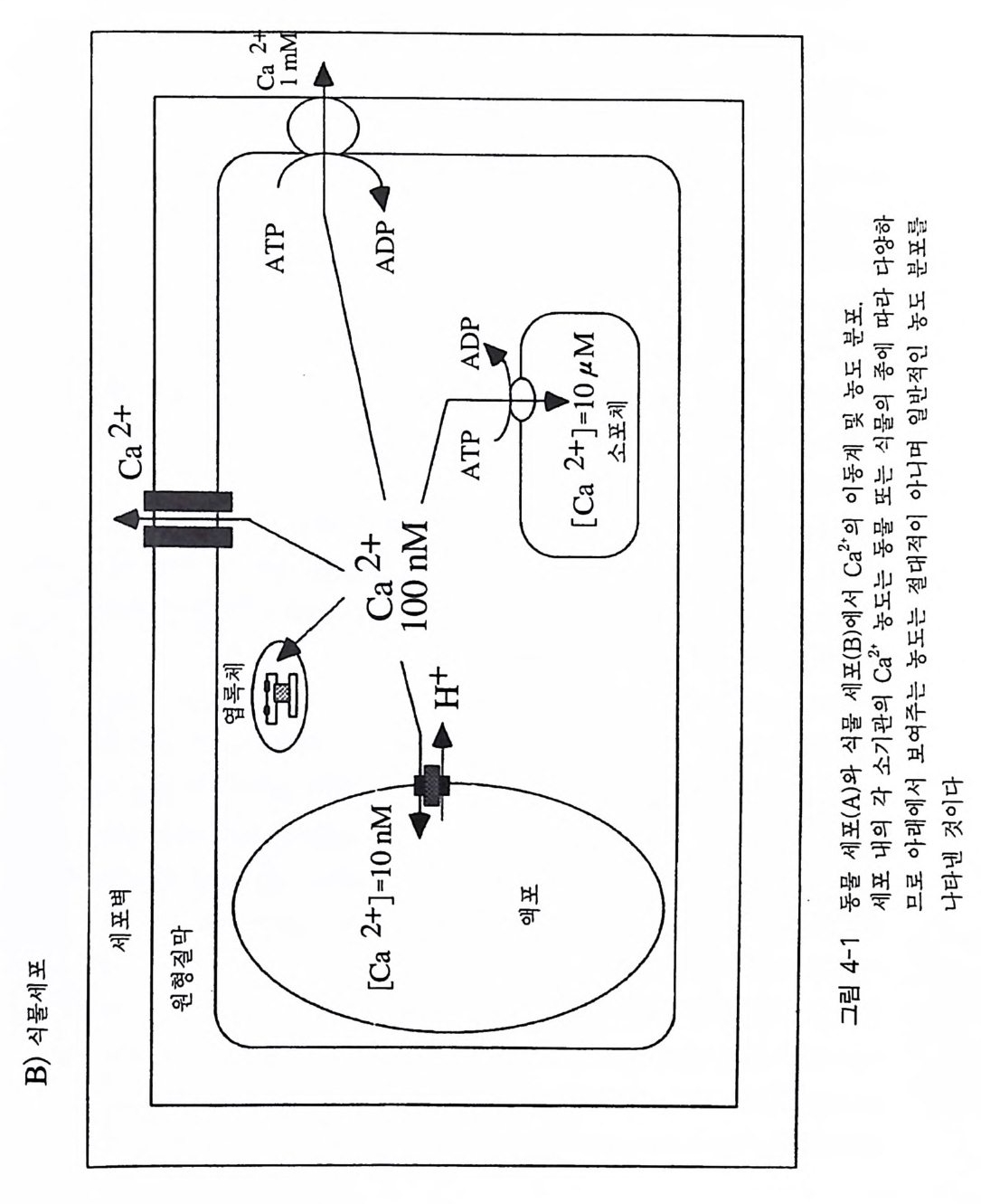
약 10 µM 정도인 것으로 나타났다(그림 4-l). 세포질 내의 Ca2 ’ 농도는 세포 외부에 비해서 약 10,000 배 정도나 낮은데 세포질 내의 높은 Ca2+ 농도는 세포에 치명상을 입히게 된다. 따라서 제 2 전령으로서 Ca 2’ 이 작 용할 때에는 순간적으로 세포질 내의 Ca2 令 농도가 증가하였다가 빠론 시 간 내에 다시 정상 수준으로 돌아와야 하는데 세포 는 복잡하고 다양한 경로를 통해서 Ca 2+ 의 농도를 조절하게 된댜 세포 자체는 생 존옹 위해 항상 Ca2 + 의 항상성을 유지하며 제 2 전령으로 작용한 때 증가 또 는 감소 하였다가 다시 항상성을 유지하는 진동 또는 파동이 잘 발달되어 있다. 즉 Ca2° 의 이동 경로는 매우 복잡하고 다양하면서 동시에 섬세하게 이루 어지고 있음을 보여주고 있다(그림 4-2). 그림 4-2 에는 이 둘 다양한 경 로를 통해 이루어지는 Ca 언의 이동을 보여주고 있는데, Ca20 의 이동은 크 게 세 가지로 나누어서 생각할 수 있다. 첫번째는 Ca2+ 의 동원 (mob ili za ti on), 즉 소포체(ER), 근소포체 (SE R), 또는 다른 세포 내 소기관으로부터 Ca 2· 이 세포질로 나오는 경우이며, 이때 세포질 내 Ca 2+ 의 양이 오랜 시간 동안 증가 상태를 유지하면 세포 가 치명상을 입기 때문에 제 2 전령으로서의 역할을 한 후, 빠 른 시간 내 에 다른 세포 내 소기관으로 들어가는데, 이 경우도 여기에 포함된다(그 림 4-2, CT)-@, ®). 두번째로는 소포체의 경우 Ca2+ 농도가 항상 mM 정 도를 유지하는데 Ca 앙 의 동원시 소포체의 Ca2• 농도가 낮아지 게 된다. 이 경우 세포질 내 Ca2 • 이 ca2 •- ATPase 에 의해서 소포체로 들어가는 경우 (Ca2• 동원)도 있지만 세포 바깥의 Ca 안 이 원형질막을 가로질러 세포 내 로 들어오기도 하는데 이를 Ca2+ 유입이라고 한다(그림 4-2 , (2), ®, ®). 마지막으로 외부에서 세포질 내로 들어온 Ca 양이 그들의 생리 반응을 조 절한 후 세포질 내의 Ca2• 의 농도는 항상 100~300nM 의 농도를 유지하 여야 하기 때문에 다시 빠른 시간 내에 세포 외부로 Ca2 + 이 나가야 하는 데, 이 경우를 Ca 얀 유출이라 한다(그림 4-2 CD, @, @). 따라서 세포질 내 Ca2 냉 의 이동은 크게 세 가지로 나누어지는 이들 경로를 통해서 이
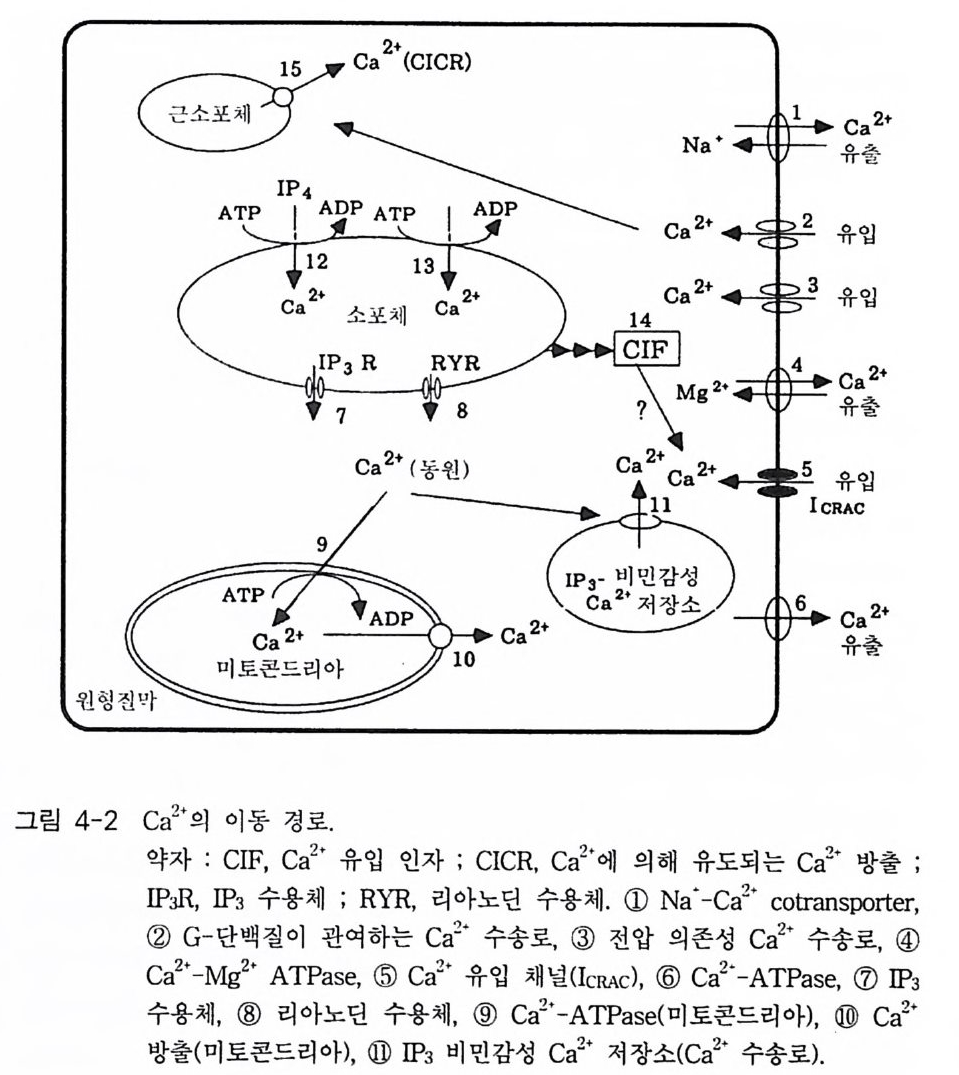 Ca2-+ ( CICR)
Ca2-+ ( CICR)
루어지게 된다 본론에서는 이 들 경로에 관여하는 다양한 신호 전달 기 작뿐만 아니라 단백질과 이 들 구성 물질에 이 르 기까지 좀 더 상세히 알 아보고자 한다. 4-1 IP3 에 의한 Ca2+ 의 동원 IP 파 이노시톨에 특이성을 가지는 Ca2 t 저장소(i nos it ol sensiti ve ca2' poo l, 예를 들어 소포체)로부터 Ca 2+ 을 동원시키는 제 2 전령으로서 작용한 다는 첫 보고(B e nidg e, M. J., 1984) 가 있은 이래, 십년 동안 Ca 2’ 의 동원 에 관한 연구는 끊임없이 이어져 왔다 (5). 그 이후 IP3 에 의해 Ca 2 t 이 세포 내 저장소로부터 동원되기도 하지만 세포 외부의 Ca 2 t 이 세포 내로 들 어 오는 데에도(아마도 간접적으로) 관여하고 있음이 밝혀졌다. 주로 IP :l ― 민감 성 저장소에서 Ca2 + 의 동원이 일어날 때 약 30~50% 가 이루어지며, 나머 지 50~70% 는 Ca2 • i ono p hore 에 의해서 이루어진다. 이 결과는 lP 3- 민감 성 저장소로부터 Ca2+ 이 동원되고 있음을 시사해 주고 있다. IP3- 특이성 항체를 사용한 면역 세포 화학적 연구 결과에 의하면 푸르 키네 세포(p ur ki n j e cell) 의 경우 IP3 수용체가 핵막과 소포체에 존재하고 있음을 보여주었다 (6). 또 다른 lP3 一민감성 Ca2+ 저 장소로서 perithe ral ti ssue 의 경우 calc i some 을 들 수 있는데 calc i some 이란 근소포체와 비슷 한 성질을 가지는 조그마한 소포로서 Ca2+ 결합 단백질인 calseq u estr in 울 갖고 있다 (7). 그러나 calc i some 이 IP3- 민감성 저장소인지는 아직까지 명확하지는 않댜 Ca2+ 이 동원되기 위해서는 IP3 가 IP3- 민감성 Ca2+ 저장소에 존재하는 血 수용체에 결합하여야 하는데, IP3 수용체는 곧 4 개의 폴리펩티드로 구성된 Ca2+ 수송로를 의미한다(그림 4-3). 다시 말해 lP3 수용체는 4 개 의 血 결합 자리를 갖는데 여기에 IP3 가 결합했을 때 구조적 변화가 일
 삭용
삭용
어나서 닫혀 있는 Ca2+ 수송로가 열리게 되며, 따라서 소포체 또는 세포 내 저 장소에 있는 Ca2+ 이 세포질로 나오게 된다 (8). 다양한 세포에 존재 하는 IP3 수용체의 결합 자리는 C- 형 IP3 보다 D- 형 IP3 에 더욱 잘 결합 하는 입체 특이성을 갖고 있으며 (9, 10), 헤파린은 IP3 가 이 수용체에 결 합하는 것을 억제할 뿐만 아니라 간세포에서 Ca2+ 의 동원도 억제한다 (11). IP 려 결합 양상은 매우 높은 협동성을 갖고 있는데 Ca2+ 채널이 열리기 위해서는 적어도 세 분자의 IP3 를 요구하고 있다. 죽, 적어도 세 분자의 IP3 가 IP3 수용체의 소단위체에 결합하여야만 IP3- 수용체 채널이 열리게 된다 (12). IP 려 의한 Ca2+ 의 동원은 여러 생리적, 약리적인 시약 의 영향을 받게 되는데 기존에 알려진 Ca2' 채널 억제제들에 의해서는
전혀 영향을 받지 않지만(1 3, 14), 홍미 롭 게도 I( 채 널 억제제인 TEA( t e tra e thy lammo ni um) 이 나 cin n a rizi n e (l 3) , fl un ari z i ne04) 에 의 해 억 제된댜 Ca2 + 을 동원시키는 데 관여하는 제 2 전령인 IP : 1 의 생성과 그 에 관한 신호 전달 경로에 관해서는 3 장 포스포이노시티드에서 이미 언 급한 관 계로 여기서는 더 이상 언급하지 않기로 하 겠 다. 또한 앞에 서 언 급한 것 처럼 IP37 } Ca2 ♦ 을 동원시키지만 세포 외부의 Ca2 ’ 이 세 포 내 부로 돕 어오 는 데도 관여한다. 즉 IP 3 에 의한 Ca2 ’ 유입에 관해서는 다음 절 인 Ca2 , 유입에서 언급하기로 하겠다. 4-2 리아노딘 수용체 채널 鵬 수용체와 리아노딘(ry anod y i ne) 수용체는 Ca2 ’ 동원에 관여하는 세 포 내 Ca2+ 수송로로서 그 역할을 수행하고 있는 대표적인 수용체들이 댜 골격근의 수축은 Ca 2+ 이 근소포체로부터 동원되고 곧이어 t ransver 一 se-tu b ule(T-tu b ule) 이 탈분극화 (de po l ari za ti on, 15, 16) 되 면 서 이 루어 지 는 데, 이 결과는 T- tu bule 과 jun cti on al 근소포체 사이의 정보 교환을 동해 서 이루어지고 있음을 의미한다. 식물에 존재하는 알칼로이드인 리아노 딘을 jun cti on al 근소포체에 첨가하였을 때 Ca2 • 이 동원되는 결과가 관찰 되었다 (l7) . 그 이후 리아노딘은 jun cti on al 근소포체뿐만 아니라 심근 소 포체 등에서도 Ca2• 을 동원시키고 있음이 확인되었다 (18). 1980 년대 중반 이후 여러 종류의 세포로부터 리아노딘 수용체가 분리 정제되었는데, 이들 수용체는 lP3 수용체와 구조적으로나 기능적인 면에 서 동질성이 있음이 밝혀졌다(그림 4-4) 09, 20). lP3 수용체는 C- 말단 부위에 막 관통 영역을 가지고 있으며 네 개의 소단위체가 막에 박혀 있 음으로써 lP3 一민감성 Ca 양 채널로서의 역할을 수행하고 있다 lP3 결합
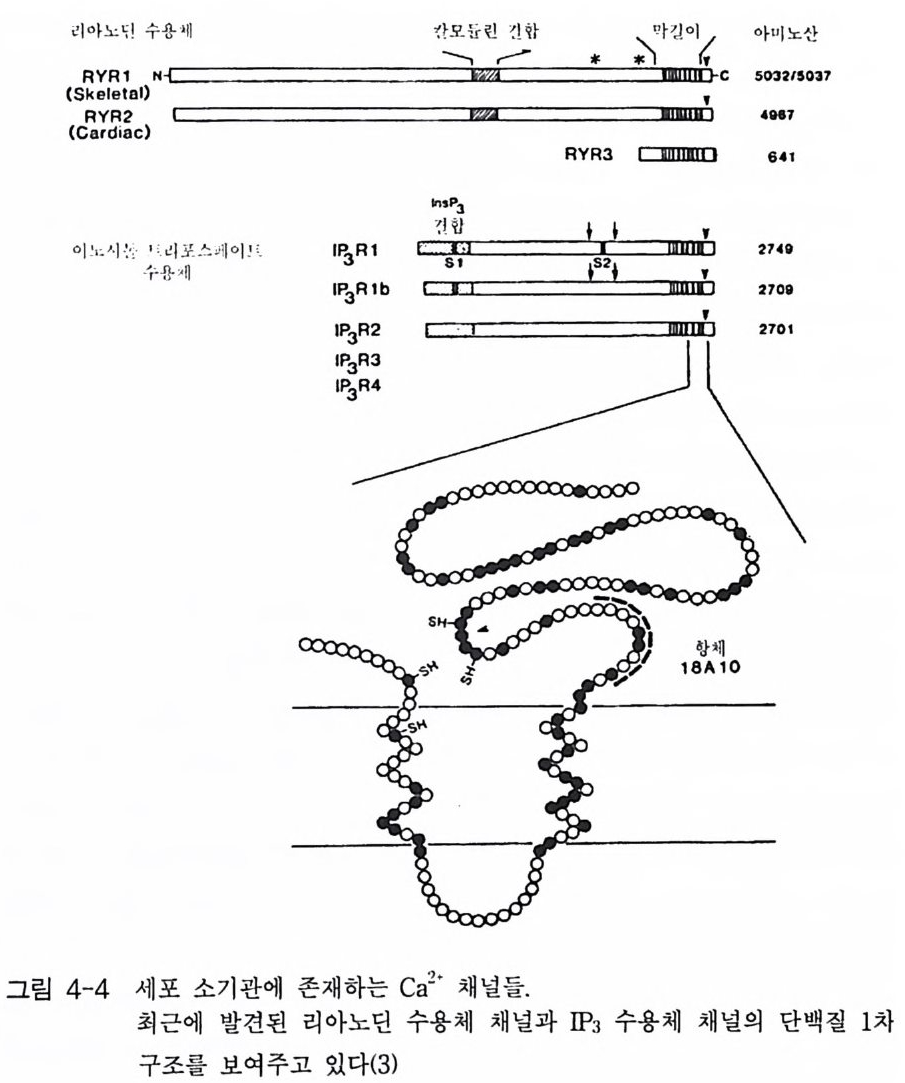 리R아Y 노R 1빈 수H용~ 사 1 칸-모- ,듄를 , '런/A r 신합 * *\막 I. 1길 1U 1이111 ( ... c 아50미32노/5 산0 3 7
리R아Y 노R 1빈 수H용~ 사 1 칸-모- ,듄를 , '런/A r 신합 * *\막 I. 1길 1U 1이111 ( ... c 아50미32노/5 산0 3 7
자리는 세포질 쪽에 위치한 N- 말단 부위에 존재한다(그림 4-4). 또 다른 Ca2+ 동원에 관여하는 리아노딘 수용체는 구조적인 면에서 크게 3 가지로 나눌 수 있는데 골격근에서 발견된 RYRl 과 심근에서 분리한 RYR2, 그 리 고 변형 성 장 인자- /3 (TGF-fl , trans fo rming grow th fac t or) 에 반응하
는 몇몇 세포에서 발견되는 RYR3 가 있는데 이 RYR3 는 다 른 RYR 에 바 해서 약간 작은 것으로 나타났다 (21) (그림 4-4 ). 또 한 신경 세 포 나 개 구 리 난세포에서 분리된 수용체의 구 조는 심장의 RYR2 와 비 슷합을 보여 주고 있다 (22, 23). 이들 리아노딘 수용체 역시 lP3 수용체와 마찬가지 로 C - 말단 영 역 에 막 관통 영역을 갖고 있으며 N - 말단 은 세 포질을 향하 고 있 는 4 개의 소 단위체로 구성되어 있다. 그러나 이 들 리아노딘 수용체 는 칼모듈린 결합 자리를 갖고 있는 것이 !P3 수용체와 다 른 점 이며 일반적 으 로 리아노딘 수용체가 IP3 수용체에 비해 약 2 배 정도가 크 다( 그립 4-4). 식물에서 분리한 리아 노 딘은 동 물 에서 는 발견 되 지 않 는 다 . 그렇 다면 실제 동물 세포에서 리아노딘으로 작용하는 즉 리아 노 딘 수용체에 결합 하는 대사 물질은 무엇인가? Lee 등 ( 24 ) 이 개구리 난세 포로 부터 분 리 한 마이크로솜에 NAD 를 첨가하였을 때 Ca 2+ 의 변화 는 일어나지 않 았 지 만 (그림 4-5A), IP 훑 첨가하였을 때에는 Ca 2+ 이 동원되었다 . 이번에 는 개 구리 난세포로부터 추출한 추출물로부터 얻은 상등액 을 NAD 와 혼합 시 킨 후 다시 미립체에 넣어 주었을 때 Ca 2+ 이 동원되었으며 곧이어 !P 3 를 첨가하였을 때 역시 Ca 2+ 이 동원되었다(그림 4_5B). 이 실험 결 과 는 NAD 가 아닌 NAD 대사 산물이 리아노딘 수용체에 결합함으로써 Ca 2· 의 동원을 일으키며 IP3 에 의해 일어나는 Ca2+ 동원과는 다른 경로에 의해 이루어지고 있음을 시사해 주고 있다. 1989 년 Lee 등 (25) 은 NMR 과 질량 분석기를 이용하여 NAD 대사 산 물이 시클릭 ADP - 리보오스 (c y c li c ADP- ri bose) 임을 밝혔는데 그림 4-6 에서 보는 바와 같이 NAD 대사 산물 (E - NAD) 의 질량 분석기의 스펙트 럼과 ADP- 리보오스의 그것과 정확하게 일치함을 보여주고 있다 . 따라 서 시클릭 ADP- 리보오스는 NAD 로부터 가수분해되어 생성된 대사 산 물이며 그림 4-7 은 시클릭 ADP- 리보오스의 구조를 보여주고 있다. 그 러나 지금까지 알아본 시클릭 ADP - 리보오스가 리아노딘 수용체에 결합
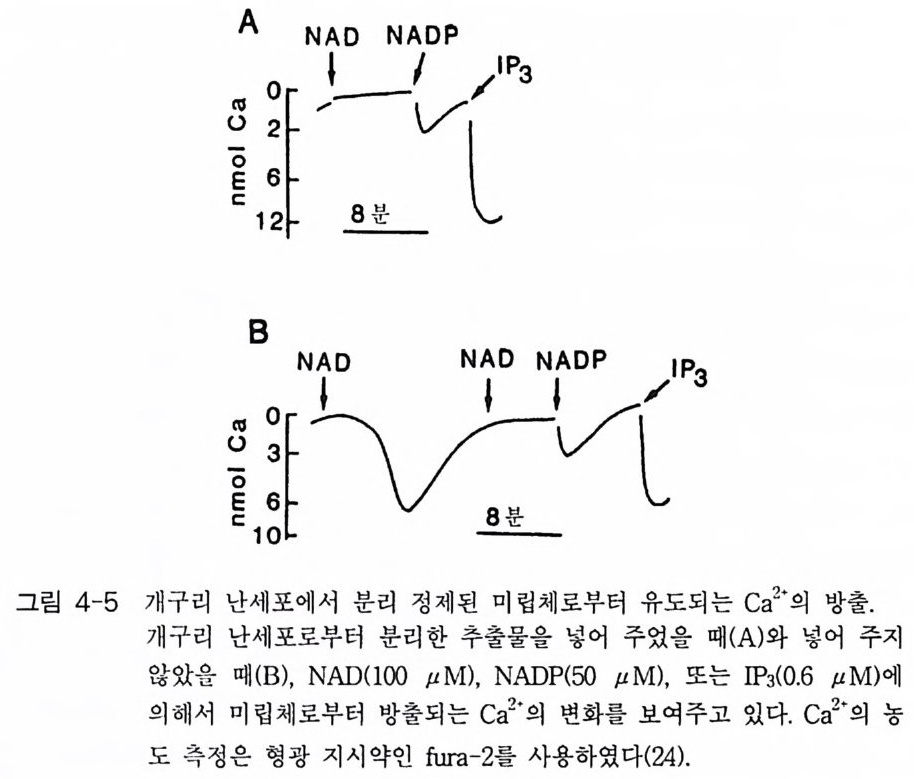 iA :N[AD 二NA仁DP〔 P3
iA :N[AD 二NA仁DP〔 P3
함으로써 일어나는 Ca2• 동원에 관여하는 신호 전달 경로는 밝혀진 바가 없다 . 최 근에 다시 Lee 등 (26) 은 시 클릭 ADP- 리 보오스가 결합함으로써 유 도되는 리아노딘 수용체의 활성화는 Ca 안 결합 단백질인 칼모듈린에 의 해 조절되고 있음을 보여주었다 . 앞으로 리아노딘(또는 시클릭 ADP- 리 보오스)에 의해 이루어지는 Ca2• 동원에 관여하는 기작의 규명이 이루어 질 것으로 생각된다.
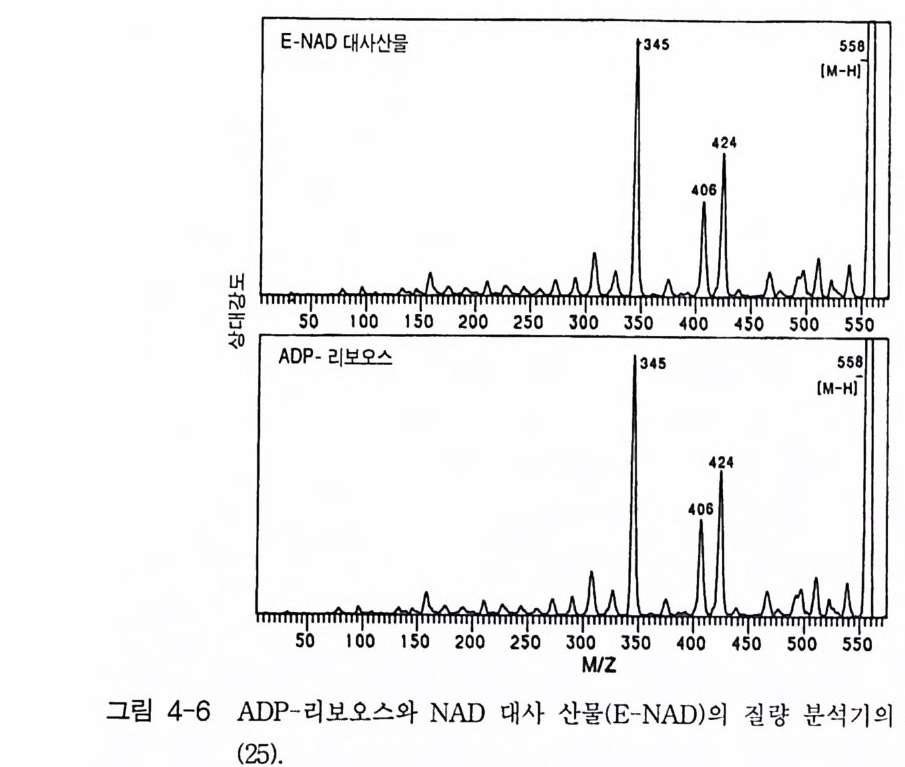 E - NAD 대사산물 345 558
E - NAD 대사산물 345 558
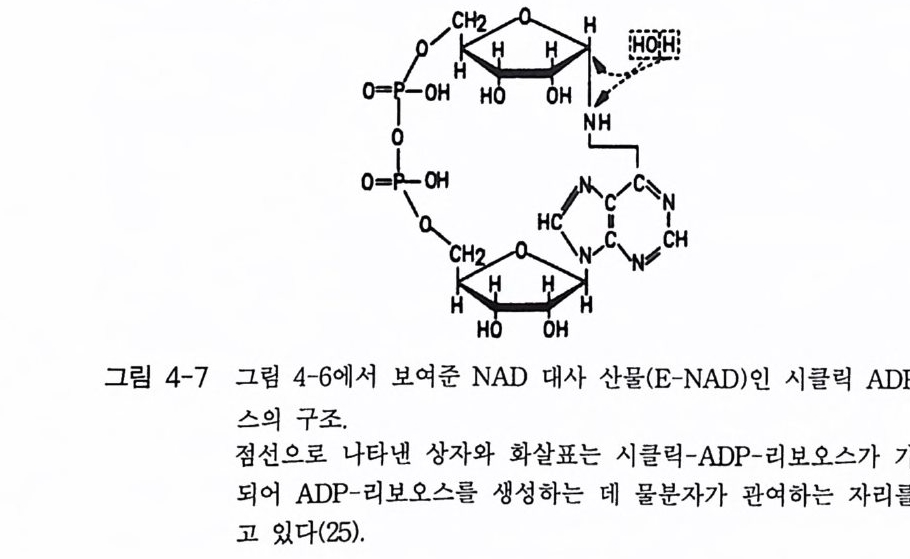 그림 4-7 그림 4 - 6 에서 보여준 NAD 대사 산 물 (E - NAD) 인 시 클 릭 ADP - 리보오
그림 4-7 그림 4 - 6 에서 보여준 NAD 대사 산 물 (E - NAD) 인 시 클 릭 ADP - 리보오
4-3 Ca 2+ 에 의해 유도되는 Ca 2 + 의 방출 (CICR) 지 금 까지 알아본 IP3 수용체 와 리아노딘 수용체들의 경우 분자의 구조 적 동질성과 Ca2’ 동원 에 관한 기능에서 비 슷함을 공유하고 있는데, 이들 두 수용체는 그 기작에서 차이점을 보여주고 있다. 그림 4-3B 에서 보는 바와 같 이 신경세 포 나 심근에 존재 하 는 리아노딘 수용체는 전압에 의해 열리는 Ca2’ 채널 (vo l t a g e- g a t ed Ca2· channel) 이 열려, 적은 양의 Ca 2+ 이 세포 내부 로 둘 어 오면 리아노딘이 활성화 되어 Ca 안을 동원 (ca2 • ind uced Ca 2 令 r e l ease) 시키는 CICR 의 양상 을 보여주고 있다 . 이에 비해 골격근의 경우에는 원형질막에 존재 하 는 디히드로피리딘 수용체(di hy dro pyridi ne rece pt or) 가 외 부 신호에 의한 전 압의 변화에 따라 구조적인 변화가 유도 되며 이 구조적 변화가 리아노딘 수용체를 활성화 시키며 Ca 안 이 동원되 고 있다(그림 4 一 3A). IP 려 경우 CICR 의 양상을 따르는 것이 아니라 활 성제에 의한 Ca2 ’ 의 방출 (a g o ni s t-i nduced calciu m release) 양상, 즉 외부 신호에 의해 수용체가 활성 화되면 IP 3 가 생성되고 이것은 신호 전이 경 로를 통 해 소포체에 존재하는 IP3 수용체에 결합하는 기작에 의해 Ca 안 을 동원시키고 있음을 보여주고 있다(그림 4-3C ). 골격근 에 존 재하는 리아노딘 수용체나 IP3 수용체의 경우, 그 주된 기 작은 CICR 이 아닌 활 성제에 의한 Ca 안 의 방출 양상을 보이지만 이들 역 시 Ca 안 의 영향을 받고 있다. 리아노딘 수용체의 경우, Ca 2• 의 양이 po- siti ve fee dback 과정 을 통하여 관여 하며 , IP3 수용체 역 시 골격 근의 리 아 노딘 수용체와 마찬가지로 Ca 안 에 특이적인 성질을 갖고 있다 . IP3 에 의 해 유도되는 Ca2• 동원의 가장 홍미로운 특징은 <전부 아니면 전무>라 는 성질일 것이다 만약 주입을 통해 세포 내 IP3 의 양을 증가시키면, Ca 양 이 순간적이면서도 거의 최대로 동원된다('2:/). Con foc al 현미경 연구 에 의하면 개구리 난세포의 경우, Ca 양 동원이 두 가지 양상을 보여주고 있는데, 먼저 Ca 안 의 방출에 의해서 어떤 최소한의 농도 이상이 되면 작
은 점을 보여주는데 이 들 점 이 갑자기 <전부 아니면 전무> 반응, 즉 Ca 안 이 파도를 치는 것같이 증감이 계속적으로 일어난다 (28, 29, 30). 이 러한 < 전부 아니면 전무 > 반응은 Ca 2+ 의 방 출 이 적은 양의 C 武 자신에 의해서 자극되는 것을 보여주 는 데 , Ca 인 이 존재하지 않을 때 IP : l 에 의한 Ca 2· 의 동원은 아주 미미하지만 , Ca 안 이 증가하기 시 작하면 갑자기 Ca21 농도가 최대 300nM 에 이 르기까지 증가하며 그 후 다시 감소하는 양상 을 나타낸다 (31) . 경우에 따라서 IP3 수용체 역시 리아노딘 수용체처럼 CICR 기작을 따르는 것으로 보여지는데, 이 CICR 기작은 앞으로 어떻게 세포가 칼슘 진동을 유도하는지 또는 세포 내의 복잡 다양한 칼슘의 변 화 를 이해하는 데 중요한 기작으로 등장할 것이다. 4-4 G- 단백질에 의해 조절되는 Ca2+ 채널 신경 전달 물질이나 호르몬을 포함한 많은 외부 신호가 Ca 2+ 의 농도를 조절하고 있음이 발견되는데, 많은 경우에 G - 단 백질의 활 성화가 여기에 관여하게 된다. 따라서 원형질막에 존재하면서 세포 밖에 있 는 Ca2’ 을 세 포 내부로 들어오게 하는 데 (Ca 2+ inf1 ux) 에 관여하는 채널은 제 2 전령이 나 G - 단백질의 영향을 직접 또는 간접으로 받게 될 것이다. 지금까지 G- 단백질이 Ca 양 채널에 영향을 미친다는 연구 결과는 많이 있다. 신경 전 달 물질인 노르아드레날린 (noradren alin)은 Ca2• 채널을 열리 게 하는데, 이때 Gs 를 경유한 cAMP 의존성 인산화에 의해 이루어진다 (32) . 이외에 도 G 를 경유한 cAMP 의 증가에 의해 활성화되는 Ca 2 ♦ 채널에 대해서는 다양한 세포에서 많이 알려져 있다 (33, 34, 35). Gs 를 매개하고 cAMP 에 의해서 활성화되는 Ca2 ♦ 채널 이외에도 단백질 키나제 C 에 의해서 활성 화되는 채널이 존재하는데 이 경우 Ca2 ♦ 동원에 관여하는 것이 대부분이 다. 그러나 최근 연구 결과에 의하면 소마토스타틴 (soma t os tati n) 이나 카 바콜 (carbachol) 에 의해 원형질막의 L- 유형의 Ca2 ♦ 채널을 저해하는데 이
때 G - 단백질의 ao 소단위체가 여기에 관여하는 것으로 알려졌다 (36, 37). 지금까지 살펴본 Ca 2 ♦ 채널 들은 제 2 전령의 생성에 의해 G _ 단백질의 간접적인 영향에 의해서 조절받게 되는데, G _ 단백질은 항상 제 2 전령을 통 해 간접적으로 Ca 2 ♦ 농도를 조절하는 것인지, 아니면 G - 단백질이 직접 c 武 채널을 조절할 수도 있 는지 에 대해 살펴보기로 한다 . 병아리의 지 각 신경 세포와 교감신경 세포 를 배양시킨 후 , 다시 cell free p a t ch 를 만 든 다 음 (o u t s i de out pa tc h ) 외부에 도파민 (do pami ne) 을 넣어 주었을 때 c 武 채 널을 닫게 하였으며 (38), ins id e out p a t ch 를 만든 후 GTP 비가수 분해 물질 인 GTPrS 를 넣어 주었을 때 역시 Ca 양 채널을 닫게 하였다 (39). 제 2 전령이나 수용성 보조 인자들이 존재하지 않는 cell free pa tc h 에서 수용체, G - 단 백질 그 리고 Ca2 + 채널이 직접 작용하고 있음을 명확 하게 보여주는 연구 결과들이다. 그렇다면 G - 단백질이 Ca 양 채널의 어느 부위에 직접 작용하여 Ca2t 채널을 활성화 또는 억제시키는지를 알아보 기로 하겠다 신경 세포에 존재하는 Ca2 ’ 채널 (L- 유형)은 G- 단백질에 의 해 억제되는데, 이는 G- 단백질과 Ca 안 채널의 리간드 결합 자리와의 상 호작용에 의해 이루어지는 것으로 밝혀졌다 (40, 4ll . 이 L- 유형 Ca 양 채 널은 활 성제에 의해 닫히게 되는데 GTPrS 가 세포 내부에 존재하는 경 우에는 닫힌 상태가 더욱 지속되었다. 이들 활성제나 GTPrS 에 의한 Ca2+ 채널에 대한 효과는 백일해 독소에 의해 억제되었는데 (42), 이는 활 성화된 G- 단백질이 활성제로서 Ca 안 채널의 리간드 결합 자리와 상호 작용하거나, G- 단백질이 Ca 양 채널에 있는 결합 자리의 구조룰 변화시킴 으로써 활성제가 잘 결합할 수 있도록 하는 데 관여할 것으로 여겨진다 (41). 비록 제 2 전령을 경유하지 않고 G- 단백질이 Ca 양 채널의 리간드 결합 자리와 상호 작용함으로써 Ca2• 채널을 조절하고 있음이 보고된 바 있지만 (41), Ca2+ 채널과 G - 단백질 사이의 상호작용 기작은 정확하게 밝 혀진 바는 없댜 Berga nasch i 등 (43) 은 G- 단백질이 Ca 안 채널에 억제제 인 디히드로피리딘 결합 자리에 직접 결합하고 있음을 보여 주었는데,
G- 단백질과 Ca2 ’ 채널의 리간드 결합 자리와의 상호작용에 대한 기작이 곧 밝혀질 것으로 기대된다 . Ca2t 유입에 관여하는 원형질막에 존재하는 Ca 2 ♦ 채널 들 중에는 지금 까지 살펴본 G- 단백질에 의해 조절되는 채널뿐만 아니라 전압에 의해 열리는 Ca2t 채널도 존재한다 . 그러나 전압에 의해 열리는 채널에 대해 서는 6 장 이온 채널에서 언급하기로 하고 Ca2 ’ 유입 체널에 대해서 알 아보기로 하겠다. 4-5 Ca2+ 유입 채널 Ca2+ 동원에서 살펴본 바와 같이 IP 3 나 리아노딘에 의해 Ca 2· 이 동원 되면 세포 내 저장소(예 를 들어, 소포체나 근소포체) 들 이 고갈 상태가 될 것이다. 이때 이들 저장소에 Ca 2+ 이 다시 채워지기 위해 세포 외부의 용 액에 존재하는 Ca 안 이 원형질막을 통과하여 유입된다 . 여기에 관여하는 Ca2+ 채널을 일반적으로 Ca2+ 유입 채널이라 한다. 그러나 JP 3 나 리아노 딘에 의해 Ca2+ 이 고갈 상태가 되었음을 어떻게 감지하여 원형 질막 에 존 재하는 Ca2+ 유입 채널이 열려지는가에 대해서는 Ca2+ 연구자 들 의 큰 관 심거리로 남아 있다. 1986 년 미국 국립 위생연구소에 있는 Pu t ne y (44) 는
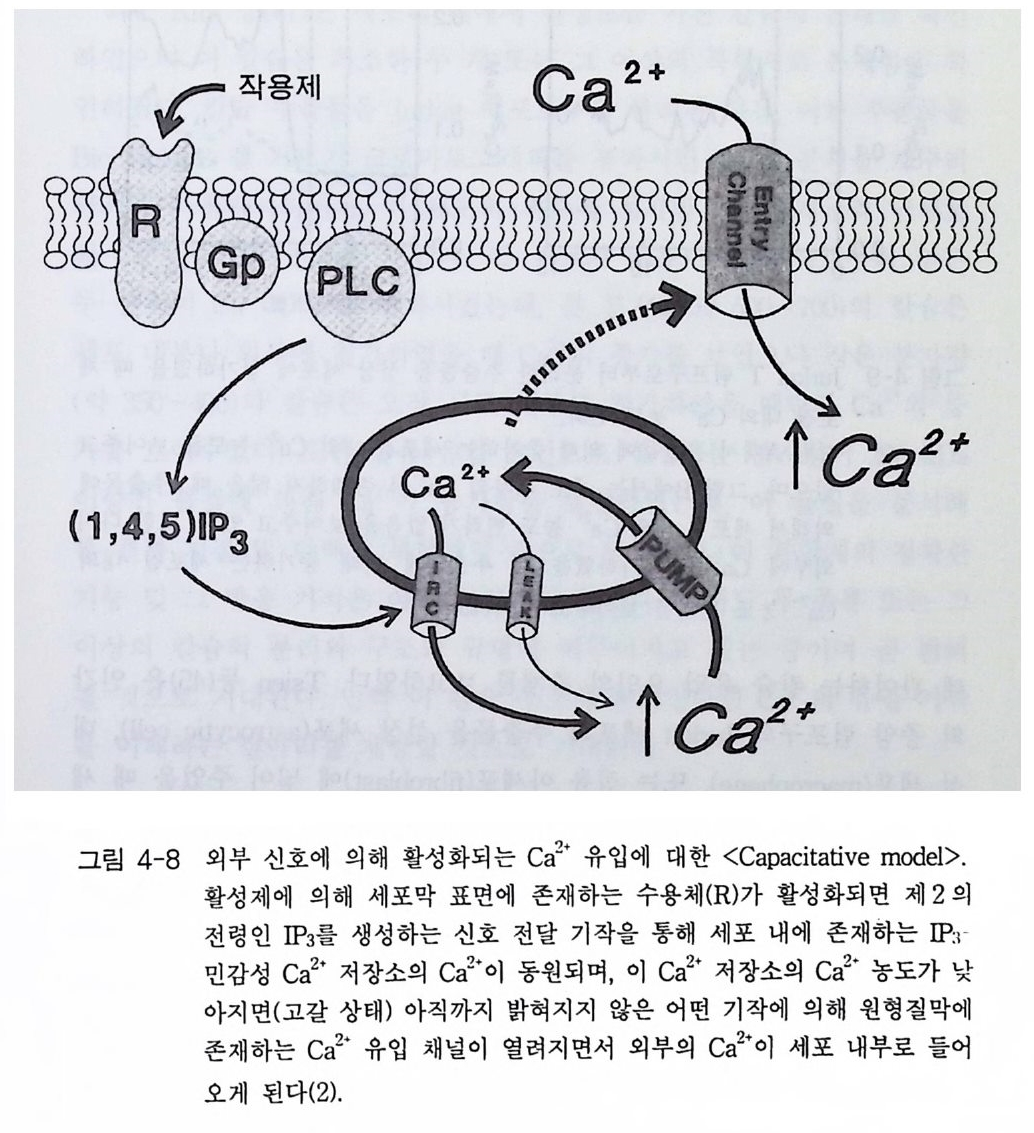 Ca2+
Ca2+
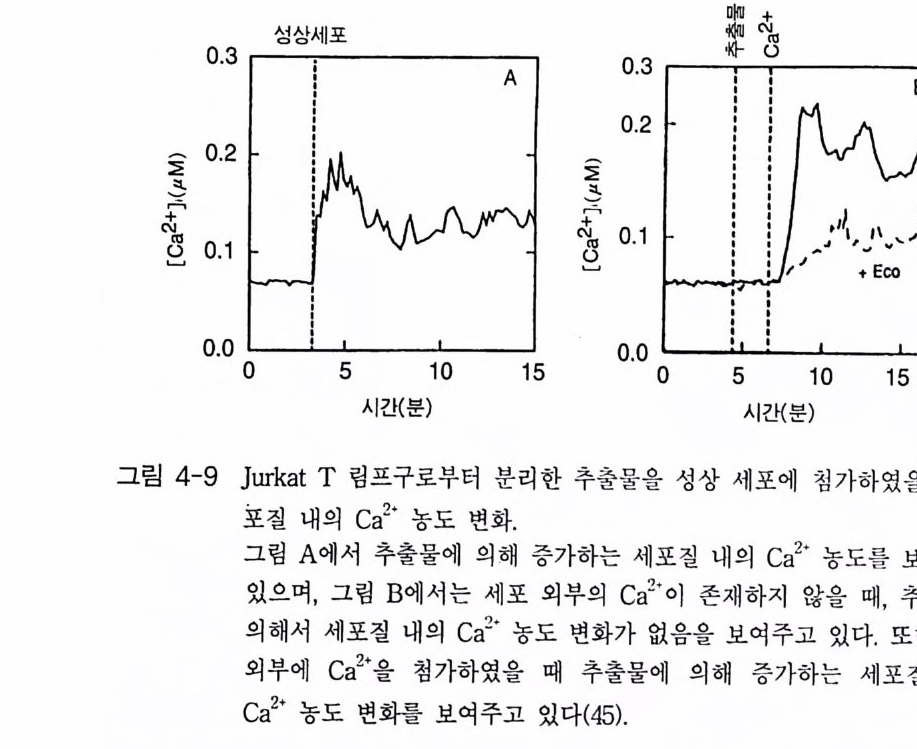 o.3 I A I 0.3 룬당 8
o.3 I A I 0.3 룬당 8
데 관여하는 칼슘 유입 요인의 존재를 보고하였다. Tsie n 등 (45) 은 인간 의 종양 림프구의 Jur kat 세포의 추출물을 성상 세포 (as tr oc yti c cell), 대 식 세포 (macrop ha g e), 또는 섬유 아세포(fi broblas t)에 넣어 주었을 때 세 포 외부 영역에 있는 Ca2+ 이 유입됨을 관찰하였다(그림 4-9). 그림 4-9A 에서 보는 바와 같이 Jur kat 추출물을 성상 세포에 첨가하였을 때 세포 내 Ca2+ 농도가 증가함을 보여주고 있다 이번에는 Ca2 + 이 없는 용액을 만든 후 추출물을 넣어 주었을 때 세포 내 Ca2+ 의 변화는 없었다(그림 4-9B). 다시 외부에 Ca2+ 울 첨가하였을 때 세포 내의 Ca2+ 의 양이 증가 하였다 . 이는 추출물에 존재하는 칼슘 유입 요인에 의해 세포 바깥의 Ca2+ 이 Ca2+ 유입 채널을 통해 세포 내부로 들어오고 있음을 시사해 주 며 유입 기작에 관여하는 물질인 칼슘 유입 요인의 존재를 확인하였다.
그러나 이 조 그마한( 분 자 량 이 500 이하) 음전하 를 띤 분자가 무엇인지는 밝혀지지 않은 상태이다. 최 근 Kim 등 (47) 은 세포질 내에서 활 성도 를 가진 칼슘의 존재를 확인 하 였으 며 이 칼슘 은 최 소한 두 개 또 는 그 이상의 복합체로 존재함을 확 인하 였 다 칼슘 추출물을 Jur kat 세포로부터 분리한 다음, 이들 추출물을 B i o 一 G e l P2 겔 거 르 기 크로마토 그 래피 를 통과시킨 후 각 분획을 개구리 난세 포 에 첨 가시키거나, 이 세 포 의 외부에 첨가함으로써 개구리 난세포 의 C a 안 농도 의 변 화 를 보았댜 겔 거 르 기 크로마토그래피로부터 얻은 두 분획 이 Ca 2 · 의 양 을 변화시켰 는 데, 큰 분자량(약 600~700) 의 칼슘은 세 포 내 부 나 외부에 첨 가하였 을 때 Ca 앙 의 중가 를 보였으나 작은 분자량 ( 약 35 0 ~4 00 ) 의 칼 슘은 오직 세포 내부에 첨 가하였을 때만이 Ca 양 의 증 가 를 보여 주 었다. 또한 칼슘 유입 요인으로 추정되는 분자량이 200 kDa 이상인 물질 에 의해 Ca 안 이 증가함을 발견하였는데, 이 물질을 분석해 본 결 과 지질 및 단백질 복합체인 것으로 밝혀 졌 다. 이 복합체의 정확한 기 능 및 그 반응 기 작 은 아직 밝혀지지 않았다 . 적어도 두 종류 또는 그 이상의 칼 슘의 분리와 구조의 규명이 이루어지고 있는 중이며 곧 밝혀 질 것으로 기대된다. 만약 이 칼슘 구조가 밝혀진다면 Ca 앙 의 유입 기작 을 이해하는 실마리 를 제공할 것으로 기대된다 . 4-6 이노시톨 포스페이트에 의한 Ca2+ 유입 제 2 전령을 경유하는 수용체에 의해 조절되는 원형질막에 존재하는 Ca2+ 채널 또한 세포 외부에 있는 Ca 앙 을 세포 내로 들어오게 하는 데 관여하는 기작의 하나로 고려할 수 있는데, 이때 관여하는 제 2 전령으로 서 잘 알려진 것은 이노시톨 포스페이트인 IP3 와 IP4 이다 (48, 49). 몇몇 세포의 경우, 이들 이노시톨 포스페이트들이 원형질막에 존재하는 Ca2+
채널을 직접 조절하고 있음을 보여주고 있다(그림 4-10). 림프구에 존 재 하는 IP3 에 의해서 Ca 2+ 이 세포 내부 로 들 어오게 되 는 데, 이때 새 롭 게 발 견된 원형질막에 존재하는 IP3 수용체 (Ca 2 t 채 널 )가 관여하는 것으로 여 겨진다 (50). 또한 후각세포의 원형질막에는 IP 3 에 의해 조절되는 Ca2t 체 널이 존재하는 것으로 보고되었다 (51, 52, 5.3). 후각세포의 경우 에 는 이 옵 단백질(여기서는 IP 3 나 IP4 가 결합할 수 있는 원형 질 막에 존 재하 는 IP:l 또는 鵬 수용체)은 IP3 나 IP4 모두에 대해 거의 같은 비 율로 민감하게 반옹하 여 이들 제 2 전령을 수용할 수 있는 데 (52) 반해 다 른 세 포, 예 를 들 어 내피 세포의 경우 원형질막에 존재하는 IP -1와 결합 하 는 Ca2 ’ 채널은 lP3 의 영 향을 전혀 받지 않는다 (54) . 이 들 결 과 를 종합해 볼 때 IP 3 나 IP4 에 의해 직접 조절되는 Ca2 • 채널이 원형질막에 존재함을 알 수 있다. IP3 가 직접 관여하는 경우와 IP 3 가 간접적으로 관여하는 경우가 있는 데 후자의 경우는 소포체를 고려해야 하는 좀더 복잡한 경우가 되겠다 . Pu t ney 가 제시한 cap a cit ative en try(그림 4-9 와 참고문헌 44) 와 궤 를 같 이 하는데, 소포체 막에 아주 가까이 존재함으로써 IP3 가 소포체에 결합 되어 Ca2+ 을 동원시킴으로서 소포체가 고갈 상태가 되면 소포체가 원형 질막에 있는 채널에 영향을 줌으로써 Ca 2+ 이 세포 내로 들어온다는 모델 이다(그림 4-10). 즉 IP3 수용체는 소포체와 원형질막 사이에서 정보를 교환할 수 있는 머리 부분을 세포질 쪽에 가지고 있을 것이라는 가능성 이 제시되고 있다 (48, 55). 소포체에 존재하는 Ca2 •- ATPase 의 특수한 억제제인 tha p s ig a rgi n( 56, 57, 58, 59), 2, 5-di -tert-b uty lh y d roq uino ne(59), 또는 calciu m i ono p hore 인 i onom y c in (58) 을 첨가하였을 때 소포체는 Ca2+ 이 고갈 상태로 되며 이때 세포 외부의 Ca2+ 이 세포 내부로 들어오고 있음을 확인하였다. 만약 소 포체가 Ca2+ 으로 충분히 채워지면(약 10mM), Ca2+ 의 유입은 중단되며, 다시 !P3 oJ ] 의해 소포체에 존재하는 Ca2+ 이 동원되고 소포체에 존재하는 Ca2 + 이 감소하게 되면 Ca2+ 의 유입 채널은 다시 열리면서 소포체가 Ca2+
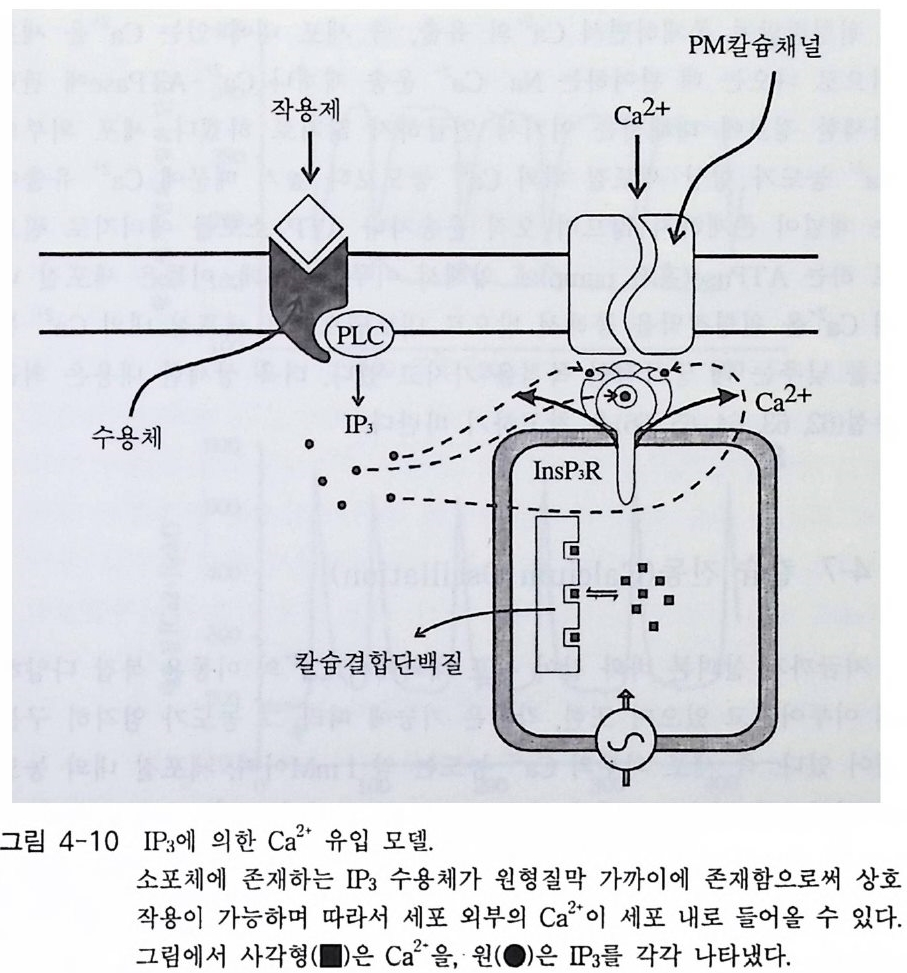 PM 칼슘채널
PM 칼슘채널
으로 채워진다. 이러한 기작에 의해 Ca 안 이 조절되고 있음이 누세포 (acri na l cell, 57) 나 비만 세포 (mas t cell, 58) 등에서 발견되었다. 또한, 다 른 연구자 (60) 들에 의해 JP 4 를 이용하는 경로를 통해서 간접적으로 Ca 안 유입이 이루어지는 현상도 발견되었다. lrvine (49, 61) 은 이들 두 이노시 톨 포스페이트에 의해 직접 또는 간접적으로 조절되는 Ca2• 유입에 관한 분석을 세부적으로 잘 기술해 놓았으므로 참고하기 바란다.
원형질막에 존재하면서 Ca 2+ 의 유출, 즉 세포 내에 있 는 Ca 안 을 세포 밖으로 나오는 데 관여하는 Na +- Ca 인 운송 체계나 ca2' - ATPase 에 관한 자세한 정보에 대해서는 여기서 언급하지 않기로 하겠다. 세포 외부의 Ca2• 농도가 항상 세포질 내의 Ca2+ 농도보다 높기 떄문에 C 武 유 출 에 는 채널이 존재하지 않으며 오직 운송자나 ATP 소모 를 에너지로 필요 로 하는 ATPase( 혹은 p um p)에 의해서 이루어지는데, 이 들 은 세포질 내 의 Ca 안을 원형 질막을 통해서 밖으로 내보냄으로써 세 포질 내의 Ca2 t 농 도를 낮추는 데 궁극적인 목적을 가지고 있다 . 더욱 상세한 내용은 최 근 총설 (62, 63, 64, 65, 66) 을 참고하기 바란댜 4 구 칼슘 진동 (Calc i um Oscil lat i on ) 지금까지 살펴본 바와 같이 세포 내외에서 Ca 2+ 의 이동은 복잡 다양하 게 이루어지고 있으며 또한, 각각은 기능에 따라 그 농도가 엄격히 구분 되어 있댜 즉 세포 외부의 Ca2+ 농도는 약 lmM 이며, 세포질 내의 농도 는 외부보다 약 10,000 배가 낮은 100~200nM 이며, Ca2+ 저장소 중의 하 나인 소포체는 상당히 높은 lOmM 정도이고, 다른 세포질 내의 저장소 인 미토콘드리아의 경우는 10 µM 정도로 잘 구분되어 있다(그림 4-1) . 세포질 내의 Ca2+ 이 높게 되면 세포에 치명상을 입히게 되는데, 이는 세 포 내의 에너지원으로서 작용하는 ATP 에 결합하거나 떨어지는 자유 인 산기가 Ca2+ 과 결합하여 인산 칼슘을 형성하기 때문인 것으로 추정된다. 세포 반응을 조절하는 데 제 2 의 전령 또는 중간체로서 작용하는 Ca2+ 은 빠른 시간 내에 증가하며 중가된 Ca2+ 은 그들의 역할을 수행한 후, 빠른 시간 내에 다시 평형 상태 즉 항상성을 유지하여야 한다. 세포 내 의에서의 Ca2+ 은 그 이동이나 역할이 복잡하고 다양한 기작에 의해 이루 어지고 있다. 그림 4-11 에서 보는 바와 같이 노르에피네프린 (nore pin e-
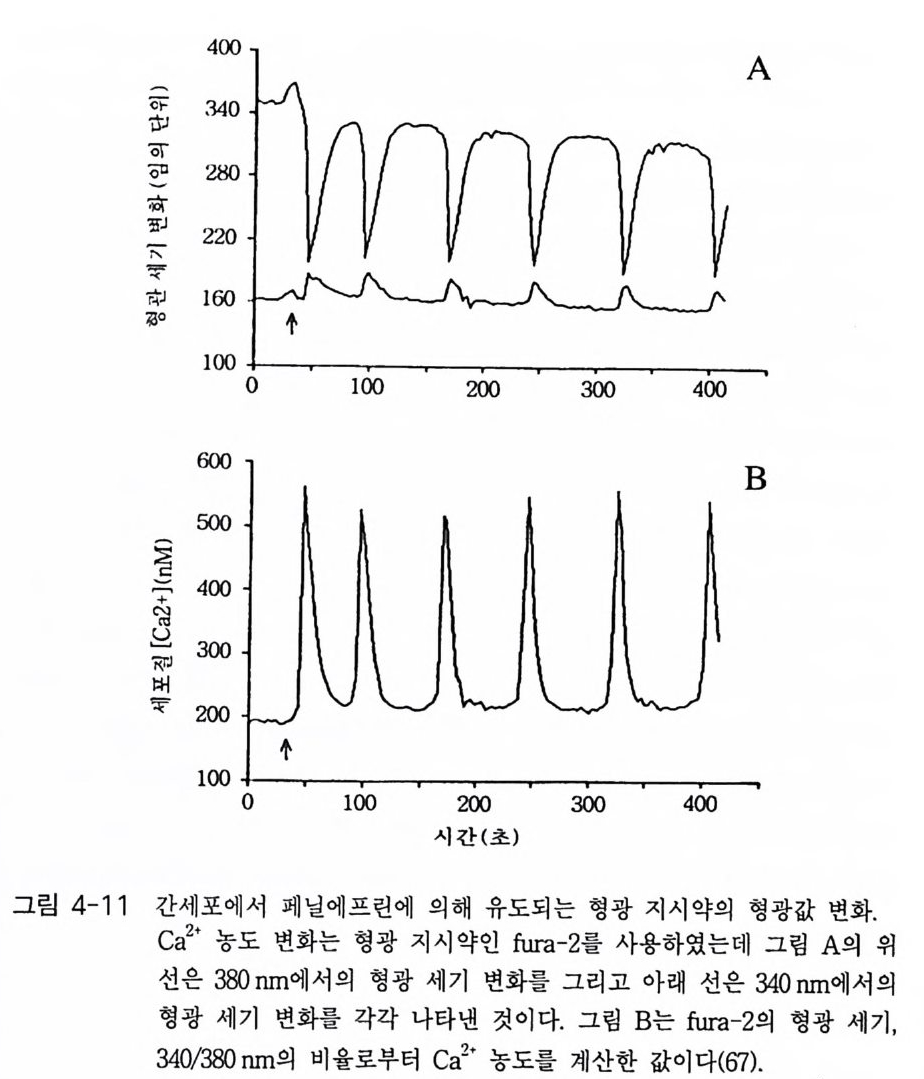 400 A
400 A
phri ne) 인 페닐에프린(p hen y le phrin e) 을 간세포 (he p a t oc yt e) 에 첨가하였을 때 세포질 내의 Ca2• 농도는 파도를 이루는 것처럼 중가와 감소가 반복 해서 일어나고 있는데 (67), 이를 Ca2• 진동이라고 한다.
4-8 세포질 내의 진동 각각의 세포에 따라 또는 외부 신호에 따라 Ca2’ 의 진동 양상은 매우 다양하게 나타나고 있댜 물론 이러한 다양성은 Ca2 1 의 이동이 서 로 다 른 기작에 의해서 이루어지기 때문이다. Ca2 + 의 진동 양상은 크게 사인 파 진동과 일시적 진동 두 가지로 나눌 수 있다. 사인파 진동은 일반적 으로 Ca 2+ 의 농도가 최대에 이르기까지 증가한 후 Ca2’ 파도 를 이 루는 데 이때 세포질의 Ca2+ 농도는 증가된 상태 를 유지하게 된다(그림 4-12). 일 시 적 진동(또는 base-lin e s piki n g)은 그림 4 - 12 에 서 보는 바와 같이 신호 에 의해 세포질의 Ca 안이 일시적으로 증가한 후 다시 정상 수준에 이르 기까지 감소한 다음 다시 비슷한 수준의 증가와 감소를 반복하는 양상 을 보이고 있다 . 이들 두 진동 양상은 같은 세포에서 다론 신호나 자극 에 의해서 일어날 수도 있는데, 예를 들어, 췌장 세포의 경우 아세틸 콜린 에 의해서 이루어지는 Ca24 이동은 사인파의 양상을 보이는 반면, 콜 레 시스토키닌 (cholec y s t o kini n) 에 의해서는 일시적 진동을 따 른 다 (69). 이 들 두 양상 모두 진동으로 간주되지만 엄격한 의미에서의 진동이란 일시적 진동을 의미하게 되며 대부분 신호 전달에 의해서 이루어지는 Ca 2’ 의 진 동은 일시적 진동에 의해서 이루어지고 있다. 따라서 이 장에서는 일시 적 진동만을 다룰 것이다. 4-9 진동과 신호 전이 기작 가장 널리 알려진 진동은 아들레날린 수용체, 바소프레신 (vaso p res s in)과 엔지오텐신(angi o te ns in) 수용체의 활성화에 의해서 이루어지는 세포질 내의 Ca2+ 농도의 증가 때 나타나는데, 이들은 앞에서 살펴본 포 스포이노시티드 경로를 통해서 이루어지는 대표적인 예들이다 (70, 71,
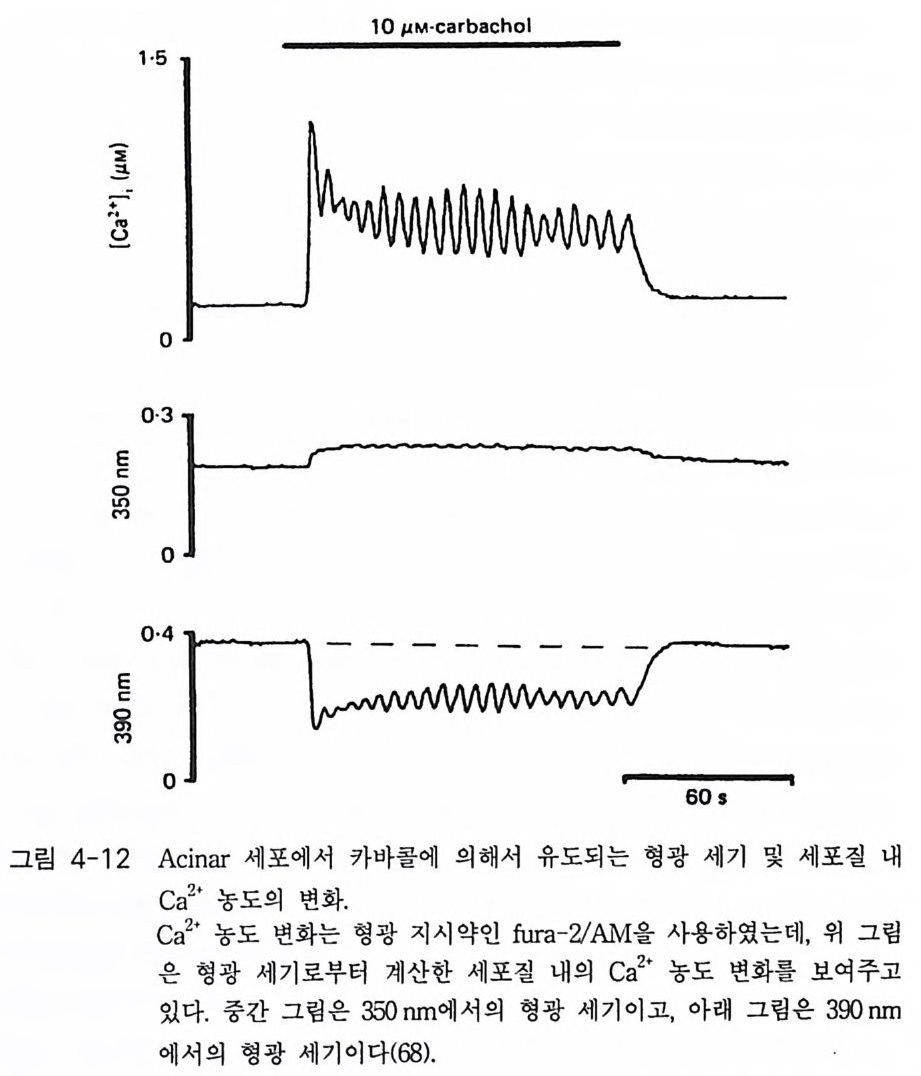 10 µM -ca rbachol
10 µM -ca rbachol
72). 특히, 포스포이노시티드 경로는 성장 인자에 의해 조절되는 세포 반 응이나 수정을 위한 세포 반옹에 신호 전이 기작으로 많이 나타나는데, 이때 Ca2+ 진동이 발생하는 것으로 여겨진다 (73 - 77) . 대식 세포는 lP3 가 형성되면 아주 큰 Ca 양 진동이 일어나는데, lP3 를
세포 내에 주입하거나 G_ 단백질의 비가수분해 활성 물질인 GTPrS 를 첨가하였을 때에도 같은 양상의 Ca 언 진동이 일어난다 (78 - 80). 이 들 모든 실험 결과는 Ca2 t의 진동이 3 장에서 살펴본 포스파티딜 이노시톨 기작을 통한 신호 전이 반응에 의해 이루어지고 있음을 시사해 주고 있다. 포스 포이노시티드의 또 다른 제 2 전령안 DAG 에 의해서 활성화되는 단백질 키나제 C 역시, Ca2 t의 진동에 관여하기도 하는데, 이는 세포 종에 따라 크게 좌우되는 것으로 밝혀졌다. 예를 들어 쥐의 난세포 (81) 나 성상 세포 (astr oc y te, 82) 에서는 단백질 키나제 C 의 활성 인자인 포볼 에스터에 의 해 Ca2+ 의 진동이 일어나지만 간(8.3), 섬유 아세포 (84), 그리고 쥐의 난세 포(8.5)에서는 Ca2 + 의 진동이 오히려 저해되었다. Ca2• 진동을 조절하는 모델로서 크게 두 가지가 있는데, 하나는 수용 체에 의해 조절되는 진동과 제 2 전령에 의해 조절되는 진동이 그것이다. 수용체에 의한 Ca2+ 진동을 다시 2 가지로 나눌 수 있는데 그 하나가 음 제어 모델 (ne g a ti ve fee dback model) 이고, 다른 하나는 양 제어 모델 (pos it ive fee dback model) 이다. 먼저 음 제어 모델의 경우, 외부 신호에 의해 포스포이노시티드 대사 (PI turn over) 를 통해서 PIP2 가 IP3 와 DAG 로 분해되면 IP3 가 세포질 내의 Ca2• 을 증가시키고 이때 DAG 가를 통해 PLC 를 저해시킴으로써 Ca2• 진동을 조절할 것이라는 모델이다. 탈인산 화가 이 저해를 다시 제거함으로써 새로운 신호 전달 순환이 시작되고 다음 단계의 IP3 가 형성되는 것을 나타내는 모델이다. 또 다른 모델인 양 제어 모델에서는 PI 대사에 의해 생성된 적은 양의 IP3 가 다시 Ca2+ 의존 성 PLC 를 활성화시킴으로써 많은 양의 IP3 가 생성되고 세포질 내의 Ca2+ 의 농도가 증가하는데, 증가된 세포질 내의 Ca2+ 은 미토콘드리아와 같은 IP3_ 민감성 저장소로 들어감으로써 감소하게 되고, PLC 를 활성화 시킬 수 있는 농도보다 낮아졌을 때 IP3 의 생성은 중단된다. Ca2+ 이 소포 체로 전달되면서 소포체에 Ca2+ 이 채워지고 다시 PI 순환에 의해 Ca2+ 의 이동이 시작된다는 모델이다 (87).
일반적으로 세포질 내의 lP3 양은 외부 자극인 활성제의 양에 의해 결 정되는데, 앞에서 언급한 두 모델 즉, 음 제어나 양 제어 모델을 통해서 는 이 들 활성제와 IP3 양과의 관계 를 명확하게 설명할 수가 없다. 이 점 을 보완할 수 있 는 모델로서 제 2 전령에 의해 조절되는 Ca 2• 의 진동 모 델을 생각해 볼 수 있다. 이 모델에서 는 적어도 두 개의 칼슘 저장소가 존 재하고 있음 을 전제하는데, 즉 IP 3_ 민감성 저장소와 lP3- 비민감성 저 장소가 그것 이다 (88). 그 러나 아직까지는 정확하게 이들 두 저장소가 존 재하 는지, 아니면 하나의 저장소가 때에 따라 다른 역할을 하는지는 알 수가 없다. 예 를 들 어, 평활근 (smoo t h muscle) 은 단 하나의 칼슘 저장소 를 갖고 있는데 이 저장소는 lP 3 에 대해 반응할 뿐 아니라 카페인에 대 해서도 반옹하기 때문이다 (89). 이 모델에서는 lP 3 _ 민감성 저장소는 원형 질 막에 가까이 있음으로 해서 PI turn over 에 의해 Ca 양 이 생성되면 주로 Ca 2 · 의 유입에 관여하고, 원형질막으로부터 비교적 멀리 떨어져 있는 IP a ― 비민감성 저장소는 CICR 의 기작을 통해서 Ca 양의 이동이 진행된다 고 설명하는 모델이다 이 경우 Ca 안 이 진동하는 동안 lP3- 민감성 저장소 에 의한 Ca 2+ 의 이동은 비교적 일정한 양을 유지하는 데 반해 lP3 ― 비민감 성 저장소의 경우는 톱니 형태 (sa wt oo t h p a tt ern) 를 보인다는 것이다 (88). 그림 4 - 13 에서 보는 바와 같이 소포체 막에 존재하는 lP3 수용체 (Ca2 + 채널)에 lP3 가 결합하게 되면 Ca 안 이 동원되면서 소포체는 고갈 상태가 되며 이때 칼슘이 생성되어 원형질막에 존재하는 Ca2• 유입 채널을 열어 주면 Ca2• 이 들어오게 되는 하나의 가능성이 있다. 또 다른 가능 경로로 서는 소포체가 고갈 상태가 될 때, 고갈 신호가 소포체 막에 있는 어떤 단백질 또는 lP3 수용체 자신이 원형질막의 Ca2• 유입 채널과 직접 상호 작용하여 Ca 양이 세포 내로 들어온다는 가능성을 고려할 수 있다 . Confo c al 현미경 실험 결과에 의하면 외부 Ca2 + 이 Ca 안 유입 채널을 통해서 소포체에 채워질 때 세포질 내의 Ca 양 농도의 증가가 발견되지 않았는데, 이는 외부 Ca2• 이 직접 소포체로 들어갈 가능성을 내포하고
 CIF •
CIF •
있댜 이 경우 후자의 가능성으로 설명이 가능해진다 (48). 최근 많은 Ca 2 + 연구자들에 의해서 이에 대한 연구가 활발히 진행되고 있으므로 여러 가능 기작들이 곧 밝혀질 것으로 기대된다. 지금까지 살펴본 Ca2+ 의 이 동에 관여하는 반응 중에서 가장 핵심적인 역할을 하는 제 2 전령은 lP3 이다. lP3 가 세포 내에서 중간 전령으로서 많은 세포 표면에 존재하는 수 용체와 세포질 내의 Ca2+ 저장소에 있는 Ca2+ 의 동원 사이에서 그 중추 를 담당하고 있음을 알아보았댜 Ca2+ 연구에서 두 가지 밝혀지지 않은 의문점을 안고 있는데, 그 첫째가 Ca2+ 유입에 대한 문제이다. 죽, lP3 생
성에 의해 소포체에 있는 Ca 2+ 이 동원될 때, 세포 외부에 존재하는 Ca21 이 세포 내부로 들 어오 는 데 (Ca 2 수 유입), 그 작용 기작이 분명치 않다는 사 실 이댜 이 작용 기작을 설명 하 는 모델로서 Pu t ney (2) 의
8) lVIIg n eD' , G . A. and Sii dh of, T. C. 0990) EMBO ]. 9, 3893 9) Ghosh, T. K, Mullaney, J. M., Tarazi, F. I. and Gil l, D. L. 09 89) Natu r e 340, 236 10) Str upish , J, Cooke, A. M., Pott er , B . V. L., Gig g, R. and Nal1orski, S. R. ( 1988) Bio c hem ]. 253, 901 11) Hill, T. D., Bergg ren , P. 0. and Boy n to n , A. L. 09 87) Bi uc hem Bi op h ys. Res. Commun. 149, 897 12) Meye r , T., H olowka, D. and Str yer , L. (19 88) Scie n c e 240, 65.3 13) Seile r , S. M., Arnold, A. J. and Sta n to n , H. C. 0987) Bi oc hem PIY irm acol. 36, 3331 14) Shah, J. and Pant, H. C. 0988) Bi oc hem ]. 250, 617 15) Endo, M. 0977) Ph ys io l. Rev. 57, 71 16) Ma rton si, A . N. (19 84) Phsio l. Rev. 64, 1240 17) Procita , L. (19 56) ]. PIY irm acal. Exp. Ther. 117, 363 18) Hillyar d, I. W. and Procita , L. (1959) ]. Pmrmacol. Exp. Ther. l 없 22 19) Renzi, V. and Macdennoff , A R. (19 92) Neuroscie n ce 46, 251 20) Tsie n , R. W. and Tsie n , R. Y. 0990) Ann Rev. Cell Bi ol . 6 , 715 21) Gia nnini, G., Clementi, E., Ceci, K., Marzia li, G. and Sorren t i no , V. (19 92) Sc ien ce 257, 91 22) Walto n , P. D., Airey , J. A, Sutk o, J. L., Beck, C. F., Mign ery , G. A., Sti dh of, T. L., Deerin c k, T. J. and Ell ism an, M. H. (19 91) J Cell Bi ol . 113, 1145 23) McPherson, S. M., McPherson, P. S., M ath ew , L., Camp b ell, K. P. and Long o, F. J. (1992) J Cell Bio l. 116, 1111 24) Clapp er , D. L, Walseth , T. F., Dargi e, P. T. and Lee, H. C. (19 87) J Bi ol. C hem. 262, 9561 25) Lee, H. C., Walseth , T. F., Braf f, G. T., Hay es , R. N. and Clapp er , D.
L. 09 89 ) ]. Bi ol . C hem 264, 1608 26) Lee , H. C., Aarhus, R., Graeff, R., Gurnack, M. E. and Walseth , T. F. 0994 ) Na tu r e 370 , 307 27) Mi ya za ki , S. Y. (19 88 ) ]. Cell Bi ol . 106, 345 28) Pa rk e r, I, Ya o, Y. 0991) Proc. R. Soc. Land B 246, 269 29) Lechlei th e r , J. D., G ir a rd, S., Peralta , E. and Claph an, D. E. 0991) Scie n c e 252, 123 30 ) Lec hl eit he r , J. D. and Clap ha n, B. E. (1992) Cell 61, 1 31 ) lino , M. 0990) ]. Gen Ph ys io l . 9 5, 1103 32) Ka m eya ma, M., He sch el e r , J., Hofm ann, F. and Trautw ein , W. (1986) Pf/ilge rs Arch. 407, 123 33) Chad, ]. and Eckert , R . 0980) ]. Ph ys io l. 378, 31 34) Dolph in, A C., McGu irk, S. M. and Scott , R. H. (19 89) Br . ]. Plurmacol. 97, 263 35) Gray, R. and Joh nsto n , D. (1 9 얽) Natu r e 3'2: 1, 620 36) K.leu ss, C., Heschreler, J., Ewel, C., Rosenth a l, W., Schultz , G. and Wi ttig, B. (19 91 ) Natu r e 353, 43 37) K.leu ss, C., Scherubl, H., Hescheler, ]., Schultz, G. and Wi ttig, B. (19 92) Natu r e 358, 424 38) Marchett i, C ., Carbone, E. and Lux, H. D. (19 80) Pfluge r Arch 406, 104 39) Dolph in, A C., Scott , R . H. and Woott on , J. F. (19 89) ]. Ph ysi o l. 410, 169 40) Dolph in, A C. and Scott , R H. (1989) J Ph ys io l . 4 13, 幻 41) Scott , R . H. and Dolph in. A C. (19 87) Natu r e 330, 760 42) Scott , R . H. and Dolph in. A C. (19 88) Neurosci. Lett. 89, 170 43) Berga naschi , S., Govon i, S ., Com ine ri, P., Parenti, M. and Trabucchi ,
M. (19 88) Bi oc hem Bio p h y s . Res. Commun. 56, 127 9 44) Putn e y, J. W. Jr. (19 86) Cell Calci um 7, 1 45) Rand ria mamp ita, C. and Ts ie n , R. Y. 09 93 ) Na tu r e 364, 806 46) Parekh, A. B., Terlay , H. and Sti ihm e r, W. (19 93) Natu r e 364, 814 47) Kim, H. Y., Thomas, D. and Hanley, M. (19 95 ) J Bio l. Ch em subm itted . 48) Irvin e , R. F. (19 90) FEES Lett . 2 63 , 5 49) Irvin e , R. F. (19 91 ) Bi os says 13, 419 50) Khan, A. A., Ste i n e r, J. P., Klein , M. G., Sc hnei d e r , M. F. and Sy n der, S. H. (1992) Sc ien ce 257, 815 51 ) Fadool, D. A. and Ache, B. W. 0992 ) Ne uron 9, 907 52) Ka lino ski , D. L., Aldi ng e r, S . B, Boy le , A. G., Huq u e, T., Ma rec ek , J. F., P restiw ich , G. D. and Restr ep o , D. (1992 ) Bi oc hem J 281 , 449 53) Restr ep o , D. J., Miyam oto , T., Bry an t, B. P. and Teete r , J. H. (19 90) Scie n ce 249, 1166 54) Lti ck hoff , A. and Claph a n, E. D. (1 992) Natu r e 335, 356 55) Berr idge , M. J. (19 90) J Bi ol. Chem. 265, 9583 56) Clementi, E., Scheer, H., Eacchett i, D., Fasolato , C., Poeean, T. and Meldolesi, J. (19 92) J Bi ol. Chem. 267, 2167 57) Bir d, G. st J., Rossie r , M. F., Hug h es, A. R., Shears, S. B., Armstr on g , D. L. and Putn e y, J. W. Jr. (19 91 ) Natu r e 352, 162 58) Hoth , M. and Penner, R. (19 92) Natu r e 355, 353 59) Robin so n, I. M., Cheek, T. R. and Burgo y n e, R. D. (1992) Bi oc hem ]. 288, 457 60) Chang a, L., Gallacher, D. V., Irvine, R. F., P ott er, V. L. and Pete r sen, 0. H. (1989) J Memb. Bi ol. 109, 85 61) Irvine , R. F. (1992) FASEB. J 6, 3085
62) Grover, A. K. and Khan, I. (19 92) Cell Calci um 13, 9 63) Inesi, G., Sumbil la , C. and Kirtle y, M. E. (19 90) Ph ys io l. Rev. 70, 749 64) Schatz m ann, H. (19 89) An n. Rev. Phys io l. 51, 473 65) Phil ip s o n, K. (19 & 5) Ann Rev. Ph ys io l. 47, 561 66) Carnfo li , E. 0987) An n. Rev. Bi oc hem. 56, 395 67) Rooney , T. A., Sass, E. J. and Thomas, A. P. (1989) ]. Bi ol. Chem 264, 17131 68) Gray, P. T. A. (19 88) ]. Ph ys io l. 406, 35 69) Osip ch uck, Y. V., Wak 띠, M., Yule, D. I., Gallacher, D. V. and Pete r sen, 0. H. 0989) EMBO ]. 9, 697 70) Woods, N. M., Cuth b erdson, K. S. R. and Cobbold, P. H. (19 ITT) Cell Calciu m 8, 79 71 ) Rooney, T. A., Sass, E. J. and Thomas, A. P. (19 89) ]. Bio l. Chem. 264, 17131 72) Kawan ish , T., Blank, L. M., Harootw nian , A. T., Sm ith, M. T. and Tsie n , R. Y. (19 89) ]. Bi ol. Chem. 264, 12859 73) Cuth b ert so n, K. S. R., Whittingh am, D. G. and Cobbold, P. H. (19 81) Natu r e 294, 754 74) Miyaz a ki, S. I. (1988) ]. Bi ol. Chem. 106, 345 75) Wi lso n, H. A., Greenblatt , D., Poen ie, M., Fin kel man, F. D. and Tsie n , R. Y. (1 9 初 ]. Esp. Med. 166, 601 76) Pallotta , T. and Peres, A. (1989) ]. Ph ys io l . 416, 589 77) Lew is, R. S. and Cahalan, M. D. (1989) Cell Regu l. 1, 99 78) Kruskal, B. A. and Ma rxfield , F. R. (19 87) ]. Bi ol. Chem. 105, 268 .5 79) Oron, Y., Dascal, N., Nadler, E. and Lup u , M. (19 &5 ) Natu r e 313, 141 80) Cornell-Bell, A. H., Fin kb ei ne r, S. M. Coope r, M. S. and Sm ith, S. J. (1990) Sc ien ce 247, 470
81) Cuth b ert so n, K. S. R. and Cobbold, P. H. (1985) Natu r e 316, 541 82) Macvic a r, B. A, Cri ch to n , S. A, Burnard, D. M. and Tse, F. W. Y. (19 87) Natu r e 329, 242 8.3) Woods, N. M. , C uth b ert so n, K S. R. and Cobbold, P. H. (1987) Bi o- chem ]. 246, 619 84) Harootu nian , A T., K ao, J. P. Y. and Tsie n , R. Y. 0988) Cold Sp r in g Harbor sym p . Qu ant Bi ol . 5 3, 935 &5) Swann, K, Igu sa , Y. and Miyaz aki , S. 098.9 ) EMBO ]. 8, 3711 86) Cobbold, P., Cuth b ert so n, R. and Woods, N. (1988) in Procee ding s of the 12th Sy mpos iu m on Harmones and Cell reg u lati on (Nunez, J., Dunont, J. E. and Caraf oli , J. E. eds) p 134, Joh n Libb ey Eurote x Ltd, Pa ris 87) Meye r , T. and Str yer , L. (1988) Proc . Natl. Acad Sci . USA . 磁 5051 88) Berr idge, M. J. and Ga lion e, A (1988) FASEB ]. 2, 3074 89) Iino, M. (1987) Bi oc hem Bi op h ys. Res. Commun. 142, 47 90) Tayl e r, C. W. (1984) TIPS. 19, 'Zll
제 5 장 단백질 인산화와 단백질 키나제 단백 질 인산화(p ro t e i n p hos pho ry la ti on) 는 세포에서 단백질의 기능을 예민하게 조 절 하는 가장 중요한 반응이라고 말해도 과언이 아니다 . 단백 질 의 다 른 자리 입체성 조절(예, alloste r ic re gul a ti on) 의 경우 주로 항상 성 기능에 관여하는 반면 , 단백질의 인산화 반응은 한 상태에서 다른 상 태로 세포의 활성도를 바꾸어 주는 역할에 많이 관여한다. 두 가지 중요 한 기능을 다음과 같이 제시할 수 있다 . 1) 호르몬이나 성장 인자들과 같 은 세포 외부의 신호가 세포 반응으로 이어지는 중간 단계에 관여하 는 중요한 반응이다. 2) DNA 합성이나 세포 분열과 같은 세포 주기에서 반드시 일어나야 하는 사건들의 시간 맞추기에 꼭 필요한 반응이다. 세 포의 분열이나 대사 과정에서 중요한 역할을 담당하고 있는 단백질의 인산화 반응은 단백질 키나제들에 의해 진행되며 , 단백질 포스파타제 (pro te in p hos ph a ta se) 에 의해 역으로 진행되는 탈인산화 (de p hos p ho ry lati on ) 반응을 일으켜 대사 조절을 하게 된다. 지금까지 적어도 200 개 이 상의 단백질 키나제들이 DNA 의 염기 서열 분석에 의하여 일차 구조가 밝혀졌으며, 앞으로도 빠른 속도로 이 효소들의 구조 및 기능에 관한 연 구가 진행될 것이다. 단백질 포스파타제에 관한 연구 결과는 현재까지
그리 많은 편은 아니지만 앞으로 괄 목 할 만한 연구 결 과 들 이 나타 날 것 으로 기대된다 많은 단백질 키나제들이 보고되어 있으나 본 장에서는 가장 대 표적 인 몇몇 단백질 키나제 (cAMP 의존성 단백질 키나제, Ca2 + / 칼모듈린 의 존성 단백질 키나제, 단백질 키나제 C, 그 리고 단백질 티로신 키나제) 들 에 관하 여 그들의 구조와 기능에 관해서 기술할 것이다. 부가하여 단백질 포스 파타제에 관한 내용도 간단히 기술하고자 한다. 5 기 cAMP 의존성 단백질 키나제 최초로 발견된 단백질 키나제 중의 하나가 cAMP 의존성 단백질 키나 제인데, 이 효소의 경우 제 2 의 전령 중의 하나인 cAMP 에 의하여 그 활 성도가 조절되는 것이다. cAMP 가 발견된 이래 많은 다양한 키나제들이 확인되고 있는데, 거의 모든 키나제들은 포스페이트 (HPO 43 - ) 그 룹을 단 백질의 세린/트레오닌 또는 티로신 잔기에 공유결합으로 옮겨 주는 것으 로 알려져 있다. 어떤 키나제들은 제 2 의 전령(예, cAMP, Ca2 \ DAG 등) 에 의해 활성화되는 반면 또 다른 어떤 것들은 성장 인자들과 같은 일차 적인 신호에 의해 활성화되기도 한다. cAMP 의존성 단백질 키나제는 모든 키나제 종류들을 대표한다고 말 할 수 있는데, 그 활성화 메커니즘이 특이하며 단백질 키나제들 가운데에 서도 유일성을 가지고 있는 효소이다 . cAMP 가 존재하지 않을 경우 이 효소는 두 개의 조절기능을 갖는 소단위체와 두 개의 촉매 기능을 갖는 소단위체들로 구성된 비활성의 사량체로 존재한다 . 세포 내 cAMP 의 농 도가 증가하면 활성화되기 시작하며, 세포에서는 cAMP 가 결합되는 부위 가 R- 소단위체 (re gul a tory sub unit)임이 밝혀졌다. cAMP 가 R- 소단위체 에 결합을 하면 이 부분의 입체 구조 변화가 일어나며 그 결과는 C- 소단
위체 (ca t al y ti c s ubun it)에 대하여 약한 친화력을 갖는 구조적 안정을 가 져와 전체 효소 콤플렉스 의 분해를 촉진시키게 된다 . 이때 R - 소단위체로 부터 분리된 C- 소단위체 (Mr : 38,900) 는 촉매적으로 활성화된다. cANIP R2 C 2 cAMP- R 2 + C2 비 활성 활성 단백질 키나제족의 다양성에도 불구하고 그들의 구조와 기능적 측면 은 상당한 공통성이 있는 것으로 알려져 있으며, 특히 모든 단백질 키나 제 둘 은 보존된 촉 매적 핵심 부위를 가지고 있다. 이 사실은 이들 효소들 이 하나의 공통된 원조에서 진화된 것으로 추측하게 한다. 촉매의 기능 울 갖는 소단위체 (C-subu nit)는 다른 모든 키나제들의 촉매 기능을 갖는 부위와 아미노산 서열의 상동성이 높으며, ATP 결합 또는 촉매작용에 필수적 인 아미노산 잔기 들도 모든 종류의 키나제 족들에서 잘 보존되는 것으로 보고 되어 있다. 5-1-1 단백질 키나제들의 상동성 그림 5 기에 몇 개 키나제들의 아미노산 서열 배치를 요약 표시하고 있댜 cAMP 의존성 단백질 키나제와 가장 큰 유사성을 갖는 키나제가 cGMP 의존성 단백질 키나제이다. 이 효소도 시클릭 뉴클레오티드에 의 하여 활성화되는데, 이 효소의 경우는 뉴클레오티드의 결합 부위가 c- 말단에 위치하여 촉매 기능을 보유한 영역을 포함하고 있는 연속적인 폴리펩티드 사슬의 한 부위에 있댜 Ca 2+/ 칼모듈린 의존성 단백질 키나 제(예, my o sin ligh t -c ha in ki nase) 들은 C_ 말단에 Ca2+ /칼모듈린 조절 부 위를 가지고 있다 (1).
 -'귁J노 ’’’ ’c AM P조측 의 에절 작邑작용옹 뻥소소단집단위 위 서시키 나서
-'귁J노 ’’’ ’c AM P조측 의 에절 작邑작용옹 뻥소소단집단위 위 서시키 나서
그 러나 단백 질 키 나제 C(PKC) 는 Ca2\ DAG 그리고 PS 와 같은 조절 인자 들 이 결합 하 는 조절 부위가 촉 매 기 능을 가지고 있는 부위의 앞에 위치하 고 있다 (2 ). EGF 수용체나 인 슐 린 수용체와 같은 경우는 막을 가 로지르는 단 일 펩 티 드 의 세포 외 영역에 호르 몬의 결합 부위 를 가지고 있으며, 단백 질 키나제의 활 성도 를 갖는 세포 내 영역을 가지고 있다. 5-1-2 활성화 자리 Zoller 등 ( 3) 이 최초로 뉴 클 레오티 드 결합 부위에 있는 특정 아미노산 잔기 를 실험적 으 로 확 인하 였는 데 , 그 들 은 ATP 와 유사한 화합물인 p_ fluo ro- su l fo n y l benzoy l 5' - ad e nos i ne(FSBA) 에 의해 화학 양론적으로 공 유 결 합되 는 아미노산 잔기가 L y s - 72 임을 밝혔다. 그 후 FSBA 에 의해 변화 된 촉 매 기 능을 갖 는 소단위체에는 Mg - ADP 또는 M g -ATP 가 더 이상 결합할 수 없으나 AMP 와 아데노신은 결합할 수 있다는 사실이 확 인되었다 . 이 사실 은 L y s_72 가 ATP 의 /3— 또는 r ― 포스페이트와 가까 운 최적 위치에 놓 여 있다는 사실을 말해 주는 것이다. 촉매 기능을 가 지고 있는 소단위체는 ATP 의 r-® 로부터 ®그룹을 기질 단백질의 세 린 또 는 트레오닌 잔기의 -O H 그룹으로 옮겨 주며, ®가 옮겨가는 부위 앞에는 보 통 두 개의 염기성 아미노산(보통은 아르기닌 잔기)들이 놓여 있다 . 기질과 유사한 구조를 갖는 분자로 친화성 표지를 하여 연구하는 방법 이외에 활성화 자리에서 목표가 되는 기능성 아미노산 잔기를 알 아보기 위하여 그룹 특이성 시약들을 사용하기도 한다. 촉매성 소단위체 에 의한 반응의 pH 의존성은 메커니즘에 일반 염기를 포함한다는 사실 을 말해 주는 것이다. 촉매성 소단위체에서 특이한 반응성을 갖는 -COOH 그룹은 분자 내부의 교차 결합 때문에 DCCD(di cy c lohe xylc a r-- bo diirni de) 에 의한 변형으로서는 확인될 수 없다. 따라서, 이것을 피하기 위 하여 효소의 어 떤 반응성 리 신 잔기 들도 aceti c anh y dri de 로 처 리 하여
차단시킨 후 반옹을 시킨다. 5-l-3 보존된 아미노산 서열과 필수 기능과의 관계 화학적 방법에 의한 구조 수정 연구 (che mi cal mo difica ti on ) 결 과 촉 매 성 소단위체의 구조가 예상되었댜 그 결과 N - 말단 부위에 뉴 클 레오티 드 가 결합하고 있으며, 펩티드 결합과 촉매 반응은 분자의 중앙 부위에서 일어납을 알았댜 특히 세 개의 아미노산 잔기 (L y s - 72, Asp- 8 4, Cy s- 199) 들이 활성화 부위에 위치해 있음을 확인했다. 많은 단백질 키나제 들 을 살 펴볼 때 뉴클레오티드의 결합과 촉매적 메커니즘에서 같은 일반적 양상 들이 유지되고 있음을 발견했다 . 만일 단백질 키나제 들 의 보존된 아미노 산 서열 부위를 선택적으로 관찰해 보면, 매우 높게 보존되며 어떤 아미 노산들은 동일한 위치에서 변하지 않는 특정한 부위가 있음을 명확히 발 견할 수 있다. 예를 들면 ATP 결합에 참여할 것으로 생각되는 리신 - 72 같은 것은 모든 단백질 키나제들에서 변하지 않는다 . pp6 0v - s nc 에서 리신 -296 이 치환되면 효소의 활성도가 없어지며 전이 능력도 없어진다 . EGF 수용체 와 인슐린 수용체 들에 서 상동성 이 있는 리 신을 site - di rec te d 돌연 변이 방법으로 치환시키면 효소들이 비활성화되며 호르몬 유도성 효과 들도 사라진다. As p -184 도 많은 단백질 키나제들에 공동으로 존재하는 불변성 아미 노산 잔기이댜 따라서 이 아미노산 잔기도 촉매반옹에서 매우 중요한 역할을 할 것이 기대된다 . 그림 5-2 에서 보는 바와 같이 Asp- 1 84 근처 의 아미노산 서열이 매우 높게 보존되어 있다. As p -184 와 L y s-72 와는 다르게 C y s-199 는 높은 보존성이 없다. C y s-199 가 촉매 기능 면에서 중 요한 역할을 함에도 불구하고, 이 역할이 많은 단백질 키나제들에서 보 존이 되지 않고 있는 것이다. 각각의 키나제들에서 펩티드 인지의 가변 성은 펩티드를 인지하는 부위가 다룰 것이라는 사실을 암시하는 것이다.
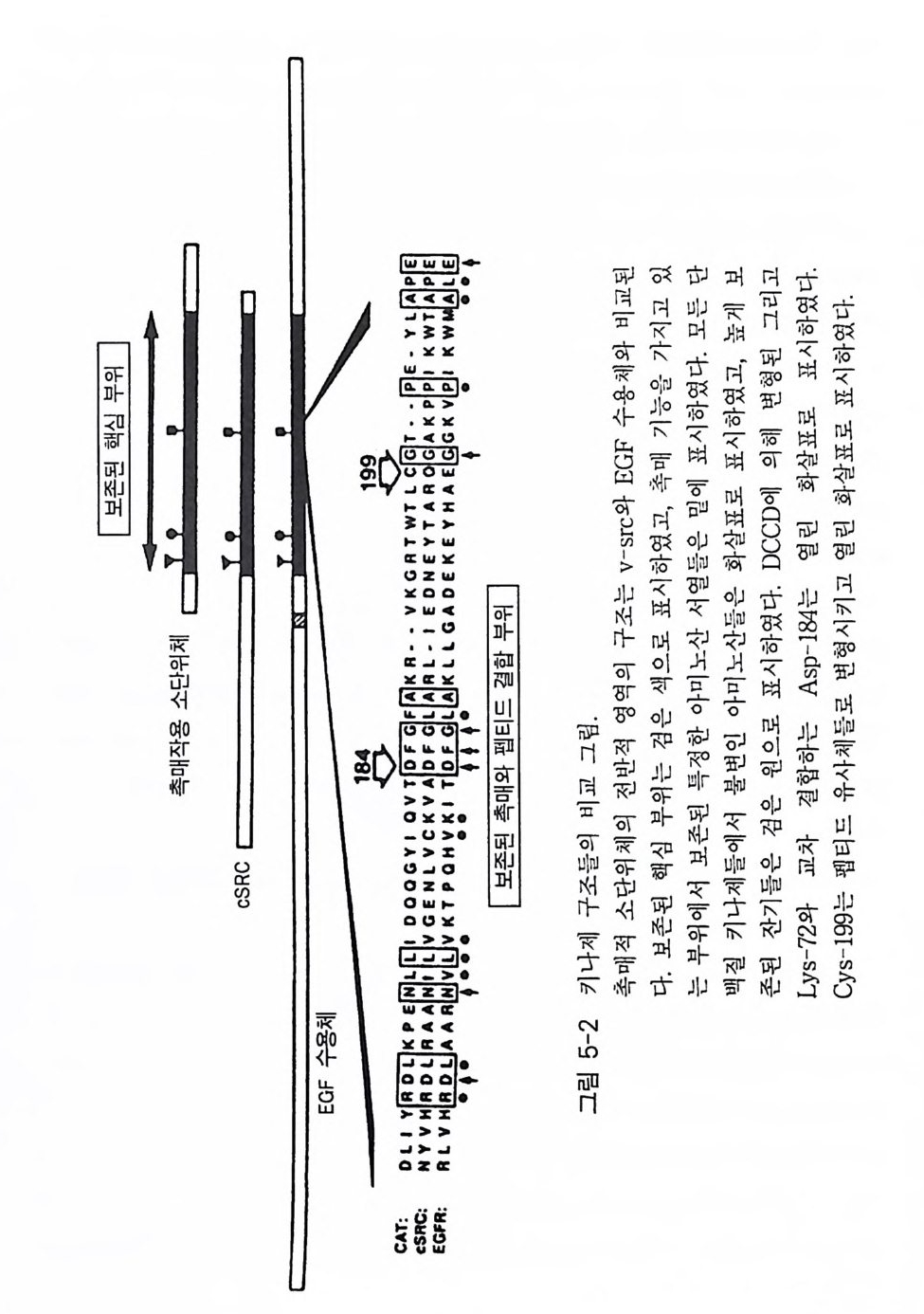
이와 유사한 가변성은 세린 단백질 분해 효소 (Se ri ne p ro t ease) 에서도 나 타난다. 촉매 기능을 가지고 있는 소단위체를 DCCD 로 처리할 때 분자 내 가 교 결합 반응에 의해 억제가 기대되었고, 실제 가교 결합 이 확인되었다. As p - 184 의 -COOH 그룹이 DCCD 와 반응하여 acy li so urea 중간체릅 형 성하며, 이 친전자성 중간체가 As p 一 184 와 L y s ― 72 의 € - 아미 노 그룹과 의 가교 결합을 형성하게 한다 . 이 가교 결합의 확인은 활성화 자리에서 이 들 두 개의 아미노산 잔기가 최적 거리에 있음을 시사하는 것이다. 앞에 서도 강조한 바와 같이 이들은 촉매 기능을 가지고 있는 소단위체에서 매우 잘 보존된 두 개의 부위에 있으며, 리신과 아스파라진은 모든 키나 제들에서 불변성을 갖는다. 촉매 기능의 일반적인 매커니즘이 그림 5 궁 에 표시되어 있댜 이 반응은 직접 운송 메커니즘에 의해 진행되며, 그 결과 r-® 그룹 의 배치가 전도되는 일이 일어난다 . 이 메커니즘에 의하면 M g 一 A TP 가 우선적으로 결합하여 리신구 2 의 곁가지와 상호작용을 한다. As p -184 는 일반적인 염기로 작용하게 되며, 따라서 세린의 -OH 그룹에 있는 산소 룰 ATP 의 r-® 그룹과 반응하는데 더욱 친핵성이 되게 만든다. 5-1- 4 E. coli 에서 촉매 기능을 가지고 있는 소단위체의 발현 제시된 메커니즘을 테스트하고 주어진 아미노산의 특정한 역할을 결 정하는 데 필요한 한 가지 방법이 돌연변이이다. C ―소단위체는 특정 돌 연변이와 효소의 기능적 변화와의 관계를 정립하는 데 좋은 모델로서 제공된다. 이 작업을 위하여 필요한 선결 과제가 돌연변이된 효소를 충 분히 얻을 수 있는 발현 벡터를 개발하는 것이다 . lac 촉진 유전자(p romo te r) 또는 t:ac 촉진 유전자를 가지 고 있는 pU C 벡터로부터 촉매 기능을 갖는 소단위체의 발현은 많은 양의 바수용성
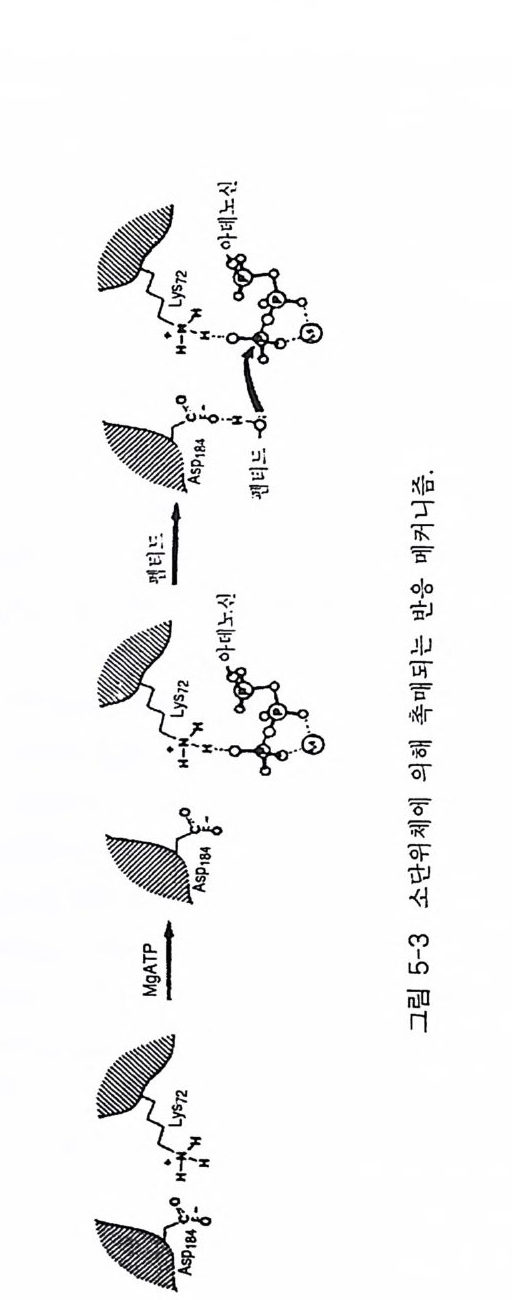
단백질을 생산하였다. 활성을 나타내며 수용성인 효소 를 얻 는 데 중요한 인자 중의 하나는 E col i의 균주이다. E. col i에서 촉 매성 소단위체의 발 현과 연관하여 용해도 문제를 해결하기 위하여 촉 매성 소단 위체 를 코드 하는 cDNA 를 p TI - 7 의 Nde I 부위에 삽입하 는 것이댜 이 벡터는 TI RNA 폴리머라제 촉진 유전자 를 포함하고 있으며 , E. co l i에 전 이가 용 이 하다 (4). TI 폴리 머 라제 가 i so p ro p y l - D 一 t h i o g alac t o p y ra no s i d e 에 의 해 유도된 후 전사가 TI 프로모터로부터 진행된다 . 따라서 이 발현계는 온 도 상승과 같은 것이 필요하지 않다 . E. coli BL2l (D E -3) 에서 pT I-7 벡 터를 이용하여 촉매성 소단위체의 유도는 많은 양의 단백질을 발현 시켰 고, 발현된 단백질의 상당한 부분 (20 - 30 % )이 수용성이며 활 성을 띠고 있었다. 이 효소는 순수하게 정제되었으며 반응 속도론적으로 포 유동물 의 조직에서 정제된 효소와 유사성을 나타낸다. 포유동물의 효소에서는 아미노말단 잔기가 미리스틸화 (m yri s t y la ti on) 되어 있는 반면 (5), E. coli 에서 발현된 효소는 말단의 Gly 잔기에 자유 a- 아미노 그룹을 가지고 있다 . N- 말단 잔기의 미리스틸화의 정확한 기능 및 역 할 이 분명하지는 않으나 효소룰 막으로 이동시키기 위한 것으로 사려되고 있다. 일반적으 로 촉매성 소단위체는 세포질에 존재하는 효소로 알려져 있기 때문에 이 효소의 미리스틸 그룹은 다른 기능을 가질 것으로 생각된다. 발현된 효소의 촉매적 소단위체와 포유동물의 소단위체 사이의 명확한 차이점 으로는 약간 감소된 안정성을 들 수 있는데, 49•c 에서 발현된 효소의 경 우 t l/l 이 0.7 분인데 반해서 포유동물의 것은 3.9 분이었다. 완충 용액에 0.01 %의 Tr iton X - 100 을 첨 가했을 때 발현된 효소의 경 우 안정 성 이 크 게 감소한 반면 포유동물의 것은 크게 영향을 받지 않았다. 이 사실은 미리스틸 그룹이 효소의 안정성에 어떤 역할을 한다는 사실을 시사하는 것이다. 촉매적 소단위체에 몇 개의 돌연변이를 유발시켜 보았는데 첫 번째 의도는 용해도를 개선하고자 하는 것이었다. 특히 C y s-199 와 C y s-343 의 잔기들 중 이 효소의 활성 화 자리로서 중요한 잔기는 Cy s -
199 로 알려져 있댜 C y s - 199 와 C y s-343 은 최소한 33 A 의 거리로 떨어 져 있음이 밝혀졌으며 C y s - 343 은 활성화 자리에 가깝게 놓여 있지 않고 단백 질 의 입체 구조 변화에 의해 보호되고 있다. C y s - 343 을 Ser 잔기로 치환 할 경우 단백 질 의 용해도가 증가되었다. As p - 184 와 L y s-72 의 역할 에 대해서 도 연구가 진행되었으나 아직 확실한 결론이 없는 상태이다. 5 기 -5 촉매적 소단위체의 활성 억제 촉 매적 소단위체의 활 성 억제에 관하여 두 개의 알려진 생리적 메커 니즘이 있 는 데, 하나 는 cAMP 가 없는 상태에서 R- 소단위체와의 상호작 용이고, 다 른 하나는 열에 안정한 단백질 키나제 억제제와의 상호작용이 다 (6). R - 소 단위체와 단백질 키나제 억제제는 매우 다른 두 개의 분자임 에도 불구 하고 촉 매적 소단위체의 활성을 저해하는 메커니즘은 매우 유 사하다. 다 른 단백 질 키나제들과 비교해서 A- 키나제의 특이한 차이점은 조절 부 위가 하나의 연속된 폴리펩티드로 구성되지 않고 분리될 수 있 는 소단위체로 구성되어 있다는 것이다 . 몇 가지 다른 형태의 R- 소단위체가 만들어지는데, 모든 R - 소단위체 들은 한가지 공통된 구조를 갖는 영역을 가지고 있다 . 예를 들면 폴리펩 티드 사슬의 C- 말단의 2/3 정도는 보존이 되어 있고, 두 개의 cAlVIP 결 합 부위 를 나타내 는 두 개의 tand em ge ne-dup lica te d 부위 를 가지 고 있 댜 R - 소단위체의 N- 말단 부위(가변성)는 단백질 가수분해 효소에 민감 하며, 이량체 상호 작용 부위를 가지고 있다. 몇몇 경우 R- 소단위체의 이 부분은 자동 인산화 부위가 되며, 다른 어떤 경우는 유사 인산화 자 리를 가지고 있다. 모든 경우 이 부위는 촉매적 소단위체에 의해 인지되 는데 꼭 필요한 Arg 잔기를 두 개 가지고 있다. 유형 II 로 분류되는 R_ 소단위체의 경우 이들 Arg 잔기들 뒤에 Ser 이 따르는데 이것은 촉매적 소단위체에 의해 쉽게 인산화된다 (7). 그러나 유형 I 의 R- 소단위체의 경
 /)丈근:;:백리 키나세 억 제재
/)丈근:;:백리 키나세 억 제재
우 Ser 이 Ala 으로 치환되어 있어 자동 인산화가 불가능하다. R _ 소단위 체는 펩티드 기질에 대해서 경쟁적 억제제이며, 전체 효소 복합체에서는 촉매적 소단위체의 펩티드 결합 부위가 이곳에 위치해 있다. 단백질 키 나제 억제제 또한 같은 메커니즘으로 촉매적 소단위체를 저해하는데, 유 형 I 의 R- 소단위체들과 같이 단백질 키나제 억제제도 유사 인산화 자리 를 가지고 있으며 합성된 펩티드 유사체들을 가지고 연구한 결과 이 펩 티드 인식 부위가 저해에 필수적이라는 사실을 확인하였다 (8). 단백질 키나제 억제제 또한 펩티드 기질에 대해여 경쟁적 억제제임이 알려져 있다. 돼지의 심장에 존재하는 유형 II 의 R_ 소단위체를 단백질 가수분해시 킬 경우 세 개의 아미노산 잔기가 다른 두 개의 조각으로 만들어지는데, 보다 큰 조각은 As p -91 이 절단되 어 만들어 지 며 Ser-95 가 자동 인산화 위치가 된다(그림 5-4). 결국 C- 말단을 가지고 있는 조각은 촉매적 소단 위체를 저해하는 능력을 보유하게 된다. 반면, Val-94 에서 절단되고 두
개의 아 르 기닌이 없 는 유사한 조각은 촉매적 소단위체와 높은 친화력을 갖 는 복합체 를 만 들 지 못한다. 따라서 두 개의 Arg 잔기들이 R- 소단위 체와 c - 소단위체 사이의 상호작용에 필수적인 것으로 사려된다 . 5, 5'- dit hi o b is - 2 - n it ro - be nzoic 산이 존재하거나 C- 소단위체의 -S H 그룹이 변하게 되면 유형 II 의 R 소단위체와 C 소단위체의 재결합은 소단위체 간 의 -s- s - 결 합 형 성 쪽으로 유도된다. 이 _s-s- 결 합은 유형 II R 소단위체의 C y s - 97 과 C - 소단위체의 Cy s -199 사이에서 형성되며, 이 사 실 은 R 소단위체의 꺾쇠(hi n g e) 부위가 C ―소단위체의 펩티드 결합 부위 를 점유하고 있다는 가설 을 지지하는 부가적 증거가 되는 것이다 (9). R 소단위체의 기능성 부위 를 찾기 위한 노력의 일환으로 소의 유형 I 의 R 소단위체에 대한 발현 벡터가 만들어졌고, 이 pU C 벡터를 이용하 여 R 소단위체 를 30m g(l L 의 배양액에 대하여)까지 발현시키는 데 성공 하였댜 이때 발현된 단백질은 수용성이었으며 활성을 잘 나타내었다. 이 발 현 벡터(p LST2) 를 이용하여 몇 가지 R 소단위체의 돌연변이체가 만 들 어졌 는 데 이들로부터 억제 메커니즘에 관한 이해가 증진될 수 있었 댜 이 들 돌연변이체들을 두 가지 유형으로 나눌 수 있는데, 첫째는 경첩 부위의 point 돌연변이를 포함하는 것들로서 C 소단위체와의 상호작용의 성질이 바뀌는 경우이고, 두번째 경우는 c- 말단과 N- 말단의 제거를 통 한 돌연변이체들로서 C 소단위체를 필수적으로 안지하는 핵심 부위만을 남겨 놓은 것이다 . 경첩 부위의 알라닌을 세린으로 치환한 유형 I R- 소단위체의 돌연변 이체를 만들었는데, 이것은 cAMP 의존성 단백질 키나제에 대한 좋은 기질이 되는 안정한 단백질이었다 . 이 돌연변이체의 R- 소단위체는 단일 인산화 자리를 제공할 수 있는 것이다. 이 돌연변이체의 경우 R_ 소단위 체와 C_ 소단위체 사이의 상호작용을 변화시킨다는 사실을 두 가지로 입 증할 수 있었다. 예를 들면, 원래의 R- 소단위체는 0.5 M M g Ch 의 존재 하에서는 분해되지 않았는데, 돌연변이체의 R 구소단위체를 가지고 있는
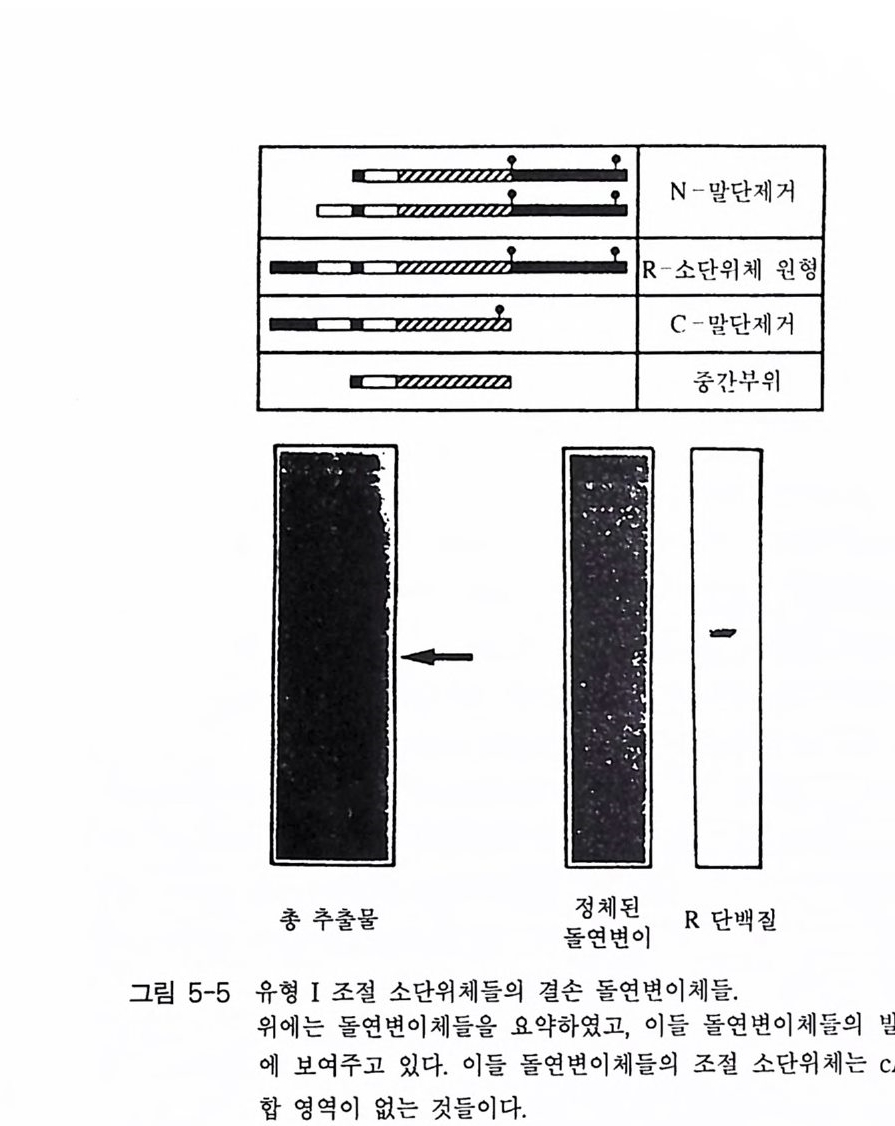 I ■■■ ---V/////盆// 모’; ‘;; cN -- 말말단단제제거거
I ■■■ ---V/////盆// 모’; ‘;; cN -- 말말단단제제거거
효소의 경우 이들 조건에서 거의 다 분해되었다. 돌연변이체의 R_ 소단 위체를 가지고 있는 전체 효소의 경우에서는 자동 인산화가 쉽게 일어 나며 전체 효소의 분해가 요구되지 않는다. 이 사실은 자동 인산화 자리를 포함하고 있는 R- 소단위체의 부분은 전체 효소에서 펩티드 결합 부위를 점유해야 한다는 사실을 암시하는 것이다. 결손 돌연변이체 또한 C 一 소단위체와의 상호작용에 꼭 필요한
R - 소단위체의 부위가 어디인지 알아보는 데 많은 도움을 주었다. 경첩 부위에 위치한 아 르 기닌 잔기들 앞의 N- 말단 부위가 C- 소단위체와 상 호 작용하는 데 꼭 필요한 부위가 아니라는 사실이 입증되었고, Arg- 94 와 Ar g - 95 가 중요한 아미노산 잔기라는 사실도 알려졌다. 그림 5-5 에 결손 돌 연변이체 들을 보여주고 있는데 이들은 유형 I 의 R- 소단위체로부 터 만 들 어진 것이다. 세번째 칸의 돌연변이체는 아미노산 잔기 260 번째 에 정지 코돈을 삽입한 것인데, 이 경우 두번째 cAMP 결합 영역을 모 두 삭제시키게 된다. 아 단백질은 안정하며 완전하게 정제되었다. 이것 은 Mg - A TP 존재 하에서 C - 소단위체와 복합체를 만들 수 있었으며, 이 복합체는 cAMP 에 의해서 분해되었다. 제일 밑의 칸에 있는 구조는 cAMP 에 의해 분해될 수 있는 C- 소단위체와 복합체를 이룰 수 있는 최 소한의 구조이다. R- 소단위체에서 이들 유형의 돌연변이체들이 C- 소단 위체와 상호작용을 하는데 있어서 중요한 구조적 면모를 제공하는데 도 움을 주었다. R- 소단위체의 다른 부위들도 C- 소단위체와 큰 친화력으로 복합체를 형성하는 데 중요하지만, 저해롤 위한 필수적 요구는 R- 소단 위체에 의한 C- 소단위체의 펩티드 결합 부위의 점령인 것이다. R- 소단 위체의 이 부위는 자동 인산화 또는 유사 인산화 자리가 될 수 있는 경 첩 부위가 되는 것이다. 5-2 Ca2+ /칼모듈린 의존성 단백질 키나제 세포의 신호 전이 반응에서 Ca2+ 의 역할과 중요성은 여러 번 언급한 바 있으며, 세포 내에서 Ca2 • 의 기능이 다양한 방법을 통하여 나타나는 데 그 중에서도 가장 대표적인 경우가 Ca2+ -수용체인 칼모듈린이라는 단백질에 Ca2 + 이 결합하여 생성되는 Ca2+-CaM 복합체를 통한 효소의 활성을 통한 것이댜 Ca2 W/ CaM 에 의해 활성화되는 효소들 중 대표적인
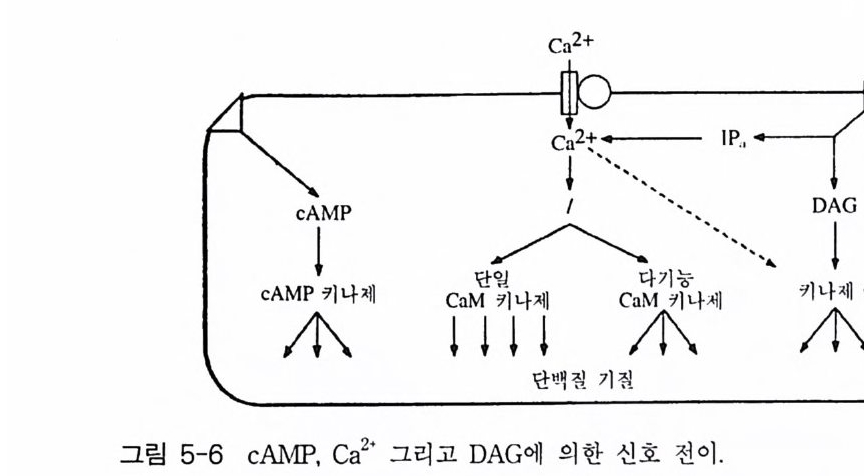 Ca2+
Ca2+
것이 단백질 키나제들인데 그 효소를 Ca l\1 키나제라고 부르며 동물, 식 물, 미생물 등 다양한 생명체의 다양한 조직에 분포되어 있다 CaM 키 나제의 종류는 크게 분류하여 두 종류가 있는데 하나는 단일 기질을 인 산화시키고 조절하는 종류 [my os in ligh t cha in kina se (MLCK), ph osph ory la se kina se, CaM 키나제 m 등]와 또 한 종류는 다기 능 단백 질 키나제 (CaM 키나제 II, 유형 II CaM 키나제)인 것이다. 이 들 의 기능을 그림 5-6 에 나타내었다. 칼모듈린 키나제는 자연에 넓게 존재하며 Ca2• 신호에 대하여 매우 다 양한 단백질들을 인산화시키며 다양한 기능을 조절한다. 이 효소가 조절 하는 다양한 기능들은 탄수화물, 지질, 아미노산과 같은 물질의 대사 조 절을 비롯하여 신경 전달 물질의 방출, 합성의 조절, 이온 수송로의 조 절, Ca2• 항상성 조절 그리고 유전자 조절 등 매우 다양하다. 이 효소는 세포 내 자유 Ca2• 농도를 증가시키는 다양한 신호들에 의해 활성화된 다. 이제 이 효소는 제 2 의 전령에 의해 많은 세포 반응들을 조절시키는 3 개의 주요한 키나제들 중의 하나로 잘 정립된 효소이다. 지금까지 칼모 듈린 키나제들에 관한 연구 결과들이 매우 다양하며 그 분량도 상당히 많은 편이 데, 본 장에서는 Hanson 둥 (10) 이 보고한 신경 세포의 칼모듈
린 키나제 들 에 대하여 간단히 살펴보기로 하였다. 5-2-1 정제와 특성 다기 능 성 칼 모 듈 린 키나제는 시냅스의 신경 말단의 붕괴에 의해 생긴 막 들 에서 확 인되었으며 그 후 많은 다른 조직들의 막에도 존재한다는 사 실 이 밝혀 졌 다 . 이 효 소는 몇 가지 다른 단백질들을 포함해서 막과 결 합하고 있 는 시냅신 I(sy n a ps in I) 을 인산화시킨다는 사실이 밝혀졌으며, 이 들 중 2 一 3 개의 단백 질들 은 효소 자체의 소단위체가 자동 인산화된 것 으로 밝혀 졌 다. 다기 능 성 칼 모듈린 키나제는 쥐 뇌세포의 세포질로부터 순 수하게 분리 정제되었 는 데 , 이때 사용한 몇 개의 기질들을 살펴보면 my o sin lig h t cha ins (ll), syn aps in 1(12 ), tub lin ( 13), micr otu b ule-associ- ate d p ro t e i n - 2(M 사 ) - 2)(14) 그리고 casein ( 1 5 ) 등이 있다 . 이들 모든 키 나제 들 은 광범위한 기질 특 이성을 가지고 있는 다기능성 칼모듈린 키나 제인데 지 금 은 동일한 효소로 인지되고 있다. 토 끼의 근 육과 간에서도 다기능성 칼모듈린 키나제의 이성질체들인 Ca 2+ / 칼모듈린 의존성 글리코겐 합성 효소의 키나제의 정제가 이루어졌 다(1 6). 그 후 다기능성 칼모듈린 키나제의 조직 특이성을 갖는 이성질 체 들 이 개의 심장, 닭의 모래주머니, 쥐의 췌장과 허파 둥에서 정제된 바 있다. 이들의 성질을 비교하면 뇌에서 정제한 것과 소단위체의 크기 가 약간 다를 뿐 매우 유사하였다. 분리한 칼모듈린 키나제의 경우 a- 소단위체 (50~54 kDa) 과 B- 소단위체 (58~60 kDa) 의 비율이 3~4 : 1 로 구성되어 있다 . Ca 2+ /칼모듈린은 이 효소의 두 소단위체 모두의 자동 인 산화를 촉진하며, a 와 8 소단위체의 자동 인산화는 SDS- 켈로 두 소단 위체를 분리한 후에도 일어나는데 이 사실은 이들 소단위체 모두가 촉 매적으로 활성화된다는 사실을 확인하는 것이다. 쥐의 뇌에서 정제된 칼 모듈린 키나제의 분자량은 460,000~ 的 0,000 범위에 있는데 10 개의 소단
위체 또는 18 개의 소단위체일 것으로 생각된다. 몇 개의 칼모듈린 키나제 이성질체 들 이 클로 닝되어 생화학 적 분석을 위한 야생형(wi ld - 유형)과 돌연변이체 칼모듈린 키나제 들을 과 발현 시키 거나 신속한 정제를 가능케 하였다. a - 소 단위체만 을 가지고 있는 a - 칼 모듈린 키나제를 동물 세포에서 발현시켜 만 들 수 있었으며 , 이것은 기질 의 인산화, 자동 인산화, 칼모듈린에 의한 활 성화 등을 나타내었다. /3- 칼모듈린 키나제 또한 동물 세포에서 발현시켜 얻었으며, 이 효소는 a- 칼모듈린 키나제와는 다르다는 것이 확인되었다. 효소 전체의 조 성은 뇌 의 부위에 따라 다른데 수많은 뇌의 부위에서 Ca 언/칼모듈 린에 의해 자 극되는 자동 인산화를 조사해 보면 다양한 a : /3 소단위체의 비율을 나타내었다. a- 소단위체 또는 f3 - 소단위체에 특 이한 항체 를 사용하여 면역성 침전을 시도할 경우 소뇌 (cerebellum) 와 전뇌(fo rebr ai n) 로부터 얻 은 효소 모두를 침전시켰는데, 이 사실은 두 개의 소단위체 들 이 각각의 효소에 존재한다는 사실을 말해 주는 것이다. 양이온 교환 수지인 s- se p harose 를 사용 이 효소의 f3-소단위 체 의 함량에 기 초하여 이 효소를 분리하는데, 다양한 a : /3 비율 (6 : 1 에서부터 8 : 1 까지)을 함유한 몇 개의 효소 po ol 을 분리할 수 있었다. 이 사실은 칼모듈린 키나제가 다양 한 동질 효소 소단위체를 함유하고 있다는 사실을 말해 주는 것이다. 최 근 EM 연구 결과에 의하면 칼모듈린 키나제는 8 개 또는 10 개의 정 렬된 촉매적 입자들이 모여 있는 8 개 또는 10 개의 소단위체로 구성되어 있음 이 밝혀졌댜 a- 소단위체에 특이성을 보이는 항체는 10 개의 소단위체에 만 결합하는 것으로 보아 10 개의 소단위체는 주로 a- 소단위체로 구성 되어 있으며 f3-소단위체는 8 개의 소단위체로 구성되어 있다는 것이 판 명되었다.
5-2-2 cDNA 클론들의 분석 쥐의 뇌로부터 4 개의 명확한 칼모듈린 키나제 이성질체들을 발현시키 는 cDNA 들을 클론 하고 그 염기 서열을 분석하였다 . a - 칼모듈린 키나 제 cDNA 는 478 개의 아미노산으로 구성된 단백질 (Mr : 54,111) 을 발현하 며, 8 - 칼 모 듈 린 키나제 cDNA 는 542 개의 아미노산으로 구성된 단백질 (Mr : 60, 3 33) 을 발현시켰다 a 와 8 의 아미노산 서열이 매우 유사한데 N - 말 단의 경우는 91 % 의 동일한 아미노산 서열과 C- 말단의 경우는 76 % 의 상동성 을 가지고 있다 (17) . 쥐의 뇌에서 두 개의 다른 이성질체들인 y와 8 도 클론되었는데, Nort he rn blo t의 결과에 의하면 이들 두 개의 소단위체 들 은 광범위한 조직 분포 를 보였다. Y_cDNA 는 5 업개의 아미 노 산으 로 구성된 단백질 (Mr : 59,038) 을 만들며 8-cDNA 는 533 개의 아 미노산으 로 구성된 단백질 (Mr : 60 , 080) 을 만들어 낸다. 이성 질 체 들 사이에서 주된 차이점은 칼모듈린 결합 영역의 끝에 위치 한 가변성 영역들이다(그림 5 구). 크기 면에서 클론된 이성질체들과 상응 하 는 칼모듈린 키나제의 소단위체들이 발견되지 않고 있는데, 이 사실은 이 들 이성질체들이 명확한 유전자 산물이거나 아니면 알려진 이성질체 들 의 접합 변이형일 가능성이 높은 것이다. 예를 들면 시상하부에 존재 하는 자동 인산화된 칼모듈린 키나제의 경우 a- 의 다른 종일 가능성이 있는 56kDa 소단위체가 그 역할을 주로 나타낸다. 이 소단위체는 11 개 의 아미노산이 두번째의 가변성 영역에 존재하는 a 에 삽입된 원숭이 뇌의 cDNA 에서 확인된 PCR 생성물에 해당될 수 있는 것이댜 사람의 임파 세포와 쥐의 심장에 존재하는 이성질체를 비롯하여 지금까지 확인 된 동물의 모든 이성질체들은 같은 구조적 구성을 하고 있고, 칼모듈린 결합 영역의 끝에 촌재하는 삽입체들의 크기와 기본적 성질은 서로 다 르댜 최근 초파리(D rosop h i la melano ga s t er) 로부터 a- 소단위체를 발현 시키는 cDNA 를 분리하였는데 쥐의 뇌에서 분리한 것과 77% 의 동일한
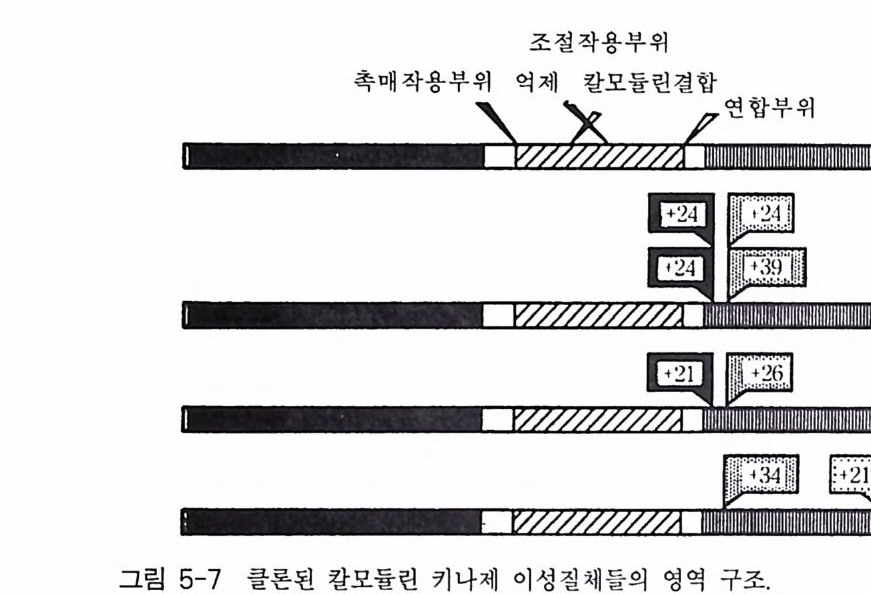 조절작용부위
조절작용부위
염기 배열을 가지고 있었다. 이 단백질 키나제의 촉매 기능 부위는 각 소단위체의 N- 말단 1/2 지점에서부터 발현되는데 아미노산 순서로 보면 a -소단위 체 의 1-(263-274) 위 치 이 댜 이 키나제의 부분적인 가수분해에 의하면 이 영역만을 포함한 촉매직 으로 활성인 부위가 생성된댜 이 촉매성 영역의 아미노산 순서를 보면 다른 칼모듈린 의존성 단백질 키나제 (IvlLCK 와 포스포리파제 키나제)들과 대부분 상동성을 가지고 있다. 아미노산 275 로부터 314 까지의 영역은 자 동 저해 및 칼모듈린 결합 부위를 포함한 조절 영역이다. 나머지 C- 말단 영역은 회합과 중합 (o lig ome ri za ti on) 영역이며, 소단위체들이 완전 효소 (holoen zy me) 에 회합하는 데 요구된다. 이 영역이 없이 만들어진 키나제 는 Ca2+ /칼모듈린에 의해서 완전히 활성화되나 다량체가 아니고 단량체 임이 확인되었댜
5-2-3 촉매적 활성도와 Ca2+ /칼모듈린에 의한 조절 작용 다기능성 칼모듈린 키나제의 메커니즘에 관한 연구와 Ca 2+ / 칼모듈린 에 의한 이 효소의 활성화 연구는 칼모듈린 키나제가 자동 억제 영역의 존 재에 의해 비교적 비활성이라는 증거 를 제시하기 위한 모델을 제공하 고 있댜 Ca 2’/ 칼 모듈린의 결합은 이와 같은 억제적 속박을 제거해 주며 키나제로 하여 금 그 기질을 인산화시키게 하며 자기 자신 또한 인산화 가 되게 한다 이 자동 인산화는 매우 홍미 있는 사건이다. 자동 인산화 로 인하여 칼모듈린의 해리가 매우 늦어지게 되며 따라서 Ca2 t 의 수준이 활성화를 위하여 필요한 양보다 낮아질 때라도 칼모듈린을 잡을 수 있 게 된댜 한번 칼모듈린이 분리되면, 칼모듈린 키나제는 탈인산화될 때 까지 Ca 2’ 에 독립성을 나타낸다. 정제된 칼모듈린 키나제는 Ca 안 과 칼모듈린이 없이는 본질적으로 비 활성이댜 칼모듈린으로 포화되어 있을 경우 최대 활성도의 1/ 2 은 자유 Ca2· 농도가 0.5-1 µM 에서 일어난다. 칼모듈린 1 분자에 네 개의 Ca2 + 이 결합하며, 칼모듈린 키나제와 같은 목표 효소에 대한 칼모듈린의 친화력 을 증가시키는 구조적 변화를 야기시킨다. 칼모듈린에 의한 칼모듈린 키 나제 의 활성 화는 양의 협 동성 (pos it ive coo pe ra tivity)을 나타낸다. 칼모듈 린 키나제의 자동 인산화와 기질의 인산화는 Hill 계수 1. 6 으로 협동성을 나타낸다 (18) . 칼모듈린 키나제의 완전한 활성은 칼모듈린의 화학 양론 적 결합을 요구한다. 용액 상태에서 칼모듈린 키나제에 결합하는 칼모듈 린을 직 접 측정 하기 위 하여 형 광 aniso t rop y 방법 이 이 용되 었다 . 모델 펩 티드를 이용하여 연구하고 확인한 바에 의하면 칼모듈린은 이 효소의 염기성이며 소수성인 영역에 결합한다. 칼모듈린 결합에 핵심적인 영역 은 a- 소단위체에 존재하는 아미노산 296-309 에 해당된다 (19). 마지막 5 개의 아미노산 잔기들이 소수성을 나타내는데 칼모듈린 결합에 중요하 다. 칼모듈린 결합에 대한 氐 값이 0.1 ~ 0.3 nM 이다. 칼모듈린과 단백질
과의 상호작용 연구에 칼모듈린 돌 연변이체 를 이용하여 좋은 결 과 를 얻 었다 칼모듈린 키나제의 경우 칼모듈린의 중앙에 위치한 헬릭스를 돌 연 변이시켰을 때 다 른 칼모듈린의 목표 부위 를 돌 연변이시킨 경우보다 덜 민감하였고, c- 말단의 돌연변이의 경우 민감함 을 나타내었다 (2 0) . 칼모 듈린과 상호 작용하는 결정적 부위는 확인된 칼모듈린 결합 영역에서 발현되는데, MLCK 의 칼모듈린 결합 영역을 칼모듈린 키나제의 것 (아미 노산 296-314) 으로 치환할 경우 칼모듈린과의 친화력이 좋게 나타났다 . 5-2-4 자동 인산화에 의한 칼모듈린 키나제의 조절 Ca 2+ / 칼모듈린에 의해 자국되는 자동 인산화가 다기능성 칼모듈린 키 나제의 독특한 특성이다. 정제된 칼모듈린 키나제의 경우 자동 인산화가 여러 곳에서 일어나는데, 아마도 효소 1mole 당 42mole 의 인산기가 결 합하는 것으로 알려져 있다 . 자동 인산화의 반응속도가 효소의 농도에 의존하지 않는 것으로 보아 이 반응은 효소 안에서 일어나는 분자 내 반 응으로 판단된다. 1985 년 Sa itoh 등이 칼모듈린 키나제의 자 동 인산화 효과에 관한 보고를 최초로 하였다 (21) . Ca 2+ / 칼모듈린이 없을 때의 활 성 도(< 5 %)가 Ca2 + /칼모듈린 이 존재 할 때 활성 도의 74 %까지 증가한다. 칼모듈린 키나제를 Ca 안 에 독립적인 것으로 바꾸어 준다는 사실이 많 은 연구를 수행하게 할 수 있었던 원동력이었다 . Ca 2+ /칼모듈린이 칼모 듈린 키나제의 자동 인산화를 자극하며 이 자동 인산화는 이 효소로 하 여금 Ca 2+ 과 무관하게 기질을 인산화시킬 수 있게 한다 . Ca2 + 에 의해 자 극되는 키나제와 비교하여 자발적이거나 또는 Ca 양 에 독립성을 나타내는 키나제의 경우 Km 값이 2-5 배 크며 그 값은 기질에 따라 바뀐다. 전형 적으로 관찰되는 Ca 양 비의존성 키나제의 활성도는 완전하게 Ca 양 에 의 해 자극되는 효소의 활성도에 20-80% 범위에 있다 . 쥐의 전뇌로부터 분리한 수용성 효소를 제외한 칼모듈린 키나제들은 자동 인산화가 되며
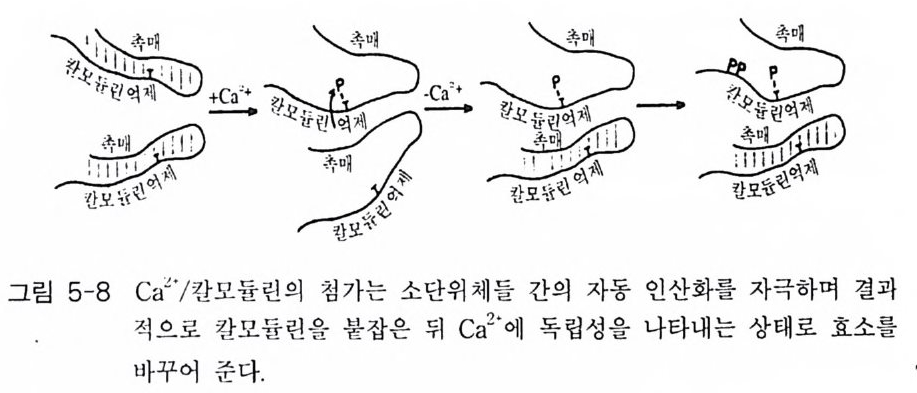 三三무T, 一
三三무T, 一
Ca 2 + 과 독립적인 활성도 를 나타낸다. 이 사실은 이 성질이 동질 효소들 간에 보존됨을 시사하는 것이다 . 칼모듈린 키나제의 소단위체들에서 자동 인산화와 Ca 안 비의존성 활 성도 를 이끄는 일련의 메커니즘이 그림 5-8 에 나타나 있다. 하나의 효소 에서 두 개의 인접한 소단위체들의 활성화와 비활성화를 표시하고 있다. Ca 2 ' / 칼모듈린에 의한 활성화 이전에는 소단위체들은 비활성을 나타낸 댜 Ca 2 ’ 의 존재 하에서 칼모듈린은 두 개의 소단위체들에 결합하며 그 들 의 자동 저해 영역을 밀어내고 기질과 ATP 에 그들의 촉매적 부위를 열어 준댜 소단위체 간의 자동 인산화는 활성화된 소단위체가 칼모듈린 의 결합에 의해서 인접한 소단위체로부터 Thr 286 을 제공받을 경우만 진행된댜 순간적으로 Ca2• 농도가 증가하는 동안 자동 인산화가 되지 않는 소단위체는 Ca 앙 농도의 수준이 떨어지거나 칼모듈린이 분리될 때 급속히 비활성화된다. 반면 자동 인산화된 소단위체는 칼모듈린이 잡혀 있는 동안(수 십초) 최대로 활성을 유지하며 칼모듈린이 서서히 분리된 후 Ca2• 과 독립적인 활성도를 유지한다. 이 활성화된 소단위체의 칼모듈 린 결합 영역이 비게 되면 Ca2• 과 독립적인 반옹으로 Thr 305 또는 Thr 306 이 빠르게 자동 인산화되며 칼모듈린에 의해 이 소단위체는 더이상 자극되지 않는다
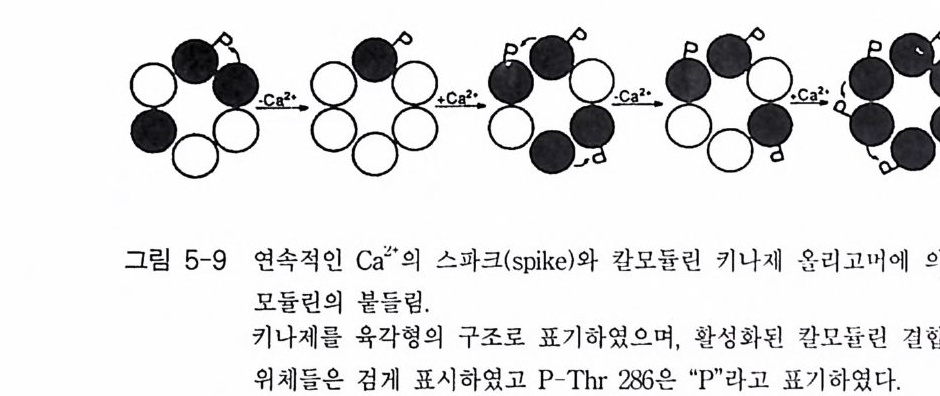 :무 8:f ':?':무 0
:무 8:f ':?':무 0
칼모듈린 키나제의 활성에서 칼모듈린의 협동적 포획이 그림 5 - 9 에 표시되어 있댜 Ca2+ 수준이 감소하면 자동 인산화된 소단위체를 제외하 고 모든 소단위체들로부터 빠른 속도로 칼모듈린이 해리된다 . 만일 1~ 10 초 사이에 Ca2+ 수준이 올라가면, 칼모듈린은 다시 몇몇 소단위체에 결합하게 된다 . 따라서 반복적인 Ca 앙 신호들은 그 올라가는 주기가 높 을 경우 칼모듈린 키나제에 의한 칼모듈린의 격리를 유도하게 된다. 만 일 Ca2+ 의 신호 주기 가 낮으면 연속적 인 Ca2+ 의 스파크 사이 의 시 간이 잡아 둔 칼모듈린의 해리를 허용하는 데 충분하게 된다 . 자동 인산화의 협동성과 칼모듈린의 포획은 이 효소의 주파수 조절을 가능하게 할 수 있다. 5-3 단백질 키나제 C 단백질 키나제 C(Prote in kina se C, PKC) 는 호르몬, 신경 전달 물질, 성장 인자 등 다양한 활성제들의 신호전이에 참여하는 효소이다. 이 효 소는 세포막 성분 중의 하나인 이노시톨 인지질들의 가수분해에 의해 생성되는 DAG 라는 화합물의 증가에 따라 활성화된다 (22). 그러나 다른
지질 들 특 히 포스 파티 딜 콜 린 (PC) 의 경우도 신호전이의 비교적 후반부 에서 DAG 를 생성시키며, 이 반응에 관여하는 효소인 PLD 도 신호 전이 에서의 어떤 역 할 이 제시된다. PKC 의 지속적인 활성화는 세포 분열과 분화 등과 같은 후속 반응에 필수적 이다. PLA J. 또한 이노시톨 인지질의 가수 분 해 를 유도하는 많은 활성 제 들 에 의해 활성 화된다 (23). PLA2 에 의 한 PC 의 가수분해로 생성 되 는 몇 가지 cis 불포화 지 방산과 Jy so-PC 도 PKC 를 활 성화시킨다 아 직도 이 들 인지 질 가수분해 효소들 간의 상호작 용에 관한 생화학적 메커니 즘 등은 확실히 밝혀져 있지 않은 상태이며 신호 전 이에서 이 효소둘 의 역할이 중요하다는 사실은 확실히 인지되고 있는 상황이다. 5-3-l DAG 와 PKC 의 활성화 세 포를 자극시키면 DAG 는 다양한 세포 내 소기관들에서 세포가 반응 하는 동안 각기 다 른 시간대에서 검출된다. 활성제와의 반응에서 DAG 는 이노시 톨 인지 질들 특히 PIP 2 의 가수분해 결과로 초기에 생성된다 (24). 이 렇게 생성된 DAG 는 보통 순간적으로 존재하며 시간적으로 lP3 의 생성과 상옹된다. 보통 잠시 후에는 더 이상의 지속적안 DAG 의 증가 가 나타난다(그림 5-10). 지방산 조성을 연구한 결과 이 단계로 생성되는 DAG 의 경우 PC 의 가수분해로 생성되는 것으로 판단되었다. 포스파티딜 에탄올아민 (PE) 의 경우는 DAG 생성에서는 거의 작용되지 않는 것으로 생각된댜 DAG 의 지속적인 증가는 PKC 의 활성을 유도하는 유사분열 촉진 인자(mit o g en), 성장 인자, 포볼 에스터 그리고 Ras 등의 작용으로 일어나는 것으로 밝혀졌다 . 방사성 동위원소 표지에 의한 연구를 통하여 세포 내에서 DAG 는 빠 른 속도로 대사되는 것이 확인되었다. 혈소판에서는 DAG 가 DAG 키나 제에 의해 포스파티딕산 (PA) 으로 전환되었다가 이노시톨 인지질로 바뀐
 A
A
다는 사실이 확인되었고, T 임파 세포에서는 외부에서 첨가한 DAG 가 DAG 리파아제와 에스테르 가수분해 효소에 의해 빠르게 가수분해된다 는 사 실 이 확인되었다. 종양을 유발시키는 포볼 에스터에 의해 PKC 가 활 성화되며 이것에 의한 세포 반응들은 DAG 에 의한 세포 반응들과 약 간 다 르 다 는 사 실 도 확인되었다 (25). 막투과성 DAG 를 여러 번 첨가하는 실험 을 통 하여 확인된 사실은 PKC 의 지속적인 활성이 T 임파 세포의 활 성화라 든 가 HL- 60 세포 를 마크로파지로 분화시키는 데 먼저 요구된 다 는 것이다 반면에 포볼 에스터는 유사한 세포 반응을 나타내는 데 단 한번의 주입으 로 가능하다는 것이다. 5-3-2 PKC 활성화에서 PLD 의 역 할 활 성제에 의해 PC 로부터 DAG 의 생성 메커니즘에 관한 가상적인 내 용이 그림 5 - 11 에 표시되어 있다. PLD 에 의해서 PC 가 가수분해되며 그 결 과 PA 가 생성되고 그것은 포스포모노에스터라제의 의해 DAG 로 바뀐
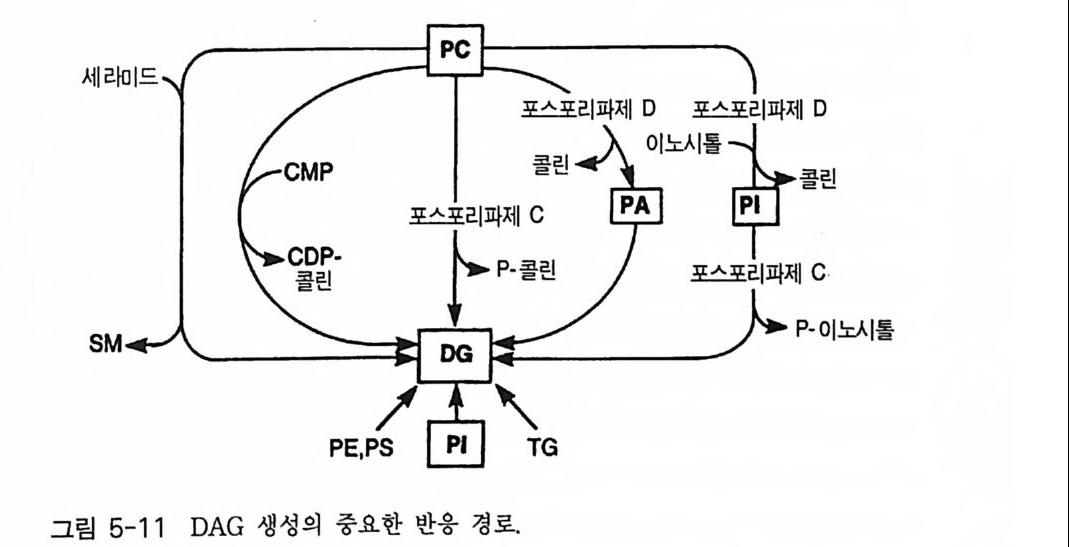 세라 □ I 드 D 놔추卓潘頭뻑言제 11 i D C0
세라 □ I 드 D 놔추卓潘頭뻑言제 11 i D C0
댜 동물의 PLD 는 쥐의 뇌에서 검출되었으며 그 후 다양한 조직과 세포 들의 균질물 (homo g ena t e) 과 막에서도 검출되었다 이 효소는 최초에 세 포막에서 발견되었고, 쥐의 뇌, 사람의 에오신 기호성 백 혈구 그리고 쥐 의 에오신 기호성 백혈구로부터 부분 정제되었다. 그러나 수용성 PLD 의 경우 소의 조직에서 검출되었다. 쥐 뇌의 시냅스 신경 말단과 간세포의 원형질막으로부터 분 리 된 PLD 의 경우 Ca 안 을 요구하나 l µM 보다 낮은 농도에서 큰 활성도 를 나타낸 댜 그러나 PLD 의 반응 속도론적인 성질은 조직에 따라 다 른 데 이 사 실 은 이 효소의 광범위한 불균일성을 시사하는 것이다. 이 효소는 PC 와는 잘 반응하나 PE 와는 반응성이 매우 낮다. 포유류 조직 의 PLD 는 염기 교 환 반응(tr ansp hos p ha ti d y la ti on) 의 촉매작용을 하며 코린, 에탄 올 아민, 세 린 등을 인지질에 결합시키는 역할을 한다. 염기 교환 반응은 대부분의 인지질을 합성하는 데 필요한 하나의 반응이다 . 염기 교환 반응에 대하 여 다른 반응 속도와 분명한 기질 특이성을 가지고 있는 효소들이 다 른 세포 내 위치를 가지고 있는 다양한 조직들에 존재하고 있다. 몇 가지 종류의 세포에서 포볼 에스터들은 PC 로부터의 콜린과 콜린 포스페이트 생성을 촉진한다 PLD 는 포볼 에스터와 막투과성 DAG 에 의해서 활 성 화되며, 때로는 Ca2• i ono p hore 에 의해 상승적으로 활성화되기도 한다. 여러 종류의 막분획에서 염기 교환 반응과 PLD 의 활성도는 GTP 유도 체들에 의해 자극되어 진다 (26) . PLD 와 염기 교환 반응을 측정하기 위한 동정 방법이 개발되었다. 사 람의 neu tr o phil과 HL-60 세포와 같은 세포들을 泊 또는 32 p로 표지된 1-o- alky l-2-l y so 一 sn- g l y cero-3- p hos p ho ry lcho li ne 과 함께 배 양한다. 이 때 이들은 알킬-인지질의 형태로 PC 에 선택적으로 결합하게 된다('Zl). 이 방법에 의해 표지된 막에서 PA 생성과 염기 교환 반응은 GTP 유사 체와 포볼 에스터에 의해 활성화된다. 포볼 에스터에 의한 이 활성화는 ATP 를 필요로 하며 PKC 의 활성을 억제하는 s ta uros pori ne 과 펩티드에
의해 저해된다. 그러나 아직까지 PKC 가 직접 PLD 를 인산화시키는지 여 부는 모르는 상태이다. PC 에서 코린을 자유 이노시톨로 교환하며 포스 파티 딜 이 노시 톨 (PI) 을 만들며 , 이 교환 반응은 포볼 에 스터 와 막투과성 DAG 에 의해 자극된다. 따라서 세포를 자극하면 PLD 에 의해 PC 가 PI 로 바뀌고 PI 는 PLC 에 의해 가수분해되어 DAG 와 IP 3 로 바뀐댜 세포 내에 서 m y o ― 이노시 톨 의 농도는 약 l mM 이댜 PC 로부터 DAG 가 생성되는 이 메커니 즘 이 많은 다른 조직과 세포들에서 그대로 작용된다면, 이노시 톨 인지 질 이 분해된 후 해당 PA 로부터 단순하게 재합성이 안될 것이라 는 예 측 이 맞는 것 같다 (28). 그러나 이노시톨 인지질의 가수분해가 활 성제에 의해 유도되는 PC 가수분해에 항상 필수적이며 충분할 수만은 없댜 활 성제에 의해 유도되는 PLD 활성화에 대한 몇 가지 메커니즘이 제시되고 있댜 PLD 활성화에 단백질 티로신 인산화가 필요하다는 것이 다 ( 29 ). 이노시 톨 인지질의 가수분해에 의해 활성화되는 PKC 가 PLD 의 활 성화에 참여한다는 주장도 있다 . 이 사실은 DAG 의 계속적인 생성과 오래 계속되는 PKC 의 활성화의 결과일 수 있는 것이다. 5-3-3 PKC 활성화에서 PLA2 의 역할 인지질을 가수분해시켜 자유 지방산과 라이소인지질을 만드는 PL fu 는 동물 조직에서 혼하게 발견되는 효소이다. 이노시톨 인지질을 가수분 해시키는 활성제는 보통 아라키돈산의 방출을 유도한다. 아라키돈산이 DAG 리파아제에 의해 DAG 로부터 생성될 수도 있지만 주로 이것은 PLA2 의 작용에 의해 인지질로부터 만들어진다. 막에서 생성되는 DAG 는 PKC 에 대한 Ca2 + 의 친화력을 증진시키며, µM 농도의 Ca2+ 존재 하에서 효소를 활성화시키게 된다. 몇 종류의 불포화 지방산들은 PKC 를 활성화 시키며, 따라서 자유 지방산의 제 2 의 전령으로서의 역할이 제시되고 있 다 (30). 비선택성형의 PLk 의 작용에 의해 생성되는 불포화 지방산(올레
산, 리놀레산, 리놀렌산, 아라키돈산) 들 은 PKC 의 DAG 의 존성 활성을 증 진시킨댜 그리고 PKC 로 하여금 Ca 2+ 의 농도가 l µM 보다 적은 범위에 서 거의 완전한 활성도를 나타내게 한다. 사람의 혈소판을 가지고 반응 속도론적 연구를 수행한 결과 막투과성 DAG 가 존재할 경우 PKC 의 활 성을 증진시키는 것으로 나타났다 Ca 2+ 에 민감한 형광 지시약인 fur a -2 라는 화합 물을 이용하여 세포 내 Ca2+ 농도를 측정 해 보니 혈소판이 DAG 와 cis 불포화 지 방산의 동시 첨 가에 의해 세포 내 Ca 2 ♦ 농도의 증가 없이 활성화되는 것 이 확 인되었다 (31). 그러나 포화 지방산과 tran s 불포 화 지방산 들은 이러한 효과를 나 타내지 못했다. cis 불포화 지방산에 의한 세포 반응 들 이 사 람 의 T 림프 구에 의해 합성되는 DAG 유도성 인터루킨 -2 와 Hermi ss enda 광수용체 세포에서 DAG 유도성 K 채널 전도도 감소 현상에 관여할 수 있을 것 이라는 보고들이 있다. 자극된 세포에서 PKC 의 활성도는 이 노 시 톨 인지 질의 가수분해 결과 증가되는 세포 내 Ca2+ 농도와 DAG 에 의해 초기 에 는 증가하는 것으로 사려된다. 만일 DAG 와 cis 불포화 지방산들의 농도 가 어느 정도 유지될 수 있다면 세포 내 Ca2+ 농도가 더이상 증가하지 않더라도 PKC 의 활성도는 유지될 수 있다. PC 가 PLA2 의 작용을 받아 생성되는 l y so-PC 는 세포의 분열 및 분화 와 같은 시간이 많이 소요되는 세포 반응을 일으킬 수 있다. 예 를 들면 l y so-PC 는 사람의 T 림프구의 활성을 증진시키며 HL-60 세포가 분화되 어 마크로파지로 전환되는 것을 자극하기도 한다 . 두 가지 경우 모두 l y so-PC 가 DAG 와 i on~m y c i n 이 존재할 때 효과를 나타내는데, 이 사실 은 l y so-PC 가 PKC 경로와 상호작용을 한다는 것을 암시하는 것이다. 아 직까지 lys o -PC 효과에 관한 생화학적 메커니즘이 설명되고 있지 못하 나 DAG 의존성의 PKC 를 직접 활성화할 가능성이 제시되고 있다 그러 나 in v itr o 와 in v i vo 에서 속도론적인 연구를 실시해 보면 c i s- 불포화 지 방산과는 달리 l y so-PC 의 경우는 PKC 활성화에서 Ca2 + 의 민감도를 증
가시 키 지 않는다 이 결과들을 종합해 보면 PLA 2 의 경 우 PKC 를 통해 신호 전이에 참여할 것이 확실하다. 세포 내에 존재하는 PLA2 의 분자량 은 301
표 5-1 포유류 동물 조직들에서의 PKC 아종 들 . Subspe cies Aamciidn o siMz eo l(eccau ilcad r. ) Acti va to r s exTp irse ss useio n resid u es (dalto n s) Group A: classic a l PKCs( cPKC) a 672 76, 799 PFSF,A C, iL 'y, s oD APGC, Univ e rsal pfl III 667713 7766,, 799303 PPFFSSFF,,A ACC ,, aa 隨L 2·y ,, ss DDoo AAPPGGCC,, !SVol amnye ttiissss uu ee ss r 6g 78, 366 PFSF,A C, aL~·y, soD APGC, Brai n only Group B: new PKCs(nPKC) TJ 8c。(L ) 776680737337 78781737,,,, 955477711427 PS, PDS,A ??DG A, GF FA LBSurknaeigU nl( ,em nta saiav n kl iedin nmr l s,yo au) thl sh ce el aer rs t Group C: aty pica l PKCs (aPKC) g 592 67, 740 PS, FFA Un ive rsal A 586 67, 200 ? Ova ry, tes tis , etc . 영역으로 구분된다. cPKC 효소들은 Ca2+, PS, DAG 또는 포볼 에스터에 의해 활성화되고 이 활성은 cis 불포화 지방산과 L y so-PC 에 의해 더욱 증진된다. 그룹 B 에 속하는 nPKC 효소들은 Q 영 역 이 없으며 Ca2+ 을 요 구하지 않는다. 이 효소들은 PS 와 DAG 로 구성된 미셀 또는 포볼 에스터 에 의해 활성화된다. c 아속들은 cis 불포화 지방산들에 의해 활성화되 는 반면에 8 아속들은 그렇지 못하다. 8 와 c 아속들은 생체 조직 내에
 O f종 조절작용부위 단백질 키나제 부위
O f종 조절작용부위 단백질 키나제 부위
서 인산화된 상태로 존재하고 전기 영동 후 이중 밴드로 나타난다. 그룹 C 에 속하는 aPKC 효소들은 한 개의 Cy s -ric h Zn fing e r mo tif을 가지고 있으며 PS 에는 의존성을 보이나 DAG, 포볼 에스터, Ca2 • 에는 영향을 받 지 않는댜 g 아속의 효소들은 cis 불포화 지방산에 의해 활성화된다. 아직까지 그룹 C 에 속하는 효소들을 활성화시키는 신호는 알려져 있지 않댜 지금까지 알려진 PKC 족에 속하는 모든 효소들은 PS 에 의존성을 보이 는 반면, 그들의 활성화를 위한 인지질 대사 물질의 요구는 다르게 나타 난다. 이들은 아마도 Ca2•, PS, DAG 그리고 다른 인지질 분해 생성물들 의 다양한 조합에 다르게 반응할 것이 기대된다.
5-4 수용체 티로신 키나제 수용체 티로신 키나제(Re ce pt or Ty ros in e Ki nas e ) 는 수용체의 기 능 과 효소의 기능을 동시에 가지고 있는 분자로서 많은 성장 인자 들 의 신 호 전이가 이 분자를 통하여 일어난다. 지금까지 몇 개의 확실 한 수용체 티 로신 키나제들이 확인되었다(그림 5- 13 ). 수용체 티 로 신 키나제의 다양 성에도 불구하고 이들 단백질 들 에 의해 시작되 는 세 포 내 신 호 전이의 유형들은 상당한 공통성을 가지고 있다. 포유 류 에서 생화 학적 그 리고 분 자 생물학적 분석에 의하면 모든 수용체 티로신 키나제 둘 의 경 우 세포 외부 영역에 리간드가 결합함으로써 세포질 영역에 존 재하 는 티 로 신 키 나제를 활성화시킨다는 것이다 . 이 결과는 많은 수의 신호 전이 분자 들 을 활성화시키게 된 다. 자 주 활 성화되는 단백질들로서는 PLC- r , PI-3 키나제 , GTPase 활 성화 단백 질, pp60 c-src, p2 1 ras, Raf- 1 키나제, ERK1 과 ERK2 키나제 (MAP 키나제) 들 그리고 S6 리보조멀 키나제 등이 있다 . 최종적으로 이 들 분자 를 포 합 한 신호 전이 과정들의 활성화는 유전자 발현에 변화 를 주며 세포의 상 태가 가시적으로 변하게 되는 것이다 . 한가지 종류의 수용체 티로신 키 나제가 다른 세포의 종류에서는 다른 생물학적 반옹을 유발한다는 사실 이 흥미롭다. 수용체 티로신 키나제의 신호 전이 영역은 최근 5 년 사 이에 엄청나게 확대되었댜 5- 4 기 수츠용체 티로신 키나제 연구를 위한 유전계 신호 전이 분자들의 활성화는 지렁이 (C ele ga ns) 와 초파리(D rosop h i la melano ga s t er) 에서 유전 분석을 통하여 독립적으로 입증되어 왔댜 이들 연구 결과에 의하면 수용체 티로신 키나제 분자들이 세포 유형들의 발 달적 특이성에 매우 중요하며, 이들 생명체에서의 수용체 티로신 키나제
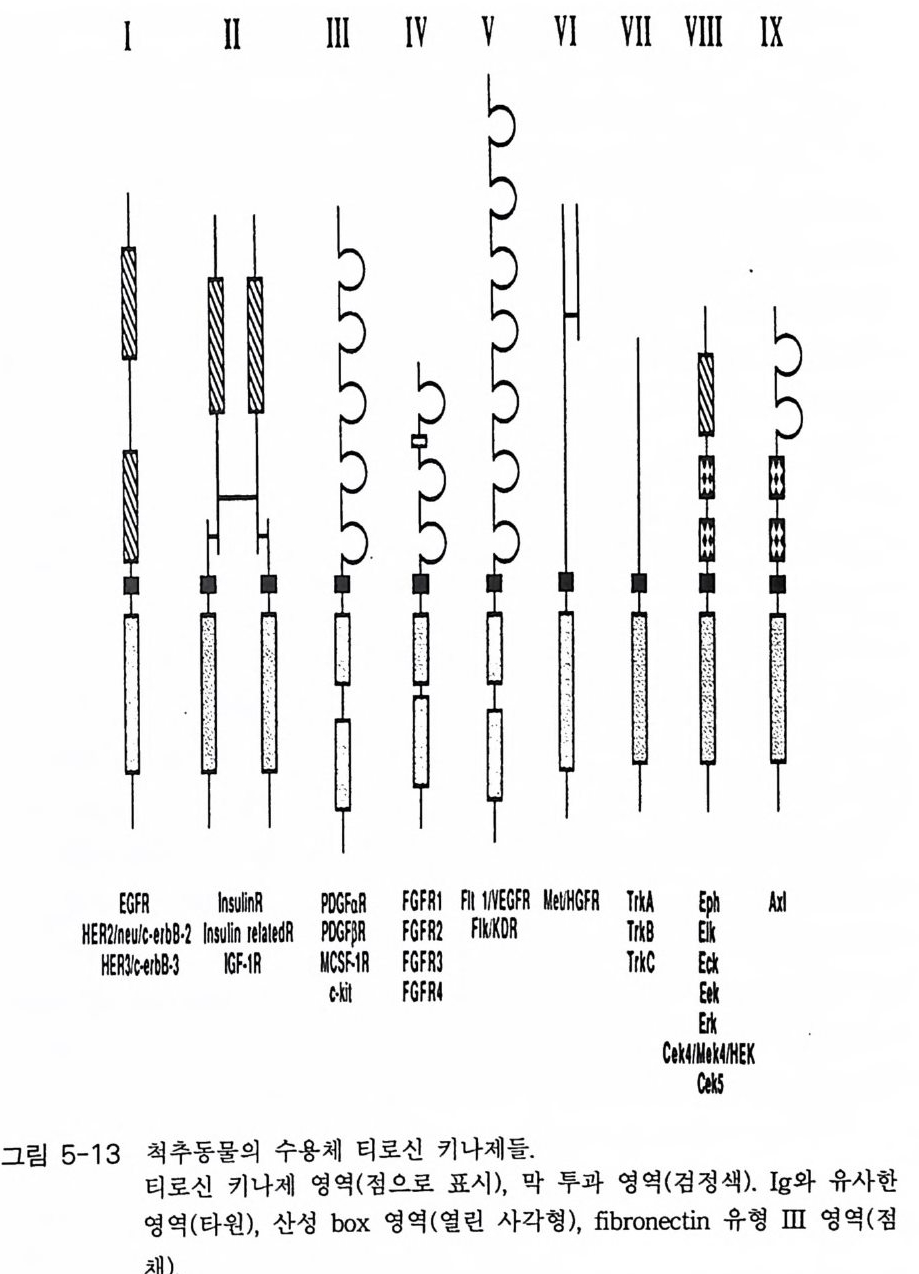 II III IV V VI VII VIII IX
II III IV V VI VII VIII IX
들의 신호 전이 과정들이 포유류 동물계에서의 것 들 과 상당히 유사합이 발견되었다. 예를 들어 지렁이에서 lin - 3 , let- 2 3 그리고 let- 6 0 와 같은 유전자들의 생성물들이 표피 성장 인자, 표피 성장 인자 수용체, Ras 와 구조적으로 상동성을 나타낸다. 유전적 연구에 의하면 /e t - 60(ras) 가 li n-3 (E GF) 와 le t -23 (E GFR) 에 대하여 우위라는 사실이 확인되었 는 데, 이 사실은 그것이 신호 전이 과정에서 아래쪽에 위치해 있다 는 사실 을 암시하는 것이댜 let- 6 0 유전자 산물은 sem - 5(SH2 / SH3 를 포 함하고 있 는 단백질)로부터 아래쪽에서 나타난다 (33) . 초파리에서 R7 광수용체의 발달은 구조적으로 c-ros 와 인슐린 수용체 족과 상관성이 있는 수용체 티로신 키나제인 sevenless 유전자 산물의 기능에 의존성을 가지고 있다. 몇 개의 신호 전이 분자 들 중 sevenless 로 부터 아래쪽에 위치한 것들로서 SOS 단백질 (son of sevenless), Gap 1, Rap 1 그리고 ras 1 과 같은 것들이 있다. SOS 단백질은 구아닌뉴클레오 티드 교환 인자들과 상동성을 가지고 있으며 ras 1 을 활성화시키는 기능 을 가지고 있다. Gap 1 과 Rap 1 은 아마도 ras 1 의 신호를 부정적으로 조 절하는 작용을 할 것으로 판단되는데, 이것은 ras 의 기능을 억제하는 데 있어 그들의 카운터 파트들의 알려진 생물학적 활성도와 일치한다. 초파 리 tor so 유전자 산물인 수용체 티로신 키나제는 혈소판-유도 성장 인자 수용체족과 유사하며 포유류 동물의 c-Ra f 1 과 유사체인 D-r af와도 유 사하고 과실 파리 의 배 에 서 ante r i or -JX )s te r i or 축을 발달시 키 는 데 중요 한 역할을 한다. 유전학적 그리고 생화학적 연구를 병행하면 서로 다른 수용체 티로신 키나제 분자들의 신호가 공통된 신호 전이 분자들의 활 성화를 통하여 전달된다는 사실이 명확하게 제시될 수 있다. 5-4- 2 신호 전이의 생화학적, 세포학적 연구 리간드가 결합하면 수용체 티로신 키나제들은 스스로 자기 자신의 티
로신 잔기를 인산화시킨다. 이 과정을 자동 인산화라고 정의한다. 어떤 수용체 티로신 키나제 들 의 경우는 리간드가 결합하면 수용체 분자의 이 량화를 유도한다 (34). 자동 인산화 후에는 수용체의 세포질 영역에 위치 한 개개의 인산화된 티로신들이 특정한 세포질 내 분자들과 상호작용을 하 는 데 있어 매우 높은 선택적 결합 부위를 제공하게 된다. 이들 신호 전이 분자둘은 성장 인자에 대한 세포 반응들을 중개한다. 신호 전이 분 자들이 직접 수용체 티로신 키나제와 결합하며 이 결합이 키나제들의 어떤 특정한 영역 을 포함하고 있다는 첫번째 실마리가 자동 인산화된 혈소판 - 유도 성장 인자 f3 -수용 체가 PI-3 키나제와 결합한다는 관찰로 부터 풀렀다 (35). 세포질 영 역의 부분이 잘라진 혈소판-유도 성장 인자 f3 - 수용체의 돌 연변이체의 경우 티로신 키나제의 활성도를 가지고 있으 며 PLC- y와 같은 신호 전이 분자는 활성화시킬 수 있는데도 불구하고 PI-3 키나제와는 결합하지 않는다. 돌연변이 연구를 통하여 PI-3 키나제 는 키나제 삽입 부위에서 두 개의 특정한 부위(티로신 708 과 719 : 쥐의 /3 -수 용체) 모두에 결합할 수 있거나 아니면 둘 중의 하나에 결합할 수 있다는 사실이 확인되었다(그림 5-14). GTPase 활성화 단백질 (GAP) 과 같은 신호 전달 분자는 티로신 739 에 결합하며 977 번과 989 번째 티로신 두 개에 PLC- y가 결합하는 것이 알려졌다. 신호 전달 분자들과 상호 작용하는 수용체 분자의 부위를 가지고 있 는 합성 펩티드들이 수용체 티로신 키나제와 신호 전이 분자들 사이의 상호작용의 특이성을 연구하는 데 구조적인 면을 보여줄 수 있는 유용 한 수단이 된댜 티로신이 인산화된 아미노산 5 개짜리 펩티드의 경우 수 용체 티로신 키나제와 신호 전이 분자들과의 상호작용을 선택적으로 막 울 수 있는데, 이는 수용체의 아미노산 순서를 인지하는 신호 전이 분자 의 부위를 이 펩티드가 점유하기 때문이다. 펩티드가 신호 전이 분자에 결합하는 것은 매우 특정하며 매우 낮은 펩티드의 농도(1 -10 µM) 수준 에서도 일어난다. 그러나 결합은 펩티드의 핵심이 되는 티로신 잔기가
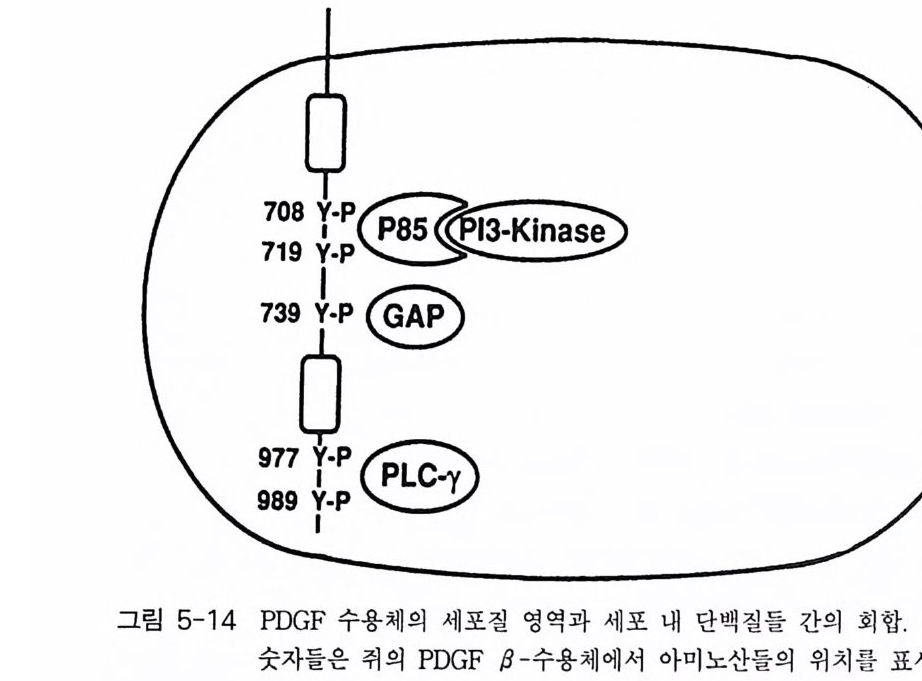 :。7;39다 :f. •• P: PPE ®@S졸
:。7;39다 :f. •• P: PPE ®@S졸
인산화되었을 때만 일어난다. 예를 들면 혈소판-유도 성장 인자 /3 ― 수 용체의 경우 PI-3 키나제에 대한 두 개의 결합 부위의 아미노산 배 열 순위 는 PYV_P-M-L 과 PYM-D-M-S 이 다 . 상기 의 배 열 중 하나로 구성 된 펩티드의 경우는 PI—3 키나제가 수용체에 결합하는 것을 막을 수 있 으나 GTPase 활성화 단백질이나 PLC- r 에 대한 결합은 막지 못한다. PI-3 키나제와 결합하는 데 최소로 필요한 아미노산의 개수가 5 개라는 사실도 확인되었다. C- 말단 쪽에 위치한 ®-Ty r 잔기들이 N- 말단 쪽에 있는 ®-Ty r 잔기들보다 상호작용에 있어 더욱 중요한 역할을 한다고 보고되었다 . 수용체 티로신 키나제에 결합하는 것으로 알려진 많은 신호 전달 분 자들의 한 가지 공통점은 이들이 SH2 영역들을 가지고 있다는 것이다. SH2 영역이란 c-src 종양 단백질에 존재하는 비촉매적 영역과 유사한
100 개 의 아미 노산으로 구성 된 영 역 을 말한다 (36). crK SH2 영 역 들이 전 이된 세포 들 에서 ®- T y r - 단백질에 직접 결합한다는 보고가 최초의 것 이었다 (37). 최근의 많은 연구 결과들은 SH2 영역들이 ®―T yr-수용체들 에도 결합한 다 는 사 실을 입증하였다. NMR 과 X- 선 연구 결과에 의하여 ® - T y r 에 대한 결합 포켓이 밝혀졌댜 ®- T y r 을 포함하는 부위와 SH2 영역 사이의 특정한 상호작용의 구조적 메커니즘은 아직 확정되지 않고 있다. SH2 영역 을 가지고 있는 많은 수의 단백질들이 확인되었고, 이들 단백질 들 이 인지하고 결합하는 특정 아미노산 부위가 PI-3 키나제, PLC- r 그 리고 GAP 에 대하여 확인되었댜 수용체 티로신 키나제와 결 합하며 SH2 를 합유하고 있는 몇 가지 단백질들이 효소적 활성도를 가지 고 있 는 것으로 알려져 있다. 예를 들면 PLC-r 는 PIP2 를 기질로 이용 하며, GTPase 활성화 단백질은 p21 ras 를 기질로 이용한다. SH2 를 가지 고 있 는 다른 어떤 단백질들은 수용체와 효소 사이에서 link er/ada pt or 로 서 역할을 한다는 사실도 알려져 있다. 예를 들면 PI-3 키나제의 촉매성 소단위체인 p llO 은 PDGF 수용체와 p85라는 소단위체를 통하여 연결되 어 있는데 이 p85는 두 개의 SH2 영역과 한 개의 SH3 영역으로 구성되 어 있다(그림 5-14). 수용체와 신호 전달 분자간의 회합의 기능적 결론은 명확히 내릴 수 없으나, 이들 회합이 신호 전달 분자들을 그들의 기질에서 가까운 부위 에 위치하게 할 수 있는 가능성이 있다고 말할 수 있다. 예를 들어 PLC-r 또는 PI-3 키나제와 같은 분자들은 원형질막에 있는 기질을 이 용한다는 것이댜 수용체 티로신 키나제와 신호 전달 분자가 만든 복합 체의 다른 가능한 기능은 신호 전달 분자들로 하여금 티로신 키나제 영 역의 더욱 좋은 기질이 되도록 이들의 위치를 정해 주는 것이다. 최근 연구 결과에 의하면 수용체 티로신 키나제의 티로신 키나제 활성도는 두 가지 기능을 가지고 있는 것으로 밝혀졌다. 첫째는 신호 전달 분자들 에 대한 높은 친화력을 갖는 결합 부위를 창출하는 것과 둘째, 티로신
키나제는 인산화로 신호 전달 분자를 변형시칸다는 것이다. 5-4-3 수용체 티로신 키나제 아과들 (Sub fa m ili es of RTKs) 표피 성장 인자 수용체 표피 성 장 인자 수용체(Epi dermal Grow th Facto r Rece pt or) 는 170 I
성장 인자의 중개에 의한 세포질 내 Ca2+ 농도의 증가 현상에 관여하는 것으로 생각된다. 여러 개의 신호 전달 분자들이 활성화된 표피 성장 인자 수용체들과 회합하는 것으로 보고되어 있다. 세포를 표피 성장 인자로 처리했을 때 PI 대사가 활성화되는데, 그 이유는 표피 성장 인자의 티로신 992 와 PLC- r 사이의 강한 상호작용 때문이다.' PLC-r 또한 티로신 잔기가 인산화된다. 표피 성장 인자에 의해 중재되는 세포의 성장에 있어서 PI 전환 반응의 정확한 역할은 아직 모르고 있는 상황이다. 분자량 46,000, 52,000 그리고 66,000 을 갖는 SHC 단백질들이 생체 내에서 그들의 SH2 영역을 통하여 활성화된 표피 성장 인자 수용체들과 회합하는 것으로 발견되고 있다. SHC 단백질들도 티로신 잔기들이 인산화되는 것으로 알 려져 있다. SHC 단백질 들 은 한 개의 SH2 영역과 한 개의 프롤린/글리 신이 풍부한 영역으로 구성되어 있으며, 알려진 촉매 영역은 없는 것으 로 보고되어 있댜 따라서 그들은 PI-3 키나제의 p85 소단위체와 유사한 lin k er /ad ap tor 단백질의 역할을 하는 것으로 되어 있다 . GTPase 활성화 단백질과 표피 성장 인자 수용체와의 복합체는 아직 보고된 바 없으나, GAP 과 그의 회합된 단백질들인 p6 2 와 p l90 은 표피 성장 인자에 의한 자극 후에 티로신과 세린 잔기가 인산화되는 것으로 알려져 있다. 표피 성장 인자 수용체에 의한 PI-3 키나제의 활성화는 세포의 유형에 따라 다른데, PC12 세포는 표피 성장 인자 수용체에 의해 활성화되며 다른 성 장 인자들의 반응속도와 유사한 양상으로 활성화된다. 인슐린 수용체족 (Insu li n Recep to r Fami ly ) 인슐린 수용체는 두 개의 a 소단위체와 두 개의 /3 소단위체로 구성 된 불균일성 사량체로서 그 기능을 발현하는 수용체 티로신 키나제족의 대표적인 수용체이다 세포 외부의 리간드 결합 소단위체는 막을 가로지 르는 /3 소단위체와 -s-s-결 합을 이루고 있다. 다른 종류의 IR 티로신
키나제 족으로는 인슐린과 같은 성장 인자-l(i nsul i n - li ke gro wt h fac to r - 1, IGF-IR) 과 ins ulin - re late d rece pt or (I RR) 가 있다 인슐린이 그 수용체 에 결합하면 다양한 반응들이 야기되는데 그 반웅 들 은 대사적 효과 들 과 성장 촉진 효과들로 나누어질 수 있다 . 대사적 효과 들로 서는 글루코스 의 수송과 글리코겐의 합성이 포함된다. 인슐린에 의해 활성화된 단백질 키 나제는 단백질 포스파타제 유형 l 을 인산화시키고 그것은 글 리코겐 합 성 효소의 세린 잔기의 탈인산화를 시킴으로써 효소의 활성도를 올려 주는 것으로 알려져 있다 . 또 다른 인슐린에 의해 중재되는 대사적 효과 돌은 지방 생성 , 지방 분해 그리고 단백질 합성 등이 있다. 성장 촉 진 효 과들로서 DNA 합성, 세포 분열, 분화 등이 포합된다. 다른 성장 인자들과 마찬가지로 인슐린과 IGF - 1 은 그들 각각의 수용 체들의 세포 외부 영역들과 반응한다. 두 수용체들의 세포 외부 영역에 서 구조적인 요소들이 보존됨에도 불구하고 인슐린과 IGF-1 은 각각의 a 소단위체들의 구별되는 영역에 결합한다. 리간드의 결합은 수용체의 B 소단위체의 자동 인산화를 자극하며 세포질에 존재하는 신호 전달 분 자들을 향하여 키나제를 활성화시킨다. 몇 가지 연구 결과에 의하면 인 슐 린 결합은 각각의 8 소단위체들을 분자 내 cis 반응으로 그 자신을 인산 화시킬 수 있다는 것이다. 또 다른 연구에 의하면 B 소단위체의 인산화 는 분자간의 트랜스 인산화 반응 메커니즘을 통하여 일어난다는 것이다. 인슐린 수용체의 키나제 활성도는 인슐린에 의해 중재되는 세포 반응 들에 필수적이다. 인간의 B 소단위체에서 티로신 인산화의 중요한 자리 들은 두 개의 영역으로 나누어지는데, C - 말단 영역(티로신 1316 과 1322) 과 티 로신 1146, 1150, 1151 을 포함하는 영 역 이 다. 티 로신 1316 과 1322 를 제거했을 때 rat- 1 섬유모에서 인슐린 의존성 유사분열이 증가하였다 (39). /3 소단위체의 마지막 43 개의 아미노산(티로신 1316 과 1322 를 포함) 들을 제거하였을 때 중국산 쥐의 난세포에서는 정상적으로 작용하는 인 슐린 수용체가 만들어졌다. 티로신 잔기 1146, 1150 그리고 1151 의 인산
화 는 f3 소 단위체의 키나제 활 성 도를 올 려주 는 데 꼭 필 요한 것 으로 보 고되 고 있댜 인 슐 린 수 용체 신호 전 이의 홍 미 로 운 점은 막 영역 가까이 에 있 는 세포 질 영역의 티로신 들 이 생 물 학 적 반응 들 을 중재하 는 데 중 요한 것 으 로 생 각 되 고 있다 . 막 가 까 운 영역에 위치한 티로신 960 을 돌 연 변 이시키 면 인 슐린 에 의해 중 재되 는 수용체의 자동 인산화 또는 키나 제 활 성 도 에 아 무런 효과도 주지 않 는 다 . 혈소판 유도 성장 인자 수용체 혈소판 - 유 도 성 장 인자 ( Pla t ele t -de ri ved Grow th Facto r Rece pt or) 는 평 활근 , 신 경교 세 포 (g l i al cel l) , 섭유아세포(fi broblas t cell) 그리고 내피 세 포 ( end o t h e l i al cel l) 등 에서 중 요한 유사분열 촉 진 인자이다. 혈소관 - 유 도 성장 인자 는 적 어도 세 개의 이량 체 로 발견되는데, A 사슬 또는 B 사 슬 이 -s- s -결 합으 로 연결되는데 AA/BB 형으로 존재하는 경우와 AB 형으 로 존 재한다 . 혈 소판 - 유도 성장 인자 수용체는 두 가지형이 있는데 하나 는 혈 소판 - 유도 성장 인자 a 수용체이고 다른 하나는 혈소판-유도 성장 인자 /3 수용체이다 . a 와 /3 수용체들은 아미노산 서열이 매우 유 사하며 구조적 영역의 같은 배치 를 가지고 있다. 이들 두 가지 종류의 수용체 들 에서 중요한 차이점들은 리간드 결합 특이성과 조직에서의 발 현 양상이 다르다는 것이다. a 와 /3 수용체 모두는 혈소판 - 유도 성장 인자의 자극에 의한 유사 분열을 중재하는데 반하여 /3 수용체만이 골 격근에서 리간드에 의해 유도되는 변화를 중재한다. a 와 /3 수용체들에 의해 인산화되는 단백질의 양상은 유사하나 동일하지는 않다. 혈소판 - 유 도 성장 인자가 결합하면 혈소판-유도 성장 인자 수용체들은 비공유성 이량체롤 형성한다. 혈소판-유도 성장 인자의 다른 2 가형의 존재 하에서 이량체의 형성은 A 사슬 리간드가 혈소판-유도 성장 인자 a 수용체에 만 결합하고 , B 사슬 리간드는 혈소판-유도 성장 인자 a 수용체와 혈소 판-유도 성장 인자 /3 수용체 모두에 결합함을 시사한다. 따라서 리간드
결합에 대한 반응으로 생성되는 수용체 이량체 (aa , bb, ab) 의 형태 는 주 어진 세포에서 발현되는 수용체의 유형에만 의존하지 않고, 세포 를 자 극 할 때 사용되는 혈소판-유도 성장 인자 이량체 (AA , BB, AB) 의 형태에 도 의존성을 나타낸댜 최근의 연구 결과에 의하면 세포질과 막 통과 영역이 절단된 혈소판 유도 성장 인자 돌연변이 수용체가 용액 내에서 혈소판 - 유 도 성장 인자 의존성 이량체를 형성한다는 것이다 . 따라서 세포 질과 막 투 과 영역에 존재하는 아미노산들은 리간드에 의해 유도되는 수용체 이량화에 요구 되지 않는다는 것이다. 신호 전달 분자들이 수용체 티로신 키나제와 직 접 결합한다는 최초의 증거는 PI-3 키나제와 혈소판 - 유도 성장 인자 /3 수용체 간의 상호작용 연구로부터 나왔다. 그 후 혈소판-유도 성장 인자 수용체는 PLC-r, GTPase 활성화 단백질, raf 그리고 pp60 c- sr c 티로신 키나제들과 결합한다는 사실이 보고되었다. 혈소판 - 유도 성장 인자 수용 체에 대한 PI-3 키나제, GTPase 활성화 단백질 그리고 PLC- r 의 결 합 자리들은 한쪽에 모여 있으며 신호 전이의 모델이 그림 5-14 에 나타나 있댜 섬유 아세포 성장 인자 수용체 섬유 아세포 성장 인자 수용체 (F i broblas t Grow th Facto r Rece pt or) 들 은 세포의 분열, 분화 그리고 생존 등 다양한 생물학적 반응들을 중재한 댜 또한 섬유 아세포 성장 인자는 다양한 생명체들에서 혈관 형성 유도 능력을 가지고 있으며 개구리에서 중배엽을 유도하는 능력도 있다. 섬유 아세포 성장 인자족은 산성의 섬유 아세포 성장 인자 (aFGF), 염기성 섬 유 아세포 성장 인자 (bFGF), int - 2 종양 유전자 생성물, hst 종양 유전자 생성물, 섬유 아세포 성장 인자 5, 섬유 아세포 성장 인자 6 그리고 kerati no cyt e gro w th fac to r( KGF) 둥이 알려져 있고, 4 종의 수용체 유전 자(섬유 아세포 성장 인자 수용체 1, 섬유 아세포 성장 인자 수용체 2, 섬유
아세포 성장 인자 수용체 3, 섬유 아세포 성장 인자 수용체 4) 들이 확인되 었다 이 유전자 들 의 생성물 들 은 구조적으로 상관성이 있으며, 티로신 키나제의 활성도를 나타내며 다양한 조직에서 다르게 발현된다. 전형적인 섬유 아세포 성장 인자 수용체는 한 개의 막투과 영역을 포 합한다. 수용체의 세포 외부 부위는 I g와 같은 세 개의 공통된 영역을 포합하고 있다. Ig 영역 I 과 II 사이에 산성 영역이라 불리는 짧은 영역 이 존 재한다 . 섬유 아세포 성장 인자 수용체 1 단백질의 경우 이 영역은 8 개의 연속적인 산성의 아미노산 잔기들로 구성된 핵심 부위이다. 수용 체의 세포질 부위는 티로신 키나제의 촉매 영역을 포함한다 . 티로신 키 나제 영역 뒤에 는 아미노산 55-65 개로 구성된 C- 말단 영역이 있다. 섬 유 아세포 성장 인자 수용체 l 과 섬유 아세포 성장 인자 수용체 2 유전 자 들 의 경우 섬유 아세포 성장 인자 수용체의 다중형들이 교차 접합에 의해 생성된댜 교차 접합은 섬유 아세포 성장 인자 수용체 1 과 Ig 영역 I 이 있는 경우와 없는 경우의 섬유 아세포 성장 인자 수용체 2 그리고 산 성 영역이 있는 경우와 없는 경우의 섬유 아세포 성장 인자 수용체 2 를 생성시킨댜 Ig 영역 I 또는 산성 박스 영역의 제거는 aFGF 또는 bFGF 에 대한 섬유 아세포 성장 인자 수용체 1 또는 섬유 아세포 성장 인자 수용체 2 의 결합력에 영향을 미치지 못한다. 이 사실온 이들 영역들이 리 간드 결합에 관계하지 않는 역할을 할 수 있음을 암시하는 것이다 . 섬유 아세포 성장 인자가 그들의 수용체들에 결합하는 것은 수용체 티로신 키나제 활성도를 올려 주며 티로신 잔기의 자동 인산화를 촉진 한다 . 또한 수용체의 이량화도 촉진한다. 이량화된 수용체의 인산화는 분자간 트란스 인산화 메커니즘에 의해 일어난다. 섬유 아세포 성장 인 자들의 자극은 세포 내 p H 와 Ca2+ 의 수준을 올려 주며, PI 전환 반응이 증진되고, 세포 내 몇몇 단백질들의 인산화를 증가시킨다. 섬유 아세포 성 장 인자의 작용으로 인산화되는 단백 질들은 PLC-r , Ra f-1 , ERKl, ERK2 그리고 S6 리보조멀 키나제 등이 있다. 이들 단백질들의 효소적
5-5 단백질 탈인산화 효소
단백 질의 인산화는 단백 질 인산화 효소(p ro t e i n ki nase) 와 단백 진 탄인 산화 효소 (Pro tei n Phos p ha ta se) 의 상대적인 활성도에 의해 결정된 다( 그 림 5-15). 단백질 탈인산화 효소는 어느 아미노산에 결합된 인산기 릅 때 어 내는가에 따라 크게 두 그룹으로 분류할 수 있다. 단백질의 세린 /토 레 오닌에 결합된 인산기를 제거하는 효소인 세린/트레오닌 특 이성 단백질 탈인산화 효소가 첫번째 부류이고 두번째 부류로 티로신 특이성 단백질 탈인산화 효소는 티로신에 결합된 인산기를 특이적으로 제거한다.
5-5-1 세린/트레오닌냐두이성 단백질 탈인산화 효소들
세린/트레오닌-특이성 단백질 탈인산화 효소는 일반적인 효소와는 달
활성도들이 증가하며, PLC - r 는 리간 드 자 극 후 에 섬유 아세 포 성상 인 자 수용체와 안정한 복합체를 만 든 다 . 섬유 아세 포 성장 안자 수용체 와 PLC - r 의 회합은 PLC - r 의 SH2 영역에 의한 수용체 c - 만민 영역에 존재하는 한 개의 인산화된 티 로신 잔기를 인지합으 로 서 가눔하게 원나, 티로신 766 을 페닐알라닌으 로 교체한 돌 연변이 체릅 만 .,`}1!! PLC r 와 회합도 하지 않고 인산화도 시키지 못 하 는 수용체 단백전이 왼더. 합 - 안 변이된 수용체의 경우 리간드 의 존 성 PI 전환도 못 시키미 섀 AE 내 Ca 언 수준도 증가시키지 못한다. 그러나 이 돌연변 이 수용제논 사동 인산화되 고 세포 내 다른 단백질의 인산화 릅 중재하며, 세포 분연도 중재한 다 . 이 결과들은 섬유 아세포 성장 인자가 L6 세포와 CHO 세 포듄 에서 세 포 분열을 촉진시키는 능력이 Pl 가수분해와 Ca2 ’ 의 동원과는 무관하다는 사실을 말해 주는 것이다.
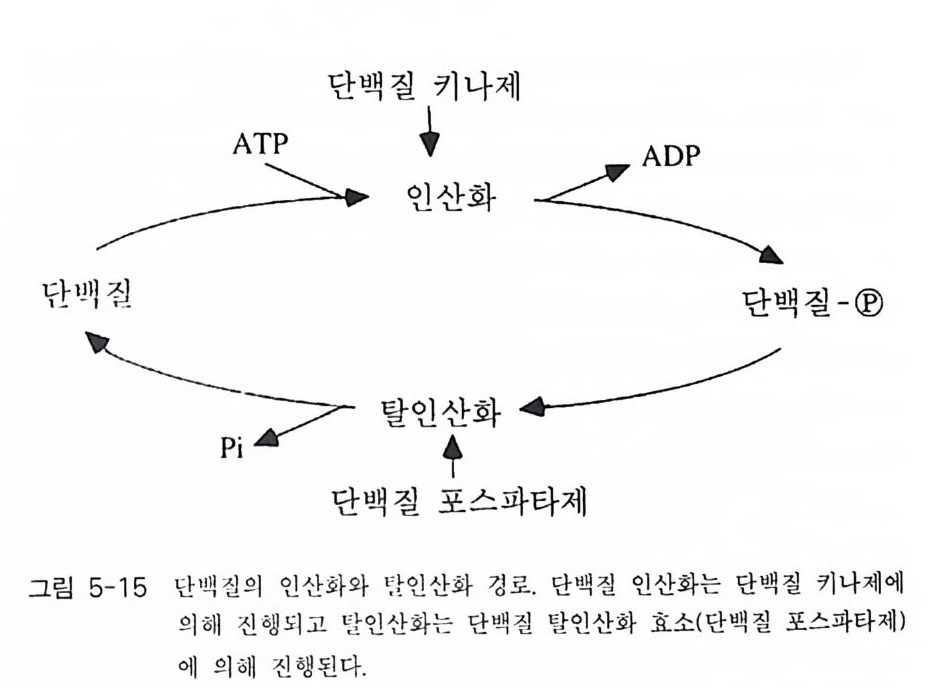 단백질 키나제
단백질 키나제
리 기 전 에 대한 특 이성이 약하다. 생체 밖에서 확인된 이 효소에 대한 기 진 북 이성은 여러 종 의 기질에 중첩되고 있다 . 이러한 이유 때문에 이 부-\}의 효소 몰 분류 하기 위해 특 이적인 억제제나 활성제가 요구된다. 특 이 적 인 억제제나 활 성제 를 이용하여 진핵세포로부터 네 종류의 단백질 탈 인산화 효소 를 확인 했다. 유형 1 탈인산화 효소 (PPl) 는 ph osph ory la se 키나제의 8 - 소단위체 를 특이적으로 탈인산화시켰으며 먀 l I 수준의 열에 안정한 단백질 억제제 -l 과 억제제 -2 에 의해 억제되었다. 반면에 유형 2 탈인산화 효소 (PP2) 는 ph osph ory la se 키나제의 a- 소단위체를 탈인산화 시키며 억제제 -1 과 억제제 -2 에 의해서는 영향을 받지 않는다. 유형 2 탈 인산화 효소는 다시 활성화에 필요한 양이온에 따라 세 종류 (PP2A, PP2B, PP2C) 로 구분된다. PP2A 는 PPl 과 같이 활성화를 위해 이가 양이 온을 필요로 하지 않는다. 그러나 PP2B 의 활성화를 위해서는 Ca 2+ / 칼모 듈린이 필 요하며 PP2C 의 활성화를 위해서는 M g 안 이 필요하다.
희석된 조직 추출물 에서 단백질 탈 인산화 효소률 확인하고 정망합 수 있는 개선된 방법이 최근 보고되었다 (40) . 억제제 _ 1 과 집는 PP! 의 환상 을 효과적으로 억제하며, okadaic ac i d 는 I 1 11\ 1 의 낮은 농도로도 Pl)'2 A 의 활성도를 완전하게 억제시 켰댜 PPI 의 활성도률 억제시키기 위해시·,급 높은 농도의 okada ic ac i d 가 필 요하다 (1 w = l0 ~ 1 5 nM ). 반면에 Ply2 B·: :- PPl 보다 okadaic ac i d 에 대한 민감도가 떨 어 진다. 그리고 Pl 꼈3 C 쓴 ok;l· daic ac i d 의 영향을 받지 않는댜 그러므로 PP2C 는 l\ l g :’ 에 의 .;{근성 · 안 가 지며, okadai c ac i d 에 비 특 이성 을 가지는 목 성웅 이 용하여 학인한 수 있 다 . PPl 에 대한 억제제 1과 집의 민감도나 PPl 과 PP2A 에 대 한 okadaic ac i d 의 민감도는 주목할 만하며 이러한 득 성 을 이 용하 여 동물 이나 식물 (41 ), 그리고 효모 (42) 에 함유되어 있는 단백질 탈 인산화 효소가 밝혀졌 다. 그러나 예외적인 경우도 보고되고 있는데 짚신벌레 ( Param e ci u m ) 에 함유되어 있는 탈인산화 효소는 PP2A 와 비 슷한 특성을 가지고 있지만 okada ic ac i d 에 의해 활성 저해를 보이지 않는다. 5-5- 2 제 2 의 전령에 의한 단백질 탈인산화 효소의 활성 조절 네 개의 세린/트레오닌 -특 이성 단백질 탈인산화 효소 중 두 개 (PPI, PP2B) 는 제 2 의 전령인 cAMP 와 Ca 안 에 의해 활성도가 민감하게 조절된 댜 PP2B 는 Ca 2 t 에 의존성이며, 칼모듈린에 의해 활성이 증 가되 는 효소 이며 칼모듈린이 존재하지 않아도 칼모듈린과 유사한 Ca2· 결합 소단위 체 (19 ada) 에 의해 활성도가 조절된다 . PP2B 는 다른 세 종류의 단백질 탈인산화 효소에 비해 기질 특이성이 더 약하다. PP2B 에 의해 탈인산화 되는 것 중 상당수의 단백질이 cAMP- 의존성 단백질 키나제 (PKA) 에 의 해 인산화된댜 이 러 한 현상은 PP2B 가 제 2 의 전령 인 Ca 2+ 을 통해 cAMP 의 효과를 억제시키도록 유도하고 있음을 시사한다 (43) . PP1 의 활성도는 PP2B 와는 달리 cAMP 와 Ca 안 모두에 의해서 복잡한
경로률 동해 조절 되고 있다. 또한 조직의 종류에 따라서도 활성화되는 양상이 차이가 있음을 보여주고 있다. G - 소단위체와 같은 소단위체의 인산화 룹 동한 조절 방식 이 그 중 하나이 다(그림 5- 16 ). 골격 근육에 아 드 래난런이 분바되면 PPl 의 G _ 소단위체의 세린 잔기는 PKA 에 의해 인 산아가 된댜 G 소단위체의 인산화 는 G ― 소단위체로부터 C - 소단위체 (ca t al yti c sub- un it) 선 해리시키 세 포질로 이 동 시킨다. 이 단계에서 c - 소단위체의 활성 도는 어새재 - 1 에 의해 억제된다(억재제 - 1 은 PKA 에 의해 인산화된 후 C_ 소단위세의 강리한 억제재가 됨). G - 소단위체로부터 c - 소단위체의 해리 는 글 리코겐 대사 합 위 한 효소둘 의 탈인산화를 효과적으로 억제할 수 있 는 메커니 즘 이다 . PPl 의 분 자 는 간장의 글리코겐에 결합되어 있으며 이러한 형태는 글 리코겐 합성 효소의 활성도를 향상시켜 준다. 동시에 기 질을 탄 인산화시키는 능력은 nl\I 수준의 ph osph ory la se a 에 의해 억제 되고 있다. 이와 같 이 글 리코겐 분해가 활성화되어 글리코겐 합성이 억제 되 는 매커니 즘은 중요한 조절 단계라 할 수 있을 것이다. Ca 2 님 과 cA l\tIP 에 의해서 증 가된 호르몬은 ph osph ory la se a 의 농도를 증가시키기 때문 에 간장의 글 리코겐에 결합된 PPl 의 활성도는 이들 제 2 의 전령에 의해 억제될 수 있다. Phosph on1I a se a 에 의한 간장의 PPl 활성도의 억제는 아마도 다른 소단위체에 의해 제공되는 것으로 생각된다 . G - 소단위체와 억제제 -1 을 탈인산화시키는 주된 효소는 PP2A 와 PP2B 이다 (44). 여기에서 PPl 은 다른 종의 단백질 탈인산화 효소 (PP2A, PP2B) 에 의해서 간접적으로 조절되고 있다(그림 5-16). PP2B 에 의한 G- 소단위체와 억제제 -l 의 탈인산화는 Ca 안 에 의한 PPl 의 활성도 증가와 cAMP 활성 도 감소를 유도하였다 (44). PP2A 와 PP2B 에 의 한 PPl 의 탈인 산화는 PPl 을 활성화시켰으며 이 탈인산화 효소는 탈인산화 반옹에 참 여하게 된다. PPl 의 활성도가 다른 경로(인슐린)를 통해 조절되고 있음 이 보고되어 있다 (45). 많은 세포에 존재하는 PPl 의 비활성형 (PP li)은 억
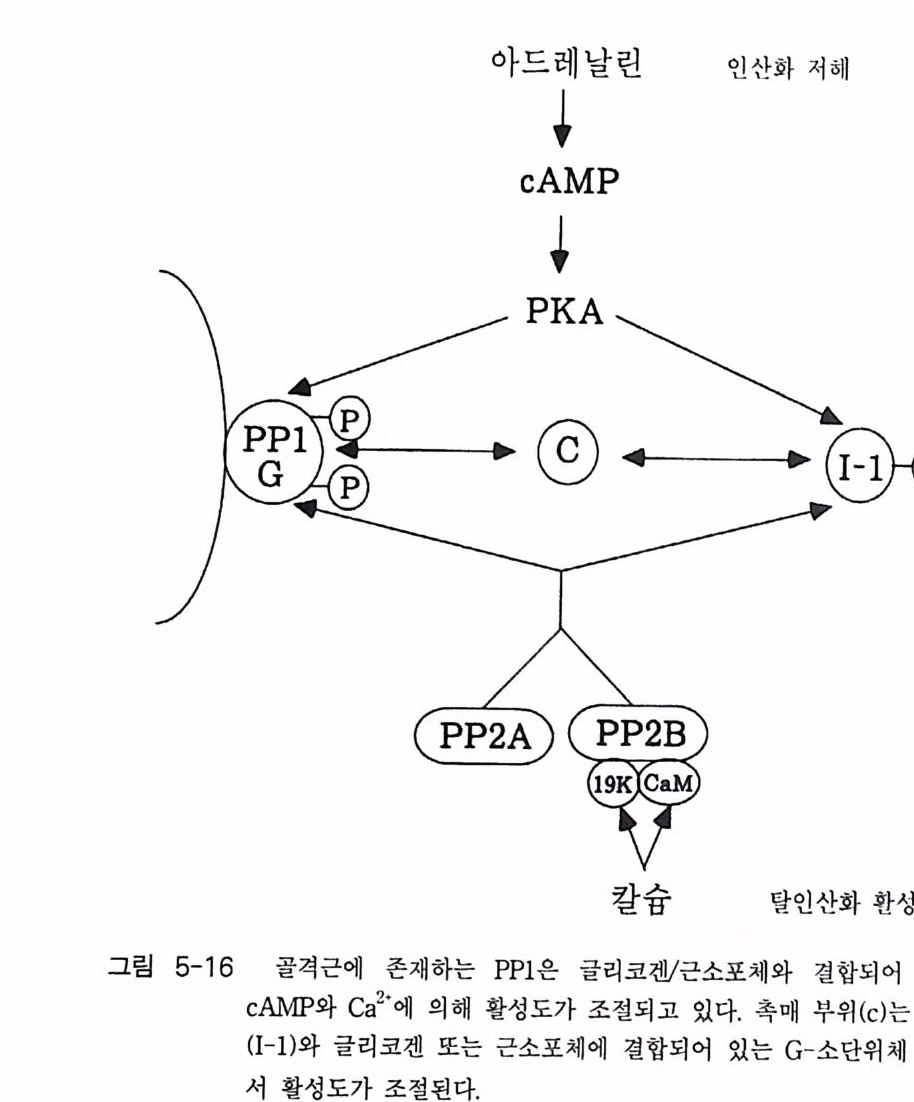 。` k_c드 _러~날 린인산화 저 해
。` k_c드 _러~날 린인산화 저 해
제제 -2 와 C- 소단위체 사이에서 평형을 유지하고 있다. 이 단백질 탈인 산화 효소 1 의 활성은 억제제 -2 의 인산화에 의해 생성된다. 그러나 인슐 린이 PPl1 를 통해 PPl 의 활성도를 증가시키는지 여부는 아직까지 명확 하지 않다. PPl 의 C- 말단 근처의 티로신이 in v itr o 에서 piffl v 작 C 에 의해
인산화되 는 것과는 달리 PP2B 의 C ― 소단 위체 는 칼모듈린 - 의 존성 단백질 키나재에 의해 인산화된댜 두 경우 의 인산화 는 기질의 Km 값 을 두 배 정도 증 가시켜 준 댜 그라 나 이러한 안산화가 in v i vo 에서도 동일하게 반생되고 있는지 여부 는 명확하지 않다. 아 도 래난린과 급부 카 곤( g luca g on) 에 의한 acety l- C oA 카복시라제의 인산화가 cAMP 에 의한 PP '2A 활성도 저해를 추측할 수 있도 록 해주며 이 니한 산상은 지방세포와 간세포에서 관찰할 수 있다. 5-5-3 유형 l 과 유형 2 단백질 탈인산화 효소 이성질체들 PPl, PP2A, PP2B 그리고 PP2C 둘 의 이성 질체는 포유동물 조직에서 적어도 2 개씩 발견되었다 . PPl 의 이성 질체들은 매우 유사하며( > 85% 유사성) PP 2A 의 이성 질체들도 역 시 매우 유사하였다( > 97% 유사성). 이 뜹 이성전체 돕은 N ― 말단과 C - 말 단만이 차이가 있음이 밝혀졌다 . PPl 과 PP3A 의 각 이성 질체둘을 CD;\A 클로 닝과 No rt he rn blott ing 등을 기초 보 연구하였으 나 다 른 작용을 할 만한 구조적인 차이점은 발견하지 못 했다 그 러나 PP2A a 이성 질체 의 m 印 \A 는 여러 조직 내에서 PP2A {3 이성 전체보다 10 배나 많이 존재하고 있었다. PP2B 촉 매 부위의 cDNA 클로닝으로부터 교차 접속에 의해 적어도 2 개 (58, 59kDa) 의 PP 가 발현되었다. 58kDa 단백질은 PP2Bw 로 명명되었 으며 PP2B 와는 54% 의 유사성을 보인다. PP2Bw 의 아미노산 서열은 PP2B 의 CaM 결합 부위와 매우 비슷하며 또 다른 이성질체로 생각된다. 그러나 촉매 부위의 유사성은 PPl 또는 PP2A 의 이성질체들 사이의 유 사성보다도 낮았다. PP2C1 과 PP2C 2 로 명명된 PP2C 의 이성질체가 토끼 의 골격근에서 발견되었다. 이 들 의 분자량은 각각 44, 42kDa 임이 확인 되었댜 이 들 이성질체의 펩티드 배열은 80% 의 유사성을 보여주었다. 쥐의 간에서 발견된 PP2C1 은 토끼의 PP2C1 과 100% 동일하며 토끼의
PP2 C ~ 와 는 75 % 유사성을 보여 주었다 (46), 5-5-4 PPX, PPY, PPZ 최근 PPX, PPY 그리고 PPZ 로 명명된 단백전 탄인산화 효소 휴 매 소 단위체가 cDNA 클로 닝으로부터 확인되었으며 이 것은 PP! 이나 PP 2 J\와 매우 유사하댜 토끼의 간에서 추 출 된 PPX 의 cDNA 배 인은 PP! 보다는 PP2A 에 더 유사했다 (표 5- 2) . ppy (초파리)와 PPZ ( 토끼)의 배연은 PP2A 보다는 PPl 에 더 유사했댜 이 들 촉매 소단위체 는 낮은 기질 득 이성과 적은 양의 존재, 다양한 세포에 존재하지 않는 점 그리고 억제 소단 위체 와 상호 작용하지 않는 성 질 때문에 쉽게 확 인되 지 못한 것 같다. 5-5- 5 단백질-티로신 탈인산화 효소 (PTPase) 단백질 - 티로신 탈인산화 효소의 기질은 단백질 내 p ho s p ho ty ros i n e 이 다. 지금까지 밝혀진 단백질-티로신 탈인산화 효소로는 7 가지가 보고되 어 있다 (Drosop hi la pro te in tyros in e ph osph ata s e, DPTP ; DLAR ; leukocyt e common an tig en(LCA) 一 rela t ed molecule, LAR ; CD 45, T cell PTPase, PTPase lB, PTPase lA). PTPase 1B 가 태반에서 발견 되었 는 데 PTPase 1B 의 아미노산 서열은 세린/토레오닌 특 이성 단백질 탈 인산화 표 5-2 최근 발견된 단백 질 탈 인산화 효소 와 PPl 또는 P P'2 A 와의 유사성 . PPX , PPY 와 PPZ 는 토끼 의 간에 서 추출되 었으며 SIT 4 는 효모 (Sacch - arom yce s cerev i s iae) 에서 클로닝되었다. PPZ PPY PPX SIT4 6945 E3i9O 4565 5417
효소의 촉 매 부위와 아무런 유사성이 발견되지 않았다. 그러나 백혈구 세 포 표면 에 존 재하 는 단백질 (CD45) 의 원형질 방향에 위치한 부위와 상 당히 유사합이 알려졌댜 이것은 CD45 가 PTPase 의 활성도를 가지고 있 옹 것 임 웅 시사한다. 태반에서 LAR 단백질이 발견되었는데 세포질 영역 은 CD45 와 비 교 하여 높은 유사성을 보인 반면 세포 외부 영역은 전혀 유사상이 먄견되지 않았 다 다가 음이온(po l y a ni on) 억제제를 이용하여 l y「 Pa se IA 와 Iyr Pasc lB 가 구별되었는데 이 두 PTPase 는 구조적으로 도 차이가 있음 이 밝혀졌댜 T cell PTPase 가 PTPase 1B 를 이용하여 확 인되었다. 이 P1`Pasc 는 PTPase 1B 보다 C - 말단 부위가 10 kDa 더 크 며 아미노산 서열의 유사성은 65 % 정도이다. 참고문헌 I ) Tal
10) Hanson. P. I. and Schulman, H. 0992 ) An nu. Rm Bi oc hem. 61. 559 11 ) Fukunag a, K, et al. ( 19 82) ]. Neu rosci. 3 9, 1607 12) Bennett, lVI . K., et al. ( 19 83) ]. Bi ol . Chem 258, 127.荀 13) Golderu ing , J. R., et al (19 8 .3) ]. Bi ol. Chem. 258, 126 32 14) Schulman, H. 0984) J. Cell. B io l. 멕 11 15) Kuret, J. and Schulman, H. (19 84) Bio c he m i st ' } ' 2 1 [).I\ Ii 16) l\' IcG 떠 nne ss, T. L., et al. (19 83) FEBS Lett . H i.1 . :t~\l 17) Bulleit, R. F., et al. (19 88) Neuron _ 1 , (3.1. 18) Levin e , H., Sahy o un , N. E. and Cuatr l' Ca sa~. P. (H)8( 1) Proc Na tl . Acnd Sc i. USA 8.3, 2253 19) Hanley, R. M., Means, A. R., Ke m p , B. E. and Sh en o lik a r, S. 0988) Bio c hem Bi op h ys. Res. Commun 152 . 122 20) VanBerkum, M. F. A., George , S. E. and Mean s, A. R. 0990) ]. Bio l . Chem 265, 3750 21) Sa itoh , T. and Schwa rtz, J. H. 0985) ]. Cell. Bi ol . 1 00, 8.3.5 22) Nis h i zu ka, Y. (1984) Natu r e 308. 693 23) Den nis, E. A., Rhee, S. G., Bil lah , M. M. and Hannun, Y. A. (19 91) FASEB ]. 5, 2068 24) Berr idg e, M. J. and Irvin e R. F. (1984) Natu r e 312, 315 25) Sha riff, A and Luna, E. J. 0992) Sc ien ce 256, 245 26) Sid d iqui, R A. and Exto n , J. H. 0992) ]. Bi ol. Chem. 267, 575 .5 '1:7) Olson, S. C., Boeman, E. P. and Lambeth , J. D. (19 91) ]. Bi ol . Chem 266, 17236 28) Prescott , S. M. and Maje r us, P. W. (19 81) ]. Bi ol. Chem 256. 579 29) Un igs, I. J., et al. (19 92) Bi oc hem ]. 281, 597 30) Khan, W. A., Blobe, G. C. and Hannun, Y. A. (19 92) ]. Bi ol. Chem 267, 3605
31 ) Yoshid a , K., As ao ka, Y. and Ni sh i zu ka, Y. (19 92) Proc. Natl. Acad. Sci. USA . 89, 6443 32) Nis h z uk a, Y. 09 88) Na tu r e 334. 661 3:3) Paws on , T. 099 2) Natu r e 356, 285 34) Uen o, H., C olbert , H. A. Es co bedo, J. A. and Wi lli a m s, L. T. (19 91 ) Scie n ce 252, 844 35) Coug h lin , S. R, Escobedo, J. A. and Wi lli a m s, L. T. 0989) Sc ien ce ‘시 3, ll()1 36) Pa wson , T., ( I! 麻 2! Curr. Op in Str u ct. Bi ol . 2 , 4 37) Mats u d a, M. , May e r, B. J.. Fukui, Y. and Hanafu s a, H. 0990) Sc ien ce 248. 153 7 38) Ullri ch , A. and Schless in g e r. J . (19 90) Cell 61, 203 39) Takata , Y., Webste r , N. J. G. and Olefs k y , J. M. (1991) ]. Bi ol. Chem 266, 9135 40) Cohen, P., Klump p, S. and Schellin g , D. L. 0989) FEES Lett . 2 50, 59G 41) Mackin t o s h, C. and Cohen, P. 0989) Bi oc hem ]. 262, 335 42) Cohem, P., Schellin g , D. L. and Sta r k, M. J. (1989) FEES Lett . 2 50, 601 43) Cohen, P. (1988) Proc. R. Soc. Land B Bi ol. Sc i. 234, 115 44) Cohen, P. (1988) Mal. Aspe cts Cell. Reg ul. 5 , 123 45) Cohen, P. (19 89) Annu Rev. Bi oc hem 58, 453 46) Cohen, P. and Cohen, P. T. W (1989) ]. Bi ol. chem 264, 21435
제 6 장 이온 채널 어 느 생물학자의 이야기이다. < 지금 카네기홀에서 음악 연주회가 있 다고 가정하자. 모든 사람은 누가 지휘하는 어떤 교향악단이 누구의 곡 윤 연주하는 데 관심이 있으며 또한 그 음악회의 질은 바로 이 요소들로 결정된 댜 물론 관객의 수준도 중요하지만 어느 누구도 카네기홀 입구에 서 표률 받는 사 람 에게는 관심이 없다. 여기서 우리는 입구에서 표를 받 는 사람에게 지휘자, 악단, 곡, 그리고 관객을 선택할 수 있는 권한을 부 여했다고 가정하자. 이 음악회의 수준은 표를 받는 사람의 능력에 따라 결정될 것이댜> 그동안 생명 현상을 연구하는 생화학자나 생물학자에 게는 생체막에 대해서는 별 관심이 없었다. 대부분이 유전자와 단백질에 초점을 맞추어 이것들로부터 생명 현상을 규명하고자 하였다. 그러나 불 행하게도 인간 사회와는 달리 생체막에는 물질, 특히 이온들의 이동을 가능케 하는 여러 단백질들이 존재하며 이들을 통해서도 생명 현상들이 조절되고 있다. 생체막에 존재하는 단백질인 이온 채널에 의해서 이온들 의 이동이 이루어지며 이들에 의해서 생명 현상이 조절되고 있음을 강 조하는 이야기이댜 외부 신호가 지금까지 살펴본 신호 전달 메커니즘에 의해서 생체 내
에서 일어나는 수많은 반응을 조절하는 데 , 크게 두 가지 범주로 나 누 어 서 생각할 수 있댜 하나는 생체막에 존재 하 는 이온 체 널 이나. 운송자 (tran sp orter ), 그리 고 펌 프(p um p, ATPase) 를 활성 화시 킴 으로씨 이 온의 이동을 조절하는 빠른 반응 (sho rt ter m, 빠 른 시 간 내에 이 무 어지 는) 이며 다른 하나는 수송(tr ans port)과 전이(t ransduc ti on) 릅 거 쳐 단백 전 합상 반응을 조절하는 느린 반응 Oon g tem 1, 단기에 비해서 긴 시 간 · 홍 요하는) 이다 . 본 장을 통해서 전기 생리학에 관한 기본적인 개념과 이온의 이 동 에 가장 중요한 이온 채널, 그리고 여기에 관여하는 신호 전단 메커니즘에 대해서 알아보기로 한다 . 먼저 전기 생리학적인 개념에 대해 살펴본 다 음, 생체가 가지고 있는 네 개의 이온 채널인 K\ Na\ Ca2’ 그리고 Cl- 채널에 대해서 그 구조와 이온의 이동 메커니즘에 대해서 소개하기로 한댜 끝으로 이들 조절에 관여하는 신호 전달 메커니즘에 대해서 G 一 단 백질을 중심으로 몇 가지 범주로 나누어서 살펴보기로 하겠다. 6-1 전기 생리학에 관한 일반적인 개념 생체막에 존재하면서 이온, 물질 등의 이동에 관여하는 단백질에는 크 게 세 가지로 나누어 생각할 수 있는데, 이온 채널, 운송자, 그리고 펌프 (ATPase) 가 그것이댜 일반적으로 이온 채널이나 운송자는 수동 수송에 관여하며 펌프는 능동 수송에 관여하고 있다 . 수동 수송이란 물이 높은 곳에서 낮은 곳으로 흐르는 것과 같이 농도가 높은 곳에서 낮은 곳으로 이온이나 물질이 이동하는 과정을 말하며 능동 수송은 농도가 낮은 곳 에서 높은 곳으로 이온이나 물질이 이동하는 과정인데 이 경우 필수적 으로 에너지(생체 에너지에서는 ATP) 의 소모를 동반하게 된다. 예를 들 어서, 일반적으로 세포 외부의 Ca2• 의 농도는 약 l mM 정도이며 세포질
내의 Ca 2’ 의 농도는 약 100- 30 0 n1vI 정도이다(제 4 장 칼슘 이온 참조). 따 라서 원형질막에 존재하는 Ca2 ’ 이온 채널은 세포 외부로부터 세포질로 Ca 2’ 이 이 동하는 데 관여하는 이온 채널만이 존재하며 세포질에서 원형 진막으로 이동하 는 Ca 2’ 은 이온 채널을 통해서 이동하는 것이 아니라 c}' - A TPa se 와 같은 펌프를 통해서 이동하게 된댜 그랑다면 이 온 채널과 운송자의 차이점은 무엇인가? 이들 두 생체막 단백전은 정확히 구분하기란 쉬운 일이 아니지만 일반적으로 운송자는 이 동하는 이 온 이나 물질 이 운송자의 용질 결합 부위에 결합하면 이 운 송자의 구조직인 변화가 일어나며, 그 후 이온이나 물질이 반대 방향으 로 빠져나가게 된다. 이에 반해 이온 채널의 경우에는 이온이 수송로 단 백질의 구조적 변화 를 유도하는 것이 아니라 수송로의 생체막 부위에 구멍 이 존재 하 는 데 이 구멍은 물로 채워져 있다. 따라서 이온 채널이 열 려 있다면 이온 들은 물로 채워져 있는 구멍을 통해서 자연스럽게 통과 하게 된다 운송자 의 이온 또는 물질 수송 메커니즘을 살펴보면, 운송자를 통한 이온의 이동은 구조적인 변화에 의해서 이루어지기 때문에 두 가지 구 조적인 상태 를 고려할 수 있다. 탁구 시합에서 탁구공의 이동처럼, ping 상태와 pon g 상태를 생각할 수 있다. 그림 6-1 에서 보는 것과 같이, pon g 상태란 이동하고자 하는 물질 A 가 결합할 수 있는 또는 결합되어 있는 상태로서 막의 바깥쪽(물질 A 의 농도가 높은 쪽)을 향해 열려 있는 상태이댜 Ping 상태란 물질 A 의 결합 자리가 반대쪽(물질 A 의 농도가 낮은 쪽)을 향해서 열려 있는 상태이다. 따라서 운송자를 통한 물질 수송 은 운송자의 pong 상태에서 가 운송자의 A 결합 자리 에 결합하게 되면 구조적인 변화가 유도되어 ping 상태로 바뀌게 되면 는 반대 방향으로 나가게 된댜 전형적인 동물 세포의 경우 세포 내의 K+ 농도가 세포 외부보다 약 10 배에서 20 배정도 높으며 Na • 의 경우는 그 반대이다. 원형질막에 존
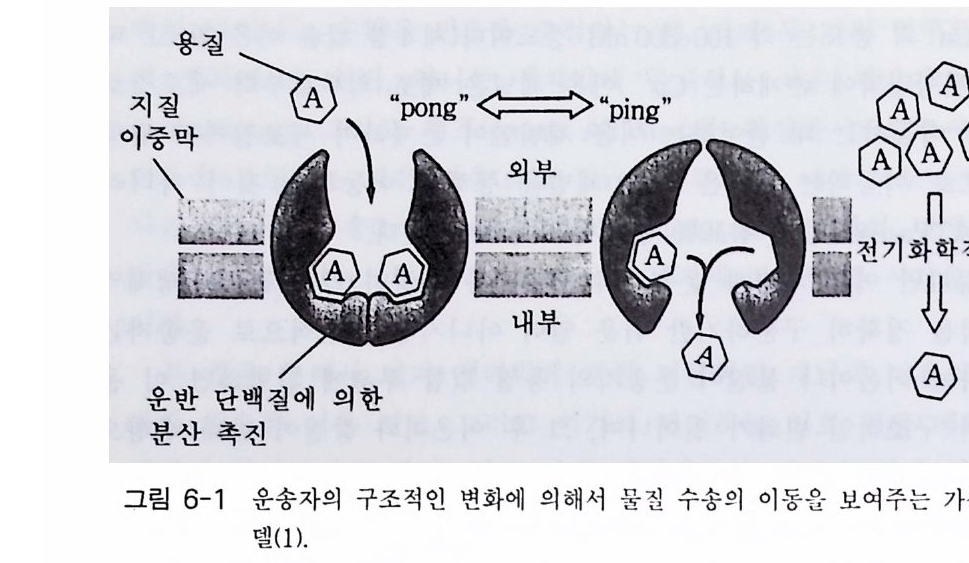 용질
용질
재하는 Na+- K 펌프(또는 Na·-K ' ATPase) 는 세 포 외부에 존재하는 2 분자의 K 홀 세포 내부로 이동시키는 동시에 세포 내부에 있는 3 분자의 Na+ 울 세포 외부로 이동시키는 데 관여하는 대표적인 펌프이다. 앞 에서 언급한 것처럼, 이 경우 ATP 의 가수분해를 수반하게 되 는 데 그 작용 기 작은 다음과 같다. 그림 6-2 에서 보는 바와 같이 Na + 이 ATPase 의 세 포 질 쪽에 결합하게 되면 ATPase 의 아스파르트산 (as partic a ci d) 이 인산화 되며, 이 Na+ 의존성 인산화가 ATPase 의 구조적인 변화 를 유도하게 되 며 동시에 Na + 이 세포 외부로 나가게 된다. 한편, 세포 외부의 K 이 결합 자리에 결합하면 K 의존성 탈인산화가 일어나며 이때 바뀐 ATPase 의 구조가 원래 상태로 돌아가며 K 이 세포 내부로 들어오게 된다 . 본 장에서는 이온 채널과 그곳에 관여하는 신호 전달 기작에 초점을 맞추고자 한다. 따라서 이온 채널을 이해하는 데 필요한 몇 가지 전기 생리학에 대한 개념 또는 용어를 살펴보기로 한다. 활동 전위 (ac ti on pote n ti al) 란 이온의 이동에 따라 생성되는 파로서 다
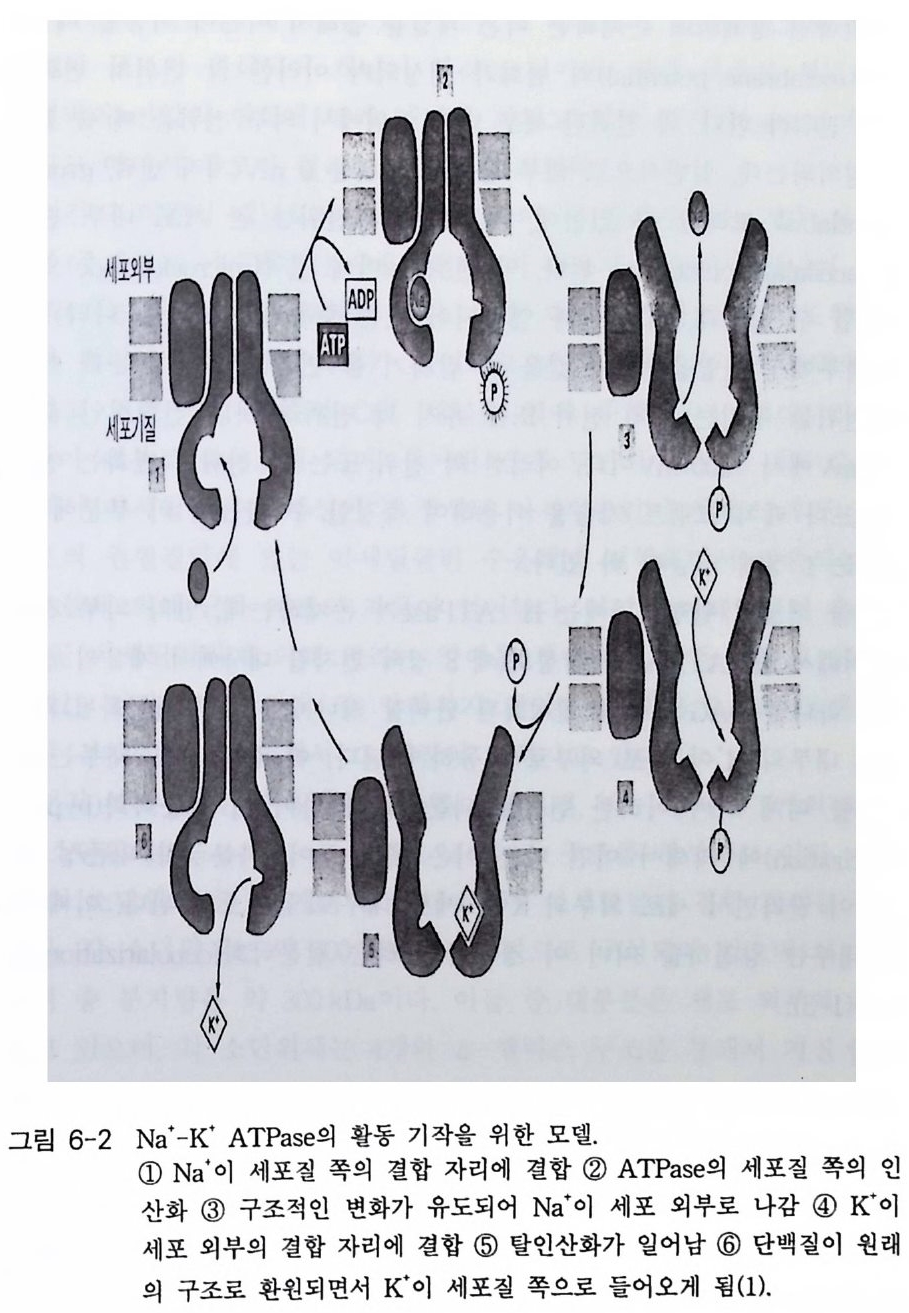 ir[7, \
ir[7, \
시 말하면 생체막에 존 재하 는 이온 채 널을 통해서 이온이 이 동할 때 박 전위 (membrane pot en ti al) 의 변화가 생성되며 이러한 막 전위의 변화릅 활동 전위라 한댜 막 전위란 세포 내부 전위에서 외부 전위를 빼 준 값으 로 정의되는데, 일반적으로 외부 용액의 전위 를 0 mV( 기저 전위, gr ound pot en ti al) 로 고려할 수 있는데, 이 경우 막 전위는 곧 세 포 내 부 신 위 (int r ac ellular pot en ti al) 가 된댜 막 전위는 미세 전극 (m i crocle ct rocle) 으로 측정할 수 있는데, 이 전극과 연결되어 있 는 증폭기가 0 값윤 나타내다 가 외부에서 전압을 변화시켰을 때 갑자기 음 변화 ·릅 보여 주는 데 이때 막 전위 를 우리는 휴지 전위 또 는 휴지 막 전위라 하며 전형적 인 값은 -40 mV 에서 -100 mV 이다 이러한 막 전위 또는 막 전위의 변화 는 전압 크램프나 패치 크램프 기술을 이용하여 측정할 수 있 는 데 이 부분에 관 해서는 l 장에 언급된 바 있다. 식물 세포의 원형질막에는 H ♦ _ ATPase 가 존재하는데, 만약 외부 자 극 에 의해서 H ' -ATPase 가 활성화(제 3 장의 인지 질 대사에서 제 2 의 전령 중의 하나인 DAG 에 의해 활성화된 단백질 키나제에 의해 활 성화됩)되면 세포 내부의 H + 이 세포 외부로 이동하게 된다 . 이 경우 세포 내부 는 음 전하를 띠 게 되 며 이 러 한 현상을 과분극화라 하며 이 과분 극화 (h ype r po l ariz a ti on) 에 의해서 어떤 다른 이온 예를 들어, 과분극화 의 존 성 K' 채널이 열리면서 세포 외부의 K 이 세포 내부로 들어오게 된다. 이때 세 포 내부는 양전하를 띠며 이 경우를 우리는 탈분극화 (de po l ari za ti on) 라 한다(1 -3). 6-2 어떻게 채널이 열리고 닫히는가? 이온 채널은 열리고 닫히는 기작에 따라 리간드-의존성 채널 (l ig and_ ga te d channel) 과 전압-의존성 채널 (vol tag e- g a ted channel) 로 나눌 수 있
다 . 리간 드 - 의존성 채널이란 리간드가 그 수용체에 결합함으로써 채널 의 3 차 구조가 변화되어 채널이 열리는 것이며, 전압 一 의존성 채널이란 생체막의 전압의 변화에 따라 채널이 가지고 있는 갑지기 (sensor) 에 인 지되고 따라서 동로가 열리는 것으로 여겨진다. 리간 드 - 의존성 채널로서 그 작용 가작이 잘 알려져 있는 것은 신경세 포 에 촌재하 는 아세틸 콜 린 수용체인데, 이 수용체를 통해서 채널이 열리 고 단히 는 기작 윤 살펴보기로 한다. 신경 자극이 신경 말단에 도착하게 되면 원형 질 막에서 탈분극화가 일어나고 이 탈분극화가 원형질막에 존 재하고 있 는 전압 - 의존성 Ca2· 채널을 열어 주게 된다. 이 때, 외부의 Ca 2· 이 내부로 들 어오게 되며, 층가된 신경 말단의 세포질 내의 Ca 안에 의해서 아세틸 콜 린이 생성된다. 생성된 아세틸콜린이 시냅스 후부 근육 세포의 원형질막에 있는 아세틸콜린 수용체에 결합하면서 방출되는 양 이온 들 에 의해 근육 세포의 자극이 일어난다. 여기서 아세틸콜린 수용체 는 곧 아세틸콜린에 의해 열리는 양이온 채널이다. 이들 채널의 열리고 닫히는 기 작은 지금까지 잘 알려지지 않았는데, 최근 9 A의 분해능을 가진 전자현미경에 의해서 그 기작이 밝혀지고 있다 (4). 먼저 아세틸콜린 수용체의 구조를 살펴보면, 이 수용체는 5 개의 막 관 몽 소단위체 (a, a, /J, r, 그리고 8) 가 링 구조를 형성하고 있다. 이들 5 개의 소단위체 중 두 개의 a 소단위체에 아세틸콜린 결합 자리를 갖고 있댜 각 소단위체는 약 500 개의 아미노산으로 구성되어 있으며 이 수용 체의 총 분자량은 약 300kDa 이다. 이들 중 대부분은 세포 외부에 위치 하고 있으며, 각 소단위체는 4 개의 a- 헬릭스 구조를 통해서 지질 2 중 층을 가로지르고 있다. 이들 4 개의 a- 헬릭스 중 오직 한 개의 a- 헬릭 스에 많은 극성 아미노산이 있는데, 각 소단위체에 존재하는 극성 a_ 헬 릭스 5 개가 모여 이온의 통과에 관여하는 수용성 구멍의 벽을 형성하고 있다(그림 6-3). 아세틸콜린 수용체의 3 차원적 구조를 살펴보면, 세포 외부는 매우 불
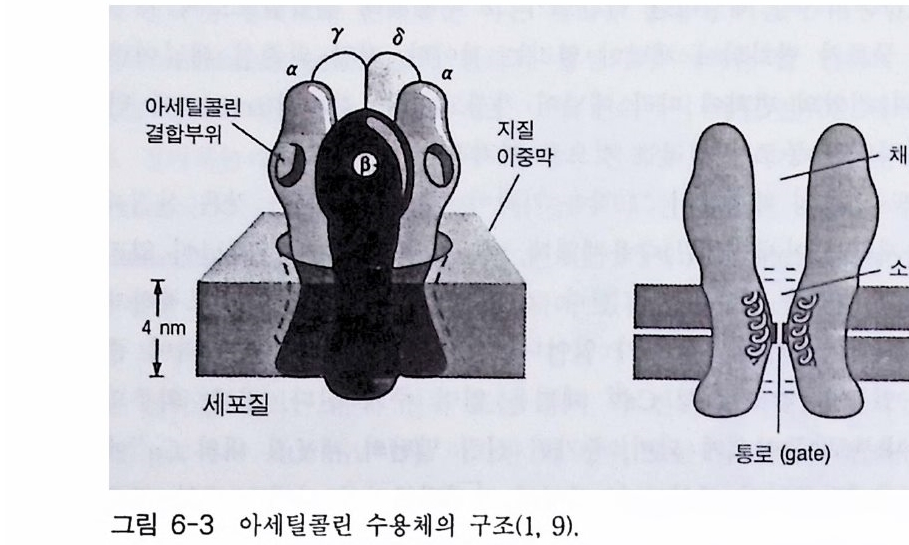 r 8
r 8
규칙적인 반면 세포 내부는 비교적 배열이 규칙적으로 이 루 어져 있다. 그림 6-4 에서 보는 바와 같이 이 이온 채널의 입구 쪽은 직경이 약 20-25 A 이며, 아세틸콜린 결합 자리는 막 표면으로부터 비교적 멀리 떨 어진 거리로서 약 20-30 A 정도이다 (5) . 구멍을 이루는 a - 헬릭스 구조 는 4 개의 막 관통 부위 중 2 번째 (M2) 로 앞에서 언급한 것처 럼 극성을 띤 아미노산이 비교적 많이 존재하는데, 이것이 이온 채널을 열고 닫히 게 하는 데 매우 중요한 역할을 하고 있다. 이들 수용체의 세포질 부분 은 다양한 세포 골격 분자나 다른 조절 분자들, 즉 단백질 키나제와 같 은 분자들과 작용하고 있다 (6, 7). 이러한 구조를 가진 리간드에 의해 열리는 이온 채널이 어떻게 열리 고 닫히는지를 살펴보기로 한다. 먼저 세부적인 구조를 살펴보면, 앞에 서 언급한 것처럼 이온 채널의 입구는 20-25 A 으로서 막 표면으로부터 비교적 많이 떨어져 있는데, 이 부분은 일차적으로 적절한 이온을 통과 시키는데 그 역할이 있는 것으로 추정된다. 즉, 이 부분의 표면에는 비
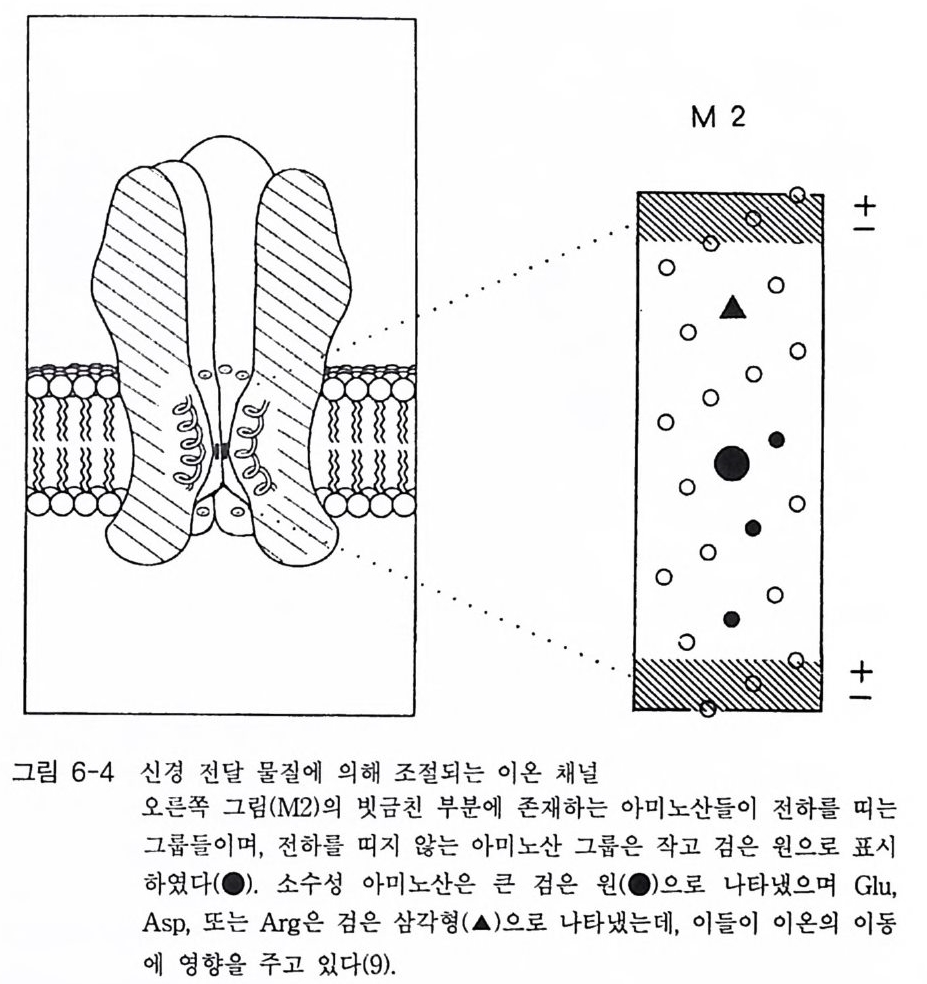 M2
M2
교적 음전하를 띠고 있는데 인력에 의해 양이온을 끌어 모으고 반발력 에 의해 음이온을 분산시키고 있다 (8). 다음 부분이 입구와 구멍 사이의 막 표면에 위치한 부분으로 비교적 좁은 상태인데 M2 단편의 끝부분으 로서 음전하를 띤 아미노산인 글루타민산이 존재한다. 마지막으로 가장 중요한 부분이 구멍으로서 극성을 띠는 M2 헬릭스와 각각 이온의 수화 된 표면 사이의 작용을 통해서 이온을 통과시키거나 통과시키지 않거나
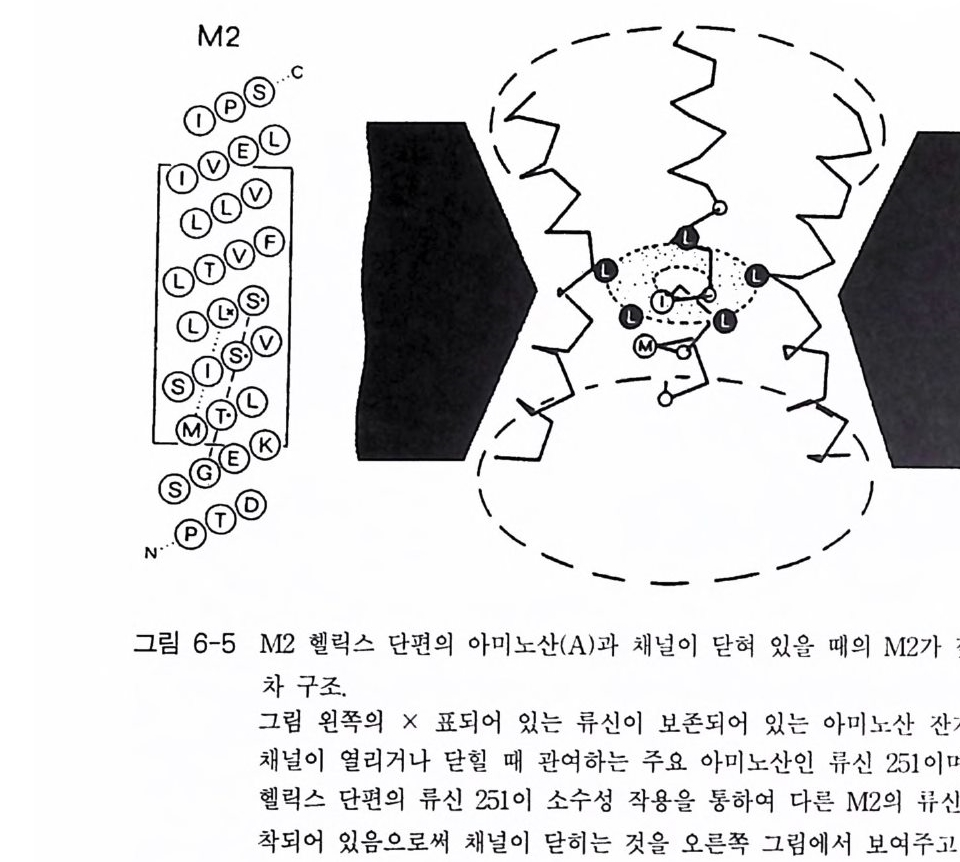 s
s
를 결정한다. M2 헬릭스 단편에는 소수성 아미노산인 류신 251 이 있는 데 이 부분이 소수성 상호작용을 통해서 다른 M2 헬릭스의 류신과 강하 게 밀착되어 있기 때문에 a- 헬릭스 구조가 이 부분에서 휘어지게 되며 이온 채널이 닫혀지게 되면 수화된 이온들이 통과할 수 없게 된다(그림 6-5). 아세틸콜린이 수용체에 결합하게 되면, M2 단편의 또 다른 중요한 아미 노산인 트레오닌 244 가 류신 251 과 작용함으로서 류신 251 간의 소 수성 상호작용이 붕괴되면서 M2 의 a- 헬릭스가 바깥쪽으로 회전하게 된다. 따라서 이 a- 헬릭스의 회전이 소수성 상호작용에 의해서 밀착되 어 있는 류신 251 의 통로를 붕괴시키면 이온 채널이 열리게 된다 (9).
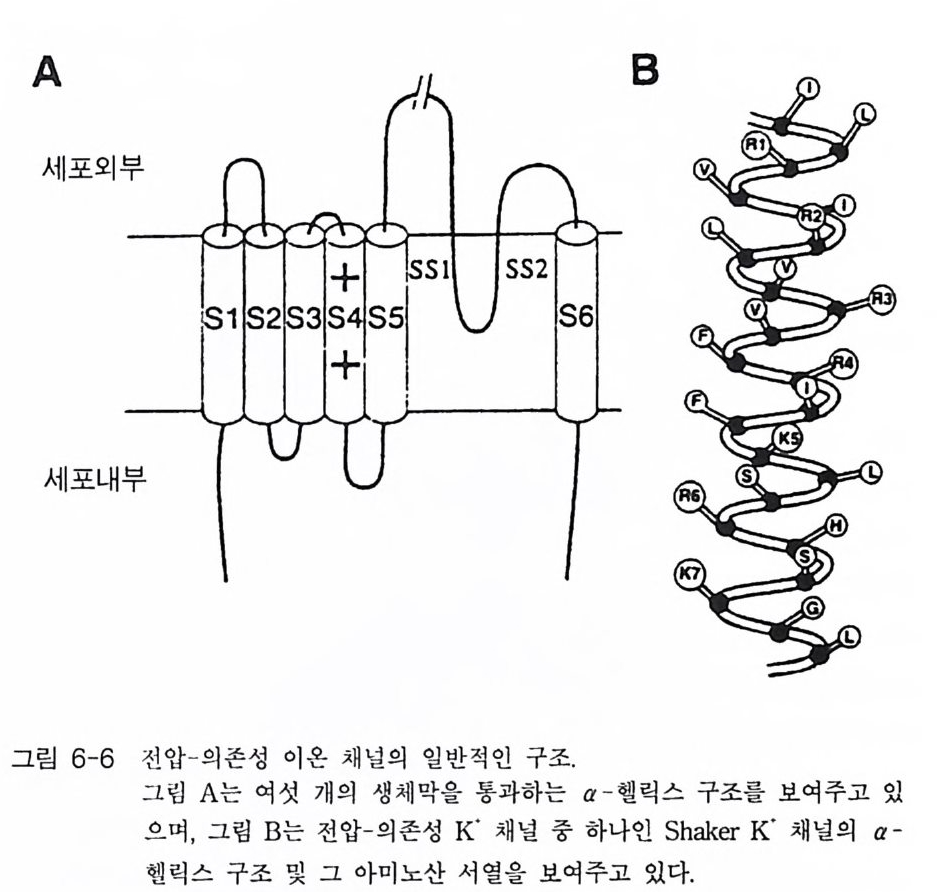 A B
A B
다음은 전압-의존성 이온 채널이 열리고 닫히는 데 관여하는 작용 기 작을 살펴보기로 한다. Na•, Ca2•, 그리고 K' 채널을 포함하는 전압-의 존성 이온 채널의 경우 공통적인 구조를 포함하는 6 개의 생체막을 통 과하는 a- 헬릭스 구조를 갖고 있으며 이들 a - 헬릭스 구조가 (S1 으로부 터 S6 까지, 그림 6-6 참조) 원통형의 통로를 형성하는 구조이다 (10, 11, 12). N갑 채널의 경우 6 개의 이들 a- 헬릭스 중 두 개 (S5 와 S6) 는 친수 성 단편으로서 전하를 띤 아미노산 잔기를 갖고 있으며, 또 다른 3 개 (Sl, S2, 와 S3) 는 비록 소수성 단편이지만 약간의 전하를 띤 아미노산 잔기를
 그림 6-7 전압-의존성 이온 채널의 중심부 를 생체막 의부에서 내려다 본 3 차 구조
그림 6-7 전압-의존성 이온 채널의 중심부 를 생체막 의부에서 내려다 본 3 차 구조
갖고 있 는 것으 로 밝혀 졌 다 03, 14). 반면 S4 는 양전하 를 띤 아미노산 잔 기뿐만 아니라 소수성 아미노산 잔기도 갖고 있다. Sl 과 S6 는 세포질 쪽 에 인산화 자리 를 갖 고 있으며 S5 의 세포 외부 쪽에는 글리코실화 반응 부위 간 가지고 있다 04, 15, 16). S5 와 S6 사이에는 아주 짧은 두 개의 단 선 , SSI 과 SS2 가 존 재하 는 데 이 들 은 생체막을 통과하는 것이 아니라 a - 헨릭스 미리핀 (a - h e l i cal hair pin) 구 조로서 양전하 를 띤 S4 와 소수성 딘편 사이에서 완 충 역 할을 하며 특 히 SS2 는 음전하 를 띠면서 채널을 동 과하 는 잉이온음 선택하 는 데 관여하 는 것으로 밝혀졌다(1 7). 앞에서 언 급 한 것처럼 이 둘 단편 들 이 원통형의 구조 를 형성하고 있는 데 이 들 구조 를 살펴보기 로 한다. 그림 6 - 7 에서 보는 바와 같이 비교적 소수성 단편 들 인 Sl, S2, S3 와 S5 는 원통의 외각을 형성하며 중앙에는 SSl 과 S6 가 서 로 상호작용하고 있고 가장 안쪽, 즉 이온들이 통과하는 구 명 부위에는 S 4 와 SS2 가 존 재한다. 그림 6 - 7 에서 S6n 이란 S6 단편의 - 말 단 부위가 위쪽으 로 노 출 되어 있음을 의미하며, 그림 6- 7 A의 S4h 란 S4 단편 중 양전하 를 띠지 않는 중간 부위를 의미하며 그림 6-7 B 의 S4c 는 양전하 를 띤 C - 말단 부위 를 의미하고 있다. 그 렇다면 이러한 구조를 가진 전압-의존성 이온 채널이 어떻게 열리 고 닫히는가에 대해서 살펴보기로 한다 . 먼저 그림 6-7 A 에서 보는 바 와 같이 S4 단편의 양전하 부위가 SSl 이나 S6n 의 음전하 부위에 상호 작용함으로써 S4h 가 구멍 쪽으로 모이면서 생체막과는 수직 형태를 유 지한댜 따라서 구멍의 지름이 비교적 좁은 상태를 유지하고 있다. 이온 채널이 열릴 때에 S4 단편의 a- 헬릭스가 회전되면서, 마치 S4 의 a- 헬 릭스가 막과 수직 상태에서 막 표면의 바깥쪽으로 이동하는 것처럼 되 면서 S4C 가 노출되 고, S4C 의 f3-구조가 SS2 의 f3 -구조와 상호 작용함 으로써 구멍의 크기가 증가하면서 이온 채널이 열리게 된다 (12) .
6-3 이온 채널 사실 1960 년대 중반까지는 이온 들 이 어떻게 세포막 을 통과하여 이 동 하는지에 대해서 잘 알려지지 않았다. 단지, 약리학 적 실험을 동해 서 어 떠한 이온들이 막을 통과하는지 또는 통과하지 못하는지릅 알게 되었다. 따라서 이온 채널의 분류 및 특 성을 이해하가 위해서 는 약품이나 독성 물질을 포함하는 약리 시약과의 관계를 먼저 이해하여야 한다. 1964 년 Narahasi(2 0) 등이 테트로도 독소(t e t rodo t ox i n, TI'X) 는 바다 가재의 거대 축색 돌기(l obs t er gian t axon) 에 존 재하 는 Na’ 체 널을 선택 적으로 억제하지만 K 채널에는 영향을 미치지 않는다는 사 실을 전압 크램프 실험을 통해서 처음 밝혔다 . 그 후 Hi lle 은 신경세포에서 TTX 에 의해 Na 令 채널은 억제되었지만 K 채널은 영향을 받지 않았다 는 결과 (21) 를 보고함으로써 확인하였고, TEA( t e tra e t hy larnmo ni um) 에 의 해 K 채널은 억제되었으나 Na 令 채널은 억제되지 않았다는 실험 결과를 보고 하였다 (22). 이 들 독소 이외 에 도, 또 다른 중요한 독소는 삭시 독소 (s axit o xi n) 인데, 이 STX 는 TTX 처럼 Na• 채널을 억제하는 것으로 나타 났다 (23, 24). 그 의에도 무기 양이온인 Cs t 나 Ba2t 또한 K 채널 을 억제 하며 프로카인(p roc ain e) 은 Na+ 채널을 억제하고 있다. 이들 시약의 작용 메커니즘은 이들이 이온 채널의 입구(이온 선택 필터)에 결합함으로써 이온 채널을 억제하는 것으로 여겨진다. 본 절에서는 Ca2+, K\ Na+, 그리고 er 채널에 관해서 알아보았는데 이들 이온 채널은 일반적으로 억제제의 종류 즉, 약리 시약에 의해서 분 류되며 이온의 이동 방향, 막 전위, 또는 이온 채널에 결합하는 리간드 에 의해서도 분류된다.
6-3-1 Ca2+ 채널 평상시 Ca2 ’ 채널은 닫혀 있는데, 외부 자극이나 신호에 의해 채널이 연리면 Ca 2 ’ 의 전기 화학적 기울기에 의해 채널을 통해서 초당 수 백만 개의 C 같이 세포 내로 들 어가게 된다 Ca 2 ♦ 채널은 일반적으로 원형질막 에 존 재하 는 데 세포 소기관의 막에도 존재한다. 이들의 역할은 세포 소 기관( 소포 체나 다 은 소기관)으로부터 Ca 2+ 을 세포질 내로 이동시키는 데 관여 하고 있다 (25, 26). Ca2’ 채널은 열리고 닫히는 매커니즘을 기초로 하여 크게 2 가지 유형 으로 나 눌 수 있는데, 전압 - 의존성 C 訖 채널과 수용체가 직접 작용하는 Ca2’ 채널이 그것이다(그림 6-8, 업). 전압-의존성 Ca2+ 채널은 생체막의 탈분극화에 반응하여 열리는데, 이들 채널의 전압 민감도, 운동 성질, 그 리고 약리 시약에 대한 민감도에 따라 다시 L- 형, T- 형, N- 형으로 구분 된다. 수용체가 직접 작용하는 Ca 안 채널 (rece pt or-ope ra ted Ca2• channel) 은 IP3 수용체 채널이나 리아노딘 수용체 채널처럼 수용체 의존성 기작 에 의해서 열리는 채널을 말한다. 전압 - 의존성 C 武 채널에 대해서는 지금까지 다양하게 연구되었는데 (28, 29, 30), 그림 6-8 에서 보는 바와 같이 L- 형은 높은 전압(― 2 - -10 mV) 에서 활성화되며, 비교적 천천히 반응하는 채널인데, 큰 전기 전도 력 (conduc tan ce, -25 p S) 을 갖는 특성이 있다. T- 형은 낮은 전압 (-7 - -70 mV) 에서 활성화되며, 일시적인 전류를 갖고 비교적 빠르게 반옹한 댜 이 유형의 채널은 적은 양의 전기 전도력(― 9 pS)을 갖는다 . 끝으로 N- 형은 비교적 높은 전압(> -30 mV) 과 T- 와 L- 형의 중간 정도에 해 당되는 일시적인 전류 (-15 pS)를 갖는다. 대부분의 세포는 하나, 또는 그 이상의 전압_의존성 Ca2• 채널을 갖고 있다. 예를 들면 감각 뉴런 (sensory neuron) 에는 T, N, 그리고 L- 형의 Ca 안 채널 모두를 갖고 있는 데 (29, 30, 31), 교감 신경세포 (s ymp a th e ti c neuron) 의 경우에는 T- 형은

존재하지 않고 L ― 과 N - 형만이 존재하는 것으로 알려졌다 (32). 결국 이 둘 각각의 유형 들 은 서로 다른 고유의 기능을 갖고 있는 것으로 알려져 있 는 데 (33, 34), 각기 다른 세포에 존재하는 이들 각 유형의 Ca 2 令 채널의 정확한 기능에 관해서는 좀더 많은 정보가 요구되는 실정이다. 수용체가 직접 작용하는 Ca 2 令 채널에는 크게 두 가지로 나눌 수 있는 데 그립 6 - 8 에서 보 는 바와 같이 리간드에 의해서 활성화된 수용체가 Ca2’ 채년을 열리게 하는 채널과 제 4 장 Ca 인 에서 살펴본 수용체 그 자 체가 Ca2’ 채 널 인 IP:i 수 용체나 리아노딘 수용체 채널을 들 수 있다. 후 자에 관해서 이미 언급한 관계로 여기서는 전자에 대해서만 언급하기로 한댜 이러한 유형의 채 널 에는 니코틴 아세틸콜린 수용체와 결합하고 있 는 Ca 언 뿐만 아니라 다 른 양이온들도 이동할 수 있는 비특이적 이온 채 널이 여기에 속한다 (35). 또 다른 예로서 ATP 수용체의 활성화에 의해 서 열리는 C 武 채널이 평활근 세포에서 발견되었다 (36). 비록 수용체가 직접 작용하는 Ca2` 채널에 비해서 정보가 부족하지만 현재 다양하게 연 구되고 있다. Ca2' 채널에 영향을 미치는 시약들은 크게 세 가지 계열로 나눌 수 있 는데, 1, 4-di hy d r op yridine (D H P) 유도체 계열, ph eny la lk yla m ine , 그리고 benzoth iaz epi ne 등이 댜 Nit ren d ipine , nimodipine , PN200-110 과 BayK 8644 등이 DHP 유도체에 속하며, verapa mil, D - 600 과 D-888 등은 p hen y lalk y l ami ne 에 속한다 . 이들 약리 시약들은 특별한 유형의 Ca 안 채 널들을 저해하고 있댜 DHP 유도체들은 오직 L- 형 Ca2 令 채널을 저해하 기 때문에 흔히 L- 형 채널은 dihy d r op yridine -sensiti ve ca2 ♦ 채널이라 일 컬어지기도 한댜 그러나 이들 시약들이 Ca2+ 채널을 저해만 하는 것이 아니라 때로는 활성화시키기도 하며 세포에 따라, Ca2+ 채널의 종류에 따라 그 작용 기작이 다르게 나타나는 것으로 알려졌다 (37). Ca2+ 채널을 조절하는 또 다른 시약으로서 (1)- cono t o xi n( (1) -CT) 을 들 수 있는데, (1)-C T 또한 L- 형을 조절하는데 DHP 와는 다른 자리를 갖고
있다 (38). (L) - CT 은 N- 형의 Ca2 ’ 채 널 에도 억제제 로 서 작용 하 는 데 요 도 화 형태의 (L) -CT 는 N- 채널의 분리와 생화학적 특 성 음 규명하는데 아주 중요한 도구로 사용되고 있다 (39) . 왜냐하면 L - 형 의 경우보다는 N - 형의 채널에 (L)- CT 결합 자리가 훨 씬 많이 있으며, 또한 N - 유형의 경우 (L)- CT 결합 자리가 다양하고 폭넓게 분포되어 있기 때 문 이다 (40). 이들 세 가지 유형의 C 武 채널이 각각 다 른 특 성 을 갖지 만 , 공몽적인 운동 성질을 갖고 있다. 이 들 모두 는 막의 탈분극화에 의해 환성화 되 는 데, 가장 높은 탈분극화가 일어날 때 이 들 채 널 이 최대로 열리게 된다 (4l). 그러나 Ca 안 채널은 탈분극화가 일어나자마자 열리는 것이 아니라 약간 지체된 후 나타나는데, 신경 세포에 있 는 T - 형 Ca2 ’ 채 널 의 열리고 닫히는 시간은 축색돌기에 있는 N 집 채널보다 최대 50 배 정도 느린 것 으로 나타났다 (41) . Ca 언 채널도 N 터이나 K ' - 채널처럼 막이 재분 극화 (repo la r iza ti on ), 즉 음 전위를 가질 때 닫힌다. Na' 채 널 과 마찬가지 로 Ca2+ 채널은 전압의 변화에 따라 닫힌 상태, 열린 상태, 그리고 바 활성화 상태로 구분된댜 그러나 Ca 안 채널이 단순히 전압의 변화에 영향 을 받 는 것만은 아니댜 막을 통과하는 Ca2• 전류에 의해서도 채 널 의 상태가 변화되는데, 세포 내부의 Ca2+ 농도가 높으면 높을수록 막을 통 과하 는 Ca2+ 전류는 적 어 진다 (42-44). 6-3- 2 Na+ 과 K+ 채널 본 절 앞부분에서 약리 시 약에 따라 구별되는 Na• 과 K+ 채널에 관해 서 간단히 언급하였다. 본 절에서는 이들 채널의 구조와 활성화 메커니 즘, 그리고 세포 내에 존재하는 이들 채널의 다양성에 관해서 언급하고 자 한다. l
몇 N 비 채널의 주요 소단위체 를 클로닝하기에 이르렀다. 이들 결과로부 터 전압 - 의 존 성 N터 또는 K 채널의 가상적 수송 메커니즘을 유추할 수 있 는 데, 그림 6 - 9 에서 작동 가설을 보여주고 있다. 채널은 막을 가로지 르는 단백질로서 세포 바깥 표면에는 많은 글리코실화 반응을 하는 자 리가 있으며 세포 내부 는 고정 (anchor) 단백질과 결합하고 있거나 세포 곱격 과 연건되어 있다. 이온 들 이 막을 통과할 수 있는 물로 채워진 통로 로 이 부 어져 있으며, 이 들 채널의 기능 부위로서 이온을 선택할 수 있는 필 터, 통로, 그 리고 감지기가 촌재한다(그림 6-9 참조). Na’ 과 I( 채 널 이 구조적인 면에서 비슷함에도 불구하고, 서로 다른 전압 의 존 성 방식을 보여주고 있는데, 대부분의 세포에서 N타 채널의 열 림은 -8 0mV 로부터 —4 0 mV 사이에서 탈분극화에 의해서 유도되는 데 반해 K 채널의 열림을 위한 전위 범위는 -100 mV 로부터 +50 mV 이 다 (2) . 전압 - 의 존성 K 채널은 N 집 채널에 비해서 다양성을 가지고 있는 데, 대부분의 경우 막의 탈분국화에 의하여 열리는 데 반해, 몇몇의 경우 과 분국화 에 의해서 열린다. 표 6-1 에서 다양한 그 채널을 저해하는 시약 등을 보여주고 있다.
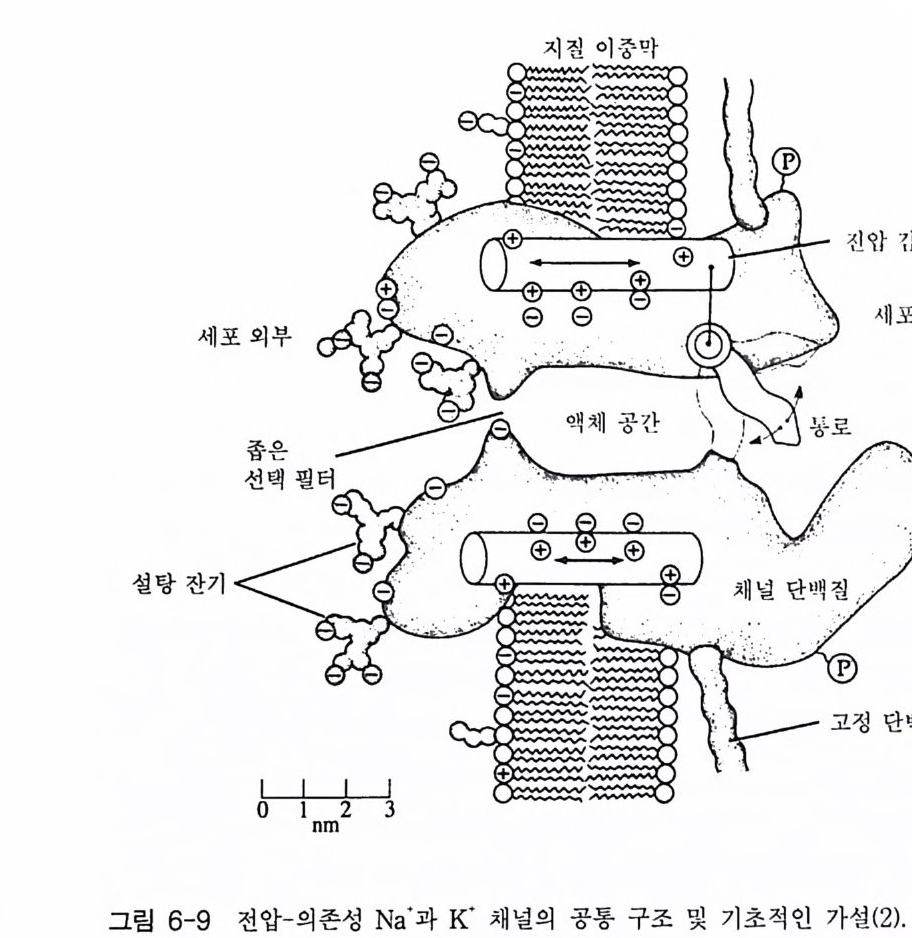 지질 이 중 막
지질 이 중 막
Ca 2• - 의존성 K 채널의 활성화는 A 채널과는 달리 상당히 길 고 많은 양 의 K 전류가 흐른다 (49). 이외에도 다양한 K 채널이 존재하고 있는데 반해 Na• 채널은 K' 채 널과 비교하여 그리 다양하지 못하다. TTX 에 빠르게 반응하는 Na• 채 널과 느리게 반응하는 N 깊 채널이 존재하며 (50), 비교적 빠르게 반응하 는 채널과 느리게 반응하는 채널이 있다 (51) . 일반적으로 Na• 채널은 0 rnV 에서 거의 95 % 이상 비활성화되는데, 오징어 거대 축색돌기에 존재
표 6-1 K 채널의 억재재 (2) 들 약자 ; TEA, tel raeth y la mmoniu m QA, qu ar tem a ry ammoniu m ion s relate d to TEA Pota s s iu m Membrane- cha n n e l Acti ng from outs id e Acti ng from ins i d e perm eant Delay ed TEA TEA and QA 4-A mino p yridine re'Ct ifier Cs \ H', B a2· cs·, Na·, Li, Ba2· Str ych n ine Cap sa i c in (f ~ ) Quini d ine Dendroto x in s (J i ) Noxiu s t o x in A TEA TEA 4-A rnino p yridine De nc lroto x in s Quinid ine ? K(Cal TEA(I 3K J TEA Quinid ine cs· Na·, Ba2· Ap amin( SK) Cha ryb doto x j n( B K J Inward TEA H·, r v1 g2 · ? rec ti fi er cs·, R b. Na· K(ATP) BTaE2A· ’ Sr2· TEA Tolbuta mide Cs\ Ba2· Na', l\1g2· Gli be nclam ide Quinidine 하는 한 Na• 채널은 +80mV 에서도 Na• 전기 전도력이 남아 있다 (52). N 검 채널의 이온 선택성은 K 채널의 선택성에 비해 특이성이 적은데, 작은 금속 이온의 선택 순서는 Na' ::::: Li' > Ti ' > K+ > Rb+ > Cs • 이 댜 또한 hy dr oxy la mmon iur n, hy dr azin iur n, ammo ni um 과 같은 비메틸화 유기 양이온도 Na+ 채널을 통과할 수 있는데 이는 최소 구멍의 크기가 3 A x 5 A( 채널의 이온 선택 필터)임을 암시하고 있다 (53). 메틸암모늄 과 같은 메틸화 유기 양이온은 Na+ 채널을 통해서 막을 통과할 수 없다 는 사실 또한 이를 뒷받침하고 있다.
지 금 까지 생체막 생화 학 자나 전기 생리학자 들 의 가 장 풀 리 지 않은 의 문 중의 하나 는 < 왜 K · 보다 크기가 작은 N a 이 K 채 널을 봉 과 한 수 없느냐 > 하는 것이었다 . 최 근 에 발 표 된 두 개의 논문 이 이 의 문점 에 대 한 실 마리 를 제공하고 있다 ( 54, 55). N 집의 지 름 이 약 1.9 A 이며 K 의 지 름 은 2.7 A 이다. Toney( 5 4) 등은 I( - 특 이적 결합 자리 를 갖고 있 는 단 백 질 인 dialk y lg ly c in e decarbox y las e (D GD) 을 통 해서 K 또 는 Na’ 과의 상호작용에 따 른 구조 를 규명하였다. DGD 의 K 전합 자리 는 3 개의 카 르보닐기 (O = C), 1 개의 카 르 복실기 (O - C - A s p - 0) , 1 개의 히 드록 실 기 ( 0 —S er), 그리고 물분자의 산소와 함 께 6 개의 산 소로 구 성 됨 으 로 서 K ’ 과 배위 결합을 형성하는데 이는 I( - 선택성 i on o p hor e 인 va li nom y c i n e 의 구 조와 비슷하다 (v ali nom y c i ne 의 경우 , 6 개의 산 소 와 K 이 배위 결합을 형 성 하고 있음). 이때 이 결합 자리는 8 면체 구조를 이 루 고 있다 . D G D 의 K' 결합 자리는 매우 높은 K 선택성을 갖 고 있는데 , 예 를 들 어 용 액에 7.5 mM K 따 75mM Na • 이 있음에도 불구하고 K 만이 선택 적 으 로 결합된 다. 만약 이 용액의 K 을 제거하면 DGD 의 결합 자리에 어떤 변화가 생 길 것인가? Toney (5 4) 등의 결과에 의하면 용액에 K • 을 제거하 였을 때 , DGD 의 결합 자리가 형성하는 8 면체 구조가 정확하게 0.8 A 줄 어 둘면 서 삼각-양추(trig onal- bip yramida l) 구조로 바뀌 게 된다. 따라서 K 에 비 해 서 0.8 A 작은 Na 이 팔면체 구조를 통과할 수 있지만 그 구 조 가 바뀜 에 따라 결합 자리에 밀접하게 결합함으로서 통과할 수 없게 된다. 비 록 이러한 구조 변화가 K 채널의 구조 를 통해서 연구된 것은 아니지만 K• 채널과 Na+ 채널 사이에서, 그리고 이들 채널의 이온 선택성을 이해하는 데 실마리를 제공해 주고 있는 것은 사실이다. 6-3- 3 er 채널 생체 내에서 가장 널리 생리학적으로 이용되는 이온이 Cl - 이다 . 동물
세포에서 세 포질 내의 C 「 농도는 항상 세포 외부의 Cl~ 농도보다 낮은 데(포유 동물 의 골격근 의 경우 세포 외부의 Cl~ 농도는 123mM, 세포질 내 의 Cl- 농 도는 4.2m ivI), 평형 전위는 거의 휴지 전위와 일치한다 (-90 mV). Cl 의 중 요한 역할은 pH 조절, 세포 부피의 조절, 그리고 분비샘으 로부 터 분 비액을 생산하는 데 관여하는 것으로 알려져 있다 . Cl 채널은 크 게 네 가지 로 구분할 수 있는데 리간드에 의해 열리는 채 널로 서 r - 아미 노부 티 르 산( r-a m ino buty ric acid , GABA) 이 리간드로 작용하는 GABA - 의존성 채 널 (GABA- g a t ed channel), 분비성 (secre t o ry) 의 CI 채널로서 CFTR( 소낭 섬유증 막 통과 전기 전도력 조절자, cys t ic fibr osis tra nsmembrane conducta n ce reg u lato r , )과 Ca 2+ 에 의해 활성화되 는 er 체널, 그리고 전압-의존성 er 채널이 있다. 이들 중에서 GABA- 의 존성 채 널, CFTR 과 Ca 2 에 의 해 활성 화되 는 er 채 널 (Ca2 - -ac ti va t ed er chann e l) 에 관해서 간단히 알아보기로 한다. 앞에서 살펴본 아세틸콜린과 같은 신경 전달 물질은 이들이 수용체에 결합 하여 양이온 채널을 열어 줌으로써 신경 물질 전달에 관여하는 데 비해서, GABA 는 수용체에 결합함으로써 수용체와 연결되어 있는 er 채널을 열어 주게 되고, 따라서 Cl - 이 세포 내부에 들어오게 됨으로써 신경 전달 물질의 전달 반응을 저해하는 데 관여한다. 이 GABA 수용체 채널의 구조는 다른 리간드-의존성 수용체안 아세틸콜린 수용체와 비슷 한 것으로 알려져 있다. GABA 수용체는 대뇌 피질로부터 분리 정제되 어졌는데, 아미노산 서열이 거의 비슷한 3 개 또는 4 개의 소단위체 유형 으로 구성된 중합체이다 (5b, 5f) . a, fJ, 그리고 r- 소단위체로 구성된 GABA 수용체의 각 소단위체는 GABA 결합 자리를 갖고 있으며, GABA 수용체의 활성 기작 역시 아세틸콜린 수용체에서 보여준 활성화 기작과 비슷한 것으로 알려져 있다. 소낭 섬유증 (c y s ti c fibr osis , CF) 은 신경 과학자의 관심을 끌기에 충분 한데, 왜냐하면 질병과 관련된 이온 채널과 연결되어 있기 때문이다. 소
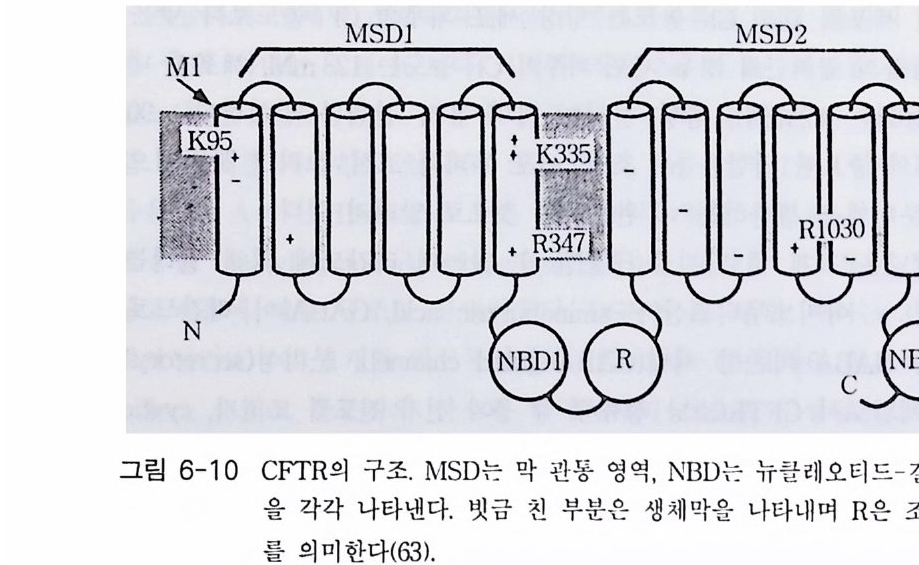 I MS D 1 \ / MS D 2 \
I MS D 1 \ / MS D 2 \
낭 섬유증은 췌장 , 침샘 , 기공 점 액, 그리고 땀 샘 분비성 코일과 같은 몇 몇 상피 조직의 분비 기능을 손상시키 는 것 으 로 알려져 있다 . 최 근 에 CFrR 을 만드는 유전자가 발견되었으며 (58), 그 리고 소 낭 섬 유 증 관련 돌연변이체만도 200 개가 넘는 것으로 보고되었다 (59). CFrR 은 그림 6-10 에서 보여주는 바와 같이 두 개의 막 관통 부 위 (MSDl 과 MSD2) 를 갖고 있다 이 들 각각은 6 개의 막 통 과 단 편 (Ml -M12) 으로 구성되어 있다. 또한 이들 각각은 뉴 클 레오티드 결 합 자리 (NBDl 과 NBD2) 를 갖고 있으며 MSDl 과 MSD2 의 연결 루 프 부분에 하 나의 조절 부위(R)를 갖고 있다. 이 CFrR 이 er 채널이기도 하다. 이 CFrR 이 Cl- 채 널이라는 사실은 정상 세포에서는 CFrR 이 존재하지 않 는 NIH3T3, CHO 세포, 그리고 개구리 난세포 등에 CFrR 유전자를 넣 어 줌으로써 cAMP 에 의 해 활성 화되 는 Cl - 의 이 동을 확인함으로써 밝혀 졌다 (60, 61, 62). 이 CFrR 의 돌연변이가 소낭 섬유층의 원인이 되며 궁 극적으로 관련 질병을 유발하게 되는데, 이들 돌연변이체는 크게 4 가지
로 구분된댜 유전자 결합 에 의해 이 CFrR 자체에 결 합이 생기는 경우, 생성된 CFrR 이 소포체에서 골지체로 진행되는 과정에 결함이 생기는 경우, N BDl 이나 NB D2 의 돌 연변이에 따 른 ATP 결합이 불가능하게 되 면서 조전 기능이 상실되는 경 우, 그리고 막의 구멍을 이루고 있는 아미 노산의 듄연변 이에 따른 Cl 의 이동이 불가능한 경우 등에 의해서 주로 소낭 심유증의 원인이 되 는 것으로 알려졌다 (63). 이 듈 중 Cl 의 이 동과 직접 관련이 있는 조절 결함과 전기 전도력 결 함을 내 포 하 는 돌연변 이체 를 통해 C 「 이동 기작을 알아보기로 한다. 조 절기능에 결함 이 있는 경우는 다시 두 가지로 나누어서 생각할 수 있는 데 , ATP 가 결합 하 는 NBDl 이나 NBD2 의 돌 연변이에 의한 경우 조절 부 위 (R)의 결합 에 의해 인산화가 불가능한 경우이다. 먼저 NBDl 의 551 번째 아미 노산 굴리신 이 아스파라진이나 세린으로 바뀐 돌연변이는 혼치 않댜 NBD2 의 1244 번째 굴 리신이 글루 타민산으로, 세린 1255 가 프롤린으 로 또는 글 리신 1349 가 아스파라진 등으로 돌연변이되는 경우인데 이것 도 혼치는 않다. 이 들 돌연변이체들은 ATP 가 결합 자리에 결합할 수 없 기 때문에 cvrR er 채널을 열어 주지 못하게 됨으로써 Cl - 의 이동이 어 립 게 된다. 또 다른 돌연변이로서 조절 부위의 결함에 의해 유도되는 경우를 들 수 있는데, 조절 부위의 돌연변이체가 보고되었으나, 다른 부 위의 돌연변이에 비해서 크게 치명적이지 못한데 이는 인산화의 한 기능 이 소낭 섬유증을 유도하는 데 충분하지 않음을 시사해 주고 있다. CFrR 의 구멍 부위 죽 , MSD 의 돌연변이에 의한 Cl - 의 이동이 억제됨 으로써 소낭 섬유증을 유도하는 경우안데, MSDl 의 117 번째의 아르기닌 이 히스티딘으로, 334 번째의 아르기닌이 트립토판으로 , 그리고 347 번째 의 아르기닌이 프롤린으로 바뀐 경우가 보고되었다 (59) . cAMP 의존성 인산화 기능과 ATP 결합이 정상이면서 단지 이들 돌연변이체의 er 이 동 양을 측정 해 보면 R 347 P > R 117 H > R 334 W 순으로 나타났다. 이는 CFrR 의 구멍을 구성하는 양전하의 아르기닌이 Cl- 의 이동에 관여
하고 있음을 시사해 주고 있다 (64). 기 금 까지 돌 연변이체 를 봉 해서 CFTR er 채널에 대해서 살펴보았는데 , 간략하게 이 채 널 의 기작을 정 리해 보면, ATP 의 결합에 의해 활 성화되면 CFTR er 채 널 이 열 리게 되 며, cAMP 의 생성이 유도되고 이것에 의해 채 널 이 조절 되 는 것 으 로 여 겨진댜 그러나 아직까지 그 정확한 기작은 밝혀지지 않 고 있다 . 끝으로 Ca 2 t -의존성 er 채널에 대해서 알아보기 로 하 겠 다 . C a2’ 에 의 해 활성화되는 er 채널은 간상 세포 광수용체와 개구리 난세포에서 처 음 보고되었는데 (65 , 66), 그 후 많은 신경세 포, 분 비 세 포, 근육 세 포 등 다양한 세포에서 그 존재가 확인되었다 (67 - 69). 이 채널은 CI . 뿐만 아니 라 많은 작은 분자의 음이온도 폭넓게 통과시키며 Ca 2 t 의 증가에 의해서 뿐만 아니라 탈분극화에 의해서도 열려지는 것 으로 밝혀 졌 다 (68). 이 채 널은 또한 전압 의존성은 약한 반면 Ca2‘ 결합에 의해서는 강하게 작용 하지만 다른 전압-의존성 채널인 Na', K' , 그 리고 Ca2’ 채널에 비해서 는 약한 것으로 알려졌다 . 최근에는 개구리 난세포에 있는 이 Ca 양 에 의해 활 성화되 는 er 채널 은 니플름산(niflumi c ac i d) 이나 플루페남산(fl u f en ami c ac i d) 에 의해서 억 제 되 고 있음이 밝혀 졌다 (70). 또한 포스파틱산이 나 라이소포스파틱 산에 의해서 이 채널이 활성화되며, 세포 바깥에 Ca 양 이 존재하지 않더라도 이들 지질에 의해서 활성화되지만 Ca2• 킬레이터인 BAPTA(bis ( o- amino -p h enocy ) -eth a ne N, N, N', N'-te t r aa ceti c ac i d) 를 세포 내에 넣 어 주었을 때는 이들 지질에 의해서 이 채널이 활성화되지 않음을 보여 주었다 (71). 이는 이들 지질에 의해서 활성화되는 er 채널은 세포 외부 의 Ca2• 유입에 의해 활성화되는 것이 아니라 Ca2• 저장고의 Ca2• 동원 에 의해서 활성화되고 있음을 시사해 준다. 개구리 난세포에 존재하는 이 er 채널의 cDNA 가 최근 밝혀졌는데 13 개의 막 관통 부위를 가진 805 아미노산으로 구성되어 있는 것으로 알려지고 있으며 이 채널의 연 구가 다양하게 이루어지고 있다 (72).
6-4 신호 전달 기작 앞에서 살펴본 여러 장을 통해서 이미 언급한 것처럼 외부 신호가 그 수용체에 결합 하면 세포막 효소에 의해 제 2 의 전령이 생성되고 그 다 음 세 포 반옹이 일어나는 경로로 신호가 전달된다 . 이때 수용체와 막 효 소를 연결하는 단백질이 G- 단백질이댜 여기에 관여하는 G - 단백질은 3 개의 소단위체 (a, B, Y) 로 구성되는데, 이들의 목적은 아데닐레이트 시 클라제 와 같은 세 포 막 효소를 활 성화시키는 것이다. G- 단백질은 이종 삼량체 로 구 성된 큰 G - 단백질과 큰 G - 단백질의 a 소단위체와 동질성 을 갖고 있 는 하나의 폴 리펩티 드로 되어 있는 작은 G- 단백질이 있다 . 최근에 이 들 G ― 단백질들이 세포막 효소에 관여할 뿐 아니라 이온 채널 도 조절하고 있는 것으로 알려졌다. 따라서 저자는 G- 단백질을 중심으 로 어떻게 이온 채 널 이 조절되고 있는지에 관해서 알아보고자 한다. 6-4- 1 작은 G- 단백질에 의한 이온 채널의 조절 Ras p 21 으로 대표되는 작은 G- 단백질은 자체가 GTPase 활성도를 갖 는 데, 큰 G - 단백질과 마찬가지로 GTP 가 결합되면 활성화되며, 활성화된 ras 가 Ra f 를 활성화시키고 활성화된 Raf는 MEK(MAP 키나제)를 인산화 시킴으로써 활성화시키며, 이 활성화된 MEK 에 의해서 MAP 키나제 [유 사 분열 인자(mit o g en) 에 의해 활성화되는 단백질 키나제]가 안산화됨으로 써 활성화되어 이 효소가 핵 내의 전사 요소들을 활성화시킨다. 따라서 ras 와 같은 작은 G- 단백질에 의한 신호 전달 기작은 종양 유전자의 생 성, 변형 등과 같은 성장 인자와 관련되어 있는 세포 반응에 많이 관계 하는 것으로 알려져 있다. 최근에 이 Ras G- 단백질에 의해서 채널이 조 절되고 있음이 밝혀졌다. 아세틸콜린에 의해 활성화되는 K+ 채널이 ros p2 1 단백질에 의해 억제되고 있음이 보고되었다 (73) . 이 억제 효과는 ros
뿐만 아니라 GTPase 를 활성화시키는 단백질 (GAP) 을 동 시에 필 요로 하 는데, 비가수분해 G- 단백질 활성 인자인 GTPrS 가 이 채 널을 활 성화시 키고 있을 때에는 억제 효과가 없었다. 이 채널의 활성화는 아세틸 콜린 이 그 수용체에 결합하면 큰 G - 단백질이 활성화되어 이루어지 는 데 , 이 반응을 억제하는 데 관여하는 ras 및 GAP 는 아마도 수용체와 큰 G - 단 백질 사이에서 작용할 것으로 여겨진다. 그러나 이러한 전 과가 어떠한 생리학적 의미를 지니고 있는지에 대해서는 아직까지 밝혀지지 않고 있 다. 현재로서는 ras-GAP 에 의해서 K 채널이 조절되고 있는 점뿐만 아 니라 서로 다른 G- 단백질(큰 것과 작은 것)에 의해서 이루어지는 경로가 서로 작용하고 있다는 사실은 매우 홍미로운 일아다. 최근에는 생체막의 탈분극화와 Ca2’ 유입 (L- 형의 Ca 2 令 채널)에 의해서 MAP 키나제 경로를 활성화시키고 있음이 밝혀졌다 (76). 일반적으로 PC12 세포에서 ras 의 활성화는 NGF( 신경 성장 인자, nerve gro w th fa c t or) 에 의해서 이루어지는 것으로 알려져 있는데, 생체막의 탈분극화 에 따른 L- 형의 Ca2+ 채널의 활성화에 의해서도 ras 가 활성화되고 있음 을 의미한다. 그러나 Ca2+ 유입에 의한 ras 활성화는 NGF 에 의해 활 성 화되는 경로와는 구분되는 것으로 알려졌다. 왜냐하면 L - 형의 채널 억 제제인 nifedipin e 이나 EGTA 에 의해서 M 사) 키나제의 활성도나 MEK 의 활성도, 그리고 ras 의 활성도가 억제되었는 데 비해 NGF 에 의해 활성화 된 이들 활성도를 이들 시약은 억제하지 못했다 (76). 아직까지 그 기작은 명확하지 않지만 Ca2+ 유입이 GEF( 구아닌 뉴클레오티드 교환 인자, gu a- nine nucleoti de exchang e fa c to r) 를 활성 화시 킴 으로써 ras 의 GDP 를 GTP 로 바꿔 주는 단계에 관여하거나 GAP 를 억제하는 반응에 관여할 것으 로 여겨진다. 비록 그 기작은 아직 확실하지 않지만, L- 형의 Ca2+ 채널 에 의해서 MAP 키나제 경로가 활성화되고 있음은 앞에서 살펴본 이온 채널에 의해서 ras 의 활성화가 억제되고 있는 결과와 함께 의의가 있으 며 앞으로 계속되는 연구가 채널과 ras 에 의한 MAP 키나제 경로와의
관계 를 명 확 히 밝혀 줄 것 으 로 기 대된다 .
6-4-2 이종 삼량체의 G_ 단백질 (he t ero t r i mer i c G- p ro t e i n) 에 의한 이온 채널의 조절
다양 한 G ― 단백 질둘 이 다양한 경로 를 통하여 이온 채널을 조 절 한다는 사 실 이 밝 혀 진 바 있다. 또 한 이러한 다양한 경로의 존 재가 당연한 것으 로 여 겨지는 것은 무 리가 아니다. 왜냐하면 지금까지 밝혀진 바에 의하 면 최소 한 40 개의 다 른 활 성제 , 70 개의 수용체, 15 개의 서로 다른 G- 단 백 질 , 약 100 여 개의 단백 질 키나제, 그리고 수백 개의 이온 채널이 존재 함이 밝 혀 졌 는데 (77) , 하나의 수 용체가 한 개 이상의 G- 단백질과 작용하 고 , 하나의 G - 단백 질 이 서 로 다 른 이온 채널과 작용하기도(예 를 들어 Gs 는 Ca 2’ 채널 뿐만 아니라 Na· 채널 도 조절한다) 한다. G - 단백 질 은 간접적으로 이온 채널을 조절할 뿐 아니라 직접 이온 채 널을 조절 하기도 한댜 전압 - 의 존 성 Ca2+ 채널이 G- 단백질에 의해서 직 접 조절 되고 있음이 보고되었다 (74). 또한 G - 단백질에 의해 활성화된 포 스포 리파제 A 에 의해 생성된 아라키돈산 (arac hi do ni c ac i d) 에 의해서 이 온 채 널 이 조절되는 간접적인 경우도 있다 (75). 그림 6 - 11 에서 보는 바 와 같 이 G - 단백질에 의한 이온 채널의 조절에 관여하는 경로를 크게 4 가지로 나누어 생각할 수 있다. 먼저, G- 단백질이 직접 이온 채널을 조 절하는 경로를 고려할 수 있을 것이다(® 一 @ - @). 두번째로 G- 단 백질이 생체막에 존재하는 효소(예 를 들어 아데닐레이트 시클라제, . 포스포 리파제 C) 를 활성화시킴으로써 생성된 제 2 의 전령에 의해서 이온 채널 이 조절되는 경우이다(® 一 ® 一 ® 一 @ -@ ). 다음으로 고려될 수 있는 경로는 앞에서 언급한 아라키돈산에 의해 조절되는 경우처럼 G- 단 백질에 의해 활성화된 효소가 제 2 의 전령을 생성하고 다시 제 3 의 전 령이 생성됨으로써 이에 의해 이온 채널이 조절되는 경우이다(® 一 ®
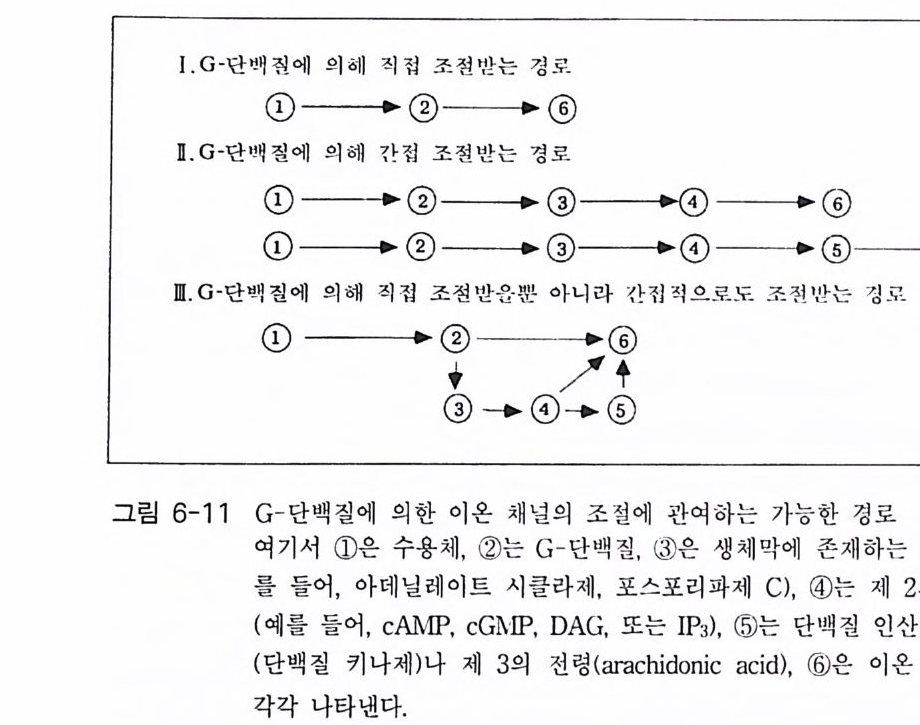 I. G- 단백질에 의해 직접 조전받는 경로
I. G- 단백질에 의해 직접 조전받는 경로
一 ® 一 ® 국 5 一 ®). 끝으로 G- 단백질이 직접 또는 간접적인 경로와 함께 이온 채널을 조절하는 경우가 있다(® 一 @ 一 ®과 ® 一 @ 一 ® 一 @ 一 ® 一 ® 또는 CD - @ - ® - @ - @). 앞에서 언급한 것처럼 G- 단백질과 이온 채널의 조절에 관여하는 경로 는 매우 다양하고 복잡하기 때문에 이들 네 가지 경우로 나누어서 G - 단 백질에 의해 조절되는 이온 채널에 관여하는 신호 전달 경로를 살펴보 기로한댜 G- 단백질에 의해 직접 조절되는 이온 채널의 대표적인 예로서 아세틸 콜린 수용체에 의해 활성화된 G- 단백질(G. 또는 G) 에 의해 조절되는 K 채널을 들 수 있다 (78). 척추동물의 심장 세포에 있는 Ca2+ 채널의 경 우도 G- 단백질에 의해 직접 활성화된다 (78). 이외에도 G- 단백질에 의해
직접 이온 채 널 이 조절 되 는 경우 는 신경 세 포, 근 육 세포뿐만 아니라 많 은 세 포 에서 발견 되었다 ( 8 0) . 이 들 의 확 인은 재구성 실험 방법에 의해 수행되 는 데, 즉 분 리 정 제한 G - 단백 질 또는 a - 소단위체와 이온 채널을 지 진 이 중구조 를 가 진 인공막이나 분리한 막에 넣은 후, G- 단백질과 이 온 채 널 과의 상 호작 용 을 알아 볼 수 있다. 제 2 의 전령융 통 해 간 접 적으 로 G - 단백질의 영향을 받는 이온 채널로 서 망막 세 포 ( r e ti n a l c e ll) 에 있 는 양이온 채널이 대표적인 경우이다. 광 수용 체인 로돔신은 광 자에 의해 활 성화되는데 이 활 성화된 로돕신은 G- 단백 질 (G1) 을 활 성화시키며, 활 성화된 G t 는 포 스포디에스터라제 (PDE) 를 활 성화시켜 세 포질 내 c G MP의 양을 조 절 함으로써 Na+ 채널을 조절하는 것 이다 ( 8 1) . 또다 른 예 로 서 노르 에피네프린 (nore pi ne phri ne) 은 8 - 아드레 너 직 수용체에 결 합하는데, 이때 G- 단백질 (G s ) 이 활성화된다. 이 G s 의 a 소단 위체 는 아데 닐 레이트 시 클 라제를 활성화시키며 cAMP 를 생성하 면 Ca 언 채 널을 조 절 하게 된다 ( 81) . 또 다른 G- 단백질에 의해 조절되는 이 온 채 널로 서 앞에서 언급한 PLA 2 에 의해 생성된 아라키돈산에 의해 활 성화되 는 경우이다 . 만약 제 2 의 전령인 cAlvIP, cGMP, 또는 다른 물 질 이 단백질 키나제 를 조절함으로써 이온 수송을 조절하는 경우도 여기 에 해 당된다 (81, 82). 끝으로 단백질에 의해 직접 이온 채널이 조절될 뿐만 아니라 제 2 의 전령이나 제 3 의 전령에 의해서도 동시에 조절 받는 경우가 있다. B- 아들레날린 수용체에 의해 활 성화되는 G s 는 직접 Ca2+ 채널(8.3)과 Na+ 채널 (84) 을 조절하는데, 동시에 G s 에 의해 활성화된 아데닐레이트 시클 라제에 의해 생성된 제 2 의 전령 (cAMP) 이나 제 3 의 전령에 의해서도 이돌 채널들이 조절되고 있다. 무스카린 수용체는 G i나 Go 와 결합함으로 써 심장 세포의 이온 채널을 직접 조절할 뿐만 아니라 cAMP 및 PKA 로 이어지는 경로에 의해서도 조절되고 있다(8.5).
6-4- 3 G- 단백질의 /3, y 소단위체에 의한 이온 채널의 조절 Log o th e ti s( 86) 등은 소의 대뇌 피질로부터 분리 정제한 G - 단백질을 병 아리 배의 심방 세포 (c hi ck embry o nic atr ial cell) 에 접맥시켜 무스카린 에 의해 활성화되는 K 채널을 확인하였는데, 이때 G - 단백질의 a 三 소단 위체 에 의해 활성화된 것이 아니라 B y 소단위체가 아세 틸콜린 에 의해 활성 화되는 K 채널을 간접 적으로 조절하고 있음이 보고되었다 (87). 이 는 f3 r 소단위체에 의해서 PL A.z가 활성화되는데 활성화된 PLA 哀근 아라키돈 산을 생성하며 이 아라키돈산은 리폭시게나제Oipo x yg enase) 에 의해 HETE 유도체가 만들어지거나, 시클로옥시게나제 (c y cloox yg enas e) 에 의 해 HEPE 유도체 또는 프로스타클란딘(p ros t a g lan di n) 을 생성하게 된다. 시클로옥시게나제에 의해 생성된 프로스타글란딘은 이 K+ 채널에 아무 런 영향을 미치지 않았지만 리폭시게나제에 의해 생성된 HETE 유도체 에 의해서 K 채널이 활성화되고 있음을 보여주었댜 이외에도 /3 r 소 단위체에 의해서 이온 채널이 조절 되고 있음이 여러 세포에서 발견되 었다 (75, 88, 89). 일반적으로 B r 소단위체의 이온 채널에 대한 역할에 대해서는 아직 불확실한 상태로 남아 있다. 왜냐하면, 비록 8 r 소단위 체에 의해 PLA2 의 대사 물질인 HETE 유도체에 의해 K 채널이 조절되 었지만, 무스카린이나 다른 활성제에 유도되는 K+ 채널을 조절하는 반응 에는 아무런 영향을 미치지 못했다. 6-4- 4 Ga 소단위체와 이온 채널과의 작용 기작 S盧 e r K• 채널의 N- 말단(세포질 부위)으로부터 20 개의 아미노산이 열려져 있는 K 채널을 비활성화시키는 것으로 알려져 있는데, 죽 이 20 개의 아미노산으로 구성된 펩티드가 K+ 채널의 구멍과 작용함으로써 K+ 채널이 닫히는 것으로 생각된다 (90). 심방 세포의 무스카린 K 채널은
활성화된 G - 단백질 (G aK) 에 의해 열리는 것으로 알려져 있다. 만약 앞에 서 살펴본 20 개의 아미노산으로 구성된 펩티드(비활성 펩티드)가 채널을 닫히게 하는 역할을 한다면, 이 비활성 펩티드가 제거되었을 때 K 채널 은 열린 상태 를 유지할 것 이다 . 이러한 가정 아래 Ki rsch 와 Brown(91) 은 트립신을 사용하여 K' 채널을 활성화시켰댜 그러나 열에 의해 변성된 트립신 이나 트립 신 억제제 를 동시에 넣어 주었을 때에는 그 활성화 효 과가 없었다. 트립 신 또한 G - 단백질에 의한 K 채널 활성을 억제하였댜 트립신은 단백질의 시스테인이나 아 르 기닌 잔기를 끊어주는데, 아르기닌 과 특 이하게 반응하 는 시약인 글리옥살(g l y oxal) 이나 페닐글리옥살(p he n y l g l y oxal) 은 K' 체 널을 활 성화시키지 못했댜 이 실험 결과는 G- 단백 질과 이온 채 널 의 작용 메커니즘에 대해서 간접적으로 설명하고 있다. 즉, G a K 가 존 재하지 않을 때 이 채널이 닫혀져 있는데, 이때 비활성 펩 티 드가 이 채널의 구멍 영역과 작용하고 있다. 그러나 활성화된 GaK 가 이 비 활성 펩티드와 작용하거나 또는 비활성 펩티드가 채널의 구멍 영 역과 작용하는 것을 억제함으로써 채널을 활성화시키는 것으로 여겨진 댜 아울러 세포의 내부에 촌재하며 트립신에 의해 끊어질 수 있는 리신 이 존 재하는 (Shaker K. 채널의 경우 10 번째 Ly s) 부위가 채널을 억제하 며 동시에 G- 단백질과 작용할 가능성을 시사해 준다. 그 동안 이온 채널의 중요성에 비해서 연구가 활발히 진행되지 못한 것은 사실이다. 그러나 최근에 상당히 많은 생명 과학 분야에서 다각도 로 연구되고 있다. 채널의 활동 메커니즘에서부터 그것을 조절하는 전달 메커니즘에 이르기까지 많은 결과들이 발표되고 있다 . 최근에는 종양 유 전자 생성으로 대표되는 MAP 키나제 경로도 채널과 상호작용하고 있음 이 보고되었다. 그러나 많은 연구들이 전기 생리학 측면에서, 그리고 그 조절 경로를 밝히는 신호 전달 체계에 집중되고 있다. 생리학적 또는 생 화학적인 측면에서 여러 연구가 진행되고 있음에도 불구하고 아직까지 는 채널의 열리고 닫히는 정확한 기작이 불확실하며, 이온 채널을 조절
하는 경로 각 단계에 존재하는 단백질이나 여러 요인 들 의 생화학적 규 명도 앞으로 해결되어야 할 과제라 여겨진다. 그러나 채널의 다양성이나 조절 기작의 복잡성을 고려해 볼 때, 진행되고 있는 연구에 대해 희망적 이라 하지 않을 수 없다. 채널 단백질의 구조와 기능 , 이 들 채 널 의 이온 선택성에 함유된 기작, 많은 억제제에 의해 채널이 연구되어 오고 있 는 데 억제 기작은 어느 정도 알려져 있지만 개폐 기작, 그 리고 진화직인 측면에서 그 채널의 기원에 이르기까지 이 들 문제가 해 깅 되어야 합 과 제들이다 . 생화학 및 생물학적 연구가 이 들 문제 해 결 에 근 원적인 역할 을 담당하고 있으며, 분자, 세포 및 진화적인 접 근 또한 이온 채널의 넓 고도 다양한 중요성의 해결에 기여할 것으로 기대된다 . 참고문헌 1) Albert s, B., Bray, D., Lew is, J., Raff, M., Robert s, K. and Wats o n, ]. D. (19 94). Molecular Bio l og y of the Cell Garland Publis h i ng Inc. N.Y . and London p 507 2) Hille, B. (19 92) Ion ic Channels of Exc itab le Membranes 2nd. ed. Sin a uer Associa t e s Inc. Sunderland, Mass 3) Neher, E. and Sakmann, B. (19 92) Scie n ti fic Ameri ca n, March, p 44 4) Unw in, N. (1993) J Mo!. Bio l. 229. 1101 5) Herz, ]. M., Joh nson, D. A and Tayl e r, P. (19 89) J Bi ol. Chem 264. 12439 6) Hu ganir, R. L. and Greeng a rd, P. (1990) Neuron 5, 55.5 7) Froehner, S. C. (19 91) J Cell Bi ol. 114, 1 8) Unw in, N. (1989) Neuron 3, fi65 9) Unw in, N. (1993) Cell 72 (sup pl.) 31
10) Salkoff , L., Butl e r, A., Wei, A., Scavarda, M., Baker, K., Pauron, D. and Sm ith, C. 0987) Trends Neu rosc i. 10, 522 11) Catt er all, W. A. 0980) Ann. Rev. Plrzrmacol. Toxia z l. 20, 15 12) Guy , R. H. and Conti , F. (1990) Trends Ne urosci. 13, 201 13) Noda, M., Sh imizu , S., Tanabe, T., Taka i, T., Kay an o, T., Ikeda, I., Tskahasi, H., N akay am a, H., Kanaoka, Y., Mina m ino , N., K ang a wa, K. etc s 0984 ) Natu re 312, 121 14) Nod a, M., Ikeda, T., Kay an o , T., Suzuk i, H., Takeshi ma , H., Kurasak i, M. , T akash i , H. and Numa, S. 0986) Natu r e 320, 188 15) Catt er all, W. A. (19 88) Sc ien ce 274, 50 16) Stu t m e r, W, Conti , F., Suzuk, H. and Wang , X. (1989) Natu r e 339, 597 17) Guy, H. R. and Seeth a ramulu, P. (19 86) Proc. Natl. A azd Sc i. USA 83, 580 18) Armstr o ng , C. M. (1981 ) Ph ysi o l. R ev. 61, 昭 19) Zag o tt a, W. N. and Aldr ich , R. (1990) J Gen. Ph ysi o l . 95, 29 20) Narahashi , T., M oore, J. W. and Scott , W. R. (1964) ]. Gen. Ph ys io l . 47, 965 21) Hille , B. (19 66) Natu r e 210, 1220 22) Hille , B. (19 67) ]. Gen. Ph ysi o l . 50, 1'2Z 7 23) Narahasi, T., Hass, H. G. and Therr ien , E. F. (10 07) Sc ien ce 157, 1441 24) Hille, B. (19 68) ]. Gen. Ph ysi o l . 5 1, 199 25) Imag a wa, T., Sm ith, J. S., Coronado, R. and Camp b ell, K P. (1987) ]. Bi ol. Chem 262, 166 .36 26) Palade, P. (19 87) ]. Bi ol. Chem 262, 6142 27) Hosey, M. M. and Lazdunski , M. (19 88) ]. Memb. Bi ol. 1 04, 81
28) Mccleskey, E. W., Fox, A. P., F eldman, D. and Tsie n , R. W. (19 86) J Exp. Bi ol. 124, 177 29) Fox, A. P., Now yck y , M. C. and Tsie n , R. W. (19 87) ]. Phys i o l . 3 94, 149 30) Fox, A. P., Now yck y , M. C. and Tsie n , R. W. 0987) ]. Phys i o l . 394, 173 31) Novry c ky, M. c., Fox, A. P. and Tsie n , R. W. (19 &5 ) Natu re 316 , 440 32) Wanke, E., Ferron i, A., Malga r oli, A., Ambrosin i , A., Pozz an, T. and Meldolesi, J. (1987) Proc. Natl. Acad Sci. USA . 84, 4313 33) Perney, T. M., Hirning , L. D., L eeman, S. E. and Mille r, R. J. (1986) Proc Natl. Acad Sc i. USA . 83, 55.56 34) i\'1ille r, R. J. (19 87) Scie n ce 235, 46 35) Chang eu x, J. P., Devil ler s-T h iery, A. and Chemo 띠Iii , P. (1984) Scie n ce 225, 133 .5 36) Benham, C. D. and Tsie n , R. W. (1 9 얽) Natu r e 328, '275 37) Tr iggle , D. J, Janis, R. A. (19 87) Ann Rev. Pharmacol. Toxic o l . 27, 347 38) Rivi e r , J, Gay le an, R., Gray, W. R., Azir ni-Z onooz, A., Mxjn t o s h, M., Cruz, L. J. and Oli ve ra, B. M. (19 87) ]. Bi ol. Chem 262, 1194 39) Cruz, L. J. and Oli ve ra, B. M. (19 86) J Bi ol. Chem 201, 6230 40) Wagn er , J. A, Snowman, A. M., Bis w as, A., Oli ve ra, B. M. and Smy d er, S. H. (19 88) J Neurosci . 8, 33.54 41) Coulte r, D. A., AHu gu enard, J. R. and Princ e, D. A. (1989) ]. Ph ys io l . 414, 5ITT 42) DeFelic e , L. J. (19 93) J Memb. Bi ol. 133, 191 43) Sta nd en, N. B. and Sta nfield , P. R. (1982) Proc R. Soc Lond B217, 101
44) Ma zz an ti , M. , De fe li c e , L. J. and Liu , Y. -M . (19 91 ) ]. Ph ys io l . 443, 307 45) Ho dg kin, A. L., Huxley , A. F. and Katz , B. 0949) Arch Sc i. Ph ys io l . 3, 129 46) Hi lle , B. 09 67 ) ]. Gen Ph ys io l. 50, 1287 47) Won g , B. S. and Bin s t o c k , L. (19 80 ) Bi op h ys. ]. 32, 1037 48) Nehe r , E. 0971 ) ]. Gen Ph ys io l. 58, 36 49) Blat z , A. L. and Ma g le b y , K. L. 0987 ) Trends Neurosci . 10, 463 50 ) We is s , R. E. and Ho m , R. 0986) Scie n ce 233, 361 51) Barres , B. A., Che n, L. L. Y. and Corey, D. P. (1989) Neuron 2, 1375 52) Sh ouk im as, J. J. and Fren c h, R. J. (19 80) Bi op h ys. ]. 32, 857 53) Hille , B. 0971) ]. Ge n Ph ys io l. 58, 599 54) To n ey , M. D., Ho h en e s te r , E., Cowan, S. W. and Jan son ius , J. N. (19 93) Scie n ce 261 , 756 55) Kump f, R. A. and Doug h ert y, D. A. 0993) Sc ien ce 261, 1708 56) Sc hofi eld , P. R., Darlis o n, M. G. Fujit a, N., B u rt, D. R., Ste p h e nson, F. A., Rod rigu ez, H., Rhee, L. M. , Ramachandran, ]., Reale, V., Glen c orse , T. A., Seeburg, P. H. and Barnard, E. A. (19 얽) Natu r e 328, 221 57) Pri tch e tt , D . B., S onth e im e r, H ., Sh ive rs, B. D., Y mer, S., Kette n man, H., Schofi eld , P. R. and Seeburg, P. H. (1989) Natu r e 338, 582 58) Rior dan, J. R., Rommens, J. M. , K erem, B. S., Alonm, N., Rozmahel, R., Grzelczak, Z., Zie le nski , ]., Lok, S., Plavsic , N., Chou, ]. L., Drumm, M. L., Lannuzzi, M . C., Coll ins , F. S. and Tsui , L. C. (1989) Sc ien ce 245, 1066 59) Tsui , L. C. (19 92) Hi u n Muta t. l , 197 60) Anderson, M. P., G reg or y , R. J., Thomp so n, S., Souza, D. W., Paul,
S., l\foll ig a n, R. C., Sm ith, A. E. and Welsh, Ivl. J. 0991) Sc ien ce 253, 202 61 ) Tabcharani , J. A., Chang , X. B., R ior dan, J. R. and Hanrahan, J. W. (19 91) Natu r e 352, 628 62) Bear, C. E., Dug u ay, F., Na ism ith, A. L., Ka rtne r, N., Hanu·a h a n, J. W. and Rior dan, J. R. 0991) ]. Bi ol. Chem 266, 19142 63) Welsh, M. ]. and Sm ith, A. E. 0993) Cell 73, 125 1 64) Shepp a rd, D. N., Rich , D. P., Oste dga ard, L. 0., Greg o r) ', R. ]., Sm ith, A. E. and Welsh, M. J. (1993) /\i,atur e 362, 160 65) Bader, C. R., Bert ran d, D. and Schwa rtz, E. A. (1982 ) ]. Ph ys io l . 3 31, 253 66) Miledi, R. 0982) Proc. R. Soc. Lond. B215, 491 67) May e r, M. L. 098. 5) J Ph ys io l . 3 64. 217 68) Evans, M. G. and Ma rty, A. (1986) J Ph ys io l. 378, 437 69) Hurne, R. I. and Thomas, S. A. (19 89) J Ph ys io l. 417, 241 70) White, M. M. and Ay lw i n, M. (19 90) Mo/. Pharmacol. 37, 720 71 ) Fergu so n, ]. E. and Hanley, M. R. (1 992) Arch Bi oc hem Bi op h ys. 297, 388 72) Jen ts c h, T. ]., Ste in me y er , K and Schwa rtz, G. (1990) Sc ien ce 348, 510 73) Yata mi, A, Okabe, K, Polak is, P., Halenbeck, R., McCorm ick , F. and Brown, A M (1990) Cell 61, 769 74) Hamilton , S. L., Codina , J., Hawkes, M. ]., Yata ni, A., Sawada, T., Str ick land, F. M., Froehner, S. C., Sp ieg el , A. M., Toro, L., Ste f a ni, E., Bir nb aurner, L. and Brown, A. M. (19 91) J Bi ol. Chem. 266, 19528 75) Kurach i, Y., Ito , H., Sug imo to , T., Sh imizu, T., Miki, I. and Ui, M.
(19 89 ) Na tu r e 337, 555 76) Rosen, L. B., Gin t y , D. D., Weber, M. J. and Greenberg, M. E. 0994) Neuron 12, 1207 77) Bim baume r, L., Abrmow itz, J. and Brown, A. M. (19 90) B i oc 玩 Bio p h ys. Acta 1031, 163 78) Brown, A. M. and Bim baumer, L . 0988) Am J Ph ys io l . 254, H401 79) Yanta m i, A., Co dina , ]., Imoto , Y., Reeves, J. P., Bim bumer, L. and Brown, A. M. 0987) Sc ien ce 238, 1288 80) Brown, A. M. and Bim baurner, L. (19 90) Ann Rev. Ph ysi o l . 5 2, 1<5 7 81) Re u te r , H. (1987) NI PS 2, 168 82) Trautw ein , W. and Hesc h eler, J . (1990) Ann Rev. Ph ysi o l . 5 2, 257 8.3) Matt er a , R., Grazia n o, M. P., Yata ni, A., Zhou, Z., Gra f, R., Codina , ]., Bim baurner, L., Gil ma n, A. G. and Brown, A. M. 0989) Sc ien ce 243, 804 84) Schubert , B., VanDong e n, A. M. ]., Kirsc h, G. E. and Brown, A. M. 0989) Scie n ce 245, 516 85) Yata n i, A. and Brown, A M. (1990) Am. J Ph ys io l. 258, Hl947 86) Log o th e tic , D. E., K urachi , Y., Galpe r, J., Neer, E. J. and Claph am, D. E. (1987) Natu r e 325, 321 87) Kim, D., Lew is, D. L., Gra ziad ei, L., Neer, E. J., Bar-S a gi, D. and Clap h am, D. E. ( 1989) Natu r e 337, 5.57 88) Bourne, H. R. (19 89) Natu r e 337, 504 89) Hamm, H. E., Deretic , D., Hofm a nn, K P., S chleic h er, A. and Kohl, B. (19 88) J Bi ol. Chem. 262, 10831 90) Zag o tta , W. N., Hoshi , T. and Aldr ich , R. W. (19 90) Sc ien ce 250, 568 91 ) Kirsc h, G. E. and Brown, A. M. (19 89) Am J Ph ysi o l . 257, H334
제 7 장 신호 전이와 유전자 발현 유전자는 특정 단백질을 발현할 수 있는 정보를 담고 있으나 많은 유 전자가 동시에 발현되는 것이 아니고 외부 환경이나 내부 환경(신호 전 이 기작)에 의해 각 유전자의 발현이 조절되고 있다. 유전자 발현은 외부 환경 인자 들 에 의한 다양한 기작에 의하여 폴리펩티드가 발현되는 과정 이 복잡하게 조절되고 있음이 보고되어 있고, 원핵 세포와 진핵 세포는 각기 다른 조절 기작을 가지고 있음이 보고되어 있다 . 원핵 세포에서 유 전자 발현의 조절이 이루어지는 단계 중 하나의 예로 오페론설 (o pe ron t heo ry)을 들 수 있다. 오페론설에 의하면 유전자는 구조 유전자 (s tru c tural ge ne), 조절 유전자 (re gul a t o ry ge ne) 그리 고 작동 유전자 (o pe ra t or g ene) 로 구성되어 있는데, 단백질을 만들기 위한 유전 정보를 갖고 있는 유전자는 구조 유전자이고 이 구조 유전자 앞에는 작동 유전자가 존재 한다 . 작동 유전자는 단백질을 합성하게 하거나 또는 억제하게 하는 스 위치의 기능을 하고 있다. 조절 유전자는 작동 유전자의 작용을 억제하 는 억 제 물질 (re p ressor) 을 만든다. 유도 물질(in ducer) 은 조절 유전자가 만든 억제 단백질과 결합하여 유도 물질-억제 물질 복합체를 만들어 억 제 단백질이 작동 유전자의 억제 활동을 못하게 하여 구조 유전자는 유
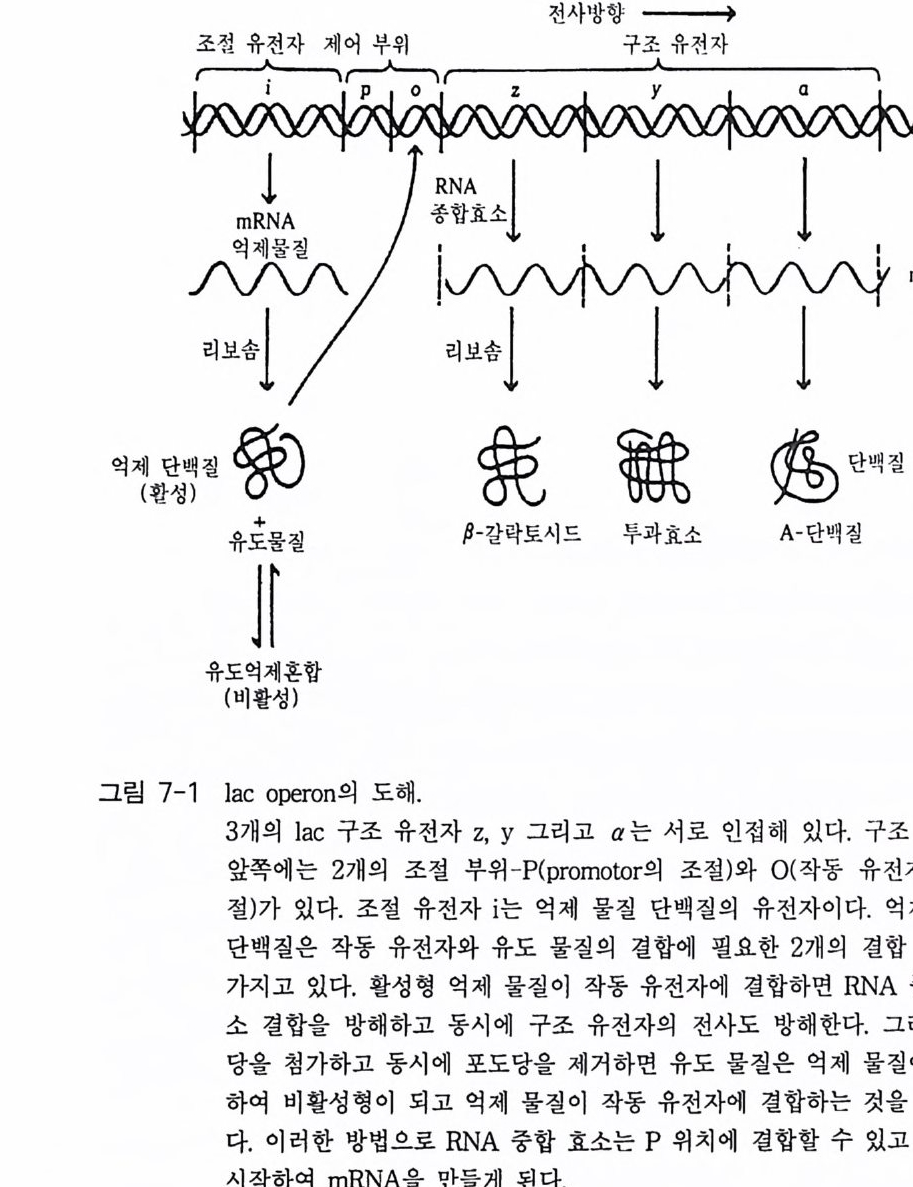 전사방향
전사방향
전자 발현을 할 수 있게 된다(그림 7-1). 유전자는 폴리펩티드 한 개를 발현하는 데 필요한 유전 정보를 의미 한댜 대장균에는 3000-4000 개의 유전자가 한 개의 DNA 에 배치되어 있 댜 이 모든 유전자들은 동시에 모두 mRNA 로 전사되는 것이 아니라 조 건에 따라 한 개의 유전자 (mono g en i c mRNA) 나 또는 여러 개의 유전자 가 동시에 rnRNA(po ly g e nic rnRNA) 로 전사된다 대장균은 포도당 배지 에서 배양하면 /3 - g alac t os i dase 를 발현시키지 못하므로 젖당을 분해하 지 못하나 배지에 탄소원으로 젖당을 첨가하면 젖당 분해 효소인 /3- g alac t os i dase 를 만들어 젖당 Oac t ose) 을 과당(g alac t ose) 과 포도당으로 분 해하여 에너지원으로 사용한다. 효소의 생성을 유도한 젖당을 유도 물질 이 라 하며 이 러 한 현상을 효소 유도 (en zym e i nduc ti on) 라고 한다. 한편 대장균은 트립토판을 합성할 수 있는 효소가 있어 대장균을 배양할 때 트립토판을 주지 않아도 성장할 수 있다. 그러나 배지에 트립토판을 넣어 주면 트립토판 합성 효소가 만들어지지 않는데, 이때 트립토판을 억제 물 질이라 하고 트립토판 합성 효소 (T rp s ynth e t ase) 와 같이 유전자 억제가 일어나 합성이 억제되는 것을 효소 억제 (e nzym e re p ress i on) 라고 한다. 고등 동물과 식물에서 단백질 발현의 조절은 훨씬 복잡할 뿐 아니라 박 테리아에서의 조절과는 다르다. 고등 생물의 유전자 DNA 는 원핵 세포와 는 달리 히스톤(hi s t one) 이 함께 있다. 염기성 단백질인 히스톤은 다섯 종 류가 있는데 종이나 세포의 종류에 관계없이 유사하다. 히스톤 중 DNA 를 둘러싸고 있는 것이 유전자의 작용을 억제하는 역할을 하고 있다. 유전자 발현은 생명체가 정상적인 생명 활동을 영위하기 위하여 정교 하게 조절되어야 한다. 유전자 발현의 촉진 또는 억제는 세포 의부의 신 호들에 의하여 조절된다. 세포의 성장을 촉진하는 인자로 표피 성장 인 자, 혈소판 유도 성장 인자, 섬유 아세포 성장 인자 둥이 있고, 성장을 억제하는 인자로는 형질 전환 성장 인자(tran s forming growth fac to r - /3, TGF-/3 ), 인터페론, 종양 회사 인자(turn ornecros i s fac to r , TNF) 동이 있
댜 성장 인자가 원형질막에 있는 수용체에 결합되면 세포 내 단백질들 과 2 차 전령들의 단계적인 활성에 의해 세포 성장이 일어난다. 성장 인 자 수용체가 활성화되면 여러 효소들의 활성도가 증가되며 2 차 전령둘 을 만들어 낸댜 2 차 전령들은 단백질 인산화 효소(단백질 키나제)등을 활성화시키며 이 신호는 핵 내의 전사 조절 인자(tr ansc ripti on fa c t or) 를 인산화 등의 방법으로 조절한다. 이러한 조절 과정을 통해 DNA 복제 및 세포 분열의 세포 주기 진행에 관련된 유전자 발현이 유도되고 세포 는 증식을 하게 된댜 한편 세포 성장을 억제하는 인자 들 이나 세포간의 접착 등에 의해서는 세포의 증식이 억제된다. 세포 성장시 신호 전달에 관련된 단백질들의 활 성화와 비활성화와의 균형이 깨지면 특정 단백질들의 영구적인 활성화 또는 비활성화가 유발 되어 세포는 정상 활동을 벗어나게 된다. 특정 단백질의 이상은 유전자 의 변화(poi n t 돌연변이, 유전자 증폭, 유전자 재배열 삭제)에 의해 발생되 는데 암 발생에 관련된 유전자를 종양 유전자 (onco g ene), 암 억제에 관 련된 유전자를 종양 억제 유전자(tum or sup pre ssor g ene) 라 한댜 Proto - onco g ene 과 종양 억제 유전자가 세포의 신호 전달 과정과 이에 의한 세 포 주기에 관련된 유전자임이 밝혀지면서 세포의 암 발생이 신호 전달 체계의 이상에 의하여 이루어진다는 사실이 명백해지고 있다. 앞에서 기술한 바와 같이 세포 내 유전자 발현은 크게 구분하여 신호 전이(그림 7-2) 단계와 전사(그림 7-3) 단계에서 조절될 가능성이 있는 것으로 알려져 있다. 본 장에서는 신호 전이 과정이 유전자 발현에 미치는 영향과 전사 과 정에서의 유전자 조절을 다루려고 한다. 그러나 아직까지 특정 유전자 발현과 관련하여 신호 전이 과정이 완전하게 밝혀진 예는 찾아보기 힘 든 형편이다. 그러므로 본 장에서는 신호 전이의 특정한 일부 단계와 유 전자 발현과의 관계를 논하고자 한다.
 외부XR cAMP 뮴 조 절 하는 Ca2+ 물 동원하는 성장인자
외부XR cAMP 뮴 조 절 하는 Ca2+ 물 동원하는 성장인자
7-1 진핵생물의 신호 전이 및 유전자 발현 7-1-1 아메바 발생 과정에서 유전자 조절 사회성 아메바 (soc i al amoeba, Di cytos te l iu m di sco i deum) 는 세포와 세 포 사이의 신호에 의해 세포 분화와 유전자 발현이 조절되고 있음이 비 교적 잘 알려져 있다 (1-6). 아메바의 발생 과정 중 나타나는 유전자 발 현 현상은 지난 수 십년간 연구되었다 . 먼저 생화학적 또는 면역학적 연
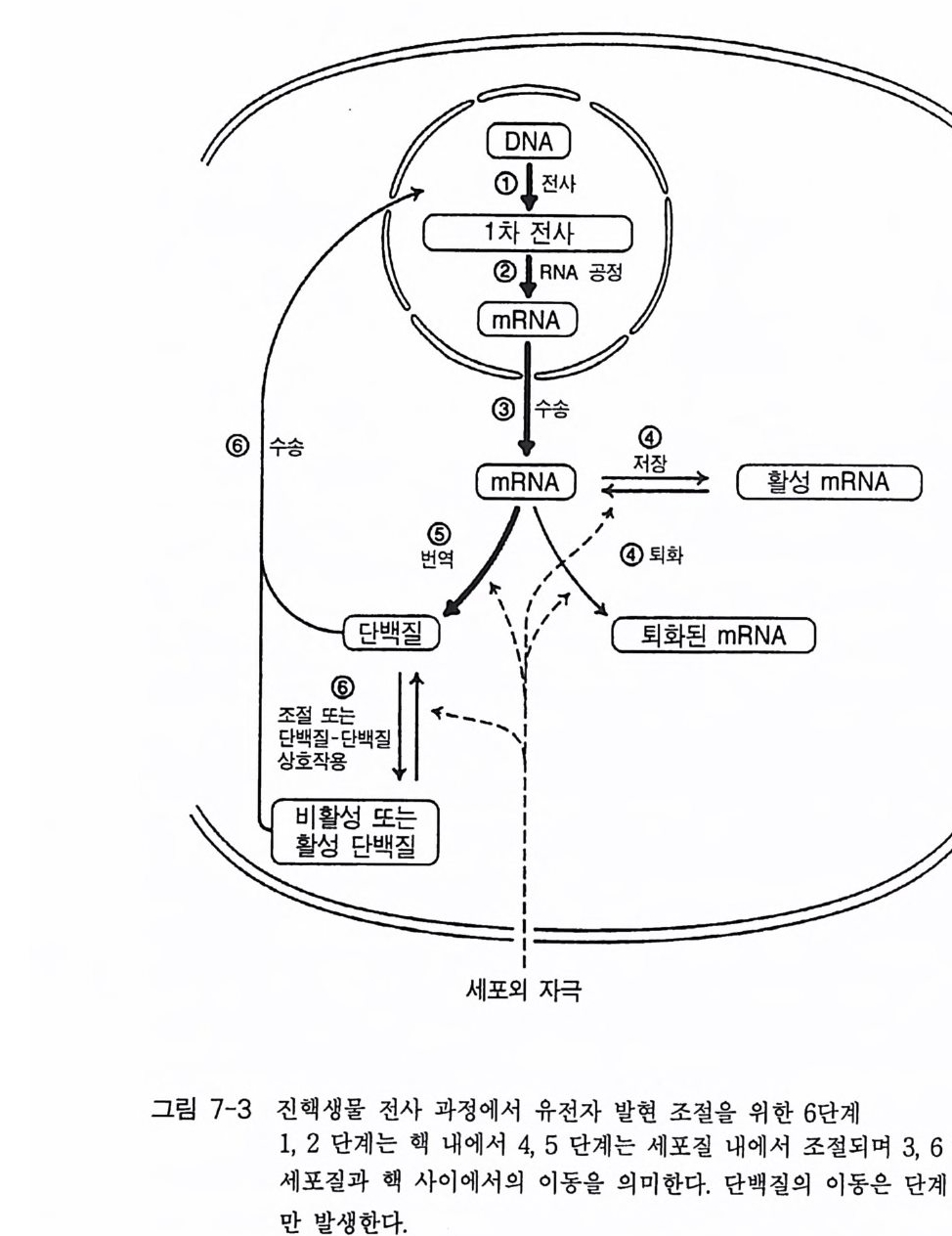 ( 1 차 전사 )
( 1 차 전사 )
구 방법 들로 발생 을 조 절 하는 효소와 항원을 밝혀 냈고, 2- D SDS— PAGE 로 발생 과 정 중 단백 질 합성의 변화 형태 를 분석할 수 있었다. 현재 발 생 과 정 에서 조절 되 는 많은 유전자들이 클론되어 있으며 이들 유 전 자 발 현 을 조절 하 는 인자 들 이 연구되고 있다 . 이 들 연구를 요약하면 cAMP 와 호르몬은 유 전 자 발현을 위해 중요한 역 할 을 하는 것으로 나타 나 있댜 아메바 는 단식 (s ta rva ti on) 에 의해 발생 과정에서 특정한 유전자의 발 현이 감소 되 는 반면 dis c o id in I, a- m annosid a se, cAMP 포스포디에스터 라제 (PDE ) 억제제 I 의 유전자 들 은 발현이 증가된다 (l) . 이들 유전자 발 현 은 분 비 물질 (PSF , CMF) 이나 아미노산의 결핍 등에 의해 유도된다. 그러나 이러한 유전자 발현은 일시적이며 대부분 cAMP 에 의해 유전자 발현 이 유 도 된다. 한편 다 른 종류의 유전자 (cAMP 수용체, 시클릭 뉴클레 오티 드 PDE, adhe si v e co n ta c t sit es A, G- 단백질 a 소단위체)들이 4 시간 동 안의 단 식에 의해 발현이 증가되었다 (2) . 단식 세포 (s tarv ed cell) 에서 이 들 응 집 성 유전자 (a gg re g a ti v e g ene) 들의 발현은 일정한 수준의 cAMP 가 미리 첨 가된 배지에서는 영향을 받지 않았으나 수 nM 수준의 cAMP 펄스 (p ulse) 에 의해서는 유전자 발현이 유도되었다 . 응집이 이루어지는 동안 세번째 유형의 유전자 (C y s 단백질 분해 효소 , ras p ro t oonco g enes) 들 이 pre sta lk 영역에서 우선적으로 발현되었다 . 이들 p res talk에 풍부한 유 전자들은 외부에서 첨가해 준 cAMP 에 의해 발현이 증가되었다 (3). 응집이 형성된 후 응집성 유전자의 발현은 감소되고 비특이적인 유전 자 즉, spo r e-sp ecific 유전자들이 발현되 었으며 이 들 유전자의 mRNA 는 수 µM 의 cAMP 에 의해 다시 증가되었다 (4). 또한 ecm A 와 ecm B 와 같은 sta lk- sp e cific 유전자들이 응집이 형성되는 동안 전사되었다 (5). 이 유전자들의 발현은 DIF(d iffer enti at i on ind ucin g fac t or) 에 의 해 유도되 었 으며 DIF 에 의 해 유도된 sta lk 세포 분화와 sta lk-s p ecific 유전자 발현 은 암모니아나 cAMP 에 의해 억제되었다 (6). 이와 같이 세포 밖에 존재
하는 암모니아 또는 cA l\1P , 아데노신의 양은 아매바의 유전자 발현 의 조절자로서의 역할을 하고 있다. 7-1-2 세포 의부의 cAMP 수 µM 수준의 cAl\ 1P 를 사용한 농도 의 존성 연 구로 아매바의 발생 과정에서 pos ta g g re ga tiv e 유전자가 발현되고 있음이 관찰되었다 (7). 변 형된 cAMP 유도체를 이용하여 여러 종류의 세포에 존재 하 는 cAMP 수 용체의 뉴클레오티드 결합 특이성을 연구한 결과 비 슷한 양상 을 보였으 나 세포질 내 cAMP 결합 단백질인 PKA 와 cABPl(cAMP- bin d i ng pro te i n 1) 에서는 결합 특이성이 구별되었다 . 이러한 결 과 들은 유전자 조 절이나 신호의 막 투과에 cAMP 가 강력한 첫번째 전달자(frr s t messen- ge r) 임 을 보여 주고 있다. 응집과 관련된 유전자 발현은 수 nM 의 cAMP 펄스와 같은 주화 성 (chemota xis) 신호에 의해 유도되며 이와 같은 신호는 주화성의 cAMP 수용체에 의해 인지된다. 그러나 몇몇 보고들은 이러한 수용체의 존 재 를 부정하고 있다. 두 개의 cAMP 유사체 (8 - bromo_cAMP 와 N;_ mono- buty ryl cAMP) 가 cAMP 보다 10 배나 많은 양의 site A(csA ) 유전자 를 발 현시켰다. 이 cAMP 유사체는 cAMP 보다 수용체에 대한 상대적인 결합 이 약하댜 이러한 사실은 csA 유전자 발현이 다른 수용체에 의해 유도 되고 있음을 시사해 주고 있다 (8) . 아메바에서 세포 외부의 cAMP 는 1000 - 2000 개의 유전자 발현에 관련 되어 있다. 그러므로 여러 개의 수용체가 각기 다른 경로로 활성화되거 나 수용체에서 유전자까지의 신호 전달 과정이 각기 달라야 한다. 즉 cAMP, cGMP, DAG, lP3 또는 lP3 유도체, Ca2+ 또는 cAMP 에 의 해 유도 된 이온들이 세포 내 중간체(i n t erm edi a t or) 로 작용할 수 있다. cAMP 수 용체의 활성화에 의해 합성된 cAMP 는 유전자 조절을 위한 후보자로 작
용한댜 그러나 이 후보와 관련이 있는 2 차 전령은 더욱 세분화되어 있 으며 중 요한 역 할을 수행하고 있다. 수용체에 의해 증가된 아데닐레이트 시 클 라제의 활 성 도는 카페인 또는 cAMP ― 유도 pre sta l k 또는 cAMP 에 의해 유 도된 pre s po re 유전자에 의해 감소되었다. 이러한 결과는 아데닐 레이 트 시 클 라제의 활 성화가 이 들 유전자의 발현을 위해 요구되는 것은 아님 을 시사해 주고 있다. 7-2 고등 식물의 신호 전이 및 유전자 발현 빛에 의한 식물의 유전자 발현은 4 개의 광수용체(p ho t ochloro p h y ll ide , 피 토크롬 , 청색 광 수용체, UV— B 수용체)가 관여하는 것으로 알려져 있지만 적색광 수용체인 피토크롬 외에는 그 분자적 성질이 자세히 밝 혀진 바 없다(그림 7-4). 식물체의 발아, 생장, 개화, 결실 등의 광형태 형성(p ho t omo rp ho g en e s i s) 은 광 신호가 염색체의 휴면 유전자 발현을 유도함으로써 일어 난다(표 7-1). 한편 호르몬 등에 의해서도 유전자 발현이 조절되는데 이 는 신호 전이 단계와 밀접한 관계를 가지고 있다. 7-2-1 적색광과 유전자 Ri bu lose-1,5-bis p h osp ha t e Carboxy la se-Oxy ge nase(Rubis c o) Rub i sco 는 광합성에 관여하는 단백질로서 빛에 의해 합성이 조절된다. 이 단백질은 두 개의 소단위체 (rbc L, rbc S) 로 구성되어 있으며 각각 8 개의 소단위체가 모여 4 차 구조를 형성한다. 큰 소단위체는 엽록체 유전 자로 존재하며 작은 소단위체는 핵 게놈(g enome) 에서 다유전자 (rnul tig ene fami l y)로 존재한댜 두 소단위체의 유전자는 각기 다른 경로를 통해 발
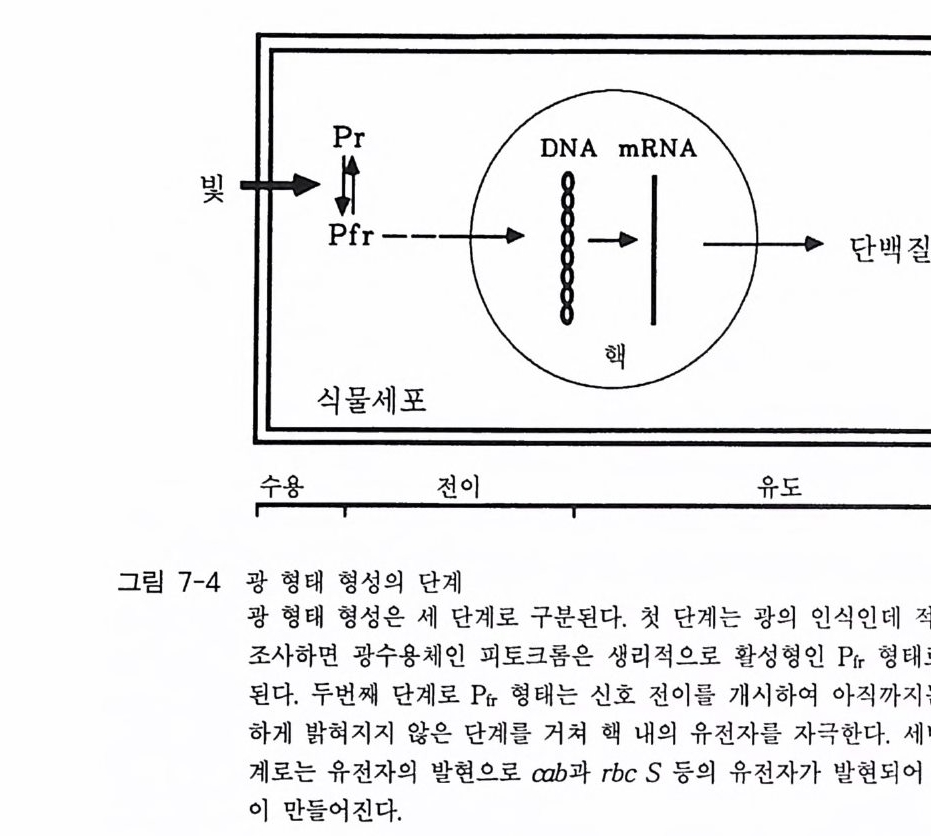 Pr
Pr
현이 조절되며 큰 소단위체 유전자의 발현이 선행된다. 큰 소단위체의 발현은 작은 소단위체의 발현에 조절 인자로 작용하고 있음이 밝혀졌다. 즉 엽 록체 인자가 핵 유전자 발현을 조절하고 있다 (9) . rbc S 유전자는 적색광에 의해 전사가 18 배 증가되며 원적색광에 노 출되면 처음 상태로 환원된다 . 이러한 사실로부터 rbc S 유전자의 발현 은 피토크롬 이 관여하는 광 형태 형성임을 알 수 있다. 그러나 최근 청 색광 수용체에 의해서도 발현이 조절되고 있음이 보고되었다(1 0) . 빛에 의해 유전자가 발현되는 것들에는 5I-fla nking 광 조절 부위에 여러 종 류의 보존된 서열 (conserved s eq uence) 이 존재하며 여러 종류의 조절 인
표 7-1 광에 의해 조절되는 유전자 (9) 유전자 (조+절/-)작 용 cPhhryo tmo-e Bligluhe t UB- B rl6 + + pS lAl + + pS lA2 + + cfo III + + cn A + + rbcL + + pG 32 + + rbcS + + + CAB + PEP GPDH Phy toc h rome +/- Proto c h lorop hy lide + r 려 uc t ase Chalcone + +/- -/+ Sy n ta s e PAL + + 4CL + + 자가 있음이 보고되었다. 가장 잘 알려진 GT-1 인자는 GGRRAA 서열을 포함하는 다양한 종류의 GT-1 부위에 특이적으로 결합한다(그림 7-5). GT-1 부위는 여러 개가 중첩되어 나타나는데 완두 rbc S-3A 유전자 에는 5 개가 존재함이 알려져 있다. GT-1 부위의 일부를 삭제시키거나 치환시키면 광 조절 기능을 잃으며 GT-1 사량체를 -90 CaMV. 35 s 촉 진 유전자에 연결시키면 광 조절 기능을 갖는 것으로 보아 이 부위는 식물의 광 조절 부위임을 알 수 있다. GT-1 결합 부위와 유사한 염기 서열은 빛에 의하여 조절되는 다른 유전자에서도 발견되었다. Gr-1 결합 부 위에는 부위 II(GTGTGGITAATAG A), 부위 ll(ATCATTTTCACT) 가 있
 2 3
2 3
으며 피토크롬에 의해 조절된다. 그러나 빛과는 무관하게 GT- 1 결합 부 위를 갖는 유전자도 발견되어 GT-1 이 일반적인 전사 요인일 가능성도 있다 (11). lig h t- h arvesti ng chlorop h y ll a/b(Cab) Cab 의 mRNA 는 적은 양의 적색광에 의해서도 증가되고 있음이 밝혀졌 다. 벼 의 CablR 촉진자에 존재하는 AGCTCACCCCAAGCTCA-C CAAG 라는 반복 배 열 (oc tam er repe at : OCT-R) 이 빛 에 의 한 cis - a cti ng 요소
라는 것이 돌연변이 실험을 통해 밝혀졌다 (13). 피토크롬 유전자 피토크 롬 유전자는 적색광에 의해 발현이 감소된다. 피토크롬 유전자 의 mRNA 전사율은 적색광에 의하여 급격히 줄어들며(1 4), 원적색광에 의해 쉽게 회복될 수 있다. 피토크롬 유전자의 5' 에는 GT- 1 부위 III, 부 위 IJ, G - 부위, AT- 1 결합 부위 등과 유사한 배열이 있음이 밝혀졌다. 앞에서 기술한 바와 같이 적색광이 유전자 발현 (rbc S, cab, phy)에 미치 는 영향은 비교적 잘 알려져 있지만 신호 전이 단계와 유전자 발현과의 관계는 아직도 더 연구되어야 할 과제로 남아 있다. 적색광과 신호 전이 피토크롬에 의한 신호 전이에 G - 단백질이 관련되어 있음이 최근 알려 졌다. 이 보고에 의하면 24 kDa 의 분자량을 가지는 이 G- 단백질이 콜레 라 독소에 의해 ADP 리보실화(ri bos y la ti on) 되었다. 또한 적색광에 의해 유도되는 클로로필 a/b_결합 (Cab) 유전자 발현의 증가와 피토크롬(phy) 유전자 발현의 감소가 콜레라 독소를 이용한 실험에서 관찰되었다(1 5). 그러나 아직까지 이 G- 단백질이 따 b 과 phy 유전자 발현에 직접적으로 관여한다는 증거는 얻지 못했다. 그 외에 피토크롬에 의한 신호 전이 과 정에 G- 단백질이 연관되어 있다는 몇몇 보고는 있지만 G- 단백질이 유 전자 발현에 기여하고 있다는 명백한 중거는 아직까지 얻지 못했다. 동물의 신호 전이에서 원형질막에 존재하는 PIP2 가 PLC 에 의해 분해 되어 lP3 와 DAG 가 생성된다는 것은 잘 알려진 사실이다. 식물에서도 이 러한 반응이 일어나고 있음이 보고되었다. 최근 보고에 의하면 옥수수 (Zea may s) 의 잎에서 PIP2 가 적색광에 의해 빠르게 증가되었다가 감소 되고 있음이 관찰되었다(1 6). 또한 lP3 가 피토크롬에 의한 반응과 관련이 있다는 간접적인 증거가 제시되었다. 그러나 아직까지 적색광에 의해 활
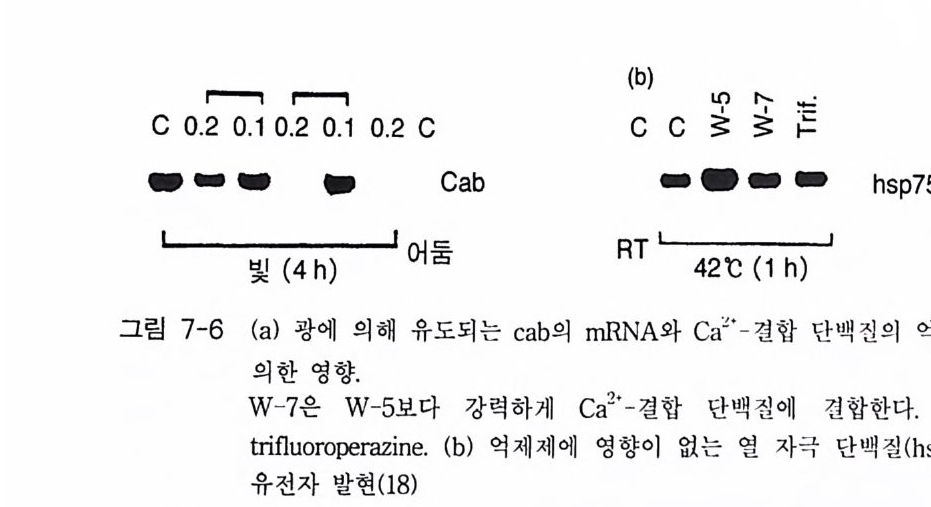 --r--_ , 『'., _.-, (b) --'gN - L'N- .-u L hsp 75
--r--_ , 『'., _.-, (b) --'gN - L'N- .-u L hsp 75
성화된 PI- 순환이 유전자 발현과 관련이 있는지 여부는 모르는 상태이 다. 피토크롬에 의한 신호 전이에 Ca 2· 이 중요한 역할을 하고 있다는 것은 잘 알려진 사실이다 . 세포질 내의 Ca2• 농도는 적색광에 의해 30nM 에서 51 nM 로 증가하였다(1 7). 한편 Chua 는 Ca2 누결합 단백질의 억제제(칼모 듈린 길항자)인 W-5, W-7 과 trifl uoro pe raz i ne 을 이용하여 광에 의한 세 포질 내 Ca2+ 농도 중가가 mb 과 hsp 7 5 유전자 발현에 미 치 는 영 향을 관 찰하였다. 그림 7-6 에서 보는 바와 같이
등에 의하면 칼슘 i ono p hore 인 A23187 이나 i onom y c i n 에 의해 cab 유전 자의 전사가 증가되는 결과를 보임으로써 Chua 의 결과를 재확인해 주고 있댜 단백질 인산화도 피토크롬에 의한 신호 전이에 중요한 단계임이 알려 졌댜 그러나 구체적으로 어떤 단백질의 인산화가 유전자 발현의 중요한 인자 로 작용할 것인지는 모르는 상태이다 . 귀리의 원형질체에 적생광을 조사하면 15 종 이상의 단백질의 인산화가 관찰되지만 그 중 2 개 단백질 (27, 32 kDa) 만이 피토크롬의 홉수 스펙트럼과 일치하는 작용 스펙트럼 (acti on s pect rum) 을 보여주고 있음이 알려졌다(1 9) . 그러나 이 단백질들 의 인산화가 유전자 발현과 구체적으로 어떤 관계가 있는지 여부는 모 르고 있다. 이와 같이 최근 피토크롬에 의한 신호 전이 현상의 연구에도 불구하고 신호 전이와 유전자 발현의 관계는 더 연구해야 할 과제로 남 아 있댜 7-2-2 청색광과 유전자 청색광 수용체와 신호 전이 고등 식물에서 청색광 수용체의 정체는 아직까지 명확하게 알려진 바 가 없다. 가능성이 있는 것으로 f3기베타카로틴과 리보플라빈을 들 수 있 댜 그러나 최근 청색광에 의해 조절되는 몇몇 신호 전이 현상이 발표되 었댜 이돌 보고에 의하면 첫째, 원형 질막에 존재하는 단백질의 인산화 가 관찰되었으며 (20), 둘째, 원형질막에 존재하는 G- 단백질의 GTPase 의 활성도가 변화하였고 (21), 셋째, 청색광에 의해 유전자 발현의 조절이 관 찰되었다 (22). 완두의 클로로필 a/b 단백질 (Cab) 유전자의 전사율이 청색 광에 의해 증가되었댜 완두의 빛에 의한 mRNA 생성량을 관찰하기 위 해 7 일 동안 적색광 하에서 키운 후 24 시간 동안 청색광을 조사하였다. 그 결과 청색광을 조사하지 않은 완두보다 청색광에 노출된 경우에 rbc
S 의 mRNA 가 6 배 증가하였댜 그러나 천연의 완두에서나 또 는 암실에 서 키운 완두의 경우 24 시간 청색광 조사에 의해 rbc S - 3A 나 rbc S- 3C 의 mR1 사 A 는 변화되지 않았다 (23). 이러한 현상은 적색광에 의해 유전자 가 조절된 후 청색광에 의해 재조절되고 있음을 시사해 주고 있다. 다섯 종류 이상의 피토크롬 존재 (24) 와 청색광에 의한 피토크 롬 의 영향은 청 색광/적색광 상호작용에 의한 유전자 조절 가능성을 높여 주고 있다. 이 러한 가능성은 다음과 같은 신호 전이의 존재 를 의미한다. ® 몇몇 청색 광에 의한 유전자 조절은 피토크롬의 활성도가 높아진 후 나타난다. @ 한 종류 또는 그 이상의 피토크롬종은 활성도가 높아지기 위해 청색광 수용체의 활성도가 높아져야 한다. ® 신호 전이 과정에 여러 경로가 존 재해야 한다. 그러나 이러한 가설을 확인하기 위해서는 좀더 많은 연구 가 요구된다. 지금까지 본 바와 같이 수용체에 신호가 인지된 후 휴면중 인 유전자까지 신호가 전달되기 위해서는 한 개 이상의 경로 를 사용할 수 있으며 동시에 여러 단계에서 유전자 조절을 할 가능성이 있으므로 완벽한 경로를 확인하는 작업은 앞으로 많은 연구가 필요하다 하겠다. C i s- 와 Trans-Acti n g 요소 청색광에 의해 조절되는 유전자의 촉진 유전자 연구가 cis - acti ng 요 소를 밝히기 위한 수단으로 수행되었고, tran s-acti ng 요소를 밝힐 수 있 는 가능성을 제공하였다. 돌연변이 식물인 Arabid o p s is t/-a l i ana 에서 CHS : GUS 의 5' 촉진 유전자를 연구하여 CHS 촉진 유전자의 523b p를 GUS 에 연결시 켰다 (25). 16 시 간 동안 빛을 조사하면 GUS 의 활성 도는 50% 중가되었다. 한편 48 시간 동안 빛을 조사하면 암실에서 자란 것보 다 활성도가 3-4 배 중가하였다. 촉진 유전자의 186b p를 제거하자 청색광 에 의해 유도되던 CHS 가 발현되지 않았다. CHS 유전자의 5' 부위는 다 른 모든 CHS 유전자에서도 발견되었고 대부분의 rbc S 촉진 유전자에 서도 발견되 었 다. 완두의 rbc S-3A 와 rbc S-3C 의 촉진 유전자를 제거 한
유전자 역시 광특이성 cis - a c ti ng 요소 를 연구하기 위해 사용되고 있지 만 아직까지 보고된 인자는 없는 상태이다. 7-2-3 Abscis i c a ci d 와 유전자 Absci si c acid ( ABA, 그림 7 - 7) 는 지금까지 발표되었던 식물 호르몬 중 에서 실용적으로 이용되지 않았던 유일한 화합물이다 . 식물체 내의 ABA 함량은 1 ppm 이하이며 낙엽의 형성, 휴면, 기공의 폐쇄 등 억제적 이며 가역적으로 작용하는 경우가 많다. Posit ive reg u lati o n ABA 에 의해 조절되는 몇 개의 유전자(E m, rab, De 3) 로부터 cis - acti ng 요소 (ABRE) 가 확인되었고 (26) DNA 의 cis - acti ng 요소에 결합하 는 tra ns-a cti ng 요소는 핵에 존재하는 단백질임이 보고되었다 (Zl). 몇몇 핵단백질이 특이적으로 ABRE 에 결합하고 있었는데 그 중 하나인 Em BP - 1 은 ABRE 가 가지고 있는 G-box 에 8 개 염기와 특이적으로 결합하 여 ABA 에 의해 조절되는 전사 활성화 안자로 작용하고 있음이 확인되 었다 ABA 에 의해 유도되는 많은 유전자들이 식물체를 성장시킬 수 있
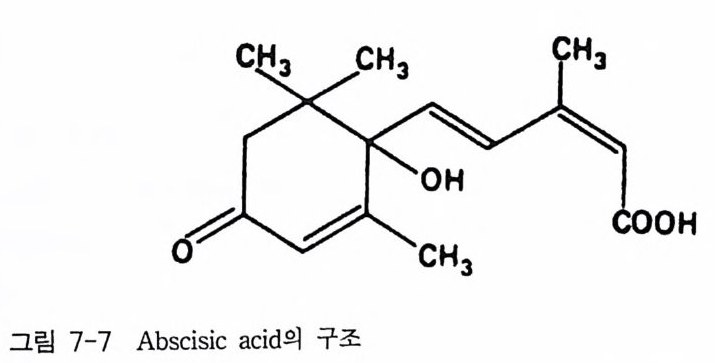 OH
OH
는 다른 자극(탈수 반응, 높은 삼투압, NaCl, 낮은 온도 그리고 열 자극) 들 에 의해서도 조절되고 있음이 밝혀졌다. 대부분의 경우 ABA 에 의해 조 절되는 유전자 발현은 ABA 의 양과 관계가 있댜 그러나 몇몇 유전자 들 마의 토발에현 존은재 앞 하에는서 AB열A거 에한 의다 :n른 유자도극되에 는 의유해전 자영(p향 L을E4 ,받 p지L E 1않6,고 p L있 E2다5) . 토발 현은 ABA 양과 항상 일정한 관계로 나타나지는 않는다 비 록 이 세 유 전자가 ABA 에 의해 발현되기는 하지만 ABA 양과 이 유전자의 mRNA 양과의 사이에 상관관계가 없는 것으로 보아 다 른 자 극 역시 유전자 발 현에 조절 인자로 참여하고 있음을 알 수 있다 (28 , 29). Neg a ti ve reg u lati on 몇몇 유전자들은 탈수 반응과 같은 자극 하에서도 ABA 에 의해 발현 이 증가되었댜 그러나 유전자 발현이 감소되는 예도 밝혀졌다. 광합성에 필요한 유전자 (cab, rbc S) 들은 탈수 반응과 ABA 에 의 해 발현이 감소되 었다 (30, 31 ). 또 다른 경우로서 ABA 는 GA3( gi bbere lli n) 에 의해 유도되 는 유전자 발현을 감소시켰다. 이상에서 본 바와 같이 유전자의 발현은 한 개 이상의 단계에서 복잡하게 관여하고 있음을 알 수 있다. 7-3 암과 유전자 발현 생명체의 정상적인 세포 활동은 의부 환경에 잘 적응하기 위해서 정 교하게 조절되고 있다. 세포의 성장과 증식은 증식을 유발하는 암 유전 자 (onco g ene, 표 7-2) 와 중식을 억제하는 종양 억제 유전자(tum or sup pre ssor ge ne) 사이의 균형에 의해 조절된다. 세포의 성장을 촉진하는 인자로는 EGF, PDGF, FGF 둥이 있고 성장 울 억 제 하는 인자로는 TGF-/3 (tran sfo rming grow th fac to r -/3 ), 인 터 페
표 7-2 종 양 유 전 자 Onc og e n e Prot o (- w o hn ceo reg ekn n eo wF unn) c ti on SoVu ri crue s of Vi ruT s u-m in do ur ced ab/ pro te in kin a s c( ty ro s in e ) mo u s e pre - B - c ell leu kem ia cat sa rco m a ak( ? mo u s e T- c e ll lym p ho ma erk ac ti va to r of tyr o s in e -sp ecific chic k e n sa rcoma pro te in kina s e(s ) erb - A thy ro id ho n no n e rec ep tor chic k e n (su p ple ments acti on of v- e rb- B ) erb - B pro te in kin a se (tyro s in e ). chic k e n ery thro leu ke m ia: ep id e rm a l gro wt h fac to r (E GF) fibr os a rcoma rec ep tor ets nuclea r pro te i n chic k e n (su p ple ments acti on of v- m yb) fes / f p s pro te in kina s c( ty ro s in e ) ca t /ch ic k e n sa rco m a fgr pro te in kina s e( ty ro s in e ) cat sa rcoma fm s pro te i n l
 성장인자
성장인자
론, TNF(tu mo mecrosis fac to r, 종 양 회사 인자) 등이 보고되 었다. 정상 세 포는 ® 세포 주기의 이상, ® 신호 전이 경로의 이상, ® 암 유전자의 활성화 등에 의해 암세포로 전환되나 여기에서는 주로 신호 전이와 암 과의 관계(그림 7-8) 를 다루고자 한다.
7-3-1 수용체 수용체 는 각기 다른 세 가지 방법으로 수용체에 인지된 의부 신호를 첫번째 분자에 전달한다 . ® 채널과 연결되어 있는 수용체는 신경 전달 물질 과 관련된 신호 전이에서 보이는 형 태로 신경 전달 물질 - 의존성 이 온 채 널 의 문을 열거나 닫는다. ® 촉매 기능을 가진 수용체는 주로 티 로신 -특 이성 단백 질 (T y r - s pe c ifi c p ro t e i n) 이며 목표 단백질의 티로신을 직접 인산화시킨다 ® G - 단백질과 연결되어 있는 수용체는 G- 단백질을 활성화시킨 후 이 단백질에 의해 원형질막에 결합되어 있는 효소나 이 온 채널이 활 성화된다 . 세포의 성장 조절에서 자극이 세포 표면의 수용 체에 의해 인지된 후 이 신호는 일련의 세포 내 신호 전이 과정을 거쳐 핵 내의 유전자까지 전달되며 이 과정에서 세포 내에 존재하는 물질의 변화 및 새로운 물질의 생산으로 자극에 의한 세포 반응을 하게 된다 . 암과 관련하여 지 금까지 보고된 수용체는 ros, erbB, c-er bB-2, fins, met, trk , sea, kit , ret 등이 있으며 주로 촉매 기능을 가진 수용체 (cata l yt ic rece pt or) 에 속한댜 성장 인자의 수용체는 세포 외부 영역, 막 관통 영역, 세포질의 키나제 영역으로 구성되어 있으며 신호의 전달을 위하여 목표 단백질을 인산화한다. 수용체의 자동 인산화된 티로신은 목 표 단백질의 SH2(src) 영역과 결합함으로써 신호가 전달되며 활성화된 수용체와 결합하여 인산화되는 목표 단백질로는 포스포리파제 C-r, ras-GTPase 활성 단백질 (ac ti va ting pro te i n ) , 포스포이노시톨 -3- 키나제, Uav, Grb- 2 동이 알려 져 있다 (32). 최근 인터페론 수용체의 신호 전이 연구를 통해 JA K-STATS(j an us kina se-sig na l tran sducti on trans ducer and acti va to r of tran scri ption ) 경 로가 알려졌다 (33). JA K-STATS 경로를 이용하는 cyt ok i ne 수용체들은 세포질 쪽 부위에는 효소 기능이 없으며 cyt ok i ne 결합 시 세포질에 존 재하는 JA K 족의 티로신 키나제들과 결합하여 J AK 를 인산화시킨다.
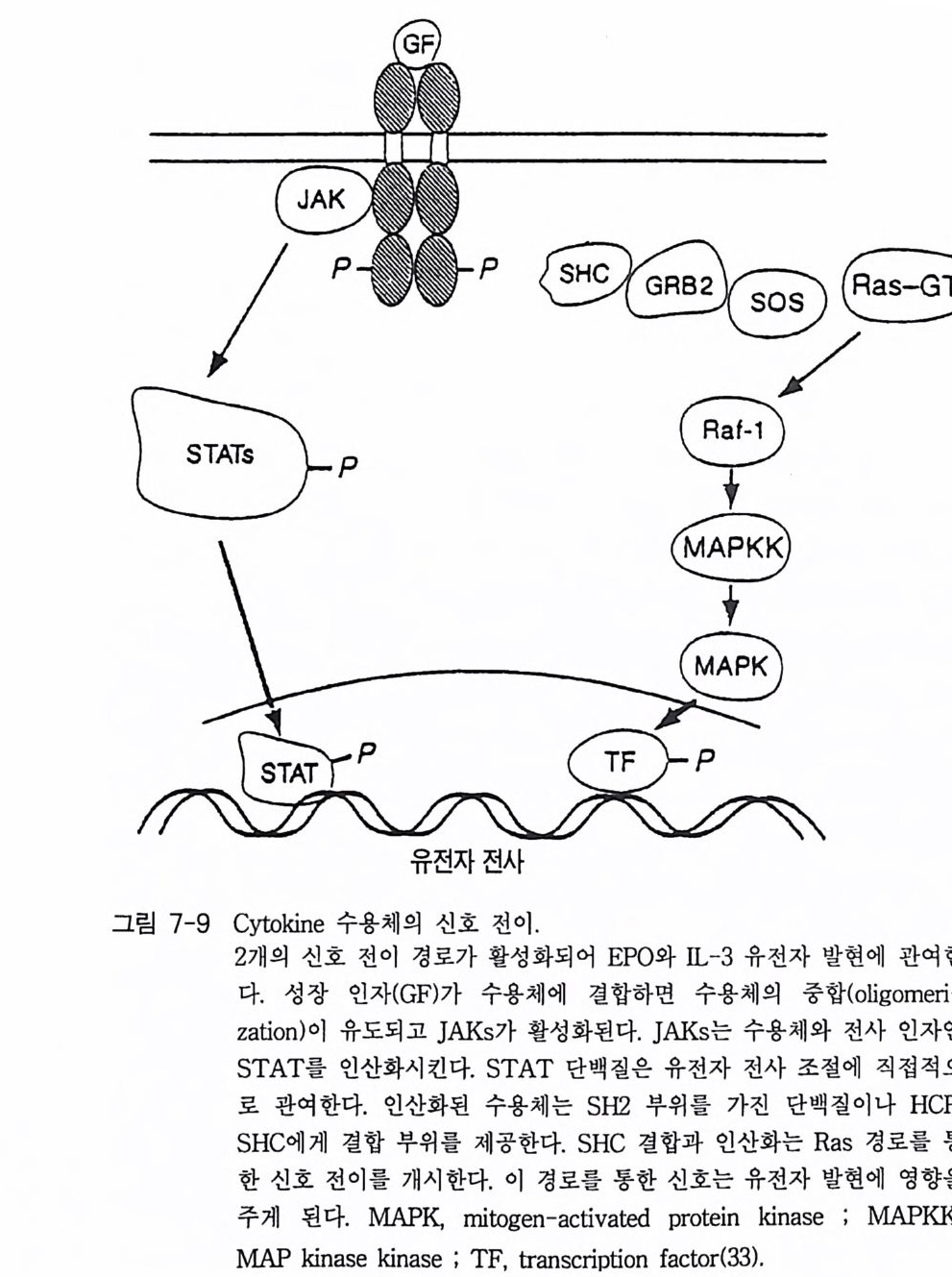 P p )?/ 三p
P p )?/ 三p
J AK 는 STAT 에 속하는 전사 요인을 인산화시키고 STAT 는 핵으로 이 동하여 다른 전사 인자와 결합하여 c yt o ki ne 에 의 한 유전자 발현을 조절 한다(그림 7-9). 7 一 3 - 2 G 전백질 G - 단백질은 수용체에 인지된 신호를 effe c to r 분자로 전달하여 주는 역할을 수행하고 있댜 신호가 수용체에 인지되면서 세포 내로 신호가 전달되는 첫 단계로 이 수용체와 관련이 있는 G- 단백질이 반응을 시작 한다 G - 단백질에 신호가 전달되면 비활성형인 GDP 결합 G- 단백질이 활성형인 GTP- 결합 G- 단백질로 바뀌면서 신호를 전달한댜 G_ 단백질 에 의해 인지된 신호는 다음 단계로 세포 내에 존재하는 eff ec to r 분자로 전달되어 신호를 증폭시킨다. 활성화된 G- 단백질은 아데닐레이트 시클 라제와 PLC 또는 이온 채널들을 활성화시켜 cAMP, DAG, lP3 등을 생 산한댜 세포의 성장과 관련이 있는 G- 단백질은 ras(34, 35) 로서 티로신 키나제 수용체에 의해 활성화된다(그림 7-10). Ras 단백질의 분자량은 21 kDa 이며 원형질막의 세포질 쪽에 위치하고 있댜 ras 가 활성화되려면 SH2 와 SH3 부위로 구성되어 있는 She 나 Grb-2 등의 adapt or 단백 질 이 필요하다 (36). ras 의 활성 도가 adap tor 단 백질을 이용한 단백질-단백질 간의 상호작용에 의해 증가됨이 알려졌다. 티로신 키나제인 수용체가 리간드의 결합에 의하여 자동 인산화되면 Grb-2 단백질이 수용체에 결합하게 된다. Grb-2 의 SH3 부위에는 SOS (son of sevenless) 단백질들이 결합되어 있으며 이 SOS 가 ras 를 활성화 시킨댜 SOS 는 GDP 가 결합된 비활성 ras 로부터 GDP 를 분리하고 GTP 를 결합시킨다. ras 는 ra f와의 기능과도 관련이 있는데 티로신 키나제인 수용체의 자동 인산화에 의하여 ras 가 활성화되면 세린/트레오닌 키나제 죽 MAP 키나제(rnit o g en acti va te d ki nase) 의 활성이 증가된다.
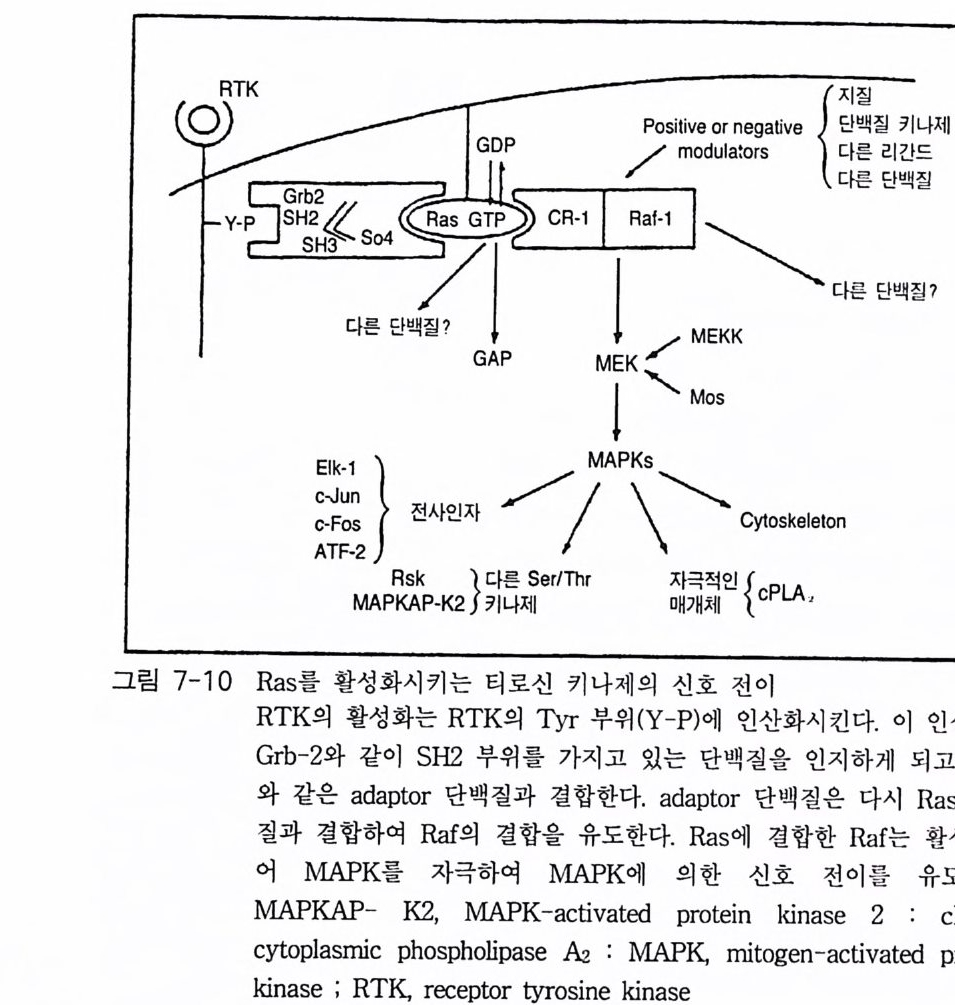 〉S l:Vo?나 ?sahve 麟지질 제
〉S l:Vo?나 ?sahve 麟지질 제
7-3-3 포스포이노시톨 대사 활성화된 G- 단백질은 원형질막에 존재하고 있는 포스포리파제 (PLA1, PLA :;,, PLC, PLD) 들을 활성화시킨다. 이들 포스포리파제는 인지질들을 가수분해하여 신호를 전달하는 새로운 분자들을 생성한다. 이중 특정 포
스포리파제는 다 른 종류의 인지질과도 반응한다. PLC 는 PIP2 를 가수분 해 하여 막에 남게 되 는 DAG 와 수용성 인 lP3 를 만든댜 DAG 와 lP3 는 제 2 의 전령으로서 DAG 는 PKC 를 활성화시키고 lP 3 는 세포내 칼슘 저장소 로부터 C 같을 동원시켜 외부 자극에 대하여 세포 내 반응을 개시한다 (그립 7- 1 1). ras 암 유전자의 경우, 정상 ras 유전자는 G- 단백질을 암호화하고, 변 형된 ras 는 PI 대사의 기능에 악영향을 주는 단백질을 암호화하는 것으 로 알려졌댜 즉, 생쥐 세포에 변형된 ras 를 넣어 주면 성장 인자가 없어 도 포스포이노시돌의 양이 증가되었다. 이러한 결과는 변형된 ras 유전 자의 산물이 PLC 를 활성 화하고 있음을 의 미 한다(그림 7-12). 이 러 한 현 상은 성장 인자에 의해 자극을 받지 않아도 PI 대사가 작동하는 것으로 서 암세포의 제어되지 않는 성장을 설명할 수 있다. 한편 PDGF 에 의해 PI 대사가 활성화되면 fa s 와 my c 과 같은 암 유전 자가 발현되는데 이렇게 발현한 단백질은 다른 유전자의 발현을 조절할 가능성이 있고, 이러한 가능성은 세포 대사의 변화를 의미한다. 7-3-4 단백질 키나제 세린/트레오닌 키나제 세린/트레오닌 단백질 인산화 효소는 단백질의 세린 또는 트레오닌 위치에 인산기를 결합시키는 효소이며 활성을 증가시키는 요인에 따라 단백질 키나제 A(cAMP 에 의해 활성화됨), 단백질 키나제 G(cGMP 에 의 해 활성화됨), Ca 인 /CaM- 의존성 단백질 키나제로 구분된다. PKC 는 암 촉진 인자인 포볼 에스터의 세포 내 수용체임이 밝혀졌다. 외부 신호를 받아들인 수용체가 G- 단백질을 통해 혹은 Ca2+ g a t e 를 통해 PI 에 특이 성을 가지는 PLC 를 활성화시키면 PIP2 로부터 DAG 와 lP3 를 생산한다. DAG 는 세포 내에서 단시간 내에 분해되는 데 반해 포볼에스터는 DAG
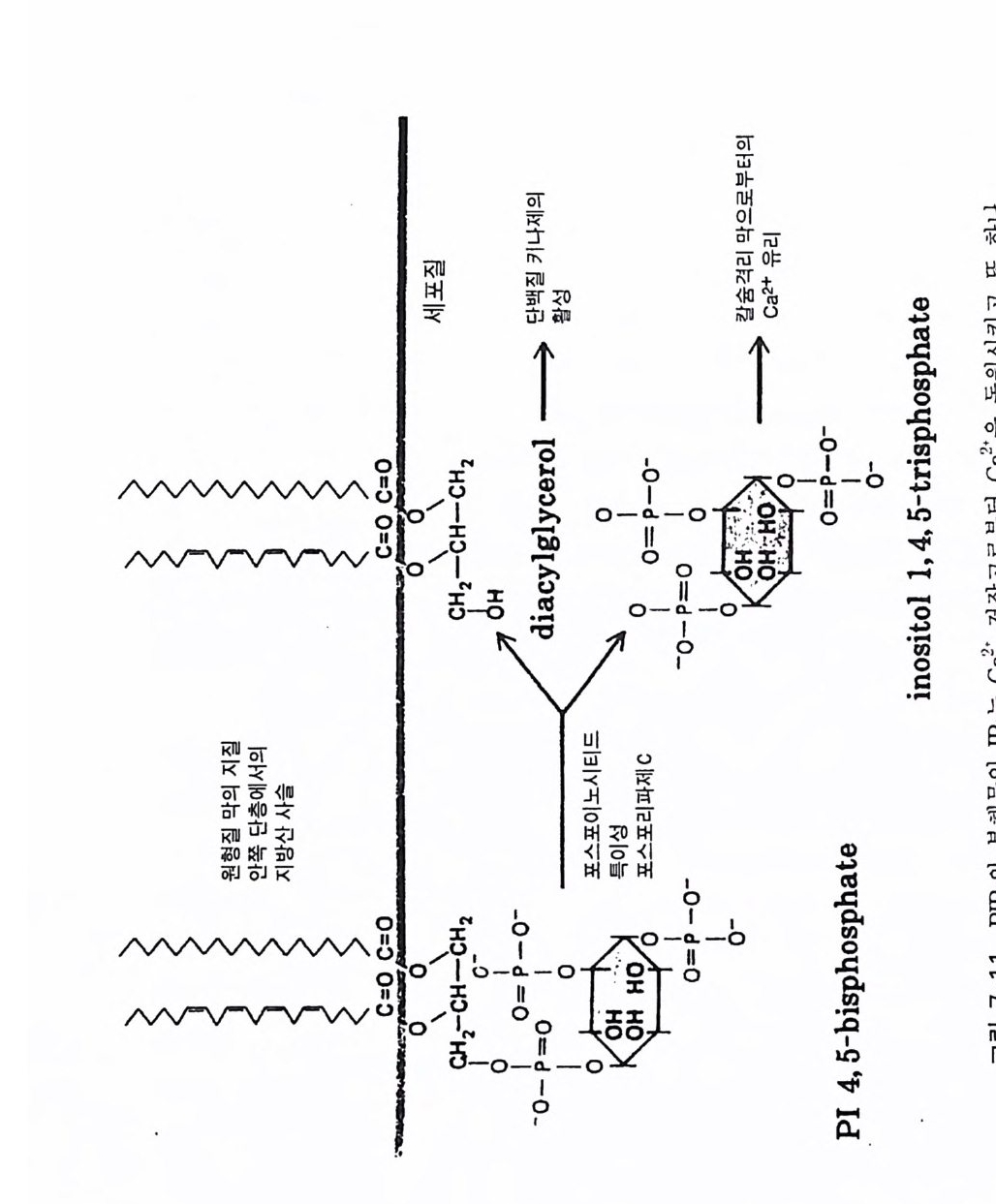 의
의
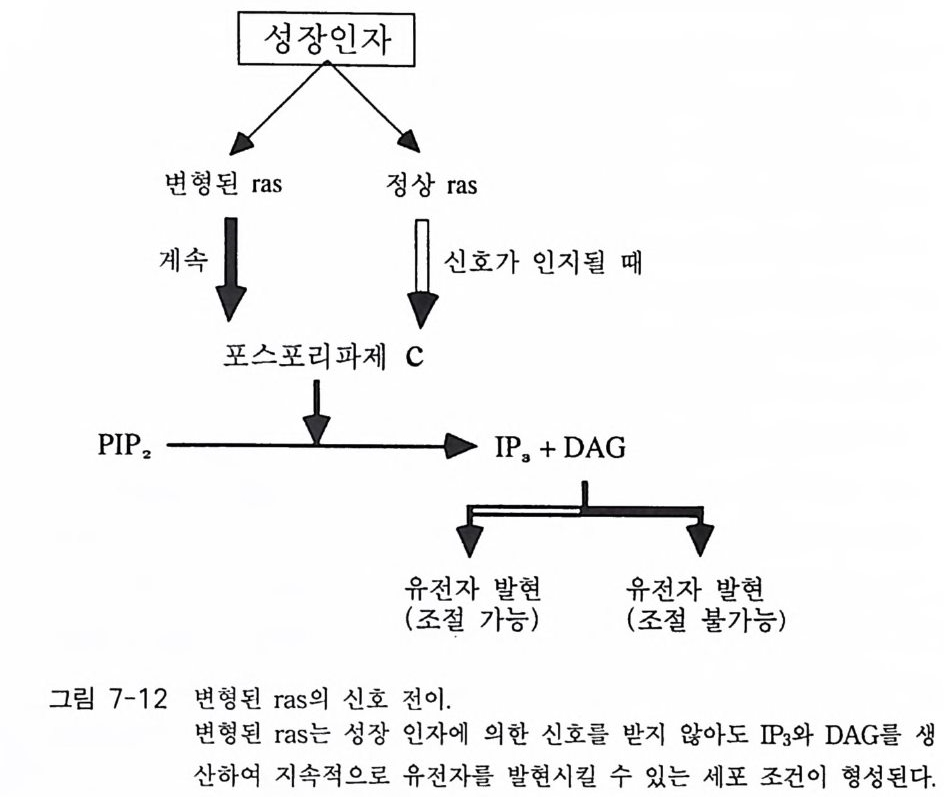 성장인자
성장인자
와 동일한 작용을 하면서 분해되지 않아 PKC 를 통한 신호 전달 경로와 암의 발생 경로가 비슷한 과정을 거칠 수 있다는 추측을 낳게 하였다. 실제로 몇몇 p ro t oonco g ene 의 전사 후 변형에 PKC 가 관여한다는 것이 알 려졌다. PKC 의 작용은 특히 유전자의 발현에서 중요한데 inter leuk in- 2 수용체 의 유도나 c_fO S , c-m y c, c-j un 과 같은 p ro t oonco g ene 의 활성 화에 작용하고, 섬유 아세포에서 PKC 아속들의 과발현 (over expr ess i on) 을 통해 PKC 가 성장 조절에 중요한 역할을 한다는 것이 알려졌다. 최근 보고에 의하면 c-fo s 는 PKC 에 의해 인산화되며 역시 인산화된 전사 인자 API / c-j un 과 복합체를 이루어 특정 enhancer elemen t (TGACTCA) 에 붙어서
meta llo th i o n ein Ila 나 colla g enase 의 전사를 조절하고 있댜 한편 int e r l eu- ki n2 와 이 수용체의 a - 소단 위체 , 그리고 /3-인터페론 유전자의 다면 발 현 중계자(p le i o tr o pi c m edi a t or) 인 nuclear fa c t or - kB 의 경우 세포질에서 억제 단백질과 결합하고 있다가 PKC 에 의해 인산화되면서 억제 단백질 과 분리되어 핵으로 이동하여 여러 유전자의 발현을 돕는다고 밝혀졌 다. 그 밖에 도 lute in izin g hormone, gly c o p h ori n, pro lacti n, calcit on in , pla srn ino g e n acti va to r , om ithi n decarboxy la se , r -in t e r fe r o n, his t i d i n e decarboxy la se, seroto n in N-ace ty l tr ans f erase 의 유전자 발현 에 PKC 가 관 여하고 있음이 알려졌다 (37) . 한편 PKC 는 EGF 수용체를 반복적으로 인산화시켜 EGF 에 대한 친화 도를 약화시키고 수용체 자체의 티로신 키나제 활 성도 를 방해하여 결국 수용체의 기능을 약화시킨다 . 이외에도 GnRH 수용체, 무 스카린 아세틸 콜린 수용체, AVP 수용체, CRF 수용체, a1- 아 들 레날린 수용체, /3 - 아 들레날린 수용체에 의해 인지된 신호가 PKC 에 의하여 약화 될 가능성이 있는 것으로 보고된 바 있다. Raf는 위에서 언급한 바와 같 이 R as 의 기 능 약화를 위한 중계자이며 신호가 인지되면 M 사) 키나제가 순차적 으로 활성화되어 세포핵에서의 유전자 발현을 조절한다 (33) . 티로신 키나제 티로신 키나제와 포스포티로신 포스파타제는 상호 조절되어 목표 단 백질의 티로신 잔기에 인산기를 더하거나 제거시켜 신호의 전달을 정상 적으로 수행한다 . 세포의 성장에 관여하는 티로신 키나제의 인산화는 세 포가 분화 단계에 있을 때 티로신 포스파타제에 의하여 탈인산화가 되 어 야 한다 PTPlB(ph osph oty ros in e ph osph ata s e 1B) 와 같이 탈인산화 활 성이 상실되면 계속적인 인산화를 유발시켜 세포의 성장을 조절할 수 없게 된다. 많은 종양 유전자가 티로신 키나제임이 잘 알려져 있으며 PTPlB 가 탈인산화 효소의 하나라는 사실은 이러한 경로가 암 유발에
중요한 단계임을 시사해 주고 있다. 티로신 키나제는 src 키나제라고 불리고 있으며 세포질이나 원형질막 에 존재하는 수용체와 직접 결합을 하지 않더라도 의부 신호를 매개 또 는 증폭시킬 수 있댜 티로신 키나제에 의해 인산화되는 단백질로 Abl 이 보고되어 있는데 DNA 에 결합하는 능력이 있는 것으로 보아 세포질에서 전달되 는 신호 를 핵 안의 유전자에게 전달하는 단백질일 것으로 추측된 댜 src 종양 유전자 산물은 특히 단백질의 티로신 잔기의 인산화에 관 여하며 그 외에 Ab!, Jes , erbB 암 유전자들도 여기에 관여하고 있음이 알려졌댜 7-3-5 유전자의 전사 신호가 수용체에서 인지된 후 원형질막과 세포질까지 전달되는 과정 에서 앞에서 언급한 암 유전자들의 산물이 작용하고 있음이 알려져 있 으나 아직 밝혀지지 않은 물질들이 많이 있다. 이중에는 핵에 존재하는 암 유전자 산물이 있는데 이들은 주로 DNA 에 결합하는 능력이 있으며 주로 유전자의 전사를 조절할 수 있는 단백질로서 세포의 성장 분화에 관여하는 유전자의 발현을 조절한다. 전사 인자로서의 암 유전자들은 이 들 자체의 발현이나 기능이 세포 조직에 특이하게 또는 세포 주기에 따 라 조절되어 직접적으로 성장 및 분화에 관여한다. 이들은 DNA 에 결합 하는 부위와 단백질-단백질 결합 부위를 가지고 있으며 성장 인자의 자 극이 전달되면 곧바로 DNA- 단백질 또는 단백질-단백질 상호작용을 통 해 유전자 발현을 조절한다. 이 조절이 평소에는 억제되어 있다가 과발 현이나 과소 발현 (undere xp ress i on) 되면 이 억제는 풀리며 암세포로 전 환되어 직접 유전자 발현에 기여한다. 그 예로 AP-1, fos , jun 동의 암 유전자 산물은 유전자 전사를 활성화시켜 암세포를 유도한다. 이들은 DNA 에 직접 결합할 능력을 가지고 있으며 PKC 에 의해 조절된다. 핵에
존재하는 암 유전자의 산물은 직접 다른 유전자의 전이를 조절하므로 전이 인자로서의 역할을 하고 있고 이 균형에 이상이 발생되면 세포 성 장의 균형이 깨진다. Reti no blasto m a(R b ) 유전자는 암 유발에 관련 있는 유전자의 발현을 억제하고 있다가 그 억제 기능의 상실로 유전자 발현 을 촉진시킨다. 이와 같은 암 억제 유전자들은 세포 주기에 따라 인산화 정도가 변화되어 Rb 의 활성화와 세포 주기가 관련이 있음을 시사해 주 고 있다. 7-4 전사 인자 원핵 세포의 유전자는 여러 개의 소단위체로 이루어진 한 종류의 RNA 중합 효소에 의해 DNA 에서 RNA 로 전사된댜 유전자의 선택적인 발현 은 원핵 세포의 RNA 중합 효소와 6 인자족 중에서 특정 (J 인자와의 상호작용으로 촉진 유전자를 인지하여 DNA 로부터 RNA 를 합성한댜 대 장균의 경우 일반적인 배양 조건에서 전사에 관여하는 6 인자는 a70 이 댜 a 70 은 촉진 유전자에 결합하지 못하나 RNA 중합 효소 - 6 복합체 형성시 촉진 유전자에 결합하여 전사 기능을 수행한다. 한편 질소원이 결핍된 배지에서는 a54 와 복합체를 형성하여 다른 촉진 유전자 DNA 를 활성화시킨다 즉 원핵 세포에서의 전사는 한 종류의 RNA 중합 효소와 조건에 따라 선택된 6 인자와의 상호작용으로 유전자 발현이 조절된다. 한편 진핵세포 유전자의 전사는 세 종류의 DNA- 의존성 RNA 중합 효소에 의해 조절된다. 큰 리보소멀 RNAs(Large ribo somal RNAs) 의 전 사를 담당하는 RNA 중합 효소 I , mRNA 와 대부분의 작은 핵 RNAs (small nuclear RNAs) 의 전사룰 담당하는 RNA 중합 효소 Il, 작은 리보 소멀 RNA 와 tRNA 및 U6 snRNA 생성 을 담당하는 RNA 중합 효소 III 가 있으며 이들은 프로모터로부터 전사를 수행하기 위해 여러 종의 보
조 단백질을 필요로 한다. 보조 단백질로는 일반 전사 인자, enhancer 인 자 둘 전사 중개 인자, TATA - 결 합 단백질과 회합하는 인자 (TAF) 들 등 이 알려져 있다. 한편 최근 일반 전사 인자에 속하는 TATA- 결합 단백 질 ( TBP) 이 세 종류의 RNA 중합 효소( I , II, III) 에 의한 복합체에서 공 통적인 구성 요소로 존재함이 밝혀졌다. 여러 종 의 진핵세포를 사용하여 RNA 중합 효소 II 유전자의 촉진 유 전자를 관찰한 결 과 유전자의 발현 조절을 위한 두 가지 특징이 밝혀졌 댜 이 TATA box 와 전사 개시 부위를 포함하는 pro moto r pro x ima l elemen t와 enhancer 또는 up s tr e am acti va ti ng 서 열 이 라 하는 DNA 조절 인자이다 . Enhancer 는 유전자에 따라서 대체로 촉진 유전자와 멀리 떨어 져 있고 방향성과 위치에 관계없이 유전자 발현에 영향을 미친다. RNA 중합 효소 II 의 전사 작용을 조절하는 전사 인자도 두 종류로 나뉘는데 이 는 기본 전사 인자와 전사 활성제이다. 기본 전사 인자는 전사가 정확 한 부위(i n iti a ti on s it e) 에서 시작되게 하고 일반적으로 모든 유전자 발현 에 필 요하며 일반 전사 인자라고도 한다. 전사의 활성제는 전사 작용을 활 성화시키며 유전자마다 특유의 인자가 존재하나 몇몇 경우에 있어서 는 여러 개의 유전자에 동일하게 사용되기도 한다. 활성 단백질은 DNA 결합 부위와 활성 부위로 구성되어 있으며 활성 부위와 유전자 발현을 활성화한댜 최근 활성제와 일반 전사 인자 사이에 me diat o r , adap tor , 또 는 보조활성제 등이 작용하는 밝혀져 있고 염색체의 소단위체 구조까지 가세하여 전사 인자간의 복잡한 상호작용에 의하여 유전자 발현이 조절 되는 것으로 알려져 있다 . 7-4-1 일반 전사 인자 RNA 중합 효소 II 에 의한 전사의 시작은 일반 전사 인자가 순차적으 로 복합체 (tran scri ption pre in itiat i on com p lex) 를 형 성 함으로써 이 루어 진
댜 아직까지 모든 요인들의 기작이 밝혀지지 않았지만 , 9 종 이상이 존 재하는 것으로 보인다(표 7- 3) . Promoto r pro x im al elem e nt 중 TATA 부 위는 RNA 중합 효소 II 유전자에 존재하며 TATA 부 위 결 합 단백 질 과 TFIID 복합체가 결합한 후 일반 인자와 RNA 중 합 효소 II 가 순 서 적 으 로 복합체 를 형성한다(그림 7-13). 일반 전사 인자 중 TFIID 복합 체인 TBP 은 유일한 서열 특이성 DNA 결합 요소이댜 일반 전 사 인자 들 은 기초적인 전사 또는 전사 억제에 관여하며 전사 활 성화 는 전 사 활 성제 와 일반 인자의 상호작용에 의해 유도된다. 7-4-2 전사 인자 단백질 인산화 효소에 의해 인산화된 단백 질 의 과인산화된 영역은 히 스톤에 대한 결합 부위로써 작용할 가능성이 있고 특정한 유전자 를 활 성화하는 전사 인자를 조절할 수 있다. DNA 에 결합하 는 활 성제 들 의 경 우 여러 종류의 DNA 결합 형태가 존재하는데 helix - tu m- h elix , zin c fing e r, homeodorn ain, 스테로이드 호르몬, he li x- 루프 - hel i x, leu ci ne zip per 등이 알려 져 있댜 DNA 결합 단백 질의 구조는 DNA 염 기 서 열 을 어떻게 인식하는가에 따라 몇 개의 유형으로 분리되었다. helix - tu m- heli x 구조의 단백질은 구조의 유사성으로 비교적 쉽게 확 인되었지만 다 른 유형의 구조는 구조 연구를 통해 확인한 후 서열을 바교하여 밝혀지 게 되었다. Helix - tu rn-helix ( HTH) HTH 구조는 DNA 인식을 위해 존재하는 구조 중 처음으로 밝혀진 형태이며 이 이론으로부터 많은 HTH 단백질과 단백질 -DNA 복합체를 확인하였다. HTH 단백질의 구조를 상세히 분석한 결과 다른 유형의 DNA 결합 단백질들이 s ite -s pecifi c 한 방법으로 DNA 를 인식하고 있다
표 7-3 RNA 중합 효소 II 의 전사 인자들 (38) Mammalia n Functi on Drosoph il a Yeast IIA To fac ili t a t e IID int e r acti on IIA IlA wi th the pro mote r /t e m p la te . IIB Bind s to RNA poly m erase II. IIB RAP 30/1 0 Re quire d for pre - in itiat i on comp le x for mati on . IID I3in d s to the TATA- ho molog y. B IID May fun cti on like the bacte r i al sig m a fac to r to pos it ion poly m erase on the pro mote r / tem p la te . IIE Bin d s to the RNA poly m e rase. IIE RAP 30/7 0 Re quired for pre -in itiati on comp le x for mati on IIS Elong a ti on fac to r ; not req uire d for pre - in itiat i on comp le x for mati on . RAP, RNA poly m erase-b i n d i ng pro te i n 는 생각을 할 수 있게 되었다. ACro 단백질, E. coli CAP 단백질, A 억 제 물질의 DNA 결합 부위와 같은 DN A 결합 단백질의 결정 구조가 알 려졌다. 세 단백질의 DNA 인식 부위를 관찰한 결과 이 부위는 a- 헬릭 스와 turn 그리고 두번째 a- 헬릭스로 구성되어 있었다(그림 7-14). 이 러 한 구조는 lac 억 제 물질, 434 억 제 물질, 434Cro, Trp 억 제 물질, 그리고 Fis 단백질과 같은 다른 HTH 단백질에서도 동일했다. Homeodomain Homeodom ai n 은 진핵생물에 존재하는 DNA 결합 단백질의 한 구조 이다. 초파리의 발생 과정에서 처음 밝혀진 이후 진핵생물에 널리 분포
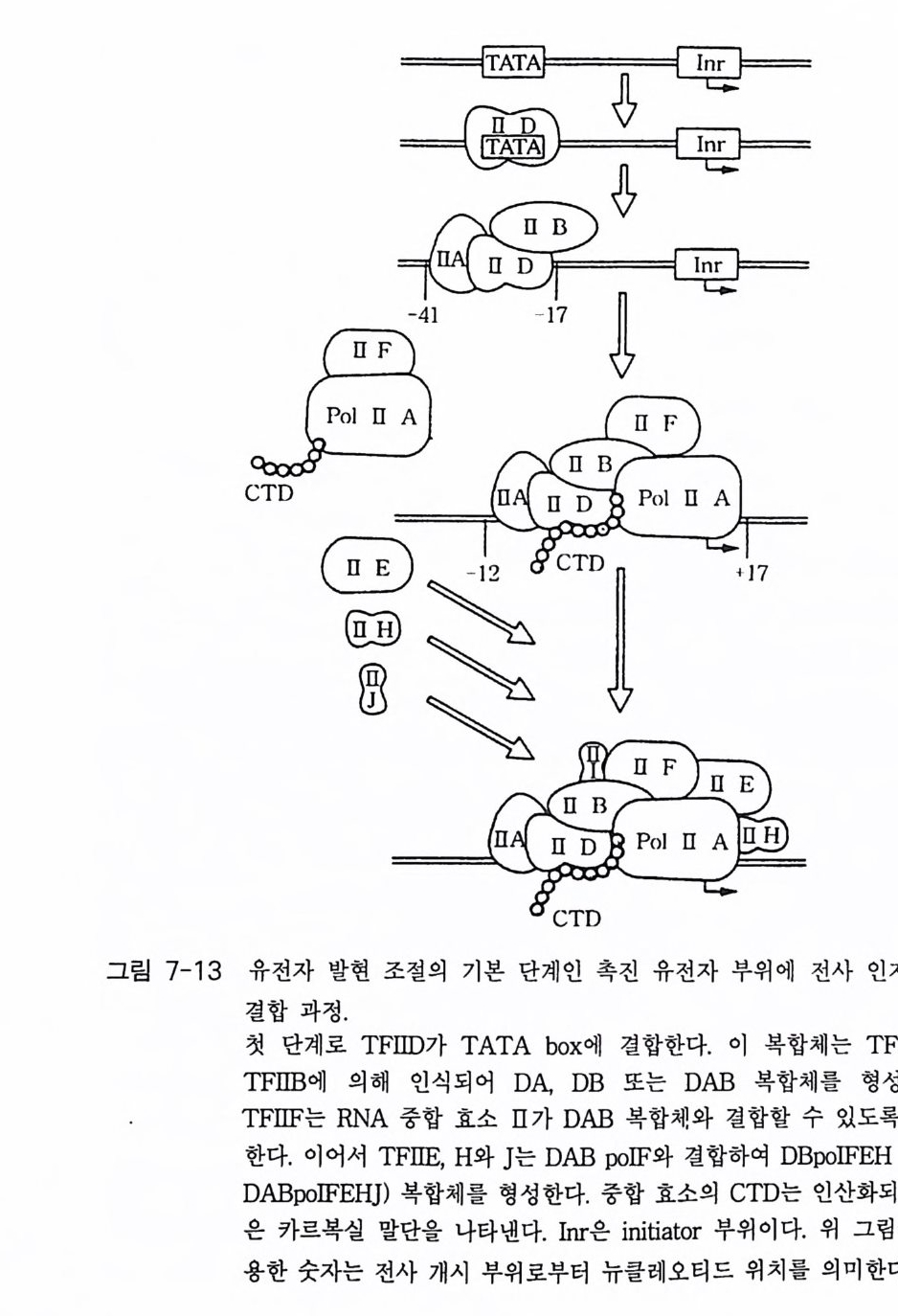 -41 -1 7
-41 -1 7
되어 있음이 확인되었다(그림 7-15). Homeodom ai n 의 아미노산을 분석한 결과 이 부위에는 HTH 구조가 포함되어 있음이 확인되었다. 그러나 HTH 와는 달리 60 개 의 잔기 로 구성 된 Homeodom ai n 은 스스로 DNA 와 결합할 수 있는 능력을 가지고 있음이 밝혀졌다. 그리고 단백질 결정 구 조로부터 확인된 homeodom ai n 은 N- 말단 부위와 3 개의 a 一헬릭스로 구 성되어 있음이 보고되었다. Zin c Fin g e r 단백 질 - DNA 상호작용에 관련된 중요 구조 중의 하나인 zin c fi n g er 의 구조가 개구리 (Xenop us) 의 전사 인자 IIIA(TFIIIA) 에서 발견되었다. 한 편 이와 동일한 구조가 pro to o ncog e ne, 일반 전사 인자 등에서도 밝혀졌 다 (42). Zin c fi n g er 의 구조는 30 개 아미노산 잔기가 반복해서 위치하고 있으며 각 구조에 는 C y s 一 Xz or 4-Cy s-X12- Hi s-X3- sHi s( 그림 7-16) 가 있 댜 이 구조 내에 위치하고 있는 2 개의 C y s 와 2 개의 Hi s 는 z in c 와 결합 을 형성하고 있다. 그러나 이 구조는 아직까지 3 차원 구조가 밝혀지지 않은 관계로 정확한 DNA 결합 형태가 알려져 있지 않은 상태이다 . 스테로이드 수용체 스테로이드 수용체는 스테로이드 호르몬, 레티노이드, 비타민 D, 타이 로이드 호르몬 등 그 외 많은 물질의 수용체이며 중요한 조절 단백질이 댜 이 수용체는 호르몬 결합 부위, DNA 결합 부위, 전사 활성 부위로 구성되어 있음이 보고되었다. 70 개 아미노산으로 구성되어 있는 DNA 결합 부위는 8 개의 시스테인이 함유되어 있다. 글루코코르티코이드(g lu cocort ico id ) 수용체의 DNA 결합 부위는 z in c 가 결합되어 있는데 이 부 위는 특이적으로 DNA 결합 부위를 인식하고 있다 . 스테로이드 수용체는 2 쌍씩 4 개 시스테인을 가지고 있어서 이 부위에 2 쌍의 zin c finger 가 있는 것처럼 보이지만 서열 형태는 TF ill A의 zinc
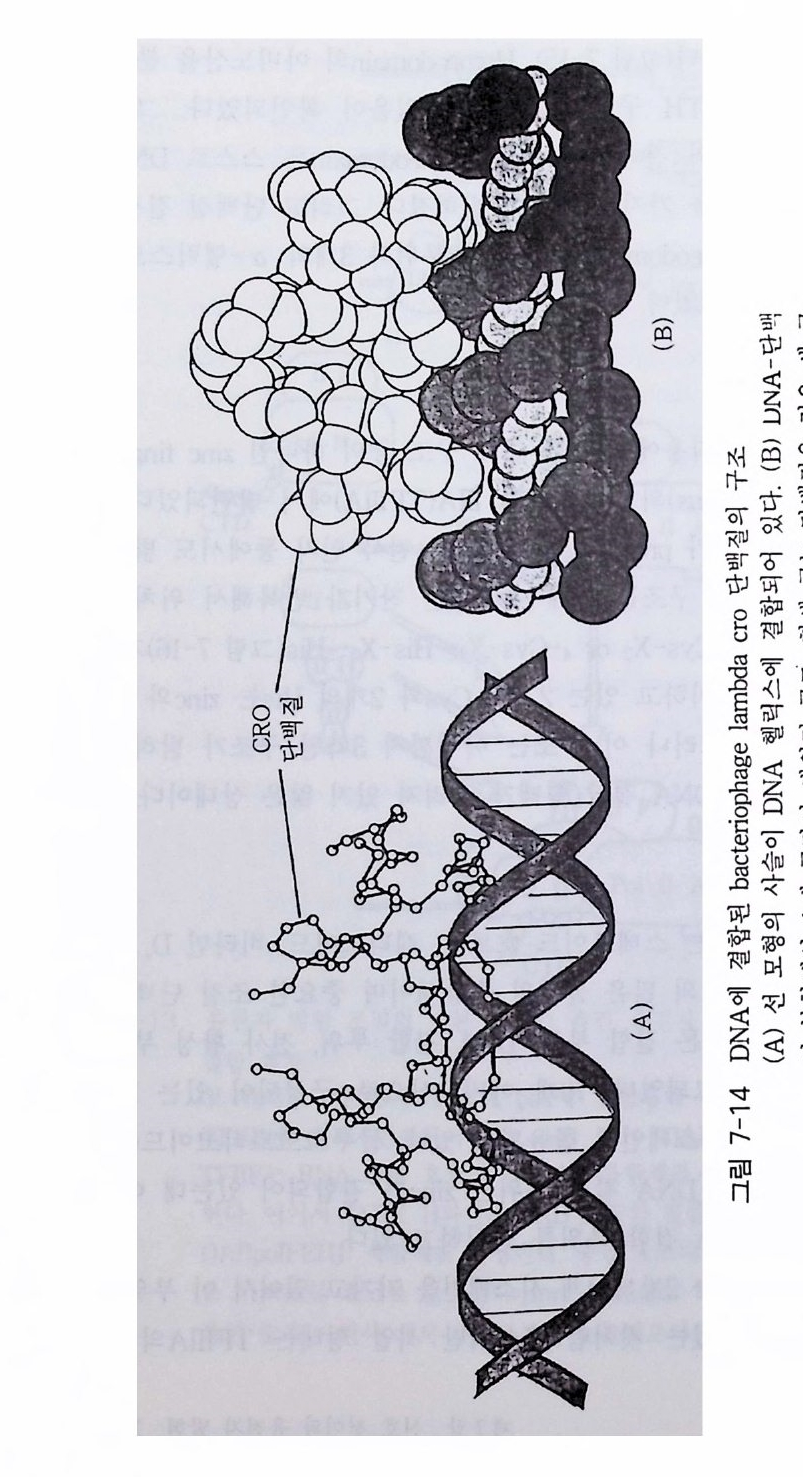
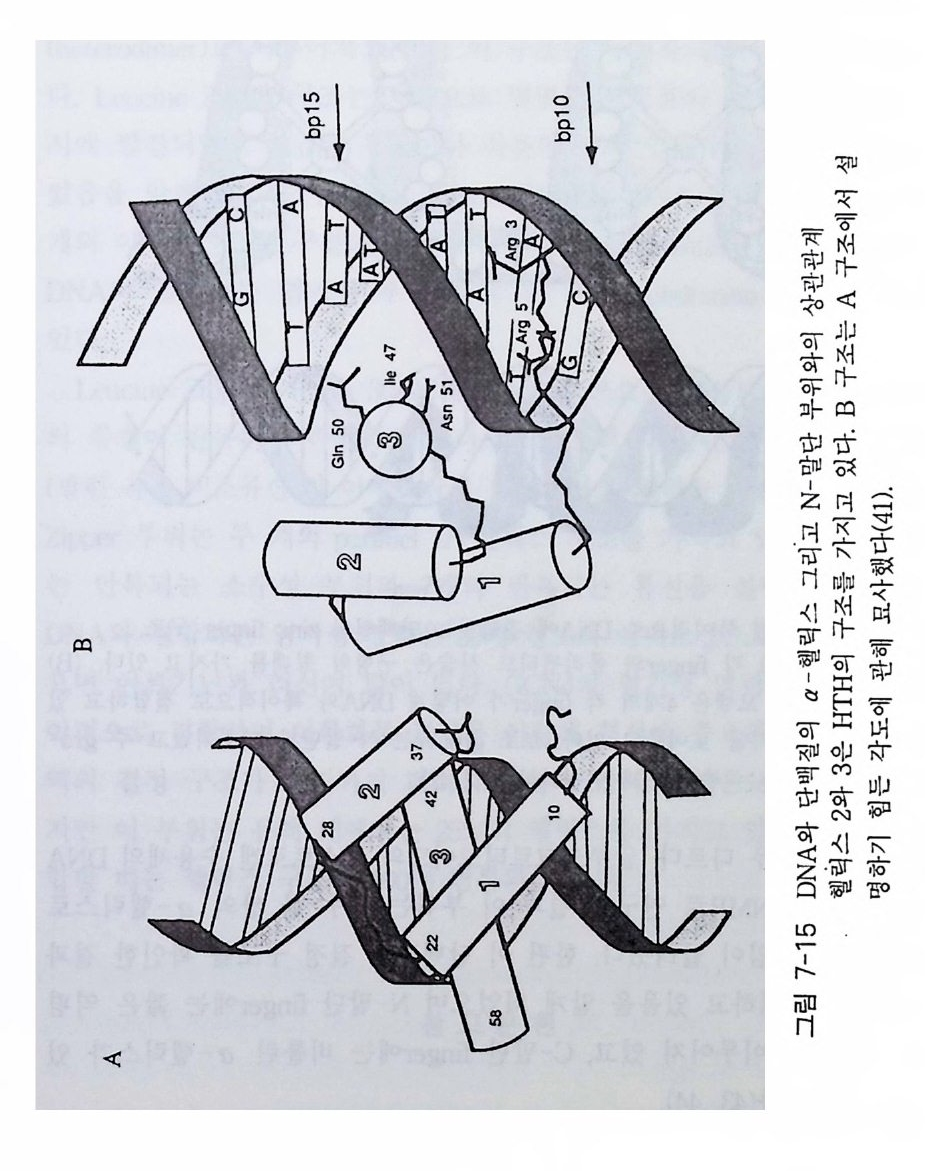 .. p51 b - pb 10 一빼 설
.. p51 b - pb 10 一빼 설
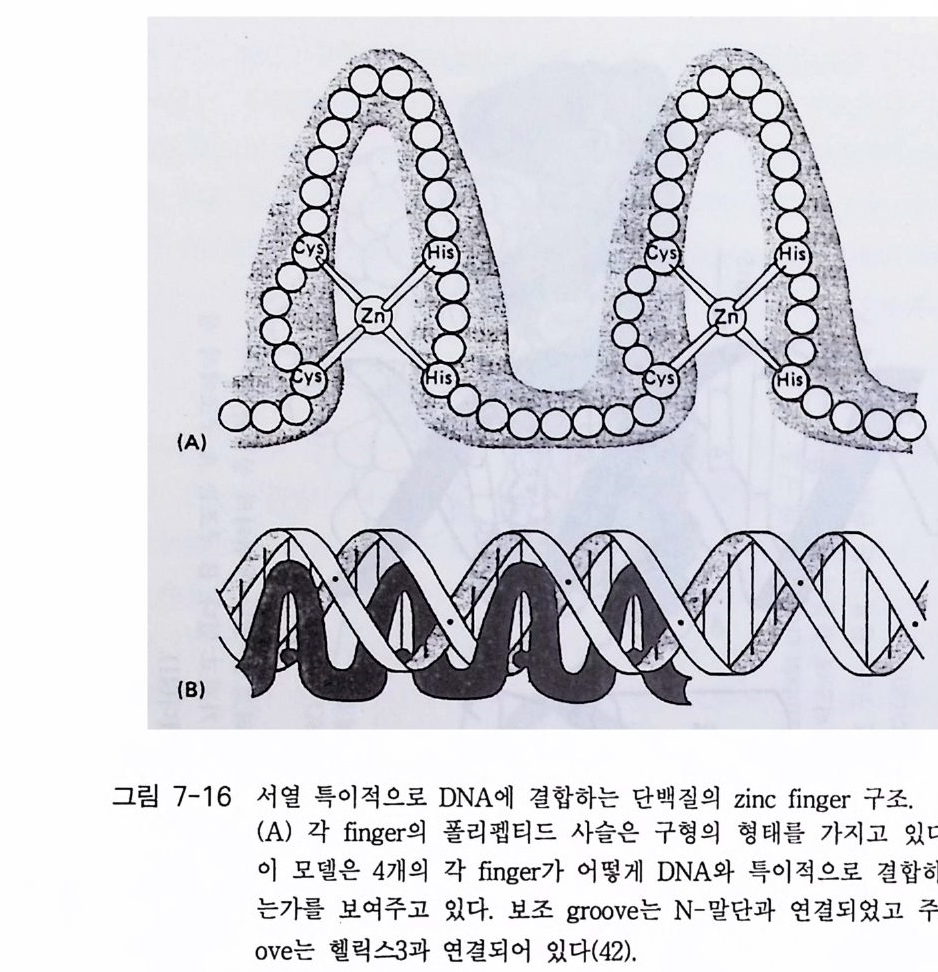 ‘\' 톤./ `• •d
‘\' 톤./ `• •d
fing er 와는 매우 다르다. 글루코코르티코이드와 에스트로겐 수용체의 DNA 결합 부위를 NMR 로 연구한 결과 이 부위는 모두 한 쌍의 a- 헬릭스로 된 단일 구형임이 알려졌다. 한편 이 단백질의 결정 구조를 확인한 결과 이량체로 존재하고 있음을 알게 되었으며 N- 말단 fi n g er 에는 짧은 역평 행 8 구조로 이루어져 있고, C- 말단 fing er 에는 비튤린 a- 헬릭스가 있 음이 밝혀졌다 (43, 44).
Leucin e Zi ppe r Leucin e Z ippe r(45) 와 hel i x- 루프 -hel i x(46) 형태를 가진 단백질들은 세 포의 성장과 분화에 중요한 역할을 하고 있다. 이 구조들은 이종 이량체 (he te r odi mer) 로 이루어져 있으며 이 구조는 유전자 발현 조절에 중요하 댜 Leuc ine Zip per 구조는 처음으로 몇몇 진핵생물의 전사 인자에서 동 시에 발견되었고 지금은 동물이나 식물의 전사 인자에서 넓게 분포되어 있음 을 알게 되었다. Leuci ne Zip per 단백질의 DNA 결합 부위는 60-80 개 의 아미 노산으로 구성 되 어 있으며 이 량화(dim e ri za ti on) 를 위 한 영 역 과 DNA 와 결합하는 염기성 부위 등이 두 개의 subdo main으로 구성되어 있댜 Leucin e Zip per 서 열은 30-40 개 의 아미 노산으로 구성 되 어 있으며 7 개 의 류신이 반복하여 존재하고 있다. 또 류신의 N- 말단 부위에는 소수성 (발린 혹 은 이소류신)의 아미노산이 반복해서 존재하는 경향이 있다. Leu Zip per 부위는 두 개의 par allel a- 헬릭스 구조를 가지고 있는데 이 구조 는 반복되는 소수성 부위와 7 개의 반복되는 류신을 설명할 수 있다. DNA 와 결합하는 염기성 영역은 30 개 정도의 아미노산으로 구성되어 있 으며 아르기닌과 리신이 많이 있다 . GCN4 의 염기성 영역은 DNA 와 특 이적으로 결합하며 이황화물 결합은 이량체 형성에 중요하다. 염기성 영 역의 결정 구조가 아직까지 밝혀지지 않아 상세한 것은 밝혀지지 않았 지만 이 부위는 용액 내에서는 25% 의 헬릭스를 가지고 있고 DNA 와 결 합할 때는 헬릭스 구조로 100% 변화되고 있다. 참고문헌 1) Sin gle to n , C. K, Delude, R L. and McPherson, C. E. (19ITT) Dev. Bio l. 119, 433
2) Kumag ai, A ., Pup illo, M., Gundersen, R., l\1iak e- L y e, R., Dev reote s , P. N. and Fir tel, R. A. (1989) Cell 57, 265 3) Pete r s, D. J. M. , V an Lookeren Camp ag n e, M. M., Van Haas te r t , P. J. M., Sp ek , W. and Schaap, P. 0989) ]. Cell Sci. 9 3, 205 4) Ha riba bu, B., R ajk o vic , A. and Dott in, R. P. (1986) Dev. Bi ol . 113, 436 5) McRobbie , S. J,, Jen ny n, K A., Duff y, K., Blig h t, K and Wi lli a m s, J. G. 0988) Develop m ent 104, 275 6) Wang, M. and Schaap, P. 0989) Develop m ent 105, 569 7) Oy am a, M. and Blwnberg, D. D. 0986) Proc. Natl. Acad Sc i. U.S .A. 83, 4819 8) Ma, P. C- C . and Siu , C-H. (1990) Mo!. Cell. Bi ol. 10, 3297 9) Sim pso n, J. and Herrera-Estr el la, L. (1990) Criti ca l Rev. Plant Sci. 9, 5 10) Short , T. W. and W. R. Bri ggs (1994) Annu Rev. Plant Ph ysi o l . Plant Mo!. Bol. 45, 143 11) Cuozzo-Davi s, M. , Yong , M-H., Gil ma rt in, P. M., Goy va ert s, E., Kuhlemeie r, C. Sarok in, L. and Chua, N-H. (19 90) Photo c h e m Photo b io l. 52, 43 12) Gil martin, P. M. , M emelin k, J., Hirat s u ka, K., Kay, S. A. and Chua, N-H. 0992) Plant Cell 4, 839 13) Luan, S. and Bog o rad, L. 0992) Plant Cell 4, 971 14) Qu a il, P. H. 0984) TIES. 9, 450 15) Romero L. C., Bis w al B. and Song , P.-S. (1991 ) FEES Lett. 282, 347 16) Guron, K., Chandok, M. R. and Sop or y , S. K. (1992) Photo c hem Photo b io l. 56, 691 17) Chae, Q., Park, H. J. and Hong, S. D. (19 90) Bi oc hem Bio p h ys. Acta 1051, 115
18) Lam, E., B enedy k, M. and Chua, N.-H. 0989) 1vlol. Cell Bi ol. 9, 4819 19) Park, M.-H . and Chae, Q. 0989) Bio c hem Bio p h ys. Res. Commum. 162, 9 20) Short , T. W. and Bri ggs, W. R. (19 90) Plant Ph ys io l. 92, 179 21 ) Wa rpeh a, K. M. F., Hamm, H. E., Raseni ck , M. M., Kaufm a n, L. S. (] 991 ) Proc. Natl. Amd Sci. USA 88, 8925 22) Thomp so n, W. F., K aufm an, L. S., Wats o n, J. C. (19 85) Bi oE ssay s 3, 153 23) Fluhr, R. and Chua, N- H . 0986) Proc. Natl . A 따 Sci . USA 83, 2358 24) Sharrock, R. A., Qu ai l, P . H. 0989) Genes Dev. 3, 1745 25) Fein b aum, R. L., Sto r z, G., Ausubel, F. M. (1991) Mo!. Gen Genet. 226, 449 26) Gu ilti n a n, M. J.. Marcott e, W. R., Qu atr ano, R. S. 0990) Sc ien ce 250, 269 27) Hamson, S. C. 0991) Natu r e 353, 715 28) Cohen, A., Plant, A. L., Moses, M. S. and Bray, E. A. 0991) Plant Ph ysi o l. 97, 1367 29) Plant, A. L., Cohen, A., Moses, M. S. and Bray, E. A 0991) Plant Ph ysi o l. 97, 900 30) Ba rtho lomew, D. M. , Ba rtley , G. E., Scoln ik, P. A. 0991) Plant Ph ysi o l. 96, 291 31) Qu atr an o, R. S., Ballo, B. L., Wi lliam son, J. D., Hambli n, M. T. and Mansfie ld , M. 0983) Plant Molecular Bio lo g y(G lodberg, R ed) p 343 New York, Liss 32) Pawson, T. and Gis h , G. D. (1992) Cell 71, 359 33) Ihle, J. N., Wi tthu hn, B. A., Qu elle, F. W., Yamamoto , K, T hi쿄e der, W. E., Kreid e r, B . and Sil ve nnoin en , 0. 0994) TIES. 19, 222
34) Barbaci d, M. (19 87) Annu Rev. Bi oc hem. 56, 779 35) Cantl e y, L. C., Au ge r, K R., Ca rpen te r , C., Duckwort h, B., Grazia n i , A., Kape ll er, R., and Solto f f, S. (1991) Cell 64, 281 36) Clark, S. G., Ste m , M J. and Horv itzd , R. 0992) Natu r e 356, 340 37) Muraka mi, Y., Sata k e, M., Yamag u shi -I wa i, Y., Sakai, M. , Mura- mats u , M. and Ito , T. (19 91 ) Proc. Natl. Arod Sci . USA 88, 3947 38) Parker, C. S. (1989) Current Op inio n in Cell Bi ol og y 1, 512 39) Zawel, L. and Rein b erg, D. (1992) Cur. Bi ol . 4, 488 40) Anderson, W. F., Ohlendorf , D. H., Takeda, Y. and Matt he ws, B. W. (1981 ) Natu r e 290, 754 41) Kiss eng e r, C. R., Liu , B. S., Ma rtin- Blanco, E., K ornberg, T. B. and Pabo, C. 0. (1990) Cell 63, 579 42) Klug , A and Rhodes, D. (1987) Trends in Bi oc hem Sc i. 12, 464 43) Hard, T., Kellenbach, E., Boelens, R., Maler, B. A. and Dahlman, K (1990) Sc ien ce 249, 157 44) Lu isi, B. F., Xu, W. X., Otw ino wski , Z., Freedman, L. P. and Yama- rnoto , K R. (1991) Natu r e 352, 497 45) Landschulz, W. H., Joh nson, P. F. and Mckn igh t, S. L. 0988) Sc ien ce 240, 1759 46) Murre, C., Mccaw, P. S. and Baltim o re, D. (1989) Cell 56, 777
제 8 장 박테리아의 신호 전이 박테리아는 갑작스런 환경 변화 또는 악조건인 환경에서 살아남기 위 해서 매우 섬세하고도 완벽한 신호 전달계를 가지고 있으므로 환경 변 화에 잘 적 응하여 살아남을 수 있다. 아울러 주위 환경 변화를 빠르고 민감하게 감지함으로써 자신이 좋아하는 환경을 만났을 때에는 그 방향 으로 이동하고 , 자신이 싫어하는 환경을 만났을 때에는 피하거나 포아를 형성함으로써 살아 남는 기능 또는 적응 능력이 잘 발달되어 있다. 따라 서 박테리아는 다양한 주위 환경의 변화 또는 의부 자극, 죽 화학 물질, 빛 , 삼투압 , 온도 , 전기장 그리고 자기장과 같은 외부 환경의 변화 속에 서 가장 살기가 좋은 환경을 찾아가는 능력 또는 환경이 좋아질 때까지 기다리는 능력을 가지고 있는 것이다. 이 능력을 위해서는 신호 전달 기 능이 잘 발달되어 있어야 하는데, 따라서 박테리아는 완벽하고도 체계화 된 이들 기작을 갖고 있다. 박테리아는 이러한 이유들 때문에 반옹 기작 을 분자 수준에서 이해하는 데 좋은 모델로 이용되고 있으며 또한 신호 전달 기작의 연구에도 널리 이용되고 있다. 그 동안 박테리아의 신호 전달 체계는 다른 생물들, 죽 진핵세포의 신 호 전달 체계와는 많은 차이점이 있는 것으로 간주되기도 하였는데 다
양한 연구가 진행됨에 따라 다른 생물계의 그것과 비교해서 공통점이 많을 뿐만 아니라 일치점도 있음이 밝혀지고 있는 만큼 박테리아의 신 호 전달 체계를 통해서 다른 생물의 그것을 이해할 수도 있을 것이다 . 본 장에서는 단백질 인산화 를 중심으로 하여 크게 3 가지 계로 나누어 생리학적, 구조적, 그리고 기계적인 측면에서 이 들 에 대해서 알아보고자 한댜 8-1 단백질 인산화와 신호 전이 기작 1978 년 Koshland 에 의해서 박테리아에도 단백질 키나제가 존재하고 있음을 발견하기 전까지는 이들 존재가 고려되지 않았다(1), 1986 년 Krebs 는 박테리아에서의 단백질 인산화 체계는 고등 생물의 그것에 비 해서는 훨씬 존재 정도가 적으며 또한 단순하다고 이야기하였다 (2). 그 러나 이 이론에 반하는 많은 연구가 보고되면서 박테리아나 다른 원핵 세포에서의 단백질 인산화가 고등 생물의 그것과 비교해 볼 때 결코 뒤 지지 않고 있음이 폭넓게 제기되고 있다. 지금까지 여러 장을 통해서 살펴본 바와 같이 진핵 세포에서는 외부 자극이 신호 전달 기작을 통하여 세포 내부로 전달되면 단백질 인산화 가 일어나고 세포 반응을 조절하는 것이 기본적인 기작의 하나이다 . 최 근 몇 년 동안 박테리아의 신호 전달 체계 역시 진핵 세포의 그것들과 같은 주요 조절 요인으로서 단백질 키나제가 고려되었다 (3, 4). 동물이나 식물의 단백질 키나제와 같은 인산화 효소들이 박테리아에서도 탄수화 물 수송, 유전자 전사, 그리고 세포 분화 둥에 관여하는 것으로 알려졌 다. 이뿐만 아니라 이들 인산화 효소들이 박테리아만이 갖고 있는 특별 한 반응, 죽 주화성, 박테리오파지 감염, 전염성, 박테리아 특유의 광합성 올 통한 C 아 고정 둥에 관여하고 있음이 밝혀졌다 (3, 4, 5, 6, 7).
인산화 를 중심으로 크게 3 가지 체계로 나누어서 박테리아의 신호 전 달 기작을 알아보기로 하겠다. 그 림 8 - 1 은 이들 3 가지 체계인 단백질 인 산화 효소와 탈인산화 효소계, 감지기와 반응계, 그리고 인산 전이 효소 (p hosp ho t rans f erase) 계를 계략적으로 보여주고 있다 (8). 그림 8-1 A 는 고전적인 단백질 인산화 효소 및 탈인산화계 (class i cal ATP - 의 존 성 단백 질 키나제 / 포스파타제)를 나타낸 것으로 이들 효소들은 진핵세포와 마찬가지로 단백질의 세린, 트레오닌 , 또는 티로신 잔기를 인산화시키거나 탈인산화시킨다 . 모든 박테리아의 단백질 키나제는 인산 기 주게 (donor) 로서 ATP 를 이용하고 있다 박테리아의 경우, 단백질 키 나제와 포스파타제가 분리된 두 개의 단백질로 존재하면서 반응을 조절 하기도 하고, 또는 하나의 단백질로 두 가지 기능인 인산화 및 탈인산화 반응 을 촉 매하기도 한댜 그림 8-1 B 는 감지기와 반응계 (sensor- ki nas e/ resp o n se reg u lato r s y s t em) 를 나타내는데 일반적으로 < 두 개의 성분계 (tw o comp on ent s y s t em) > 로 잘 알려져 있댜 이 계에서는 감지기-키나 제의 Hi s 가 인산화되는데 이때도 역시 인산기 주게로서 ATP 가 사용된 댜 이 인산기가 다시 반응 조절자의 아스파르트산에 전달된다. 따라서 반옹 조절자의 인산화가 생리 반응의 활성도를 조절하게 된다. 이뿐만 아니라 몇몇 반응(예, 질소 고정이나 주화성)에서는 이들 감지기나 조절 자 이외에도 3 개 또는 그 이상의 세포질 내 단백질이 관여하고 있다. 자 세한 내용은 8-4 에서 언급하기로 한다 . 그림 8-1 C 는 PEP(ph osph o-enolpy ru vate ) 의촌성 인산 전이 효소에 의한 단백질 인산화 및 세포 조 절을 보여주고 있다. 이 계에서는 PEP 에 의해 인산기가 계속 다음 단계 로 전달된다. 즉 PTS 인산기 전달 사슬을 통해서 전달되는데 이때 5 개 의 단백질이 관여하고 있다. 이들 단백질을 통해서 당이 전달된다.
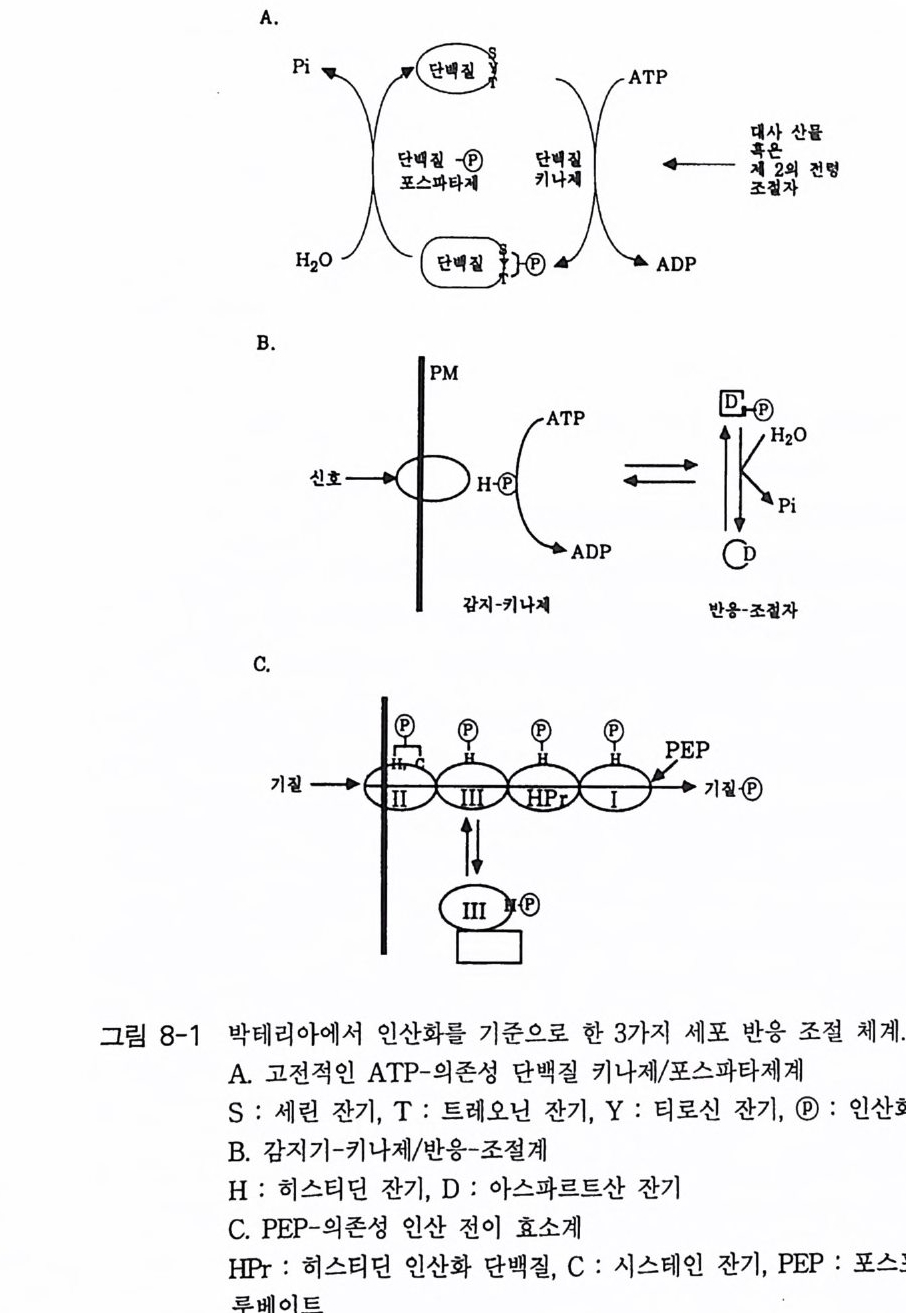 A.
A.
8 오 고전적인 단백질 키나제와 포스파타제계 고전적인 단백질 키나제, 죽 ATP 소모에 의해 단백질의 세린, 트레오 닌 그리고 티로신 잔기의 인산화가 이루어지는 계로서 크게 3 가지로 나 누어 살펴보고자 한댜 ATP 의존성 단백질 인산화 효소의 종류 및 그 특 성, 이 체계의 대표적인 예로서 IDH( 이소시트레이트 탈수소 효소, iso - cit ra te dehy cl rog e nase) 안산화 사슬, 그리고 박테리아의 사회적인 행동 에 관여하는 신호 전달 기작의 주요 부분을 차지하는 세린/트레오닌 키 나제에 관해 !vly x ococcus xan t hus 를 통해서 살펴보기로 하겠다. 8-2-l ATP 의존성 단백질 키나제 Nucleosid e trip hospha t e 로부터 인산기를 기질 단백질의 아미노산에 전 달하는 데 관여하는 효소인 단백질 키나제는 크게 5 가지 유형으로 나눌 수 있는데, 첫째 세린이나 트레오닌의 알코올기에 인산기를 전달하는 효 소(단백질_세린/트레오닌 키나제), 둘째 티로신의 페놀기에 인산기를 전 달하는 효소(단백질 - 티로신 키나제), 셋째 히스티딘의 l 혹은 3 번 위치, 아르기닌의 g u ani do 기, 또는 리신의 NH2 기에 인산기를 전달하는 효소(단 백질-히스티딘 키나제), 넷째 아스파르토산이나 글루타민산의 아실기에 인산기를 전달하는 효소, 끝으로 시스테인 잔기에 인산기를 전달하는 효 소가 그것이다 (9). 박테리아에서 발견되는 대부분의 단백질 키나제는 ATP 의 r 위치의 인산기를 인산기 주게로 이용하기 때문에 ATP 의존 성 인산화 반응이라 표현한다. 물론 몇몇의 경우는 ATP 를 인산기 주게 로 사용하는 것이 아니라 다른 반응 중간체나 대사 산물, 예를 들어 PEP, 아세틸 포스페이트 (ace ty l ph osph ate ) 또는 카바모일 포스페이트 (carbamoy l p hos p ha t e) 를 사용하기도 한다(1 0, 11). 단백질-히스티딘 키나제는 신호 전달계 중 <두 개의 성분 조절계>로
잘 알려져 있는 세포 반응을 조절하는 계에 관여하는 것이 대 표적 이다 . 이들 조절계는 적어도 20 개 이상의 다른 기능을 조절하는 데 관여하는 것으로 알려져 있는데, 예 를 들어 주화성, 질소 고정, fore ig n 유전자 발 현, 포자 형성 (s po rula ti on), 그리고 분비 단백질 (exo p ro t e i n) 합성 등 다양 하댜 이 계의 신호 기작은 다음과 같다 먼저 단백질 키나제(감지기)가 외부 환경 변화 또는 외부 신호를 인지하면 자동 인산화 (au t o p hos p hor y 一 la ti on) 가 일어난댜 감지 단백질 키나제의 히스티딘 잔기가 인산화되면 반응 조절자의 아스파르트산 잔기 에 위 의 포스포히 스티 딘(p hos p hoh i s tidi ne) 의 인산기가 전달된다 그 후 조절 작용이 진행되면 끝으로 단백 질 포스파타제가 조절 단백질에 작용하여 탈인산화를 시키면 이 단백질 은 비활성화 상태로 돌아가 다음 신호를 기다리게 된다 . 감지기로 작용하는 단백질-히스티딘 키나제의 일반적인 구조적 특징 은 C- 말단의 6 개의 아미노산 중 하나의 아스파라진을 가지고 있다(1 2). 대부분 이 키나제는 세포막과 결합되어 있는데 2 개의 소수성 막 관통 배 열을 가지고 있댜 세포 바깥에 위치하는 N- 말단 부분은 외부 신호 를 받고 세포질에 위치하는 C- 말단은 키나제나 포스파타제의 활성도를 조 절하는 기능을 가지고 있다(1 3). 그러나 주화성에 관여하는 Che A( 키나 제)나 질소 고정에 관여하는 N tr B 는 세포질 단백질로서 신호 를 세포 내 에서 받기도 한다 (12, 14). 홍미로운 사실은 인산화된 Che A 가 인산기를 질소계인 N trC에 직접 전달하기도 하는데, 이는 박테리아의 성장 및 대 사에 서로 다른 경로가 직접 연결되어 있음을 보여주고 있다 (15). 박테리아에 존재하는 많은 단백질 키나제들이 단백질 세린/트레오닌 키나제에 속한다. 박테리아의 경우 단백질의 트레오닌보다는 세린에 더 많이 또는 더 자주 인산화가 이루어지고 있다(1 6). 단백질 키나제가 어디 에 존재하느냐에 따라 두 그룹으로 분류할 수 있는데, 하나는 세포질에 존재하며 다른 하나는 리보솜이나 막에 결합되어 있다 07, 18). 박테리아 에서 발견되는 이들 키나제들은 어디에 존재하느냐에 관계없이 인산기
주게 로 서 대부분 ATP 를 사용하는 것과 자동 인산화가 잘 일어나지 않 는 특 징이 있댜 많은 단백 질 세린 / 트레오닌 키나제가 여러 종의 박테리 아에서 발견 되었 는 데, 진핵세 포 의 키나제와 아미노산 서열에서뿐만 아니 라 조절받는 요인 들 에까 지 비 슷 한 것 으로 보고되었다 . 예 를 들 어 My x o- coc cus xan t hu s 로부 터 단백 질 세린 / 토레오닌 키나제 를 발현시키는 유전 자인 p knl 의 아미노산 서 열 이 진 핵세포 키나제의 촉 매 부위의 그것과 거의 일치 하 는 것으로 나타 났 다(1 9) . 이 유전자의 생성물인 Pknl 은 세린 과 트 레오닌 잔 기 모 두 에 자 동 인산화가 일어나며 분화 를 조절하는데 중 요 한 역 할을 하 는 것으 로 알려 졌 다 . E. col i로부터 단백질 키나제 C 와 같은 효 소가 발견 되었 는 데 ( 2 0), 이 효소는 동물의 단백질 키나제 C 와 마 찬 가 지로 Ca2’ 및 인지 질 의 존 성이며, DAG 나 포볼 에스터에 의해 활성 화되기도 한다. 이러한 발견 은 적어도 단백질 키나제의 몇몇 종류는 진 핵 세 포 의 그 것 들 과 비 슷 한 것 으로 여겨진다. 박테리아의 단백 질 트 레오닌 키나제 활성도가 E. col i에서 처음 보고 된 이래 (2 1), 여러 종의 다른 박테리아에서 발견되었다. 예 를 들어 Rho-dosp iril l u m rubrum(22), Rhodomi cr obiu m vannie l ii( 23 ), Clostr idi u m the rmosu[fu r ic u m(24), S. pyo g e nes(25), Pseudomonas aerug ino sa(26) 등 이 그것이다. 홍미 있게도 이 들 키나제는 진핵세포의 그것과는 기능 면 에서나 아미노산 서열에서도 비슷한 점이 없으며 특히 동물의 그것에 작용하는 활성제나 억제제에도 반응하지 않는 것으로 나타났다 . 그러나 아직까지 박테리아의 단백질 티로신 키나제의 분리 정제나 유전자 클로 닝에 관해서 보고된 바가 없다 . 따라서 그 효소의 구조나 기능의 이해는 좀더 기다려야 할 것이다. 박테리아의 ATP 의존성 인산화 효소는 인산기 주게로서 ATP 를 사용 하지만, 몇몇의 경우는 주게로서 다른 뉴클레오티드를 사용하기도 한다. P. aeru gz· nosa 에서 발견된 단백질 Al g R2 는 주게로서 ATP 뿐만 아니라 GTP 도 사용하고 있다('2:7). 또한 Leg ion ella m i cdade i에 존재하는 PK2 는
cAMP 뿐만 아니라 cGMP 의존성 인산화 단백질이다 (2 8 ). 또 다 른 박테 리아의 단백질 인산화 효소는 진핵세포의 키나제와는 달리 외부 단백질, 예를 들어 카세인 (case i n), 히스톤(hi s t one), 프로타민(p ro tami ne), 또는 포 스비틴(p hosv iti n) 등은 인산화시키지 못한다 (3) . 이러한 이유로 해서 이 들 단백질을 기질로 하여 박테리아의 키나제 활성도 를 측 정한 초기 연 구에서는 단백질 키나제들을 발견하지 못하였다. 그러나 최 근 에 예외적 인 사실이 발견되었는데 S. py o g enes 는 히스톤과 프로타민 을 각각 인산 화시키는 두 개의 키나제를 가지고 있음이 보고되었다 (25). 박테리아에서 발견되는 단백질 안산화 효소는 종에 따라 다양할 뿐만 아니라, 지금까지 살펴 본 바와 같이, 진핵세포의 그것과 비슷한 면도 있 으나 박테리아 자신만이 가지는 특이성도 동시에 가지고 있다. 따라서 이들 키나제의 구조와 기능 나아가서 세포 반응 조절 기작을 이해하기 위해서는 좀더 기다려야 할 것 같다. 8-2-2 이소시트레이트 탈수소효소 인산화 순환 생명체에서 대부분의 생명 현상을 조절하는 기작 중의 하나가 단백질 의 인산화이다 (29, 30). 원핵 세포에서 처음으로 밝혀진 인산화에 의해 조절되는 기작이 E col i에서 발견된 이소시트레이트 탈수소 효소 (ID H) 가 관여하는 경로이다 (30, 31). IDH 의 인산화 순환은 이소시트레이트가 글리옥실레이트(g l y ox y la te)를 생성하는 경로를 조절하는 것인데, 죽 이 경로(g l y o xy la te c y cle) 는 식물이나 미생물 계에서 발견되는 것으로서 아 세테이트나 지방산과 같은 탄소원을 축적하는 데 필수적인 경로로서 Krebs 회로가 진행되는 것이 아니라 글리옥실레이트 회로로 진행됨으로 써 75% 의 에너지를 저장할 수 있게 된다 (32, 33, 그림 8-2). IDH 는 활성화 자리에 있는 세린 113 에서 유일하게 인산화가 일어나는 데 (33, 34), 많은 다른 인산화 효소와는 달리 IDH 가 인산화될 때 비활성
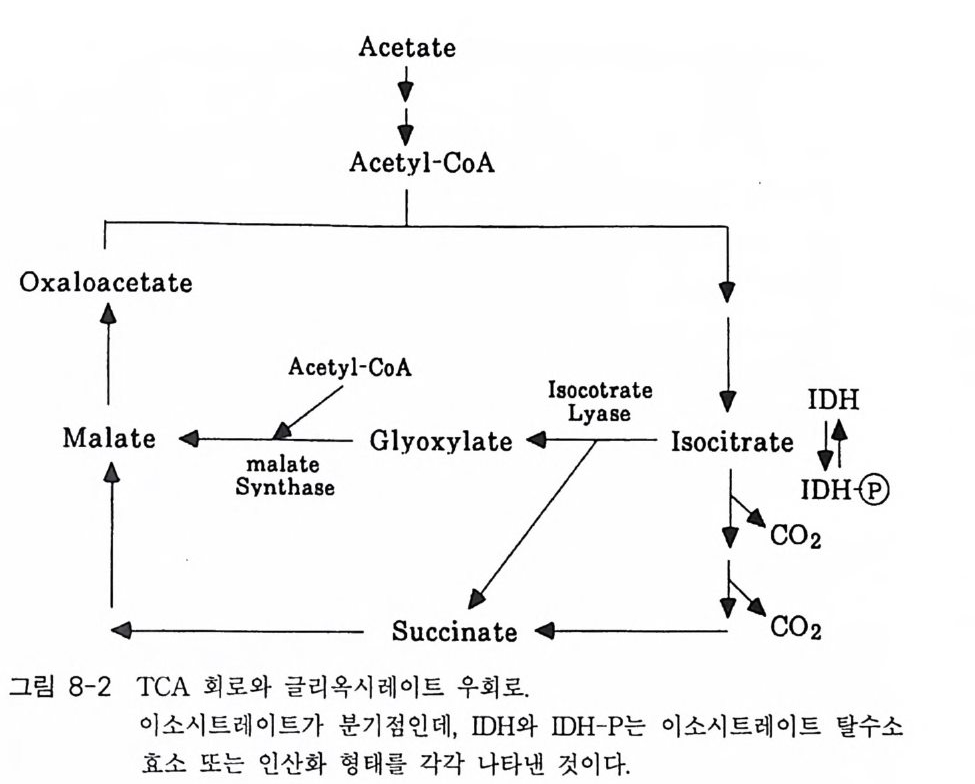 Acet소 atcee- Cl
Acet소 atcee- Cl
화가 된다 (33, 35). 세린 113 을 아스파르트산으로 바꾸었을 때에도 이 효 소는 비 활 성화가 되는데, 이는 이 부분의 아미노산 잔기가 음전하를 가 질 때 비 활 성화가 됨을 보여주고 있다 (34). IDH 의 활성화 자리에 존재하 는 세린 113 이 기질인 이소시트레이트와 수소결합을 하는데, IDH 가 인 산화되어 비활성화되면 이소시트레이트는 입체 장애와 정전기적 반발에 의해서(인산기와 citrat e ) 세린 113 과 결합할 수 없게 된다(그림 8--J , 36). IDH 의 인산화 및 탈인산화는 하나의 단백질이면서 두 개의 기능을 가 지 는 효소인 IDH 키 나제/포스파타제에 의 해 촉매된다 (37). 이 효소는 키 나제와 포스파타제의 활성도를 동시에 갖는 하나의 단백질로서 같은 활 성화 자리를 가지고 있다. 즉, 같은 활성화 자리에서 인산화 및 탈인산화 를 위해 두 개의 기질이 작용한다는 것이다. 이 효소는 또한 특이하게도
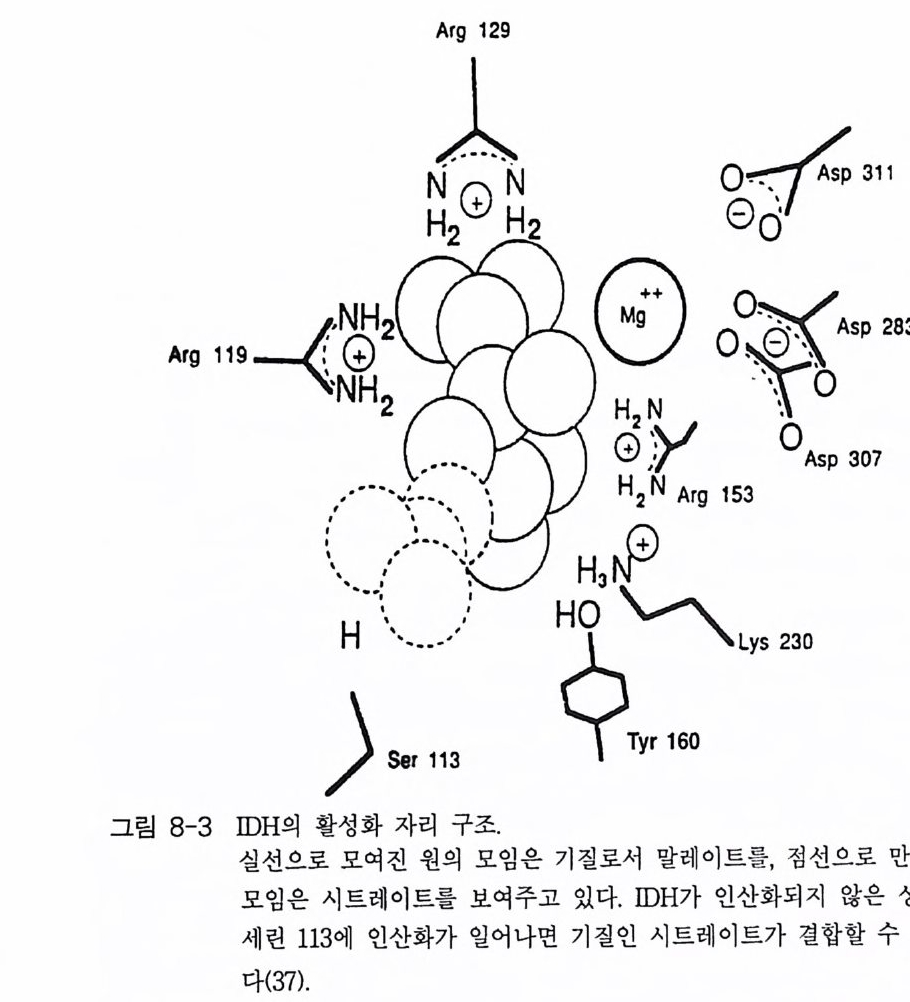 Arg 129
Arg 129
ATPase 의 활성도를 가지고 있는데, 이 효소의 활성도는 ATP 또는 ADP 의 세포질 내 농도의 영향을 받게 된다. 동시에 이 효소의 ATP 결합 자 리 역시 하나로서, 이 효소는 하나의 기질 결합 자리 및 하나의 ATP 결 합 자리를 가짐으로써 세포 반응을 조절한다 . 즉, 탈인산화 반응은 먼저 이 효소 (IDH 키나제/포스파타제), ADP 및 인산화 ID H(p hos p ho-IDH) 의 4 개 복합체를 형성한다. 그리고 인산화 -IDH 의 인산기가 ADP 에 전달되고
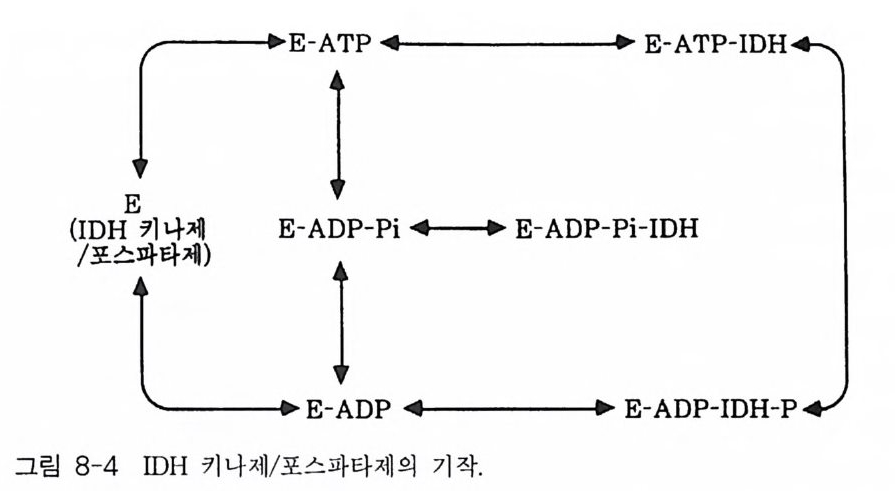 E广 E-Af P ◄ ► E-ATP-1
E广 E-Af P ◄ ► E-ATP-1
다시 물 분자에 전달된다. 이 연쇄 반응은 마침내 인산화 -IDH 의 탈인산 화 를 유도하게 된다(그림 8-4, 38, 39). 이러한 IDH 인산화 순환은 이소시트레이트가 글리옥실레이트 순환으 로 가느냐 Krebs 회로로 가느냐를 결정하는 중요한 단계가 된다. 인산화 에 의해 IDH 가 저해되면 이소시트레이트는 Krebs 회로로 진행될 것이 다 (32). 이러한 경로의 선택을 조절하는 가장 중요한 요인 중의 하나로 서 AMP 를 들 수 있다. AMP 는 IDH 포스파타제를 활성화시키지만 IDH 키나제 를 저해시킨다. 즉 세포 내에 AMP 가 많으면 세포는 에너지를 필 요로 하게 되는데, 이때 AMP 가 IDH 포스파타제를 활성화시킴으로써 이소시트레이트는 Krebs 회로로 진행되며 따라서 세포가 필요로 하는 에너지롤 생성하게 된다. 반대로 세포 내 AMP 의 농도가 낮아지면 IDH 키나제가 활성화되면서, 이소시트레이트는 글리옥실레이트 순환으로 진 행되며 에너지를 축적하게 된다 . 따라서 세포 내의 이 효소 활성도는 세 포 내 에너지 존재 (ATP/ADP, 또는 ATP/AMP 의 비)와 밀접한 관계가 있는데, 죽 현재 대사 산물을 통해서 에너지를 필요로 하느냐 또는 에너 지를 저장하느냐에 따라 결정된다고 할 수 있을 것이다 (40).
8-2-3 단백질 세린/트레오닌 키나제 그람 음성 박테 리 아인 My x ococcus xan t hus 는 특이 한 삶의 순환과 사 회적 행동성 때문에 많은 과학자들의 관심을 끌고 있다 . 영양이 충분치 못할 때 이들은 한 곳으로 모여들어 자실체(fruiti n g bod y) 를 형성한다. 이 자실체 안쪽에는 막대 모양의 영양 세포 (ve g e t a ti ve rod- sha 1.le d cell) 들이 모여 있으며 열이나 건조한 악조건에서도 생존하게 된다(그림 8-5). 이들 점균 포자 (m yx os po re) 는 영양이나 기타 조건이 좋 아지면 다시 성 장을 계속한다 (42). M xan th us 의 발달 주기는 매우 특 이한 프로그램에 의해 진행되는데, 특히 막대 모양 세포 를 형성할 때나 점균 포자를 형성 할 때 관여하는 여러 다른 유전자가 관여하며 또한 이에 의해 일시적으 로 조절된다 (43) . 이들 M xan t hus 의 발달 순환 과정과 많은 세포들이 모이는 형 태 형성 현상들은 진핵세포의 Di ct y o ste l iu m d i sco i deum 과 같 은 곰팡이의 그것과 매우 비슷하다 (41, 44). D. d i sco i deum 은 신호 전달계의 구성 물질인 수용체, G- 단백질, 조절 자, 그리고 다양한 단백질 세린/트레오닌 키나제를 가지고 있으며 이 들 이 발달이나 생활 주기에 중요한 역할을 하고 있는 것으로 알려져 있다 (45). 최근 M xan th us 에서 진핵세포의 그것과 거의 비슷한 단백질 Ser/Thr 키나제가 발견되었다 (46). PCR(Polym erase Cha in Reacti on ) 기술을 이용 하여 얻은 결과에 의하면 M xan t hus 는 적어도 3 개의 진핵세포의 그것 과 비슷한 효소가 존재하는 것으로 밝혀졌다 (47). 그 첫번째 단백질 인 산화 유전자가 p knl 인데 DNA 서열에 의해 유추한 아미노산 수는 693 개로 나타났으며 N- 말단 쪽의 절반은 진핵세포의 단백질 세린/트레오닌 키나제의 촉매 부위의 아미노산 서열과 거의 일치함을 보여주고 있다 (48). 이외에도 이 인산화 효소는 RXXS/T 의 아미노산 서열을 인지할 수 있으며 이 서열 내의 세린이나 트레오닌울 인산화시킬 수 있다 (49).
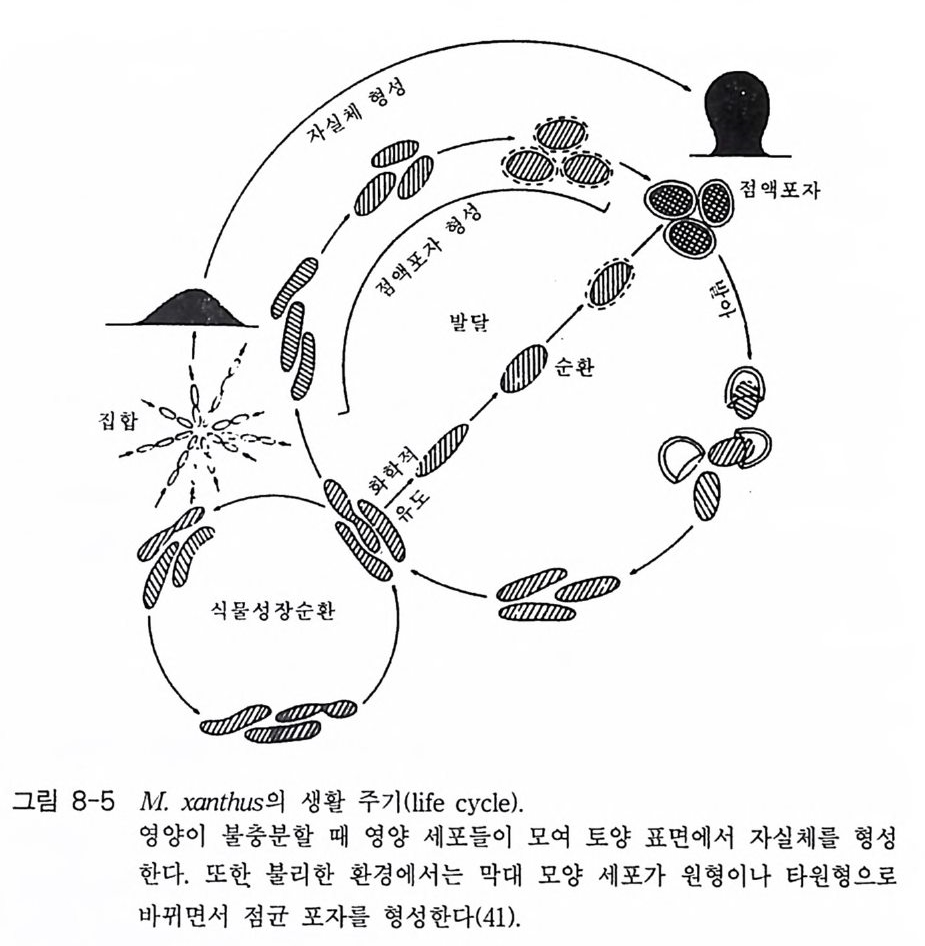 자
자
즉 p knl 으로부터 생성된 단백질인 Pknl 은 3 개의 RXXS/ T 배열을 가지 고 있는데 RQ RS( 아미노산 517-520), RLRT(540-543), 그리고 RARS (689- 6 92) 가 그것이다 (47). 이는 진핵세포의 세린/트레오닌 키나제 중에 서도 CAM - 키나제 II( 칼모듈린 - 키나제 II) 와 아미노산의 서열이나 영역의 구조가 비슷한데, 칼모듈린은 Ca 2+- 결합 단백질인데 , 이 박테리아가 점 균 포자를 형 성 할 때 Ca 2+ 을 필요로 하고 있다 (50). Pknl 의 역할을 알아보고자 결손 돌연변이체인 L1Pknl 를 제조하였고
이 유전자를 가지고 있는 돌연변이 세포는 풍부한 영양 상태에서 정상 적으로 성장하였다. 그러나 자실체를 충분히 형성하지는 못하였다. 이 돌연변이 세포는 정상 세포보다 4_8 시간 일찍 응집을 시작하였고 자실 체는 훨씬 작았으며 단단하지 않았다 . 또한 포자 형성은 정상 세포보다 더 빨랐다. 따라서 포자의 형성률이 낮았는데 정상 세포의 35% 정도밖 에 형 성 치 못하였다 (47). 따라서 M. xan t hus 의 자실 체 와 포자 형 성 에 진 핵세포의 단백질 세린/트레오닌 인산화 효소와 같은 세린 / 트레오닌 키나 제(특히 p lml) 가 관여하는 것으로 여겨진다. 그러나 아직까지 박테리아 에서 신호 전달 기작에 관한 정보는 매우 부족한 상태이다. 즉, 이 형태 형성을 위한 외부 신호, 그것을 받는 수용체, 진핵세포에서와 비슷한 역 할을 하는 G 一단백질, 그리고 조절자 등 그들의 존재 확인 및 반응 경로 등에 관하여 더욱 많은 연구가 진행되어야 할 것이다. 8-3 감지 와 반응계 (sensor-kin a se/resp o nse-reg u lato r sy st e m ) 많은 박테리아의 신호 전이에 관여하는 단백질은 두 가지로 구성되어 있는데 감지기로서의 기능을 가지는 전달자와 반옹 조절자로서의 기능을 가지는 수신자가 그것이다. 그림 8-6 에서 보는 바와 같이 비공유 결합을 통해 의부 신호가 정보로서 전달되면, 인산화 반응을 통해서(전달자 부분 의 인산화) 수신자와 정보 교환을 하며 그 정보가 세포 반응과 연결되는 데 이는 <두 개의 성분 신호계(tw o-com po nen t sig naling s y s t em) >로 널 리 알려져 있다. 감지기는 전형적으로 C- 말단(세포 내부)에 전달 영역과 N- 말단(세포 외부)에 수신 영역(i n pu t dom 책 1) 을 가지고 있다. 반응 조절 자는 N- 말단의 수신자 분자와 c- 말단의 출력 영역 (ou tp u t dom ai n) 으 로 구성되어 있다. 감지기의 입력 영역과 통신을 함으로써 감지기에 입 력된 신호가 이들 영역을 거쳐 증폭되어 출력 영역을 통하여 세포 반응
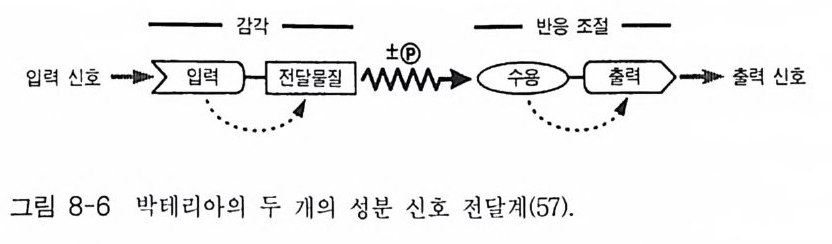 감각 - 반응조절 -~
감각 - 반응조절 -~
울 조절 하게 된댜 전달자와 수신자의 정보 교환을 위한 유일한 기작에 는 인산화 및 탈인산화 반응이 관여하고 있다. 먼저 이 인산화 및 탈인 산화 반응에 대해서 살펴보고 박테리아에서 이 신호 전달계에 속하는 대표적인 세 가지 반응, 질소 고정, 주화성, 그리고 삼투 조절의 신호 전 달 기작에 대해 알아보기로 한다. 전달자가 수신자의 인산화 상태를 조절하는 기작은 그림 8-7 에서 보 는 바와 같이 진행된댜 첫째는 인산화 반응으로, 전달자 자신은 자동 키 나제 (au t o ki nase) 활성도를 가지는데, ATP 로부터 인산기를 받아 자신의 His 잔기에 인산화가 일어난다 (51). 이 인산화 Hi s 는 인산기를 수신자의 As p에 전달하는데 있어서 고에너지 중간체로 작용한다 (52). 두번째는 탈 인산화 반응으로, 전달자(몇몇 경우, 또는 많은 경우)는 포스파타제 활성 도 를 가지는데 (53), 이 분자는 수신자의 인산화된 Asp 잔기를 탈인산화 시킨다. 지금까지 알려진 전달자로 작용하는 단백질은 약 50 개 이상이 밝혀졌 다. 이 단백질의 아미노산은 약 240 개로 되어 있으며 전형적으로 N- 말 단 부분에 히 스티 딘 인산화 자리 를 가지 고 있다(그림 8-7). 그림 8 구에서 C- 말단 쪽의 네 부분 (N , Gl , F , G2) 은 촉매 자리를 나타내는데, 두 개의 G(Gl 과 G2) 는 글리신이 풍부한 영역으로서 뉴클레 오티드 결합 자리이다 (54). 수신자는 약 120 개의 아미노산으로 구성되어 있으며 N- 말단 가까이에 아스파르트산(두 개)을 가지고 있다(5.5). 또한 c- 말단 가까이에 리신을 가지고 있고, 중간 부위의 인산화 자리에 아스
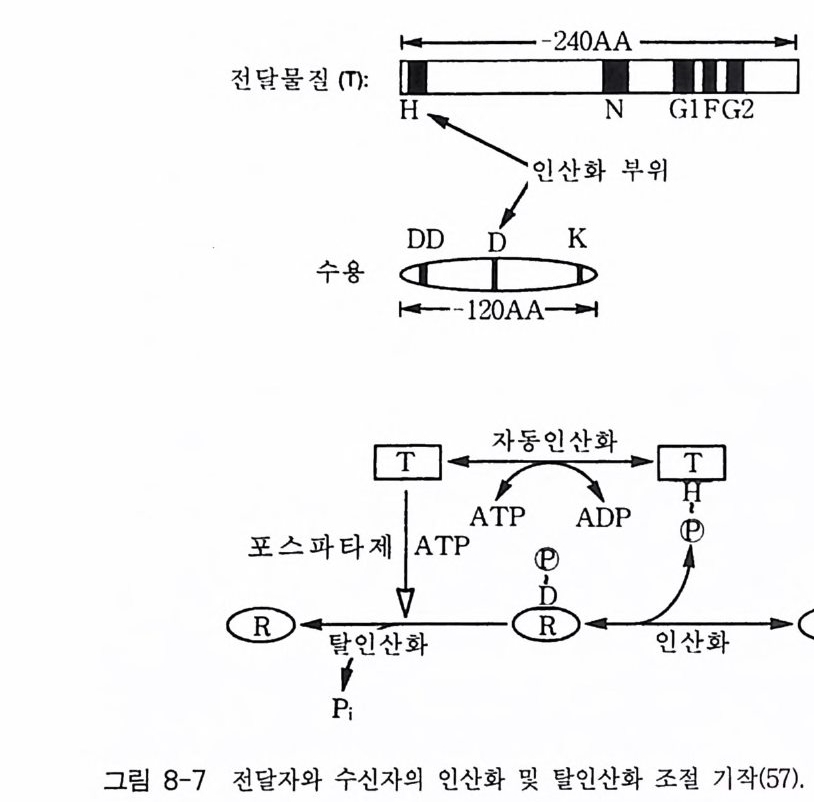 전달물전 (T): |' .I. -2 40AIA -I-I- I- i
전달물전 (T): |' .I. -2 40AIA -I-I- I- i
파르트산을 가지고 있다(그림 8 구). 수신자는 전달자에 비해서 비교적 구조가 잘 밝혀져 있는데, 이들 3 차 구조를 살펴보면 /3- sheet 와 a- 헬 릭스의 5 개 세트가 통과 같은 구조를 형성하고 있다 . /3 -shee t는 안쪽에 서 소수성 내부의 핵심을 형성하고 a- 헬릭스 구조에 의해서 바깥쪽이 둘러싸여 있다 (56). 이들 두 분자(전달자와 수신자)를 통해서 진행되는 신호 전달 기작은 앞에서 언급한 3 가지 예를 통해서 살펴보기로 하겠다. 8-3-1 질소 이용을 위한 조절 기능 (N it rore g ula ti on) 박테리아의 질소 대사에 관여하는 가장 중요한 효소는 글루타민 합성
효소(g lu t a mi ne s yn t he t ase) 로서 질소는 글루타민산염 과 암모니 아로부터 글루 타민이 합성되는 경로 를 통해서 생성된다. 세포가 질소를 필요로 할 때, 글 루타민 합성 효소 를 만드는 유전자인 gin A 가 발현되면서 이루어 진다. 질 소 조 절 을 위한 반응 조절자는 NRI 으로서 전사 활성화 단백질 이다. 즉 NRI 이 인산화되면 gin A 촉진 유전자에 결합함으로써 전사 (gin A ) 가 이 루 어진다 NRI 의 인산화는 히스티딘 키나제인 NRII 에 의해 조절 된댜 이 NRII 의 활 성도는 세포 내 탄소와 질소 대사 사이의 균형에 의해 조절 되 는 데 이 조절 기작에 대해서 살펴보기로 한다. 세포 내 탄소 및 질 소 대사의 비율이 두 개의 기능을 가지는 효소 (bif un cti on al enz y m e) 인 UTase/U R(uridy ly It r an sfe r ase/ uridy ly !r em ov ing e n z y me) 의 활 성도 를 조 절 한다. 이 효소는 다시 조절 단백질인 PII 의 티 로 신 잔기에 우리딜기 를 붙이거나(uri d y la ti on) 우리딜기를 제거 (de uri d y la ti on) 시킴으로써 히스티딘 키나제인 NRII 의 활성도를 조절한다. 만약 세포가 질 소가 필요하게 되면 UR 의 활성도가 증가함으로써 PII-UMP 에 서 우리 딜 화 반응이 일어나면서 PII 가 되며 NRII 의 활성도를 증가시키게 된다(그림 8-8). 이때 PII 가 세포 내 질소의 필요성을 감지하는 감지기 로 작용하고 있다. N 血가 활성화되면 자신의 히스티딘 잔기에 자동 인산화가 되며 이 인산기가 반응 조절자인 NRI 의 As p를 인산화시킴으로써 전달된다. NRII 는 또한 자신이 포스파타제 활성도를 가지고 있다. NRI 의 인산화는 글루타민 합성 효소의 유전자인 gin A, NRII 의 유전자인 gln L, 그리고 NRI 의 유전자인 gln G 를 전사시킴으로써 질소 대사룰 조절하는 단백질 들을 생성함으로써 세포 내 질소의 양을 증가시키게 된다 (3, 57). 8-3-2 박테리아의 주화성 (Chemota x is ) E. coli 나 Salmonella typhi, mu ri um 은 다양한 물리 화학적 자극에 반
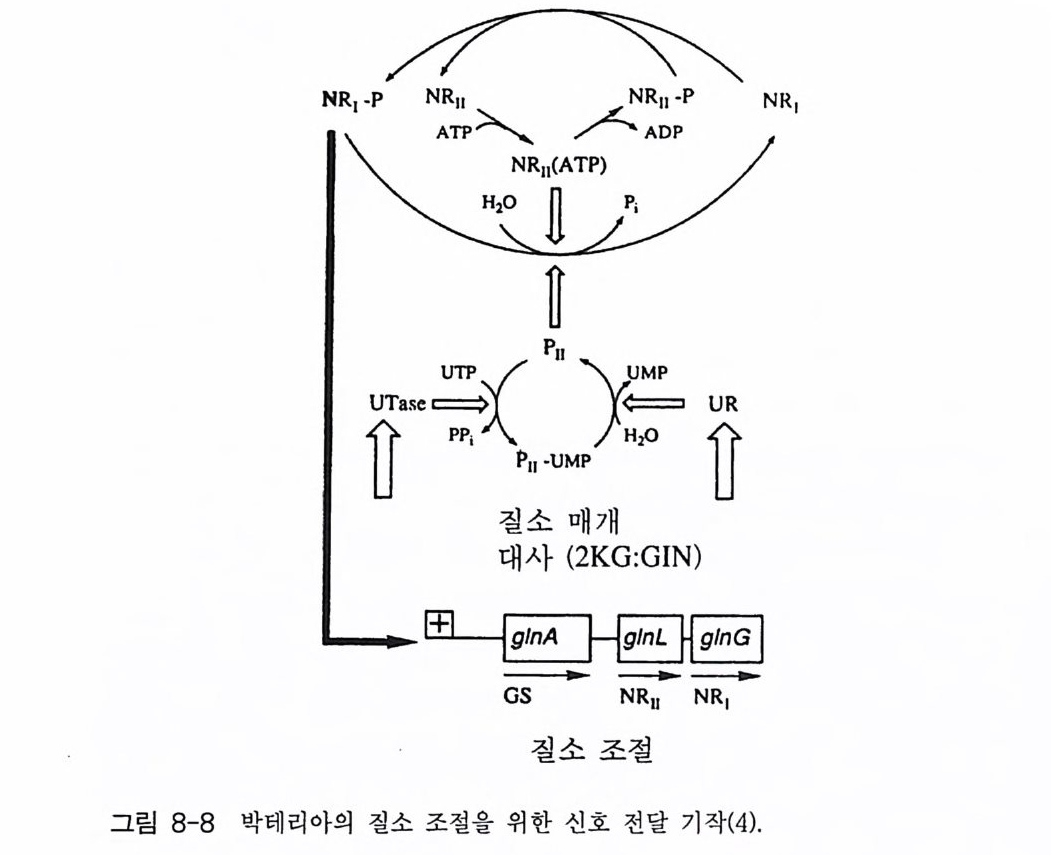 N RI TUPANnTR \NR1 I_zuI g〈 N RADnP N RI PN
N RI TUPANnTR \NR1 I_zuI g〈 N RADnP N RI PN
응하여 그들의 진행(수영) 방향을 조절한다. 이들은 회전할 수 있는 helic a l 편모(fl a g ellar) 필라멘트(마치 배에 있는 프로펠라와 같은 기능을 가진)에 의해서 수영을 하는데, 이 편모의 회전이 반시계 방향 (coun t er clock wise , CCW) 일 때는 계속 앞으로 진행하는 데 반해 , 회전이 시계 방 향 (cloc kwi se, CW) 일 때는 세포의 진행 방향을 돌리거나 텀불(tum ble) 하 게 된다 (58). E. col i는 자신이 좋아하는 여 러 가지 당이나, 아미노산과 같은 환경을 만나면 편모가 반시계 방향으로 회전하여 계속 진행하지만 자신이 싫어하는 지방산, 알코올, 또는 다른 독성 물질을 만나면 이 편
모가 시계 방향으로 회전하면서 멈추어 다른 방향으로 가게 된다. 지금부터 이 주화성에 관여하는 신호 전달 기작에 대해 알아보기로 한다 주화성의 신호 전달계에 관여하는 단백질이나 다른 구성 성분들은 위에서 언급한 감지기와 수신자 이외에 더 많은 세포질 내의 단백질을 필요로 한댜 먼저 많은 박테리아에서 발견된 다양한 외부 자극을 수용 할 수 있는 수용체(막 수용체 단백질)에는 4 개의 다른 단백질이 관여하고 있음이 확인되었는데 세린과 반응하 는 Tsr, 아스파르트산이나 말토오스 와 반응하는 Tar, 리 보오스나 갈락토오스와 반응하는 Trg, 그리 고 디 펩 티 드( dipepti de) 와 반응하는 Ta p가 있다 . 이 막 단백질들은 약 550 개의 아미 노산으로 구성되어 있으며 세포 바깥쪽에 감지기 또는 입력 영역을, 세포 안쪽에 출력 또는 신호 영역을 가지고 있다 (59) . 이 수용체 또는 변환 단백질은 Che R 에 의해 메틸화됨으로써 활성화 되며 che B 에 의해 탈메틸화됨으로써 비활성화된다. 이들 두 단백질은 세 포질 단백질로서 Che R 은 메틸 전이 효소 (me thy l tr ans f erase), Che B 는 메틸에스터라제 (me thy les t erase) 의 활성도를 각각 가지고 있다 (60). 그림 8 - 9 에서 보는 바와 같이 세포질 단백질은 5 개로 되어 있는데 이 들 중 Che B 를 제외한 Che A, Che W, Che Y, 그리고 Che Z 가 신호를 전달하는 데 관여하며 이들을 통해 신호가 전달되어 편모가 회전하기까 지는 약 0.1 초가 소요된다. 앞에서 언급한 Che B 는 전달자로서의 역할 보다는 전달자의 활성화를 조절하는 조절자로서의 역할을 수행하고 있 다. 먼저 Che R 에 의해 메틸화됨으로써 외부 신호가 전달자의 활성화를 거쳐 Che W 에 전달되며, 다시 Che A 에 전달되는데 이들 두 단백질은 막에 있는 전달자와 결합하고 있다 (61). Che A 는 자동 인산화를 수행할 수 있는 단백질 인산화 효소로서의 기능을 가지고 있는데, M g 양 과 ATP 가 존재할 때 , ATP 의 인산기가 Che A 의 His 48 에 전달되어 인산화 효 소의 중간체 를 형 성 하게 된다 (62). 인산화된 Che A 는 인산기를 다시 Che B 나 Che Y에 전달할 수 있다.
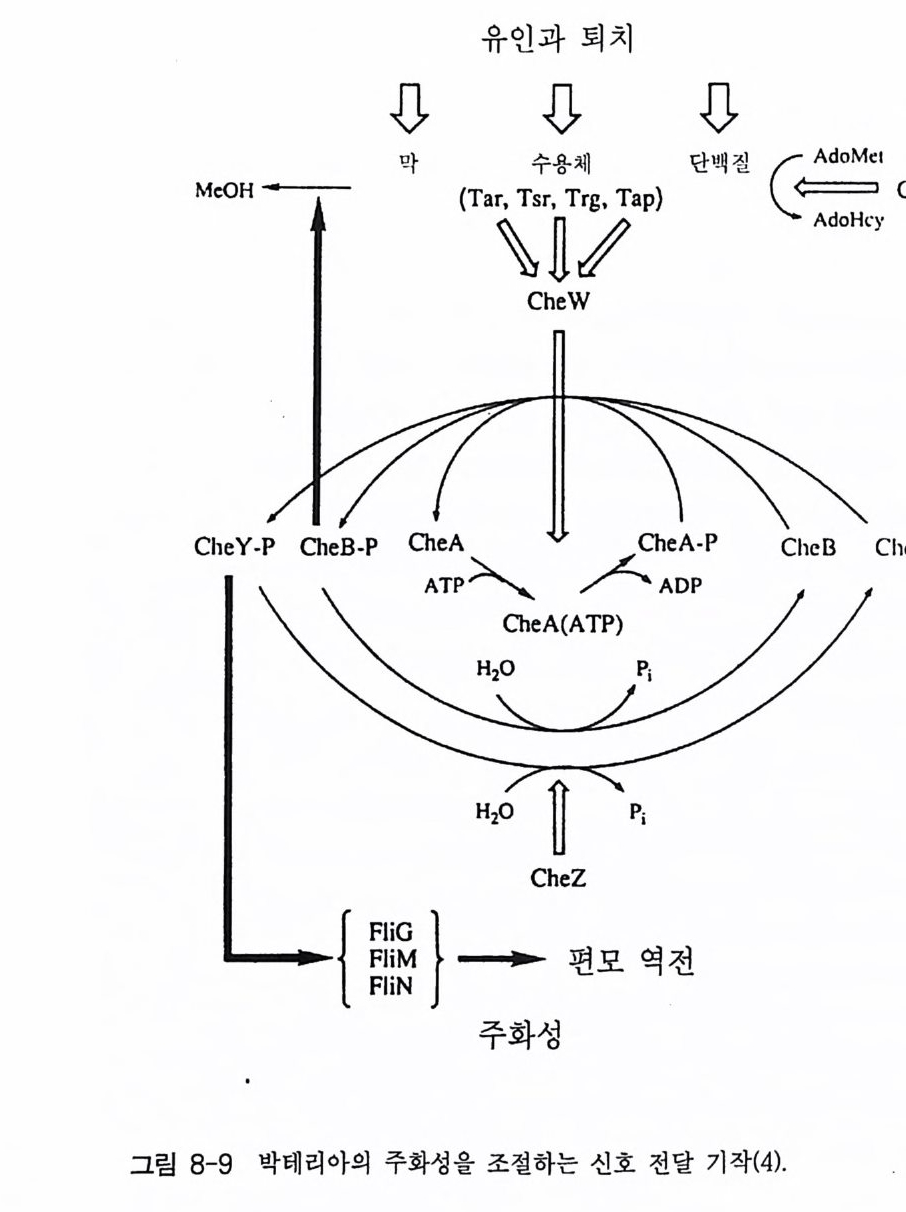 유인과 퇴치
유인과 퇴치
이 Che B 와 Che Y 의 인산화는 불안정 하며 쉽 게 가수분해 되 어 인산화 단백질에서 인산화되지 않은 상태로 쉽게 돌아간다 (hal f - lif e time : 10 s). 편모는 생체막에 존재하는 스위치 단백질과 결합되어 있는데, 인산화 된 Che Y 가 이 단백질과 작용함으로써 신호가 전달되어 편모 운동은 CW 방향으로 회 전하게 된댜 그 후 Che Z 가 Che Y 를 탈인산화시 킨다 (Che Z 는 Che B 는 탈인산화시 키 지 못함). 따라서 Che Z 는 포스파타제 활 성화 를 가지고 있다. Che B 의 인산화는 전달자의 탈메틸화를 유도하여 정상 상태로 돌아가 는 데 관여하고 있다. 이외에 Che W 는 Che Y 의 인 산화에 필요한 단백질인데 아마도 Che A 의 자동 인산화 반응에도 관여 하 는 것으로 여겨진다 (4, 12). 8-3-3 삼두 조절 E. col i와 같은 박테리아는 두 개의 세포막을 가지고 있는데, 세포질의 구성은 peripla sm ic 영역에 의해 둘러싸여 있다. 안쪽 막, 죽 세포질 쪽의 막은 수많은 여러 투과 효소(pe rmease) 들에 의해 이온이나 다른 분자들 이 능동 수송 기작을 통해 세포 내로 들어올 수 있다. 반면, 외막에는 po re 를 형성하는 단백질이 많이 존재하면서 작은 분자들이 수동 확산 (pa ssiv e diffu s i on) 에 의해서 peripla sm ic s p ace 로 들어온다. E. col i는 삼 투압 조절에 밀접한 관계가 있는 두 개의 주요한 porin 단백질이 있는데, Omp F 와 Omp C 가 그것이댜 Omp F 의 po re 가 Omp C 의 그것에 비해 약간 더 큰 것으로 알려져 있다. 박테리아는 배양액이나 외부 환경의 삼 투압에 반응하는데 이는 이 두 단백질인 Omp F 와 Omp C 의 비가 변함 에 따라 외부 삼투압 변화에 적응하여 생존하고 있다. 박테리아가 삼투 압 변화에 적응하며 반응하는 데 관여하는 신호 전달 기작에 관해 살펴 보기로 한다 배양액의 삼투압이 낮은 경우에는 Omp F 가 많이 존재하며 삼투압이
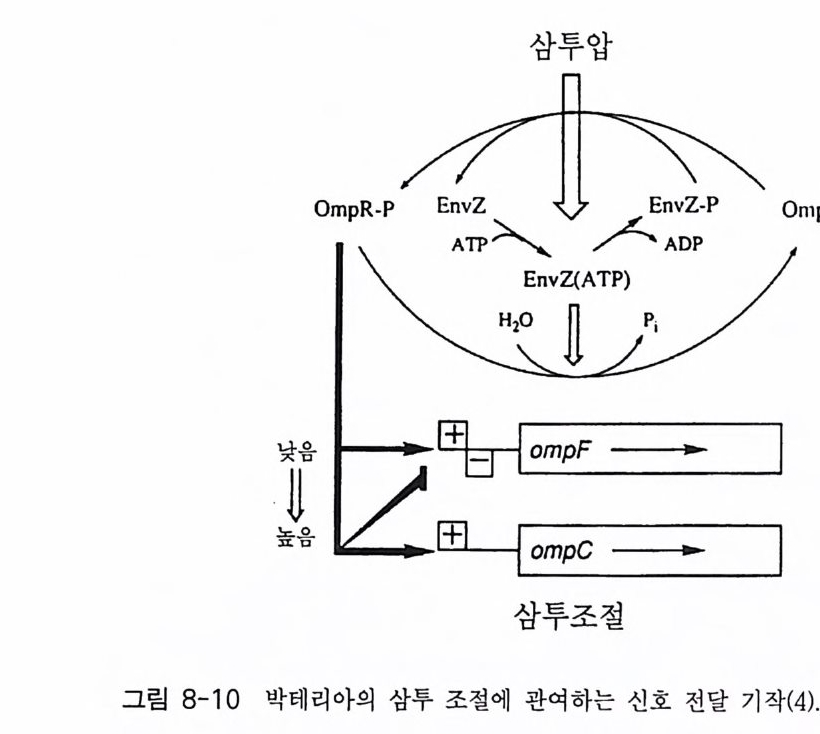 삼투압
삼투압
높은 경우에는 Omp C 가 많이 존재한다 . 이는 삼투압의 변화가 이들 porin 단백질을 생성하는 유전자인 porin 유전자의 발현을 조절하기 때 문이다. 예를 들어 삼투압이 높은 경우, 이 신호가 신호 전달 기작을 거 쳐 omp C 유전자의 발현을 증가시 키 고 omp F 유전자 발현을 억 제하고 있다. 그림 8-10 은 삼투압 변화가 omp F 와 omp C 유전자 발현에 관여 하는 신호 전달계를 보여주고 있다. 여기에 관여하는 두 개의 단백질이 있는데 Env Z 는 내막의 감지기로서, Omp R 은 세포질 내의 반응 조절자 로 작용하고 있다. Env Z 는 본 절의 질소 조절이나 주화성에서 살펴본 바와 같이 두 개의 주요 부위를 가지고 있는데 C- 말단 부분의 운송자로 서 작용하는 부위와 N- 말단의 감지기로 작용하는 부위가 그것이다. 배 양액 또는 외부 삼투압의 변화가 감지기 부분에 의해 감지되어 운송자
부분으로 전달되는데 그 기작은 아직까지 알려져 있지 않고 있다 (63). Env Z 단백질은 두 가지 효소 기능을 가지고 있는데, 단백질 키나제 의 활 성도와 포스파타제의 활성도이다. 죽, 높은 삼투압은 Env Z 의 자동 인산화 를 증가 시키고 , 따라서 반응 조절자인 Omp R 을 인산화시킨다. 반 면 낮은 삼투압일 때 는 이 Env Z 가 Omp R 의 탈인산화를 증진시키고 있다 (57). Omp R 은 N - 말단에 수용체 영역과 C - 말단 에 DNA - 결합 영역 을 가지 고 있댜 또한 porin 유전자는 omp F 와 omp C 촉진 유전자의 up s tr e a m 부위에 Omp R 의 결합 자리를 가지고 있다 . 이 결합 자리는 omp 촉진 유전자의 -3 5 consensus 부위 에 있는 것으로 알려 졌는데 (64), 이 는 Omp R 이 RNA 중합 효소가 촉진 유전자에 결합할 수 있도록 도와 줌으로써 전사를 조절하고 있 는 것으로 여겨진다. 탈인산화 형태의 Omp R 이나 인산화 형태(인산화 -Om p R) 모두 이 부위(또는 결합 자리)에 결 합할 수 있으나 인산화 Omp R 이 훨 씬 높은 찬화력을 가지고 있다 (65). 결론적으로 이야기하면 배양액의 삼투압이 높을 때 Env Z 의 자동 인산 화가 유도되 고 다시 Omp R 을 인산화시 키 며 이 인산화된 Omp R 이 porin 유전자의 촉 진 유전자의 u p s tr eam 에 결합함으로써 omp C 유전자 의 전사를 증가시킴과 동시에 omp F 유전자의 전사를 저해하고 따라서 세포막에 존재하는 Omp C 를 증가시키고 Omp F 는 감소시킴으로써 삼 투압 변화에 적응하게 된다. 8-4 인산 전이 효소계 이 계에서 가장 잘 알려져 있는 것으로 당 전달계를 들 수 있는데, 그 림 8-11 에서 보는 바와 같이 p hosp hoenol pyru va t e(PEP) 로부터의 인산기 가 PTS(ph osph otr an sfe r ase sys t e m ) 사슬을 거쳐 전달됨으로써 당의 전 이(tr ansloca ti on), 죽 당이 세포막을 가로질러 세포 내로 들어오게 된다 .
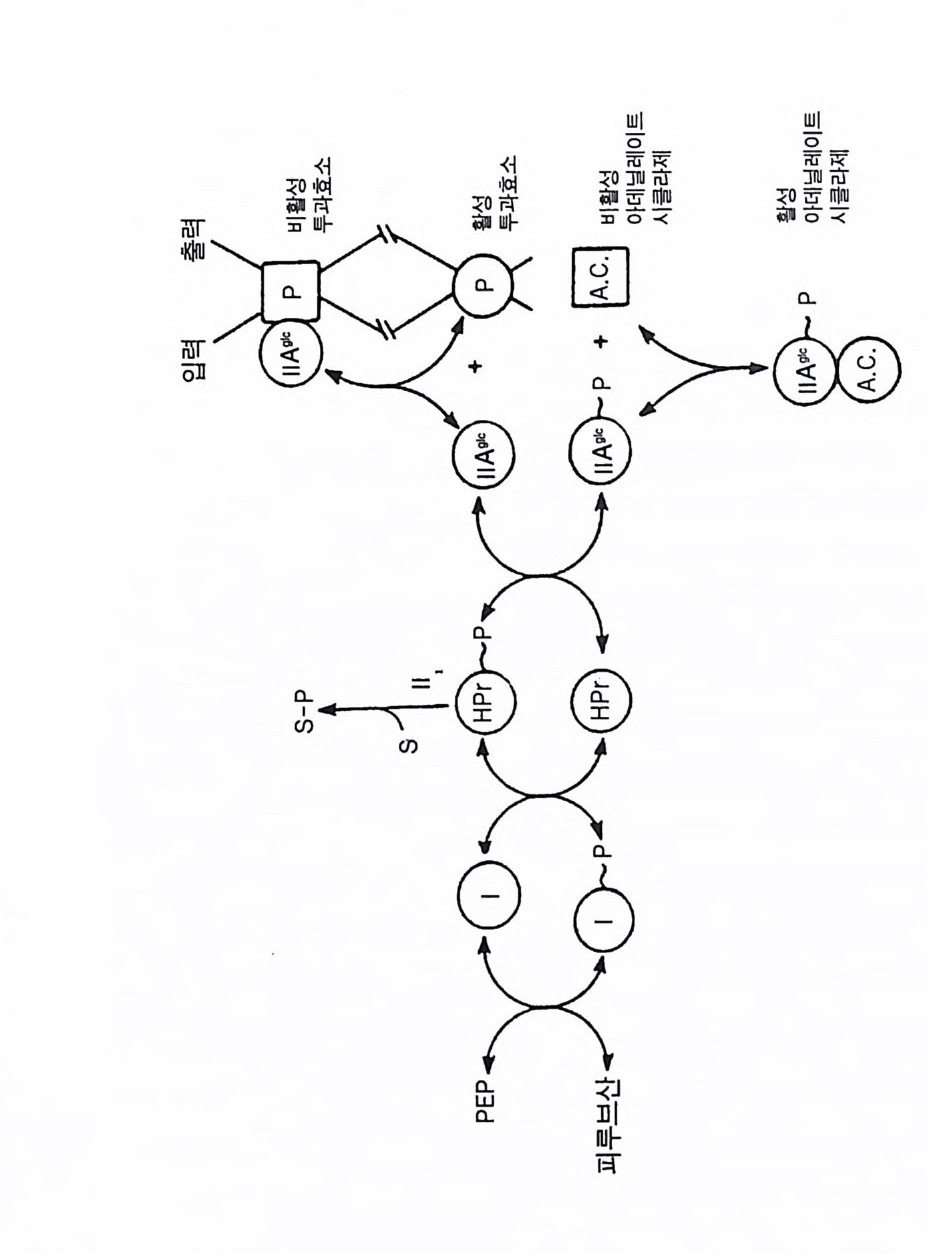 이트:; : 트 이:겁:
이트:; : 트 이:겁:
PTS 에서 인산기 전달 사슬은 일반적으로 다섯 개의 단백질에 의해서 이루어지는데, Enzy m e I 과 HPr 은 당에 대한 특이성은 존재하지 않으며 단지 에너지 전달에 관여하는 단백질이다. 이에 반해 Enz yme IIA, B, 그 리고 C 는 당에 대한 특이성을 가지고 있다. PTS 의 에너지와 관련 있는 이 단백질 들 은 Hi s 잔기의 인산화에 의해 이루어지고 있다. Hi s 의 이미 다 졸 링(imi dazole ri n g)의 인산화는 N-1 이나 N-3 위치에서 일어나는데, 이는 고에너지 포스포아미데이트(p hos p ho arni da t e) 결합을 형성함으로써 당 전달에 소모되는 에너지원으로 이용되고 있다. 본인은 본 절에서 장 내 세균의 박테리아에 있어서 PTS 와 PTS 에 의한 주화성 조절에 관여 하는 신호 전달 기작을 살펴보기로 하겠다. 8-4-1 장내 세균의 인산 전이 효소계 (PTS) 박테리아에서 탄수화물은 다양한 기작에 의해 전달되는데 그 중 하나 가 당 인산 전이 효소계 (PTS) 이다. 이 PTS 는 또한 PTS 에 관련이 없는 효소인 아데닐레이트 시클라제, 글리세롤 키나제 그리고 탄수화물 투과 효소 등의 활성도도 조절하는 것으로 알려져 있다 (5, 10). E. col i에서 당 특이성 PTS 단백질은 En zyme IIA g 1c( 글루코스 특이성)인데, PEP 의존성 기작에 의해 히스티딘 잔기에 인산화가 일어난다 (66). En zyme IIA g lc 의 탈인산화 형태가 세포질 내의 이화 효소 (ca t abo li c e nzym e) 나 막 통과 단백질인 투과 효소의 세포질 쪽에 결합하여 그들의 활성도를 저해한다. 반면 이 효소 (IIA g 1c) 의 히스티딘 잔기에 인산화가 일어날 때 아데닐레이 트 시클라제에 결합함으로써 활성화시킨다(그림 8-11, 5). 최근에 이 효 소 IIA g 1c 의 3 차 구조가 X- 선 결정학 및 NNIR 연구 결과에 의해 밝혀졌 는데 (67), 이 효소를 중심으로 PTS 계의 구조적인 측면, 그리고 생리 반 응 기작에 대해서 알아보고자 한다. 이 효소의 조절 기작은 PEP 로부터 인산기가 En zyme I, HPr 에 연쇄적으로 전달(이들 En zyme I 이나 HPr 은
PTS 단백질임)되어, 이 효소 (IIA g!c)의 인산화가 이루어짐으로써 세포질 이나 막에 존재하는 단백질의 활성도를 조절하고 있다(그림 8-11). 인산화된 HPr 로부터 인산기가 IIA g!c의 활성화 자리에 있는 His 잔기 에 전달되어 인산화 효소가 아데닐레이트 시클라제 를 활성화시키는데, Gly4 7 또한 활성화에 필수 아미노산이댜 돌연변이 연구에 의하면 Gly4 7 을 Ser 로 바꾸었을 때 IIA g 1c 의 구조가 변화하는 것으로 나타났다. 이는 Gl y 47 이 이 효소의 구조 유지와 밀접한 관계가 있는 아미노산으로 추정 된다. 젖당, 과당, 멜리비오스 (mel i b i ose) 그리고 글리세롤을 만드는 데 조절 자로 작용하는 유전자는 각각 lac, ma!, me!, 그리고 g[p인데 이들 유전 자의 전사는 CRP(cAMP 수용체 단백 질)과 cAMP, 그리 고 유도 물질 (i nducer) 로 작용하는 탄수화물 특이성 억제 단백질에 의해서 조절되고 있댜 따라서 당의 생성은 세포질에 있는 이 유도 물질과 cAMP 양과 밀 접한 관계가 있댜 또한 PTS 를 거쳐 생성되는 당이 PTS 를 거치지 않고 생성되는 당 (non-PTS 당)으로 전달되는데, 즉 non-PTS 당의 생성을 위 해 PTS- 당이 이용되고 있다. 따라서 IIA g 1c 에 의해 조절되는 기작은 세 포질에 유도 물질의 생성과 cAMP 합성에 밀접한 관계가 있다 . 죽 세포 바깥에 있는 당이 세포 내로 들어오면 세포 내의 non-PTS 당의 생성 이 필요치 않기 때문에 이 효소 IIA g 1c 에 의해 세포질 내의 유도 물질과 cAMP 의 생성이 억제된다. 그 기작을 살펴보면 다음과 같다. 세포 바깥 의 당이 세포 내에 들어오게 되면 HPr 의 인산화 Hi s 가 탈인산화되는데 이때 인산기가 당에 전달된다(그림 8-11). HPr 의 인산화 양이 적을 때에 는 IIA g lc 의 인산화가 줄어든다. 죽 세포 내 IIA g lc/ 인산화 IIA g1 c 의 비율은 HPr/ 인산화 HPr 의 비율과 일치한다. 따라서 IIA g 1c 이 인산화되지 못하면 세포 내 아데닐레이트 시클라제의 활성화가 되지 않는다. 결국 IIA g lc 의 탈인산화는 non-PTS 탄수화물 투과 효소나 글리세롤 키나제의 저해 원 인이 되는 것이다. 세포질 내의 cAMP 와 유도 물질의 감소는 non-PTS
re g ulon 에 의 한 유전자의 전사 속도를 감소시 킨다. 따라서 PTS 와 non - fYf S 는 서로 상반된 기작에 의해 연결되어 있다. 죽 PTS 의 활성화 는 non - fYf S 의 비활성화를 촉진하고 PTS 의 비활성화는 non-PTS 의 활 성화 를 유도한다. 8-4-2 주화성의 조절을 위한 인산 전이 효소계 PTS 에 의해 조절되는 주화성의 신호 전달 기작은 앞 절 감지기와 반 응계에서 살펴본 주화성의 그것과는 명확하게 구별된다. 앞에서 살펴본 주화성을 PTS 에 의해 조절되는 주화성과 구별하기 위해 MCP( 메틸 수 용 주화성 단백 질, meth y l- accept ing chemota x is p ro t e i n) 에 의 한 주화성 으로 명명하기로 하겠다. PTS 에 의한 주화성은 그람 양성 세균 (68, 69, 70) 뿐만 아니라 gr am- po s iti ve 박테리아 (71) 에서도 발견되었다. PTS 에 의한 주화성에는 2 개의 일반적인 단백질인 효소 I(EI) 과 HPr, 탄수화물 특이성 효소인 효소 IIABC 복합체(IJA, IIB, ITC) 들, PEP 그리고 기질로 서 탄수화물이 포함되 어 있다(그림 8-12). PEP 로부터 인산기 가 EI 의 히스티 딘 잔기 에 전달되며, 이 인산화된 EI 에 의해 다시 HPr 의 히스티딘으로 전달된다. 이 인산화된 HPr 의 인산기 가 막 통과 단백질인 IIABC 복합체에 다시 전달된다. 복합체 단백질은 20 개 이상의 서로 다른 유전자로부터 아미노산 서열이 밝혀졌는데 홍미 있게도 어떤 경우에는 IIABC 가 하나의 폴리펩티드로 구성되어 있었다 (예, 만니톨에 관여하는 IIABC). 몇몇의 경우에는 두 개의 폴리펩티드(예, 포도당에 관여하는 IIA 와 IIBC) 그리고 몇몇의 경우에는 3 개의 각각 다 른 폴리펩티드로 구성되어 있는데 cellob i ose 의 수송 및 주화성에 관여하 는 IIA, IIB, 그리 고 IIC 가 그것 이 다 (66, 72). 효소 IIA 의 인산화는 인산화 HPr 에 의해 히스티딘 잔기에 일어난다. 이어서 이 인산화는 IIB 의 시스 테인이나 히스티딘에 전달되는데 단백질에 따라 시스테인 또는 히스티딘
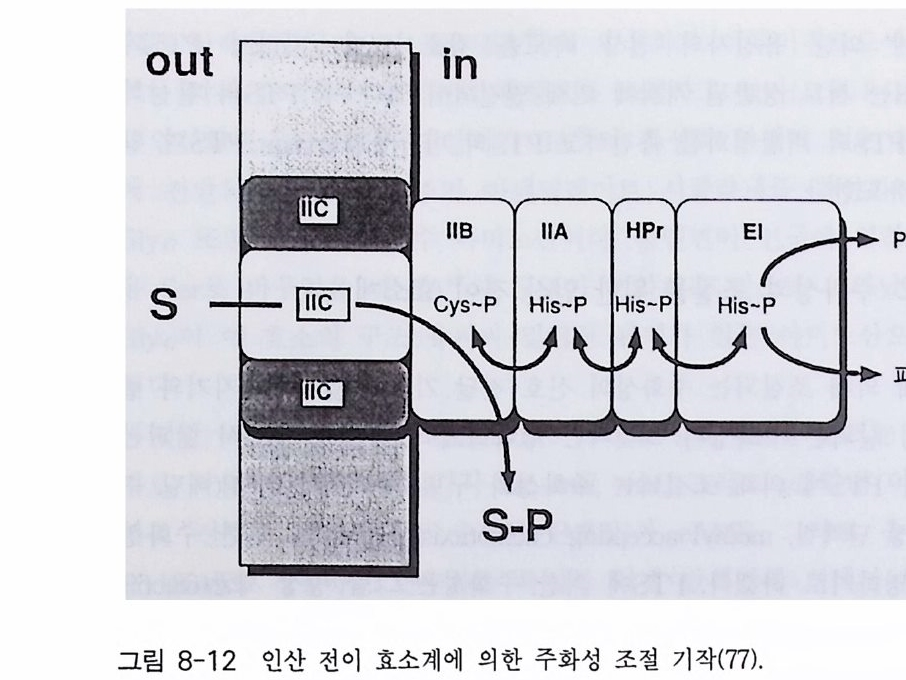 out in
out in
이 결정된다. 유일한 소수성 영역을 가지고 있는 IIC 는 기질의 결합과 수 송에 관여하는 것으로 여겨지는데, 이 IIC 가 11B 로부터 인산기 를 받아서 당(기질)에 전달하는 것으로 알려져 있다. 홍미롭게도 MCP 에 의한 주화 성과 Prs 에 의한 주화성은 정확하게 구분되며(결코 상호 의존적이지 않 음), 이 두 계에 의한 주화성의 반응 강도도 다른데, MCP 에 의한 주화성 이 Frs 의 그것보다 적어도 다섯 배 이상 강한 것으로 나타났다 (73). 四 S 에서 어느 단백질이 주화성과 당 수송에 관여하는가를 알아보았 다. 먼저 EI 을 생성하는 유전자인 pts 1 의 인산화가 부족한 유전자를 발 현시켰을 때 Frs 단백질의 인산화와 주화성 반응이 일어나지 않았으나 약간의 당 수송은 일어났다. 이는 화학 물질의 수용 (chemorece pti on) 과 인산화 그리고 수송은 상호 밀접한 관계가 있음을 의미한다. 이번에는 주화성 의 반응을 하지 않는 박테 리 아인 Klebsie ll a p necemon i ae 로부터
PTS 의 단백질인 II 를 발현시키는 유전자를 E. col i에 전이시킨 후 인산 화 및 주화성 반응을 검토해 보았을 때 인산화 및 주화성 반응이 관찰 되었다 (74) . 이 결과는 IIABC 복합체가 신호 전달 기작에 간접적으로 참 여하고 있음을 의미한다. 즉 신호 전달 기작의 중요한 중재자가 아닌 당 수용체로서의 역할만 담당하는 것으로 여겨진다 . 그렇다면 어떻게 PTS 에 의해 주화성이 일어나는가? 여기에 대한 실 험 결과는 명 확하지 않으나, PCP( 포스포릴-주화성-단백질)가 PTS 와 MCP 계 를 연결하는 단백질 또는 연결자로서 작용한다는 것이 모델로 제 시되고 있다 (75). 이 모델에 의하면 PTS 의 IIABC 에서 HPr, 그리고 EI 에 전달되 고 다시 EI 에 전달된 신호가 앞에 서 언급한 PCP 에 전달된다. 이 PCP 는 MCP 의 Che A 나 Che Y 와 작용하여 편모 운동이 일어난다는 가 정이댜 이 가정의 가능성에 대해서는 생화학적안 방법과 유전자 이용을 통한 방법을 동원하여 좀더 연구되어야 할 것으로 사료된다. 최근 Fox (76) 등은 EI 의 인산기가 세포질 단백질인 아세틸포스페이트와 아세틸 키나제 를 거쳐 MCP 계의 Che Y 에 전달된다는 연구 결과를 제시하였다. 이는 앞으로 언급한 PTS 에 의한 주화성 반응은 PTS 의 마지막 효소인 EI 가 MCP 계의 신호 전달 경로와 간접적으로 연결되어 있음을 시사해 주고 있다. 지금까지 본 장을 통해서 박테리아에서 일어나는 기작을 크게 3 가지 로 나누어 살펴보았다 ATP 의촌성 단백질 인산화, IDH 인산화 순환, 그리고 단백질 Ser/ Th r 키나제를 포함하는 고전적인 단백질 키나제/포 스파타제계는 진핵세포에서 발견되는 신호 기작과 거의 비슷한 반면, 질 소 조절, 주화성 그리고 삼투압 조절을 포함하는 감지기국기나제/반응 조 절자계는 이들 현상들이 박테리아만이 가지는 독특한 생명 현상이므로 이에 포함되는 신호 전달 기작은 진핵세포의 그것과는 다른 기작에 의 해서 이루어지고 있다. 그러나 최근 진핵세포에서도 메틸화 반응에 의한 생명 현상이 발견되고 있는 만큼 단정할 수는 없을 것 같다. 또한 최근
에 Koshland(78) 는 진핵 세포에서의 두 개의 구성 성분계에 대해 언급한 바가 있댜 연구 결과(원핵 세포와 진핵세포)의 상호 보완 겁정을 통해 생명 현상의 이해에 접근해야 할 것으로 생각된다 . 그러나 아직까지도 몇 가지 측면에서 박테리아에서 일어나는 신호 전 달 기작이 명확하게 밝혀져 있지 않은 상황이다. 예 를 들 어 주화성에서 Che Y 단백질과 편모의 운동을 유도하는 운동 단백질과의 작용 기작, MCP 계와 PTS 간의 연결 기작, 그리고 지금까지 살펴본 각 신호 진달 기작에 관여하는 단백질들의 정확한 활동 기작 등은 아 직도 연구되어야 할 과제로 남아 있다. 참고문헌 1 ) Wang, J. Y. J. and Koshland, D. E. Jr. (19 78) J Bi ol. Chem. 253, 7605 2) Krebs, E. G. (1986) In Boye r , P. D. and Krebs, E. G. eds. The En zym es. Vol. XVII. San Die g o , Academi c Press. 3) Cozzone, A J. (19 88) Ann Rev. Mi cr obia l. 42, 97 4) Sto c k, J. B., Sto c k, A M. and Mott on en, J. M. (19 90) Natu r e 344, 395 5) Sa ier , M. H. Jr. (19 89) Mi cr obia l. Rev. 53, 109 6) Burbulys , D., Trach, K A. and Hoch, J. A. (1991 ) Cell 64, 545 7) Grois m an, E. A and Sa ier , M. H. Jr. (1990) Trends Bio c hem Sci. 15, 30 8) Sa ier , M. H. Jr. (1993) J Cell Bio c hem 51, 1 9) Hunte r, T. (19 91) Meth o ds En zym ol. 200, 3 10) Sa ier , M. H. Jr, Wu, L. F. and Reiz er, J. (19 90) TIES 15, 391 11) Lukat, G. S., Mclear y, W. R., Sto ck , A. M. and Sto c k, J. B. (1992) Proc Na tl. A 따 Sci . USA . 89, 718
12) Sto c k, J. B., Nin f a , A. J. and Sto c k, A. M. (1989) Mi cr obia l. Rev. 53, 450 13) Forst, S. and Inouy e, M. (19 88) Ann Rev. Cell Bi ol. 4, 21 14) Mag a san ik, B. (19 89) Bio c him i e 71, 1005 15) Wanner, B. L. (1992) ]. Bacte r ial . 174, 2053 16) Cort ay, J. C., Rie u !, C., Duclos, B. and Cozzone, A. J. (19 86) Eur. ]. Bio c hem 159, 227 17) Manai , M. and Cozzone, A. J. (1982) Bi oc hem Bi op h ys. Res. Commun. 107, 981 18) Mirnu ra, C. S., Poy, F. and Jac obson, G. R. (19 87) ]. Cell Bi oc hem 33, 161 19) Munoz-Dorado, J., Inouy e, S. and Inouy e, M. (19 91) Cell 67, 995 20) Norr is, V., Baldw in, T. J, Sweeney, S. T., Wi lliam s, P. H. and Leach, K. L. (19 91 ) Mo!. M icr obia l. 5, 2977 21) Mana i, M. and Cozzone, A. J. (19 83) FEMS Mi cr obia l. Lett . 17, 87 22) Vallejo s , R. H., Holui gu e, L., Lucero, H. A. and Torruella, M. (1懿) Bi oc hem Bi op h ys . Res. Commun 126, 685 23) Turner, A. M. and Mann, N. H. (19 86) ]. Gen Mi cr ovio l. 132, 3433 24) Londesboroug h , J. (19 86) ]. Bacte r i al. 1 65, 595 25) Ch ian g , T. M., Reiz e r, J. and Beachey, E. H. (1989) ]. Bi ol. Chem. 264, 2957 26) Kelly- W i nt e n berg, K., Anderson, T. and Monti e, J. C. (19 90) ]. Bacte r i al. 172, 5135 '2:1) Roy c housur y, S., Sakai , K., Chakraba rty, A. M. (19 92) Proc. Na tl. Ac ad. Sci. USA . 89, 2659 28) Saha, A. K., Dowli ng, J. N., Mukhop a dhy ay , N. K and Glew, R. H. (1988) ]. Gen M icr obia l. 134, 1275
29) Edelman, A M., Blumenth a l, D. and Krebs, E. G. 0987) Ann. Rev. Bi oc hem. 56, 567 30) Bennett , P. M. and Holms, W. H. ( 1975) J Gen. Mi cr obia l . 8 7, 37 31 ) Garnak, M. and Reeves, H. C. (1979) Sc ien ce 203, 1111 32) Lap orte, D. C., Walsh, K and Koshland, D. E. Jr. 0984) ]. Bi ol. Chem. 259, 14068 33) Bort hw ick , A C., Holms, W. H. and Nim mo, H. G. 0984) Bi oc hem ]. 222. 797 34) THorsness, P. E. and Koshland, D. E. Jr. 0987) J Bi ol. Chem. 262, 10422 35) Lapo rte, D. C. and Koshland, D. E. Jr. 098. 3) Natu r e 305, 286 36) Dean, A M. and Koshland, D. E. Jr. (19 90) Scie n ce 249, 1044 37) Lapo rte, D. C. and Koshland, D. E. Jr. (19 82) Natu r e 300, 458 38) Lapo rte, D. C., Stu e land, C. S. and Ikeda, T. (19 89) Bio c him i e 71, 1051 39) Stu e land, C. S., Eck, K R., Ste ieg l b auer, K. T. and Lap orte, D. C. 0987) ]. Bio l. Chem 262, 16095 40) EL-Mansi, E. M., Nim mo , H. G. and Holms, W. H. 0986) ]. Gen. Mi cr obia l. 132, 797 41) Kaise r, D. (19 86) Ann Rev. Genet. 20, 539 42) Srumkets , L. J. (19 90) Mi cr obia l. Rev. 54, 473 43) Kroos, L., Kuspa , A and Kaise r, D . (19 86) Dev. Bi ol . 117, 252 44) Derreote s, P. N. (1989) Sc ien ce 245, 1054 45) Ha riba bu, B. and Dott in, R. P. 0991 ) Proc Natl Aa ul. Sc i. U SA . 88, 1115 46) Zha ng, W., Munoz-Dorado, J., Inouy e, M., Inouy e, S. (19 92) ]. Ba cter i al. 173, 5450
47) Munoz- D orado, ]., I nouy e, S. and Inouy e, M. (19 91) Cell 67, 995 48) Edelman, A. M. , B lumenth a l, D. K. and Krebs, E. G. (19ITT) Ann Rev. Bio c hem 56, 567 49) Colbran, R. J., Schworer, C. M., Hashi mo to , Y. Fong, Y. L., Rich , D. P., S wi th, M. K. and Soderlin g , T. R. (19 88) Bi oc hem ]. 258, 313 50) Tein t z e , M.,In o uy e, M. and Inouy e, S. (19 88) ]. Bio l. Chem. 263, 1199 51) Nin f a , A. ]. and Be nn ett, R. L. (1991) ]. Bi ol . Chem. 26, 6888 52) Sanders, D. A., Gil le ce, C. B., Burlin g am e, A. L. and Koshland, D. E. Jr. (1992) ]. Bacte r i al. 1 74, 5117 53) Aiba , H., Nakasai , F., Mizu shi ma , S. and MiZu no, T. 0989) J Bio l. Chem. 264, 14090 54) Yang , Y. and Inouy e, M. (1991 ) Proc Natl. Amd Sc i. USA 88, 11057 55) Bri ss ett e, R. E., Tsung, K. L. and Inouy e, M. 0991) J Bacte r i al. 1 73, 601 56) Sto c k, A. M. , M ott on en, ]. M., Sto c k, ]. B. and Schutt , C. E. 0989) Natu r e 337, 745 57) Parki ns on, ]. S. 0993) Cell 73, 8.57 58) Ste w a rt, R. C. and Dahlqu ist, F. W. (19 ITT) Chem Rev. 紅 997 59) Hazelbauer, G. L. (19 92) Curr. Op in, Str uc t. B io l . 2 , 505 60) Lup as , A. and Sto c k, ]. (1989) ]. Bi ol . Chem. 264, 17'3 '57 61) Maddock, J. R. and Shapi ro, L. (19 93) Sc ien ce 259, 1717 62) Hess, J. F., Bourret, R. B. and Sim o n, M. I. (1988) Natu r e 336, 139 63) Toki sh i ta, S. I., Koji ma , A., Aiba , H. and Mizuno, T. 0991) ]. Bi ol. Chem 226, 6780 64) Maeda, S. and Mizu no, T. (1990) J Bacte r i al. 1 72, 501 65) Aiba , H., Nakasai , F., Mizus hi ma , S. and Mizuno, T. 0989) ]. Bio c hem 106, 5
66) Sa ier , M. H. Jr. and Reiz e r, J. (19 92) ]. Bacte r ial . 174, 1433 67) Chen, Y., Fa irb roth e r, W. J. and Wr igh t, P. E. 0993) ]. Cell. Bi oc hem. 51, 75 68) Adler, ]. and Ep st e in, W. 0974) Proc: Natl. A(X Jd Sc i. USA . 71, 2895 69) Leng e ler, J. (1975) ]. Bacte r ial . 124, 26 70) Bassler, B. L., Gib b ons, P. ]., Yu, C. and Roseman, S. 0991 ) ]. Bi ol. Chem. 266, 24268 71) Thoelke, M. S., Caspe r, J. M. and Ordal, G. W. 0990) ]. Bacte r i al. 172, 1148 72) Leng e ler, J. W., Tit ge meye r , F., Vog le r, A. P. and Wohrl, B. M. (1990) Ph il. Trans. R. Soc: Lond. B326, 489 73) Vog le r, A. P. and Leng e ler, J. W. (1987) ]. Bacte r ia l. 169, 593 74) Vog le r, A. P. and Leng e ler, J. W. (1991) Mal. G en Genet. 230, 270 75) Leng el er, J., Auburge r, A. M., Maye r , R. and Pecher, A. (1981) Mal. Gen Genet. 183, 163 76) Sa ier , M. H. Jr., (1993) ]. Cell. B i oc hem. 51, 62 77) Tig e meye r , F. (1993) ]. Cell. Bi oc hem 51, 69 78) Koshland, D. E. Jr. (19 93) Sc ien ce 262, 헛 2
제 9 장 식물의 신호 전이 최근의 연구 결과들에 의하면 식물계에서도 동물의 신호 전이 과정과 유사한 반응들이 일어나고 있음이 확인되고 있으나, 아직 확실한 반응 경로는 어느 신호의 경우에서도 완전히 이해되지는 못한 상황이다. 식물 계에서 지금까지 연구된 신호로서는 빛, 호르몬, 병원균, 중력 등을 들 수 있댜 빛의 경우 자외선 , 청색광, 적색광을 신호로 이용하여 식물의 성장, 발달, 발아, 개화 및 결실 등의 생명 현상을 조절하고 있으며, 식물 호 르 몬의 경우 지베렐린(gi bbere llin)과 옥신 (au xi n) 의 신호 전이 과정에 관한 연구 결과들이 보고되고 있으며, 엘리시토 (e licit or) 신호 전이 과정 을 이해하려는 연구 그리고 중력에 의한 뿌리의 굴중성(g ra vitr o pi sm) 에 관한 신호 전이 연구 둥이 진행되고 있다 . 현재 식물계에서의 신호 전이 연구는 신호와 현상 발현이 어떤 것이 든 간에 동물 신호 전이의 기본 반응들이 식물에서도 일어나고 있는지 확인하고 있는 단계이다. 그 연구 내용들을 요약하면 ® 식물 세포에서 도 G- 단백질이 존재하며 그 역할이 무엇인지에 관한 연구, ® 이노시톨 인지질 대사 과정에 관한 연구 , ® 세포질 내 Ca2+ 농도 변화와 그 역할 이 무엇인지에 관한 연구, @ 단백질 인산화 반응과 단백질 키나제들에
관한 연구, ® 신호에 의해 그 발현이 조절되는 유전자 들 에 관한 연구 등이 진행되고 있댜 본 장에서는 현재까지 식물계에서 진행되고 있는 광신호 전이에 관한 연구들을 요약해서 기술하고자 한다. 9-1 신호와 수용체 식물계에서는 수용체의 종류, 정체를 비롯하여 수용 메커니즘 등이 거 의 이해되고 있지 못한 상태이다. 몇 가지 성장 조절제들과 당들이 어떤 수용체를 가질 것이라는 보고가 있고, 질산(nitr a t e) 은 니트레이트 리닥타 제(nitrate reduc ta se) 에 의해 인지될 수 있다는 설이 있을 뿐이고, 광 수 용체 중에서 적색광 수용체인 피토크롬(p h yt ochrome) 만이 그 정체가 밝 혀져 있을 뿐이댜 청색광 신호도 식물계에서 매우 중요한 역할을 하고 있음이 분명하나 아직도 그 수용체가 밝혀져 있지 않은 상태이다 . 피토 크롬의 경우 그 구조를 비롯해서 일차 광반응에 관한 연구 결과들이 비 교적 많이 보고된 반면 생리적으로 활성형인 피토크롬 P f r 형으로부터 시 작되는 신호 전이 과정에 관한 연구는 이제 시작 단계에 있다. 식물의 외부 신호를 수용하는 수용체 분자에 관한 충분한 연구 결과는 매우 부 족한 상태임에 틀림없으나, 신호가 제 2 의 전령(예, Ca2• , abscis i c acid , au xin, gibb erell in 둥)을 통하여 전달될 것이라는 내용들이 많이 보고되 고 있댜 동물계의 신호 전이에서 중요한 제 2 의 전령으로서는 cAMP 와 Ca 안을 열거할 수 있는데, 식물계에서는 cAMP 의 존재 및 역할이 거의 알려져 있지 않은 상황이며, Ca 안이 가장 중요한 제 2 의 전령으로서 널 리 알려져 있는 상황이다. 신호 전이 과정에서 중요한 역할을 담당하는 Ca2• 은 세포질 내 자유 Ca 양이며, 이 자유 Ca2+ 의 농도 조절은 세포 의부 로부터 Ca2• 채널을 통해서 유입되거나 유출되어 조절되거나, 세포 내
Ca2+ 저장고(소포체 또는 액포)로부터 동원되어 조절되는 것으로 알려져 있댜 세포 내 Ca 안 저장고로부터 Ca 안 이 세포질로 동원되기 위해서는 외부 신호가 PLC 까지 전달되어 막 성분 중의 하나인 PIP 2 를 분해시켜 생성되 는 수용성 생성물인 lP 3 가 Ca2• 저장고 막의 lP3 수용체에 결합함 으 로 써 일어난댜 신호에 의해 증가된 세포질 내 자유 Ca 앙 은 Ca2• 의존 성 단백 질 키나제 를 활성화시켜 단백질의 인산화를 촉진시키는 것으로 보고되고 있댜 지금까지 식물 세포에서 보고된 Ca 인 의존성 단백질 키 나제 들 의 종류와 기능이 다양한데 이 내용에 관해서는 다음 절에서 자 세히 기 술할 것이다. 9-2 G- 단백질 동물 세포에서의 신호 전이를 논할 때 G- 단백질에 관한 언급을 하지 않 을 수가 없는데, 그 이유는 많은 신호 수용체들이 신호를 수용한 후 초 기 단계에서 G- 단백질을 경유하여 그 신호를 전달하기 때문이다 . 최근에 식물 세포에서도 G- 단백질을 통하여 신호를 전달하는 수용체들이 존재 한다는 실험적 결과들이 나타나고 있는 상황이다. G- 단백질이란 구아닌 뉴클레오티드의 결합에 의해서 그 활성이 조절되는 단백질로서, Rodbell 등이 1971 년 처음으로 이 단백질을 통한 신호 전이 경로롤 시사하였다. 지금까지 G- 단백질에 관한 연구는 주로 동물 세포에서 진행되어 온바 그 결과를 토대로 G- 단백질의 일반적 성질 및 종류 등을 기술하고 그 동 안 식물 세포에서 연구된 G- 단백질에 관하여 기술하고자 한다. 9-2-1 G- 단백질의 일반적 성질 G- 단백질의 경우 그 분자의 크기에 따라 크게 두 종류로 나누어진다.
분자량이 비교적 큰(약 80kDa) 이종 삼량체 (he t ero trirn e ri c) 의 G - 단백질 (af J r 소단위체)과 분자량이 작은 ras-lik e G - 단백질(약 20kDa) 인데, 이 절에서는 신호 전이에서 중요한 역할을 담당하고 있는 이종 삼량체 의 G- 단백질에 관해서만 기술하고자 한댜 세포의 원형질막에 결합하고 있는 신호 수용체와 직접 상호작용을 통하여 신호 전이에 참여하는 G- 단백질은 모두 이종 삼량체의 G- 단백질인데 , 8 r 소단위체 는 주로 막 이중층에 박혀 있으며 , a- 소단위체는 세포질 쪽으로 노출되어 GDP/ GTP 가 결합하는 부위를 가지고 있댜 수용체가 신호 를 받지 않았을 경 우 G- 단백질의 a - 소 단위체에는 GDP 가 결합되어 비활성을 나타내며, 수용체가 신호를 받고 활성화된 후 그 신호가 G - 단백질에 전해지면 G- 단백질의 입체 구조 변화가 일어나게 되고 그 변화는 G ― 단백질의 친화 력을 증진시키는 방향으로 일어나게 되어 a - 소단위체에 GTP 가 GDP 대신 결합하게 되며, 이때 G- 단백질은 활성화된댜 GTP 의 결합으로 활 성화된 G- 단백질은 그 옆에 결합되어 있는 eff ec t or 분자(주로 효소계)를 활성화시켜 그 다음 반응을 촉진시키게 된다. 신호 전달이 끝난 다음 다 시 비활성형의 GDP 가 결합되어 있는 G- 단백질로 돌아가기 위해서는 G- 단백질의 GTPase 기능에 의해 결합된 GTP 를 가수분해시켜 GDP 로 바꾸어 주는 것 이 다(그림 9-1). G- 단백질과 연결되어 있는 수용체로서 많은 연구가 되어 있는 것들은 /3-아들레날린 수용체들, a- 아들레날린 수용체들, 로돕신 그리고 무스 카린 아세틸콜린 수용체들이댜 G- 단백질들을 조절하는 수용체들은 대체 적으로 그 구조 및 기능 면에서 많은 유사성을 가지고 있다. 예를 들면, ® 분자량의 유사성 (40~50 kDa), (2) 막을 7 번 가로질러 통과하는 유사 성, ® N- 말단에 gly c o sy la te d res i due(s) 를 가지고 있는 유사성, @ c- 말 단 근처에 몇 개의 세린/트레오닌 잔기를 가지고 있는 유사성 등이다. 어떤 수용체이든 신호를 받으면 수용체는 활성형의 구조로 바뀌게 되 며, 활성화된 수용체는 a B r 소단위체가 함께 결합되어 있는 G- 단백
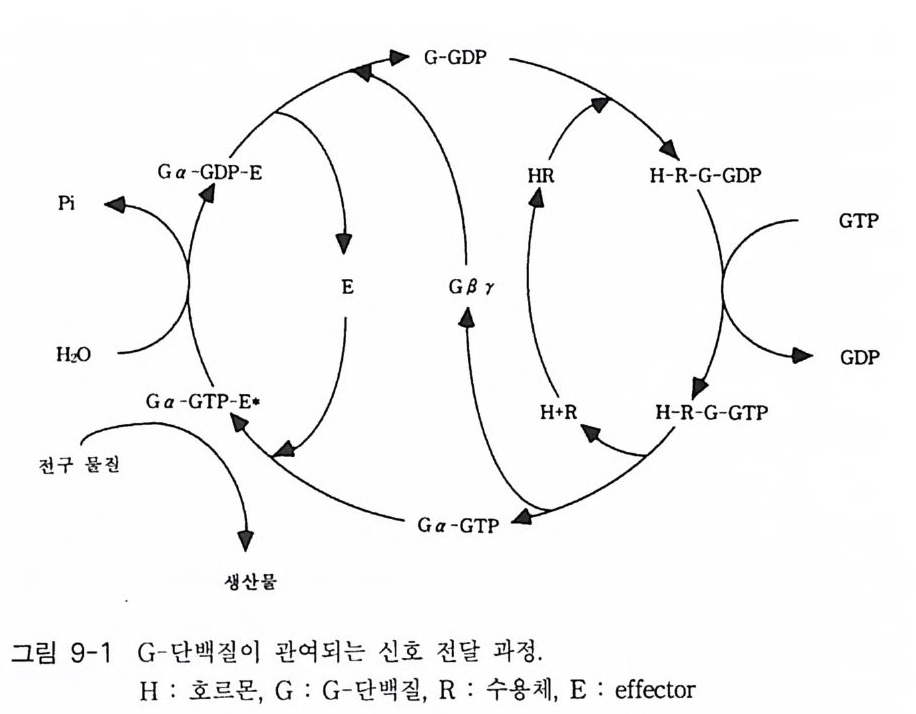 G- G DP \
G- G DP \
질 과 높 은 친화력을 갖게 되며, 이때 a- 소단위체에 결합되어 있는 GDP 의 방 출을 촉 진시켜 GTP 결합 부위 를 비어 있게 만들고 GTP 와의 결합 력을 증진시킨다. a- 소단위체에 GTP 가 결합하게 되면 a- 소단위체와 /3 r 소단위체 간의 결합력이 약화되면서 a- 소단위체는 그들로부터 떨 어지게 되며, GTP 가 결합되어 있는 a - 소단위체는 eff ec to r 분자와 상호 작용을 하게 되며 이 분자 를 활성화시킨다. G- 단백질을 세포로부터 정제할 때 확인하는 동정 방법으로는 몇 가지 가 보고되고 있는데 , 첫째는 비가수분해성 GTP 유사체인 [r_l5S]GTP rs 의 결합으로 확인하는 방법이 있고, 둘째로는 G - 단백질의 경우 GTPase 활성도를 나타내는데 이 성질을 이용하여 결합된 [r- 허기 GTP 로부터 유리되어 나오는 32 p의 방사능을 측정하여 확인하는 방법이 있으
며, 셋째로는 GDP 또는 GTP 그리고 M g안과 같은 성분을 첨가하면서 트립토판 잔기의 형광 변화를 측정하여 확인하는 방법, 그리고 넷째는 박테리아 독소(콜레라 독소 또는 백일해 독소)들과 NAD 의 첨가로 ADP- 리보실레이션되는 것을 확인하는 방법 등이다. 위에 기술한 몇 가지 동 정 방법 중에서도 G ―단백질의 특이성을 확실하게 확인하는 방법이 독소 에 의한 ADP- 리보실레이션(그림 9-2) 인데, G 」단백질의 종류에 따라 리 보실레이션시키는 독소의 종류가 다르기 때문에 가능하다 . 9-2-2 G- 단백질의 종류 G- 단백질들은 그들의 a- 소단위체로 구별되면서 지금까지 보고된 바 에 의하면 9 개의 다른 유전자들이 a- 소단위체 를 발현시키는 것 으로 알 려져 있다. 그러나 G- 단백질들의 종류를 구분하여 명명하는 것은 a - 소 단위체와 상호 작용하는 effe c to r 분자(주로 효소계)들이 무엇이냐에 따 라 결정한다(표 9-1). 동물 세포에서 G- 단백질에 의해 조절되는 eff ec to r 분자들은 아데닐레 이트 시클라제 (AC), PLC, cGMP PDE, PLA .z 그리고 이온 수송로 (K, Ca2+ 수송로) 등이다. 아데닐레이트 시클라제를 활성화시키는 G- 단백질 과 상호작용을 하는 대표적인 수용체계로는 /3-아들레날린 수용체계 (ag o n ist : ca tec hol amin es) 인데 에피네프린 (e pi ne phri ne) 과 같은 호르몬이 수용체와 결합을 하게 되면 수용체는 G- 단백질 (Gs) 로 하여금 G sa 에 GTP 가 붙기 쉬운 입체 구조 변화를 유도하게 되며, Gsa 를 활성화시켜 아데닐레이트 시클라제를 활성화시키게 된다. 따라서 세포질 내의 cAMP 의 농도를 증가시키며 cAMP 의존성 단백질 키나제 (A 홉]나제)의 활성도가 올라가게 되고 단백질의 인산화 반응이 일어나게 된다. G 구간 백질과 연결된 신호 전달에서 가장 많이 연구된 수용체계가 시각 현상 의 신호 전달계인데, 이 현상의 광수용체 분자는 로돕신 (rhodo p sin ;
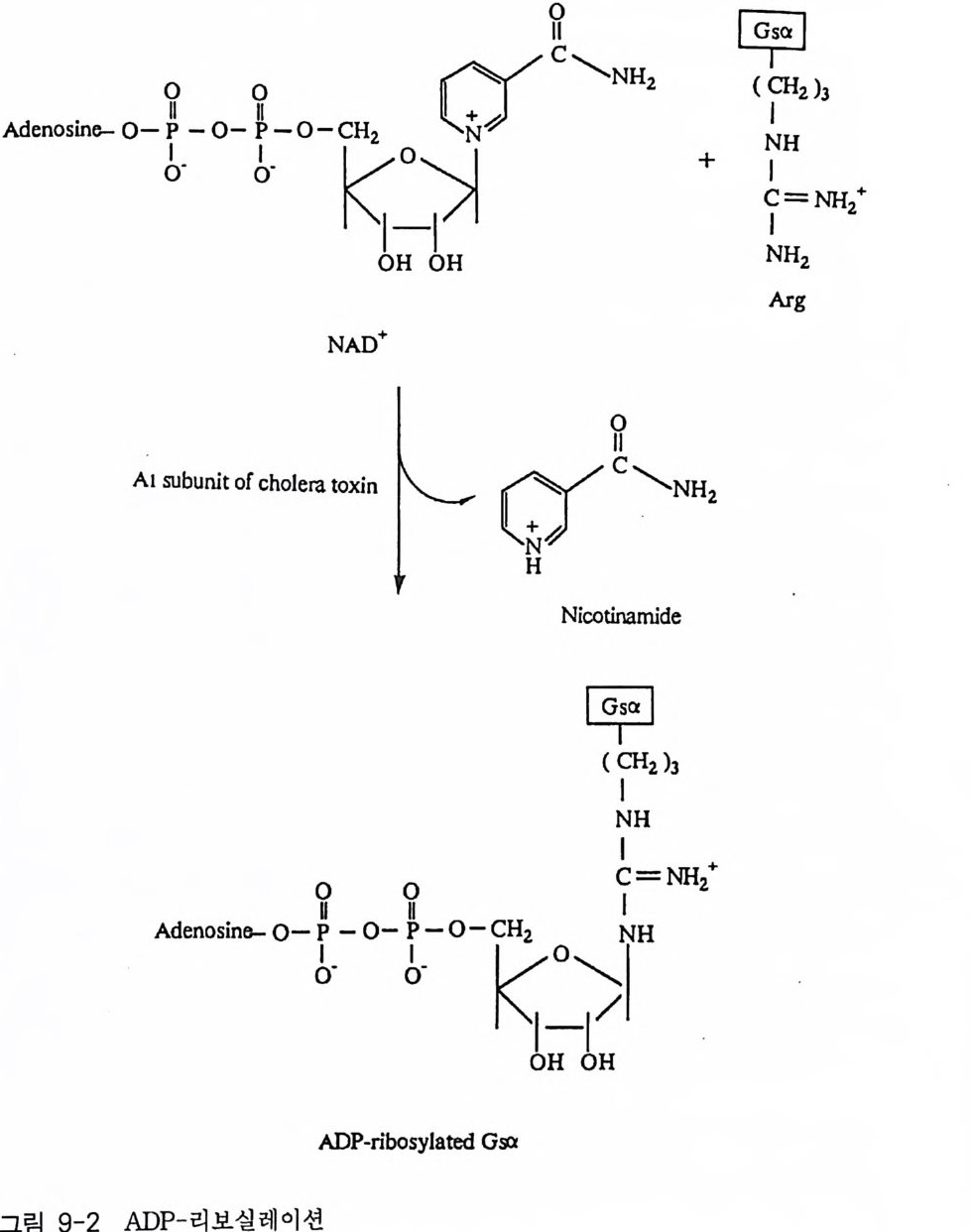 Adenosmeo_ 『O -O-l-oO· -CHk2 0 >: 망\ NH2 + 무( CNCII H=HN2 )H3 2+
Adenosmeo_ 『O -O-l-oO· -CHk2 0 >: 망\ NH2 + 무( CNCII H=HN2 )H3 2+
-9fEf1 rt .표 에 른자따 분류o 질-e의백단 종Gc A %mo niHcpsnreccv tiitIub a• ys /saM sFTxoin srsitbioi uindutesTorleEf)/fr@U u•Dl ta Jr (mOku J X 'Iidadc ett nyii re)ec[rs ot G sC2 ss()(XIa244.0 01CTXq giUbo guuistdoncBl, A,a uH lcdAecnleys(ctaya +) ( d L s) 2)C(X 47,a. Cch·T. 5nC aX. uibUls(en)q+stoiu Hsr,oTS the N 'acn2ahJ-esn( l .44 7 8C8XrI T oCcOlrtoeoy-n ura dnortOata)ydylac+ A(ecesefl n iheemtul ip G i .3P40TaX 0 10 Nuiou ibsaq uytlre li a0.4 5P C8T; 8-XuuibU qstoh:a ,! MoR ,A'Knn+ l(ashceJ2 i a5 . 04· chPT. 9,n XC.aa4nlreN)sile siuot( y -aqubu reosth 3i satyl(ycA))cn(el d aee-? AaC o 4.3 TP700X, ihoetrnrasB2 n,-EetkMP HAaha+o )(seps)?olhpi(C n aC o 14 XTP.7 30o narriseB th,e rshtoohslpohPi+)(2Jspe?a (A u0 a4 natiR eXP,T68CX Tlos d rRpspsomo d-hPMcG cfieci a . 104X TXP,C 8 6Tnlties R naxloCP( ranioopdnehs se)s se+phoi te:!t {?TCX0 5.4) a 67. etsaTad suTbs ?)(et XTP0 69a .04 za ,inraBMl anerd J(?hoyl,.£;,ndaeAe) -? (syc (c)late letaPles)?rssh(ethtore to Gq 24abu rlaeN0 01uoyutiiq1M sA Ia ol ,hoPRhCps. ohpiC1 3-se.a/ q a88 24 ubuyrlaeNqitho sou tuiJ rs-e 2, P/-he otrs.1 ,59g7.14 aiknuL Mnd ?r veli,e y 75 43 ,sl1ec By eidollm a5 ? slelc? l .5346a,sllce8 T 5 ? lsmel cdieol y /olhs-espaohPCpi3,I B- :, ·B-3 2 1G 41 001 4 2asutoiuqibU ? ‘) 7 6 44suotiuqibaU 3 1 ?? A ieddiaco nm ni%yitt; 은 것의위 장 가의lyim fa각 의때 유 했로으010 값 a elrhoCb isssin(xotXPTn(xiottruep 과X)T)C기s잔 C와X)TC(기g잔rr A는(tiay,xli-,PU As의서에lx)rFno다한매·누 훈 응반 p lirmos . atsna vhceS
vita min A aldehy d e + p ro t e i n) 이며, 이 수용체와 상호 작용하는 G- 단백 질은 t ransduc i n(G1) 이고, eff ec to r 분자는 cGIYIP 특이성 포스포디에스테 라제 (PDE) 이댜 소의 눈 세포에서 정제한 G1a(39kDa), G1p (3 6kDa) 그 리 고 G1 r (8 kDa) 의 cDNA 들은 모두 클로닝 되 었다(표 9-1). G 를 통한 시각 현상의 반응 경로는 다음과 같댜 R 一hu R* . ― ➔ Gta GTP 一 PDE* 一 cGIYIP ! 一 Na • channel closure 一 membrane hyp erpola r iza ti on G - 단백질에 의해 활성화된 PDE 는 cGlVIP 의 수준을 감소시키게 되며 그 신호는 Na ♦ 채널에 전달되어 N 깊 채널을 닫히게 하는데 그 분자적 메커니즘은 확실시되고 있지 못하다 . N 깊 채널이 닫히게 되면 시각 세포 막을 중심으로 막 전위차가 생기게 되며, 이 전기적 신호가 신경세포로 전달되게 되는 것이다. 지금까지 열거한 두 가지 경우는 수용체에 의해 서 활성화된 G- 단백질의 신호가 eff ec to r 분자로 연결되는 대표적인 예 이고, 무스카린 아세틸콜린 수용체들과 연결된 G- 단백질의 경우 활성화 된 G ― 단백질의 신호가 이온 채널 (K • 또는 Ca2• 채널)들을 조절하는 기능 과 eff ec to r 분자계(아데닐레이트 시클라제 또는 PLC) 를 조절하는 기능 등 두 경우로 대별된다. G- 단백질이 이온 채널을 조절하는 경우 간접적 으로 조절하는 경우와 직접적으로 조절하는 경우로 나누어지는데, 간접 적으로 조절하는 경우 막에 결합된 효소계를 자극한 후 세포질 내 제 2 의 전령(예, IP3 또는 Ca2•) 수준을 조절하여 단백질 키나제의 활성도를 조절함으로써 채널 단백질의 인산화 조절을 통하여 이온 채널을 조절하 게 된다. G- 단백질과 직접 상호작용을 통해서 조절되는 이온 채널의 경 우 막의 탈분극화가 채널을 여는 필수적인 자극이 된다 . 이종 삼량체의 G- 단백질들 중 eff ec to r 분자의 활성을 억제시키는 기 능을 가지고 있는 G- 단백질(Gi)이 있는데 대표적인 것이 a2- 아들레날린
수용체와 연결되어 있는 G- 단백질이며, 이 G - 단 백질의 경우는 백일해 독소(pertu ss i s t o xi n) 에 의 해 ADP- ri bos y la ti on 이 되 는 것 으 로 알려 져 있 댜 a 2 - 아들레날린 수용체 외에 musca rinic cholinergic 수용체, dop a- mine 수용체, opi at e 수용체들과 연결된 G _ 단백질 들 이 G, 인데 eff ec to r 분자는 모두 아데닐레이트 시클라제이며 활성제가 이 들 수용체에 결합 할 때 G- 단백질은 아데닐레이트 시클라제의 활 성 을 억제하 는 방향으 로 반응을 진행시킨댜 G s 와 G i의 경우 Gp r 복합체는 같은 것 으 로 밝혀졌 으며, Ga 가 서로 다른 구조 를 가지고 있는 것으로 알려져 있댜 세포의 원형질막에 결합되어 신호 전이에 참여하는 이 종 삼량체의 G- 단백질은 분자량이 비교적 큰 G- 단백질들이고, 세포질 내에서 세포 분 열 등의 신호 전이에 참여하는 분자량이 비교적 작은 G - 단백질 들 이 있 댜 그 중 가장 대표적인 것이 ras 종양 유전자의 산물인 p21 단백질인 데 이들의 분자량은 21 kDa 이며, GDP / GTP 가 결합하는 단백질이댜 이 들 p21 단백질들의 아미노산 서열과 이종 삼량체의 G - 단백질 들 의 a - 소 단위체의 아미노산 서열은 상동 관계가 낮은 편이나 구아닌 뉴 클 레오티 드 결합 부위의 아미노산 서열의 상동 관계는 높은 편이다. 이상에 언급 한 G- 단백질들이 동물 세포에서는 그 연구가 상당히 진척되어 있는 반 면, 식물 세포에서는 이제 그 존재의 확인을 시작으로 그 기능 연구가 진행되고 있는 실정이다. 9-2-3 식물계 G- 단백질 식물계에서 최초로 확인된 GTP 결합 단백질의 경우는 Pisu m sat i- vum 에서 [35S]GTPrS( 비가수분해형 GTP 유사체)를 이용하여 확인하였 으며 (1), 그 후 Zucc hini의 배축 미크로좀 분획 (h ypo co ty l microsomal fr ac ti on) 에서 분자량이 작은 G- 단백질 (23kDa-28kDa) 들이 확인되었다 (2). 식물 세포에서 최초로 클로닝된 이종 삼량체의 G- 단백질은 Arabi-
dop s is t ha li ana 으로부터 얻었는데, 그 Ga1 단백질의 a- 소단위체의 아미 노산 서열과 동물의 것을 비교해 볼 때 36% 의 서열 상동 관계 를 나타내 었댜 식물 세포 들 의 경우도 다양한 신호(예 , 광선, 중력, 미생물 , 호르몬 등) 들 과 민감하게 반응하며, 생리 / 생화학적 연구 를 통하여 이들 반응에 대한 많은 정보 가 보고되어 있는데 반하여, 이 들 신호를 받아들인 후 진 행되 는 신호 전이의 반응 경로 및 반응 메커니즘에 관한 연구는 동물 세 포의 경우 와 비교하여 매우 초보적인 상태이다 . 최근에 식물계에서 신호 전이 과정을 이해하기 위하여 많이 이용하는 접근 방법 중 의 하나 는 신호 전이 반응에서 결함을 갖는 돌연변이체를 만 들 어 분석하는 것 인데, 이 연구 결과들로부터 신호 전이에 관한 생리 적 / 유 전적 정보는 비교 적 많이 얻고 있으나 , 신호 전이의 반응 메커니즘 에 관한 정보는 그 습득이 매우 부족한 상태이다. 생명체의 신호 전이 형태 는 매우 다양한데 그 중에서 가장 많이 연구가 되어 있는 경우가 세 포의 원형질막 표면에서 신호가 수용되며 그후 신호 전달 분자들에 의 한 생화학적 반응들을 통하여 그 신호가 전달되어 가는 경우인데 이때 신호 전달에 참여하는 중요한 분자가 G- 단백질이라는 사실은 부정의 여 지가 없다. 그러나 식물 세포의 신호 전이에서는 이 단백질의 참여 여부 조차도 확실한 상황이 아니다 . 그러나 최근에 식물 세포들에서도 호르몬 또는 광선 신호 전이 등에 G- 단백질이 관여할 것이라는 보고들이 나타 나고 있는 실정이다. Bossen 등 (4) 의 보고에 의하면 암소에서 성장한 밀 의 잎으로부터 분리한 엽육 (Meso ph yll) 세포가 적색 광선의 조사에 의해 그 부피가 증가하는 현상을 발견하였는데, 그 현상이 GDP /J S 에 의해 억제됨을 관찰하였다. 그와는 대조적으로 암소에서 또는 원적색광 조사 후 GTPrS 를 첨가해 보았을 때 세포의 부피 증가 현상이 적색광 조사 후 관찰되는 정도와 같게 나타남을 발견하였다. 이 사실온 Pfr 형의 피토 크롬이 세포의 부피 증가 (swe lli n g)에 관여한다는 증거를 제시함과 동시 에 어떤 메커니즘인지는 아직 확실치 않으나 피토크롬 신호가 G- 단백질
을 통하여 세포의 부피 증가 현상을 유발한다는 증거도 되는 것이다. 이 종 삼량체의 G- 단백질이 식물 세포의 원형질막에도 존재한다는 사실을 발견한 이후, 청색 광선에 의해 활성화되는 G - 단백질이 완두의 원형질 막에 존재함이 확인되었다 (5). G - 단백질(tr ansduc i n) 의 a 三 소단위체에 대 한 폴리클로널 항체(po l y clonal an ti bod y)에 의해 인지되 는 40l ill a 의 폴 리펩티드를 확인하였고, 이 펩티드가 콜레라 독소 (cholera t ox i n) 에 의해 ADP - 리보실레이션되는 기질이라는 사실도 확인하였다. 이 펩티드 (40 kDa) 가 콜레라 독소에 의해 리보실레이션(ri bos y la ti on) 되 는 능릭이 청색 광선의 조사에 의존성을 보인 사실은 이 펩티드 (40l ill a) 가 청색 광선에 의해 활성화되는 G_ 단백질의 a- 소단위체라는 사실을 확인한 것이다. 청색광을 조사한 시료에서만 비가수분해성 GTP 유사체가 이 펩티드에 결합한다는 사실이 확인되었는데, 이러한 결과들은 고등 식물에서도 신 호 전이에 참가할 수 있는 이종 삼량체의 G- 단백질이 세포의 원형질막 에 존재한다는 사실을 강력히 시사하는 것이다. 청색광 신호 전이에서 광수용체 분자가 어떤 것인가 아직 밝혀져 있지 않은 상황인데, 최근에 폴라보 단백질(fl avo p ro t e i n) 이 Pis u m sa ti vum 에서 청색광 수용체 역할 울 하여 이 식물의 원형질막에 GTPrS 의 결합을 중재할 것이라는 보고 가 있었다 (6). 식물의 성장과 분화에 청색광보다 중요한 광선이 적색 광 선이며, 적색광 수용체로서는 피토크롬이라는 색소 단백질(분자량 : 124 kDa) 이 모든 고등 식물에 분포되어 있다. 피토크롬에 의해 조절 받는 현 상은 매우 다양한데 그 모든 현상 발현 과정이 적색광 신호 전이 과정 이라고 말해도 과언이 아니다. 그런데 아직도 피토크롬 신호 전이 현상 에 G- 단백질이 관여한다는 실험적 사실들은 많지 않은 상태이다. 최근 에 귀리 세포에서 피토크롬에 의해 활성화되는 분자량이 작은 ras like G- 단백질 (24 kDa) 이 존재하는 사실이 보고된 바 있다 (7). 어떤 종류의 G- 단백질이 관여하는지는 모르지만 피토크롬에 의해 조절되는 대표적 인 유전자인 mb 유전자 발현에 G- 단백질이 관여한다는 사실을 대두의
세포에 콜레라 독소 / 백일해 독소와 같은 G- 단백질의 활성을 조절하는 박테리아 독소 를 세포 내에 넣고 cab 유전자가 발현되는 현상을 Nort he rn blot 방법으로 알아본 것이다 광 신호 전이(청색광, 적색광) 과 정에 G - 단백질이 관여한다는 사실 이외에도 Faba bean 의 공변세포의 K' 채널의 전류 흐름을 G- 단백질이 조절한다는 보고 (8) 와 Commelin a communis L. 의 기공의 개폐가 G - 단백질에 의해 조절된다는 사실도 최 근 에 발표되었다 (9). 이상 식물 세포의 여러 가지 현상 조절에 분명히 G ― 단백질 들 이 관여한다는 실험적 증거들이 제시되고 있으나, 아직도 식 물계에서는 관여하는 G - 단백질의 종류, 특징, 수용체와의 상호작용, eff ec to r 분자의 작용 등 구체적으로 해결되어야 할 문제점들이 그대로 남아 있는 상태이다. 9-3 이노시톨 인지질 대사 회로 식물, 동물, 미생물 등 거의 모든 생명체의 세포막을 구성하는 안지질 중 PI (4, 5)P2 (그림 9 一 3) 라는 인지 질이 소량 존재하고 있다. 세포의 신호 전이에서 이 인지질의 순환 대사 산물인 lP3 와 DAG 가 제 2 의 전령으로 서 중요한 역할을 담당하게 되는 것이다(그림 94). IP3 는 세포 내 Ca 안 저장고(소포체 또는 액포 등)의 막에 그 수용체가 존재하며, 이 수용체에 IP 따 결합하게 되면 저장고에 저장되어 있던 Ca 양이 세포질로 방출되게 되며, 증가된 Ca2+ 은 Ca2+/ 칼모듈린과 같은 단백질의 기능을 조절하거나, Ca2+ 의존성 단백질 키나제의 활성을 조절하여 단백질의 인산화 반응을 조절하게 된다. DAG 는 증가된 세포질 내 자유 Ca 안과 함께 단백질 키나 제 C(PKC) 의 활성을 증가시켜 단백질 인산화를 촉진시키며 그 후의 대 사 조절을 가능하게 하는 것이다. Boss 둥(1 0) 이 식물 세포에서 PIP2 의 존재를 최초로 확인한 이후 인지
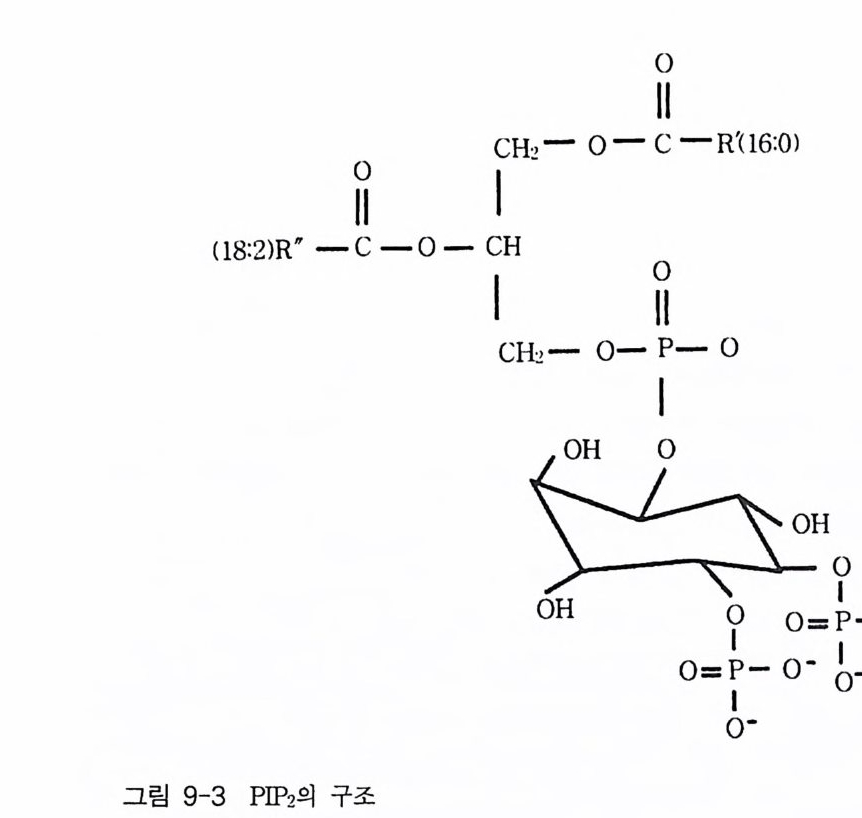 CH1 - o-ic- R ,(16:0 )
CH1 - o-ic- R ,(16:0 )
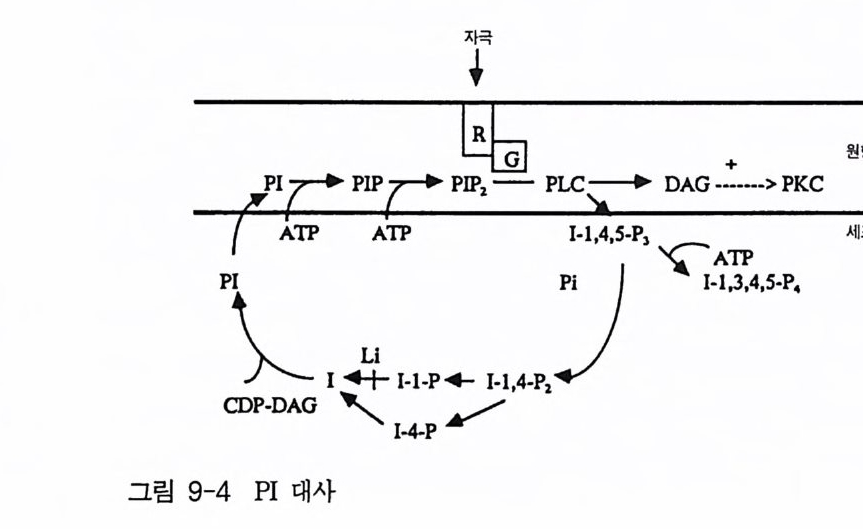 三/二 :\\.:::c 원힝질 막
三/二 :\\.:::c 원힝질 막
질의 존재가 고등 식물 (ll) 과 조류 (al g ae) 에서 결정적으로 다시 확인되었 는 데, 아직도 이 작은 양의 지질이 모든 식물에서 세포의 생리 반응을 조절할 것인지는 미지수로 남아 있는 실정이다. 특히 이노시톨 인지질 대사 반옹이 식물 세포에서도 신호 전이 과정의 중요한 역할을 하는지 여부에 관한 연구 결과들 이 동물 세포들의 경우와 비교하여 매우 부족 한 상태이다. 동물 세포에서 PIP 2 의 대사 과정이 관여되는 신호 전이 과정을 보면 환 경적 신호 를 받아 활성화된 수용체는 원형질막에 결합되어 있는 이종 삼 량체의 G - 단백질을 활성화시키 며, 이렇게 활성화된 G - 단백질은 PLC 를 활성화시켜 이 효소의 기질인 PIP 2 를 분해시키며 그 산물로 수용성의 IP3 와 지질에 녹는 DAG 를 생성시키게 된다. IP3 는 세포 내 Ca 안 저장고인 소 포체의 Ca2+ 채널을 여는 작용을 하며, 세포질 내 자유 Ca2• 농도를 증가 시키게 되며 , 세포의 생리 반응을 조절하게 된다 . IP3 는 IP3 키나제의 작용 을 받아 IP4( ln s 1, 3, 4, 5 P4 ) 로 전환되며, IP 4 는 IP 3 와 함께 세포질 내 Ca 안 농도 를 증가 시키는 역할을 하게 된다. DAG 는 자유 Ca 양 과 함께 단백질 키나제 C(PKC) 의 활성을 올려 단백질 인산화 반응을 촉진하게 된다. 9-3-1 이노시톨 인지질의 생성 및 대사 모든 이노시톨 인지질들의 합성에 전구 물질인 PI( ph osph atid y l ino - s it ol) 가 식물에서도 합성이 된다. CDP-DAG 로부터 DAG 가 이노시톨로 옮겨감으로써 합성되는 것이다. 이 반응은 소포체에서 일어나는 것으로 알려져 있다 (12 ). PI 가 만들어지면 이노시톨 인지질에 특이한 키나제들 에 의해 연속적으로 인산화 반응이 일어나 각종 이노시톨 인지질들이 생성된다. 아직 식물에서는 동물의 경우에 확인된 각종 PI 키나제들이 확인되어 있지는 않으나 존재할 것으로 생각된다. 밀의 뿌리에서 지질에 [ r -32P]ATP 로부터 32 pi가 빠르게 결합하는 현상을 발견하였는데, 인산
화된 이 지질들이 TLC 분리시 P I( 4)P 와 PI( 4, 5)P 2 와 같은 위치에 나타 나 는 사실이 확인되었다(1 3) . 이 사실로 미루어 보아 식물 에서 도 PI 키 나제 들 이 존재하여 PI 를 인산화시키는 반응 들 이 일어날 것 이라 는 강한 추측을 일으키는 것이다 . 당근 세포에서 분리한 원형 질 막에서 는 lys o PI 키나제의 활성도가 관찰되었는데(1 4), 아직까지 이 경우 PI 키나제에 의 한 촉매작용으로 나타난 것인지 아니면 lys o PI 에 특 이 한 키나제가 존재 하는 것인지에 대한 확증은 없는 상태이다 . PIP, lys o PI 그 리고 lys o PIP 의 인산화 반응 속도론적 분석에 의하면 lys o PI 의 인산화가 lys o PIP 생성의 주요 반응 경로일 것이라고 시사하고 있다(1 4). Gross 등(1 5) 이 당근의 원형질막에서 PI 키나제의 활성도가 PL A-!.에 의해 10 % 까지 수용성화될 수 있다는 사실을 발견하였는데, PL& 에 의한 키나제의 수 용성 화에 관한 가능한 설 명 은 PL A-!.가 PC(ph osph ati dy l choli ne ) 또는 PE(ph osph ati dy l e t hanol ami ne) 와 같은 막 구성 인지 질을 파괴시켜, 키나 제를 l y so- 인지질의 미셀(mi celle) 로 방출시키기 때문인 것으로 설 명하고 있다. 동물계에서는 이노시 톨 인지질 키나제들의 작용과 포스파타제 들 의 작 용이 동적 평형을 유지하는 것으로 알려져 있는데 반하여 식물에서는 이노시톨 인지질에 특이한 포스파타제는 한 가지 경우만 보고되어 있다 (16). PI 는 소포체에서 합성되는 데 반하여 인산화된 이노시 톨 인지질이 나 그 키나제들은 원형질막에서 발견된다는 사실은 PI 의 합성 장소로부 터 원형질막까지 운반하는 기작이 틀림없이 존재한다는 것이다. Morre 등 (17) 은 소포체로부터 원형질막까지 PI 의 수송은 두 개의 평행한 길을 통하여 일어나는 것으로 보고하고 있다. 하나는 골지체 를 통한 vesic u lar traffi c 을 통한 것 이 고, 다른 하나는 지 질 운반 단백 질을 통하거 나 막들 사이의 접촉 부위를 통하여 직접 수송되는 경우일 것이라고 생각하고 있다. 신호 전이에서 핵심적 반옹 단계가 PLC 에 의한 이노시톨 인지질의
가수분해이다 따라서 동물 세포의 경우 이노시톨 인지질 특이성 PLC 의 동질 효소 둘 의 종류가 다양한데, 그 이유는 신호의 다양성에 따른 다양 한 조절 기 능 이 필요하기 때문이다. 일반적으로 알려진 PLC 의 동질 효 소 둘 은 f], Y 그리고 8 형이다 f]형의 PLC 는 이종 삼량체의 G - 단백질 들 에 의 해 활 성 화되 며 , 7 형 의 PLC 는 PTK(pr o te i n tyros in e kina se, 단백 전 터 로 신 키나제)와 연결된 수용체에 의해 활성화되고, 8 형 효소는 그 활성 화 매커니즘이 알려져 있지 않다. 이들의 조절 방법은 다르지만 세 가지 유형의 PLC 모두는 같은 촉매적 성질을 가지고 있다. 그들은 모두 이노시 톨 인지 질 에 특 이적으로 작용하여 PI, PI( 4) P 그리고 PI( 4, 5)Pz 를 가수분해시키는데 3 - P i 를 가지고 있는 이노시톨 인지질은 가수분해시키 지 못한댜 이것 들 의 활성도는 Ca 앙 에 의존성을 나타내며, 그들의 기질 특이성들도 Ca 양 수준에 의해 조절된다 보통 인산화되어 있는 이노시톨 인지질 들 의 가수분해는 Ca 인 농도가 µmole 수준에서 잘 일어나는 반면, PI 의 경우 mmole 수준의 Ca2+ 농도에서만 일어난댜 이노시톨 인지질에 대한 PLC 의 활성도들이 피자 식물 (an gi os pe rms) 의 뿌리, 싹, 꽃, 꽃가루 등에서 발견되고 있으며 (18), 단세포 조류인 D. sal i na06) 에서도 발견되었다 . 동물의 경우와는 달리 두 가지 식물 모두 에서 수용성 효소 (soluble enz y me) 가 비수용성 효소(parti cula t e enz yme s) 에 비하여 PI 에 대한 활성도가 인산화된 유도체에서 나타내는 것보다 크게 나타났댜 또한 셀러리 줄기로부터 추출한 수용성 효소의 경우 어 떤 동정 조건에서도 PI( 4) P 또는 PI( 4, 5)P 2 를 가수분해시키지 못했다 (19 ). 밀의 뿌리와 싹 (20), 그리고 귀리의 뿌리(1 8) 세포들의 원형질막에 서 확인된 PLC 들은 매우 유사한 성질을 가지고 있다 이들은 모두 Ca양 에 의존성을 보이며 PI 에 바하여 인산화된 이노시톨 인지질을 월등히 가수분해시키는 성질을 가지고 있다. 귀리 세포에 존재하는 PLC 의 경우 P I( 4)P 와 PI( 4, 5)Pz 에 대한 가수분 해 능력은 Ca 양 농도가 10-100 µM 에서 최대값을 나타냈으며, PI 에 대해
서는 mM 의 Ca2t 농도 단위에서 최대값을 나타냈는데 (21), 이 현상은 동 물 세포의 경우와 유사한 것이댜 식물 세포의 경우는 아직도 PLC 가 완 전히 정제된 바 없으며, 이 효소의 생리적 역할 및 조절에 관한 생화학 적 메커니즘을 확실하게 말할 수 있는 단계가 아니다. 동물 세포의 PLC /3는 이종 삼량체의 G- 단백질을 통하여 활성화되며, PLCr 는 단백질 티로신 키나제 수용체와의 상호작용을 통하여 활성화되는데, 식 물 에서는 아직 이와 같은 반응 경로가 밝혀지지 않은 상태이다 . 신호 전이에서 이 노시톨 포스페이트의 역할이 매우 중요하여 동물의 경우는 그 연구가 상당히 진척되어 있는 반면, 식물에서는 이들이 생성되는 데 참여하는 키나제들에 관한 연구를 비롯하여 그 반응 경로 등도 아직은 확실히 밝 혀져 있지 않는 상태이다. 가장 중요한 이노시톨 포스페이트인 IP 3 의 경 우 광합성 능력이 있는 C re i마 nrd tii에서 확인된 바 있으며 (22) , 여기서 연구자는 HPLC 분리시 표준 IP3 와 동시에 이동하는 화합물을 발견하였 고, 그것은 IP3 수용체에 강하게 결합한다는 사실을 확인하였다 . 만일 이 노시톨 포스페이트들이 식물에서도 PLC 에 의해 만들어진다면, 1 : 2 시 클릭 포스페이토 유도체들이 만들어져야 하는데 아직 식물에서는 이와 같은 화합물들이 발견되고 있지 않은 상황이다. 이 화합물들의 경우 산 촉매 가수분해에 의해 쉽게 분해가 되기 때문에 분리하는 과정에서 소 실될 가능성도 있다. 1(1, 4, 5}P3 는 탈인산화되어(1, 4)bis p h os-p ha t e 와 (4, 5)b i s phos p ha t e 를 만들 수 있는데, 완두 뿌리의 경우 4, 5 이성질체가 우세하게 많이 존재하며 1, 4 이성질체의 경우는 소량만이 존재하는 것 을 확인하였다 (23). 반면 C eu ga me t os 의 수용성 추출물의 경 우는 1, 4 이성질체가 우세하게 많이 존재하며 4, 5 이성질체는 소량 존재하는 것 으로 밝혀졌으며 (24), 담배 세포의 수용성 추출물에는 이들 두 이성질체 가 동일한 비율로 존재하는 것으로 확인되었다 (25). 식물 세포에서도 동 물 세포의 이노시톨 포스페이트 순환 대사 과정과 유사한 반응들이 일 어날 것이라는 생각으로 현재 많은 연구들이 진행되고 있으나, 이 반응
들 에 참여하는 효소계를 비 롯 하여 확실한 반응 경로가 밝혀져 있지 못 한 상태이다. 9-3-2 신호 전이에서 이노시톨 인지질의 생리적 역할 식물이 외부 신호 를 감지하여 반응을 일으킬 때 Ca 앙 의 역할에 관해서 는 오랫동안 중 요하게 인식되어 왔다 (26) . 보통 자극을 받지 않은 세포들 의 경 우 세포 질 내 자유 Ca2• 농도는 100-200nM 의 낮은 농도를 유지하 며, 자 극을 받았 을 때 순간적으로 크게 Ca2+ 농도가 증가한다는 것이다. 예 를 들 어 Ca 2 + 에 민감한 단백질인 a eq uo ri n 이 주입된 식물의 경우 의부 자 극( 바람 , 접촉, cold-shock, elic i t or 등)에 의해 Ca 2• 의 농도가 크게 증가 되 는 것을 발견하였다 (27). 식물 세포의 경우도 신호수용 후 생성되는 IP 3 가 액포막의 IP3 수용 체에 결합함 으로써 액포의 막에 결합되어 있는 Ca 양 을 세포질로 방출한 다 는 사 실 이 확인되었다 (28). 액포의 막에 결합되어 있는 Ca2+ 채널들은 µM 수준의 lP 3 에 의해 열리는 반면 다른 이노시톨 포스페이트들의 경 우는 그 농도가 20 배 이상 되어도 아무런 효과를 주지 못함을 발견하였 다. 그러나 세포 내 다른 소기관으로부터 IP 3 에 의해 유도되는 Ca 안 의 방 출과 원형질막을 통한 Ca2+ 유입 여부는 확실히 밝혀져 있지 않다. 식물 에서 IP3 수용체의 정제와 특성화가 조속히 이루어져야 할 것이다. PIP 2 가 PLC 에 의해 가수분해될 때 IP3 와 DAG 가 생성되는데, DAG 는 단백질 키나제 C 의 활성화를 통하여 세포의 생리 반응을 조절하는 제 2 의 전령으로 알려져 있다. 식물 세포에서도 신호 수용 후 DAG 농도 증 가 현상은 몇 가지 보고되어 있으나 PKC 는 아직 확인하지 못하고 있는 실정이다. 그 동안 식물에서 확인된 많은 Ca2+ 의존성 단백질 키나제들 의 경우, 그 생화학적 성질 및 아미노산 서열이 동물의 PKC 와 비교할 때 유사성을 가지고 있지 않음이 밝혀졌다. 특히 낮은 Ca 안 농도에서
DAG 에 의해 활성화되는 단백질 키나제가 식물에서는 밝혀진 바 없는 상황이댜 식물의 신호 전이에서 이노시톨 인지질 대사 반응과 Ca 2 + 의 역할아 중요하다는 사실이 확인되면서 이 분야의 연구가 활발히 진행되 어 왔으나, 아직도 신호 수용, IP3 생성, Ca2 ’ 방출 그리고 세포 반응 사 이의 연결 문제가 그렇게 명확한 상태는 아니다. 이노시 톨 인지질 대사 와 신호 전이와 관련된 연구가 몇 가지 식물계에서 수행된 바 있 는 데 이 장에서는 세 가지 경우의 연구 결과들을 간단하게 소개하고자 한다 . 그 첫번째 예가 공변 세포에서 청색광 또는 abscis i c ac i d 에 의해 팽압 (turg or) 과 세포 부피가 빠르게 변화하는 현상인데, 신호 수용 후 세포질 내 Ca2+ 농도의 변화가 기공 개폐를 조절하는 핵심적 생화학 / 생리적 반 응 단계임을 시사하는 것이다 (29). 최근에 Lee 등 (30) 은 공변 세포 반응 에서 G- 단백질이 참여한다는 사실을 보고하였는데 아직은 G- 단백질의 eff ec to r 분자가 PLC 인지는 확실하게 밝히지 못하고 있는 상황이며 몇 종류의 G- 단백질이 참여하는지도 확실하지 않은 상황이다. 두번째 예로 서 조류의 일종인 D. sal i na 의 경 우 삼투압의 변화에 따라 신속한 막 전 위의 변화 (31), 원형질막의 투과도 (32), 세포 내 pH 및 Na' 농도 변화 등 이 일어나는데, 이러한 변화들이 이노시톨 인지질 대사 과정을 통하여 일 어 나는 것 으로 보고되 어 있다. Chlamy d omonas re i nhard tii의 defl ag e ll- ati on 현상이 G- 단백질에 의해 조절된다는 보고도 있고 (33), IP3 의 생성 과 Ca2+ 이 관련된다는 보고도 있다 (33). 9-4 신호 전이 에서 Ca2+ 의 역 할 다양한 외부 신호들이 수용되어 신호 전이 과정을 거쳐 세포 반응으 로 나타날 때 Ca2+ 이 세포 내에서 제 2 의 전령 역할을 하고 있다는 사실 은 모든 생명체에서 보편적으로 인정되고 있다. 식물의 경우 세포 분열
(34), 광형 태 형성 현상 (35), 중력 수용 현상 (36), 세포간 정보 교환 (37) 그리고 노화 현상 (38) 등에 관계되는 신호 전이 현상들에서 Ca2 • 이 제 2 의 전령 역할을 한다는 사실이 보고되어 있다. 세포 내 Ca2 令 중에서도 세 포 질 내 자유 Ca 2 ’ 의 농도 변화가 신호 전이 과정에서 중요한 역할을 하고 있 는 것이다 외부 신호에 따라 세포질 내 자유 Ca 2 令 농도의 증가 는 크 게 두 가지 경로 를 통하여 가능한데, 하나는 세포 내 Ca2+ 저장고 로 부터 세포질로 방출되는 경우이고, 또 다른 한 가지는 세포 외부로부 터 막에 걸합된 Ca2’ 통로 를 통하여 유입되는 경우이다. 식물 세포의 세 포질 내 평형 Ca2’ 농도는 보통 0.1 ~1.0 µM 정도인데 이 농도는 주로 소포체, 액포, 미토콘드리아, 원형질막 등을 통한 Ca2• 수송 (mob ili za ti on, inf l ux , up tal
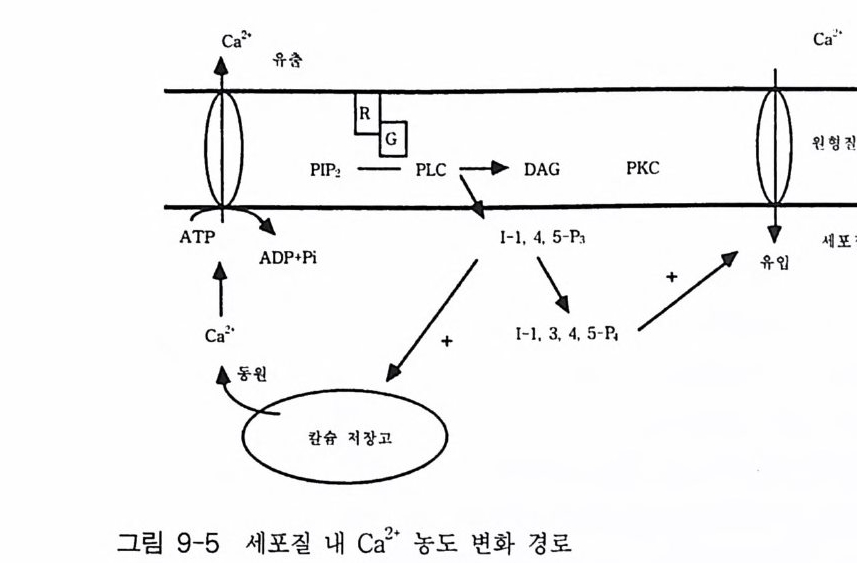 Ca’. ca'·
Ca’. ca'·
포에서 제 2 의 전령으로 그 중요성이 강조되는 cAMP 와 같은 화합물의 존재 및 기능이 식물에서는 아직도 미지수로 남아 있기 때문이다. 식물 세포에서 많은 생리 작용들이 Ca 2• 의 조 절로 진행되고 있는데, 예를 들면 세포 분화, 효소의 분비, 호르몬 작용, 괭압 조절, 빛과 중력에 의한 움직임, 효소의 활성도 조절 등의 현상들이다. 그러나 아직까지도 Ca2 • 의 조절 메커니즘이 완전히 이해되고 있지 못한 상태이다 . Ca 2’ 의 조절 메커니즘을 이해하는 데 가장 중요한 실험은 세포질 내에 존재하 는 자유 Ca2• 농도를 정확하게 측정하는 것인데, 현재까지는 세포막을 투과하여 세포질 내에 존재하여 Ca 양 과 결합함으로써 강한 형광을 내는 Ca2• 특이 성 형 광 지 시 약들(Quin 2, Fura 2, Fluo 3 등)을 사용하여 이 실 험을 수행하여 왔으나, 아직도 몇 가지 문제점들이 해결되지 않고 있는 상태이다. 최근에 세포의 Ca2• 연구는 주로 con foc al mi crosco py를 이용 한 연구들이 각광을 받고 있으며, 이 기술을 이용한 세포 내 Ca2• 분포 및 이동 현상의 확인 실험 둥은 앞으로 Ca2 • 의 조절 메커니즘을 연구하 는 데 큰 도움을 줄 것으로 기대된다 (42).
트로포닌 C(tr op o nin C) 와 칼모듈린과 같은 세포 내 Ca2• 수용체의 존 재와 그들의 작용 메커니즘 등이 발견된 후, 각종 세포들의 기능 발현에 대한 Ca 언 의 역할의 이해가 좀더 쉬워졌고, 지난 수 년 동안 다른 Ca 양 결합 단백질 들 이 발견 (43) 되어 식물에서도 이 분야의 연구가 활발히 진 행되어 왔댜 칼모듈린 이외에 식물에서 발견된 Ca2• 결합 단백질로서 calcim edi n( 44), qu in a te : NAD o 처 doreduc t ase(45) 그리 고 각종 Ca2• 의 존성 단백질 키나제 (46) 들이 있으며 , 이들에 관한 연구가 활발히 진행되 고 있다 칼모듈린은 다양한 고등 식물들, 녹색 조류 그리고 곰팡이류 등에서 확인 및 정제되었고 특 성화되었다. Manne 등 (47) 은 호박에서 칼모듈린 을 정제한 바 있는데 SDS-PAGE 결과 Ca 2+ 의 존재 하에서 그 분자량이 14,500Da 이었다 그 외에도 다른 식물에서 분자량이 다른 칼모듈린을 정 제한 바 있다 . 식물에서 정제한 칼모듈린들의 아미노산 조성을 분석한 결과 동물의 것과 비교하여 매우 유사한 조성을 가지고 있으며 (47), 특징 적인 것은 두 개의 프롤린 잔기와 하나의 트리메틸 리신(trim e thy l Ly s) 잔기 그리고 상당 양의 음전하를 띤 아미노산들을 가지고 있으며, 트립 토판 잔기가 없다는 사실이다. 시금치로부터 정제한 칼모듈린의 아미노 산 서열의 경우 소의 뇌에서 정제한 것과 비교해 볼 때 13 군데 중에 12 곳이 Ca 2+ - 결합 부위 또는 flanking a- 헬릭스 부위에 있다는 것이다. 식물 세포에서 칼모듈린에 의해 조절되는 대표적인 효소계들인 [Ca2• + Mg 2• ] ATPase, NAD 키나제들 그리고 단백질 키나제들이 있다. Diet e r 등 (48) 은 호박의 세포질 분획에서 수용성 NAD 키나제를, 옥수수의 미토 콘드리아 외막에서 비수용성 NAD 키나제를 분리하였고, Sim o n (49) 등 은 완두의 엽록체에서 비수용성 NAD 키나제를 확인하였다. 최근 식물에 서도 Ca2 + 에 의존성을 나타내는 많은 단백질 키나제들이 정제되고 특성 화되고 있는데, 그 효소들은 크게 세 가지 유형 (Ca2• 의존성, Ca2+ /칼모듈 린 의존성, Ca2+/ 인지질 의존성)으로 나누어진다. 이들 효소에 관한 자세
한 내용은 다음 절에서 단백질 인산화와 함께 기술하고자 한다. 식물에 서 대표적인 신호 수용체인 피토크롬의 신호 전이 과정에서 피토크롬이 적색광을 흡수한 후 초기 단계에서 세포질 내 Ca2' 농도 를 증가시킨다는 보고 (50) 들이 최근에 나타나고 있으며, 증가된 Ca 언 은 어떤 Ca2 + 의존성 단백질 키나제의 활성을 높여 주는 작용을 할 것이라는 가정을 하고 있 댜 그러나 아직도 Ca2 ' 증가의 구체적 경로 및 메커니 즘 그 리고 어떤 단백질 키나제가 활성화되는지는 확실히 밝혀져 있지 못한 상태이다. 9-5 단백질 인산화와 단백질 키나제 동물 세포의 신호 전이에서 단백질의 인산화 과정이 가장 핵심적인 생화학 반응이라는 사실은 이미 보편적으로 알려져 있으며, 다양한 단백 질 키나제들이 이들 단백질 인산화 반옹에 참여하여 신호의 증폭에 중 요한 역할을 하고 있음이 잘 알려져 있다. 세포 외부의 신호는 세포막에 결합되어 있는 신호 전달 체계를 활성화시켜 적은 수의 화학적 매개체 또는 제 2 의 전령을 생성시키며, 이들은 각종 단백질 키나제들과 단백질 포스파타제들의 활성을 조절하여 세포 내 단백질들의 인산화 상태를 변 화시켜 대사 조절을 하게 되는 것이다 (51) . 단백질 키나제들은 그들을 활성화시키는 안자들 (e ff ec t or molecule) 에 의해 몇 가지로 구분된다 (cAMP 의존성 단백질 키나제, Ca2+ /칼모듈린 의존성 단백질 키나제, cGMP 의존성 단백질 키나제, Ca2+/ D A G 의존성 단백질 키나제, 인지질 의 존성 단백질 키나제, 단백질 티로신 키나제 등) . 그러나 식물에서는 아직 도 매우 제한된 종류의 단백질 키나제들만이 보고되어 있는 실정이다 (52). 호박(헛)과 Amaran t hus(54) 에서 Ca2+ 과 인지질에 의존성을 보이는 단백질 키나제를 확인한 바 있으며, 이 단백질 키나제가 동물의 PKC 항 체와 교차 반응 (cross-reac ti on) 하는 것을 확인하였다 (55). 최근에
Sussman 등 (56) 은 귀리의 뿌리에서 막에 결합되어 있는 단백질 키나제 중 Ca 2 t 과 인지 질 에 의해 활성화되는 단백질 키나제 (79kDa) 를 부분 정 제 하여 특 성 화한 연구 결과 를 보고한 바 있고 , Chae 등 (57) 은 귀 리 의 coleo p tile 세 포질 에서 79 kDa 의 Ca 2+ /P S 의존성 단백질 키나제를 부분 정제하여 특 성화 한 연구 결 과 를 보고하였다 . 동물 에서 는 상당히 많은 Ca 2 ’ / 칼모 듈 린 의존성 단백질 키나제들과 단 백 질 키나제 C 계열 효소 들 의 구조 및 기능에 관하여 연구된 반면 식물 에서 는 그 연구 결 과 들 이 매우 부족한 형편이다. 동물 세포들에서 확인 된 C a2’/ 칼모듈 린 의 존 성 단백질 키나제 들 은 세 가지 다른 유형 (C ai\1 키 나 제 I , Ca i\1 키나제 II 그 리고 Ca i\1 키나제 m) 들이 있으며, 이들은 정 제되고 특 성화되었다. Ca i\1 키나제 m 는 몇 개의 단백질들을 인산화시키 는 다기 능 성 단백 질 키나제이며 (58), Ca i\1 키나제 I 과 Ca i\1 키나제 II 는 어떤 특 정한 단백 질 만을 인산화시킨다. 동물 에 비하여 식물의 경우 신호 전이 자체에 관한 연구 결과가 초보 적 안 상태에 있기 때문에 신호 전이와 관련되어 연구된 단백질 인산화 에 관 한 연구 결과도 매우 적은 편이다. 단백질 인산화에 관련된 단백질 키나제의 종 류 및 정제에 관한 확실한 결과들도 부족한 상태이며, 인산 화되는 기질로서의 단백질의 정체 및 그 기능도 아는 것이 거의 없는 상태이다. 따라서 여기서는 몇 가지 제한된 단백질 키나제들에 의한 단 백질 인산화와 신호 전이에서 그들의 가능한 역할에 대하여 간단히 논 의하고자 한다 . 각종 식물에서 수용성 단백 질 및 막 결합 단백 질들의 인산화가 Ca 2+ 의 농도 증가에 따라 증가하는 현상을 관찰 (52) 하였고 , 어떤 경우는 칼모듈 린 억제제에 의해 그 인산화가 저해되는 현상도 관찰되어 Ca 2+ 에 의한 단백질 인산화에 칼모듈린이 참여하고 있다는 사실을 입증하는 것이다 . 그러나 Ca 2+ 에 의해 증진되는 단백질의 인산화가 모두 칼모듈린을 통한 것이 아니고, Ca 2+ 과 다른 어떤 화합물(인지질 등)에 의존성을 보이는 단
백질 키나제에 의한 경우도 발견되고 있다 (57). 식물의 신호 전이 현상 들 중에 광 신호 전이(청색광 , 적색광)에 관한 연구 결과들 가운데 광선 신호가 단백질의 인산화와 직결된다는 보고 (59, 60) 들이 최근에 많이 나 타나고 있다. 이 경우에도 초 기 신호인 광선이 수용체에 의해 홉수된 후 어떤 경로를 통해서든 세포질의 Ca 안 농도를 변화시켜 그 에 따 른 단백질 인산화의 변화가 일어날 것으로 생각하고 있는데 , 아직 도 이 반응에 참 여하는 확실한 단백질 키나제의 종류 및 구조 등은 모르고 있 는 상태이 다. 그러나 지금까지 보고된 식물에서의 인산화 반응들의 경우 모두 Ca 안 이 크게 영향을 준다는 사실은 틀림없는 것 같 다. 이 사실은 식물 세포의 경우 제 2 의 전령으로 Ca 안 의 역할이 신호 전이 과정에서 매우 중요함을 나타내는 것이다 . Ca 2+ 에 의해 증진되는 단백질의 인산화 반응 들은 세포질 내 자유 Ca 양 농도가 lµM 과 같이 낮은 농도에서 일어나는 데, 이 사실은 식물 생리적 측면에서 그 중요성이 인정되는 것이다. 지금까지 식물의 경우 인산화되는 기질 단백질들이 많이 알려져 있지 않은데 Ca 2+ / 칼모듈린 의존성 단백질 키나제들의 기질로서 quina te : NAD 산화 환원 효소 (61), 포스포에놀피루베이트 카복실라제 (62), [H' ] ATPase(56) 등이 보고되어 있을 뿐, 신호 전이에서 유전자 발현 단계인 전사 과정 의 tran s-actin g 요소로 작용할 가능성 이 있는 인산화된 단백 질은 확실히 그 정체가 파악되지 않았다. 최근에 식물 세포에서는 Ca2 + /칼모듈린 의존성 단백질 키나제 또는 Ca2 + / 인지질 의존성 단백질 키나제 이의에 새로운 형태의 Ca2• 의존성 단백질 키나제 (CDPK) 가 정제되고 특성화되었다 (59). 대두로부터 CDPK 의 cDNA 클론이 얻어졌으며 이것으로부터 이 효소의 아미노산 서열이 결정되었는데, 아 효소는 단백질 키나제 촉매 영역과 칼모듈린과 유사한 Ca2+ 결합 부위를 가지고 있는 것이 밝혀졌다. 이 효소의 분자적 구조는 Ca2+ 에 의한 이 효소의 직접적인 활성화 현상을 설명할 수 있으며, 이 효소가 앞으로 식물의 신호 전이룰 비롯한 다른 생리 반옹에 참여하는
단백질 인산화 과정에 중요한 단백질 키나제로서의 참여 가능성이 높아 지고 있는 실정이다. 현재까지 10 여 종의 다른 식물체들로부터 CDPK 가 분리 정제되어 특성화되었다(표 9-2 ). 이 장에서는 지면 관계로 이 효소 들 의 구조, 생화학적 성질, 세포 내 위치 및 생리적 기능 등에 관한 자세 한 내용의 언급은 생략하고자 한다. 마지막으로 식물에서의 신호 전이와 관련된 단백질 인산화 반응을 적 색광 신호 전이의 경우를 예로 선택하여 조금 자세히 기술하고자 한다. 현재 식물의 신호 전이 현상 중 가장 관심의 대상이 되는 경우가 적색 광 수용체인 피토크롬에 의한 신호 전이 현상이다 . 식물의 성장 및 분화 등 피토크 롬 에 의해 조절 받는 현상들은 이루 헤아릴 수 없을 정도로 많 고 중요한데, 아직도 피토크롬이 적색광( Amax : 660nm) 을 흡수한 후 생리적으로 활성형의 피토크롬 (P f r 형)으로 전환된 후 어떤 생리/생화학 적 반응 경로를 거쳐 세포 반응을 일으키는지에 관한 신호 전이 과정을 거의 파악하고 있지 못한 상태이다. 그러나 이 신호 전이 과정을 이해하 는 데 가장 확실하고 매력적인 한가지 과정은 Ca 양 이 제 2 의 전령으로 작용할 것이라는 가설이었고, 이를 입증하기 위해 지난 10 년 동안 많은 논문들이 발표되었다. 따라서 피토크롬이 적색 광선 수용 후 변화되는 세포질 내 Ca2• 농도가 어떤 생화학적 반응으로 연결될 것인지가 많은 관심의 대상이 되어 왔다. 그 관심의 대상 중의 하나가 Ca 양 과 연관성을 갖는 어떤 단백질 키나제의 활성 변화를 통한 단백질의 인산화 반응으 로 나타날 것이라는 생각을 여러 연구실에서 하게 되었다. Datt a 등 (63) 은 완두의 핵에서 그 인산화가 적색광과 Ca2• 에 의존성을 보이는 세 개의 다른 단백질들 (47kDa, 64kDa 그리고 77kDa) 을 확인하 였는데, 이들의 인산화는 원적색광의 조사와 Ca 양 제거제인 EDTA 와 같 온 물질의 첨가시에는 전혀 증가 현상을 보이지 않았음을 관찰하였다. 같은 실험 대상으로부터 폴리아민(po l yamin e) 에 의해 활성화되는 단백질 키나제를 발견하였고 90% 의 순도로 정제한 바 있으나 (64), 아직까지도
m clCuaeicE tff aCclruemumn eqitie R )M(µ ,KK奭)5 1-1 0 02 HO .30 51. .62f)(lf-Si OO(e! cs)ani 3 .0 .05 05.(C-0K.4 )5J 2) (ccn.30sai ) S05-A(1I .08 (cme0.3a)s A) IISa)(- 찍
9 에물一2.표서 식성질의나키백의존 단 제 종 류Ca' 2 p .ct.esAcSe i1.f od~l ( g oµm! Dkm)nmOa) (-1 1smoubTl essgluiS rniayteim aiiNv oancaitit ll oe lacllucstlbluear5-00uffae6 220 .0 acel xoabe ptmeepuf nirtmrr3 09. -050었 ) y bauv-serodll4oeaa elltes el5be it'r/.奭0 4Sl'rman-mee b5 函0. mlceo5ec5 1oo- 8020 suotil0olbe0l.. p. 24. mam5 ener5- 81b '1.05004.9 ldnuelullsbeloa aW708. iO 4 ao.09 0meose6g(u1tb4l-iu) KMlo 40 ssealv9b o0e0 oa.le7 lu t80 (7J or.araboeommp 3 t en6t01 5.5 -20rpwo ea<5eal umbcnsl(PCIa3ic0s)nae i3 .100 fi-6f(50. )S crnamhonluw e-itlp 80ape0 1. )안 acs edaosit oseallv versbbueesleIl e10 -6003 t 02.0i5 0I7O 05-I O 3.00'2 IP nerabme .mp 33502.0 80 P-803Sl W9 II.0 O ys4-uloodC Kso( eln) bueb15el10 a30 l.-n yseturl50c ello ae-bs7 c eulnu blo 1.001-탔25 ya 7 ANo5Dc anPKeDbCs70 oem e seanahki Ielbubwlso 04ry(9tcanse Ji 7(Il-S)A ahewc ob50mI I esnaik-amoerhint0 00 6ry8 t-12 . ssa4 -edtaSocA iJ(JI enlO)(c asi e falaehws leubol 10 810t0. 43 ec ~p c bS•ificnosh S-IIIe ns htiivctaot.i 이적 지른다별는 tyi 한 는없H 는또-측 .다하여용사 였웅정1하 loF- d재 이niwlcca 은niotavic존ta성환 의서에건조 는않 지도하c 대한 에한재존 이miucal의 .때이비 의도성환 다 l a-malhimxaf값 C이ytiivtca 은들에또 .;:)oK(도농 는되구요 해대 a해먼a 는대 yt에vitimac ml요)`이다It(도농 는되 .구LL es d c ttnye nosh; etiehppiti: 와51-KC 어약 는41-MK S-AII 와S-l는ilp. 다s이ontiara per이 효소가 피토크롬에 의해 조절되는지의 여부는 미확인 상태이다. 그 후 피토크롬의 작용에 의해 그 탈인산화 (29kDa, 30kDa) 와 인산화 (30 kDa) 가 조절된다는 사실을 암실에서 성장한 귀리 조직으로부터 확인하 였고 (65), 귀리의 세포로부터 피토크롬의 작용에 의해 인산화가 조절되 는 단백 질 (2 7 kDa 와 32 kDa) 들 이 존재 한다는 사실을 보고한 바 있다 (66). 박 등은 위의 보고에서 귀리 세포에서 피토크롬의 작용이 PKC 의존 성 단백질 인산화일 것이라는 가능성을 제시한 바 있다. 피토크롬에 의 해 조절 되 는 반응 과정에 PKC 가 참여할 수 있다는 가능성은 몇몇 연구 실에서 보고한 바 있다 (4). Haas 등 (67) 은 PKC 억제제인 s t auros pori ne 의 이 용으로 피 토크롬에 의 해 중재 되 는 Dr yop t er i s filix - mas L. 포자의 Ca2+ 의존성 발아가 감소하는 현상을 관찰한 바 있다 . 한때 피토크롬 자 신이 단백질 키나제의 역할을 겸하고 있다는 설이 제시된 바 있으나 (68), 곧 이어 이 사실은 피토크롬을 정제할 때 피토크롬과 결합되어 있는 단 백질 키나제가 같이 정제되기 때문이라는 반론이 제기되었다 (69) . 어쨌 든 이 들 의 견해 차이는 제시되었으나, 피토크롬 분자 자신이 단백질 키 나제의 기질이 될 수 있는 가능성을 제시해 준 것으로 사료된다. Mc- Mi chael 과 La gari as(70) 는 다가 양이온에 의해 자극되는 어떤 단백질 키 나제가 귀리에 있는 피토크롬의 N- 말단의 세린이 풍부한 부위를 인산화 시 킨다는 보고도 하였다. Romero 등 (7) 은 피토크롬에 의해 조절되는 단백질의 인산화가 G- 단 백질을 통하여 일어나는가를 확인하기 위하여, 귀리에서 분리한 핵을 사 용하여 콜레라 독소 처리에 따른 단백질의 인산화 결과를 분석해 보았 는데 두 단백질(1 0kDa, 54kDa) 의 인산화가 증가하는 사실을 확인하였 고, 두 개의 다른 단백질 (60 kDa, 75kDa) 의 인산화는 저해되는 사실을 발견하였다. 광에 의해 조절되는 유전자 발현에 핵단백질의 인산화 결과 가 관여될 것이라는 가정은 Datt a 등 (71) 에 의해 제시된 바 있다. 가장 최근에 Fallon 둥 (60) 은 적색광에 의존성이며, Ca2 + 에 민감한 단
백질의 인산화 현상을 발표하였는데, 여기서 그들은 적색광에 의해 유도 되는 Ca 언 농도 변화는 2 분 이상을 지속하지 못하기 때문에 인산화 반응 도 이 시간 내에 완결되어야 한다는 결론을 내리고 있다. 적색 광선 신 호와 단백질 인산화에 관한 실험 결과들이 아직도 확실한 기질의 제시 를 비롯한, 참여 단백질 키나제의 정체를 제시하지 못하고 단지 단백질 인산화 반응이 일어난다는 사실을 암시해 주는 것이며, 특히 인산화된 단백질의 다음 역할에 관해서는 전혀 모르고 있는 상태이다. 청색 광선 신호 전이와 단백질의 인산화 반응에 관해서는 Bri ggs 연구실에서 많은 연구 결과 (59) 들을 제시하고 있는데, 120 k.D a 의 단백질의 인산화가 청색 광에 의해 유도된다고 주장하고 있다.
9-6 신호와 유전자 발현 동물에서 신호 전이의 경로 및 분자적 반응 메커니즘 연구가 상당한 수준에 도달하여 최초의 신호가 유전자 발현까지 연결되는 과정이 비교 적 많이 이해되고 있는 반면, 식물의 경우는 신호와 유전자 발현에 관한 연구 결과들이 매우 제한되어 있다. 이 장에서는 비교적 그 연구가 많이 진행된 적색광 신호 전이와 광 유도성 유전자 발현에 관한 내용을 간단 히 기술하고자 한다. 제 5 절까지에서 기술했던 신호 전이의 생리/생화학 적 반옹 경로들이 과연 유전자 발현에 어떻게 연결될 것인지가 이 분야 연구의 관심의 대상인데, 특히 인산화된 단백질의 역할이 무엇인지가 연 구의 초점이 되고 있다. 빛에 의해 조절되는 대표적인 유전자들은 광수확 엽록소 a/b-결합 단 백질들을 발현시키는 rob 유전자들, 캘빈 사이클에서 중요한 효소인 리 뷰로스비 스포스페 이 트 카복실라제/옥시 게 나제 (ribu lose bis p h osph ate car- boxy la se/ o xyg enase) 를 발현시키는 rbc S 유전자들 그리고 피토크롬을발현시키는 phy 유전자들이 있는데, 이들 유전자들은 촉진 유전자 부위 에 몇 개의 다른 mo tif를 가지고 있으며, 이들이 유전자의 전사 조절에 참여할 것으로 예상되는 단백질 인자들의 결합 부위로서 그 중요성을 갖는 것으로 사료된다 (72). 예를 들면 담배의 azb E 촉진 유전자에서 DNA 와 상호 작용하는 단백 질 인자들로서 GBF, GA-1, AT-1 그리 고 GT- 1 등이 보고되어 있다 (73). ACGT 의 염기 서열을 포함하고 있으며 GBF 가 결합하는 G box 는 Arabid o p si s rbc S-lA 유전자 발현에 중요한 요소로 알려져 있다 (74). 두 개의 다른 인자 (LRF ― l 과 ABF-1, LRF-1 인 자는 Lemna rbc S 유전자에 결합하는 활성도를 가지고 있으며, ABF-1 인 자는 완두의 azb 유전자에 결합하는 활성도를 가지고 있음)들도 발견되었 는데, 이들의 함량이 광의 존재 하에서 성장한 식물과 암소에서 성장한 식물의 경우 각각 다름을 확인할 수 있었다. 광 조절 경로를 이해하기 위한 강력한 접근 방법 중 한 가지가 정상 적인 조절이 변화된 돌연변이체를 분리하는 것이다. Arab i do p s i s 에서 발 견된 두 개의 홍미 있는 돌연변이 체가 det 돌연변이 체 (75) 와 cop 돌연변 이체이다 (76). 이들 돌연변이체들은 광선이 없는 조건에서도 광선의 존 재 조건에서 자라는 야생형(wi ld 유형)의 여러 가지 발달이 그대로 재현 되는 것이댜 이와 같은 돌연변이체들을 연구함으로써 광 신호 전이에 중요한 역할을 수행하는 인자가 무엇인지를 쉽게 찾을 수 있는 것이다. 예를 들면 이들 돌연변이체들은 암소에서 azb RNA 를 높은 수준으로 발 현시키는데, 이 사실은 암소에서 일어나는 이 유전자 전사의 정상적인 억제 과정이 돌연변이체들에서는 없어졌다는 것이다 (77). 인산화된 단백질이 rbc S-3A 유전자 (166 개의 뉴클레오티드가 잘라진 촉진 유전자를 가지고 있는 rbc S) 의 어느 부위에 결합하여 유전자 발현 특히 전사 단계를 조절할 것인지를 알아보는 연구를 Chua 등 (78) 이 실 시하였는데, 두 개의 단백질 (3AF5, 3 .AF.:})이 결합하는 부위가 두 개의 box(box II : -151 ~ _ 138 : GTGTGGTIAATATG top stra nd, box ill :
_125~— 114 : AGTGAAAATGAT bott om str an d) 상에 있다 는 사실을 확인하였댜 그들은 3AF3 가 그 결합 부위에 붙 은 것이 인산화에 의 존 성 을 나타내는 사실을 발견한 반면 3AF5 의 경우 는 그것이 인산화 상태에 의의 해단 백아질무의런 영인향산을화 가받 지— 1않66 는 rb다c는 S -사 3A 실 을유 전확자인 하발였현다에. 요이 구결되 과 는 는 사두항 이개 지만, 3AF5 와 3AF3 의 활성을 조절하는 인산화의 메커니 즘은 다 르 다 는 사실을 입증하는 것이다 . 피토크롬의 신호가 세포질의 Ca2+ 농도 변화로 이어 지며 변화된 Ca2 · 농도는 Ca 안 의존성 단백질 키나제의 활성을 올려 주고 어떤 단백질의 인산화 반응이 일어날 것이라는 가정을 기술한 바 있 는 데, 인산화된 단 백질의 기능에 대한 의문이 제기된 바, 위에서 기술한 내용이 그 해답이 될 수도 있다는 가능성을 제시하는 것이다. 최근에 Chua 등 ( 79) 은 피토 크롬 신호 전이에 G- 단백질이 관여하며 이들은 적어도 두 개의 다른 경 로로 그 신호를 전달하는데, 한가지 경 로는 Ca 2+ /칼 모듈린을 통하여 cah-Gus 유전자의 발현을 조절하는 것으로 밝혀졌고, 다른 하나의 경로 는 안토시아닌 (an th oc yani n) 생합성을 조절하는 경로인데 Ca 양을 요구하 지 않는다는 것이다 . 현재까지 알려진 피토크롬 유전자는 다섯 종류(plry A, plry B, plry C, plry D, plry E) 가 있으며, 따라서 피토크롬의 종류도 다섯 종류가 세포 내에 공존하는 것으로 알려져 있는데, 식물이 처해 있는 환경 조건 특히 광선의 유무에 따라 어떤 종류의 피토크롬이 많이 존재하느냐가 결정된 다(그림 9-6). 예를 들면 광선의 존재 하에서 성장한 식물의 경우에는 plry B 의 전사에 의해 생성되는 피토크롬이 우세하게 많으며, 암소에서 성장한 식물의 경우는 plry A 의 전사에 의해 생성되는 피토크롬이 우세 한 것으로 알려져 있다. 현재 많은 이 분야의 연구자들은 다른 피토크롬 에 의한 신호 전이 과정들이 서로 다를 것으로 생각하고 있으나, 그 구체 적인 반응 경로 및 반응 결과들이 무엇인지는 모르고 있는 상태이다.
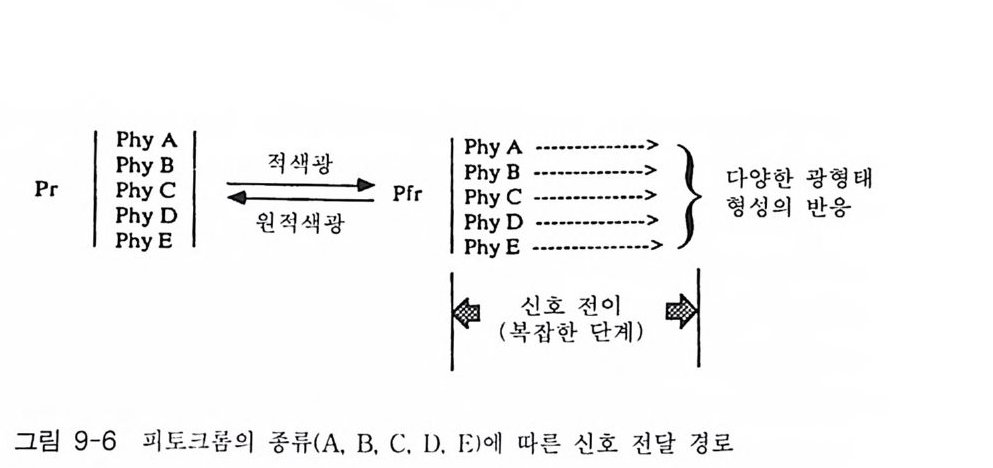 그림Pr 9-6 PhP피yh P토yAhPyB크hyPC몸hy D빼 의 E 원종 적적류색(색광A광, ~B, CP,f r D . E5) p에h~ yI,, pCDAEB 따h복 y| p른ii잡안iiih y ph신二한 三yp호iii털 iihy 1계 i ~~ti전 _一). V달..V }경VV로다형V 성T양 의한 광반형응태
그림Pr 9-6 PhP피yh P토yAhPyB크hyPC몸hy D빼 의 E 원종 적적류색(색광A광, ~B, CP,f r D . E5) p에h~ yI,, pCDAEB 따h복 y| p른ii잡안iiih y ph신二한 三yp호iii털 iihy 1계 i ~~ti전 _一). V달..V }경VV로다형V 성T양 의한 광반형응태
식물의 깅 우는 신호 전이 과정의 생리 / 생화학적 연구 자체가 동물에 비하여 초 · I,l· 적인 단계에 놓여 있는 상태이기 때문에, 신호 전이의 생화 학적 반응 경로와 유전자 발현과의 상관성 연구는 더욱이 미진한 상태 이다 그리나 앞으로 이 분야의 연구가 활발히 진행될 것으로 기대된다. 참고문헌 1 ) Hasunma, K, Furukawa, K, Tom ita, K., Muta ki, C. and Nakamura, T. 0987) Bio c hem Bio p h ys. Res. Commun 148, 133 2) Drobak, B. K, Allan, E. F., Comerf ord , J._G ., Robe rts, K and Dawson, A P. (1988) Bio c hem Bio p h ys. Res. Commun 150, 899 3) Ma, H., Yanofs k y, M. F. and Mey er ow itz, E. M. (1990) PriJC Natl. Acad Sci . USA 87, 3821 4) Bossen, M. E., Kend rick , R. E. and Vredenberg, W. J. (1990) Ph ysi o l og ia Planta ru m 80, 55 5) Wa rpeh a, K M. F., Hamm, H. E., Rasen ick , M. M. and Kaufm a n, M.
S. 0991) Proc Natl. Acad Sci. USA 88, 8925 6) W arpeh a, K. M. F., Kaufm an, M. S. and Bri ggs , W. R. 0991 ) Photo c hem Photo b io l. 55, 595 7) Romero, L. C., Sommers, S. D., Gato r , C. and Song , P. S. (1991 ) FEES Lett 282, 341 8) Fa irle y -G renot, K. and Assmann, S. M. (19 91 ) Plant Cell 3, 1037 9) Lee, H. J., Tucker, E. B., Crai n, R. C. and Lee, Y. 0993) Plant Ph ysi o l. 102, 95 10) Boss, W. F. and Massei, M. 0. (1985) Bio c hem Bi op h ys . Res. Comm 血 132, 1018 11) Cote ' , G. G., Morse, M. J., Cra in, R. C. and Satt er , R. L. 0987) Plant Cell Rep. 6, 352 12) Moore, T. S., Jr. (1990) Inosit ol Meta b olism in Plants , New York ; Wi ley - L is s . p 107 13) Sandeliu s , A S. and Somma rin, M. (1986) FEES Lett. 201, 282 14) Wheeler, J. J. and Boss, W. F. (1992) Bio c him Bi op h ys. Acta 1134, 73 15) Gross, W., Yang , W. and Boss, W. F. (1992) Bio c him Bi op h ys. Acta 1134, 73 16) Ein s pa h r, K J., Peeler, T. C. and Thomp so n, G. A Jr. (1989) Plant Ph ysi o l. 9 0, 1115 17) Morre, D. J., Penel, C., M orre, D. M. and Sandeliu s , A S., 0991) Proto p l a sma, 160, 49 18) Tate , B. F., Schaller, G. E., Sussman, M. R. and Crain , R. C. (1989) Plant Ph ys io l. 91, l'l7 5 19) McMUITay, W. C. and Irvine , R. F. (1988) Bi oc hem ]. 249, 877 20) Melin , P. M., Pic a l, C., J er gi l, B. and Sommr uin, M. , (19 92) Bi oc hi m
Bi op l zys. Acta 1123, 163 21 ) Tate , B. F. (19 90) Cmracte r iz a ti on and par tia l p u rifi따 on of a ph osph olip ase C from the pla sma membrane of Avena sati va Ph. D the si s , Un iv. Connectic u t, Sto r rs, p 117 22) Qu annby, L. M. (1990) Inosit ol ph osph olip id sig nall in g in Clilamy- domonas rein h ardti i, Ph. D the sis , Un iv. Conneti cu t, Sto r rs, p 71 23) Drobak, B. K., Watk ins , P. A C., Chatta w ay , J. A., Robert s, K. and Daws on, A P. (19 91) Plant Plz ys io l . 9 5, 412 24) Irvin e , R. F., Letc h er, A J., Ste p h e ns, L. R. and Musgr a ve, A. (19 92) Bi oc hem ]. 281, 261 25) Jos eph , S. K., Esch, T. and Bonner, W. D. Jr. (19 89) Bi oc hem ]. 264, 851 26) Robert s, D. M. and Hannon, A C. (1992) Annu Rev. Plant Plz ys io l. Plant Mo!. Bi ol . 4 3, 375 27) Knigh t, M. R., Sm ith, S. M. and Trewavas, A.- J . (1992) Proc Natl. A( Xld Sci . USA 89, 4967 28) Alexandre, J., Lassalles, J. -P. and Kado, R. T. (19 90) Natu r e 343, 567 29) Lee, Y. and Assman, S. M. (19 91 ) Proc Na tl. A 따 Sc i. USA . 88, 2127 30) Lee, H. J., Tucker, E. B., Cra in, R. C. and Lee, Y. (1993) Plan t Plz ys io l. 102, 95 31) Oren-Sha mir, M., Pick , U. and Avron, M. (19 90) Plant Plz ys io l. 93, 403 32) Weis s , M., Benta l, M. and Pick , U. (19 91 ) Plant Plz ys io l. 97, 1241 33) Qu annby, L. M., Yueh, Y. G., Cheshi re, J. L. et al. (19 92) J Cell Bio l. 116, 7~
34) Hepl e r, P. K 0985) ]. Cell Bi ol. 100, 1363 35) Roux, S. J. (1984) Bio S ci. 3 4, 25 36) Sie v ers, A, Belrrens, H. M., Buckhout, T. J. and Gradman, D. (19 84) Zeit sc hrift f Pjla11 2en Phys i o l. 114, 195 37) Mein e rs, S., Baron-Ep ei, 0. and Schin d ler, M. 0988) Plant Phys i o l. 88, 791 38) Fergu son, I. B. 0984) Plant Cell Envir o n 7, 477 39) Drob 책, B. K. and Fergu son, I. B. (1985) Bi oc hem Bio p hy s . Res. Commun 130, 1241 40) Reddy, A S. N. and Poova iah , B. W. 0987) ]. Bi oc hem(Ty ok o). 101, 569 41) Rinc on, M. and Boss, W. F. 0987) Plant Ph ysi o l. 83, 395 42) Brain , M. 0993) Cell Bi ol og ica l Ap pli ca ti on of Confo c al M icr oscopy , Academ ic Press, Inc., p 268 43) Diet e r , P. and Manne', D. (1986) Plant Cell Ph ys io l. 27, 1327 44) Dauwalder, M., Roux, S. J., Hardi so n, L. K. and Redman J. R. (19 86) ]. Cell Bi ol. 103, 453a. 45) Grazia n a, A, Dil len schneid e r, M and Ranje v a, R. (19 84) Bi oc hem Bi op h ys. Res. Commun 125, 774 46) Bri ggs, W. R., et al, 0992) Annu Rev. Plant Ph ysi o l . and Plant Mo!. Bi ol. 43, 375 47) Manne', D. and Diet e r , P. (19 8.3) Role of Ca2• and Calmodu lin in Plants . In Cheung WY(ed) : Calci um and Cell Functi on s, Vol. 4, New York : Academ ic Press, p 263 48) Diete r, P. and Manne', D. (1980) Ann NY Acad Sc i. 356, 371 49) Sim o n, P., Bonzon, M. , Grepp in, H. and Manne', D. (19 84) FEES Lett 167, 332
50) Chae, Q., Park, H. J. and Hong , S. D. (19 90) Bi oc him Bi op h ys. Acta 1051, 115 51 ) Nis h iz u ka, Y. 0986) Sc ien ce 233, 305 52) Poovaia h , B. W. and Reddy, A. S. N. 09얽) Calci um Messeng e r Sy st e m in Plants , CRC Cri t. Rev. Plant Sci., 6, p 47 53) Schafe r , A., By gra ve, F., Matz e nauer, S. and Marme', D. 098. 5) FEES Lett. 187, 25 54) Ellio t, D. C. and Kokke, Y. S. 0987a) Bi oc hem Bi op h ys. Res. Com-mun 145, 1043 55) Ellio t , D. C. and Kokke, Y. S. (1987b) Ph ytoc hemi st r y 26, 2929 56) Schaller, G. E., Harmon, A. C. and Sussman, M. R. (1992) Bi o- chemi str y 31, 1721 57) I<.im , T. I., Cho, T. J. and Chae, Q. 0994) Mo!. Cells 4, 159 58) Colbran, R. ]., Schworer, C. M., Hashi mo to , Y., et al, 0989) Bi oc hem ]. 258, 313 59) Palmer, J. M., Short , T. W., Gallagh er, S. and Bri ggs , W. R. 0993) Plant Ph ys io l . 1 02, 1211 60) Fallon, K. M., Shacklock, P. S. and Trewavas, A. J. 0993) Plant Ph ysi o l. 101, 1039 61) Ranje v a, R. and Boudet, A. M. (1983) Annu Rev. Plant Ph ysi o l. 38, 73 62) Echeva rria, C., Vid a l, J., et al. (1988) Bi oc hem Bi op h ys. Res. Com-mun 155, 8.35 63) Datta , N., Chen, Y. -R. and Roux, S. J. 098. 5) The Plant Cell l, 1069 64) Li, H. and Roux, S. J. 0991) Plant Ph ysi o l. 96(sup pl.), 66 65) Ot to, V. and Schafe r , E. (1988) Plant Cell Ph ysi o l. 29, 1115 66) Park, M. H. and Chae, Q. (1989) Bi oc hem Bi op h ys. Res. Commu n.
162, 9 67) Haas, C. J., Scheuerlein , R. and Roux, S. J. (1991) ]. Plant Ph ysi o l. 68) Wong, Y. S., McM ich ael, R. W. and Lag arias , J. C. 0989) Plant Ph ysi o l. 91, 709 69) I
약어표 AC adeny la te cyc lase ACh acety lc holi ne Ala alan ine AR adrenergi c recep tor Asp aspa rtic acid ADP adenosim e diph osph ate 編 adenosim e monop h osph ate ATP adenosin e triph osph ate BAETA bis ( o-am ino p h enocy ) -eth a ne N, N, N' , N-te t r aa ceti c aci d BDNF brai n- dr ive d neurotr op hic fac to r cA 輝 cyc lic adenosin e monop h osph ate cDNA comp le menta ry DNA CDP cys ti dine diph osph ate CFTCR cys ti c fibr osis tran smembrane conducta nc e reg ulat o r CICR calciu m -in d uced calciu m release ; Ca2+ 에 의해 유도되는 Ca2+ 의 방출 CIF calciu m influx fac to r Cy s cys te i n e D aspa rtic aci d DAG diac yl gly c erol DGD dialkylgly c i n e decarbox yla se
dGMP gu anosin e 3, 5-cy cl ic monop ho s ph ate DLAR Drosoph il a leukocy te common anti ge n (LCA)-r e late d molecule DPTP Drosop h ila pro te in tyro sin e ph osph ata s e EGF epi de rmal gro w th fac to r EGFR epi de rmal gro w th fac to r recep tor EGTA eth yle ne gly c o l-bis ( /3 건 n li noe t hy l eth e r N, N, N', N'-t e t r aa ceti c Acid ER endop la snl ic reti cu lum FGF fibr oblast gro w th fac to r GABA r -am ino buty ric acid GAP GTPase-acti va ti ng pro te i n GDP gu anosin e diph ospb a te GMP gua nosin e 5' -monop h osph ate GEF gua n ine nucleoti de exchang e fac to r GNRP guanine nucleoti de releasin g pro te i n GTP gua nosin e triph osph ate GTPase gua nosin e triph osph a ta s e HPLC high perfor mance liquid chromato g ra ph y I(l)P ino sito l 1-monop h osph ate 1(1, 2, 4, 6)P4 ino sito l 1, 2, 4, 6-te t r a k isp h osph ate 1(1, 3)Pz ino sit ol 1, 3-bis p h o sph ate I(l, 3, 4, 5,)P4 ino sito l 1, 3, 4, 5,-te t r akisp h osph ate 1(1, 3, 4, 5, 6)Ps ino sito l 1, 3, 4, 5, 6-pe n ta kisp h osph ate 1(1, 3, 4, 6)P4 5-ki na se ino sito l 1, 3, 4, 6-te trakisp h osph ate 5-ki na se I(1, 4)P2 ino sit ol 1, 4,-bis p h osph ate 1(1, 4, 5, 6)P4 ino sito l 1, 4, 5, 6-te trakisp h osph ate I(1 ; 2 시클릭, 4, 5)P3 ino sito l( ! ; 2 cyc l ic 4, 5)tr iph osph ate 1(3, 4)P2 ino sit ol 3, 4-bis p h osph ate
1(3 , 4, 5)P:i ino sito l 3, 4, 5-t r iph osph ate 1(3 , 4, 5, 6)P4 ino sit ol 3, 4, 5, 6-te t r a k isp h osph ate I(4) P ino sit ol 4-monop h osph ate IGF- lR ins ulin - lik e gro w th fac to r -1 recep tor IP ino sit ol 1-monop h osph ate IP2 ino sit ol 1, 4-b is p h o sph ate IP3 ino sit ol 1, 4, 5,-tri ph osph ate lPJ 3- lu nase ino sit ol 1, 4, 5,-tri ph osph ate 3-ki na se IP4 ino sit ol 1, 3, 4, 5,- te t r akisp h osph ate lP5 ino sit ol pen ta kisp h o sph ate IP6 ino sit ol hexa kisp h osph ate IR ins u lin recept or IRR ins ul in- relate d recep tor Kd diss ocia t i on consta nt L leucin e Leu leucin e Ly s lys i n e M meth ion ine mAChR musca rinic acety lc holin e recep tor rnRNA messeng e r RNA MSD membrane spa nning doma in nAChR nico ti nic acety lc holin e recep tor NAD nico tin amide aden ine dinu cleoti de NBD nucleoti de bin d ing doma in NDF neu differ enti at i on factor NGF nerve gro w th factor NMR nuclear magn e ti c resonance NT-3 neurotr op hin- 3 NT-4 neurotr op hin- 4
NT-5 neurotr op h in- 5 P pro li ne PA pho sph a rtic aci d pA pico Amp ere PC pho sph ati dy lc holi ne PDE pho sph od ies te r ase PDGF pla te le t deri ve d grow th fac to r PE pho sph a ti dy le th a nolam ine PHA phy toh emagg lu ti nin PI pho sph a ti dy lino sito ! PI( 3) P pho sph a ti dy lino sito l 3-p h o sph a te PI( 3, 4)P2 pho sph a ti dy lino sito l -3, 4,-bis p h o sph a te PI( 3, 4)P2 pho sph a ti dy lino sito l 3, 4-bis p h o sph a te PI( 3, 4, 5)P3 pho sph a ti dy lino sito l 3, 4, 5-tri ph osph a te PH3, 5)P2 pho sph a ti dy lino sito l 3, 5-bis p h o sph a te PI (4) pho sph a ti dy lino sito l( 4) PI( 4) 5-ki na se pho sph a ti dy lino sito l( 4) 5-ki na se PI( 4) P pho sph a ti dy lino sito l 4-ph o sph a te PI( 4, 5)P2 pho sph atid y lino sito l 4, 5-bis p h o sph a te PH4, 5)P-5 pho sph a ti dy lino sito l 4, 5-bis p h o sph a te - 5 PI 3-ki na se pho sph a ti dy l ino sito l 3-ki na se PI 3_P pho sph a ti dy lino sito l 3-ph o sph a te PI-3-P 4-ki na se pho sph a ti dy l ino sito l 3-ph o sph a te 4-ki na se PI 4-kin a se pho sph a ti dy lino sito l 4-k i na se PI 4-P pho sph a ti dy lino sit ol 4-ph osph a te PI-4-P 5-ki na se pho sph a ti dy lino sit ol- 4 -P 5-ki na se PIP pho sph a ti dy lino sito l pho sph a te PIP2 pho sph a ti dy lino sito l 4, 5-bis p h o sph a te PKA pro te in kina se A
PKC pro te in kina se C PLA2 pho sph o lip as e A2 PLC pho sph o lip a se C PLCr pho sph o lip a se C r PLD ph osph o lip a se D pp 1 pro te in pho sph ata s e 1 PP 2A pro te in pho sph ata s e 2A PP 2B pro te in pho sph ata s e 2B PP 2C pro te in pho sph ata s e 2C PS pho sph a ti dy ls eri ne RTK recep tor tyro sin e kina se s senne SDS- P AGE sod ium dodecyl sulfa te- po ly a c ry la m ide gel electr op h oresis SH2 src homolog y reg ion 2 sos son of sevenless STP sig n al trans fe r particle STX sa xitox in TEA tetrae th y la mmon ium -K' channel blocker TLC thin laye r chromato g r a ph y TTX tet r od oto x i n Ty r tyros in e V va line Y tyros in e
용어해설 l - 포스포모노에 스터 라제 1-ph o sph omonoeste r ase 2-D SDS-PAGE 2-d i m ensio n al sodi um dodec y l sul fa t l' -1x i l y a c 1y - )amide gel electr o p h oresis 2 가형 diva lent fon n 3 차원적 구조 confo n nati on ; 3-di m ensio n al arrang em ent of at- oms in a stru c tu re 3 차원 적 인 구조 변화 confo n natio n al chang e 3- 포스포이 노시 티 드 3-ph osph oin o sit ide 4- 포스포모노에 스터 라재 4-p h osph omonoeste r ase 5' flanking 광 조절 부위 5'-fla nking ligh t- s ensiti ve element Abscis i c acid ( ABA) hormone pre sent in many pla nts wh ich pro mote s senescence, lea f fall , dormancy in buds, and anta go ni ze s the effe c t of the gro w th- pr o moti ng hormones ADP- 리보실레이션 ADP-ri bo syl a ti on Ae qu ori n a calciu m -bin ding pro te in tha t em its a flas h of ligh t when it bin d s Ca2' ATP- 의 존성 인산화 반응 ATP-depe n dent ph osph ory la ti on A 채 널 A channel A- 키나제 pro te in kina se A Ca2 + -결합 단백질 ca2'- bin d i ng pro te i n ; any pro te in tha t bin d s ca2' with a confo r ma- tion al chang e, wh ich eith e r acti va te s or ina cti va te s the pro te i n
Ca· 동원 Ca ' mobil iz a ti o n ; Ca2· p ool 로부터 의 Ca2· 방 출 Ca 2 ·- 민감성 형 광 지 시 약 ca2·- se nsit ive fluo resc enc e ind i ca to r (Qu in 2, Fura 2, Fluo 3) Ca2· 수송 로 Ca')·, channel ; ion channel in a bio lo g ica l mem-brane wh ich allows the pas sag e of calciu m ion s Ca?’ 유입 ci • inf l ux ; 세포 외부로부터의 C 誌 유입 CCaa22’‘ 유저 총장 소 Ccaa .,·.· esftof lru ex ; 세포 내부로부터 의 Ca2’ 유 출 Ca2’ 킬 래이터 Ca~., . c helato r 따유전자 chlorop h y ll alb-bin d ing pro te i n ge ne Calcim edi n Ca') ,• - b in d ing pro te i n in pla nt Calcis o me ci •- b in d ing pro te i n cAl\ 1I P - 의 존성 단백 질 키나제 pro te i n kina se A, A-ki na se cA l\1IP 펄스 cAMP pu lse cAMP 포스포디 에 스터라제 cAlvI P ph osph o dies te r ase inhibi t or I 억제재 I Cru\1I 키나제 Ca° /ca lmodulin - d epe n dent pro te i n kina se Coleop tile pro te c ti ve sheath sUITound ing the plu mule (ge rm ina ti ng shoot) of some monocoty le donous pla nts such as gra sses Cy s 단백질 분해 효소 Cy s pro te a se c - 말단 C-te r m ina l DHP deri va ti ve s 1, 4-di hyd rop )rridine 유도체들 Down reg u lati on reg ulat i on of a cell' s sensit ivity to a hormone by reducin g the number of sp ecific recep tor s on • the cell su rfac e Downstr ea m DNA seq u ences, contr ol sit es , etc . on the dist a l sid e of any give n point in relati on to the direc ti on of trans cri ption . Generally refe r s
to point s aft er the sta rtpoint of tran scri ption . Eff ec to r 분자 아데닐레이트 시클라제 adeny la te cyc l ase(AC) cGMP- 특이성 cGl \1P -spe cific pho sph o c lies te r ase 포스포디에스터라제 포스포리파제 A2 ph osph o lip a se A!. 포스포리파제 C pho sph o lip a se C 이 온 수송로 ion channel GABA( r -아미노부티르산) r-am ino buty ric acid , GABA ; an amino acid wh ich acts as an inh i bi t or y neurotr a nsm itter in the centr al nervous sys t e m GABA- 의존성 수송로 GABA-ga t e d channel Gli al cells any of the var iou s cells of the neurog lia the centr al nervous sys te m and sim ila r cells associa t e d with the periph eral nervous sys t e m , e.g. in gut Glyc o g en olys i s 글리코겐 분해 반응 Granulocyt e 과립 성 백 혈 구 GTPase 활성화 단백질 (GAP) GTPase acti va tin g pro te i n Ionomy ci n calciw n ion oph o re Ionoph ore small hyd r op ho bic molecules tha t diss olve m lipid bila y e r s and inc rease the perm eabili ty of the membrane to ion lP3 ino sito l- 1,4 ,5 -tr isp h o sph a te Jur ket Cell human tumo r T-lym p ho cyt e K 채널 K• channel KGF keratin o cyt e grow th fac to r LAR leukocyt e common anti ge n (LCA)-relate d mol-
ecule Ly s lys i n e Ly so PI 키나제 lys o pho sph a ti dy l ino sito l kina se MAP 키 나제 mitog e n - ac ti va te d pro te in kina se Mo nog e ni c contr o lled by a sin g l e gen e ; pro ducin g off sp r ing all of the same sex My ri st o y l a ti on the covalent add ition of my risti c acid to a pro te in , tho ug h t to be importan t in atta ch i ng some pro te ins to cell membranes No rt he r n Blott ing tech ni qu e in wh ich RNAs sepa r ate d by gel electr op h o resis are tran sfe r red to a sui tab le me dium for subseq u ent hyb r id iza ti on with radi o- acti ve pro bes for ide nti fica ti on and iso latio n of Rt'l'As of int e r est, named by analog y with the South e rn blott ing techniqu e. N - 말단 N-te rmina l Olig o de nd rocy te type of small neurog lial cell pre dom ina nt in wh ite matt er of the centr al nervous sys t e m, where the y form my el in sheath s around axons, collecti ve ly known as olig o dentr og l ia PCR poly m e rase cha in reacti on PEP pho sph o enolpy ruv ate phy 유전자 ph yt oc hrome gen e PPoI in키 t 나 돌제연 변이 Pphooinstp h ma utitd a ytiloinn o s;i to al mkiunta a steio n inv olvin g a cha nge at a sin gle base-pa ir in DNA . Polyg e ni c contr ol led by many differe nt gen e Positi ve coop erativity the bin ding of one substra te to one acti ve site on a pro te in raise s the affinity of the oth e r
act ive site ( s ) for sub st ra te Proto - o n cog e ne the n01mal cel lu lar ge ne from wluch an onc o- gen e has bee n der iv e d Quina te : NAD oxi do - ca2· - bi n d i ng pro te in in pla nt reducta s e Ras pro te i n pro te in encoded by the ras ge ne rbc S 유전자 ribu lose bis p h o sph a te carbox yl a se /o x y g e n a s e sm all subun it gen e RNA 중합 효소 RNA poly m erase R - 소단위체 reg u lato r y subun it S6 리보조멀 키나제 S6 ribo somal kina se sevenless R7 cel l is miss in g Sit e- c li rec te d 돌연변이 site - di rec te d muta ge nesis , a ge ne r a l ten n cov e r- ing var io u s tec hn iqu es by wh ich spe cific chang es can be int r od uced int o iso l ate d DNA in vit ro Sp licin g RNA spl icin g ; the pro cess by whic h int r a ns are removed from the prin1ary RNA tran scri pts of euka ryo tic gen es, in wh ich the int r an s are cut out at pre cis e ly defi ne d spl ice point s and the ends of the rema ining RNA rejo i n e d to fon n a conti nu ous rnRNA, rRNA or tRNA Sta u rospo r in e • pro te in kina se C inhibi to r Thaps i g a rgi n( Tg ) inhibit o r of Ca 양 -ATPase in ER Trans-acti ng element gen es or the ir pro te in pro ducts pro duced by one chromosome and coope ra ti ng with or actin g on gen es elsewhere T- 림프구 T-lym ph ocyt e(T cell) ; a type of small anti ge n-spe cific lym ph ocyt e orig ina ti ng in thym us(in
mammals) and pre sent in seconda ry lym p ho id tiss ue s (e.g. lym p h modes, spl e en) and blood, and wh ich is inv olved in cellular immu ne reacti on s and aiding the pro ducti on of anti bo d ies . Val valin e Wcslem blott ing tec hn iqu e used to tran sfe r the pa tt er n of pro te i n s sepa rate d by electr op h oresis to a medi um in wh ich the y can be furthe r analys e d X- ra y 결정학 X- ra y cry s ta ll og ra p h y ; tec hn iqu e for dete r- min ing the thr ee- di m ensio n al ato m ic str u ctu res of molecules tha t can be cry s ta llize d, from the diffra cti on pa tt er ns of X ray s pa ssed thr oug h the cry st a l. a - 헬릭스 a -he lix ; reg ular period ic seconda ry str uc tu re common in pro te i n s in wh ich the poly p eptide backbone is twist e d in a righ t- h anded spi ral to form a rigid rod-lik e str uc tu r e a- 헬릭스 머리핀 a -helic a l ha irpin f3 - 병풍구조 /3- sheet f3 - 아 들 레날린 수용체 /3 -adrenergi c recep tor 6 인자족 a fac to r s 간상체 rod cell 간세포 hepa to c y te 감각뉴런 sensory neuron 감압 sucti on 감지기 sensor 거 대 축색 돌기 gian t axon ; large nerve fibr es in annelid s . 겔 거르기 크로마토그래피 gel filtration chromato g r aph y 결손 돌연 변 이 deleti on muta tion ; muta t i on inv olvi ng loss of
part of a chromosome, or a base or base s in a DNA seq u ence. 결합 부위 bin d ing site 결합포켓 bin d i ng pock et 경쟁적 억제제 comp etitive inhibi t or 고정 단백질 anchor pro te i n 골격근 skeleta l muscle 골지체 gol gi body 과당 gal acto s e 과발현 overexpr e ss1on 과분극화 hyp erpola ri za ti on 과소발현 underexp re ssio n 관강 lumen 광수용체 pho to r ecept or 광형태형성 pho to m orp h og en esis ; any eff ec t on pla nt gro w th pro duced by ligh t 교감 신경 세포 sym p at h e ti c neuron ; part of the auto n om ic ner- vous sys t e m comp risin g nerve fibr es tha t leave the spi na l cord in the tho racic and lumbar reg ion s and supp ly vis c era and blood vessels by way of a chai n of sym pa th e ti c gan g lia runn ing on each sid e of the spi na l column wh ich commu nica te with the centr al nervous sys t e m via a branch to a correspo n di ng spi na l nerve. 교차 대화 cross-ta lk 교차 접합 alte rn ati ve spl icing 구멍 por e 구아닌 뉴클레오티드 guanine nucleoti de 구아닌 뉴클레오티드 gua ny l nucleoti de exchang e factor
교환 인자 구조 유전자 str uc tu r al ge ne ; a ge ne tha t codes for an en- zym e or oth e r pro te i n equired for a cell's str u ctu re or meta b oli sm , or for tRNA or rRNA . 굴중 성 gra vit rop i sm 근소포 체 (SE R) smooth endop la sm ic reti cu lum 굴루 코코르티코 이 드 glu cocort ico id ; any of the ste ro id hormones pro duced by adrenal cort ex and wh ich inf l ue nce carbohy dr ate meta b oli sm , as the form ati on of carbohy d rate from fat and pro te i n , and wh ich inc lude cort ico ste r one, cort iso ne etc ., but not aldoste ro ne, wh ich is a mine ralocort ico id . 글루 타민 glu ta rnine 글루 타민산 glu ta rnic acid 글루 타민 합성효소 glu ta rnine syn th a se 굴 리세 롤 키나제 gly c e rol kina se 글 리신 gly c ine 글 리옥 살 gly o x al 글 리옥실레이트 gly o x y la te 굴 리코겐 gly c o g en 글 리 코겐 합성 gly c o g e n syn the sis 글 리코실화 gly c o syl a ti on 기공 점액 airwa y mucosa 기저 전위 grou nd poten ti al 기질 substra te 억제제 anta go n ist ; a muscle workin g agains t the acti on of anoth e r ; any substa nc e tha t counte r acts the eff ec ts of a hormone, neurotr ans -m itter , drug, etc .
나선 helix 내피 세포 endoth e lia l cell 높은 삼투압 hyp erton ic 뉴로트로핀 neurotr op h in 뉴클레오티드 nucleoti de 뉴클레오티드 트리포스페이트 nucleoti de triph osph a te 능동 수송 acti ve tra nspo rt ; the movement of substa n ces across bio lo g ica l membranes int o cells or orga nelles oth e r tha n by pa ssiv e dif fus io n or pas siv e tran spo rt, oft en occuni ng ag a in s t concentr at i on gra di en ts . It inv olves ca rrier pro te i n s and req uires energy . 니코틴 아세틸콜린 nico ti nic acety lc holin e 니코틴 nico ti ne ; an alkaloid obta ine d from the tob acco pla nt, Ni co tz' an a tab acum, tox ic because of its blocki ng of the acti on of the neurotr an sm itter acety lc holi ne 니트레이트 리닥타제 nitrate reducta s e 니플람산 niflumic acid 다른 자리 입체성 단백질 alloste ric pro te i n 다른 자리 입체성 조절 alloste r i c regu lat i on ; refe r s to the abil ity of an inter acti on at one site of a pro te i n to influe nce the acti vity of anoth e r site 다면 발현 ple io t r op y , ple io t r op i sm ; muti ple eff ec ts of a sin gle gen e wh ich aff ec ts more tha n one ph enoty pic characte r 다면 발현 중계자 ple io t r op i c me diat o r 다유전자 multig e ne family 단량체 monomer ; molecule consis t i ng of a sin g le unit,
as e.g. a pro te in cons is ti n g of one poly p eptide chai n. 단백 장 단백 질 결합 부 위 pro te in - p r o te in bin d i ng site 단 백 질 접 합 pro te i n fold in g 단 백 질 키 나제 pro te in kina se ; any enzym e tha t pho sph o ry la te d spe cific amino acid resid u es in a pro te in , as pro te in - s e ri ne kina se, pro te in - t y ro sin e kina se 단백 질 키나제 C pro te i n kina se C 단백 질 키나제 억제재 pro te in kina se inhibi to r (PKI) 단백 질 탈 인산화 효소 pro te i n pho sph a ta s e(PP) 단백 질 티 로신 키 나재 PTK , pro te in tyros in e kina se 단백 질- 티 로 신 포스 파타제 pro te i n - ty ros in e pho sph a ta s e (PTPase) 단백 질 포스파 타제 pro te i n pho sph a ta s e 단 백 질- 히 스 티딘 키나제 pro te i n - h i sti d ine kina se 단식 세 포 sta rved cell 단일 항체 monoclonal anti bo dy ; anti bo dy pro duced by a sin g l e clone of B cells and thu s consis ti n g of a popu lati on of ide nti ca l anti bo dy molecules all spe cific for a sin gle anti ge ni c dete r m ina nt Produced from cultu red hyb ri do ma cell line s for research and commercia l pUIJ)Os es. Wi de ly used in research and me dica l diago ni st ic s as high ly spe cific rea ge nts in the assay and ide nti fica tio n of macromolecules, virus es, etc . or for accurate ly pinp o inting stru c tu ral fea tu res of cells •i n such tec hriiq u es as immu nofl uo rescence micr oscopy . 당 인산 전이효소계 PTS, ph osph o tr ans fe r ase sys t e m 당 전달계 glu cose trans po rt sys te m 대뇌 피질 cerebral cort ex
대사 과정 meta b oli sm 덤블 tumb le 도파민 dop amine 독소 tox i n 동질 효소 iso enzym e, iso z3rme ; any one of several differe nt form s in wh ich some enzy m es may be fou nd, each havi ng a sim ilar enzym e spe cif icit y but differi ng in pro p erties such as opt im wn pH or iso electr ic point . 디아실글리세롤 diac y lg ly c e rol 디히드로피리딘 dehy dr op yridine 땀샘 분비성 코일 sweat gla nd secreto r y coil 라이소 포스파티딕산 lys o -ph o sph ar tic acid 레티노이드 retin oi d 로돕신 rhoclop si n 류신 leuci ne 루프 loop 리간드 liga nd 리간드-의존성 수송로 liga nd- ga t e d channel 리 놀 렌산 (L in ole ni c acid ) 18 carbon fatty acid with 3 double bonds(bond pos iti on ; a -ty pe : 9, 12, 15 carbon , r -type : 6, 9, 12 carbon) 리놀레산 (L in ol ei c acid ) 18 carbon fatty aci d with 2 double bonds(bond pos iti on ; 9, 12 carbon) 리보오스 ribo se 리 불로오스 비 스포스페 이 트 ribu lose bis p h o sph a te carboxy la se/oxy ge nase 카르복실라제/옥시 게나제 리신 lys i n e 리아노딘 ryan o dine
리포 솜 lipo s ome 리폭시게나제 lipox y g e nase 막 membrane 막 관통 영역 membrane- sp a nning doma in 막 대 모 양의 영양 세 포 veg e ta t i ve rod- sh ape d cell 막 전 위 membrane poten ti al ; electr ica l poten ti al dif- fer ence pre sent across the pla sma membranes of all livi n g cells, so tha t the cy top la sm ic sid e of the membrane is neg a ti ve with respe ct to the exte r i or . It is ge nerate d by the movements of ion sOarge l y Na· and K ) in and out of the cell, and in most euka ryo ti c cells is ma int a ine d by the acti vity of membrane Na 令 -K ' ATPase 막 투 과성 신 호 전이 membrane-pe rm eable sig n al tran sducti on 만니 톨 ma nnitol 말 레이 트 malate 말토 오 스 malto s e 망막 세 포 reti na l cell 매 트릭스 matr ix 메 틸 수용 주화성 단백질 MCP, meth yl- a c cep ting chemo-ta xis pro te in 매 틸 에 스터 라제 meth y le ste r ase 메 틸 전 이 효소 meth ylt ra ns fe r ase 메 틸 화 meth yla ti on 멜리비오스 melib io s e 면역학적 전자현미경 immu noelectr on micr oscop y 목표 단백질 targe t pro te in 무스카린 musca rinic ; Acety lc holi ne (ACh) recep tor s blocked by muscru ine and sim ilar drugs (as opp os ed to the nico ti nic ACh recept or s)
무스카린 수용체 musca rinic recept or 무스카린 아세틸콜린 musca rinic acet rlc h olin e recept or 수용체 무스카린 콜리 너 직 수용체 musca rinic cholin e rgi c recep tor 미 립 체 ( 미 크로좀) micr osomes ; the smallest siz e pat i cl es spu n down from cell homog en ate s in the ultr ac entr i- fuge and inc lud ing broken parts of oth e r frac - tion s esp. endop la sm ic reti cu lum with ribo somes atta c hed ; fon nerly used by cyt olo g ist s for any small gran ules in the cyt op l a sm, now usually restr ict e d to pero x iso mes 미세 전극 micro electr od e 미세 피펫 micro p ipette 미셀 mice lle ; orderly arrang em ent of molecules as in cellulose micr ofi br i ls in pla nt cell walls, or pho sph o lip ids in aqu eous soluti on . 미엘린 my el in 미토게네시스 mitog e nesis 미토콘드리아 mitoch ond ria 바소프레신 vasopr e ssin ; peptide honnone pro duced by the neurohyp oph y si s ( th e pos te r i or lobe of the pitui固y) . It stim u late s smooth muscle blood vessels and rai se s blood pre ssure, and has an anti diur eti c eff ec t by causin g wate r resorp tion in kidn ey tubu les. 바소프레신 수용체 vasopr e ssin recept or 받게 accept or 발달주기 developm enta l cyc l e
발린 valin e 발전판 electr op l a x 발현 exp re ssio n 방사성 동위원소 표지 radi o- is o to p e labellin g 배우자 형성 ga meto g e nesis ; ga mete for mati on 백일해 독소 pertus sis tox i n 번역 tran slati on 보조인자(보조단백질) cofa c to r (cop ro te i n ) 보존된 서열 conserved seq u ence 복합체 comp le x 봄베신 bombesin 부신 피질 adrenal cort ex 분비 단백질 exopr o te i n 분화 differe nti at i on 비수용성 효소 particu late enz ym e 사량체 tet r am er 삭시 독소 STX, sax itox i n 삭제 deleti on 산성 아미노산 acid amino aci d 삼각구양추 구조 trigo nal-bip yramida l str uc tu re 삼량체 trime r 상동성 homolog y 서열 상동관계 S 띠 uence homolog y 서열특이적 S 힉 uence-s pecifi c 섬유아세포 fibr oblast ; a flat t en ed, irregular sha 函 connec- tive tiss ue cell, ubiq uitou s in fibr ous connecti ve tiss ue and wh ich secrete s comp on ents of the extrac ellular matr ix, incl ud ing type I collag e n and hy al uron ic aci d.
섬유아세포 성장인자 fibr oblast gro w th fac to r (FGF) ; pro te i n pro duced by many cells and wh ich among s t oth e r eff ec ts , stim u late s the divi s i o n of fibr oblasts . A sim ila r pro te i n in amp hibi a n egg s is tho ug h t to act as a morp h og en . 성게 난세포 Xenop u s oocy te 성상 세포 astr oc y te 성장 인자 g row 由 fac to r ; orga nic comp ou nds oth e r tha n tho se req uired as carbon and ene rgy sources wh ich are needed by many orga ni sm for pro pe r gro w th and develop m ent, a nd wh ich may inc lude vitamins amino acid s , purine s, pyrimidine s, etc . ; gen eral ter m for spe cific peptide s or pro te i n s req uired by particu lar cells for divi s i o n and /or differ enti at io n , e.g. nerve gro w th fac to r , epi de rmal gro w th fac to r . 성장 인자 수용체 gro w th fac to r recept or 세린 serin e 세린/트레오닌 키나제 serin e/threo n ine kina se 세린 단백질 분해효소 ser ine pro te in pro te as e 세제 dete rg e n t 세포 골격 cyt osk eleto n ; intern al pro te i n a ceous fram ework of a euk aryot i c cell. It is comp os ed of •a cti n micro fi lam ents , interm e diat e filam ents and micr o-tu b ules and give s shape to a cell, pro v ide s supp ort for cell exte n sio n s such as villi and axons of nerve cells, is inv olved in cell movement, in interac ti on s with the substr at u m on wh ich the cell is lyi ng , and in int r ac ellular
tran spo rt. The cyt o - s k eleto n is not usually a per manent stru c tu re but is conti nu ally bein g disa ssembled, reassembled and rearrang ed . 세 포 내부 전 위 int r ac ellular poten ti al 세 포 분 열 cell divi s i o n ; spl itting of a cell int o two com- ple te new cells : by bin m y fiss io n in bacte ria and oth e r pro - km yo te s , and by divi s io n of both nucleus and cy top la sm in eukm yo tic cells 세 포 외 부 영 역 cel l- su rfac e reg ion 세 포 주기 cel l cyc l e ; collecti ve ly the chang e s tha t tak e pla ce in a cell in the period betw e en its for - mati on as one of the pro ducts of cell divisio n and its own subseq u ent divisio n , and wh ich in all cells inc lude repl ica ti on of the DNA . In eukm yo ti c cells the cell cyc l e is divide d into ph ases term ed Gl, S, G2, and M. Gl is the period immediat e l y after mitos is and cell divi s io n when the newly form ed cell is in the diplo id sta te, S is the ph ase of DNA syn th e sis wh ich is foll owed by G2 when the cell is in a tetraplo id sta te, mitos is ( M) foll ows to resto r e the diplo id sta te, accomp anied by cell divisio n . 세포질 cyt oso l, cy top l a sm 소낭섬유증 CF, cys t ic fibr osi s 소단위체 subu nit 소마토스타틴 somato s ta tin ; 14- am ino aci d peptide hormone, pro duced by hypotha lamus, inhibit i ng the secre- tion of growth hormone, ins ul in and glu ca go n 소선 gla ndule
소중합 핵산 olig o nucleoti de 소포체 ER, endopl a sm ic reti cu lum 수동 수송 pas siv e tran spo rt 수동 확산 pas siv e diffus io n 수송로(채널) channel ; pore in bio lo g ica l membrane for med by some membrane pro te i n s whic h allows the sim ple diffusi o n of cert ain solute s across the membrane. 수용성 구멍 aqu e ous pore 수용성 효소 soluble enzym e 스트리키닌 stry ch n ine 시냅스 syn a ps e ; come int o conta c t with each oth e r app li ed to nerve end ing. 시냅스후부 pos ts y n a ps e ; cell or part of cell on the receiv i n g sid e of a syn a ps e in nervous sys t e m or at a neuromuscular jun cti on . 시냅토솜 syn a pt os ome ; membrane-bounded str u ctu r es, repr e sentin g pinc hi ng off nerve ter m ina ls and pos t syn a p tic membrane, form ed when brai n tiss ue is homog e ni zed . 시스테인 cys t e ine 시클로옥시게나제 cyc l oox yge nase 시클릭 1(1, 2)P2 cyc l ic ino sito l 1, 2~bis p h osph ate 시클릭 뉴클레오티드 cyc l ic nucleoti de 시 클릭 뉴클레오티드-특이성 cyc l ic nucleoti de -spe cific PDE 포스포디에스터라제 시클릭 포스페이트 cyc l ic pho sph ate 시클릭 이노시톨 포스페이트 cyc l ic ino sito l pho sph a te 시 프 염 기 Sch iff-b ase
신경 교세포 glial cell ; any of the va riou s cells of the neurog lia of the centr al nervous sys t e m and sim ilar cells associa t e d wi th the periph eral nervous sys t e m , e.g. in gu t 신경 말단 nerve end ing (ter m ina l) ; the ter m ina l portion of axon of a neurone, mo dified in va riou s way s. 신경 성장 인자 nerve gro w th factor (NGF) ; pro te i n homo dime r pro duced by some nerve cell targe t tiss ues, such as smooth muscle, wh ich is needed for ma int e - nance of some types of neurone, esp. sym p at h e tic and sensory neurones. It also stim u late s the outg row th of neu rites from develo-pi ng neurones of the se types. 신경 전달 물질 neurotr an sm itter ; chem ica l libe rate d by axon termina ls in respo n se to an electr ica l impu lse in tha t neurone and by wh ich neuronal sig n als are tran s-m itted across a syn aps e to anoth e r neurone or muscle fibr e, some common neurotr ans m itters bein g acety lc holin e, noradrena line (norepi -n eph rine ), dop amine, and 5-hyd r ox y-tryptamine (seroto n in) . 신호 영역 sig naling doma in 신호 전이 sig nal transd ucti on 아고니스트 ago n ist ; substa nc e respo n sib l e for trigge rin g a respo n se in a cell, such as a hormone, neurotr ansm itter etc . ; a prime mover or muscle direc tl y respo n s ibl e for a chan ge in pos it ion of a part. 아데노신 adenosin e
아데닐레이트 시클라제 adeny la te cyc l ase 아드레날린 수용체 adrenergi c recep tor ; any of several typ es of spe cific recept or for adrena- lin e and noradrena line , on the su rfac e of a vari et y of cells. /3 -ad renergi c recep tor s and a -adr energi c recept or s are the t\vo ma in clas ses and the y me diat e the ir eff ec ts tlrr oug h differ e nt int r ac ellular second me sseng e r pa th w ay s. 아라키 돈산 (arac hi do ni c 20 carbon fatty acid with 4 double bonds( bo nd acid ) pos iti on ; 5, 8, 11, 14 carbon) 아르기닌 argi nine 아미 노산 amino acid 아미 노산 서 열 amino acid seq u ence 아미 노산 잔기 amino acid resid u e 아민기 amine gro up 아세틸콜린 acet 1lc h olin e( ACh) ; a neurotr an s-m itter , acety l este r of choli ne , released at the t ern 加 als of nerve fibr es inn ervati ng skeleta l muscle, at syn aps e in auto n om ic gan g lia and by the pos tg a ng lion ic pa rasym -pa th e ti cs , nerve fibr es secretin g acety lc holi ne bein g known as cholin e rgi c. 아세틸 키나제 acety l kina se 아세틸포스페이트 acety l ph osph ate o} 과 subfa mily o} 스파라진 aspa r ag me o} 스파르트산 aspa rtic acid 아실기 acyl gro up 아종 subspe cies
안타고니 스트 anta go n ist ; a muscle worki ng aga ins t the acti on of anoth e r ; any substa n ce tha t counte r acts the eff ec ts of a hormone, neuro- tr an sm itter , drug , etc . 안 토 시아닌 anth o cy a ni n ; any of a gro up of important pla nt pigm ents fou nd in flow ers, fruits, leaves and ste m s, wh ich are sap -s oluble flav onoid gly c o sid e s givi n g scarlet, purple and blue colours, also fou nd in some ins ects , absorbed wit h pla nt foo d. 알라닌 alan ine 암 억제 유전자 tumo r sup pr essor gen es ; ge nes belie v ed to be inv olved in the develop m ent of ·som e familial cancers. Hete r ozy go te s inh eri ting a defe c t in one cop y of such a ge ne show a much grea te r pre -di s(X )si ti on to develop va riou s types of cancer. The develop m ent of the cancer seems to be due in many cases to subseq u ent loss or ina cti va -tio n of the go od cop y of the ge ne in cert ain somatic cells, from wh ich the cancer the n develop s. 액틴 actin 야생형 wild- ty pe ; the orga nism ca nying the normal (unalte red) form of a ge ne or ge nes. 억제 물질 repr e ssor ; in bacte r i a, a pro te in wh ich shuts down(repr e sses) trans cr iption of an ope ron by bin d ing to the ope rat o r reg ion on DNA and wh ich is produ ced by a regu lat o r y ge ne spe cific for the ope ron ; a pro te in wh ich inhibit s
tran slati on of mRNA by bin d i ng to mRNA 억제제 inhibi t or 에스트로겐 수용체 estr og e n recept or 에피네프린 epi ne ph rin( e) ; pre fe r red name for adrenalin e in Nort h Ameri ca 엔지오텐신 ang iot e n sin ; eithe r of the 2 short poly p eptide s ang iot e n sin I (ina cti ve ) or II(ac ti ve honnone) released in the blood by acti on of renin on ang io- te n sin o g en , ang iot e n sin II bein g fan ned from ang iot e n sin I and fou nd only in people with high blood pre ssure and acti ng on blood vessels, causin g constr ict i on and a rise in blood pre ssure. It also causes contr ac tio n of the ute r us and stim u late s aldoste r one secreti on from the adrenal cort ex . 엘리시토 elic it o r 역 유전자 방법 reverse gen eti cs 역평형 8- 구조 antip a rallel /3- stru c tu re 열 자극 단백질 heat shock pro te in 염기성 부위 basi c reg ion 엽록소 a/b-결합 단백질 chloroph y ll alb-bin d ing pro te i n 오페론 ope ron ; a type of gen eti c unit in bacte r i a, in wh ich several gen es cod ing for the enzym e s of a meta b oli c pat h w ay are cluste r ed and tran scri be d toge th e r into a poly c istr on i c mRNA The tran scri p-tion of each ope ro n is initiat e d at a pro mote r regi on and contr ol led by a neig h bow ing reg u lato ry pro te in(a repr e ssor or apo ind ucer) wh ich bin d s to an ope r ato r seq u ence
in the ope ro n to respe ctive ly pre vent or allow its tran scri ption . 오페 론설 ope ro n the ory 옥신 aux in 올 레 산 (ole i c acid ) 18 carbon fatty acid with 1 double bond(bond pos iti on ; 9 carbon) 용질 결합 부위 solute bin d i ng sit e 우리딜기 uridy l resid u e 운동 뉴런 moto r neuron ; nerve cell tha t ca rries impu lses away from the centr al nervous sys t e m (brai n and spi na l cord) to an eff ec to r muscle. 운송자 tran spo rter 원적색광 far -red ligh t 원조 ong m 원형질막 pla sma membrane 유도물질 ind ucer ; any comp ou nd wh ich spe cifica lly causes the syn the sis of an enz yme , cf repr e ssor ; in bacte r i a, any small molecule tha t spe cifica lly causes the exp re ssio n of ge nes spe cifying the enz yme s req uired to meta b oli ze it ; any chem ica l or ph y si c a l stim u lus tha t causes the expre ssio n of a spe cific gen e ; in embry ol og y, any substa nc e pro duced by cells wh ich influe nces nei gh bom ing cells or tiss ues. 유도물질-억제물질 복합체 ind ucer-repr e ssor comp le x 유사분열 mitos is ; the typica l pro cess of nuclear division in euka ryo ti c cells, in wh ich each member of a dup lica te d chromosome seg reg a te s into a daug h te r nuclei conta ining ide nti ca l sets of
chromosomes ide nti ca l to tha t of the par ent nucleus, and wh ich is foll owed by cell divi s io n . 유사 분열 촉진 인자 mitog e n ; any substa n ces tha t causes mitos is and(usually) cell divi s i o n 유전자 재배열 gen e rearrang em ent ; e.g. im muno- gl o bulin ( Ig ) gen es -They comp rise many sim ila r but not ide nti ca l gen e seg m ent for par t s of the lg molecule. DNA rearrang em ents dw ing lym p ho - cyt e develop m ent bri ng tog e th e r one of each type of gen e segm ent to fon n a comp le te heavy or ligh t cha in gen e. 유전자증폭 gen e amp lifica ti on ; the repe a te d dup lica tio n of a gen e to pro duce a number of ide nti ca l cop ies in the nucleus. 유전자 클로닝 gen e clon ing 음 변화 neg a tiv e chang e 음이온 교환 칼럼 anion exchang e colwnn 응집 aggreg a t io n 옹집성 유전자 agg reg a tiv e gen e 이량화 dime riz a tio n 이 미 다졸 링 irnida zole ring 이 성 질 화 반응 iso meriz a tio n 이 소류신 iso leucin e 이소시트레이트 탈수소 효소 IDH , iso cit rate dehy dr og en ase 이소프레닉화 iso pr e ny la ti on 이 온 강도 ion i c str en g th 이 온 선 택 필터 ion selecti ve filter 이온수송로 ion channel 이종삼량체 hete ro tr ime r
이 종 이량체 he te r od ime r 이화 효소 cata b olic enzy m e 인산 전이 효소 pho sph o tr an sfe r ase 인산화 자리 pho sp h o ry la ti on site 인슐린 ins ul in 인터페론 int e r f er on ; any one of a gro up of small pro te i n s pro duced by vert eb rate cells natu ral ly and in resp o n se to vira l muti plica ti on , and also havi ng eff ec ts on cell grow th and the immu ne sys t e m . 일차 구조 prim a ry str u ctu re 림프구 lym p h ocy te ; small mononuclear wh ite blood cell pre se n t in large numbers in lym ph oid tiss ues and cir cu lati ng in blood and lym ph . There are two ma in fun cti on al types , B lym ph ocy tes and T lym p h ocy tes , wh ich take part in anti ge n-spe cific immu ne reacti on s. Natu ral killer cells are a type of non-spe cific lym ph ocy te. 입체 장애 ste r eoh ind rance 입체 특 이성 ste r eospe cificit y 자동 인산화 auto p h osph o ry la ti on 자실체 fruiting body 작동 가설 worki ng hyp othe sis 작동 유전자 ope r ato r ge ne ; regi on of DNA fou nd in many bacte rial ope ron s to wh ich the repr e ssor or apo ind ucer bin d s, thu s pre venti ng or allow ing trans cri p-tion of the op eron . 작용 스펙트럼 acti on sp ectrum 잔기 resi du e 재분극화 repo la r ization
저장소 pool, sto r e 적색광 red-lig h t 적혈구 ery throc y te 전기 생리학 electr op h y s i o lo g y 전기 전도력 conducta nc e 전기 화학적 기울기 electr oc hem ica l gra di en t 전뇌 fore brain 전달자 tran sducer 전사 tran scrip tion 전사(조절) 인자(전사 요소) tran scri ption fac to r 전사 개 시 부위 tran scri ption initiat io n codon 전사 요소 tran scrip tion fac to r 전사율 tran scrip tion rati o 전사 활성화 인자 tran scrip tion acti va tin g fac to r 전압-의존성 채널 volta ge -ga te d channel 전압 클램프 volta ge clamp 전해질 electr oly t e 점균 포자 my xo spo re ; a spo re of a slim e mould ; a spo re sepa r ate d off by slim y disi n t e g r a ti on of the hyp h a. 정지 코돈 sto p codon ; ter m ina ti on codon 젖당(락토오스) lacto s e 젖당 분해 효소 f3 -ga lacto s id a se 제 2 전령 second messeng e r 조류 alga e 조절 영역 regu lat o r y dom ain 조절자 regu lato r 종양유전자 oncog en e ; a gen e can ied by a tumo ur virus or a cancer cell, wh ich is solely or partly respo n -
sib l e for tumo ri ge nesis . Many oncog e nes have been ide nti fied as alte r ed versio n s of normal cellular ge nes inv olved in the contr ol of cell divi s io n or differ en-tia t i on . The oncog en es in RNA tumo ur vir use s deri ve from cellular gen es wh ich have been pick ed up du ring virus inf e c ti on of a cell. The normal counte r p art to an oncog en e is sometim e s known as a pro to - oncog en e, but the term oncog en e is oft en used to denote any gen e, alte r ed or not, wh ich is a poten ti al oncog en e. Vir al oncog en es are sym boli ze d as v-onc, where one may be a wide rang e of gen es. The normal counte rpart is oft en sym boli ze d as c-onc. 종양 회사 인자 TNF, tumo r necrosis fac to r ; a lym ph ok ine pro -duced by acti va te d macrop ha g es . It also has direc t anti tumo ur acti vit y . 주게 donor 주화성 신호 chemota xis ; reacti on of moti le cells or micr o-orga nism s to che mica l stim uli by mov ing tow ards or away from source of che mica l. 중간자 me diat o r 중배엽 mesoderm ; the laye r of embry o ni c cells lyin g betw e en ecto d erm and endoderm in ga str ula, and from wh ich muscle, blood, connecti ve tissu es, vascular sys t e m and hear t, much of the kidn ey, and the de rmis of ski n develop in vert eb rate s . 중합 olig o me rizat i on 중합체 olig o mer
지각 신경 세포 sensory neuron ; nerve cell concerned wit h car- rying impu lses from a sense orga n or sensory recept or to the centr al nervous sys t e m . 지방산 fatty acid 지방 세포 adi pocyte ; an ani ma l cell spe cial iz e d for fat (lipid) sto r ag e, conta ining large glo bules of trigly c e ri de s in the cy top l a sm . 지수 분석 exp on enti al analys i s 지질 lipid 지체기 lag ph ase 척수 spi na l cord 청색광 수용체 blue ligh t recept or 촉매적 소단위체 cata lytic subu nit(C -subun it) 촉진(유전)자 P, pro moto r ; DNA regi on inv olved in and nee 一 essar y for initiat i on of tran scri ption , and ind uct - ing the RNA poly m erase bin d ing sit e, the sta rt- point of transc ri ption and va riou s oth e r site s at wh ich gen e reg ulat o r y pro te ins may bin d ; in carcin o g en esis , any age n t tha t haste n s the pro cess of carcin o ge n esis wh ile not bein g a carcin og e n on its own ; a pro tr ac to r muscle. 축색돌기 axon ; cyt op l a sm ic pro cess wh ich ca nies irn-pu lses away from the cell body of neurone, may be up to several mete rs lon g in the case of moto r neurones of large anima ls. 충돌-결합 메커니즘 colli sion -coup ling mecha nism 친수성 hy dr op hilic 친전자성 중간체 electr op hilic interm e diat e 친핵성 nucleop hilic
친 화성 크로 마 토그 래피 aff inity chromato g ra ph y 카 르 보 닐 기 carbony l gro up 카르 복 실가 carboxy l gro up 카바모일 포 스 페이트 carbamoy l pho sph ate 카바 콜 carbachol ; 2-hy d rox yph enol 카세인 casein ; mixt u re of milk pro te i n s pre cip itated by the acti on of renn in. 카테 콜 아민 cate c holam ine ; a gro up of chem ica ls actin g as neurotr a nsm itter s or hormones, wh ich are amine deri va t i ve s of cate ch ol( 2- h y d roxy -ph enoD and inc lude adrena line , noradrena line and dop amine . 칼모 듈 린 calmodu lin ; ubiq uitou s calciu m -bin d ing pro te in abundant in euka ryo ti c cells, forming the regu lato ry subun it of gly c o g en pho p ho ry la se. Undergo es a confo r mati on al chang e on bin d ing ca2· and associa t e s with many oth e r pro te in s, me diat i ng reg u lati on of the ir acti vi t y by ca2·. 칼슘 진동 calciu m oscill at i on 사인파 진동 sin u soid a l oscill at i on 일시적 진동 tran sie n t oscill at io n 콜 래라 독소 cholera tox i n 콜레시스토키닌 cholecys t o k i nin( CCK) ; a peptide hormone pro duced by duodenal cells and actin g on pa ncreati c acin a r cells to ind uce secreti on of dige stiv e enz yme s, also ind uces concentr ation of gal l bladder and relaxati on of sph inc te r around the duodenal end of the common bil e duct. also pre sent in the centr al nervous sys t e m where its role is not yet lmown.
클로닝 clon ing 클론 clone 티로이드 호르몬 thyro id hormone ; the hormones secrete d by the thyroid gla nd- ch i ef ly thy r o x ine and tri-i o d oth y - ron ine . 탄수화물 carbohyd r ate 탈갑현상 desensiti za ti on 탈메틸화 demeth yla ti on 탈분극화 depo la ri za tio n 탈인산화 deph o sph o ry la ti on 테트로도 독소 TIX, tet r od oto x i n 투과 효소 perm ease ; gen eral term for any pro te i n tha t spe cifica lly tran spo rts a solute across the pla sma mem-brane ; any of var iou s •p ro te i n s in bacte r ia respo n sib le for car rying solute s int o the cell. 트레오닌 threo n ine 트로포닌 C trop o nin C, intr a c ellular Ca2G*· recept or 트롬빈 throm bin ; a pro te ina se pro duced from pro - throm bin at a wound, wh ich convert s the soluble pro te in fibr in o -ge n to ins oluble fibr i n in blood clot form atio n . 트리메틸 리신 trime th yl lys i n e 트립신 trypsi n ; pro te oly ti c diges tiv e enz yme fou nd in pan creatic juice of mamrnals(and sin illar enz yme s fou nd in oth e r anima ls and in pla nts ) , form ed from an ina cti ve pre cursor, trypsi n o g en , by enzym ati c cleavage in small intes tin e by ente rop e ptida se. 트립토판 tryptoph an
트립토판 합성 효소 Trp syn th e ta s e 티로신 tyro sin e 티로신 키나제 tyro sin e kina se 티로신 포스파타제 tyro sin e pho sph ata s e 패치 클램 프 기술 pa tc h clamp techniqu e ; tec hn iqu e in neurop h y si - olog y wh ich iso late s a tiny portion of nerve cell membrane allow ing recordi ng from sin g l e ion channels. 팽압 turgo r 페닐 글 리옥살 ph eny lg l y o x al 펩티드 peptide 평형 전위 equilibr i um poten ti al 평활 근 smooth muscle 평활근 세포 smooth muscle cell 포도당 glu cose 포볼에스터(p horbol este r ) este r of pho rbol, ~야, some are tumo r p romo 血~ comp ou nds 포스비틴 ph osvi tin 포스파디드 산 pho sph a tid ic acid 포스파티딜이노시톨 ph osph atid y lino sito l 3-ki na se 3- 키나제 포스파티딜 이노시톨 ph osph ati dy lino sito l ph osph ate 포스페이트 포스파티 딜 이 노시 톨 4- ph osph atid y lino sito l 4-mono-ph osph ate 모노포스페이트 포스파티딜이노시톨 4, 5-p h osph ati dy lino sito l 4,5-bis - ph osph ate 비스포스페이트 포스페 이트 -5- 포스타제 ph osph ate - 5-ph osph ata s e 포스포글리세라이드 ph osph og ly c e r ide
포스포디에스터 pho sph o d ies te r 포스포디에스터라제 pho sph o d ies te r ase 포스포리파제 Cr pho sph o lip a se C r 포스포리파제 pho sph o lip a se 포스포리파제 C pho sph o lip a se C 포스포릴-주화성-단백질 PCP, pho sph o ry l- chemota x i s pro te i n 포스포모노에스터라제 pho sph o monoeste r ase 포스포아미데이트 pho sph o a mida te 포스포이노시톨 -4- 키나제 pho sph o in o sit ol -4-ki na se 포스포이노시톨 키나제 pho sph o in o sito l kina se 포스포이노시티드 pho sph o in o siti de 포스포이노시티드 대사 PI turno ver 포스포이노시티드 키나제 ph osph o in o sit ide kina se 포스파타제 •p h osph ata s e 포스포티로신 포스파타제 pho sph o ty ros in e pho sph a ta s e 포스포히스티딘 pho sph o-hi sti d ine 포아 spo re ; a small, usually uni ce llular, repr o ducti ve body from wh ich a new orga nism arise s, pro - duced by some pla nts ( fe r ns and mosses), fungi, bacte ria and pro to z oa. 포자형성 spo ru latio n ; the pro cess of spo r e form ati on ; libr atio n of spo re s ; in bact er i a, the seg reg a t io n of the DNA to one part of the cell where it is sUITounded by a spo re coat, forming an endo- spo re ; brood form ati on by multip le cell fiss io n (in some pro to - zoans). 폴리클로널 항체 poly c l onal anti bo dy ; deri ve d from several cell clones 폴리펩티드 poly p eptide
표적 세포 tar ge t cell 표지 pro be 표피 성장 인자 epi de rmal gro w th fac to r (EG F) ; a poly p eptide tha t sti m ulate s the divi s io n of cells of ecto d ermal and mesodermal ori gin, and pro mote s pre cocio u s eye l id ope ning in mice . 표현형 ph enoty pe ; the vis ib le or oth e rw ise measurable ph y si c a l and bio c hem ica l characte r i st i cs of an orga n ism , a result of the int e ra cti on of gen oty pe and envir o nment ; a gro up of ind ivi-d uals exh ibit ing the same phe noty pic characte r s. 푸르키네 세포 pu rki nj e cell ; type of neurone fou nd in cere-bellwn, whose cell bo dies constit ute a disti nc t lay er in cerebellar cort ex betw e en the molecular and gra nular(nulear) lay er s, and whose axons ca rry the outp u t from cerebellwn. 프로스타글란딘 pro sta gla nd in ; any of a gro up of comp ou nds form ed from C2 0 fatty aci ds and conta ining a 5-carbon ring. There are fou r ma in classes, PGA, PGB, PGE and PGF. They are pre sent in many mamma lian tiss ues. They mo dify the eff ec ts of oth e r hormones, stim u late contr ac ti on of smooth muscle of ute r us, ind uci ng labour or abort ion , and are also inv olved in infl amr 떠t o ry reacti on s. 프로카인 pro ca ine 프로타민 prot a mine ; any of a grou p of small high ly basic argi nine -ric h pro te i n s associa t e d with DNA in fish spe nn in a similar manner to hist o n es in
oth e r euka ryo tic DNAs. 프로테오글리칸 pro te o g ly c a n ; any of a class of comp o unds consis t i ng of poly s a ccha-ri de (95 %) and pro te i n (5 %) units, forming the gro und substa n ce of connecti ve tiss ue, im p ortan t in dete r -m ini n g the visc oelastic pro p erties of join t s etc . 프롤린 pro li ne 풀라보 단백질 flav opr o te i n 플루페남산 fluf e n a mic acid 피자 식물 an gios pe rm s 피토크롬 phy toc hrome ; red ligh t recep tor in pla nt Pr for m ; ina cti ve form of phy toc hrome Pfr form : acti ve form of ph1 rt oc hrome 항상성 homeosta s is 항원 antig e n 항-유전자 anti -ge ne 항체 anti lxx ly 핵 게놈 nuclear ge nome 헤파린 hepa rin ; a poly s a ccha ride (a gly c o s-am ino g ly c a n) fou nd in mast cells and wh ich has anti co ag u lant activ ity, inhibi t ing blood clott ing by inc reasin g the rate of ina cti va ti on of throm bin by anti throm bin ill. 현탁액 suspe n sio n 혈관 형성 angiog e n esis ; the form ati on of new cap illaries by spr o utin g from pre -ex ist i ng small blood vessels.
혈소 판 - 유 도 성 장 인자 pla te l et - d eri ve d gro w th fac to r (PDGF) ; a gly c o p ro te i n pro duced by pla te le ts and oth e r cells, and wh ich stim ulate s the pro life r ati on of cells of mesenchy m al orig in and wh ich has been implica te d in repa ir of the vascular sys t e m in viv o . 협동적 포획 coope r ati ve trap p ing 형질 전환 tran sfo rm ati on ; the gen eti c mo difica -tio n of a bacte r i um by DNA added to the cultu r e and wh ich ente r s the bacte r ia l cell. It can occur natu rall y, dur ing mixed inf e c ti on s, and is used in exp erime nta l bacte r i al gen eti cs and to pro duce bacte r i a conta ining artifi-ciall y pro duced recombin a nt DNA ; the chang e s tha t occur in cultu red cells after infec ti on with tumo ur vir use s, trea tm e nt with carcin o g en s etc ., in particu lar the abil ity to divi d e ind efe n itely , and wh ich sometim e s result in a cell tha t can form a ma lign ant tumo ur is trans pl a nte d int o an animal. 형질 전환 성장 인자 TGF- S , trans fo rming gro w th fa c t or 내 ; a poly - peptide pro duced by cancerous and embry on i c cells, wh ich inhibi t s the grow th of some cells and stim u late s divisi o n in oth e rs, depe n d ing on what oth e r grow th fac to r s are pre sent. 호모 이량체 homo dime r 혼성 분자 chi me ri c molecule 확인자 marker 활동 전위 acti on poten ti al a poten ti al differ ence pro duced acrss the pla sma membrane of nerve or muscle
cells when the y are stim u late d , reversin g the restin g poten ti al from about -70 mV to about+ 30 mV, and bein g an easily measured manif est a t io n of a nerve im p u lse. 활성 단백질 acti va ti ng pro te in 활성도 acti vity 활성제 acti va to r , ago ni st 활성형 억제 물질 acti va te d repr e ssor 활성화 자리 acti ve site ; reg ion of an enzy m e molecule at whlch substra tes are bound and acti va ti on and chem ica l reacti on of substr at e take s pla ce ; on an anti bo dy molecule, the anti ge n-bin d i ng site . 효소유도 enzy me ind ucti on 휴지 전위 또는 휴지 막전위 restin g poten ti al or restin g membrane poten ti al ; the poten tia l differ ence across a nerve or muscle cell membrane when it is not bein g stim u late d , and wh ich is usually about -70 mV in a nerve cell. 홉수 스펙트럼 absorp tion spe cb um 히드록실기 hyd o x yl gro up 히스톤 histo n e 히스티딘 histi d ine 집고문인 Henderson's diction a ry of bio lo g ica l tenns eel, Eleanor Lawrence, Longm an Sin ga po re Publis h ers Pte Ltd ., Eng la nd(1989)
찾아보기
기 GABA 28 GABA 의 존성 수송로 227 간세포 98 감각 뉴런 219 감지기 211, 300 겔 거르기 크로마토그래피 131 결손 돌연변이 4 과분극화 210 과소발현 업 4 광수용체 完 3 광형태형성 25.3 구아닌 뉴클레오티드 52 구조 유전자 245 굴중성 321 근소포체 120 글루타민 합성 효소 303 글리신 30 글리옥살 237 글리옥시레이트 294 기저전위 210 L 내피세포 43 nort he rn blott ing 331 뉴로트로핀 44 니코틴 아세틸콜린 18
니트레이트 리닥타제 322 nitro regu lat io n 302 E: 다른자리 입체성 단백질 149 다른자리 입체성조절 149 다 유전자 253 단백질 인산화 149, 288, 344 단백질 접힘 4 단백질 키나제 149, 269, 344 단백 질 키 나제 A(cA fvIP 의 존성 단백 질 키나제) 150, 291 단백질 키나제 C 172 단백질 키나제 G(cGMP 의존성 단백 질 키나제) 업 1 단백 질 탈인산화 효소 149 단백질 티로신 키나제 182 단백질 티 로신 포스파타제 201 단백질 포스파타제(단백질 탈인산화 효소) 149, 194 단백질 히스티딘 키나제 291 단식세포 251 단일항체 31 동질효소 82 디아실글리세롤 81, 173 디히드로피리딘 58, 125
근 Ras 단백 질 38, 62, 268 로돕신 9, 326 leucin e zip per 283 루프 6 리간드 의존성 수송로 210 리뷰로오스 비스포스페이트 카보실라 제/옥시게나제 350 리아노딘 120 리포좀 23 리폭시게나제 236 □ 막대모양의 영양세포 298 막 전위 210 메틸 수용 주화성 단백질 313 메틸에스터라제 305 메틸전이효소 305 메틸화 305 멜리비오스 312 면역학적 전자현미경 31 무스카린 수용체 13 무스카린 아세틸콜린 수용체 13 미세전극 210 미세 피펫 26 미셀 336 미엘린 105
my rist o y la ti on 55, 158 미토콘 드 리아 105 닌 바소프레신 138 박테리아 287 발전판 19 발현 245 배우자 형성 85 백일해 독소 52 분비단백질 292 비수용성 효소 337 人 site - di rec te d 돌연변이 154 삭시독소 218 삼각양추구조 226 삼투조절 3(17 상동성 4, 70, 151 섬유아세포 43, 129 섬유아세포 성장인자 43, 46, 192 성상세포 129 성장인자 262 세린/트레오닌 키나제 150, 269, 298 세린 단백질 분해효소 156 sevenless 184 세포주기 299
세포질 13.5 소낭 섬유증 227 소단위 체 52, 56, 74, 156 소선 13 소포체 118 수동확산 '307 수송로 (채 널) 205 수용성효소 337 수용체 1, 265, 322 sta u rospo rine 177 sp licin g 56 시냅토좀 105 시크로옥시 게나제 236 신경교세포 43 신경성장인자 232 신경전달물질 213 신호전이 3, 245, '2K1 스테로이드 수용체 'l79 。 아고니스트 4 아데닐레이트 시크라제 2 아드레날린 수용체 2 아라키도닉산 235 아메바 2A9 absci sic aci d 261 아세틸콜린 211 아세틸포스페 이트 291
ion omy ci n 133 ion oph o re 118 IP3 81 아종 32, 179 암 억제 유전자 262 야생형 7 억제물질 245 에피네프린 2, 326 ADP - 리보실레이션 52, 3'l7 effe c to r 분자 2, 2fi6, 344 엔지오덴신 138 엘리시토 321 엽록소 alb- 결합 단백질 256, 350 오페론설 245 옥신 321 olig o dendrocyt e 43 우리딜기 303 운송자 2OO 원적색광 254 원형질막 259 유도물질 %5 유도물질_억제물질 복합체 245 유사분열 231 유사분열 촉진인자 173 유전자 발현 245 응집성 유전자 251 이노시톨 시클릭 포스페이트 101 이노시톨 포스페이트 대사 96 이량화 沈 3
이미다졸 링 311 이성질화 반응 10 이소시트레이트 탈수소 효소 294 이소프레닐화 46 이온 채널 205, 218 인산 전이 효소 289, 309 인슈린 42, 190 인터페론 247 大 자동인산화 170, 292 자실체 298 작동 유전자 245 작용 스펙트럼 259 재분극화 222 저장소 104, 119 적색광 253 전기 생리학 24, 208 전기전도력 219 전뇌 166 전사 250 전사인자 248, 'Z14 전압 의존성 채널 210 점균 포자 298 젖당 247 젖당 분해 효소 247 제 2 전령 2, 196, 322 조류 幻 5
종양 유전자 248 종양회사인자 247, 26-5 jur kat 세포 131 주화성 신호 252, 303 중합 168 G - 단백질 51, 266, 323 GTPase 활성화 단백질 67 zin c fing e r 初 9 犬 채널 16 청색광 수용체 259 촉진유전자 156 축색돌기 118 충돌一결합 메카니즘 29 친화성 크로마토그라피 29 =, 카바콜 l 업 카세인 294 카테콜아민 2 칼모듀린 163 calci so me 118 칼슘 결합 단백질 칼슘 동원 82, 118 칼슘 민감성 형광 지시약 136 칼슘 유입 114
칼슘 유 출 114 칼슘 이 온 113, 340 칼슘 저 장소 118, 130 칼슘 진동 135 칼슘 채 널 119, 126, 219 칼슘/칼모듀린 의존성 단백질 키나제 163 칼슘 킬레이터 230 cab 유전자 350 콜 레라 독소 52, 332 콜레시스토키닌 137 er 채널 226 E 탈분극화 120, 210 탈 인산화 195 tha ps ig a rgi n 133 테트로도 독소 118 두과효소 307 트레포닌 C 343 tra ns-actin g element 260 트립토판 합성효소 247 티 로신 키 나제 40, 182, '2:12 티 로신 포스파타제 201 패치 클램프 24 페닐글리옥살 237 평활근 43 포볼에스터 얽
포스비틴 294 포스파타제 194 포스파티딜 이노시톨 포스페이트 84 포스파티 딜 이 노시톨 4- 모노포스페이 트 84 포스파티딜 이노시톨 4,5- 비스포스페 이트 84 포스포디에스터라제 2 포스포리파제 A2 2, 177 포스포리파제 C 90 포스포리파제 Cr 92 포스포라파제 D 175 포스포릴-주화성-단백질 315 l- 포스포모노에스터라제 96 4- 포스포모노에스터라제 96 포스포아미 데이 트 311 포스포이노시톨 -4- 키나제 86 포스포이노시톨 키나제 85 포스포이노시티드 81 포스포이 노시 티 드 대사 84, 269, 333 포스포이노시티드 키나제 85 포스포 티 로신 포스파타제 202 포스포히스티딘 292 포자형성 292 표피 성 장인자 40, 93, 188 프로스타그란딘 236 프로카인 218 프로타민 294 프로테오글리칸 47
PCR 298 피자식물 337 피 토크롬 25.3, 322 ,10 항체 332 helix -tum- helix m 혈소판-유도 성 장 인자 43, 92, 191 형질 전환 성장 인자 247
homeodoma in 獨 혼성 분자 33 확인자 222 활동전위 208 활성제 99 효소 유도 247 후라보 단백질 332 5'fla n k ing 광 조절 부위 254 후루해나믹산 230 히스톤 294
지은이 약력 채쾌는 서울대학교 화학교육과 (B .S) 와 서강대학교 화학과 (M. S.) 를 졸업하고 미국 텍사스 주립대학 화학과에서 박사학위를 취득하였으며 연세대학교 조교수 , 충북대학교 생화학과 교수를 역임하였댜 김학용은 충북대학교 농화학과 화학과 (M.S. )를 졸업하고 미국 코네티컷 주립대학교에서 박사학위를 취득한 후 현재 캘리포니 아 대학에서 연구원으로 있다. 박문환은 충북대학교 과학교육과와 한양대학교 화학과 (M. S. ) 를 졸업하고 충북대학교 화학과에서 박사학위를 취득하였으며, 미국 네브라스카 주립대학에서 연구원을 역임한 후, 현재 태산정 밀 부속 생명공학연구소에 재직중이다 .
생명체의 신호전이 대우학술총서 자연과학 118 1 판 1 쇄 펴냄 ―一 - 1998 년 4 월 30 일 지은이 -―― 채쾌 김학용 박문환 펴낸 이 -朴孟浩 펴 낸 곳―-―(주) 민음사 출판등록 1966. 5. 19. 제 16-490 호 서울 특 별시 강남구 신사동 506 대표전화 515-2000, 팩시밀 리 515- 2 007 값 24,500 원 ® 체쾌 김학용 박문환, 1998 생화학 KDC/472.1 9 3 Printed in Seoul, Korea ISBN 89-374-3618-3 94430 89-374- 3 000-2 ( 세 트)
| 대우학술총서(자연과학) |
1 소립자와 게이지 상호작용 김진의 2 동력학특론 이병호 3 질소고정 송승달 4 상전이와 임계현상 김두철 5 촉매작용 진종식 6 외스바우어 분광학 옥항남 7 극미량원소의 영양 승정자 8 수소화봉소와 유기봉소 화합물 윤능민 9 항생물질의 전합성 강석구 10 국소적 형태의 Ati ya h- si n ge r 지표이론 지동표 11 Mucop ol y sacchar i des 의 생화학 및 생물리학 박준우 12 천체물리학 홍승수 13 프로스타글라딘 합성 김성각 14 천연물화학연구법 우원식 15 지방영양 김숙희 16 결정화유리 김병호 17 고분자에 의한 화학반응 조의환 18 과학혁명 김영식 19 한국지질론 장가홍 20 정보이론 한영열 21 원자핵반응론 정운학 22 파괴역학 김상철 23 분자궤도 이론 이익춘 24 반응속도론 정경훈 25 미분위상수학 이현구 26 자기공명방법 조성호 27 플라스마 물리학과 핵융합 최덕인 28 천문관측과 분석 이시우 29 석탄에너지변환기술 김상돈 30 해양미고생물학 백광호 31 편미분방정식론 김종식 32 대통일 이론 소광섭 33 금속전자계의 다체이론 김덕주 34 액정중합체 진정일 35 복합재료 권숙인 36 단백질 생합성 박인원 37 한국의 광물종 김 수진 38 일반상대론 이철훈 39 레이저 광산란 분광학 김종진 40 복소다양체론 김 상문 41 역학적 연구방법 김일순 42 핵구조물리학 민동필
43 후리에 해석과 의미분 작용소 김도한 44 한국의 고생물 이하영 45 질량분석학 김명수 46 급변론 박대현 47 생체에너지 주충노 48 리이만 기하학 박을룡 49 군표현론 박승안 50 비선형 편미분 방정식론 하기식 51 생체막 김형만 52 수리분류학 고철환 53 찰스 다윈 정용재 54 금속부식 박용수 55 양자광학 이상수 56 효소반응 속도론 서정현 57 화성암 성인론 이민성 58 확률론 구자홍 59 분자 분광학 소현수 60 벡터속 이론 양재현 61 곤충신경 생리학 부경생 62 에너지띠 이론 모혜정 63 수학 기초론 김상문 64 신 경 과학尸 김 흥 업 박찬웅 65 BCH 부호와 Reed- Solomon 부호 이 만영 66 양자 전기역학 김영덕 67 군환론 박재걸 68 대수기하학 조영현 69 양자장이론 이재형 70 해앙오염과 생태계 십재형 71 비기체 연소합성 ( SHS ) 여철현 72 크로마토그래피 이대운 73 곤충의 사회행동 추종길 74 동위원소 지질학 김규한 75 X - 선 결정학 김양 77 통계역학 조순탁 78 고분자의 구조와 형태학 이석현 79 LC 에 의한 광학 이성질체의 분리 현명호 80 신경전달물질 서유헌 81 발생과 유전자 발현 이양림 82 스테로이드 화학 감완주 김득준 83 다체계론 엄정인 84 중핵반응론 김병택 85 비가역 열역학 이철수
86 등각장론 임채호 87 방사선생물학 남상열 88 석유지질학 이용일 89 베르누이 시행의 통계적 분석 배도선 김성인 90 신경세포생리학 강만식 91 생리활성을 가진 C ― P 화합물의 화학 김용준·강익중 92 생물유기화학 서정헌 93 조직배양 김승업 94 유기전이금속화합물 조남숙 외 95 실내환경 과학 김윤신 96 유한요소법 정상권 97 대수적 위상수학 우무하 • 김재룡 98 파인만 적분론 장건수 99 응용 미생물학 박무영 100 리보플라빈 이 상선 101 노화 김숙희 • 김화영 102 매트릭스 격리분광학 정기호 103 신경계 조직배양 김승업 104 지구화학 김규한 105 은하계의 형성과 화학적 진화 이시우 현정준 · 윤홍식 · 홍승수 107 액체의 미립화 이상용 108 점토광물학 문희수 109 중국수학사 김용운 • 김용국 110 퇴적암석학 유강만 • 우경식 111 로렌츠 기하학 김종철 112 몬테카를로 방법의 물리학적 응용 김재삼 113 천체역학 최규홍 114 확률마분방정식 김재희 115 전자현미경의 원리와 응용 이정용 116 미세구조유체 흐름의 원리 양승만 · 박오옥 117 고분해능 분자분광학 아상국