
김규한 연세대학교 지질학과 및 동 대학원 졸 업 일본 나고야대학 지구과학과 ( 이학박사 ) 미국 캘 리포니아 공과대학 ( CALTEC H ) 방문 연구교수 현재 이화여자대학교 과학교육과 교수 『 동위원소지질학 』 『 한국의 지질과 광물자원 』 등의 저서와 『 현대 광상학의 기초 』 『 점토광물학 』 등의 역서 그리고 Oxy ge n Isot o p i c C omp osition s of M esowic G ranit ic R oc ks in S outh Korea 외 다수의 논문
지구화학 
 지구화학
지구화학
책 머리에 지구는 크게 암석권, 수권, 생물권 및 대기권으로 구분된다. 여기에다 정신권을 포함시키는 학자도 있다. 지구화학은 지구의 각 물 질권에서 일어나는 물질의 생성, 이동, 소멸 등의 지구화학적 현상뿐만 아니라 지구 물질권과 정신권 간에 일어나는 사회 지구화학적 문제까지 다루고 있다. 지구 물질의 지구화학적 과정의 이해를 위해서는 우주 태 양계 물질의 지구화학을 동시에 이해해야 한다. 지구화학적 과정은 각 물질권 간에 물질평형과 화학평형이 진행되는 쪽으로 일어나고 있다. 지 구와 우주 물질계에서 일어나는 지구화학적 현상은 시공간의 변화에 따 라 일어나는 과정이므로 시공간적인 물질 시스템의 도입이 필요하다.,. 최근 지구 물질의 기원, 생성 환경, 물질의 분배 및 물질의 거동을 정 량적으로 해석할 수 있는 연구 방법의 개발로 지질시대에 일어난 지질학 적 및 지구화학적 과정이 정량적으로 해석되고 있다• 따라서 이 책에서는 일반화학과 지질학의 기초를 가진 독자는 누구나 지구 물질의 화학적 시스템을 이해하기 쉽게 지구의 탄생과 지구 물질의 진화, 광물 열역학, 상률과 상률도, 동위원소 지구화학, 지구 물질의 원 소 분배, 물의 화학, 광물의 결정화학, 지각과 맨틀의 화학 성분, 해양 화학, 생물 지구화학, 환경 지구화학 등의 문제를 기본적으로 다루었다. 지질학적 과정과 지구화학적 과정에서 물과 미생물의 역할이 점점 중 요해지고 있다. 또한 과학 문명의 발달과 함께 환경 지구화학의 문제가 복잡하게 대두되고 있다. 따라서 미래 지구화학의 주요 대상인 물과 미
생물 지구화학을 소개하고 지구화학과 우리 생활 환경과의 관련성을 이 해할 수 있게 하였다. 지구화학을 공부하는 학부 고학년 학생과 대학원 학생뿐만 아니라 전 문 연구기관의 연구자들이 지구화학적 과정과 지질 현상과의 관계를 이 해하기 쉽게 지구화학의 기본 개념, 이론 및 실례를 함께 다루·었다. 그 러나 국내의 지구화학 연구 역사가 짧기 때문에 국내 연구 자료의 부족 으로 의국의 연구 사례를 주로 인용하게 됨을 안타깝게 생각한다. 지구 화학의 범위가 너무 방대하여 각 단원 간에 연계성과 체계성의 결여가 영려된다. 지구화학적 연구 방법이 지질 현상 해석에 중요함을 생각하여 부족한 마음으로 집필의 과욕을 부려 보았다. 이 책이 지구화학과 지구과학 분 야의 연구자에게 조금이라도 도움이 된다면 더없는 영광이겠다. 전략광 물자원 연구센터의 지원과 원고 정리에 협력해 준 이화여자대학교 교육 대학원생 신유희, 박성숙, 하우영, 이은정, 이지현, 안은선 양에게 고마 움을 전한댜 끝으로 이 책의 출판을 지원해 준 대우재단과 민음사에 사 의를 표한다.
차례
책 머리에•5제1장 지구의 탄생과 지구 물질의 진화 111-1 지구화학적 시스템 121-2 지구화학의 역사 141-3 원소의 기원 171-4 운석 231-5 원시 지구의 화학적 특징 35제2장 광물 열역학 412-1 열역학 시스템 422-2 열역학 제1법칙과 엔탈피 432-3 열역학 제2법칙과 엔트로피 442-4 Gibbs 자유에너지 472-5 화학퍼텐셜, 퓨가시티, 활동도와 표준상태 502-6 광물 평형과 평형상수 522-7 화학반응속도론 682-8 G-x 다이어그램과 T-x 다이어그램 712-9 지질온도계와 지질압력계 82제3장 상률과 상률도 91
3-1 상률 913-2 상률도 933-3 그래프 표시법 111제4장 동위원소 지구화학 1154-1 질량 분석 1164-2 방사성 동위원소 1184-3 안정 동위원소 145제5장 지구 물질의 원소 분배 1695-1 원소 분배의 열역학적 콘트롤 1705-2 원소 분배의 반응속도론적 콘트롤 1715-3 마그마의 분화와 미량원소의 분배 181제6장 물의 화학 1876-1 용해도와 용액 1886-2 산화 환원 평형 2056-3 화학적 풍화 과정 2196-4 퇴적물의 속성 작용 2336-5 열수의 지구화학 241제7장 광물의 결정화학 2517-1 결합 구조와 이온 반경 2527-2 광물의 화학적 전이와 구조적 전이 2547-3 규산염 광물의 결정화학 2647-4 점토 광물의 광물화학 270제8장 지각과 맨틀의 화학 성분 277
8-1 암석권의 구성 성분 2788-2 지각과 맨틀의 상호 반응과 진화 2838-3 마그마의 기원 2898-4 원소의 이동과 농집 2978-5 광상의 형성 302제9장 해양화학 3099-1 해수의 화학 성분 3109-2 해수의 화학 성분의 변화 3139-3 해수 중 원소의 평균 체류시간 3259-4 해양 퇴적물 326제10장 생물 지구화학 33310-1 물질의 순환 33410-2 미생물 지구화학 34010-3 석탄, 석유 및 천연가스의 성인 35510-4 지구 생원소계의 진화 361제11장 환경 지구화학 36911-1 대기권에서의 환경 문제 37111-2 토양 오염 37311-3 수질 오염 37811-4 수질 평가 37911-5 음용수의 적합성 38311-6 방사성 폐기물 오염 38511-7 지구 환경의 보전 398참고문헌•403
부록•423찾아보기•439제 1 장 지구의 탄생과 지구 물질의 전화 인류는 우주와 지구의 신비에 많은 꿈과 기대감을 가지며, 우주와 자 연에 도전적으로 끊임없는 탐구에 전력을 기울여 왔다. 아폴로 11 호가 달의 수수께끼를 풀었고 심해저 탐사선에 의해 해저 신비의 베일이 벗겨 졌으며, 고압 • 고온 실험장치 개발과 전자현미경, 가속기와 질량분석기 등 분석기기의 정밀화로 우주와 지구 물질의 기원과 물질의 거동이 정량 화되기 시작하였다. 지구화학은 우주와 지구에서의 물질의 분포, 기원, 전화, 이동, 상호 작용 등을 화학적인 수단으로 탐구하는 지구과학의 핵 심 전문 분야 중의 하나이다. 지질학적 모든 현상과 갑이 지구화학적 현상은 시공간상에서 일어나기 때문에 시스템 개념을 도입하여 정량화하는 것이 유용하다. 지구화학적 시스템 개념, 지구화학의 역사 그리고 태양계 초기 물질을 대표하는 운 석과 선캄브리아대 지층 중의 기록으로 지구 물질의 역사를 알아보자.
1-1 지구화학적 시스템 약 150 억 년전 대폭발 (b ig ban g)에 의하여 생성된 수많은 원소가 지구 와 우주에 존재하고 있으며 이들 원소의 분포와 원소의 거동은 열역학 (th ermod yn a mi cs) 이나 운동역학 (k i ne ti cs) 과 같은 지구화학적 변화 원리 에 따라 변화하고 있다. 따라서 지구화학자들은 우주와 지구의 물질계에서 일어나고 있는 다양 한 변화의 과정 (pa th w ay s of chan g es) 에 홍미를 가지게 된다. 지구화학 (g eoche mi s try)은 지구의 내의부에서 일어나고 있는 지질학적 현상을 화 학적인 수단을 이용하여 해석하는 지질학과 화학이 바탕이 되는 중간 학 문이다. 따라서 화학의 기본 개념과 이론을 도입하여 지질학적 사건이나 지질 학적 환경을 해석하게 된다. 화산 활동의 근원지인 마그마 방 (ma gm a chamber) 의 환경 , 유용 금속 광물이 농집 된 광상의 형 성 환경 이 나 호수 나 심해저 퇴적물의 되적 환경 해석에 이르기까지 지질학의 다른 분야에 서 해석된 내용에 추가하여 지구화학의 새로운 개념을 도입하게 되면 보 다 더 정량적인 많은 유익한 정보를 얻게 될 것이다. 특히 화학 퍼텐셜, 광물 열역학, 반응속도론, 원소의 분배, 동위원소 지구화학, 미량원소 -REE 원소, 지구화학 분야가 지질학 문제 해석에 크게 기여하고 있다. 지구화학은 화학 분석법과 분석기기의 개발에 힘입어 광물화학, 암석 화학, 결정화학, 수질화학, 해양화학, 생물 지구화학, 미생물 지구화학, 동위원소 지구화학, 유기 지구화학, 환경 지구화학, 사회 지구화학 등의 여러 지구화학 분야로 세분화되어 가고 있다. 특히 지구화학적 모든 과정은 대상이 우주나 지구 같은 방대하고 무한 한 크기의 공간에서부터 미세한 점토 광물의 입자까지를 포함하며, 특히 모든 지구화학적 과정은 시간에 따라 변화하기 때문에 지구화학은 시스
템 (s y s t em) 의 개념울 도입하여 지구화학적 시스템의 범위에서 다루지 않 으면 안 된다. 이때에는 질량이나 체적과 같은 시스템의 크기를 한정짓 는 시량성 변화 (ex t ens i ve varia b le) 요소와 시스템의 크기와 무관한 온도 와 압력 같은 시 강성 변화 (int e n siv e varia b le) 요소가 대 단히 중요하게 된 다. 지구 시스템 및 지구화학 시스템에서 여러 과정은 시간과 공간상에서 다루어져야 한다. 일반적으로 지진, 화산, 대기의 대류 등 미세한 지구 현상은 좁은 시공간상에서 다루어지며 판구조 운동, 빙하기, 생물의 변 천, 생명의 기원 등 거대한 현상과 사건은 넓은 시공간상에서 취급된다 (그립 1-0).
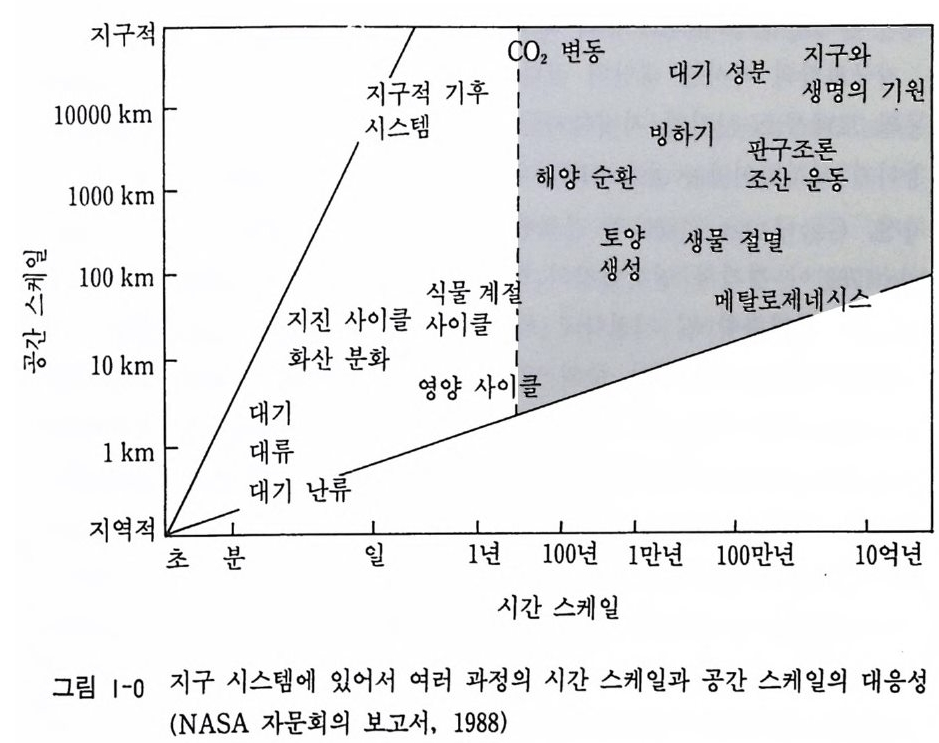 1000지0 구km적 시지스구템적 기후 C11|| O 2 변동 빙대하기기 성판분 구조생지론명구 의와 기원
1000지0 구km적 시지스구템적 기후 C11|| O 2 변동 빙대하기기 성판분 구조생지론명구 의와 기원
1-2 지구화학의 역사 고대 희랍에 Thales( 기원전 624 - 546) 는 물질의 근원을 〈 물 〉 에 두었고, Anax i menes( 기원전 588-524) 는 〈 공기 〉 에, Herakle it os( 기원전 541-475) 는 〈 불 〉 에, Em p edokles( 기원전 483-433) 는 〈 흙 〉 에 두어 4 원소설을 제창했 다. 이 4 원소설을 후에 Ar i s t o t eles( 기원전 384-322) 가 받아들였으며 원소 사이에 상호 변환이 가능함에 착안하여 14-15 세기에 유럽 문화는 Kheme i a( 연금술)의 전성기를 맞게 된다. 납이나 철을 금, 은으로 바꾸 는 중세의 연금술은 후에 불가능함을 알게 되 었으나 황산, 초산, 왕수 등의 개발 및 야금, 유리 제조, 착색 기술 등에 큰 성과를 가져와 근대 적인 물질관을 도입하고 근대 화학의 기초를 만들게 되었다. 지구화학의 역사는 대단히 젊다. Ste n o, Nic o laus, Ag rico la, Georgi us 등의 르네상스 시기의 지질학자들이 자연에서 원소의 산출과 습성을 관 찰하기 시 작하여 Lavois ie r (17 74) 의 질 량보존의 법 칙 , Dalto n (18 03) 의 원 자설, Ga y -Lussac(1809) 의 기체반응의 법칙 등의 개념이 나왔으며 Del' lsle(1783) 이 결정의 면각일정의 법칙을 발견하고 결정 관찰을 함으로써 광물학, 결정화학 및 지질학에 화학적 개념이 도입되기 시작하였다. 지 구화학이란 용어는 대기 중의 오존 발견으로 유명한 스위스의 화학자 Schonbein ( 17 99-1868) 이 1838 년 처 음으로 그의 논문에 서 사용하였으며 Ro th (1859-1893) 는 광물 암석의 분석치를 Allge m ein e und Chemis ch e Geolog ie 에 수록하였다. 이 무렵 1884 년 미국 지질조사소와 1904 년 카 네기 연구소에 지구화학 실험실이 만들어졌다. Goldsc hmi d t (1888-1947) 는 지구화학에 의한 결정구조 결정의 중요성을 강조한 정량 지구화학의 시조로 스위스 취리히에서 태어나 노르웨이의 크리스티아나(현재의 오슬로)에서 Konta k tm eta m orph o se in Kris t ia n a Geb i e t e” 이라는 학위 논문을 쓰면서 화학평형론을 암석의 생성 변화 기
구의 해석에 적용하여 변성암석학의 근대적 기초를 만들었으며, 1914 년 에 오슬로 대학의 교수가 되었다. 특히, Sto f f w echsel der Erde” 라는 논문에서 지구에서 원소의 순환 모델을 설정하고 원소의 순환 속도의 개 념 을 도 입 하 였 다. 그 리 고 Geochemi sc he Verte l ung sg e s etz e der Elemen t e” 이라는 논문도 고전으로 높이 평가받고 있다. 미국의 Clarke(1847 - 1931) 는 1908 년 워싱턴 대학 광물화학 교수로 재 직하면서 세계 각지의 광물, 암석, 해양, 대기 등의 화학 분석치를 수집 하여 The Data of Geochem istry를 출판하였으며 미국 지질조사소에서 수차례 개정 출판되었다. 그가 설정한 지각, 해양, 대기의 지구 표층부 의 원소의 평균 존재량의 비율을 가리키는 〈 클라크 지수 〉 는 지구화학의 기본적인 수치로 사용되고 있다. 1880 년대에 수립된 G i bbs 의 열역학의 이론에 근거하여 Roozeboon, Eskola 등은 지구화학을 바탕으로 변성상 (meta m orp h ic fad es) 의 개 념 을 도입 하였다. 한편 이 시기의 소련의 대표적인 지구화학자는 Vernadskii (1 863-1945) 로 1885 년 이후 모스크바 대학의 교수로 재직하였고 1908-1910 년에는 지 각에 있어서의 화학 원소의 역사를 연구하였으며 1922 - 1926 년에는 프랑 스 소르본 대학에서
1921 년 「동양산 함희토류 원소 광상의 화학적 연구」로 지구화학 연구가 시작되었고 1926 년 ((국민신문))에 지구화학을 소개하였다 . 1926 년 『 무기 화학 요람 』 에 지구화학의 단원을 넣어 일본의 지구화학의 발전에 공헌하 였으며 1953 년 지구화학 연구회(일본 지구화학회)를 발족시켰다. 1930 년 대에 와서 다시 2 차 세계대전 때 고압 하에서 처음으로 철 합금이 개발 되었다. 이때 미국의 Brid g e m an, Bowen 등은 하부 지각과 상부 맨틀 에 상응하는 압력과 온도에서 광물 조합을 합성하였다. Clarke 의 책 이 후에 미국 지질조사소의 Wede p ohl (1 969 - 1978) 에 의해 편집된 Handbooll of Geochemistry라는 책은 현재 지구화학 자료 를 참고하는 데 가장 많이 이용되고 있다. 19 세 기 말에 Ruth e rf or d, Bequ e rel, Curie s 등의 방사성 동위 원소 발 견에 의해 지구연대학(g eochronolo gy)이 연구되고 1936-1939 년 N i er 에 의한 질량분석기의 개발로 동위원소 지구화학의 시대가 열리게 되어 1940 년대 Urey 등을 시초로 안정 동위원소가 광상학, 환경 지구화학, 암석학 등에 광범위하게 이용되게 되었다. 최근에는 U-Pb, Sm- N d, Rb-Sr 과 같은 방사성 동위원소의 정밀 측 정이 가능하여져 l“Nd/l“Nd, “Sr/86Sr, 207Pb/204Pb 등의 동위원소비가 지각과 맨틀 등의 지구물질의 화학적 경로 (che mi cal p a th wa y)의 추적자 로 높이 평가받고 있다. 1950 년대에 와서 지구화학자들은 열역학을 이용한 광물의 안정도, 화 학 반웅, 실험암석학 분야에 초점을 맞추었다. 1928 년 Bowen 에 의해 출판된 The Evoluti on of Ign eous Rock 과 1952 년 Mason 에 의 해 출판 된 Pr inc i ple of Geochem istry가 이를 말해 주고 있다. 이어서 Garrels 과 Ch rist( 1 9 65), Krausko pf(1 967) 는 열역학과 용액 화학을 중요하게 다 루는 지구화학 관련 저서를 출판하였다. 20 세기에 들어와 지화학 탐사와 환경 화학분야의 연구가 활발해지면서 지구화학은 동위원소 지구화학, 유기 지구화학, 무기 지구화학, 지구화학 탐사, 환경 지구화학, 미량원
소 지구화학, 우주 지구화학 등으로 세분되어 연구가 심화되고 있다. 대표적인 지구화학 관련 전문 논문지는 Geochemi ca et Cosmochim i ca Acta , Chemi ca l Geology , App li ed Geochemi str y , Geochemi str y Inte rn a- tion al, Geochemi ca l Jou rnal 등이 있다. 1-3 원소의 기원 우주 초기 약 150 억 년전 고온에서 평형상태에 있던 양자, 중성자, 전 자, 뉴트리노 등의 소립자가 우주 괭창이 시작되면서 평형이 깨어져 중 성자의 일부는 f3붕괴를 하고 양자는 중성자를 포획하여 중양자를 만드 는 과정이 반복되어 연속적으로 점차 무거운 원소가 다음과 감이 합성되 었다. f H+!H 一iH+{3 + +v f H+!H ―내 He+r me+me 一 ;He+iH + !H me+me 一 !Be !Be+ 홍 He 一 A2C+ r i2C +!H 一 PN+ r 散 :+me 一 160 l60+me 一나 8Ne 등 우리는 이 러 한 과정 울 대폭발설 (big bang the ory ) 이 라고 하며 1957 년에 B2FH(Burbid g e , Burbid g e , Fowler 와 Hoy le ) 등에 의해 제출되었다. 대폭발이 일어날 때 만들어진 대부분의 원소는 대폭발 과정에서 재분 해되었으며 C, Be, M g와 같이 붕소보다 무거운 원소는 대폭발에서 만 들어진 가벼운 원소가 별의 내부에서 수소와 헬륨과의 핵융합 과정을 거
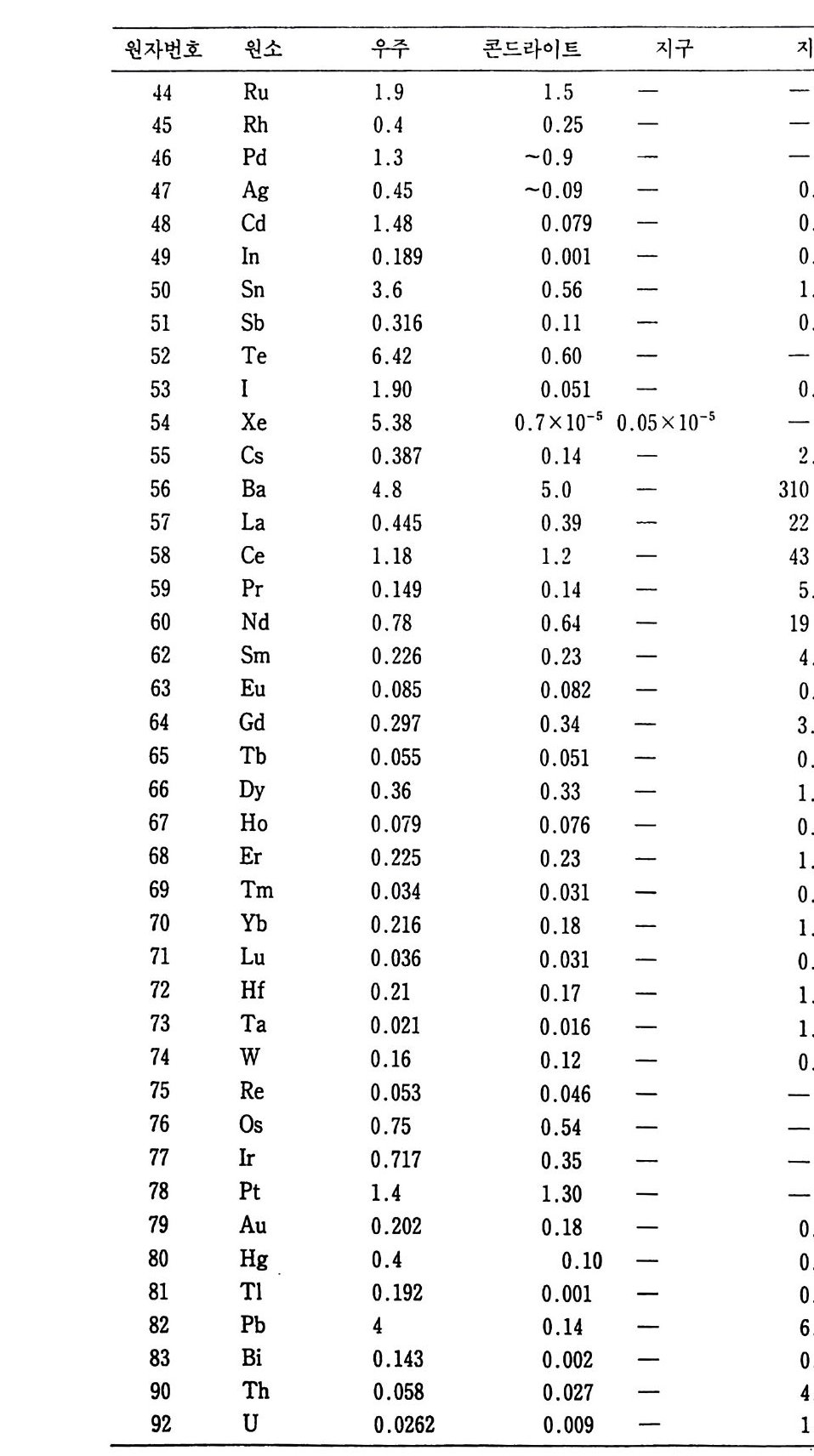
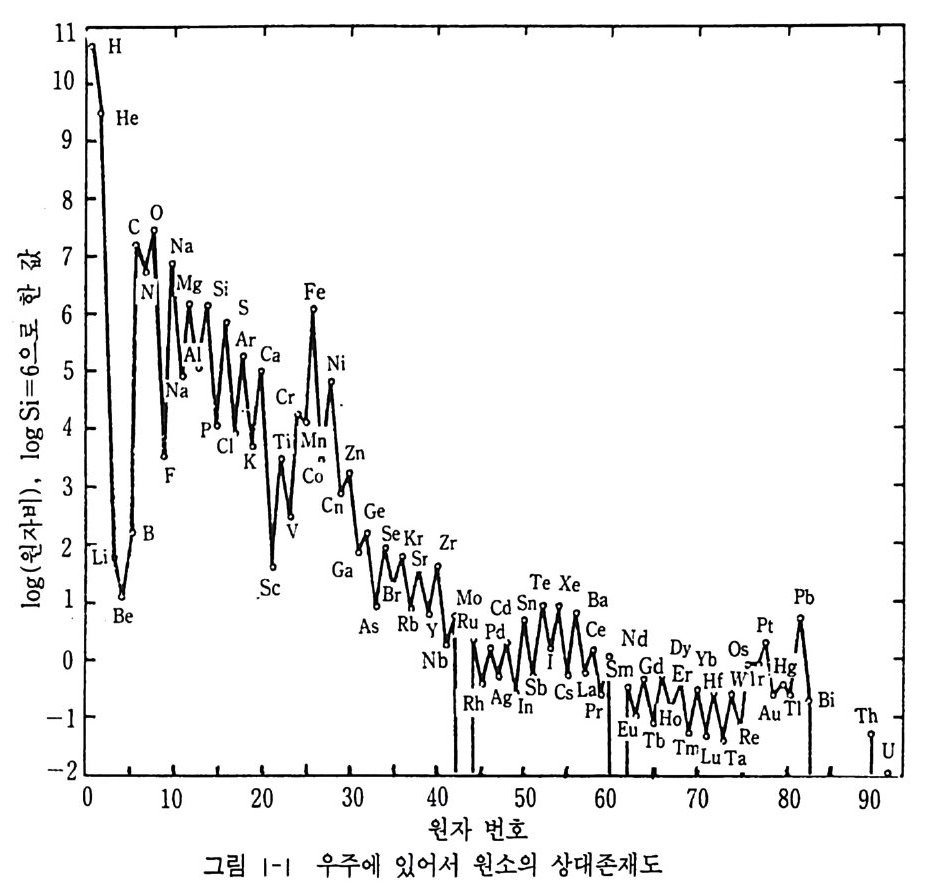
치면서 만들어졌다. 그리고 Fe 보다 무거운 원소는 S - 과정 (slow pro cess) 에서, B i보다 무거운 원자핵은 R- 과정 (rap id pro cess), 112Sn 은 P- 과정에 서 만들어진다. 죽 H, He 등 일부 경원소를 제의한 모든 원소가 별의 내부에서 초신성의 폭발과 원자핵 반응에서 만들어전 것이다. 현재까지 107 원소가 보고되어 있으며 우주의 원소 성분은 표 1 - 1 과 같다. 우주의 원소 성분은 주로 H(3. 18 x 1 010), He(2.21 x 109) 으로 구성되어 있고 콘드 라이트와 지구물질의 Na, Mg , Al, Si, K, Ca 등의 대부분의 원소의 존재도는 대단히 유사하다. 이와 같이 콘드라이트 성분과 우 주 의 원소 성분은 대단히 유사하다. 그러나 지구의 원소 성분은 이들과 상당한 차 이가 있다. 즉 지구 물질은 지구 탄생 후 물질이 진화되었음을 알 수 있 다. 우주의 원소 성분은 행성에서 뜨거워진 원소가 발하는 각 원소의 특유 한 파장을 광스펙트럼 분석 (spe c tr os cop ic analys i s) 에 서 알 수 있는데 , 그 파장에서 원소의 종류를 연구하고 스펙트럼의 강도에서 그 원소의 존재 비를 추정할 수 있다. 또 다른 방법은 지구 밖에서 지구로 떨어지는 운 석 (mete o ri te) 연구에서 알 수 있다. 이같은 원소의 존재도를 보면 몇 가 지 특성이 나타난다. 첫째, 수소와 헬륨이 99.8 % 이상을 차지하고 있 으며 나머지 원소의 존재도는 대단히 낮다. 둘째, 일반적으로 원자번호 가 증가함에 따라 존재도가 감소한다. 셋째, Li, Be, B, Sc 등은 예의 적으로 낮은 존재도를 나타내는 반면에 Fe, Ni, Pb 등은 높은 존재도 를 나타내며, 존재량은 원자번호 40(Zr) 정도까지는 지수함수적으로 감 소하고 있다(그림 1-1 ) . 넷째, 짝수 원자번호의 원소의 존재도가 홀수 원 자번호의 존재도보다 높게 나타나 지그재그 (z ig za g)형을 나타내는 오도 -하킨스 (Oddo-Hakk i ns) 규칙이 성립하고 있다. 원소의 우주존재도 중 지구 구성 물질에 가장 중요한 Mg , Fe, Si 등 의 비휘발성 원소의 비는 Mg : Fe : Si= l : 0.9 2 : 1 이다. 이 비율은 지 구의 전체 화학 조성을 고려할 때 중요한 의미를 가진다. 만일 Fe 가 핵
 표 |기 우주, 운석, 지구 및 지각에서의 원소의 분포 (Cameron , 1973, Ehmann,
표 |기 우주, 운석, 지구 및 지각에서의 원소의 분포 (Cameron , 1973, Ehmann,
 원자번호 원소 우주 콘드라 o J트 지구 지각
원자번호 원소 우주 콘드라 o J트 지구 지각
(지구 질량의 92. 4 %)의 주된 구성 원소가 되었을 때 맨틀과 지각의 화학 량론 (s t o ic h i ome t r y)은 휘석 (M g S i 03) 으로 된 콘드라이트 모델이 되며 Clarke 와 R i n gw ood0964) 가 제안한 파이로라이트(pyr o lit e) 모델의 Mg 2S iQ 4 조성이 되지 않는다. 콘드라이트질 지구 (M g : (Fe+Ni) : Si= 1 : 0.92 : 1) 에서 M g 2S i O 검 맨틀을 만들려면 핵의 밀도를 낮추기 위하여 핵에 S i를 넣을 필요가 있다 . 그러나 핵의 밀도를 낮추는데 S 나 O 를 도 입시키면 화학적으로 더욱 합리적이다. 이때에는 M g 2S iQ 4 질 맨틀로 된 지구로서 전체적으로 비콘드라이트질이 되어버리는 양면성이 있어 콘드 라이트 모델과 파이로라이트 모델 사이에 본질적인 문제는 여전히 미해
 101 h H
101 h H
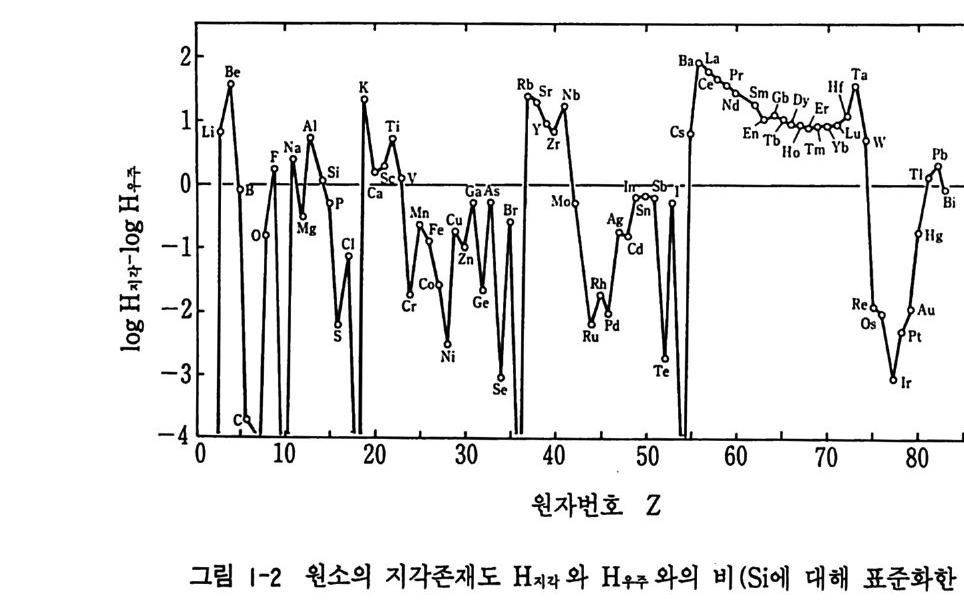
결로 남아 있게 된다. 대신에 원소의 우주존재도와 지각존재도를 비교하여 지구에서의 원소 의 존재도 이상을 추정하기 위하여 원소의 지각존재도와 우주의 존재도 의 비를 원자번호순으로 나타내었다(그립 1-2). 그 결과 홀수 원자번호의 원소가 비교적 강한 농집을 나타내고 있다. 그리고 홀수 전하 원소의 대 표적인 알칼리 금속 원소의 농축은 위의 효과에도 불구하고 Rb 과 Sr, Cs 과 Ba 처럼 짝수 전하의 Sr, Ba 이 Rb, Cs 만큼 농축되어 있어 지구 전체는 알칼리 금속 원소의 존재도 이상이 나타나고 있다 (Ma t su i, 1992). 죽 지구의 재료 물질은 콘드라이트에 비해 상대적으로 알칼리 금속 원소 가 결핍되어 있었다. 지구, 달, 평균 0- 콘드라이트 사이의 원소의 존재 도 이상은 표 1-2 와 같다.
 2.L꿍i1 0l2K 3 Thg u
2.L꿍i1 0l2K 3 Thg u
지구와 달에서 알칼리 금속 원소의 결핍은 콘드라이트에서는 현저하지 않다. 콘드라이트에 현저한 In, Tl, Bi 등의 결핍은 지구와 유사하나 달에서는 국단적으로 결핍되어 있다. 죽 지구와 달의 비교행성학적으로
도 생성 기구가 복잡하였음을 알 수 있다.
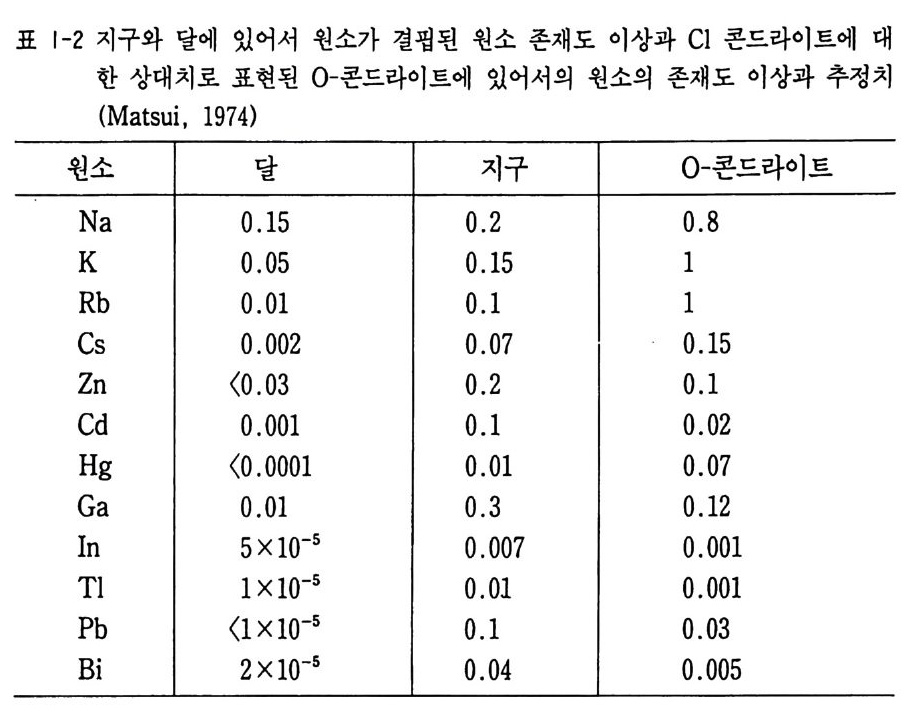 표 1-2 지구와 달에 있어서 원소가 결핍된 원소 존재도 이상과 Cl 콘드라이트에 대
표 1-2 지구와 달에 있어서 원소가 결핍된 원소 존재도 이상과 Cl 콘드라이트에 대
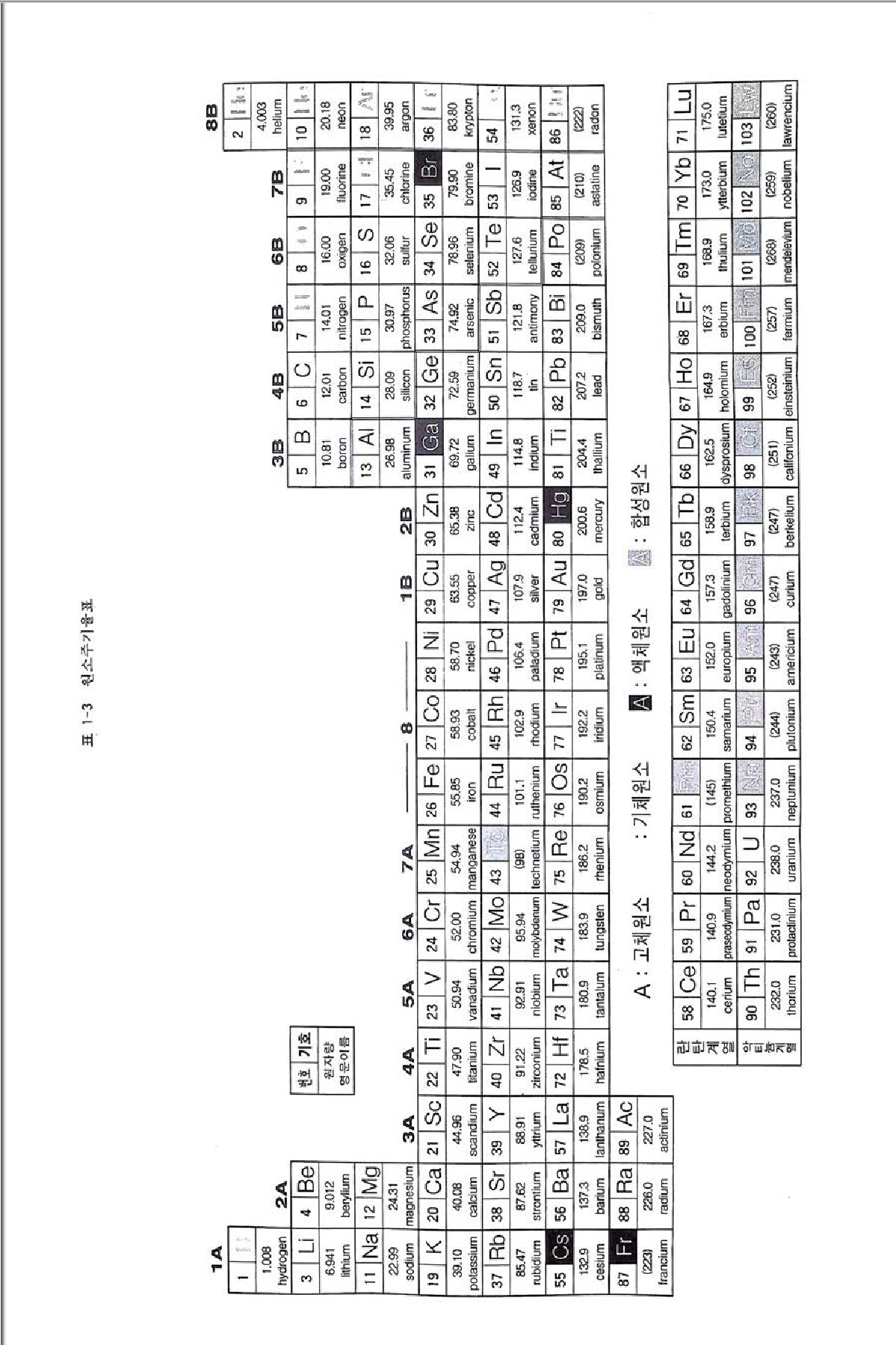
원소 주기율표 1869 년 초 러 시 아의 화학회 에 서 MendeleevUa34-1907) 는 원소 주기율 표를 발표하였다. 또한 비슷한 시기에 독일의 Me y er (1 830-1895) 가 1869 년 12 월에 주기율표를 발표하였다. 사실은 Mendeleev 이전에 주기율을 제창한 학자는 프랑스의 지질학자인 샹그르드와이며 1863 년에 주기율표 를 발표하였으나 화학회지에 게재되지 않아 화학자들에게 알려지지 않은 불운한 선구자가 되었다. 원소들을 원자량 증가순으로 배열한 결과 물리적 및 화학적 성질의 주 기성이 나타나 비슷한 성질을 가지는 원소들을 족으로 구분하였다. 이때
핵의 전하수, 죽 중성 원자 속에 들어 있는 전자수가 원소의 중요한 성 질이 되고 있다. 표 1 - 3 에서와 갇이 1A 족부터 7A 족까지와 0 족을 대표적 원소라 하며 lB 족에서 7B 족까지와 7 족을 전이원소(t rans iti on elemen t s) 라 한다. 58Cl 부터 71Lu 까지의 원소들은 란탄 다음에 들어가는 원소들로서 란탄족 또 는 희 토류 원소 (rare-eart h elements ) 라 부른다. 그리 고 g oTh 에 서 103Lr 까 지는 악티늄 (89Ac) 다음에 들어가는 원소로 악티늄족이라 부르고 있다. 그리고 lA 족 원소들을 알칼리 금속, 2A 족 원소들을 알칼리토 금속, 7A 족 원소들을 할로겐, 0 족 원소들을 0 족 기체(비활성 기체)라 한다. 또 주 기율표 왼쪽의 원소들은 금속 원소이고 오른쪽은 부도체인 비금속 원소 이다. 이들의 중간 성질의 Ge, Se 등의 중금속은 주로 반도체로 이용되 고 있다. 지질학자들은 원소 주기율표에서 자연계의 원소의 거동과 습성 울 쉽게 이해한다. 이온의 크기나 이온의 전하는 광물의 결합과 치환 등 의 이온 화합물의 특성 연구에 대단히 중요하다. 루비듐은 칼륨 광물에 미량원소로 들어가 있으며 스트론튬은 칼슘 광물, 브롬은 영소 광물에서 산출되는 사실을 쉽게 이해할 수 있게 된다. 따라서 다양한 지질학적 과 정에서 원소의 농도가 변화될 수 있지만 어떤 원소들의 특성의 유사성에 서 원소의 비가 물질의 역사를 해석하는 데 이용될 수 있다. 예를 들면 마그마 결정사 해석에 K/Rb, 안정 동위원소비, 방사성 동 위원소비 등이 이용될 수 있다. 따라서 지질학자들은 원소의 특성뿐만 아니라 압력, 온도, 화학적 환경 해석에 원소 주기율표를 유용하게 이용 하고 있다. 1922 년 Goldschm i d t는 많은 운석 분석 치 에서 각 원소들이 산소에 대 하여 친화성이 다르다는 점에 착안하여 친철원소 (s i dero p h il e), 친동원소 (chalcop hi le ) , 천석원소(lith o phi le), 친기원소 (a tm o p h il e) 로 구분하였다 (표 1-4).
8B
〔〔昌
〉〔〕〉\ \:;l \:1:\| \ \11\ 三「
표율기주소원 -3
 二H 2`t 403.0 B7 B46B BB53 lhumeiA2 oer ygInhd ” 떠H., t L 1 8i0I 79 65 기)호B 번IC호 I I I3e B4I 920..068001 1101 011.810021..4 1902.1 1 6 .4I9자 량원 lonu reenoeoexonn rn non rbt ibrooicinggaf m luem uIhb yitliir 룽문영이 p i gt 51仁!17 S1 18A 6SA 1 l13 4a 12//M N11/ 9553 93..54` .093.922 .3 780609 862 43..221 I29 9 2B rIo n-B eI8asg7uh nA-Ir osA uuolrhh socl if s5pn lnpuom4rui mllc IAaI IAG 13 iAiiosmeamunsudm l liig li1C li Vi K i I3Il 3IS leGI4I6 l53233 IG1A3lI 3seII 293 Iu nZIINI Co s I2o F I26l 12ICnI I Me 3 T2II 25Ir 2I I4C Ic I0 a 1 2II2S2I2IC 91 IJ s. 7_I3.ao . 0_II9 8974I 2 9 7III.59_ 1926 3 I3 126.6I 659:85 05 . 85I.s5I 55.I98 7834_ o2.45I .5I .I~ 9004I4 0~s 97I.o. 4 I 1oI09. 304 .nomrIIboe n k I rcalpt mmyme eenlils rruIl un snaeeoIir nciig um alz Ic nke cI lo bclI aInp ogiipr mit m1i sane na uo ch 1Idummerum guvca Iinmania Id asnI m I uacpm li1itutssiocaii j j j jj g j Y登、1『.,5311,1 I 54 I51nSe15T215l0l bSA1Cn 1 I49lds1144d16l1hR45l4uP1R44 43 oM 42 bNr 41 rZ 40 39 78bR3 3 S II I 3 7.3.6129II611228I 8.111.11I 74.8 I 1 1.10I 6109.2t 17I I 2.910I 10I 8) (9. 1.42I .9495I .919I 21 .42 7 I 7 2889.( .918I .68514. II n on xemon I m ryullun eeoI IIa nditi iI umnid tI m undmca usv I laa m uodtiiIei imI l r dii pir I umnheru I umehnec hI u mdenitttyblI mm uobn I mnu ocozirI mrn s Ibrom iiiiduuIm uutiiititryt l m11t iti Jlt W fa HII 8 I ;, l 61 B I83 I II 8o P I A845I I bP I82I I T 81 80A I19I P I18I Ir I I u11I sO I16 I e R I 15I I 1 I aI T 13I I 12 4I a65 55I L 57 I aI B II 22l (2.o092I II 9l(200)(I 21 1.202I 420I 0.6207.o9I 5.119I 2 .2119I 0.210I 6.218I 3.9 .I418 0918I 8.5.17II 913I9 18.13I 7.32.3 asIIII m d o e nulonn oI aratulmbI dleaI im uatihp sI h ldoI m inualllitcu ermI I m uenryo gipI umdI m utsmiirirh en s1nuI m lunIaaIi m iuba m tttianh I umanhangI lI umuescftrii .n1 cA 8 87I 89 l aI 8R : : 소원성합 점소원체액屋 소원 :체기 소원체고: A 7.o22 22) 23(26.0 rad Imm unacI umucnraitiiif
二H 2`t 403.0 B7 B46B BB53 lhumeiA2 oer ygInhd ” 떠H., t L 1 8i0I 79 65 기)호B 번IC호 I I I3e B4I 920..068001 1101 011.810021..4 1902.1 1 6 .4I9자 량원 lonu reenoeoexonn rn non rbt ibrooicinggaf m luem uIhb yitliir 룽문영이 p i gt 51仁!17 S1 18A 6SA 1 l13 4a 12//M N11/ 9553 93..54` .093.922 .3 780609 862 43..221 I29 9 2B rIo n-B eI8asg7uh nA-Ir osA uuolrhh socl if s5pn lnpuom4rui mllc IAaI IAG 13 iAiiosmeamunsudm l liig li1C li Vi K i I3Il 3IS leGI4I6 l53233 IG1A3lI 3seII 293 Iu nZIINI Co s I2o F I26l 12ICnI I Me 3 T2II 25Ir 2I I4C Ic I0 a 1 2II2S2I2IC 91 IJ s. 7_I3.ao . 0_II9 8974I 2 9 7III.59_ 1926 3 I3 126.6I 659:85 05 . 85I.s5I 55.I98 7834_ o2.45I .5I .I~ 9004I4 0~s 97I.o. 4 I 1oI09. 304 .nomrIIboe n k I rcalpt mmyme eenlils rruIl un snaeeoIir nciig um alz Ic nke cI lo bclI aInp ogiipr mit m1i sane na uo ch 1Idummerum guvca Iinmania Id asnI m I uacpm li1itutssiocaii j j j jj g j Y登、1『.,5311,1 I 54 I51nSe15T215l0l bSA1Cn 1 I49lds1144d16l1hR45l4uP1R44 43 oM 42 bNr 41 rZ 40 39 78bR3 3 S II I 3 7.3.6129II611228I 8.111.11I 74.8 I 1 1.10I 6109.2t 17I I 2.910I 10I 8) (9. 1.42I .9495I .919I 21 .42 7 I 7 2889.( .918I .68514. II n on xemon I m ryullun eeoI IIa nditi iI umnid tI m undmca usv I laa m uodtiiIei imI l r dii pir I umnheru I umehnec hI u mdenitttyblI mm uobn I mnu ocozirI mrn s Ibrom iiiiduuIm uutiiititryt l m11t iti Jlt W fa HII 8 I ;, l 61 B I83 I II 8o P I A845I I bP I82I I T 81 80A I19I P I18I Ir I I u11I sO I16 I e R I 15I I 1 I aI T 13I I 12 4I a65 55I L 57 I aI B II 22l (2.o092I II 9l(200)(I 21 1.202I 420I 0.6207.o9I 5.119I 2 .2119I 0.210I 6.218I 3.9 .I418 0918I 8.5.17II 913I9 18.13I 7.32.3 asIIII m d o e nulonn oI aratulmbI dleaI im uatihp sI h ldoI m inualllitcu ermI I m uenryo gipI umdI m utsmiirirh en s1nuI m lunIaaIi m iuba m tttianh I umanhangI lI umuescftrii .n1 cA 8 87I 89 l aI 8R : : 소원성합 점소원체액屋 소원 :체기 소원체고: A 7.o22 22) 23(26.0 rad Imm unacI umucnraitiiif
1표
: :I:〔i[ :I
5
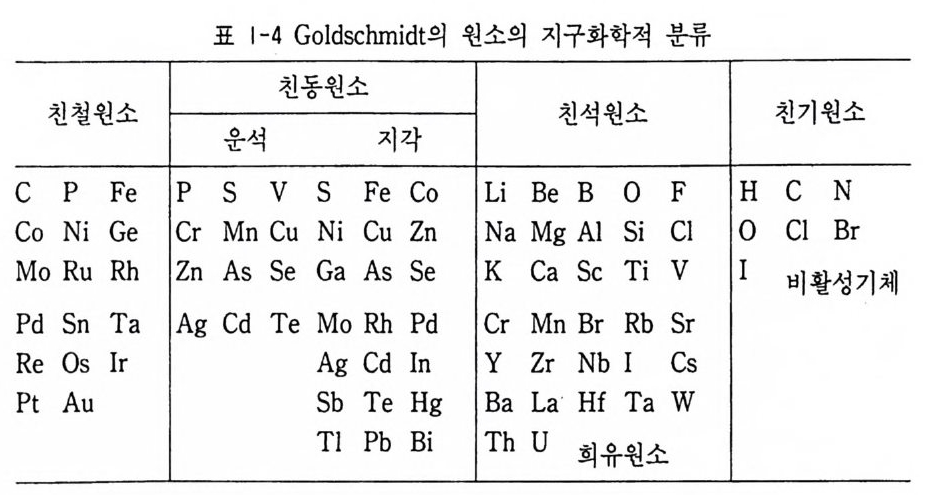 표 1-4 Goldschm i d t의 원소의 지구화학적 분류
표 1-4 Goldschm i d t의 원소의 지구화학적 분류
예를 들면 니켈은 철과 강한 친화성을 가지며 산소와는 친화성이 낮기 때문에 백금족 원소는 운석 중의 주로 중금속상에 농축된다. 이같은 원 소를 친철원소라 한다. 황화물을 만들기 쉬운 원소는 천동원소, 규산염 염상에 친화성을 나타내는 원소는 천석원소이며, 액화되기 어려운 원소 나 휘발성 화합물에 해당하는 헬륨, 아르곤, 수소, 질소 등은 친기원소 이다. 물론 이 Goldschm i d t의 분류는 지구에서보다 더 환원성 환경에서 만 들어전 운석의 분석치에서 분류한 것이므로 지구 물질에 그대로 적용될 수는 없지만 이 분류가 지구의 진화에 따른 원소의 거동을 연구하는 데 대단히 유용하게 적용되고 있으며 지구화학적으로도 의미가 있다. 1-4 운석 운석은 태양에서 2-4AU 거리에 있는 궤도를 돌고 있는 다수의 소행 성군 (as t ero i ds) 이 지구 궤도에 진입한 것으로 생각하고 있다. 옛 체코슬
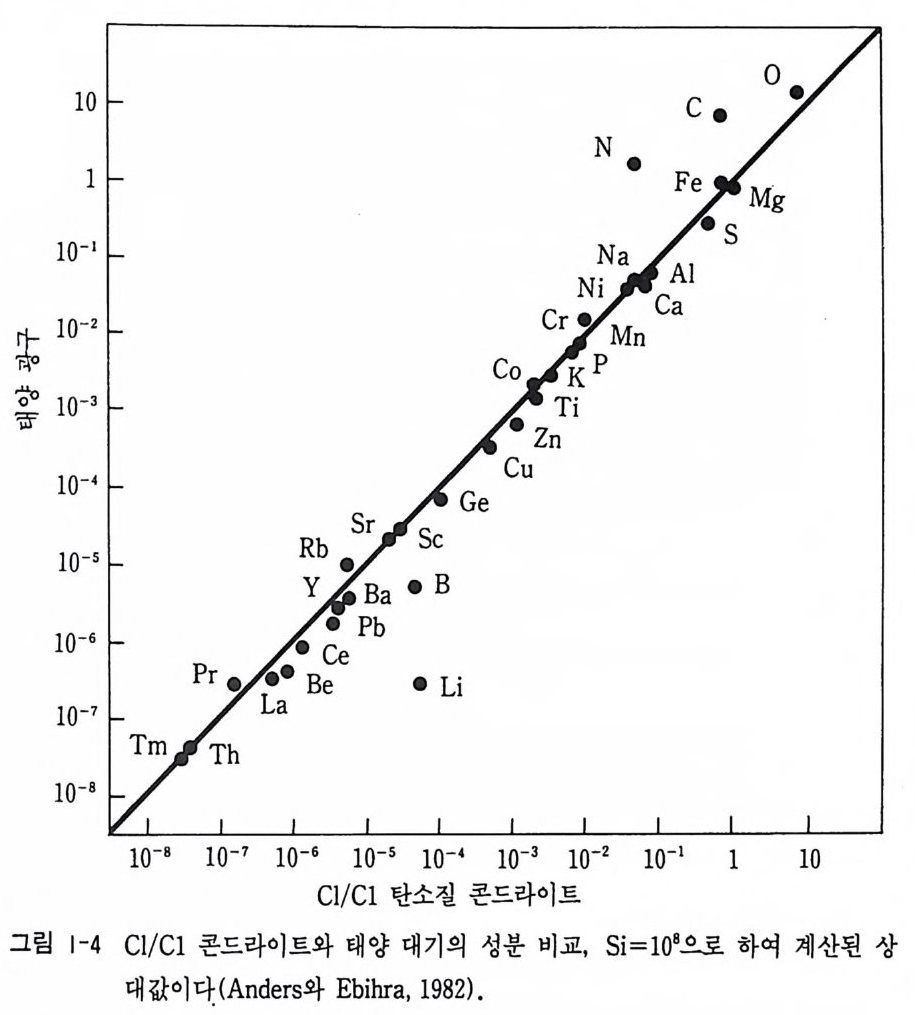
로바키아 프라하 부근의 프리브램 (Prib r am) 마을에 10 k g의 운석이 떨어 졌을 때 관측 촬영된 사진에서 프리브램 운석의 기원은 그림 1-3 과 같이 소행성의 조각으로 해석되고 있다. 46 억 년전 태양계가 형성된 이후 지구와 달에서는 화성작용이 장기간 활발하게 일어나 초기의 물질의 특성은 모두 없어졌다. 그러나 운석은 긴 지질시대 동안 변성작용을 거의 받지 않아 태양계의 초기의 정보를 얻을 수 있다. 태양광 스펙트럼 해석에서 얻어진 태양 표면의 원소의 존 재도와 Cl 탄소질 콘드라이트의 분석치 사이에 나타난 높은 상관성에서 콘드라이트가 우주 성분과 유사하고 운석 연구에서 태양계의 초기 우주 원소 성분 추정이 가능함을 알 수 있다(그림 1-4).
 \,I'/ '
\,I'/ '
2
 10 c •
10 c •
(1) 운석의 종류 운석은 금속철과 규산염 광물의 비율에 따라 철운석 (iro n mete o r ite) , 석 철운석 (sto n y -iro n mete o r ite) , 석 질운석 (sto n e mete o r ite) 등으로 구분된 다(표 1-5).
 표 1-5 운석의 종류
표 1-5 운석의 종류
콘드라 01 트 (chondri te) 운석 중에 가장 혼한 유형으로 감람석, 휘석, 유리질 또는 장석으로 구성된 밀리미터 크기의 둥근 콘드률 (chondrule) 을 다량 가지는 운석이 다(그림 1-5). 콘드라이트는 주로 Fe-Ni 합금, 트로이라이트 (FeS), 감람 석, 사방휘석, 사장석 등으로 구성되어 있다. 콘드라이트는 용융이나 분화가 일어나지 않은 45 - 46 억 년전의 운석으 로 태양계의 초기 물질의 상태를 가장 잘 보존하고 있다. 그립 1-4 에서 처럼 태양 대기와 직선 상관성을 나타내며 탄소, 질소, 산소 등의 기체 원소는 태양에 더 많기 때문에 콘드라이트는 가스가 증발해 버린 태양계
조각으로 생각할 수 있다.
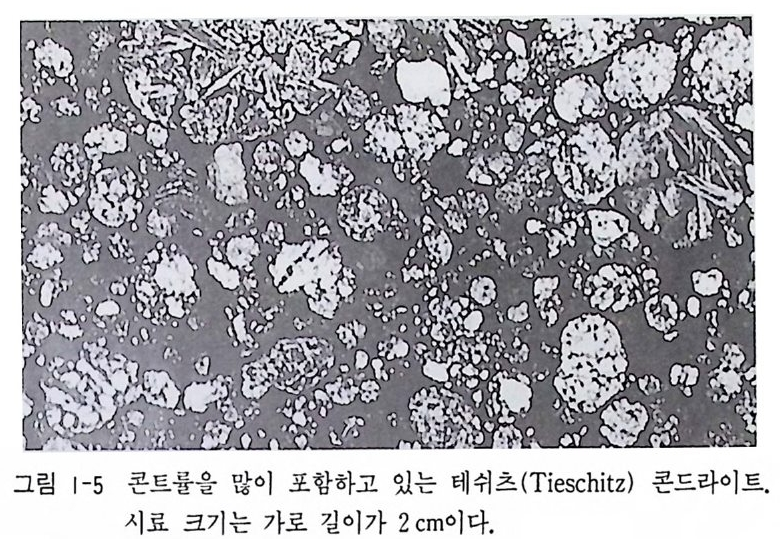 그림 ,-s 콘트률을 많이 포함하고 있는 테쉬츠 (T i esch it z) 콘드라이트.
그림 ,-s 콘트률을 많이 포함하고 있는 테쉬츠 (T i esch it z) 콘드라이트.
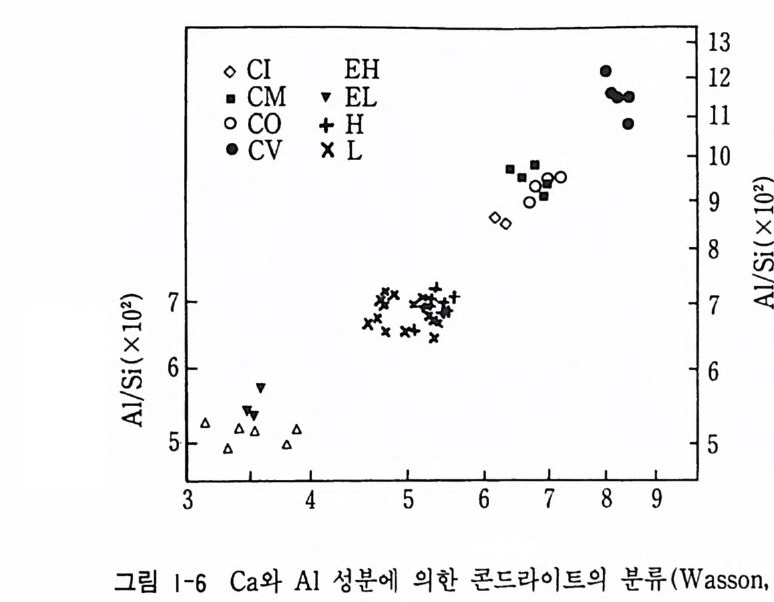
한편 Li, B, Be 등의 원소는 태양보다 콘드라이트에 더욱 많이 포함 되어 이 세 원소가 핵 입자와 상호 반응에 와해 태양에서 체계적으로 파 괴된 것으로 보여 콘드라이트가 현재의 태양의 성분보다도 과거의 태양 의 성분을 잘 기록하고 있는 것 같다. 콘드라이트는 탄소질 콘드라이트 (C) , 보통 콘드라이트 (0) , 엔스타타 이트 콘드라이트(E) 등으로 구분된다. 이들은 Ca, Al 의 함유량에 따라 구분된다(그림 1-6). 탄소질 콘드라이트는 Al 함량에 따라 Cl, CM, CO, CV 네 종류로 구분되며 이들은 콘드라이트 중에서 가장 산화형이다. 보통 콘드라이트 는 철 함량에 따라 H, L, LL 로 구분된다. 엔스타타이트 콘드라이트는 환원형으로 금속철만이 존재하며 철 함량에 따라 EH, EL 그룹으로 구 별된다. 탄소질 콘드라이트는 철은 대부분 Fe2+ 상태로 사문석과 유사한 광물로 존재하고 금속철은 거의 존재하지 않는다. 특히 물과 유기물이
다량 포함되어 있다. 보통 콘드라이트는 철의 함량의 변화가 커 금속철이 28 % 정도 포함 된 H 콘드라이트, 22 % 정도 포함된 L 콘드라이트, 철과 금속 함량이 대단히 낮고 규산염 광물 내에 산화물 형태로 존재하는 LL 콘드라이트 등으로 세분하고 있다. 에 01 콘드라 01 트 (achond rite) 콘드률을 가지지 않는 석질운석으로 지구상의 암석과 유사하다. 에이 콘드라이트는 HED 에이콘드라이트, 엔스타타이트 에이콘드라이트, 유 레이라이트 에이콘드라이트 등으로 세분된다. 금속 광물과 규산염 광물 이 비슷한 함량으로 구성된 석철운석은 메소시데라이트, 팔라사이트가 있다. 철운석은 거의 Fe-Ni 합금만으로 된 운석으로 미량원소의 함유량 에 따라 13 그룹으로 세분된다 (Wasson, 1985).
 듭X 7 o0•■ CCCcVIoM +X• HLEEHL念 합 O 。• •。 냥 •` • 」 11891711302 :gTX
듭X 7 o0•■ CCCcVIoM +X• HLEEHL念 합 O 。• •。 냥 •` • 」 11891711302 :gTX
(2) 콘드라이트의 응축 모델 별은 고온이기 때문에 기체 상태의 물질로 되어 있으며 모든 분자들이 원소로 분리되어 있다. 일단 고온 (2000 'K) 가스상의 원소들이 별에서 추 출되어 나오면 별은 냉각되어 고체의 금속 또는 화합물로 응축된다. 우 주에서는 압력이 너무 낮기 때문에 평형상태에서는 액체상이 생성될 수 없다. 성간 먼지와 성간 가스가 집합되어 새로운 별을 만들고 다시 뜨거워 진다. 우주의 가스 성분이 응축되는 모델을 Grossman(1 9 72) , Ste v en 등 •( 19 89) , Oshim a (19 92) 등은 다음과 갇이 계 산하여 검 토하였 다. 소행성으로 존재하던 마립자들이 지구 궤도에 유입되어 콘드라이트가 만들어졌다는 것이 〈 콘드라이트 응축 모델 〉 이다. 고온 가스가 냉각될 때 고체상이 생성되는 온도는 고체상의 증기압에 따라 결정된다. 금속철의 경우에 Fe( 고체상 )=Fe( 기체상) 평형이 성립될 경우 평형상수는- K= PF e 포화 가 된다. 여기서 PF e£.화 는 철의 증기압이며 aFe 는 철의 활동도이 aF e 다. 순수한 금속철의 활동도 aFe 는 1 이다. 평형상수 K 는 온도와 압력에 따라 결정되며 Gib b s 자유에너지 (LJ G) 에서 K=exp ( 겅? )=P 타 가 얻어진다. 또 원시 태양계 성분의 압력은 거의 0 에 가까우므로 금속철의 포화수 증기압은 온도만의 함수로 생각해도 좋다. 고온에서 모두 기체상에 있는 성운 가스 중의 철의 분압은 우주 원소 존재도에서 PFe 성운=겅A겨(간FIe)) X PH2
에서 얻어진다. 여기서 A(Fe) 와 A (H)는 각각 철과 수소의 원 소 존재도이고 PH 2 는 원시 태양계 성분 중의 수소 분자의 분압이다. 성운이 냉각될 때 포화수 증기압은 급속히 감소하게 되어 어느 온도에서 PF c.!l.화
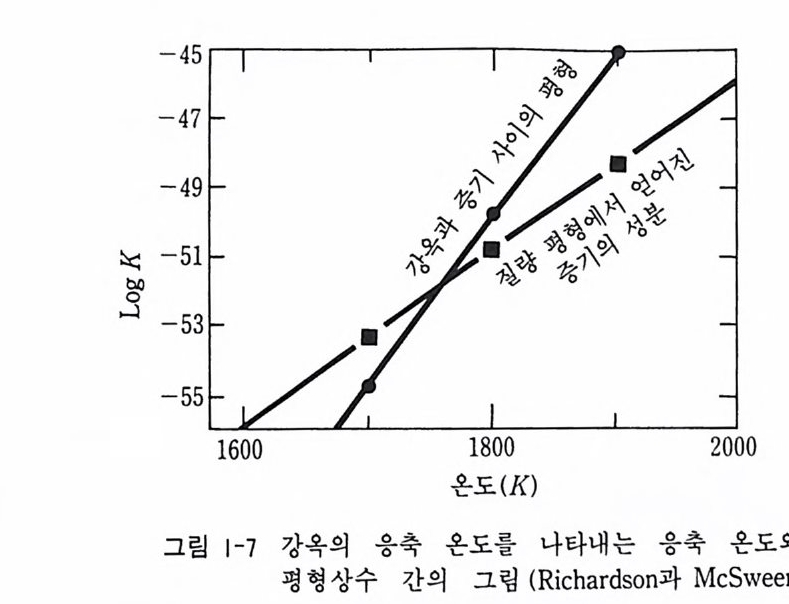
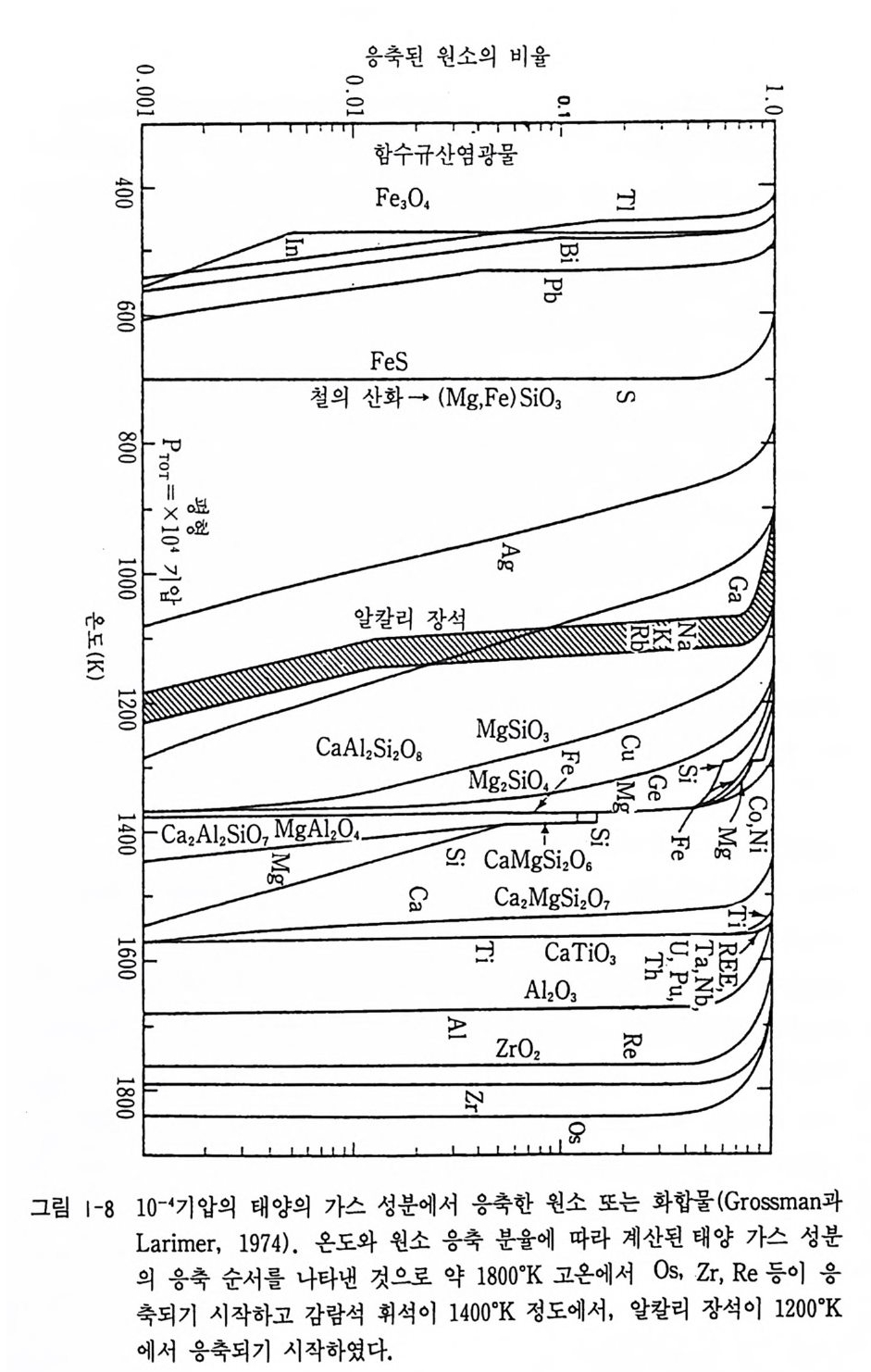
로 쓸 수 있다. 이때 평형상수는 K=(~。 ) 가 된다. 이상기체 방정식을 적용하면 NH2o=KN2H2N。 (RT )2 가 된다. 같 은 식으로 하여 기타 가스 종에 대해서도 같은 관계식이 얻 어질 수 있어 Nj Ola1 이 계산될 수 있다. 다음 고체인 강옥과 가스 사이에는 Al 2 야 ,s, ----+ 2A(g> + 30(g> 가 성립되고 log K eq = 2log P ,11 + 3lo g?i。 -log aA 1203 가된다. 순수한 결정질 강옥의 활동도는 일정하기 때문에 log K eq =Z log P A,+3 lo g Po 로 쓸 수 있다. 열역학 자료에 의하여 다양한 온도에서 lo g Ke q가 계산될 수 있다(그립 1-7). 물론 강옥에 대해서도 lo gKe q값을 계산할 수 있다. 이같은 열역학적 계산에 의하여 얻어진 각종 원소나 화합물이 응축한 결과가 그립 1-8 이다. 이 그림에서 가장 고온에서 응축하는 것은 Os, Re, Al, Ca, Ti 등이다 . 이같은 물질이 포함된 Ca-Al 이 많이 함유된 포유물 (CAI) 이 1969 년 떨어진 알렌드 (Allende) 운석 중에서 발견되었다. 이 모델을 이용하면 감람석 (M g 2S iQ 4), 금속철 등은 1350 °K 정도 고온에 서 응축된다. 알칼리 장석은 1100 °K 에서 응축되며 Tl, Bi, In 과 같은 휘발성이 높은 원소는 450°K 정도에서 응축됨을 알 수 있다.
 _45 47495153
_45 47495153
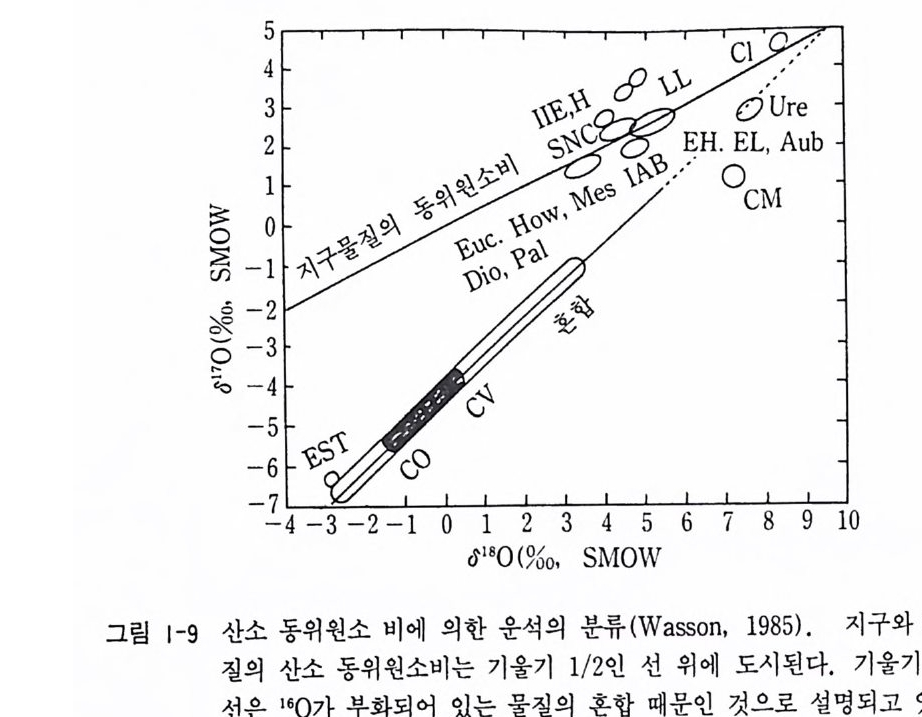
(3) 불균질한 운석 여러 행성 물질의 산소 동위원소 성분을 보면 지구는 C2 콘드라이트 나 C3 콘드라이트와는 현저히 다른 성분을 나타낸다. 지구와 달의 물질 의 산소 동위원소비 0180-0110 그립에서 기울기가 1/2 인 질량 의존성 분별을 나타내지만 C2 콘드라이트와 C3 콘드라이트의 고온 광물(감람석, 휘석 콘드률)은 기울기 1 의 직선을 나타내 질량 분별 과정을 나타내지 않 는다. 그러나 C2 콘드라이트의 기질 광물은 지구 물질과는 다른 기울기 1/2 의 직선을 나타내고 있다(그림 1-9). 이와 같은 산소 안정 동위원소비의 차이는 첫째, 동위원소 분별 과정, 둘째, 혼합, 셋째, 우주선과의 반응 등으로부터 생길 수 있다. 그림에서 기울기 1 의 직선은 지구물질과 다른 동위원소 성분을 가지는 두 성분의 혼합선이다. 하나의 단성분은 지구 물질의 기울기와 교차하는 점을 나타 내는 180 이 결핍된 성분 A 이고 또 다른 단성분은 180 이 많은 B 이다. A
 O 응축된 원소의 비율
O 응축된 원소의 비율
단성분은 C3 운석 중의 멜리라이트 (mel ilit e) 의 값이고 B 단성분은 스피 넬과 휘석의 값이다. Ca-Al 이 많이 함유된 포유물이 혼합선에 나타난다 (Clay ton 등, 1973). 이를 연장하면 순수한 막)에 이른다. 순수한 180 는 초신성이 폭발할 때 형성된 것이다. 그렇다면 Ca-Al 이 많이 함유된 포 유물은 성간 입자 내에 초신성 폭발에서 생성된 것으로 산소가 포함되었 다는 야야기가 된다. 소멸 핵종인 26Al 에서 생성된 26M g이 포유물 속에 다량 발견된 사실에서 핵융합 반응 직후에 태양계 성운 (solar nebula) 이 형성된 사실을 알 수 있다. 26Al 역시 탄소 핵융합 반응에서 생성된 것 으로 태양계 성운의 시대 결정에 중요한 자료가 되고 있다.
 층 :5 I 二:三u ;eub
층 :5 I 二:三u ;eub
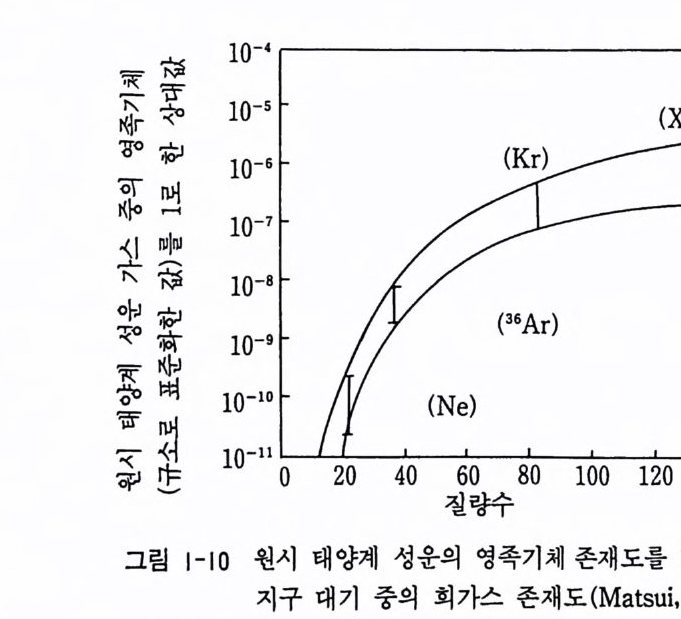
1-5 원시 지구의 화학적 특징 원시 지구는 가스와 먼지로 구성된 원판상의 성간운이 회전할 때 중력 에 의해 미립자가 운동 충돌함으로써 생성된 것으로 생각하고 있다. 즉 미립자가 저온에서 천천히 집적되어 행성이 형성되었다는 저온설과 직경 수 km 정도의 미행성 (~10 1 5k g)이 충돌과 집적을 반복하여 커다란 행성 을 형성하였다는 미행성설이 있다. 수치 시뮬레이션에 의하면 106~108 년 정도의 짧은 시간에 미행성이 충돌하여 지구가 만들어지게 된다. 지 구 표면에는 충돌할 때의 열에너지와 CO2 에 의한 온실 효과에 의해 마 그마 오션 (ma g ma ocean) 이 형성된 것으로 생각하고 있다. 이때 원시 태 양계는 주로 H2, He 으로 된 가스로 포획되어 1 차 원시 지구 대기가 만 들어지계 된다. 이때 존재하던 105~106 Pa 정도의 대기압울 가지는 1 차 원시 대기는 T- 타우리 (Tauri) 시기의 강한 태양풍에 의하여 태양 형성 후 10 년이 지난 기간 동안에 다 없어지게 된다. 오늘날의 지구 대기는 T- 타우리 시기 이후에 지구 내부에서 탈 가스 (de g as) 되어 형성된 2 차 대기이다. (1) 원시 대기의 성분 오늘날의 지구 대기는 지구 형성 초기에 형성된 1 차 대기가 아니고 지 구 형성 후 지구 내부에서 탈 가스되어 형성된 2 차 대기이다. 왜냐하면 원시 태양계의 영족기체와 지구 대기 중의 영족기체의 존재도의 비교에 서 성분이 현저히 다르기 때문이다(그림 1-10). 그리고 현재의 대기의 “Ar/36Ar 츠 295.5 와 상부 맨틀의 “Ar/36Ar= 20000 을 비교해 보면 초기에 36Ar 이 탈 가스된 것임을 알 수 있다. 40Ar 은 K 이 방사성 붕괴하여 생성된 것으로 시간이 지남에 따라 증가하여 맨틀의 40Ar/a6Ar 의 값은 크고 초기 에 탈 가스된 대 기 중의 40Ar/a6Ar 의
값은 작기 때문이다. 성간 가스나 먼지에서 지구가 집적될 당시에 포획되어 있던 H2, He 과 마그마 오션에서 탈 가스된 기체는 T- 타우리 시기에 모두 태양풍에 의 해 없어졌다. 세계에서 최고기의 퇴적암의 연령이 3.8X109 년인 점을 고 려하면 마그마 오션이 고화되는 데에는 4-5 억 년이 걸린 것으로 추정된 다. 마그마 오션이 냉각되어 1400°K 정도가 되어 금속철, 산화철, 석 영, 자철석, 감람석 광물 등이 정출될 때 고온에서 방출된 기체와 화학 평형에 있었다고 가정하면 3Fe+ 和근 3Fe0 0.1) 3FeS i O 곱iD 2 ~ Fe3Q 4 + 3Si0 2 0 . 2) 2Fe2SiQ 4 (ss) ~ 2Fe(s) +2FeSi0 3 (ss) +02(g) (1.3) 등의 식으로 표현할 수 있다 (Ma ts uo, 1989). 이 식에서 /s02/ftt 2s, fco2 /
 10410S
10410S
fc。, fCH4 / fc o2 , fo2 등이 각각 계산된다(표 1-6). 여기서 ss 는 고용체, s 는 고체, g는 가스를 의미한다. (1. 3) 식에서 fo 2 를 열역학적으로는 계산할 수 없다. 그러나 다음과 같이 fo 2 를 계산할 수 있다. (1. 3) 식에서 평형상수는 Kp = a 2 Fe • a 2F eSl03 • f야 aFeSJO , 가 된다. 여기서 a 는 활동도, f는 퓨가시티이다. K흡 lo, 가 되어 1400 ° K 에서 KP 값에서 lo, 는 1 x 10-12Pa 가 계산된다 (Ma ts uo, 1989). 이 lo, 값 은 마그마 오션에서 탈 가스되는 기체의 산화 환원 상태를 콘트롤하게 된다. 죽
H2 0 :;=== 比+-½o 2, CO2 :;=== CO+ 伊 2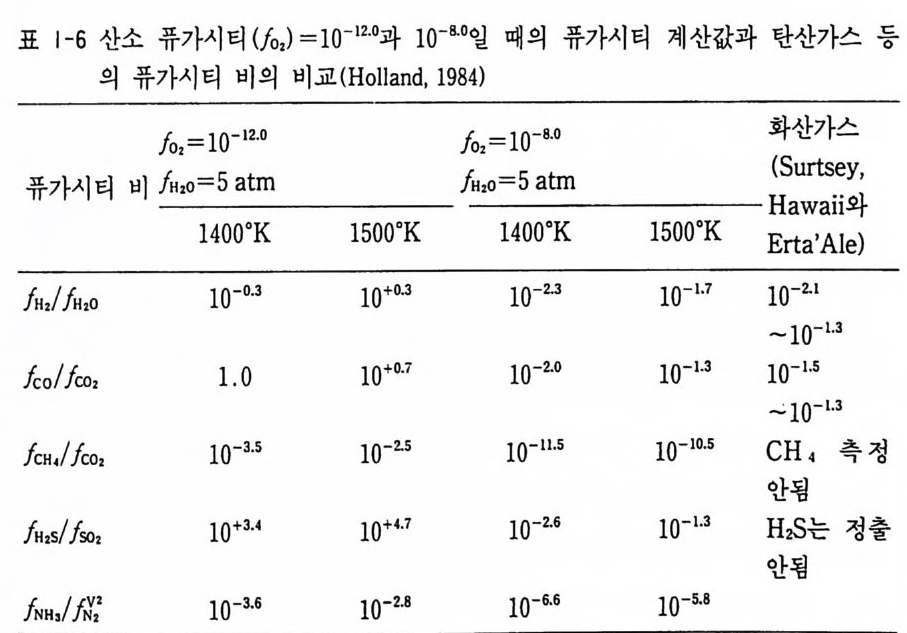 표 |-6 산소 퓨가시티 (/o,) =10 - 1 2. 0 과 10 - s. o 일 때의 퓨가시티 계산값과 탄산가스 등
표 |-6 산소 퓨가시티 (/o,) =10 - 1 2. 0 과 10 - s. o 일 때의 퓨가시티 계산값과 탄산가스 등
두 반응식 에 서 140 『 K에 서 평 형 상수와 /02 에 서 각각 A,2/ IH :::::: 4 x 102 Pa 및 fc。 //co 츤 8Xl02Pa 가 결정된다. 그러나 마그마 오션 표충에서 금속 철이 침강하여 없어지고 난 후의 마그마 오션의 /02 를 결정하는 반응은 2Fe30 ◄ + 3Si0 2 :;:== 3Fe2Si0 4 + 02 가 되어 소위 FMQ 버퍼로 지배될 때 l400K 에서 평형상수는 2X 1 0- 10 이 된다. 즉
?3 F e2SIO4 冷 =2 X 10-io a-Fe30, • a-S 10 2 가 된다. aFesO ◄ 와 SI02 는 각각 1 이고 aFe 2 SIO, 를 0.1 로 하면 lo,= 2 X 10-10 Pa 가 되 어 IH J IH2o 와 le 。/fc o2 는 각각 약 10-3 이 된다. 이상에서 마그마 오션에 금속철이 존재하는가에 따라 가스의 성분이 영향을 받게 됨을 알 수 있다. 금속철이 침강해 버린 후 탈 가스된 기체 의 양은 H20>H2, CO2>CO 가 된다. 같은 식의 계산에서 C02~ C H47)- 얻어진다. 조암광물의 정출이 시작될 때 마그마 오션과 화학평형에 있던 대기의 성분의 함량은 H20>C02>HCl>S02~N2>H2>CO 순으로 추정된다 (Mats u o, 1989) . 초기 지구 대기의 성분은 H20, H2, CH ◄, NH3, CO2 등과 같이 환원 형 대기였다. 이때 태양의 자의선이 지구 표층부까지 도달하여 H20 一 H2+0 로 수증기가 광분해되어 수소는 대기권으로 사라지고 자유 산소 원자가 산소분자 (0+0=02) 를형성하고 02+0--0a 과정에서 오존이 형성되어 지구 상층부에 오존층이 형성된다. 태양 자의선이 이 오존층에 의해 홉수되고 에너지만 지구 표면에 도달하게 되어 지표에는 에너지를 이용한 광합성 과정이 일어나 대량의 식물이 출현하게 된다. 이와 함께 지구의 대기는 환원형 대기에서 산화형 대기로 변화되어 오늘날과 같은 산화형 대기의 성분으로 변하게 된다. (2) 원시 바다의 형성 세계의 최고기의 암석은 서부 오스트레일리아의 규암충의 저어콘 연령 으로 4.1~4. 2 X1 0 년이며 그린란드의 이수아(l sua) 지방의 퇴적변성암의 절대연령이 3.8 X l09 년으로 알려져 있어 이미 3.8 X 109 년 전에 바다가 형성되어 있었음을 알 수 있다. 해양의 형성 조건은 첫째, 마그마 오션이 냉각되어 지표의 온도가 물 의 임계 온도인 647 °K 이하여야 하고 둘째, 647 °K 에서 H20 가 액상이 되기 위해서는 수증기압이 물의 임계압력인 2.21x107Pa 보다 커야 한다 (Mats u o, 1989) . 초기의 해양은 고온의 바다였을 것이다. 고온의 해양이 되려면 적어도 1.1 X 1 021 k g의 수증기가 대기 중으로 없어져야 한다. 아 양은 지구 전체 물의 총량의 1/2 정도에 해당되는 양이다. 지표면의 온도가 647°K 까지 낮아질 시기에 지구상의 물의 전량인 2.04Xl021 k g의 물이 기화되었다면 그때의 수증기압은 2.21Xl07Pa 이 된다. 이 압력을 제의한 수증기가 응축하여 물이 되었다고 가정하면 뜨 거운 원시 바닷물의 양은 0.9 3 Xl021 k g이 된다. 이 양은 현재의 해수와 빙하를 포함한 양 0.40X1021 k g)의 약 66 % 에 해당된다. 뜨거운 원시 바 다는 HCl 이 용해되어 있어 약산성이었으나 규산염 광물 +H+= =드고령 토+점토 광물에서의 반응처럼 해수가 해저의 암석과 상호 반응하여 중 화되었을 것으로 본다. 중화된 NaCl 로 구성된 해수는 온도가 저하됨에 따라 S02, CO2 의 용해 량이 증가하여 다음과 감은
3H2S03 一 2H2S04 + S + H20 4H2S03 一 3H2S04+H2S 산화 환원 반응에 의해 S 나 so~- 가 생성되고 해수의 증발에 의하여 해 수의 Ca2+ 와 so~- 가 결합하여 무수석고 (Caso ◄) 와 석고 (Caso ◄ • 2H20) 를 침전시키게 된다. 그리고 해수의 Ca2+ 와 H2C03 가 CaC03 로, Fe” 와 HC03 에서 FeC03 등을 침전시키게 되었다 (Ma t suo , 1989). Hanks 와 Anderson(1969), Sk i nner 와 Pa rt er(l987) 에 의하여 얻어진 3 . 6-4 . 6 억 년 의 지온 구배를 보면 선캄브리아 초기에는 지구 내부의 온도가 높았다. 그리고 30 억 년전의 해수온은 Knau th와 Lowe (l 978) 의 처트의 0180 값에 서 75~110°C 정도가 얻어져 역시 따뜻한 해수로 추정되었다. 점차 해수온이 낮아지면서 시생대 시기의 그린란드의 이수아 지방의 호상 철광충 (35-38 억 년)의 황화 광물의 o36S=+O.5~o.9%0, 아프리카 의 남부 스와질란드의 중정 석 (32 억 년) 의 o34S= + 1. 7 %0, 황철석 -3 %。 로 모두 O%o 에 가까운 값을 가지던 황 동위원소값이 변화되기 시작하게 된다. 이는 황 환원 박테리아의 작용 때문으로 보인다. 또 이때 대량의 호상 철광충 (banded iro n fo rma ti on) 이 바다에 퇴적된다. Fe2+ 가 Fe3+ 로 다음과 감은 산화 반응에 의하여 Fe2++H+ +靜 0 一 Fe3++H20 가 된다. Fe3+ 는 Fe(OH)3 로 침전된다. 이때 대량의 산소가 생성되면서 대기 중에 오존층을 형성하게 되어 지구 표면이 생물이 존재할 수 있는 환경으로 변화하게 된다.
제 2 장 굉물 열역학 지질 현상은 온도, 압력, 에너지, 암석 광물의 구성 성분 사이에 열역 학적 평형이 이루어지는 쪽으로 진행된다. 많은 지질학적 과정은 열과 일, 진행 방향 사이에 일어나는 열역학적 평형 과정이다. 지구화학 시스 템의 열역학적 평형에서 지구 물질의 거동과 상호 반응, 물질이 형성될 때의 물리화학적 조건 등의 많은 지구화학적 문제를 정량적으로 풀 수 있게 된다. 이 장에서는 열역학 법칙, 엔트로피, 자유에너지, 화학 퍼텐셜, G-x 다이어그램, T-x 다이어그램, 화학반응속도론 등을 다루고 그의 응용 으로 지질온도계와 지질압력계를 설명한다. 지구화학 시스템은 동적 시스템 (dy na m ic sys t e m ) 으로 성분이 시공간상 에서 변화하는 비가역 변화이다. 이런 비가역 변화를 지구화학적 진화 (ge ochem ica l evoluti on ) 라 한다.
2-1 열역학 시스템 열역학(th ermod y nam i cs) 은 자연계의 물질의 조합과 그 물질의 형성 조 건을 추정하는 데 유용한 수단이 되고 있다. Eskola0920) 는 임의의 온 도와 압력 조건에서 평형상태에 있는 변성암의 광물 조합을 추정하는 데 화학 열역학을 이용하였다. 마그마에서 냉각되어 화성암을 형성할 때 광 물 사이에는 화학평형이 이루어진다. 변성암은 특정한 온도, 압력에서 변성 광물들이 안정하게 평형상태에 이르게 된다. 열역학의 원리 를 이들 암석에 적용하면 화성암의 결정사(結晶史)와 변성작용에 의하여 변성암 이 형성될 때의 온도와 압력 등의 변성 환경을 해석할 수 있게 된다. 물론 열역학은 화학평형 상태에 있는 경우에만 유용한 정보를 주게 되 며 반웅의 중간 과정이나 준안정 상태의 정보를 주지는 않는다. 수용액, 가스, 광물, 이온 등의 열역학적 성질이 얻어지게 되어 이들 에 의해 구성된 암석이나 광물 등의 온도와 압력에 따른 구성 원소나 이 온의 분포, 거동 등이 이 열역학적 방법으로 설명되게 되었다. 광물 열역학을 공부하기 위해서는 먼저 계 (s y s t em) 를 정의하지 않을 수 없다. 계(系)라는 것은 우리가 대상으로 하고 있는 원자, 분자, 광 물, 암석이 될 수 있다. 또한 암석 전체의 노두가 될 수 있고 하나의 광 물이 계 가 될 수 있다. 계 를 둘러 싸고 있는 부분을 주위 (surroundin g ) 라 고 한다. 계 안에서 일어나는 변화는 주위 물질과 반응을 할 수도 있고 하지 않을 수도 있다. 계는 주위에서 에너지와 물질이 유입되는가에 따 라 개 방계 (op en sys t e m ) , 폐 쇄 계 (closed sys t e m ) , 고립 계 (iso late d sys t e m ) 로 세분할 수 있다. 예를 들면 석회암과 화강암이 접촉하고 있을 때, 화강암체가 주위의 석회암에 에너지와 물질의 교대를 일으키는 일을 하여 스카론 광물이 형 성될 때 개방계가 된다. 그리고 폐쇄계 조건이 되면 주위의 석회암에 물 질의 이동은 일어나지 않고 마그마의 뜨거운 에너지만 전달됨으로써 재
결정 작용이 일어나 대리암이 될 수 있다. 고립계는 물질과 에너지의 교 환이 일어나지 않는 상태로 접촉부에 아무런 광물학적 변화가 일어나지 않게 된다. 이때에 열역학적으로는 열평형 상태로 가게 된다. 열역학에 이용되는 상태량은 온도, 압력, 밀도, 굴절률과 갇이 계 안의 물질의 양 에 관계 하지 않는 시 강성 상태 량 (int e n siv e pro p er ty ) 과 체 적 , 질 량, 내 부 에너지, 엔탈피, 엔트로피 등과 같이 물질의 양에 관계하는 시량성 상태 량 (ex t ens i ve p ro p e rty)이 있다. 에너지는 두 가지 성질의 상태량을 가지 고 있다. 열역학적으로 상태 A 에서 상태 B 로 변화할 때 계 안에서는 열 의 출입이 일어나고 일을 하게 된다. 2-2 열역학 제 1 법칙과 엔탈피 계의 열역학적 상태 A 에서 상태 B 로 변화될 때 계에 출입하는 열 Q 와 한 일 W 의 합은 일정하다. 죽 내부에너지의 변화 (LlE=Ea-EA)= 열(Q)+일 (W) 이 된다. 이를 에너지 보존의 법칙 또는 열역학 제 1 법칙 이라 하며 LlE=Q -W 로 표현할 수 있고 W=PL J V 이므로 LlE=Q _PL1V 로 표현할 수도 있다. 2s·c, 1 기압에서 아라고나이트가 방해석 으로 상전이할 때 59 ca l/ mo! 의 홉열반웅으로 체적이 2.78 cm3/mol 이 변화하기 때문에 내부에너지의 변화 (LlU) 는 위 식을 이용하여 계산하면 58.933 ca l/ mo! 이 얻어진다. 같은 방법으로 25°C, 1 기압에서 흑연과 다이아몬드의 동질이상에서 상전이할 때 내부에너지의 변화는 453.046ca l/ mo! 이 얻어져 아라고나이 트에서 방해석으로 상전이하는 경우보다 흑연에서 다이아몬드로 상전이 할 때 400cal/ mo ! 정도 더 많은 에너지가 필요함을 알 수 있다. 따라서 자연계에서 방해석은 가끔 아라고나이트의 가상(p seudomo rp h) 으로 산출 되지만 흑연과 다이아몬드 사이에 가상은 발견되지 않는다. 내부에너지
는 체적이 변화되지 않는 반응에서 유용하며 이때 내부에너지의 변화가 바로 열류량이 된다. 죽 LlE= Q가 된다. 그러나 대부분의 화학 반응이 나 상전이는 압력이 일정한 계에서 일어나기 때문에 엔탈피 (enth a lpy , H) 라고 하는 또 다른 함수 H= U+PV 를 도입하여 LlH= U+LlE+PLlW + VL J P 라는 식을 얻게 되며 열역학 제 1 법칙을 여기에 적용하면 LlH= LJQ+ VL J P 가 얻어진다. 압력이 일정할 때에는 LlH= L]Qp =CP LJ T 가 된 다. 여기서 G 는 정압 비열이다. 정압일 때에는 엔탈피의 변화 4H 가 흡수된 열량과 같기 때문에 엔탈피는 열 함량과 같게 된다. 정압일 경우 반응열이 발생하여 상태 A 에서 상태 B 로의 반응이 일어날 때 엔탈피의 변화는 LlH=HA-HB 이다. 4H 와 L]Qp의 값이 부(―) 인 과정을 발열 과 정 (exoth e rm ic pro cess) 이 라 하고 정 ( + ) 인 경 우를 홉열 과정 (endoth e rmi c pro cess) 이 라 한다. 예를 들면 실험적으로는 어렵지만 이론적으로 25·c, 1 기압에서 1 몰의 흑연이 1 몰의 다이아몬드로 변할 때 452cal 의 열이 필요하게 된다. 즉 C( 흑연) +02 ~ CO2(L1H=-94052 cal) (2.1) C( 다이아몬드) +02 ~ C02(L1H=— 9 4504 cal) (2.2) 일 때 (2.2) 식에C서( 흑 연(2). 1=) =식 C을( 다빼이면아 몬드) (L1H=452 cal) 가 얻어진다. 2-3 열역학 제 2 법칙과 엔트로피 열역학 제 2 법칙은 자연계에서 일어나는 현상의 방향을 경험적으로 적 용한 원리로 〈엔트로피 증대의 법칙〉을 의미한다. 즉 임의의 등온 변화 에 대한 Q/T 라는 양을 생각해 보면 바가역으로 변화가 일어날 때 Qre v
가 최대가 되므로 비가역 변화일 때는 編T > 요T 가 되며 가역 변화일 때는 編T= QT 가 된다. 엔트로피의 변화량 (4S) 도 마찬가지로 4S= 編T 로 정의할 수 있다. 바가역 과정에서 엔트로피는 반드시 증대한다. 즉 LlS > 유 이다 . 이갇은 열역학 제 2 법칙을 수식화하기 위하여 Claus i us (1 865) 는 엔트로피라는 상태량을 도입하였다. 계의 온도가 h 에서 h 로 변화할 때 엔트로피의 변화를 다음과 같이 계 산할 수 있다. 위 식에서 엔트로피의 변화는 dS= 辛dT 로 표현할 수 있다. 압력이 일정할 때 Qp=LJH 이므로 dH= TdS 가 된 다. 정압 비열 c p=dH評 로 정의되므로
dS = 유 dT 로 표현할 수 있다. 온도 h 에서 t 2 까지 적분식으로 쓰면 4S=1홉 dT 가 되어 4S 를 계산할 수 있다. 절대 영도에서는 고체의 모든 열운동이 정지되어 격자의 전동이나 원 자 운동에 의한 무질서는 일어날 수 없다. 완전한 결정의 절 대 영도에서 의 엔트로피는 0 아다. 이것이 열역학 제 3 법칙이다. 따라서 순수한 결정 질 물질의 엔트로피는 So(O °K) = O 이라는 가정에서 열 함량을 측정하여 직접 그 값을 얻을 수 있다. Ro~ i e 와 Waldbaum (19 68) 은 지 질학에 유용한 많은 결정 질 상에 대 하 여 298. 15 °K 와 더 높은 온도에서 엔트로피의 값을 계산하여 표 를 만들 어 놓았다(표 2-1 과 부록 참조). 계에서의 무질서도는 고체, 액체, 기체 에서의 원자와 분자의 진동 • 회전운동에 따른 열적 무질서 (the rmal dis o rder) 와 엔트로피 의 혼합 (mixi n g of entr o p y) 의 관점 에 서 정 량적 으로 다룰 수 있다. 예를 들면 감람석 고용체 (M g x Fe1- x ) 2 S i 0 4 에서 M g와 Fe 의 혼합이 일어나 순수한 단성분에서 존재하지 않는 본질적인 무질서 를 일으킨다. 자연계의 많은 광물이 복합 고용체이기 때문에 암석에서의 엔 트로피 혼합이 대 단히 중요하다. 엔트로피의 압력에 의한 변화도는 L1S=S2— S1 =- R In 융 식에서 계산할 수 있다. 이 식에서 S1 과 요는 각각 압력 R 과 R 에 있어 서의 엔트로피 값이다. 일반적으로 단위질량당 체적이 크면 무질서도도 크게 된다. 죽 동질이상 사이에 체적의 차가 크면 클수록 엔트로피의 차
도 커진다. 또 광물의 체적이 크면 엔트로피가 크다고 할 수 있다. 만일 광물에 압력을 가하면 체적이 감소하여 엔트로피는 감소한다. 물론 광물 에서는 화학 성분, 결정구조, 고용체의 정도, 결합 유형 등에 따라서도 엔트로피 값이 변화된다. 2-4 Gib b s 자유에 너 지 열역학 제 1 법칙 LlE= Q -W 에 열역학 제 2 법칙울 대입하고 계에서 한 일이 압력과 온도에서 체적 변화의 일을 한 것으로 가정하면 LlE= TLJ S — P4 V 식을 얻을 수 있다. 이 석을 엔탈피의 형태로 변형하면 LlE + PLl V+ VLlP=LlH= TLlS-PLl V+ PLl V+ VLJ P = TLJ S + VLJ P 가된다. 이 식에서처럼 엔탈피는 압력과 엔트로피의 값이 변화되는 계의 연구 에 유용하다. 만일 온도와 체적이 변화하는 계를 필요로 할 때는 헬름홀 츠(H elmbol t z) 함수 (A= U-TS) 가 유용하다. 여기서 4A=_S4T— PL J V 가 얻어진다. 지질학에 이용되는 대부분의 화학 반응 현상은 압력과 온 도가 변화하는 조건에서 다루어진다• 따라서 이를 위해 Gibb s 함수가 도입되었다. Gibb s 자유에 너 지는
G= U+PV-TS=H— TS =Q -W +PL1V-TL1S 로 표현되고 이를 미분하면, dG= VdP-SdT, 그리고 4G= V4P_S4T 관계가 얻어진다. 임의의 화학 반응식에서 반응 자유에너지의 변화 (L1G) 는 위 식의 4H, 4S 에서 계산될 수 있다. 예를 들면 석회암과 화강암의 접촉대에서 접촉변성작용에 의하여 규회 석과 갇은 스카른 광물이 형성될 때 각 온도에 따라 4G 값을 계산할 수 있다. CaC03 (방해 석 ) +S i0 2 (석 영 ) 혹쁜 :CaS i 02 (규회 석 ) +C O2 (가스) 25•c1 1 기압에서 4G=4H— T4 S 식에서 LJ G=+10034cal 가 계산된 다. 650°K 에서는 f650K dH=f 650K Gd?, f650K dS=f 650K 유 dT 298. !S'K J 298. JS' K • J 298. IS' K J 298. JS'K 를 계산하면 4G6500K 값이 LJ G=,::O 으로 계산된다. 여기서 L1G= Q-TL 1S, L1S= 유 식을 참고하면 LJG =Q -Qre v 이다. 가역 변화일 때 Q=Q rev 가 되어 LJ G=O 이 되고, 비가역 변화일
때는 Q< Qre v , LJ G < O 이 된다. 즉 LJ G=O 일 때는 위의 반응이 평형으로 암석 시료 내에 방해석 + 석영 +규회석 광물상이 공존하게 된다. LJ G
2- 5 화학 퍼텐셜, 퓨가시티, 활동도와 표준상태 암석의 화학 변화의 방향을 결정하기 위하여 암석 구성 성분들의 화학 퍼텐셜(µ,)의 개념을 도입할 필요가 있다. 전기적 퍼텐셜이나 중력 퍼텐 셜과 같이 계의 서로 다론 부분의 성분의 µ 2 를 측정하여 물질의 이동이 나 반응의 경향을 추정할 수 있다. 화학 퍼텐셜은 G 값을 n, 에 대하여 편미분한 값으로 µ, = (훑 )P , T, nJ 식으로 표현된다. 여기서 1 1 i 는 i종 이의의 성분, P 는 압력, T 는 온도 를 의미하며 이들 값이 일정한 조건일 때 자유에너지의 부분 몰량을 화 학 퍼텐셜이라 한다 . i 종의 성분으로 구성된 계의 자유에너지는 LlG101 a1 =~n#,로 표현된다. 죽 감람석 고용체의 경우에 Mg 2S i 0 4 n , 몰과 Fe2 S i O ◄ n2 몰로 구성되었을 때 자유에너지는 Gto t a 1 = n1µ ~ k ,o . + n2µ f ~s1 0. 가 된다. 공존 광물상의 화학 퍼텐셜이 같을 때 각 광물은 평형에 있게 된다. 예를 들면 방해석과 아라고나이트의 동질이상의 광물에서 d ~co 3 = 站臨 (Llµ=O) 이면 평형상태에 있음을 의미한다. 이상기체의 상태방정식은 PV=n R T 이다. 이상기체들의 혼합으로 된 기체일 경우에는 이들 이상기체 중의 기체 i의 화학 퍼텐셜은 µi= µ~+RTlnPi
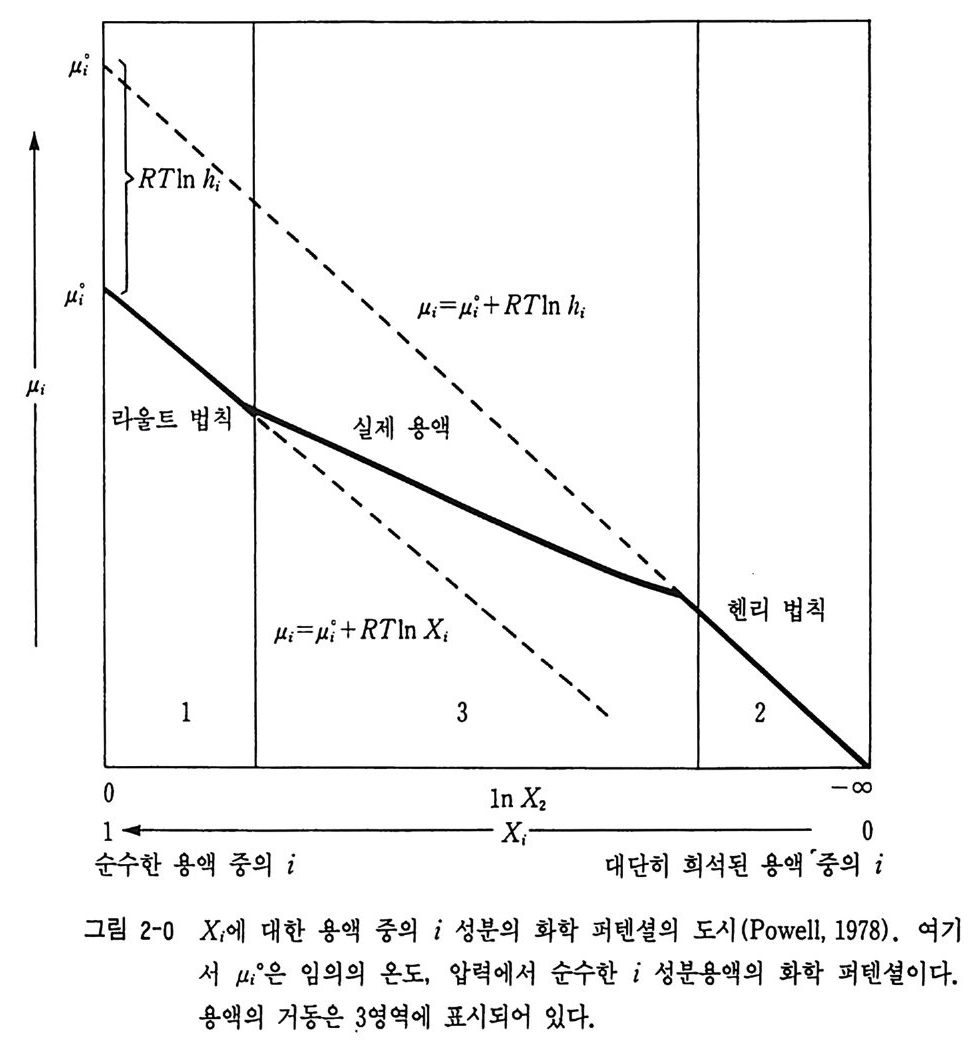
로 표시할 수 있다. 여기서 µi는 표준압력에서 혼합 기체 중의 기체 i의 화학 퍼텐셜이며 E 는 기체 i의 분압이다. 그러나 비이상기체일 경우에 화학 퍼텐셜은 µ;=µ1+RTI 내 로 표현할 수 있다. f,는 기 체 i의 퓨가시 티 (fuga ci ty) 이 며 I10 은 온도 T 에 서 의 표준압력 의 성분 i의 퓨가시티이다. 퓨가시티 (/)와 이상기체의 분압 사이에는 /.-= r i P, 이다. r, 는 퓨가시티 계수이며 이상기체일 경우에는 r i =l 이다. 용액 과 평형에 있는 기체의 경우에는 이상용액에서는 기체 중의 성분 i의 분 압 P i =X, 이다. 여기서 X는 용액 중의 i의 몰분율이다. 이 관계를 라 울 (Raoul t)의 법칙이라 한다. 이와 갇이 용매 A 에 비휘발성 물질 B 를 녹이면 그 증기압은 내려간다. 이때 용액은 대단히 뭄은 상태이므로 A 의 증기압 저하 비율은 용질 B 의 몰분율 xB 와 같다. 즉 임의의 온도에 서 용매 A의 증기압을 R 라 하고 이 온도에서의 용액의 증기압을 PA 라 하면 라울의 법칙은 (P').-P A) IP'). = Xp 가 된다. 우리가 디루는 지화학 시스템이 용액일 경우에 이상용액 중의 i의 화학 퍼텐셜은 µi=µ 1+RTlnX 로 표현되며 X 는 용액 중의 임의의 성분 i의 몰분율이다. 실제 용액에 서는 용질과 용매 등의 상호 반응으로 위의 관계가 성립되지 않으므로 G. Lew i s 는 활동도 (a) 를 도입하였다. 즉 비이상용액 중의 i의 화학 퍼 텐셜은
µ; =µ ~ + RTin a ; 이다. 여기서 a, 는 성분 i의 활동도이다. X 와의 관계는 a,=r,x, 로서 r j는 활동도계수이며 이상용액 일 경우 r1=1 이다. 용액 중의 a, 와 X, 의 관계는 X값 이 낮은 용액일 때는 a;=knXi 관계가 성립한다. 이 관계를 헨리 (He nry)의 법칙이라 하고 kn 는 헨리 정수라 한다. X 와 µ, 사이의 관계는 그립 2-0 과 같다. 그림에서 보면 실제용액 (real solu ti on) 은 다음 과 같은 특성을 가진다. 성분 i가 용매이면 Xi 는 1 에 가까우며, 성분 i 가 용질이면 X가 대단히 작다. 그리고 X 는 라울의 법칙과 헨리의 법 칙의 중간 특성을 가진다. 용질 B 도 휘발성인 경우에는 PA 는 용액과 평형에 있는 기체 중의 용 매 증기의 분압이다. 여기에 XA+xs=l 을 적용하면 PA=RxA 가 된다. 용액 중의 각 성분이 이같은 라울의 법칙을 따르는 용액을 아상용액 (ide al soluti on ) 이 라 한다. 지구화학에서 열역학 문제를 다룰 때 여러 다른 화합물의 열역학 자료 와 비교하기 위해서는 어떤 한 성분 i(압력 P, 온도 T, 성분 C) 의 화학 퍼텐셜 µj의 기준값을 취하는 것이 편리하다. 계산할 때에 이 µ,값을 표 준상태의 값으로 하면 편리하다. 일반적으로 이 조건은 25°C 와 1 기압 (101. 325 KPa) 이 다. 이 런 조건 에 있는 물질을 표준상태 (sta n dard sta t e ) 에 있다고 한다. 즉 편의상 취한 것으로 최종 결과에는 아무런 영향을 주지 않는다. 열역 학 자료는 lbar, 298 °K, 순수한 성분을 표준상태로 하여 많은 실험 자료가 나와 있다. 2-6 광물 평형과 평형상수 일정한 성분으로 된 광물상들이 평형상태에 있을 때 Gib b s 자유에너
지 값으로부터 평형상수를 계산할 수 있다. 하나 이상의 상의 용액이 화 학평형을 이루고 있을 경우에는 화학 퍼텐셜울 이용하면 편리하다. 예를 들면 반응식이 aA+bB=cC+dD 일 때 평형상수
 µ;
µ;
[A]a_[~] b K= 亢門前- 이다. 위 반응식에서 자유에너지 (G) 는 G = n 也 + 11BµB + nck + 11Dµ D 이며 이들이 평형상태일 때는 4G 尸 (nc/.4 :.+ no 찌 —( 11AµA+ 11B 띠 =O 이다. 또한 등온, 등압 조건에서 비반웅계의 평형 조건은 ~µ;dn;=O 일 때이며 반응계에서는 2I 輝i =O 일 때이다. 여기서 v,는 성분 i의 화학량론 계수 (s t o i ch i ome t r ic coeff i- ci en t)로서 반웅물의 이 값은 부(-)이며 생성물의 값은 정 (+)이 된다. 그리고 화학 퍼텐셜 µi=µ杓 +RTlna i 이다. 이때의 에너지 평형은 4µ=2I l/ i(µ ?+RTlnai) =O 일 때 이루어진다. 다르게 표현하면 2 叫 !+RTlnILar i =O 으로 표현할 수 있다. 여기서 Il;ar i는 활동도의 적이다. 그리고
2v, 짜 = 4G?= _RTlnII,at'. i 관계로 표현할 수 있다. 일정한 온도의 표준상태에서 LJ GO 값은 일정한 값을 가지므로 II,a t'값 역시 일정하게 된다. 이 값이 평형상수 K 이다. 즉
LJG ~= -RT inK 또는 L1G~= -2 . 303RT iog K 이다. 그러면 상평형이 지구화학적으로 어떤 의미를 가지고 있는가를 생 각해 보자. 순수한 이상기체 반응에서의 평형상수는 K= (Pc)C(P訂 (P사 a (PB) b 가 된다. 여기서 P 는 분압을 의미한다. 비이상기체일 때 퓨가시티(/)를 도입하면 K= (fe )C( f記 (/A) a (/s) b 가 된다. 예를 들어 327·c 에서 CO, 02, CO2 가 서로 평형에 있을 때 평 형상수를 계산하고 기체 전압이 1bar 이며 P。 2 가 0.8bar 라고 가정하였을 때 CO 와 co 려 분압을 계산할 수 있다. 이때 이들 기체를 이상기체로 간주하면 327 ·c 에 서 L1G1co. = -94 . 445 kcal mol-1, L1G10.=-39.3 0 8 kcal mol-1, L1G10. =0 .0이다. 이들 기체 사이의 화학평형은 다음 반응식과 감이 co+ 伊 2~C02, K=ex p(궁問)=〈陶 로 표현할 수 있다. 우선 327°C 에서 이 반응식의 LJ GO 값을 계산하면 L1G0 = L1Gf c o2 -LJG fc o —十4 G J O2 =— 55.137 kcal mol-1 가된다. 따라서 Keq= exp ( ) =1.22 X 1020 가 얻어진다. Pco,+Pco+Po,=1 bar 라 가정하였으므로 위 식에서 Pco= l. 833 X l0- 21 bar, Pco,=0 . 2 bar 가 얻어진다. 고체 광물상에서의 평형상수는 일정 성분을 가진 결정질상으로만 구성 된 변성 반응에서 평형상수를 구할 수 있다. 예를들면
3CaAhSi2 0 a;=:=:Ca3AhSb012 + 2AhSiO s + Si0 2 (아놀사이트) (그로슈라) (남정석) (석영) 의 변성 반응식에서 평형상수 (K) 는 a 후(溫:j) 2a:!영 K= (蟲노 )3 이 된다. 여기서 남정석과 석영은 임의의 P, T 에서 순수한 상이므로 일정한 활동도를 가진다. 따라서 K= a 꾸석유슈석라 (蟲노 )3 이 된다. 위의 변성 반응식이 평형에 있을 때 석류석과 사장석의 성분은 쉽게 측정할 수 있으나 측정 성분에서 활동도로 변환은 어렵다. 따라서 분배 계수 (KD) 와 활동도계수 사이의 관계에서 다음과 감이 평형상수를 추정 할수 있다. KD= X 麟 (x: 昆노 )3 Ka=KDKA 여기서 X는 성분의 몰분율이고 Ka 는 활동도계수의 비이며 Ki= I 零A} 꾸석류이슈석트라 ) 3
이다. 분배계수 (KD) 는 온도와 압력의 함수이므로 지질온도계와 지질압 력계로 응용되고 있다. 수용액 이온종 사이의 반응에서의 평형상수 (K) 는
K= (ac)C(aD)d (aA) a(a 이 b 가된다. 예를 들면 알루미늄 수화 반웅인 Alftq > + H20 ~ Al (OH ) 갑q) + Ht aq) 에서 평형상수는 K-aA 1<0H i 2 +a 드 ZAl(OH)2+ YAl(O H )2+ 11ZH• YH ♦ aAIaH2 0 111Ai 3+ /Ai 3+ 1nH20 /H20 가 된다. 여기서 y는 각 이온종의 활동도계수이다. 많은 지구화학적 반응은 광물과 수용액 사이에서 일어난다. 형석의 용 해를 예로 들어 보자. 반응식 CaF2(s) = C 삶굶) + 2F1aq ) 에서 평형상수는 K=acaF~2 가된다. 또 다른 예로 석회암 지역에 분포하고 있는 어느 동 광산 갱내에서 홀 러나온 지 하수에서 공작석 (malachit e) 이 침 전된 경 우를 들어 보자. 이 때 공작석 광물의 침전은 다음과 같은 광물평형 반응식을 생각할 수 있다. 2Cu2++coi- + 20H-1 ~ C112(0H)2COa (공작석)이들이 상온에서 화학평형에 도달하였다면 LJ G0=-46.020cal 가 얻어 진다. 여기서 평형상수 K=l033.7 이 계산된다. 평형상수는 K=[C-u2= (0H 1) 2CQ0 3 ] -33.7 이다. 동 광산이 석회암 지역에 분포하고 있기 때문에 지하수의 p H 는 약 8 정도로 가정할 수 있고 이 조건에서 co~-이 온 농도는 10-6mol/l 로 추 정할 수 있다. 따라서 (Cu 짜= ~=10-313.7 0 -15.7 로 Cu2+ = 1o-1-85mol/ l 로 광산 지하수 중의 구리 (Cu2+ ) 농도를 추정할 수가 있다. 이처럼 Cu2+ 이온이 대단히 미량이라도 공작석 광물이 침전될 수 있다. 이같은 현상 을 광산 갱 내에서 흘러나오는 물의 수로 바닥에서 흔히 관찰할 수 있 다. (1) 공존 광물들의 상평형 경계의 계산 광물들의 표준상태에서의 엔탈피의 값과 엔트로피 값 등의 열역학 자 료를 이용하면 공존 광물쌍의 반응 평형 경계선을 그릴 수 있다. 예를 들어 알바이트, 제이다이트, 석영이 공존할 경우 상평형 경계를 계산하 여 구해 보자. 이들 광물 사이의 반응식은 다음과 같다. NaAlSi3 0 8 == NaAlSi2 0 6 + Si0 2 (알바이트) (제이다이트) (석영)
이들 광물이 모두 순수한 광물상이라고 가정하고 평형상태에 있다면 LJG = µ~~AISI06 + µ~~6 -µ~~AISl30e = 0 이 된다. 죽 L1G = G 교 + Gqz —Ga b = Q 이다. 표 2-1 의 Rob i e 와 Waldbaum0968) 의 열역학적 자료를 이용하여 계산하면 4HL298= 一 375 cal mol-1 이 되고 L1S1. 2 9s=-8.43 cal mol~i d eg -1 가 얻어진다. 앞에서 dG = -L1SdT + L1 VdP 식에서 평형일 경우 dG=O 이다. 따라서 dP L1S dT LJV 식 이 얻 어 진다. 이 식을 클라우지 우스 클라페 이론 (Clausiu s -Clape y r o n) 방정식이라 부르며 임의의 온도 (T) 와 압력 (P) 에서의 반응 경계선의 기 울기가 된다. 죽 4S 와 4V 값에서 기울기가 계산된다. 4CP=0 이라고 가 정하면 1bar 에서의 평형 온도 T 가 다음과 같이 계산된다. L1G=L1H1bar-T L1S1bar=O T=LL11HS ~내= —. 4~32 7c5 a= cl aml 4oml-o14ld-1e g.- 15 °K 반응의 경계선의 기울기는
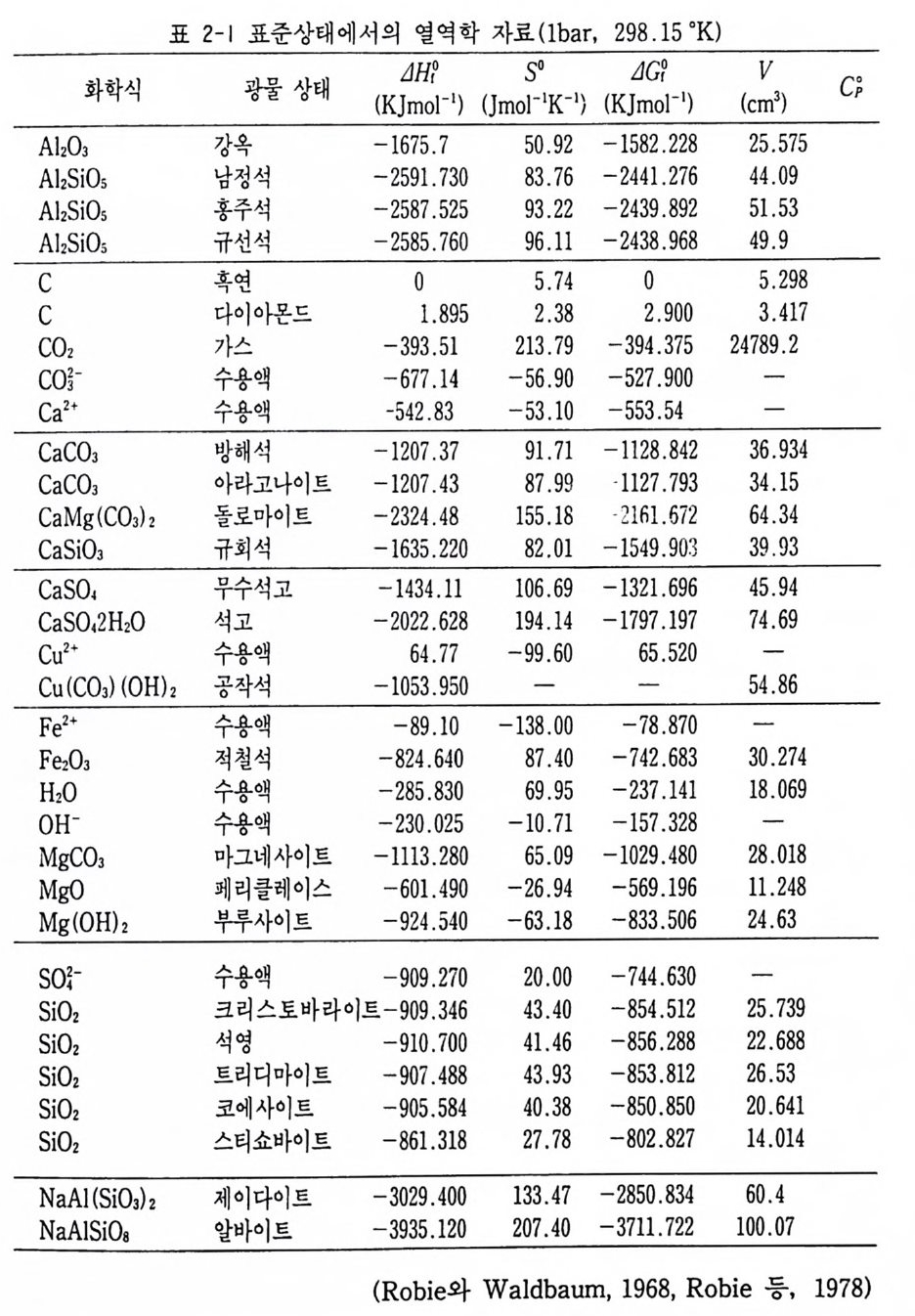 표 2 기 표준상태에서의 열역학 자료 Obar, 298.15 °K)
표 2 기 표준상태에서의 열역학 자료 Obar, 298.15 °K)
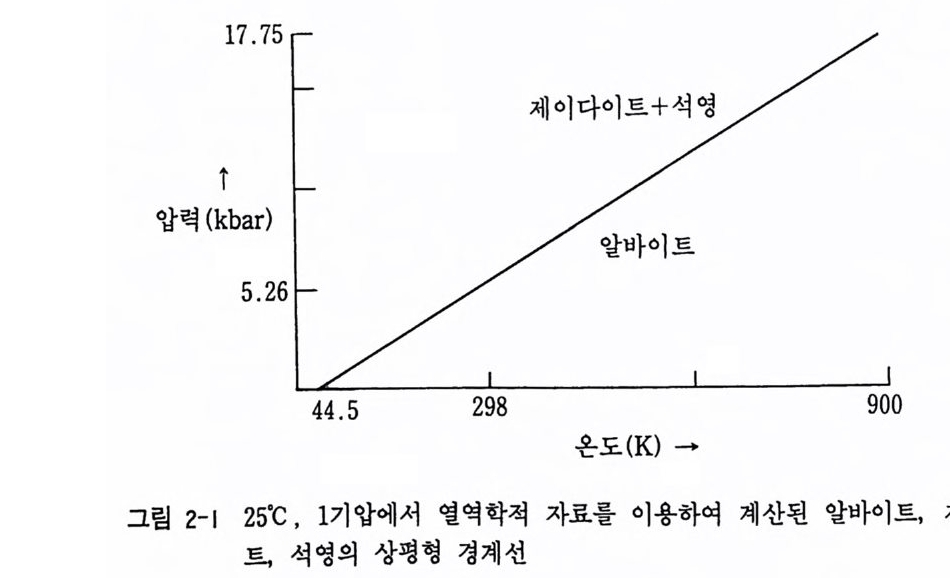
쁘dT= —- .0....... ~4058 c=al mo12-1bar-10 .75 ba r deg - 1 가 된다. 이보다 더 높은 온도에서의 압력 계산은 다음의 ip 1dP= 흙j IT2dT, P 기 =1+ 흠 (T2-T1) 식에서 계산된다. 예를 들면 298 °K 에서 5.26 kbar, 900 °K 에서 17.75 ° kbar 가 각각 얻어진다. (그림 2-1)
 17.75
17.75
그리고 광물상의 안정 영역은 L1G=L1H-TL1S+ (P— l)L J V 식에서 판정할 수 있다. 죽 4S 와 4V의 값이 부(―)이므로 압력이 높아 질 때 LJ G
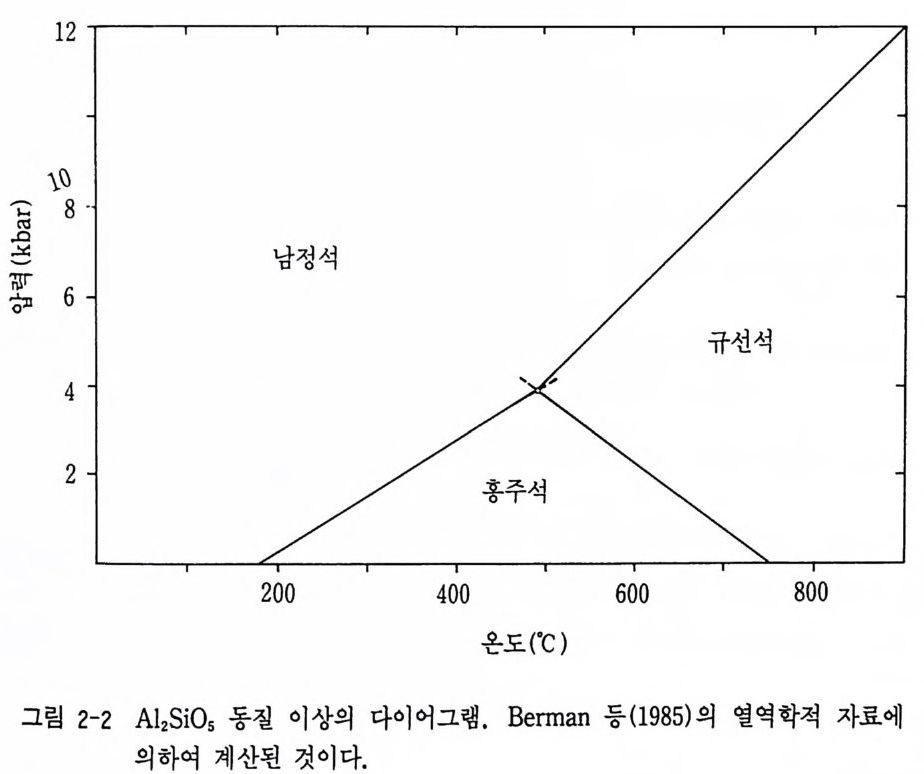
있다. 같은 방법으로 Al2S i 05 의 동질이상인 남정석, 규선석, 홍주석 사 이의 상평형 경계선도 계산으로 그릴 수 있다. 얻어진 결과는· 그림 2-2 와같다.
 12
12
(2) 유체상을 가지는 광물 조합의 상평형 경계선 계산 변성 반응에서 H20( 유체)나 CO2( 유체) 상과 같은 유체상(fl u i d pha se) 울 가지는 반응식에서의 반응 경계선 계산은 성분 광물의 활동도가 고려 되어야 한다. 예를 들면
(마챔8 鬪? ~l 트) = 깁爵레이:)(羅 (2.3) (C방a해C석03) + (S석i0영 2) 一<—_ (C규aS희i석0 )3 + (c유o체2) (2 . 4) 식에서와같이 탈탄산가스 (decarbona ti on) 변성 반응식과 같은 경우이다. 폐쇄계에서 이들 광물들이 공존하면서 평형상태에 있다고 가정하면 t 4$겁 8 서이스 + t{t싫 - u; 益 덟} 이 n =LlG=O 站짧 03 + 瓜區 —函 co3- µ器 2 =LlG =O 이 된다. (2 . 4) 식의 경우만을 예를 들어 반응 경계선의 작성을 설명하여 보자. 활동도와 화학 퍼텐셜 관계에서 µ-!=µ?+ R Tin a 1, 떠 =ex p(덮-『) 와 같이 j상의 광물 중의 i 성분의 화학 퍼텐셜과 활동도를 알 수 있다. 이를 위의 (2. 4) 식의 변성 반응에 적용하면 불 a~Cas0130-, +R TR i nTa~ i ~nCa0 『3 —墨µ g+ , d0b22- +RT R i nTai 蟲n a t=bO 2 ~as10, + 處 這 aCOs- JJ.?. ,02=L1G0= -RTin ( 言~) (2 . 5) 의 관계식을 얻을 수 있다. 이들 광물들이 순수한 광물상으로 구성되어 있다고 가정하면 1bar, 온도 T 의 표준상태에서 다음과 같이 LJ GO 을 계산할 수 있다. 4G f, T=4 庄, T_ T4S 우
LIC p =O 이라 가정하고 표 2-1 의 열역학 자료를 이용하여 900 °K 에서 4Hf9 00 = H젊 + H9 ~앙, _ H9cto - H 9%는 19343 cal 4S 옮。 =35 . 07 cal mol-1deg -1 가 계산된다. 그리고 J4 =µ?+RTln 짜 와
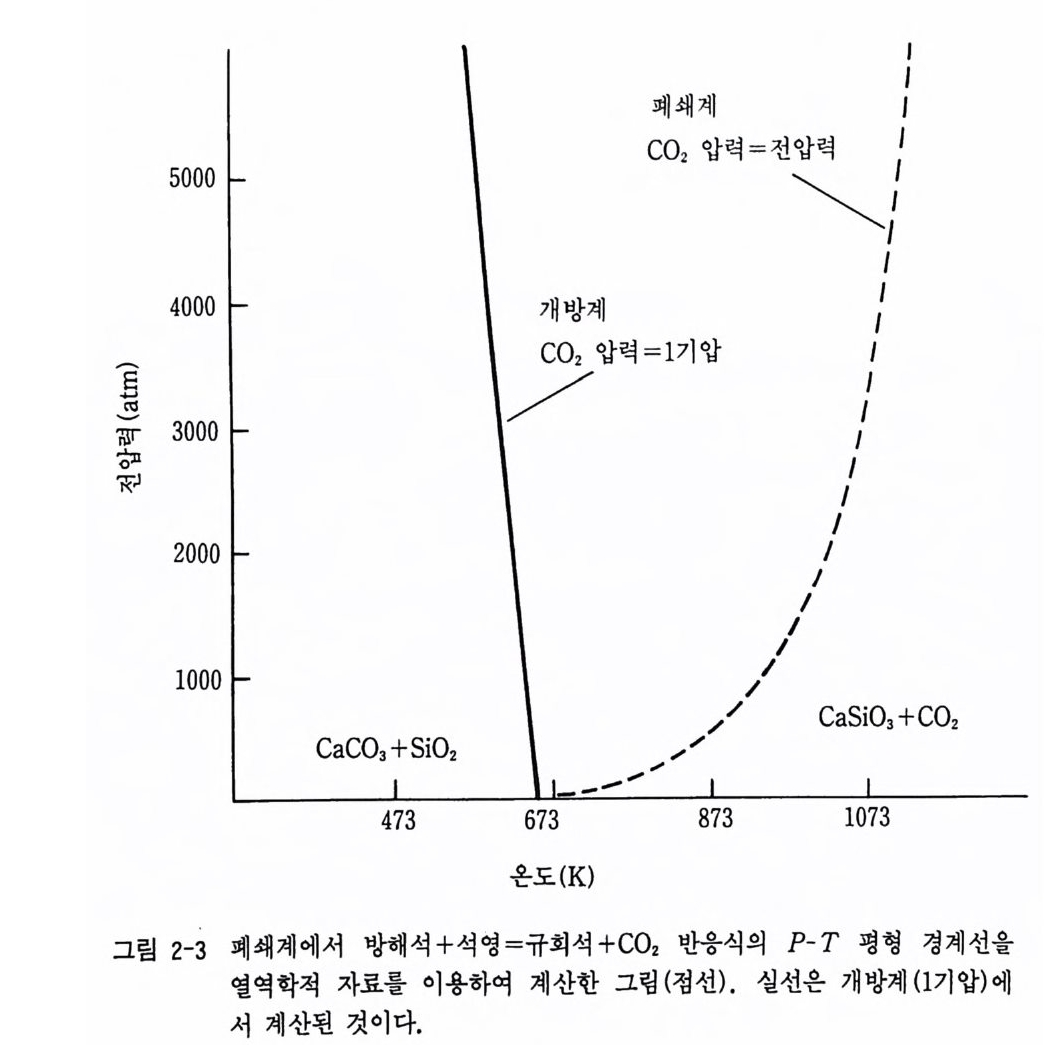
(µ{) p, r=µ?+ JP ½d P l 식에서 RTln 떠= VJ( P-1) 의 관계를 얻을 수 있다. 또한 고체 광물 성분의 활동도는 각각 RT ina gi co .= (P-1) Vee RT i na 쁜~i 103= (P-1) Vwol RT i na 蜀 2= (P 기) Vqz 의 관계가 얻어진다. 여기서 CO2 를 완전 기체라 가정하면 CO2 의 활동도 는 바로 P 와 같게 된다. 위 (2.5) 식에서 4Gf, T =4Hf, T -T4Sf,T == -—RRTT iinn PP ccoo,,--((PP--ll)) (V Vwwo1o+1 -(PV —e e1-) V V .e리e + (P— l) Vqz ( 2.6) 가 얻어진다. L1Vsoud= Vwoi -Vc c-V qz =-19. 69 cm3(-0.47065 cal-1)와 L1Hf 900, L1SP9oo, L1 V 를 (2 . 6) 식 에 대 입 하면 19343— T( 35.07) = -RT inP + (P-1)0. 4 7065 (2 . 7) 가 얻어전다. 이 식에서 임의의 압력을 대입하면 그 압력에서 온도가 계 산되어 P, T 의 관계가 얻어진다. 즉 2 kbar 에서 T=922 °K, 1 kbar 에 서 T=884 °K, 1 bar 에서 T=552 °K 가 계산된다. 이를 P-T 다이어그
 Il
Il
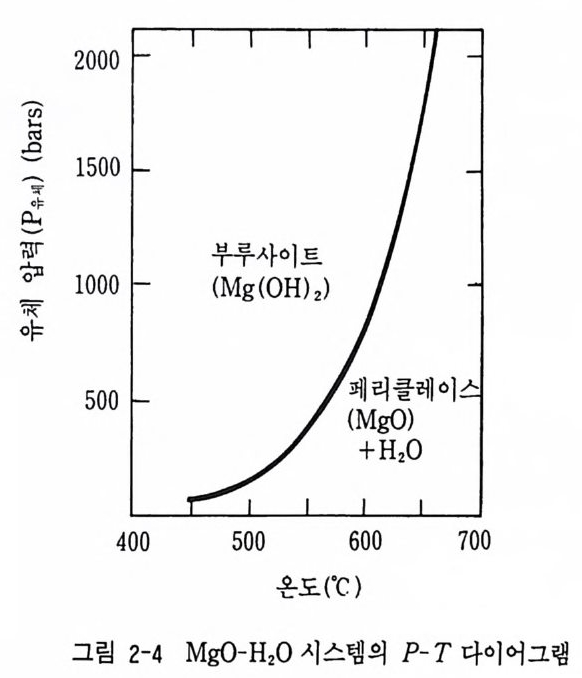
램으로 표시하면 그림 2-3 과 같다. 이는 Harker 와 Tu ttl e(1956) 의 실험 연구에서 얻은 결과와도 잘 일치하고 있다. 그러나 유체상을 가지는 변 성 반응식에서도 개방계인 경우에는 CO2 압력이 1 기압으로 유체상을 가 지지 않는 반응에서와 같이 계산된다(그립 2-3). 같은 방법으로 부루사이 트 (bruc ite) , 페 리 클레 이 스 (pe ric la se) 사이 의 반응식 에 서 Mg (OH ) 2 ~ Mg O + H20 (부루사이트) (페리클레이스) 계산된 결과의 P- T 다이어그램은 그림 2-4 와 같다.
 ’:롭누 -- 、 211 005000 000 上 부(M루g 사(O 이H트)2 )
’:롭누 -- 、 211 005000 000 上 부(M루g 사(O 이H트)2 )
2-7 화학반응속도론 이상에서 설명한 것과 같이 암석 광물은 온도, 압력에 따라 여러 가지 화학 변화를 일으킨다. 화학 변화는 물질 사이의 화학 반응에 의하여 일 어난다. 저온인 지표 환경에서 물과 암석 상호 반응이 일어날 때에는 화 학평형에 도달하지 못하는 경우가 많으므로 반응속도론적 연구의 중요성 이 증가되고 있다. 화학 반응은 일정한 조건에서 화학평형에 이르게 된 다. 일반적으로 화학 반응은 다음과 같이 표현된다. aA+bB+… … :;:::== dD+e E … … 여기서 A, B 는 반응물의 화학종이며 D, E 는 생성물의 화학종이다. 그리고 a, b, d, e 는 화학량론 계수 (s t o ic h i ome t r ic coe ffici en t)이다. 위 의 반응에서 좌 또는 우로 향하는 반응 속도가 갇울 때 열역학적으로는 LJG =O 일 때이다. 이때 화학평형 상태 (v+=v- )에 있게 되며 화학평형 상수 (K) 는 [[AD ]F a[[EB]] eb =K 로서 물질의 농도와 양의 함수로 질량작용의 법칙이 성립된다. 화학평형 에 도달하는 데 걷리는 반응 속도는 반응 물질의 농도, 온도, 촉매, 빛 등에 의해 영향을 받는다. 반응 속도 (v) 는 v= 고팔 =k[A]n'[B 〕 n2 … 로 표현된다. 여기서 [A], [B] 는 반응 물질의 농도이며 k 는 반응속도정수이다. 그 리고 nI, n2 는 반웅의 차수로서 n=O 인 경우를 0 차 반응, n=l 인 경우
를 1 차 반응, n=2 인 경우를 2 차 반응이라 한다. 기체 반응인 경우에는 물질의 농도 대신에 분압을 사용한다. 1 차 반응은 단일 물질의 농도와 시간과의 관계로, N 을 반응 물질의 농도라 하면 쁘dt =-11N 가 된다. 초기 농도 No 가 시간 t만큼 경과한 후의 변화는 위 식을 적분 한 형태로 f:=A i tdt 가된다. 이 식을풀면 t=1t =I nNN。 가 얻어진다. 반응 물질의 초기 농도 No 가 반으로 줄어드는 데 걸리는 시 간을 반감기 (half l ife) 라 하며 tl/2 =—I nK 2 = 0.6K9 3 이 된다. 이 관계식은 방사성 동위원소를 이용한 암석 절대연령 측정의 기본 원리가 된다. 2 차 반응은 二d=t 싸 으로서 반응 속도가 하나의 반응 물질의 농도의 제곱에 비례하는 경우이 다. 2 차 반응에서는
근慕=뿡 =ANANB 와 같이 반웅 속도가 서로 다른 두 반응 물질의 농도 NA, NB 의 곱에 비 례하는 경우가 있다. 이런 경우는 주로 기체상과 액체상의 2 차 반응에서 그 예가 많다. 일반적으로 지질학에서 반응 속도는 방사성 동위원소의 붕괴, 광물의 용해, 침전, 핵형성, 결정 성장 등이나 물-암석 상호 반웅, 암석의 풍 화, 열수 변질, 토양 형성 과정 등의 반응 경로 해석이나 진행 과정을 연구하는 지구화학 분야에 이용되고 있다. 그리고 유기 물질과 무기물질 이 상호반응할 때 반웅 기구와 반응 속도는 대단히 중요하다. 예를 들면 탄질물과 같은 유기물에 있어서 우라늄의 흡착과 환원에 관 한 실험을 들 수 있다 (Nakash i ma, 1992). 탄화도가 낮은 아탄은 아래 반응에서와 갇이 상온에서도 20 시간 정도 지나면 0.2m mo l/g의 우라닐 이온이 흡착되며 수용액에는 동시에 0.4 m mol/ g의 수소 이온이 증가한다. 2RCOOH + UO 출+ 一 RRccoooo-->u m++ zH+ 그리고 아탄에 의해 다음과 같이 우라닐 이온이 환원될 때 RH2+U00~+ __. R+2H++U02 환원 반웅속도는 d[:?g+ ]= -k[UO 訂 • [RH나 식에서 계산될 수 있다. 여기서 k 는 반응속도정수이며 RH2 는 단위체적 중의 아탄의 중량이다. 지구화학에 반응속도론의 적용에는 반웅 중간 생 성물의 동정이 어렵고, 반응시 속도 정수, 빈도 인자, 활성화 에너지 결
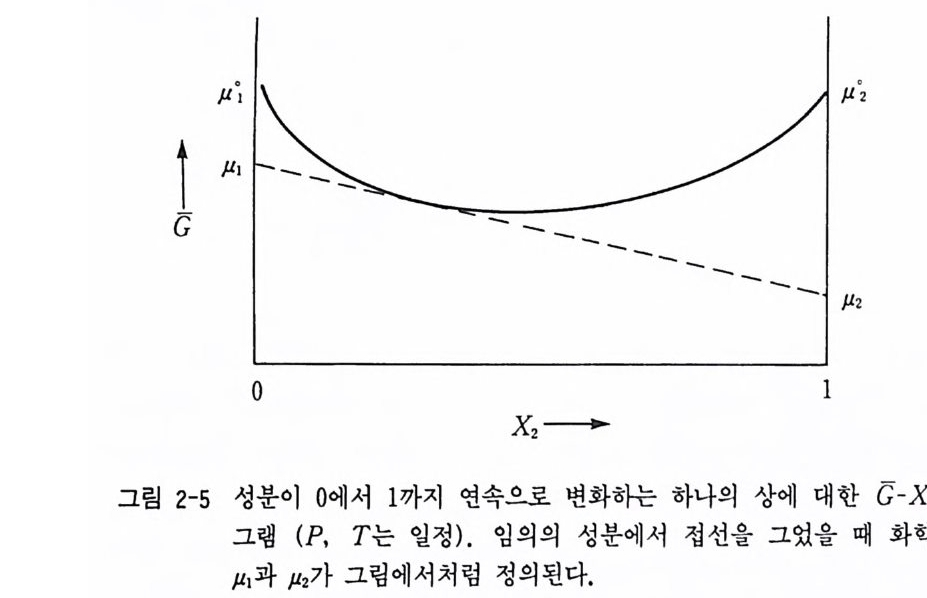
정이 어려워 많은 문제가 있다. 지금부터 실험연구 결과가 기대되는 분 야 중의 하나이 다 Oiyam a, 1994) . 2-8 G-x 다이어그램과 T-x 다이어그램 지구화학 시스템에서는 보통 온도와 성분 (T-x), 압력과 성분 (P-x) 또는 P- T 관계를 그래프로 표현할 수 있다. 죽 지구화학적 적용에서 압력 (P), 온도 (T) , 성분의 몰분율 (x) 로 표현하면 대단히 편리하다. Gib b s 자유에너지는 G=G(P, T, X2) 의 함수 관계에 있다. 그러므로 주어진 온도와 압력 조건에서 Gib b s 자유에너지 (G) 와 성분 X 의 함수 관계가 얻어진다. 그림 2-5 의 G-X 다이어그램은 일정한 온도 (T) 와 압력 (P) 조건에서 성분 X가 1 에서 2 까지 변화하고 있는 경우이다. 온도, 압력이 고정되어 있을 때 G=G(X2) 의 관계에 있게 된다. 단 일 광물상이 성분 X2=0 과 X2=l 사이에 연속적으로 변하는 혼합 모델 에서 Gib b s 자유에너지는 G (X2) = µfX1 + µ8X2 + R T (XdnX1 + X2InX2 + Xdn111 + X2ln112 =µf+ X2(µ8-µf) +RT([l-X2] 〔 ln(l-X2) 사 +X2 [I nX2 却 로 표현할 수 있다. 여기서 A 는 활동도 계수이다. 이룰 그림으로 표현하면 그림 2-5 와 같다. 그림 2-5 에서 성분 X 에서 접선을 그리면 성분 X2=0 과 X2=l 에서 각각 화학 퍼텐셜 µ1 과 µ2 가 y 축 좌표계에 교차한다. µ1 값은 점점 감소하여 가고 µ2 값은 점점 증가 하면서 C 값은 커브의 국소점에 이르게 된다. 순수한 단성분 X2=0 과 단성분 X2=l 에서의 화학 퍼텐셜의 값은 각각 µf과 째이다. 고용체와 유사하게 순수한 성분이 아니고 성분이 변화할 때 안정한 광물상 A 는
C 값의 극소점에서 이루어진다. 단성분 1 과 2 사이의 A, B 두 상을 가 지는 2 성분계의 G-x 다이어그램은 그림 2-6 과 같다. 두 상의 성분을 몰 수로 표현하면 A 상의 성분 1 과 2 사이에는 n1A, n2A 로 표현할 수 있고 B 상의 경우에는 nIB, n2 쵸i 표현할 수 있다. 한편 몰분율로 표현하면 각 각 XIA, X2A, XIB, X2B 로 표현할 수 있다. 여 기 서 nlA X1A= n1A+n2A 이다. 물론 X1A+X2A=l 이다. GA 와 G 는 A 상과 B 상의 Gib b s 자유에너 지 이다.
 l µµI ~ l -— - ---- 』 µµ2° 2
l µµI ~ l -— - ---- 』 µµ2° 2
이것을 화학 퍼텐셜 µ로 표현하면
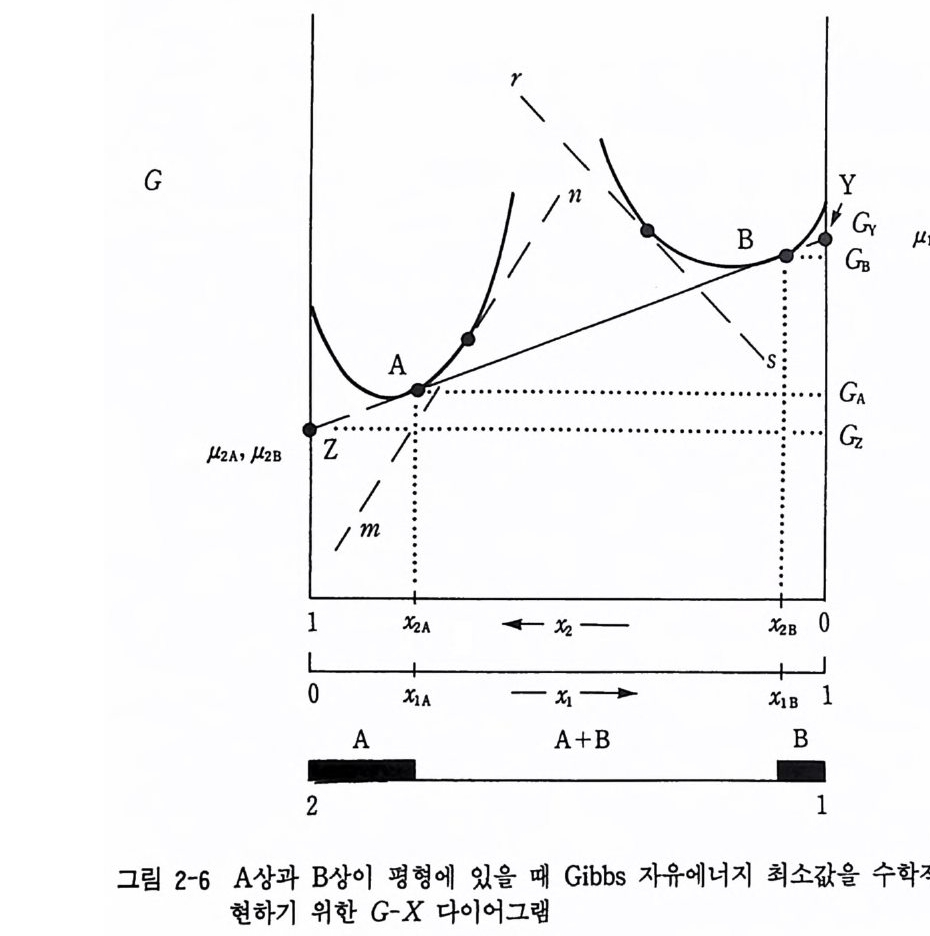
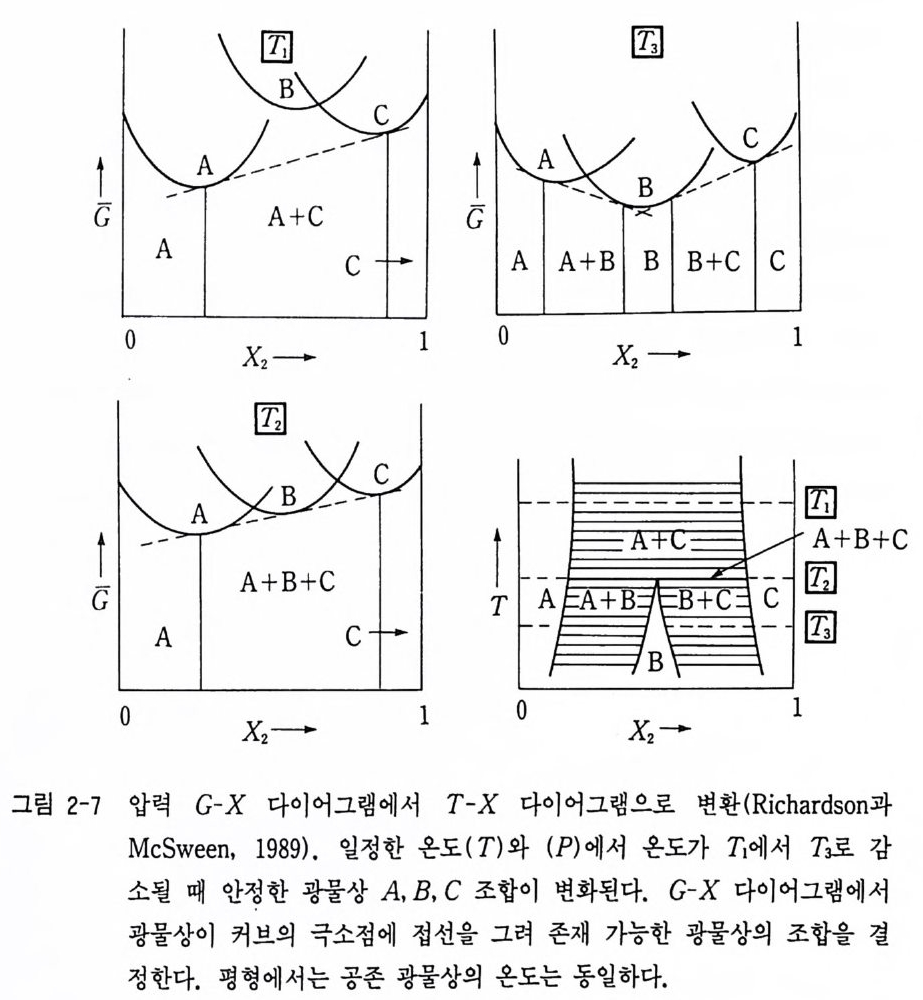
µIA=(~)n2A, µ2A=(~)n1A, µ1s=(~;』 2B) 이 n2A, µ2s=(~) 이 nlB 가된다. G-x 그림에서 접선(즉 자유에너지의 국소값)을 그으면 A 상과 B 상이 공존하며 평형일 때는 µIA = µIB, µ2A = µ28 가 된다. 그림 2-6 에서와 같이 A, B, C 세 광물상이 서로 공존하는 경우 각 온도에서의 c-x 그림을 생각하여 보자. 그림 2-7 에서 A, B, C 상의 국소점을 연결한 접선을 그으면 T3 온도 에서 존재 가능한 광물상은 A, A+B, B, B+C, C 상임을 알 수 있 다. 같은 방법으로 m 온도에서는 A, A+C, C 상이 안정하다. 온도의 변화에 따라 C 커브가 상하로 움직이지만 이 경우 B 상의 이동이 다른 두 상의 커브에서보다 빠르다. T2 에서는 3 상이 동일 접선 위에 놓일 경 우로 µu=µrn=µ1c 일 때이다• 이때는 A+B+C 상이 공존 평형에 있는 영역이 생긴다. 이 를 온도 (T) 와 성분과의 관계 그림으로 그리면 그림 2-7 과 같이 된다. 이것이 T-x 다이어그램이다. 위에서처럼 압력 (P) 와 성분 (X) 이 일정한 조건에서 온도에 대한 자유 에너지의 변화량은 層 )Px= ― 5
로서 엔트로피의 값이 양의 값이므로 온도 변화에 따라 G (x ) 커브가 아래 위로 움직일 수 있게 되기 때문에 G-x 다이어그램에서 T- x 다이 어그램으로 변환시킬 수가 있다. 물론 T, X 가 일정한 조전에서의 압력 에 대한 자유에너지의 변화량이 (:衍 rx = v 로서 V 의 값이 양의 값을 가지기 때문에 T-x 다이어그램에서와 같이 P-x 다이어그램도 G-x 다 이어그램에서 유도해낼 수 있다. 그러나 P-x 다이어그램은 T- x 다이어 그램과 같이 모양이 거꾸로 될 것이다. 왜냐하면 고온일수록 V 와 5 의
 r
r
값이 크고, 고압일수록 V 와 5 값이 작아지기 때문이다. P- x 다이어그 램은 지화학적 문제 해결에 별로 이용되지 않고, 보통 압력의 효과나 영 향은 P-T 다이어그램에서 판단한다.
 ml
ml
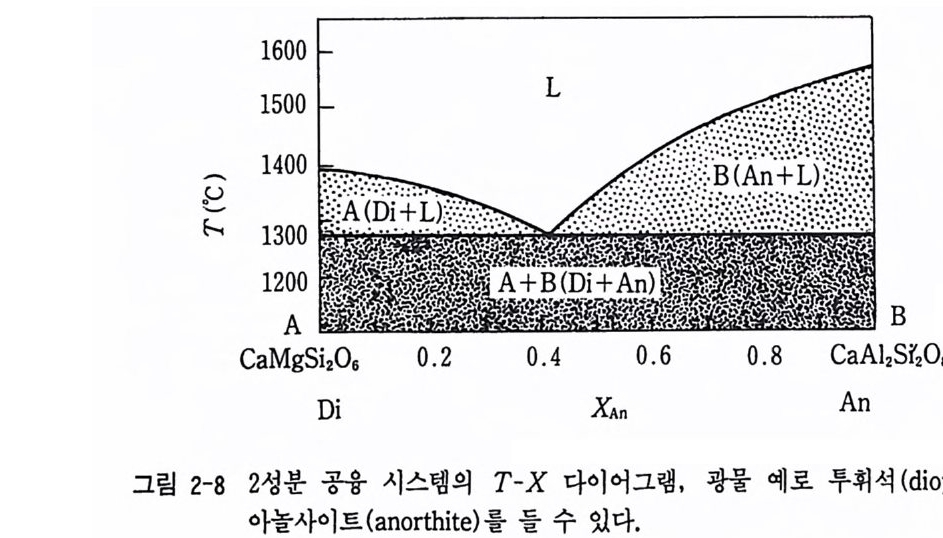
(1) T-x 다이어그램의 실례 상률도(p hase d i a gr am) 는 1 성분계, 2 성분계, 3 성분계 그리고 다성분계 로 구분하여 생각할 수 있다. 2 성분계 이상의 모든 다성분계 상률도에서 는 성분의 변화와 온도와의 관계를 생각하여 볼 수 있다. 몇 가지 유형 의 T-x 다이어그램을 생각하여 보자. 첫째, 2 성분 공융 관계에 있는 3 상 평형, 둘째, 2 성분 포정반응 시스템, 셋째, 2 성분 고용체 시스템, 넷 째, 3 성분계 및 다성분계 T-x 다이어그램을 들 수 있다. 그 중 2 성분 A, B 의 공융 (eute c ti c) 관계 에 있는 A, B, L 상의 3 상 상률도 중에 가 장 단순한 경우의 T-x 다이 어그램 이 그림 2-8 과 같다.
 1600 L
1600 L
고온에서 성분 X건 (Ai .2B0.s) 액체상이 온도가 내려가면 결정 B 가 정 출되기 시작한다. TE( 공융 온도)에 이르기 전까지는 고체상인 B 결정이 계속 정출된다. 그러나 따 온도에 이르게 되면 잔액에서 A 결정이 정출 되기 시작하여 고체인 A 와 B 그리고 잔액인 액체상과 세 상이 TE 온도 에서 공존하게 된다. 이를 공융 (eute c ti c) 이 라 한다. E 온도 이 하로 온
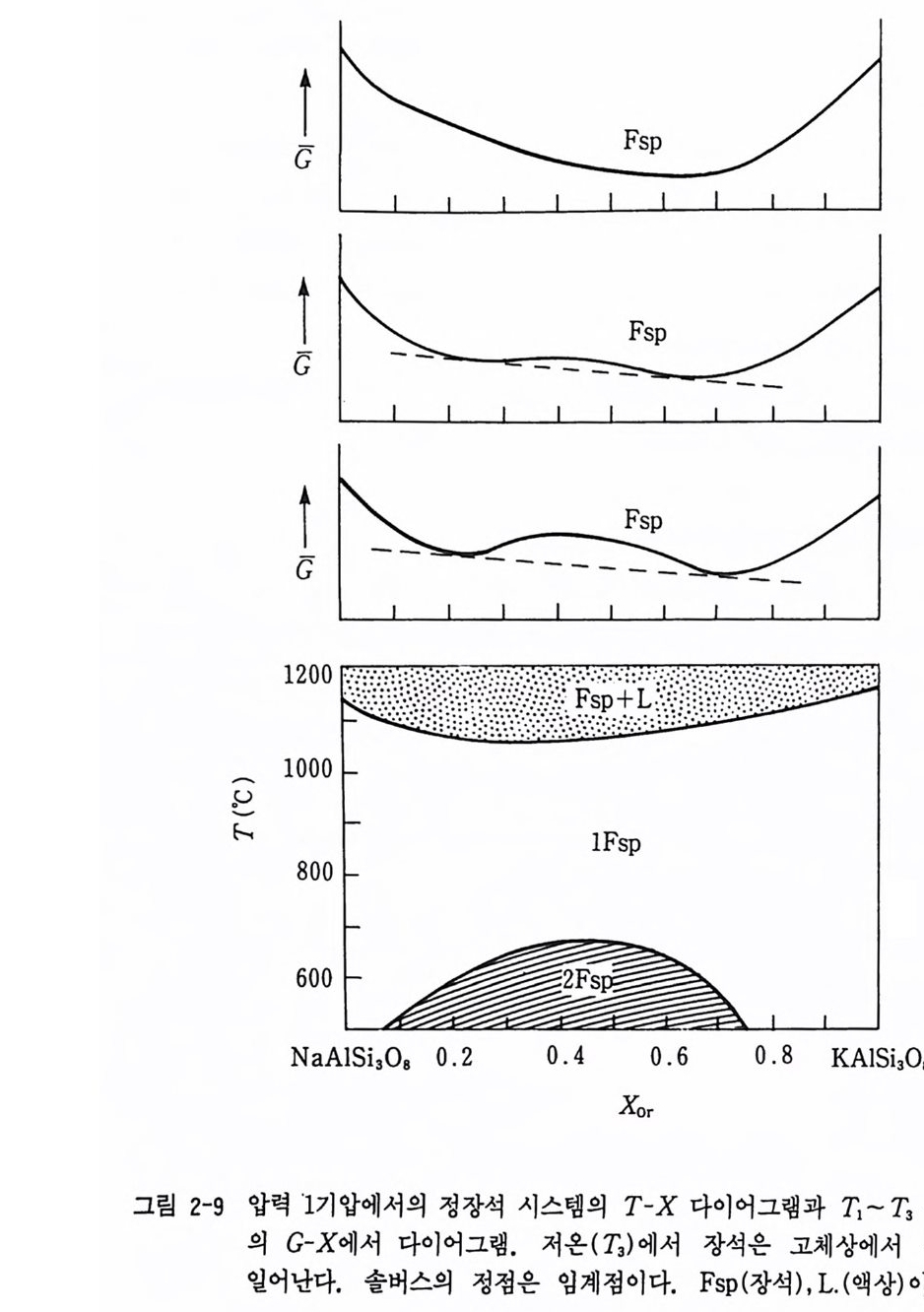
도가 내려가면 잔액이 소진될 때까지 A 결정이 정출되어 초기의 액의 성 분과 동일한 고체 결정 A, B(Ao . 2B0 . s) 가 정출되어 A, B 고체상이 만들 어진다. 여기서 액체상 L 과 B+L 또는 A+L 상과의 상경계선을 액상선 (iiqu id u s li ne) 이라 하고 액체상이 더이상 안정할 수 없는 A+L, B+L 상 이하의 A+B 경계선을 고상선 (so li dus li ne) 이라 한다. 암석학에서 고 체의 성분과 액의 성분이 동일하게 정출 또는 용융되는 과정을 조화 융 해 과정 (cong rue nt melti ng pro cess) 이 라 한다. 암석 광물의 간단한 실례는 두휘석 (CaM g S i 20s) 과 아눌사이트 (CaAl2S i 2 아) 사이의 공융 관계를 들 수 있다. (2) 솔버스 커브의 G-x 다이어그램 알칼리 장석 솔버스 (solvus) 에서처럼 용리 (exsoluti on ) 현상이나 액체 불혼화 현 상 (im mi sci bi li ty ) 이 일 어 난다. 이 경 우에 는 임 계 점 (cri tical p o i n t)을 가지는 점이 앞의 여러 경우와는 다르다. 알칼리 장석 솔버스 의 T-x 및 G-x 다이어그램은 그림 2~9 와 같다. 이 그림에서 정장석과 알바이트가 평형 공존하는 조건은 8G 겅 r= /Jo r-µAb Ol 다. 一정ax G2 =O 인 곳은 변곡점이 얻어지게 되어 T-x 곡선이 바이노달 (b i noda l) 곡선 또는 솔버스가 된다. 변곡점 내측 부분은 〈스피노달 (s pi noda l) 곡선〉이 된다. 고온에서는 알바이트와 정장석 광물이 고용체를 이루고 있으나 저 온에서는 알바이트와 정장석의 2 종류의 장석으로 분리된다.
 凰
凰
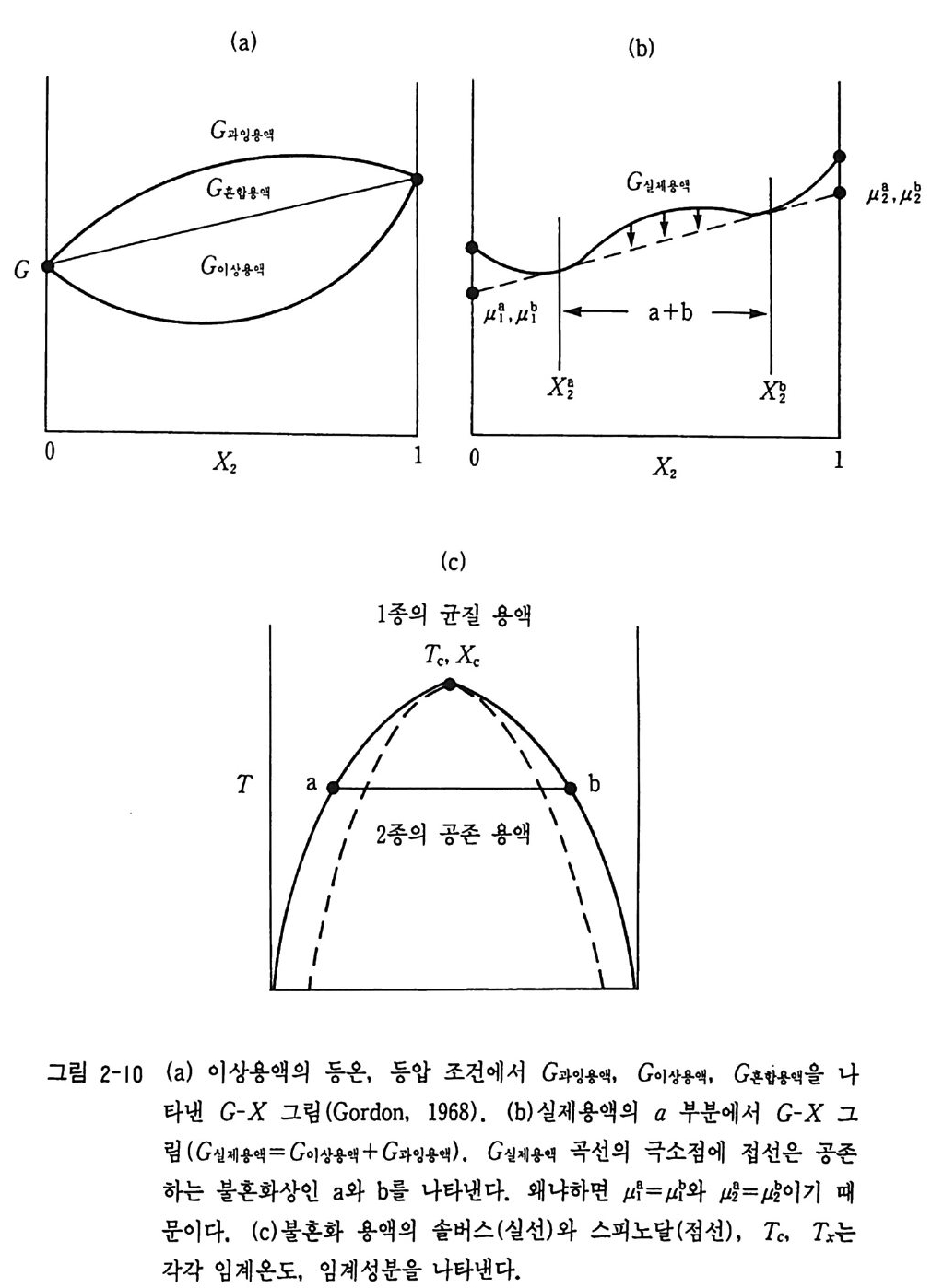
G- x 다이어그램을 보면 고온에서는 완전히 액상이지만 온도가 내려가 면 변곡점이 생긴다. 이 변곡점이 바로 임계점이다. 이 두 변곡점을 잇 는 접선을 그으면 두 종류의 장석 고체상이 얻어진다. 온도가 내려갈수 록 변곡점 사이의 간격이 넓어지게 된다. 이같은 결과로 생긴 현상이 화 강암에서 흔히 관찰되는 퍼사이트(p e rthit e) 조직이다. (3) 용액의 분리와 혼합 위와 같 은 현상은 2 성분 용액의 혼합 때문에 일어난다. 이상용액 (ide al solu ti on) 의 화학 퍼텐셜은 µ i이상 =µ f +RTlnX 이다. 그리고 자유 에너지의 혼합은 4G 혼합 =4H 흔 E T4S 혼 합 O] 다. 4G1 이 상혼합 =RT2XJ n Xi 로 표현되며 여기서 C이 상 =2X 뼈 +RT2XJ nX, . 를 얻을 수 있다. 성분 1 과 성분 2 항을 X1=l-X2 로 바꾸어 넣으면 C 이상= (1 ― X2)µ f +X따 ~+1 泊 (l-X2)ln(l-X2) +X2lnX』 관계가 얻어진다. X1=X2=0.5 일 때 4G 이상혼합는 그립 2-10 과 같이 된 다. 여기서 G 과잉 (G 과 잉 =G 이 상 _G 이상)를 대입하면
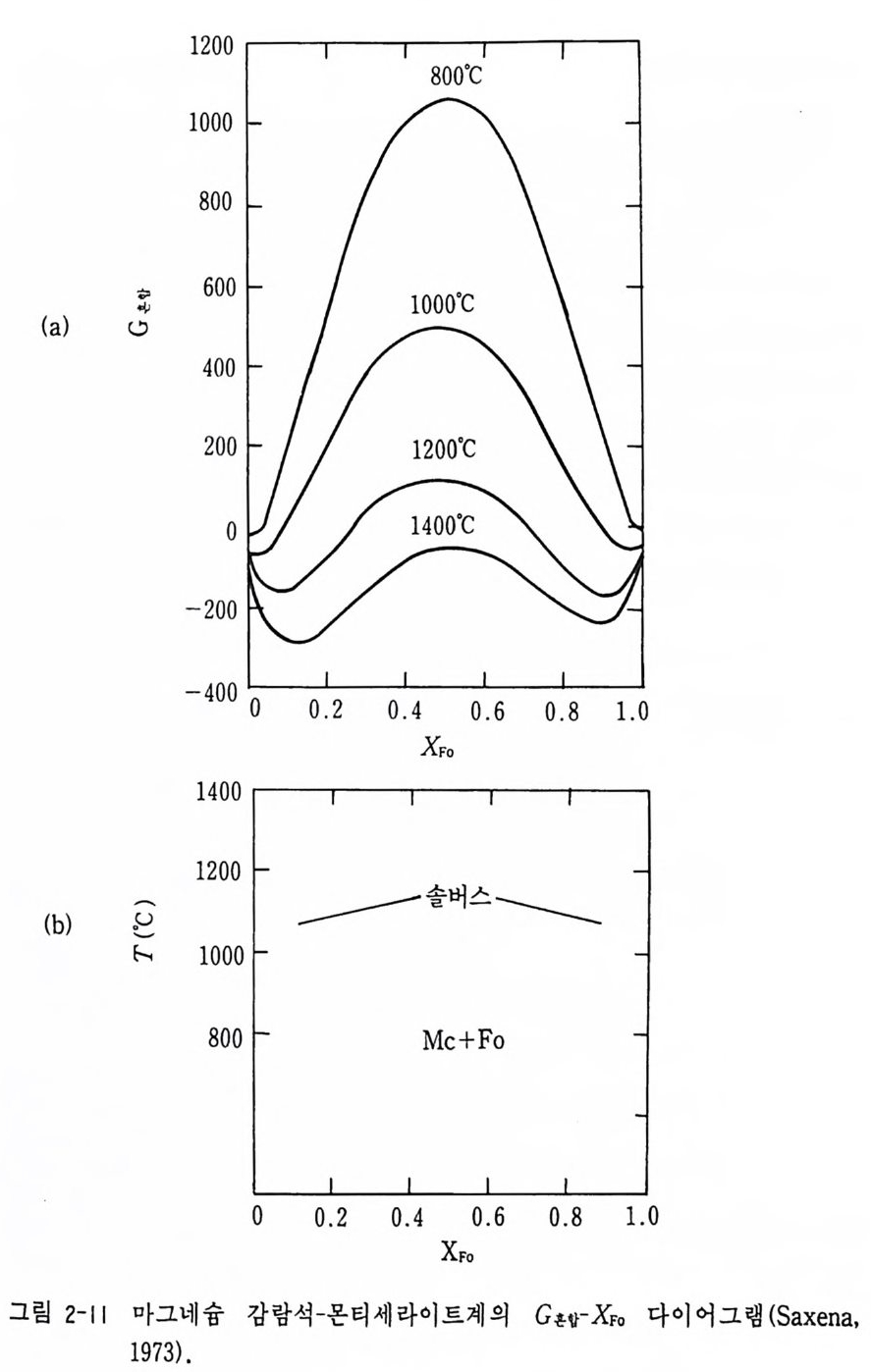
틀) = µ~ + R Ti n 倍+(體) 가 얻어지며 이것을 2 차 편미분을 하면 露정 G= 露R+T ( 장綴 G 과 )잉 가 된다. 여기서 이상용액이라면 G 혼 합 =0 이 되어 2 차 편미분 값은 항상 양의 값이 되어 자유에너지 커브는 위로 볼록하게 된다(그립 2-1 0 ). 그립 2-10 에서는 실제 2 성분 용액에서의 G- x 다이어그램과 G 혼 합, G 이상, G 利 관계를 비교하고 솔버스 커브를 동시에 보여 주고 있다. 실 제용액 a 부분 (G 선제 =G 이상 +G 과 잉)의 G-x 다이어그램은 그림 2-10(b) 와 같다. G 실 제 곡선의 극소점에 접선을 그으면 µ f =µf와 µ 정 =µ # 이기 때문에 공존하는 a 와 b 의 불혼화상이 형 성 된다. 이 때 T-x 다이 어그램 에 불혼 화 용액의 솔버스와 스피노달이 그림 2-10(c) 에서처럼 얻어진다 . 스피노 달은 열역학적으로 불안정한 상태에 있는 변곡점 (s pi node) 을 이은 그림 울 말한다. 그리고 2 상 공존 영역 경계를 그린 것을 바이노달이라 한다 (그림 2-lO(c)). 이 그립에서 TC 와 Tx 는 각각 임계온도와 임계성분을 나 타내고 있다. 감람석 (fos te r it e, Mg 2S iO c ) 과 몬티 셀 라이 트 (monti cel li te, CaMg S i0 4 ) 사이 의 2 성분 혼합으로 계산된 G-x 다이어그램의 실례를 들어 본다. Saxena (19 73) 에 의 해 얻어진 5 kbar 에서 온도 의 존 반응 파라미 터 (int e r acti on par amete r ) 값은 [W=35000 ― 37247(T • 1000- 1) +13094(T • 1000-1)2]c al mol-1, 1073 °K 에서 W=IOI09 cal moJ- 1 , 1273 °K 에서 8804 cal mol 가 1473 °K 에서 8546 cal mol-1, 1673 °K 에서 9335 cal mol-1 이다. 감람석의 Gib b s 자유에너 지는 Go1 = XFoµFo + XMc/lM c =XFoGFo+XMcCrnc+XFo R Tln XFoYFo+XMcRTln XMcYM c
 (a) (b)
(a) (b)
로 표현된다. 이를 정상용액 (regu la r solu ti on) 의 모델 RTin r ;= WXJ = W (l-XJ) 로표현하면 C 혼합 =RT(XMcln XMc+Xroln Xro) + WXMcXro 가 된다. 이 식을 이용하여 계산된 G-x 다이어그램은 그림 2-11 과 같다 (Saxena, 1973) . 2-9 지질온도계와 지질압력계 (1) 지질온도계 평형상수의 온도, 압력, 성분 의존성을 이용하여 평형상태에 있는 광 물종에 대하여 그 광물이 형성될 때의 온도와 압력을 계산할 수가 있다. 이 를 지 질온도계 (ge oth e rrnomete r) 와 지 질 압력 계 (ge obaromete r ) 라 한다. 물론 지질온도계로 이용되려면 반응이 압력에 무관하고 온도에만 영향을 받아야 하며 지질압력계는 반대의 경우라야 한다. 열역학 상태 함수인 Gib b s 자유에너지에서 L1G0=L1H— TL 1S 이다. 그리고 반응이 평형일 때 4G!= -RTlnKD 이다. 여기서 lnKD= -L下1H T~ +, 켕L1S―~
 11020000 I / soo·c
11020000 I / soo·c
로 표현할 수 있다. 이 식은 lnKo=Ar +B 가 되어 평형상수 K마 온도의 함수임을 알 수 있다. 따라서 광물 평형 에서 엔탈피와 엔트로피 값을 알면 온도와 KD 관계를 얻을 수 있다. L1CP 의 값이 알려져 있지 않을 때는 보통 4C p =0 으로 가정한다. 예를 들면 단사휘석 (C p x) 과 사방휘석 (O p x) 이 공존하고 있는 경우 이 들이 화학평형에 있으려면 공존하는 단성분 E, 모두에 대하여 화학 퍼텐 셜이 갇아야 한다. 즉 µ옹 ?X=µ 응 ?X 이다. 그 중 단성분 엔스타타이트 (M g 2S i 206, En) 에 있어서 G~~x+RT i na~ 堅= 며쁜 x + R Ti na 옹안 식이 성립된다. l 霞a콘 窓= - G8XR -TG 옹 :x = -스R산iT L 만일 2 종류의 휘석이 이상 고용체 (ide al soli d solu ti on) 라면 a=x 가 되 어 l 겔=-磐=맹原+챙 가 얻어진다. CaM g S i 206-M g 2S i 206 계의 실험에서 LJ HEn 와 4SEn 가 얻어 진다. 그러면 자연에서 산출되는 2 종류의 휘석의 분석에서 :『몰 얻어 온도 (T) 를 얻을 수 있다. 그러나 단사휘석이 이상 고용체가 아닌 제한 점이 있다. 또 다른 예는 공존하고 있는 흑운모와 석류석 사이에 M g와 Fe 의 분
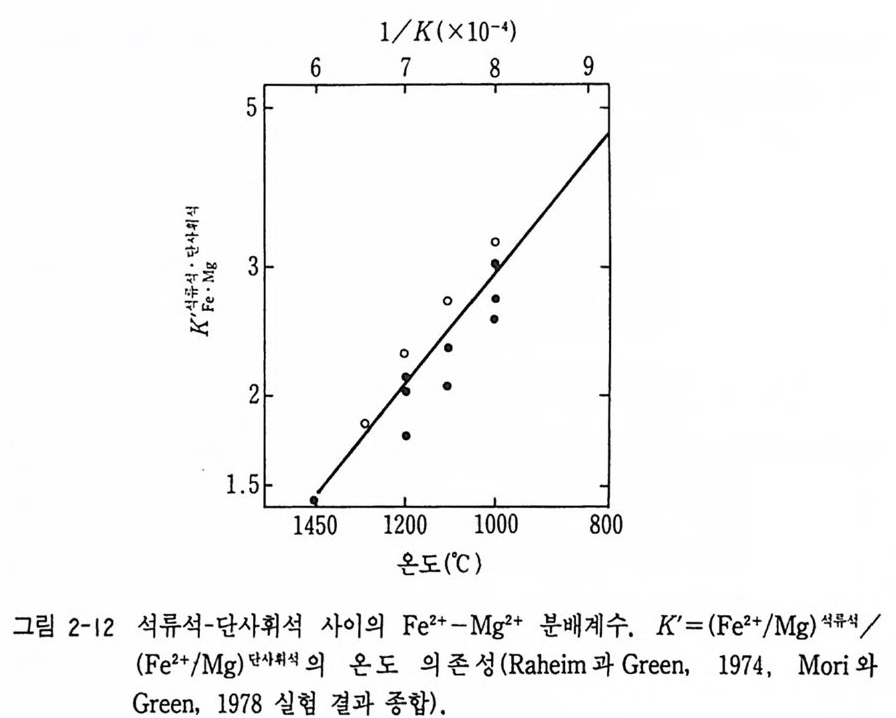
배를 이용한 것으로 Fe3AbSi3 0 12 + KM g述 lS i 3 아 (OH ) 2; ;:::=Mg ~ bSb012 + KFe3A!Sb01o (OH ) 2 (석 류석 ) (혹운모) (석 류석 ) (흑운모) Ferr y와 S p ear0978) 에 의한 교환 반응 실험에서 얻어진 lnKo= -2109/ T+O .78 2 식을 이용하여 온도를 구할 수가 있다(그립 2-12). 여기서 lnK[l = (XM g/ XFe) 석 유 석/ (XM s/XF e) 혹운모 이다.
 1 / K( x lO 기
1 / K( x lO 기
(2) 지질 압력계 일정한 온도에서 자유에너지의 압력 영향은 (1 맡 )T=4VT 로 표현된다. 이 식에 4G!= _ RTlnKD 를 대입하면 ( 8(l:D) )T= ―앱 가 얻어진다. 그리고 4VT 가 압력에 영향을 주지 않는다면 압력 변화에 따른 변화는 앞의 식을 적분하면 lnKP2-lnKP1=- 禍問 -R) 이 얻어져 평형상수가 압력에 의존함을 알 수 있다. 물론 평형 반응시의 Gib b s 자유에너지 변화는 4G!=-RTlnKD=4H— T4 5+P4V 이다. 여기서 일정한 압력 (P) 과 온도 (T) 하에서 편미분하면 (營 )P= 흙 와 (틀 )T=- 暮
가 얻어져 4H 값이 큰 광물 조합은 온도 의존성이 커서 지질온도계로 유용하고, 4V 값이 큰 광물조합의 경우에는 압력 의존성이 크기 때문에 지질압력계로 적합함을 알 수 있다. 지질압력계의 한 예를 들면 사장석 -석류석-석영-단사휘석과 공존하고 평형에 있을 때 다음과 감은 반응식 을 생각할 수 있다. 3CaAl2SE08+ 3CaMg S i2 0 6=2Ca3Al2Si3 0 l2 + Mg 3A 12Si3 0 n + 3Si0 2 (사장석) (단사휘석) (그로슈라 석류석) (파이로프 석류석) (석영) 이들이 평형에 있을 때에는 4V 값의 변화가 대단히 크다. Ne wt on 과 Perk i ns(1982) 가 이를 이용하여 구한 지질압력계 P (bar) = 675 + 17 .179 T (K) + 3 . 5962 Tln Keq 식을 이용하여 압력을 계산할 수 있다. 여기서 Keq = (a~aa~1g ) 석류석/ (aca) 사장석 (acaMg ) 단사휘석 이다. 그러나 이 경우에는 여러 성분의 활동도 값 (a citi v ity coe ffici en t)의 결정이 어렵다. 석류석 내의 Ca 와 Mg 혼합은 비이상 (non i deal) 임이 밝 혀져 (Ne wt on 과 Perkin s, 1992) 다음과 같은 파라미터를 제안하였다. Wca-~18 석류석 = 3306-1. 5 T (K) W 값은 (Ca,M g )A12/3S i 04 의 calmol-1 이다. 물론 그로슈라, 파이로 프, 알만딘과 갇은 석류석군 광물에는 Fe, Al 성분도 포함되어 있지만 Fe-M g와 Fe-Ca 교환의 상호 반응 파라미터 값이 Ca-M g의 경우보다 작기 때문에 무시할 수 있다. 따라서 정상용액 모델 (re gu lar soluti on model) 을 적용하여 석류석 의 Ca 와 Mg 활동도계수를 RT i nrca 석류석= Wca-Mg ( X~+XM gX Fe)
식과 RTln rM g석류석 = Wca-Mg X la +X caXFe) 에서 각각 계산할 수 있다. 그리고 사장석의 활동도계수는 aca 사장석 = YAnXAn (l +X An) 2/4 에서 계산한다. 여기서 rAn 은 R Tin rAn = XJ.b ( 2625 +9 442XAn) 에서 구하고 활동도 a 값은 aca-M g단사휘 석 = XMg M , XcoM2 에서 구한다. 여기서 M1~ M2 는 휘석의 두 결정구조의 위치이며 Ca, Mg , Mn, Fe2+ 는 M2 구조 위치로 Mg , Fe2+, Ti, AI 과 잔여 Fe” 는 M 려 구조 위치로 배분한다. 이들 값은 모두 위의 Ke q값 계산에 이용하 고 마지막으로 위의 지질압력계 식에 대입하여 이들 광물이 평형에 있는 압력을 계산한다. (3) 티타노마그네타이트 지질온도계 화성암과 변성암에서는 함티탄 자철석 (titan omagn e tit e, Fe3Q 4 -Fe2TiO .) 과 헤모일메나아트 (hemo i lmen it e, F 터 03-FeT i 03) 의 함티탄 자철석 산화 물의 두 고용체 광물이 관찰된다. 이들 사이의 반응식은 6Fe2Ti0 4 ~ 02 = 2Fea0• + 6FeTiO a (2 . 8) (함티탄 자철석) (액체) (함티탄 자철석) (헤모일메나이트) Fe203 + Fe2TiO . ~ FeaO• FeTiO a (2 . 9) (헤모일메나이트) (함티탄 자철석) (함티탄 자철석) (헤모일메나이트)
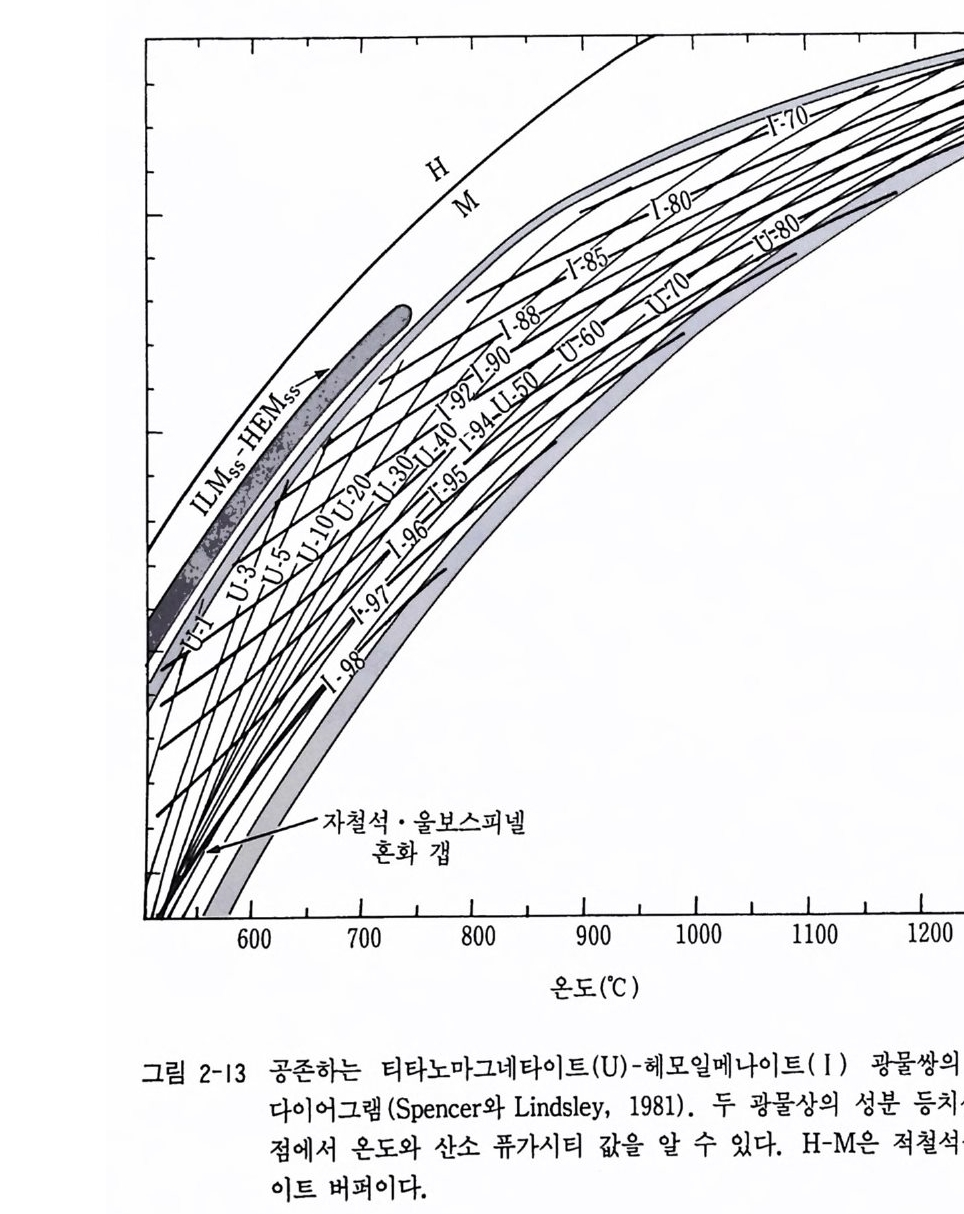
이다. 이들 광물둘이 평형에 있다면 lnK= -4R1T¥ -' -+R뿌 _Jfp P1 2 끄RT 의 온도, 압력과 평형상수 관계식을 이용하여 온도 (T) 와 /02 의 관계를 얻을 수 있다. (2.8) 식에서 평형상수 K= _ia]_ l,십 쩝2 o .~ 10•. a• !;a!6l0: 3 를 얻을 수 있고, (2.9) 식에서 평형상수 K= aFHeI 3 04 • aFTMe2 TI O4 aFTMe3 0 4 • aFTeM2 T l04 를 얻어 대입하고 또 온도에 따른 열역학 자료를 대입하여 계산하면 된 다. 위의 반응식 대신에 다음의 반응식을 이용하여도 좋다. Fe304Mr + FeTi0 3 HJ ;:::::::::=: Fe2Ti 04 Mr + Fe203H1 4Fe3Q 4 Mr+02 ;:::::::::=: 6Fe203HJ S p encer 와 L i ndsle y(1 981) 에 의하여 얻어진 T-foz 다이어그램은 그립 2-13 과 같다. 이 그림은 지질온도계와 산소분압계를 동시에 이용할 수 있는 장점이 있다.
 석·울보스피넬
석·울보스피넬
제 3 장 상률과 상률도 암석을 구성하고 있는 공존 광물 사이에는 상평형이 이루어지는 쪽으 로 반응이 진행되면서 광물 조합이 안정하게 된다. 이때 압력, 온도, 광 물 성분이 변수로서 작용한다. 보통 P-T 관계로 광물의 안정 상태를 표현하며 이를 상률도(p hase d i a gr am) 라 한다. 자연계의 다양한 광물 조 합은 다성분계 시스템이다. 여기서는 P-T 다이어그램 1 성분계, 2 성분 계 포정반응 시스템, 2 성분계 고용체 시스템, 3 성분계 시스템, 다성분계 시스템을 다룬다. 3-1 상률 암석은 광물의 집합체이며 광물은 다성분의 화학 성분으로 구성되어
있다. 따라서 다성분계 다상 평형으로 취급할 수밖에 없다. 열역학에서 소개한 바와 갇이 계에서 가장 안정한 광물상은 주어진 P, T 에서 Gib b s 자유에너지 (G) 값이 최소일 경우이다. P, T 의 함수로 계의 안 정상태를 표현하는 방법이 G i bbs 가 1878 년에 도입한 상률도이다. n 개의 성분으로 구성된 a, b, c, …… 2 상이 공존하고 평형상태에 있다면 모 든 성분의 화학 퍼텐셜(µ)은 계 안의 모든 상에 있어서 같다. 즉, µf=짜=µf=……µf µ정=µf=µf=… •• 짜 짜=짜=µ든•• ••.• µ; 가된다. 여기서 1, 2, …… n 은 성분을 나타낸 것이다. µf는 a 상의 성분 (x f, 처, …… x i -1 과 T, p와는 함수이다. 여기서 xf, xl, …• •• x i -1 는 a 상 중의 각성분의 몰분율이다. 물론 x f +x 打+ ……짜 =1 이기 때문에 성분을 나타내는 변수는 n_1 이 된다. 상 a, b, c …… 2 의 총수를 p라 하면 이 계를 표현하기 위해서는 p( n-1) +2 개의 변수가 필요하게 된다. 위 의 식에서는 c( p _1) 개의 방정식이 포함되어 있다. 변수의 수와 방정식 의 수의 차는 계의 상태를 결정하는데 필요한 변수의 수, 죽 자유도(/) 가된다. 죽 /={p( n— 1) +2}— n( p키) =n+2-P 로 표현된다. 이 식이 G i bbs 의 상률이다. 자유도는 T, P, xf, xJ, …… x 晶 등의 독립으로 선택 가능한 시강 변수 (示强變數, int e n siv e vari ab le) 의 수이 다. 보통 f칙 0 이므로 상의 수와 성분의 수와의 관계는 Psn+2 이다. 암석 이 생성될 때 P, . T 는 독립적으로 취급하므로 /~2 이다. 따라서 암석에 서는 p ~n 의 관계가 성립된다. 이를 Goldsc hmi d t의 광물학적 상률 (mine ralog ica l pha se rule) 이 라 한다. 이 처 럼 상률은 광물의 공존 관계 등
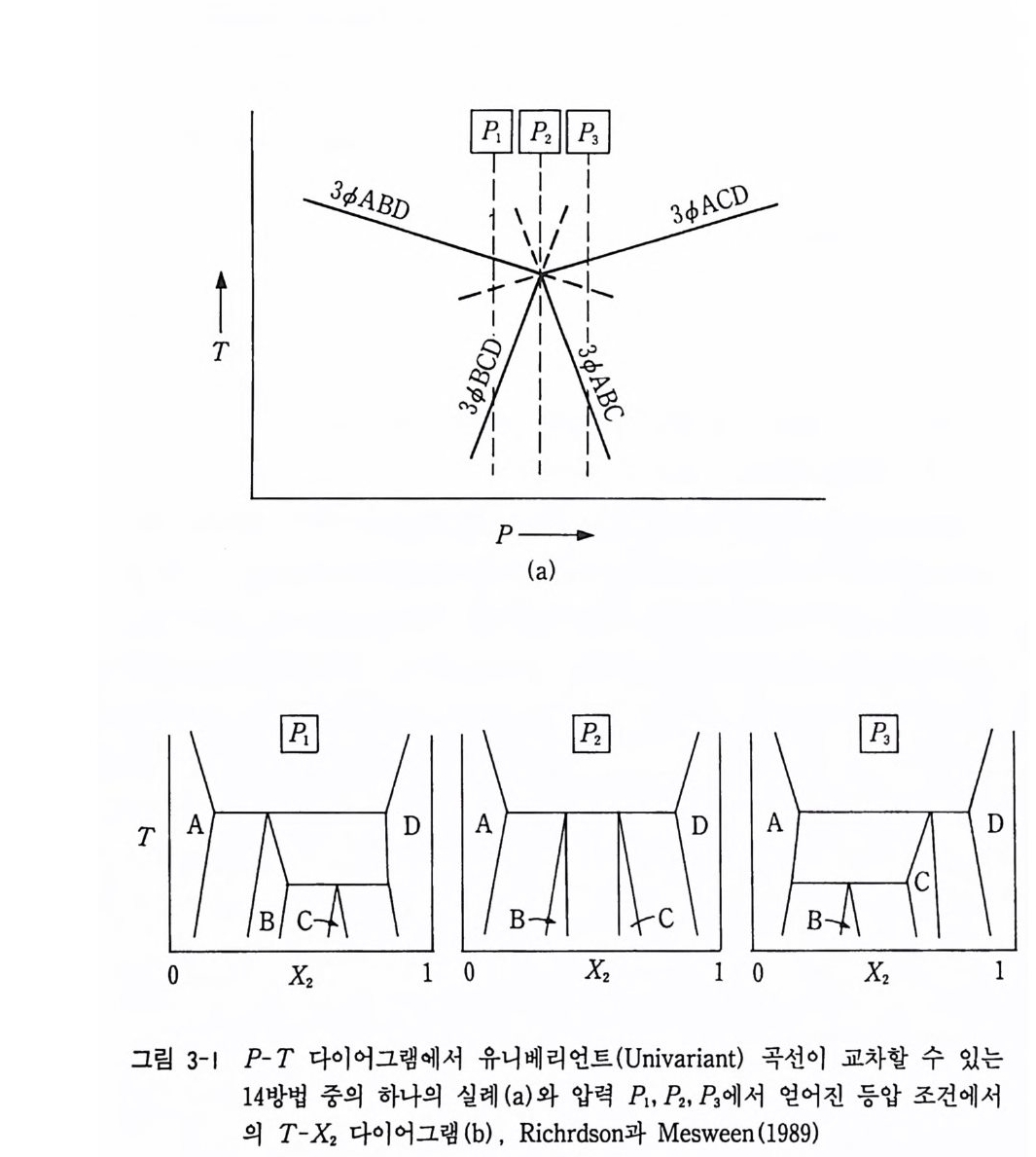
을 고려할 경우에 어떻게 하여 계의 상태가 정해지는가를 나타내는 중요 한 법칙이다. 3-2 상률도 (1) P-T 다이어그램 어떤 암석 광물이 안정상 A, B 와 평형에 있을 때 (L1G= O , µA=µa) 온도와 압력에 대하여 그림으로 나타낼 수 있다. 물의 액체상, 기체상, 고체상의 3 상이 평형에 있을 때나 Al2Si0 5 동질 이상 광물에서 규선석, 홍주석, 남정석 3 상이 공존할 때 그림 2-2 와 같 이 된다. 이때 3 상이 공존할 때는 G i bbs 의 상률 U=c + 2- p, I = 자유도, c= 성분의 수, p=상의 수)에 의하여 f =O 이 된다. 자유도가 0 인 경우를 삼중점 (trip le poi n t , i nv aria n t poi n t) 이 라 한다. 2 상이 공존하는 경 우에 는 / = 1 이 되어 일변선 (un i var i an t l i ne) 이라 한다. 1 상만이 존재하는 경우 에는 /=2 가 되어 이변선 (b i var i an t l i ne) 이라 한다. 앞에서 동일한 압력 에서의 T-x 다이어그램을 공부하였다. 만일 상이한 압력에서의 T-x 다이어그램이 얻어지면 많은 독특한 기하학적 위상법(t o p olo gy)에 의하 여 그림 3-1 에서처럼 일변 곡선들이 P-T 다이어그램 위에 교차할 수 있다. 그림 3-1 에서 압력 P1 에서 3 상이 공존하는 2 개의 일변선이 나타난다. 낮은 온도에서 BCD 가 안정하게 공존하며 높은 온도에서는 ABD 가 안정 한 상으로 존재한다. 높은 압력인 R 에서는 낮은 온도에서 ABC 가, 높 은 온도에서 ACD 가 공존하고 있다. 그리고 R 압력에서는 ABCD 의 모 든 상이 안정하게 공존하고 있다. 반응에서 이들 일변선이 가지는 의미 는 ABD 3 상선은 B=A+D 의 반응으로 B 가 A 와 D 를 형성하는 데 쓰여
 m回_因___ '_
m回_因___ '_
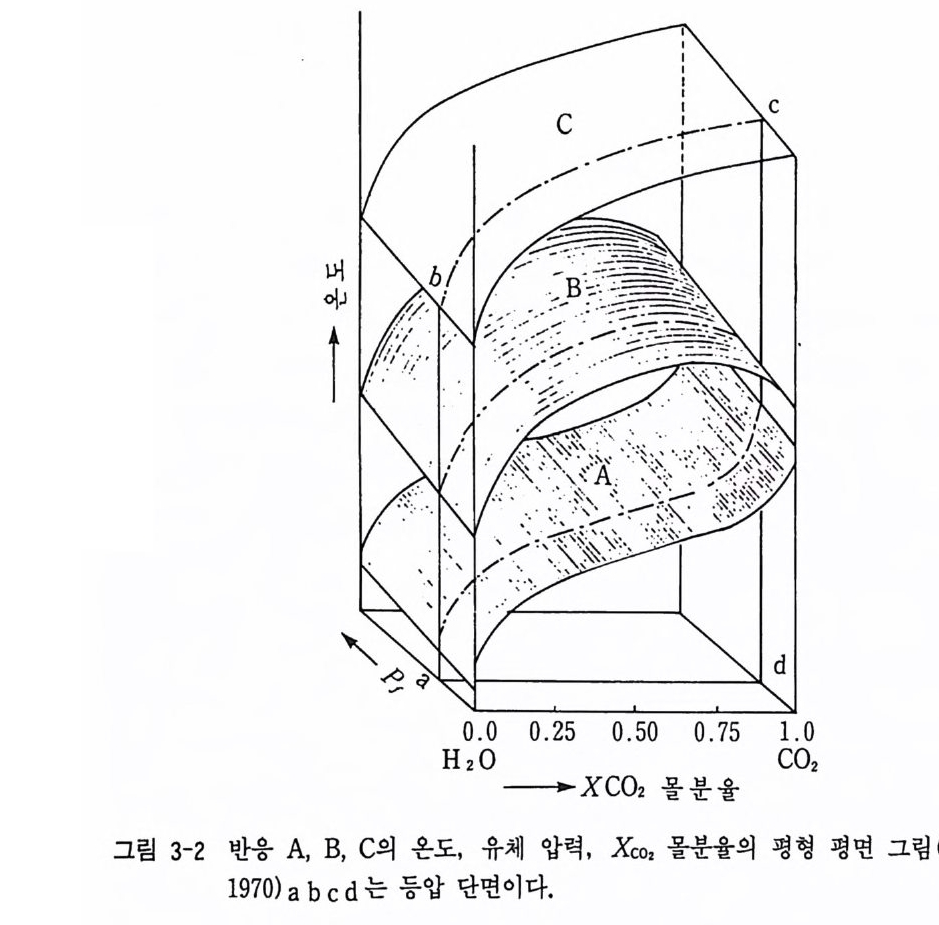
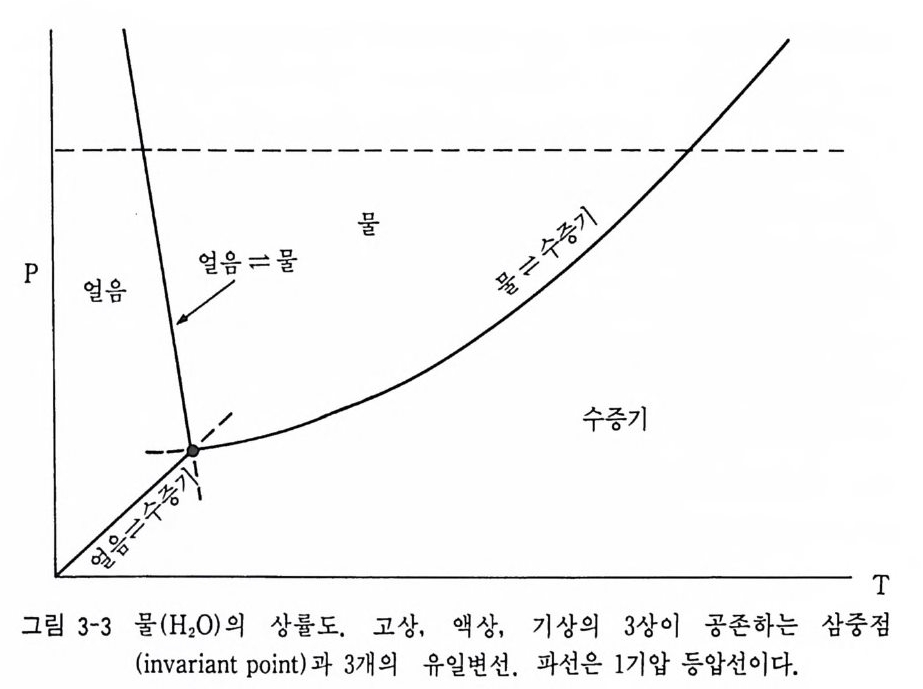
지 게 된다는 것 이 다. ABC, ACD, BCD 3 상선 역 시 B, C, D 상이 반응 에서 각각 소비됨을 의미한다. 삼중점 ABCD 4 상 존재 지역은 A+D= B+C 반응으로 C 와 B 가 소비되어진다. 이같이 상이한 압력에서 얻어진 T-x 다이어그램에서 P-T 다이어그램이 유도될 수 있고, 역으로 P-T 다이어그램에서 T-x 다이어그램을 추론할 수 있다. 물론 P-T-x 다이 어그램을 3 차원 상에 표현할 수도 있다. 예를 들면 P-T-Xco, 를 들 수 있다(그림 3-2). 이는 탄산염암의 변성 반응에서 유용하게 이용된다. P-T 다이어그램 의 다른 예로 그림 9-21 에서처럼 Ca0-Mg 0 -Fe0-Ab0a-Si0 2 -H20 시스 템의 P-T 다이어그램과 각 광물상 간의 반응 및 광물 조합을 나타낼 수도 있다. P-T 다이어그램은 열역학 자료로 그려질 수도 있고 실험에 의해서도 그려질 수 있다. 지질학적 현상은 일반적으로 온도와 압력에 의해 크게 변화하고 있으므로 암석 광물의 생성 환경 해석에 P-T 다이 어그램이 많이 이용되고 있다. 그러나 반응식에서처럼 지구화학적인 반 응은 P, T 이의에 fo,, Pco,, pH 등의 많은 조건에 의하여 영향을 받 고 있으므로 최근의 많은 연구에서 fo, -T 다이어그램, fs2 -T 다이어그 램, XC02- T 다이어그램 등이 연구되어 있다. (2) 1 성분 시스템 성분의 수는 화학평형 상태에 존재 가능한 모든 상의 화학 성분을 표 현하는 데 충분하고 독립으로 변화시킬 수 있는 화학 성분의 최소수의 성분 수를 말한다. 예를 들면 물은 액체상, 기체상, 고체상이라도 모두 화학 성분은 H20 로 표현할 수 있어 1 성분이다. Si0 2 광물상, Al2Si0 5 광물상도 같은 경우이다. 1 성분계 의 물의 상률도는 그림 3-3 과 같다. 물은 1 기 압 100 ·c 에 서 액 체상과 기체상이 평형(비등)에 있게 된다. 또는 1 기압 0°C 와 교차하는
univ a ria n t 곡선에서 고체상인 얼음이 녹기 시작한다. 비등 곡선과 멜트 곡선이 273.16 °K, 0. 0016 bar 에서 교차한다. 물론 승화 곡선도 이 교차 점을 통과한다. 이 점이 J =O 인 3 중점이다. 1 성분계에서는 p + /=3 이 다. 공존 평형상태에 있는 상의 수가 증가하면 자유도의 수는 감소한다.
 lJ三...• . •_ . :->: ·c _ ... : ./ -c;.: .:-- •:; . : - · ..i. ....
lJ三...• . •_ . :->: ·c _ ... : ./ -c;.: .:-- •:; . : - · ..i. ....
 P , 얼음
P , 얼음
(3) 2 성분 포정 반응 시스템 포정 반응 시스템은 앞의 공융 관계에서와는 다르게 단성분 A 와 B 사 이에 중간 성분인 고체상 AB 가 형성되는 점이 다르다. xD 성분 (Ao.3B 0 . 7) 의 고온의 액체상이 온도가 내려가면 먼저 A 고체상이 결정되기 시작 한다. 접점 온도가 내려가서 Tp 온도에 이르면 먼저 정출된 A 결정과 액이 반응하여 중간 성분인 AB 고체상이 결정된다. TE 온도에 이르면 AB 고체상과 잔액에서 B 고체상이 정출되고 잔액 모두가 B 결정을 정 출하면 최종적으로 AB 와 B 고체상이 만들어져 처음 액의 성분과는 다 론 중간 성분 AB 가 만들어지게 된다. 이때 E 에서 일어나는 반응을 포 정 반응 (pe rite c ti c reacti on ) 이 라 한다. 거 꾸로 온도가 상승하여 고체 인 광 물이나 암석이 융해될 때 처음 고체상과 후의 액체상의 성분이 다르게
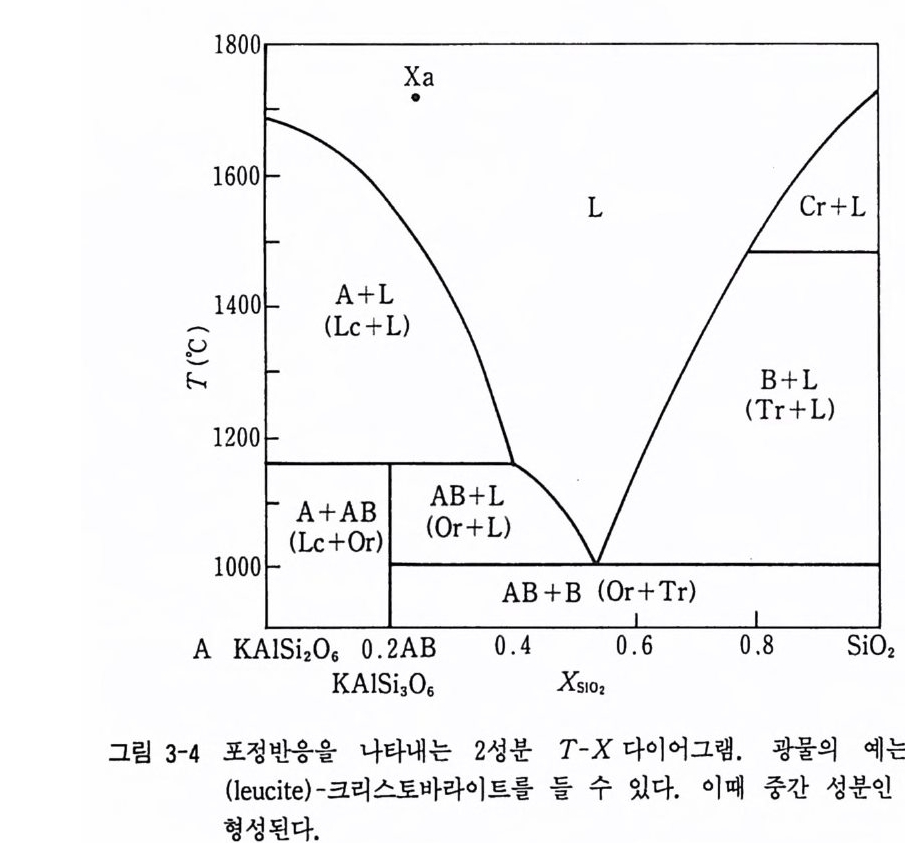
되 는데 이 과정 을 비 조화 융해 과정 (inc ong ru ent meltin g pro cess) 이 라 한 다. 암석 광물의 실례로 준장석-실리카(i uec it e - s il i ca) 계 를 들 수 있다(그 림 3-4). 그림 3-4 에서 처음 고온에서는 준장석 (KAIS i 2 0 G ) 이 정출되지만 Tl’ 온 도에서 준장석과 액 이 반응하여 중간 성분인 정 장석 (KAISiJ O s ) 을 정 출 시 키게 된다. 물론 실리카의 몰분율 (Xs10 2 ) 에 따라 정 출 결과가 다 르 다. 초 염기성암 내에 감람석 주위에 휘석의 반응연 (reac ti on r i m) 을 관 찰 할 수 있는데 포정반응의 좋은 실례이다.
 1800 ’ X•a
1800 ’ X•a
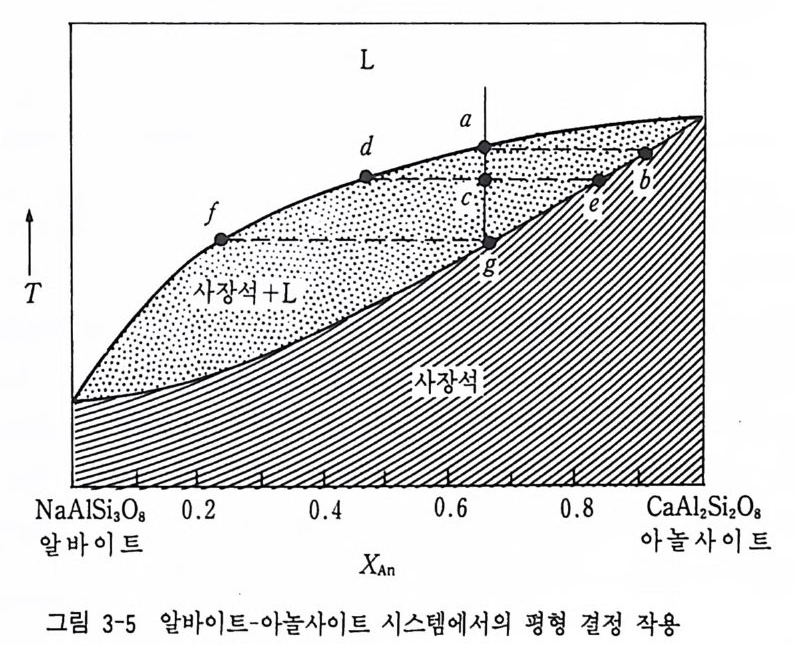
(4) 2 성분 고용체 시스템 2 성분 고용체의 경우 T_x 다이어그램과 G-x 다이어그램은 그림 3-5 와 같다. 성분 1 과 성분 2 의 고용체로 된 A, B 상에서 정출되는 고용체 광물은 고체상선과 액체상선이 각 단성분 (Xx=O, Xx=l) 에서 정출되는 고용체 고체상 광물이 단성분과 감은 순수 성분 Xx 를 가질 수 없는 한 정된 값을 가지는 특징을 가진다. 즉 G-x 다이어그램에서 A 상과 B 상의 2 상의 커브가 순수 단성분에서 만나게 된다. 이와 같은 고용체의 실례는 사장석 이 다 (그립 3~5 ) .
 L
L
XAn=O.5 인 고온의 액이 냉각될 때 평형 정출 과정이라면 먼저 d 점에 이르면 고용체 성분 e 광물 (Anao) 이 정출되기 시작한다. 온도가 내려감 에 따라 액의 성분은 d ➔ f 커브로 변하고 고체 광물의 성분은 e ➔ g 로 향하여 변화된다. Ta 온도에서 액이 전부 없어질 때까지 A 店 o 의 사
장석이 정출된다. 마그마가 냉각될 때 액체상과 결정이 서로 평형상태에 있을 경우와 비 평형 상태에 있을 경우에 따라, 고용체에서도 다른 현상이 일어난다. 알 바이트와 아놀사이트 계에서 결정이 정출된 후 중력에 의해 침전되어 계 에서 빠져나가면 잔액에는 알바이트 성분이 점점 부화된다. 계속적으로 정출된 결정이 계에서 빠져나가면 최종적으로 남은 잔액은 순수한 알바 이트 성분이 될 수 있다. 결정과 액 사이에서 바평형 과정으로 정출이 계속되면 하부에 침전된 사장석에는 아놀사이트 성분이 많고 상부에 침 전된 결정에는 알바이트 성분이 우세해지게 된다. 그러나 광물이 액에서 느린 속도로 빠져나가면 액과 결정 사이에 부분적인 반응이 일어나 사장 석의 누대 구조 (zonal s t ruc tu re) 가 발달하게 된다. 고용체와 공융계의 복합상 또는 2 개의 공융점을 가지는 복공융계 (double eute c tic ) 등이 있다. 복공융계의 경우 실리카-네펠린 계를 예로 들 수 있다(그림 3-6). 실 리 카 (Si0 2 ) 와 네 펠 린 (NaA!S i O ◄) 계 에 서 는 2S i 0 곱 NaA1Si0 4 = NaAISia O s 과 같은 반응에서 알바이트 상이 형성될 수 있다. 상률식에 의하면 3 개 의 상이 공존할 수 없다. 왜냐하면 액체상과 합해서 4 상이 되기 때문에 /=c-P+1=2 ― 4+1 에서 /=-1 이 된다. 따라서 실리카적알바이트 또는 네펠린-알바이트는 공존할 수 있 으며 그 광물상의 쌍이 그립에서와 같이 복공융점을 형성한다. 이 경우 에는 초기의 액의 성분은 순수한 알바이트 성분과 바교해서 실리카 포함 량의 다소에 따라 결정된다. 이 상률도에서 3 개 고체 광물이 공존 불가 능하며 실리카와 네펠린이 동일한 멜트로부터 동시에 정출될 수 없음을 말해 주고 있다.
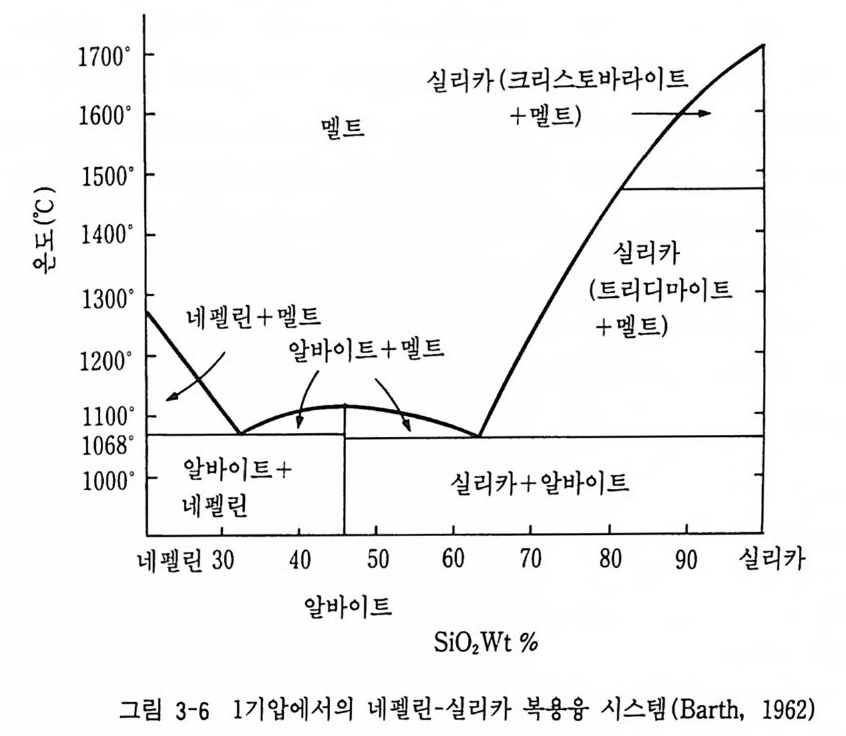 1700'
1700'
(5) 3 성분 시스템 액체상이 포함된 3 성분계의 T-x 다이어그램은 1 성분이나 2 성분계에 서와는 달리 3 차원 입체적인 그림이 얻어진다(그림 3-7). 이는 일정한 압 력에서 얻어진 A-B, B-C, A-C 3 개의 2 성분계를 조합하면 된다. 이 그 림에서 점선은 등온선을 나타낸다. 그림에서처럼 A-B, B-C, A-C 각 공융점에서 3 상 공융점을 잇는 선을 그림의 위쪽에서 아래쪽의 A, B, C 3 상 삼각도에 수직으로 두영하면 3 성분계 싱물도가 얻어진다. 아놀사이트 (CaAl2S i 2 아)-두휘석 (CaM g (S i 03)2)- 마그네슘 감람석 (Mg S i0 4 ) 계의 3 성분 상률도의 실례를 들면 그립 3-8 과 같다.
액의 성분 a 인 마그마가 냉각되면 먼저 마그네슘 감람석이 정출되고 b 점까지 온도가 내려가면 투휘석이 정출된다. 계속 온도가 내려가면 액 의 성분은 g -d 선을 따라서 변화되면서 d 점에 이르면 아놀사이트가 정 출되어 최종 정출 산물은 마그네슘 감람석 - 두휘석 - 아놀사이트가 된다. 평형 정출 (e qu il i br i um crys t a l l iza t ion ) 과정이면 처음 액의 성분과 동일한 비를 가지는 마그네슘 감람석-두휘석-아놀사이트가 정출되고, 분별 정 출 (frac ti on al cry st a l l iza t ion ) 과정인 경우에는 처음 액의 성분과는 상이한 d 점에 해당되는 레버 룰 Oever rule) 에 따라 계산되는 비율의 세 광물이 정출된다.
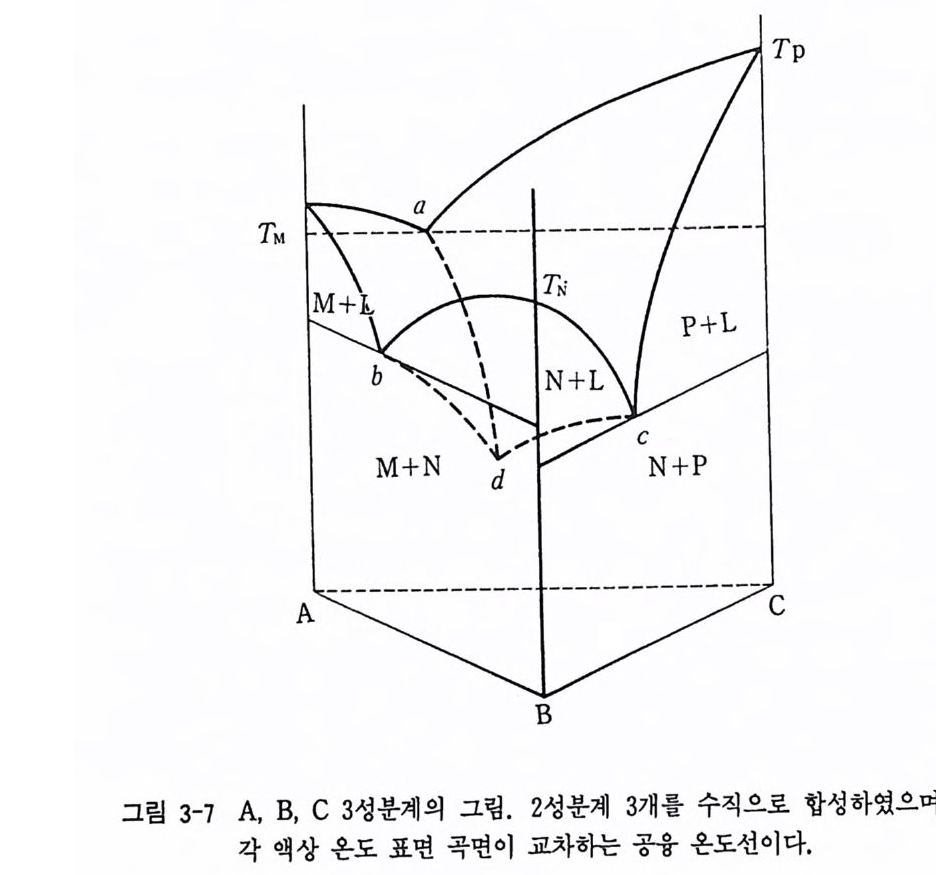 Tp
Tp
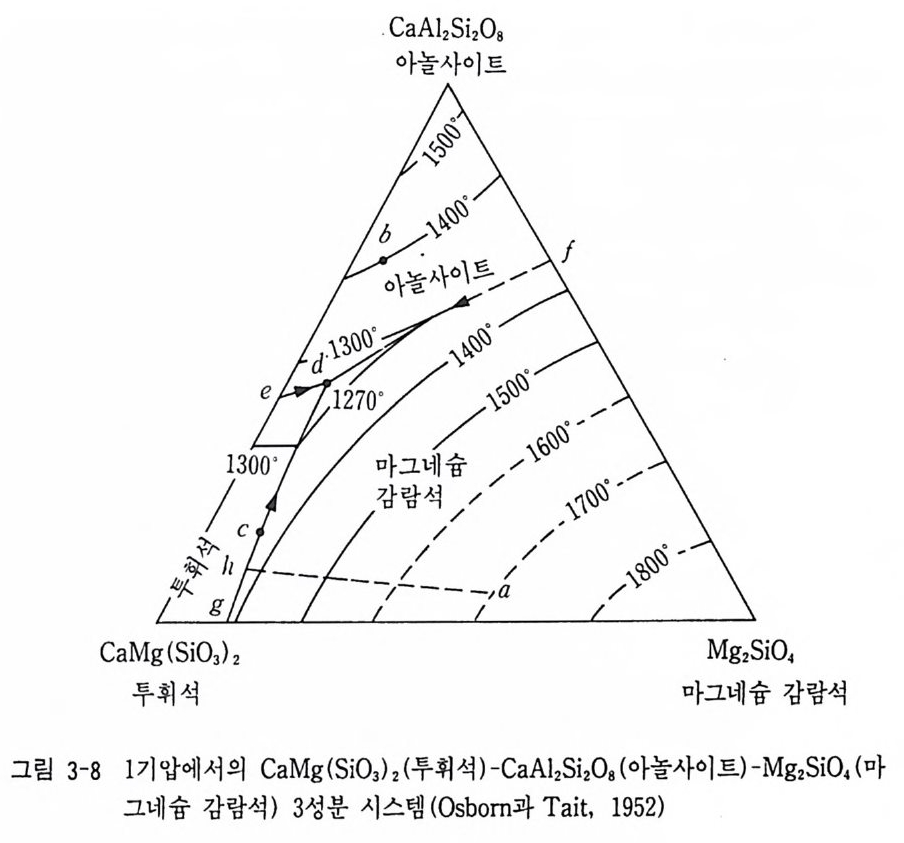 CaAbSi2 0 8
CaAbSi2 0 8
3 성분계에서 고온 액체상(마그마)에서 온도 저하에 따라 광물이 정출 될 때 냉각 과정은 다음과 같다. 그림 3-9 의 A, B, C 3 성분 상률도에 서 광물상을 각각 M, N, P 상이라 하자. 성분 x 인 액체상이 1400·c 이상에서는 액체상만이 안정하다. 그러나 1400·c 에 이르면 100 % C 성 분인 P 상의 광물이 정출되기 시작한다. C 와 x 를 잇는 직선을 따라 온도 가 계속 내려가면 P 상의 결정의 정출량은 증가하게 된다. 1300·c 에 이 르면 액의 성분은 x 점의 성분에서 y점의 성분으로 변하고 정출된 P 상의 양은 레버 룰에 의하여 x y/C y가 되며 잔액의 양은 Cx/C y가 된다. 계속 온도가 내려가면 1200·c 인 2 점에서는 100% B 성분인 N 상이 정출되기
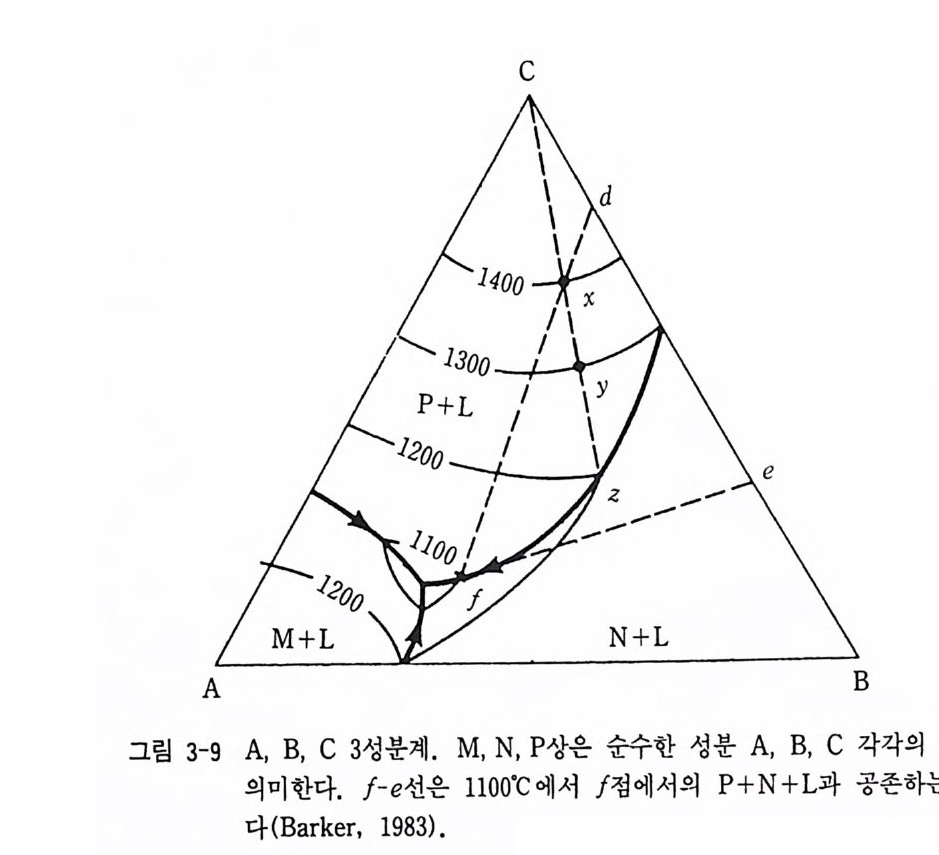 c
c
시작한다. P 상 광물과 N 상 광물은 공융선인 P+N+L 선을 따라 그 광 물이 계속 정출된다. 점 I(1100·c) 위치까지 정출이 계속되었다면 이때 까지 정출된 P 와 N 의 양의 비는 Bd 와 Cd 의 레버 룰의 비가 된다. 11oo·c 가 된 순간 정출되는 P 상과 N 상의 양의 비는 1 점에 접선이 BC 선 상에 만나는 e 접인 Be 와 Ce 가 된다. 온도가 계속 3 공융점으로 진행 되면 3 공융점에서 100 % A 성분인 M 상의 광물이 정출된다. 이때 잔액 이 소진될 때까지 M, N, P 가 정출된다. 폐쇄계의 평형 정출 과정이라 면 최종 정출된 광물상의 조합 M+N+P 의 비는 최초 액의 성분 x 점의 성분비와 동일하게 된다. 그러나 분별 정출 과정이라면 최종 광물상의
조합의 양의 비는 3 공융점에 해당하는 비가 된다.
 CaMg (SiO l ) 2
CaMg (SiO l ) 2
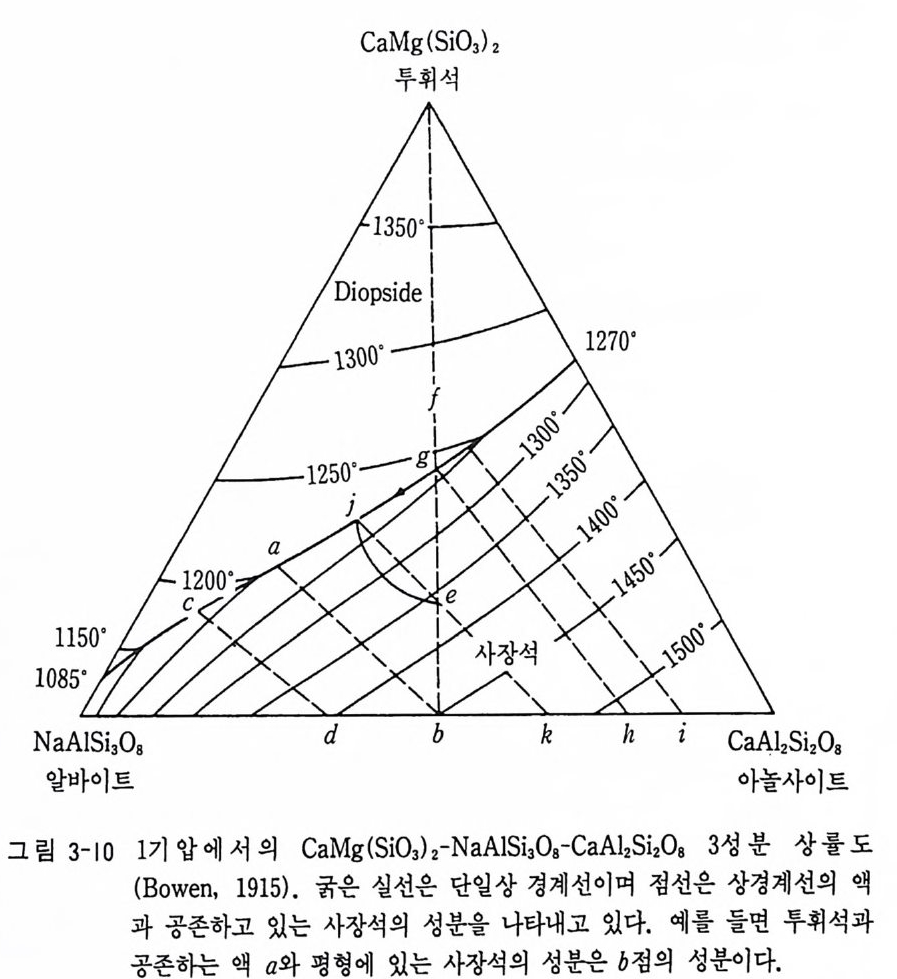
고용체를 수반하는 3 성분계의 예는 투휘석-알바이트-아놀사이트 계의 예를 둘 수 있다(그림 3-10). 이 경우 1 점에 해당하는 성분의 마그마가 냉 각되 어 액 상 표면 (liqu id u s sur fac e) 에 도달하면 두휘 석 이 정 출되 기 시 작한다. 온도가 계속 내려가 g접에 이르기까지 두휘석의 정출은 레버 룰 에 따라 정출량이 증가하고 g점 온도에 이르면 h 점 성분의 사장석 이
정출되기 시작한다. 온도의 저하에 따라 액의 성분은 g-+ a 를 따라 변 화하며 사장석의 성분은 h-+ b 로 변화하게 된다. a 점의 온도에서 잔액 이 모두 소진되고 최종 사장석 (b 점의 성분)의 정출로 결정화가 끝난다.
 `` J2` %\ o\\ B\
`` J2` %\ o\\ B\
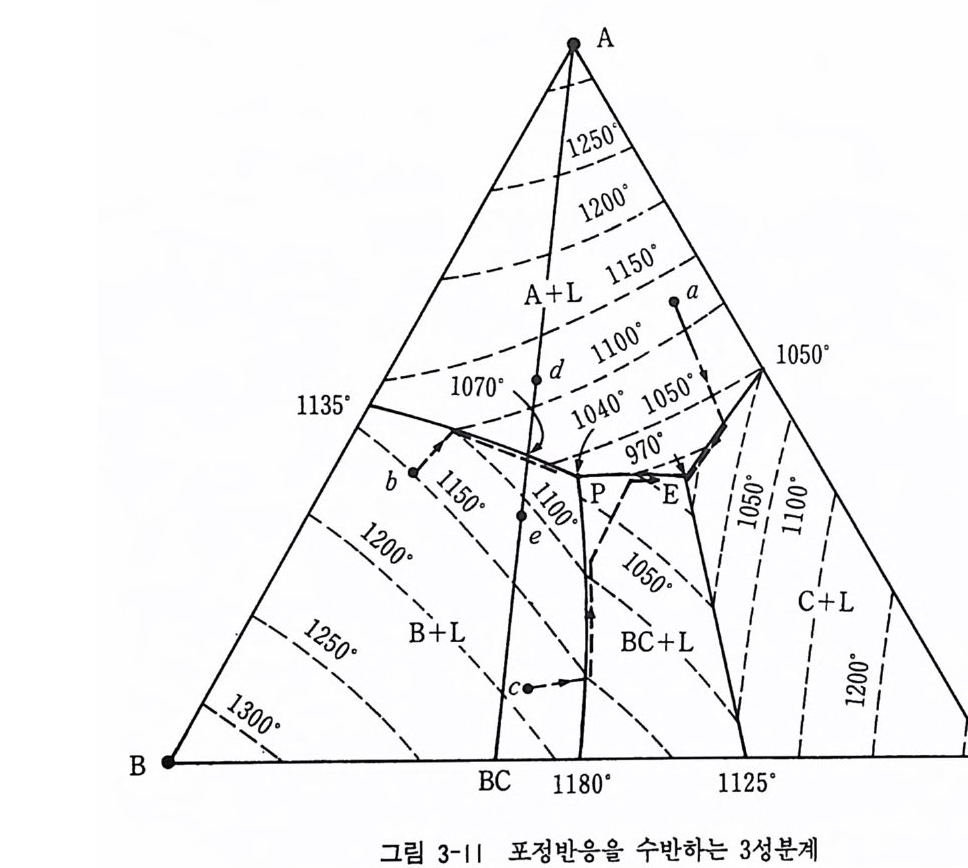
포정 반응을 수반하는 3 성분계의 마그마에서 광물 정출이 일어나는 과 정을 알아보자. 포정 반웅울 수반하는 3 성분계 상률도 그림 3-11 에서, 표시된 a, b, c, d 의 각 성분 마그마가 냉각될 때 일어나는 결정화 과 정을 설명하면 다음과 같다. 성분 a 인 마그마는 112s·c 에 이르면 A 상 의 결정이 정출되기 시작하여 1020·c 온도에 C 상과의 경계선에 접할 때 까지 계속 A 상이 정출되다가 C 상과의 경계에 접하면 C 상이 A 상과 함께
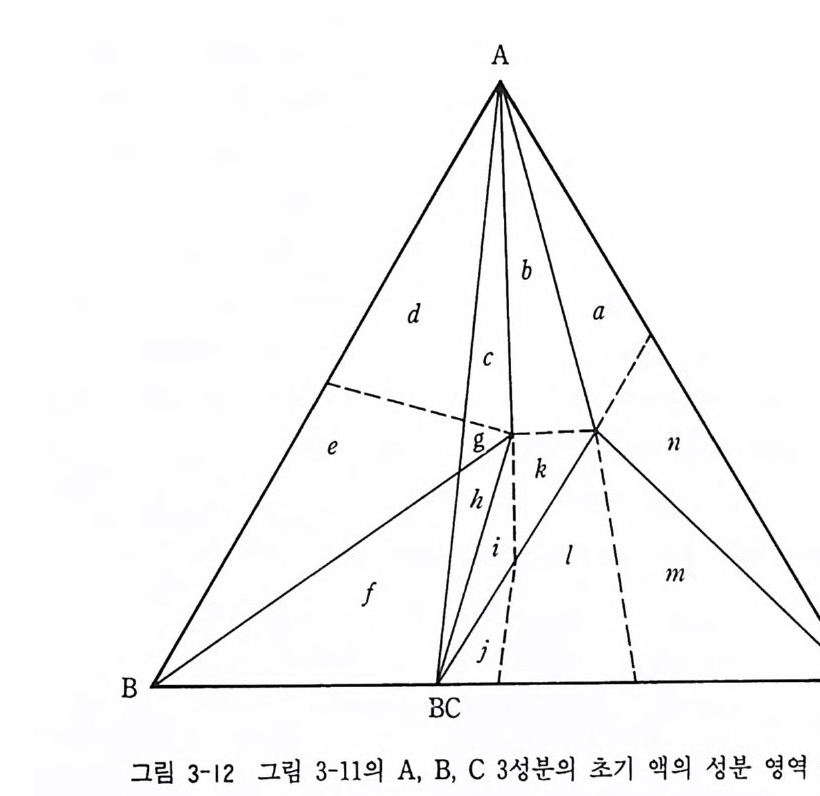
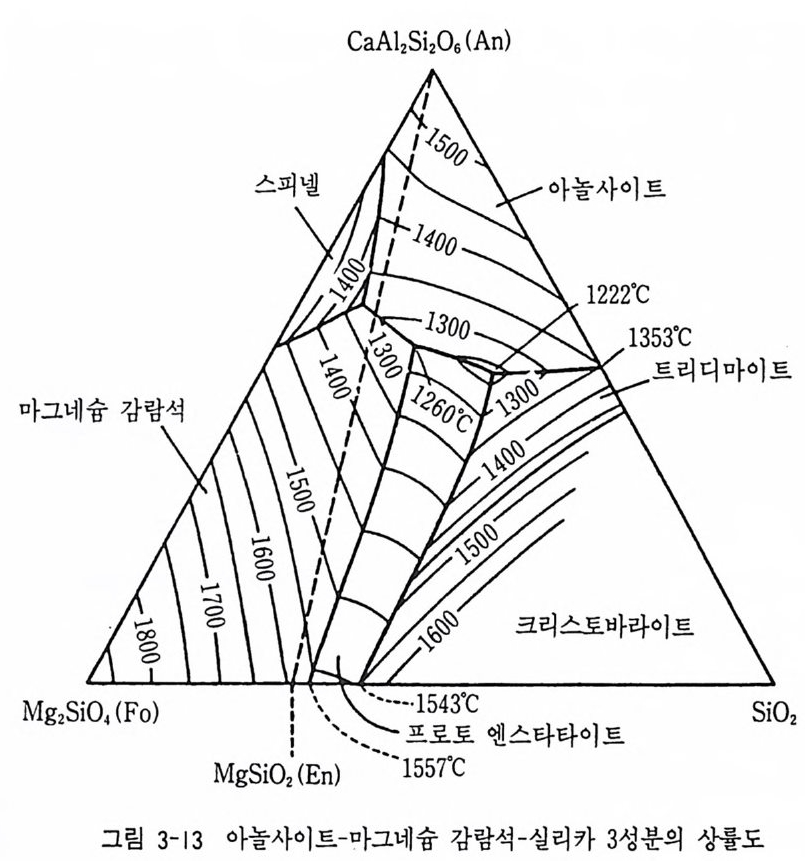
E 점 (970 ·c) 에 이를 때까지 정출된다. E 점에서 BC 상이 정출되어 최종적 으로 A+BC+C 상이 정출된다. 성분 c 인 경우 1185·c 의 온도 곡면에 이르면 B 상의 정출이 시작된다. 1150·c 까지 B 상이 계속 정출되며 l150°C 에 이르면 B 상과 액이 반응(포정반응)하여 BC 상이 만들어진다. c 점 과 BC 점을 잇는 선과 만나는 11oo·c 온도에서 B 상의 결정이 모두 포정반응으로 BC 상으로 변하여 10oo·c 의 A 상 영역에 이를 때까지 BC 상의 정출이 계속된다. 1000·c 에서 A 상과 BC 상이 계속 정출되어 E 점 에 이르면 C 상이 정출되어 최종적으로 A+C+BC 상이 정출된다. 이와 같이 광물의 최종 정출 산물은 액의 성분에 따라 다르다. 예 를 들 면 그립 3 - 12 에서처럼 초기의 액의 성분에 따라 최종 결정 광 물상은 다음과 감은 정출 과정으로 최종 광물 조합이 결정된다. a L= A , L= A + C , L= A+B C+ C b L= A , L= A + B C, L= A+B C+ C C L= A , L= A+B . L+ B = A+B C. L=A+ B C, L=A+ B C+ C d L= A , L= A + B , L+ B = A+B C e L= B , L= A+B , L+ B = A+B C I L= B , L+ B = B C, L+ B = A+B C g L= B , L= A + B , L+ B = A + B C, L=A+ B C, L =A+ B C+C lI L= B , L+ B =BC, L+ B = A+B C, L=A+ B C, L= A +BC+ C L= B , L+ B = B C, L= B C, L=A+BC, L=A+BC+ C j L= B , L+ B =BC, L=BC, L =BC+ C ,L=A+BC+ C k L=BC, L=A+BC, L= A + B C+ C l L= B C, L=BC+C, L=A+ B C+ C )I1 L=C, L=BC+ C , L=A+ B C+ C n L=A, L=A+C, L=A+ B C+C 실제 포정반응을 수반하는 광물의 상률도는 아놀사이트-마그네슘 감람 석 -실리카―엔스타타이트 계를 들 수 있다(그림 3-13). 실제 초염기성 암석에서 감람석 주위에 휘석의 반응연 (reac ti on ri m) 이 관찰된다.
 A
A
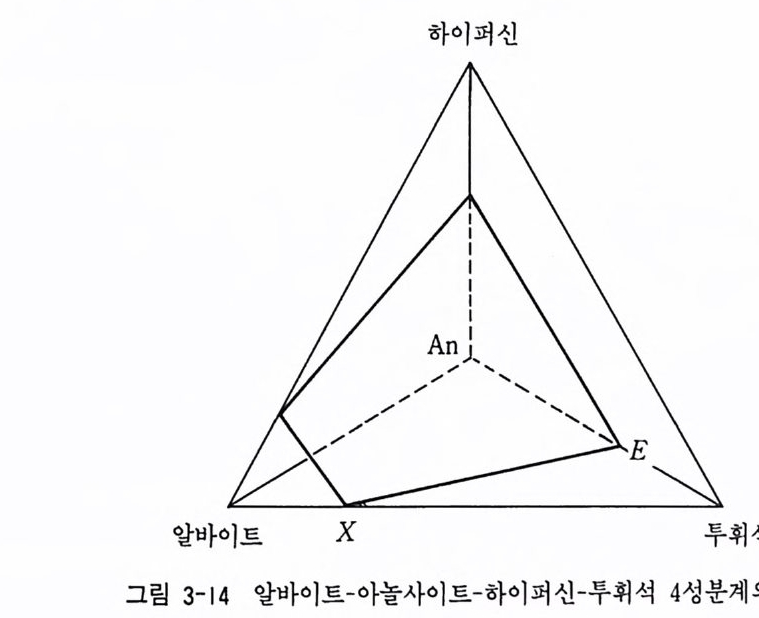
(6) 다성분계 지금까지 고려한 성분은 현무암질 마그마 성분에 유사한 Si0 2 , Al203, Mg O , Ca0, Na20 의 다섯 가지의 산화물의 예로 설명하였다. 그러나 실제 현무암은 이 성분 이의에도 FeO, Fe20a, K20, H20, Ti0 2 등과 같은 중요 구성 성분을 가지고 있다 . 보다 실제 암석에 가까운 상률도를 만들려면 가능한 한 많은 구성 성분의 수가 고려되어야 하고 온도, 압 력, 가스 성분 (CO2, H20 등) 조건 등도 다양하게 고려되어야 한다. 3 성 분 이상의 다성분계가 되면 평면상에 나타내기 어려워지게 된다. 예를 들면 알바이트-아놀사이트-하이퍼신-두휘석의 4 성분계는 그림 3-14 와 같
이 나타낸다.
 CaAl2Si2 0 s (An)
CaAl2Si2 0 s (An)
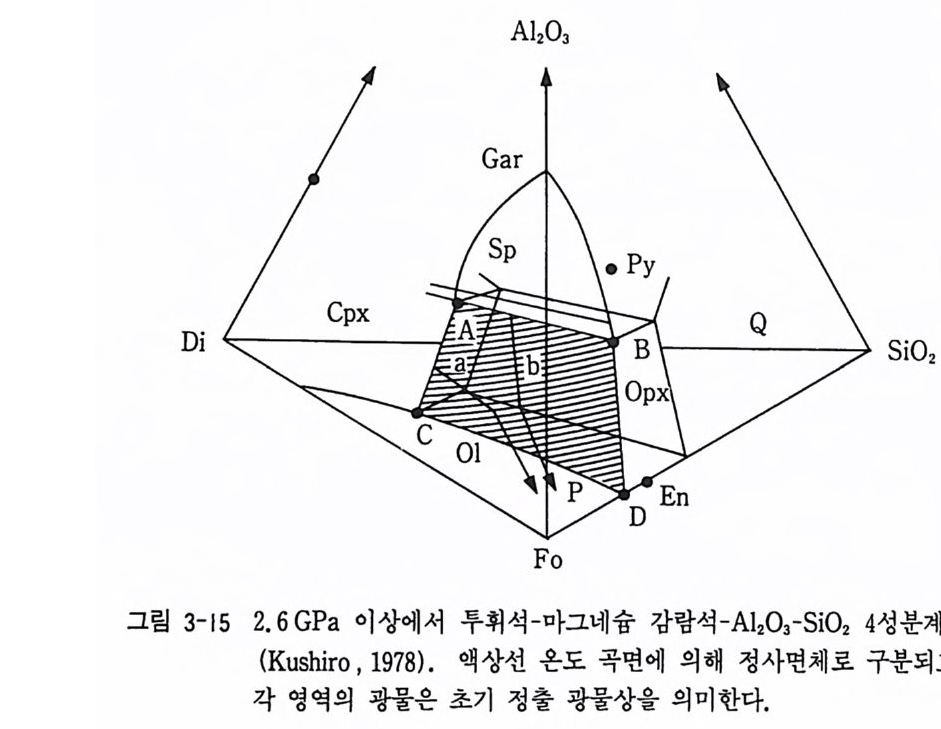
페리도타이트가 분별 융해되어 현무암질 마그마를 형성할 때 투휘석 -마그네슘 감람석 -Ab03-S i 02 의 4 성분계를 예로 들어보자. 그림 3-15 는 Kushir o (19 78) 에 의 하여 압력 2. 6 GPa 이 상에 서 만들어 진 4 성 분 상평 형 도이다. 상부 맨틀 구성 암석인 페리도타이트 암석의 성분 (P 점)이 부분 용융되어 현무암질 마그마 (A 점의 성분)를 형성할 때의 평형 용융 과정은 다음과 같다. 만일 P 점 성분을 가진 암석에서 평형 용융 작용이 일어난 다면 용융된 멜트의 성분은 최초의 A 성분에서 화살표 방향으로 광물
 하이퍼신
하이퍼신
 Al2°3
Al2°3
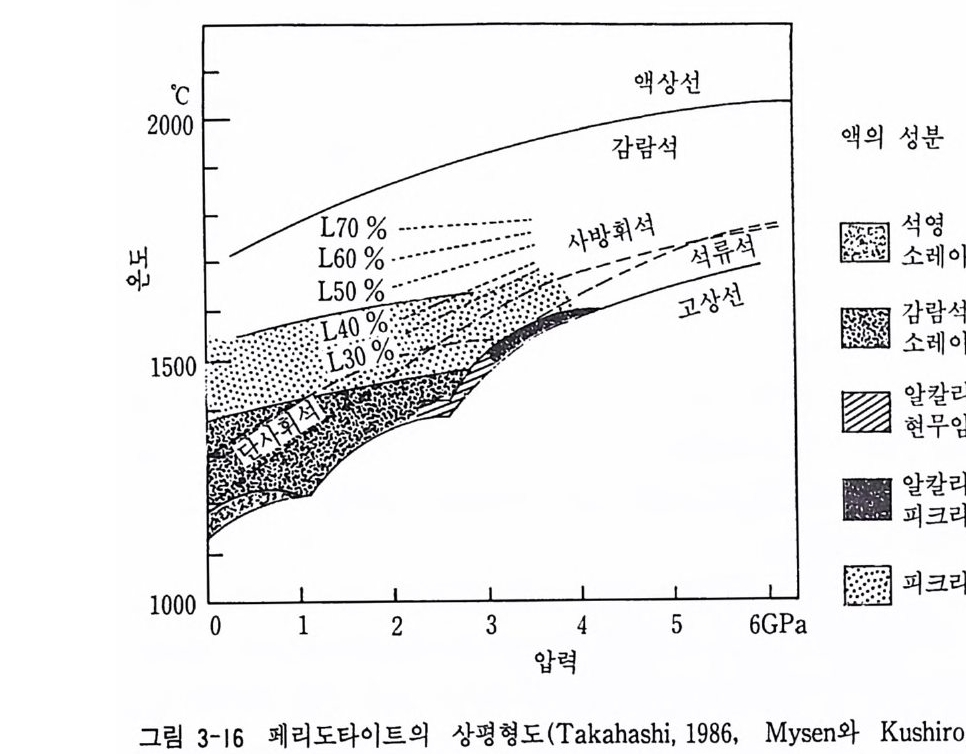
결정과 계속 반응 평형이 유지되면서 최종 P 의 멜트가 된다. 멜트비는 CaO, Ah03 성분이 포함되어 있으므로 저압에서 사장석이 정출되며 A 의 성분은 염기성 (ma fic)이 된다. 만일 분별 용융 과정이라면 멜트 A 가 암석에서 점차 제거되어져 고체 광물 성분은 변화되지만 각 단계에 형성 된 멜트는 A 로 계속된다. 계속 멜트가 일어나 암석 중의 두휘석 광물이 전부 녹아 없어지면 멜트의 성분은 B 로 변화하고, 광물 중의 Al2 야 성 분이 전부 없어지면 멜트는 C 로 점프된다. 또한 B 의 멜트가 녹아 광물 중의 Al203 성분이 전부 없어질 경우 D 로 점프한다 (Su gi mura. 1987). Fe 와 M g의 상호 치환에 의하여 그림에서 두휘석이 되어 단사휘석이나 엔 스타타이트 등이 형성된다. 위의 상평형도에서는 초염기성암의 주요 성 분인 Fe 가 빠져 있다. 다성분 의에 온도와 압력 조건의 변화가 마그마의 성분 변화에 영향을 준다. 예 를 들면 Takahashi 0 986) 와 M y sen 과 Kushir o (1977) 의 페 리 도 타이트의 상평형도(그림 3-16) 에서 P, T 조건에 따라 안정 광물상과 액 상의 성분이 표시되어 있다. 죽 저압, 저온 조건에서는 주로 감람석-소 레아이트질 마그마가 형성되며 이때 고체 광물인 감람석, 사방휘석, 단 사휘석이 이들 마그마와 평형상태에 있다. 그러나 온도와 압력이 변화되 면 알칼리 현무암질 또는 감람석이 많은 피크라이트질 마그마 성분이 된 다. 3-3 그래프 표시법 액체상이 포함되지 않은 3 성분계에서는 고체상만의 광물상으로 삼각 다아어그램을 그린다. 공존하는 상의 성분은 동일 직선으로 서로 연결한 다. 그러므로 작은 삼각형 모양은 평형에 있는 광물 조합을 의미한다. ACF 다이어그램은 그 한 예로서 변성암석학에서 많이 이용되고 있다.
 ·c 액상선
·c 액상선
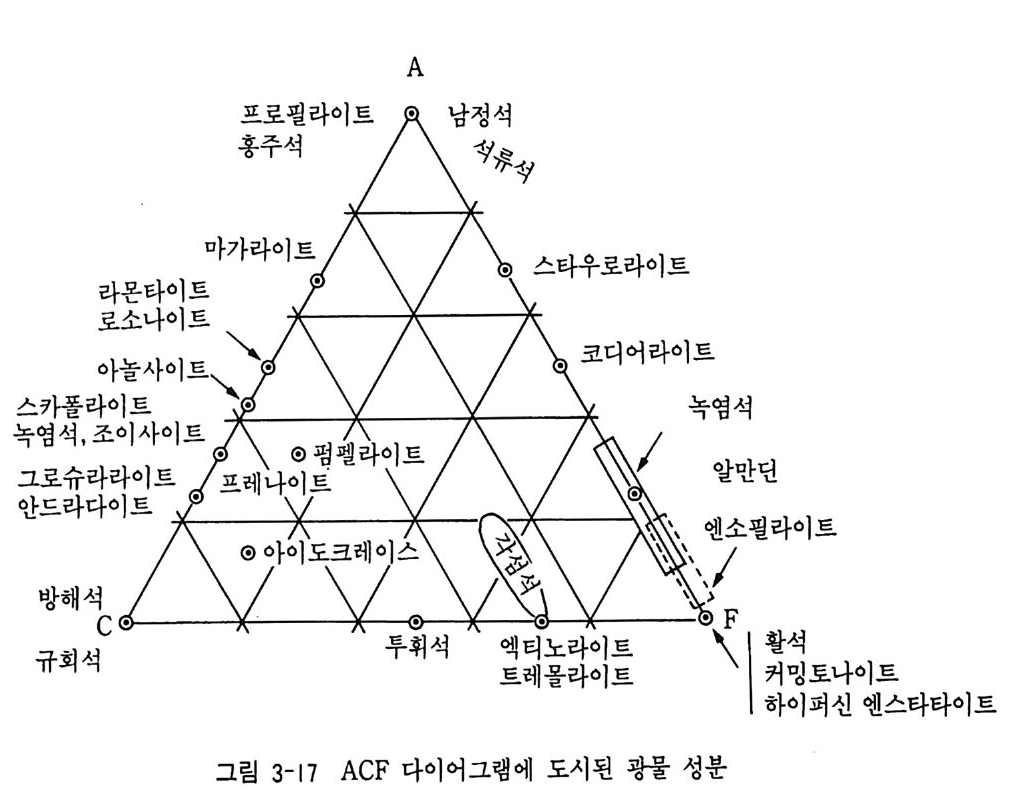
ACF 의 3 성분은 A=Ab03 + Fe203 -Na20 —K2 0 C=Ca0-3. 3P20s F=FeO+Mg O +MnO 변성 반응의 P-T 다이어그램에서 나타난 ACF 다이어그램의 예는 그림 3-17 과 같다. 이 ACF 다이어그램은 등온, 등압에서 얻어전 것으 로 물론 P, T 가 변화되면 광물 조합이 달라진다. 이처럼 변성 조건의 변화에 따른 변성상 연구에 ACF 다이어그램이 대단히 유용하게 이용되 고 있다. 이의에도 변성 광물의 공생 관계 표시에 AFM 다이어그램과 AKF 다이어그램 등이 사용되고 있다.
 A
A
제 4 장 동위원소 지구화학 동위원소란 용어는 영국의 Sodd y가 처음 사용하였으며 원자번호는 같 지만 중성자 수가 다르기 때문에 질량수가 다른 원자나 원자핵을 동위원 소(i so t o p e) 라 한다. 멉 0 처럼 표시하며 18 은 질량수, 8 은 원자번호롤 가 리킨다. 예를 들면 산소 동위원소 1:0, 1~0. 1go , 수소 동위원소 iH, fH (D), fli, 탄소 동위원소 1lc, 방 C, 1tc 등이 있다. 일반적으로 동일한 원소의 동위원소들은 그 화학적 성질이 유사하지만 위에서 예시한 수소 의 f H 과 탄소의 1 t C 은 기타 예시한 동위원소들과는 핵의 안정성과 화학 적 성질에 큰 차이가 있다. 즉 동위원소는 3H 나 14C 처럼 핵종이 반감기 로 붕괴 하는 불안정 한 방사성 동위 원소 (radio a cti ve iso to p e ) 와 lH, D, 12c, 13c 등과 갇이 핵종이 안정한 안정 동위원소 (s t able i so t op e) 로 대분된다. 동위원소는 암석의 절대연령 측정, 트레이서, 암석의 열역사 해석, 암 석의 성인 연구 , 물질의 기원, 암석 광물의 생성 환경, 물질의 순환, 환
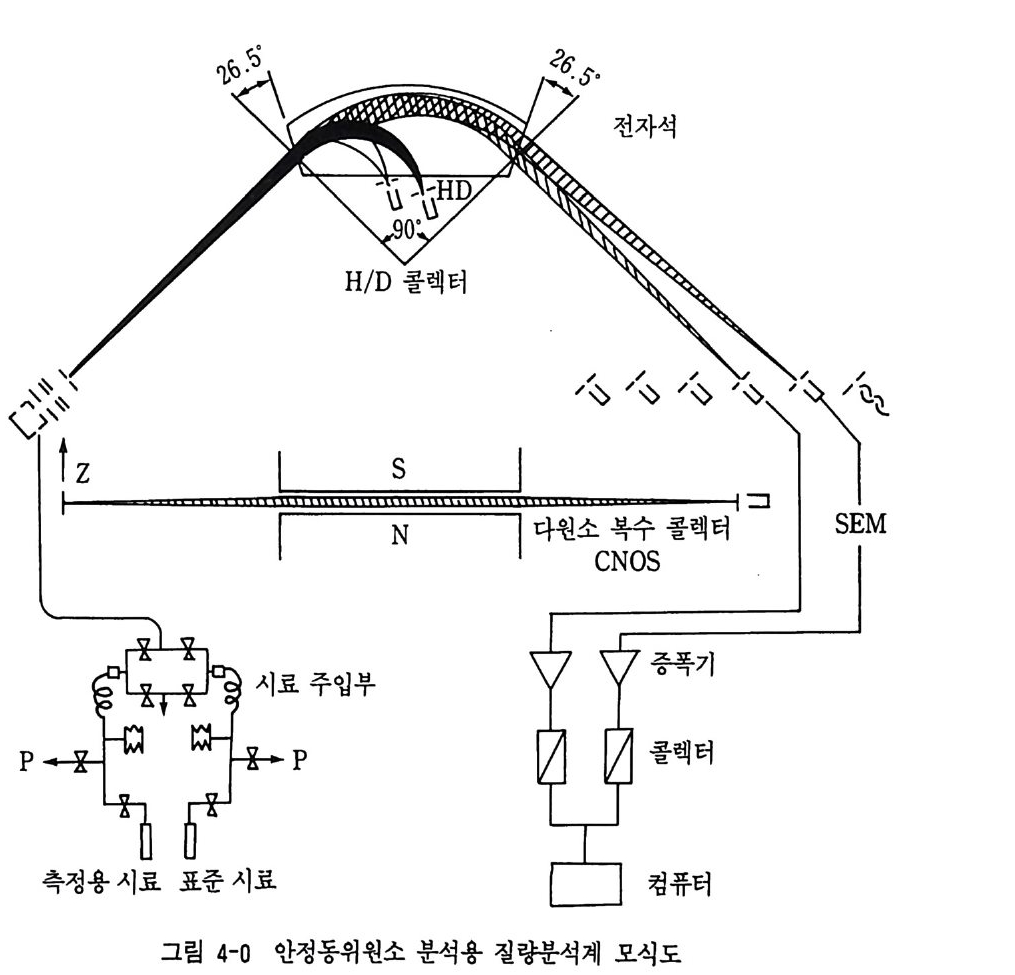
경 오염 연구 등 지구과학의 많은 분야에서 이용되고 있으며 지각, 해 양, 지구의 전화 연구와 우주의 전화 연구에 크게 기여하고 있다. 4-1 질량 분석 동위원소는 중성자 수의 차에 기인한 질량의 차이로 구분할 수 있으므 로 질량 분석법의 개발로 정량화될 수 있게 되었다. 지구과학에 많이 사 용되고 있는 질량분석기는 가열 이온화 질량분석기 (the rmal ion iz a ti on mass spe c tr om ete r ) 와 가스용 질 량분석 기 (ga s source mass spe c tr o mete r ) 이 다. 질량 분석 장치는 크게 표준 시료와 측정 시료를 질량분석기로 도입 시키는 시료 주입부 (source), 편향 자장에 의해 질량별로 분리시키는 분 석부 (anal y zer) 및 이온을 검출하는 측정계 (collec t or) 로 구성되어 있다 (그립 4-0). 가스용 질량분석 기는 고전류 (3kV 정도) 하에서 시료 가스를 이온화시켜 편향자장 내에서 질량별로 분리시킨다. 질량 m인 이온을 전 위차 V 로 가속시킬 때 필요한 에너지 E 는 E=eV=—12 mv 2 이다. 여기서 v 는 이온의 속도이고 e 는 전하이다. 동일한 전위차 V 에 의해 가속되기 때문에 동일 전하를 가지는 이온은 동일한 운동에너지를 가지고 이온원을 통과한다. 그러나 질량이 다를 경우 v=2P !- 에서처럼 그의 속도가 다르다. 이온이 자장 내를 통과할 때 HeV=V~r2
 전자석
전자석
조건에 맞게 타원형으로 편향된다. 여기서 r 은 휘어진 자석의 반경이며 H 는 자장의 강도이다. 이 관계에서 m H2r2 e 2v 이 얻어진다. 이를 반경 또는 H 에 대하여 정리하면 r=l43H95 른 와
H=l43.95 广 r v e 가 된다. 죽 이온화된 가스는 질량이 큰 가스 조합이 가벼운 것보다 더 큰 원을 그리며 편향자장 내를 통과하게 된다. 또 v, r 을 일정하게 고 정시키면 m/e 의 차이는 H 의 변화로 나타나 측정부에서 이온 전류의 강 도비를 측정하여 질량으로 환산하게 된다. 4-2 방사성 동위원소 방사성 동위원소는 붕괴할 때의 반감기를 이용하여 지구 및 우주연대 학 연구에 많이 이용되고 있다. 장반감기 방사성 동위원소는 주로 지구 및 태양계 구성 물질의 절대연령 측정과 지각, 맨틀의 진화, 우주의 진 화 연구에 이용되며 단반감기 동위원소는 고고학에 이용된다. 운석 등에 서 29I, 2sAl 과 같은 소멸 핵종은 태양계 형성 초기물질의 동정에 이용된 다. 또한 방사성 핵종이 지구화학적 트레이서로 이용되어 맨틀 물질의불균질성, 광상구의 구분, 마그마의 혼합, 해수의 혼합, 탈가스, 지각과 맨틀 물질의 순환 연구에도 응용되고 있다. 지구과학에 많이 이용되고 있는 방사성 동위원소의 종류와 반감기는 표 4-1 과 갇다. 방사성 동위원소의 붕괴 속도는 앞장에서 설명한 화학 반응의 반응 속 도 관계식인 뿜=潭 에서 유도된 것으로, t 시간 붕괴 후에 암석 광물의 시료 속에 들어 있 는 방사성 동위원소의 수 N, 붕괴 전(t =O) 에 시료 속에 포함되어 있는 동위원소의 수 No 를 적분구간으로 적분하면 1No 짱= —Aj ::Od t 의 관계로 표현된다. 이 식의 해는 log frNo =— At 이다. 우변을 상용대수로 취하면 N=Noe~u (No=Neu) 가 된다. 붕괴 전과 붕괴 후의 동위원소 값의 차이를 딸원소라 하며 D=No-N 이다. D=N(eu— 1) 이 되어 t에 대해 풀면
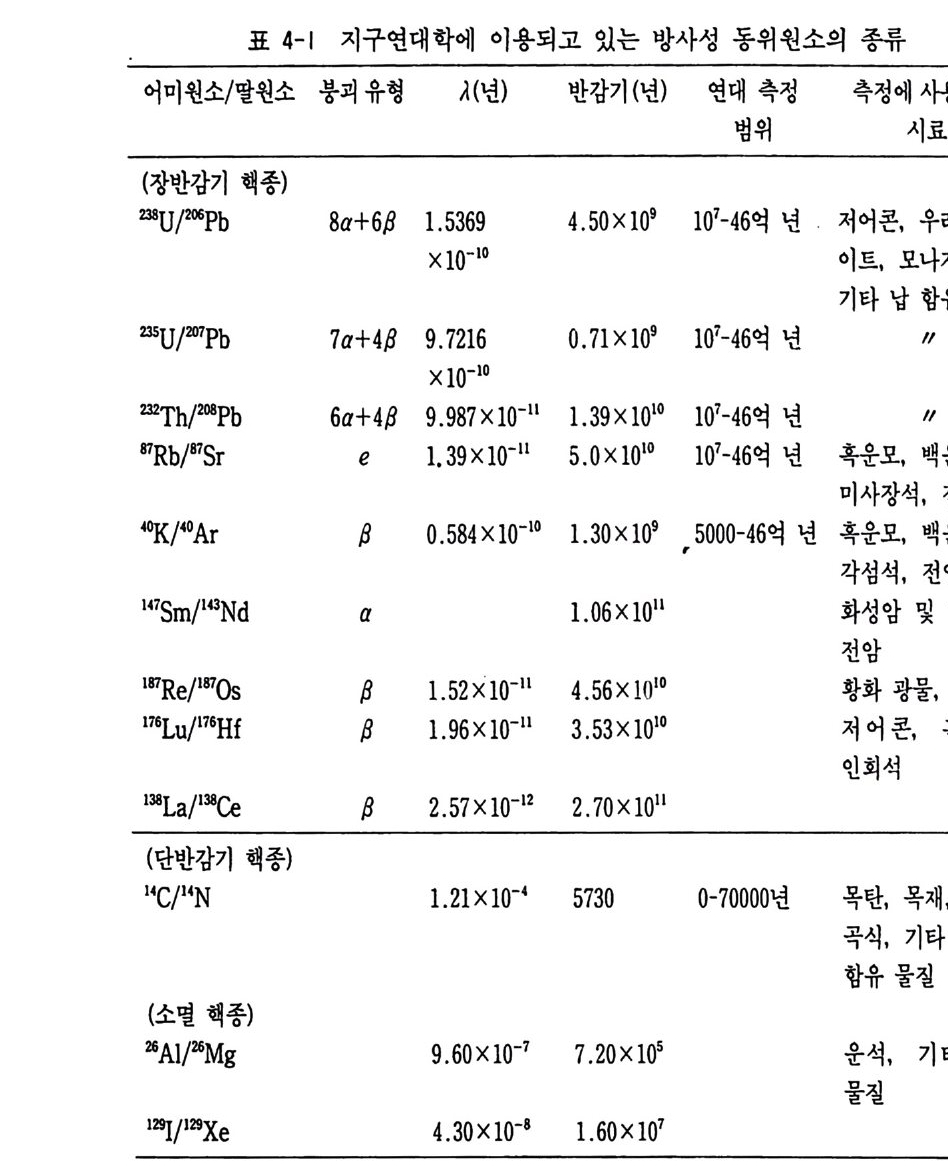 표 4-1 지구연대학에 이용되고 있는 방사성 동위원소의 종류
표 4-1 지구연대학에 이용되고 있는 방사성 동위원소의 종류
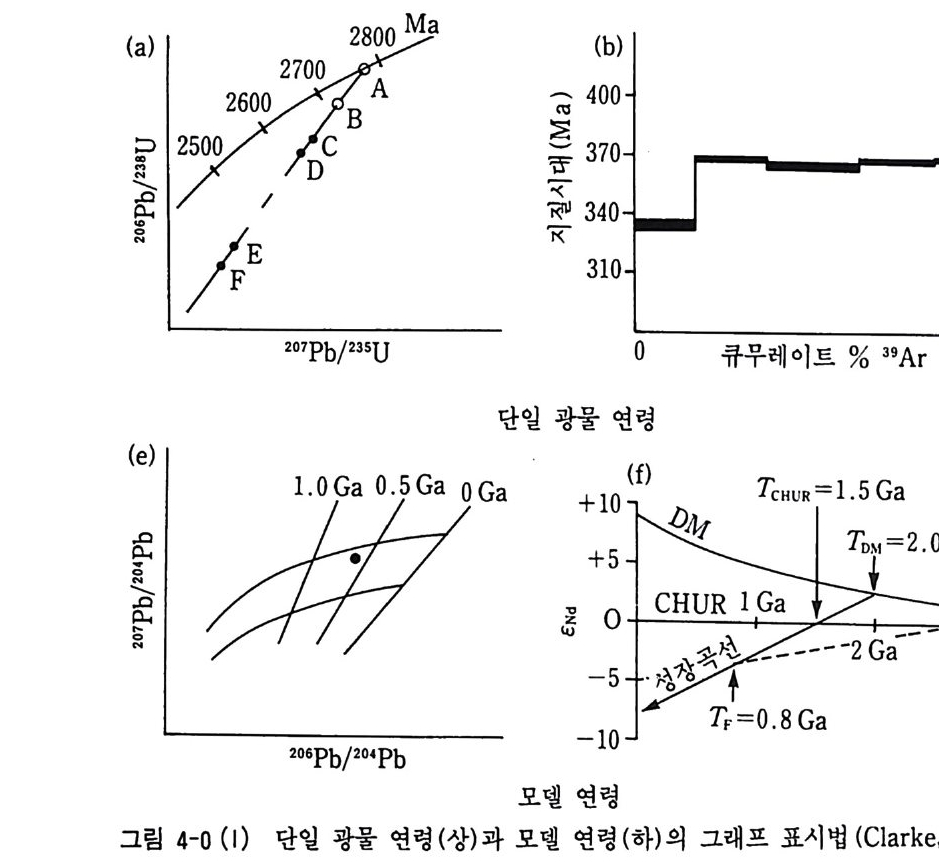
t=l].lo g (, Dw+ 1) 이 얻어진다. 이 관계식이 암석 절대연령 측정의 기본 원리가 되는 식이 다. 반감기 U1,2) 는 부이다. 암석의 절대연령은 단일 광물 연령 (sin g l e mine ral age s ), 아이소크론 연령 (iso chron age s ) 및 모델 연령 (model age s ) 이 있다. 광물 연령은 임의의 광물이 다루고자 하는 동위원소계에 대해서 폐쇄 계를 이루는 온도, 죽 동결온도 (block i n g tem p er atu r e) 이하부터의 연대 이다. 단일 광물 연령 측정은 U-Th— Pb 계와 K— Ar 계에서만 가 능하다. 왜냐하면 광물 결정구조 내의 방사성 동위원소의 존재 범위와 측정시까지의 방사성 기원 딸원소의 보존 범위에 따라 적용 여부가 결정 되기 때문이다. 예를 들면 저어콘과 인회석은 U— Th— Pb 계에서는 이용 가능하나 석영과 사장석은 이용 불가능하다. 반대로 K— Ar 계에 서는 K —장석, 흑운모, 백운모는 사용 가능하나 모나자이트와 저어콘 은 이용 불가능하다. u— Th— Pb 계에서 이용되는 광물은 보통 무시 해도 좋을 정도의 소량의 보통 납 (common lead) 을 가지고 있거나 공존 광물 중에 우라늄을 함유하고 있지 않은 황화 광물이나 K ―장석과 같 은 광물에서 보통납의 양을 측정해서 시료 광물에서 측정한 값에서 빼주 므로 광물 형성시의 보통납의 양을 정량할 수 있다. K— Ar 계에서는 동위원소의 동결온도 이상에서는 방사성 기원의 아르곤이 광물 내에 전 혀 포함되어 있지 않은 것으로 가정하여 보통 아르곤 (common ar g on) 의 보정이 필요 없다. 206Pb/238u_207 p b/235u 의 광물 연령과 Ar 유출 (Ar -release) 스펙트럼 연령은 그림 4-0 (l)과 같다. 아이소크론 연령은 Rb_Sr 과 Sm— Nd 시스템에서 많이 아용된다. 자 세한 내용은 Rb-Sr 시스템에서 설명한다. 모델 연령은 Sm-Nd 계, Rb— Sr 계, Pb_Pb 계에서 주로 적용이 되며 우리가 다루는 지각 암석
이 초기에 Nd, Sr, Pb 의 저장소(콘드라이트질 지구, 맨틀 (de p le t ed mantl e) 또는 전형적인 조산대가 될 수도 있음)에서 형성되어 현재까지 동위원소계 가 유지되었다고 가정한 연대로 지각 정체 연령 (crusta l resid e nce tim e) 또는 맨틀 유래 연령이 될 수 있다. 단일 스테이지 모델 연령과 2 스테 이지 모델 연령이 제안되어 있다. 모델 연령의 그래프 표시법은 그립 4-0(1) 과 같다. 댜에 지구과학에서 많이 이용되는 방사성 동위원소에 대하여 암석 절대연령 측정에 대한 적용 원리와 측정 결과 해석에 대하여 설명한다.
 (a) 曲
(a) 曲
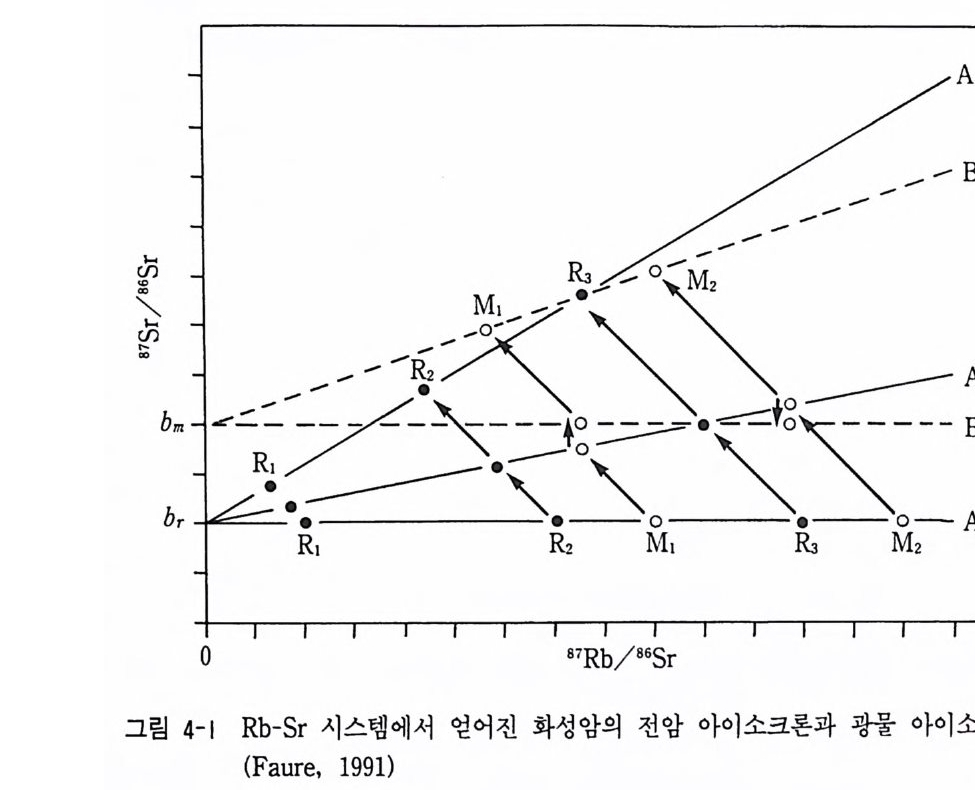
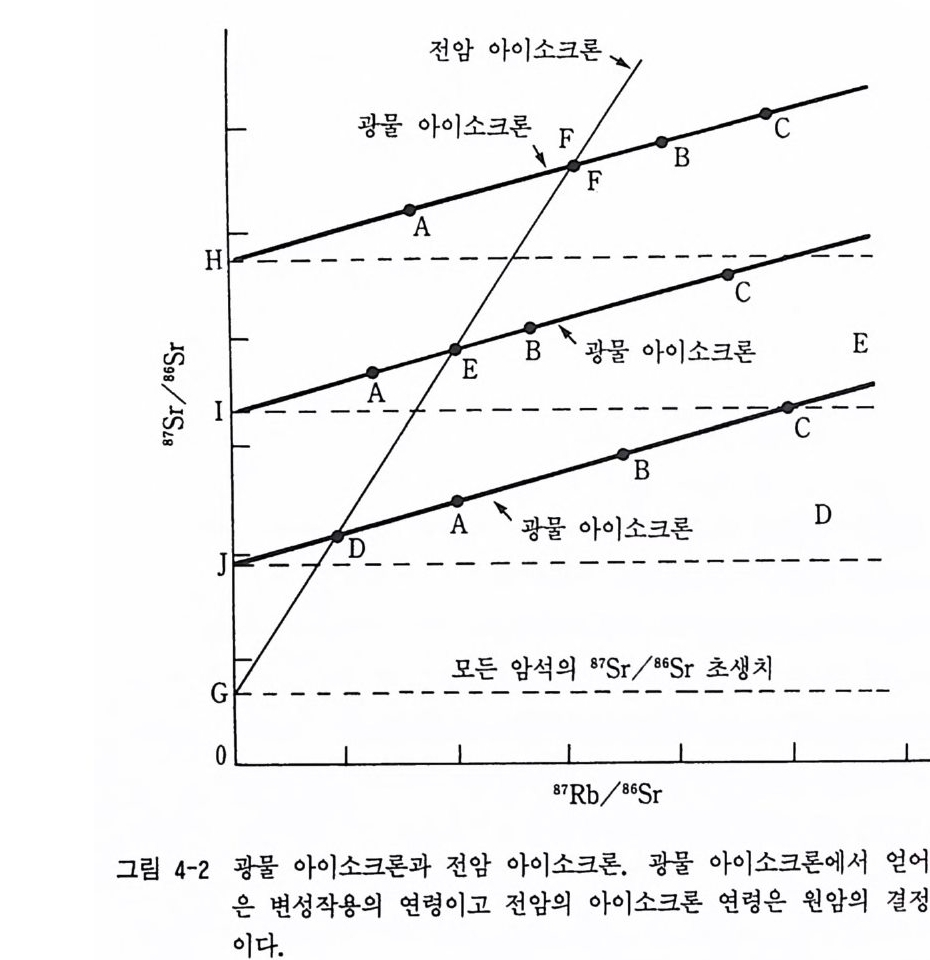
(1) 루비듐-스트론튬 시스템 자연계에서 루바듐은 동위원소가 85Rb, 87Rb 이 있으며 스트론튬은 “Sr, 86Sr, 87Sr, 88Sr 이 알려져 있다. “Rb 이 붕괴하면 87Sr 으로 된다. 이때 s1sr=s1Rb(eu —1) 관계 를 적용할 수 있다. 시료가 생성 초기에 원래부터 가지고 있는 동위 원소 를 초생치 (ini ti al ra ti o) 라 하며 87Sr 에는 81Rb 에서 생성된 87Sr 과 스 트론튬의 초생치 ( s 1sr,) 가 포함되어 있다. 따라서 87S r =“Sr, +“Rb (eAt -1) 가 된다. 동위원소는 두 동위원소의 비를 정량하는 것이 편리하고 정도 가높으므로 톱=(홀),+雪 (e-1) 의 관계가 얻어진다. :룹과 ;嬰봅 각각 y축과 x 축으로 잡으면 위의 식은 1 차식의 관계가 된다. 그러므로 동일한 암석 시료에서 서로 다른 광물이나 전암의 이들 동위원소비를 분석하여 나타내면 그림 4-1 처럼 직 선으로 나타난다. 이 직선을 아이소크론(i sochron) 이라 한다. 즉 기울기 가 암석의 생성 연대이며 87Rb/86Sr=O 인 y축에 얻어진 절편의 값이 초 생치 (87Sr /87 Sr), 이다. 초생치는 마그마의 기원과 지각과 맨틀 물질의 전 화 해석에 유용하게 이용되고 있다. 광물에서 얻어진 아이소크론을 광물 아이소크론(mi neral i sochron) 이라 하고 전암 시료에서 얻어진 아이소크 론을 전암 아이소크론 (whole rock iso chron) 이 라 한다.
 A3
A3
그림 4-1 에서 화성 암 시료 RI, R2, &와 R3 암석 중의 광물 M1 과 M2 를 표시하였다. 두 축의 축척은 같게 하였다. 화성암이 형성 당시 최초 에는 암석이나 광물이 모두 동위원소 값이 기울기가 0 이고 절편이 b r 인 A1 아이소크론에 나타난다. 그러나 시간이 지남에 따라 AI 직선 상의 모든 광물과 암석은 화살 표시 방향으로 이동하여 경과 시간에 따라 기 울기가 다른 & 아이소크론이나 如 아이소크론을 만들게 된다. 물론 기 울기가 큰 값인 A 아이소크론이 & 아이소크론보다 연령이 오래된 것 이다. 아직 절편은 같다. 이때 열변성 작용에 의하여 방사성 87Sr 동위 원소의 확산이 일어나 M1 광물과 M2 광물 내의 Sr 동위원소 성분이 변 화되어 두 광물과 & 암석이 변성작용 마지막 시기에 절편 bm 에 해당하
는 동일한 87 Sr /8 6Sr 를 가지게 된다. 그 결과 R3 암석과 광물 M1 과 M2 가 동일한 B1 아이소크론에 나타나게 된다. 그러나 R3 암석은 & 아이 소크론에 놓여 있다. 지질시대가 더 경과하면 전암 시료는 결정화 연령 이 A3 아이소크론을 만들게 되며 절편은 아직 br 이다. 그러나 M1 광물 과 庫 광물은 현재 시점에 B 2 아이소크론을 형성하게 된다. B2 아이소 크론은 동위원소 재평형에 걸린 시간으로 기울기는 A3 아이소크론보다 완만하다. B 2 아이소크론의 절편 b m 은 br 보다 큰 값이다. 왜냐하면 R3 암석의 87 Sr /86 Sr 비와 동위원소 재평형 후에 이루어진 광물의 동위원소 값이기 때문이다. Rb- S r 시스템의 전암 아이소크론은 화성암이나 고변성도 변 성암의 결정화 연령인 반면에 광물 아이소크론은 변성작용과 같은 동위 원소 재평형의 마지막 에피소드의 연령이다. 암석 형성 후에 변성작용이나 지각 변동과 같은 지질학적 사건에 의하 여 조암 광물 내의 이들 동위원소비의 재분배가 일어난다. 예를 들면 그 립 4-2 에서처럼 대규모의 화강편마암체에서 위치가 다른 가, 나, 다 세 지점에서 시료를 채취하여 이를 동위원소비를 분석하면 각 지점의 각 광 물 또는 전암 시료의 동위원소비가 다르다. 그러나 각 지점 시료의 광물 아이소크론의 기울기는 같다. 그러나 전암 아이소크론은 광물 아이소크 론보다 기울기가 급하다. 즉, 화강편마암체의 전암 아이소크론은 변성작 용을 받기 전의 화강암의 관입 연령을 의미하고 광물 아이소크론은 변성 작용이 일어날 때의 연령을 의미하여 변성 시기 해석에 이용될 수 있다. (2) 우라늄(토륨)-납 시스템 자연에서 우라늄 계열 동위원소는 238u, 23Su, 232Th 이 알려져 있다. 이들이 여러 단계 a 및 f3붕괴를 거쳐 안정한 납 동위원소인 2osPb, 201Pb, 2os p b 로 각각 변한다. 자연에서 우라늄 계열의 동위원소의 존재량
 전암 아이소크론 `
전암 아이소크론 `
은 238U 99. 2139 %, 235U o.1204 %, 232Th 100 %로 구성되어 있다. 저 어콘, 우라니나이트, 스핀, 인회석, 모나자이트 등이 우라늄 함유 광물 이다. 루비듐―스트론듐 계에서와 유사하게 시료 속의 206Pb 동위원소 는 206Pb=238u (eA238t -1) 로 표현되며 시료에 원래 포함되어 있던 206Pb 의 초생치를 고려하면
206Pb 측정치 =206 p초생치 +23su (i238t - l) 의 관계식이 얻어진다. 204Pb 는 동위원소비로 분석되므로 (206Pb/204Pb) 측정치 = (2osp b /204Pb) 초생치 +238U/204Pb (eA238t _ l) (4 .l) 이 되어 루비듐-스트론튬 시스템에서처럼 아이소크론이 얻어전다. 23su 와 232Th 의 경 우에 도 유사하게 (201p b /204Pb) 속정치 = (201Pb/204Pb) 타치 +235U/2“Pb (eA235t _ 1) (4 . 2) (208Pb/204Pb) 측정 치 = (2osp b/2 04p b) 조생 치 十 232Th/2 0 4Pb (emu -1 ) (4 . 3) 이 각각 얻어진다. 위의 (4.1) 식에서 (4.2) 식을 나누면 ((220016p Pb b//220044PPbb)) 측측정정치치 -― ((2200 16PPbb//2 200 44PPbb)) 초초생생치치 =(西235汀 U) 측정치 (~eA238t 一 1) (4.4) 의 Pb-Pb 의 동위원소 측정만으로 암석의 연대가 얻어진다. 이를 201p b _206Pb 연대 측정법이라 한다. 현재의 235U/238U 의 값은 1/137.88 이다. 이 방법은 시료 중에 Pb 가 존재하는 시료의 Pb 동위원소비를 측정하기 때문에 지질시대 동안에 Pb 의 유실(l ead loss) 의 영향을 적게 받는 장점 이 있다 . 지질시대 동안에 어떤 지질학적 사건에 의해 시료에서 Pb 의 유실이 일어나는 경우 시료의 참연령보다 젊게 얻어지게 될 것이다. 이와 같 이 변성작용, 동화작용 또는 지각 변동에 의해 Pb 의 유출입이 일어나면 238u _ 206p b, 236u _ 207Pb, 232Th-208Pb, 207Pb-206p b 법 에 의 하여 얻 어 진 연령은 서로 일치하지 않을 것이다. 이를 불일치연령 (dis c ordant a g e) 이 라 한다. 그러나 Pb 유실이 일어나지 않은 경우에는 이들 동위원소비의 연령이 일치하는 일치연령 (concordant a g e) 이 얻어진다.
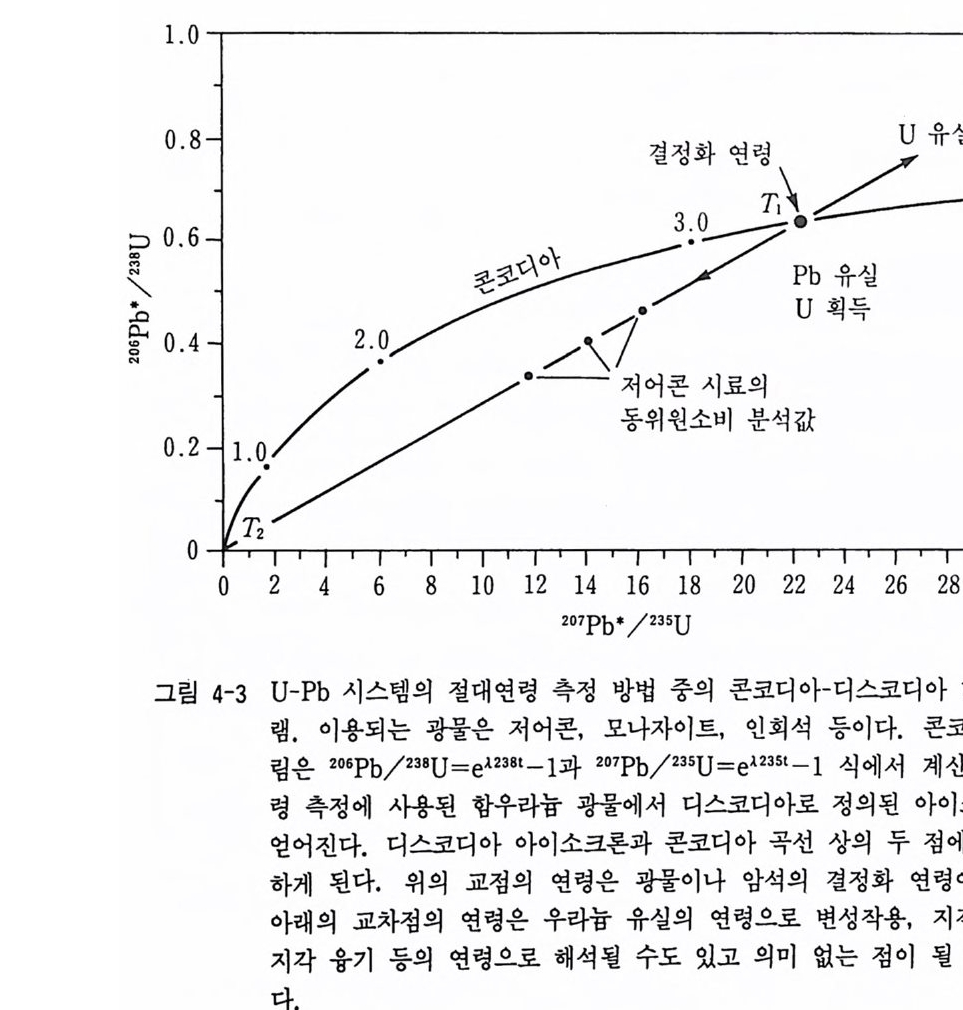
콘코디아 -디스코디아 다이어그램 이상적인 폐쇄계에서는 206Pb/238u=eA2381 ― 1 과 201Pb/23su=e,23s1_1 에 서 얻어진 연령은 일치할 것이며 그림 4-3 에서와 같이 시간의 변화에 따 라 일치연령의 곡선, 죽 콘코디아 (concord i a) 곡선이 얻어지게 되어 폐 쇄계의 시료의 연령 측정에 이용된다.
 1.0
1.0
그러나 그림에서처럼 많은 시료는 변성작용이나 풍화작용 등의 지질학
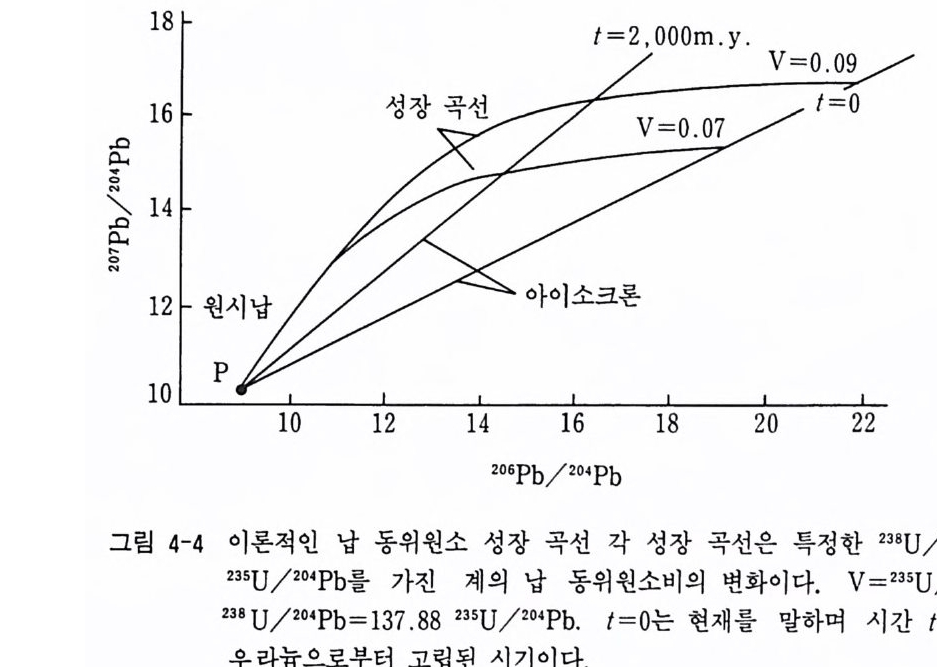
적 사건에 의하여 Pb 의 유실이 일어나 콘코디아 곡선 위에 나타나지 않 는 아이소크론이 얻어진다. 이를 디스코디아 (d i scord i a) 라 한다. 이 디스 코디아 아이소크론 직선과 콘코디아 곡선은 의삽법으로 연장시키면 T1 과 T2 에서 만나게 된다. 이때 T1 은 암석이 결정화된 시기이고 T2 는 변 성작용 같은 Pb 의 유실 시기가 된다. T2 의 Pb 의 유실의 방식은 학자들 에 따라 그 해석이 다르다. 납의 유실 방식을 순간적인 Pb 의 유실 (ep iso dic lead loss) , 연속 확산에 의 한 Pb 의 유실, 팽 창 모델, 화학적 풍화 등에 의한 Pb 의 유실이 제안되고 있다. 확산에 의해 Pb 이 유실되 었다면 T2 의 지질시대는 아무런 지질학적 의미를 가지지 못하게 된다. 납 동위원소의 성장 납 (Pb) 동위원소는 태양계 형성 초기물질 내에 포함되어 있는 원시납 (pr im ordia l lead) 의 동위 원소비 206P b/2 0 4 Pb = 9 . 307, 201Pb/ 20 4Pb = 10 . 294, 208Pb/2 ° ~Pb = 29 . 476 에서 지질시대 동안에 붕괴하는 과정에서 그 함량이 변화하여 오늘날 암 석 광물에 포함되어 있는 현생납 (modern lead) 이 된다. 이같은 변화를 Pb 동위원소의 성장이라 한다. 보통 원시납은 캐년 다이아브로 (Can y on Diab lo) 철운석의 동위원소바로 대표된다. 그리고 보통납 (common lead) 은 암석 광물이 생성된 이후에 방사성 기원의 Pb 가 생성되기 이전에 광 물 내에 존재하는 Pb 를 말하며 방연석, 칼리장석, 운모류와 같이 우라 늄을 포함하지 않은 광물의 Pb 동위원소 값이다. 그림 4-4 에서 처 럼 원 시납에서 현생납으로 오면서 Pb 동위원소비가 점점 증가하고 있다. 이 감이 지질시대에 따른 납 동위원소비의 변화 곡선을 납 동위원소 성장 곡선 (lea d iso to p e grow th curve) 이 라 한다. 이 는 지 각과 맨틀의 진화, 지 구물질의 진화 연구에 이용된다.
 18 I f= 2 , 000m . y.
18 I f= 2 , 000m . y.
피션 트랙 측정법 우라늄 계열의 자발적인 핵분열이 일어날 때 발생하는 에너지에 의 하여 광물의 결정 격 자에 손상을 일으켜 결정 면에 흔적 (fiss io n tra ck) 을 만든다. 이 흔적의 양과 광물 내의 우라늄 계열의 원소의 함량 간에는 Ts( 피션 트랙의 수)=4A-a 238u(eAa t -1) 의 관계가 얻어져 시간의 함수로 표현된다. 여기서 Aa 는 238u 의 a 붕괴의 붕괴상수이다. 따라서 광물 연마면을 질산, 염산 등과 같은 부식용 시약 울 사용하여 부식시킨 후 현미경으로 피션 트랙의 수를 측정하여 암석의 연대를 측정한다. 보통 많이 사용되는 광물은 저어콘, 인회석, 녹영석, 스펜, 화산성 유리질 물질 등이다.
(3) 칼륨-아르곤 시스탬 칼륨 (K) 은 39K, ◄ oK, 41K 의 세 동위원소가 알려져 있다• 그 중 K 은 전자 포착 방식의 붕괴 과정에서 ◄ oAr 이 생성되고 8 붕괴에 의해 “Ca 이 만들어지는 2 가지 방식의 붕괴를 하게 된다. 40K 一 40Ar 일 때의 붕괴상 수는 Aec = 5. 8 X 10- 11 이고 K - 4°Ca 일 때의 붕괴상수는 A/I= 4. 962 X 10-io 이며 이들 사이의 분리 비율은 0 . 117 이다. 40K-4 0Ar 방법에서 얻어지 는 연령(t)은 !=~loge [1+(~ 내40 ] (4 . 5) 에서 계산된다. 위의 붕괴상수 값을 (1) 식에 대입하면 t = l. 804 X 109!og e( 9 . 54~ + 1) (4 . 6) 이 얻어진다. 측정에 이용되고 있는 시료는 운모류, 각섬석류, 칼리장석, 사장석, 휘석, 해록석 등 K 함유 광물이 사용되며 화산암의 전암 시료도 사용된 다. K-Ar 방법에서는 “Ar 이 비활성 가스이므로 암석이 용융될 때 쉽 게 시스템 밖으로 날아가 버리기 때문에 기존 딸동위원소는 고려하지 않 아도 된다. 이 방법은 K 원소가 암석 내에 혼하게 들어 있어 측정이 쉽 고 5 천 년에서 46 억 년된 시료까지 연대 측정이 가능하므로 지질학에서 많이 이용되고 있다.
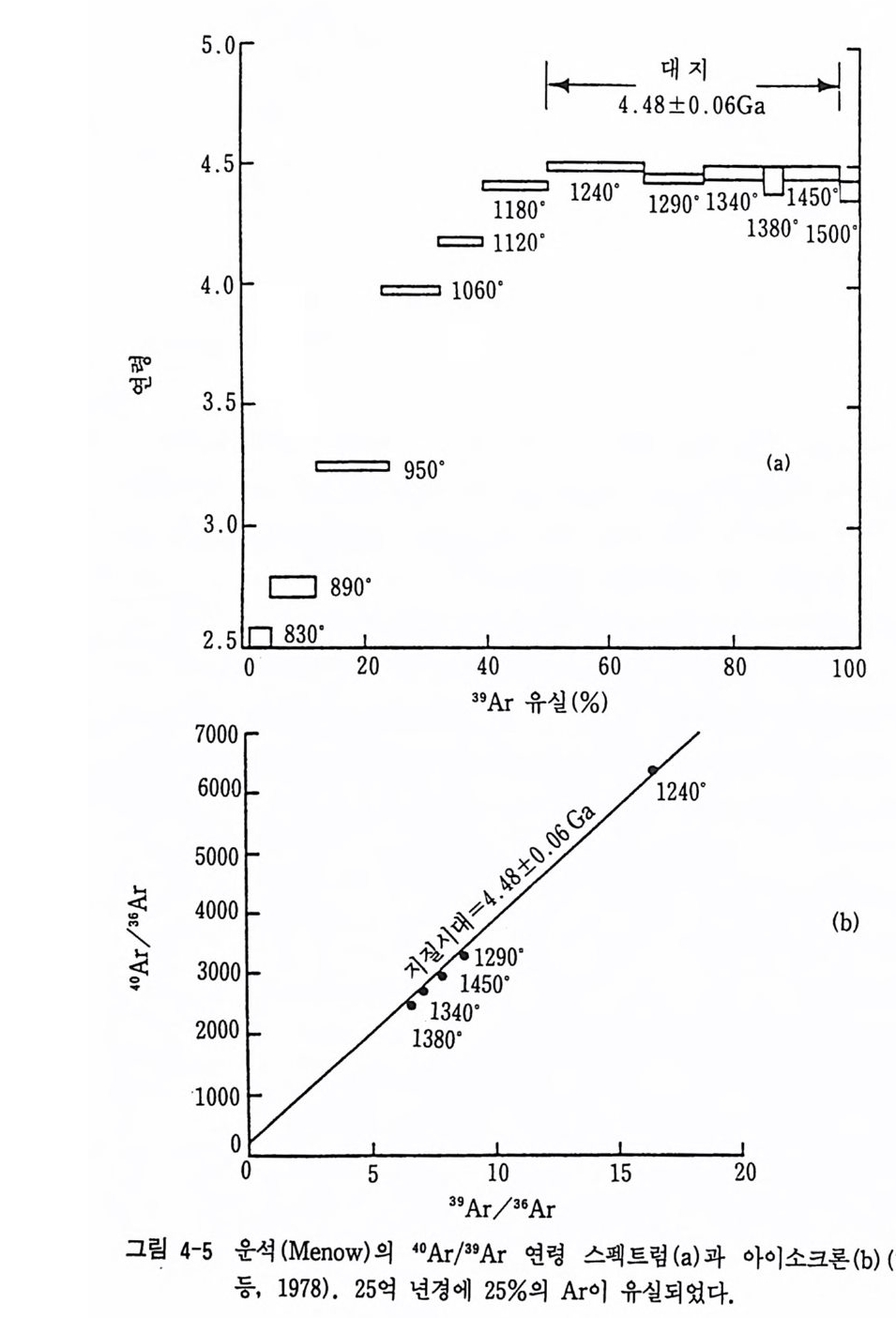
그러나 변성작용이나 기타 지질학적 사건에 의해 Ar 유실이 쉽게 일 어나므로 변성암에서는 적절하지 못하다. 보통 화산암이나 오래된 암석, 운석 및 달 암석 등의 연대 측정에 이용되고 있다. 광물에 따라 Ar 유 실의 정도가 다르며 장석과 운모류보다는 각섬석 광물이 Ar 유실이 바 교적 적어 연대 측정에 유용하다. 그러나 40Ar/3 9 Ar 연대 측정법이 개발 되어 암석 형성 후의 지질학적 과정의 가열에 의해 일어나는 Ar 유실의 문제점을 해결해 주고 있다. 40Ar/39Ar 법 40Ar/39Ar 방법은 K— Ar 법의 하나로 시료 속의 K 울 정량하는 대신 시료를 원자로 속에서 빠른 중성자로 조사, Ar 으로 변환시켜 40A r/3 9 Ar 비를 측정하는 방법아다. 연령은 t=1. 804 X l09lo g e ( 홉40 . J+ 1) (4 . 7) 식에서 계산된다. 여기서 J는 상수로서 중성자 조사 동안 3 9 Ar 으로 변환 된 39K 의 분율 (frac ti on ) 이 다. J=~LJT j rp( c) o(c) dz 으로 표현되며 연대가 알려진 시료에 조사시켜 구할 수 있다. 이 방법은 K-Ar 방법보다 정밀도가 높을 뿐만 아니라 온도를 변화시켜 가면서 추 출된 가스의 동위원소비를 분석할 수 있으므로 각 온도 단계에서 연령 계 산이 가능하다. 즉 단계 적 가열 방법 (inc rementa l heati ng tec hniq u e) 으 로 폐쇄계에 있지 못했던 시료에 대해서도 연령 측정이 가능하며 동시에 이들 연령의 유효성이 확인될 수 있다. 즉 온도에 따라 유출되는 39Ar 의 양과 연령 사이에 연령 스펙트럼 (age s p ec t rum) 이 얻어진다. 그립 4-5 는 Menow 운석 의 40Ar/39Ar 스펙 트럼 과 아이 소크론이 다. 연령 스펙 트럼 의
형태에서 약 25 % 의 Ar 유실을 계산할 수 있다. Turner 등 (1978) 는 악 2.5Ga 시기에 다른 천체에 의한 충돌 때문에 일어난 가열에서 Ar 유실 이 초래된 것으로 생각하고 있다. 그러나 고온에서는 Rb-Sr 측정법에서 얻어진 연령과 동일한 40Ar/3 9 Ar 연령이 얻어져 운석의 연령을 알 수 있 다. 폐쇄계에서 암체 내의 Ar 이 고온에서도 유출되지 않는 온도인 동결온 도 (blockin g tem p er atu r e) 를 각 광물에 서 구하면 화성 암체 의 냉 각사를 해 석할 수 있다. 예 몰 들면 미국 유타 주의 신생대 화성암 복합체의 연구 (Ne il son 등, 1986) 에서 각 광물의 Ar 동결온도, 각섬석과 혹운모의 K_Ar 연령과 저어콘과 인회석의 피션 트랙 연령 특성 자료 사이의 관계가 그림 4-6 과 같이 얻어졌다. 즉 각섬석과 흑운모의 K— Ar 연령은 각각 11. 8 m . y 와 10.8m. y이며 이들의 Ar 동결온도는 각각 s2o·c 와 275·c 였다. 이 그림에서 보면 soo·c 이상에서 400 만 년 시간 간격 동안에 1oo·c 정도씩 화성암체가 느리게 냉각되었음을 알 수 있다. 주로 융기와 침식 에 의한 냉각으로 지하 중온율을 30·c km-1 으로 가정하면 이 기간에 0.6-1.1 mm/ 년 속도로 융기가 일어난 것으로 계산이 된다. (4) 사마륨-네오디뮴 시스탬 141Sm 이 a 붕괴를 하면 143Nd 이 된다. Rb-Sr 방법에서와 유사하게 국i=( ::접 )1+ 틀 (eAI-1) 관계식에서 아이소크론이 얻어진다. 반감기는 1. 06X1011 로 대단히 길기 때문에 오래된 암석의 절대연령 측정에 유용하다. 시료 중에 Rb/Sr 의 함량이 낮아서 연령 측정에 부적합한 시료일지라도 Sm-Nd 법은 이용될
 5.0 尸 대지 __+
5.0 尸 대지 __+
수 있다. 특히 스트론튬 동위원소 (87Sr/86Sr) 나 납 동위원소 (206Pb /2 07Pb) 비 와 함께 트레아서로서 암석의 기원, 지각과 맨틀 물질의 진화 연구에 많 이 이용되고 있다. 왜냐하면 Nd, Sr 과 갇이 원자량이 큰 원소의 동위원 소비는 기존 물질의 혼입이 없으면 화성암과 마그마가 형성된 장소에서 그 값이 일치하므로 이들 동위원소비에서 마그마의 직접적인 정보를 얻 울 수 있기 때문이다. 또한 Sm-Nd 법은 방사성 붕괴의 어미원소와 딸 원소 모두 희토류 원소로 어미원소와 딸원소 간에 성질이 다른 K-Ar, Rb ― Sr 법과는 달리 변성작용이나 지질학적 사건에 영향을 적게 받는 장 점이 있다. 때문에 지각, 맨틀의 전화, 고기 지각의 존재 확인, 마그마 동화 및 혼합 등의 해석에 CNd-87Sr/86Sr 다이어그램이 많이 ` 이용된다.
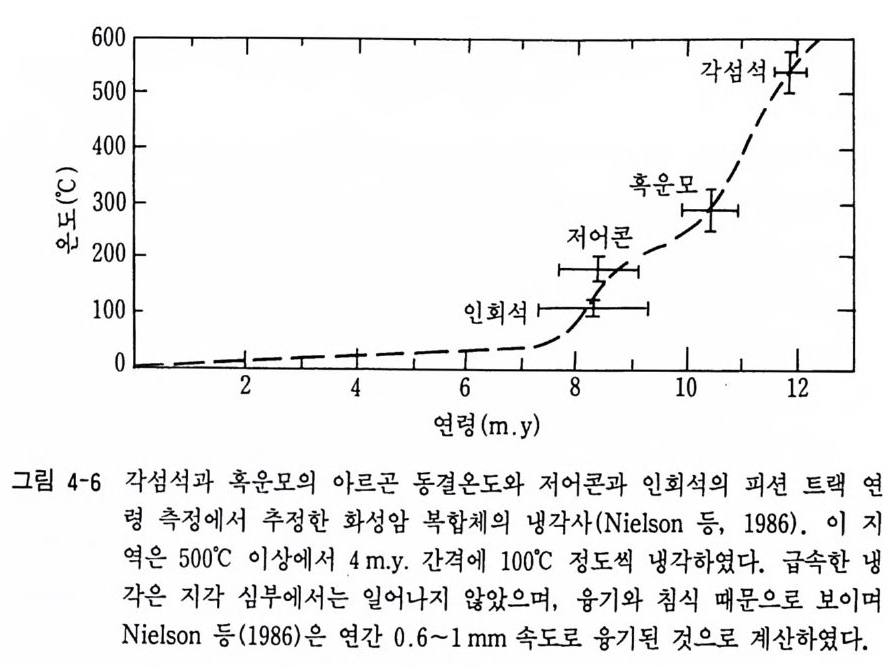 : 654231 。。。。。。 卜LI _ 각 섭 I석 I I
: 654231 。。。。。。 卜LI _ 각 섭 I석 I I
여기서
cNd =[~-}]X} Q4 으로 정의된다. 14aNd 은 14 1 Sm 이 방사성 붕괴로 생성된 것이며 l 4 4Nd 은 안정동위원소이기 때문에 l43Nd/144Nd 비는 암석의 연대가 오래된 것일수 록 이 값이 크게 된다. 위 식은 CNd 값은 시료 중의 14aNd/144Nd 값이 지구 전체 또는 운석의 14aNd/144Nd 값보다 얼마나 Sm/Nd 이 높거 나 또는 낮은 영 역 에 서 만들어 진 것인가를 지시하는 값이다. 맨틀 물질이 부분 용융되어 마그마가 형성될 때 Sm, Nd, Rb, Sr 등 의 원소의 분별이 일어남이 확인되었다. 즉 이온 반경이 Sm 보다 약간 큰 Nd 이 마그마(액상)에 더 농축되어진다. 또한 Sr 보다 약간 이온반경 이 큰 Rb 이 마그마에 더 농집된다. 그러므로 맨틀에서 부분 용융되어 마그마가 만들어질 때 맨틀에는 Nd 과 Rb 이 감소하게 되어 (결핍맨틀이라 함) 143Nd /14 4Nd 값은 지구 전체의 평균값보다 증가하고 87Sr/86Sr 은 감소 하게 된다. 그렇다면 cNd-87Sr/86Sr 다이어그램에서 맨틀의 값은 좌측 상단에 나타나야 할 것이다. 바로 이 위치가 MORB( 중앙해령 현무암, mido ceanic ridg e basal t)의 위치와 일치하므로 MORB 가 상부 맨틀의 동 위원소비를 대표한다고 생각하면 상부 맨틀에서 만들어진 마그마가 지각 울 형성하게 된 셈이 된다. 그런데 그림 4-7 에서 보면 젊은 연대를 가지 는 해양섬 현무암은 MORB 에 근접한 영역에 나타나 맨틀 기원의 현무 암은 CNd=- Q .37csr 의 직선적인 배열인 멘틀 배열선 (man tl e arra y)을 나 타내고 있다. 그런데 CNd 一 “Sr/86Sr 다이어그램에서 CNd=O 부근과 이보 다 값이 작은 부근의 위치와 87Sr/86Sr 값이 큰 영 역 에 나타나는 현무암도 조사되었다. 이는 MORB 를 대표하는 물질에서만 부분 융융되어 마그마 가 만들어진 것이 아니고 미분화 상태의 지구 (cNd=O 에 해당함)나 미분화 된 지구보다도 Rb, Nd 이 많이 농축된 부화 (enr i ched) 맨틀의 영향도 존재함을 가리킨다(그립 4-8). 부화 맨틀의 기원은 맨틀 내에서의 변성작
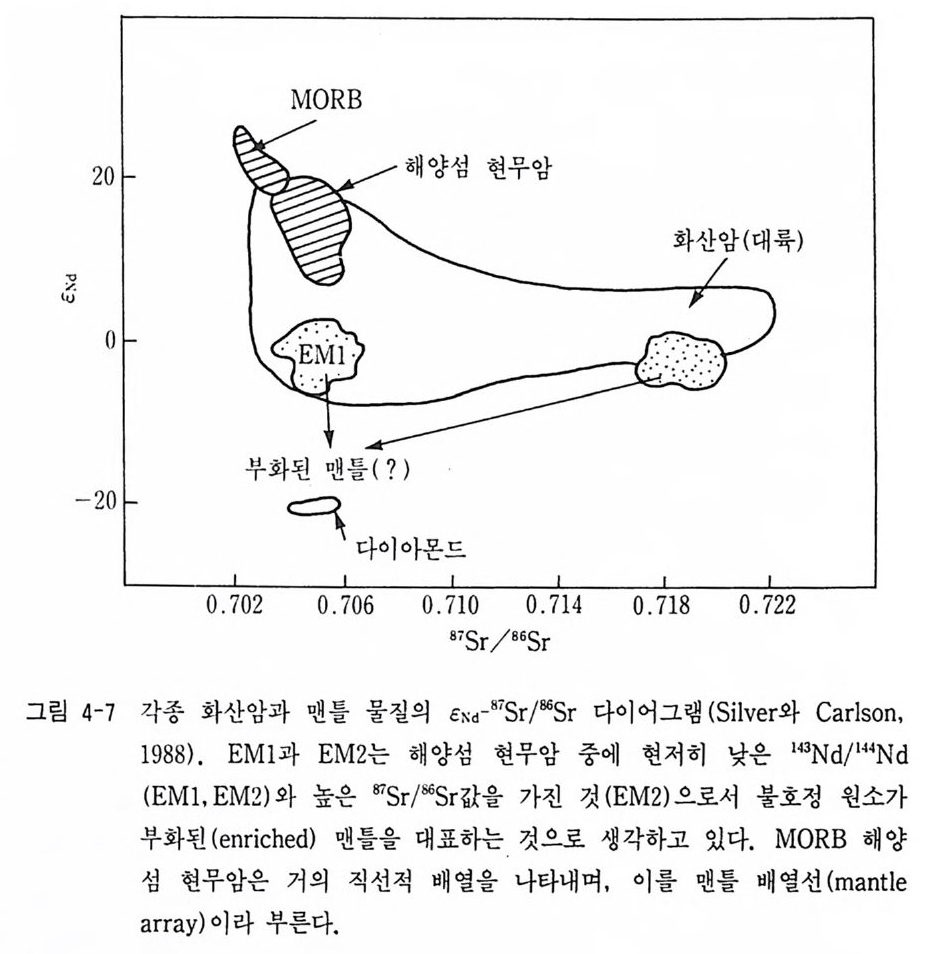 MORB
MORB
용으로 인하여 평균적인 맨틀에서보다 Rb, Nd 이 농축되었든가, 판의 섭입에 따른 지각 물질이 맨틀 혼입 등으로 인하여 만들어지는 것으로 해석하고 있다. 맨틀 배열선의 기원이 완전히 규명되어 있지는 않지만 맨틀 배열선에서 맨틀은 지구 탄생 후 대규모의 분화 작용을 계속해 왔 으며 이로 인하여 지각이 형성되었으며 지각을 만들고 남은 맨틀은 결핍 (de p le t ed) 맨틀이 되거나 위에서 설명하는 부화맨틀로 존재하는 것으로
생각할 수 있다. 그러나 이 문제는 아직 지각과 맨틀의 진화의 중요한 연구 과제로 남아 있다.
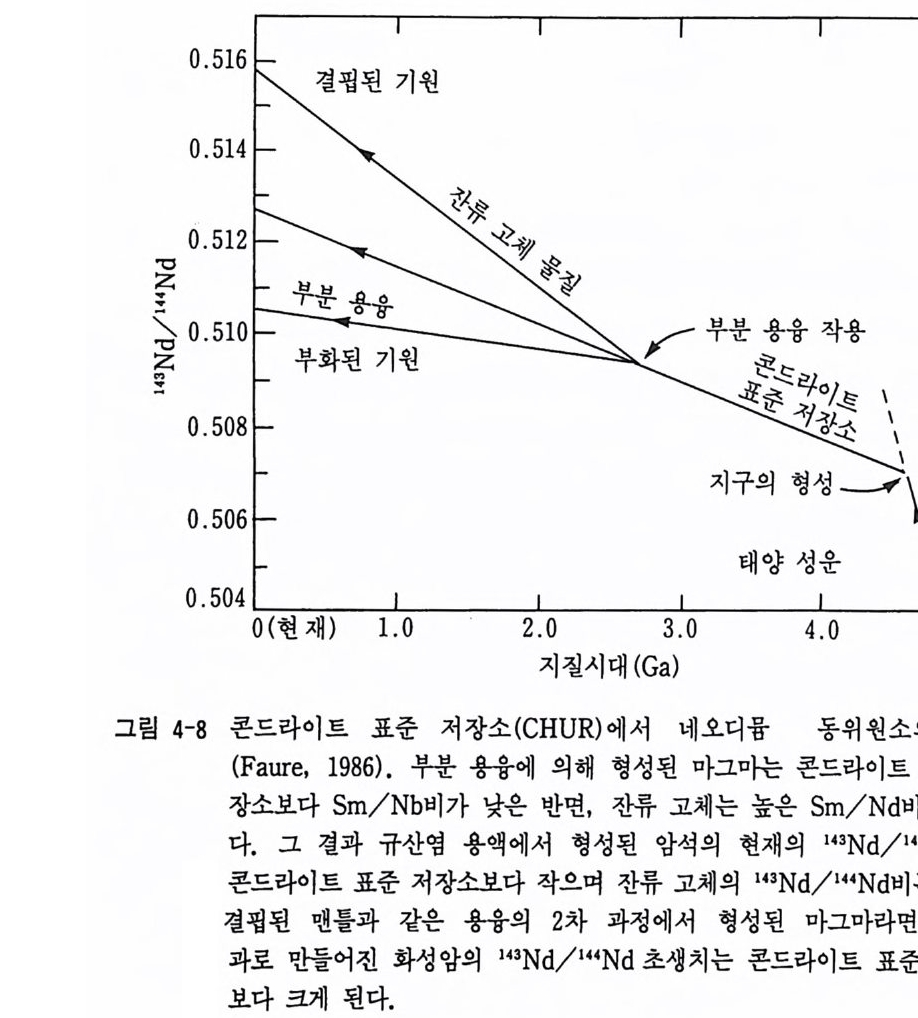 0.516
0.516
네오디뮴 모델 연령 모델 연령 (Tt H dUR) 이란 시료의 현재의 Sm/Nd 과 14aNd/144Nd 비가 CHUR(chondri te un iform reservo i r) 의 14aNd/144Nd 비와 동일하였던 시기
를말한다. 이 연령은 ItH UR = I 선 HUR - (특 ):HUR ( eAI —1) 로 표시한다. 여 기 서 NHuR 는 과거 의 특정 t 시 기 에 서 의 CHUR 의 143Nd/144Nd 비 이 며 I견 HUR 는 현재 의 CHUR 의 143Nd/14 ◄ Nd 비 로서 0 . 512638 이 다. ( I1 二 ):HUR 은 석질 운석의 분석에 의한 CHUR 의 현재의 값은 o. 1967 이다. 암석의 모델 연령은 위 식을 t에 대하여 푼 것으로 다음 식과 같다. t=丁1 ln[ (홀 )( :::-:접( ): 틀-I견 HUR ) :HUR +1] 이 방법으로 측정된 연령은 측정하고자 하는 암석이 콘드라이트 저장 소에서 Nd 이 분리된 시기 이후에는 Sm/Nd 비가 변화되지 않았을 경우 에만 지질학적으로 의미를 갖는다. 이런 조건은 희유 원소의 지화학적 특성이 알칼리 금속과 알칼리토류 금속과 대단히 유사하므로 Rb 과 Sr 보 다 Sm 과 Nd 이 더욱 적합하다. 그러나 최근에는 결핍 맨틀 저장소 (dep le te d mantl e reservoir ) 와 대 륙지 각의 형 성 에 관한 많은 정보가 얻 어 져 TCN如 연대보다 결핍 맨틀 모델 연대 ( T曲 ) 가 이용되고 있다. J acobsen(1988) 에 의한 결핍 맨틀 모델 연대의 계산식은 다음과 같다. T溫 =六 1n[1+~}:;:: 二 {::멀~]
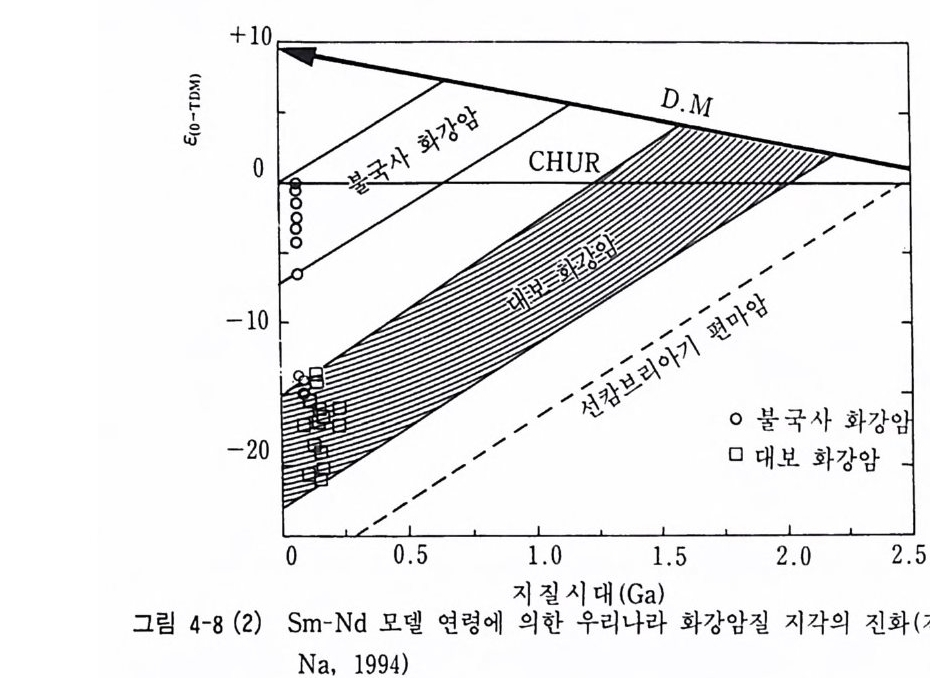
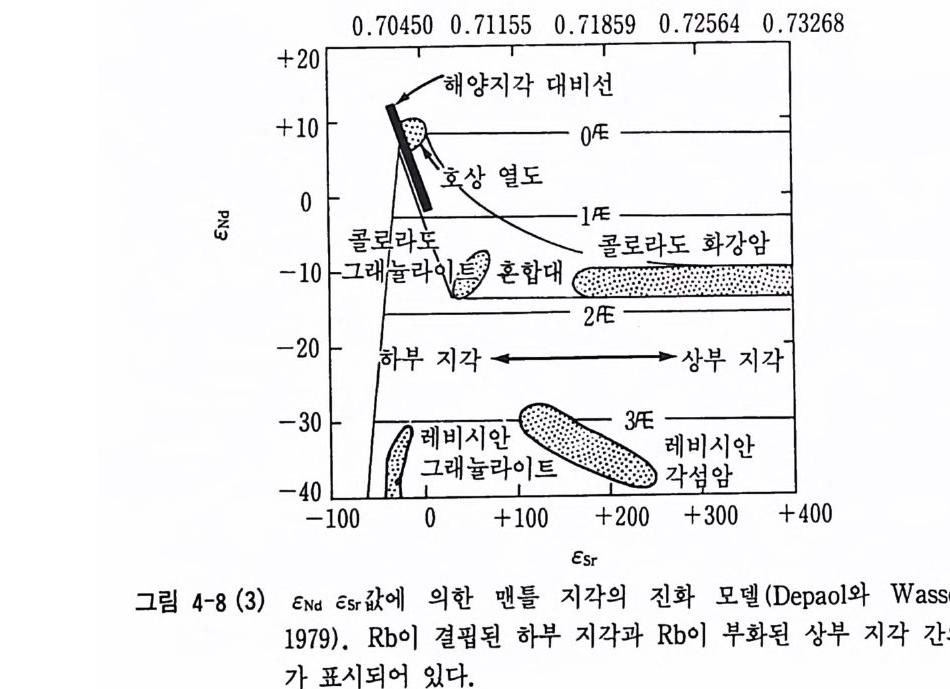
여기서 Asm=6.54 X 10-12/ 년, (14 3Nd/144Nd)o M =O .513114 (c= +8. 74) 와 (l47Sm/l“Nd)DM=O. 222 를 사용하였다. 그러나 LREE 부화된 광물상의 분리로 인하여 Sm/Nd 분별이 일어나 고 하부 지각 그래늄라이트(gr anu lit e) 암석이 부분 용융에 의해 화강암 질 마그마를 형성할 때 Sm-Nd 분별이 크게 일어나고 있다. Sm/Nd 비 가 증가할 경우 늙은 모델 연령이 얻어지고, 감소할 경우 젊은 연령이 얻어지게 됨을 알게 되었다. 그래서 이를 보정한 모델 연령이 2 스테이 지 모델 연 령 ( T晶 ) 이 다 (Ja cobsen, 1988) . T蟲 = T도 ( T값 1- Ts1ar1) [~] 여 기 서 f는 부화 파라미 터 (enric h ment par amete r ) 로 pm1 N? = H:: 問j:::삽i \1; ]-1 로 계산된다. 전형적인 대륙지각의 f' m/Nd 값은 -0.39UoM=O.12862 사용)이다. T .구 만 1 (멜팅), T溫 T2성 잃 사이의 관계는 그림 4-8 (1)과 같다. 한반도의 대표적인 지각 구성 암석의 2 스데이지 모델 연령은 선캄브 리아 기반암 (2.6-2.lGa, Na, 1994) 과 김규한 등(1 994) 에 의하여 대보 화 강암류(1. 6 ― 2.2Ga), 경상 분지 내의 불국사 화강암류 (0.5- 1. l Ga) 가 얻어져 이미 원생대 중기 시기에 지각이 전화되었음을 의미하고 있다(그 립 4-8 (2)). ENd-ESr 다이어그램 ENd-ESr 다이어그램, (1 ◄ aNd/1 ◄◄ Nd) 초생 *1- (87Sr /86 Sr) 나치 다이어그램 등이 암석성인론에 이용되고 있다. 일반적으로 정의 ENd 값과 부의 Esr 값 을 가지는 화성암은 맨틀 기원 물질에서 유래한 것으로 해석되고, 정의
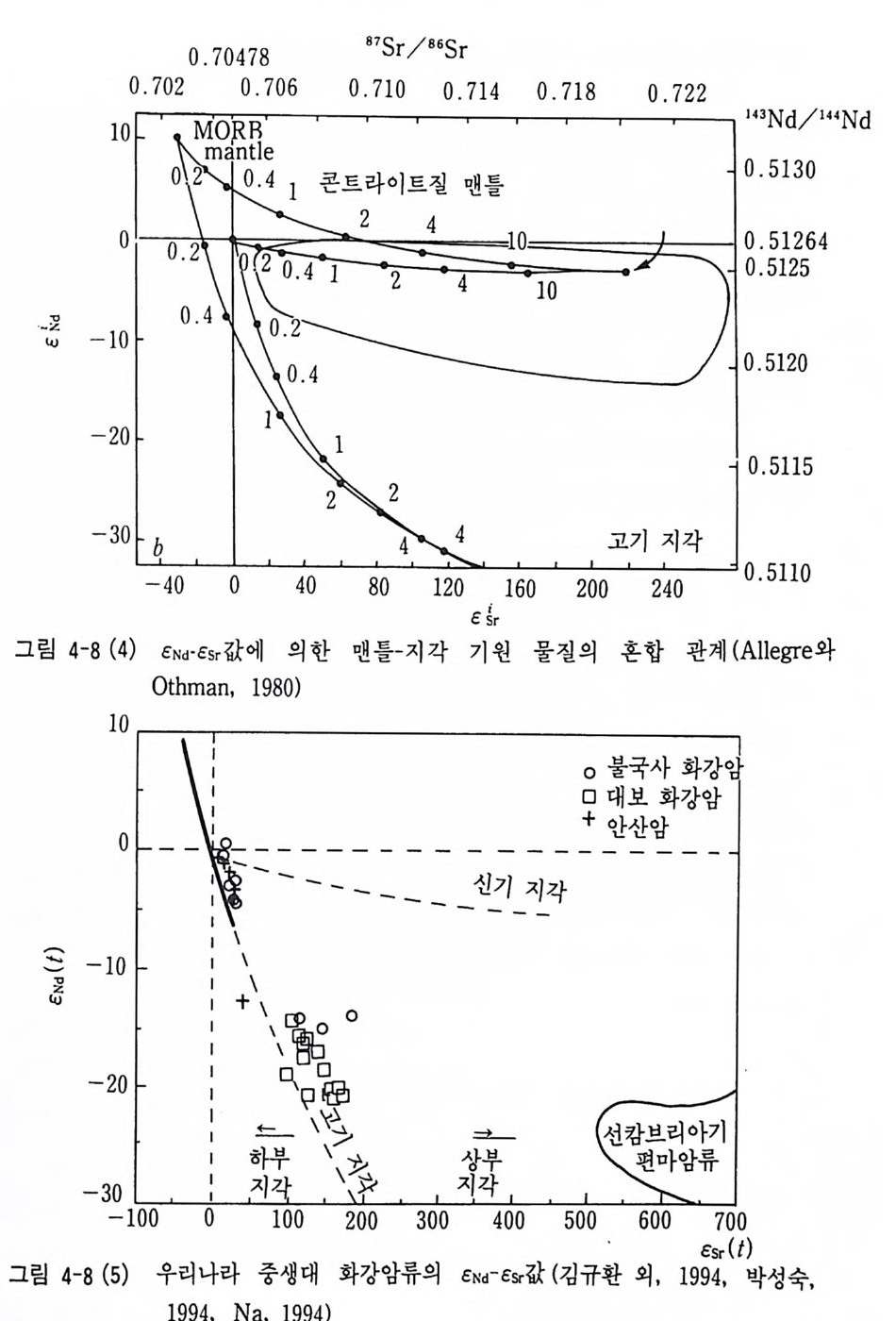
csr 값 과 부의 C Nd 값을 가지는 화성암류는 지각 기원 물질의 부분 용융 산 물로 해석되고 있다(그림 4-8(3)). 그리고 CN d -CSr 다이어그램을 이용하여 MORB, 맨틀 기원 물질과 지각 기원 물질의 혼합 또는 콘드라이트질 맨틀 물질 기원과 지각 기원 물질의 혼합 관계를 해석하고 있다(그림 4-8 (4)) . 그림 4-8(5) 에 서 와 같이 우리 나라의 중생 대 화강암류의 CN d -CS r 값의 특 징은 대단히 홍미 있는 결과로 경상 퇴적분지 내의 불국사 화강암류는 맨틀 기원 물질에서 유래하였고 대보 화강암류와 경상 퇴적분지 밖에 분 포하는 불국사 화강암류는 고기 하부 지각 기원 물질에서 유래한 것으로 해석하였다(김규한 등, 1994, 박성숙, 1994, Na, 1994, 권성택, 1992).
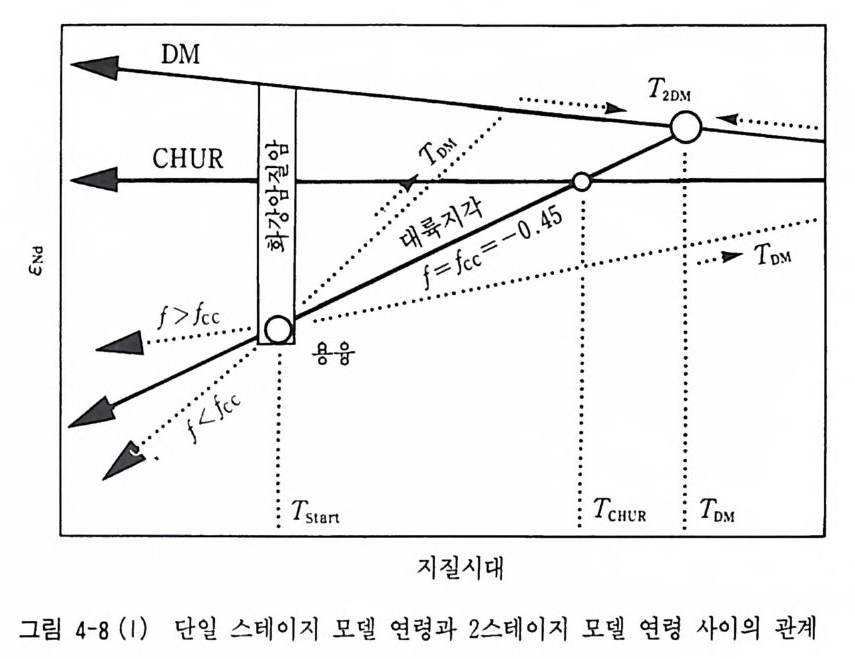 CHUR 守守
CHUR 守守
 +10
+10
 0.70450 0.71155 0.71859 0.72564 0.73268
0.70450 0.71155 0.71859 0.72564 0.73268
 0.7 04 78 s1s r/ 8 6Sr
0.7 04 78 s1s r/ 8 6Sr
(5) 기타 장반감기 핵종을 이용한 연대 측정법 앞에서 설명한 측정법 의에 레늄-오스뮴 측정법, 루데뮴 - 하프늄 및 란 탄-세륨 측정법 등이 있다. 레늄 (187Re) 은 /3붕괴로 1870s 이 된다. 반감기 는 4.56X1010 년이다. 레늄-오스뮴 연령 측정 ::훈(閃 ) 1 + : : :問 (e• t- 1) 의 관계식에서 아이소크론이 얻어진다. 그리고 루테튬 (1 16 Lu) 은 /3붕괴로 116H f가 되며 반감기는 3. 53 X 1010 년이다. 대=( 問 {) 1+ : 情 ( e u ― 1) 의 석에서 아이소크론이 얻어지게 되며 란탄 - 세륨의 경우에는 꾼=(꾼 )1+ 선국 :( eA I_1) 의 관계식에서 아이소크론이 얻어진다. 레늄은 운석 내의 황화 광물 등 에 많이 포함되어 있으며 루테뮴, 란탄은 저어콘, 혹운모, 인회석 등에 함유되거나 기타 REE 와 흔히 수반된다. 스트론튬, 네오디뮴 동위원소 와 함께 암석 절대연령 측정과 암석 성인 해석 및 지각의 전화 연구에 이용되고 있다. (6) 단반감기 핵종을 이용한 연대 측정법 상충 대기권에서 질소 (l4N) 가 중성자 포획 반응으로 인하여 탄소 동위 원소 (uc) 가 만들어진다.
1~N+An=13C+IH 이 때 만들어 진 탄소는 산소와 결합하여 14C02 가 되고 다음과 같은 식 물의 광합성 작용에 의해 14C02+H20= (14CHO) +02 가 되어 식물이 살아 있을 때는 대기 중의 14c 가 식물체의 14c 와 동위원 소 평형에 있게 된다. 그러나 식물이 죽게 되면 14c 은 방사성 붕괴를 시작하여 그 양이 변화 된다. 이때 연령 (t)은 t= -8.2 6 6ln—NN 。 에서 얻어진다. 여기서 N/No 는 대기 중의 14c 의 농도와 시료 중의 14c 농도의 비이다. 탄소 동위원소의 반감기는 5730 년으로 대단히 짧다. 그 러므로 0~50000 년 정도의 젊은 연대를 가지는 시료의 연대 측정에 주로 이용된다. 14c 연대 측정을 위해 과거에는 8 선 계측법을 이용하였으나 최 근 가속기 질 량 분석 (AMS, accelerato r mass spe c tr o metr y) 을 이 용하여 측정 감도가 1000 배 이상 높아졌고 사용 시료의 양도 1/1000 정도 줄어 들었으며 측정 가능한 연대 범위도 6 만 년까지 가능하게 되어 제 4 기 지 질학이나 고고학 분야에서 많이 이용하고 있다. 4-3 안정 동위원소 지구과학 및 환경과학 분야의 연구에 주로 탄소, 수소, 산소, 질소, 황 등의 경원소 환경 동위원소가 많이 사용되고 있다. 안정 동위원소는 물질의 기원, 물질의 혼합, 물질 간의 상호 반웅 및 물질의 생성 환경
해석 등에 유용한 수단으로 지구과학 분야에 이용되고 있다. 방사성 동 위원소와는 달리 안정 핵종으로 구성되어 있는 원소임에도 불구하고 물 질 간에 상이한 동위원소비를 가지게 된다. 지질학적 과정, 지구화학적 및 환경화학적 과정 등의 여러 과정이 일어날 때 이런 동위원소비의 변 화를 가져오기 때문에 지질학적 사건의 문제 해결의 수단이 될 수 있게 되었다. 현재 안정 동위원소 분석을 위하여 가 스 용 질량분석기(g as source mass s p ec tr ome try)가 많이 이용되고 있다. 그러므로 모 든 시료는 CO2, H2, S02, N2 등과 갇이 가스화되 어 야 한다. 준비된 가스 시료는 표준 시료와 교대로 질량분석기에 도입, 질량 분 석을 하게 된다 . 분석된 안정 동위원소비는 표준 시료와 분석용 시료 간 의 천분율 편차로 다음과 같이 너 RR표 ;:료 _ 1)1000 (% 0 ) 로 표현한다. 산소의 경우에는 818O 로 표현하며 R 대신 180/1 6 O 로 바꾸어 넣으면 된다. 수소 8D 는 D/H, 탄소 813C 는 13c;12c, 황 834S 는 “S/32s , 질소 815N 는 15N/14N 등으로 위 식에 대입하면 된다(표 4-1 ) . 환경 동위원소의 종 류와 존재량, 표준 시료, 측정 대상 시료 등이 표 4 - 1 에 요약되어 있다. 산소와 수소는 표준 시료로 표준 평균 해수 SMOW(Sta n dard Mean Ocean Wate r ) 또는 V-SMOW 를 사용한다. 탄소는 미국 남부 캐롤라이 나 주의 백 악기 의 피 디 충 (Pee Dee Formati on ) 중의 벨럼 나이트를 표 준 시료로 사용하고 있다. 황은 캐년 다이아브로 운석 중의 트로이라이 트를, 질소는 대기 중의 질소를 표준으로 하고 있다. 분석된 시료의 산소 동위원소 값이 8180=-8%0 이라면 해수 (SMOW) 에서보다 측정용 시료에 가벼운 동위원소가 많이 농집되어 있고 +8% 。 이라면 해수에서보다 상대적으로 무거운 동위원소가 측정 시료에 더 많 이 들어 있음을 의미한다. 그러면 자연계의 물질에 있어 안정 동위원소
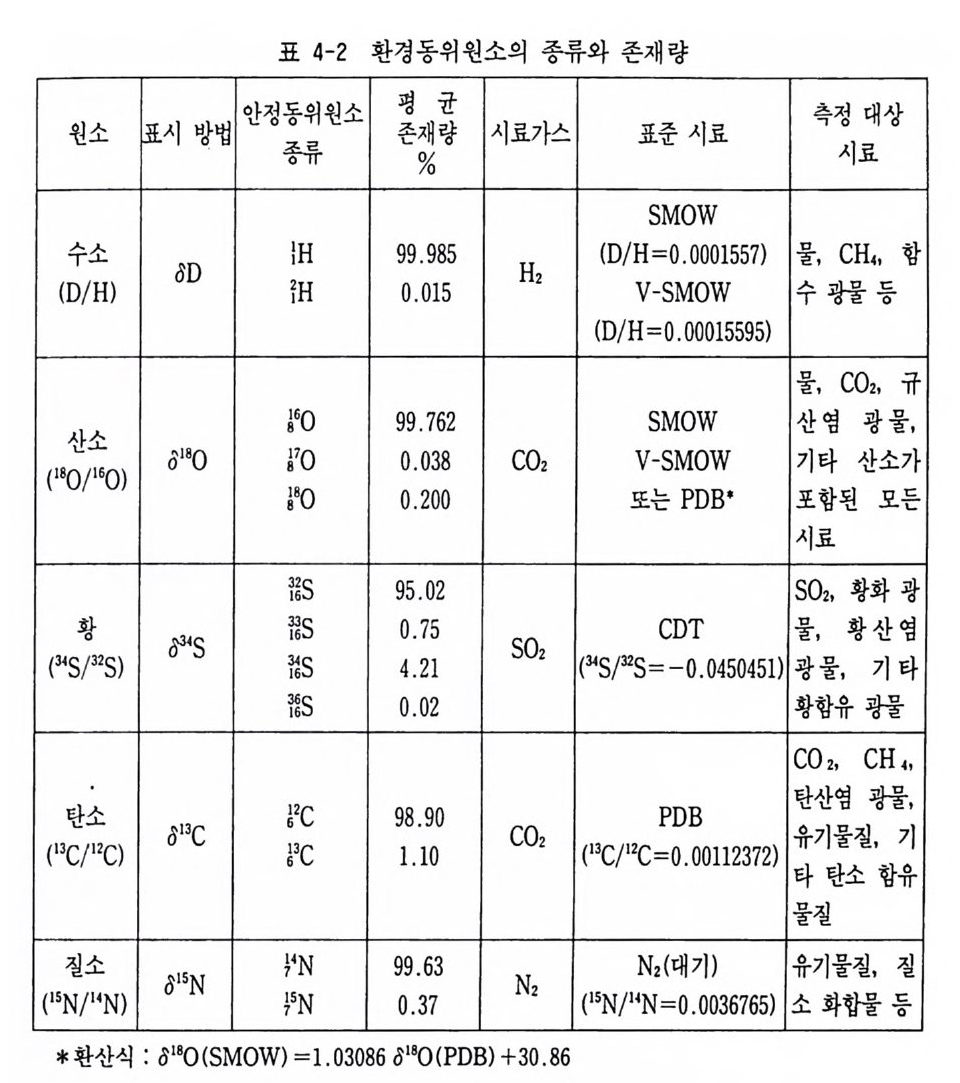 표 4-2 환경동위 원소의 종류와 존재 량
표 4-2 환경동위 원소의 종류와 존재 량
비가 다른 이유는 무엇일까? 이 이유가 바로 지구과학적 문제 해석에 대단히 중요한 의미를 가지고 있다. 즉 반응속도론적 동위원소 과정 (kin e tic iso to p i c pro cess) , 동위 원소 평 형 분별 과정 (iso to p i c equ i li br i wn frac ti on ati on pro cess) 그리고 생성물이 이동되거나 평형이 계속적으로 변
하거 나 하는 물리 화학적 영 향 (ph ys i co chemi ca l eff ec ts ) 에 의 하여 물질 내 에 가벼운 동위원소와 무거운 동위원소 간에 서로 동위원소의 차등 분배 가 일어난다. (1) 안정 동위원소비의 변화의 원인 반응속도론적 동위원소 효과 동위원소 효과(i so t o pi c e ff ec t)라 함은 원소의 질량차로 인하여 일어나 는 물리화학적인 차이를 말하며 반응속도론적 동위원소 효과에는 증발, 확산, 생물학적 과정 등에서와 같이 비가역적 화학 반응에 수반되어 일 어난다. 기체 분자 운동의 경우 분자의 운동 방식에는 병진운동(t ransla ti on), 회전운동 (ro t a ti on), 진동운동 (v i bra ti on) 방식이 있다. 분자의 병진운동 속도는 T= 塾m 관계에 있다. 여기서 m 은 기체 분자의 질량, T 는 절대온도, k 는 볼츠 만 상수이다. 질량이 작은 분자일수록 병전운동 속도가 크다. 죽 기체의 동위원소 분자 중에 상이한 동위원소를 L( 가벼운 동위원소)과 H( 무거운 동위원소)로 구별하면 분자의 평균 병전운동 속도바는 룹=: 가된다. 예를 들면 수증기의 동위원소 분자 IH2160 와 H2180 를 비교하면 :=濬 =1.054
로서 lH 쁜 0 가 H2180 분자보다 5.4 % 평균 병전운동 속도가 빠르다. 즉 물의 비 평 형 증발이 일어 날 때 머 2160 가 1H2180 보다 빠르게 확산된다. 화학 반응이 일어날 때 화학 결합이 파괴되는대 보통 가벼운 동위원소를 포함한 결합이 무거운 동위원소를 가전 결합보다 먼저 파괴되어 다른 물 질과 우선적으로 반응한다. 즉 결합이 파괴될 때 필요한 에너지를 해리 에너지라 한다. 두 원자 간에 퍼텐셜 에너지와 분자 결합 거리 사이의 에 너 지 우물 (energy well) 의 그림 은 그림 4-9 와 같다.
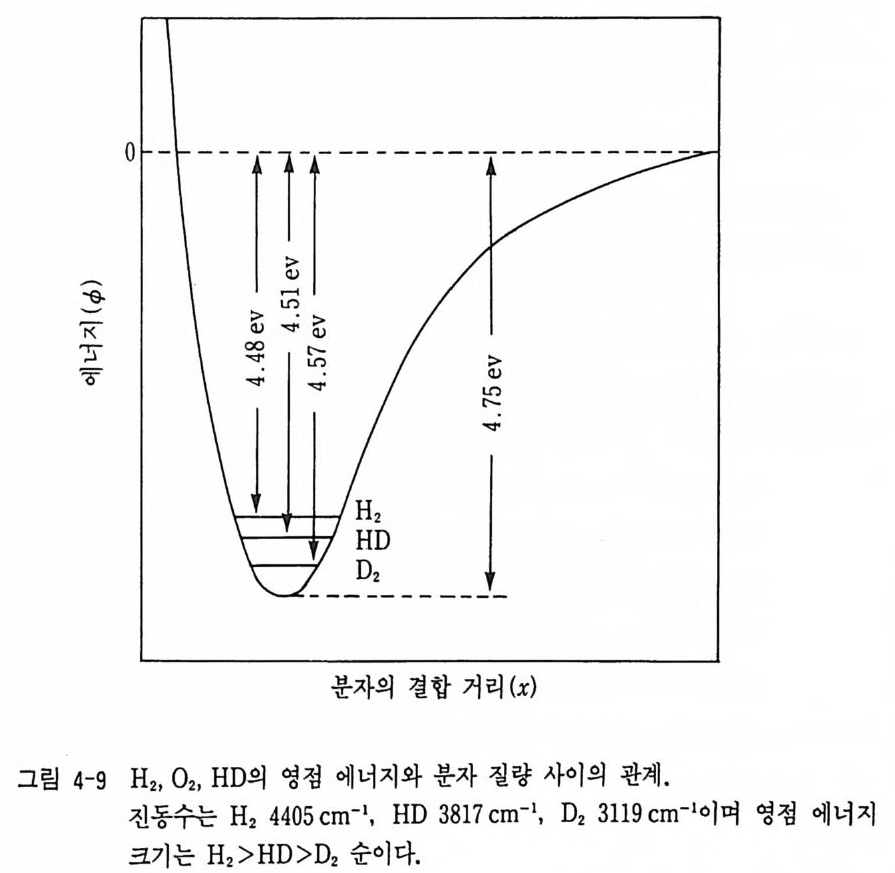 鳳 昌- -
鳳 昌- -
그림 4 - 9 에서처럼 각 분자들 간에는 영점 에너지 (zero poi n t ener gy)의
차이가 있다. 영점 에너지란 기저 상태에서의 에너지 준위와 퍼텐셜의 국소점 간의 차이를 말한다. 가벼운 원자로 된 H2 분자의 영점 에너지 가 D2 분자의 영점 에너지보다 크다. 즉 해리 에너지는 가벼운 동위원소 를 포함한 결합의 경우에 그 값이 더 작고 분열되기가 더욱 쉬워 다른 물질과 반응하기 쉬움을 알 수 있다. 생물학적 과정에 의한 반웅속도론적 동위원소 효과의 한 예는 황 환원 박테리아에 의해 황산 이온에서 황화수소가 만들어지는 것이다. 23so4 노 H 곤 S 와 “S04 쓰 H234S 와 같은 비가역 반응에서 k i/ k2=1.002 로서 32s 가 3 ◄ s 보다 2 . 2 % 반응 속도가 빠르기 때문에 그만큼 32s 가 농축되 기도 쉽 다. 또한 광합성 작용의 경 우에 도 12C02 와 13C02 사이 에 12C 0 27t 13C02 보 다 농축 속도가 빠르므로 대다수의 식물이 가벼운 탄소 동위원소를 많이 가지게 된다. 동위원소 평형 분벌 과정 화학적 동위원소 평형 분별의 하나로 H2180+\o 든 H2160+ 店 1802 와 같은 동위원소 교환 평형 반응을 생각할 수 있다. 이때 평형정수 (K) 는
[C180 i/ C160 며 (180/160) CO2 K= [H2180/H 몬이 = (180/“O) H20 = a 가 된다. 여기서 두 화합물 간의 동위원소비로 표시된 쩌롭 동위원소 분 별정수(fr ac ti ona ti on fa c t or) 라 한다. 평형정수 K 는 반응할 때의 자유에 너지 변화 관계식lnK= -LRJTG O 에서와 갇이 온도의 함수이다. 위의 반응식에서처럼 동시에 교환하는 원 자수가 1 일 때에는 K=a 가 된다. 즉 a 도 온도의 함수이다. 그러므로 온도의 변화에 따라 물질 사이에 동위원소 분별이 일어나게 된다. 따라 入 1 1000 In a=A10r6+ B 의 온도 관계식이 얻어져 동위원소 지질온도계 (iso to p e geo th e nnomete r ) 로서 널리 이용되고 있다(그림 4-10). 또한 유체 포유물의 균일화 온도와 함께 광상학에서 광화 작용시의 온도 추정과 속성작용, 열수변질작용, 화성작용, 변성작용 등의 지질학적 과정의 온도 추정에 유용하게 이용되 고 있다. 화학 성분과 결정구조에 따른 동위원소비 번화 일반적으로 이온 퍼텐셜이 높고 원자의 질량이 작은 이온의 결합으로 된 광물은 진동 빈도가 높고 무거운 동위원소를 더 많이 함유하는 경향 이 있다. 예를 들면 180 가 많은 광물은 결합력이 강하고 전하가 높은 양 이온과 결합을 하게 된다. 따라서 S i 02 와 Fe3 Q 4 를 비교하면 S i O 전] 항 상 무거운 산소가 더 많이 결합되어 있다. 그리고 평형상태에 있는 섬아 연석과 방연석을 비교하면 ZnS 쪽에 항상 “S 가 더 많이 들어 있어 질량 의 영향을 크게 받고 있다. 이를 질량 효과라 한다. 보통 광물의 결정구 조가 밀착되게 결합되거나 질서도가 높은 구조를 가지는 광물일수록 무 거운 동위원소가 더 많이 들어 있다.
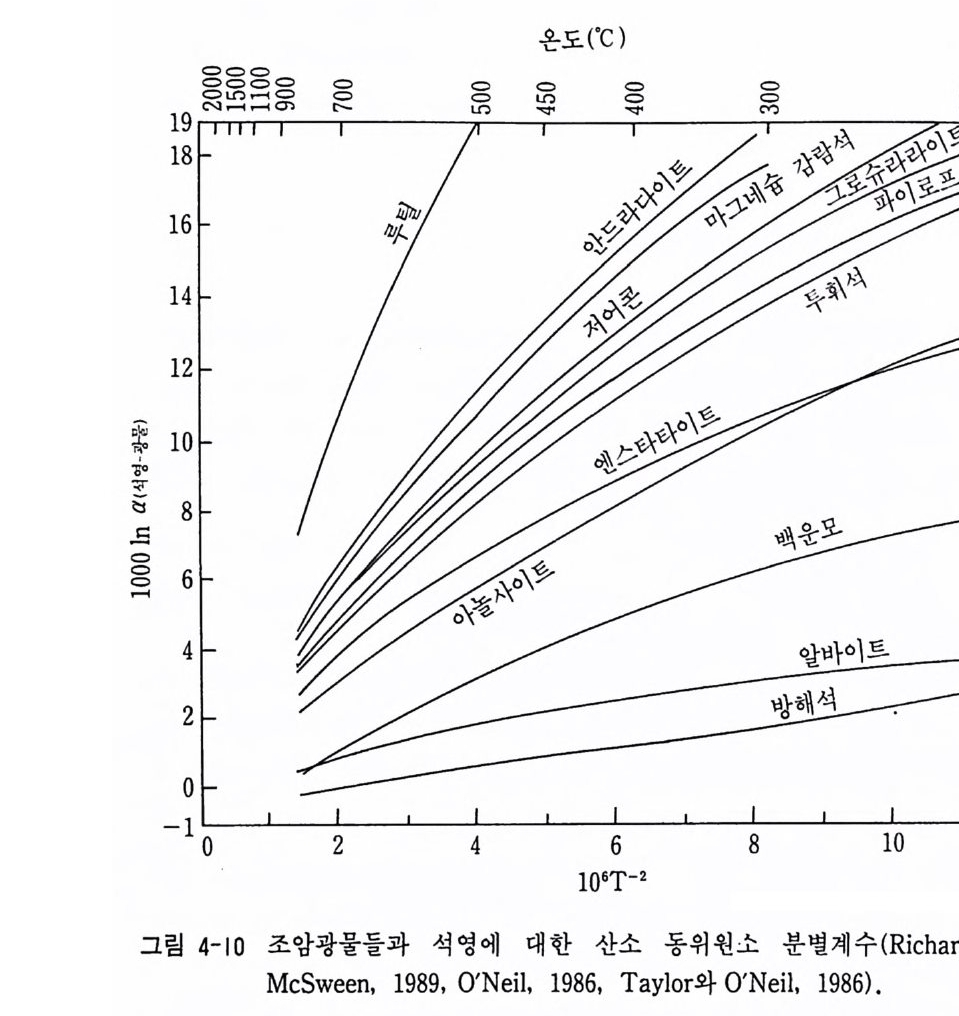 온도 ( °C )
온도 ( °C )
(2) 자연계 물질의 안정 동위원소 성분 수소 및 산소 안정 동위원소비 자연계의 구성 물질은 대부분 산소를 가지고 있으며 지구의 수권, 대 기권, 암석권에서 산소와 수소가 중요한 구성 성분으로 되어 있다. 자연 계 물질의 산소 동위원소비 (8180) 는 해수 O% o, 순환수 +10~ -45 %0, 현무암 +8~+9%o, 퇴적암 +40~+10% 。 내의의 값을 가진다. 그리고 수소 동위원소비 (oD) 는 초생수 -40~-80%0, 화성암 및 변성암 -50~-120%0, 퇴적암 —30 ~-150%0 등을 가진다. 이처럼 수소 및 산소 동위원소비가 상이하므로 지질학적 여러 과정에 서 트레이서로 이용될 뿐만 아니라 물질의 생성 환경 해석에 유용하게 이용된다. 수권과 대기권에서 산소와 수소의 동위원소비는 증발, 응축 과 정에 의하여 동위원소 분별이 일어나 지표수, 강수, 지하수 등의 180/0 • 와 D/H 비가 변화한다. 물 (H 2 0) 은 IH2160, IH2110, IH21so, HD160, HD110, HD180, D2160, D/70, D/80 의 질량이 다른 물이 존재한다. 25·c 에서 해수가 증발하여 만들어진 수증기단의 oD=-80%0, a180 =-9%o 내의이다. 이 수증기단은 온도에 영향을 받아 위도 효과, 고도 효과와 내륙 효과가 나타나고 우량 효과, 모세관 효과에 의해 동위원소 값이 변화한다. 수증기단이 응축되어 강우 현상을 일으킬 때 응축 후 남 은 수증기단은 동위원소비가 점접 가벼워져 응축이 진전됨에 따라 접점 동위원소 값이 가벼운 비를 내리게 한다. 이때 응축 전 수증기단의 동위 원소비 (Ro) 와 응축 후의 남은 수증기의 동위원소비 (R) 사이에는 R= Ro f' a-1) 의 레 일 리 증류방정 식 (Ray le ig h dis t il lat i on equ a ti on a) 이 성 립 된다 (그립 4-11). 여기서 f는 남은 수증기의 몰분율이고 쩌큰 동위원소 분별 정수이다. 예를 들어 25·c 에서 _9%o 인 수증기단이 75% 응축하여 강우가 일어 났을 때 수증기단의 동위원소비는
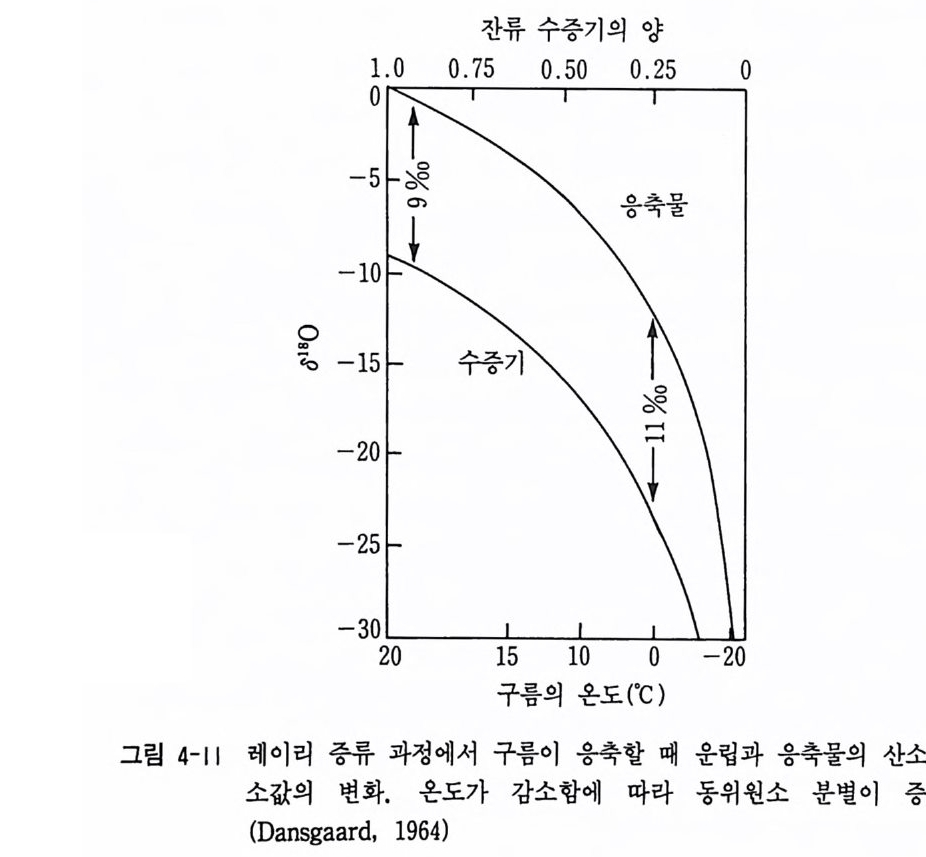 잔류 수증기의 양
잔류 수증기의 양
요R 。= f a-( 0I180=) 。 +~ 100 0 식에서 0180=-2 1. 6% 이 얻어지고 이 수증기단이 농축한 빗물의 동위 원소값은 (180/160) 비 a= (180/160) 웁 기 에서 818 어 =_12, 6 % 。
이 얻어진다. 이때 동위원소 분별정수 (a) 는 1.0092 가 사용되었다. Cra ig (l961) 는 순환수의 동위원소 값이 온도 효과에 의해 0D=80180 +10 관계식 (mete o ric wate r li ne) 을 나타냄울 조사하였다. 적도 지방에 비해 극지방으로 갈수록 위도 효과에 의해 가벼운 동위원소를 가지며 위 도에 따라 평행한 등치선을 나타낸다. 그러나 북미와 우리나라에서처럼 내륙 효과 및 고도 효과에 의해 동위원소 등치선이 변화하고 있다(그림 4-12). 그러나 열수의 경우에는 물-암석 상호 반응에 의하여 열수가 그 지역 의 지하수나 지표수보다 무겁게 나타나는 산소 편이 (oxy ge n shif t) 현상 이 나타난다(그림 4-13). 이에 열수변질을 받은 암석에서 물/암석의 비를 정량화할 수 있다.
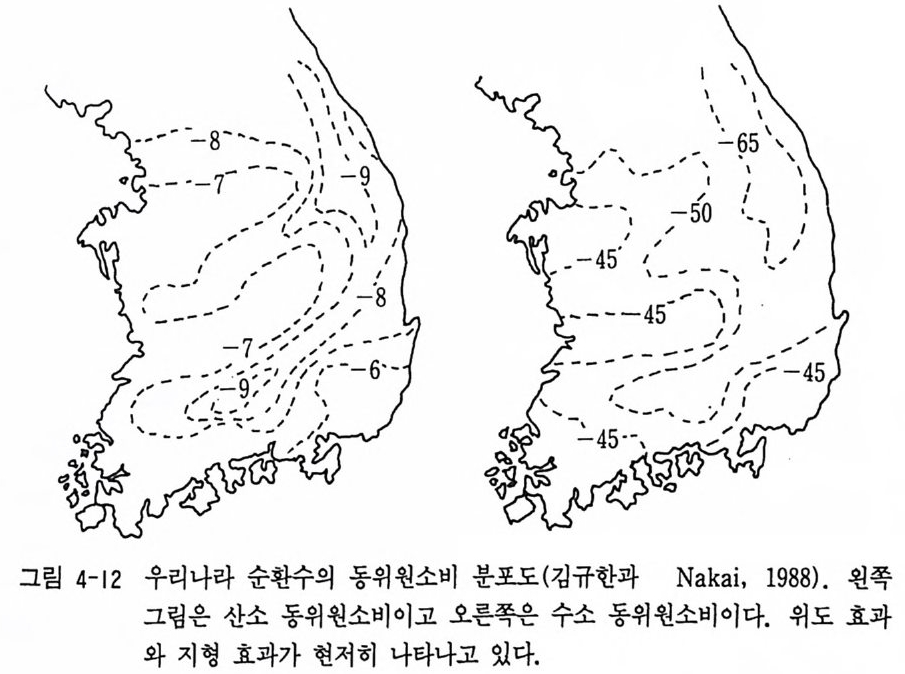 O 「------ --, '-- ,8 7, ` 一'` /I `一- ? / 一~\,,`1,,\ 仁z, :`\ `/ `/ `` ;- I, I \1.` : `1'/I•,. ` T ,I`, 1 -I\` ` III 9 _\`I\ `' ·’8 I I I _-4-5-.` i, 1` ' -.I—' -’r 5--/0 -`I `’、 I I _ .` \`§, ` , 5 ``I `、 I I 1\I ` \, I' II'
O 「------ --, '-- ,8 7, ` 一'` /I `一- ? / 一~\,,`1,,\ 仁z, :`\ `/ `/ `` ;- I, I \1.` : `1'/I•,. ` T ,I`, 1 -I\` ` III 9 _\`I\ `' ·’8 I I I _-4-5-.` i, 1` ' -.I—' -’r 5--/0 -`I `’、 I I _ .` \`§, ` , 5 ``I `、 I I 1\I ` \, I' II'
그러나 우리나라의 온천수는 산소 편이 현상이 거의 나타나지 않는다
(그림 4-14). 온천수의 기원이 온천 지역 부근의 순환수이며 저온에서 물 의 순환 속도가 빨라 물―암석 반웅의 영향이 나타나지 않기 때문으로 해 석 된다 (김 규환, Nakai, 1981 ) . 물-암석 상호 반응 지질학적 시스템에서 다양한 종류의 물과 암석 사이에 지하에서나 해 저에서 상호 반응 (wa t er-rock i n t erac ti on) 이 일어나게 된다. 폐쇄계에서 물-암석 사이에 동위원소 교환이 일어날 경우에 물/암석 비에 따른 동위 원소값의 변화를 Tayl o r(1974, 1977) 는 다음과 갇이 정량적으로 계산하 였다.
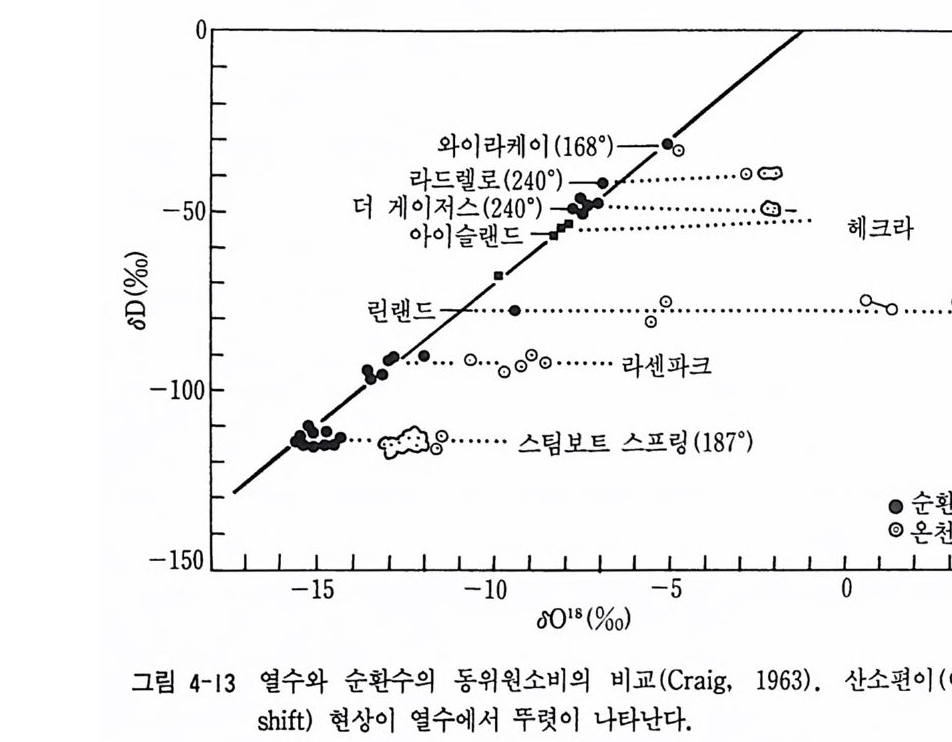 。
。
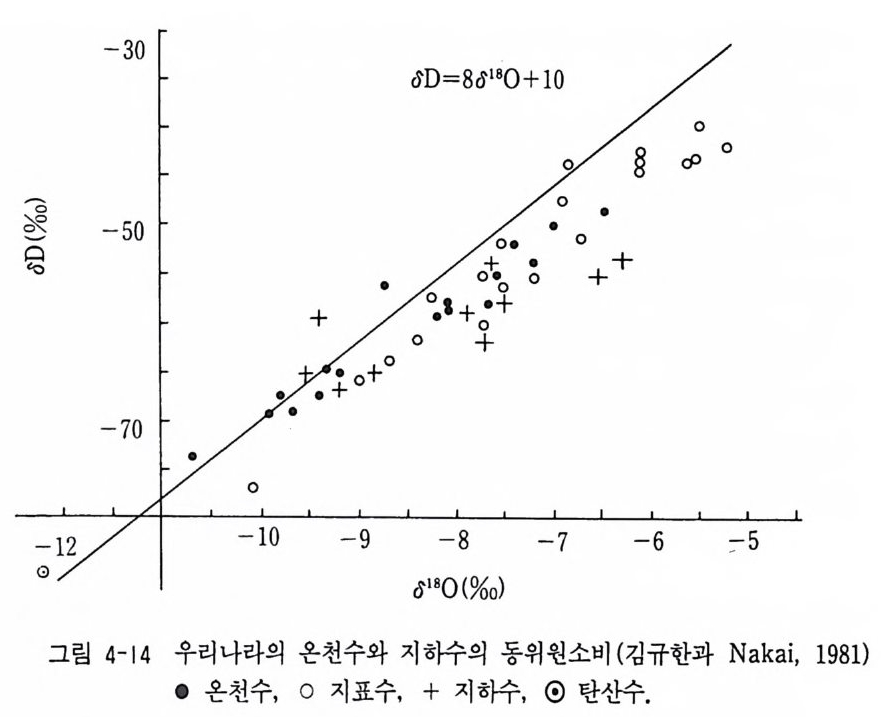 —30 0D=80180+10
—30 0D=80180+10
w-R 8Rf _ 8Ri 8Wi _ (8Rf _ 4) 여기서 8W, 와 8R i는 각각 동위원소 교환 반응 전에 존재하였던 물과 암석의 동위원소 값이다. 그리고 Rf 는 교환 반웅 후의 암석의 동위원소 값이며 4 는 동위원소 분별정수이다. 예를 들면 순환수 (oD=-12 %0, 0180 =一 16%0) 기원의 열수에 의해 화강섬록암 (0180=+8~9%o, oD=-65 %。) 이 열수변질을 받았을 때 W/R 비의 변화에 따른 동위원소 값의 변화는 그림 4-15 와 갇다. 그림에서 보면 W/R 비가 낮은 조건에서는 산소 동위원소 값은 변화가 적고 수소 동위원소 값은 변화가 크다. 그러나 W/R 비가 증가함에 따라 암석의 8180 값의 가벼운 산소 동위 원소에 의한 영 향이 크게 나타난다.
이갇은 현상은 미국의 아이다호 저반의 화강암질 암석의 열수변질에서도 잘 나타나고 있다. 우리나라의 화강암류의 산소 동위원소비의 분포(그림 4-16) 에서도 석영 의 동위원소 값은 균일한 데 비하여 전암의 산소 동위원소 값의 변화는 심하다. 이는 순환수 기원의 열수변질에 기인하는 것으로 해석되었다 (Ki m 등, 1992) .
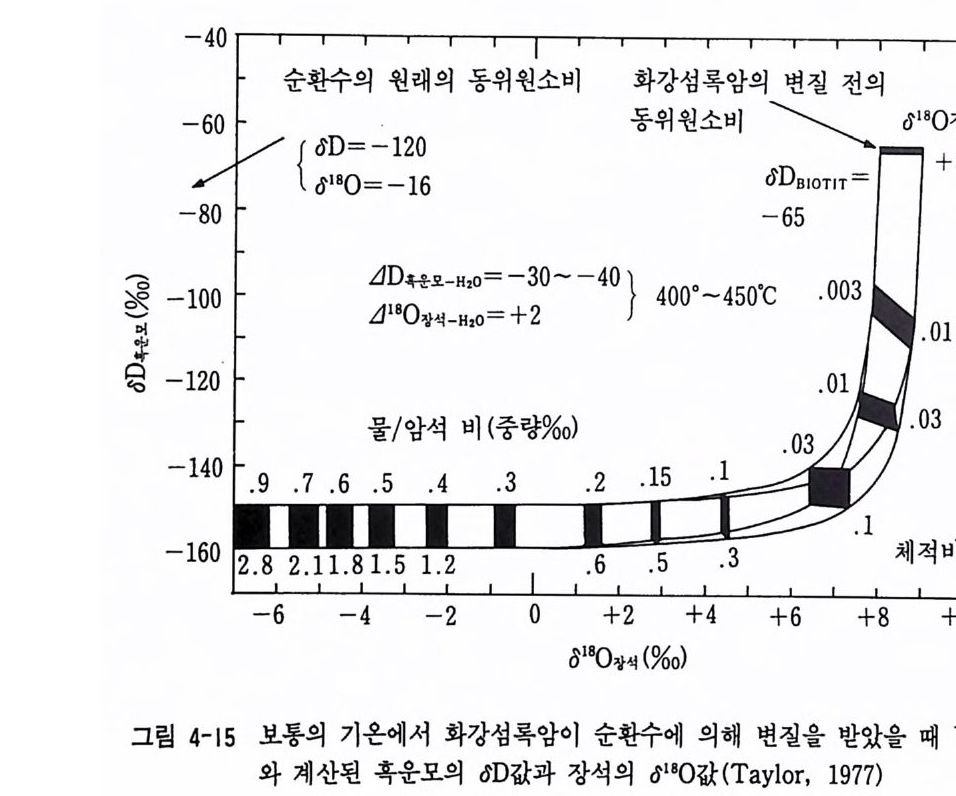 -40
-40
Camp be ll 등 (1984) 은 페루의 산크리스토발 (San Cris to b al) 함혹중석 석 영맥 광상의 광화 작용시의 열수의 기원과 W /R 바를 추 정하였다. 산크 리스토발 지역의 신선한 화강암의 동위원소 값 (a1 8 0 = +7 % , oD= - 70 %0) 과 중정석 내의 유체포유물의 물의 동위원소 값 (oD =- 14 % 0 , 0180 =
-20 %0) 을 초기 순환수로 가정 하고 흑운모-물과 사장석-물 사이의 동위 원소 분별을 이용하여 계산된 온도 673°K 에서 W/R 변화에 따른 열수 의 동위 원소 값의 변화를 계 산하여 나타내 면 그립 4 - 17 과 같다. 실제 혹 중석과 석영이 평형상태에 있었던 열수의 동위원소 값과 비교하여 보면 중석 광화 용액의 물/암석 비는 0.0 0 1~0.003 정도이며 혹중석은 순환수 와 마그마수의 혼합에 의하여 침전된 것으로 해석하고 있다.
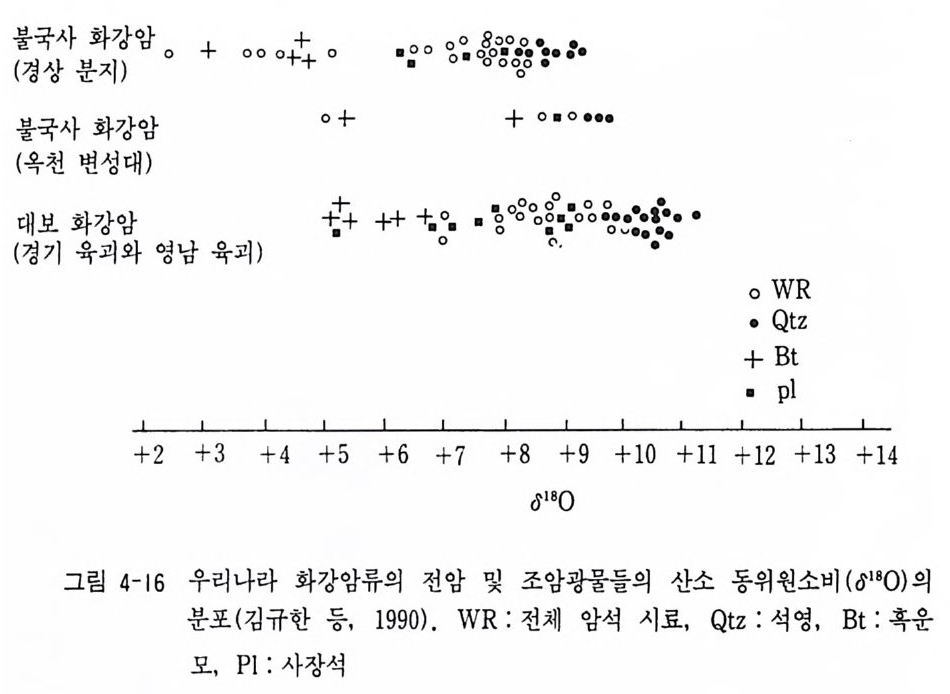 불(경국상사분 화지)강 암 。 + oo o++ + o • •O O 앙 건 。80 g .0o0.。0 o .•• “ &
불(경국상사분 화지)강 암 。 + oo o++ + o • •O O 앙 건 。80 g .0o0.。0 o .•• “ &
저온에서는 점토 광물이 물과 동위원소 교환이 일어난다. 그림 4-18 에 서처럼 풍화 산물인 퇴적 점토 광물의 동위원소비는 순환수선과 평행하 게 나타난다 . 즉 고령토선, 몬모릴로나이트선, 순환수선과 평행하여 점 토 광물이 형성될 때의 기후 조건을 잘 반영하여 주고 있다.
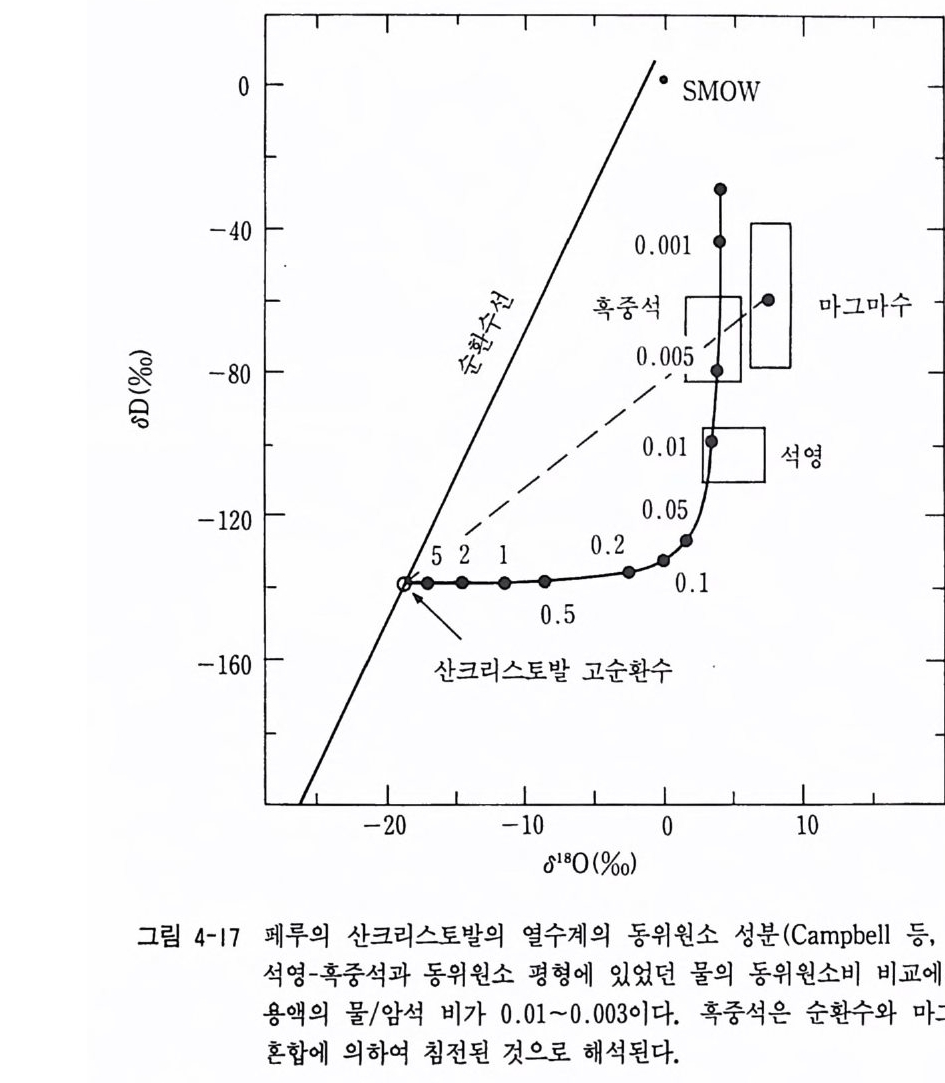 。 • SMOW
。 • SMOW
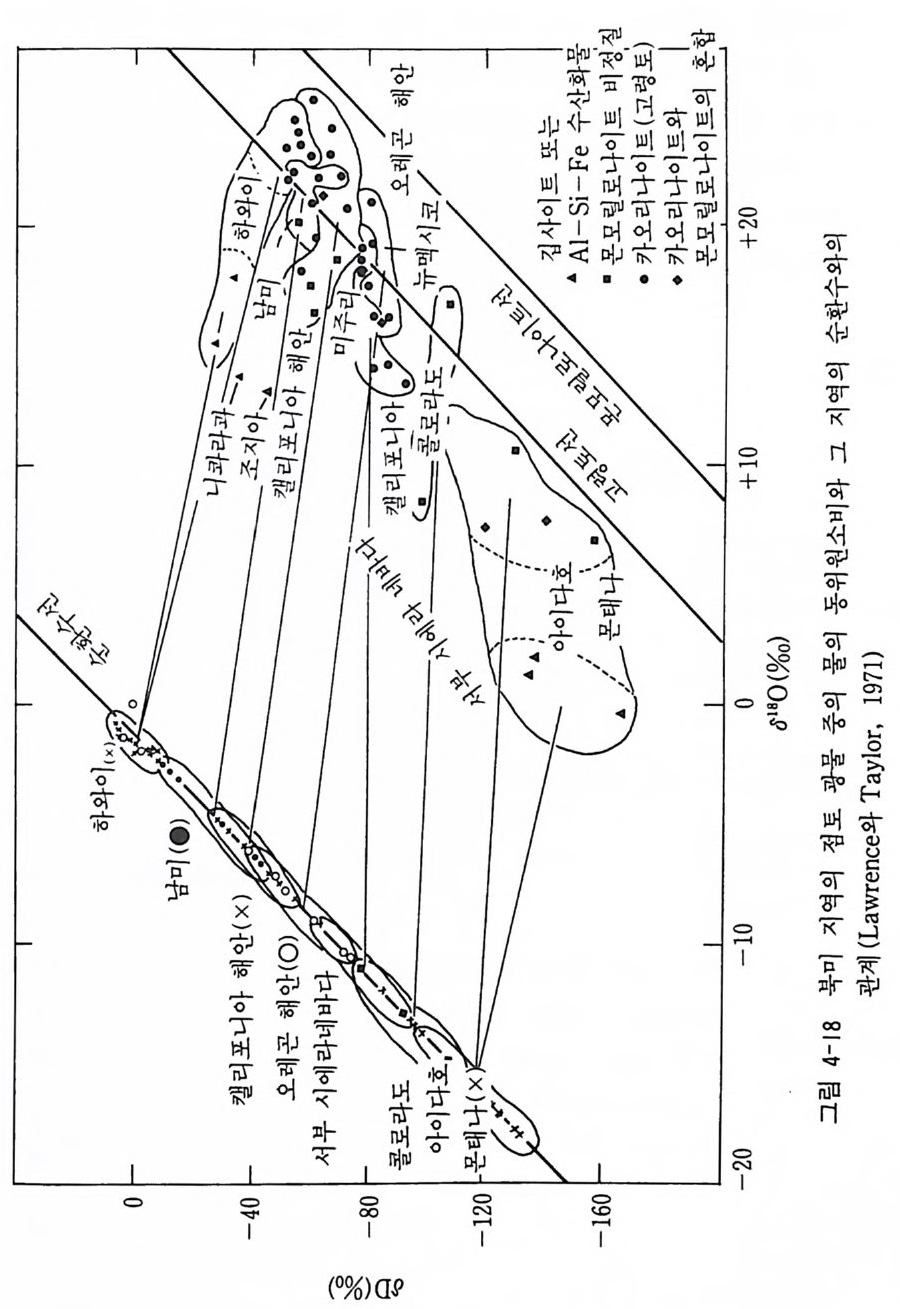 r·。〈삐버{「-매 γ·며시m킹’‘l때|국뻐 -헨때{얘•멤K며머미{」。메 h(미띠어{{。뎌뻐{」){•암 -」떼{•어{-κ띠。{.{어 。w{ι¢·」미때이-‘맨머메{’ ”g+ -이·{+{어#{이ψ
r·。〈삐버{「-매 γ·며시m킹’‘l때|국뻐 -헨때{얘•멤K며머미{」。메 h(미띠어{{。뎌뻐{」){•암 -」떼{•어{-κ띠。{.{어 。w{ι¢·」미때이-‘맨머메{’ ”g+ -이·{+{어#{이ψ
 cS3'S% o (CDT)
cS3'S% o (CDT)
황 동위원소비 황과 탄소 동위원소는 이들 원소의 순환, 지질시대에 있어서의 동위원 소의 진화 및 광상에서의 광화 용액의 기원의 해석 등에 이용되어 왔다. 왜냐하면 자연계의 물질에서 황이나 탄소의 동위원소비가 물질에 따라 차이를 보이고 있기 때문이다. 황은 산화 환원 반응과 황 환원 박테리아 에 의하여 동위원소 분별이 크게 일어나기 때문에 다양한 지질학적 환경 과 지구화학적 과정에 의해 황 동위원소비는 변화가 크게 일어난다. 운
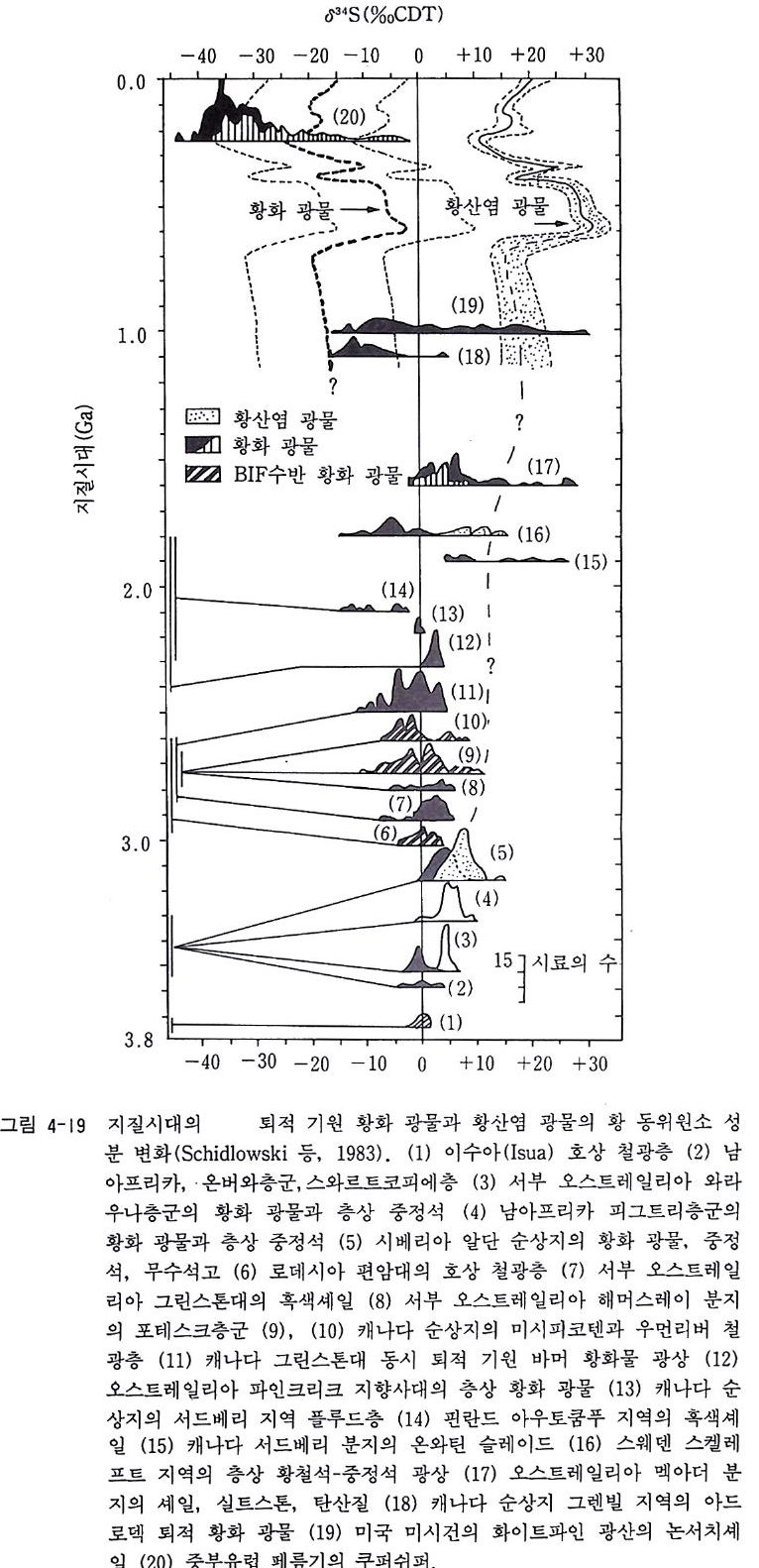 cS 'S(%oCDT)
cS 'S(%oCDT)
석이나 화성 기원의 황은 o34s 값이 O% o 에 수렵하면서 그 변화폭이 대단 히 작은 반면, 퇴적 기원의 황은 생물학적 과정 때문에 o34s 값이 -50~ +40 % 0 로 변화 폭이 크다. 해수 중의 so~- 의 o34s 값은 약 +2 0 %。 내의로 대단히 균질하지만 여러 지질시대에서 형성된 증발 잔류암의 o34s 값은 지질시대에 따라 지구 전체의 산화 환원 환경 변화에 따라 크 게 변동하고 있다(그림 6-10). 황화 광물 사이의 동위원소 분별 실험 및 이론 연구가 많이 이루어져 황 동위원소 지질온도계가 광상학에서 유용하게 이용되고 있다(그림 4-19) . 우리나라의 금속 광상에서 산출되는 황화 광물은 o34s 값이 +4~5 %。 정도로 대다수 화성 기원의 황이며 한강물에 용존하고 있는 sm- 의 o34s 값이 이 값과 일치하고 있어 한강물에 용존하고 있는 so~- 는 광상 황화 광물에서 유래하고 있음을 알 수 있다. 그리고 해운대 온천수 중 so~- 의 B3 4 S 값은 +20 % 0 로 동해 바다의 해수 기원의 so~- 가 혼입되었음을 알 수 있다(그림 4-20). 이처럼 자연계의 황을 함유하고 있는 모든 물질의 o34Srs 값의 분석에 서 트레이서로서 그 기원을 해석할 수 있어 광상 황의 기원, 환경 오영 원의 추적, 물질의 순환 등의 연구에 많이 이용되고 있다. 탄소 안정 동위원소비 탄소는 대기권, 생물권, 수권, 및 암석권에서 여러 가지 형태로 존재 하며 4.5 년을 주기로 순환하고 있다. 대기 중의 CO2 나 맨틀 기원의 다 이아몬드나 카보나타이트에서는 813C 값은 시공간적으로 비교적 변화폭이 좁다. 그러나 운석과 달 등의 의계 물질과 퇴적성 탄소는 o13c 변동폭이 크다. 광합성에 의해 생성된 식물에서는 그 값이 대단히 작다. 식물 중 에서도 C3 식물(대다수의 육상 식물)과 C4 식물(옥수수 등)과 CAM 식물 간에 013C 값이 차이가 있어 질소 동위원소비 (015N) 와 함께 고고학에서
고생태계의 물질 순환 연구에 이용되고 있다 (DeN i ro 와 Hastr o t, 1 985 Wada, 1986) . 황 동위원소와 함께 광상에서의 광화 용액의 기원 연구나 지질시대의 환경 변화에 따른 o1 3 c 값의 변화, 저온에서의 탄소의 기원이나 탄소의 순환 등의 연구에 이용되고 있으나 화성 기원의 탄소나 맨틀 기원의 탄 소 기원 규명에는 많은 문제점이 제기되고 있다. 질소 안정 동위원소비 생물권에서 질소고정 반응, 질산화 반웅, 탈질산화 반응 등에 의한 동 위원소 분별 작용과 신진대사 작용과 같은 생화학적 반응에 의하여 반응 속도론적 동위원소 분별 작용이 일어나 자연계의 물질이 상이한 동위원 소비를 가지게 된다• 질소 안정 동위원소비 (01sN) 분석으로 생명 활동과 물질 순환, 동물의 영양 관계, 토양 오염 연구 등에 이용하고 있다. 그 러나 아직 질소 동위원소 분별의 실험 연구가 별로 이루어져 있지 못하 다. (3) 동위 원소 지 질온도계 공존하는 두 물질 A, B 사이에 동위원소 평형이 이루어졌을 때 동위 원소 분별정수 (a, iso to p i c frac ti on ati on fa c t or) 는 RA aA-B=7 죠 로 정의된다. 여기서 RA 와 RB 는 상 a 와 b 내의 원소의 무거운 동위원 소와 가벼운 동위원소 사이의 비 (예를 들면 180/“O, “S/32S 등) 이다. 동위 원소 표시법 (8) 의 식을 여기에 대입하면
8a-b= 1l000000++8 oba 가 된다. 보통 a=K i 의 관계에 있으며 n 은 동위원소 교환이 일어난 원 자의 수를 말한다. a 의 값은 보통 l. OOX 로 표현되며 25° C 물과 수증기 에서는 a 노 =~=1.0092 이다. 여 기 서 R * 기 , R 군은 각각 수증기 상과 액 체 상의 180/160 값이 다. 평 형 상수 K=ex p( - LJ G0 / RT) 로 온도의 함수이므로 a 역시 온도의 함수이 다. 동위원소 교환 평형을 이용한 온도 변화에 따른 동위원소 분별정수 의 결정을 실험에서 구할 수 있으며 보통 1000 ln aA-B = A T• 120 6 + B 의 관계로 표현된다. 여기서 A 와 B 는 상수이며 T 는 온도이다. lOOOlna= 10001n (1. OOX) 값 와같으므로 a g― 1= 운 1=¥, a 운 1= 8Ob+a1-O00b0 가 얻어진다. 만일 a g가 1. 010 보다 작으면 Ob + 1000 ~ 1000
이 된다. 따라서 at- l ~ oIaO-OOOb 가된다. ag ~1 + &100겁0 ' In ag ~Jn (1+1 益 )=1000 In ag ~o a- o b 가 얻어진다. Oa- o b=L )g 라놓으면 1000ln at ~ 4gA XT 12 06 +B 가 되어 동위원소 평형에 있는 공존 2 광물상의 8 값의 차이는 온도가 증 가함에 따라 감소하는 관계가 얻어진다. 대단히 높은 온도가 되면 4 의 값은 0 에 가까워진다. 그러나 대다수의 공존 광물 사이에 C, H, 0, N, S 의 동위원소비는 차이가 있어 동위원소 평형 온도를 계산할 수 있 다. 지구과학 분야에 많이 이용되는 동위원소 분별은 표 4 - 3 과 갇다. 그러나 동위원소 지질온도계로 이용되려면 첫째, 공존하는 2 광물쌍이 동위원소 교환 평형상태에 있어야 하고 둘째 , 사용된 광물은 순수한 광 물 시료라야 한다. 그리고 셋째, 공존 광물상이 형성된 후에는 지질학적 사건에 의해 동위원소 교환이 일어나지 않아야 한다. 그 의에는 동위원 소 분별정수의 온도 의존성이 크고 동위원소 분별이 분석할 때의 실험 오차보다 커야 하는 조건이 필요하다. 동위원소 지질온도계를 사용할 때 공존 광물 사이의 동위원소 비평형을 쉽게 인지할 수 있다.
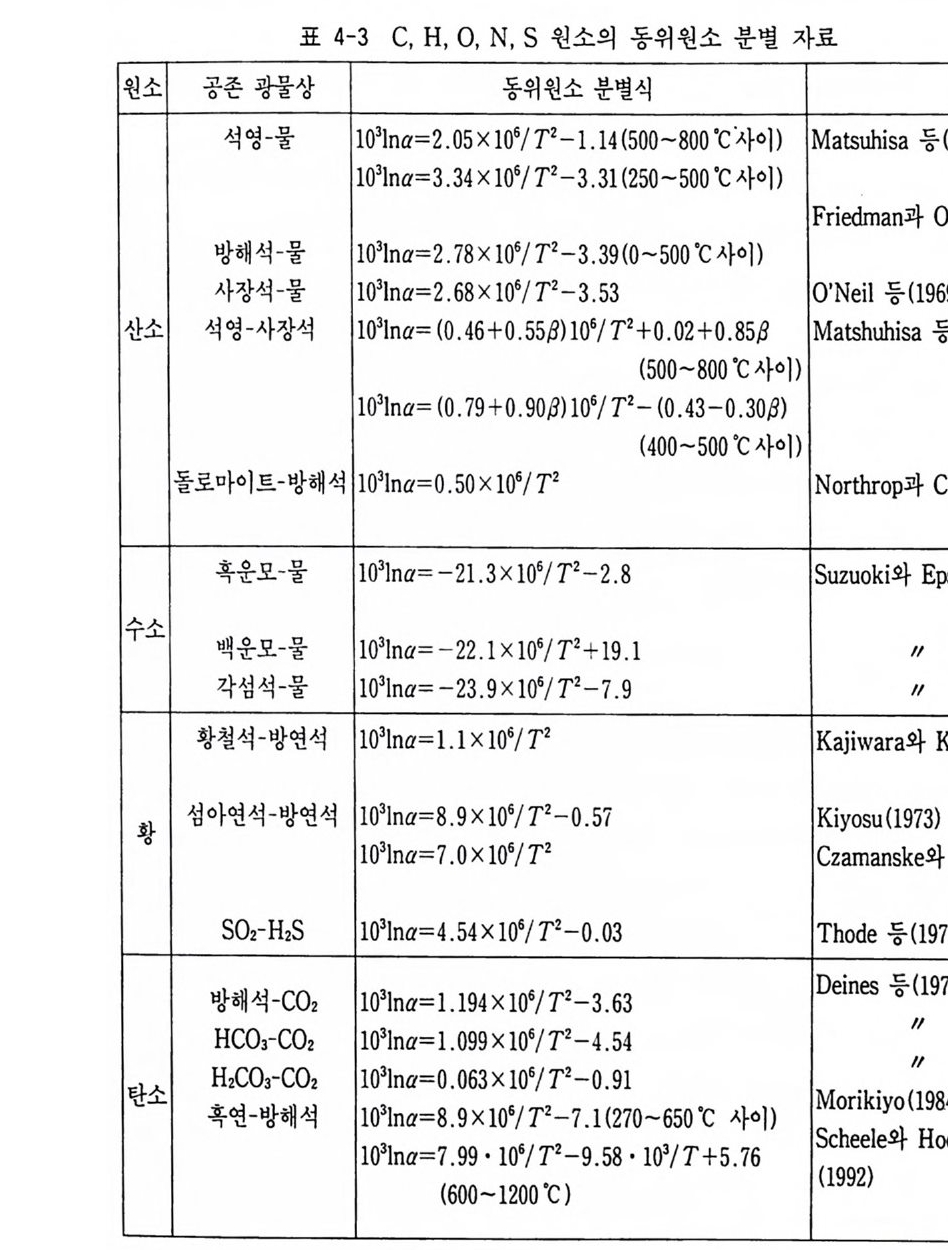 표 4-3 C, H, 0, N, S 원소의 동위원소 분별 자료
표 4-3 C, H, 0, N, S 원소의 동위원소 분별 자료
(4) 헬륨 동위원소비 헬륨 동위원소비 (3He/4He) 는 위에 설명한 C, H, 0, N, S 의 동위원 소와는 다르게 반응에 따라 동위원소비가 변화하지는 않는다. 지 구물질 중의 He 동위 원소비 분포 (그립 4-21) 에 서 보면 대 기 중의 3He/ 4He 비는 1.4Xl0-6Ra t m 이며 해령, 열점, 베니오프대 등지에서는 이 값 이 1 보다 훨씬 크고 대륙지각의 기반암이나 천연가스의 3He /4 He 비는 1 보다 작다. 그리고 지질시대와 이 값이 상관성이 있다. 이는 맨틀에는 지구 형성 초기의 원시 헬륨이 남아 있는 반면 지각에는 초기에 격렬한 탈가스에 의한 유실과 우라늄 굉물의 방사성 붕괴로 인하여 생성된 4He 의 영향이 크게 나타나고 있음을 말해 주고 있다 (Ma t suo, 1989). 지구 심부 기원의 가스 동정이나 지진 예지를 위한 지구화학적 연구 수단으로도 이용되고 있다•
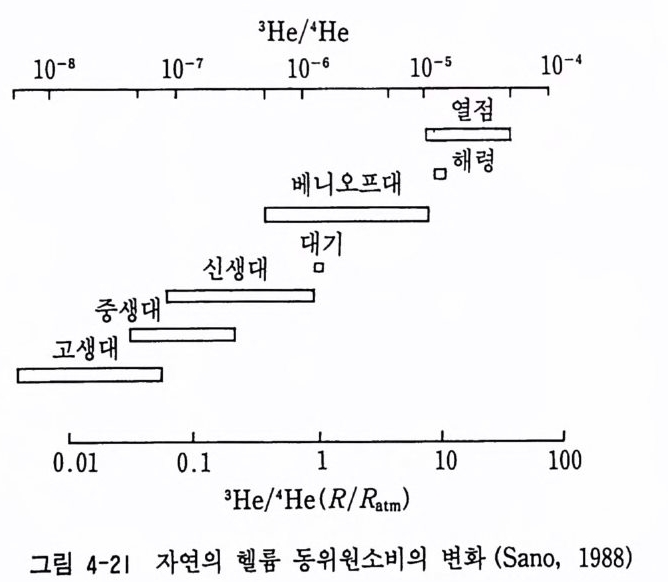 3He/'He
3He/'He
제 5 장 지구 물질의 원소 분배 화성암이나 변성암이 형성될 때에 확산이나 결정 성장 등에 의해 원소 의 이동이 일어나게 된다. 이같은 원소의 이동 속도나 원소의 분배 비율 등이 지질학적 환경에 따라 다르기 때문에 변성작용이나 마그마 작용이 일어날 때의 암석 성인사 해석에 이들이 응용될 수 있다. 즉 원소의 분배 연구에서 마그마가 생성될 때의 기원 물질의 특성, 용 융 속도 및 용융될 때의 물리화학적 조건을 해석할 수 있다. 또한 마그 마의 이동과 고결 작용이 일어날 때의 마그마와 모암과의 반응, 결정 분 별 작용, 상이한 기원의 마그마의 혼합, 결정화 작용이 일어날 때의 물 리화학적 조건, 마그마의 결정 작용 속도 및 냉각 속도, 분별 결정 작용 의 규모 등의 연구에 원소의 분배 연구가 유용하게 이용되고 있다.
5-1 원소 분배의 열역학적 콘트롤 어떤 성분(B)이 공존하는 2 광물상 (a 와 b) 에 포함되어 있는 것을 분배 (p a rtiti on) 라 한다. 이때 a 상과 b 상에 있어서의 B 의 화학 퍼텐셜은 µg( a)=µg( a) +RTlnxAa), µg( b)=µg( b) +RTlnxAb) 로 표현된다. 온도와 압력이 일정할 때 분배 평형이 이루어지기 위해서는 µg( a)= µg (b) 가 되 어 야 하므로 µg(a ) _ µg(b ) = RTln xAb)/xAa) 가된다. 죽
홉 =ex p{~써 (b) }=K 가 된다. 이것을 네론스트 (Nems t) 분배법칙이라 하고 이때 K 를 분배평 형정수라 한다. 원래 활동도로 표시되지만 여기서 편의상 2 상 중의 농도 의 비로 생각하여 x!b) 굽 =Ko 로 표현하고 이 Ko 를 분배 계 수 (dist r ibu ti on coeff icien t) 라 한다. 분배계수는 온도나 압력에 의하여 변화하므로 지질온도계와 지질압력 계로도 이용된다. 네른스트 분배법칙은 분배 성분이 2 상 사이에 공존하 는 성분의 이동에 한하여 적용되지만 특정 이온만이 이온 교환 반응에 의하여 분배가 일어난다. 예를 돌면 방해석과 무수석고 사이에 다음과 같이 이온 교환 반응이 일어난다.(Ca2+) 방해석 + (Sr2+ ) 석 고= (Sr2+ ) 방 해석 + (Ca2+) 석 고 이때 분배평형정수 (K) 는 K= (XSr) 방해 석 (XCa) 퓨석고 (Xca) 방해석 (Xsr) 유석고 =exp (~—µgrS04 ) 이 된다. 이들 2 상 사이의 2 성분의 농도비로 표시하면 분배계수는 Ko=(¾)~M 석/(홉)석고 가 된다. 그 의에도 공존하고 있는 흑운모와 각섬석에서 Co 의 분배, 암 염과 수용액 사이의 K + 의 분배, 마그마와 알바이트 사이의 Rb+ 의 분 배, 감람석과 휘석 사이의 Mg 2+, Fe2+ 의 분배, 감람석과 마그마 사이의 M 군, Ni2 + 분배 등의 예를 들 수 있다. 분배계수 (KD) 는 온도의 함수이 므로 미량원소 분배를 이용한 지질온도계가 보고되어 있다. 미량원소 분 배의 온도 의존성이 높은 원소는 사장석 내의 Sr, Ba, 휘석 내의 Cr, 석류석 내의 일부 희토류 원소 등이 있다. 현무암질 멜트와 장석 사이의 Sr 분배 의 지 질온도계 는 그림 5-1 과 같다. 5-2 원소 분배의 반응속도론적 콘트롤 지구화학적 과정은 보통 평형 조건에 이르게 되었을 때 지질 현상이 그 시공간상에서 종결이 된다. 그러나 많은 지질 현상은 반응속도론적 요소 (k i ne ti c fa c t or) 들에 의해 지배를 받는다. 예를 들면 저온에서 천천 히 일어나는 속성작용이나 열수변질작용에서 고온의 마그마의 결정화 작
용이나 변성암의 재결정 작용에 이르기까지 비가역적인 반응 속도의 영 향을 크게 받는다. 변성작용이나 마그마 결정화 작용과 같은 속도 콘트 롤 과정은 속도정수의 온도 의 존성 이 중요하다. Arrheniu s 0889) 는 일찍 이 반응속도정수 (K) 와 온도 사이의 관계 K=Aexp —f4 rG* 를 제안하였다. 여기서 A 는 빈도정수(fr e q uenc y fac to r ), LJ G* 는 가속 에 너지 (acti va ti on energy ), R 은 기체상수, T 는 절대온도이다. 반응 속도 과정 (rate pro cess) 에 는 확산 (dif fusi o n ) , 핵 생 성 (nucleati on ) , 결 정 성 장 과정 (cry st a l grow th) , 변 형 (tran sfo n nati on s) , 결 정 분별 작용 (frac ti on al cry st a l li za ti on ), 용융(fu s i on) 등이 있다.
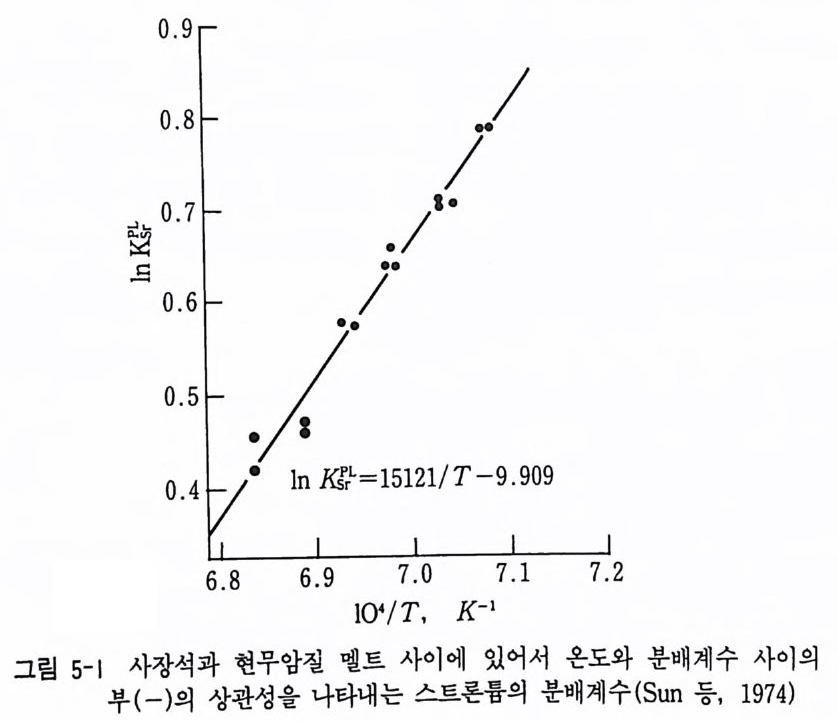 0.9 I
0.9 I
(1) 확산 과정 지질학적 과정에서 반응 속도는 계내의 화학 성분의 확산 방식이나 확 산 속도에 따라 다르다. 확산 방식에는 성분의 이동이 입자의 표면에서 일 어 나는 표면 확산 (surfa c e dif fus io n ) 과 입 자 경 계 를 따라 일 어 니는· 입 자 경 계 확산 (grai n b oundary dif fus io n ) , 입 자 내 부나 액 체 내 부를 통과하여 이동하는 체적확산 (volume dif fus io n ) 등이 있다(그림 5-2). 입자경계확산 과 체적확산 방식은 고온 환경의 지질학 시스템에서 대단히 홍미있는 방 식 이 다. 체 적 확산 기 구에 는 교환, 공국 이 동, 공국 충전 (int e r sti tialc y ) , 공동으로 이동 (vacanc y) 등의 4 가지 유형이 있다. 체적확산의 경우에는 장석 내에 산소가 확산되는 것처럼 동일한 원소로 구성된 시스템 내를 원자나 이온이 이동하는 자발확산 (sel f -d iff us i on) 과 감람석에서 Mg - Fe 교환이 일어나는 것처럼 한 성분이 다른 성분과는 독립적으로 확산되는 상호확산 (int e r dif fusi o n ) 을 구분해 서 다루는 것 이 효과적 이 다. 확산계수 (D) 의 표현에서 자발확산은 보통 트레이서 확산계수(t racer dif fus io n coeff icien t, D* )로 표현한다. 예를 들면 산소로 구성된 규산염에 서 180 이 이동하는 경우나 철감람석에서 55Fe 동위원소 이동 (55Fe2S iQ 4 -56Fe2SiQ 4) 을 들 수 있다.
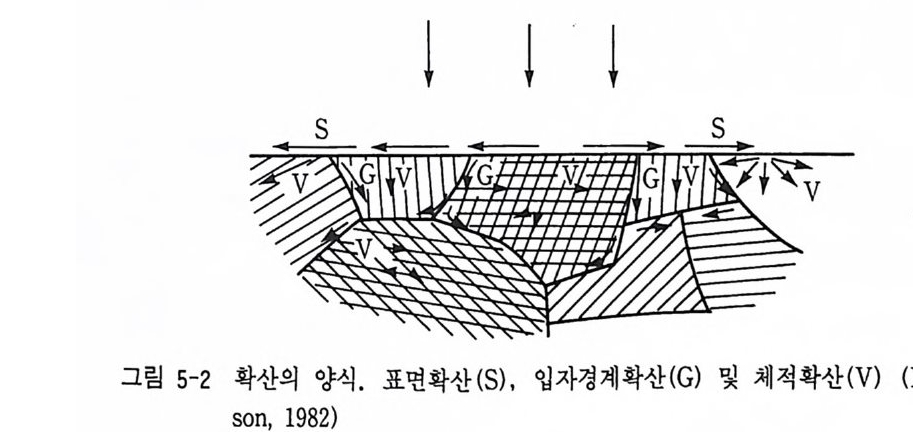 · 曺 曺 s
· 曺 曺 s
이온종 1, 2 의 상호 반응시의 상호확산에는 상호확산계수 (DE2) 를 사 용한다. 두 확산계수 사이의 D1-2= n1Dni*1 ++ nn22 Di* 관계에서 지질학 시스템 내의 상대적인 존재도로서 상호확산계수를 계산 할 수 있다. 그러나 지질학적 시스템에 적용하기에는 다량의 실험 자료 등이 요구되므로 대단히 어렵다. 때문에 금속학자들이나 세라믹 연구자 둘이 이용하고 있는 원자 수준에서 기계적인 접근 (mechan i s ti c per - spe ctive ) 방식 의 확산울 이용하기 시 작하였다. Talyo r 등 (19 77) 과 Buenn i n g과 Buseck 0973) 등은 원소의 확산으로 마그마의 냉각 속도 등을 추정하였다. 확산계수 D 와 온도 사이에 다음 과 같은 확산방정식을 이용하면 감람석 결정의 성분 변화에서 마그마의 냉각 속도를 계산할 수 있다. 릅=훑 {D 』 C (x) , T (t) ]틀} 여기서 C 는 감람석 중의 철의 농도이며 Da 는 결정축 a 를 따라 일어 나는 확산계수(결정축에 따라 확산 속도가 달라 c 축의 Dc 가 a 축의 Da 보다 크다)이다. 냉각 속도가 다른 몇 가지의 경우 결정의 핵에서 가장자리까 지의 거리와 감람석의 성분 변화 사이에 계산된 모델은 그림 5 - 3 과 같 다. 달에서 가져온 현무암 내의 감람석 결정의 EPMA 분석 자료에서 얻 어진 결정 성분 자료들의 모델과 비교하면 달 현무암의 최저 냉각 속도 는 5°C/ 일로 추정된다.
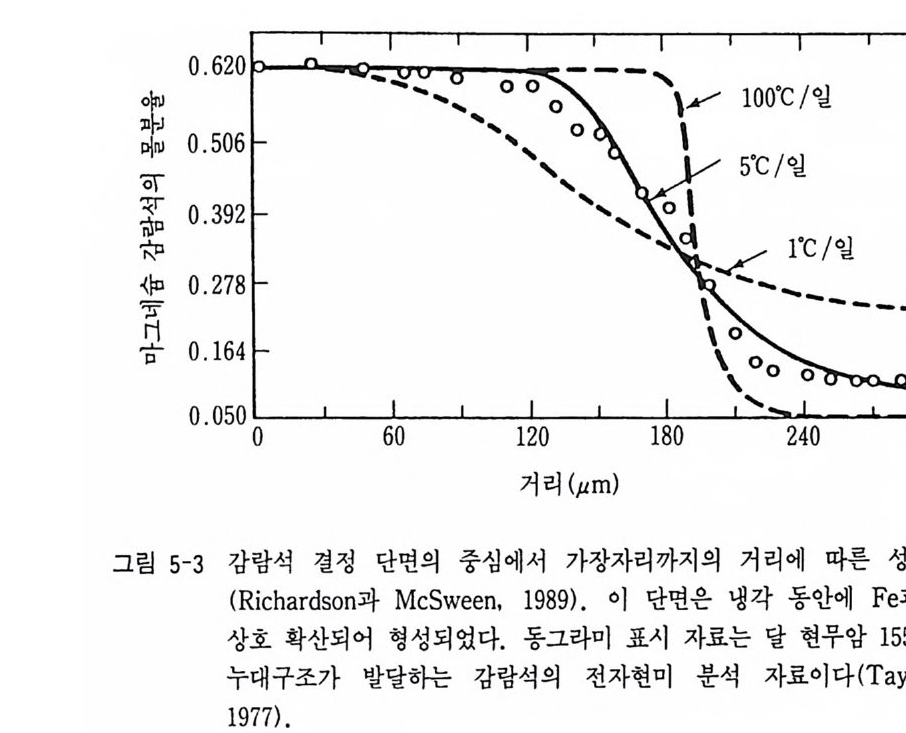 ;孟<히守더Itii 000。 ....2563 7029 8620 ` ......... `` `o ` ` o` o` - ` -` --、..'. \\ /< 1 0.0..° C:./C二 일
;孟<히守더Itii 000。 ....2563 7029 8620 ` ......... `` `o ` ` o` o` - ` -` --、..'. \\ /< 1 0.0..° C:./C二 일
(2) 결정 분별 과정에서의 원소 분배 그린란드의 스케어가드 충상관입암체에서처럼 마그마가 냉각됨에 따라 먼저 형성된 결정이 침전되므로 잔액의 성분이 점진적으로 변하여 온도 가 내려감에 따라 결정되는 결정 작용에서 만들어진 암석은 분별이 잘 일어난 암석이 된다. 이와 같은 분별 결정 과정에서 미량원소의 분배 과정을 정량적으로 생 각하여 보자. 처음 Lo 의 마그마인 액체상에서 W( g)의 고체상(결정)이 정출되었다 고 하면 이때 액체상은 L=L 。 -w 가 된다. 액체상 L 과 고체상 S 사이 에 열역학적 평형이 이루어진다. 그리고 각 상에서는 Ws, WL( 중량)의
미량원소가 포함되어 있다면 고체상의 미량원소 농도 (CS) 와 액체상의 미량원소 농도 (Cl) 사이에 미량원소의 농도비는 K= 몽, cs= 唱 cl= 干 (5 .1) 가 되 며 여 기 서 K 는 분배 계 수 (pa rtit ion coeff icien t) 이 다. 결 정 이 계 속 정 출되어 dW 만큼 정출되고 dW 중에 미량원소가 dW 만큼 포함되어 있 다면 결정된 부분에서의 농도는 C 됴盟 WS (5 .2) L 。― W 가 된다. 결정화 작용이 순간순간마다 액체상과 평형상태를 유지하면서 진행된다고 가정하면 K=—CC L5 =-- ( Wo-dWW 5)5I/d(WL 。 - W) (53()54 ) dWs= ( 隋- WS) =K • (Lod_ww) · 가된다. 초기 조건 t =O 에서 W5= W=O 를 이용하여 위의 식을 풀면 l 」 =KIn L 。£ 0 W (5 . 5) 가 된다. 이때 결정화의 정도를 F=1 ―션L\ 。 로 놓은 (5.5) 식에서 百CL=- WW o//LL 。 = (F) K-1 (5'·16)L5·7 ) 웁 =K. (F)K-I
과 갑이 레일리 증류방정식과 유사한 결과가 얻어진다 (Oz i ma 등, 1990). 여기서 일단 광물이 정출되면 결정이 계에서 빠져나가 버리므로 물질 교 환이 더이상 일어나지 않는다.
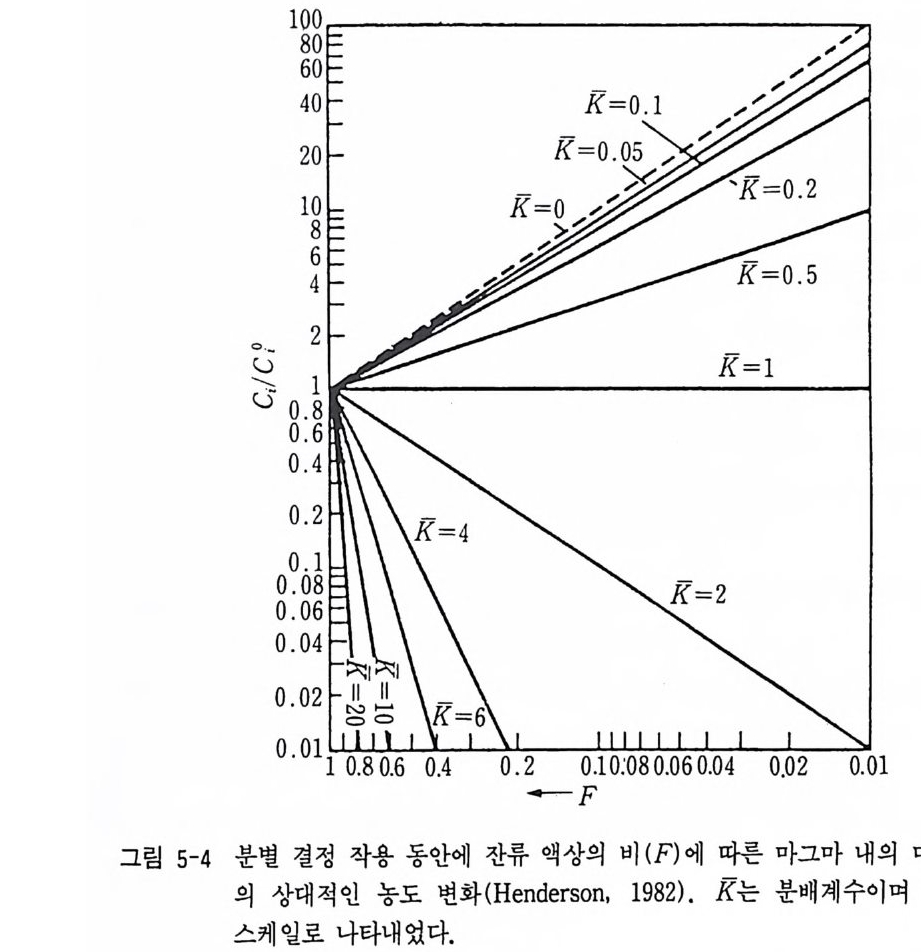 ,,,,
,,,,
그림 5 - 4 는 위의 (5.6) 식의 이론적 모델에서 상이한 K 값에 대하여 잔액의 비율에 따른 Ci / CY( 또는 Cs/C? )의 변화를 나타내고 있다. K= 0 이상에서는 액체상 중의 원소의 상대적 농도는 더이상 증가하지 않는 다. 폐쇄계라면 위의 식에서 K 값의 변화는 온도, 압력, 액의 성분, 결
정 성장 속도 또는 서로 다른 결정 광물의 비 등과의 함수 관계를 가지 게 되어 암석학에 응용될 수 있다. 결정화가 진행될 때 초기에 집적된 결정들에 분배된 미량원소의 함량과 후기에 정출된 결정 내의 미량원소 의 분배를 조사하여 마그마의 결정화 비율을 추정할 수 있다. 현무암질 마그마에서 분별 결정 작용에 의해 형성된 초염기성암으로 된 캐나다의 Muskox 관입암체에서 결정 분별의 예를 들어 보자. 4 회 사이클을 나타내는 5~20 m 충후의 암석 내의 충준 고도에 따른 Ni 함량이 불연속적인 변화를 나타내고 있다(그립 5-5 ) . 이는 이 시점마 다 새로운 마그마가 공급되었기 때문이다. Ni 함량이 하부에서 상부로 감에 따라 체계적으로 감소하는 현상은 결정화가 진행됨에 따라 N i이 마그마에 비해 결정에 우선적으로 분배되어 제거되었기 때문으로 해석하 였다. 만일 1220~1320 m 간의 100 m 충 사이에 Ni 함유량이 3100 ppm 에서 1700 pp m 으로 감소하였다면 위 식에 Ni 함량값과 noo·c 의 감람 석 그래스의 분배계수의 실험치 K=15 를 대입하면 CcVsl 5=15F14. F=O. 960 이 계산된다. 이는 이 구간에 분출된 화산 활동이 일어날 때에는 본원 마그마 약 4 % 정도가 결정화되었음을 가리킨다. (3) 부분 용융시의 미량원소의 분배 마그마에서 결정 분별 과정의 역으로 일어나는 과정이 부분 용융 과정 이다. 예를 들면 고체 물질 Wo( g)이 부분 용융되어 L( g)의 액상이 만 들어졌다면 액상의 분율(fr ac ti on, F) 은 F=WL~o (5 .8)
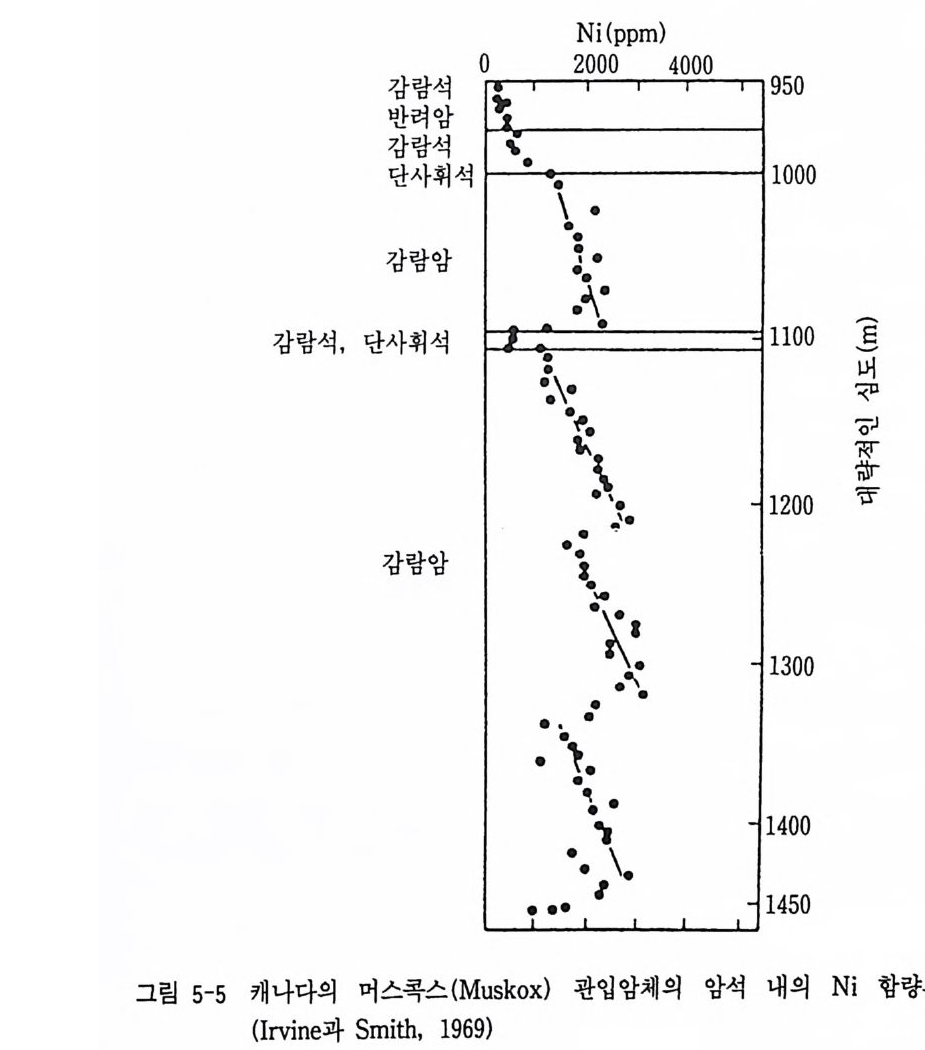 Ni( ppm )
Ni( ppm )
이 된댜 용융이 계속 진전되어 dL 만큼 액상이 증가하고 이때 dL 중에 미량원소가 dWl 만큼 녹아 있다고 하면 dL 중에 미량원소의 농도t el) 는
CL= 싼dL (5.9) 가 된다. 분배계수 (K= 응)를 고려하면 ddWL Kl WWoo--WL (5 .10) 의 관계가 얻어진다. 여기서 초기 조건 L=O, W= H1a, W= Wo 을 이용 하여 적분하면 lnWwo =K1l.n 而w 훑(溫 )1/K (5 .11) 가 얻어진다. 여기에 액체상의 분율 (F) 을 고려하면 cs 1 국c。 =(1-F) 亡 욕C=o. l.K. (1-F) 志 (5.12) 가 된다. 만일 분리된 액체상이 한 곳의 마그마 방에 모여 있다면 이 용 액 중의 미량원소의 농도식 (5.12) 는 F 로 적분되어 요C=o _lF_ (1- (1 -F))½ 이 얻어지고 액체상과 고체상이 공존할 경우에는국8GCo== —>K1 ((11 一- FF)) 了*-l 이 된다. 부분 용융시 액체상이 몰분율 F 만큼 계에서 빠져나갔으면 그때의 고 체상과 액체상에서의 미량원소의 농도 硏 융=*(l -F) ( {-1) 이 된다. 또 잔류 고체 광물 중에서의 미량원소의 농도는 욕Cs =(1-F) 軒) 이 된다 (Oz i ma 등, 1990). 5-3 마그마의 분화와 미량원소의 분배 마그마가 냉각, 결정화 작용이 일어날 때 미량원소 중에서 광물 결정 격 자 내 에 쉽 게 들어 갈 수 있는 원소를 호정 원소 (comp at i ble element) 라 하고 그렇지 못한 원소를 불호정 원소(i ncom p a ti ble elemen t)라 한다. 마 그마에서 광물이 결정화될 때에 미량원소의 분배가 일어날 때 분배계수 는 (KD) 액겅정 고액체체상상 중중의의 미미량량원원소소의의 농농도도 로 표현된다. 여기서 분배계수 Ko>l 인 원소를 호정 원소라 하며 Ni,
Cr 등이 여기에 해당된다. 불호정 원소는 KD < 1 인 원소로 LIL(Large ion litho ph i l e ) 인 K, Rb, Sr, Ba, Zr, Th, REE 등의 원소들이 있다. 부분 용융시나 분별 결정 작용시에 고체상 잔유물에 우선적으로 남는 원소는 호정 원소이 다 (그립 5-6) . 란탄 계열 원소 또는 희토류 원소 (REE, rare earth elemen t s) 인 La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy , Ho, Er, Tm, Yb, Lu 는 모두 불호정 원소이다. 그러나 달이나 지구 맨틀에서처럼 환원 환경에서 는 Eu2+, Eu3+ 상태로 존재할 수 있으며 Eu2+ 는 Ca2 + 과 이온반경이나 전하가 유사하기 때문에 환원 조건에서 서로 치환되므로 이들 원소는 호 정 원소처럼 행동한다. 산화 환경에서 Ce 는 Ce” 로 산화된다. Ce 는 해양에서 망간단괴에 침 전되어 해수에서 Ce 이 결핍된다. 해수 기원 열수 용액에서 함금속 퇴적 물이 되적되기 때문에 중앙해령에 퇴적되고 있는 합금속 퇴적물에도 Ce 이 결핍되어 있다. 이처럼 환원 환경의 Eu2+ 와 산화 환경의 Ce” 를 제의 한 모든 REE 는 불호정 원소의 거동을 한다. 여러 광물상에 있어서 REE 의 KD 값은 결합 특성보다도 이온반경의 크 기에 더 많은 영향을 받는다(표 5-1). 일반적으로 광물의 결정구조 중에 존재하는 양이온 사이트의 크기와 유사한 이온반경을 가지는 원소는 고체 광물상에 분배 농집되기 쉽고 그 렇지 않은 원소는 잔액상에 남기 쉬워진다. 각 광물에 있어서 광물-멜트 사이의 원소 분배의 특칭에서 마그마의 분별 결정 작용시에 마그마 중의 원소의 성분의 변화를 예상할 수 있다. 초기에 정출되는 감람석과 휘석 등에 Cr, Ni, Se 이 분배되기 쉬우므 로 분화가 진전됨에 따라 이들 원소는 감소하게 된다. Ti, V 은 자철석 정출시에, P 는 인회석 정출시에 각각 제거되므로 이때부터 이들 성분이 감소하게 된다. 그러나 불호정 원소인 Ba, REE, Y, Zr, Nb, K, Rb, Cs, Ta, U, Th 등의 원소는 잔액에 농집되므로 분화 후기로 갇수록
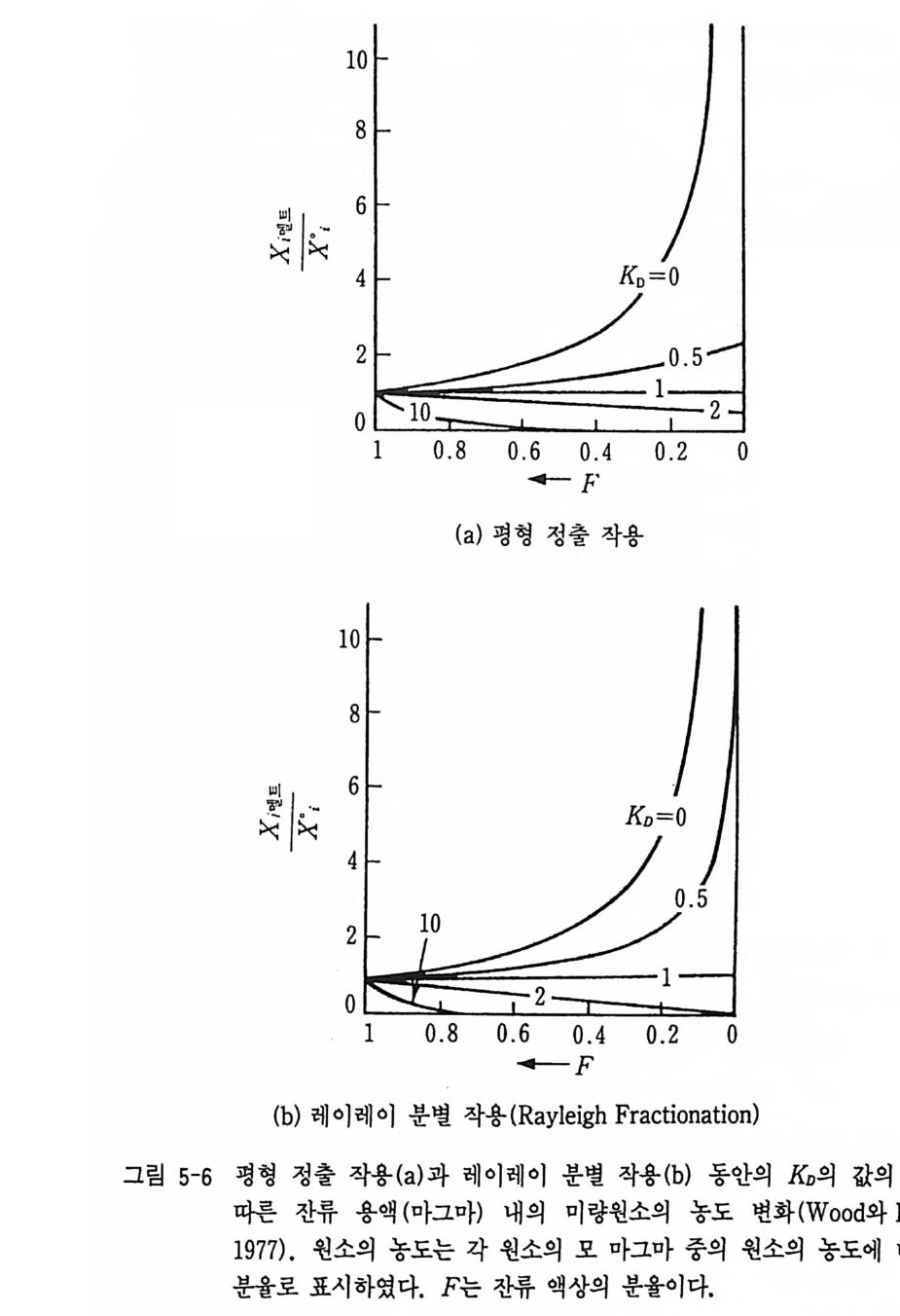 10
10
증가한다 . 물론 부분 용융시에는 불호정 원소는 초기에 생성된 액에 농 집되게 된다. REE 는 맨틀에서의 부분 용융과 마그마 분별 작용에 대한 암석 성인 모델 연구에 대단히 유용하다. REE 는 변성작용 조건 하에서 비교적 불 용성인 특성을 가지므로 변성암의 원암(p ro t o lit hs) 추정에도 유용하다 . 란탄 계열의 원소는 지표 조건에서 불용성 이 므로 퇴적물에서의 이들 함 량이 바로 평 균 지각의 함량을 나타낸다. 그 리고 해수에서 REE 의 정체 시간이 짧기 때문에 해수의 혼합 추정에도 이용될 수 있다 . 미량원소나 R EE 가 화성암 암석 성인 모델 해석에 이용된 예로 인도 양에 있는 Reu ni on 섬의 현무암 용암에 대 하여 알아보자.
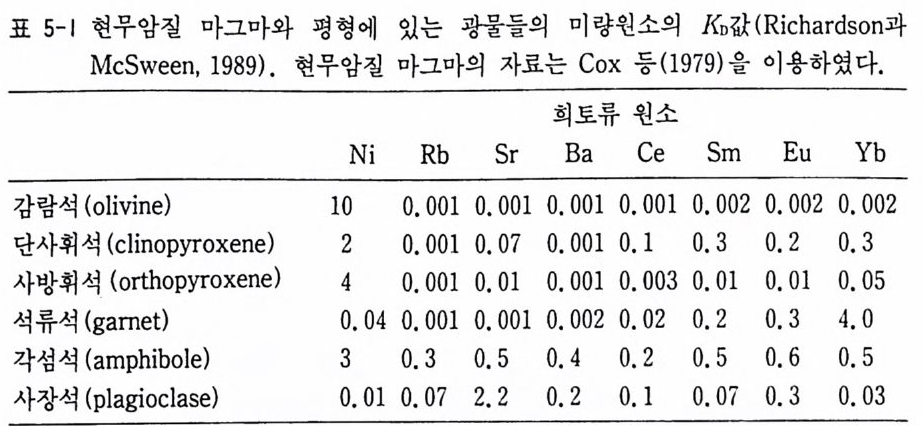 표 5-1 현무암질 마그마와 평형에 있는 광물들의 미량원소의 K0 값(Ri chardson 과
표 5-1 현무암질 마그마와 평형에 있는 광물들의 미량원소의 K0 값(Ri chardson 과
Z i el i nsk i(1 975) 는 이 지역의 현무암 시료의 REE 와 미량원소 분석을 실시하여 이들 성분의 변화를 그림 5-7 과 같이 나타내었다 . 그림에서 보 면 REE 의 값 은 1 에서 8 로 가면서 평행하게 증가하고 있다. 이는 불호 정 원소인 REE 는 잔류 마그마로 갈수록 증가해야 하기 때문이다 . 시료 8 번에서 Eu 부 의 이상은 대량의 사장석이 정출, 제거되었기 때문이다. Eu 이상 해석에서 마그마 중의 산소 분압의 정보를 얻을 수가 있다 . 미 량원소 중에도 U, Th, Ba 은 다른 원소에 비해 불호정 원소의 특칭을
200 ( a )삐 100 l50 0
l뼈]ilU{ 20 Y10 5 La Ce Nd Sm Eu Gd Tb Dy Yb Lu 1200 (b) 흥 800 Q.d 400 2 3 4 5 6 7 8 시료 그림 5-7 인도양의 리뮤니온섬의 현무암의 분석치 Oizl in s ki, 1975) 를 콘라이트 값 으로 표준화한 희토류 원소의 변화 패턴 (a) 와 기타 미량 원소의 변화도 (b) (R ic hardson 과 McSween, 1989). 이 패턴은 시료 3~8 이 시료 2 의 성분을 가지는 액상 마그마의 접전적인 분별 결정 작용에 의해서 형성된 모델과 일치 한다. 시료 l 은 큐무레 이트 암석 인 것으로 나타났다.가지므로 후기에 분출한 충준으로 감에 따라 점진적으로 증가하고 있다. 그러나 Ni, Cr 은 호정 원소의 특징을 나타내며 1 번 시료는 추정된 모델 계산에서 얻은 값이 본원 마그마에서보다 더 높은 값을 가지고 있었다. 왜냐하면 이 암석은 큐무러스상을 다량 가지고 있기 때문으로 보인다. 이같은 결과는 KD 와 잔류 마그마의 분율 (F) 값을 이용하여 모델 계산을 하여 추정한 마그마의 분별 과정에서의 미량원소의 변화 경향과도 일치 하고 있다.
제 6 장 물의 화학 지구 내의부에서 물은 끊임없이 순환하고 있으며 물의 순환 과정에서 물질의 순환이 함께 일어나고 있다. 모든 지질학적 현상은 물의 순환과 밀접히 관련되어 있다. 지표에서의 생물의 발생과 전화 , 풍화 , 침식 , 퇴 적작용 등이 물에 의하여 일어나고 있으며 광물의 침전, 결정 성장, 마 그마 활동, 변성작용과 암석의 형성에도 물의 역할은 대단히 중요하다. 지표 환경에서 일어나는 수문학적 과정을 다루는 분야를 수문학 (hy dr olog y) 이 라 한다. 물의 특칭 중의 하나는 다른 용액과는 다르게 자 연의 물질을 용해시켜 다양한 특성을 가지는 수용액을 만든다는 것이며, 이것은 순수한 물과는 다른 물리화학적 특징을 가지게 되어 자연계의 지 질학적 과정을 일으키게 한다. 따라서 물을 연구하는 지구화학자들은 석 고충과 평형에 있는 지하수의 황산염의 농도나 열수 광화 용액 중에 운 반될 수 있는 불소의 양에 홍미를 가지게 된다. 또 해수의 증발 과정에
서 형성될 수 있는 광물의 종류와 형성 순서, 광화 용액의 이동 중에 한 금속 원자가 주위에 있는 몇 개의 음이온이나 중성 분자와 결합하여 이 루어진 착이온의 거동과 광석 광물의 침전 메커니즘이 밀접한 관련을 가 지고 있다. 폐기물 처리장에서의 화학적 누수 현상이 주위 암석이나 토 양의 안정도에 주는 영향과 오염 현상 등에도 홍미를 가지게 된다. 6-1 용해도와 용액 (1) 용해도 순수한 물 속에는 다양한 물질이 녹아 있다. 100 g의 용매를 포화시키 는 데 필요한 용질의 그램수를 용해도 (solub ility)라 한다. 이렇게 포화에 도달한 용액을 포화용액 (satu r ate d soluti on ) 이 라 한다. 포화용액 을 만들 면 해리된 이온과 녹지 않은 고체 사이에 다음과 같은 동적 평형이 이루 어진다. AB( 고체) =A + +B- =鬪써衍 =Ks p 즉 일정 온도에서는 해리된 이온의 농도의 곱은 일정하다. 이 를 용해 도곱 상수 (solubil ity p roduc t」 G p) 라 한다. 용해 도곱 상수와 이 온 농도의 곱의 대소 관계에서 [A+ ][ B- ] < Ksp 일 때에는 불포화용액으로 AB 고체상이 침전되지 않는다. 그리고 [A+ ][ B-]=Ksp 일 때에는 포화용액이 되고
[A+ ][B - ] > K sp 일 때에는 과포화용액으로 AB 고체상이 침전된다.
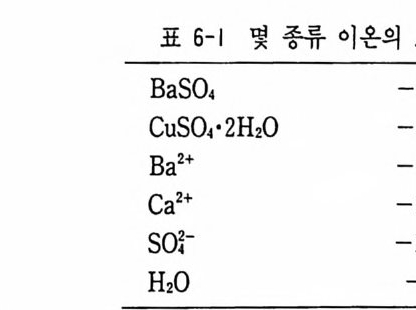 표 6-1 몇 종류 이온의 4E; 값
표 6-1 몇 종류 이온의 4E; 값
25· c 물에서의 중정석과 석고의 용해도를 다음 표 6 - 1 의 열역학 자료 룰 이용하여 계산할 수 있다. 예를 들면 중정석의 용해도 계산울 위해서 BaS04 ~ Ba2+ + SO!- 반응식에서 LlG~ = —1 34 .02+ ( —1 77. 97) —( —3 25. 6) = 13 . 61 kca lmol-1 log K sp = _~4C!= 래 . 98 (Ksp = 1. 0 4 X1 0- 10) 를 계산한다. 용액이 이상용액이라 가정하면 중정석의 용해도는 [Ba+] = [c1-] =~=1.02 x 1 0- s m ol kg- 1 이 된다. 이 값은 Blou t U977) 의 실험에서 추정한 값인 1.0 6 X 1 0-5mol k g -I 과도 유사하다. 이 값을 m B a2+ 로 표현하면 1. 02 x 10-s mol kg- 1 x 137 . 34 gB a mol-1
로 1.40 ppm Ba 에 해당되고 2.39 ppm BaS04oJ ] 해당되는 값이다. 그리고 석고의 경우 25·c 에서 용해도를 계산하면 CaS04 • 2H20 :;:::=:= Ca2++soi- + 2H20UGp = 2.45X l0 -5) 이며 용해도는 [Ca2+ ]= [SOi -] =~ 이 얻어전다. 25·c 에서 얻어진 일부 광물의 용해도곱의 자료는 표 6-2 와같다.
 표 6-2 25C 에서 계산된 일부 광물의 용해도곱
표 6-2 25C 에서 계산된 일부 광물의 용해도곱
용해도곱은 용액 중에 기타의 염이 공존하여도 항상 일정하다. 예를 들면 A g Cl 의 침 전과 평 형 에 있는 포화용액 이 있다면 [Ag +] [Cl-] =Ksp 이다. 여기에 HCI 이나 A g N03 를 소량 추가하면 용액 중에 [A g + ]나 [cr] 가증가하여
[Ag +] [C i -] >K sp 가 되어 침전이 일어난다. 이처럼 임의의 염과 양이온이나 음이온을 첨가하면 원래의 염의 용해 도가 감소한다. 이를 공통이온효과 (common ion e ff ec t)라 한다. 이 효과 는 분석화학에서 널리 이용되고 있다. 착이온과 용해도 열수 용액에서 금, 은, 동 등 많은 금속 이온은 착이온의 형태로 이동 되는 것으로 알려져 있다. 따라서 광화 용액 중의 착이온의 거동은 금속 광물 침전에 있어서 대단히 중요하다. 많은 금속 이온, 특히 전이원소의 이온들은 다른 분자나 이온과 결합하여 Au(CN)2-, Au( HS 2)-, AuCl4, AuF1, Cd(CN)~-. Co(NH3H+ , Ag (N H3)2+ , Ag (C N)2-, Zn(OHH-, ZnCi t Cu(CN)2, Cu(NH3)~+ , Ni (N H3)2+ 등과 같은 착이온을 만든다. 용해되지 않는 염의 용액에서 금속 착이온이 만들어질 때 금속 이온의 농도는 감소하게 된다. 따라서 금속 이온 농도가 Ksp 평형에 이르게 될 때까지 주위 암석에 있는 물질이 용해된다. 그러므로 용해되지 않는 염 의 용해도는 착이온이 만들어질 때 증가하게 된다. 일반적으로 NH3 나 CN 등은 착이온을 쉽게 만들기 때문에 NH3 가 존 재하면 A g자은) 이온은 쉽게 Ag + + 2NH3;:::::::::::::Ag (NH3) t 와 같은 착이온을 만들게 된다. 따라서 NH3 나 CN 등이 금속 이온의 용해도에 크게 영향을 준다.
탄산칼슘의 용해도 물에 용존하고 있는 탄산 이온에는 C02( a q ), H2C O ; , HCO;, co~- 등이 있다. 이들 탄산 이온 사이에 일어나는 주요 화학 반응은 다음과 같다. CO2 (ga s) ~ CO2 ( aq) C02(aq) + H20 ~ H2C03 CO2(ga s ) +H20 ~Ka,, H2C03 H2C03 ~K, HC0;1 + H+ H2C03 ~K HC0;1 + H+ 위의 각 반응식에서 평형상수는 각각 Kco2 = aH2COs = 10-1.4 7 I,L6 .,1,,I6 .` 2.63 Kl = = aHCa0t3t 2 C• 0 3a H + = l0-6.35 _`1 ,'__, .&=~a=HC108 0-10.33 ‘,`' ,I 이다. 위의 평형상수는 용액의 p H 에 따라 변화함을 알 수 있다. 용존 전 탄 소종의 농도를 10-2 (1 0-2=a tt 2co,+a tt coa+aco,_) 라 가정하면 (6.2) 식에서 25°C 에서 쁘aHCO=3 쁘K+I =10 + 6 . 4 . a~ (6. 4) 가된다. pH 6 . 4 에서 H2C03 의 활동도는 HCOa 의 활동도와 같게 되 어
aaHH2CC0083 =l 이 된다. 따라서 aH,COo + aHCOa = 10-2 aH2C03 = aHCOa = 10-2·3 이 된다. 상이한 p H 에서 얻어진 H2C03 의 활동도는 각각 다음과 같이 계산된 다. pH 5.4 일 때 att 2 co,=O.1X10-2=10-3 pH 4. 4일 때 att ,C 03 = 10-2·004 , aHCO: i = 10-4 pH 7.4 일 때 aH2C03=10-J att co 3 = 10-2·0 5 pH 8.4 일 때 aH2C03=10-4 aHC03 = 10-2·0 04 이 결과에서 탄산종의 활동도와 pH 관계가 그림 6-1 처럼 얻어진다. 자연계의 대부분의 물 속에 용존하는 탄소종은 co~ -농도에 비해 HCOi 농도가 높음을 알 수 있다• p H 가 9 이상인 염수에서만은 예의이다. 현 재의 대기 중의 Pco2 는 빗물과 대기 중의 CO2 가 평형상태에 있다는 가정 하에 빗물의 pH 측정 (a 는 10-5.65) 에서 Pco2= (mH+)3/Keo.Ki (mw+2K2) 식에서 계산할 수 있다. 위 식을 계산하면 대기 중의 Pco.=3.31 pp m 이 된다. 지금부터 탄산칼 슘의 용해도를 검토해 보자. 방해석이나 아라고나이트가 용해될 때
CaC03( 방해석) ;:== Ca2+ + co}+, K 방 해석 =Ca2 ++ co i CaC03( 아라고나이트) ;:== Ca2+ + Co}- 와 갑은 평형이 이루어진다.
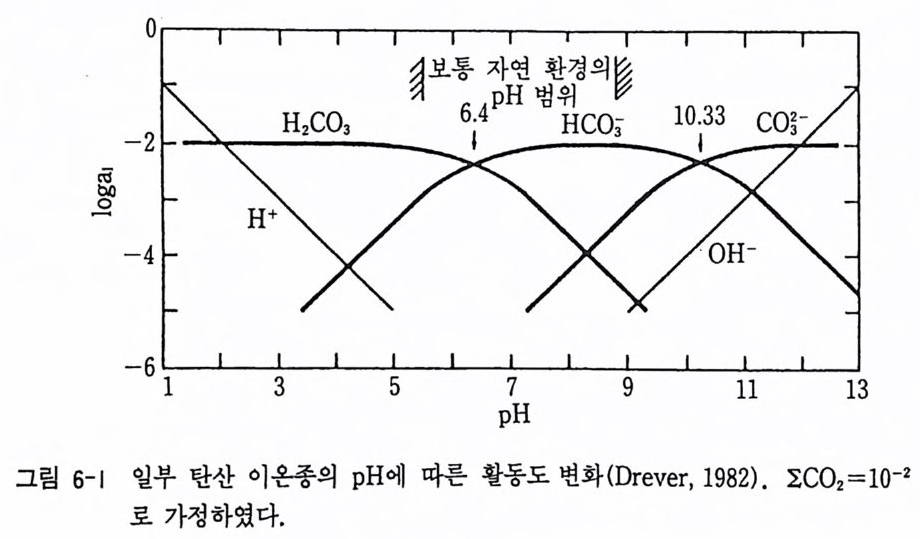 。 I 4 보통 자연 환경의『’
。 I 4 보통 자연 환경의『’
위의 탄산종의 관계식에서 蟲+广= K 방 해석 KIKc o 2 PC02 K2 이 얻어진다. 위의 식은 천연수의 특성을 이해하는 데 중요하다. 탄산의 농도와 pH 는 PC02 와 11ZHC 야 관계식으로 생각할 수 있다. 광합성 작용은 용존 CO2 를 감소시키므로 탄산염 광물의 포화도를 증 가시킬 것이다. 반면에 호흡 작용과 부식 작용은 용존 CO2 를 증가시켜 포화도를 감소시킬 것이다. 황산염 의 환원과 함께 형 기 성 분해 (anaerobic decay) 가 일어 날 때 , 즉 S0:;-2 +2Cors+2H20 ~ H2S+ZHCQ 3
로 탄산염 광물의 포화도를 증가시키게 될 것이다. 방해석과 평형에 있는 순수한 물 속의 Ca2 + 의 농도와 p H 가 Pco, 의 변 화에 따라 변화하는 경향을 알아보자. 앞의 (6.1) ~ (6.4) 식에서 acol-= K1K2Kco,Pco,/ai. 가 얻어진다. 여기서 aco 3- 를 방해석의 용해도의 곱의 표현과 합쳐서 소거하면 전하 균형 식 (charge balance) 에 서 mw + 2 mca2+ = mt tc o; + 2 mco, + mott - 가된다. 해수의 p H 는 7 과 9 사이이므로 mw, moH-, mco3- 의 값은 1ncaz+ 나 mHC05 보다 훨씬 작으므로 무시하고 2mca2+= mt tco ; 나
2 aca•• _ att co , rca2+ 1Pco3- 로 표현할 수 있다. 위의 식을 종합하면 p H 의 식으로 ai+ = Plo2 福 K갛 rca2+ 2K 방해석 r ic o3 가 얻어전다. 25·c, 1 기압에서 PC02 의 값은 rca2•=rHco; 로 가정해서 구한 값이고 rca” 와 rHco; 는 디바이-휘켈 식에서 계산된 것이다. 표면수에서는 대 체 로 Pco2 값이 10-2 와 10-3.5 사이 에 해 당되 어 이 같은 Pco2 를 가지 는 물 이 방해석과 평형상태에 있다면 p H 는 7.3 과 8.4 가 될 것이다. 표면수의p H 가 이 값의 범위를 가지므로 낮은 p H 값을 가지는 물 속에서는 방해 석이 불포화 상태에 있게 됨을 알 수 있다. Py tko wi cz (19 83) 의 해 수 합성 실 험 자료에 서 활동도계 수를 이 용하고 Yca2 ♦ =0.26 1, YHco,=0.532 라 가정하면 해수의 p H 는 8.39 가 된다. 만일 해수에서 방해석이 존재한다면 해수의 p H 는 \8?5 의 적정점 가까이에 있는 경우가 된다. 그리고 방해석의 용해도는 해양의 심도에 따라 변화한다. 이는 죽은 유기 물질의 계속적인 침전과도 밀접히 관련되어 있다. 즉 심도에 따른 알칼리도와 ~CO2 의 변화에서 mco1-/1nHco, 의 비가 심도가 깊어침에 따라 감소하는 결론이 얻어졌다. 실제는 해저 바닥 심층수에 용존 전 탄소의 농도가 IO % 높지 만 mco i - 는 2/3 정 도 낮다. 남대 서 양에서 mcoco3- 의 수 칙 단면도에서 보면 파도에 의해 혼합되는 표면수에서는 mco J-값이 급격 한 변화를 나타내며 500m 이하에서는 점진적으로 감소하고 있다(그림 6-2). 진하게 그린 방해석과 아라고나이트의 포화선의 오른쪽은 해수이며 이 들 탄산영 광물이 과포화되어 있고 그 왼쪽은 불포화상태에 있음을 의미 하고 있다. 따라서 3.3km 이하에서 아라고나이트는 해수에 용해되어 있지만 탄산염 입자들이 침강하면서 핵이 성장하게 된다. 4.3 km 이하 에서는 방해석 역시 불안정하여 이 이하에서는 탄산염 광물이 안정할 수 없다. 이 심도를 탄산염 보상 심도 (carbona t e comp en sati on dept h, CCD) 라 한다. CCD 는 탄산염 광물의 성 장과 용해 속도가 평 형 에 있는 반웅 속도론적 개념을 가진다. 2°C 에서 반응 속도는 대단히 느리므로 CCD 이하에서도 일부 탄산염 광물 입자들은 심해 퇴적물에 포함되어 있을 수 도 있다.
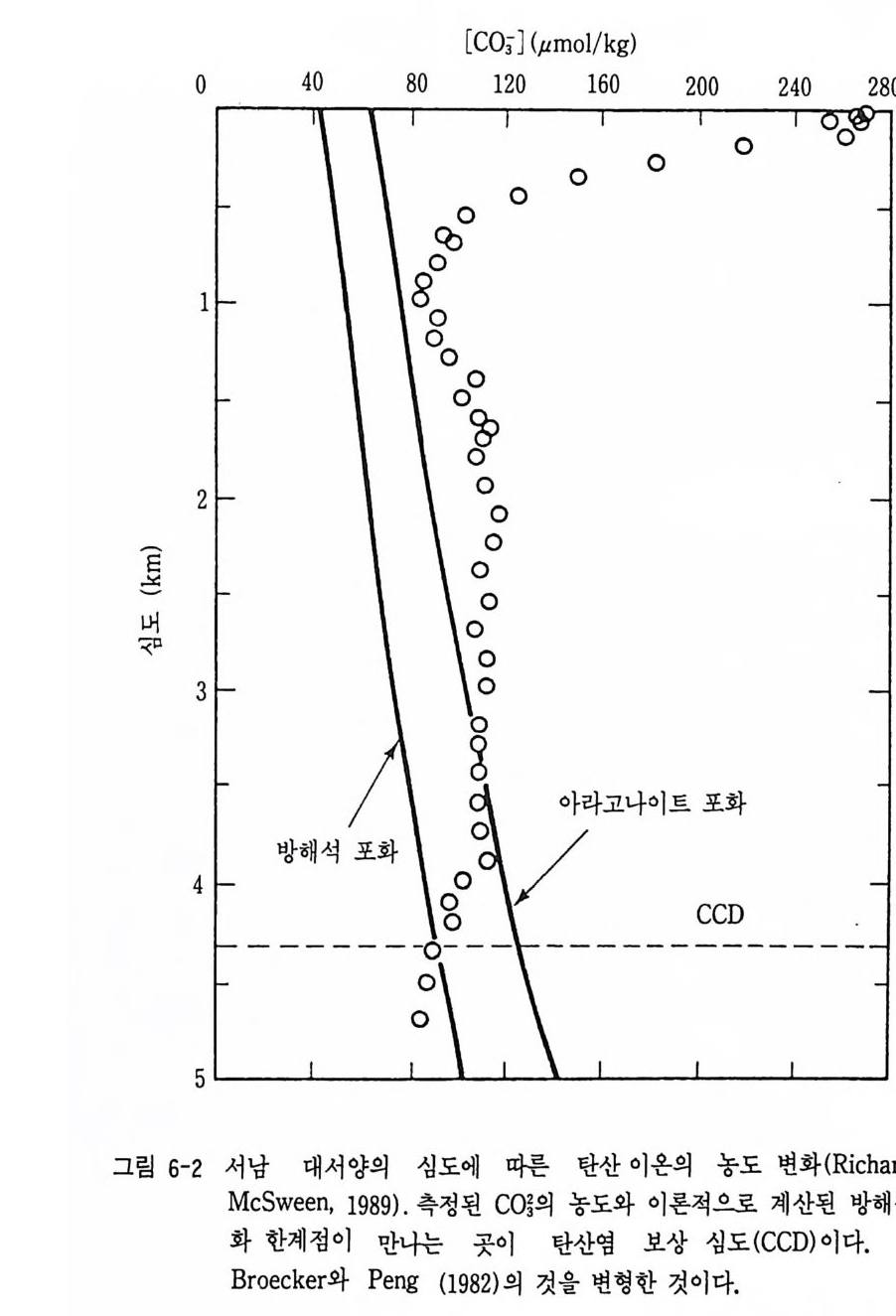 [ CO 깁 (µmol /kg )
[ CO 깁 (µmol /kg )
(2) 용액 일반적으로 균일한 액체상을 만드는 혼합물을 용액이라 한다. 임의의 액체에 고체, 액체 및 기체 물질이 용해되어 용액이 될 때 녹이는 액체 롤 용매라 하고 용해된 물질을 용질이라 한다 . 지구화학에서 대상이 되 는 물질의 대부분의 상(相)은 일정한 성분을 가지고 있지 않다. 즉 멜트 용액 , 전해질 용액, 가스 혼합 용액, 결정질 및 비정질 고용체 등 다양 한 용액들이 존재하고 있다. 석영을 제의한 대부분 조암광물은 고용체로 구성되어 있다. 이들 고용체의 용액의 성분은 이온의 전기적 성질 , 이온 의 크기, 결정구조 등의 구조 화학의 법칙에 따라 변화한다. 멜트 용액 x- 선 회절법과 분광 분석법의 개발로 규산영 멜트 구조나 특성이 점 차 알려지게 되었다. 규산염 광물은 Si0 4 사면체를 중심으로 양이온들이 여러 가지 형태로 결합되어 규산염 광물을 이루고 있다. 결합 구조의 강 도는 Si, Al 과 같은 결정 구조 형 성 원소와 M 굽\ Fe2+ , Ca2 +, Na+ , K+ 등과 같은 결정구조 변형원소들에 따라 달라진다. 실리카가 많은 규산염 멜트는 S i -0 의 공유결합을 중십으로 이루어져 많은 수의 산소가 Si0 4 사면체 단위에 연결되어 있기 때문에 이들 멜트는 점성은 높으나 전기 전도도는 낮다. 그러나 Na20 나 기타의 양이온이 여기에 추가되면 멜트 의 점성이 낮아지는 반면에 멜트의 전도도가 증가한다(그림 6-3 ) . 그래서 규산염의 중합(p ol ym er i za ti on) 정도를 낮추게 된다. 또 이로 인하여 규 산염 멜트의 점성이 낮아지게 된다. 물이 규산염 멜트의 구조 변형 요소로 작용하여 다음과 같이 결합 구 조 중의 산소와 반응하여 OH 형태의 구조로 바꾸어진다.
H20 +S IIi 一 OII ― SII i —2( —SIIi - O H) 그림 6-3 규산영 멜트의 구조 결정질 고용체 고성능 전자현미경에 의해 결정질 고용체 (crys t a l li ne soli d solu ti on) 의 결정구 조 가 규명되어 광물학에 크게 기여하고 있다. 조암광물들이 대다 수 고용체 를 이루고 있기 때문에 전자 현미 구조에서의 미세 결정구조를 알 수 있게 되었다. 규산염 광물에서 결합구조 형태는 이온의 전하와 이 온의 크기에 따라 크게 영향을 받는다. 사장석의 경우 알바이트 (NaAl2S i 3 야)와 아놀사이트 (CaAl2S i 2 야)의 두 단성분 사이에 Na+ Si 4 + ;:== Ca2+Al3+ 의 복치환이 일어난다. 가스 혼합 용액 저압에서 가스는 독립된 분자로서 혼합되어 있다. 대기 중의 가스나 높은 에너지 환경에 있는 화산 가스 등은 가스 혼합 용액으로 되어 있 다. 이들 가스들은 암석의 풍화 반응이나 마그마 방 내의 물리화학적 조 건 변화와 같이 지구화학적 작용을 하게 된다. 예를 들면 어느 지역의 화산 지역의 가스가 600' t/ °K 에 co, 02, co3 종이 공존, 평형상태에 있다고 가정하자. 또 가스의 전압력은 lbar 이고 Po 2 는 0 . 8bar 였다면 이 때의 CO 와 co 려 분압을 다음과 같이 계산할 수 있게 된다.
co+ 군1 )2 =K co2 K=exp ( 강?° )= PCP:沿 L1G0=-55.137 kcal mol - 1 이고 K=l . 22 X 1020 이 얻어진다. Pco2 + Pco + R。 , = lbar o] 므로 1. 22 X 1020Pco2 + Pco + R。 2 = lbar, Pco =l . 833 X1 0-21 bar, Pco2 ~ 0. 2 bar 가 얻어진다. 이와 같이 화산 지역에서의 마그마 방의 압력을 추정할 수 있어 화산 활동의 특성을 예측할 수 있게 된다. 전해질 용액 전해질 (elec tr ol yt e) 용액이란 용질이 용매 분자층으로 구성되어 있는 모유체 내에서 이온의 형태로 존재하는 용액을 말한다. 지구화학에서는 해수나 열수 용액과 같은 액체상 유체를 말한다 . 전해질 용액은 멜트나 고체 내에서 대규모로 주기적인 구조를 나타내지는 않는다. 이온과 용매 분자는 독립된 종의 기계적 혼합으로 다룰 수 없다. 용매와 용질 화학종 간의 전기적 상호 반응은 용액 내의 자유 용질 이온의 농도에 한하여 일 어날 수 있다. 예를 들면 해수 중의 황산나트륨의 용해도의 추정에 대하 여 알아보자. 결정 질 황산나트륨이 보통 Na2S04 • mH20 를 만드는 반웅 울무시하면 Na2SO. ― ➔ 2N!+So!-
와 같은 화학 반응이 일어난다. 이때 용해도곱 상수 (K이 는 Ksp = (aNa+ ) 2 aso i- / a Na,s o , 가 된다. 일반적으로 이온들이 전기적으로 상호 작용을 하기 때문에 희 석 용액이 아닌 경우에 이온종들은 이상용액으로 작용하지 않는다. 이온 전하 평형이 항상 계속적으로 유지되어야 하기 때문에 용액 내에 음이온 조절 없이 Na + 와 같은 양이온의 농도를 변화시킬 수가 없기 때문에 개 개의 용존 이온의 활동도를 측정할 방법이 없다. 그러므로 해수 증발 과 정 동안에 aN a· 증가에 기인한 퍼텐셜 자유에너지의 변화를 결정할 수 없고 ac, -, aso i- 등 의 음이온의 활동도의 증가량도 계산할 수 없다. 이를 해결하기 위하여 평균 염액법 (Mean salt m e th od) 과 디바이 휘켈법을 이 용하고 있다. 디바이 휘켈법 디바이-휘켈 (Deb y e-H ti cke l) 이론은 단일 이온의 활동도와 이온들의 자유에너지를 가지고 이온들 사이의 전기적 상호 작용의 효과를 계산하 는 모델이다. 전기적인 견인 및 반발력의 부합 효과를 계산하기 위하여 다음과 갇은 용액 화학에서 사용하는 활동도계수와 이온강도(i o ni c str en g th, I) 를 도입하였다. 즉 이 관계에서 log Y i= -AZNT 의 디바이 휘켈 방정식이 얻어진다. 여기서 %는 이온종 i의 활동도계수 이며 A 는 P, T에 따라 변화하는 상수이다. 그리고 Z i는 특정 이온의 전하이며 I 는 이온강도이다. 이온강도는 l=½2mi z :
로 표현된다. 용액 내의 이온들은 그들 주위의 전기장에 영향 을 받는다. 다가 이온 ( ! Zl > l) 은 1 가의 이온보다 주위에 더 큰 전기적인 힘이 작용한 다. NaCl 1 몰 용액의 이온강도는 1 이며 Na2S04 는 3, M g S04 는 4 이다. 디바이 휘켈 방정식에서는 전해질 용액의 이온강도뿐만 아니라 수화 이 온의 크기를 고려하여 인접 이온의 수를 추정하고 있다. 각 온도에서 디 바이 휘켈 방정식에 사용되는 각종 상수는 표 6-3 과 같 다. 크기 단위 로 A 울 사용한다. 그리고 온도와 압력만의 함수인 경험지수 A, B 값이 사용된다. 그리고 이온 i 의 활동도계수 (r , ) 는 log Y i= 1_+ABZa°N 汀T (6 . 5)
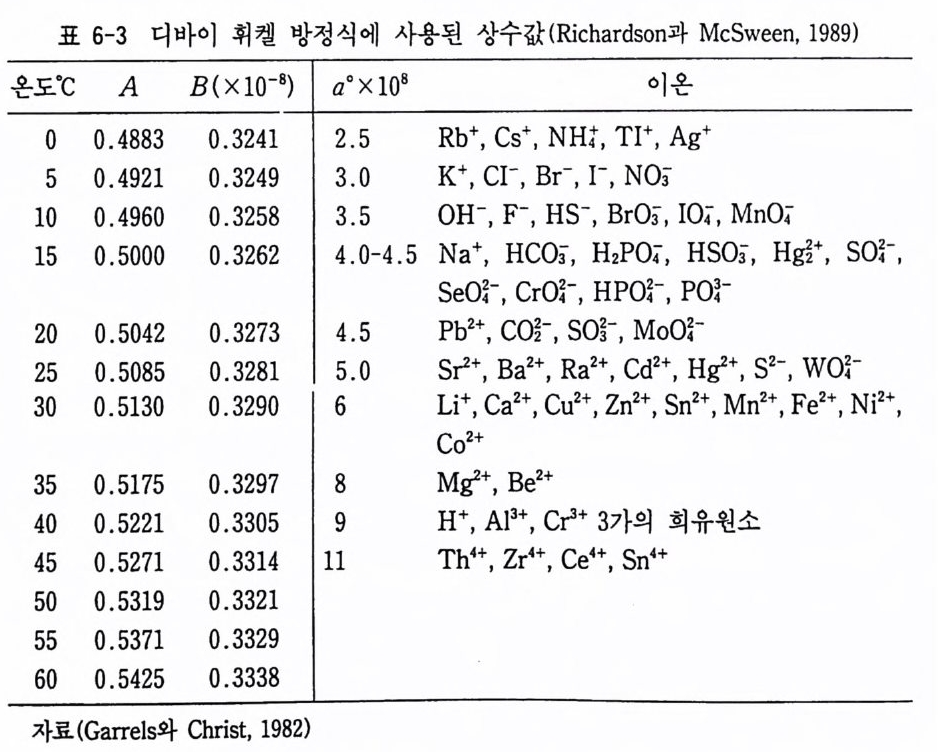 표 6-3 디 바이 휘 켈 방정 식 에 사용된 상수값 (Ri chardson 과 McSw ee n, 198 9)
표 6-3 디 바이 휘 켈 방정 식 에 사용된 상수값 (Ri chardson 과 McSw ee n, 198 9)
로 표현된다. 위 식을 이용하여 25·c 에 석고와 평형상태에 있는 Ca2 + 와 SO t의 활동도계수를 계산하면 다음과 같다. 반응식 CaS04 • 2H20 ;:== Ca2+ + So~-+ 2H2 0 와 열역학 자료를 이용하여 석고의 용해도곱 (Ks 값을 계산하면 10 - 4 . 61 이 된다. 여기서 mc a2, = mso i- = 00-4 · 51) 강 =4. 98 X 10-3 으로 가정하면 /=21( 4. 95 X 10-3 X 4 +4. 95 X 10-3 X 4) =1. 98 X 10-2 가 얻어진다. 표 6-3 의 값을 (6. 5) 식에 대입하면 log rc a•• = -0. 224 log rs oi- = —0 , 242 Ycn z+ =O. 597 rsoi- = O. 573 이 각각 얻어진다. 이 값을 이용하여 Ca2 + 와 SO t의 농도를 계산하고 더 정확한 이온 강 도의 값을 계산할 수 있다. 즉 m(cm ac 2a ♦ ,=. X m Oso. 5i-9 =7 )( ( 。 m .~so i- X O. 5)73) == 100 .- 844·67 1 X l0-2 이 되고 이온강도는 J= 3.39 X l0-2 rca2+ = 0 . 531 rsoi- = O . 499
가 얻어진다.
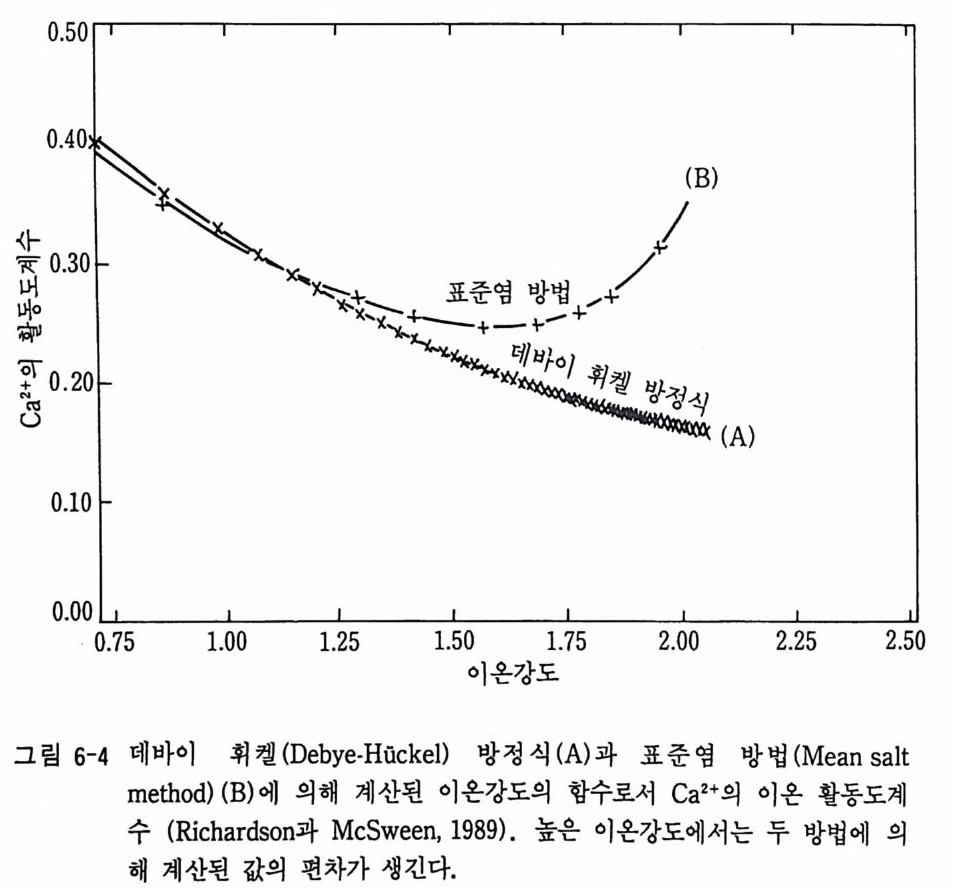 0.50
0.50
그리고 25·c, o.o5 몰의 CaCl2 수용액에서 Ca2+ 의 활동도계수를 계산 하면 I=0 . 15 에서 log rca•• = -0 . 447, rca•• = O. 357 이 얻어진다. Ca2+ 이온의 이온 강도와 활동도 계수 사이의 관계는 그립 6-4 와 갇다. Ca2+ 의 이온강도가 클수록 활동도 계수가 감소한다. 높은 이온강도에서는 평균 염액법이나 디바이 휘켈법 사이에 계산된 값의 편
차가 크게 나타난다. 6-2 산화 환원 평형 (I) Eh 의 정의 탄산염과 규산염 광물의 용해도는 산을 중심으로 한 반웅이었으나 산 화 환원 (redox, Eh) 반응은 산소의 전이를 포함한 반응이다. 예를 들면 자철석이 산화되어 적칠석이 되는 경우에서와 같다. 2Fe304 +z1- 02 : ;::::::= 3Fe203 2Fe2++i- 02+ 2H+ :;::::::= 2Fe3++H20 또는 다음과 갇아 전자의 전이로 생각할 수도 있다. 2Fea04+H20 ~ 3Fe20a+2H++2e- Fe2+ ~ Fe3+ +e- 이 반반응이 일어날 때 그림 6-5 에서처럼 용액에 백금선 전극을 담그 면 두 전극 岭와 Vi 사이에 전기적인 일 (W) 을 하게 된다. 즉 W=(½-V i)Q =EQ 여기서 Q는 전류 (elec tricity)이다. 전류 Q =NF 로 정의되므로 전기적 인 일은 W=NEF 가 된다. 여기서 N 은 전하의 수이며 F 는 패러데이 (Faraday) 상수아다. 25 ·c 에서는 F=23969 cal/vol t이다. 헬름홀츠 (He lmholtz) 자유에너지 변화(LJ A) 는
4A=-S4T— P4 V 로 정의된다. 산화 환원 반응에서는 체적 변화의 일과 전기적인 일을 동 시에 하게 된다. 따라서 L1A0 =NE2F-PL1 V 로 표현할 수 있다. 여기서 기전력 (E°) 은 표준수소의 반세포 (hal f cell) 를 기준으로 하여 Eh 로 표현하였다.
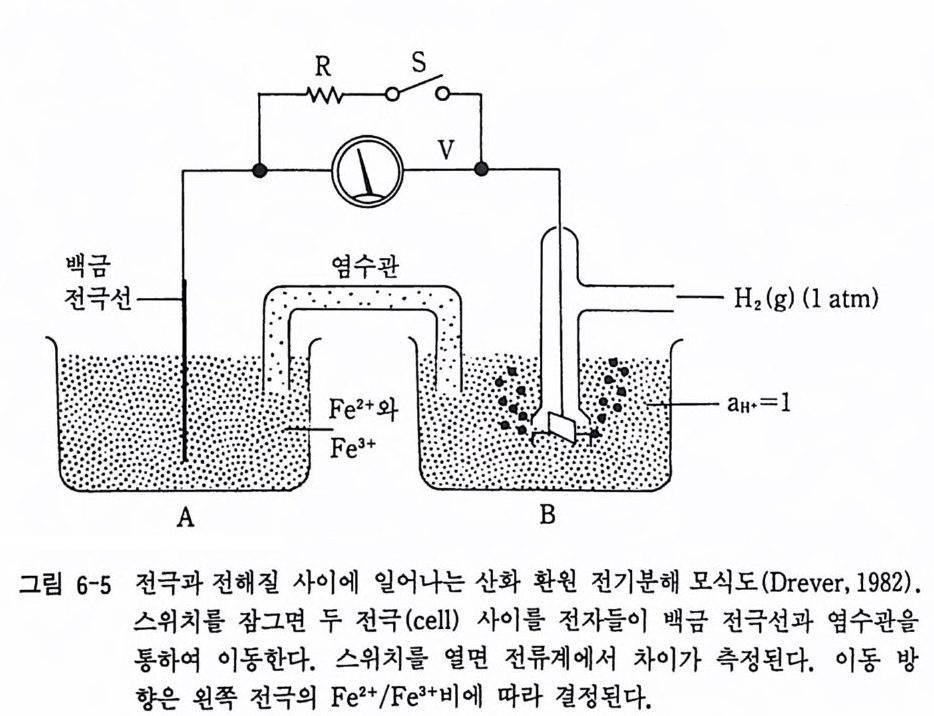 s
s
E 快는 수소의 반반응 (H2~2H++2e 기에서 0.00 볼트인 표준전위 (sta n dard p o t en ti al) 의 값이다. 기타 반반응에서의 기전력의 표준전위의 값은 표 6-3 (1)과 같다. L1NE2F = L1A0 + PL1 V = L1G0 이므로
NE2F= 一 RTlnK 이다. 그리고 NEhF=LIG 이므로 b.G r=b .G 0 +RTln (仁訖갑衍) 로 표현된다. PH,=aw=l 이므로
 표 6-3 (l} 25°C 에서의 표준환원전위 반반응에 대한 기전력 표준전위의 값
표 6-3 (l} 25°C 에서의 표준환원전위 반반응에 대한 기전력 표준전위의 값
L1Gr=L1G0+RT in ~ aFe3 令 가 된다. 따라서 NEhF=L1G0 + RTln 쁘aFe으3+ Eh=E0+N~FI n 쁘aFe” Eh=E0+ 특N lo g aaFFee23 ++ ((환산원呼종의의 활활동동도도)) 가된다. 일부 수질화학자들은 Eh 대신에 p e 를 사용하기도 한다. Pe= ― lo g[디 관계에 있다. Fe3+ + e- = Fe2+ 반응식에서 예를 들면 K= afa eF o+ ea Ee - ’ _l_= K aFe3• , ae- are•• Pe=Iog K +log aF~e2 + 로 표현된다. 일반적으로 산화종 +Ne-= 환원종, 죽 pe= iJ1 iogK +iJ1 log ((산환원화종종의의 활활동동도도))
로 표현할 수도 있다. p e 와 Eh 간에는 pe =~hh 관계에 있다. 다음에 Eh 의 지질학 적용의 예를 몇 가지 들어 보자. 첫째, 하천수에는 Cu+ 와 Cu2+ 가 용존되어 있다. 만일 하천에서 측정 한 Eh 값이 0.20 볼트였다고 가정하면 위의 Eh 식에서 cu+=cu2++e-, +0 . 20=-0.16+~lo g願 관계가 얻어진다. 經f= 106.l ::::: 1259000 로서 그 하천수에는 Cu2 + 가 우세하게 용존하고 있음을 알 수 있게 된다. 둘째, 소태지 퇴적물에서 측정된 Eh 값이 +0.36 볼트이고 p H 가 7 이었 다. 이 소태지 지역의 환경이 산화 환경 (aerob ic)인지 환원 환경 (anaerobic ) 인 지 판정 하여 보자. 2H20 :;=:::::! 02( 가스) +4H++4e-
+ 0 . 36 = + 1. 00 +뚜 lo g [H+]4 .Pc야 lo g P。 2 = -15, P。 , = 10-15 기 압 이 얻어진다. 헨리 법칙에서 02( 가스) ==02( 수용액) 사이에는K= 02 (수용액 ) 츠 10- 2 P야 이므로 P。 2=10-17 로 산소가 거의 존재하지 않는 협기성 (anaerobic ) 환경 임을 알 수 있게 된다. 셋째, 하천수에는 철과 망간이 용존하고 있다. 그러나 하천수가 바다 로 유입될 때 철은 해안 부근에 철산화물과 철수화물의 형태로 침전되 고, 망간은 가용성인 Mn2+ 형태로 심해까지 이동하여 망간단괴를 형성 하는 데 사용된다. 그 이유에 대하여 알아보자. Fe2+ ;:::::= Fe3+ + e- Q) (£0=+o.77 볼트) Mn2+ ;:::::= Mn02+4H+ + 2e- @ (£0= +1. 25 볼트) 위 의 두 식 에 서 전자를 소거 하면 통합반응식 (net reacti on ) Mn02+4H++2Fe2+~Mn2+ +2 H20+2Fe3+ @ 이 얻어진다. 엔탈피나 자유에너지에서와는 달리 ®식윤 2 배하여도 전 기력 볼트는 곱의 값이 아니다. 따라서 통합반응식의 E0=0.77-1. 2 3= -0.46 볼트가 된다. 이를 Eh 식에 대입하면 다음과 갇다. ® Eh=-0.46+~log aH.a~Fe2+ 해양의 만에 유입되는 하천수의 p H 가 6 이었고 농도가 lOµg /1 (1. 8 X 10-1mo l/ 1) 였다고 가정하고, 세계의 하천수 중의 평균 철과 망간의 비 는 대략 50 : 1 이라고 가정하자. 여기서 aFeh + aFeh = 9 X1 0-5 로 추정하였다. 그리고 하천수 중의 aFe•+/aFez+=l : 6 으로 aFe•+=l.3X 10-6, aFez+=7.7X10-6. 으로 가정하였다. 이 값들을 모두 위의 @의 Eh
식에 대입하면 Eh =0 . 46- 〉0 . 0 ―59 , l_o g__ 4 1. 8 X 1 0♦ (-9 7 (x1 .1 30- X6) 1 20- 6) 2 가된다. p H = 6 에서는 E 습 0 이다. 이 하천수가 바다 심부로 유입되어 보다 알 칼리 해수 속으로 유입되면 이 값은 점점 부의 값을 가지게 될 것이다. 즉 p H = 7 에서 Eh= - 0.121 볼트, p H=8 에서 Eh= - 0.239 볼트가 된 다. 4G 에서와 같이 부의 Eh 값은 앞의 ®반응식의 반응을 오른쪽으로 진행시켜 Fe2+ 대신에 Fe3 + 를 형성하여 퇴적물에 침전시키고, 생성된 Mn2+ 이온은 그대로 남아 먼 바다로 흘러들어가게 된다. (2) Eh-pH 다이어그램 Eh 식을 이용하여 이론적으로 물 (H20) 의 Eh 의 상한과 하한을 계산할 수 있고 광물의 안정 영역을 계산할 수 있다. 물의 Eh 상한 경계는 2H20 ~ 02 +4 H+ + 4e-, £0=+1 .23 V Eh= l. 23+ 汀덴 lo g [H+]4Pc。 2 , P。 2= 0.2 Eh=l .22 — 0.0 5 9 pH 가 된다. 그리고 물의 Eh 하한 경계는 H2 ~ 2H++2e-, £0=0.00 V Eh=0. 00+ 무 lo g桐, PH2=l = -0 . 059 pH 一 _0.205I9 o g PH 2
Eh= -0 .059 pH 가된다. Fe2+ 와 Fe3+ 의 경 계 는 Fe2+=Fe3++e-, E0= +O.77 V Eh=O.77+0.059lo g[F存e 가四 回[Fe 가 =l Eh=O.77 V 이다. 자철석과 적칠석의 경계는 Fe3Q 4 + z1- 02; :::::::::= 3Fe203 Fe3Q 4 +H20 ;:::::::::= 3Fe203+2H++2e- Eh=0.22+ 묘2괜 lwo gi::, aFe3~0,aH20 =0.22-0.059p H 가 되고, 적칠석과 Fe2+ 의 경계는 Fe2++3H20 ;:=:= Fe203+6H++2e- Eh=0 . 73+ 끄2괜 lo gaF*e = O. 73-0 . 059log aF e2+ - 0 .177 pH 가된다. 그림 6-6 에서는 aFe2+=10 군으로 가정하여 Fe2+ 와 적칠석의 경계선을 가정하여 그렸다. 적칠석과 Fe3+ 의 반웅 경계선은
Fe20 a + 6H + ;=:::! 2Fe3+ + 3H20 log K =2 .; 겁 ?°T =log aa옵 H e:++ = —1. 4 5 pH = 一 0 . 018 —31l og aF e3+ aFe 3.= ― 10-6 으로 가하면 p H= l. 82 가 된다. 이상의 계산에서 얻어진 반응 경계선의 결과로 작성된 Eh-pH 다이어 그램은 그립 6 - 6 과 같다. 이 그림에서 각 광물의 안정도를 쉽게 이해할 수 있다. 우라늄 광물 및 함우라늄 산화물의 Eh-pH 안정도 그림은 6-7 과 갇 다. 우라늄 광물 자원은 주로 우라니나이트 (uran i n it e, U0 2 ) 로 채광되고 있다. 우라늄은 U 와 u6+ 상태가 가장 중요하다. U” 는 U02F+ 형태나 환원 환경 에 서 는 U” 이 온으로 존재 한다. u6+ 는 U02 (COaH-, U02cog 형 태 로 CO:-, HC03, SOt , POt 등에 서 처 럼 강한 복합 화합물을 형 성 하고 있다. pH 변화에 따라 다양한 형태의 우라늄 복합 화합물이 존재 하고 있다(그립 6-8). 사암형 우라늄 광상에서 우라늄의 1 차 기원은 화강암질 암석 (2~15 ppm U) 이다. Eh=0.4V 이상인 지표수(p H 5~6.5) 에 의해 화강암이 풍 화되 면 우라늄은 그립 6-7 에 서 와 같이 쉽 게 uo2cog나 U02 (COaH- 형 태로 물속에 안정하게 존재하게 된다. 또한 알루미늄 규산염 광물이 풍 화가 계 속되 면 p H 가 증가하므로 U02 (COa) ~- 형 태로도 많이 존재 하게 될 것이다. 함우라늄 복합 이온둘은 철, 탄소, 황 등의 산화 작용과 함 께 다음과 같이 우라니나이트 형태로 침전된다. 4[U02(C02H-J+ H s-+15H+ ;=:::! 4U02+So~-+12C02+8H20 [U02 (COa) 디 + 2Fe2+ + 3H20 ;=:::! U02 + 2Fe (OH ) a+ 3C02 위의 반응에서 황 환원 박테리아 작용과 Fe2+ 의 산화 작용 과정에서
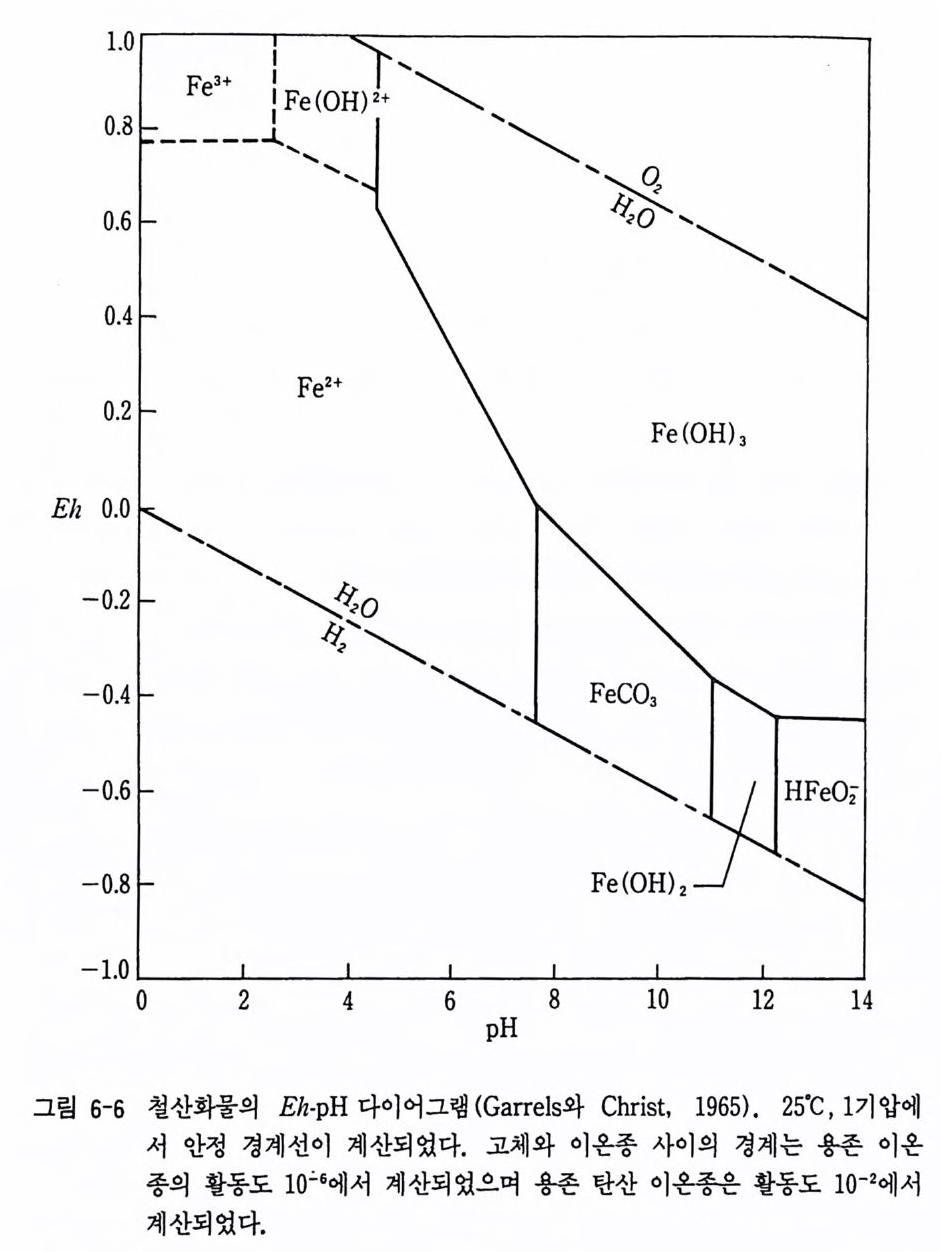 LO,
LO,
우라니나이트가 침전된다. 이 과정의 역으로 사암형 우라늄 광상에 높은 불소 함유 산성 용액을 시추공에 넣어 U02~, U02F+ 형태나 uo t의 복 합체로 만들어 추출하므로 우라늄 광석을 굴착채광하지 않고 쉽게 액상 형태로 된 우라늄을 추출하는 채광법이 이용되기도 한다.
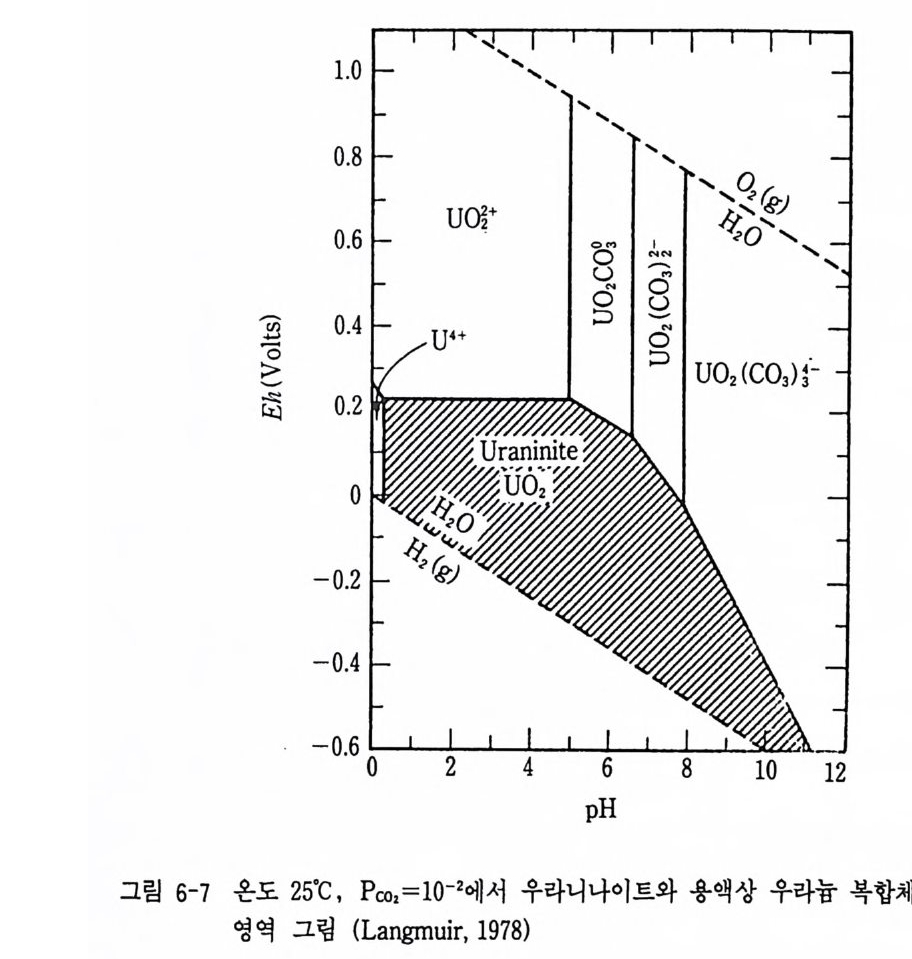 001...068 U 여` +` `` `` ``O `M`O U`z'`(ogEn O :`))z%`o
001...068 U 여` +` `` `` ``O `M`O U`z'`(ogEn O :`))z%`o
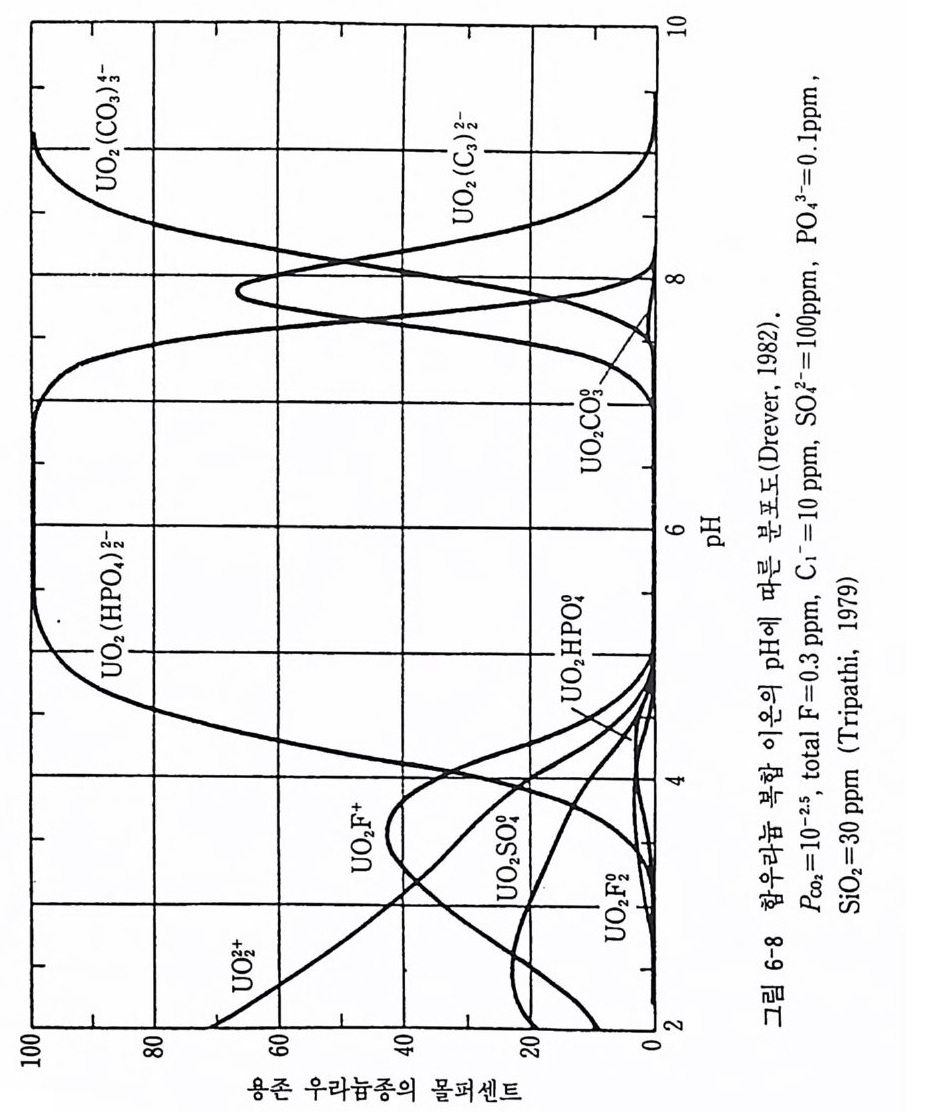 cF 녁>
cF 녁>
(3) 황화 광물의 Pe-pH 다이 어 그램 황화 광물에서 H2s- s o~-, Hs--so~-, H2S-Hs-, so~- -s0, s0 一 H2S, Fe2+ -FeS2, Fe203-FeS2 등의 안정 영 역 의 반응 경 계 선은 그 림 6-9 와 같다.
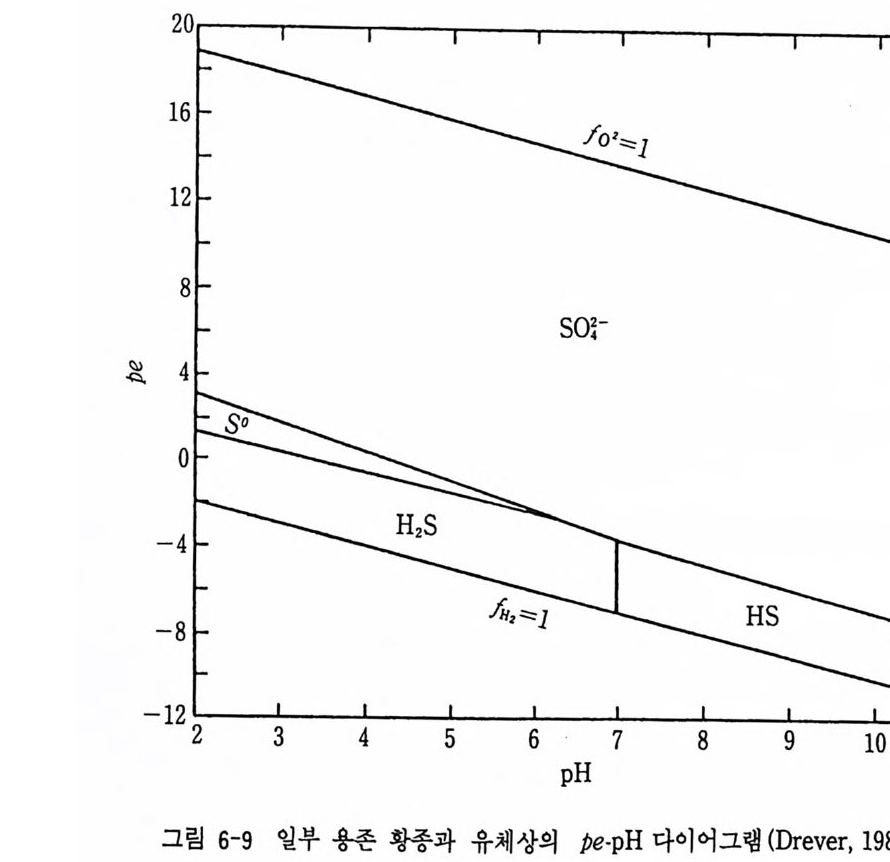 16
16
각 황화 광물 및 황종 사이에 안정 영역의 반응 경계선은 다음과 갇이 계산된다. srn- - H 2 s 의 경 우
sm-+se-+ IOH+ ;:== H2S+4H20 lo g K=lo g(a뿌so니i- ,1 쁘asoi드- 1 Pe=S.13-fp H H2S-HS- 의 경우 log K =log (~)-pH , pH =7.0 0 SO i ~HS- 의 경우 Soi- + 9H++se-~ HS-+4H20 log K=l og (~) +9p H p e=4.25 ―정9 p H SO t-안의 경우 sm-+sH++6e-~ S( 고체) +4H20 log K =8p H +6pe - aso1-, aso1- =1 0-2 pe= 5.71-43 p H H2S-S0 의 경우 S( 고체) +2H++ze-=H2S log K =log a H2s+2p H +Zp e, aHs=l0-2 pe= 3.40— pH 이와 같이 Eh-pH 다이어그램이나 pe- pH 다이어그램은 광물의 침전 자연 환경과 용액과 광물의 화학적 특성 해석에 대단히 유용하게 이용된
다. 자연 환경에서는 여러 요인에 의해 Eh 나 p H 가 변화된다. Eh- p H 에 영향을 주는 요소는 첫째, 광합성 작용, 호흡 작용, 부패 등과 같은 유기적 과정, 둘째, 철, 황, 탄소를 포함한 산화-환원 반응, 셋째, 물속에 용존하고 있는 C 아와 CaC03 의 평형 등이 있다. 6-3 화학적 풍화 과정 지표에서 물은 암석과 화학적으로 상호 반응하여 토양을 형성하게 된 다. 이 같은 과정 을 화학적 풍화 (chem i cal weath e rin g ) 라 한다. 지표에서 일어나는 화학적 풍화 과정은 우리의 생활과도 밀접하게 관련되어 있다. A즉의h 0오지3염 표一,수 (나N풍a 화2지0 ,하잔 K수류2의0 )광 —물진화의H,2 0 형 생계성물에 권과서에정 일대등어한은나 는저영 향온반,에 웅서지 과의표정 의S의 i 0안 2산 정—물 성들,M이 g 다 O토 .—양 화학적 풍화 과정은 점토에서 발생해서 점토로 소멸되는 인류의 생활 사 이클의 모체가 되며 점토 광물과 환경은 경제적인 면에서도 대단히 중요 하다. 화학적 풍화에 영향을 주는 요소는 모암의 종류, 기후, 온도, CO2, 유기 산 등이 있다. 예를 들면 정장석 (K 서 S i 3 아)이 물과 반응하여 ' 수화 작용을 일으켜 고령토로 된다. 2KA1Sb0a+2H++9H20 :;=:=! AbShOs(OH) ◄ +4H ◄ S i 0.+2K+ (정장석) (고령토) 이때 K+ 이온은 이동성이 큰 양이온으로 정장석 내에서 모두 빠져나 간다. 그러나 전조 기후 지역에서는 K+ 이 잔류되어 일라이트(i ll it e, KAl3 Sb01o(OH)2) 를 형성하게 된다. 양이온의 이동 속도는 (Ca2+, M,j -+, Na+) >K+>Fe2+>S i + ◄ >T i + ◄ >Fe+3>A1+3 순이다. 그러므로 풍화 토양에는 이동성이 낮은 Fe3+, Al3+ 등이 다량 포함되어 있다. 다음에 암석의 주
된 구성 광물의 하나인 석영 (S i 02) 과 김사이트-물 사이의 용해도 평형과 알루미늄 • 마그네슘 규산염 용해도 평형에 대하여 알아보자. (1) 규산염의 용해도 평형 석영과 물 사이에 pH 9 이하에서 다음과 같은 반응이 일어난다. Si0 2 + 2H20 ~ H4Si0 4 이 반응은 용해 된 화학종만을 만드는 반응이므로 조화 반응 (cong rue nt reac ti on) 이라 한다. 2s·c 에서 석영의 평형상수는 K=aH.s iO .(aH,o=1 로 가정 )=lxl0-4 이며 비정질 실리카의 평형상수는 K=2X10-3 이다. H4S i 04 는 약산이므로 pH 9 이상에서는 다음과 같이 용해가 일어난 다. H ◄ S i O ◄ ~K, HaS i O ◄ + H+ 25·c 에서 K1=a~H,=s101, 2.6Xl0-9 이 되고 H3S i 04 는 다시 H3SiO . ~K2 H3Sim -+H+ 이 된다. 용해된 실리카의 전농도는 m1 :s1 02 = mH2SI04 + mHsSIOJ -+ mH2SIOi 이다.
위 식에서 활동도계수를 소거하면 mi: s1 0, = mH,s10,( 1 +~+¥) 가된다.
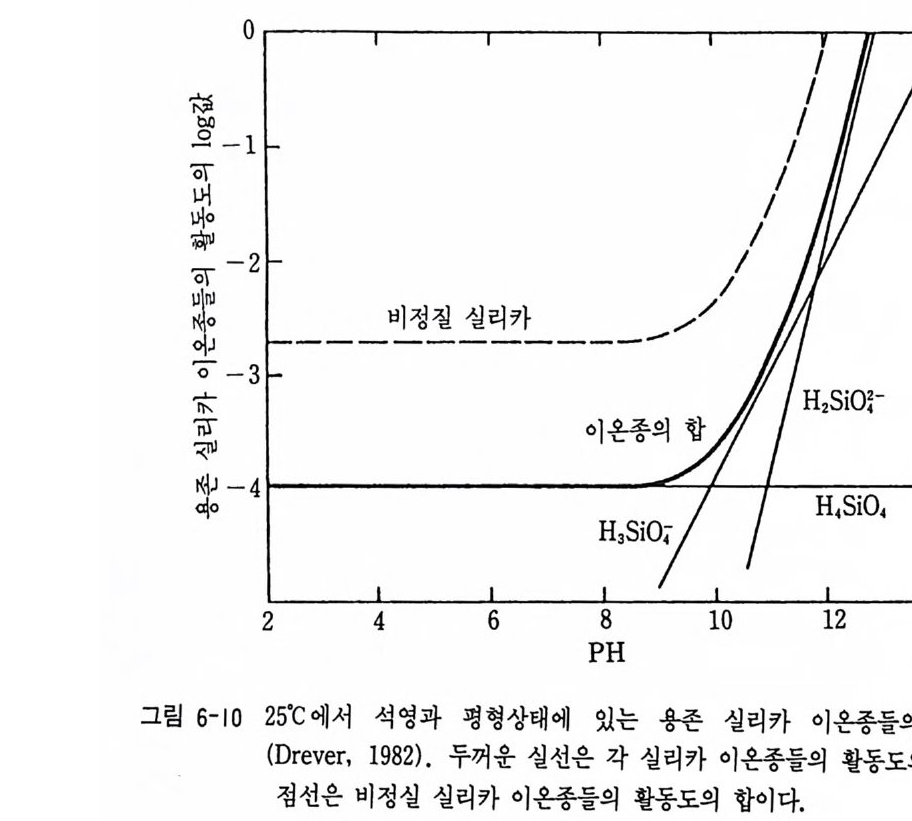 k탕버 。1 234 /' I
k탕버 。1 234 /' I
탄산염 계에서도 이와 유사하게 mi: co , =m H, co ,+(1+~+¥) 가 얻어진다. 이 관계를 그립으로 나타내면 그림 6-10 과 같다. 용해된 실리카의 전농도는 알칼리수에서는 대단히 높지만 물속에서의 H4S i 04 의
활동도가 크다는 의미는 아니다. 즉 pH 9 이 하에 서는 H4S i 04 만이 m~s10 , 에 영 향을 주지 만 pH 9 . 9 에 서 는 111H2SI04 = 11lH3SIO i가 되 어 관계 식 이 교차하고 있다. 그리고 pH 11.7 에서는 HaS i 04=mH,s10 J - 가 된다. 이와 같이 실리카-물 계에서는 천연수의 p H 가 버퍼 역할을 하고 있다. (2) 김사이트의 용해도 평형 함수산화 광물인 깁사이트(gi bbs it e, A l(QH) 3) 가 용해되면 Al3 + 가 물과 반응하여 Al3+, Al (O HH, Al (OH )i 등의 형태를 만든다. 알루미늄 규 산염 광물에서와 같이 깁사이트의 용해도는 p H에 의해서만 변화되지 않 고 공존하고 있는 복합 알루미늄 이온종 사이의 평형에 크게 영향을 받 는다. p H 의 변화에 따른 용존 Al 이온종의 활동도를 알아보자. pH 5 이하에서는 Al3+ 가 우세한 종으로 다음과 갇은 용해 반응이 일 어난다. Al( O H)3+3H+ ~K, Al3++3H20 K1= 도ai누+ (6 . 6) pH 5 내의에서는 Al(OH) ;가 우세하다. Al(OH)3+H+ ;::K= 2= Al (O H)2+H20 K2= 年Q出만 (6 . 7) a 記 그리고 pH 7 이상에서는 A l( OH) i가 안정하기 때문에 Al( O Hh+H20 ;=K5= Al( OH )i + H+
2
와 같은 평형 반응이 일어난다. K3= aA1 c oHl,a w (6. 8) 따라서 깁사이트와 평형에 있는 물속에 용해된 알루미늄 이온종의 전 농도는 m:i :A I = aA J3+ + aA l(O H) 2 + aA l(O H) i 이다위.의 (6. 6) —(6.8 ) 식울 여기서 대입하면 ~AI=K晶 +K2aw+aw~ 가된다.
 표 6-4 알루미늄 이온종의 열역학적 자료
표 6-4 알루미늄 이온종의 열역학적 자료
알루미늄 이온종의 열역학 자료 표 6-4 를 이용하여 각 반응식의 평형 상수를 계산하면 K1 =1. 27 X 108 = 욕aw 누 K2=4. 28 x 1 0- 3 =aw~ K3=2. 34 x 10- 16 =aA1<0H>,aw
가 얻어진다. pH 6 에서 ~Al=l. 27 X1 0- 10 +4 . 28 X1 0-9+2 . 34 X1 0-10= 4 . 64 X1 0- 10, pH 4 에서 ~Al=l.27X 1 0-4 가 계산되어 al1/ aA 1 ( 0 H) 2 = 297 X1 0- 4 이 얻어전다. 이를 p H-lo g a 용 해된 알우 미 늄 화학종 그림으로 나타내면 그림 6-11 과 같다. 그림 6-11 에서 보면 ~CO2 나 ~S i O 제서와는 달리 높은 산성수와 높 은 알칼리수에 깁사이트의 용해도가 크고 보통의 하천수나 지하수의 pH 범위인 5~8 에서는 용해도가 낮음을 알 수 있다. (3) 마그네슘 규산염의 용해도 평형 사문석, 세피오라이트, 활석, 부루사이트 등의 마그네슘 규산염 점토 광물이 저온에서 용해평형이 일어날 수 있다. 사문석은 감람석이 열수변질받아 형성되며 다시 다음과 갇이 용해된 다. M g 3S i 2 야 (O H) 4+6H + ;::::::= 3M g2 ++2H ◄ S i 0 ◄ +H20 (사문석) K 따 = aM3 g 2♦ .6aH22 SIO4 aH+ log aH.s1 0. 건 lo g K A 陸석 군 lo g(훈) 세피오라이트의 경우에는 다음과 같다.
Mg 4S is 0 1 s (O H )2 • 6H20+ 8 H+ + H20 ;== 4M g 2+ + 6H4 Si0 4 (세피오라이트) K 세피 오 라이트 = aM4 g 2 * a• 8w a H64 SIO , lo g a H,s 10,=½lo g K 세피 오 라이트 _f 1o g ( 7♦ ) 활 석의 경우에는 다음과 같다. Mg 3S i4 0 1 o ( OH ) 2+ 6H+ + 4H2 0 ~ 3M 균 + 4H4 Si 0 4 (활석 ) K 황석 = a3M g2 + • aH4 & l0 4 a~ 솔
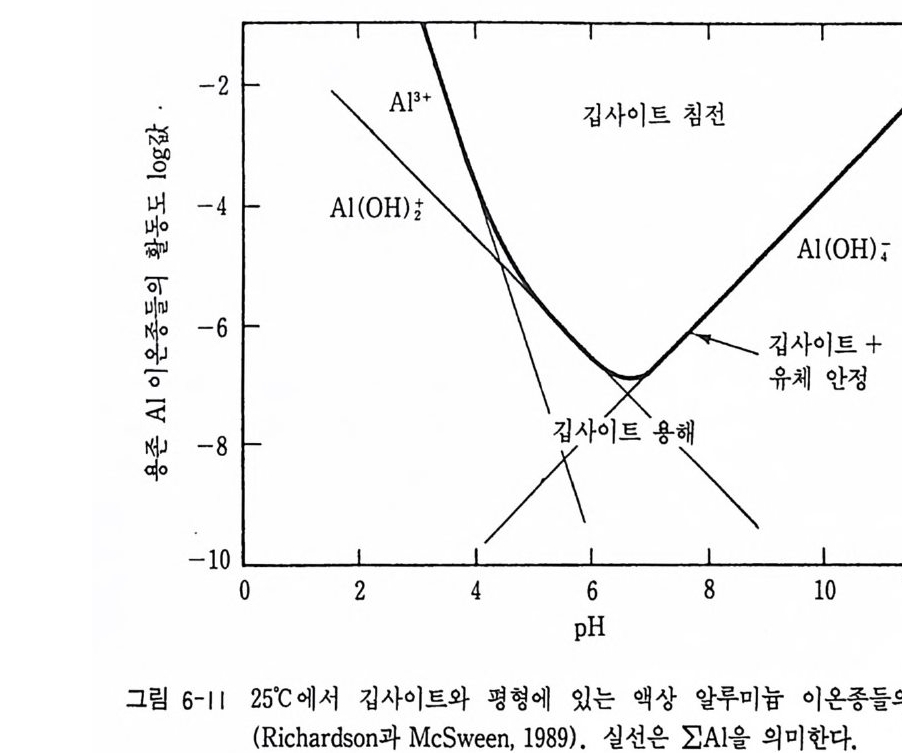 ? -2 I \ AIJ T \ 깁사이트 침 전
? -2 I \ AIJ T \ 깁사이트 침 전
log a H,s10 , =¾lo g K 황 석 -¾lo g(던) 부루사이트의 경우에는 다음과 갇다. (부루사이 트M) g =(O =Hh M , t++ 2o w. K 터-사이 트 =ll M g h ll b H - Mg 2( 0 H )2 +2W =M, j++2 H 20 , K 뮤사 이 트 =°a門w 이들 관계식을 lo g(면『)와 lo g aH,s 1 0 , 에 대하여 그립으로 나타내면 그 림 6-12 와 갇다. 그림 6-10 에서 이미 H4S i 04 가 용해되었기 때문에 pH 9 이상에서는 석 영의 용해도는 lo g H4S i 04 와 무관하다. 마그네슘 규산염 용해도 평 형 은 칙선으로 표시되어 y축 절편의 값은 K 의 값과 같다. 기울기는 용해 도 반웅의 규산염 광물 중의 M g /S i비 의 화학량론 (sto i c h io m etr y) 에 따라 변화된다. 용해된 화학종은 반응 경계선의 왼쪽에서는 안정하다. 그러므로 반응 경계선의 오른쪽 상부 영역에는 유체 내에 규산염 광물이 과포화되어 있 고 왼쪽 아래 영역은 이들이 불포화되어 있음을 말한다. 부루사이트-사 문석-활석 - 석영을 잇는 반응 경계선은 유체와 광물 사이에 log a H,s10 , -Io g (aMB 나命)값에 대한 안정 영역 경계선을 의미한다. 세피오라이트 는 25°C 물과 접촉부에서는 불안정(준안정) 상태에 있다.
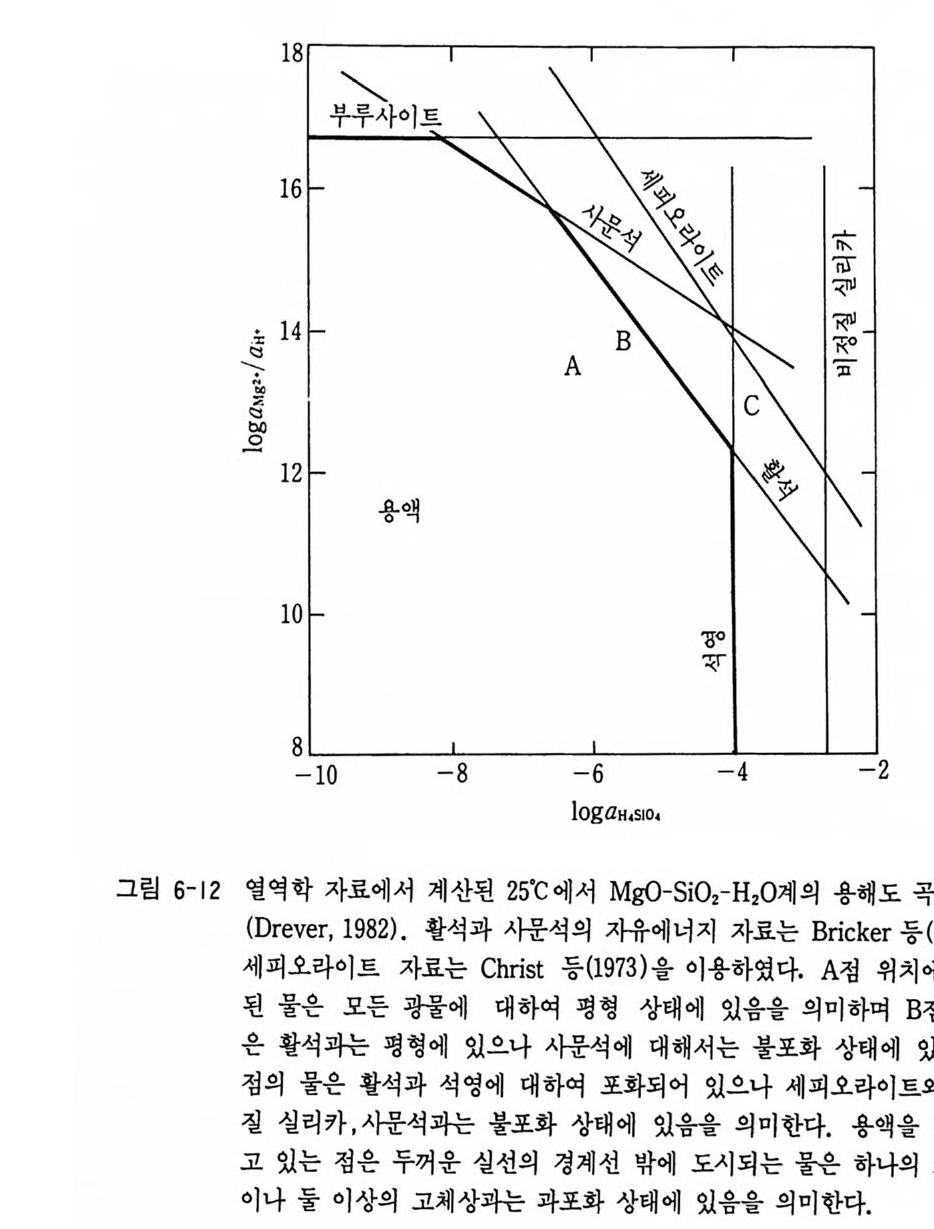 18
18
(4) 알루미늄 규산염 광물의 용해도 평형 점토 광물 중 1 : 1 층형인 고령토와 2 : 1 층형의 운모류는 풍화에 의해 형성된 대표적인 점토 광물들이다. 알루미늄 규산염 점토 광물에서 용해 된 알루미늄의 농도는 대단히 낮기 때문에 알루미늄 이온종이 고체상과 평형에 있게 되어 단일한 광물의 침전과 용해만을 고려하는 것이 아니라 그 광물상 이 의 의 반응을 고려 하여 야 하는 비조화 용액 (inc ong rue nt soluti on ) 을 생 각하지 않을 수 없다. 예를 들면 다음과 같다. 5AbSi4 0 10(0H )2 +2.5H20 ~ Al(OH) J +H4Si0 4 (고령토) (깁사아트) K 고령토 -김사 이 트 = aH,s10 ,= 10-4· 2 (25 ·c ) 0 . 5A'2 S i4 0 1o (OH ) 2+ 2 . 5H20 ;::::::::= A'2 S i2 0 s (OH ) 4+ H4Si0 4 (고령토) (영납석) K 고령토무 팔라이트= aH,5 1 0, = 10-3-2 (25 ·c ) 2KAISia O s + 2H+ + 9H20 :;::::= AhSbOs (O H) 4+ 2K+ + 4H4Si0 4 (정장석) (고령토) K 정장석 -고령토 = a t s,o, • 坐aw KAlS i 3 아 + H+ + 2H20 ~ 0 . 5AbS i ◄ 010 (OH ) 2+ K+ + H ◄ S i O ◄ (정장석) (영납석) K 정장석-영납석 =aH.s10. 겔a꼬H+ KAlS i 308+2H 나 12H20 :;:=:= KAbSb01o(OH )2 +2H++6H4Si0 4 (정장석) (백운모) K 정장석 -백 운모= at s10 , 겔a몬i2i •
2
KAISb01o (OH ) 2+ ZH+ + 3H20 ;::==: 3AlzSi2 0 s (OH ) 4+ 2K+ (백운모) (고령토) K 백운 오 -고 령토 =aa국Hw2+ KAISh010+H+ + 9H20 :;::::::=: 3Al(OH )3 +K+ + 3H4Si0 4 (백운모) (김사이트) K 백운모김 사이 트 =a~,s10 , • ~aw 열 역 학적 자료를 이 용하여 위 의 각 반응식 의 K 를 계 산하여 log aH , s10 , =at s10 , • ~aw 다이어그램을 그리면 그림 6-13 과 같이 된다. 그림 6-13 에서 고령토는 기타 광물에 의해 둘러싸여 있어 어느 광물보 다도 안정하다. 이 그림은 화학적 풍화 과정의 해석에 적용할 때는 지하 수나 하천수가 풍화된 암석과 화학적으로 평형에 있다는 가정 아래서 이 루어져야 한다. 그러나 여기에 CaO 나 Na20 성분을 고려에 넣으면 그래 프로 표현이 더욱 복잡해진다. ai-a •I aw 성분 변화를 더 추가하여 25·c 에서 Na - 알루미늄 규산염 광물과 K- 알루미늄 규산염 광물 사이의 안정 도 그림을 입체적으로 그리면 그림 6-14 와 갇다. 그러나 안정도 그림 해 석은 언제나 주어진 조건에서 이루어져야 한다. 특히 총상 규산염 광물 은 양이온과 음이온 치환이 빈번히 일어나고 대부분의 점토 광물은 혼합 충 광물의 구조를 이루고 있기 때문에 열역학적 자료로 작성한 알루미늄 규산염 계의 안정도 그립의 해석에는 주의를 요한다. 그러나 Nor t on (1 974) 은 푸에르토리코의 Rio Tanama 의 하천수의 pH , 용존 실리 카, 양이온을 분석 하여 그림 6-15 와 같은 축을 잡고 나타낸 결 과 고령토와 Ca- 몬모릴로나이트의 안정도 영역에 도시되어 이론적인 안 정도 영역과 일치하고 있음을 확인하였다. 이와 갇이 2 : 1 형 점토 광물 은 교환 가능한 이온이나 분자를 가지고 있기 때문에 기타 점토 광물보
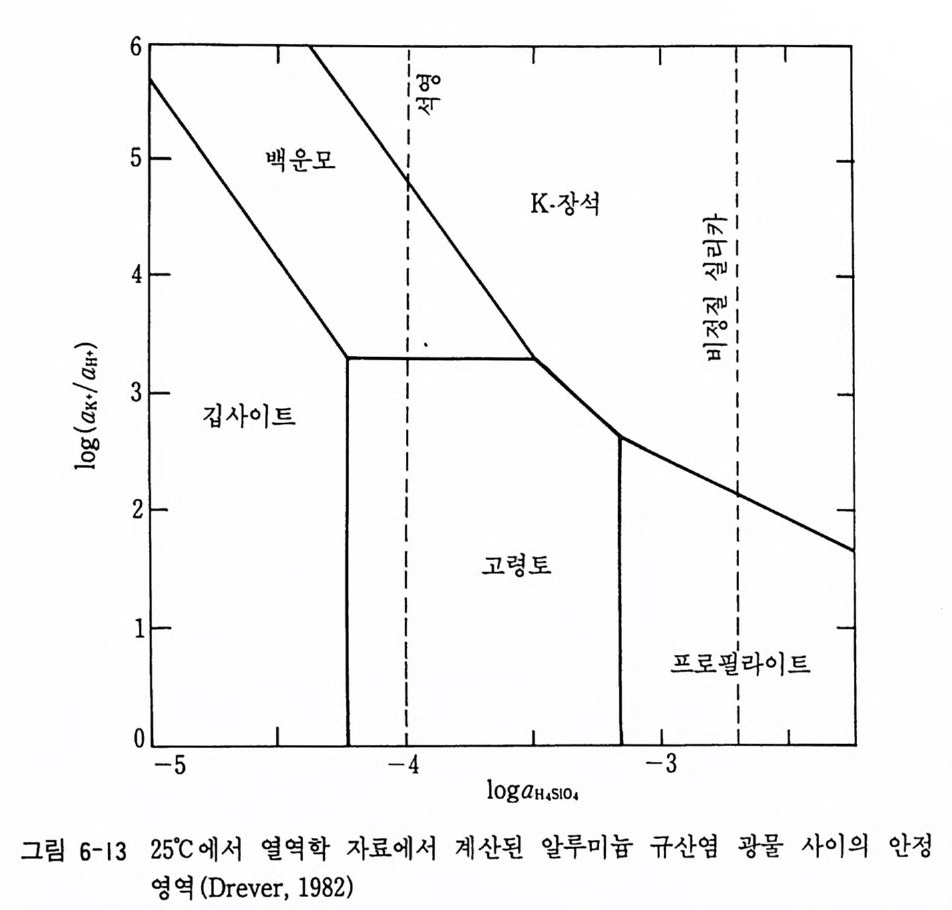 6
6
다 지화학적 환경 변화에 민감하다. 이들 점토 광물들이 평형을 이룰 때 주위 환경에서 이온을 흡수하여 이온 교환을 일으키게 된다. 이온 교환 이 비교적 빨리 일어날지라도 팔면체 시트와 사면체 시트의 화학 성분을 일으키는 반응은 대단히 느리게 일어난다. 그래서 자연계의 점토 광물은 주어진 환경에서 상호간에 평형에 있지 못한 혼합 점토 광물을 형성하게 된다. 이 때문에 주어진 환경에서 안정한 점토 광물을 확인하고 점토 광 물 사이에서 일어나는 반응의 방향을 알기 위하여 위와 같은 활동도 다 이어그램을 이용하게 된다. 활동도를 이용한 안정도 다이어그램은 화학
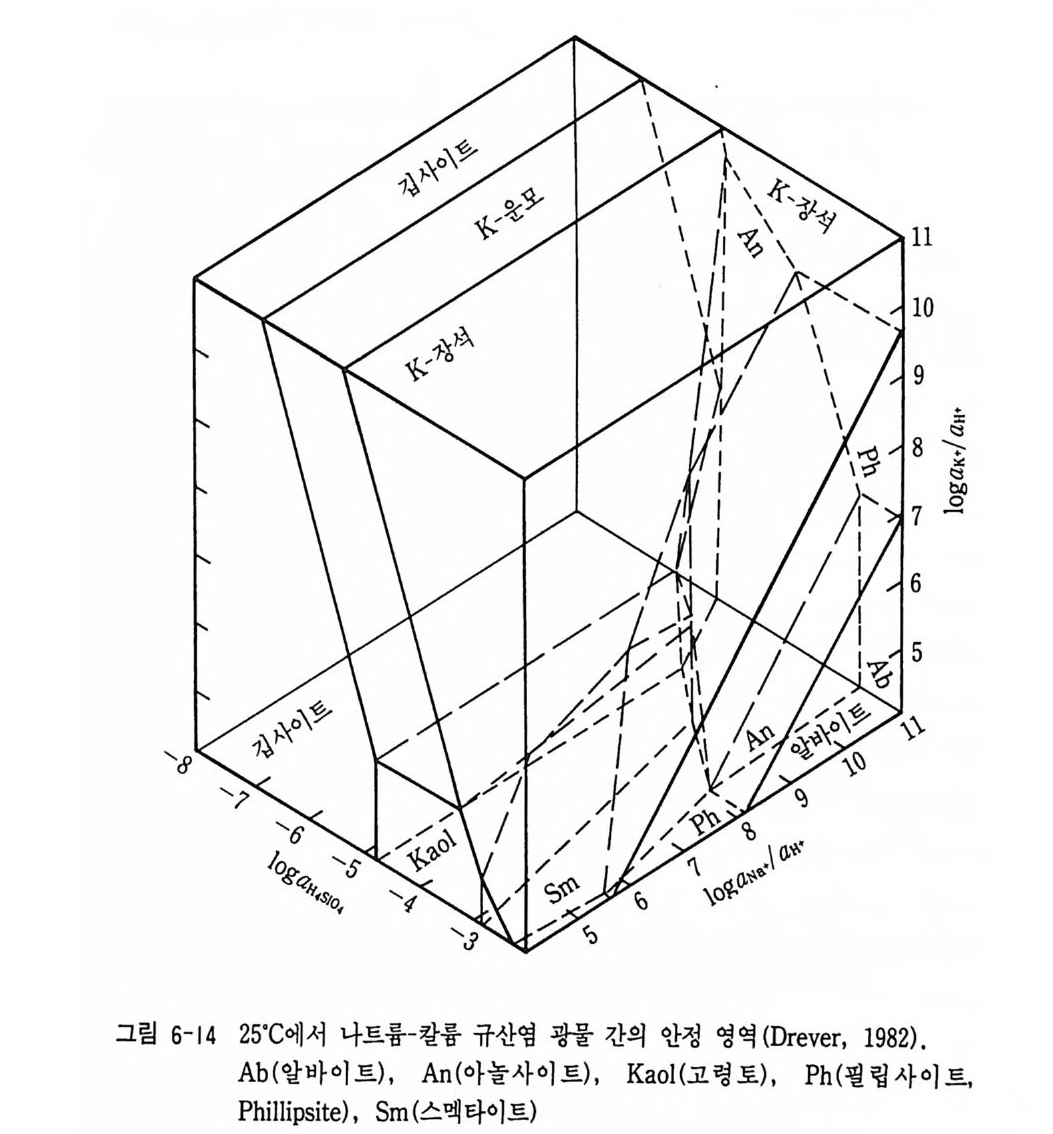 11
11
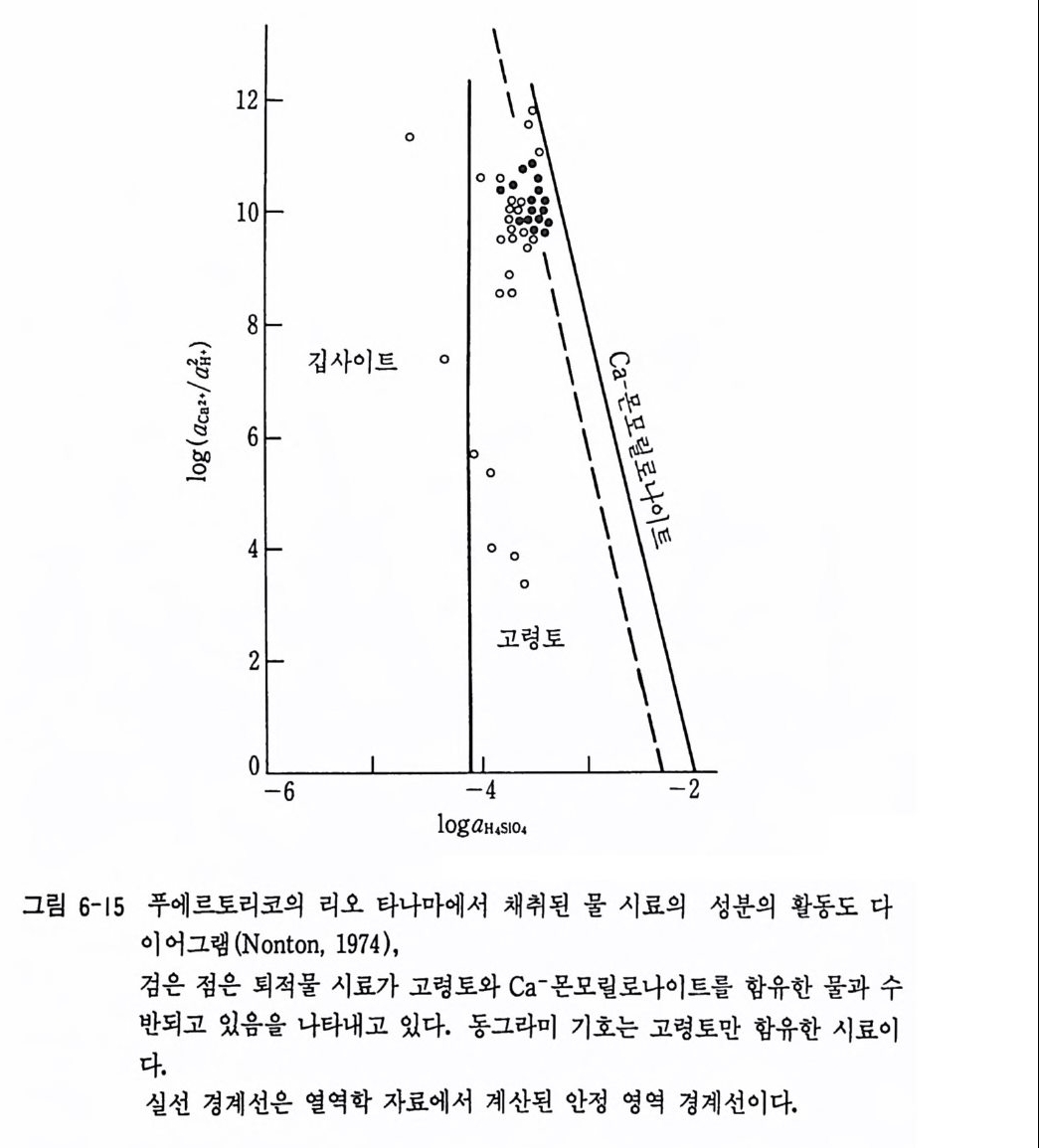 \
\
적 풍화 과정, 풍화의 정도, 풍화의 진행 방향, 풍화대의 구분 등의 해 석에 유용하게 이용될 수 있다. 6-4 퇴적물의 속성 작용 퇴적물이 저온에서 다져지는 작용 (com p ac ti on), 교착작용 (cemen t a tion ) , 재 결 정 작용 (recrys t a l li za ti on ) , 자생 광물 형 성 작용 (auth ige nic mine r- aliz a ti on ) , 노듈의 성 장 등과 같이 천천히 암석 화되 어 가는 작용을 속성 작용 (d i a g enes i s) 이라 한다. 퇴적물 내에는 유기 화합물이 함유되어 있기 때문에 속성작용의 과정을 추적할 수 있으며 퇴적암의 기원은 물론 천연 가스와 석유 탐사에 유용한 추적자로 이용될 수 있다. 속성작용은 보통 20 ·c ~200 ·c 의 온도 범위에서 일어나며 전압력은 1 kbar 이하인 지표 환경에서 주로 일어난다. 그러나 5kbar 정도의 퇴적층 심도까지에서도 일어날 수 있다. 속성작용의 과정은 퇴적물 입자 사이의 퇴적수 (form ati on wa t er) 가 침전되거나 퇴적수가 퇴적물 입자들과 반응에 의하 여 고화(固化)된다. 이때 퇴적물 입자 사이에서 확산 (d iff us i on) 이나 이류 (移流 advecti on ) 에 의 하여 반응속도론적 과정으로 물질의 이동이 일어 난다. 이런 내용을 다루는 분야가 물질이동학(物質移動學)이다. 속성작 용의 확산 과정은 고정되어 있는 되적물 입자 사이를 이온이나 분자가 확산되는 과정을 말하며 계내의 온도나 화학 퍼텐셜에 크게 영향을 받는 다. 그러나 이류 과정에 의한 물질의 이동은 이온이나 분자가 정수압 (hy dr osta t ic pre ssure) 에 의 하여 퇴 적 물 입 자 내 에 서 되 적 물 입 자와 함께 이동하는 과정을 말한다. 되적층에서 일어나는 확산 과정이나 이류 과정 의 예를 들어 보자.
(1) 퇴적층에서의 확산 과정 퇴적층 단면(그림 6-16) 에서 4x 만큼 떨어진 XA 깊이와 XB 깊이에서 이 온이나 분자의 확산이 일어날 때 이들의 각 플럭스(fl ux) ]1 와 h 는 갇지 않다. 죽 x 가 같은 값일 때 ]A=]a-LJx (a]/ax) 로 표현될 수 있다. 깊이가 다른 두 위치에서 플럭스 값이 다르기 때문 에 어떤 이온종의 농도는 임의의 시간 간격 동안에 퇴적물의 전체의 체 적을 변화시킨다. 따라서 퇴적층의 단위 단면적을 가정하면 그의 영향으 로 변화된 체적은 lX LJx 이며 그 변화량은 (]A-]이 =4x (8c/8t) = —L1x (a]/ax)
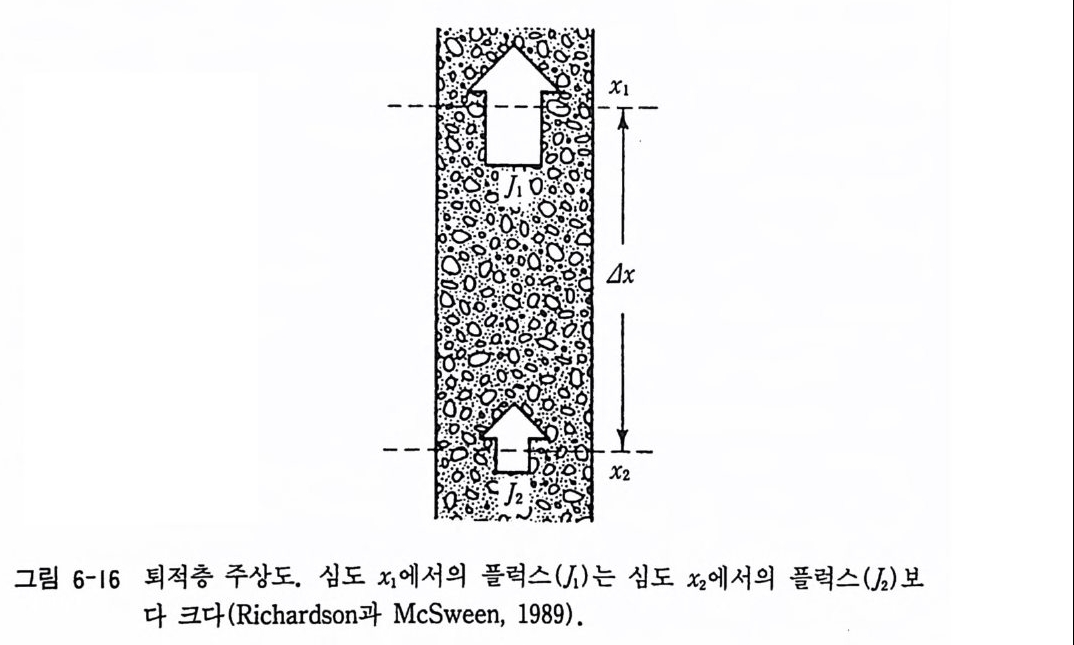 -li_--一{鼻l心XI _, -
-li_--一{鼻l心XI _, -
가 된다. 여기에 F i ck 의 제 1 법칙인 J= -D(ac/a x ) 를 대입하면 퇴적층에서의 시간 변화에 따른 이온종이나 분자종의 농도 변화는 (틀)=틀)(~) 가 된다. 이를 연속방정식 (conti nu it y equ a ti on ) 또는 Fic k 제 2 법칙이라 한다. 위의 식은 1 차원에서의 확산이고 3 차원에서의 확산 과정식은 信)=나)(着)+불)(峰)+나)(전) 으로 표현할 수 있다. 실제 퇴적층에서 일어나는 확산 속도 계산의 실례를 들어 보자. 해저 의 적색 점토충의 공국수에서 Mg 2+ 농도를 측정한 결과 Mg 2+ 농도는 해저 표면에서 1300 pp m 이고 lm 깊이의 점토충에서 1057 pp m 이었다. 만일 M 균 이온이 확산 과정에 의하여 이동되었다고 가정한다면 적색 점토충에서의 M g 2 + 의 확산 속도는 Fic k 제 1 법칙에 의하여 다음과 같이 계산할 수 있다. J= -Ds (8c/ax) 이때 M 균의 확산계수는 Ds = 1. 6 x 10-6cm2sec-1 이며 농도 변화는 243 ppm m-1(=1 .0 x 1 0-2 mol1-1m-1, =O.1 µmol cm 기 이다. 그리고 틀)값이 깊이에 따라 변화하지 않으므로 되적물에서 Mg 2+
아온은 정상 상태 플럭스 (s t ead y sta t e fl ux) 이므로 위의 식에 대입하면 퇴적충에서 M g2넥 확산 속도가 J= -0 .12 mg cm2y r-1 로 계산된다 (R ic hardson 과 McSween, 1989). (2) 퇴적층에서의 이류 과정 해저나 호소성 환경에서 퇴적물이 다져지는 작용 (com p ac ti on) 이나 지 하수면의 변화 등으로 인하여 퇴적물 내에 공극을 통하여 물이 이동된 다. 이때 용존 화학종이 운반되어 퇴적물과 반응한다. 일반적으로 퇴적 충 공국 내에서 유체의 이동은 대단히 느리게 일어나기 때문에 퇴적물이 다져지는 과정 실험에 의한 이론적 모델로 유체의 이동 속도를 추정할 수 밖에 없다. 퇴적물과 공국수의 매몰 속도를 각각 s, p의 기호로 표시하면 다져짐 이 진행될 경우 공국률(rp)은 비동시성 한계점 (asy m p tot i c lim i t, S d=Pd) 울 향하여 점점 감소하고 %, S 및 P 값도 감소한다. 퇴적층의 심도에 따라 공국률의 변화가 대단히 작을 경우에는 P q; =
V= 요¢ &-S (6 .11) 가된다. 예를 들면 마국의 Puzzle p ond 의 퇴적충 주상단면에서 측정한 공국률 의 변화에서 q;( x) =~1 x p(내 . 05x) +0.2 (6 .12 ) 의 경험적인 관계식이 얻어졌다. 여기서 x 는 되적층의 깊이이다. 이 관 계를 이용하여 퇴적층 내의 다져짐 과정에 의하여 유출된 유체의 속도를 추정할 수 있다. 정상상태 다져짐작용에 의하여 이류 현상이 일어났다고 가정하면 ~a=x O (6 .13) 가 얻어진다(B erner, 1980). 여기서 [l- rp (x)]S(x) 는 일정하다. 퇴적층 표면 (x=O) 에서 측정한 S 값은 퇴적물의 퇴적 속도와 같다. S(O) 의 값을 So 로 표현하면 위의 (6.13) 식의 실측치 값의 식에서 rp (O) 가 계산되어 [l-rp( x)]S(x) =0.3So 가 된다. 퇴적 주상단면에서 퇴적물의 매몰 속도 (S) 는 S= [8-5exp3 (S-。 O . 05x) ) 가된다. Puzzle p ond 의 퇴적 속도는 O.Z c m yr -1 이고 표면에서 60 rn 심도까지 위 식에서 ¢와 S 값이 %=0.22 와 Sd=0.077cm yr -1 으로 거의 일정한 값이 얻어졌다(B erner, 1980). 따라서 이를 (6.11) 식에 대입하면 v= 오p顯 0 . 077 cm yr-1 ) -S
가 얻어져 퇴적층의 임의의 깊이에서 유체의 이류 속도가 계산될 수 있 으며 그 결과는 표 6-5 와 같다. 이류 속도가 모두 부(―)의 값을 나타내 는 것은 퇴적수가 위로 유출되기 때문이다. 그러나 유체의 이류 현상은 입자 크기, 분급도, 퇴적 속도 등에 의하 여 크게 영향을 받기 때문에 반경험적인 모델밖에 수립할 수 없다. 그러 나 퇴적물 내에서의 확산과 이류 현상을 비교해 보면 이들이 속성작용 동안에 물질의 이동의 주요 메커니즘임을 알 수 있다.
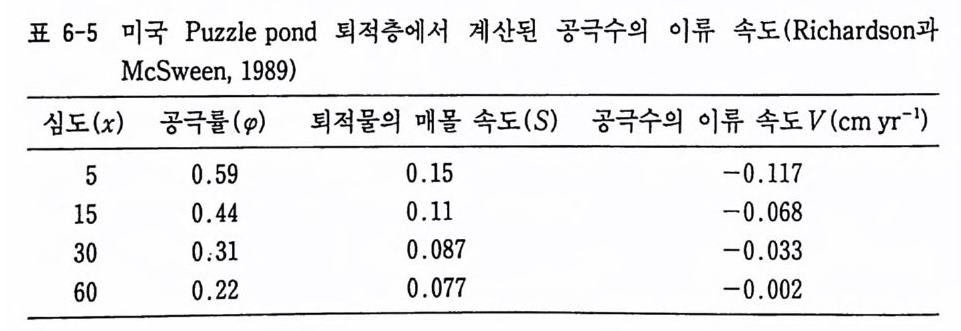 표 6-5 미국 Puzzle pon d 되적층에서 계산된 공국수의 이류 속도 (R i chardson 과
표 6-5 미국 Puzzle pon d 되적층에서 계산된 공국수의 이류 속도 (R i chardson 과
(3) 퇴 적물의 교착작용 속성작용 과정에서 퇴적물 입자 사이에서 CaC03, Si0 2 성분의 교결 물질이 화학적으로 퇴적물 입자를 교착시키는 작용을 교착작용 (cemen t a ti on) 이라 한다. 퇴적물 표면에서 산화 상태에 따라 전이 금속 이온들이 재아동하여 침전된다. 해저 퇴적층 표면에 박테리아에 의해 산소가 급속 히 소모되어 광물의 용해 반웅이 일어나 퇴적층 내에서 철 (Fe2 + )과 망간 (Mn”) 등은 산화되지 않고 이동성이 큰 이온 상태로 존재한다. 그러나 이들 이온은 확산에 의해 퇴적층 표면으로 이동하여 Fe3+ 와 Mn” 로 산 화되어 침전되어 Fe-Mn- 옥시수산화물충을 만들어 심해저에 망간 노듈 과 같은 것을 형성하게 된다. 심해저 퇴적물에서 시간에 따른 망간의 분 포 변화를 볼 수 있는데 대서양 적도 지역의 퇴적물 코아 시료에서 심도
에 따른 재분포 모델을 Berner(1980) 와 Burd ig e 와 G i erskes(1983) 이 설 정하였다(그립 6-17). 심도에 따른 망간의 분포는 룹)= (CLi G) (6 .14 ) 이다. 여기서 CL 과 Co 은 x =L 과 x =O 에서의 Mn2 + 의 농도이다. 어떤 시점 x= O 에서 용존 Mn 의 플럭스는 Fic k 제 1 법칙에서 다음과 갇이 계 산될 수 있다. lo= —Ds (ac/a x ) = ― D 三 (6 .15 ) 시간의 변화에 따라 전이대의 두께 (L) 의 변화는 ]o 와 비례한다. 孟dL -=VT T山 T\ 5 ( cFl -dL C o) (6 .16) 여기서 Vd 는 1 몰의 Mn 2 + 를 함유한 용해되고 있는 광물의 체적이며 Fd 는 전체 퇴적물 중에 용해되고 있는 물질의 체적분률이다. 같은 식으로 ox y h y drox i de 충 (l) 의 충의 두께 가 다음과 같이 증가한 다. 河dl =Vp D 广(C了L—江 C_o ) (6 .17) 여기서 Vp 와 Fp 는 각각 Vd, Fd 와 유사한 의미로 사용되었으며 침전 대의 광물질에 대한 이들의 값을 의미한다. 전이대의 두께는 (6.16) 식을 적분하여 계산할 수 있다. 이때 t =O 에서 적분구간 (boundra y cond iti on) 은 L=O 이고 t=t일 때 L=L 이다. 즉 L=[ 망 S (CL_C 가 (6 .18)
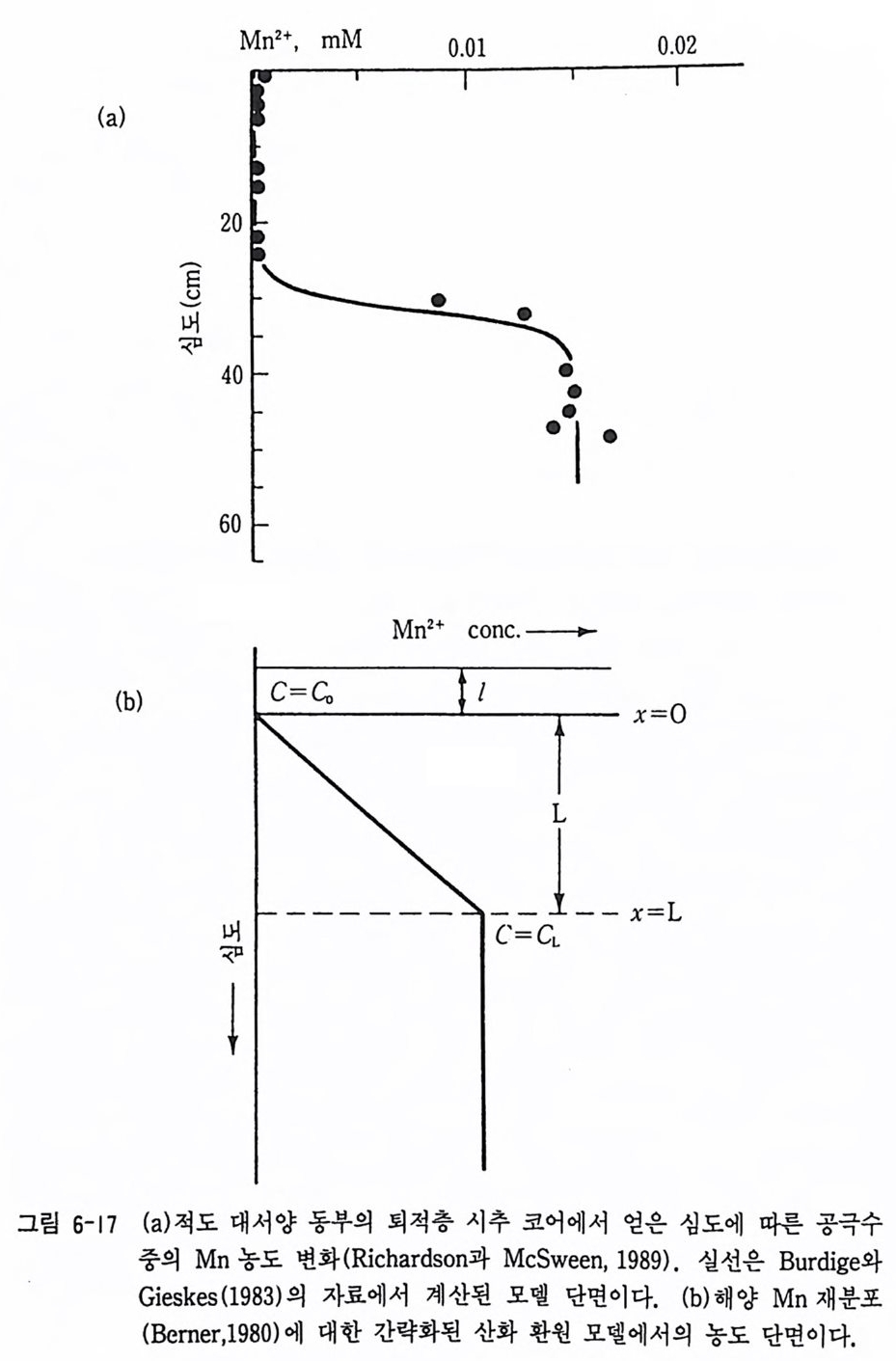 Mn2+ , mM 0.01 0.0 2
Mn2+ , mM 0.01 0.0 2
이다. (6.18) 식을 (6 . 17) 식에 대입하고 t =O 일 때 l=O, t=t일 때 l=l 인 적분구간에서 적분하면 옥시수산화물 (ox y h y drox i de) 충의 형성에 걸린 시간(t)은 2 Vi F FJ FJds 2( CvLd -C o) (6 .19) 이 된다. 예를 들면 1 cm 두께의 산화표면충이 형성될 때 걸린 시간을 계산할 수 있다. Ds=2. 4 X 1 0-6(cm2sec~1 ) , Vp =Vi=2 0cm3mol-1 , FP =0. 2, Co= O .O M 등의 수치를 사용하여 계산된 t와 L 은 표 6 - 6 과 갇 다.
 표 6-6 계산된 t와 L( Ri chardson 과 McSween, 1989)
표 6-6 계산된 t와 L( Ri chardson 과 McSween, 1989)
6_5 열수의 지구화학 열수의 지구화학은 주로 지열수의 특징에서 체계화되었으며 물의 기원 과 지열수의 역할, 열수 겨 암석 상호반응, 화산 분출시 물의 역할, 화산 분화의 예측과 방제, 온천 개발, 지열 발전, 광상 생성 메커니즘 해석, 광상 탐사법 등에 응용될 수 있다. 물은 임의의 온도에서 압력을 높이면 액체로 존재하지만 압력을 낮추 면 비등 현상이 일어나 수증기로 존재한다. 이 특정한 압력을 이 온도에
서의 포화수증기압이라 한다. 압력과 온도를 계속 높이면 어느 온도에서 는 압력을 아무리 변화시켜도 물이 액체의 수증기 상태와 구별되지 않게 된다. 이 점 을 임 계 점 (criti ca l poi n t ) 이 라 한다. 물은 374 'C , 21. 8 MPa 가 임계점이다. 열수와 수증기는 현저한 밀도차가 있다. 열수는 암석과 의 반응성이 대단히 높기 때문에 암석을 용해시킨다. 석영의 포화수증기 압에서 열수에서의 용해도를 보면 온도가 증가함에 따라 S i 0 2 의 용해도 가 증가한다. 그러나 약 340° C 이상에서는 용해도가 급격히 감소한다. 600 ppm S i 02 의 용해도를 가진 340 ·c 내의의 고온의 열수가 200 °C 정 도로 온도가 낮아지 면 S i 0 2 의 용해도가 260 pp m 으로 떨어 지 게 되므로 결국 340 pp m 의 S i 0 2 는 침전되어 수정이나 오팔 등을 형성하게 된다. 이때 온도가 천천히 낮아지면 수정 결정이 형성되고 온도가 급격히 낮아 지면 오팔과 같은 비정질 실리카가 정출된다. (1) 지열수와 암석의 반응 지열수의 화학 성분은 지열수의 성인, 용존 화학 성분의 기원 등에 따 라 다양하다. 지열수의 화학 성분은 주로 양이온으로 Na+, K+ , Mg 2+ , Ca2+ , Fe2+ , Fe3+ 등이 용존하고 있다. 그리고 음이온으로 Cl\ SOt , HCOa 등이 있다. 양이온은 지하에서 광물 및 암석과 반응하며 반응한 암석 광물과 성분이 평형에 있게 되나 음이온은 원래의 기원 고유의 특 칭을 가지고 있는 경우가 많다. 따라서 용존 성분의 기원 추정에는 음이 온의 구성 성분의 동위원소비가 많이 이용되고 있다. 조암광물의 성 분은 Si0 2 , AhOa, K20, CaO, Mg O , FeO, Fe2 아, P205 등으로 되 어 있다. Si0 2 , Ah 아, K20, H20 계 의 구성 광물은 칼리장 석, 칼리운모, 고령토 등이 있다. 앞에서 칼리장석의 화학적 풍화에서와 같이 열수의 H+ 가 칼리장석과 반응하여 칼리운모를 만들게 된다. 반대 로 열수의 K 겨t 방출, 칼리운모와 석영이 반응하여 칼리장석이 생기게
되기도 한다. 즉 칼리장석이 H+ 이온 농도가 높은 산성 지열수와 반응 하면 다음 반응석에서와 같이 칼리운모가 생성되고 지열수의 K+ 농도는 높아짐을 알 수 있다. 3KA!Sh0a+2H+ ~ KAbSh01o(OH )2+ 2 K+ +6 H20 (칼리장석) (칼리운모) (석영) 2KAhSh010(0H )2 +2H++3H20 ~ 3AhSi2 0 s(OH )4 +2K+ (칼리운모) (고령토) K20— AJ iQ3 -Si0 2 -H20 계에 있어서 열수의 성분과 공존 광물 사이 의 관계는 그림 6 - 18 과 같다. Io g (mK•lmw) 와 온도 사이의 관계에서 고 온에서 K 농도가 높은 조건에서는 칼리장석이 안정하고 온도와 K 농 도가 낮아지면 칼리운모 (KA6S iJ 01o(OH )z) 그리고 고령토 (Al2S iz Os(OH)4), 납석 (AbSi4 0 10(OH )2) 및 홍주석 (AhS i O 이이 각각 안정하게 된다. 이들 광 물은 열수와 공존하고 있다. 열수와 공존하는 세 광물은 K + 을 함유하지 않는 Al, S i로 구성 된 광 물들이다. 온도가 높아지면 납석에서 물이 빠져나가 홍주석이 된다. 열 수의 K\ H 농도가 어느 정도일 때 열수와 이들 광물이 공존 가능할 것인지 250°C 에서의 예를 들어 보자. 칼리장석과 칼리운모의 경계에서 log (m K+ /mw) =4.1 이다. 즉 열수가 칼리장석과 공존하기 위해서는 K. 농도가 H 농도의 104.1 배(약 13000 배) 이상 함유되어야 한다. 그 이하에 서는 칼리운모와 공존하게 된다. 물론 log (m K+/mt t+) 츠 10“ 일 때에는 칼리장석과 칼리운모가 공존하게 된다. log (m K•lmw) 츠 2.4 일 때 칼리운모와 고령토가 공존하게 된다. 만 일 열수의 p H 가 7 인(H+ 농도가 10-1mo!K g기 중성 열수에서 칼리운 모와 칼리 장석 이 공존할 경 우에는 K+ 농도가 10-1 mol K g -1 의 13000 배 인 약 50 pp m 이 된다. 같은 식으로 생각하면 칼리운모와 고령토가 공존 할 때에는 K+ 농도가 약 l pp m 이 된다. 그러므로 중성 열수가 칼리장석
과 공존 평형에 있으면 K+ 농도는 50p pm 이상이 되고 칼리운모와 공존 평형에 있으면 50 pp m~1 pp m 의 값을 가짐을 의미한다. 열수변질 광물 은 반암동 광상이나 열수 광상, 스카론 광상 등에서 광화 작용의 지시자 가 되기 때문에 광상 탐사에 대단히 중요하다.
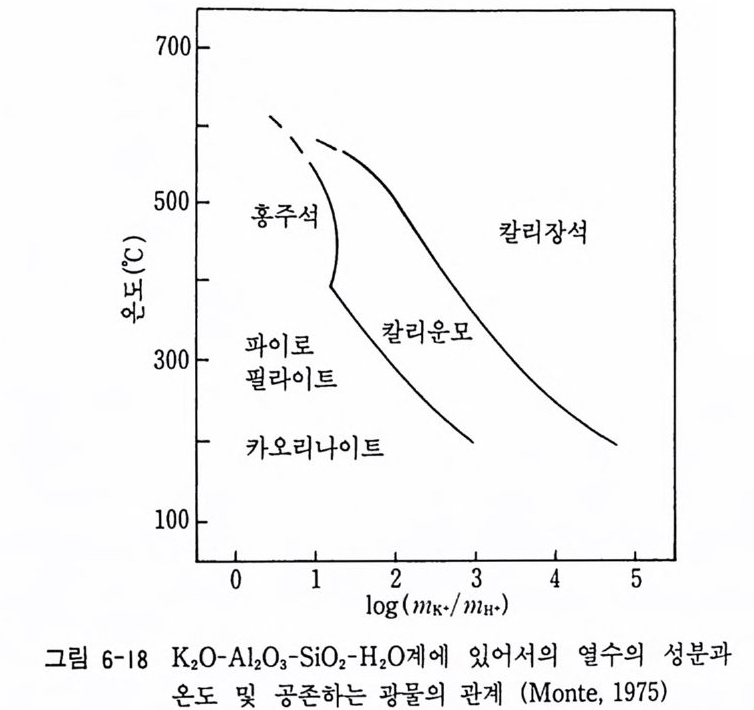 700
700
실험에서 해수와 안산암 분말의 고온 • 고압 반응에서 형성되는 열수의 화학 성분 변화는 그립 6-19 와 같다 (Endo, 1980). 가열 시작 10 시간 후 230~300·c 에서 M i' + 가 급격히 감소하고 K + 은 증가하고 있다. Na+ 도 약간 변화하며 Ca2+ 는 급격히 감소한 후 증가하 고 있다. 이는 SOt 등의 성분의 농도 변화와 함께 고려하면 반응이 시 작될 때 최초로 안산암 중의 휘석, 사장석, 유리질 물질이 녹기 시작하 여 용출된 Al3+ , Fe2+ , Fe3+, M 굽+ 등의 이온과 S i O 가 스멕타이트
(smec tit e) 를 형성하기 시작한다. 따라서 안산암에서의 Na+, K+, Ca2+ 성분이 열수에 첨가되고 M ,j- + 는 열수에서 제거된다. 300 시간이 지나면 M 균는 감소하고 K+, Ca2+ 는 증가하며 N 갑가 다시 감소하기 시 작한 다. 1000 시간 후 M ,j-宅 전부 없어지고 Ca2+, Na + 가 감소하기 시작하 며 K 만 증가하게 된다.
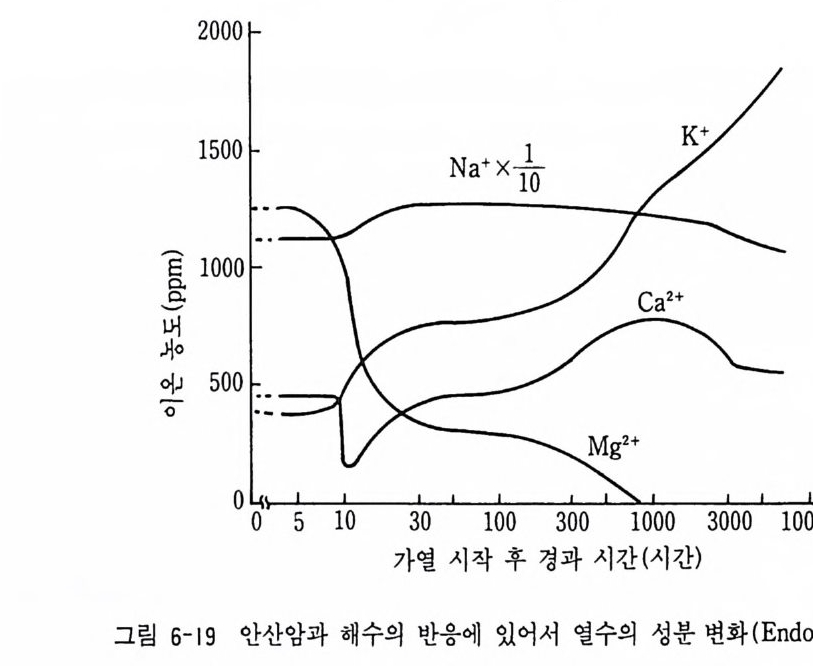 2000
2000
이같은 현상은 약 1000 시간 후 열수 중에 M ,j-+가 없어지고 난 후 스 멕타이트가 새로 생성되지 않고 스멕타이트의 이온 교화성의 반응만이 일어나게 되어 스멕타이트에서 K + 이 열수 속으로 이동하고 열수 중의 Ca2+, Na 까 스멕타이트 속으로 들어가게 되기 때문인 것으로 추정하고 있다.
(2) 열수-암석 상호반응과 안정 동위원소비의 변화 화성암과 물 사이의 상호 반응에 의해 일어난 수소 및 산소 안정동위 원소비의 변화가 Tay lo r0974, 1977) 에 의해 정량화되었다. 열수와 암석 사이의 반응에서 다음과 갇은 동위원소 교환 반응이 일어난다. ½si0 1 602 + mso ;::::::::= ½si1 8 02 + m60 특히 180 가 결핍된 순환수 기원의 열수가 암석과 반응할 때는 산소 편 이 (oxy ge n shif t) 현상이 현저 하게 나타난다. 이 같은 현상은 많은 반암동 광상이나 미국의 아이다호 화강암 저반, 옐로스본, 스팀보트스프링, 라 센파크 등의 지열수 지역 등지에서 현저하게 나타난다. 폐쇄계에서 열수 와 암석 사이에 동위원소 교환이 일어날 경우 반응 전후의 암석 시료의 안정동위원소비 분석에서 물-암석의 비 ( W/ R) 를 다음 식에서 계산할 수 있다. W/R=[ 』I _ R( 걸낀 4) ] (6.20) 여기서 &W와 &R 은 동위원소 교환 반응 전에 존재했던 물과 암석의 동위원소 값이다. 그리고 &R 동위원소 교환이 일어난 후의 암석의 동 위원소비이며 4 는 해당 온도에서의 물-암석 (광물) 사이의 동위원소 분별 정수이다. 변질받기 전의 신선한 화강섬록암이 180 가 결핍된 순환수와 400~45o•c 온도에서 동위원소 교환이 일어날 경우 물/암석 (W/R) 의 변 화에 따른 조암광물의 동위원소비 변화를 (6.20) 식의 동위원소 질량평형 식에 의하여 계산하면 그림 4-15 와 갇다. 신선한 섬록암 중의 장석의 8180= +8~9 %o 과 혹운모 8D= -65 %0 를 사용하고 8D= -120 %0, 818 0=-16%0 인 순환수를 사용하여 계산하였다. W/R 비가 낮은 조건에서
는 수소 동위원소값의 변화가 현저하고 W / R의 비가 점차 증가함에 따 라 산소 동위원소비가 변화하고 있다 . 이와 같은 모델 계산 결과는 미국 아이다호 저반의 화강암질 암석의 열수변질에 의한 동위원소비의 변화 경향과 잘 일치하고 있다 (Cr i ss 와 Tayl o r, 1983). 우리나라의 중생대 대보 화강암류와 불국사 화강암류에서도 열수변질 에 의하여 전암의 산소 동위원소비는 土 2.38~+1 1. 0 % 0 로 변화폭이 크 다. 그러나 동위원소 교환에 비교적 안정한 석영의 0180 값은 +8.73 ~ + 11.10 %0 로 비교적 균질하다(그립 4-1 6 ). 그리고 경상 퇴적분지 내에 분포하고 있는 안산암질암의 01 8 0 값 一 3.1~7.6 % 0 로 변질받지 않은 안 산암의 818 0 ::: ::: +6 % 값과는 대조저으로 180 결핍된 순환수 기원의 열수 에 의한 변질을 심하게 받고 있다(김규한과 이전수, 1993).
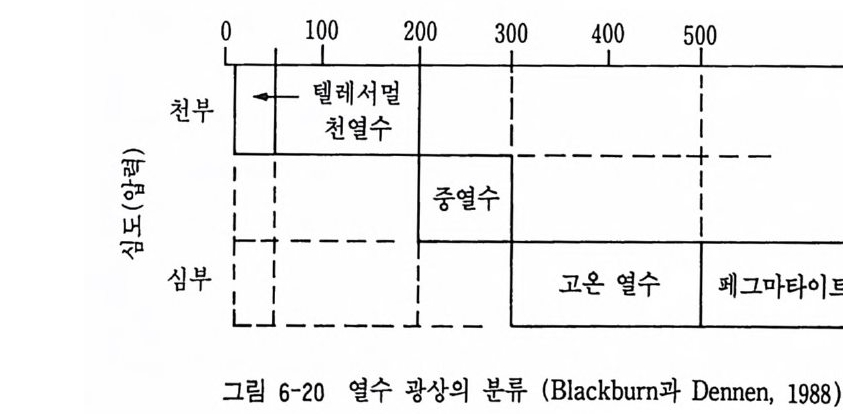 。 100 200 300 400 500
。 100 200 300 400 500
(3) 열수 광상의 형성 열수 광화 용액이 공국률이 큰 모암의 파쇄대에 유입되어 맥상, 망상 (sto c kworks) , 판상 등의 열수 광상을 형 성 한다. 열수 광상은 광화 심도 와 온도에 의 하여 천 열수형 (ep ithe rmal) , 중열수형 (mesoth e rmal) , 심 열수 형 (hy po th e rmal) 등으로 구분한다 (그림 6-20) .
열수 광화 용액의 주요 성분은 Au, Ag , W, Fe, Ni, As, Pb, Zn, Sn, Bi, Cu, Co, U 등으로서 열수 용액에 포함되어 착화합물의 형태로 운반되다가 새로운 환경에 이르면 금속 산화물의 형태로 침전된다. 침전 울 일으키는 화학적 원인은 Eh, p H 의 변화, 고체와의 반응, 다른 유체 와의 반응 등이 있다. 그리고 물리적 원인으로는 온도 저하, 압력 변화, 불포화수의 희석과 박테리아 활동과 같은 생물학적 원인 등이 있다. 그 러나 열수 광화 용액의 기원이 마그마 기원인지 또는 마그마에 의해 뜨 거워진 지하수가 암석과 반응하여 만들어진 열수인지 확실하지 않다. 유 용 금속 성분의 기원 역시 마그마에서 유래한 것인지, 물-암석 반응에 의해 암석에서 추출된 것인지는 미해결의 문제로 남아 있다. 광물 중에 는 열수 용액에서 광물이 정출될 때 광물 내에 포획된 유체포유물(fl u i d i nclus i on) 이 많이 관찰된다. 유체포유물의 영농도와 균일화 온도 측정에 서 열수 용액의 특성이 고온에서 고영농도의 유체임아 확인되었으며 저 영농도의 지하수와 혼합에 의하여 영농도가 낮은 유체포유물도 많이 존 재하고 있음이 보고되어 있다. 유체포유물의 산소 및 수소 안정 동위원 소비 분석으로 열수 광화 유체의 기원이 규명되어 마그마 기원, 순환수 기원, 순환수와 마그마 기원 열수의 혼합, 암석과 열수의 반응 등의 결 과가 규명되어 있다. 일본의 쿠로코형(黑鑛型) 광상, 반암동 광상, 괴상 황화물 광상 등에 서 열수와 순환수의 혼합에 유용 금속 광상이 형성된 예가 많이 알려져 있다. 그리고 해저 화산 활동에 의해 형성된 고영농도의 열수가 홍해의 열곡 대에서 발견되었으며 대량의 황화 광물이 침전된 퇴적물이 알려졌다. 또 해 령 부근에 황화 광물을 다량 침 전시 킨 블랙 스모커 (black smoker) 가 확인되었다. 열수가 지표 부근까지 상승하면 압력 저하로 비등현상이 일어나 2 차적 인 열수가 형성되어 천열수형 광상을 형성하게 된다. 천열수형 광상으로
는 일본의 히 시 카리 (his h ik a ri) 광상과 같은 금은 광상이 잘 알려 져 있 다.
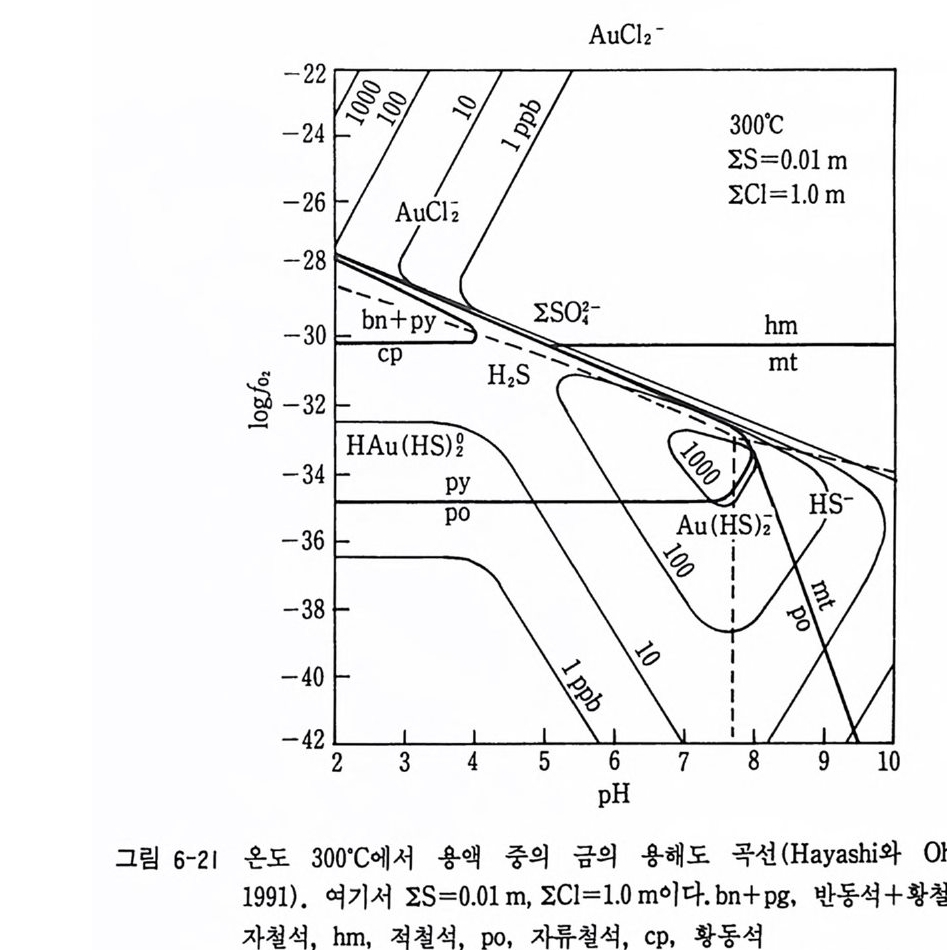 AuCl2-
AuCl2-
금은 AuCl2- 와 같은 영화물 착화합물이나 Au (H S) i와 같은 황화물 착 화합물의 형태로 광화 용액에서 이동된다. 그림 6-21 은 300·c 에서 AuCl i 의 염화물 착화합물과 Au( HS )i 황화물 착화합물의 용해도를 pH -log/ 0 2 관계 그림으로 나타낸 것이다. AuCl2 착화합물의 용해도는 pH 가 높고 환원적 환경이 될수록 낮아지며 p H 가 중성 부근에서는 용해도 가 현저히 낮아진다. 반대로 Au( HS )i 착화합물의 용해도는 중성 부근
에서 대단히 높다. 황철석이나 자류철석이 존재하는 열수계에서 Au 는 광화 용액 중에 Au (HS)2 와 감은 착화합물로 존재 할 것 이 다. 2Au(H S )2+2H++H20 =소 2Au+4H2S+ 拉 또는 다음과 갇다. 2Au (H S)2+H 나上2 H2 =~ 2H2S+Au HAu (HS ) g+ 卓 H2 ~ Au + 2H2 S Ha y ash i와 Ohmo t o0991) 의 금의 용해도 실험에 의하면 금의 용해도 와 H+, Cl- 의 활동도는 무관하며 H 2 S 의 활동도가 중요한 요인 이 며 금 은 HAu (H S) g의 형태로 용존하고 있는 것으로 나타났다. H2S 활동도가 Au 의 용해도를 증가시키고 있다. 열수가 파쇄대를 따라 지표 부분까지 상승하면 비등 현상이 일어나고 이때 용존하고 있던 열수 중의 H2S 는 밖으로 유출된다. 이와 함께 열수 의 온도가 저하되면 H2S 의 저하가 현저하여 금의 용해도가 현저히 낮아 져서 열수 용액에서 금이 다량 침전하게 된다. 그리고 열수계에서 금의 침전은 환원, p H 의 변화 , H2S 의 유실, 온도 변화 등에 대한 금의 용해 도의 변화에 따라 일어나고 있다 . 이처럼 H2 의 활동도가 증가(fo , 감소) 하면 금의 용해도가 감소할 것이다. Au(HS)2 가 우세한 광화 용액에서 는 p H 가 증가할 때 금의 침전이 일어날 것이고 금이 HAu (H S) g의 형태 로 존재할 때는 p H에 무관하며 Au (H S) ;가 우세 하게 존재 하면 p H 가 감소할 때 금이 침전하게 될 것이다.
제 7 장 광물의 결정화학 결정화학에서는 고체 광물의 구조와 화학 성분 사이의 관계를 다룬다. 지 질학적 과정 에 서 광물 결정구조의 안정 성 (sta b il ity) 과 광물의 거동 (mi ne ral behav i or) 은 물질과학 분야의 광물학, 금속학, 고체물리학 및 고체화학 분야의 기본이 되고 있다. 광물의 화학적 전이와 구조적 전이에서 지질학적 과정의 물리화학적 조건을 해석할 수 있으며 광물의 안정도를 해석할 수 있다. 전자현미경 의 개발로 광물의 미세 결정구조의 연구에 큰 발전을 가져왔다. 여기서 는 광물의 거동과 규산염 광물의 결정화학을 중점적으로 다룬다.
7-1 결합구조와 이온 반경 광물의 결합은 원자 사이의 전기음성도 값의 차가 큰 경우 이온결합을 이루고 두 원자가 유사한 전기음성도 값을 가질 때에는 공유결합을 하게 된다. 그리고 금속 이온 사이에 금속결합이 이루어진다. 소금의 결정은 Na+, c1-이 온이 이온결합을 하고 있다. 결정 중에 이온이 반대 전하의 이온으로 둘러싸인 것을 배위라 하며 반대 전하의 이온의 수를 배위수 (coordin a ti on number) 라 한다. Na+ 와 Cl- 은 각각 6 배 위 이 다. 즉 배 위 하 고 있는 6 개의 이온이 팔면체를 형성하고 있다. 이때 두 이온 사이의 퍼 텐셜 에너지 (E) 는 E= _ARE 냥 +BTe2 이다. 여기서 R 은 이온 사이의 거리이고 A 는 결정구조에 따라 정해지 는 마델룽 (Mardelung) 정 수이 며 n 은 7~ 12 까지 의 값을 가지 며 이 온의 전자 배열에 따라 다른 값을 가진다. e 는 전하, z 는 이온의 가수이며 B 는 개체의 결정에 의해 정해지는 정수이다. 양이온과 음이온의 거리가 짧을수록 결합력은 강하다. 이온 반경은 양이온과 음이온 간에 정전력으 로 결합된 두 이온의 양이온과 음이온의 반경 거리를 말한다. 동일한 원 소의 이온이라도 이온의 가수가 크면 정전기력이 강하여 이온 간의 거리 가 짧아져 이온 반경이 작아지며 배위수가 크면 이온이 넓은 공간을 차 지하므로 이온반경이 커진다(표 7-1). 화학 결합에 있어 Paul i n g(1 960) 은 〈안정한 배위 구조 중에는 인접하고 있는 양이온에서 1 개의 음이온에 작 용하는 결합의 강도 총합은 음이온의 전하와 같다〉는 등의 5 가지의 Pau li n g의 법칙을 세워 결정구조 추정에 유용한 자료로 사용하였다. 즉 이온 반경에 따라 광물의 배위수, 결합력 등의 광물의 결정화학적 성질이 달라진다. 이온 반경의 비에 따라 이온결합 결정의 배위수가 결
 표 7-1 원 소 의 이온반경과 배위수
표 7-1 원 소 의 이온반경과 배위수
정된다. 양이온 반경 (R e ) 과 음이온 반경 (R 사의 비가 0.155 이면 양이온 주위에 음이온이 3 개 결합되는 삼각형이 되고, 0 . 225 일 때에는 양이온 주위에 4 개의 음이온이 결합하는 사면체형, 0 . 414 일 때는 6 개의 음이온 이 결합되는 팔면체형, 0.732 일 때는 8 개의 음이온이 결합되는 입방체를 이룬다. 안정된 팔면체형을 이루려면 0 . 4l4 < RclRa < O . 732 이어야 한다. 따라서 광물의 안정도는 원자의 상대적 크기에 의해 결정되는 기하학 적 특칭과 전자의 전하수, 전기음성도, 결합 형태 등과 감은 전기적인 특칭과 열역학적인 특징에 의해 결정된다. 7-2 광물의 화학적 전이와 구조적 전이 광물의 화학적 전 이 와 구조적 전 이 (mine ral tra nsfo r mati on ) 가 온도나 압력 등의 환경 변화에 따라 일어난다. 예를 들면 온도와 압력 변화에 따라 구조가 변화하는 동질이상(p ol ym o rp h), 질서 - 무질서 (order-d i s - order) , 고용체 (soli d soluti on ) 등을 들 수 있 다. (1) 동질이상 화학 성분은 같으나 결정구조가 다른 광물상으로 C( 다이아몬드와 혹 연), AbS i Os( 홍주 석 , 남정석, 규선석), S i 02(a - 석영, f3-석영, 트리디마이 트 크리스토바라이트 등)의 동질이상을 둘 수 있다. 그립 7-1 에 동질이상 관계에 있는 Si0 2 광물상을 압력과 온도에 따라 나타내었다. 이를 이용하여 공존 광물 종류에 따라 그 광물이 결정화될 때의 온도 나 압력을 추정할 수 있기 때문에 광물학에서 대단히 중요하다. 지표 환 경에서는 a- 석영과 같이 특정 온도와 특정 압력에서 단 하나의 광물상 만이 안정하다. 그러나 지표의 암석에서는 트리디마이트, 크리스토바라
이트와 코에사이트 등의 광물이 산출된다. 이들 광물은 지표 환경에서는 모두 a- 석영으로 전이되어야만 하나 이들 광물의 전이가 저온에서는 대 단히 느리기 때문에 준안정 상태 (meta s ta b le s t a t e) 로 존재하게 된다. 이 는 반응속도론적 문제가 된다.
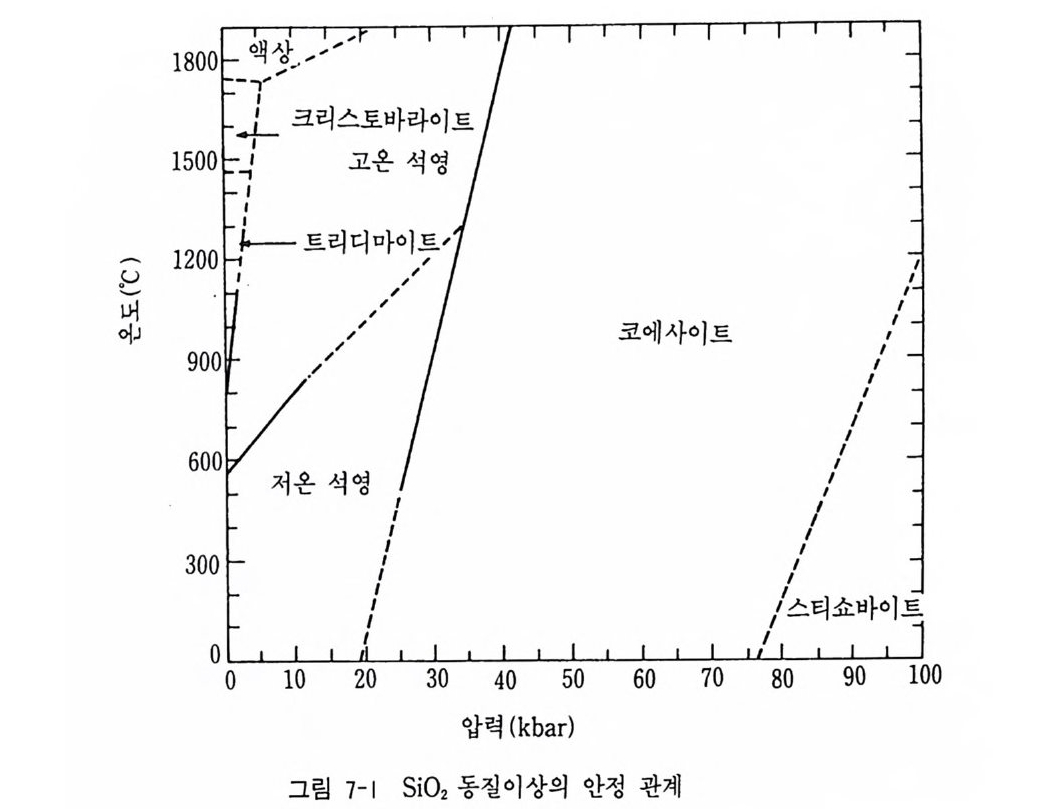 18001- --1액 ,-상-. . ,/zz 2
18001- --1액 ,-상-. . ,/zz 2
(2) 질서-무질서 전이 단일한 광물 안에서도 질서-무질서 전이 (order-di so rder tran s fon nati on ) 가 일어나고 있다. 금속결합에서 흔히 관찰되는 현상으로 두 원소 사이
가 높은 온도에서 완전히 무질서해질 수도 있고(그립 7-2) 저온에서 질서 상태에 이를 수도 있다. 물론 특정 온도에서는 이들의 중간 상태가 존재 할 수도 있다. 장석류와 휘석류의 광물에서 대단히 느린 광물의 상전이 가 일어나고 있다. 이는 광물의 결정 열역사 해석에 대단히 중요한 현상 이다.
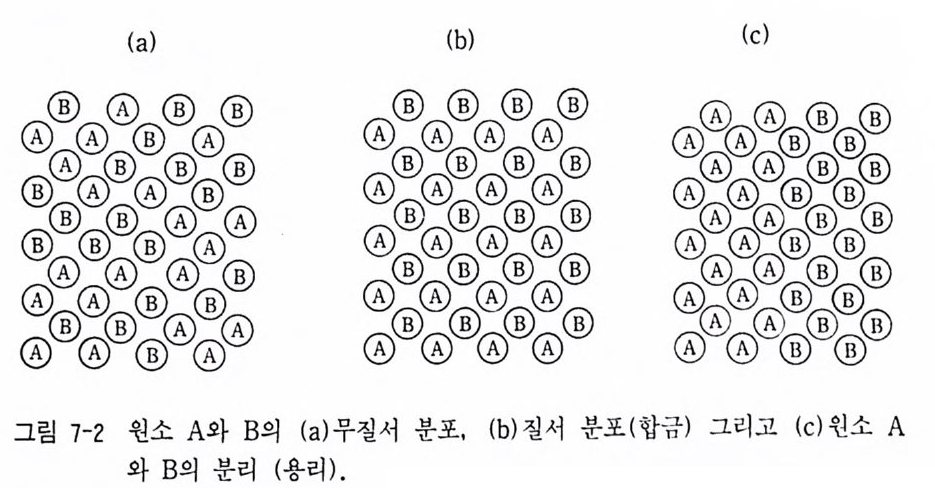 (a) (b) (c)
(a) (b) (c)
위의 그림 7-2(a) 와 7-2(b) 에서는 원자들이 큰 이동 없이 전이가 일 어나 국부적으로 화학 성분은 변하지 않았다. 그러나 이갇은 균질한 광 물상이 새로운 환경에서는 화학 성분이 다른 부분으로 분리될 수도 있다 (그립 7-2 (c)). 이런 현상은 광물에서 용리 (exsoluti on ) 현상이라고 한다. 주로 결정 내에서 원자의 이동이나 확산에 의해 용리 구조가 형성되지만 대부분의 광물에서 그 형성 속도가 대단히 느리다. 이처럼 광물의 상전 이 현상은 모두 반응속도론적 과정으로 귀결된다. 따라서 시 간-온도-전 이 (tim e-te m p er atu r e-tr a nsfo rm ati on , T- T -T) 그 림 으로 표현한다(그림 7-3). 그림 7-3 에서 스피노드식 분해의 경우와 균질핵 형성 경우의 TTT 다 이어그램으로 스피노드식 분해의 경우 E는 열역학적으로 이상적인 전
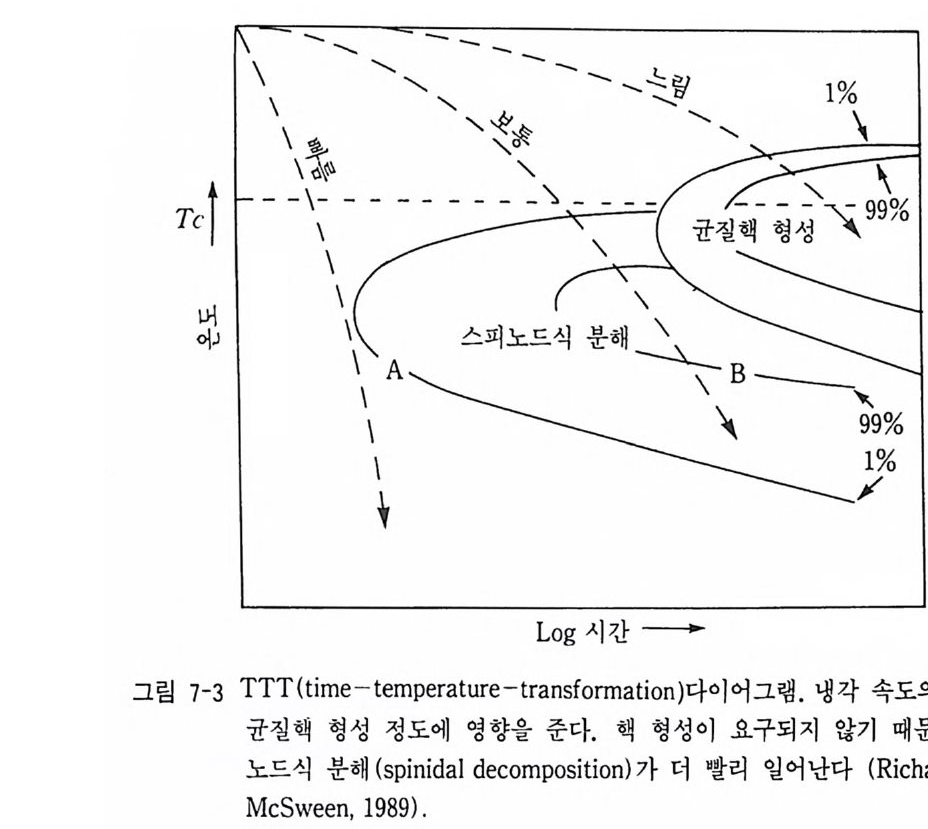 Tca \- \ - \\`多적-\ ` ` `-` -\-\- - \-〈-漆\- ':,- ---- -- `- 느-\ 립 \ ` 璃\ `
Tca \- \ - \\`多적-\ ` ` `-` -\-\- - \-〈-漆\- ':,- ---- -- `- 느-\ 립 \ ` 璃\ `
이 온도로 최종 광물상이 모체 광물상과 완전히 평형상태에 있음을 말한 다. 처음 A 선은 전이 산물이 처음 관찰되는 온도이며 B 선은 반웅이 종 결된 때의 곡선이다. A 와 B 의 중간 점 찍은 부분은 전이의 양을 나타낸 것이다. E 부근의 온도에서는 전이 속도가 대단히 느리고 저온에서는 전이 속도가 빨라지며 온도가 더 낮아졌을 경우에는 전이 현상이 일어나 지 않는다. 이 룰 반응속도론적 중간 온도 (kin e ti c cut off tem p e ratu re ) 라 한다. 그림 7-3 에서처럼 용리 현상이 일어날 때 TTT 그림으로 나타내 는 것이 유용하다. 이 그림은 실험에서 얻어진 값으로 1 % 용리 산물이 형성되기 시작한 경우와 99 % 용리 산물이 만들어진 경우를 나타낸 것
이다. 이처럼 용리 생성시의 냉각 속도와 온도 사이의 관련성이 검토될 수 있다. 느린 냉각 속도에서는 균질 핵생성이 스피노드석 분해 (spi no id a l decomp os it ion ) 보다 우세 하게 일 어 난다. 반면 에 보통의 냉 각 속도에서는 그와 반대 현상이 일어난다. 빠른 냉각 동안에도 스피노드식 분해는 불완전하게 일어난다. 고온에서 균질 핵생성 이전에 불균질 핵형 성을 추정할 수는 있으나 실험으로 재현이 불가능하므로 TTT 그림에 나타낼 수 없다. TTT 커브는 실험 광물학에서 실험적으로 결정할 수 있다. 광물을 특 정 온도에서 급냉시켜 그때 형성된 미세 구조를 전자현미경으로 관찰함 으로써 전이의 특칭을 연구하고 있다. 이같은 연구는 광물 암석의 열역 사 해석에 크게 기여하고 있다. (3) 고용체 광물 안에서 이온 반경과 원자가가 유사한 원자들이 상호 치환되어 무 질서한 고용체를 이루고 있다. 대부분의 광물에서 고용체의 구조는 특정 한 구조형 내에서 하나 또는 그 이상의 양이온이 무질서한 구조로 나타 나고있다. 고용체 는 원자 치 환에 의 한 고용체 (ato m ic substi tut io n soli d soluti on ) , 결손 고용체 (om iss io n al soli d soluti on ) , 간극 고용체 (int e r nal solid solu- tion ) 등의 종류가 있다. 치환 고용체에서는 원자의 이온반경과 원자가에 따라 유사한 것들이 치환되는 것으로 Fe2+( 0. 74A) 대신에 Mg 2+(0. 66 A), Si4 +(0. 40A) 대신 에 Al3+(o.39A) 가 치환된다. 감람석 [(Fe, M g )2S i 04) 의 경우 M g 2 S i 04 와 Fe2Si0 4 간의 고용체가 형성된다. 그 의에 치환이 쉬운 원소는 Na+ -Ca2+, Ba2+-ca2+, Mn2+-Fe2+, Mn4+ - Fe3+, Ca2+-Fe2+, Al3+-Fe3+, Al3+-Si4 + 등이 있다.
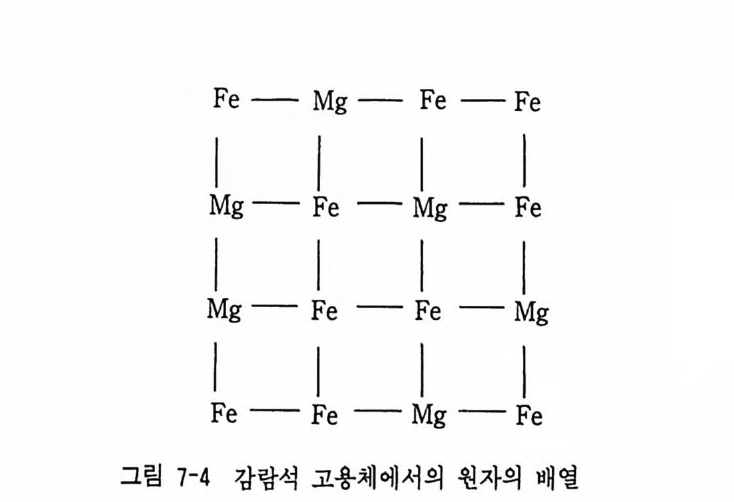 Fe—|IMFi— e ——F—F—ee—||F—F—ee— | F——e| —
Fe—|IMFi— e ——F—F—ee—||F—F—ee— | F——e| —
결손 고용체는 자류철석 (Fe1-xS), 뮬라이트 (mu llit e) 등의 광물에서 볼 수 있다. 뮬라이트의 경우 3Ah03 • 2Si0 2 -+ 2Al2 아 • Si0 2 성분 변화시에 2Si4 + + 02-;: :::=: 2Al3+ + D 에서와 같이 열역학적으로 고용체 형성시 자유에너지 변화와 광물 성분 의 혼합과의 관계가 있다. 감람석의 경우 Fe2S iQ 4 와 M g 2S iQ 4 의 단성분 이 혼합될 때 엔탈피 또는 내부에너지 변화, 엔트로피 변화, 자유에너지 변화를 G 혼합 =H 혼합 -TS 혼합 으로 표현할 수 있다. 그림 7-4 에서와 같은 간단한 Fe 와 M g의 혼합시 의 엔트로피의 변화를 생각하여 보자. 결정 내에 N 개의 원자가 N 위치 에 들어갈 수 있게 되어 있다면 Fe 의 원자가 들어갈 수 있는 수를 xN 이라할 때 M g의 원자가 들어갈 수 있는 수는 (1-x)N 이 된다. 여기서
x 는 0 과 1 사이의 값이다. xN 과 (l -x )N 개의 원자가 N 위치에 배열될 때 배열의 수는 배열의수= (xN ) ! [N(1!- x)N] ! 이고 이때 원자 배열 엔트로피 혼합 (4S) 은 원자 배열 엔트로피 (confi gura ti on al entr op y ) 로서 LJS =klog eW =klog e ~N! ! 로 표현할 수 있다. lo gJv =Nlo gJv -N 이라는 스터링 (St irli n g ) 이론을 도입하여 이 식을 간략화하면 LJS = -Nk{x lo g e W+ (l- x ) log e (1 - x) } 로 된다. 그림 7-4 에서와 같아 성분 x =0.5 에서 엔트로피 혼 합이 최대 가된다. 다음과 같이 고용체가 형성될 때 내부에너지와 엔탈피의 변화 를 생각 하여 보자. 감람석 광물 결정에 Fe 와 M g가 다음처럼 배열되어 있을 때 Fe— F e 결합의 Fe 원자들이 인접하는 반응 에너지를 VF e - F e 라 하고 M g - M g가 인접할 때의 반웅 에너지를 VM g -M g 로, Fe-M g이 서로 인접할 때의 반 웅 에너지를 祚 e- M g라 하자. 고용체 내에 임의의 어떤 원자 다음에 올 수 있는 Fe 원자의 수를 Zx 라 하면 Mg 원자의 수는 Z(l - x) 가 될 것이다. 전체 원자의 수가 N 개 일 때 Fe 원자는 xN 개가 되고 Mg 원자는 (1- x )N 개이므로 두 성분쌍 인 Fe-Fe 쌍, M g -M g쌍 Fe - M g쌍의 수는 다음과 같다.
1ZFe-Fe1= 2xNZx=NXx22 nM g -M g=了l (l ― x)NZ (1 -x) =NZ(E7x )2 1lFe-Mg = xNZ( l-x ) =NZx(l-x) 이때 두 원자의 혼합 에너지를 인접하는 원자와의 반응 에너지의 합으 로 가정하면 총에너지는 다음과 같이 계산된다. 총에너지 =~[x2 VFe-Fe+ (l-x)2 ¾18-Mg + 2x(1-x) 祚 e-Fe] =TZ[NxV Fe-Fe+ (1- X) V.'-lg- Mg +X (l-x) (2 VFe-Mg - VFe~Fe VMg -M g ) ] 가 된다. 처음 두 항은 순수한 단성분이 혼합되기 전의 에너지인 t1 NZx VFe-Fe 와
군1 NZ(l-x) Vr.18 -M& 이다. 세 번째 항인 군1 vZx(l-x) (2 VrH1 g-祚 e-Fe- VM g-Mg) 의 부호는 고용체의 에너지가 분리된 단성분의 에너지보다 높은지 또는 낮은지에 따라 다음과 같이 결정된다.2 Vre-Mg > 祚 e-Fe + VMs-Mg 인 경 우 H 혼합 >O 2 Vre-Mg < 祚 e-Fe + VMs-~18 인 경 우 H 혼합 < o 2 Vre-Mg = 祚 e-Fe + VMg -Mg 인 경 우 H!-=O 이때는 최대수의 Fe-Mg 결합의 질서 화합물을 형성하며 내부에너지 와 원자의 분포와 무관하다. 이 관계를 자유에너지 변화의 식 G(x) =H 혼합_ TS 혼합에 적용하면 G (x) =견ZN― [x 祚 e-Fe + (1-x) VMs-Ms + X (1-x) (2 祚 e-M g- Vre-Fe-V M g-Mg) ] -RT[xio g e X+ (1 ― x)lo g e(1 급)] 로 표현할 수 있다. 성분 (x) 와 에 너 지 좌표에 H 혼합과 TS 혼합에 대 하여 나타내 면 그림 7-5 와 갇다. 이 커브의 기울기는 껍합 0::1 _2x 당o:: lo g e(1 一 x) —l og eX 가된다. 성분 0 에서 1 까지에서 SH 흔단 1 기울기가 H 혼합의 기울기보다 훨씬 크 고 지유에너지의 변화는 엔트로피 항에 의해 좌우된다. 엔트로피 값은 고용체의 두 번째 성분의 낮은 농도에서도 항상 감소되고 있다. 이 사실 은 다른 원자와의 혼합 없이 순수한 단성분이 얻어지기 어려움을 의미한 다. 죽 적은 양의 불순 성분이 포함되면 자유에너지롤 낮추어 광물을 더 욱 안정하게 한다. 그립 7-5 에서 G(x) 값은 H 혼합 =O, H 혼합 <0, H 혼합 >O 의 경우를 나타낸 것으로 H 혼합 =0, H 혼합 <0 인 경우에 고용체의 자유에 너지 G(x) 는 언제나 분리된 단성분의 자유에너지보다 낮다. 따라서 고 용체는 항상 균질하게 잔류할 수 있게 된다. 그러나 H 혼합 >0 인 경우에
2
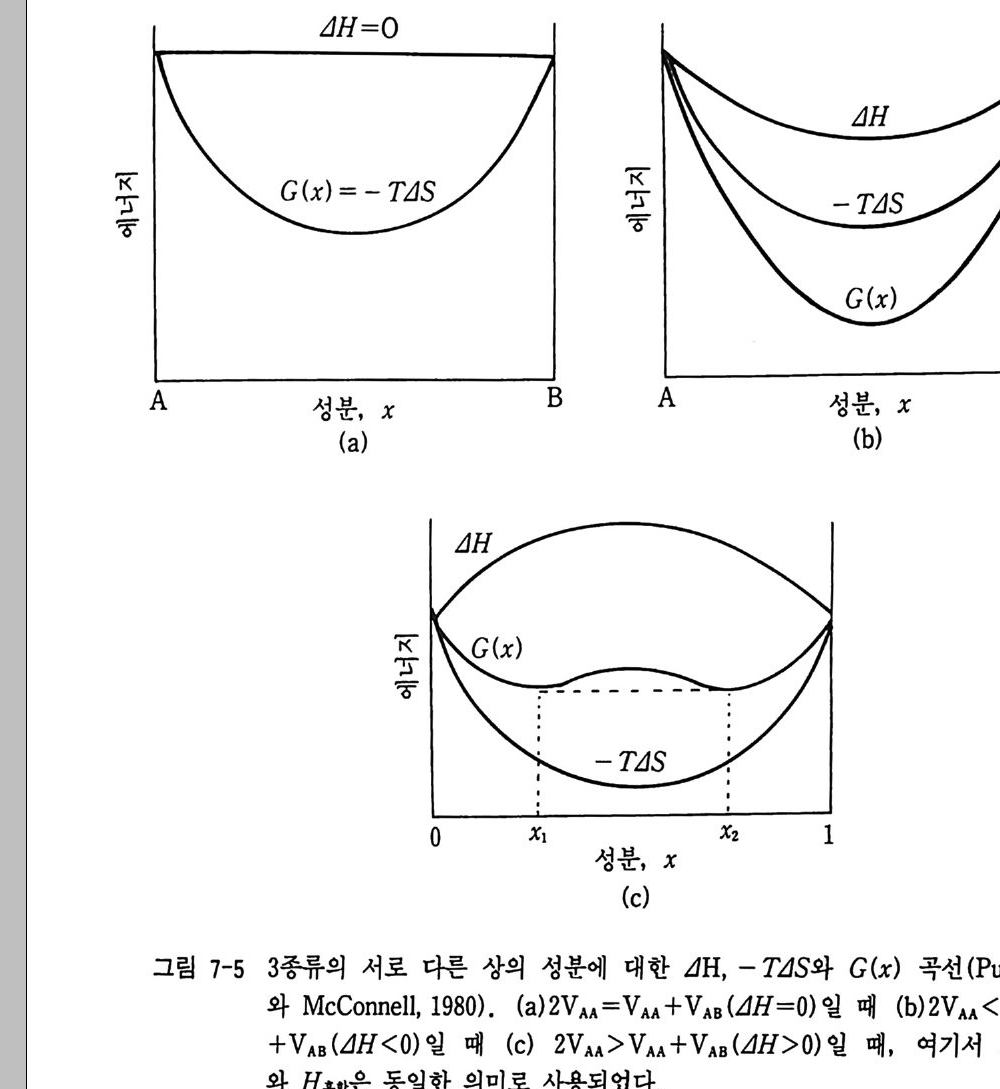 L1H=O
L1H=O
는 Fe-Mg 원자 사이에 견인 작용이 일어난댜 견인 작용이 강할 때 Fe 와 Mg 원자는 결정구조의 위치에 교대로 들어간다. 7-5(c) 에서처럼 H 혼합 >0 일 때 G(x) 의 값이 정(+)의 커브를 나타내기도 한다. 이때는 불혼합 (umn i x i n g)이 일어난다. 성분 x 가 0 에서 X1 까지와 X2 에서 1 까지는 고용체가 균질하게 잔류하지만 X1 과 X2 사이에는 원래 고용체가 균질이 었던 것이라도 불혼합이 되어 X1 성분과 X2 성분으로 분리된다. 이런 불혼 합 현상이 G-x 다이어그램과 T-x 다이어그램에서 온도 변화와 함께 단계적으로 진행되는 과정을 그림 7-6 에서 알 수 있다. 불혼합 현상은 암석학에서 알칼리 장석의 퍼사이트 조직의 형성, 규산염 마그마에서 철 산화물 광화 용액의 불혼화(분리) 현상 설명에도 대단히 유용한 과정이 다. 7-3 규산염 광물의 결정화학 Bra gg(l 930) 은 규산염 광물을 Si0 4 사면체 구조의 중합 방식에 따라 구분하였으며 그 후 Zolt ai( 19 60), Lie b au( 19 85) 등이 이를 발전시켰다. Bowen 의 불연속 반응 계열과 Si0 4 사면체의 결합 형태와의 관련성이 감람석 (독립사면체형) 一 휘석 (단쇄형) 一 각섬석 (복쇄형) 一 운모(충상구조 형) 一장석 (망상구조형)으로 나타나고 있다. Si0 4 사면체가 중합된 규산염 광물은 독립사면체형 (nesosil ica t es ), 복 사 면 체 형 (solosil ica te s ) , 쇄 상 구 조 형 (ino sil ica t es ) , 충 상 구 조 형 (ph y llo sil ica te s ) 및 망상구조형 (tec to s il ica t es ) 등의 구조형으로 구분된다. 독립사면체형은 Si0 4 사면체가 서로 연결되지 않고 M1, M2 위치에 양이온이 연결된 구조형으로 감람석이 그 예이다. 그림 7-7(a) 에서와같 이 감람석은 M1 위치에 Fe2+, M, j-+ 또는 Ca2+ 가 위치하여 M g 2S iQ 4( 마 그내슘-감람석), Fe2SiQ 4( 철-감람석), CaM g S i 04( 몬티셀라이트, monti ce l-
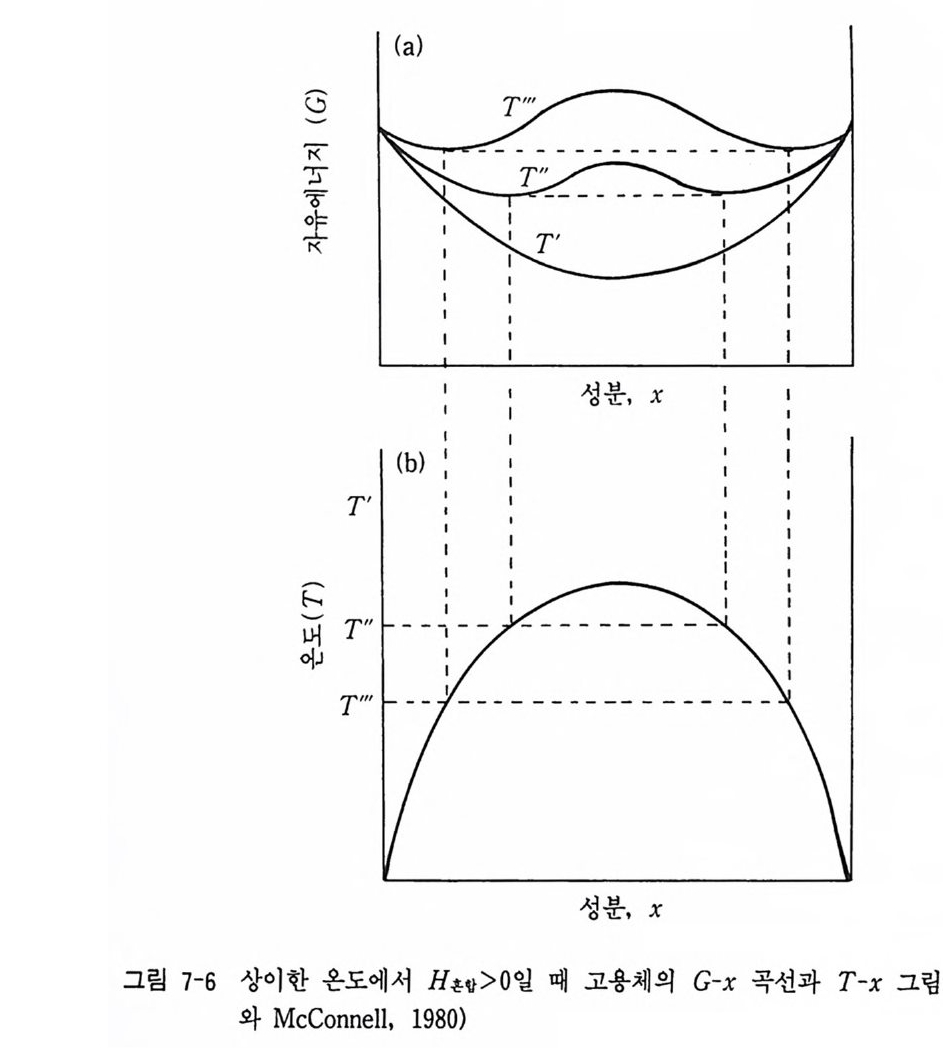 (a)
(a)
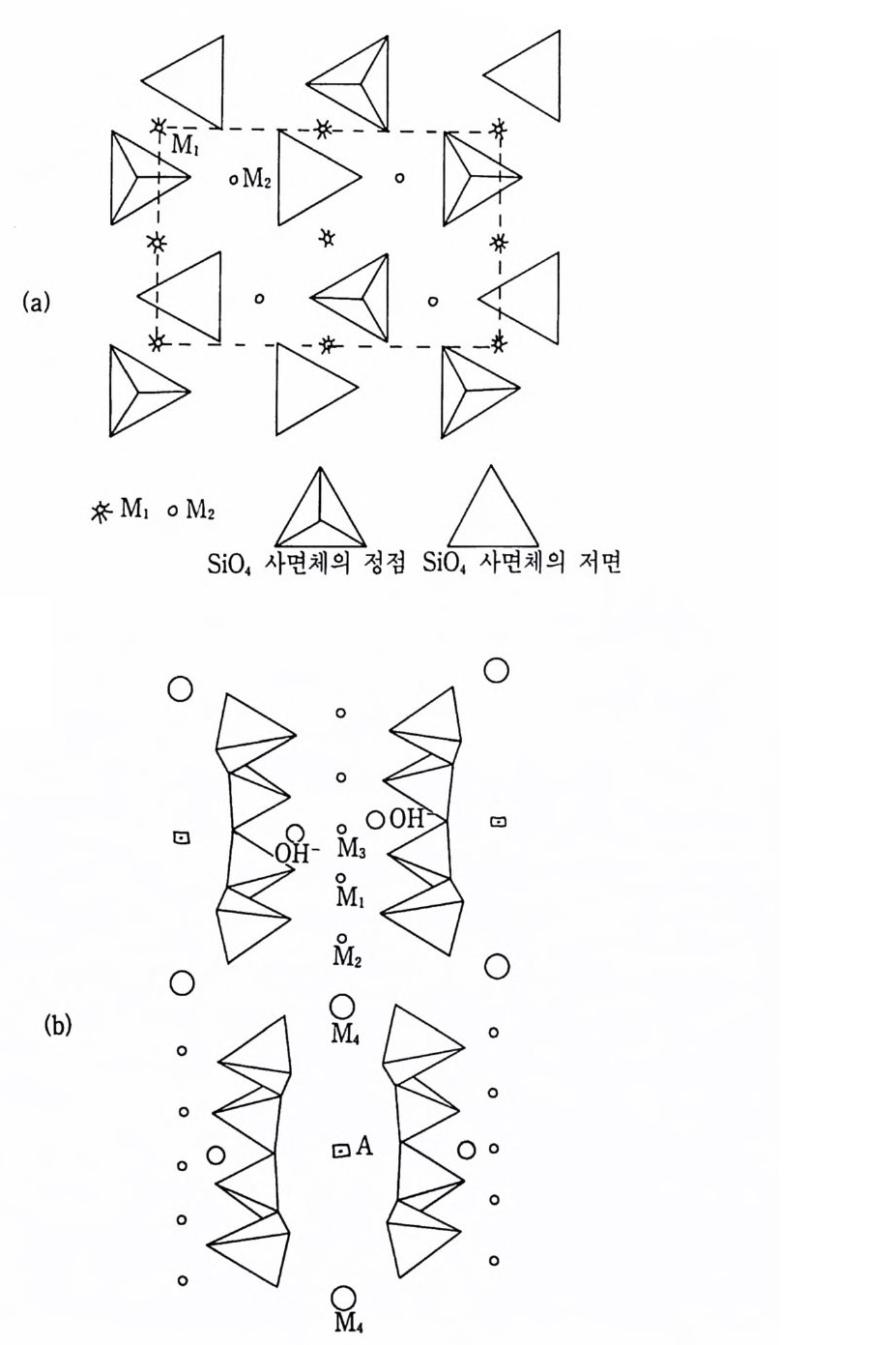 ;((-M , , M, 乙\ /\
;((-M , , M, 乙\ /\
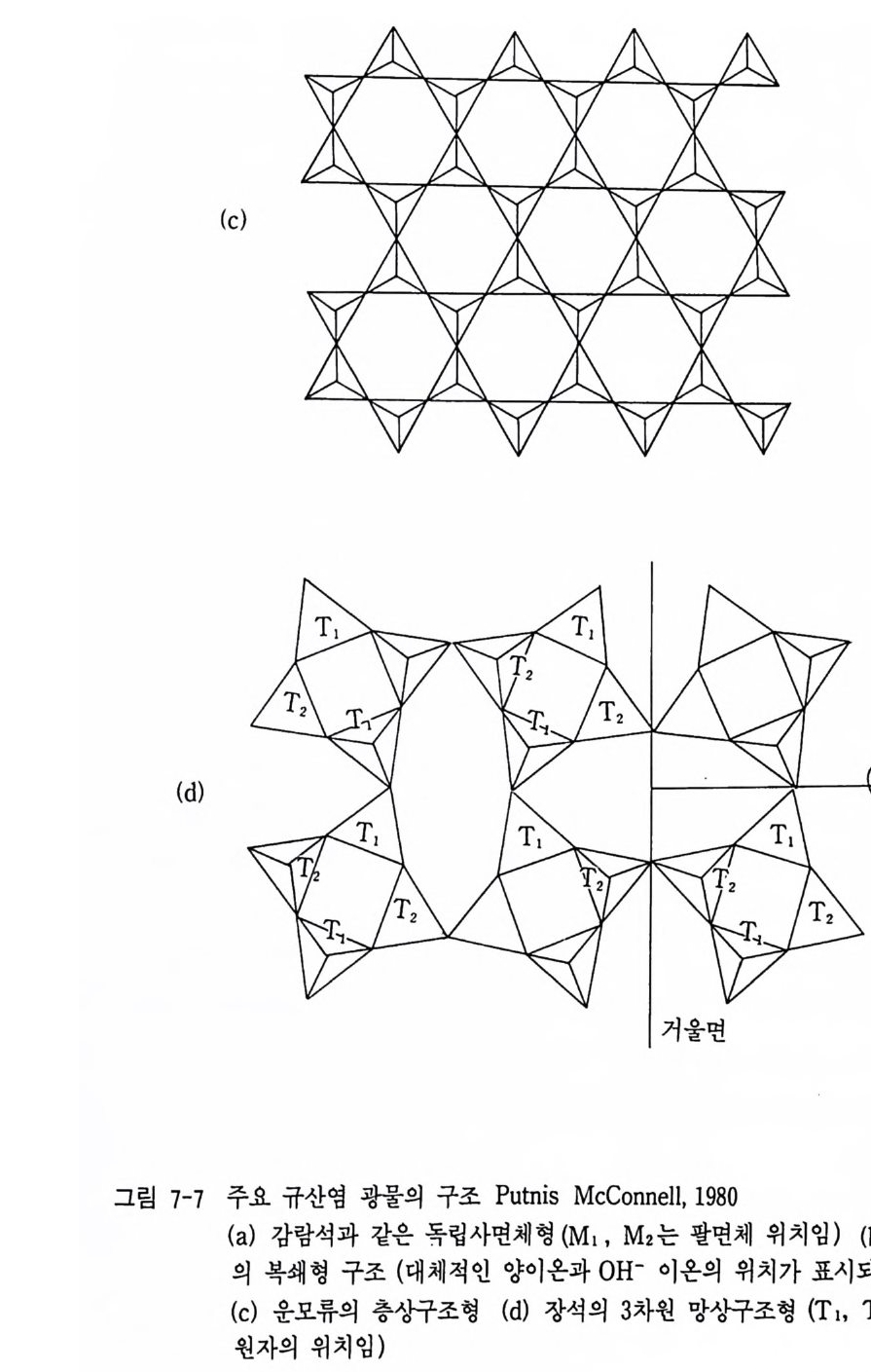 (c)
(c)
lite) 등을 만든다. Ca 함유 감람석은 M2 위치에 Ca2+ 이 둘어간다. 석류석, 저어콘, 규선석 등이 이 형에 속한다. 석류석의 경우 일반식은 A~+B 꾼 S i 3 아로 A~+=Ca2+, M 균, Fe2+ 또는 Mn2+ 이고, B: + 는 Al3+ ' Fe3+ 또는 Cr3+ 이 다. 석류석 광물은 그로슐라(gr ossular, Ca3Alz(S i O ◄ )3), 안드라다이트 (an dradit e, Ca3Fd+ (S i O ◄) 3) , 스페 서 틴 (sp es sar tine , Mn3Alz (S i O ◄) 3} , 알만딘 (almand ine , F~+Alz (S i O ◄) 3} , 파이 로프 (pyro p e, Mg 3A lz (S i O ◄) 3) , 우바로바 이트 (uvaro vit e, CaaCr2(S i O ◄ )a) 등이 있다. 석류석의 단위포 구조는 그림 7-8 과 같다.
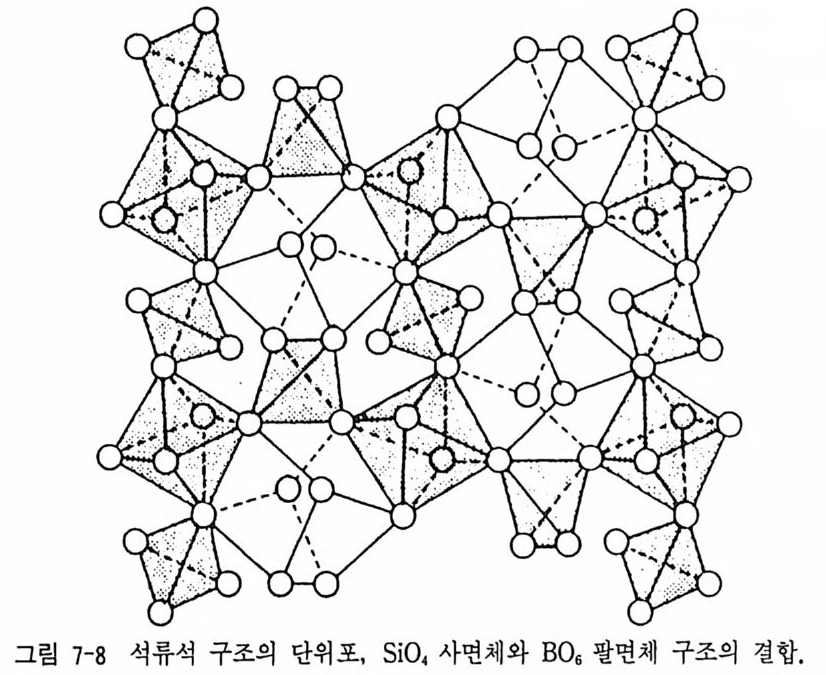 그립 7-8 석류석 구조의 단위포, Si0 4 사면체와 B06 팔면체 구조의 결합.
그립 7-8 석류석 구조의 단위포, Si0 4 사면체와 B06 팔면체 구조의 결합.
복사면체형은 24 개의 사면체가 한 정점을 공유하고 있으며 녹영석, 멜 리나이트 (me lli n it e) 등이 있다 쇄상구조형은 사면체가 2 개의 정점을 공유하면서 연결되는 단쇄형과
단쇄형 둘이 겹쳐진 복쇄형 구조가 있다. 휘석군 광물이 단쇄형에 속하 며 각섬석군 광물은 복쇄형에 속한다. 각섬석군 광물의 구조형은 그립 7-7 (b) 에 서 처 럼 OH- 를 가진 함수 광물이 다. 일반형은 wo_IX2KZ8%(OH, F)2 로서 W 위치에 Na, K 가, X 위치 에 Ca, Na, Fe2+ 또는 M g가, Y 위치에는 Mg , Fe2+ , Fe3+ , Al, Ti, Mn, Cr, Li, Zn이, Z 는 사면체 내의 Si, Al 이다. 각섬석의 화학식은 NaCa2Mg sS i1 0 22 (OH ) 2 이 며 트레 몰라이 트(t remo lit e) 는 Ca2Mg sS i a0 22 (O H) 2 이다. 운모충상류구가조 여형기 (에S i O s속 )n한2n다- .에 서일는반 충식이은 2 W차o원-1 적}';으_3로(Z4 0연10속) 된(O다H(, 그F)림2 이7며-7 ( cw)),. Y, Z 위치에 들어가는 원소에 따라 단성분이 다음 표 7-2 와 같이 결정 된다.
 표 7-2 운모군 광물의 각 원소의 위치
표 7-2 운모군 광물의 각 원소의 위치
망상구조형은 Si0 4 사면체가 3 차원적으로 연속 연결되는 형태로 장석, 석영 등이 3 차원 망상구조 규산염 광물(fr amework s ili ca t es) 이다. 그립 7-7(d) 는 장석의 구조형으로 사면체 내에 Si ” 대신 Al3+ 이, 그리고 격 자 간극에는 Na+, K+, Ca2+ , Ba2+ 이온 등이 채워져 있다. 새니딘 (KAlS i 3 아), 알바이트, 아놀사이트의 단성분이 있다. Haw t horne(1983) 은 규산염 광물의 구조는 높은 결합력을 가진 배위다 면체의 중합체에 따라 구조형태학적으로 구분할 수 있다는 가정을 하였 다. 그에 의하면 배위다면체 (coordi na ti on p ol y hedra) 의 배열의 결합 원칙 (bond balances) 은 S J >S&-1 인 경우에는 SJ (i=l, n) 에 의해 표현될 수
있으며 원자의 합이 SHS 『 < IV 음이온 |일 때는 중합(p ol y mer i za ti on) 이 만 들어질 수 있다. 그는 다양한 구조 단위 (str uc tu r al un it)들이 중합 양식에 따라 독립 배위다면체, 유한 클러스터 (fini te c luste r ), 유한 쇄상형, 유한 충상형, 유한 망상형 등으로 구분하고 화학양론적으로 사면체형은 M (Tfb 4 )< Pn , 팔면체형은 M(T fb 4) 2
라이 트 (sep iol it e) 와 팔리 고르스카이 트 (pa lyg o rskit e) 와 갇은 섬 유상 점 토 광물, 셋 째 , 알로팬 (allop ha ne) 과 감은 바 정 질 점토 광물 등으로 구분된 다. 충상 점토 광물은 Si0 4 사면체가 평면적으로 연결된 충상 규산염이다. 충상 규산염은 사면체 시트와 팔면체 시트가 합쳐져 1 : 1 층 또는 2 : 1 층 구조를 이루어 3 차원에서 중첩된 구조를 이룬다. 사면체 시트는 Si- 0 사면체가 2 차원적으로 망상으로 연결된 구조를 말하며 사면체 시트 (tet r a hedral shee t)와 Al-0 등의 팔면체의 망상 결합을 팔면체 시트 (octa h edral sheet) 라 한다. (2) 층상 규산염 점토 광물의 기본 구조와 화학 성분 I : I 형 점 토 광물과 2 : I 형 점 토 광물 카올리 나이 트 (kaolin it e ) , 디 카이 트 (dic k it e) , 내 크라이 트 (nacrite ) , 할로 이사이트 (hallo y s it e) 와 같은 카울린 광물군과 크리소타일 (ch ryso ti le), 리 자다이 트 Oiza rdit e) , 안티 고라이 트 (antig o rite ) , 그린 알라이 트 (gree nali te) 등의 사문석군 광물들이 대표적인 1 : 1 점토 광물이다. 1 : 1 층은 1 매의 사면체 시트와 1 매의 팔면체 시트 사이에 음이온을 공 유하므로 두 시트가 연결된 것이다. 그리고 1 매의 사면체 시트와 1 매의 팔면체 시트가 결합되면 2 매의 사면체 시트가 정점을 향해 합쳐져 2 매의 팔면체 시트를 포함하여 결합되는데 이를 2 : 1 층이라 한다(그림 7-9). 1 : 1 층이 반복 중첩되어 만들어진 구조를 1 : 1 형 구조 (2 층 구조)라 하 고 2 : 1 층이 중첩되어 기본 구조를 형성한 것을 2 : 1 형 구조 (3 층 구조)라 한다. 1 : 1 층은 2 팔면체 시트를 가지며 화학 성분은 AhS i 205(OH)4 이 다. 일반식은 X2~3(Si, A l) 20s(O H) 4 로 표현되며 X 에는 Al, Mg , Fe2+ 등이 들어간다. 팔면체 시트의 OH 기는 사면체의 정점 산소와 동일 평 면상에 위치하거나 팔면체 양이온의 의측에 위치한다.
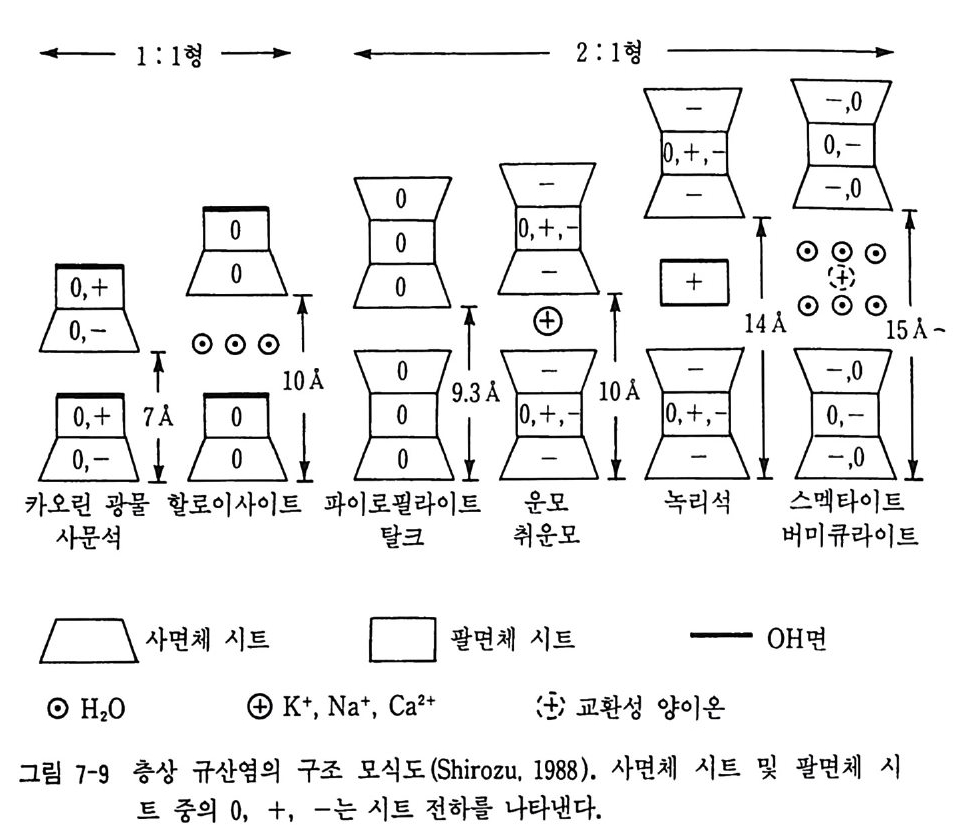 -1 : 1 형巴 ___+ 円빼 巴二2 : 1「 f형 f:i_홍:§「
-1 : 1 형巴 ___+ 円빼 巴二2 : 1「 f형 f:i_홍:§「
2 : 1 층의 일반식은 X2~3(Si, A l) ◄ O,o(O H) 12 로 OH 기는 내측의 것만으 로 1 : 1 층에서보다 그 수가 적다. 카울린 광물의 화학식은 AhSi2 0 6 (OH) 4 이며 사문석은 M g 3S i 2 야(OH) 4 이다. 카울린 광물층 사이에 1 매의 물 분자층이 있는 광물이 할로이 사이트 (Al2S i 206 (OH) r 2H20) 이 다. 이 물 분자는 탈수되기 쉬워 IOA 의 저면 간격이 탈수 후에 7.2A 으로 된다. 유기물 분자와 교환이 일어나 에틸렌글리콜 처리를 하면 저면 간 격이 11A 으로 팽창한다. 할로이사이트는 판상결정구조를 나타내지만 카 올리나이트는 판상구조이나 화학 성분은 동일하여 동질이상이지만 그 광 물들의 생성 환경에 차이가 있다•
사문석은 카울리나이트와 같이 1 : 1 형 충상 규산염 광물이지만 김사이 트 충이 부루사이트로 치환되어 있다. 따라서 사문석의 화학석에서 보면 사면체 시트에 S i와 0 의 특칭적인 비율을 가지고 있으며 팔면체 시트에 는 2 개의 Al3+ 가 3 개의 M 균에 의해 치환되어 +6 의 양전하를 가진다. 그린알라이트는 화학식이 Fe~ + S i 20s(O H) 4 로서 3 개의 Fe2+ 이온이 2 개 의 AI3+ 이온을 교대하고 있다. 2 : 1 형 광물의 대표적인 예는 파이로필라이트(pyr o p h llit e), 활석 (tal c), 스멕 타이 트 (smect ite) , 버 미 큘라이 트 (vermi cu li te) , 운모류 (mi ca ) , 녹니 석 (chlorite ) 등이 있다. 파이로필라이트는 AlzSi 40 10(OH )2 화학석으로 팔면체 시트와 사면체 시트에 이온의 치환을 허용하지 않는 2 : 1 형 광물의 기본 유형이다(표 7-3). 활석 은 Mg 3S i 40 10 (OH ) 2 로 3 개 의 M 군 이 온을 2 개 의 Al3+ 가 치 환하고 있다. 스맥타이트는 팔면체 시트 내의 Al3 + 의 부분 치환과 사면체 시트 내의 S i의 부분 치환으로 다양한 화학 성분을 가지는 다수의 광물종이 있다. 예를 들면 Al3 + 가 팔면체 시트에 위치할 때 세 위치 중에 두 위치에만 채워지기 때문에 2 팔면체 (d i oc t ahedral) 구조를 이루게 된다. Al3+ 가 Fe3+ 나 다른 3 가의 이온으로 치환되면 광물은 2 팔면체 구조로 유지되지만 2 개 의 Al3+ 이 온이 Fe2+, Mg 2+, Zn2+ 등과 같은 2 가의 3 개 이 온과 치 환 이 되면 팔면체 시트 중의 양이온이 채워질 세 위치가 모두 채워져 3 팔 면체 (trioc ta h edral) 광물이 된다. 이 기준에 의하면 파아로필라이트는 2 팔면체 광물이며 활석은 3 팔면체 광물이다. 스멕타이트 그룹 광물은 2 팔 면체 (몬모릴로나이트, 바이 델라이트, 논트로나이트) 과 3 팔면체 (사포나이트, 헥토라이트, 사우코나이트)가 있다. 이들은 충전하의 차이에 의해 구분할 수있다. 스멕타이트 그룹의 일부 광물의 화학식은 디옴괴· 같다.
 표 7-3 접토 광물에 관계 있는 층상 규산영의 분류 (AIPEA 명명위원회에 의함)
표 7-3 접토 광물에 관계 있는 층상 규산영의 분류 (AIPEA 명명위원회에 의함)
Mg -버 미 큘라이 트 [Mg o.a a ] 0+[Mg a ( Sb .a. Alo.7 7) 010 (OH) 2)0- 6 6-• 4. 5H20 몬모릴로나이 트 [ (Na, Ca112) 。 . 33 )0- 33+[ (Alo.1 1M g o.3 3) Si4 0 10 (OH) 2]0·33- 바이 델라이 트 [ (Na,_ C a112) 。 .33 )0- 33+[ (Ah (Aia .6 1Alo.33) 010 (O H ) 2]0·33- 사포나이 트 [ (Na, Ca112) 。 . 33]0 .3 3+[ (M g o 죠 (Sh .61 Alo.3 3) 010 (OH) 2]0·33-
이들 광물들은 대다수 충간수를 가지거나 몬모릴로나이트와 같이 물에 서 쉽게 양이온 교환이 일어난다. 이 때문에 충간의 간격이 변화하여 괭 창하는 특성을 가진다. 이와 같은 팽창성의 특성을 이용하여 버미큘라이 트 등은 균종 배양, 토양 계량, 원예, 건축 내장재, 방음제, 보온제, 경 량 골재, 흡착제 등으로 다양하게 이용되고 있다.
제 8 장 지각과 맨틀의 화학 성분 지구의 내부 구조는 지진파의 속도 변화에 의해 지각, 맨틀, 의핵, 내 핵으로 구분되었다. 심도 100~200km 내의에 지전파 속도가 감소하는 저 속도층 (Low veloc ity zone) 이 알려 져 이 지 역 의 물질 이 부분 용융과 현 무암질 마그마의 형성에 밀집한 관계가 있는 것으로 생각하고 있다. 지 구 내부의 구성 물질의 물성과 화학 성분은 탄성파의 특성에 의한 추정 과 심부에서 유래한 초염기성암이나 운석의 연구에서 추정하고 있다. 최 근 고온고압 합성 실험에서 맨틀 물질의 화학적 특칭이 규명되고 있다. 지각, 맨틀, 핵의 구성 광물과 화학 성분에 대하여 알아보자.
8-1 암석권의 구성 성분 (1) 지각의 화학 성분 지각은 크게 화강암질암으로 구성된 대륙 지각과 현무암질암(반려암질 암)으로 구성된 해양 지각으로 구분된다. 지각의 평균 화학 성분은 Poldervaart 0955) 와 Ronov 와 Yaroshevsky (1976) 에 의 해 계 산되 었 다. Ronov 와 Yaroshevsk y 0976) 는 지 각 구성 암석 의 광물 구성 비 율을 석 영 (12 )' 알칼리 장석 (12), 사장석 (39), 휘석 (11)' 운모류 (5), 각섬석류 (5), 감람석 (3)' 점토 광물 (5), 탄산염암 (2) 및 기타 부속 광물로 잡아 계산하였으며 그 결과는 표 8-1 과 같다. 대륙지각은 해양지각에 바하여 Si0 2 , K20 함량이 높고 Cao 는 낮다. 지 각 중의 천석 원소는 마그마 분 화의 후기 분화 산물에 부화되는 경향이 있어 대륙지각에 그 함량이 대 단히 높다. 이온 반경이 큰 천석원소 (LIL 원소)나 불호정 원소인 K, Rb, Cs, Sr, Ba, Y, REEs, Zr, Hf, Nb, Ta, W, Th, U 등은 큰 원자 부화 요소를 가지므로 지각에 다량 농집되어 있다. LREE 가 HREE 에 비해 지각에 더 부화되어 있다. 주성분 이의에도 미량원소는 암석 성인 해석에 중요한 지시자가 될 뿐만 아니라 지구상에서 일어난 지질학적 사건의 증거가 되기도 한다. 지각의 미량원소 중 Ir 은 지각에 국소량이 포함되 어 있으며 태 양계 물질의 1/12500· 밖에 포함되 어 있지 않다. 그런데 Alvarez 등 (1980) 에 의해 백악기-제 3 기 경계에서 Ir 의 부 화대가 발견되어 이 시기에 지구에 운석 충돌 사건이 있었음을 지지하고 있다. (2) 맨틀의 화학 성분 맨틀의 구성 암석은 주로 페리도타이트(p e ri do tit e) 와 에클로자이트
(eclo git e) 이다. 맨틀에서 온 킴버라이트 중의 포획암의 연구와 초고압 • 고온 실험 결과에 의하면 맨틀 암석은 주로 감람석 ((Mg , Fe)2S i O.) 과 사 방휘 석 ( (Mg , Fe) Si0 3 ) 으로 구성 되 어 있으며 소량의 단사휘 석 ( (Ca, Mg , Fe)2Sh06-NaAISh06) 와 석류석 ((Mg , Fe, Cah(Al, Fe3+, Cr)2Sb0,2) 등으로 구성되어 있는 것으로 추정하고 있다.
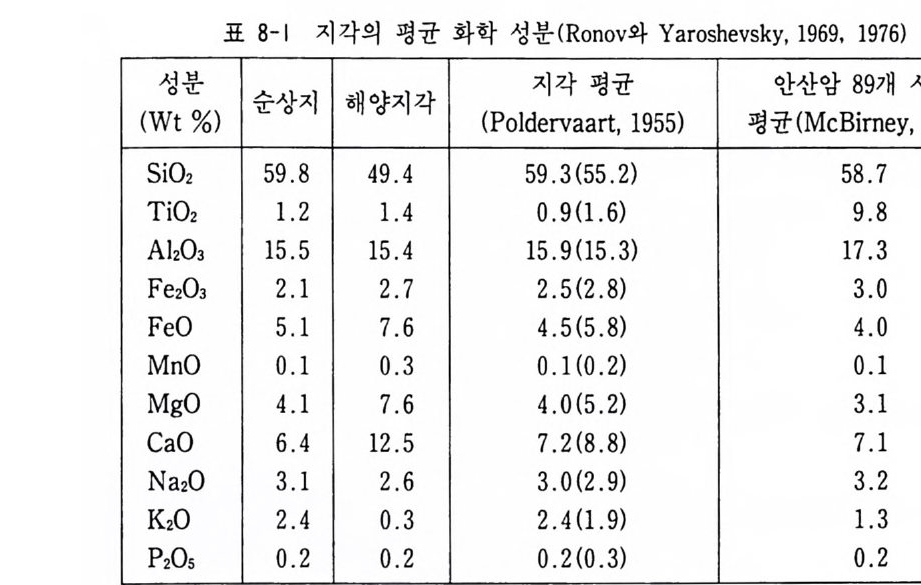 표 &l 지각의 평균 화학 성분(R onov 와 Yaroshevsky , 1 969. 1976)
표 &l 지각의 평균 화학 성분(R onov 와 Yaroshevsky , 1 969. 1976)
맨틀 물질을 대표하는 암석은 페리도타이트이다. 페리도타이트는 스피 넬예리도타이트와 석류석-페리도타이트의 2 가지 유형으로 구성된다. 스 피넬-페리도타이트는 M g-감람석 (60-70 %), 엔스타타이트 (10-30 %), 두 휘석 (diop s i d e , 8-12 %), Cr-A l 스피넬 (3-13 %) 등으로 구성되어 있으며 석류석-페리도타이트는 감람석 (48-67 %), 엔스타타이트 (28-47 %), 두휘 석 (~3 %), 파이로프(pyr o p e) -석류석 (2-5 %) 등으로 구성되어 있다. 주된 구성 광물아 감람석과 휘석이지만 소량으로 포함된 스피넬과 석 류석이 대단히 중요하다. 왜냐하면 다음 반응식에서처럼 초염기성암에서 사장석은 Al 을 가지는 저압상이지만 고압상인 스피넬과 석류석이 만들
어지기 때문이다. 2CaAbSbOs+2Mg 2S i0 4 一--+ CaMg Sb 06 • xCaAbSi0 6 (아놀사이트 )(M g- 감람석) (Al-단 사휘석) +2Mg S i0 3 • xMg A bSi0 6 + (l-x )CaAbSb06 (Al-사 방휘석) 아놀사이트(잔류) + (l-x) Mg A b04 _--+ 2CaMg 2A '2 S b012 (스피넬) (석류석) 페리도타이트 포획암의 화학 성분과 맨틀의 평균 성분은 표 8 - 2 와 같 다.
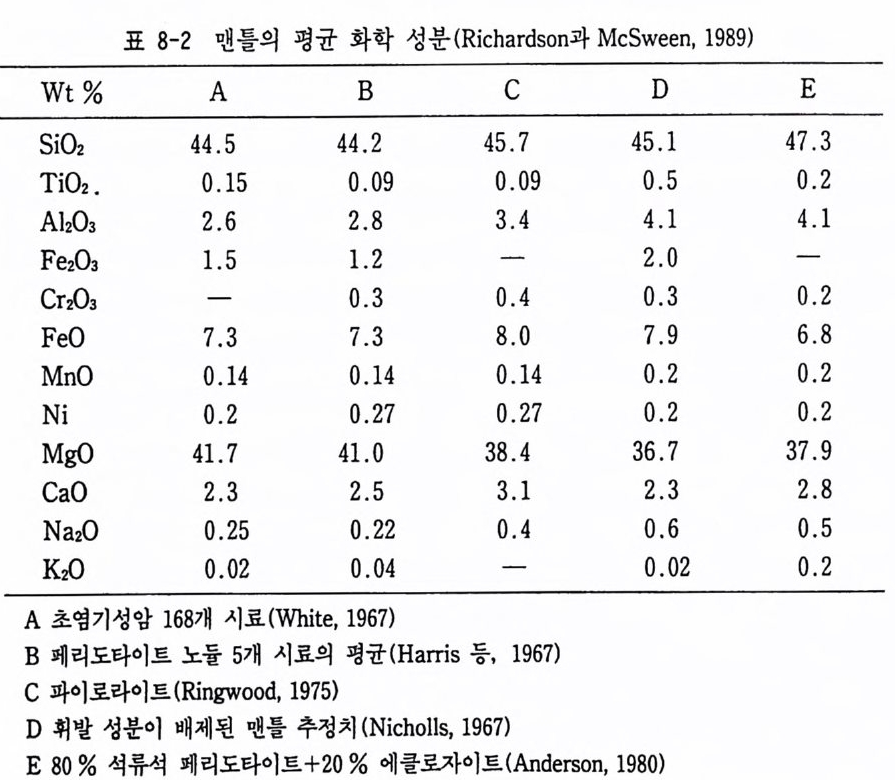 표 8-2 맨 틀 의 평균 화학 성분 (R i chardson 과 McSween, 1989)
표 8-2 맨 틀 의 평균 화학 성분 (R i chardson 과 McSween, 1989)
맨틀 화학 성분을 추정할 때 현무암질 마그마 형성시에 이미 Ca, Al
이 사용되었기 때문에 스피넬이나 석류석을 가지지 않는 페리도타이트와 현무암질 멜트를 계속 형성할 수 있는 페리도타이트의 비율을 결정하기 가 어렵다. 그래서 R i n gw ood(1962) 는 원시 맨틀 물질이 휘석과 감람석 으로 구성된 파이로라이트(py rol it e) 모델을 제안하였다. 그는 페리도타 이트와 현무암의 비율을 3 : 1 로 잡고 맨틀의 평균 화학 성분을 추정하였 다. 그리고 현무암은 마그마의 형태로 맨틀에서 유출되어 베니오프대에 서 에클로자이트 형태로 유입되기 때문에 에클로자이트와 페리도타이트 의 혼합된 모델을 Anderson0980) 이 제안하였다(표 8-2). Rin g w o od (1975) 는 맨들의 심도에 따른 광물의 상전이를 제안하였다(그립 8-1). 모 호불연속면 아래의 저속도충에서 지진파 속도 감소와 밀도 변화는 부분 용융 때문으로 해석하고 있다• 상부 맨틀은 감람석, 사방휘석, 단사휘 석, 석류석 등으로 구성되어 있다. 그러나 300km 와 400km 심도에서 각각 휘석 一 석류석 一 감람석 一 8 감람석으로 상전이가 일어난다. 그리 고 650-750 km 에서 r 감람석이 페리클레이스(p er ic lase), 스티쇼바이트 (sti sh ovit e, S i 02) 로 상전이되며 M g-석류석이 일메나이트 구조로 변하게 된다. 이보다 더 하부에서는 페리클레이스, 스티쇼바이트, 일메나이트, 페로브스카이트 (pe rovskit e, (Ca, Fe) Si0 3 ) 가 안정 하다. 멘틀 물질은 광물 학적으로나 화학적으로 대단히 복잡하다. 일반적으로 맨틀 기원의 중앙 해령 현무암 (MORB) 은 해양성 현무암에서보다 불호정 원소가 결핍되어 있다. 또한 87Sr/86Sr, 206Pb/204Pb 동위원소비도 맨틀 기원의 현무암질암 내에서도 현저하게 다르다. 이갇은 사실은 모두 맨틀 내의 물질의 불균 질성 (mantl e he t ero g en ity)울 말해 주고 있다. (3) 핵의 화학 성분 핵은 액체상인 의핵과 고체상인 내핵으로 구분되며 주로 운석에 근거 하여 Fe-Ni 합금으로 구성되어 있을 것으로 추정하고 있다. Rin gwo od
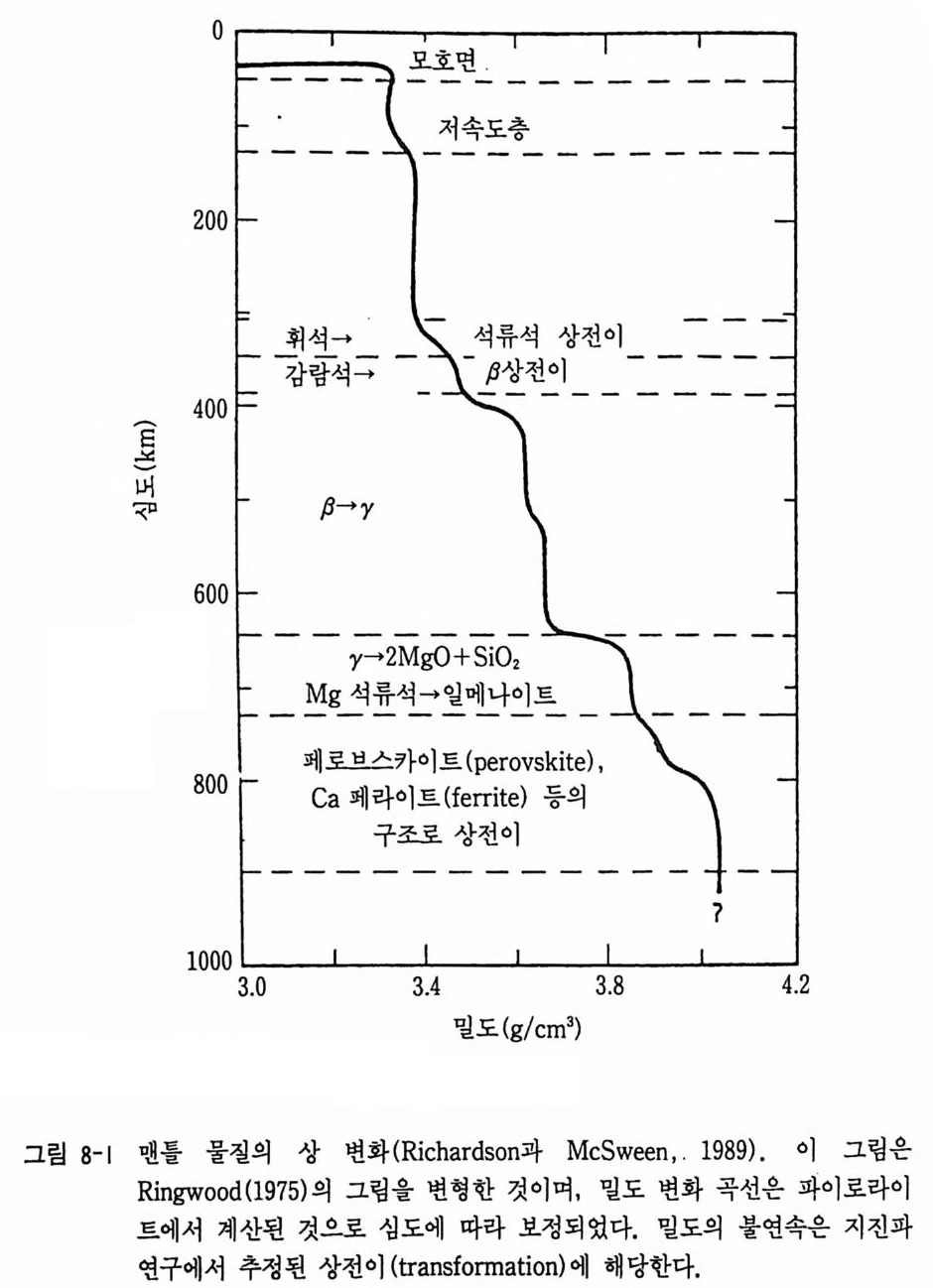 。
。
(1 966) 는 Fe-Ni 합금에 S i가 혼재되어 있음을 주장하였으나 Mu rt h y와 Hall0970) 은 Si 대신에 운석 중에 S 가 2 % 함유되어 있으므로 S 가 혼 재되어 0, H 와 함께 밀도를 낮추는 역할을 한 것으로 추정하고 있다(표 8-3).
 표 8-3 핵의 화학 성분 (Ms t suo, 1989)
표 8-3 핵의 화학 성분 (Ms t suo, 1989)
8-2 지각과 맨틀의 상호 반응과 진화 판구조 운동에 의하면 중앙해령이나 열점 (ho t s p o t)에서는 맨틀에서 부 분 용융된 마그마가 상승하면서 지각 물질과 상호 반응하게 되며 섭입대 (subducti on zone) 에 서는 해 양지 각 물질이 해 양 퇴 적물과 함께 맨틀로 섭 입되어 맨틀 물질과 상호 반응하게 된다. H, C, 0, S, Ne, Ar, Kr, Xe 등과 갇은 휘 발 원소들의 재순환이 지각 맨틀 진화에 중요한 역할을 할 수 있다. 지구 내부에서 이들 원소 둘이 해양이나 대기로 탈가스되기도 하고 일부는 암석권에 포획되어 탄 산염 광물, 각섬석, 황화 광물 등을 형성하기도 한다. 또한 해저에서 황
화 광물이나 탄산염 패각 및 퇴적물을 만들게 된다. 섭입대에서 해양 되 적물은 다시 맨틀로 되돌아가게 되어 지각과 맨틀 물질 간에 순환이 일 어난다. 그러나 많은 지구화학자들은 정상 상태에서 비가역적인 진화를 주장하고 있다. Di ck i nson 과 Lu t hU971) 와 Gas t 0972) 는 맨틀의 70 %가 비가역으로 진화된다고 주장하고 있다. 즉 일단 형성된 화강암질 대륙 지각은 다시 섭입되기에는 밀도가 너무 낮다는 것이다. 일단 대륙 지각 이 형성되면 지표에 그대로 잔존하게 된다는 것이다. 판구조 운동에 의해 지각 물질이 순환하고 있음에도 불구하고 대부분 의 순상지의 변성암류의 지질시대가 20~35 억 년이며 그린란드의 이수아 (Isua) 지역 퇴적 기원의 편마암에서 38 억 년의 절대연령이 얻어져 38 억 년전에 이미 지구상에 해양이 존재하였음을 의미하고 있다. 오스트레일 리아 나레마운틴 (M t. Narrye r ) 지역 변성퇴적암 중의 저어콘에서 41~42 억 년 절대연령 (Froude 등 , 1983) 아 보고되어 42 억 년 전에 이미 대륙지각이 존재하였음을 암시하여 주고 있다. 맨틀 기원의 초염기성 포 획암의 연령이 10~30 억 년으로 얻어졌으며, 킴버라이트 중의 다이아몬 드 내의 포유물을 사용한 연령 측정에서 약 30 억 년이 보고되어 있다 (Rich ardson 등, 1984) . 따라서 이들 시료를 포함하고 있던 리소스피 어 는 적어도 30 억 년전에 이미 형성되어 있었을 것으로 추정된다. 맨틀과 핵 의 분리 시기는 38 억 년전 그린란드의 변성암이 지구 자장을 가지는 점 에서 38 억 년전에 이미 자장 형성이 가능한 액체의 핵이 분리, 존재하였 음을 의미하고 있다. 지각과 멘틀 물질의 기원과 진화 연구에 스트론튬 (“Sr/ 8 6Sr), 네오디뮴 (143Nd/1«Nd), 납 (206Pb/204Pb) 등의 동위원소비가 많이 이용되고 있다. 암 석 광물 중의 87Sr 은 87Rb(A=1 . 42X10 - ll/ 년)이 방사성 붕괴되어 생성된 87Sr 에 지구 물질이 원래부터 가지고 있던 초생기원의 87Sr 이 포함되어 있 다. 태양계 초기물질은 87Sr/86Sr 비가 대단히 균일하였다. 예를 들면 현무암질 에이콘드라이트 운석 (basaltic achond rite best ini t ial, BABI) 은
0 . 69897 土 0.00003 으로 대단히 균일하여 이 값은 태양계 형성 초기 성운 의 동위원소 값으로 잡고 있다. 맨틀 기원인 현무암은 87Sr/86Sr 의 초생 치가 비교적 균일하였으나 지질시대가 젊어침에 따라 약간 값이 커지고 있는데 대륙 지각 물질에 비해서는 균일한 값을 가진다. 지각의 화강암 질 암석에는 Sr 보다 Rb 이 부화되어 있어 지구 역사 초기로부터 Sr 동위 원소 전화가 일어났다(그림 8-2 ) . 그림에서 보면 대륙지각의 87Sr/86Sr 동 위원소 성분은 대단히 불균일한 특칭을 가지며 지각의 다양한 암석에서 도 그 성 인에 따라 87Sr/86Sr 동위 원소비 가 다르다.
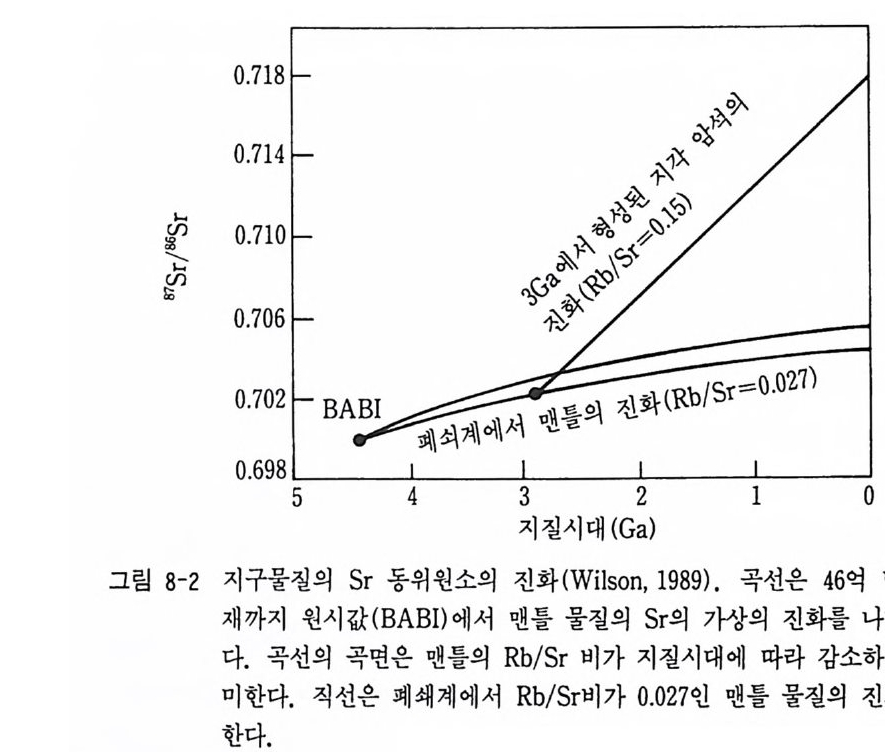 0.718
0.718
87Sr 은 87Rb 의 방사성 붕괴 산물이므로 지 질시 대 가 젊 어 짐 에 따라 87Sr/86Sr 비는 증가한다. 맨틀에서보다 지각에는 알칼리 금속이 많이 포
함되어 있기 때문에 Rb/Sr 함량이 맨틀에서보다 높다. 그리고 14aNd 은 wsm 이 방사성 붕괴로 만들어 진 것 이 기 때문에 87Sr 과 경 향이 유사하며 !43Nd/144Nd 연대와 함께 증가한다. Sm 과 Nd 은 희토류 원소로 화학적 특성이 대단히 유사하기 때문에 변성작용과 같은 지질학적인 사전 변화 에도 물질 내에서 원소가 교란되지 않고 일정하게 보존되기 때문에 운석 의 14aNd/144Nd 값이 지구 전체의 값을 대표할 수 있다. 따라서 시료 중 의 l“Nd/1Nd 이 지구 전체의 14aNd / 144Nd 값에 얼마나 차이가 나 는 지 를 c N d 로 다음과 갇이 표현하고 있다. CNd = [ ((l1“4NaNdd/1/14N4Ndd)) C 시HU료 R -l] x 104 여 기 서 CHUR (chondriti c unif orm reservoir ) 는 콘드라이 트질 평 균값이 다. 시료가 지구 평균값보다 Sm/Nd 이 높은 지역에서 만들어전 것이라면 143Nd/144Nd 값이 커 져 €Nd 값은 큰 값을 가지 게 될 것 이 다. Sm 과 Nd 의 화학적 특성은 유사하지만 맨틀 물질이 부분 용융되어 마그마가 형성되 는 과정에서 이들 원소의 원소 분별이 일어난다. 즉 이온 반경이 약간 큰 Nd 이 Sm 보다 액체상인 마그마에 더 많이 농집된다. Rb, Sr 에서도 이온 반경이 큰 Rb 이 Sr 보다 마그마에 우선적으로 농집된다. 따라서 마 그마 형성 후 잔류 맨틀 내에는 Nd, Rb 이 상대적으로 감소하게 되어 지구 전체의 평균 14aNd/144Nd 값보다 잔류 맨틀의 14aNd/ 1 44Nd 값은 증가 하고 87Sr/86Sr 값은 감소하게 된다. 따라서 MORB의 위치가 14aNd/144Nd -87Sr/86 S r 그림에서 €Nd=-0.36csr 의 부의 직선적인 상관성을 나타낸 다. 이를 맨틀 배열선 (man t le arra y)이라 한다. 그림 4-7 에서와 갇이 MORB 와 대부분의 현무암이 결핍 맨틀 (de p le t ed man t le) 에서 유래한 것 이며 케르구엘렌 (Ker gu elen) 해양섬의 현무암이나 콜롬비아 리버프라토 우 현무암과 갑은 대륙 지역 현무암은 맨틀 배열선 이의 지역에 도시된
다. 결핍 맨틀이란 맨틀에서 부분 용융에 의해 MORB 등 현무암과 칼은 화산암류를 형성하여 지각을 만들게 되면 남은 잔류 맨틀에는 Rb, Nd 등이 상대적으로 결핍되어 있게 되는데 이같이 Rb, Nd 이 결핍된 맨틀 영역을 말한다. 한편, 미분화 상태의 지구(c. Nd =O) 나 미분화의 지구에서 보다 Rb, Nd 이 더 농집 되 어 있는 영 역 을 〈 부화 맨틀 (enric h ed mantl e) > 이라 하여 네오디뮴이 지각과 맨틀의 상보적인 저장소 (reservo i r) 로 동위 원소 진화 곡선을 해석하고 있다(그림 8-3 ). 그림에서 하부 맨틀 CNd = O 와 상부 맨 틀 의 C. N d =+ 12 로 구분했을 때 하부 맨틀은 형성 후 원시 상 태로 그대로 유지된 곳이며 상부 맨틀은 판구조 운동에 의해 물질의 순 환이 일어나는 곳이다. 상부 맨틀의 + l2c N d 와 — l5 c. N d 값이 균형을 이루 며 기타의 지구조 지역에서 산출되는 해양 현무암은 두 맨틀 물질의 혼 합으로 보고 있다. Wasserbur g와 DePaolo(1979) 는 이같이 현무암들이 상이한 Nd 동위 원소 값을 가지는 것은 총상 맨틀의 용융 과정의 차이에 기인하는 것으 로 추정하였다. 그러나 Menz i es (1 983) 에 의하면 대륙 지각 하부의 리소 스페어 (subconti ne nta l lith os p here) 에서 스피넬-석류석 레르조라이트 포획 암(l herzo lit e xeno lith)의 동위원소 자료도 MORB 와 겹쳐져 이들 역시 부 화 맨틀 저 장소 (enrich ed mantl e r eservoir ) 로 생 각하고 있다. Zin d ler 등 (1982) 은 Nd— S r— P b 동위원소를 함께 고려하고
(conta m ina ti on ) 에 의 한 암석 성 인 해 석 을 하고 있다.
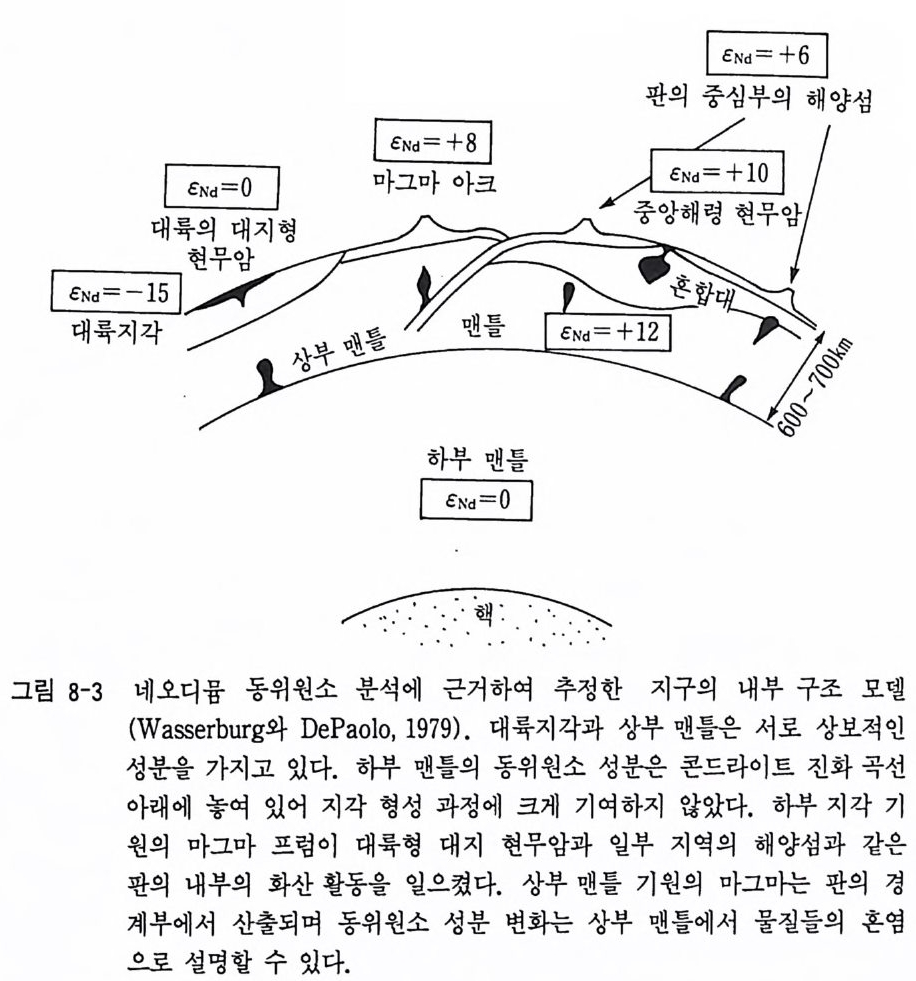 판의 중巳심부의 해 양섬
판의 중巳심부의 해 양섬
지 각 물질의 143Nd/144Nd, s1sr/s6Sr, 206Pb/2 0 4Pb 동위 원소비 모두가 지 질시대가 젊어짐에 따라 원시값에서 그 값이 증가하고 있다. 이둘 동위 원소 성분은 태양계 초기물질에서 다양한 지각의 물질로 진화되고 있음 울찰보여주고있다.
8-3 마그마의 기원 판구조 모델에 의하면 마그마의 생성은 공간적으로 첫째, 중앙 해령과 감이 판이 갈라지는 경계에서 부분 용융에 의해 현무암질 마그마가 발생 하고, 둘째, 판이 수령하는 베니오프대에서 화강암질 마그마나 안산암질 마그마를 형성하며, 셋째, 판의 내부에 위치한 열점 (ho t s po t)에서는 맨 톨 열류의 상승에 의해 하와이 군도의 화산섬 형성과 같은 현무암질 마 그마가 생성되고 있다(그림 8-5). 즉 마그마는 상부 맨틀이나 하부 지각 물질이 부분 용융(p a rti al fu s i on) 되어 지표로 분출하거나 지하에서 결정 분화된다. 마그마의 부분 용융시 기원 물질의 종류나 용융 정도와 압력 등에 따
I As E면GA•. . I R 疆疆疆副疆 PNm/PNm 그립 8-4 해령과 해양성의 현무암의 206Pb/2 ° 'Pb, 143Nd/1Nd, 87Sr/86Sr 동위원소 비 의 3 차원 도시 (Zin d ler 등, 1982)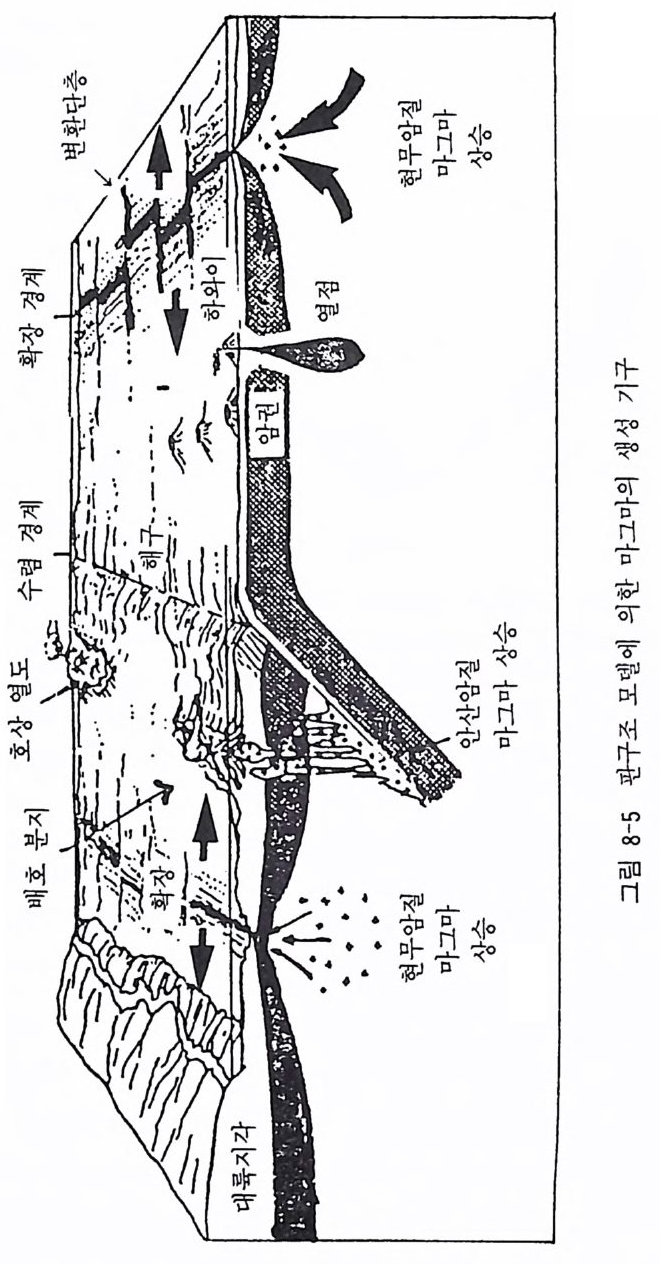 ·J종 마W해양{ P。며{{ -“치- <
·J종 마W해양{ P。며{{ -“치- <
라 다양한 마그마를 만들게 된다. 상부 맨틀이나 하부 지각에서 부분 용 융에 의해 생성된 마그마가 상승 도중 마그마 방에서 주위 암석과 동화 (ass i m il a ti on) 되거나 상이한 마그마와 혼합됨으로써 마그마의 성분이 변 화된다. 형성된 마그마는 분별 결정 작용에 의해 초염기성암에서 산성암 에 이르기까지 다양한 화성암울 형성하게 된다. (1) 상부 맨틀에서의 부분 용융 지진파의 복성과 고압 고온 합성 실험 및 현무암질 암석의 산출 상태 등을 종합하면 현무암질 마그마는 감람석, 휘석, 스피넬 또는 석류석과 같은 고알루마늄상의 광물의 부분 용융 산물임을 지지해 주고 있다. M ysen 과 Kush i ro (1 977) 와 Kush i ro(1994) 의 페리도타이트의 부분 용융 실험에 의하면 10 kbar 와 15 kbar 에서 사장석, 석류석, 스피넬 등이 12oo·c 에 서부터 용융하기 시 작하여 액상의 마그마를 생 성 하여 단사휘 석 (Cp x) , 사방휘석 (Op x) 순으로 용융이 진행되었다. 부분 용융의 정도가 변화되면 마그마의 성분도 변하게 된다. 부분 용융 정도가 동일하여도 압력이 다르면 마그마의 성분이 변화된다(그림 8-6). 상부 맨틀에서 부분 용융으로 형성된 마그마는 마그마의 고결 과정에 서 마그마의 분리 상승, 마그마 방에서의 동화 등에 의해 다양한 과정으 로 그 성분이 변화하게 된다(그림 8-7 ) . 부분 용융 과정에는 평형 용융(equili br i um fu s i on) 과 분별 용융 (frac ti on ati on al fus io n ) 이 있다. 평형 용융 과정 부분 용융되어 형성된 멜트와 잔류 결정 사이에 평형이 계속 유지되면 서 생성된 마그마액은 모암과 항상 평형상태에서 접하고 있다 . 그림 8-8 에서 암석 성분 X(A 40 %, B 30 %, C 30 %)가 부분 용융되어 최초로
형성된 멜트는 E1 성분의 액은 a, b, c 상의 고체 광물과 접하여 평형 에 있게 된다. 최초의 용융은 공융점 (1150°C) 에서 시작되어 b 상이 먼저 용융 소진되고 온도가 상승하면 Y 점의 온도에 이를 때까지 액의 성분은 a+c+ 액 공융점 쪽으로 이동한다. E1 과 Y 구간의 온도에서 c 상이 액 속에 용해되고 마지막 c 상이 Y 점에서 소진된다. 온도가 계속 상승되면 (Y 점의 온도에서 X 점의 온도까지) 고체인 상이 액에서 용해되어 온도 1250 · c 가 될 때까지 성분 X 안 마그마가 형성된다.
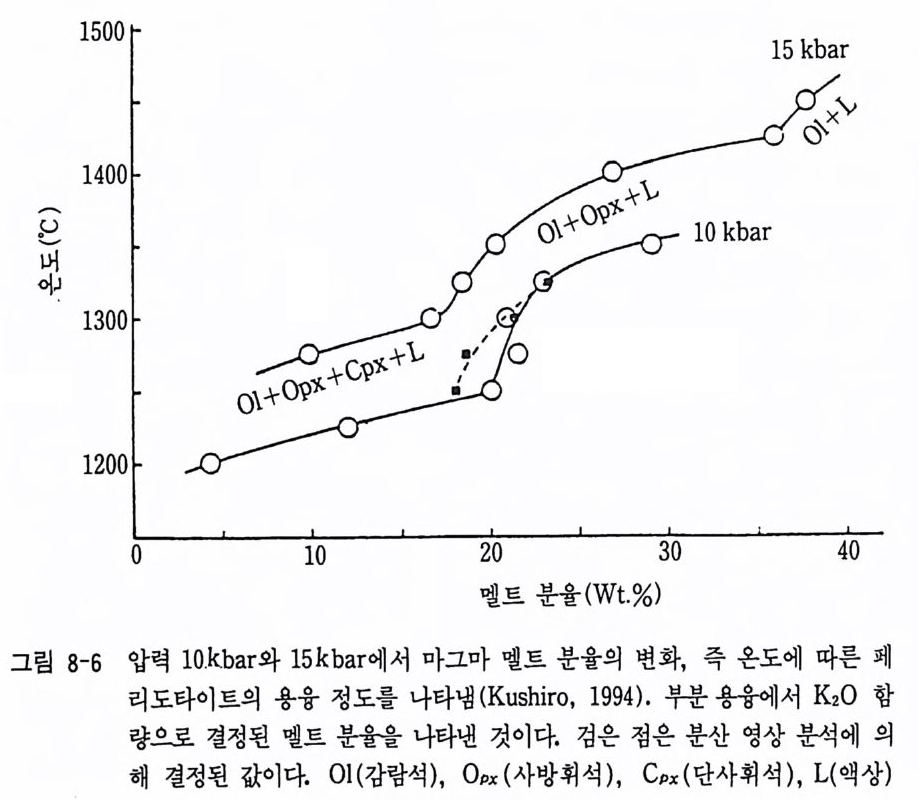 1500 15 kbar
1500 15 kbar
분벌 용융 과정 마그마 형성 과정에 가장 많이 적용되는 메커니즘이다. 마그마 멜트가
형성된 후 곧 모암인 암석에서 액이 제거되어져 마그마의 형성 온도나 형성 단계에 따라 마그마의 성분이 불연속적으로 변화하는 과정이다. 예 룰 들면 그림 8 - 8 에서 X 성분의 광물상 a, b, c 가 공융점 E1 에서 액의 성분 E,(A 19 %, B 50 %, C 31 %)인 마그마가 형성되며 곧 액은 잔류 결정만 남기고 이동되어 버린다. E1 의 멜트 내에 b 상(B 성분)이 모두 소전될 때까지 멜트화되면서 액은 계속하여 없어진다. B 성분이 E1 의 기본 성분이기 때문에 B 성분이 모두 사용된 후에는 더 이상 멜트가 형 성될 수 없다. 이 단계에서 원래 암석 질량의 50 % 정도가 멜트로 만들 어져 없어지고 남은 고체상의 성분은 E1 점을 떠나 X 점 (A 39%, B 31 %, C 30 %)에서 X' 점 방향으로 이동된다(그림 8-8).
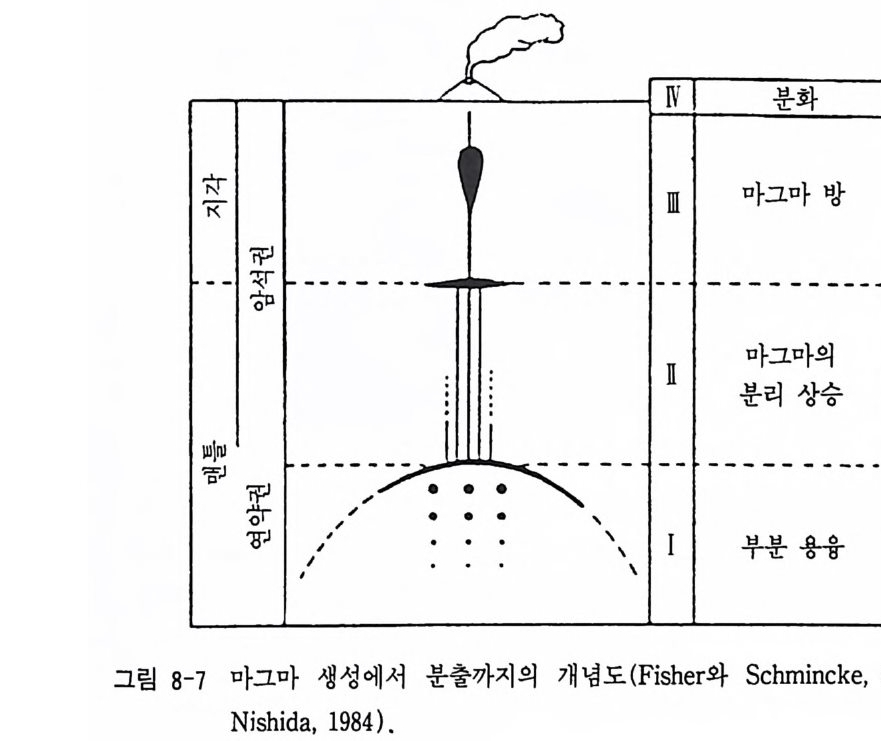 古下-- 더 ------- y’- --- -- T二-- -방------ --
古下-- 더 ------- y’- --- -- T二-- -방------ --
온도가 계속 상승되어 A, B 2 성분 공융계에서 공융 온도 k 에 이를
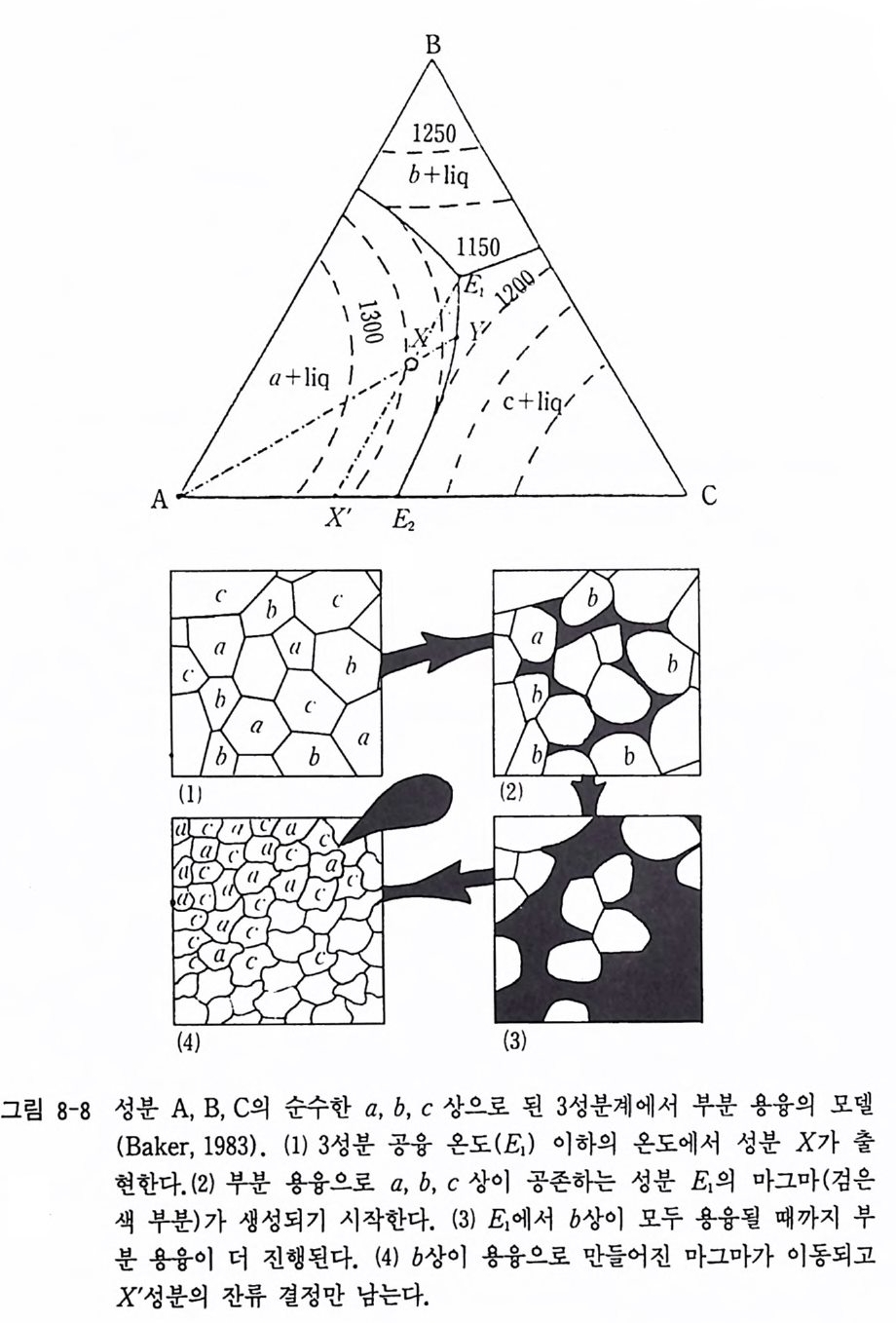 B
B
때까지는 멜트가 형성되지 않는다. k 점 온도에 이르면 멜트의 성분인 A 30. 4 % , B 69. 6 % 가 생성되며 생성되자마자 곧 이동되어 고체상의 잔 류상의 성분은 k 에서부터 순수한 A 로 변화된다. 계에서 약 63% 가 액 k 로서 제거되었을 때 남은 고체상은 순수한 A 성분이다. 1350·c 의 온 도에 이룰 때까지 멜트화되지 않는다. 따라서 순수한 A 성분의 고체는 용융된 멜트의 성분이 E1, k, A 로 불연속적인 경로로 변화하여 온도가 상승되어도 액상이 형성되지 않는 간격이 있다. 그러나 잔류 고체 결정의 성분은 X, X', A 로 연속적으로 변화된다. (2) 마그마의 분화와 원소의 이동 마그마가 냉각 고결될 때 중력 작용, 결정-액 분별 작용 (cr y s t al- liq u i d frac ti on ait on ) , 압축여 과작용{filt er pre ssin g ) , 액 체 불혼화(liq u i d imm i s- cib il i t y ), 확산 (d iff us i on) 등의 과정에 의해 단일한 초생 마그마에서 다양 한 화성 암울 만들게 되 는 과정 을 마그마의 분화 (ma gm a tic dif fere nti a- ti on) 라 한다. 마그마의 성분 변화에 따라 알칼리암 계열과 비알칼리암 계열의 솔레아이트(t hole iit e) 계열과 칼크 알칼리암 계열 등으로 구분하 고 있다. 마그마의 분화에 수반되어 원소의 화학적 분별이 일어난다. 특 히 이때에는 결정구조의 지배를 받게 되며 광물 결정구조 중의 양이온 반경과 유사한 이온반경을 가지는 원소가 고체 광물에 우선적으로 농집 된다. 이런 원소를 호정 원소 (com p a ti ble elemen t)라 한다. 크기가 다른 이온은 액체상에 남게 되며 이런 원소들을 불호정 원소(i ncom p a ti ble element) 라 한다. 예를 들면 솔레아이트 계열 마그마가 결정 분화될 때 수반되는 마그마 의 성분 변화를 보면 그림 8-9 와 갇다. 초기에 정출되는 감람석과 휘석에 호정 원소인 Cr, Ni 등이 우선적으
로 분배되기 때문에 결정 분화가 진행됨에 따라 Cr, N i가 감소하게 된 다. 그러 나 불호정 원소인 REE 와 Ba, Y, Nb, Zr, Rb, K, Cs, Ta, Th, U 등의 이온반경이 큰 LIL 원소는 마그마 분화시 후기 정출 광물 에 분배되어 분화 후기로 감에 따라 이들 원소는 증가하고 있다. 불호정 원소 중에서도 REE 는 마그마 분화의 많은 정보를 주고 있다. REE 패 턴에 따라 부분 용융의 정도나 마그마의 혼합 등을 추정할 수 있다. REE 패턴 중에 Eu 부의 이상이 나타나는 경우가 있는데 3 가의 Eu 대신 에 2 가의 Eu 이 사장석 정출시에 사장석 중의 K 와 치환되어 제거되기 때 문에 마그마 중의 산소 분압 증가의 정보도 얻을 수가 있다.
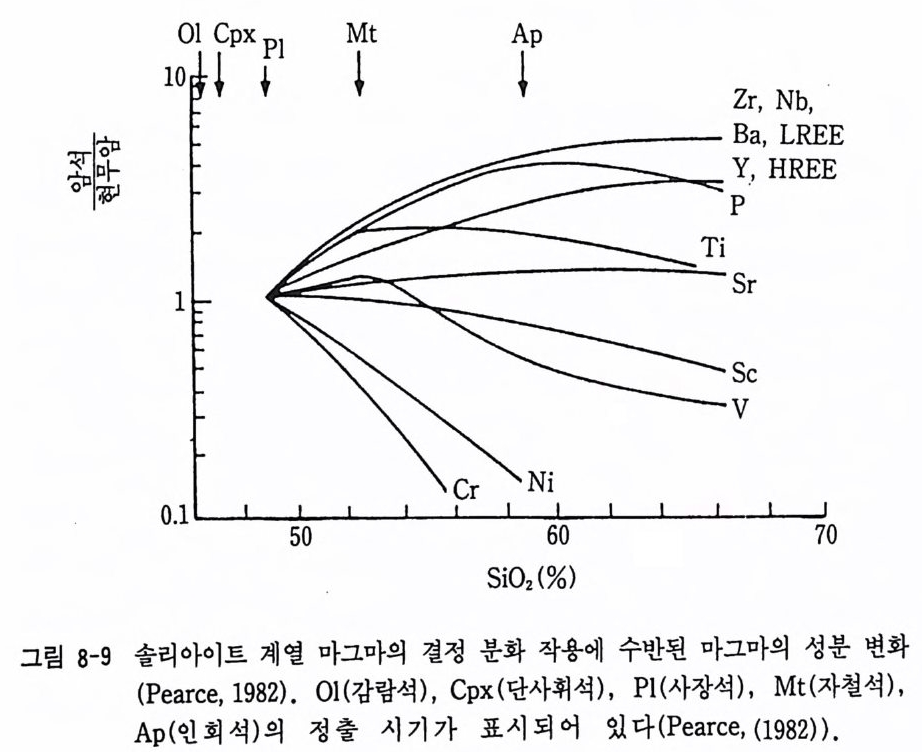 100 1바 C p x P| I Mi t Aip Zr, Nb,
100 1바 C p x P| I Mi t Aip Zr, Nb,
화성 암에서 일반적으로 Fe, Co, Ni, Au, Pt 등과 같은 친철원소 (sid e rop hi le e lements ) 는 초염 기 성 암류에 부화되 어 있고, Cu, Zn, Ag , Cd, S, As, Sb 등와 같은 친동원소 (chalco ph il e elemen ts)는 현무암이나 중성 화성암에 부화되어 있다 (Faure, 1991 ). 그리고 천석원소Oith o p h il e elements ) 중 LIL 은 후기 분화 산물인 화강암류에 부화되어 있다. 그러 나 Na, AI, Ca, Sc, Ti, V, Mr, Sr 등은 현무암질 암석 에 부화되 어 있으며 초영기성암이나 저칼슘 화강암류에는 일반적으로 결핍되어 있다. 8-4 원소의 이동과 농집 지구의 구성 원소 중 지각 내에서나 지표에서 원소의 이동에 의해 특 정 원소가 지구 평균 원소의 함량보다 높게 농집되는 경우가 있다(표 8-4 ) . 이 중에서 경제적으로 이용 가치가 있는 원소들로 된 광물의 집합 체를 광석 (ore) 이라 하고 광석이 부존된 곳을 광상 (ore de p os it s) 이라 한 다. 원소의 이동과 농집은 마그마의 결정 분화 작용이나 변성작용시에 일 어날 수 있으며 열수, 지하수, 지표수의 작용에 의해서도 일어날 수 있 다. 마그마의 결정 분화시에 정출된 결정과 잔류 멜트 사이에 금속 원소 의 분배가 일어난다. 초기 정출 광물인 감람석에 이온 반경과 전하가 유 사한 Ni, Cr 등이 우선적으로 분배된다. 예를 들면 남아프리카의 부시 벨트 복합체 (Bushveld comp le x) 와 같은 곳의 충상관입 암체 중 백금족 원 소를 다량 함유한 머 렌스키 리프 (Merensk y reef) 충과 크로마이트암층이 알려져 있다. 마그마 중의 S 는 fo 2 의 상승, Fe 함량 저하 및 온도 저하 등의 요인에 의해 황화물 멜트와 규산염 멜트로 불혼화 현상이 일어난 다. 이때 마그마 내에 존재하고 있던 Fe, Ni, Cr, Cu, Co 등의 금속 원소는 두 멜트 내에서 분배가 일어난다. 예를 들면 N i의 경우는 다음
과갇다. N i S( 황탸 멜트) +겅1 -0 2=N i O( 규산영 멜트) +겅l- S2 (8 .1) N i O( 황화물 멜트) + FeO( 규산염 멜트) =N i O( 규산영 멜트) + FeS( 황화물 멜트) (8.2)
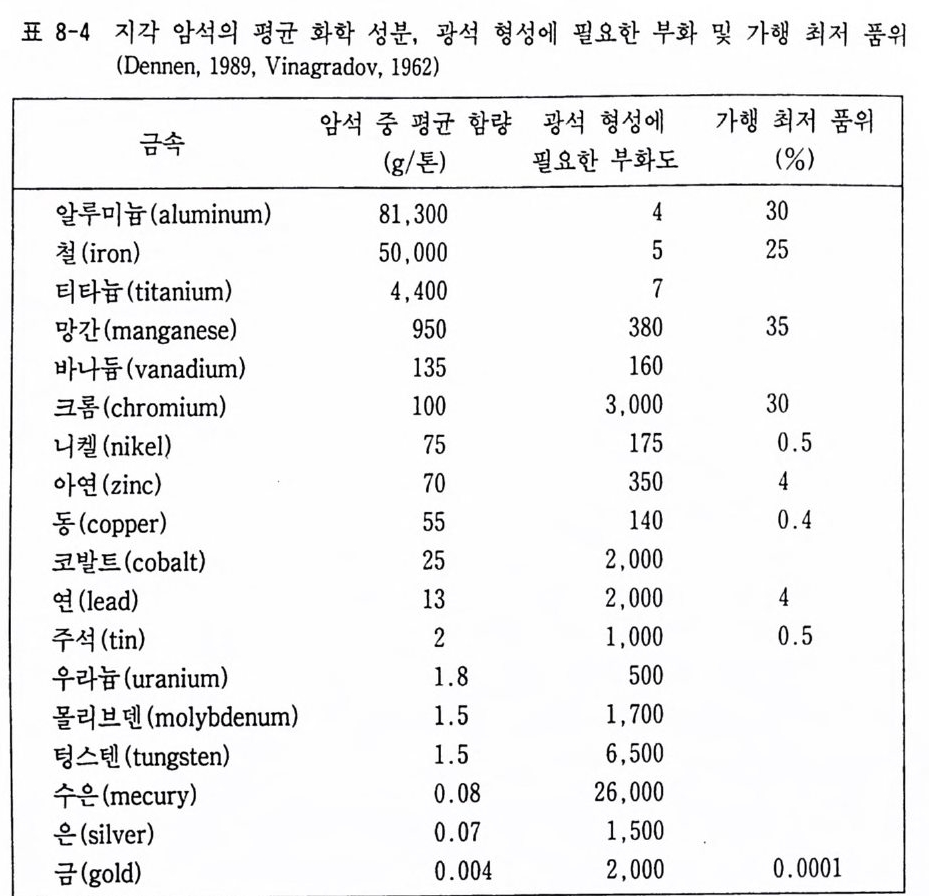 표 8-4 지각 암석의 평균 화학 성분, 광석 형성에 필요한 부화 및 가행 최저 품위
표 8-4 지각 암석의 평균 화학 성분, 광석 형성에 필요한 부화 및 가행 최저 품위
이때 분배계수 (KD) 는 다음과 갇다. KD= MMs • MFeo MN10 • MFeS
여기서 M은 미지 광물 성분의 몰분율이다. 위의 (8.1), (8.2) 식에서 분배계수는 f°” fs2, T, P, 성분 등의 함수임을 알 수 있다. 1255 ° C 에 서 현무암 멜트 성분에서의 규산염 멜트와 황화물 멜트 사이에 금속 원 소 Ni, Cu, Co 의 분배계수 KD 가 42, 35, 15 로 각각 얻어졌다 (Ra j aman i 와 Naldrett , 1 978). 순수에서 황화 광물의 용해도는 낮지만 염소나 황을 함유한 열수 용액 중에서는 이들 광물의 용해도가 순수에 비해 대단히 높다. 왜냐하면 ZnCl+, ZnCli , ZnCb- 등 의 클로르착체를 형성하기 때 문이다. 많은 광산에서의 석영 중의 유체포유물의 화학 분석에서 c1-함 량이 27400 pp m~197000 pp m 으로 높게 함유되어 있음이 알려져 있다(표 8-5). 따라서 규산염 멜트 중에는 H20 의에 Cl- 이 용존하고 있어 유체/ 멜트 사이에 Cl 의 분배비가 30~100 이므로 이들 멜트가 분리될 때에는 유체상에 Cl 아 이동하게 된다. 열수 유체 중의 c1- 이 온은 유체 중의 금 속 이온의 용해도를 상승시킨다. 이때 두 상 사이에 금속 이온 M 의 분 배비 (DM) 는 다음과 같은 유세 凡= m : 재 =k x (m [i 세 ) n 1M 의 관계가 얻어진다(H olland , 1972). 여기서 m 갑 ,1 1 은 유체 중의 Cl— 이온 농도이며 m 은 금속 이온 M 의 전 하, k 는 정수이다. 그립 8-10 에서 유체상중의 c1-이 온 농도에 따른 규 산염 멜트와 유체 사이의 금속 이온의 분배비를 나타냈다 (Ma t suo, 1989) . 클로르착체 형태로 열수 유체상에 용존하고 있는 금속 원소는 다음과 갇이 황화 광물인 방연석을 침전시킨다. PbCI~-n+H2S(aq )-+ PbS+2H+ + nc1- 물론 열수 유체 중에 용존하는 이온종에 따라 다음과 같이 다양한 금
속 광물이 침전될 수 있다. Ba2+ + soi- ---+ BaS04 (중정 석 ) Zn2+ + soi- ---+ ZnS + 02 (섬 아연석 ) 3FeS2+6H20---+ Fea04+6S2-+12H++02( 황철석과 자철석 공존)
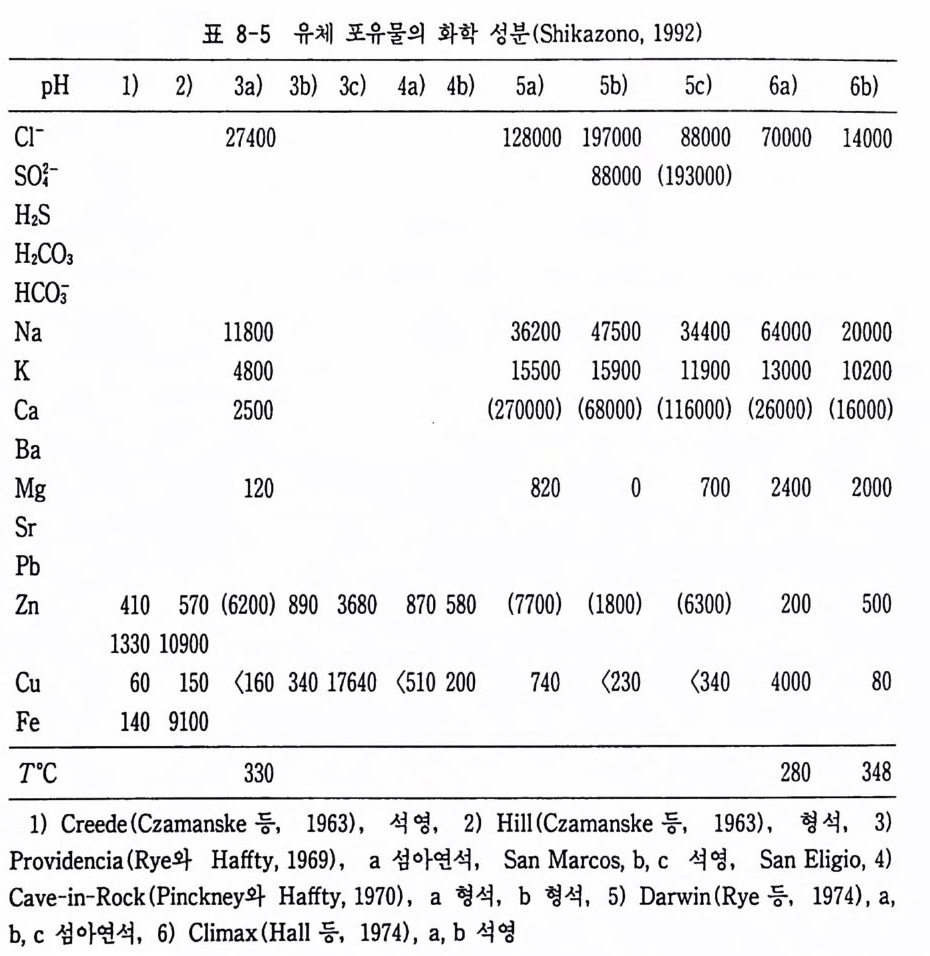 표 8-5 유체 포유물의 화학 성분 (Sh i kazono, 1992)
표 8-5 유체 포유물의 화학 성분 (Sh i kazono, 1992)
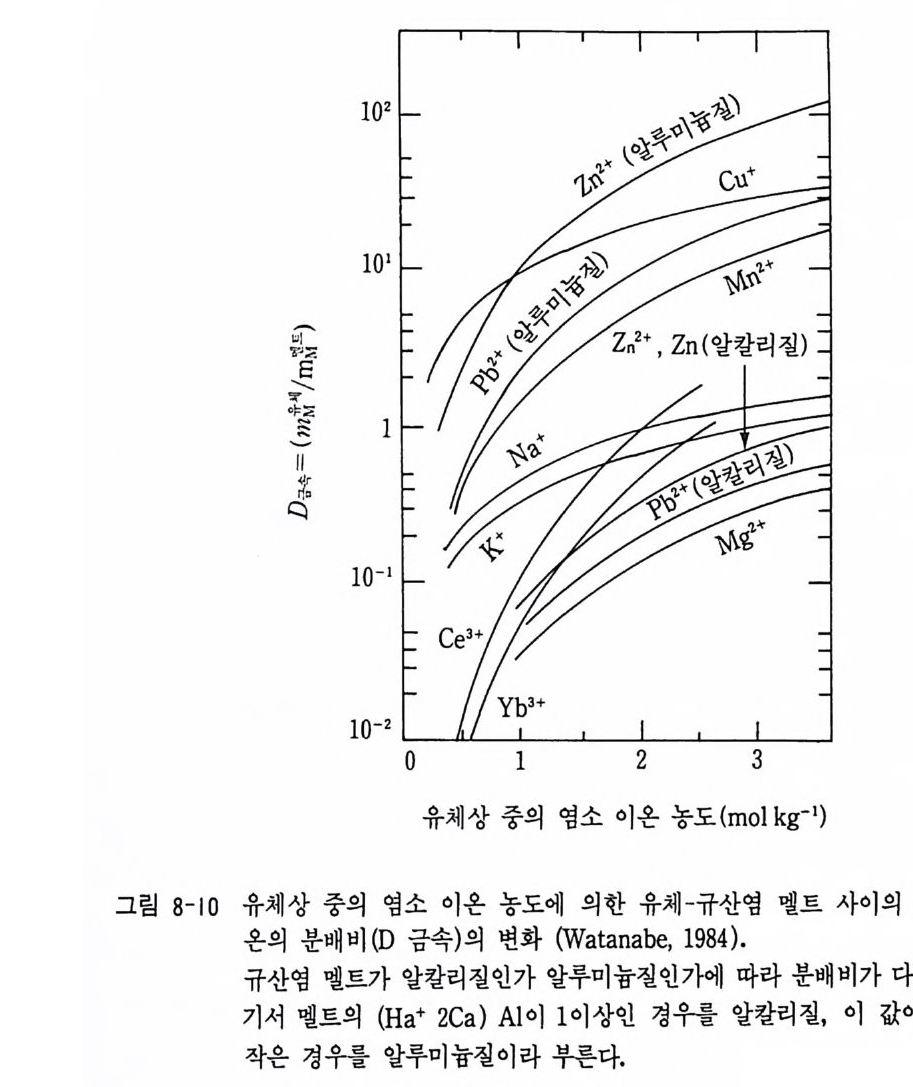 l02
l02
위의 반응식에서 열수 유체에서 광물이 침전될 때 영향을 주는 요인으 로는 p H 와 Eh 변화, 모암인 암석과의 반응, 비등 현상, 다른 유체와의 반응 등의 화학적 원인과 온도 및 압력의 변화 , 순환수의 혼입으로 인한 희석 작용 등의 물리적 원인 및 박테리아 활동 등의 생물학적 원인 등이 있다. 8-5 광상의 형성 (1) 순환수 유입과 광물의 침전 금속 광물을 침전시키는 다양한 요인과 메커니즘이 알려져 있지만 안 정 동위원소 분석 연구로 마그마 기원의 열수계에 순환수의 유입으로 인 하여 광물이 침전되는 기구가 잘 알려지게 되었다. 예를 들면 마그마에 서 방출된 유체상에 금속 원소가 농집되어 황화 광물을 침전시킨 반암동 광상(p o rp h yry cop pe r de p os its)에서 순환수의 유입으로 물리화학적 변화 롤 주어 대량의 Cu, Mo 황화 광물을 침전시키게 되었다. Tay lo r0974) 에 의 해 북미 다수의 반암동 광상의 oD, 0180 의 값은 그 지 역 의 순환수 와 유사하며 물-암석 반응으로 산소 편이 현상이 나타났다(그림 8-1 1 ). 반암동 광상에서 모암의 변질에 의해 다량 산출되고 있는 석고 (gypsu m) 는 마그마에 서 방출된 유체 의 S02 가 분해 되 어 형 성 된 H 2 SO ◄ (4S02+4H20--+ H2S+3H2SO ◄) 가 모암과 반응하여 모암 중의 Ca 2+ 울 방 출하여 석교를 정출한 것으로 알려져 있다. 반암동 광상에서는 모암의 변질대가 잘 발달하고 있으며 내측에서 의측으로 감에 따라 칼륨 변질 대 , 필릭 변질대, 점토화 변질대 , 프로필라이트화 변질대 등으로 구분된 다 (Lowell 과 Guil be rt , 1970). 변질대 내측은 마그마수가 우세하고 외측은 순환수가 우세하다. 필릭 변질대는 마그마수와 순환수의 혼입 부분으로
Cu 황화물의 침전이 다량 일어난다. 열수 광맥 광상의 경우에도 Au, Ag , Cu, P, Zn, Sn, W 등의 금속 원소가 열수 용액 에 의해 운반되어 모암 중의 파쇄대나 구조대를 충전하여 광맥형 광상을 형성한다. 이때 열수의 기원은 마그마에서 분리된 열수와 모암 내에 순환하고 있는 지하 수가 고온에서 암석과 반응하여 생성된 열수가 제안되고 있다. 최근 동 위원소 분석 연구와 유체포유물의 연구에서 후자의 기원이 더 많이 고려 되 고 있다. 캐 나다의 애뮤레 트 광산의 애 뮤레트 A 광체 (Shepp a rd 1977, Tay lo r 1979) , 미국 콜로라도 주의 크리드 광상, 상동 중석 광상(Ki m 등, 1988) 등의 연구에서 순환수가 금속 원소의 침전에 중요한 역할을 한 것으로 해석되었다. 무국 금은 광상(김규한 등, 1990) 과 논산, 원주,
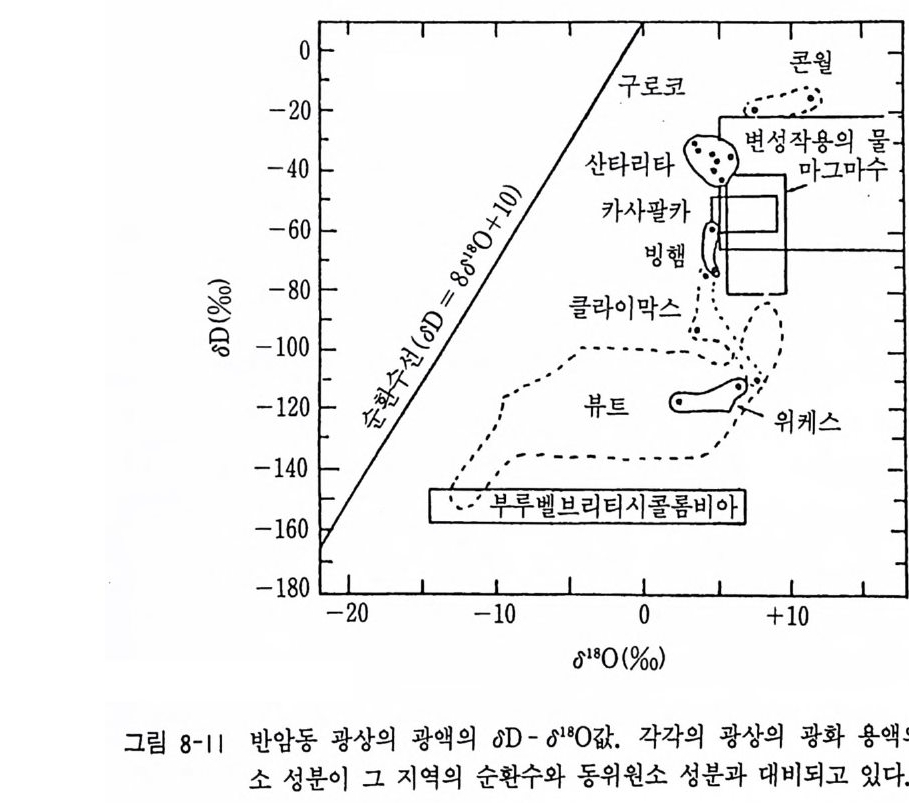 000000
000000
여주 등의 금은 광상 (So 등, 1988) 등에서도 금은 광물의 침전에 순환수 가 크게 기여하였음이 조사되었다. 특히 일본의 히시카리 천열수 금은 광상에서는 지표 부근에서 열수와 순환수의 혼합과 비등 현상으로 2 차적 인 열수가 형성되어 금은 광물 침전에 영향을 주었다. (2) 해령 열수계와 광물의 침전 동태평양 해령과 대서양 중앙 해령에서 황화물과 황산염을 다량 포함 하고 있는 350·c 의 열수 분출이 해저 탐사선에 의해 관측되었다. 황동 석, 섬아연석 등의 황화 광물이 우세한 검은 열수 분출을 블랙 스모커 (black smoker) 라 부르며 중정 석 , M g - 규산염 광물과 비 정 질 실 리 카가 우세 한 흰 열수 분출을 화이트 스모커 (whit e smoker) 라 한다(그림 8-1 2 ) . 해령 부근의 열수계에서 섬아연석, 황동석, 자류칠석, 황철석 등 여러 종류의 황화 광물이 산출되고 있다. Pt 0. 32 %, Ag 0. 20 %를 함유한 황동석도 보고되었다. Fouq ue t 등 (1993) 의 연구 결과에 의하면 23°N 대 서양 중앙해령에서 발견된 비하이브사이트(B eeh i ve s it e) 에서의 블랙 스 모커는 중심부가 345•c 이고 의측은 70°C 였다. 유체가 느린 속도로 회전 하면서 상승하는 과정에 해수와 혼합되어 수직연동 (ch i mne y) 구조가 형 성된 것이 해저 참수 담사선에 의해 조사되었다(그립 8~13). 연통의 상부 에는 다량의 Zn 과 Cd, Pb, Ag , Sb, Au 원소들이 수반되고 있다. 황화 광물로는 섬아연석, 자류철석, 황철석, 백칠석 등이 산출되었다. 황화 광물 중에는 Au 이 포함되어 있으며 연통에 1.8 p pm , 괴상 Zn 황화 광 물에 3.4p pm , 괴상 Fe 황화 광물에 0.75p pm , Cu-Fe 괴상 황화 광 물에 1.4 ppm 등이 포함되어 있다 (Fou que t 등, 1993). 해저 열수계와 관 련된 광물 침전은 홍해의 고영수 광상, 키프러스 (C yp rus) 와 오만 등지의 광상에서 발견된 오피 올라이트 (o ph i o lit e) 에 수반되는 괴 상 황화 광물 광 상, 일본의 벳시형 동 광상과 쿠로코(黑鑛) 광상 등이 알려져 있다. 해
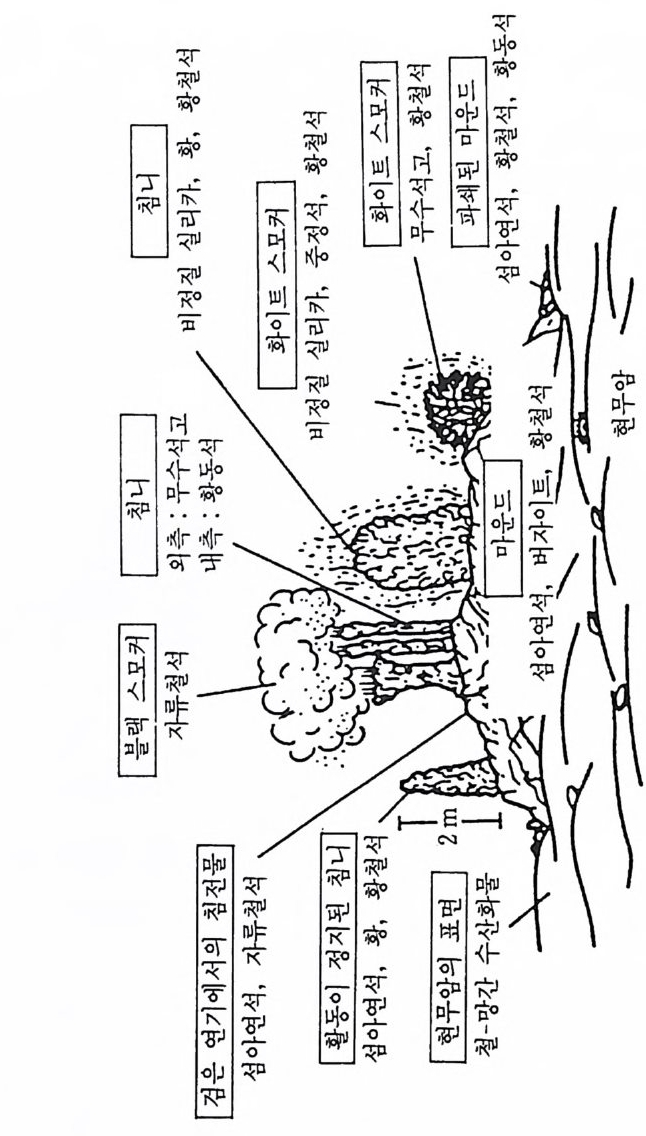 맞「
맞「
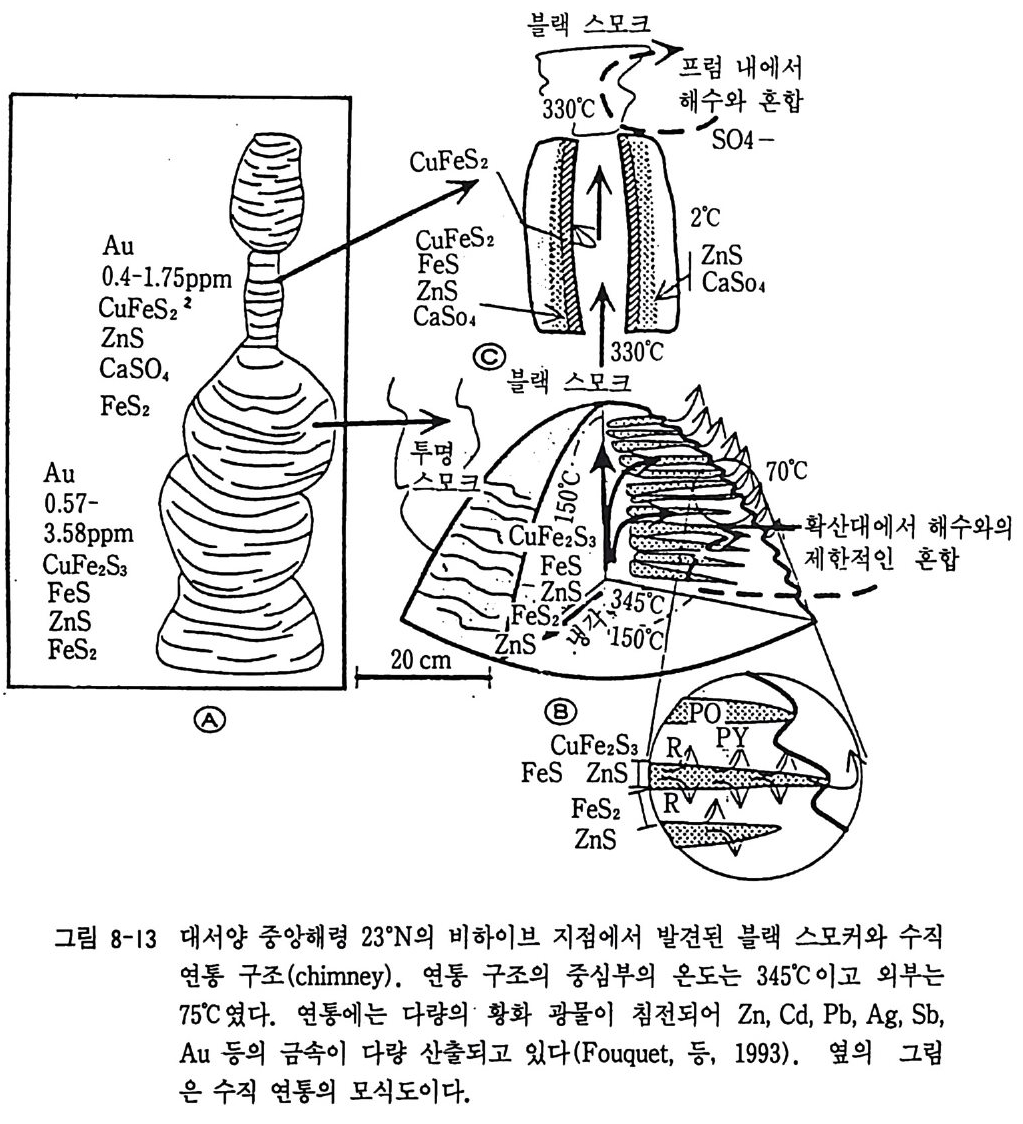 )戶혼_에서합
)戶혼_에서합
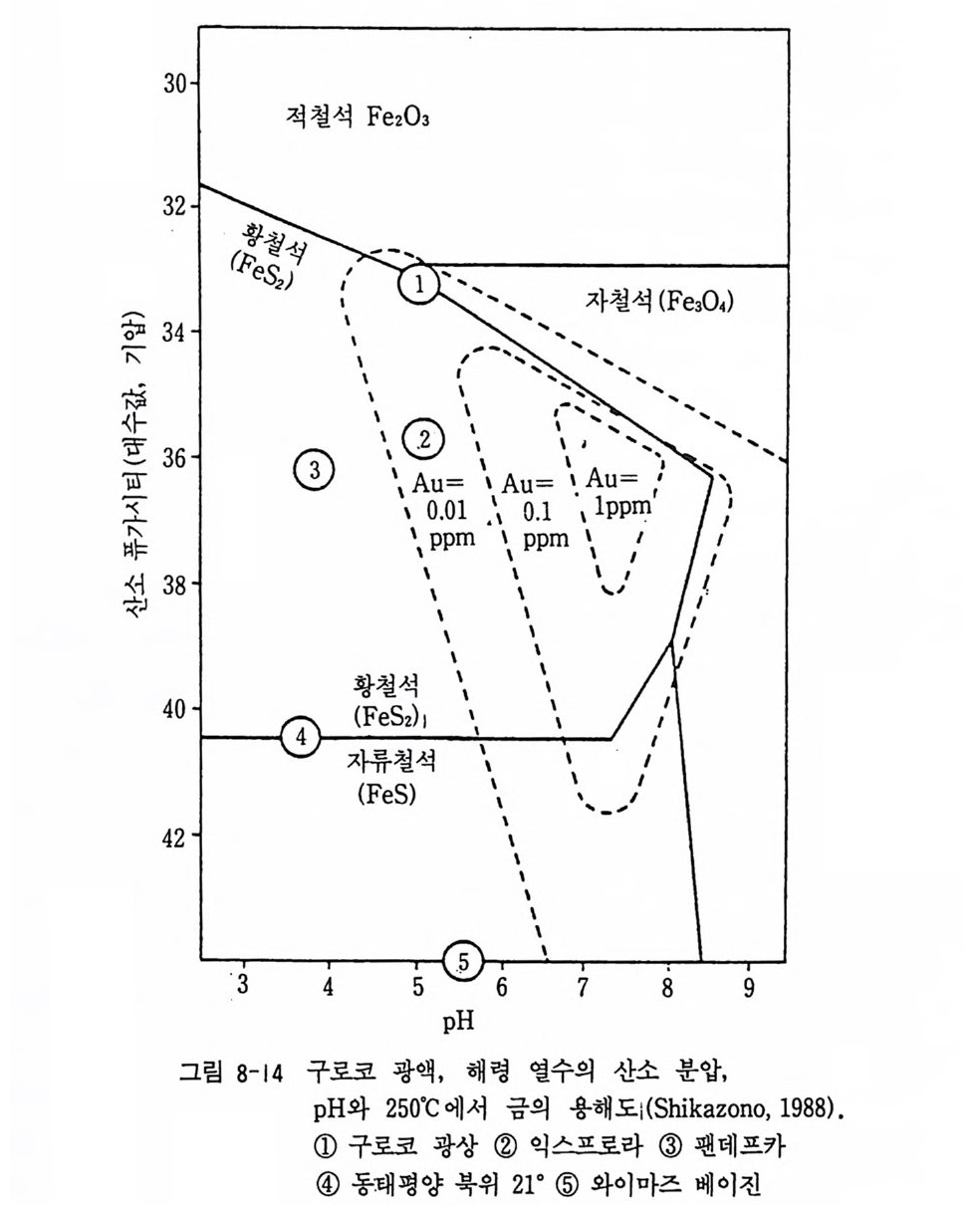 30
30
령 열수계의 광상과 쿠로코 광상은 모두 해저 화산 활동과 관련되어 형 성된 광상이지만 모암의 성질, 구성 광물 및 광물의 침전 환경 조건이 현저히 다르다. 쿠로코 광상에서는 금은 광물, 적철석, 중정석, 석고 등이 우세한 반 면, 해령 광상에서는 자류철석이 관찰된다 (Sh i k q zono, 1988). 또한 섬아 연석의 FeS mol% 가 해령 열수 광상에 비해 쿠로코 광상이 현저히 낮 다. 이와 같은 차이는 FeS 량= FeS2 (자류철석) (황철석) (F황e철S석2) +—23 0 2 = (F적e칠2 야석) + 2S2 의 반응식에서 임의의 온도에서 PS2, fo2 등의 차이에서 오는 광물의 안 정도 때문으로 해석하고 있다. 죽 쿠로코 광액의 산소 분압과 황 분압이 해령 열수계의 것보다 높았기 때문으로 해석하고 있다(그립 8-14 Shik a zone, 1988) .
제 9 장 해양화학 수권에서 해수의 역할은 대단히 중요하며 해수는 하천수나 호수의 화 학 성분과는 달리 대단히 균질하고 일정한 화학 성분을 가진다. 주로 Na+, Ca2+ , M 균, K+, c1-, so~-. HCOa 등으로 구성 되 어 있으며 해 수의 95 % 이상이 염분도가 35 土 7 %죠i 일정하다. 그리고 용존 고형 물 질의 함량도 대단히 낮다. 따라서 해수는 해양화학에서 평균적 화학 특 성으로 취급되고 있다. 그러나 해양에서는 대기, 해수, 지각의 물질의 순환과 상호 작용이 계속적으로 일어나고 있어 해수의 화학 성분에 변화 를 일으킨다. 특히 그림 8-5 에서처럼 판구조 운동과 해양저 확장에 수반 되어 해양 되적물의 퇴적과 퇴적 물질의 순환이 계속적으로 일어나고 있 다. 해수와 대기 간의 화학평형은 대기의 전화와 거시적인 지구물질 순 환에 대단히 중요하다. 여기에서는 해수의 화학 성분, 해수의 화학 성분의 질량평형, 해수의
화학 성분의 변화 과정과 해양 퇴적물 등에 관하여 설명한다. 9-1 해수의 화학 성분 해수의 용존 화학 성분은 대부분 Na+ , Ca2+, Mg 2+ , K+, c1-, So}-, HCO i'와 같은 육수의 용존 성분과 감은 화학 종류로 구성되어 있다. 그 러나 그 함량은 표 9-1 에서처럼 c1-, Na+, Mg 2+ , So}- , Ca2 +, K+ , HCOi ' 순으로 육수의 성분과 크게 다르다. 해수의 주성분은 그 함량이 대단히 높기 때문에 의부에서 유입되는 화 학 성분에 의한 변화가 적다. 해수의 주성분은 NaCl 로 염분도 35 %o 이 며 c1-, Na+ 논 해수에서 자유 이온(fr ee i on) 으로 존재하지만 so i-와 같 은 많은 이온종은 자유 이온과 이온쌍(i on i c p a i r) 으로 구성되 어 있다. 즉 황의 경 우 sm-, Na+so:. CaSOt Mg SO ~ 등의 이 온종으로 되 어 있다 . 그리고 탄소종의 경우에는 HCOi ', co~- , CO2 의 형태로 해수에 존재하 고 있으며, 인의 경우에는 HPoi- , Po!-, H2PO:. 형태로 해수에 용존되 어 있다. 그리고 해수 중의 Br, HBOa, Sr, Rb+ 등과 같은 미량 성분 ( 〉 l µm)은 주성분에 비하여 장소에 따라 또는 원소 종류에 따라 변화가 심하다. 이처럼 해수 성분 원소 중에 어떤 성분 원소는 일정하고 어떤 성분 원소는 크게 변화하고 있다. 이같은 해수 성분의 변동은 하천수의 유입이나 화산암과 해수와의 반응에 따른 성분 원소들의 교대 정도, 교 대 시 간 (rep la cement time ) 또는 체 류시 간 (resid e nce time ) 의 차이 때 문에 일어나는 것으로 본다. 즉 주성분 원소는 해수 중의 함량이 대단히 높기 때문에 해수의 균일화에 걸리는 교대시간이 길며, Fe 와 같은 미량 성분 은 체류시간이 짧기 때문에 지역적으로 그 성분의 변화가 심하게 나타난 다(표 9-2). 해수에서 주요 원소들의 유입과 유출 과정은 표 9-2 와 갇다. c1 - 은 주
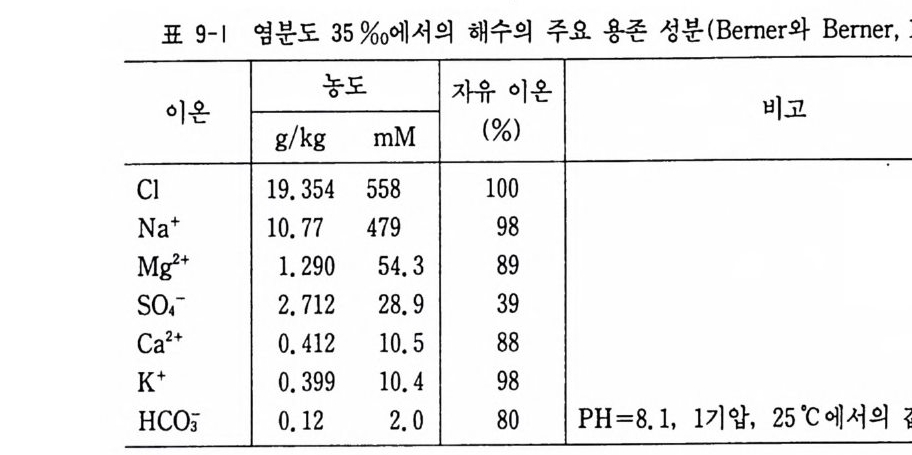 표 9-1 영분도 35 % 0 에서의 해수의 주요 용존 성분 (Berner 와 Berner, 1987)
표 9-1 영분도 35 % 0 에서의 해수의 주요 용존 성분 (Berner 와 Berner, 1987)
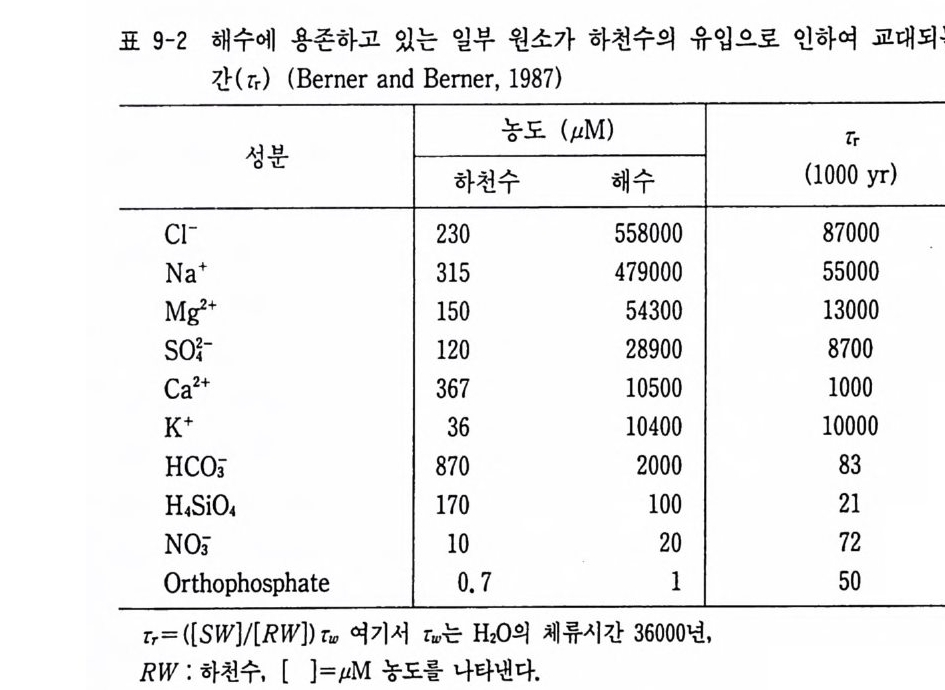 표 9~2 해수에 용촌하고 있는 일부 원소가 하천수의 유입으로 인하여 교대되는 시 •
표 9~2 해수에 용촌하고 있는 일부 원소가 하천수의 유입으로 인하여 교대되는 시 •
로 하천수로 유입되며 암염 퇴적이나 공국수, 해수-대기 간의 전이 등에 의해 유출되어 해수에서 Cl- 의 원소 평형이 이루어진다. 그러나 Cl- 은 8700 만 년의 긴 체류시간 때문에 그 농도가 점점 증가하여 비평형상태가 되고 있다. 죽 유입 증가량만큼의 현생 암염 퇴적분지가 형성되고 있지 않으며 인 공 오염으로 유입되는 Cl- 의 양이 조철될 시간이 없어 해수에서 c1- 양 이 증가하여 비평형이 이루어지고 있다. 예를 들면 해양에 유입되는 Cl 의 전량은 308T g CI-/ 년이고 해수-대기 전이와 공극수로 인한 유출 총 량은 57T g CI-/ 년이므로 많은 양의 차이로 Cl 의 비평형이 이루어지고 있다(B erner 와 Berner, 1987). 이렇게 증가한 c,- 의 양은 Na 와 함께 증발 암 퇴적분지에서 주기적으로 암염을 퇴적시키면서 지질시대 동안에 해수 에서 염분도와 c1- 의 평균 함량이 정상상태평형 (ste a dy sta t e balance) 을 유지하여 왔다. 특히 Na 는 암염 의에 규산염 광물의 주된 구성 성분이 므로 암석의 풍화, 양이온의 교환, 암석-해수 반응 등에 의해서도 변화 되는 원소이다. N 찰은 Cl- 과 함께 증발암으로 퇴적되며 암석-해수 반응 에 의하여 N 잘 이온이 유출된다. 반면에 Ca2+ 이온은 하천에서 유입되 는 양 (550), 화산암-해수 반응(1 8 1), 양이온 교환 과정 (37) 에서 유입되는 총유입량이 778 T g Ca2+I 년이며 천해 CaC03 퇴적 (520), 심해 퇴적 (440) 으로 총 유출량 960T g Ca2 + I 년으로 오늘날 해수에서 Ca2+ 유출량이 유 입량을 초과하고 있다. 즉 후빙하기의 빠른 해수면 상승으로 대륙붕에 CaC 아의 빠른 침전이 일어나고 있기 때문이다. 그리고 대부분 CaCOa 는 유공충과 같은 플랑크톤 유기물에 의해 사용되므로 심해 퇴적물에 퇴적 되는 양은 적다. 때문에 심해 해수에는 CaC03 가 불포화되어 Ca 물질이 어느 심도에 이르면 용해되어 버리는 탄산염의 보상 심도 (carbona t e comp en sati on dep th, CCD) 라는 개념이 나오게 되었다. 그 때문에 태평양 이나 대서양의 심해에서는 퇴적물에 CaC03 가 없는 퇴적층이 분포하고 있다. 심해에서는 광합성 작용에 의한 CO2 제거 없이 호흡 작용에 의해
co 가 생성되기 때문에 이 CO2 는 탄산을 형성하여 다음과 갇이 CaC03 를 용해시키게 된다. CO2+H20+CaC Q 3 一 Ca2++2HCQ j 또한 CaCO 려 용해도는 압력이 증가함에 따라 증가한다. 때문에 심해 저에서는 평균 400 기압이기 때문에 CaC03 의 용해도가 천해에 비해 2 배 로 증가하여 CaC03 가 쉽게 용해된다. 9-2 해수의 화학 성분의 변화 (1) 생물학적 과정에 의한 해수의 화학 성분의 변화 생물학적 과정에 의한 해수의 화학 성분의 변화나 하천 유입에 의한 해수 성분 변동 의에 다론 이유는 생물학적 과정으로 표면수에서 생물들 이 질소, 산소, 규소와 같은 성분을 섭취하므로 이들 성분이 결핍되고 이들 원소가 생물이 죽은 후에 침강 분해되어 다시 심층수에서는 증가하 게 된다. 해수의 수직적 혼합 속도보다 생물학적 과정의 속도가 빠를 때 용존 02, CO i-와 같은 원소의 수직적 변화가 일어난다. 그리고 화산암 -해수와의 반웅, 대륙에서 운반된 고형 물질과의 반응에 의해 해수의 성 분이 변화하기도 한다. 그 의에 pH , 온도와 압력 등이 해수의 성분 변 화에 영 향을 준다. 해수의 화학 성분 중에 서 Ca2+, SO!-, HCOj , CO2, 02, NOj , HPO:i 등은 생화학적 과정에 의해 영향을 받는다. 그리고 Cu, N i와 같은 미량원소도 생물학적 활동에 크게 영향을 받는다 (Bo y le 등, 1977, Bo y le 과 Edmond, 1976) . 주로 연질 조직 이 나 유기 물 합성 과 정, 유기물질의 박테리아 분해, 경골질부의 분해 과정에서 성분 변화가 초래된다. 해수의 표충수에는 인산과 질산이 많이 포함되어 있어 광합성
이 촉진된다. 여기서 이들 원소를 소모하게 된다. 그러나 죽은 유기물질 이 심층수로 침전되면 박테리아에 의한 호흡 작용에 의해 CO2, NOJ , HPO:i 등을 만들어내고 아를 소비한다. 그 결과 그림 9-1 에서처럼 십해 수에는 NOJ , HPO:i , CO2 의 농도가 높고 02.Q J 농도가 낮게 나타난다.
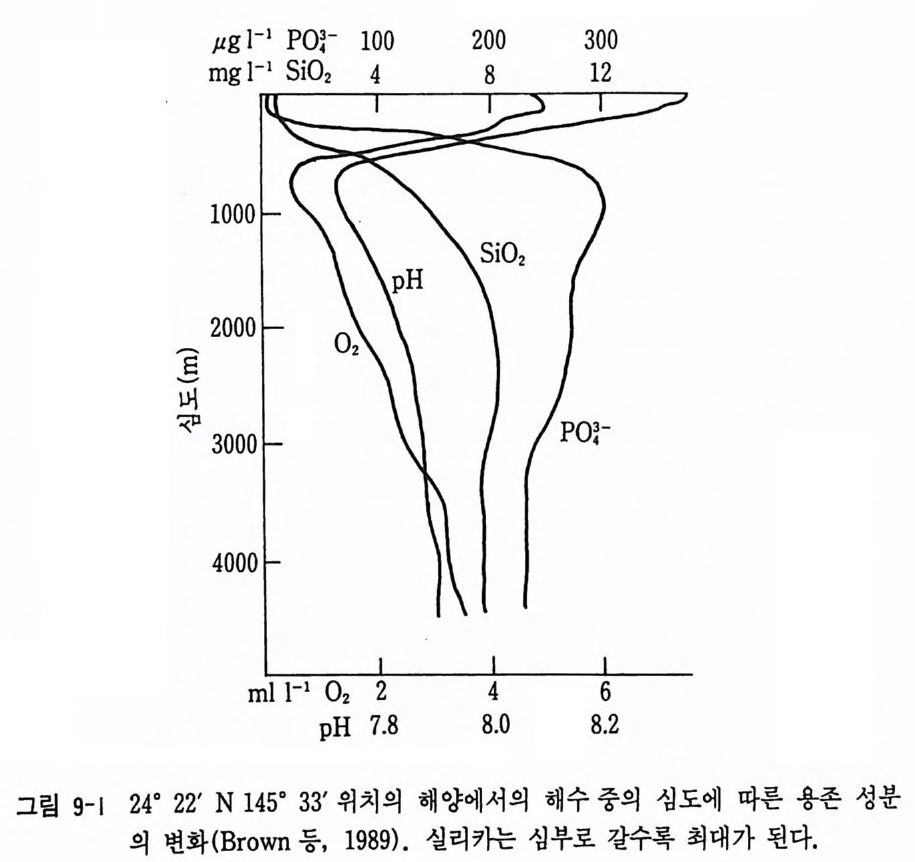 µg 1-1 POt 100 200 300
µg 1-1 POt 100 200 300
해양 퇴적물 중의 유기물은 주로 박테리아 작용에 의해 분해된다. 예 를 들면 황 환원 박테리아에 의해 2CH2o+so~-一 H2s+2HC05 가 되어 SO t에서 H2S 가 다량 생성된다 (Cla yp ool 과 Kap la n, 1974, Berner,
1980). 박테리아 작용에 의해 형성된 H2S 가 철 함유 광물의 Fe2+ 와 반 응하여 2H2S + Fe2+ 一 FeS2 + 2H2 와 같이 퇴적 기원의 황철석을 침전시킨다. 따라서 퇴적물 중의 황철석 의 양은 퇴적지 내의 유기물의 존재량, so~- 의 양 및 철 함유 광물의 존재 량에 크게 영 향을 받는다. 이 의에도 퇴적물 중의 유기물의 분해 과정은 CH20 + 02 一 CO2 + H20 (oxy ge nati on ) CH20 + 2Mn02 + 3C02 + H20 一 2Mn2+ + 4HCOi 5CH20+4NOi 一 2N2+C02+4HCOi + 3H20 CH20 + 4Fe (OH ) 3 + 7C02 一 ➔ 4Fe2+ + 8HCOi + 3H20 2CH20 一 CH4+C02 등이 있다. (2) 암석-해수 반응에 의한 해수의 화학 성분 변화 판구조 운동에 의하면 해양저가 확장되는 중앙해령이나 호상 열도 등 의 해양에서는 화산 활동이 대단히 활발하게 일어나고 있다. 동태평양 해령 부근의 심해저에서 발견된 블랙 스모커 (blacksmoker) 나 화이트 스 모커 (wh it esmoker) 에서처럼 350·c 내의인 열수의 검은 연기와 흰 연기 가 분출하고 있으며 이 주위에 Pb, Zn, Ag 황화 광물의 침전이· 일어나 고 있다(그립 9-2). 고온에서 현무암-해수 반응에 의해 해수에서 Mg 2 +, SO t가 유출되고 암석 에서 Ca2+, H4SiQ 4 , K+ 등의 이온이 해 수로 유입되는 현상이 실험에서도 입증되었다(표 9-3) (Bi sche ff와 Dick son, 1975, Mott le 등, 1979) .
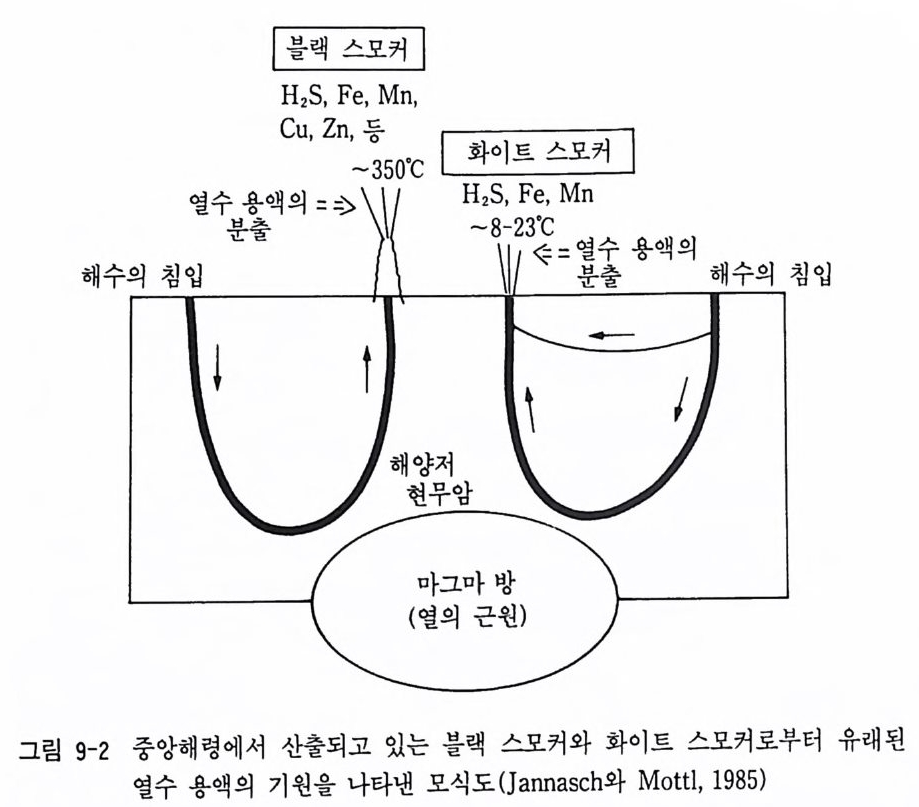 |블랙 스모커 |
|블랙 스모커 |
저온 (50°C) 에서의 현무암-해수 반응에서는 해수에서 K+ 를 받아들이고 암석 에서 Ca2+, Mg 2+ , H ◄ S i O 를 해수로 방출하는 결과 (Thom p son, 1983) 가 얻어져 고온에서의 현무암-해수 반응에서 일어나는 K + 과 Mg 2+ 의 거동과는 반대 경 향이 얻어졌다. Li+, Rb+, Ba2+ 이온의 경우에서도 고온에서는 이들 이온이 해수로 유출되었으나 저온에서는 현무암 내에 흡수되는 결과가 얻어졌다. Crovis ie r 등(1 983) 에 의한 저온에서의 실험 결과 해수로부터 M g2+울 취하여 변질 현무암질 유리질 표면에 Mg 함유 광물충이 형성된 것이 현미경으로 관찰되었다. Ge i skes 와 Lawrance (1981) 에 의하면 화산재로 된 퇴적층에서 심도가 깊어질수록 Mg 2+ (K+ )
가 감소하고 Ca2 + 은 증가하는 경향이 얻어졌다(그림 9-3). 화산성 퇴적 물과 간극 해수의 반응으로 스멕타이트가 형성되어 물의 산소 동위원소 비도 변화하고 있다.
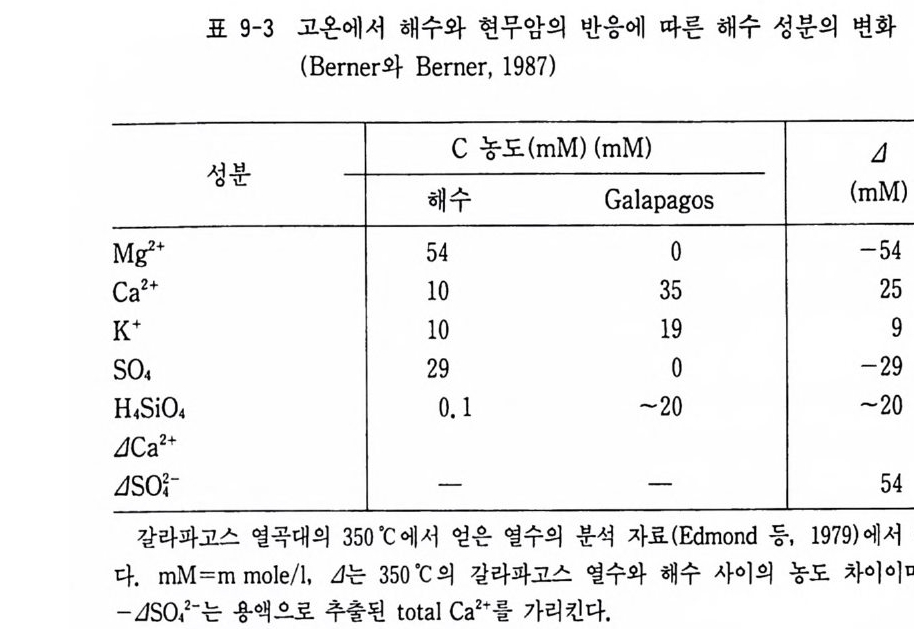 표 9-3 고온에서 해수와 현무암의 반응에 따른 해수 성분의 변화
표 9-3 고온에서 해수와 현무암의 반응에 따른 해수 성분의 변화
(3) 육성 기원 물질과의 반응에 의한 해수 성분의 변화 하천에 의해 유입된 점토 광물과 감은 육성 물질은 해수와 평형에 있 지 못하기 때문에 바다에 유입되면 해수와 반응을 일으키게 된다. 이 과 정은 풍화의 역과정으로 이온 교환이나 흡착과 같은 과정으로 일어난다. 예를 들N면a + N+aH+C 의O i 경+우Al -다 규음산과염 같—이- NN aaAAll-- 규규산산염염 을+C 만02들+게H 2된0다 .
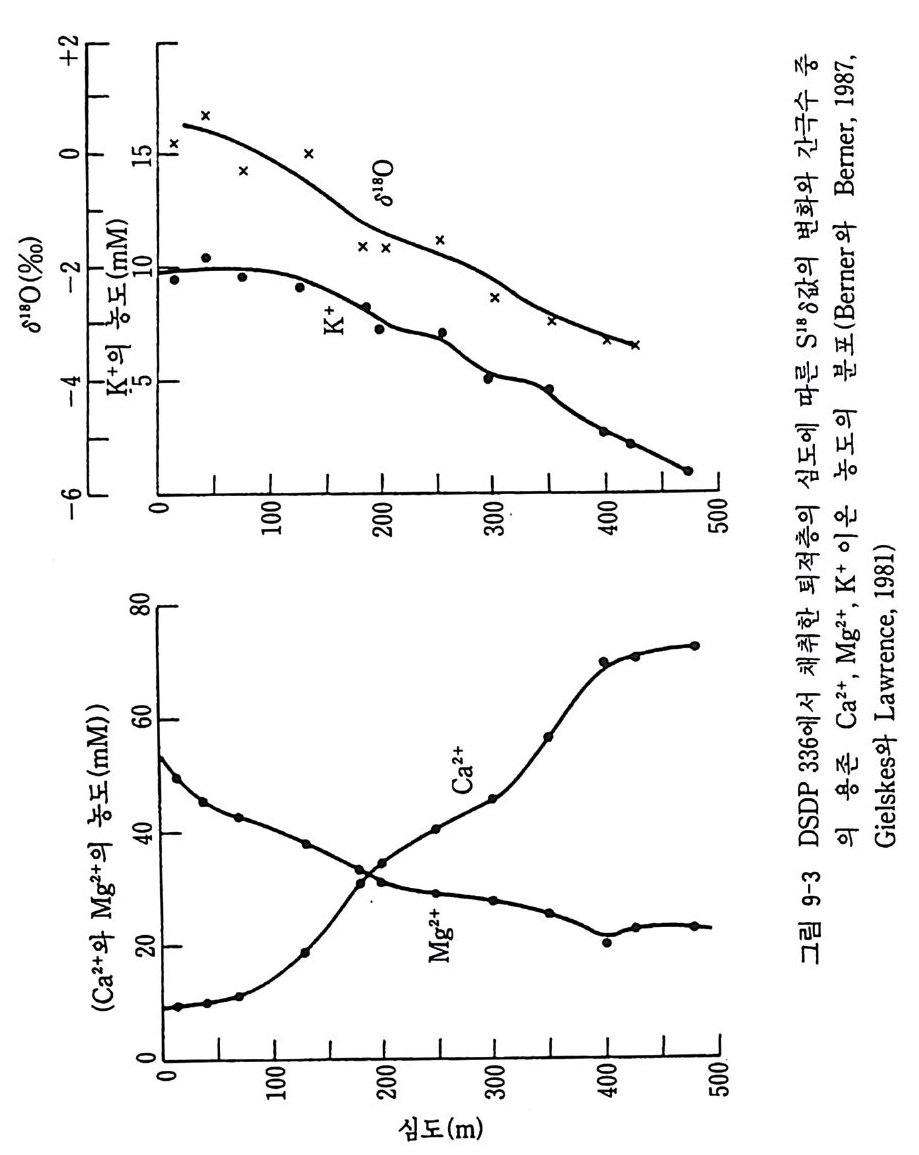 。+ a 배 .
。+ a 배 .
Sa y les0981) 는 대서양 심해저 퇴적층에서 용존 Mg 2+, K+, Na+, Ca2+ , HC03 이온들의 농도 변화를 조사하였다(표 9-4, 그림 9-4). 그 결과 Mg 2+, K+, Ca2+ 화산성 퇴적암의 분석 결과와 유사하게 M 답+와 K+ 은 퇴적물이 취하고 Ca2+ 은 퇴적물에서 유출되었다. 이는 저 온의 화산재-해수 반응에서 일어난 화학 성분 변화와 유사하게 동일한 방향으로 변화가 일어났으므로 이 결과 역시 해수-퇴적물 상호 반응에 의한 것으로 추정하게 되었다. Drever 등 (1988) 에 의하면 화성암이 풍화되어 해양에 유입되거나 퇴적 암으로 퇴적될 때 정상상태 (ste a dy s t a t e) 에서의 원소의 지구화학적 순환 이 일어날 때에는 다음과 같은 질량평형 관계가 성립한다. M 화요 =M 외J:a j C~ + M 해 M 화 = 풍화 받은 대륙지각의 화성암의 전량 C 는 지각의 화성암 중의 i 원소의 함량 M 되= 해양 퇴적물을 포함한 현재의 퇴적암의 전량 C 논 해양 퇴적물과 퇴적암 중의 i 원소의 함량 M 해= 해양에서의 물의 질량 어= 해수에서 i 원소의 함량 aj= 상이한 되적암과 해양 퇴적물의 질량분률 (mass frac ti on ) 위 식에서 다음의 M 되 = 2. 5土 0. 4 X 1024g (Li, 1972, Ronov와 Yaroshevsky, 1976) M 화 =0. 88M 되 (Li, 1972) M 해 = 1. 4 X 1024g (Suerdrup 등, 1942) 와 퇴적암의 종류에 따른 비율인 셰일:사암:탄산염암:증발암 =74: 11 : 15 : 2(Garrels 와 Mackenzie , 1971) 를 이용하여 계산된 질량분율 (a j)의 값인 a 셰(셰일) =0.725, a 란(탄산영암) =0.147, a 사(사암) =0.108, a 증(증발
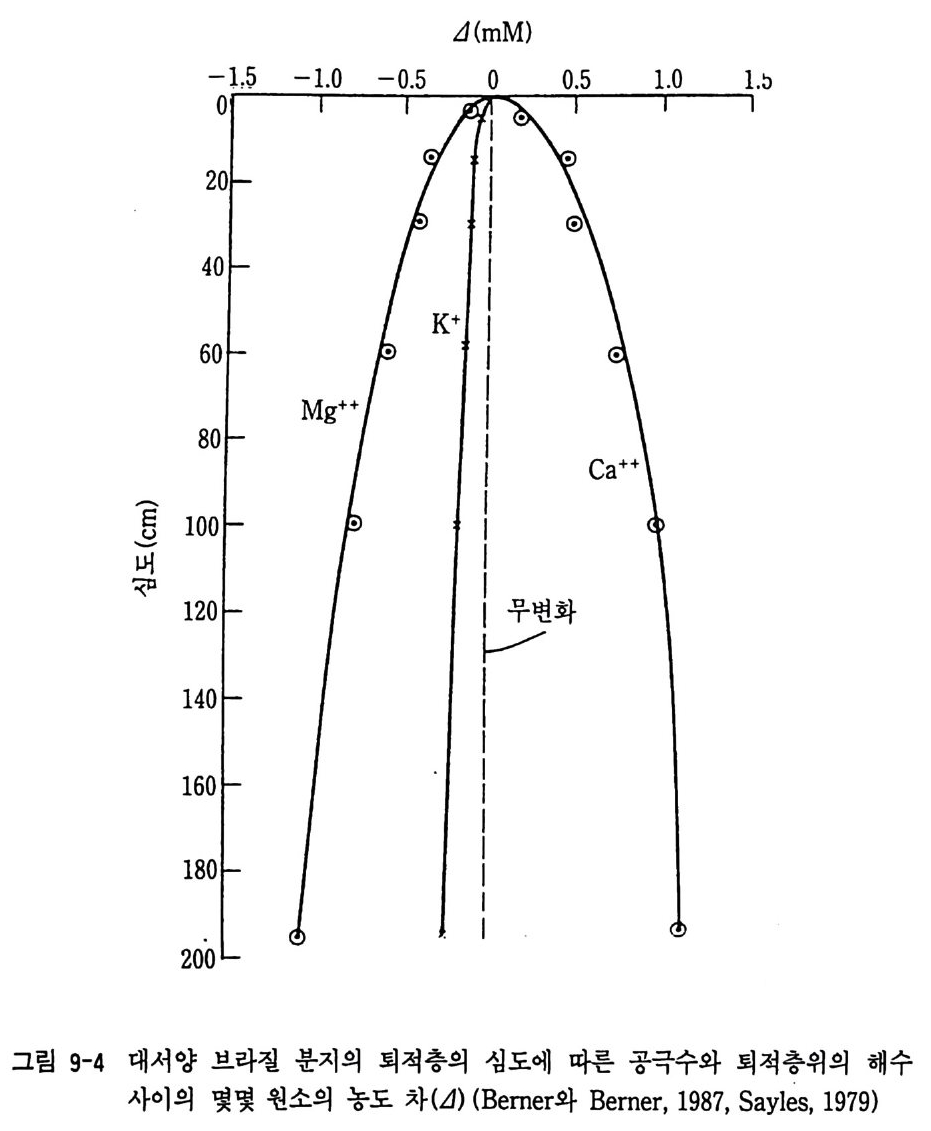 L1(mM)
L1(mM)
암) =0. 020 을 각각 대 입 하면 0. 88C~f = O . 702C ~ +0.108C 묘 f +o.122c~+o. ooze~+o. 024c 싫 +o. 024c~+o. 56C~i 의 물질평형 관계식이 얻어진다. Co p'와 C0CI 는 각각 해양 되적물과 해 양 탄산염 퇴적물 중의 i원소의 함량이다 . 이 식은 해수와 암석 간의 각 원소의 지화학적 평형 계산에 이용될 수 있다. 완전 평형이 이루어진다 면 댜 =0.88C 화가 얻어져야 하나 사용된 성분 자료나 질량분율의 부정 확성 때문에 이 값이 o. 8~1 . 30 이 얻어졌다(D rever 등, 1988).
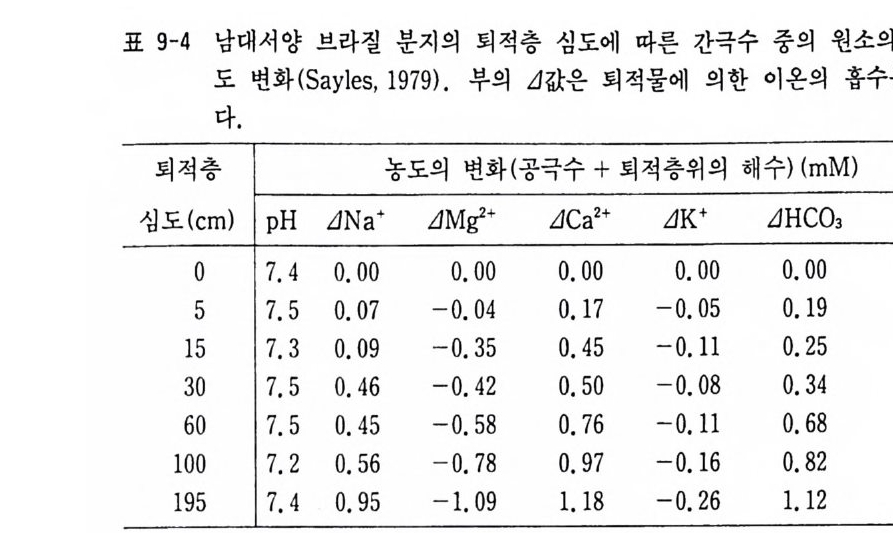 표 9-4 남대서양 브라질 분지의 퇴적층 심도에 따른 간극수 중의 원소의 이온 농
표 9-4 남대서양 브라질 분지의 퇴적층 심도에 따른 간극수 중의 원소의 이온 농
정상상태에서 지구화학적 순환이 일어날 경우 해양에서 원소의 유입량 과 유출량이 감아야 한다. 원소의 유입은 주로 하천수에 의해 일어나고 유출은 퇴적물이 매몰될 때 공극수, 이온 교환 반응, 속성작용, 화학적 침전 등에 의해 일어난다. 일부 이온들의 유입량과 유출량은 표 9-5 와 갇다. N 갑 이온을 보면 유출량보다 유입량이 많기 때문에 해수에서 N 잘 농
도가 계속 증가하고 있다. 그 의에 Mg 2+, ca2+ , ci- , HCOa, so~-등 도 증가하고 있으며 K+ 과 H.S i 04 는 거의 평 형 에 가깝다. N 갑의 증가는 c1-증 가와 상응되며 Ca2+ 는 so~-증 가량과 상응되기 때문에 결국 이들 이온들은 해양 되적분지에 석고 (CaSO. • 2H20) 나 암염 (NaCl) 을 퇴적시키 게 되어 물질평형에 이르게 된다. 그리고 M, t+ 이온은 해령의 고온의 현무암과 해수와의 다음과 감은 반응에서 활석을 만들게 된다. 6M, t+ +4CaAbSiz O a + H20 ~ 2Mg 3S i4 0 1o (OH) 2+ 4Alz03 + 4Ca2+ + 4H+ (아놀사이트) (활석)
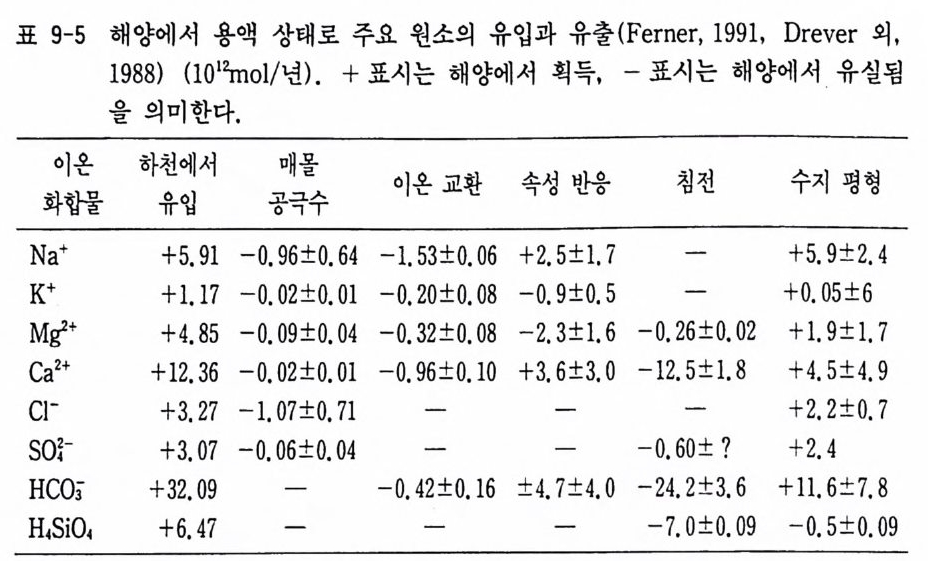 표 9-5 해양에서 용액 상태로 주요 원소의 유입과 유출 (Ferner, 1991 , Drever 의,
표 9-5 해양에서 용액 상태로 주요 원소의 유입과 유출 (Ferner, 1991 , Drever 의,
그리고 현무암 중의 감람석과 sot, M¢+ 이온과의 다음과 같은 복잡 한 반응에서 세피올라이트 (se pi o lit e), 황철석, 비정질 실리카, 자철석 등 울 형성하게 된다 . 11Fe iSi 0 . +2Mf + +2S 야 +2H20 ~ Mg 2S hO& (OH ) • + FeS2 + 8Si0 2 + 7FeD. 이같은 해수와 암석의 반응에서 해수의 M, t+, so~-, N 갑 이온은 감
소하는 반면 Ca2+, K+ 이온은 증가하게 된다. 지질시대 동안 해양에서의 주원소의 유입량과 유출량은 평형이 유지되 어 왔으며 하천수에 의해 연간 유입되는 양에 비해 해양은 너무나 방대 한 양의 주원소의 저류 장소이므로 해수의 화학 성분은 변화가 없다.
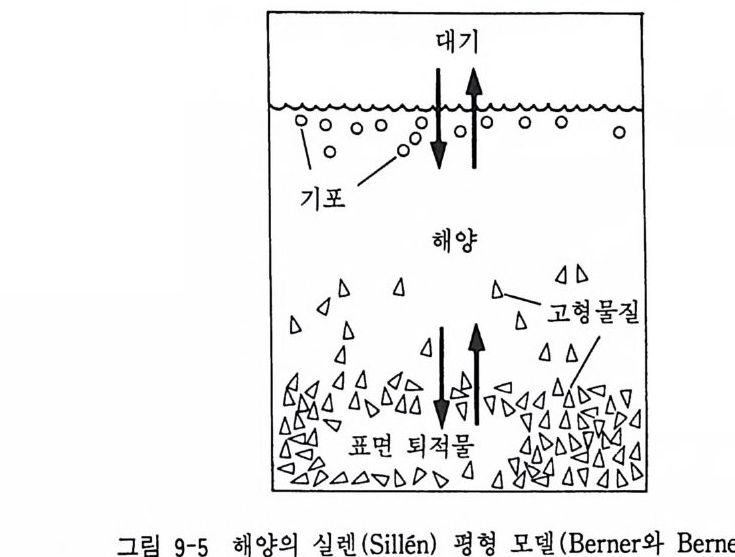 대기
대기
이갇은 해수 화학 성분 설명을 위하여 첫째 , 실렌 평형 모델 (S ill en's equ i l ibr iu m model) , 둘째 , 해 양 상자 모델 (oceani c box models) 이 제 안되 고 있다. S ill en(1967) 은 대기, 해수, 해양저 퇴적물 사이에 단순한 화학 평형을 가정하였다(그림 9-5). Broecke(1971), Garrels 등 (1975) 은 해양을 균일한 성분을 가지는 몇 지역으로 구분하고 이들 지역 내에 성분의 유 입 속도와 유출 속도 차를 이용하여 성분의 변화 속도를 계산하는 정상 상태 상자 모델링 (ste a dy sta t e box mode lli n g)을 제안하였다(그림 9:_6).
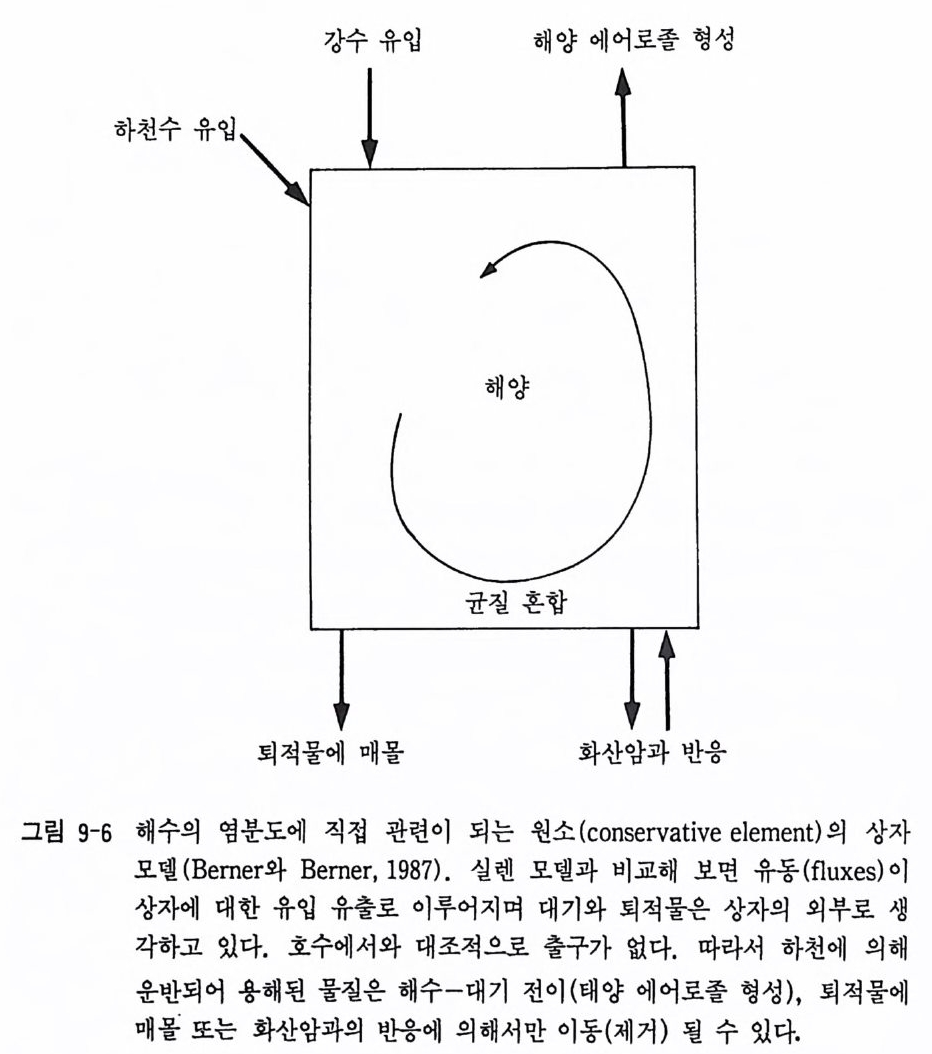 강수유입 해양 에어로졸 형성
강수유입 해양 에어로졸 형성
9-3 해수 중 원소의 평균 체류시간 대기권, 생물권, 수권, 암석권 간에 물질의 순환이 일어나고 있다. 각 권에서 물질이나 원소의 체류시간 (res i dence ti me) 은 다음 식으로 계산된 다. 원소의 평균 체류시간 (T 년) 단위해시수간 에중 의해 수성분로 유i의입 되전량는 양 해수 중의 성분 i의 전량 단위시간에 해수로 유출되는 양 여기서 평균 체류시간은 연 단위로 하고 유입량과 유출량은 동일하며 해 양에 서 어 떤 성 분의 농도는 일정 한 정 상상태 (ste a dy sta t e ) 라는 가정 이 필요하다. 어떤 성분 i의 평균 체류시간 (T) 은 T( 년) 하천수 중의해 수i 성중분의의 i 평성균분 의농 도평 X균 세 농계도의 X 전전 하해천수의량 연간 수량 해수 중의 i 성분의 평균 농도 X 전 해수량 해저 퇴적물 중의 i 성분의 평균 농도 X 연간 퇴적량 전 해수량 l, 37X1021/ 와 연간 육지에서 풍화된 암석량 2.0X1015g, i 성분의 해수 중의 농도를 mµg /1 , 지각 중의 그 농도를 Cµ g /1 라 하면 T(년) 12. . 3o7x X101 01251 xX Cm =6.8X10 멸 이 얻어전다 (N i sh i mura, 1992). Nis h im ura (1 992) 는 알루미늄 평균 체류시간 T=60 년과 지각의 알루 미늄 농도 81300 pp m 과 해수의 알루미늄 농도 1 µg /l 를 이용하여
T (년) =4. 1 X 105쁘 C 울 얻었다. 위 식을 상용대수를 취하면 lloogg mT== lloogg C(4 1- x(6 1 . 06 시— + lolog gT m) - lo g C 가 된다. 이 관계식에서 보면 동일한 체류시간을 가지는 원소 는 기울기 가 같다. 죽 지각 중에 농도가 높은 원소가 해수 중에 높고 체류시간이 긴 원소가 해수 중에 높은 농도를 나타낸다(그립 9-7 ) . 해수와 하천수의 평균 화학 성분과 계산된 원소의 평균 체류시간 (MORT) 은 표 9-6 과 갇다. 9-4 해양 되적물 해양 퇴적물은 해저 퇴적 지형에 따라 천해성 대륙봉 퇴적물과 심해 생물 기원 퇴적물로 대분된다. 대륙붕에서는 주로 셰일, 사암류, 탄산암 류가 퇴적되고 대륙사면에서 슬럼프 (slum p s) 퇴적물과 저탁충(tu rb i d it es) 이 되적된다. 십해 해양분지에서는 방산층 연니 (radio l arian ooze), 유공 충 연니 (fora m infer a ooze), 규조 연니 (dia t o m ooze) 와 같은 심해성 퇴적 물(pe la gi c sedim en t)이 되적된다. 대륙 주변부에 심해 퇴적물 중의 퇴적 후 과정 (po st- d epo s it ion al p rocess) 에 의해 네펠로이드 충 (ne p helo i d laye r ) 이 형성되기도 하고 심해저에서는 망간 단괴 등이 형성되기도 한다.
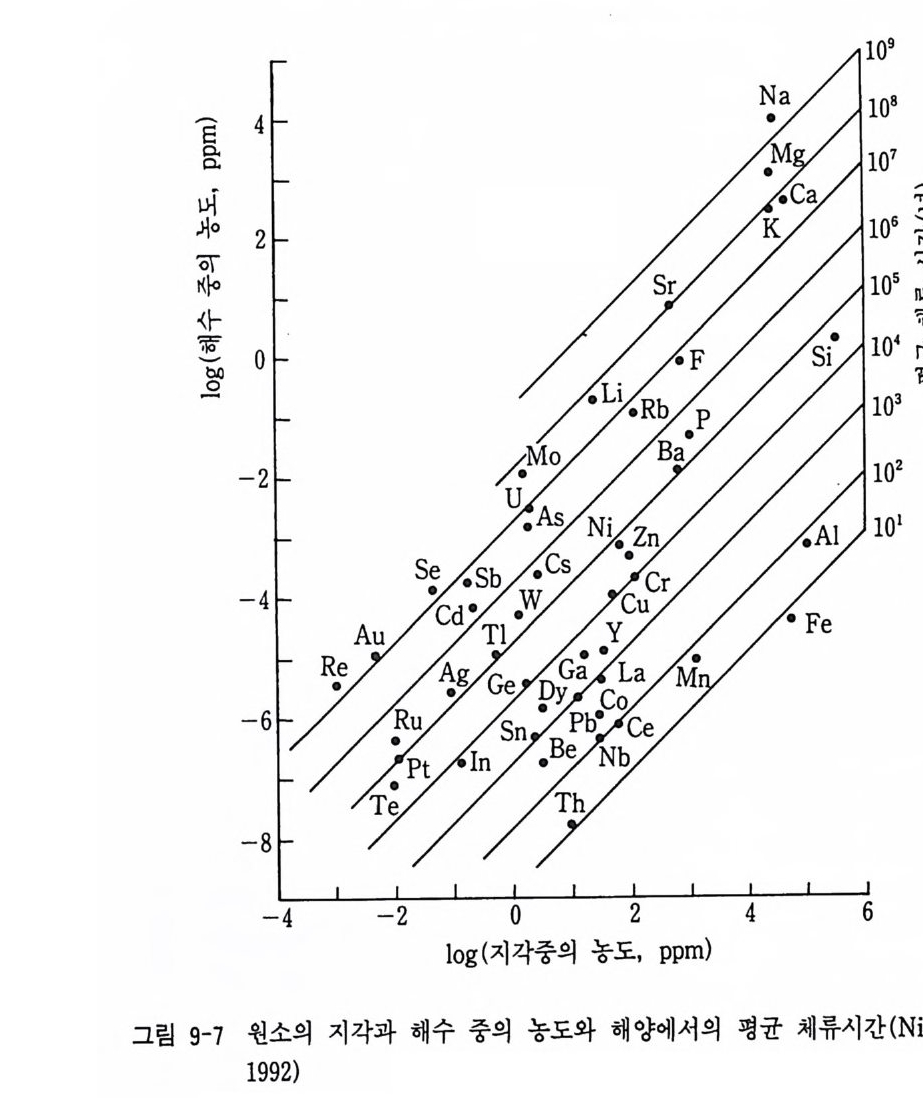 ~g 41 - . / A l11000987
~g 41 - . / A l11000987
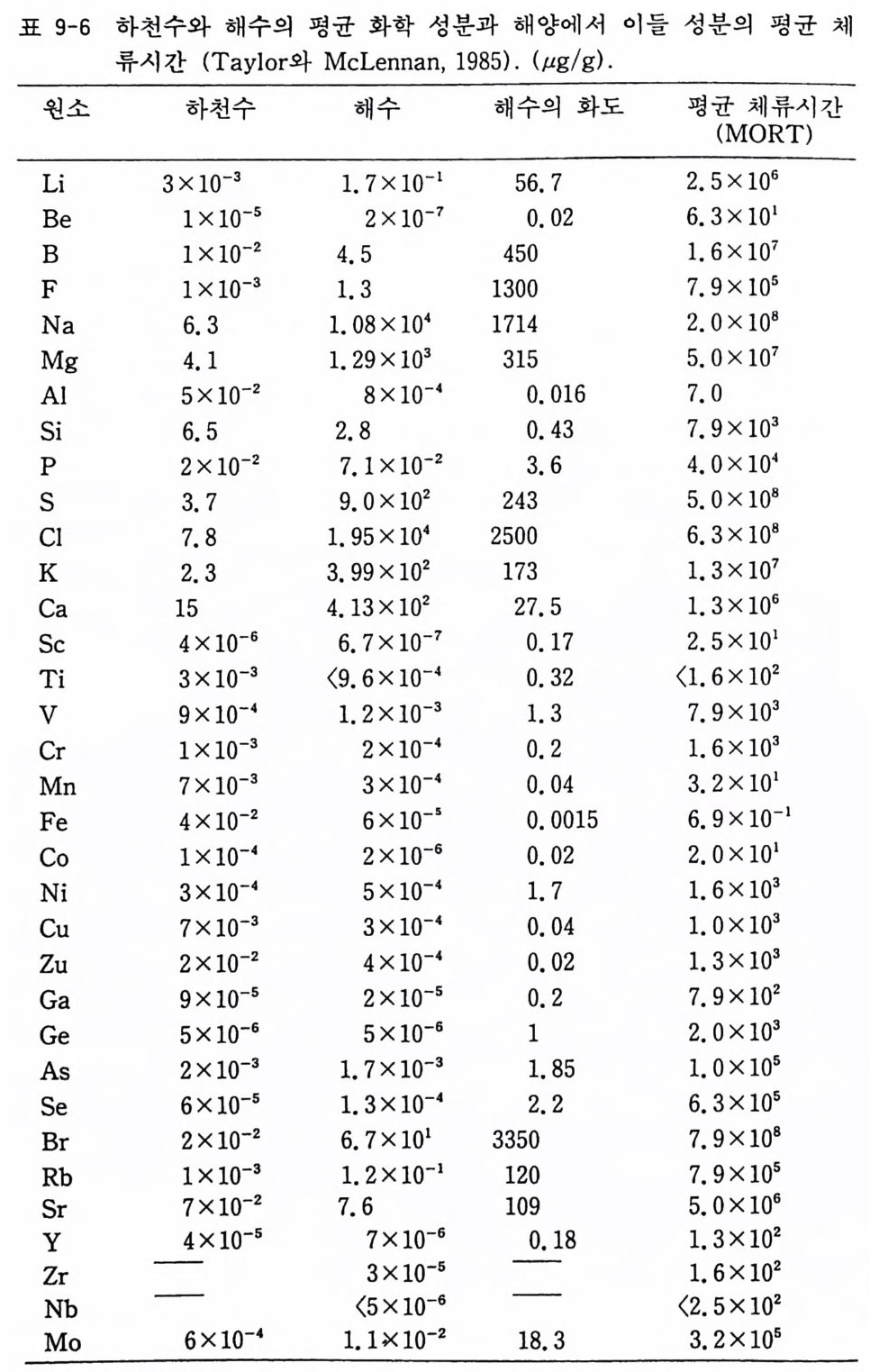 표 9-6 하천수와 해수의 평균 화학 성분과 해양에서 이들 성분의 평균 체
표 9-6 하천수와 해수의 평균 화학 성분과 해양에서 이들 성분의 평균 체
 원소 하천수 해수 해수의 화도 평균 체류시간
원소 하천수 해수 해수의 화도 평균 체류시간
(1) 대륙붕 지역 퇴적물 대륙붕 지역에는 주로 대륙 지역에서 풍화 침식된 퇴적물이 운반, 퇴 적된다. 해수면이 낮을 때에는 조립질 퇴적물이 퇴적되고 세립질 퇴적물 은 파도나 해류에 의해 대륙붕 끝부분 (she lf ed g e) 에 재되적된다. 대륙붕 끝부분은 불안정하여 저탁류에 의해 조립질과 세립질 퇴적물이 대륙사면이나 대 륙융되 (conti ne nta l rise ) 지 역 에 저 탁충을 대 량 되 적 시 킨 다. 이 지역에서는 해저 석유 또는 천연가스 포함 지층이 부 존 될 수 있 다. (2) 대양저 평원 퇴적물 대양저 평원에는 대량의 생물 기원 퇴적물이 퇴적되며 유공충, 방산 충, 익족류(pt ero p od), 규조류 등의 미생물의 유해로 구성된 석회질 연 니충이 퇴적된다 . 심해 퇴적층 중 저서성 유공충 퇴적물 등의 산소 동위 원소 분석 연구로 과거 해양의 해수면의 변동, 해수온 등의 환경 변화의 . 많은 정보를 얻고 있다. 그리고 심해저에는 자생 기원 퇴적물 (au thig en ic sedim ents ) 로 망간단괴 (mang an ese nodule) , 제 올라이 트 (zeoli te) , 필 립 사 이트(p h yllip s it e) 등이 퇴적된다. 구형의 노둘로 된 망간단괴가 대서양과 태평양 심해저에서 대량 발견 되었다. 수 µm 에서 10cm 이상 크기의 망간단괴는 동심원상으로 망간, 철 산화물과 수산화물의 혼합총으로 이루어져 있으며 대다수는 화산성 단괴로 되어 있으나 생물 기원의 단괴도 있다. 방사성 동위원소(책 Th, 10Be) 에 의해 측정된 망간단괴의 성장 속도는 l~10m/106 년 정도로 대 단히 느리다. 망간단괴의 화학 성분은 표 9-7 과 같다. 망간단괴의 성분은 Mn, Fe, Ni, Cu 등으로 구성 되 어 있으며 높은
함량의 Ni, Co, Cu 등으로 경제성과 개발의 홍미의 대상이 되고 있다. 망간단괴는 퇴적 환경에 따라 그 성분이 현저히 다르다. 참도 (seamount) 나 해 령 에서 성 장한 노듈에는 Cu, N i보다 Co 함량이 높다. 그러 나 Mn/Fe 의 비는 심 해 성 망간단괴 (aby ss al nodule) 와 큰 차이 가 없다(표 9-7).
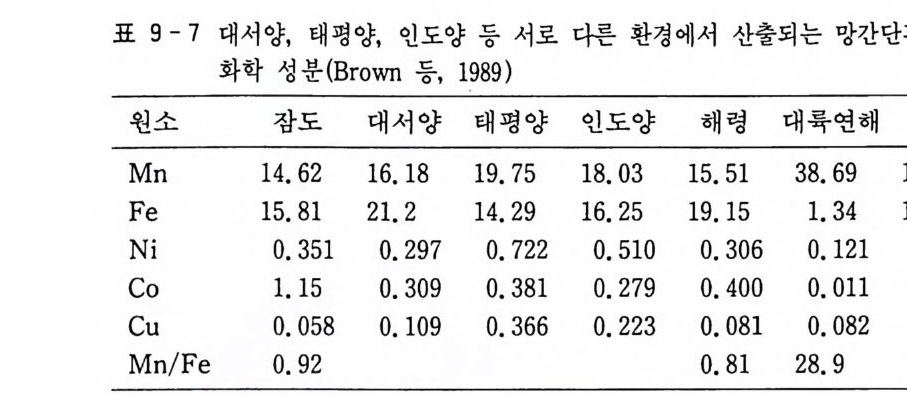 표 9 -7 대서양, 태평양, 인도양 등 서로 다른 환경에서 산출되는 망간단과의 평균
표 9 -7 대서양, 태평양, 인도양 등 서로 다른 환경에서 산출되는 망간단과의 평균
망간단괴의 단면을 조사해 보면 유공충 껍질, 부석 조각, 상어 치아, 산호 조각, 고래 뼈나 먼저 형성된 노듈 조각을 핵으로 해서 노듈이 성 장한 것을 알 수 있다. 망간 광물은 토도로카이트(t odorok it e) , 버네 사이 트 (b i rness it e) 와 o-Mn02 등으로 구성되어 있다(B urns 등, 1974). 노듈의 전자현미경 연구에서 노듈의 껍질에 다양한 박테리아가 관찰되 었다(그립 9-8) (Burne tt와 Nealson, 1981). 즉 Mn( Il ) 산화형 박테리아, Mn(N) 환원형 박테리아와 비산화형 Mn(Il) 및 비환원형 Mn(N) 의 3 종류의 박테리아가 망간 노듈 형성에 작용하고 있음이 밝혀졌다. 예를 들면 모든 Mn(Il ) 산화형 박테리아 군은 퇴적물이나 노돌에서부터 고립 되 어 Mn( N) 산화물각의 Mn2+ 만을 산화시켜 철망간 산화물의 노듈의 껍질을 만든다. 중성과 알칼리 p H 에서 Mn(N) 산화물은 Mn2+ 이온이나 양이온 제거
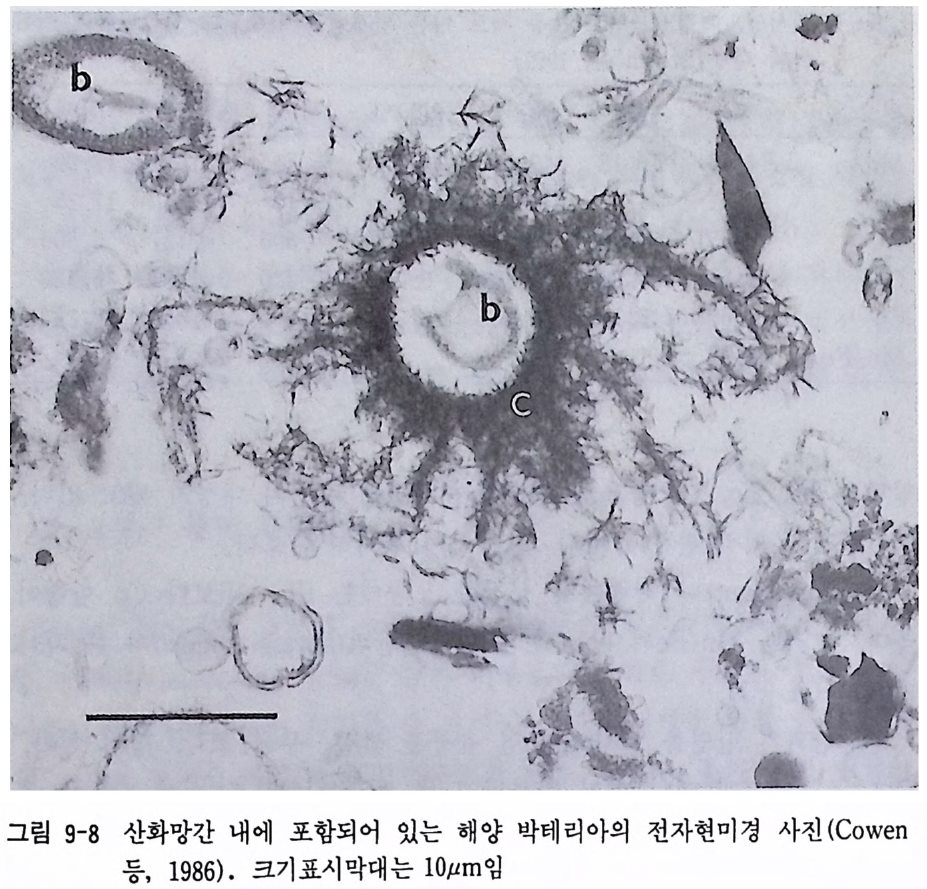 혼 `、 · J.
혼 `、 · J.
제의 역할을 한다. Mn(N) 산화물은 망간 산화 작용의 산물로 이 산화 작용 과정에서 새로운 양이온 제거 부분이 될 껍질을 만들게 된다. 이러 한 과정에서 망간단괴는 계속 성장하게 된다. Mn(N) 산화물의 양이온 제거 작용 (scaven gi n g acti on ) 과정 에서 다음과 같이 기 타 양이 온들도 노 듈에 들어가게 된다. H2Mn03+X2+ ;::=::= XMnOa+2H+ 여기서 x2+ 는 Co2+, Cu2+, Ni 2+ 이온 등이다.
제 10 장 생물 지구화학 대기권, 수권, 생물권 및 암석권 사이에는 뭉질의 순환이 일어나고 있 으며 이들 각 권 사이에 물질평형이 유지되고 있다. 또한 대기권, 생물 권, 수권, 암석권에서는 많은 유기 물질 등이 지질 과정 변화에 영향을 주고 있다. 지표의 많은 생물과 미생물들이 지표의 변화와 대기의 환경 변화, 지 구 생물계의 변화에 영향을 주고 있다. 퇴적암 내에서 산출되는 유기 화 합물은 퇴적 환경사 해석에 중요하게 이용되며 유기 퇴적물은 석탄, 석 유, 천연가스 등의 화석연료 자원을 형성하게 된다. 이와 같이 생물의 활동에 의해 일어나고 있는 지구상의 물질의 변화나 지질 현상을 연구하 는 학문이 지구생물학(g eob i olo gy)이며 이들을 화학적 방법으로 해석하는 학문이 생물지구화학 (b i o g eoche mi s try)이다. 그리고 자연에 산출되는 탄 소질 물질의 지구화학적 연구가 유기 지구화학 (or g a ni c g eoche mi s try)이
다. 최근 다양한 미생물들이 지질 작용과 환경 변화에 작용하고 있어 지 구미생물학(g eom ic rob i olo gy)이라는 새로운 학문이 탄생하였다. 10-1 물질의 순환 (1) 탄소의 순환 대기의 화학 성분은 질소 78. 08 %, 산소 20.95 %로 전체의 99 %를 차지하고 있으며 나머지 1 %가 아르곤, 이산화탄소, 수증기, 네온 등으 로 되어 있다(표 10-1). 대기중의 CO 2 는 320 pp m/ 체적, 약 0.0 3 %로 미 량 존재하지만 생물의 광합성 작용이나 유기물의 기본 구성 원소로 대단 히 중요하다. 탄소는 무기기원 및 유기기원의 탄소가 있으며 가스상의 CO2 와 HCQ 3 -H2C 0 3 등의 다양한 형태로 존재한다. 탄소는 지구물질 중 탄산염 퇴적암과 생물체, 죽은 유기물질(단백질, 탄수화물, 부식산, 탄 화수소, 탄산칼슘) 등에 주요 성분으로 포함되어 있다. 대기의 C 아와 해양에 용존하고 있는 CO2 는 범지구적으로 평형에 있 다. 그리고 용존하고 있는 기타 탄소종 사이에도 다음과 같은 평형을 생 각할 수 있다. CO2 (ga s) ~ CO2 (aq) (10·(1,’1·0, l (2l01(3 0 4 H2C02 ~K, HCOa + H+ ,I` HCOa -k= co~-+ H+ ·1·’ CO2+H20 ~ H2COa `d_ _ 25·c 에서 위의 (10.2) 와 (10.3) 반응식의 평형상수는 각각
Kl = aHC05 , aw = 10_6.3 5, att 2C 03 K2=~=10-10.33 aHco, 이며 반응식 (10.4) 의 CO2 평형상수는 Keo 톤 aH2C03 = l0-I.47 Pco, 로 계산된다. 위의 평형상수 관련 (IO.I), (10.2), (10. 3) 식에서 Pcoz, H2C03, HCOa, CO i-의 활동도와 p H 의 미지수가 있어 2 가지의 미지수 의 정보가 얻어지면 각 탄소종의 활동도를 결정할 수 있다. 예를 들면 강수의 p H 를 측정하면 현재 대기 중의 PC02 를 계산할 수 있다. 물론 이 때에는 현재의 대기 중의 CO2 와 강수의 CO2 가 평형에 있다는 가정이 필 요하다.
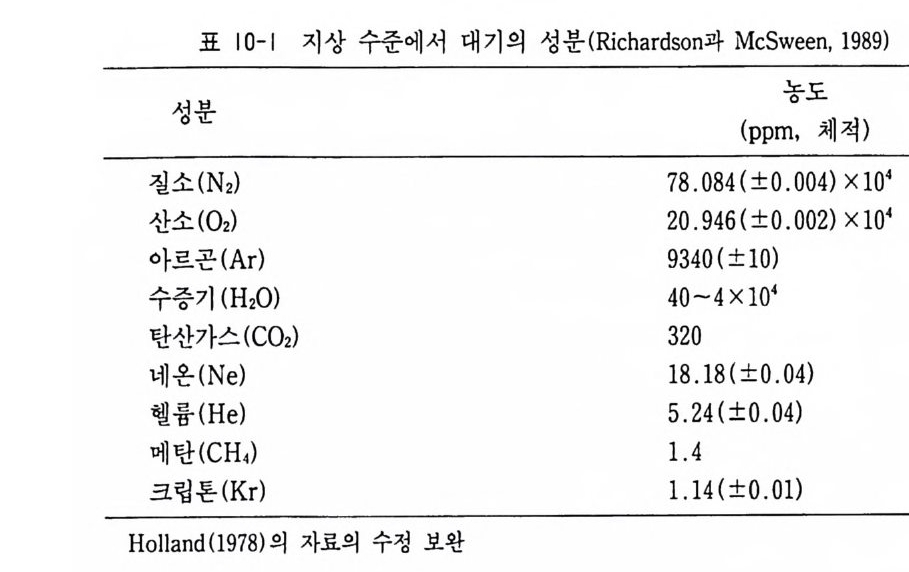 표 10-1 지상 수준에서 대기의 성분(Ri chardson 과 McSween, 1989)
표 10-1 지상 수준에서 대기의 성분(Ri chardson 과 McSween, 1989)
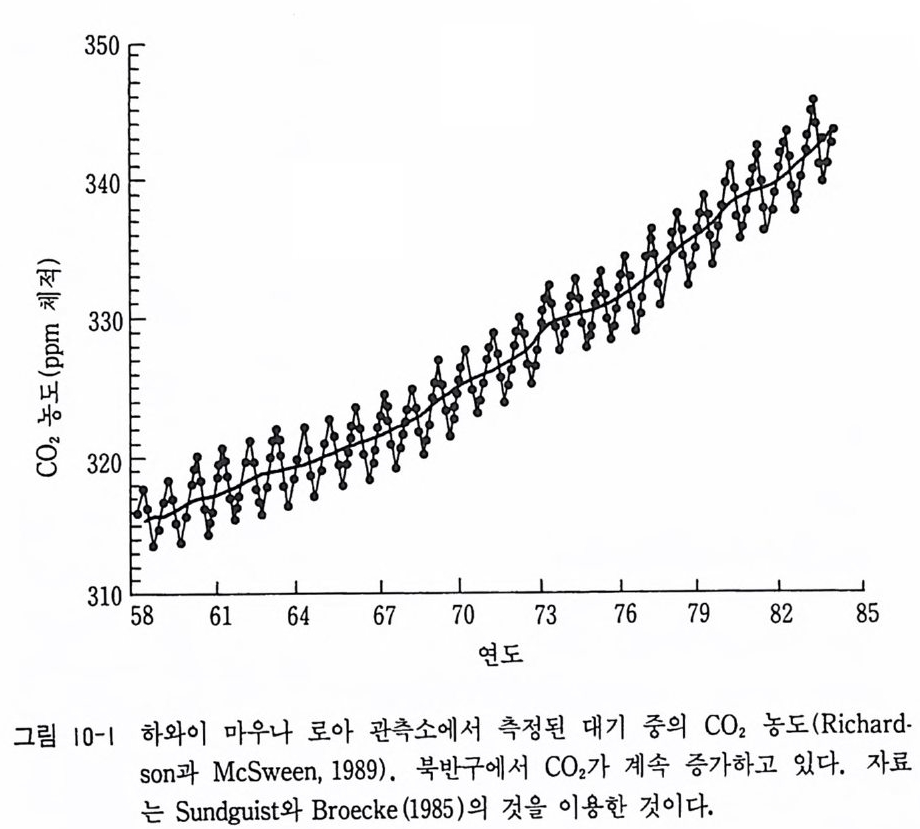 350
350
강수의 aw=l0-5'65 , mw=m tt co3+2mco J-를 위의 식에 고려하면 5 개의 미지수와 5 개의 식이 되어 PC02 의 해가 다음과 갇이 얻어진다. ( mw) 2= mtt co 3 ( mw + 2K2) mtt co , = Pco2Kco2K1/ mH + Pco, Kco2K1/ m(mw3 H ++ 2K2) 측정된 pH =5.65 값을 대입하면 Pco2=331 pp m 이 얻어진다. 실제 하와이의 마우나로아에서 측정 된 대 기 중의 CO2 의 농도는 1958 년 315 pp m 에서 1980 년 339 pp m 으로 매년 증가하고 있다(그립 10-1) . 대
기 중의 co 가 광합성과 호흡 작용에 의해 매년 약 6p pm 증감의 지그 재그 패턴을 나타내고 있다. 이는 화석연료의 사용 증가로 대기 중의 co 가 증가하였기 때문이다. 이 기간 동안 사용된 화석연료는 84.5X 1015 g C(Marland 와 Rott y, 1984) 로 51 X l015 g C 의 co 가 생성되었으며 이 중 60 %가 대기 중에 잔존하고 있다. 나머지 40 %는 탄소의 순환에 사 용되었다. 지구의 탄소의 최대 저장소로는 대기권, 수권(해양) 및 암석 권이다(그립 10-2). 이 중 해양이 가장 큰 CO2 순환(교환) 저장소이다.
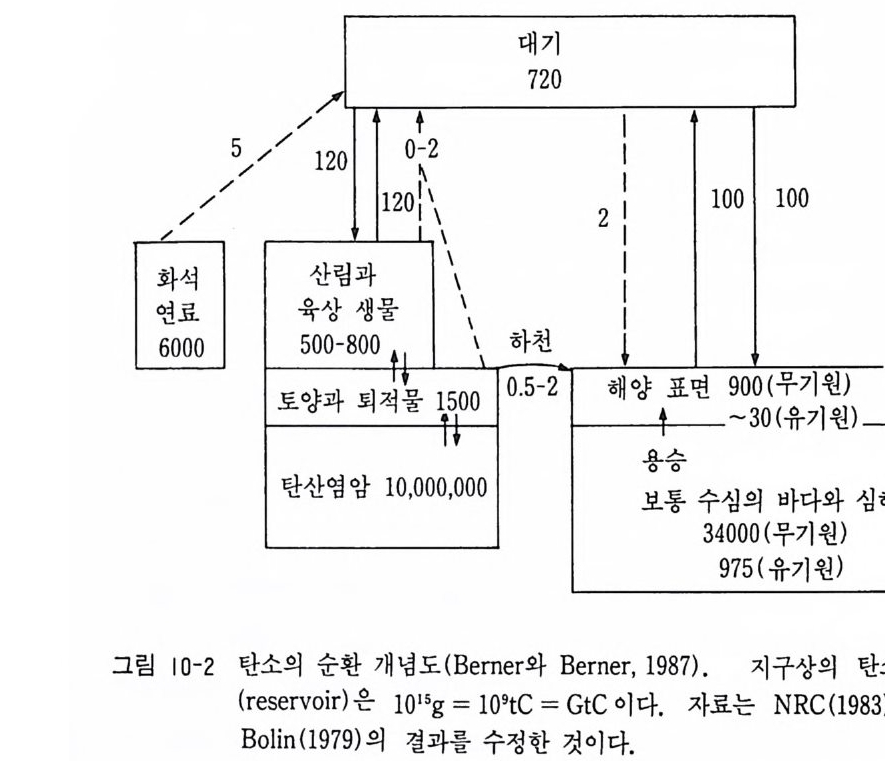 대기
대기
죽해수에서 CO2 +coi- + H 2 0 —+ 2HCOa
로 대기-해수 CO2 평형에서 과잉 CO2 는 Ca2+ 이온과 함께 다시 탄산염 암으로 침전되어 암석권으로 되돌아가게 된다. 물론 탄산염 침전 의에도 해양 생물의 광합성 작용이나 육지의 산림, 토양 등의 생물권에도 다량 의 탄소가 저장된다. 그러나 Woodwell 등(1 983) 에 의하면 산림벌채 (defo r esta t io n ) 로 발생 한 CO2 에 서 조림 (fore sta t io n ) 시 에 생 성 된 CO 2 를 뺀 값인 1. 8~4.7 X l015 g C / 년의 CO2 가 대기로 방출된다고 보고하였다. 즉 인간활동에 의해 증가되는 CO2 (a nth ro p og e n ic CO 2 ) 는 A 는 F - S-B 로 계산된다. 여기서 A 는 대기 중의 연간 CO2 증가량, F 는 연간 화석연료 에 의해 발생되는 CO2 양, S 는 해양에 연간 저장되는 양, B 는 생물권 에 사용되는 CO2 양이다. 열대 립의 급속한 파괴와 화석 연료 사용으로 증가된 CO2 가스는 CH4 , N02 등의 가스와 함께 온실효과 (gree nhouse effe c t) 를 일으키 게 되 며 2665 년경에는 대기 중의 CO 2 의 농도가 600 pp m 이 넘어 지표의 기온이 2.0~3.o·c 증가 (NRC, 1983) 할 것으로 추정하고 있다. 이같은 기온의 증가로 그린란드나 남극의 빙하가 부분적으로 녹고, 가열로 인해 해수가 증가하여 해수면이 다음 세기에는 0.7 m 상승하여 지구 규모의 물의 순 환 (h y drolo gi c c y cle) 에도 영향을 주게 될 것으로 추정하고 있다 . (2) 탄소의 순환과 미생물 광합성 , 동물의 호흡, 공업 활동 등이 탄소의 순환에 주는 영 향에 비 하면 미생물에 의한 영향은 적다. 그러나 미생물은 생명현상에 필요한 에 너 지 ATP (adenosin e trip h osph a te ) 를 발효, 호흡 광합성 과 감은 방법 으로 얻기 때문에 탄소의 수지에 영향을 준다. 예를 들면 메탄 생성 세균이 H2 를 CO2 로 산화시켜 ATP 를 만드므로 C 아를 호흡하게 되어 CO2 를 소비하게 된다. 미생물 중에는 광합성을 하 는 조류나 광합성 세균이 있어 C 아를 사용한다. 광합성을 하지 않는 미
생물은 유기물을 분해시켜 CO2 를 만든다. 독립영양 화학합성 세균은 빛 의 유무에 관계없이 CO2 를 사용하는 미생물이다. Meth a nobact er i um omel i ansk ii와 같은 메 탄 생 성 세 균은 CO2, 착산, 메탄올, 메틸아민 등의 탄소 화합물을 이용하여 CH4 를 만든다. 따라서 최근 대 기 중에 CO2 뿐만 아니 라 CH4 의 양이 증가하고 있다. 이와 같이 고등식물, 조류, 광합성 세균, 독립영양 화학합성 세균 등이 CO2 를 이 용하여 생체를 구성하는 유기물을 만들기 때문에 토양, 하천, 해양 등에 널리 분포하고 있는 미생물이 지표의 CO2 를 소비하고 02 를 생성하여 지 구 환경 변화에 영향을 주고 있다. (3) 질소의 순환 질소는 탄소와 같이 동식물의 중요 구성 성분으로 자연계에서 미생물 학적 지구물질 순환을 계속하고 있다. 질소는 N2, N20, N02, NO, NH3 형태로 산출되며 80 % 이상이 질소 기체로 존재하는데 화학적으로 비반응성이므로 생물체가 이용하기 위해서는 H, C, 0 와 결합하는 생물 학적 질소고정 작용 (bio lo g ical nit rog e n fixa ti on ) 이 대 단히 중요하다. 주요 질소고정 작용은 표 10-2 와 같다. 자연계에서 청록 조류식물에 의해 대부분 질소고정이 일어나며 콩의 재배와 같은 과정에서 약 30 %의 질소고정이 일어난다. 고정된 N 는 탈 질소화 작용 (den it r ifi ca ti on) 아나 박테리아에 의한 질산 환원에 의해 다시 대기로 환원되어 순환이 일어난다(그립 10-3). 화석연료 사용 및 산업화 에 따라 대기 중에 NOx(N02, NO) 가 1940 년 2x1012 g N/ 년에서 1980 년 약 6 . 3 X1 012 g N/ 년으로 계속 증가하고 있으며 대 기 중의 NH3 은 대 기 중의 H2S04 에어로졸과 반응하여 (NH4)2S04 에어로졸울 형성하여 대기 오염에 관여하고 있다. 인간활동에 의해 증가된 NOx 는 아시아 대륙 오염 지역에서는 NOa 5
mg /I 포함된 강수에서 연간 2.2T g N이 되적되어 생성과 되적이 평형에 가깝다. 그러 나 토양이 나 방전 (ligh tn ing ) 과 같은 자연 발생 NOx 는 25 % 내의이고 화석연료 사용으로 NOx-N 생산이 대단히 증가하여 산림 연소 에서 생성된 것과 합하면 NOx-N 생성의 75 %가 인간활동에 의해 형성 된 것이다. 즉 인간활동에 의해 질소의 지구화학적 순환의 불균형이 초 래되고 있다.
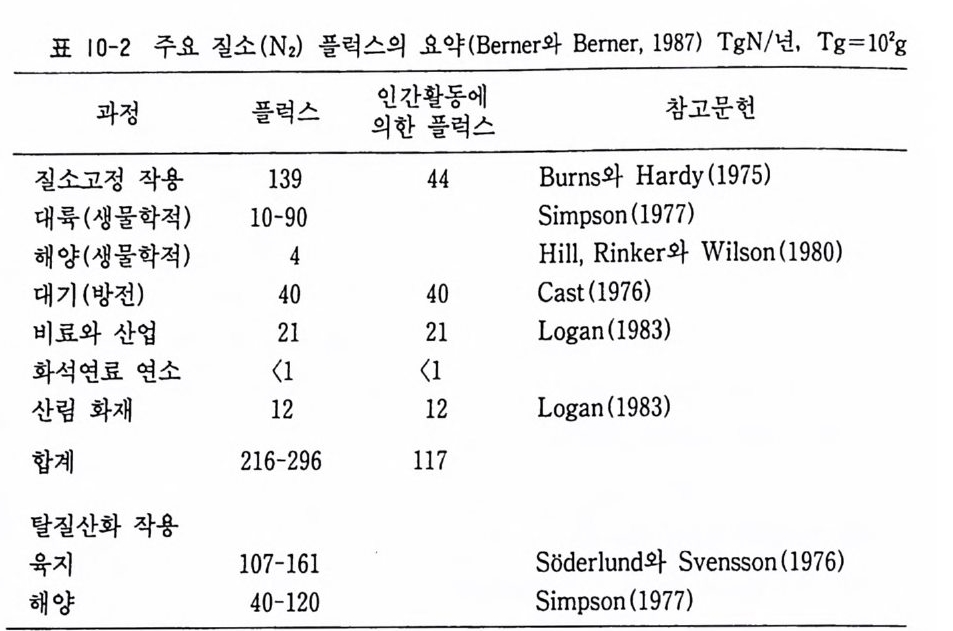 표 10-2 주요 질소 (N2) 플럭스의 요약(B erner 와 Bemer, 1987) T g N / 년, Tg = l02g
표 10-2 주요 질소 (N2) 플럭스의 요약(B erner 와 Bemer, 1987) T g N / 년, Tg = l02g
10-2 미생물 지구화학 다양한 미생물들이 암석의 풍화, 토양과 퇴적층 형성과 변형, 광물의 생성, 화석연료의 생성 등의 여러 지질학적 과정에 작용하고 있다. 미생 물들은 생명현상에 필요한 에너지 (ATP) 를 발효, 호흡, 광합성과 갇은
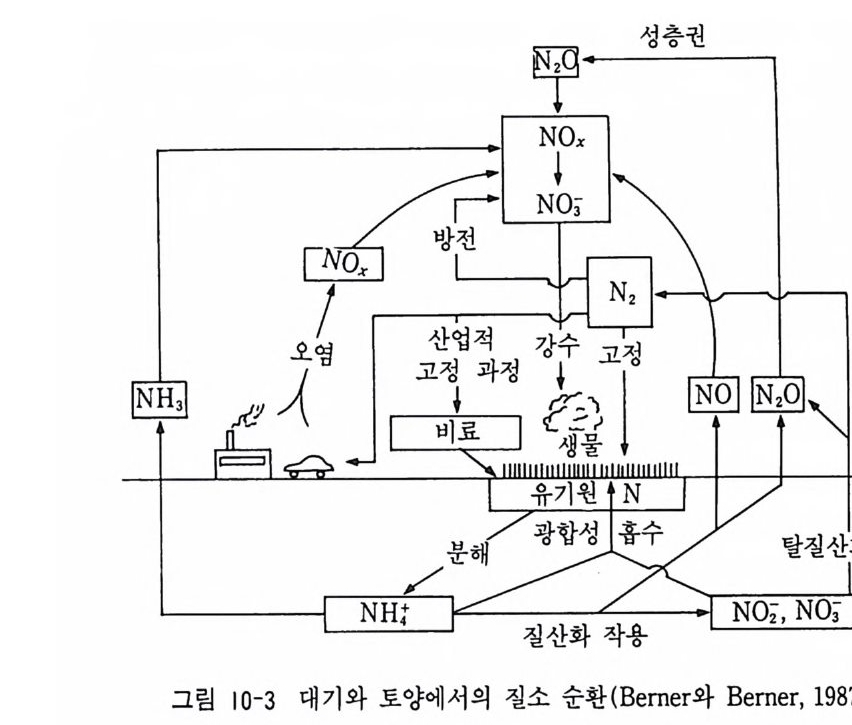 麟 성층권
麟 성층권
방법에서 얻는다. 최근 생물지구화학 분야와 밀접하게 지구미생물학, 미 생물 생태학(mi crob i al ecolog y), 미생물 생물지구화학(mi crob i al bio g e o - chemi str y ) 등의 학문 분야가 생기게 되었다. 마생물이 현재나 과거 지 질시대의 지질 과정에 작용한 역할을 연구하는 새로운 학문이 지구미생 물 학 (ge om icr obiC Jl og y) 이 다 (Ehrlig h, 1990, Beerstr ec her, 1954, Kuznets o v 의, 1963). 원핵세포생물(p roka ry o t es) 과 진핵세포생물 (euka ryo t es) 과 같 은 미생물이 광물을 산화시키거나 환원시키기도 한다. 생물권에서 미생 물은 물질의 농집제 (ag en ts of concentr at i on ) , 물질의 확산제 (age n ts of dis p e r sio n ) 및 물질의 분별제 (age n ts of frac ti on ati on ) 등으로 작용하여 암 석 화 작용 Oithifica ti on ) , 광물의 형 성 , 암석의 풍화, 속성작용, 퇴 적작용 등에 직접적으로나 간접적으로 작용한다. 또한 미생물은 지구화학적 과
정의 촉매제의 역할을 하기도 한다 . 미생물은 발효 작용과 같이 직접적 으로 지질 과정에 영향을 주기도 하며 미생물의 물질대사 산물의 화학적 작용이나 세포 표면에 불용성 물질을 농집시키거나 지질 환경의 Eh -pH 조건을 변화시키는 등의 간접적인 영향을 주기도 한다. 물질대사는 호기성 또는 협기성 (aerobic or anaerobic ) 조건에서 동화작 용 (anabo li sm) 이나 이화작용 (ca t abol i sm) 을 일으킨다. 체세포 분열을 하 는 뚜렷한 핵이나 염색체를 가지고 있지 않은 원핵세포의 호흡 작용에서 일부 무기화합물을 산화시키거나 환원시켜 침전이나 용해시킨다. 일부 화학무기 영 양 박테 리 아와 혼합영 양 박테 리 아 (chemoli tho tr o p hi c and mix - atr op h i c bact er i a) 는 H2, Fe ( Il ) , Mn ( Il ) , H2S, S0 등과 같은 일부 무 기 물질이 산화할 때 발생하는 에너지롤 사용한다. 광무기영양 박테리아 (ph oto l it ho tr op h i c bacte r ia) 는 황이 퇴 적 되 거 나 CO 2 가 동화될 때 의 환원 력으로 H2S 를 사용한다. (1) 독립영양 박테리아 무기 화합물을 02, NO i나 빛 에너지를 이용하여 산화시키고 CO2 에서 세포의 구성 성분을 합성하는 박테리아를 독립영양 박데리아라고 한다. 독립영양 박테리아는 자연계 물질의 거동과 관계가 깊다. 예를 들면 암 모니아 산화 박테리아 및 아초산 산화 박테리아는 각각 NH3 및 NO i를 산화시킬 때의 에너지를 이용하여 ATP 및 CO2 환원에 필요한 NAD (P)H 를 생성한다. 독립영양 화학합성 박태리아는 보통 무기 화합물에서 만 생 육한다 (그립 10-4) . 주요 독립 영 양 화학합성 박테 리 아의 종류는 표 10-3 과 같다. 협기성 호흡 유기물은 대기 중의 산소가 결핍된 환경에서 유기물질의 광화 작용에 대단히 중요하다. 호기성 조건에서 미생물에 의한 유기물질 의 광화 작용으로 C02, H20, N05, SOt , POt 등이 형성되는 반면에
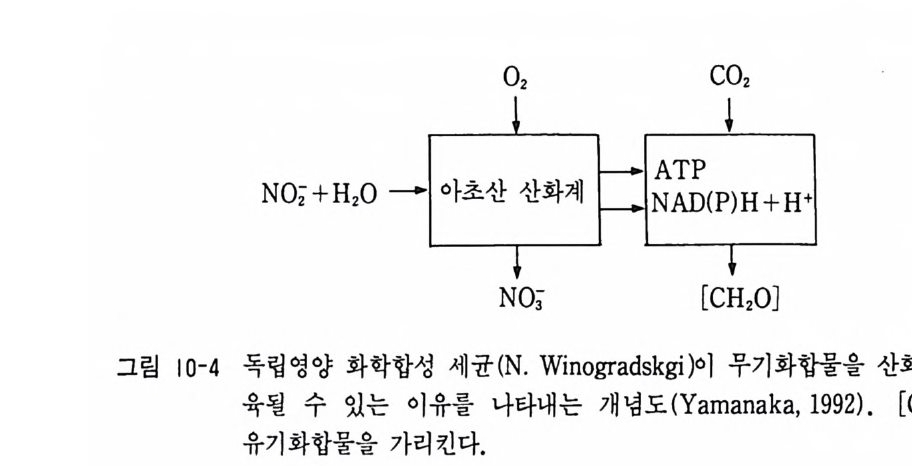 02 ci 0'2
02 ci 0'2
 표 10-3 주요 독립영양 박테리아의 종류 (Yamanaka, 1992)
표 10-3 주요 독립영양 박테리아의 종류 (Yamanaka, 1992)
협기성 조건에서는 CH ◄, CO2, NH3, H2S 등이 형성된다. 화학 합성 박 데리아와 광합성 박테리아와 같은 지구미생물은 환경 연구, 금속 자원의 농축, 지구의 생명의 진화 등의 연구에 크게 기여하게 될 미래의 연구 개발 대상이다. (2) 미생물의 지구화학적 작용 미생물은 지구물질의 농집, 확산, 분별 등의 지질 작용과 지구화학 작 용에 중요하게 작용하고 있다. 미생물은 발효, 호흡, 광합성의 과정에서 생명현상에 필요한 에너지인 ATP 를 만든다. 발효는 산소가 없는 곳에 서 유기화합물을 유기화합물로 산화시켜 ATP 를 만드는 에너지를 얻는 과정 이다. 호흡은 유기화합물이나 무기화합물을 02, so~-, NOa 등으로 산화시켜 ATP 를 생성하는 과정이다. 그리고 광합성은 빛에너지를 이용 하여 ATP 를 만든다. 그림 10-5 에서 ATP 에서 세번째의 인산이 가수분해되어 ADP 가 되는 데 이때 약 8kcal/mo! 의 자유에너지를 방출하게 된다. 즉 ADP 와 인산 에서 ATP 가 합성되 려 면 발효, 호홉, 광합성 등의 과장에서 8 kcal/ mo ! 이상의 에너지를 공급받아야 된다. 발효, 호흡, 광합성 과정에서 ATP 형성 방법과 마생물과의 반응의 실례는 표 10-4 와 같다. 모든 유형의 박테 리 아를 포함하는 원핵세포생물과 조류 (al g ae) , 곰팡 이, 원생동물 등의 진핵세포생물과 같은 미생물이 메탄 형성이나 황 환 원, 철 산화 등의 지질 작용에 작용한다. 원핵세포생물의 한 종류인 유우박테리아 (eubac t er i a) 와 고박테리아 (archaebacte r ia ) 인 화학무기 영 양 생 물 (chemoli tho tro p hs : 철박테 리 아, 황세 균, 수소세균과 같이 무기물로부터 에너지를 얻어 자가영양하는 생물)은 무기 화합물의 산화와 같은 물질대사 과정에서 에너지를 얻으며 CO2, HCOa,
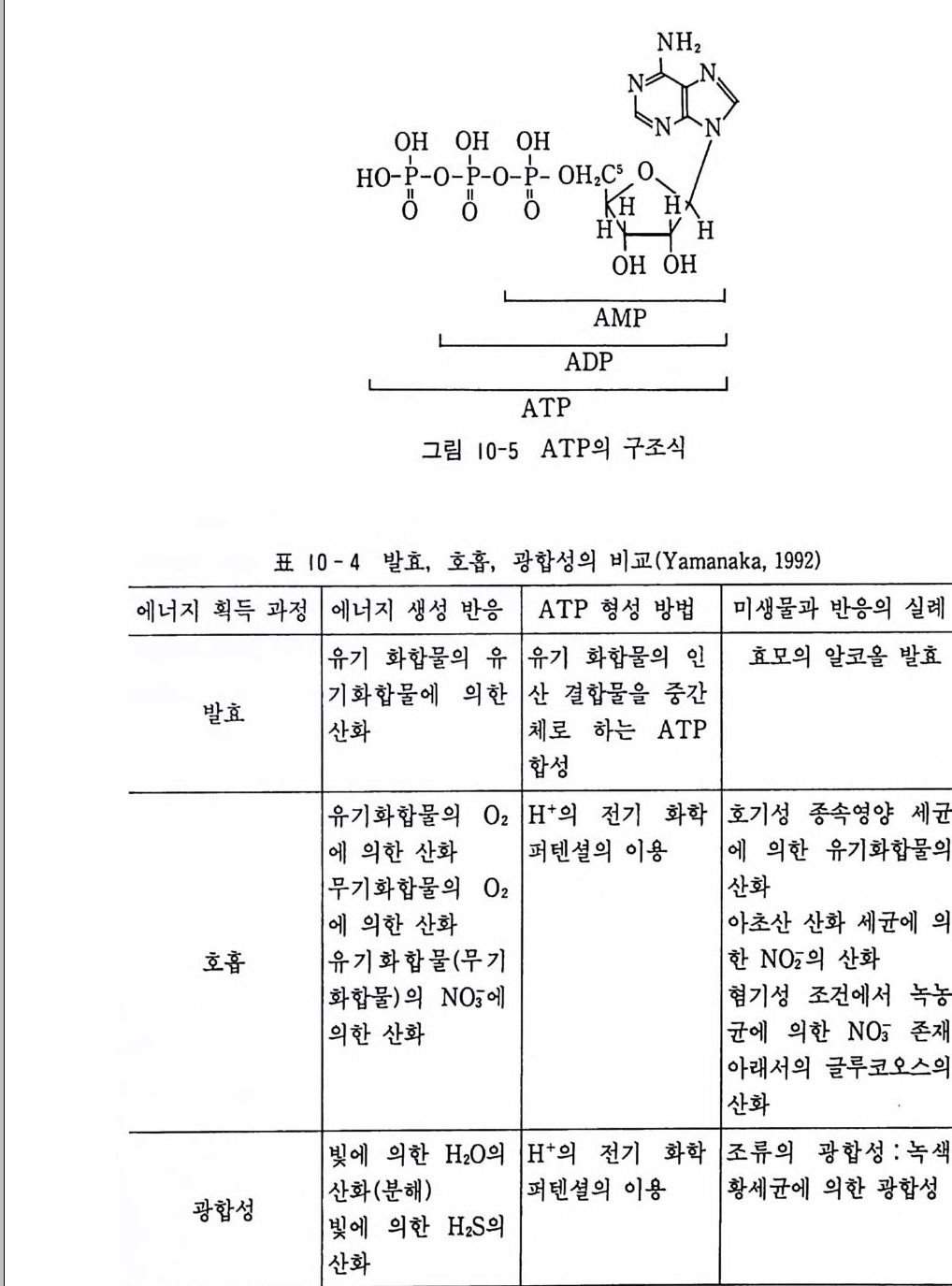 H 。 'P-I그I。O_립 _P-I0IO- 0oAD5― ―MA 二O〔\H T-\Ni\H식 OHP 2A N \/TN/ /~H
H 。 'P-I그I。O_립 _P-I0IO- 0oAD5― ―MA 二O〔\H T-\Ni\H식 OHP 2A N \/TN/ /~H
COt -동 의 탄소와 동화된다 (Wood, 1988) . 유우박테 리 아만으로 된 광무 기영양 생물(p ho t o lith o tr o p hs) 은 방사에너지를 화학에너지로 변환하는 물 질대사 과정에서 에너지를 얻으며 CO2, HCOa, coi- 등 의 탄소와 동화 한다 (그립 10-6) .
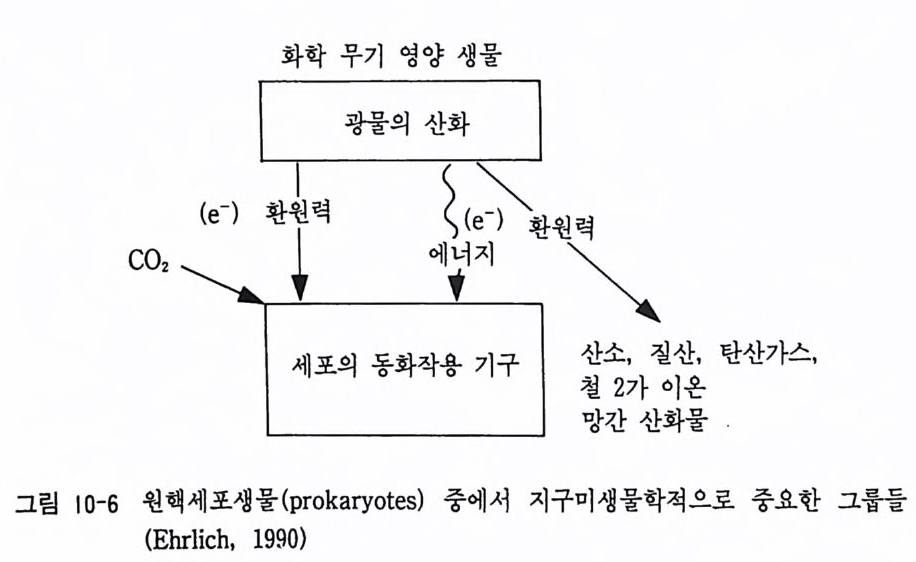 CO2 , I|」臼|화_ v 학력 釋 무7· 의영 에 양-:門i(1入 e 지 〉 o 뭄」 환원 력\
CO2 , I|」臼|화_ v 학력 釋 무7· 의영 에 양-:門i(1入 e 지 〉 o 뭄」 환원 력\
많은 미생물은 생물권과 수권에서 물질의 농집제, 물질의 분산제, 물 질의 분별제 등의 지질학적 작용제 (ge olog ica l a g en t s) 로 작용한다. 농집 과정의 예로 황박테리아는 무기 물질을 세포 간극에 집적시키며 박테리 아질의 CaC03 침전에서처럼 의부에서 세포 속으로 불용성 화합물의 침 전을 가속시킨다. 그리고 철 산화물과 망간 산화물에서처럼 금속 이온이 세포 표면에 흡착되거나 박테리아와 곰팡이에 의해 수은이 세포 내에 고 정되거나 흡착된다. 분산 과정의 예는 미생물이 CaC03, 철 산화물, 망 간 산화물 등의 불용성 물질의 용해를 촉진시키는 것이다. 분별 과정은 미생물이 혼합물에서 선별적인 화학 변화를 촉진시키거나 무기 화합물의 혼합에 선별적으로 작용하여 선별적인 농집아나 분산을 일으키는 과정이 다. 예를 들면 Thio b aci llu s fe rroox i dans 에 의한 유비칠석의 산화 작용이
나 철망간단괴에서의 Fe(Ill) 보다 Mn(N) 의 우선적인 환원, “so~- 보다 32SO t의 우선적인 환원, 13C02 보다 12C02 의 우선적인 동화작용 등을 둘 수 있다. 그리고 미생물은 지구화학적 과정에서 촉매 작용을 한다. 물질대사 과 정 (meta b oli sm ) 중 이화작용 (ca t abol i sm) 에 의해 철, 망간, 황 등의 산화 작용이 일어난다. 또한 동화작용에 의해 석탄, 석유 등의 화석연료 형성 과 같은 유기 화합물이 형성된다. 이때 작용하는 미생물은 대기 중의 산소의 유무에 따라 다르게 활동한 다. 따라서 미 생물은 산소를 필요로 하는 유기물 (aerobes) , 산소가 불필 요한 유기물 (anaerobes), 소량의 산소만을 요구하는 무기물 (m ic roaero phi l lic orga n is m ) , 산소 유무에 무관한 유기 물 (fac ulta t i ve orga n i sm ) 등으 로 구분한다.
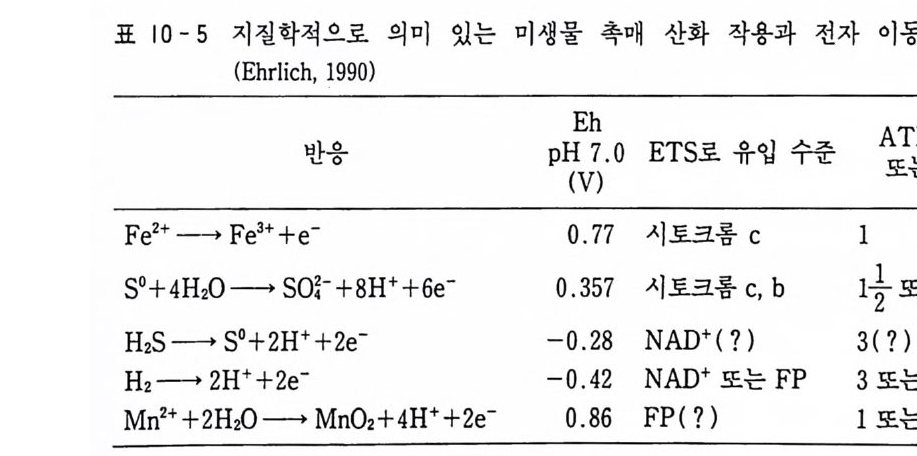 표 10-5 지질학적으로 의미 있는 미생물 촉매 산화 작용과 전자 이동 시스템
표 10-5 지질학적으로 의미 있는 미생물 촉매 산화 작용과 전자 이동 시스템
이화작용 반응시에는 수소 원자의 환원 또는 산화시에 전자의 방출 등 으로 전 자 이 동 시 스템 (electr o n tra nspo r t sys t e m ) 이 성 립 한다 (표 10-5) . 무기 물질과 유기 물질이 미생물의 작용에 의해 죽은 유기 물질을 완전 히 광화 (mi ne rali za ti on ) 시 켜 CH4, CO2, H20, H2, NHa, H2S, POt 등 을 형성하기도 한다. 이와 같은 미생물의 활동에는 온도, pH , Eh 등이
대단히 중요하게 영향을 준다.
(3) 생물 기원 탄산영암의 퇴적 카보나타이트 (carbona tit e) 와 같은 마그마에 의해 형성된 일부 탄산염 암울 제의하고 지표의 대부분의 탄산염암은 해수에서 침전된 석회암이거 나 생물 기원의 퇴적 탄산염암이다. 박테리아, 곰팡이, 조류 등과 갇은 미생물에 의해 생물학적으로 탄소고정작용이 일어나 탄산영암이 만들어 지기도 한다. 유공충과 조개류 등도 CaC03 로 형성되어 있다. 박테리아 나 곰팡이의 작용에 의해 다음 몇 가지 과정에서 미생물에 의한 탄산염 광물이 침전된다. 첫째, 중성 또는 알칼리 환경에서 탄소 화합물이 호기성 또는 협기성 산화 작용에 의해 Ca 또는 M g와 함께 아라고나아트와 같은 탄산염 광 물을 침전시킨다. 둘째, 유기 질소 화합물의 호기성 또는 협기성 산화 작용에 의해 탄산 염이 침전된다. 셋째, 황산염 환원 박테리아에 의한 CaS04 의 환원에 의하여 CaS 가 형성되고 다음과 같은 과정을 거쳐 CaCO 가 침전된다. CaS0.+2(CH2 0) 麟 CaS+2C02+2H20 CaS + 2H20 一 Ca (OH) 2+ H2S C02+H20 一 H2C03 Ca(OH )i +H2C03 一 CaCOJ + 2H20 넷째, 요 (urea) 의 수화 작용에 의해 암모니아 탄산염이 형성된다. NH2(CO)NH2+2H20 一 (NH4)2C03
다섯째, 2HC03 :;:::== CO2+H20+co~- 와 같은 반응식에서 HC03 함유 용액에서 CO2 의 유출 과정 등에 의해 탄산염 광물이 박테리아의 작용에 의해 침전된다. (4) 철-미생물 지구화학 철은 지각 구성 원소 중 네 번째로 많은 원소이며 많은 광물과 암석, 토양, 퇴적물에 포함되어 있다. 지표에 산출되는 철의 일차적 기원은 마 그마 활동의 산물이다. 그러나 휘석류, 각섬석류, 감람석, 운모류 등의 조암광물과 철 함유 광물이나 암석이 풍화되어 능철석 (s i der it e, FeC03), 침칠석 (go eth ite, Fe20 3 • H20 ) , 적철석 (Fe20 3 ), 자철석 (Fe30 ◄), 황철석 (FeS2), 티탄철석 (FeTiz 0 4), 자류철석 (FeS) 등의 광물로 구성된 퇴적 철 광상을 형성하고 있다. 광산 폐수 등에 용존하고 있는 Fe2+ 는 H2S04 가 포함되어 산성(p H=2) 이므로 공기 중에서도 Fe3+ 로 산화되지 않는다. 그러나 철은 pH 5 이하 에 서 Thio b acil lu s ferr ooxid a ns, Le ptos p irillu m Jerr oox ida ns 등의 철 박테 리아와 감은 미생물에 의해 비효소적으로 산화될 수도 있다. 또한 철은 산화 환원 퍼텐셜이나 p H 를 증가시켜도 미생물에 의해 비효소적으로 산 화될 수도 있다. Fe2+ 은 킬레이트 화합물 형성에 의해 용액에서 안정될 수 있다. Fe2+ 침전은 킬레이트 화합물이 형성될 때, 미생물에 의한 분해에서도 일어날 수 있다. Fe2+ 은 세포 표면에 흡착되어 국부적으로 농집되기도 한다. 퇴 적 환경에서 철의 미생물학적 형성과 침전은 다른 중금속 이온과 함께 철함수산화물로 동시에 침전되기도 한다. 미생물에 의한 철의 산화 • 환원 반응은 자연계의 철의 순환에 대단히
중요하다. 미생물은 철의 이동성과 철의 지역적 침전에 영향을 준다• 일 부 퇴적 철광의 형성은 철-미생물이 직접 작용하였다. 퇴적 철 광상에서 화석화된 미생물이 발견되고 살아 있는 철 산화 박 테리아가 존재하는 등의 박테리아 활동에 의해 퇴적된 증거가 많이 발견 되고 있다. 선캄브리아기의 퇴적 철 광상인 호상 철광충 (banded iro n fo rma ti on) 의 형성에서도 생물 활동이 기여하였음이 주장되고 있다 (Walker 등, 1983). 소태지원 철광상 (Bo g iro n de p os it s) 에서는 thi o b acill u s, ferr ooxid a ns, s i deroop sa 의 ge m i na t a 와 같은 철박테 리 아가 작용하였다. 박테 리 아와 곰 팡이류는 광석, 토양, 퇴적물 내의 철 광물에서 많은 양의 철을 이동시 킬 수도 있다. 철 산화 세균에 의한 금속의 침출 Thio b aci llu s fe rroox i dans 와 감은 철박테리아는 0.01~1 mM ZnS04, 0.1~10 mM CuS04, 0.1~10 mM Cr(SQ 4 )a, 0.1~10 mM CdS04, 1 µ M Hg N Oa 등이 포함된 환경에서 정상적으로 생육할 수 있다. 또한 철 박테리아는 여러 금속 이온에 대해 내성이 강하다. 황동석 (CuFeS2) 과 감은 광석 은 Fe3+, H2S04, 027}. 존재 하는 환경 에 서 다음과 같이 CuS04 를 만든다. CuFeS2 + 2Fe2 (SQ 4 ) a+ 2H20 + 302 一 CuS04 + 5Fe2SOt + 2H2S04 이 반응에 서 Fe3+ 는 Fe2+ 로 환원되 지 만 H2S04 가 존재 하여 반웅 용액 이 산성이므로 Fe2+ 는 공기가 있어도 거의 산화되지 않는다. 그런데 T. fe rroox i dans 의 미 생물이 번식 하고 있으면 공기 중의 Fe2+ 가 Fe3+ 로 산화 되기 때문에 연속적으로 Cu 가 Cu2+ 로 변화되어 Cu2+ 가 침출된다 (Yamanaka, 1992). 이는 자연에서 일어나는 현상이지만 인공적으로 미생 물을 이용하여 Cu, Mn, Bi, Zn Mo 등의 금속을 침출시킬 수 있다.
이 갇은 과정 을 박태 리 아 리 청 (bacte r ia leachin g ) 이 라 한다. 우라늄 광석 에서도 U02 + x 의 성분을 가지는 섬우라늄 광물에서 철 산화 세균을 사용 하여 U02S04 와 같은 형태로 U 울 침출시킬 수 있다. T. fe rroox i dans 는 U” 를 u6+ 로 산화시킬 수 있으며 이때 발생하는 에너지를 사용하여 CO2 룰 고정해서 미생물을 살려 번식을 계속시킬 수도 있다. Ochre(FeOOH ) 형성은 철박테리아의 산화 작용과 밀접하게 관련되어 있고 그레이 작용(gr e yi n g)은 철박테리아의 환원 작용과 밀접하게 관계 되어 있다. 환원 환경에서 호흡 작용과 같은 박테리아에 의한 철 환원 작용은 협기성 광화 작용을 증진시킴과 동시에 탄소 순환에도 중요한 기 여를 하게 될 것이다. (5) 황의 미생물 지구화학 지각에 평균 520 ppm (Goldschmi dt , 1954) 정도로 소량의 황이 포함되어 있지만 화성암아나 퇴적암에는 270-2400p pm ( Bo wen, 1979) 으로 비교적 다량의 황이 농집되어 있다. 그러나 무기기원의 황은 전하가 _2, -1, +2, +4, +6 가를 가져 자연 환경에서 다양한 황 화합물을 만든다. H2S 나 so 는 soi- , S20 i-나 Thio b acil lu s fe rroox i dans 와 같은 황 산화 박테리아나 광합성 박테리아에 의해 산화되어 so!- 가 된다. 이들 박테 리아는 이때 발생한 에너지를 이용하여 생존하고 있다. 또 SO t는 Desulf ovi b r io desulf uri ca ns 황 환원 박테리아(그림 10-7) 에 의해 환원되 어 H2S 가 형성되거나 박테리아에 의해 동화되어 함황 아미노산이 된다. 죽, 다음과 같다. S0+ 2GSH —-+ H2S +GSSG H2S+6Fea+ + 3H20 麟 Soi- + 6Fe3++8H+ Soi- + H20+2Fe 짜 麟 SO!-+2H+2Fe2+
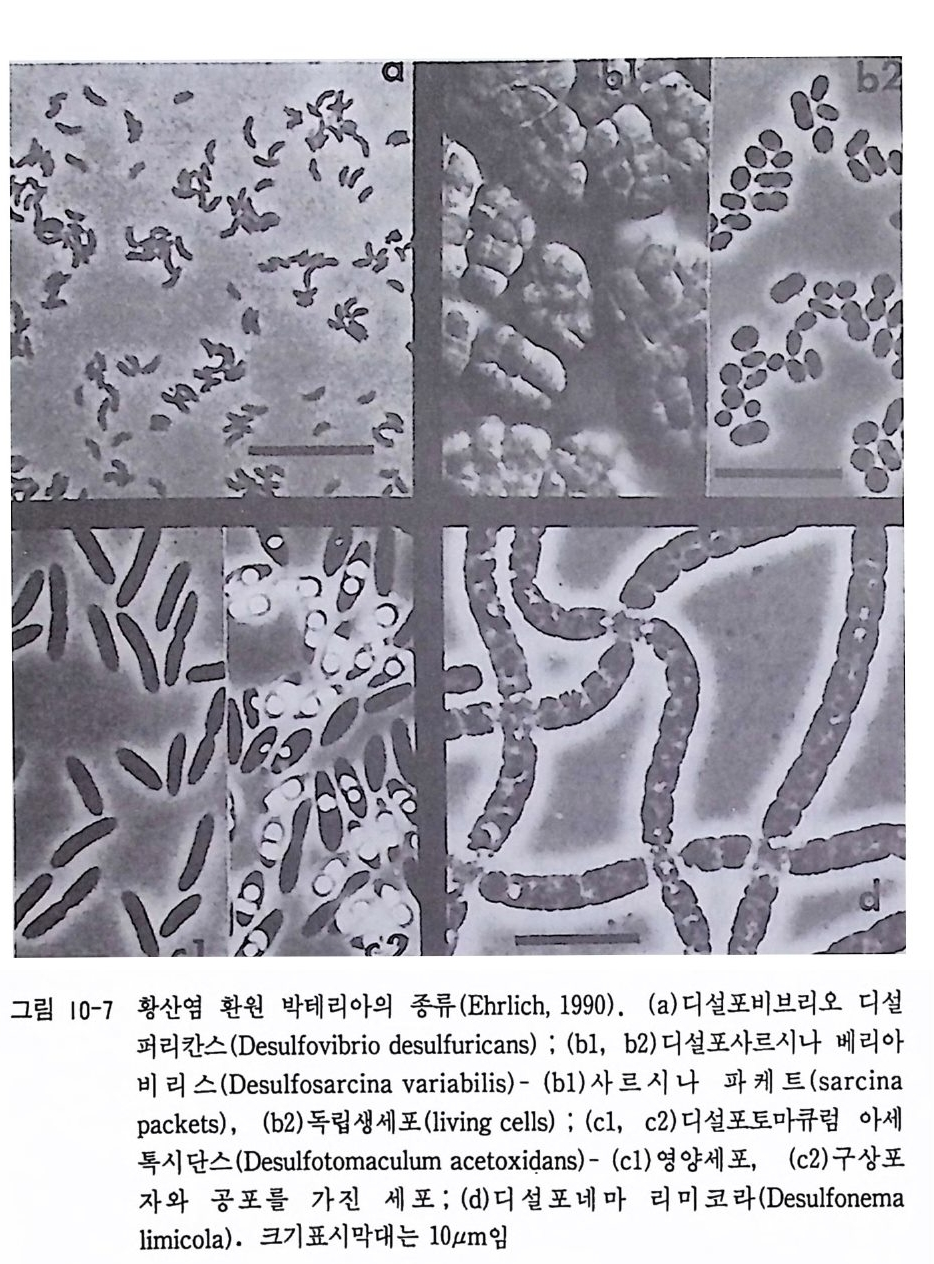 ’ ;-싼( A(`Pf`一 `* v,
’ ;-싼( A(`Pf`一 `* v,
8Fe2+ + 8H+202 ~뜨브, 8Fe3+ + 4H20 s2- 一 S0+2e S0+H20+02--+ zH++so~- S20~-+ 황 결합 단백질--+ 황 결합 단백질 -s+sm so~- + H20 一 sot + 2H+ + 2e 황철석이 다량 포함된 무연탄충이나 탄질 셰일이 분포하는 탄전 지역 의 노천 채탄장에 물이 고이면 이와 같은 황 산화 박테리아 작용에 의하 여 황철석이 산화 H2S04 를 형성하여 환경 오염원이 된다. 한편 H2S 를 산화시카는 광합성 박태리아는 호수 바닥에서 발생하는 H2S 를 산화시켜 지구 환경의 H2S 오영을 막아 주고 황 환원 박태리아에 의해 H2S 를 생 성시킬 때 유기 화합물을 소비하여 CH4 발생을 감소시키기도 한다. 그 리고 황 산화 박테리아인 Thio b acii lztS novell ZtS에 의하여 황 화합물이 위 의 반응과 같이 산화되 어 so~ - 가 만들어 지 기도 한다. 박테리아에 의한 황 광상의 형성 박테리아에 의해 형성된 호수의 CaS04 등이 황 환원 박테리아에 의해 H2S 를 형성하고 H2S 가 산화되어 so 이 만들어져 북마 텍사스 주의 천연 황 광상을 만들었다. 현재에도 CaS04 가 포화되어 있는 북아프리카의 리 비 아, 시 레 나이 칸 (C yr ena ic an) 호수에 서는 황 환원 박테 리 아에 의 한 다음 과 같은 반응에 의해 H2S 가 다량 만들어지고 있으며 호수면에 홍색 황 박테리아와 녹색 황박테리아가 덮여 있어 광합성 박테리아가 태양광을 이용하여 호수 바닥에서 상승하는 H2S 를 산화시켜 so 와 유기물을 만들 고 있다(그림 10-8). 2C02+4H2S ~ 2(CH20) +4S0+2H20 2(CH20) +so~-+2H+ ~ H2S+2H20+2C02
이와 갇은 생물 기원의 황은 황 동위원소비 (034S) 가 넓은 변화폭을 보 이며 부(내의 값을 가진다. 한편 화성 기원의 황과 미생물 기원의 황은 a3 4 S 값이 변화폭이 좁고 0 %0 에 수렴하는 정 ( + )의 값을 가지는 특징에 서 이들과는 쉽게 구별될 수 있다.
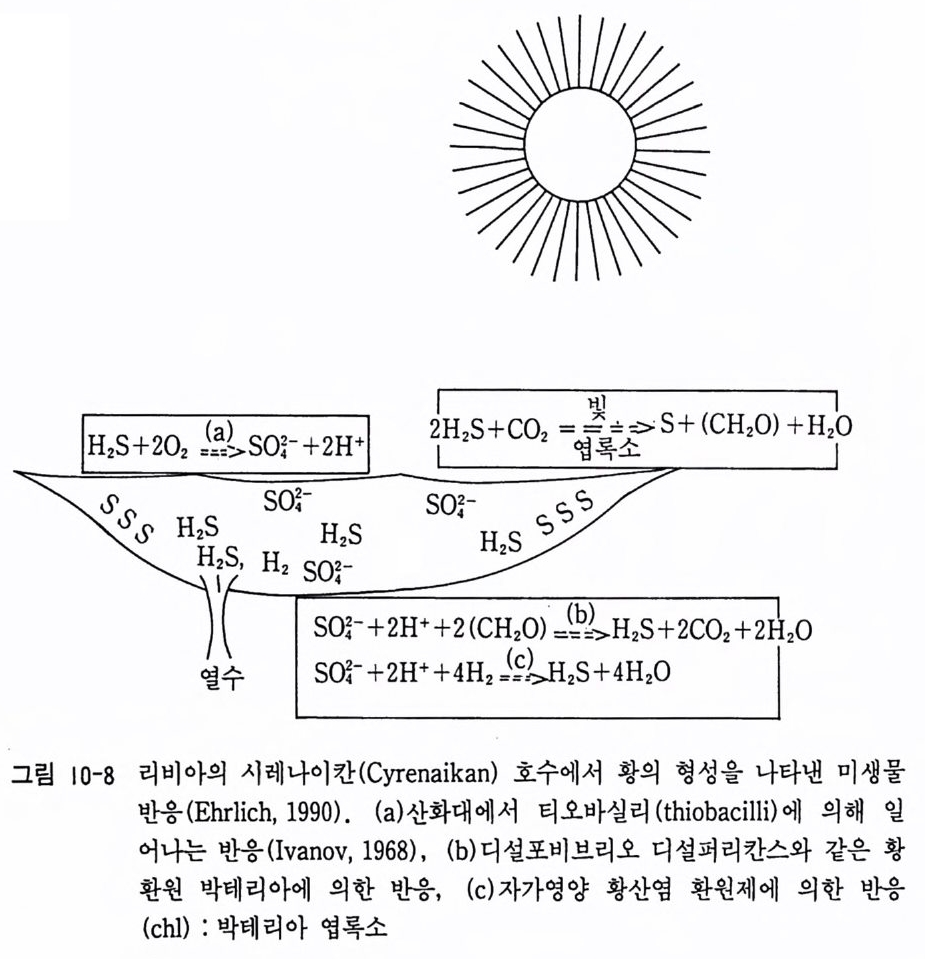 H2S+202 =(?=L s o:-+ 2H+ 2H2 S+ C02 =영 측닌록 l :소=. ~s + (CH2 0) +H 20
H2S+202 =(?=L s o:-+ 2H+ 2H2 S+ C02 =영 측닌록 l :소=. ~s + (CH2 0) +H 20
10-3 석탄, 석유 및 천연가스의 성인 오늘날 우리 인류의 주요 에너지원아 되고 있는 석탄, 석유, 오일셰 일, 천연가스 등의 화석연료 자원은 과거 생물 활동에 의해 지충 중에 퇴적된 유기물 기원에서 만들어전 것이다. 화석연료는 지형적으로 생물 의 유체 (這體 )가 되적되기 쉬운 곳인 분지나 소택지와 같은 환경과 육지 에서 멀리 떨어진 해분, 내만(內 it¾ ) 등의 유기물이 찰 분해되지 않는 곳 에서 주로 형성된다. 따라서 화석연료 유기 광상의 형성 조건은 생물의 생산 속도가 느리거 나 주위 환경에서 생물 유체의 공급이 많고 이질 퇴적층 퇴적분지에서 퇴적이 계속되는 퇴적지라야 한다. 이런 지역에 퇴적된 하부 지층은 협 기성 ( anaerob i c) 이 되어 이질 지층 중에 포함된 유기 물질이 비트민 (bit um en) 이 나 케 로전 (kerog en ) 과 같이 고분자화된다. 고분자화된 유기 물은 지하 심부에서 속성작용이나 변성작용을 거쳐 화석연료화된다(그림 10 선). (1) 석탄의 성인 현재 알려져 있는 세계적인 큰 규모의 탄전은 대부분 넓은 소택지대에 형성되어 있으며 석탄 형성 지질시대는 고생대의 석탄기와 페름기, 중생 대의 트라이아스기와 주라기, 신생대의 고제 3 기 (Paleog en e) 등이다. 석탄의 원물질은 고식물 중의 셀룰로오스와 리그닌이 석탄화된 것으로 생각하고 있다. 전자를 셀룰로오스설이라 하고 후자를 리그닌설이라 한 다. 셀룰로오스설은 셀룰로오스와 리그닌에 물을 첨가시키고 온도, 압력 울 증가시킨 실험에서 리그닌은 소실되고 셀룰로오스가 석탄화되었다는 것이다. 한편, 리그닌설은 리그닌이 화학적으로 안정하기 때문에 보다 불안정한 셀룰로오스가 분해, 소실된다는 것이다 (Ta gu ch i와 Aih a ra,
1992) 〈 셀룰로오스설 〉 식물질 〔셀수룰지무류-―-―+ 당류 --+ 부식산--- `+ 역부청식 질 ] --+석탄 리 그닌 -+ CO2 , H20 , CH4 -+ 소실 〈 리그닌설 〉 식물질 〔셀룰푸스 --+C0 2 , CH4, 지방산--+ 소실 수지류 역청 ] --+ 석탄 리그닌_~부식산_부식산_부식질 CH3CLO OH CH2L 0 H HL20
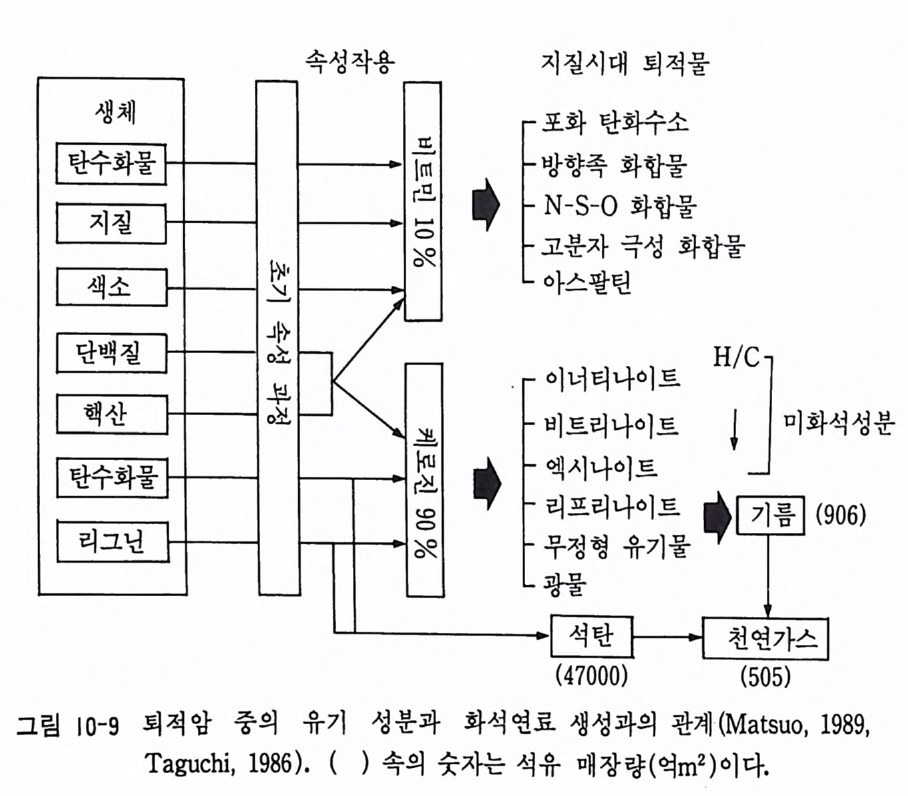 생체 半一j村0부x7A 속A'JO 작 용1 Jo%프柚0 “”: t- 엑 :리포방지N아 고-;시프화 스질향분S:-나리 : 자 팔-족탄0시이나나 -나트이”화협呼틴화 ; 트:貸적소臼화 물합 Hn 尸;/물 J祠C f l미 화( 9석06성) 분
생체 半一j村0부x7A 속A'JO 작 용1 Jo%프柚0 “”: t- 엑 :리포방지N아 고-;시프화 스질향분S:-나리 : 자 팔-족탄0시이나나 -나트이”화협呼틴화 ; 트:貸적소臼화 물합 Hn 尸;/물 J祠C f l미 화( 9석06성) 분
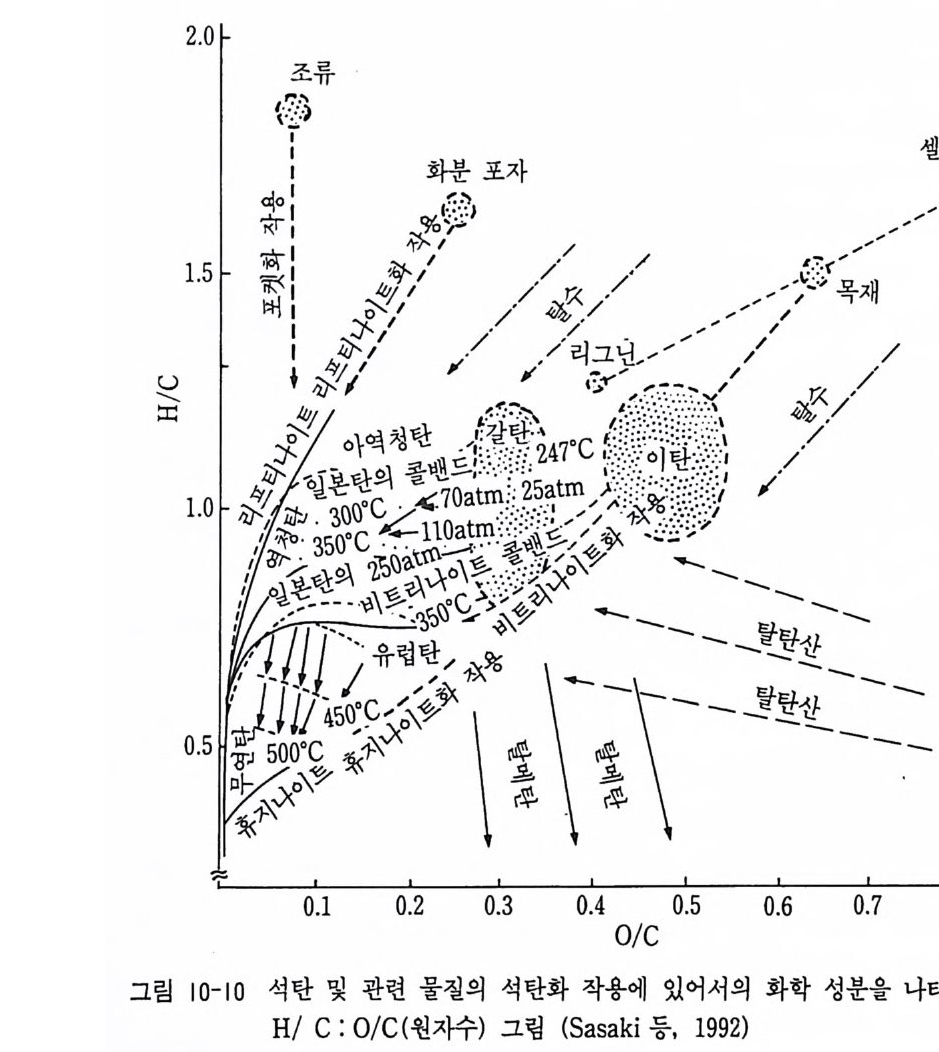 2.0
2.0
석탄의 주된 구성 원소는 C(78-9 1 %), H(5-6.3 %), 0(3-15 %), N 0-2 %), S(0.2-1 %) 등이며 탄화도가 증가함에 따라 석탄 중의 H/C, 0/C, H/0 비가 감소한다(그림 10-10). 그립 10-10 은 주요 단위 성분에 상당하는 현생 식물에서 석탄화가 진행됨에 따라 H/C 와 0/C 의 변화를
나타낸 것이다. 식물의 종류와 부위에 따라 화학 성분이 현저히 다르며 석탄화 진행 단계에 따라 반웅 생성물이 연속적인 대상분포를 나타내는 소위 콜밴드 (Coal band) 가 나타나고 있다. (2) 석유 • 천연가스의 기원 석유가 대량 산출되는 지역 역시 이질 퇴적층과 사질 퇴적층이 두껍게 퇴적된 퇴적분지이다. 해저 유전은 대륙지각 연변부의 해저 퇴적분지에 서 산출된다. 세계 유전의 50-60 %는 제 3 기 지층에서 산출되며 그 중 마이오세 (Mi oc ene) 지층에서 30-40 %가 발견되고 있다. 석유나 천연가스가 다량 산출될 수 있는 지역은 유기물이 다량 포함된 세립질 점토질암인 셰일이나 탄산영암의 근원암이 존재해야 하며 이들 저류암에서 이들울 보존해 주는 덮개암 (seal) 이나 모암 (ca p rock) 이 존재 해야 한다. 그리고 이들이 저장되기 쉬운 지질 구조인 배사구조가 발달 해야한다. 석유의 근원 물질, 변화 과정 및 집적 과정에 대하여 여러 학설이 있 다. 석유의 기원은 유기기원설과 무기기원설이 있으나 Abelson(1963) 이 제안한 퇴적물 중의 케로진이 지열에 의해 열분해되어 석유 탄화수소가 생성되었다는 케로진 유기 기원설이 가장 유력하다. 케로진은 퇴적물 중 에 잘게 분산 존재하는 유기 용매, 알칼리 수용액에 불용성인 고체 유기 물을 총칭한다. 이와 같은 케로진 근원설의 근거는 첫째, 석유, 천연가 스가 해성 퇴적암 지층에 부존되며, 둘째, 석유 중에 클로로필 골격으로 된 폴피린 스데로이드 왁스 등이 존재하고, 셋째, 원유는 편광을 회전시 키는 선광성 (旋光性, laevorata t io n ) 을 가져 무기 적으로 합성 되 기 어 려 우 며, 넷째, 현재의 해저나 호저 이질 퇴적층 중에도 액상의 탄화수소가 보편적으로 발견되고, 다섯째, 원유의 탄소 안정동위원소 값 (813c) 이 -22% 。 ~-36%0 로 보통 유기물의 813C 값인 -15~-30%0 과 유사하며
화성 기원의 탄소에 비해 13c 이 결핍되어 있다는 점이다 (Thgu ch i, 1986). 케로진의 유형 케로진은 H/C 와 0/C 비에 따라 3 가지 유형으로 구분하고 있다(그림 10- 11 ) .
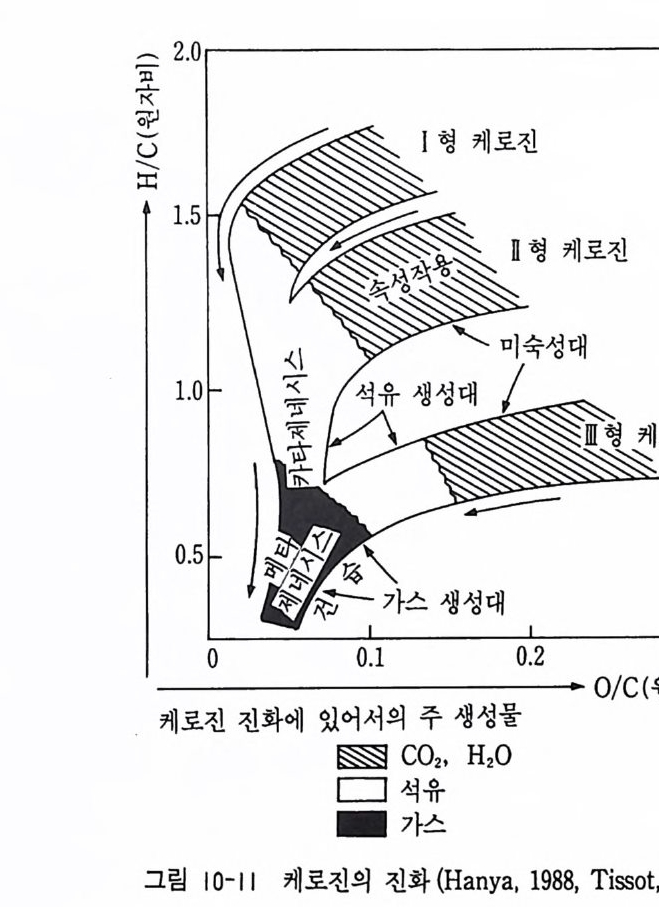 (lR 2015
(lR 2015
1 형 케로진 오일셰일형, 지질형, 조류형 등으로 불리며 디론 - 형에 비 해 축합아환방향족이나 헤테르 화합물이 적고 메틸렌이 많은 특징을 가 진다. 산소의 대부분은 에스데르로 존재한다. H/C 비 (1 . 65) 가 높고 0/C
비 (0 . 06) 는 낮다. 이 유형의 케로전은 조류 등의 비정질 성분, 화분, 포 자 등의 지 질 부분에서 유래 하여 조류질 케로진 (alog al kerog en ) 이 라 하 기도 한다. 오일셰일 중의 케로전이 대부분 여기에 속하며 탄화수소 발 생이 가장 양호하다. Il 형 케로진 석탄질 오일셰일형, 리프티나이트형 등으로 불리며 환원 환경에 침적된 플랑크톤, 박테리아 등의 유기 기원으로 보인다. H / C 비 는 1. 28 이며 0/C 비는 0.10 이다. 원유와 가스를 생성시킨다. 매형 케로진 석탄형, 부식형, 탄수화물一리그닌형으로 불리우며 아환 방향족 구조가 많다. 낮은 H/C 비 (0 . 84) 와 높은 0/C 비 (0 .13) 를 가진다. 이 유형의 케로진은 육상이나 해상 고등식물의 질소질 및 부식질 부분에 서 유래하여 부식질 (hum ic) 케로진이라 한다. 전류시에 석유 발생은 낮 다. 케로진 기원 탄화수소의 형성 유기 퇴적물은 매몰 심도에 따라 속성작용, 변성작용을 거쳐 유기물 一분해 작용一이질충一초기 속성작용一퇴적암一후기 속성작용一원 유一변성작용一 CH4, 흑연 등으로 반응이 진행된다. 속성작용 초기에 는 케로진의 카르보닐기와 카르복시기 등아 제거되고 0 가 H20, CO2 형 태로 없어진다. 이때 N2, CH ◄ 등 가스도 없어진다 . 매몰 심도가 증가하 여결 합속이성 작파괴용된이다 .진 전C되— 어C 온결도합가이 5파0~괴2o되o고·c 에N , 이0르, 면S 등케의로 진원 중자의가 많없어은 지며 탄화수소, 쇄식 화합물 C 가 생기게 된다. 이 단계가 석유 발생 단 계 이 다 (그립 10-12) . 이때 발생한 탄화수소는 n- 해트란, 1-2 환 시클로파라핀, 톨루엔, 크 실렌 등의 특칭이 나타난다. zoo·c 이상의 변성작용에 이르게 되면 c-c 결합이 파괴되고 메탄의 주성분인 드라이 가스가 생성된다. 천연가스에는 CH4 이 주성분인 탄전
가스와 CH 서 C2Hs, C3Ha 등의 파라핀계의 탄화수소로 된 유전 가스가 있다. 유전 가스의 성인은 석유와 유사하다• 그러나 탄전 가스는 석탄화 과정에서 생성된다.
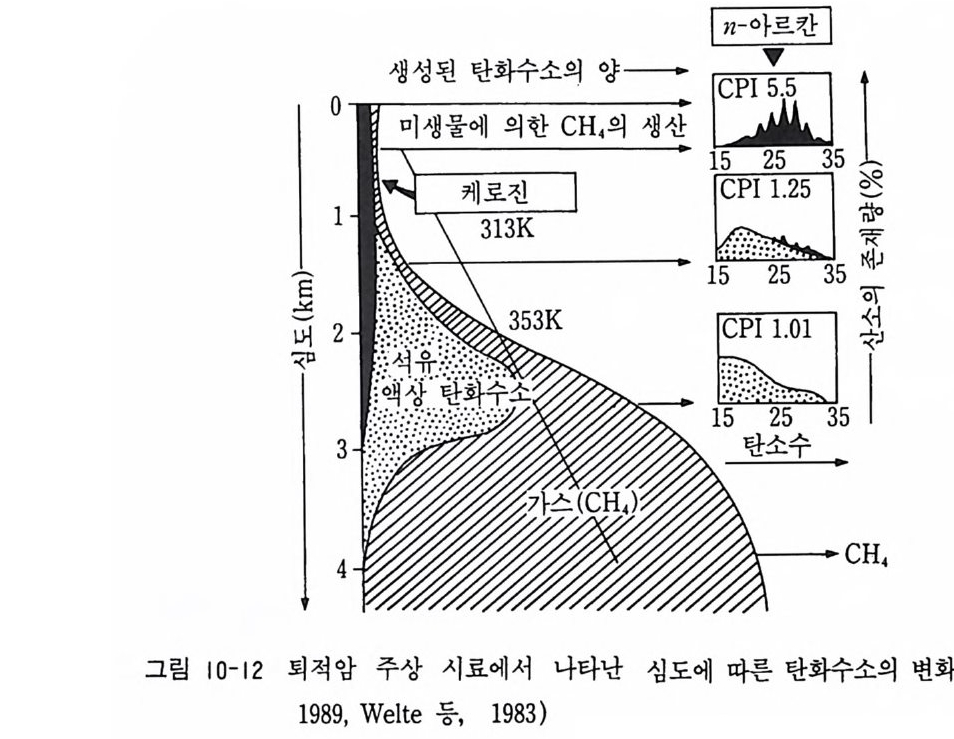 守버) 3 _Jg .-.: 생:생: :::C의 H 40:: :三言;\ 』
守버) 3 _Jg .-.: 생:생: :::C의 H 40:: :三言;\ 』
10-4 지구 생원소계의 전화 (1) 지구 대기의 진화 46 억 년전 지구가 형성된 후 지구의 초기 대기는 Tauri 시기의 강한 태양풍에 의해 모두 지구상에서 없어지고 오늘날의 지구 대기는 지구 내
부에서 탈가스에 의해 형성된 2 차 대기로 구성되었다고 해석하고 있다. 초기 지구 대기는 CH4, NHa, H20, CO2, CO, H2, N2 등으로 구성 된 환원형 대기로 이루어져 있었으며 태양의 자의선에 의한 수증기의 광 분해에 의해 발생한 수소 분자는 우주 공간으로 사라지고 02 가 상충 대 기에 공급되었다. 02 는 화산성 H2 와 수증기의 광화학 반응 (2H20 一 H202+H2) 과 Fe2+ 의 광 산화 작용 Fe2+ +H + 一 Fe + 3+ 靜 에 의해 형성된 수소와 반응해서 소비되어 없어지고 지표에 도달하는 양 은 극히 소량이었다. 약 30 억 년전의 암석에서 H2S 과 같은 환원성 화합물을 사용한 최초의 광합성 박테 리 아에 의 해 형 성 된 스트로마토라이 트 (str o mato l it e) 가 발견 된 사실이 지표에 산소가 증가하였음을 암시해 주고 있다. 20~30 억 년 사이에 P。 2 가 점점 증가하여 지표에서 화학적 풍화가 진 행되었으며 광합성에 의해 다량 형성된 02 는 해양에서 호상 철광충 (banded iro n form ati on ) 을 퇴 적 시 키 는 데 거 의 사용되 었 다. 이 같은 사실 은 남아프리 카의 위 트워 터스렌드 분지 (W itwa te r srand basin ) 와 캐 나다의 엘리엇 호수 (Ell i o t lake) 와 브라인드 리버 (Blind r i ver) 에서 발견된 23~27 억년 된 석영으로 된 역(礎)에서 우라니나이트 (uran i n it e) 와 황철석이 발 견되어 이 시기를 지표에 산소가 없었던 마지막 시기로 추정하고 있다. 왜냐 하면 우라니나이트는 p H<5 에서 아와 결합, 용해성 U02 (C03)g -이 온을 쉽게 만들게 되며 황철석은 보통의 p H 와 현재와 같은 환경에서는 쉽게 산화되어 버리기 때문이다. Holland (1 984) 는 U 야의 용해 속도 실험 자료를 이용하여 그 당시 의 PO2Pco2 를 10-4.9 표.8로 계산하였다. 현재의 P。 2Pco2 는 600 에 가깝다. 이리
하여 지구의 대기는 환원형 대기에서 산화형 대기로 변화되면서 태양 에 너지를 이용한 광합성이 활발하게 일어나기 시작하였다. 또한 상충 대기 권의 03 층이 형성되어 대기 중에 02 의 축적을 증가시키게 되었다. J un g e(l975) 는 지구 형성 후 대기 중에 시간 변화에 따라 축적된 산소 의 양 (02)1 을 다음 식으로 계산하였다. (02) 1=0.03 XO .2 X 룹 M1 p (l 一 e-AI) (10 . 5) =O .Ol6M1p ( l-e-u) 여기에서 0.016 Mt p는 현재까지 대기 중에 방출되어진 산소의 총량 (02) tp을 말한다. 지구 역사를 통하여 풍화된 화성암의 양, 즉 생성된 퇴적암의 양이 지구 내부에서 방출된 산성 기체 (CO2, HCI 등)의 양과 비 례한다고 가정하였다. 그리고 지구 내부에서 기체의 압축량은 지구 형성 후 시간이 지남에 따라 지수함수적으로 감소한다고 가정하여 지구 형성 후 t년 지난 후의 되적암의 양 (Mt )을 다음 식으로 계산하였다. M1=M1p (l— e-AI) (10 . 6) 여기서 Mt p는 현재의 퇴적암의 양 (2.4 X 1021k g)이고 A 는 지구 내부에서 기체의 방출속도 정수(l. 16 X 10-9 년)이다. 퇴적암에 평균 3 % 탄소가 탄 산염과 유기물 형태로 포함되어 있으며 그 중 유기물이 20% 포함된 것 으로 가정하였다. 위와 같이 되적 매몰된 유기탄소 1 몰당 1 몰의 산소가 대기 중에 축적 (C02+H2 0- --+ CH20+02) 되었다는 가정에서 계산된 것이 다. (10.5) 의 관계를 그립으로 그리면 그림 10-13 과 같다. 이 결과에서 보면 30 억 년전에 (02) tp의 80 % 정도가 이미 대기 중에 축적되었어야 한다. 그러나 이 산소는 대기 중에 축적되지 못하고 거의 해양의 Fe2 + 나 S2- 를 산화시켜 호상 철광충이나 우라늄 광상을 형성하는 데 사용되었다. 이같은 광상 형성이 20 억 년에 거의 끝나고 그 후부터
과잉 산소가 대기 중에 축적되기 시작하였으며 이로써 지표의 암석이 풍 화되기 시작하여 적색사암이 18 억 년전까지 형성되었다. 이처럼 약 30 억 년전부터 광합성이 시작되었으며 광합성 식물의 출현으로 지구의 환경이 산화적 환경으로 변화되어 생물 체계에 큰 변화를 가져오게 되었다.
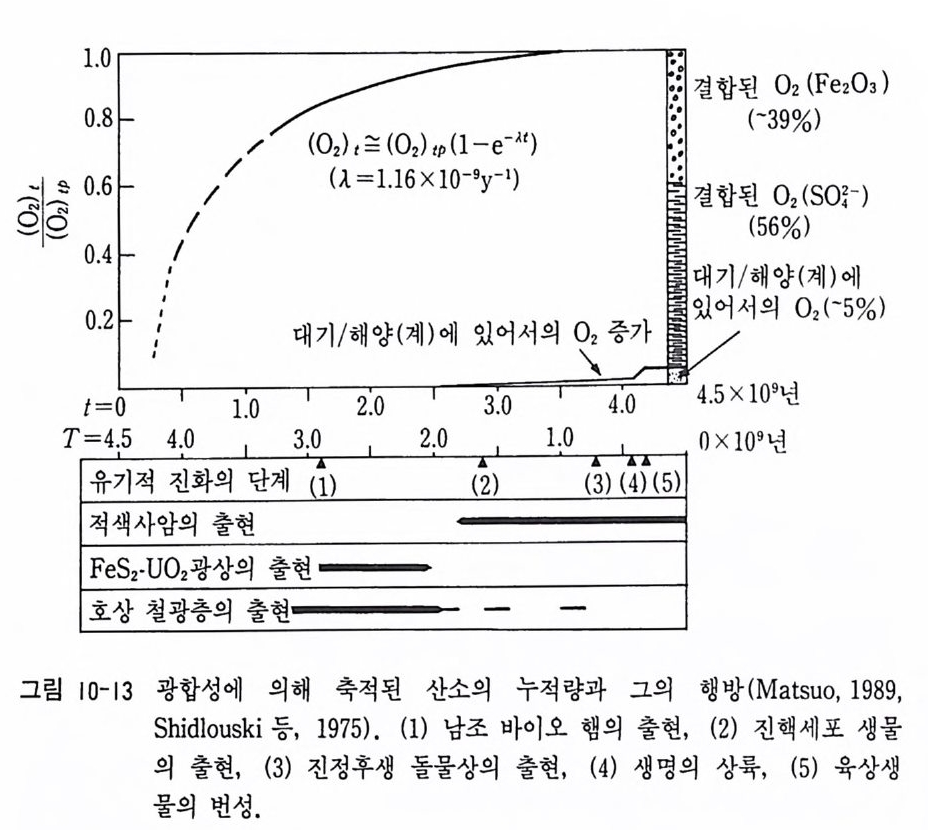 l·00·8
l·00·8
(2) 생명의 기원 생명의 발생과 기원은 지구 대기의 전화와 밀접한 관련이 있다. 생명 의 기원설에는 첫째, 신에 의해 창조되었다는 특수창조설과 둘째, 다른 천체에서 탄생된 배자가 지구에 도착·진화되었다는 판스퍼미아설
(Panspe r mi a) , 셋째, 대폭발 과정의 핵융합 과정에서 분자를 형성한 후 생물 출현으로 이어지는 화학적 전화, 넷째, 유기물 수프 기원 (ora gnic soup scenario ) , 다섯 째 , 표면 물질대 사 기 원 (surf ac e meta b oli sm scenari o) 등이 있다. 지금까지 생명의 기원과 진화의 연구의 기초는 과거 지질시대 지충에 서 관찰되는 미화석이나 지질기록 및 지구화학적 자료에 근거하였다. 죽 첫째 , 선캄브리아기 지충에서 발견되는 Gunfi nti a m i nu t a 와 같은 마화 석과 둘 째, 선캄브리아기 암석의 안정 동위원소 (C, H, N, S) 지구화학 적 연구에서 암석 중의 이들 원소가 생물 기원임을 동위원소 분별을 이 용하여 구별할 수 있게 되었고, 셋째, 케로전과 같은 유기 지구화학적 연구와 분자생물학적 연구, 넷째, 고박태리아 등의 연구에 기초하여 유 기물 수프 기원설과 표면 물질대사 기원설 등을 제안하고 있다 (Ehr li ch, 1990). 대표적인 생명 기원설은 다음과 같다. 유기물 수프설 초기 지구 표면을 덮고 있던 유기물 수프에서 생명이 발생하였다는 설 로 생명의 기원을 설명하는 데 광범위하게 받아들여지고 있다. 생명체를 구성하고 있는 거대분자(D NA, RNA, 단백질 , 지방, 탄수화 물)의 구성 성분인 아미노산, 푸린 및 피리미딘 염기, 단당류, 글리세 롤, 지방산 등의 환원성 원시 대기 구성 성분이 열, 전기 및 빛에너지에 의하여 화학 반응을 일으켜 축적되어 수프를 이루고 있었다. 이러한 물질들은 선캄브리아기의 시생대 (4.5-3.9b y)기에 나타났다. 그 후 이 물질들이 중합을 일으켜 단백질 및 고핵산이 만들어졌으며 이 때 점토가 촉매나 주형 에 중요한 역할을 하였다. 이 중합분자(p ol ym e ri c molecules) 가 자발생성 (sel f -re p roduce) 되었다. 세포 생명체가 유기물 수 프 내의 자발생성체의 재질막(lipi d membrane) 내에 포집되었다. RNA 나 DNA 같은 분자는 스스로 복제 능력 (self r epr o duc ibl e molecule) 을 가지
고 있으며 초기 생성된 여러 가지 핵산 분자들은 구성 성분인 뉴클레오 티드 (nucleo ti de) 와 경쟁을 하게 되며 복제 능력이 강한 분자들이 선택되 어졌다. 이러한 과정에서 단백질이 강력한 촉매로 작용하여 복제 효율성 울 높여 주었으며 단백질과 핵산의 관계가 형성되었다. 핵산과 단백질의 복합체가 지질로 구성된 막으로 둘러싸여 초기 생명체가 탄생하였다. 이 최초의 생명체는 원핵세포(p roka ryo tic cell) 이며 무기호흡을 하는 타가영 양체 (hete r otr op h ) 였다. 시생대 (2.5-4.5b y)시기에 이르러 세포 군집이 계 속 증가하여 비 생물적으로 만든 단위 체 (monomers) 의 공급이 부족해 지 면서 스스로 필요한 영양분을 만들 수 있는 자가영양체가 출현하게 되었다. 이러한 자가영양체는 무기화합물을 산화시켜 그 에너지를 이용하는 화학합성 자가영양 체 (chemosyn t h e tic auto t r o p h) 와, 태 양 에 너 지 를 화학에 너 지 로 전 환시 켜 그 에너지를 이용하여 C 아를 환원형 유기 탄소로 전환시키는 광합성 자 가영 양체 (ph oto s yn the tic auto t r op h ) 로 나눌 수 있 다. 화학합성 자가영양체에는 4H2+C02 一 CH4+2H20 와 같은 반응 과정을 통하여 메탄을 합성하는 박테리아로 고박테리아가 있다. 광합성 자가영양체는 빛에너지를 이용하여 2H2S + C02 一 (CH20) + H20 + 2S 와 같은 반응을 통하여 유기물을 합성하는 시아노박테리아 (c y anobac t er ia) 계열과 H20+C02 一 (CH20) +02 의 반응을 거쳐 유기물을 합성하는 생명체로 나눌 수 있다. 물을 분해하여 광합성을 하는 생명체가 증가하여 대기 중에 산소가 축 적되면서 무기호흡을 하던 생명체에서 유기호흡을 하는 생명체가 출현하 게 되었다. 좀더 복잡한 반웅울 수행하는 생명체가 출현하면서 세포막의
기능이 분화되어 유핵세포가 출현하게 되었고, 초기 무기호흡을 하는 유 핵세포와 유기호흡을 하는 박테리아 또는 광합성을 하는 박테리아가 세 포내 공생 (endosy m bio s is ) 을 하게 되 어 이 러 한 박테 리 아로부터 오늘날 동 식물 세포인 엽록체나 미토콘드리아가 생성되었다. 표면 물질대사설 유기물 수프설보다 더 새롭고 열역학적으로도 합리적인 표면 물질대사 설 이 Waech t ershaeuser(1988) 에 의해 제안되었다. 표면 물질대사는 효 소나 주형이 없이 스스로 촉매 반응을 하는 반응이다. 표면 물질대사에 의해 형성된 모든 유기분자는 세포질액 (sy tos ol) 내의 양전하를 띤 광물 표면과의 상호 작용에 의해 형성된 것이다. 즉 표면 물질대사에서는 CO2 , CO, NH3, H2S, H2, H20 등을 재료 로 스스로 영양분을 만들 수 있다. 예를 들면 Fe2 + 와 H2S 의 반응에서 황철석이 생성되는 것과 같은 것이다. Fe2+ + H2S 一 FeS2+ 4H+ + 2e 이와 같이 생성된 물질대사 산물이 인지질 세포막으로 둘러싸이게 되 면 광물 표면으로부터 떨어져 나가게 되고 세포질액아 세포막으로 둘러 싸고 있는 형태에서 유전 기구가 발달하며 효소와 주형도 점차 형성된 다. 이와 같이 효소나 주형이 형성되기 전까지는 표면 물질대사 과정이 생명의 중심이 된다. 세포질액에 효소가 생긴 후에는 새포 내의 광물 입자에서 표면 물질대 사가 점차 에너지 발생 반웅으로 전환이 되어 호흡 체계가 생겨나게 된 다. 최초에 형성된 세포는 자가영양 생물이다. 표면 물질대사설에서도 세포는 협기성 화학합성 자가영양 세포가 호기성 광합성 자가영양 세포 보다 먼저 형성된 것으로 생각하고 있다.
제 11 장 환경 지구화학 과학 기술의 발달과 함께 인구 증가 및 화석연료 자원의 고갈, 핵연료 와 같은 대체 에너지 개발 등과 산업화에 따라 발생하고 있는 공해 문제 와 환경 문제가 인류 생활에 중요한 영향을 미치고 있다. 따라서 자연과 인류가 공생할 수 있는 지구의 미래를 만드는 것이 가장 중요한 문제로 대두되고 있다. 지구 환경 문제에는 독성 화학 물질에 의한 해양 오염, 지구 온난화, 열대립의 파괴, 생태계의 파괴 등 다양한 문제들이 서로 상호 연쇄적으로 밀접히 관련되어 있다(그림 11-1). 따라서 대기권, 수권, 생물권, 암석권 환경에서 화학적 성분의 상호 반응과 지구 환경에 미치는 영향을 연구하는 환경화학 (en vi romnen t al g eoche mi s try)의 중요성이 증가하고 있다. 환경 문제는 대기, 수질, 토 양, 생물 등의 대상에 대하여 시 • 공간적 차원에서 다루어져야 한다. 즉 단기, 중기, 장기 또는 현재, 과거 등의 시간 단위에서와 함께 소규모
지역적인 공간에서 광역적인 지구 규모에 이르는 공간 규모에서 취급되 어야한다.
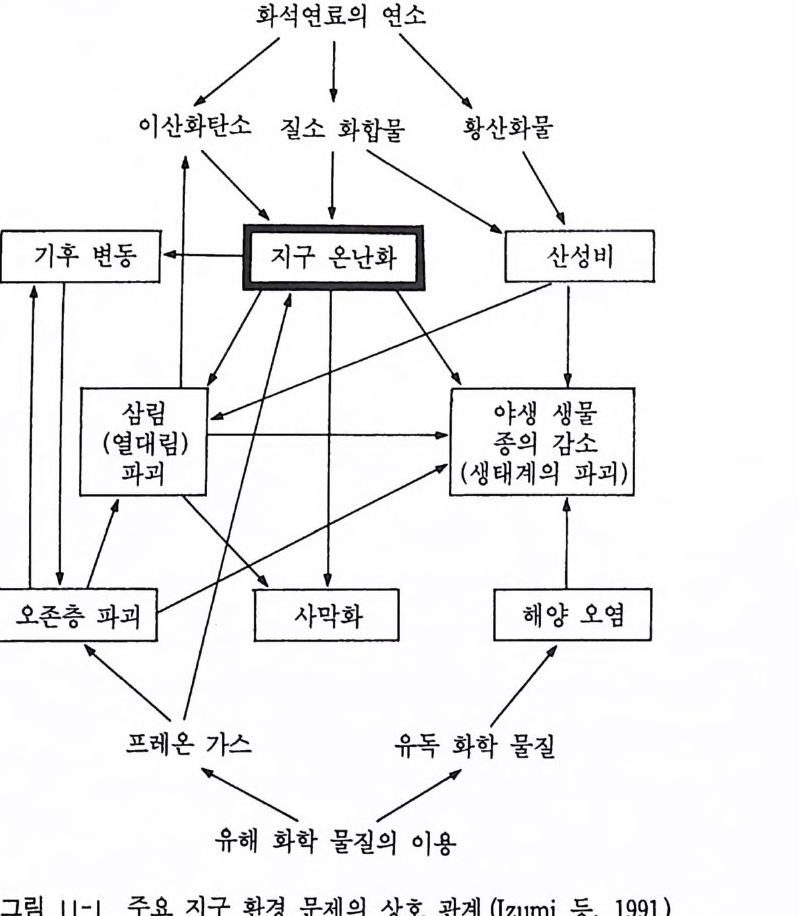 /화석i연료의 \연소
/화석i연료의 \연소
11-1 대기권에서의 환경 문제 (1) 지구 온난화 화석연료의 사용과 농업 및 공업 활동 등의 인간활동에 의하여 대기 중의 CO2 가 증가하고 이로 인한 온실효과로 지구 온난화가 가속되고 있 다. CO2 이 의 에 도 CCbF, CF3Br, CH4, H20, 03, N20 등의 가스도 자의선은 홉수하고 가시광선은 통과시키므로 온실효과에 가세하고 있다. 1980 년대에는 CO2 49 %, CH4 18 %, N20 6 %, CFCb 14 %, 기타 13 %로 지구 온난화에 기여하였다 (Sh i kazono, 1992). 과거 100 년간 (18 80-1980) 측정된 대기 중의 미량 성분 가스 농도의 증가와 지표 온도 의 변화는 표 11-0 과 같다. Hansen 등 (1988) 에 의하면 지구 온난화에 따른 온도 상승률이 2000 년대 이전 100 년간 (0.4~0 . 6°C) 보다 금후 100 년 (0.9~1·c) 이 현저히 클 것으로 추정하였다. 500km 부근의 상충 대기권의 오존층은 자의선을 막아 지표의 생물을 보호하고 있다. 그러나 최근 CCbF, NO 와 감은 인공 화학 물질이 다음 과 같은 반응에서 오존층을 파괴하고 있음이 보고되고 있다.
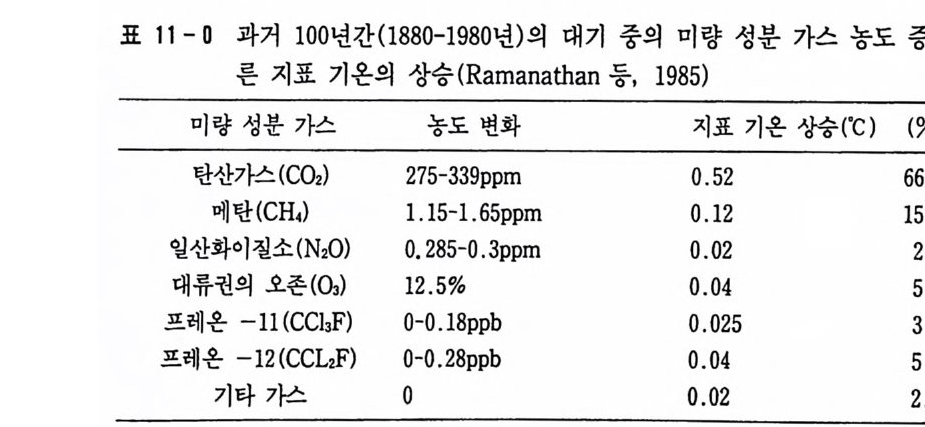 표 11-0 과거 100 년간(1 880-1980 년)의 대기 중의 미량 성분 가스 농도 중가에 따
표 11-0 과거 100 년간(1 880-1980 년)의 대기 중의 미량 성분 가스 농도 중가에 따
CCbF 一자의 ➔선 CClzF +Cl 03+Cl 一, CI0+02 CIO+O 一 Cl+ 0 2 N0+03 一 N02+02 여기서 CClaF 는 냉장고, 에어컨, 전자회로 정밀부품, 세척제 등에서 사용되고 있으므로 이들에서 발생하고 있으며 NO 는 초음속기의 성층권 비행시 배기 가스로 방출되고 있다. (2) 산성비 순수한 물은 보통 pH 7 이다. 그러나 대기 중의 물은 CO 2 로 인하여 탄산(H 2C03) 이 형성되 어 산성화된다. 즉 다음과 갇다. CO2( 가 스) ~ CO2( 용액) CO2( 용액) + H20KI ~ H2C03 H2C0/2 ~ H+ + HCOa 상온에서 K1=10-1·5, K2=10-6 '4 가 되고 현재의 대기의 CO2 의 농도를 325 pp m 으로 가정 하면 Pco2= 10-3 · 5 가 되 어 [H+ ]= 2 .1 X1 0-6 mol/ 1=1 0-5·61 이 되어 p H=5 . 7 이 된다. 오염이 없는 건조 지역에서 고농도의 CaC 아로 된 풍성충에 의해 CaC03 + H+ 一 Ca2+ + HCOa 가 되어 강우의 형태로 중성화시키거나 생물학적 분해 작용이나 농업 활 동에 의해 암모니아 가스 (NH3) 가 다량 방출되는 지역에서는
NH3+H + 一 NHt 가 되어 강수가 중성화된다. 그리고 해양 환경에서도 해영 에어로졸이 형성되어 해양의 강수는 중성화될 수 있다. 그러나 인간활동에 의해 배출되는 S02, H02, NO, HCI 가스 등에 의해 다음과 같이 대기 중의 수증기단이 산성화되어 pH 5 . 7 보다 낮은 산성비를 만들고 있다. S02+0H 一 比 S04 H2S04 一 2H++srn- N02+0H 一 HN03 HN03 一 H++No3- HCI 一 HCI HCI 一 H++Cl 그 결과 유럽 지역에서는 p H < 4.6 인 산성비가 보고되어 있다(Li kens, 1976). 또한 겨울은 p H 가 높고 여름은 낮은 계절 변화도 보고되고 있다 (Kallend 등, 1983). 우리나라의 경우에도 서울 지역에서 p H<4 . 7 의 산 성비가 보고되었다(김규한. Nakai, 1988). 이와 같은 산성비는 생태계의 파괴뿐만 아니라 구조물의 부식 및 파괴, 암석의 풍화 등을 가속시켜 토 양 유실량을 증가시키고 지표의 지형 및 환경의 변화를 가속시킨다. 11-2 토양 오염 지역의 지질에 의한 자연적 조건에 의해 토양 중에 Cd, Hg , Pb, Se, As, Co 등의 중금속 오염이 일어나는 자연적 요인과 공장 폐수, 광산 폐수, 농약 오염 등, 인간활동에 의한 인위적 요인에 의한 오염이 점점 증가하고 있다. 토양은 이런 중금속 이온들을 흡착하는 성질이 있어 일 단 오염되면 이들 원소를 제거하는 데 긴 시간이 필요하며 제거하기가 대단히 어렵다. 산화 • 환원 조건에서 중금속 이온들이 산화물이나 황화 물 형태로 토양 중에 고정된다. 공장 폐수, 광산 폐수, 농약 중에 다량
포함되어 있는 중금속 이온의 일부는 지하수나 하천수로 유입되고 일부 는 토양이나 하상 되적물, 호수 퇴적물, 해저 되적물 등에 흡착되어 2 차 오염의 주요 원인이 된다. 토양 내의 다양한 원소 중에 식물이나 동물 성장에 필요한 원소와 Cd, Hg , Tl, Cu, Zn, Mo, Se 등과 같은 독성 원소들과 동물아나 인 간의 건강에 영향을 주는 As, I, Cr 등이 있다. 토양 중의 이와 같은 유해 원소들은 주로 그 지역에 분포하는 지충 기반암에서 유래한다. 그러나 농업 활동, 선광장, 제련소, 골프장 등의 인위적인 원인에 의 해서도 유해 원소들이 토양에 농축되어진다. 특히 광종에 따라 차이가 있지만 광화 지역의 토양에는 Cd, As, Pb, Cu, Zn, Mo, Se 등의 유 해 금속 이온들이 농집되어 식물을 통하여 간접적으로 인간에게 섭취되 거나 하천의 작용 등으로 하천수에 유입되어 지하수계 오염원이 되기도 한다. (1) 카드뮴 중금속 중 카드뮴은 화강암 0.1~0.2p pm , 셰일 0.3~11p pm , 비오염 토양 0.27~0.55 ppm , 망간단괴에는 5.1~8.4 pp m 이 포함되어 있다. 카 드뮴 함유 광물로는 그리노카이트(gr eenock it e,CdS), 옥타바이트 (oc t av it e , CdC03), 산화카드뮴 (CdO) 등과 같이 광물로 산출되거나 섬아연석 [(Zn, Fe, Cd)S] 중에 Zn2+ 를 치환하여 비교적 많은 양이 산출되며 방연석, 보우렌저 라이트 (boulange r ite ) , 보우르노나이트 (boumon it e) , 산화망간, 갈칠석 등에서도 소량 산출된다. 카드뮴은 수용액 중에서 암모늄, 시안 화물, 염화물 이온과 착이온을 형성한다. 카드뮴 오염으로 잘 알려진 일 본 도야마(富山) 지역에 있는 가미오카 광산(神岡鑛山)의 아연 선광 폐기 물은 진즈가와(神通川) 수계 지역의 토양을 오염시켜 〈이타이이타이 병〉 울 발병시켰으며 이 지역의 농경지에는 2 차 대전 이후 지금까지 벼농사
를 하지 못하는 논이 많다. 보통 현미 중에 카드뮴 1 ppm 이상이면 오 영 지역으로 간주되며 음용 수질 기준치는 0.01p pm 이하라야 한다. 우 리나라의 장항 제련소 부근과 삼보 광산 주위의 토양도 카드뮴이 1. 6~27 . 2 pp m 으로 기타 중금속과 함께 오염되어 있다(김주용, 전효택, 1993, 김상현, 전효택, 1993). 카드뮴은 토양 중에서 주로 산소가 부족한 논에 서 H2S 와 반응 (Cd + H2S - ---+ CdS) 하여 난용성 인 CdS 를 만든다. 그 러나 대 기 중의 산소나 박테 리 아에 의 하여 황산카드뮴 (CdSO ◄) 을 만든 다. 황산카드뮴은 물에 쉽게 녹아 Cd2 + 로 벼와 같은 농작물에 쉽게 흡수 되어 쌀에 유입된다. (2) 수은 카드뮴과 동족 원소인 수은은 독성 원소로 잘 알려져 있다. 수은은 상 온에 서 액 체 금속이 며 휘 발성 원소이 다. 수은 광물은 진사 (cinn abar, H g S) 와 액상 자연 수은이 있다. 수은 화합물은 Hg > Hg 2 Ch>Hg C h> Hg S >Hg O 순으로 기화되기 쉽다. 암석 중의 수은 함량은 100p pb ~20 ppm 정도이며 보통 평균값이 0.1p pm 이하가 많다. 토양 중의 수은 함 유량은 0.1p pm 이하이나 수은 광산 부근의 토양에서는 10~lOO pp m 정 도가 검출되는 곳도 있다. 액상 수은이나 염화제일수은 (H g 2Cl2), 황화수은(Hg S) 은 난용성으로 체 내에 흡수되기 어려우며 독성이 없으나 염화제이수은 (H gC I2) 과 유기수은 은 독성이 강하다. 수은은 광산 폐수나 공장 폐수에서 다량 방출되며 이 둘이 해저나 호수 퇴적물에 축적되고 메탄 생성 박테리아에 의해 메틸수 은 (CHsH g CI) 으로 변화된다. 이것이 어패류를 거쳐 인간의 몸에 섭취되 는 경우가 있다. 일본에서 수은 중독으로 발병된 〈미나마타 병〉은 세계적으로 잘 알려 져 있다. 어패류 중의 총 수은의 양은 0.4 ppm , 메틸수은( Il )은 0.3
ppm 정도가 허용 한계치이며 체중이 50 k g인 성인의 경우에 1 주일 간의 총섭취량의 한계치는 메틸수은 210 µg 정도이다. 대부분의 중금속은 생 물학적 반감기가 길기 때문에 일단 체내에 유입되면 축적되어 인체에 크 게 영향을 준다. (3) 납 납은 주로 방연석 (PbS) 광물로 산출되며 드물게 세루사이트 (ceruss it e, PbC03) , 엔그레 사이 트 (ang le sit e,P bS04) , 파이 로모르파이 트 (pyrom orp h ite , Pbs(PO.AsO ◄ )3C I) 등으로 산출된다. Pb2 + (이온반경 1.2 0A), K+( l.3 3A), Ca2+ (0 .99A) 은 이온 반경이 서로 유사하여 사장석, 각섬석, 휘석 중에 서로 치환되어 들어 있다. 암석 중에는 화강암 30p pm , 염기성암 5~9p pm , 석회암 5~10p pm , 셰일 20 ppm 정도 포함되어 있다. 납은 암석이 풍화되는 환경에 따라 그 거동이 다르다. 따라서 토양 중에 납의 함유량은 2~200 ppm 정도이 다. 산성에서는 수용성으로 존재하며, 알칼리성에서는 불용성 황화 광물 울 형성한다. 중성~약알칼리성에서는 수산화물로 침전되거나 점토 광물 에 흡착된다. 해수 중의 납의 함유량은 0 . 03 ppb 이며 보통 하천수 중에 는 3 ppb 정도 함유되어 있다 (Tarek i an, 1969). 최근 환경 오염에 의하여 납은 식물에서보다 대기 중에서 과잉 섭취되고 있다. 주로 광산에서나 혹은 안료, 축전지 제조 공장 등에서 납중독이 많이 발생한다. 최근 도 시화로 인한 화석연료 사용에 따른 교통량 증가에 의해서도 도시 지역에 납 오염이 발생하고 있다. 정상적인 사람의 혈중 납의 농도는 0.20p pm 이하이다.
(4) 비소 비소 (As) 가 함유된 광물로는 유비칠석 (arsenop yrite, FeAsS2) 이 대표적 이며 황동석, 방연석, 섬아연석 내에서도 소량 산출된다. 비소의 환경 오염은 제초제, 살충제, 살균제 등의 농약 오염원에서 주로 일어나고 있 다. 비소는 이온 반경이 As3+ 0.58A, Ass+ 0.46A 으로 Si4 +(0. 43A), AJ3 + (0 . 51 A), Ti4 +(0. 68A), Fe3+( 0. 64A) 등과 유사하므로 광물 중에 이 둘 원소와 치환되어 방연석 중에 50~10000p pm , 섬아연석 중에 5~10000 pp m 이 산출된다. 화성암 중의 As 함량은 2 pp m 이며 토양 중 에는 5 ppm 정도이다. 일본의 보통 비오염 경작지의 비소 함유량은 10.3 pp m 이다(山縣 1977). 비소 함량이 높은 유비칠석, 방연석, 섬아연 석 등과 같은 황화 광물 중의 비소는 용해도가 낮지만 As20s, H3AS04, H3As03 등의 비 소 산화물은 용해 도가 높아 As3+, As5+ 이 온은 수산화 철이 침전될 때 쉽게 흡착 침전되어 퇴적 철 광상에 비소 함량이 높게 나타난다. 해수 중의 비소의 함량은 1~5 ppb 이며 심해저 퇴적 점토에는 11 ppm 정도 함유되어 있다. 비소는 제철소, 비료 공장, 지열 발전소와 화학연료 사용으로 대기 중 에 오영된다. 일본의 미야자키현에 있는 연아연 비소 광산지역의 토양은 비소 함량이 44. 2~ 1,302 pp m 이며 주변 마을의 토양에서도 17.6~83.1 pp m 이 산출되었다. 일본에서는 비소가 수질 환경 기준치인 50 ppb 를 초 과한 지하수도 보고되어 있다. 이로 인하여 이 지역 주민들은 빈혈, 피 부 각화, 탈모 등의 환자가 발생하였다. A~2 아는 As20s 보다 10 배 정도 독성이 강하며 As2 아 최저 치사량은 0.4mg /k g 정도이다. 즉 체중 60 k g인 사람이 24m g의 비소를 섭취하면 생명이 위험하다.
(5) 셀렌 오염 토양에 셀렌 (Se) 함량이 높은 지역에서는 목장의 가축이 중독되거나 사람들의 오중에 셀렌 함량이 높은 경우가 있다. 셀렌에 오염되면 장 질 환, 피부영 등이 발병하기도 한다. 셀렌은 적색을 띠며 금속상의 셀렌은 대단히 안정하다. 그러나 황화 광물에 황과 함께 수반되는데 제련시에 H2Se03+2S02+H20 一+ Se+2H2S04 과정으로 셀렌이 만들어진다. 셀렌은 H2Se, Se02, Se03, H2Se03, H2 Se04 등의 형태로 산출되는데 Se03 는 황색 분말로 홉습성이 있으며 물 에 용해되어 H2S04 가 된다. 11-3 수질 오염 하천수, 지하수, 해수, 호소수 등의 오염은 주로 공장 폐수, 광산 폐 수 및 생활 폐수에 의하여 일어난다. 공장에서 유출되는 Cr6+, 트리할로 메탄 (CH&), 트리크롤에틸렌 (C2HC6), 데트라크롤에틸렌 (C2Cl4) 등의 독 성 유기 할로겐 화합물의 하천 유입으로 오염이 되며 PCB(C12HmCli o-m ), 다이옥신, 농약 오염도 물의 주요 오염 요인이다. 선박 등에서 기름이 유출되어 해수를 오영시키고 있다. 석탄 광산의 황철석이 다음과 같이 산화되어 산성의 광산 폐수를 만들기도 한다. (F황e철S석2)+ 묘4 국 H20 一 Fe(OH)2+2H++2HSO ◄ 상수도에는 시 안 이온, 유기 인, Pb, Cr6+, Cd, As, F, Cu, Hg 등
과 같은 병원성 생물 오염 물질이 함유되어 있어서는 안 된다. 수돗물의 살균 처리를 위하여 보통 염소를 많이 사용하고 있으며 급수지에서 0.1 pp m 의 유리 잔류 염소가 유지되도록 하고 있다. Cb+ H20 ~ HCI + HCIO HCIO~HCI+O 위와 같이 영소의 수용액인 염소수는 산화 작용을 하여 살균 소독제로 효과가 크다. 유리 산소 (0) 가 물 속의 유기 물질을 산화시키고 염산 용 액으로 변한다. 수돗물을 끓이면 Cl2 나 HCIO 가 제거된다. 수도의 살균 처리용으로 사용하는 염소가 수돗물 중의 미량의 후민아류의 무기물과 반응하여 발암성 트리할로메탄류를 만드는 경우도 있으므로 주의를 요한 다. 11-4 수질 평가 지구 내의부에서 지질 현상을 일으키는 요인으로서 물의 역할이 중요 할 뿐만 아니라 물은 인간 생활에 있어 가장 중요하다. 상수도, 농업용 수, 공업용수 및 교통 수단 등으로 다양하게 이용되고 있다. 수량과 수 질에 따라 그의 이용은 제한을 받게 된다. 수질은 물리적 특성, 화학적 특성 및 생물학적 특성에 의하여 평가될 수 있다. 물리적 특성에 의한 수질 평가 기준은 물의 혼탁도(tur b i d ity), 고형 물질 (so li ds) 의 양, 색, 냄새와 온도 등이 있다. 혼탁도는 콜로이드 입자들이 침전되면 물의 투명도가 떨어져 혼탁도가 증가한다. 혼탁도는 상수도의 수질 평가에 중요한 요소 중의 하나이다. 고형 물질은 크기나 상태, 화학적 특성에 따라 평가되어야 한다. 색은 보통 용존 유기 물질에 의하여 다르게 나타나며 산업 폐기물에 의해 오 염된 경우 그 원인에 따라 다양한 색을 나타낼 수 있다.
냄새의 원인은 주로 아민 (CH3(C H) 2nNH2), 암모니아 (NH3), 유화수소 (H2 S) , 유기 황화물 ( (CH3) 2S) 등의 성 분 때 문이 다. 화학적 특성은 암석 광물의 풍화에 의해 형성된 Ca2+ , Na+, K+ , HCO;, sot, c1-, NO; 과 같은 주요 용존 이 온종과 Al3+ , NHt , As+, Ba2+, BO 仁 Cu2+ , Fe2+, Fe3+, Mn2+ , HSOi , Co~-. F-, HPol-, Poi- , soi- 등 과 같은 부성분 이온종에 의해 수질의 특성이 달라진다. 또한 인간활동으로 인해 유입된 As3+ , Ba2+ , Cd2+ , Cr3+ , Cr6+ , Pb2+ , Hg 2+; Ag 2+ , Se, Zn2+, CN-등 의 유해 성분과 NH3, NO;, N02 등의 유기 질소 성분 그리고 Na3P04, Na2HP04 등의 인산이 수질 평가에 중 요한 성분이 된다. 방사성 원소 (90Sr, 226Ra, 131!, 187Cs) 가 원자력 발전소, 의학, 농업 등에 이용되고 있으며 동시에 이들이 붕괴할 때 발생한 동위원소가 지하수계 에 유입되어 지하수를 오영시키고 있다. 물의 수소이온 농도는 자연계에 서 보통 6.5~8.6 범위이다. 우리나라의 지하수의 평균 p H 는 6.9~7.0 이다(김규한과 Nakai, 1988). 그러나 산성비나 환경 오염 등에 의해 물이 산성화될 수 있다. 강수의 수소이온농도는 주로 대기 중의 CO 2 의 함량 에 따라 결정된다. 즉 대기 중의 co 제 의하여 주로 지배받기 때문에 예를 들어 25°C 에서 강수의 p H 는 다음과 같이 계산된다. =K, [H 기=均關曾니 위의 식에서 빗물의 수소이온농도를 추정할 수 있다. 그런데 빗물에서 수소 이온과 평형에 있는 음이온은 [H+) = [OH-] + 2[CO;] + [HCO;] 이 있다. 많은 빗물 측정에서 p H 가 7.0 정도였다. p H<7 . 0 이라면 [OH-] 와 CO t-는 무시 될 수 있으며
[H+ ] ~ [HCO 디 이 된다. 따라서 [H+ ]2 =K • [H2C03] 가 되어 여기서 [H2CO 리가 다음 과정에서 계산된다. 빗물 중의 CO2 몰 건'!cl 건O_ 亡0 x(co2 )aq = KRRcodaq 식에서 계산될 수 있다. 여기서 X(C02)a q는 액상과 평형에 있는 C 아의 몰 분율이고 K茂 헨리 법칙의 상수이고 Rco2) 는 대기 중의 CO2 분압이다. 대기 중에 CO2 가 0.0 3 % 함유되어 있다고 가정하면 X(co2Ja q = 6. ll X1 0- ◄ a t om-1 (0 . 0003 atm ) = 1. 84 X1 0-1 이 된다. 그리고 [CO 』 a q의 몰농도는 X( co 이 ::::c [C02] 나 [H2 이 = [C02)aq/ 55 . 56 [C02)aq = (1. 84 X 10 기 (55 . 56) = 1. 02 X 10-s mol/ 1 가 된다. H2C 아의 몰농도는 [[HC20C2O]aJq =K 에서 [H2COa] = (1. 58 X 10-3) X (1. 02 X 10-5) =1. 61 X 10-s mol/l 가 얻어진다. 따라서 [H2COa] = [C02)aq + [H2COa] = (1. 02 X 10-5) + 1. 61 X 10-s
=1. 02 X 10-s mo!/l [H+ ] = (4 . 47 X 10 기 (1. 02 X 10- 5) [H+ ] = 2 .13 X 10-6 mo!// 그러므로 빗물의 수소이온 농도는 pH 5.67 이 얻어진다. 최근 산업화에 따라 화석연료 사용이 증가하여 이로 인한 SOa, NOx 가스가 대기 중으로 대량 방출되어 강수의 p H 가 5.6 보다 낮은 산성비가 오고 있다. 미국 북동부의 에이디론덱 마운틴 (Ad i rondack Mounta i n ) 지 역에 pH 1.5 까지 산성비가 보고되었으며 우리나라에서도 p H 가 4.7 까지 보고되어 있다. 물이 산성화가 되면 생태계에 큰 영향을 준다. 호수의 연어는 pH 5.0 이하가 되면 살 수 없다. 또한 독성 금속의 용해도가 산성수에서 대단히 크므로 토양에서 이들 금속 이온의 침출로 환경 문제의 심각성을 더하여 주게 된다. 알칼리도 (A, alca li n ity)는 A, eg/ m 3= (HC Oa) + (Co~-) + (OH 기 에서 계 산된다. 전기전도도 (conduc tivity)는 용존 이온종에 따라 다르다. 그리고 물의 경도 (hardness) 는 H, eg/ m 3= (Ca2+ ) + (M 균) 에서 계산된다. 보통 물속의 CaC02 의 농도 (m g/!)가 < 50 이면 단물, >150 이면 센물로 구분 하고 있다. 그리고 수질 평가에는 유기물질의 정량이 대단히 중요하다. 대부분의 자연수에는 유기 물질의 함량이 낮다. 그러나 물 속에 유기 물 질이 존재하면 색, 냄새, 맛, 산소 결핍 초래, 정수 처리의 방해, 할로 겐 화합물 형성 등에서 많은 환경 문제를 야기시킨다. 수중의 유기 물질 의 함량울 측정하기 위 하여 화학적 산소 요구량 (COD, chem ica l oxy ge n demand) , 생 물학적 산소 요구량 (BOD, bio c hemic a l oxyg e n demand) , 전 유기 탄소량 (TOC, tota l orga n ic carbon), 전 산소 요구량 (TOD, tot a l oxyg e n demand) 등을 측정하여 유기물 함량의 척도로 삼고 있다. COD 의 예를 들어 보면 유기물에 의한 화학적 산소요구량을 Cr20~- 시 약을 사용하여 측정한다.
CAHsOc+Cr20~- + H+ ―촉가―매열 ➔ Cr+3 + H20+CO2 실험 전과 실험 후의 Cr 2 m- 울 정 량하여 CO2 , H20, NH \ PO 仁 so~-등 과 같이 유기물질이 산화되는 데 쓰여진 산소의 양을 정량하여 COD 값을 정하고 있다. 또한 BOD 는 다음과 같이 유기물질 +0 곱영양 물질 °」!:!° C0 2+ H20+ 새로운 세포+영양 물질 생물학적으로 변화될 수 있는 유기물의 물질대사 과정에 사용된 산소의 양을 말하며, 보통 유기화합물의 탄소질 물질의 산화에 요구된 산소량을 측정 하므로 CBOD (ca rbonaceous bio c hemi cal oxy ge n demand) 라 부르기 도 한다. 수질의 생물학적 특성은 동식물 기원에서 유래한 수중의 미생물의 존 재에 따라 다르다. 특히 박테리아, 곰팡이류, 규조류, 원생동물, 지렁 이, 바이러스류 등은 전염병의 전파와 독성이 있을 뿐 아니라 물의 맛, 지표수와 지하수의 냄새, 부식, 정수 처리 시스템이나 냉각 시스템의 표 면의 열전도 방해 등에 크게 영향을 준다. 11-5 음용수의 적 합성 지하수 및 하천수의 수질 특칭은 그 지역의 지질, 지표의 생물 환경 등에 의하여 변화하게 된다. 음용수로 이용 가능한 물은 일반적으로 혼탁도 (NTU) 가 <1, 고형 물 질 500 g/m 3, 색 도 < 15, 냄 새 <3 , c1-2 50 g/m 3, 질산 10 g/m 3, 황산 영 250 g /m 리 pH 6.0-8.5, pes tic ide s 0.5, 페놀 0.001 g/m 3, 산소> 4.0 g /m 라 박테리아<1. 0 MPN/100 ml 등이어야 한다(부록 2). 그 의의
중금속 함유량의 한계치는 표 11-1 과 같다.
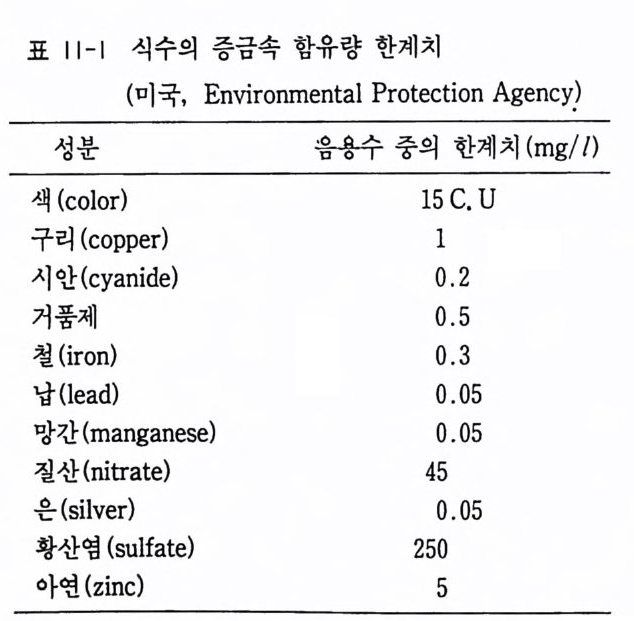 표 1| -l 식수의 증금속 함유량 한계치
표 1| -l 식수의 증금속 함유량 한계치
수돗물(음용수) 중에는 그 지역의 지질에 따라 칼슘, 마그네슘, 철 등 이 다량 함유되어 있는 광천수 (m i neral wa t er) 가 있다. 광천수는 사람에 따라 부적합한 경우도 많다. 물론 순수(증류수)의 경우에도 유사하다. 따라서 수돗물은 인간의 건강을 해치지 않는 성분을 가져야 하고 마실 때 불쾌감이 없어야 한다. 죽 음용수는 표 11-1 에서와 같은 시안 이온, 수은, 유기 인산, 납, 크 롬 (Cr6 + ), 카드뮴, 비소, 불소, 구리 등 유해성 원소의 함유량이 식수의 한계치를 넘지 않아야 하고 염화물 이온, 유기 물질, 일반 세균, 대장균 류 등의 함유 한계치를 넘지 말아야 한다. 그리고 pH , 냄새, 맛, 색도, 탁도, 증발 잔류 물질, 페놀류, 계면활성 물질 등의 값이 기준치를 유지 하여야 한다. 하시모도 등 (19 88) 에 의 하면 맛이 있는 물은 수중에 Ca, K, Si0 2 총
량이 M g와 so~- 의 총량의 2 배 이상이어야 한다는 지표를 수립하였다. 죽 맛있는 물의 지표는 Ca+K+Si0 2 느 2.O M g +SO ◄ 이다. 보통 음료수의 p H 가 6 . 85- 중성에서 약간 알칼리 쪽인 수질 지역 주 민의 평균 수명이 길며 장수촌 지역의 물은 Ca 이 Mg , Na 보다 상대적 으로 많이 포함되어 있다 (Su g ano , 1989). 수돗물에 살균 소독제로 염소 가 많이 이용되고 있으나 발암성 물질을 만들 우려가 있는 것으로도 알 려져 있다. 또 미국의 일부 주에서는 충치 예방의 효과가 있는 불소를 수돗물에 소량 넣기도 한다. 즉 물의 화학 성분은 그 지역의 지질, 기 온, 강우량, 지표 및 대기 환경 등에 의해 달라지며 사용하는 대상에 따 라 물이 좋은 영향을 줄 수도 있고 나쁜 영향을 줄 수도 있다. 11- 6 방사성 폐기물 오염 지질학적 재해 중에는 지전, 홍수, 매스 무브먼트 (mass movement) , 화산 폭발 등이 있다. 인구 증가와 인간 생활 향상을 위하여 식량, 물, 공기, 주택, 도구, 기구 운송 등의 자연 자원의 사용이 급증하고 에너지 의 수요량도 크게 증가하여 재생 불가능한 화석연료 자원 (nonrenewable foss il fue l resources) 의 고갈로 원자력 대 체 에 너 지 의 이 용이 중가하게 되 었다. 이로 인하여 지화학적 재해 (ge ochemi ca l hazards) 가 증가하기 시작 하였다. 장반감기 핵종인 U, Th 과 T, ,oB, 14c 와 같이 우주방사성 핵 종에 의해 방출되는 이온화된 방사선이 생물체에 큰 영향을 주고 있다 (Faure, 1986). 그리고 특정 원소의 과잉 또는 결핍 현상이 의학적 문제
를 일으킨다 (Cannon, 1974). 어떤 박테리아에 의해 형성된 독성 물질이 생물체에 위험 요소가 되기도 한다. 환경 지질학자와 환경 지구화학자들 은 이 같은 인 간에 의 해 발생 하고 있는 재 해 (anth ro p og e n ic hazards) 를 감 소시키기 위하여 끊임없이 연구를 하고 있다. 특히 원자력 에너지의 이 용아 급증함에 따라 원자로에서 핵분열이 일어날 때 발생하는 방사성 물 질이 위험한 물질이므로 방사성 폐기물의 문제가 심각한 환경 문제로 등 장하고 있다. 일반적으로 암석 내의 우라늄 함량은 화강암 (3 .5 p p m 내외), 셰일 (3.2 ppm 내의), 탄산염암 (3 . 2 pp m 내의) 순으로 화강암 내에 U 의 함량이 높 다. Th 역시 화강암 08.0 pp m 내의), 셰일 (1l . 0 pp m 내의)에 많이 함유 되 어 있으며 스웨 덴의 S t r ip a 의 화강암은 U 44 .1 pp m 과 Th 33 . 0 pp m 으 로 대단히 높은 방사성 원소를 함유하고 있음이 보고되었다 (Andrews 등, 1989) . 우리나라 옥천 변성대 내의 창리층 중의 흑색셰일 및 탄질 셰일 0 충에 서도 우라늄의 함량이 높게 나타나고 있다. 소련의 체르노빌, 미국의 드리마일 섬의 원자력 발전소의 방사능 유출 사고와 방사성 폐기물의 재처리 및 처분 문제 등은 지구 규모의 환경 문 제뿐만 아니라 플루토늄 재처리로 핵무기 개발이 국제적인 문제가 되고 있다. 방사성 원소에 의한 오염 및 재해는 U, Th 등의 방사성 원소가 붕괴할 때 방사되는 방사능 피해뿐만 아니라 원자력 발전소에서 발생하 는 핵 폐기물 중 Th, Pu, 137Cs 등이 생태계를 파괴한다. 플루토늄은 +3, +4, +5, +6 가의 산화 상태로 무기 및 유기물과 복합 이온을 형 성하여 콜로이드상으로 부유하며 유동성이 대단히 크기 때문에 생태계에 쉽게 유입되어 순환한다. 따라서 고준위 방사성 폐기물은 해양저나 두수 성이 낮은 암석으로 구성된 육상의 지하에 폐기하여 생물권과 격리시켜 야한다.
(1) 고준위 방사성 페기물 원자로에서 우라늄이 붕괴될 때 많은 열(에너지)이 발생함과 동시에 원자핵 반응로의 연료봉에 플루토늄 (Pu), 넵투늄 (N p), 아메리슘 (Am), 퀴륨 (Cm) 등의 초우라늄 원소(t ransuran i um elemen t)가 축적된다. 따라 서 연료봉은 이들 원소들의 붕괴 결과로 강한 방사성을 가진다. 방사성 폐기물은 방사 독성이 강할 뿐만 아니라 많은 양의 . 열울 방출한다. 때문 에 안전을 위하여 붕괴 속도가 우라늄 광석 수준에 이를 때까지 이들 방 사성 폐기물을 특정 장소에 격리 보존하여야 한다. 방사성 동위원소에서 방출되는 방사선은 농업, 공업, 생물, 의학, 첨 단 산업 등에 이용되어 인류 생활 향상에 크게 기여할 뿐만 아니라 붕괴 할 때 발생하는 에너지는 발전에 이용되고 있다. 방사성 동위원소가 붕 괴할 때 발생하는 방사선과 방사성 동위원소는 한편으로는 생물계에 위 험한 환경 오염의 근원이 되기도 한다. 방사선 핵종이 붕괴할 때 발생하는 a, {], r, X 선 등의 방사선의 강 도 (radia t i on dose) 의 단위 는 Gy (gray ) 이 다. 이 는 1 J/k g, 100 rad 와 동일 하다. 1 rad 는 흡수물의 g당 1X 1 0-sJ 에너지를 방출하는 데 필요한 방 사량을 말하며 100 렘 (rem) 은 SV(s i eve rt)이며 X 선이나 西]의 1 rad 울 렘 이라 한다. 방사선은 방사선 발생지와의 거리에 따른 방사 에너지의 강 도에 따라 피해 정도가 다르다. 방사선의 강도에 따른 영향은 표 11-2 와 갇다. 방사성 폐기물은 원자로 연료 사이클 과정에서 생성된다. 물론 우라늄 광산에서 폐석이나 선광 후 폐기물에도 방사성 폐기물이 포함되어 있다. 우라늄 연료 사이클 중에 가장 위험한 고준위 방사성 폐기물(H LW) 은 연료 원소의 초기 제작시에 만들어진다. 또한 원자로에서 사용 후에 재 처리 과정에서도 만들어지며 재처리하지 않고 폐기하였을 때도 발생한 다. 핵연료 처리 과정과 가압 경수로형의 원자로의 모식은 그림 11-2 와
같다.
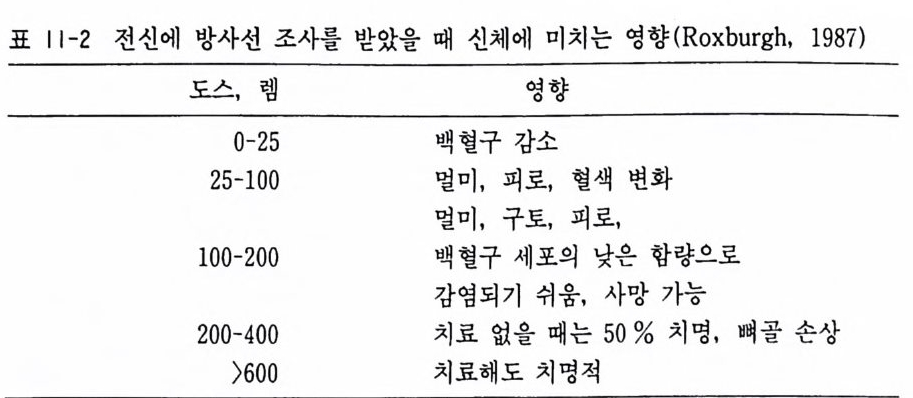 표 11-2 전신에 방사선 조사를 받았을 때 신체에 미치는 영향 (Roxbur g h, 1987)
표 11-2 전신에 방사선 조사를 받았을 때 신체에 미치는 영향 (Roxbur g h, 1987)
원자로 속의 천연 연료 우라늄에서 23Su 이 소진되면 연료봉을 반응로 에서 제거하고 이를 반응로 사이트에서 방사성의 강도가 떨어질 때까지 5 년 정도 저장한다. 그 다음에 연료 원소를 재처리하여 우라늄과 플루토 늄을 회수한다. 이를 위하여 우라늄 연료는 금속 보관기에서 꺼내어 질 산으로 용해시킨다. 용액에서 트리부틸 인산(tri bu ty l phosp ha t e , TBP) 과 무향 케로진 (OK) 용매로 우라늄과 플루토늄을 분리시킨다. 잔류 질산 용액에는 99.9 %의 비휘발성 붕괴 산물과 0.1 %의 우라늄, <1 %의 플 루토늄과 기타 초우라늄 원소 등이 포함되어 있다. 이들 방사성 핵종의 붕괴에 의해 생성된 열 때문에 잔류물은 보론규산염 그래스로 옮겨 방사 성 폐기물 저장고에 보관한다. 회수된 U 는 23su 를 정재하여 재사용하며 반응로에서 238U 에서 생성된 239Pu 는 원자핵 무기 제작에 사용된다 (Blasew itz 등, 1983) . 원자력 발전에서 전력 1 GWe( lG W=109W) 생성할 때 6m3 의 고준위 방사성 폐기물이 생성되며 ~50 m3 정도의 a 선 방출 방사성 농축물이 형 성된다. NEA(nuclear energy a g enc y)에 의하면 방사성 폐기물 1 메트릭돈 울 재처리하면 고준위 방사성 폐기물이 5m3 정도가 생성된다. NEA의
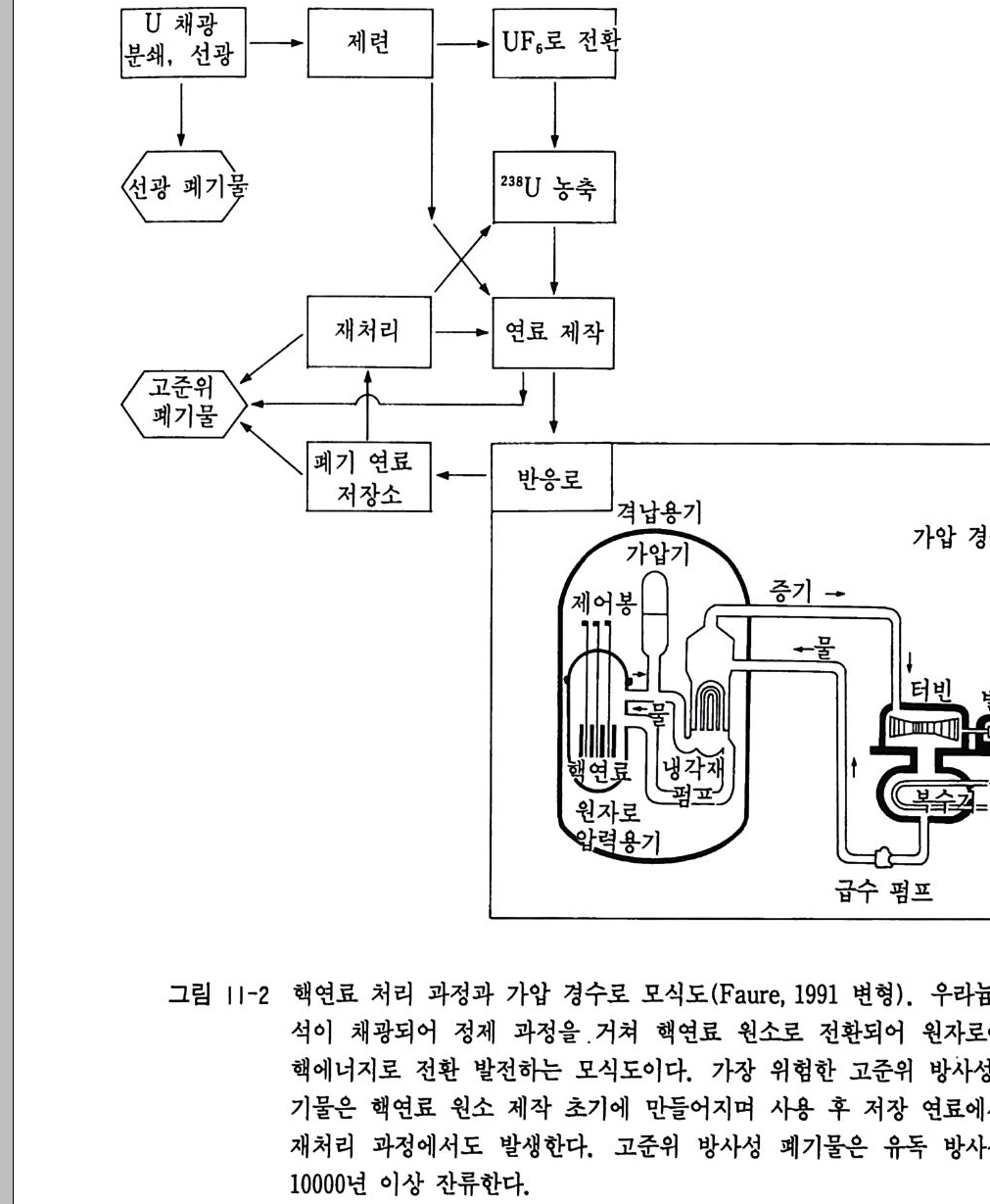 一三曰jx一~l三
一三曰jx一~l三
추정에 의하면 2000 년대 세계에서 원자력 발전 용량이 600GWe( 연간 15000metr ic t on 의 핵연료 처리시에 생성될 수 있는 양)가 될 것으로 추정하 고 있다. 만일 이때 사용되는 방사성 물질을 반 정도만 재처리한다 해도 세계적으로 연간 750m 떡 고준위 방사성 폐기물이 생성된다. Roxburgh (1987) 에 의 하면 2000 년 경 미 국에 서 발생 하는 126000 MCi 강도의 고준위 방사성 폐기물이 10500m3 가 생성될 것으로 추정 보고하였다. 그리고 기타 방사성 폐기물 2.28 X 106m3 를 더 고려하면 미국에서만 4735X 1 018 Bq (b ecq ue rel, IC i(큐리) =3.70 X 1010B q)의 방사성이 축적되게 된다. 고준위 핵 폐기물의 붕괴 산물인 방사 화학 성분은 연료 중의 235u 동 위원소의 존재량에 의하거나 반응로의 중성자 에너지 스펙트럼 등에서 추정할 수 있다. 1 Mwe 1 년간 가동 후 핵 반응로에서 제거한 후에 발 생하는 방사성 핵종과 시간이 지남에 따라 발생한 방사성 동위원소 활동 도의 추정 량은 표 11-3 과 같다. 방사성의 활동도와 방사성 유해성과 딸원소는 시간이 지남에 따라 감 소하고 있다. 원자로에서 발생한 폐기물을 냉각시켰을 때 냉각 100 일 후 방사성 핵종의 활동도 (ac tivity) 는 처 음보다 23 % 감소하며 활동도가 약 190TB q인 5 년 후에는 원래 값에서 0.84 % 더 감소하게 된다• 냉각 5 년 후에 고준위 폐기물에 잔류하고 있는 주요 방사성 핵종은 Pm, Pr, Ce 과 같은 회토류 원소 일부와 Pu, Rh 와 같은 백금족 원소, Sr, Ba 과 같 은 알칼리토류 원소, 기타 Kr, Y, Cs 등이다. SURF(spe n t unrepr o cessed fu el) 에는 악티늄족의 원소인 23sPu, 240Pu, 2“Am, 237Np , 238u, 잔류 235u 등이 포함되어 있다. 이들은 대부분 장 반감기 핵종이다. 따라서 SURF 가 HLW 에서보다 방사성이 더 강하고 재처리한 HLW 에서보다 방사성 활동 기간이 길다(그림 11-3). 그림 11-3 에서 보면 HLW 와 SURF 의 핵분열 산물은 1 TB q로 붕괴 되는 데 1000 년도 걸리지 않지만 SURF 의 악티늄족은 10000 년 이상이 걸린다.
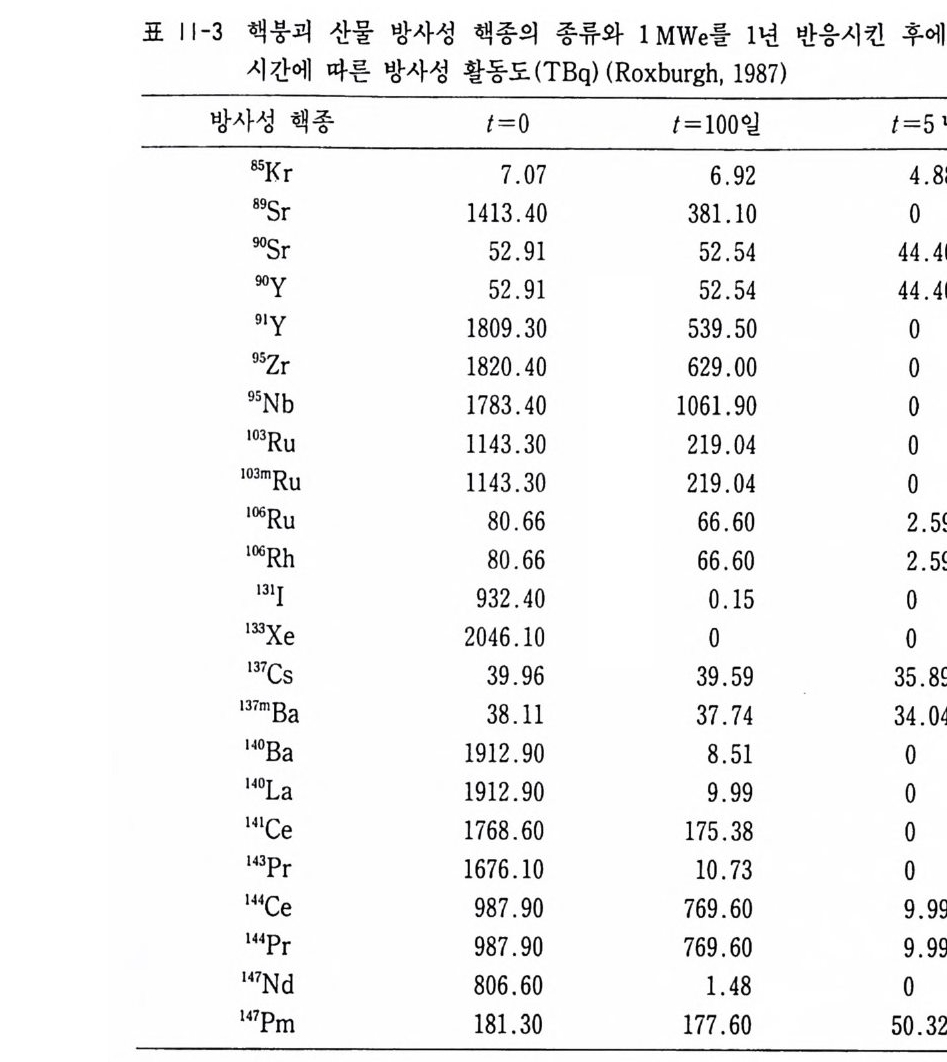 표 11-3 핵붕괴 산물 방사성 핵종의 종류와 l MWe 를 1 년 반응시킨 후에 나타난
표 11-3 핵붕괴 산물 방사성 핵종의 종류와 l MWe 를 1 년 반응시킨 후에 나타난
(2) 방사성 페기물의 지질학적 처리 방사성 폐기물은 원자로를 떠난 후 10000 년 이상 생물계에 영향을 준 다. 따라서 폐기물은 반드시 생물계와 격리시켜야 한다 (Cham p man 과
Mackin le y, 1987). 방사성 핵종은 지하수를 통하여 오염이 일어날 수 없 는 불투성충으로 특수 설계된 지하 공간에 폐기하여야 한다. 지하 폐기 방법 의에 심해저 해구, 대륙 빙하, 해양 속으로 주입하는 등의 폐기 방 법도 고려될 수 있다. 그러나 지하 저장 방법이 현재 가장 안전하게 활 용되고 있다. 이유는 지질학적으로 적합한 지역에 특수 공법에 의해 건
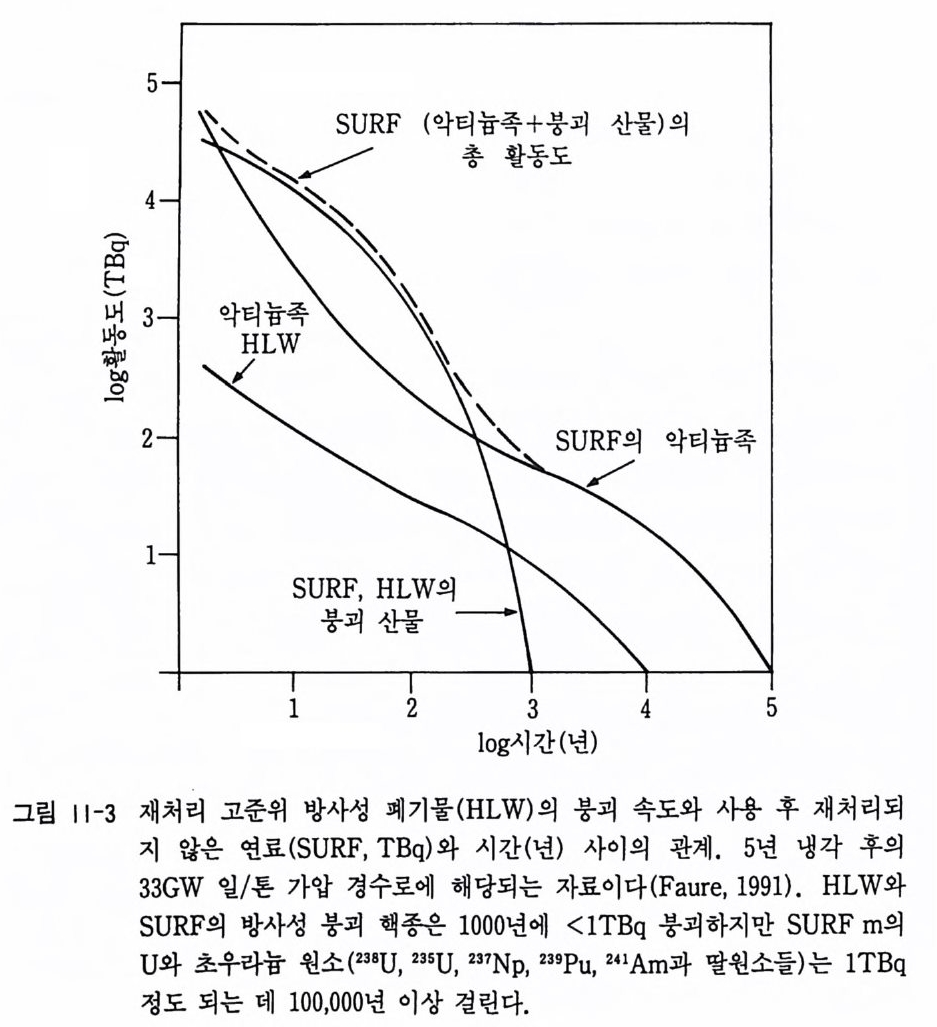 5
5
설된 지역에 폐기하므로 안정성이 높다는 점이다. 그리고 지하 저장법은 관리 유지비가 들지 않고 건설 장소의 선정에 편리함과 융통성이 있다. 왜냐하면 대상 지역의 암석도 화강암 지역, 암염과 같은 증발암 지역, 셰일 , 응회암, 현무암 지역 등을 목적에 맞게 선정할 수 있고 위치 선정 등도 편리하다. 더욱이 지하에 건설할 때는 광산 공법의 적용이 편리한 점 등이 있다. 그리고 지하 공간에 폐기할 때는 지화학적 모델링으로 미 래의 폐기물에 의한 오영을 예측하여 사전에 예방할 수 있다. 그리고 원자력 발전소의 구조물 설치 지역은 지진, 태풍, 해일 등 지 질 재해에 안전한 지역으로 견고한 암반 위에 설치되어야 하며 방사성 폐기물 처리 지역 역시 위와 같은 지질학적 조건을 만족하는 지역이어야 한다. (3) 플루토늄의 지구화학 Np , Pu, Am, Cm 등의 초우라늄 원소들은 원래 태양계 성운에 존재 하였으나 이들은 모두 방사성 동위원소이기 때문에 방사성 붕괴가 일어 난다. 2 38U(4 .4 7 X 10 년)과 235U(7.04 X l0 년)은 반감기가 길기 때문에 현 재 까지 존재 하고 있으나 244Pu ( 1}=8 . 3 X1 0 년) 은 존재 하지 않는다. Np , Pu, Am, Cm 등은 반감기가 짧기 때문에 일부 원소만이 지구 물질 내 에 소량 존재하고 있다. 피치블렌드(pit chblende) 와 카노타이트 (camo tit e) 와 같은 우라늄 광물 내에 239Pu( 1} =2 . 44 X l0 년)이 확인되었다 (Seabor g 와 Perlman, 1948, Gamer 등, 1948) . 초우라늄 원소들은 우라늄 광물 내 에 존재할 뿐만 아니라 원자로에서나 핵폭발 실험시에 형성될 수 있다. 초우라늄 원소의 동위 원소 중 그림 11-4 에 검 게 표시된 부분의 동위 원소 는 방사성 폐 기물과 SURF 에서 산출될 뿐만 아니라 238Pu 과 함께 RTGS (방사성 동위원소 열발전기)에서 태울 때 발생한다. 따라서 최근에는 지구 환경에서는 자연 방사성 동위원소보다 인공 방사성 기원의 동위원소가
더 많이 존재하고 있다(H arle y, 1980). 핵무기 실험이나 원자력 발전소의 방사성 폐기물의 재처리 과정에서 발생한 다양한 방사성 핵종이 해양과 호소성 퇴적물의 연령 측정에 사용될 뿐만 아니라 남극이나 그린란드의 빙하 연대 측정에 사용되고 있다 (S t anners 와 Astm , 1984 , Koid e 등, 1985). 플루토늄 동위원소에는 238Pu, m pu, 24oPu, 241Pu, 242Pu 등이 있다. 핵무기 실험시에 발생한 플루토늄 동위원소의 비는 240 Pu/2 39 P u= 0 . 18 土 0 . 002, 242Pu/ 2 39Pu=0 . 004 土 0 . 001 이다. 플루토늄 동위원소가 존재 하려 면 238 Np , 239Np , 24°Np , 2Np 등과 같은 단반감기 동위 원소가 존재 하고 있어야 한다 . 241Pu 는 2 ◄ o p u 에 의해서 형성되며 2 41Pu 은 f3붕괴로 24'Am 이 된다. 241Am 은 방해석이나 아라고나이트 결정 표면에 쉽게 흡착 (Shambha g와 Morse, 1982) 될 뿐만 아니라 해수에서 쉽게 퇴적물로 흡수되기도 한다 . 플루토늄은 핵실험, 원자력 발전소, 방사성 함유 암석 등에서 자연 환 경으로 유입된다. 플루토늄은 +3, +4, +5, +6 가의 산화 상태로 존재 할 수 있으며 유기물과 무기물 리간드(lig ands) 와 복합 이온을 형성하거 나 콜로이드질 부유물을 형성할 수도 있다(그립 11-5). 때문에 플 루토늄 은 다양한 환경 조건에서 이동성이 크기 때문에 해양 생물계의 먹이사슬 에 쉽게 전이될 수 있다. 따라서 어류나 해산물이 쉽게 플루토늄으로 오 염된다. 플루토늄은 해양에서 생물 입자들에게 쉽게 흡수될 수 있는 반 면 퇴적물로 퇴적되면 분해되어 다시 해수로 유출되어 심해수에 용액 상 태로 존재한다. 따라서 플루토늄의 해양에서의 거동은 대단히 복잡하다. (4) 소련의 체르노빌 원자로의 방사성 물질 유출 사고 키에프 부근에 위치한 옛 소련의 체르노빌 원자력 발전소에서 가동 중 인 RBMK 형 4 개의 원자로는 연료봉이 고압 경수 펌프의 파이프 내에
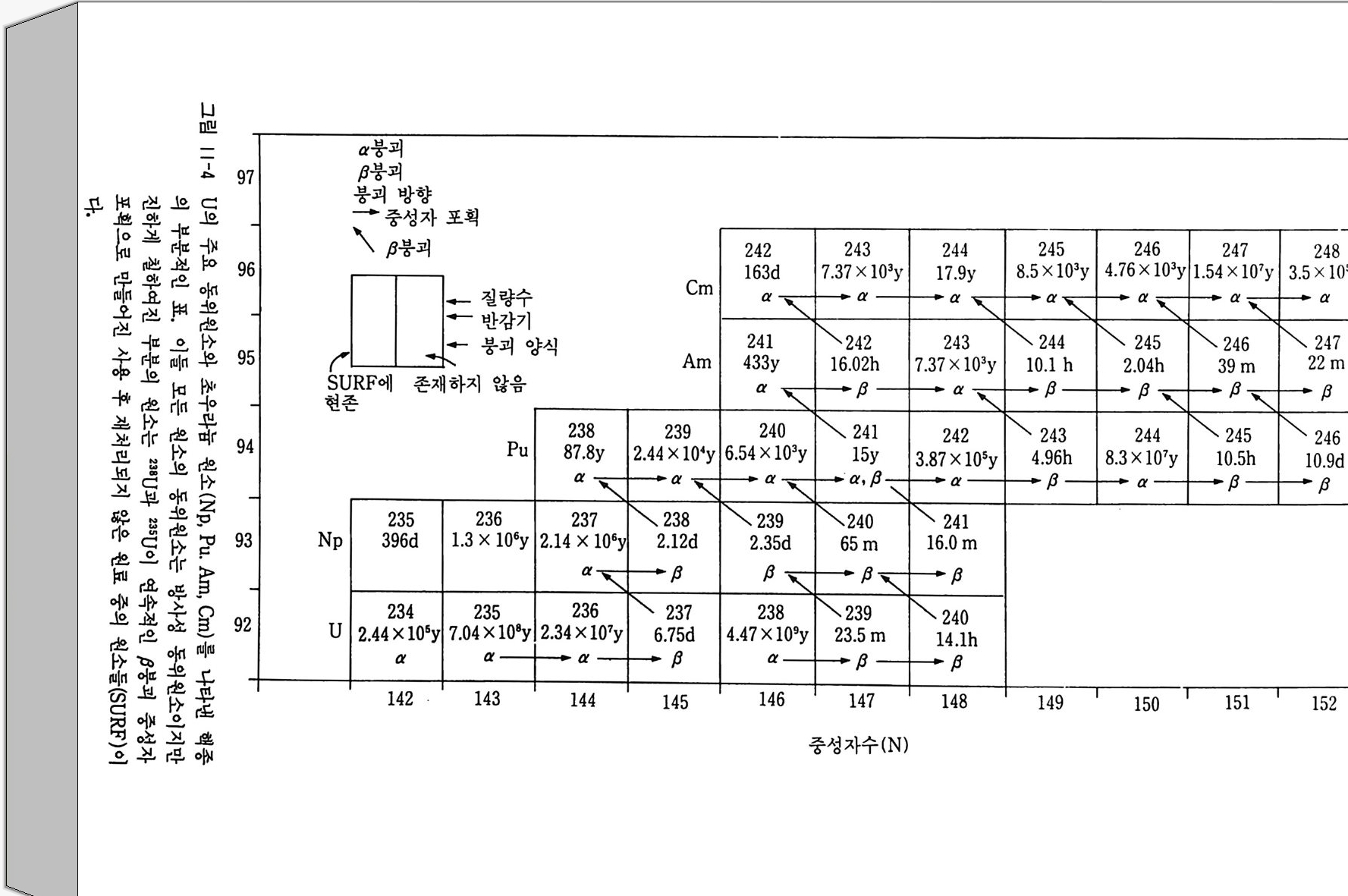 F h
F h
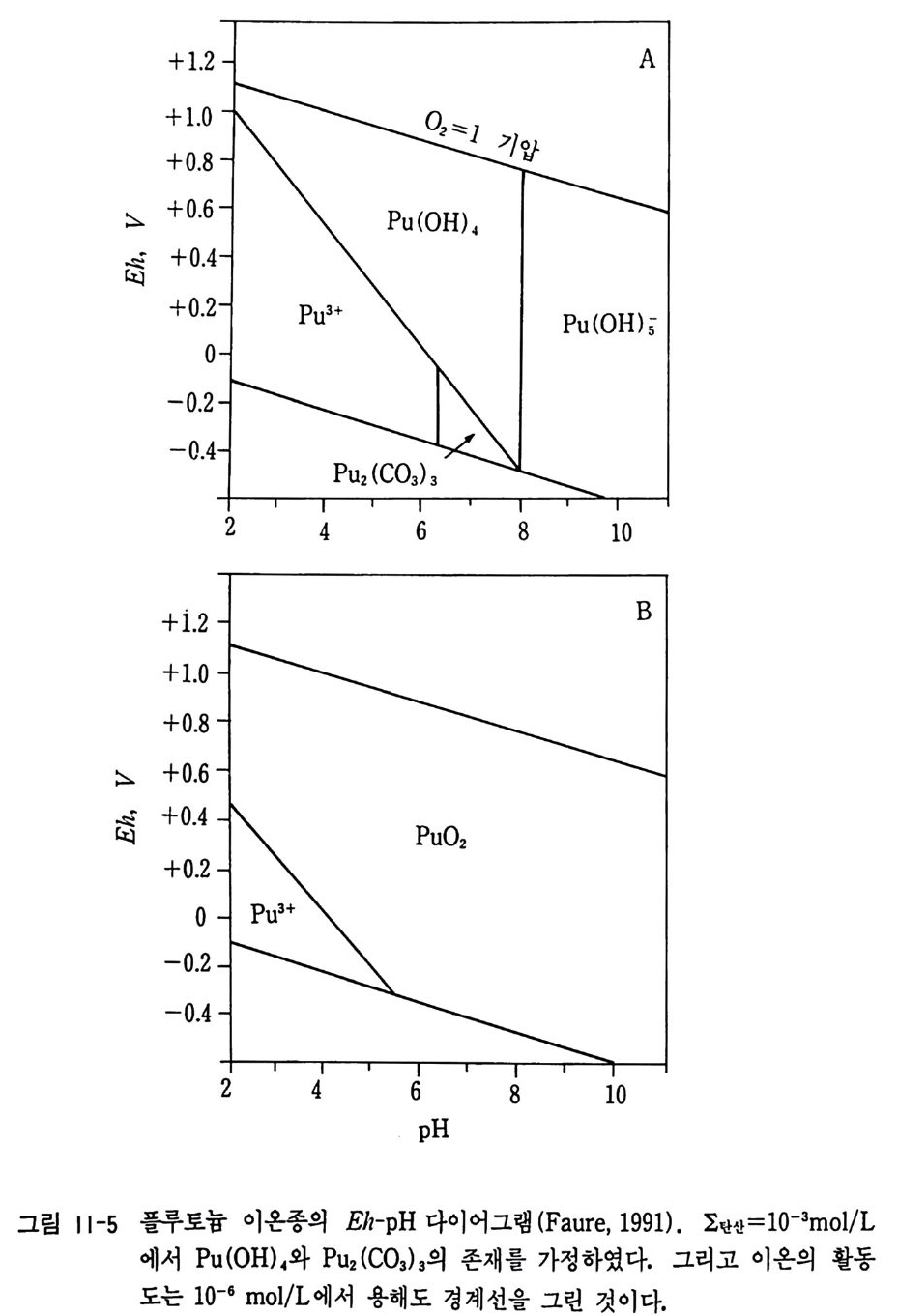 +l 2L0o8o50A020020A A
+l 2L0o8o50A020020A A
장착되어 있었다. 우라늄 연료 집합체는 흑연 속에 장착되어 있었다. No4 원자로는 114.7 kg 우라늄을 채운 1659 핵연료 집합체로 되어 있었 다. 핵 연료는 610 일간 반응로에 서 반응하였으며 90Sr 과 137Cs 를 포함한 200 종의 방사성 동위원소 핵종을 생성하고 있었다. 원자로 가동 관리자가 반응로의 흑연로심의 열이 주발전기의 작동에 충분한지 여부를 점검하는 과정에서 오조작으로 에너지 유출이 3 초 사이 에 200 에서 530 메가와트로 급증하여 반응로의 작동이 중지되고 노심의 온도가 3ooo · c 로 증가하였다. 이로 인해 증기압에 의한 압력 용기가 파 괴되었으며 핵연료의 피복제 연료 원소와 압력 찬넬의 지르코늄 (Zr) 이 물과 화학 반응하여 지르코늄 산화물을 형성하여 H2 가스를 방출, 이것 이 02 와 폭발적으로 반응, 반응로심의 2500 톤의 감속제용 흑연으로 채 워 진 철제 원자로 건물이 1986 년 4 월 26 일 폭발하였다. 이 때 우라늄 연료 원소와 반응 핵종들이 대량 유출되고 250 톤의 흑연이 연소되었다. 폭발 후 며칠간 계속 원자로의 온도가 상승하여 방사성 동위원소가 붕괴되었 으며 폭발로 냉각 시스템이 파괴되었다. 유출된 방사성 핵종은 온도 상 승에 따라 폭발 후 급격히 감소하고 9 일 후에야 초기 상태로 회복되었 다. 이곳에서 2 차적으로 비활성 가스, 1311 , 134Cs, 137Cs 그리고 소량의 sgs r, go Sr, 141Ce, l44Ce, 238Pu, 239Pu, 24op u 등의 원소들이 방출되 었다. 방사성 핵종은 스웨덴, 핀란드까지 빠르게 이동되었다. 그리고 러시아의 서부 지역과 대부분의 유럽 국가에 낙진되었다. 이때 북반구에 떨어진 137Cs 의 총량은 10X1016B q이었다 (Ans p au gh 등, 1988, Baie r , 1989). 이들 은 러시아의 서부와 유럽에 79%, 아시아에 20%, 캐나다와 미국에는 각각 2.5X1014 와 2.8Xl014 Bq 낙진되었다. 이 폭발 사고로 31 명이 사망하고 237 명이 방사성에 감염되고 그리고 10000 명 이상이 이주하였다. 경제적 손실은 150 억 달러로 추정되었다. 러시아 이의의 국가에서 방사성 감염의 보고는 없지만 방사성 암 발생이
유럽에서 0 에서 0.2 %로 증가하였다 (Ans p au gh 등, 1988). (5) 원자력 발전소의 현황 1988 년 말 세계의 원자력 발전소는 420 기 가 운전 중에 있으며 전력 공 급의 18 %인 326,168,000 kW 의 전력을 생산하고 있다. 건설중인 것이 118 기, 계획중인 것이 88 기로 총 626 기, 총발전 용량은 523,721, 00 0 kW 로 추정하고 있다(한국전력공사, 1990). 미국이 126 기, 소련 96 기, 프랑 스 67 기, 영국 45 기, 일본 36 기, 한국 14 기 등이 가동 중에 있다. 우리나라에서는 고리 원자력 발전소 4 기, 월성 원자력 발전소 1 기, 울 진에 2 기, 영광에 4 기 등이 있다(표 11-4). 월성의 가압중수소로 1 기를 제의하고는 모두 가압경수로형이다. 냉각제와 감속제로 물(H 2 0) 을 사용 하며 핵연료는 저농축 235U(3 %)을 사용하고 있다. 11-7 지구 환경의 보전 지구는 보통 암석권, 대기권, 생물권, 수권으로 구분하고 있다. 여기 에 Chard i n (1 881-1955) 은 사고력의 피막이란 의미의 정신권 (noos p here) 을 추가하였다. 정신권은 철학적인 용어라기보다는 인간 활동을 중심으로 한 정신권 지구화학, 즉 사회 지구화학 분야라고 생각할 수 있다. 인류 사회와 지구물질계의 진화와의 관련성과 자연 개조를 연구하는 학문의 한 분야로 등장하고 있다(H an y a, 1988). 지구 환경 문제는 특정 국가의 문제가 아니며 전세계적인 문제임과 동 시에 복합 작용으로 그의 원인과 결과가 초래되기 때문에 환경 윤리의 중요성은 더욱 증대되고 있다. 지구 온난화, 사막화, 산성비, 해양 오 영, 대기 오영, 토양 오염, 수질 오염, 오존층의 파괴 등이 산업혁명 이
후 인구 증가, 과학 문명의 발달과 함께 급속히 증대하고 있다.
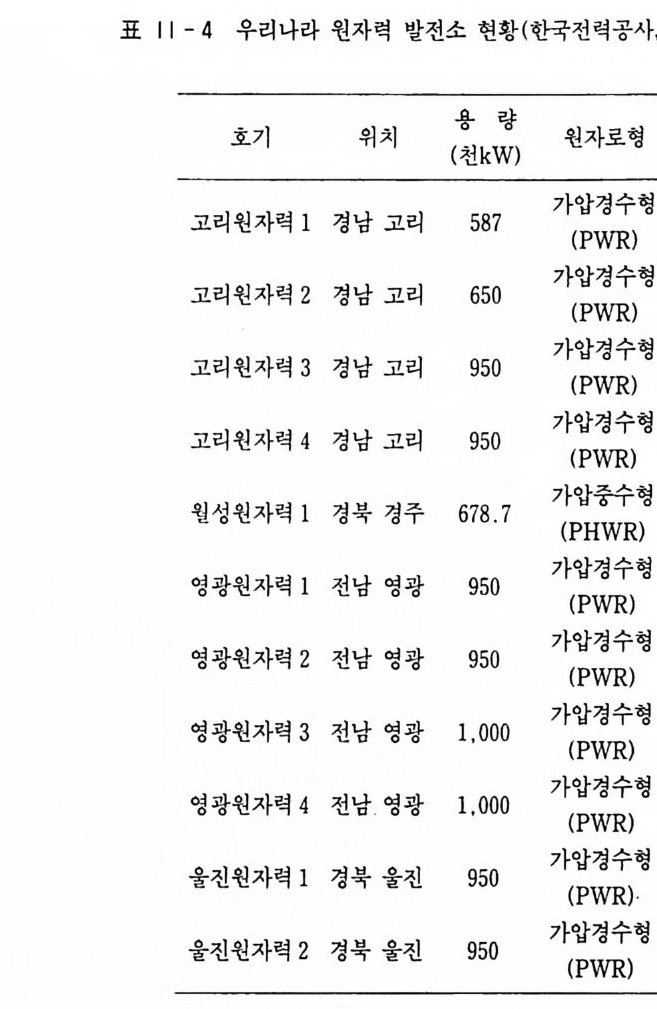 표 11 -4 우리나라 원자력 발전소 현황(한국전력공사, 1990)
표 11 -4 우리나라 원자력 발전소 현황(한국전력공사, 1990)
산업혁명 이전에는 지구의 암석권, 대기권, 생물권, 수권, 정신권의 각 권 사이에 물질 평형이 이루어져 있었다. 그러나 산업혁명 이후 정신 권에 큰 변화가 왔다. 죽 인간 생활의 향상을 위하여 화석연료의 사용 급증, 인구의 증가, 급속한 공업화, 생존 경쟁에 의한 핵무기의 개발 등
이 이루어지면서 고도로 발달한 과학 기술이 자연을 급개조하여 각 물질 권 사이의 평형이 깨어지기 시작하였다. 서기 2000 년 경에는 지구상의 인구가 60 억을 넘게 될 것이다. 그러나 식량 생산량의 증가는 인구 증가 와는 달리 둔화되어 지역적으로 식량 부족과 과잉 생산 지역이 발생함으 로써 지구상에는 식량의 불균형이 일어날 것이다(그립 11-6). 죽 자연계 의 탄소, 질소, 산소, 황의 순환과 같은 원소의 순환, 물의 순환, 판구 조 운동에 의한 지각물질의 순환 등의 물질의 순환 속도에 큰 변화가 일 어났다. 자연적으로 조화(평형)될 수 있는 순환 속도가 인간활동으로 인 해 인위적으로 변화되면서 자연의 조화와 질서가 파괴되기 시작하였다 .
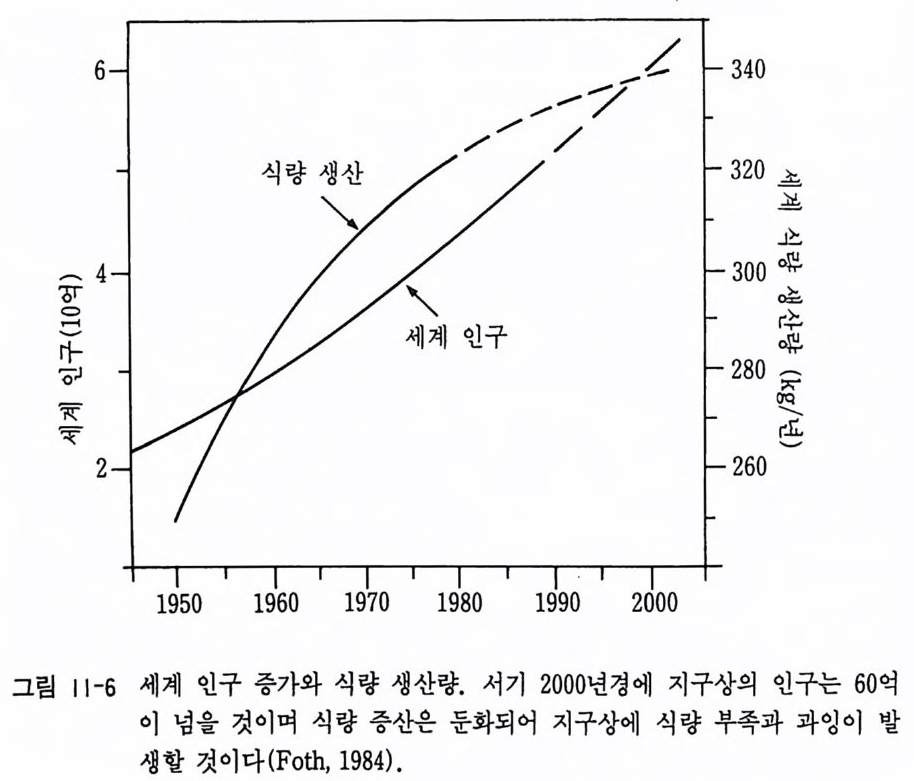 6 니 .,,,,.-7-~ I-34 0
6 니 .,,,,.-7-~ I-34 0
따라서 지구 환경 보전은 정신권의 안정과 정상화가 우선되어야 하고 지 속 가능한 자연 개발과 자연과의 공생을 위하여 〈 자연의 보전 = 자연의 개발 = 자연의 이용 〉 의 평형 (조화)을 유지시키는 데 우리 인류의 모든 연 구력을 집중시켜야 된다고 본다. 때문에 오늘날 정신권 내에서도 많은 갈등이 초래되고 있다. 이를 위하여 필자는 우주와 거대한 자연의 평형, 인간과 자연의 조화 그리고 자연의 수수께끼와 신비를 푸는 일 등이 동 위원소와 갇은 미세한 물질의 단위의 연구와 개발에서 가능해진다고 믿 고 있다. 뿐만 아니라 자연계 질서 유지에 생물계의 박테리아, 곰팡이류 와 같은 미생물의 역할이 대단히 크기 때문에 박테리아와 같은 미생물을 지혜롭게 조절함으로써 생물과 자연의 조화를 함께 찾아야 할 것으로 믿 고있다.
참고문헌 권성택 (1991) 우리나라 현생 화강암질에 대한 사마륨-니오디미움 동위 원소 연구 : 지각의 성인 및 구조고찰. 제 46 차 대한지질학회 학술 발표 회 초록집 , p. 528. 김규한, 中井信之 (19 88) 「남한의 지하수 및 강수의 안정동위원소 조성」 지질학회지 24(1) pp.3 9-46. 김규한 (19 90) 무극 금은 광상에 대한 유체포유물 및 안정동위원소 분석 연구」 광산지 질 23, pp. 1-9. 김규한 (1991) 동위원소지질학, 민음사, p. 552 김규한 (19 92) 米占土鑛物學(번역서), 춘광, p.1 9 0. 김규한, 박성숙, 나춘기 (1994) 남한의 중생대 화강암류의 Nd, Sr 동위 원소 및 유체모유물연구, 대한지질학회 학술발표 요약집. 김규한, 이진수 (1993) 경상되적분지내에 분포하는 백 악기 화산암류의 암석지구화학적 연구, 지질학회지 29(1), pp. 8f- 9 6. 김상현, 전효택 (1993) 삼보 연 - 아연-중정석 광산주변토양에서 중금속오 영 연구, 한국자원공학회 지 30, pp. 228-237. 김주용, 전효택 (1993) 장항제 련소제 역 토양과 분전 중의 Cu, Pb, Zn 및 Cd 의 지구화학적 분산과 산출상태. 광산지질 26, pp. 175-185. 이용일 (1993) 석유지질학, 민음사, p. 310. 전효택 (1991) 鑛物探査를 위 한 岩石地球化學, 機電硏究社, p. 469. 전효택, 김종대, 김옥배, 민경원, 박영석, 윤정환 (1993) 應用地球化學,
서울大學校出版部, p. 380. 전효택 (1993) 환경지구화학과 건강, 서울대학교 출판부, p. 139. 최진범 김우한, 좌용주, 1993, 지구라는 행성. 춘광, p. 204. 谷山鐵郞 (1991) 地球環境保全槪論, 東京大學 出版會, p. 181 . 鹿園直建 (1992) 地球〉久子소 科學入門, 東京大學 出版會. 松尾植士 (1989) 地球化學, 講談社 甘 4 .:r. > 子 1 711, p. 2 66. 山縣 登 (1977) 微量元素-環境科學特論-産業圓曹 p. 2 86. 木村 俊 (1990) 微量元素(TJ世界, 裝華房, p. 190. 西村雅吉 (1992) 環境化學, 裝華房, p. 156. 松葉谷治 (1991) 熱 7k (7) 地球化學, 袋華房, p. 139. 小嶋 稅 (1991) 地球物理學槪論, 東京大學 出版會, p. 423. 松井義人 • 坂野昇平 (1992) 岩石, 鑛物(7)地球化學, 岩波書店, p. 304. 鹿園直建 (1988) 地(7)底(7)杓 〈김 l-;.' 袋華房, p. 182. 正田 誠 小林孝彰 (1985) 環境(7)科學, 學會出版七 > 夕一, p. 2 10. 半谷高久 (1988) 地球化學入門,丸善株式會社, p. 211 . 石川洋平 (1991) 黑鑛, 共立出版株式會社, p. 120. 佐佐木照 石原舜三, 關陽太朗 (1992) 地球(7)資源, 地表(7)開發, 岩波뺨 店, p. 310. 山 中健生 (1992) 入門生物地球化學, 學會出版七 > 夕―, p. 134. 小山忠四郞 (1980) 生物地球化學, 東京大學出版會, p. 258. 森本信男 (1989) 造岩鑛物學, 東京大學出版會, p. 239. 一國雅巳 (1972) 無機地球化學, 培風館, p. 1 48. 高橋博彰, 新田信, 松本和子, 伊藤 一, 多田 意 (1989) 現代(7)基礎化學, 朝倉書店, p. 199. 飯山敏道, 河村雄行, 中嶋 悟 (1994) 實驗地球化學, 東京大學出版會, p. 233. 渡邊淳夫 (1993) , 基礎敎養環境化學, 內田老鶴圓 p. 185.
久城育夫 荒牧重雄 (1991) 火成岩 k 군 (J)生成, 岩波 普 店, p. 268. 立見辰雄 (1980) 現代鑛床學(J)基礎, 東京大學出版會. 松井孝典 (1987) 水惑星iit문生圭 n t묘#, 講談社. 久城育夫 (1978) 地球(J)物質科學 Il 岩波講座 3 岩波書店 13-40, 93-117. 高橋榮一 (1986), 火山 第 2 集 30 S17-S40. 杉村 新 (19 78) 變動寸 5 地球 I 岩波講座 10 岩波書店 pp. 159-181. 山 口 喬 (19 81) 入門化學熱力學, 培風館, p. 214. 千原秀昭 崎山 秘 (1975) 化學平衡, 化學同人, p. 235. 萩野一善 (1984) 化學熱力學講義, 東京化學同人, p. 146. 牛來正夫 (1990) 大陸地穀進化論序說, 共立出版株式會社, p. 221 . 白 水晴雄 (1988) 帖土鑛物學, 朝倉 書 店, p. 185. 佐野有司 (1988) 地球化學, 22p . 4 金奎漢 • 中井信之 (1981) 韓國(J)溫泉 7k (J) 7k 素, 酸素 及伊琉黃同位體比. 地球化學, 15, pp. 6-16. 和田英太郞 (19 86) 生物界(J) 1sN : 13c(J ) 分布t:!!寸 5 總設. Radio - iso to p e s 35, pp. 166-147 泉邦秋本 實 森泉, 廣井敏男,岩田進年, 川崎 健 (1991) 今 日 m 地球環境 新日本新畵 浦邊 微郞 (1984) 鑛山地質, 34, p. 3 26 玲木靜夫 (1994) *(J)環境科字, 內田老鶴園. p. 305. 橋本 外 (1988) 水處理技術, 29, p. 26 管野 明男 (1989) J;,4.,-tt 층 , p. 829 Alleg re, C. J. and Turcott e, D. L. (1985) Geodyn a mi c mix i n g in the mesosph e re boundary laye r and the orig in of oceanic isla nd. Geop hy s . Res. Lett , 12 . pp. 207-210. Allegr e, C. J. and Hart, S. R. (1978) Trace elements i n igne ous pet r o log y, Elsevi er Sci en ti fic Pub. Co., p. 272.
Alleg re, C. J. and Ben Uth ma n, D. (19 80) Nd-Sr iso to p i c relati on ship in gran i toi d rocks and conti ne nta l crust develop m ent : a chemi ca l ap- pro ach to orog en esis . N atu r e, 286. pp. 335- 34 2. Alvarez, L. W. , A lvarez, W. Asaro, F., Mi ch el, H. V. (1980) Extr a te r res- trial cause for the Creta c eous-Tertia r y exti nc t ion . Scie n ce, 208, pp. 1095-1108. Anderson, D. L. (19 83) J. Geop hy s . R es. 38. b-50. Anderson, 0. L. (1980) The tem p er atu r e pro fi le of the upp e r mantl e , J. Geop h ys . 85. pp. 7003-7010. Anderson, 0. (19 15) Amer. Jou r. Sci ., 3 9. pp. 407-4 54 . Anspa u g h , L. R., Catl in, R. J., and Goldman, M. (1988) The glo bal im p ac t of the Chenoby l reacto r accid e nt. Sci en ce, 242. pp. 1513-1519 Barker, D . S. (19 83) Ign e ous rocks, Prentic e Hall, p . 417. Barth , T. F. W. (19 62) Theoretic al pet r o log y 2nd ed., Joh n Wi le y & Sons, Inc., N ew York. Bear, J. ( 1979) Hy dr auli cs of grou dwate r , M cGraw Hil l Inc., p. 567 Bearman, G. (1989) Ocean chem istr y and deep- s ea sedim ents , Perga m on Press, p. 134. Beerstre cher, E. (1954) Petr ol eum mic r obio l og y. Elsevie r , New York. Berman, R. S. and Brown, T. H. (1985) Heat capa c it y of min e rals in the sys t e m Na20-K20-CaO-Mg O -FeO-Fe20a-AlzOa-Si0 2 -Ti0 2 -H20-C02, J. Pet. 29. pp. 445-522. Berner, E. K. and Berner R. A. (1987) The glo bal wate r cyc l e, Prenti ce Hall, p. 396. Berner, R. A., (1980) Early dia g e n esis : A the oretic al app ro ach. Pri n- ceto n , N. J. Pri nc eto n Un iv. Press. Bis c hoff , J. L. and Dick son, F. W. (1975) Seawate r -basalt i nt e r acti on at
zoo·c a nd 500bars : Imp li ca ti on s for orig in of sea floo r heavy meta l dep os it s a nd regu la ti on of seawate r chemi st r y. Earth Planet. Sci. L ett . 25. pp. 385-397. Blackburn, W. H. and Dennen, W. H. (1988) Prin c i ple of mi ne ralog y. Wm C. Brown Pub. Blasewit z, A . G., Dav is , J. M. and Smi th, M . R. (1983) The tre atm e nt of radio a cti ve waste s . S pr i n g e r -V e rlag, New York, p. 658. Bowen, N. L. (1915) Amer. Jou r. Sci . 4 p. 40 Fig 5. Bowen, R. (19 91) . Isoto p e s and clim ate s . Elsevie r . p. 483. Boy le , E. A., Sclate r , F . R. and Edmond, J . M. (1977) The dis t r ib u ti on of dis s olved cop pe r in the Pacif ic. Earth Planet. Sci . lett 37. pp. 38- 54 . Broecke, W . S. (1971) A kin e ti c model for the chemi ca l comp os it ion of seawate r . Qu artn a ry. Res. 1. pp. 188-207. Broecke, W, S. and Peng, T. H. (19 82) Tracer in the sea. New York : Eldig io Press, Columbia Univ . Brown, H. J. M. (1979) Env iro menta l chemi str y of the elements . Aca- demi c Press. London. Brownlow, A. H. (1979) Geochemi str y, Prenti ce Hall, p . 498. Buennin g , D. K. and Buseck, P. R. (1973) Fe-Mg latt ice dif fus io n in oliv i n e . J. Geop h ic s Res. 78. pp. 6852-6862. Bugrann eitst m, sB .a sRs.o cai nadt e dN ewailtsho n m, aKn.g aHn .e s(e1 9n8o1d) ulOesr.g aD n eice p f iSlmea s. Raneds. m28iAc r. o popr.- 637-645. Burns, R. G., B urns, V. M. and Smig , W. (1974) Ferro mang an ese nodule min e ralog y : Sugg e ste d ter m ino log y of the pri n c ip a l mang an ese oxi de pha se. Abstr . Ann. Meet. Geo!. Soc. Am. Cameron, A. G. W. (1973) Cosmic , ine xp lo siv e nucleosyn the sis ,
Schramm and Arnett eds., U niv e r sity of Texas Press Austi n, T ex. pp. 3-6 . Camp b ell, A. Ry e. , D . and Pete r son, U. (19 84) A hyd r og en and oxy ge n iso to p e stu d y of t he San Cris t o b al mi ne , Peru : Imp li ca ti on s of the role of wate r to rock rati o for the gen esis of wolfr am i te dep os it s. E con. Geo!. 79. pp. 1818-1832. Carmi ch ael, I. S. E. and H. P. Eug st e r (19 87) Thermody na mi c modelin g of g el og ical mate r ia l s ; mi ne ral, flui d s and melts, Mi ne ralog ica l Soc i- ety of Americ a , p. 499 Champ m an, N. A. and Mackin l ey, I. G. (19 87) The geo log ica l dis p o sal of nuclear waste . Wi le y . New York. p. 232. Chatt er je e , N. D. (1991) Ap pli ed min e ralog ica l the rmody n ami cs , Sp ri n g e r -V e rlag, p. 3 21 . Clarke, D. B. (1992) Granit oi d rocks. C hap m an & Hall. p. 2 83. Clayt on , R. N., G rossman, L. and May ed a, T. K. (19 73) A comp o nent of pri m it ive nuclear comp os it ion in carbonaceous mete o rite s , S ci en ce 182 pp. 485-488. Coutu r ie r , Y. Mi ch ard, G . and Sarazin , G. (1984) . Conta n es de for mati on des comp le xes hyd roxy de s de !'al u mi nu m en soluti on agu e use de 20 a 75°C Geochim . Cosmoch im . Acta 48. pp. 649- 66 0. Cowen, J. P., Massoth , G. J. and Baker, E. T. (1986) Bacte r ia l scaveng- ing of Mn and Fe in a mid- to far- fi eld hyd roth e rmal Partil e plu me, Natu r e(London) 322. pp. 169-171. Cox, K, G., Bell, J. D. and Pankhurst, R. J. (1979) The int e r p re ta t i on of igne ous rocks. L ondon. Allen and Unwi n. Craig , H. (1961) Isoto p i c varia t i on s in mete o ric wate r s. Sci en ce 133. pp. 1702-1703.
Craig , H. (1963) The iso to p i c geo chemi st r y of wate r and carbon in geo th e rmal areas. pp. 117- 53 in Nuclear Geolog y in Geoth e rmal areas. Tong ior gi , E . ed. Spo l eto Pis a , Consig li o. Nacio n ale della Ric e rche Laborato r ie de Geolgi a Nucleare. Cris s , R. E. and Tayl o r, H. P. (1983) An 180 / 160 and D/ H stu d y of Tertia r y hyd r oth e rmal sys t e m s in the South e rn half of the Idaho bath o lit h. Geo!. Soc. Am. Bull 94. pp. 640-653. Crovis ie r , J. L., T homassin , J. H., Jut e a u, T., Eberhart, J. P., Touray, J. C. and Bail lif, P. 0983) Exp er im enta l seawate r -basaltic gla ss int e r ac- tion at 50'C , Geochim . Cosmochim . Acta 47 pp. 977-988. Czamanske, G. K. and Ry e, R. 0. (1974) Exp er im enta l ly dete r mi ne d sulfu r iso to p e frac ti on ati on s betw een sph alerite and gal ena in the tem p er atu r e rang e 600' to 275'.C . Econ. Geo!. 69. pp. 17-25. Dalrym p le , G. B. (19 91) The age of the Eart h, Sta n fo r d Univ . Press, p. 474. Dansgg a ard, W. (19 64) Sta b le iso to p e s in pre ci pp. itat i on . Tellus 16 (4) pp. 436- 46 8. Dein e s, P., L angm u ir , D. and Harmon, R. S. (1974) Sta b le carbon iso to p e rati os and the exis te n ce of a gas ph ase in the evoluti on of carbonate grou ndwate r . Geochir n . Cosrnochir n. Acta 38 pp.1 147-1164. Den iro , M., Jan d Hastr o f, C. A. (1985) Alte r ati on of 15N/14N and 13C/12 C rati os of pla nt matt er durin g the initial sta g e s of diag e n esis . Geo- chir n , Cosrnochir n Acta 49 pp. 97-115. Dennen, W. H. (1989) Mi ne ral resources, Tayl o r & Franci s, p. 255 Dep ao lo, D. J. and Wasserburg, G. J. (1979) Petr o g en etic mix i n g models and Nd-Sr iso to p i c pa tt ern s. Geochim . Cosmochi m . Acta ., 43 pp. 615 -62 7.
Dic k en (1995) Dadio g e n ic iso to p e geo log y Cambrid g e Univ . Press. Dick in s on, W. R. and Lath , W. C. (1971) A model for pla te tec to n ic evoluti on of mantl e lay er s. Sci en ce 174 pp. 400-404. Drever, J. I. (19 82) The Geochemi st r y of natu r al wate r s. P renti ce Hall, p. 3 88. Drever, J. J. (1988) Crust and the oceans. I n C. B. Grego r , R. M., Garrels, F. F., M ackenz and J. B. Mayn a rd(Eds). Chemi ca l cyc l es in the evolu- tion of the earth . pp. 17-53 Wi le y, New York. 2769. Edmond, J. M., Messures, C., McDuff , R. E., C ham, L. H., Collie r , R., Grant, B., Gordon, L. J. and Corliss , J. B. (1979) Rid g e crest h yd r oth e r- mal acti vi t y and the balances of the majo r and mi no r elements in the ocean ; The Galapa g o s data . E arth . Planet. Sci Lett . 46 pp. 1-18. Ehler, E. G. and Blatt , H. (19 80) Petr o log y, igne ous, sedim enta r y and meta m orph i c . W. H. Freeman and Co., p . 7 32. Ehmann, W. D. (19 68) Chondrite s and eart h crust, in Encyc l op ed ia of the chemic a l elements Hamp el ed., Van Nostr a nd Rein h old, New York. pp. 568-570. Ehrlic h , H. L. (1990) Geomi cr obio l og y, Marcel Dekker, Inc., p. 646 Faure, G. (1986) Prin c i ple s of iso to p e geo log y, Joh n, Wi ley & Sons, p. 584. Faure, G. (1991) Prin c i ple s and app li ca ti on s of ino rga n ic geo chemi st r y , Macm illa n, Pub. Co. p. 626. Ferry, J. M. and Sp ea r, F. S. (1978) Exp er im enta l calib r ati on of the par t ition of Fe and Mg betw een bio t i te and gar net. Contr ib. Mi ne ral. Petr o l. 66 pp. 113-117. Fouqu e t, Y., Wafi k, A., Cambon, P., Mevel, C., Mey er , G., and Gente , P. (1993) Tecto n i c s ett ing and mine ralgi ca l and geo chemi cal .z o nati on in
the Snake pit sulfid e dep os it (M i d- A t la nti c Rid g e at 23°N). Econ Geo!, 88. pp. 2018-2036. Fraser, D. G. (19 77) Thermodyn a mi cs in geo log y, D. Reid e l Pub. Co., p . 410. Fried man, I. and O'Neil , J . R. (1977) Comp ila ti on of sta b le iso to p e frat i on ati on fac to r s of g eo chemi ca l int e r est i n : Date of Geochemi str y 6th ed. M. Fleis c her ed. U. S. Gov. Prin t i ng Off ice . W ashin g t on , D. C. Froude, D. 0., I reland, T. R., Kin n ey, P . D ., W i lliam s, I. S. a nd Comp st o n , W. (1983) Ion mic ro p ro be ide nti fica ti on of 4,100-4,200 My r- old Terres- tria l zirc ons. Natu r e. 304 . pp. 616- 61 8. Gamer, C. S., B onner, i\. A. and Seaborg, G. T., (1948) Search for elements 94 and 93 in natu r e pre sence of 239 P in camoti te. J. Amer. Chem. Soc. 70. p. 3453. Garrels, R . M. and C. L. Chris t , ( 1965) Soluti on , min e rals and equ i li b r ia , A Harpe r & Row, p. 450. Garrels, R. M. and Mackenzie , F. T. (1971) Evoluti on of sedi m enta r y rocks. A new app ro ach to the stu d y of mate r ia l tra nsfe r and chang e thr oug h tim e. Nort on , New York. p. 397. Garrels, R. M. Mackenzie , F. T. and Hunt, C . (1975) Chemi cal cyc l es and the glo bal envir o nment : assessin g human influe nces. Kaufm a nn Los alto s , CA. p. 266. Gast, P. W. (19 72) The chemic al comp os it ion of the eart h,-the moon and chondriti c mete o rite s. In the natu r e of the solid eart h ed. E. C. Robert - son. pp. 19-40 New York McGraw-Hi ll. Geis k es, J. M . and Lawrence, J. R. (1981) Alte r ati on of v olcan ic m att er in deep sea sedim ents : Ev ide nce from the chemic a l comp o sit ion of int e r sti al wate r s from deep sea drill ing cores. Geochim . Cosch im. Acta
46 pp. 377-388. Gordon, P. (1968) Eq ui li b r iu m the mody na mi cs in pet ro log y. An int r o ducti on . Harpe r & Raw. p. 287 Grossman, L. (19 72) Condensati on in the pri m it ive solar nebula. Geo- chim . Cosmochim . Acta 36 pp. 597-619. Hanks, T. C. and Anderson, D. L. (1969) The early the rmal his t o r y of t he eart h. Phys . Earth Planet. Inte r io r s 2 pp. 19-29. Harley, J. H. (1980) , Pluto n iu m in the envir o nment a revie w J. Raclia t . Res. 21 pp. 83-104. Harris, P. G., Reay, A. and Whit e, I. G. (1967) Chemi ca l comp o sit ion of the upp e r mantl e. J, Geop h ys . Res. 72 pp. 6359-6369. Hay as hi, K. I. and Ohrnoto , H. (1991) Solubil it y of go ld in Nac1-a nd H2s- b earin g aqu eous soluti on s at 250-350°C . Geochim . Cosmochim Acta . 55 pp. 2111-2126. Helge s on, H. C., Delang, J. M. , N esbit t, H. W. and Bir d , D. K. (1978) Summary and Criti gue of the the rmodyn a mi c pro p er tie s of rock form - ing min e rals. A rn J. Sci. 278A pp. 1-229. Henderson, P. (1982) Inorga ni c geo chemi str y , Perga m on Press, p. 353 Hess, P: C. (1989) Orig ins of i gneo us rocks, Harvard Univ . Press, p. 335 Hoefs , J. (1987) Sta b le iso to p e geo chemi st r y , Spr i n g e r-Verlag, p. 241 Holland, H. D. (1972) The geo log ic his t o r y of sea wate r on att em p t to solve the pro blem. Geoch im. Cosmochim Ac ta. 28 pp. 1287-1302. Holland, H. D. (1984) The Chemi ca l evoluti on of the atm osph ere and ocean. Prin c eto n Univ e rsity Press. Irvin e , T. N. and Smit h, C. H. (1967) Ultr a mafi c rocks of the Muskox int r us io n . Nort hw est Territo r i es , Canada. In ultr a mafi c and relate d rocks(ed P. J. Wy llie) pp. 38-49.
Jac obsen, S. B. (1988) Isoto p i c constr a in t s on crusta l grow t h and recy- clin g . Earth Planet. Sci. Lett . 90 pp. 315-329. Jan nasch, H. W. and Moth , M. J. (1985) Geomi cr obio l og y of deep sea hyd roth e rmal vents . Sci en ce 229 pp. 717-725. Jµn g e, C. E., Shid l ouski, M. and Eic h nam, R. J. (1975) Geop h ys i c a l Res. 80 p. 4542. Kaji wa ra, Y. and Krouse, H. R. (1971) Sulfu r iso to p e pa rtit ion in g in meta l lic sulfid e sys t e m s. Canadia n J. Earth Sci. 8 pp. 1397-1408. Kallend, A. S., Marsh, A. R., P ic k les, J. H. and Procto r , M. V. (1983) Ac idi ty of rain in Europ e. A t om os. E nvir o n. 17 pp.1 27-137. Kearey, P. and Vin e F. J. ( 1990) Global tec to n ic s . Blackwell Scie n ti fic Pub. p. 302 Kim , K. H., Kim , 0. J., Nakai, N. and Lee, H. J. (1988) Sta b le iso to p e stu d ie s of the Sang d ong tun g st e n ore dep os it s. South Korea. Mi ning Geo!. 38 pp. 473- 48 7. Kim , K. H., S ata k e, H. and Mi zu ta n i , Y. (1992) Oxy ge n iso to p i c comp os it ion s of Mesozoic g ran it ic r ocks in South Korea. Mi ni n g Geo!. 42 pp. 311-322. Kim , K. H., Mi zu ta n i, Y. and Moon, H. S. (1995) Oxy ge n and sulfu r iso to p i c comp os it ion s of gua rt z, barite a nd sulfid e mi ne rals from the Sambo Pb-Zn-barite o re dep os it s, South Korea. G eochem ica l Jou rnal, 29 (5) . Kim m, V. J. (1976) Nati on al int e r in pri m ary drin k in g wate r regu la ti on s. Envir o nmenta l Prote c ti on Ag ne cy, EPA-570/9-76-003, p. 159 Kiy os u, Y. (1973) Sulf ur iso to p e frac ti on ati on among sph alerite , ga lena and sulfid e ion s. Geoch. J. 7 pp. 191-199. Koid e , M., Bert ine , K. K., Chow, T. J. and Goldberg, E. D. (1985) The 240
Pu/2 3 9Pu rati o, a po te n ti al geo chronomete r . Earth Planet. Sci. Lett . 72 pp.1 -8. Krauskop f, K. B. (1985) Intr o ducti on to geo chemi st r y , McGraw-H ill Book Co., p . 617 Krouse, H. R. and V. A. Grin e nko (1988) Sta b le iso to p e s ; Natu r al and anth r op og e n ic sulph ur in the envir o nment, Joh n, Wi le y & Sons. Kushir o , I. (1994) Recent exp er im enta l stu d ie s on pa rti al melti ng of mantl e per id o ti tes at hig h pre ssures usin g dia m ond agg reg a te s . J. Geol. Soc. Jap a n 100 pp. 103- 11 0. Kuznets o v, S. I. and Romaenko, V. I. (1963) The mi cr ob~olog ica l stu d y of inl and wate r s. lzvddate l 's tv o Akad. Nauk. SSSR . Moscow- Lenin g r ad . Maid m ent, D. R. (1993) Handbook of hyd rolog y, McGraw-H ill, Inc. Mason, B. (1966) Prin c i ple of geo chemi st r y , 3rd ed., J oh n Wil e y & Sons, Inc., New York, p. 5 2. Mats u h isa , Y., Goldsm ith, J. R. and Clay ton , R. N. (1979) Oxy ge n iso to p e frac ti on ati on in the sys t e m qu artz - albit e-a north i t e-w ate r . Geochi m. Cosmoch im Acta . 43, pp. 1131-1140. McBi m ey, A. R. (19 69) Comp o sit ion al varia t i on s in Cenozoic calc- alkali ne suit es of Centr a l Americ a, Orego n Dep t. Geol. Mi ne ral Ind. Bull, 65, pp. 185-189. Menzie s , M. A. and Wass, S . Y. (1983) CO2 ric h mantl e below easte r n Austr al i a ; REE, Sr and Nd iso to p e stu d y of Cenozoic alkalin e mag- mas and apa ti te ric h xenoli tws ., South e rn High lands pro vin c e, New South Wales, Austr a li a. Eart h Planet Sci . Lett . 65, pp. 287-302. Metz , P. (1970) Cont. Mi ne rl Petr o l., 28, pp. 221-250. Montg o mery , C. W. (1989) Envir o nmenta l geo log y, Wm C. Brown Publ,
p.4 76 Mori, T. and Green, D. H. (19 78) Laborato r y dup lica ti on of ph ase equ i li b r ia observed in n atu r al ga rnet Iherzolite s. J. Geo!., 8 6, pp. 83-97. Morik i y o , T. (1984) Carbon iso to p i c stu d y on coexis ti n g calcit e and grap h it e in the Ry o ke meta m orp h ic rocks north e rn Kis o dis tr i c t , Centr a l Jap a n . Contr i b. Mi ne ral Petr o l. , 8 7. pp. 251-259. Mott !, M. J., Holland, H. D. and Crarr, R , F. (1979) Chemi ca l exchang e durin g hyd r oth e rmal alte r ati on of basalt by sea wate r , Il . Exp er - im enta l results for Fe, Mn, and sulfu r spe c i es . Geochim , Cosmochim Acta , 43, pp. 869-884. My se n, B. 0. and Kushir o , I. (19 77) Comp os it ion al varia t i on s of coexis t- ing pha ses wit h deg ree of p er id o ti te in the upp e r mantl e. Am . Mi ne ral. 62, pp. 843- 86 5. Na, C. K. (1994) Genesis o f gran it oi d bath o lit hs of O kchon zone, Korea and its i m p li ca ti on s for crusta l evoluti on . Ph D. the sis , Tsukuba Univ . , p.1 54. Newt on , R. C. and Perkin s , D. Ill. (1982) Thermodyn a mi c c alib r ati on of geo baromete r s based on the assemblage s ga rnet-p la g ioc lase- orth p y ro xene(clin o p yrox ene)-qu a rt z. Amer. Mi ne ral., 67, pp. 203- 22 2. Nic h dls, G. D. (1967) Geochemi ca l stu d ie s of the ocean as evid e nce for the comp o sit ion of the mantl e, In mantl e s of t he eart h and ter restr i a l pla nets ed. S. K. Runcorn, pp. 285-304, New York, Wi ley - l n te r sci en ce. Nie ls on, D. L., Evans, S. H. and Sib b ett , B. S. (1986) Magm a ti c, stru ctu r - al, and hyd roth er mal evoluti on of the Mi ne ral mounta i n s int r u siv e comp le x, Utah . Geo!. Soc. Amer. Bull, 97, pp. 765-777. Nie r enberg, W. A. (19 92) Encyc l op ed ia of earth sys t e m scie n ce, Aca- demi c Press. Inc., Vol 1-4.
Nnauth , L. P. and Lowe, D. R. (19 78) Oxy ge n iso to p e geo chemi str y of cherts f rom the Onverwacht Group (3 .4 bill ion yea rs), Transvaal, South Afr ica , wit h i m p li ca ti on s for secular varia t i on s in the iso to p i c comp o- siti on of cherts . E arth . Planet. Sci. Lett , 41, pp. 209-222. Nordstr o m, D. K. and J. L. Munoz (1985) Geochemi ca l the rmodyn a mi cs , The Benja m i n/ Cummi ng s Pub. Co, Inc, p. 477 North ro p , D. A. and Clayt on , R. N. (1966) Oxyg e n iso to p e frac ti on ati on s in sys t e m s conta i n i n g dolomi te. J. G eo!., 74, pp. 174-196. Nort on , D. (1974) Chemi ca l mass tra nsfe r in the Rio Tanama sys t e m , west- c ontr a ! Puert o Ric o , Geochim , Cosmochim , Acta 38, pp. 267-277. O'Neil, J. R., Clay ton , R. N. and May ed a, T. K. (1969) Oxy ge n iso to p e frac t ion ati on in div a lent meta l carbonate s , J. C hem, Phy s. 51, pp. 5547- 5558. Osborn, E. F. a nd Tait, D. B. (19 52) Amer, Jou r. S ci. Bowen Volume, Fig 4. Pearce, J. A., (1982) Andesite , Orog en ic andesit es and relate d rocks. p p. 541, Joh n Wi ley & Sons. Poldervaart , A. (1955) Chemi str y . o f the eart h's crust : In crust of the Eart h-a sym po siu m (ed. Poldervaart) , pp.1 19-144, Geol. Soc. Am. Spe c . Pa p. 62. Powell, R. (19 78) Eq ui li b r iu m the rmodyn a mi cs in pet r o log y. Hap er & Raw, p. 287 Pric e, G. D. and N. H. Ross. (1992) The sta b il ity of min e rals, Champ - man & Hall, p. 368 Putn is, A. and J. D. C. McConnell (19 80) Prin c ip le s of m in e ral behavio u r, Blackwell Seie n ti fic Pub. p. 257 Raheim , A. and Green, D. H. (1974) Exp er im enta l dete r mi na ti on of the
tem p er atu r e and pre ssure depe n dence of the Fe-Mg par tit ion coexis t- ing ga rnet and clin o p yrox ene. Contr i b . Mi ne ral. Petr o l. , 48, pp. 179- 203. Reesman, A. L., Pic k ett , E. E. and Keller, W. D. (1969) Alumi nu m ion s in aqu e ous soluti on s. Amer. J. Sci ., 267, pp. 99-113. Ric h ardson, S. H., Gurney, J. J., Erlank, A. J. and Harris, W. (1984) Orig in of dia m onds in old enric h ed mantl e. Natu r e 310, pp. 198-202. Ric h ardson, S. M. and McSween, H. Y. Jr. (19 89) Geochemi st ry , Path - way s and Processes, Prenti ce Hall, p. 488. Rin g w ood, A. E. (1975) Comp os it ion and pet r o log y of the eart h mantl e . New York, McGraw Hill. Rin g w ood, A. E. (19 62) A model for the upp e r mantl e . J. Geop hy s . Res., 67, pp. 857-866. Rin g w ood, A. E. (1975) Comp os it ion and pet r o log y of the Eart h mantl e . McGraw-H ill, New York, p. 619. Robie , R. A. and Waldbaum, D. R. (1968) Thermodyn a mi c pro p er tie s of mi ne rals and relate d substa n ces at 298. 15K and one atm o sph e re pre ssure and at hig h er tem p er atu r es. U. S. Geol. Survey Bull, 1259. Robie , R. A., Hemi ng w a y, B. S. and Fis h er, J. R. (1978) Thermodyn a m ic pro p er tie s of mi ne rals and relate d substa n ces at 298.1 5 K and I bar pre ssure and at hig h er tem p er atu r es. U. S. Geol. Surv. Bull, 1452. Ronov, A. B. and Yaroshevsky, A. A. (1976) A new model for the chemi ca l stru ctu r e of the Eart h's crust. Geochem. Int., 13, pp. 89-121 . Roxburgh , I. S. (1987) Geolog y of hig h level nuclear waste disp o s al. Chapm an & Hall, London, p. 229. Sayl e s, F. L. (1979) The comp os it ion and dia g e nesis of int e r stit ial soluti on s : I. Fluxes across the sea wate r sedi m ent int e r f ac e in the
At la nti c Ocean. Geochim . Cosmochim . Acta , 45, pp. 1687-1703. Saxena, S . K . 0973) Thermodyn a mi cs of rock-fo r mi ng crys t a l lin e solu- tion s. New York Spr i n g e r -Verlag. Saxena, S. K. (1982) Advances in ph ys i c a l geo chemi str y , Spr i n g e r - Verlag, p. 353. Scheele, N. and Hoefs , J. 0992) Carbon iso to p e frac ti on ati on betw een calcit e, grap h it e and CO2 : an exp er im enta l stu d y. Contr i b . Mi ne ral. Petr o l. , 112, pp. 35-45. Schid l owski, M., Haye s , J. M. and Kap la n, I. R. (19 83) Isoto p i c inf e r - ences of ancie n t bio c hemi st r ie s : carbon, sulfu r, hyd r og en and nit ro - gen . In Schop f, J. W. ed. Earth ' s earlie s t bio s ph ere : Its orig in and evoluti on . Prin c eto n Univ . Press, pp. 149-186. Schop f, J. W. (19 83) Earth 's earlies t bio s ph ere, its orig in and evoluti on , Prin c eto n Univ . Press. p . 542. Seaborg, G. T. and Perlman, M. L. (19 48) Presence of 239Pu in pitch blen- de. J. Amer. Chem. Soc. 70, p. 1571 . Shambhag, P. M. and Morse, J. W. (1982) Americ ium int e r acti on wit h calcit e and arago nit e surf ac es in seawate r . Geochim . Cosmochim . Acta , 46. Sil len , L. G. (1967) The ocean as a chemi cal sys t e m . Sci en ce, 156, pp. 1189-1197. Skin n er, B. J. and Porte r , S. C. (1987) Phys i c a l geo log y. Joh n Wi le y & Sons. So, C. S., Ch i, S. J. and Choi, S. H. (1988) Geochemi ca l stu d ie s on Au-Ag hyd r oth e rmal vein depo sit s. Rep u blic of Korea : Jina n-Je o ung eu p mine rali ze d area. J. Mi n. Petr . Econ. Geol. , 83, pp. 449-471 . Spe n cer, K. J. and Lind sley, D. H. (1981) A soluti on model for coexis t in g
iro n-ti tan iu m oxid e s : Amer. Mi ne ral 66, p p. 1189-1201. Sta n ner, S . D. A. and Asto n , S. A. (19 84; The use of r epr o cessin g eff lue nt radio nuclid e s in the geo chronolog y of recent sedim ents . C hem. Geo!., 44, pp. 19-32. Sun, C. 0., Wi lli a n s, R . J. and Sun, S. S. (1974) Distr ib u ti on coeff ici e n ts of Eu and Sr for pla g ioc lase-liq u id and clin o p yro xene-liq u id equ i li br ia in oceanic rid g e basalt : An exp er im enta l stu d y. Geochim . Cosmochim . Acta 38, pp. 1415-1433. Suzuoki, T. and Clay ton , R. N. (19 66) Oxy ge n iso to p e frac ti on ati on s betw e en OH bearin g min e rals and wate r . Geochim . Cosmochim . Acta ., 40, pp. 1229- 12 40. Tayl o r, H. P. 0974) Oxy ge n and hyd r og en iso to p e evid e nce for large scale circ ulati on and int e r acti on betw een grou ndwate r s and igne ous int r u sio n s wit h pa rtic u lar refe r ence to the San Jua n volcanic field . Colorado, In Geochemi ca l tra nspo r t and kin e ti cs . Carnegi e Inst. Washin g t on , p. 634, pp. 299-323. Tayl o r, H. P. (1977) , Wate r /rock int e r acti on s and orig in of H20 in gran it ic bath o lit hs . J. Geo!. Soc., 133, pp. 509-558. Tayl o r, L. A., Onorato , P. I. K. and Uhtm ann, D. R. (19 77) Cooli ng rate esti m ati on s based on kin e ti c modell ing of Fe-Mg diffus io n in oliv ine . Proc. Lunar Sci . C onf. 8th , p p. 1581-1592. Tchobanog lo us, G. and E. D. Schroeder (1985) Wate r qua lit y. Add iso n- Wesley Pub. Co., p. 768. Thode, H. G., Craig , C. B., H ulsto n , J. R. and Rees, C. E. (1971) , Sulfu r iso to p e exchange betw een sulfu r dio x id e and hyd r og en sulfid e , Geo- chi m. Cosmochim . Acta 35, pp. 35-45. Thomp so n, G. (1983) Basalt-s e a wate r reacti on . In hyd r oth e rmal pro ces-
ses at seafl oo r spr e adin g cente r s, ed P. A. Rona, K. K. Bustr o n, L. Laubie r and K. L. Smi th, pp. 225-278, NATO conf. Ser. 4 v. 12 New York : Plenum Press. Tis s ot, S. P. and Tis s ot, P. H. (1984) Potr o leum form ati on and occurren- ce. 2nd revis e d. Sp ri n g e r -Verlag. Tucker, M. E. and V. P. Wrig h t, (1990) Carbonate sedim ento l og y. Blackwell Scie n ti fic Pub., p . 482. Turner, G., Enrig h t, M. C. and Cadog on , P. H. (1978) The early his t o r y of chondrite pp. arent bodie s inf e r red from •0Ar-39Ar age s . Proceed- ing s of the nin t h Luna and Planeta r y Scie n ce Confe r ence, pp. 989-1025. Waechte r , S, G. (1988) Befo re enzym e s and tem p lt es : Theory of surfa c e meta b olism . Mi cr obio l. Rev., 52, pp. 452-484. Walker, J. C. G. (1986) Eart h his t o r y, The several age s of the earth . Jon es and Bart le tt , Pub. Inc., p . 199. Walker, J. C. G., Klein , C., Schid l owski, M., Schop f, J. W., Ste v enson, D. J. and Wate r , M. R. (1983) Envir o menta l evoluti on of the Archean- early P rote r ozoic earth . In : J. W. Schop f ed. Earth ' s earlie s t b io s ph e re. Prin c eto n Un iv.- P r ess, pp. 260- 29 0. Wasserburg, G. J. and Dep ao lo, D. J. (19 79) Models of eart h str u ctu r e infer red from neodym ium and stro nti um iso to p i c abundances. Proc. Nat. Acad. Sci . USA ., 76, pp. 3594-3598. Wasson, J. J. (1985) Mete o rite s the ir record of early solar-sys t e m histo r y, New York, Freeman. W 血 e, I. G. (1967) Ultr a basic rocks and the comp os it ion of the upp e r mantl e . Eart h Planet, Sci . Lett ., 3, pp. 11-18. W血 e, W. M. (1985) Sources of ocean ic basalts : radio g e n i c iso to p e evi de nce. Geolog y, 13, pp. 115-118.
Wi lso n, M. (19 89) Ign e ous pet r o g en esis . U nwi n Hy ma n, p. 466. Wi nk ler, H. G. 0979) Petr o g en esis of meta m orph i c rocks. Sp ri n g e r - Verlag, p. 348. Wood, B. J. and Fraser, D. G. (19 77) Elementa r y the rmody na mi cs for geo log ist s. Oxfo rd Univ . Press, p. 303. Zie l in s ki, R. A. (19 75) Trace element evaluati on of a suit e o f r ocks from Reunio n lsland, India n Ocean. Geochim . Cosmoclt im . Acta . , 39, pp. 713- 734. Zin d ler, A. and Hart, S. (1986) Chemi ca l geo dyn a mi cs . A nn. Rev. Eart h. Pp an et. Sci , 14, pp. 493- 57 1 . Zolta i , T. (1960) Classif ica ti on of sili ca te s and oth e r mi ne rals wit h tet r a hedral str u ctu r es. Amer. Mi n. , 4 5, pp. 960-973.
 부록 |
부록 |
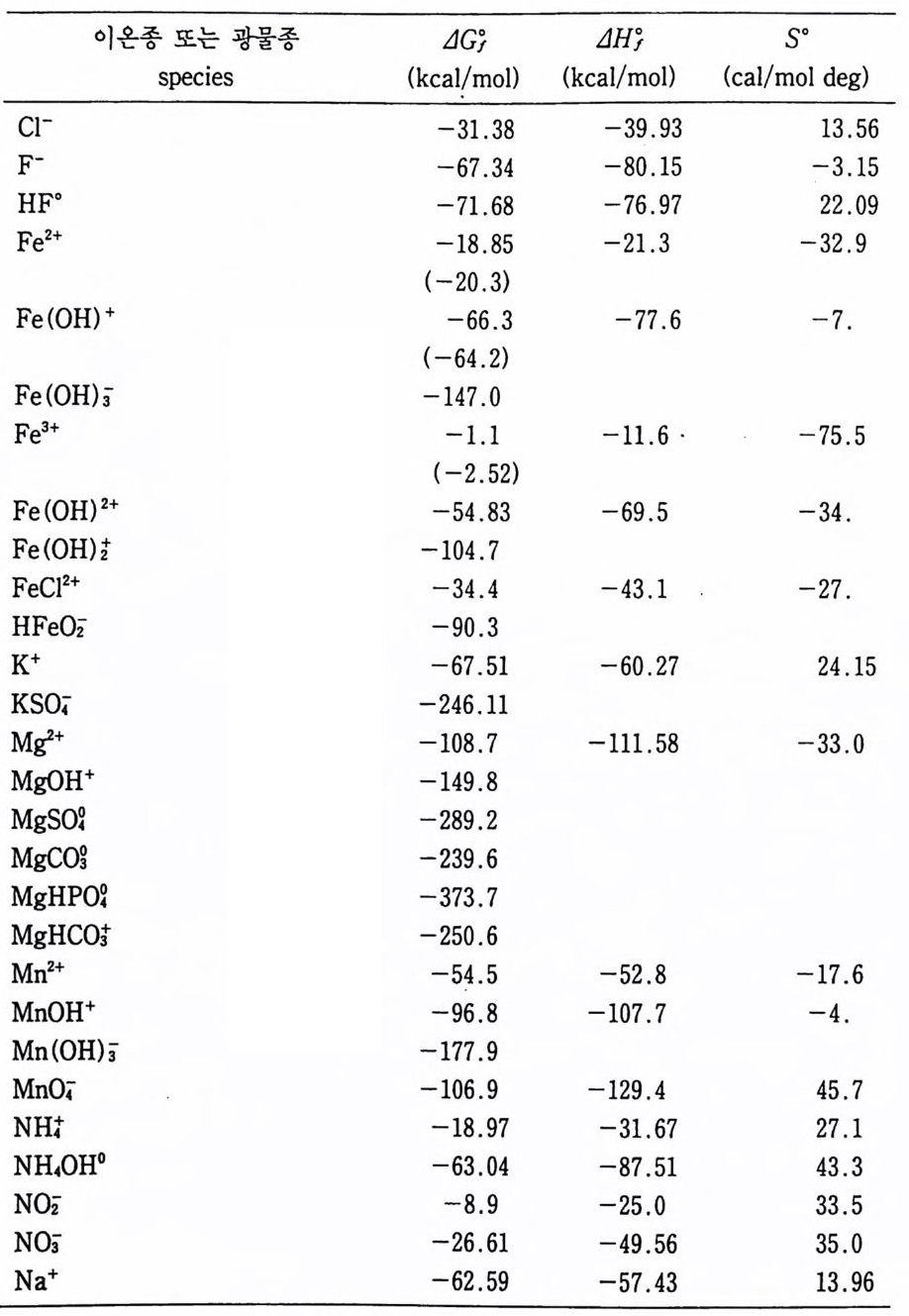 이온종 또는 광물종 L1G; L1H1 s·
이온종 또는 광물종 L1G; L1H1 s·
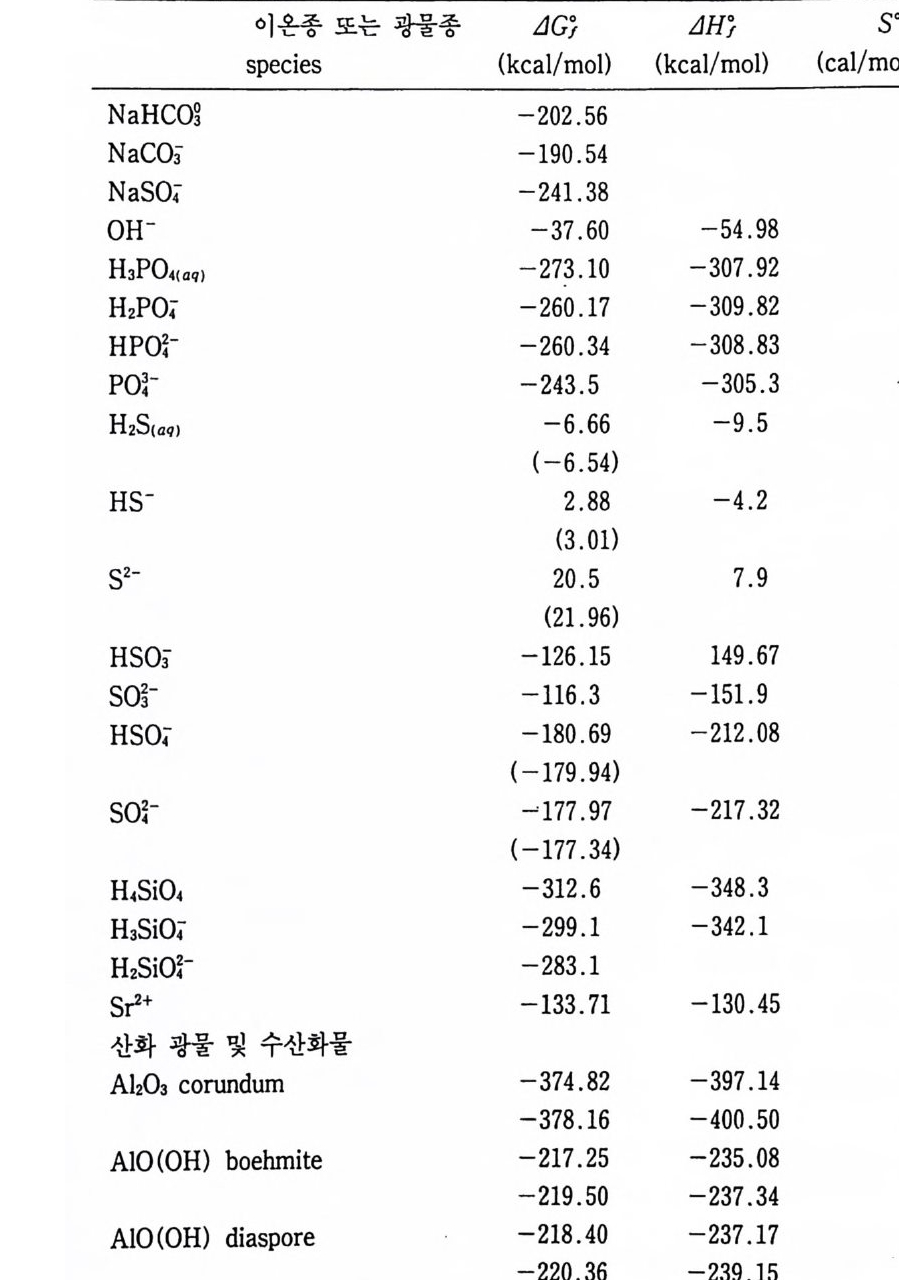 이온종 또는 광물종 L1G1 4H} S°
이온종 또는 광물종 L1G1 4H} S°
 이온종 또는 광물종 L1G1 4H} s·
이온종 또는 광물종 L1G1 4H} s·
 이온종 또는 광물종 4G} 4H; s·
이온종 또는 광물종 4G} 4H; s·
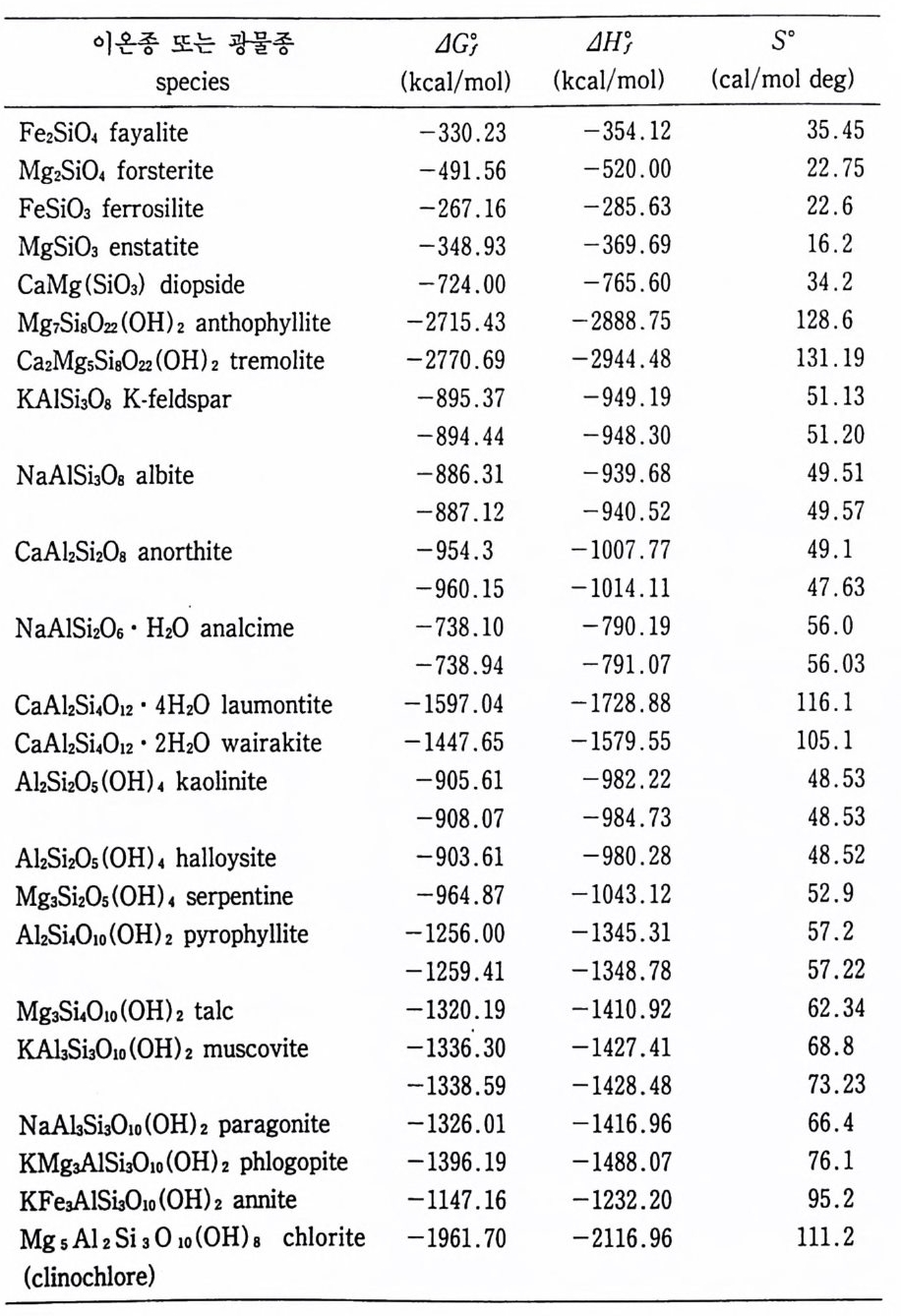 이온종 또는 광물종 4Gj L1H1 s·
이온종 또는 광물종 4Gj L1H1 s·
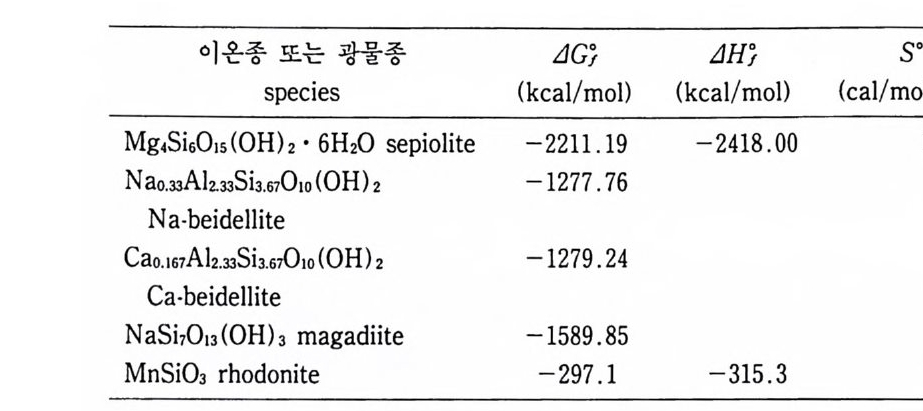 이온종 또는 광물종 4G, 4H} S°
이온종 또는 광물종 4G, 4H} S°
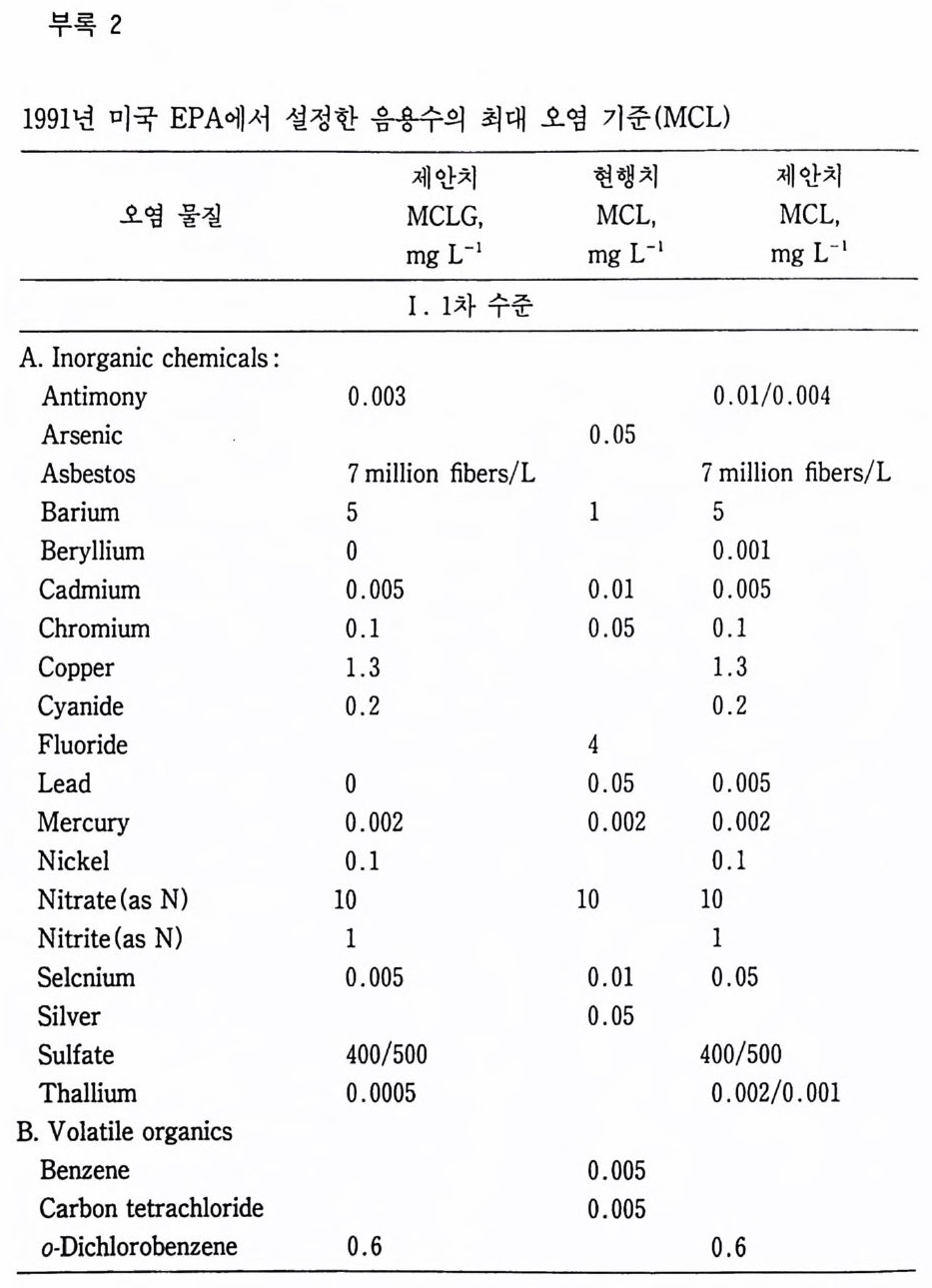 부록 2
부록 2
 제안치 현행치 제안치
제안치 현행치 제안치
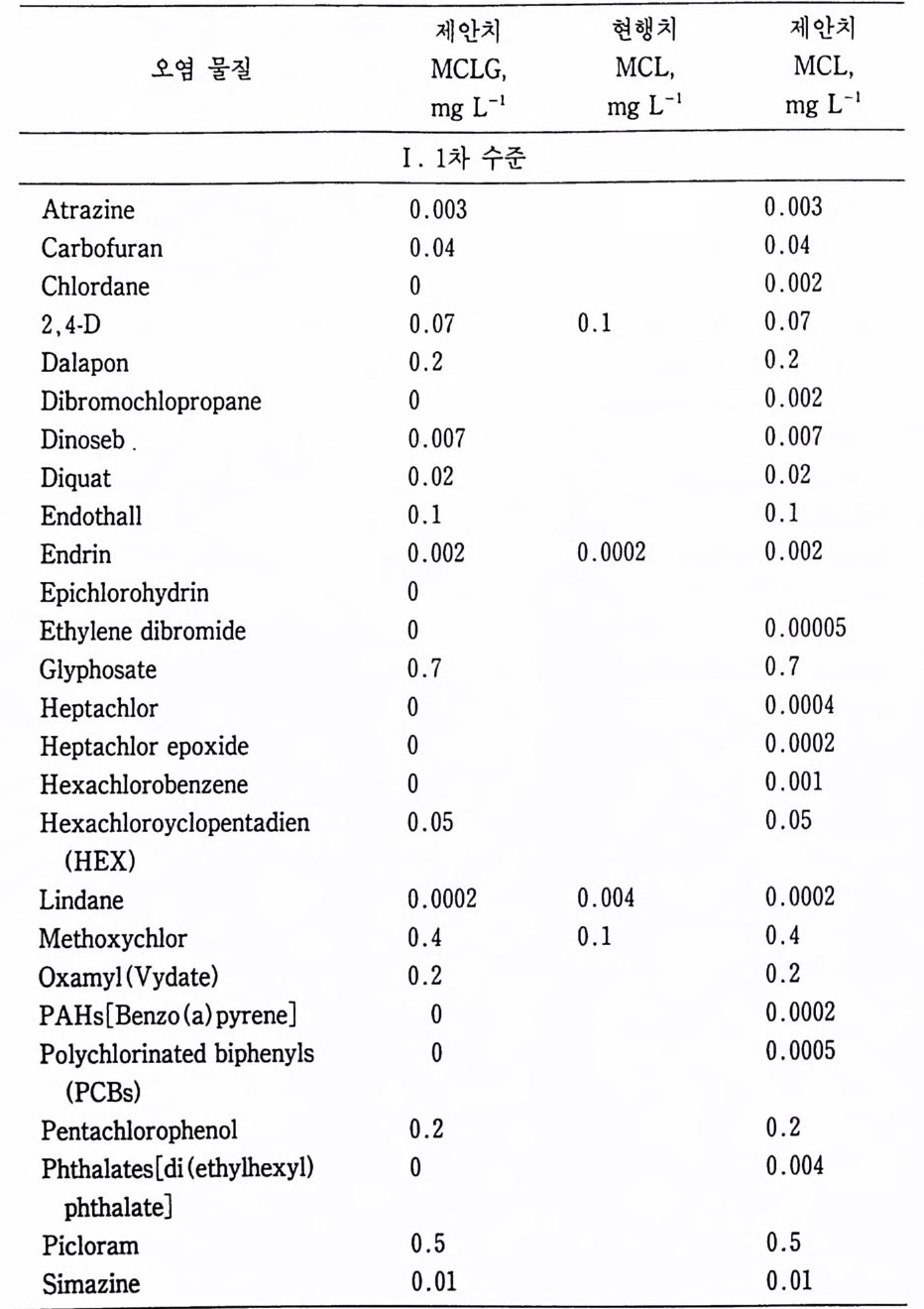 제안치 현행치 제안치
제안치 현행치 제안치
 제안치 현행치 제안치
제안치 현행치 제안치
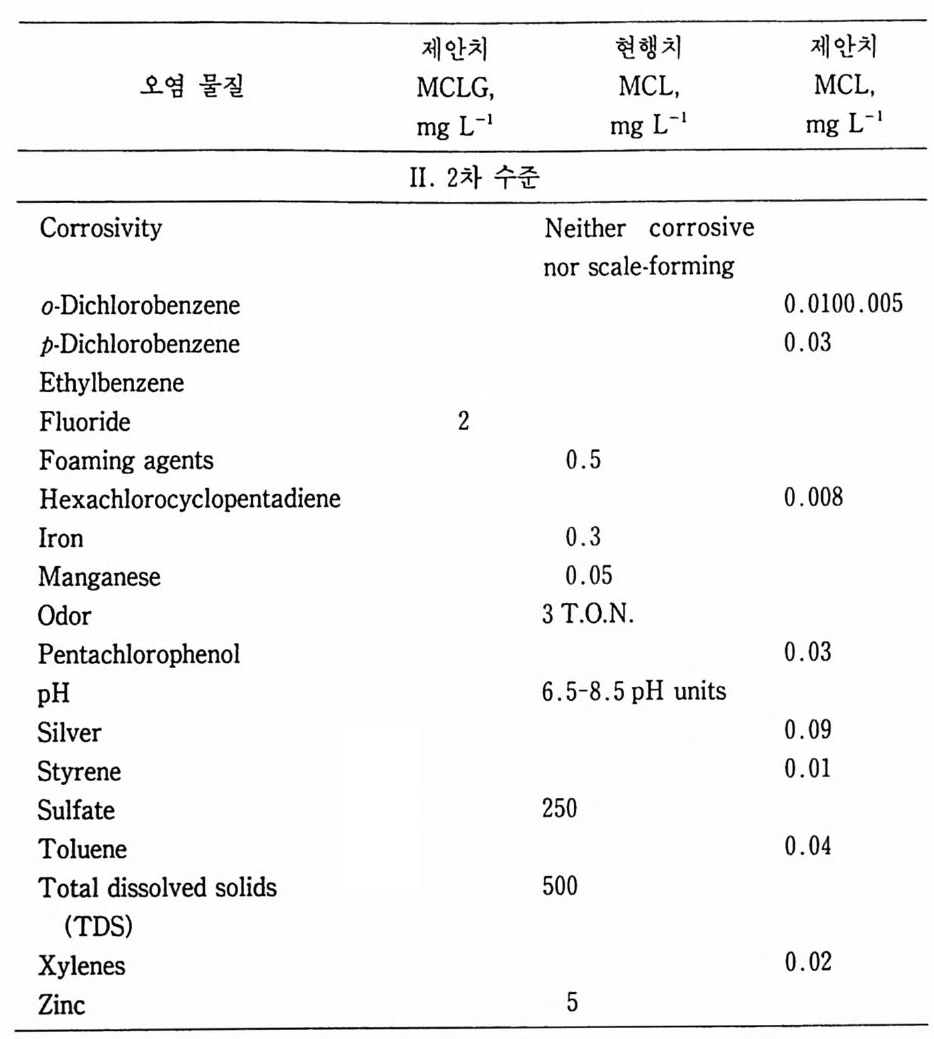 제안치 현행 치 제안치
제안치 현행 치 제안치
 부록 3
부록 3
 3 단위 환산
3 단위 환산
 F. 방사능
F. 방사능
찾아보기
 기
기
 E:
E:
 모델 연령 121
모델 연령 121
 산화형 대기 39
산화형 대기 39
 액상선 77
액상선 77
 이상용액 52, 80
이상용액 52, 80
 질량효과 151
질량효과 151
 E
E
 풀루토늄 394
풀루토늄 394
 환원형 대기 39
환원형 대기 39
김규한 연세대학교 지질학과 및 동 대학원 졸업 일본 나고야대학 지구과학과(이학박사) 미국 캘리포니아 공과대학 (CALTEC H) 방문 연구교수 현재 이화여자대학교 과학교육과 교수 t 동위원소지질학 』 『 한국의 지질과 광물자원 』 등의 저서와 년대 광상학의 기초 』 『 접토광물학 』 등의 역서 그리고 Oxy gen Isoto p i c Comp os it ion s of Mesozoic Granit ic Rocks in South Korea 의 다수의 논문 지구화학 대우학술총서 자연과학 104 1 판 1 쇄 찍음―― 1996 년 1 월 5 일 1 판 1 쇄 펴 냄 __ 1996 년 1 월 15 일 지은이一―김규한 펴낸이_朴孟浩 펴낸곳――(주)민음사 출판등록 1991 . 12. 20 제 16-490 호 서울특별시 강남구 신사동 506 강남출판문화연구소 대표전화 515-2000, 팩시밀리 515-2007 값 23,000 원 © 김규한, 1996 지구화학일반 KDC/451. 9 Prin t e d in Seoul, Korea ISBN 89-374-3604-3 94450 89-374-3000-2 (세트) 지은이와 합의하여 인지를 붙이지 않습니다•
대우학술총서(자연과학) 1 소립자와 게이지 상호작용 검진의 52 수리분류학 고철환 2 동력학특론 이병호 53 찰스 다윈 정용 재 3 질소고정 송 승달 54 금속부식 박용수 4 상전이와 임계현상 김두철 55 양자광학 이 상 수 5 촉매작용 진종식 56 효소반응 속도론 서정현 6 뫼스바우어 분광학 옥항남 57 화성암 성인론 이 만 성 7 극미량원소의 영양 승정자 58 확률론 구 자 홍 8 수소화봉소와 유기봉소 59 분자 분광학 소 현수 화합물 윤능민 60 벡터속 이론 양 재현 9 항생물질의 전합성 강 석구 61 곤충신경 생리학 부경생 10 국소적 형태의 Ati ya h-sin g e r 62 에 너 지띠 이론 모혜정 지표이론 지동표 63 수학 기초론 김 상 문 11 Mucop ol y s acchar i des 의 64 신경과학 김승 업 · 박찬웅 생화학 및 생물리학 박준우 65 BCH 부호와 Reed- 12 천체물리학 홍승수 Solomon 부호 이 만 영 13 프로스타글라딘 합성 김 성 각 66 양자 전기역학 김영덕 14 천연물화학연구법 우원식 67 군한론 박재걸 15 지방영양 김숙희 68 대수기하학 조영현 16 결정화유리 김 병 호 69 양자장이론 이재형 17 고분자에 의한 화학반응 조의환 70 해양오염과 생태계 심재형 18 과학혁명 김영식 71 비기체 연소합성 ( SHS ) 여 철 현 19 한국지질론 장 기 홍 72 크로마토그래피 이대운 20 정보이론 한영열 73 곤충의 사회행동 추종길 21 원자핵반응론 정운혁 74 동위원소 지질학 김규한 22 파 괴 역학 김상 철 75 X- 선 결정학 김 양 끊용자구 11 노 _ O I 른 오比 遠 24 반응속도론 정경훈 78 고분자의 구조와 형태학 이석현 25 미분위상수학 이현구 79 LC 에 의한 광학 이성질체의 26 자기공명방법 조성호 분리 현명호 27 플라스마 물리학과 핵융합 최덕인 80 신경전달믈짙 서유헌 28 천문관측과 분석 이시우 81 발생과 유전자 발현 3290 해석양탄미에고너생지변물환학 기백술광 호김 상돈 8832 스다테체계로론이드업정 인 31 편미분방정식론 김종식 84 중핵반응른김병 32 대통일 이론 소광섭 85 비가역 열역학 33 금속전자계의 다체이론 김덕주 86 등각장론입채호 34 액정중합체 진정일 87 방사선생률학 35 복합재료 권숙인 88 석유지철학이 36 단뷁질 생합성 박인원 89 베르누이 시행 333444444444172956843087 검급복질후생한리역한레핵일도이국이량국학변체리소구반한의저의에적론분다만에조상 너물양석 대광고기해광박연지론리체학대생산하물구석 학 른 현종주란학과물김방이 명충철법 민 김분의박김이노훈수동상 을하수광미김 필문영진룡일분학 순 작김 종용진소 999999919991105620789340 1 0 화유실유파응조배생생대신 노리도학기내한물리수인직경용 화선전김환요적세만유활배미· 경 소 김0용기성포양김 적 법화을생준성깁 인 리학 7 학 455190 군비생선체표형현막 론 김편 형박미만승분 안 방 정식론 하기식 110023 신대트경릭계스