 이 철수
이 철수  이 철수
이 철수
서 울대학교 화학공학과 졸업 플로리다주립대학교 화학공학과 졸업 (석사, 박사) 한국원자력연구소 책임연구원(실장) 현재 고려대학교 화학공학과 교수 저서 『신 과학운동 』 (공저) 역서 『화 학공학 열역학 』 (공역)
 비가역 열역학
비가역 열역학
 비가역 열역학
비가역 열역학
책 머리에 열역학은 기본적으로 두 개의 변화의 법칙을 제시한다. 하나는 제일 법칙으로 표시되는 에너지의 보존 법칙이고 다른 하나~ 제이법칙으로 표시되는 전화의 법칙이다. 보존의 법칙은 일반적이다. 그러나 진화 의 법칙은 경계조건의 지배를 받는다. 〈 고립계의 엔트로피는 증가한 다났근 단순한 형석의 진화의 법칙은 바로 고립계라는 경계조건에서 성 립하는 진화의 법칙을 의미한다. (평형)열역학이 동역학과 크게 구별되는 점의 하나는 보존의 법칙에 추가하여 전화의 법칙을 제시한다는 것이다. 우리가 살고 있는 세계가 비평형 세계인 만큼 일반적 진화의 법칙을 (평형)열역학에서와 같이 단순한 형식으로 제시할 수 있다면 우리가 얻을 수 있는 대상에 대한 이해는 훨씬 깊어질 것이다. 불행하게도 지금까지는 이러한 전화의 법 칙은 제한된 형식으로만 발견되어 있다. 이것은 우리가 살고 있는 세 계가 단순한 것이 아니고 복잡한 것이라는 결론을 강요하는 것처럼 보 인다. 근래에는 〈 복잡성의 과학 〉 이 많이 논의되고 있다. 열역학의 영역을 평형, 평형 근처 그리고 평형에서 멀리 떨어전 영 역의 세 개로 니누어 생각하면 편리하다. (평형)열역학의 영역을 확장 해서 평형 근처의 영역에 들어가면, 이러한 영역에서는 열역학이 두 가지의 중요한 법칙을 제시한다. 이 영역에서는 전화의 법칙이 평형계 에서와는 달리 엔트로피의 생성속도에 의하여 규정될 수 있다. 또한 소산 과정 (Diss ip a ti ve Process) 의 연계성을 말할 수 있고 소산 과정 울 기술하는 선형 법칙들의 계수에 관해 온사거의 대칭성 관계를 논의 할 수 있다. 평형 근처의 영역에 대한 이러한 능력은 동역학 또는 유
체역학과 다른 열역학의 고유의 것 이라고 말할 수 있다 . 평형 근처의 영역을 넘어서서 평형에서 멀리 떨 어전 영역으 로 들 어 가면 열역학이 해결 방법을 제시할 수 있는 문제들은 방법 은 다 르지만 많은 경우에 동역학이 할 수 있는 것과 중복된다. 아직까지 는 동역학 만큼 일반적이지 못하다는 표현이 더 적합할 것이다. 이러한 상황에서 평형에서 멀리 떨어진 영역에 열역학을 적용하고자 시도하는 것이 의 미가 있겠는가 하는 의문이 생길 수 있다. 아마도 이러한 의문 때문에 평형에서 멀리 떨어전 영역에 대한 열역학이 주로 프리고전 그룹에 의 해서만 주도되어 온 것이 아닌가 생각된다. 그리고 이러한 이유 때문 에 어떤 비평형 열역학의 책들에서는 평형에서 멀리 떨어진 영역에 관 한 논의를 피하는 것으로 생각된다. 이들의 방법은 프리고전 -글 란스 도르프 가설이라고도 불리는 일반적 진화의 법칙에 근거하고 있다. 평형에서 멀리 떨어전 영역에서 정상 상태가 불안정해지면 어떻게 될 것인가 하는 문제는 일반적으로 안정성 이론으로 답할 수 있는 문 제는 아니다. 근래에 〈 이상한 유인자 〉 라고도 불리는 혼돈 상태에 도 달하는 과정이 많이 연구되고 있다. 혼돈 상태에 도달하는 대표적 과 정은 파이젠바움 수열과 관련되어 알려져 있는데 이 과정에서는 한 정 상 상태가 불안정해지면서 주기가 배가 되는 다른 정상 상태로 전이하 여 궁극적으로 주기가 무한대가 되는 상태에 도달하고 이 상태가 혼돈 상태 이다. 따라서 하나의 소산 구조 (Di ss ip a ti ve Str u ctu r e) 또는 정 상 상태가 불안정해지면 다른 소산 구조가 나타나는 경우가 많다. 이 책 에서는 화학 반응과 기본적인 유체 역학계의 소산 구조를 논의하지만 이 현상은 혹성의 구름 무늬 (Trit ton _a n d Davis , 1985) 또는 지상에서 발견되는 여러 기하학적 무늬 (Krantz et al, 1988) 의 이해뿐만 아니라 생명체의 구성 (Prig o g ine and Ste n g e rs, 1984) 과 같은 현상의 원인으로 생각되고있다. 소산 구조는 비가역 과정에서 자기 구성 (Se lf -or g an i za ti on) 된다. 이 구성 과정에서 요동의 역할이 중요한 것으로 생각되고 있다. 자기 구성과 비평형 상전이를 대상으로 최근에 활발한 학제적 연구들이 진
행되고 있고 그 중 하나는 시너제틱 스 (S y ner g e ti cs) 라고도 불린다. 저지는 평형에서 멀리 떨어진 영역에 대해 열역학이 무엇을 말하고. 있는지 개관하는 것 은 충분히 가치있고 또한 홍미있는 일이라고 생각 한다. 더욱이 유체 역학, 반응 속도론 등 여러 분야에서 논의되고 있 는 비평형 현상 들 특히 근래에 여러 분야에서 관심을 보이고 있는 소 산구조와 안정성에 관한 논의들을 열역학의 틀에서 정리하고 이들 방 법 들을 비교 검 토하는 것은 의미있는 일이라고 생각한다. 이렇게 생각하면 비평형 열역학은 공학 또는 과학의 고급 과정에서 한번쯤 개관할 필요가 있는 주요 기초 분야의 하나로 생각된다. 그러 나 현재 저자가 알고 있는 책들은 선형 영역만을 다루고 있거나 또는 줄거리의 이해에 는 꼭 필요하지 않은 것으로 생각되는 많은 논의들을 포함하는 등 이러한 목적에는 적합하지 못하다. 1981 년에 발간된 크 로이저가 쓴 『 비평형 열역학과 통계역학적 근거 』 의 비평형 열역학 부 분이 이러한 목적에 접근하지만 통계 역학 부분에 역점을 둔 책이고 비가역 열역학 부분은 잘 쓰여져 있지 못하였다. 이 책을 대학원 과정 의 교재로 사용해 보았지만 만족스럽지 못하였다. 이 책을 쓴 목적은 평형 근처와 평형에서 멀리 떨어전 영역에 적용되는 열역학을 세부에 너무 신경을 쓰지 않고 함께 개관하며 기본 원리를 이해하는 데 도움 울 줄 수 있도록 하기 위한 것이다. 기본 원리가 최근에 변한 것은 없 고 근본적으로 새로운 원리가 발견된 것도 없으므로 이 책의 많은 부 분은 잘 알려진 책들 특히 핏츠 (Fit ts, 1962) , 하세 (Haase, 1969) , 글 란人두 근 立와 프리고진 (Glansdorf and Prig o g ine , 1971), 그리고 크로 이저 (Kreuzer, 1981) 의 책에 근거하였으며 이 책들에서 인용되는 경우 에 꼭 필요하다고 생각되지 않으면 원 문헌을 밝히고자 노력하지 않았 다. 평형에서 멀리 떨어진 영역의 논의는 프리고전과 글란人두근立의 책을 주로 참조하였으며 그 이후의 발전에 관한 문헌들이 검토되어 있 다. 가능한 한 주요한 유도 단계를 포함시키고자 노력하였으며 또한 부분적으로 유도 과정이나 결과가 원 문헌과 일치하지 않는 것들이 있 고 새로 계산해서 삽입한 그림들이 포함되어 있다.
저자가 비가역 열역학에 관심을 갖기 시작한 것은 대학을 졸업하고 재대 후 원자력연구소에 근무하던 시절에 고 깅~-기 박사가 이 분야에 관심을 유도하던 20 년이 넘는 옛날로 돌아간다. 이 인연 때문에 대학 원에서 열역학과 응용통계역학 관련의 연구를 한 것이 아닌가 생각되 기도 한다. 그리고 유학해서 대학원 공부를 할 때 강의 내용에 비가역 열역학이 포함되어 접할 기회가 있었다. 비가역 열역학에 대한 저자의 본격적인 관심은 1982 년 대우재단의 〈 불우부전한 〉 분야에 대한 연구 지원으로 고 강웅기 박사를 비롯한 여러 공학 분야의 사람들이 비가역 열역학 연구회를 구성하고 같이 토론하기 시작할 때부터이다. 그러나 저자는 이러한 책을 쓰기에 적합한 배경을 가지고 있다고 주장할 근거 가 없다. 순수과학을 하는 분들이 많은 관심을 갖 는 분야도 아니고 〈첨단기술 〉 의 개발에 바쁜- 공학 연구인들이 저술을 할 만큼 홍미있는 분야도 아니기 때문에 어떻게 하다가 저자가 이 일을 하게 된 것뿐이 다. 그리고 사실을 말하면 긴 저술 과정에서 이러한 책을 쓰기에는 능 력이 부족하다는 것을 실감한 적이 한두 번이 아니다. 그렇다고 계속 붙잡고 있을 수도 없고 포기할 수도 없으므로 어느 정도 만족스러운 선에서 일단 끝내기로 하였다. 집필 예정 기간을 많이 초과해도 참고 집필을 지원해 주신 대우재단 에 감사드리고 또한 집필을 강하게 권유하고 추천하여 주신 김용준· 교 수께 감사드린다. 유체 역학계의 안정성 논의에 도움을 주신 최창균 교수에게도 감사드린다. 1993 년 2 월 이철수
비가역 열역학
차례 책 머리에 5 사용기호 12 제1장 서론 ―― 17 1 서론 17 2 열역학의 기본 법칙들 19 3 비가역 열역학의 역사적 발전 22 4 엔트로피 24 5 국소 평형 28 6 열역학의 기본 방정식 32 7 정리 38 제2장 수지식 ―― 39 1 서론 39 2 표기법과 일반적 수지식 40 3 물질 및 운동량 수지식 43 4 에너지 수지식 47 5 엔트로피 수지식 50 6 다른 수지식들 52 7 정리 53 제3장 선형 열역학 ―― 55 1 서론 55 2 흐름의 플럭스와 힘 56 3 큐리의 정리 594 온사거의 상호관계 60
5 변환 성질 63 6 정리 71 제4장 선형 열역학의 응용 ―― 73 1 서론 73 2 화학반응 75 3 다성분 등온 동압계내의 확산 80 4 다성분 등온계내의 침강과 확산 86 5 열확산 89 6 열전 효과 93 7 정리 95 제5장 진화와 안정성 ―― 97 1 서론 97 2 안정성 이론 100 3 평형 상태의 안정성 103 4 비평형 열역학 계의 안정성 107 5 일반적 진화의 법칙과 안정성의 판정 기준 111 6 동역학적 안정성 이론 114 7 정규 모드에 근거한 열역학적 방법 115 8 국소 퍼텐셜 119 9 정리 122 제6장 화학반응의 안정성과 시간적 질서 ―― 125 1 반응 속도와 안정성 125 2 로트카-볼테라 모델 127 3 화학 진동과 극한 싸이클 134 4 로트카-볼테라 모델과 극한 싸이클 142 5 벨루소프-자보틴스키 반응과 오레고네이터 반응 기구 143 6 정리 146제7장 화학반응의 다중 정상 상태 및
공간적 질서 ―― 147 1 서론 147 2 비평형 상전이와 다중 정상 상태의 화학적 모델 148 3 대칭성 파괴의 불안정성 158 4 대칭성 파괴 불안정성의 열역학적 검토 161 5 공간적 소산 구조 164 6 정리 166 제8장 베나드 대류 ―― 167 1 서론 167 2 선형화된 과잉 수지식 171 3 선형 이론의 정규 모드 해석 173 4 수력학계의 열역학적 안정성 이론 178 5 안정성 교환 원리의 열역학적 검토 182 6 소산 구조와 비평형 안정성 이론 184 7 정리 188 제9장 층류의 안정성과 국소 퍼텐셜 ―― 189 1 서론 189 2 일반화된 국소 퍼텐셜 191 3 등온 충류의 안정성 199 4 수직 온도 구배를 가진 층류의 안정성 202 5 수치 해석 206 6 검토와 정리 211 참고문헌 213 찾아보기 219사용기호 A 총헬름홀츠자유에너지 A1 i번째 반응의 화학 친화력 G, 총정부피열용량 Q 총정압열용량 Dij 질량 평균 속도에 대한 확산계수 Du' 용매의 속도를 기준으로- 한 확산계수 Dij 부피 평균 속도에 대한 확산계수 F 파라데이 상수 G 총깁스자유에너지 H 총엔탈피 J 화학반응속도 J1 i번째 반응의 반응속도 Llj 선형 계수 M1 성분 i의 분자량 N 총입지수 P 총엔트로피의 생성 속도 p 압력 Pr 프란틀수 R 기체 상수 Ra 레일리 수 s 총엔트로피 T 절대온도 u 총내부에너지 V 총부피
v + 특성 속력 Z1 =z1F/ M 1 a 무차원파수 aI i번째 반웅의 선형 반응 속도식의 속도 상수 Cv 정부피 비열 dcS 총엔트로피 흐름의 미분 d1S 총엔트로피 생성의 미분 kB 볼츠만상수 m 입자의 질량 mI 성분 i의 질량 q 계에 전달된 열 qrc v 가역과정에서 계에 전달된 열 s 단위 질량 당의 엔트로피 S1 성분 i의 소레이 계수 t1 성분 i의 침강 계수 u 단위질량 당의 내부 에너지 V 속력 VI 성분 i의 부분질량부피 Vz z 방향의 속도 성분 w 정규모드의 고유치 Wad 단열과정에서 계에 전달된 일 WI 고유치의 허수부분 W1 성분 i의 질량분율 Wr 고유치의 실수부분 Wrev 가역과정에서 계에 전달된 일 Wz z 방향의 와류도 성분 Zl 이온 i의 전하수 2 총엔트로피의 흐름속도 。 리아푸노프 함수, 동역학 퍼텐셜 함수 1 국소퍼텐셜
J 백터 성 분 이 Y1 인 플럭스 벡터 w 오 H수 도 D 변형 속도 텐서 I 단위 텐서 L 선형 법칙의 계수 행렬 P 압력 텐서 pd =P - p l 상첨자 * 공액 정규모드- 하첨자 C 임계접의 성질 N 성분의 수 。 기준상태
제 1 장 서론 I 서론 열역학은 거시적이고 현상적인 변화의 법칙을 탐구하는 과학의 한 분야이다. 거시적이란 분자나 소립자가 아닌 많은 분자로 이루어진 거 시적인 계를 대상으로 한다는 것을 의미하고 현상적이란 법칙들이 근 본 원리에서 유도된 것이 아닌 경험적이라는 것을 의미한다. 거시적 현상의 원인은 미시적 현상에서 설명될 수 있어야 하고 이러한 설명은 통계 역학의 영역에 속한다. 통계 역학은 열역학이 제시하는 개념들을 분자의 성질들과 관련시키고 있고, 거시적 계의 성질들을 분자들의 성 질로부터 계산하는 데 부분적으로 성공하고 있다. 열역학에서 대상으로 하는 변화를 두 가지로 나누어 생각하면 편리 하다. 하나는 무한히 느리게 일어나는 변화이고 다른 하나는 유한한 속도로 일어나는 변화이다. 무한히 느린 변화는 현상계에서 일어날 수 있는 변화를 이상화한 것이고, 이러한 변화 과정에서 계는 거의 평형 상태를 유지할 수 있다고 생각한다. 우리가 열역학이라 부르는 평형
열역학에서는 이러한 변화 과정이 취급된다. 평형 열역학의 이러한 특 성 때문에 평형 열역학에서는 내부 에너지의 변화가 관심의 주 대상이 되며 시간은 변수에서 제의된다. 반면에 유한한 속도로 변화하는 계는 평형에서 떨어져 있고 따라서 평형을 거의 유지하는 변화 과정이라고는 생각할 수 없다. 이러한 계 에는 농도, 온도 또는 속도의 구배가 존재하여 계가 균질성을 유지하 지 않고 있어서 안정한 상태로 변화하려고 하거나 또는 조성이 평형 조성에서 떨어져 있어서 화학반응이 일어난다. 유한한 속도 로 변화하 는 계 중에는 겉보기에 시간에 따르는 변화가 없는 것처럼 보이는 정 상 상태 (Ste a dy S t a t e) 에 있는 계도 있다. 정상 상태는 평형 상태오片근 다르게 계내에서 화학 반응이 진행되거나 계의 경계면을 통해서 물질 또는 에너지가 출입하고 있으며 계의 균질성이 보장되지 않는다. 이러 한 계와 관련된 여러 문제는 비평형 열역학의 취급 대상에 포함된다. 비평형 열역학은 비가역 열역학이라 불리기도 한다. 평형 열역학에서와 같이 비가역 열역학에서도 대상을 계와 주위 (Env i ronmen t)로 나누어 생각한다. 계가 주위와 열을 교환하면 열적 (Thermal) 접촉 그리고 일울 교환하면 기계적 (Mechanic a l) 접촉을 한다고 말한다. 열적 접촉이 있으면 전열(Di a t hermal) 계이고 없으면 단열 (Ad i aba tic)계이다. 계가 주위와 물질울 교환하면 열린 (O p en) 계 이고 물질울 교환하지 않으면 닫힌 (Closed) 계라고 말한다. 열적 또는 기계적 접촉이 없는 닫힌 계는 고립계라 불린다. 평형 열역학에서는 계가 구성 화학 성분들의 양에 추가하여 두 개의 독립변수로 정의될 수 있다는 것이 경험적으로 알려져 있다. 그러나 비가역 현상은 내부 이완 작용을 포함한다. 따라서 비평형 열역학에서 는 비균일계도 취급하게 되며 변화 과정을 기술하기 위해서 시간과 위 치 에 따라서 변화하는 장변수 (Fie l d Varia b le) 의 도입 이 필요하다. 우 리에게 익숙한 열역학 변수들은 이제 일반적으로- 위치와 시간의 변수 가 되어야 한다. 그러나 열역학 변수들은 많은 분자들의 성질을 표현 하고 있는 것이고 위치를 표시하는 수학적인 점의 성질로 정의되는 것
은 아니다. 열역학 변수가 장변수가 되기 위한 조건은 국소 평형 (Local E q u i l i br i um) 의 조건으로 알려져 있다. 이에 관해서는 4 절에서 다시 검토하기로한다. 거시적 변화는 변화를 제한하는- 두 종류의 법칙의 지배를 받는다. 하나는 보존의 법칙이고 다른 하나는 진화의 법칙이다. 전화를 인정하 는 것은 비가역성을 인정하는 것과 같다. 비가역성은 뒤에 다시 논의 되겠지만 여기에서는 간단히 시간의 일방성으로 생각할 수 있다. 비가 역 과정에서는 시간이 증가하는 방향의 변화는- 시간을 거슬러 과거로 전행할 때 생각할 수 있는 변화와 명확히 구별된다. 나이를 먹으면서 늙어가는 것은 허용되지만 젊어질 수는 없다. 뉴턴의 운동방정식에서 와 같이 미시적인 법칙에는 비가역성이 존재하지 않는데 어떻게 거시 적인 계에서 비가역성이 가능한가 하는 것은 통계 역학의 문제의 하나 이고 프리고전의 책 (Prig o g ine , 1983) 에서 이 문제를 상세히 검토하고 있다. 평형 열역학의 제일법칙인 보존의 법칙은 내부 에너지에 한정되지만 비가역 열역학에서는 총에너지와 운동량 등에까지 확장될 수 있다. 그 리고 평형 열역학의 제이법칙인 전화의 법칙은 단열된 닫힌계에 대한 것이지만 비평형 계에서도 성립한다. 그러나 비가역 열역학에서 관심 울 갖게 되는 다양한 경계 조건은 많은 경우에 평형 열역학의 경계 조 건과 다르기 때문에 적합한 진화의 법칙을 찾는 것은 중요한 문제의 하나이다. 다음 절에서 평형 열역학의 보존 법칙과 진화 법칙을 간단 히 살펴본다. 2 열역학의 기본 법칙들 에너지 보존의 법칙은 평형 열역학이나 비평형 열역학의 기초가 되 는 법칙의 하나이다. 그러나 평형 열역학에서는 퍼텐셜 에너지나 운동 에너지를 무시하고 내부 에너지에 주로 관심을 갖는다. 단열 과정에서
계가 얻은 미분 일 dwa o.? :- 계의 내부 에너지의 미분 변화 dU 와 같다 고 생각하여 내부 에너지를 정의하고 도입한다. dU = dwad (1. 1) 다음에 일과 열을 주위와 교환할 수 있는 계에서 같은 내부 에너지 의 변화를 수반하는 변화에 대하여 다음과 갇이 열의 개념을 도입한 다. dU = dw+dq (1. 2) 이 식은 열역학 제일법칙으로 알려진 에너지의 보존 법칙이다. 이 식에서 dw 와 d
한다. 에너지가 보존되는 여러 변화 중에서 제이법칙에 따르는 변화만 이 허용된다. 제이종 영구 기관은 바로 허용되지 않는 에너지의 이동 에 근거한 것이고 따라서 실제로는 불가능·하디는· 것이 경험적으로 알 려져 있다. 클라우시우스는 단열된 닫힌계의 특수한 경우인 고립계에 대해 〈 (고립계인) 우주의 엔트로피는 항상 증가한다 〉 고 선언하였다. 이러한 진화의 법칙은 안정성에 관한 논의를 내장하고 있다는 것에 유의할 필요가 있다. 죽 단열된 닫힌계에서 엔트로피가 더 이상 증가 할 수 없으면 계는 더 이상 변화하지 않는다는 것은 이렇게 도달한 계 가 요동에 대해 안정하다는 것을 의미한다. 열역학의 제일법칙과 제이법칙을 함께 생각하면 변화 과정에서는 에 너지가 보존되며, 단열된 닫힌계에서는 엔트로피가 증가하는 방향으 로만 변화가 일어날 수 있다는 것을 의미하고 있다. 엔트로피가 더 이 상 증가할 수 없으면 계는 변화가 없는 평형 상태에 도달한다. 이러한 변화의 법칙은 단열된 닫힌계에 대한 일반적 전화의 법칙이고 평형 열 역학과 바평형 열역학에 같이 적용된다. 우리의 관심이 단열된 닫힌계에 한정된 것은 아니다. 계가 단열된 닫힌계가 아니라면 변화의 법칙은 어떻게 될 것인가? 보존 법칙들이 성립하지 않을 이유는 없다. 그러나 전화의 법칙인 제이법칙은 이제 단열된 닫힌계가 아니면 경계 조건에 변화에 따라 변화되어야 한다. 제이법칙이 처음에 고립계에 대해 선언되었지만 고립계가 아닌 다른 닫힌계들에 대한 진화의 법칙들도 우리는 알고 있다. 예를 들면 온도 와 압력이 일정한 닫힌계에서는 깁스 에너지가 최소가 되려는 방향으 로 계가 진화한다. 전화가 끝난 상태가 평형 상태이다. 이 경우는 계 의 균질성이 보장된다는 특징을 갖고 있고, 이 경우에 해당하는 진화 의 법칙은 제이법칙의 다론 표현에 지나지 않는다. 5 절에서 이들 다 른 표현식들을 르장드르 변환에 의해 체계적으로 도출할 수 있다는 것 울 알게 될 것이다. 또한 다른 닫힌계도 생각할 수 있다. 양면의 온도가 서로 다르게 일 정하게 유지되어 있는 평판을 생각하자. 이 경우에 깁스 에너지가 최
소가 된다는 전화의 법칙은 계의 온도가 일정하지 않기 때문에 도움을 주지 않는다. 또한 이러한 계의 진화 조건은 평형 열역학의 어떠한 함 수들을 써서도 표현할 수 없다. 그렇다면 계의 전화는 어떤 법칙의 지 배를 받을 것이며 전화가 끝나는 상태가 촌재한다면 이 상태의 안정성 은 어떻게 판별될 수 있을 것인가. 더욱이 열린계에 관해서는 무엇을 말할 수 있을 것인가. 제이법칙에 해당하는 전화의 법칙과 안정성의 문제를 비가역 현상에 대해 더 일반적으로 논의하는 것은 비가역 열역 학의 주요 과제의 하나이다. 3 비가역 열역학의 역사적 발전 역사적으로 비가역 열역학의 근원은 뉴턴의 점성 흐름의 법칙, 푸리 에의 열전도 법칙, 피크의 확산 법칙, 움의 전기 전도 법칙에서 찾을· 수 있다. 뉴턴의 법칙이 17 세기 후반에 발견된 것을 제의하고는 이들 법칙들은 19 세기 초반에서 중반에 걸쳐 발견되었다. 이들 법칙들에서 는 흐름(또는 변화)과 이 흐름을 일으키는 힘 사이에 선형 관계가 존 재한다. 따라서 이러한 법칙들은 2 장에서 취급되는 선형 현상적 법칙 들의 예가된다. 이후의 중요한 진전은 엔트로피의 변화 d 혀춘 생성 부분 d1SS 斗 흐름 부분 deS 로 구분한 것이며 이는 베르트란드 (Ber t rand, 1887) 에 의한 것으로생각되고있다. dS = d1S+deS (1. 4) 단열된 닫힌계에서는 엔트로피의 흐름이 없으므로 엔트로피의 생성 만이 엔트로피의 변화에 기여한다. 따라서 엔트로피의 생성은 비가역 과정과 관련되고 이 양은 비가역 과정에서는 항상 0 보다 크며 가역 과 정에서는 0 이 된다.
d1S~ O (1. 5) 이 식은 또한 제이법 칙 의 다른 표현으로 생각할 수 있다. 한편 열전 효과 (Thermoelectr i c Eff ec t, T homson, 1854) 같은 연계 된 이동 현상들이 발견되었다. 여기에서 연계된 이동 현상이란 예를 들면 온도차와 전위차가 있는 계에서 온도차는 열 흐름을 일으킬 뿐만 아니라 전류의 흐름을 일으키며 또한 전위차는 전류는 물론 열의 흐름 울 일으키는 것과 같은 현상을 의미한다. 온사거 (Onsag e r, 1931a, 19 3 1b) 는 평형 근처의 이들 연계된 이동 현상에 대해 잘 알려진 상호 관계 를 발전하였다. 그는 연계된 전달 현상의 선형 계수들 사이에 어 떤 대칭성 관계 를 발견하여 미시적 물리학과 열역학의 기본적 관계를 수립하였다. 온사거의 업적으로 비가역 열역학은 학문적 형태를 갖추 게 된 것으로생각된다. 여기까지의 발전은 선형 열역학의 영역이라 불리는 평형 근처에서의 비평형 거동을 대상으로 이루어졌으며 그 이후에는 평형에서 멀리 떨 어전 영역까지 바가역 열역학이 확장되었다. 영역의 문제는 전화의 법 칙 및 안정성과 깊은 관계를 갖는다. 열역학 제이법칙에 따르면 단열 된 닫힌계에서 전화의 방향은 엔트로피가 증가하는 방향이고 전화가 끝난 평형 상태는 요동에 대해 안정하다. 고립계에 대한 이 법칙은 영 역과 무관하게 유효하지만 경계 조건이 변화하면 이 법칙이 적용~ 수 없다. 선형 열역학 영역의 정상 상태가 한 예인데 이 상태를 나타낼 수 있는 계는 분명히 단열된 닫힌계가 될 수 없으므로 엔트로피로 표 시되는 전화의 판정 기준이 적용될 수 없을 뿐만 아니라 엔트로피가 계속해서 생성되므로 엔트로피의 증가가 정지되는 평형 상태까지의 전 화가 허용되지도 않는다. 이러한 계는 엔트로피의 생성 속도가 감소하 는 방향으로 전화하고 엔트로피의 생성이 최소가 되는 정상 상태에 도 달한다. 이 상태에서 계가 안정하다는 것을 뒤에 보이게 될 것이다. 정상 상태에서는 평형 상태의 안정성 논의에서 엔트로피가 사용된 것 과 비슷하게 엔트로피의 생성 속도가 이용되었다는 것에 유의하자.
평형에서 멀리 떨어전 계의 거동은 더욱 복잡해진다. 이러한 계에서 는 앞에서 언급한 엔트로피의 생성 속도와 관련된 전화의 법칙도 다시 생각할 필요가 있다. 더 일반화된 진화의 법칙을 말할 수는 있지만 실 제적인 응용에는 큰 제한이 따른다는 것을 알게 될 것이다. 평형 상태 의 엔트로피 또는 선형 열역학의 엔트로피 생성 속도와 같이 전화를 규정하는 일반적인 함수가 평형에서 멀리 떨어진 영역에서는 발견되지 않는다. 또한 이 영역에서는 소산 구조 (D i ss ip a ti ve S t ruc t ure) 라 불리는 비 평형 구조가 생성될 수 있고 이 구조가 불안정해지면 비평형 상전이에 의해 다른 구조로 전이될 수 있다. 이 상전이는 평형 상전이와는 달리 두갈래치기 (B ifu rca ti on) 의 특성을 갖는다. 이 영역에서의 열역학적 진화의 법칙과 안정성의 연구에는 프리고전 등의 브러셀 학파가 크게 기여하였다. 그리고 이러한 현상은 생물학과 사회과학의 영역에까지 응용이 시도되고있다. 4 엔트로피 엔트로피의 변화는 계가 가역적으로 받은 열량 Gre/ 4 온도 T 의 함 수로 위에서 (1. 3) 식으로 정의되었다. 5 장에서 안정성의 검토와 관련 되어 언급되는 바와 같이 자연계에서 허용되는 변화에 대한 리아푸노 프 함수와 관계가 있는 엔트로피라는 함수는 유도되었다기보다는 〈발 견〉된 것이다. 여기에서 자연계에서 허용되는 변화의 예는 열이 온도 가 높은 곳에서 낮은 곳으로 흐른다든지 또는 열을 전부 일로 전환시 킬 수는 없다는 것과 같은 경험에 근거한 현싱들이다. 엔트로피의 증 가는 무질서도의 증가로 이해되기도 하는데 계가 열을 받아 온도가 높 아지면 구성 분자들의 무질서도가 증가한다. 이러한 엔트로피의 증가 가 무질서도의 증가를 의미한다는 것은 통계 역학에 의해서도 분명해 진다.
가역 과정은 주위에 이차 항 이상의 작은 변화만을 남기고 원래의 상태로 복원될 수 있는 과정이라고 정의될 수 있다 (Mode l! and Reid , 1983). 이 조건은 주위와 계가 거의 같은 상태에 있을 것을 요구한다. 일에 대해서는 계의 압력을 P 라 할 때에 주위의 압력이 P+oP 이면 계는 수축하고 P ― oP 이면 계는 팽창한다. 따라서 팽창하고 있는 계 를 반전시키기 위해서는 이차항 oPoV 만큼 주위가 계에 일을 해주어 야 한다. 열전달 과정에서는 계의 온도를 T 라 할 때 주위의 온도가 T+oT 이면 주위에서 계로 열이 전달되고 T ― oT 이면 계에서 주위로 열이 흐른다. 계가 열을 주위로 전달하고 있는 과정을 반전시키기 위 해서는 이차항 oTos 만큼만 주위에서 계로 추가적인 열을 공급-하면 된다. 가역 과정에서는 계가 평형 상태를 거의 유지하면서 변화한다. 엔트로피의 변화는 엔트로피의 흐름에 의존하며 가역 과정에서는 엔트 로피가 생성되지 않으므로 (1. 3) 식의 엔트로피 변화는 (1. 4) 식의 엔트 로피 흐름에 해당한다. 그리고 가역 과정은 엔트로피가 생성되지 않는 과정이라고 말할 수 있다. 가역 과정에 대해 정의된 엔트로피가 비가역 변화의 척도가 될 수 있다는 것은 홍미로운 것이다. (1. 3) 식으로 정의된 엔트로피는 엔트 로피의 흐름을 표시하고 있다. 그러면 엔트로피의 생성은 어떻게 가능 한가 또는 어떻게 정의될 수 있는가하는 문제가 대두된다. 결론부터 말하면 계내에 엔트로피의 흐름이 있는 계는 전체로서는 엔트로피를 생성할 수 있다는 것이다. 특수한 경우로 닫힌 단열계를 생각하면 계 내에서 엔트로피의 흐름이 존재하면 이 계는 전체적으로는 엔트로피를 생성한다. 다시 말하면 전체 계의 엔트로피 생성은 국소적인 엔트로피 의 흐름을수반한다. 이룰 이해하기 위해 다음과 같은 변화 과정을 생각해 본다. 초기 온 도가 서로 다르고 동일하고 온도에 의존하지 않는 열용량 C p를 갖는 두 부분계로 구성된 단열된 닫힌계를 생각하자. 이 부분계들이 열적 접촉을 통해 평형에 도달한다고 하면 이 과정에 대한 계의 엔트로피의 변화는 (1. 3) 식을 전체계에 적용해서는 구할 수가 없다. 이 경우에는
계가 받은 열도 없고 또한 초기 상태가 평형 상태가 아니므로 변화 과 정이 가역적일 수가 없기 때문이다. 그러나 이 변화 과정에서 각 부분 계는 초기 상태와 최종 상태가 평형 상태이므로 가역적 변화과정을 통 해 이 최종 상태에 도달할 수 있고 (1. 3 ) 식에 의해 엔트로피의 변화가 계산된다. 초기에 비평형인 상태가 평형 상태로 진화하는· 과정의 엔트 로피 변화가 (1. 4) 식의 엔트로피 생성에 해당한다. 반면에 (1.3) 식으 로 계산될 수 있는 두 평형 상태의 엔트로피 차이는 (1 .4) 식의 엔트로 피의 흐름에 해당한다. 엔트로피의 생성을 계산하기 위해 (1. 3) 식을 계에 직접 적용할 수는 없지만 이 식을 부분계 (Subsy st e m ) 각각에 적용하는 것은 허용된다. 각각의 부분계에 대해 한 평형 상태와 다론 평형 상태의 엔트로피의 차를 생각해 보자. 부분계는 평형 상태를 유지하고 있으므로- 압력이 일정하게 유지되면 dq re v= C p dT 가 된다. 따라서 다음 식이 성립한 다. b..S = J (Cµ/ T ) dT (1. 6) 두 부분계의 초기 온도를 T1, 따라 하고 T1 > T 2 라 하자.두 부분계 를 의부와 절연시킨 조건에서 열적 접촉을 시키면 최종 온도 (T1+T2 ) /2 에 도달한다. (1. 6) 식에 의해 부분계 l 의 엔트로피 변화는 다음과 같이 된다. !:::.S1 = Cp ln (T1+T2)/2T1 부분계 2 의 엔트로피 변화는 우변 분모의 Tl 대신 T2 를 쓴 다음 식으로표시할수있고 !:::.S2 = Cp ln (T1 + T2) /2T2 따라서 총 엔트로피 변화는 다음과 같다. !:::.S = ZCP ln (T1 + T2) /Z (T1T2) 0·5 > 0
계 전체로 보면 열의 출입이 없으므로 이 엔트로피 변화는 엔트로피 의 생성에 해당한다. 이 과정은 분명히 자발적이고 비가역적인 과정이 며 엔트로피의 증가가 수반되었다 . 전체계를 구성하는 각 부분계에서 일어나는 변화가 가역적인데 전체적으로는 비가역적이므로 비가역성 은 접촉하고 있는 계면에 있다고밖에는 생각할 수 없다. 이것은 전체 적으로는 비가역적인 과정의 엔트로피 변화를 가역 경로를 따라 계산 하기 때문에 발생한 것이지만 다음에 보이는 바와 같이 실제로 전체 계의 앤트로피 변화를 반영하고 있다. 같은 문제를 조금 더 실제에 가깝게 생가해 보자. 부분계 1 과 2 가 각각 균일한 온도를 유지하면서 열이 전달된다고 생각하는 것보다 각 부분계 를 다시 각각 2 개로 나누고 이렇게 나누어진 부분계를 11, 12, 21, 22 라 하자. 그리고 각 부분계내의 온도 분포가 균일하다고 생각 해 보자. 각 부분계의 초기 온도는 위에서와 같고 최종적으로 도달한 평형 온도도 동일하다. 그러면 각 부분계의 엔트로피 변화의 총합은 디음과 같이 표시할 수 있다. t::,,.S = (Cp / 2) fnl Tl+T Z >l 2 ( dTu/ T 11 +dT1z /T 12+dT21/T21 +dT2z/ T2 2) = 2Cp ln (T1 + T2 ) / 2 (T1T2) 0·5 이 결고性근 예상할 수 있는 것과 같이 위에서 두 부분계로 구성된 계에 대해 계산된 것과 동일하다. 그러나 이제는 앞에서와 다르게 제일 단 계에서는 초기의 계면에 집한 두 부분계 12 와 21 이 열적 접촉에 의해 먼저 평형에 도달하고 다음 단계에서 모든 부분계가 열적 접촉을 해서 열이 11 에서 12 와 21 을 통해 2 2i료 전달된다고 생각하자. 그리고 제이 단계에서 부분계 12 과 21 의 상태는 변화하지 않는다고 생각한다. 그 러면 제일 단계와 제이 단계에서 생성된 엔트로피는 각각 t::,,. S/2 이고 계의 총 엔트로피 변화는 A 없근 위에서와 같다. 그러나 두 부분계만울 생각할 때는 모든 엔트로피가 하나의 계면에서 생성되었다고 생각해야 하지만 이제는 같은 엔트로피가 세 계면에서 나누어 생성되었다. 이렇게 부분계를 계속 분할해서 부분계의 수가 아주 큰 값을 가질
때에는 엔트로피가 비가역 현상이 일어니~ 전영역에서 생성되지만 생 성된 총 엔트로피의 값은 일정하게 된다는 것을 알 수 있다. 또한 엔 트로피의 생성은 유한한 계면에 한정된 것이 아니고 비가역 과정아 진 행되는 전체 계에 걸치고 있음을 알 수 있다. 그리고 분할된 계는 국 소 평형 상태에 있다고 간주된다. 위의 예에서는 균일하지 않은 계가 균일한 평형 상태로 변화하는 과 정의 엔트로피 생성을 임의의 부피 요스커 1 대한 엔트로피의 흐름에서 계산할 수 있었다. 2 장에서는 이러한 엔트로피의 생성이 계내에 존재 하는 온도, 농도, 속도 등의 구배의 내부 이완 현상 (Relaxa ti on) 과 관계가 있음을 알게 될 것이다. 그러나 한 평형 상태의 엔트로피와 이 상태가 도달할 수 있는 다른 평형 상태의 엔트로피의 차는 임의의 가 역 과정에 대해 계산될 수 있다. 이 값은 엔트로피의 흐름을 나타내고 있으므로 이 값으로부터 자발적인 변화의 방향을 판정할 수는 없다• 또한 두 개의 서로 다르고 고립되지 않은 비평형 상태에 대해서 엔 트로피의 차를 계산할 수 있다고 하더라도, 이 값이 자발적 변화의 방 향울 판정할 근거가 될 수는 없다. 생명체는 고도로 조직되어 있어 낮 은 엔트로피의 상태로 볼 수 있지만 계속 엔트로피를 생성하고 있는 비평형 상태에 있고 의부로부터 적합한 물질이나 에너지의 공급이 계 속되는 한 이 상태를 유지할 수 있다• 이 경우에 엔트로피가 낮은 생 명체는 분명히 엔트로피가 더 높은 상태의 구성 성분들로부터 생성된 것이다. 생명체가 수명을 다한 후에 구성 성분들로 분해되는 것은 자 연 발생적 변화이지만 또한 구성 성분들로부터 생명체가 생성될 수 있 는데 분명히 이러한 현상은 가능하다. 5 국소 평형 비가역 열역학이 장이론이리는 것과 장변수가 정의될 수 있기 위해 서는 국소 평형의 조건이 성립해야 한다는 것을 앞에서 언급하였다.
이에 앞서 평형 열역학에서 대상으로 하는 가역 변화를 먼저 생각해 보자. 가역 과정은 앞절에서 논의한 바와 같이 평형 상태를 거의 유지 하면서 일어나는 변화물 의미하고 있다. 이에 필요한 조건은 계의 요 동에 비하여 계에 존재히는 비균질성이 충분히 작아야 하고 또한 변화 가 무한히 조금씩 그리고 무한히 천천히 일어나야 한다는 것이다. 계 에 항상 존재하는 요동이야말로 보편적인 가역 현상이므로 이를 기준 으로 가역성을 검토하는 것은 자연스러운 일이다. 국소 평형의 가정은 거시적 길이 척도에 비해 무시될 만큼 작은 부 피 요소를 생각하고 이 부피 요소에서 일어나는 변화를 가역 과정으로 볼 수 있다는 것을 의미한다. 따라서 국소 평형의 조건은 이 작은 부 피 요소에서 일어나는 요동을 기준으로 허용되는 계의 비균질성과 변 화의 속도를 제시한다. 여기에서 생각하는 작은 부피 요소는 열역학적 으로 의미를 가질 만큼 충분히 커야 한다. 통계 역학에 의하면 이 조 건이 구체적으로 표시될 수 있고, 크로이저 (Kreuzer, 1981) 의 책에 검 토되어 있다. 국소 평형의 가정을 검토하는 것은 원칙적으로 비평형 통계역학의 문제이고 여기에서는 유도 결과를 간단히 정리하여 검토하 기로 한다. 이들 조건의 유도에 관해서는 예를 들면 티엔과 린하드 (Tie n and Lie n hard, 1979) 의 책을 참조할 수 있다. 국소 평형 상태의 부피 요소는 정의에 의해서 열린계이다. 열린계가 열역학적으로 의미를 갖기 위해서는 분배함수 (Par titi on Func ti on) 가 정의될 수 있어야 하고 입자수의 상대 요동이 1 보다 아주 작아야 한 다. 입자수 N 의 상대 요동의 크기는 다음 식으로 표시되며, oN/N = (kaTxT/V) 1'2 (1. 7) 여기에서 k 긁큰 볼츠만 상수, XT = —(8 V/8 p )T/V 로 등온 압축 계수 를 의미한다. 입자수 밀도를 N/V 라 하고 작은 부피 요소의 특성 길 이를 r 이라 하면 이 부피 요소내의 입자수 Nr 은 다음과 같으므로 Nr = (N/V)r3 (1. 8)
(oN / N) ~ l 의 조건에서 특성 길이의 개략적 크기는 밀도의 함수로 구해진다. 이제 이 부피 요소에 대해서 임의의 열역학적 특성 A 의 요 동 oA 를 통계 역학적 방법에 의해서 계산한다. A 는 다음 조건을 만 족해야한다. oA/ A ~ I (1. 9) 그리고 의부적으로 제어되는 경계조건에 의해 계내에 A 의 구배 gra d A 가 결정된다면 허용되는 최대 구배는 다음 조건을 만족해야 한다. r (gra d A) /A = !:!,.A/A < oA/ A ( 1.1 0) 이 식은 좌변에 표시된 부피 요소내의 구배에 의한 차이는 우변에 표시된 요동의 한계내에 있어야 한다는 것을 의미한다. 온도와 압력에 대한 상대 요동 크기의 통계역학적 유도 결과는 다음과 같다 . 8T/T = (kB/mcv) Il2 1',1 ·'1 11`/` ’1 2 8p /p = (ksTcp/ Vp 2C vXr) 112 ,'' , · · \.,' 여기에서 Ci r2f Cv 는 각각 단위 질량 당의 정압비열과 정부피비열이 고 m 은계의 질량이다. 기체에 대해서는 이상 기체를 가정하고 특성 길이로 평균 자유 행정 울 택할 수 있다. 액체에 대해서는 평균 자유 행정을 택히는 것이 의 미가 없으므로_ oN/N 을 .01 과 같은 1 보다 작은 값으로 가정하고 작 은 부피 요소의 특성 길이를 계산할 수 있다. 이러한 해석에 의하면 밀도가 아주 낮아지면서 특성 길이가 아주 길어지고 국소 평형의 가정 아 성립하지 않게 됨을 알 수 있다. 평균지유행정 A 눈· 기체 분자운동 론에 의한 다음 식으로 쉽게 계산될 수 있다. Ar = V/ (2°·57rN( J2 ) (1. 13) 여기에서 6는 분자의 직경이다. 실온과 대기압에서 이 식에 의한
알곤의 평균자유행정은 10-5 c m 정도아다. 그리고 평균자유행정을 한 변으로 하는 정육면체 부피 요소내의 분자수는 2. 7Xl04 개이다. 평균 자유행정을 기준으로 한 부피를 이용하면 (1. 7) 식에 의해 oN/ N = 6 x10 - 3 을 얻는다. 이 값은 1 에 비해 충분히 작으므로 부피 요소의 길 이 척도로 평균자유행정을 택할 수 있다. 특성 길이가 거시적 길이 척도보다 충분히 작아 국소 평형이 성립하 떤 디음 문제는 (1. 10) 식에 의해 허용되는 최대 구배를 계산하는 것이 다 . 이제 (1 .11) 식과 (1 . 1 2 ) 식에서 T 와 p가 주어졌을 때에 oT 와 op 를 계산할 수 있고 이로부터 계에 허용되는 최대의 온도와 압력의 구 배 를 계산한다. lgr a d Tl = oT 1 1 0-s = 1. 4Xl05K/ cm lgr a d Pl = op / 1 0-s = 7 . 4Xl02bar/cm 이들 값들은 충분히 크기 때문에 우리가 관심을 갖는 대부분의 경우 에 국소 평형의 가정은 문제를 제기하지 않을 것으로 예상된다. 특성 시간으로 분지들의 충돌 사이의 시간을 택하면 이 값은 대부분 의 경우 거시적 시간 척도보다는 충분히 작으므로 국소 평형의 가정은 특수한 문제를 제기하지는 않는다. 기체 분자운동론에서 주어지는 다 음 식으로 충돌 사이의 시간 re 를 계산할 수 있다. re = (8ksT/ 7r ff i) 112/ II (1.14) 예를 들면 실온 대기압에서 알곤 분자들의 충돌 사이의 시간은 이 식으로부터 2.sx10-10 초 정도라는 것을 알 수 있다. 거시적 전화의 속도는 (1 . 10) 식과 비슷하게 다음 식의 제한울 받지만 특성 시간 (r) 울 충돌 사이의 시간보다 길게 하더라도 아 값이 아주 작기 때문에 별 문제를 제기하지 않는다. r (dA/dt) /A < oA/A (1.15) 원칙적으로 국소 평형이 타당한 가정이 될 수 있는가 하는 것은 우
리가 비가역 열역학을 적용하고자 할 때마다 검토되어야 하겠지만 밀 도가 아주 낮은 기체의 경우나 구배가 아주 큰 충격파와 같은 경우를 제의하고는 이 가정이 타당하다고 생각되고 있다. 국소 평형의 조건은 일차적으로 장변수들이 도입될 수 있는 조건을 제시하지만 이차적으로는 이들 장변수 사이에 비평형 상태에서도 평형 열역학의 기본 관계식들이 적용될 수 있다는 것을 의미한다. 5 장에서 논의되는 일반적 진화의 법칙은 이차적 의미의 국조 평형 조건은 필요 로하지 않는다. 6 열역학의 기본 방정식 제일법칙과 제이법칙의 결합 형식인 열역학의 기본 방정식은 (1.2) 식을 열린계로 확장하고 우변을 가역 경로를 택해서 표시하면 얻어진 다. dU = dWrev+dQ r ev+~µ1dm1 (1. 16 ) 여기에서 m 는 성분 i의 질량이고 µ1 = (aU/am1)s , v, m 논- 성분 i의 단위 질량 당의 화학 퍼텐셜을 의미한다. 이 도함수는 열역학에서 혼 히 쓰이는 몰 수에 관한 것이 아니고 질량에 관한 것임에 유의해야 한 다. µ는 다음과 같이 표시될 수도 있다. µ1 = (oG/am,)T, P, mJ (1.1 7) 이 정의식은 화학 퍼텐셜울 깁스 에너지의 부분몰 성질 (Parti al Molar Pro p e rty)이 아니고 부분 질량 성질 (Parti al Sp e ci fic Prop - e rty)로 나타내고 있다. 단위 질량 당의 화학 퍼텐셜은 질량 농도와 다음과 같은 관계를 갖는다. µ1 = µ10 + (RT/M1) ln (C1 r1/C10) = µ10 + (RT/M1) In ( Pi r1/M 요) (1.18)
여기에서 C 놉 성분 i의 몰농도이고 沿근 성분 i의 활동도 계수이다. 그리고 µ1 0 는 단위 농도 C1 0 인 이상 용액의 화학 퍼텐셜이다. 이상 용 액을 가정하면 활동도 계수는 1 이 된다. 일정한 온도와 압력에서 열역학적 시량 성질 F 는 다음과 같은 성질 울갖는다. F (kmi , km2 , … , kmn) = kF (mi , m2, … , m 깁 (1. 19 ) 이러한 성질을 갖는 함수를 일차 제차함수 (Homo g eneous Fune- ti on) 이라 부른다. 오일러 정리에 의하면 일차 제차함수는 다음 성질 을갖는다. F = ~ml ( aFI a m1h, P, mj = ~m1f 1 ( 1. 20) 이 식은 바로 시량 성질 F 와 부분질량 성질을 i의 관계를 표시한 다. 또는 F 의 단위 질량당의 값을 f라 하면 다음 관계식을 쓸 수 있 고, f= 2wIfl (1. 21) 여기에서 W 는 성분 i의 질량분율이다. 부분 질량 성질을 도입하는 이 유는 다음 장에서 검토되는 바와 같이 반응계에 대해서도 수지식에서 총 질량이 보존되는 성질을 이용하여 식들을 간편하게 표시하기 위한 것이다. 가역 경로에 대해서는 dWrev = ―p dV 이고 dQ r ev = TdS 이므로 (1. 16) 식은 다음과 같이 된다. dS = dU/T + (p/ T) dV —~ (µi/T ) dm1 (1. 22) 그리고 국소 평형의 조건이 만족될 때 열역학의 기본 방정식인 (1.22) 식은 국소 형식으로 다음과 같이 표시된다. ds = du/T + (p/ T) dv— ~ ( µ1/ T ) dw1 (1. 23)
비가역 과정에서는 이들 변수가 장변수가 되어 위치와 시간의 함수 가 되며 S, U, V 는 단위 질량에 대한 내부 에너지와 부피를 표시한다. 단위 부피에 대한 국소 형식의 표현도 가능하다. d (ps ) = d (pu ) /T— ~ (µ,/T) dp , 0 . 24) 이들 국소 형식으로 표시된 기본 방정식은 앞으로 중요한 역할을 한 다. 앞에서 평형 열역학은 내부 에너지의 변화가 중요한 변화의 현상적 법칙이라고 생각할 수 있디는· 것을 언급한 바 있다. 비가역 현상을 취 급할 때에는 기계적 에너지와 운동량도 고려할 필요가 있고 따라서 2 장에서 검토되는 바와 같이 속도도 장변수로 도입된다. (1. 4) 식에 따라 d~ 즌 일반적으로 d,~ de& 기 합이지만 (1. 22) 식의 우변은 4 절에서 논의한 것과 같이 de 없룹 표시한다. 변화 과정이 가역 경로를 따르는 변화만으로 구성될 수 있는 경우에는 계가 평형을 유지 한다. 따라서 (1. 22) 식이 성립한다. 그러나 가역경로를 띠를 수 없는 부분이 존재하면 이 부분에 대한 엔트로피의 생성 d1 없룹 (1. 22) 식의 양변에 더해 주어야 총 엔트로피의 미분 d Si룹 표시할 수 있다. 따라 서 엔트로피의 생성항을 포함해서 (1. 22) 식을 다시 쓰면 디음과 같다. dS =d,S+deS = d,S + dU/T + (p/ T) dV-~ (µ1/T) dm1 (1. 25) 이제 열역학 제아법칙은 d1S~O 이므로 (1 .25) 식으로부터 U, V, m 가 일정한 경우에는 다음과 같이 표시될 수 있다• (6.S )u , v, m~O (1. 26) 이 식에서 엔트로피 없근 U, V, m, 의 함수로 표시되었지만 U 를 S, V, m 려 함수로 표시할 수도 있다. 이때에는 (1. 25) 식으로부터 다음 식을얻는다. (6.U ) s, v,m~O (1. 27)
경계 조건이 다른 경우에 대한 제이법칙의 표현식들도 알려져 있다. 이러한 표현식들을 얻기 위해서는 다른 독립변수의 함수로 표시되는 열역학 함수들을 발견해야 한다. 엔탈피, 헬름홀츠 에너지, 그리고 깁스 에너지는 이 목적에 적합한 함수들이며 르장드르 변환 (Le g endre Trans fo rma ti on) 에 의해 엔트로피 또는 내부 에너지의 표현식으로부 터 얻어질 수 있다. 르장드르 변환은 기본 관계인 S(U, V, m) 을 이와 동등하지만 다른 독립 변수들을 갖는 함수로 변환한다. 르장드르 변환 의 열역학적 응용에 관해서는 예를 들면 모델과 리드 (Modell and Reid , 1983) 의 책을 참조할 수 있다. 함수 y(O )(X1, X2, …, Xn) 은 르장 드르 변환에 의해 함수 y(k )(g I, g2, … , Sk, XK+h XK+2, … , Xn) 으로 다 음식에 의해 변환된다. y
dG = -SdT+Vdp + ~µ,dm, (1. 34) (1. 25) 식을 얻은 것과 같은 방법에 의해 (1 . 32) 식을 다시 쓰면 다음 과같다. dS == dd,,SS ++d deHS /T —(V /T) dp -~ (µi/T ) dm, 0 . 35) 이 식으로부터 다음 결과를 얻는다. (!:::.S) H,P,m ~ 0 (1. 36) (!:::.H)s,P,m~O (1. 37) A 의 정의식 (1. 29) 로부터 정온에서 /J,. A= /J,. U ― T !J,. S 라 쓰고 (1. 25) 식을 이용하면 V, m 가 일정할 때에 다음 관계식을 얻을 수 있 다. (~A) r,v,m 회 0 (1. 38) 또한 정온에서 AG=AH ― T t:,. S 라 쓰고 (1. 25) 식울 이용하면 V, m 가 일정할 때에 다음 식을 얻는다. ( AG) T,P,m 칙 0 (1. 39) (1. 26) 식과 (1. 36) 식을 함께 생각할 수도 있다. 실제로 모델과 리드 (Modell and Reid , 1983) 는 단열된 닫힌계에 대해 다음 식이 성립하는 것을보이고있다. !1S 2 :0 (1. 40) 르장드르 변환의 특수한 경우의 하나는 (1. 28) 식에서 k = n+2 인 때 01 다. y(n +2) ( g1, & , … , Sn+2) = y
면 s1=T, s2= -p, ti= µ1 (i= 1, …, n) (1.42) 이다. 따라서 0 = U-TS+p V — 2µ ImI (1. 43) 이다. 이 식에서 U ― TS+ p V 는 정의에 의해 깁스 에너지 G 이고 G 는 (1 . 20) 식에 의해 ~µ1m 이므로 (1. 43) 식의 좌변은 0 이 된다. 그리 고 이 식의 미분과 (1. 34) 식에서 다음의 깁스곡국엠 (Gi bb s-Duhem) 식 울얻는다. ~m1dµ1 = -SdT+Vdp (1. 44) 이 식은또한다음과같이 쓸수도있다. ~W1dµ1 = —sd T+vdp (1.4 5) ~w1d(µ,/T) = pu d(l/T) +d(p/ T) (1.4 6) (1. 26) 식과 (1. 30) 식은 각각 내부 에너지, 부피 및 각 성분의 질량 이 일정한 계와 엔탈피, 압력 및 각 성분의 질량이 일정한 계에서 엔 트로피는 증가하는 방향으로만 변화하고 변화가 끝나면 엔트로피는 최 대가 된다는 것을 의미한다. (1.2 7), (1. 37)-( 1. 39) 식도 비슷한 의 미를 가지며 예를 들면 깁스 에너지는 온도, 압력 및 각 성분의 질량 이 일정한 계에서 감소하며 깁스 에너지가 최소인 상태는 더 이상 변 화하지 않고 안정하다. 이들 식들은 전화의 방향을 제시하고 있으므로 진화의 법칙이라 부를 수 있다. 열역학의 기본식들은 (1. 23) 식 또는 (1. 24) 식과 비슷한 형식의 국소 형식으로 쓰일 수 있고 이 형식들에 의해 열역학 변수들의 상호 관계 를 표시할 수 있지만 위치와 시간에 따르는 열역학 성질의 변화를 표 시하기 위해서는 다음 장에서 검토되는 수지식을 도입해야 한다.
7 정리 열역학은 거시적이고 현상적인 변화의 법칙을 대상으로 하는 과학의 한 분야이다. 평형 열역학에서는 이러한 변화 중에서 거의 평형 상태 룰 유지하는 변화 과정을 주로 다룬다. 비가역 열역학에서는 국소 평 형의 가정에 근거하여 실제의 변화 과정을 연구한다. 실제로 일어나는 거시적 변화 과정은 엔트로피를 생성한다는 특징을 갖는다. 변화의 법칙은 보존의 법칙과 진화의 법칙으로 나누어 생각할 수 있 다. 전화는 비가역성의 근원이라고 생각할 수 있으며 평형 열역학과 비가역 열역학에서 중요한 역할을 한다. 평형 열역학에서는 진화의 법 칙이 열역학 제이법칙으로 비교적 단순하게 주어진다. 비가역 과정에 대한 보존의 법칙과 진화의 법칙을 찾는 것이 바가역 열역학의 주요 관심이 된다. 전화의 법칙은 안정성과 밀접한 관계가 있다. 더 이상 진화할 수 없 는 상태는 안정한 상태이다. 평형 열역학의 평형 상태는 전화가 끝난 상태이고 안정하다. 비평형계에서는 경계조건에 의해 계가 평형 상태 에 도달할 수 없는 경우가 있다. 이러한 계의 안정성은 비평형계에 대 한 진화의 법칙과 관계를 갖는다.
제 2 장 수지식 I 서론 1 장에서 거시적 변화를 기술하기 위해서는 보존의 법칙과 전화의 법 칙이 필요하고 또한 비가역 과정에서는 열역학의 법칙들을 국소 형식 으로 표시할 필요가 있다는 점을 언급한 바 있다. 그러나 1 장에서는 열역학 법칙들을 국소 형식으로 표시하였을 뿐이고 변화를 기술하는 데 필요한 시간에 대한 의존성은 논의되지 못하였다. 이러한 시간적 변화는 수지식을 이용해서 검토된다. 수지식은 보존의 법칙을 일반화 한 것으로, 생성과 소멸의 속도가 0 이 되는 성질에 대한 수지식은 보 존의 법칙이 된다. 비평형계에서는 또한 평형계와 달리 속도장을 고려 할 필요가 있고 이에 따르는 양들이 도입된다. 따라서 운동량의 수지 식이 검토에 포함된다. 이 의에도 물질 수지, 에너지 수지, 그리고 엔 트로피 수지가 고려되는데 이들은 각각 질량 보존의 법칙, 열역학 제 일법칙 그리고 제이 법칙을 일반화한 것으로 생각할 수 있다. 이러한 수지식을 검토하는 이유는 두 가지로 생각할 수 있다. 하나는 엔트로
피 수지식의 구체적인 표현식을 발견하는 데 이용하고자 하는 것이고 다른 하나는 수지식을 근거로 계의 동역학과 안정성을 검토하고자 하 는것이다. 2 표기법과 일반적 수지식 이 책에서는 성분 표기법이 아닌 백터 표기법을 널리 사용하기로 한 다. 백터를 표기하기 위하여 A, lB, C, D .• …. . 와 같은 문자를 사용하 고 이계 텐서 또는 다이아드 (d y ad) 를 의미하기 위하여 A, B, C, D, ……와 같은 문자를 사용한다. 삼차원 공간에서 벡터를 다음의 열 백 터 (Column Vec t or) 로 표시하거나 A = 門門 (2 .1) 또는 다음의 행 백터 (Row Vec t or) 로 표시한다. A = [Ax ,A y , A 』 (2 . 2) 벡터들의 A벡B터 =곱 : A::B: 와 :스:칼::라 곱: :A: ]• B 는 다음과 같이 정의되(며2 . 3) zBx AzBy AzBz A•JB = AxBx+AYBY+AzBz (2 . 4) 이러한 곱은 A 가 벡터 연산자 V 일 때에도 적용된다. 연산자 V 의 원 (Elemen t)을 열 벡터로 표시하면 다음과 같다.
V원_== `'울이이이a8aAzyx '` A l (2 . 5) 행 렬 A 의 표 하면 홉 `과 같 댜A/A zXxxy AAA zyx yyy xZA, (2 . 6) 또한 행렬A의· B곱 = A[x Z·IBA 와x1 B Alx : AYZB2 를IA X정IB의l한y 다2.IA xlBIz 麟 ,B,x A~1Ay 1 B1y ~1Ay 1 B1z (2 . 7) 21AZIBlx z21AzlBiy 21AzIBIz] AA ·: BB == '~21`AA2x,BA: 21xA z+ ~ 1Ay 1 B1y + ~1Az1B1z (2 . 8) 이 식들로부터 A·B 는 이계 텐서이고 A : B 는 스칼라라는 것을 알 수 있다. 또한 이계 텐서와 백터의 곱을 정의할 수 있다. (2 . 9) B · A = 쭈BAlBIX`AiBIYlA I,Z (2 .10) 분명히 A·B =t= B·A 이고 또한 행렬 A 의 트랜스포즈 (Trans p ose) 를 A 타 하면 A·JB = lB·AT 이다. 대칭행렬에 대해서는 A = A 되므로 A·B = B·A 이다. 이러한 표기법에 의한 계산은 폴리아덕 대수 (Polya d ic Al _~ ebra) 라고도 불리며 선형 대수와 벡터 해석을 같이 생각 할 때에 널리 쓰이는 표기법이다. 블럭 (Block, 1962) 의 얇은 책에 기
술되어 있으며 여러 책 (예를 들면 Fit ts, 1 962 ; Slatt er y, 1972) 에서 쓰 이고있는표기법이다. 이제 비가역 과정의 열역학적 해석에 필요한 수지식들을 일반적으로 고려하기 위해 표면 S 로 둘러싸인 부피 요소 V 를 생각하자. 위치 벡 터 R 과 시간 t에 의존하는 밀도 p( R, t)와 단위 질량당의 시량 변수 f (R, t)의 부피 V 에 대한 값 F( t)는 다음 식으로 주어진다. F (t) =f f (JR, t) p (JR, t) dV (2 .11 ) 또한 F 의 시간에 대한 변화율을 다음과 같이 표시하기로 한다. dF/dt = P(F) +~ (F) (2 .12) 여기에서 P 와 Z 는 각각 부피 요소내에서 F 가 생성되는 속도와 부 피 요소의 계면을 통과해서 F 가 흐르는 속도를 나타내는 항이고 다음 식들로표시된다. P(F) = J야 dV (2 .13 ) ~ (F) = JJF ·NdS = JJF ·d§ (2 .14 ) 여기에서 N 은 표면적 요스: dS 에 수직인 부피 요소에서 밖으로 향 하는 단위 벡터이다. 이 식들에서 6 達t J습근 각각 단위 부피당의 F 의 생성속도와 단위 표면적당의 F의 흐름 속도 또는 플럭스를 표시한다. (2.12) 식을 국소 형식으로 표시하기 위해 디음과 같이 표시되는 벡 터해석의 발산 정리 (Dive rge nce Theorem) 를 이용하여 본다. JJF ·d§ = f'v·JF dV (2 .15) 이 관계식에 의해 (2.14) 식의 표면 적분은 부피 적분으로 변환될 수 있고, 따라서 (2.11) ― (2.14) 식으로부터 다음과 같은 국소 형식의 수 지식을 얻게 된다. 8(p f)/at+'il•JF = (JF (2 .16) 이 식은 일반적인 수지식이고 이 식을 우리가 관심을 갖는 특정한
성질에 적용하기 위해서는 해당하는 성질에 대한 f,
_ ).Il2 AI _ ).I2 2A2— …… = ).Ir + I , 2A r+l + ).Ir+ 2, 2Ar+2+······ - Y1nA1 - ))2nA2 - …… = ))r+h nAr+l + ))r+ 2, nAr+2 + …… (2 . 20) 이 화학 반응식은 ~r=l l/ijnl = 0 (j = 1, 2, 3, …… , R) 와 같이 표 시할 수 있고 n 는 성분 A1 의 몰수이고 양론 계수 l/의 부호는 반응물 에 대해 음(陰)이고 생성물에 대해 양(陽)이다. j번째의 반응 속도 Jj 는 다음과 같이 정의되며 한 반응에서는 성분에 무관하게 된다. Jj = (dni/ dt ) / vu (2 . 21) (2 . 19) 식은 단위 시간당 생성 또는 소멸되는 성분 i의 몰수를 표시 하는 반응 속도 J 1 에 대한 표현식을 알아야 완결된다. 이 문제는 다음 장에서 생각한다. 위의 표시 방법은 고정된 좌표계 또는 오일러 (Euler) 계에 대한 것이 고 같은 수지식을 질량 중심의 속도로 움직이는 좌표계에 대해서 표시 하는 것이 편리할 때도 있다. 이 질량 중심의 속도 V 로 움직이는 좌 표계는 라그란지 (La gr an g e) 계라고도 불린다. 라그란지계에서 수지식 을 얻기 위해 다음과 같이 도함수를 정의한다. 이 도힘수는· 물질 도함 수 (Substa n ti al Deriv a ti ve ) 라고도 불린다. D/Dt = aIat+ V.'v (2 . 22) 또한 다음 정의식을 이용하면 p = ni=l P t (2.23) pV = 고= l pIV I (2.24) 총물질 수지식과 성분 i의 물질 수지식은 각각 다음과 같이 표시된다. Dp /D t +p'v• V = 0 (2.25) Dp ,/ Dt +p,'v • V+'v ·J,d l ff = ~=l l/lJ M1J J (2.26) 여기에서 Jt dl”은 다음 식에서 정의되는 확산에 의한 성분 i의 흐름
을표시한다. J전 = P1(V1-V) (2 . 27) 그리고 고정된 좌표계에 대한 성분 i의 질량 속도를 J 1 라 하면 J전 = P1V1-P1V = J1— (p1 /p )~f=l PJ V j = J 1 一 W1~ f= 1 JJ (2 . 28) 이고 여기에서 w 는 질량 분율이다. 따라서 이렇게 정의된 확산 속도 는 질량 평균 속도를 기준으로- 한 확산 속도이다. (2.26) 식에서 J,d lff 와 JJ의 표현식을 쓸 수 있으면 이 식은 완결된다. 의력이 없고 압력 과 온도가 균일한 2 성분계에 대한 J ,dl”는 피크의 경험적 법칙으로 다 음과같이 표시된다. JId Iff = - Dljv pI (2 . 29) 여기에서 D1 눈- 확산 계수이다. 그러나 일반적인 경우의 Jt dl ff에 대 한 표현식은 연계된 전달 현상 때문에 훨씬 복잡하게 되며 4 장에서 검 토한다. 성질 f에 대한 수지식은 (2 .16) 식 대신 이 식으로부터 유도할 수 있 는 다음 관계식을 이용하면 더 쉽게 얻어진다. p( Df /D t ) = 8p f/8 t+ v·pv f = 6F_v· (JF _vp f) (2.30) (2.30) 식은 흐름 JF 대신 확산 흐름 JF dlff = J'F -Vp f.£ 표시되어 있다. 확산 흐름은 여기에서 질량 평균 속도로 유체와 같이 흐르는 흐 름에 대한 상대적인 흐름으로 다성분계에서의 확산은 물론 고체내에서 열이 전달되는 경우의 열흐름과 같이 전도에 의한 흐름을 일반적으로 의미한다. 확산 흐름의 기준이 되는 흐름은 여기에서와 갇이 질량 평 균속도를 가질 수도 있지만 몰 평균 속도 또는 부피 평균 속도와 같이 다른 평균 속도를 가질 수도 있다. 이때에는 (2.30) 식의 표현이 변한 다. 라그란지계에서나 오일러계에서 생성항은 변하지 않는다.
f = V 이면 운동량 수지식을 얻게 된다. 각 성분의 단위 질량에 작 용하는 힘의 크기를 E 라 하면 힘이 운동량의 생성항에 해당하게 된 다. 또한 운동량의 전도에 의한 흐름을 압력 텐서 P 로 표시한다. -P 는 응력 (Str e ss) 텐서라고 불리기도 한다. 따라서 (2.30) 식을 이 용하면 운동량 수지식은 다음과 같이 쓸 수 있다. p( DV/Dt ) = XF=I PIFl_v·P (2 . 31) 이 표현식은 일반적이며 점탄성류 (V i scoelas tic Flu i d) 에까지 적용될 수 있다. 점성류 (V i scousFlow) 의 경우에는 P 를 다음과 같이 두 부 분으로 나누어 표시한다. p = pl + pd (2 . 32) 여기에서 읽근 압력이고 I 는 단위 텐서이며 p d 는 점성에 의한 운동 량의 흐름을 표시한다. p d는 잘 알려진 바와 같이 점성류의 특수한 경우인 뉴턴 유체에 대해 다음과 같이 표시된다. pd = -[?;-(2 /3) 씨 ('v• V) l-2 µD (2.33) 여기에서 D = [vV+ (vV ) 기 /2 (2 . 34) 그리고 g는 벌크 점도 (Bulk Vi sc osit y), µ는 전단 점도 (Shear V i scos ity)이다. 人두 더 ~(S t okes) 의 가설에 의하면 t는 0 이고 실제 로 이 값은 낮은 밀도의 기체에 대해서는 0 이 된다는 것이 알려져 있 다. 이 경우에 위의 식은 다음과 같이 된다. pd = -2µ[D -(1 /3) ('1· V)I] (2 . 35) 이 식에 관한 논의는 여러 유체 역학 책에 취급되어 있다(예를 들면 Slatt ery , 1972) . 다음 관계식을 이용하면 V·D = [V2V+V(V·V)]/2
밀도가 일정한 유체에서는 'v • V = O 이므로 (2 . 35) 식과 (2 . 32) 식을 (2.31) 식에 대입하고 물질도함수의 표현식 (2.22) 를 이용하면 다음 식을 오일러 좌표계에서 얻는다. pa v/ at+ pV •'v V = ~=I p, F,-'v p+ 2µ'v · D =~f=l p ,lF',-'vp+µ'v2V (2. 36 ) 이 식은 나비에-人두더 !::..(Nav i er - S t okes) 식으로 알려져 있다. 성분의 물질 수지식도 (2.30) 식의 형식으로 표현이 가능하다. (2.26) 식으로부터 다음 식을 얻는다. p( Dw,/Dt ) +'v·J전 = ~R=I l.lu M,Ji (2. 37 ) 위의 운동량 수지식은 국소 질량 평균 속도 V에 관한 것이다. 다성 분계에서는 각 성분의 속도가 다르므로 각 성분의 단위 부피당의 운동 량 p lv1 도 생각할 수 있다. 베어만과 커크우드 (Bearman and Ki rk wood, 1958) 는 통계역학적 방법으로 성분의 운동량 수지식을 유 도한 바 있다. 이렇게 유도된 식은 복잡하고 여기에서는 이 식을 논의 하지 않지만 성분의 속도가 다르기 때문에 발생할 수 있는 문제점들은 후에 논의된다. 4 에너지 수지식 기계적 에너지의 수지식은 (2.31) 식의 양변에 V 를 곱하면 얻을 수 있다. pD (V•V/2)/Dt = pV ·DV/Dt = TI'=1 piV• F,-V· (V·P) = (Jk — V · (P·V) (2.38) 여기에서 생성항을 정리하면 다음과 같게 된다.
(Jk = P : vv +~ r=l p,F ,·v = p(v'•v ) +Pd : vv +~r= l p,JF',• v (2. 39 ) 이 식은 기계적 에너지의 순 (ne t) 생성을 표시하고 우변의 첫항은 내부에너지의 변환에 의한 기계적 에너지의 생성을 나타내며 둘째 항 은 점성에 의해 기계적 에너지가 열 에너지로 소산되는 것을 나타낸 댜 그리고 우변의 끝항은 의력에 의해 기계적 에너지가 생성되는 것 울의미하고있다. (2 . 30) 식에서 f='1이고 V 가 퍼텐셜 에너지 밀도를 나타낸다면 퍼 텐셜 에너지 수지식을 얻는다. 디성분계에서 V 는 성분 i의 퍼텐셜 에 너지 밀도이다. p D'l / Dt = (Jp- V• (~~=I 'l 1 J전) (2 . 40) 퍼텐셜 에너지의 생성항 (Jp의 계산을 위해 다음과 같이 성분 i의 퍼 텐셜 에너지 수지식에서 시작한다. p,D 'l ,/ Dt = a(p, '1,) /at + V· (p,'liV) (2 . 41) 그리고 다음의 정의식을 사용하여 (2.41) 식을 모든 성분에 관하여 합하면 (J려 표현식을 얻을 수 있다. p'l' = ~r= I P1' l'1 (2 . 42) 계산결과는다음과같고 (Jp = -~p1lF ' 1· V-~1=1N J1d 1rr·lF '1+ ~~=1 ~f=1 vu' l'1J1 (2.43) 여기에서 우변의 첫항은 퍼텐셜 에너지가 기계적 에너지로 전환되는 것을, 둘째 항은 확산에 의해 퍼텐셜 에너지가 내부 에너지로 전환되 는 것을, 그리고 끝항은 화학반응에 의해 퍼텐셜 에너지가 생성되는 것을나타내고있다. f = u 이고 U7} 내부 에너지 밀도를 나타낸다면 다음 내부 에너지 수지식을 (2.30) 식으로부터 얻는다.
p Du/ D t =
되는 바와 같이 Jq의 표현식은 훨씬 더 복잡한 식이 된다. 이제 (2.44) 식을 (2.45) 식 및 (2.47) 식과 결합하면 내부 에너지의 수지식을 다음과같이 쓸수있다. p Du/Dt = p Dq /D t -pd : \JV +~r=l J/lff•JP1 — pV V : I (2.49) 위 식의 우변의 끝항은 p V•V 와 같다. 그리고 p- 1 = V 이므로 연속 방정식 (2.25) 식을 다음과 같이 표시하고 'v· V = p Dv/Dt (2.50) 이 관계식을 이용해서 다시 내부 에너지 수지식을 정리하면 다음과 같 은 열역학 제일법칙이 확장된 국소 형식을 얻게 된다. Du/Dt = Dq /D t -p Dv/Dt -v(Pd : VV) +v(~=l J1d t rr ·lF1) (2.51) -Pd : vv 항은 (2.39) 식에서와 같이 점성 소산에 의해 기계적 에 너지가 내부 에너지로 전환되는 것을, 그리고 ~ J 1dl ff •lF1 항은 확산에 의해 퍼텐셜 에너지가 내부 에너지로 전환되는 것을 나타내고 있다. 내부에너지의 변화가 중요한 (평형) 열역학에서는 이 두 항을 무시할 수 있고 따라서 이 경우에 (2.51) 식은 우리가 잘 알고 있는 열역학 제 일 법칙과 동일하게 된다. 5 엔트로피 수지식 엔트로피의 수지식을 라그란지 계에서 다음과 같이 표시하자. p Ds/Dt = 6s-V·Js d Iff (2 . 52) 여기에서 J sdl”는 엔트로피의 확산 플럭스를 표시한다.
Jsd lf f = Js —ps V (2 . 53) (J s 와 J?”는 각각 엔트로피의 생성항과 확산 플럭스을 나타내며 이 양들의 표현식을 얻기 위해서 먼저 국소 형식의 기본 방정식인 (1. 23 ) 식을 라그란지 계에서 표시한다. 결과는 다음 식과 같다. T (Ds/D t ) = Du/Dt + p (Dv/Dt ) —~~ = 1 µ, (Dwi /Dt ) (2 . 54) 성분 물질 수지식 (2.26) 과 내부 에너지 수지석 (2 . 51) 을 (2.54) 식에 대입하고 (2.52) 식의 형식으로 정리하면 다음 엔트로피 생성의 표현식 을얻는다. Os = Jq• v' (1/ T ) + (1/T ) TI1=1 J,d lff • F,-~l=t J,d lff •v' (µ,/T) 一 (1/T)p d : v'V + (1/ T )~=I J,A , (2.55) 여기에서 끝의 합은 約사의 화학 반응에 관한 것이고 A 는 i번째 반 웅의 화학 천화력이며 M 롤 성분 j의 분자량이라 할 때 다음 식으로 정의된다. Al = — 2?=I VlJM j µj (2 . 56) 또한 엔트로피의 확산 플럭스는 디옴- 식으로 표시된다. J전 = Jq/ T -~ f=l µ1J /1 ff /T (2 . 57) (2.52) 식의 우변을 엔트로피의 생성항 (2.55) 식과 흐름항 (2 . 57) 식 으로 나누는 방법은 임의성을 내포하고 있는 것처럼 보인다. 형식적으 로는 벡터장의 발산은 흐름항으로, 그리고 나머지는 생성항으로 분류 하였다. 이러한 방법에 의하여 엔트로피의 생성 속도가 항상 0 보다 크 거나 같게 된다. 또한 1 장에서 분류한 엔트로피의 생성과 흐름의 분류 와도 관련을 찾을 수 있다. (2 . 52) 식은 (2.55) 식 및 (2 . 57) 식과 함께 질량 평균 속도로 움직이고 있는 부피 미분 요소에 대한 기본 방정식 의 국소 형식으로 볼 수 있다. 단지 여기에서는 물질의 확산에 의한 영향이 추가되어 있다.
고정된 좌표계에 대해서는 (2.12)-(2.14) 식에서 F = S 라 해서 다 음식들을얻는다. dS/dt = d,S/dt + deS / d t (2.58) dde,SS//ddtt == J—as !dJ rV s• d=S P = ( S~) (S) ((22.. 5690 )) 제 1 장에서 제이법칙이 d1S~O ¾ 의미한다는 것을 지적하였다. 따라 서 시간이 증가할 때 자연적 진회에 대해 다음 관계식이 임의의 적분 구간에서 성립한다. d,S = J P (S) dt ~ O (2.61) 그러므로 엔트로피의 생성속도 P(S) 가 0 보다 크거나 같아야 한다. 비슷한 논의에 의해 (2.59) 식의 적분이 적분구간에 상관없이 0 보다 크 거나 같으므로 다음 관계식이 성립한다. (Js ~O (2.62) 이 부등관계를 만족하는 엔트로피의 국소 생성 속도는 다음 장의 선 형 열역학에서 중요한 역할을 한다. 6 다론 수지식들 위에서 질량, 운동량, 에너지 수지식을 검토하였다. 이 의에도 각 (角)운동량 수지식을 생각할 수 있으며 고체의 격자 뒤틀림에 의한 응 력 등 다른 영향둘을 고려할 수도 있다. 여기에서는 이들 다른 수지식 에 관해 구체적인 언급은 피하기로 하고 일반적인 기술만을 소게한다 (Kreuzer, 1981). 주어전 계에서 천천히 일어나는 과정을 거시적으로 기술하기 위해 질량, 운동량, 에너지 이의에 필요한 거시적 변수들을 g라 하자. 그러면 g는 국소 수지식인 (2 . 16) 식 또는 (2.30) 식을 만족
해야한다. p (Dg / D t ) = i)pg/ i) t+ ' \J• pV g =
시간에 의존하는 열역학 변수들의 관계를 제시할 수 있어야 한다. 이 장에서 제시한 수지식들은 앞으로 논의할 비가역 과정의 기술에 기초 가된다.
제 3 장 선형 열역학 I 서론 평형 근처에서 성립하는 비가역 열역학을 프린고진에 따라 선형 열 역학이라 부르기로 하자. 선형 열역학의 영역에서는 평형 상태를 향해 변화하는 흐름 또는 변화가 이 흐름을 일으키는 힘의 선형 함수로 표 시될 수 있다. 선형 열역학의 영역에서 변화의 법칙은 두 가지의 중요 한 성질을 갖는다. 하나는 4 장에서 예시하고 검토하게 되는 바와 같이 선형 현상적 법칙들이 연계되어 있고 연계된 현상법칙들의 선형 계수 들 사이에 온사거의 상호 관계로 알려진 대칭성 관계가 성립한다는 것 이다. 연계되어 있다는 예는 열의 흐름을 일으키는 힘이 확산을 일으 킬 수 있다는 것이고 또한 확산울 일으키는 힘이 열의 흐름을 유발시 킬 수 있다는 것이다. 그리고 다른 하나는 평형계에서와는 다르게 최 소 엔트로피 생성의 정리에 의해 계의 진화가 결정된다는 것이다. 2 장에서 국소 엔트로피의 생성 속도 6g l-흐 름의 플럭스과 힘의 곱 으로 표시된다는 것을 알았다. 그러나 해당하는 항을 플럭스와 힘으로
나누는 유일한 방법이 있는 것은 아니다. 그 러 므로 어떠한 흐 름 과 힘 의 짝에 대응하는 선형 계수들 사이에 온사거의 관계가 성립할 것 인가 하는 것 이 문제가 된다. 온사거 관계의 유도 과정에서도 이 문 제 는 밝 혀지지 않는다. 간접적으로 이 문제는 플럭 스 와 힘의 변환 성 질 을 구 명하여 해결될 수 있다. 어떤 제한 조건에서 한 세트의 힘과 플 럭스에 서 정의된 선형 계수들 사이에 온사거의 관계가 성립한다면 이 플 럭 스 와 힘의 선형 변환에 의해 얻어지는 다른 세트의 플럭 스 와 힘에서 결 정되는 선형 계수들 사이에도 온사거의 관계가 성립함을 보일 것 이다. 이 점은 온사거의 관계를 응용하는 데 가장 중요한 문제의 하나가 될 것이다. 이 장과 다음 장에서는 온사거의 관계 를 중심으로- 선형 열역 학의 문제들을 검토하기로 한다. 선형 열역학의 다른 하나의 중요한 문제인 진화와 안정성의 문제는 5 장에서 검토한다. 2 흐름의 플럭스와 힘 푸리에의 열전도 법칙 (2.48 식), 뉴턴의 점성법칙 (2. 3 ~). 피크의 확산 법칙 (2.29 식) 등은 흐름의 플럭스가 흐름을 일으키는 힘의 선형 함수로 표시되므로 선형 현상적 법칙이라 불린다고 2 장에서 언급한 바 있다. 그러나 온사거의 관계를 적용하기 위해서는 이둘 경험적 법칙에 서 나타나는 플럭스와 힘의 곱이 엔트로피 생성 속도의 표현식에 나타 나는 항과 일치할 필요가 있다. 이 조건에서 이들 법칙의 힘과 흐름의 플럭스를 다시 정리해서 아래의 표 l 과 같이 표시할 수 있다.
표 l 흐름의 플럭스와 힘 플럭스 YI 힘 X1 선형계수 푸리에의 법칙 Jq v (1/T) xT2 뉴턴의 법칙 pd -D 2µ
피크의 법 칙 Jid lf f -9 (µ1/ T ) Du p J R 화학반응 JI A1/ T Jno /R
여기에서 의력이 확산에 미치는 영향은 표시되지 않았으며 화학반 응의 힘 A 는 i번째 반응의 화학 친화력 (Af fini t y) 이다. 화학반응 속 도의 선형계수는 아직 도입되지 않았지만 평형 근처에서는 화학반응 속 도 를 천화력의 선형 함수로 표시할 수 있다 (Glansdor f and Pri- go g ine , 1971). 이때에 선형계수는 표에 주어전 것과 같이 평형에서의 반응 속 도 를 써서 표시될 수 있으며 양수이다. 이 문제는 4 장에서 화 학반응을- 취급하면서 검토된다. 이제 (2.55) 식으로 표시된 엔트로피 의 생성항 6 s 을 ( 2 .29) 식, (2 . 35) 식, (2.48) 식과 비교하여 보면 엔트 로피의 생성 속도가 위에서 정리한 흐름의 플럭스와 해당하는 힘의 곱 으로 표시되어 있음을 확인한다. 이러한 발견에 따라 엔트로피의 생성을 다음과 같이 일반화된 힘과 이에 대응하는 흐름의 플럭스의 곱으로 표시하는 것이 가능하다. as = ~ X,Y1 = X• Y 2:0 (3 .1 ) 또한 Y 는 XI 등의 함수이므로 YIo를 중심으로 전개해서 다음 근사 식 을 얻는다. Y, = Y,o+~(aY, /aX i) X i=X io Xj = ~ Lu X i 또는 Y =L·X (3 . 2) 평형에서 YIo 는 0 이고 또한 평형에서 계산된 도함수인 계수는 힘을 포함할 수 없다. 이 식은 또한 Y 가 X 는 물론이고 X 세도 영향을 받 는다는 것을 의미하고 있다. 이러한 연계성은 비평형 통계역학에서 밀 도가 낮은 기체에 대한 통계역학적 이론의 볼츠만 방정식에서도 제시 되지만 거시적 과학의 틀에 의해 설명하는 방법은 비가역 열역학에 의
하는 것이다. (3.1) 식과 (3 . 2) 식에서 디음 식이 성립한다. as = ~~ LuX1Xi = X·L·X 착) (3 . 3) 이 식의 구체적 표현식은 디옴- 장에서 논의하고 다음에 이 식의 일 반적 성질에 관해서 검토한다. (3.2) 식은 흐름의 플럭스 Y 가 이 흐름에 대응하는 힘 X 는 물론이 고 다른 힘 X 세 의해서도 일어난디는 것을 의미한다. 이러한 힘과 흐름의 연계성은 다음 철에서 간단히 검토되는 바와 같이 큐리의 정리 에 의해 제한을 받는다. (3.1) 식으로 표시된 쌍선형 형식 (Bi li n e ar Form) 은 (3.2) 식으로 표시된 선형 현상적 법칙들과 결합되면 이차 형 식 (Qu adrati c Form) 을 구성한다. 이러한 이차 형식에서 L 은 대칭 행 렬이 되는데 그 이유는 다음과 같다. 임의의 행렬 L 은 대칭 (s ym me t r i이 행 렬 L5 (Lu = L 사 와 반대 칭 (skews y mme t r i이 행 렬 U (Lu = 一 L j l) 의 합으로 표시할 수 있다. L=V+La (3 . 4) 그러나 반대칭 행렬은 이차 형식에서 상쇄되고 대칭 행렬만이 남는 다. 그러므로 3 . 3 절에서 취급될 온사거의 상호관계 (Onsag e r, 1931a, 1931b) 에 따라 (3.2) 식의 선형 계수들 사이에 다음의 중요한 관계식이 성립한다. Lu=Li1 (3 . 5) 따라서 (3.3) 식의 계수 행렬은 (3.2) 식의 계수 행렬과 동일하다. 그 리고 이 대칭성 관계는 (3.3) 식의 부등 관계와 함께 성립되어야 한다• 죽 모든 힘이 0 이 되는 평형 상태를 제외하고는 (3.3) 식의 이차 형식 은 항상 0 보다 커야 한다 (Pos iti ve Defi ni t e) . 선형 대수학의 이론에 의하면 이 조건이 만족되기 위해서는 NxN 행렬인 L 의 계수 (Rank) 가 N 이 되어야 하고 또한 E 긱 고유치가 모두 0 보다 커야 한다. L 긱 계수가 N 이 되기 위해서는 (3 . 2) 식에서 X 와 Y 가 모두 선형 독립인
벡터가 되어야 한다. L 키 고유치가 모두 0 보다 크기 위해서는 L 의 주도 소행 렬식 (Leadin g M i nor) 가 모두 0 보다 커야 한다. 이 점은 京J 에서 다시 논의된다. 4 절에 주어진 온사거 관계의 증명은 이러한 관계의 존재를 미시적으 로 증명하지만 힘과 흐름의 플럭스를 어떻게 선택할 때에 아 관계가 성립하는지를 제시하지는 않는다. (3 . 1) 식을 만족하는 힘과 플럭스의 구성은 임의성을 가지고 있다. 3.5 절에서는 힘과 흐름의 플럭스가 모 두 선형 독립일 때는 한 세트의 힘과 흐름의 플럭스에 대해 온사거의 관계가 성립하면 (3.1) 식을 만족하는 어떤 다른 세트의 힘과 흐름의 플럭스에 대해서도 이 관계가 성립함을 보일 것이다. 따라서 힘과 흐 름이 선형 독립일 때는 온사거의 관계를 만족하는 힘과 흐름의 선택에 아무런 문제가 제기되지 않는다. 4 장에서는 연계된 전달 현상 중에서 힘 그리고/또는 흐름의 플럭스 가 선형 독립이 아닌 경우가 발생한다는 것을 알게 될 것이다. 이러한 경우에 온사거의 관계는 어떻게 적용될 것인가 하는 문제를 검토해야 한다. 온사거의 관계와 이러한 제한 사항을 이 장에서 검토하고 다음 장에서 연계된 전달 현상에서 중요한 역할을 하는 이 관계의 응용 예 를 취급할것이다. 3 큐리의 정리 (3 . 2) 식은 흐름의 플럭스가 모든 힘의 선형 함수로 표시될 수 있다 는 것을 의미하고 있다. 그러나 이러한 전달 현상의 연계성은 큐리의 정리로 알려진 제한 조건의 지배를 받는다. 큐리의 정리는 전달 현상 의 연계성이 같은 텐서의 성격을 같는 힘과 흐름의 플럭스 사이에서만 존재 가능하다는 것을 의미하고 있다(더 정확히 말하면 전달 현상의 연 계성은 텐서 계수의 차가 짝수인 힘과 흐름 사이에서만 가능하다).
(Js = ~ X,Y,+~ X, ·Y , + ~ X, : Y, (3.6) 이 식에서 2 칭에서 설명한 바와 같이 XI 와 Y 는 스칼라 양을, X 와 Y 는 벡터 양을 그리고 X 와 YI 는 이차 텐서를 의미한다. 이 정리는 다음과 같이 증명된다. 텐서 계수가 n 인 흐름의 플럭스 Y 를 생각하자. 만약 이에 대응하는 힘 X 가 같은 텐서 계수 n 을 갖 는다면 선형 계수 LIJ- 2 스칼라 양이다. LIJ- 2 위에서 밝힌 바와 같이 평형에서 계산되는 물성으로 등방성이므로 힘, 죽 구배를 포함할 수 없고 스칼라 양은 이 조건과 부합되어 일반적으로 0 이 되지 않는다. 같은 논의에 의해 힘과 흐름의 플럭스의 텐서 계수 n 의 차가 짝수일 때는 L1 놉 짝수 텐서 계수의 양으로 되어 등방성의 조건이 만족될 수 있고 따라서 이러한 선형 계수는 일반적으로 0 이 아니다. 반면에 힘과 흐름의 플럭스의 텐서 계수 차가 홀수이면 이때의 선형 계수 L1J -2 홀 수 텐서 계수의 양이 되어 등방성 조건에 부합되지 않으므로 0 이 되어 야만한다. 4 온사거의 상호관계 3.2 절에서 선형 계수 행렬 L 에 부과되는 조건의 하나로 온사거의 상호관계에 의해 이 행렬이 대칭행렬이 된다는 것을 언급한 바 있다. 이 대칭성은 미시적 가역성의 원리에 근거한 것으로 회전계의 코리올 리 힘이나 자력장의 로렌츠 힘과 같은 시간에 대해 기함수인 힘이 작 용하는 계에는 적용되지 않는다. 카시미르 (Cas i m i r, 1945) 는 온사거의 관계를 이러한 힘이 작용하는 계에까지 확장하였다. 이러한 관계는 온 사거-카시미르의 관계라고도 불린다. L1k (JB, W) = E1 EkLk1 ( 一 lB, _ w) (3 . 7) 여기에서 B 는 의부 자력장, W 는 계의 각속도이고 이들 이의에도
시간 역전에 대해 부호가 바뀌는 성질들을 포함할 수 있지만 여기에서 는 생략하였다. 또한 c 는 해당하는 힘 X 가 시간 역전에 관해 부호가 바뀌면 ― 1 이고 그렇지 않으면 +1 이다. 따라서 두 힘 모두 시간 역 전에 대해 같은 성질을 가지면 L,k(B, W ) = Lk,(-B, -W) (3 . 8) 이다. 그리고 두 힘이 시간 역전에 대해 다른 성질을 가지면 L,k(B, W) = -Lk1(-B. -W) (3 . 9) 이다. 위의 두 식에서 두 힘이 자력장 또는 각속도와 무관하더라도 B 와 W 의 부호가 바핀다는 것에 유의해야 한다. 자력장 또는 각속도와 같은 시간 역전에 대해 부호가 바뀌는 성질이 없는 계에서는 온사거의 관계는 (3.5) 식으로 표시한 것과 같이 단순하게 된다. 고전 역학이나 양자 역학에서 입자들의 운동을 기술하는 법칙은 시 간 역전에 대하여 불변이다. 예를 들어 다음의 고전 역학적 운동 법칙 울생각하자. F = md2X/dt2 (3 .10) 이 식에서 ~ -t의 시간 역전에 대해 F 와 X 의 관계는 변화하지 않는다. 그러나 각속도가 W 인 원심력장에서 회전축으로부터의 위치 가 고정 좌표계에서 R 로 표시되는 질량 m 인 질점에 작용하는 코리올 리 힘은 다음과 같이 표시되므로 W 의 부호가 변하지 않을 때에 시간 역전에 대해 F 와 R 중 하나의 부호가 변한다. F = 2m (dIR/dt) x w (3 .11) 따라서 (3.8) 또는 (3.9) 식에서와 같이 W 의 부호가 반전되어야 한 다. 懿l-oJ]서는 원심력장에서 일어나는 침강 현상을 검토하게 되지만 이때에는 코리올리의 힘이 원심력에 비해서 무시되므로 각속도의 부호 에 관심을 가질 필요가 없게 된다.
온사거의 관계는 미시적 가역성에 근거하고 있다. 열역학 변수의 요 동 a1( t)와 ai (t +r) 의 교차 상관 계수 를 다음과 같 이 정의하자. @ (t) aJ (t + T) >= 四 +1Ta, (t) a』 (t + r) dt (3 .12) 다음에 〈 a i(t )a1( t + r) 처t 생각하자. 이 표현식과 (3 . 12) 식의 차이 는 시간적인 순서에 있으며 r 대신에 ―례t 대입하면 미시적 가역성 으로부터 두 표현식이 같게 된다.
니고 요동이 일어날 확률의 밀도 함수 W 에 관한 평균을 다음과 같이 취한다.
정의되는 선형 계수들 사이에도 온사거의 관계가 성립한다는 것을 언 급하였다. 이 절에서는 힘과 흐름의 플럭스의 변환 성질에 의해 이 점 울 보인다. 더욱이 힘과 흐름의 플럭스가 동시에 선형 종속이 아니면 (3.1) 식을 만족하는 어떠한 힘과 흐름의 플럭스의 세트에서 결정되는 선형 계수들 사이에도 온사거의 관계가 성립하는 것을 보일 것이다. 선형 독립인 힘과 흐름의 플럭스, X’ 와 Y' 에 대해 (3.2) 식과 같은 선형 관계가 성립하고 이때에 선형 계수들 사이에 온사거의 대칭성 관 계가 성립한다고 생각한다. 그리고 (Js = X·Y 이고 각각 선형 독립인 또 다른 힘과 흐름의 플럭스의 세트 X 와 Y 를 생각하자. (Js = X·Y = X'•Y' 착) (3 . 21) 그리고 두 세트의 힘과 흐름의 플럭스 사이에 다음 변환 관계가 성 립한다고하자. X' = A·X = X·AT (3.22) Y' = B·Y = Y·BT (3 . 23) 그러면 선형 변환 A 와 E 큰 정방 행렬로 표시되고 이들의 행렬식은 IAI=I= 0 , IBI =I=떠 조건을 만족한다. 이제 엔트로피의 생성 속도는 두 표현에서 같아야 하므로 다음 관계가 성립한다. (55 = X•Y = X'•Y' = X• (AT,B ) •Y (3.24) 따라서 A 와 B 사이에 디음 관계가 성립한다. AT·B=I (3 . 25) 이제 디음 식에 의해 L 을 정의하고 Y=L·X (3 . 26) 이 식과 선형 현상적 (3.2) 식을 (3.21) 식에 대입하면 다음 관계식을 얻는다.
(J5 = X'•Y ' = X'•L '•X ' = X •AT•L '•A •X = X •L•X (3.27) 이 관계로부터 L'=L'T 일 때에 L=LT 인 것을보이기 위해 LT 을 계산한다. LT = (AT·L '·A )T = AT·L '·A = L (3. 28 ) 이 식으로부터 L = LT 이고 대칭성 관계가 성립하는 것을 확인한 다. 다시 말하면 하나의 선형 독립인 힘과 흐름의 플럭스의 세트에 대 해 온사거 관계가 성립한다면 같은 엔트로피를 생성하는 어떤 선형 독 립인 힘과 흐름의 플럭스의 세트에 대해서도 온사거의 관계식이 성립 한다. 이것은 또한 (3.1) 식을 만족하는 어떤 선형 독립인 힘과 흐름에 대해서도 흐름을 힘의 선형 함수로 표시할 때에 선형 계수들 사이에는 대칭성 관계가 성립한다는 것을 확립한다. (3.22) 식과 (3.23) 식의 변환 관계는 힘과 흐름의 플럭스가 선형독립 이 아닌 경우에도 유효하다. 먼저 힘이 선형 독립이고 흐름의 플럭스 가 선형 독립이 아닌 경우를 생각하자. A·Y =O (3 . 29) 여기에서 A = (a1, a2, a3, …… , aN) 이고 선형 종속의 정의로부터 a1, a2, a3, …… , aN 중에서 적어도 하나는 0 이 아니다. N 차원의 흐름 의 플럭스 벡터 Y ' 가 선형 종속이고 (N-1) 개의 독립적 성분을 갖고 있다면 엔트로피의 생성을 다음과 같이 표시할 수 있다.
L' 과 A 를 알면 (3.27) 식을 이용해서 L 을 계산할 수 있다. L 키 원 을 계산한 결과는 다음과 같다. Lu = Lu'(i = 1, …… , N-1, j = l, …… , N-1) LL1NN1 == —一 Z즈麟 麟 갑 LLijj1 ' 'aa JJ aaNN LNN = 책감 ~f=11 Li1 'Lu'aia 1/ai (3.32) 따라서 L jl’ 가 온사거의 관계를 만족하므로 Lj1 역시 온사거의 관계 롤 만족함을 알 수 있다. 이 결과로부터 온사거의 관계식은 흐름의 플 럭스가 선형 독립이 되지 않는 경우에도 성립함을 확인한다. 비슷한 방법으로 흐름의 플럭스가 선형 독립이고 힘이 선형 독립이 아닌 경우에도 온사거의 관계가 성립함을 확인할 수 있다. 이 경우를 생각하기 위해 (3.29) 식 대신에 디옴- 식을 쓸 수 있다. B•X=O (3.33) (3·29) 식에서와 비슷하게 B의 성분 b1, b2, …… , bN 중에서 적어도 하나는 0 이 아니다. (3 . 30) 식은 다음과 같게 된다. as=Y·X= 麟 Y1X1= 雲 1Y,X1+ YNxN = 2!f=11 X1(Y1-b1/bN.y N ) (3.34) 이 식으로부터 (3.23) 식의 행렬 B 를 다음과 같이 쓸 수 있다. B = 「1 0… … 0 —b1/ bN 0 1… … 0 一 b2/bN (3 . 35) 0 0… … 1 -bN-1/bN 이제 선형 독립인 힘과 흐름의 관계를 아래와 같이 쓰고 X' = (L')-1·Y' 선형 종속인 힘과 선형 독립인 흐름의 관계를 디음과 같이 쓰면
X=H·Y (3 . 36) 이 식들을 (3.21) 식에 대입해서 다음 관계를 얻는다. 6s = Y'•X' = Y'• (L')- 1•Y' = Y•BT• (L')-1•B•Y = Y·H·Y (3.37) 따라서 H=BT, (L')-1•B (3 . 38) 이 식을 이용하면 B 라 (L')-1 이 알려져 있으므로 H 를 구할 수 있다. (L') -1 과 H 의 원을 각각 lu 와 Hu 이라 하면 계산 결과는· 다음과 같 다. HHuIN = = lu— 2(i? =다 1l, 晶… / ,b NN — 1, j = 1, … , N-1) HNl = —Z 冒 llJb j/ bN HNN = ~~;;II zr감 1 j lll j b j bl/b N2 (3.39) 이 식에서 L' 이 대칭 행렬이고 따라서 (L')-1 이 대칭 행렬이므로 또한 H 도 대칭 행렬이 된다. 일반적으로- H 의 역행렬은 존재하지 않 지만 다음 관계식을 만족하는 L 은 구할 수 있다. L·H=I (3 .40) (3.36) 식에 의해 이 석을 만족하는 L 은 (3.26) 식의 선형 계수가 된 다. (3.40) 식으로부터 다음 식을 쓸 수 있다. LT = L·H·LT (3 . 41) 양변의 트랜스포즈를 취하면 H 가 대칭 행렬이므로 다음 식이 성립 하고, L = L·HT-LT = L·H·LT (3 . 42)
따라서 L = LT 이므로 L 은 대칭 행렬이고 온사거의 관계를 만족한다. 그러나 힘과 흐름의 플럭스가 동시에 선형 종속인 경우에는 온사거 의 관계가 일반적으로 성립한다고는 말할 수 없다. 힘과 흐름이 모두 선형 독립이 아닌 일반적인 경우를 생각하고 이때에 힘과 흐름이 각각 X 와 Y 이고 이들의 원 N 개 중에서 각각 N-1 개만이 독립이라고 하 자. 이들의 종속 관계를 (3.29) 식과 (3.33) 식으로 표시할 수 있다고 생각하고 엔트로피의 생성을 계산한다.
그러나 여기에서 A’ 와 B' 는 Nx (N-1) 의 행렬이며 X 와 Y 는 (N 다―. 1 ) 차(3 원. 4의8) 식벡에터서이 1고 는 적(N어— 도1 )이 X 들( N벡-1터) 의중 에단서위 하행렬나이는 고선 따형 라독서립 A이' 와 B' 중에 하나가 주어질 때에 다른 것이 결정되는 방법이 여럿 존재 한디는 것에 유의한다. 이제 (3 . 26) 식을 (3 . 47) 식과 결합해서 다음과 갇이쓰자. B'•Y' = L· (A'·X') (3. 49) 이 표현식에서 A’ 이 주어져 있다고 해도 (3.48) 식에 의해 B' 을 유 일하게 결정할 수는 없으므로 L 역시 유일한 것은 아니다. (3.49) 식의 양변에 A'T 를 좌측에서 곱하고 (3.48) 을 이용하면 다음 결과를 얻는 다. Y' = (A'r•L·A') ·X' = L'·X' (3.50) 이 식으로부터 L 이 대칭 행렬이면 L'은 온사거의 정리를 만족한다. 그러나 일반적으로 선형 독립인 힘과 흐름의 플럭스에 대한 L' 은 대칭 행렬이지만 이때에 L 은 유일한 것이 아니며 대칭 행렬이 될 수도 있 각지각만 반(N드— 시1 ) 그 X 러(N한 ― 것1) 은과 아N니x다N. 의 이행 렬점이을라 생는각 것하에기 유위의해한 L다'. 과 대L칭 이 행렬 L’ 에 대해 (3.50) 식의 L' = A'T•L·A’ 의 관계를 만족시키는 L 의 원의 수 NxN 은 이들을 결정하기 위한 식의 수 (N-1)x (N _1) 보다 크므로 L 이 하나 이상 존재한다. 이 중에는 물론 대칭인 것 이 포함되어 있지만 일반적으로 대칭성이 보장되지는 않는다. 엔트로피 생성 속도가 다음과 같이 표시되는 계를 예로 생각하자. as = X1Y1+X2Y2+X3Y3 (3 . 51) 이 계에서 힘과 흐름의 플럭스가 선형 독립이 아니고 다음 관계를 갖고있다고생각한다. a2x2 + a3x3 = O
Y2+Y3 = 0 (3. 52 ) 이 관계식들을 쓰면 엔트로피 생성 속도는 다음과 같이도 표시된다. as = X1Y1+ (1 + a) X2Y2 = Xi 'Yi '+ X/Y2' (3 . 53) 여기에서 a = a2/a3 이다. 편의상 (l+a)X 2’ 를 힘으로 생각하면 Xi ' = X1 : Xi ' = O+a)X2 = X2 一 x3 Y1' = Y1 ; Y2' = Y2 (3.54) 이다. 또한 A’ 와 B' 는 다음과 갇이 된다. A' = [i —a1 /I:\\+aa:] , B' = [i] ] (3.55) 그리고 독립적인 힘과 흐름의 플럭스에 대해 다음과 같은 선형 현상적 법칙들을쓸수 있다. YI' = Lu'XI' + L12'X2, Y2' = L21'XI'+L22'X2, (3. 56 ) 이 식들에 대해서는온사거의 대칭성 관계가성립하고 L12' = L21’ 이다. 이 관계는 (3 . 50) 식을 쓰면 다음과 같은 Llj 사이의 관계로 표시될 수 있다. L' = A'T·L·A' Ln (L1(21 一+ aaL)1 j) (L21 _ aL31) (L22 _ a (L23 + aL32) + #L33) (l+ a) (l+ a)2 (3 . 57) 따라서 온사거의 관계는 다음 식으로 표시된다.
L21 一 aL3 1 = L12 - a L13 (3.58) 이 식의 특수한 경우로 Lu=L J 1 가 성립할 수는 있지만, 일반적으로 는 Lu 사이에 직접 온사거의 관계가 성립하지 않는다. 6 정리 엔트로피의 생성 속도 6s 는 힘과 이에 해당하는 흐름의 플럭스의 곱 으로 표시된다. 한 흐름은 계에 작용하는 힘들의 선형식으로 표시될 수 있으며 같은 텐서 차수의 힘과 흐름 사이에 연계 관계가 발생한다. 여러 단계의 복잡한 반응 사이의 연계 관계가 가능하고 또한 여러 성 분의 확산과 열흐름 사이에도 연계 관계가 생긴다. 힘과 흐름의 플럭스를 관계시키는 선형 계수들에 부과되는 조건이 두 가지 있다. 하나는 엔트로피의 생성 속도가 0보 다 크거나 같도록 되어야 한다는 것이고 다른 하나는 온사거의 대칭성 관계를 만족시켜 야 한다는 것이다. 힘이나 흐름의 플럭스가 동시에 선형 종속이 되는 경우를 제의하고는 엔트로피의 생성 속도 6s 에서 정의되는 힘과 흐름 의 선형 관계식의 계수들 사이에 온사거의 대칭성 관계가 성립한다. 또한 이 경우에 온사거의 관계가 성립하는 힘과 흐름의 한 세트가 알 려져 있으면 선형 변환에 의해 온사거의 관계가 성립하는 다른 힘과 흐름의 플럭스의 세트를 구할 수 있다. 힘과 흐름이 동시에 선형 종속 인 경우에는 선형계수들 사이에 일반적으로는 온사거의 관계가 성립하 지 않는다.
제 4 장 선형 열역학의 응용 I 서론 3 장에서 도입한 선형 열역학의 방법은 연계된 소산 과정에서 선형현 상적 법칙들을 쓸 수 있게 하고 선형 계수 사이의 부등 관계를 제시한 다. 또한 온사거의 상호 관계는 선형 법칙이 적용되는 영역에서 독립 적인 선형 계수의 수를 줄일 수 있는 방법을 제공하고 있다. 연계된 소산 과정은 여러 책 (예를 들면 Haase, 1969 ; Fit ts, 1962) 에 상세히 취 급되고 있고 여기에서는 이 대표적인 문제들을 예시하는 정도로 만족 하기로 한다. 소산 과정의 연계성은 비평형 통계역학에서 볼츠만 방정 식의 풀이로부터 밀도가 낮은 기체에 대해 유도될 수 있지만 (Chap m an and Cowl ing , 1939) 여기에서 논의하는 것보다 훨씬 복잡한 과정이 요구되며 또한 일반성에 제약을 받는다. 선형 법칙들을 쓰기 위해서 (2.55) 식의 양변에 T 를 곱하고 다시 정 리해서 다음과 같이 쓴다.
Tas= -Jq • VlnT— ~ ~=I J1d lff [T V (µ1/T) -F'』 一p d : \IV +~r=l J 1A1 칙 0 (4. 1) 이 식에서 필요하면 (2. 63) 석에 따라 다른 힘과 흐름을 추가할 수 있다. 이제 큐리의 정리에 따르는 제한 조건하에서 연계된 식들을 쓸 수있다. Y1=~LuXj (4. 2) 여기에서 XJ -i=- 이에 대응하는 Y 가 YI 와 같은 차수의 텐서인 경우 에 한한다. 따라서 (4. 2) 식에서 연계될 수 있는 흐름은 Jq와 J만이 다. 이러한 연계성을 검토하기 위해서는 v (µ1/T) 가 온도, 압력의 영 향을 포함하므로 다음 전개식을 이용해서 (4. 1) 식을 변형시키는 것이 편리하다. v (µ1/T) = v (µ1/T) T.P- h1v ( 1/T) + (vi/ T) vp (4. 3) 여기에서 h~ V 는 각각 부분 질량 엔탈피와 부분 질량 부피이다. 이 식을 (4.1) 식에 대입하고 정리하면 다음 식을 얻는다. T< Js = — (Jq— ~r=l h,J ,d lff ) • vln T -~r=l J,d tr r. [v( µ,)T.P+v,v p- F,] —pd : vV +~r=l J,A , =_Q .VlnT- 모 F=I JId Iff .V (µ!')T_F : vv+ 고晶 JIA I ~o (4. 4) 이 식에서 Q는 물질의 확산에 의해 전달되는 열량이 제의된 전도에 의한 열흐름이고 v (µ1'h 는 정온에서 계산된 확산을 일으키는 힘이며 각각 다음과 같이 정의된다. Q=Jq- ~~l h1J 1d lff (4. 5) \I (µ1') T= \I (µ1) T,P+V1 \Ip— E (4. 6)
(4. 2) 식의 선형 현상 적 계수 들 사이에 온사거 관계 를 적용하기 위해 서는 이 관계가 3 장에서 검토한 바와 같이 힘과 흐름이 모두 선형 종 속인 경우에는 일반적으로 적용될 수 없으므로 적합한 변환에 의해 이 관계가 적용될 수 있도록 할 필요가 있다. 그러나 힘 또는 흐름 중에 서 하나만이 선형 종속인 경우에는 선형 독립인 힘과 흐름에 대해서만 온사거의 관계를 적용할 수도 있지만 그대로도 온사거 관계를 적용할 수 있다는 것 을 3 장에서 보인 바 있다. 온사거의 관계 를 적용하는 데 있어서 또 하나의 문제는 (4. 1) 석에 나타나는 힘 들 이 경험적 선형 법칙들 예를 들면 푸리에의 법칙이나 피 크의 법칙에 나타나는 힘들인 농도 구배나 온도 구배와 다르다는 것이 다. 선형 법칙을 (4.2) 식과 같이 쓰고 온사거 관계를 구체적으로 발견 하는 것은 어렵지 않다. 그러나 이러한 계에 적용되는 경험적으로 편 리한 법칙들이 일반적으로 온사거의 관계를 논의하기에 가장 적합한 형식은 아니므로 적합한 변환이 필요하다. 이 장에서는 이러한 문제점 둘을 구체적인 응용 예를 통해 살펴보기로 한다. 2 화학반응 여기에서는 농도가 균일한 등온계에서 일어나는 화학반응을 생각한 다. 다른 변화가 없을 때에 화학반응에 의한 엔트로피의 생성만을 포 함하는 엔트로피 생성은 (4. 1) 식에 의해 다음과 같이 표시된다. Tcrs=~r=l J 1A1 착) (4. 7) 여기에서 11 는 i번째 화학 반응의 속도이고 A 1 = ―~jl/tj M Jµi는 i번 째 화학반응의 천화력이다. 평형 상태에서는 J 1=A1=0 이 되고 평형 에서 벗어나면 (4. 7) 식이 만족되어야 한다. 평형 근처의 선형 영역에 서 현상적 법칙을 다음과 같이 쓰자.
J 1=~ 晶 LIJA j (4. 8) 이 식은 約 H 의 화학반응으로 구성된 복합 반응에서 J 1 가 AJ (j= l, 2, ……, R) 에 의존함을 표시하고 있다. 복합 반응의 특수한 경우로 i=j일 때만 Lu 가 0 이 아닌 값을 가진다면 이 복합 반응을 구성하고 있는 기초 반응들은 연계된 것이 아니다. 먼저 하나의 반응에 대해 선형 관계를 구해 보자. (n+l) 개의 변수 {x t}의 함수로 표시된 반응 속도를 다음과 같이 표시하자. J=g(X 1, X2, Xa, ……, Xn, Xn+1) (4. 9) 힘 A롤 다음과 같이 {x1} 의 함수로 표시할 수 있으므로 A=h(xi, X2, X3, ……, Xn, Xn+1) (4. 10) 이다. 위의 두 식에서 Xn+l 을 소거해서 다음과 같이 쓸 수 있고 J=f(X 1, X2, X3, ……, xn, A) (4. 11) 이 식에서 A=O 일 때 J =O 이므로 다음 관계식이 성립한다. O=f (X 1, X2, X3, ……, Xn, A=Q ) (4. 12) 평형 상태를 기준으로 속도를 힘에 대해 전개해서 일차항만을 취하 면 J= (at/ a A)A=aA (4. 13) 이다. 이 식은 힘과 흐름(여기에서는 반응 속도)이 선형 관계임을 의미 한다. 그리고 이 식에서 편도함수는 (4.12) 식을 만족하는 일정한 xh X2,x3, …… ,Xn 에서 구한 것이라는 점에 유의하자. 위의 논의는 형식적인 것으로 반응속도식의 구체적인 형태와는 무관 한 것이었다. 이제 하나의 기초 반응에 대해 선형 계수를 계산하는 방 법을 예시해 보자. 화학 퍼텐셜울 이상 용액에 대해 단위 농도 이상 용액의 화학 퍼텐셜 µ10 울 기준으로 해서 (1. 18) 식으로부터 CIo 를 Ei 하고 다음과 같이 표시한다.
µ,=µ1 0+ (RT/M 1)l n(C1 ) (4. 14) 여기에서 C 는 성분 i의 몰농도이다. 그러면 친화력은 다음과 같이 된다. A=-~vj[ M jµJO +RT ln(Cj ) ]=RT In (K/IICji ) (4.15) 여기에서 평형 상수 K는 다음과 같이 정의되고 K=exp (—t::.G o/RT) (4.16) AGo 는 다음과 같이 정의되는 표준 반응 깁스 에너지이다. ~Go=~lliM i µJo (4. 17) 이제 다음과 갇이 표시되는 기초 반응식에 대해 ~f=I l.11 R1 =0 (4.18) 농도의 함수로 표시된 반응속도식이 다음과 같다면 J= J,-Jb = kIIreacta nt C 1111— k'I lpr o ductC i 1 11 =J, (1-K-1II~:J C11 11) (4. 19) 이 식은 (4.15) 식에 의해 다음과 같이 표시된다. J= J r[l 一 exp (— A/RT)] (4. 20) 평형에서의 정반응의 속도를 JfO라 하고 위 식의 우변을 평형 상태 롤 기준으로 A/RT 에 대해 전개하면 A/RT 《 1 일 때 다음 근사식이 성립한다. J=Jro A/RT (4. 21) 따라서 선형 법칙의 속도 상수는 다음과 같게 된다. a=J ro /RT (4. 22)
R 개의 기초 반응으로 구성되는 복합 반응에서는 각 기초 반응을 다 음과같이 표시한다. ~~=I l.11JR 1=0 (j= 1, 2, 3, ……, R) (4. 23) 여기에서 N 은 반응에 참여하는 성분의 수이다. 그러면 하나의 기초 반응에 대해 3 장에서 도입한 미시적 가역성의 원리를 도입해서 다음 식을 쓸 수 있다. 이 원리는 거시적 열역학의 평형 조건에서 유도되지 않는다는 것에 유의할 필요가 있다. J1= Or10/RT) A1 = a1A1 (i= 1, 2, 3, …… , R) (4. 24) 이 식에서 J 1 는 A1 에만 의존하므로 이 수준에서 온사거의 관계를 논 하는 것은 의미 없는 일이다. L 와 A1 가 각각 모두 선형 독립이라면 더 이상 진행시킬 논의는 없다. 이제 R 개의 반응 중에서 r 개만이 선 형 독립인 반응이라고 하면 r
이 식에 의해 행렬 L로부터 온사거의 관계를 논의하기에 적합한 행렬 L'을 얻을수 있다. 다음 반응에 대해 이 결과를 예시해 보자. MLN===MLN AAA2,3= ==µµ µLNMMMMNLM ———µµµMLNM MMMNL =—(A 1十&)(((444... 323901))) 이 반응에서는 흐름과 힘이 모두 선형 독립이 아니고 다음과 같이 쓸수있다. AI+A2+A3=O (4. 32) J,+12+Ja=O (4. 33) 이 식들을 써서 국소 엔트로피의 생성 속도를 표시하면 다음과 같 다. CJs=J,A, +J2A2+J3A3 = (2J,+J2)A,+ (J,+J2)A2 =JI'AI'+L'A2, (4. 34) 이 식으로부터 A, A', J 및 J'을 다음과 같이 정의할 수 있다. A'= [AI',A깁 = [A1,A』
A = [Ai,A2, A3J JJ'= [J1', J리 = [2J1+J2, J1+2J2] JJ = D1, J2, J』(4. 35) 이 그 고러면 昆 힘A=과 / ―흐A 101`름J一 에`L1 대 ,.B해 =r 」 률卜ll1l2I과제3장 ――같。l3/2떼가 험I31/ 14 (용 4· 36) 9L = /a`lo0oo8 `o0 , aJ (4. 37) 그러면 (4. 28) 식을 써서 다음 관계를 얻는다. L'=[ ;: 二:〕: :2 :」 \=[::+a3 : :+a ] (4. 38) (4. 38) 식은 이 경우에 온사거의 관계가 성립함을 확인하고 있지만 새 로운 정보를 제시하지는 못하고 있다. 그리고 만약 L 이 대각선 행렬 이 아니었다고 하더라도 L' 은 온사거의 관계에 의해 대칭 행렬이 된 다. 또한 (4.1) 식에서 다음 부등 관계가 성립한다. a1+a3>Q ; a2+a3>Q ; (a1+a3)(a2+a3)— a1 a3>Q (4.39) 그리고 (4. 35) 식과 (4. 38) 식으로부터 독립적인 힘과 흐름에 대한 선 형 법칙을 다음과 같이 쓸 수 있다. 2J 1+ J 2= (a1+a3)A1+a3A2 J1+ 2J2 = a3A1+ (a 곱 a3)A2 (4. 40) 여기에서 반응 속도 2 J,+J 2 와 J ,+2 J 2 는 각각 J 1- J 3 와 J 2- J 3 로 쓸 수 있는데 이들은 J 3 를 기준으로 한 반응 속도를 나타내고 있다. 이 식들은 또한 힘 A1 과 A 가 0 이 되는 평형에서는 J,=J 2= J a 이고 이 값은 (4.27) 식에 의해 0 이 되어 평형에서 모든 반응들의 속도가 0 이 된다는 것을 의미하고 있다. 3 다성분 등온 등압계내의 확산 엔트로피의 생성을 표시하는 (4.1) 식은 등온 등압의 확산계에서 다
음과 같이 간략히 표시된다. as= (1/T) ~~=l J1d t r r _ [lF'1 -'1 (µ1h pJ (4. 41) 여기에서 J Id1 와 V 는 2 장에서 정의되었다. J전 =P1( V 1- V ) (2. 27) v = 고點 P1V 1 /~~=I Pi (2: 2 4) (2. 27) 식의 확산 흐름이 질량 중심의 속도 V 를 기준으로- 정의되어 있다는 것에 유의할 필요가 있다. 질량 중심의 속도 이의에도 몰 평균 속도, 부피 평균 속도 또는 용매의 속도와 같은 여러 기준 속도에 대 해 확산 속도를 정의하는 것이 가능하지만 먼저 질량 중심 속도를 기 준으로 논의한다. 의력 E 가 없는 계에서 온도와 압력이 일정하면 (4. 4) 식은 다음과 같이 표시된다. Tas= —L}r= I J1 dlrr. V(µ1h ,p (4. 42) 따라서 흐름은 Ji dl 이고 힘은 (VµI)T, p이다. 이 식에서 힘과 흐름 둘아 모두 선형 독립이 아닌 것에 유의하자. (2. 27) 식에서 J전”를 모 든 성분에 대해 합하면 0 이 된다. ~~=l J,d l ff = O (4. 43) 그리고 깁스스유엠식 (1. 43) 으로부터 정온 정압인 경우에 다음 관계 가성립한다. ~r=I P1' v{ µ1h.P=o (4. 44) 이 식에 의하면 N 성분으로 구성된 확산계에서 선형 독립인 힘과 흐 름은 각각 (N-1) 개가 된다. (4. 42) 식을 (4. 44) 식을 이용해서 독립 된 힘과 흐름에 대해 표시하면 다음 식이 된다. T&=-2f=-1 I NJ 1d lff .v'(µ 1h,P (4. 45) 여기에서 N J전”은 성분 N 을 기준으로 한 확산 흐름을 의미하며 다
음과같이 정의된다. N Jt d lff=Jt d lff一 (pl/ PN)J N dlff =p, (V,-VN) (4. 46) 이 식으로부터 하나의 확산 흐름을 서로 독립인 (N - 1) 개의 힘에 대해 표시하면 다음과 같다. N .lf ldl ff=― 2 f갑 Llj'V (µj) T ,P = — Z 冒 L ij '2 麟 µjkV Pk =—~t=l D1k'V Pi< (i= 1,2,… , N— 1)(4.47) 여기에서 DIk'=2f갑 Lu'µJk (4. 48) 또한 (4. 47) 식의 유도에서 다음 관계식을 이용하였다. 'vµj= ~ (aµJ a P i<) 'vPi<= ~µJk 'v Pi< (4. 49) D 퍼, Lu', µ;k 로 구성되는 행렬을 각각 D', L', M이라 하면 (4. 48) 식으로부터 다음 관계식을 얻을 수 있다. L'=D'•M-1 (4. 50) 그러면 L IJ '=L il’의 관계가 성립하므로 확산 계수 사이에 성립하는 대칭성 관계를 유도할 수 있다. 정온 정압의 다성분계에 대한 피크의 법칙은 경험적으로 다음 식과 같이 표시할수 있다. J전= -2f.;-1 1 D1 JV Pi (i= 1, 2, ……, N) (4. 51) 그러나 실험적 확산 계수는 용매 또는 부피 평균 속도를 기준으로 한 확산 속도로부터 더 편리하게 측정될 수 있다. 용매 (성분 N) 의 속 도를 기준으로 한 성분 i의 확산 플럭스 N J전”는 (4. 47) 식으로 표시되 었다. 부피 평균 유속에 대한 확산 플럭스는 다음과 같이 표시될 수 있다.
v J전 = P1 (V 1— Vv) = -~r =-1 1 Du 'vP i (i= 1, 2, ……, N) (4. 52) 여기에서 부피 평균 유속 V v 는 다음과 같이 정의된다. Vv= ~ 1N=1 P1V 1 V1 (4. 53) (4.52) 식의 양변에 v t를 곱하고 i에 관해 합하면 다음 관계식을 얻는 다. ~ ~=I V1 v J전 =O (4. 54) 이 식을 이용해서 확산 계수들 사이의 변환 관계도 유도할 수 있다. NJ / l ff= vJ 1 d1rr_ (p1/ P N ) vJ N dl ff = vJ /1 rr+ (p1 /PN ) ~~갑 (vk/vN) vJ kd l !f = 一 ~f; /[D u + (p1 /PN ) ~~다 Dk t (vk/vN)]VPi =—~f= l DI J' Vp ; (4. 55) 그러면 Du'=Du+ (p 1/P N )~ 訂 Dk/' (vk/v 사 (4. 56) 이다. 이성분계에서 피크의 법칙 (4. 51) 식을 다음과 같이 쓰자. 』 1d I ff= — DIIVPI Jr2d lff := -D22'\ Jfh= —D 2 2 ( oP i/o p 1) VPi (4. 57) 이 식과 (4. 43) 식으로부터 확산 계수 사이에 다음 관계식을 얻는다. D11/D22= 一 (aP i/a p 1 ) (4. 58) 한편 계의 부피에 관한 깁스뮤연]식에서 온도와 압력이 일정하면 d P1 과 dp i7l-서 로 독립적으로 변할 수 없으므로 ~r=l v1dp 1 =0 (4. 59)
이 식을 쓰면 (4. 58) 식은 다음과 같이 된다. D11/D2 2= V1/V2 (4. 60) 이 관계는 온사거의 관계 를 이용하지 않고 얻어진 것이리~ 점을 유 의할 필요가 있다. 그리고 두 성분의 부분 질량 부피가 같지 않으면 두 확산 계수는 같지 않다. 비슷한 계산을 반복히면 부피 평균 속도를 기준으로 한 확산 흐름에서는 두 확산 계수가 같아지는 것을 보일 수 있다. D11/D22= 1 (4. 61) 또는 (4. 56) 식을 이용하면 다음 관계를 얻는다. D11'/D22'= p따/()2 V2 (4. 62) 삼성분계에 대해 온사거 관계를 식으로 표시하기 위해 먼저 (4. 50) 식을다음과같이 쓴다. 亡: ::「鬪::: ::::[: :: 二 丁 =D.-1 問::: 訂µ―2 2::〕 (4. 63) 여기에서 µu=8µ 1 /8 pj이고 A=µIIµ22 ― µ21µ12 이다. 그리고 온사거 의 상호 관계는 다음 식으로 표시된다. µuD1i '+ µ21D2i' = µ12D11'+ µ2 2D 2i ' (4. 64) 만약 경험적 피크의 법칙을 다론 기준에서 정의하였다면 이 표현식 은 달라졌을 것이다. 또한 (4.1) 식으로부터 다음 부등 관계가 성립한 다. Lu'>O ; L2i' >O ; Lu'L22'-L1i' L2 1'>0 (4. 65) 피츠 (F itt s, 1972) 는 NaCl-KCl-H20 계에 대한 확산 실험 결과
(Fuigt aand Gos i t ,ng 1960) X� t����� (4. 64) ��<�\� \������ (Ƭ�p� X� �m�1� �Ĭ� ���� $�( � tǴ���� 1���\�䲔� ��D� �t�� ���. ̹}� (4. 47) � ����� �L�D� ��D� ���t� t �L���
� � ��Y�@� Ż�� �� \����p� Ĭ��@� (Ƭ�p�X� �Ĭ|� `�|� ��x�� XՔ� 8��|� ��� t����. J1dlff = -~f~ 1 LIJ"v�J (i= l, 2, & & , N) (4. 66) t� ��@�( 4. 4)7 ��� � 첬� �� �ȍ�x� � �� �P��ׄ� \� ��t���. ��1� �Ĭ��� ��t � �X��0� �t� ���� ׄPD�� �L�� ��t� ��\X��. X'= ["v�i, "v�0X= ["v�I, "y�2, "y�3] Jdlff'= [NJIdIff,NJ2dIfT = [JIdIff_ aJ3dIff, J�"- az Jp� "T Jdlff = [J1d1rr, J2d1rr, Jp� "T (4. 67) ��0���� al= pJgt��. ���t �(3. 46)�� �(.�3 47) � �< 0 �1\N1�l�(�40.� 6'8)A=\ t ��\.l, Bt'�= A -\1��D��� � U\��x���\0���. A�'\T�" (B4'.= I38 )x� �� �� D���XՌ� �L� Ĭ��D� `� �L1 2 一 L13a2-L32a1 + L32a1a2 = L1 z' - L 23a1- L31a 2+ L33a1a 2 (4. 70) 이 식은 L21=L12, L13 =L 13, L23=L 32 가 성립하기 위한 필요 조전 은 되지만 충분 조건은 되지 않는다. 3 장에서 검토한 바와 같이 선형 종속인 힘과 흐름에 대한 선형 계수인 Lu 는 일반적으로는 온사거 관 계를따르지 않는다. 실제의 다성분계 확산은 훨씬 더 복잡한 문제가 된다. (4. 49) 식으로 표시되는 피크의 법칙보다는 다음과 같이 표시되는 스 테판-맥 스 웰 (S t e fa n ― Maxwell) 식이 기체에 대해 더 적합하다는 것이 알려져 있 다. X1=~i= 1N ( 1/cDu) (x1J 1 — XJ JJ) (4. 71) 이 식에서는 X1 는 몰분율, Jf I 는 몰 플럭스, c 는 총몰농도 그리고 D ij는 2 성분계의 확산 계수이다. 이 식에서 온사거의 관계를 유도하는 것도 가능하다. 또한 다성분계에서 질량 평균 속도 대신 부피 평균이 나 몰 평균 속도가 기준 속도로 많이 사용되고 이러한 계로의 변환도 가능하다. 물질과 열이 같이 전달되는 다성분 계에 대한 스테판_맥스 웰 표현식도 알려져 있다 (St an dart et al, 1979) . 4 다성분 등온계내의 침강과 확산 침강은 중력장 또는 원심력장내에서의 확산으로 생각할 수 있다. 먼 저 비전해질에 대해 중력장의 영향을 생각하기 위해서 E 를 중력 G 로 바꾸고 벌크 흐름과 반응이 없는 등온계에 대해 (4. 4) 식을 쓴다. as=-( l/T)~f= 1 J1 dm·V(µ1'h (4. 72) 한편 (2. 31) 식의 운동량 수지에 의하면 각 성분의 속도가 충분히 작 아 기계적 평형을 가정할 수 있울 때에 다음 식이 성립한다.
I:r=l P1F1-'v P = pG — 'vp= O (4. 73) 이 식은 의력이 작용하면 계내에 압력 구배가 존재함을 의미하며 기 계적 평형인 계에서는 (4. 6) 식의 확산을 일으키는 힘은 다음과 같이 표시되며 'v (µ1') r= 'v (µ1) T,P+v1'v p- G ='v( µ1hp + (V1-p -1 )'v p (4. 74) 여기에서 V1 는 기준 압력에서의 성분 i의 부분질량 부피이다. 중력장 대신에 원심력장도 생각할 수 있다. 이 경우려]는 코리울리의 힘을 무시하면 G 대신에 원심력 硏 R 을 생각하면 된다. 또한 (4. 74) 식 에서 압력 대신 다음과 같이 정의되는 침강 퍼텐셜 ¢룰 사용하기도 한다 . vp= pv ¢ (4. 75) 침강 퍼텐셜울 써서 V(µ 1 'h 를 다시 표시하면 다음 식이 된다. V(µ t ')T=V( 미 T,P+ (V1 p크 )V¢ (4. 76) 등온 침강 평형에서는 힘이 0 이 되어야 하므로 다음 석이 성립한다. (1 一 pV 1 ) y ¢=y (µ1h.P (4. 77) (4.76) 식의 양변에 p I 를 곱하고 모든 성분에 대해 합하면 깁스곡꼭엠 식 (1. 48) 과 (4. 73) 식에 의해 다음 식을 얻는다. 2~=i PIV(µl') T =p G — 'vp= O (4. 78) 이 관계식은 기계적 평형에 있는 계에서는 힘 v (µ1'h 이 서로 선형 독립이 아닌 것을 의미한다. 또한 흐름의 합 ~J전도 0 이므로 흐름 도선형 독립이 아니다. 이제 선형 현상적 법칙을 쓸 수 있다. 기계적 평형에 있지 않는 계 에서는 N 개의 힘이 독립이 되지만 여기에서 생각하는 기계적 평형에
있는 계에서는 선형 독립인 (N 一 1) 개의 흐름에 대해 (4. 72), (4. 74), (4.75) 식으로부터 다음과 같이 쓴다. NJ tdl ff =~~=_i1 Lu[(1 ―p v j )V¢ ― V(µ j )T. 나 (j= l, 2, …… , N-1) (4 . 79) 그러면 Lh=L J로 온사거의 관계가 만족된다. 중력장이나 원심력장에 추가하여 정전기력장도 생각할 수 있다. 정 전 퍼텐셜을
(1- p v l)G= V (µ1) T,P = 2j= I N-Iµ1j v pj (4. 84) 이 식으로부터 VP j를 계산한 후에 이 값들을 (4. 83) 식에 대입하면 t1 를 표현하는 식을 얻을 수 있다. 그 결과는 다음과 같고 t1= (p 1µ)-l~~ 갑 µkD1/' (4. 85) 여기에서 µ와 µk 는 다음과 같이 주어진다. µ= [
= -O·VlnT— ~ I=! N J1 dl ff. '\ J( µ1' ) T (4. 87) 이 식으로부터 Ji dl ff와 Q(=JJQ -~h1 JJ전)는 VlnT, V(µI)T,p , v p 그리고 E 에 의존함을 알 수 있다. 또는 다음과 같이 흐름을 표시 할수도 있다. J전= JId l f f(D )+ JId l f f( P) + JId l f f(F) + JId l FF (T) (4. 88) Q=Jq(C )+J q(P )+J q(F )+J q (D ) = Jq< Cl+ Jq(D u fou r) (4. 89) (4. 89) (4, 88) 식에서 Jidl ff( D)' J1 dlff (P ), Jidl ff (F > , Ji d l ff (T ) 는 각각 V (µ1) T,P, 'vp, Fi , 그리고 'v lnT 에 의존하며 보통 확산, 압력 확산, 강제 확산, 그리고 열확산이라 불린다. (4. 77) 식에서 전도에 의한 열 의 흐름은 lnT 에 의존하는 Jq(C ) 그리고 '\l (µ1h ,P, 'vp, F 에 의존하 는 J /Du f our) 의 합으로 표시된다. 온도 구배에 따르는 물질의 열확산 현상을 소레이 (Soret) 효과, '\l(µ 1h ,P, 'vp, F1 에 의존하는 열의 흐 름을 두푸르 (Dufo u r) 효과라 부른다. J i dl ff (D) 는 피크의 확산 법 칙으로 그리고 Jq (C) 는 푸리에의 전도 법칙으로 경험적으로 주어진다. 다성분 계에서 두푸르 효과를 제의한 다론 플럭스에 관한 경험적 표현식들은 예를 들면 버드 등의 책 (Bi rd , St ua rt and Ligh t foo t, 1960) 에 소개되어 있으나 여기에서는 취급하지 않고 온사거의 관계와 관련된 검토로 넘 어가기로한다. (4. 87) 식에서 확산과 관련된 힘과 흐름을 살펴보자. (4. 4 3) 식에서 ~J 1dl ff =O 이고 (4. 73) 식으로부터 기계적 평형에 있는 계에서는 ~Pl V(µl')T=0 이므로 힘과 흐름이 모두 독립적인 양들이 아니다. 따라서 독립적인 선형식들은 다음과 같이 쓸 수 있고 O=-L qq'v lnT 一Z 麟? Lq 1'v (µ1' ) T N J전=― L1 q'v lnT-~ f다 LI J'v(µi'h (i=1 ,2,… … N-1) (4.90) 여기에서 V(µ ! \는 (4. 6) 식으로 주어진다. (4. 6) 식을 이용해서 위
의 두번째 석을 다음과 같 이 다시 쓴 다. NJ1d 1 rr= -L,q' v ln T— z: ? 각 Di jv Pj _2JN= -I I L I[ vlvp -F 』 (i=1,2 ,… … N-1) (4. 91) 여기에서 D u = :E 麟 L,k µ k j (4. 92) 이다. (4. 91) 식은 열확산 계수 D1, 열확산 비 Kk, 소레이 계수 Sk 등 을 다음과 같 아 정의하여 다시 쓸 수 있다. D1 =L 1q / p1 T (4. 93) Spk 1 =D1 —= K~k 麟/P kK k D lk ((44.. 9954)) 그러면 N J I d i =一 2 冒 D1i ( VPi -pls iV T) - ~ 冒 Lu[v 1 V p -F 』 (4. 96) 이다. 의력이 없고 압력이 일정한 경우에 확산 흐름이 없으면 위의 식 으로부터 소레이 계수를 다음 식으로 표시할 수 있다. Sj= dlnp j/d T (4. 97) 열의 흐름을 생각하기 위해 의력이 없고 압력이 균일한 경우에 대해 (4.90) 식의 첫째 식을 다음과 같이 쓴다. Q = -xVT-~ ~갑 DIT vp I (4. 98) 여기에서 열전도도 x 와 D 1 T 는 현상적 계수들과 다음과 같은 관계가 있다. x=Lqq / T (4. 99) D1T= ~腐 Lq jµJt (4.100)
이제 일정한 온도 구배가 경계 조건에 의해 유지되는 경우 를 생각하 자. 의부로부터의 물질의 출입이 없다면 시간이 충분히 흐른 후에 정 상 상태에 도달하고 질량의 확산 흐름이 없게 된다. 그러면 농도 구배 와 온도 구배는 (4. 97) 식에 의해 연관된다. 이 조건에서 (4. 98) 식을 다시쓴다. Q=— (K+~~국 ! D?s1p 1) '\ IT (4. 101) 이 식은 열전도도가 초기의 전 l 서 시간이 지나면서 감소한다는- 것 을 의미하며 온사거의 관계와는 관계없이 얻어지는 결과이다. 이성분 계에서는 (4. 93) 식과 (4. 100) 식을 쓰고 온사거 관계를 적용하면 다음 관계를얻는다. P1D1T=L1q = Lq1 =D1T/µII (4. 102) 이 관계를 이용해서 (4.101) 식을 이성분계에 대해 다시 쓴다. Q=— (x+D1P12S1Tµ11)'v T (4. 103) 여기에서 -P1S1Tµ11 는 전달의 열 (Hea t o f Trans p or t)이라 불리기 도한다. 소레이 계수가 0 이 아니면 (4.96) 식에 의해 온도 구배가 물질의 확 산을 일으키는 힘이 된다는 것을 알 수 있다. (4. 103) 식에 의해 소레 이 계수가 열전도도에 미치는 영향은 두푸르 효과를 반영하고 있으므 로 이를 검토하면 온사거의 관계를 확인할 수 있다. 여러 기체 혼합물 과 액체 혼합물 및 전해질 수용액에서 소레이 계수가 실험적으로 결정 되었고 하세의 책 (Haase, 1969) 에 검토되어 있다. 또한 이로부터 전 달의 열이 계산될 수 있지만 실험적인 어려움 때문에 전달의 열이 직 접 측정되지는 못하였다.
6 열전 효과 도체내에 온도 구배와 정전 퍼텐셜이 존재하는 경우를 생각하자. 이 문제를 일반적으로 검토하기 위하여 이 계에 대한 엔트로피의 생성을 (4.4) 식에 따라 표시한다. 그러면 T6s= —Q.vln T— 고 r= I JId Iff .V (µtEC ’) T (4. 104) 이다. 이 식에서 µ1EC’ 는 등온에서의 전기화학 퍼텐셜을 의미하며 장 의 세기가 F 인 전기력장에서 (4. 6) 식으로부터 다음 식으로 주어지고, VµIEC'=V(µi) T,P+vlvp _ zIE =V (µ,)T,p+ v,Vp + Z,Vrp (4. 105) 여기에서 µ1EC’ 은 µ1’ 과 유사하지만 성분 i에 작용하는 의력이 정전 기력으로 대치되어 있다. 또는 針三 정전 퍼텐셜이고 Z1=z1F/M1 (4. 106) 이다. ZI 는 성분 i의 단위 질량 당의 전하이고 전하수 z1 에 파라데이 상수 F 를 곱하고 분자량 M 로 나눈 값이다. z1 값은 전자에 대해 음의 부호를 갖는다. 이제 압력과 전자의 밀도가 균일하고 생각하면 (4. 104) 식은 디움과 같이 된다. To ;;= -Q•'v lnT-Je d l ff•Z e'v
만약 전자의 확산에 관한 힘과 흐름을 각각 J edI f『와 Ze 'vrp으로 생각 한다면 다음 식들을 얻는다. Q = —L q q 'V lnT —L q e 'Zev rp (4. 110) I = 一 Le/Zev InT-Le e 'Ze2v cp (4. 111 ) 그리고 온사거의 상호 관계는 힘과 흐름을 나누는 방법에 상관 없이 다음식이 된다. Le/Ze= Leq = Lq e = Lq e 'Ze (4. 112) 또한 푸리에의 열전도 법칙 (Q =_XVT) 과 움의 전기전도 법칙 (I= 一 aZe2V rp)을 기본으로 다음과 같이 연계된 선형 법칙을 쓰면 Q= _xvT— f]'Z e2\1 rp= -xT\1 l nT— B 'Ze2Vr p (4.ll3) I=_BVT— aZe2Vr p= -BTVlnT_aZe2Vr p (4.1l4) 이다. 따라서 온사거의 관계는 위의 식들과 비교할 때에 다음과 같이 표시된다. BT=B'Ze2 (4. 115) 전류 밀도가 0 이지만 온도 구배가 유지되고 있어서 열이 흐르고 있 는 일차원의 정상 상태를 생각하자. 그러면 (4. 109) 식에서 A< p/A T= —L eq / (LeeT) (4. 116) 이다. 이 식은 온도 구배가 존재하면 퍼텐셜의 차가 생성된다는 것을 의미하고 있으며 이때에 발생한 정전 퍼텐셜울 열전 퍼텐셜 (Thermoelectr i c Pote n ti al) 이라 부른다. 이 현상은 금속 A 와 B 가 연 결되어 있고, A 중간에 이상적 축전기 C 가 설치되어 있는 간단한 열 전대 (Thermocou p le) 에서 관찰된다. A 와 B 의 두 점점을 서로 다른 온도로 유지하면 전류의 흐름을 일으킬 수 있는 퍼텐셜이 발생한다. 이 현상은 시벡 (seebeck) 효과로 알려져 있다. 반면에 (4.108) 식과 (4. 109) 식에서 온도 구배가 0 인 경우에는 디음
과 같이 펠티에 계수 Il7} 정의된다. Il = Q/ Il = Lqe /L ee (4. 117) 이 식은 온도 구배가 없더라도 정전 퍼텐셜의 구배가 존재하면 열의 흐름이 있다는 것을 의미하고 있다. 또한 이러한 현상은 펠티에 효과 (Pelti er E ff ec t)로 알려져 있으며 1824 년 펠티에가 발견하였다. 한편 (4. 116) 식 , (4.117) 식 및 온사거의 관계식을 이용하띤 다음 관 계식 을 얻는다. D.
경험적 현상적 법칙들은 엔트로피의 생성속도에서부터 도출된 선형 관계와 다른 형식으로 표현되는 경우가 많다. 이러한 경우에는 적합한 변환에 의해 두 식을 비교하고 온사거의 관계 를 적용한다.
제 5 장 진화와 안정성 I 서론 지금까지 우리는 평형과 평형 근처에서의 거동을 살펴보았다. 평형 상태는 고립계에서는 엔트로피가 더 이상 증가될 수 없는 상태이다. 이미 알고 있는 바와 같이 고립계의 전화 조건은 dS>O 이며, 여기에 대응하는 평형 상태의 평형 조건은 dS=O 이고 안정성 조건은 교란에 대해 t::,. S
피의 생성 속도 P[8S] 를 정의할 수 있고 안정성의 판별에 이용할 수 있다. 힘과 흐름이 선형 관계를 갖고 온사거의 관계가 성립하는 평형 근처의 상태에서는 기준 상태로 평형 상태를 선택할 수 있다. 그러면 과잉 엔트로피의 생성 속도는 엔트로피의 생성 속도 P[ 히가 된다. 선 형 열역학의 영역에서 계는 경계 조건이 허락한다면 평형 상태를 향해 서 진화하거나 또는 비평형 정상 상태를 향하여 진화한다. 이때의 전 화는 계의 엔트로피의 생성 속도가 감소하는 방향이라는 것을 알게 될 것이다 . 진화가 끝나면 엔트로피의 생성 속도는 상수가 된다. 평형 상 태에 도달할 수 있으면 P 〔히= 0 이 되고 경계 조건에 따라 비평형 정 상 상태에 도달할 수 있으면 이때에는 P[S] 가 0 보다 큰 최소값을 갖 게 된다. 평형 근처의 선형 열역학의 영역은 열역학적 가지라고도 불 리는데 여기에서는 계가 엔트로피의 생성 속도를 증가시키는 요동에 대하여 안정하다. 평형 근처에서는 엔트로피의 생성 속도가 전화의 기 준이 될 수 있지만 평형에서 멀리 떨어지면 임의의 상태를 기준으로 한 과잉 엔트로피의 생성 속도가 안정성의 판별 기준아 될 수 있다. 이 기준은 제한된 경우에는 직접 적용될 수도 있지만 선형화된 계에 대해 혼합 과잉 엔트로피의 생성 속도를 계산하는 방법으로 적용될 수 도있다. 작은 요동에 대한 비평형 계의 안정성 논의는 선형화된 계를 대상으 로 논의할 수 있다. 선형화된 계에 대한 정규모드 해석이 이 방법의 대표적 방법이 된다. 그러나 정규모드에 근거한 열역학적 방법도 가능 하다. 위에서 언급한 과잉 혼합 엔트로피의 생성 속도를 이용하는 방 법은 과잉 엔트로피의 생성 속도와 정규 모드의 거동을 근거로 발전되 었다. 과잉 혼합 엔트로피롤 이용하는 방법은 정규 모드의 개념을 이 용하고 있지만 고유치를 구하지 않고 적용될 수 있다. 이 방법들에 의 해 안정성을 논할 수 있고 기준 상태로부터 요동에 의해 생성될 수 있 는 시간적 구조를 판정할 수 있는 방법을 검토할 것이다 . 작은 요동에 대해 안정한 계가 큰 교란에 대해서도 항상 안정한 것 은 아니다. 교란에 대한 안정성을 포함한 비평형 계의 일반적 안정성
의 논의는 열역학적으로 어려운 문제이다. 리아푸노프의 방법으로 알 려진 동역학의 일반적 안정성 판정 방법이 존재하지만 이 방법에 근거 한 안정성의 해석은 특수한 경우에만 단순한 방법이 된다. 동역학 퍼 텐셜을 이용하는 방법이 예가 된다. 열역학적으로는 프리고진 등이 제 시한 일반적 진화의 법칙에 근거한 해석이 가능하다. 평형에서 멀리 떨어진 영역을 포함한 일반적인 계의 전화를 규정하는 법칙울 발견할 수는 있지만 어떤 일반적 퍼텐셜 함수를 써서 진화를 기술할 수 없다 는 것 을 알게 될 것이다. 따라서 비평형 상태의 안정성 논의는 열역학 적으 로 어려운 문제가 된다. 이 장에서는 일반적 진화의 법칙을 제시 하고 이 를 근거로 한 두 가지 방법 즉 운동론적 퍼텐셜 (K i ne ti c Pote n - ti al) 을 이용하는 방법과 국소 퍼텐셜을 이용하는 방법을 논의한다. 운 동론적 퍼텐셜은 독립변수가 하나일 때에 유용하다. 국소 퍼텐셜은 한 계 안정성 조건을 계산할 수 있는 방법에 적용될 수 있다. 안정성 논의를 위해 퍼텐셜 함수들을 쓰는 방법을 일반적으로 열역 학적 방법이라 부르기로 한다. 평형 열역학의 엔트로피, 내부 에너 지, 엔탈피, 헬름홀츠 에너지, 깁스 에너지 등은 적합한 경계 조건에 서 진화물 기술하는 퍼텐셜 함수의 예가 된다. 평형 근처에서의 엔트 로피 생성 속도나 평형에서 멀리 떨어전 영역에서의 과잉 엔트로피의 생성 속도는 퍼텐셜 함수의 다른 예가 된다. 주어전 경계조건에서 전 화의 법칙은 퍼텐셜 함수의 단순 증가 또는 단순 감소로 표시된다. 반 면에 요동의 시간에 따르는 거동을 해석해서 안정성을 판별하는 방법 을 동역학적 방법이라 부르기로 한다. 계의 교란에 대한 안정성은 일반적으로 교란의 크기에 의존한다.우 리는 성질 A의 작은 교란을 요동이라 부르고 oA 로 표시하며 큰 교란 울 교란이라 부르고 AA 로 표시하기로 한다. 요동은 2 차항 이상의 영 향을 무시할 수 있는 교란을 의미하기로 한다. 요동에 대한 안정성은 안정성을 검토하고자 하는 계의 동역학을 선형화해서 취급할 수 있고 이러한 방법은 선형 안정성 이론으로 불린다. 이러한 검토 방법은 평 형계, 선형 열역학계 또는 평형에서 멀리 떨어진 계를 대상으로 할 수
있다. 그러나 교란에 의한 안정성은 선형화된 계를 대상으로 판정할 수 없고 일반적으로 비선형 안정성 이론으로 취급된다. 선형 열역학은 힘과 흐름 사이에 선형 관계를 가정할 수 있는 경우에 적용되고 따라 서 선형 열역학의 영역과 선형 안정성 이론의 영역은 별개이다. 선형 열역학의 범위를 벗어나더라도 요동에 대한 안정성은 선형 안정성 이 론으로 검토될 수 있다. 비선형계를 포함한 이들 문제들을 일반적으로 취급하기 위하여 동역학계의 일반적 안정정 이론을 다음 절에서 도입 한다. 평형 상태에서 멀리 떨어진 비평형 정상 상태는 요동에 대해 불안정 해지면서 다른 안정한 정상 상태에 도달할 수 있다. 또한 평형에서 멀 리 떨어진 정상 상태는 공간적 또는 시간적 질서를 유지할 수 있다. 이러한 질서는 소산 구조라 불리며 다음 장에서부터 논하게 된다. 2 안정성 이론 리아푸노프의 제이 방법으로 알려진 안정성 판별법은 여러 책에 기 술되어 있으며 여기에서는 노프스와 윌크스 (Kno p s and W ilk es, 1973) 에 따라 개략적으로 기술하기로 한다. 다음 미분 방정식으로 표시되는 동역학계를생각하자. dX/dt= F (X, t) (5. 1) 여기에서 X 는 이 미분 방정식에 의해 적당한 초기 조건 및 경계 조 건과 함께 주어졌다고 생각한다. X1 에 해당하는 해를 ({)1(t o, t)= ({)1 (t。+t)라 하면 ({)1 는 실수 t를 X 로 사상하는 함수의 집합{cp}의 원소 가 된다. 안정성을 논의하기 위하여 메트릭이 정의될 수 있는 함수공 간 {rp}에서 다음과 같은 성질을 갖는 메트릭 p(안 %)을 정의하자.
p(rp1, rpz ) =O rp1 = ({J z 일 때에 한해 (5. 2) p(안%) ~o (5.3) p(안 rp,z)=p(rpz, rp1 ) (5.4) p(안 作)::;;;p(안 %)+P((/> 3, rp,z) (5.5) 또한 같은 함수 공간 {rp}에 속하는 임의의 함수 ¢에 대해 硏구위의 반경 r 인 근방 혀 E 다음과 같이 정의하자. S(rp , r) ={p(¢, rp)
상태의 해가 될 수 있으므로- 이러한 상태 를 기준으로 한 요동에 대해 계가 안정할 것인가 하는 문제도 리아푸노프 함수 를 발견할 수 있으면 리아푸노프 정리에 의해 판별될 수 있다. 이때에 (5. 9) 식은 요동에 대 한 제한조건을 그리고 (5.10) 식은 전화의 법칙을 의미하게 된다. X 가 시간 t에 직접적으로 의존하지는 않는 경우에 (5. 1) 식은 다음 과같이쓸수있다. d:X / dt= F (X ) (5. 11) 이 석의 특수한 경우로 다음과 같은 선형계를 생각하자. dX/dt= A • X. (5. 12) 이 계에 대하여 리아푸노프. 함수를 디음과 같이 정의할 수 있다. = X ·Q ·X (5. 13) 呼 임 의의 0 보다 큰 (Posit ive Defi ni t e) 행 렬 Q에 대해 항상 0 보다 크게 된다. 그리고 O 의 도함수는 다음과 같이 계산된다. dcI> / dt= (dX/dt) • Q • X+X • Q • (dX / dt) =X • (A • Q+ Q • A) • X (5. 14) >O 이므로 선형계의 안정성은 다음 조건에서 보장된다. d / dt< O (5. 15) 이 조건은 행 렬 (A • Q+ Q • A) 이 0 보다 작을 (Neg a ti ve Defi ni t e) 것을 요구한다. 그리고 이 조건은 행렬 A 의 성질에서 결정된다. 이제 일반적 경우인 (5.11) 식에 대해 동역학 퍼텐셜 (D y nam ic Pote n ti al ) 함수 ®를 다음과 같이 정의할 수 있다고 가정해 본다. 동 역학 퍼텐셜은 일반적으로 쓰이는 용어는 아니고 이 책에서는 5. 5 절 에서 논의되는 운동론적 퍼텐셜 (Ki ne ti c Po t en ti al) 과 구별하기 위해서 쓴다. 운동론적 퍼텐셜은 프리고진 그룹에서 쓰고 있는 용어이다.
'\!= —F (5. 16) 그러면 퍼텐셜 ®의 시간에 대한 도함수는 다음과 같이 된다. d / dt = 'v • dX /dt = -F • F ~ O (5. 17) 이 식에서 등호는 X = O 일 때만 성립한다. 그리고 시간에 따라 변하 지 않는 기준 상태가 안정하기 위해서는 (5.17) 석이 항상 성립하므로 디옴 식의 성립만이 요구된다. A 中 츠 0 (5. 18) 리아프노프 함수 를 발견하는 한 방법은 이상에서 논의한 바와 같이 적합한 퍼텐셜 함수 를 발견하는 것이다. 그러나 일반적으로 (5.16) 식 으로 정의되는 퍼텐셜 함수의 존재는 종속 변수가 하나인 경우를- 제의 하고는 보장되지 않는다. 벡터 해석에 의하면 (5.16) 식은 d 룰 다음 과 같이 전미분으로 표시할 수 있다는 것을 의미한다. def >= -lF • dX (5. 19) 리아푸노프 함수는 일반적으로- 유일한 것이 아니며 또한 안정성의 충분 조건을 제시한다는 것에 유의할 필요가 있다. 3 평형 상태의 안정성 고전 열역학의 안정성 이론은 단열된 닫힌계에서 엔트로피는 증가하 고 더 이상 증가할 수 없는 상태가 안정한 평형상태가 된다~ 것이다. oS=O 인 상태가 일반적으로는 안정한 상태가 아니라는 것은 다음 해 석에 의해 알게 될 것이다. 평형 상태의 안정성에 대한 수학적 표현은 S>O 인 엔트로피에 대해 다음과 같다. oS=O, t::.S
여기에서 A 없즌 평형 상태로부터의 교란을 의미한다. b,. S < 0 가 의 미하는 바를 살펴보기 위해 단위 부피당의 엔트로피 p s=S/V 를 생각 하자. 그러면 임의의 부피에 의해 b,. S= Jb,.(p s)dV 이므로 AS < 岭근 A( p s) <어 의미하고 또한 v8 p s=8s 이므로 b,. s < O 임을 인정할 수 있 다. 그리고 8S= 岭근 os= 어十 의미한다.따라서 6.s = os+ (1/2) 성 s+ …… = (1/2) 성 ~ < O (5. 21) 이 식은 평형 상태에서 일어나는 엔트로피의 국소 요동에 대한 제한 조건이다. 정효] 표현식을 구해 보자. (1. 23) 식에서 os= (1/T) ou+ (p/ T) ov— ~f = I ( µ1/T) ow, (5. 22) 독립 변수에 대한 이차 미분은 0 이 되므로 정 u= 정 v= 정 w i =0 이다. 그러므로 성 s= o (l/T) ou+ o (p/ T) av- L !f=l o (µ,/ T ) ow, =-(1 /T)[(cv/ T ) (0T)2+ (p /x이 (ov)2 +L!t=lN L!J= lN µIi OW10W 』 (5. 23) 이다. 이 식의 유도는 o(µ , /T) 를 o(l/T) 과 o(p / T) 및 ow 에 관해 서 전개한 후 열역학의 항등식들을 사용해서 얻어전다. 이 식에 안정 성 조건 (5. 21) 식을 적용하면 다음 결과들을 얻는다. Cv> O, XT= - (小 /8 p) T,c/v> 0; 2:f=I z:f= I µIJ 8w1 8Wl>0 (5. 24) 죽 oS=O 인 상태라고 해도 (5. 21) 식의 조건이 만족되지 않으면, 구 체적으로는 (5.24) 식의 조건들이 만족되지 않으면 계는 불안정하다. (5. 24) 식의 마지막 조건은 쌍이차 형식이 항상 0 보다 클 조건이고 3 장 에서 논의된 바 있다. 이 조건은 구체적으로 아래 (5. 72) 식으로 주어 전다. 독립 변수로 u, v, w, (i= l, 2, ……, N) 대신에 pu , pw , (i= 1, 2,
……, N) 을 변수로 택할 수도 있다. 후자는 단위 부피당의 성질을 나 타내고 전자는 단위 질량당의 성질을 나타낸다. 단위 부피당의 성질에 대해서 기본 방정식은 (1. 24) 식에서 다음과 같다. 8ps = (1/T) 8pu -~r=18(µ1/T) 8p1 (5. 25) 따라서 (5. 22) 식을 얻을 때와 같은 방법으로 (5. 22) 식 대신 다음 식을얻는다. 청p s= o (l/T ) op u 一 ~~=I o (µi/T ) OPt (5. 26) 깁스스유엠식 (1. 46), (5. 23) 식 및 (5. 26) 식에서 p성 S= 성(p s) 인 것을 보일 수 있고 따라서 (5, 26) 식에 의해서도 (5. 24) 식과 같은 결과 를보일수있다. 이 안정성 이론을 위에서 정리한 리아푸노프의 정리에 따라 다시 구 성해 보자. 평형 상태의 값을 기준으로- 한 -AS 를 리아푸노프의 함수 로 택한다떤 안정성 조건은 (5.9) 식과 (5.10) 석으로부터 다음과 같이 생각할수 있다. AS 三 0, 8AS/8t= 8S/ 0t 느 0 (5. 27) 이 식은 엔트로피가 평형에서 최대가 되어야 하므로 요동에 대해 앞 의 관계가 성립하고 뒤의 관계로 표시된 전화의 법칙에 따라 계는 평 형 상태로 되돌아간다는 것을 의미한다. 제이 법칙은 실제로 (5.27) 식 을 만족하는 리아푸노프 함수로 엔트로피의 차를 정의할 수 있다는 의 의를 갖는다. (5.27) 식의 둘째 조건을 (2.58) 식에 따라 다시 써보면 8S/8 t =P[ 히 +~[S J ~O (5. 28) 이다. 여기에서 P 固=J asdV (5. 29) ~[SJ =—JJs ·d§ (5. 30) 이다. 또한 dS 는 2 장에서와 같이 Nd~ 춘 의미하며 N 은 dS 에 밖으
로 수직인 단위 벡터이다. 이제 앤트로피를 평형 상태의 값을 기준으 로 전개하면 다음 식이 되고 S=S 。+ oS+ (1/ 2) 청 S+ …… (5. 31) 따라서 다음식을쓸수있다. as;at= aos/at + (1/2) a 성 S/a t (5. 32) 흐름항을 다음과 같이 일차항과 이차항으로 나누어 표시하고 2 [S] = 2(I)[ 언 + ~(2)[S ] (5. 33) (2. 53) 식과 (2. 57) 식을 결합하면 다음 식을 쓸 수 있으므로 Js = ps V+J q/ T— ~ f=I µ1J 1 dlff /T (5. 34) 짝히는 (5. 30) 식의 정의에 따라 다음과 같이 표시된다. ~[S]=— J(ps V+J q/ T— xr=l µIJ I dl/T) ·dS (5. 35) T_1 과 µT-1 을 평형값을 기준으로 표시하면 다음과 같고 T-1= (T-1) 。+t::. (T-1) (5. 36) µT-1= (µT-I) 。+!:::. (µT-1) (5. 37) 따라서 V=O 인 닫힌계에 대해서는 합 !)[S]= f(Jq /T 。―:EN =! J ,d lff (µ,/T) 。) ·dS (5. 38) ~(2) [히=J(Jq /A(T-1)-l=~l J,d t rft::.( µ,/T)) ·dS (5. 39) 이다. (T 기려 (µT 기제 해당하는 엔트로피의 생성 속도는 0 이다. 그러므로 P[ 히는 이차항이 된다. (5. 32) 식의 일차항과 이차항을 정리 하면다음과같다. aos/ 洪 =Z(1)[S 〕 (5. 40) (1/2) a 성 S/ at= P[S 狂 ~(2l[SJ (5. 41)
(5. 40) 식 을 적분 형 식 으로 쓰면 8S = J2 (I)[ S ] d t (5. 42) 고립계의 평형 상태 또는 계의 엔트로피의 요동이 엔트로피의 흐름 에 의해 상쇄되는 계에서는 고 ( 1 )[S]=0 이므로 oS=O 이 되어 깁스의 평형 조건 을 다시 얻게 된다. 또한 이 경우에 (5. 32) 식은 다음과 같이 표시된다. as; a t= (1/ 2) a 성 S / a t = P[S 狂 2 (2) [S 〕 20 (5. 43) J q와 Jidl 또 는 t:,. (1 / T) 와 t:,. (µ 1/ T) 이 0 이 되어 ~( 2) 〔히 = 0 이거나 요동의 시간 척도보다 큰 시간 척도에 대해 J ~<2>[S]d t =O 이 되면 이 식은 P 隣 〕 2 0 이 된다. 그리고 (5. 43) 식을 적분하면 AS 에 관한 안정 성 조전을 얻을 수 있다. A 없근 평형 상태를 기준으로 한 교란을 의미 하므로 계가 안정하다면 복원 과정에서의 엔트로피 변화와 AS 의 합이 0 이 되어야 한다. 따라서 A 없즌 엔트로피의 생성 속도를 진행하는 시 간 방향에 대해 적분한 값과 반대의 부호를 갖게 된다. AS= —J P [S] dt = - (1/2) 정 S :s: o (5. 44) 이 식의 국소형식은 (5. 21) 식과 동일하므로 이상에서 우리는 깁스의 안정성 이론과 리아푸노프의 방법에서 같은 결과를- 얻는다는 것울 확 인한다. 그리고 (5. 4 3) 식에서 엔트로피의 생성속도 P[ 언가 안정성 판 정기준이 될 수 있다는 것을 알수 있다. 4 비평형 열역학계의 안정성 앞절에서 검토한 안정성 이론울 비평형 상태로 확장하기 위해서는 국소 평형의 가정과 리아푸노프 함수의 개념을 이용한다. 평형에서 떨 어져 있는 계를 기준 상태로 택하면 oS 가 0 이 되지 않으므로 as/ 承를
(5. 40) 식아나 (5. 41) 식과 같이 나누어 쓸 수 없다. 따라서 (5. 44) 식도 성립되지 않는다. 비평형 상태의 안정성은 국소 평형 상태의 안정성 조건에서 시작한다. V =O 인 순수한 소산계를 생각하면 이러한 계의 어떤 비평형 상태가 안정하기 위해서는 국소 평형 상태가 안정해야 한 다. 국소 평형 상태 안정성의 필요 조건은 평형계의 국소 평형 조전과 같아야 할 것이므로 평형계에 대한 디옴- 식에서 시작한다. t::.S = (1/2) 성 S= (1/2) J 82 p sdV 악) (5. 45) 이 관계가 임의의 부피 요소에 대해 성립해야 한다. 따라서 성p s~O (5. 46) 총 엔트로피를 이용한 평형 상태의 판정 기준은 단열된 닫힌계에 대 한 것이지만 국소 평형인 부피 요소는 열린계이다. (5.46) 식은 이러한 열린계에 대한 관계식인 것에 유의해야 한다. 우리의 비평형 계에 대 한 기술은 국소 평형인 계에 대한 것이므로 이 관계식은 국소 평형인 비평형계의 부피 요소에 대해서도 조건 없이 적용되어야 한다. 또한 p가 항상 0 보다 크고 p샹 s= 성(p s) 이므로 다음 식도 성립한다. 성 s~O (5. 47) 이 식은 (5. 21) 식과 동일하다. 그리고 이 식의 구체적 의미는 평형 계에서와 같이 (5 . 23) 식으로 주어전다. 이제 기준 바평형 상태가 안정 하다면 항상 0보 다 작은 (Ne g a ti ve Defi ni t e) 함수 o2p S 또는 장 s를 리아푸노프 함수로 볼 수 있을 때 ao2p s /at ~O (5. 48) 또는 a 성 s/ at ~O (5. 49) 의 관계식이 성립해야 한다. (5. 49) 식의 표현식은 (5. 23) 식을 시간에 대해 편미분해서 얻을 수 있다.
(1/ 2) 8 성 s / a t = - (cv /T ) oT aoTI at— (p / x 깁 ov aov/ a t - ~ ~= I ~ 7= t µuOW t aow 』 /a t =0 (1/T) (aou/ a t)+ o (p / T ) (aov/at) —~~= ! ~f= l O(µ1/T) (aowdat) (5. 50) 한편 (5. 23) 식에서 (5. 50) 식을 얻는 것과 같은 방법으로 (5. 48) 식의 편도함수를 표시할 수도 있다. (1/2) ao2 p s /at= 0 (1/T) a(op u) /at •- ~~=I 0 (µ1/T) a(op w 1) /햐 (5. 51) (5. 50) 식 또는 (5. 51) 식에 해당하는 과잉수지식들을 계산해서 정리 하여 (5. 48) 식 또는 (5. 49) 식의 구체적인 표현식을 얻을 수 있지만 더 직접적인 방법은 (2.52) 식에서 유도될 수 있는 다음의 과잉 엔트로피 수지식을 이용하는 것이며 ao2p s /at= -'v • (장 L) ) + as (as) (5. 52) 여기에서 과잉 엔트로피 흐름 성J s 은 (2. 57) 식에서 V=O 인 경우에 다 음과같고 정J s= oJ qo (l/T) — o (µi/T ) 0J 1d 1f f (5. 53) 그리고 과잉 엔트로피 생성 속도는 다음 식으로 표시된다. as (os) = ~0X10Y1 (5. 54) (5. 52) 식을 계의 부피에 관해 적분하면 다음에 주어전 전체 안정성 기준에 도달하고 정 s;a t =P[o 히=f dV~oX10Y1 책 (5.55) 이 식에서 계면에서의 요동은 억제되어 고정된 경계 조건이 적용된다 고 가정하였다. 계면에서 요동이 억제될 수 없는 경우에는 (5. 52) 식의
발산항의 부피에 관한 적분이 0 보다 커야 한다는 조건이 추가된다. -f'v· (청Js)dV= J ( - o Jq o(l/T)+~~= l o(µ,/T) o J전) ·d§ 착) (5. 56) 과잉 힘과 과잉 흐름은 예를 들면 XIo 를 기준으로 8X i = Xl-X i 0 등 과 같이 표시되어 있다. (5. 46) 식과 (5. 48) 식을 같이 생각할 때의 의 미는 다음과 같다. 안정한 기준 상태에서는 요동에 의해 과잉 엔트로 피가 0 보다 작아지면 0 보다 큰 과잉 엔트로피의 생성 속도에 의해 계 의 과잉 엔트로피는 증가하다가 더 이상 증가할 수 없는 과잉 엔트로 피가 0 인 원래의 기준 상태에 도달한다. 과잉 엔트로피의 생성이 정지 되는 계는 더 이상 변화할 수 없으므로 기준 상태인 정상 상태를 유지 한다. 정상 상태에서는 위 식의 적분내의 oY 는 정상 상태의 Y 가 되 지만 oX 가 0 이 되어 과잉 엔트로피의 생성 속도가 0 이 된다. 과잉 엔트로피의 생성이 항상 0 인 정상 상태에서는 (5. 43) 식에 의해 과잉 엔트로피의 생성이 항상 0 과 같거나 클 수밖에 없으므로 엔트로피의 생성 속도가 최소가 되어야 한다. 정상 상태는 항상 안정한 것이 아니 고 그 주위에서 (5. 55) 식이 만족되지 않으면 불안정하게 된다. 선형 열역학의 영역에서는 정상 상태를 기준으로 (5.55) 식이 다음과 같이 표시된다. P[a 인 =Jd V~Lu8X,8XJ 킥 0 (5. 57) 이 경우에 피적분 함수는 &와 같은 쌍이차 형식이 되어 (3. 3) 식에 의해 이 조건이 항상 만족된다. 다시 말하면 고정 경계 조건과 V=O 이고 의력장의 영향이 없는 경우에 선형 열역학계의 정상 상태는 안정 하다. 그리고 (5. 57) 식은 정상 상태에서 엔트로피의 생성이 최소가 된 다는 것을 의미하고 있다. 이것은 최소 엔트로피 생성의 정리로 알려 져 있다. 란다우어 (Landauer, 1975) 가 이 법칙의 유효성을 논의한 바 있다.
5 일반적 진화의 법칙과 안정성의 판정 기준 지금까지는 평형계와 비평형계에 대한 안정성과 진화를 작은 요동에 대하여 생각하였다. 작은 요동은 선형화에 의해 취급될 수 있다. 그러 나 어떤 비평형 상태는 선형화에 의한 작은 요동의 해석뿐만 아니라 유한한 요동 죽 교란을 고려한 해석이 필요하다. 이러한 계를 일반적 으로 검토하기 위하여 엔트로피 전개식과 상관 없는 부등문尻 l 를 유도 하여 보자. 성분 물질 수지식 (2. 26) 과 에너지 수지식 (2. 46) 를 V= 0 인 경우에 대해서 다음과 같은 형태로 쓰자 . 8p I /8t = 2f= I UuMJ j_V · J Id Iff (5. 58) 8p u /8t= 2f= l JIdl ff . FI-V·Jq (5. 59) (5.58) 석에 a(µ1 / T);a t를 그리고 (5.59) 식에 a(l/T)Ia t를 곱하여 더하고 계의 부피에 대해서 적분한다. Jd V[ ( aT-1/at) (ap u /at) —~ l=lN { a (µ1/T) /at} (ap 1 /at) ] :..:..:Jd V[ (~f=1 l.l u JJ M 广 V • J전) a(µ1/T);at + (~~=I J1d l ff • JF'1— v • Jq) a (1/T) /at] =-JdV [Jq • avU/T);at- ~~=' J/lff • a(µ1VT-1-T-1IF '1 )/at +~f=, J 1a(A1T-1)/ 組 (5. 60) 이 식은 고정된 경계 조건을 택하여 계면에서의 화학 퍼텐셜과 온도 의 요동을 무시하고 의력 E 가 시간에 의존하지 않는다고 하면 부분 적분에 의해 유도될 수 있다. 프리고전과 글란人두근立 (Pr ig o gi ne and Glansdorf, 1971) 는 이 식에서 시작하여 일반적 전화의 법칙을 제 시하였다. 먼저 이 표현석의 부호를 결정한다.
Jd V[ (aT- 1 /at) (ap u /at) —~f =1 { a (µ1/T) /at} ( ap 1/ a t) ] =一J dV( p /T) 〔 (cv/T) (aT/at) 2 + (p /X 깁
다음 석으로 정의되는 퍼텐셜 함수 cl>p를 발견할 수 있는 경우에는 일반적 전화의 법칙을 근거로 직접 관련된 안정성을 논의할 수 있다. 프리고진은 이러한 퍼텐셜 함수를 운동론적 퍼텐셜 (Kin e ti c Pot en ti al ) 이라부르고 있다. dxP = cd< I>p (5. 63) • 여기에서 c 는 0 보다 큰 함수이고 적분 인수에 해당한다. 그러면 (5. 62) 식은 다음 조건으로 변화한다. d
선형 영역의 정상 상태에서 P = P o 라 하고 oP = P ― Po 라 정의하면 oP~O 일 때 계는 (5. 67) 식에 의해서 안정하다. 그리고 이 안정한 정 상 상태에서는 엔트로피의 생성이 최소가 되므로 4 절에서 언급한 바와 같이 최소 엔트로피 생성의 정리가 된다. 이 경우에 야p는 P 가 된다. 선형 영역 밖에서는 온사거의 정리가 성립되지 않으며 선형 계수의 대칭성이 보장되지 않고 또한 퍼텐셜 함수의 존재도 변수가 하나인 경 우를 제의하면 보장되지 않는다. 그러나 일반적 전화의 법칙은 교란에 대해 적용될 수 있으므로 요동에 대해서도 적용이 가능하다. 이 장에 서는 앞으로 일반적 진화의 법칙과 이와 관련된 안정성을 선형호匡 1 계 에 적용하는 문제를 검토할 것이다. 6 동역학적 안정성 이론 이 절에서는 안정성 판정의 디른· 방법인 동역학적 안정성 이론을 소 개하기로 한다. 이 방법은 동역학계의 고전적 안정성 판별방법이며 정 규 모드 해석에 근거하고 있다. 2 절에서는 동역학계가 (5.1) 석과 같 이 일반적으로 주어져 있지만 여기에서는 다음과 같은 선형계를 생각 한다. 선형계는 비선형계를 어떠한 기준 상태를 중심으로 선형화해서 얻을 수 있으며 따라서 요동이 선형화에 의해 근사적으로 기술되는 영 역내에 있을 때는 이 절에서 취급하는 방법에 의해 기준 상태의 안정 성을 판별할 수 있다. 선형계와 선형 열역학계는 구분되어야 하며 선 형 열역학이 적용되지 않는 평형에서 떨어전 계라 하더라도 그 계의 어떤 상태를 기준으로 선형화하는 것은 가능하다. dX/dt= A • X (5. 68) 여기에서 A 는 상수 행렬이다. 적합한 경계 조건이 주어져 있을 때 이 식의 해롤 구하기 위해 다음과 같은 변수 변환을 한다.
llJ= B • X, X= B-1 • llJ (5. 69) 이 석을 (5. 67) 식에 대입하고 양변에 B 를 좌측에 곱하면 dU /dt = B • A • B- 1 • U (5. 70) 행렬식이 0 이 아닌 행렬 A의 고유치 중에 서로 같은 값이 없을 때에 는 행렬 B • A • B - 1 가 대각선 행렬이 되도록 하는 B 를 발견하는 것 이 가능하다. 이 대각선 행 렬 을 W라 하면 이 행렬의 대각선 요소 wi 는 A의 고유치가 된다. 그러면 (5. 70) 식의 해는 디음과 같이 쓸 수 있다. u i =U i 。 exp (w 1t ) (5. 71) 이 식들은 정규 모드라 불린다. 모든 정규 모드가 안정하면 (5. 69) 식 에 의해 X 를 U 의 선형 결합으로 표시할 수 있으므로 (5. 68) 식으로 표시된 계가 안정해진다. 그리고 이 안정성은 모든 고유치 A 의 실수 부분이 0 보다 작아야 보장된다. n x n 행 렬 A 가 실수 부분이 0 보다 작은 고유치만을 갖게 되는데 필요한 조건은 다음과 같다. An> O , IAII A1 2 >O , …, An A12··… · Am > O A2 1 A22 I IA2••1• •• A•2•• 2• •…•••…•• •A• •2••n • (5. 72) An1 An2 …… Ann (5. 71) 식에서 고유치의 허수 부분은 주기운동과 관계를 갖고 있음이 분명해진다. 7 정규 모드에 근거한 열역학적 방법 다음과 같은 정규 모드를 생각한다.
dA/ d t= (wr+i w ,)A dA*/dt= (Wr- i w ,) A* (5. 73) 이 식에서 양 A 가 (wr+ i w1) t에 의존한다면 A* 는 (Wr- i w i)t에 의 존하는 양이다. 그리고 이 표기법에 따라 oP = J dV~[oY,oX 』를 근 거로 다음과 같은 혼합 미분둘을 정의한다. &nP = (1/2) Jd V~[oY,oX,*+ oY,*oX 』 (5. 74) &nQ= -(i/2 ) J dV~ 醫 Y18X1 *_ 8Y1 *8X 』 (5. 75) 정규 모드의 해석 방법을 비평형계의 열역학적 안정성 판별에 적용 하기 위하여 일반적 진화 법칙의 근거가 되는 (5. 60) 식을 (5. 61) 식 및 (5. 62) 식과 함께 과잉 성질에 대해 다음과 같이 쓰고 dxoP/dt = Jd V~ oY1d ox1/dt = 一J dV (p/ T) [(c v/T) (aoT-1/8t) 2+ (p /x 이 (88 p -1 庫) 2 +~f=l ~f=l µ1J (aow1/at) (aowi /at) ]책 (5. 76) 이 식으로부터 다음 관계를 구성한다. -JdV (p/ T) [(c v/T) (aoT 크 /a t)
한편 (5. 74) 식의 힘에 관한 부분을- 시간에 대해 미분하고 (5. 77) 식 울 이용하면 다음 결과를 얻게 되며 dx& nP /dt= (l /2) J dV~ 〔紋 1doX1·/d t+ oY1*doX1/dtJ =-JdV (p/ T)[ (cv/T) (aoT-1/at) (aoT•-1/at) + (p /x깁 (88p - 1/8t) (88p * -1/at ) + ~r=l ~f= 나i u (aow1/at) (aow//a t)]::;; ; 0 (5. 79) 이 식은 일반적 진화의 법칙인 (5. 62) 식과 유사하지만 그러나 선형화 된 계에 적용이 제한된다. 하나의 정규모드에 대해 위의 식은 또한 다음과 같이 표시될 수 있 다. dx8mP/dt = (1/2) JdV ~[8Y,d8x,*/dt + 8Y,*d 8x,/dt] = (wr-iw ,) (l/2) JdV 8Y,8x,* + (wr+ iw i) (l/2)J d V8Y,*8x, =wr&n P +w,&n Q ~O (5. 80) (5. 77) 식과 (5. 80) 식으로부터 다음 관계를 얻는다. (Wr2+w12) 합 S=wr &n P+w1 &nQ ~O (5. 81) (5. 78) 식을 시간에 관해 미분하면 다음 관계식을 얻고 a 핥 S/a t =2Wr 핥 S=2P[ &n S]=2 &n P (5. 82) 이 식의 양변에 Wr 을 곱하면 다음 식이 된다. Wr2 핥 S=wr &n P~O (5. 83) 여기에서 부등호는 (5.78) 식에 의해서 결정되었다. 그리고 Wr 이 ' O 보다 작아서 계가 안정한 조건은
&nP ~ O (5. 84) 이다. 또한 &n P 의 시간에 대한 도함수를 구하고 이 식에 의해 부호를 결정하면 디옴 식을 얻는다. a& nP Iat = 2wr&n P = 2w/&n S s : O (5. 85) 이 식과 (5. 84) 식은 &n P 이 리아푸노프 함수가 된디는 것을 의미하 고 있다. 이 해석 방법은 정규 모드에 근거하고 있지만 정규 모드의 고유치를 구하지 않고 &n P 의 부호를 결정할 수 있으면 안정성을 판별 할 수 있도록 한다. 요동이 존재할 때에는 (5.78) 시게 의해 &2S< o 이므로 8mP=O 이면 (5. 83) 식에 의해 Wr=O 가 된다. 또한 (5. 81) 식과 (5. 83) 식에서 다음 관계를 얻고 W12 핥 S=w1 &nQ sO (5. 86) 여기에서 부등호는 (5. 83) 식에서와 같이 (5. 78) 식에서 결정된다. 이 식에서 wI 는 회전의 방향과 관계가 있고 &nQ의 부호는 w1 의 부호를 결정한다. &nQ =O 이면 W i =0 이며, 위상 공간에서 기준 상태는 회전 하지 않는다. 위에서와 같이 &nQ의 부호를 결정할 수 있으면 고유치 롤 구하지 않고 정규 모드가 위상 공간에서 회전하는지 여부를- 결정할 수있다. &n P 과 &nQ의 부호를 함께 생각하면 정규 모드의 특성을 알 수 있 다. &nQ이 0 이 아니고 &n P=O 이면 기준 상태는 요동에 의해 전폭이 결정되는 새로운 상태로 변화하여 변화된 상태는 위상 공간에서 회전 하는 시간적인 주기 운동을 나타낸다. &nQ이 0 이 아니고 &n P>O 이면 기준 상태는 안정하고 요동에 의한 상태는 회전 운동을 하며 기준 상 태로점근한다. 위의 논의는 선형화된 계에 대한 것이므로 (5. 74) 식과 (5. 75) 식에 다음 선형관계를 대입하면 oY=M • oX (5. 87)
(5. 74) 식과 (5. 75) 식 대신에 다음 관계식들을 얻게 되고 &,,P= (1/2)Jd V~~M0n[oX10XJ *+ 0X1*oX 』 (5. 88) &,,Q= - (i/2) J d V~~MllJJ[ o X10X)*— 0 X1*0X 』 (5. 89) 여기에서 M (lj)과 M11 JJ은 각각 M을 대칭 행렬 M(S) 와 반대칭 행렬 M(a) 의 합으로 표시하였을 때에 이 대칭 행렬과 반대칭 행렬의 요소이 다. 위의 두 식에 의해 &,,P 와 &,,Q의 부호가 결정되면 (5. 84) 식과 (5. 86) 식에 의해 Wr 과 W1 의 부호를 결정할 수 있고 또한 계의 안정성 과 해가 위상 공간에서 회전하는지의 여부를 결정할 수 있다. (5. 87) 식이 과잉 힘과 과잉 흐름의 선형 관계를 표시하고 있지만 이 관계는 평형에서 멀리 떨어진 영역에서도 유효하고 행렬 M 은 일반적으로는 온사거의 관계를 만족하지는 않는다. 선형 영역에서 이 판정방법이 적 용되는지 확인하기 위해 정상 상태를 기준으로 생각하면 M 은 온사거 의 관계에 의해 대칭 행렬 L 이 되어 &Q는 0 이 되고 W1 도 0 이 된다. 또한 (3. 3) 식에 의해 &,,P 는 항상 0 보다 크게 되어 안정성 조건을 만 족한다. 이 방법은 선형화된 계에 대한 정규 모드의 고유치를 직접 계산하지 않고 고유치의 실수 부분과 허수 부분의 부호를 결정할 수 있는 방법 을 제시한다. 이 방법에 의한 해석은 6 장에서 화학 반응계의 시간적 질서를 논의하면서 실제로 검토될 것이다. 8 국소 퍼텐셜 평형계나 선형 열역학계에는 잘 정의된 진화의 법칙과 안정성의 판 별 기준이 존재한다. 평형계에서는 장 S::;;o, P[S J =a 정 S/a t ~O, 선형 열역학계에서는 이차의 작은 교란에 대해서는 장 s::;;o, P[o 언=J dv ao2s/at ~ O, 그리고 유한한 교란을 생각할 때는 t::,.P ~O, dP/dt: :;;~ 조건이 존재한다. 이들 세 쌍의 식들에서 처음 식들은 교란의 조건을
그리고 둘째 식들은 진화의 법칙을 제시하고 있다• 평형에서 멀리 떨 어전 계를 포함해서 일반적으로 성립하는 일반적 진화의 법칙은 (5. 62) 식에서 dxP/d t~~료 알려져 있다. 그러나 안정성 판별을 위해서 는 교란의 조건이 필요하고 위에서 언급한 바와 같이 이 식에 대응하 는 교란의 조건은 제한된 형식으로만 제시된다. 국소 퍼텐셜은 우리가 관심을 갖는 기준 상태의 해를 구하는 방법을 제시한다. 기준 상태는 정상 상태가 될 수도 있고 시간에 의존하는- 상 태도 될 수 있다. 국소 퍼텐셜 그 자체로서 안정성 판별의 조건을 제 시하지는 않는다. 그러나 정규 모드를 기준 상태로 하고 이 정규 모드 룰 국소 퍼텐셜을 이용해서 구할 수 있다면 국소 퍼텐셜을 이용한 안 정성의 판별이 가능하다. 열 전달을 예로 국소 퍼텐셜의 문제를 생각 해보자. - 순수 성분계에서 V=O 이고 경계면에서 온도가 일정한 순수 열 전 달계를 생각하자. 그러면 (2. 55) 식에서 o;;=Jq·'1(1/ T) =Yq X q (5. 90) 현상적 법칙을 다음과 갇이 쓰면 Jq= —x'1 T =xT2'1 ( 1/T) (5. 91) 진화의 조건은 다음 식으로 주어진다. dxP/dt= (l/2)J d VxT2 (o/at ) ['v (1/T) ·'v (1/T)] :::;;; o (5. 92) 정상 상태는 에너지 수지식 (5. 59) 에서 시간 의존 항이 0 이 될 때이 다. 따라서 정상 상태의 온도 분포를 To 라 하면 To 는 다음 식의 해로 주어진다. . '1•Jq=-'1( x'1 T o) =O (5. 93) xT 떻 다음과 같이 전개하고 x (T)T2=x (To)T 。 2+ o(xT2) (5. 94) 이 식을 (5.92) 식에 대입하면 다음 관계를 얻는다.
dxP /dt =+ ((1 1// 22)) J(dd/V do t) ( JxdTV 2 )[ x (a (/T a 。t) ) T[ v。 2 ('\/l /(1T /)T ·)v · (vl /(1T/) T] )s ] o (5. 95) 위 식의 우변 첫항의 적분을 국소퍼텐셜 1 라 하면 아는 T 와 To 의 함수이다. 그러나 일반적으로 우변의 둘째 항이 0 세 비해 무시되는 것은 아니므로 위 식이 d 1 /dt s 0% 의미하는 것은 아니다. 만약 이 것이 사실이었다면 우리는 전화를 기술하는 퍼텐셜 함수를 발견한 것 이고 따라서 안정성 조건은 리아푸노프의 방법에 따라 1> 但냐 1 주 어졌을 것이다. 국소 퍼텐셜 1 (T, To) 로부터 함수 A< I>I (T, T 。)를 다음과 같이 정 의한다. ~1 (T, T 。)= 1(T, T 。)一 1 (To, T 。) = (1/ 2) Jd V[x (T 。) T 。 2 v (1/T) .v (1/T)] — (1/2) J dV 〔짜 To) T 。 2 v (1/To) .v (1/To)] (5. 96) 또한 T-1 을 T 。 - I 를 기준으로 다음과 같이 전개해서 T-1= T 。 -1+AT _ I (5. 97) (5.96) 식에 대입하면 경계조건이 고정되어 있으므로」 다음 관계식을 얻고 AOI (T, To) = (1/2) f d 마 x (To) T 。 2 '\l (AT-1) •v( AT- 1 )] >0 (5. 98) 이 식에서 다음 관계도 성립한다. f:::..
는 함수 T+ 를 발견할 수 있다. T+ 는 일반적으로 To 9-~ 다르지만 T 。 가 정상 상태의 해일 때에는 T+ 가 To -2t- 같게 되도록 국소 퍼텐셜을 정의할 수 있다. 이 경우에는 국소 퍼텐셜을 이용한 정상상태의 해가 가능해진다. 더 일반화된 국소 퍼텐셜에 관한 논의는 9 장에서 충류의 안정성 문제와 함께 고려된다. 국소 퍼텐셜은 알려지지 않은 안정한 정상상태의 해를 구하는 방법이 될 수 있고, 또한 이렇게 구해전 정상 상태의 안정성 판별방법이 될 수 있다논 것을 알게 될 것이다. 9 정리 안정성의 논의에는 전화의 조건이 필요하다. 안정성을 판별하기 위 해서는 동역학에 적용되는 리아푸노프의 일반적 방법이 적용될 수 있 다. 그러나 리아푸노프 함수를 항상 발견할 수 있는 것은 아니다. 평 형에서 멀리 떨어진 계의 안정성 검토에 많이 쓰이는 직접적인 동역학 적 방법은 선형화된 계에 대해 정규 모드 해석 방법을 적용하는 것이 다. 이 방법에 의하면 정상 상태의 안정성을 판별할 수 있고 또한 정 상 상태로부터 요동에 의해 생성될 수 있는 상태를 제한적으로 알 수 도있다. 단열되고 닫힌 평형계의 안정성은 엔트로피 판별 기준을 써서 논의 할 수 있다. 국소 평형의 가정은 비평형계에도 적용되어야 하므로 비 평형 계의 안정성은 국소 평형의 가정에 의해 논할 수 있다. 이때에 는 안정성 조건으로 과잉 엔트로피의 생성 속도 P[oS] 가 0 보다 클 것 울 요구한다. 평형 근처 선형영역의 비평형 정상 상태의 안정성 판별 에서는 과잉 엔트로피의 생성 속도는 엔트로피의 생성 속도 P[S] 가 된 다. 평형에서 멀리 떨어전 계의 안정성 판별에는 과잉 엔트로피의 생성 속도나 과잉 엔트로피의 생성 속도와 정규 모드의 개념이 결합된 혼합 과잉 엔트로피의 생성 속도가 적용될 수 있다. 일반적인 안정성은 열
역학적으로 엔트로피 생성 속도의 힘 부분에 대한 시간 도함수의 부호 로 표시된 일반적 전화의 법칙을 근거로 검토가 가능하다. 그러나 아 법칙을 칙접 적용하는 것은 어렵고 계가 하나의 상태 변수에 의존하는 특수한 경우에는 운동론적 퍼텐셜을 이용하거나 또는 더 일반적으로 국소 퍼텐셜의 방법을 이용해서 일반적 전화의 법칙을 안정성 판별에 적용할 수 있다. 이 장에서 검토한 안정성 판별 방법들은 이 책의 후 반부에서 중심적인 역할을 한다. 그러나 이 방법들은 기준 상태가 불 안정해지면서 나타날 수 있는 가능성에 대해서는 정보를 제공하지 못 한다.
제 6 장 화학 반응의 안정성과 시간적 질서 I 반응 속도와 안정성 먼저 2 장에서 검토한 것과 같이 約서의 연계된 화학 반응식을 일반 식으로 다음과 같이 표시한다. ~r=1111J R i= O (i= l, 2, ……, R) (6.1) (6.1) 식으로 표시된 반응에서 i번째 반응의 화학 친화력 A 는 4.2 절에서 정의된 바 있다. A1=-~=1 vuM 먀 (6. 2) 그리고 (2. 55) 식의 엔트로피 생성 속도항을 이 반응계에 대해 표시 하면 디음식을얻는다. P=d1S/dt= <1/T) fav ~r=1 A1J i ~o (6. 3) 평형 근처에서는 (4. 21) 식으로부터 반응속도 L 를 친화력의 선형
함수로표시할수 있다. J1= Orio/ RT)A1=a1A1 (6. 4) 여기에서 JflO는 평형 상태에서의 정반웅의 속도이다. 이 식을 (6. 3) 식에 대입하고 (5. 62) 식으로 주어진 전화의 법칙을 적용하면 다음 식을얻는다. dxP/dt= Jd V (1/T) ~晶 (dA1/dt) J1 = Jd V (l/2T) ~r=l a1d (A12) /dt = (l/2) dP/dt ::;;; Q (6. 5) (6. 3) 식과 (6. 5) 식에서 P 는 리아푸·노프 함수를 정의하고 있다. 그 리고 평형 근처의 화학 반응은 선형 열역학 영역에서 예상할 수 있는 바와 같이 최소 엔트로피 생성 정리를 만족한다. 즉 경계조건이 엔트 로피 생성이 0 이 되는 상태까지의 진화를 허용하면 엔트로피의 생성 속도가 감소하여 계는 평형에 도달하고 이 평형 상태는 안정하다. 열 린계에서 경계조건이 엔트로피 생성이 0 이 되는 상태까지의 전화를 허 용하지 않으면 계는 엔트로피 생성 속도가 일정해지는 정상 상태까지 엔트로피의 생성 속도가 감소하면서 전화하고 이 상태는 안정하다. 그러나 평형에서 멀리 떨어전 계에서는 (6. 4) 식과 같이 반응 속도를 친화력의 선형 함수로 표시하는 것이 허용되지 않는다. 따라서 (6. 5) 식에 첫번 관계로 표시된 일반적 전화의 법칙에 근거한 전화와 안정성 의 논의가 필요하다. 5 장에서 논의한 바와 같이 (6. 5) 식에 근거해서 안정성을 직접 논의하기 위해서는 운동론적 퍼텐셜울 이용할 수 있어 야 한다. 이 장에서 검토하는 문제들은 두 개의 중간 생성물의 농도에 의존하므로 운동론적 퍼텐셜의 이용은 일반적으로 불가능하다. 이 장에서는 평형에서 멀리 떨어전 계의 전화와 안정성을 선형화된 계에 대해 동역학적 방법인 정규 모드 해석 방법과 정규 모드에 근거 한 열역학적 방법에 의해 검토하고자 한다. 5 장에서 언급한 바와 같이 정규 모드 해석은 임의의 기준 상태를 중심으로 한 요동이 시간에 따
라 어떻게 변하는지를 검토하는 것이다. 그리고 이에 근거한 열역학적 방법은 &n P 와 &nQ의 부호로부터 기준 상태의 안정성과 요동에 의해 생성되는 구조를 검토하는 방법으로 정규 모드의 고유치를 직접 구하 지 않고 부호를 열역학적 방법에 의해 결정하는 것이다. 계산으로 볼 때에 열역학적 방법이 더 편한 것으로 생각되지는 않지만 고유치 문제 와 독립적인 열역학적 방법이라는 점에 의의가 있는 것으로 생각된다. 평형에서 멀리 떨어진 계의 정상 상태는 불안정해질 수 있고 이로부터 공간적 질서 또는 시간적 질서가 생성될 수 있다. 이 장에서는 화학 반응으로부터 생성되는 시간적 질서를 검토하고 공간적 질서는 디옴 장에서 검토한다. 2 로트카-볼테라 모델 다음과 같은 자촉매 (Auto c at al ys i s ) 반응 단계들로 구성된 반응을 생각한다. A+X=2X (속도 상수 k1, L1) X+Y=2Y (속도 상수 k2, k_2) Y=E (속도 상수 k3, k_3) (6. 6) 이들 반응의 총괄식은 A=E 이며 이 모델은 시간적 질서 또는 구조 를 나타낸디는 접에서 홍미롭다. 평형 상태에서는 총괄 반응식으로부 터 계산된 총 친화력이 0 이 된다. A=A1+A2+A3 =RT ln [ (k1k2k3/k_ 1 k-2k_3) (A/E)] =O (6. 7) 또한 총괄 반응을- 구성하는 각 기초 반응 속도들도 평형에서 0 이 되 므로 평형 조성을 계산하면 다음과 같다.
(A/E) eq= k_, k_2 k-3 /k ,k2k3 Xe q= (k,/k_,)Ae q Ye q= (k,ki/ k_,k _2)Aeq (6. 8) 평형 조성이 알려지면 평형 근처에서 (6.5) 식에 따라 선형 법칙들을 쓸수있다. J1= (k1AeqX eqQ ) A1/RT=a1A1 J2= (k2XeqY eq) Ai /RT =a2A2 J3= (k3Yeq) A3/RT=a3A3 (6. 9) 이제 앞절에서와 같은 논의에 의해 평형 근처의 열린계에서 정상 상 태가 존재한다면 이 정상 상태는 안정하다. 그러나 다음에 보이는 바 와 같이 평형에서 멀리 떨어진 정상 상태의 안정성은 보장되지 않는 다. A와 E를 일정하게 유지할 수 있는 열린계에서 중간 생성물 X 와 Y 의 시간에 따른 변화를 역반응을 무시할 수 있다고 생각하고 평형에서 멀리 떨어진 상태의 반응 속도롤 디움 식으로 표시하자. ddXY//ddtt== k k12AXXY—— kk32Y X Y (6. 10) 이 반웅 모델은 로트카쉽匡]라 (Lo t ka-Vol t era) 모델로 알려져 있으 며 이 모델은 환경 시스템의 모델로 제안되었다. 죽 X 가 A 를 먹이로 번식하고 마찬가지로 Y 가 X 를 먹이로 번식하며 Y 는 일정한 속도 상 수를 갖고 사멸하는 먹이와 먹는자의 거동을 설명하기 위해서 도입되 었으나 생물학적 시계나 신경 계통과 같은 생물학적 현상을 논의하기 위해서도 사용되었다. 이 식들로부터 dX/d t =dY/d t =O 인 정상 상태 의 해는 쉽게 구할수 있고그 결과는다음과같다. Xo=k3/k2, Y 。= (k1/kk)A (6. 11) 정규 모드 해석에 의한 안정성을 검토하기 위해 정상 상태를 기준으
로한 X, Y 롤 oX, oY 로 표시하고 (6.10) 식을 선형화해서 다시 쓰면 다음식을얻는다. doX/dt = (k1A- k 2Yo) oX-kkX 。 oY doY/dt = k2Y 。 oX+ (k2X 。 -k3) oY (6. 12) (6.11) 식을 (6.12) 식에 대입하고 (6.12) 식을 다시 쓰면 다음과 같 이 된다. doX/dt= 一 k2X 。 oY = oJ 1一 싸 2 doY/dt= k2Y 。 oX= o J 2 一 싸 3 (6. 13) 이 연립 미분 방정석의 해는 5 장의 정규 모드 해석에서 검토한 바와 같이 다음 식으로 표시할 수 있다. 8X= 8X 。 exp (wt ) 8Y = 8Y 。 exp (wt ) (6.14) 여기에서 oXo 와 %는 요동의 초기 크기를 의미한다. w 는 (6.14) 식을 (6.13) 식에 대입해서 구할 수 있으며 다음 행렬의 고유치가 된 다. [°k2Y 。 o-k2x 。] (6.15) 이 행 렬의 고유치는 다음 특성 방정식 (Characte r is t i c Eq u ati on ) 의 해로표시된다. w 드 -k1k2A (6. 16) 분명히 두 고유치는 허수가 되므로 oX 와 oY 는 초기 요동의 크기 oXo 와 昴%에 따라 전폭이 변치 않고 전동하게 되며 시간을 소거한 위상 공간에서는 폐곡선을 따르는 회전 운동을 하게 된다. 정규모드에 근거한 열역학적 방법을 검토하기로 한다. (6.10) 식으 로 표시된 반응 속도식은 평형 근처의 속도식 (6.10) 으로부터 유도될
수 있는 것은 아니다. 그러나 기준 상태를 중심으로 선형화한 힘을 이 용해서 과잉 반웅 속도를 표시할 수는 있다. 이를 위해 과잉 엔트로피 생성 속도의 표현식을 구한다. P[o 히 = f dV 江 F= I 8J 18 Al (6. 17) 이 식에 A 와 E 가 일정할 때에 성립하는 다음 관계식을 대입하고 정리한다. ~r=l 0A1=0 (6. 18) 그러면 P[8S] =Jd V (8]1— 8 12) 8A1/T+ (8]3-8]2) 8A3/T =Jd V (8J ,— 8]2) 8A,/T+ (8]2-8]3) (국 )A3)/T (6.19) 이다. 한편 8A1 과 8A3 를 계산하면 다음과 같다. 8A 尸 (RT/X 。) 8X 8A3= 一 (RT/Y 。) 8Y (6. 20) 0A1 과 一 8A3 은 각각 oXx, oX y 0l 고 (6. 13) 식의 반응 속도들은 각 각 과잉 반응 속도 oYx, oY 러므로 힘과 흐름의 선형 관계를 디음과 같이쓸수있다. oY=M • oX (6. 21) 여기에서 M 은 다음과 같다. M= [0k 2X&/R -k。2 X0Yo/R] (6. 22) 여기에서는 현상적 법칙들의 계수는 평형 근처에서 평형 상태를 기 준으로 선형화한 속도식들에 대한 것이 아니므로 대칭성 관계롤 만족 하지 않는다는 점에 유의한다. M 으로부터 M(S) 와 M(a) 롤 구성하면 다 음과같다.
M (S)= O M(a)=M (6. 23) 이 결과를 이용해서 (5. 88) 식으로 표현된 &,P 를 계산하면 대칭 행 렬의 요소가 모두 0 이므로 0 이 된다. &,P= (1/2) Jd V1 :1:M< u>[oX10Xi *+ 0X1*0X 』 (6. 24) =O 이 결과는 (5. 85) 식에 관한 논의로부터 Wr=O 이 된다는 것을 의미 한다. 이는 요동이 시간에 따라 전화하지 않는다는 것을 의미한다. 또 한 반대칭 행렬 요소의 값들과 (6.17) 및 (6.18) 식을 이용해서 (5.89) 식으로 표현된 &Q를 계산할 수 있다. &,Q= —( i /2) f dV I:I: M1u1[0X10X1*-oX1*oX 』 = - (i/2 ) J dV[ 一 (oXxoXy * -oXx*oXy ) + (oX., ,oX x*-o Xy * oXx)] (k2X 。 Y 。 /R) =ifdV k2R(oX*oY-0XoY*) (6. 25) 위에서 Wr=O 이 되었으므로. (6.13) 식으로부터 다음 식들을 얻는다. -iw1 ( 0Xr-io X 1) =-k2X 。 (0Yr-io Y 1) -iw1 ( 0Yr-io Y 1) =k2Y 。 (0Xr-io X 1) (6. 26) 위의 두 식은 예상할 수 있는 바와 같이 동일하다는 것을 쉽게 확인 할 수 있다. 그리고 이 식들로부터 다음 결과를 얻는다. oY!= —(k2 Yo/W1) oXr 8X 尸 (k2Xo/W1) oYr (6. 27) 결과를 (6. 25) 식에 대입하고 (6.11) 식을 써서 정리하면 다음 식울 얻는다. &nQ= - (2k2R/w1) Jd V[k3 (oYr) 2+ (wi2 / k3) (oXr) 기 (6. 28)
(5. 86) 식에서 w1& Q < 0 의 관계가 항상 성립해야 하고 위의 식에서 &nQ는 0 보다 작으므로- w, 는 항상 0 보다 크다. 따라서 요동은 위상 공간에서 회전하고 W1 의 부호는 회전의 방향을 결정한다. 다음에는 선형화되지 않은 원래의 속도식을 써서 무엇을 알 수 있는 지 검토한다. 로트카웃匡]라 모델의 위상 공간에서의 거동을 살펴보 기 위해서 (6. 14) 식에서 반응 속도 상수들을 1 로 하고 또한 A= l 인 경우를생각하자. 견dX =XXY-X ― YY (6. 29) 이 식의 해는 변수 분리에 의해 쉽게 구해진다. x - 1 exp (X ) =CY exp ( - Y ) (6. 30) 여기에서 C 는 초기 조건에 의해 결정되는 상수이다. 이 식은 그림 6-1 에 보인 바와 같이 초기 요동에 따라 결정되는 폐곡선의 일족을 나 타낸다. 그림에서 K 는 ln C 를 의미한다. (6.10) 식을 다음과 같이 N 성분계로 일반화해서 선형화되지 않은 계의 시간 의존 특성을 해석할 수 있다 (Goel et al, 1971). dN1/dt= k1N1+/3 1 -1~ f =1 auN,Nj (6. 31) 여기에서 au= ― a j 1 이고 a11=0 인 제한 조건을 가정한다. 정상 상태 에서는 이 식은 다음과 같이 표시된다. N,0 (k,/31 +~=1 ali N i o ) =O (6. 32) 이제 다음과 같이 vI 를 정의한다. v,=ln(N,/N10) (6. 33) 그러면 (6. 31) 식과 (6. 32) 식에서 다음 식을 얻는다. /31 dvi/ dt = (/31 /N1) (一 ln N1 o) dN1/dt = ~J=t N atJN J o (exp VJ - 1) (6. 34)
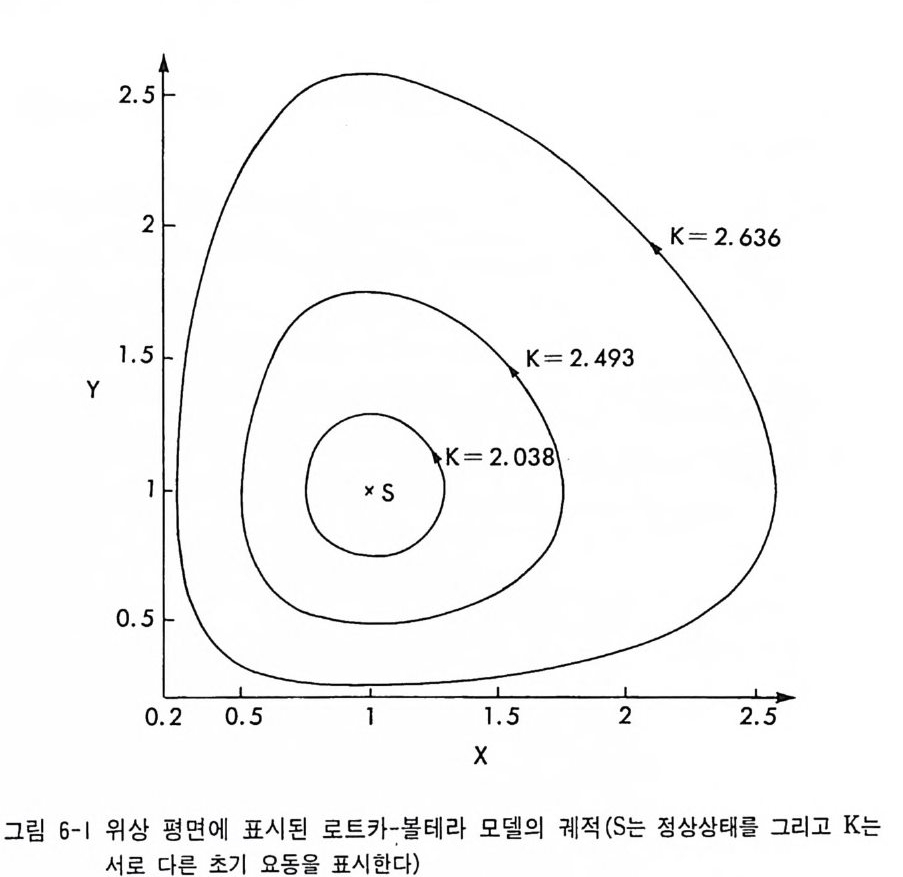 2.5
2.5
이 식의 양변에 NIO(exp V 1 -l) 를 곱하고 i에 관해 합한다. (dv1/dt) ~~=1 /31 N10 (exp V1-l) =d[ ~~ =1 /3iiN 1 0 ( exp V1-v1)]/dt =~~=1 ~f=1 auN J。 (ex p vi - 1) (exp V1 - l) =O (6. 35) 위의 식이 0 이 되는 이유는 au= ― a j 1 의 관계가 성립하기 때문이다• 이제 G 를 디움과 같이 정의하면
G= ~~=I {J1N 10 (exp v,-v1) (6. 36) 분명히 G>O 인 상수이고 따라서 dG/d t =O 이다. G 는 한계 안정성을 나타내고 있는 리아푸노프 함수가 된다. 로트카국며라 모델의 또 하나의 특징을 살펴보기 위해 (6. 31) 식의 양변을 t= O 에서 t까지 적분하고 匡그 나눈 다음에 t-+ 00 이 되는 극한 울취해 보자. l뽀 (/31 /t) [ In N1(t) — In N1(0)]=k1/3 1 +~f= 1 a1J
명과 관련을 맺고 있는 것이 홍미롭다. 브럿셀레이터 반응은 다음 반 응기구로 표시되는 자촉매 반웅이다. A=X 2X+Y=3X B+X=Y+D X=E (6. 41) 총괄 반응식은 A+B=D+E 이며 둘째 반응이 자촉매 단계이고 또 한 둘째 반응과 셋째 반응은 X 와 Y 가 서로 교차로 촉매 역할을 한 다. 문제를 단순하게 하기 위해 모든 정반응의 속도 싱수를. 1..£ 그리 고 모든 역반응의 속도 상수를 臣료 가정하고 중간 생성물 X 와 Y 의 농도 변화를 표시하면 다음과 같다. dX/d t =A+X2Y-BX ― X+k(YD+E-X ―처) dY/dt= BX-X2Y+ k (X3-YD) (6. 42) A, B, D 및 E 가 일정할 때 정상 상태에서는 X0= (A+kE) / (l+k) , Yo=X 。 (kX2+RD) / (X 。 2+kD) (6. 43) 이다. 여기에서 R=B/D 로 표시했다. 더욱이 A 와 E 긱 관계가 평형 에서와 같이 질량 작용의 법칙에 의해 결정된다고 가정하면 A=k2E (6. 44) 이다. (6. 42) 식을 정상 상태를 기준으로 선형화하면 다음 식이 되고 doX/dt= [2X 。 Y 。 _B-1-k(l+3X 。 2) 〕 oX+ (kD+X 。 2) oY doY/dt= [B-2X 。 Y 。 +3kX 。기 oX-( X 。 2+kD) oY (6. 45) 이제 정규 모드 해석에 의해 선형화된 계의 고유치를 다음 특성 방정 식에 의해 계산한다.
w2+ [X 。 2+RD+ l-2X 。 Y 。 +k (3X 。 2+D+ l)]w +x 。 2+k(X 。 2+D)=O (6. 46) 주어전 D 에 대해 일차항의 계수는 R에 따라 변화한다. 일차항을 0 으로 하는 R 값을 Re 라 하면 R doY/ dt = 0]3- o J2 =— BoX— A 20Y (6. 50) 고유치 w 는 다음 특성 방정식의 근이 되며 w 탸 (A 도 1 ― B)w+A2=0 (6. 51) w 의 실수 부분이 0 보다 커서 계가 불안정해지는 조건은 B> B c=l+A2 (6. 52) 이다. (6. 50) 식의 좌변을 각각 oYx, 昴 8 라 표시하고 해당하는 힘 8 Xx, oX 틀 앞절에서와 같이 구한다• 여기에서는 반응식 (6. 41) 로부 터 다음 관계 를 얻고 0A1+0A4 = 0, 0A2+0A3=Q (6. 53) (6. 50) 식에 따라 독립된 흐름을 구성하고 (6. 53) 식의 관계를 써서 독 립된 힘과 흐름에 대한 엔트로피의 생성 속도를 표시하면 다음 식이 된다. H 祠 =Jd v~oX10Y1= (0J 1+ 0J2 -0J3 — 0J 4 ) 0A1/T + (0J3 -ol2) ( 0A1-0A2)/T (6. 54) 이제 힘을 계산하면 다음과 같고 oXx= 0A1/T=-(1 /T) oµx= —(R /A) oX oXv= (0A1-0 A2) /T= -( 1/T) oµv= -(RA/B) oY (6. 55) (6.21) 석으로 정의된 것과 같은 흐름과 힘 사이의 선형 계수 행렬 M 울 쓰면 다음과 같이 표시된다. M= [A_B\\B— 1)/R —::;:] (6. 56)
M(s)= [ —: (B— 1)/ R A~/Rl (6. 57) M(a)= [A:/R _:B/R] (6. 58) 그리고 (5. 88) 식과 (5. 89) 식의 정의에 따라 &n P 과 &Q를 계산하면 결과는 다음과 같이 쓸 수 있다. &nP = (R/AB)Jd V{B(l-B) oXoX*+A4oYoY*} (6. 59) &nQ=i(R A) Jd V(oX*oY-oXoY*) (6. 60) A 와 因큰 농도이므로 양수이고 oXoX* 와 oYoY* 는 항상 0 보다 크 다. 그러므로 다음 관계가 &n P 을 0 보다 크게 하는 충분 조건 죽 정규 모드의 실수 부분 Wr 이 0 보다 작게 되는 조건이 되고 따라서 안정성 의 충분조건이 된다. B
&nP =J d V[A/(1+A2)][ (A2-w12) (oYr) 기 = O (6. 64) 이 결과는 Wl= 土 A 를 의미하고 특성 방정식 (6. 51) 로부터 얻는 결 과와 동일하다. 또한 이 조건에서 (6. 60) 식으로부터 &Q를 계산하면 다음관계를 얻는다 . &nQ= ― 2RA J dV[oXroY1-oX 1 0Y 』 =— 2RAw1J dV (oYr)2 (6. 65) !)
또는 w,& nQ= -2 RAw,2J d V (0Yr) 2힉 0 (6. 66) 이 식에서 W1 의 부호가 결정되고 따라서 회전방향이 결정된다. 고 유치 문제에서와 같이 여기에서도 W1 의 부호는 두 가지가 되며 실제 로 나타나는 계는 두 부호 중에서 하나를 선택한다. 6. 2 절의 로트카 볼데라 모델이 임의의 요동에 대해 진동을 나타내는 것과는 다르게 여기에서는 B=Bc 인 경우에만 비슷한 거동을 나타낸다. 그리고 B> B 러면 정상 상태가 불안정해진다는 것을 알 뿐이다. 정상 상태가 불안정해지면 어떻게 될 것이가 하는- 문제는 선형 안정 성 이론의 한계를 벗어나는 문제이다. 선형화되지 않은 (6.42) 식에서 역반응을 무시하고 X 에 관한 2 차 상미분 방정식을 얻어 해석한 결과 는 극한 싸이클이 나타날 수 있음을 보이고 있다. 그란人두근立와 프 리고진의 책에 소개된 이 문제를 간략히 검토하기로 한다. (6.42) 식에 서 역반응을 무시하고 두 식을 합하면 다음 식을 얻는다.
1) 이 식의 계수는 프리고진과 글란스도르프의 책에 주어진 결과와 차이 가있다.
dX/dt+ d Y/dt= A -X (6. 67) 또한 Y= (BX— dY /dt) / X2= (BX+dX/dt+ A- X )/X2 (6. 68) (6. 42) 식의 첫째 식을 미분하고 (6. 67) 식과 (6. 68) 식을 대입하면 d2X/dt2 = X+2 2 ([ A(B-XX+— ddXX //ddtt+ ) A— X) /X 國 X/d t (6. 69) 一 (B+l)dX/dt 이다. 이 식을 x=X-A 라 정의하고 x 에 대해 다시 쓰면 d2x/dt2 + (—x+ZAd x)-/d!t[]x ( 3d+x3/Adtx) 2 ++x( (3xA+2A-)B2 ―= l0 ) x+A(A 드 B+(l6). 70) 이다. 다시 ~>-1/A 에 대해 E 를 다음 식과 같이 정의하고 x= —A2 ~ / (l+A~) (6. 71) (6. 70) 식을 다시 쓴다. d2;/dt2 + [A 키 (l+A;) 2+2A;— B+ 1] (d;/dt) +A;/(l+A;) =O (6. 72) 일반적으로 다음 형식의 미분 방정식에서 d2t; /d t2 + f (I;) (dl; /d t) +g (I;) = O (6. 73) 적어도 하나의 주기적 해가 존재할 조건은 f(0 )
족된다. 다시 말하면 정상 상태가 불안정해지면 주기적 해가 나타난 다. 이 주기적 해의 특징은 수치 해석에 의해 밝혀질 수 있다. 그 결 과는 그림 6-2 에 보인 바와 같이 여러 개의 초기 요동에서 초기 조건 에 상관 없이 하나의 극한 싸이클로 점근한다.
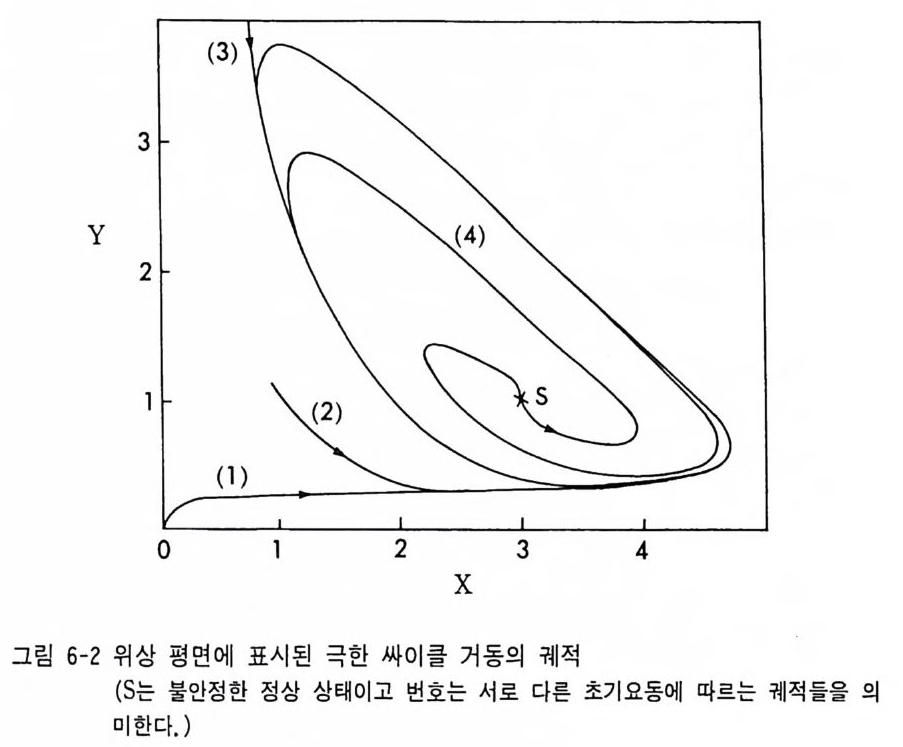 (3)
(3)
복잡한 열린계인 생물계에서 관찰되는 여러 주기적인 현상은 생물학 적 시계 (Bi ol og ica l Clock) 라고도 불리는데 진동하는 화학 반응에 대 한 연구에 의해 궁극적으로 이러한 현상을 이해할 수 있을 것으로 생 각되고 있다 (Eige n, 1971) .
4 로트카-볼테라 모델과 극한 싸이클 로트카윤톄라 모델과 브럿셀레이터 반응의 차이는 전자가 정상 상 태의 주위에 무한히 많은 주기적 해를 갖는 반면에 후자~ 정상 상태 가 불안정해지면서 하나의 극한 싸이클을 갖는다는 것이다. 그러나 브 럿셀레이터 반응도 한계 안정성 조건에서는 로트카令柱 1l 라 모델과 마 찬가지로 무한히 많은 주기적 해를 갖는다. 이러한 성질은 운동의 상 수의 존재와 관계가 있다. 로트카읍困 1 라 모델의 (6.30) 식에서 C 는 운동의 상수이다. 한계 안정성 조건의 브럿셀레이터 반응에서도 디옴 과 같은 운동의 상수가 존재함을 보일 수 있다. V= (l+A2) (oX)2/2+A2(0Y)2/2+A2 0 XoY (6. 76) 브릿셀레이터 반응에서 반응계가 불안정해지기 전에는 정상 상태는 안정하다. 한계 안정성 조건은 두갈래치기점 (Bif urc ati on Po i n t)에 해 당한다. 안정한 정상 상태는 두갈래치기점을 지나면서 안정한 극한 싸 이클과 불안정한 정상 상태 중에서 안정한 상태를 택하게 된다. 프리 고진과 글란人두 근 立는 이 현상을 다음과 같이 제시하였다• 안정한 초점―」二안정한 극한 싸이클 불안정한초점 여기에서 초점 (Focus) 이란 그림 6-3 에 표시한 바와 같이 위상 공간 에서 점으로 표시되는 정상상태를 기준으로 한 요동의 정규모드의 허 수부분이 0 이 되지 않는 경우를 의미하며 다음 장에서 논의되는 노드 (Node) 와 비교된다. 이것은 두갈래치기점을 지나면서 일어날 수 있는 현상의 한 형태이며 두갈치기점을 지나면서 나타나는 현상은 다양하 다. 조셉 (Jo seph , 1985) 은 유체 역학계 및 다론 계에서 나타날 수 있 는 두갈래치기 현상을 종합적으로 검토하였다.
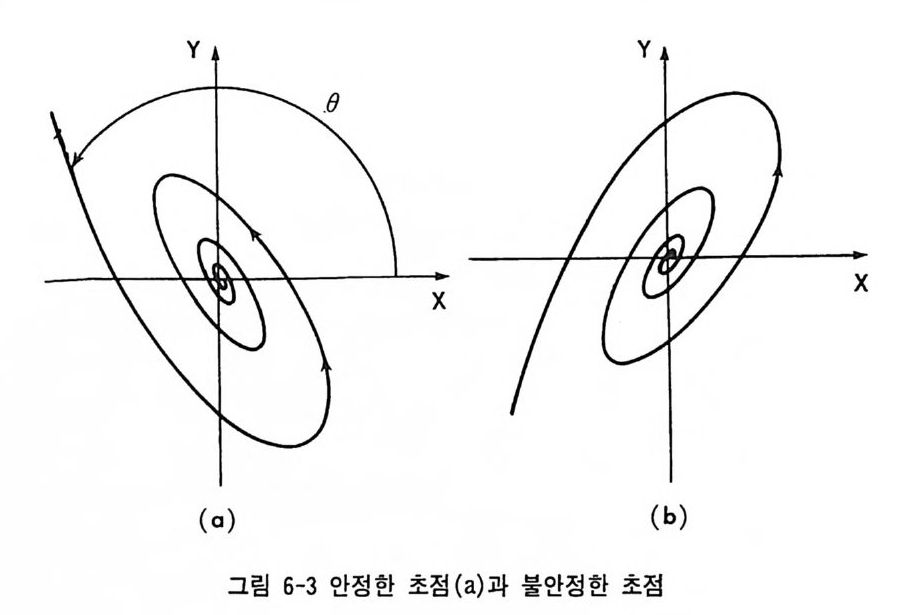 Y Y
Y Y
~l B 롭 지나서 더욱 증가하면 어떠한 일이 생길 것인가 하는 문제도 생각할 수 있다. 열역학적 방법은 첫번 두갈래치기점까지만 시 도되어 있고 따라서 평형에서부터 첫번 두갈래치기점까지를 열역학적 가지 (Thermody n ami c Branch) 라 부르기도 한다. 이 문제는 다음 절 에서 간략히 언급하고 유체 역학계의 안정성 문제를 검토할 때 다시 생각하기로한다. 5 벨루소프-자보틴스키 반응과 오레고네이터 반응기구 시간적 질서를 나타내는 실제 반응계의 대표적인 예는 벨루소프-자 보틴스키 반응 (De gn, 1972) 으로 알려져 있다. 이 반응은 황산 세륨과 브롬산 칼륨이 존재할 때에 말론산이 산화하는 반응이며 이 반응에서
황산 세륨은 촉매 작용을 한다. 이 반응은· 복잡한 반응이지만 다음 반 응 단계들이 중요한 역할을 하고 있는 것으로 추정된다. (a) 말론산의 산화 CH2 (COOH)2+6Ce 4+ +2H 2 0 ⇒ 2C02+HCOOH+6Ce3++ 6 H+ (6. 77) (b) 세륨 이온의 산화 lOCe3++2HBr03+lOH 드 ⇒ lOCeH+Br2+ 6H2 0 (6. 78) (c) 말론산이 브롬말론산으로 변화 CH2 (COOH) 2+ Br2 ⇒ CHBr (COOH) 2 (6. 79) 단계 (a) 에서 생성된 3 가 세륨이 단계 (b) 에서 반응하므로 자촉매 작 용이 중요한 역할을 하고 있다는 것을 알 수 있다. 단계 (b) 에서 생성 된 세륨 4 가 이온은 단계 (a) 에서 다시 37} 이온으로 환원된다. 실험적으로는 황산 세륨, 브롬산 칼륨, 말론산 및 황산의 농도가 각 각 0. 12 mmol/ dm 3 , 0. 60 mrnol/dm3 , 48 mmol/dm3 , 1. 5 mol/ dm 낀 용액을 60°C 에서 잘 혼합된 상태를 유지하면 초기의 유도 기간 울 지난 다음에 3 가 세륨의 농도가 일정한 주기로 지속적으로 진동하 는 것이 발견된다. 몇 방울의 Ferro i n 러t 산화환원 지시약으로 가하 면 3 가 이온이 과량으로 존재할 때는 적색 그리고 4 가 이온이 과량일 때는 청색이 되는 지속적인 진동이 관찰된다. 주기는 초기 농도와 온 도에 따라 다르지만 위의 조전에서는 4 분 정도이다. 이 실험은 닫힌계 에서 일어나므로 브롬말론산이 생성되면서 반응은 평형에 접근한다. 그리고 이 실험은 동일한 실험 조건하에서 갇온 진폭, 형태, 주기를 갖는 진동을 재현할 수 있으므로 극한 싸이클의 존재를 확인한다. 이 반웅의 정량적 해석이 시도되었고 이를 위한 대표적인 모델로 필 드와 노이스 (F i eld and Noy es , 1974) 의 오레고네이터 반응기구를 들 수 있다. 오레고네이터 반응 기구는 다음과 같은 반응둘로 표시되며 세 개의 연립 미분방정식을 구성한다.
A+Y=X X+ Y =P B+X= 2 X+Z 2X=Q Z= f Y (6. 80) 여기에서 X= 〔 HBrC 』, Y= [ Be], Z= 2[CeHJ , A= B=[BrO 깁 그리고 P 와 Q는 생성물들의 농도를 표시한다. 또한 타이슨 (T y son , 1976, 1978) 은 수정된 오레고네이터 반웅기구 를 제시한 바 있다. 타이슨의 모델에서 디음-과 같은 속도석들을 쓸 수 있다. dcc'(Z (d/dXdYt/ /ddt t) ) === Xµ—Y(µlY-— X— ZY)X —+Y XZ+ f( Zl- Z )rX2 (6. 81) 여기에서 매개 변수들의 영역은 다음과 같은 값의 근방이다 ; c'~5 xl0-6, c~l0-3, µ~2x10-s, r~l, f~l. 이 매개 변수들의 커다란 차아 때문에 미분 방정석의 수치해를 구하기 위해서는 아주· 짧은 시간 간격을 사용해야 하는 어려움이 있다. 얻어진 해에서 국한 싸이클의 존재를 확인할 수 있다. 그러나 열역학적 해석은 시도되지 않은 것으 로 생각된다. 앞절에서 언급한 바와 같이 열역학적 방법은 열역학적 가지 죽 매개 변수가 변화하면서 처음 생기는 소산구조가 안정한 영역에서만 가~f하 다. 그러나 열역학적 가지를 넘어서서 죽 처음 두갈래치기점을 지나서 일어나는 현상에도 최근 많은 관심이 표시되고 있다• 어떤 동역학 모 델들에서는 두갈래치기가 계속되어 〈 이상한 유인자 (S t ran g e At tra c- t or) 〉 라고 불리는 혼돈 (Chaos) 에 도달하는 과정이 알려져 있다. 혼돈 은 일종의 극한과정으로 생각할 수 있으며 타이슨의 수정 오레고네이 터의 수치해도 두갈래치기를 계속하면서 혼돈에 도달할 것으로 생각되
고있다. 6 정리 이 장에서는 정상상태에서 발생할 수 있는 두 가지의 시간적 소산구 조와 그 안정성을 정규 모드에 의한 해석과 열역학적 해석 방법으로 검토하였다. 로트카 볼테라 모델은 정상상태 주위에 무한히 많은 진동 상태를 갖는다. 반면에 브럿셀레이터 반응은 정상상태가 불안정해지 는 한계 안정성 조건에서는 로트카 볼테라 모델과 같은 거동을 보이지 만 한계 안정성 조건을 넘어서면 단 하나의 극한 싸이클에 접근한다. 혼합 과잉 엔트로피의 생성 속도를 이용하는 열역학적 방법은 선형 화된 계의 고유치의 부호를 고유치를 직접 계산하지 않고 일반적 진화 의 법칙에서 유도된 방법에 의해 판정할 수 있는 방법이다. 이 방법이 계산상으로 더 간편한 것은 아니지만 평형에서 멀리 떨어전 계에 대한 열역학적 판정 방법이러는 접에서 의의가 있다고 하겠다.
제 7 장 화학반응의 다중 정 상 상태 및 공간적 질서 I 서론 앞장에서는 정상 상태가 불안정해지면서 나타날 수 있는 시간적 질 서에 관해서 검토하였다. 시간적 질서는 공간적인 균질성를 전제로 검 토되었지만 이 장에서는 공간적 균질성이 깨어지는 확산에 관한 안정 성의 문제를 검토한다. 열역학적 평형에서 멀리 떨어진 상태에서는 자 촉매 단계를 포함하는 복잡한 화학반응에서 국소적 요동에 의해 반응 계가 확산에 대해 불안정해지면 물질의 분포가 균일하지 않은 안정한 정상 상태가 나타날 수 있다. 이러한 전이에 의해 생성된 상태는 전이 전보다 덜 대칭적이므로 이와 관련된 불안정성은 대칭성 파괴의 불안 정성 (Sy m metr y Breakin g Ins t ab ility)이라 불린다. 정상 상태가 불안 정해지면서 나타나는 시간적 질서는 앞장에서 논의되었다. 공간적 대 칭성 파괴의 불안정성은 앞장에서 논의한 브릿셀레이터 반응에 확산항 이 추가되면 나타날 수 있다. 대칭성 파괴의 불안정성은 안정성 교환의 원리 (Pr i nc ip leo f
Exchang e of S t ab il ty) 를 따르는 것으로 알려져 있다. 안정성 교환의 원리는 하나의 안정한 정상 상태가 불안정해지면서 다른 정상 상태로 주기적인 운동을 수반하지 않고 전이되는 현상을 가르키는 것으로 정 규 모드 해석에서 고유치의 허수 부분이 임계점에서 0 이 된다는 것을 의미하고 있다. 이에 대비되는 전이현상은 과도 안정성 (Over St ab i- l ty)으로 과도 안정성을 보이는 계는 새로운 정상 상태로 감쇄 진동을 하며 접근한다. 공간적 질서는 확산을 수반하는 계에서 가능하며 대칭성 파괴의 불 안정성에 의해서 생성될 수 있을 뿐만 아니라 또한 계에 다~ 정상 상 태가 존재하면 확산에 의해 생성될 수도 있을 것으로~ 생각되고 있다. 다중 정상 상태를 논의하기 위한 실뢰글 모델과 에델시타인 모델에서 는 요동이 하나의 변수로 표시되므로 우리는 5 장에서 논의한 운동론적 퍼텐셜 힘수를 이용할 수 있다. 공간적 질서를 생성할 수 있는 다른 반응들도 글란人두 근 立와 프리고진의 책 (Glansdorf and Prig o g ine , 1971), 니콜리와 프리고진의 책 (Ni co lis and Prig o g ine , 1977) 과 논문 (Ni co lis, 1978) 에 논의되어 있다. 2 비평형 상전이와 다중 정상 상태의 화학적 모델 이 절에서는 다중 정상 상태를 나타낼 수 있는 화학반응의 모델로 실뢰글 모델과 에델시타인 모델을 생각한다. 이들 반응에서 반응물과 생성물은 열린계에서 일정하게 유지된다. 그리고 다중 정상 상태가 존 재할 수 있는 조건을 검토한다. 실뢰글 모델 (Schlog l, 1972) 로 알려진 다음 반응식들로 주어지는 연 립 반응계를생각하자. A+2X=3X B+X=C (7. 1)
이 반응은 생성물 X 가 빈응에 참여하는 자촉매 반응의 하나로 총괄 반응식은 A+B=C 이댜 첫째 반응은 삼분자 반응이고 일어날 가능 성이 희박하지만 A+X = Y ; Y+X = 3X 와 갇이 두 단계로 일어나 고 이 중에서 앞의 반응이 사전평형 (Pree qu i li br i um) 에 있다고 생각하 면 설명 이 가능하다 (Haken, 1978) . 연속적으로 A 와 B 가 공급되고 C 가 제거되는 반응기에서 이 성분들의 농도를 일정하게 유지한다고 하 자. X 의 농도만이 변할 수 있다고 할 때 정상 상태에서는 dX/dt = 0 이 된다; 정상 상태를 벗어나면 X 의 농도의 변화는 첫째 반응과 둘째 반응의 차로 표시될 수 있다. dX/ d t = k1AX2-k 김전 — k2BX+k _ zC (7.2) 여기에서 k 와 k _ 는 각각 i번째 반응의 정반응꾀- 역반응오의 반응 속 도 상수이다. 이 식에서 k1A = 3, k2B = {], k_ zC = r, k-1 = 1 이 라 하자. 그러면 (7.2) 식은 다음과 같이 된다. dX/dt = 3X2-X3-{3 X + r = -'l'(X ) + r (7.3) 정상 상태에서는 dX/dt = 0 이므로 다음 식을 얻는다. r = 'l'(X ) = X3-3X 탸{3 X (7.4) 쩌 X 의 함수로 도시하면 그림 7-1 과 같아지는데 /3 ~3 이면 r 값에 대응하는 X 값이 하나 존재한다• /3< 3 이면 Y는 극대값 (r2) 과 극소값 (r1) 을 갖는다. r1
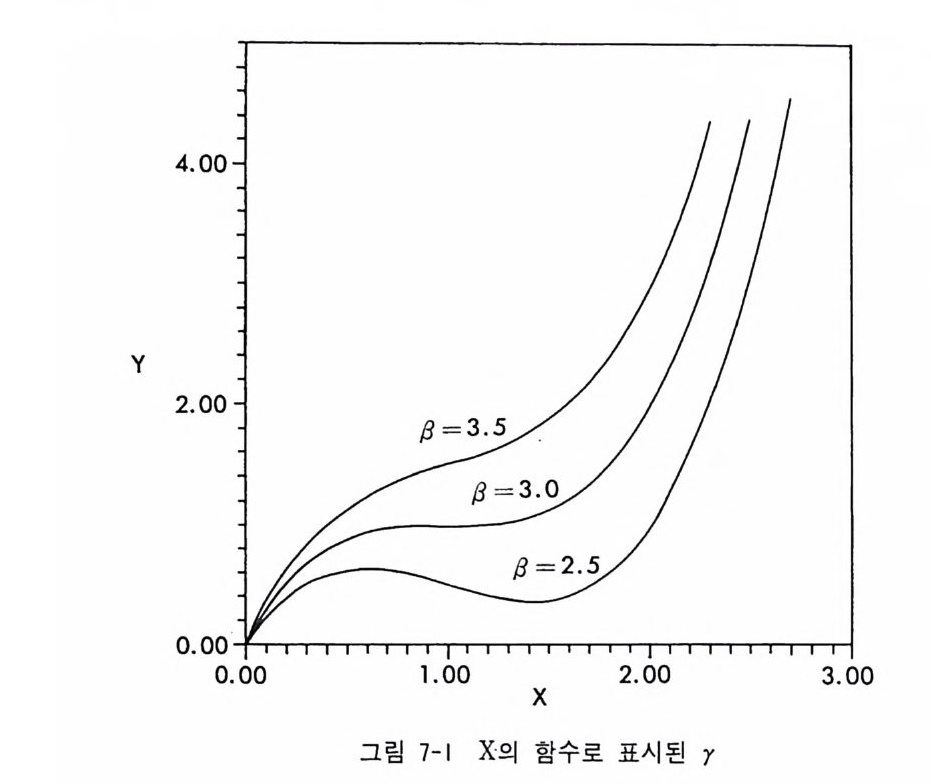 4.00
4.00
검토하였다. /3 = 3+ o ; r = 1+ o' : x = 1+x (7.6} 이 식들을 (7.3) 식에 대입하면 다음 식을 얻는다. dx/dt = -x3— XO — 8+ 8' (7. 7) 정상 상태에서는 다음 식이 유효하다. x3+xo = o'-o (7.8) 8= 8' 일 때에 x 를 계산하면 o~O 이면 하나의 실근이 그리고 o
(3=3 ;y = l;X=l (7. 9) 이 결과는 (7.5) 식에서 얻은 결과와 동일하다. 그림 7-2 에는 8— 8' 평면에 근의 특성을 도시하였다. 임계점이 원점이고 o>O 에서 원점으 로 접근하는 임의의 곡선을 따라서는 x 의 실근이 하나 존재하지만 8
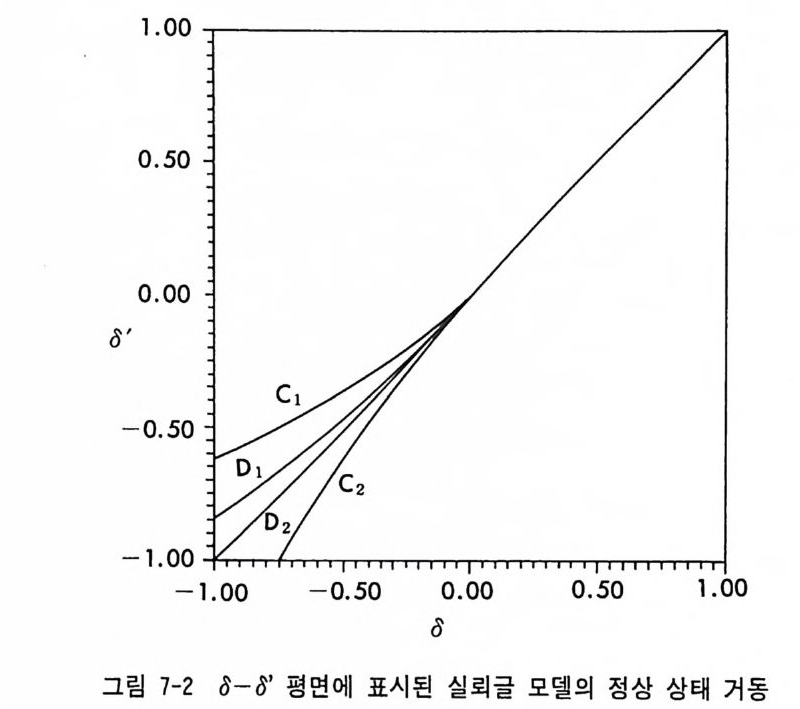 1.0 0
1.0 0
이들 X( 또는 x) 값에 해당하는 상태는 정상 상태이며 정상 상태의 안정성을 정규모드 해석 방법에 의해 검토하기 위하여 X 의 정상 상태 Xo 를 기준으로 한 요동 8X 를 다음과 같이 생각하자. X=X 吐 ax (7.10) 그러면 (7.3) 식에서
doX/ d t = dX/dt ~ 'l'(X ) -' l'(X 0 ) = (d 'l' /dX) 。 oX (7.11) 이다. 여기에서 (d 'l' /dX)o 는 정상 상태에서 계산된 도함수 값을 의미 한다.따라서 ax = ax 。 exp [ (d l'/d X) 。t〕 (7.12) 이다. 이제 8X 의 전화는 (d 'l' /dX) 려 부호에 따라 결정된다. 죽 (d 'l' /dX)o<0 이면 시간이 지나면서 요동이 사라지고 계는 안정하다. 위의 해석에서 실근이 하나인 경우에는 이 근에 해당하는 상태가 안 정하고 근이 세 개인 경우 즉 /3 <3 이고 r1 < r < r 2 일 때는 가운데 근 에 해당하는 상태는 불안정하고 나머지 두 개의 근에 해당하는 상태는 안정하다. /3 = 3 은 불안정이 나타날 수 있는 임계값이다. /3 > 3 일 때 에는 하나의 안정한 정상 상태만이 존재한다. 또한 (7.5) 식 또는 그림 7.1 에 예시된 이러한 거동은 다음에 주어진 제삼 비리알 계수까지를 포함하는 비리알 (V iri al) 식과 같은 3 차 상태 방정식에 의한 p-p 선 도와유사하다. p = RT p -3 p토p 3 (7 .13 ) 이 계의 정상 상태의 안정성을 판정하는 또 하나의 방법은 리아푸·노 프 방법을 이용하는 것이다. 이 경우에는 독립변수가 하나이므로 5. 2 절에서 검토한 방법에 따라 다음 식에 의하여 동역학 퍼텐셜 함수 0 를정의할수있다. dcf? / dX = 'l' (X) -y (7 .14) 그리고 이렇게 정의된 心는 X 가 (7. 3) 식에 의해 주어전 t의 함수일 때 에 5.2 절에서 보인 바와 같이 d~/d t ~O 의 조건을 항상 만족하므로 안정성 조건은 다음과 같이 된다. A >O (7.15) 정상 상태를 기준으로 생각하면 이 식은 안정한 정상 상태에서는 中
가 최소가 되어야 한다는 것을 의미한다. 위의 반응 모델에서는 요동을 나타내는 변수가 하나뿐아므로 우리는 5. 5 철에서 언급한 운동론적 안정성 이론을 이용할 수 있다. 운동론적 퍼텐셜은 다음 식에서 시작하여 결정할 수 있다. dxP[ 히 = JI ( dA1/T) +J2 (dAz /T ) = (J1 -Jz ) (dA1/T) (7 .16) 이 식의 유도에서 성분 A, B, 0 긱 농도가 일정하므로 dA1+dA2 = 0 인 관계를 이용하였다. 그러면 dX/dt = J1 -J2 = r- 'l' (X) 이므로 (5.63) 식에 따라 운동론적 퍼텐셜은 다음 식으로 주어진다. Ed
d
r = [ln(Xz /X 1)J -1J ['l'(X )/X]dX (7.24) 이 식에서 계산된 B 와 7 사이의 관계 즉 8 와 8' 사이의 관계를 그 림 7-2 에 곡선 D1 으로 표시하였다. 이 결과에서 두 퍼텐셜이 정상 상 태의 안정성 판별에는 동일한 결과를 주지만 퍼텐셜이 같아지는 8 와 8' 의 값 또는 정상 상태의 X 값은 약간 다르게 제시한디는 것을 알 수 있다. 코바타케 (Kobata ke, 1970) 는 운동론적 퍼텐셜이 동일한 두 정 상 상태가 다공성 멤브레인의 양쪽에서 실현될 수 있다고 지적하였다. 니콜리와 터너 (Ni co lis and Turner, 1977) 는 또한 임계점 근처에서는 요동의 역할이 증대되며 두 안정한 상태 사이의 요동이 중요하고 계의 거시적인 성질이 하나의 안정한 상태의 성질과 다르게 될 수 있다는 것을보였다. 다중 정상 상태를 나타내는 다른 모델로 에델시타인 (Edels t e i n) 의 다음반응모델이 프리고진과글란人두근立의 책에 인용되어 ' 있다. A+X = 2X X+E=C C=E+B (7 .25) 이 반응 모델의 총괄 반응은- A = B 이고 E 는 효소로 그리고 G 즌 효소와 기질 X 의 복합체라 생각한다. 그러면 총 효소의 양 T는 일정 할 것이므로 다음 식이 성립한다. E+C=T= 일정 (7.26) 앞의 실뢰글 모델에서와 같이 A, B 의 농도가 일정하게 유지된다면 다음 석이 성립한다. dA1+dA2+dA3 = 0 (7. 27) 이 관계를 이용해서 dxP 를 쓴다. dxP = ~J, (dA,/T)
= (JI — J2 ) ( dA1/T) + (}3 - J 2) (dA3 /T ) (7.28) 이제 모든 반응 속도 싱수들을 1 이라 하면 반웅 속도식들을 다음과 같이쓸수있다. dX/dt = J1 -J2 = AX-X2-XE+C dE/dt = J3— L = —X E— B E+2C (7.29) 정상 상태의 X 와 政값은 이 두 식에서 dX/dt = dE/dt = O 일 때에 얻어진다. X 의 농도는 E 를 소거한 다음 식의 해로 주어진다. X 프 (2+B— A) X2+[ T — A( 2+B)]X - B T= 0 (7.30) X 가 구해지면 다음식에 의해 E 긱 농도를 구할 수 있다. E = 2T/(X+B+2) (7 . 31) 이제 반응식 (7.25) 에서 효소 반응의 미카엘리스-멘튼 (M ic hae li s -Mento n ) 기구에서와 같이 활성 중간 생성물인 C 에 대해 정상 상태 가정 (Ste a dy Sta t e A pp rox i ma ti on) 을 도입한다. 이 가정은 디음 관계 롤의미하고 dC/dt = J2 -J3 ~ Q (7 . 32) 따라서 dE/d t ~O 이 성립되며 (7.31) 식음 정상 상태를 벗어나더라도 유효하게 된다. 그러면 c = l 이라 하고 운동론적 퍼텐셜을 다음과 갇 이 쓸수 있다. d«l> p = —[ (AX ― X2-XE+C)/X 〕懿 (7 . 33) I) 이 식에서 E는 (7.31) 식에 의해 X 의 함수가 되고 C 는 (7 . 26) 식에 서 E 라 함수가 된다. 이 퍼텐셜 함수 아를 A=8.5, B=0.2, T=30
1) 프리고진과글란소干己立의 책에는한항이 추가되어 있다. 이들은 (7.32) 식 으로 표시되는 정상 상태 가정을 형식적으로는 이용하지 않고 (7.31) 식에 따르 는 X와 距 관계를 이용했다. 그러나 정상 상태를 벗어나서 (7.31) 식을 이용하 는 것은 (7 . 32) 식을 이용하는 것과 동일하다.
일 때에 X 의 함수로 계산한 결과를 도시하면 그림 7- 料} 같다. 여기 에서 임의로 X=0.1 일 때에
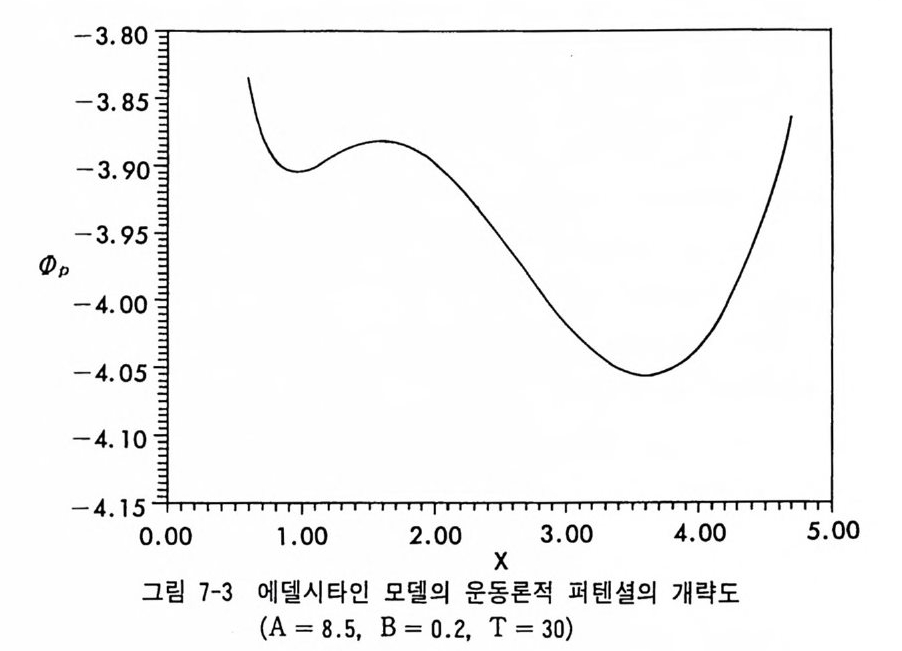 -3 .80
-3 .80
dp/ dX = 匡 주거지는 정상 상태는 (7.18) 식에서와 갇이 d2< I>p/ dX2> 떠 조건이 만족되면 안정하다. 그림에서는 중앙의 정상 상태는 불안정하고 양쪽 두 개의 정상상태는 안정하다는 것을 알 수 있다. 여 기에서도 앞의 실뢰글 모델에서와 같이 동역학 퍼텐셜 0 또는 운동론 적 퍼텐셜 야가 같게 되는 공존 상태를 얻을 수 있을 것이고 확산이 중요한 계에서 이들 상태가 공간적 구조를 나타낼 수 있음을 생각할 수 있다. 앞의 실뢰글 모델에서와 같이 운동론적 퍼텐셜과 리아푸노프 함수로 제시되는 퍼텐셜은 정상 상태의 안정성에 관해서는 같은 결과 를 주지만 퍼텐셜이 같아지는 X 값은 다르게 제시한다. 이 점과 관련 된 문제점들은 니콜리와 레페버 (Ni co li s a nd Lefe rv er, 1977) 가 논의한 바 있다• 실뢰글 모델과 에델시타인 모델에 대응하는 반응은 실험적으
로는 확인되지 않은 것으로 보인다. 다중 정상 상태의 모델은 또한 생 체 분리막을 통한 물질의 변환과 이동의 설명을 가능하게 하는 한 모 델로도 생각되고 있다. 평형 근처에서는 정상 상태가 항상 안정하다는 것을 우리는 알고 있 다. 그러나 평형에서 멀리 떨어진 정상 상태의 안정성은 일반적으로 보장되는 것은 아니다. 위에서는 정규모드 해석에 의해서 정상 상태의 안정성을 검토하였으며 또한 리아푸·노프의 방법과 일반적 전화의 법칙 에 근거한 운동론적 퍼텐셜을 이용해서 정상 상태의 안정성을 살펴 보 았다. 다중 정상 상태를 나타내는 계의 또 하나의 특징은 히스데리 현 상을 보일 수 있다는 것이다. 확산이 없을 때 디중· 정상 상태가 존재 하면 일종의 히스테리 현상이 존재하는데 위의 예에서는 Y 가 정상 상 태를 유지하면서 서서히 변화하면 하나의 정상 상태의 가지에서 다른 가지로 그림 7-1 에 보인 바와 같이 서로 다른 경로를 따라 변화하는 것을알수있다. 3 대칭성 파괴의 불안정성 6. 4 절에서 검토한 브럿셀레이터 반응식을 다시 생각하자. A=X 2X+Y=3X B+X=Y+D X=E (7.34) 여기에서는 모든 역반응을- 무시하고 확산항을 추가해서 중간 생성물 X 와 Y 에 관한 속도식을 다음과 같이 쓰자. ax/at = A+X2Y-BX-X+Dx a2X/ar2 aY/at = -X2Y+BX+Dv a2Y/ar2 (7. 35)
여기에서 확산항은 일차원 좌표계에 대해서만 고려하였고 6.4 절에 서와 같이 모든 반응 속도 상수들을 1 이라 하였다. 먼저 정규 모드 해석을 시도해 본다. 정상 상태를 기준으로 선형화 한식은다음과 같다. doX/dt = 〔 2XoY 。 ._ B-l]oX+X 。 20Y+Dx 장 X/ 記 doY/dt = [B ― 2X 。 Y 。 ]oX-X 。 28Y+DY 꾼 Y/a 군 (7.36) 다음과 같이 oX 와 oY 를 가정한다. ax = (ax) 。 exp (wt+i r/ .-1) 8Y = (8Y) 。 ex p (wt+i r/ .-1) (7 . 37) 여기에서 A 는 비균일성의 파장이다.이 식을 (7.36) 식에 대입하면 다음 특성 방정식을 얻게 된다. w2 + [A2 + 1-B + a + b] w +A2(1+a) + (1-B)b+ab = 0 (7 . 38) 여기에서 a = Dx/A2 ; b = Dv/112 (7 . 39) A... ... 00 이면 시간에만 의존하는 요동이 되고 분산 방정식은 k = O 일 때 의 (6.46) 식과 같게 된다. 이 계는 (7. 38) 식의 일차항의 계수와 상수항이 모두 0보 다 크거나 같을 때 안정하다. w의 실수부분이 0 이 되는 한계 안정성 · 조건의 거 동으로 두 가지롤 생각할 수 있다. 하나는 (7.38) 식의 일차항의 계수 가 0 이 되고 상수항이 0 보다 큰 경우이다. 그러면 근은 허수가 되고 한계 안정성의 상태는 과도 안정성을 보인다. Be’ 과 BC” 를 다음과 같이 표시하면 Be ' = l+A2+a+b Be = (A2+b) (l+a)/b (7.40)
Be’ 은 일차항의 계수를 但냐 1 하는 값이고 Be 은 상수항의 값을 0 으로 하는 값이다. 이때에 계가 불안정해지는 조건은 다음과 같이 된다. BC'< B (7 . 41) 두번째는 상수항이 0 이고 일차항의 계수가 0 보다 큰 경우로 이때에 는 한 근이 반드시 0 이 된다. 따라서 한계 안정한 상태는 안정성 교환 의 경우가 된다. 이 경우에 불안정성 조건은 디움과 같이 된다. BC'’
댜 위에서는 반응 속도 상수들을 l 로 놓고 검토하였지만 이제 이들을 포함한 석을 쓰면 (7.44) 식과 (7.45) 석은 다음과 같이 된다. Ac = (k4/ k /k2) 0 ·5 (Dx D v) 0·5/A (7 . 46) Be r = [ (k4/ k 3) + A (k1/k4) (kz /k 3 ) 1 12 ( Dx/Dv) 112] 2 (7 . 47) 이 식들에서 보면 불안정성이 화학반응과 확산의 협동 효과라는 것 을알수있다. 4 대칭성 파괴 불안정성의 열역학적 검토 이제 열역학적 방법으로 대칭성 파괴의 불안정성을 검토해 보자. 5 장에서 검토한 바와 같이 (5.55) 식의 안정성의 조건은 다음- 식으로 표 시된다. P[o 인 = J ~oX10Y1dV 착) (7 .48) 먼저 (7.42) 식으로 주어지는 불안정성의 조건을 검토하자. 앞에서 와 마찬가지로 역반응을 무시하고 확산항은 유지한다. 그러면 정상 상 태 를 기준으로 한 요동에 대해 다음의 과잉 엔트로피 생성속도식을 얻 는다. P 醫 S J = (1-B) (oX)2/A+A2(0Y)2/ B +Dx(oX)2/.-l2 A +Dv(oY)2/.-l2 B . (7. 49 ) 여기에서 반응 속도 상수들과 RT를 1 로 생각하였으며 이 식은 (6 . 53) 식에 확산항을 더한 형식으로 표현되어 있다. 그리고 확산항은 과잉 농도 구배를 선형화해서 표시하고 있다. 이 식에서 다음 두 점에 유의하자. (1)-B(oX)2/A 로 표시되는 음수의 항은 X 의 저촉매 반응에서 기 인한다. 이 항은 안정성에 위험을 주는 요소이다.
(2)D/A2 에 비례하는 확산항은 양수이다. 따라서 불안정성이 있다면 D 가 증가할 때 임 계 파장 A 죠- 증가한다. 대칭성 파괴의 한계 안정성 조건에서는 Wr=W1=0 이고 (7. 36 ), (7 . 37) 식에서 디움 관계가 성립한다. oY = —(1 +Dx/A 아 / (DY/A2) 8X (7.50) 따라서 이 관계를 (7 . 49) 식에 대입하면 다음 식을 얻는다. {P [ oS] }s= B cr = 0 (7.51) 6 장에서와는 달리 대칭성 파괴 안정성의 한계 조건은 과잉 엔트로피 의 생성 속도가 0 이 된다는 조건으로 표시된다. 또한 확산에 관한 불안정성에 대해 임계 천화력을 6 장에서와 같이 계산할 수 있다. 그러면 (6.47) 식 대신 다음 식을 얻는다. Re = (l/k3 y A 2D) {2k2[r (l+k)]l l2 [ 2k9D3+5k6ND2 + 4k3A4D + A 기 1/2 + k7D2 + kT2A2+ k2 Y ( l + k) +3k 입\.2 ]D+kA2[A2+k2 y (l+k) +krA 기 } (7.52) 여기에서 Y = DY/Dx 이다. 또한 해당하는 임계 파장은 다음 식으로 주어전다. 않 = k3r(2k3D+A2)Dx2/[(k1D2+2k4A2D+kA4) (l+k)] (7.53) 懿테서 검토한 것괴는 다르게 (7.53) 식은 제한된 D 값의 범위에 한 정된 것이 아니다. (6.48) 식에서 k3D>A2 이면 정상 상태의 계는 불 안정해진다. 그러나 위 식의 임계 파장은 그러한 조건과는- 상관이 없 으므로 k3D>A2 인 경우에는 반응과 확산의 간섭이 존재하지 않고 확 산 계수가 같다고 하더라도 계는 균일하지 않은 교란에 대해서만 불안 정해질 수 있다. 硏k ] 서 검토한 거동과 비교하면 다음 현상을 발견한다. 여기에서
는 안정한 정상 상태는 A 값의 어떤 영역에서는 불안정해지면서 안정 한 공간 구조로 전이된다. 한편 6 장에서는 안정한 정상 상태가 불안정 해지면서 극한 싸이클로 전이된다. 여기에서는 정규모드의 고유치가 임계점에서 허수부를 갖지 않지만 6 장에서 검토한 시간적 구조를 나타 내는 불안정성에서는 허수부를 갖는다. 이 차이는 위상 공간에서 거동 의 차이를 나타내며 요동이 허수부를 갖는 경우의 정상 상태를 초점 (Focus) 그리고 허수부를 갖지 않는 경우의 정상 상태를 노드 (Node) 라 부른다. 그림 7-4 에 노드를 표시하였다. 또한 로트카국t테라 모델 의 정상 상태는 중심 (Cen t er) 이라 불린다. 6 장에서 검토한 바와 같이 극한 싸이클로 표시되는 시간적 구조를 갖는 계는 두갈래치기점에서 안정한 초점이 불안정한 초점이 되며, 이 장에서 논의한 공간적 구조 롤 생성하는 두갈래치기는 다음과 같이 표시할 수 있다. 안정한노드—」二 불안안정정한한공노간드구 조 위의 논의는 선형화된 계의 정규 모드에 관한 것이었다. 문제는 원 래의 비선형계의 거동이 선형화된 계의 거동과 어떤 관계가 있는가 하
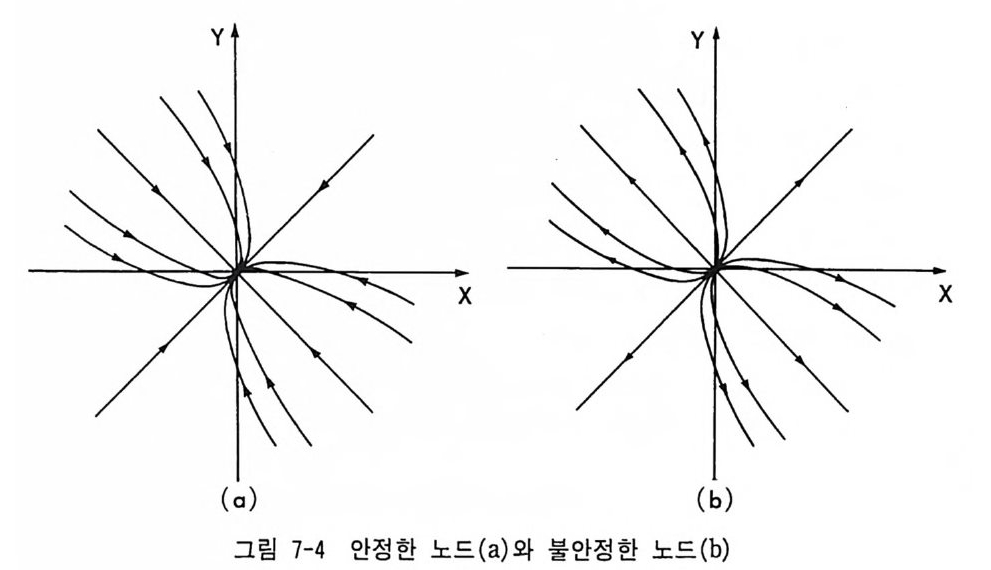 Y Y
Y Y
는 것이다. 일계 이원 비선형 상미분 방정식으로 표시되는 계의 거동 과 선형화된 계의 거동 사이에는 다음 관계가 있다는 것이 알려져 있 다 (Ledermann and Vajd a , 1982). 선형화된 계의 중심은 비선형계의 중심 또는 초점, 선형화된 계의 노드는 비선형계의 노드 또는 초점이 된다. 그러나 선형화된 계의 초점은 비선형계의 초점이 된다. 5 공간적 소산 구조 7.4 절에서는 확산항을 포함한 브럿셀레이터 반응의 안정성을 정규 모드 해석에 의해 검토하였다. 실제로 공간 구조의 해석을 위해서 여 기에서는 브릿셀레이터에 대한 (7.35) 식 대신 다음 식을 생각하기로 하자. dX1/dt = A+X/Y)— BX 1-X1+Dx(X2-X1) ddXY2i //ddtt == ABX +1 X— zX 2Y/Yz1-B+XDzv —(YX22 -+Y D1x) (X1 —X2 ) dY2/dt = BXz— X /Y2+Dv(Y1-Y2) (7.54) 이 식들은 원래의 문제를 단순화시켜 두 개의 상자를- 생각하고 각 상자의 농도는 균일하며 두 상자 사이에 확산이 가능하다고 생각한 것 이다. 위의 식에서 하첨자 l 과 2 는 상자 1 과 2 를 의미한다. 또한 앞 에서와 같이 역반응을 무시하고 반응 속도 상수들을 1 이라 하였다. 두 상자를 가정한 해석은 분명히 너무 간단해 보이지만 이러한 관계식들 울 인접한 두 상자에 적용하고 상자 수를 증가시키면 실제계의 거동에 가까운 수치해를 얻을 수 있다. 이 식의 시간에 의존하지 않는 정상 상태의 해는 균일한 상태에 대 해 다음과같다. X1 = A ; Y, = B/A (i = 1, 2) (7 . 55)
이제 디음 값들을 가정한다. Dx = 1 ; A = 2 (7. 56) 그러면 이제 남는 매개변수들은 B 라 D 려고 이 값들이 정상 상태의 성질을 결정한다. (7.54) 식에 (7 . 56) 석의 값들을 대입해서 정상 상태 에 대해 정리하면 다음 석들을 얻는다. 3X 2 드 30X2 나 [96+2Dv (B+3) 〕 X2 드 [96+ 12Dv (B+3)]X z2 +l6Dv(B+6)X2-96Dv = 0 (7.57) X1 = 4 一 X2 (7.58) Y2 = B(8Xg -4 DY— l6 X2_x23)/[8 X 23-3Xz2(Dy + 8) +8Dy ( X2-2) -X 리 (7.59) Y1 = Y2+ (X/Y2— BX 2)/Dv (7. 60) 이 석들의 해는 두 종류가 있는데 하나는 (7.55) 식으로 주어전 것과 같은 균일한 계에 대한 것이고 다른 하나는 균일하지 않은 계에 대한 것이다. 상자 1 과 2 에 대한 농도는 상자 l 과 2 가 대칭이므로 불균일 한 계에 대한 해는 다음 조건을 만족한다. X1>X2 ; Y1
(7.47) 식에서와 같이 Dx 와 A 가 주어지면 (7 . 62) 식과 (7.63) 식에서 D 와 B 에 따라 정상 상태의 종류에 따르는 안정성이 결정된다. 이 결 과는 D-B 평면에 여러 영역으로 표시된다. 글란人두근立와 프리고 진 (Glansdorff an d Prig o g ine , 1971) 의 책에 이 영역들을 그림으로 표 시하고검토하였다. 6 정리 이 장에서는 공간적 구조를 가질 수 있는 두 그룹의 반웅 모델들을 검토하였다. 공간적 구조에 도달하기 위해서 확산의 역할이 중요하다 는 것은 공통적이지만 실뢰글 모델이나 에델시타인 모델에서는 디중 정상 상태를 통해서 그리고 브럿셀레이터 반응에서는 대칭성파괴의 불 안정성을 통해서 공간적 소산구조에 도달한다• 대칭성 파괴의 불안정 성은 안정성 교환의 원리를 따르며 안정한 노드가 불안정한 노드가 되 거나 안정한 소산 구조를 생성하는 두갈래치기점에서 소산구조를 택하 는쪽으로변화한다• 이 두 경우의 안정성 해석에는 선형화된 계에 대한 정규 모드 해석 방법이 이용될 수 있다. 그러나 변수가 하나인 다중 정상 상태 를 나타 내는 계에서는 동역학 퍼텐셜이나 운동론적 퍼텐셜이 직접 이용될 수 있다. 대칭성 파괴 불안정성의 한계 안정성 조건은 정규 모드 고유치 의 실수부와 허수부가 각각 0 이 된다는 조건에서 과잉 엔트로피의 생 성 속도가 0 이 되는 조건으로 표시될 수 있다•
제 8 장 베나드 대류 I 서론 두 평판 사이에 정지된 유체가 채워져 있고 밑으로부터 가열되는 계 롤 생각한다. 밑면의 온도와 윗면의 온도를 각각 일정하게 유지할 수 있다고 가정한다. 유체의 열전도도가 일정하다면 충분한 시간이 지난 후에 유체충의 온도 분포는 잘 알려진 바와 같이 직선 분포를 보이게 된다. 이러한 온도 분포는 밀도의 차를 유발시키고 중력장에서 아래에 있는 유체가 부력의 영향으로 위로 움직이려 하~근 경향이 생간다. 그 러나 이러한 경향은 온도차가 작을 때에는 점성력에 의해 억제되어 정 지되어 있는 구조가 안정하지만 온도차가 어떤 한계 이상이 되면 불안 정해진다. 그 결과로 유체가 더 이상 정지해 있는 것이 아니고 일정한 형태의 유선을 그리는 대류 오동 을 보이게 된다는 것이 알려져 있다. 베나드 (Bernard, 1900) 는 상충이 실온에 노출된 얕은 유체충을 밀에서 가열할 때 유체가 육각주의 규칙적 형태를 유지하면서 운동하게 되는 것을 발견하였다. 육각형의 크기는 대략 유체충의 두께와 같았으며 유
체는 육각주의 중심 부분에서 상승하고 상부에서는 밖으로 흘러나가서 아래로 육각주의 의면을 따라 내려온다. 이 현상의 해석은 레일리 (Ray le ig h , 1916) 가 한 이후에도 확장되어 왔고 찬드라세커 (Chandraseker, 1961) 의 고전적 책에 기술되어 있다. 근래에는 부스 (Busse, 1985) 에 의해서도 개관되었다. 이러한 구조는 온도차가 증가함에 따라 다시 불안정해지고 궁극적으로는 난류 유동 현상에 도달한디는 것이 알려져 있다. 이 장에서는 검토되는 문제논 밀면이 충분히 천천히 가열되어 일정한 온도 구배에 도달할 수 있는 경우에 정지된 유체가 불안정해지는 조건만을 정규 모드 해석에 의한 방법과 열역학적 방법에 검토하기로 한다. 가열 조건이 급격할 때에는 시간 의존적인 온도 구배에서 불안정성이 발생할 수도 있고 이러한 현 상도 많이 연구되고 있다. 베나드 문제 또는 베나드-레일리 문제로 알려진 이 유체의 불안정성 문제를 생각하기 위해 먼저 비압축성 유체에 대한 질량보존식을 생각 한다• 그러면 (2.25) 식으로부터 다음 식을 얻는다. '\l·V = 0 (8 .1) 그리고 (2.36) 식으로 표시된 비압축성 유체에 대한 운동량 보존식은 의력이 중력 G 인 단일 성분계에 대해 다음과 같이 표시되며 po V/ot+ pV •v 'V = pG -v'p + 2µv '•D (8 . 2) 여기에서 D = [v'V + (W) 지/2.£ 2 장에서 정의된 바 있다. 이 식은 또한 (2.36) 식으로 주어진 나비에—人두더 ~(Nav i er-S t okes) 식의 형 식으로 표시될 수 있다(예를 들어 Slatt er y, 1972 참조). p[ o(V)/at+ V·v'V ] +v'p = pG +µv '2V (8 . 3) 또한 (2.46) 식으로 표시된 내부 에너지 보존식은 단일 성분 비압축 성 유체에 대해 디음과 같이 표시된다. o(p u )/a t+v'· (Jq+pu V) = —pd : v'V (8.4)
이 식에서 Jq는 (2.48) 식으로 주어진 푸리에 법칙으로 다음과 같이 표시될 수 있다고 생각한다. Jq = —xv T (8 . 5) 그리고 내부 에너지의 밀도 u 는 다음식으로 표시한다. u=cvT (8 . 6) (8.5) 식과 (8.6) 식을 (8.4) 식에 대입하면 x, P, Cv 가 온도에 의존 하지 않을 때에 다음 식을 얻는다. aT/at+ V VT = (x/pC v) V 2T (8 . 7) 여기에서 (8.4) 식의 pd : vV 항은 (8.10) 식의 내부 에너지 수지식 에서 전도의 영향을 나타내는 항 AV2T 에 비하여 작다고 가정하고 생 략하였는데 2 장에서 생각한 바와 같이 pd : vV 항은 기계적 에너지가 내부 에너지로 소산되는 효과를 나타내고 있다. 실제로 다음 표현식의 값은 I( Pd : vV ) / (xv 2 T) I (8.8) 유체의 깊이가 1cm 정도일 때에 액체 헬리움을 제의하고는 10 - 9 에서 10-1 정도로 무시할 만하다• 이제 문제를 단순하게 하기 위하여 부시네스크 (Bouss i nes q)의 근사 법으로 알려진 가정을 도입한다. 이 가정에 의해 p의 온도에 따르는 변화를 운동량 보존식에서만 (8.3) 식에 의해 고려하기로 한다. 이를 위해 유체의 밀도를 온도의 선형 근사식으로 다음과 같이 표시한다. p (T) = Po[l— a(T— E )] (8 .9) 그러면 (8.1) 식은 그대로 유효하고 (8.3) 식과 (8.7) 식은 다음과 같 게 된다. Po[a(V)/at+ V•v V] +vp = (po +8p ) G+µv 2 V (8.10)
aTIat + V ·'v T = (xi Po Cv )'12 T (8 .11) 부력과 점성력의 비를 레일리 (Ra y le ig h) 수라 부르고 R ai료 표시하 기로한다. Ra = lop G /Pol/lµV2V /Po l (8 .12) (8.9) 식으로부터 다음 관계를 쓸 수 있다. op /po = at: :.T = a/3 d (8 .13) 여기에서 fJ = l '1 TI 츠b. T/d 이고 d 는 유체충의 깊이이다. 또한 연 산자 V 는 유체충의 깊이 土료 나누는 것에 상당하므로 (8.11) 식으로부 터 다음관계를 얻는다. IV I 타 / (poC v d ) (8 .1 4) 중력 가속도의 절대치를 g, 그리고 동점도 v = µ / Po 를 써서 표시 하면 (8.12) 식의 레일리 수는 (8.12) 석과 (8.13) 식을 이용해서 다음과 같이쓸수있다. Ra = a/3 gpo Cvd4/ lJX (8 .15) 여기에서 (x/PoCv) 는 열확산 계수로 묶어 표시되기도 한다. 레일리 수는 물성이 일정한 계에서 실험적으로 역온도구배 B 를 조절하여 변 화시키는 것이 가능하며 이 수가 임계 레일리 수 Rae 보다 커지면 정 지된 유체충이 불안정해지고 대류가 시작된다. 문제는 Rae 를 계산하 는것이다. 이 장에서는 정규 모드 해석 방법과 과잉 엔트로피의 생성 속도에 의한 열역학적 판정 기준을 이용한다. 여기에서 검토하는 안정성 문제 는 안정성 교환의 원리를 따르는 것으로 알려져 있고 이 원리가 적용 된다는 것을 보일 것이다. 다음 장에서는 같은 문제를 국소 퍼텐셜울 이용해서 해석하는 방법도 제시하게 된다.
2 선형화된 과잉 수지식 찬드라세카 (Chandrasekhar , 1961) 에 의한 논의에 따라 선형화된 과 잉 수지식들과 경계 조건들을 검토하기로 한다. 부시네스크 식 (8.9) -(8.11) 의 정지 상태의 해는 쉽게 구해진다. T = T 。 - {J z (8 .16) p = p。 ( 1 + a{J z ) (8 .17) p = p。 - gp。 (z+a 합 /2) (8 .18 ) 이러한 해는 온도 구배가 작은 경우 즉 레일리 수 Ra 이 작은 경우 에 실현 가능하지만 Ra 이 증가해서 Ra e 보다 커지면 요동에 대해 불 안정해진다. 작은 요동에 대한 안정성을 검토하기 위해서 여기에서는 부시네스크 식을 정지 상태 를 기준으로 요동에 대해 선형화해서 속도 V(z, t), 압력의 요동 op, 그리고 다음 식으로 주어지는 온도 분포의 요동 0 에 대해 표시한다. T = T 。―[3 z+ 0 (z, t) (8 .19) 이제 정지 상태 해의 안정성을 검토하기로 한다. 기준 상태가 정지 상태이므로 속도 벡터가 직접 요동 속도를 의미한다는 것에 유의한다. 그러나 밀도의 독립적 요동은 고려하지 않고 부시네스크의 가정에 의 해 온도 함수 0(z, t)에 의존하는 것만 포함시키기로 한다. p( z, t) = Po[l+a{/ 3 z -0(z, t)}] (8 .20 ) 그러면 이들 변수에 대한 선형화된 부시네스크 식은 다음과 같게 된 다. Vav·V/a =t = 0 —(1/ Po)V(op ) + (µ/Po)V2V+g aB lf z ((88..2221)) ae/at = {J v 급 (x/ p oCv) 한 0 (8.23)
여기에서 rr z 는 z 방향의 단위 벡터이고 중력의 반대 방향이 양의 방 향이다. 압력의 요동을 소거하기 위해서 (8.22) 식의 양변의 curl 을 취 한 후에 z 성분만을 표시한다. 속도의 curl 인 VX V 이 와류도 (Vortic ity) W 가 되고 발산의 curl 은 0 이 되므로 다음 식을 얻는다. owz/ot = (µ/Po) '12 W z (8. 24 ) 또한 (8 . 22) 식의 curl 을 두 번 취하면 a('v 2 Vz)/at = ll 'v 4V z + g a( 장 /ax2+ 장 /a y 2 ) O (8.25) (8.21), (8.23), (8.24), (8.25) 식들이 필요한 과잉 수지식들이다. 다음에 자유 경계면과 고정 경계면에 대한 경계 조건들을 각각 생각 한다. 유체의 윗면과 아랫면의 온도는 일정하고 또한 이 경계면에서는 유체가 밖으로 나갈 수 없다. Vz= 0=0 Z=0 Z=d (8 . 26) 또한 윗면은 대기에 접해 있으므로 자유 경계면이고 아랫면은 고체 와 집하고 있으므로 고정 경계면이다. 고정 경계면에서는 Vx = Vy = 0 이고
cJvx /az = avy/ a z = 0 (8 . 30) 필요한 다른 경계 조건들도 얻을 수 있다. (8 .28 ) 식의 z 에 관한 도함 수를 취하면 다음 석이 성립한다. 장 V z /3 균 = O (8 . 31) 와류도 W 의 정의와 위의 식들에서 지유 경계면에 대해 다음 관계 가성립한다. awz /a z = 0 (8 . 32) 3 선형 이론의 정규 모드 해석 정규 모드 해석을 위해 다음과 같이 표시되는 이차원 요동을- 생각하 자. Vz = V (z) exp [i (kxx + ky y) + ft] Wz = W (z) ex 碩 (kxx + ky y) + ft] 0 = 8 (z) exp [i (kxx + ky y) + f디 (8 . 33) 여기에서 주파수 f는 복소수가 될 수 있지만 파수 kx, k y는 x, y 의 존성이 실험 결과와 일치하게 주기적이라 하면 실수가 되어야 한다. 이 식들을 (8. 23 ) — (8.25) 식에 대입하면 다음 식들을 얻고 f 8(z) = (JV (z) + (11/ p。 C p) (d2/dz2-k2)8(z) (8.34) f W (z) = v (d2/dz2 玉) W (z) (8 . 35) f (d2/dz 드 k2)V(z) = —ga k28(z) + 11 (d2/dz2-k2 ) 2V (z) (8 . 36) 여기에서 k2=kx2+k y 2 이다. 앞절에서 논의한 경계 조건들은 다음과 같이 정리해서 표시된다.
8=V=O z=O z=d (8 . 37) W = dV/dz = O 고정 경계 면 (8 . 38) dW/dz = d2V/dz2 = 0 자유 경 계 면 (8. 39 ) 이제 무처원 변수들을 다음과 같이 도입한다. [즈, x, 김 = [x/d, y/d , z/d] ! = t/ (d2p oC p / X) ~ = 8/ ((Jd /Ra) a = kd ;
F(z) = (D2- a 2 - a/P r)G(z) (8 . 46) 그러면 (8 . 43) 식은 다음과 같이 표 시된다. F (z) = a28 (z) (8 . 47) @에 대한 경계 조건에서 F 에 대한 경계 조건도 생각할 수 있다. F=Oz=Oz= l (8 . 48) (8.44) 식을 다시 쓰면 (D2 - a2 -6 )F(z) = —R a a2V(z) (8 . 49) 이다. 이 식의 양변에 F(z) 의 공액 복수二 함수 F(z) *를 곱하고 유체 충에 대해 적분한다. Jd zF (z) * (D2 - a2 - 6) F (z) = —R a a2J d zF (z) *V (z) (8 . 50) 다음에 좌변의 첫항을 부분 적분한다. Jdz F (z) *D2F (z) = F (z) *DF (z) I01 -Jdz lDFl2 (8 . 51) 이 식의 우변의 첫항은 경계 조건 (8 . 48) 식에 의해 0 이다. 이제 (8 . 50) 식의 우변을 적분한다. Jd zF (z) *V (z) = Jd zV (z) (D2-a2-6 * /P r) G (z) * = Jdz G (z) * (D 드 a2 - 6* /P r) V (z) (8 . 52) 이 식에서 둘째 줄의 표현식은 앞 식을 두 번 부분적분해서 얻는다. G 의 정의식을 이용하면 이 식을 두 부분으로 나누어 쓸 수 있다. Jdz G (z) *G (z) — ( 6*/Pr) Jd zV (z) G (z) * = Jd zG (z) *G (z) — ( 6*/Pr)J d zV (z) (D 드 강) V (z) * = Jd zG (z) *G (z) + (6*/Pr) Jdz (IDV (z) l2+ a2IV (z) 12) (8 . 53) (8.51) 식과 (8.53) 식을 (8 . 50) 식에 대입하면
Jdz [IDF (z) l2 + (a2 + 6) IF (z) |기 = Ra a2J d z[IG (z) l2+ (6*/Pr)[IDV (z) l2+ a2 IV (z) l2]] (8.54) 이다.또는 Jd z[IDF (z) 12+ a2IF (z) 12-Ra2IG (z) 円 = —a*aJf d d z z (lRFa (z2)/ P12 r) [|D V( z) 12 + a2IV (z) 12]_] (8 . 55) 이 식의 허수 부분을 취하면 좌변이 실수이므로 다음 식이 성립한 다. Im(
(8. 4 5) 식은 (J = 0 이면 다음 식이 된다. (D2-a 2) 3 V (z) = -R a a2V (z) (8 . 57) 이 식이 프란툴 수에 무관한 것에 주목하자• 이 식은 (8 . 37) 식과 (8 . 39) 식의 경계조건에 대해 풀어야 한다. 레일리 (Rail e y, 1916) 가 생 각한 고전적인 문제는 윗면과 아랫면이 모두 지유- 경계면인 경우이다. 두 면이 모두 자유 경계면인 경우는 실험적으로 실현되기는 어려운 경 우이다. 이 경우에는 (8.37) 식과 (8.39) 식에 추가해서 디~ 경계조건 이 성립된다. (D2- a 2) 2 V (z) = 0 z = 0 z = 1 (8 . 58) 이들 경계 조건에 대해 (8 : 57) 식의 해는 다음과 같이 주어진다. V (z) = V 。 sin (nJ fz) (8 . 59) 여기에서 고유치 Ra 은 n 과 다음식으로 관련된다. Ra = (n 2 군 +a 2 ) 3 /a2 n = l, 2, 3, …… (8. 60 ) 가장 작은 Ra 값은 n = O 일 때 a2 에 대해 최소화된 값이다. Rae = 27 군 /4 츠 657.511 (8. 61) 그리고 이때의 무차원 파수 ac 는 다음 식으로 주어진다. ac = 군 /2 (8 .62) 양면이 고정 경계면인 경우의 해는 찬드라세카가 구한 바 있고 또한 고정 자유 경계면에 대한 해도 구해졌다. 여러 가지 경계 조건에 따르 는 임계 레일리 수들은 표 8-1 에 정리되어 있다. 정규 모드 해석에 의 한 결과는 다음과 같이 정리할 수 있다. 레일리 수가 작아서 Ra
으로 생기는 것이 아니고 안정성 교환의 원리에 따라 갑자기 생긴다. 이 대류 구조는 유한한 크기의 세포로 구성되며 이 세포의 특성 길이 는 Le = 2 교 /ac 이다. 그러나 아직도 해답이 구해지지 않은 다음과 같 은 문제들이 있다. 이렇게 생긴 대류 구조는 어떠한 것인가? 이렇게 생긴 구조는 어떤 레일리 수까지 안정할 것인가? 레일리 수가 더욱 증가하면 어떠한 현상이 일어날 것인가? 이러한 구조는 실험적으로 관찰되는 것인가? 이러한 질문들의 해답에 앞서 다음 절에서는 열역 학적으로는 안정성에 관해 무엇을 말할 수 있는지 먼저 살펴보기로 한 다.
표 8-1 베나드 대류에서 여러 경계조건에 따른 임계 레일리 수 경계 조건 Rae ac 자유-자유 657.511 2.2214 고정-자유 1100.650 2.6820 고정-고정 1707.762 3.1170
4 수력학계의 열역학적 안정성 이론 5 .4절에서 검토한 글란人두근立와 프리고전의 안정성 이론에 따르 면 비평형 기준 상태의 안정성 조건은 다음 식으로 제시된다. 82s-::;;:o (8 . 63) a 성 s/ at ~O (8 . 64) (8.63) 식은 국소 평형인 계에서 항상 성립되므로 요동이 (8.64) 식을 따르는 계는 안정하다. 그러나 과잉 엔트로피의 표현식에는 대류의 영 향이 포함되지 않고 있으므로 이 식들이 대류가 존재하는 계들에 적용 될 수는 없을 것으로 보인다. 대류를 포함하는 경우에 속도 요동의 제
곱인 (ov)2 을 생각하면 이 양이 리아푸노프- 함수가 될 수 있을 것으 로생각된다. (ov) 2:: :::: o (8 . 65) 이 관계는 항상 성립하므로- 안정성 조건은 다음 식으로 표시된다. a (ov) 2/at : :;;; o (8 . 66) (8.65) 식은 분명히 성립하며 (8.66) 식은 기계적 에너지의 소산을 의 미하므로 역시 성립해야 한다. 부시네스크의 가정에 따라 (8.64) 식을 구체적으로 써보자. (5.41) 식을 단일 성분계에 대해 다시 쓰면 (1/2) ao2p s /at = 0(1/T) a(op u )/ at (8.67) 정상 상태를 기준으로 할 때 oT = fJ라고 표시하면 부시네스크의 가 정에 따라 다음 관계가 성립한다. op u = Cvp o oT = Cvp o 0 (8 .68) 이 식과 (8.23) 식을 (8.67) 식에 대입하면 다음과 같이 쓸 수 있다. (1/2) ao2p s /at = —(Cv p o 0/T2) (ae/at) = 크나 /T2)[ /3 VZ+ (x/PoCv)V 뀜〕 = -[/ 30 vz + (x/po C v) 0'\1 2 0 ] (CvPo/T2) = [ (x/po C v) (v0 )2+ v· (0v 0 ) -/3 0v 』 (Cvp o /T2) ;;;::,;o (8 . 69) 이 식을 적분하면 우변 괄호 속의 두번째 항인 발산항이 경계 조건 에 의해 0 이 되므로 이 조건은 또한 다음 부등 관계를 의미한다. Jd V[ ('vfJ )2 ― CvPo f3 0v 』 /T2 칙 0 (8 . 70) 한편 (8.66) 식은 (8.22) 식으로부터 다음과 같이 표시된다.
a(ov)2/at = (2ov) aov/at = 2V· [ (1/P o) 'v (op ) + (µ/po) 'v 2V+ g a0IT 』 = (2/po )'v · [Vop + µV •VV] -2[ (op /po )V·V+ (µ/po) (VV : VV) -ga 0V·llz] ~ o (8 . 71) 이 식을 적분형식으로 표시하면 위에서와 같이 발산항이 경계조건에 의해 0 이 되고 또한 V·V = 0 이므로 다음 식을 얻는다. f[( µ/Po) (VV : VV)- g a0V·ll 』 dz 착) (8.72) 안정성 조건 (8.64) 식과 (8.66) 식은 다음과 같이 리아푸노프 함수를 정의하면 결합될 수있고 성p z = 꿉 %s- 平 (ov)2 착) (8 . 73) 여기에서 규와 E2는 가중 함수로 8 규와 8E2 가 0 이 되도록 정의되었다. 그러면 안정성 조건은 다음 식이 된다. a 정p z/ at: ~O (8 . 74) 다음과 같이 r 와 혀끝 택하면 군 = T 。 c2 = T 。 2/T+ T+ = Cv(J / ag (8 . 75) 안정성 조건 (8. 74) 식은 (8. 69) 식과 (8. 71) 식을 이용해서 (5. 43) 식과 비슷한 적분 형식으로 표시될 수 있다. P[8Z ] =당f악尸 dV = f{러/3 0vz+ (x/po Cv) ('v 0) 기 +군[(µ/p o) ('vV : 'v V)- g a0V·[ 』 }dz = Pol[ (1/Ra) (g2 a2d4/ 11) ('v 0) 2 +v('vV : 'v V)-2 g a0v 』 dz 킥 0 (8.76)
이 식은 (8. 70) 식과 (8. 72) 식의 결합된 형식에 해당한다. 이 석에서 (7 . 51) 식과 같은 대칭성 파괴 불안정성의 한계 안정성 조건을 표시하 면 디움식이 된다. f[ (1/ Ra) (g2 a2d4I ll) (V 0) 2+ l/ (VV : VV) —2g a 0vz] dz = 0 (8 . 77) 이 식을 정리해서 레일리 수 Ra 에 대해 풀어 쓰면 다음과 같다. Ra = (ga ) 2d4 J (V 0) 2dz/[2g a llf 0 vzd z —l/2J V V : VV dz] = I1/lz (8 . 78) L 과 Iri: -위 식의 분모와 분자를 각각 의미한다. 이제 레일리 수의 최소값을 구해 보자. 극값은 다음 조건으로 주어진다. oRa = (1/12 ) (011— R aolz) = 0 (8 .79) 따라서 0l1 一 Raol2 = 0 (8 .80) 이 문제를 풀기 위해 다음과 같은 해를 가정해 본다. () = aoexp [i(a x x +ay y)]¢ (z) Vx = a1exp [i (axx + ay y)]d < f;/ dz Vy = a2exp [i(a xx+ay y)]d ¢/dz Vz = a3exp [i(a xx+ay y) ]¢(z) (8 .81) 또한 꿉춘 다음과 같은 다항식으로 가정해 본다.
그러면 ¢ (0) = ¢ (d) = ¢ (0) = ¢ (d) = 0 (8 . 84) 이 조건에서 ¢(z) 의 표현식이 결정된다. ¢ (z) = 7 (z/d) —1 0 (z/d) 3+ 3 (z/d) 5 (8 . 85) 이 식을 써서 (8.78) 석의 적분 L 과 I2 를 계산하고 그 결과식을 ao, aI, a2, a3 에 관해 최소화한다. A, B, C, D-를 다음과 같이 정의할 때 A = J[d ¢(z/d)/d(z/d)]d(z/d) 헉 27.43 B = J[d 2¢ (z/d) /d (z/d) 2] d (z/d) ~ 274 . 3 C = J ¢2(2/d)d(z/d) 츠 2.752 D = J rp (z/d) [d¢2 (z/d) /d (z/d) 2] d (z/d) 츠 27. 4 (8 . 86) Ra 는 다음과 같이 정리된다. Ra = (A + a2C) (4A + B/a2 + a2C + 2D) /a2 (8 . 87) 여기에서 a2 = ax2+a y 2 이다. 이제 이 식을 강에 관해 최소화하면 a2 과 임계 레일리 수 Ra 혼 근사값을 얻는다. a2 츠 4 .99 Rac~672.15 (8 . 88) 이 값들은 정규 모드 해석에서 얻은 결과인 (8.61) 식과 (8.62) 식의 4 . 935 및 657 과 비교될 수 있다. 5 안정성 교환 원리의 열역학적 검토 7 장게서 검토한 안정성 교환 원리의 열역학적 검토는 베나드 문제와 같이 대류가 포함된 계에 확장될 수 있다. (8.22) 식과 (8.23) 식에 각 각 -p ooV*/ 犯斗 (ag /c v(J ) O0* /孔를 곱하고 하나의 정규모드에 대
해 정리하면 다음 식을 얻을 수 있다. —2 ( w/+wi2 ) Ipo [ (ag/ /3) 00* + V· V *]d V = (wr-iw 1HPo[(g a )2h 4 / vR il0 ·'\l 0 *+vil V : '\JV * -ga( vz0 * +vz* 0)]d V + (wr+i w1 )f po [(ga )2h4/vR '\10 •'\1 0 *+v'\J V : '\JV * 一g a(v z 0* +vz* 0 )]dV = 2w r f p。[ (g2 clh4 / v Ra) '\l0 ·'\l0* + v'\J V : '\JV * -ga (vz0 *+vz* 0 )]dV (8.89) 이 식은 다음에 다시 표 시한 (5.81) 식과 같은 형식이다. (W r2 + w12) 핥 Z = WrPm[ 泣 ~ + w1Q m [& 汀 ~ o (8 . 90) 여기에서 핥 Z = -2!Po [ (ag/ /3) 00* +V · V 기 dV~O (8.91) 이다. 또한 하나의 정규 모드에 대해 (5.4 5) 식과 비슷한 다음 관계식 이 성립한다. a 핥 Z/a t = 2w r 핥 Z = 2Pm[ &~ = 2omP 〔幻 (8 .9 2 ) 이 관계석으로부터 (5.83) 식 및 (5.86) 식과 비슷하게 (8 . 90) 식의 부 등 관계는 다음과 같이 나누어 쓸 수 있다. Wr2 핥 z = WrPm[ oZ ] s: o (8 .93) W12 핥 Z = w1Q m [o Z J 책 (8.94) (8 . 93) 식은 다음을 의미하며 정규 모드의 안정성 판별 기준이 되고 Pm[oZ ] >O 이면 Wr
하면 Qm [oZ ] = 0 이다. ( 8 .91) 식 에서 om 2 Z < 0 이 므 로 다음 식이 성립 해야한다. W I= O (8 . 96) 이 결과는 바로 8 . 3 절에서 검토한 안정성 교환의 원리가 성립하는 조건이다. 죽 이 조건은 정지된 유체충이 불안정해지면서 다음 안정한 상태로 전동 없이 점근한다는 것을 의미한다. 이러한 해석 방법은 정규모드의 개념을 이용하고 있기는 하지만 8 . 3 절과는 다른 방법으로 안정성 교환의 원리가 성립함 을 보이고 있 다. 8.4 절의 안정성 한계에 대한 계산과 함께 생각해 보면 열역학적 방법이 정규모드에 의한 해석 방법보다 더· 좋다는 결론을 내리기는 힘 들다. 더욱이 열역학적 방법의 성공은 임의성이 있는 것으로 생각되는 함수 左斗 가중 함수 e2 과 군의 선택에 의해 가능하였다. 또한 열역학 적 방법은 열역학적 가지인 첫번 임계점까지만 적용이 가능하며 다음 절에서 언급하게 되는 바와 같이 생성된 구조가 어떤 것인지 그리고 이 구조가 어떤 조건에서 불안정해지는지 하는 문제에 대한 대답을 할 수 없다. 열역학적 방법의 의미는 크로이저의 의견과 같이 안정성 판 별을 위한 독립적인 변분 원리가 존재한다는 것에서 찾아야 할 것으로 생각된다. 6 소산 구조와 비선형 안정성 이론 앞절들에서 검토한 선형화된 이론은 한계 안정성 조건 즉 임계 레일 리 수의 근처에서 유효하다. 그러므로 한계 안정성 조건 근처에서 나 타날 수 있는 구조의 해석에 적용될 수 있다. 그러나 어떤 레일리 수 까지 이 구조가 안정할 것인지에 대한 해답은 비선형 이론에 의해 가 능하다. 레일리 수가 증가하면서 일어날 수 있는 현상을 검토하기 위 해서는 (부시네스크 가정에 근거한) 비선형 이론이 필요하게 된다. 이
러한 문제들은 비평형 열역학의 범위를 넘어서고 있지만 여기에서 간 략히 살펴보기로한다. 선형 이론에 의해 생성되는 구조를 알기 위해서는 안정성을 위해 계 산한 Vz , Wz , 0 이의에도 vx -2-} V y 를 알아야 한다. 속도장이 밀도가 일정하기 때문에 솔레노이드 장(v · V = 0) 이 되므로 V 를 다음과 같이 두 스칼라장 +E< p (8 .9 7) 여기에서 연산자 lD 와 E 는 다음과 같이 정의된다. JD = 'v X ('v X liz< /> ) (8 . 98) E = 'vX liz< p (8 .99 ) 그러면 (8 . 97) 식의 속도 성분 vx -2-} V y는 다음과 같게 된다. Vx = o' /o x+ O< p/a y (8 .100) vy = o' /a y - a
것이라는 근거는 없다. 대칭성의 입장에서 본다면 삼각주, 사각주 및 육각주도 가능하다. 이러한 해는 (8 . 101) 식과 (8.102) 식으로부터 쓸 수 있는 다음 식들에서 시작하면 적합한 경계 조건에 대해 풀 수 있 다. (장 /ax 탸 장 /a y 2) ¢'+a2 섭 = O (8 .109) (장 /ax 묘 장 /ay 2) rp+ a2rp = 0 (8 .llO) 찬드라세커의 책에 육각주 소산 구조의 해가 소개되어 있으며 여기 에서는 논의하지 않는다. 이러한 논의에서 선형이론의 한계가 분명해진다. 이렇게 생성된 소 산 구조에서는 속도 벡터 V 가 0 이 되지 않으므로 소산 구조의 안정성 은 이제 선형화된 식 (8.22) 와 (8.23) 에 근거할 수 없고 비선형 이론 에 의해서 가능하다. 비선형 이론의 한 방법은 교란 전개 (Pertu r ba- tion Exp a nsio n ) 에 의하는 것이다. 이 전개 방법에 의해 일차항만을 취하면 운동량과 에너지의 수지식은 기준 상태의 해가 알려져 있을 때 에 요동에 대한 선형 편미분 방정식이 된다. 아직 연구된 바는 없는 것으로 보이지만 기준 상태의 해와 선형화된 편미분 방정식을 쓰면 다 음 장에서 논의되는 국소 퍼텐셜의 방법을 적용해서 안정성을 검토하 는 것이 가능할 것으로 생각된다. 그러나 이 방법도 레일리 수가 임계 레일리 수보다 아주 커지면 효용성이 감소한다. 따라서 수치해에 의존 하게 된다. 불안정성울 넘어서서 생성되는 소산 구조들의 안정성 문제 는 아주 복잡하며 부스 (Busse, 1985) 의 총설에서 검토하고 있다. 이러 한 안정성 문제와 관련된 중요한 문제의 하나~ 소산 구조가 어떻게 궁극적으로 난류 유동에 이르는 것인가 하는 것이다. 많은 실험적 연구가 대류에 의해 생성되는 소산 구조와 이 구조들의 전이에 관해 발표되었다. 육각형의 세포구조가 베나드에 의해 1901 년 에 발표되었지만 이 구조가 과연 중력장에서 부력에 의해 생성된 것인 가 하는 문제는 논쟁의 대상이 되어 왔다. 온도차로 인한 표면장력의 불균일성이 이러한 구조를 생성할 수 있다는 것이 우주선내에서 실시
된 무중력 상태의 실험에서 확인되었다 (Grod z ka and Bannis t e r, 1 972). 그러나 솜머스케 일과 도허티 (Sommerscale and Doug h erty , 1970) 는 부력에 의해 이러한 구조가 생성될 수 있다는 것을 확인하였다. 이 구 조는 유체충의 점도와 같은 물성이 가열 중에 대칭 상태에서 조금 벗 어나면 발생될 수 있는 것으로 생각되고 있다. 초기조건이 잘 제어되 는 대부분의 실험에서는 이차원의 롤이 생성되는 것이 관찰되었다. 이 와 관련된 안정성과 전이의 실험적 논의는 역시 부스 (Busse , 1985) 의 총설에서 논의하고 있다. 7 정리 이 장에서는 정지된 유체의 온도 구배에 대한 열적 안정성을 검토하 였다. 부시네스크의 가정에 따라 온도의 변화는 밀도의 변회를· 통해서 계에 영향을 준다고 생각하고 선형화된 수지식들을 이용한다. 먼저 이 불안정성이 안정성 교환의 원리를 따르는 것을 보이고 다음에 고유치 의 허수 부분을 邸로 놓은 후에 정규 모드 해석에 의해 안정성을 검 토할 수 있다. 열역학적 방법으로는 이 경우에 과잉 엔트로피롤 확장 해서 이의 생성 속도가 0 보다 클 때에 계가 안정하다는- 조건을 이용하 였다. 그러나 과잉 엔트로피롤 확장하는 과정에 임의성이 있는 것으로 생각된다. 안정성 해석의 결과는 온도의 구배가 포함된 무차원 수인 레일리 수로 나타낼 수 있으며 임계 레일리 수는 계가 불안정해지기 시작하는 조건을 의미한다. 불안정한 계가 어떻게 될 것인지는 정규모드 해석이나 열역학적 해 석으로는 알 수 없고 추가적이거나 독립된 해석이 필요하며 이러한 해 석에 의해 이차원 롤이나 육각 원주가 발생한다는 것을 보일 수 있다.
제 9 장 층류의 안정성과 국소 퍼텐셜 I 서론 이 장에서는 두 개의 고정된 수평 평판 사이룰 흐르는 비압축성 유 체의 포아서유 (Po i seu ill e) 흐름의 두 가지 안정성을 검토한다. 하나 는 등온 포아서유 흐름에서 유속이 증가하면서 충류가 불안정해지고 난류가 발생하는 것이고 다른 하나는 일정 유속의 포아서유 흐름에서 밑면과 윗면의 온도차가 증가하면서 중력 방향의 대류 흐름이 발생하 는 것이다. 관련되는 문제는 고정된 평판과 움직이는 평판 사이의 꾸 에트 (Coue tt e) 흐름의 안정성 문제와 경계층 흐름인 블라우시우스. (Blausiu s ) 흐름의 안정성 문제 등이 있으며 또한 중심이 같은 두 개 의 구와 축을 공유하는 두 개의 원통 사이의 유체의 안정성 문제가 있 지만 여기에서는 논의하지 않는다. 근래에 유체역학에서 많이 연구되 고 있는 문제는 아랫면의 온도가 윗면의 온도보다 크게 높은 경우인데 이때에는 불안정성이 계 전체에서 시작되기 전에 경계층내에서 시작하 게 된다. 이러한 경우에 대한 열역학적 해석은 발표된 바 없다.
온도차에 의해 발생하는 불안정성은 앞장의 베나 드 문제와 유사하며 안정성 판별에 중요한 판별기준은 레일리 수 Ra 와 관계가 있을 것으 로 생각할 수 있다. (8.15) 식으로 주어전 레일리 수의 정의 를 다시 쓰 면 Ra = ag poC v (t::.T ) h3/ v x (9 .1) 이다. 또한 평판 포아서유 흐름은 레이놀즈 (Re y nolds) 수, Re 라 불 리는 무차원 수에 따라 특칭지울 수 있고 Re = hV+ p /µ = hV+ /v (9 . 2) 여기에서 h 는 특성 길이, V + 는 유체의 특성 속도, 点 근 유체의 밀도, 産 유체의 점도 그리고 )) ( = µ/p)는 동점도이다. 8 장에서는 기준 상태가 정지된 유체이었지만 여기에서는 정상 상태 의 포아서유 흐름이므로 정상 상태를 기준으로 한 과잉 수 지 식들을 유 도할 필요가 있다. 8 장에서 주어전 부시네스크의 근사법에 의해 관계 되는 수지식들 (8.1), (8. 10 ), (8 . 11) 식을 기준으로 과잉 수지식들을 도입한다. 부시네스크의 가정에 의해 p의 온도에 따르는 변화를 운동 량 보존식을 제의하고는 무시하기로 한다. 그러나 기준 상태가 여기에 서는 정지 상태가 아니므로 운동량 보존식에 압력 경도항 v p가 포함 된다. v· oV = 0 (9 . 3) Po[a (oV) Iat+ V 。 . vov + oV • v`]+ v· op = (po +op ) G+µ\1 2 0V (9.4) 80/ at +V 。.v 0+oV· v To= (x/po C v)\1 2 0 (9. 5) 여기에서 0 = T-T 。이고 하첨자 匠는 기본 흐름의 값을 의미한다. 이 장에서는 등온계에서 난류가 발생하는 문제와 포아서유 흐름에서 밀면과 윗면의 온도차에 의해 대류가 발생하는 문제를 나누어 생각하 기로 한다. 앞의 문제에 대해서는 정규모드 해석에 의한 린 (Lin,
1955) 의 고전적 해가 알려져 있다. 후자의 해석은 국소 퍼텐셜의 방법 에 의한다. 이 문제는 이차원의 문제이며 흐름의 방향을 x 좌표로 그리고 흐름 에 수직이고 중력의 방향과 반대 방향을 z 좌표로 생각한다. 평판 사이 의 간격은 d 이다. 기본 흐름과 경계 조건은 좌표계를 다음과 같이 두 방법으로 설정하여 표시한다. 방법 l )에서는 원점을 아래 평면에 고 정시키고 방법 II )에서는 원점을 두 평면의 중앙에 고정시킨다. 방법 l )과 II )에서 특성 길이와 특성 속도는 다음과 같이 택한다. 방법 I ) h = d V+ = Vmax/2 방법 Il ) h = d/2 V+ = Vmax 여기에서 d 와 Vm a x는 각각 평판 사이의 간격과 최대 속도를 의미한 다. 국소 퍼텐셜의 방법은 온도구배에 대한 충류의 안정성 해석에는 물 론이고 8 장에서 검토한 베나드 문제와 이 장에서 검토하는 등온 충류 계의 안정성 해석에도 적용될 수 있다. 다음 철에서는 먼저 5 장에서 열전달 현상을 예로 소개된 국소 퍼텐셜의 개념을 확장한다. 2 일반화된 국소 퍼텐셜 5 장에서 정상 상태를 기준으로 한 국소 퍼텐셜을 도입하였다. 국소 퍼텐셜 아은 기준 상태에서 첸 ?1 = 0 이고 그 이의에서는 A cp 1>O 이 되는 성질 때문에 기준 상태의 해를 구하는 데 쓰일 수 있다. 만약 정 규 모드를 기준으로- 국소 퍼텐셜을 구성한다면 국소 퍼텐셜을 이용해 서 정규 모드의 고유치를 구할 수 있다. 이 경우의 국소 퍼텐셜은 과 잉 국소 퍼텐셜이 되는데 그 이유는 정상 상태에서 교란된 정규 모드 의 요동으로부터 퍼텐셜이 구성되기 때문이다. 그리고 이때에는 수지 식 대신 과잉 수지식이 국소 퍼텐셜을 구성하는 근거가 된다.
8 장에서 검토된 베나드 문제와 9 장에서 검토할 충류의 전이 및 충류 의 온도 구배에 대한 안정성 해석에는 5 장에서 열전도를 예로 논의된 국소 퍼텐셜의 개념이 적용될 수 있다. 이 목적을 위해 국소 퍼텐셜을 일반화시키기로 한다. 먼저 변분법을 간단히 생각해 보자. 경계치 문제를 구성하는 많은 미분 방정식들은 변분원리를 따라서 표시될 수 있다. 다음 정적분을 생각한다. I = JF (x, y, Yx)dx (9 . 6) 다음에 주어지는 오일러-라그란지 식은 주어전 구간에서 위의 적분 이 극값을 갖도록 하는 함수 y를 구할 수 있는 조건을 제시한다. aF/ ay —d/d x ( aFI ayx ) = 0 (9 . 7) 함수 y가 X1, X2, X3, …… 에 의존할 때에는 위의 식은 디음과 같이 되고 aF/ 的 _V• 〔~ (aF 傾罰 )ll1] = 0 (9 . 8) 여기에서 I 는. i 방향의 단위 벡터이다. 이 미분방정식이 해석적으로 풀리지 않을 때에는 수치해에 의존할 수 있다. 미분 방정식의 경계조건을 만족하는 완전한 직교함수계 (Comp le te Orth o g o nal Sy s te m ) {
이제 a2를 구하기 위해 Y2 = Y1+a2¢2 라 놓고 al/ aa 2 = 0 인 조건에 서 a2를 구한다. 이러한 절차는 반복될 수 있고 이렇게 얻어전 해는 수렴한다는 것을 보일 수 있다. 국소 퍼텐셜은 변분원리와 비슷하지만 다음의 (5.96) 식에서와 같이 구하고자 하는 함수 T 이의에 기준함수 따를 포함한다. 아 (T, T0) = JL { T , T0}dV (9 .12) 5 장의 열전달 문제에서 국소 퍼텐셜 아 (T, To) 의 첸가 = 0 이 되는 해 T + 는 E 에 의존하며 To7} 정상상태의 해이면 T+ = To7} 된다는 것을 예시하였다. 라그란지안 L 이 다음 식으로 주어진다고 생각하면 L = (l/2) xoT 。 2 (VT- I) 2 (9 .13) 그러면 (9 . 7) 식의 오일러 ― 라그란지 식은 디음과 같이 된다. aL/aT-1 = 짜 xoT 。 2VT 려 = O (9.14) 이 조건을 만족하는 해 To 를 대입하면 다음 석을 얻고, v [xo v T 。] = O (9.15) 이 식에서 To7} 정상 상태의 해인 것이 분명하다. T 가 알려져 있지 않을 때에 국소 퍼텐셜은 변분법에서와 같이 수 치해를 구하는 방법을 제시한다. To = ~Clko , /aa1=0 (i= 1,2,… … ,n) (9.16) 이 결과는 디음과 같은 연립 방정식을 구성한다. fi({ a1}, {aw}) = 0 (j = 1, 2, ……, n) (9.17) 이제 다음 조건을 적용하면
dj = aIO (i= 1,2 ,… … ,n) (9.18) 처음에 알려지지 않았던 aIO 를 구할 수 있다. 따라서 n 항 까지의 To 에 대한 근사식을 얻게 된 것이다. 이것은 정상 상태를 기준으로 한 국소 퍼텐셜로부터 주어진 E 에 대해 o = o 의 조건을 만족하는 해 T + 를 구할 수 있지만 To7} 주어져 있지 않으면 T+ = T 려 조건 이 만족되 도록 구한 해가 바로 정상 상태의 해가 된다는 것을 의미한다. 국소 퍼텐셜이 변분원리를 수정한 것이라면 왜 처음부터 변분원리를 적용하지 않고 국소 퍼텐셜을 도입하였는가 하는 의문이 생긴다. 이에 대한 대답은 비가역 열역학에 도입되는 수지식들이 고전적 변분원리를 적용하기에 적합하지 않다는 것이다. 이제 남은 문제는 어떻게 국소 퍼텐셜을 일반적으로 구성굴H 근가 하는 것이다. 국소 퍼텐셜의 일반적 표현식을 얻기 위해 2 장에서 도입된 수지식들 울 다음과 같이 다시 표시하자. ap1 /at = —V ·Piv i +~R= I l/UM JJ pa V/at = pV •v' V +p F -v'p +v'·P d a(pu)/a t = —pd : v' V ― pv' ·V+ 홉 Jidi C C ·Fi -v'• (p uV+ Jf갑 (9 .19) 에너지 보존식에서 E 가 성분에 의존하지 않을 때에는 우변의 셋째 항이 0 이 된다. 昭》버]서 열전도에 대한 국소 퍼텐셜을 얻기 위해 J [{a( pu)/a t }aT- 1 J dV 에서 시작했던 것을 기억하고 여기에서는 (9.19) 식들의 양변에 각각 -8(µ1/T), -T 。 -1av, aT - 1 을 곱하고 적분하여 다음 식을 얻는다. l = J[— (8p I/ 8t) 8(µJ T ) -p (8V/8 t )T 。 -1av +{a( p u)Ia t }aT 거 dV (9.20) 이제 이 식에서 시작하여 다음 형식의 국소 퍼텐셜을 찾고자 한다.
(9.20) 식에 (9.19) 식들을 대입하고 흐름들에 관해 부분적분한다. 결과식은다음과같다. l = J{ \l • [ —Jqo T- 1+ ~J1dl ffo (µ1/T) +T 。 - 1 (Pd· ov ) J + [Jq. V8T-I _ 2 Ji dIrr. 합 (µ1/T) -T 。 -1 (Pd : '1a v)] +~]10(Ai /T )-[\l• (pu V) +pd : \l민 oT - 1 + ~\!• (piV) 0 (µ1/T) + [ (pV •\JV -plF ' + \lp) T 。 -I - p d. \J T 。 - 1]·oV}dV (9.22) 이 식에서 계에 작용하는 힘 F 는 화학성분에 의존하지 않는다고 생 각하였다. (9.22) 식의 첫줄은 계의 경계면을 통과하는 흐름을 나타낸 다. T, µ1, V 가 일정하거나 계면을 통과하는 흐름을 무시할 수 있는 경우에 이 줄은 무시된다. 둘째 줄을 다음과 같은 선형 현상적 법칙들 과 Jq = xT2'v y- 1 J전 = —D 1' v( µ1/T) Pd = —2 µD (9. 23) 또한 懿테서와 같이 다음 전개식을 이용해서 다시 쓴다. xT2 = xoT 。 2+ o (xT2) ; D1 = D10+ oD 나 µ = J.Lo+ oµ (9. 24 ) 그리고 적분 I 의 나머지 항들의 계수를 위 식들과 같이 전개한 후에, 하첨자 記냐 1 표시된 계수들울 포함하는· 적분 L 과 나머지 부분 I~ 합으로 적분 I 를 표시한다. 다음에 하첨자 0 이 없는 변수들에서 8 롤 제거하여 국소 퍼텐셜 1 를 구성한다. 그 결과는 다음과 같다. 1 = f{ (1/2)XoT 。 2(VT-1)2+ (1/2)~D10 〔짜µi /T)]2 + J.Lo T 。 -1 (D : D) +~J10 Ai /T _[ V ·(p u V) +Pd : VV] 。 T-1 +2[V· (piv )]0 ( µ1/T)+ 〔(p V•VV―p F+V p )T 。 -1
-Pd• \l T 。 - I] 。 .V } dV (9.25) 이제 다음 조건들을 만족하는 해 T+, µ占 V+ 를 구한다. o1 = o (9 . 26) T+ = T 。 ; µl+ = µ10 ; v+ = Vo (9 . 27) (9.25) 에 이 해들을 대입하고 오일러-라그란지 식을 계산하면 다음 과같게 된다. aL/a(µ,T-1) = [V· (piV)]。 +[V· (J 1dl)] 。 -~110M1 JJ 0 = -[ap, / at] o = 0 aL/av = [v• (PdT-1)] 。+ [ (pV •VV-pF +Vp ) T 。 - I -Pd•vT-1:] 。 = T 。기 V•Pd+ p V•VV ―p F 〕 O = -T 。 -1[ p (av/ 社)〕 0 = 0 aL/aT-1 = -[V· (pu V) +Pd : vv+ p V V]。― (V• Jq)。 = (a( p u)/a t)。 = 0 (9.28) 이 식들은 각각 정상 상태의 성분의 질량, 운동량 그리고 에너지 수 지식과 갇다. 따라서 (9.26) 식과 (9.27) 식을 만족하는 해는 정상 상태 의 해가 된다는 것을 확인한다. 정상 상태에서 국소 퍼텐셜이 최소가 되는 것을 보이기 위해 다음과 같이 정상 상태를 기준으로 한 변수들을 정의한다. 01 = µi/T -µ, o/T 。 oV=V-Vo 0-1 = T-I -T 。 -1 E=D-D 。 (9 . 29) 그리고 (9.25) 식으로부터 다음 식을 얻는다.
+ µT 。 - l (E : E) + xoT 。 2VT 。 •' v 0- 1 +~Dw 'v (µ1/T) 。.'v 01 - 1+2 1.1-0 T 。 -l (E。 : E) +~J10 A1/T-['v · (pu V) +pd : 'v V] 。 T-1 +2[V· (pIV )]o ( µi/ T) + [(p V· 'v V ―p F+ 'vp )T 。 -I _Pd.VT 。 - 1] 。 .V } dV (9.30) 이 식에서 01, oV, 0 의 경도(gr ad i en t)를 포함하는 항들을 부분적 분하면 경계 항들이 없어진 후에 다음 석을 얻는다. A 아 =中 I_®IO = f{ (1/2) XoT 。 2 ('v0 - 1) 도 (1/2) ~D1o['v ( 01)] 2 +µT 。 - I(E : E) } dV 착) (9. 31) 따라서 아가 국소 퍼텐셜이라면 (5.98) 식과 (5.99) 식을 만족해야 한다. 또는 Yk = Yko (k = 1, 2, 3, ……)에 대해 다음 조건들이 만족되 어야한다. 8 아 =O (9 . 26) A 이 >O (9.32) 그리고 우리는 (9 . 25) 식이 정상 상태를 기준으로 한 국소 퍼텐셜의 일 반 형식이 되는 것을 확인한다. 국소 퍼텐셜의 개념은 시간에 따라 변화하는 계에 대해서도 일반화 된다. 시간에 따라 변화하는 계에 대한 라그란지안 £울 다음과 같이 정의하자. £ = L+ µ,~T- 1( ap w /at) +poT -1V• (aVo/at) -T-1a( p u) 。/洪 (9. 33) 그리고 다음 적분 V를 생각하자. '11' = f£ {T, T 。 ; µ,, µw ; V, V 。 }dV (9 . 34)
이 적분에 대한 오일러-라그란지 식을 계산하면 a£/a(µ,T-1) = 크 a p ,/a t)。+ (ap w /at) = 0 a£/av = ― PoT-l(av/a t)。 +PoT - 1(av 。 /a t) = o 篠 /aT-1 = T 막 a( p u)/a 니。― T-1a( p u) 。 /a t = O (9. 35 ) 따라서 8'!' = 0 가 되도록 하는 함수들은 수지식의 해와 일치한다. 더욱이 다음 조건이 성립하는 것을 보일 수 있으므로 !J.-qr > 0 (9 . 36) V 는 수지식의 해에서 극소값을 갖는다. 또는 中롤 최소로 하는 해는 수지식을 따르는 해가 된다. 그러므로 中를 국소 퍼텐셜이라고 생각할 수있다. 일반화된 과잉 국소 퍼텐셜도 과잉 수지석둘을 근거로 도입될 수 있 다. 시간에 의존하는 과잉 국소 퍼텐셜을 이용하면 정규 모드 해석에 근거한 임의의 정상 상태의 안정성 문제를 근사적으로 풀 수 있다. 선 형화된 과잉 수지식들을 (9.19) 식으로부터 얻어 다음과 같이 표시한 다. 88p i/8 t = -8[V·PiV J +2l/U M 18J j pa ov/at = o[pV ·'v V ] +Fop —'vo p +'v· oPd oo(pu )/ot = 一 8 〔p d : 'iJ민 -o[ p'v •V] + Z:: 0J 1d l ff • Fi - 'v • oJq (9 . 37) 여기에서 8 룰 써서 표시된 양들은 정규 모드와 같이 시간에 의존하 는 교란양둘을 표시한다. 또한 이 교란의 요동을 8' 을 써서 표시하기 로 한다. 이 식들의 양변에 각각 -8'[o (µi/ T) ], -T 。 -1o'[ov J, o' (oT-1) 을 곱하고 적분하면 다음 식을 얻는다. 1 = J[-~ (aop 1 /at ) o'{o(µ i/ T)}-P
여기에서 8' 은 교란에 대한 요동을 표시하기 위해서 도입되었다. 이 식에서 시작하여 (9. 25) 식으로 표현된 국소 퍼텐셜을 얻는 것과 비슷 하게 디음 형식의 과잉 국소 퍼텐셜을 찾고자 한다. , = ff. e { oT, oTo ; oµ,, oµ,o ; oV , oVo} dV (9 . 39) (9 . 37) 식들로 표시된 과잉 수지식은 구체적으로 표현되어 있지 않고 따라서 여기에서는 과잉 국소 퍼텐셜의 구체적 표현식은 유도하지 않 는다. 뒤따르는 응용에서는 계에 적합한 단순화된 과잉 수지석을 먼저 유도하고 이에 따라 각 문제에 적합한 과잉 국소 퍼텐셜의 표현식을 구하는 방법을 쓸 것이다. 또한 과잉 국소 퍼텐셜은 시간에 의존하는 계를 기준으로 하고 있으므로, 수지식 대신 과잉 수지식에서 얻은 라 그란지안 L 로부터 (9.33) 식에 따라 다음과 같이 구한다. £ = L+~o(µ i/ T) { a(o p 1) 。 /a t }+o( p oT-1V) •{a(oV) 。/at} -o(T-1){a(o p u) 。/at} (9. 40 ) 3 등온 층류의 안정성 평행인 평판 사이를 흐르는 2 차원의 등온의 포아서유 흐름을 먼저 생각하자. 그러면 해당하는 수지식은 (9.3) 식과 (9.4) 식이고 의력을 무시할 수 있을 때에 등온계에서 (9 .4)식은 다음과 같이 표시된다. p o 〔짜 ov)/a t +v 。.v oV+oV· v Vo] +vo p = µv2 0V (9.41) 이 식을 무차원 변수들을 도입해서 다시 쓰면 88V/8t = ― V 。.v oV-oV·v Vo-v oP+ (1/Re)v 2 oV (9.42) 이다. 여기에서 y_ = V/V+, ~ = hv , ! = t/ (h/V+) , f = p/ (poV +2) (9 . 43)
이며 좌표계는 9 . 1 절의 방법 l )에 의해 선택하였다. 아 경우에 특성 속도 V 적 특성길이 h 를 다음과 같은 방법으로 정의한다. V+ = Vmax/2 와 h = d( 평판 사이의 간격) (9.44) (9 . 3) 식도 무차원 변수를 써서 표시할 수 있다. 'v·o V = 0 (9 . 45) 이제 av 의 흐름에 평행인 x 성분을 8vx, 흐름에 수직인 z 성분을 8 따라 하고 속도와 압력의 요뚱의 푸리에 성분을 다음과 갇 이 생각하 자. o'!_x = U( 낌 ex p[i a( 꼰― C!)] (9 . 46) 8 又 z = W< i )ex p[i a( 혼- 야)] (9 . 47) of = II( 쯔 )ex p[i a( 프 -C!) 〕 (9 . 48) 여기에서 쩌근 피수이고 요동은 x 방향의 주기성을 갖도록 좌표계를 택하였다. 또한 좌표계의 선택에 의해 기본 흐름 벡터는 다음과 같다. y。 = [~xo (낌 , 0] (9 . 49) 그리고 8Y = [8y_x , &성 (9 . 50) P = P 。 +oP (9.51) 이 식들을 쓰면 연속방정식 (9.45) 식은 다음과 같이 된다. ia U+DW=0 (9.52) 또한 (9.42) 식의 x 와 z 성분은 각각 디움과 같이 된다. [D2_#— ia Re(Vxo-c)]U = Re(Dvxo)W+i aR eII (9.53) [D 2_# —ia Re(Vxo-C)]W = ReDII (9 .'54) 위의 세 식에서 D = d/dz 이다. 여기에서 c는 일반적으로 복소수인
고유치이고 (8. 40) 식에서 정의된 6 와 다음 관계를 갖는다. a = -iac (9. 55 ) (9.53) —(9 .54) 식에서 U 와 II 를 소거하면 다음 식을 얻는다. (D2-a2)2W = iaR e[(vXO— C) (D2_#)W 一 (D2vxo)W J (9.56) 그리고 경계 조건은 다음과 같다. W=DW=0 z=O z=1 (9 . 57) (9 . 56) 식은 잘 알려진 오르븀군머펠드 (Orr-Sommer fe ld) 식이다. 이 식과 경계 조건 (9.57) 식은 8 장의 베나드 문제와 비슷한 고유치 문 제를 구성한다. 린(Li n, 1955) 의 해법은 댜] 허수 부분 C1 를 但냐 1 놓 고것이 실다.수 의( 9a.4 값6)과 — R(9e. 에48 ) 대식해에 서g ]지 실수 수함 부수분 항 의Cr 을 시 고간유의치 계문수제는로 _푸ia는c 이므로 C1 이 0 보다 크면 계는 불안정하고 0 보다 작으면 계는 안정하 다. C1 = 0 인 경우에 a_Re 의 관계에서 가장 작은 Re 값은 임계 레이 놀즈수 Rec 가된다. 이 문제는 과잉 국소 퍼텐셜울 이용해서 풀 수도 있다. 과잉 국소 퍼텐셜을 구하기 위해 먼저 적분 I 를 (9.38) 식으로부터 단일 성분 등 온계에 대해 성분 물질 수지식 대신 총 물질 수지식을 생각하고 여기 에 8' 야를 곱해서 다음과 같이 쓰고 l = J[— (88p /at) a'{ 8p } -P
-y•안’ {전) • 선드 [무· 8' (8 프] [쪼· 인] —8 .P[Y· 8' (8 모)] + (2Re)-1o'[Y 찐 : 쩐 Y] _8 프전 o'(o f)} 이 식으로부터 고정된 경계 조건에 대해 발산항을 무시하고 8'8y 의 계수를 기준 상태의 값으로 하첨자를 써서 표시한 후에 (9. 22) 식에 서 (9.25) 식을 얻은 것과 같은 방법으로 라그란지안을 얻는다. 그리고 (9.40) 식에 따라 시간의존성을 고려한 항을 더해 주면 다음의 국소 퍼 텐셜 표현식을얻는다. 1 = f-—{仁VYo o8 • .·\Y1 _ a o(•y 8포 HV ( )8l •·Y 8 )aV 모·o o포} —一 8(f 8 . oY{ _ 모o ·· a 전y }) ( l· Y!!) + (2Re) -1{\1 a v : vav} ― 8 프o · 프 (8E) +{a(8 프 o)/a t}{ (8 모)}〕 dV (9.59) 이 식에 (9.4 6)-(9.48) 식으로 주어전 정규 모드식들을 대입해서 정리하면 정규 모드에 대한 과잉 국소 퍼텐셜을 얻는다. 여기에서 Vo 와 8V 志 각각 (9.4) 식과 (9.42) 식을 만족한다. 여기에서는 이들 해법은 검토하지 않고 다음 절에서 수직 온도 구배 를 가진 충류의 안정성 거동을 기본적으로 검토한 후에 국소 퍼텐셜 방법을 이용한 해법을 함께 생각한다. 4 수직 온도 구배를 가진 층류의 안정성 여기에서는 온도 구배를 고려해야 하므로 부시네스크 가정에 의한 (9.3), (9.4), (9.5) 식이 기초가 된다. (9.3) 식은 변하지 않고 (9.4) 식과 (9.5) 식을 평판 포아서유 흐름에 적용하고 무차원 변수로 표시하 면다음과같이 된다.
aav Iat = —R eoV · V V 。― Re Vo ·Vo V- VoP Prae/at =+ —VP20e VV•+VR0a+Bwil z+ V20 ((99 .. 6601)) 여기에서 Iz는 z 방향의 단위 벡터이고 무차원 변수들은 다음과 같이 정의하였다. oy = oV I (x/h) ' 쯔 = h쪼, ! = t/ (h2/ 11) , f = p/ (h2/px 1 1) , 0 = oT/AT (9 . 62) 여기에서 AT 는 두 평판의 온도 차이고 앞절과 다르게 좌표계를 방 법 l )에 따라 선택한다. 그리고 특성 길이 h 와 특성 속도 V + 는 다음 과 같은 방법으로 정의된다. V+ = Vma 려 h = d/2 (9. 63) 또한 기본 흐름의 속도는 앞절에서와 같이 특성 속도 V+ (= Vmax/ 2) 로 나누어 무차원 속도 又료- 표시하였고 프란틀수와 페클레수는 이 경우에 다음과 같이 정의된다. Pr = 11/x, Pe = V+ h /x (9. 64) 식 (9 . 60) 과 (9.61) 에는 네 개의 무차원 그룹이 포함되어 있지만 Pe = (Re) (Pr) 이므로 이 중에서 세 개만 독립적이다. 이제 무차원 요동을 다음과 같이 표시하자. 짝 = U(~)ex p(i a쪼 +야) (9 . 65) 싼'!: = W( 으 )ex p(i a판 야) (9 . 66) §_ = e (~) exp (i a쯔 + a!) (9. 67) 8 문 = l1 (즈) exp (i a쯔 + 야)(9.68) 여기에서 z2t X 는 앞절에서와 같이 각각 흐름에 수직인 방향과 흐 름에 평행인 방향의 좌표이다. 또한 空十 쯔는 각각 z/h, x/h 를 의미 한다• 그러나 z = 低근 이제 평판 사이의 중앙에 위치한다. 연속방정
식 (9 . 45) 에 의하면 8 釣도 /8 곤 = 88 도 / 8 쯔이므로 U 와 W 사이에는 다음 관계가있다. U = (i/a ) (dW/d~) (9 . 69) 이 문제에 대한 국소 퍼텐셜의 구성 방법을 검토하자. (9.38) 식으로 부터 (9.58) 식 대신 다음 식을 얻는다. 1 = J [-P(aav/a t )T 。 -10'{av }- o(T - 1) { a(o p u) 。 /a t } ]dV (9.70) 위 식에서 총질량의 보존식이 제외되었으며 이는 정규 모드를 대입 할 때에 고려될 수 있다. 이 식에 (9.60) 과 (9.61) 식으로 표시된 운동 량 보존식과 에너지 보존식을 대입한다. 또한 에너지 보존식이 O 로 표시되어 있으므로_ o(T- 1) 대신에 O 를 쓰기로 한다• 그러면 디~ 식 울얻는다. I = [〔 {Reo 프전 프 +Re 포g·모낀+한 E ―짠짠一 Ra0Kz } • (o'oV ) +{ P eV•'v 0 ― w- 'v 20 } o' 。〕 dV (9. 71 ) 이 식에서 시작해서 (9.59) 식을 얻는 절차를 따라 과잉 국소 퍼텐셜 을 얻고 정규 모드 (9. 65 ) -(9.68) 식을 대입한다. 다음에 (9.60) 식과 (9 . 68) 식을 써서 Ilo 를 소거한다. 결과식은 디음과 같다. '1>1 = J[R eVo • (VoVo) • oV + ReoVo • (VVo) • oV +-VRao8P。 。 l ·lz·o oV V一+ oPVe·V (V 。·2 (0VV o0)o ) 0-wo0— 0 V20]dV = J{ [a2+a+i a U] [W 。 W+ (1/a2) (DW 。) (DW)] +〔 #+Pr(a+ i aReU) 〕@。硏 (1/2) [(D W)2+ (D@) 가 -RaBoW-W 。@- (1/2a2) (D2W)2 + (2/a2) (D2Wo) (D2W) — (iR e/a) (DU) (DW)W 。 }dz (9 . 72) 이 식은 충류의 역온도구배에 대한 안정성 해석에 사용될 수 있다.
이 식의 두 극한 경우는 또한 베나드 문제와 등온 충류의 안정성 해석 에도 이용될 수있다. 베나드 문제에서는 기본 흐름이 없고 레이놀즈 수가 0 이 된다. (9.72) 식에서 Re = 0 라 하고 o = o 의 조건을 만족하도록 한 후에 W + = Wo, @+ = @가 되도록 한다. 그러면 오일러 라그란지 식은 다음과같이 된다. o / oe = o (9 . 73) o/ ow = o (9 . 74) 이 식 들 로부터 다음 식을 얻는다. (D2_ g_ (JP r) 8 = -W (9. 75 ) (D2_ 갈) (D2 _ g_ (J)w = Racle (9 . 76) 이 식은 베나드 문제의 에너지와 운동량에 관한 수지식으로 무차원 변수의 정의 차이로 다르게 표시되어 있지만 (8 . 41) 식과 (8 . 43) 식에 해당한다. 그리고 이 경우에 적합한 과잉 국소 퍼텐셜은 U 를 但냐i 놓아다음과같게 된다. , = ! { [a 모 어 [WoW+ (1/cl) (DW 。) (DW)] +—[R#a + 8P0Wr6-W]8o0@8 +—( (11/ /22)c[ / ()D (DW2)W2)+2 ( D8) 기 + (2/cl) (D2W 。) (D2W) }d z (9 . 77) 등온 충류의 안정성 문제에서는 (9.72) 식에서 Ra=O 이고 또한 @ = O 이다. 8 = 0 의 조건을 만족하도록 한 후에 W+ = Wo 라 놓고 오 일러 라그란지 식 8< I>/o W = 眞卜 이용하면 다음 식을 얻는다. (D2-c f)2 W = ia Re[(U+a/ia R e) (D2 군 )W ― (D2U)W ] (9.78) 이 식에서 무차원 변수의 차이를 다음 식으로 고려해 준다. a= -i aR e c (9. 79)
그러면 (9 . 78) 식이 (9.56) 식으로 표시된 오르븀f머펠드 식이 된다 는 것을 확인할 수 있다. (9.78) 식을 쓰고 양변에 #을 곱해서 이 경 우에 대해 과잉 국소 퍼텐셜을 표시하면 (9.72) 식으로부터 디음괴- 같 다. <1'1 = J{詞+i a3Re(U-c) 〕 [WoW+ (1/a2) (DW0) (DW)] + (cr/2) (DW) 드 (1/2) (D2W)2 + (2/cl) (D2Wo) (D2W) — (iR e/a) (DU) (DW) W 。 }dz (9. 80) 이 식은 충류의 안정성을 검토하기에 적합한 과잉 국소 퍼텐셜이다. 5 수치 해석 (9과.65잉) —국(소9. 6퍼8) 텐의 셜z을 에 이의용존한하 는안 정부성분 을해 석구은하 는정 규과 정모에드서를 표일현정하한 는레 이식 놀즈 수, 프란틀 수 또는 레일리 수에 대해 a 및 6( 또는 c) 를 구하는 것이다. 그리고 6( 또는 c) 의 실수 부분이 0 이 되는 조건이 한계 안정 성 조건이 된다. 먼저 과잉 국소 퍼텐셜이 (9.80) 식으로 표시되는 등온 충류의 안정 성을 검토하기 위해 2 절에서 제시된 방법을 따르기로 한다. a 와 Re 는 주어져 있다고 생각한다. U는 평판 사이의 포아서유 흐름의 속도 분포이므로 9.1 절의 방법 Il) 에 따라 좌표계를 설정하고 무차원화하 면 디음과 같이 표시되며, U=l 一꾼 (9.81) 여기에서 ~ = ~이다. 그리고 W와 W 。롤 다음과 같이 가정한다. Wn = l+a1
여기에서 (f) k 는 경계 조건을 만족하는 임의의 함수로 디음- 형식을 7 肉한다. (f)k = (1- 꾼 )2 [;2 (k 一 I) (9.83) D = d/de 이므로 위의 세 석을 (9 . 80) 식에 대입하고 oil> = o 인 조 건 죽 디음 조건들을 적용한다. a«t >/ aa1 = a«t >/ aaz = …… = a«t >/ aan = 0 (9.84) 이렇게 얻어진 n 개의 식에서 a10, ……, ang } 알려져 있을 때에 n7B 의 a1 값을 구할 수 있다. 그러나 a i 0 은 알고 있다고 생각하였을 뿐이고 실제로는 알려진 값이 아니므로 이 값들을 알기 위해 추가 조건 w+ = W 。률 적용한다. 이 조건은 다음을 의미한다. al = aIO (9.85) 그러면 미지수 Il7n (aIo, ……, ano) 에 대한 Il7 ij의 식을 다음과 같이 얻 게 된다. ~aio Y J t = 0 (i = 1, 2, ···, n) (9 .86) 여기에서 Yjl = f{ [a 4+i a 3Re(U-c)] [rpjrp,+ (1/#) 아rp』 + (a2/2) (짜) 2 - (1/ 2) (합 )2+ (2/#) (합) (합) - (iR e/a) (— 2~) (rpi') rpj} d~ (9.87) 이 Il7n 의 선형 연립 방정식은 제차 방정식이며 주어전 a와 Re 값에 따라 결정되는 싱수 c 를 포함하고 있다. 이 값은 n 이 증가하면서 수 령하는 것으로 알려져 있다. 이 연립 방정식이 해를 가질 수 있논 조 건은 (9 . 86) 식의 계수 ru 에서 결정되는 행렬 F 의 행렬식이 0 이 되는 것이다. 그리고 이 조건으로부터 상수 O 卜 결정된다. 플라톤 (Pla tt en, 1970, 1971) 은 a-Re 평면에서 450 개의 점에 대해
c 값을 계산하고 이로부터 불안정성이 시작되는 가장 낮은 레이놀즈 수인 임계 레이놀즈 수를 계산하였다. 계산이 어려운 영역이 존재하지 만 n 을 20 정도로 하여 계산한 결과는 다음과 같고, 5600 < Rec < 5900 (9.88) 이 결과는 토마스 (Thomas, 1953) 의 5780 과 비교될 만하다. (9.77) 식으로 주어진 국소 퍼텐셜울 아용하면 베나드 안정성을 검토 할 수 있다. 여기에서는 좌표계를 8 장에서와 같이 9 . 1 절의 방법 I ) 과 같이 택하고 윗면과 아랫면이 단단한 표면인 경우의 경계 조건을 생각한다. DW = W = 0 ; e = 0 z = 0 와 z = l 에 대해 (9.89) 그리고 경계 조건을 만족시키는 다음 함수들을 생각한다. ({)k = (1 ― z)2 균 (2z ― 1)2(k-l) (9 . 90) ¢k= (l-z)z(2z-l)(k-ll (9 . 91) 다음에 W 러 @옳 이 함수들을 써서 표시한다. Wn = a1 q; 1+ …… +a 따 (9. 92 ) Bn = b1¢1+… … +bn'P n (9.93) W 과 @국 윗식들의 계수의 하첨자에 떼「 더한 것으로 표시된다. 8 장의 정규 모드 해석에서는 안정성 교환의 원리에 의해 6 의 허수 부 분이 0 이 되므로 임계 안정성 조건은 6 의 실수 부분을 但포료 하는 조 건이 되었다. 이 조건은 다시 레일리 수의 고유치를 찾는 문제가 된 다. 여기에서는정규모드해석에서와같이 a=3 . ll7 로하고주어전 Ra 값에 대해 6 의 고유치를 찾는 문제로 생각한다. 그러면 앞에서 논 의한 등온 충류의 안정성 조건을 찾는 문제와 비슷한 수치 해석 방법 울 따라 해를 구할 수 있다. 셰히터와 힘멜블라우 (Schech t er and Himm elblau, 1965) 가 얻은 계산 결과는 n = 3 일 때에 R,a = 1710 에서
최소 6 의 값이 0 이 되고 따라서 Rae= 1710 이 된다. 이 값은 표 8.1 에 주어진 챤드라세커의 값 170~ 찰 일치한다. 아랫면의 온도가 높고 윗면의 온도가 낮은 온도 분포에 대한 충류의 안정성 문제도 생각할 수 있다. 이 문제를 국소 퍼텐셜을 이용해서 풀 기 위해서는 (9.72) 식을 이용해야 한다. 이 문제는 천천히 흐르는 포 아서유 흐름에서 이차원의 롤이 생성되는 불안정성을 논의하는 것이고 풀라톤 (Pla tt en, 1970) 은 Wn, ®n, Wno 및 @격 전개식의 첫항만을 사용하여 해를 구하였다. 레이놀즈 수와 프란툴 수를 변화시켜 가면서 임계 레일리 수 Rae 를 계산한 결과는· 그립 9-1 에 표시되어 있다. 여 기에 표시된 무차원 수는 다음의 특성 길이와 특성 속도에 근거하였 다. v+ = 4Vmax ; h = d (9.94)
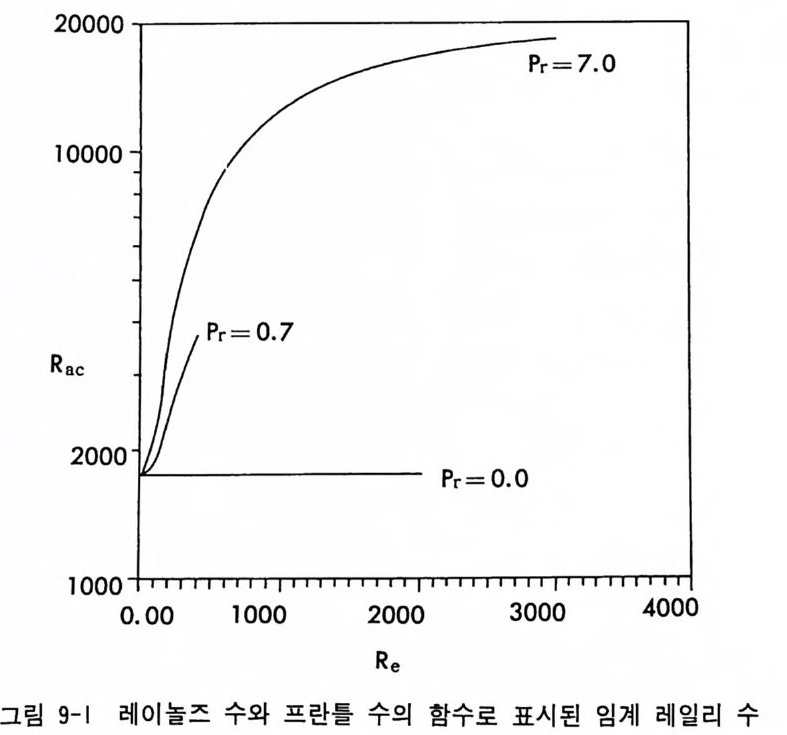 20000
20000
이 그림에서 레이놀즈 수가 0 일 때에는 결과는 페클레 수에 의존하 지 않고 베나드 불안정성에 대한 임계 레일리 수 를 제시한다. 그리고 레이놀즈 수가 증가하면서 임계 레일리 수가 증가하는 것을 관찰할 수 있다. 한편 찬드라 (Chandra, 1938) 의 고전적 실험 결과가 알려져 있 고 게이지와 리드 (Ga g e and Reid , 1966) 의 해석 등 여러 연구 결과에 의하면 임계 레일리 수는 프란툴 수의 영향을 받지 않고 170~ 유지 되다가 레이놀즈 수가 5380 에 이르면 난류로 전이되는 것으로 알려져 있다. 이 결과는 일반적으로 인정되고 있는 것으로 생각된다. 플라든 과 레그로스 (Pla tt en and Leg ros , 1984) 는 이 문제를 실험과 삼차원 계산을 포함하여 더 깊이 연구하고 정리하였다. 이차원 롤 은 축이 흐 름 방향에 수직인 가로 롤 (Transverse Roll) 과 흐름 방향에 평행인 세 로 롤 (Long itud in a l Roll) 이 가능하다. 다른 사람들의 연구 결과는 더 불안정한 평행인 롤에 대한 것이고 그림 9-1 에 표시된 결과는 수직인 롤에 대한 것이다. 그러므로 그림의 결과가 일반적으로 알려진 결과에 위배되는것은아니다. • 평판 위를 흐르는 유체의 열적 불안정성은 경계층 이론을 중심으로 이론적 또는 실험적으로 많이 연구되어 왔다. 이러한 연구에서 관심은 가열이 시작되는 위치롤 기준으로 해서 어느 위치에서 불안정성이 시 작되는가 하는 것이고 수평 평판은 물론이고 경사전 평판 위를 흐르는 흐름도 연구의 대상이 되어 왔다. 여기에서 논의하는 불안정성은 이와 는 달리 완전히 발달된 정상 상태의 온도분포를 갖는 포아서유 흐름이 어떤 조건에서 불안정하게 되는가 하는 것이고 경계층 이론과 직접적 인 관계를갖지 않는다. 윗면의 온도가 높고 아랫면의 온도가 낮아서 레일리 수가 음수가 될 때의 충류의 안정성도 검토되었다. 이 경우의 안정성은 충류가 난류로 전이하는 것에 대한 안정성을 의미한다. 이 문제는 (9 . 72) 식의 국소 퍼텐셜을 사용하면 풀릴 수 있고 이때에 (9.92) 식과 (9.93) 식은 여러 항을 포함하는 형식으로써 쓸 필요가 있다. 이 식들을 n 항까지 포함
하는 형식으로 쓰면 국소 퍼텐셜의 극값을 구하는 조건에서 2nX2n 행렬식을 얻을 수 있으며 레이놀즈 수, 프란톨 수, 레일리 수 및 며t 변화시켜 가면서 이 행렬식의 값을 但냐i 하는 a를 찾고 6 의 실수부 가 0 이 되는 조건에서 한계 안정성을 결정하는 것이다. 6 검토와 정리 이 장에서는 국소 퍼텐셜을 이용한 평판 포아서유 흐름의 안정성 해 석 문제를 중점적으로 검토하였다. 즉 등온계에서 충류가 불안정해지 는 조건과 역온도구배가 있을 때에 충류가 불안정해지는 조건을 검토 하고 특수한 경우로 유속이 0 이 되는 경우의 역온도구배에 대한 안정 성을 검토하였다. 국소 퍼텐셜은 국소 평형에 근거한 열역학 관계식과 는 관계가 없으므로 국소 평형의 가정이 적용되지 않는 경우에도 적용 될 수 있다. 국소 퍼텐셜을 이용한 방법은 또한 선형화된 수지식 또는 과잉 수지식의 해를 구하는 변분 원리의 하나로 생각할 수 있다. 8 장에서 논의된 것과 같이 선형화된 이론의 적용은 한계를 가지고 있다. 문제점의 하나는 안정성 해석의 결과가 요동의 전폭에 상관 없 고 또한 이 전폭은 시간에 따라 변화하지 않는디는 것이다. 그 결과로 고유치 문제에서 결정되는 요동의 시간적 거동은 무한히 지속되는 지 수적 증폭이나 감쇠 거동을 보이는데 이는 실험적 관찰 결과와 일치하 지 않는다는 것이다. 따라서 마스로우 (Maslowe, 1985) 의 총설에 개관 된 바와 같이 비선형 이론들아 발전되었다.
참고문헌 Bearman, R. B., J . G. Ki rk wood, Sta t i st i ca l mechnic a l the ory of tra ns- p o rt pr ocesses XI . eq u ati on of tra np o rt in mult ico mp o nent sys te m , Chem. Phy s. , 28, 136 (1958) . Benard, H., Les tou rbil lo ns cellulair e s dans une nap pe liq u id e , Revue Generale des Scie n ces Pures et Ap pli q u ees, 11, 1261 and 1309 (19 00) ; Ann. Chem. Phy s. , 23, 62 (19 01) . Bertr a nd, J. L. F., T hermody n ami qu e, Paris ( 1887) . Bi rd , R. B., W . E. Ste w art a nd E. N. Lig h tf oo t, T ransp o rt P henom- ena , W ile y, New York (19 60) . Block, H. D., Intr o ducti on to Te nsor Analys i s, C. E. Merrill Books, Columbus (19 62) . Busse, H, F., T rasit ion to tur bulence in Ray le ig h -Benard convec- tion , in Top ic s in Ap pli e d Phys i c s , ed. H. L. Swi nn ey and J. P. Gollub, Sp r in g e r, B erlin (1985) . Casim i r, H. B. G., On Onsag e r's pr in c ip le of mi cr oscop ic rever-sib i l it y , Rev. Mod. Phy s ., 17, 343 0945) . Chandra, K., I nsta b il it y of flui d s heate d from below, Proc. Roy . Soc., A 164, 231 (1938) . Chandraseker, S., Hy d rodyn ami c and Hy d romagn eti c Sta b il it y , Clarendon, Oxfo r d (1961) . Chap m an, S., T. G. Cowlin g , The Math e mati ca l Theory of Nonunif orm Gases, Cambrid g e Press, New York (1939) . Curi e, P., Jou rnal de Phy si q u e, 3 d seri es , 3, 393 (1894) , Oeuvres de
Pie r re Curz·e, pp.1 18-141 , Gauth i e r -Vi llar s, Paris ( 19 08) . Deg n, H. , O scil lat i ng chemi ca l reacti on s in homog e neous ph ase, J. Chem. Educ., 49, 301 (1972) . Eig e n, M., Selfo r ga niz a ti on of matt er and the evoluti on of bio l og i- cal macromolecules, Di e Natu r wi ss enschaft en , 58, 465 (1971) . Fie l d, R. J., R. M. Noy e s, Oscil lat i on in chemi ca l sys te m s. IV. Lim i t cy c le behavio r in a model of a real chemi ca l reacti on , J. Chem. Phy s. , 60, 1877 (19 74) . Fit ts, D. D., N onequ il i b r i um Thermodyn ami cs , McGraw-Hi ll, New York (1962) . Fug ita, H., L.G osti ng , Inte r pr eta t i on of data for concentr a ti on dep e ndent free dif fus io n in tw o comp o nent sys te m , J. Phy s. Chem., 64, 1256 (1960) . Gag e , K. S., and W. H. Reid , The sta b il it y of the rmally str a ti fied pla ne Pois e uil le f low , J. F uid Mech., 33, 21 (1968) . Glansdorf, P., I. Prig o g ine , Thermodyn ami c Theory of Str u ctu r e, Sta b il it y and Fluctu a ti on s, W ile y -I n te r sci en ce, London (1971) . Goel, N. ~-, S . C. Mait ra , and E. W. Montr o ll, On the Volte r ra and oth e r nonli ne ar models of int e r acti ng po p u lati on s, Rev. Mod. Phy s ., 4 3, 231 (1971) . Grodzka, P. G., a nd T. C. Bannis t e r , Heat flow and convecti on demonstr a ti on exp e rim ents aboard Ap o llo 14, Scie n ce, 176, 506(1972) . Haase, R., Thermodyn ami cs of Irreversib l e Processes, Addis o n-Wesley (1969) . Haken, H., Syn erge ti cs, Sp r in g e r-Verlag, Berlin ( 1978) . Jos ep h, D. D., Hy d rody n ami c Sta b il it y and Bif ur cati on , in Top ics in Ap pli e d Phys i c s , ed. H. L. Swi nn ey and J. P. Gollub, Sp r in g e r-Verlag, Berlin ( 1985) .
Knop s, R. J., E. W . Wi lk es, Theory of elasti c sta b il ity, in Han-dbuch der Phy s ik , Vla 3 : Mechnic s of Soid s III ed. C. Truesdell, Sp r in g e r, Berlin ( 1973) . Kobata k e, Y., Transit ion betw een tw o sta d y sta t e s in po rous charge d membrane, Phy si c a , 48, 301 (1970) . Krantz , W. B., K. J. Gleason and N. Cain e , Patt er ned Ground, Scie n ti fic Americ a n, December, 44 (19 88) . Kreuzer, H. J., Nonequ i l ib r iu m Thermodyn ami cs and its Sta t i sti - cal Foun-dati on s, Clarendon, Oxfo r d (1981) . Landauer, R., Phy s. Rev., Inadeq u acy of entr o p y and entr o p y deriv a ti ve s in charate r iz i n g the ste a dy sta t e s , A 12, 636 (1975) . Ledermann, W., S. Vajd a ed., H andbook of Ap pli c a ble Math - emati cs IV. Analysy s , W ile y, New York (1982) . Lin , C. C., Theory of Thermodyn ami c Sta b il it y , Cambrid g e Univ e r-sit y Press, Cambrid g e (1955) . Maslowe, S. A., Shear flow ins ta b il i ti es and tra nsit ion , in Top ics in Ap pli e d Phys i c s , ed. H. L. Swi nn ey and J. P. Gollub, Sp r in g e r-Verlag, Berlin (19 85) . Mi ller , D. G., Thermody n ami cs of irr eversib l e pro cesses : The exp e rim enta l verif ica ti on of Onsag e r rec ipr ocal relati on s, Chem. Rev., 60, 15 (1960) . Modell, M., R. C. Reid , Thermodyn ami cs and its Ap pli ca ti on , 2nd ed. , Prenti ce -Hall, Eng le wood-Clif fs ( 1983) . Ni co lis, G., Patt er n for mati on in reacti ng and dif fus in g sys te m s, Adv. Chem. Phy s. , 38, 263 (1978) . Ni co lis, G., I. Prig o g ine , Self- or ga niz a ti on in Nonequ i l ib r i um Sys t e m s, Wi le y, New York (1977) . Ni co lis, G., and J,S. Turner, Sto chasti c analys is of a noneq u il i- briu m ph ase tra nsit ion : Some exact result s, Phy s ic a , 89A,
326 (1977) . Ni co lis , G., R. Lefe v er, Comments on the kin e ti c p o te n ti al and the Maxwell constr u cti on in noneq u il ib r iu m ph ase tra nsit ion s, Phy s . Lett ., 62A, 469 (1977) . Onsag e r, L., Recip r ocal relati on s in irr eversib l e pro cess.II, Phy s. Rev., 38, 2265 (1931b) . Onsag e r, L., Recip r ocal relati on s in irr eversib l e pro cess. I, Phy s. Rev., 37, 405 (1931a) . Patt en , J. K., J.C . Leg ro s, Convecti on in Liq u id s , S p r in g e r-Verlag, Berlin (1984) Platt en ,]., These de doctr a t, Chim i e- Phsys iq u e, Univ e rsit e d e Bruxel-les ( 1970) . • Platt en , J. K., On varia t i on al for mulae for hy d rody n ami c sta b il - ity, Int. J. Eng . Sci. , 9 , 37 (1971) . Prig o g ine , I., From Bein g to Becomi ng , Freeman, New York (1983). Prig o g ine , I., Intr o ducti on to Thennodyn ami cs of Irreversib l e Processes 3rd ed., Inte r scie n ce, New York (1967) . Prig o g ine , I., I. Ste n g e rs, Oder out of Chaos, Banta m Books, New York (1984) . Ray le ig h , Lord, On convecti on current in a horiz o nta l lay e r of flui d when the hig h er tem p e ratu r e is on the up pe r sid e , Phil . Mag. , 32, 529 (1916) . Schechte r , R. S., D.M. Hi m melbrau, Local po te n ti al and sys te m sym metr y , Phy s. of Fluid , 8, 1431 (1965) . Sehl gl, F., Chemi ca l Reacti on models for noneq u il ib r iu m ph ase tra n-sit ion , Z. Phy s ik , 253, 147 (1972) . Slatt er y, J. C., Momentu m , Energy , and Heat Transfe r in Conti n- ua, McGraw-Hi ll, New York (1972) . Sommerscale, E. F. C., T. S. Dohert y, Observed flow pa tt er ns at
rne m1-t1 a t1 o n ot convecti on in a horiz o nta l liq u id lay e r heate d from below, J. F luid Mech., 4 2, 755 (1970) . Sta n dart, G . L., R . Tayl o r, R . Kris h na, The Maxwell-Ste f a n for- mulati on of irr versib l e th ermody n ami cs for sim ulta n eous heat and mass tra nsfe r , C hem. Eng . Commun., 3, 277 ( 1979) . Tadzhib a ev, P. A., Realiz a ti on of crit er ia of the evoluti on of the Glansdor f-P r ig o g ine hy po th e sis for a Ray le ig h ga s wi th chemi - cal reacti on s and an exte r nal pa rti cl e source, Zh. Fiz . Khim ., 61, 263 (1987) . Thomas, L . H., The sta b il it y of pla ne Pois e il le flow , Phy s. Rev., 91, 780 (19 53) . Thomson, W., Exp e rim enta l researches in th ermo-electr i c ity, Pro. Roy . Soc. (Edin b urgh ) , May (1854) . Ti en , C. L., J. H. Lie n hard, Sta t i sti ca l Thermodyn ami cs, Hemi - sp h ere, Washin g ton ( 1979) . Ty so n, J. J., O n the ap pe arance of chaos in the Belousov reac- tion , J. Math . Bi o. , 5, 351 (1978) . Ty s on, J. J., The Belousov-Zhaboti ns kii reacti on , Lectu r e Note s in Bi om ath emati cs , vol 10, Sp r in g e r,· Berlin (1976) .
기 가로롤 (Transverse Roll) 210 가역 과정 (Reversib l e Process) 20, 2 5 각속도 (Ang ul ar Velocit y) 60 계 (Sy st e m ) 18 고유치 (Eig e n Value) 13 5 공간적 질서 (Sp ac e Order) 14 7 과도 안정 성 (Oversta b il it y ) 148, 176 과잉 수지식 (Excess Balance Eq n) 171 과잉 국소 퍼 텐셜 (Excess Local Pote n ti al ) 198, 205, 206 과잉 엔트로피의 생성 (Excess Entr o p y Producti on ) 169 과잉 엔트로피의 생성 속도 98, 109, 129 과잉 엔트로피의 흐름 109 과잉 혼합 엔트로피 (Excess Mi xe d Entr o p y) 98 교란 (Pertu rbati on ) 98 국소 안정 성 (Local Sta b il it y ) 조건 116 국소 엔트로피 (Local Entr o p y) 79 국소 퍼 텐셜 (Local Pote n ti al ) 99, 119, 189, 191 국소 평 형 (Local Eq ui l ib r iu m ) 19, 28 , 97 극한 싸이클 (L i m it Cy c le) 134 ,14 2 기 계 적 에 너 지 (Mechanic a l Energy ) 34 기 계 적 접 촉 (Mechanic a l Conta c t) 18 기 계 적 평 형 (Mechanic a l Eq u il ibr iu m ) 87, 90 기본 방정식 (Fundamenta l Eq n) 32 기체분자 운동론 (K i ne tic Theory) 30 깁 스 에 너 지 (Gi bb s Energy ) 3 5 깁스-두엠식 (Gi bb s-Duhem Eq n ) 37, 81, 83
L 나비에-스토크스식 (Navie r -Sto k es Eq n ) 47, 168 내부 에너지 수지식 48 내부 에너지 (Inte r nal Energy ) 18, 20 노드 (Node) 14 2, 163 C 다성분 등온계 86 다성분 등온등압계 80 다중 정상 상태 (Multip le Ste a dy sta t e ) 14 7 단열계 (Adia b ati c Sy s te m ) 18 닫힌계 (Closed Sy st e m ) 18 대칭성파괴의 불안정성 (Sy mm etr y Breakin g Insta b il ity) 14 7, 158, 161 • 동역학 퍼텐셜 (D y nam i c Pote n ti al ) 102, 152 동역학적 안정성이론 114 두갈래 치 기 (Bi furc ati on ) 24, 14 2 두프르 효과 (Dufo u r Ef fec t) 90 등온충류의 안정 성 199 근 라그란지 계 (Lag ran g e Sy st e m ) 44 라그란지 안 (La gr an gi an) 193, 197, 199 레 이놀즈수 (Re y nolds Number) 190 레 일리수 (Ra y le ig h Number) 169 로트카-볼테 라 모델 (Lotk a-Volt er a Model) 127, 142 롤 (Roll) 185 르장드르 변환 (Le g endre Transfo r mati on ) 35 리아푸노프 방법 158 리아푸노프 제이방법 (Liap o unov Second Meth o d) 101
리아푸노프 함수 103, 105, 157 □ 무질서도 24 물질 도함수 (Substa n ti al Deriv a ti ve ) 44 물질 수지 식 (Mass Balance Eq n ) 43, 44 미카엘리스-멘튼 반응기구 (M i chae li s-Men t on Mechanis m ) 156 밀도 (Densit y) 42 1::1 반응 속도 (Reac ti on Rate ) 44, 75, 125 반응 속도식 (Reacti on Rate Eq n ) 77 발산의 정 리 (Dive rge nce Theorem) 42 벌크점도 (Bulk Vis c osity ) 46 베나드 대류 (Bernard Convecti on ) 167 베나드-레 일리 문제 (Bernard-Ray le ig h Problem) 168 벨루소프-자보민스키 (Belusov-Zhaboti ns ki) 반응 143 변분원리 (Varia t i on al Prin c ip le ) 191 변환성 질 (Transfo r mati on Prop e rty ) 63 보존의 법 칙 (Conservati on Law) 39 부분몰 성질 (Parti al Molar Prop e rty ) 32 부분질량 성 질 (Partia l Sp e ci fic Prop e rt y) 32 부시 네 스크 근사법 (Boussin e sq Ap pr oxim ati on ) 169, 190, 202 부시네스크식 171 분배 함수 (Part ition Functi on ) 29 브릿셀레이터 반웅 (Brussela t or Reacti on ) 158 브릿셀레이터 반응기구 135 비 가역 과정 (Irreversib l e Process) 22 바가역 열역학 (Irrevers i ble Thermody n ami cs ) 18, 22 비 가역 성 (Irreversib i l it y ) 27
비 리 알식 (Vi rial Eq n ) 152 비선형 안정성이론 184 바 평 형 상전이 (Nonlin e ar Phase Transit ion ) 148 비 평 형 열 역 학 (Noneq u il ibr iu m Thermody n ami cs ) 18 비평형계의 안정성 107 人 사전평 형 (Preeq u il ib r iu m ) 149 선형 열역학(Li near Thkermody na mi cs ) 55, 73, 110 선형화된 과잉수지식 171 세 로를 (Long itud in a l Roll) 210 소레 이 계 수 (Soret Coeff ici e n t) 90, 91 소산 구조(Di ss ip a ti ve Str u ctu r e) 24, 164, 184 수지식 (Balance Eq n ) 42 스테판-맥스웰식 (Ste f a n -Maxwell Eq n ) 86 스토크스 가설 (St ok es Hy po th e sis ) 46 시 간적 질서 (Tim e Order) 12 5 시 강성 질 (Inte n siv e Prop e rt y) 3 3 시 량성 질 (Exte n siv e Prop e rty ) 3 3 시 벡 효과 (Seebeck Ef fec t) 9 5 실뢰글 모델 (Schlog l Model) 148 。 안정성 (Sta b il it y ) 97, 100, 111, 125, 189, 199 안정성교환의 원리 (Prin c iple of Exchang e of sta b il ity) 147,176, 182 에너지 보존의 법칙 19 에너지 수지식 47 에 델시 타인 모델 (Edelste i n Model) 15 5 에르고드 가설 (Ergo dic Hy po th e sis ) 63 엔탈피 (Enth a lpy ) 3 5
엔트로피 (Entr o p y) 20 , 24 엔트로피 생 성속도 (En t ro py Producti on Rate ) 23, 55, 65, 89, 98, 105, 107 엔트로피 수지식 39, 50 엔트로피의 생성 22, 50, 51, 75 엔트로피의 흐름 22 연계된 화학반응 (Cou p led Chemi ca l Reacti on s) 43 연 계 된 흐름 (Coup le d Flow) 74 열 (Heat) 20 열 린 계 (Op en Sy st e m ) 18 열역학 제이법칙 21 열역학 제일법칙 20 열역학적 가지 (Thermody n ami c Branch) 143 열역학적 안정성판별 116 열적 접촉 (Thermal Conta c t) 18 열전 퍼 텐셜 (Thermoelectr i c Pote n ti al ) 94 열전대 (Thermocoup le ) 94 열전도 법칙 56 열전효과 (Thermoelec t r i c Ef fec t) 23, 93 열확산 (Thermal Diffus io n ) 89 오레고네이터 반응 (Ore g ona t or Reacti on ) 14 3 오르-솜머 펠드식 (Orr-Sommerfe l d Eq n ) 201, 205 오일러-라그란지식 192, 196, 198 오일러계 (Euler Sy st e m ) 44 온사거 - 카시 미 르 관계 (Onsag e r-Casim i r Relati on ) 60 온사거의 상호관계 (Onsag e r Recip ro cit y relati on ) 23, 60, 84 요동 (Fluctu a ti on ) 28, 29, 63, 98 운동량 수지식 45 운동량 (Momen t um) 43 운동론적 퍼텐셜 (K i ne ti c Pote n ti al ) 99, 102, 113, 153, 156 원심력장 (Cen t r ifug al Force field ) 87, 88 유선함수 (S t ream Functi on ) 185 이상한 유인자 (S t ran g e At tra cto r ) 145
이완현상 (Relaxa ti on Phenomenon) 28 이 차형 식 (Qu adrati c Form) 5 8 일 (Work) 20 일반적 진화의 법 칙 (General Evoluti on Theorem) 111 일반화된 국소퍼텐셜 191 임계레일리수 182 임 계 점 (Crit ica l Poin t ) 151 大 자촉매 반응 (Auto c ata l yt ic Reacti on ) 13 s 장변수 (F i eld Varia b le) 18, 28 전기 화학 퍼 텐셜 (Elecrochemi ca l Pote n ti al ) 88 전단점도 (Shear Vi sc osit y) 46 전달의 열 (Heat of Transpo rt) 92 전열계 (Di at h e rrnal Sy s te m ) 18 점 성 법 칙 (Vi sc osit y Law) 5 6 점 탄성 류 (Vi sc oelastic Flow) 46 정 규모드 (Normal Mode) 98, 115 정규모드 해석 126, 169, 173 정 부피 바 열 (Consta n t Volume Heat Cap a cit y) 30 정상상태 (Ste a dy Sta t e ) 18, 120, 139, 147, 153, 159, 196 정 암비 열 (Consta n t Pressure Heat Cap a ci ty) 30 제이종 영구기관 21 제일종 영구기관 20 제 차함수 (Homog e neous Functi on ) 3 3 주위 (Env iro nment) 18 진화 (Evolu ti on) 21, 97 전화의 법칙 (Law of Evoluti on ) 21, 126 질량농도 (Mass Concentr at i on ) 32
云 초점 (Focus) 142 충돌 사이 의 시 간 (Tim e betw een Coll isio n s) 31 충류 (Lam i nar Flow) 의 안정성 189,2 0 2 친화력 (Affini t y) 77 침강 퍼텐셜 (Sedim enta t i on Pote n ti al ) 87 침 강 (Sedim enta t i on ) 86 = 큐리 의 정 리 (Curie ' s Theorem) 59, 74 E 통계 역 학 (St at i st ic a l Mechanic s ) 17, 29 튜링 불안정 성 (Turin g Insta b il it y ) 160 특성 방정식 (Characte r is t i c Eq n ) 129 고 파라데 이 상수 (Faraday Consta n t) 88 퍼 텐셜 에 너 지 (Pote n ti al Energy ) 19, 48 펠 티 에 효과 (Peltie r Ef fec t) 95 평 균 자유행 정 (Mean Free Path ) 30 평 형 (Eq u li br iu m ) 21 평형상태의 안정성 103 포아서유 흐름 (Po i seu ill e Flow) 189 푸리 에 법 칙 (Fourie r 's Law) 49 프란들 수 (Pran t dle Number) 174 피크의 법칙 (Fick 's Law) 45, 82, 83
-lo 헬름홀츠 에 너 지 (Helmholtz Energy ) 3 5 현상적 계수 (Phenomenolo gi cal Coeff ici e n t) 75 현상적 법 칙 (Phenomenolog ica l Law) 56 혼돈 (Chaos) 14 5 혼합미분 (M i xed Di ffer enti al ) 116 화학 친화력 (Chemi ca l Affini t y) 57 화학 퍼텐셜 (Chemi ca l Pote n ti al) 32, 35 화학반웅 (Chem ic al Reacti on ) 75, 125, 147 화학반웅계의 안정성 125 화학진동 (Chem i cal Oscil lat i on ) 134 확산 (Diffus io n ) 80, 86 확산법칙 56 흐름의 플럭스 55, 56 힘 (Force) 55, 56
이철수 서울대학교 화학공학과 졸업 풀로리다주립대학교 화학공학과 졸업 (석사, 박사) 한국원자력연구소 책임연구원(실장) 현재 고려대학교 화학공학과 교수 저서 『 신과학운동 』 (공저) 역서 『 화학공학 열역학 』 (공역) 외 비가역 열역학 대우학술총서 • 자연과학 85 초판찍음 -1993 년 2 월 10 일 초판펴 냄 - 1993 년 2 월 20 일 지은이―-―이철수 펴낸이——朴孟浩 펴낸곳-(주) 民音社 출판등록 1991 . 12. 20 제 16-490 호 우편대체번호 010041-31-0523282 은행지로번호 3007783 135-120 서울시 강남구 신사동 506, 강남출판문화센터 515-2000~2 (영 업부) , 515-2003~5 (편집부) 515-2007, 2101 (팩시밀리) 값 8,500 원 Prin t e d in Seoul, Korea © 이철수, 1993 열역학 KDC/426.7 ISBN 89-374-3585-3 94430 ISBN 89-374-3000~2 (세트)
대우학술총서 (자연과학) 1 소립자와 게이지 상호작용 김진의 44 한국의 고 생물 이 하영 2 동력학특론 이병호 45 질량분석학 김명수 3 질소고정 송승달 46 금변론 박대현 4 상전이와 임계현상 김두칠 47 생체에너지 주충노 5 촉매작용 진종식 48 리 이만 기하학 박을룡 6 뫼스바우어 分光學 옥항남 49 君表理論 박승안 7 극미량원소의 영양 승정자 50 비선형 편미분 방정식론 하기식 8 수소화봉소와 유기봉소 51 생체막 김형만 화합물 윤능만 52 수 리 분류학 고철환 9 항생물질의 全合成 강석구 53 찰스 다윈 정용재 10 국소적 형태의 Ati yah -sin g e r 54 금속부식 박용수 지표이론 지동표 55 양자광학 이상수 11 Mucop ol y sacchar i des 의 56 효소반응 속도론 서정현 생화학 및 생물리학 박준우 57 화성암 성인론 이만성 12 천체물리학 홍승수 58 확률론 구자홍 13 프로스타글라딘 合成 김성각 59 분 자 분광학 소현수 14 天然物化學硏究法 우원식 60 벡 터 속 이론 양재현 15 脂訪營養 김숙회 61 곤충신경 생리학 부경생 16 結 晶 化유리 김병호 62 에너지띠 이론 모혜정 17 고분자에 의한 화학반응 조의환 63 수학 기초론 김상문 18 과학혁명 김영식 64 신경과학 김승업 ·박찬웅 19 한국지질론 장가홍 65 BC H 부호와 Reed- 20 정 보 이론 한영열 So l omon 부호 이만영 21 원자핵반응론 정운혁
