

이양림 서울대학교 문리과대학 동물학과를 졸업하고 미국 워싱톤대학교에서 발생생물학을 연구하여 석·박사 학위를 받았댜 현재 이화여자대학교 생물과학과 교수로 재직하고 있으며 논문으로 「난자형성중 유전자 발현의 변화에 대한 연구」 외 20 여 편이 있다.
발생과 유전자 발현 
 발생과 유전자 발현
발생과 유전자 발현
『발생과 유전자 발현 』 正誤表 페이지 행 訂正내용 19 上 1-2 (誤) 고 있다. 이를 회색신월대(g ra y crescen t)라고 하는데, 낭 배형성시 합색소가 산만하게 분포되어 있는데. 적도면 바로 밑에반월모양을하 (正) 색소가 산만하게 분포되어 있는데, 적도면 바로 밀에 반월 모양을하고있다.이를회색신월대(g ra y crescen t)라고하 는데,낭배형성시함 31 | 上 l (誤) 대한 연구로 클레멘트의 연구를 계속하였다. (正) 대한 연구로 윌슨의 연구를 계속하였다.
책 머리에 생물학에서 생명현상에 대한 현상론적 설명은 어렵지 않으나 기구 론적 설명은 대단히 어렵다. 한 개의 세포가 다세포화하면서 일어나 는 세포운명결정에 대한 기구론적 설명도 쉬운 일이 아니다. 일반적 으로 기구론에 대한 설명이 어려운 이유는 아마도 생물학에는 생명현 상을 설명할 수 있는 생물학적 법칙이나 원리가 결여되어 있기 때문 아 아닌가 생각된다. 생물학에는 현상에 대한 개념은 있으나 현상의 원인을 설명할 수 있는 법칙이나 원리가 거의 없다. 그렇기 때문에 생물학자들은 생명현상을 설명하기 위하여 물질과학에 있는 법칙이나 원리를 빌려온다. 물론 생물체내에는 어느 정도 물질의 법칙에 따르 는 현상이 있으나, 사실상 물질의 법칙에 따라 생명현상을 설명하는 데에는 한계가 있다. 지난 200 여년 동안 세포운명결정에 대한 기구론 적 설명에 어려움이 있는 것도 이러한 이유때문이 아닌가 생각된다. 일반적으로 세포특이 단백질이 특정한 세포에 존재하면 그 세포의 기능이 부여된다고 생각하는 것이 발생학적 견해이다. 동일한 조성의 유전자를 가지고 있을지라도 선택적으로 조절되는 유전자 발현의 결
과로 세포특이 단백질이 생성되기까지 정교하고 섬세하면서도 폭넓게 작용하는 조철요인들을 전제하지 않고는 세포운명결정의 조절기구를 설명할 길은 없다. 조절요인의 정체는 무엇이며, 조절요인이 어떻게 작용하여 그와 같은 현상을 일으킬 수 있는가 ? 필자는 이 책에서 지금까지의 발생생물학의 놀라운 발전에 따른 새 로운 업적들뿐만 아니라 아직도 발생학자의 도전의 대상이 되는 넓은 미지의 세계가 있음을 보여주고저 노력하였다. 아직도 도전하는 과학 의 폭보다는 생명 속에 담겨져 있는 전실의 폭이 더 크기 때문인지는 알 수 없으나, 이룬 것 보다는 이루어져야 할 것이 더 많은 것처럼 느껴진다. 끝으로 이 책의 저술을 위하여 지원해 준 대우재단의 도움과 이 책 을 출간해 준 민음사의 노고에 감사한다. 1992 년 6 월 이양림
발생과 유전자 발현
차례 책 머리에 • 5 제 1 장 서론 11 제 2 장 결정요인의 선택적 분배 17 1 난자의 세포질 이동 • 17 2 멍게 발생배에서의 세포질 분배 • 20 3 세포 계보 • 26 4 연체동물과 절지동물 발생배에서의 세포질 분배 •28 5 유즐동물의 발생배에서의 결정요인의 선택적 분배 • 40 6 생식세포 결정요인의 선택적 분배 • 41 (1) 선충에서의 생식세포 결정요인 • 42 (2) 곤충에서의 생식세포 결정 요인 • 44 (3) 양서류에서의 생식세포 결정요인 • 51 7 쌍시목 곤충류에서의 결정요인의 분배 • 55 8 결정요인의 정체 • 57 참고문헌 • 59제 3 장 유전자 동질성 67
1 유전자 동질성 • 68 (1) 핵이식 • 69 (2) 운명 전환 • 80 (3) 유전자 동질성에 대한 분자생물학적 증거 • 83 참고문헌 • 90 제 4 장 전사수준에서의 유전자 발현의 형태 93 1 게놈의 부분적 불활성화 • 93 (1) 쥐똥나무벌레에서 부계 염색체의 이질 염색질 • 94 (2) 포유류의 X염색체의 불활성화 • 96 2 유전자 변경 • 102 (1) 유전자 손실 • 102 (2) 유전자 증폭 • 102 (3) 유전자 재배열 • 106 3 순차적 유전자 발현 • 116 (1) 다사영색체 • 117 (2) 성게 발생에서의 순차적 유전자 발현 • 125 (3) 양서류 발생에서의 순차적 유전자 발현 • 128 참고문헌 • 131 제 5 장 순차적 유전자 발현의 조절 137 1 염색질의 구조 • 137 2 진핵세포 게놈의 특징 • 1433 DNA 재결합 • 145
4 순차적 유전자 발현의 조절요인 • 154 (1) 세포질 요인 (cytoplasmic factor) • 154 (2) 염색질의 구조적 변화 • 158 (3) 비히스톤 단백질 • 161 (4) 호르몬 • 163 (5) 글로빈유전자의 전사 • 172 (6) 전사조절 단백질 • 175 (7) Switch genes • 181 참고문헌 • 184 제 6 장 진핵세포 유전자의 분자 구조와 유전자 발현의 조절 195 1 진핵세포 유전자의 분자 구조 • 195 2 promoter의 구조와 기능 • 203 (1) promoter의 구조 • 203 (2) trans조절 단백질과 promoter의 결합 • 206 3 enhancer의 구조와 기능 • 208 (1) 발생단계 특이 enhancer • 210 (2) 조직 특이 enhancer • 211 (3) 호르몬 특이 enhancer • 215 (4) Immunoglobulin경사슬유전자의 전사 • 218 (5) 메칠기 첨가반응 • 223 참고문헌 • 231제 7 장 RNA processing에서의 유전자 발현의 조절 241
1 heterogeneous nuclear RNA • 241 2 nRNA processing에 의한 유전자 발현의 조절 • 246 3 순차적 RNA processing • 253 4 RNA processing과정과 성 결정 • 259 5 3'말단의 결정 • 261 참고문헌 • 262 제 8 장 해독 및 후 해독 수준에서의 유전자 발현의 조절 275 1 해독 수준에서의 유전자 발현의 조절 • 275 (1) 단백질 합성의 협조적 관계 • 275 (2) mRNA 의 선택적 붕괴 • 282 (3) 해독 수준에서의 유전자 발현의 조절의 예 • 284 2 후 해독 수준에서의 유전자 발현의 조절 • 308 (1) 후 해독에 의한 단백질의 활성화 • 309 (2) 후 해독에 의한 단백질의 불활성화 • 311 (3) 세포내 단백질의 위치결정 一막과 리소좀을 위한 표적단백질 • 316 참고문헌 • 327 찾아보기 • 333제 1 장 서론 발생생물학의 핵심적인 주제는 단순한 구조와 기능을 가진 한 개의 세포로부터 복잡한 구조와 놀라운 기능을 가지는 고도의 생물학적 질 서인 다세포의 개체를 구현해내는 생물학적 기구에 있다. 100 조의 세 포로 구성된 사람일지라도 0 . 2mm 의 작은 한 개의 세포로부터 시작 하여 성체가 된다. 난자와 정자의 결합으로 이루어전 한 개의 세포는 세포분열을 동하여 증식됨으로써 여러 개의 세포가 되고, 여러 개의 세포는 배영 형성을 통하여 유사한 세포의 모임인 세포군으로 나뉘어 진다. 이러한 세포군들로부터 특정한 구조와 기능을 갖는 조직이나 기관이 형성되면서 개체 형성이 완성된다. 개체 형성은 크게 보아 성 장과 분화의 두 가지 과정에 의해서 성취된다. 성장이란 세포분열을 통해서 세포의 수를 증가시키는 과정을 의미하는데, 개체 형성은 단 순한 성장만으로는 불가능하다. 증식하는 세포가 정해전 질저에 따라 조절되지 않으면 무질서한 세포의 덩어리밖에는 될 수 없다. 증식된 세포들은 일정한 방향으로 조절됨으로써 한 개의 수정란으로부터 근
세포, 표피세포, 신경세포, 적혈구 등을 포함한 다양한 세포들로 분 화한다(표 l). 이와 같이 세포들이 다양한 방향으로 분화될 수 있도 록 조절되지 않으면 생물학적 질서의 구현은 불가능하다. 이러한 생물학적 질서의 구현은 반드시 세포분화를 수반하고, 세포 분화에는 반드시 세포운명의 결정이 선행되어야 한다. 17 세기에 등장 한 전성설에 의하면 이미 난자나 정자 속에 굉장히 작은 소화상의 생 물이 둘어 있다가 수정이 되면 성장함으로써 개체 형성이 가능한 것 으로 설명되었다. 그러나 19 세기 말에 등장한 후성설에 의하면 개체 형성은 소화상의 단순한 성장이 아니고 세포 운명의 점진적인 결정과 함께 다양한 방향으로의 세포분화에 기인한다고 설명되었다. 지난 반 세기 동안 세포운명의 결정기구는 발생생물학자의 관심의 초점이 되 어 왔다. 아직도 세포운명결정의 구체적인 기구에 대해서는 완전히 파악되지 않고 있으나, 개념적으로 그리고 현상적으로는 그 모습을 보이고 있다. 발생과정에는 크게 보아 두 가지 큰 특칭이 있다. 첫째는 발생과정 이 불연속적인 발생학적 사건들의 연결이라는 점이다. 발생과정 자체 는 사건들의 연결로서 전행되지만 발생학적 사건들간의 관계는 반드 시 연속적이 아니다. 죽 한 가지 발생학적인 사건을 통하여 다음에 일어난 발생학적인 사건을 예측할 수 없다는 점에서 발생과정은 불연 속적이다. 수정을 통하여 난할을 예측할 수 없고, 난할을 동하여 다 음에 일어날 세포군 형성 죽 배영형성을 예측할 수 없을 뿐만 아니 라, 배영형성을 통하여 기관형성도 예측할 수 없다. 이와 같은 관점 에서 볼 때 발생과정은 격변적으로 일어나는 불연속적 사건들의 연결 이라고 할 수 있다. 두번째 특칭은 불연속적인 발생학적 사건들이 단 순한 물질과 에너지의 공급만으로 그 연결이 불가능하다는 점이다. 죽 발생과정에서 나타나는 생물학적 질서의 구현은 물질과 에너지 공 급 이상의 생물학적 요인에 의한 조절이 필요하다. 죽 한 개의 세포 가 개체로 발전하는 과정이 에너지에 의한 물질의 복잡화와 같이 열
역학적 법칙에 따른 질서의 구현만으로는 설명이 불가능하다는 것이 다. 물론 발생이 진행되기 위해서는 기본적으로 적절한 물질과 에너 지의 공급이 필요하지만 그러한 공급만으로는 불연속적인 발생학적 사건들의 연결을 가능케 할 수 없다. 일반적으로 물질과 생물학적 에너지 이의의 디른· 생물학적 요인이 반드시 발생과정에 개입될 것이라는 생각이 지배적이다. 이러한 요인 울 결정요인(決定要因, morp h og en eti c de t e nni nan t)이라고 한다. 따라 서 발생생물학의 주제는 구체적으로 결정요인의 정체와 작용기구를 알아내는 데 있다 . 아리스토텔레스에 의해 처음으로 발생기구에 대하여 언급되기는 하 였으나 본격적으로 관심을 두고 견고한 설명을 시도한 때는 17 세기 중반이다. 정자나 난자 속에 이미 존재하고 있던 개체의 소화상이 단 순히 성장함으로써 개체를 형성한다는 전성설(前成說, pre fo n nati on theo ry ) 이 있었으나 전성설은 인정을 받지 못하였다. 전성설은 발생 기구에 대한 핵심적인 문제점은 인식하고 있었으나 문제점에 도전하 는데 있어서 방법론적인 문제가 있었다. 2 세기 후인 19 세기 말에, 발 생이 진행됨에 따라 구성이 점차 복잡하게 변함으로써 개체가 형성된 다는 후성 설 (後成說 epig e nesis ) 이 제 기 되 었고 현재 까지 인정 되고 있 다. 원래 후성설에 대한 생각은 아리스토텔레스에 의해 발상된 것이 지만 독일의 발생학자 울프 (Kas pe r Fri ed r ich Wol ff)에 의해 본격적으 로 제창되었다. 울프는 닭의 발생과정을 관찰하고 성체에서는 찾아볼 수 없는 조직으로 부터 심장, 혈관, 및 장과 같은 기관이 새롭게 형 성 되는 사실을 관찰하고 어떤 알지 못할 기본적 인 힘 (Vis e ssenti al is ) 에 의해서 발생이 수행된다고 생각하였다. 블루멘바하(J ohann Fri edrich Blumenbach, 1752~1840) 는 이러한 힘 울 발생 력 (Bi ldu ng strieb : developm ent forc e) 이 라고 불렀고 종에 따 라 이미 정해진 발생력에 힘입어 발생이 수행된다고 하였다. 현재는 기본적인 힘이나 발생력에 해당하는 결정요인이 세포의 운 명결정에 어떻게 작용하는지에 따라 발생기구론이 크게 두 가지로 나
뉘어지고 있다. 다양한 세포가 형성되기 위해서는 세포가 분화되어야 하며 세포가 분화되기 위해서는 세포의 운명이 우선 결정되어야 한 다. 이때 세포의 운명은 결정요인의 선택적 분배 혹은 세포간 상호작 용에 의한 유도에 의해서 결정된다. 결정요인의 선택적 분배에 대한 생각은 바이스만 (Au gu s t Weis m an, 1834~1914) 의 생식질설(生殖質說 ger m pla sm th eo ry)로부터 출발하였 다. 그 당시 후성설로 발생중 나타나는 변화를 설명하는 데에는 큰 무리가 없었으나, 결정요인의 세대간 연속성은 쉽게 설명되지 않았 다. 바이스만은 그 당시 발표된 염색체설에 힘입어 다음 대에 전승될 요소 즉 결정요인이 염색체에 잠재해 있다고 함으로써 이 문제에 대 한 답을 추구하였다. 죽 개체 형성에 필요한 결정요인이 유전적으로 생식세포를 동해서 다음 세대로 전승됨으로써 세대간 연속성이 이루 어진다고 설명하였다. 또한 그는 발생에 필요한 정보가 세포분열시 오른쪽 할구와 왼쪽 할구 속에 각기의 다른 결정요인이 분배된다고 가정함으로써 다양한 세포의 운명결정을 설명하였다. 결정요인이 염 색체에 있다는 생각은 잘못된 것으로 후에 판명되었으나, 그의 결정 요인의 선택적 분배에 대한 생각은 아칙도 인정할 만하다. 루후 (Wi lhe lm Roux) 는 이와 갇은 현상을 직접 실험적으로 보여주었다. 개구리의 2~4 세포기의 발생배의 일부를 파괴시키고 그 나머지를 발 생시켰을 때 그 일부가 결손된 상실배를 얻음으로써 바이스만의 생각 을 확인하였다. 1900 년대에 들어서면서 결정요인의 선택적인 분배를 통해 세포의 운명결정이 이루어질 것이라고 보베리 (Bover i), 핍 (Loeb), 모르간 (Mor g an) 등도 강하게 주장하였다. 결정요인의 선택 적 분배에 대한 생각은 사실상 결정요인이 유전자 그 자체가 아니고 세포질 속에 있으면서 세포의 운명 결정에 관여하는 것으로 이해되고 있다. 따라서 발생이 시작하기 이전에 이미 생식세포 특히 난자에 결 정요인이 준비되었다가 수정과 함께 결정요인이 세포에 따라 다르게 분배됨으로써 세포의 운명이 다르게 결정된다고 생각되고 있다. 이러 한 주장은 그 모양은 다르나 전성설과 어느 정도의 맥을 갇이 하는
 표 1-1 분화된 세포형과 주 생성물
표 1-1 분화된 세포형과 주 생성물
점을 찾아볼 수 있다. 그러나 세포간 상호작용에 의한 유도에 의해서 세포의 운명이 결정 된다는 생각은 앞에서 언급한 생각과는 상당한 대조를 이루고 있다. 세포간 상호작용이 세포의 운명결정에 중요한 역할을 할 것이라고 처 음 착안한 학자는 드리쉬 (HansD ri esch) 였다. 드리쉬는 루후가 개구 리알을 가지고 수행한 결손실험과 유사한 실험을 성게알을 가지고 하 였다. 즉 2, 4 및 8 세포기의 성게알의 할구를 분리하여 배양해 본 결
과 각각의 분리된 할구는, 발생하여 완전한 유충인 풀루티우스 (p lu t eus) 를 형성하였다. 이러한 실험결과는 루후의 실험결과와 대조 적이었다. 그후 호르스타디우스 (Sven Hors t ad i us) 에 의해서 발견된 성 게 알에 서 의 이 중구배 설 (double grad ie n t the ory) 과 슈페 만 (Hans S p emann) 의 유도현상의 발견은 세포간 상호작용으로 세포의 운명이 조철 및 결정된다는 생각을 견고하게 해 주었다. 본 저서에서는 결정요인의 선택적 분배에 따른 순차적 유전자발현 의 조절 문제를 분자생물학적인 측면에서 다루었다. 아직까지 이 문 제에 대한 궁극적인 해결을 얻지 못하였으나, 이러한 발생학적 주제 가 어떤 맥락 속에서 어떤 내용으로 연구되고 있는지를 취급하였다.
제 2 장 결정요인의 선택적 분배 루후의 실험 그 자체는 실수였으나 그의 실험 결과는 결정요인의 선택적 분배가 세포의 운명 결정의 원인일 가능성을 보여주었다. 결 정요인을 가정하지 않고는 세포운명의 결정과정을 생물학적으로 설명 할 길이 없었기 때문에 무엇보다도 결정요인의 실재를 확인하는 것은 중요했다. 루후 이후 많은 실험발생학자들에 의해서 여러 종류의 동 물의 발생중 세포질의 선택적 분배가 세포운명결정에 중요한 역할을 한다는 사실이 확인되었다. 비록 결정요인의 물질적인 정체와 선택적 분배 과정의 실제에 대하여 분명히 알려진 바는 없었지만, 결정요인 의 선택적 분배에 대한 관찰은 발생학자들에게 커다란 가능성과 희망 울 던져 주었다. 1 난자의 세포질 이동 멍게의 난자에서는 수정되는 죽시 세포질 이동이 일어난다. 멍게
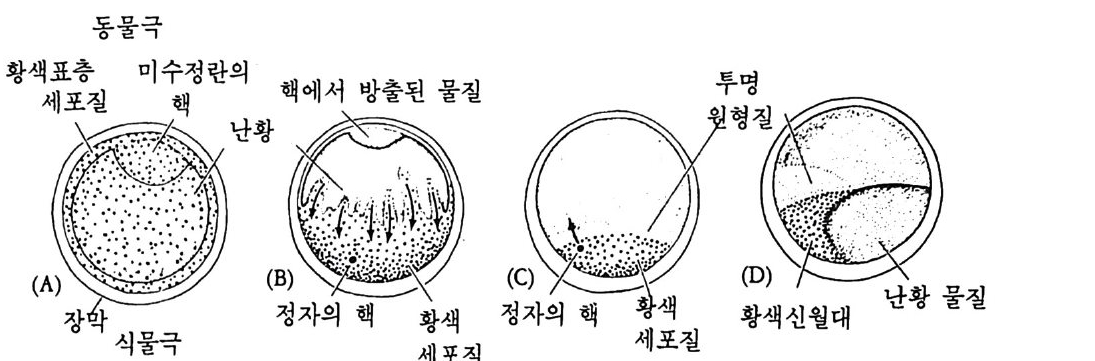
난자에는 종에 따라 독특한 색깔의 색소가 있는데 이 색소는 미수정 란에서는 난자 전체에 고루 분포되어 있다. 일단 수정이 일어나면 색 소의 이동이 일어난다. 이러한 색소의 이동과 함께 결정요인의 이동 울 직접적으로 관찰할 수도 없고 색소자체가 결정요인으로 확인된 바 없으나, 이러한 세포질의 이동은 나중에 세포의 선택적 운명 결정에 중요한 역할을 한다는 사실을 확인할 수 있었다. 가장 뚜렷한 예는 콩클린 (Conk li n) 에 의해 1905 년에 멍게의 일종인 Sty e la p a rtita 에서 관찰된 것이다. St y ela 의 미수정란에는 중앙에 회색의 세포질이 있고 그 주위를 황색의 지방립이 둘러싸고 있다. 핵은 동물극쪽에 위치하 고 있는데 배란직후 투명물질을 방출하면서 붕괴된다. 이미 마수정란 에 극성 (p ola rity)이 정해져 있으며, 정자의 전입이 식물극 쪽에서 일 어난다. 수정 전까지는 세포질에 아무런 변화가 없으나 정자의 진입 후 5 분 이내에 황색 및 두명 세포질이 식물반구로 이동하여 정자 진 입부위에서 황색 세포질과 두명 세포질이 포개전 형태로 모이게 된 다. 동시에 회색 세포질은 중앙에서 동물극쪽으로 이동한다. 식물국 쪽으로 진입한 정자의 핵이 적도면을 향하여 이동하여 난자의 핵과 융합하는데, 이때 황색 세포질은 정자의 핵을 따라 적도면 쪽으로 흐 름으로써 적도면에서 식물극에 이르는 황색 세포질의 신월대가 형성 된다(그림 2-1 ). 발생이 진행되면서 이들 색소 세포질은 64 세포기에 5 종류로 발전하고, 후에 분배받은 세포질의 종류에 따라 세포의 운명 이 다르게 결정된다. 세포질 이동은 양서류의 난자에서도 관찰되었다. 양서류의 미수정 란을 보면 동물 반구는 검고 식물 반구는 밝은대, 이러한 차이는 표 층에 분포된 멜라닌 색소의 정도 때문에 생긴다. 정자는 동물반구 어 디에서나 진입하는데, 일단 수정되면 세포질의 이동을 멜라닌 색소의 변화를 통해 관찰할 수 있다. 죽 표충 세포질과 중심 세포질이 이동 하여 색소로 덮혀 있던 부위가 색소가 없는 표층으로 대치된다. 정자 의 전입부위 반대편에 새로이 노출된 부위에 있는 세포질에 회색의
 도o口 .멸:,:,i
도o口 .멸:,:,i
그림 2-1 Sty e la par ti ta 난자에서의 세포질 이동. (A) 수정 전에는 황색의 표 충 세포질이 회색의 세포질을 둘러싸고 있다. (B) 수정 직후 황색의 표충 세포질과 핵의 붕괴로 방출된 두명한 세포질이 식물국을 향하여 이동한다. (C) 정자의 핵이 동뭉국쪽으로 이동할 때 황색 세포질과 두명 세포질도 함 께 이동한다. (D) 황색 및 무명 세포질이 결국 안정된 자리를 잡는다. 후에 무명 세포질은 중배영으로, 황색 세포질은 근육세포로 분화된다 (Conk li n, 1905).
고 있다. 이를 회색신월대(gr a y crescen t)라고 하는데, 낭배형성시 함 색소가 산만하게 분포되어 있는데, 적도면 바로 밑에 반월 모양을 하 입이 처음으로 일어나는 부위이며, 후에 올챙이의 등쪽을 형성하게 된다. 수정 후 표충의 세포질만이 이동하는 것이 아니고 중십 세포질에도 변화가 나타난다. 양서류 미수정란의 세포질은 여러 충의 세포질로 구성되어 있다. 동물반구에는 멜라닌 색소총 의에 감수분열 전에 핵 속에 있던 물질을 포함한 두명 색소충, 리보솜과 미토콘드리아를 포 함한 세포질층 및 글리코겐 입자, 지방립, 작은 난황립이 포함되어 있는 충이 있다. 반면에 식물반구에는 세포질 성분은 거의 없고 크기 가 큰 난황립이 있다. 수정 후 이러한 세포질충에는 세포질 이동에 의해 많은 변화가 일어난다. 회색 신월대에서는 가장 동물국 충의 세 포질이 가장 식물국 층의 세포질과 집하게 되는 반면, 반대편에서는 미수정란의 상태를 그대로 유지하게 된다 (Kla g and Ubbels, 1975 ; Gerhart et al., 1983} .
세포질 이동의 기구에 대한 정보가 지금까지 알려지지 않았으나 근 래에 미세소관( 微 細小 管 mi cro tu bule) 의 개입에 기인한다고 실험적으 로 입증되었다 (Gerha rt et al., 1981}. 멍게나 양서류의 알에서 난할이 일어나면 난할의 함입부위가 알의 정중선을 따라 알을 똑같이 두 개 의 부분으로 나눈다. 이때 첫번째 난할의 함입 부위도 임의로 정해지 는 것이 아니고 정자의 진입과 그 후에 일어나는 세포질의 이동에 따 라 정해지는 것으로 생각되고 있다. 개구리의 알을 콜히친 (col chici ne) 으로 처리하면 성상체도 형성되지 않을 뿐만 아니라 세포질 이동도 일어나지 않는다. 따라서 정자의 중심립이 세포분열과 세포질 재분배에 관여하는 것으로 추측되고 있다. 2 멍게 발생배에서의 세포질 분배 멍게의 2 혹은 4 세포기의 알로부터 할구를 분리하여 배양하면, 정 상적인 발생에서 나타나는 그 부위의 구조가 그대로 형성되고 다른 할구에서 형성되는 구조는 전혀 형성되지 않는다. 콩클린은 1905 년 수정란에서의 세포질 이동에 관해서 뿐만 아니라 수정 후 세포질 분배 에 관해서도 연구하였다. 세포분열과 함께 나타나는 색소의 특정된 할구로의 분배를 발생단계를 따라가며 추적하였다. 첫번째 세포분열 에 의해서는 좌우상칭으로 나누어진다. 황색 및 회색 신월대까지도 모두 좌우상칭으로 나누어침으로써 세포질이 동일하게 두 개의 할구 로 분리된다. 두번째 세포분열은 동 • 식물축에 평행하나 첫번째 세포 분열면에 대해서는 직각인 면에서 이루어전다. 그러나 세포분열면이 알의 뒷쪽으로 치우쳐져서 알의 크기가 동일하지 않게 된다. 따라서 두 개의 작은 할구에는 황색 신월대의 세포질이 그리고 큰 두 개의 軒는· 회색신월대의 세포질이 분배된다. 세번째 세포분열은 적도면 에서 일어나는대, 동물 반구의 두명 세포질과 회색 신월대의 윗부분 이 동물극 할구로 들어 가고, 식물극 할구로는 회색 신월대의 아랫부
 도o . 놀0 - 그기
도o . 놀0 - 그기
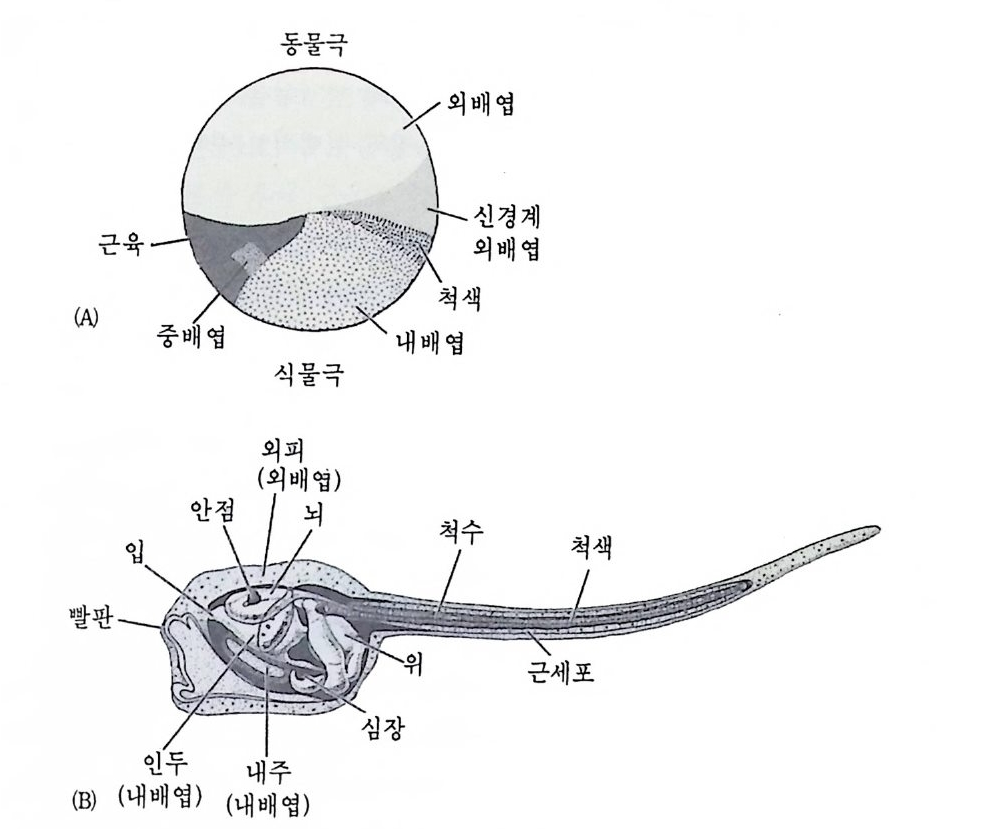
그림 2-2 결정요인의 선택적 분배. (A) 멍게 (Sty e la p a rtita)의 수정란에서의 세포질의 예정된 운명에 따른 위치 (B) 멍게의 유생에서의 기관
분이 들어간다. 이와 같은 세포질의 분배가 난할의 진행과 함께 계속 된다. 결국 황색 세포질의 신월대로 부터는 근세포, 적도면의 회색 세포질의 신월대로부터는 척색과 신경판, 동물극의 두명 세포질로부 터는 유생의 표피세포, 그리고 난황이 많은 회색의 식물국 부위로부 터는 유생의 장이 형성되는 사실을 관찰하였다. 콩클린은 이와 같은 관찰만으로는 세포질의 선택적 분배가 세포 운명 결정의 원인이 될 수 있다고 확신할 수 없었다. 그는 할구를 선택적으로 제거시키거나 파괴시킨 후 남은 할구만을 배양한 결과 언제나 불완전한 발생배가
형성됨을 관찰하였다. 또한 원심분리기를 이용하여 세포질을 이동시 킨 후 배양시켜 본 결과 비정상적인 유생의 발생됨을 관찰할 수 있었 다. 콩클린은 세포의 운명 결정은 세포질의 선택적인 분배에 그 원인 이 있다고 결론지었다. 리베버리 (Reverber i)와 민간티 (Mi ng a n ti ) (1946) 도 멍게 발생에서의 세포운명결정에 대한 분석을 일련의 할구 분리 실험을 통하여 수행하 였다. 8 세포기의 발생배의 할구를 두 개씩 묶음으로 하여 4 부분으로 나눈 다음 각각의 할구 묶음이 발생하여 생성하는 세포들의 종류를 조사하였다. 리베버리와 민간티도 원칙적으로는 콩클린과 동일한 결 론에 도달하였다. 죽 동물국 할구로부터는 의배영세포가 그리고 식물 극 할구로부터는 내 배 영 과 간충직 (mesenchym e ) , 근육조직 이 예 정 배 역도에서 예상한 대로 형성된다. 그러나 신경세포는 이러한 원칙과는 다론 방법으로 형성되는 것을 관찰하였다. 죽 식물극의 세포만이나 혹은 동물국의 세포만으로는 신경세포가 형성되지 않고, 두 종류의 세포가 함께 존재할 때에만 신경세포의 형성이 가능하였다. 즉 세포 질의 선택적 분배에 의해서 세포의 운명이 결정되는 멍게의 발생에서 도 부분적으로는 세포의 상호작용에 의해서 세포의 운명이 결정됨을 보여주었다. 오토라니 (Or tol ani, 1959) 도 64 세포기까지는 의배영이 신 경세포로 그 운명이 결정되는 것이 아니라는 점을 보여 주었다. 멍게 발생에서 대부분의 조직이 선택적 세포질 분배에 의해서 세포의 운명 이 결정되지만, 어떤 조직의 운명은 유도작용에 의해서 점진적으로 결정된다. 대체로 콩클린의 결론이 멍게의 경우에서는 옳다는 것이 생화학적 인 방법에 의해서도 증명되었다 (Wh itt aker, 1977). S ty ela 의 발생과 유사한 발생 양상과 세포질의 구성을 가진 멍 게 의 일종인 Cio n a i n te s tin al is의 발생 단계에 따라 일어나는 근육 결정 요인의 분배 과 정 을 조직 화학적 인 방법 으로 알아보았다. acety lc holi ne ste r ase (AchE) 가 직접 근육세포의 결정요인이 될 수 없으나, 근육세포에는
반드시 AchE 가 존재한다는 점을 이용하여 AchE 의 분포의 변화를 발생과정을 통해 알아보았다. 8 세포기의 발생배에서 B4-1( 그립 2-3) 에 해당하는 세포 즉 콩클린에 의해서 황색 신월대의 세포질이 들어 있는 할구로서 후에 근육조직으로 발생하는 세포만을 배양했을 경우 AchE 양성반응을 보이는 유생으로 발생하나 B4-1 을 제의한 나머지 부분은 AchE 음성반응을 보이는 유생으로 발생함을 관찰하였다.
 도o 멸0 T-=,
도o 멸0 T-=,
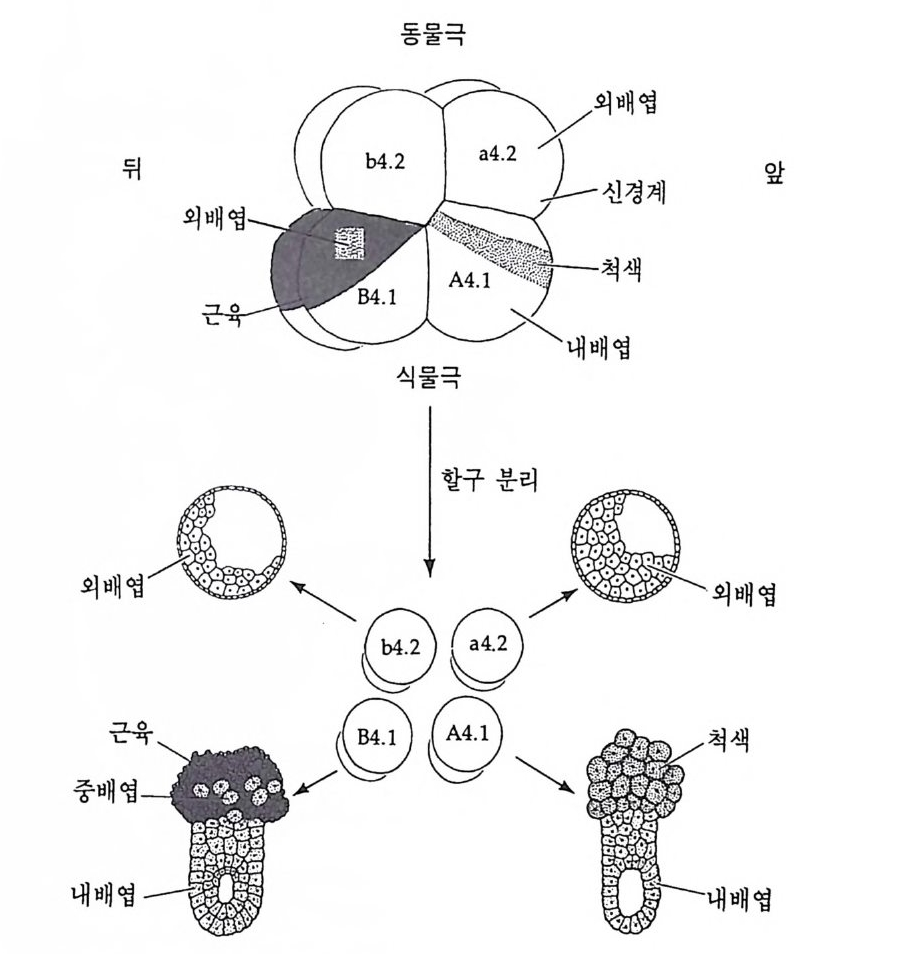
그림 2-3 멍게 발생배에서 분리된 할구의 운명 (Reverberi and Min ga nti ; 1946)
휘 데 이 커 (Whit tak er) 는 cy toc halasin B 를 처 리 한 다음 세 포분열 이 억제된 발생배에서의 AchE 의 분포를 조사하였다. AchE 는 바록 세 포분열이 억제된 발생배에서까지도 정상적인 발생배에서와 같이 선택 적으로 분포되었다. 2 세포기까지는 알 전반에 걸쳐 AchE 가 분포되
 분유리리 한바 늘B4로.l ::::::===-.,__~
분유리리 한바 늘B4로.l ::::::===-.,__~
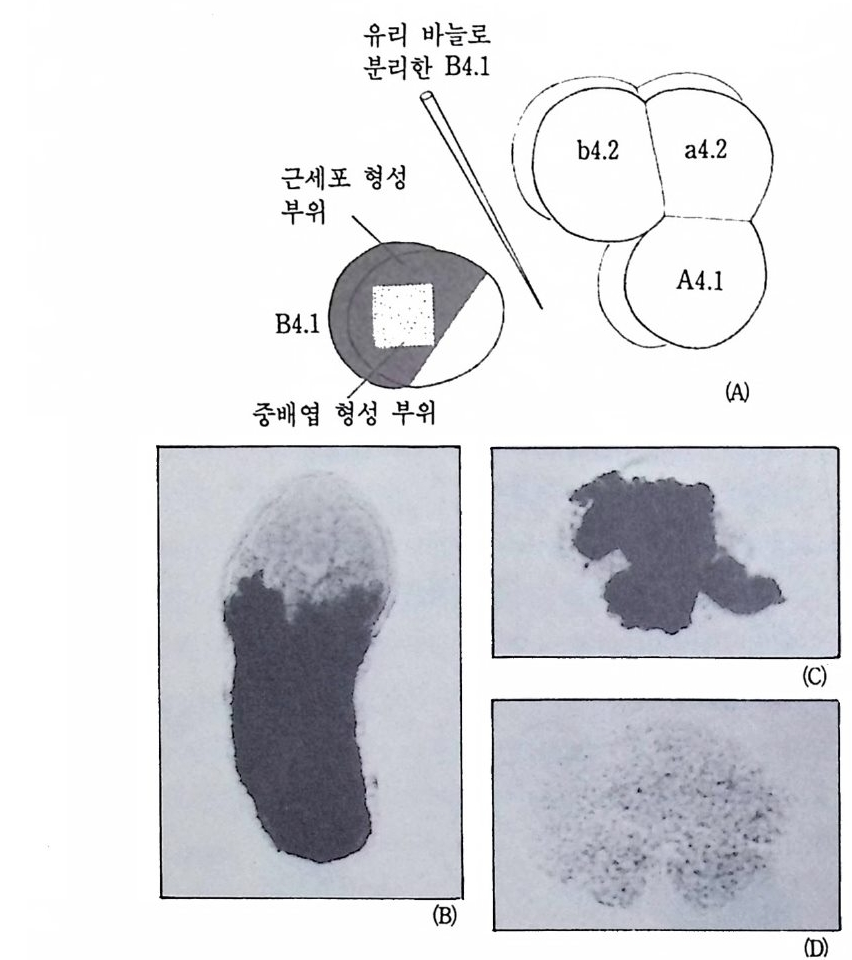
그림 2-4 멍게 발생에 따른 근세포 계보의 할구에서의 ace ty lcho lin es t erase 의 선택적 분포. (A) 8 세포기로부터 B4 • 1 할구의 분리 (B) 멍게 유생 꼬리근 육에서의 ace ty lcho lhi nes t erase 의 선택적 분포 (C) 분리된 B4 • 1 항구에서 의 ace ty lchol in es te rase 의 분포 (D) 나머지 할구에서는 acety lc holin e str as e 생성되지 않음.
어 있으나 4 세포기에는 식물국쪽에서 그리고 8 세포기에는 정확하게 B4-1 에 해당하는 부위에서 그 분포가 확인되었다(그립 2-4). 이와 같
 (A) (B) (C)
(A) (B) (C)
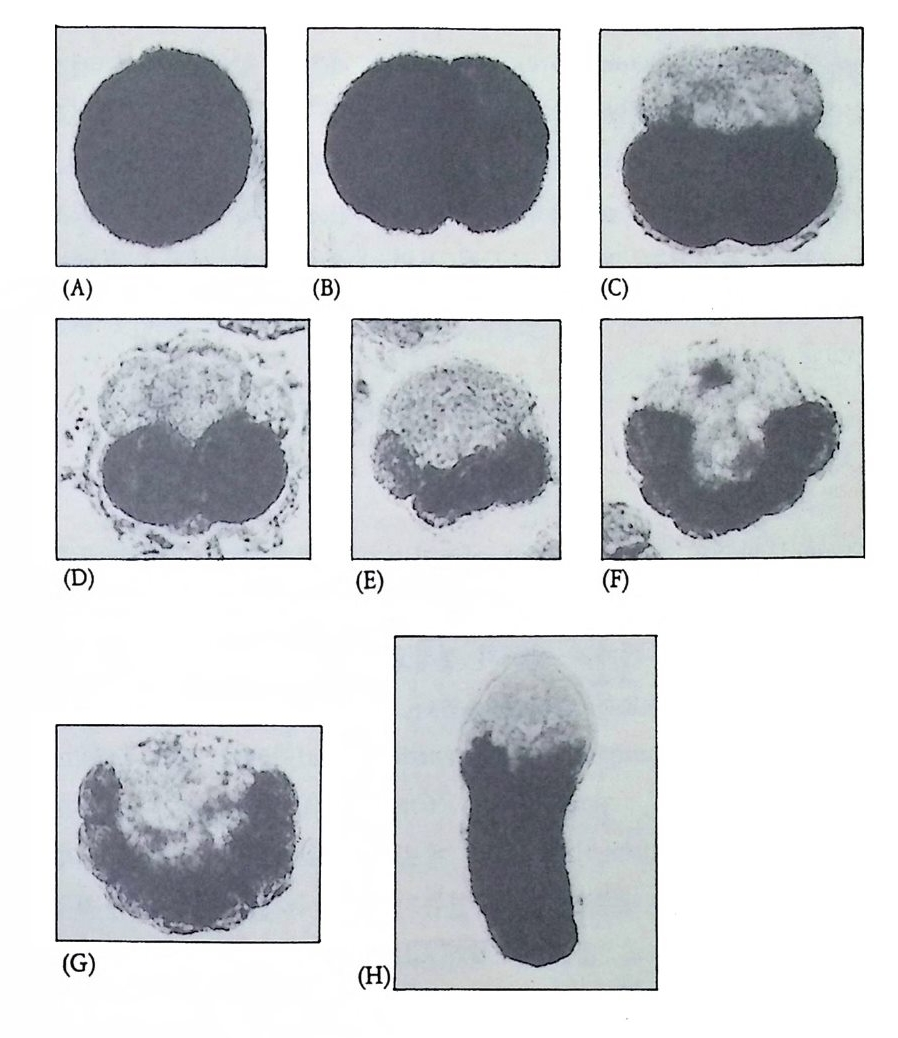
그림 2-5 멍게의 발생단계에 따른 ace ty lcho li nes t erase 의 선택적 분포. 발생배 룰 단계 별로 cyt oc halasin B 로 처 리 한 다음 ace ty lcho li nes t erase 의 분포를 조사함. (A) 1 세포기 (B) 2 세포기 (C) 4 세포기 (D) 8 세포기 (E) 16 세포 기 (F) 32 세포기 (G) 64 세포기 (H) 9 시간된 발생배
은 관찰로부터 이미 2 세포기 이전에 근육조칙의 분화능력이 형성되고 4 세포기 부터는 특정된 식물극의 할구에만 분배된다는 사실을 알 수 있다. 분화된 할구에서까지도 AchE 가 형성되는 시기가 정상배에서와 동 일하게 나타났다 (Sa t oh, 1979). 또한 핵을 제거한 할구에 다른 세포 의 핵을 이식시켜 배양시키면, 그 세포는 핵을 제공한 세포의 운명으 로 발생하지 않고 오히려 세포질을 제공한 세포의 운명으로 발생하는 사실을 관찰하였다 (Tun g et al, 1977}. 이러한 관찰에 근거하여 세포 의 운명이 결정되는 과정을 생각해 보면 우선 특정된 세포로 분배된 결정요인이 선택적 유전자 발현을 유발함으로써 세포의 운명이 결정 된다고 할수 있다. 3 세포 계보 1800 년 말부터 1900 년 초기에 이르기까지 수종의 선구 무척추 동물 발생배의 세포 계보 (cell li nea g e) 에 대해 대단히 자세하게 연구되었는 데, 사실상 이러한 기재적 연구가 결정요인의 선택적 분배에 대한 개 념을 설정하는데 중요한 역할을 하였다. 연구된 동물로서는 절지동물 에 서 Cles pine (Whitma n, 1878) , Arenic o la (Chil d, 1900) 및 Tubif ex (Penners, 1922) 이며, 연체동물에서 Crep idu la(Conkli n, 1897) 그리고 미색류(Whitt aker, 1979) 이다. 세포 계보에 따르면 특정된 세포가 발 생초기에 어느 세포로부터 출발하였는지를 알 수 있다. 선구 무척추 동물에서는 2 세포기의 할구를 AB 와 CD 로 그리고 4 세포기의 할구를 A, B, C, D 로 명명한다. 8 세포기에서 나타나는 소할구에 대해서는 소 문자로 대할구에 대해서는 대문자로 기술하고, 알파벳 문자 앞에 숫 자로서 4 세포기의 각 할구로부터 유래한 차례를 나타낸다. 그리고 알 파벳 문자의 오른쪽 상단에 작은 글씨로 나타낸 숫자는 딸세포를 표 시한다.
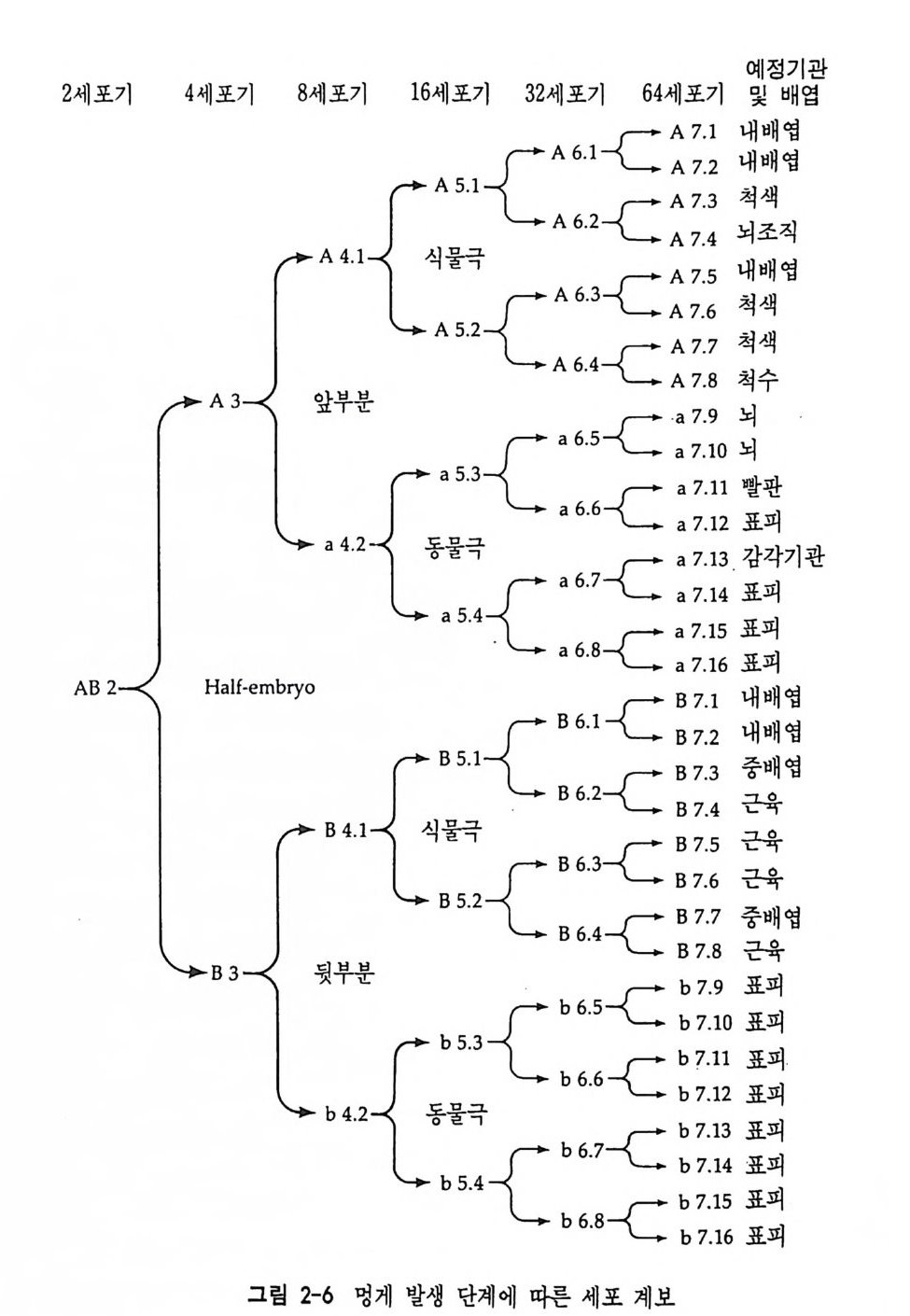 예정 71 관
예정 71 관
미색류에서의 세포계보 표시법은 다소 선구 무척추 동물의 경우와 다르다. 2 세포기의 발생배는 동일한 AB 의 두 개의 세포 즉 A2 와 B2 로 이루어전다. 4 세포기에 A3 세포 두 개와 B3 세포 두 개, 8 세 포기에 A4-l, a4-l, B4-1, b4-l 각각 두 개씩의 세포로 발생배가 이 루어진다. 크게 두 종류의 세포 계보에 따르며 이를 알파벳 문자 A 와 B 로 나타내었다. 알파벳 문자 다음에 오는 첫번째 숫자는 세포분 열의 차례이고 다음 숫자는 같은 계보의 세포의 차례를 의미한다. 이 러한 세포 계보를 통해 구체적으로 어느 세포가 후에 어떠한 조직이 나 세포로 분화하는지를 알 수 있다. 4 연체동물과 절지동물 발생배에서의 세포질 분배 연체동물과 절지동물은 선구 무척추 동물의 대표적인 예로서 나선 난할 (螺旋卵割 I, spi ra l cleavage ) 을 하며 후구 무척 추 동물인 성 게 의 알 은 방사난할(放射卵割 radia l cleava g e) 울 한다. 세포분열면을 이루는 방추사의 각도가 대각선으로 형성됨으로 인하여 발생이 진행됨에 따 라 할구가 나선형으로 분포되는 것이 나선난할의 특칭이다. 이러한 특칭을 가진 연체동물과 절지동물의 발생에서 세포의 운명은 초기부 터 대단히 결정적이다. 이러한 모자이크난의 특징을 윌슨 (W i lson , 1904) 은 연체동물인 Pate ll a coerulea 의 발생배에서 할구를 분리 배양 함으로써 확인하였다. 분리된 할구는 정확하게 정상적인 발생과정에 서 정해지는 운명의 세포로 분화할 뿐만 아니라 세포분열의 횟수까지 도 분리된 후 남아 있는 발생배의 세포들의 것과 동일하였다. 윌슨은 난할의 형태와 리듬, 그리고 후에 나타나는 분화의 특칭과 복잡성을 조절하는 요인이 둘러싸고 있는 다른 세포들과는 상관없이 독립적으 로 할구들 그 자체 속에 있다고 결론지었다. 윌슨은 처음에는 tr ochoblas t의 분화에 대해서만 연구하였으나 후에 다른 세포를 가지
 hoblast 7
hoblast 7
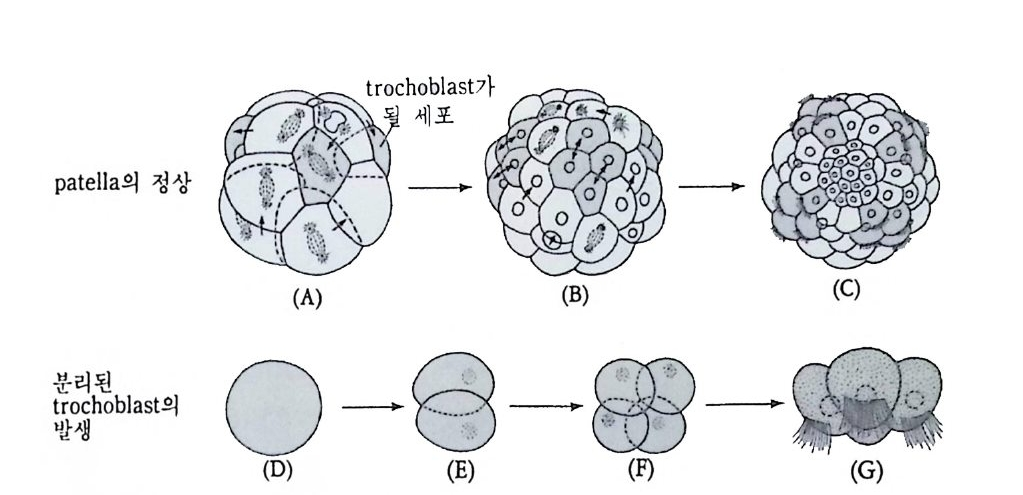
그립 2-7 Pa t e lla 의 정상적인 발생과정에서의 tr ochoblas t의 분화. (A-C) 와 분 리하여 시험관내에서 배양한 t rochoblas t의 분화 (D-G), (A) 16 세포기 (B) 48 세포기 , (C) 동물국에서 본 유생, tr ochoblas t에 섭모가 나 있다. (D) 분리된 tro choblast. (E), (F) 1 차와 2 차의 세포분열, (G) 분리된 tro chob- las t에서도 섬모가 적절한 시기에 생겨남
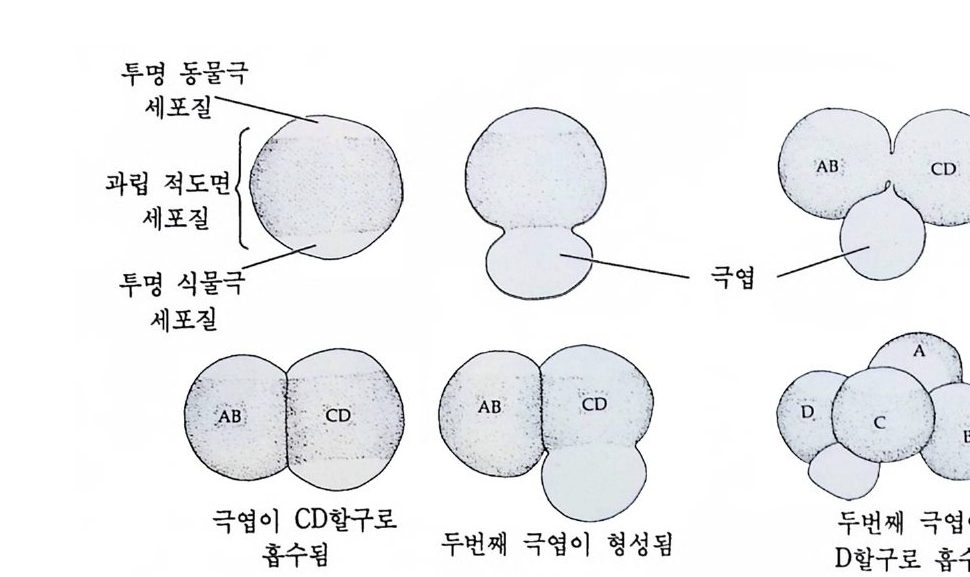
고 실험하였을 때에도 동일한 결과를 얻었다. 연체동물과 절지동물의 발생배의 또 하나의 다른 특징은, 모든 종 류에서 형성되는 것은 아니나, 극영 (極葉 pol ar lobe) 의 형성이다. 첫번째 난할이 일어나기 직전에 세포질의 일부가 혹처럼 나오는데 난 할이 끝날 무렵 CD 세포와 가느다랗게 이어져 발생배는 클로바잎 모 양을 하다가 세포분열이 끝나면 CD 세포 속으로 흡수된다. 이 시기를 삼영기 (三葉期 tref o il s t a g e) 라고 한다. 이때 혹처럼 나왔다가 들어가 는 구조를 국영이라고 하는데, 그 속에 핵은 없고 세포질로만 구성되 어 있다. 2 세포기에 AB 세포보다 CD 세포의 크기가 더 크다. 극영은 두번째 난할이 일어나기 전에 한 차례 더 형성되었다가 D 세포 속으 로 흡수된다. 따라서 D 세포는 다른 할구보다 그 크기가 언제나 크 다. 비록 국영을 형성하지 않은 종류에서도 D 세포는 다른 할구보다 크다. 4 세포기 이후에는 더 이상 극영이 형성되지 않고 담륜자 유생 (擔輪子幼生, tro chop ho re larva) 으로 발생 한다.
 두명 동물극
두명 동물극
그립 2-8 Den ta l i um 의 난할중에 나타나는 국영 (Wi lso n, 1904)
윌슨 (W il son, 1904) 은 극영을 제거한 후에 결손되는 유생의 구조를 관찰함으로써 극영의 발생학적인 중요성을 보여주었다. 극영이 제거 된 발생배일지라도 나선난할을 계속하여 담륜자 유생으로 발생하지 만, 주로 중배엽으로부터 형성되어야 할 구조들 즉 근육, 입, 난각선 (90 穀線), 운동기관 등이 결손되었다. 유사한 실험으로 2 세포기에 AB 세포와 CD 세포를 분리하여 배양하였을 경우 AB 세포는 중배염성 기관이 결손된 불완전한 유생으로 발생하였다. 4 세포기에 단지 D 세 포만을 제거한 후에 나머지 발생배를 배양할지라도 AB 세포를 배양 했을 경우와 유사한 결과를 초래하였다. 이와 같은 실험 결과에 근거 하여 윌슨은 극영의 세포질 속에는 중배영성 기관에 대한 결정요인이 들어있다고 결론지었다. 수정 직후 즉시 중배영성 결정요인이 D 할구 속으로 분배될 세포질에 집중됨으로써 할구의 세포분열 속도와 중배 영 세포의 분화에 필요한 요인이 D 할구 속에 들어갈 것이라고 윌슨 은 생각하였다. 클레멘트 (Clemen t, 1968) 는 연체동물인 Jly a n assa obsole ta의 발생에
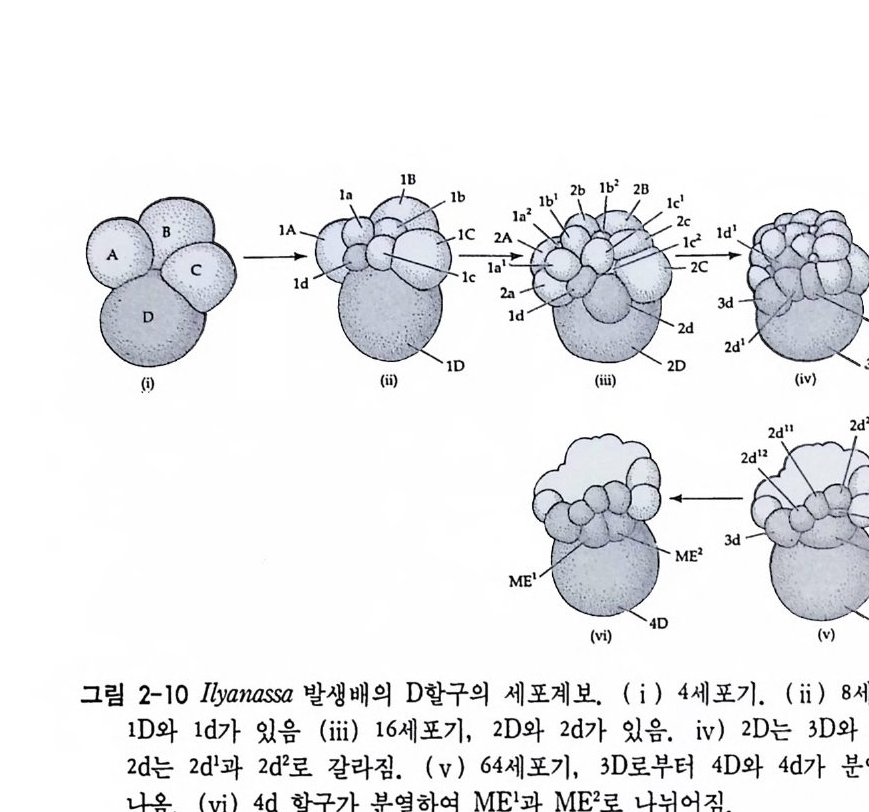
 (B)
(B)
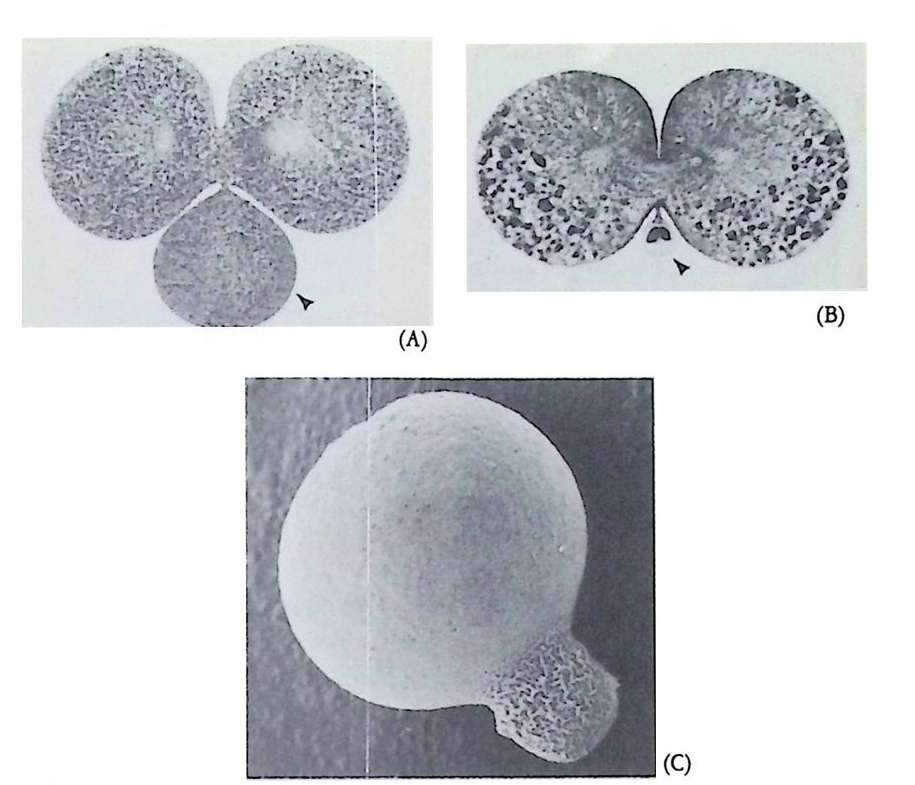
그림 2-9 연체 동물의 국영. (A) Den ta li um 의 극영 (B) B it hyn ia의 극영. (A) 와 (B) 는 hema t ox y l i n - eos i~로 염색됨 (C) Bucci nu m unda t um 의 국 영의 주사 현미경 사진.
대한 연구로 클레멘트의 연구를 계속하였다. 죽 클레멘트는 극영에 들어 있는 중배영성 결정요인이 세포분열이 계속될 때 어떠한 세포의 계보를 따라 선택적으로 분배되는지를 추적하였다. 각 세포기에서 D 세포를 제거한 다음 배양하여 얻은 유생에서 결손된 구조를 조사함으 로써 어느 결정요인이 세포분열시 어느 할구로 전달되는지를 확인할 수 있었다. 세번째 난할이 일어나면 D 세포는 1D 의 대할구와 ld 의 소할구로 분열하는데 이때 1D 만을 제거한 후 나머지 발생배 (ABC+ ld) 를 배양하면 4 세포기의 D 세포를 제거하고 배양했를 때와 동일하 게 중배영성 기관이 결손된 유생이 형성되었다. 죽 내배엽성 조직,
 ~°@
~°@
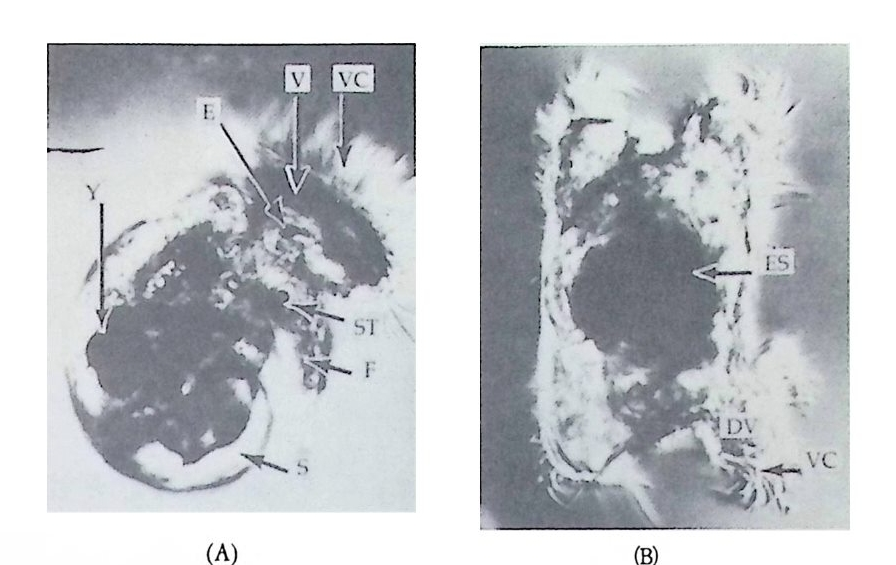
색소세포, 신경계, 근육, 위는 가지고 있으나 연막( 緣膜 , velum), 심 장, 장, 이포(耳胞 oto c y st ) , 난각 및 눈과 같은 기관이 결손된 피면 자(被面子, ve lig er) 가 형성되었다(그림 2-1 1). 그러나 2D 세포만을 제 거 시 키고 ABC 세포와 ld, 2 cl.i료 구성 된 발생 배는 최소한도 난각 (shell) 울 형성하는 유생으로 발생하였다. 그리고 3D 세포만을 제거시키고 3d 세포를 발생배에 포함시켰을 경우 D, 10, 2D 를 제거하였을 때 결 손되었던 기관 죽 연막, 눈, 난각, 운동기관이 형성되었다. 그러나 아직도 심장과 장이 결손되었다. 다음 세포분열 후 4D 세포를 제거할 지라도 더 이상 유생에 중배영성 기관의 결손이 일어나지 않았다 . 오 히려 4d 세포를 제거하면 결손이 일어나는 것을 관찰할 수 있었다. 4d 세포는 한번 더 분열하여 두 개의 세포로 되는데 이 세포를 mesen t oblas t라고 하며 이 세포로부터 심장과 장이 형성된다. 이와 갇은 윌슨과 클레멘트의 연구를 통해서 세포분열의 단계에 따
 (A) (B)
(A) (B)
그림 2-11 정상 적 인 되명자유생 ( A) 과 국영 혹은 D 세포의 제거에 따른 이상되 명자유생 (B). E : 눈, F : 발, S : 껍질, s t : S ta t oc y s t , V : 연막, Ve : 연 막섬모, Y : 난 황 , ES : 뒤집힌 입.
른 결정 요인의 선택적인 분배를 확인할 수 있었다. 일단 D 세포에 분배된 결정요인이 D 의 소할구 (d 세포)에 순차적으로 분배되는 현상 울 알 수 있었다. 그러나 세포간 상호작용을 통한 유도현상도 나타났 는데, 예 를 들어 눈의 발생이다. 눈은 A 와 B 세포가 D 의 소할구와 작용하여 형성된다. 사실상 4D 가 제거되었을지라도 정상적인 발생배 가 형성된다는 실험결과는 세포간 상호작용이 있음을 의미한다. 쿨레멘트는 결정요인이 세포질에 들어 있다는 전제하에 만약 세포 질을 인위적으로 이동시켜 주면 결정요인 분배의 선택성이 붕괴되기 때문에 세포 운명 결정에 변화가 있을 것이라는 예상을 하고, Ily anassa 의 알을 원심분리하여 식물국의 세포질을 동물국쪽으로 이 동시켰다. 정상적인 발생배와 다른 세포질의 분포를 가전 알을 배양 시킨 결과 국영은 비록 식물국의 세포질을 상실하였으나 식물극에서 형성되었고, 후에 유생에서도 기관이 전혀 결손됨이 없이 완전한 발
 표 2 기 연체동물의 발생단계에 따른 D 할구 제거의 효과
표 2 기 연체동물의 발생단계에 따른 D 할구 제거의 효과
생배가 형성되었다. 원심력으로 결정요인의 위치를 변경시킬 수 없었 던 원인은 결정요인이 움직일 수 없는 구조에 결합되었기 때문이라고 풀이하였다. 즉 원심력에 의해서 이동이 불가능한 표충 (co rt ex) 에 결 정요인이 결합되어있을 것이라고 추측되었다. 그러나 이러한 클레멘 트의 실험은 사실상 결정요인이 표충의 어떤 구조와 결합되어 있기 때문에 이동하지 못한 것인지 혹은 클레멘트가 사용한 원심력이 결정 요인을 이동시키기에 충분치 못했는지는 알 수 없다. 비록 현미경적 으로 구별할 수 있는 식물극의 세포질이 동물극 쪽으로 이동하였다고 하여 반드시 식물극에 있는 모든 세포질이 이동하였다고는 생각할 수 없다. Bit hy n ia te n ta cula ta도 연체 동물로서 극영 이 난할중에 형 성 되 며 , 비록 크기는 작으나 Jl y anassa 의 알에서 볼 수 있는 중배영성 기관에 대한 결정요인이 들어있다. 극영을 제거시키면 mesen t oblas t와 중배 영성 기관이 형성되지 않는다 (Verdonk and Cath e r, 1 973). J ly anassa 와 다른점은 극영의 결정요인이 C 와 D 세포로 분배되어 C 세포와 D 세포 가 발생학적으로 동일한 의미를 갖는다 (Verdonk and Cath e r, 1973). 따라서 극영세포질이 B it hy n i a 에서는 C 와 D 세포에 분포되 어 있는 반 면에 Ily anassa 와 Den tali um 에서는 D 세포에만 분포되어 있다. Bi th y nia의 국영은 세포학적으로 특징적인 구조를 가지고 있다.
 o
o
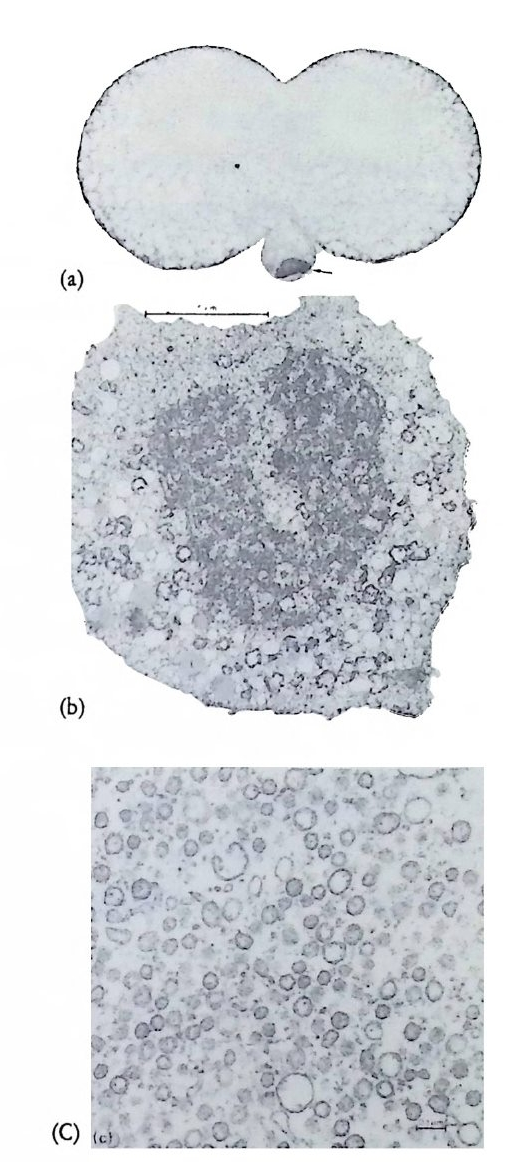
그림 2-12 B it hy nia극영의 미세구조. (a) 1 차 난할시 형성된 극영. meth yl- gree n pyron i ~ RNA 를 염색한 식물국쪽의 식물극체 (vege ta l bod y')가 RNA 에 대한 양성반응을 보이고 있다. (b) 극영 세포질의 전자현미경사진. A'l:할구에 부착된 부위. L: 지방, M: 미토콘드리아 X6300(C) 식물국체 의 미세구조. 대부분의 소낭둘은 RNA 일 가능성이 있는 물질로 가득차 있 다. x6s,2so(Dohmen and Verdonk, 1974).
RNA 에 대하여 강하게 반응하는 구조를 가지고 있는데 이를 식물국 체 (veg et a l bod y)라고 부른다. 식물극체를 전자현미경으로 보면 작지 만 막으로 둘러싸인 소포 (vesic le ) 와 막과 상관없는 거의 갇은 크기 의 입자로 이루어져 있다. 식물국체는 첫번째 난할시 CD 세포로 분배되 고 두번째 난할이 일어나서 C 와 D 로 갈라지기 전에 사라진다. 유사 한 막상 구조와 입자가 Denta l iu m (Reverberi, 1970), Ilya n assa(Pucci -Mi na fr a et a l., 1969) 및 Crep idu la(Dohman and Lok, 1975) 에서도 발 견되었다. 특히 Cre pi dula 에서는 생석세포의 결정요인으로 알려진 극 입자 (po lar gran ule) 와 유사한 모양의 막이 없는 입 자도 찾아볼 수 있 었다. 발생학적인 의미에서는 물론 구조적인 면에서까지도 다른 세포질과 는 디른 특칭적인 세포질을 가전 연체동물의 극영은 분자발생학자들 에게는 대단한 관심거리였다. 무엇보다도 중요한 이유는 극영의 분리 가 기술적으로 가능하다는 점이었다. 지금까지 가장 많이 사용된 동 물은 lly a na.ss a 로서 정상배와 극영이 제거된 발생배의 차이를 여러 가 지 생화학적인 기준하에서 비교하였다. 대체로 발생속도나 세포의 증가율 및 DNA 합성률, 최소한도 24 시간 후에야 나타나는 rib o somal DNA 의 합성률은 두 종류의 발생 배 사이 에 큰 차이가 없 었다 (Koser and Coll ier, 1972 ; Coll ier, 1975a ; Newrock and Raff , 1975) . 극영의 세포질이 세포분화에 특이한 질적 변화를 유발하는 것은 확실 하나, 발생초기에는 극영 세포질의 생화학적 특징을 포착하기가 힘들 었다. 성장률의 변화도 기관형성이 시작되면서 나타나는 것으로 기관 이나 조칙의 결손으로 인한 이차적인 현상으로 생각되었다. 극영이 제거된 발생배에서 기관이 결손되는 현상은 단백질의 성분 에 변화가 생겼기 때문아라고 쉽게 생각할 수 있었다. 프리먼 (Freeman, 1971) 은 alkali ne p hos p ha t ase 와 es t erase 의 동위효소의 분 화에 대하여 연구하였다. lly a na.s sa 의 정상배에서 alkalin e pho s- p ha t as 탸 발생 초기에 한 종류로 나타나서 7 일째까지 큰 변화를 보
 (a)
(a)
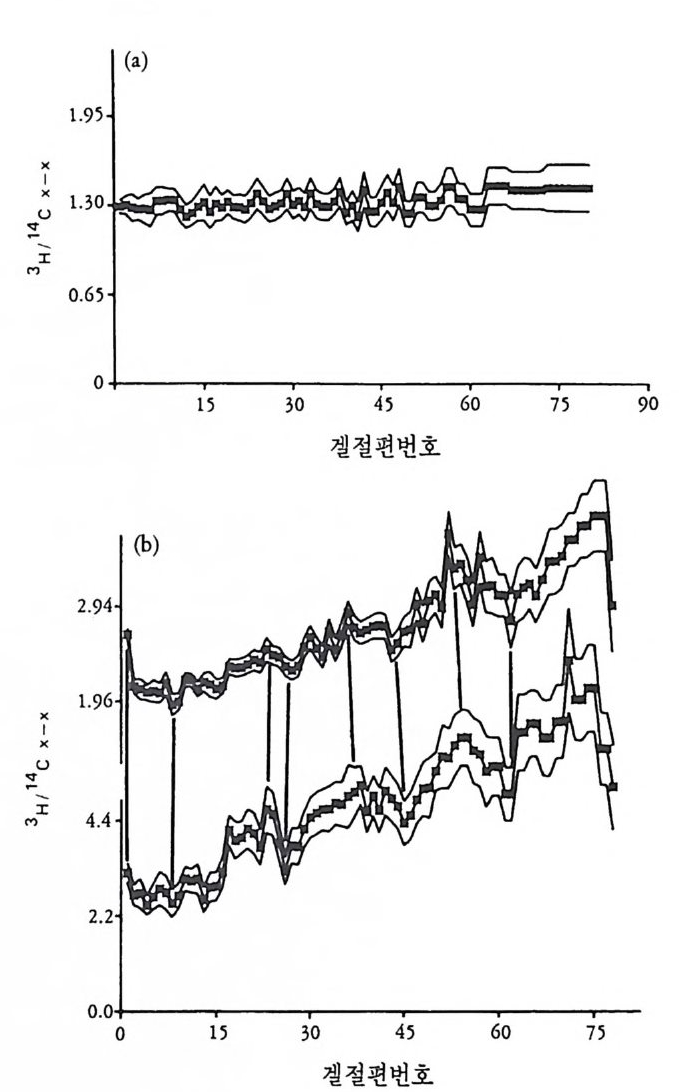
그림 2-13 Ily anassa 의 정상 및 부분 발생배에서의 단백질 합성 비교 (a) 초기 난할기에 100 분 동안에 합성된 단백질. 166 개의 3H-leuc in인i로 표지된 발 생배와 89 개의 “C-Ieu ci ne 으로 표지된 발생배로부터 단백질을 추출하여 함 께 전기영동함. (b) AB 할구에서 출발한 발생배와 CD 할구에서 출발한 발생 배에서 합성된 단백질의 차이. 146 개의 CD 와 104 개의 AB 에서 합성된 단백 질(위의 그림)과 99 개의 CD 와 118 개의 AB 에서 합성된 단백질(아래 그림). 단백질의 종류에 따라 AB 와 CD 간에 차이를 보이고 있다 (Donohoo and Kafa tos , 1973) .
 겹 1.0 II .: 閑)
겹 1.0 II .: 閑)
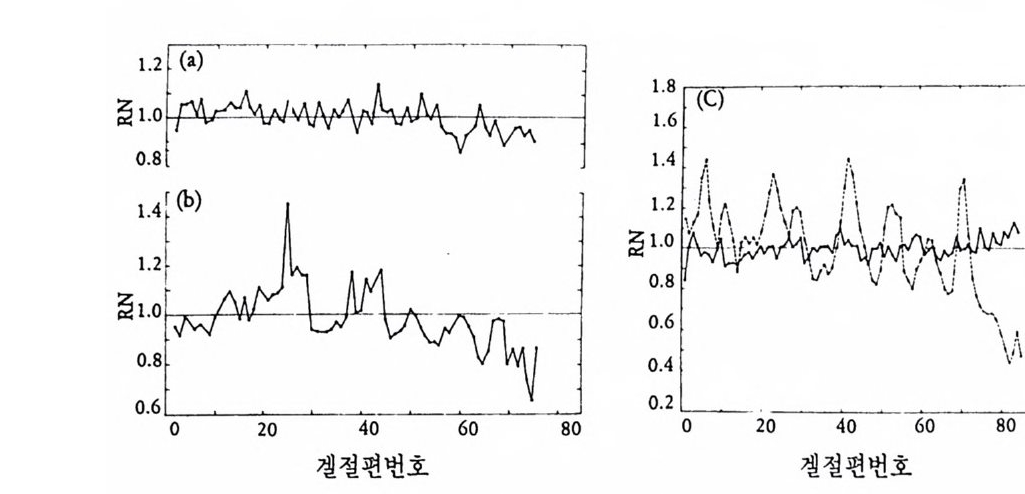
그림 2-14 (a) 24 시간 된 정상 발생배에서의 l ◄ c- 과 3H-leuc i ne 으로 표지된 단 백질의 전가영동에 의한 분석. RN 은 l ◄ c- 과 3H-leu ci ne 으로 각각 표지된 단 백질을 함께 전기영동한 다음 전기영동띠의 “C/ 3H 바 (b) 24 시간 된 국영 이 없는 발생배를 3H-leuci n ~ 표지하고 같은 단계의 정상 발생배를 l ◄ c - leuc i n 무 표지한 다음 두 단백질을 함께 전기영동함. (c) 48 시간 된 발 생배에 acti no my cin D 를 수정후부터 처리하면서 3H-leu ci ne 으로 표지한다 음 이들 단백질을 함께 전기영동함 (Newrock and Raff . 1 975}.
 1.2
1.2
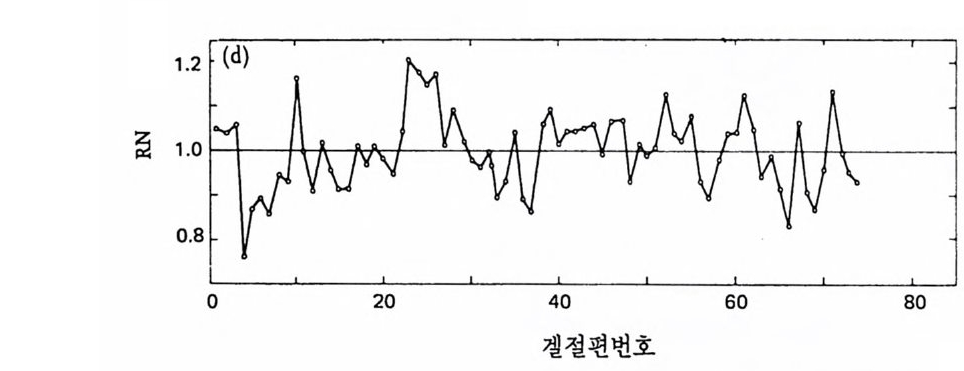
(d) 수정 후 24 시 간 동안 acti no my cin D 를 처 리 하면서 배 양한 발생 배 를 14C-leu ci n~ 료 표지하고 극영이 없는 발생배에 acti no my cin D 을 24 시간 동안 처리한 다음 3H-leu ci ne 으로 표지한 다음 두 단백질을 함께 전기 영동함.
이지 않다가 9 일째에 최소한도 3 종류의 동위효소의 형태로 나타났다. 그리고 es t erase 는 5 일째 까지는 단일 동위 효소의 형태로 나타나나 7 일째에 최소한도 7 종류로 분화하였다. 그러나 극염을 제거한 발생배 에서는 alkali ne p hosp ha t ase 는 10 일째가 되도록 처음에 나타난 한 종류 의 에는 더 이 상 분화하지 않고, es t erase 도 7 종류 중 2 종류가 나타나지 않았다. 전체적인 단백질 합성 양상도 연구된 바 있는데 4 일째가 되는 기관 형성이 시작될 무렵부터 단백질 합성에 차이가 생긴다 (Te it elman, 1973 ; Newrock and Raff , 1975). 발생 5 일째에 정상배에서의 단백질 합성 양상은 극영이 제거된 발생배의 것과 뚜렷하게 다르다. 그러나 초기에서부터 극영에서의 단백질 합성이 다른 할구의 것과 다르다는 실험적 증거가 이중 표지법을 이용하여 가능하였다. 즉 2 세포기의 Ily anassa 의 알을 AB 세포와 CD 세포로 분리 한 다음 AB 계통의 세포 는 14C- 아미노산으로, CD 계통의 세포는 3H- 아미노산으로 표지한 다 음 표지된 단백질을 각각의 세포군으로부터 추출하여 전기영동한다. 다음 전기 영동 겔울 일정한 크기로 자른 절편의 14C 과 3H 의 방사능 울 측정하여 3H/'4C 의 비를 구한다. 만약 국영을 포함하는 CD 계통의 세포에서 합성되는 단백질이 AB 계통의 세포에서 합성되는 것과 양 적으로나 질적으로 다르면 그 비가 일정하지 않고 다르게 나타난다. 도노후 (Donohoo) 와 카파토스 (Ka fat os, 1973) 는 이러한 실험을 통하여 AB 계통의 세포와 CD 계통의 세포가 초기부터 단백질 합성 양상을 달리함을 보여 주었다. 유사한 실험방법으로 정상배와 극영을 제거한 발생배의 단백질 합성을 비교했을 경우에도 낭배기 이전에 이미 차이 가 있음이 나타났다 (Newrock and Raff , 1975). 이러한 결과는 국영내 에 다른 할구와 다른 모계의 mRNA 가 선택적으로 분배되었을 가능 성을 강하게 암시해 주었다. 혹은 국영내에 유전자를 선택적으로 발 현시킬 수 있는 요인이 선택적으로 분배되었을 것이라는 생각을 강하 게 해 주었다.
5 유즐동물 (C t ene p hore) 의 발생배에서의 결정요인의 선택적 분배 유즐동물은 이 방사 상청 (二放射相稱 bir a dia l sym me tr y) 의 간단한 동물로서 발생중 유생기에 즐판(節板 comb p la t e) 과 광세포(p ho t oc yt e)
 (a)
(a)
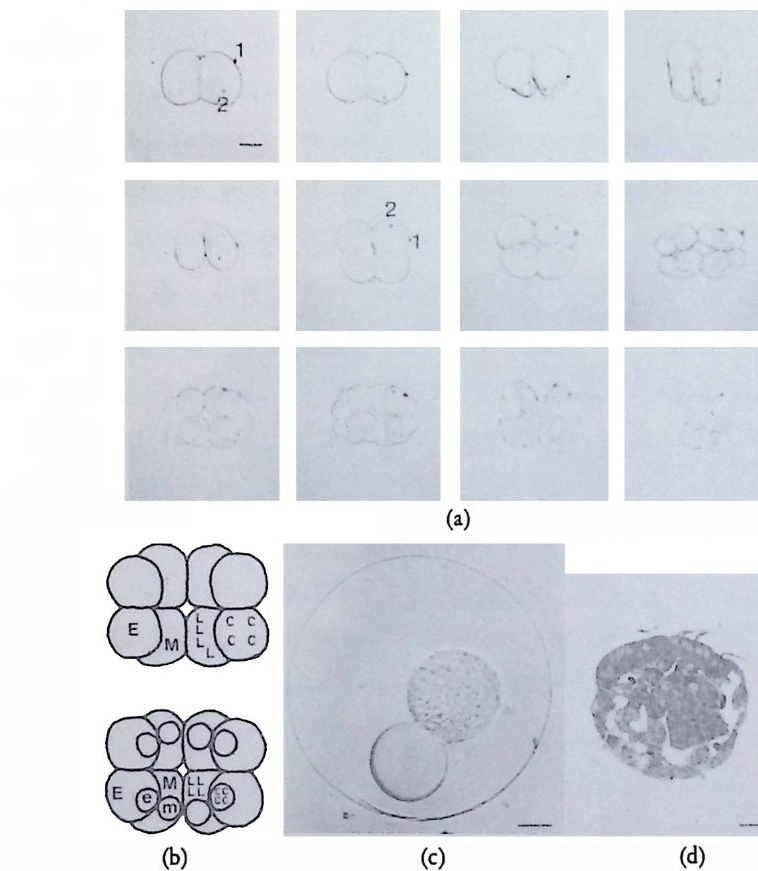
그립 2-15 유즐동물의 발생과 난파편 (e gg fr a gm en t)의 발생. (a) 정상발생, 2 세포기에 두 개의 분필입자를 삽입시킴 (1 과 2 로 표시함). 16 세포기가 되는 동안 한 개의 분필입자는 E 세포로 다른 하나는 M 세포로 분배됨. (b) 8 세 포기와 16 세포기에 광세포와 줄판 세포의 결정성. L 은 광세포로 분화할 부 위를 지시하고, C 는 즐판세포로 분화할 부위를 지시함. (c) 원심분리에 의 해 형성된 모양, 약 10 분 후 원래의 모양으로 환원됨• (d) 2s 시간 된 발생 배의 단면. 줄판세포가 보임.
가 분화하는데, 결정요인의 선택적 분배에 대한 연구에 대단히 중요 한 자료로서 이용되어 왔다. 즐판은 섬모를 가진 운동기관이고 광세 포는 광을 발하는 세포이다. 할구 분리법을 이용하여 오래 전부터 세 포의 결정성에 대하여 연구되었다 (Chun, 1880, Drie s ch and Morga n , 1896;Fis c hel, 1898, 1903;Yats u , 1912), 그리고 근래에는 리베버리 (197la) 에 의해서 연구되었고, 세포계보는 오토라니 (1964) 에 의해 밝 혀진 바 있다. 8 세포기의 발생배는 안쪽에 자리하고 있는 M 세포 4 개 와 M 세포 양쪽 바깥쪽에 자리하고 있는 E 세포 4 개로 구성되어 있 다. 후에 M 계통의 세포와 E 계통의 세포의 운명은 다르게 나타난다. 즉 세번째 난할 후부터는 결정요인이 엄격하게 분배된다. 세포분열에 의 해 e 소할구는 E 대 할구로부터 분리 되 어 즐판으로 분화하고, m 소할 구는 M 대할구로부터 분리되어 광세포로 분화한다. E 세포나 M 세포 를 분리하여 배양하면 E 세포로부터는 즐판이 그티고 M 세포로부터는 광세포가 형성되고, 절대로 역분화가 일어나는 경우를 찾아볼 수 없 었다. 그러나 2 내지 4 세포기 초기에 반구국(反口極, aboral p ole) 의 세포질 즉 E 대할구로 분배되는 세포질을 제거하면 줄판 형성 능력 이 어느 정도 감퇴되나, 만약 첫번째 난할이 일어날 때 제거되면 줄 판 형성에 큰 영향을 주지 못한다 (Freeman, 1976 a, b). 이러한 관찰 에 근거하여 유즐동물의 발생배에서의 결정요인의 분배는 난할 이전 부터 엄격하게 일어나는 것이 아니고 난할과 함께 점전적으로 일어나 는 것으로 생각되었다. 광세포의 결정요안도 수정 이후 8 세포기에 이 르기까지 점진적으로 일어나고 8 세포기에 이르러 M 세포로 엄격하게 일어나는 것으로 추측되고 있다. 6 생식세포 결정요인의 선택적 분배 생식세포 결정요인의 분배는 동물계에서는 상당히 보편적으로 일어 나는 현상으로 알려져 있다. 생식세포(生殖細胞 ger m cell) 는 생식질
(生殖質, ger m p lasm) 이라고 하는 특수한 세포질에 의해서 결정된다. 난자 형성 기간 동안 형성된 생식질이 수정 후 난할 기간 동안에 특 정된 세포 죽 원시 생식세포(原始生殖細胞 pri m ordia l ger m cell) 로 분 배된다. 생식질에 대한 개념은 19 세기 바이스만으로부터 시작되었는 데, 그는 생식질을 구성하는 요소가 부모의 생식세포로부터 자손의 생식세포로 전달됨으로써 세대간 생식세포의 연속이 가능하다고 하였 다. 원시 생식세포 형성에 대한 연구가 1800 년대 말부터 활발하게 시 작되었는데 원시 생식세포는 체세포와 별도로 만들어지며, 이 세포는 간혹 특별한 형태의 세포질을 가지고 있는데, 이러한 세포질은 아미 수정란 속에 존재하며 세포분열중 생식세포 계통의 세포로 분배된다. (1) 선충에서의 생식세포 결정요인 선충의 일종인 회 충 Ascaris mega loc ejJ hala 의 발생 중 생 식 세 포가 어디에서부터 출발하는지 보베리 (Boveri, 1862~1915) 는 염색체의 행동 에 대하여 연구하던 중 알아내었다. 반배수체가 2 이기 때문에 발생중 일어나는 염색체의 변화를 쉽게 추적할 수 있었다• 보베리는 이 연구 롤 통하여 생식세포의 형성이 2 세포기에서부터 출발한다는 사실을 알 아내었다. 회충에서의 첫번째 난할면은 적도면에 형성되는데 흔히 찾 아볼 수 없는 경우이다. 그러나 좀더 놀라운 사실은 그 다음 2 세포기 의 할구들이 세포분열할 때 일어나는 염색체의 행동이다. 즉 동물극 쪽에 형성된 할구에서 이질 염색질쪽의 염색체가 부분적으로 본체로 부터 떨어짐으로써 본래의 염색체의 크기가 감되하는 현상이 일어난 다. 이 러 한 현상을 염 색 체 감되 (chromosome dim unit ion ) 라고 부른다. 따라서 새로 형성되는 핵은 본래의 유전자에서 상당수의 유전자를 상 실한 염색체를 가지게 된다 (Tobler, 1972). 한편 식물극 할구내의 염 색체는 정상적으로 유지된다. 2 차 세포분열에서 동물극 할구는 정중 선에 따라 그리고 식물국 할구는 적도면을 따라 분열한다. 이때 동물
 囚 염색체 감되
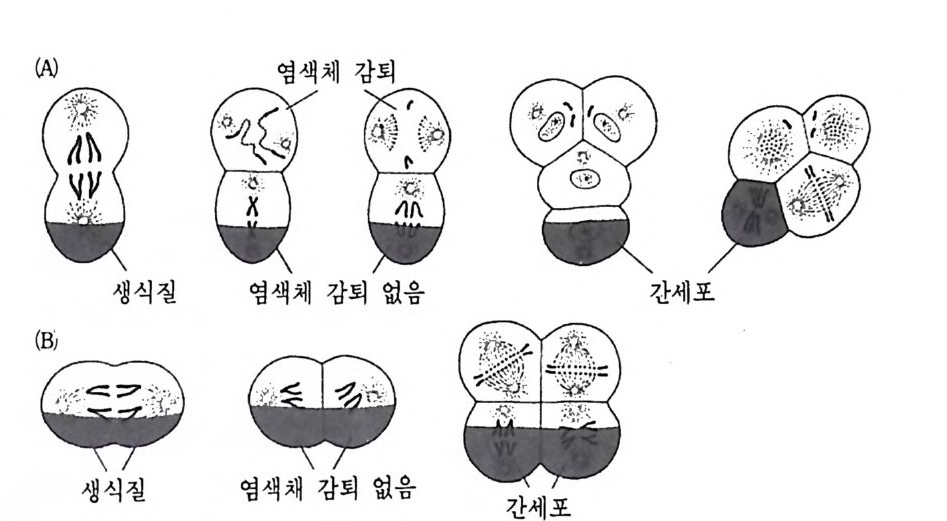
囚 염색체 감되
그림 2-16 Asca ris의 정상 발생과정 (A) 과 원심분리된 접합자에서의 생식질 분 배 (B). 생식질은 식물극 세포에만 분배되며, 생식질이 결여된 동물국 세 포에서는 염색체 감되현싱이 일어난다. 원심분리로 눕혀진 접합자에서는 생식질이 두 개의 세포 모두에게 분배되었기 때문에 염색체 감되가 이 두 개의 간 세포 모두에서 일거나지 않는다.
국쪽으로 치우친 3 개의 할구에서는 3 차 세포분열전에 다시 염색체가 감되한다. 그래서 4 세포기어 I 가장 식물국쪽에 자리하는 할구만이 원래 의 유전자를 가진 염색체를 유지하게 된다. 난할이 계속되는 동안 체 세포의 핵에서는 16 세포기까지 계속 염색체 감퇴현상이 일어나는 반 면에 단지 두 개의 세포만이 감퇴하지 않은 온전한 염색체를 유지하 게 된다. 이들 할구 중 하나가 생식세포를 형성하게 된다. 그리고 다 른 할구는 결국 염색체 감퇴로 인해 체세포를 형성한다. 32 세포기 이 후 한 개의 생식세포는 계속 증식하여 다수의 생식세포를 이루게 되 는데, 이 때 염색체 감되는 더 이상 일어나지 않는다. 보베리는 회충의 알에서 일어나는 염색체 행동이 세포질에 의해 결 정될 것이라고 가정하였다. 염색체 감되를 억제하는 식물국 세포질이 난할중 특별한 할구로만 선택적으로 분배되기 때문에 그 세포질을 부 여받은 세포는 염색체를 온전히 유지할 뿐만 아니라 생식세포로 운명
지어진다는 것이다. 사실상 식물국쪽에 분포된 세포질에 그러한 능력 이 있는지 알아보기 위하여 보베리는 1 차 세포분열이 일어나기 직전 알을 원심분리하였다. 원심분리된 알에서는 방추사의 위치에 변화가 생겼다. 죽 방추사가 40° 정도 희전하여 세포분열이 정중선에서 일어 나면서 식물극 세포질이 동일하게 두 개의 할구로 분배되었을 뿐만 아니라 두 개의 할구에서는 전혀 염색체 감되 현상을 보이지 않았다. 다음 4 세포기에서는 계속 식물극에 있는 두 개의 세포에서는 염색체 감되현상이 일어나지 않고 동물극 세포에서만 일어남을 관찰할 수 있 었다. 보베리는 이와 같은 실험을 통해 식물극 세포질에는 염색체 감 되 현상으로부터 핵을 보호하고 생식세포로의 운명을 결정하는 요인 이 포함되어 있을 것이라고 결론지었다. (2) 곤충에서의 생식세포 결정요인 어떤 곤충의 알은 회충의 경우에서와 감은 생식질을 가지고 있는
 그4S4 림 감 는의~四麟年1 핵i체위》TJK 『 둘 수- 벳따떠競 에가 지적정라결 이후서_기기|긴〔:\감국2 〔.門三\川~Tii뉵 분차 K의례 핵i핵 回의핵 세후서 側〔i:어〔떠田 0\ 正” 錢디广广\섭判10 핵구냐回 극어깁 p 『질斜州g°l1 요 는때따u· 군묘입虹1 40 체에개써-
그4S4 림 감 는의~四麟年1 핵i체위》TJK 『 둘 수- 벳따떠競 에가 지적정라결 이후서_기기|긴〔:\감국2 〔.門三\川~Tii뉵 분차 K의례 핵i핵 回의핵 세후서 側〔i:어〔떠田 0\ 正” 錢디广广\섭判10 핵구냐回 극어깁 p 『질斜州g°l1 요 는때따u· 군묘입虹1 40 체에개써-
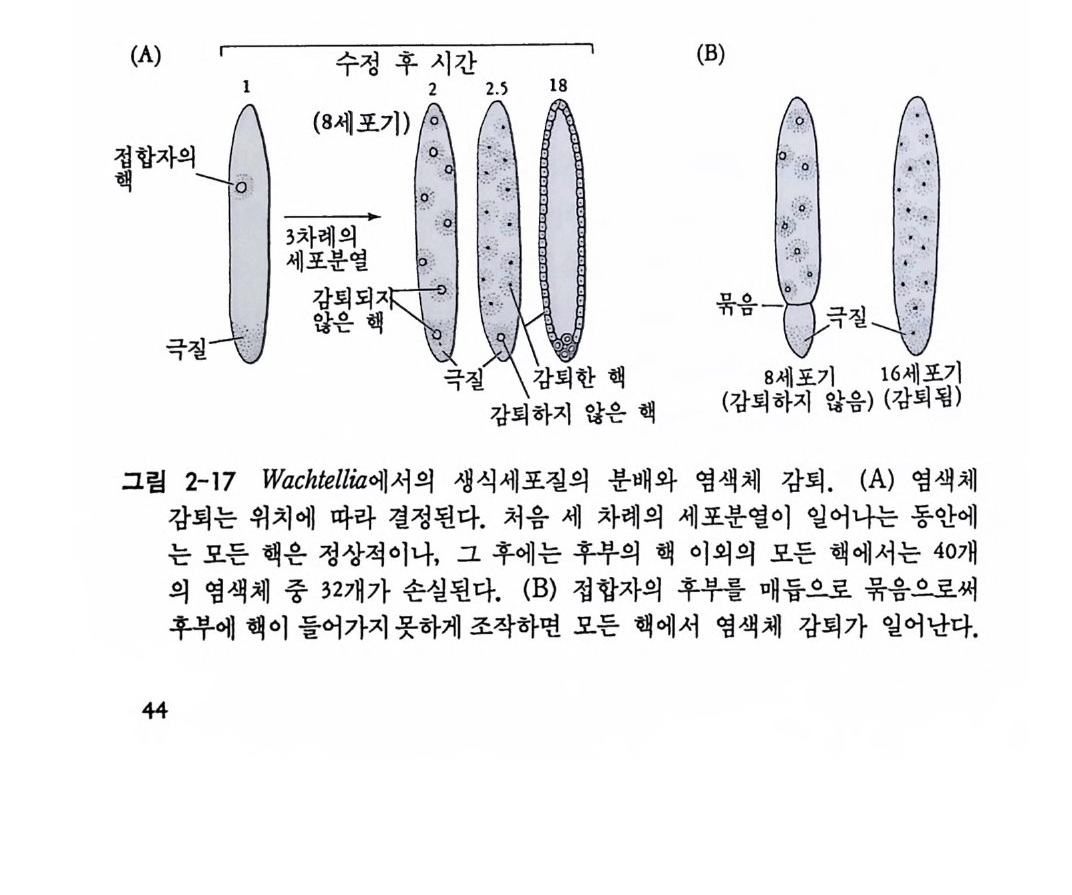
것으로 알려졌다. 작은 곤충의 일종인 Wachti ell a p e rs i ca ria e 에서는 발생중 40 개의 염색체중 32 개가 사라지는 감되 현상이 일어난다. 그 러나 알의 후부에 자리하고 있는 두 개의 핵에서만이 염색체 감되 현 상이 일어나지 않고 후에 생식세포가 된다. 만약 알의 후부를 끈으로 잡아매어 중으로써 이 두 개의 핵이 후부로 이동하는 것을 막아 주면 이 핵에서도 염색체 감되 현상이 나타나며 후에 불임성의 개체로 발 생한다. 얼마 후에 매듭을 풀어 줄지라도 염색체가 감퇴한 이들 핵으 로부터는 생식세포로서의 기능을 갖춘 세포가 형성되지 않는다 (Gey er -D uszyr nsk a, 1959). 쿤쯔 (Kunz) 와 그의 공동연구자들은 후에 감퇴한 염색체 속 에는 생식세포 형성 기간에 활발하게 발현되는 유전자가 포 함되어 있음을 규명하였다. 곤충의 생식질은 다른 세포질과 다르다. 헤그너 (Hegn e r, 1 911) 는 처 음으로 생식질이 생식세포 형성에 관여함을 밝혀냈다. 죽 극세포가 발생배에서 형성되기 전에 생식질을 제거하거나 파괴하면 생식세포가 형성되지 않는다. 죽 알의 후부에 위치하는 생식질 즉 극질(p olar pla sm) 속에는 생식세포 결정요인이 특수하게 자리하고 있는 것으로 풀이되었다. 전자현미경으로 알의 후부를 관찰해 보면 보통 다론 세
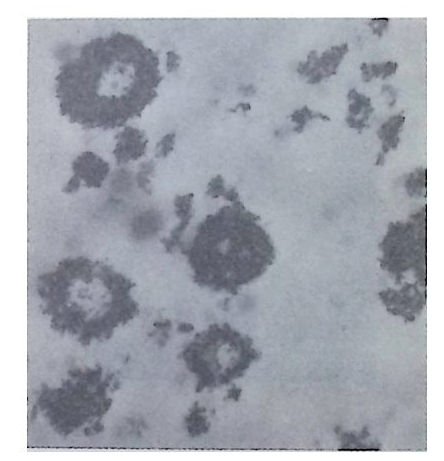
그립 2-18 초파리 국세포에서 관찰된 국입자의 전자현미경 사진
포질에서는 발견할 수 없는 특수한 구조 즉 리보솜으로 둘러싸여 있 으나 막이 관여하고 있지 않은 구조를 찾아볼 수 있는데 (Mahowald , 1968), 이 구조가 세포분열중 선택적으로 앞의 후부말단에 위치하는 국세포 (po le cell) 로 분배 되고 국세포는 후에 생 식 세 포로 분화한다. 이러한 구조를 국입자(p olar gr anule) 라고 하며 생식세포 결정요인이 들어 있다고 생각되어 왔다. 그러나 아직까지로 국입자가 어떻게 작 용하여 국세포를 생식세포로 분화시키는지 분명치 않다. 근래에는 국세포의 세포질에 대한 연구가 초파리의 발생배에 집중 되었다. 초파리의 발생배는 수정 후 처음 두 시간 동안은 세포질 분 열은 하지 않고 핵분열만 반복하여 다핵 세포를 이룬다. 결국 약 3500 개의 핵을 가지는 배반영 (旺盤葉 blas t odenn) 을 형성하게 되는 데, 이 때 핵이 모두 표면에 자리하게 되고 핵 사이에 세포막이 형성
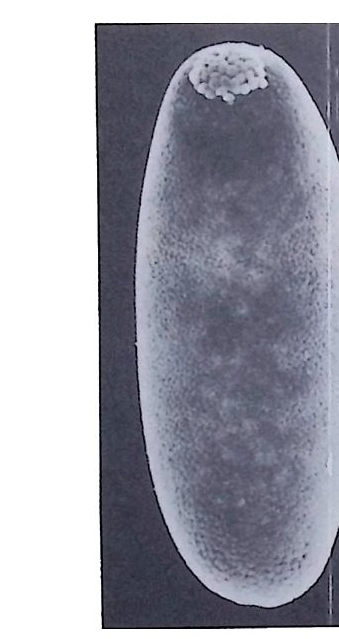
그립 2-19 난할을 끝내기 직전의 초파리 발생배의 주사현미경 사진. 사전의 꼭대기에 국세포가 보임
 (A)
(A)
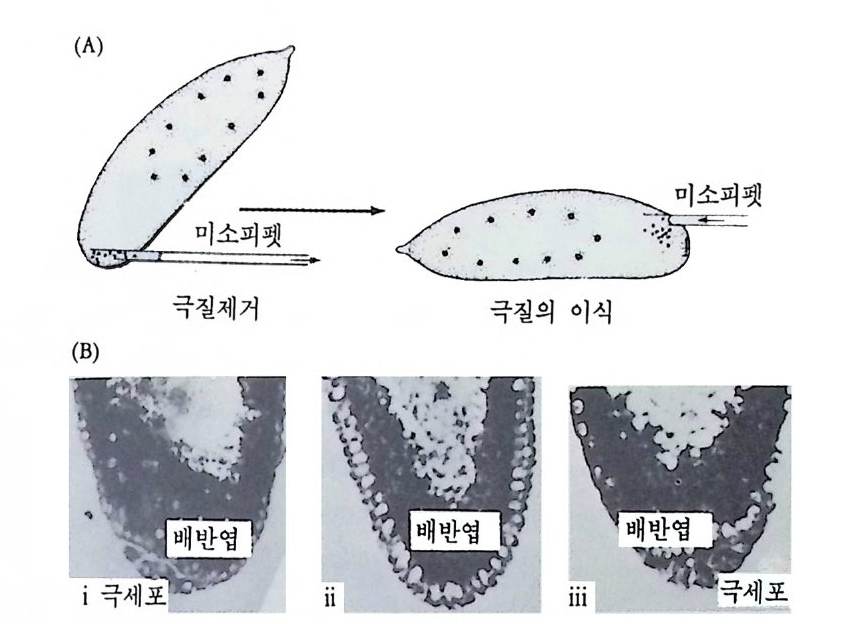
그림 2-20 초파리 발생배의 국질의 역할. (A) 극질 이식의 기술 (B) 국질 이 식의 효과. ( i ) 국세포를 가지고 있는 배반영 (ii) 자의선 조사로 국세포 가 제거된 배반영. (iii) 초기 난할 시기에 자의선을 조사한 다음 국질을 이 식함 (Okada et a l., 1974).
되면서 비로소 세포성 배반영으로 발전한다. 다핵 세포 시기의 핵을 이식하여 발생능을 보면 모든 핵은 분화능 면에서 동일할 뿐만 아니 라 전능성 (全能性, t o tip o t enc y)을 가지고 있다 (Zalokar, 1971 ; Illmensee 1968, 1972), 그러나 세포성 배반영의 단계에 이르면 운명은 결정된 다. 죽 다핵 세포 단계에 있는 핵 속에서는 염색체감되가 일어나지 않고 이들 핵은 생식세포나 체세포 어느 쪽으로 분화될 수 있다. 그 리고 세포의 운명 결정은 그 핵이 이동하여 발생배의 어느 세포질과 접하느냐에 달려 있다. 즉 다핵 세포 시기의 핵 중 어느 핵이든지 발 생배의 후부의 세포질과 집하면 생식세포의 핵으로 분화된다. 가이기 (Geig y, 1931) 는 자의선으로 생식질을 조사하면 불임성 개체가 형성된 다는 사실을 처음으로 발견하였다. 오카다 (Okada) 와 그의 공동연구
 국질이식
국질이식
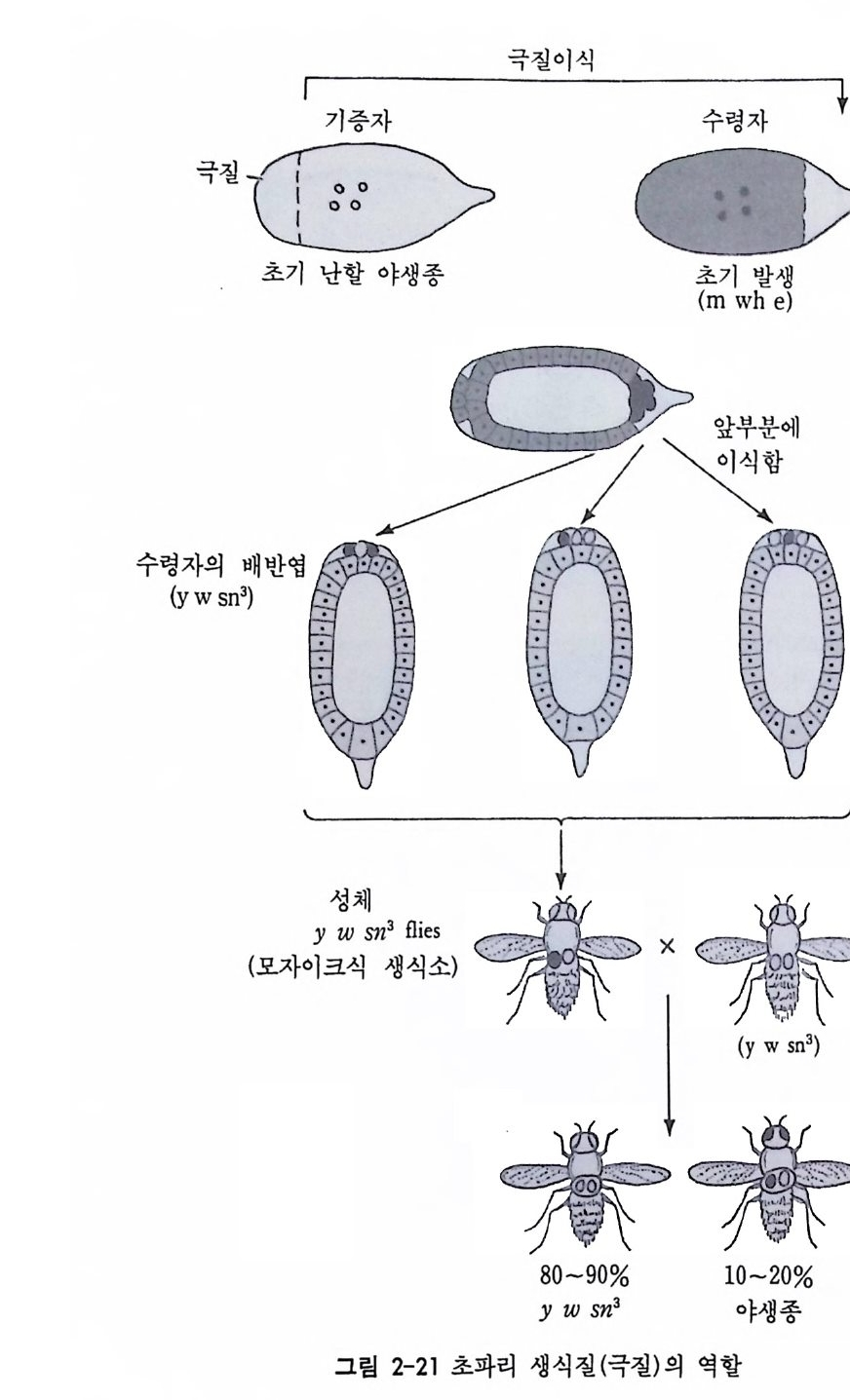
자들은 자의선을 이용한 실험을 통해 자의선으로 인해 불임 상태가 된 배반영에 국질을 이식시켜 줌으로써 불임성으로부터 회복시킬 수 있었다. 그러나 다른 어떠한 세포질로도 불임성의 치료는 불가능하였 다. 이러한 극질의 특이성 즉 초파리의 어느 핵이라도 생식세포의 핵으 로 운명 지 어 줄 수 있는 국질의 능력 이 일멘제 (Illrnensee) 와 마호왈드 (Mahowald, 1974) 의 정교한 실험을 통해 재확안되었다. 우선 야생종 의 초파리의 발생배의 후부로부터 세포화 (cellula ri za ti on) 가 일어나기 직전 극소량의 세포질 (5~lOO p l) 을 취하여 유전적으로 표시가 있는 돌 연 변 이 종 (mwh e ; multip le win g hair and ebony body) 의 배 반 영 전 부 (前部)에 이식하였다. 이때 배반영 전부에 이식한 이유는 전부에 형 성된 국세포는 수령자의 후부(後部)로 이동하기가 용이하지 않으므로 수령자의 생식세포와 구분될 수 있었기 때문이다. 세포성 배반영이 형성된 후에 수령자의 전부에 형성된 세포는 기증자의 후부의 국세포 와 유사한 형태적인 특칭을 가지며 국질을 함유한다. 이들 세포가 사 실상의 생식세포의 전구 세포의 역할을 하는지롤 알아보기 위하여 마 호왈드와 일멘제는 mwhe 돌연변이 발생배의 전부에서 분리하여 유 전적으로 다르게 표시 되어있는 돌연변종(y w sn3 ; yel low body wh ite eye s and sin g e d br i s t les) 의 세포성 배반엽의 후부에 이식하였다. 이 발생배들은 후에 모두 y w sn3 돌연변이종으로 발생하였다. 그러나 야 생종의 국세포를 수령하고 있는 y w s 균 돌연변이종끼리 교배시켜 보 았더니, 92 개체 중 88 개체가 y w s 균의 돌연변이종으로 그리고 4 개체 가 야생종으로 나왔다. 이러한 실험결과는 1) 극질이 배반부 전부의 핵을 생식세포의 핵으로 운명지울 수 있고, 2) 국질의 특성이 수령자 의 세포질에 흡수되지 않고 독립적이며, 3) 극질의 독립적인 특이성 이 세대간에 전달될 수 있다는 점을 보여주었다. 무엇보다도 생식세 포 결정요인이 국부적으로 집중되어 있다는 접이 강하게 반영되었다. 생식세포 결정요인은 수정이전에 기능적으로 마련되어 난황물질이 난
모세포의 후부로 이동하는 때에 후부로 집중된다 (Illmensee et al., 1976) . 극질과 국세포에 있는 극입자가 생식 세포 형성에 결정적인 역할을 한다는 사실은 여러 가지 다른 실험을 통해서도 입증되었다. 초파리 에서 gran dchil d less 돌연변이의 동형 접합자인 암컷을 정상적으로 숫컷과 교배시켰을 때 정상적이나 불임성인 자손을 낳는다 (GG( 수 컷) X gg(암컷 )-+G g(불임성)) (Mahowald et a l 1979). 그 이유는 이 발 생배의 핵은 후부로 이동하지 않음으로 인하여 국세포가 형성되지 않 기 때문이다. a g arne ti c 이라는 돌연변이종이 있는데, 이 종에서는 자 손의 생식소에 생식세포가 나타나지 않는다. 그 이유는 국세포가 형 성되기는 하지만 수정 후 곧 국입자가 퇴화하기 때문이다 (En g s t rom et a l., 1982). 즉 국질에 이상이 생길 경우에는 직접 생식 세포 형성 에 반영된다. 초파리에서 국입자를 분리하여 화학적인 성분을 조사하여 본 결과 단백질과 RNA 임 이 밝혀졌다 (Wa ri ng et a l., 1978). 이 단백질의 분자 량은 95,000 이며 염기성을 띠고 있고, 난자 형성 기간 동안에 새로이 합성되는 것으로 직접 알의 세포질을 통해서 전해지지 않는다. 국입 자에서 확인할 수 있는 RNA 는 일단 극세포가 형성되면 더 이상 찾 아볼 수 없지만 (Mahowald, 1971 a, b) 아마도 생식세포 형성에 대단히 중요할 것으로 생각되고 있다. 일단 극세포에 자의선을 조사하여 국 세포를 제거시킨 다음 초파리의 초기 발생배의 세포질을 주사해 주 면, 국세포를 상실했던 발생배가 극세포를 회복하고, 생식세포를 가 지는 성체로 발생한다 (Okada and Kobay as hi, 1987}. 수정 전에 이 국입자에 또 다른 변화가 일어난다. 즉 미토콘드리아 근처에 막으로 둘러싸인 질은 입자들이 핵이 극으로 이동하기 이전에 산만하게 퍼지는 것을 관찰할 수 있다. 결국은 국세포가 이 입자를 흡수하게 되는데 , 국세포가 생 식융기 (go nadal ridg e ) 에 도착하기 전에 일종의 섬유구조 (nua g e) 로 변한 다음 핵막에 모인다. 유사한 구조를
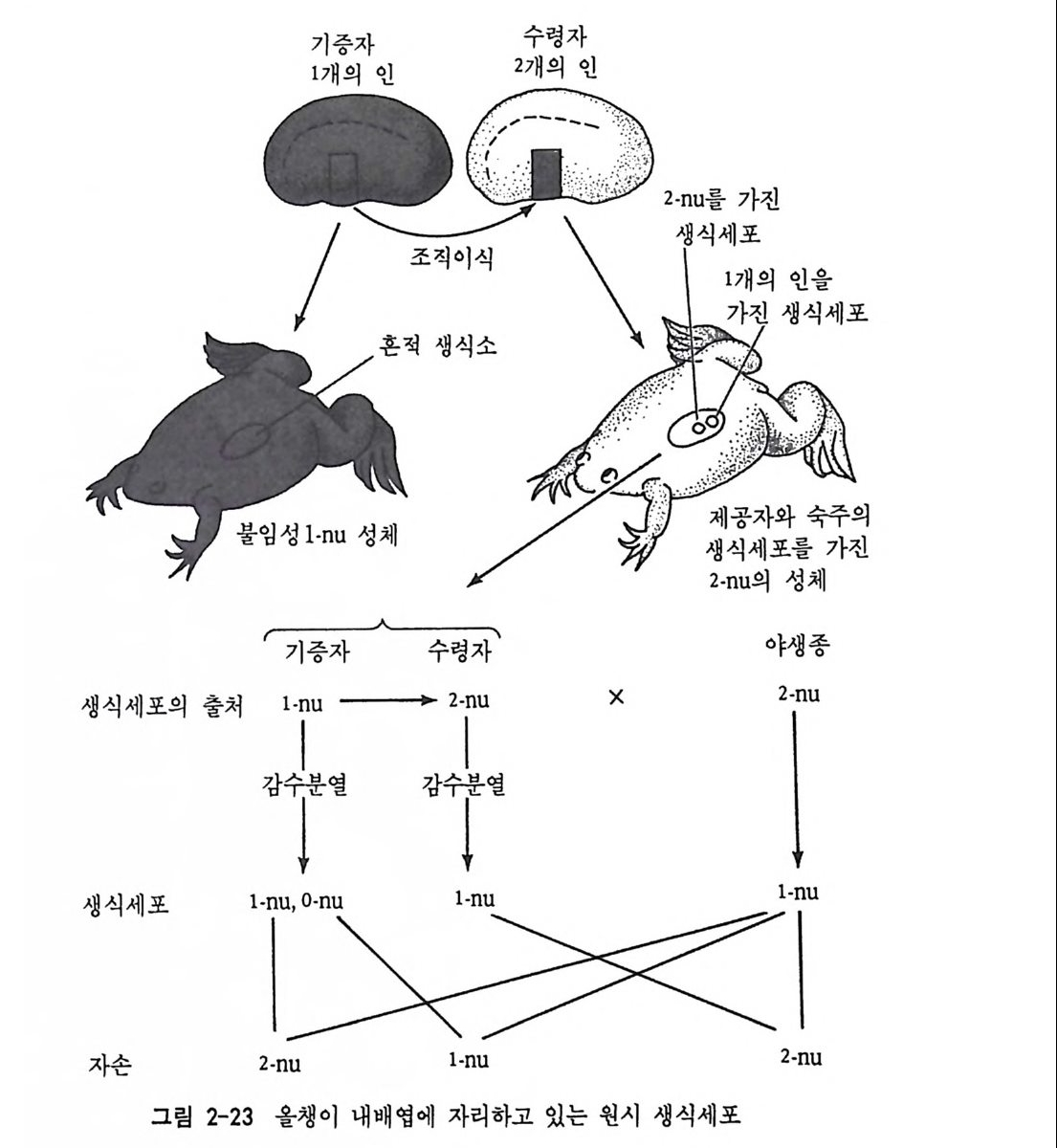
양서류의 국입자에서도 찾아볼 수 있는데 섬유구조 물질이 언제나 핵 막과 결부되어 있는 미토콘드리아에 부착되어 있다. 이러한 현상을 동물계에서는 흔히 찾아 볼 수 있는데 생식세포 형성에 중요한 역할 울 하는 것으로 생각되고 있다. (3) 양서류에서의 생식세포 결정요인 생식세포 결정요인의 선택적 집중 및 분배 현상을 척추동물의 발생 배에서도 찾아볼 수 있다. 보누르 (Bounoure, 1934) 는 곤충의 국질과 감은 염색 성질을 가진 물질을 아직 난할을 시작하지 않은 개구리의 수정란의 식물국 쪽에서 관찰하였다. 이러한 물질은 표충질(表層質) 로서 앞으로 내배영을 이루는 세포로 분배되었다가 생식융기(g e nit al r i d g e) 로 이동한다. 블래클러 (Blackler, 1962) 도 이러한 물질을 가진 세포들이 흔히 원시 생식세포가 되는 것을 확인하였다. 즉 한 개의 인을 가진 돌연변이종의 신경배로부터 내배영을 분리한 후 두 개의 인을 가진 야생종의 신경배의 내배영에 이식하였더니, 돌연변이종인 기증자에서는 생식세포가 생성되지 않은 반면에 야생종인 수령자에서 는 생식세포가 형성되었다. 뿐만 아니라 이러한 야생종을 다른 정상 적인 야생종과 교배시켰을 경우 그 자손에는 한 개의 인을 가전 개체 와 두 개의 인을 가진 개체가 섞이어 나타났다. 이러한 실험결과는 한 개의 인을 가전 기증자의 내배영으로부터도 생식세포가 형성되었 음을 말해주는 것이라고 할 수 있는데, 만약 기증자로부터 이식된 내 배영에서 생식세포가 형성되지 않았다면 수령자로부터 나온 자손은 모두가 두 개의 인을 가졌었어야만 했을 것이다. 보누르 (1936) 는 후에 개구리 수정란의 식물국쪽에 자의선을 조사하 여 중으로써 불임성 개체를 얻을 수 있었다. 스미스(Smith, 1966) 도 개구리 발생배의 여러 부위를 자의선으로 조사함으로써 보누르와 같 은 실험결과를 얻었는데, 동물 반구에 조사했을 경우에는 생식세포
 난황립 춧생식 질 广건홉
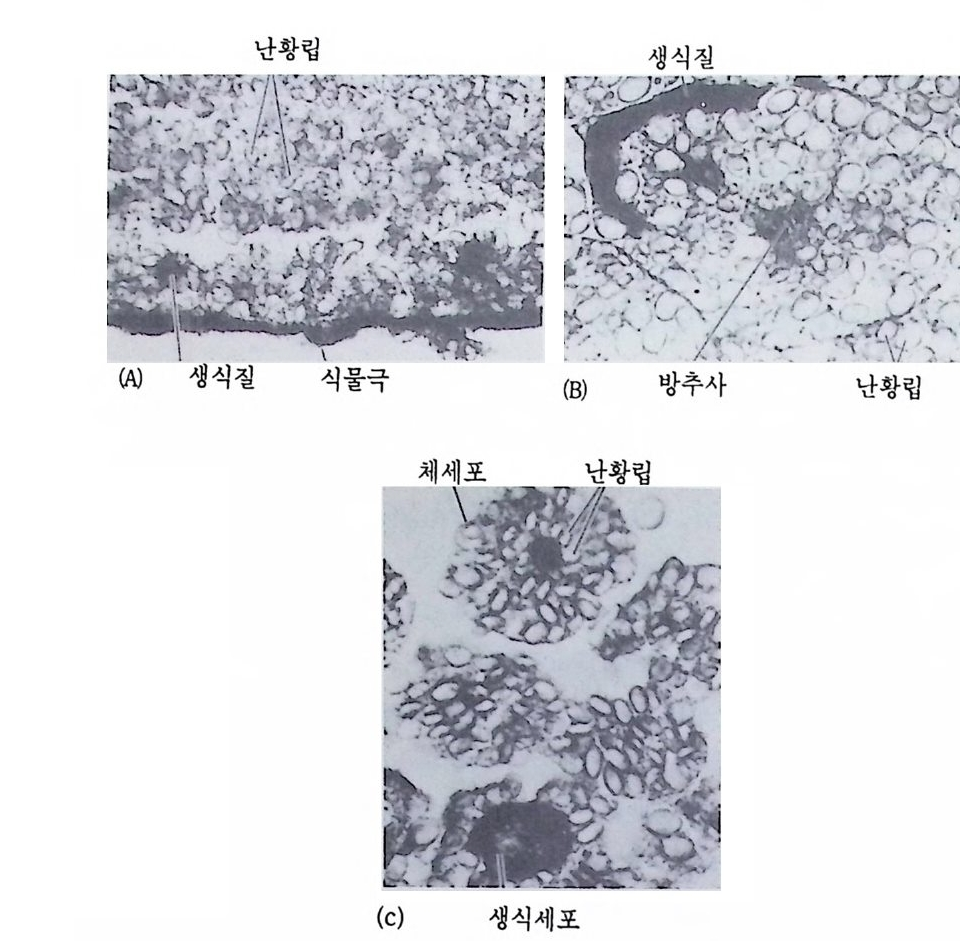
난황립 춧생식 질 广건홉
그립 2-22 개구리 발생배의 생식질. (A) 수정란의 식물극쪽에 자리한 생식 질. (B) 포배의 내배영 부위에 생식질을 포함하고 있는 세포. (C) 초 기 낭배에 나타난 원시 생식세포와 체세포.
형성에 아무런 영향을 주지 못하였으나 식물 반구를 조사하였을 경우 에는 올챙이에서 생식세포의 흔적을 찾아볼 수 없었다. 또한 생식융 기로의 생식세포 이동도 관찰할 수 없었다. 스미스는 이러한 실험을 연장시켰는데, 정상배의 세포질을 자의선을 조사한 배의 식물극에 이 식한 후 생식세포가 형성되는지를 관찰하였다. 기대한 바대로 동물국
 수령자
수령자
의 세포질을 이식하였을 경우에는 아무런 영향을 주지 못하였으나 식 물극의 세포질을 이식하였을 경우에는 생식세포가 형성되었다. 또한 2~4 세포기에 자의선으로 조사된 발생배를 발생시켰을 경우에 생식세
포가 생식융기로 이동하기는 하나 이들 세포의 수가 정상적인 것에 비해 10 분의 1 밖에 되지 않으며 핵의 모양도 비정상적이었다. 이와 같은 점으로 보아 개구리의 수정란도 초파리의 경우에서와 같이 생식 세포 결정 요인을 가지고 있으며 결정요인의 이동이 자의선에 예민하 게 영향 받음을 알 수 있었다.
 .. , t' 住 .t.
.. , t' 住 .t.
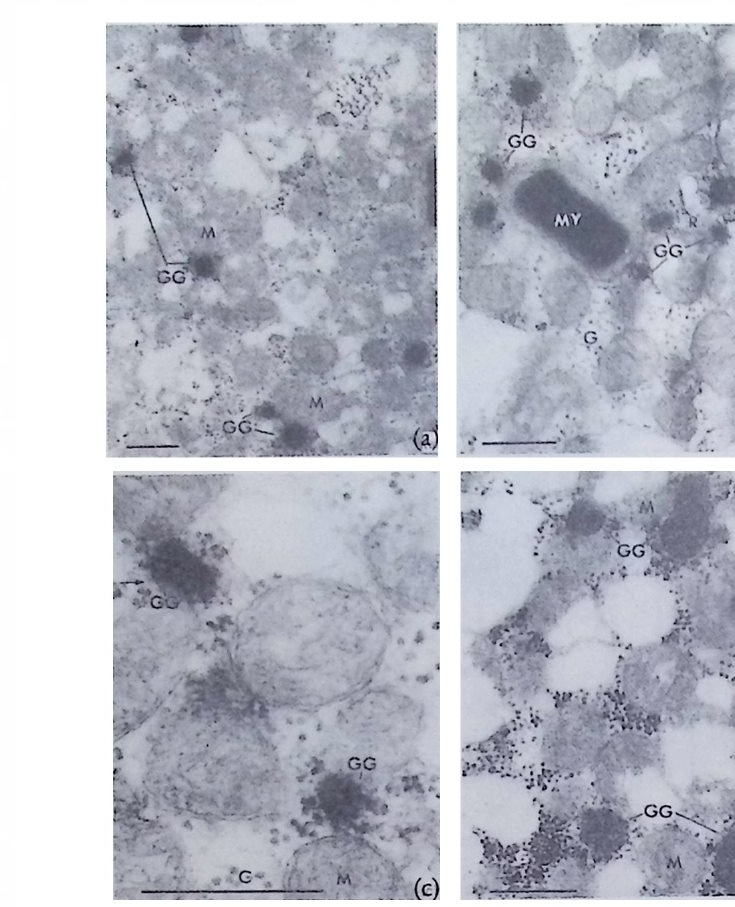
그림 2-24 양서류 수정란에 있는 국입자의 미세구조. (a) 수정 후 1 . 5 시간 (b) 2 세포기 (c) 4 세포기 (d) 16 세포기, GG : 국입자 M : 미토콘드리아, MY: 난황을 함유하고 있는 미토콘드리아, R: 리보솜 , G: 글리코겐, 화살표 는 국입자와 리보솜울 포함한 부위를 가리키고 있다. 막대 길이는 0.5µm (Wi lliam s and Sm ith, 1971) .
양서류의 생식질은 이러한 기능적인 유사성에서뿐만 아니라 구조적 인 면에서도 곤충의 극입자와 대단히 흡사하다. 즉, 미수정란과 초기 발생배에서 미토콘드리아와 결합되어 있으면서 리보솜에 둘러싸여 있 는 섬유 구조를 찾아볼 수 있다. 원시 생식세포가 생식융기로 이동할 즈음에는 과립성 구조는 사라지고 단지 섬유 구조만이 핵막 근처에서 미토콘드리아와 결합되어 있는 모양을 볼 수 있다. 이와 같은 섬유 구조는 난원세포와 초기의 난모세포에서도 나타나는데 초파리의 난원 세포와 난모세포에서 볼 수 있는 것과 대단히 유사하다. 섬유 구조는 생식질로부터 유래된 것이라고 추측은 되나 아직 확실한 증거는 없 다. 그러나 생식질이 호르몬 처리에 의해 난모세포 성숙 과정에서 다 시 나타나는 점과 초파리의 극입자와의 유사성에 비추어 볼 때 양서 류에서의 생식질 생성은 난자 형성중에 일어나는 것으로 추측된다. 난할중 내배엽 세포로 분배되고 생식질을 받은 세포는 생식세포로 결 정되는 것으로 생각된다. 생식질을 부여받아 앞으로 생식세포가 될 세포는 생식융기로 이동하는데 일단 생식융기에 도달하면 생식질은 더 이상 보이지 않는다. 아마도 섬유 구조 물질로 전환되어 있다가 난모세포 성숙기간에 다시 나타나는 것으로 추측된다. 그러나 이러한 설명에서 한 가지 어려운 점은 생식질이 사실상 섬유 구조로 확실히 전환하는지 분명치 않은 점이다. 섬유 구조는 초파리와 양서류에서뿐만 아니라 포유류를 포함한 여 러 종류의 동물에서 볼 수 있는데, 이러한 점으로 비추어 보아 섬유 구조의 형성은 거의 모든 동물에서 생식세포 형성에 공통적인 의미를 가지는 것으로 생각된다. 7 쌍시목 곤충류에서의 결정요인의 분배 선구동물의 하나인 곤충의 발생중에도 세포질의 선택적 분배로 인 하여 세포의 운명이 결정되는 경우를 찾아 볼 수 있다. 키로노무스의
일종인 Sm ittia 의 발생중 전부 결정요인 (前部決定要因, ante r i or i zi n g fac t or) 이 선택적으로 분배된다. 전부 결정요인을 어떠한 방법으로든 지 파괴시키면 앞부분의 형성이 불가능해진다. 자외선으로 Smi ttia 알의 앞부분을 조사한 후에 발생시키면 이중복 유충(二 重 腹幼蟲 double abdomen larva) 을 형 성 하게 되 는데 , 앞부분을 자의 선 조사함 으로써 전부 결정요인이 파괴되었기 때문에 전부(前部)형성 능력을 상실하고 후부(後部)를 형성함으로써 두 개의 복부를 가진 결과를 초 래한다 (Kal th o ff and Sander, 1968). 따라서 이중복 유충에서는 머리, 가슴 및 앞부분이 복부로 대치됨으로써 전후 상칭의 모양을 나타낸
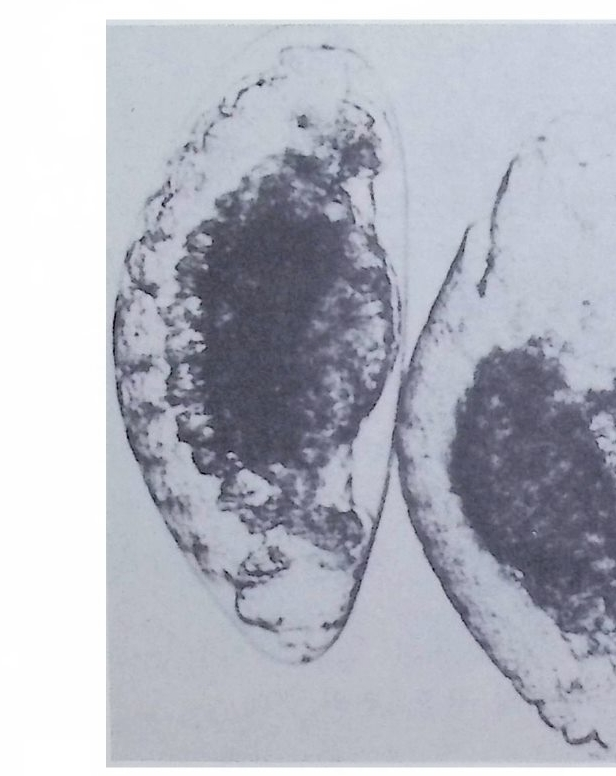
그립 2-25 Sm itta.의 이중복 유충 오른쪽 : 정상적인 체절을 가진 유충 왼쪽 : 이중복 유충 길이 noµm (Kalth o ff , 1971a)
다. 죽 전부 결정요인이 결여될 경우 앞부분도 뒷부분과 갇이 분화한 다는 것이다. 바늘로 앞부분을 찌르면 이중복 유충이 형성될 수도 있 다 (Schm i d t et al., 1975). 알의 앞부분에서 어떤 특별한 구조를 찾아 볼 수는 없으나 (Z i ssler and Sander, 1973), 칼토프 (Kal th o ff, 1971b) 는 알 속에 자의선에 특별히 민감한 부분이 있다고 하였다. 그리고 자의 선의 침두거리가 5µm 이하인 점을 감안해 볼 때, 전부(前部) 결정 요인은 앞의 표층에 위치하는 것으로 추측되었다 (Kal th o ff. 1971a, 1973), 또한 전부 결정요인은 RNAse 에 의해 쉽게 파괴되는 것으로 보아 일종의 RNA인 것으로 짐작되었다. 죽 RNAs 여t 전부에 처리 하였을 경우 이중복 유충이 형성되었다. 8 결정요인의 정체 발생학적 정보가 결정요인의 형태로 생성되어 보존되었다가 발생 기간중 작용하는 것으로 일반적으로 인식되고 있으나 사실상 결정요 인의 정체 죽 화학적 성분에 대해서는 아는 바가 거의 없다. 초파리 와 양서류의 생식세포 결정요인의 생성에서 본 바와 같이 결정요인은 난자 형성중에 준비되는 것으로 생각되었다. 그러나 발생학적 정보가 저장되는 형태는 다양한 것으로 보였다. 멍게에서 근육 결정요인은 선택적인 유전자 발현을 유발하는 물질로 생각되었다. 즉 acti no my cin D 를 멍게알에 처리하여 DNA 로부터의 RNA 전사를 억제시키면 아세 틸콜린 에스테라아제 (ace ty lcho li nes t erase) 의 효소활성도가 발생중 나 타나지 않는다. 또한 C i ona 의 여러 단계의 발생배로부터 RNA 를 추 출하여 양서류 난모세포에서 해독시킨 다음 단백질을 분석하여 본 결 과 C i ona 의 발생배가 낭배기에 이를 때까지는 아세틸콜린 에스데라 아제의 합성을 찾아볼 수 없었다 (Meedel and W 血 aker, 1983). 죽 아 세틸콜린 에스데라아제가 합성되기 위해서는 새로운 RNA 합성이 먼 저 일어나야만 한다는 접을 보여주고 있다. 따라서 멍게 근육 결정요
인은 아세틸콜린 에스데라아제를 포함한 단백질의 유전자를 선택적으 로 활성화하는 물질로 생각되었다. 그러나 같은 멍게의 발생배에 있 어서도 장(腸)의 알칼린 포스파타아제의 경우는 다르다. 이 효소는 유생 내배영에서 합성되어 장을 형성하는 세포로 분배된다. acti no my ci n D 는 이 효소의 합성 에 아무런 영 향을 주지 못하고 단지 해독 억제제만이 이 효소의 합성을 억제하였다(Whitt aker, 1977). 따 라서 장의 알칼린 포스파타아제의 발생중 합성은 이미 난자 형성 기 간 동안에 합성된 mRNA 의 존재에 기인하는 것으로 생각되었다. 즉 알칼린 포스파타아제의 mRNA 가 특정한 할구로 분리되었다가 해독 되는 경우로서 결정요인이 mRNA 형태로 생각되었다. 그러나 이러한 mRNA 가 해독되지 않고 있다가 수정 후 특정된 세포에서만 해독하 도록 작용하는 요인이 무엇인지는 알지 못하고 있다. 앞에서 기술하였지만, mRNA 의 분포가 발생배의 부위에 따라 다 르게 나타나는 현상을 여러 가지 경우에서 찾아볼 수 있다. Bit hy n ia 의 극영에 RNA 가 치우쳐 있는 것 의에도 Ily anassa 의 정상배와 극 엽울 제거한 발생배간에 단백질 합성이 양적으로 크게 차이가 나는 경 우를 볼 수 있다 (Brandhors t and Newrork, 1981) . 콜리 어 (Coll ier ) 와 맥카시 (McCart hy, 1981) 는 극영 속에 전사와 해독을 조절하는 요인이 들어 있을 것 이 라고 추측하였는데 그 이 유는 act ino my ci n D 를 처 리 한 발생배로부터 극영을 제거시키면 해독률이 증가되기 때문이었다. 성게에서도 16 세포기에 소할구의 mRNA 는 다른 할구의 것과 다르다 (Rodge r s and Gross, 1978 ; Mizu no et al., 1974). mRNA 의 선택적 분배 가 발생학적 결정요인의 선택적 분배와 동일한 것인지는 확실히 말할 수 없으나, mRNA의 분포가 달라질 때 세포의 운명이 달라지는 경 우로 보아서 mRNA 의 분포적 차이와 결정요인의 선택적 분배 사이 에 상관 관계가 있을지도 모른다는 가능성을 생각하였다. 앞에서 기 술한 Sm ittia의 경우에서도 전부 결정요인이 자의선에 의해서 파괴된 다는 것이 RNA 의 파괴에 기인되었을 가능성이 농후하지만 특별히
RNAse 에 의해서 결정요인이 제거된 실험결과는 결정요인이 RNA 의 형태로 보존됨을 강하게 암시한 경우라고 하겠다. 곤충의 동배축의 결정도 모계 RNA(mate m al RNA) 에 기인하는 경 우를 찾아볼 수 있다. 초파리의 snake 라는 돌연변이 종에서는 동형 접합체로서의 암컷의 알이 배쪽은 상실하고 완전히 동쪽으로만 이루 어진 발생배로 발생한다. 따라서 배쪽의 큐티클충을 포함한 구조가 보이지 않는다. 이러한 돌연변이 종의 알은 정상적인 야생종의 알의 세포질을 조금 이식시켜중으로써 구제될 수 있다. 혹은 야생종의 알 로 부터 mRNA 를 추출하여 돌연변이 종의 알 속으로 주사해 주면 배쪽을 상실한 비정상적인 발생으로부터 회복시킬 수 있다는 것이다 (Anderson and Nusslein ~ V orhard, 1984) . 참고문헌 Anderson, KV. and Nti ss lein - Volhard, C. (1984) . Inf or mati on for the dorsal-ventr a l pat t er n of the Drosop hi la embry o is sto r ed as mate r nal mRNA . Natu r e 311: 223-227. Blackler, A.W . (1962) . Transfe r of pri m ordi al ger m cells betw e en tw o subspe c ie s of Xenopu s laelvis . ]. Embry o! . 母 Morp h ol. 10: 641 -65 1. Bounoure, L. (1934) . Recherches sur la lign e e ge rrnin a le chez la gren ouil le r ousse aux pre mi er s sta d es du develop pe ment. Ann Sci . Natl. 1oe wer. 17: 67-248. Bounoure, L. (1939) . L'o ri g ine des Cellules Re pr oductr ies et le Prolb- leme de la Lig n ee Germi na te . Gauth ier -Vi llars , Pari s. Boveri, T. (1910) . Uber die Teilu ng centr ifugier t er Eie r von Ascaris mega l ocep h ala. Wi lh elm Roux Arch. Entw ick lun gsme ch. Org. 30: 101-125.
Brandhorst, B.P. and Newrock, K.M . (1981). Post- tra nscrip tion al regu la ti on of pro te i n syn the sis in llyan assa embryo s and iso late d po lar lobes. Dev. Bio l. 83: 250-254. Chi ld, C.M . (1900) . The early develop m ent of Arenic o la and Ste r- napsis. Arch. Entw ick lun gsm ech. Org. 9, 587. Chun, C. (1880) , Di e C te n op ho ren des Golf es von Neape l . Fauna und Flora des Golfe s von Neape l , Monog r. I. Eng el mann, Leip z ig . Clement, A.C. (1968) . Develop m ent of the vege t a l half of the Ilyan as- sa egg aft er removal of most of the yol k by centr if u ga l forc e, comp ar ed wit h the develop m ent of anim al halves of s im il a r vis ib le comp os it ion . Dev. Bio l. 17: 165-186. Coll ier, J.R., and McCart hy , M.E. (1981) . Regu la ti on of pol yp e pt ide syn thes is durin g early embry o ge n esis of llyan assa obsoleta . Dif fere nti ation 19, 31. Conklin , E.G . (1897) . The embry ol og y of Crep idu la. A contr ib u ti on to the cell line age and early develop m ent of some marin e gas te r- opo d s. ]. Morp h ol. 13, 1. Conkli n, E.G . (1905a) . The orga n i za ti on and cell line age of the ascid ian egg . ]. Acad. Nat. Sci . Phil a. 13: 1-119. Dohmen, M.R. , and Lok, D. (1975). The ultr a str u ctu r e of the po lar lobe of Crep idu la forn ic a ta (Gaste r op od a, Prosobranchia ) . ]. Em- bry ol . Exp. Morp h ol. 34, 419. Dohmen, M.R. , and Verdonk, N.H. (1974). The stru ct u r e of a mor- pho g en etic • cyt op l a sm, pre sent in the po lar lobe of Bit hy n ia ten ta cula ta (Gastr o p od a, Prosobranchi a) . ]. Embry o! . Exp. Mor- pho l. 31, 423. Donohoo, P., and Kafa tos , F.C. (1973) . Differe nces in the pro te i n s syn thes iz e d by the pro g en y of the firs t t wo blasto m eres of llyan as-
sa, a mosaic embryo . Dev. Bio l. 32, 224. Drie s ch, H., a nd Morga n , T.H . (1896) . Zur Analys i s der erste n Entw ic k elung ss ta d ie n des Cte n op ho reneie s . I. Von der Entw ic k - elung ein z elner Cte n op ho renblasto m eren. Arch. Entw i c k lungs m ech. Org. 2, 2 04. Eng st ro m, L., C aulto n , J.H ., U nderwood, E.M . and Mahowald, A.P . (1982) . Dev el op m enta l lesio n s in the aga m eti c muta n t of Droso- phi la melanoga s te r. Dev. Bio l. 91: 163-170. Fis c hel, A. (1898) . Exp er im ente l le Unte r suchung en am Cte n op ho r- ene. IL Von der Kti ns tl ic h en Erzeug ung (halber) Dop pe l-u n d Mi ssb il d ung en . III. Regu la ti on der Entw ic k elung . IV. Ober den Entw ic k elung sg a n g und die Orga n is a ti on s-stu fe des Cte n op ho r- eneie s . Arch. Entw i c k lung s m ech. Org. 7, 557. Fis c hel, A. (1903) . Entw ic k elung und Orga n -d iffer enzir u ng. Arch. Entw i c k lungs m ech. Org. 15, 670. Freeman, S.B. (1971) . A comp ar iso n of cert ai n iso zym e pat t er ns in lobeless and normal embry o s of the snail, Ilyan assa obsoleta . J Embry o! . Exp. Morp h ol. 2 6, 339. Freeman, G. (1 976a) . The role of cleavage in the locali za ti on of develop m enta l po te n ti al in the cte n op ho re Mnemi op s is leid y i. Dev. Bio l. 49, 143. Freeman, G. (1976b). The eff ec ts of alte r in g the pos it ion of c leavage pla nes on the pro cess of localiz a ti on of develop m enta l pot e n ti al in cte n op ho res. Dev. Bio l. 51, 332. Hegn e r, R .W . (1911) . Expe r im ents w it h chr yso melid beetl e s. I II. The eff ec ts of kil ling par t s of the egg s of Le ptino ta r sa decemlin e ata . Bio l. Bull. 20, 237-251. Geig y, R. (1931) . Acti on de !'ultra -vi ol et sur le po le ger m ina l dans I'
oeuf de Drosoph i la melanoga s te r (castr a ti on et muta b il it e ) . Rev. Suis se Zool. 38: 187-288. Gerhart, J ., Black, S., and Scharf, S. ( 1983) . Cellular and pan cellular orga ni za ti on of the amp h ib i a n embryo . In Modem Cell Bio l og y. Sp a ti al Orga ni za ti on of Eukaryo t i c Cells (R. McInto s h, ed.) , Vol. 2, p. 483. Alan R. Liss, New York. Gerhart , J., Ubbels, G ., Black, S., H ara, K., and Kir s chner. M. (1981) . A rein v esti ga ti on of the role of the grey crescent in axis f or mati on in Xenop us laevi.s . Natu r e(London) 292, 511 . Geye r -Duszyn s ka, 1. (1959) . Exp er im enta l research on chromosome dim i nu ti on in Cecid o mi idae (Di pter a) . ]. Exp. Zoo!. 14I: 3 81- 44 1 . Illmensee, K. (1968) . Transpl a nta t i on of embryo n ic nuclei int o unfe r - tilize d egg s of Drosoph i la melanoga s te r. Natu r e 219: 1268-1269. Illmensee, K. (1972) . Develop m enta l po te n cie s of nucleif rom cleav- age , pre blasto d erm, and syn c yt ial blasto d erm tra nspl a nte d int o unfer t ilize d egg s of Drosop hi la me lan og a s te r . Wi lh elm Roux A rch . Entw ick lungs m ech. Org. 110: 267-298. Illmensee, K. and Mahowald, A.P. (1974) . Transpl a nta t i on of po ste - rio r po lar pla sm in Drosoph i l a . Inducti on of ge rm cells at the ante r i or po le of the egg . Proc. Natl. Acad. Sci. USA 71: 1016-1020. Illmensee, K., Mahowald, A.P. and Loomi s, M.R. (1976) . The onto g e n y of ger m pla sm durin g oog en esis in Drosop hi l a . De v. Bio l . 49: 40-65. Kalth o ff , K. (1971a) . Photo r eversio n of UV ind ucti on of the malfo r- mati on double abdomen in the egg of Sm i血 spe c . (Dipter a, Ch iro nom ida e) . Dev. Bio l. 25, 119. Kalth o ff, K. (1971b) . Posit ion of tar ge ts and pe rio d of comp e te n ce for UV- in d ucti on of the malfo rm ati on double abdomen in the
egg of Smi ttia spe c . (Di pter a, Chir o nomi da e) . Wi lh elm Roux' Arch. Entw i c k lungs m ech. Org. 168, 63. Kalth o ff , K. (1973). Acti on spe c tr a for UV ind ucti on and ph oto r - eversal of a swi tch in the develop m enta l pro g ram of the egg of an ins ect (Smi ttia) . Photo c hem. Photo b io l . 18, 355. Kalth o ff . K., and Sander. K.(1 968). Der Entw ic k lung sg a ng der Mi /3 bild ung Dop pe labdomen im UV-bestr a hlen Ei von Smi ttia pa r- the noge nic a (Di pt. Chir o nomi da e). Whlhelm Roux Arch Entw ic k - lungs m ech. Org. 161 . 129. Klag , J.J., and Ubbels, G.A . (1975). Reg ion al morp h olog ica l and cyt ol og ica l dif fere nti at i on of the fer t iliz e d egg of Dis co g lo ssus pictu s (Anura) . Dif fere nti at io n 3, 15. Koser, R.B. , and Collie r , J.R. (1972) . Characte r iz a ti on of the rib o somal RNA pre cursor in llyan assa. Exp. Cell Res. 70, 124. Mahowald, A.P. (1968) . Polar gran ules of Drosop h ila . II. Ultr as • tru ctu r al chang es dur ing early embry og e nesis . J F,xp. Zoo!. 167, 237. Mahowald, A.P. (1971a) . Polar gran ules of Drosop hi la . III. The conti nu it y of po lar gran ules durin g the life cyc l e of Drosop h ila . J 均. Zoo!. 176: 329-343. Mahowald, A.P. (1971b) . Polar gran ules of Drosop hi la . IV. Cy to- chemi ca l stu d ie s showi ng loss of RNA from po lar gran ules du ring early sta g e s of embry og e nesis . ]. Exp. Zoo!. 176: 329-343. Mahowald, A.P. , Caulto n , J.H . and Gehrin g , W. J. (1979) . Ultra s- tru ctu r al stu d i es of oocyt es and embry os deri ve d from fem ale flies carryi ng the gra nd chil d less muta t i on in Drosop h ila subobscura. Dev. Bio l. 69: 118-132. Meedel, T.H. and Whittak er, J.R. (1983} . Develop m ent of tran -
scrip tion ally acti ve mRNA for larval muscle acety lc holin e ste r ase durin g ascid i a n embryo g e n esis . Proc. Natl. Acad. Sci. USA so: 4761 -4765. Mi zu no, S., Lee, Y.R., Whit ele y, A.H ., and Whit ele y, H.R. (1974) . Cellular dis t r ibu ti on of RNA po pu lati on s in 16-cell sta g e embryo s of the sand dollar, D endraste r excentr icttS . Dev. Bio l. 37, 18. Newrock, K.M . and Raff , R.A. (1975) . Polar lobe spe c if ic r egu la ti on of tra nslati on in embry o s of Ilya n assa obsoleta . Dev. Bio l. 42: 242 -261. Okada, M., Klein m an, I.A. and Schneid e rman, H.A. (1974) . Resto - rati on off ert il ity in ste r ili z e d Drosop hi la egg s by tra nspl a nta t i on of po lar cyt op l a sm. Dev. Bio l. 37: 43-54. Ort ol ani , G. (1959) . Ric h erche sulla ind uzio n e del sis te m a nervoso nelle larve delle Asci die. Boll. Zoo!. 26: 341-348. Or tol ani , G. (1964) . Orig ine dell'orga n o api ca le e di d eriv a ti mesoder- mice nello svi lu p po ernbrio n ale di cte n op h ori. Acta Embry o! . Morp h ol. Exp. 7, 191 , Penners, A. (1926) . Expe r im ente l le Unte r suchunge n zum Dete r - mina ti on spr o blem am Keir n von Tubif ex n·vulorum Lam. II. Die Entw ick lung tei lw e is e abg et o tet e r Keim e. Z. Wis s. Zoo!. 127, 1. Pucci -Mina fr a, I., Mi na fr a, S., and Coll ier, J.R. (1969) . Dis t r i b u ti on of rib o somes in the egg of Ilya n assa obsoleta . Exp. Cell Res. 57, 167. Reverberi, G. (1970) . The ultr as tru c tu r e of Denta li um egg at the trefo il sta g e . A cta Embry o! . Exp. p. 31. Reverberi , G. (1971a) . Cte n oph o res. In Expe r im enta l Embryo l og y of Mari ne and Fresh-Wate r Invert eb rate s (G. Reverberi, ed.) . p. 83. Nort h-H olland Publ., Amste r dam. Reverberi, G. and Mi ng a n ti, A. (1946) . Fenomeni di evocazio n e nello
svil u pp o dell'uovo di Ascid i e . Ris u lta t i de ll'ind ag ine spe r menta l e sull'ouvo di Ascid i e ll a aspe rsa e di Ascid ia malaca allo sta d io di 8 blasto m eri. Pubbl. Sta z . Zoo!. Napo li 2 0: 199-252. (Qu ote d in Rever- beri , 1971, p. 537) . Rodg er s, W. H. , and Gross, P.R . (1978) . Inhomog en eous dist r ibu ti on of egg RNA sequ e nces in the early embry o. Cell 14, 279. Sato h , N. (1979). On the clock mechanis m dete r mi ning the tim e of tiss ue-spe c i fic develop m ent durin g ascid i a n embry og e n esis . I. Acety lc holin e ste r ase develop m ent in cleavage - a rr este d embry os . J Embry o! . Exp. Morp h ol. 54: 131-139. Schmi dt , 0., Zis s ler, D., S ander, K., and Kalth o ff, K. (1975) . Sw itch in pa tt er n for mati on aft er pun ctu r in g the ante r io r pol e of Smi ttia egg s (Chir o nomi da e, Dip ter a). D ev. Bio l. 46, 216. Smi th, L.D . (1 966) . The role of a ge rmi na l pla sm in the form ati on of pri m ordia l ger m cells in Rana pipien s. Dev. Bio l. 14: 330-347. Teit elm an, G. (1973) . Prote i n syn the sis durin g Ilya n assa develop- ment: Eff ec t of the pol ar lobe. J Embry o! . Exp. Morp h ol. 29, 267. Tobler, H., Smi th, K.D . and Urspr u ng , H. (1972) . Molecular aspe c ts of c hromati n elim in a ti on in Ascaris lumbr ico id e s. Dev. Bio l. 27: 190 -203. Tung, T.C. , Wu, S.C ., Yel, Y.F., L i, K.S. and Hsu, M.C. (1977) . Cell dif fere nti at i on in asci dian s stu died by nuclear tran spl a nta t i on . Scie n ti a Sin i c a 20: 222-233. Verdonk, N.H., and Cath e r, J.N . (1973) . The develop m ent of i so late d blasto m eres in Bit hy n ,ia ten ta c ulata (Prosobranch ia, Gastr op o da) . ]. Exp. Zool. 1s6, 47. Verdonk, N.H. and Cath e r, J.N . (1983) . Morp h og en i c dete r m ina ti on and dif fere nti at i on . In N.H. Verdonk, J.A .M. van den Big ge laar
and A.S. Tomp a (eds.) , The Mollusca. Academi c, New York, pp. 215-252. Waring , G.L ., Allis , C.D . and Mahowald, A.P. (1978). Isolati on of po lar gran ules and the ide nti fica ti on of po lar gran ule-spe c if ic pro te i n . Dev. Bio l. 66: 197-206. Whitma n, C.O . (1878} . The embryo l og y of Cleps i n e . Q.]. Mi cro sc. Sci. 18, 215. Whit tak er, J.R . (1977) . Segr eg a ti on durin g cleavage of a fac to r dete r mi ning endoderrnal alkalin e pho sph a ta s e develop m ent in ascid i a n embry os . ] . Exp. Zool. 202: 139-153. Whit tak er, J.R. (1 979) . Cy top l a smi c dete r mi na nts of tiss ue dif fer- enti at i on in the asci di a n egg . In S. Subte l ny and I. R. Konig sb erg (eds.) , Dete rm i na nts of Spa tia l Orga n iz a ti on . Academi c, New York, pp., 2 9-51 . Wi lliam s, M.A. , a nd Smi th, L.D . (1971) . Ultr a str u c tur e of the 'ger - mina l pla sm' durin g matu r ati on and early eleavage in Rana pipien s. D ev. Bio l. 25, 568. Wi lso n, E.B. ( 1904} . Exp er im enta l stu d ie s on ger mi na l localiz a ti on . I. The ger m regi on s in the egg of Denta li um . II. Expe ri me nts on the cleavag e- mosaic in Pate ll a and Denta li um . ]. Exp. Zoo!. 1: 1 구 2 . Yats u , N. (1912} . Observati on s and expe r im ents on the Cte n op h ore egg . III. Expe r i m ents on ger m ina l locali za ti on of the egg of Beroe ovata . Ann. Zool. J pn . 8, 5. Zalokar, M. (1971) . Transpl a nta t i on of nuclei in Drosop h ila melanoga s te r. Proc. Natl. Acad. Sci. USA 68: 1539-1541 . Zis s ler, D., and Sander, K. (1973) . The cyt op l a smi c arch itec tu re of the egg cell of Smi ttia spe c . (Dipter a, Chir o nornid a e) . Wil h elm Roux' Arch. Entw i c k lun gsm ech. Org. 172, 175.
제 3 장 유전자 동질성 한 개의 세포로부터 다양한 종류의 세포가 분화될 수 있는 기구에 대한 설명은 유전자 작용에 대한 연구가 활발해지면서부터 비록 개념 적이나마 가능해졌다. 유전자가 세포분열중 서로 다르게 분배되어 딸 세포로 들어가서 유전적인 조성을 다르게 해 주기 때문에 세포분화가 가능하다고 생각한 때도 있었다. 그러나 세포분화의 가장 근본적인 원동력은 유전적 조성의 변화가 아니라 루후 (Roux) 나 바이스만 (We i sman) 의 가설에서 제시된 바와 같이 오히려 결정요인의 선택적 분배로 인하여 나타나는 유전자 작용의 차이라고 일반적으로 생각되 고 있다. 종류가 다른 세포에서 합성되는 단백질의 종류가 다른 이유 는 유전자의 조성이 세포의 종류에 따라 다르기 때문이 아니고 발현 되는 유전자의 종류가 각기 다르기 때문이다. 적혈구에서는 헤모글로 빈이 그리고 표피 세포에서는 케라틴이 주로 합성되는 것은 적혈구와 표피세포의 유전적 조성은 같으나 발현되는 유전자가 다름을 의미한 다. 유전자의 조성 이 동일한 현상을 유전자 동질성 (ge nome equ i v a -
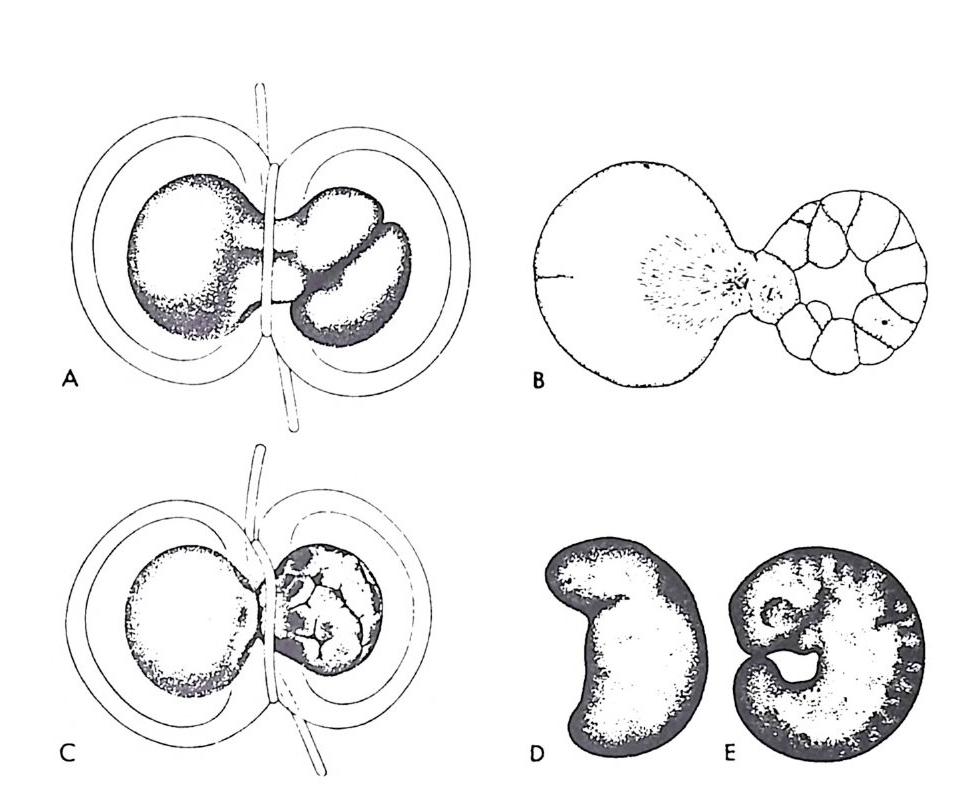
lence) 이라고 하며, 다르게 나타나는 유전자의 작용을 순차적 유전자 발현 (dif fere nti al gen e exp re ssio n ) 이 라고 한다. 순차적 유전자 발현은 한 개체를 이루는 다양한 세포에서 공간적으로 다르게 나타날 수도 있고, 발생중 시간적으로 다르게 나타날 수도 있다. 수정란은 한 개체를 이루는 데 필요한 모든 종류의 세포를 생성할 수 있는 잠재력 즉 전능성 (全能性, t o tip o t enc y)를 가지고 있다. 그러 나 발생이 진행되면서 이러한 능력이 세포에 따라 다르게 제한됨으로 써 유전적 작용이 다르게 나타나며 그 결과 세포의 운명이 결정된다. 세포의 운명 결정은 사실상 세포분화의 방향의 결정과 다름이 없다. 이미 분화의 방향이 결정된 세포의 핵은 동물의 경우에는 거의 비가 역적이다. 1 유전자 동질성 유전자 동질성 (ge nome e q u i valence) 에 대한 실험적 증거는 1914 년 슈페만 (S p emann) 의 실험에서 찾아볼 수 있다. 그는 Tr it urus 의 알을 머리카락으로 묶어서 핵이 한 쪽으로 치우치게 한 다음 어느 정도 세 포분열이 진행된 다음 분열된 세포 하나를 지금까지 핵의 결핍으로 전혀 세포분열이 없었던 쪽으로 이동시켜 준 다음, 매듭울 좀더 좁혀 서 알을 둘로 나누어 발생을 시키면 두 부분이 모두 올챙이가 된다. 비록 세포분열을 거듭한 세포의 핵이지만 전능성을 유지하고 있다는 것은 핵이 세포분열을 통하여 변하지 않고 처음의 상태를 그대로 유 지하고 있음을 의미하는 것이다. 드리쉬 (D ri esch) 도 성게의 4 세포기 할구가 전능성을 가지고 있다고 하였는데, 이러한 현상은 핵의 조성 이 세포분열을 통하여 변하지 않고 그대로 유지됨을 보여준 예이다.
 : I‘II
: I‘II
그림 3-1 슈페만 (S p emann) 의 핵 이동 실험. 수정란을 매듭으로 묶어서 핵을 한쪽에만 가두고 발생시키다가 32 세포기에 세포 한개를 핵이 없는 쪽으로 이동시키면 양쪽이 모두 정상발생을 한다.
(1) 핵이식 슈페만의 생각은 후에 브리그스 (B rigg s) 와 킹(King)의 핵이식 (nuclear tran spl a nta t io n ) 실험을 통해 더욱 견고해졌다. 이미 분화한 세포로부터 얻은 핵아 수정란의 핵과는 기능적으로 전혀 다르게 변했 는지를 이 실험을 통해 알아냈다. 1936 년 슈페만은 핵이식의 가능성 울 암시하였는데 16 년 후에 브리그스와 킹은 직접 핵이식에 성공하였 다. 만약 분화된 세포의 핵이 아직도 전능성을 가지고 있는 수정란의
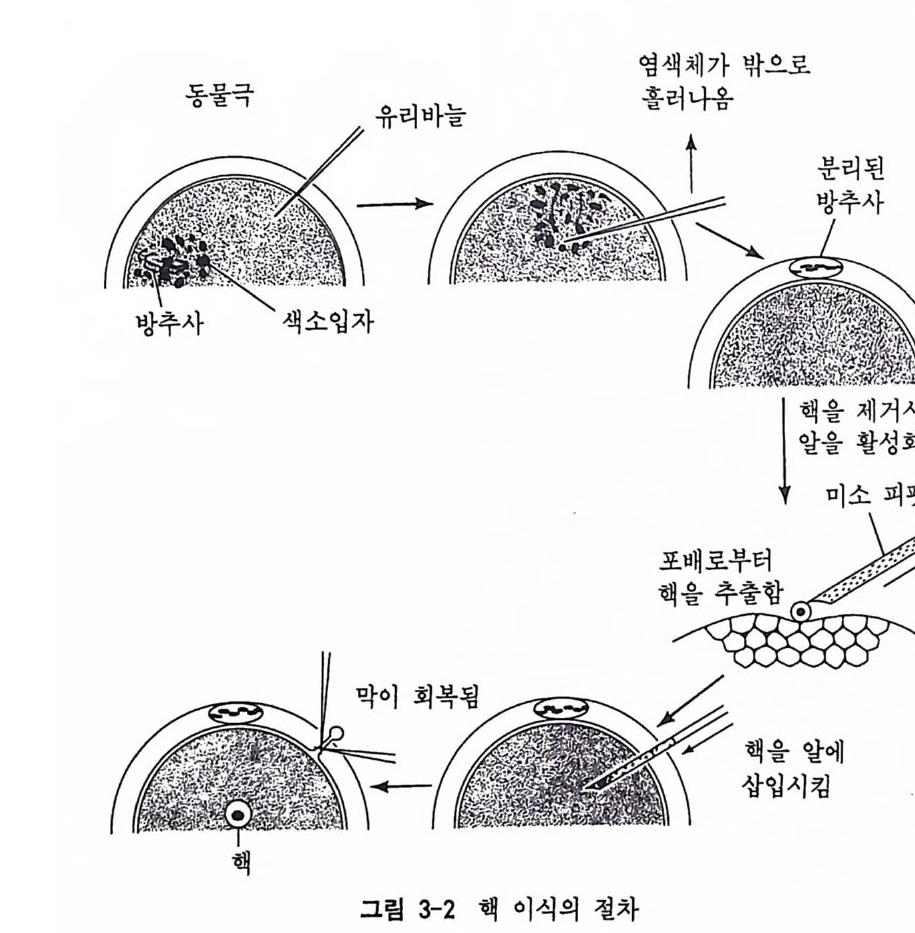
핵과 발생학적으로 다름이 없다면 유전적인 조성이 발생과정을 통해 계속 유지된다는 접을 확인할 수 있을 것이라고 기대하였다. 핵이식 과정은 크게 세 단계로 이루어지는데 첫째는 수정란의 핵을 제거시키는 것 (enuclea ti on) 이고, 둘째는 분화된 세포로 부터 핵을 뽑 아내는 것이고, 세째는 그 핵을 수정란 속에 넣어주는 것이다. 브리 그스와 킹은 개구리 의 일종인 Rana pipi ens 의 미수정 란을 유리바늘 로 찔러중으로써 단순히 단성 생식법으로 활성화시켜 수정과 관계되 는 모든 세포학적 및 생화학적 변화를 유발시킬 수 있었다. 즉 표충 립반응, 세포질 이동 및 감수분열 등을 확인할 수 있었다. 특히 감수
 염색체가 밖으 로
염색체가 밖으 로

그림 3-3 핵을 제거시킨 난자에 포배의 핵을 이식시켜 얻은 개구리 성체 (Rana pipiens )
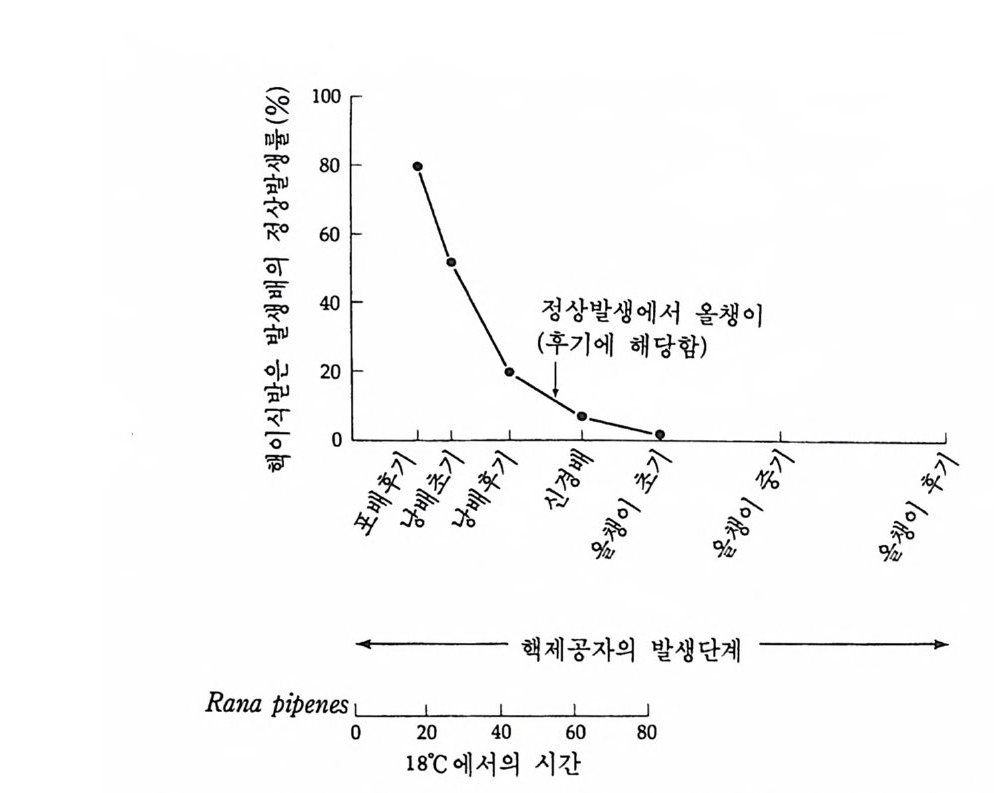
분열이 동물극 쪽에서 일어나는데 가느다란 유리바늘로 이 부위를 찔 러서 방추사와 염색체를 알 밖으로 빼낼 수 있었다. 이와 같은 알은 비록 발생학적으로 활성화되었으나 핵을 상실한 상태에 처하게 된다. 핵 기증 세포에 미소 피펫(mi cro pip e t)을 찔러 핵을 피펠 속에 담은 다음 피펠을 미리 준비된 수령세포 속으로 찔러서 핵을 옮겨 준다. 물론 이때 얼마의 세포질이 핵과 함께 들어가지만 거의 무시할 정도 의 소량으로 수령세포의 세포질의 10-s 정도에 지나지 않는다. 이러한 방법으로 브리그스와 킹은 포배 세포의 핵을 이식시켰는데 이 방법으로 완전한 올챙이가 형성됨을 관찰하였다. 포배의 세포는 아직 그 운명이 결정되지 않은 것으로 다능성 (多能性, p lu rip o t enc y)을 가지고 있기 때문에 정상적으로 발생할 수 있다고 슈페만이 예견한 바와 같이 핵을 이식받은 알의 60% 가량이 완전한 올챙이로 발생하 였다. 그러나 포배기의 핵을 이식한 실험결과와는 달리 좀더 발생이 진행 한 내배엽 세포의 핵을 이식하였을 경우에는 정상적인 올챙이의 발생 률이 엄청나게 떨어지는 현상을 볼 수 있었다. 이러한 현상은 발생이 더 진행된 세포 죽 좀더 분화된 세포의 핵을 이식하였을 경우 더 십 각하게 나타났다. 올챙이의 체세포의 핵을 이식하였을 경우에는 전혀 정상적인 발생이 일어나지 않았다. 단지 올챙이의 생식세포의 핵만은 발생한 포배의 40% 한도에서 정상적인 발생을 유발하였다. 이와 같
 (1008060
(1008060
그림 3-4 핵 기증자의 발생단계에 따른 핵 이식이 정상발생율에 미치는 효과 (McK innel l, 1978) .
이 발생이 진행되면서 핵의 발생능이 점차 제한되는 현상을 볼 수 있 는데, 이는 핵 조성에 변화가 있기 때문이 아니고, 유전자 조성에 동 질성은 유지되나, 아마도 염색질의 상태에 변화가 일어났기 때문인 것으로 생각되고 있다. 죽 염색질의 응축으로 인해 DNA 의 복제가 일어나기 어렵게 되기 때문인 것으로 보고 있다. 언제나 DNA 의 복 제가 일어나기 위해서는 염색질의 풀림 (decondensa ti on) 이 먼저 일어 나야한다. 발생이 진행됨에 따라 핵의 발생능이 감소하는 현상은 비가역적이 며 조직에 따라 특칭적으로 나타난다. 이러한 현상은 대를 거듭하여 연속적으로 핵을 이식시켜봄으로써 알 수 있는데, 이렇게 핵의 발생
 [[
[[
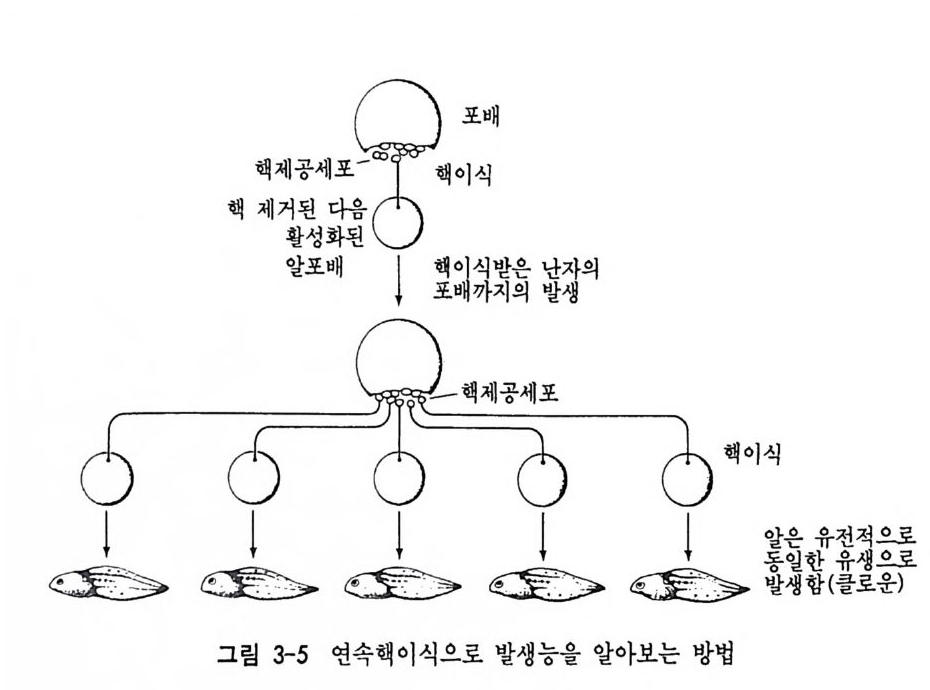
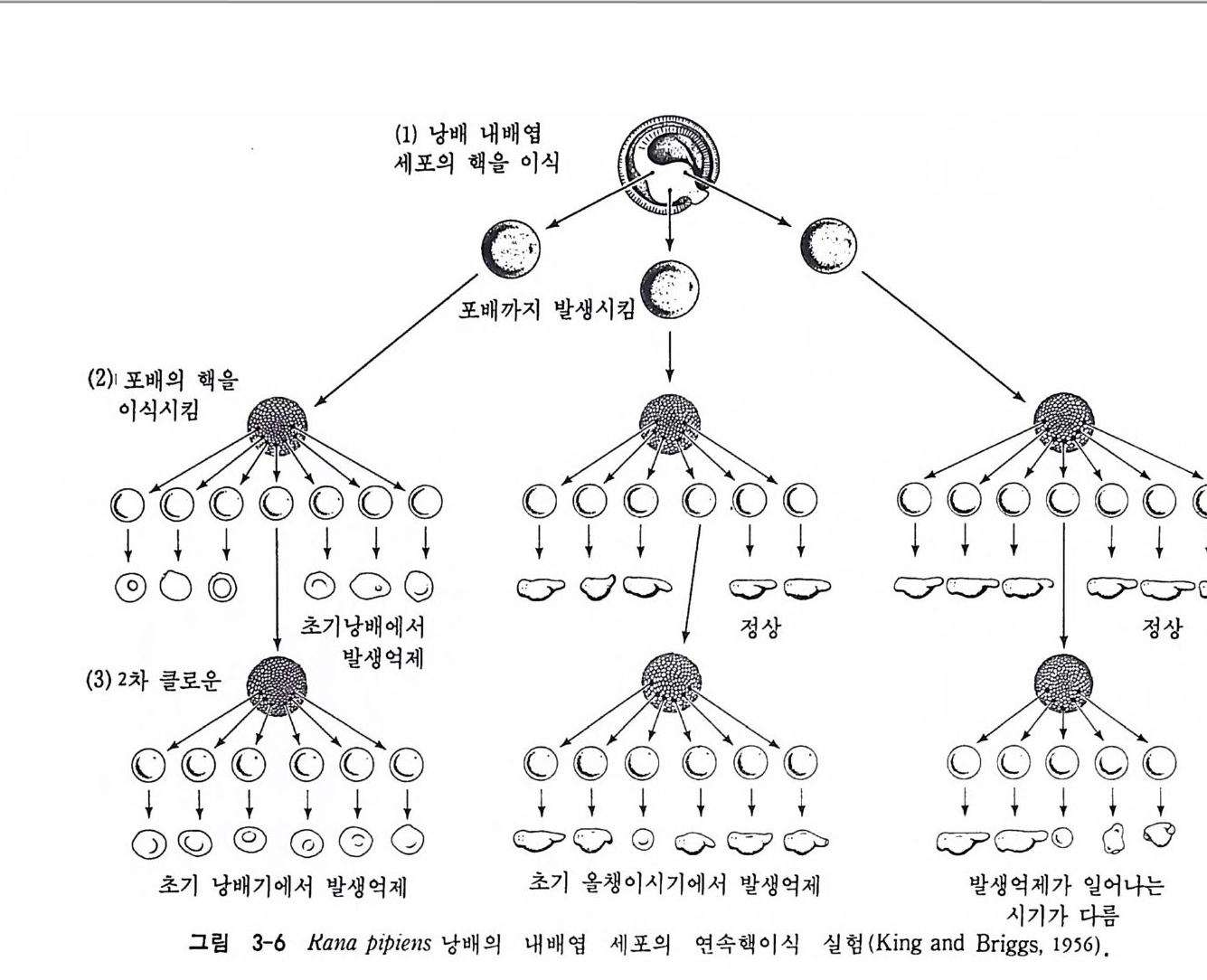
능을 평 가하는 방법 을 핵 클로운닝 (nuclear clon ing ) 이 라고 한다. 우 선 낭배 후기의 발생배로부터 내배영 세포의 핵을 취하여 핵이 없는 활성화된 알에 이식하여 준다. 다음 이 알이 발생하여 포배기에 도달 하면 다시 이 포배로부터 핵을 취하여 새로운 알에 이식시켜 준다. 이 러 한 대 를 거 듭한 연속핵 이 석 (seri al tran spl a nta t i on ) 을 반복하여 여 러 대에 걸쳐 수행할 수 있다• 연속핵이식을 시작하기 전 처음 이식 하였을 때에는 핵에 따라 발생되는 정도가 폭넓게 나타난다. 죽 어떤 핵은 올챙이의 단계에 이르기까지 발생시키는가 하면 어떤 핵은 단지 낭배기 정도까지만 발생한다. 처음 이식한 핵에 의해서 발생한 세포 의 모임을 클로운 (clone) 이라고 할 수 있는데, 비록 내배영 세포의 핵으로부터 얻은 클로운들 사이에서는 발생정도의 차이가 나타났지 만, 하나의 클로운내에서는 거의 차이가 보이지 않았다(그림 3-6). 대 부분의 경우 내배영 세포의 핵을 일단 클로운닝시킨 다음 다시 핵을 이식시켜 얻은 발생배가 발생할 수 있는 정도는 유사하다. 이러한 현
 0 : Kn(i
0 : Kn(i
상은 여러 대를 거듭하여 핵을 이식하여 발생시켜볼지라도 똑같이 나 타난다. 죽 연속핵이식에서 일단 비정상적인 발생배로 발생되면, 그 발생배로부터 핵을 취하여 이식해 줄지라도 계속 이상형의 발생배가 나타난다는 것이다. 따라서 내배영 세포의 핵으로부터 시작한 연속핵 이식에서는 올챙이가 주로 내배영성 구조로 이루어져 있고 중배염과 의배영성 구조는 결여되어 있다. 디버라르디노 (D iB erar di no) 와 킹 (1967) 은 외배영 세포의 핵으로 시작한 연속핵이식에서도 유사하게 발생능이 상실되는 현상을 관찰하였다. 죽 의배영 세포의 핵으로 클 로운닝한 올챙이에서는 내배영성 구조가 결여되는 반면 의배엽성 기 관인 신경계는 월등하게 분화된다. 발생이 진행함에 따라 핵의 발생 능에 제한성이 점진적으로 종가하는 것이 통례아다. 거든 (Gurdon) 은 브리그스와 킹의 것과는 다소 다른 방법으로 핵이 식을 시도하였다. 분화된 세포의 핵에 발생능이 제한적으로 형성되는 이유는 염색질의 응축에 있다. DNA 복제가 일어나기 위해서는 반드 시 염색질이 응축의 상태에서 풀려나와야만 하는데, 난할기에 세포분 열의 빠른 속도에 병행하여 염색질이 응축상태에서 풀려나지 못하기 때문에 염색체 절단 (chromosome breaka g e) 으로 인한 염색체 이상이 유발된다. 사실상 핵클로운닝으로 얻은 올챙이의 세포에서 염색체 이 상을 흔히 찾아볼 수 있다. 그러나 거든이 제한된 발생능을 회복시킬 수 있다고 생각한 근거는 그가 사용한 동물재료에 있는 것으로 평가 되고 있다. 거든이 사용한 재료는 남아프리카 종인 Xenopu s laevis 였다. Xenop us 는 Rana 와는 다른 양서류로서 눈까풀, 고막, 및 혀를 가지고 있지 않다. Xenop us 는 발생학적으로도 Rana 와는 다른 특칭 울 가지고 있다. Xenop us 에서는 사지의 재생력이 강하고 초기발생의 속도가 Rana 에 비해 3 배만큼 빠르다. Rana pipi ens 에서는 올챙이시 기까지 발생하는 데 80 시간이나 걸리는 데 비해 Xen op us 에서는 갇은 시기까지 단지 26 시간밖에는 걸리지 않는다. 따라서 Xenopu s 올챙이 의 내배영 세포 핵은 마치 Rana 의 낭배초기의 것과 상태가 비슷하다 (McK inn ell, 1978) .
 100
100
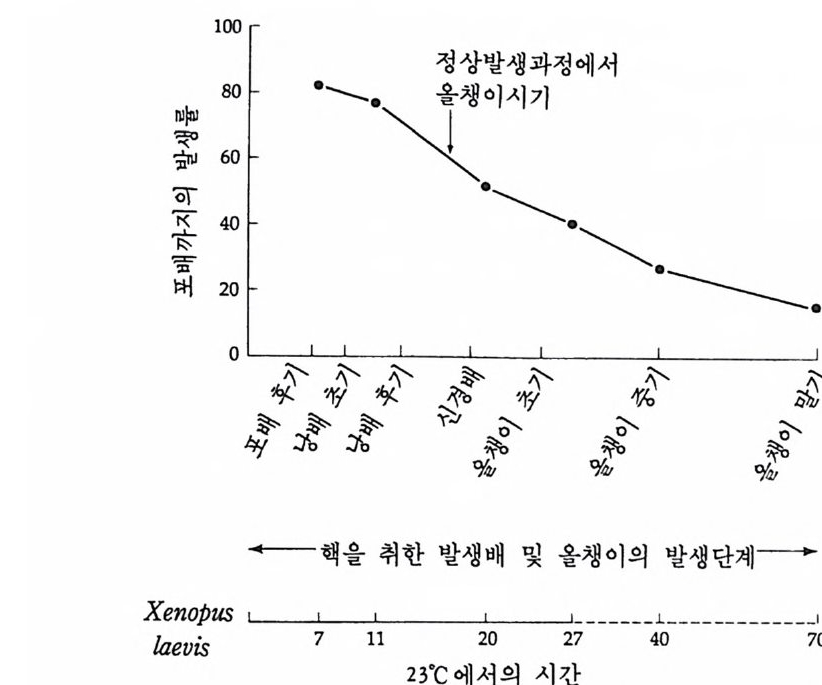
그림 3-7 Xenop us Laev is의 발생단계에 따라 핵이식으로 성공한 발생률 (Mck inn el, 1978).
또한 Xen opus 의 경우에도 속도는 Rana 의 것보다 느리지만 발생에 따라 발생능이 점진적으로 상실되는 현상을 거든 자신이 관찰하였다. 그러나 장 내배 영 세포(int es tin al endoderm) 의 핵으로 클로운닝시 켰을 경우에만 예의가 나타났다. 장내 배영 세포의 핵을 핵이 제거된 Xen oj)us알에 이식시켰다. 이때 거든은 기증세포와 수령세포를 구별 하기 위하여 기증세포를 유전적으로 표시하였다• 즉 인이 한 개만 둘 어있는 돌연변이 종을 기증자로 사용하였다. 726 회의 이식실험에서 올챙이 시기까지 발생한 경우는 10 회였다. 그리고 연속핵이식을 통하 여 올챙이까지의 발생율을 7% 가량 증가시킬 수 있었다 (Gurdon, 1962). 어떤 경우에는 장 내배영 세포의 핵을 이식시킴으로써 신경세 포 및 혈구를 포함하는 거의 모든 세포가 올챙이에서 형성되었다. 그
 미。수정란 (2 - nu) <혼올챙노이 (I 二-nu) 춧
미。수정란 (2 - nu) <혼올챙노이 (I 二-nu) 춧
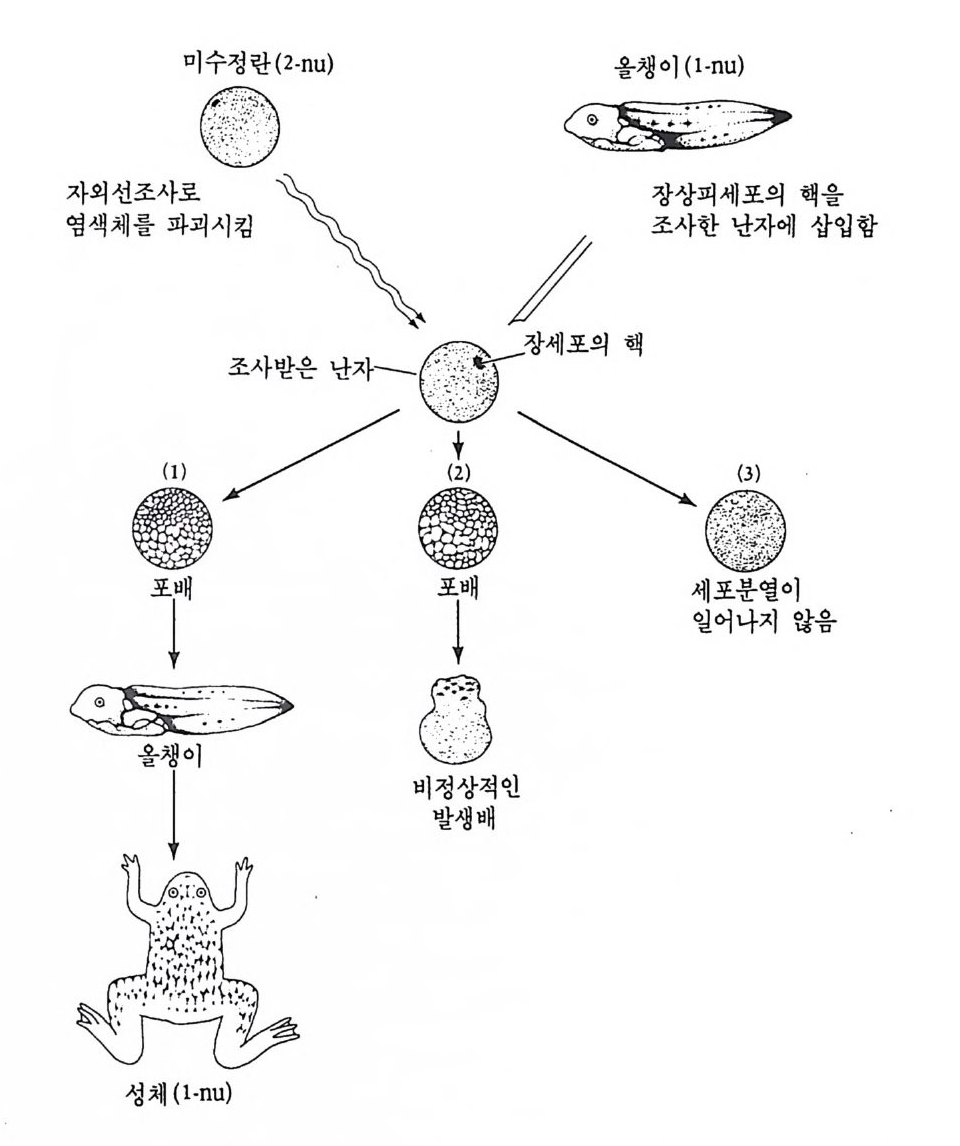
그림 3-8 l(eno p u s 올챙이의 장 세포의 핵을 이식하여 개구리 성체를 발생시키 고저 사용한 방법. 두 개의 인을 가진 야생종의 알을 자의선으로 조사하여 모계 염색체를 파괴시킨 다음, 1 개의 인을 가진 올챙이의 장 세포로부터 핵 울 이식함.
리고 이들 중 생식이 가능한 성체로까지 발생한 경우가 7 번이나 있었 다고 보고하였다 (Gurdon and Dehli ng e r , 1966). 죽 이러한 장 내배영 세포의 핵은 전능성을 보존한다고 주장하였다. 그러나 킹은 거든의 실험을 다음과 같은 점에서 비판하였다. 죽 첫 째는 원시 생식세포의 핵이 이식실험에 사 용되지 않도록 충분한 주의 를 기울이지 않았다는 것이다. 원시 생식세포는 이동하는 도중 장에 머무를 수 있으며, 생식세포의 핵은 다른 분화된 세포의 핵과는 달리 전능성을 유지하고 있다. 둘째는 올챙이의 장 내배영 세포는 아직도 완전히 분화된 세포로 볼 수 없다는 것이다. 즉, 이 시기의 세포 들 에 는 아직도 난황립 이 들어 있다(Di Berard i no and Kin g , 1967 : McKi nn ell, 1978 ; Brigg s, 1979) . 이러한 바판을 극복하기 위하여 거든은 개구리 성체의 발에 있는 물갈퀴의 상피세포로부터 핵을 얻어 핵을 제거시킨 알에 이식시켰다. 이들 상피세포는 성체 표피 세포의 특징인 케라틴을 합성하는 것으로 보아 분화된 세포로 생각되었다. 그러나 이러한 실험결과는 거든의 생각을 적국적으로 뒷받침해 주지는 못했다. 제 1 대의 이식에서는 신경배 이상 발생하지 못했고, 연속핵이식 실험에서도 울챙이 시기까 지 발생한 경우가 있기는 하였으나 먹이 섭취 시기에 이르기 전에 발 생배 모두가 죽었다 (Gurdone t a l. ,1975). 이러한 발생억제는 (develop m enta l arrest) 림 프구 핵 {lymph ocy te nucleus) 을 사용한 이 식 실험에서도 유사하게 나타났다 (Wabl et al., 1975). 이러한 핵 클로운 닝 실험에서 두 가지 점을 인식할 수 있다. 첫째는 발생진행에 병행 하는 발생능의 점진적인 상실이다. 이러한 발생능의 제한도 유전적으 로 결정되는 것으로 모든 기증 세포의 핵의 특징이다. 둘째로는 비록 분화된 세포에서일지라도 유전자 조성 자체로 보아서는 올챙이의 모 든 세포를 생성할 수 있는 발생능을 소유하고 있다고 할 수 있다. 분 화된 세포의 핵이 전능성을 상실하였지만 이들 핵이 다능성을 유지하 고 있는 것만은 틀림없다. 따라서 표피나 림프세포에서 사용되지 않
 __ .. . -7 ··:- z
__ .. . -7 ··:- z
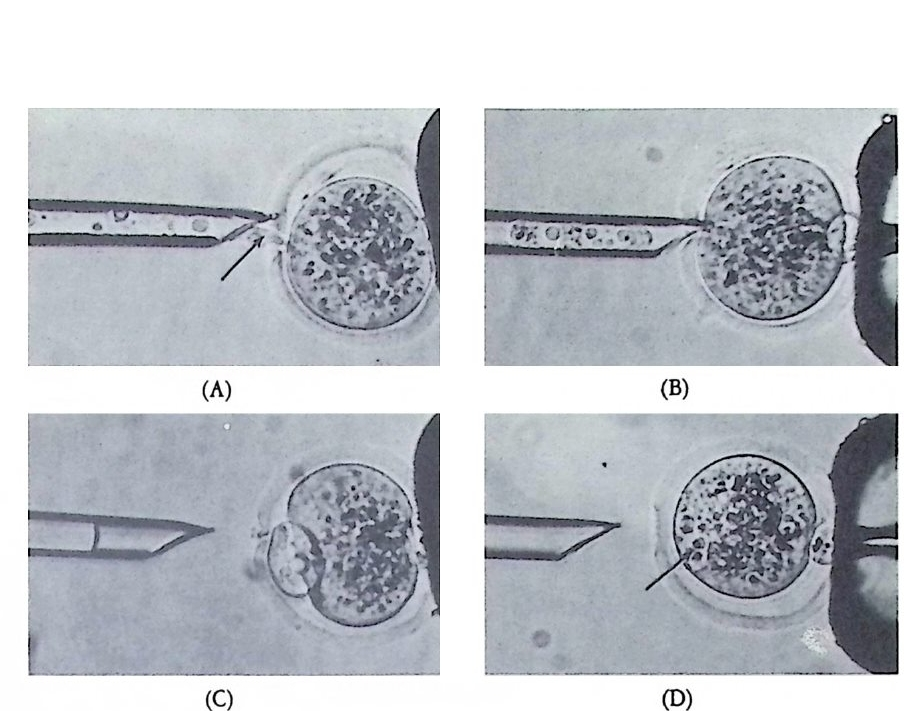
그립 3-9 포유류 알 속으로의 핵 이식 절차. colcem i d 와 cyt oc halasin B 로 세 포분열을 억제시킨 알을 피펫에 홉인력을 이용하여 고정시킨 다음, 끝이 날 카로운 미소 유리 피펫울 알 속에 삽입시켜 핵을 제거시킨다 (A). 다른 세 포에서 얻은 막으로 둘러싸안 핵과 Sendai vi rus 를 함께 zona pe lluc i da 와 핵을 제거시킨 알사이에 넣어주면 (B, C) 전핵과 알이 융합되어 전핵이 알 속으로 전입하게 된다 (D). 화살표는 알 속에 들어간 전핵을 지시한다. (McGrath and Solte r , 1983) .
은 유전자가 재활성화만 된다면 신경계, 위, 심장 등의 세포를 생성 할 수 있는 참재력을 소유하고 있다는 가능성을 배제할 수 없다. 바 록 분화된 세포에서일지라도 유전적인 발생능(g ene tic p o te nc y)에는 세포의 종류를 막론하고 동일한 것으로 인정되고 있다. 그러나 발생 학적 발생능 (develo p men t al p o t enc y)은 발생단계에 따라 제한된다. 즉 분화의 원인은 순차적인 유전자의 상실에 있지 않고 비록 유전자 조 성으로는 동일할지라도 적절한 조건 하에서의 선택적인 유전자 발현 에 있기 때문이다.
 (2) 운명 전환(tr ansde t erm i na ti on)
(2) 운명 전환(tr ansde t erm i na ti on)
 입
입
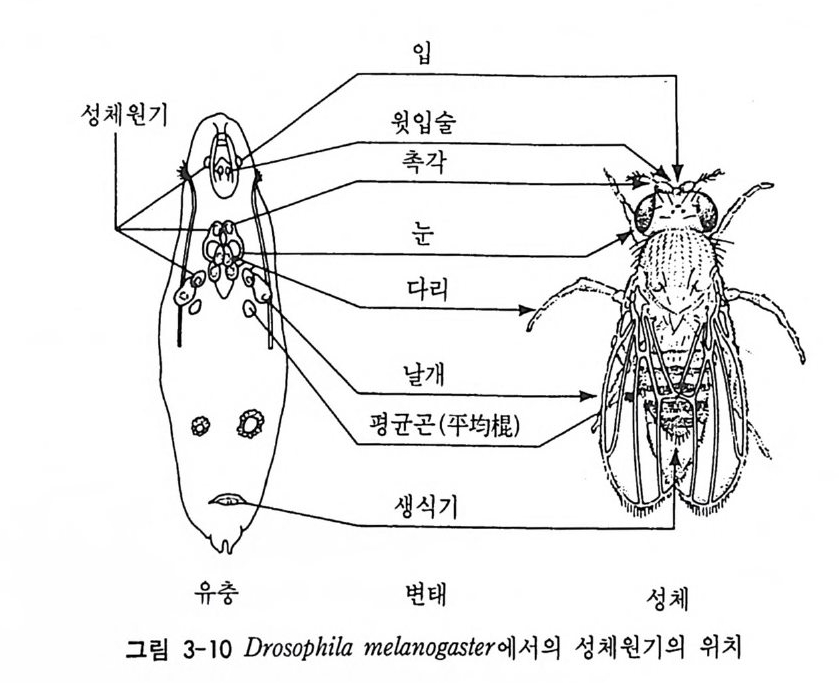
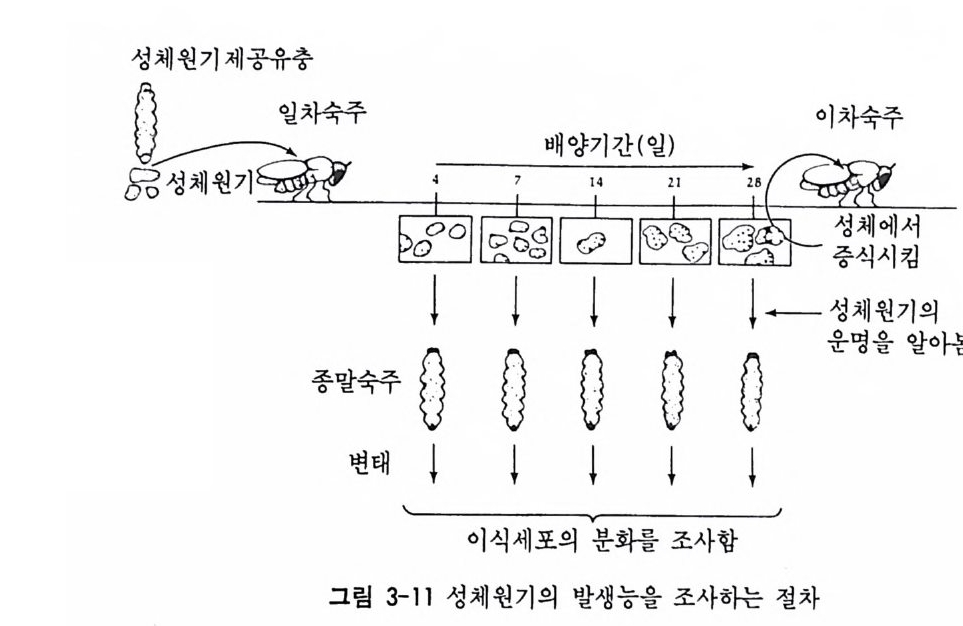
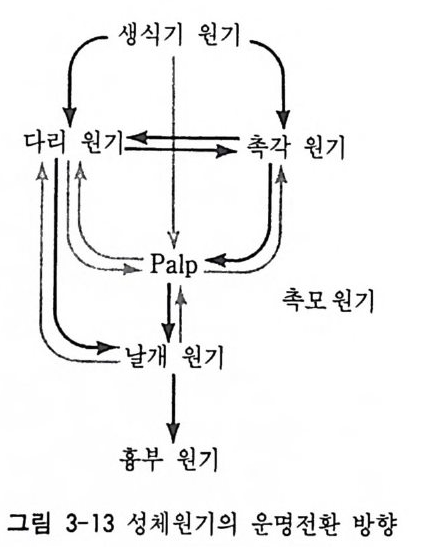
呼 (Radom , 1968) 은 이러한 성체 원기를 이용하여 세포의 운명이 바뀔 수 있는지에 대하여 알아보았다. 일반적으로 정해전 운명은 몇 대에 걸친 연속 이식에서도 변하지 않고 유지되었다. 죽 촉수 성체 원기를 성체의 복부에서 대를 거듭하여 배양하면서 성체 원기 세포를 변태중에 있는 유충에 이식시켰을 때마다 계속 촉수가 형성되었다. 그러나 아주 드물게 일어나지만 촉수 성체 원기로부터 다리, 입, 혹 은 날개가 형성되는 경우가 있다. 이러한 현상을 운명전환 (tra nsdete r m ina ti on ) 이 라고 한다. 본래 정 해 전 운명 으로서 의 기 관을 형성하는 대신에 다른 기관을 형성한다. 일단 운명 전환이 일어나면, 그 운명 전환의 상태는 안정적이다. 즉 여러 대에 걸친 세포분열에서 도 계속 전환된 운명이 그대로 유지된다. 여러 종류의 성체 원기를 가지고 실험을 거듭한 결과 운명전환이 일어나는 데에는 어느 정도 방향성이 있음을 알게 되었다. 죽 날개성 체원기는 흉부구조로 그 운명이 전환될 수 있다. 그러나 흉부 성체
 성체원기제공유충
성체원기제공유충
 :빼
:빼
그립 3-12 촉각과 다리사이의 운명전환. (A) 촉각 성체 원기를 이식하여 나타 난 운명전환. 정상적인 촉각구조 (Am, Ar) 부절강모(附節剛毛, tar sal brist le , Ta) 와 같은 다리 구조도 함께 나타남. (B) ante n nape d ia 돌연변 이를 일으킨 성체의 머리. 이러한 돌연변이종에서는 촉각이 정상적인 다리 로 전환되어 있다. 이러한 돌연변이를 homeoti c mu t a ti on 이라고 하는데, 물 론 운명전환과 homeoti c mu tati on 은 다르지만 이들은 모두 성체 원기에서 의 운명 전환의 가능성을 보여주는 것이다 (Ge hri n g, 1969).
 흉부i 원기
흉부i 원기
원기가 날개로 전환되는 경우는 지금까지 관찰되지 않았다. 생식기관 성체 원기 (ge nit al d i sc) 는 촉수나 다리로 그 운명이 전환될 수 있으나 어떤 종류의 성체 원기도 생식기관으로 전환되는 경우는 찾아볼 수 없다. 아직 운명전환의 원인에 대해서는 별로 아는 바가 없으나, 운 명전환 현상을 통해 알 수 있는 사실은 비록 운명이 결정된 세포도 정해진 운명 이의의 다른 운명으로 분화될 수 있는 유전자를 내포하 고 있다는 점이다. 즉 유전적인 발생능은 어떤 종류의 세포에서나 동 일하나 발생학적인 발생능은 일단 운명이 결정되면 그 결정된 범위를 능가하지 못한다. 그러나 일단 운명전환이 일어나면 제한되었던 유전 적 발생능에 변화가 일어난다. 죽 운명전환 현상도 유전자 동질성에 대한 증거이다. (3) 유전자 동질성에 대한 분자생물학적 증거 핵이식에서 나타나는 현상과 운명전환 현상을 통하여 유전자 동질 성을 생물학적인 견지에서 살펴보았다. 그러면 유전자 동질성은 생화
학적으로도 증명될 수 있는 현상인가? 발생생물학자들은 분자생물학 적 인 방법 죽 핵 산 재 결 합법 (nucleic aci d hyb rid i z a ti on or renatu r ati on ) 과 유전자 클로운닝법 두 가지 방법으로 아 문제를 살펴보았다. 핵산 재결합법은 DNA 와 RNA 혹은 DNA 와 DNA 를 상보성 (com p lemen t ar ity)에 따라 결합시킴으로써 핵산 배열순서가 DNA 와 RNA 사이 혹은 DNA 와 DNA 사이에 동일한지를 검출할 수 있는 방법이 다. 우선 DNA 를 일정한 길이로 그러나 짧게 자론 다음 변성 (dena tu ra ti on) 시킨다. 이때 변성이란 이중나선 (double s tr and) 을 단일 나선 (s i n g le s t rand) 으로 풀어내는 과정인데, 이중나선의 DNA 를 알칼 리로 처리하거나 끓이면 DNA 는 변성된다. 짧게 잘렸고 변성된 DNA 를 일정한 조건(온도와 이온의 농도)에 노출시키면 단일 나선의 DNA 조각은 서로 상보적인 짝을 찾아 결합하게 된다. 또한 변성된 DNA 에 RNA 를 주면 시간이 지남에 따라 RNA 는 자신이 전사되어
 5' l; l;m:니 RNtA :급: 분AA리A한0다 3 '
5' l; l;m:니 RNtA :급: 분AA리A한0다 3 '
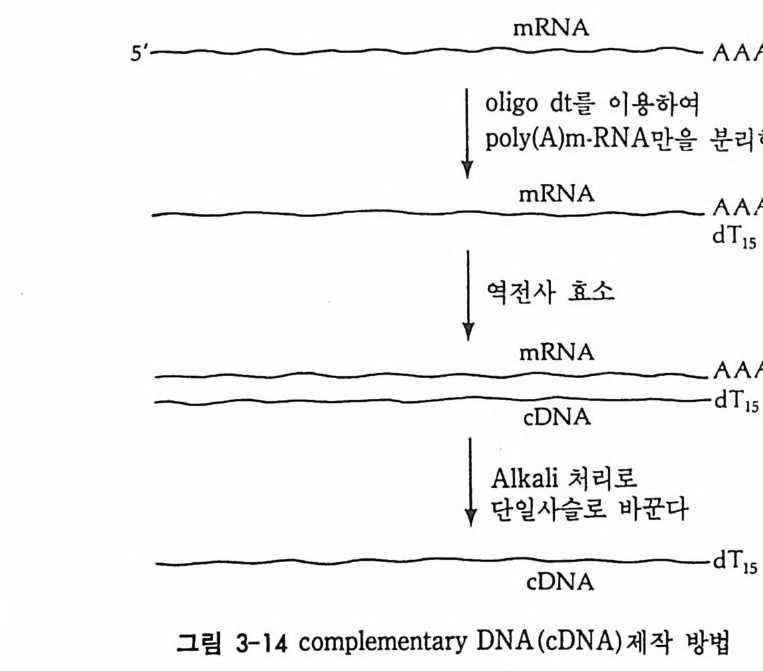
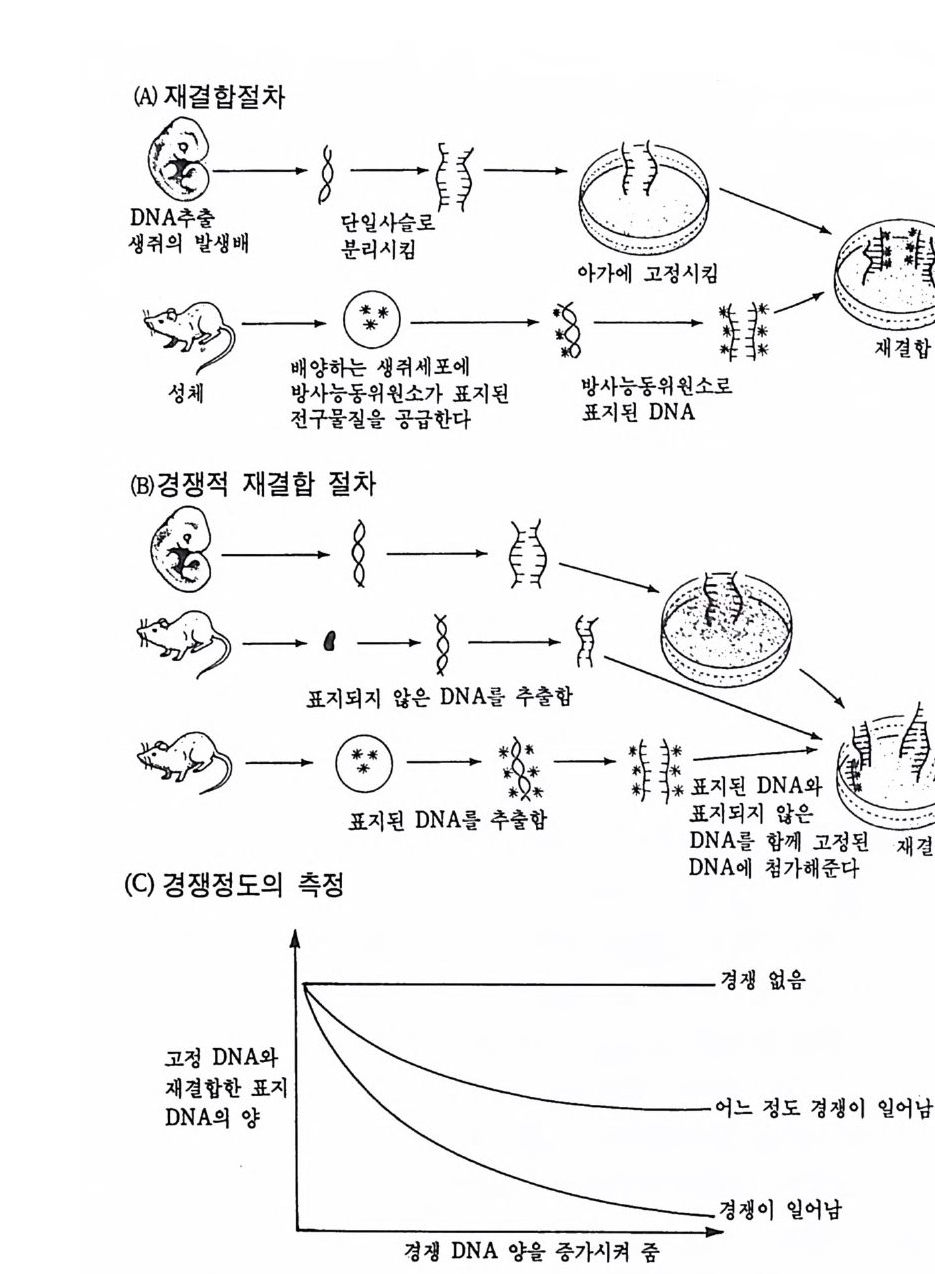
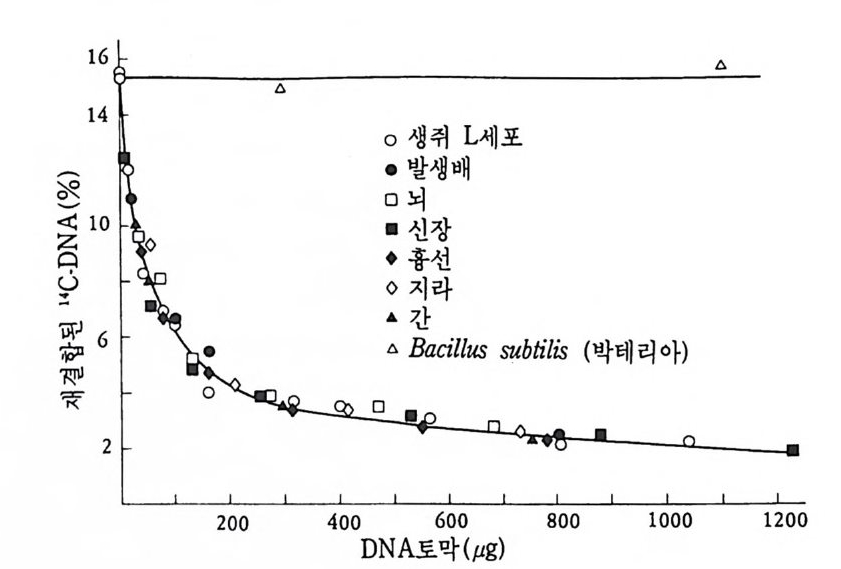
나온 DNA 부위와 결합하게 된다. RNA 와 DNA 간의 결합반응에서 흔히 RNA 의 양적 부족으로 인해 반응자체를 수행시키기 힘든 경우 가 있다. 그러한 경우에는 mRNA 를 분리하여 mRNA 로부터 comp le menta r y DNA(cDNA) 를 시험관에서 인위적으로 합성하여 RNA 와 DNA 간의 결합반응을 수행 함으로써 RNA 와 DNA 간의 관계 를 알아낸다. RNA 로부터 cDNA 를 합성하는 데에는 역전사효소를 사용한다. 핵산 재결합법을 이용하여 모든 세포가 수정란과 동일한 유전자 조 성을 소유하고 있다는 점을 보여줄 수 있었다. 가장 처음으로 시도된 예는 생쥐의 여러 종류의 조직에서 DNA 는 동일하다는 점을 핵산재 결합법으로 보여준 것이다 (McCa rthy and Hoy er , 1964). 우선 생쥐의 DNA 를 짧게 짜르고 변성시켜 아가 (a g ar) 접시에 고정시킨 다음 여 기에 방사능 물질로 표지한 동일한 생쥐의 DNA 를 노출시키면 고정 된 DNA 와 표지된 DNA 사이에 상보적인 결합반응이 일어난다. 결 합되지 않은 표지 DNA 를 씻어서 제거시킨 다음. 고정된 DNA 와 결 합된 표지 DNA 를 측정함으로써 결합 정도를 알아낸다. 이때 표지 DNA 의 양을 점차 증가시켜 주면 고정된 DNA 를 전부 결합시킬 수 있는 포화상태에 이른다. 이러한 반응에 여러 조직에서 추출한 DNA 를 짧게 짜르고 변성시켜 양을 조금씩 늘려가면서 넣어 준다. 만약 조직에서 추출한 DNA 와 표지 DNA의 염기 배열순서가 동일하면 표 지 DNA 와 고정 DNA 간의 결합반응이 경쟁적으로 억제된다. 이때 여 러 조직에서 추출한 DNA 가 모두 갇은 정도로 표지 DNA 와 경쟁한 다면 이돌 DNA 는 모두가 동일한 염기배열순서를 가졌다고 할 수 있 다. 사실상 생쥐의 조직이 어느 것이든지 상관없이 이들 조직으로부 터 추출한 DNA 는 동일한 정도로 표지 DNA 의 결합을 억제시킨다. 그러나 박테리아의 DNA 는 비록 그 양을 증가시키면서 반응시킬지라 도 생쥐의 표지 DNA 와 경쟁하지 못한다. 이것은 비상보적 DNA 간 의 결합반응은 일어나지 않기 때문이다. 그러나 한천을 이용한
 昌囚广재:결합절\차 :三로《 1 一 :ui 广;\;] 威\학
昌囚广재:결합절\차 :三로《 1 一 :ui 广;\;] 威\학
그림 3-15 DNA 재결합 방법울 이용하여 DNA 염기 서열을 확인하는 방 법. (A) 고정된 DNA 에 표지 DNA 를 결합시키는 절차. (B) 경쟁적 재결 합 절차. 표지되지 않은 DNA 를 경쟁자로 이용하여 재결합을 측정한다. (C) 경쟁적 재결합법을 이용하여 얻을 수 있는 결과.
 1614
1614
그림 3-16 경쟁적 재결합 실험 결과. 여러 종류의 기관에서 추출한 DNA 를 경 쟁자로 이용하여 고정 DNA 와 표지 DNA 사이의 결합을 억제시켰다 (McCarth y and Hoy er , 1964)
DNA- DN A 재결합반응에서는 단백질의 아미노산 배열순서의 결정을 직접 지시하지 않는 리보솜 RNA 와 같은 RNA 를 전사하는 반복성 유전자 (re pea t ed g enes) 의 결합만이 반영되며, 사실상 단백질의 아미 노산 배열순서를 지시하는 유일성 유전자(uniq ue g enes) 의 결합은 반 영되지 않는다. 유전자 동질성은 파두 (Pardue) 와 골 (Gall, 1970) 에 의해서 개발된 in sit u 재결합법에 의해서 확인되었다. in sit u 재결합법은 영색체 전체 룰 술라이드 위에 울려놓고 가열하거나 알칼리를 처리하여 단일 사슬 로 변성시킨 다음, 특정된 단백질에 대한 mRNA 나 cDNA 를 염색체 상 상보적 부위에 결합시키는 것이다 . 이때 mRNA 나 cDNA 를 미리 방사능 동위원소로 표지하여 사용하면, 상보적 DNA 부위에 결합시킨 다음 자기방사법 (au t ora di o gr a p h y)으로 그 부위를 확인할 수 있다. 자기방사법이란 방사능동위원소로 표지된 RNA 나 DNA 가 결합한 다
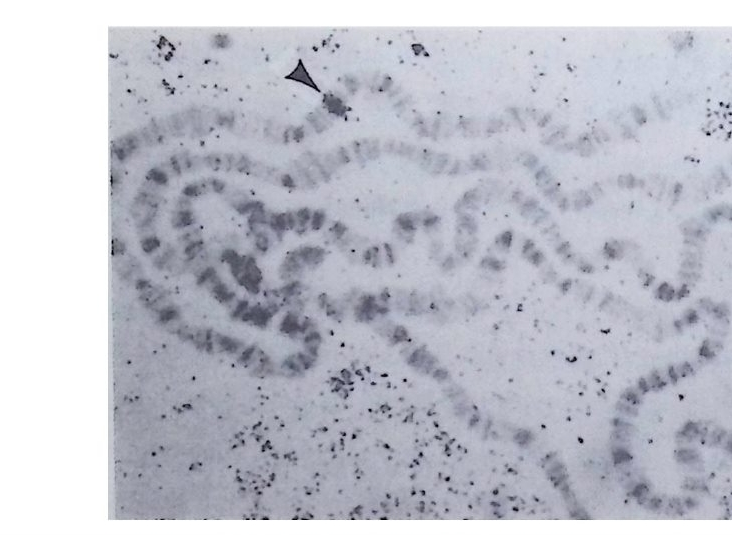
음 방출하는 방사능에 대해 예민하게 반응하는 사진 emuls i on 에 감 광시킴으로써 결합한 부위를 정확하게 알아내는 방법이다. 이러한 방법을 이용하여 초파리의 난소 조직에서만 만들어지는 난 황 단백질에 대한 DNA 위치를 비난소 조직에서도 확인할 수 있었다. 우선 초파리의 DNA 를 제한효소로 끊어서 유전자 재조합법으로 클로 운시킨 다음 난황 단백질 mRNA 와 결합시켜 . 보면 여러 종류의 DNA 가 난황단백질 mRNA 와 결합하는 사실을 알 수 있다. 이러한 클로운만을 골라서 방사능 동위원소로 표지시킨 다음 초파리의 침샘 의 다사염색체와 in sit u 재결합시켰다. 원래 난황단백질은 난소에서 만 만들어지고 침샘에서는 합성되는 것이 아니지만 , 침샘에서도 이와 같이 in situ 재결합법으로 난황 단백질 유전자의 존재를 확인할 수 있었다. 비록 침샘에서는 난황 단백질 유전자가 발현하지는 않지만 그 유전자가 포함되어 있다는 것은 유전자 동질성을 시사하는 것이다 .
 .
.
그립 3-17 Drosop h ila 유충 침샘의 다사영색체에 대한 난황단백질 cDNA 의 in s itu재결합. 머리화살표가 cDNA 가 결합한 부위를 지시한다 (Branett et al., 19so) .
 一 r .L'• •\ 下·· k ; ' '- —戶
一 r .L'• •\ 下·· k ; ' '- —戶
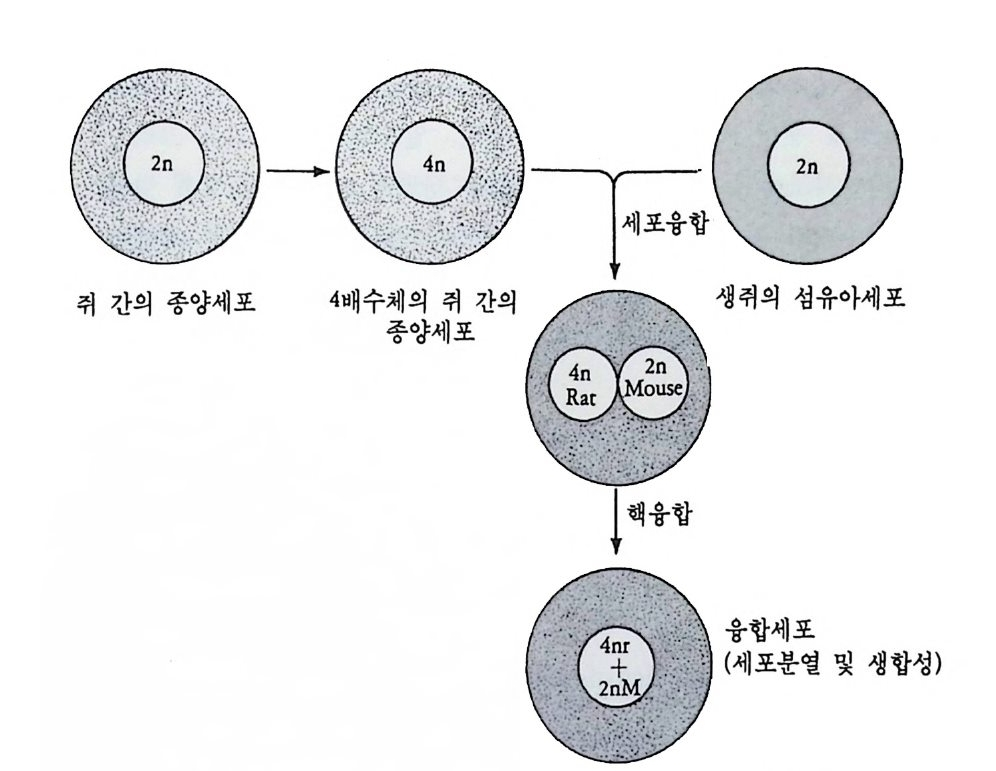
그립 3-18 체세포 융합으로 불활성화된 유전자를 활성화시킴. 쥐의 4 배수성 간 종양세포와 생쥐의 이배수성 섭유적아세포를 융합하면, 융합 세포에서 생쥐 의 간 특이 유전자가 발현된다.
유전자 동질성을 보여주는 또 다른 방법은 세포 융합 (cell fus ion ) 이 다. 분화된 세포에서 지금까지 전혀 발현되지 않았던 유전자가 세포 융합으로 새로운 조건이 주어질 경우 새롭게 발현될 수 있다. 세포융 합은 Sendai vi rus 나 pol ye t h yle ne g l y col 을 매 개로 가능한데 , 세포융 합을 시키면 두 개의 핵은 공통적이며, 새로운 세포질 환경에 접하게 된다. 적절한 조건 하에서 두 개의 핵이 합쳐져서 한 개의 잡종핵이 형성되면서 세포분열에 들어간다. 이러한 경우 잡종세포는 모세포의 특칭을 상실한다. 바이스 (We i ss) 는 쥐의 종양세포와 생쥐의 섬유적아 세포를 융합하여 4n 에 해당하는 간의 염색체와 2n 의 생쥐의 염색체 를 가지는 잡종세포를 만들었다. 이러한 잡종세포에서는 알부민, 알
도라제, 티로신 아미노 트랜스퍼라제 (TAT) 와 같은 쥐 간세포의 특 이 단백질 뿐만 아니라. 생쥐의 알부민, 알도라제 및 TAT 그리고 섬유적아세포에서 합성되지 않던 새로운 단백질 세 종류도 함께 합성 되었다. 이와 같이 생쥐의 섬유적아세포는 간 특이 유전자를 적철한 조건에 따라 발현할 수 있다. 죽, 세포분화는 일어날지라도 비가역적 인 유전적 변화는 일어나지 않으며, 모든 유전자는 보존된다. 참고문헌 Brigg s, R . (1979) . Geneti cs of c ell type dete r mi na ti on . Int. R ev. Cyt ol. [Su p pl.]9 : 101-121. DiB e rardi no , M.A. and Kin g , T.J . (1967) . Develop m ent and cellular dif fere nti at i on of neural nuclear tra nspl a nts of known karyo t y pe s. Dev. Bio l. 15: 102-128. Gehrin g , W.J. (1969) . Problems of cell diff ere nti at i on in Drosop hi la . In E.W . Hanley (ed.) , Problems in Bio lo gy : RNA in Develop m ent. Un ive rsity of Ut ah Press, Salt L ake Cit y, pp. 231: 244. Gurdon, J.B . (1962) . The develop m enta l capa c i ty of nuclei tak en from int e s ti na l epi thel ia l cells of f ee di ng tad p o les. ] . E mbry o l. E xp. Mo,r ph ol. 10: 622-640. Gurdon, J.B. Laskey, R.A . and Reeves, O.R . (1975) . The develop - menta l capa c i ty of nuclei tra nspl a nte d from keratin ize d cells of adult f rog s . ]. Embry ol . Exp. Mo,rp h ol. 3 4: 93-112. Gurdon, J.B. and Uehlin g e r , V. (1966) . Fert ile int e s tin a l nuclei. Natu r e 210: 1240-1241 .
Hadorn, E. {1968). Transdete r mi na ti on in cells. Sci. Am. 219(5): 110 -120. Kin g , T.J. and Brig gs, R. {1956) . Seria l tra nspl a nta t i on of e mbry on i c nuclei. Cold Spr ing Harbor Sym p. Quan t. Bio l. 21: 271-289. McCarth y , B.J. and Hoye r , B.H. (1964) . Identi ty of DNA and dive r- sity of messeng er RNA molecules in normal mouse tiss ues. Proc. Natl. Acad. Sci. USA 52: 915-922. McKi nn ell, R.G . (1978) . Clonin g ; Nuclear Trans pla nta tion in Am- phi b ia . U niv e rsity of Mi nn esota Press, Mi nn e apo l is. McGrath , J. and Soit er, D. (1983) . Nuclear tra nspl a nta t i on in the mouse embry o by mic ro surge r y and cell fusi o n . Sci en ce 220: 1300 -1302. Pardue, M.L. and Gall, J.G . {1970) . Chromosomal localiz a ti on of mouse sate l li te DNA . Scie n ce 168: 1356-1358. Wabl, M.R. , Brun, R.B . and DuPasqu i e r , L. (1975) . Lym ph ocy tes of the toa d Xenopu s laevis have the gen e set for pro moti ng tad po l e developm ent. Scie n ce 190: 1310-1312.
제 4 장 전사 수준에서의 유전자 발현의 형태 전사 수준에서 나타나는 유전자 발현을 조절하는 형태에는 크게 나 누어 (1) 게놈의 부분적 불활성화 (2) 유전자 변경 (ge ne alte r ati on ), (3) 순차적 유전자 발현(diff eren ti al gen e ex p reS5 i on) 의 세 가지가 있다. 1 게놈의 부분적 불활성화 염색질은 세포주기의 간기에 응축 정도에 따라 크게 두 부류로 구 별된다. 세포분열기에 응축되었다가 간기에 풀리는 염색질 부위가 있 는데 이러한 염색질을 진정 염색질(眞正染色質 euchroma tin)이라고 하고, 간기에서도 응축 정도의 변화없이 풀리지 않은 부위의 염색질 울 이 질 염 색 질 (異質染色殊 hete r ochromati n) 이 라고 한다. 이 질 염 색 질은 그 응축 정도가 높기 때문에 염색 정도도 진정 염색질보다 높 다. 이질 염색질이 진정 염색질과 다른 점은 (1) RNA 를 전혀 혹은 거의 합성하지 않으며, (2) 세포주기 간기에 DNA 합성이 제일 마지
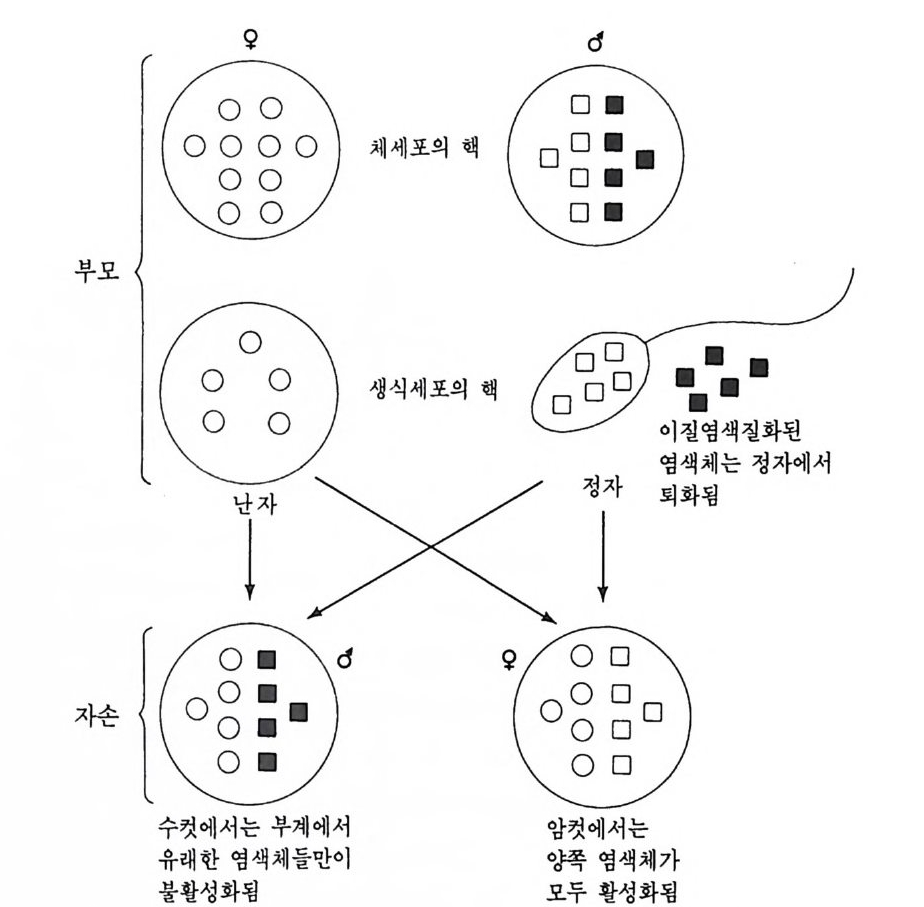
막으로 일어나고 (3) 감수분열시 염색분체의 교차를 억제한다는 것이 다. 이질 염색질에는 두 종류가 있다. 죽 구성적 이질 염색질 (cons tit u tive hete r ochromati n) 과 임 의 적 이 질 염 색 질 (fac ulta t i ve hete r ochro ma ti n) 이 있다. 구성적 이질 염색질은 항상 있는 것으로 상동염색체 모두에 갇은 위치에 존재하는 것이다. 구성적 이질 염색질은 주로 동 원체 (cento r mere) 근처에 존재하며 대단히 반복적인 DNA 로 구성되 어 있다. 임의적 이질 염색질도 구성적 이질 염색질과 성질상으로는 동일하나 고정적으로 존재하는 것이 아니고 발생과정중 특정된 시기 에 염색질 응축으로 형성되며, 상동 염색체 중 한쪽 염색체에서만 일 어난다. 이와 같이 DNA 의 일부가 이질 염색질화함으로써 실제 유전 자로서 발현되지 못하게 되는 경우가 있다. (1) 쥐똥나무벌레 (meall y bu g)에서 부계 이질 염색질 쥐똥나무벌레 (Planococcus citri. )의 수컷에서만 임의적 이질 염색질 화 현상이 일어나는 것을 관찰할 수 있다. 원래 임의적 이질 염색질 이 없었으나 수컷에서만 부계로부터 유래한 반배수의 염색체가 이질 염색질화한다. 이 염색체가 부계에서 진정 염색질이었을지라도 일단 정자를 통해 다음 대의 수컷으로 전승되면 이질 염색질로 전환된다. 그러나 수컷에 전승된 · 모계의 반배수의 염색체는 진정 염색질을 그대 로 유지한다 .• 수컷에서 감수분열중 이질 염색질의 염색체는 붕괴하고 진정 염색질의 염색체만이 남아서 정자 속으로 들어간다. 만약 정자 가 수컷인 자손쪽으로 들어가면 이 정자에 의해 전승된 염색체가 이 질 염색질화한다. 따라서 수컷에서 발현되는 유전자는 모계로부터 전 승된 염색체의 것뿐이다. 부계로부터 전승한 염색체가 이와 같이 유 전적으로 불활성화되는 현상을 실험적으로 보여준 예가 있다 (Brown and Nelson-Rees, 1961). 이들은 쥐똥나무벌레의 수컷과 암컷울 X- 선
 0+ d
0+ d
그림 4-1 작은 진디 (meally bu g)의 수컷에서 부계로부터 유래된 염색체의 이 질 염색질화. 수컷에서는 반배수체의 염색체만이 활동적인데, 이들 전정 영 색체가 정자에 분배되었다가 이 정자에 의해 다음 대가 ' 수컷이 되면, 이들 진정 염색체는 모두 이질 염색질화한다.
으로 조사하고 X- 선으로 조사하지 않은 배우자와 교배시킨 다음 생 산되는 자손의 사망률을 조사하였다. 만약 암컷이 조사되었을 때에는 자손 중 수컷과 암컷 모두가 사망하는 것을 관찰할 수 있었다. 그러 나 수컷을 X- 선으로 조사하였을 경우에는 자손 중 수컷이 사망하는 예는 거의 없고, 암컷은 거의 모두 죽었다. 이때 사망원인은 X- 선에
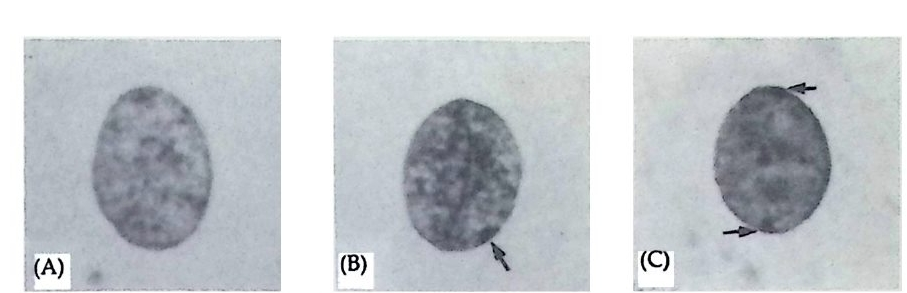
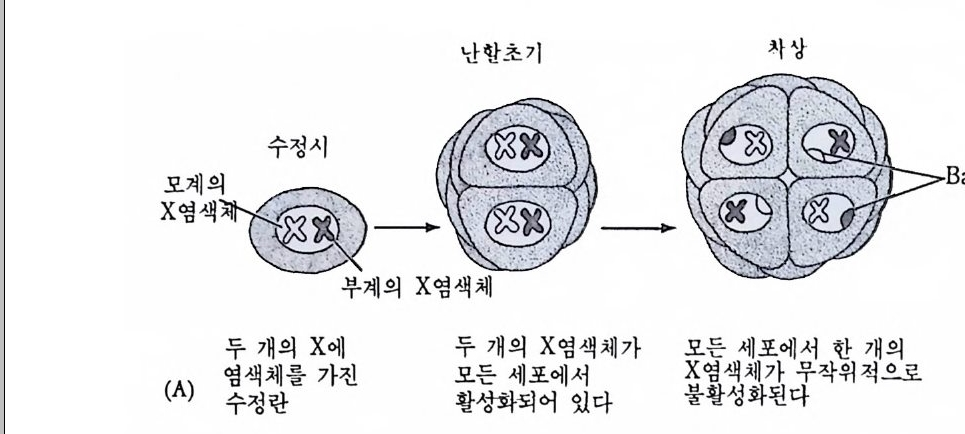
의한 우성치사돌연변이로서 수컷 자손에 전승된 모계의 염색체는 X -선으로 조사되지 않은 반면에, 조사받은 부계에서 전승된 염색체는 이질 염색질화됨으로써 우성치사들연변이의 효과가 예방된 것으로 해 석되었다. (2) 포유류의 X 염색체의 불당성화 포유류의 X 염색체에서 임의적으로 나타나는 이질 염색질이 발견되 었다. 1749 년 바르 (Barr) 와 버트람 (Be rtr am) 은 암컷 고양이의 뉴우런 의 핵막에 붙어 있으면서 질게 염색되는 핵체 를 발견하고 Barr 체 (Barrbod y)라고 하였다. 흔히 Barr 체는 사람을 포함한 여러 종류의 포유류의 암컷에서 발견되었는데 불활성화된 X 염색체임이 알려졌다. 죽 암컷 세포는 두 개의 X 염색체를 가지게 되는데 그 중 하나만이 전사될 수 있다. 그렇기 때문에 X 염색체가 들어 있는 수컷에서 X 염 색체상에 있는 유전자에 의해 지시되어 합성되는 단백질의 양은 암컷 의 것과 동일하다. 죽 암컷과 수컷에서 유전자 수에 관계없이 표현형 이 동일하게 나타난다. 이와 같은 현상을 유전자 양적보정 ( 造傳子臨 的補整 dosage comp en sati on ) 이 라고 한다. 유전자 양적보정을 처음으로 제 안한 학자는 라이온 (L y on , 1961) 인 데, 그는 생쥐의 털 색깔무늬를 관찰하고서 이러한 가설을 제안하였 다. 만약 생쥐의 털 색소를 조절하는 유전자가 이형 접합자로서 상영 색체에 있다면 양부모 중 한 쪽을 닮든가 혹은 양부모의 중간색의 털 울 가지게 된다. 즉 생쥐의 털색은 단색일 뿐이다. 그러나 생쥐의 털 색 유전자가 이형 접합자로서 X 염색체에 있을 때, 두 개의 X 염색체 중 하나가 발생 도중에 불활성화된다면 그 결과가 다르게 나타날 수 있다. 죽, 한 가지 색의 털이 아니고 두 가지 색이 모자이크 모양으 로 섞여있을 수 있다. 라이온은 이러한 현상을 다음과 같이 설명하였 다. 죽, 포유류 암컷의 초기 발생 시기에는 X 염색체 모두가 활성화
 (B) (C)
(B) (C)
그림 4-2 사람의 구강 상피 세포의 핵. (A) 정상적인 XY 수컷 세포, Barr 체가 없다. (B) 정상적인 XX 암컷 한 개의 Barr 체가 보인다. (C) 비정상적인 XXX 암컷 두 개의 Barr 체가 보 인다. (Moore, 1977)
되어 있었으나, 발생이 진행되면서 두 개의 X 염색체 중 하나만이 불 활성화된다. 이때 불활성화되는 X 염색체가 고정적으로 정해진 것이 아니고 세포에 따라 임의로 정해진다면 세포에 따라 부계의 X 염색체 가 불활성화될 수도 있고 모계의 X 염색체가 불활성화될 수도 있다. 그러나 이러한 과정아 비가역적이며 일단 발생과정중 특정된 시기에 어떤 세포에서 어느 한 X 염색체가 불활성화된다면 그 세포에서 유래 한 모든 세포에서는 동일한 X 염색체가 불활성화된다. 따라서 두 가 지의 색이 점으로 나타나지 않고 넓은 조각으로 나타난다(그림 4-3). 생화학적인 연구를 통해서도 유사한 결론을 얻었다. 사람의 유전병 중에 Lesch-Ny ha n 증후군(症侯群 s yndrome) 이라는 병이 있는데, 이 유전 병 은 X 염 색 체 에 연 관된 효소 hy po xanth ine -gu a nosin e pho sp h orib o sy l t rans fe rase(HGPRT) 의 유전자가 결핍됨으로써 유발 되는 것으로, X 염색체를 통해 다음 대로 전승된다. 즉 HGPRT 유전 자에 돌연변이가 남성에서 일어나면 남성은 이 질병에 걸려 죽는다. 그러나 여성에서 한쪽 X 염색체에 이러한 돌연변이가 일어나고 다론 X 염색체에는 돌연변이가 일어나지 않는다면 이 여성에서는 돌연변이 의 효과가 나타나지 않을 수도 있다. 그러나 이 여성은 돌연변이 보 존자 (carr i er) 로서 남아 있게 된다. 그래서 이 여성의 자손 중 아들에
 난항초기 사상
난항초기 사상
 (B)
(B)
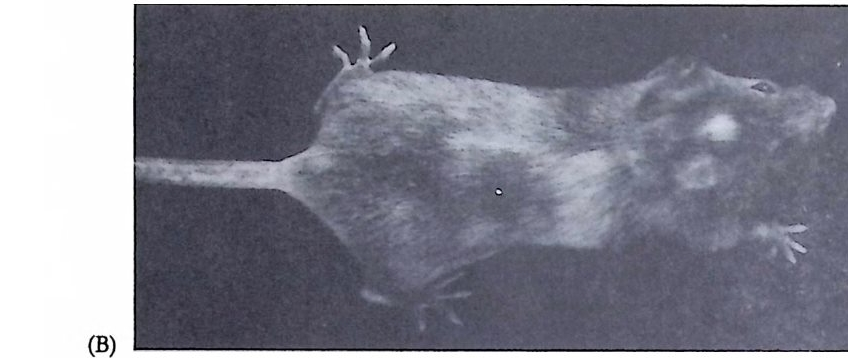
그림 4-3 포유류에서의 X 염색체 불활성화. (A) 무작위적인 X 염색체 불활성화에 대한 도해 (B) X 연관 유전자인 털색 dapp led 의 분포를 보여 주는 이형 접합자의 생쥐 암컷.
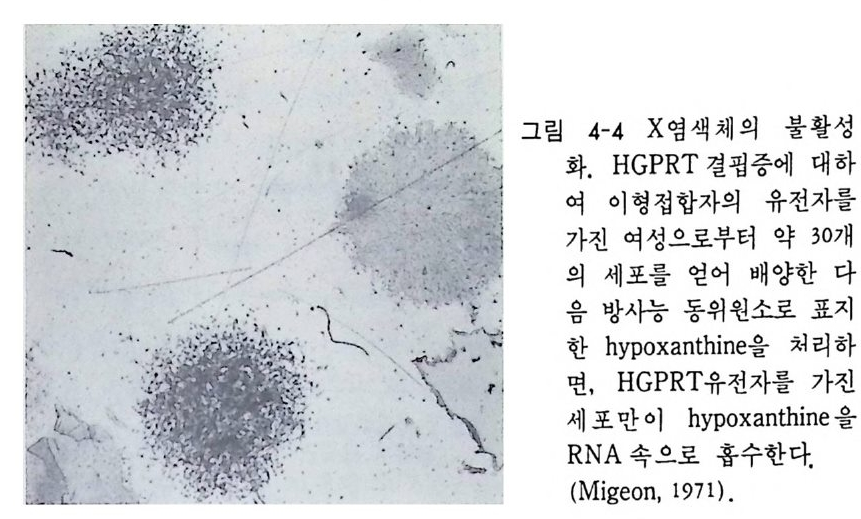
서는 다시 이 질병이 나타날 수 있다. 라이온의 가설에 따르면 여성 의 세포는 그 세포 속의 어느 X 염색체가 불활성화되었는지에 따라 HGPRT 생성이 좌우된다. 미게온(Mig eon, 1971) 은 HGPRT 유전자에 대해 이형 접합자인 암컷의 표피세포를 배양하여 각 세포로부터 클로 운을 형성시킨 다음, 클로운을 염색함으로써 HGPRT 의 존재여부를 검출하였다. 그 결과 클로운 중 반은 양성반응을 보였고, 반은 음성 반응을 보였다(그림 4-4). 즉 두 개의 X 염색체 중 어느 염색체가 불 활성화되었는지에 따라 그 결과가 다르게 나타났다.
 --..-. ..· .., ~ . · ·- ••. •/,J .} ,/ .•` ·> ·. ..모\ •l o '':c../ , . ..·- . .`, • . \.,*,-,, 쇼'':.m 년.. . .. ?. . ,i•-• ::, \. _- ·, ·. ·. .•\r.파i. . 노·,/•,‘ :· ? - \〉c.• 4J.I 그립 가화여의. 진4 -세 이4H여 포G형성PX를접 R으염 합T얻로색자 결어부체의핍 터의 배증 유에양약불전 한 활자3대 0성 를개하다
--..-. ..· .., ~ . · ·- ••. •/,J .} ,/ .•` ·> ·. ..모\ •l o '':c../ , . ..·- . .`, • . \.,*,-,, 쇼'':.m 년.. . .. ?. . ,i•-• ::, \. _- ·, ·. ·. .•\r.파i. . 노·,/•,‘ :· ? - \〉c.• 4J.I 그립 가화여의. 진4 -세 이4H여 포G형성PX를접 R으염 합T얻로색자 결어부체의핍 터의 배증 유에양약불전 한 활자3대 0성 를개하다
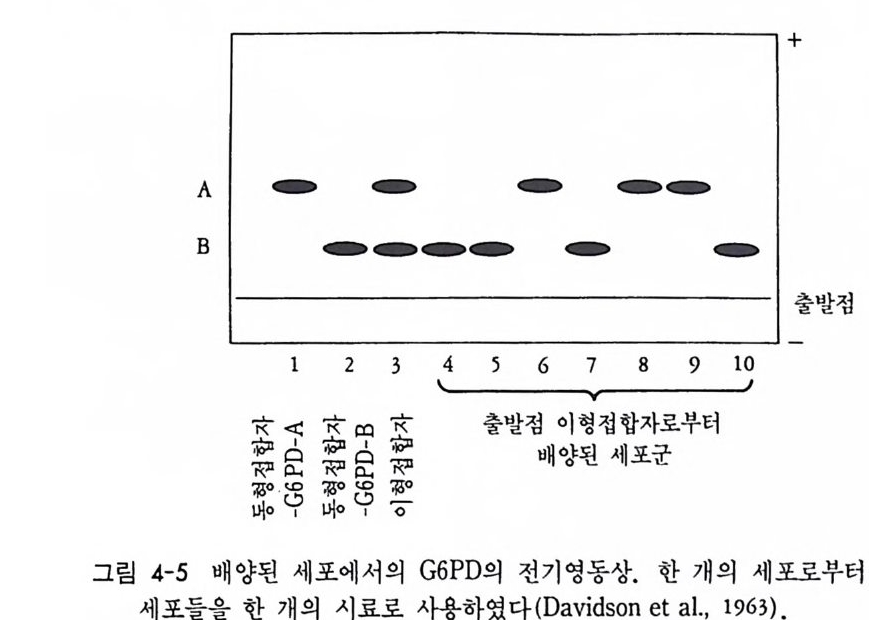
또 다른 예로서는 X 염색체에 그 유전자를 가지고 있는 glu cose-6 -ph o sph a te dehy dr og en ase (G6PD) 에 관한 것 이 다. G6PD 는 전기 영 동상에 두 가지 형 태 즉 G6PD-A 와 G6PD-B 로 나타난다. 즉, 수컷 에는 A 나 혹은 B 가 나타날 수 있으나, 암컷에서는 A, B, 혹은 AB 의 형태로 나타날 수 있다. 이형 접합자인 암컷의 표피세포를 취하여 배양함으로써 클로운을 형성시킨 다음 그 클로운으로부터 G6PD 를 분리하여 전기영동함으로써 표피세포에 따른 G6PD 형을 확인하였다. 이러한 실험 결과 암컷의 표피세포는 A 형 혹은 B 형의 G6PD 를 가지 고 있고, 두 가지 형을 동시에 가지는 경우는 나타나지 않았다 (David s on et a l., 1963). 이러한 결과는 X 염색체 중 어느 염색체가 불 활성화되느냐에 따라 다른 형으로 표현되는 것으로 풀이되었다. X 염색체 불활성화에 대한 라이온의 가설은 전사수준에서의 유전자 발현의 조절을 설명해 주고 있으나 다음과 같은 예의적인 현상을 찾 아볼 수 있다. 첫째는 X 염색체 불활성화는 체세포에서만 일어난다. 암컷의 생식세포에서는 감수분열이 시작되기 직전 불활성화되었던 X 염색체의 재활성화가 일어난다 (Kra tz er and Chapm an, 1981 ; Gart ler et
 +
+
al., 1980). 그래서 마지막 단계에 있는 난모세포에서는 X 염색체 모두 가 활성화되어 있다. 체세포에서는 G6PD 가 A 형으로나 혹은 B 형으 로 나타난다. 죽 이형 접합자인 암컷에서 G6PD 가 어떤 세포에서는 A 형으로만, 어떤 세포에서는 B 형으로만 구성되어 있다. 그러나 난 모세포에서는 A 형과 B 형 모두 나타난다. 이것은 난자형성중에는 두 개의 X 염색체 모두가 활성화되어 있음을 의미한다 (Ga rt ler et al., 1973 ; Mi ge on and Jela lia n , 1977) . 두번째의 예의적인 특칭은 X 염색체 불활성화가 무작위적으로 일어 나지 않고 부계에서 유래한 X 염색체에 선호적으로 일어난다는 것이 다. 암컷 생 쥐 의 영 양아충조직 (trop h o blast tiss ue) 에 서는 주로 모계 의 X 염색체가 활성화되어 있고 부계의 X 염색체는 거의 모두가 불활성 화되어 있다. 유대류(有袋顯 marsu pi al) 에서도 주로 부계의 X 염색체 가 불활성화된다 (Shannan, 1971 ; Coop er et al., 1 971). 셋째로 X 염색체의 불활성화는 반드시 염색체 전반에 걸쳐 일어나
지 않는다. ste r oid sulfat ase 의 유전자는 X 염색체의 단완에 자리하 고 있는데 일단 불활성화가 일어나면 다른 부위의 유전자는 아직 활 성화되어 있으나 ste r oid sul fat ase 의 유전자는 불활성화되는 것으로 보아 불활성화가 부분적으로 일어나는 것을 알 수 있었다 (Mohandas et al., 19so) . 네번째 예의적인 특칭으로는 고양이와 갇은 포유류의 수컷에서 X 염색체가 불활성화되면 나타날 수 없는 털 색깔의 무늬가 나타난다. 물론 이러한 색깔의 무늬가 암컷에서는 당연히 나타나지만 X 염색체 가 불 활 성화된 수컷도 암컷과 동일한 털색깔을 갖는 경우가 있다. 이 경우에는 수컷의 성 염색체가 XXY 인데 Y 염색체에 의하여 수컷으로 성이 결정되고, 두 개의 X 염색체 중 하나는 불활성화되지만, 나머지 다른 하나는 암컷에서와 마찬가지로 불활성화되지 않기 때문에 Barr 체를 가지면서 동시에 암컷의 특칭이 수컷에서 나타난다 (Cen t erwall and Ben irs chke, 1973) .
 AA
AA
그림 4-6 포유류 난모세포 내에서는 두 개의 X 염색체 모두 활동적이다. 14 주된 태아의 폐 세포에서 A(AA) 와 B(BB) 두 가지 형태의 동질 이량체로 존재하지만 난소 세포에서는 두 가지 동질 이량체 의에도 AB 의 이질 이량체가 존재한다.
물론 이질 염색질화가 전사수준에서의 유전자 발현 조절의 전부는 아니다. 염색체 불활성화에 의해 다수의 유전자가 동시에 불활성화되 는 것은 관찰할 수 있으나, 선택적인 유전자의 불활성화는 일어나지 않는 것으로 생각되고 있다.
2 유전자 변경 기본적으로 유전자 조성은 모든 세포에 있어서 동일하다. 그러나 특정된 세포에서 일부 유전자가 변경되는 것을 관찰할 수 있는데, 이 러한 유전자의 변경 (ge ne al t era ti on) 도 유전자 발현을 변화시키는 근 거로 볼 수 있다. 물론 모든 세포에 적용되는 것이 아니고 일부 특정 된 세포에서 특정된 유전자에 한해서 적용되는 것이기 때문에 유전자 조절기구에 대한 일반화된 설명은 될 수 없다. 그러나 유전자 변경으 로 인하여 유전자 발현에 변화를 준다는 점에서 유전자 변경이 유전 자 발현의 부분적인 조절기구로서 관심을 모을 만하다. 크게 3 종류의 유전자 변경 즉 유전자 손실(g ene deleti on ), 유전자 증폭(g ene amp lifica ti on ) 및 유전자 재 배 열 (ge ne rearrange m ent) 을 들 수 있다 . (1) 유전자 손실 선충(線蟲 Nemato d e) , 갑각류 혹은 곤충류에서 발견된 것으로 난 할 초기에 체세포 계열에서만 게놈의 일부가 선택적으로 손실되고 반 면에 생식세포 계열에서는 게놈 전부가 보존되는 현상을 관찰할 수 있다. 이러한 게놈의 손실은 대체로 단번에 과격하게 일어나는 사건 으로 선택적인 유전자의 손실로는 볼 수 없다. 따라서 이것은 선택적 인 유전자 발현의 조절기구로서 인정하기는 아직도 이르다. (2) 유전자 증폭 유전자 증폭은 특정된 RNA 에 대한 유전자를 다수로 복사하여 다 량의 RNA 합성을 가능케 하는 방편이다. 유전자 증폭도 보편화된 현 상은 아니며 곤충과 양서류에서 rRNA 유전자와 초파리와 같은 곤충 에서 의 융모막 (織毛膜 chori on ) 유전자에서 와 갇아 극히 국한된 범 위
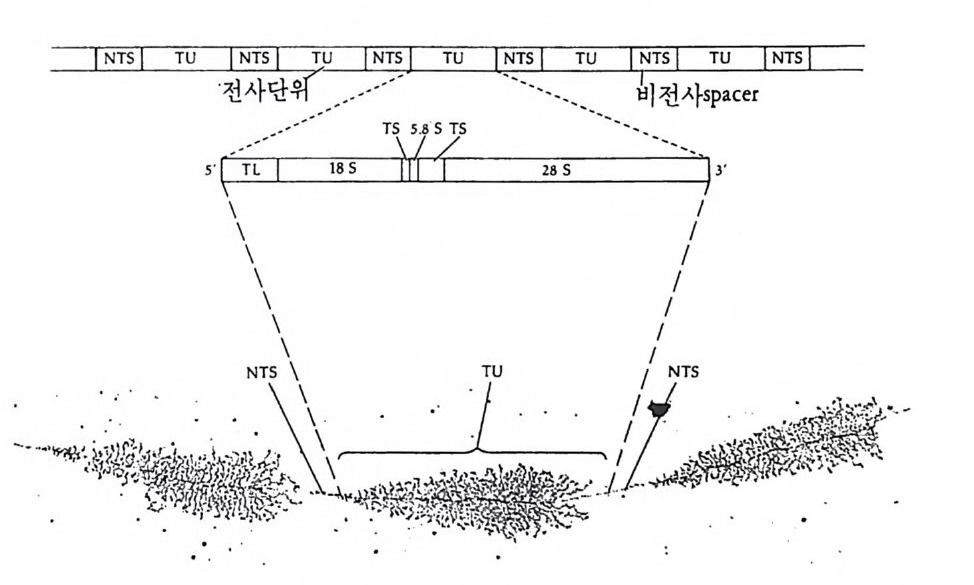
내에서만 찾아볼 수 있는 현상이다. 양서류의 경우 난모세포에서 특 히 rRNA 합성이 엄청나게 일어나는데 리보솜의 수가 보통 유충 세포 에 비하여 200,000 배나 더 많다. rRNA 합성은 주로 복사기 (複絲期, dip lo te n e sta g e ) 에 수개 월 에 걸 쳐 일어 난다. rRNA 의 유전자에 대해서는 Xenop us laev is에서 가장 잘 연구되어 있다. rRNA 유전자는 일정한 간격을 두고 반복적으로 분포되어 있는 데 (tan dem repe t it ion ) 전사단위 (tra nscrip tion unit , Tu) 와 비 전사 spa c er(nontr a nscrib e d spa c er, NTS) 가 번갈아 자리하고 있다. 비전사 s p acer 는 전사되 지 않으나 pol ym e rase I 울 인식 하는 부위로 알려 져 있다 (Moss, 1983). 전사 단위만이 전사되는 부위로서 전사 단위에는 전사 개시 부위에 이어 1sS rRNA 에 대한 유전자가 있고, 18S rRNA 유전자에 이어 전사 spa c er, 5.S S rRNA 유전자, 다시 전사
 NT S I TU I NT S I TU I NTS I TU I NTS I TU I NTS I TU I NTS
NT S I TU I NT S I TU I NTS I TU I NTS I TU I NTS I TU I NTS
그립 4-7 양서류 rRNA 유전자의 구성. 전사단위 (tran scri ption al unit , TU) 는 비전사 s p acer(NTS) 에 접하고 있고, leader sequ e nce(TL), lBS, 58S 및 28S 유전자와 전사되는 s p acer(TS) 를 포함하고 있다 (Wats o n, 1976).
spa c er 그리고 마지막으로 2sS rRNA 의 유전자가 자리하고 있다 . 전 사단위는 한꺼번에 4oS 의 RNA 로 전사된 다음 3 종류의 rRNA 로 성 숙한다. 개구리의 이배수체의 세포에는 rRNA 유전자가 모여 있는 부위가 두 군데 있다. 각 부위마다 450 개의 전사단위로 이루어져 있는데, 비 전사부위의 길이가 언제나 일정하지 않다. 난자형성 기간은 감수분열 기의 일부에 해당됨으로 이 기간중의 난모세포내의 유전자는 반배수 의 염색체에 4 배가 됨으로 450 X 4=1800 의 rRNA 유전자를 기대할 수 있으나 실상은 훨씬 더 많다. 수천 개 정도가 아니고 백만 개 정도의 rRNA 유전자가 난모 세포내에 형성된다 . 인 (nucleolus) 도 4 개가 아니 고 수천개로 늘어나면서 염색체에 부착되지 않고 독립적으로 존재한 다. 인 속에 rRNA 유전자가 존재한다는 사실이 DNA- R NA 재결합 법으로 확인되었고 양서류 난모세포 속에 인이 약 1500 개로 늘어나는 점으로 보아, rRNA 유전자는 반배수체의 염색체에 들어 있는 rRNA 유전자의 1500 배에 해당하는 유전자의 함량으로 증폭하는 셈이다. 만 약 인 한 개 속에 들어 있는 rRNA 유전자수를 450 이 라고 하면, 6.
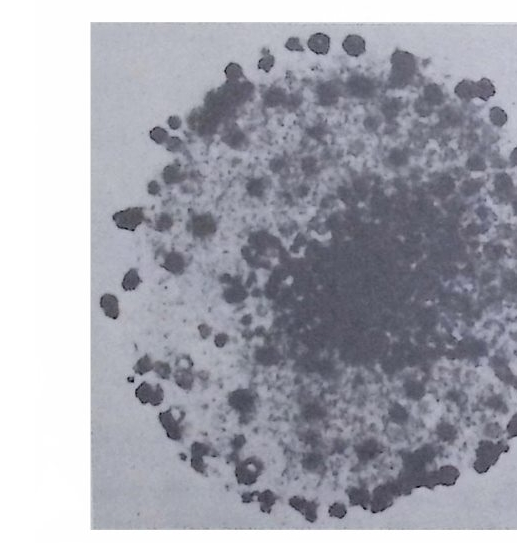
그림 4-8 Xenop us Laevis 난모 세포의 핵 핵 속에는 많은 수의 인이 있다 (Brown and Dawi d, 1968) .
 dAT Cop ol ym er
dAT Cop ol ym er
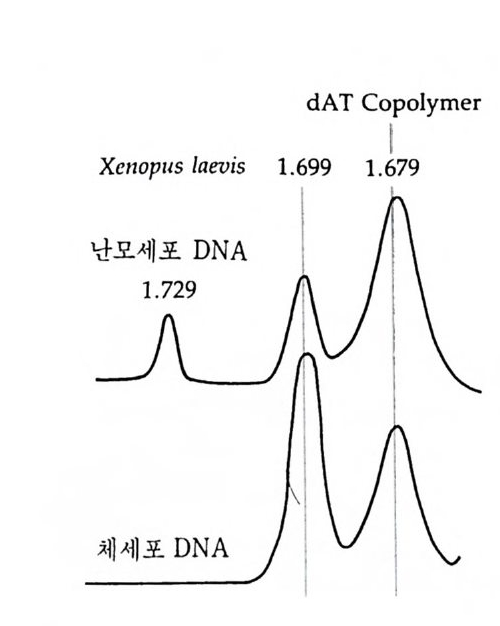
그림 4-9 인에 존재하는 염색체 의 rDNA 의 분리. 체세포와 난모세포 의 핵으로부터 DNA 를 분리하여 CsCI 원심분리로 분석하였다. 난모 세포에는 밀도가 높은 DNA 가 있다 (Brown and Dawi d, 1968) .
8 X l 한개의 유전자로 증폭하는 셈이다. rRNA 유전자의 증폭은 CsCI 구배를 이용한 분석 초원심 분리에 의 해서도 확인되었는데, Xenop us laev i s 의 체세포와 난모세포에서 DNA 를 추출하여 토막을 낸 후에 CsC! 구배에서 초원심분리하면 체 세 포에 서 는 평 균 부력 밀도 (buoy an t density ) 가 l. 699 g /cm3 인 DNA 만 이 존재하는 반면, 난모세포에서는 이와 같은 평균 부력밀도의 DNA 이의에 또 하나의 다른 부력밀도를 가진 위성 DNA 를 찾아볼 수 있 다. 이 위 성 DNA 의 염 기 성 분 (base comp os it ion ) 은 Xenop us 의 염 색 체 DNA 에 바해 훨씬 높다. 즉 염색체 DNA 의 GC 성분은 40% 인 반면에 위성 DNA 의 GC 성분은 67% 로 그 밀도가 훨씬 높다 (1,729 g/ cm3). 위성 DNA 를 또한 분리하여 DNA-DNA 재결합법으로 전체 DNA 에 재 결합시 켜보면 rDNA 에만 재 결합한다. rRNA 유전자 의에 초파리의 융모막 유전자 (chor i on g ene) 도 증폭 하는 것으로 알려져 있다. 융모막 단백질이 여포세포에서 합성된다. 융모막 유전자가 발현되기 직전 여포세포의 게놈 전부가 DNA 합성을 통해 96 배로 늘어난다. 그후 융모막 유전자만이 선택적으로 10 배로
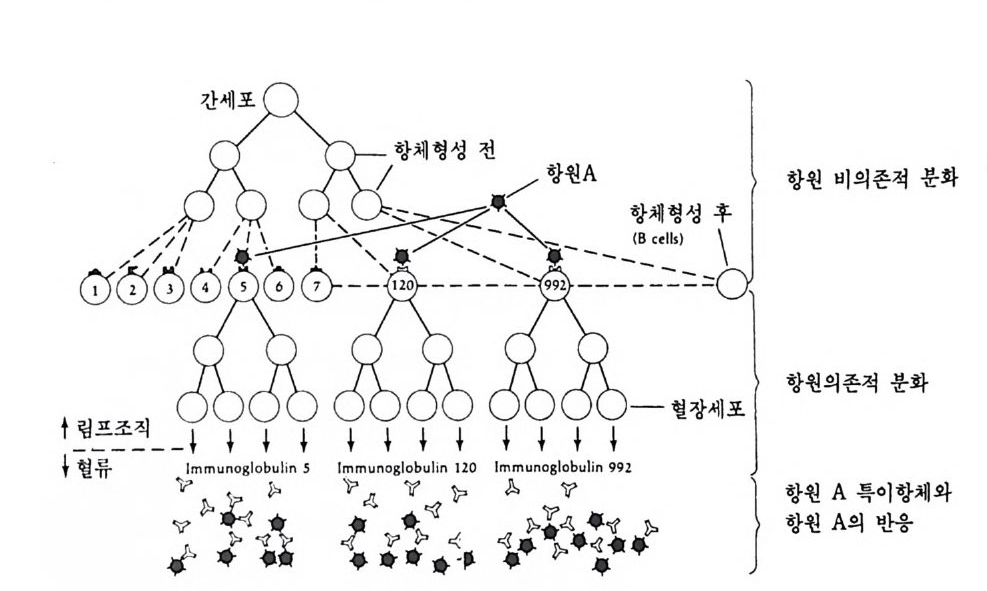
증폭하는데, 이 러 한 증폭은 여포세포에 서 만 일어난다 (S p rad li n g and Mahowald, 1980). 증폭된 DNA 가 가지모양으로 염색체에 붙어 있는 데, 융모막 유전자에서만 DNA 합성이 일어나서 중폭된 것으로 생각 되고 있다. 유전자 증폭이 어떠한 기구에 의해서 일어나는지 알 수 없을 뿐만 아니라, 지금까지 알려진 예로는 rRNA 유전자와 초파리의 융모막 유 전자의 증폭 뿐이다. 이것은 모든 유전자에 일반적으로 적용될 수 있 는 현상이 아니다. 글로반 단백질을 생성해내는 적혈구나, 난알부민 울 합성하는 수란관세포나, fi bro i n 을 합성하는 누에의 fi bro i n 선에서 는 유전자가 증폭되기 때문에 단백질을 다량 합성해 낼수 있는 것이 아니다. (3) 유전자 재배열 1) 림프구의 항체 유전자에서의 유전적 조성의 변화 유전자 조성 자체에 변화가 일어남으로써 유전자 조성이 다른 세포 의 것과는 달라지는 경우가 유일하게 림프구에서 발견되었다. 항원 (anti gen ) 이 의 부로부터 들어 와서 림프구와 접 하면 림프구에 서는 항 체 (an ti bod y)가 만들어진다. 항원과 접하기 전에도 림프구는 항체를 만든다. 그러나 항체를 분비하지 않고 세포막에 삽입시켜 보관한다. 림프구는 모두가 항체를 생성하지만 한 종류의 림프구는 한 종류의 특이한 항원만을 인식하는 항체를 생성한다. 따라서 pol io v i rus 의 표면 단백질을 인삭할 수 있는 항체는 E. coli 막 , 콜레라 독소 혹은 인플루엔자 바이러스 등을 인식할 수 없다. 일단 막에 부착되어있는 항체가 항원과 결합하면 그 때 부터 이 림프구는 여러 차례 분열하여 항체분비 혈장 세포 (an tib od y -secre ti ng pla sma cells) 가 된다. 림프구 중 특정한 항원과 결합된 림프구만이 분열하며 항체를 분비한다. 이 러한 설명 즉 클로운 선택설 (Burne tt, 1959) 에 의하면 항원과 결합하
 항원 비의존적 분화
항원 비의존적 분화
그림 4-10 쿨로운 선택 모형의 항체 형성. B 림프구는 항원과 접하기 전에 이 미 표면 특이성을 가지고 있다. 막에는 단 한 종류의 항체만이 있는데, 이 항체가 항원과 결합하면 그 세포만이 증식하면서 동일한 항체를 형성한다 (Edelman, 1970) .
 (A) (B)
(A) (B)
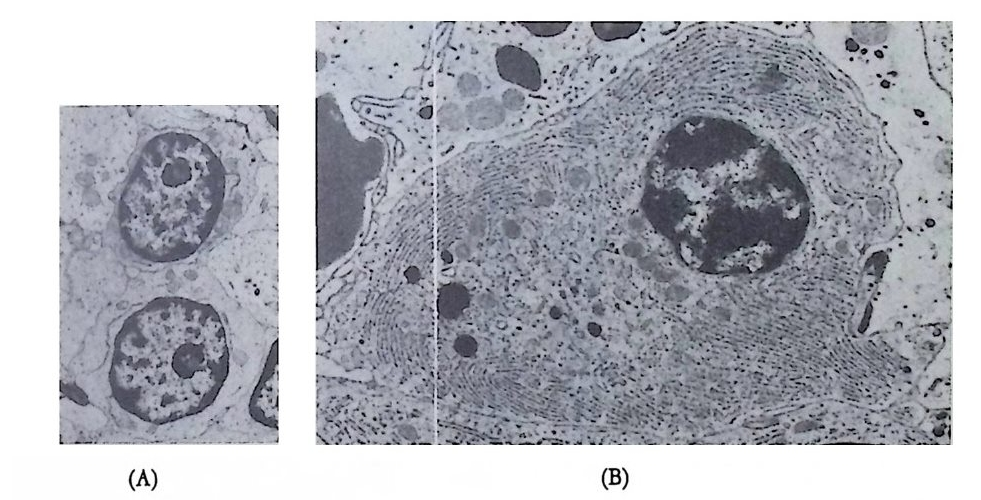
그림 4-11 B 림프구 (A) 와 혈장 세포 (B). B 림프구가 항체 분비 혈장 세포로 분화 하면서 조면 세포체가 많이 발달한다.
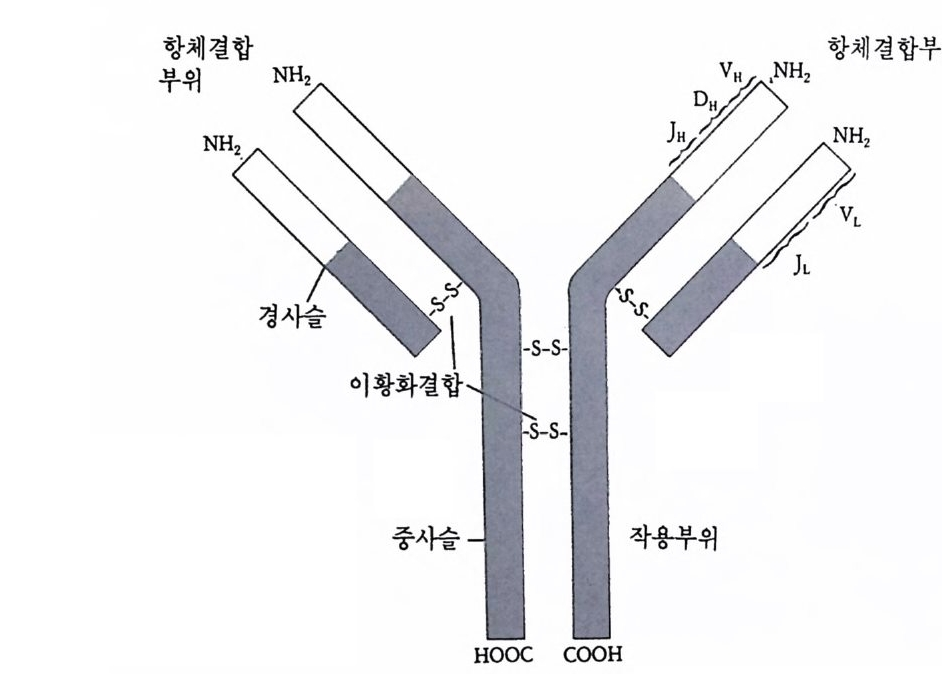
기 전에 이미 림프구는 그 자체의 항원 특이성을 형성하고 있다. 각 림프구는 수백만 종류의 항체 중 한 종류만을 생성하여 이미 그 표면 에 항원특이성을 가진 항체를 준비하고 있다. 이러한 항원 특이성은 림프구가 분화하는 동안 새로운 유전자를 형 성함으로써 가능하다. 림프구 표면의 항체 단백질은 두 쌍의 폴리펩 티드 죽 한 쌍의 중사슬과 한 쌍의 경사슬로 이루어져 있다. 이들 사 슬은 이황화물 결합 (d i sul fi de bond) 으로 결합되어 있으며, 이러한 항 체 혹은 i mmuno g lobul i n 의 특이성은 변이부위 (varia b le re gi on) 의 아 미노산 배열순서에 따라 결정된다. 중사슬과 경사슬 모두에서 그 말 단은 아미노기 말단이 며 변이부위 가 고정 부위 (consta n t regi on ) 에 부 착되어 있다. 중사슬의 고정부위가 세포막에 삽입됨으로써 항체가 세 포 표면에 고정된다.
 부항위체 결합 뿐 屈 결 합부 위
부항위체 결합 뿐 屈 결 합부 위
그림 4-12 전형적인 항체(imm uno g lobul in)의 구조. 두 개의 동일한 중사슬이 이황화 결합으로 연결되어 있다.
 D量NA言 -DN+A -토 막 큰 토막의 작은 토막의 子〕겔 一절편冒 등:에 :이용: 충
D量NA言 -DN+A -토 막 큰 토막의 작은 토막의 子〕겔 一절편冒 등:에 :이용: 충
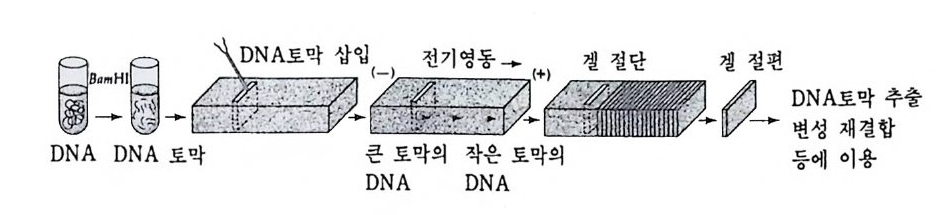
그립 4-13 크기에 따른 DNA 토막 분리
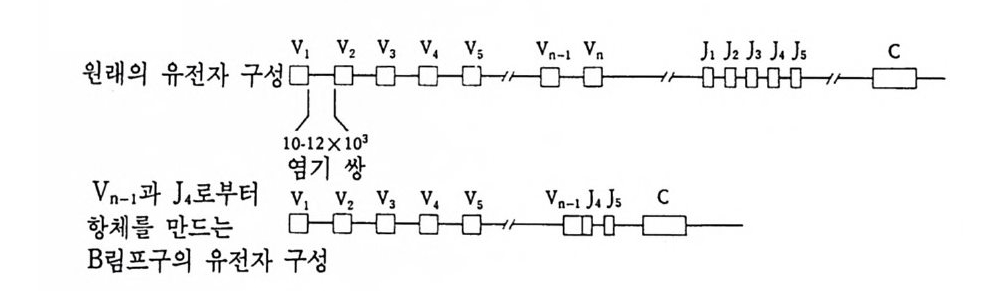
중사슬과 경사슬의 유전자 모두가 림프구에 따라 다르게 형성된다• 우선 경사슬 유전자 형성에 대하여 살펴보기로 하자. 경사슬 유전자 는 크게 세 개의 부위 즉 변이부위, J부위, 및 고정부위으로 이루어 져 있다. 변이부위는 항체의 처음 97 개의 아미노산의 배열순서를 지 시하는 염기배열로 약 200 종이 있다. J부위는 변이부위의 마지막 15 ~17 개의 아미노산을 지시하는 염기배열로 4~5 종이 있다. 고정부위 는 언제나 일정하며 모든 림프구에서 공통적이다. 림프구 분화과정에 서 200 종의 변이부위 중 하나와 J부위 중 하나가 조합하여 항체의 변 이부위를 이루는데, 이때 V 부위와 J부위는 그 사이에 있는 인트론 (i n t ron) 을 제거시키면서 결합한다. 호주미 (Hoz umi)와 토네가와 (Tone g awa, 1976) 가 처음으로 이러한 유전자의 재배열을 보여주었다. 이들은 생쥐의 발생배와 특이한
 V1 V2 V3 V, V; V0_1 V0 J1 ] 2 J, J, ], C
V1 V2 V3 V, V; V0_1 V0 J1 ] 2 J, J, ], C
그림 4-14 B 림프구 분화중 일어나는 경사슬 유전자의 재배열 항원과의 결합 에 의해 촉진되기 전에 200 혹은 그 이상의 V 유전자 중 하나가 5 종류의 J 유전자 층 하나와 결합한 다음 고정 유전자 (C) 쪽으로 가까이 이동한다.
 (A) 실험고안
(A) 실험고안
 (B) 결과 분자량 (x 10 ... )
(B) 결과 분자량 (x 10 ... )
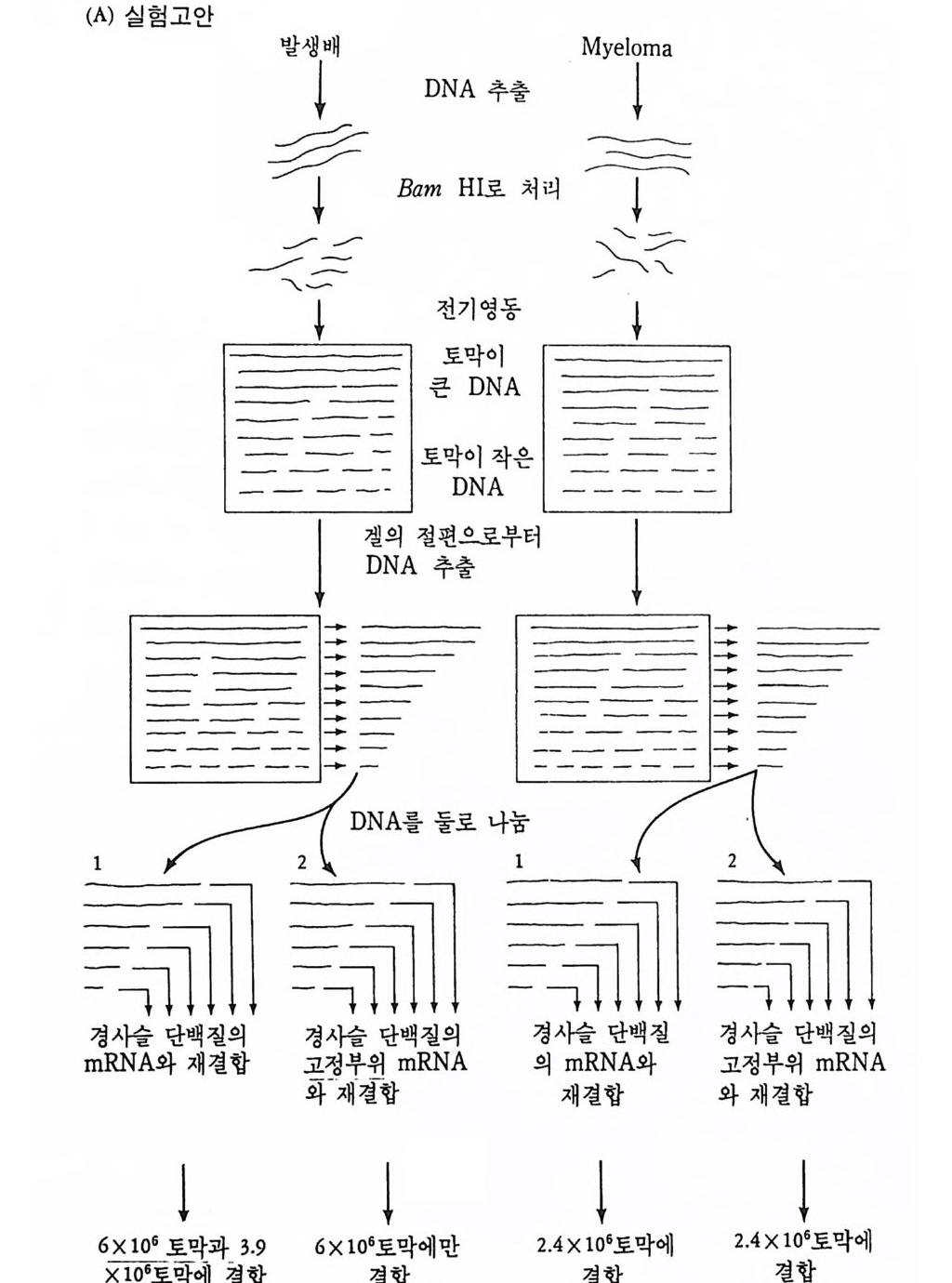
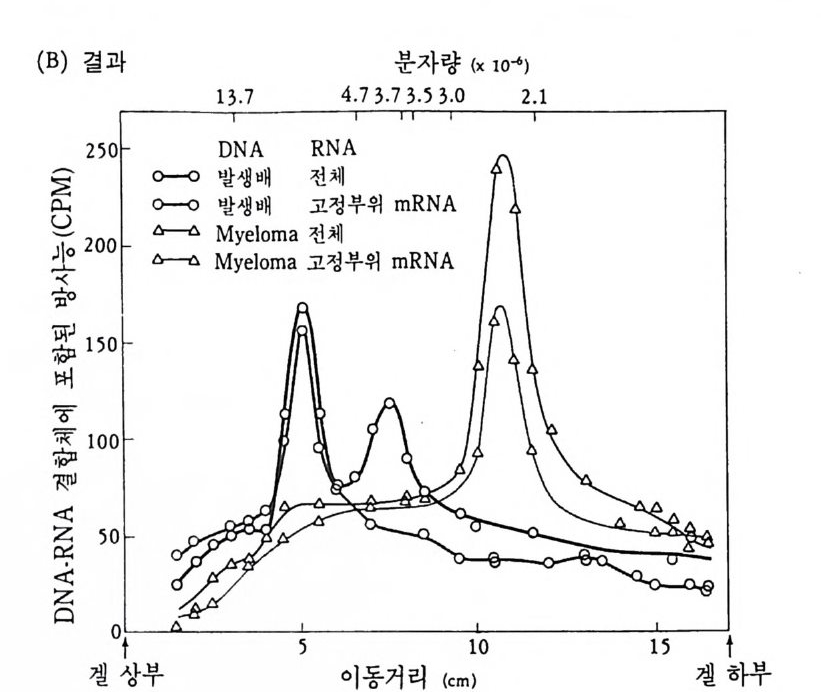
그림 4-15 Hozum i와 Tone g awa 의 실험고안과 결과. 생쥐 발생배와 my el oma 의 DNA 를 BamHI 로 처리하여, 전기영동하고 분리 추출하였다. 각각의 DNA 시료를 항체 경사슬의 V 와 C 부위에 대한 mRNA(l) 그리고, 경사슬 단백질의 고정부위만을 지시하는 mRNA(2) 에 재결합시켰다. 발생배의 DNA 에서는 경사슬 단백질의 변이 (V) 및 고정 (C) 부위가 서로 다른 DNA 토막에서 발견되었으나, 림프구에서는 고정부위와 변이 부위가 동일한 DNA 토막 (2 .4 X 106) 에서만 함께 발견되 었다 (Hozum i and Toneg aw a, 1976).
i mmuno g lobu li n 을 다량 생 성 하는 경 사슬 분비 B 종양 세포로부터 DNA 를 추출하여 제한효소 Barn HI 으로 처 리하여 특별히 GGATCC 에서 DNA 를 토막내었다. 이들 DNA 토막들을 다시 겔 전기영동법 으로 크기에 따라 분리하여 전기영동 겔 절편으로부터 추출하고 변성 시킨 다음 원래 방사능으로 표지한 B 종양 세포의 전체 경사슬 RNA 와 재결합시켰다. 물론 고정부위에 대한 RNA 가 재결합하였으
나, 이 의에도 발생배의 DNA 는 겔상 두 군데에서 RNA 와 재결합하 는 것을 관찰할 수 있었다. 이때 재결합한 DNA의 분자량은 각각 6 X 106 과 3 . 9 X 10 6 이었다. 이들 DNA 를 각 각 고정부위의 mRNA 나 혹은 경사슬 단백질에 대한 전체 mRNA 와 결합시켜 보았더니, 고정 부위는 6 X 106 분자량의 DNA 에만 재결합하고 경사슬 전체 mRNA 를 사용하였을 경우에는 6 X 106 혹은 3 . 9 X W6 의 DNA 에 모두 재결합하는 것을 알았다. 이와 같은 결과로서 고정부위는 6x 1 06 DNA 에만 있고 변이 부위는 3.9 X l 06 DNA 와 6X 1 06 DNA 모두에게 있음 을 알 수 있었다. 그러나 림프구 종양세포의 DNA 는 발생배의 DNA 와 는 전혀 다른 실험결과를 보여주었다. 죽 경사슬 mRNA 에 결합할 수 있는 유일한 림프구의 DNA 는 분자량 2 .4 X 106 이었다. 2.4 X 1 06 DNA 는 고정부위 (C)RNA 와 결합하는 것은 물론 변이부위 (V) 와도 결합하는 것으로 보아 2.4 X 106 DNA 속에 C 부위와 V 부위의 DNA 가 모두 있는 것으 로 생각할 수 있었다. 이와 같은 실험결과는 아마도 두 개의 토막 죽 경사슬 C 부위의 한 토막과 V 부위의 한 토막이 결합하여 하나의 새로 운 유전자가 형성되었기 때문에 얻어진 것이라고 해석되었다 (Brack et al., 1978 ; Bernard et al., 1978 ; Seid m an et al., 1978, 1979) . 죽 림 프구 가 분화하는 동안 유전자 재배열에 의해 유전자가 새로이 형성된 것 이라고 생각되었다. 중사슬 유전자는 그 토막수가 경사슬의 유전자보다도 더 많고 분 화 과정이 다양하다. 중사슬 유전자는 V 부위, D 부위 J부위 및 고정 부위로 이루어져 있다. V 부위는 처음 97 개의 아미노산을 지시하는 부위로서 200 종의 다른 염기배열로 이루어져 있고 , D 부위는 3~14 아미노산울 지시하는 부위로서 10~15 종의 다른 염기배열로 이루어져 있으며, J부위는 15~17 아미노산을 지시하는 부위로 4 종의 염기배열 로 이루어져 있다. 그 다음으로 고정적인 C 부위가 연결되어 있다. 중사슬에서의 V 부위는 하나의 V 배열 부위와 하나의 D 배열 부위가
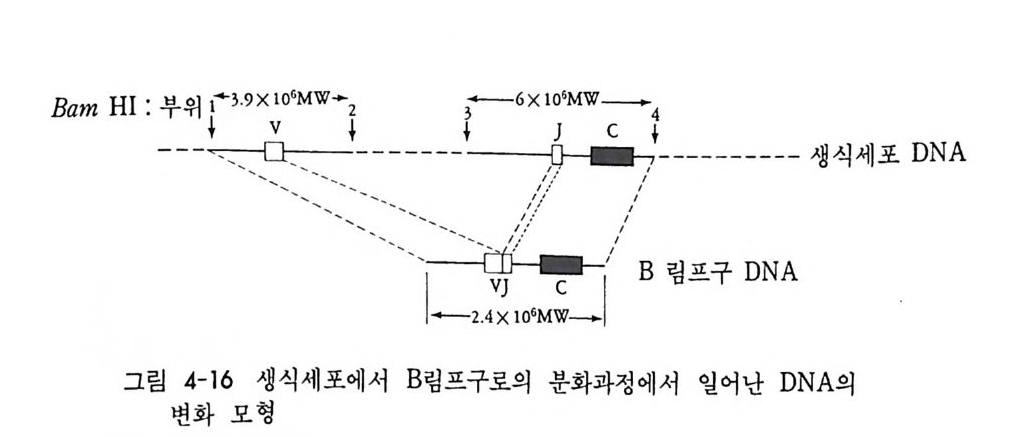 Bam HI : _부_위 - 1~+59규 X 王10 6 ―MW_ 칼_ _ _ ___ 「― 6 -X- DI0 -6 M -W-4 I ----------생 식세포 DNA
Bam HI : _부_위 - 1~+59규 X 王10 6 ―MW_ 칼_ _ _ ___ 「― 6 -X- DI0 -6 M -W-4 I ----------생 식세포 DNA
하나의 J배열 부위에 부착됨으로써 이루어진다. 이와 같이 중사슬의 V 부위와 C 부위는 림프구 분화중 형성된 두 개의 유전자로부터 지시 받아 형성된 것이다. 이때 항체의 C 부위는 세포막에 삽입되고 V 부위 는 항원 수용체로서 작용한다. 림프구가 항원과 접촉하게 되면 림프구는 분열하면서 항체분비 혈 장세포로 분화한다. 이들 세포에 의해 생성되는 항체에는 C 부위가 있다. 그러나 항체합성이 계속되면 C 부위는 변할 수 있다. 첫번째 C 부위를 mu 고정부위 (Cµ) 라고 하며, 두번째 C 부위는 분비될 때 다소 변경된 mu 자체이거나, Cr, Cc 혹은 Ca 부위이다. 그래서 중사슬의 변이 부위는 처음에는 µ고정부위에 나타나고, 다음에 r 고정부위에 나타난다. 이러한 현상을 class sw it c hi n g이라고 한다. 이때 고정부 위가 달라짐에 따라 중사슬의 작용양식에 변화가 생긴다. 즉 고정 부 위가 µ와 r 이면 항체의 분해, 응고 및 식세포에 의한 소화 등이 촉 진되고, €사슬이면 염증반응을 유도하게 되고, a 사슬이면 점액, 눈 물, 땀 및 젖으로의 항체 분비가 촉진된다. class s wt c hi n g은 변이부 위의 유전자 (VD J)를 止고정부위 앞에서부터 r, a, 혹은 €고정부위 앞으로 이동시킴으로써 성취한다. 이러한 접으로 보아 혈장세포의 유전적 조성은 다론 세포의 것과는 판이하게 다르다. 첫째로 림프구의 변이부위의 유전자를 구성하는
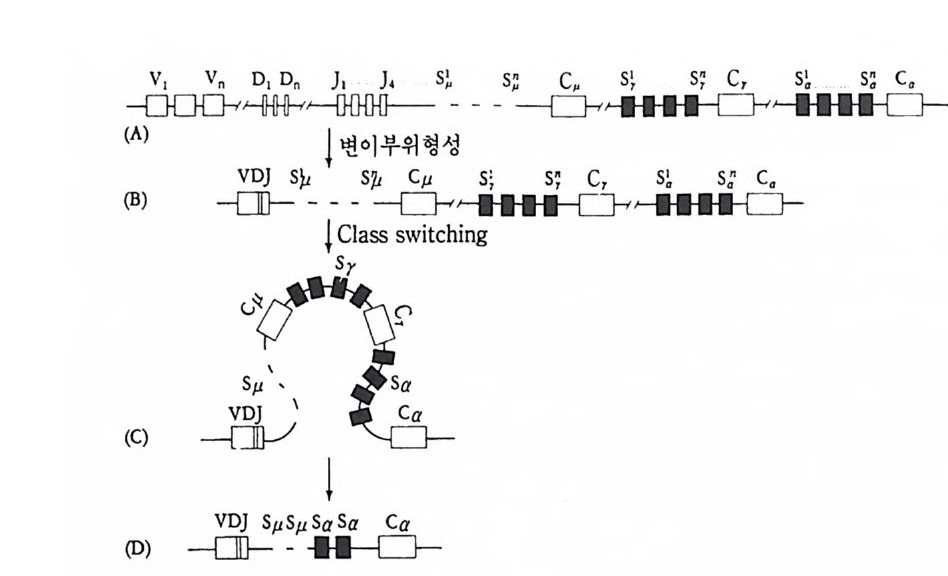 V, V0 D1 D0 J, J, S~ sz C, S\ s; C, S~ . S~ C0
V, V0 D1 D0 J, J, S~ sz C, S\ s; C, S~ . S~ C0
그립 4-17 변이부위 유전자형성과 항체의 중사슬 생성중 일어나는 class swi tch ing , 중사슬유전자는 변이부위인 V, D, J와 고정부위 를 포함한다. 4 종류의 주요 항체는 고정부위에 근거하여 분류된다. 죽 I g A 는 요를 , IgM 은 Cµ 룰 그리고 I gG는 CT 를 포함한다. 변이부위는 한 개의 V, 한 개의 D 그리고 한 개의 J로 구성된다. 항체출현 이전에는 VDJ 유전자가 mu 고정 부위에 인접하면 , 이 항체는 세포막에 자리한다. 항제출현 이후에는 DNA 가 고리를 형성하면서 VDJ 유전자는 고정부위에 인접한다. 만약 pha 고정 부위에 인접하면 분비형의 항체가 된다. class sw it ch i n g은 고정부위 앞에 있는 일련의 swi tch 부위 (S) 에 의해 조절된다 (Dav i s et al. , 19soa, b).
DNA 토막둘이 다른 세포에서는 서로 떨어져 있으나, 림프구에서는 떨어져 있는 DNA 토막이 한군데에 모여 새로운 유전자로 구현된다. 둘째로 대부분의 혈장세포에서는 중사슬의 µ고정부위와 같은 게놈의 일부가 핵으로부터 제거될 수 있다. 죽 혈장세포에서는 유전적 조성 의 일부가 분화과정에서 결손될 수도 파괴될 수도 있는 반면에 새로 운 유전자가 탄생될 수도 있다. 대부분의 분화된 세포의 공통점은 유전적 조성은 동일하나 세포의 종류와 분화의 시기에 따라서 유전자의 발현이 선택적으로 일어난다. 그러나 림프구에서 나타난 유전적 조성 자체의 변화가 분화의 형태로
나타났다는 점은 대단히 획기적인 사실이라고 할 수 있다. 분화의 결 과로 나타난 유전적 조성의 변화는 분화의 결과가 단순히 선택적인 유전자 발현만으로 나타나는 것이 아니라 유전자 자체의 변화로도 나 타날 가능성을 강하게 암시하였다. 이러한 현상이 발생이 진행되면서 할구의 전능성을 제한하며 분화세포의 비가역적인 변화를 일으키는 것인지도 모른다. 2) 림프구 이외의 세포에서 유전적 조성의 변화 분화의 결과로 유전적 조성의 변화를 일으키는 예가 림프구 이외의 다른 세포에서도 관찰된 바가 있다. 말라리아 기생충인 Try pa nosoma bruse i에서도 유전적 조성이 바뀜으로 인해 새로운 표면 당단백질을 형성하는 예를 찾아볼 수 있다. 또한 효모균에서도 유사한 기구에 의 해서 교집 형 (mati ng type) 에 변화가 일어난다 (Hoe ij makers et al., 1980 ; Haber et al., 1980 ; Str a th e m et al., 1979). 죽 교집형은 교접형 유전자 (mati ng type gen e) 가 염 색 체 상에 위 치 하는 부위 에 따라 달라진다. 따 라서 제 1 대에서는 a 교집형 유전자가 on 위치에 있었지만 다음 대 에는 그 자리를 a 교집형 유전자와는 다른 a 유전자가 차지함으로써 교집형아 바뀌는 현상이 일어난다. 이때 이들 유전자들은 주로 세포 표면의 인식기구를 바꾸어 준다. 이러한 현상이 척추동물의 발생과정 에서도 나타나는 것으로 보아 아마도 이러한 바가역적인 유전적 조성 의 변화로 인하여 전능성이 상실되는 것인지도 모른다. 앞에서 설명 한 유전자 토막의 재조합 현상으로 유전적 조성이 변경되는 것 이의 에도 림프구 B 세포가 혈장세포로 분화하는 동안 많은 점 돌연변이 (po in t muta t io n ) 가 일어 남으로써 다양한 항체 형성 이 가능하다 (Crews et a l., 1981) . 유전적 조성을 변경시키는 또 하나의 특별한 예는 도약 유전자 Gump ing gen e) 혹은 트란스포손 (tran spo s on 혹은 tran spo s able ele- men t)인데, 트란스포손은 일종의 DNA 토막으로 이동하면서, 게놈
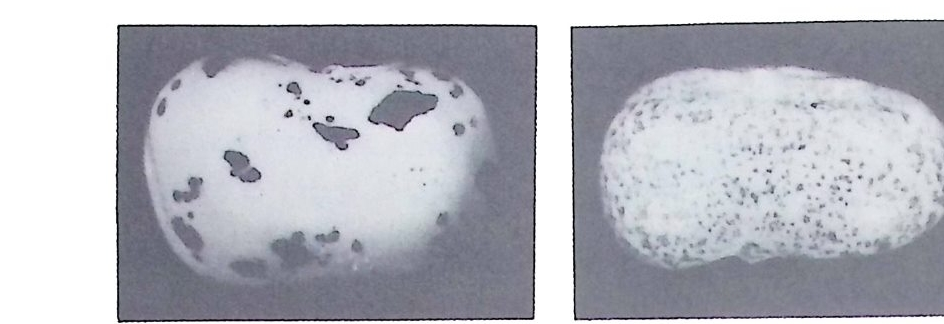
그림 4-18 옥수수 씨의 색소 유 전자 발현에 미 치는 t rans p oso n 의 효과 . 흰 부 위는 t ransp oson 에 의해서 색소유 전 자가 불 활성화 됨으 로 나타난 효과 이 다 (Pete r son, 1977) .
안으로 삽입되어 게놈의 염기배열순서를 바꾸어 준다. 트란 스 포손이 구조 유전자 사이에 삽입되면 구조유전자 는 불활 성화될 수 도 있다. 이러한 현상은 박테리아, 옥수수 (ma i ze), 초파리에서 그 예를 찾아볼 수 있다. 옥수수에서 씨의 색소유전자에 트란스포손이 삽입되면 무색 의 씨가 생성된다 (McC li n t ock, 1952 ; Pete r son, 1980). 그러나 이 트란 스포손이 그 위치에서 이동하면 색소합성이 회복된다. 초파리에서도 백색 유전자 (w hit e g ene) 에 트란스포손이 삽입됨으로 돌연변이가 일 어나는 경우가 있다 (Green, 1980 ; Gehrin g and Paro, 1980). 아직까지 트란스포손의 이동으로 발생의 방향이 정해지는지에 대하여 아 는 바 가 없으나, 트란스포손으로부터 mRNA 가 합성되는 것으로 보아 (Rubin e t al., 1980) , 트란스포손의 작용으로 발생 의 방향이 정 해 질 수 있을런지도 모론다는 가능성은 배제할 수 없다 (Sh i mo t ohno and Tem in, 1 980) . 3 순차적 유전자 발현 앞에서 설명한 게놈의 부분적 불활성화와 유전자 변경이 세포운명 결정에 대한 부분적 설명이 될 수는 있으나 모든 경우에 적용될 수
있을 만큼 보편적이지 못하다. 물론 이러한 현상에 대한 기구론적인 설명이 없기도 하지만 특수한 경우에만 그 설명이 가능할 뿐 모든 경 우 를 설 명할 수 있 을 정도의 일반성이 결여되어 있다. 그러나 순차적 유전자 발현 (D iff eren ti al gen e ex p ress i on) 은 아직까지 기구론적으로는 설명이 어렵지만 현상적으로는 가장 보편적으로 관찰되기 때문에 세 포운명의 결정에 가장 가능한 선택적 유전자 발현의 형태로 인식되고 있다. 분화된 세포는 그 종류에 따라 특이한 단백질을 합성한다. 즉 적혈 구 는 신경세포에서 찾아볼 수 없는 글로빈 단백질을 합성한다. 또한 발생배에 서 합성되는 단백질을 단계별로 보면 단백질의 양상이 다르 게 나타난다. 이와 같 은 공간적으로나 시간적으로 다르게 나타나는 단백질 합성 양상의 차이는 순차적 유전자 발현에 기인한다. 이것은 동일한 조성의 유전자가 발생과정을 통해서나 혹은 세포의 종류에 따 라 다르게 발현되기 때문에 나타나는 현상이다. 일단 발현되어야 할 유전자가 결정되면 발생의 방향 즉 세포운명이 결정된다. 그리고 결 정된 방향으로 세포는 분화하여 특정된 기능을 가전 세포가 된다. 여 기서는 순차적 유전자 발현을 몇 가지 예를 통하여 현상학적으로만 살펴보기로 하겠다. (I) 다사 염색체 순차적 유전자 발현이 발생단계에 따라 시간적으로 나타난다는 사 실을 가장 잘 보여준 예는 다사염색체 (po Mene chromosome) 에서 찾 아볼 수 있다. 다사염색체란 초파리나 Ch i ronomus 와 같은 쌍시류(雙 超羅 d ipt eran) 의 침샘세포에서 찾아볼 수 있는 특수한 염색체이다. 동원 체 (動原 體 , centr om ere) 의 응집 으로 형 성 된 염 색 질 핵 소체 (chromocente r ) 에 서부터 4 개 의 염 색 체 가 방사형으로 분포되 어 있고, 상동염색체가 짝을 이루고 있다. DNA 복제는 일어날지라도 염색체는
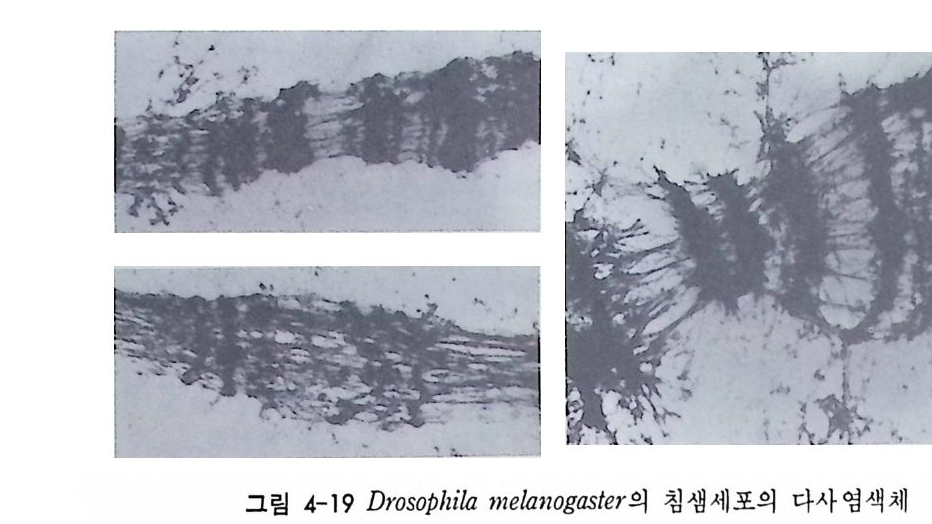 그 립 4-19 Drosoph i l a m e lano g as t er 의 침 샘 세 포의 다사 염 색 체
그 립 4-19 Drosoph i l a m e lano g as t er 의 침 샘 세 포의 다사 염 색 체
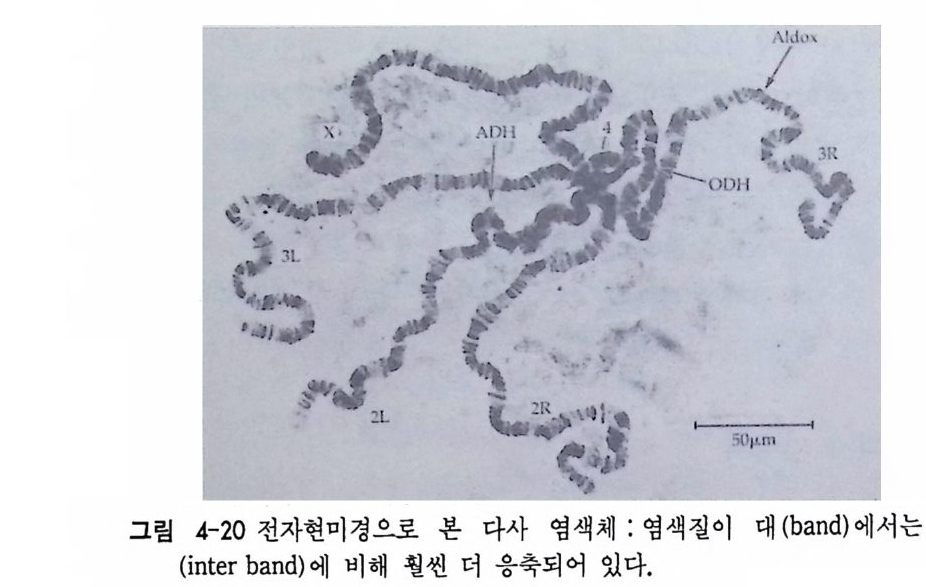 I 궐 I I' m I
I 궐 I I' m I
분열하지 않은 내분열(內分裂 endo mit os i s) 을 하기 때문에 DNA 함 량이 512 배, 1024 배 혹은 그 이상으로 증가한다. 이러한 염색체는 그 후 더 이상 분열하지 않은 채로 남아 있게 되는데 그 크기가 거대하 여 광학 현미경 하에서도 관찰할 수 있을 정도이며, 가장 의미있는
특칭은 염색체상에 있는 대 (band) 이다. 초파리의 염색체에는 반배수 체의 게놈당 5150 개의 대가 존재하는데, 이러한 대는 무작위적으로가 아니고 규칙적으로 배열되어 있다. 대 사이에는 간대(i n t erband) 가 있 는데, 대와 간대의 차이는 DNA 의 농도에 달려 있다. 즉 염색분체가 대에서는 접혀 있는데, 이러한 접힘(fo ld i n g)의 모임으로 인해 대가 형 성되며, 염 색분체의 개 별적 인 접힘을 염색소립(染色小粒, chromomere) 이라고 한다. 간대에서 염색분체는 접히지 않은 채로 평 행적으로 분포되어 있다. 대를 구성하는 염색소립의 모양은 염색체를 인위적으로 잡아당겨 주었을 때 더 분명하게 나타난다. 조금 잡아당 겼을 때에는 염색소립의 모양이 잘 나타나나 좀더 세게 잡아당기면 염색소립의 모양을 상실하게 되는데, 접혀 있던 염색질이 풀려서 간 대와 비슷한 모양이 되기 때문이다. 비어만 (Beermann, 1952) 은 다사 염색체의 대의 모양이 일정하며 세포 종류에 따라 염색체 손실이 전 혀 일어나지 않음을 보여주었다. 그러나 그는 이러한 대가 부풀어 오 르는 현상을 관찰하였다. 이러한 부풀림 (p u ff)은 대를 구성하는 염색 소립이 풀려나오면서 부풀어오르는 것으로 그 크기가 염색소립이 풀 려나는 정도에 따라 다르게 나타난다. 비어만은 부풀림을 전사과정의 형태적인 표현이라고 생각하였는데, 여러 가지 유전학적인 연구를 통 해 대와 유전자간에 밀접한 관계가 있음이 발견되었다(J udd and Young , 1973 ; Swanson et al., 1981), Chir o nomus 침샘 염색체 4 번에서 거 대 한 부풀림 인 Balbia n i rin g 2 (BR2) 가 형 성 될 때 대 가 부풀어 오 르는 것을 관찰하였다(그림 4-21). 가장 간단하면서도 직접적인 증거 는 방사능 RNA 전구체로 유충을 처리하여 RNA 를 합성시킨 다음 자 기방사법으로 표지부위를 알아내는 것인데, 이러한 방법을 다사염색 체에 적용시켰을 경우 부풀림만이 선택적으로 표지되어 있음을 알 수 있었다. 그러나 전사 억제제인 a-ama niti n 이나 acti no my ci n D 를 처 리하면 RNA 전구물질의 표지가 부풀림에서 완전히 억제되었다 (Beermann, 1971 ; Holt a nd Kaijp er s, 1972) . 부풀림 이 풀려 나오는 것은
 (A)
(A)
그림 4-21 Chir o nomus p all i di v itattatus의 침샘 염색체 4 번 기부말단에 자리한 Balbia n i ring 2 (A) 위상차 현미경사진 (B) 단계적으로 부풀고 있는 Balbia ni ring 2.
염색질을 전사시키는 여건을 마련하는 것이라고 볼 수 있는데, 전자 현미경으로 Balbia n i r i n g을 관찰해 보면 풀려나온 염색질에 전사활 동이 활발한 전사단위 (tran scrip tion al unit) 가 많이 있음을 찾아볼 수 있다(그립 4-2 2). 부풀립에서 mRNA 가 합성된다는 사실은 실험적으로 증명되었다. Chir Q n omus t en ta ns 에서 Balbia n i rin g 2 부풀립 (BR2) 은 그 크기가 대단히 크기 때문에 현미경 하에서 분리가 가능하다. BR2 를 분리하
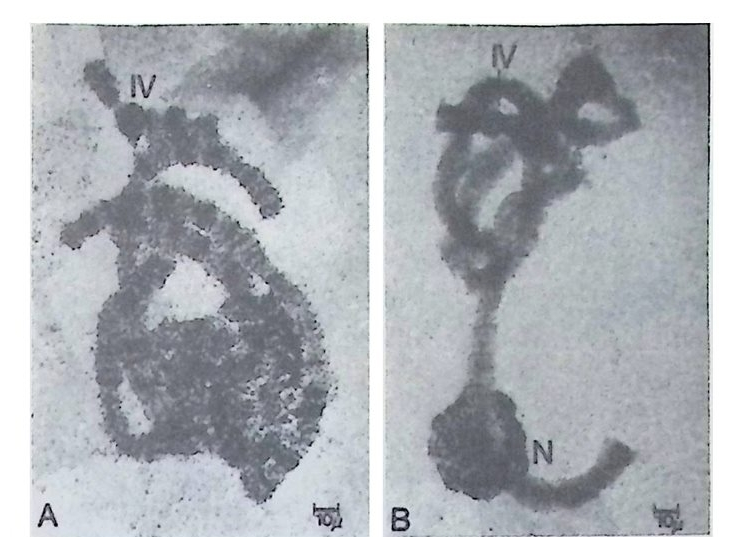
그립 4-22 Chir o nomus p all id i v ittat us 의 침샘 염색체에서의 3H-u ridine 흡수에 미치는 a-aman iti n 의 효과. (A) 대조군 (B) a-aman iti n 을 처리한 염색체. N : 인, IV : 4 번 염색체에서의 Balbia n i rin g ( Beermann, 1971).

그림 4-23 Chir o nomus te n ta ns 의 4 번 염색체에서 발현중인 전사단위 (Lamb and Daneholt, 1979) .
여 전기영동법으로 분석하였는데, 75S 의 침강계수를 가진 50 , 000 개의 염기로 이루어진 대단히 큰 RNA 가 BR2 에서 합성된다는 사실을 알 게 되었다. 방사능 RNA 전구체로 RNA 를 표지한 다음 BR2 를 분리 하여 추출함으로써 얻은 순수한 75S RNA 를 염색체에 in sit u 재결 합시켜 자기 방사법으로 재결합 부위를 알아보았더니, 75S RNA 는 반드시 BR2 에만 결합되는 사실을 알 수 있었다 (Lambe rt, 1972 ; Lambert and Danholt, 191s). 75S BR2 ~NA 는 다른 RNA 와는 달리
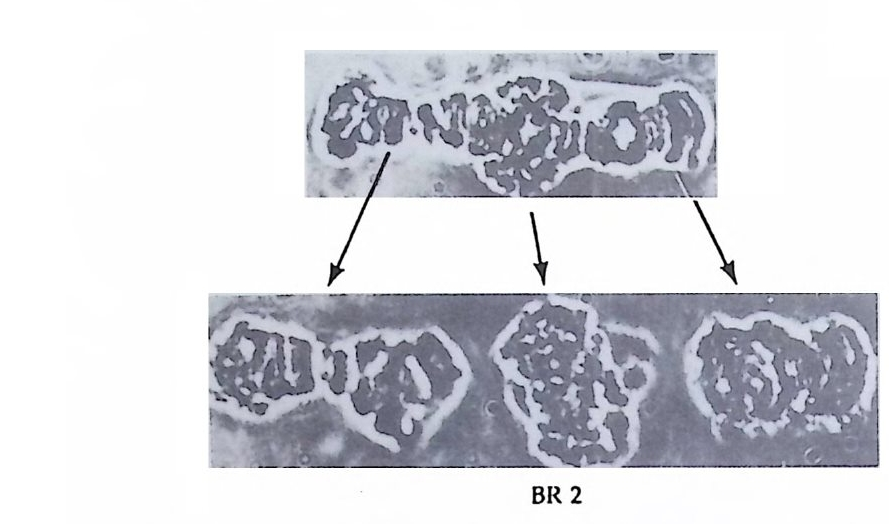 BR 2
BR 2
그림 4-24 Chir o nomus tenta ns 의 BR2 의 분리 (Lambert a nd Daneholt, 1975) .
핵에서 세포질로 이동하는 동안 그 크기가 감소하지 않는 것으로 나 타났다. 이러한 점은 RNA 를 분석하는 데 대단히 중요했다. 이와 같 이 거대한 RNA 가 리보솜과 결합하여 형성한 폴리솜은 거대할 것으 로 예측되었다. 침샘세포를 방사능 RNA 전구체로 표지한 다음 세포 질 폴리솜을 설탕 구배 원심분리 (sucrose grad i en t cen trifug a ti on) 로 분 석하여 보면 거대한 폴리솜울 얻을 수 있는데, 이 거대 폴리솜으로부 터 추출한 RNA 의 침강계수는 75S 였다. 또한 이 RNA 를 다시 염색
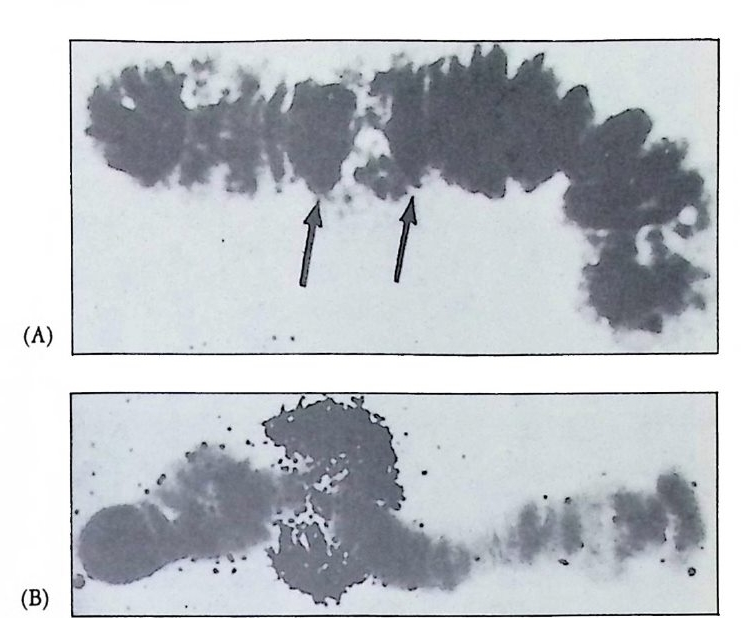 (A)
(A)
그림 .4- 25 Chir o nomus lenta n s 침샘 염색체 4 의 BR2 에서의 전사. (A) tolu id ine blue 로 염 색 한 염 색 체 . in vit ro 에서 의 RNA 합성을 시도하기 위 해 화살표 부위를 절단하였다. (B) 표지된 BR2 RNA 로 in situ 재결합시킨 다 음 자기 방사법으로 RNA 합성 부위를 검출하였다 (Lambe rt, 1972) .
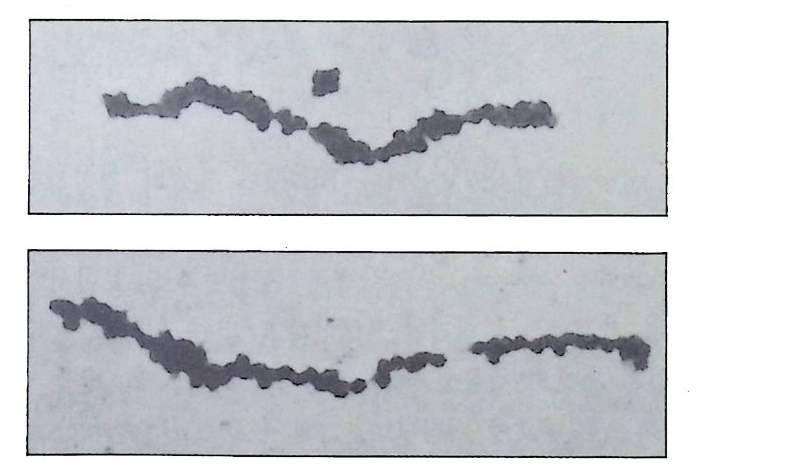 `• 1
`• 1
그림 4-26 Chir o nomus ten ta n s 4 번 염색체의 BR2 에서 얻은 거대 폴리솜의 전 자현미 경 사진 (Daneholt, et al. 1976)
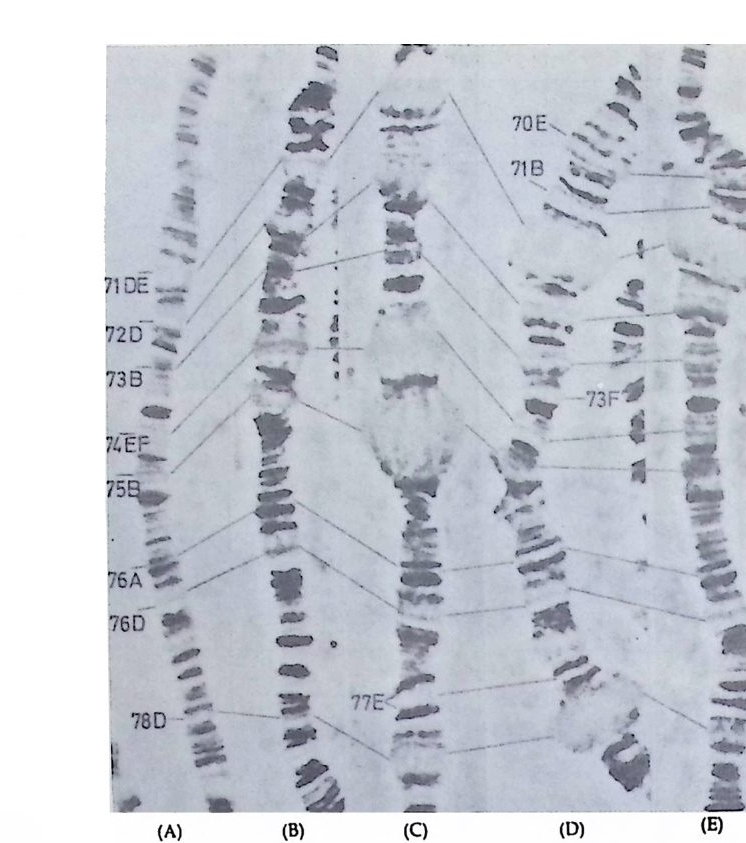 70E
70E
그림 4-27 Drosop hila melanog as te r 침샘 염색체의 3 번 영색체에서 단계에 따 라 일어나는 순차적 부풀림, A 와 B, 110 시간 유충, C, 115 시간 유충, D, O 시간 번데기. E, A 시간 번데기
체에 in sit u 재 결합시켜보았더니 BR2 에만 특별히 결합하였다 (W i es lander and Daneholt, 1977). 이 RNA 는 후에 침샘세포에서 단백질 합 성에 이용되고 있는데, 이와 같은 실험결과로 보아서 부풀림은 rnRNA 를 합성하는 형태적인 표현이라고 할 수 있었다. 부풀림은 조직의 종류에 따라 공간적으로 다르게, 발생 단계에 따 라 시간적으로 다르게 나타난다. 그림 4-27 은 Drosop hi la melanoga s - t er 의 침샘염색체 3 에서 일어나는 부풀림이 발생단계에 따라 다르게 일어남을 보여주고 있다.
(2) 성게 발생에서의 순차적 유전자 발현 성게 발생에서 유전자가 순차적으로 발현되는 사실을 핵산 재결합 법으로 알아냈다 (Galau et a l., 1976). 발생중 상당한 부분의 RNA 는 발생단계를 막론하고 공통적으로 존재하나 RNA의 일부는 단계에 따 라 그리고 조직에 따라 다르게 나타나는데 이러한 현상은 유전자의 순차적 발현에 기인한다. 이 실험은 성게 낭배의 mRNA 의 유전자인 유일성 DNA(uniq u e DNA) 에 여러 단계의 발생배나 종류가 다론 조 직에서 얻은 RNA 를 재결합시켜봄으로써 수행되었다. 이러한 DNA 를 낭배 특이 유일성 유전자라고 불렀는데, 그 복잡도 (com p lex ity)는 17 X 10 명기로서 마지막 단계의 난모세포의 mRNA 복잡도의 반 정 도에 해당한다. 우선 낭배로부터 세포질 RNA 를 추출하여 유일성 유 전자와 결합시킨다. 이때 RNA 는 완전히 순수한 mRNA 는 아니지만 일단 유일성 유전자와 결합시켜서 얻은 RNA 는 mRNA 로 간주할 수 있는데, 그 이유는 유일성 유전자는 구조 유전자 (s truc t ural g ene) 로서 직접 mRNA 를 전사시킴으로써 단백질의 아미노산 순서를 지시할 수 있기 때문이다. 유일성 유전자와 낭배 RNA 의 결합으로 이루어진 RNA - DNA 를 RNAse 로 강하게 처리하여중으로써 일단 DNA 에 결 합된 RNA 를 제거시킨다. 이와 같은 방법으로 얻은 DNA 는 낭배 mRNA 를 전사하는 부위로서 낭배 mDNA 라고 불렀다. 그리고 낭배 mRNA 와 결합하지 않은 DNA 를 낭배 null mDNA 라고 불렀다. 각 단계의 발생배와 여러 종류의 조직에서 추출한 RNA 를 낭배 mDNA 혹은 낭배 null mDNA 와 결합시킴으로써 낭배기에 발현되는 DNA 가 다른 발생 단계와 다른 조직에서도 공통적으로 발현되는지 혹은 낭배 기에서는 발현되지 않은 유전자가 다른 발생단계와 다론 조직에서는 발현되는지를 알아보았다. 그림 4-28 에서 회색대로 표시한 부분이 낭 배 mDNA 에 결합되는 정도를 그리고 백색대로 표시된 부분이 낭배 null mDNA 와 결합하는 정도를 나타낸다. 난모세포에서의 유전자 발
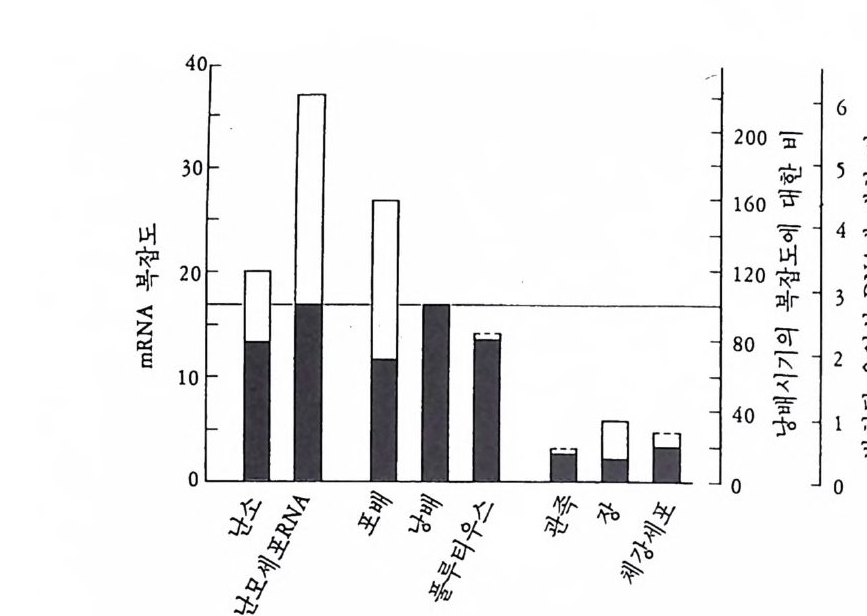 40I -·1
40I -·1
그립 4-28 여러 종류의 조직에서 mRNA 로 발현된 구조유전자. 회색대는 낭배 의 mRNA 와 동일한 mRNA 의 양을 의미하고, 비 회색대는 낭배 mRNA 와 다른 종류 mRNA 의 양을 의미한다. 복잡도 (com p lex ity)는 낭배 mRNA 의 복잡도를 100% 로 간주하고 산출한 것이다 . (Galau et a l., 1976)
현정도는 낭배에서 발현되는 것의 두 배로 난모세포에서는 낭배에서 발현되는 모든 유전자가 발현될 뿐만 아니라 낭배에서 발현되지 않은 유전자까지도 발현된다. 낭배 mDNA 와 재결합하는 포배의 mRNA 가 수정 후 포배기에 이 를 때까지 계속 전사되었을 가능성을 배제할 수는 없으나, 아마도 포 배의 mRNA 의 대부분은 난모세포에서 합성되었다가 수정 후 어느 정도 소모되는 것으로 보인다. 전반적으로는 난모세포에서 전사된 mRNA 종류가 수정 후 감소하는 경향을 보인다. 그러나 포배기에 아직도 낭배에 없는 전사체가 상당히 남아 있다. 낭배에 달하면 난모 세포에서 합성된 낭배 null mDNA 의 전사체는 완전히 고갈되고, 낭 배 mDNA 의 재발현을 유발함으로써 수정 후 감소된 낭배 mRNA 를
충당한다. 낭배 이후 낭배 mRNA 가 점차 고갈될 뿐만 아니라 낭배 null mDNA 가 발현함으로 낭배 의 것과는 다른 종류의 mRNA 가 합 성된다. 성체의 조직으로부터 얻은 mRNA 를 비교해 보면, 대부분의 낭배 mDNA 의 발현이 이러한 성체조직에서 위축되어 있다. 전반적 으로 보아 낭배 mDNA 가 공통적으로 발현되기는 하나 단계에 따라 또한 세포의 종류에 따라 특이한 DNA 가 발현된다. 아마도 공통적인 DNA 의 발현은 공통적인 대사과정을 위한 효소와 구조단백질에 대한 전사체의 합성과 관계되고 비록 양적으로는 적어도 특이하게 발현되 는 DNA 는 아마도 발생단계와 조직에 따라 특이한 형질 발현을 위한 단백질 합성과 관계되는 것으로 생각되었다. 성게 발생중에 나타난 유전자 발현은 공간적으로 선택적이다. 성게 의 게놈에는 6 종류의 액틴 유전자가 있는데, 이들 유전자 발현은 세 포의 계보에 따라 특이하게 나타난다. 그 중 한 개는 근육 액틴 유전 자 (M) 이고, 나머지 5 개는 세포 골격의 액틴 유전자 (C y)이다. M유 전자는 근육 세포에서만 발현되고 Cy I , Cy I la,Cy I lb,Cy lI Ia,Cy lI I b 등의 C y유전자가 발현되는 시기와 세포의 종류는 각각 다르다• Cy I 과 C y Il 는 발생초기에 포배 간충직 세포에서 그리고 배발생 후에 는 입부분을 구성하는 의배영과 장에서, 그리고 성체에서는 장과 관 족에서 발현된다. C y lll 는 발생 초기에는 동물극의 한 개의 세포로부 터 유래한 항문을 구성하는 의배영에서만 발현되고, 그 후에는 전혀 발현되지 않는다. 이러한 사실이 유전자 재조합법을 이용하여 확인되 었다 (Dav i dson et a l., 1985, 1986). 먼저 미수정란을 p ro tami ne 을 입힌 접시에 고정시키고 수천 개의 DNA 분자를 주사해 준 다음 수정시킨 다. 이때 의부에서 넣어 준 DNA 는 성게알의 핵 속에서 재조합되고 복제된다. 또한 열충격 단백질 (hea t - shock p ro t e i n) 에 대한 유전자를 박테 리 아의 chloramp he n ico l tran sfe r ase (CAT) 의 유전자에 재조합 시켜 성게알에 주사한 다음 발생시키면서 열충격을 주면 CAT 유전자 가 발현되어 CAT 효소가 생성된다. 죽 의부에서 주입된 유전자가 밖
에서부터 주는 자국에 대하여 반응을 보이고 조절될 수 있음이 확인 되었다. 이와 같은 실험방법을 이용하여 Cy매 a 유전자의 발현의 선택성에 대하여 데이비드슨 (Dav i dson) 등은 연구하였다. C y IIIa 유전자에 박테 리아 CAT 유전자를 재조합하여 성게의 미수정란에 주입시킨 다음 수정시켜 발생시켰다. 이 재조합유전자는 세포분열과 함께 복제되고 세포로 분배되기 때문에 내인성 Cyll la 유전자가 발현되는 시기와 세 포에서는 함께 발현될 것으로 기대되었다. 재조합된 C y Illa 유전자에 도 해독 개시코돈인 ATG 가 있지만 CAT 유전자에도 개시코돈이 있 기 때문에 C y llla 유전자의 발현 여부는 CAT 효소 를 검출함으로써 확 인이 가능하였다. 이러한 실험으로 C y Illa 유전자 발현은 수정 후 20 시간 이내에 최고조에 달하는 것을 확인할 수 있었다. 또한 방사능 동위원소로 표지된 CAT 유전자로 in situ 재결합시켜 본 결과 CAT mRNA 의 합성은 항문을 구성하는 의배영에서만 선택적으로 일어난 다는 사실을 확인하였다. 이러한 실험결과로 보아 C y llla 유전자 발현 은 시간적으로 그리고 공간적으로 정확하게 조절되는 순차적 유전자 발현임을 알수 있었다. (3) 양서류 발생에서의 순차적 유전자 발현 사아젠트 (Sar g en t)와 다빗 (Da wi d, 19s3) 은 특정된 발생단계에서만 발현하는 유전자를 재조합하여 이용함으로써 양서류 발생과정에서 일 어나는 순차적 유전자 발현을 관찰하였다. 죽 Xenop us 의 낭배에만 존재하는 mRNA 를 추출 및 분리하여 이 mRNA 에 대한 cDNA 를 만든 다음 이 cDNA 에 다량의 난모세포 mRNA 를 첨가해 중으로써 낭배 mRNA 에 대한 cDNA 중 난모세포 mRNA 에 상보적 인 cDNA 는 모두 난모세포 mRNA 와 결합하도록 유도했다. 그 다음 결합된 cDNA mRNA 에서 mRNA 를 제거시킴으로써 수정 후 낭배기 이전
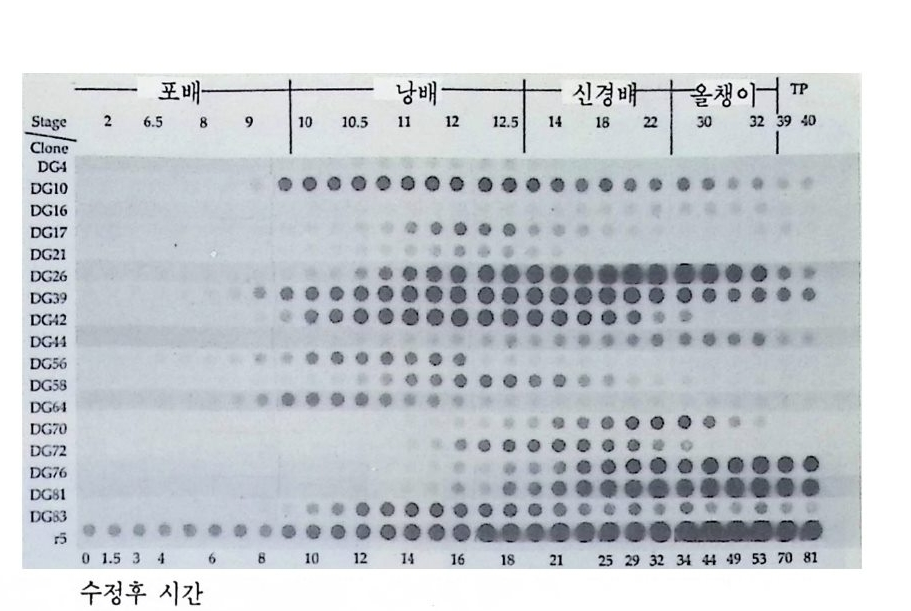 -DDDDDDDDDDCDDDD5DlLGGCGGGGGGGGGGGo .lC&274 7i865n這r IllJ . 24”O 66056』c271IeJ 6.5 포 배 8 o-•. ••.•-l••• .••。 ••••.•1•••0•.•..5 • •.••.•• ~••• .•.• H•• •..• i•• •.•.•j•••• .:••.••0•• .- ••.•••••• :. •.••• ••仁. ••••••.•• . ••••••산.• • •. ••1••.•• .••.•.••• H를.•.••••• • .•.•••~••'C ! ! ••. •••.. 쟁 •.•••. ,0 •.• •鬪•.• .•• . 9, T•.••P따
-DDDDDDDDDDCDDDD5DlLGGCGGGGGGGGGGGo .lC&274 7i865n這r IllJ . 24”O 66056』c271IeJ 6.5 포 배 8 o-•. ••.•-l••• .••。 ••••.•1•••0•.•..5 • •.••.•• ~••• .•.• H•• •..• i•• •.•.•j•••• .:••.••0•• .- ••.•••••• :. •.••• ••仁. ••••••.•• . ••••••산.• • •. ••1••.•• .••.•.••• H를.•.••••• • .•.•••~••'C ! ! ••. •••.. 쟁 •.•••. ,0 •.• •鬪•.• .•• . 9, T•.••P따
그림 4_29 X e no pt lS 의 발생 단계 에 따른 17 종류의 유전자 발현의 변화. 각 단계 로부터 추출한 RNA 와 방사능 동위원소로 표지한 DNA 를 dot blo tting법으 로 재결합시켜 유전자 발현 여부를 알아내었다 (Sar g en t and Daw id, 1983).
에 새로 발현된 유전자를 cDNA 의 형태로 분리해낼 수 있다. 이렇 게 분리된 cDNA 를 유전자 재조합법으로 증폭시켜 발생 단계에 따라 특이하게 발현되는 mRNA 의 종류를 알아내는 데 이용하였다. 이러 한 기술을 subtr ac ti on clo ni n g이라고 한다. 사아젠트와 다빗는 1 세 포기에서 tai lb ud s t a g e 에 이르는 발생배로부터 mRNA 를 단계별로 분리 하여 nit ro cellulose memberane fi l t er 에 s p o t하여 한 장의 filte r 에 모든 단계의 mRNA 가 포함되도록 하였다. 그 다음 subtr a cti on t echn iq ue 과 유전자 재조합법으로 증폭시키는 과정에서 방사능 동위 원소로 표지 한 낭배 특이 cDNA 에 mRNA 가 s p o t된 nitro cellulose filt er 를 넣 어 줌으로써 상보적 인 DNA 와 RNA 사이 에 재 결합이 이루 어지도록 하였다. 재결합되지 않은 cDNA 는 씻어버리고 결합된 cDNA 만울 자기 방사법으로 x-ray fi lm 에 옮겨 관찰함으로써 낭배 기 에 특이하게 발현되는 유전자가 다른 단계의 발생배에서도 발현되는
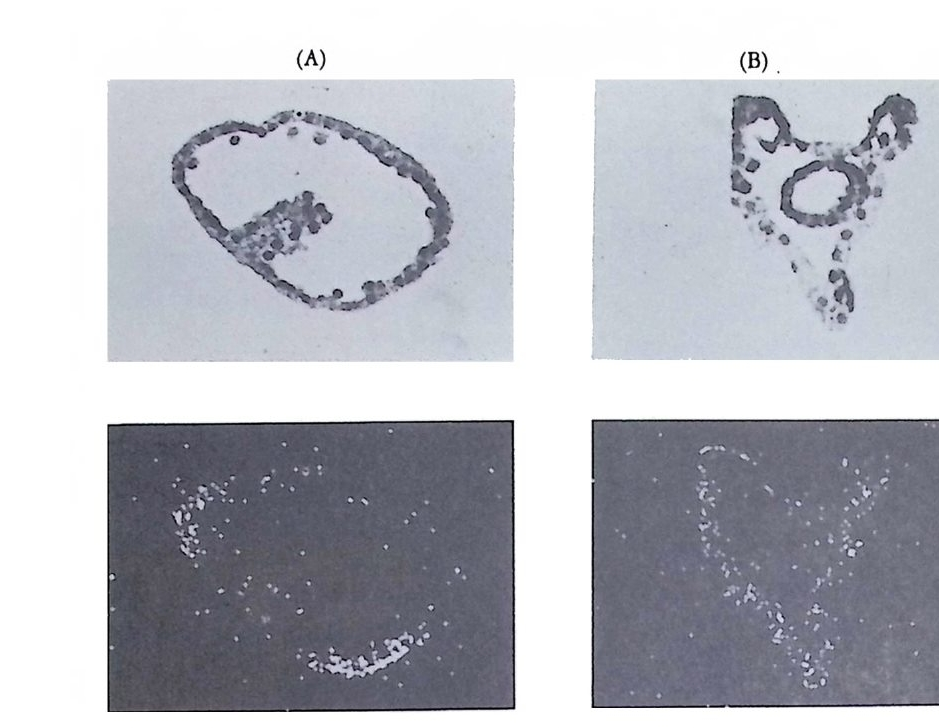 (A) (B) .
(A) (B) .
그립 4-30 성게의 의배영 특이 mRNA의 분포. 낭배중기 (A) 와 풀루티우스 유 생 (B) 에 분포되어 있는 의배영 특이 mRNA 를 in situ 재결합법으로 확인 하였다 (L ynn et al., 1983) .
지의 여부를 확인할 수 있었다. 그림 4-30 은 17 개의 유전자가 발생과 정중 어느 단계에서 특이하게 발현되는지를 dot blott ing 기술을 사용 하여 보여준 실험결과이다. 이들중 어느 유전자도 수정 후 7 시간의 포배 전이 (midb lastu la tr ans iti on) 시기 이전에 발현되지 않았다. 그러 나 DG64, DG39 와 같은 유전자는 포배 전이 시기직후 발현되기 시작 하였고, DG72, DG81 과 같은 유전자는 낭배중기에 발현되는 것으로 나타났다. 어떤 유전자는 일단 발현되기 시작하면 지속적으로 발현되 는 것으로 나타났고, 어떤 유전자는 그 발현이 순간적으로만 나타났 다. 그러나 지속적으로 발현되는 유전자도 앞으로 계속적으로 발현될 것인지는 알 수 없다. 이와 같은 Xenop us 의 예는 특별히 유전자 발 현의 시간적 선택성을 보여주는 좋은 예라고 하겠다.
참고문헌 Bemrnoaursde, i m0. m, oHuonzougm lo ib , uNlin: a lingdh t Tc hoanieng ga we n ae, s Sbe. f o( 1r9e 7 a8n) d. Safetq e ur e snocmesa toi cf chang e. C ell 15: 1133- 1 144. Brack, C., Hir a ma, M., Lenhard-Schuller, R. and Tonega w a, S. ( 1978) . A comp le te im munog lo bulin gen e is create d by somati c recombin a ti on . Cel l 15: 1~ 1 4. Brown, D. D. and Dawi d, LB. (1968). Spe c if ic gen e amp li fi ca ti on in oocyt es . Scie n ce 160: 272-280. Brown, S.W. and Nelson-Rees, W. A. (1961) . Radia t i on analys i s o f a lecanoid gen eti c sys t e m n. Geneti cs 46: 983- 1 007. Burkholder, G.D . (1976) . Whole mount electr o n mic r oscop y of pol yt en e chromosome from Drosop hi la melanoga s te r. Can. ]. Genet. Cyt ol. 1s: 67-77 . Burnett, F.M. (1959). The Clonal Selecti on Theory of Immunity . Vanderbil t P ress, Nashv ille . Cente r wall, W .R. and Benir s chke, K . (1973) . Male tor t oi s e shell and calico (T-C) cats . ]. Hered. 64: 272-278. Coop er , D. W., Vandeberg, J.L., Shannen, G.B. and Poole, W.E. (1971) . Phosph o g ly c e rate kin a se pol vrnorp h is m in kanga r oos pro - vid e s fur th e r evid e nce for pat e r nal X ina cti va ti on . Natu r e new Bio l. 230: 155-157. Crews, S., Griff in, J ., Huang, H., Calame, K. and Hood, L. (1981) . A sin g l e 따 gen e segm e nt encodes the im mune respo n se to pho sph o r- ylc holin e : Somati c muta t i on is correlate d wit h the class of the anti bo dy. Cell 25: 59-66.
Daneholt, B., Case, S.T., Hy de , J., Nelson, I and Weis la nder, L. (1976). Producti on and fate of Balbia n i rin g pro ducts . Prag. Nucleic Acid Res. 19: 319-334. Dav ids on, R.G ., Nit ow sky, H.M. and Ch ild s, B. ( 1963) . Demonstr a ti on of tw o po pu l ati on s of cells in the human fem ale hete r ozyg o us for glu cose-6-ph o sph a te dehyd r og en ase varia n ts . P roc. Natl. Acad. S ci . USA 50: 481-485. Davi s, M.M., Calame, K., Early, P.W. , L iv a nt, D.L. , Joh o, R., Weis s- man, I.L. and Hood, I. (1980) . An irn munog lo bulin heavy chain gen e is f orm ed by at least t w o recombin a ti on al events . Natu r e 283: 733-739. Davi s, M.M., Kim , S.K . and Hood, L. (1980) . Immunog lo bulin class swi tch i ng : Develop m enta l ly regu la te d DNA rearrange m ents durin g differ enti at i on . Cell 22: 1-2. Edelman, G.M. (1 970) . The stru c tu re and func ti on of anti bo die s . Sci . Am. 223 (2) : 34-42. Galau, G.A . , Klein , W.H., Davi s, M.M., Wold, B.J. , B ritt en , R.J. and Davi ds on, E.H. (1976) . Str uc tu ral gen e sets acti ve in embry o s and adult t issu es of the sea urchi n. Cell 7: 487-505. Gart ler , S.M. and Rig gs, A.D . (1983) . Mannalia n X-chromosome ina cti va ti on . Annu. Rev. Genet. 17: 155-190. Ga rtler , S.M., R ive st M. and Cole, R.E. (1980) . Cy tolo g ica l evi de nce for an ina cti ve X chromosome in mu rine oog on ia . Cyt og e n et. Cell Genet. 28: 203-207. Gehrin g , W. J. and Paro, R. (1980) . Isolati on of a hyb r id pla smi d wit h homolog ou s sequ e nces to a tran spo sin g element of Drosop hil a , melo ,no g as te r. Cell 10: 897-904. Green, M.M. (1980) . Transpo s able elements in Drosoph il a , and oth e r
dip ter a. Annue Rev. Genet. 14: 109-120. Grossbach, U. (1973) . Chromosome puffs and gen e exp re ssio n s in pol yt en e cells. Cold Spr ing Harbor Sym p. Quan t. Bio l. 38: 619-627. Hoeij m akers, J.H .J., Frasch, A.C.C., B ernards, A., borst, P. and Cross, G.A .M . (1980) . Novel exp re ssio n -lin k ed cop ies of the gen es for varia n t surf ac e anti ge ns in trypa nosomes. Natu r e 284: 78-80. Hozumi , N. and Tonega w a, S. (1976) . Evi de nce for somati c re- arrange m ent of im munog lo bulin gen es codin g for varia b le and consta n t regi on s. Proc. Natl. Acad. Sci. USA 73: 3628-3632. Jud d, B.H . and Young, M.W. (1973). An exami na ti on of the one cist ro n-one chromomere concept . Cold Spr ing Harbor Sym p. Qu ant. Bio l. 38: 573- 5 79. Kratz e r, P .G. and Chap m an, V.M . (1981) . X-chromosome reacti va - tion in oocy tes of Mus caroli. Proc. Natl . A cad. Sci. USA 78: 3093 -3097. Lambert , B. (1972) . Rep ea te d DNA sequ e nces in a Balbia n i rin g . J Mol. Bio l. 7 2: 65-75. Lambert, B . and Daneholt, B. (1975) . Mi cr oanalys i s of RNA from defi ne d cellular comp on ents . Meth o ds Cell Bio l. 10: 17-47. Ly on , M. F. (1961) . Gene acti on in the X-chromosome of the mouse (Mus mztS c ulus L.) . Natu r e: 190: 372-373. McClin t o c k, B. (1952) . Chromosome orga n i za ti on and gen i c e xpr e s- sio n . Cold Spr ing Harbor Sym p. Quan t. Bio l. 16: 13-47. Mi geo n, B.R. (1971) . Stu d i es of ski n fibr oblasts from ten familie s wit h HGPRT defi ci e n cy, wit h refe re nce to X-chromosomal ina cti va ti on . Am. J Human Genet. 2 3: 199-209. Mig eo n, B.R. and Jela lian , K. (1977) . Evi de nce for tw o acti ve X- chromosomes in gen n cells of f em ale befo re meio t ic entr y. Natu re
269: 242-243. Mohandas, T., Sp a rkes, RS., Helkuhl, B., Brzesch ik, K.H . and Shapi ro , L.J. (1980) . Exp re ssio n of an X-lin k ed gen e from an ina cti ve human X chromosome in mouse-human hyb r id cells: Fu rthe r evi de nce for the non-in a cti va ti on of the ste r oid sulfa tas e locus in man. Proc. Natl. Acad. Sci . USA 77: 6759-6763. Moore, K.L. (1977) . The Develop ing Human, Saunders, Phil a delph ia . Moss, T. (1983) . A tra nscrip tion al fun cti on for the repe t it ive rib o somal spa cer in Xenop us laevis . Natu r e 302: 223- 22 8. Pete r son, J.A . and Weis s, M. C. (1972) . Exp re ssio n of dif fere nti at e d fun cti on s in hep a to m a cell hyb r id s : Inducti on of mouse albumi n pro ducti on in rat hep a to m a-mouse fibr oblast hyb r id s . Proc. Natl. Acad. Sci . USA 69: 571- 57 5. Rubin , G.M., Brosein , W.J. , D unsmuir , P., F lavell, A.J., Lavis , R., Str ob el, E., Toole, J.J. and Young, E. (1980) . Cop ia-1 i ke tra nspo sa- ble elements in Drosop h ila gen ome. Cold Spr ing Harbor Sym p. Quan t. Bio l. 45: 619-628. Sarge n t, T.D . and Dawi d, I. (1986) . Differ enti al gen e expr e ssio n in the gas tru la of Xenopu s laevis . Scie n ce 222: 135-139. Seid m an, J.G ., Max, E.E . and Leder, P. (1979) . A im munog lo bulin gen e is form ed by site -s pe c i fic recombin a ti on wit ho ut furthe r somati c muta t i on . Natu r e 2so: 370-375. Sharman, G.B. (1971) . Late DNA rep lica ti on in the pa te r nally der- ive d X chromosome of fem ale kang a roos. Natu r e 230: 231-232. Sh im oto h no, K., and Tern in, H.M. (1980) . Evoluti on of retr o v iru ses from cellular moveable gen etic elements . Cold Spr ing Harbor Sym p. Quan t. Bio l. 45: 719-730. Spr a dlin g , A.C. and Mahowald, A.P. (1980) . Amp lifica ti on of gen es
for chorio n pro te i n s durin g oog en esis in Drosoph i la me lan oga s te r. Proc. Natl . A cad. Sci. USA 77: 1096-1100. Str at h e rn, J.N . , New ton , C.S ., Herskowi tz, I. and Hic k s, J.B . (1979) . Isolati on of a cir c ular deriv a ti v e of y ea st c hromosome. I ll. lmp li ca - tion s for the mechan ism of mati ng type int e r conversio n . Cell 18: 309-319. Swanson, C.P ., M erz, T. and Young, W.J. (1981} . Cyt o g e n eti cs: The Chromosome in Div is i o n , Inherit an ce, and Evoluti on , Second Edi· tion . Prenti ce -H a ll, Eng le wood Cli ffs, N J . Wats o n, J.D . (1976). Molecular Bio lo gy of the Gene, Th ird Edit ion . Benja m i n / Cummi ng s , Menlo Park, CA . Weis la nder, L. and Daneholt, B . ( 1977} . Demonstr a ti on of Balbia n i rin g RNA sequ e nce in pol ys o mes. ]. Cell Bio l. 7 3: 260-264.
제 5 장 순차적 유전자 발현의 조절 진핵생물에서의 세포분화는 시간과 공간에 따른'순차적 유전자 발 현에 기인한다고 할 수 있다. 발현될 유전자가 선택되어 전사된 다 음, RNA pro cessin g , 해독 및 후 해독과정을 거쳐 기능을 가전 단 백질이 만들어진다. 이러한 여러 과정을 거쳐 나타나는 유전자 발현 이 그 과정을 거칠 때마다 알맞게 조절됨으로써, 발생단계에 따라 그 리고 세포 종류에 따라 선택적 발현이 가능하다. 물론 유전자 발현의 조절기구가 현대 발생학에서 완전히 파악되기는 어렵지만, 이러한 문 제에 대한 개념적 이해를 돕기 위해서 우선 염색질의 물리적 구조와 유전자의 화학적 성질에 대하여 알아보는 것이 기본적으로 중요하다. 1 염색질의 구조 세 포주기 (cell cyc l e) 를 통해 염 색 체 의 크기 가 응집 (condensati on ) 정 도에 따라 다르게 나타난다. 세포분열기에 응집되고, 합성기 (S 기)에
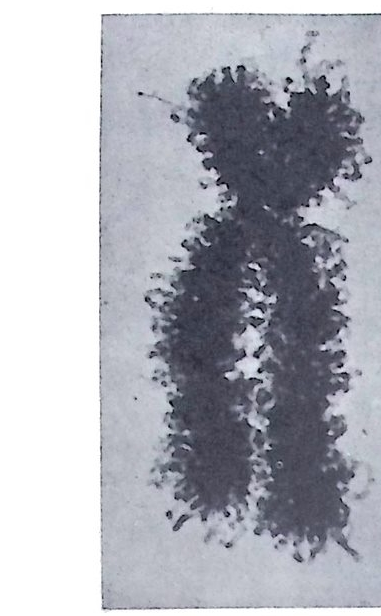
그림 5-1 전자현미경으로 본 사람의 염색체 x2 9,6 0 0 (DuPraw. 1970)
풀린다. 그러나 풀리는 정도는 제한되어 있기 때문에 염색체를 이루 는 DNA는 핵 속에서 완전한 길이로 풀리는 경우가 없다. 인위적으 로 사람의 염색체를 풀어놓았다고 할 때 염색체를 이루는 DNA 의 길 이는 1. 4~7.3cm 에 달한다. 그러나 이러한 염색체는 세포분열 중기 죽 염색체가 가장 응집된 상태에 있을 때 2~lOX10-4cm 에 그친다. 죽 염색체를 이루는 DNA 길이의 1.4 ~36X 10-3 배로 그 길이가 줄어 드는 셈이다. 세포주기를 통한 염색체의 길이의 변화나 염색체 응집을 일으키는 물리적인 힘의 출처는 염색질의 화학적인 조성에 있다. 염색질은 DNA 와 히스톤(hi s t one) 단백질의 결합으로 이루어져 있다. 히스톤은 리신이나 아르기닌과 같은 염기성이며 양성으로 하전된 아미노산아 다량 들어 있어 단백질 전체가 염기성을 띠고 있다. 히스톤은 리신과 아르기닌의 양적 비율에 따라서 달라지는데, 리신이 아주 풍부한
Hl, 리신이 적당히 들어 있는 H2A 와 H2B, 그리고 아르기닌이 풍 부한 H3 와 H4 의 5 종으로 나뉜다. 일반적으로 동물, 식물 및 원핵 생 물에서 이 5 종의 히스톤이 공통적으로 발견되는데, 조류와 양서류의 적혈구와 같은 몇 종류의 세포에서 H5 가 발견되었다. H5 는 H1 을 대신하는 히스톤으로 H5 가 들어 있을 경우 DNA 의 응집정도는 대단 히 높다. 히스본의 역할은 DNA 와 결합하여 DNA 를 응집시키는 것 인데 , 염색질은 DNA 가 일정한 간격으로 꼬인 모양으로 나타난다. DNA 응집의 가장 기본적인 단위인 꼬임의 구조를 누클레오솜 (nucleosome) 이라고 한다. 누클레오솜은 직경이 125A 인데 단백질 분 해 효소인 트립신을 처리하면 구형(球形)의 모양이 풀리는 것으로 보 아서 이러한 구형의 누클레오솜 구조는 DNA 와 히스톤의 결합으로 인하여 생기는 구조임을 알 수 있었다 (Sahasrabuddhe and Van Holde, 1974) .
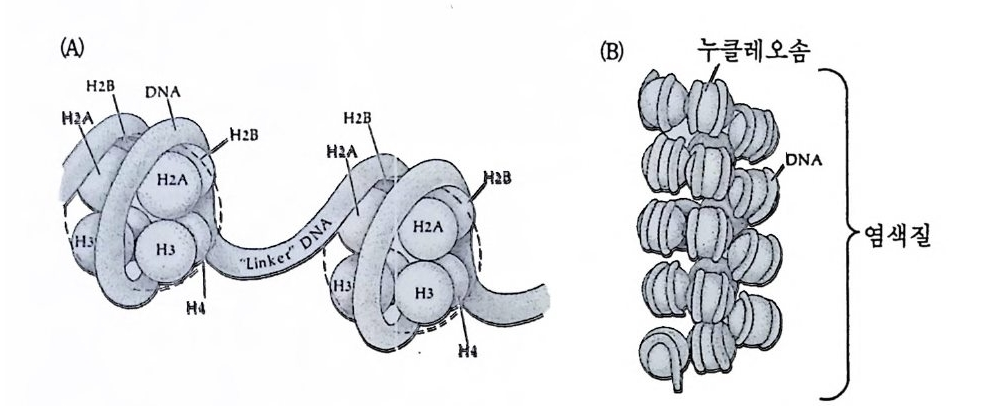 h (B) 누쿨레오솜
h (B) 누쿨레오솜
그립 5-2 누클레오송의 모형 (A) , 누곧레오송의 배열에 대한모형 (B) (Wolf e, 1983 ; Ste w art and Hunt, 1 982} .
누클레오솜의 구조를 알아내는 대 여러 가지 방법이 사용되었다. 가장 유용한 방법 의 하나는 염 색 질을 DNAse (micr ococcal nuclease) 로 처리한 다음 토막난 염색질을 관찰하는 것이었다. DNAs 여卜 아주 간 단히 처리한 다음 토막난 염색질을 설탕구배에 얹어 원심분리하여 얻
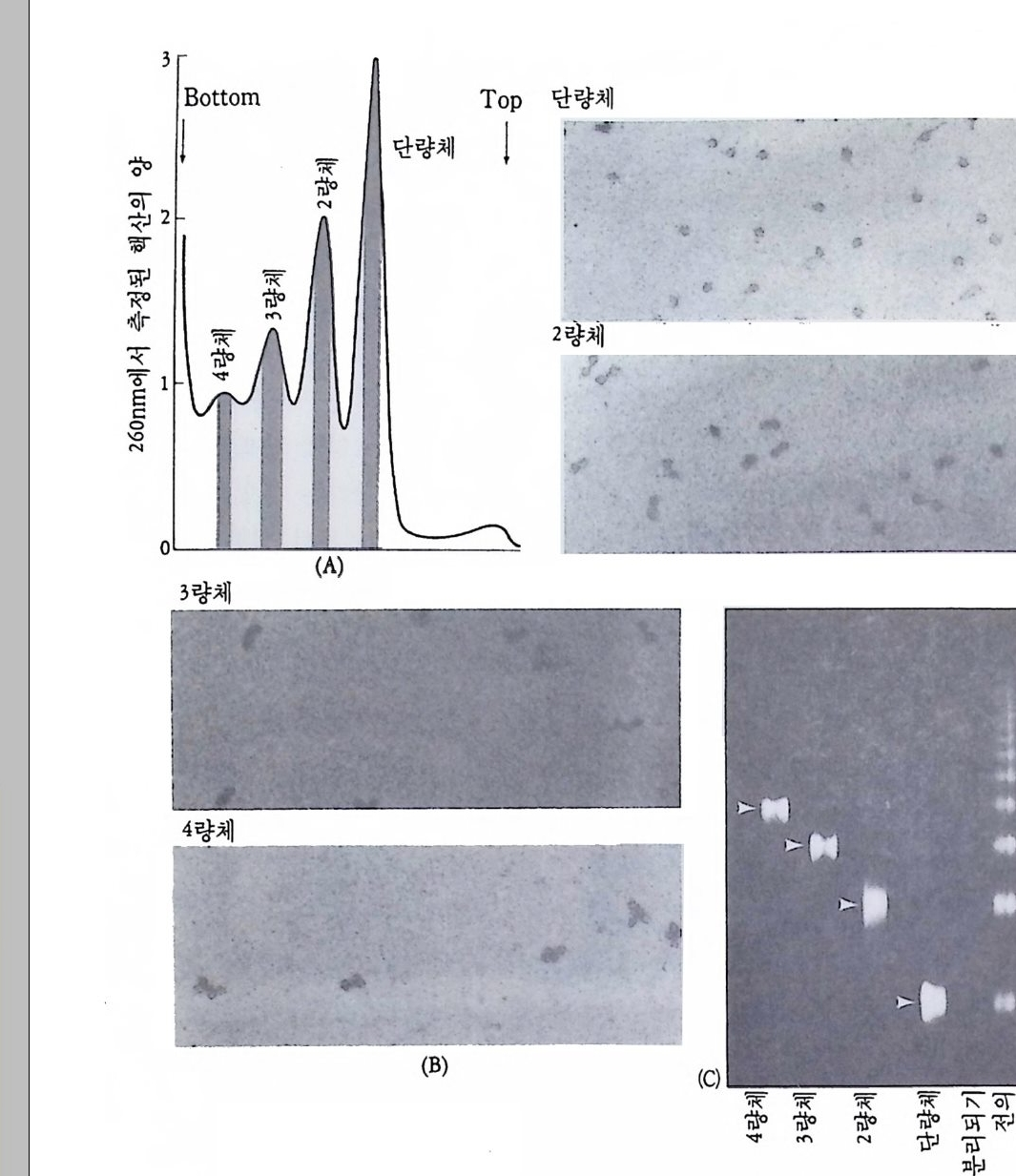 3
3
그립 5-3 누클레오솜 다량체의 특칭. (A) 쥐 간세포의 염색질을 DNAse I 으로 처리한 다음 설탕 농도구배로 분석한 결과 (B) 설탕농도구배로 분리한 4 개 의 pe ak 를 전자현미경으로 관찰한 결과 (C) 설탕농도구배의 각 pe a k.2로부 터 DNA 를 추출하여 전기영동으로 분석한 결과. 겔의 오른쪽 줄은 설탕농 도구배로 분리하기 전 DNAse 로 처리하여 전기영동한 것임 (Fin c h et al., 1975)
은 염색질 토막을 전자현미경으로 관찰하였다• 설탕구배를 260run 의 파장으로 scan 하여 여러 개의 p eak 를 관찰할 수 있었고, 각 p eak 의 염색질 토막을 전자현미경으로 관찰하여 몇 개의 누클레오솜으로 이 루어진 토막인가를 알아내었다. 다음 각 구배의 p eak 로부터 분리한 염색질 토막으로부터 DNA 를 추출하고 전기영동하여 한 개의 누클레 오솜울 이루는 데 필요한 DNA 의 염기수를 알아내었는데, 그 수는 200 염기쌍 (base p a i r) 에 달했다 (He wi sh and Burgo y n e , 1973 ; Noll, 1974). DNAse 를 처리한 염색질 토막을 전자현미경으로 다시 관찰해 본 결 과 200 개의 염기쌍을 가진 염색질 토막은 짧은 꼬리가 달린 구형의 모양을 가지고 있었고 400 개의 염기쌍을 가전 토막에는 두 개의 구형 체, 600 개의 영기쌍을 가진 토막에는 3 개의 구형체가 관찰되었다 (Fiu n ch et al., 1975). 따라서 누클레오솜 한 개는 200 염기쌍으로 이루 어져 있고, DNAse 에 의하여 200 염기쌍의 단위로 해체되는 것으로 풀이되었다. 그러나 DNAse 를 좀더 강하게 처리해 주면, 한 개의 누클레오솜에 관여하는 영기쌍 수가 점차 감소하는데, 감소의 한계가 140 염기쌍에 서 나타난다. 즉 140 염기쌍 이하로는 DNAse 에 의해 분해되지 않은 사실을 알게 되었다. 이와 같이 두 단계의 DNAse 를 처리한 다음 140 염기쌍과 결합되어 있는 히스톤을 분석하여 140 개의 염기쌍당 H2A, H2B, H3 및 H4 가 각각 두 개씩 들어 있음을 알 수 있었다 (Thomas and Kornberg, 1975). 즉 한 개의 누클레오솜은 140 개의 염 기쌍과 8 량체의 히스몬 (8 량체 =4 량체 X2) 으로 이루어져 있고, 200 개의 염기쌍 중 140 개를 제의한 60 개의 염기쌍은 은 누클레오솜 사이를 이 어주는 연결체 (li nker) 의 역할을 하고 있다. DNAse 로 강하게 처리하 기 전 200 개의 염기쌍을 가지고 있는 염색질 토막으로부터 단백질을 추출하여 분석해 보면 4 종류의 히스톤의에 Hl 이 들어 있음을 알 수 있었다. 즉 연결체인 60 개의 염기쌍에 Hl 이 결합되어 있다. 시험관 에서 히스톤과 DNA 를 적절한 조건 하에 둠으로써 누클레오솜을 인
위적으로 합성시킬 수 있었다 (Kornber g and Thomas, 1 97 4) . 우선 H2A, H2B, H3 및 H4 를 섞 어 주면 H2A 와 H2B 의 4 량체 및 H3 와 H4 의 4 량체가 형성된다 . 여기에 DNA 를 넣어 주면 물리적 및 화학 적인 성질이 정상적인 누클레오솜과 동인한 구조를 형성한다. 이와 같은 결과로서 DNA 가 히스톤의 8 량체를 둘러싸서 누클레오솜을 형 성하며 누클레오솜은 일정한 간격을 가지고 반복되는 것을 알 수 있 었다.
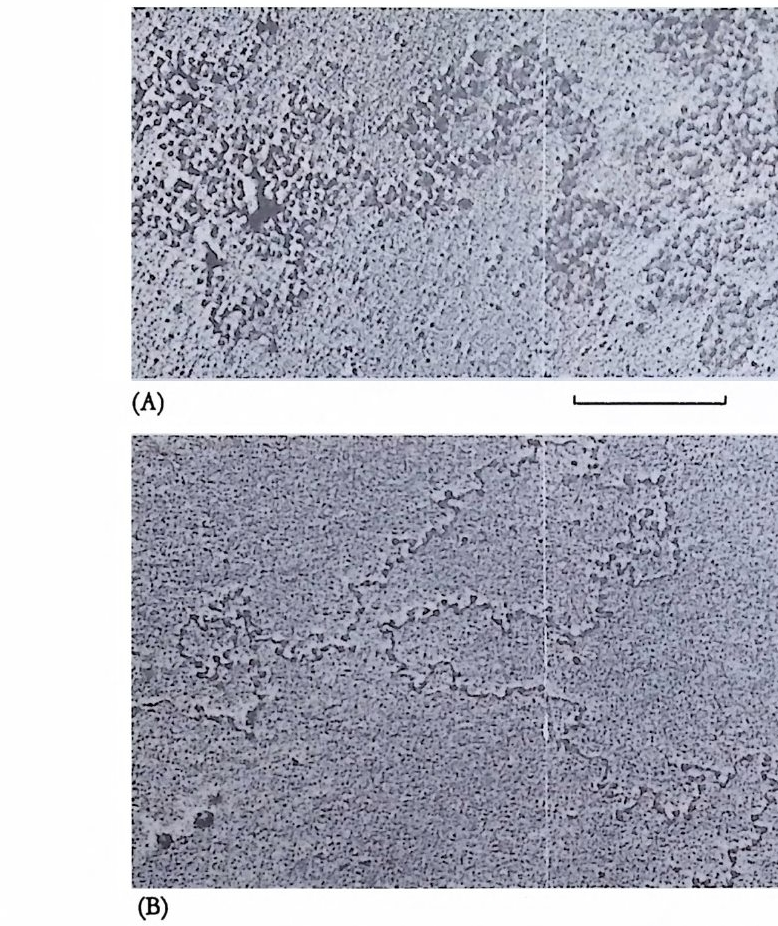 (A) ’ ’
(A) ’ ’
그림 5-4 염색질을 응축시키는 Hl 히스돈의 역할. (A) 닭의 간세포로부터 추 출한 염색질 (B) Hl 만을 제거시켰을 때의 영색질 (Ou tl e t et al., 1975)
Hl 은 연결체에 결합되어 있는데, Hl 이 결핍될 경우 염색질에 구 조적인 변화가 일어난다. 핵에서 직접 얻은 염색질을 전자현미경으로 보면 대단히 심하게 응집되어 있는 염색질을 볼 수 있는데, 만약 Hl 울 제거시키면 염색질은 상당히 긴 연결체에 누클레오솜이 비교적 잘 드러나는 모양을 가진다. 이러한 점으로 보아서 Hl 은 특별히 염색질 울 응집시키는 것으로 생각된다. 세포분열시 일어나는 염색체의 응집 현상은 Hl 히스톤에 의해서 가능한 것으로 보인다. 또한 진정 염색 질과 이질 염색질에 응집 정도의 차이가 있는데 이것도 Hl 의 변화에 의하여 조절되는 것으로 생각되고 있다. 이와 같 이 염색질은 누클레오솜이라는 단위로 일차적으로 꼬여 있 으나 꼬임은 그 위에 여러 차례 가중되어 핵 속에서의 염색질의 구조 는 복잡하다. 그러나 이들 염색질을 이루는 DNA 로부터 선택적으로 유전자가 발현된다. 누클레오솜은 고르게 염색질을 따라 형성되어 있 고 누클레오솜에 관여하는 히스톤의 성분이 동일한 것으로 보아 누클 레오솜 자체가 선택적인 유전자 발현에 조절 역할을 할 것이라고 기 대하기는 어렵다. 히스몬이 DNA 에 강하게 밀착되어 있는 한 DNA 는 전사되지 않는 다. DNA 가 전사되기 위해서는 우선 RNA 중합효소가 DNA 에 부착 되어야 하는데, 누클레오솜이 있는 한 RNA 중합효소의 부착은 불가 능하다. 그러나 누클레오솜에 변화를 주면 RNA 중합효소의 부착이 가능해지고 DNA 는 전사된다. 2 진핵세포 게놈의 특징 진핵세포의 게놈과 원핵세포의 게놈 사이에는 구조적인 면과 기능 적인 면에서 대단한 차이가 있다. 이러한 차이는 유전자 발현의 조절 기구의 차이룰 반영하는 것으로 진핵세포 게놈의 특칭을 이해하는 것
은 중요하다. 진핵세포의 게놈은 일반적으로 원핵세포의 게놈에 비하 여 엄청나게 크다. 예를 들어 Esclwr ich ia col i의 게놈의 크기는 4. 2X10 명기쌍인 데 비하여 사람의 게놈크기는 3 . 3X10 명기쌍으로 거 의 800 배나 더 크다. 게놈 크기 (ge nome s i ze) 는 반배수체의 염색체에 들어 있는 DNA의 함량을 길이, 무게, 혹은 염기쌍의 수로 표시한 것이다. 그러나 놀라운 사실은 비록 원핵세포의 게놈 크기가 작을지 라도 진핵세포에서 합성되는 효소를 거의 모두 합성한다는 것이다. 전통적인 유전학적 방법으로 사람의 유전자의 수를 산출해 보면 약
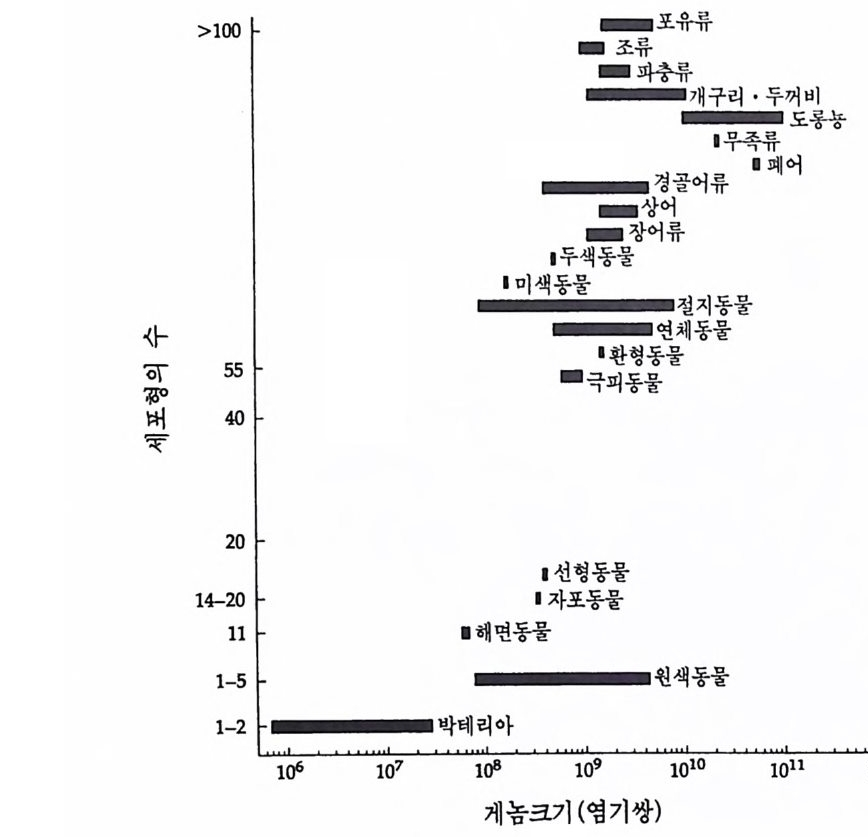 >100 -포유류
>100 -포유류
그립 5-5 여러 종의 생물의 게놈 크기 비교 (Ra ff and Ku nfma n, 1983).
5 X l 어 정도라고 하는데 사람의 게놈 크기로 최소한도 2 X 106 개의 유 전자가 이론적으로 가능한 점으로 보아 진핵세포의 게놈 크기가 필요 이상으로 크다는 점을 알 수 있다. 그러나 이러한 현상이 세포분화의 관점에서 볼 때 어떠한 의미를 가지는지는 아직 분명치 않다. 또한 고등한 동물의 게놈 크기가 하등동물의 것보다 일반적으로 크다는 사 실을 알 수 있다. 그러나 양서류와 같은 종류에서는 게놈 크기의 폭 이 대단히 크다. 특별히 도롱뇽의 게놈 크기는 사람의 것보다 100 배 이상이나 크다. 이러한 현상은 양서류가 사람보다 더 많은 유전자를 필요로 하는 것이라고 보기는 어렵다. 3 DNA 재결합 진핵세포의 DNA 의 특징을 알아내는 데에는 DNA 재결합법 (DNA rena t ura ti on) 을 이용해 왔다. 이 방법은 DNA 이중나선의 상보성을 이용한 것인데, 단일 나선의 DNA 조각들이 농도와 시간에 따라 재 결합하는 속도를 기준하여 동일한 염기서열을 가진 DNA 의 반복정도 를 측정함으로써 DNA 를 분류할 수 있다. 그러나 동일한 염기서열을 가진 DNA 의 재결합이 빠른 속도로 일어나기 때문에 일단 재결합반 응이 부분적으로 일어나면 나머지 부분의 재결합반응은 물리적으로 불가능해진다. 일정한 길이로 DNA 를 토막내지 않으면 동일한 서열 울 가진 DNA 토막끼리의 충돌을 좀더 효과적으로 유발시킬 수 없다. French p ress 나 초음파분쇄기 (ul tr aso ni ca t or) 를 이용하여 450 염기쌍의 크기로 DNA 를 토막낸 (shea ring) 다음 90° 이상의 열을 가하든가 알칼 리를 처리하여 단일나선으로 변성 (dena tur e) 시켜준다. 열을 이용하여 이중나선을 결합시키고 있는 수소 결합을 끊어중으로써 DNA 가 변성 되는 것인데, 이때 온도 변화의 중간 온도를 DNA 의 융점 (mel ting tem p er atu re, Tm) 이라고 한다. 변성 직후 온도를 Tm 에서 20~25° 이 하로 떨어뜨려 주면, DNA 토막들이 짝을 찾아 재결합하기 시작한
다. 재결합 정도를 측정하는 데에는 두 가지 방법이 있다. 파장 26orun 에서 DNA 는 변성 정도에 따라서 파장 흡수도가 달라진다. 이 률 hyp o chromi c sh ift라고 하는데 변성 전 DNA 의 흡수도에 바 하여 약 40% 가 증가한다. 따라서 재결합 반응에 따라 감소하는 흡수도로 부터 재결합 정도를 산출해낼 수 있다. 또 다른 방법으로는 hydroxy a p a tit e( 일종의 calciu m p hos p ha t e) 를 이용하는 것이다. hy drox y a p a tit학근 인산 완충용액 (ph osph a te bu ff er) 의 낮은 농도에서 는 단일 나선만을 통과시키고 이중나선을 보유하며, 높은 농도에서는 이중 나선까지 모두 통과시키는 성질을 가지고있다. 일정한 시간 동 안 반응한 DNA 용액을 hyd r oxy ap a t i te column 에 얹어 단일 나선과 이중 나선을 분리하여 각각을 측정함으로써 재결합 정도를 측 정할 수 있다. 재결합 반응은 상보적인 두 종류의 분자간에 일어나는 것이므로, 그 반응속도가 이 차 반응속도 (second order reacti on ) 를 따른다. 반응 속도는 반응시간과 DNA 의 농도에 따라 변한다. 반응시간을 오래 끌 면 재결합 정도가 시간에 따라 증가할 것이고 DNA 농도를 높이면 재결합 반응속도가 빨라진다. 따라서 재결합 반응속도는 반응시간과 DNA 농도의 복합적인 요인에 의해서 좌우된다. 재결합 반응을 시작 할 때의 DNA 농도 (Co) 에 시간(t)을 곱해준 Co t를 기준으로 반응속 도를 평가함으로써 한 종류의 DNA 를 염기서열의 반복 정도에 따라 분류하거나 혹은 서로 다론 DNA 를 비교할 수 있다. 만약 한 게놈에 서 염기서열의 반복정도가 높은 DNA 부위가 있다면 이 부위의 DNA 토막의 용액내에서의 농도는 높을 것이고 반응속도도 빨라진다. 따라 서 Co t값이 낮을 때 이미 반복적 인 DNA의 재 결합은 끝난다. 반대 로 거의 반복성이 없고 유일하게 게놈 속에 존재하는 부위의 DNA 토 막의 농도는 대단히 낮을 것이므로 반응속도는 엄청나게 느리다. 따 라서 Co t의 값이 높은 때에만 이러한 DNA 의 재결합 반웅이 일어난 다. 이와 같이 재결합법으로 게놈내의 DNA 의 반복정도에 따라
DNA 를 분류할 수 있다. 즉 DNA 를 이루는 영기서열의 복잡도 (DNA com p lex ity)를 알 수 있다. 또한 이러한 방법으로 게놈의 크기 도 알아낼 수 있다. DNA 복잡도는 생물의 종류에 따라 다른데, 특 히 진핵세포와 원핵세포 사이에는 뚜렷한 차이가 있다. 만약 영기배열 순서가 반복되지 않고 유일하게 존재하는 유일성 DNA의 경우에서는 재결합 반응에 대한 Cot curve 가 두 단계의 log ar ith m i c scale 에서 표현된다. 그러나 유일한 배열순서의 DNA 만 이 아니라 여러 단계의 반복정도를 가진 반복 배열 순서의 DNA 의 Cot curve 는 더 광범위한 log a rith m i c scale 에 넓게 퍼져서 나타난다. 우선 유일성 DNA 에서의 재결합반응의 예를 들어 보기로 하자. 원 핵세포의 DNA 는 거의 모두가 유일성 DNA 이므로 2 단계에 걸친 이 상적 인 Cot curve 로 재 결합 반응을 일으킨다. 박테 리오파아지 인 T4 는 1.5 X 10 명기쌍의 게놈 크기를 가전 DNA 이고, E. co i l 는 4.2X106 염기쌍의 게놈크기를 가전 DNA 이다. 이들 DNA 의 재결합은 모두 이상적인 Co t곡선을 따라 일어나는데, 반응이 일어나는 Co t의 영역 이 게놈 크기의 차이에 따라 다르게 정해진다. T4 의 Co t곡선이 E.
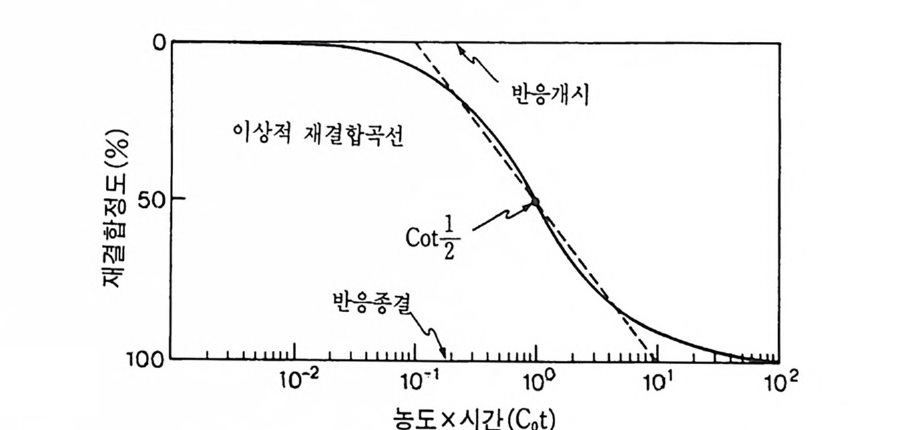 。
。
그립 5-6 이상적 Co t곡선. 백분율로 나타낸 재결합 정도를 DNA 의 농도와 시 간의 곱인 Co t에 따라 그리면 두 단계의 log ar it hmic scale 에 분포하는 그 립이 나온다 (B ritt en and Kohn, 1968}.
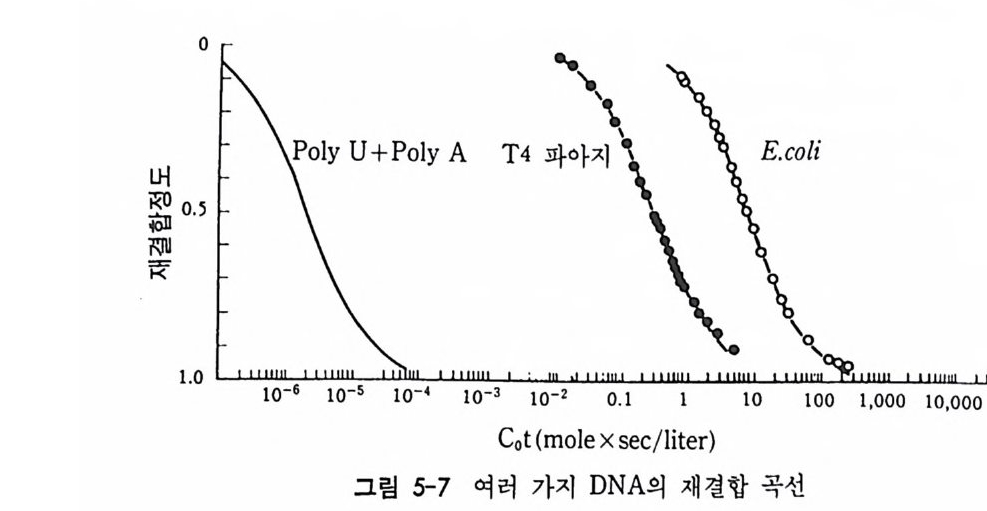 。
。
Col i의 것에 비해 낮은 Co t영역에서 일어난다. 이러한 Co t영역의 차 이룰 직접 비교하기 위하여 Co 담 (hal f Co t)를 이용하는데, 재결합이 50% 까지 일어났을 때의 Co t의 값을 Co t卓이라고 한다. T4 DNA의 Co t21一 는 0.3 mole x sec/l it er 이며 E. coli D NA의 Co t1j 는 T 4 의 30 배인 10 molexsec/l it er 이다. 따라서 한 종류의 게놈 크기를 알면 Co t곡선을 비교하여 다른 종류의 게놈 크기를 알 수 있다. 이러한 게놈크기의 산출은 사실상 이상적인 Co t곡선을 가지는 DNA 에서만
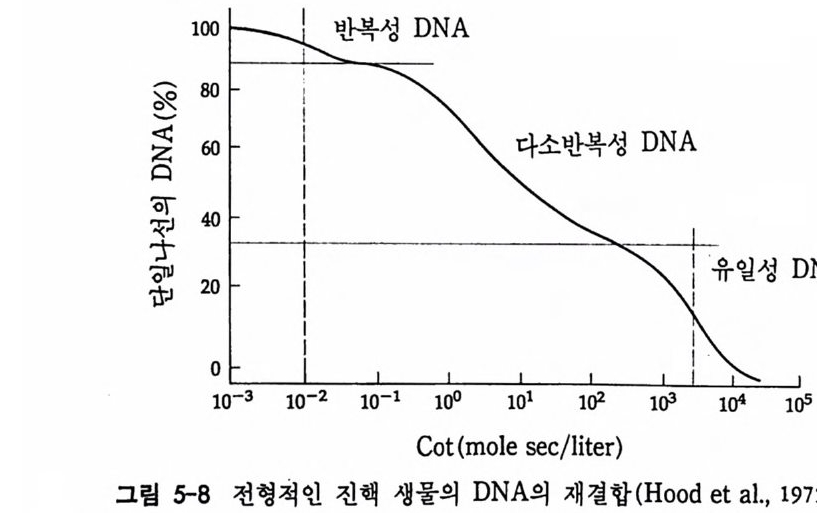 100
100
가능한데 그 이유는 반복정도의 차이로 DNA 의 Co t곡선이 두 단계 이상의 log ar ith m i c scale 에 걸쳐 나타나 사실상 Co t- 21 로 게놈 크기 를 비교할 수 없기 때문이다. 일반적으로 진핵세포 DNA의 Co t곡선은 크게 3 부분으로 나뉘어진 다. Co t곡선 전체는 6~7 단계의 !og ar ith rn ic scale 에 분포되어 있다. Co t값이 낮은 부위에서 재결합된 DNA 는 대단히 반복적인 것으로 반복정도가 106 이다. 이러한 DNA 는 전사되지도 않고 단백질합성에 있어서 아미노산 서열을 지시하지도 않는 것으로 세포분화와 관계가 없다. 염색체내에서는 주로 동원체 부위에 자리하면서 세포분열시 영 색체 를 보존하는 역할을 하는 것으로 알려져 있다.
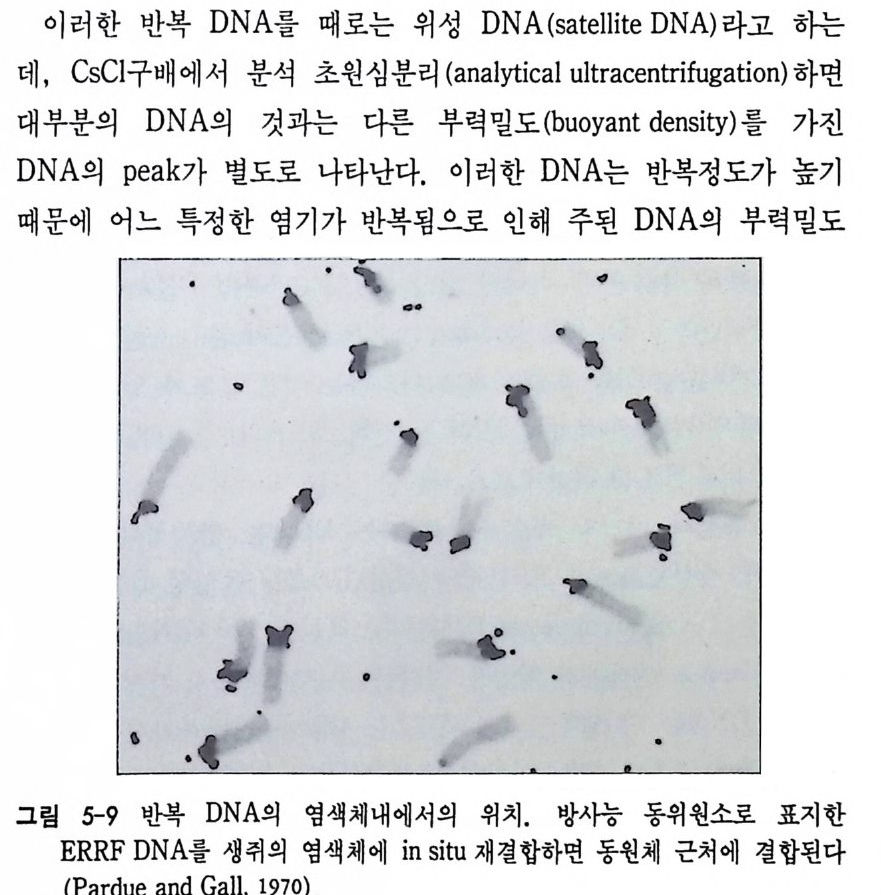 이 러 한 반복 DNA 를 때 로는 위 성 DNA(sate ll ite D NA) 라고 하는
이 러 한 반복 DNA 를 때 로는 위 성 DNA(sate ll ite D NA) 라고 하는
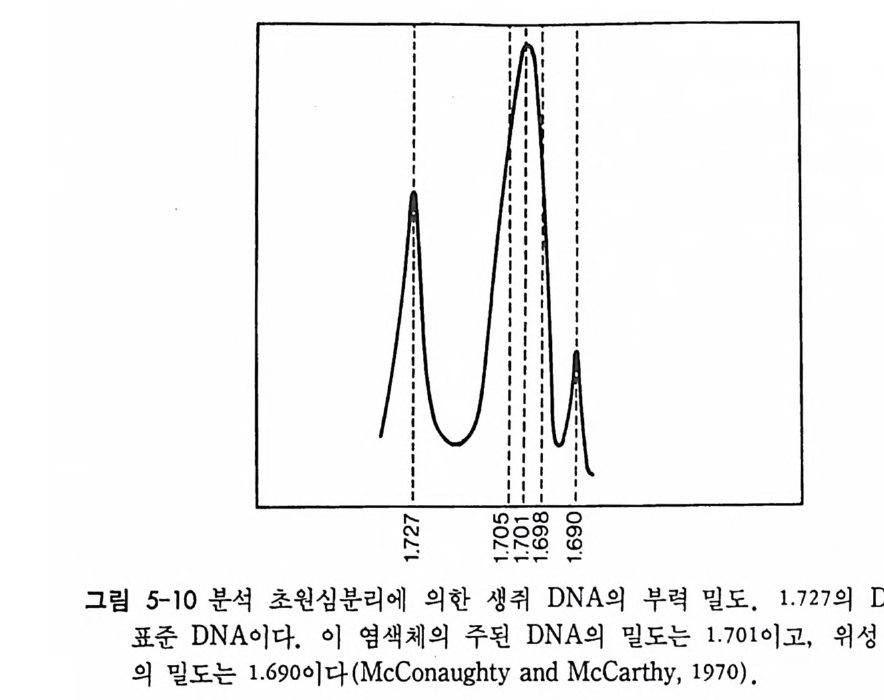 그림 5-10 분석 초원심분리에三 의한 생广쥐 DN A 의 부력 밀도. 1. 72 7 의 DNA 는
그림 5-10 분석 초원심분리에三 의한 생广쥐 DN A 의 부력 밀도. 1. 72 7 의 DNA 는
와 다르게 나타난다. 이러한 위성 DNA 가 반복성 DNA 이다. 이러한 사실은 반복성 DNA 를 h y drox y a p a tit e 로 분리 하여 부력 밀도를 측정 해 보면 위성 DNA 와 동일하게 나타나는 것으로 보아 알 수 있었다. 생쥐에서 가장 반복적인 DNA 는 전체 DNA 의 약 10% 에 해당하며 106 의 반복정도를 나타내고 있다. Co t곡선의 마지막 부분에 나타나는 DNA 는 반복성이 거의 없기 때문에 재결합속도가 느리다. 이러한 DNA 를 유일성 DNA 혹은 비 반복성 DNA(non-r e pe a te d DNA) 라고 하는데 , 이 DNA 는 대 부분의 효소와 구조 단백질의 합성을 지시하는 유전 정보를 가지고 있다. 유 일성 DNA 는 한 게놈당 1 회 혹은 2~3 회 이상 반복하지 않는다. 포 유류에서 게놈당 50% 이상이 유일성 DNA 에 속한다. 만약 mRNA 룰 분리하여 DNA 에 재결합시키면 mRNA 는 유일성 DNA 에 특이하 게 결합하는 현상을 찾아볼 수 있다 (Goldlber g et a l., 1973), 적혈구로
부터 헤모글로빈 mRNA 를 추출하여 DNA 와 재 결합시 키면 거의 대 부분이 유일성 DNA 와 결합한다 (Dav i dson and Bri tten , 1973). 그러나 히스톤 mRNA 의 경우는 다르다. 히스몬 mRNA 는 다소 반복성 DNA(moderate ly repe a te d DNA) 와 결합하는데 히스톤 DNA 는 수백 배에 해당하는 반복성을 지니고 있다 (Kedes, 1976). 유일성 DNA 가 구조 유전자 (s t uc t ural g enes) 에 해당한다는 사실은 mRNA 와의 재결 합 실험에서뿐만 아니라 mRNA 에 대한 cDNA 와 DNA의 재결합 실 험 에서 도 나타났고, DNA 재 조합법 (recombin a nt DNA meth o d) 을 이 용하여서도 확인되었다. 특정 구조 유전자를 진핵세포의 유전자로부 터 분리하여 DNA 재조합법으로 증식시킨 다음 DNA 와 재결합시켜 봄으로써 구조 유전자는 유일성 DNA 로 구성되어 있음을 알 수 있었 다. DNA 의 세번째 부류로서는 다소 반복성 DNA 를 들 수 있는데, Co t곡선에서 중간부분에 나타나는 DNA 로서 반복성도가 103~105 이 다. 포유류에서는 게놈당 15% 가량이 이 범주에 속한다. 다소 반복 성 DNA 중 지금까지 알려진 구조 유전자로서는 히스톤 DNA 뿐이며 대부분의 다소 반복성 DNA 는 단백질 합성 지시 역할을 하지 않는 다. rRNA 나 t RNA 에 대한 유전자가 다소 반복성 DNA 에 속하는 것으로 알려져 있는데, 이러한 DNA 는 비교적 한군데 모여 있으며, 일정한 간격을 두고 반복되는 것이 특칭이다. 43 종의 t RNA 에 대한 유전자는 각 유전자당 평균 200 회 반복함으로써 전체로서는 8600 tR NA 유전자가 존재한다 (Clarkson et a l., 1973). 5S, 18S, 28S 의 rRNA 의 DNA 도 다소 반복성 DNA 에 속하는데, 특히 l8S 와 2sS rRNA 의 유전자에 대 한 연구가 많이 되 어 있다. rRNA 유전자는 염색체상에서는 인 형성체 (nucleolar or g a ni zer) 부위 에 위치하고 있는데, 수백회 반복되어 있다. 대개의 경우 인 형성체 가 반배수체의 염색체 중 하나만 존재하는 것이 보통인데 그 예를 Xenop us 나 초파리에서 찾아볼 수 있다. 인 형성체의 위치는 rRNA 와 염색체의 DNA 간의 in situ 재결합법과 자기방사법으로 밝혀졌다
(Pardue, 1973). rDNA 는 염색체상에 산만하게 퍼져 있는 것이 아니 고, 한군데에 집중적으로 모여 있다. t RNA 와 rRNA 의 유전자가 특정된 위치에서 반복되는 반면에 나 머지 다소 반복성 DNA 는 유일성 DNA 사이에 산만하게 흩 어져 있 다는(i n t erd i s p erse) 사실이 밝혀졌다. 대부분의 유일성 DNA 는 다소 반복성 DNA 로 둘러싸여 있다 (Dav i dson, 1973 a and 6). 이러한 사실 은 이중 재결합 실험 (double renatu r ati on exp e ri men t)을 통해 증명되 었다. 우선 DNA 를 3700 염기쌍의 크기로 토막을 내고 단일 나선으 로 변성시킨 다음 다소 반복성 DNA 와 재결합할 수 있는 정도의 Co t수준까지 재결합 반응을 허용한다. 재결합된 이중나선의 DNA 토막둘을 hy drox y a p a tit e 로 분리한 다음 다시 변성시키고 450 염기쌍 의 크기로 토막낸다. 이들 DNA 토막을 한번 더 재결합시켜 보았더 니 45% 만이 이중나선을 형성하였다. DNA 토막의 길이가 길수록
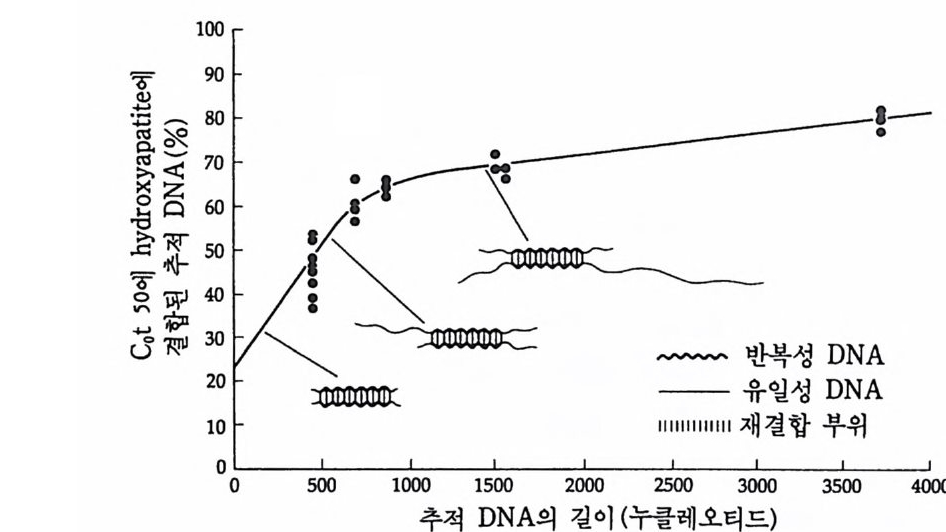 100
100
그람 5-11 유일성 DNA 와 다소 반복성 DNA 의 산재성. DNA 가 hyd rox- y a p a tit e 에 붙둘리는 대에 DNA 토막의 크기가 미치는 영향을 조사함으로 써 유일성 및 다소 반복성 DNA 의 산재성을 알아내었다 (Da vi dson , 1973}.
이중나선 부위에 붙어 있는 단일 나선의 길이가 긴 것을 전자현미경 으로 확인할 수 있었다. 즉 DNA 토막의 길이가 짧을수록 다소 반복 성 DNA 와 유일성 DNA 가 h y droxy a p a tit e 에 의해 분리되는 점을 관찰할 수 있었다. 이러한 실험결과는 다소 반복성 DNA 와 유일성 DNA 가 서로 나란히 자리하고 있기 때문에 나타나는 것으로 해석되 었다.
 I I
I I
그립 5-12 전자현미경으로 관찰한 유일성 및 다소 반복성 DNA 의 산재성 (Dav ids on et a l., 1973) .
다소 반복성 DNA 의 산재성 (散在性 i n t er di s p ers i on) 은 전자현미경에 의해서도 확인되었다 (Chambela i n et a l., 1975). 2500 염기의 Xenop us DNA 토막을 낮은 Co t까지 재결합시킨 다음 전자현미경으로 관찰하 였다. 이중 나선으로 재결합된 대부분의 DNA 토막둘은 H 자 모양 즉 이중 나선 부위 양쪽에 단일 나선의 꼬리가 달린 모양을 하고 있 었다. 이중 나선 부위는 다소 반복성 DNA 에 해당하며 단일 나선 꼬 리는 유일성 DNA 에 해당하는 것으로 풀이되었다. 이러한 다소 반복 성 DNA의 산재성은 Xenop us 에서뿐만 아니라 비록 그 양상에 다소 차이가 있으나 초파리, 성게, 곰팡이, 쥐의 DNA 에서도 발견되었다 (Mann ing et a l., 1975 ; Klein , e t a l., 1978 ; Consta n ti ni et a l., 1978 ; Kimme l and Fir tel. , 1 979 ; Zucker and Lod ish , 1981) . 다소 반복성 DNA 의 기 능 에 관해서는 아직까지 확실치 않으나 이 DNA의 전사체가 주로 핵
속에 남아 있으면서 해독되는 경우가 거의 없는 것으로 알려져 있다 (Ry ffel et al., 1981). 아마도 이들 전사체들은 유전자 발현의 조절 역 할을 담당할 것으로 짐작되어 대단한 주목을 끌고 있다. 4 순차적 유전자 발현의 조절요안 대부분의 유전자는 손실되거나 변경됨으로써 선택적으로 발현되지 않는다. 적혈구에서 단백질의 98% 이상이 글로빈으로 구성되어 있 고, 누에에서 명주 단배질인 fi bro i n 을 엄청나게 생산해낼 수 있는 원인은 이들 단백질에 대한 유전자가 특별히 증폭되기 때문이 아니고 선택적으로 발현되기 때문이다. 세포분화의 방향성이 유전자 손실이 나 유전자 , 변경이 일어나기만 하면 크게 영향받는 것은 확실하나 유 전자의 손실과 변경은 분화의 결과를 설명하는 데 있어서 아직까지 지나치게 국부적인 현상이기 때문에 일반화된 조절기구로 받아들이기 는 어렵다. 오히려 다양한 세포분화의 방향성을 설명해 주는 공통적 인 기구는 물론 완벽한 것은 아니나 선택적인 유전자 발현을 동해서 그 방향이 정해진다. 물론 선택적인 유전자 발현 그 자체는 세포분화 의 원인이 아니고 결과이다. 따라서 세포분화 기구의 핵심적인 문제 점은 〈특정된 세포에서의 유전자 발현을 선택적으로 유발시키는 원인 이 무엇인가?〉에 귀결된다. 아칙까지 결정요인의 정체를 파악하지 못한 실정이기 때문에 결정요인과 선택적 유전자 발현의 요인이 구체 적으로 어떻게 연관되는지 알 수 없으나, 개념적으로는 결정요인의 작용에 의해 유전자가 선택적으로 발현되는 것으로 인식되고 있다. (1) 세포질 요인 (cy top l a smi c fac to r ) 핵 속에서 일어나고 있는 생리적인 활동이 핵을 둘러싸고 있는 환 경요인 죽 세포질에 의해서 좌우된다는 생각이 오래 전부터 있었다.
단순히 세포질을 바꾸어 중으로써 핵의 형태적 및 생화학적 변화를 관찰하고 아마도 유전자 발현을 조절하는 요인이 세포질 속에 있을 것이라고 추측하였다. 세포질의 조성은 핵과 세포질간의 상호작용에 의해서나 혹은 세포간 상호작용에 의해서 변화받을 수 있고, 변화받 은 세포질 요인은 핵과 상관하여 핵내의 활동을 조절할 것이라고 생 각되었다. 세포질요인이 핵내의 활동에 크게 영향을 준다는 사실이 크게 두 가지 방법 즉 핵 이식과 세포융합 (cell fu s i on) 에 의해서 확인 되었다. 우선 핵 이식 실험을 위하여 Xenop us 의 포배세포의 핵을 난모세포 에 이식하였다. 난모세포의 특칭은 핵의 크기가 크고 RNA 를 다량 합성하는 것이고 포배세포의 특칭은 세포분열을 계속하고 있는 세포 이기 때문에 핵의 크기는 작고 RNA 의 합성은 거의 일어나지 않는 것이다. 그런데 포배세포의 핵을 난모세포에 이식하면 핵의 크기가 커지고 RNA 합성이 급격히 증가하며, 인이 새로 나타나고 염색질이 분산된다. 즉 포배세포의 핵이 난모세포의 핵과 유사해진다. RNA 합성이 난모세포에 이식한 포배의 핵에서 급격히 증가하는 현 상을 자기방사법을 이용하여 알아낼 수 있었다. 핵을 이식한 난모세 포에 3H-ur i d i ne 과 같은 방사능 RNA 전구물질을 주어 RNA 합성 에 참여시킨 다음 난모세포를 슬라이드 . 위에 고정시키고 그 위에 사진 에멀죤을 입혀 RNA 에 침투한 3H- uri d i n~ 료부터 방사되는 방사능 울 에멀죤에 감광시킨다. 감광된 입자 즉 은입자 (s il ver gra i ns) 의 위 치와 양을 확인함으로써 RNA 합성부위 및 대략적인 양적 차이룰 알 아낼 수 있다. 난모세포에 이식한 포배세포의 핵에서 RNA 합성이 급 격히 증가하는 반면에 난모세포의 핵과 같이 DNA 합성은 억제된다. 3H- t h yrni d i ne 으로 표지한 후 자기 방사법 으로 조사해 보면 3H -thyrnidi ne 이 난모세포의 DNA 합성에 전혀 참여하지 않음을 볼 수 있었다. Xenop us 의 콩팥세 포의 핵 을 Pleurodeles wal tii의 난모세 포에 이 식
하여 주고 난모세포에서 합성되는 단백질을 조사해 보면 Xeno p us 단 백질의 합성을 찾아볼 수 있는데, 이것은 Pleurodeles 의 세포질에 의 해 Xenop us 의 콩팥세포의 핵 이 활성화된 것이 다. 더구나 단백 질은 콩팥세포에서 합성되는 것이 아니고 Xenop us 난모세포에서 합성되는 종류와 흡사하였다. 콩팥세포에서 억압되었던 유전자가 새로운 세포 질 환경인 난모세포질내에서 새롭게 활성화된 것이다. 세포융합법에 의해서도 세포질 요인에 의하여 RNA 및 DNA 합성 이 조절되는 현상을 찾아볼 수 있었다. 일단 융합이 일어나면 서로 다른 두종류의 핵이 한 세포 속에 들어 있을 뿐만 아니라 두 종류의 세포질이 합쳐진 새로운 세포질 환경이 이루어진다. 이러한 상황에서 는 융합 이전 각각의 세포질에서 일어나던 것과는 다른 새로운 변화 가 핵에 일어난다. 사람의 조직 배양 세포인 HeLa 세포와 닭의 적혈 구를 융합해 주면 적혈구의 핵에 큰 변화가 일어난다 (Harr i s, 1967, 1968). 적혈구에 센다이 바이러스몰 처리하면 적혈구의 원형질 막이 터져서 세포질이 밖으로 유출된다. 따라서 융합세포의 세포질은 거의 HeLa 세포의 것이 다. HeLa 세포는 DNA 와 RNA 합성 이 대 단히 활발 한 세포로서 핵의 크기가 크다. 반면에 적혈구의 핵은 작고 DNA 와 RNA 합성률은 대단히 낮다. 적혈구의 핵이 융합에 의해 HeLa 세포 의 세포질에 들어가게 되는 셈인데, 융합후 적혈구의 핵은 커지고 염 색질이 분산되며 RNA 와 DNA 의 합성률이 높아진다. 또 하나의 다른 예로서는 쥐 의 간 종양세 포 (live r tum or cell) 와 생 쥐 의 섬 유아세 포 (織維茅細胞 fibr oblast) 의 융합의 경 우이 다 (Pete r son and Weis s , 1972 ; Brown and Weis s , 1975). 바이스 (We i ss) 는 이 융합세 포가 쥐의 간세포에서 특별히 합성되는 쥐의 albumi n, aldolase, tyros in e ami no tr ans fe rase(TAT) 뿐만 아니라 섬유아세포에서는 전혀 합성 되 지 않는 생 쥐 의 albu min, aldolase 및 tyros in e am ino tr a ns- fe rase 가 합성됨을 발견했다. 이것은 섬유아세포내에서 쓰이지 않았 던 유전자들이 새로운 세포질 환경에서 발현된 것으로 풀이되었다.
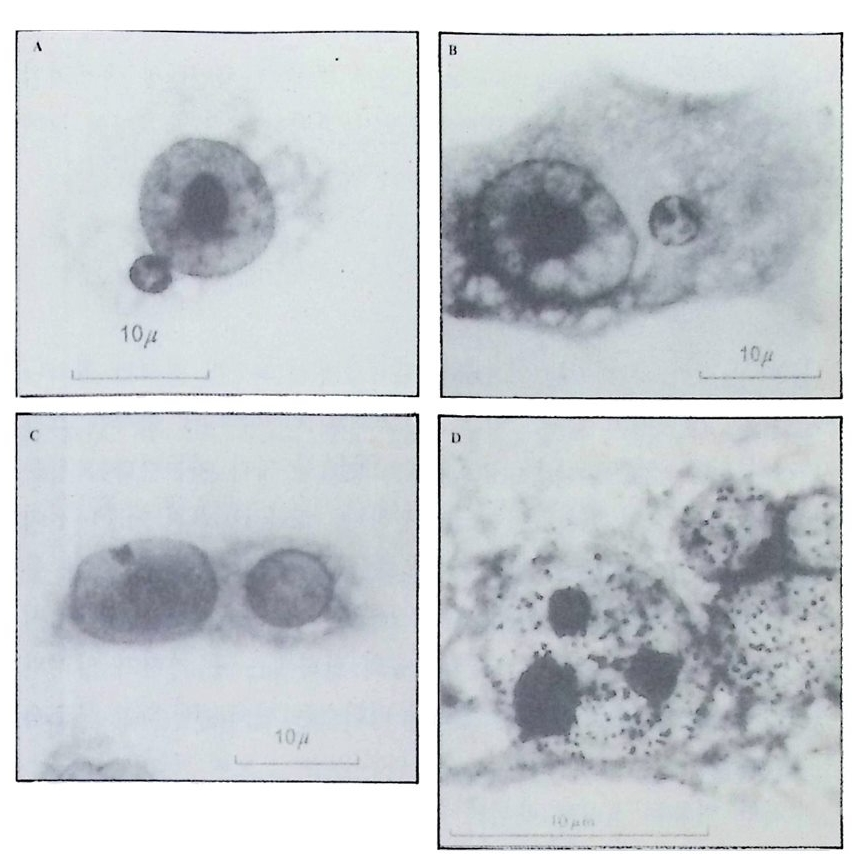 10,,
10,,
그림 5-13 HeLa 세포와 적혈구를 세포 융합하여 얻은 hete r okary o n. 세포 융 합 직후에는 적혈구 핵의 크기에 큰 변화가 없으나 (A) 시간이 지남에 따라 접차 커진다 (B, C). 세포 융합 이후 적혈구 핵에서의 RNA 합성을 3H ur i d i ne 으로 표지하여 자;「방사법으로 확인하였다 (D) (Harr is, 1967, 1968)
비록 세포의 종류는 다르나 특정된 세포에서 발현되는 유전자가 다 론 세포의 핵 속에도 불활성화된 상태로 숨어 있다. 바아넷 (Barne tt, 1980) 은 이와 같은 사실을 실험적으로 보여주었다. 바아넷은 초파리 의 지 방체세포(fat body cell) 로부터 얻은 난황단백 질의 mRNA 에 대 한 cDNA 를 준비하여 in s itu재결합법으로 침샘세포의 염색체와 결합 시킴으로써 지방체세포에서만 발현되는 난황단백질 유전자가 비록 침
샘세포에서는 발현되지 않을지라도 존재하고 있다는 사실을 알아냈 다. 즉 지방체세포에서는 세포질 요인에 의해 난황단백질 유전자가 발현되며, 침샘 세포에서는 지방체세포가 가지는 세포질 요인이 결여 되어 있기 때문에 난황단백질 유전자의 발현이 억제된다. (2) 염색질의 구조적 변화 DNA 가 전사되기 위해서는 우선 염색질에 구조적인 변화가 일어나 야 된다고 생각되고 있다. 예를 들어 RNA pol ym e rase 분자가 크기 가 거의 같은 누클레오솜울 감고 있는 DNA 를 따라 이동한다는 것은 염색질에 구조적인 변화없이는 불가능하다. 또한 DNA 의 이중나선이 전사될 나선과 전사되지 않을 나선으로 분리되어야 하는데, 이와 같 은 이중나선의 분리도 누클레오솜의 구조적 변화에 의해서 아루어지 는 것으로 생각되고 있다. 누클레오솜의 변화에는 두 가지가 알려져 있는대, 누클레오솜의 수적인 변화와 비히스톤 단백질에 의한 구조적 인 변화이다. 수적인 변화는 전사될 부위의 염색질에 누쿨레오솜이 없어지는 것 인대, 이러한 염색질 부위는 RNA 중합효소 (RNA p ol y merase) 에 대 한 친화성이 높기 때문에 전사활동이 활발해진다. Oncop elt u s fa sc iat us 라는 곤충에서 rRNA 유전자를 가진 게놈 부위는 누클레오솜 울 거의 가지고 있지 않은 것으로 관찰되었는데, 이 부위의 DNA 만 이 활발하게 전사된다. Oncop e lt us 의 게놈에서 이 부위 의 에는 누클 레오솜이 결핍된 부위가 없는 점으로 보아서 이 동물에서의 rRNA 유전자에게만 특이하게 일어나는 것으로 생각되었다 (Foe et a l., 1976). Oncop e ltu s 이의의 다른 종류의 생물에서도 이와 같이 특이한 현상이 보이기는 했으나 (Labha rt and Koller, 1982} 이것은 보편적으로 일어나 는 현상이 아니다. 오히려 대부분의 경우는 rRNA 유전자가 누클레오 솜과 결합되어 있을지라도 전사가 가능하다. 또한 적혈구의 글로빈
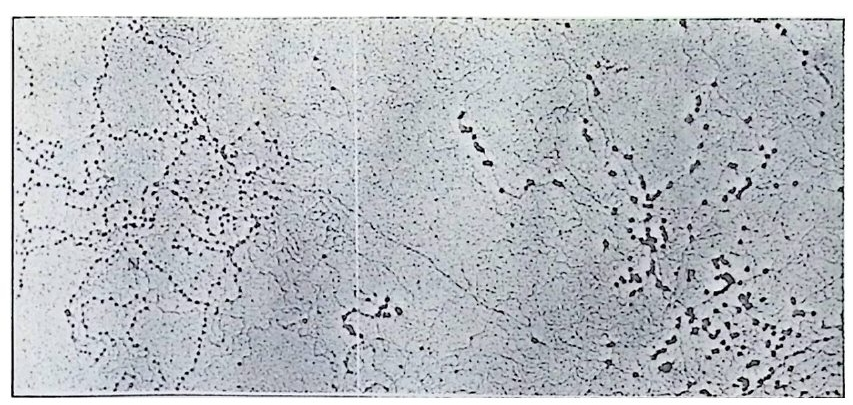
그립 5-14 Xen o p ztS 게놈의 활성 부위와 불활성 부위. 염색질을 분리하여 RNAse 로 처리한 다음 전자현미경 관찰을 위하여 조작하였다. 염색질의 두 가지 특 징적인 부위가 관찰되었다. 그립의 오른쪽 P 라고 표지한 부위의 염 색질에는 RNA 중합효 소 라고 생각되는 분자의 크기가 큰 단백질이 있는 활 성부위와 왼쪽 N 이라고 표 지 한 부위의 염색질에는 중합효소는 보이지 않고 다만 누클레오솜만이 있는 불 활성부위가 있다 (Labha rt and Koller, 1982).
유전자와 같은 유일성 유전자도 누클레오솜이 부착되어 있는데도 불 구하고 전사되는 것으로 보아 누클레오솜이 없어져야 하는 것이 전사 에 꼭 필요한 조건은 아니다. 누클레오솜이 부착된 상태로 전사가 일어나는 부위는 반드시 다른 누클레오솜과는 다르게 누클레오솜에 변화가 일어나는 것으로 생각되 었다. 즉 특정된 비히스몬 단백질이 특정된 유전자에 부착되어 있는 누클레오솜과 결합하여 유전자와의 부착에 변화를 줄 것이라고 생각 되었다. 이러한 예측에 대한 실험적 증거는 대개 세포 종류에 따라 다르게 나타나는 특정 유전자에 대한 DNAse 의 민감도 (DNAse sens iti v ity)를 측정함으로써 알게 되었다. 전사하고 있는 유전자 부위 만 DNAse 에 의해 쉽게 붕괴되고 다른 부위의 DNA 는 히스톤에 가 려져서 효소에 의해 붕괴되지 않는다는 전제하에 우선 조직으로부터 새롭게 얻은 염색질을 낮은 농도의 DNAse I 으로 처 리한다. 효소로 처리된 염색질로부터 단백질을 제거시키고 DNA 를 추출하여 방사능
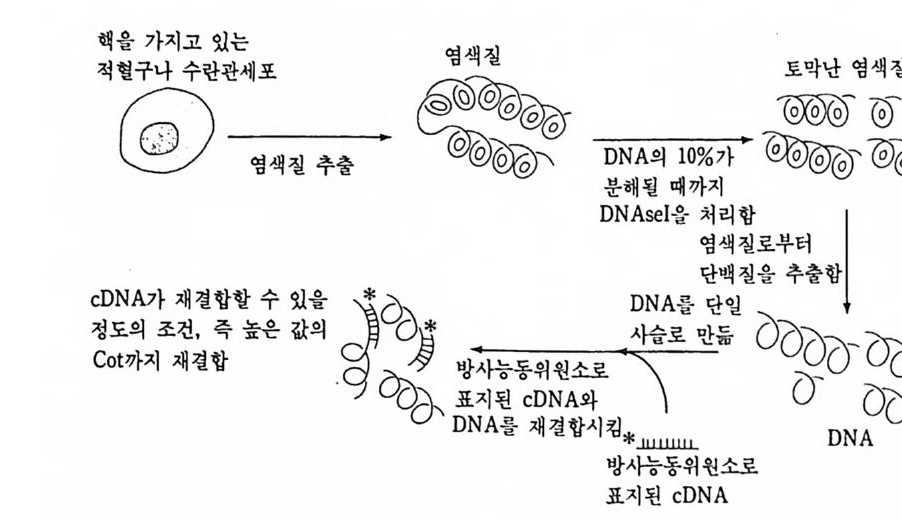 적핵 혈을@ 구가나지 고수 란있관는세 二포 〈\촐 二 三--..영 i:函
적핵 혈을@ 구가나지 고수 란있관는세 二포 〈\촐 二 三--..영 i:函
그림 5-15 염색질에 대한 DNAse I 의 민감도 를 측 정하 는 실험고안
으로 표지한 cDNA 와 재결합시킨다. 만약 전사한 부위의 DNA 가 DNAse I 에 민감하여 붕괴되었으면 방사능 cDNA 와의 재결합은 일 어나지 않을 것이다. 따라서 DNAse 민감도를 측정함으로써 비록 누 클레오솜이 부착되어 있다고 할지라도 활성화된 DNA 부위에서는 RNA p ol ym erase 와 같은 효소를 부착시 킬 수 있을 만큼 누클레오솜 에 변화가 일어났다고 짐작할 수 있었다. 와인트라우브 (We intr aub) 와 그라우딘 (Grou di ne, 1976) 은 닭의 적혈 구의 염색질을 DNAse I 으로 처리한 다음 DNA 를 추출하여 방사능 글로빈 cDNA 와 재결합시켰다. 사실상 DNAse I 으로 처리받은 DNA 는 방사능 글로빈 cDNA 와 거의 재결합하지 않았다. 물론 DNAse ~로 처 리받지 않은 적 혈구 DNA 나 혹은 DNAse I 으로 처 리받은 뇌세포 및 섬유아세포의 DNA 는 글로빈 cDNA 와 결합하였 다. 죽 섭유아세포와 뇌세포의 글로빈 DNA 는 전사되고 있지 않았기 때문에 DNAse I 에 의해 제거되지 않았다. 같은 방법으로 수란관세포의 염색질에서 활발하게 전사되는 난알부
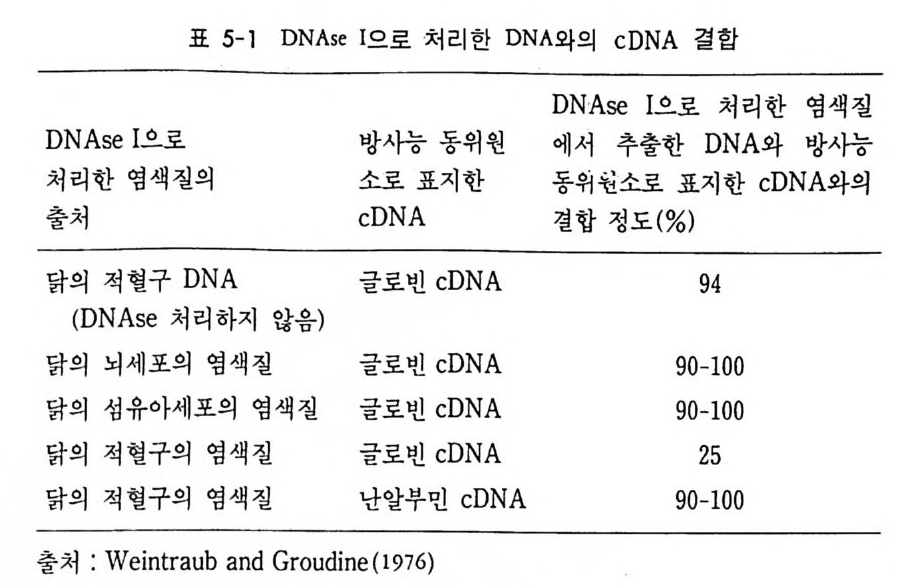 표 5-1 DNAse I 으로 처리한 DNA 와의 cDNA 결합
표 5-1 DNAse I 으로 처리한 DNA 와의 cDNA 결합
민유전자의 DNA 를 DNAse I 으로 제거시킬 수 있었다. 그러나 적혈 구에 내재 하는 난알부민유전자는 DNAse I 에 의해 분해 되 지 않았다 . 즉 난알부민 cDNA 는 적혈구 DNA 에는 재결합되었으나, 수란관 염 색질로부터 추출한 DNA 에는 재결합되지 않았다. (3) 비히 스 톤 단백질 핵 속에는 히스톤단백질 이의에 비히스톤단백질 (no nhi s t one pro te i n s ) 이 있는데 , 비 히스몬 단백 질은 영 색 질의 구조 변화에 영 향을 주어 선택적 유전자 발현에 관여하는 것 으 로 생각되고 있다 . 즉 적혈 구에는 크게 나누어 비히스톤 단백질에 HMG(hig h mobil ity grou p ) -14 와 HM G - 17 의 두 종류가 있는데, 이들 HMG 단백질의 존재 여 부 에 따라 글로빈 유전자의 발현이 결정된다. 염색질을 o.35M Na Cl 로 처리하면 분자량이 낮은 단백질들이 추출되는데, 이와 같은 방법으로 비히스몬 단백질을 제거시키고, DNAse I 에 대한 민감도를 조사해
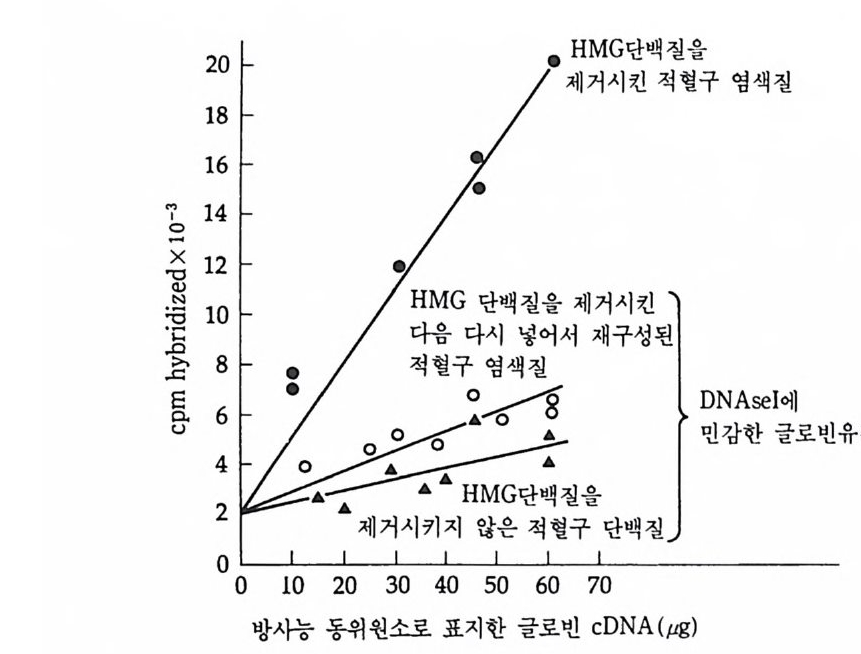 20181614 • HMG 단백질을
20181614 • HMG 단백질을
그림 5-16 글로빈유전자에 대한 DNAse I 의 민감도. 닭의 적혈구 염색질에서 HMG 단백질을 제거시킨 다음, 둘로 나누어 한쪽에는 HMG 단백질을 다시 넣어 주고, 다른 한쪽에는 HMG 단백질을 넣어 주지 않았다. 이와 같이 처 리한 두 부류의 DNA 와 HM G-를 처음부터 추출하지 않은 적혈구 염색질에 각각 DNAsel 를 작용시킨 다음 방사능 동위 원소를 표지 한 cDNA 와 재 결합 시켰다 (We i sbrod and Wein t r au b, 1979).
봄으로써 비히스톤 단백질의 존재와 선택적인 유전자 발현과의 관계 를 침작할 수 있었다. HMG 단백질을 적혈구 염색질로부터 제거시키 면 글로빈유전자는 DNAse I 에 의해 분해되지 않았다. 그러나 이들 단백질을 다시 넣어 주면 글로빈유전자의 DNAse I 에 대한 민감도가 회복됨을 관찰할 수 있었다 (We i sbrod and Wein t r au b, 1979 ; Gazit et al., 19so). 그러나 뇌세포에서 추출한 HMG-14 와 HMG-17 은 적혈구 의 글로빈유전자의 DNAse I 에 대한 민감도를 회복시킬 수 있었으 나, 적혈구의 HMG 단백질로서는 뇌세포 유전자의 DNAse I 에 대한 민감도를 회복시키지 못했다. 이 두 종류의 비히스톤 단백질이 여러
종류의 조직에서 유전자 발현을 유발시키는 데 필요한 것이지만, 세 포의 종류에 따라서는 이들 단백질만 가지고는 선택적 유전자 발현의 유발이 어려웠다. (4) 호르몬 비히스본 단백질 이의에도 호르몬이 유전자 발현을 조철하는 요인 으로 알려져 있다. 지금까지 가장 잘 연구된 호르몬은 엑디존과 에스 테로겐아다. 초파리 침샘세포에서의 부풀림이 엑디존에 의해서 조절 되는 예와 닭의 수란관에서 다량 합성되는 난알부민의 유전자 발현이 에스테로겐에 의해서 조철되는 예가 그러한 경우이다. 1) 엑디존에 의한 부풀림 양상의 변화 초파리 발생중 용화기에 나타나는 부풀림 양상의 변화는 엑디존의 분비 시기와 일치할 뿐만 아니라 엑디존의 분비 없이는 용화가 일어 나지 않는다. 베커 (Becker, 1959) 는 이러한 사실에 근거하여 부풀림 형성이 엑디존에 의해 조절된다고 가정하였다. 엑디존은 전홍선 (pro th o raci c gla nd) 에서 분비 되는 호르몬이 다. 초파리 유충의 중간을 가는 끈으로 매어서 전홍선에서 분비되는 엑디존이 유충 뒷부분으로 의 이동을 제한하고 앞부분으로의 이동만을 허락하였다. 그리고 유충 의 앞부분과 뒷부분의 세포내 염색체를 관찰하였는데, 앞부분에서만 정상적인 발생단계 특유의 부풀림 형성이 가능했을 뿐 뒷부분에서는 매듭(lig a ti on) 짓기 전과 동일한 양상의 부풀림을 보였다. 죽 부풀림 의 형성은 엑디존에 의해 조절됨을 보여주었다. 또한 침샘을 다른 개 체로 이식하면 숙주의 것과 동일한 부풀림 양상이 이식 세포에서도 나타남으로 보아 엑디존은 부풀림을 조절하는 호르몬임을 확인할 수 있었다. 엑디존의 역할에 대해 좀더 직접적인 증거는 in vitr o 실험에서 얻
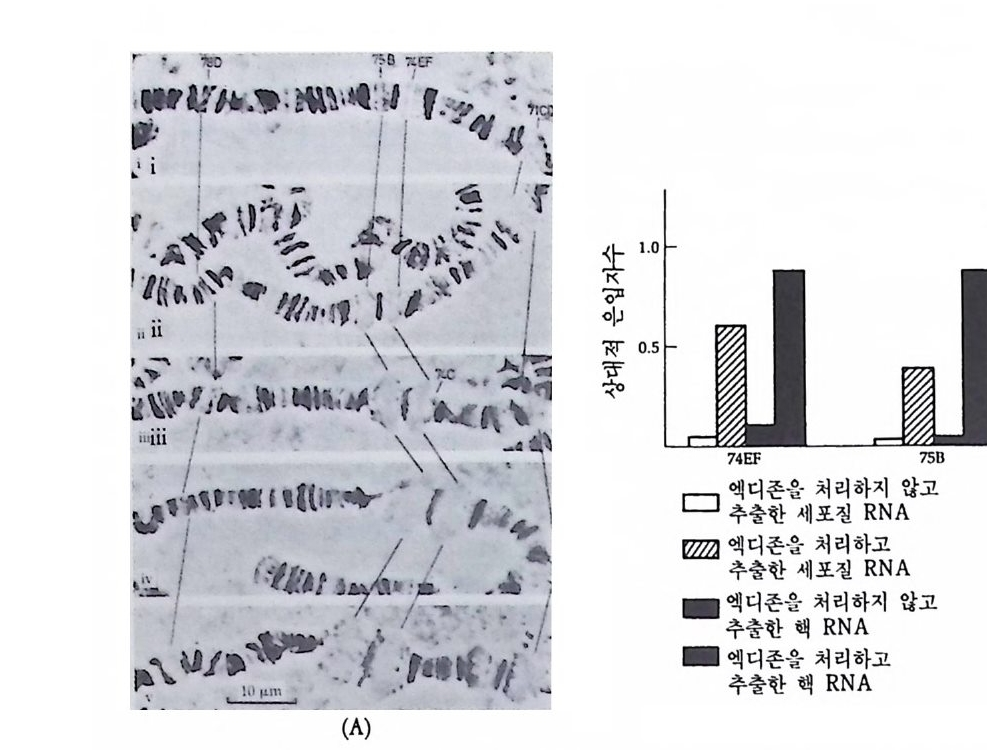 협'•같,r , i '•따. . mI꿉1: , DA -- \ : ` . `-1• ~,녔 :; -I 책\ 유 1rC; ' f ., ?꾸 .이 . ^ .` . .4나,I : ,. .! . Y oloJFKF량f i 74EF 758
협'•같,r , i '•따. . mI꿉1: , DA -- \ : ` . `-1• ~,녔 :; -I 책\ 유 1rC; ' f ., ?꾸 .이 . ^ .` . .4나,I : ,. .! . Y oloJFKF량f i 74EF 758
그림 5-17 D. melanog as te r 의 배양된 침샘 세포에서 엑디존으로 유도된 부풀 림. (A) 부풀림의 순서가 엑디존에 의해 유도된다. (i) 엑디존을 처리하 지 않음. (ii-v ) 25 분, 1 시간, 2 시간, 4 시간 동안 엑디존으로 처리된 후의 부풀림. (B) 엑디존을 처리하였을 때와 처리하지 않았을 때 743EF 와 75B 에 in situ 결합한 RNA 의 양을 은입 자의 수로 나타냄 (Bonner and Pardue, 1977J .
울 수 있었다. 엑다존을 미성숙한 유충에 직접 주사해 주면 단계 특 유의 부풀림이 나타난다 (Clever and Karlson, 1960 ; Clever, 1961). 또한 침샘을 분리하여 i n vitr o 에서 엑디존에 넣어 줄지라도 부풀림이 유 발된다. 그림 5-19 은 이와 같은 실험에서 엑디존에 의해 부풀림이 단 계에 따른 특유의 변화를 보여주고 있다. 특히 대 (band) 74EF 와 75B 에서의 부풀림의 변화는 특기할 만하다. 부풀림이 엑디존에 의해 조절될 때에는 엑디존이 염색체상 특정된 부위와 결합한다. 우선 엑디존을 인식하는 토끼의 항체를 초파리 침
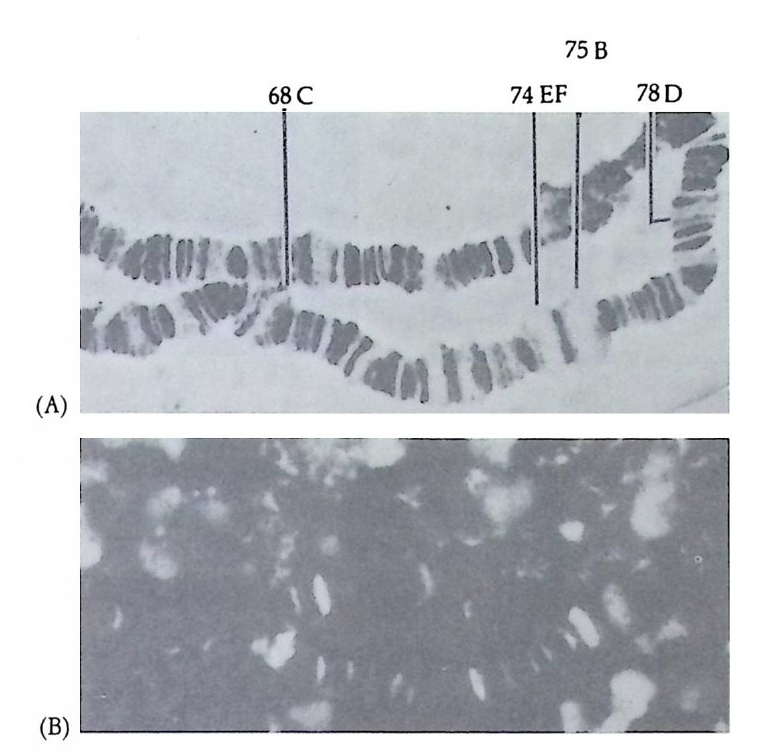 75 B
75 B
그립 5-18 엑디존과 결합하는 초파리 염색체 상의 위치. 일단 염색체를 엑디 존으로 처리한 다음 엑디존에 대한 형광항체를 결합시켜 위치를 확인하였 다. (A) 침샘염색체의 위상차 현미경 사진. (B) (A) 의 염색체에 나타난 엑디존 결합부위를 확인한 형광현미경 사진.
샘에 넣어준 다음 토끼의 항체를 인식하는 형광물질이 표지된 염소의 항체를 넣어 주면, 염색체상에 엑디존이 결합되어 있는 부분에 형광 물질이 나타난다. 이와 같은 방법으로 엑디존에 의해 조절되는 부풀 림 부위가 엑디존과 결합되어 있음을 확인하였다 (Groneme y er and Pongs , 1980). 엑디존에 민감한 부풀림은 크게 3 종류 죽 엑디존에 의해 유발되는 부풀림, 엑디존에 의해 억제되는 부풀림 그리고 엑디존에 의해 처음 몇 시간만 유발되는 부풀립이 있다. 두번째 범주에 속하는 부풀림의 예로서 염색체 3 의 68C 를 들 수 있다. 이 부풀림은 번데기
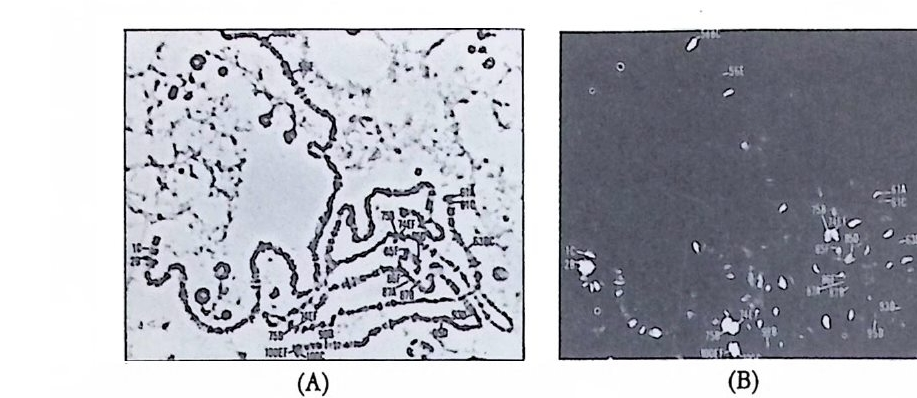 m
m
그림 5-19 초파리 염색질에 DNAseI 을 처리할 때 방출되는 단백질의 위치 결정. 그 단백질에 대한 항체를 만들어 염색체에 결합시킨 다음 , 다론 형광항체를 이용하여 그 위치를 확인하였다. (A) 위상차 현마경 사진 (B) 엑디존 결합부위 (May field et al., 1978).
껍질을 딱딱한 표면에 부착시키는 풀의 역할을 하는 단백질에 대한 유전자 Sgs 3 로서 마지막 유충 시기에 침샘세포에서 부풀어 오른다 (Korge , 1975). 침샘을 in v it ro 상태에서 배양하면서 엑디존을 넣어 주 면 곧 그 부풀림이 사라지면서 동시에 이 유전자로부터의 전사활동도 중지된다 (Me y ero witz and Rog ne ss, 19s2). 즉 이 풀 단백질은 유충을 딱딱한 표면에 부착시키기 위해 필요할 때에만 합성된다. 엑디존이 염색체상 특정 부위에 결합되는 것은 비히스톤 단백질에 의해 매개되 는 것처럼 보인다. 초파리의 염색질은 DNAse I 으로 처리하면 63KD 의 단백질이 떨어져 나오는데, 이 단백질은 제 3 유충기에 엑디존에 민 감한 염색체 부위에 결합하여 유전자의 특칭적인 염색질의 구조를 유 지 시 키 는 데 도움을 준다 (May field eta !., 1978) . 2) 에스테로겐에 의한 난알부민유전자 발현의 조절 닭은 난소에서 난자가 배란되면 수란관의 앞부분에 해당하는 누두 (漏斗, infundibu lum) 에서 수정 된 후 수란관을 따라 내 려 가면서 여 러
종류의 껍질이 수란관으로 분비되어 난자를 둘러싸게 된다. 그 중 흰 자위의 주성분인 난알부민 난자가 통과하는 시기에 수란관 세포에서 전체 단백질의 50% 이상이 합성 분비되는데 이와 같이 시기에 맞추 어 이루어지는 난알부민의 합성은 에스테로겐에 의해 촉진된다. 즉 아직 성숙하지 못한 암닭에 에스데로겐을 주사해 주면 수란관 세포에 서 난알부민의 합성이 급격히 증가되는 것을 관찰할 수 있었다
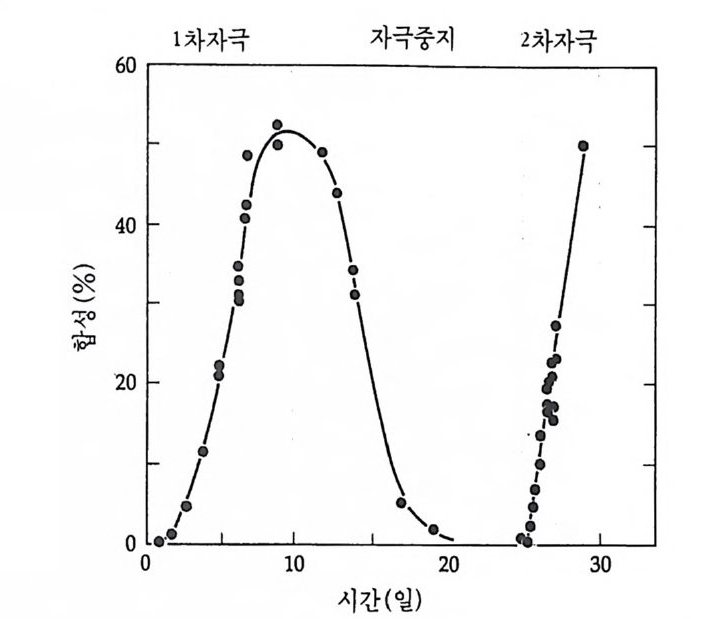 1 차자 국 자극중지 2 차자극
1 차자 국 자극중지 2 차자극
그립 5-20 4 일된 병아리 수란관에서의 난알부민합성에 미치는 에스테로겐의 영향. 처음 10 일 동안 매일 병아리에게 에스데로겐을 주사하였다 (l 차 자 국) . 2 주 동안 주사하지 않다가 다시 주사하였다 (2 차 자극) (Palm iter and Schim ke, 1973) .
(Palm iter and Schim ke, 1973). 에스데로겐울 주사한 후 18 시간만에 난 알부민의 합성이 관찰되기 시작하였고 그 후 에스데로겐을 계속 처리 하는 동안 난알부민의 양이 급격하게 상승하여 새로 합성되는 단백질 의 거의 대부분을 충당하였다. 그러나 에스테로겐 처리를 중단하면
난알부민의 합성이 급격히 감소하는데 만약 에스데로겐을 다시 공급 해 주면 단백질 합성이 회복된다. 이와 같은 실험결과로 보아 난알부 민의 합성은 에스데로겐에 의해 조절된다고 할 수 있다. 그런데 에스 데로겐의 효과는 a-aman iti n 이나 acti no my ci n D 에 의해서 저지되는 점으로 보아서 에스데로겐이 난알부민유전자의 전사에 관여한다는 점 울 알게 되 었다 (O'Malle y and Means, 1974 ; E-delman, 1975) . 즉 에스 데로겐에 의한 난알부민유전자의 선택적 발현으로 난알부민 mRNA 의 합성이 촉진된다. 이러한 결론은 난알부민 mRNA 에 대한 cDNA 와 수란관세포에서 추출한 난알부민 mRNA 와의 재결합 실험을 통해 mRNA 분자의 수 롤 알아냄으로써 확인할 수 있었다. 우선 수란관 세포의 세포질로부 터 전체 RNA 를 추출하여 olig o -d e ox:i1 :h ym i di n e (olig o -dT)-cellulose bead 를 통과시킨다. mRNA 중 p ol y (A) 가 3 ' 말단에 꼬리처럼 부착 되 어 있는 pol y (A) mRNA 는 pol y (A) 와 ol ig o-dT 간의 결 합으로 인 해 ol ig o-dT 에 붙잡히고, 나머 지 RNA 는 통과한다. 고 농도의 영 류 용액을 사용하여 ol ig o-dT 로부터 pol y (A ) mRNA 를 회수하고 전기 영동을 이용하여 종류별로 분리한 다음 전기영동대에서 개별적으로 mRNA 를 추출한다. 각각의 pol y (A) mRNA 를 in v it ro 에 서 해 독시 키고 다시 전기영동하여 어느 전기영동대에서 추출한 pol y (A ) rnRNA 가 난알부민 mRNA 인지를 확인할 수 있었다. 이와 같이 준 비 된 rnRNA 로부터 역 전사효소 (reverse tra nsrp ipa ta s e) 를 사용하여 cDNA 를 만든 다음, cDNA 와 수란관 세포로부터 추출한 난알부민 rnRNA 를 재결합시켜 봄으로써 mRNA 의 분자수를 산출할 수 있었 다. 이러한 실험을 통해서 에스데로겐 처리 여부에 따라 난알부민 rnRNA 분자가 급격하게 변한다는 사실을 관찰할 수 있었다. 즉 에 스테로겐을 처리하기 전에는 mRNA 분자수가 수란관의 상피세포당 30 분자에 지나지 않았으나 (Moen and Palm iter , 1980), 에스테로겐을 주사한 18 일 후에는 50,000 분자로 증가하였다 (O'Malle y et al., 1975) .
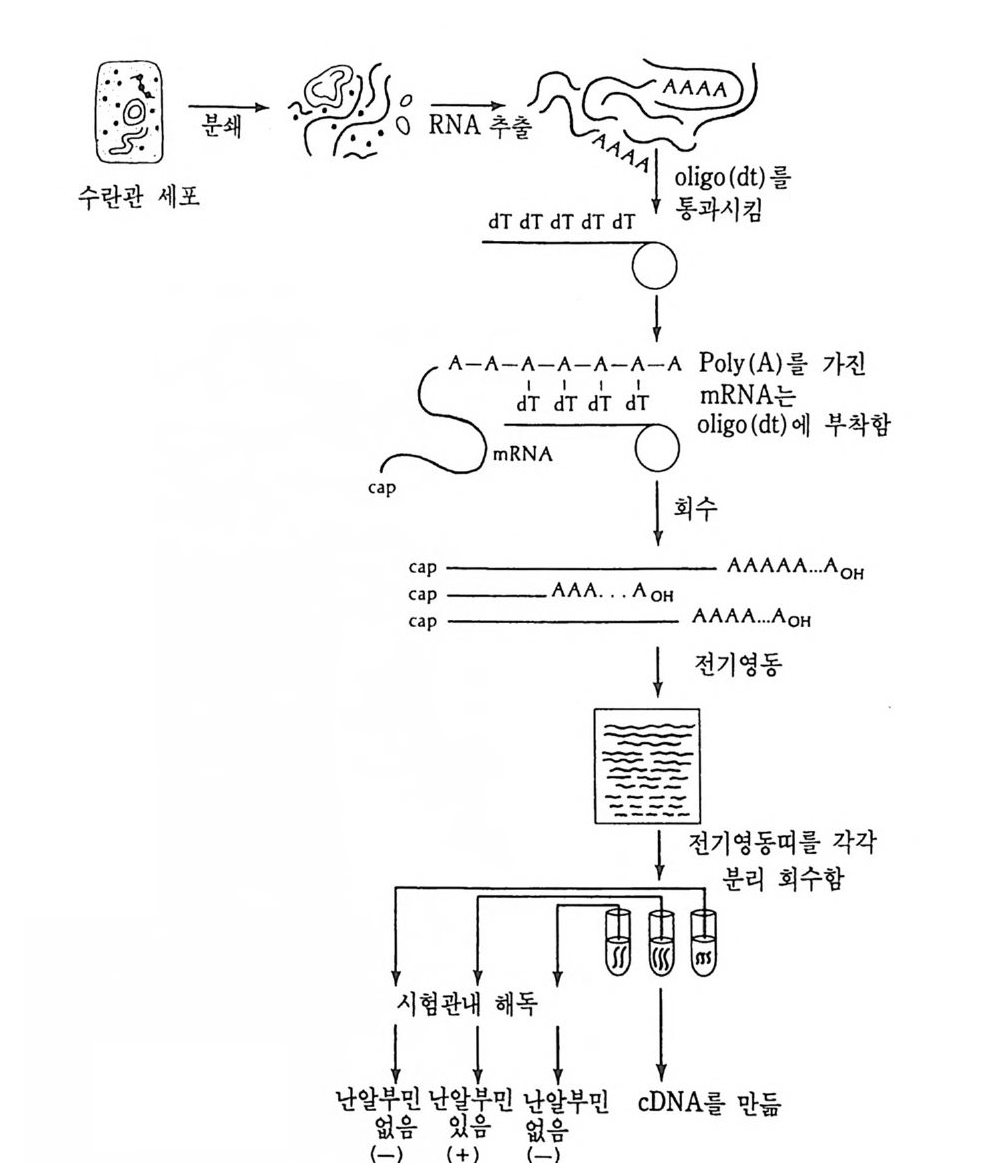 수]란관 세포T 亨g三 ~줄dm T:- d公T dT三〈 dT
수]란관 세포T 亨g三 ~줄dm T:- d公T dT三〈 dT
그림 5-21 수란관 세포로부터의 난알부민 mRNA 추출 및 cDNA 제조법.
또한 에스테로겐의 처리를 중단하면 난알부민 mRNA 분자수는 60 에 지나지 않았다 (Mck nig h t et al., 1975). 해리스 (H arri s, 1975) 등과 루프 (Roop, 1978) 등도 이와 유사한 결과를 얻었다(표 5-2). 특히 루프의
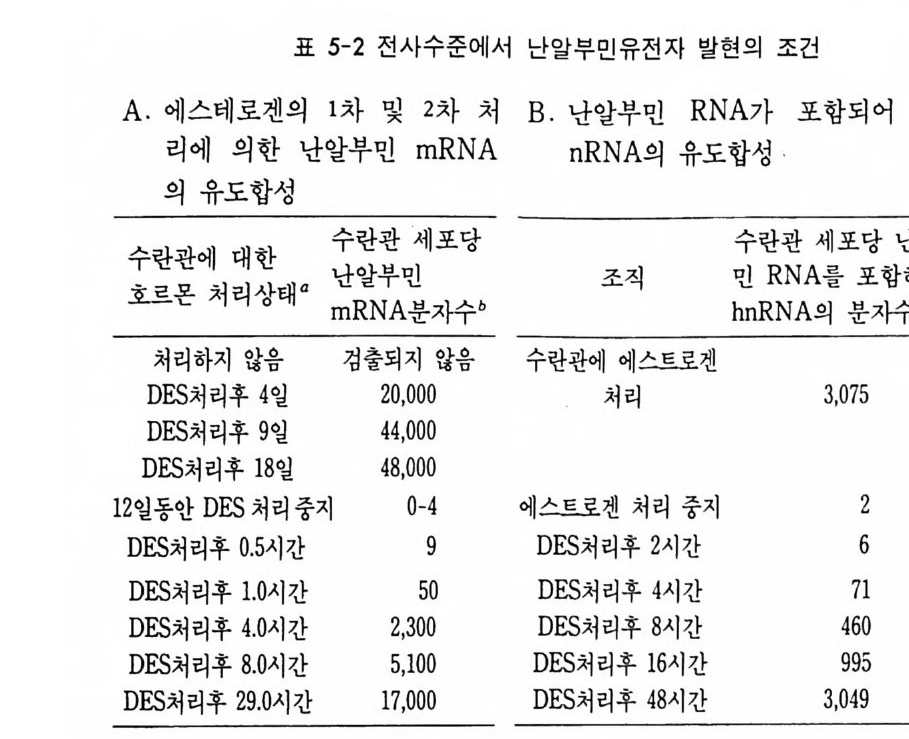 표 5-2 전사수준에서 난알부민유전자 발현의 조건
표 5-2 전사수준에서 난알부민유전자 발현의 조건
A 의 출처 : Harris e t al. (1 975). B의 출처 : Roop et al. (1 978). a. 10 일된 White Leg h orn 병아리에 die th yls ti lbe str ol (D E S, 일종의 합성 에스트 로겐) 2.5m g을 주사한 다음 정해전 시간에 따라 희생시켰다. 에스트로겐의 2 차 처리 실험을 위해서는 병아리를 먼저 2 . 5m g의 DES 로 10 일 동안 처리한 다음, 11 일 동안 처리중지하였다가 12 일째 되는 날에 한 번의 2.5mg DES 를 주사하고 정해진 시간에 희생시켰다. b. 난알부민 mRNA 에 대한 3H-cDNA 를 지시한 대로 호르몬 처리를 받은 병아 리의 수란관 RNA 와 결합시켰다• c. 난알부민 cDNA 와의 재결합실험으로 결정하였다.
실험에서는 에스트로겐에 의해 난알부민 cDNA 와 재결합할 수 있는 핵 RNA 가 합성됨을 보여주었다. 이러한 실험 결과를 종합해 볼 때 수란관 세포에서의 난알부민 합성은 에스테로겐에 의해 조철되는 것 임을 알수 있었다.
에스데로겐에 의해 난알부민 mRNA 의 합성이 촉진되는 사실은 in situ 재결합에 의해서도 확인되었다. 즉 에스테로겐으로 처리된 수란 관 세포에서는 방사능물질로 표지된 cDNA 와 결합하는 난알부민 mRNA 가 다량 나타났고, 에스테로겐 처리를 중단한 세포에서는 은 입자가 거의 보이지 않았다. 그러나 프로게스테론으로 다시 촉진시켰 울 경우 mRNA 은입자가 보이기 시작했다 (She p herd et a l., 1980}. 아직까지 에스데로겐이 어떻게 수란관 세포에서만 난알부민 mRNA 합성을 촉진시키는지에 대해서는 확실히 알 수 없다. 아마도 에 스 테로겐과 수용분자 간의 복합체가 염색질과 결합함으로써 선택적 인 유 전 자 발현이 유발될 것 이라고 생각되고 있을 뿐이다. 특별히 수
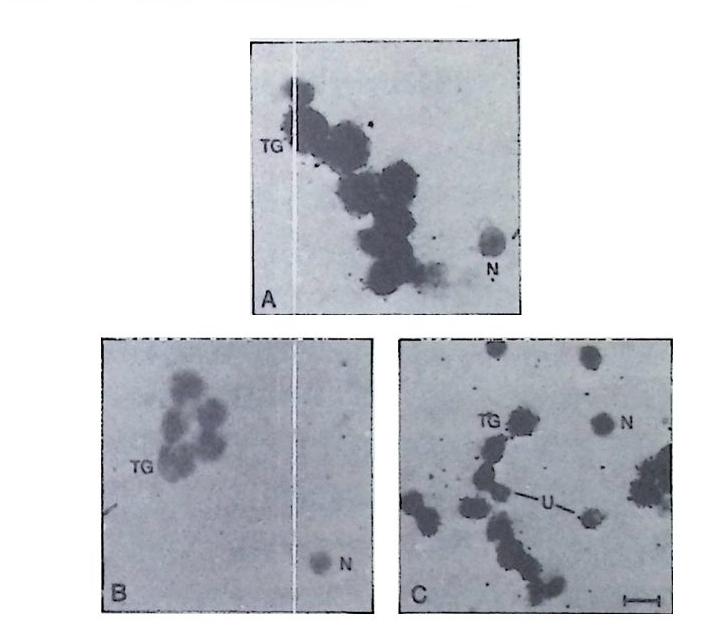 l
l
그림 5-22 난알부민 cDNA 와의 in situ 재결합법으로 알아낸 난알부민 mRNA 의 위치. (A) 수란관 세포 (TG) 에는 에스테로겐 처리 후 강하게 표지됨. 비 수란관 세포 (N) 는 표지되지 않음. (B) 에스데로겐을 제거시키면 거의 표지되지 않음. (C) 프로게스테론을 다시 처리해 주면 수란관 세포에 표지 2가µ. m많( S이h ep나 h타e 남rd. e t 두a l. , 개 1의98 0)확. 인되지 않은 세포 (U) 도 관찰됨. 눈금의 길이는
란관세포에서만 난알부민유전자가 발현되는 이유는 표적세포의 특이 성 때문이라고 생각되고 있다. 즉 표적세포의 세포질에 있는 수용분 자의 특이성 때문에 에스데로겐이 수란관세포에만 선택적으로 수용될 수 있다. 일반적으로 스데로이드 계통의 호르몬이 핵 속으로 들어가 서 염색질에 결합하기까지는 두 단계의 반응이 일어나는 것으로 생각 되고 있다. 첫 단계에는 호르몬의 표적세포로의 두과이다. 스데로이 드계의 호르몬은 표적세포와 비표적세포에 모두 확산해서 들어가지 만, 비표적세포에서는 수용분자가 없기 때문에 호르몬이 세포내에 보 존되지 못하고 표적세포에서는 수용분자가 있기 때문에 보 존 된다. 단 백질로 생각되는 수용분자와 호르몬간의 결합으로 세포질에서 복합체 가 형성된다. 두번째 단계로는 핵 속으로 복합체가 이동하여 염색질 과 결합한다. (5) 글로빈유전자의 전사 유전자 발현이 전사수준에서 조절되는 예로서 가장 잘 연구된 경우 는 발생단계에 따른 글로빈유전자의 순차적 활성화에서 찾아볼 수 있 다. 닭이나 사람의 경우 헤모글로빈 합성은 발생과정에 따라 변한다. 닭에서는 계배의 암구 (area opa c a) 후부에 자리하고 있는 혈도 (blood i slands) 에서 헤모글로빈이 만들어지는데, 20 내지 23 시간 경과한 계 배에서는 아직 글로빈유전자가 전사되지 않지만, 약 35 시간이 경과하 면 두 차례의 세포분열을 더 하게 되는데, 이때부터 이들 적아구(赤 茅球 e rythr oblas t)에서 헤모글로반이 상당히 빠른 속도로 합성된다. 죽 발생 35 시간만에 글로빈유전자가 처음으로 활성화된다. 점차 발생이 진행됨에 따라 글로빈유전자의 전사는 또 다른 형태로 조절된다. 닭과 사람을 포함하여 여러 종류의 동물에서는 발생배 혹 은 태아의 헤모글로빈이 성체의 적혈구 헤모글로빈과 다르다. 사람의 발생배 헤모글로빈은 두 분자의 제타 (ze ta, t) 글로빈과 두 분자의 입
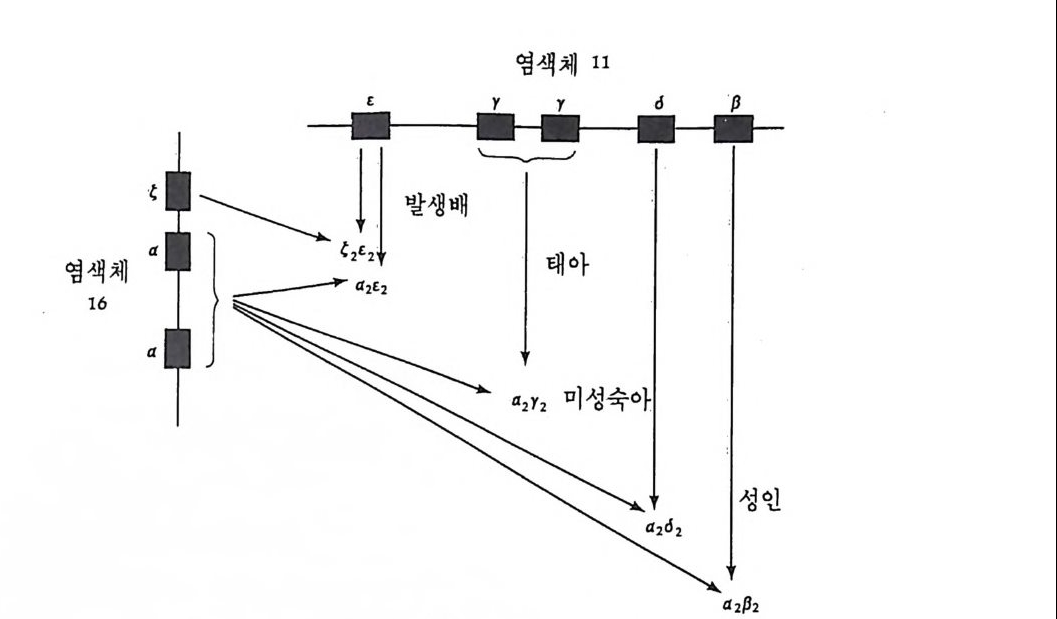 염」제:’ : | :` ;\ a2 y 2 미성숙:아
염」제:’ : | :` ;\ a2 y 2 미성숙:아
그림 5-23 발 생에 따른 글로빈유전자의 순차적 활성화
실론 (e p s il on , E) 글로빈 및 석손자의 행으로 구성되어 있다. 그러나 임 신 2 개월 정도 지나면 t와 c 글로빈의 합성은 갑자기 중지되고, 그 대신 알파 (al p ha, a) 와 감마(g amma, r) 글로빈의 합성이 증가한다. 두 분자의 y글로빈과 두 분자의 云군로반이 결합하여 한 분자의 태아 헤 모글로빈을 이루게 된다. 임신 3 개월부터 베타 (be t a, f3)글로빈과 델타 (delta , o) 글로빈유전자가 활성화되면서 r 글로빈유전자의 발현은 중 지된다. 분만 후에는 더 빠른 속도로 태아의 헤모글로빈이 성체의 헤 모글로빈의 형태로 바뀐다. 즉, 정상적으로 성체의 헤모글로빈은 97% 가 a2/J 2, 2~3% 가 a282 그리고 l% 가 a2 Y2 로 구성되어 있다. 사람에서는 t와 a 글로빈유전자는 16 번의 염색체에 자리하고 있고, €, r, 8 및 8 글로빈유전자는 11 번의 염색체에 순서대로 자리하고 있 다. 이러한 점으로 보아 11 번의 염색체에 있는 이들 글로빈유전자들 이 발생배에서 태아의 글로빈 형태로 그리고 태아에서 성체의 글로빈 형태로 순서에 따라 발현되는 데에는 반드시 이러한 발현 순서를 조
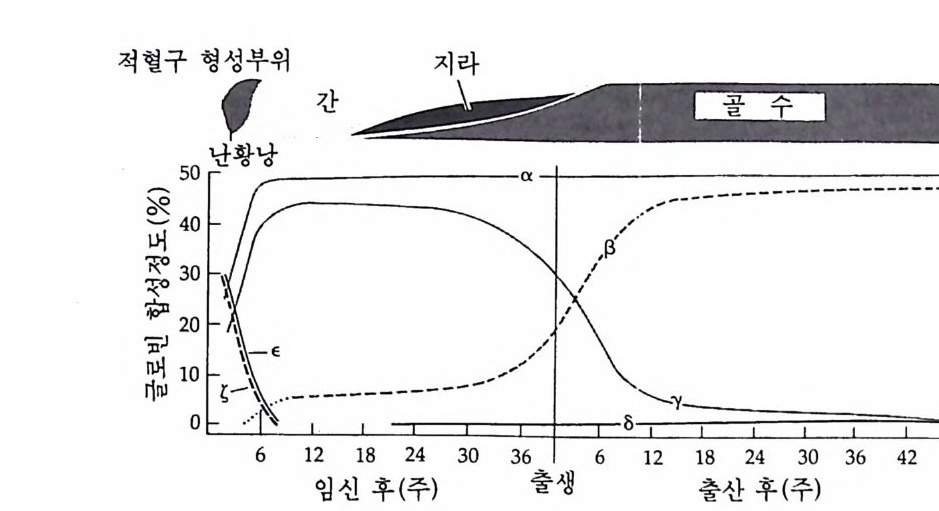 적혈 구 난형,呼 위 간 지`라
적혈 구 난형,呼 위 간 지`라
그림 5-24 발생 에 따른 글로빈유전자와 순차적 활성 화
절하는 특별한 기구가 있을 것으로 생각되고 있다. 그러나 아직 이러 한 기구는 모른다. 모든 면에 있어서 정상적이지만, 태아의 헤모글로 빈 합성만은 비정상적으로 성체에서까지도 중지하지 않고 계속하는 개체에서 유전자 발현 조절기구와 관련되는 단서를 얻을 수 있었다. 즉 동일한 계보의 세포에서 태아의 글로빈으로부터 성체의 글로빈으 로 전환하는 것이 적아구에 선천적으로 주어진 기구에 기인할 것이라 는 단서가 최근 관찰되었다. 사람의 발생배의 난황낭(y olk sac) 으로 부터 적혈구의 전구 세포를 분리하여 배양해 보면 그 중에는 발생배 의 헤모글로빈을 합성 하는 세포들과 함께 간 세포 (s t em cells) 가 나타 난다. 이들 간 세포들은 후에 태아의 글로빈 그리고 성체의 글로빈을 합성하는 적혈구가 된다 (S ta ma t o y anno p oulos et al., 1987). 사람의 태 아 적아구와 생쥐의 적아구 종양세포를 융합하면 처음에는 사람의 태 아 헤모글로빈이 융합세포에서 만들어진다. 그러나, 이들 융합세포가 계속 세포분열하면 나중에는 성체의 글로빈 단백질을 합성한다. 대개 15-20 주의 사람의 태아 적아구를 사용하여 이와 갇은 조작을 하면, 8 -10 주의 태아를 가지고 하는 것보다 글로빈 형태의 전이과정이 더 빠
르게 나타남을 관찰할 수 있다. 이러한 관찰로부터 그 세포에 선천적 으로 내재하고 있는 시계와 같은 기구가 있을 것이라는 생각이 가능 하였다 (Pa p a y anno p oulou et a l., 1986). (6) 전사조절 단백질 유전자가 전사될 때 조절 단백질의 개입으로 인하여 그 전사가 조 절될 수 있다는 가능성이 5S rRNA 유전자의 전사과정에서 관찰되었 다. 즉 5S rRNA 유전자는 발생과정중 전사수준에서 조절된다 (Xom, 1982). 반 배수체의 게놈 속에는 20,000 개의 난모세포형의 5S 유전자 와 400 개의 체세포형 5S 유전자가 있는데, 난자형성 초기에는 이들 유전자 모두가 전사된다. 그러나 난자형성 후기에 모든 5S 유전자의 발현은 중지되고 포배 전이 시기까지 다시 발현되지 않는다. 포배기 에 다시 난모세포형과 체세포형의 5S 유전자가 발현되지만 포배기가 끝날 무렵 체세포형의 5S 유전자만이 발현된다. 5S 유전자의 발현을 조절하는 RNA 중합효소는 RNA 중합효소 l11 인데 이 효소는 특이한 p romo t er 에만 결합한다. 죽 RNA 중합효소 l 과 Il 의 p romo t er 는 유전자의 5' 쪽의 가장자리 에 자리 하고 있지 만, RNA 중합효소 Ill 에 대한 p romo t er 는 유전자의 가운데 에 자리 하고 있다. 이러한 사실은 Xen op us 의 5S rRNA 유전자를 부분적으 로 결손시킨 다음 그 유전자가 아직도 전사능력을 유지하는지롤 살펴 봄으로써 알아낼 수 있었다. 즉, 5S 유전자의 5' 쪽의 가장자리나 혹 은 3' 쪽의 가장자리를 효소로 제거시킨 다음 RNA 중합효소 l11 을 넣 고 전사시켜 보면, 5S 유전자의 전사는 정확하게 일어난다. 그러나 5S rRNA 유전자의 가운데 부위에 해당하는 누클레오티드 번호 50 에 서 83 의 누클레오티드를 제거시킨 다음, 전사시켜 보면 5S rRNA 유 전자는 전혀 전사되지 않는다 (Sakon j u et a l., 1 980 ; Bog en hage n et a l., 1980). 더구나 RNA 중합효소 Ill 에 의해 전사되는 유전자내에는 보
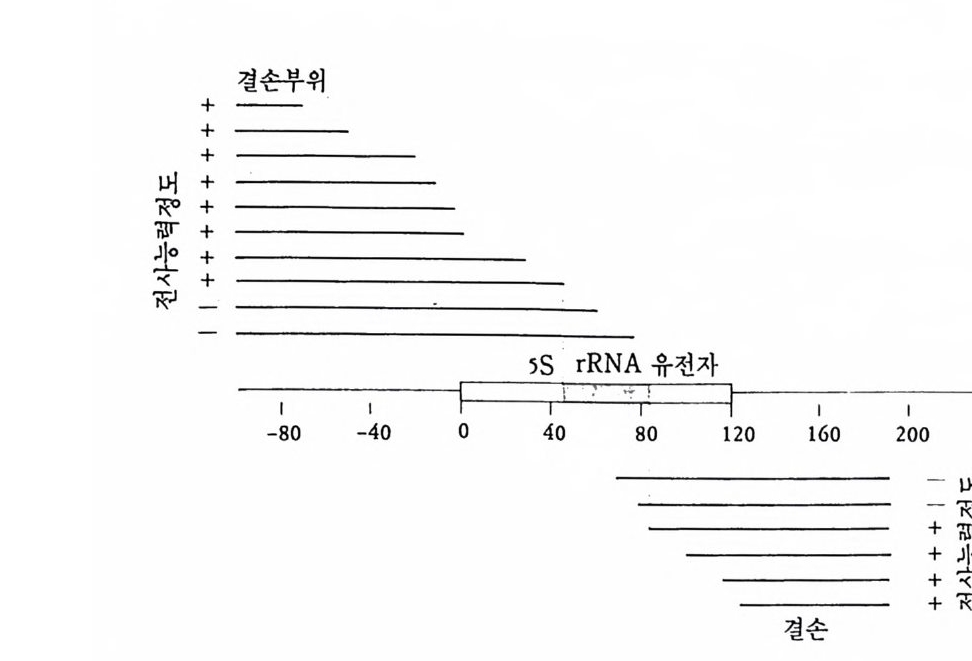 결손부위
결손부위
그림 5-25 Xenopu s laevis 5S rRNA 유전자에 대한 결손지도. 5S rRNA 유전자 를 프라스미드에 조합시켜 증폭시킨 다음 시험관내에서 전사능력을 측 정하 였다. 이때 5S rRNA 유전자를 상위에서부터 그림에 표시한 선에 해당하는 부위만큼씩 결손시키면서 전사능력을 측정함으로써, 5S rRNA 유전자의 위 치를 확인할 수 있었다. 특별히 하위 50~83 염기쌍을 결손시키면 , 유전자는 전사능력을 상실한다. +는 전사능력 있음을 그리고 -는 전사능력이 없음 을 나타낸다 (Brown, 19s1).
존적인 부위가 있는 것으로 관찰되고 있다. 죽 AGCAGGGT 와 갇은 염기배열이 Xenoj)u s 5S rRNA 유전자의 영기서열번호 55 와 62 사이 에서 관찰되었고 유사한 염기서열이 누에 (Bomb yx mo ri)의 tyros in e t RNA 와 adenov iru s VA-1 유전자에서도 관찰되었다. 박테리아의 RNA 중합효소는 DNA 에 직접 결합되지만, 진핵세포 의 RNA 중합효소는 p romo t er 에 직접 결합되지 않고 특별한 단백질 에 의해 중개 된다. 죽, Xen oj)us의 5Sr RNA 유전자에 RNA 중합효 소 따울 인위적으로 첨가해 줄지라도, 정확한 전사는 일어나지 않는
다. 그러나 5S rRNA 유전자에 핵 추출물을 함께 넣어주면 전사가 정확하게 일어난다. 이때 5S rRNA 유전자 조절부위에 특별히 결합 하는 38,5KD 의 단백질이 있는데, RNA 중합효소 IIl 을 p romo t er 에 결합시키는 역할을 하는 것으로 보인다 (N g et a l., 1979 ; Eng el ke et al., 1980). 이 단백질이 없으면 sSrRNA 유전자의 전사도 일어나지 않는 다. 이 단백질은 TFIIIA 라고 불리는데, 5S rRNA 유전자에만 특이하 게 작용하는 전사 조절 단백질로서 발생중에 단계에 따라 작용된다. 즉 sS rRNA 가 다량 합성되는 난자형성 초기에는 TFIIIA 단백질은 다량 존재하나, 5S rRNA 합성은 난자형성 말기에는 대단히 낮은 수 준으로 떨어진다 (G i nsber g et a l., 1984). 5S rRNA 유전자 발현은 핵 속에 존재하는 TFIIIA 의 양과 관계되 는 것으로 보인다. 즉 유전자 재조합법으로 클로운된 난모세포형 및 체세포형 5S rRNA 유전자를 난모세포와 포배세포의 핵 속으로 주입 시키면 TFIIIA 는 난모세포형에 대해서보다도 체세포형에 대해서 약 200 배나 더 높은 친화력을 가지고 있는 것을 알 수 있다. 따라서 TF IIIA 의 농도가 낮을 때에는 체세포형의 유전자에만 결합하지만 농도 가 높을 때에는 체세포형은 물론 난모세포형의 5S rRNA 유전자도 TFIIIA 의 결합에 의해 활성화된다. 체세포형 5S rRNA 유전자만이 활성화되어 있는 후기 포배세포의 핵 속으로 순수한 TFIIIA 를 다량 주입하면 난모세포형의 유전자도 함께 활성화된다. 5S rRNA 유전자내의 TFIIIA 결합부위를 돌연변이 분석, DNAseI foo tp ri n t i ng , gua nosin e meth yla ti on 및 pho sph a te blockage 등과 갇은 방법 으로 알아내 었 다 (Sakon j u and Brown, 1982 ; Pie l er et a l., 1985). 돌연변이 분석법으로 전사가 적절하게 일어나는 데 필요한 부 위 세군데 즉, 누클레오티드 배열 번호 50~61, 70~71 그리고 80 ~89 를 알아내었다. 누클레오티드 배열 번호 50~61 은 RNA 중합효 소 Ill 에 의하여 전사되는 모든 다른 유전자에서도 발견되었다. 체세 포형 sS rRNA 유전자와 난모세포형 5S rRNA 유전자는 이 결합부위
가 서로 다른데 아마도 이러한 차이 때문에 TFIIIA 에 대한 친화도도 다를 것이라고 생각되고 있다 . DNAse I fo o tp r i n ti n g도 DNA 상의 단밸질과의 결합부위를 찾아내 는 방법이다. TFIIIA 와 같은 결합 단백질을 방사능 동위원소로 표지 된 DNA 에 결합시킨 다음 별로 특이성이 없는 일반적인 DNAse 로 처리하여 전기영동법으로 분리하면 크기가 다른 여러 종류의 ol ig onucleo ti des 를 얻을 수 있다. 이 때 ol ig onucleo ti des 간의 염기
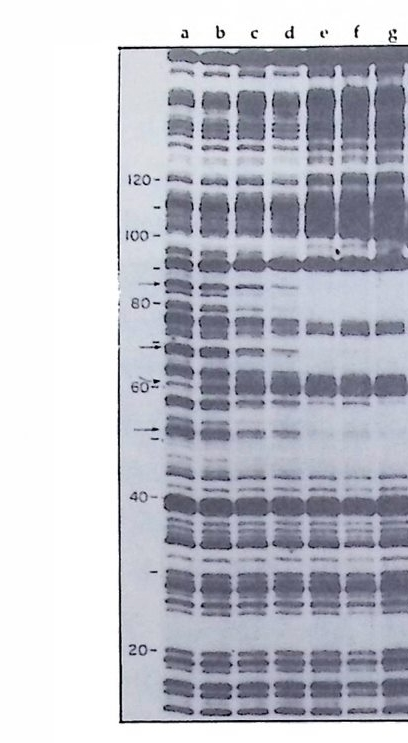 • b C
• b C
그림 5-26 5S DNA 내 TF fil A 결합부원 방사능 동위원소로 표지한 5S DNA 를 TFIIA 로 처리한 다음, DNAse 로 분해시켰다. 분해된 DNA 토막을 전기영동 하여 자기방사하였다. TF fil A의 농도를 증가시켜주면 (a-h) 전기영동띠가 없는 빈자리가 나타나는데, 이 자리에 있는 D NA 토막이 TF fil A에 보호받음으로 전 기 영동띠가 나타나지 않았다 (Sakonju and Brown, 1982) .
수의 차이는 일반적으로 한 개 정도에 지나지 않지만 , 만약 결합단백 질에 의해 DNA의 결합부위가 보호되면, DNAse 에 의해 분해되지 않기 때문에 바로 해당하는 부위의 ol ig onucleo ti des 가 전기영동판에 나타나지 않는다. 이러한 분석을 TFIIIA 단백질을 이용하여 시행하 므로써 역시 세 군데의 결합 부위가 있음을 확인할 수 있었다. 결합 부위를 알아내는 또 하나의 다른 방법은 gu anos i ne 에 메칠기 롤 첨가시키든가 혹은 인산기에 에칠기를 첨가시킴으로써 이러한 첨 가반응이 TFIIIA 결합에 어떤 영향을 주는지를 관찰하는 것이다. 배 열번호 70, 71 그리고 80~89 의 gu anos i ne 에 메칠기를 첨가하고 배열 번호 70, 71 그리고 80~87 의 인산기에 에칠기를 첨가하면 TFIIIA 결 합이 억제되기 때문에 TFIIIA 에 의한 세 군데의 DNA 부위의 보호가 불가능해진다. 5S rRNA 유전자의 p romo t er 에는 TFIIIA 에 대한 결합부위가 세 군데 있는 반면에 TFIIIA 단백질에는 9 개의 DNA 결합부위가 있다. DNA 결합부위는 주로 영기성 아미노산울 주요 아미노산으로 하는 구형 모양의 부위 이 다 (glo bular domain ) . 이들 구형 부위 는 각각 Zn 이온을 중심으로 안정되어 있고 9 개의 구형부위는 일정한 간격울 가 지고 반복된 배열을 하고 있다(t andom array) . 이러한 배열로 인하여
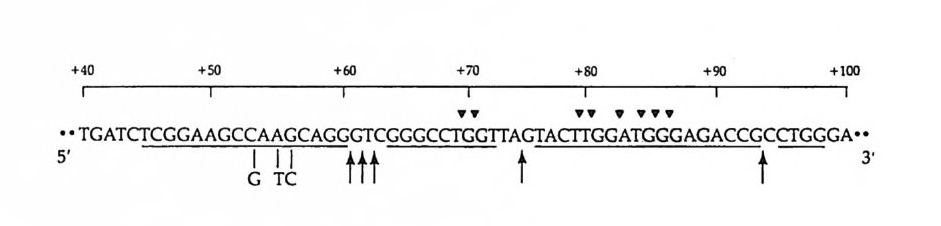 +40 +50 +6 0 +70 +80 +90 +100
+40 +50 +6 0 +70 +80 +90 +100
그림 5-27 Xenopu s lae v is의 5SrRNA 유전자의 조절부위와 TFil lA 사이의 상 호작용. 회색상자 : gua nosin e 잔기가 메철화되면 TF ill A의 결합울 방해한 다. 삼각형 (T) : TF ill A 와 접촉을 가진 DNA 의 인산기 , 믿줄 : TF ill A의 결합으로 DNAse I 의 작용으로 보호받은 부위. 화살표로 지시된 염기는 난 모세포형의 5S rRNA 유전자에서는 다르다 (Sakon j a and Brown, 1982).
RNA 중합효소가 DNA 를 따라 이동할 때 DNA 를 고정시키는 역할 울 하는 것으로 생각되고 있다. 즉 TF ilI A 가 DNA 에 결합하여 이중 나선을 분리시키는 것과 갇은 sS rRNA 유전자의 구조적 변화 (con fon nati on al chang e) 를 유발하는 것으로 해석되고 있다(Kmi ec and Worcel, 1985 ; Kmiec et al., 1986) . 그러 나 이 러 한 해 석 에 반론이 제 기 된 경우도 있다 (Wol ff e et al., 1987).
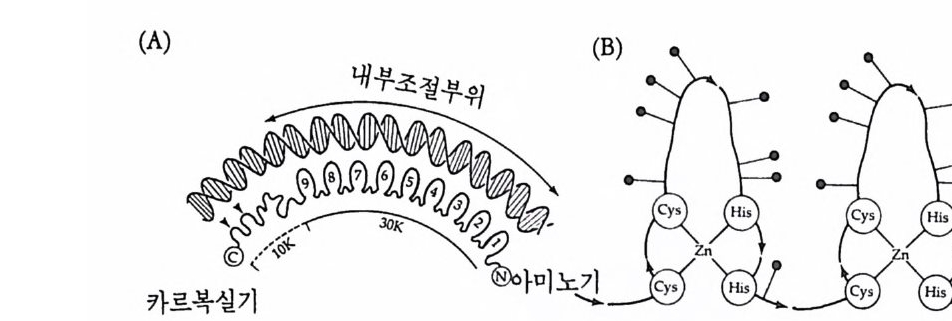 (A)
(A)
그립 5-28 전사조절단백질 TFlIIA 의 구조. (A) DNA 와 TFlIIA 단백질의 상대적 배열. 9 개의 손가락과 갑은 구조가 TF 때 A 에서 나와 5S p romo t er 와 결합한다. (B) DNA 과 결합하는 손가락 과 감은 구조를 아연 (Zn) 으로 안정시키고 염기성 산기(혹색의 원)가 DNA 와 접촉을 이룬다 (M ill er et a l., 1985).
5S rRNA 의 유전자 발현이 TFllIA 단백질에 의해 조절된다는 사 실은 상당한 의미를 내포하고 있다. 아직까지 결정요인의 정체와 작 용기구에 대해서 전혀 모르고 있는 실정에서 이러한 선택적 유전자 발현의 조절 단백질에 대한 확인을 결정요인의 정체와 작용기구를 보 여주는 것처럼 받아들여질 수 있다. 물론 세포의 운명결정은 세포의 기능부여와 동일한 의미를 가지고 있으며 세포 특유의 기능부여는 단 백질의 종류에 기인한다고 할 수 있기 때문에 선택적 유전자 발현의 조절기구를 규명하는 것은 대단히 중요하다. 그러나 5S rRNA 유전 자 발현을 조절하는 TFllIA 단백질의 합성조철 죽 TFllIA 유전자의
선택적인 발현조절이 규명되어야만 궁극적으로 5S rRNA 유전자 발 현조절로 설명될 수 있다는 점을 감안할 때 세포운명결정을 위한 선 덱적 유전자 발현의 조절기구를 밝힌다는 것은 그렇게 쉬운 일이 아 니라는 점을 실감케 한다. (7) swit ch gen es swi tch g enes 이란 이 유전자의 생성물의 유무에 따라 세포의 분화 방향을 변경시키는 유전자를 의미한다. 즉 swi tch g ene 의 생성물은 두 가지 종류의 세포로 분화할 수 있는 잠재력을 가진 세포의 방향을 한쪽으로 고정시켜 준다. swi tch g ene 의 가장 좋 은 예는 환형동물 홉충류의 일종인 Caenorhabdit is e leg a ns 의 Iin- 12 유전자에 관한 것이다 (Greenwald et al., 1983). C. e leg a ns 의 야생종의 발생배에는 Zl. PPP 와 Z4. aaa 라는 두 종류의 세포가 형성되는데 두 종류의 세포 중 한 종류는 자궁 갈 고리세포 (u t er i ne anchor cell, ac) 가 되고, 다른 종류의 세포는 복면 자 궁 (ven tr al ute r i ne , vu) 의 모세포가 된다. Ii n-12 의 열성 돌연변이종에 서는 이 유전자가 전사되지 않으며, 두 종류의 세포는 모두 갈고리세
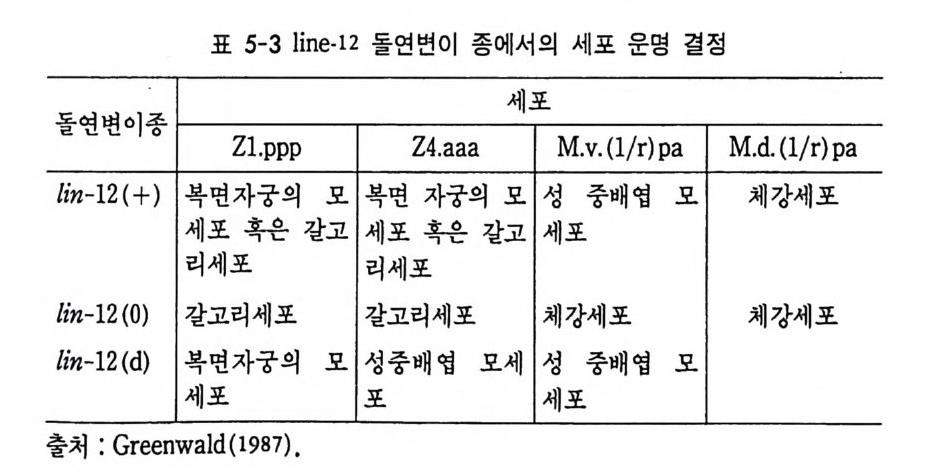 표 5-3 line -12 돌연번이 종에서의 세포 운명 결정
표 5-3 line -12 돌연번이 종에서의 세포 운명 결정
포로 분화한다. 그러나 우성 돌연변이종에서는 !i n ~ 12 의 전사정도가 높으며 그 결과 두 종류의 세포는 모두 복면자궁의 모세포가 된다. 이러한 관찰로부터 lin- 12 유전자는 두 가지 발생 방향 중 하나를 선 택해 주는 역할을 한다. lin - 12 유전자는 이 의에도 다른 종류의 세 포에서도 유사한 역할을 하는 것으로 관찰되었다. 죽 복측과 배측의 m(l/r)pa 세포는 각각 성 중배엽 모세포 (sex mesoblas t)와 체강세포 (coelomoc yt e) 가 되지만 우성 !in~ 12 돌연변이종은 모두 성 중배엽 모 세포가 되는 반면에 열성 돌연변이종은 모두 체강세포가 된다. 초파리 의 Notc h 유전자도 일종의 swi tch g ene 으로 알려 져 있다. 낭배기 직후 발성성배의 배측 정중선을 따라 자리하고 있는 1800 개의 의배엽 세포들은 배측 신경색 (背側神 經 索, ventr a l nerve cord) 을 형성 하는데, 이들 중 25% 가량의 세포는 신경 원세포 (neuroblas t)가 되 고, 그 나머지는 하피(下皮 hyp erde rmi s) 의 전구 세포가 된다. 즉 신
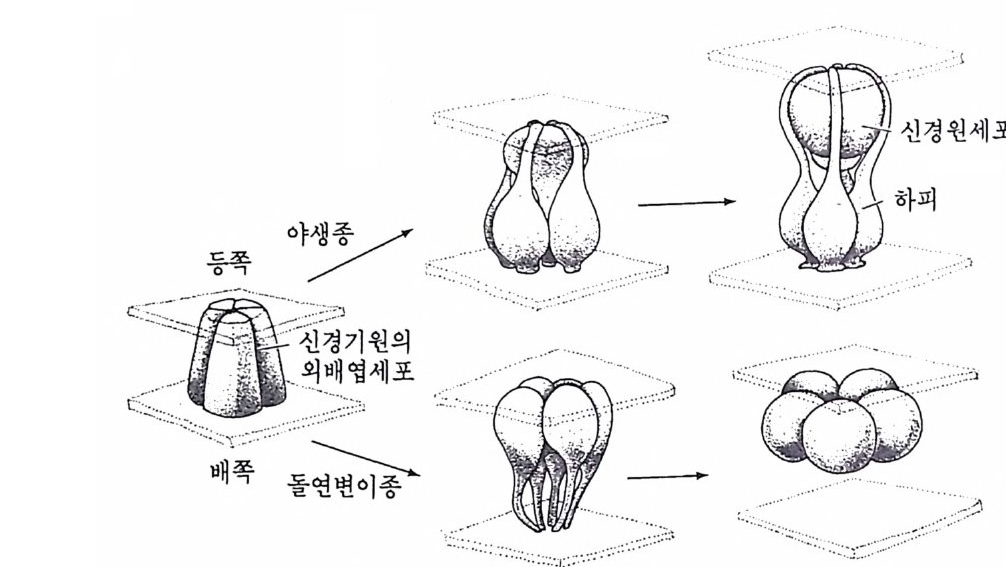 ·l
·l
그림 5-29 Notc h 돌연변이의 효과. 야생종의 발생배에서는 신경기원의 의배영 세포로부터 신경원세포와 하피 (下皮) 세포가 분화된다. 그러나 Notc h 발생 배에서는 모든 신경기원의 의배영세포는 신경원세포로만 분화한다.
경계 형성 부위의 세포들은 표피 혹은 신경계의 전구 세포가 된다 (Hart en ste in and Camp os -Or teg a , 1984). 그러나 Notc h 유전자가 발생 중 전사되지 않으면, 이들 세포들은 모두 신경계 전구 세포로 분화된 다 (Lehmann et al., 1983 ; Artav ari s-T sakonis e t a l., 1983). 이러한 발생 배에서는 배측 및 머리 부위의 표피 세포를 모두 신경계 세포로 전환 시켜 신경계 세포가 과잉으로 생산되기 때문에 이 발생배는 결국 죽 게 된다 (Poulson, 1937 ; Hop pe and Greenspa n , 1986) . Notc h 유전자를 클로운하여 조사해 본 결과 발생 초기에 전사되는 것으로 관찰되었다 (Ki dd et al., 1983 ; Yedvobnic k et al., 1985) . Notc h 유전자와 lin- 12 유전자는 모두 표피 생 장요인 (ep ide nnal grow th fac to r , EGF) 의 유전자의 염기 배열과 상당히 유사한 것으로 나타났다. Notc h 단백질 N- 말단 부위는 EGF 와 같은 펩티드를 36 군 데에서 반복적으로 가지고 있는데, 이 펩티드의 특칭은 세포막 밖으 로 돌출된 모양으로 막에 부착되어 있다 (Wha rt on et al., 1985). lin - 12 유전자의 생성물도 최소한도 11 개의 EGF 와 유사한 펩티드를 가지고 있으며 막에 부착되어 있는 것으로 생각되고 있다.
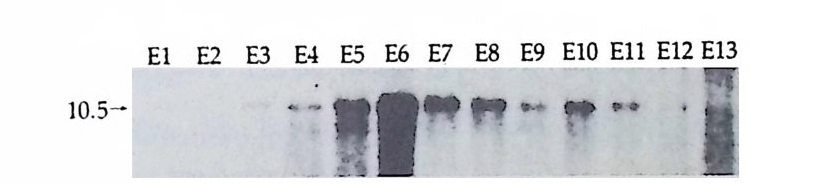 10.5 一 El E2 E3 E4~ ES :EI6 E7 ES E...9.. ,ElO E..l.l E12 E13
10.5 一 El E2 E3 E4~ ES :EI6 E7 ES E...9.. ,ElO E..l.l E12 E13
그림 5-30 초파리 야생종에서의 배발생중 No t ch 유전자 발현의 변화. Noth e m blo t법으로 측정하였다. 숫자는 2 5°C 에서의 발생시간을 의마한다 (Yedvob nic k et a l., 1985) .
sevenless 라는 swi tch g ene 에서도 막에 부착되 어 있는 성 장요인 수 용분자와 갇은 단백질이 만들어진다는 사실이 알려지고 있다. 이 유 전자는 초파리 의 마지 막 유충기 의 눈 성 체 원기 (ey e im ag ina l disc ) 에서 발현되는대, 망막 세포가 자의선 광수용 세포나 혹은 비신경성 추세
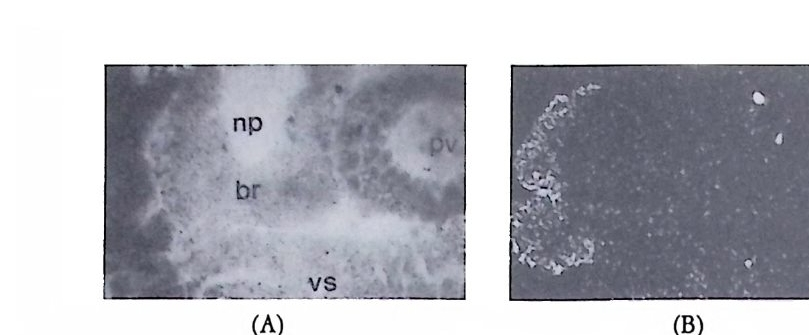 ?`ir , ,i i ‘`.‘. ’.
?`ir , ,i i ‘`.‘. ’.
그림 5-31 Sevenless mRNA 의 위치. 야생종의 Sevenless DNA 울 방사능 동 위원소로 표지하고 제한효소로 토막내어 in situ 재결합하여 자기방사하였 다. (A) 유충의 뇌 부위 (br, pv, vs) 와 눈 성체 원기 (ed). (B) 표지된 DNA 가 눈 성체원기부위의 mRNA 에만 재결합한다 (Ha f en et a l., 1987).
포 어느 쪽으로 분화할 것인지를 결정하는 역할을 한다. 만약 sevenless 유전자가 전사되면 이들 세포들은 신경세포로 그 운명이 결정되고, 만약 전사되지 않으면 추세포로 그 운명이 결정된다 (Banerj ee et a l., 1987 ; Hafe n , et a l., 1987}. 세포의 가능한 분화 방향이 두가지일 때 lin- 12, Notc h 및 sevenless 유전자는 그 방향을 결정해 준다. 이러한 유전자의 생성물이 작용하는 과정에서 대단히 중요한 공통점은 세포 상호작용으로 생각되고 있는데, 그 이유는 이들 조절 단백질이 막에 부착되어 있어 다른 세포의 표면과 상호작용을 할 수 있도록 되어 있기 때문이다. 참고문헌 Artav ani s- Tsakon is, S., Muskavi tch , M.A.T. and Yedvobn ick , Y. (1983) . Molecular clon ing of Notc h , a locus affe c ti ng neurog en esis in Drosop h ila melanoga s te r. Proc. Natl. Acad. Sci . USA so: 1977
-1981 . Ashburner, M. (1972a) . Patt er ns of puf f ing acti vity in the saliv a ry gla nds of Drosop hi la . VI. Inducti on by ecdy so ne in saliv a ry gla nds of D. melanoga .ster cultu r ed in vitr o. Chromosoma 38: 255-281. Ashburner, M. (1972b) . Puff ing pat t er ns in Drosop hi la melanoga .ster and relate d spe c i es . In W. Beerman (ed.) , Develop m enta l Stu d ie s on Gia n t Chromosomes, Spr i n g e r -Verlag, Berlin , p p. 101-151 . Ashbumer, M. (1974) . Seq ue nti al gen e acti va ti on by ecdy so ne in pol yt en e chromosomes of Drosoph i la melanoga .ster . I I. Eff ec ts of inh ib i t or s of pro te i n syn the sis . D ev. Bio l. 39: 141-157. Banerjee , U., Renfr an z, P.J., Pollack, J.A. and Benzer, S. (1987) . Molecular characte r iz a ti on of sevenless, a gen e inv olved in neur- onal pat t er n for mati on in the Drosop hi la eye . C ell 49: 281-291. Barnett, T., Pachl, C., Gerge n , J.P. and Wensin k , P.C. (1980) . The iso lati on and characte r iz a ti on of Drosop hi la yol k pro te i n gen es. Cell 21: 729-738. Beermann, W. 1971. Eff ec t of a-aman itine on pu ff ing and int r a nu- clear RNA syn the sis i n Chir o nomus saliva ry gla nds. Chromosoma, 34: 152-167. Bog en hage n , D.F., Sakonju , S. and Brown, D.D . (1980) . A contr ol regi on in the cente r of the 5 S RNA gen e Bonner, J.T . and Pardue, M. L. (1977) . Ecd y sone-s ti m따 a t ed RNA syn the sis in saliv a ry gla nds of Drosoph i la melanoga .ster : Assay by in situ hyb rid i z a ti on . Cell 12: 219-225. Britt en , R.J. and Davi ds on, E.H . (1971) . Repe t it ive and nonrepe t i tive DNA sequ e nces and a s pec따 a ti on on the orig ins of evoluti on ary novelty. Q. Rev. Bio l. 46: 111-133. Britt en , R.J. and Kohne, D.E. (1968). Repe a te d sequ e nces in DNA.
Sci en ce 161: 529-540. Brown, D.D . (1981) . Gene exp re ssio n in eukaryo t e s . S cie n ce 211: 667 -674. Chamberlain , H.E. , Britt en , R.J. and Dav ids on, E .H. (1975) . Sequ e nce orga n iz a ti on in Xenop us DNA stu d ie d by the electr o n mi cr oscop e. ]. Mol. Bio l. 96: 317-334. Clarkson, S.G . , M .L. Bir n sti el , a nd V. Serra. 1973. Reit er ate d tra nsfe r RNA gen es of Xenop us laevis . J. M ol. Bio l. , 79: 391-410. Clever, U. 1961. Genak ti v it셨t en in den Rie s enchromosomen von Chir o nomus ten ta n s und ihr e Bezie h ung en zur Entw ic k lung. I. Genakti vier ung en durch Ecdy so n. Chromosoma, 12: 607- 67 5. Clever, U., and P. Karlson. 1960. Indukti on von Puff .ve randeri lng e n in den Spe i c h eldri lse nchromosomen von Chir o n om us ten t a n s durch Ecdy so n. Exp. Cell. Res., 2 0: 623- 62 6. Consta n tin i, F.D., Scheller, R.H. Britt en , R.J. and David s on, E.H . (1978) . Rep et it ive seq ue nce tran scrip ts in the matu r e sea urchin oocyt e. Cell 15: 173-187. Davi ds on, E.H ., and R.J . B rit ten . 1973. Orga n iz a ti on , tra nscrip tion , and regu la ti on in the ani m al gen ome. Q. Rev. Bio l. , 48: 565- 61 3. Davi ds on, E.H ., Graham, D.E. , New feld , B.R., Chamberlain , M. E., Amenson, C.S ., Houg h, B.R. and Britt en , R.J. (1973a) . Arrang e- ment and characte r iz a ti on of repe ti tive sequ e nce elements in ani- mal DNAs. Cold Sp ring Harbor Sym p. Quan t. Bi ol. 38: 295-301. Davi ds on, E.H ., Houg h, B.R., Amenson, C.S . and Brit ten , R.J. (1973b) . General int e r spe r sio n of repe t i tive wit h nonrepe t i tive sequ e nce elements in the DNA of Xenopu s. ]. Mol. Bio l . 7 7: 1-2 4 . DuPraw, E.J . 1970. DNA and Chromosomes. Holt , Rin e hart & Wi n- sto n . New York.
Edelman, LS. 1975. Mechanis m of acti on of ste r oid hormones. J. Ste r oid Bio c hem., 6: 1 47-159. Eng el ke, D.R ., Ng , S. -Y., Shastry , B.S. and Roeder, R.G . (19so) . Spe c i fic int e r acti on of a pur ifi ed tra nscrip tion fac to r wit h an int e r nal contr o l regi on of 5S RNA gen es. Cell. 19: 717-728. Fin c h, J.T ., Noll, M. and Kornberg, R.D . (1975) . Electr o n mic r oscop y of d efi ne d leng ths of c hromati n. Proc. natl . A cad. Sci. USA 72: 3320 -33 22. Foe, V.E., Wi ki n s on, LE. and Lair d , C.D . (1976) . Comp ar ati ve orga - niz a ti on of a cti ve tra nscrip tion unit s i n Oncop e ltu s fasc ia tus. Cell 9: 131- 14 6. Gazit , B., Panet, A. and Cedar, H. (1980) Reconsti tut i on of deoxy r- ibo nuclease I-se n sit ive stru ctu r e on acti ve gen es. Proc. Natl. Acad. Sci. USA 77: 1787-1790. Gin s berg, A.M. , K in g , D.O . and Roeder, R.G . (1984) . Xenop u s 5S gen e tra nscrip tion fac to r , TFIIIA: Characte r i za ti on of a cDNA clone and measurement of RNA levels throu g ht o u t develop m ent. Cell 39: 479-489. Greenwald, LS. (1987) . The lin- 1 2 locus of Caenorhabditi s elega n s. Bio E ssays 6: 70-73. Greenwald, LS., Ste r nberg, P.W . and Horv itz, H.R . (1983) . The lin- 12 locus spe c i fies cell fates in Caenorhabditi s eleg a ns. Cell 34: 435-444. Gronemeye r , H. and Pong s, 0. (1980) . Localiz a ti on of e cdys t e r one on pol yt en e chromosomes of Drosop hil a melanoga s te r. Proc. Natl. Acad. Sci. USA 77: 21os-2112. Gurdon, J.B . 196Ba. Chang es in somati c cell nuclei inse rt ed int o grow i ng and matu r in g amp hibi a n oocyt es . J.Em bry o l. Exp. Mor- pho l., 20: 401-414.
Gurdon, J.B. 1968b. Transpl a nte d nuclei and cell dif fer enti at i on Sci. Am. , 2 19(6) : 24-35. Hafe n , E., Basler, K., Edstr o em, J-E . and Rubin , G.M. (1987} . Sev en- less, a cell-spe c i fic homeoti c gen e of Drosop hi la , encodes a pu ta t i ve tra nsmembrane recep tor wit h a tyros in e kin a se domain . Scie n ce 236: 55-63. Harris, S.E ., Rosen, J.M ., Meens, A.R. and O'Malley, B.W . (1975}. Use of spe c i fic pro be for ovalbumi n messeng er RNA to qua nti tat e estr o g en -in d uced tra nscrip ts. Bio c hemi stry 14: 2072-2081 . Harte n ste i n , V . and Camp o s-Orte g a , J.A. ( 1984} . Early neurog en esis in wild- ty pe Drosop hi l a melanoga s te r. Wi lh elm Ro 邸 Arch. Bio l. 193: 308-325. mic r oscop e analys i s. ]. Cel l Sci . 44: 87-101 . Hewi sh , D.R . and Burgo yn e , L.A . (1973} . Chromati n substr u ctu r e. The dige sti on of chromati n DNA at regu la rly spr e ad site s by nuclear DNase. Bio c hem. Bio p h y s . Res. Commum. 52: 504- 51 0. Hood, L.E. , Wi lso n, J.H . and Wood, W.B. (1975}. The Molecular Bio lo gy of Eukary o tic Cells. Benja m i n, New York. Hop pe , P.E . and Greenspa n , R.J. (1986} . Local fun cti on of the Notc h gen e for embry on i c ecto d ermal pat h w ay choic e in Drosop hi la . Cell 46: 773-783. Karlsson, S. and Nie n haus, A.W . (1985} . Developm enta l regu la ti on of human glo bin gen es. A nnu. Rev. Bio c hem. 54: 1071-1108. Kedes, L.H . 1979. Histo n e gen es and hist o n e messeng er s Ann. Rev. Bio c hem., 48: 837-870. Kid d , S., Lockett , T.J. and Young, M.W. (1983) . The Notc h locus of KiDinrmoseo lp, hAi .lRa . maenlda nFoigr a tse tle, rR. .CAe. ll( 13947:9 4) 2.1 A-4 3fa3m. ily of short int e r spe r sed repe a t sequ e nces at the 5' end of a set of 屈 c ty os t el i um sin g l e cop y
mRNAs. Cell 16: 787-796. Kmi ec , E.B ., Razvi, F. and Worcel, A. (1986). The role of DNA -media t e d tra nsfe r of TFIIIA in the concert ed gyrat i on 1nd dif fere nti al acti va ti on of the Xenop us 5S RNA gen es. Cell 45: 209 -218. Kmi ec , E.B. and Worcel, A . (1985) . The pos it ive tra nscrip tion fac to r for the 5S RAN gen e ind uces a 5S DNA- sp e c if ic gyrat io n in Xenop us oocyt e extr a cts . Cell 41: 945-953. Korge , G. 1975. Chromosome puf f acti vi ty and pro te in syn the sis in larval saliv a ry gla nds of Drosoph il a melanoga s te r. Proc. Natl. Acad. Sci. U.S.A . , 72: 4550-4554. Korge , G. 197 7. Dire ct correlati on betw e en a chromosome puff and the syn the sis o f a larval saliv a pro te i n in Drosop hi la melanoga s te r . Chromosoma, 62: 155-174. Korn, L. (1982) . Transcrip tion of Xenop us 5 S rib o somal RNA gen es. Natu re 295: 101- 10 5. Labhart, P. and Koller, T. (1982). Str u ctu r e of the acti ve nucleolar chromati n of Xenop us laevis oocy tes . Cell 28: 279-292. Lehmann, R., Jim enez, F., Diet r ic h , U. and Camp o s-orte g a , J.A. (1 983) . On the phe noty pe and develop m ent of muta n ts of early neurog en esis i n Drosop hi la melanog as te r. Wil h elm Roux Arch. Dev. Bio l. 192: 62-74. May field , J.E., Serunia n , L.A., Silv e r, L.M . and Elgi n, S.C.R. (1978) . A pro te i n released by DNase I dig es ti on of Drosop hil a nuclei is pre fe re nti all y assoc iat e d wit h puf f s. Cell 14: 539-544. McKnig h t, G.S., P. Pennequ i n , and R.T . Sch im ke. 1975. Inducti on of ovalbw nin m RNA sequ e nces by estr og e n and pro g es te r one in chi ck ovi du ct as measured by hyb r id iza ti on to comp le menta r y DNA . J.
Bio l. Chem. , 2 50: 8105- 8 110. Meye r owi tz, E.M . , a nd D.S. Rog ne ss. 1982. Molecular orga n iz a ti on of a Drosop hila pu ff site tha t respo nds to ecdy so ne. Cell. 2 8 : 165- 1 76. Moen, R.C., and R.D. Palmi ter. 1980. Chang es in hormone respo n - siv e ness of chi ck ovid u ct durin g pri m ary stim ulati on wit h estr og e n . Dev. Bio l. , 7 8: 450-463. Mi ge on, B.R., Schmi dt , M., Axelman, J. and Cullen, C.R. (1986) . Comp le te reacti va ti on of X chromosomes from human chorio n ic villi with a swi tch to early DNA repl i ca ti on . Proc. Natl. Ac ad . Sci. USA 83: 2182-2186. Mi geo n, B.R., Wolf , S.F., Axelman, J., Kaslow, D.C . and Schmi dt , M. (1985) . Incomp le te X chromosome dosage comp e nsati on in chor- ion i c villi of human pla centa . Proc. Natl. Acad. Sci . U SA 82: 3390 -3394. Mi ller, D.L , Jr. and Beatt y, B.R. (1969) . Vis u aliz a ti on of nucleolar gen es. Sci en ce 164: 955-957. Mille r, J., M cLachlan, A.D . and Klug , A. (1985) . Repe t i tive zin c -bin d in g domain s in the pro te i n tra nsci rp t ion fac to r IIIA from Xenop us oocy tes . EMBO J 4: 1609- 1 614. Monk, M. and Harp e r, M.I. (1979) . Sequ enti al X chromosome ina cti va ti on coup le d wit h cellular differ enti at i on in early mouse embry o s. N atu r e 281: 311-313. Moore, K.L. (1977) . The Develop ing Human. Saunders, Ph ila delph ia . Morga n , T.H. (1934) . Embry ol ogy and Geneti cs. Columbia Un ive rsit y Press. New York, pp. 9-10. Ng , S-Y., Parker, C.S. and Roeder, R.G . (1979) . Transcrip tion of cloned Xenopu s laevis RNA po lym e rase III in reconsti tut e d sys - ter ns. Proc. Natl. Acad. Sci. USA 76: 136-140.
Noll, M. (1974) . Subunit stru ctu r e of c hromati n. Natu r e 251: 249-251 . O'Malley, B.W. et al. 1975. Ste r oid hormone regu la ti on of spe c i fic messeng er RNA and pro te i n syn the sis i n eucaryo t ic cells. J. C ell. Phy si o l. , 8 5: 343-356. Outl et, P., Gross-B e llard, M. and Chambon, P. (1975). Electr o n mic ro scop e and bio c hemi ca l evid e nce tha t chromati n s tru ctu r e is a repe a ti ng unit . Cell 4: 281-300. Palmi ter , R.D . and Schim ke, R.T. (1973) . Reg ula ti on of pro te i n syn t h e sis in chic k ovid u ct. III. Mechani sm of ovalbumi n supe r in d ucti on by acti no my cin D.J Bio l. Chem. 248: 1502-1512. Papa y a n nop ou lou, T., B ric e, M. and Sta m ato y a n nop ou los, G. (1986) . Analys i s of human hemog lo vin swi tch in g in MEL X human fet a l eryth ro id cell hyb r id s . Cell 46: 469-476. Pardue, M.L. and Gall, J.F. (1 970) . Chromosomal localiz a ti on of mouse sate ll ite DNA . Scie n ce 168: 1356-1358. Pardue, M.L . 1973. Localiza ti on of repe a te d DNA sequ e nces in Xenop us chromosomes. Cold Spr i n g Harbor Sym p. Qu ant. Biol. , 38: 475-482. Pardue, M.L ., D.D. Brown, and M.L. Bim stie l. 1973. Locati on of the gen es for 5 S rib o somal RNA in Xenop us laevis . Chromosoma, 42: 191-203. Pardue, M. L., and JG . Gall. 1972. Chromosome stru ctu r e stu d id e d by nucleic aci d hyb r id i sa ti on in cyt ol og ica l pr~ p ar ati on s. Chromo- somes Today; 3: 47-52. Pie le r, T., Oei, S. -L., Hamm, J., Eng el ke, U. and Erdmann, V.A. (1985) . Functi on al domain s of the Xenop us laevis 5 S gen e pro - mote r . EMBO J 4: 3751-3756. Poulson, D.F. (1937) . Chromosomal defi cie r ci es and the embry o ni c
develop m ent of Dr os op h ila me la n og a ,ster . Proc. Natl . Acad. Sci . USA 23: 133-137. Raff , R.A. and Kaufm an, T.C. (1983) . Embry os , Genes, and Ev ol uti o n . Macmi llan , New York. Roop , D.R. , Nordstr o m, J.L., Tsai, S.Y. , T sai, M-J. and O'Malley, B. W. (1978) . Transcrip tion of s tr u ctu r al and int e r venin g sequ e nces in the ovalbumi n gen e and ide nti fica ti on of po te n ti al ovalbumi n mRNA pre cursors. Cel l 15: 671- 68 5. Rubin , G.M., Brosein , W.J. , Dunsmuir , P., Flavell, A.J ., Lavis , R., Str o bel, E., Toole, J.J. and Young, E. (1980) . Cop ia- li ke tra nspo s a- ble elements in Drosop h ila gen ome. Cold Spr ing Harbor Sym p . Qu ant. Bio l. 45: 619-628. Ry ffel, G.U ., Muellener, D.B. , Wy le r, T ., W ahli, W . and Weber, R . (1981) . Transcrip tion of sin g l e -cop y vit ell og en i n gen e of Xe nop u s inv olves expr e ssio n of mid d le repe t i tive DNA . Natu r e 291: 429-431. Sakonju , S., Bog en hage n , D.F. and Brown, D.D. (1980) . A contr ol regi on in the cente r of the 5 S RNA gen e dir e cts spe c i fic ini t iat i on of tran scrip tion . I. The 5'border of the regi on . Cell 19: 13- 25 . Sakonju , S. and Brown, D.D. (1982) . Conta c t po in t s betw een a po si- tive tra nscri ption fac to r and the Xenop u s 5 S RNA gen e. Cell 31 : 395-405. Sheph e rd, J.H . et al. 1980. Com mitm ent of chic k ovid u ct tub ular gla nd cells to pr? duce ovalbumi n mRNA durin g hormonal wit h- drawal and restim ulati on . J Cell Bio l ., 87: 142- 15 1. Sh im oto h no, K., and Tem in, H.M. (1980) . Evoluti on of retr o v iru ses from cellular moveable gen eti c elements . Cold Spr ing Harbor Sym p. Quan t. Bio l 45: 719-730. Sta m ato y a n nop o ulos, G., Consta n to u lakis , P., Bric e . M. , K urachi , S.
and Papa ya n nop o ulou, T. (1987) . Coexp re ssio n of embry o nic , fet a l , and adult glo bin s in ery throi d cells of human embry os : Relevance to the cell-lin e age models of g lo bin swi tch in g . Dev. Bio l. 123: 191-197. Thomas, J.O . , a nd A.J, A. Khabaza. 1980. Cross-lin k in g of hist o n e HI in chromati n. Eur. J.B i oc hem., 112: 501-511 . Thomas, J.O . , a nd R.D . Kornberg. 1975. An oct am er of his t o n es in chromati n and free in soluti on . Proc. Natl . Acad. Sci . U.S .A., 72: 2626~2630. Wein t r a ub, H. and Groudin e , M. (1976) . Chromosomal subunit s in acti ve gen es have an alte r ed config ura ti on . Scie n ce 193: 848-856. Weis b rod, S., G roudin e , M. and Wein t r a ub. H. (1980) . Inte r acti on of HMG 14 and 17 wit h acti ve ly tra nscrib i n g gen es. Cell 19: 289-301 . Weis b rod, S. and Wein t r a ub, H. (1979) . Isolati on of a subclass of nuclear pro te i n s respo n sib l e for con fer rin g a DNase I-sensit ive str u ctu r e on glo bin chromati n. P roc. Natl . A cad. Sci. USA 76: 630 -6 34. Wharto n , K.A., Joh ansen, K. and Ar tav anis - Tsakonas, S. (1985) . Nucleoti de sequ e nce from the neurog en ic locus Notc h im p li es a gen e pro duct whic h shares homolog y wit h p ro te i n s conta i n ing EGF -lik e repe a ts . Cell 43: 567-581. Wollff e, A.P. , Andrews, M.T., C raw for d, E., Losa, R. and Brown, D. D. (1987) . Nega t i ve sup er coil in g is not requ i re d for 5 S RNA tra nscrip tion in vitro . Cell 49: 301-303. Yedvobnic k , B., Muskav itch , M.A . T ., Whart on , K.A ., Halpe r n, M. E., Paul, E., Grim wade, B.G . and Artav anis - Tsakonas, S. (1985) . Molecular gen eti cs of D rosop hi la neurog en esis . Cold Sp ring Harbor Sym p. Quan t. B io l. 50: 841-854.
제 6 장 진핵세포 유전자의 분자 구조와 유전자 발현의 조절 1 진핵세포 유전자의 분자 구조 1970 년대까지 유전자 구조에 대한 지식은 주로 원핵세포의 유전자 구조에 의존해 왔다. 즉 단백질의 아미노산 서열과 이를 지시하는 유 전자의 염기서열은 언제나 병행하며, mRNA 의 5' 쪽이 단백질의 아 미노기 말단을 지시하기 시작하여 각 코돈 (codon) 이 순서에 따라 카 르복실기 말단까지 아미노산으로 해독된다는 것이었다. 그러나 진핵 세포 유전자의 분자적 구조의 특징이 이러한 원핵세포의 유전자의 것 과는 다르다는 점을 알게 되었다. 죽 진핵세포의 구조 유전자들은 서 로 인접되어 있지 않고 대부분의 경우 분리되어 있다. mRNA 의 5' 과 3' 쪽이 각각 이러한 부위의 유전자에서 유래하며 단백질을 지시하 는 DNA 부위 죽 exon 사이에 단백질의 아미노산 서열과는 아무런 관계가 없는 i n t ron 이 삽입되어 있다. 사람의 8- 글로빈유전자의 분자
구조적 특칭을 보면 다음과 같다. CD pro moto r : RNA 중합효소의 결합부위로서 f3 - 글로빈유전자에 서는 전사 개시 부위 전 95 번에서 26 번에 자리하고 있는 영기쌍으 로 이루어져 있다. ® 전사 개시 부위 : ACATTTG 의 염기서열을 가지는 전사 개 시 부위는 cap 배열이라고도 하는데, 일단 전사되면 RNA의 5 ' 말 단에 위치한다. ® ATG 코돈 : 해독 개시 부위로서 전사 개시 부위 후 50 번째의 염기쌍에 자리하고 있다. 전사 개시 부위와 해독 개시 부위 사이의 50 개의 영기쌍으로 구성된 i n t ron 은 leader se q uence 라고 불린다. © exon : 글로빈의 아미노산 서열을 지시하는 염기쌍들로서, f3-글로빈유전자에는 3 개의 exon 이 있다. 첫번째 exon 은 글로빈 단백질의 구성 아미노산 1 번에서 30 번을 지시하는 90 개 염기쌍으로 되어 있고, 두번째 exon 은 구성 아미노산 31 번에서 104 번을 지시 하는 222 개의 염기 쌍으로 되어 있고, 세번째 exon 은 구성 아미노 산 105 번에서 146 번까지 지시하는 126 개의 영기쌍으로 되어 있다. @ int r on : exon 사이에 자리하고 있으며 전사는 되지만 아미노 산을 지시하지 않는 부위이다. f3-글로빈유전자에는 두 개의 int r o n 이 있는데, 첫번째 i n t ron 은 130 개의 염기쌍으로 이루어진 첫번째 exon 과 두번째 exon 사이에 자리하는 것이며, 두번째 i n t ron 은 두
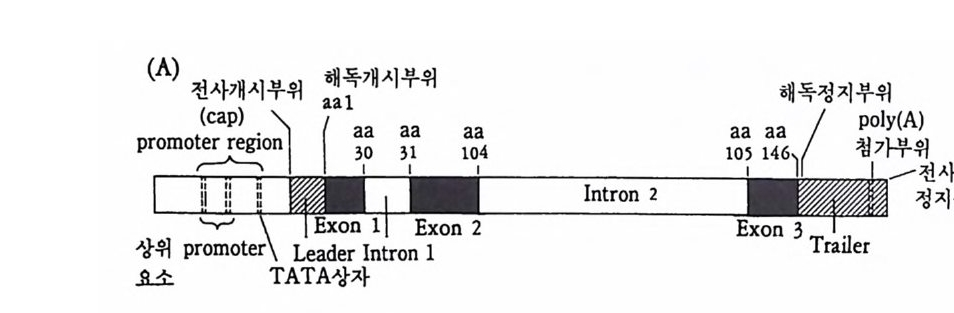 p(roA m) o전te 사r r개eg시i o부n 위I a(해 a독l! ~개 시:부f위 f0a’4 Intr o n 2 감I 나:해1독( 정 지부二I위 / ;전정 사지부 위
p(roA m) o전te 사r r개eg시i o부n 위I a(해 a독l! ~개 시:부f위 f0a’4 Intr o n 2 감I 나:해1독( 정 지부二I위 / ;전정 사지부 위
 (B) cccc g,gg三t a gggttg죤호 c t ac t ccca gg a g ca ggg a ggg ca gg a g cca ggg c tgg로호프]
(B) cccc g,gg三t a gggttg죤호 c t ac t ccca gg a g ca ggg a ggg ca gg a g cca ggg c tgg로호프]
그림 6-1 사람의 8- 글로빈유전자의 누클레오티드 배열순서. (A) p romo t er 부 위, 전사개시부위 (cap ), leader seq ue nce, exon, i n t ron 의 위치. exon 의 양쪽에 있는 숫자는 아미노산의 순서에 해당한다. (B) 누클레오티드의 배 열순서. pro mot er 부위 개시 및 정지코돈에 대한 누클레오티드 배열순서 (ATG, TAA) 는 모두 조그만 상자 속에 넣었다. 대문자는 exon 에 해당하 며, 그 위에 지시되는 아미노산을 약자로 표기하였다. 소문자는 i n tr on 에 해당한다. 대문자로 표기했으나 아미노산이 없는 부분은 전사는 되지만 해 독되지 않은 부위이댜 여기에는 p ol y aden y la ti on 에 필요한 hexanu- cleo ti de 가 있다. 첫번째 i n tr on 에 자리하고 있는 G( 화살표)가 A 로 돌연변 이되면 p+th alassem i a 를 일으킨다 (Lawn et al ., 1980).
번째 exon 과 세번째 exon 사이에 자리하는 850 개의 염기쌍에 해당 한다. ® 해독 정지 코돈 : 세번째 exon 의 3 ' 말단에 인접해 있는 TAA 로 되어 있다. (j) trai le r regi on : 세번째 exon 의 3' 말단에서 전사가 끝나는 것 이 아니고 비록 단백질로 해독되지는 않아도 전사되는 부위가 있 다. 이 염기 부위에는 특별히 AATAAA 가 있는데 RNA 로 전사된 후 200~300 개 정도의 아데노신 염기를 꼬리로 붙이는 데 필요한 부위이다. p ol y (A) 꼬리는 AAUAAA 부위에서 하위로 20 개 염기 떨 어진 부위의 RNA 에 삽입된다. 그러나 전사는 AATAAA 에서 끝 나지 않고 이 부위를 지난 다음에도 약 1000 개의 염기로 된 부위에 걸쳐 일어난다. 만약 AATAAA 부위에 돌연변이가 일어나면 전사 는 되 지 만 po ly ( A) 꼬리 는 첨 가되 지 않는다, trai l e r re gi on 에 는 성 체 적혈구세포에서의 /3 - 글로빈유전자 발현조절에 필요한 부위로서 AATAAA부 위로부터 600 내지 900 염기쌍에 해당하는 enhancer 가 있다 (Trudel and Consta n ti ni, 1 987) . 이러한 유전자가 전사되면 전사체인 nuclear RNA(nRNA) 는 cap 염 기 부위 , leader sequ e nce, exon, int r o n 및 3' 말단에 해 독되 지 않는 염기 부위로 이루어진다. 전사 후 양 말단에 변화가 일어나는데, RNA 의 5' 말단에 있는 ca~ 본 메철화된 gu anos i ne 이 RNA 염기의 결 합방향과는 반대방향으로 결합된다. 죽 모든 염기가 5' 에서 3' 으로 결합되는 반면에 ca p에서는 5 ' 에서 5 ' 으로 결합된다. 따라서 nRNA 에는 5' 인산기가 없다. messeng er RNA 에도 ca p이 있는데 이 ca p이 nRNA 의 것과 동일한 것인지는 확실치 않다. rnRNA 에서의 5'ca 硏본 rnRNA 가 리보솜에 안착할 때 필요한 것으로 이해되고 있다 (Sha t k i n, 1976) . 3' 말단은 약 200 개 정도의 아데노신 영기가 주로 핵내에서 첨가됨 으로써 변화된다 . 아들 아데노신 염기의 첨가는 유전자에 의해 조절
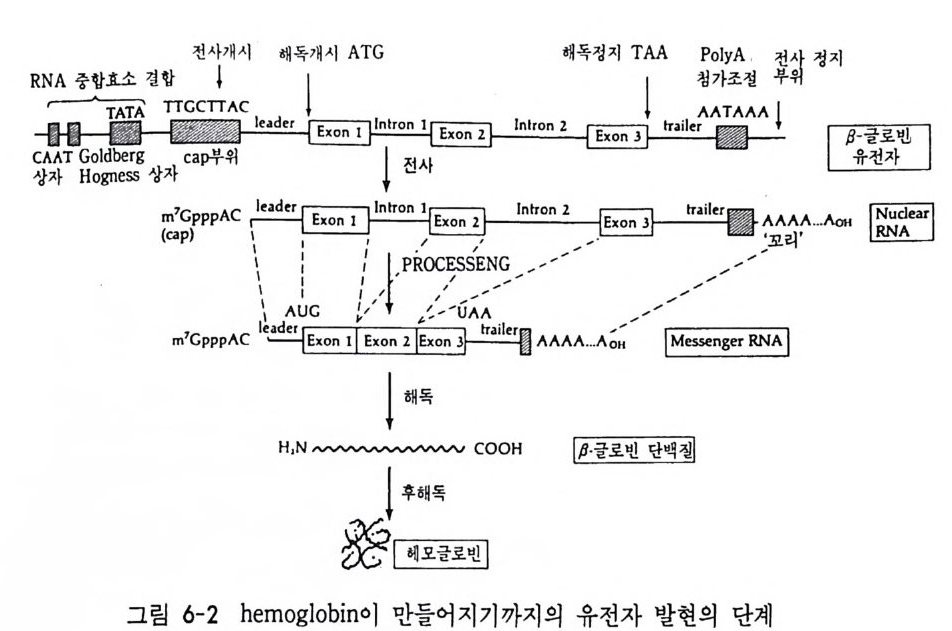 RNA 중합요소 경합TT C건CT사Tl개A 시C 해독I개 시 ATG 해독정지 TAA 첨APAo가lTy조AA 정A ‘ A 부전^J 정지
RNA 중합요소 경합TT C건CT사Tl개A 시C 해독I개 시 ATG 해독정지 TAA 첨APAo가lTy조AA 정A ‘ A 부전^J 정지
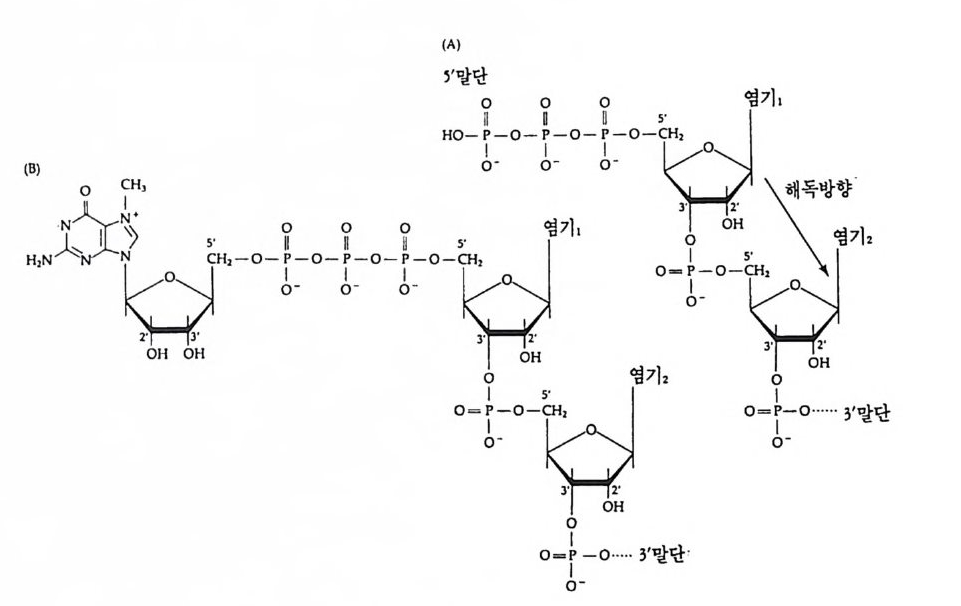 (A)
(A)
그림 6-3 진핵세포의 mRNA 5' 말단에서의 capp ing , (A) ca ppi n g전의 5' 말단, (B) 5'cap, 7-me thy l gu anos i ne 이 mRNA 의 5' 말단과 5'-5' 의 결합을 하고 있다. (Rott ma n et al., 1974)
되는 것이 아니고 전사 후 효소에 의해 성취된다. 이러한 RNA 의 5' 과 3' 말단에서의 변화 때문에 RNA 는 exonuclease 로부터 보호를 받 는 다 (Shein e ss and Darnell, 1 973 ; Gedamu and Dixo n, 1978) . 즉, pol y (A) 첨가로 인하여 mRNA 가 안정된다. 그러나 시간이 지나면 Poly (A) 꼬리는 점차 짧아지면서 안정성을 잃게 된다. 새로 합성된 글로 빈 m-RNA 의 pol y( A ) 꼬리는 처음에는 150 개의 아데노신으로 이루 어져 있으나 시간이 지남에 따라 100 개 , 60 개 혹은 40 개의 아데노신 으로 감소하는 경우도 찾아볼 수 있다 (Merkel et a l., 197 5 ; Nokin et al., 1976). p ol y (A) 꼬리가 결여된 글로빈 mRNA 를 X e no p u s 의 난모 세포에 주사해 주면 mRNA 는 쉽게 붕괴된다. 따라서 p ol y (A) 는 mRNA 를 안정시키는 역할을 하는 것으로 생각되고 있다. mRNA 는 핵 속에 갇혀 있는 한 그 기능을 발휘할 수 없다. 원핵 세포에서는 전사와 해독이 거의 동시에 일어날 정도로 밀접하게 연결 되어 있지만 진핵세포의 RNA 는 원핵세포의 것과는 달리 반드시 핵 밖으로 나와야만 그 기능을 발휘할 수 있다. 지난 수년 동안에 누적 된 연구결과에 의 하면 i n t ron 이 mRNA 를 핵 에서 세포질로 이동시 키 는 데 중요한 역할을 하는 것으로 생각되고 있다. mRNA 의 전구체 에 i n tr on 이 존재한다는 사실은 전자현미경으로 쉽게 확인될 수 있 다. 즉 B- 글로빈 mRNA 에 대 한 cDNA 를 준비 하여 핵의 RNA 전구 체에 결합시킨 후 전자현미경으로 확인해 보면 i n t ron 이 결합되지 못 하고 고리모양(l oo p)으로 밀려나오는 것을 관찰할 수 있는데, 이러한 i n t ron 은 mRNA 전구체가 핵을 탈출하는 데 필요한 것으로 생각되 고있다. 가장 직접적인 증거의 하나로서 글로반유전자를 바이러스에 삽입시 킨 후 i n t ron 의 유무에 따라 출현하는 굴로빈 mRNA 의 존재를 확인 하는 것이다. 우선 글로빈유전자를 삽입시킨 후 그 바이러스를 진핵 세포에 감염시키고 그 유전자로부터 전사된 RNA 를 관찰한다. 만약 바이러스의 유전자나 글로빈유전자에 i n tr on 이 존재하면 글로빈
mRNA 가 세포질에 출현하지만 i n t ron 이 어느 유전자에나 결여되어 있으면 글로빈 mRNA 는 전혀 생성되지 않는다. 또 다른 실험적 증거는 /3 + 탈라세미아(/3 + -t halassem i a) 질병에 관한
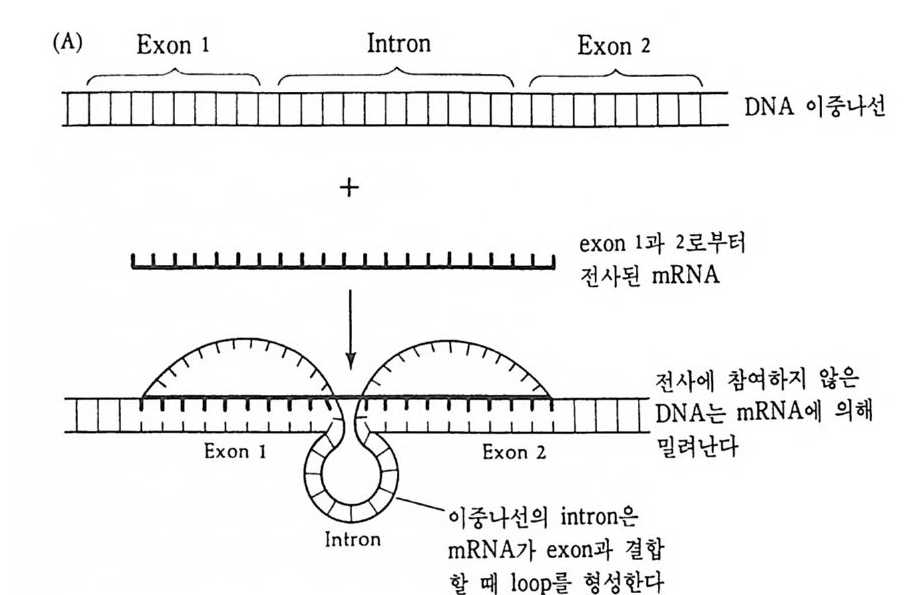 (A) Exon I Intr o n Exon 2
(A) Exon I Intr o n Exon 2
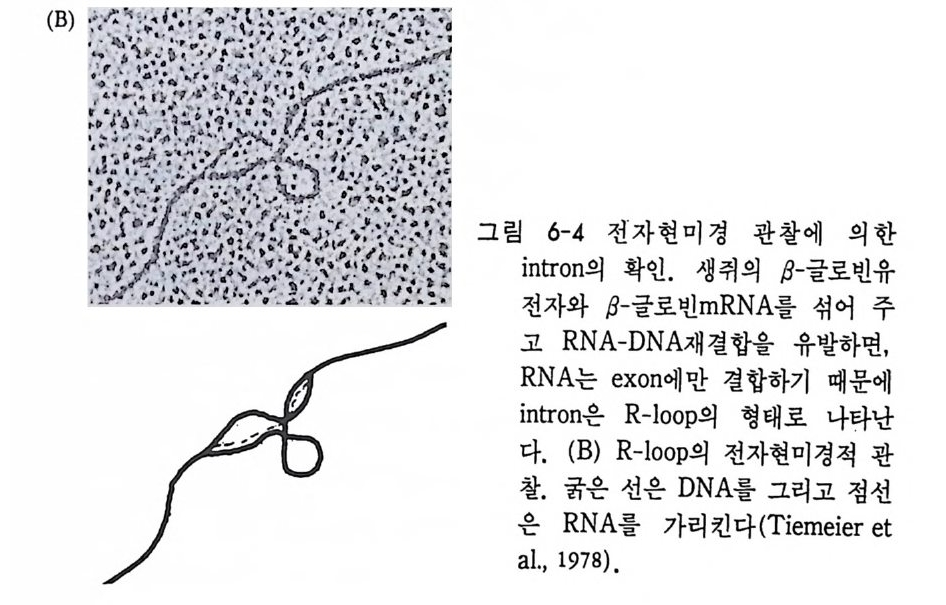 (B)
(B)
연구로부터 얻을 수 있는데, 이 질병을 앓는 환자에게는 8- 글로빈의 생성이 대단히 낮다. 이러한 이유는 환자에게 8- 글로빈유전자가 결 핍되어 있기 때문이 아니고 RNA p rocess i n g에 문제가 있는 것으로 알려졌다. 8+ 탈라세미아 환자의 8- 글로빈유전자는 정상적으로 전사 하며, 전사된 mRNA 는 정상적으로 해독될 수 있다. 그러나 문제는 g-글로빈 mRNA 가 양적으로 대단히 적다는 데 있다. 8- 글로빈 mRNA 의 양적 부족을 pul se-chase 실합을 통해 알아냈다 (Ma q ua t et al., 1980) . 즉 환자의 골수로부터 적 혈구를 분리 하여 12 분 동안 방 사 능 동 위 원 소 를 표 지 한 염 기 로 짧 게 표 지 (pu lse) 한 다 음, acti no my cin D 를 처리하여 전사를 중지시켰다. 그 후 시간 간격을 두고 세포로부터 RNA 를 추출하여 전기영동으로 분리시킨 다음 그 RNA 와 8- 글로빈 cDNA 를 결합시켰다. 정상인에서는 표지 직후 cDNA 와 결합하는 RNA 의 염기수가 1900 개이지만 얼마 후에는 1550, 1150, 960 및 880 염기로 염기수가 감소하였고 2~3 분 이내에 85% 의 RNA 가 mRNA 로 존재하는 것을 관찰할 수 있었다. 맑탈라 세미아 환자의 적혈구에서도 RNA의 중간형이 형성되기는 하지만 30 분이 지나도록 메시지 크기의 RNA 는 보이지 않는 점으로 보아 아마 도 중간형의 RNA 가 mRNA 로 성숙하지 못하여 세포질 속으로 나오 지 못하고 핵 속에 그대로 남아 있는 것으로 생각되었다 (Ma q ua t e t al., 1980_; K anto r et a l., 1980}. 따라서 8+ -탈라세 미 아는 8 곱굴로빈 mRNA의 p rocess i n g에 결함이 있기 때문에 일어나는 질병으로 생각 되었다. 그러나 8- 글로빈유전자의 염기 배열 순서를 조사해 보면 첫 번째 i n t ron 에 돌연변이가 일어난 것을 알 수 있는데, 아마도 이 질 병은 돌연변이로 인하여 RNA p rocess i n g에 관여하는 i n t ron 의 기능 이 상실되었기 때문에 일어난 것으로 추측되고 있다.
* p luse-chase 실험 : 방사능 전구물질로 짧은 기간 동안 표지한 다음 표지 되지 않은 전구물질에 옮겨 놓음으로써 일단 표지된 방사능 전구물질을 추적하는 실험.
2 p romo t er 의 구조와 기능 (1 ) p romo t er 의 구조 유전자 발현 조절 요인에는 크게 나누어 ci s 조절요인과 t rans 조절 요인의 두 종류가 있다. 즉 c i s 조절요인은 인접 유전자에 작용하여 유전자 발현을 조절하는 특정 DNA 부위에 해당한다. t rans 조절요인 은 DNA 로부터 만들어졌으나 염색체에 작용하여 유전자 발현을 조철 한다고 생 각되 는 RNA 와 단백 질과 같은 요인 이 다. E. col i의 lac o p eron 에 의한 선택적 유전자 발현 유도과정에서 억제단백질이 t rans 조절요인에 해당하며 작동유전자는 c i s 조절요인에 해당한다. 진핵세포의 구조 유전 자 에는 두 가지 형태의 ci s 조절인자 즉 p romo t er 와 enhancer 가 있다. 진핵세포에서 p romo t er 는 전사 개시 부위 에서 상위 (up st re am) 에 자리 하는 약 100 개의 염 기쌍에 해 당한다. 구조 유전자의 p romo t er 는 RNA 중합효소 Il 가 결합되는 부위로서 정확한 전사 개시를 돕는디. enhancer 는 p romo t er 를 활성화시켜 전 사의 능률 및 속도를 조절한다. 그러나 enhancer 는 반드시 전사 개 시 부위의 상위에 자리하거나 혹은 동일한 DNA 사슬에 자리하지 않 을 지라도 그 역할을 수행할 수 있다 (Ma ni a ti s et a l., 1987). 비교적 다량의 mRNA 를 전사하는 p romo t er 들은 공통적인 부위를 가지고 있다. 한때는 TATA 상자나 Goldber g -Ro gn ess 상자로 알려졌 던 ATA 염기배열은 전사 개시 부위에서 상위로 30 염기쌍 떨어전 곳에 자리하고 있고, 그 위로 한 개 혹은 그 이상의 상위 pro mote r 가 있을 수 있다. 상위 p romo t er 는 CAAT 배열의 변이형태이지만 이 의 에 도 다른 종류의 상위 p romo t er 가 발견되 기 도 한다 (Gros. 5Che dl and Bir n stie l, 1950 ; McK nigh t a nd Tji an , 1986) . /3-글로빈유전자의 p romo t er 가 처음으로 분석되었다. 클로운된 유 전자를 양서류의 난모세포나 섬유아세포의 핵 속에 혹은 세포 상등액
에 누클레오티드와 RNA 중합효소와 함께 넣어 주면 이 유전자는 정 확하게 전사한다 (Was y l y k et al., 1980}. 이와 같이 이 유전자로부터 정확한 전사를 할 수 있다는 것이 확인되면, 제한효소를 사용하여 이 유전자의 특정 부위에 결손을 일으킨다. 그 다음 이러한 결손이 정확 한 전사에 어 떻게 영 향을 주는지 재 확인하고 분석 함으로써 pro mote r 의 위치와 영기수를 알아낼 수 있다. 즉 이러한 연구결과 /3-글로빈 유전자의 p romo t er 는 cap 부위에서 상위쪽으로 109 개의 염기쌍으로 이루어져 있다는 사실을 알게 되었다 .(Grosveld et al., 19s2 ; Dier ks et al., 1983} .
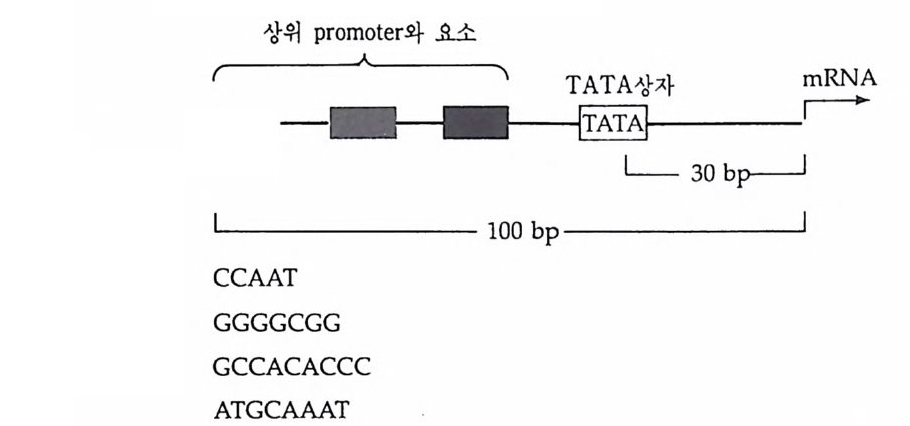 상위 p romo t er 와 요소
상위 p romo t er 와 요소
그림 6-5 진핵세포 유전자의 전형적인 pro mote r 부위. 여기에 TATA 상자와 세개의 p romo t er 요소가 포함된다 (Man i a ti s et al., 1987).
최근 마이어스 (M y ers, 1986) 등은 이러한 분석법을 좀더 다듬어서 생쥐의 글로빈유전자의 전사 개시 부위에서 상위에 자리하는 106 번째 영기쌍으로부터 475 번째 염기쌍에 이르는 첫번째 exon 을 분석하였 다. 우선 생쥐의 글로빈유전자를 클로운시킨 다음 이들 쿨로운된 유 전자에 시험관내에서 인위적으로 돌연변이룰 유발시켰다. 이러한 방 법으로 pro moto r 부위에만 130 개의 단일 염기치환을 일으킬 수 있었 다. 이와 갇이 처리된 유전자를 enhancer 를 포함하고 있는 풀라미드
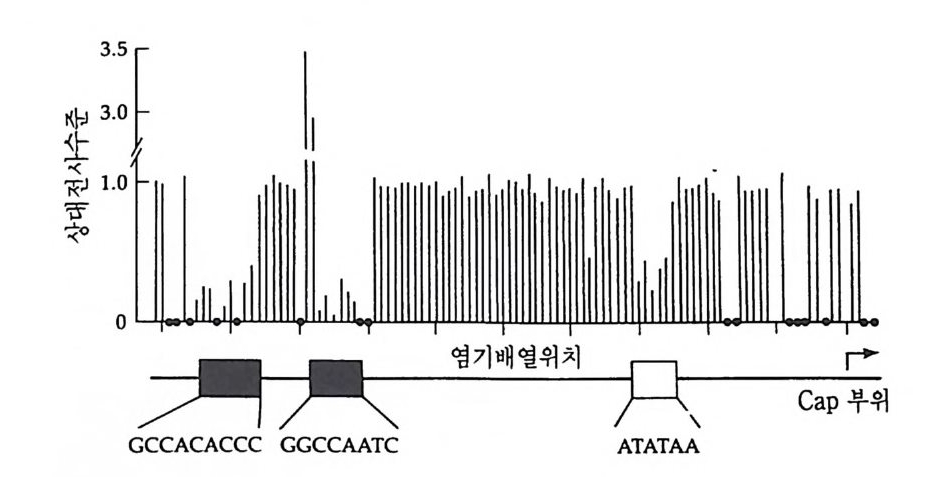 효-_JJ
효-_JJ
그림 6-6 생쥐 B- 글로빈 p romo t er 부위의 접돌연변아가 전사능력에 미치는 영 향. 수직선은 p romo t er 부위에 점돌연변이를 일으켰을 때의 정상에 대한 상 대적인 전사수준을 의미한다. 혹색접은 돌연변이가 발생하지 않은 누클레오 티드를 가르킨다. 아래에 있는 그립은 TATA 상자와 두 개의 p romo t er 요소 의 위치를 보여주고 있다 (Man i a ti s et a l., 1986).
에 삽입시켜 글로빈단백질을 합성하지 않는 세포에 넣어준 다음, 글 로빈 단백질이 그 세포에서 합성되는지의 여부를 검출하였다. 대부분 의 경우 5' 말단의 가장자리 부위에 돌연변이를 일으키면 이것은 글로 빈유전자의 전사에 영향을 주지 못했다. 그러나 세군데의 특별한 부 위에 점 돌연변이를 일으키면 전사가 크게 저해되는 것을 관찰할 수 있었다. 이와 같이 돌연변이에 예민한 반응을 보이는 부위 중 첫번째 것 은 Goldberg- R ogn e ss TATA 상자, 두번 째 것 은 CAAT 상위 pro mote r 그리고 세번째 것은 ca p부위에서 상위로 95 번과 87 번 사이 에 자리 하고 있는 GCCACACCC 이다. CAAT 와 TATA 상자는 여러 종류의 진핵세포 유전자의 pro mote r 에서 대단히 중요한 공통적인 염기서열로 알려져 있다 (E fs tr a ti a di s et al., 19so). 그러나 GCCACACCC 서열은 8- 글로빈유전자 의의 다른 유전자에서는 거의 찾아볼 수 없다. 사람에서 이 부위의 돌연변이로 인하여 8- 글로빈유전자의 전사가 전적으로 억제되는 경우도 찾아볼
 표 6-1 프로모우터의 공통적인 염기서열
표 6-1 프로모우터의 공통적인 염기서열
수 있는 반면 (Ork i n and Kazazia n , 1984), 전사개시부위에서 상위로 78 과 79 번째의 누클레오티드에 돌연변이가 일어나 오히려 전사가 촉 진되는 경우도 찾아볼 수 있다. 아마도 이러한 현상은 p romo t er 와 tran s 조절 단백질간의 상호작용이 촉진핀 데에서 바롯된 것으로 생 각되고 있다. (2) tran s 조절단백질과 p romo t er 의 결합 진핵세포에는 세 종류의 RNA 중합효소가 있는데, mRNA 를 전사
하는 데 필요한 효소는 RNA 중합효소 Il 이다. 그러나 RNA 중합효 소를 순수하게 추출하여 넣어주면 이 효소는 p romo t or 를 인식하지 못하기 때문에 전사 개시가 무작위적으로 일어날 뿐만 아니라 정확한 전사가 일어나지 않는다. 그러나 RNA 중합효소 n 와 핵 추출액을 함 께 넣어 주면 정확한 전사가 일어난다. 이러한 관찰로부터 RNA 중 합효소가 p romo t er 를 인식 하는 데 에는 효소와 pro mote r 이 의 에 핵 속에 있는 다른 요인이 있음을 알 수 있었다. 파커 (Parker) 와 토폴 (Topo l , 1984) 은 초파리의 핵으로부터 히스톤유전자와 액틴 유전자를 포함하는 여러 종류의 유전자 전사를 위해 필요한 조절요인 두 종류 룰 분리 하였다. 그 중 하나는 상위 p romo t er 와 결합하고, 다론 하나 는 TATA 상자와 결합한다. 지금까지 포유류에서 TATA 상자에 대 한 결 합 단 백 질 (David s on et a l., 1983 ; Shi et a l., 1986) , CAAT 상 위 p romo t er 에 대한 결합단백질, 특별히 GGGCGG p romo t or 에 대한 결합 단백질인 S p l 이 분리되었다 (Dyn anandTj i an, 1985;J on eset a l., 1987). 핵 속에는 이 의에도 DNA 와 직접 결합하지는 않을지라도 RNA 중합효소와 안정된 결합을 하는 단백질도 있다 (Zhen g e t a l., 1987). 이러한 tra ns 조절요인들은 모든 세포에서 특이성 없이 발견 되기 때문에 순차적 유전자 발현을 선택적으로 조절한다고는 할 수 없다. 그러나 이들 단백질들은 p romo t er 와 enhancer 사이에 개입되 어 특정된 유전자의 순차적 유전자 발현을 유발하는 것으로 생각되고 있다. 제한된 종류의 세포에서만 조직 특유의 유전자 발현에 관여하는 핵 단백질이 발견되었는데, 뇌하수체 전영세포에서 찾아볼 수 있는 GHF-1 이 그러한 예이다. GHF-1 은 사람의 성장 호르몬 유전자의 상위 p romo t er 에 결합한다. 이 유전자를 클로운하여 뇌하수체 이의 의 세포에 넣어 주면 이 유전자는 전사되지 않지만 뇌하수체 전영세 포에 넣어 주면 전사된다. 만약 GHF-1 를 뇌하수체 이의의 세포의 핵 추출액에 넣어 주면 성장호르몬 유전자는 전사될 수 있다 (Boder
an건 Ka ri n, 1987). 따라서 뇌하수체 전영에서 성장 호르몬 유전자가 선택적으로 발현되는 것은 조직 특유의 pro mote r 결합 단백질에 기 인하는 것으로 생각되고 있다. 3 enhancer 의 구조와 기 능 enhancer 는 pro mote r 이 외 의 또 다른 cis 조절 부위 라고 할 수 있
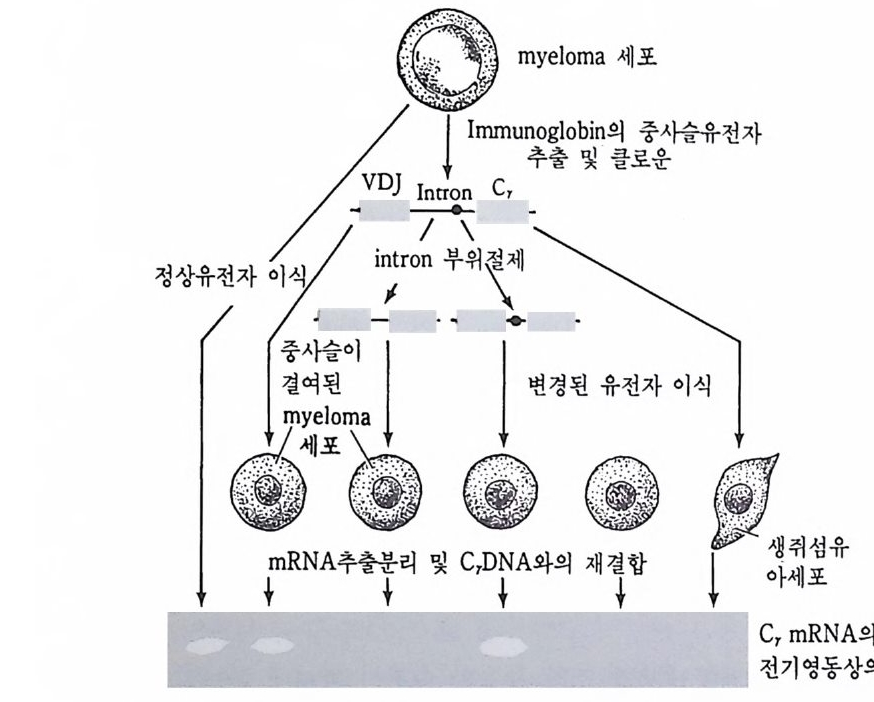 my el oma 세포
my el oma 세포
그림 6-7 enhancer 작용의 조직 특이성을 알아보기 위한 실험고안. m y eloma 세 포로부터 imm uno g lobul i n 의 중사슬유전자를 분리 하여 클로운시 킨 다음 VD J와 Cr exon 사이에 자리하고 있는 i n tr on 을 여러 종류의 제한효소로 절단하여 다시 imm uno g lobul in유전자를 상실한 my el oma 세포 내로 넣어 준다. 클로운된 DNA 부터 합성된 mRNA 를 전기영동으로 분리하여 nitroc ellulose p a pe r 에 blo t한 다음 제한효소를 절제한 Dr 부위를 재결합시 킨다. 이러한 실험 고안으로 Cr 메시지가 i n tr on 을 가지고 있는 DNA 에서 만 전사된다는 사실을 확인할 수 있다.
다. 처음에는 바이러스에서 발견됐으나 후에 진핵세포에서도 발견되 었다• 가장 먼저 알려진 enhancer 의 하나는 i mmuno g lobu li n 유전자 의 전사를 세포 특이적으로 조절하는 것이다. 길리스 (G illi es, 1983} 등은 쿨로운된 i mmuno g lobul i n 의 중사슬유전자를 중사슬 합성능력 을 상실한 /3-림프구 종양세포에 넣어 주면 이 m y eloma 세포는 중사 슬 합성능력을 회복한다. 그러나 만약 변아유전자와 고정유전자 사이 의 i n t ron 부위를 상실하게 되면 이 유전자의 전사는 거의 찾아볼 수 없게 된다. 즉 전사를 위해서 i n t ron 이 필요하다. 이 int r o n 속에 는 enhancer 가 존재 하는데 enhancer 에 의 해 조직 특유의 전사가 일어난다. i mmuno g lobu li n 유전자의 전사에는 반드시 enhancer 가 필요하고 class sw it ch i n g시 에 도 VD J부위 에 enhancer 가 그대로 남아 있다. 특히 enhancer 는 조직 특유의 전사와도 밀접한
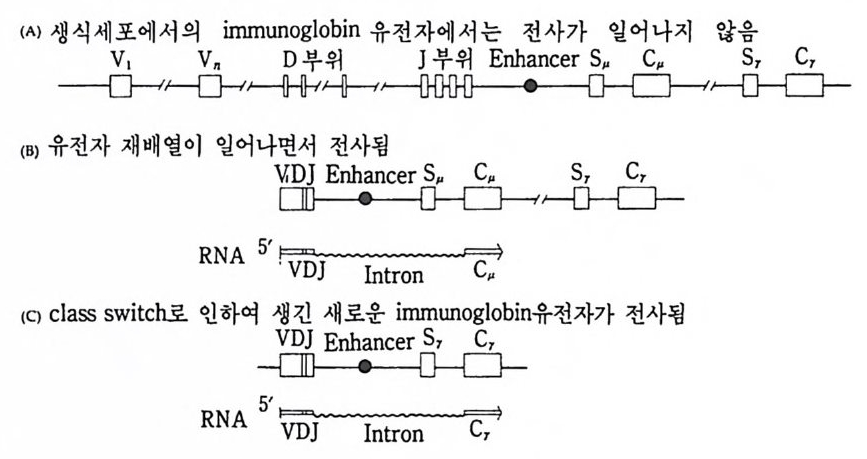 (A) 생식세포에서의 irnmu nog lo bin 유전자에서는 전사가 일어나지 않음
(A) 생식세포에서의 irnmu nog lo bin 유전자에서는 전사가 일어나지 않음
그림 6-8 im munog lo bulin e nhancer 활성도의 모형. (A) 재배열 되기 전의 i mmuno g lobu li n 중사슬유전자. enhancer 가 J부위와 Su(sw itch 부위) 사이에 자리하고 있다. 만약 enhancer 가 없어지면 전사활 동이 급격히 감소한다. p romo t er 는 V 부위에서 상위방향에 자리하는데 enhancer 로부터는 먼 거리에 있다. (B) 재배열된 후의 imm uno g lobul i n 중 사슬유전자와 유전자의 전사. (C) class sw it ch 를 일으킨 immu nog lo bulin 유전자. class s wit ch 가 일어나는 동안 VD] 가 Cr 와 접근할 때 enhancer 는 VD] 를 따라간다.
관계를 가지고 있는데 클로운된 i mmuno g lobul i n 유전자를 B- 림프구 의의 다른 세포에 넣어주면 전사가 일어나지 않는다. 더구나. i mmuno g lobul i n 중사슬유전자의 enhancer 를 /3 듭 글로빈유전자에 삽입 시켜 주면 글로빈유전자의 전사를 m y eloma 세포에 삽입`시켰을 때보 다 100 배 정도는 촉진시킬 수 있다. (1) 발생 단계 특이 enhancer 발생단계에 따라 혹은 세포의 종류에 따라 선택적 유전자 발현을 조절하는 enhancer 가 발견되었다. 발생단계에 따라 유전자 발현의 양상을 바꾸는 가장 좋은 예는 양서류 초기 발생과정에서 나타나는 포배 전이 (midb lastu l a tra nsiti on ) 이다. 크리그 (Kr i e g)와 멜론 (Mel t on, 1987) 은 포배기에 특이하게 enhancer 가 작용하는 유전자를 발견하였 다. 이들은 이와 같은 전이 과정에 활성화되는 유전자를 쿨로운하여 이들 유전자의 5' 쪽 처음 500 개의 염기쌍에 해당하는 부위를 Xenop us fJ-글로빈 유전자에 조합시 켰다. 8- 글로빈유전자는 비 록 Xenop us 의 수정란에 주입되었다고 할지라도 발생 후기까지는 보통 전사되지 않는다. 그러나 포배 전이 시기에 활성화된 유전자에 단계 득이 enhancer 가 들어 있다면 주입 된 재조합 유전자로부터 글로빈 단 백질 합성을 기대해 볼 수 있다. North e rn blot 분석법으로 검출해 본 결과 기대했던 바와 갇이 재조합 유전자로부터 B- 글로빈유전자의 발현을 확인할 수 있었다. 포배기까지는 글로빈유전자는 전사되지 않 았다. 그러나 포배기부터 새로운 글로빈 mRNA 가 검출되기 시작하 였다. 포배 특이 유전자에 대한 결손실험을 수행해 본 결과 이 유전 자의 enhancer 는 p romo t er 에서 상류로 700 번째 염 기 쌍이 되는 부위 에 94 개의 염기쌍 배열으로 이루어져 있다. 사람의 8- 글로빈유전자 에서는 단계 특이 enhancer 가 p ol y (A) 부위에서 하위로 600 번과 900 번의 염기쌍 사이에 자리하고 있다. 만약 이러한 enhancer 부위를
사람의 r- 글로빈유전자에 삽입시키면, 8- 글로빈이 정상적으로 발현 하는 시기에 태아의 r - 글로빈유전자도 발현된다 (Trudel and Con- sta n ti ni, 1987) . (2) 조직 특이 enhancer 조직 특이 enhancer 로 발견된 가장 좋은 예는 i mmuno g lobul i n 중 사슬 유 전 자 의 enhancer 이 다. 췌 장 에 서 chym o tr yps in , amy la se, t r yp s i n 과 같은 의분비 세포의 단백 질 유전자는 내분비세포의 단백 질 인 i nsul i n 유전자의 것과는 다른 enhancer 를 가지고 있다. 이들 두 종류의 enhancer 는 모두 유전자의 5 ' 쪽 측면 부위 (flan kin g regi on ) 에 자리하고 있다. 워커 (Walker, 1983) 등은 포유류의 세포에서는 찾 아볼 수 없는 박테 리 아의 chloramp he nic o l acety lt ra nsfe r ase (CAT) 의 유전자에 ch ym o tryp s i n 과 ins ulin 유전자의 측면 부위를 조합시켜 난소 세포, 내분비 세포 및 의분비 세포에 각각 주입시킨 다음, 표시 효소인 CAT 의 활성도를 각각의 세포에서 측정 함으로써 enhancer 의 조직 특이 성 에 대 하여 알아보았다. i nsu li n 유전자나 ch ym o tryp s i n 유 전자의 인접 부위에 조합된 CAT 유전자를 각각 난소세포에 주입시켰 을 경 우 i nsul i n 유전자와 ch ym o tryp s i n 유전자의 enhancer 는 작용하 지 않았다. 그러나 내분비세포에서는 i nsul i n 유전자의 인접 부위가 CAT 유전자를 발현시킨 반면에 ch ym o tryp s i n 유전자의 인접부위는 CAT 유전자를 발현시키지 못했다. 반대로 의분비 세포에서는 ch ym o tryp s i n 유전자의 인접 부위가 CAT 유전자를 발현시키는 반면 에 i nsu li n 분바 유전자의 인접 부위는 CAT 유전자를 발현시키지 못했 다. 이러한 점으로 보아 췌장의 내분비 세포와 의분비 세포의 유전자 발현은 서로 다른 enhancer 에 의해서 조절되는 것으로 생각되었다. 동일한 단백질의 합성이 한 종류 이상의 세포에서 일어나는 경우를 초파리의 난황 단백질에서 찾아볼 수 있다. 난황 단백질의 유전자로
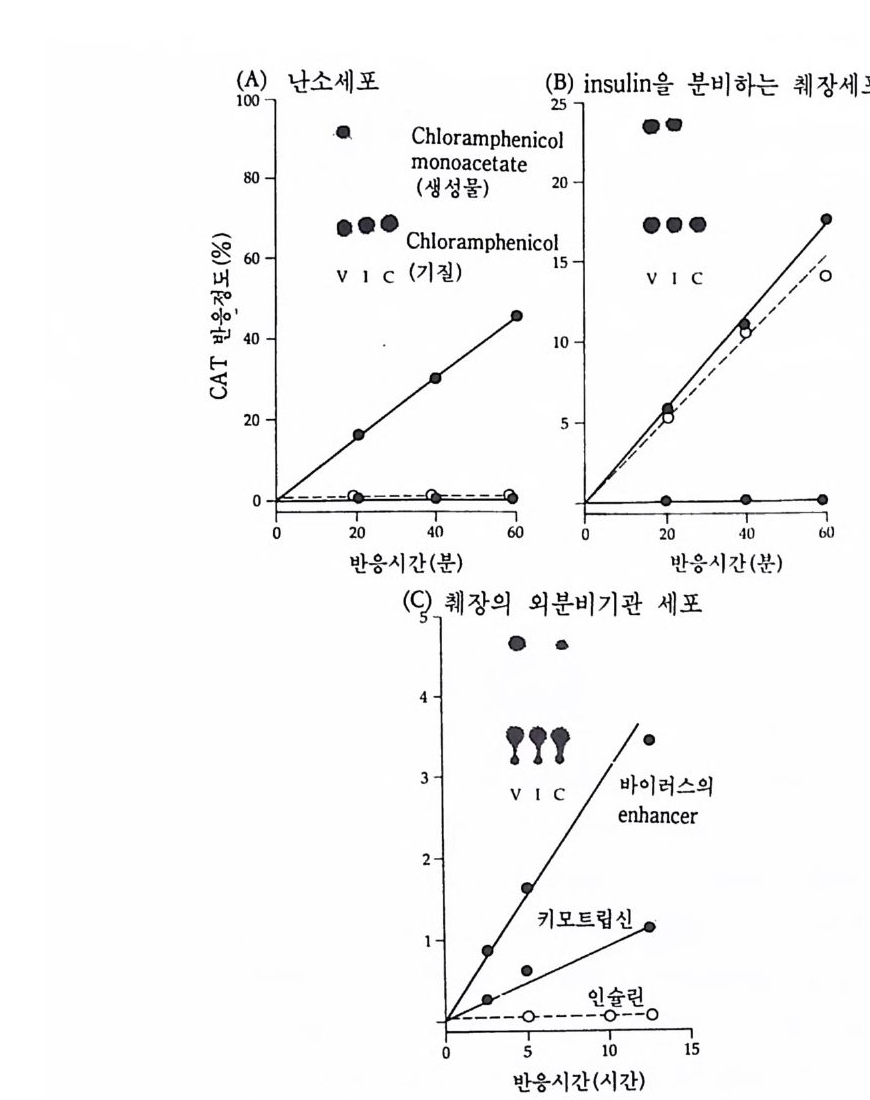 ~토:`버JQ~ ,(J O46A8O0 00 ) 난소세.•V ` 포 •I • C C(mC(h기ho생l질lono성)rora물 aammc)ep pt hah ete nen i ci c o(o. 22l1 1B l5500 ) 7 i nsul i n•• v을 •• /• 분/ c/ 비 /. / /하 는// ~/췌 / / 장 /O 세 포
~토:`버JQ~ ,(J O46A8O0 00 ) 난소세.•V ` 포 •I • C C(mC(h기ho생l질lono성)rora물 aammc)ep pt hah ete nen i ci c o(o. 22l1 1B l5500 ) 7 i nsul i n•• v을 •• /• 분/ c/ 비 /. / /하 는// ~/췌 / / 장 /O 세 포
그림 6-9 췌장유전자의 enhancer 의 조직 득이성. 인슐린유전자 (I) 와 키모트립 신유전자 (C) 의 5' 말단 부위를 . 개별적으로 박테리아의 chloramp h enic o l ace ty l tr ans fe rase(CAT) 에 삽입시킨다. 또한 대조군으로서 Rous Sarcoma vi rus(V) 의 enhancer 를 CAT 유전자 옆에 삽입시킨다. 그 다음 이들 세 종 류의 클로운을 세 종류의 세포에 넣어주고 CAT 활성도를 측정한다. 그림 속에 삽입한 조그만 사진은 방사능 동위원소로 표지된 chloram phe ni col 을 기질로 사용하였을 때 생성물로 나타나는 chloramp he n ico l monoace t a t e 를 크로마토그래피로 분리하여 자기방사법으로 확인한 사진이다 (Walker et al., 1983} .
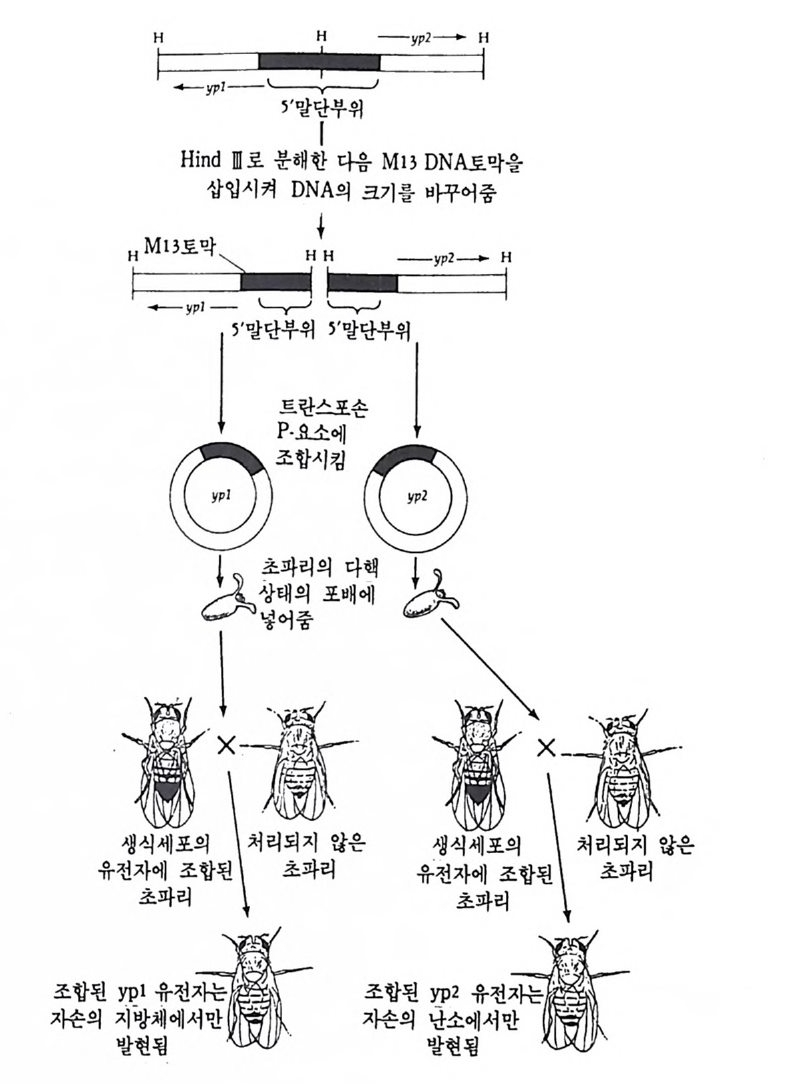 H - yp1 -'-- -H,— — J― y p 2 一 H
H - yp1 -'-- -H,— — J― y p 2 一 H
그립 6-10 난황단백질 유전자 전사의 조직특이성을 조절하는 두 종류의 enhancer 를 확인하는 실험고안. Hi ndlll 와 같은 제한효소를 이용하여 난황 단백질 유전자와 5 ' 부위의 요소들을 분리시킨 다음 (H i n d ll[로 분해된 부위 를 H 로 표시 함) tran spo son p - 요소에 조합시 켜 다핵 상태의 포배 (syn c yt ial blas t oderm) 에 넣어주면 초파리는 p-요소를 생식세포의 유전자에 흡수한 다. 이와 갇이 처리한 초파리를 처리하지 않은 초파리와 교배시키고, 자손 의 눈 색깔을 확인함으로써 p-요소를 받은 자손을 확인할 수 있다. 그리고 각 기관에서 yp l 과 yp 2 의 전사체의 존재여부를 조사할 수 있다.
는 YP1 과 YP 려 두 종류가 있는데 난소와 지방체에서 이들 유전자는 서로 인접해 있으면서 반대 방향으로 전사된다. YP1 과 YP2 유전자를 제 한효소를 이 용하여 분리 시 킨 다음, tra nspo sable P-element vect or 에 클로운시켜 초파리 난자의 유전자에 삽입시켰다. 또한 클로운시키 기 전에 pla smi nd DNA 를 yp유전자에 삽입시켜 이들 유전자의 생성 물을 내인성 유전자의 생성물과 구별하였다. 이들 유전자는 물론 암 컷에서만 단계 특이적으로 발현되었지만. YP2 mRNA 는 난소에서만 그리고 YP1 mRNA 는 지방체에서만 합성되었다. 이것은 난황 단백질 유전자가 5' 말단에 두 개의 enhancer 를 가지고 있으면서 하나는 난소 에서 그리고 다른 하나는 지방체에서 전사과정을 조절하는 것으로 생 각되었다. YP1 유전자의 지방체 특이 enhancer 는 ca p부위에서 상위로 196 번과 321 번의 염기쌍 사이에 자리하는 것으로 밝혀졌다. 이러한 사실은 5' 측면 부위의 DNA 토막을 여 러 가지 크기로 만들어 E. col i의
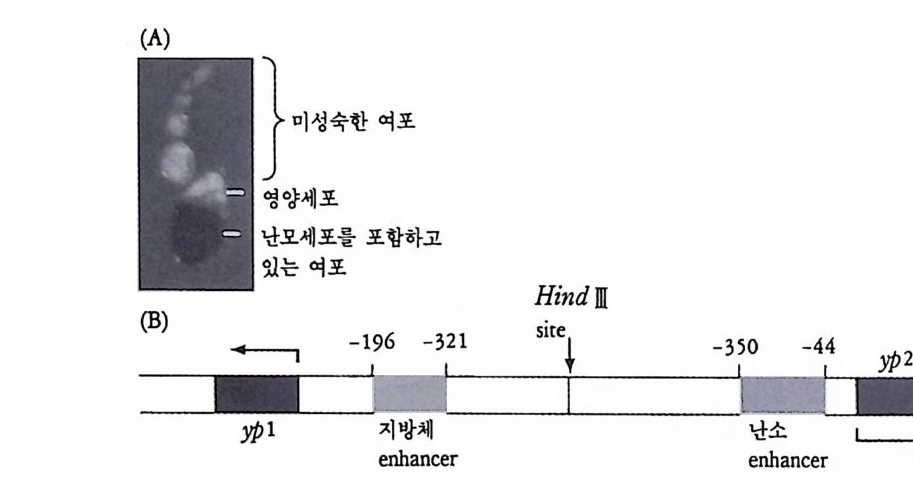 (A)
(A)
그립 6-11 난황단백 질유전자의 enhancer 의 위 치 . (A) 초파리 난소에서의 ’ 박테리아의 {3-g alac t os i dase 유전자의 발현. 이 발 현은 yp 2 유전자의 상위 - 44 에서 -350 에 이르는 부위에 enhancer 를 삽입시켰 울 때 일어난다. (B) 초파리 난황단백질 유전자의 enhancer 에 대한 요약.
f]-g alac t os i dase 유전자에 조합해 줌으로써 알아낼 수 있었다. 이러한 유전자의 5’ 측면 부위 를 E. col i의 f]-g alac t os i dase 유전자에 조합시 켜 , P-elemen t에 쿨로운시 킨 다음 발생 배 에 삽입 시 켜 주었다. 이 때 P-elemen t를 받아들인 발생배에서 생긴 개체는 f]-g alac t os i dase 에 대하여 양성 반응을 보인다 (Garabed i an et al., 1986). 그러나 5 ' 인접 부위가 없는 DNA 토막을 조합시켜 주었을 경우에는 f]-ga lacto s id a se 는 지방체나 난소에서 관찰되지 않았다. 그러나 YP1 의 5’ 인접 부위 전체를 첨가하면 지방체에서는 f]-g alac t os i dase 가 합성되지만, 난소 에서는 합성되지 않는다. 이렇게 특이한 전사는 상위 321 과 196 사이 의 DNA 토막이 사용되었을 때에만 나타난다. 이와 같은 결과를 종 합해 볼 때 지방체 특이 전사는 상위 196 과 321 사이의 125 개의 영기 쌍에 의해서 조절되는 것으로 보이며, 난소 특이 전사는 YP2 유전자로 부터 상위로 44~350 염기쌍에 자리하고 있는 enhancer 에 의해서 조 절되는 것으로 보였다. (3) 호르몬 득이 enhancer 발생과정에서 대부분의 경우 유전자 발현 조절이 협동적으로 나타 난다. 협동적 유전자 발현 조절이란, 같은 시기에 한 종류의 세포에 서 여러 개의 세포 특이 단백질에 대한 유전자 발현의 유발이나 혹은 한 종류의 호르몬에 의해 여러 종류의 세포에서 여러 종류의 유전자 발현의 유발을 의미한다. 이러한 협동적 유전자 발현 조절은 여러 개 의 다른 구조 유전자들이 같거나 혹은 여러 종류의 유전자가 유사한 enhancer 에 연계되어 있을 때에만 가능하다. 췌장에서 10 종류의 의 분비 단백질에 대한 유전자의 enhancer 가 20 개의 염기로 된 consensus se q uence 를 공유하고 있음을 볼 수 있는데 , 유사한 영 기 배열이 아마도 의분비세포의 유전자를 활성화시키는 데 작용하는 것 으로 생각되고 있다.
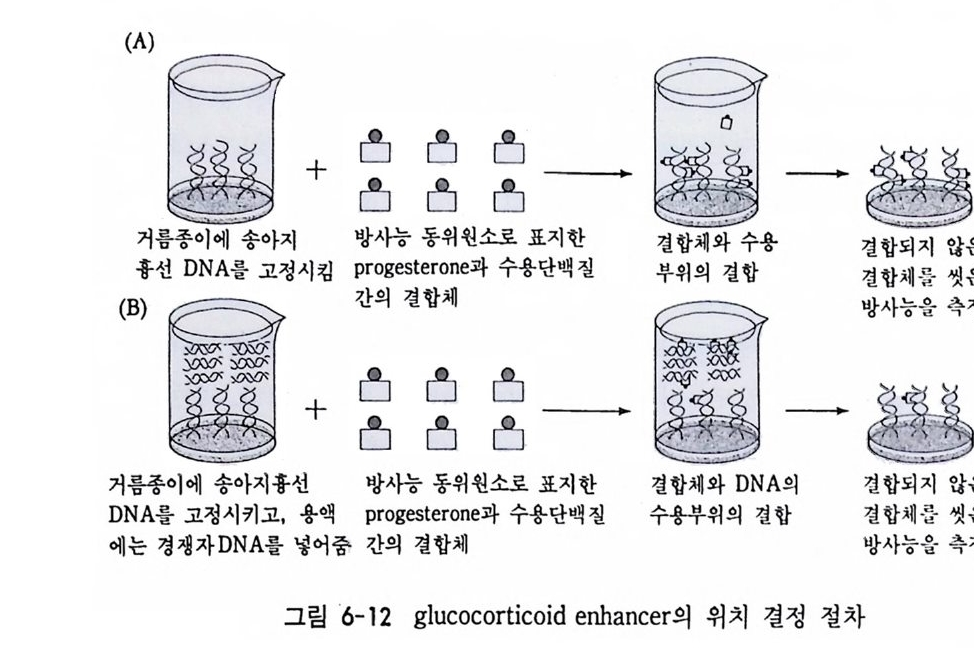 거側름( 서거 종름이선 言에 송雪尸아지흉 정 지선A+ 벼+ p방!먼 r방 사qo g사 능 e]능sq t e동 혼만r]동o위q n위 원e 원과q소 소만혼로수]로만만 용 표단표지백지한 한질 J’ 결합체鬪와二尸 DNA 의 一 一 결 합되지二二皇 않은 후
거側름( 서거 종름이선 言에 송雪尸아지흉 정 지선A+ 벼+ p방!먼 r방 사qo g사 능 e]능sq t e동 혼만r]동o위q n위 원e 원과q소 소만혼로수]로만만 용 표단표지백지한 한질 J’ 결합체鬪와二尸 DNA 의 一 一 결 합되지二二皇 않은 후
스테로이드 계통의 호르몬들은 유전자 발현을 촉진시키는 것으로 알려져 있다. 스테로이드 계통의 호르몬이 세포내로 들어오면 단백질 성 수용분자와 결합하여 핵 속으로 들어가 특정 부위의 DNA 와 결합 한다 (M i es fe ld et a l., 1986). 이러한 스데로이드 호르몬의 한 예는 gl ucoco rtic o idj쵸르몬인데, cort iso ne, h y drocor ti sone 과 일종의 합성 호 르 몬 인 dexameth a sone 이 glu cocortic o id 호 르 몬 에 속 한 다. g lucoco rti co icti.E..몬은 주로 단백 질 대 사를 조절하는 호르몬으로 모 든 세포에서 작용한다. me t allo thi onen 유전자와 바이러스 종양 유전 자를 포함하는 수종의 유전자는 g lucoco rti co id:호르몬에 의해 활성화 된다. 이러한 점으로 보아 호르몬 수용에 대한 DNA 의 결합부위가 이들 유전자 가까이 자리하고 있는 것으로 생각되고 있다. g lucoco rtic o i d 에 의 해 활성 화되 는 유전자의 enhancer 를 결정 하는 방 법으로 경쟁 결합법이 있다. 먼저 송아지 흉선 DNA 를 cellulose filt er 에 고정시킨 다음 방사능 동위원소로 표지된 g lucoco rti co i d 와
수용 단백질의 복합체를 넣어 준다. 이 복합체를 DNA 에 결합시키고 결합된 g lucoco rti co i d 의 방사능을 측정 한다. 그 다음 다른 종류의 DNA 를 과잉으로 넣어준 상태에서 DNA 에 결합된 복합체의 양을 측 정 한다. 만약 경 쟁 DNA 가 glu cocort ico id 수용분자 복합체 의 결합
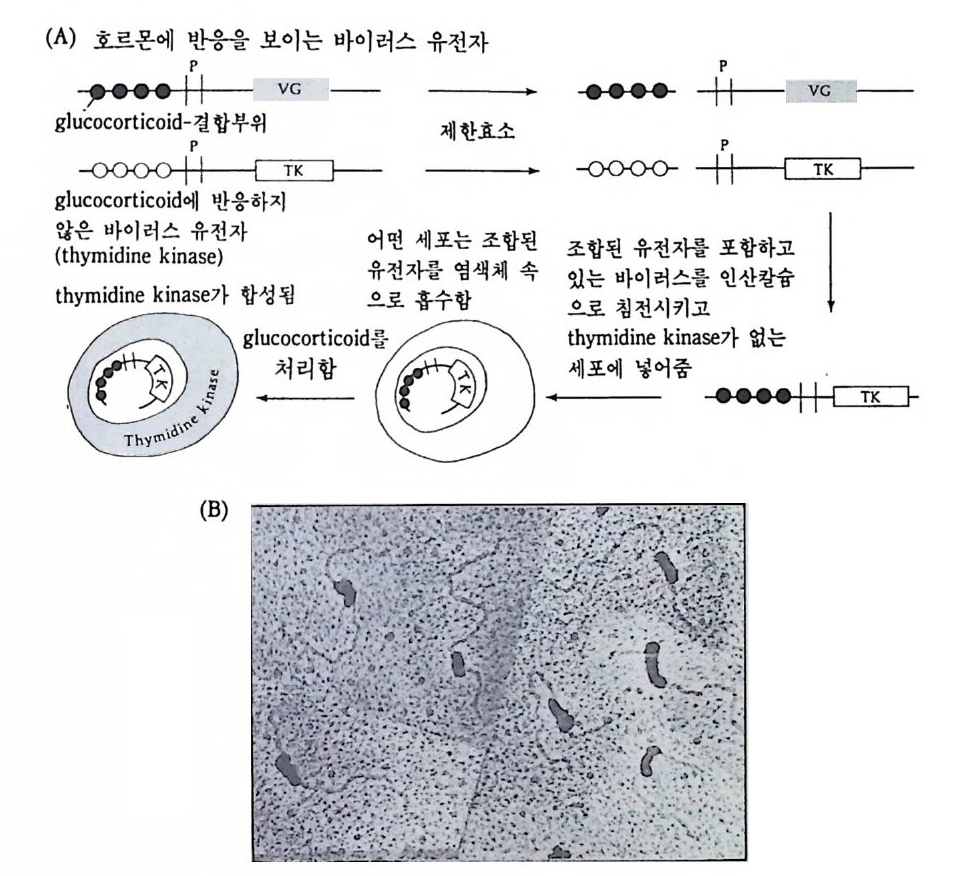 (Ag l) uc호oc르or t몬ic에 o i d -I반pp 결I 응 합 을부 위보 V이G 는 바이러스 유제전한자효 소 •••• -HpP -VC _
(Ag l) uc호oc르or t몬ic에 o i d -I반pp 결I 응 합 을부 위보 V이G 는 바이러스 유제전한자효 소 •••• -HpP -VC _
그립 6-13 glu cocort ico id enhancer 의 확인 절차. (A) 생 쥐 의 유방 종양 바이 러 스의 glu cocort ico id enhancer 와 Herp e s simp lex 바이러스의 thymidine k in as 러누전자를 조합시켜 thymidine kin as e 유전자가 결핍한 세포에 넣어준 다음, g lucoco rti co i d 를 처리하여 재조합된 유전자에서 바이러스의 thymidine k in ase 가 합성되는지 여부를 조사한다. (B) glu cocort ico id 수용체와 유전자의 결합을 보여주는 glu cocort ico id enhancer 의 전자현미경사진(A. Chandler, 1983 ; B. Payv e r et al., 1983).
부위와 동일한 결합 부위를 가졌다면 경쟁 DNA 와 cellulose fi l t er 에 고정시킨 흉선 DNA 에는 방사능 동위원소로 표지한 복합체와 결합하 는 데 경쟁적이다(pfa hl, 19s2). 제한효소를 처리하여 얻은 여러 가지 DNA 토막을 이용하여 연구해 본 결과 glu cocortic o id enhancer 는 공 통적으로 TGGTACAAATGTTCT 를 가지고 있음을 알 수 있었다 (Karin e t a l., 1984} . 이 러 한 glu cocortic o id 결 합부위 의 염 기 서 열을 보 통 호르몬에 의존하지 않은 유전자에 결합시킴으로써 이러한 결합부 위의 염기서열아 enhancer 로 작용한다는 점을 알 수 있었다 (Chandler et a !., 1983} , 스데로이드 계통 호르몬에 대한 특이 enhancer 둘은 굉 장히 비슷하 기 때문에 밀접한 관계를 가지고 있는 단백질에 의해서 인식될 수 있 다. 이러한 스데로이드 계통 호르몬의 수용 단백질에는 두 개의 기능 적인 영역 즉, 호르몬에 대한 결합 영역과 enhancer DNA 에 대한 결합 영역이 있다. 이 때 첫번째 영역과 호르몬 사이의 결합은 두번 째 영역이 특이 DNA 부위와 결합하는 데 필수적이다 (Kumar et al., 1986, 1987}. 이들 단백질의 DNA 결합 영역이 대단히 유사하지만 DNA 염기서열의 작은 변화에도 민감한 반응을 보일 정도로 그 차이 를 구별한다. 예를 들면 5'-GGTCACTGTGACC - 3' 은 에스테로겐에 강하게 반응하는 enhancer 로서 에스테로겐과 수용 단백질의 결합체 룰 쉽게 결합시킨다. 그런데 이러한 염기서열에 상칭적으로 돌연변이 가 일어나서, enhancer 의 염기서 열이 5'-GG@CACTGTG d) CC-3' 이 되면 이 염기서열은 g lucoco rtic o i d 에 민감한 enhancer 로 바뀐다 (Mart ine z et a l., 1987 ; Klock et a l., 1987} . (4) Immuno g lobul in경 사슬유전자의 전사 유전자 발현의 조절에 대하여 가장 잘 연구된 경우는 생쥐의 i rnrnuno g lobul i n 유전자에 대 한 것 이 다. 이 연구에서 8- 세포 특이 전
사에 필요한 c i s- 와 t rans - 조절요인이 확인되었다. 클로운된 유전자를 국부적으로 결손시켜 염기 서열을 알아본 결과 i mmuno g lobul i n 경 사슬의 p romo t er 에는 두 개 의 중요한 부위 즉 TATA 상자와 Oc t a 상자 라고 하는 상위 p romo t er 가 있음을 알 수 있었다. (Bergm a n et a l., 1984 ; Parslow et a l., 1984) . ATTTGCAT 의 8 개의 염기 서열때문에 oc t a 상자라고 불리는 이 특별한 염기서열은 모 든 i mmuno g lobul i n 유전자의 경사슬의 p romo t er 에서 발견되었다. i mmuno g lobul i n 유전자의 중사슬 p romo t er 는 oc t a 상자가 거꾸로 뒤 집힌 염기서열 즉 ATGCAAAT 를 가지고 있다. oc t a 상자의 위치를 글로빈유전자의 상위 로 옮기 면 글로빈유전자의 전사는 11 ~ 18 개 가량 증가한다. 이러한 증가는 림프 세포에서만 관찰되었고 섬유아세포에 서는 관찰되지 않았다 (W irth et a l., 1987). i mmuno g lobul i n 유전자의 경사슬의 enhancer 염기서열은 V J배열순 서와 고정 부위 사이에 있는 첫번째 i n t ron 내에 자리하고 있다(Q ueen and Baltim ore, 1983 ; Bergm a n et a l., 1984). 이러한 enhancer 의 염기서 열을 클로운된 글로빈유전자로 옮기면 글로빈유전자 전사는 특별히 림프구에서만 일어난다 (P i card and Schaff ne r, 1984). 만약에 유전자 재배열중에 enhancer 와 p romo t er 의 위치를 근접시 키면 전사 속도가 크게 증가하는 것을 관찰할 수 있다. 림프구에서 유전자 재배열이 일어나는 동안 enhancer 와 p romo t or 가 근접하는 데, 만약 경사슬의 유전자의 재배열중에 enhancer 와 p rorno t or 의 근 접이 일어나면, 경사슬의 핵내 전사체 양이 재배열이 일어나지 않은 사슬에 비해 16,000 배나 증가한다 (Ma ther ~d Perr y, 1982). 더구나 i rnmunog lobul i n 유전자의 경사슬 enhancer 는 SV4o 바이러스 유전자 나 rne t allo t h i one i n 유전자의 p romo t er 를 촉진하는 것에 비해 자기 자신의 p romo t er 를 20 배나 더 효율적으로 촉진시킨다. 이러한 현상 은 enhancer 와 pro mote r 사이 에 일종의 특이 한 상승작용이 있는 것 으로 보인다 (Gar ci a et a l., 1986). 재배열된 i mmuno g lobul i n 유전자는
 생쥐의 경사슬유전자 广oc t a 상자 ATG 로부터거의리
생쥐의 경사슬유전자 广oc t a 상자 ATG 로부터거의리
그림 6-14 imm unog lobul i n 유전자의 p romo t er 에 있는 oc ta상자 (Parslow et al., 1984}.
섬유아세포나 간세포에 넣어주면 활발하게 전사하지 않는 것으로 보 아 재배열 그 자체가 유전자 활성화에 충분한 조건은 아닌 것으로 생 각된다. 이러한 상승작용을 위해서는 반드시 세포 특이 tra ns 조절요 인이 있어야 할 것으로 예상된다. 1986 년 슈타우트 (S t aud t) 등에 의해서 두 종류의 pro mote r 결합요 인이 발견되었다. 슈타우트 등은 oc t a 상자를 포함하고 있는 조그만
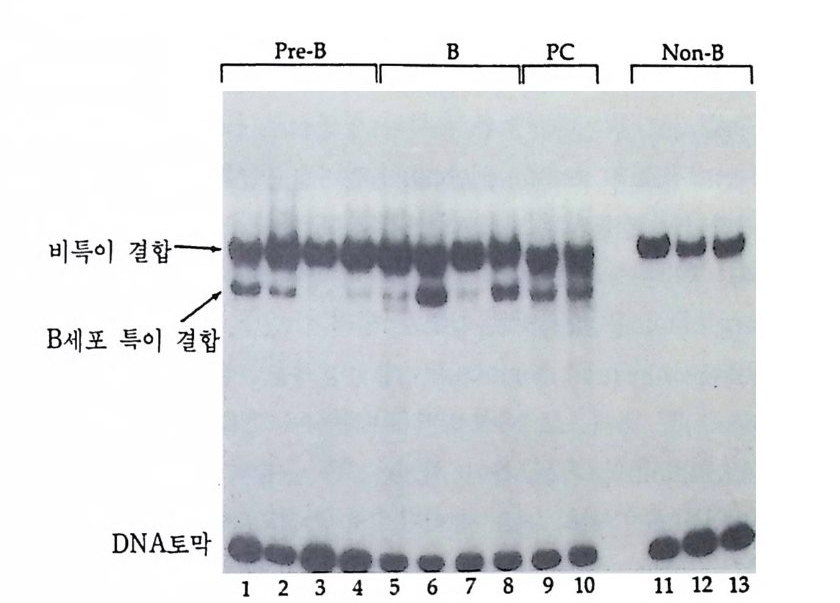 I Pre-B I B PC I Non-B I
I Pre-B I B PC I Non-B I
그립 6-15 electr o p ho retic mobil it y shi ft assay. B- 세포계통의 세포(p re-B, B, 및 혈장세포)와 비 B- 세포계통의 세포(기관지 경부세포, 섬유아세포, 적혈 구 전구세포)의 핵추출물을 8 량체 (oc t amer) 를 포함하고 있는 DNA 토막과 섞어주고 i ncuba t e 시킨 다음, 전기영동으로 분리하여, nitroc ellulose pap e r 에 blo t시켜 8 량체에 대한 상보적인 DNA( 방사능동위원소로 포지함)로 재 결합시켜 electr o p h oreti c mobil it y shift를 알아 보았다. 8 량체와 결합하지 않을 경우 DNA 토막은 빠른 속도로 이동한다. 비 B 세포계통의 세포의 핵 속에는 8 량체와 비 특이적으로 결합하는 단백질이 있기 때문에 이동속도가 저해된다. 그러나 B 세포계동의 세포의 핵 속에는 8 량체와 특이적으로 결합 하는 단백질이 있기 때문에 비특이적 결합체와는 다른 이동속도를 보인다 (St au dt et al., 1986) .
DNA 토막을 여러 종류의 세포에서 얻은 핵 추출액에 넣어 DNA 와 결합 단백질이 작용하도록 한 다음 그 생성물을 전기영동법으로 분석 하였다. 만약 핵 추출액 속에 DNA 에 결합할 수 있는 단백질이 없으 면 작은 DNA 토막은 대단히 빠른 속도로 겔을 이동해 간다. 그러나 DNA 에 단백질이 결합하면 이동 속도는 감소된다. 이러한 겔 상의 이동 속도를 분석함으로써 모든 핵 속에는 DNA 토막과 결합할 수 있 는 요인이 최소한도 한 종류 있음을 알아내었다. 그러나 B 세포 계보 에서는 oc t a 상자에 결합할 수 있는 또 하나의 요인이 발견되었다. 이 러한 단백질을 순수분리하여 확인하였는데, 특히 림프구 특이 단백질 을 NF-A2 라고 부른다. 또한 유사한 방법으로 B 세포 계보에만 제한 된 핵 단백질로서 i mmuno g lobul i n 유전자경사슬의 enhancer 에 결합 하는 단백질이 발견되었는데, NF-kB 라고 한다. 이 단백질은 성숙한 B 세포와 혈장세포(p lasma cell) 에서만 검출되었는데, 이들 세포만이 i mmuno g lobul i n 을 합성하는 것으로 알려져 있다. NF-kB 는 그의 다 론 세포에서나 im munog lo bulin 합성능력을 상실한 전구 B 세포 (pr e-B cells) 를 B 세포로 유도하면 나타나는 것을 관찰할 수 있다. i mmuno g l c,J ul i n 의 세포 특이 합성은 두 종류의 핵 단백질 즉 NF -A2 와 NF-kB 가 미리 세포 특이적으로 합성되어 준비되어 있어야만 가능하다. 아와 같이 i mmuno g lobul i n 유전자의 순차적 발현 조절에 대한 설명을 위해서는 우선 핵 단백질과 같은 조절요인이 어떻게 미 리 세포 특이적으로 합성될 수 있었는지를 설명하여야만 한다. 따라 서 NF-kB 단백질은 여러 종류의 세포 속에 불활성화된 형태로 존재 하지만 B- 계통의 세포에서 어떻게 활성화된 형태로 전환되는지 그리 고 어떻게 NF-A2 와 같은 핵 단백질 유전자가 림프구에서 순차적으 로 발현될 수 있는지에 대하여 먼저 알아야만 할 것이다. 이러한 사 실은 순차적 유전자 발현에 대한 설명이 앞으로도 얼마나 어려울 것 인가를 강하게 암시하고 있다.
(5) 메철기 첨가반응 유전자의 구조 죽 염색질의 구조를 변화시키는 또 다른 방법은 메 칠기 첨가반응 (DNA me thy la ti on) 이다. DNA 의 cyt os i ne 염기 중 5% 는 메칠기가 결합되어 있는 me t hy lc yt os i ne 의 형태로 되어 있는데, 근래 메칠기 첨가반응이 어떤 세포에서 특정된 유전자의 발현을 조절 하는데 개입될 가능성이 있다고 암시된 바 있다. 사람이나 닭의 발생 배의 적혈구 세포에서 글로빈 단백질 합성에 관여하는 DNA 에는 전 혀 메칠기가 존재하지 않으나, 글로빈을 합성하지 않는 세포에서는 동일한 유전자일지라도 메칠기가 다량 존재한다. 태아의 간세포가 헤 모글로빈을 합성하는 발생 초기에는 그 유전자에 메칠기가 전혀 첨가 되어 있지 않으나 동일한 유전자일지라도 성체 조직에서는 메칠기가 첨 가되 어 있다 (van der Ploeg and Flavell, 19so ; Groud ine and Wein - trau b, 1981}. 근래 메칠기 첨가반응과 글로빈유전자의 작용의 관계에 대해서 클로운된 글로빈유전자를 이용하여 연구된 바 있다 (Buss li n g er et al., 1983}. 태아세포의 글로빈유전자를 클로운시킨 다음 칼슘인산 에 침전시켜 세포에 넣어 주면 세포는 그 DNA 를 핵 속에까지 침투 시킨다. 일단 DNA 가 핵 속으로 들어가면 그 유전자는 전사된다. 클 로운된 글로빈유전자를 세포내로 침투시키기 전 그 유전자의 특정 부 위만을 메칠기 첨가 반응으로부터 보호하고 나머지 부위를 메칠기 첨 가 반응에 노출시킴으로써 유전자 자체는 모두 동일하나 유전자의 메 칠기 분포 양상을 다르게 만들어준 다음 각각을 전사시켰다. 전혀 메 칠기가 없는 유전자는 전사되었으나, 완전히 메칠기가 첨가된 유전자 는 전사되지 않았다. 부분적으로 메칠화된 유전자를 이용하여 실험한 결과 글로빈 유전자의 5' 부위 즉 -760 에서 +100 에 이르는 염기에 메칠기가 첨가되면 전사가 억제되는 점으로 보아 유전자의 5' 쪽에서 의 메칠기 첨가반응이 직접 유전자 발현을 조절하는 역할을 하는 것 으로 생각되었다.
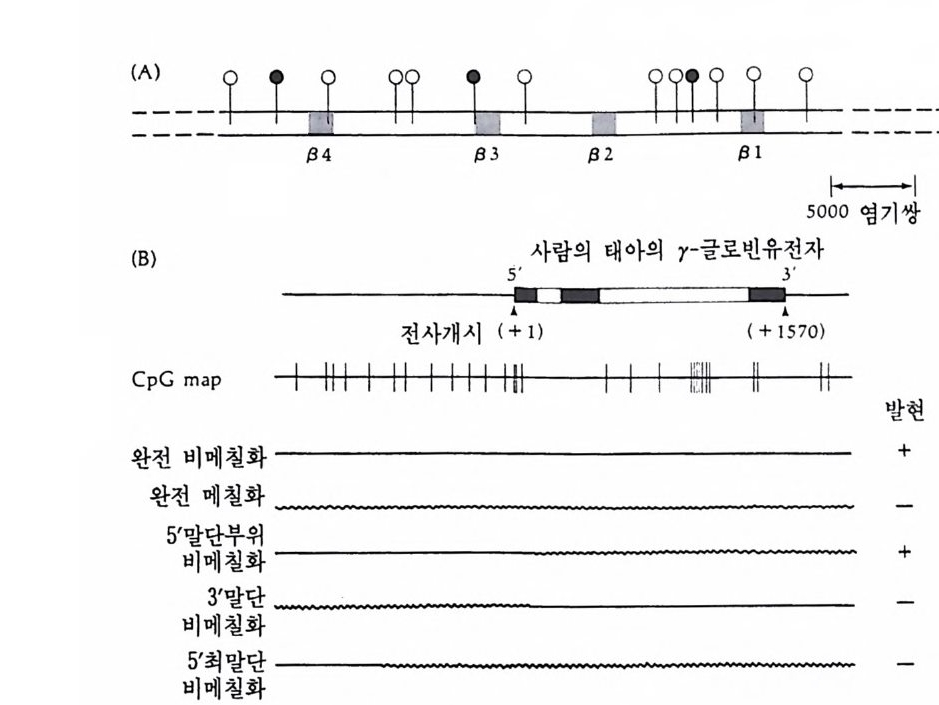 (A) 『 f L 『 『 I 二二-二二二二
(A) 『 f L 『 『 I 二二-二二二二
그림 6-16 글로빈유전자에서의 메철화현상. (A) 토끼 8- 글로빈유전자에서의 메칠화현상(f] h fJ2, f]3, {J4 ), CCGG 배열 의 위치는 ?으로 나타내었고, 메철화된 부위는 ’으로 나타내었다. (8) 클로운된 r- 글로빈유전자로부터의 전사는 메철화현상에 의해 조절된다. 꼭 대기에 있는 그림은 태아의 r- 글로빈유전자인데, 검은 부분은 exon 을 그리 고 밝은 부분은 intr on 을 나타낸다. 그 밀의 그립은 유전자내의 메칠화 부 위의 위치를 보여주고 있다. 그 다음 그립은 클로운된 글로빈을 부분적으로 혹은 천부 메칠화시킨 다음 발현에 미치는 영향을 조사한 결과이다 (Shen and Manrati s, 1980 ; Busslin g e r et al., 1983) .
기관 특이 메칠기 첨가 반응을 난알부민유전자에서 찾아볼 수 있는 데, 유전자가 수란관 세포에서는 메칠화되어 있지 않으나 다른 조직 에서는 메칠화되어 있다 (Mandel and Chambon, 1979). im munog lo bulin 합성에 있어서 class s wit c hi n g이 일어날 때 탈메칠기 반응 (deme th-
yla ti on ) 이 일어나는 것을 관찰할 수 있었다 (Ro g ers and Wall, 1981). 이 경우의 탈메칠기 반응은 쥐의 림파구에서 일어나도 금속 결합 단 백질인 meta l loth ion in e I 의 생성과도 관계되는 것으로 보였다 (Comp re re and Palm iter , 1 981}. 이러한 점으로 보아 탈메칠기 반응은 조직 특유의 유전자 발현의 유발과 관계되는 것으로 보인다. 5 - azac yti d i ne 는 me t h y l t ran f erase 의 억제제로서 탈메칠기 반응을 촉 진한다 (Raz i n et a l., 1984). 만약 5 - azac yti d i ne 을 생쥐의 섬유아세포 (C3HlOT1 /2) 에 첨가해 주면 , 이들 세포들은 근세포 (m yoc yt e), 지방 세포 (ad ip oc yt e), 연골세포 (chondroc yt e) 기능으로 전환될 수 있다 (Tayl o r and Jon es, 1982 ; Konie c zny and Emerson, 1984) . 이 와 같이 세 포의 형질전환이 탈메칠기 반응으로 가능하며, 이러한 형질전환은 상 당히 안정하다. 즉 여러 차례의 세포분열을 통해서도 전환된 형질은 그대로 유지된다. 또한 5 - azac yti d i ne 을 C3Hl0Tl/2 세포에 처리하 여 얻은 근세포로부터 DNA 를 추출하여 다른 C3Hl0Tl/2 세포에 주 입하면 이들 세포들도 근세포로 전환하는 것을 확안할 수 있었다 (Lassar, et al., 1986) . DNA 메칠화가 유전자 발현의 조절과 밀접한 관계가 있음을 시사 하는 또 하나의 유력한 예는 포유류에서 X 염색체의 불활성화이다. X염 색 체 에 연관된 유전자의 하나인 hyp o xanth ine pho sph o rib o syl - tra nsfe r ase(HPRT) 유전자를 생쥐의 세포 속으로 주입시켰을 때 불 활성화된 X 염색체에 조합되면, 이 DNA 는 숙주세포에서 전사되지 않는다. 그러나 주입된 HPRT 유전자가 활성화된 X 염색체에 조합되 면 숙주세포는 HPRT 효소를 합성한다. 5-azac ytidi ne 을 불활성화된 X 염색체에 처리하면 X 염색체가 부분 적으로 다시 활성화되는 경향을 보인다. 활성화된 X 염색체를 가진 생쥐세포와 불활성화된 X 염색체를 가진 사람의 세포를 융합한 다음 이들 융합세포에 5-azac yti d i ne 을 처리해 주면 사람의 X 염색체로부 터 HPRT 효소가 합성된다 (Mohandas et a l., 1981).
X 염색체상에 연속적으로 잇달아 자리하는 효소들 (consecu ti ve enz ym es) 의 유전자는 공통적으로 5' 말단에 G-C 가 풍부한 부위를 가 지고 있다. X 염색체가 활성화된 경우에는 최소한도 세 개의 유전자 의 5' 말단이 저메철화 (h yp ome thy la t ed) 되어 있고, X 염색체가 불활성 화된 경우에는 이둘 세 개의 유전자의 5' 말단이 메칠화되어 있다 (Wolf e t a l., 1982, 1984 ; Keit h et al., 1986) , 이 와 유사하게 3' 말단의 C p G 도 활성화된 X 염색체에서보다 불활성된 X 염색체에서 훨씬 더 많이 메칠화되어 있다. 만약 이들 불활성화된 X 염색체를 자연적으로 나 혹은 인위적으로 활성화시키면, 3' 말단의 C p G 부위의 저메칠화 현 상이 두드러지게 나타난다 (Wol f et al., 1984). t era t ocarc i noma 세포가 분화하는 도중에 X- 염색체가 불활성화되면, C p G 부위의 메침화 현상 이 나타난다 (Lock et a l., 1987). 아직까지 X 염색체의 불활성화를 유도 하는 요인에 대하여 알려진 바가 없지만, DNA 메칠화에 의해 불활성 상태가 유지되고 다음 대로 전달되는 것으로 보인다 (Kaslow and Mi ge on, 1987) . 만약 탈메철기 가설이 옳다면 메칠화된 시토신의 양상이 여러 대의 세포분열을 통해서도 다음 대에 전해져야 할 뿐만 아니라 생식세포에 서는 탈메철화로 메칠기가 제거되어야 한다. 그런데 그것이 사실이 다. 일정한 양상으로 메칠화된 DNA 를 주입하면 100 회의 세포 세대 에 걸쳐 동일한 메칠화 양상이 유지된다 (W ig ler et al., 1981 ; Ste in et al., 1982). 스타인 (S t e in)은 한쪽의 사슬만이 메칠화된 DNA (he m iinet h yla te d DNA) 를 세포 내로 주입 하면 그 세포로부터 유래 된 모든 세포에서는 모든 CG 가 메칠화되는 현상을 보인다. 정자 형성 과정에서 체세포 특유의 저메칠화 양상은 나타나지 않는 다. 글로빈 난알부민, i mmuno g lobul i n 과 같은 세포 특유의 단백질에 대한 유전자들은 모두 정자 형성 과정에서는 상당한 정도로 메칠화되 어 있다. 정모세포에서 대부분의 저메칠화된 부위는 성숙한 정자에서 는 메철화된다. 정자와 난자의 유전자간의 메칠화 정도의 차이는 그
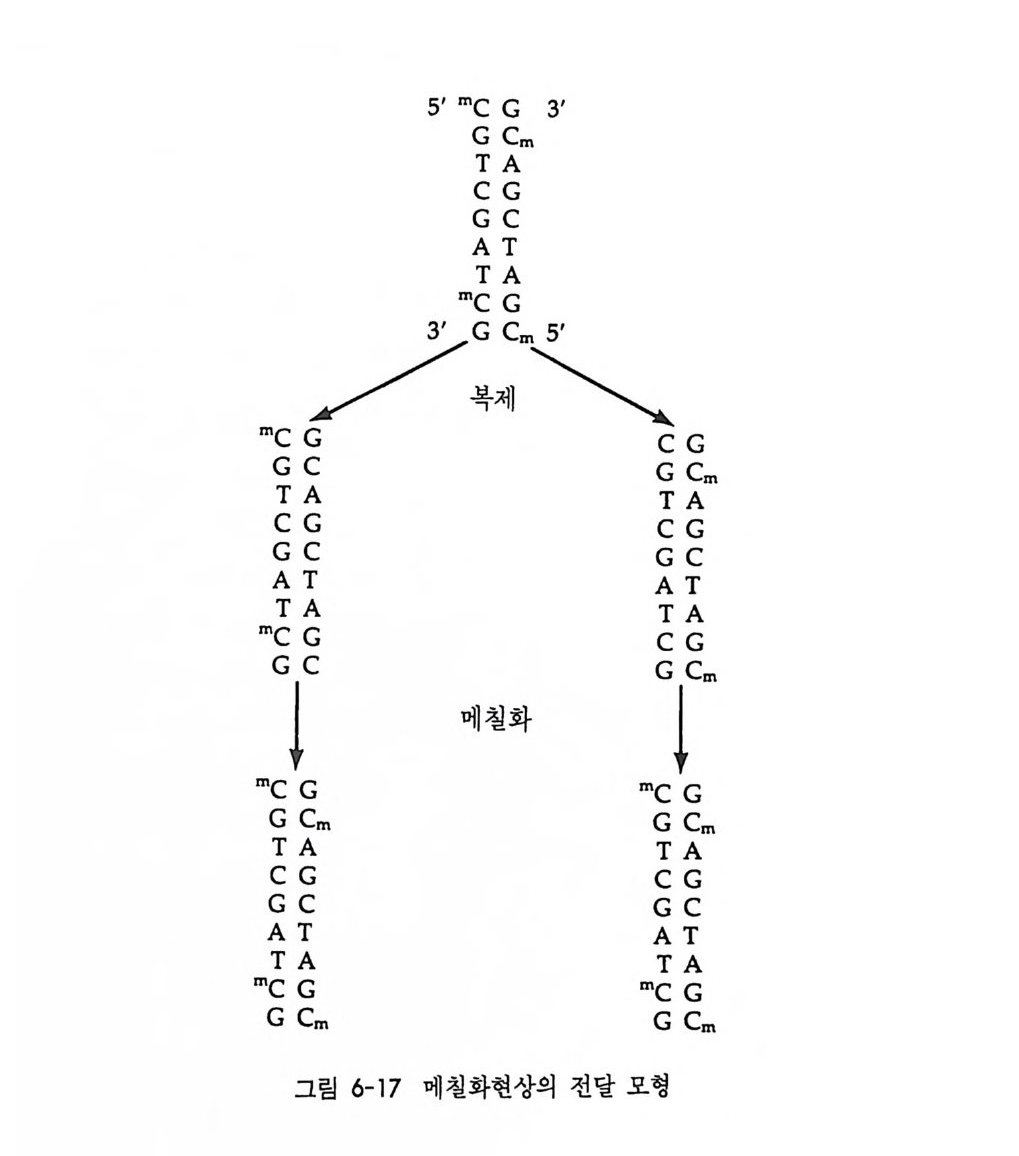 [
[
유전자가 모계에서 유래하였는지 혹은 부계에서 유래하였는지 판단할 수 있을 정도로 분명하다. 수컷 혹은 암컷의 원시 생식세포의 DNA 가 놀라울 정도로 메철화되지 않은 데 반하여 (Monk et a l., 1987), 정 자와 난자의 유전자는 상당히 메칠화되어 있다. 더구나 갇은 유전자 일지라도 정자와 난자 사이에 메칠화 양상에는 차이가 있다 (Re i k et
al., 1987 ; Sap ien za et al., 1987) . 이 러 한 모계 와 부계 의 메 칠화에 따른 착상(impri n ting)은 공간적 및 시간적 유전자의 발현조절에 대한 정보 를 유전적으로 부여하는 결과를 초래한다. 스웨인 (Swa i n, 1987) 등은 종양 세포 생성 유전자를 생쥐의 게놈에 삽입시킨 tra nsge ni c m ic e 를 만들었는데, 만약 이 종양 세포 생성 유 전자가 수컷으로부터 유래한 것이라면 특별히 십장세포에서만 이 유 전자가 발현되나, 암컷으로부터 유래한 것이라면 전혀 발현되지 않는 다. 유전자 발현양상이 메철화 정도와 밀접한 관계를 가지고 있다는 것이 분명하다. 죽 이 유전자는 난자형성 기간에는 메칠화되고, 정자 형성 기간에는 탈메철화된다. 이와 같이 생식세포에 따른 메칠화 양 상의 차이는 왜 포유류에서 단성생식이 불가능하며, 반드시 수컷과
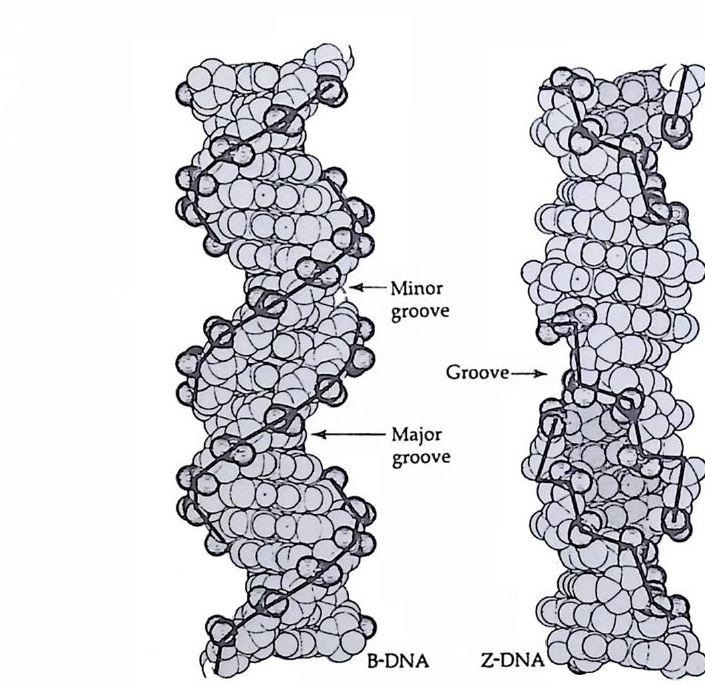
그림 6-18 우선성 B-DNA 와 좌선성 Z-DNA. 메철화현상에 의해 B-DNA 가 Z-DNA 로 전환될 수 있다.
암컷의 핵의 결합을 필요로 하는지 어느 정도는 설명해 주는 것으로 생각된다. 메칠기 첨가반응과 유전자 발현의 조절과의 관계를 보여주는 또 하 나의 중요한 예 는 Z - DNA 의 존재 이 다. 대 부분의 DNA 는 Wats o n- Cr i ck 모델에 따르는 사슬의 희전방향이 우회전하는 이중나선의 B - DNA 이다. 그러나 리치 Alexander R ic h 와 그의 공동 연구자들은 특 별히 CGCGCG 와 같이 GC 의 함량이 높은 염 기 배 열을 발견했는데 이러한 회전방향이 좌회전하는 이중나선으로 되어 있다 (Wan g e t a l. , 197 9} . 이 들 좌회전하는 DNA 의 물리적인 성질은 우회전하는 대부분 의 DNA 와 대단히 다르다. 좌회전하는 DNA 는 1 회전당 12 개의 염기 쌍이 소 요되며 지그재 그 ( z ig za g) 의 모양을 형 성하는데 이 러한 DNA 를 Z - DNA 라고 한다. Z - DNA 에는 B-DNA 에서 볼 수 있는 넓은 홈 (majo r gr oove) 이 결여되어 있기 때문에 특정된 분자의 결합이 불가 능하다. 좌회전하는 Z - DNA 는 포유류와 초파리의 게놈에서 발견되 었는데, Z - DNA 에 대한 항체 를 이용하여 초파리의 다사염색체의 간 대에만 Z - DNA 가 존재함을 발견하였다 (Nordhe i m et a l., 1981}.
그림 6-19 초파리의 다사염색체내의 Z-DNA 의 위치. Z-DNA 에 대한 형광항 체가 간대에 결합하고 있다 (Nordhe i m et a l., 1981).
B-DNA 구조를 Z-DNA 구조로 전환시킬 수 있는데, 지금까지는 영류의 농도가 높은 조건에서만 이러한 전환이 가능하였다. 그러나 근래 정상적인 생리적 영류 농도에서도 GC 중합체에서 cyt os i ne 염기 에 메칠기 첨가만 이루어지면 Z - DNA 으로의 전환이 가능한 것으로 관찰되었다 (Bebe and Felsenfe ld , 1981). 더구나 누클레오솜의 간격이 영향을 주었는데, B-DNA 에서는 누클레오솜 형성이 촉 진되고 반면 에 Z-DNA 에서는 누클레오솜 형성이 억제되는 현상이 나타난다 (Ni cko l et a l., 1 982). 사실상 히스톤이 Z-DNA 에 결합되지 않은 것 은 아니다. 그러나 히스톤의 결합이 누클레오솜의 구조로 나타나지 않는 다. 죽 메칠기 첨가반응에 의해 Z - DNA 가 형성되고 이러한 DNA 의 구조에서는 누클레오솜의 형성이 전적으로 억제된다. 누클레오솜의 구조적 변화가 유전자 발현과 대단히 밀접한 관계가 있다. 전사하지 않는 DNA 에서의 누클레오솜은 덩어리로 뭉쳐 있어 서 DNAse 로 처리하여 토막을 낼지라도 서로 엉켜서 떨어지지 않는 다. 그러나 전사하고 있는 DNA 의 누클레오솜은 DNAse 에 의해 쉽 게 분해된다. 이러한 현상은 히스톤 중 특히 H 제 의해 일어나는 것 으로 생각되고 있으며, H 례 의한 엉킴이 유전자 발현을 억제하는 것으로 추측되고 있다 (W ei n tr aub 1984). 그러나 누쿨레오솜에 의한 엉컴을 풀어주면 유전자 발현이 유발되는 것으로 보였다. 누클레오솜 의 엉킴울 푸는 방법으로는 HMG 14 혹은 17 의 결합, DNAse I 에 예민한 부위형성, 히스톤의 변화, Z-DNA, 혹은 특정 염기 부위 특 유의 결합 단백질의 결합 등이 있다.
참고문헌 Behe, M. and Felsen feld , G. (1981) . Eff ec ts of meth yla ti on on a syn the ti c pol yn u cleoti de . The B-Z tra nsit ion in pol y (dG-m5dC) • pol y (dG-m5dC) . Proc. Natl. Acad. Sci . USA 78: 1619- 1 623. Bergm a n, Y., Ric e , D., Grosschedl, R. and Baltim ore, D. (1984). Two regu la to r y elements for im munog lo bulin K ligh t chain gen e exp re s- sio n . Proc. Natl. Acad. Sci. USA 81: 7041- 7 045. Bodner, M . and Karin , M. (1987) . A pit떠t ary -s p ec ifi c tra ns-acti ng factor can stim ulate tra nscrip tion from the grow th hormone pro - mote r in extr a cts of nonexp re ssin g cells. Cell 50: 267-275. Busslin g e r , M ., Hurst, J. and Flavell, R.A. (1983) . DNA meth yla ti on and the regu la ti on of glo bin gen e expr e ssio n . Cell 34: 197-206. Chandler, V.L. , Maie r , B.A. and Yamamoto , K.R . (1983) . DNA sequ e nces bound spe c if ica lly by glu cocort ico id recept or in vitro render a hete r olog ou s pro mote r hormone respo n siv e in vivo . Cell 33: 489-499. Comp er e, S.J . and Palmi ter , R.D . ( 1981 ) . DNA meth yla ti on contr ol s the ind uc ibi li t y of the mouse meta l loth ion ein - 1 gen e in lym ph oid cells. C ell 25: 233-240. Davis o n, B.L., Edg ly , J .M ., Mulvi hill, E.R. and Chambon, P. (1983) . Formati on of sta b le pre in itiat i on comp le xes betw een eukary o tic class B tra nscrip tion fac to r s and pro mote r sequ e nces. Natu r e 301: 680-686. Die r ks, P., v an Ooy en , A., Chochran, M.D., Dobkin , C., Reis e r, J. and Weis sm an, C . (1983). Three regi on s ups t r e am from the cap site a re requ ire d for effi cien t and accurate tran scri ption of the rabbit
/3-glo bin gen e in mouse 3T6 cells. Cell 32: 695-706. Dy na n, W.S. and Tji an , R. (1985) . Contr o l of eukaryo t i c messeng er RNA syn the sis by sequ ence-spe c i fic DNA-bin d in g po rte i n s . Natu r e 316: 774-778. Efs t r at i ad is , A. and fou rte e n oth e r. (1980) . The str u ctu r e and evolu- tion of the human {]~g l o bin gen e fam il y. Cell 21: 653- 66 8. Garabedi an , M. J., Hung, M-C. and Wensin k , P.C. (1985) . Indepe n dent contr o l elements tha t dete r mi ne yol k pro te i n gen e exp re ssio n in alte r nati ve Drosop hi l a tiss ues. Proc. Natl. Acad. Sci. USA 82: 1396-1400. Garabedi an , M.J. , Sheph erd, B.M ., and Wensin k , P.C. ( 1986) . A tiss ue -spe c if ic t ra nscrip tion enhancer from the Drosop hi la yol k pro te i n 1 gen e. Cell 45: 859-867. Garcia , J.V . , Bic h -Thuy, L.T ., S ta f fo rd , J. and Qu een, C. (1986) . Syn e rgi sm betw een im munog lo bulin enhancers and pro mote r s. Natu r e 322: 383-385. Gedamu, L. and Dixo n, G.H. (1978) . Eff ec t of enzy m ati c decap ping on pro ta m i ne messeng er RNA tra nslati on in wheat- gem S-30. Bio c hem. Bio p h y s . Res. Commun. 85: 114- 12 4. Gil lies, S.D., Morriso n, S.L. , Oi, V.T. and Tonega w a, S. (1983) . A tiss ue-spe c if ic tra nscrip tion enhancer element is locate d in the majo r int r o n of a rearrang ed im munog lo bulin heavy chain gen e. Cell 33: 717-728. Grosschedl, R. and Bir n sti el, M.L. (1980) . Sp a cer DNA ups t r e am from the TATAATA sequ ence are essenti al for pro moti on of H2A his t o n e gen e tra nscri ption in viv o . Proc. Natl. Acad. Sci . USA 77: 7102-7106. Grosveld, G. C., de Boer, E., Shewmaker, C. K. and Flavell, R. A.
(1982) . DNA sequ ences necessary for the tra nscrip tion of the rabbit /3-glo vin gen e in viv o . Natu r e 295: 120-126. Groudin e , M. and Wein t r a ub, H. (1981). Ac tiva ti on of glo bin gen es durin g chic k develop m ent. Ceil 2 4: 393-401 . Jon es, K.A ., Kadonaga , J. T., Rosen feld , P.J ., Kelly, T.J . a nd Tji an , R. (1987) . A cellular DNA-bin d in g pro te i n tha t acti va te s eubar- yot ic tra nscrip tion and DNA rep lica ti on . Cell 48: 79-89. Kanto r , J.A . , T urner, P.H . and N i enh 떠 s, A.W . (1980) . /3 Thalas- semi a: Muta t i on s whic h aff ec t pro cessin g of the /3-glo bin mRNA pre cursor. Cel l 21: 149- 15 7. Karin , M ., Haslin g e r , A., Holtg rev e, H., Ric h ards, RI. , Krautn e r, P., Westp h al, H.M. and Beato , M. (1984) . Characte r iz a ti on of DNA sequ e nces thr oug h whic h cadmi um and glu cocort ico id hormones ind uce human meta l loth i o n ein - II gen e. Natu r e 308: 513-519. Kaslow, D.C. and Mi geo n, B.R. ( 1987) . DNA meth yla ti on sta b il ize s X chromosome ina cti va ti on in euth e ria n but not in marsup ial: Evi- dence for multis te p main t e n ance of mammalia n X dosage comp en sati on : Proc. Natl. Acad. Sci. U SA 84: 6210-6214. Keit h, D.H., Sin g e r sam, J. and Rig gs, A.D. (1986) . Acti ve X-chromo- some DNA is unmeth y l a te d at eig h t CCGG site s cluste r ed in a gua nin e -pl u s-cyt os in e -ric h isla nd at the 5' end of the gen ~ for pho sph o g ly c e rate kin a se. Mo!. Cell Bio l. 6: 4 122-4125. Klock, G., S tr a hle, U. and Schutz , G. (1987) . Oestr o g en and glu cocor- tico ld respo n siv e elements are closely relate d but dist in c t . Natu r e 329: 734-736. Konie c zny, S.F. and Emerson, C.P ., Jr. ( 1984) . 5-Azacyt idine ind uc- tion of sta b le mesodermal ste r n cell line age s from 10T1/2 cells: Evid e nce for regu la to r y gen es contr o llin g dete r m ina ti on . Cell 38:
791-800. Krieg , P.A. and Melto n , D.A . (1987) . An enhancer respo n sib le for acti va tin g tra nscrip tion at the mid- blastu l a tra nsiti on in Xenop u s developm ent. Proc. natl. Acad. Sci. USA 84: 2331-2335. Kumar, V., Green, S., Sta c k, G., B err y, M. , J in, J-R. and Chambon, P. (1987) . Functi on al domain s of the human estr o g en recept or . Cell 51: 941-951 . Lassar, A.B., Pate r son, B.M. and Wein t r a ub, H. (1986). Transfe c ti on of a DNA locus tha t m edia t e s the conversio n of lOTl/2 fibr oblasts int o my o blasts . Cell 47: 649-656. Lock, L. F., Takagi , N. and Martin , G.R . (1987) . Meth yla ti on of the HPRT gen e on the ina cti ve X chromosome occurs aft er chromo- some ina cti va ti on . Cell 48: 39-46. Lawn, R.M ., Efs t r a ti ad i s, A., O'Connell, C. and Man iat i s, T. (1980) . The nucleoti de sequ e nce of the human /3-glo bin gen e. Cell 21 : 647 -651. Mandel, J.L. and Chambon, P. (1979) . DNA meth y l a ti on pa tt er n within and around ovalbu min and oth e r chic k gen es. Nucleic A cid Res. 7: 2os1-2103. Ma niat is , T., Goodbourn, S. and Fis c her, J.A. (1987) . Regu la ti on of ind ucib l e and tiss ue-spe c if ic gen e exp re ssio n . Scie n ce 236: 1237 -1245. Maqu a t, L.E. , Kin nibu rgh , A.J. , Beach, L.R., Honig , G.R ., Lazerson, J., Ershler, W.B. and Ross, J. (1980) . Processin g of h uman /3-glo bin mRNA pre cursor to mRNA is defe c t ive in three pa tie n ts wit h p+ tha lassem ias . Proc. Natl. Acad. Sci . USA 77: 4287-4291 . Mart ine z, E., Giv e l, F. and Wahl, W. (1987) . An estr og e n respo nsiv e element as an ind uc ibl e enhancer: DNA sequ e nce requ i re ments a nd
conversio n to a glu cocort ico id - respo n siv e element. EMBO ]. 6: 3719-3727. Math e r, E.L. and Perry , R.P. (1982). Transcrip tion al regu la ti on of t he im rnunog lo bulin - V gen es. Nucleic Acid Res. 9: 6855-6867. McKnig h t, S. and Tji an , R.(1 986). Transcrip tion al selec tivity of v ir a l gen es in mammalia n cells. Cell 46: 795-805. Merkel, C.G ., Kwan, S. -P. and Ling r el, J.B . (1975) . Siz e of the pol y (A) regi on of newly syn the siz e d glo bin mRNA . ]. Bio l. C hem. 250: 3725-3728. Mi es fe ld , R. and seven oth e r. (1986) . Geneti c comp le menta t i on of a glu cocort ico id recept or defi ci e n cy by a cloned recep tor cDNA. Cell 46: 389-399. Mohandas, T ., Spa r kes, R.S. and Shapi ro , L.J. (1981) . Reac tiva ti on of an ina cti ve human X chromosome: Ev ide nce for X ina cti va ti on by DNA meth y l a ti on . S:i en ce 211: 393-396. Monk, M. ; B oubeli k, M. and Lehnert , S. (1987) . Temp o ral and reg ion al change s in DNA meth yla ti on in the embry on i c, extr a em- bryo n ic , and ger m celllin e ag es durin g mouse embry o develop m ent. Developm e nt 99: 371-382. My er s, R.M ., Til ly, K. and Man iat i s, T. (1 986) . Fin e stru ctu re g en etic analys i s o f a f]-glo bin pro mote r . Sci en ce 232: 613-618. Nic k ol, J., Behe, M.N. and Felsen feld , G. (19s2) . Eff ec t of the B-Z tra nsfo r mati on in pol y (dG-m5dC ) ; bip o ly (dG-m5dC ) on nucleosome form ati on . Proc. Natl. Acdd. Sci . USA 79: 1771-1775. Nokin , P., Burny, A., Huez, G. and marbaix , G. (1976) . Globin m RNA from anaemi c rabbit spl e en. Siz e of its po lya d enyl a te segm e nt. Eur. ]. Bio c hem. 68: 431-- 43 6. Nordheim , A., Pardue, M. L., Lafe r, E.M ., Moller, A., Sto l lar, B.D.
and Ric k , A. (19s1) . Anti bo die s to left ha nded Z-D NA bin d to int e r band regi on s of Drosop hi la pol yr en e chromosomes. Natu r e 294: 417-422. Orkin , S. and Kazazia n , H.H. (1984} . The muta t i on and pol ym o ph is m of the human [J-glo bin gen e and its s urroundin g DNA . Annu. Rev . Genet 18: 131- 17 1 . Parker, C.S . and Top ol , J. (1984). A Drosop hi la RNA pol ym erase II tra nscri ption fac to r contr a in s a pro mote r reg ion - sp e c if ic DNA -bin d in g acti vi ty . Cell 36: 357-369. Parslow, T.G. , Blair , D.L. , Murph y , W. J. and Granner, D .K . (1984) . Str uc tu re of the 5' ends of im munog lo bulin gen es: A novel conser- ved sequ e nce. Proc. Natl. Acad. Sci. USA 81: 2650-2654. Pfa h l, M. (1982} . Spe c if ic bin d in g of the glu cocortic o id r ecep tor comp le x to the mouse mammary tum or pro v ira l pro mote r reg ion . Cell 31: 475-482. Pic ar d, D. and Schaff ne r, W . ( 1984} . A lym ph ocy te- spe c i fic e nhancer in the mouse im munog lo bulin K gen e. Natu r e 307: 80-8 2. Qu een, C. and Baltim ore, D. (1983) . Immunog lo bulin gen e tra n- scrip tion is acti va te d by downstr e am sequ e nce elements . Cel l 33 : 741-748. Rabin o w, L. and Dic k in s on, W.J. (1986) . Comp le x cisac ti ng reg ul arors and locus struc tu r e of Drosop hi la tiss ue- sp e c if ic ADH varia n t s. G e ne t ic s 112: 523-537. Razin , A., Cedar, H. and Rig gs, A. {1984) . DNA Meth y l a ti on : Bio - chemis try and Bio lo g ica l Sig n if ican ce. Spr in g e r Verlag , New York. Reik , W., Coll ick , A., Norris, M. L., Barto n , S.C. and Surani , M.A. {1987} . Genom ic im p ri n t i ng dete m i ne s meth yla ti on of pa te r nal alleles in tra nsge n i c mic e . N atu r e 328: 248-250.
Rog e rs, J . and Wall, R. (1981) . Irnmunog lo bulin heavy ch ain gen es: Demeth yla ti on accomp a nie s class swi tch i ng . Proc. N atl . A cad. Sci . USA 78: 7497- 7 501 . Rott m an, F.A., Shatk i n , A.J . and Perr y, R.P. (1974) . Sequ ences conta i n i n g meth yla te d nucleoti de s at the 5' ter m ini of messeng e r RNAs: P ossib l e im p li ca ti on s for pro cessin g . Cell 3: 197-199. Shatk i n , A .J. ( 1976) . Cap ping of euca ryo ti c rnRNAs. Cell 9: 645-653. Shein e ss, D. and Darnell, J .E . (1973) . Polya d eny lic s egm e nt in rnRNA becomes shorte r wit h age Natu r e New Bio l . 2 41: 265- 26 8. Sapi en za, C., Pete r son, A.C . , Rossant, J. and Ballin g , R. (1987) . Deg ree of meth yla ti on of tra nsge nes is dep e ndent on ga mete of orig in. Natu r e 328: 251 - 25 4 . Shen, C.K .J. and Mania t is , T. (1980) . Tis s ue-s p e ci fic DNA meth - yla ti on in a cluste r of rabbit {]- lik e glo bin gen es. P roc. natl. A cad. Sci . U SA 77: 6634- 6 638. Shi, Z .P., L ee, R. and Weir u nann, R. (1986) . Prote i n fac to r (s) bin d i ng ind epe n dentl y to tw o dif fere nt regi on s of the adenov iru s-2 majo r late pro mote r . Nucleic Acid Res. 14: 3729-3744. Sta u dt, L.M ., S in g h , H., S en, R., Wi rth, T., Sharp, P.A . and Baltim or- e, D. ( 1986) . A lym ph oid - spe cif ic pro te i n bin d i ng to the octa m er moti f of irn munog lo bulin ge nes. Natu r e 323: 640- 64 3. Ste i n , R., Gruenbaum, Y., Pollack, Y ., Razin , A . and Cedar, H . (1982) . Clonal inh erita n ce of the pa tt er n of meth yla ti on in mouse cells. Proc. Natl. Acad. Sci. USA 79: 61-65. Swain , J.L . , Ste w art , T.A . and Leder, P. (1987) . Parenta l leg a cy dete r n ine s meth yla ti on and exp re ssio n of an auto s omal tran sge n e: a molecular mechan ism for pa renta l im p rint i ng . Cell 50: 719-727. Tayl o r, S.M . and Jon es, P .A. ( 1982) . Chang e s in ph enoty pic exp re s-
sio n in embryo n i c and adult cells tre ate d wit h 5-a z acy ti di n e . ]. Cel l Phys i ol . 111: 187-194. Tie m eie r , D.C ., Til g h man, S.M., Polsky, F.I. , Seid m an, J.G ., Leder, A., E dg el l, M .H. and Leder, P . (1978) . A comp ar iso n of tw o cloned mouse glo bin gen es and the ir surroundin g int e r veni ng sequ e nces. Cell 14: 237-246. Trudel, M. and Consta n ti ni, F. ( 1987) . A 3' enhancer contr i b u te s to the sta g e -spe c i fic expr e ssio n of the human /3-glo bin gen e. Gen e s and Dev. 1 : 954- 96 1 . van der Ploeg, L.H .T . and Flavell, R.D. (1980) . DNA meth y l a ti on in the human r-8-/3 glo bin locus in eryt hroi d and non-e r y thr oid cells. Cell i9: 9 47-958. Vog el i, G., Ohkubo, H., S obel, M .E. , Yamada, Y., Pasta n , I. and de Crombrugg h e, B. (1981) . Str u ctu r e of the pro mote r for chic k en type I collage n gen e. Proc. Natl . A cad. Sci. USA 78: 5334- 53 38. Walker, M .D., Edlund, T., Boulet, A.M . and Rutt er , W.J. (1983) . Cell -spe c i fic expr e ssio n contr ol led by the 5' flan kin g reg ion of the ins ulin and chym o tr ypsi n gen es. Natu r e 306: 557- 56 1 . Wang, A.H .J ., Q떠g le y, G.J. , Kolpa c k, FJ ., C raw for d, J.L., vanBoom, J.H ., v an der Marel, G. and Ric h, A. (1979) . Molecular stru ctu r e of a left -h anded double heli ca l DNA frag m e nt at ato m i c resoluti on . Natu re 282: 680-686. Wasyl y k , B., Ked ing e r , C., C orden, J., B ~·i so n, D. and Chambon, P. (1980) . Spe c i fic in vitro initiat i on of tran scrip tion on conalbumi n and ovalbw nin gen es and comp ar iso n wit h adenov iru s 2 early and late gen es. Natu re 285: 367-373. Wein t r au b, H. (1984) . Histo n e Ill-depe n dent chromati n supe r stru c- tures and the supp re ssio n of gen e act ivity. Cell 38: 17-27 .
Wi gle r, M., Levy , D. and Perucho, M. (1981) . The somati c r ep lica ti on of DNA meth y l a ti on . Cell 24: 33-40. Writh , T., Sta u dt, L . and Baltim ore, D. (1987) . An octa m er olig o nu- cleoti de ups t re am of TATA moti f is s uff icien t for lym ph oid - spe - cifi c p ro mote r acti vi ty . Natu r e 329: 174-178. Wolf. S .F., D int g is, S ., Tonio l o, D., P ersic o, G., Lunnen, K.D ., Axel- man, J. and Mig eo n, B.R. (1984) . Comp le te concordance betw een glu cose-6-ph o sph a te dehy dr og en ase acti vi t y and hyp o meth yla ti on of 3' Cp G cluste r s: Imp lica ti on for X chromosome dosage comp en - sati on . Nucleic Acid Res. 12: 9333-9348. Zheng, X- M ., Moncoll in, V., Eg ly , J.M . and Chambon, P. (1987) . A gen eral tra nscrip tion fac to r form s a sta b le comp le x wit h RNA pol ym e rase B (II) . Cell 50: 361-368.
제 7 장 RNA p rocess ing에서의 유전자 발현의 조절 유전자 발현은 DNA 로부터 RNA 가 전사되는 것으로 완성되지 않 고, RNA로 부터 단백 질이 생 성 된 후 단백 질 특유의 모양 (co nf onna ti on) 을 획득하거나 혹은 특유의 서열을 구현함으로써 기능적인 단백 질이 될 때 유전자 발현은 완성된다. 진핵세포에서는 유전자가 전사되면 그 전사체가 직접 해독에 쓰일 수 있는 mRNA 가 되는 것이 아니다. 전사 후에도 여러 가지 p rocess i n g을 거침으로써 드디어 단백질로 해독될 수 있는 mRNA 가 된다. 그런데 이러한 p rocess i n g도 무작위적으로 일어나는 것이 아니 고 선택적으로 일어난다. I hete r og en eous nuclear RNA 유전자가 전사되면 분자가 mRNA 보다는 훨씬 큰 nRNA 의 형태로 핵 속에 존재한다. nRNA 는 분자 크기의 변화 폭이 크고 반감기
에(h alnf-Rl i fN e)A 가 는 짧5다—. 1 9분 X 자1 03의 염크기기 는정도 m이R다N.A 가반 감보기통도 2 Xm 따RN A염 에기 서인 는반 면수 시간에 해당하는 데 비해 hnRNA 에서는 수십 분 정도에 지나지 않 는다. 성 게 란에서 mRNA 의 반감기는 5 시간인 반면에 nRNA 의 반감 기는 20 분 정도이다. nRNA 와 mRNA 의 관계가 1977 년까지도 분명치 않았으나, 그 후 cDNA 의 재결합 실험으로 일부 nRNA 는 mRNA 의 전구체임이 확인 되었다. 바스토스 (Bas t os) 와 아비브 (Av i v, 1977) 는 생쥐의 글로빈 mRNA 를 분리하여 역전사 효소를 이용하여 cDNA 를 만든 다음, cDNA 를 셀룰로스에 부착시켰다. 헤모글로빈 생성세포에 방사능 ur i d i ne 을 넣어 RNA 를 표지 한 다음, RNA 를 분리 하여 글로반 cDNA 가 부착되어 있는 셀루로스 관에 넣어 흘렸다. 글로빈을 합성 하는 RNA 는 모두 이 관에 있는 cDNA 와 결합하나, 다른 종류의 RNA 는 글로빈 cDNA 와 결합하지 않는다. 이와 같은 방법을 이용하 여 cDNA 에 결합한 RNA 를 고농도의 영류 용액으로 용출시켜 방사 능 ur idi n~ 녁i 표지된 RNA 의 크기를 측정하였다. 만약 5 분 동안만 방사능 ur idi n (0녁i 표지 하면 27S 혹은 5000 개 의 염 기 로된 RNA 에 표지된다. 이 RNA의 크기는 보통 세포질에 있는 글로빈 mRNA 보 다 거의 8 배나 더 크다. 그러나 방사능 물질 표지를 중지하고 5 분 후 에 RNA 를 추출하여 분석 하여 보면 RNA 는 15S 의 RNA 속에 들어 있고, 좀더 지나면 10S 의 세포질 글로빈 mRNA 에 들어 있는 것을 알 수 있다. 죽 hnRNA(hete r og en eous nuclear RNA) 에는 ' 글로빈 mRNA 의 전구체가 들어 있다. 분자의 크기가 엄청나게 큰 전구체인 hnRNA 가 성숙하여 실제로 단백질 합성을 지시하는 rnRNA 로 된다. 글로빈을 지시하는 15S RNA 나 혹은 10S RNA 를 추출하여 글로 빈유전자에 in situ 재 결합시켜 전자현미경으로 비교하여 보았다 (Til gh man et a l., 191sa). 15S RNA 가 결합하였을 때에는 RNA 와 DNA 간에 완전하게 결합되는 것을 볼 수 있었으나 10S RNA 와의
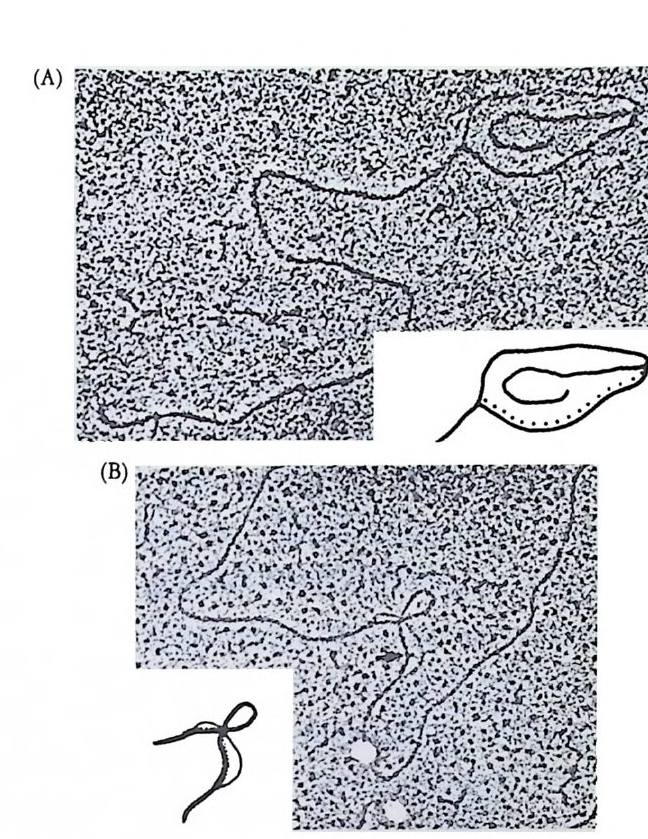 A
A
그림 7-1 생쥐 8- 글로빈유전자의 i n tr on 에 대한 전자현미경적 확인. (A) 부분적으로 변성시킨 글로빈 DNA 와 15S 글로빈 전사체의 결합, x 120,0 0 0 (해설 그립 참조) (Til g h m an et al. , 191sb). (B) 글로빈 DNA 와 글 로빈 mRNA 와의 결합. mRNA 쪽에 상보적인 영기서열의 결핍으로 재결합 되지 않음으로 DNA 에 고리가 형성된다. 이 고리가 i n tr on 에 해당한다(해 설 그림 참조). 굵은 선은 이중 나선의 DNA, 가는 선은 단일나선의 DNA, 접선과 굵은 선을 함께 그린 것은 DNA-RNA 결합부위. X78,400 (Til gh m an et al. , 1978a) .
결합에서는 불완전한 결합으로 결합되지 못한 DNA 부분이 고리모양 울 형성하는 것을 관찰할 수 있었다. 이와 같은 고리의 형성은 10S RNA 의 길이보다 글로빈유전자의 길이가 길기 때문에 나타난 것으로 해석되었다.
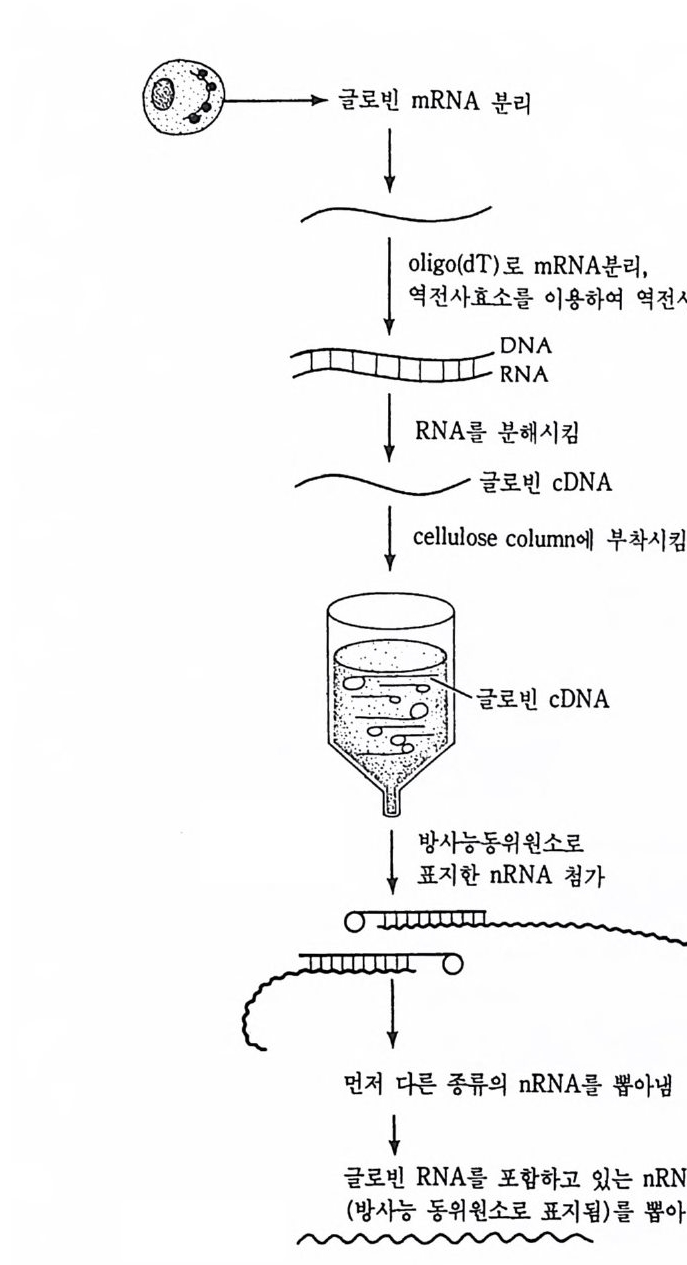 g글로빈i mRNA 분리
g글로빈i mRNA 분리
그림 7-2 글로빈 지시 서열을 포함하고 있는 핵내의 nRNA 의 분리 철차
글로빈 mRNA 에 대해서뿐만 아니 라 다른 종류의 mRNA 에 대 해 서도 전구체인 hnRNA 가 존재한다는 사실을 알 수 있었다. 즉 생쥐 배양 세포의 mRNA 전체에 대한 cDNA 를 준비하여 hnRNA 에 결합 시 켜보면 대 단히 많은 양의 cDNA 가 hnRNA 에 결합하는데, 이 러한 관찰은 핵내의 hnRNA 가 mRNA 의 전구체 임 을 보여주는 것이 라고 풀이되었다 (Hames and Perr y, 1977). 따라서 nuclear(nRNA) 에는 크게 나누어 두 종류가 있다. 즉 전체 nRNA 중 일부로서 mRNA 의 전구체 에 해 당하는 hnRNA 와 핵에만 머무는 대부분의 나머지 nRNA 이다. 이러한 사실을 알아내기 위해 서 RNA 의 다양성 즉 복잡성 (comp le xit y) 을 측정 하였다. DNA -R NA 분자 재 결 합 (molecular hyb r id iz a ti on ) 으로 RNA 의 복잡성 을 측 정할 수 있는데, 방사능 물질로 표지한 RNA 를 과량의 변성된 DNA 와 재결합시킨다. 만약 RNA 가 복잡하면 재결합 반웅 속도는 느려진 다. 즉 한 종류의 RNA 만이 존재한다고 할 때 복잡도는 1 에 해당하 는데 이러한 상황에서는 같은 영기서열을 가진 RNA 만이 존재하기 때문에 상보적 DNA 부위와의 결합이 빨리 일어난다. 그러나 동일한 양의 RNA 속에 1000 종류의 다른 염기서열이 있다면 RNA의 복잡 도는 1000 으로서 각각의 RNA 는 복잡도가 1 인 RNA 에 비해 1000 배 나 희석되어 있다고 할 수 있다. 따라서 상보적 DNA 부위와 만날 수 있는 확률이 그만큼 떨어짐과 동시에 재결합 반응 속도도 느려진다. 이와 같은 방법으로 RNA 의 복잡도를 측정해 보면 같은 세포의 mRNA 의 것 보다 nRNA 의 복잡도가 훨씬 크다는 사실을 알 수 있 다. 우선 nRNA 를 DNA 에 결합시켜 보면 nRNA 의 일부는 대단히 빠른 속도로 재결합한다. 이렇게 빠른 재결합은 nRNA 의 일부가 반 복성 DNA 로부터 전사된 것을 의미한다. 성게 포배기에 nRNA 의 25% 가량이 낮은 값의 Co t에서 DNA 와 재결합하는 반면에 mRNA 는 전혀 반복성 DNA 와 결합하지 않는다. 성게의 nRNA 에 있는 반 복성 부위의 염기수는 약 300 개의 염기로서 nRNA 의 70% 가 최소한
 표 7-1 mRNA 와 nRNA 의 특징과 상대적 복잡도
표 7-1 mRNA 와 nRNA 의 특징과 상대적 복잡도
도 한 개의 반복성 영기부위를 내포하고 있다 (S mith et a l., 1974). 그 러나 이와 같이 반복성 염기부위가 많은 mRNA 도 비반복성 DNA 와 재결합시키면, 완전히 반복성 부위를 제의한 재결합을 볼 수 있다. 이러한 유일성 nRNA 의 복잡도는 갇은 세포의 mRNA 의 복잡도 보 다 4~20 배 가량 높다. 이와 같은 방법으로 계산해 보면 nRNA 의 약 10~20% 가량만이 세포질 mRNA 로 성숙된다는 점을 알 수 있 다. 쥐의 간 세포에서는 단지 nRNA 의 11% 만이 mRNA 로 성숙되 고, 배양된 곤충세포에서는 5% 의 nRNA 만이 mRNA 로 성숙된다. 이러한 관찰로부터 핵 속에 존재하는 전사체 중에는 mRNA 의 전구 체가 될 수 있는 hnRNA 의 양이 적고 대 단히 빠른 속도로 tur n over 하는 nRNA 의 양은 많다는 사실을 알 수 있다. 이들 다량의 nRNA 는 mRNA 로 성숙되는 RNA 와는 다른 염기서열울 가지고 있다. 2 nRNA p rocess ing에 의한 유전자 발현의 조절 유전자의 선택적 발현은 전사과정에서는 물론 순차적인 pro cessin g 에서도 조절된다. 일단 nRNA 의 형태로 전사되지만 단백질의 아미 노산 서 열을 지시 하는 mRNA 는 선택 적 인 p rocess i n g에 의 해서 구현 된다. 물론 다량의 nRNA 중 일부분에 해당하는 hnRNA 로부터의
mRNA 생성 자체가 선택적이기도 하지만 최근 동일한 hnRNA 로부 터 발생 단계 와 세 포의 종류에 따라 mRNA 로의 p rocess i n g이 다르게 일어날 가능성이 성게와 쥐의 발생과정에서 제시되었다. 1977 년 클린 (Kleene) 과 험프리스 (Hum p hre y s) 는 포배의 DNA 로부 터 Cot의 값이 200 이 상인 유일성 DNA 를 분리 하여 포배 에 서 추출한 nRNA 와 재 결합시 켰다. 이 때 유일성 DNA의 15% 가 nRNA 와 결합 하였다. 유사한 방법으로 동일한 유일성 DNA 를 풀루티우스 유생의 nRNA 와 결합시켰을 때에도 DNA 의 15% 가 nRNA 와 결합하였다. 이때, 15% 의 DNA 재결합은 이중나선인 DNA 의 한쪽 사슬만이 재 결합에 사용되었으므로 실제로 게놈의 30% 가 nRNA 로 전사하였음
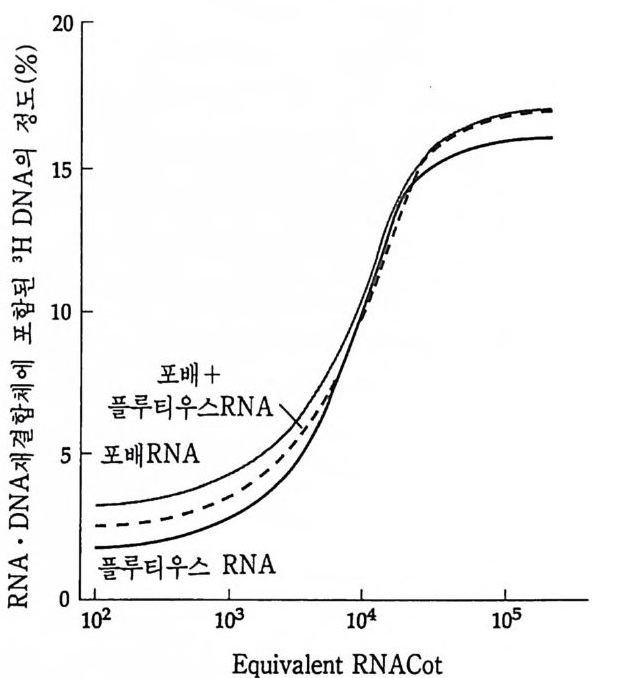 20
20
그림 7-3 유일성 3H-DNA 와 nRNA 의 재결합. 유일성 3H-DNA 와 포배 .RN A, RNA 혹은 포배와 플루티우스 RNA 의 혼합액을 섞어서 RNA 와 RNA 의 재결합을 유도한다 (Kleene and Hump hr eys , 1977).
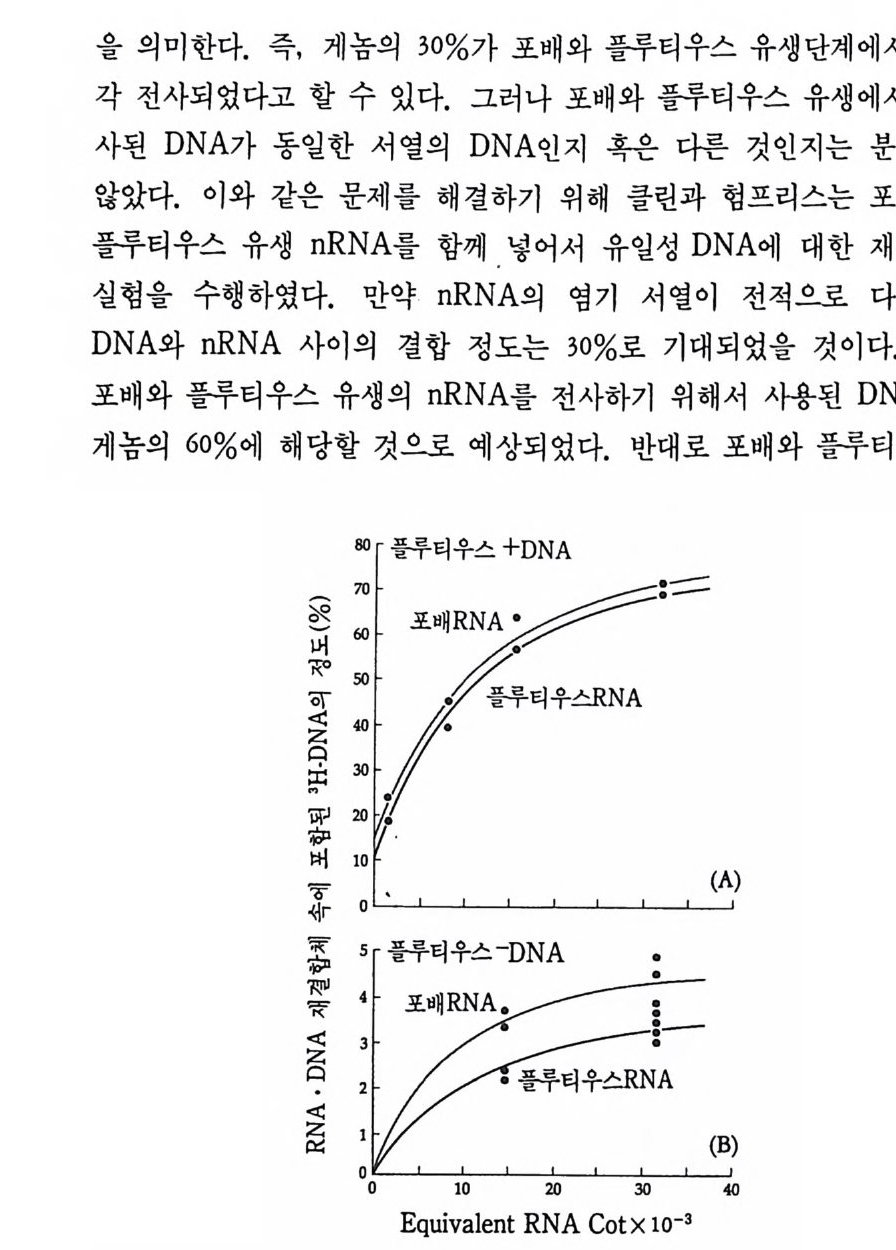 울 의미한다. 즉, 게놈의 30% 가 포배와 플루티우스 유생단계에서 각
울 의미한다. 즉, 게놈의 30% 가 포배와 플루티우스 유생단계에서 각
그림 7-4 플루티우스 +DNA 혹은 풀루티우스 -DNA 와 포배 및 플루티우스 RNA 와의 재결합. (A) 포배 및 플루티우스 RNA 와 플루티우스 -DNA 의 결합 정도는 같다. {B) 두 종류의 RNA 중 어떤 것도 플루티우스 -DNA 와 결합하지 않는다 (Kleene and Hump hr eys , 1977).
유생의 nRNA 의 염기서열이 동일하다면 15% 의 결합 정도가 기대되 었다. 실험결과 결합 정도는 15 % 로 나타났다. 즉 포배와 플루티우스 유생의 nRNA 는 동일한 염기서열을 가진 DNA 로부터 전사된 RNA 임을 알 수 있었다. 이러한 예상 의의 결과를 확인하기 위하여 클린과 험프리스 (1977, 1985) 는 방사능 동위원소로 표지한 유일성 DNA 를 플루티우스유생나 포배의 nRNA 에 결합시키는데 높은 Co t값에 이르기까지 재결합 반 응을 진행시켰다. 즉 상보적인 RNA 가 하나도 남김없이 모두 DNA 에 결 합할 수 있도록 재결합 반응을 연장하였다. . 그 다음 포배의 nRNA 와 결 합하지 않은 DNA (blastu la -n u ll DNA) 와 플루티우스 유생 의 nRNA 와 결 합하지 않은 DNA (plu te u s-null DNA) 를 분리 하여 blastu l a-n u ll DNA 를 plu te u s nRNA 에 결 합 시 켜 보 거 나 혹 은 plu te u s-null DNA 를 blastu l a nRNA 에 결 합시 켜 보았다. 이 들 null DNA 와 nRNA 사이에는 전혀 결합이 일어나지 않았다. 이러한 관찰 로부터 포배기에 전사된 DNA 가 풀루티우스 유생시기에 전사된 DNA 와 동일하다는 점을 확인할 수 있었다. 그러나 성게의 난소, 난 모세포, 포배, 낭배, 플루티우스 유생, 성체의 관족, 장 및 체강세포 에 존재하는 mRNA 를 비교해 보면 mRNA 는 발생단계와 조직에 따 라 다름을 알 수 있다 (Galau et a l., 1 976). 난모세포에는 게놈의 4.5 % 혹은 37 X 106~ 기쌍의 유일성 DNA 로부터 전사된 RNA 가 있다. 이 RNA 는 모두가 mRNA 는 아니지만, mRNA 의 역할을 할 수 있는 RNA 로서 한 개의 mRNA 의 평균크기를 2000 개의 염기라고 할 때, 약 18,500 종류의 mRNA 를 만들 수 있는 유전정보에 해당한다. 포배 의 mRNA 는 게놈의 3 . 1% 의 DNA 로부터 전사된 RNA 로서 13,000 종 류의 mRNA 에 해당한다. 낭배의 mRNA 는 게놈의 2% 의 DNA 로부 터 전사된 RNA 로서 8,000 종류의 mRNA 에 해당한다. 접차 발생 이 진행되면서 성체의 조직은 6000 종류의 mRNA 죽 게놈의 0.75% 에 지나지 않은 DNA 로부터 전사된 mRNA 를 포함하고 있는 것으로 밝
혀졌다. 죽, 세포질내의 mRNA 로 발현되는 게놈의 양이 점차 감소 하는 경향울 보였다. 이러한 세포질내의 mRNA 의 양적 감소가 전사 과정에서의 조절에 기인한 것인지 혹은 p rocess i n g에서의 조절에 기인한 것인지 알아보 기 위해서 월드 (Wold, 1978) 등은 포배의 mDNA 를 이용하여 DNA -RNA 재결합 실험을 수행하였다. 먼저 포배의 mRNA 를 추출한 다 음 방사능 동위원소로 표지한 DNA 에 전합시켰다. 재결합된 DNA -RNA hyb r i d 를 변성시켜 DNA 만을 분리하였는데, 이 DNA 는 포배 에 있는 mRNA 에 상보적이기 때문에 포배의 mRNA 와 재결합시켰 을 경우 상당히 특이하게 결합하였다. 이 포배 특이 DNA 는 장 (i n t es ti ne) 의 mRNA 에는 겨우 10% 밖에 결합하지 못하지만, 포배의 mRNA 에 대해서는 78% 까지 결합하였다. 월드 등은 이러한 포배 특 이 mDNA 를 이용하여 다른 조직이나 세포속에 포배 특이 mRNA 와 동일한 mRNA 가 존재하는지 그리고 있다면 어느 정도나 있는지에 대하여 알아보았다. 포배 특이 mRNA 가 세 종류의 다른조직에서도
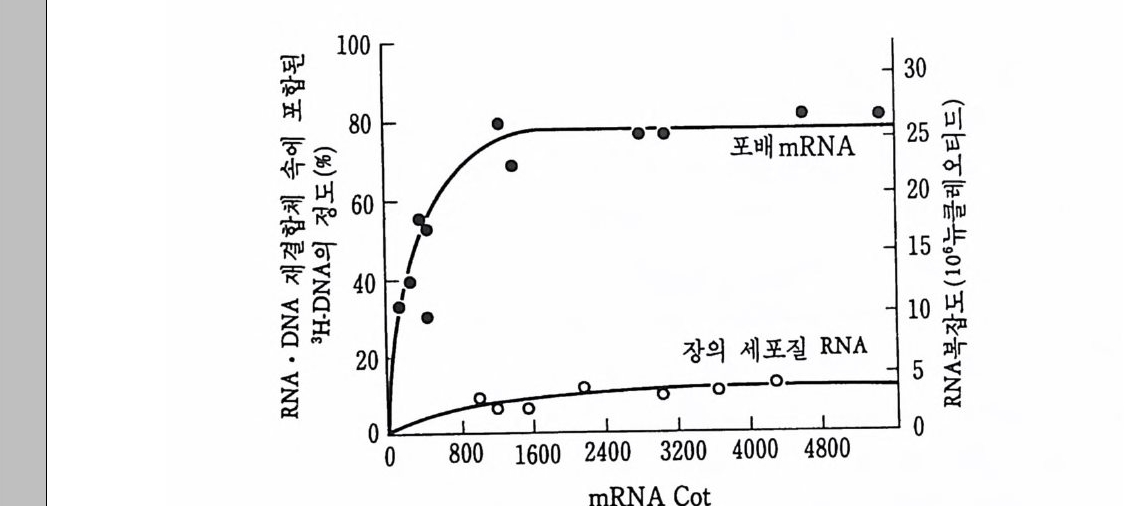 v{frl8EipFl止버=짜 • VQV N N >NGH'c (永버)혼이H 1 0820o0 ?6o 4o 포배 m•R NA • 302 5어버비F(牛守坤[h曲90[)vm 2 0151050
v{frl8EipFl止버=짜 • VQV N N >NGH'c (永버)혼이H 1 0820o0 ?6o 4o 포배 m•R NA • 302 5어버비F(牛守坤[h曲90[)vm 2 0151050
그립 혹7은-5 장성의게 세b포la질st u RlaN mAD 와N의A 의재 결특합이성 (.Wo lbdl aest tua ll.a , m19D78N).A 와 blastu la mRNA
검출되었다. 즉, 낭배 및 체강세포 등에서 추출한 nRNA 에 포배 특 이 mDNA 를 재결합시켰을 때 포배특이 mDNA 의 약 80% 가 nRNA 와 재결합하는 경향을 보였다. 그러나 장의 mRNA 에 결합하는 포배 특이 mDNA 는 10% 에 지나지 않았다. 이러한 결과는 대조군 즉 포 배특이 mDNA 와 포배의 mRNA 의 재결합 정도가 75~80% 에 지나 지 않는다는 점을 감안할 때 모든 포배의 mRNA 가 장세포, 체강세 포 및 낭배세포의 세포질 속에는 거의 결여되어 있지만 이들 세포의 핵 속에는 nRNA 의 형태로 거의 동일한 정도로 존재한다는 사실을 알 수 있었다. 분화된 체강 세포나 장 세포에서 포배 특유의 RNA 를 동일하게 전사한다는 사실로부터 실제로 단계 특이적 유전자 발현은 오히려 RNA p rocess i n g에서 일어나고 있음이 시사되었다. 더구나 쥐와 생쥐를 이용한 유사한 실험에서도 뇌, 간, 신장에서 nRNA 는 거의 동일한 것으로 밝혀졌다 (C hi kara i sh i et a l., 1978}. 생 쥐의 글로빈 mRNA 에 대한 cDNA 를 이용하여 같은 동물의 간, 뇌, 배양 세포 등에서 글로빈 mRNA 의 전구체의 존재를 확인할 수
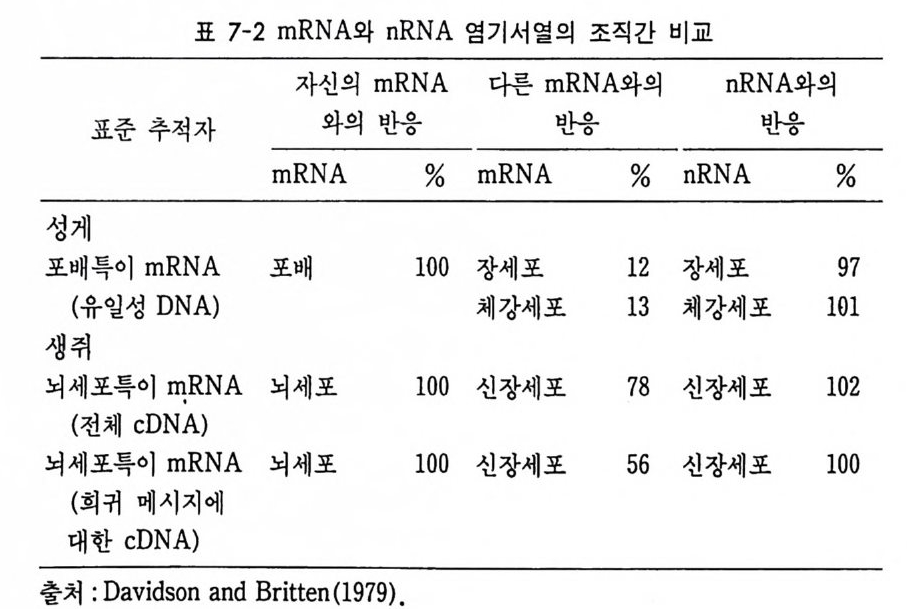 표 7-2 mRNA 와 nRNA 염기서열의 조직간 비교
표 7-2 mRNA 와 nRNA 염기서열의 조직간 비교
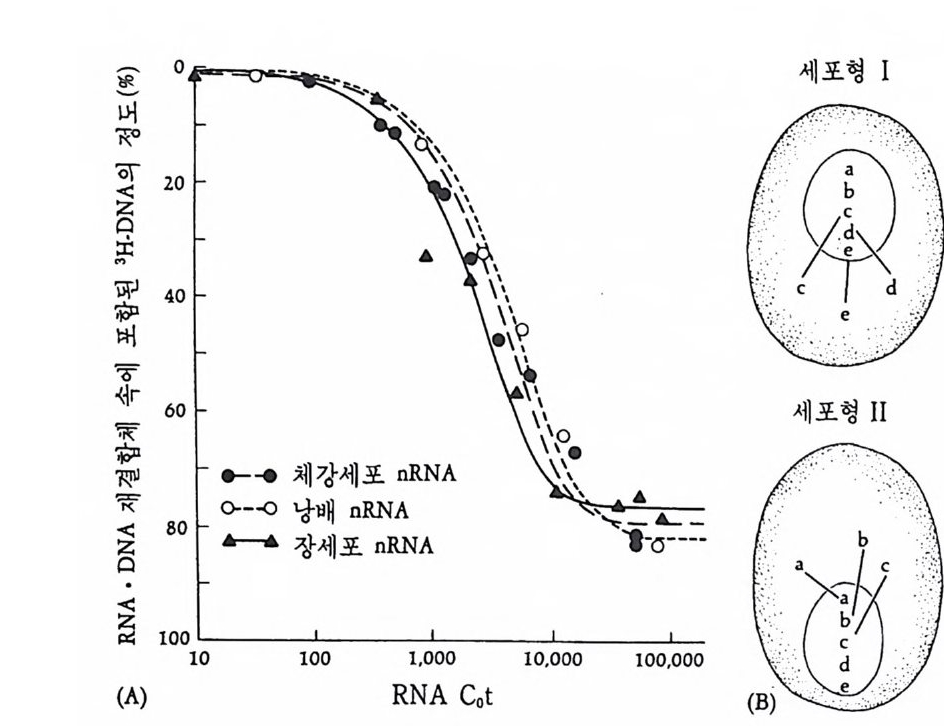 B1 0 , 00
B1 0 , 00
I 8���� II ���� 7-6 1���X� ��T�� p���(���8���, ��0�, �8����)��� �͜�\� nRNA X� ȴ�. (A) blas tula mDNA @� ��8���, ���8��� � ��0�X� nRNA @�X� �� ��i� (B) �(�� RNA p rocess ingD� $���XՔ� ���. P� ��X�X� 8��� ��P� ��� nRNA x� a, b, c, d, e �Ȭ����̹, 8���
� I ����� c, d, ̹et mR�NA 1����, 8���� Il ����a�, b c, t�̹ mRNA \ � ��1�� (Wold et al., 197)8 �.���� (Hum ph ries et al., 1976. )�, �t�@� �@� ���� �r F eind e ry ht-oerulemkia 8���X� nR NA ��� ����� Xenopus ����8����� � �� U�x�� ��� (Perlman et al., 1977 ; Gottes fe ld an dPar tin gt on, 9717 .) �� �� ��Lŀ��� �Ȑǔ� �� �� �ij� ����̹, t� �Ȑ�X� ���� �� �t� �Ŕ� �, ��|�, ̱, �¥� 8������L���ij
세포내에서의 바이러스 DNA 의 전사에 대한 관찰로부터 얻은 것이 다. 죽 pol yo m a 바이러스나 SV4o 바이러스는 세포에 감염되어 숙주 세포의 염색체에 조합되면 숙주세포의 DNA 가 전사할 때 함께 전사 되어 숙주세포의 핵 속에 바이러스의 RNA 가 존재한다. 이들 바이러 스 RNA 들도 숙주세포의 RNA 와 마찬가지 로 s p li c i n g을 거 쳐 성숙됨 으로써 숙주세포의 세포질 속에 바이러스 RNA 가 축적된다. 일반적 으로 분화되지 않은 t era t ocar ci noma 세포에 바이러스를 감염시킬지 라도 SV4o 와 pol yo m a 바이러스의 감염을 통한 유전자 발현은 일어 나지 않기 때문에 감영효과가 나타나지 않는다. 그러나 ter ato c ar- cino ma 세포를 분화시키면 이들 두 종류의 바이러스의 감영효과가 대단히 민감하게 일어난다. 이와 같이 분화되지 않은 ter ato c ar- cin o ma 세포에서 바이러스의 감염효과가 나타나지 않는 것은 RNA p rocess i n g의 결여에 기인하는 것으로 보였다. 즉 이것은 분화되지 않은 t era t ocar ci noma 세 포는 sv 40 의 RNA 를 s p l i ce 시 키 지 못하는 반면 분화된 세포는 s p li ce 시킬 수 있기 때문에 나타니는· 현상으로 생 각되 었다. 분화되 지 않은 ter ato c arcin o ma 세포에는 다량의 RNA 전구체가 nRNA 의 형태로 축적되어 있지만 결국 붕괴되어 버린다. 그러나 분화된 세포는 이러한 nRNA 가 세포질의 mRNA 로 성숙한다 (Seg al et a l., 1979) . 물론 유전자 발현을 위 하여 p rocess i n g을 필요로 하지 않는 바이러스는 분화되지 않은 세포나 분화된 세포 모두에서 성장할 수 있다. 이와 같이 분화된 세포에서만 s p l ici n g이 선택적으 로 가능하다는 사실은 순차적 유전자 발현이 spl icing enz ym e 의 발현 에 기인할 수도 있다는 생각을 강하게 암시하고 있다. 3 순차적 RNA pro cessin g 동일한 유전자로부터 전사된 전사체가 순차적 p rocess i n g을 거쳐 다양한 메시지의 역할을 한다. 가장 잘 연구된 순차적 RNA
p rocess i n g의 예는 B- 림프구 분화과정에서 나타나는 im munog - lobulin 죽 항체단백질 형성에 관한 것이다. 림프구의 분화과정에서 나 혹은 항원에 대한 반응으로 나타나는 전사 수준에서의 유전자 발 현은 유전자의 선택과 재배열 과정을 통하여 조절되기도 하지만 항체 유전자 발현은 RNA p rocess i n g에서도 조절된다. 일반적으로 B- 림프구는 항체 분비세포로 성숙하기 이전에 이미 이 세포가 앞으로 분비할 항체를 만들어 원형질막에 삽입시키고 있다. 여기에서 이들 항체는 일종의 항원 수용체로 작용한다. 항체 분화 단 계에 따라서나 혹은 항원에 림프구가 노출되었는지에 따라서 i rnmuno g lobul i n 은 l g M 이나 혹은 l g D 가 될 수 있다. 처음에는 모두 l g M 이 된다. 그러나 항원과 작용하여 반응을 일으킨 다음에는 lgM
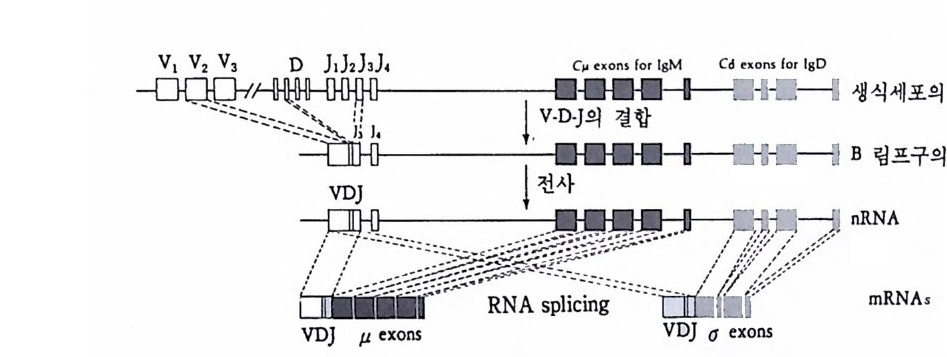 V, V, V, D JiJ,J , J , l C• uondodgM Cd «o ns f o 『 18D
V, V, V, D JiJ,J , J , l C• uondodgM Cd «o ns f o 『 18D
그림 7-7 B 림프구에서의 I g M 과 I g D 의 발현. 중사슬유전자는 림프구 분화중 V, D, J부위의 재배열에 의해서 만들어지지만, 이 유전자의 전사체가 µ 혹 은 8 고정부위 중 어느 것을 포함하느냐에 따라 IgM 혹은 I g D 가 된다 (L i u et al. , 1 980} .
과 l g D 가 동시에 생성되었다가 후에 l g D 만이 남게 된다. 이와 같은 현상은 RNA p rocess i n g에 기인한다. i mmuno g lobu li n 의 변이 부위 죽 항원 결합부위는 림프구나 그로부터 유래한 모든 딸 세포에서는 언제나 동일하지만 l g M과 l g D 사이의 sw it c hi n g이 RNA pro cessin g 에서 일어난다 (Mak i et a l., 19s1). RNA 전사체가 생성되면 이 전사
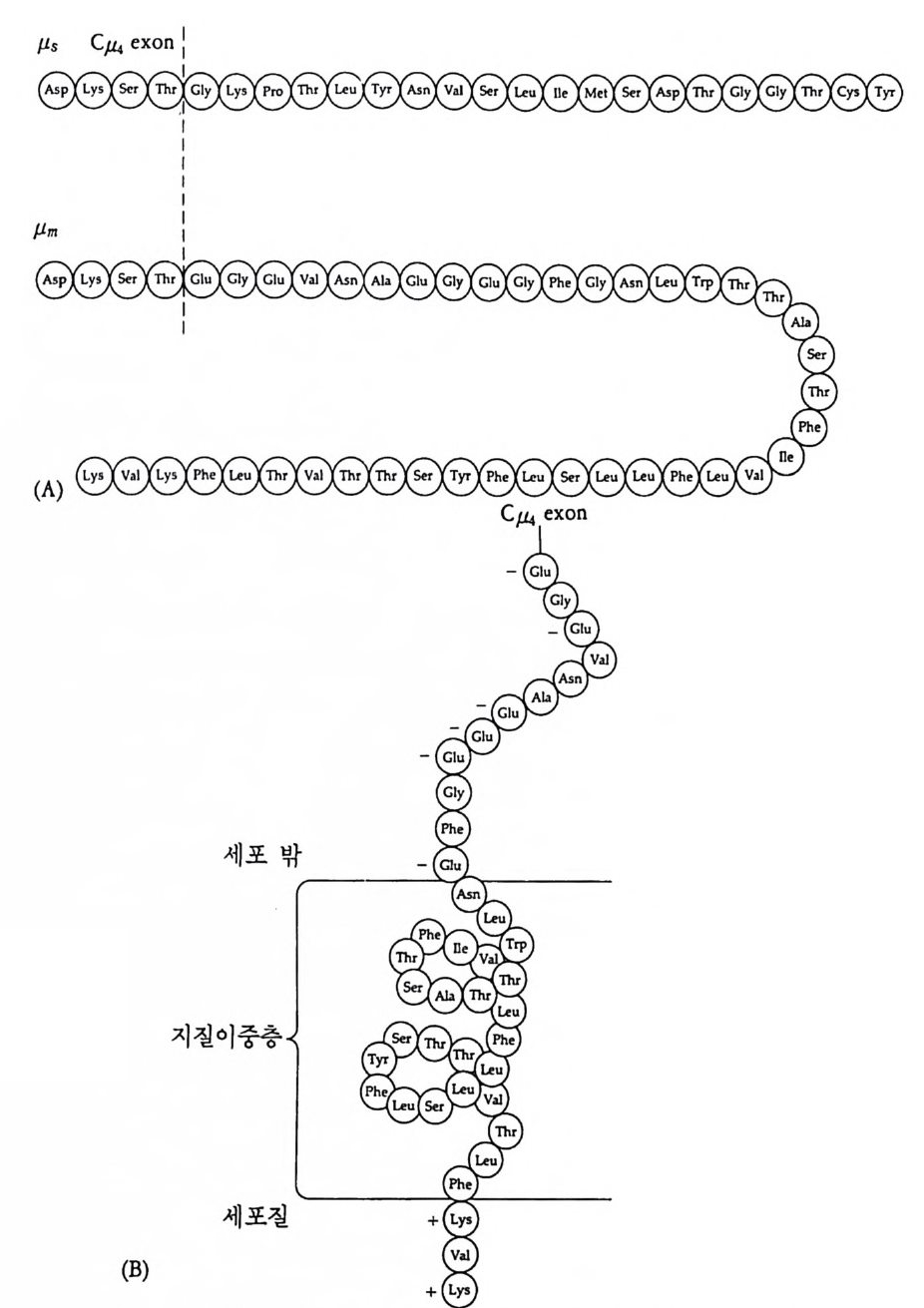 µsc山 m µex 。n ___ ____
µsc山 m µex 。n ___ ____
그림 7-8 I g M 의 막부착형 (m) 과 분비 형 (s) 의 카르복실기 말단 아미노산. (A) µs( 분비형)과 µm(막부착형)의 카르복실기 말단 (B) 막에 부착한 사슬 (Rog er s et al., 1980) ,
체에는 변이부위와 mu(lgM ) 및 delta ( IgD ) 고정부위를 지시하는 exon 과 여러 가지 i n tr on 이 있지만 세포질에 도달한 mRNA 는 IgM 혹은 lgD 중 하나롤 지시하는데, 이러한 지시 결정은 두 가지 spl ic ing enzy me 중 어 느 효소가 작용하였는지 에 달려 있다. 만약 delta ( o) exon 이 s p l ici n g에 의해 제거되면 I g M 이 만들어지며, 만약 mu(µ) exon 이 s p l ici n g에 의해 제거되면 I g D 가 만들어진다. 이와 같이 lgM 혹은 I g D 로의 결정뿐만 아니라, 이들 단백질이 원형질막 에 삽입될 것인지 혹은 분비될 것인지에 대한 결정도 RNA p rocess i n g중에 이루어진다.
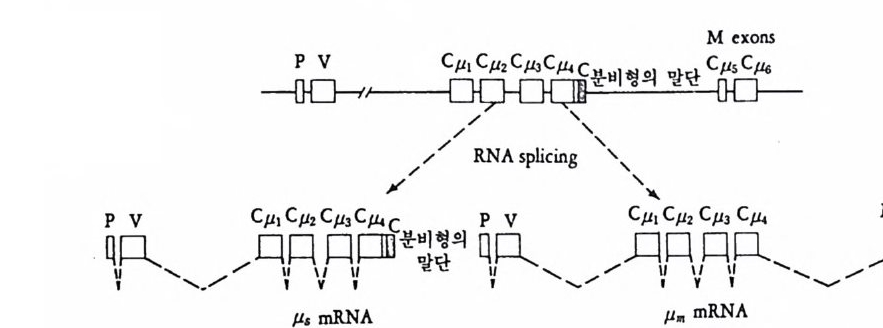 M cxons
M cxons
그림 7-9 분비 형 µs 과 막부착형 µ.m mRNA 의 spl i ci n g 양상. s p l i ce 된 부분은 접선으로 표시됨 (Early et al., 19ao).
l g D 는 주로 세포막에만 분포되어 있다. 혈청 속에 있는 l g D 는 우 연히 유출된 것이거나 혹은 세포사(細胞死)로부터 유래한 것이다. 그 러나 l g M은 결합형 (ml g M) 과 분비형 (slgM ) 두 개의 유형으로 존재 한다. 결합형 l g M 은 항원 수용체로 작용하는 반면에 분비형 l g M 은 그 생물체가 항원에 노출되었을 때 처음으로 혈액 속에 나타나는 항 체 이다. sl g M 과 mlgM 사이에는 카르복시 말단 부위 에 약간의 차이 가 있다 (S ing er et al., 19so) . ml g M 단백 질은 꼬리부분이 카르복시 말 단 부위가 소수성인 아미노산으로 구성되어 있기 때문에 막 속에 쉽
게 삽입될 수 있다. sl g M 과 ml g M 의 mRNA 는 서로 다르다. 즉, 같은 Cµ 유전자로부터 전사될 때에는 동일한 nRNA로 전사되지만 p rocess i n g에서 다르게 성숙된다 (Ro g ers et a l., 1980 ; Early et a l., 1980 ; Alt et a l., 1980) . sl g M 은 VD J유전자와 Cµi, Cµ2, Cµ3 및 c /J.I로부터 지시된 아미노산으로 구성되어 있으며 분비형의 말단부위를 가지고 있다. ml g M 은 말단 부위를 제의한 모든 구성이 sl g M 과 동일하다. 즉, sl g M 의 말단은 두 개의 G 와 C&. 부터 지시 된 아미노산들로 구 성되어 있는데, 이들 아미노산들이 소수성을 띠고 있기 때문에 림프 구의 세포막 속으로 쉽게 삽입될 수 있다. 이와 같이 slgM 혹은 mig M 의 결정은 오히려 p rocess i n g의 하나인 s p l ici n g에 의해서 이루 어전다고 할 수 있다. 항체 형성과정에서 순차적 RNA p rocess i n g이 중요한 역할을 하는 또 하나의 단계로서 allelic exclus i on 이 있다. 죽 B 림프구에 존재하는 항체가 상동 염색체 중 한쪽 염색체에 있는 항체 유전자로부터 유래하는 현상이다. 이러한 현상을 allelic exclus i on 이 라고 하는데 , allelic exclusio n £ RNA p rocess i ng 에 기 인하는 것으로 생각되고 있다. 양쪽 상동 염색체에 있는 항체 대립 인자로부터 항체 RNA 가 모두 발현되지만 그 중 한 종류는 특이한 p rocess i n g을 통해서 항체 mRNA 로 성숙되고 다른 하나는 성숙되지 못하기 때문에 결국 단백질 형태로 표현되지 못한다. 순차적 RNA p rocess i n g에 의한 유전자 발현의 조절과 관련하여 im munog lo buli n 유전자 발현에 대한 것 이의에도 50 종 이상의 단백 질의 유전자에 대하여 관찰된 바 있다 (Bre i ba rt et a l., 1987). 어떤 경 우에는 세포의 종류에 따라 다른 단백질의 합성이 RNA s plici n g에 의해서만 지배받는 경우를 볼 수 있었다. 갑상선 세포에서 calc it o ni n 의 mRNll 성숙하는 RNA 가 신경세포에서는 neurope p- ti de 의 일종인 CGRP 로 성숙되는 경우를 찾아볼 수 있다 (Amara et al., 1952 ; Crenshaw et a l., 1987). 즉, 동일한 전사체가 spl i ci n g 부위의 차이에 따라 신경세포에서는 P 물질 그리고 갑상선 세포에서는 K 물질
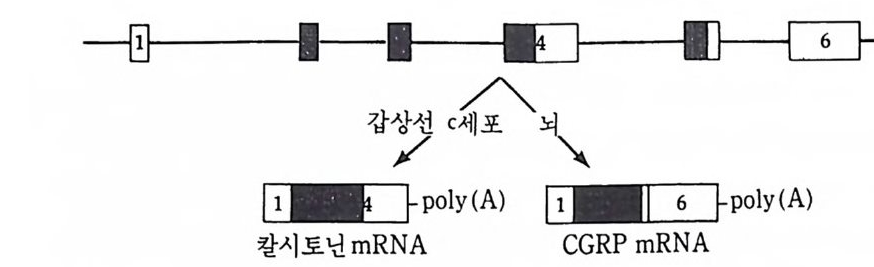 뺑 I
뺑 I
그림 7-10 s plici n g과정의 차이에 따라 다르게 구현되 는 mRNA 갑상 선 c 세포 에서는 exon 1, 2, 3, 4 가 calcit on in mRNA 를 만드는 데 이용되고 , 뇌 세 포에 서는 exon 1, 2, 3, 4, 5, 6 이 CGRP mRNA 를 만드 는 데 사용된다 ( Cren s haw et a l., 1987) .
로 발현된다. 이러한 현상은 세포 특유의 spl ic i n g 조절 요인에 기인 하는 것으로 생 각되 는데 , 이 러 한 관찰로부터 RNA p rocess i n g에 의 해 세포 특이 단백질이 생성될 수 있는 가능성이 짐작되었다. 유사한 방법으로 한 종류의 fibr onecti n 유전자로부터 5 종류의 다 른 fi bronec ti n 단백질의 생성아 가능한 것으로 관찰되었다. 즉 다양 한 형 태 의 fi bronec ti n 이 fibr onecti n mRNA 전구체 가 다르게 spl i ce 됨으로써 생긴 mRNA 에서 생성된다 (Tamkune t a l., 1984; H y ne s, 1987). 동일한 mRNA 전구체를 다르게 s pli ce 시킴으로써 여러 가지 형태의 신경 세포 응집분자 (NCAM) (Cu nning h a m et a l., 1987) 와 태아 형과 성체 형의 미오신 단백질이 생성된다 (Nabesh i ma et al., 1984 ; Rozek and Davi ds on, 1986) . 이 와 같이 한 종류의 유전자로부터 다양 한 형태의 mRNA 가 s plici n g의 차이에 의해서 생성될 수 있다. 만약 동일한 mRNA 의 전구체가 세포의 종류에 따라서 다르게 pro cessin g 됨으로써 다양한 mRNA 가 생성된다면, 세포 종류에 따라 특이하게 존재하는 세포 특유의 p rocess i n g요인이 대단히 다양할 것으로 기대 되 었다• 브라이바트 (Breib a rt ) 와 나달-지 나드 (Nadal-Gin a rd, 1987) 는 이러한 p rocess i n g요인을 간접적으로 관찰하였다. 근 세포 특유의 단
백질인 tro p on in T 의 mRNA 는 특정된 exon 을 s p l i c i n g시킴으로써 생 성 되 는데 , 이 렇 게 정 확한 p rocess i n g은 근세 포 특이 p rocess i n g요 인에 의해서만 수행되는 것으로 관찰되고 있다. tro p on in T mRNA 의 p rocess i n g은 근세포에서만 가능할 뿐, 비근세포나 혹은 단핵 근 원세포 (m y oblas t)에서는 일어나지 않고 단지 다핵의 근세포에서만 일 어난다. 4 RNA process i n g과 성 결정 최근의 연구보고에 따르면 순차적 RNA p rocess i n g이 초파리에서 성결정과 밀접한 관계가 있다고 한다 (Baker et a l., 1987 ; Bog gs et a l., 1987). 초파리에서 성의 분화는 X 염색체와 상영색체의 비를 수컷의 것이나 혹은 암컷의 것으로 전환시키는 일련의 유전자에 의해 중개된 다. 이러한 유전자 중 하나로서 성전환 유전자(tr ans fo rmer) 가 있다. 성전환 유전자는 암컷을 생성하는 데 필수적인데, 만약 이 유전자가 결여되면 염색체의 비에 관계없이 수컷울 생성하게 된다•유충기를 통 해서 성전환 유전자는 암수에 상관없이 여러 가지 형태의 mRNA 로 성숙될 수 있는 전사체를 합성한다. 그러나 암컷에서만은 이 전사체 가 특별한 형태로 s pli c i n g되어 mRNA 를 만들어내는데, 이 mRNA 만이 성전환 유전자로부터 성전환을 위해서 만들어질 수 있는 유일한 메시지이다. 수컷과 암컷 모두에서 발견되는 일반적인 mRNA 는 두 번째 exon 에 정지 코돈인 UGA 를 가지고 있다. 그러나 암컷 특이 메시지에서는 UGA 가 int r o n 속에 있기 때문에 그 메시지를 해독하 는데 문제가 되지 않는다. 그러한 mRNA 에 의해서 지시된 단백질은 196 개의 아미노산으로 이루어진 ar gini ne 이 풍부한 단백질이다. 초파리의 성결정 과정에서 성전환 유전자는 doublesex 라는 유전자 의 발현을 조절하는 것으로 생각되고 있다. 이 유전자는 암컷이나 수 컷 어느 쪽의 것이든지 성칭을 형성하는 데 필요하며, 만약
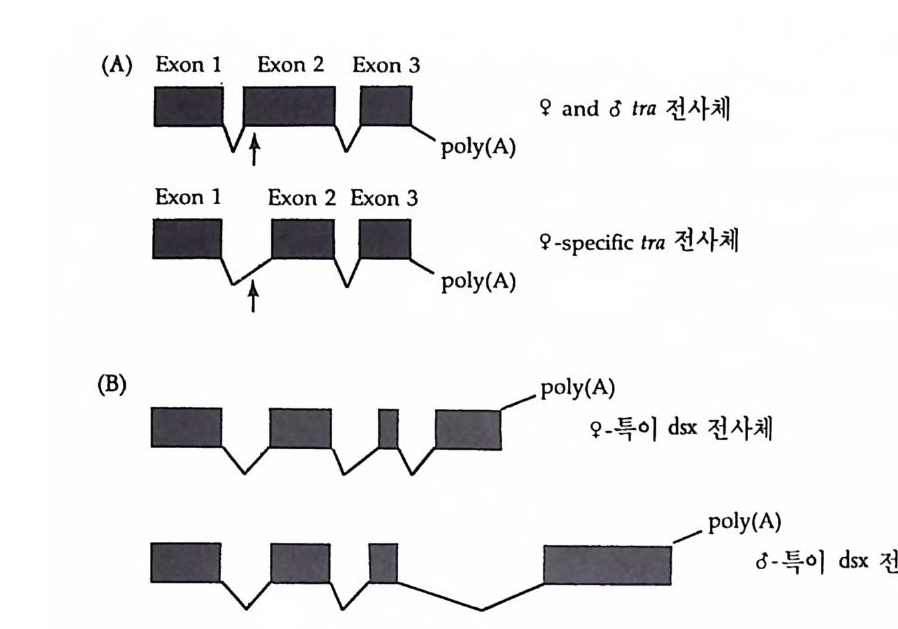 (A) ~Ex on 1 Exon 2 Exon 3 pol y( A ) 9 and o tra 전사체
(A) ~Ex on 1 Exon 2 Exon 3 pol y( A ) 9 and o tra 전사체
그림 7-11 초파리 발생에 따른 성 특이 전사체의 생성. (A) s p l i c i n g과정 의 차이 에 따라 tr ans fo rmer 유전자로부터 생 성 된 암컷 특 이 및 일반적 전사체. 화살표는 UGA 정지 코돈을 지시하는데, 암컷 특이 전사체에서는 정지코돈이 exon 안에 있지 않고, i n t ron 에 있다. (B) doublesex 유전자에서의 RNA s p l i c i n g과정. doublesex 유전자도 tr a 와 tra- 2 유전자의 활성여부에 따라 수컷 특이 혹은 암컷 특이 전사체를 합성한다 (A : Bogg s et a l., 1987 ; B : Baker et al., 1987) .
doublesex 에 돌연변이가 일어나면 정소와 난소의 형성이 억제된다. 번데기 시기에 doublesex 는 두 가지 다론 형태로 성숙될 수 있는 전 사체를 만드는데, 이 전사체는 p rocess i n g에 따라서 암컷 특이 mRNA 나 혹은 수컷 특이 mRNA 로 성숙될 수 있다 (Baker et al., 1987). 암컷과 수컷에서 처음 세 개의 exon 은 동일하지만 네번째 exon 은 다르댜 즉, 수컷 특이 RNA 에는 암컷 특이 exon 을 포함하 고 있는 RNA 전구체가 결여되어 있다. 베 이 커 (Baker) 등은 doublesex 유전자보다 먼저 작용하는 성 결정 유전자는 RNA 전구체를 암컷 특이 mRNA 로 성숙시키는 요인을 생
성할 것이라고 생각하고 있다. 만약 doublesex 유전자에 작용하는 유전 자(tr ans fo rmer 와 tran sfo rm er 2) 가 돌연변이와 같은 사건에 의해 결손 되면 doublesex 전사체는 수컷 특이 mRNA 로 성숙되어 수컷이 생성 된다. 만약 이러한 가설이 옳다면, 순차적 p rocess i n g은 발생조절에 엄청난 역할을 할 것이라고 생각된다. 그러나 순차적 p rocess i n g을 조절하는 요인은 무엇이며 어떠한 과정에 의해서 생성되는 것일까? 이러한 요인들이 단백질이라면 이러한 단백질 요인을 단계 특이적으 로나 조직 특이적으로 생성하는 대에는 어떤 특별한 과정이 필요할 까? 5 3' 말단의 결정 r i bonucleo p ro t e i n 복합체는 mRNA 의 전구체가 3' 말단에서 분리된 다음 p ol y ade ni ne 꼬리의 부착 위치결정에 중요한 역할을 한다. 최초 의 RNA 전사체는 메시지의 말단이 될 부분보다 훨씬 더 긴 3' t ra i ler 부위를 가지고 있다. t ra i ler 부위에는 AAUAAA 영기서열이 있는데, 이 염기서열은 이 부위에서 하위로 10~30 염기 떨어진 위치 에 자리하고 있는 메시지를 분리시키는 데 대단히 중요한 역할을 한 다. (Proud foo t and Brownlee, 1976). 만약 AAUAAA 에 돌연변이가 일 어나면 mRNA 의 3' 말단 형성은 억제된다 (W i ckens and Ste p h e nson, 1984 ; Orkin et a l., 1985). 사람의 f3―글로빈유전자에서 AAUAAA 부위 에 돌연변이가 일어나서 AACAAA 가 되면, 새로운 RNA 의 3' 말단은 정상적인 pol y (A ) 첨가 부위에서 하위로 900 염기 떨어진 부위에, 죽 이 유전자의 3' 쪽에 자리하고 있는 AATAAA 에서 15 개 염기 떨어진 부위 에 그 위치를 정한다. 이 러한 3' 말단 분리 와 p ol y adn y la ti on 은 spl icin g 이전에 이루어진다. 그래서 s plici n g은 p ol y aden y la t e 된 mRNA 전구체에서 일어난다. 더구나, pol y( A ) 첨가 부위가 달라질
수 있는데, 다른 형태의 pol y (A ) 부위 선택이 어떻게 조절되는지 아 직 확실치 않다. snRNP(small nuclear ri bonucleo p ro t e i ns) 가 이 p ol y (A) 부위를 인식 하는데 개입되는 것으로 알려져 있다. snRNP 에 대한 항체는 AAUAAA 를 포함하는 RNA 토막을 침 전시 키 며 (Hashi m oto and Ste itz, 19s6), U7RNP 가 성게의 히스돈 H3 mRNA 전구체를 3' 말단에 서 s p l i ce 하는 데 필요한 것으로 알려지고 있다 (S tru b and Bim stie l, 1987). 그러나 아직도 RNA 전구체가 어떻게 s p li ce 되고 p ol y (A) 꼬리 가 어떻게 붙는지는 쉽게 설명되지 않는다. 어떤 때에는 전사가 미숙한 상태로 끝나기 때문에 전사체가 pol y (A) 꼬리를 수용하지 못하는 경우가 있다. 이와 갇이 결손이 있는 메 시지는 곧 붕괴되어 버린다. 최소한도 세포 증식을 조절하는 데에는 두 가지 단백질이 관여하는 것으로 나타난다. 이들 단백질에 대한 유 전자는 증식하지 않는 세포에서는 일단 전사까지는 일어나지만 그 전 사체가 완성되지는 않는다. 그러나 증식하고 있는 세포에서는 완전한 RNA 가 만들어 진다 (Ben t le y and Groudin e , 1987 ; Bender et a l., 1987). 이러한 경우 첫번째 exon 의 3' 말단 주변에서 돌연변이가 일어나면 미숙한 전사체를 만들던 세포에서 전사체가 완전한 상태로 전사된다 (Cesarman et a l., 1987) . 참고문헌 Adamson, S.D., Y au, P.M.P., H erbert , E. and Zucker, W.V. (1972) . Involvement of hem in, a stim ulato r y frac ti on from rib o somes, and a pro te i n syn the sis inhibi t or in the regu la ti on of hemog lo bin syn -
the sis. ]. Mot. Bio l. 6 3: 247-264. Albert , B., B ray, D ., Lewi s, J., Raff , M., Robert s, L. and Wats o n, J.D . (1983) . Molecular Bio lo g y of the Cell. G arland Publish i ng , New York. Akhaya t , 0., de Sa, F.G . and Inf an te , A.A . (1987) . Sea urchin pro some: Characte r iz a ti on and change s durin g develop m ent. Proc. Natl. Acad. Sci . USA 84: 1595- 15 99. Ang e rer, L.M . and Ang e rer, R.C. (1981) . Dete c ti on of pol y A+ RNA in sea urchin egg s and embryo s by qua nti tat i ve in situ hyb r id i z a - tion . Nucleic Acid s Res. 9: 2819-2840. Audet, R. G., Goodchil d , J. and Rich te r . J.D . (1987). Eukary ot ic ini t iat i on fac to r 4A stim ulate s tra slati on in micr oin j e c te d Xenop u s oocyt es . Dev. Bio l. 121: 58-68. Bachmair , A ., Fin l ey , D . and Varshausky, A. (1986) . In vivo half- l ife of a pro te i n is a fun ct ion of its a m ino te r mi na l resid u e. Scie n ce 234: 179- 18 6. Brig gs, R. and Cassens, G. (1966) . Accumulati on in the oocyt e nucleus of a gen e pro duct essenti al for embry on i c develop m ent beyo n d ga str u lati on . Proc. Natl. Acad. Sci . USA 55: 1103-1109. Broth e rs, A.J. (1979) . A spe c if ic case of gen eti c contr ol of early develop m ent: The o mate r nal eff ec t muta tion of the Mexic a n ax ol otl . In S. Subte l ny and LR . Kon igsb erg ( eds) ., D ete r mi na nts of Spa t ia l Orga n iz a ti on . Academ ic Press, New York, pp. 167-184. Carroll, C.R. (1974) . Comp ar ati ve stu d y of the early embry on i c cyt olo g y and nucleic acid syn the sis . of Amb ys to m a m 函 can u m normal and o muta n t embry os . J Exp. Zoo!. 187: 409-422. Chen, S-H. and 12 oth e rs. ( 1987) . Ap ol ip o pr o te i n B48 is the pro duct of a messenge r RNA wit h an orga nspe c if ic in- fr am e sto p codon.
Sci en ce 238: 363-366. Clemens, M. J., Henshaw. E.C., Raha mino ff , H. and London, I.M . (1974). Met- t R N Armet bin d i ng to 40 S rib o somal units: A site for the regu la ti on of initiat i on of pro te i n syn the sis by hern in. Proc. Natl. Acad. Sci . USA 71: 2946- 29 50. Coli n, A.M ., Brown, B.D ., Dholakia , J.N . , Woodley, C.L., Wahba, A. J. and Hil le, M.B . (1987). Ev ide nce for sim ult an eous derepr e ssio n of messeng er RNA and the gua nin e nucleoti de exchange fac to r in fer t iliz e d sea urch in egg s. Dev. Bio l. 123: 354- 36 3. Dan ilch ik, M.V., Yablonka-Reuveni z, Z., Moon, R.T ., Reed, S.K . and Hil lew , M.B. (1986) . Sep a rate rib o somal poo ls in sea urch in em- bry os : Ammon ia acti va te s a movement betw een po ols. Bio c hemis - try 25: 3696-3702. Davey, J., Dim mock, N.J . and Colman, A. (1985) . Identi fica ti on of the sequ ence respo n sib l e for the nuclear accumulati on of the influe nza viru s nucleop ro te i n in Xenop us oocyt es . Cell 40: 667-675. Davi ds on, E.H . (1986) . Gene Acti vit y in &rly D evelop m e nt , 3rd Ed. Academ ic Press, New York, pp. 69-173. Davi ds on, J.M . and Berg. R.H . (1981) . Postt ra nslati on al events in collage n bio s yn the sis : In A.R. Hand and C. Oliv e r (eds.) , Meth o ds in Cell Bio lo gy , Vol. 23. Academ ic Press, New York, pp. 119- 13 6. Davi ds on, E.H., and Houg h, B.R. (1971) . Geneti c infor mati on in oocy te RNA. J Mal. Bio l. 56, 491 . Davi ds on, E.H . (1976) . Gene Ac tivity in Early Develop m ent, 2nd ed. Academ ic Press. New York. Davi s, F.C. , Jr. (1975) . Un iqu e sequ e nce DNA tran scri pts . pr esent in matu re oocyt es of Urechis caup o . Bio c him . Bio p h y s . Acta 390, 33. Deleon, C.V., Cox, K.H . Ang er er, L.M . and Ang er er, R.C. (1983) .
Most e arly varia n t histo n e mRNA is c onta ine d in the pro nucleus of sea urchi n egg s. Dev. Bio l. 1 00: 197~ 2 06. Denny , P.C. and Ty le r, A. (1964) . Acti va ti on of pro te i n syn the sis i n non-nucleate f rag m e nts of sea urchi n egg s. Bio c hem. Bio p h y s . Res. Commun. 145: 245- 2 49. de Sa, C .M ., de Sa, M. -F. G., A khaya t , 0 ., Broders, F., Scherrer, K., Horsch, A. and Schmi d, H. -P. (1986) . Prosomes: Ub iq떠ty and int r a spe c ie s stru c tur al vari at i on . ] . Mol. Bio l. 187: 479-493. Dic k erson, R.E . and Geis , I. (1983) . Hemog lo bin . Benja m in/ Cum- min g s , Menlo Park, CA. Ding w a ll, C., Sharnic k, S.V . and Laskey, R.A . (1982) . A pol yp e pt ide domain tha t s pe c if ies mig rat i on of nucleop la sm in int o the nucleus. Cel l 30: 44 9- 4 58. Duncan, R.F . ( 1978) . Mate r nal messeng er RNA in sea unch in egg s and embry o s. P h. D. Theis, Un iv. of Hawaii, Honolulu. Ecker, R .E. and Smi th, L.D . (1971). The natu r e and fate of Rana pipien s pro te i n s syn the siz e d durin g matu r ati on and early c leavage . De v. Bio l. 24: 559- 5 76. Evans, T., R osenth a l, E., Young bl om, J., Diste l , D. and Hunt, T. (1983) . Cyc l in : A pro te i n spe cified by mate r nal nRNA in sea urchi n egg s tha t is d estr o y ed at each cleavage divisio n . Cell 33: 389-396. Fil ip o wi cz , W., Sie r ra, J.J. and Ochoa, S. (1975) . Polyp eptide chain initiat i on in eukary o te s : I ni tiat i on factor MP in Ar tem i a salina embry o s. Proc. Natl . A cad. Sci. USA 72: 3947- 3 951 . Fri tz, P.L, Vesell, E., White, E.L. and Pruit, K .M . (1969) . Roles of syn the sis and deg rad ati on in dete r m ining tiss ue concentr at i on of LDH- 5. Proc. Natl. Acad. Sci. USA 62: 558-565. Galau, G., Keli n, W.H., Davi s, M.M., Wold, B., Bri tten , R.J. and
Davi ds on, E.H. (1976) . Str u ctu r al gen e sets acti ve in embry o s and adult t iss ues of the sea urchin . Cell 7: 487-505. Grace, M., Bagc h i , M., Ahina d, F., Yeage r , T., Olson, C., Cha- kravart y, I., Nasron, N., Banerje e , A. and Gup ta, N.K. (1984) . Prote i n syn the sis in rabbit reti cu locyt es : Characte r ist ic s of the pro te i n fac to r RF tha t reverses inh ib i t ion of pro te i n syn the sis in heme-defic ien t reti cu locyt e lys a te s . Proc. Natl. Acad. Sci. USA 79: 6517-6521 . Grib b le, T.J. and Schwart z, H.C. (1965) . Eff ec t of pro to p o rph yr in on hemog lo bin syn the sis . Bio c him . Bio p h y s . Acta 103: 333-338. Gross, K.W ., Jac olbs-Lorena, M., Bag lion i, G. and Gross, P.R. (1973) . Cell-fr ee tra nslati on of mate r nal messeng er RNA from sea urchi n egg s. Proc. Natl. Acad. Sci. USA 70: 2614-2618. Gross, M., Redman, R. and Kapl a nsky, D.A. (1985) . E 어 dence tha t t he prim ary eff ec ts of p h osph ory la ti on of eukary ot ic initiat i on factor 2 (a) in rabbit reti cu locy te lys a te is inh ib i t ion of the release of eukary o ti c i nitiat i on fac to r 2-GDP from 60 S rib o somal subunit s. ] . Bio l. Chem. 260: 9491-9500. Gross, P.R. •a nd Cousin e au, G.H. (1964) . Macromolecular syn the sis and the influe nce of acti on omy ci n Don early develop m ent. Exp. Cell Res. 33: 368-395. Guy et t e, W.A., Matu s ik , R.J. and Rosen, J.M . (1979) . Prolacti n -medi at e d tran scrip tion al and po st- tran -scrip tion al contr o l of casein gen e exp re ssio n . Cell 17: 1013-1023. Hall, M.N., Herefo rd , L. and Herskowi tz, I. (1984) . Targe t i ng of E. coli / 3-gla cto s id a se to the nucleus in yea st. Cell 36: 1057-1065. Ha rris, H. (1975) . Pri nc i ple s of Human Bio c hemi ca l Geneti cs. El- sevi er Nort h-H olland, New York.
Hart l, F . -U., Sch midt , B., Wachte r , E., and Neup ert, W. (1986) . Transpo r t int o mit oc hondria and int r a mi toc hondria l sort ing of the Fe/S pro te i n of u biq u in o lcyt oc hrome c reducta s e. Cell 47: 939-951 . Harvey, E.B . (1940) . A comp ar iso n of the develop m ent of nucleate and non-nucleate egg s of Arbacia pun ctu l ata . Bio l. Bull. 79: 166 -187. Herbert, E., P hil li p s, M. and Budarf . M. (1981) . Glyc o syl a ti on ste p s inv olved in pro cessin g of pro -cort ico tr o p in- endorp h in in mouse pitui t ar y tum or cells. Meth o ds Cell Bio l. 23: 101-118. Hil le, M.B., D anil ch ik , M.V., Colin , A.M . and Moon, R.T . (1985) . Translati on al contr o l in echin o id egg s and early embry os . In R.H. Saw ye r and R.M . Showman (eds.) , The Cellular and Molecular Bio lo gy of Invert eb rate D evel op me nt. Univ e rsity of South Caroli na Press, pp. 91-124. Houg h -Evans, B.R ., Wold, B.J., Ernst, S.G., Britt en , R.J. and David - son, E.H . (1977) . Ap pe arance and per sis t e n ce of mate r nal RNA sequ ences in sea urchin developm ent. Dev. Bio l. 260: 258-27 7. Houg h- E v ans, B.R . , E rnst, S.G., Britt en , R.J. , and Dav ids on, E.H . (1 979) . RNA comp le xit y in develop ing sea urchi n oocyt es . Dev. Bio l. 69, 258. Houg h -Evans, B.R., Jac ob~-Lorena, M., Cu mming s , M.R ., Brit ten , R. J., and David s on, E.H . (1980). Comp le x ity of RNA in egg s of Drosop hi la melanoga s te r and Musca domesti ca. Geneti cs 95, 81. Hump hr eys , T. ( 1971 ) . fy!ea surements of messeng er RNA ente r in g pol ys o mes upo n fer t iliz a don in sea urchi ns . Dev. Bio l. 26: 201-2os. Hu rt, E.C. and van Loon, A.P. G.M. (1986). How pro te i n s find mito- chondria and int r amitoc :1 0 ndria l comp ar t me nt. Trends Bioc hem. Sci . 11: 204-207.
Infan te , A. and Nemer, M. (1968) . Hete r og en eous RNP par t icle s in the cyt op l a sm of sea urchi n embry o s. J Mol. Bio l. 32: 543-565. Itoh, N. and Okamoto , H. (1980) . Translati on al contr ol of pro in s ulin syn thes is by glu cose. Natu r e 283: 100-102. Jac obson, A. and Favreau, M. (1983) . Possib l e inv olvement of pol y (A) in pro te i n syn the sis. Nuc[ 或 Ac ids Res. 11: 6353-6368. Kabat, D. and Chapp ell , M. R. (1977). Comp etition betw e en glo bin messenge r ribo nucleic acid s for a disc ri m in a ti ng ini t iat i on fac to r . J Bio l. Chem. 252: 2684- 2 690. Kalderon, D., Robert s, B.L. , Ric h ardson, W.D. and Sm ith, A.W . (1984) . A short amino acid sequ ence able to spe cify nuclear loca- tion . Cell 39: 499-509. Ka ribi a n , D. and London, I.M . (1965) . Contr o l of heme syn the sis by fee dback inhibi t ion . Bio c hem. Bio ph ys . Res. Commun. 18: 243- 2 49. Kaste m , W.H. , S w ind lehurst, M., Aaron, C., Hoop er , J. and Berr y, S. J. (1982) . Contr ol of m 만-.J' A tran slati on in oocy tes and develop ing embry os of g ian t moth s. I Functi on s of the 5' ter m ina l cap in the tob acco homworm Manduca sex ta. Dev. Bio l. 89: 437- 44 9. Kirsc hner, M. and Mitch i so n, T. (1986) . Beyo n d self-a s-sembly: From mi cro tub 며 es to moph o g en esis. Cell 45: 329-342. Kovesdi , I., and Sm ith, M.J. (1985) . Qu anti tative assessment of act in transcript number in eggs, embry os , and tub e fee t of the sea sta r Pisaster ochraceus, Mol. Cell. Bio l. 5, 3001 . Lee, Y.R., and Whitele y, A.H . (1984) . Gene tran scri ption dur ing oog en esis of Schi zo branchia insign is , a tub ic ul ous po lyc h aete . Forts ch r. mo!. 29, 167. Levi n, D., Ranu, R., Ernst, V. and London, I.M . (1976) . Regu lat i on of pro te in syn thes is i n reti cu locyt e lys a te s : Phosph o ry la ti on of meth -
ion y l- t R NAr , bin d ing fac to r by pro te i n kina se acti vity of tran s-lati on al inhibi t or iso late d from heme -de fi cien t lys a te s . Proc. Natl. Acad. Sc i. USA 73: 3112-3116. Lod ish , H.F. (1971). Alph a and beta glo bin messeng e r ribo nucleic acid . Di ffere nt amounts and rate s of tran slati on . ]. Bio l. Chem. 246: 7131- 71 38. London, I.M ., Clemens, M.J. , Ranu, R.S. , Levi n, D.H., Cherbas, L.F. and Ernst, V. (1976) . The role of he roin in the reg ulat i on of pro te i n syn t h e sis in ery throi d cells. Fed. Proc. 35: 221s-2222. Lop o, A.C., MacMi llan , S. and Hershey, J.W .B. (1988) . Translati on al contr ol in early sea urch in embry o ge nesis : Initiat i on fac to r eIF4F sti m ulate s pro te i n syn the sis in lys a te s from unfer t iliz e d eggs. of S. pur p u ratu s. Bio c hemi stry 21: 351-357. Lusis , A. J., T om ina , S. and Paig en , K. (1976) . Isolati on , characte r i - zati on , and rad ioi m munoassay of mu rine ega syn , a pro te i n sta b il iz- ing glu curon ida se membrane bin ding. J Bio l . C hem. 251: 7753-7760. Lusis , A.J. and Paig en , K. {1977) . Relati on sh ip betw e en levels of membrane -bo und glu curon ida se and the assoc iat e d pro te i n ega syn in mouse tiss ues. J Cell Bio l. 731: 728-735. Malaci ns ki, G.M. (1971) . Geneti c contr ol of qu a litative chang e s in pro te i n syn the sis du ring early amp hibi a n (Mex ica n axolotl ) em- bry o g en esis . Dev. Bi ol. 26: 442-4 5 1. Markert , C.L. {1968) . The molecular basis for iso z yme s. Ann. N. Y. Acad. Sci . 151: 14-40. Markert , C.L. and Urspr u ng, H. (1971) . DevelojJ mental Geneti cs. Prenti ce -H all, Eng le wood Clif fs, NJ . Meij link , F., Curran, T., Mille r, A. D. and Verma, J.M . {1985). Removal of a 67-base pair sequ ence in the non-co ding reg ion of
pro to o ncoge n e fos converts it to a tra nsfo n nin g gen e. Proc. Natl. Acad. Sci . USA 82: 4987-4991. Mermod, J.J., Schatz , G. and Crop pa , M. (1980). Sp ec if ic contr o l of messeng e r tra nslati on in Drosop hi l a oocy tes and embryo s . Dev. Bio l. 75: 177-186. Moon, R.T., Danil ch ik , M.V. and Hi lle, M. (1982}. An assessment of the masked messeng e r hyp o th e sis: Sea urch in egg megg e ng er rib o nucleopr o te i n comp le xes are eff ic:e n t tem p la te s for in vit ro pro te i n syn the sis . Dev. Bio l. 93: 389-403. Moon, R.T ., Nic o sia , R.F ., O lsen, C., Hi lle , M.B. and Jef f er y, W. R. (1983) , The cyt os keleta l fram ework of sea urchin egg s and em- bry os : Developm enta l chang es in the associa t i on of messeng er RNA . Dev. Bio l. 95: 447- 45 8. Mosto v , K.E., Breit feld , P. and Harris, J.M . (1987). An anchor-mi nu s form of po lym e ric im munog lo bin recep tor is secrete d pre domi - nantl y api ca lly in Mad in- Darby can ine kid n ey cells. ]. Cell Bio l . 105: 2031-2036. Pavlakis , G.N., Lockard, R.E ., Vamvakop ol ous, N., R ie s er, L., R ajB - handary , U.L. and Vournakis , J.N . (1980) . Secondary str u ctu r e of mouse and rabbit a-and /3-glo bin mRNAs: Differ enti al accessib i l- ity of initiat o r AUG codons tow ards nucleases. Cell 19: 91-102. Pelham, H.R .B. and Brown, D.D. (1980) . A spe c if ic tra nscrip tion fac to r tha t can bin d eith e r the 5 S RNA gen e or 5 S RNA. Proc. Natl. Acad. Sci . USA 77: 4170-4174. Pelleti er, J. and Sonenberg, N. (1985) . Insert ion al muta g e n esis to inc rease secondary stru c tu r e wit hin the 5'noncod ing reg ion of a eukary o tic mRNA reduces tran slati on al eff icien cy. Cell 40: 515 -5.26 .
Powell, L.M ., Wall is, S.C ., Pease, R.J. , Edwards, Y.H . , K nott , T.J . and Scott . J. (1 987) . A novel form of t iss ue-spe c if ic R NA pro cess- ing pro duces apo l ip o pr o te i n - B 4 8 in int e s tin e . Cell ·50: 831-840. Prockop, D.J ., Kiv irk ko, K.I., Tudeman, L. and Guzman, N.A . (1979) . The bio s yn the sis o f c ollage n and its d iso rders. N. En gl. ]. Med. 301: 13-23. Raff , R .A. (1980). Masked messeng er RNA and the regu la ti on of pro te i n syn the sis in egg s and embry os . In D.M. Prescott and L. Goldste i n (eds.) , Cell Bio lo gy : A Comp re hensiv e Treatis e, Vol. 4. Academi c, New York, pp. 107-136. Raff , R.A ., Colot, H.V., S olvig , S.E. and Gross, P.R. (1972) . Oog en eti c orig in of messeng er RNA for embryo n ic syn the sis o f mic ro tu b ule pro te i n s . N atu r e 235: 211- 21 4. Ranu, R.S ., Levi n, D.H. , Delaunay, J., E rnst, U. and London, I.M . (1976) . Regu la ti on of pro te i n syn the sis in rabbit retic u locyt e lys a te s : C haract er ist i c s of i nh ibi t ion of p ro te i n syn the sis b y a tra ns- lati on al inhibi to r from heme-defic ien t lys a te s and its r elati on shi p to the initiat io n fac to r wh ich bin d s Met- tRN Ar. Proc. Natl . A cad. Sci. USA 73: 2720-2726. Ray ch audhury, P., C haudhuri, A . and Mait ra , U. (1985) . Formati on and release of eukary o tic initiat i on fac to r 2GDP comp le x duri ng eukary o tic rib o somal pol yp e pt ide chain initiat i on comp le x fon na- tion . ] . Bio l. Chem. 260: 2140 크 145 . Rebag liat i, M.R ., Weeks, D.L. , Harvey, R.P. and Melto n , D.A. (1985) . Identi fica ti on and clon ing of localiz e d mate r nal RNAs from Xenopu s egg s. Cell 42: 769-77 7. Ric h te r , J.D . and Sm ith, L.D . (1984) . Reversib l e inhibi t ion of tran s- lati on by Xenop u s ooGy te- spe cific p ro te i n s . Natu re 309: 378-380.
Rog er s, S., Wells, R. and Rechste i n e r, M. (1986} . Amino acid sequ ences common to rap idl y degr ad ed pro te i n s : The PEST hyp o th e sis . Sc ien ce 234: 364- 3 68. Rosbash, M., and Ford, P.J. (1974} . Polya d eny lic acid - conta i n i n g RNA in Xenop u s laevis oocy tes . ]. Mal. Bio l. 85, 87. Rosbash, M., Ford, P.J., and Bis h op , J.O . (1974). Analys i s of the C -value pa radox by molecular hy br i diza ti on . Proc. Natl. Acad. Sci . USA n, 3746. Rosenth a l, E.T. and Ruderman, J.V . (1987} . Wi de spr e ad chang e in the tran slati on and adeny la ti on of mate r nal messeng e r RNA foll ow ing fertiliz a ti on of Spi sula oocy tes . Dev. Bio l . 121: 237- 2 46. Rosenth a l, E., Hunt, T. and Ruderman, J.V . (1980}. Selecti ve tra nsla- tion of mRNA contr ol s the pat t er n of pro te i n syn the sis du ring early develop m ent of the surf clam, Spi sula solid is sima . Cell 20: 487 -494. Shapi ro , D.J., Blume, J.E. and Ni el sen, D.A. (1987}. Regu la ti on of messeng er RNA sta b il ity in eukary o ti c cells. Bio E ssays 6: 221-226. Shaw, G. and Kamen, R. (1986} . A conserved AU sequ e nce from the 3' untr an slate d regi on of GM-CSF mRNA med iat e s selecti ve mRNA deg rad ati on . Cell 46: 659-667, Showman, R.M ., Wells, D.E., Anstr om , J., Hursh, D.A. and Raff , R.A . (1982} . Message - spe cific sequ estr at i on of mate r nal hist o n e mRNA in the sea urchi n egg . Proc. Natl. Acad. Sci . USA 79: 5944-5947. Shyn e-A th w al, S., R icc i o, R.P, Chakrabort y, G. and Ing ol ia , N.A. ( 1986} . Prote i n mod ifica ti on by amino aci d add ition is i nc reased in crushed scia t i c but not op tic nerves. Sc ien ce 231: 603-60_7 . Siel ar rtia o, n Ja.lM c.o, ndter o Hl baryo , p rCo .t, e Di n a tkt ain, a sAe.s ainnd A Or ctehmo ai a, Ssa. li(n1 a 9 7a7n) d. Twrhaenast-
ger m. Proc. Natl. Acad. Sci . U SA 74: 4356-4359. Skoultc h i, A. and Gross, P.R. (1973} . Mate r nal his t o n e messeng er RNA: Dete c ti on by molecular hyb r id i z a ti on . Proc. Natl. Acad. Sci . USA 10: 2840-2844. Sly, W. S., Fis c her. H.D., Gonzalez-Norieg a , A., Grubb, J.H . and Nato w i cz , M. (1981} . Role of the 6-ph o sph o mannosyl -e nz yme recept or in int r a cellular tra nspo r t and adsorp tive pino cy tos is of lys o somal enzym e s. Meth o ds Cell Bio l. 23: 191-214. Smi th, L.D. and Ecker, R.C . (1965) . Prote i n syn the sis in enucleate d egg s of Rana pipien s. Scie n ce 150: 777- 77 9. Soff er, R.L. (1980} . Bio c hemi str y and bio l og y of ami no acy l- tr an sfe r RNA- pr o te i n tra nsfe r ases. In D. Soll, J. N. Abelson, and P.R . Schi mm el (eds.) , Transfe r RNA: Bio lo g ica l As pe cts . Cold Spr i n g Harbor Laborato r y , Cold Spr i n g Harbor, NY, pp. 493- 50 5. van Loon, A.P. G.M. and Schatz , G. (1987} . Transpo r t of p ro to n s int o the mi toc hondria l int r a membranous spa c e: The sort ing domain of cyt oc hrome ci pre seq ue nce is a sto p - tra nsfe r sequ e nce spe c i fic for the mi toc hondria l inn er membrane. EMBO ]. 6: 2441-2448. Wag en aar, E.B. and Mazia , D. (1978} . The eff ec t of emeti ne on the firs t cleavage div isio n of the sea urchi n, S tr o ngy lo centr o tu s pu rp u r- atu s. In E.R. Dirk sen, D.M. Prescott and L.F. Fox (eds.) , Cell Rep r oductio n : In Honor of Danie l Mazia . Academi c, New York, pp. 539-545. Walte r , P. and Blobel, G. (1983) . Subcellular dist r ibu ti on of sig na l recog nition par t icle and 7SL-RNA dete r m ine d with pol yp eptide -spe c if ic a nti bo d ies and comp le menta r y DNA pro be. ]. Cell Bio l. 97: 1693- 16 99. Weid m ann, M., Kurzchalia , T .V., Hart ma nn, E. and Rapo p o r t , T.A .
(1987) . A sig na l seq u ence recep tor in the endop la smic retic u lum membrane. Natu re 328: 830-833. Wi lt, F.H. {1964) . Rib o nucleic aci d syn the sis durin g sea urchin embryo g e n esis . D ev. Bio l. 9 : 299-313. Wi nk ler, M. M., Nelson, E.M ., Lashbrook, C. and Hershey, J.W . B. {1985) . Multip le levels of regu la ti on of pro te i n syn the sis at fertiliza ti on in sea urchin egg s . D ev. Bio l. 107: 290-300. Wi nk ler, M.M. and Ste i n h ardt, R.A. (1981) . Acti va ti on of pro te i n syn thes is in a sea urchi n cell-fr ee sys t e m . De v. B io l. 84: 432-439. Young, E.M . and Raff , R.A. ( 1979) . Messeng er rib o nucleop ro te i n par t icle s in develop ing sea urchin embryo s . De v. Bio l. 72: 24- 4 0. Zucker, W.V. and Schulman, H.M . {1968) . Sti m ulati on of glo bin -chain ini t iat i on by hemi n in the reti cu locy te cell-fr ee sys t e m . Proc. Natl. Acad. Sci. USA 59: 582-589. Sta n dart , N., Hunt, T. and Ruderman, J.V . {1986) . Differ enti al accumulati on of r ib o nucleoti de reducta s e subun its i n clam oocy tes : The large subu nit is sto r ed as a po lyp e pt ide , the small subunit as untr an slate d mRNA . ]. Cell Bio l. 103: 2129-2136. Swank, R.T . and Paig en , K. (i97 3) . Bio c hemi cal and gen eti c evi- dence for a macromolecular /3-glu curonid a se comp le x in mi- crosomal membranes. ]. Mo!. Bio l. 77: 371- 3 89. Tennant, D.R. (1914) . The early influe nce of spe r mato z oa upo n the characte r s of echi no id larva. Carnegi e Inst. Wash. Pu hl . 182: 127 -138. Thomas, N.S.B. , Matt s, R.L. , Levi n, D.R. and London, I.M . (1985) . The 60S rib o somal subu nit as a carrie r of eukaryo tic initiat i on fac to r 2 and the site of reversin g fac to r acti vity durin g pro te i n syn thes is . ] . Bio l. Chem. 260: 9860-9866.
제 8 장 해독 및 후해독 수준에서의 유전자 발현의 조절 1 해독 수준에서의 유전자 발현의 조절 mRNA 는 전사되고 , p rocess i n g되어 핵 밖으로 나가 세포질에 자 리하게 되면 언젠가는 해독되어 단백질을 형성하게 되는데, 이때에도 유전자 발현은 조절된다. mRNA 는 세포질에서 세포질 요인에 따라 서 해독될 수도 있고 혹은 일정한 기간 동안 해독되지 않고 보존될 수도 있다. 수정 직후 단백질 합성이 즉시 필요할 경우 유전자 발현 이 해독 수준에서 조절되어 정확한 양의 단백질이 합성된다. (1) 단백질 합성의 협조적 관계 유전자는 게놈의 여러 부위에 홀어져 있지만 서로 연관성이 있는 단백질이 협조적으로 합성될 수 있도록 해당되는 유전자 발현이 조절
된다. 적혈구 세포에서 헤모글로빈이 합성될 때 우선 a- 글로빈, f]-글로빈 및 헴분자가 2 : 2 : 4 의 비율로 합성되어야 한다. 만약 이 러한 비율이 유지되지 않으면 심각한 질병이 발생한다.
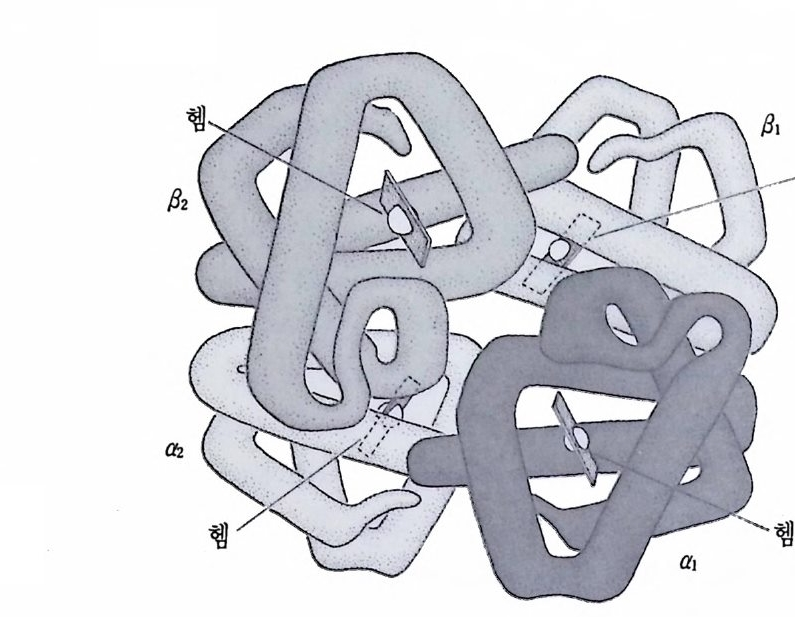 A 헴
A 헴
그림 8-1 헤모글로반 구조 (D i ckerson and Geis , 1983)
최근의 연구 보고에서 헴분자가 헤모글로빈 성분의 비례적 합성을 조절한다고 알려져 있다. 이러한 조절은 두 가지 방법으로 이루어진 다. 첫째, 글로빈과 결합되어 있지 않은 행은 행의 합성을 억제한다 (Ka ribia n and London, 1965) . 죽 헴 울 과량으로 넣 어 주면 헴 생 성 과sy n 정th 의e t a s e첫 ( D번A L째A s반yn t응he t을as e) 촉를 진불 하활 성는 화효시 킴소 으 인로 써o -a행m 의i n o l합ev성u l을in a 억te 제시킨다. 둘째, 행은 글로빈 단백질 합성을 촉진한다 (G ri bble and Schwa rtz, 1965 ; Zucker and Schulman, 1968) . 글로빈 mRNA 를 해 독시 키는 대 필요한 모든 조건과 요인을 준 다음 시험관에서 생체 밖 해
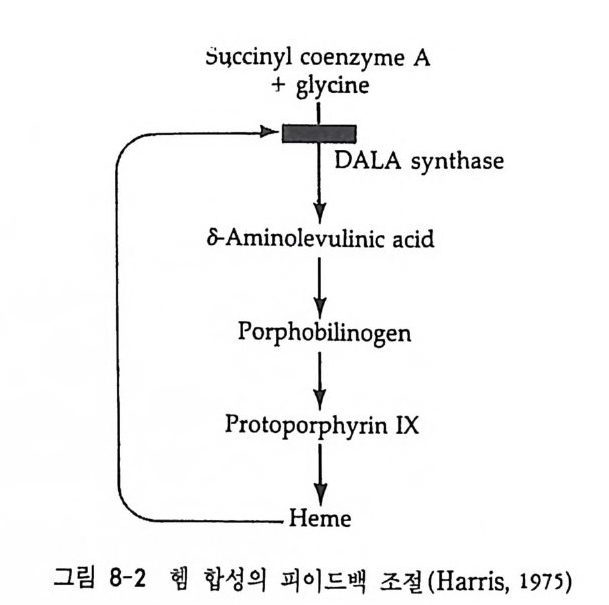 :,qcc i+ ny l c oefnz~yL mA e sAy n t h a se
:,qcc i+ ny l c oefnz~yL mA e sAy n t h a se
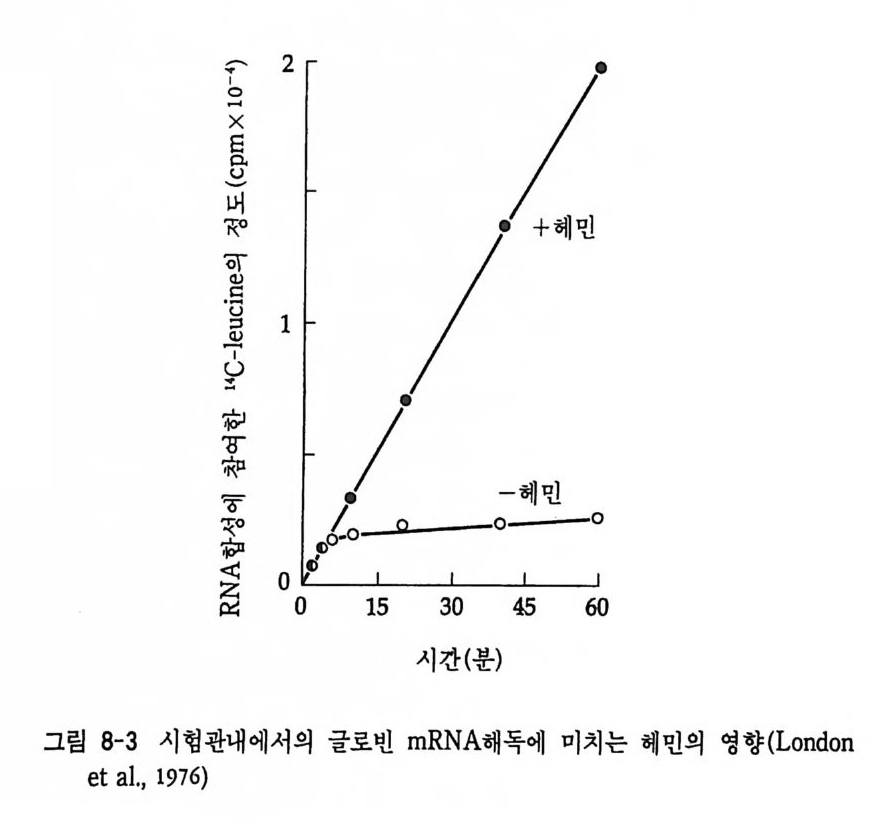 et a l., 1976) mKa'3귬n8中Hmrnlp)uf버U 12 00d•d/ q 시一I••I간 (분) 一 玉며•I
et a l., 1976) mKa'3귬n8中Hmrnlp)uf버U 12 00d•d/ q 시一I••I간 (분) 一 玉며•I
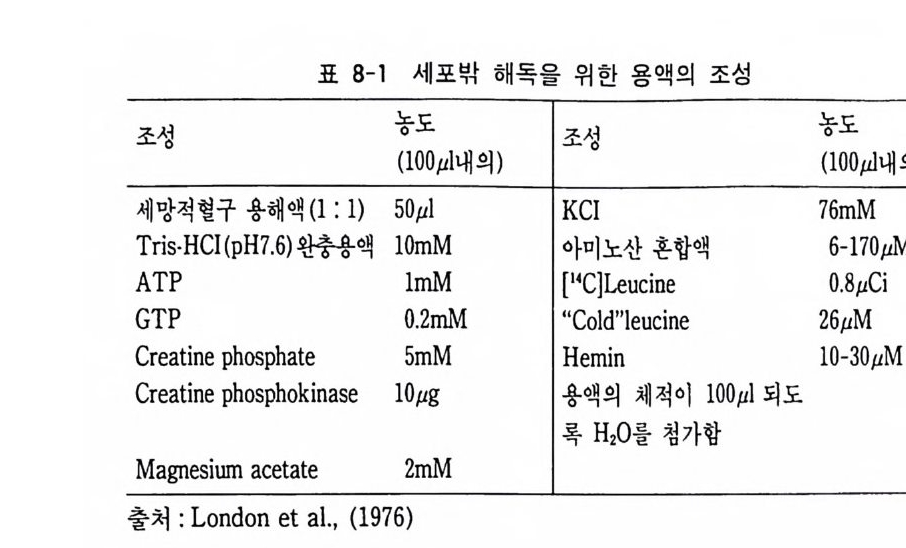 표 8-1 세포밖 해독을 위한 용액의 조성
표 8-1 세포밖 해독을 위한 용액의 조성
독 반응을 시도할 때, 헴울 첨가해 주면 글로빈 합성은 크게 촉진된 다. 그러나 헴과 결합할 글로빈이 없으면 행 합성은 억제되고 글로빈 합성은 촉진된다. 헴의 글로빈 합성에 대한 촉진 효과는 리보소말 단백질을 해독반응 용액에 첨가했을 때에도 비슷하게 나타난다 (Adamsson et aL, 1972) . 이때 이 용액 속에 여러 가지 해독 개시 요인들이 들어 있기 때문에 이들 요인을 하나씩 분리하여 개시 요인과 해독 개시의 관계를 알아 볼 수 있다. 이러한 실험을 통하여 진핵세포의 개시 요인인 eIF 2 에 의해 행이 결여된 용해액 (ly sa t e) 내에서도 단백질 합성을 회복시킬 수 있다는 사실을 알게 되었다. 이때 행과 eIF 2 사이에는 어떤 특별 한 관계가 있는 것으로 예상되는데, 이러한 관계를 알아내기 위하여 헴이 결여된 용해액를 헴울 보충한 해독반웅 용액에 첨가해 주고 글 로빈 합성이 억제되는 현상을 관찰하였다. 행이 결여된 용해액에 억 제 요인이 존재하는 것을 알게 되었고, 더구나 억제 요인에는 효소의 활성도가 관계된다는 사실도 알게 되었다 (Lev i n et al., 1976 ; Ranu et al., 1976) . 억제 요인은 eIF2 를 인산화시키는 효소인 k i nase 로 알려졌는데,
eIF 2 가 인산화되면 해독이 중지된다. 일단 리보솜의 소단위와 결합 하면, eIF2 도 GDP 와의 결합체로 방출된다 (Ray chandhur i e t a l., 1985). 방출 요인으로서 eIF - 2B 가 있는데, recyc l in g fac to r 혹은 gua nid i n e nucleoti de exchang e fac t or 라고 불리 운다. 아 요인은 eIF 2 에 결합하여 리보솜으로부터 eIF 2 를 분리시킨다. 그러나 eIF-2B 는 eIF2 가 인산화되었을 때 결합되면 eIF2 결합체가 리보솜에서 분리 되지 않고 결합된 채로 남아 있게 된다 (Thomas et a l., 1985 ; Gross et al., 1 986). 결국 모든 recyc l in g fa c t or 는 eIF 2 보다는 10~20 배 가량 낮은 농도의 불활성화된 결합체로 남아 있게 되기 때문에 eIF 2 의 기
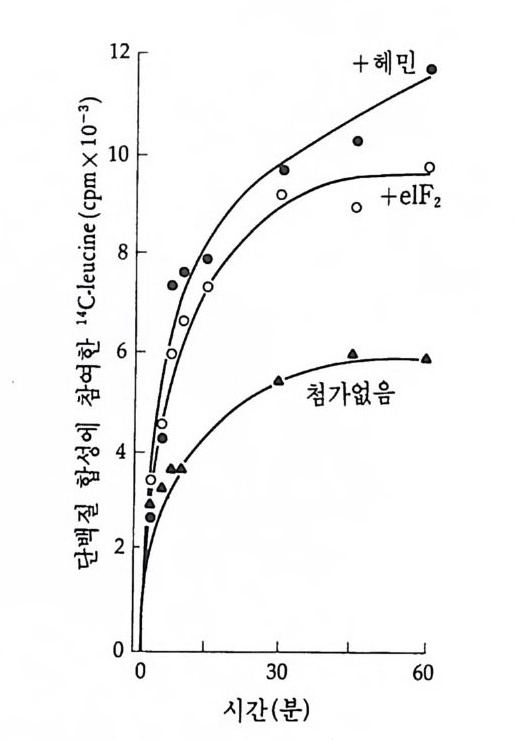 12 +혜민 •
12 +혜민 •
그립 8-4 시험관내 해독에 미치는 진핵세포 개시요인 2(eIF2) 의 영향 (Clemens et a l., 1974) .
능은 정지되고, 해독도 정지된다. 만약 행이 결핍된 용해액에 recyc l in g fa c t or 를 첨가해 주면 단백질 합성이 회복된다 (Grace et a l., 1984). 글로빈 합성의 해독 수준에서의 조절은 a_ 글로빈과 8- 글로빈간의 농도비에 관한 것이다. 죽 이배수체의 핵 속에는 a- 글로빈유전자 4 개와 8_ 글로빈유전자 2 개가 있기 때문에 만약 동일한 속도로 전사되 어 해독된다면 a- 글로빈단백질의 농도가 8 곱 E 로빈의 것에 비해 2 배 가 되어야 한다. 그러나 mRNA 는 a : /j= l.4 '. 1 이고 단백질의 비는 a : /j= l : 1 이다 (Lod i sh, 1911). 이러한 a - 와 8- 글로빈간의 평형은 해 독 수준에서 조절된 결과이다.
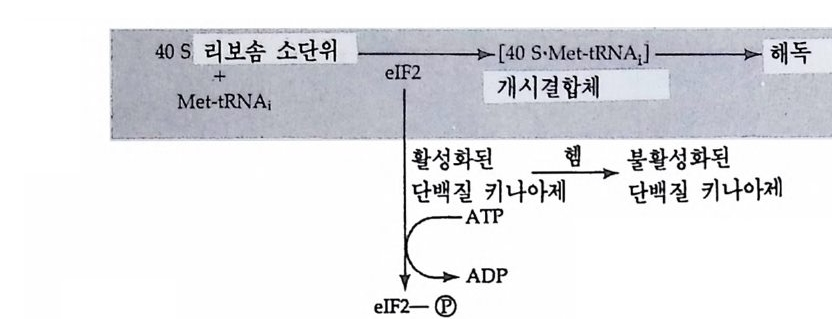 40 —S_L _린 +_ 보 .솜_. 솜—· 단 —위 _’. -_ .. ~1 _~ 1 4 - 브- ; .M-e브 뽀'.-1·_ -~] .- -;' -: ―_― _ ―一 >. .민 독
40 —S_L _린 +_ 보 .솜_. 솜—· 단 —위 _’. -_ .. ~1 _~ 1 4 - 브- ; .M-e브 뽀'.-1·_ -~] .- -;' -: ―_― _ ―一 >. .민 독
그림 8-5 글로빈 합성에 대한 해독 수준에서의 조절
a- 와 /3-글로빈의 평형은 해독이 개시될 때 이루어진다 (Kaba t and Chapp ell s. 1 977) . a- 글로빈 mRNA 와 /3-글로빈 mRNA 에 의 한 해 독 은 동일한 개시 요인에 대하여 서로 경쟁적이다 ‘ 그런데 /3-글로빈 mRNA 가 우세하기 때문에, /3-글로빈 mRNA 가 개시 요인에 의해 더 효율적으로 인식되는 동시에 더 빈번하게 해독된다. 개시 요인의 공급이 심하게 제한된 상태에서 두 종류의 mRNA 가 동일한 양으로 주어질 때 합성된 단백질의 3% 만이 a- 글로빈으로 검출되었다. 그러 나 a- 와 /3-글로빈 mRNA 로 분리하지 않고 과잉의 개시 요인을 섞
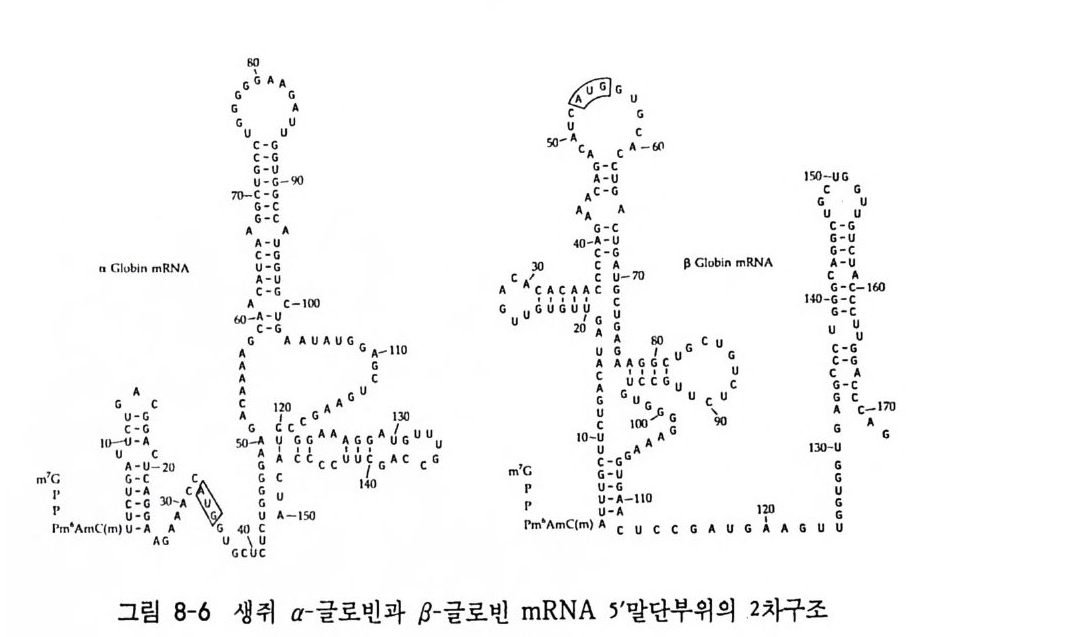 m’ crPm · ^ r’’ ` cnI G 그cluuGuGb[cAUl-^--림-- uun--G- ~-mcc一A G R G2 ^N0A8 I JA A ^U O- cC6 A `C%6생GcGG60元A^^^cA5^040 u G 8쥐C6Uc 0cCc,G- ---- ^G G-- G -J-,uA-uA--cGG c- -a-G A u cwU AA --'A5 l G0 글O AC Ac'C G^ cC Au로CUOAUcCG-cA'Au''Gu^U빈GA U C G^AGcG At과 G GG^U 2 J4UIG JO'u CcCOGG 1 0u8 /cUcG 1u '/국G cu4GU c0 몬4 A A로G빈 cA cGm9uA ’ 6 J 'PR·l ^'ulsc PuN r A C4uArfi%止EA『2,0瑟it UACGc Au止 5 m CCUUmG'GGcU A^ c -G 말GA- A'u G1 u uU c 1 0 Al G 。단G.01cA'cgi GsC^^^ u Cc U 부c G' C' ucuG G O 위U AG cG 1cI C0A의 PbuAR Ul u n 0 mGG 2R G N차A^ AG ^구u G’조, uc%叫g%' cu6^l GcuAGUcGCC c-G - - cG---c UGu- GGcGlG c^G^GuU c- u Jc UG u-c-O1c u c R 6G 0 T,^
m’ crPm · ^ r’’ ` cnI G 그cluuGuGb[cAUl-^--림-- uun--G- ~-mcc一A G R G2 ^N0A8 I JA A ^U O- cC6 A `C%6생GcGG60元A^^^cA5^040 u G 8쥐C6Uc 0cCc,G- ---- ^G G-- G -J-,uA-uA--cGG c- -a-G A u cwU AA --'A5 l G0 글O AC Ac'C G^ cC Au로CUOAUcCG-cA'Au''Gu^U빈GA U C G^AGcG At과 G GG^U 2 J4UIG JO'u CcCOGG 1 0u8 /cUcG 1u '/국G cu4GU c0 몬4 A A로G빈 cA cGm9uA ’ 6 J 'PR·l ^'ulsc PuN r A C4uArfi%止EA『2,0瑟it UACGc Au止 5 m CCUUmG'GGcU A^ c -G 말GA- A'u G1 u uU c 1 0 Al G 。단G.01cA'cgi GsC^^^ u Cc U 부c G' C' ucuG G O 위U AG cG 1cI C0A의 PbuAR Ul u n 0 mGG 2R G N차A^ AG ^구u G’조, uc%叫g%' cu6^l GcuAGUcGCC c-G - - cG---c UGu- GGcGlG c^G^GuU c- u Jc UG u-c-O1c u c R 6G 0 T,^
어 주면 , 모든 RNA 가 해독되는 효율이 동일하기 때문에 a- 와 f3-글 로빈 단백질 비율은 1.4 : 1 에 해당한다. 그러나 생체내에서는 1 : 1 의 비로 a - 와 f3-글로빈이 합성된다. 최근 보고에 의하면 cap bin d i ng p ro t e i n 이 두 가지 종류의 글로빈 mRNA 를 구별하는 개시 요인으로 생각되고 있지만, 아직도 이러한 구별이 어떻게 가능한지 별로 알려 진 바가 없다. 5' 의 leader se q uence 의 이차 구조에 따라 해독 효율 이 영향받는 것으로도 생각되고 있다 (Pelle ti er and Sonnenberg, _19 85). 그림 8-6 에서 보는 바와 갑이 a- 와 8- 글로빈 mRNA 의 5' 말단은 상 당히 다르다. 그래서 해독 개시 단계에서 a- 글로빈, f3-글로빈 및 헴 의 비율이 정해질 수 있다. 물론 헤모글로빈 합성이 전사와 RNA pro cessin g 수준에서 조절되지만 , 마지막 분자는 해독 수준에서 정교 하게 협조적으로 조절된다.
(2) mRNA 의 선택적 붕괴 해독 수준에서 유전자 발현을 조절하는 또 하나의 다른 기구는 mRNA 의 수명을 조절하는 것이다. 8- 글로빈 mRNA 와 같은 안정된 메시지는 약 17 시간의 반감기를 가지고 있는 반면에 여러 가지 성장 요인의 mRNA 는 30 분 이하의 반감기를 가지고 있다. 따라서 한 분 자의 글로빈 메시지로부터 만들어지는 단백질 양은 한 분자의 성장 요인 메시지로부터 만들어지는 단백질 양보다 훨씬 많다. mRNA 의 반감기를 조절하는 가장 중요한 요인은 mRNA 의 3' 말단쪽에 있는 미해독 부위로 보이는데, 수명이 짧은 RNA 종류는 이 부위에 AU 가 풍부한 염기 서열을 한 개 이상 가지고 있다. 만약 성장 요인 GM -CSF 유전자의 3' 말단쪽의 미해독 부위로부터 51 개의 염기쌍으로된 AT 가 풍부한 부분을 분리하여 토끼의 8- 글로빈유전자의 3' 말단쪽의 미해독 부위에 삽입시키면, 이 글로빈 메시지의 반감기는 30 분 이내 로 단축된다 (Shaw and Kamen, 1986). 그러나 유사한 영기 서열을 가 졌지만 14 개의 GC 염기쌍을 가진 부위를 8- 글로빈유전자에 삽입시키 면, 이 글로빈 메시지는 정상적으로 건 반감기를 가진다. 따라서 특 정한 메시지의 수명은 mRNA 의 3' 말단쪽의 미해독 부위에 지시된 것으로 보인다. m 만 ~A 를 순차적으로 붕괴시키는 능력은 세포 기능을 구현하는 데 아주 중요하다. 예를 들어 c-fo s 유전자는 정상적인 섬유아 세포 분 열에 필요한 핵 단백질을 지시한다 (Hol t et al. , 19s6). GM-CSF 성장 요인 메시지와 감이 c-fo s mRNA 는 AU 서 열 부위 에 3' 말단쪽에 미 해독 부위를 가지고 있는데, 만약 이 부위가 인위적으로 혹은 자연적 인 돌연변이에 의해서 소실될 경우 그 메시지의 반감기는 더 길어진 다. 결과적으로 더 많은 c-fo s 단백질이 계속 생성되면서 세포분열에 대한 지속적인 신호를 보내게 된다. 그 결과 AU 가 풍부한 3' 부위를 결핍한 c-fo s 유전자를 가전 세포에서는 세포분열의 속도가 빨라져
 A G 에 다 부 문 는 c an 존
A G 에 다 부 문 는 c an 존
종양세포가 유발된다 (Me ijli nk et al., 1985), (3) 해독 수준에서의 유전자 발현의 조절의 예 1) 초기 발생의 모계 조절과 저장 mRNA 대부분의 동물에서는 수정 직후 이배체의 염색체를 회복하지만 초 기 발생과정은 이배체의 유전자 발현에 의존하지 않고 오히려 난자 형성중 준비되어 난모세포에 저장되어 있던 여러 가지 요인에 의하여 조절된다. 이러한 사실을 입증하는 실험이 고전적인 것부터 현대적인 것에 이르기까지 다양하게 있다. 발생 초기에는 모계의 특징이 우세 하게 나타나지만 점차 부계 혹은 부계와 모계의 특칭을 모두 나타내 는 형태로 전환한다. 달팽이의 경우 난할면을 오른쪽 방향으로 (dextr al ) 혹은 왼쪽방향으로 (s i n i s tral) 정 하는 요인 이 이 미 난모세포 의 세포질내에 들어 있다. 1898 년 Hans Dr i esch 는 두 종류의 성게를 교배시켜 잡종을 만들었 는데, 그 잡종의 일차 간충직 세포(pri ma ry mesenchym e cells) 의 수는 모계의 것을 따른다는 사실을 알아내었다. 데넌트 (Tennan t, 1914) 도 C i da ris의 난자를 Ly t ech i nus 의 정 자로 수정 하여 잡종 발생 배 의 초기 발생과정을 관찰하였다. 두 종류의 염색체가 모두 할구에 지속적으로
 표 8-2 성게 잡종배에서 일차 간충직세포 수의 모계 조접에 대한 Dr i esch 의
표 8-2 성게 잡종배에서 일차 간충직세포 수의 모계 조접에 대한 Dr i esch 의
 표 8-3 성게 잡종배에서 초기 낭배과정의 모계 조절에 대한 Tennan t의
표 8-3 성게 잡종배에서 초기 낭배과정의 모계 조절에 대한 Tennan t의
보존되었지만 원장의 함입과 일차 간충직 세포의 형성시기 등에 이르 는 발생 특징은 모두 모계의 것을 따른다. 부계 유전자가 처음으로 개입하는 특징은 후기 발생과정에서 골격 세포의 위치결정에서 나타 난다.
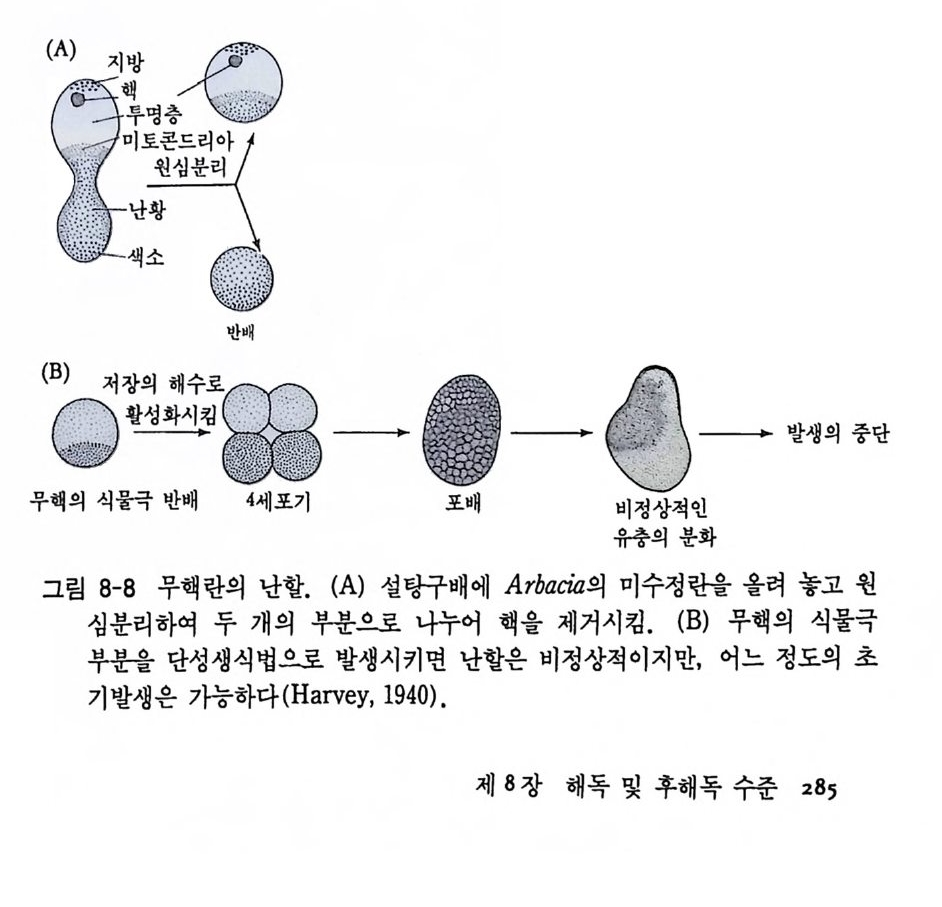 무 그핵g二三rv발언『一鬪부설 血,三제 8핵은 A 장 r\ab 一 해 정제lCU· 독 상거의 및 :円〈〉후해독白病一 수 핵느올준 려의정 발28텨놓생 식5 물고의 극중원초 단
무 그핵g二三rv발언『一鬪부설 血,三제 8핵은 A 장 r\ab 一 해 정제lCU· 독 상거의 및 :円〈〉후해독白病一 수 핵느올준 려의정 발28텨놓생 식5 물고의 극중원초 단
초기 발생과정이 모계 조절에 의존한다는 또 하나의 증거는 주로 핵 제거 연구에서 찾아볼 수 있다. 만약 수정 직후 핵을 제거할지라 도, 이 핵이 없는 수정란은 새로운 RNA 합성이 없이도 얼마 동안 발생한다. 이러한 핵 이식에는 물리적 방법, 화학적 방법 및 유전학 적 방법이 있다. 물리적 방법은 하아비 (Harvey, 1940) 에 의해서 처음 시도된 것으로, 난자와 동일한 밀도를 가진 설탕 용액에 난자를 넣고 원심분리하면, 난자는 두 부분으로 분리된다. 이때 가벼운 쪽에만 핵 이 들어가고 무거운 쪽에는 핵이 없다. 그 다음 핵이 없는 반쪽의 난 자를 저장액의 해수에 넣어 활성화시켜 발생시킨다. 이러한 반쪽 난
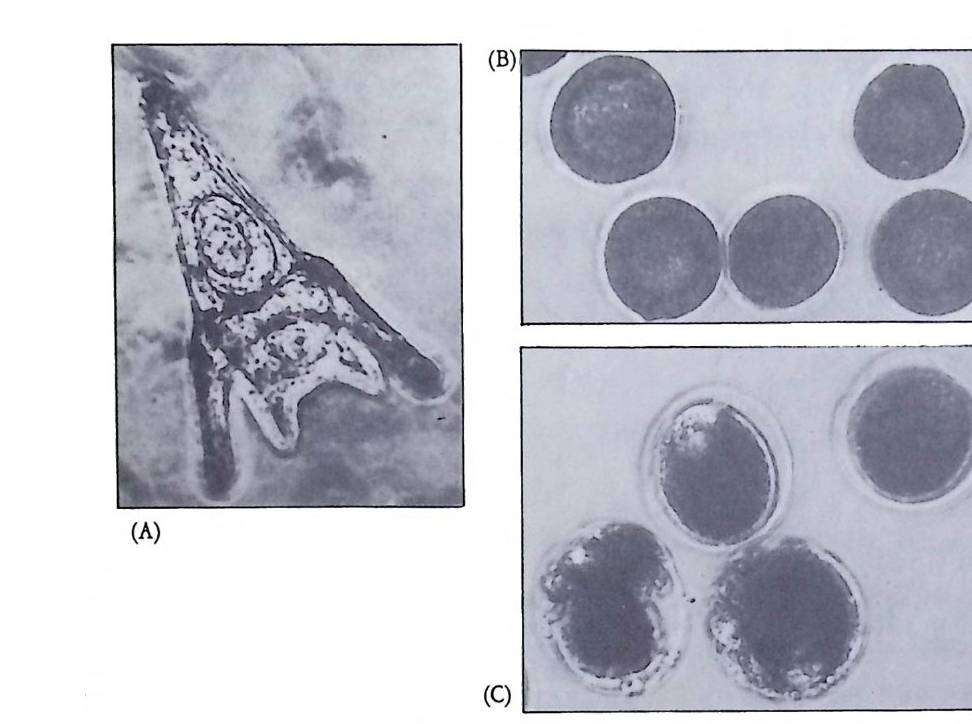 (B)
(B)
그립 8-9 성게 Lyt ech in u s 발생에 미치는 단백질합성 저해제의 영향, (A) 정상 플루티우스 유생 (B) ac ti nom y c i nD 를 처리하여 발생이 정지된 포배 (C) 해독 저 해 제 인 eme ti ne 이 나 c y clohex imi de 에 의 하여 난할기 에서 발생 이 정지된 발생배;
자를 단성 생 식 난편 발생 자 (pa rt he nog en ic merog on es) 라고 하는데 , 이 둘 단성생식 난편 발생자는 난할시 할강이 결여된 포배를 형성하나 성공적으로 부화한다. 그러나 그 이상의 발생은 진행되지 않는다. 유 사한 연구가 개구리의 난자를 이용하여서도 이루어졌는데, 난자에 중 십립을 인위적으로 제공하여 주면 염색체가 없을지라도 난할이 일어 난다. 물론 비정상적인 포배가 형성되지만, 물리적으로 핵을 제거시 켜 도 난자는 중포배 기 (midb lastu la sta g e ) 까지 발생 할 수 있다. 초기 발생이 난모세포에 저장된 mRNA 에 의해서 조절된다는 증거 를 처 음으로 제 시 한 발생 학자는 부라쉐 (Brachet) 와 그 동료들이 다 (1963), 곧 이어 데니 (Denn y)와 타일러 (Ty le r, 1964) 도 유사한 연구결 과를 발표하였다. 이러한 연구 결과에 의하면 성게의 난자로부터 핵 울 제거한 다음 활성화시킬지라도 세포질에는 RNA 가 남아 있는데, 이들 RNA 는 정상적으로 수정된 난자들과 동일한 속도로 단백질을
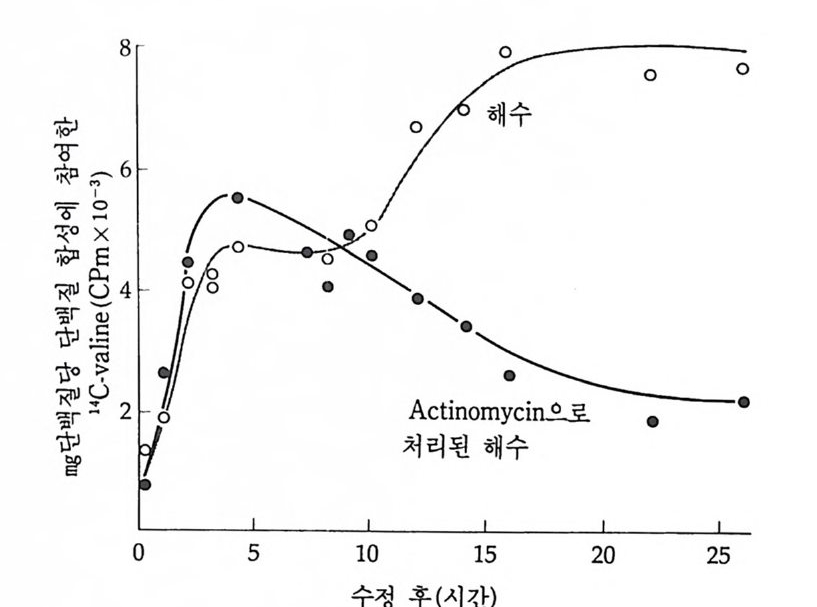 8
8
그림 8- 10 성게 Arbaci a pim ctu la ta 발생배에서의 단백질 합성에 미치는 acti no my cin D 의 영향 (Gross and Cousin e au, 1964).
합성한댜 핵이 없는 수정란에서 RNA 가 합성될 수 없기 때문에 이 러한 수정란에서의 단백질 합성은 난모세포에서 합성되었다가 저장된 mRNA 에 의존하는 것이라고 풀이되었다. 핵 제거는 물리적 방법의에 화학적인 방법으로도 가능하였다. RNA 합성을 억 제시 키는 acti no my ci n D 를 수정 란에 처 리 하면 비 록 핵이 있을지라도 전사를 94% 까지 억제할 수 있었다 (Gross and Cousin e au, 1964). 그러나 이러한 발생배는 포배까지 발생하였는데, 이러한 발생은 전적으로 저장된 메시지에 의존한다. 그렇기 때문에 단백 질 합성 억 제 제 인 eme ti ne 이 나 c y clohex i m i de 를 수정 란에 처 리 하면 발생 이 중단되지만 acti no my ci n D 를 처 리 하여 화학적으로 핵을 제거했을지라도 수정 직후 단백질 합성 정도는 정상적인 발생배에서 일어나는 정도와 동일하다. 그러나수정 후 6~10 시간 후부터는 핵이 제거된 발생배에서는 단백질 합성이 감소되기 시작하고, 포배기에 나 타나는 두번째 고조되는 단백질 합성 양상이 나타나지 않는다. 즉 두 번째 단백질 합성에 대한 메시지는 저장된 것이 아니고 수정 후 새로 합성된 것이다. 따라서 acti no my ci n D 를 처리한 발생배는 포배기까 지 발생하여 부화될 수 있으나 그 이상은 발생되지 않는다. 즉 저장 된 mRNA 를 이용하여 부화기까지 발생이 진행된다. 양서류에서는 단백질 합성이 배란에 의해서 촉진되지만 성게에서와 유사한 결과가 관찰되었다. 핵을 제거당한 양서류의 난자에서 활성화 된 단백질 합성은 양적으로나 질적으로 정상적인 수정란에서의 합성 과 동일하다 (S mith and Ecker, 1965 ·; E cker and Sm ith, 1971). 양서류에 서도 역시 난모세포의 세포질이 이미 계획되어 (pre pr o g ram med) 핵이 결여되었을지라도 어느 정도의 발생을 수행할 수 있다. 정상적인 발 생배에서의 전사 개시도 난모세포에서 준비된 모계 요인에 의해서 활 성화된다. 이러한 개념은 Mexic an axolo t l 의 0 돌연변이종에 대한 연구로부터 정립되었다. 이러한 돌연변이는 일종의 모계효과 돌연변 이로서, 이러한 변이를 가진 동형집합자의 암컷 (0/0 암컷)에서 생겨
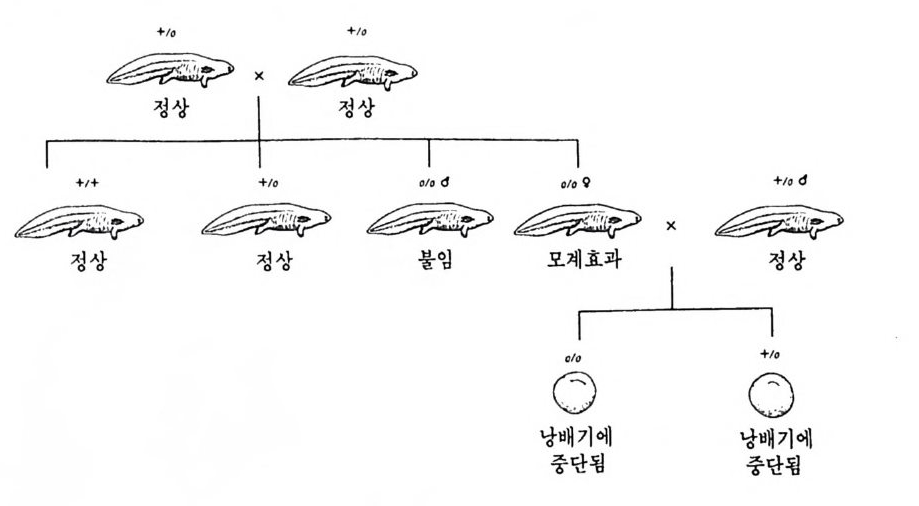 정+/ o상 l 정+/상 0
정+/ o상 l 정+/상 0
그림 8-11 양서류 Axolo tl에서의 0 돌연변이의 모계 효과. 이형 접합자의 교배 로 얻은 0 / 0 개체 중 수컷은 불임적이나 암컷은 돌연변이의 난자를 형성한 다. 따라서 이러한 난자 를 수정시켜 발생사키면 야생종의 인자가 정자로부 터 공급되었을지라도 발생이 낭배기에 중단된다 (Bro th ers, 1979).
난 알은 성공적으로 수정도 되고 정상적으로 발생하지만 난할 후기나 포배 초기 정도까지만 발생한다 (Br igg s and Cassens, 1966). 포배 중기 부터는 0/0 암컷에서 생긴 알의 세포 분열 속도는 느려지고, 원구 배순부를 형성하기는 하지만 낭배 형성에는 실패한다. 일반적으로 야생종의 암컷은 포배기에 새로운 단백질을 합성하기 시작한다 (Malac i nsk i, 1971). 그러나 0/0 암컷의 난자로부터 출발한 발생배에서는 포배기에 새로운 단백질이 합성되지 않는다. 즉 야생종 에서는 포배 후기에 다량의 RNA 가 합성되지만, 돌연변이종에서는 합성되지 않는다 (Carroll, 1974). 브리그스 (B riggs)와 카센스 (Cassen s, 1966) 는 이미 0/0 암컷은 포배기에 유전자 발현을 활성화시킬 수 있 는 요인을 가지고 있지 않기 때문에 이 돌연변이 종에서는 RNA 합 성이 일어나지 않을 것이라고 예측하였는데, 실제로 이러한 요인을 정상적인 발생배의 세포질이나 혹은 난모세포의 핵질에서 분리하여
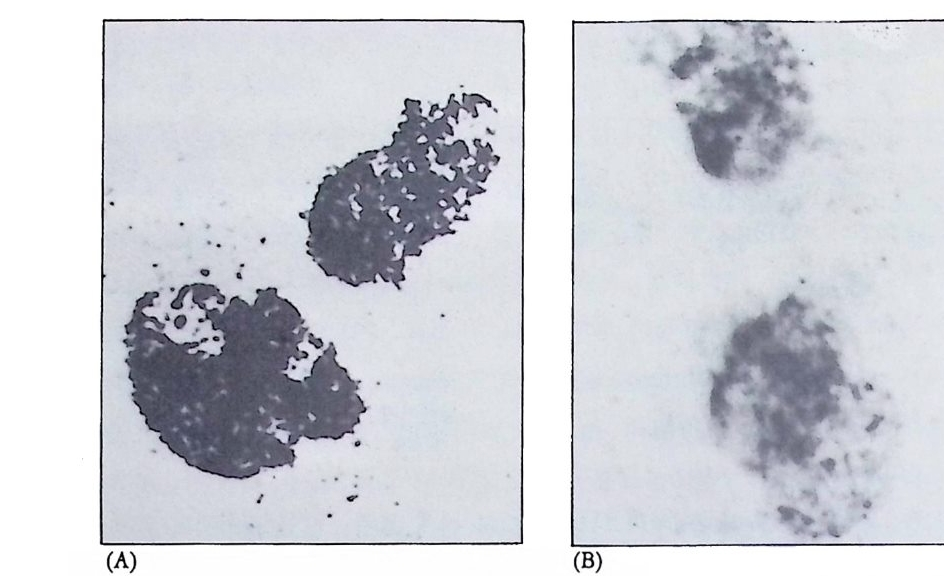 . .
. .
그림 8-12 야생종과 돌연변이종에서의 RNA 합성. 포배기의 발생배를 띤 -ur i d i ne 로 3 시간 동안 처리한 다음 자기방사법으로 관찰하였다. (A) 정상 배에는 3H-u ri d i ne 의 표지에 의한 은입자가 많이 보인다. (B) 0/ 0 암컷에서 얻은 발생배에는 전사의 흔적이 보이지 않는다 (Carroll, 1974).
0/0 난자에 주입해주면 정지된 낭배과정이 재개되어 정상적인 발생 울 회복시킬 수 있다. 따라서 양서류의 핵을 발생과정중에 활성화시 키기 위해서는 특별한 요인이 필요하다. 만약 그러한 요인이 없다면 발생은 저장된 난모세포의 mRNA 에 의해서 뒷받침될 수 있는 정도 까지만 진행될 수 있다. 죽 양서류에서는 저장된 mRNA 만으로는 낭 배 직전까지 발생이 가능하다. 그러나 새로운 단백질 합성이 일어나 지 않으면 더 이상의 발생은 진전되지 않는다. 이러한 실험결과로부터 알 수 있는 분명한 사실은 초기 발생을 조 철하는 메시지가 이미 난모세포내에 저장되어 있으며, 또한 새로운 RNA 합성을 조절하는 요인도 난모세포에 이미 준비되어 있다는 것 이다.
2) 모계 메시지의 특징 난자 형성 과정의 마지막 단계에 난모세포내에 저장되어 있는 모계 RNA 의 복잡도를 DNA- R NA 재결합법으로 측정할 수 있다. 유일성 DNA 를 방사능 동위원소로 표지하고 단일 사슬로 변성시킨 다음, 과 잉의 RNA 로 포화상태에 이르기까지 재결합시킴으로써 전체 게놈의 어느 정도가 마지막 단계에 있는 RNA 를 발현하는 데 쓰였는지를 알 아낼 수 있다. 지금까지 이와 같은 방법으로 성게 (Galau et al., 1 976 ; Houg h- Evans et al., 1977 ; Duncan et al., 1978 ; Wi lt, 1977), 불가사리 (Kovesdi and Sm ith, 1982) , 양서류 (Dav i dson and Houg h, 1971 ; Rosbash and Ford, 197 4 ; Rosbash, et al. , 1974) , 쌍 시 류 (Houg h -Evans et al., 1980), 개불 (Dav i s, 1975) 및 갯지렁이 (Lee and Whit ele y, 1984) 에서 모 계 RNA 의 복잡도가 측정되었다. 대부분의 경우 복잡도는 35 土 lO X 따 NT 로서 보라성 게 에 서 37 x 106NT, 불가사리 에 서 43 X 106 NT, Xenop us 에서 27~40 X 106NT, 초파리에서 12.1 X 106 NT, 개불에서 31~47X 106 NT, 그리고 갯지렁이에서 27X 106 NT 이다. 이러한 복 잡도의 값은 대단히 높은 것이다. 보라성게의 경우를 예로 설명하면, 보라성게의 마지막 단계에 있는 난모세포에는 20,000 내지 50,000 종 류의 RNA 가 가능하다. 즉 이들 RNA 가 단백질의 형태로 표현될 경 우 20,000~50,000 종류의 단백질이 합성될 수 있는 정보가 모계 RNA 형태로 난모세포내에 존재할 가능성이 있다는 뜻이다. 그러나 이렇게 높은 복잡도의 값을 가진 RNA 가 모두 mRNA 의 형태로 존재하는 것은 아니다. 원래 DNA-RNA 재결합실험을 위하여 난모세포로부터 추출한 RNA 가 세포질의 것만이 아니고 세포질의 것과 핵 속에 있는 nRNA 를 합한 것이었기 때문에 37X106 NT 와 같은 복잡도를 가진 모계 RNA 가 모두 mRNA 라고 단언하기는 어렵다. 일반적으로 nRNA 의 일부만이 mRNA 로 성숙한다는 사실을 전제로 할 때 실제 로 난모세포내에 저장되어 있는 mRNA 의 복잡도는 전체 RNA 의 것 에 비해 훨씬 낮을 것으로 예상된다.
난자형성 과정에서 RNA 복잡도의 변화는 기대와는 다르다. 즉 난 자형성 초기에는 대단히 높은 RNA 복잡도를 보이지만 난자형성 말 기에 접근할 수록 RNA 복잡도는 감소한다. 보라성게에서도 난자형 성 초기에는 복잡도가 16X107 NT 로 말기의 3.7X107 NT 에 비해 4 배가 높다 (Hou g h-Evans, et al., 1977, 1979). 갯지렁이의 난모세포는 난 소에 묻혔거나 난소막같은 구조에 부착되어 있지 않고 체강액에 부유 하면서 성장하기 때문에 난모세포를 단계별로 분리하여 RNA 복잡도 를 측정하기에 편리한 재료이다. 직경 25µm, soµm 및 lSOµm 의 난모 세포를 분리한 다음 각 단계의 난모세포로부터 RNA 를 추출하여 1251
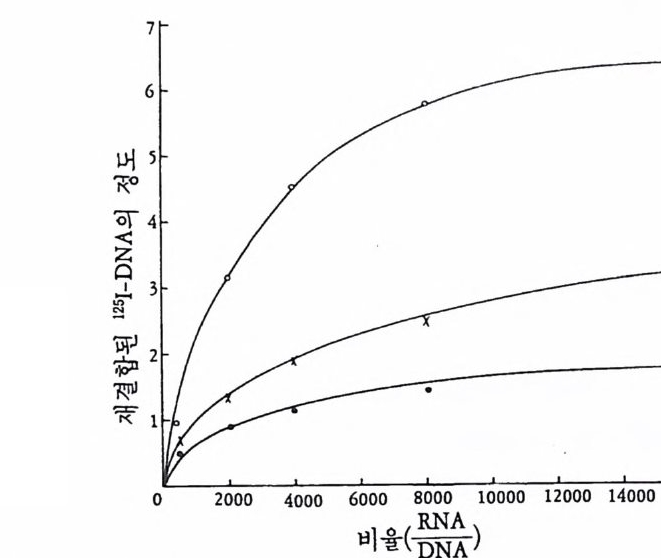 7
7
그림 8-13 난자형성 단계에 따른 유전자발현 정도의 차이. 유일성 1 하 -DNA 와 직경 25µ m (o-o), soµ m (x-x) 및 180 µm(*)의 난모세포 RNA 와의 포 화재결합반응을 일으킨 다음 따 I-DNA-RNA 결합체를 SI nuclease 로 처리하 여 검출하였다 (Lee and Whitel ey, 1984).
으로 표지한 유일성 DNA 와 재결합시킴으로써 난자형성 단계에 따른 RNA 복잡도의 변화를 관찰한 결과, 직경 25 µm의 난모세포에서 lOX107NT, SOµm 에서 5.5X107NT 그리고 180 µm에서 2.1x107 NT
로 RNA 복잡도는 난자형성 과정이 진행됨에 따라 점차 감소하였다 (Lee and W 血 ele y , 1984) . 난자형성 과정중에 다수의 메시지가 준비되지만 지금까지 알려진 것은 그리 많지 않다. 세포 밖 해독과정을 통하여 히스톤 mRNA (Skoultc h i and Gross, 1973) 와 듀블린 mRNA(Raff et a l., 1972) 가 확인 되었다. 또한 생화학적안 방법으로 rib o nucleoti de reduc t ase 와 부화 효소 (hatc h in g enzym e ) 에 대 한 메시 지 가 난모세포에 저장되 어 있음이 확인 되 었 다 (Ra ff, 19so). 조개 의 난모세 포에 서 는 rib o nucleoti de redu ct ase 가 놀라운 방법으로 저장되어 있다. 즉, 이 효소의 큰 하단 위 (lar ge subunit ) 는 단백 질의 형 태로 보존되 어 있는 반면에 작은 하 단위 (small sub unit)는 해독되지 않은 모계 mRNA 로 보존된다. 수정 이 일어난 다음에만 작은 하단위의 mRN A.로부터 작은 하단위의 단 백질이 합성되어 작은 하단위와 큰 하단위가 결합함으로써 기능을 가 진 효소가 생 성 된다 (Sta n da rt et a L, 1986) . 저장된 mRNA 는 난모세포 전체에 고르게 분포되기 보다는 RNA 종류에 따라 지역적으로 특이성있게 분포되어 있다. Xen op us 의 미수 정란에서 대부분의 모계 mRNA 는 고르게 분포되어 있지만 어떤 mRNA 는 동물국쪽에나 혹은 식물국쪽에 특이하게 분포되어 있다 (Rebag liati et a l., 1985). 레 바리 아티 (Reba gli a ti)와 그의 동료들은 Xenop us의 난모세포로부터 p ol y (A)RNA 를 추출한 다음 역전사 효 소 (reverse tran scri ptase ) 와 DNA 중합효소를 이 용하여 RNA 로부터 이중나선의 DNA 를 만들었다. 이 이중나선의 DNA 를 vec t or 에 조합 시 킨 다음 E. coli 에 넣어 증폭시 킴으로써 Xenop us 난모세포의 gen e l i bra ry를 만들었다. 이 DNA 를 두 장의 거름종이에 옮기고 단일 사 슬의 DNA 로 변성시켰다. 한편 수정란의 동물극과 식물국으로부터 각각 pol y (A ) RNA 를 추출하여, 이들 RNA 로부터 방사능 cDNA 를 만들었다; 그 다음 DNA 가 들어 있는 거름종이 한 장은 동물극의 RNA 에서 얻은 cDNA 와 항온처리시키고, 다른 한 장은 식물국의
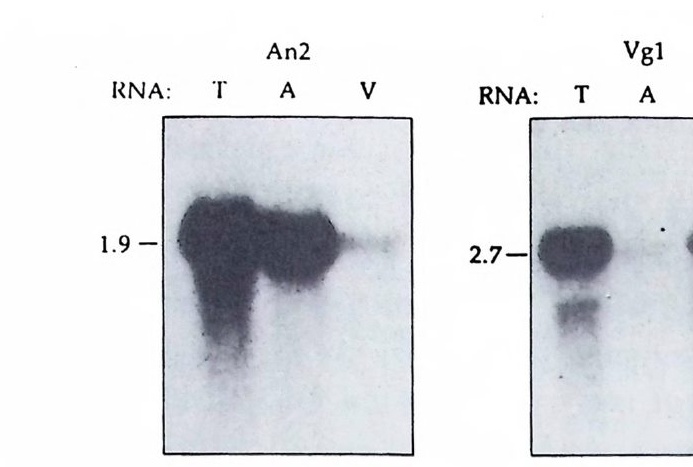 An2 Vg l
An2 Vg l
그림 8-1.4 Xenop us 난모세포의 동물국과 식물극에 분포된 특이 mRNA. RNA 를 난자 전체 (T), 동물국 반구 (A) 및 식물극 반구 (V) 에서 각각 추출하여 전기영동법으로 분리하였다. 그 다음 Nort he rn blo t방법으로 RNA 의 존재여 부를 알아내었다. 이때 사용한 DNA 는 난모세포 동물국 반구와 식물국 반 구의 메시지에 대한 cDNA 울 An2 와 V g l 을 이용하여 만든 클로운 DNA 로 방사능 동위원소로 표지한 것이다. An2 는 동물국 반구의 mRNA 와 결합하 지만 식물극 반구의 mRNA 와는 재결합하지 않는다. 반대로 Vg l cDNA 는 식물국 반구의 mRNA 와만 재결합한다 (Rebla g l i a ti et al., 1986).
RNA 에서 얻은 cDNA 와 항온처리시켜 거름종이에 있는 DNA 와 cDNA 사이에 재결합반응을 유도하였다. 재결합된 cDNA 의 방사능 울 측정하여 본 결과 대부분의 클로운은 동물극과 식물극에 상관없이 동일한 양의 cDNA 와 결합하였다. 죽 이러한 메시지가 동일하게 분 포되어 있음을 보여주었다. 그러나 클로운의 1.2 % 가량은 동물극의 RNA 에서 얻은 cDNA 에만 결합하였고 클로운의 0.2 % 가량은 식물 극의 mRNA 에서 얻은 cDNA 와 결합하였다. 이러한 결과는 수정란 의 mRNA 부위에 따라 특이하게 분포되어 있음을 보여주었다. 레바리아티와 그의 동료들은 다음 단계로 동물국이나 식물국 메시 지에 대한 특별한 DNA 를 이용하여 부위에 따라 분포되어 있는 mRNA 를 확인하였다. 즉 그들은 수정란 전체에서나 혹은 동물극이
나 식물국에서 RNA 를 추출하여 전기영동으로 분리하였다. 그 다음 이 들 RNA 를 nitr o cellulose 종이 에 옮기고 지 역 특이 쿨로운 DNA 와 재 결합시 켜 X- ra y fi lm 에 감광시 킴으로써 지 역 특이 RNA 를 확 인할 수 있었다. 3) 난모세포 메시지의 해독 조절 일반적으로 난자형성 말기에 난모세포의 mRNA 는 해독되지 않은 상태로 보존되었다가 수정 직후 해독되기 시작한다. 현재로서는 난모 세포 mRNA 의 해독 조절에 대한 가설이 다섯 가지가 있다. 그 중에 세 종류는 mRNA 의 이용도와 관계되고, 두 종류는 mRNA 해독의 효율과 관계된다. 가려 진 메시 지 (masked message s ) : 이 가설은 난모세포의 mRNA 가 단백질에 의해서 물리적으로 가려 져서 (masked) mRNA 가 리보솜에 부착될 수 없기 때문에 해독이 저 지될 것이라는 설명이다. mRNA 는 언제나 단백질과 결합되어 있는 데 , 단백 질은 RNA 의 종류에 따라 다르다. 1966 년에 스피 린 (Sp irin) 은 난모세포의 mRNA 는 infon nosome 즉 mRNA 가 단백질에 의해 서 r i boncleo p ro t e i n 의 형태로 가려진다고 하였다. 이와 같이 가려진 메시지는 리보솜에 부착이 불가능하기 때문에 해독될 수 없을 것이라 고 생각되었다. 수정시에는 메시지를 가리고 있던 단백질이 방출됨으 로써 이 메시지가 해독을 개시할 수 있을 것이라고 생각되었다. 이러한 가설을 뒷받침하는 근거로 성게 난모세포에 리보솜보다 느 리 게 침 강하는 ribo nucleop ro te i n ( RNP) 입 자가 있고, 그 입 자 속에 여러 가지 mRNA 가 존재한다는 사실이 발견되었다 (I nf an t e ahd Nemer, 196s ; Gross et al., 1973). 성게의 성숙한 난모세포의 RNP 입자에는 Poly( A ) 꼬리를 가지고 있는 mRNA 가 들어 있는데, 이들 mRNA 는 쉽게 해독되지는 않지만 이온의 변화에 따라 대단히 민감
하게 반응을 보인다. 즉 o.3 5 mM K+~ smM M g 2+ 울 포함하는 난모 세포 완충액 (난모세포의 세포질과 유사한 이온의 조성을 가지고 있는 용액)과 mRNA 로부터 단백질을 제거시킬 수 있는 0.3 5 mM Na+ 을 포함하는 용기을 이용하여 난모세포로부터 RNP 를 분리한 다음 생체 밖 해독을 시도해 보면 이온의 변화에 대한 RNP 의 민감한 반응을 알 수 있다. 난모세포 완충액으로 추출한 RNP 입자의 mRNA 의 해 독은 대단히 부전하였다. 그러나 Na + ~ 끝 포함하고 있는 용액으로 분
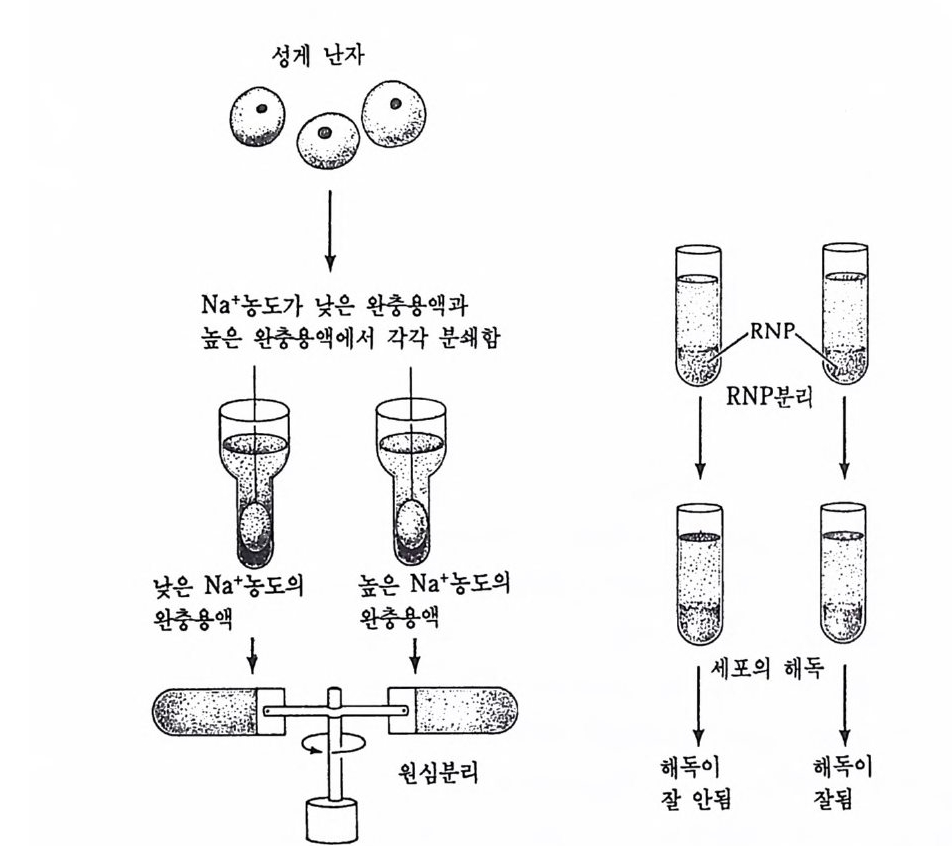 성게 난자
성게 난자
그림 8-15 RNP 내에 mRNA 의 존재에 대한 입증. 단백질과 결합한 RNA 는 Na+ 농도가 높은 완충용액에서는 해독할 수 있다. N 갑은 mRNA 를 RNP 로 부터 분리시킨다.
리한 RNP 입자의 mRNA 해독 정도는 수정 직후 수정란에서 분리한 mRNA 의 것과 유사할 만큼 활발하였다. 이러한 현상은 수정시 난자 속으로 유입되는 Na + 에 기인하는 것으로 생각되고 있는데, Na + 은 RNP 입자를 불안정하게 하여 그 속에 있는 mRNA 가 해독될 수 있 도록 작용하는 것으로 생각되고 있다 (Ra ff, 19so). 최근에는 난모세포 특유의 단백질이 난모세포에 저장된 메시지를 가리는데 (mask) 쓰이는 것으로 생각되고 있다. 난모세포는 체세포의 것과는 다른 mRNA 결합 단백질을 가지고 있는데, 이들 단백질 중 어떤 것은 mRNA 의 특별한 염기서열을 인식한다 (Aude t et a l., 1987). 즉, 굴로빈 mRNA 를 Xenop us 의 난모세포에 넣어 주면 이 mRNA 는 쉽게 해독되지만 mRNA 를 먼저 Xeno p us 난모세포의 RNP 입자로 부터 추출한 단백질과 섞어준 다음 해독시키면 이 mRNA 는 거의 해 독되지 않는다. 다른 조직으로부터 추출한 RNA 결합 단백질은 글로 빈 mRNA 와 섞어줄지라도 해독에 아무런 영향을 주지 못한다. 죽 난모세포 특유의 RNP 입자 단백질만이 모계 메시지의 해독을 조절 할 수 있다 (R ic h t er and Sm ith, 1984). 수정 직후 리보솜은 급격히 폴리솜의 형태로 바뀐다. 성게에서는 수정 전 난모세포에서 1% 의 리보솜만이 폴리솜의 형태로 존재하지 만, 수정 후 난할기에는 거의 20% 의 리보솜이 폴리송의 형태로 전환 한다. 이때 새로운 mRNA 가 합성되는 것이 아니므로, 폴리솜이 증 가하는 것은 이미 존재하던 메시지가 차출되어 폴리솜에 안착되는 것 을 의미한다. 난모세포의 RNP 입자로부터 mRNA 가 나와 폴리솜으 로 들어간다. 원래 성게 난모세포의 RNP 입자에 들어 있던 RNA 를 방사능 동위원소로 표지하여 추적하여 보면 이 RNA 가 나중에 초기 발생과정의 할구에 있는 폴리솜과 결합하는 것으로 보아 난모세포에 준비되었던 mRNA 가 RNP 입자에 저장되었다가 수정 후 차출되는 것으로 생각되었다 (Yo ung and Raff , 1979). 유사한 현상이 조개에서도 관찰되었다. 로젠탈 (Rosen th al) 과 그 동료들 (1980) 이 조개의 난모세포
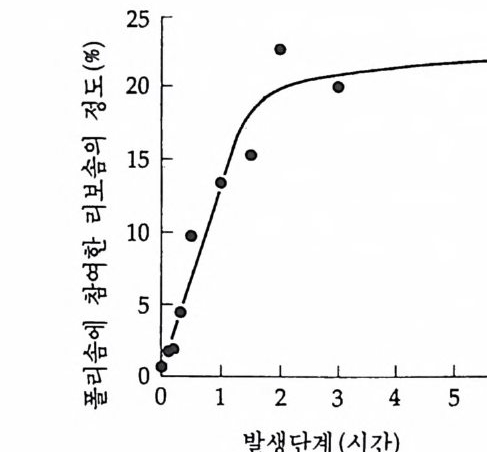 .숲버 2250 I • •
.숲버 2250 I • •
그림 8-16 성게 초기발생에 따른 리보솜으로부터 폴리솜으로의 전환
와 발생배의 RNP 입자와 폴리솜으로부터 mRNA 를 각각 추출하여 세포 밖 해독을 시도하여 본 결과 난모세포와 발생배의 mRNA 는 모 두 동일한 단백질을 지시하는 것임을 알게 되었다• 즉 난모세포와 발 생베에는 동일한 mRNA 가 들어 있지만, 폴리솜에는 각각 다른 종류 의 mRNA 가 안착되어있다. 폴리솜에 안착되어 있는 발생배 특유 단 백질에 대한 mRNA 가 난모세포에서는 RNP 입자에 자리하고 있는 것으로 나타났고, 난모세포 특유 단백질에 대한 mRNA 가 난모세포 에서는 풀리솜에서만 발견되고, 발생배의 폴리솜에서는 발견되지 않 았다. 죽 mRNA 는 RNP 입자로부터 선택적으로 차출되어 폴리솜에 안착된다. 메시지를 RNP 업자에서 선택적으로 뽑아 쓰는 현상은 초파리의 발생배에서도 관찰되었다. 머모드 (Mermod) 와 그의 동료들 (1980) 은 초파리의 난모세포와 발생배의 RNP 입자로부터 각각 p ol y (A) 를 포 함하고 있는 RNA 를 분리해낸 다음, 이돌 mRNA 를 세포 밖 해독시 켰다. 세포 밖 해독과정에서 방사능 동위원소가 표지되어 있는 아미 노산으로 단백질을 합성시킨 다음 이들 단백질을 전기영동법으로 분
석 비교하였다. 초파리 난모세포의 RNP 에서 얻은 mRNA 는 난모세 포 폴리솜에서 얻은 mRNA 에서는 합성될 수 없는 종류의 단백질을 합성하였다. 그러나 이들 단백질은 발생배의 폴리솜에서도 합성되었 다. 이러한 관찰로부터 난모세포 RNP 입자에 이미 저장되어 있던 mRNA 가 수정 후 발생배에서 선택적으로 이용된다는 점을 확인할 수 있었다 .
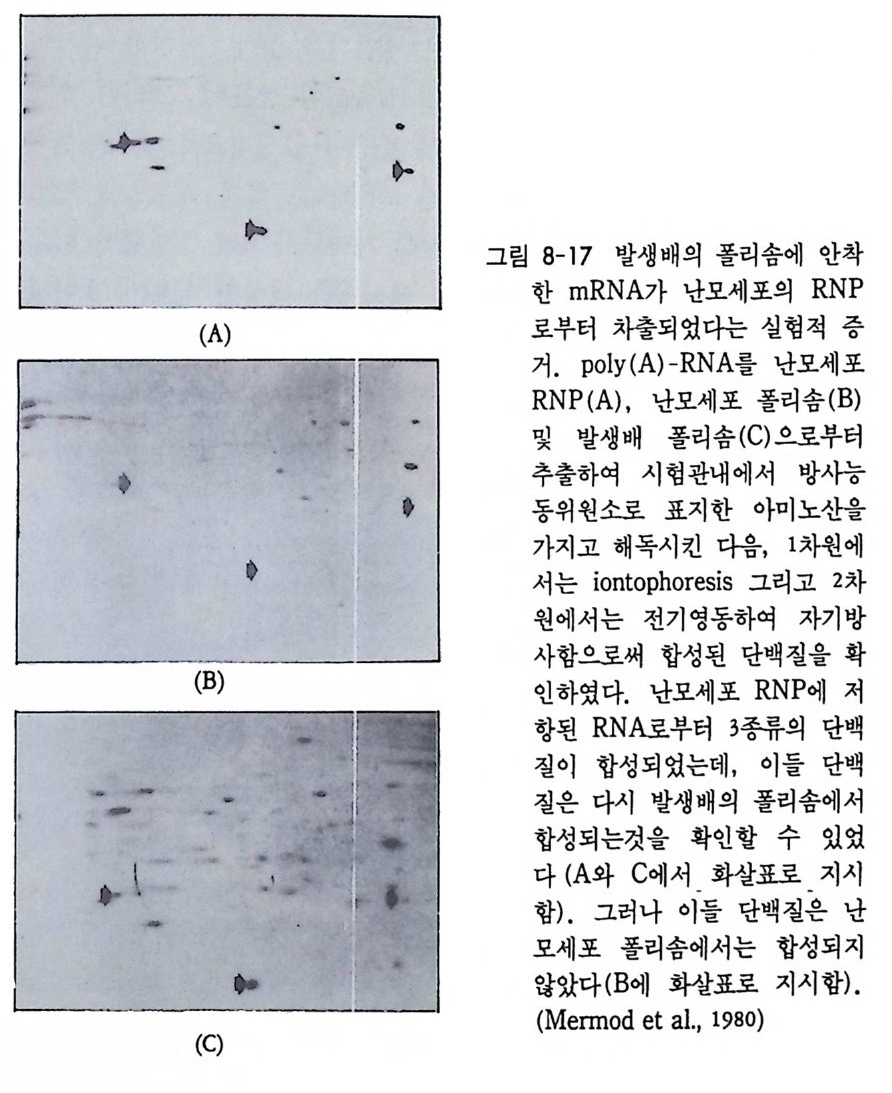 ..... ..
..... ..
Uncapp e d message s : mRNA 가 효율적으로 해독되기 위해서는 5 ' 과 3' 말단이 필요하다. Spi sula 난모세포에서는 3' 말단의 po ly (A ) 꼬리의 길이에 따라 순차 적인 RNA 해독이 영향을 받는다. 나방에서는 5'ca p의 변화를 이용하 여 해독이 조절된다 (Kas t em et al., 1982). 메시지가 효과적으로 해독 되기 위해서는 거의 모든 메시지의 5 ' 말단에 7-meth y l g u a nosin e cap 아 있어야 한다. tob acco hornworm mo th의 난모세포에 저장된 메 시지의 ca p에는 gu anos i n~ 본 있으나 메칠기가 없다. 이러한 메시지 는 세포 밖 해독과정에서도 단백질로 해독되지 않는다. 그러나 수정 시 이들 난모세포에서는 메칠기 첨가 반웅이 급진적으로 일어나면서 ca p이 완성된다. 완성된 ca p을 가전 mRNA 는 쉽 게 리보솜에 결합 되어 해독을 개시할 수 있다. 메시지를 가리든지 혹은 5' 말단이 미완 성 상태에 있든지 해독은 억제되고, 메시지는 적절한 신호가 주어질 때까지 해독되지 않는다. Seq ue ste r ed message s : 최근에는 난모세포의 RNP 입자에 둘어 있는 mRNA 가 해독될 수 없다는 데에 반론을 제기하는 연구결과가 보고되었다. mRNA 가 RNP 의 형태로 가려져 있기 때문이 아니라 오히려 단백질 합성 장치 가 구획화 (com p a rtm en ta l i zed) 되어 있어서 RNP 내에 있는 mRNA 가 리보솜에 접근하는 일이 어려워지기 때문에 해독아 억제된다는 것이 다 (Moon et a l., 1982). 성게 난모세포내의 히스톤 mRNA 가 이러한 방식으로 조절되는 것으로 보인다. 난모세포내의 히스톤 mRNA 는 세포질에서는 발견되지 않고 핵에서만 발견된다. 핵이 붕괴될 때에만 히스돈 rnRNA는 세포질 속으로 들어가게 된다 (DeLeon et a l., 1983). 이러한 경우는 다른 종류의 메시지에는 적용이 안된다. 난모세포내의 전체 mRNA 중 0.1% 이하만이 핵에서 발견되고 (An g erer and Ang er er, 1981) 액틴과 듀불린 단백질에 대한 메시지롤 포함하고 있는
 70 분 80 분
70 분 80 분
그림 8-18 성게 난모세포의 히스돈 메시지의 격리 저장• 히스돈 메시지에 대한 cDNA 를 만들어 수정 후 여러 단계의 성게 알을 고정하고 ifl situ 재결합법 으로 히스톤 메시지의 위치를 확인하였다• (DeLeon et al., 1 983).
RNP 입자들은 주로 세포질 속에 있다 (Showman et a l., 19s2). 리보솜 은 물론 모계 메시지도 세포골격 (c yt oskele t on) 에 부착되어 있다는 관 찰을 통해서 아마도 세포골격이 mRNA 를 리보솜에서 분리하는 데 관여할 것이라고 추측되고 있다 (Moon et al., 1983). 해독효율의 번화: 앞에서 설명한 해독조철에 대한 모델에서는 해독장치는 어떤 종류
의 mRNA 라도 효율적으로 해독할 수 있지만 mRNA 와 리보솜은 물 리적 혹은 화학적 방법에 의해 분리되어 있어야 한다는 점이 전제되 고 있다. 그러나 이러한 장치가 없을지라도 난모세포질의 낮은 p H 로 인해 단백질 합성이 억제될 수 있다. 성게에서는 수정시 수소이온이 방출되어 세포질의 p H 가 6.9 에서 7 .4로 상승한다. 윙클러 (W i nkler) 와 슈타인하트 (S t e i nhard t, 1981) 는 성게 난모세포질을 가지고 세포 밖 해 독장치를 준비하고 두석을 이용하여 세포질의 p H 를 바꿔가면서 방사 능으로 표지 된 va li ne 을 사용하여 단백질 합성을 측정 하였다. 즉 mRNA 를 의부에서 별도로 첨가해 주지 않을지라도 난모세포질의 pH (pH 6.9 ) 를 수정 란의 수준 (pH 7.4 ) 으로 상승시 켜 주면 수정 란에 서
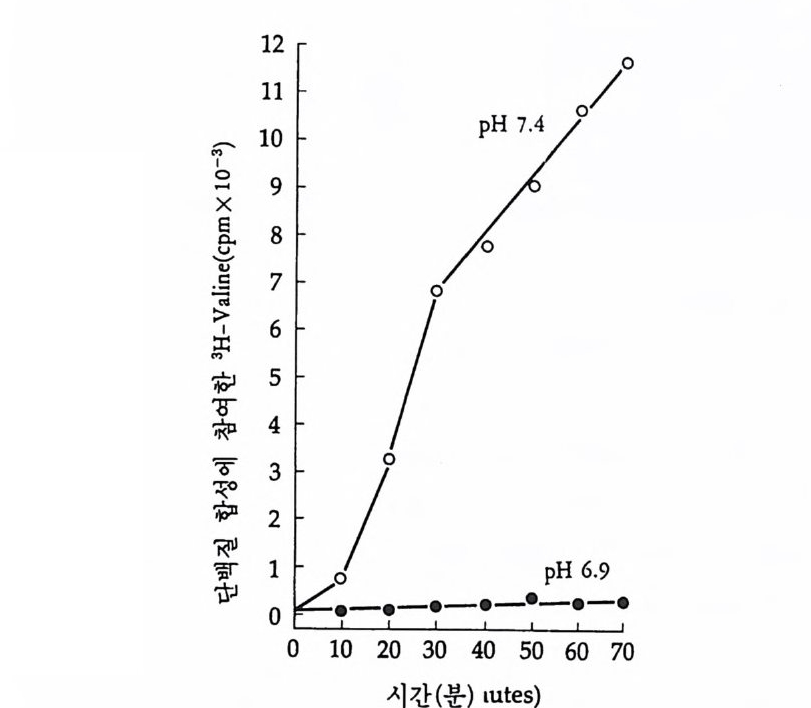 210987654321
210987654321
그림 8-19 p H 에 따른 단백질합성율의 변화 (W i nkler and Ste i n h ardt, 1981)
일어나는 정도로 단백질 합성이 폭발적으로 증가하는 것을 관찰할 수 있었다. 힐라 (H ill e) 와 그의 동료들 (1985 ; Dan ilch ik et al., 1 · 9s6) 은 아마도 p H 의 변화가 난자의 해독장치를 활성화시켰을 것이라고 주장하고 있 다. 난모세포에서 얻은 리보솜과 개시요인은 수정란에서 얻은 리보솜 보다 해독 활성도가 훨씬 낮다. 더구나 미수정란에 글로빈 mRNA 를 넣어줄지라도 단백질 합성정도가 더 이상 증가하지 않는데, 아것은 마수정란 속에 있는 해독장치의 크기가 한정되어 있기 때문에 글로빈 mRNA 가 해독될 때 나타나는 제한현상으로 보였다. 개시요인인 eIF-2B(GTP- 결합요인)나 eIF-4F(cap 결합단백질)를 미수정란 추출 액에 첨가해 주면 그 추출액에서의 해독효율이 증가 하는 것으로 보 아 제한요인은 개시요인 자체일 것으로 생각되고 있다 (Col i n et al., 1987 ; Lop o et al. , 1988). 또 다른 요인은 p H 인데, 미수정란의 pH 를 상승시켜 주면 가려졌던 mRAN 가 벗겨지고 개시요인이 활성화된 다. 즉 p H 를 울려 주면 mRNA 와 리보솜의 결합이 3 배나 증가한다 (Wi nk ler et al., 1985). 더구나 난모세포의 mRNA 가 비로솜에 결합 된 경우를 별로 찾아볼 수 없는데, 아마도 성게에서는 해독개시 요인 울 활성화시키는 것은 물론 메시지의 이용도를 변화시컴으로써 해독 을 조절할 가능성도 있다. 저장된 mRNA 를 해독 수준에서 조절하는 데에는 여러 가지 방법이 있으나 동물에 따라 다소 차이가 있다. 4) 모계 mRNA 와 난할 성게에서 난할이 일어나기 위해서는 저장된 모계 mRNA 로부터 합 성된 단백질의 지속적인 공급이 필요하다. 만약 성게알을 해독억제제 속에서 수정시키면 비록 두 개의 전핵이 융합할지라도 난할은 일어나 지 않는다. 방추사가 형성되지 않고 염색체 응축도 일어나지 않고, 핵막도 붕괴되지 않는다 (Wa g enaar and Mazia , 1978). 즉 모계 메시지 에 의해 특별히 만들어진 단백질이 세포분열에 필요하다.
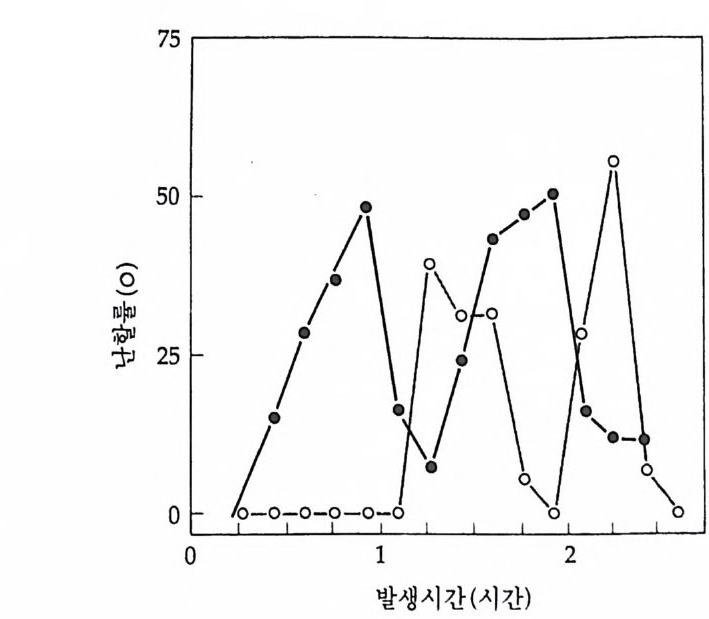 75
75
그립 8-20 성게 발생중 난할에 따른 c y cl i n 수준의 변화. 난자를 방사능 동위원 소로 표지한 아미노산으로 처리한 다음 10 분마다 세포분열하는 세포의 백분 율과 주기성을 띠고 있는 단백질의 존재여부를 확인하였다. 이러한 단백질 의 양은 세포주기중간에 가장 높고, 붕괴되었다가 다시 합성된다 (Evans et al., 1983) .
이러한 가설은 c y cl i n 이라는 단백질을 발견하게 되면서부터 크게 지지를 얻었다 (Evans et a l., 1983). c y cl i n 에 대한 mRNA 는 미수정란 에서는 검출되지 않으나, 일단 수정이 일어나면 c y cl i n 의 합성이 급 격히 증가하는 것을 볼 수 있다. c y cl i n 은 세포분열에 사용된 다음 붕괴되고 다시 모계 mRNA 에 의해 새롭게 합성되는데 c y cl i n 의 합 성은 포배 말기에 접근하면서 점차 감소하는 경향을 보인다. 처음에 는 c y cl i n 이 성게에서만 검출되었으나 나중에는 다른 종류에서도 검 출되었다. sur f clam 에서도 단백질 A 와 B 는 모두 c y cl i n 으로 세포주 기와 밀접한 관계를 가지고 있다. 수정 후 이들 단백질은 모계 저장 mRNA 로부터 지속적으로 합성되어 세포주기의 S 기와 M 초기에 축적
되었다가 세포분열중 붕괴된다. cyc l in A 를 Xenop u s 난모세포에 주 사해 주면 감수분열이 유도되는데, 이러한 점으로 보아 c y cl i n 은 세 포분열의 시간을 조절하는 것으로 생각되고 있다. 5) 기타 해독 수준에서의 조절의 예 분화된 세포에서의 유전자 발현은 호르몬에 의해 유도되는 경우가 있다. 어떤 경우에는 호르몬이 전사에 관여하지 않고 해독수준에서 작용하여 그 효과를 나타낸다. 우유의 주요 인 단백질인 case i n 의 합 성도 이러한 경우 중의 하나로서 p rolac ti n 에 의해 조절된다. 이 때 p rolac ti n 은 실제로 casein mRNA 의 전사에 있어서는 단지 2 배 정도 의 증가효과만을 나타낼 뿐이고 오히 려 casein mRNA 를 안정시켜 줌으로써 case i n 합성을 조절한다 (Gu y e tt e et a l., 1979). p rolac ti n 의 이 러한 작용으로 casein mRNA 의 수명은 다른 메시지에 비해 약 25 배 가량 더 길다. 결과적으로 casein mRNA 는 여러 차례 해독과정을
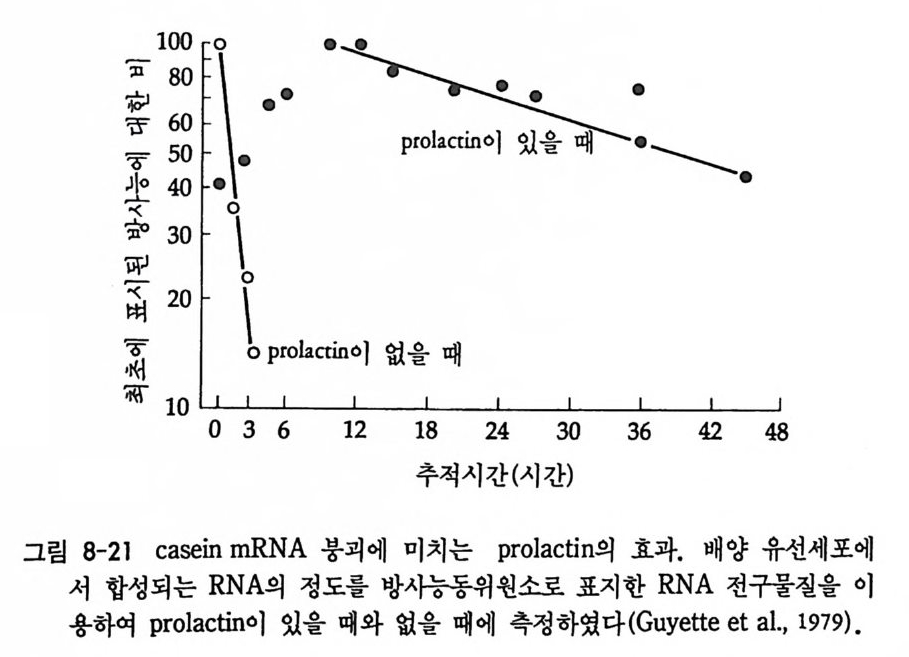 R需 plfY벼l{T守Yf止lRpl 1 008\\\0p이\\0\o0 6•0•o5la0 •二ct m14P•2。0· r 3:없01을28 60-때1024 - 3-0 3-6 •42 48
R需 plfY벼l{T守Yf止lRpl 1 008\\\0p이\\0\o0 6•0•o5la0 •二ct m14P•2。0· r 3:없01을28 60-때1024 - 3-0 3-6 •42 48
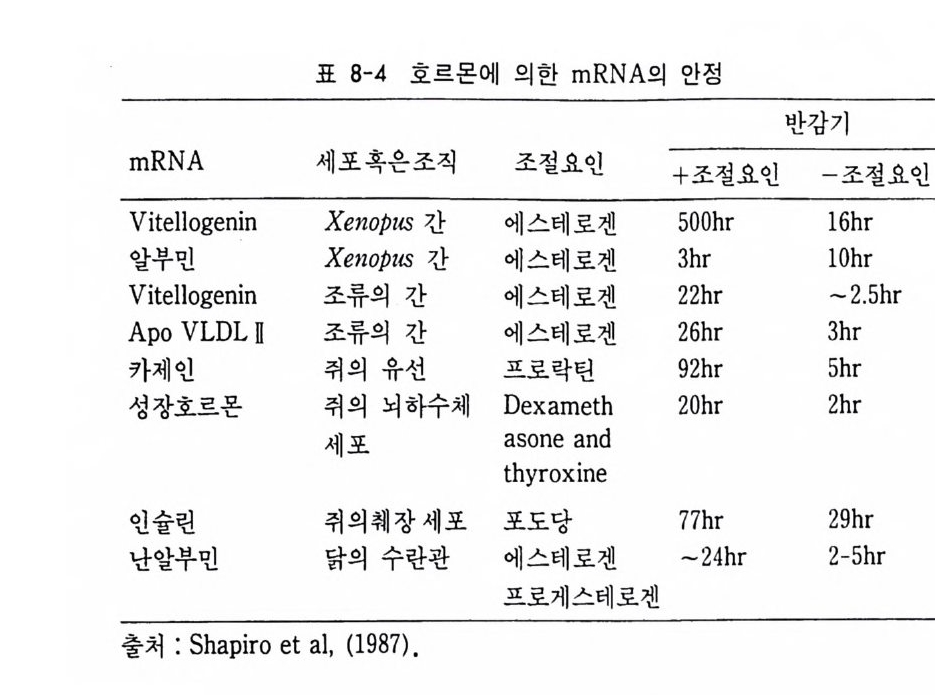 표 8-4 호르몬에 의 한 mRNA 의 안정
표 8-4 호르몬에 의 한 mRNA 의 안정
반복하므로 메시지 당 합성되는 case i n 의 분자수가 많아진다 . 해독 수준에서 유전자 발현을 조절하는 경우를 i nsul i n 합성에서도 찾아볼 수 있다. 췌 장의 8- 세 포에 서 p ro i nsu li n 이 합성 되 는데 , 이 때 포도당을 주면 p ro i nsul i n 의 합성률이 10 배 정도 증가한다. ins ulin cDNA 를 만들어 췌 장의 8- 세포 내 의 ins ulin mRNA 의 양을 측정 해 보면, B- 세포어} 포도당을 처리했을 때나 하지 않았을 때에 p ro i nsul i n 의 mRNA 양에 큰 차 이 가 나타나지 않았다 (I t oh and Oka ino to , 19so). 이러한 점으로 보아 포도당에 의한 i nsul i n 합성 촉진 은 일종의 해독 수준에서의 조절로 볼 수 있다. 적혈구와 포유류나 조류의 배 양 세포에도 prosome 이 라고 하는 mRNP 가 있는데 난모세 포의 inf ormosome 과 유사하게 RNP 에 결합된 mRNA 의 해독을 억 제하고 있다 (de Sa et al., 1986 ; Akhay at et al., 1987). 탈수된 염수산 작은 새우 (b rin e shrimp)의 발생배를 활성화시키는 것도 역시 해독 수 준에서의 조절로 생각되고 있다. 염수산 작은 새우의 발생배는 발생
을 시작할지라도 발생중에 장기간의 휴지기에 들어갈 수 있다. 휴지 기간 동안에는 발생배 속에서 단백질합성 억제제에 의해 단백질 합성 이 일어나지 않지만 일단 재활성화되면 eIF2 의 농도가 20 배나 증가 한다 (F ilip ow ic z et a l., 1975). 더구나 시에라 (S i erra, 1977) 은 이러한 억 제제가 pro te i n k i nase 일 가능성이 있는 것으로 보아 헤모글로빈 합 성을 조절하는 기구와 동일한 기구가 염수산 작은 새우의 발생배에서 도 작용할 것이라고 생각하였다. 정자에서도 어떤 유전자의 발현은 해독수준에서 조철되는 것으로 보인다. 정자에서도 난자에서와 갇이 메시지를 저장하였다가 후에 이 용하는 경우가 있다. lacta t e deh y dro g enase-X(LDH-X) 는 조류와 포유류의 정자 형성 말기에만 합성되는데, LDH-X 유전자는 정자형 성 전 과정에 걷쳐 발현되지만 (Blanco, 19so) 저장된 mRNA 의 해독 은 정자형성 말기에 일어난다. a p olip o p ro t e i n-B(A p o-B) 단백질도 해독수준에서 조절되는 단백질 중의 하나이다. Ap o- B 단백질은 혈장 내의 지방 담체로서 동맥경화 증을 일으키는 데 중요한 역할을 한다. Ap o -B 48 (4s KD) 은 장에서 합성 되 어 chy lo mi cr on 결 합체 를 이 룸으로써 콜레 스테 롤과 trig ly c e r- i des 의 흡수와 투과를 조절한다. Ap o -B 100(100 KD) 은 간에서 만들 어져서 대단히 낮은 밀도의 지방 담체 단백질의 주성분이 된다. 이들 Ap o -B 100 와 Ap o -B 48 단백 질은 모두 동일한 유전자로부터 전사된 RNA 의 해독에 의해 합성된 것이지만, RNA p rocess i n g에서도 두 종류의 mRNA 를 생산해낼 수 있는 순차성이 관찰되지 않는 것으로 보아 이들 단백질의 발현도 해독 수준에서 조절되는 것으로 생각되고 있다. Ap o -B cDNA 를 분석하여 보면 간세포에 있는 Ap o -B 메시지 는 Ap o -B 100 펩티드 전체를 지시한다. 그러나 장세포의 Ap o -B 메 시지는 간세포의 메시지와 염기 한 개만이 다르다. 죽 C 가 U 로 바뀜 으로 인하여 정상적으로는 g lu tami ne 코돈 (CAA) 인데 정 지 코돈인 U 무 바뀐다. 이러한 염기상의 차이로 인하여 장세포의 Ap o- B 48
단백질은 Ap o -B 100 보다 짧은 폴리 펩티드로 된다 (Powell et al., 1987 ; Chen et al., 1987). 지금까지는 메시지의 염기서열이 일단 형성 되면 바뀔 수 없다고 생각되어 왔는데 이 경우는 mRNA 에 직접 염 기상의 변화가 일어난 것으로 대단히 특이한 예이다. 2 후 해독 수준에서의 유전자 발현의 조절 단백질은 세포구조의 구성성부이 된다든가 혹은 효소로서 세 포 내에 서 일어나는 여러 가지 화학반응을 촉진함으로써 그 기능을 나타내게 되며, 여러 가지 단백질의 종합적인 기능이 세포의 기능으로 나타난 다. 따라서 단백질이 합성된 후에는 다른 단백질들과 관계 를 맺으며 세포 내의 복잡한 체제로 홉수되어 그 체제의 일부를 이룬다. 따라서 단백질이 합성된 후에도 적절한 기능이 부여될 때까지는 단백질에 여 러 가지 변화가 일어난다. 이러한 변화는 크게 4 가지 영역으로 나누 어 생각해 볼 수 있다. 첫째로 새로 합성된 단백질이 더 이상 변화되 지 않으면 불활성화된 상태로 남아 있게 된다. 즉 이러한 변화를 통 하여 단백질을 불활성화시키는 억제 요인이 제거되거나 혹은 작은 분 자의 화합물과 결합하여 단백질의 활성도가 회복되는 경우이다. 둘째 로, 어떤 단백질은 선택적으로 불활성화될 수 있다. 단백질 전체가 불활성화되는 경우도 있으나 어떤 때에는 inh ib i t or y l ig and 와 결합하 여 불활성화되는 경우도 있다. 셋째로, 어떤 단백질은 세포내 특별한 위치로 옮겨져야만 한다. 죽, 세포는 단순히 효소를 포함하고 있는 자루와 같은 것이 아니다. 어떤 단백질은 막 구조, 리소좀 혹은 미토 콘드리아와 감은 특정한 구조물 속에 분리 보관되어야 한다. 넷째로, 어떤 단백질들은 다른 단백질들과 결합하여 기능적인 복합체를 만들 기도 한다. 헤모글로빈, 미세소관, 및 리보솜은 모두 여러 개의 단백 질이 결합하여 형성된 기능적인 복합체의 예들이다. 이러한 관점에서
보면 후 해독 수준에서까지도 유전자 발현에 변화가 있을 수 있다는 것이다. (1) 후 해독에 의한 단백질의 활성화 많은 폴리펩티드는 새로 합성된 후에 즉시 기능적인 단백질이 되는 것이 아니고 일정한 아미노산 부위가 절단되어야만 드디어 활성화된 다. 인슐린의 전구체도 세 개의 이황화 결합을 가지고 있는 상당히
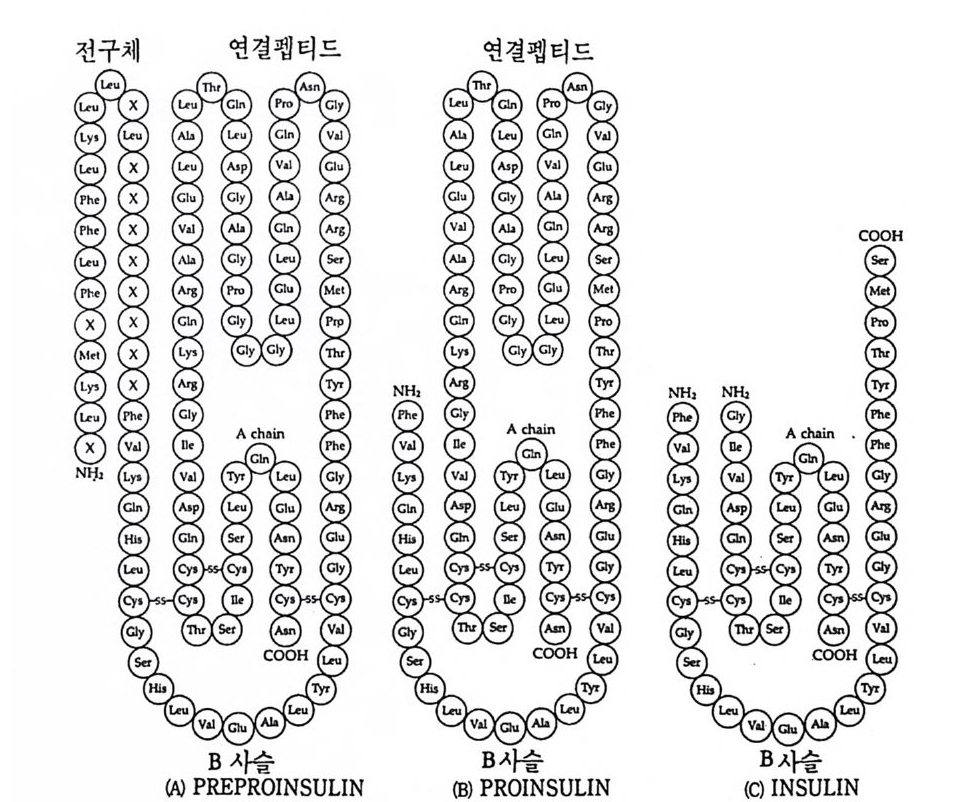 전구체 :드 연결펩티드
전구체 :드 연결펩티드
그립 8-22 쥐의 인슐린 Il 의 아미노산 배열순서(검게 칠함). 인슐린 분자는 pre pr o in s uli n 그리고 p ro i nsul in에서 아미노산의 일부가 제거됨으로써 i nsul in으로 성숙한다.
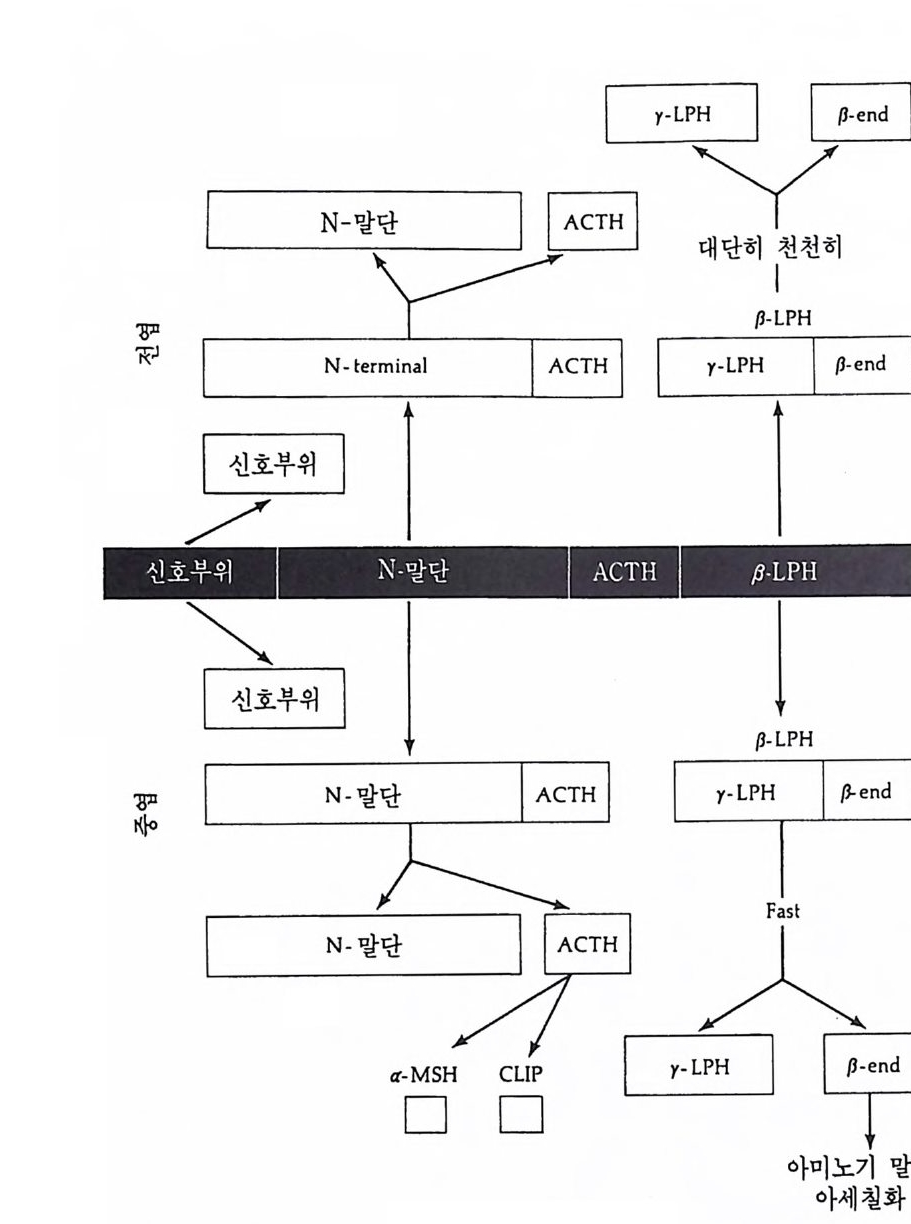 二\대단히 三 |천 천히
二\대단히 三 |천 천히
그림 8-23 취의 뇌하수체 중엽과 전염에서의 pro -ACTH-endorp hin 성숙과정. ACTH : adrenocort ico tr op i c hormone, {3- en : {3- endorph i n , r-LPH : r-lipo tr op i n, a-MSH : a-melanocyt e- stim u lati ng hormone (Herbert et al., 1981).
긴 폴리펩티드이지만 폴리펩티드의 가운데 부분과 처음 부분이 절단 된 다음에야 비로소 활성화된다. p re p ro i nsul i n 을 이루는 아미노산의 일부가 절단되면 이황화결합으로 이어진 두 조각의 폴리펩티드가 남 는데 이 것 이 활성 화된 분자이 다. pro ACTH-endor p h i n 의 경 우물 보 면 한 종류의 폴리펩티드로부터 부신피질호르몬 (adenoco rtic o t ro pi c hormone, ACTH), y-lip o tr o p in( r-LPH), 및 /3- endorph in 등의 다양 한 단백질이 절단과정을 통하여 만들어진다. 다양한 단백질 형태로의 절단은 세포의 종류에 따라 다르다. 즉, 뇌하수체 전영에서는 ACTH 가 최종적으로 생성되는 단백질이다. 그러나 중엽에서는 ACTH 는 절제되어 a- 색소세포 촉진 호르몬 (a-melanoc yt e stim ulati ng hormone, a-MSH) 으로 된다 (Herbe rt et a l., 1981). 어떤 단백질은 작은 분자와 공유결합으로 연결되어야만 그 기능을 나타내고, pho sph o r- yla se k i nase 는 인 산화되 어 야만 활성 화되 어 효소의 기 능을 나타낸다. colla g en 은 아미노산 성분 중 p rol i ne 과 l y s i ne 이 히드록실화되어야만 그 기능을 나타낸다. 만약 특정한 아미노산의 히드록실화가 일어나지 않으면, 심각한 질병이 발생한다. 후 해독 수준에서 히스톤에 변경이 생기면 전사조절이 영향받는다. 변형균의 일종인 Phys a rum p oly c ep halum 에는 세포의 경계가 없기 때 문에 모든 핵은 고르게 조절된다. 이러한 특칭 때문에 변형균은 세포 주기를 연구하는 데 대단히 훌륭한 재료이다. H4 히스톤은 아세칠화 (acety la ti on ) 정도에 따라서 여러 가지 형태로 존재하며 전사활성도 룰 촉진한다. 반대로 Hl 히스톤이 인산화되면 염색체의 응축활동은 촉진되고 전사 활성도는 위축된다. 죽, 히스톤 단백질의 인산화와 아 세칠화 정도에 따라서 전사 활성도가 조절될 수 있다. (2) 후 해독에 의한 단백질의 불활성화 이미 존재하고 있는 단백질을 변경시킴으로써 그 단백질을 불활성
화시킬 수도 있다. 즉, 개시요인 2(in i ti at in g fac to r 2) 가 인산화되면 불활성화되는데, 이러한 방법에 의해서 헤모글로빈 합성이 조절된다. gly c o g en s ynth e t ase 와 pyruv ate k i nase 도 인 산화에 의 해 서 불활성 화 된다. glu ta m i ne s ynth e t ase 는 AMP 가 첨가되면 불활성화되기 때문 에 이 효소는 AMP 의 첨가와 절단에 따라 정확하게 조철될 수 있다. 어떤 경우에는 단백질이 세포내에 필요 이상으로 존재하면 세포에 해로울 수가 있다. 즉 세포분열과 관계되는 단백질들은 DNA 합성과 세포증식간의 협동적 조화를 이루기 위해 빠른 속도로 붕괴되어야만 한다. 이 렇 게 빨리 붕괴 되 는 단백 질들은 pro lin e , glu ta m ate , serin e , th reon i ne 과 같은 아미노산이 풍부한 부위 를 가진다 (Ro dg er et a l, 1986). 오랫동안 보존되는 단백질에서는 이러한 아미노산의 모임을 찾아볼 수 없다. 단백질 수명의 가장 중요한 결정 요인은 아미노기 말단의 아미노산이다. 이러한 사실을 확인하기 위하여 바흐메어
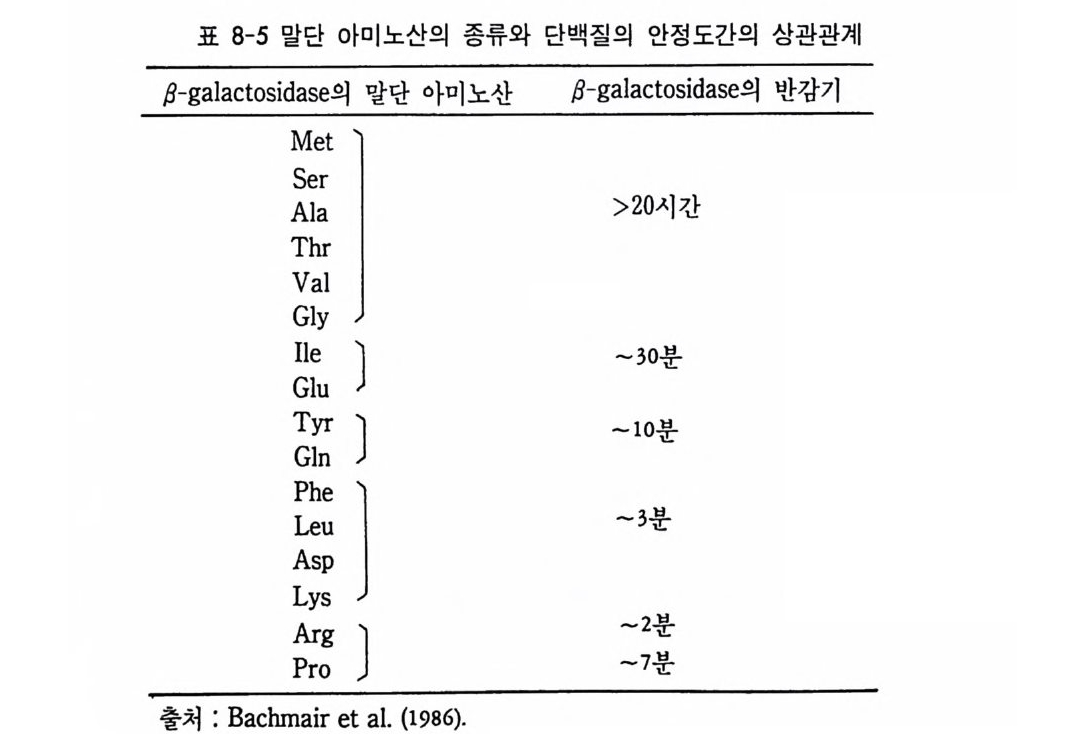 표 8-5 말단 아미노산의 종류와 단백질의 안정도간의 상관관계
표 8-5 말단 아미노산의 종류와 단백질의 안정도간의 상관관계
(Bachma i r) 는 (1986) 는 클로운된 /3-g alac t os i dase 의 유전자에 돌연변 이를 일으킴으로써 개시코돈 (AUG) 을 15 종류의 다른 아미노산을 지 시하는 코돈으로 바꾸어 해독시킨 다음 그 단백질들의 수명을 알아보 았다. 아미노기 말단 아미노산으로 me t h i on i ne 을 가진 정 상적 인 /3-g alac t os i dase 의 반감기는 20 시간인 반면에 아미노기 말단 아미노 산을 다른 아미노산으로 바꾸어 주었을 경우 반감기는 3 분 이하로 떨 어졌다.
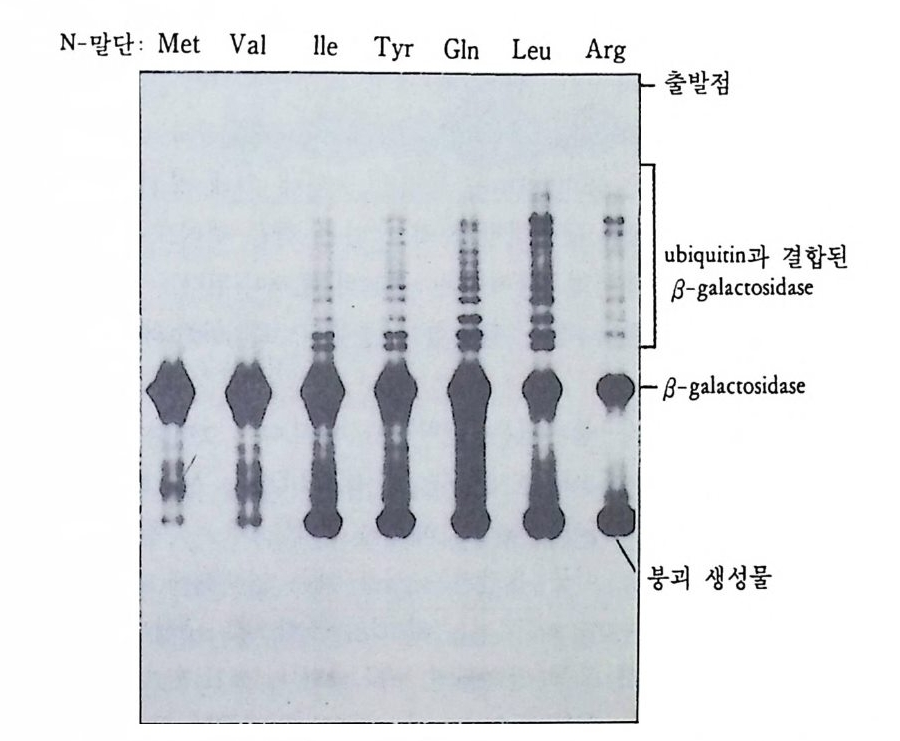 N- 말단 : M••e t V”al •lie •T디..C..y .. .• . r G•급.-』i .n L',Ie u저 A....r, Lg \.. I I\f -붕I {3출 괴/ -3g발- ga생점a la lac성 crot물so si di da as see
N- 말단 : M••e t V”al •lie •T디..C..y .. .• . r G•급.-』i .n L',Ie u저 A....r, Lg \.. I I\f -붕I {3출 괴/ -3g발- ga생점a la lac성 crot물so si di da as see
그림 8-24 아미노기 말단의 아미노산의 종류에 따른 /3-g alac t os i dase 의 붕괴 정도의 차이. 아미노기 말단의 아미노산을 다르게 지시하는 유전자를 풀라 스미드에 조합시킨 다음 효모에 삽입시켜 방사능 동위원소의 아미노산으로 이 유전자에 의해 새로 합성되는 단백질(/3-g alac t os i dase) 를 표지하였다. 그 다음 항체를 이용하여 침전시켜 항체와의 결합체로부터 /3-ga lacto s id a se 를 분리시켜 전기영동 및 자기 방사함으로서 이 효소의 붕괴 정도를 알아보 았다 (Bachma i r et al., 1986}.
단백질의 수명과 아미노기 말단 아미노산과의 관계의 예는 다른 단 백질의 경우에서도 찾아볼 수 있다. 세포가 죽을 때 단백질의 아미노 기 말단의 아미노산이 변경되는 것을 관찰할 수 있다 (So ff er, 19so ; Shyn e -Ath w al et al., 1986} . argi ni n e , lys i n e , leuc ine , phe ny la lanin e , tyros in e 등이 아미노기 말단에 자리하게 되면 그 단백질의 안정성을 해치는 결과를 초래한다. 바흐메어는 단백질의 파괴는 특별한 요인이 단백질에 결합됨으로써 유발될 것이라고 전제하면서 이러한 녹별한 요인은 아마도 아미노기 말단의 아미노산의 종류에 따라 달라질 것이 라고 주장하였다. 즉 단백질의 안정성을 해치는 아미노산이 아미노기 말단에 자리할 경우 특별한 요인과의 결합 가능성은 더 높아진다는 것이다. 이러한 요인이 일단 결합하면 이 요인은 단백질과 ubiq u it in 과의 결합을 유도한다. ub iq u iti n 은 특별한 요인에 의해 붕괴의 표적 이 된 단백질의 l y s i ne 과 공유결합을 하고 있는 작은 펩티드인데, 일 단 ubiq u it in 이 결합하면 단백질은 붕괴의 표적이 된다. /3-g alac t os i dase 단백질의 경우 많으면 15 종류의 ub iq u iti n 과의 결합 을 하기도 한다. 세포의 종류에 따라 붕괴되는 단백질도 다르다. 그러한 예로서 lacta t e dehyd r og en ase (LDH) 를 둘 수 있는데 , LDH 는 두 개 의 서 로 다른 유전자에 의해서 지시된다 . 즉 하나는 LDH - A 를, 다른 하나는 LDH-B 를 지시하는데, 이들 유전자는 서로 다른 염색체에 자리하고 있다. LDH 는 4 량체 (tet r am er) 로서 A 와 B 의 조합으로 구성 된다. 만 약 두 종류의 유전자가 모두 발현되면, A4, A3Bl, A2B2, A1B3, B4 와 같이 5 가지 상황의 LDH 동위효소가 가능하다. LDH 동위효소는 각각 세포의 형편에 따라 다른 촉매효율을 가진다. 만약 두 종류의 유전자가 동일하게 발현되고 조합이 무작위적으로 일어난다면, 동위 효소의 생성비율은 l(A4) : 4(A3Bl} : 6(A2B2} : 4(A1B3) : l(B4) 이 된다. 이때 B 형의 단백질은 A 형의 단백질보다 더 음전하를 띤다. 죽, 동위효소는 종류에 따라 다른 전하를 띤다. 이와 같은 특성을 이
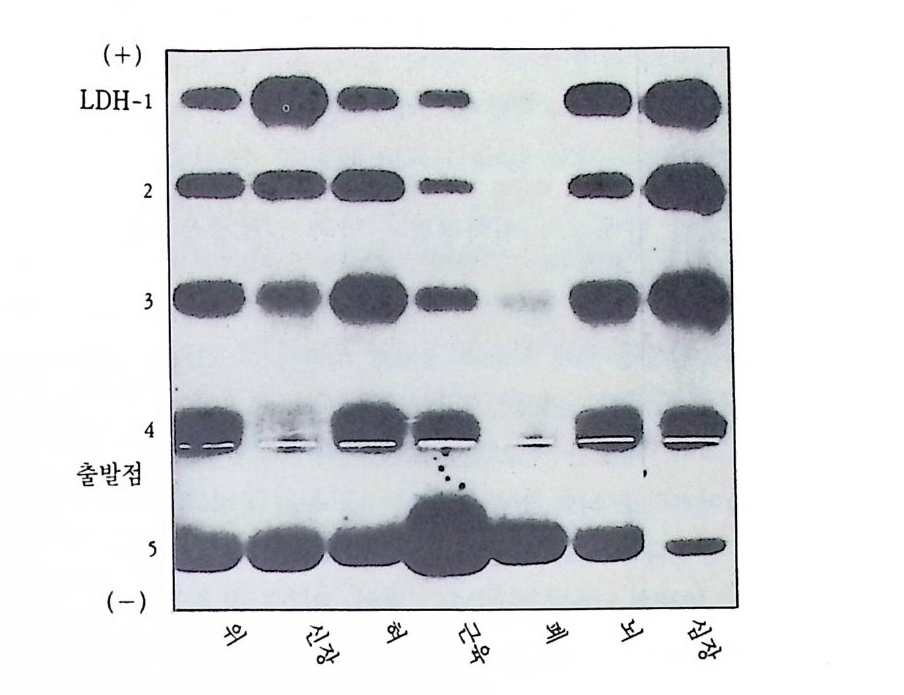 (+) •-•-』 . --
(+) •-•-』 . --
그림 8-25 쥐의 여러 가지 조직에 서 발견되는 lacta t e deh y dro g enase(LDH) 동 위 효소 의 양 적 차이 .
용하여 5 가지 형태의 동위효소를 전기영동으로 분리시켜 촉매 기능을 알아볼 수 있다. 만약에 A 형과 B 형을 동일한 양으로 섞어주면, A 형 과 B 형의 조합으로 이루어지는 동위효소의 비는 1 : 4 : 6 : 4 : 1 이다. 그러나 기관의 종류에 따라 동위효소의 비를 개별적으로 보면, 그 비 는 무작위적 조합에 의해 생긴 비와는 상당한 차이룰 보인다. 근육의 LDH 는 주로 A 형으로 이루어져 있는 반면에 정소, 심장, 신장의 동 위효소는 주로 B 형으로 구성되어 있다 (Marke rt , 1968). 프릿츠 (F rit z, 1969) 는 A 형에 대한 LDH 항체를 이용하여 여러 조 직에서의 LDH-A 의 합성율을 알아 보았는데, 그 합성율이 조직에 따라 변하지 않는다는 사실을 알아내었다. 그러나 동위효소의 붕괴울 은 조직에 따라 상당한 차이를 나타낸다. 즉, LDH-A 의 붕괴율은
골격근에서 보다 심장근에서 22 배나 높다. 이러한 점으로 보아 LDH 동위효소의 조절은 전사 수준이나 해독 수준에서 일어나는 것이 아니 고, 효소 붕괴 수준에서 일어나는 것이라고 할 수 있다. (3) 세포내 단백질의 위치결정 ―막과 리소좀을 위한 표적단백질 단백질은 합성된 후에 세포내 적절한 부위에 그 자리 를 잡게 된다. 즉 단백질은 세포질, 미토콘드리아, 리소좀, 소포체, 혹은 핵 속 에 위치하게 되며, 때로는 세포 밖으로 분비되기도 한다. 리소종이나 소 포체로 들어가기로 되어 있는 단백질이나 혹은 분비되기로 되어 있는 단백질은 합성되는 동안 일단 조면소포체내로 들어간다. 이 들 단백질 들은 약 30 개의 아미노산으로 되어 있는 신호영기서열 (s ign al se q uence) 을 가지고 있는데, 이 신호영기서열은 세포질내에 있는 신 호 수용 복합체 (sig na l recept or com p lex) 에 의해 인식된다. 이 신호 수용 복합체가 리보솜에서 성장하고 있는 폴리펩티드에 결합하면 해 독이 중단되었다가 소포체에 있는 dockin g p ro t e i n 에 결합되면서 해 독은 재개된다. 성장하는 폴리펩티드가 소포체막을 통하여 일단 소포 체 안으로 들어가면, 신호영기서열은 제거되면서 남아 있는 단백질에 변 화가 생 긴 다 (Blobel and Dobberste in , 1 975 ; Walte r and Blobel, 1 983 ; Weid m ann et a l., 1987) . 만약 단백 질에 소수성 부위 가 있다면 그 단백 질은 소포체의 막구조의 일부가 되었다가 나중에 세포막의 일부가 될 수 있다. 이러한 과정에서 한 가지 중요하면서도 풀기 어려운 문제의 하나는 어떻게 막의 특정된 부위에 단백질들의 위치결정이 이루어지 는지에 관한 것이다. 즉, 세포의 원형질막에는 세포의 종류에 따라 특이한 단백질이 막의 한쪽에만 분포되어 있는데, 어떻게 그러한 단 백질의 위치 결정이 가능한지 알 수 없다. 이와 유사한 현상을 포유 류의 초기 발생에서 할구들이 서로 밀착되기 (comp ac ti on ) 이전에 형 성되는 할구의 국성 (p olar ity)에서도 찾아볼 수 있다. 즉 세포막의 기
저부와 상위부에 각각 특이한 아미노산이 있을 것이라고 생각되고 있 는데, 이 점에 대해서는 아직 확실치 않다 (Mos t ov, 1987). 단백질을 변화시키는 방법의 하나는 mannose-8- p hos p ha t e 를 단백 질에 첨가하는 것이다. 이렇게 첨가된 당류는 당단백질을 리소좀으로 분리시키라는 신호로서 작용한다. mannose-o- phosp ha t e 는 소포체의 특정 부위에 자리하는 수용분자에 의해 인식되는데, 이러한 방법으로 소포체는 같은 신호를 가지고 있는 효소들을 한 자리에 모을 수 있 다. 그 다음 이 부위의 소포체가 떨어져 나와 리소좀울 형성하게 된 다 (Sl y et a l., 1981). 만약 수용분자와의 결합이 이루어지지 않으면 이 둘 단백질들은 세포 밖으로 분비된다. 이러한 현상에 대한 증거는 I 세포 질환이라고 하는 일종의 치사 유전 증후군에서 찾아볼 수 있는 데, 이 질환을 가진 환자는 mannose-8-ph o sph a te 신호를 단백질에
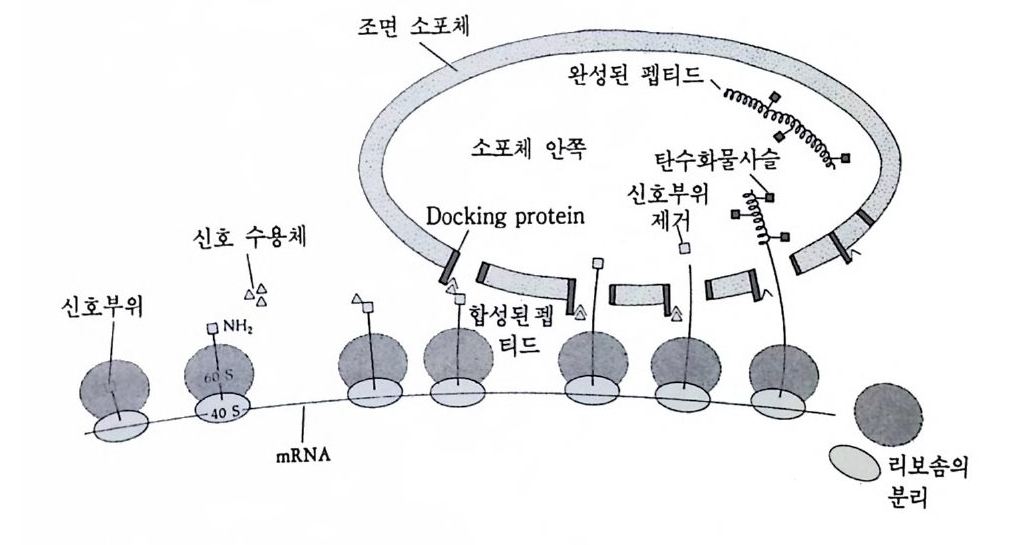 완성된
완성된
그립 8-26 분비형 단백질의 해독과 당류첨가반웅의 모형. 폴리펩티드의 처음 50 개 정도의 아미노산은 신호부위로서 조면소포체의 막 속으로 그 단백질을 인도하는 역 할을 한다. 신호부위는 신호수용체 (sig ua l recept or comp le x) 에 의해 인식된다. 일단 소포체 안으로 들어오면 신호부위가 제거되고, 풀리펩 티드 사슬의 길이가 길어지면서 당류의 잔기가 첨가된다.
붙이는 능력을 상실하고 있다. 따라서 이러한 환자의 리소좀에는 리 소좀에 들어 있어야 할 효소가 결여되고 있고, 이들 효소는 오히려 혈관 속으로 잘못 분비된다. 어떤 단백질은 특별한 결합 단백질을 가 지고 있는데, 이러한 결합 단백질 때문에 이들 단백질들의 위치결정 이 가능해진다. 생쥐의 간세포에서 (3-g lucuron i dase 는 리소좀과 소 포체 모두에 분포되 어 있는데 , mannose-o-ph o sph a te 신호에 의 해 리 소좀 속으로 들어갈 수도 있고, e g as yn이라는 특별한 단백질에 의해 소포체에 결합된 채로 남아 있을 수도 있다 (Swank and Paig en , 1973). e g as yn을 결핍한 생쥐의 돌연변이 종에서는 간의 소포체에서 (3-g lucuro ni dase 가 발견되 지 않는다 (Lus i s et a l., 1976).. (3- gl u cur- on i dase 의 위 치는 세포의 종류에 따라 다르다. e g as y n 이 풍부한 간 이나 신장과 같은 조직에서는 (3-g lucuron i dase 가 소포체에서 발견되 는 반면에 e g as yn이 결핍된 뇌와 지라와 감은 조직에서는 이 효소가 리소좀에서 발견된다 (Lus i s and Paig en , 1977). 이러한 관찰에 근거해 볼 때 단백질의 세포내 위치결정은 후 해독 수준에서 일어나는 현상 으로 세포의 종류에 따라 크게 다를 수 있다. 1) 핵과 미토콘드리아에 대한 표적 단백질 특정한 단백질을 핵 속에 축적시키기 위해서는 단백질을 핵 속으로 선택적으로 두과시키는 능력과 일단 핵 속으로 들어온 단백질을 선택 적으로 보존하는 능력이 필요하다 (D i ng wall et al., 1982 ; Kalderon et al., 1984}. 이러한 능력은 단백질에 있는 특별한 아미노산 서열에 의 해서 가능한 것으로 알려지고 있다. 1984 년 칼데론 (Kalderon) 은 핵 단백질에서 7 개의 아미노산으로 구성된 특별한 서열을 발견했는 데, 이 아미노산 서열은 세포질 단백질의 위치를 변경시킬 수 있는 성질을 가지고 있는 것으로 알려지고 있다. 이 핵 단백질은 SV4o 바 이러스에 대한 T- 항체이다. 만약 이 단백질의 유전자에 돌연변이가 일어나 128 번째 자리하는 l y s i ne 을 다른 아미노산으로 바꾸어 주면,
그 단백질은 세포질에 남아 있게 된다. 즉 이러한 사실은 128 번째의 아미노산이 핵내의 위치 결정에 상관하는 신호일 가능성을 보여주고 있다. 이러한 가능성을 직접 재조합 풀라스미드를 이용하여 알아보았 다. 죽 세 포질 효소의 일종인 pyru vate k i nase 에 대 한 유전자와 SV4o 의 T 항체의 114~138 아미노산울 지시하는 75 개 염기쌍으로 구성된 부위를 한 개의 단위로 포함하는 플라스미드를 우선 조직배양 세포내로 주사하여 준다. 그러면 재조합된 유전자가 염색체 속으로 들 어가 전사되고 해독되어 pyru vate k i nase 에 T - 항체 단백질의 25 개
 12 』 135 위치
12 』 135 위치
그림 8-27 핵에 대한 표적단백질의 아미노산 서열 (A) SV4oT 항원의 128 번째 아미노산인 l y s i ne 을 중심으로 자리하고 있는 25 개의 아미노산은 pyruv ate k i nase 를 핵 속으로 인도한다. (B-I) 어둡게 칠한 상자 속에 있는 아미노산들은 단백질을 핵 속에 축적시키는데 필요하 다 . 사진은 (H) 와 (I) 의 세포내 위치를 보여주고 있다 (Kalderon et al., 1984) .
아미노산이 붙어 있는 단백질이 만들어진다. 이러한 세포를 pyruv ate k i nase 에 대 한 형 광항체 로 염 색 하여 pyru vate k i nase 의 세 포내 위치를 확인해 보면 , 이 효소단백질이 오히려 핵 속에 들어가 있음을 볼 수 있다. 만약 T- 항체의 유전자 영기수를 감소시키면 다 른 종류의 단백질이 만들어지며, 세포내 위치도 바뀐다. 죽 아미노산 의 수를 지나치 게 줄이 면 pyruv ate k i uase 는 핵 속으로 들어 가지 못
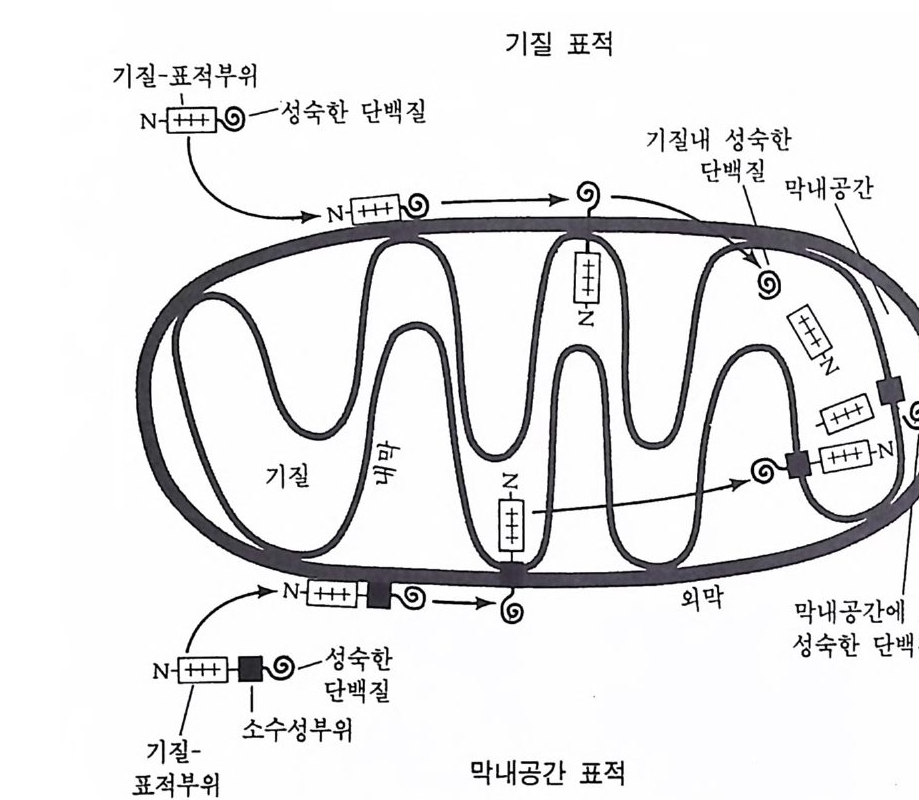 기질 표적
기질 표적
그립 8-28 미토콘드리아내 특정 부위에 대한 단백질 표적의 모형. 핵 속의 유 전자에 의해 만들어진 미토콘드리아 단백질을 모두 기질 표적부위를 가지고 있다(田田)• 만약 미토콘드리아의 기질 내표의 두과가 정지되면, 두번째소 수성 부위의 신호(.)에 의해 막에 보존된다. 이 단백질이 막 안으로 들 어갈 것인지 혹은 막에 그대로 남아있을 것인지는 단백질이 신호부위에서 분리되는데 달려 있다 (H urt and van Loon, 1986, Loon and Schatz , 1987).
하고 세 포질에 머 물게 된다. pyru vate k i nase 를 핵 속으로 유도하는 데 기 본적 으로 중요한 아미 노산은 7 개 로 p ro-l y s-l y s-l y s-ar g -l y s-val 이 다. 이러한 사실은 모든 핵 단백질아 위치 결정을 위해 이와 같이 특 별한 7 개의 아미노산을 필요로 한다는 뜻이 아니며, 모든 핵이 이러 한 아미노산만을 신호로 인식한다는 뜻도 아니다. 핵 단백질의 종류 에 따라 자신에게 적합한 종류의 신호를 가지고 있다는 뜻이다 (Hall et al., 1984 ; Davey et al., 1985) . 미토콘드리아는 의막, 내막, 막 사이의 공간과 기질의 4 개의 구획 으로 분리되어 있기 때문에 단백질의 미토콘드리아에서의 위치 결정 이 핵에 바하여 훨씬 복잡하다• 단백질을 핵으로 인도하는 신호 아미 노산 서열 부위와는 달리 미토콘드리아로 인도되는 대부분의 단백질 은 성숙한 단백질로부터 쉽게 구별할 수 있는 아미노산 서열을 가지 고 있다. 이러한 신호부위는 염기성 아미노산이 주기적으로 배열된 비교적 짧은 서열을 가지고 있다. 물론 정확한 길이와 아미노산 서열 은 미토콘드리아의 단백질 종류에 따라 다르다. 만약 신호 아미노산 부위가 단백질내에 있으면, 이 단백질은 미토콘드리아로 인도될 뿐만 아니라, 두 겹의 막을 지나 미토콘드리아의 기질 속으로까지 이동될 수 있다. 만약 성숙한 단백질과 기질로 인도하는 서열 사이에 소수성 부위가 있으면, 기질내로의 단백질의 이동은 어렵게 된다. 이와 같은 이유때문에 단백질이 미토콘드리아의 내막에 자리하게 된다. 만약 성 숙한 단백질이 소수성 부위로부터 쉽게 분리될 수 있다면, 이 단백질 은 막 속의 공간(i n t ramembranous s p ace) 에 자리하게 된다 (Van Loon and Schatz , 1987) . 2) 초분자 수분의 분자조립 후 해독 수준에서 가능한 또 하나의 조절 형태는 새로 합성된 단백 질들을 기능적인 단위로 조립하는 것이다. 단백질 중에는 스스로 조 립되어 기능적인 단위를 형성하는 경우가 있다. 예를 들어 헤모글로
빈과 lacta t e deh y dro g enase 는 모두 4 개의 폴리펩티드 사슬로 이루어 져 있는데, 이들 사슬들은 서로 비공유 결합으로 결합되어 있다. 수 축성 단백질인 튜불린과 액틴은 모두 중합된 형태로나 혹은 중합되지 않은 형태로 존재할 수 있다. 수정시 첨체 돌기가 돌출되기 위해서는 액틴 단량체가 미세소사로의 중합이 반드시 이루어져야 한다. 또한 세포분열시 듀불린이 세포 분열 장치 (mi tot ic a pp ara t us) 의 미세소관 으로 조립되었다가 세포분열이 끝날 때쯤에 다시 중합체가 단량체로 전환된다. 이들 듀불린 단량체들은 새로운 미세소관으로 조립되는 데 재이용된다.
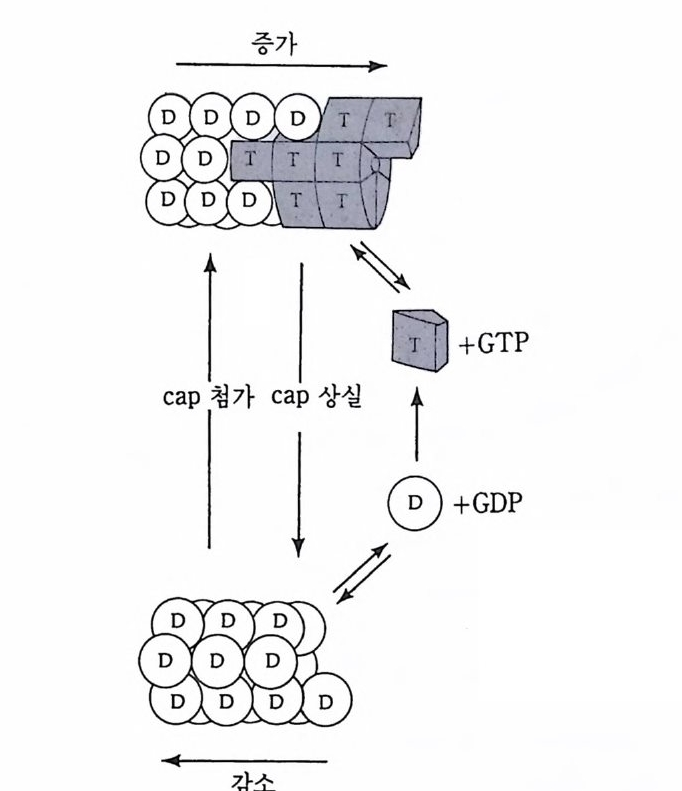 증가
증가
그립 8-29 미세소관의 형성과 분해에 대한 모형 (Kirs chner and Mit ch is o n, 1986)
미세소관 신장의 조절은 듀불린 단백질과 공유결합하고 있는 GTP 분자의 가수분해를 통하여 일어난다. 새로 중합된 튜불린은 GTP 와 결합함으로써 다른 듀불린 분자와 안정된 결합을 유지할 수 있다. 듀 불린 단백질이 오래되면 GTP 는 GDP 로 분해된다. GDP 와 결합되어 있는 듀불린은 인접하고 있는 튜불린 분자와 안정된 결합을 유지하지 못한다. 이와 같이 안정성이 감소되면 미세소관이 단량체의 듀불린 분자로 분해된다. 사실상 미세소관의 순차적인 신장은 형태형성에 대 단히 중요하다. 단백질이 섬유를 형성할 수 있는 능력은 단백질내의 비교적 작은 부위에 의존한다. 그런데 다른 단백질이 돌연변이에 의해서 이러한 능력을 획득하게 되면 해로운 결과가 나타난다. 경형 적혈구가 그러 한 예이다. 즉 글로빈 단백질을 이루는 아미노산 중 한 개의 아미노 산이 다른 아미노산으로 바뀌면({3-글로빈의 여섯번째 아미노산인 glu ta m i c ac i d 가 va li n 힙브로 대 치 됨 ) 소수성 주머 니 (hy dr op ho bic poc ket) 를 형 성 하여 산소가 방출할 때 (deoxyg e nate d ) 헤 모글로빈의 4 량체 가 상호작용하여 일종의 섬유성 구조를 가지게 된다. 이러한 섬유성 구 조에 의 해 세 포가 늘어 남으로 (str e tc h ) 겸 형 적 혈구의 독특한 모양이 만들어지고, 세포의 탄성이 감소한다. DNA 와 결합하는 히스톤 단백질도 일단 DNA 와 결합하여 누클레 오솜의 형태를 구현하지 못하면 별로 쓸모가 없다. 진핵세포의 80S 리보솜 입자도 70 종류의 단백질과 4 종류의 리보솜 RNA 로 구성되어 있다. 단백질과 RNA 가 일정한 형태로 조합되지 못하면 기능이 나타 나지 않는다. 일반적으로 이러한 조합은 세포 안에서 대단히 빠른 속 도로 그리고 능률적으로 일어난다. 난노세포에서 mRNA 를 가리고 있는 단백질들도 핵산과 결합하여 특별한 복합체를 형성할 수 있는 단백질들이다. 그리고 Xenop us 의 5S rRNA 유전자에서 5S rRNA 와 복합체를 형성하는 TFIIIA 도 역시 난모세포에서 5S rRNA 와 결합하 여 7S 입자를 형성할 수 있는 단백질이다 (Pelham and Brown, 1980).
이러한 관찰에 근거하여 볼 때 분자조립이란 또 하나의 중요한 후 해 독 수준에서의 조절 과정이라고 할 수 있다. 3) Colla g en 의 후 해독 수준에서의 조절 colla g en 의 합성과정을 자세히 살펴보면 후 해독 수준에서의 단백 질 합성조절의 중요성을 좀더 분명히 이해할 수 있다 (Procko p et al., 1979 ; Dav ids on and Berg, 1981). 첫째 단계로, collage n mRNA 가 해독되어 p rocolla g en 이 된다 .
 (A)
(A)
그림 8-30 겸형적혈구 헤모글로빈에서의 섬유형성. (A) 삼두압을 이용하여 분쇄한 적혈구에서 나오는 경형적혈구 헤모글로빈 의 전자현미경 사진 (Wellems and Jos eph s , 1979) (B) 섬유형성에 대한 모 형. 돌연변이가 생긴 8- 글로빈이 다른 8- 글로빈에 부착하여 섬유를 형성한 다(Di ckerson and Geis , 1983).
p rocolla g en 의 아미노기 말단에 신호부위가 있는데, 이 신호부위로 인하여 p rocolla g en 이 우선 조면소포체 속으로 인도된다. 신호부위가 colla g en 분자로부터 떨어져 나오면 colla g en 분자는 3 종류의 히드록 실화 효소를 만나게 된다. 이들 중 두 종류의 효소는 p rol i ne 을 3 -hyd r oxyp ro lin e 및 4 - h ydroxyp rol i n 탸냐i 히드록실화시키고, 다론 한 종류는 l y s i ne 을 h y drox y l y s i ne 으로 하드록실 화한다. 이 때 colla g en 단백질에 있는 모든 p rol i ne 과 l y s i ne 이 히드록실화되는 것이 아니고 적절한 위치에 자리하고 있는 p rol i ne 과 l y s i ne 만이 이들 효소 에 의해 인식된다. colla g en 이 히드록실화됨에 따라 당류가 h y droxy l y s i ne 에 첨가될 수 있다. 즉, g ala ct os y l t rans fe rase 에 의 해 g alac t ose 가 hyd r ox- y l y s i ne 에 그리 고 g lucos y l t rans fe rase 에 의 해 g lucose 가 hyd r ox- yly s y l g alac t ose 에 첨 가된다. 카르복실 말단 부위 는 g lucos ami ne 과 mannose 에 의해 영 향받는다. 다음 단계로 이황화결합이 형성됨으로 인하여 3 개의 colla g en 분자 로 이루어진 삼중나선(t r ip le hel i x) 이 구성된다. 이황화결합은 인접 한 colla g en 분자 사이에 카르복실기 말단에서 형성되는대, 만약 p rol i ne 이 히드록실화되면 3 개의 colla g en 분자가 접혀서 삼중나선을 구현하게 된다. colla g en 분자는 이러한 형태로 세포 밖으로 분비된다. 그러나 분비 과정에서도 단백질에 변화가 일어난다. 첫째로 두 개의 단백질 분해 효소는 아미노기 말단과 카르복실기 말단의 구형의 영 역 (glo bular doma i ns) 을 제거시킨다. 이러한 과정을 거쳐 삼중나선의 구조를 형 성하게 된다. 다음으로 이러한 구조들은 자연적으로 조합되어 섬유원 이 된다. 그러나 이들 섬유원으로서는 장력이 결여되어 있기 때문에 구조 단백질로서의 기능을 나타내지 못한다. 결국 삼중나선의 구조를 가전 여러 개의 단백질 분자들이 공유결합에 의해 결합됨으로써 기능 울 발휘하게 된다. 이러한 결합은 h y drox y l y s i ne 의 l y s i n 단+분을 효
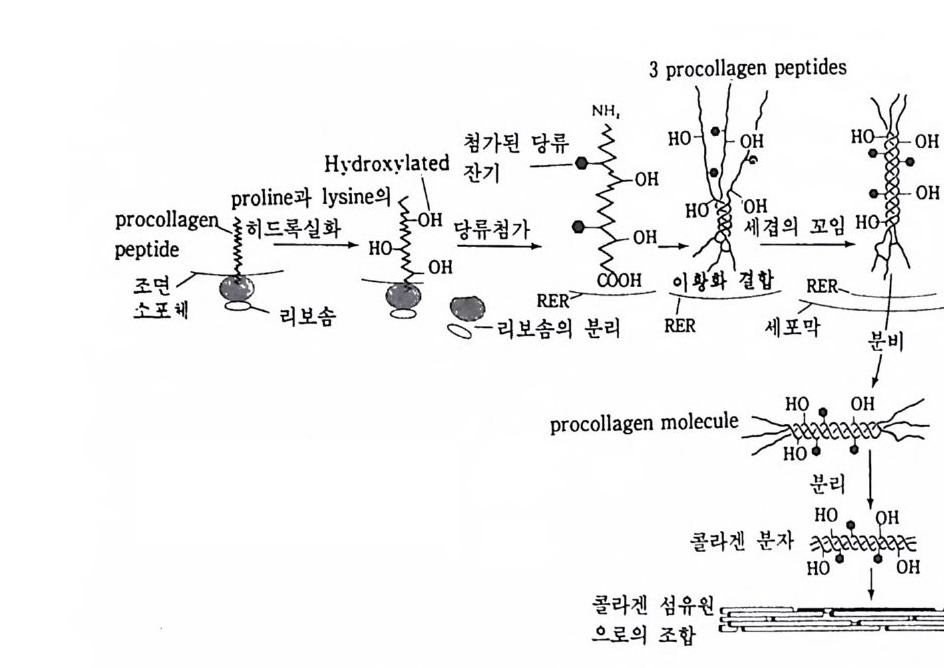 3 pro collage n peptide s
3 pro collage n peptide s
그림 8-31 후해독과정중 조면세포체내에서와 분비 후에 일어나는 콜라겐 단백 질의 성숙과정.
소로 변경시키고 이어중으로써 가능해진다. 죽 단백질이 해독된 후에 도 여러 단계에 걸쳐 성숙되어야만 드디어 생물학적으로 기능을 가진 구조가 된다. 지금까지 여러 단계에서 유전자 발현을 조절하는 과정을 살펴보았 다. 즉, 전사, RNA pro cessin g , 해독, 후 해독 단계에서 유전자의 발현이 조절된다. 이러한 유전자 발현의 조절 결과로 세포에 따라 단 백질의 종류가 결정되고 단백질의 종류에 따라 세포의 기능이 결정됨 으로써 세포의 운명이 결정되는 것으로 이해되고 있다. 일단 세포의 운명이 결정되면, 그 운명에 따라 세포가 분화한다. 그러나 이것은 유전자 발현의 조절을 현상론적인 면에서 살펴본 것에 불과하다. 앞 으로 유전자 발현의 선택성을 이해하기 위해서는 무엇보다도 유전자 발현의 조절기구가 규명되어야만 발생기구에 대한 설명이 가능할 것
으로 보인다. 그러나 이 문제는 그렇게 간단하지가 않다. 조철요인의 정체를 파악하기도 힘들지만 조절요인의 정체를 파악한다고 할지라도 조절요인의 작용을 조절하는 또 다른 조절요인을 전제하지 않고는 조 절기구를 설명할 수 없기 때문에 문제해결의 전망이 그렇게 낙관적인 것은 아니다. 참고문헌 Alt, F.W., Both w ell, A.L .M ., knapp , M.N., Sid e n, E., Math e r, E., Koshland, M. and Balt im ore, D. (1980) . Syn thes is of secrete d and membrane-bound i mmuno g lob 떠i n µ heavy chain s is dir e cte d by mRNAs tha t differ at the ir 3' ends. Cell 20: 293-301 . Amara, S.G., Jon as, V., Rosen feld , M.G., Ong, E.S. and Evans, R.M . (1982) . Alt er nati ve RNA pro cessin g in calcit on i n gen e exp re ssio n ge nerate s mRANs encodin g differ ent po lyp e pt ide pro ducts . Natu r e 298: 240-244. Axel, R., Feig le son, P. and Schutz , G. (1976) . Analys i s of the com- ple xit y and div e rsity of mRNA from chi ck en live r and ovi du ct. Cell 7: 247-254. Baker, B., Nag o shi, R.N . and Burt in, K.C. (1987) . Molecular ge neti c aspe ct s of sex dete r mi na ti on in Drosop h ila . Bio E ssays 6: 66-70. Basto s , R.N . and Av iv, H. (1977). Globin RNA pre cursor molecules: Bio s yn thes is and pro cessin g ery throi d cells. Cell 11: 641-650. Bender, T.P., Thomp so n, C.B . and Kuehl, W.M. (1987). Differ enti al exp re ssio n of c -my b mRNA in murin e B lym ph omas by a block to
tra nscrip tion elong a ti on . Scie n ce 237: 147 3-14 7 6. Bentl ey , D.L. and Groudin e , M. (1987). A block to elong a ti on is large l y respo nsib l e for decreased tra nscrip tion of c-m y c in diff er- encia c ed HL60 cells. Natu r e 321: 702- 7 06. Bog gs, R.T ., Grego r, P., Idris s , S., Belote , J.M . and McKeown, M. (1987) . Regu la ti on of sexual dif fer enti at i on in D. melanoga s te r via alte r nati ve spl i ci n g of RNA from the tra nsfo rn zer gen e. Cell 50: 739 -747. Breitb a rt , R.E. , Andreadis , A. and Nadal-G in a rd, B. ( 1987) . Alte r - nati ve spl icin g: A ubiq u it ou s mechani sm for the gen erati on of multip le pro te i n iso fo rm s from sin g l e gen es. Annu. Rev. Bio c hem. 56: 467-495. Breit ba rt , R.E. and Nadal-Gi na rd, B. (1987) . Develop m enta l ly in- duced, muscle-spe c ifi c fac to r s contr o l the dif fere nti al spl i ci n g of alte r nati ve and consti tut i ve tro p o ni n T exon. Cell 49: 793-803. Cesarman, E ., Dalla-Favera, R ., Bentl e y, D. and Groud ine , M. (1987) . Muta t io n s in the firs t exon are a_ss o c iat e d wit h alte r ed tra n- scrip tion in c-my c in Burkit t lym ph oma. Scie n ce 238: 1272-1275. Ch ika rais h i , D.M., D eeb, S.S. and Sueoka, N. {1978). Sequ e nce com- ple x ity of nuclear RNAs in ad 血 rat tissu es. Cell 13: 111-120. Crenshaw, E.B., III, R usso, A.F ., S wanson, L.W . and Rosen feld , M.G. {19 ,8 7) . Neuron-spe c i fic alte r nati ve RNA pro cessin g in tra nsge n i c mice exp re ssin g a meta l loth ion ein - calcit on i n fusi o n gen e. Cell 49: 389-398. Cun ning h am, B.A., Hemp er ly, J.J., Murray, B.A ., Predi ger , A.E., Brackenbu ry, R. and Edelman, G.M. (1 98.7 ) . Neural cell adhesio n molecule, S tr u ctu r e, im munog lo bulin - lik e domain s , cell sur fac e .ao dulati on , and alte r nati ve RNA spl icing . Scie n ce 236: 799-806.
David s on, E.H. and Brit ten . R.J. (1979}. Regu la ti on of gen e exp re s- sio n : Possib l e role of repe t i tive sequ e nces. Scie n ce 204: 1052- 10 59. Early, P., Rog er s, J., Davis , M., Dalame, K., Bond, M. , W all, R. and Hood, L. ( 1980) . Two mRNAs can be pro duced from a sin g l e im munolgl o bulin gen e by alte r nati ve RNA pro cessin g pat h w ay s. Cell 20: 313- 31 9. Galau, G.A . , Klein , W.H., Davis , M.M ., Wold, B.J. , Brit ten , R.J., and David s on, E.H . (1976). Str u ctu r al gen e sets acti ve in embry o s and adult tiss ues of the sea urchi n. Cell 7, 487. Gott es fe l d, J.M . and Part ing t on , G.A . (1977} . Distr i b u ti on of messen- ger RNA codin g seq ue nces in frac ti on ate d chromati n. Cell 12: 953 -962. Hames, B.D . and Perry, R.P . (1977} . Homolog y relati on shi p betw een the messeng er RNA and hete r og en eous nuclear RNA of mouse L cells. A DNA excess hyb rid iza ti on stu d y. ]. Mol. Bio l. 109: 437-453. Hashim oto , C. and Ste i tz , M.A. (1986) . A small rib o nucleop ro te i n associ at e s wit h the AAUAAA pol ya d envlati on sig na l in vitro . Cell 45: 581-591 . Hump h rie s , S., Wi nd ass, J. and Wi lliam son, J. (1976) . Mouse glo bin gen e exp re ssio n in. e ry throi d and nonery throi d tiss ue. Cell 7: 267 -27 7. Hy ne s, R.O . (1987) . Fib r onecti ns : A family of comp le x and versati le adhesiv e gly c o p ro te i n s deriv e d from a sin g l e gen e. Harvey Leet . 81: 133-152. Kleene, K.C. and Hump hr eys , T. (1977) . Sim ila rity of hnRNA sequ e nces in b lastu l a and plu te u s sta g e sea urch in e mbry os . Cell12: 143-155. Kleene, K.C. and Hump hr eys , T. (1985) . Transcrip tion of s im ila r sets
of rare mate r nal RNAs and rare nuclear RNAs in sea urchin blastu l ae and adult c oelomocyt es . ] . Embry o! . Exp. Morp h ol. 85 : 131 -149. Lewi n, B. (1980) . Gene Expre ssio n 2, 2nd Ed. Wi le y -l nte r sci en ce, New York, pp. 694-760. Liu, C. -P., Tucker, P .W., Mushi ns ki, F. and Blatt ne r, F.R . ( 1980) . Mapp ing of heavy chain gen es for mouse im munog lo bulin s M and G. Scie n ce 209: 1348-1353. Maki, R., R oeder, W., Traunecker, A., Sid m an, C,, Wahl, M., Rasjh - ke, W. and Tonega w a,·S . (1981) . The role of DNA rearrang em ent and alt er nate mRNA pro cessin g in the exp re ssio n of im munog - lobuli n d elt a gen es. Cell 24: 353-365. Nabeshi m a, Y., Fuji -K uriy am a, Y., Muramats u , M. and Og a ta , K. (1984) . Alte r nati ve tra nscrip tion and two modes of spl i ci ng result in tw o my o sin ligh t chain s from one gen e. Natu r e 308: 333-338. Orkin , S.H., Cheng, T-C., Anto n arakis , S.E. and Kazazia n , H.H. , J r. (1985) . Thalassem ia due to a muta t i on in the cleavage -po lya d enyl a ti on sig na l of the human {J-glo b in gen e. EMBO ]. 4: 453-456. Orki n, S.H. and Kazazia n , H.H . (1984). The muta t i on and po lym o r- phism of the human {J-glo bin gen e and its s urroundin g DNA Annu. Rev. Genet. 18: 131-171 . Perlman, S.M., Ford, P.J. and Rosbash, M.M. (1977) . Presence of tad p o le and adult glo bin RNA sequ ences in oocy tes of Xenop us laevis . Proc. Natl. Sci . USA 74: 3835- 38 39. Proud foo t, N.J. · a nd Brown1ee, G.G. (1976) . 3' Noncodin g regi on sequ e nces in eukary o ti c messeng e r RNA . Natu r e 263: 211-214. Rog er s, J., Early, P., Cart er , C., C alame, K., Bond M., Hood, L. and
Wall, R. (1980) . Two mRNAs wit h dif fer ent 3' ends encode membrane-bound and secrete d for ms of im munog lo bulin µ chain . Cell 20: 303-312. Rozek, C.E. and David s on, N. (1986) . Dif fer enti al pro cessin g of RNA tra nscrib e d from sin g l e -cop y Drosop hi la my os in heavy chain gen e pro duces fou r mRNAs tha t encode tw o pol yp e pt ide s. Proc. Natl. Acad. Sci . U SA 83: 2128-2132. Sega l , S., Levin e , A.J. and Khou ry, G. (1979) . Evid e nce for non -sp l ic e d SV40 RNA in undif fer enti at e d murin e ter ato c arci no ma ste m cells. N atu r e 280: 335-338. Smi th, M.J., Houg h, B.R., Chamberlain , M.E. and Dav ids on, E.H. (1 974) . Repe t it ive and 1on-repe t it ive seq ue nce in sea urchi n hete r oge n eous nuclear RNA . ]. Mol. Bio l. 85: 103-126. Str u b, K. and Bir n sti el, M.L (1986) . Geneti c c omp le menta t i on in the Xenop us oocy te: Co-expn ssio n of s ea urchi n his t o n e and U7 RNAs resto r es 3' pro cessin g of H3 pre -mRNA in the oocy te. EMBO ]. 5: 1675-1682. Tamkun, J.W ., Schwart zb auer, J.E . and Hy ne s, R.O . (1984) . A sin g l e rat fibr onecti n g en e gen erate s three diffee nt mRNAs by alte r nati ve spl icing of a comp le x exon. Proc. Natl. Acad. Sci . USA 81: 5140 -5144. Til gh man, S.M . et a l. 1978. Inte r ven ing sequ ence of D NA ide nti fied in the stru c tur al por t ion of a mouse {3-glo bin gen e. Proc. Natl. Acad. Sci. U .S.A., 75: 725-729. Tsai, S.Y., Tsai, M-J., Lin, C-T . and O'Malley, B.W. (1979) . Eff ec t of e str o g en on ovalbu min gen e expr e ssio n in differe nti at e d nonta r - get tiss ues. Bio c hemi stry 18: 5726-5731 . Wi ck ens, M. and Ste p h e nson, P. (1984) . Role of the conserved
AAUAAA sequ e nce: Four AAUAAA poi n t muta n ts pre vent 3' end form ati on . Scz e nce 226: 1045- 1 051 . Wold, B.J. , Klein , W.H., Houg h -E v ans, B.R ., Britt en , R.J. and David - son, E.H . (1978} . Sea urchi n e mbryo mRNA sequ e nces exp re ssed in nuclear RNA of adult tiss ues. Cell 14: 941- 95 0.
찾아보기
기 가려진 메시지 295 간세포 174 간충직 22 y-l ip o tr a pi n 311 개시요인 2 312 개시코돈 313 게놈 275 게놈 크기 144 결정요인 13 결합형 im munog lo buli n 256 겸형 적혈구 323 고정부위 108, 256 Goldberg- H og ne ss 상자 203 공유결합 311 광세포 40 구성적 이질 염색질 94 gua nid i n e nucleoti de exchang e fac to r 279 구조단백질 325 구조유전자 151 구획화 300 극성 316 국세포 46 국영 29 극입자 46 국질 45 glo bular domain 325 글로빈유전자 172
L 나선난할 28 난알부민 167 난할 287 난황낭 174 낭배형성 289 내분열 118 Nort he rn blot 분석 법 210 Notc h 유전자 182 누두 166 누쿨레오솜 139, 323 E: 다능성 71 다사염색체 117 다소 반복성 DNA 151 단량체 322 단성생식 난편 발생자 287 단핵 근세포 259 담륜자 유생 29 double sex 259 DALA syn the ta s e 276 dockin g pro te i n 316 동물극 293 동원체 94, 117 동위효소 314 동형 접합자 288 DNA 의 민감도 159 DNA-RNA 재결합법 291 DNA 의 융점 145 DNA 의 산재성 153
DNA 재결합법 145 DNA 재조합법 151 DNA 중합효소 293 deoxyg e nate d 323 2 large subu nit 293 lacta t e dehy dr og en ase-X 307 leader sequ e nce 281 ribo ncleo reducta s e 293 ribo nucleop ro te i n 295 ribo nucleop ro te i n 복합체 261 recyc l in g fac to r 279 lin-1 2 유전자 182 E, masked mRNA 295 mesento b last 32 메칠기 첨가반웅 223 모] RNA 59 모계요인 288 모계조절 286 모계효과 돌연변이 288 미세소관 308 미세소사 322 m y eloma 세포 210 미해독부위 282 n Barr 체 96 반감기 282
반복성 유전자 87 Balbia n i ring 120 발생배 284 발생억제 78 방사난할 28 방사능 동위원소 291 방출요인 279 배란 288 배반영 46 배측 신경색 182 /3-ga lacto s id a se 215 /3-글로빈 276 /3- endorp h in 311 /3누탈라세미아 202 vecto r 293 변성 291 변이부위 108 변이부위 108, 254 변형군 311 복사기 103 복잡성 245, 291 부력 밀도 105, 1.4 9 부신피질호르몬 311 부화 287 부화기 288 부화효소 293 분비 형 im munog lo buli n 256 분자조립 324 VDJ 유전자 257 B- 림프구 254 비공유결합 322 비반복성 DNA 150 바히스톤 단백질 161
人 4 량체 314 삼엽기 29 삼중나선 325 생식세포 41 생식융기 50 생식질 41 생식질섣 14 섬유성 구조 323 섬유아세포 156, 282 섬유원 325 subtr ac ti on clonin g 129 성 중배영 모세포 182 성장요인 282 성전환 유전자 259 성체원기 80 sevenless 유전자 184 세포융합 89 세포계보 26 세포골격 301 세포분열장치 322 세포사 256 세포주기 311 세포질요인 155. 세포질이동 17 세포특이단백질 258 세포화 49 소수성 주머니 323 수용분자 317 순차적 유전자 발현 68, 117 순차적 pro cessin g 253 small subu nit 293
swi tch gen es 181 swi tch i ng 2 54 spli cing 256 spli c i ng enzym e 256 식물국 293 식물국체 36 신경 원세포 182 신경세포 응집분자 (NCAM) 258 신호수용 복합체 316 신호영기서열 316 Cyc l ohexa rnide 288 Cy cl in 304 cyt oc halasin B 24 3'tra i le r 261 cDNA 293 cis 조절요인 203 CAAT 205 CGRP 257 c-fo s 유전자 282 。 acety lc holin es te r ase 22, 57 아세틸화 311 아이세포질환 I - 세포질환 317 apo l ip o pr o te i n -B 단백 질 307 actin o my cin D 57, 288 allelic exclusio n 257 RNA 중합효소 143, 158 RNA pro cessin g 254 a- 글로빈 276 a- 색소세포 촉진 호르몬 311 야생종 289 억제요인 278
eg a syn 318 SnRNP 262 에스데로겐 167 ACTH 311 hnRNA 242 ATG 코돈 196 엑디존 80, 163 exon 196 enhancer 203, 20s, 210, 211, 21s LDH 314 m-RNA 전구체 258 역 전사효소 168, 293 연속핵이식 73 열충격 단백질 127 염색질의 풀림 72 염색체 감되 42 염색체 응축 303 염색체 절단 75 영양아충조직 100 O 돌연변이종 288 5' cap 300 Oc t a 상자 219 oli go -deoxy thi m i di n e -cellulose bead 168 용해액 278 ubiq uitin 314 운명전환 81 원구배순부 289 원시생식세포 42 원장 285 위성 DNA 149 U7RNP 262 유일성 DNA 1so, 291 유일성 유전자 87
유전자 동질성 68 유전자 변경 93, 102 유전자 손실 102 유전자 양적 보정 96 유전자 재배열 102 유전자 증폭 102 유전자의 재배열 109 응축활동 311 emeti ne 288 im munog lo buli n 108, 254 이방사상청 40 이배수체 280 eIF2 278 eIF-2B 279 이중 재결합 실험 152 이중구배설 16 이중복 11 충 56 이질 염색질 93 in situ 재결합법 87 인 형성체 151 ins ulin 306 int r am embrane spa c e 321 int r on 196 inf o n nosome 295, 306 inh ib i t or y liga nd 308 일차 간충직 세포 284 임의적 이질 염색질 94 x: 자기방사법 87 재조합 플라스미드 319 저메칠화 226 적아구 172
전기영동 295 전능성 47, 68 전사 개시부위 196 전사단위 103, 120 전성설 13 전핵 303 점 돌연변이 115 정중선 20 gen e libr ary 293 Z-DNA 229 조면소포체 325 조직배양 319 조합 293 종양세포 284 중심립 287 중포배기 287 줄판 40 증폭 293 지방 담체 307 지방체세포 157 GM- C SF 2s2 전정 염색질 93 •K 첨체돌기 322 체강세포 182 체강액 292 7-m eth ylg u a nosin e cap 300 침강 295 더 casein 305
chy lo m icr on 307 calcit om in 257 cot curve 147 cap bin d in g pro te i n 281 comp ac ti on 316 comp le menta r y DNA 85 consensus sequ e nce 215 collage n 311 콜레스테롤 307 class sw itch in g 115 Chloramp he n ico l tran ste r ase 127 클로운 294 kin a se 278 E 두석 302 트란스포손 115 tr an 홉절단백질 206 trai l er reg ion 198 trop on in T 259 trigly e e ri de s 307 TATA 상자 203 TFIIIA 177 T- 항체 318 고 포배 287 포배기 288 포배전이 130 pho sph o ry la se kin a se 311 폴리솜 297
pol ya d eni ne 꼬리 261 pol ya d emy la ti on 261 표적단백질 318 표충 34 표피 성장요인 183 프로게스테론 171 pro lacti n 305 pro mote r 175, 196, 203 pro some 306 ACTH-endorp hin 311 pro in s uli n 306 pre pr o g ram med 288 pre pr o in s ulin 311 pyruv ate kin a se 319 피면자 32 fibr onectin 258 石 HMG 161 hyp o chrom ic s hift 146 하피 182 할강 287
할구 284 항체대립인자 257 항체분비 혈장세포 106 해독개시요인 278 해독억제제 303 해독장치 301 해독정지코돈 198 해독효율 281 핵 클로운닝 73 핵산 323 핵산 재결합법 84 핵이식 69, 286 핵질 289 헴 분자 276 혈도 172 형광항체 320 회색신월대 19 효소붕괴수준 316 후 해독 308 후성설 13 휴지기 307 히드록실화 311 히스톤 138
이양립 서울대학교 문리과대학 동물학과를 졸업하고 미국 워싱돈대학교에서 발생생물학을 연구하여 석 • 박사 학위를 받았다. 현재 이화여자대학교 생물과학과 교수로 재직하고 있으며 논문으로 「난자형성중 유전자 발현의 변화에 대한 연구」 의 20 여 편이 있다. 발생과 유전자 발현 대우학술총서 자연과학 81 초판 찍음 1992 년 7 월 5 일 초판 펴냄 1992 년 7 월 15 일 지은이 이양립 펴낸이 朴孟浩 펴낸곳 (주)民音社 주간 / 이영준 편집/이갑수, 윤석호 , 이남수 , 전경십, 강일철, 임인기 제작 1 권명오 출판등록 1991 . 12. 20. 제 16 -4 90 호 • 우편 대체번호 010041-3 1 -0523282 • 은행 지로번호 3007783 • 135-120 서울시 강남구 신사동 506 강남출판문화센터 5F • 515- 2000~2( 영업부) 515-2003~5( 편집부) 515-2007, 2101 (팩시밀리) 값 12,000 원 Pri nted in Seoul, Korea © 이양립, 1992 동물학 KDC/491 . 33 ISBN 89-374-3581-0 94490 ISBN 89-374-3000-2 (세트)
대우학술총서 ( 자연과학 ) 1 소립자와 게이지 상호작용 김진의 44 한국의 고생물 이하영 2 동력학특론 이병호 45 질량분석학 김명수 3 질소고정 송승달 46 급변론 박대현 4 상전이와 임계현상 김두철 47 생체에너지 주충노 5 촉매작용 진종식 48 리이만 기하학 박을룡 6 뫼스바우어 分光學 옥항남 49 君表理論 박승안 7 국미량원소의 영양 승정자 50 비선형 편미분 방정식론 하기식 8 수소화봉소와 유기봉소 미 생체막 김형만 화합물 윤능민 52 수리분류학 고철환 9 항생물질의 全合成 강석구 53 찰스 다윈 정용재 10 국소적 형태의 At iya h-sin g er 54 금속부식 박용수 지표이론 지동표 55 양자광학 이상수 11 Mucop ol y s~cc~ar i des 의 56 효소반응 속도론 서정현 생화학 및 생물리학 박준우 57 화성암 성인론 이민성 12 천체물리학 홍승수 58 확률론 구자홍 13 프로스타글라딘 合成 김성각 59 분자 분광학 소현수 14 天然物化學硏究法 우원식 60 백터속 이론 양재현 15 脂防營養 김숙희 이 곤충신경 생리학 부경생 16 結晶化유리 김병호 62 에너지띠 이론 모혜정 17 고분자에 의한 화학반응 조의환 63 수학 가초론 김상문 18 과학혁명 김영식 64 신경과학 검승업박찬웅 19 한국지질론 장기홍 65 BCH 부호와 Reed- 20 정보이론 한영열 Solomon 부호 이만영 21 원자핵반응론 정운혁 66 양자 전기역학 김영덕
 2 파괴역학 김상철 _ -- 67 단 환론 학재걸
2 파괴역학 김상철 _ -- 67 단 환론 학재걸