

배 무 동경대학교 대학원 미생물학 전공 ( 박사 ) 한국미생물학회 회장역임 현재 이화여자대학교 생물과학과 교수 교육부 유전공학 연구 평가위원 저서 『 과학대사전 』 ( 식물편, 미생물의 세계 ) 『 미생물학, 생명공학 용어집 』 ( 공동연구 ) 외 다수의 논문과 번역서가 있음
산업미생물학 
 산업미생물학
산업미생물학
책 머리에 생물공학은 21 세기 산업의 주된 영역의 하나로 기대를 받고 있는데 그 주요한 분야가 산업미생물학이다. 산업미생물학은 주류제조산업 시대에서 부터 항생물질생산시대를 거쳐 대규모화선업으로 성장하였고 식품공업, 의 약품공겁 등 주된 산업분야로 성장하였다. 최근에 와서는 산업미생물학의 가장 주요한 균주개량분야에 유전자 조작기법이 도입되면서 산업미생물학 의 혁명적 시대를 맞이하게 되었다. 그것은 균주의 생산성 향상뿐 아니라 과거에는 미생물에 의해서 생산할 수 없었던 고등동물 및 식물의 유전자 산물인 의약품을 미생물에서 생산할 수 있게 되었고 그 의 여러 종류의 화학물질을 효율성 높게 미생물로부터 생산할 수 있는 기술 개발의 가능 성이 제시되고 있다• 이 책의 제 1 부 (1 - 6 장)에서는 산업미생물학 전반에 걸친 원론을 다루었 으며 제 2 부 (7-1 (pol-)에서는 각 분야별로 일반심층내용을 정리하였는데 각 장 모두 오늘날의 미생물산업이나 미래에 더욱 발전되어야 할 분야에서 빼놓을 수 없이 중요시되는 분야이다. 일반 미생물학을 이수한 후 실질적 미생물의 응용분야에 관한 지식과 이론을 이해하고 연구하려는 미생물학자와 실용면에서 더욱 깊은 연구를 원하는 미생물분야 과학기술자를 위하여 될 수 있는 한 많은 참고문헌을 소개하였다. 산업미생물학은 특성상 미생물의 생리 • 대사의 규명, 조절, 물질의 생산 성 , 균주개량, 발효 특성 등을 다루는 up -stre am 분야와 발효균주의 생산
동역학, 대규모화 생산공정, 산물회수 및 분 리 • 정제공정을 디루는 down-s tre am 분야로 구성되며 이러한 각 분야가 합쳐 비로소 산업이 이 루어지는데 이 책은 up -s t r e am 분야를 주로 다루고 있는 것이 특징이다. 그리고 이 책을 저술함에 있어서 미생물균명을 한글화하지 않고 원명을 샤용하였으며 제 11 장을 위시하여 주된 효소명은 영문으로 표기하였다. 화 학물질명은 한글로 표기해도 이해하기 쉬운 것은 한글로 표기하였으나 첫 용어의 경우에는 괄호 안에 영문을 나타내었다. 영문으로 표기한 것은 이 책을 읽을 수 있는 정도의 학도에게는 더욱 편리하다고 판단되기에 영문 으로 표기하였으므로 양해바란다 . 끝으로 이 저술에 연구비를 지원해 주신 대우재단에 감사드리며 원고 정리에 도움을 준 아내에게 고마움을 표한다. 1991 년 11 월 배 무
산업미생물학
차례책 머리에 • 5제1부 산업미생물학 개론제1장 산업미생물학의 탄생1 발효의 탄생 152 산업미생물학의 역사 163 산업미생물학의 발전 184 산업미생물학과 그 이용 범위 214.1 미생물균체의 이용 • 224.2 미생물이 생성하는 고분자물질 • 234.3 일차 대사산물과 이차 대사산물 • 244.4 미생물 전환공정 • 26참고문헌 28제2장 새로운 대사산물의 검색과 산업균주의 분리1 대사산물 291.1 새로운 대사산물의 검색 • 291.2 화학적 전환 • 291.3 원형질체 융합에 의한 균주개량과 새물질 탐색 • 301.4 유전자 재조합에 의한 방법 • 30
2 유용미생물의 분리와 검색 312.1 검색대싱균 • 312.2 검색방법 • 323 유용미생물의 보존 및 관리 343.1 단기보존법 • 343.2 장기보존법 • 38참고문헌 43제3장 산업균주의 개량1 서론 452 일차대사산물을 생성하는 유도 돌연변이주의 선별 482.1 투과성의 변화 • 522.2 되돌림 저해물질 또는 억제물질을 생성하지 않는돌연변이주의 분리 • 532.3 저해물질과 억제물질을 인식하지 않는 돌연변이주의 분리 • 582.4 효소의 합성이 우량한 유도돌연변이주의 선별 • 633 이차대사산물의 생산수율이 우랑한 돌연변이주의 분리 673.1 영양요구 돌연변이주의 분리 • 723.2 내성돌연변이주의 분리 • 743.3 복귀돌연변이주의 분리 • 774 산업미생물 개량을 위한 재조합 체계 794.1 진균류의 유성생식에 의한 재조합 • 794.2 방선균에서의 재조합 방법의 이용 • 854.3 원형질체 융합기술의 이용 • 874.4 유전자 조작기술의 이용 • 905 산물의 수율향상 이의의 균주개량 1035.1 안정한 균주의 선별 • 1035.2 감염저항성 균주의 선별 • 104
5.3 거품 없는 균주의 선별 • 1055.4 배지성분에 내성을 갖는 균주의 선별 • 1055.5 형태학적 유용균의 선별 • 1065.6 일부 발효산물의 제거와 신발효산물 생성균주의 육종 • 107참고문헌 108제4장 발효공업에 사용되는 배지성분1 서론 1152 배지성분의 조제 1163 물 1204 탄소원 1214.1 일반적으로 사용되는 탄소원의 예 • 1214.2 탄소원의 선택에 미치는 요인 • 1234.3 산물생성에 대한 탄소원의 영향 • 1245 질소원 1245.1 일반적으로 이용되는 질소원 • 1245.2 질소원의 선택에 미치는 요인 • 1275.3 유기 질소원 • 1286 무기염류와 미량성분 1327 완충제 1348 전구물질과 대사조절 1358.1 전구물질 • 1358.2 저해물질 • 1368.3 유도물질 • 1388.4 거품소포 • 139참고문헌 141제5장 발효방법
1 서론 1492 미생물의 증식 동력학 1502.1 회분발효 • 1502.2 fed-b atc h 배양공정 • 1552.3 연속발효 • 1563 멸균 1643.1 배지의 멸균 • 1653.2 발효조의 멸균 • 1753.3 공기의 멸균 • 1764 미생물 접종 1784.1 효모의 접종 • 1794.2 세균의 접종 • 1814.3 진균류의 접종 • 1825 발효공정과 발효조 1845.1 발효공정 • 1845.2 발효조 설계의 기본 • 1865.3 발효조 본체 • 1896 통기와교반 1906.1 임계산소농도 • 1906.2 산소공급과 산소전달 • 1936.3 산소흡수율 KLa 값 측정 • 1956.4 발효조내의 KLa 값에 영향을 미치는 요소 • 200참고문헌 201제6장 발효산물의 회수
1 서론 2072 단위조작 2102.1 추출 • 2112.2 크로마토그래피 방법 • 2112.3 농축 • 2173 수율 218참고문헌 219제2부 미생물산물의 각론제7장 미생물이 생산하는 유기용매와 연료1 서론 2212 에탄올 2222.1 에탄올의 생합성 • 2222.2 에탄올 생산공정 • 2242.3 에탄올 발효의 에너지 수지 • 2283 아세본및 부탄올 발효 2293.1 생합성 • 2303.2 생산공정 • 2314 글리세롤 2335 수소가스 2355.1 조류 와 cyanbacteria • 2365.2 산소 바발생형 광합성 세균의 수소생성 • 2375.3 형기성 세균의 수소생성 • 238참고문헌 241제8장 유기산발효
1 서론 2432 시트르산 2432.1 시트르산 생산균주 • 2452.2 생합성 • 2462.3 수율 • 2472.4 영양배지 • 2472.5 생산공정 • 2512.6 산물회수공정 • 2573 글루콘산 2584 아세트산 발효 2604.1 아세트산 생합성 • 2614.2 식초생산 • 2625 젖산발효 2656 코지산 2677 이타콘산 발효 268참고문헌 270제9장 아미노산 발효1 서론 2732 아미노산의 용도 2743 생산방법 2754 아미노산 생산균주의 새로운 개량방법 2795 아미노산 생산공정 조절 2836 각종 아미노산의 생성 2836.1 L-글루탐산 발효 • 2846.2 L-리신 발효 • 294
6.3 L-트립토판의 발효 생산 • 301참고문헌 307제10장 누클레오티드, 누클레오시드 및 그 관련 물질1 서론 3092 핵산의 생합성 조절 3103 조미성분 5'-IMP와 5'-GMP의 생산 3133.1 RNA의 효소가수분해에 의한 5'-IMP 와 5'-GMP의 생산 • 3143.2 직접발효법에 의한 5'-IMP 생산 • 318 3.3 5'-GMP의 발효 생산 • 3243.4 아데노신과 아데닌 누클레오티드의 생산 • 3273.5 누클레오티드 관련 물질의 발효 생산 • 328참고문헌 329제11장 미생물효소의 생산1 서론 3312 전분가수분해 3362.1 α-amylase • 3382.2 세균 α-amylase 생산 • 3402.3 β-amylase • 3422.4 glucoamylase • 3432.5 16-glycoside 결합을 분해하는 효소 • 3443 Glucose isomerase 3453.1 bacillus의 glucose isomerase3.2 streptomyces의 포도당 이성화효소 • 3483.3 포도당 이성화효소의 고정화 • 349
4 Protease 3525 Rennin 3546 Penicillin acylase 3567 기타 미생물효소 3607.1 L-Asparaginase • 3607.2 pectinase • 3617.3 Lipase • 3637.4 Lactase • 3648 효소의 안정화와 고정화 3648.1 가용성 효소의 안정화 • 3658.2 고정화에 의한 안정화 • 366참고문헌 373제12장 비타민1 서론 3772 리보플라빈(비타민 B₂) 3782.1 분포 및 경제적 의의 • 378 2.2 구조와 생합성 • 3792.3 생산방법 • 3813 비타민 B₁₂ 3813.1 분포 및 경제적 의의 • 3813.2 생합성 • 3833.3 비타민 B₁₂ 생산 • 3854 β-카로딘 3884.1 분포 및 경제적 의의 • 3884.2 생합성 • 3894.3 β-카로틴의 생산공정 • 391참고문헌 393
제13장 항생물질1 서론 3951.1 항생물질을 생산하는 미생물집단 • 3961.2 항상물질의 분류 • 3971.3 항생물질의 이용분야 • 3981.4 항생물질 연구의 목적 • 4022 β-락탐계 항생물질 • 4032.1 페니실린 • 4032.2 세팔로스포린 • 4112.3 새로운 β-lactam계 항생물질 • 4153 아미노산과 펩티드계 항생물질 4163.1 D-서이클로세린 • 4173.2 Chromopeptide계 항생물질 • 4183.3 Depsipeptide계 항생물질 • 4193.4 선상과 환상의 deptide계 항생물질 • 4203.5 바시트라신• 4213.6 Bleomycin • 4234 탄수화물계 항생물질 4234.1 Glycoside 당유도체5 아미노글리코시드계 항생물질 4256 Macrocyclic lactone계 항생물질 4326.1 크로리드 항생물질 • 4326.2 폴리엔(polyene) 항진균 항생물질 • 4356.3 안사마이신 • 4397 테트라사이클린(tetracycline)계 항생물질 4417.1 테트라사이클린계 • 441
8 퓨린 및 피리미딘 관련 항생물질 4479 방향족 항생물질 4489.1 클로람페니콜 • 4489.2 Griseofulvin • 4499.3 Novobiocin10 기타 상업적으로 생산되는 항생물질 45110.1 Fusidic acid • 45110.2 Polyether 항생물질 • 45210.3 Mitomycin계 • 453참고문헌 454제14장 미생물이 생산하는 유용물질1 생리활성물질 4591.1 식물병원균이 생성하는 독소 • 4591.2 지베렐린 • 4622 세포 외 다당류 464참고문헌 470제 15 장 미생물의 물질전환1 서론 4732 생물학적 전환반응의 종류 4743 생물학적 전환공정 4764 스테로이드와 스테롤의 전환 4784.1 스테로이드 전환의 종류 • 4804.2 경제적으로 중요한 스데로이드 전환 • 4824.3 스테롤 (sterol) 곁사슬의 미생물적 분해 • 486
5 비스테로이드계 화합물의 물질전환 4885.1 L-Ascobic acid • 4885.2 프로스타그란딘 • 4896 항생물질의 전환 4907 살충제의 물질전환 494참고문헌 498제16장 단세포 단백질1 서론 5012 알칸 으로부터 SCP의 생산 5022.1 긴사슬 일칸의 이화작용 • 5032.2 효모를 이용한 대규모 SCP 생산 • 5043 C₁ 화합물로부터 SCP의 생산 5053.1 메탄 자화세균 • 5053.2 메탄올 발효 • 5064 셀룰로 언쓰로부터 SCP의 생산 5145 폐수로부터 SCP의 생산 516참고문헌 517제17장 폐수 처리의 새로운 방법1 서론 5212 처리공정을 위한 스타아터 배양 5223 호기적 폐수 처리-공기보급형 공정 5244 순수산소의 통기 5265 메탄생산 529참고문헌 531
제18장 광물자원 회수기술1 서론 5332 미생물학적 리칭의 원리 5343 미생물 리칭의 공정과 현실 535참고문헌 538제19장 발효공정의 수지계산과 경제성1 발효산물의 경제성 5412 산업균주와 균주개량에 의한 경제성 향상 5423 발효장치 및 발효원료의 경제성 5434 발효공정의 관리와 수지 5465 발효산물의 회수와 수지 547참고문헌 548찾아보기 551제 1 장 산업미생물학의 탄생 1 발효의 탄생 자연발효란 형식으로 인간은 미생물을 고대로부터 이용해오면서도 그 주역인 미생물에 대해서는 알지 못한 채 오랜 세월이 지나왔다. 그것은 세 균이나 효모가 매우 작은 미생물로서 육안으로는 각 개체 (세포)를 볼 수 없어 미생물이용에 관한 학문이 실증 과학으로 확립되기까지는 오랜 세월 이 소요된 것이다• 예컨대 밀가루반죽을 자연발효시킨 후 굽는 빵제법은 기원전 4000 \1 전부터 이집트인의 일상생활에 이용되었고 이집트 제笠} 조(B. C. 2400~ )의 묘벽에는 빵의 제조에 관한 조각이 새겨져 있다. 또 한 맥주와 유사한 알코올 음료를 만드는 데 효모를 자연으로부터 이용하 는 방법도 기원전 60 0¼민경의 수메르인 (Sumer i ans) 과 바빌론인 (Bab y lo ni ans) 은 알고 있었다. 발효산물인 와인은 「창세기」 에도 나타나 있고 노아가 와인을 과음한 것으로 기록되고 있다. 동양에서는 혼히 원숭이가 나뭇가지 사이에 잘 익은 나무열매를 따서 모아 두었다가 자연발효가 된 알코올성 음료를 즐겨 마셨다는 이야기가 있는데, 태고로부터 발효식품이 즐겨 이용되었을 정도라면 인간의 발효식 품에 대한 관심은 그 기원을 선사시대 이전으로 거슬러 생각할 수 있다. 특히 우리나라나 중국에서는 서력 기원전부터 누룩(곡자)을 이용하여 술 울 빚었고 메주로써 된장, 간장을 만드는 등 자연발효를 통한 종균의 조제
방법이 발달하였다. 우리나라에서는 일찍이 백제의 仁番 이 일본의 응신천왕시대에 그곳 왕 실에 술 빚는 방법을 가르쳤으며, 그 제조방법이 현대화되면서 일본청주 (sake) 로 등장한 것이 일본의 대표적 발효산물기며 오늘날 일본 발효공업 전반을 선진화시킨 원동력이 되었다고 생각해볼 수가 있다. 발효방법이 역사적으로 인간생활에 도입되는 과정에서 동서양의 차이점 을 보면 서양에서는 곡류와 같은 전분질의 맥아를 이용하여 당화시키고 그 당화액이나 포도에서 발효과정을 거쳐 알코올 음료를 제조할 때 자연 발효를 통해 효모의 발효력을 이용한 것에 비해 중국을 중심으로 한 우리 나랴게서는 쌀과 같은 곡물로부터 당화와 발효를 누룩(곡자)에 번식한 사 상균 (Rh i zo p u~) 과 효모를 함께 이용하였다. Rhi zop u ~ 곰팡이는 전분 의 당화력과 알코올 발효력을 함께 지니고 있으니 우리 조상들의 누룩제 법 (밀기울이 주성분)은 일찍이 종균의 제조로서 오늘날에도 적용되는 우 수한 종균제조방법을 고안하고 있었다고 할 수 있다 . 이와 같이 발효는 자연발효를 통해서 곡물이나 포도에 함유된 당분에서 주정성분으로, 또 주정성분으로부터 식초로, 그리고 우유의 자연발효를 통 한 요구르트나 치즈로의 가공과 같은, 자연에 존재하는 발효미생물의 이용 으로 이루어져 왔으며 〈발효(fe rmen t a ti on) 〉란 용어는 〈끓어오르다〉라고 하는 라틴어 〈fe rvere 〉란 의미에서 유래된 것으로서 효모 7} 당분을 협기 상태에서 대사시킬 때 발생하는 이산화탄소의 거품이 끓어오르는 현상에서 나온 말이다. 그러나 오늘날 발효는 미생물학자들간에는 더 광범위한 의미 에서 사용되고 있다. 2 산업미생물학의 역사 옛부터 전해지고 있는 알코올 발효를 중심으로 식초발효, 발효식품제조 동은 그 발효과정이 경험적인 바탕 위에서 간단한 기록으로 전해져 왔기
때문에 집균에 의한 오염으로 실패하는 경우가 빈번했다. 발효를 일으키는 미생물을 발견하고 그 작용을 인식하게 된 것은 그 역사가 비교적 짧다. 미생물은 오랜 세월에 걸쳐 인간이 이용해왔음에도 불구하고 처음으로 관찰하고 기록한 것은 네덜란드 사람으로, 포목상이면서 렌즈연마를 하던 현미경 제작자 Ant ho ny van Leewenhock (1 632~1723) 이다. 그는 최고 확대율이 약 27 ()ll匠인 현미경을 제작하여 자연계의 여러 시료를 관찰하였 고 또 여러 형태의 미생물을 기록하였으며, 이들 작은 움직이는 생물을 미 세동물 (an i malcules) 이라 하여 이를 Roy al Socie t y of London 에 보고. 하였다. 그러나 이들 미세한 생물이 발효, 부패 혹은 전염병의 원인이 된 다고 하는 생각에는 미치지 못하였던 것이다. 많은 사람들은 아리스토텔레 스(B. C. 384~322) 가 제창한 가설과 같이 생물이 무생물로부터 자연발생 하는 것으로 믿고 있었던 것이다 . 미생물의 작용에 의해서 발효가 일어난다는 사실을 알게 되고 마생물학 이 과학의 한 분야로서 확립되게 된 것은 그로부터 약 임 1] 기가 지난 1 양 1l 기 후반인 Pas t eur 시대에서라고 할 수 있다. 불란서의 Louis Pas t eur(1822~1895) 와 영국의 Joh n Ty nd all(1 8 20~1893) 은 자연발생설을 부정하고 〈미생물의 생명은 그 이전에 존재한 생명으로부터 발생한 것〉이란 내용을- 증명함으로써 미생물학에 대한 개념 을 창시하였는데 Pas t eur 가 미생물의 생명의 기원에 대한 연구를 하기 이전인 18371d 에 불란서의 Charles Cagn i a r d de la Taur, 독일의 The- odor Schwann (1 810~1882) 과 Frie d ric h Taugo t t Kut zi n g 등은 각각 독립적으로 〈알코올 발효중에 당을 에탄을과 탄산가스로 전환시키는 현미 경적 작은 생명체(효모)의 존재와 알코올 발효가 이 작은 생명체에 의해 서 일어나는 생리현상〉이란 내용을 보고하였다. 그런데 당시의 저명한 화학자인 Jus tu s von Lie b ig , Jo ns Jak ob Berge l i us , Frie d ric h Wohler 懿 발효는 오로지 화학적 반왕기라고 믿 고 발효액 중의 효모는 생명이 없는 오영물질에 불과한 것으로 주장했던 것이다. Pas t eur 가 이들 화학설에 대해 반증을 하는 데에는 185A 빈부터
약 2 약이란 긴 세월이 소요되었다. 그는 당시 불란서의 Lill e 지방의 포 도주 양조과정에서 포도주가 酸 Hi 를 일으키는 원인에 대하여 조사를 의뢰 받고 있었다. 그는 현미경을 통해 발효액을 조사 하 는 중에 효모 이의에도 더 작은 생물, 즉 산을 생성하는 세균이 있어 산패는 이 세균에 기인된다 는 것을 밝혔고 모든 발효과정은 미생물의 생리활동의 결과로 나타나는 것이라는 사실을 확인하였다. 이 연구의 결과 그는 〈특정유형의 발효는 각각 특정미생물에 의해 매 개되는 반응〉이란 것을 확립하였다. 즉 알코울 발효는 효모에 의해서, 젖 산은 젖산균에 의해서 생성된디는 사실을 확인하였던 것이다. 그리고 맛없 는 불란서 포도주를 조사하는 과정에서 공기를 싫어하는 세균, 즉 공기가 없는 곳에서만 살 수 있는 형기성 (anaerob i c) 세균의 존재를 발견하고 이 세균이 부티르산 (bu ty r i c ac i d) 을 생성한다는 사실을 확인하였다. Pas t eur 에 이어 독일에서도 근대세균학의 선조라 할 수 있는 Robert Koch (1 843~1910) 가 의학세균학 분야에서 많은 연구성과를 거두어 세균 학의 연구기법을 확립했다. Koehl 근 젤라틴 고형배지에 이어 한천고형배지 를 만들거 세균의 분리배양법과 순수배양법울 고안하여 (1881) 오늘날에도 순수배양에 널리 이용되고 있다• 같은 시대에 (1878) 발효분야에서도 덴마크의 Hansen 은 맥주효모의 순 수배양에 성공하였다. 한센희석법이 바로 그것이며 이어 L i ndner 는 방울 배양법을 고안하였다. 한센은 이때 이미 맥주제조에 우량효모를 순수분리 하여 이 종균을 코펜하겐의 칼스벨그 양조장에서 시험제조하여 성공하였 다. 이렇게 하여 발효분야에서도 종전의 자연발효법으로부터 순수배양법에 의한 발효의 시대로 길이 열리게 된 것이다. 3 산업미생물학의 발전 Pas t eur 와 Koch 이들 두 선구자에 의해 개척된 미생물학은 곧이어 비
약 적 발전을 초 래하게 되 었 다 . Pa s t e ur 의 중 요한 이 념은 〈 발효는 산소 가 없는 곳 에서 일어나 는 호 홉 , 즉 생 물 의 형 기성 에너지 획득 방 식 »]라 는 생 각 이 었 다. 이 생 각 은 1 8 9 7',킨 독 일의 Eduard Buchner 의 무세 포 추 출 액이 알코올 발효 를 가진다는 우발적 발견 을 초 래하게 되었다. Buchner 는 효모를 마쇄하여 살아 있는 세포를 제거시킨 효모추출액이 당 을 알코올로 변환시킨다는 사실을 확인한 후 생물학적 전환은 특정효소 의 촉매작용으로 일어나는 화학적 반응이란 사실을 알게 되었고, 이러한 이념은 효소화학적 연구와 생화학연구의 급격한 발전을 가져오게 된 기초 가 되었다. 그 대표적인 성과로서 해당과정, 알코올 발효, 젖산발효의 과정 울 규명한 소위 Embden~M ey er hof- P armas Schem 떠 확립되어 발효화 학이 생화학의 기초가 되고 산업미생물학이 생화학에 주로 기여함으로써 생화학이란 학문은 독자적 영역을 확립할 수 있게 된 것이다 . 한편 산업미생물 분야에서는 동서양을 막론하고 양조업이 기초가 되고 있 는데 Hansen 의 맥 주 효모의 순수배양법에 이어 포도주 주정 제조용 효 모, 식초 양 조 의 초산 균, 요구르트 제조용 젖산균 등이 순수분리되어 그 균 의 분류학적, 생리학적 연구가 행해지게 되었다. 산업미생물공업 분야에서는 특정대사산물을 대량 생성시키는 미생물을 자연계로부터 분리하는 탐색단계의 시대에 돌입하게 되었으나 본격적인 발 효공업의 발 전 은 제 1 차 세계대전과 관련이 있다. 대전이 벌어지자 독일에 서는 곧 폭탄제조에 필요한 글리세린의 원료인 식물유의 수입이 영국에 의해 봉쇄당하게 되었다. 독일의 생화학자인 Carl Neuber g는 알코울 발 효중개 소량의 글리세린이 생성된다는 Pas t eur 의 연구결과를 개량하여 발 효중에 sod ium b i sul fi d 례- 첨가함으로써 글리세린 생성이 증가하는 것을 발견하였고 이 결괴를 연간 12,00~ 톤의 발효공업으로 발전시켰던 것이다. 한편 영국에서는 대전이 벌어지자 (1915) 화약제조에 필요한 아세톤을 러시아 태생의 화학자 Chaim . We i zman( 후에 이스라엘의 초대 대통령이 됨 )이 토양에서 분리한 협기성 세균인 Clostr id i u m ace t obu ty r i cu m-을 이용
하겨 처음으로 발효법에 의한 아세톤 • 부탄올 제조법을 공업화시켰다. 아 세톤 • 부탄올 발효는 석유화학에 의해 대치될 때까지 중요한 아세톤의 공 급방법이 되었다. 일찍이 미생물산업에서 미생물의 대사산물을 대량 생성시켜 산업화시킨 대표적인 산물로는 유기산울 둘 수 있는데, 젖산균에 의한 젖산의 제조와 As p er gi llus 속 곰팡기에 의한 시트르산의 제조, 글루콘선균에 의한 글루콘 산의 제조, 나아가 비타민 C 의 제조공정중의 D- 소르비톨 (D-sorb it ol) 로 부터 La 수근 ~(L -s orbose) 로 산화하는 반응을 미생물을 이용한 전환 방법에 의해 달성시키는 등 미생물이용 분어의 생물전환법의 확대가 이루 어졌다. 그러나 미생물에 의한 유용대사산물의 생산을 시도하려는 개념은 차츰 미량아나마 얻기 힘든 생리활성 물질아나 의약품원료로의 미생물 생 산수단을 탐색하는 방향으로 향하게 되었다. Pas t eur 나 영국의 의사인 Wi lliam Rober t s 는 미생물간에 길항작용이 있음을 187 떠경 관찰하면서 이 현상을 치료에 쓸 수 있을 것으로 생각하 였고 이들 물질의 효과를 조사하였으나 모두 동물에 독성이 깅히여 빛을 보지 못하던 중, 192~ 영국의 Alexander Flem i n g은 Penic i ll i u m no- t a t um 이란 곰팡이가 Sta p h yl o coccus aureusr d- 포도상구균을 배양하고 있는 접시에 우연히 들어가 자라면서 포도싱구균을 녹이고 있는 것을 발견하였 다. 그리하여 이 곰팡이를 액체배지에서 배양하여 그 배양액의 여러 세균 에 대한 항균성을 조사해본 결과 여러 종류의 세균증식을 저해함을 발견하 고 이 액체 중의 활성성분에 페니실린이란 이름을 부쳐 의약으로- 쓸 수 있 울 것으로 생각하였으나 이 페니실린은 극히 불안정하고 순수분리하기에는 어려운 물질이라 판단하고 도중에서 연구를 중단하였다. 193 0t;:祖]에는 많 은 화학자들이 이 물질을 순수분리하려고 노력하였으나 성공하지 못했다. 그 후 O xf ord 대학의 Howard W. Flore y와 Ernest B. Cha i펴評 7 193 9\1에 다시 연구를 시작하여 안전한 형태의 페니실린을 만들어 임상실 험에서 항균활성이 있음을 증명하였으나 제~} 대전중에 있던 영국에서는 이 연구를 더 계속할 수가 없어 Flore y와 그 동료인 Norman Hea tl e y는
1941 년 미국으로 건너가 연구를 계속하고 194 3 \ :i 대량 생산기술을 확립하 여 공업생산이 개시되었다. 이 페니실린의 대량 생산의 성공은 전쟁에서 부상한 많은 사람의 인명을 구했을 뿐 아니라 미생물의 의약품생산에 일 대 혁명을 가져오게 하였다고 하여도 과언이 아니다. 항생물질시대가 개막되면서 Ru tg us 대학의 토양미생물학자인 Selman A. Waksman은 많은 종류의 방선균이 세균저해물질을 생성함을 조사해냈 고 이들 방선균의 한 종류인 Stre p t om y ce s gri se us7} 그람음성균과 결핵균 에 저해효과를 나타내는 스트렙토마이신 (s t rep t omy c i n) 을 생성하는 것을 발견하게 되어 이들 물질을 항생물질 (an ti b i o ti cs) 이라 부르게 되었다. 이 둘이 계기가 되어 세계 각처에서 새로운 항생물질의 발견이 속속 이어지 고 산업미생물시대에 의약분야의 개척이란 일대 혁명시대를 맞이하게 되었 다. 4 산업미생물과 그 이용 범위 미생물을 산업에 이용하여 인간복지에 기여하게 할 수 있는 것은 미생 물이 지닌 특성과 능력의 다양성이 있기 때문이다. 미생물이 지닌 가장 기본적 특칭은 세포가 작기 때문에 체적에 바해 그 표면의 비율이 크다는 것이다. 즉 표면적이 큼으로 해서 영앙소를 세포내 로 급속히 흡수할 수 있고 따라서 높은 대사속도를 지탱해낼 수 있는 것 이다. 미생물의 생합성 속도는 대단히 빨라서 1 형손 정도로 세포가 복제되 어 두 배로 증식하는 종류도 있다. 미생물은 다양한 환경에 적응하면서 긴 세월 동안 진화해온 역사를 반 영하여 고등 동식물이 적응할 수 없는 환경조건에서도 생활할 수 있는 종 류가 많은 것이 특칭이다 . 님국과 같은 얼음에서 서식하는 것이 있는가 하 면 온천수와 같은 뜨거운 물에 서식할 수 있는 종류도 있고 딥수나 염전 과 같은 곳, 공기가 있는 곳이나 없는 곳, 영양분이 많은 곳이나 결핍된
곳에서도 각기 그 환경을 극복해서 생활할 수 있는 미생물이 전화하면서 적응하고있다. 미생물은 광범위한 대사반응을 영위할 수 있기 때문에 그 적응력을 이 용하여 산업적으로 인간이 이용하고 폐기되는 영양소를 고가의 산물로 생 산할 수 있다. 예컨대 당밀이나 옥수수 침지액 (corn ste e p l iq uor) 과 같 은 폐기물에서 항생물질 아미노산류와 같은 고가의 물질을 생산할 수가 · 있다. 미생물의 생산성은 그 이용면에서 4 가지 측면으로 분류할 수 있다 (Rose, 1979). 1. 산물로서의 미생물균체 (micr obia l bio m ass) 2. 미생물이 산출하는 고분자물질 및 효소류 (m i crob i al enzy m es) 3. 미생물의 일차대사산물과 이차대사산물 (m i crob i al meta b olit es ) 4. 미생물 전환공정 (micr obia l tra nsfo r mati on ) 4.1 미생물균체의 이용 미생물균체는 용도면에서 두 가지가 있다. 그 하나는 균체를 석량자원으 로 이용하는 것이다. 미생물균체는 풍부한 단백질과 다양한 영양소롤 함유 하고 있다. 효모와 클로렐라와 같은 균체는 단백질 함량이 50% 이상에 달하며 또 여러 가지 비타민을 함유하고 있어 균체를 수집하여 식량이나 사료로 사용할 수 있고 효모에서 글루타치온이나 핵산, 그리고 비타민 B 군을 추출하여 약용원료로도 쓸 수 있다. 미생물균체의 이용을 위해서는 세균균체, 효모류, 곰팡이 및 클로렐라 등 다양하나, 독일에서는 세계대전시 효모균체를 대량 배양하여 빵이나 비 스켓 등에 혼합하여 단백질원으로서 식량으로 대체시킨 바가 있고 오늘날 에는 석유계 탄화수소로부터 효모를 대량 배양하여 사료단백질로서 이용하 고 있으며 장래 인류의 식량문제 해결의 측면에서도 대단히 중요시되고
있다. 미생물균체의 또 다른 용도로는 빵의 제조과정에서 사용되는 빵효모를 사람이나 가축이 섭취함으로써 정장작용과 같은 효과를 기대하여 생산되는 균체의 이용에 있다. 마생물균체를 이용하여 물질전환을 달성하는 부분은 항목을 독립시켜 취급하기로하겠다. 4.2 미생물이 생성하는 고분자물질 (mi cr obia l bio p o l ym er) 미생물이 생성하는 고분자물질 중 가장 중요한 것은 효소류 (enz y mes) 이다. 효소는 그 촉매의 특이성이 높고 고온을 요하지 않으며 반응효율이 나 활성이 높기 때문에 식품공업이나 화학공업 분야에서는 대단히 중요한 위치를 차지하고 있다. 효소류가 처음에는 식물이나 동물에서 추출되었으나 오늘날에는 미생물 에 의한 생산이 급속히 증대하고 있으며 대량 생산에도 최적화된 발효조 배양을 통한 단시간내 생산이 가능하기 때문예 큰 이점을 지니고 있다. 또 다른 이유는 목적으로 하는 효소를 생산하는 미생물을 분리할 수 있고 이 미생물을 유전적으로 조작하여 효소의 생산량을 개선하는 것이 가능해졌기 때문이다. 미생물에 의해서 생산되는 효소 중 최근 이용되고 있는 분야로는 양조, 빵제조, 제과, 과당제조, 섬유산업 등에 쓰이는 아밀라아제 양조, 육가공, 피혁제조, 세제 등에 쓰이는 단백질 분해효소, 치즈제조에 쓰이는 렌닌, 포 도당을 과당으로 전환시키는 포도당이성화효소 등이 있고 그 밖에 의약품, 전단용 효소류 동식물성분 추출을 위한 분해효소류의 이용분야가 확대되고 있다. 이들 효소의 생산을 위한 유전학적 혹은 유도조절을 통한 생산방법 이 크게 발달하고 있으며 이들 효소의 고정화방법에 의한 이용방법도 크 게 진전되어 경제적인 효율을 높이고 있다. 미생물이 생산하는 산업상 중요한 고분자물질 중에서 효소 이의의 중요
한 것으로 다당류가 있다. 다당류의 주요 공업원료로서는 해 초 와 같은 식 물을 둘 수 있겠으나 최근에 와서 미생물에 의해 산출되는 다당류가 관심 울 끌고 있다. 많은 미생물산출 다당류 중에서 Xanth o monas camp es tn i s 란 세균이 내는 xanth a m g um 은 점성물 질 로서 식품의 안정제 혹은 유화제 뿐만 아니라 석유채유시 사용함으로써 채굴수율을 울릴 수가 있다. 그 외 에도 의약품 , 살충제 등의 첨가제가 되는 것도 있다. 4.3 일차대사산물과 이차대사산물 미생물에 의해 대사되어 산출되는 산물은 제 1 차 대사산물(p r i mar y me - t abol it es) 과 제 2 차 대사산물 (secondan y me t abol it es) 로 나눌 수 있다 (Ki es lic r , 1982). 미생물 증식과정에서 대수증식기 (log p hase) 에 세포내에 대사생성되는 산물은 주로 세포의 증식 및 생식에 필수적인 아미노산, 핵산 관련물질, 단백질, 지질, 당질과 그 전구물질 등 세포의 구성성분이거나 그 생합성에 필요한 에너지 및 관련물질들이다. 이러한 대사산물을 제 1 차 대사산물이라 하는데(t ro p ho p hase) 제 1 차 대사산물은 발효공업에서 중요한 생산물이 되고 있다. 제 1 차 대사산물로서 가장 중요한 것으로는 아미노산, 퓨린누클 레오티드(p ur i ne nucleoti de s), 비타민류, 유기산류 등을 들 수 있다. 제 1 차 대사산물의 생산은 경제적으로 대단히 중요하다. 다만 미생물 야 생주가 일차대사산물을 합성할 때는 증식이 필요한 양만큼 생성하기 때문 에 그 대사산물의 생성량을 증대시키기 위해서는 이들 야생주의 합성조절 메커니즘을 변경시켜 유전적으로나 배양조건을 개선함으로써 그 생산성을 향상시킬 수가 있고 이러한 분야의 연구는 산업미생물학 연구자들에게 부 과된 중요한 과제 중의 하나라고 볼 수 있겠다. 증식의 정지기 (sta t i on ary p hase) 에서 미생물이 대수중식기에 생성하 지 않았던 화학물질을 합성해내며 이들 화학물질의 세포내 대사에서 그 기능이 명확하지 않는 경우가 있는데 이러한 화학물질은 대사 및 증식시
표 1.1 제 1 차 대사산물과 그 생산균 및 용도 - - 1 차 대사산물 생산균 용도 에탄올 yea st, Rhiz o p u s 알코울음료·화학공 업 시트르산 Aspe rgi llu s nig e r 식품공업원료 아세톤·부탄올 Cl. aceto b uty li cu m 유기용제 아세트산 Aceta b acte r aceti 식품가공 글루콘人J Aspe rgi llu s nig e r 식품가공 글루탐산 Mi cro coccus glu ta m i cu s 식품가공 라이신 Mi cro coccus g lu t am i c 의 묘변이주 식품 및 사료첨가제 누쿨레오티드 Breubacte r ammon i e g ene 펴 돌연변이주 증미제 xanth a n gum Xanth o monas comp es tr is 식품공업유화제 리보풀라빈 Ashby a gos syp ii 영양보강제 비타민 B12 Prop ion ib a cte r iu m shermanii 영양보강제 Pseudomonas denit rif ica ns
기와 관련해서 (idi o ph ase) 제疾} 대사산물 (secondar y me t abol it es) 이 라 한다. 제差} 대사샨물은 제 1 차 대사산물을 중간 합성원료로 하여 생성 되며 대부분 제한된 미생물 종류에서만 생성된다. 제疾} 대사산물의 특칭을 살펴보면, 1. 제疾} 대사산물은 소수의 제한된 미생물에 의해서만 생성된다. 2. 증식과 생식에 필수적인 대사물질이 아니다. 3. 환경요인에 의해서 그 생성이 좌우된다. 4. 제疾} 대사산물은 화학구조가 밀접하게 연관된 집단으로 이루어지고 있 다. 예컨대 방선균의 한 균주는 32 종의 유사구조의 안트라사이클린 (an t hrac y c li nes) 을 생성한다. 5. 미생물 중에서는 다양한 종류의 제疾} 대사물질을 생성하는 것이 있다. 6. 제~} 대사산물의 생합성 조절은 제 1 차 대사산물의 조절 메커니즘과는 다 르다.
제 2 차 대사산물 중 산업미생 물 분야의 관심대상 물질로서 대 표적 인 것 으로 항생물질 등 항미생물활성을 가전 물질, 알칼로이드류 식물생장호르 몬, 독성물질, 효소저해물질 등을 들 수 있다. 가장 대표적인 것은 이차대 사산물인 항생물질인데 이미 10,00 0-'l문 이상의 항생물질이 발견되어 있고 (미생물에서는 약 7,00 (H은) 매년 20 어]지 30 0{류가 새롭게 추가로 발견 되고 있으며 미생물 중 70% 이상이 방선균 Stre p tom y ce s4 r- 세균에 의 해 서 생성되고 있다. 이미 알려진 항생물질이 많이 있음에도 불구하고 새로운 항생물 질울 계 속 탐색하는 것은 기존 항생물질에 대해서 저항성이 강한 균이나 혹은 돌 연변이의 결과 저항성을 획득한 균에 대항하기 위해서도 필요하고 나아가 보다 안전한 약품을 공급하기 위해서도 필요한 것이다. 항생물질의 대부분 이 실질 임상시험에서 독성을 나타내거나 효력을 발휘하지 못하므로 실용 화되지 못하고 있어 화학자들은 효력을 증진시키거나 저항성 획득을 극복 하기 위해서 이들 항생물질의 구조변경을 시도하고 있다. 이렇게 해서 개발된 반합성 항생물질이 의료 분야에서 점차 중요시되고 있댜 발효공업의 생산성을 높이고 더욱이 화학공업과 대항하기 위한 가장 중요한 수단으로서 돌연변아를 들 수 있다. 산업미생물 분야 산업에서는 돌연변이유발제로 미생물을 처리함으로써 그 유전자의 발현을 몇 배 혹은 몇 십 배 증대시킬 수 있다. 페니실린공업에서는 Penic il l i u m chry so g en um 의 공업생산용 균주는 원 야생주에 비해서 약 l,OO Qil n 의 단위용량당 생산 증대를 울리고 있다. 한편 돌연변이의 결과 분자구조가 변경된 항생물질을 생산시킬 수가 있어 생산물의 개량에 이 방법이 이용되기도 한다. 4.4 미생물 전환공정 미생물에 의해서 물질을 전환시키는 것은 광의로는 미생물균체의 이용 이나 고분자물질로서 생성된 미생물효소의 이용이란 범위에 포함시킬 수가 있겠으나 화학물질의 구조전환이란 관점에서 보면 그 목적을 뚜렷하게 구
분시킬 수도 있다. 전환공정 에서 는 미생 물균체 에서 공급되는 한 종류 또는 수종류의 효소로서 화학물질을 경제적으로나 고귀한 물질로서 화학적으로 관련된 구 조를 가전 화학물로 변화시키는 반응에 미생물을 이용하는 것이 다. 여기서 사용되는 미생물은 증식균체 혹은 미중식균체, 때로는 건조균 체를 쓰는 경우도 있는데 마생물은 그 종류에 따라 어떤 종류의 반응도 수행될 수 있다 . 대표적인 반응으로서 탈수소반응 (deh ydro g ena ti on), 산화반응 (ox i da ti on), 수산화반웅 (h y drox y la ti on), 탈수반응 (deh y dra - tion ), 축합반응 (condensa ti on), 탈탄산반응 (decarbox y la ti on), 아미노화 반응 (am i na ti o11), 탈아미노화반응 (deam i na ti on), 그리고 이성질체화반응 (iso meriz a ti on ) 등을 들 수 있다. 미생물학적 전환공정은 순화학적 방법에 비해 많은 이점을 가지고 있다. 예컨대 첫째, 대부분의 미생물학적 화학반응에서는 반응용기를 가열하거나 냉각하면서 많은 에너지를 소모하는 데 반해 미생물 전환공정을 상대적으 로 낮은 온도인 상온부근게서 반응시킨다. 둘째, 화학적 전환공정에서는 반응이 보통 유기용매내에서 행해지거나 중금속과 같은 무기촉매를 요구하 기 때문에, 그 결과 이들의 제품을 오염시킬 우려가 있고 또한 필요치 않 는 부선물이 같이 생성되어 정제단계를 복잡하게 하는 경우가 많다. 그런 데 미생물학적 전환공정은 물을 용매로 하면서 상온상압인 생물학적 온도 에서 반응이 진행된다. 셋째, 미생물 전환의 특칭이면서 이접으로서의 반 응의 특이성을 둘 수 있다. 한 종류의 효소는 기질분자의 특정자리의 반응 울 촉매하여 한 가지 반응만을 일으킨다. 또한 효소는 화학물질의 특정이 성질체만을 선택하여 반응의 촉매작용을 하는 기질특이성을 가지므로 미생 물 전환으로 고수율성을 기할 수가 있다 . 미생물 전환으로 가장 오랜 세월 동안(기원전 약 50Q ld 바빌론에서도 식초제조) 인간에게 이용된 것은 주정성분으로부터 식초의 제조과정인데 최근에 와서는 포도당으로부터 글루콘산, 비타민 C 제조과정에서의 소르 비톨에서 수근 나 ? 人쿠의 전환, 의약품공업에서는 스데로이드의 전환, 반합 성 페니실린제조 등 항생물질 전환, 그리고 프로스타그란딘의 전환 등에
미생물 전환기술이 높이 평가되고 또 실용적 가치로서 평가받고 있다. 미생물 전환은 무공해성 전환방법으로서 환경오영을 초래하는 화학반응 에 점차 대치될 수 있는 방법으로 중요한 위치를 넓혀가고 있다. 집卜고문헌 Demain A. L., Industr i a l Mi cr obio l ogy , Scie n ti fic Americ a (1 9 81) vol. 11. No. 9. Sta n ie r , R. Y., et al, The Mi cr obia l World(The beg inning s of mi cr o-bio l og y), Fif th edit ion , 1987. Brock, T. D., Bio l og y of Mi cr oorga nis m s, 4th . edit ion (1984) and 5th . edit ion ( 1988) .
제 2 장 새로운 대사산물의 검색과 산업균주의 분리 1 대사산물 미생물의 물질대사 능력은 무한한 가능성을 가져 매우 다양한 화학물질 울 많은 종류의 미생물균주로부터 얻을 수 있고 또한 생성시킬 수가 있다. 따라서 산업미생물 분야 연구자가 해야 하는 분야로서 새로운 미생물 대 사산물을 탐색하기 위한 방법을 개발해내는 것이 중요한 과제가 되고 있 다. 산업미생물 분야의 개발되어야 할 분야를 요약하면 다음과 같다. 1.1 새로운 대사산물의 검색 (screenin g ) 새로운 균주분리의 검색과 새로운 검사방법을 구사하여 새로운 대사산 물을 생산하는 것으로서 이러한 과정을 통해 새로운 범주에 속하는 물질 울 발견할 수가 있다 (N i sbe t, 1982). 1.2 화학적 전환 (chem i cal modif ica ti on ) 기존 미생물 대사산물을 화학적 혹은 미생물학적(효소학적) 방법에 의 해 분자구조를 변경시켜 개량된 성질을 지닌 물질로 전환시키는 과정.
1.3 원형질체 융합에 의한 균주개량과 새물질 탐색 종간 혹은 속간 원형질체 융합(p ro t o p las t fu s i on) 으로 유전자 재조합 울 달성시켜 균주의 생산성을 향상시키고 나아가 새로운 변화된 물질을 개발하는 과정으로서 항생물질 생산이나 이차대사산물 개발에 널리 이용될 수있다. 1.4 유전자 재조합에 의한 방법 이미 알려진 물질을 생산하는 균주간에 유전자를 이동시키거나 혹은 비 생산균에 유전자를 전환시켜 화학적으로 변화한 산물잘울 생성시키려는 시 도로서 미래에 기대되는 방법이라 할 수 있다. 미생물에 의해서 생합성되 는 대사산물의 종류는 매우 다양하기 때문에 어떠한 종류의 대사산물을 검색하느냐 하는 것은 전적으로 검색하는 방법, 즉 시험방법과 검색에 사 용하는 미생물균주와 시험균주에 의존하게 된다. 의약품에 쓰이는 항생물질을 생산하는 균주분리에도 검색 (screen i n g)방 법이 주로 쓰이고 있는데 이와 같이 검색방법이 아직 쓰이고는 있지만 검 색목표의 설정은 변화하고 있다• 즉 현재 사용되고 있는 항생물질 내성균 에 유효한 항생물질과 항바이러스성 항암성 물질 검출에 많은 노력이 경 주되고 있는 실정이다. 그 결과 매년 200 내지 300-2 1 새로운 활성물질이
표 2. 1 새로운 항생물질의 출현 1962 1977 미생물 출현수 % 출현수 % Str ep t om y ce s 58 61 37 70 Str ep t om y ce s 이의의 Acti no my ce ta le s 24 25 8 15 곰팡기 10 11 7 13 Actin o my ce ta le s 이의의 세균 3 3 1 2
보고되고 있으며 그중 약 100 정도가 방선균으로부터 분리되는 것들아다 (표 2.1 참조) (Lancin i , 1980). 2 유용미생물의 분리와 겁색 2.1 검색대상균 검색계획의 성공여부는- 사용하는 미생물의 종류와 활성을 검출하기 위 한 방법에 좌우된다. 오늘날 균주의 선택이 30~40% 정도의 검사방법은 60~70% 정도의 영향을 결과에 미치고 있다. 새로운 대사산물의 분리에 있어서 극단환경의 균주들이 새로운 대사산 물을 만들 것이라는 기대에서 그러한 환경으로부터 균주를 분리하려고 노 력하고 있다. 예를 들어서 높고 냉한지, 바닷물, 심해, 사막, 간헐천, 유전 등의 미생물들이 조사대상이 되고 있다. 지금까지 새로운 종류의 화학물질 이 발견되지는 않고 있지만 강화배양에 의하여 바닷물과 물에서 Mi c- romonospo ra, Str ep t os po rang ium , 그리고 Acti no p la nes, 되비에서 The- rmoac ti nom y ce 러 1hermomonospo ra, 바닷물에서 Acti no p la nes2 } 같은 특 별한 미생물들이 분리되고 있다. 각각의 속으로부터 생성되는 대사물질의 다양성은 St rep t omy ce t e 遷 제의하고 어느 정도 한정되어 있다. 즉 Bacil - lum 주의 경우는 거의 펩티드계 항생물질만을 생성하는 것이 특칭이다. 분리된 20,000rr주 의 Ac ti no p lane 예 관한 대규모 실험에서 13,00 어芹주 의 항생물질에 대한 형성여부를 검색한 결과 l Qld이라는 기간 동안에 41 개의 새로운 항생물질이 분리되어 성질이 조사되었는데, 거의 대부분이 아 세틸말로닐 (ace ty lmalon y l) 계이거나 아미노산 유도체임이 밝혀지고 있다 (표 2. 2). 성공적인 산업적 스크리닝 계획에는 대규모 시설과 숙련된 요원이 필요 한데 오늘날 많은 산업적 스크리닝 조직의 분리 및 검사능력은 대략 연간
1,000~2,000 균주로 볼 수 있다.
SPterp u tcidtue sr 표e / D2e. p2 s i1 p3 e,0p 0t 0i deA sc ti no p la nes 균주가 생성하는 항생물질의 범g1—위 4 353222 Macrocyc l ic Lacto n es Aromati c anti bi o t i cs and qui n o ne deriv a te s Hete r ocy cl ic anti bio t i cs Polye n es Polys a ccharid e s Glyc o p ep t ide s Glyc o lip ids Ot he rs (Lancin i , 1980)
2.2 겁색방법 (tes t sys t e m s) 검색과정의 성공여부는 필요없는 항생물질들을 제의시키고 원하는 성질 의 화합물들만을 얻을 수 있도록 고안된 검사방법의 개발에 의해서 좌우 된다. 한 예를 들어보면 (Omura et al, 1979) 세포벽 생합성 저해물질을 발견하기 위한 한 검색계획의 처음 단계에서는 저해조사시험이 Bacil lu s sub ti l i邊 저해하나 Acholep la sma la i dlaw ii(세포벽이 결핍되어 있다)를 저해하지 않는 대사물질에 대해서 행해졌다. 두번째 단계에서는 세균의 세 포벽 구성성분인 mesodia m i no p im elic ac i d의 합성을 억제하면서 단백질 합성을 나타내는 류신(l euc i ne) 의 흡수를 저해하지는 않는 물질을 조사하 였다. 세번째 단계에서는 큰 분자물질은 임상적으로 사용될 때 종종 원하 지 않는 부작용을 초래하기 때문에 (분자량이 1,00 따i다 큰 물질이 여과막 入냄에서 제거되었다) 이러한 세 가지 과정에 의해서 곰팡이 세균과 Act-
i nom y ce t es 방선균 등 약 10,00 어t주의 배양 여과액 을 검색하여 새로운 항 생물질인 azureom y c i n 이 발견되었고 6 개의 이미 알려진 항생물질도 재분 리한 예가 있다. 페니실린(p en i c i ll i n) 은 l - 락탐 (P-lact am) 계 항생물 질 인데 내성을 나타 내는 하나의 이유는 '-락탐환을 끊는 효소인 P-lac t amas 태 7 생성하기 때 문기다 . 그래서 P-lac t amas 려 저해물질이 내성균에 대하여 페니실린 치 료효과에 유효할 것이라는 전제히에 미생물의 /J- lacta m ase 저해물질에 대 한 검색을 행하였다. 배양 상등액을 페니실린이나 ce p halos p or i n 함유 한 천배지, 그리고 P-lacta mas~ 생성하는 미생물균주가 접종된 배지에 펴 주었다 . 이렇게 해서 P-lac t amas 헝l- 저해되는지롤 첫번째 검색에서 결정 할 수 있었다. 한편 但 ac t amase 활성에 내성을 가진 항생물질을 찾기 위 해서는 P-lacta m ase7]-첨 가된 시험 배양이 검색에 사용되기도 한다. 함암활성을 가전 물질들을 검출하는 경우와 같이 생물학적 활성물질을 검색하기 위한 또 다론 방법으로는 분자생물학적 방법을 이용하는 수도 있다. 예컨대 프로파지 람다(p rop ha g e }c)에 의해 용원화된 E. co li균주에 서 특이하게 용균상태를 유도해낼 수 있는 화합물들을 검색해내는 것이다. 이러한 방법에서는 용원화된 E. col i의 증식을 저해하는 물질이 제거되도 록 대조구를 두고 바이러스 생성을 · 특이하게 유도하는 화합물만을 발견해 내는 것이다 또 다른 방법으로는 E.col i의 수복 메커니즘 (dark repa ir mechan i sm) 의 목]저해 (DNA 제거 )를 측정하는 방법이다. 이러한 검색방 법으로 함암활성을 가전 항생물질인 leukaemom y c i n이 발견되었다 (Fleck & Str a uss). 검색에 대한 합리적 방법에 대한 예를 제시함으로써 다른 검색계획에 대한 좋은 착상을 제공해줄 수 있는 것이다. 비록 새로운 항생물질 활성을 검출하는 데에 있어서 최근의 합리적 검 색방법이 임의 검색방법만큼 성공적이지는 않지만 임의 검색방법은 지난 3 떠 동안 대규모로 행해전 반면 합리적 검색방법은 상대적으로 새로운 접근방식임을 인식해야 할 것이다.
3 유용미생물의 보존 및 관리 대부분의 미생물학 실험에서 는 교육용, 연구용, 생 물 학적 검정용 (b i o assay ), 산업용, 그 밖에 다른 목적으로 균주들을 보 존 , 관리하고 있다. 균 주의 적절한 보관은 매우 중요하므로 장바의 표준화가 필요하다. 균주보관 의 주요목적은 미생물이 오영되지 않고 돌연변이가 일어나지 않도록 하는 것이다. 즉 원래의 미생물 (or igi nal iso late ) 상태로 보존할 필요.7~ 있다. 미생물을 보존하는 방법은 많이 제시되고 있지만 모든 종 의 미생물을 똑 같은 방법으로 보존할 수는 없다. 때때로 사용가능한 장치와 기구 보관장 소, 그리고 노동의 숙련에 따라 보존방법이 달라진다. 미생물을· 보존하는 데 있어서 보존기록은 매우 중요하지만 소홀해지기 쉽다. 대개 균주의 명 칭 (str a in des ig na ti on) 은 문자와 숫자로 표기되는데 이는 확실한 표현형 의 특성 (dist i nc t ph enoty pic charac t er i s ti cs) 을 지닌 특 수급 균주를 뜻한다. 이러한 기록에는 분리원과 그 균주를 분리한 연구자의 이름도 기 록해야한다. 3.1 단기보존법 (short- ter m meth o ds) (1) 계대배양 (subcul t ur i n g ; Li nc oln, 1960) 균주를 보존하는 전통적인 방법은 신선한 배지에 미생물을 주기적으로 옮겨주는 것으로서 이식주기는 미생물 종류, 사용되는 배지, 그리고 의부 환경에 따라다르다. 어떤 종류의 미생물은 이틀에 한 번씩 옮겨주어야 하는 반면에 보통 미 생물은 몇 주 또는 몇 달에 한 번씩만 옮겨주면 된다. 균주를 보존하는 방 법으로써 이 방법을 이용할 경우에는 세 가지 조건을 검토, 결정하여야 한 다. 죽 첫째 적당한 보존용 배지, 둘째 이상적인 보존온도, 셋째 옮겨주는 빈도이다. 보존용 배지 (ma int e n ance mediu m ) : 미생물의 대사율을 낮게 유지시
킴으로써 이식빈도 를 줄 이는 데 는 최소배지 (mi ne ral med i a) 를 사용하는 것이 좋 으나 어떤 미생 물 은 증식을 위해 복합배지 (comp le x med i a) 를 필 요로 하기도 하고 특 정한 생리적 특성을 유지하기 위해서는 배지 속 에 복 잡한 화합물을 필요로 하는 경우도 있다. 필요에 따라 복합배지가 이용될 경우에는 증식이 가속되고 대사산물이 더 빨리 축적되므로 배지를 더 자주 갈아주어야 한다 . 보관 (s t ora g e) : 미생물의 가장 간단한 보존방법은 상온에서 시험관걸이 (tes t tab e rack) 나 특별히 고안된 보존용 통에 넣어 보존하는 것이다. 이러한 방법으로 보존되는 균주들은 쉽게 건조되므로 항상 주의를 기울여 야 하며 건조의 위험을 최소화하기 위해서는 고무띠가 있는 마개를 사용 하고 파라필름으로 감싸거나 시험관을 풀러스틱 통에 넣어두어야 한다. 이 와 아울러 미생물의 대사속도를 줄이기 위해서는 냉장고 (5~8 °C )에 보관 하여야 하며 대부분의 미생물은 이 방법에 의해 3~57H 월 동안 보관될 수 있다. 계대배양 방식 (tra nsfe r schedule) : 배지를 갈아주는 시간 간격 (sub- cultu r in g i n t erval) 은 실험에 의해서 결정되는데 연속적으로 배지를 갈 아주면서 균주가 순수배양되는지를 검사하고, 표현형의 특성이 변화되었는 지를 알아보기 위해서 주기적으로. 간략한 특성판별법 (characte r iz a ti on ) 을수행하여야한다. 이러한 균주보관법을 이용할 때는 돌연변이체를 선별할 가능성이 크기 때문에 균주를 새로운 배지에 옮겨줄 때는 한 개 이상의 집락을 선별하여 야한다. 이와 같이 연속적으로 배지를 옮겨줌으로써 균주를 보존하는 방법의 단 점으로는 오염의 위험, 잘못된 표기의 가능성, 돌연변이체의 선별가능성, 균주의 손실가능성, 그리고 필요한 보관장소 등을 들 수 있다. (2) 광유 (m i neral o i l) 내 침지보존법 많은 미생물은 멸균된 광유(액체 par aff in 등)에 담그는 비교적 간단하
고 저렴한 방법으로 몇 달 내지 몇 년 동안 보관할 수 있다. 그러나 이 방법에 의해서 미생물을 보관하면 불충분하게 떨균된 광유 때문에 오염이 자주 일어나므로 170°c 의 오본에서 약 l~ 앙]간 동안 가열함으로써 광유 를 완전히 멸균시킨다. 오토클레이브 (au t oclave) 를 이용한 고온고압살균 법은 광유의 적합한 멸균법이 아니다. 이 방법으로 균주를 보관하기 위해서는 먼저 사면배지, 고충배지 또는 액체배양 등의 적당한 배지에 균주를 배양한 후 건조를 방지하고 대사활 성과 균주의 증식을 감소시키기 위해서 멸균된 광유를 적어도 2cm 깊이 이상넣는다. 광유가 덮인 균주를 냉장고에 바로 세워 보관하며 이들 균주가 잘 보관 되는지를 알아보기 위해서 주기적으로 생존실험 (via b il it y t es t)을 행하여 야 한다. 광유 아래에 있는 미생물은 접종침 (ino culati ng needle) 으로 새 배지로옮겨 쓸수있다. (3) 동결(fr eez i n g) 보존법 (Perlman, 1977) 냉장고의 냉동실이나, 일반적으로 0°C 에서 一 20°C 의 온도범위인 냉동실 (fr eezer) 에서의 균주보존은 매우 유동적이며 미생물의 종류에 따라 다른 결과가 나타난다. 일반적으로 용융 (eu t ecti c) 의 농축된 전해질 용액 (NaCl) 은 ― 20°c 의 용융온도를 지니므로 미생물이 손상을 입기 때문에 동결보관법은 바람직하지 못하다. 그러나 어떤 미생물은 이 방법에 의해서 약 핵월~썩 동안 보관될 수 있다. (4) 건조 (dr yi n g) 보존법 대부분의 미생물은 실험실에서 건조시키면 죽게 되나 이들 미생물 중에 서 특히 포자형성균주들은 적당한 용매에서 건조시킴으로써 몇 년 동안 보관할수있다. (5) 토양 (so il) 보존법 (Prid h am, 1973)
포자형성세균은 공기건조 멸균토양과 혼합해두면 수년 동안 잘 보존할 수 있다. 이 방법을 위해서는 먼저 토양을 이틀 동안에 걸쳐 여러 시간 고 압살균법 (au t o~av i n g)으로 멸균시킨 뒤에 포자용액 l m 邊 멸균토양이 들어 있는 시험관에 접종시킨 후 실온에서 충분히 마를 때까지 세워둔다. 충분히 마르면 멸균된 고무마개로 봉한 뒤에 냉장고에서 보관한다. (6) 종이 (pa pe r ) 보존법 이 방법은 멸균된 여과지 조각에서 미생물을 말림으로써 비교적 간단하 고 값싼 균주보존법이다. 이 방법에 의하면 같은 종류의 미생물을 포함하고 있는 여러 여과지 조 각을 같은 시험관에 밀봉시켜 보관할 수 있으므로 필요할 때마다 여과지 한 개를 멸균된 집게로 꺼내 적당한 배지에 접종시켜 사용할 수 있다. En t erobac t er i acea 툰 아니라 여러 종의 미생물 역시 아 방법에 의해서 몇 년 동안 잘 보존할 수 있으며 이 방법은 다음과 같다. 멸균된 여과지를 ml 당 108세 포수 (cells) 이상의 미생물을 포함하고 있 는 미생물의 배양액으로 포화시킨 뒤 공기 중에서 건조시키거나 전공전조 시킨 후 시험관에 넣어서 봉한 뒤 건조기나 냉장건조기 (des i cca t ors) 에서 보존한다. (7) 젤라틴(g ela ti n) 보존법 많은 종류의 종속영양형 세균 (he t ero t ro p h i c bac t er i a) 은 말린 젤라틴 에서 보존할 수 있다. 이때 보관온도는 매우 중요한데 일반적으로 —20° C 가 4°c 나 상온보다 더 유리하다. 이 방법은 다음과 같다. 균주를 적당한 배지에서 배양한 뒤 무균상태에서 원십분리하여 집균한 다. 이를 소량의 액체배지에 현탁시킨 뒤 30°C 에 녹은 영양젤라틴 (nutr i - ent gel ati n) 2.0~5.0ml 를 포함한 시험관에 m1 당 10 도 1010 개의 세포수 가되도록접종한다. 이러한 미생물 현틱액 중 1 방울을 멸균된 페트리 접시 (petri d i sh) 에
후퇴르 피펫 (pa ste u r pip ette) 이나 주사기를 이용하여 떨어뜨린다. 이 페트리 접시를 ph osph orous p en t ox i d 여十 넣어둔 건조기에 놓은 뒤 전공 펌프로 증발시킨다. 방울이 다 건조되면 무균상태로 이들을 멸균된 시험관 에 옮간 뒤 냉장고에 보관한다• 이들을 다시 사용하고자 할 때는 젤라틴 방울을 적당한 배지에 무균상태로 옮김으로써 미생물을 증식시킬 수 있다. 3.2 장기보존법 (lon g -ter m meth o ds) (1) 동결전조법 (lyop h il iz a ti on : Perlman, 1977) 동결전조법은 미생물을 오랫동안 보관하는 가장 경제적이고 효과적인 방법 중의 하나로서 이 방법은 생리적으로 매우 다양한 많은 미생물과 박 데리오파지를 3 0\1이 넘도록 보존할 수 있다. 또한 이 방법을 이용하면 용 기가 작아 보관하기가 유리하다. 동결전조법은 매우 간단하지만 이론적인 배경은 복잡하다. 동결건조과정 은 감압하에서 얼린 미생물 배양액으로부터 승화에 의해 물을 제거하는
 D
D
 G
G
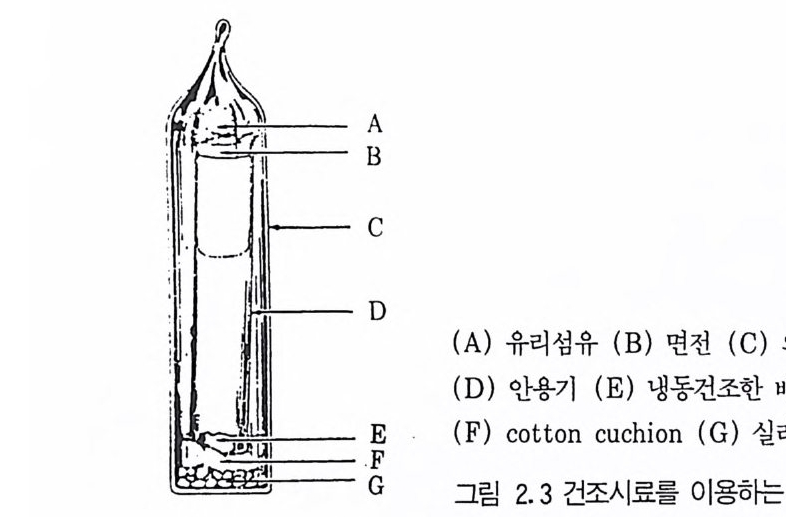
것 0] 다. 이와 같은 방법에 의해서 건조된 미생물은 산소, 습기, 그리고 빛에 노 출되지 않으면 오랜 기간 동안 보관할 수 있으며 필요할 경우 본래의 상 태로 되돌릴 수 있다. 동결건조법의 가장 간단한 장치는 미생물 현틱액을 얼릴 수 있는 동결기와 이것에 연결된 전공펌프로 구성되어 있다. 장치 : 동결건조 장치는 비교적 간단하고 건조기 -전공펌프 장치로부터 복잡한 상업용 동결전조기 (fr eeze -d r y er) 까지 다양하다. 그러나 일반적으 로는 고도진공펌프{hig h-vacuum pum p ), 냉각기 (condenser), 그리고 다 기관이나 용기로 구성된 간단한 구조로도 좋은 결과를 얻을 수 있다. 용기 : 용기의 크기와 모양은 매우 다양하지만 동결건조에 이용되는 용 기는 기본적으로 두 가지 형태이다. 미생물이 용기내에서 동결건조될 경우에는 이중용기가 적당한데(그림 2. 3) 이들 이중용기는 한겸용기에 비해서 다루기가 쉽고 오염될 가능성이 적으며 병원균을 보관하기에 더 안전하다. 이중용기의 경우 의부용기용으 로는 연질 그라스용기가 많이 이용된다. 이중용기를 만드는 방법은 다음과 같다.
의부용기 바닥에 실리카겔 조각을 깔고 그 위에 솜충을 만드는데 외부 용기를 사용하기 전에는 반드시 100 °c 에서 하룻밤을 두어야 한다. 실리카 겔은 열처리 후에 진한 푸른 색을 띠게 되는데 이 색은 미생물을 보관하 는 중에도 그대로 푸르게 유지되어야 한다.
 ABCDEFG
ABCDEFG
배양액 조제 : 동결전조에 이용되는 균주는 최적상태에서 활발히 증식하 는 미생물로서 ml 당 최소한 l08 세포가 될 때까지 배양시킨 뒤 대수증식기 후반에 수확하여 이용한다. 동결방지제 : 동결전조시킬 미생물은 동결방지제 (cryo p r o te c ti ve age - n t)가 들어 있는 배지에 현탁시킨 뒤 동결건조시킨다. Americ a n Ty pe Cultu r e Collec ti on 에서는 이중용기법 (double via l me t hod) 용으로는 20% 스킴 밀크 (sk i m mi lk ), 한겸용기법으로는 동량의 배양객으로 희석된 24% 설탕 (sucrose) 용액 (12% 설탕, 최종농도)을 사용 궁阿 생리적으로 다양한 미생물을 장기보존할 수 있다. 이 밖에 동결방지 제로는 10% 덱스트란 (de xt ran), horse serum, 이노시톨(i nos it o l) 등도 사용할 수 있다. 이중용기법의 조작은 디음과 같다. 20%(we/vol) 스킴 밀크 용액 (Difco 0032) 을 5rnl씩 분주한 뒤에
l16 °C 에서 2 어만간 떨균시킨다. 이때 밀크의 캐러멜化 (caramel ig a ti on) 가 일어날 수 있으므로 과열은 금물이다. 한천 위에서 자란 미생물의 경우에 는 20% 스킴 밀크 용액으로 무균상태에서 세척한 뒤 집균히여 이용하고 배양액에서는 무균상태로 원심분리한 뒤 침전물을 멸균된 스킴 밀크로 ml 당 10 6 세포 이상의 미생물 현탁액을 만든다. 각 용기당 0.2ml 의 미생물 현탁액을 넣은 뒤 솜마개를 하는데 미생물의 변화를 줄이기 위해서는 미생물 현탁액이 준비되는 대로 분주와 동결전조 과정 사이의 시간 간격을 최소화시켜야 한다. 한겸용기법의 경우에는 각각의 용기에 미생물 현틱액 0 .1 ml 를 넣은 뒤 용기 입구로부터 약 1.3c m 아래에까지 솜마개를 밀어넣고 위에 뒤어니온 솜털을 제거시키기 위해 불꽃.으로 태운다. 보존 (s t ora g e) : 동결전조된 미생물은 모두 5°C 이하에서 보관되어야 하며 상온보존은 꼭 피해야 한다. 그러나 —3 0~ _60°c 에서 이들이 보존 되면 더 오랜 기간 동안도 보존될 수 있다. 비록 동결전조법이 미생물의 장기보 존 법으로 많이 이용되고는 있지만 이들의 생존성여부는 동결건조 전 과 후에 꼭 확인하여야 한다. 또한 미생물의 보존기간을 알아보기 위해서 도 주기적으로 생존성 실험을 수행하여야 한다. 동결건조과정이나 보존과 정 중에 어떠한 변화가 일어났는지롤 알아보기 위해서는 특성판별법 실험 (characte r iz a ti on tes t) 또한 수행되어야 한다. (2) 초냉동보존법 (ultr a -f r ee zin g ) 동결전조법을 쓸 수 없는 미생물의 장기보존은 액체질소온도(― 196°c) 나 기체상태 ( -150°C )에서 얼린 상태로 보존할 수 있다. The Americ a n Ty pe Cultu r e Collec ti on 에서는 이 방법을 이용하여 많은 종류의 미생물 울 표현형의 특성이 변하지 않고도 15년 이상이나 보존하고 있다. 미생물의 장기보존은 또한 -70°C 를 유지하는 초저온 (ul t ra - low ter n- pe ratu r e) 냉동고를 이용하여 이루어질 수 있지만 정전이나 냉각기의 고 장이 일어나지 않도록 주의하여야 한다.
미생물의 장 기보 존 법에 액체 질소를 사 용하 는 것은 비 용 이 많이 들지 만 다루기가 매우 쉽고 생리적으로 매우 다양한 미생 물을 성공 적으로 보 존 할 수 있기 때문에 많이 사용되고 있다 (Heckl y, 197 8 ). 액화질소용기로는 보로실리케이트바이알 (boros il i ca t e-v i als) 과 이미 멸균처리가 되어 있는 폴리프로필렌튜선서떠y - p ro py lene tub es, 38m m x l2.5mm) 가 많기 이용되고 있다. 이들 용기들의 용량은 1. 2ml 이며 톱니 모양냉의동 방자지국제들 (이cr y있o p 어r o서t e c열 ti 기ve가 a g쉽e 다n .ts ) : 냉동방지제는 크게 두 종류로 나 누기전다. 즉 글리세롤(g l y cerol) 과 디메틸 술폭시드 (d i me t h y l sul- fox id e , DMSO) 같은 냉동방지제는 세포막을 쉽게 통과하여 세포 내부와 의부가 빙점 이하로 떨어지는 것을 방지하며 설탕, 유당, 포도당, 만니 톨 (mannit ol) , 소르비톨 (sorb it o l), 덱스트란 (dex t ran), 폴리비닐 피롤리 돈(p ol y v i n y l py rrol i don) 과 폴리 글리콜(p ol y g l y col) 과 같은 냉동방지 제들은 세포막 밖에서 냉동되는 것을 방지한다. 이들 중 전자의 냉동방지 제가 더욱 효과적이며 글리세롤과 DMS 아근 넓은 범위의 미생물에 다 사 용될 수 있으나 냉동방지제의 정확한 선택은 미생물 종에 따라 다르다. 새로운 종의 경우에는 냉동방지제가 유해한 영향을 미치는지를 알아보 기 위해서 내성시험 (tol erance t es t)을 행해야 하며 글리세롤과 DMSO 는 대개 10%(vol/vol) 와 5%(vo l/ vol) 의 농도로 적당한 배지에 가한 뒤 이용된다. 글리세롤은 고온고압살균법 (au t oclav i n g)으로 멸균할 수 있으며 DMS- 아 막 여과기 (membrane filt er) 로 멸균하여 5°C 에서 얼린 상태로 보존 한다 (DMS 아 l8°c 에서 언다). 배양객 준비 냉각원칙 : 미생물 배양액의 생리상태는 미생물의 액체질소 냉동시 생존에 중요한 요소로 작왕하는데, 일반적으로 대수증식기 후기의 활발히 증식하는 미생물을 이용한다. 미생물은 배양객의 경우 무균상태로 원심분리하여 수확한 뒤 펠릿 (pe l- le t)을 10% 글리세롤이나 5% DMSO 가 들어 있는 멸균된 배지에 접종
시킨다. 한천고체배양의 경우에는 냉동방지제가 들어 있는 멸균된 배양액을 이 용하여 한천 표면으로부터 미생물을 씻어내려 멸균된 용기에 ml 당 적어도 l08 세포를 포함하는 미생물 현탁액을 0 .4 ml 씩 분주한다. 병원균이 아닌 미생물의 경우에는 용기를 밀봉하기 전에 최소한 3 어손 이상 4°c 에서 미리 식힌 뒤 용기의 윗부분을 가열하여 습기를 제거시킨다. 이들은 산소가스 불꽃으로 용기의 윗부분을· 밀봉한 뒤 집게로 뜨거운 용 기를 시험관 꽂이에 울려놓고 차가운 물속에 집어넣는다. 용기가 차게 되 면 이들은 쉽게 얼 수 있는 상태가 된 것이다. 냉각속도 (cool i n g ra t e) 가 미생물의 생존에 중요한 요소로 작용하는데 일반적으로 느린 냉각속도 (1·c per m i n) 가 냉동보존법에 적당하다. 만일 프로그램이 가능한 냉동기 (pro g ra mmabe fr eezer) 가 없는 경우에 는 다음과 같은 방법에 의해서 냉각시킨다. 내용물이 들어 있는 용기를 스데인리스 스틸 (sta i n l es-s tee l) 냄비에 넣 고 이를 냉각기 ( —60° C ) 바닥에서 1 시간 동안 냉동시킨 뒤 이들을 액체질 소 속에 詩 E 동안 침수시킨다 이 방법을 이용하여 -60°C 까지 온도를 저 하시키는 속도는 대략 분당 1.5°C 이다. 얼린 미생물을 녹이기 위해서는 37°c 워터 배스 (wa t er ba t h) 에서 적 당히 흔들어준다. 그라스앰풀의 경우에는 이들을 녹이는 데 약 40~6 떠i 가 소요되며, 폴리프로필렌 바이알(p ol yp ro py lene v i als) 의 경우에는 약 60~12 陶} 소요된다. 이들이 다 녹으면 곧장 워터 배스에서 꺼내어 70% 에탄올로 소독한 뒤 뚜껑울 개봉하고 이들 미생물을 신선한 배지에 무균상태로옮긴다. 춥卜고문헌 Drew, S. W. and A. L. Dema in, 1977, Ef fec t of pri m ary meta b oli tes
on secondary meta b olis m , Ann. Rev. Mi cr obia l , 31 : 343~356. Fleck, W. and D. Str a uss, 1975, Leukaemomy c in , an anti bi o t ic wit h ant- itum or acti vit y , vol. 1, Screenin g , fer menta t i on , and bio l og ica l ac- tivi t y, Z. Alig. Mi kr obio l , 15:495~503. Heckly, R. J., 1978, Preservati on of Mi cr oorga n is m s. Adv, in Ap pl. Mi cr obia l ., 24 : 1~53. Lancin i , C., 1980, Screenin g for new anti bi o t i cs , Lectu r e, Int. School of General Geneti cs :Mi cr obia l Breedin g Il , Ju ne 3~13, 1980, Eri- ce/It aly . Lin c oln, R. E., 1960, Contr o l of sto c k cultu r e pre servati on and in- oculum in bacte r ia l fer menta t i on , J. Bio c hem, Mi cro bio l . Tech. En g. 2 : 481 ~ 500. Nis b et, L. J., 1982, Current _str a te g i es in the search for bio a cti ve micr obia l meta b olit es , Jo ur. chem 'Jec h. Bio t e c hnol. 32 : 251~270. Omura, S., H. Tanaka, R. Oiw a, T. Naga i , Y. Koy an a and Y. Tak- ahashi , 1979, Stu d ie s on bacte r ia l cell wall inh ib i to r s, vol. 11, Scr- een ing meth o d for the spe ci fic inh ibi t ors of pe pt ido g ly c an syn - the sis , J. Anti bi o t ic s, 32 ; 978~984. Perlman, D. et al, 1977, Cultu r e main t e n ance, Annual Rep o rts on Fer- ment, Process, 1, 41~48 Acad, Press, New York. Prid h am, T. G, 1933, Vi ab il ity of acti no my ce te s sto red in soil , App l. Mi cr obia l , 26 : 441~442. Zahner, H., 1979., What are secondary meta b oli tes? Folia Mi cr obio l , 24 : 435~443.
제 3 장 산업균주의 개량 1 서론 자연에서 분리한 균주는 식품공업에 사용되는 소수의 균주를 제의하고 는 산업적으로 유용한 산물을 저농도로 생산하므로 생산성을 증가시키기 위한 노력을 기울이게 된다. 수율증가는 배지와 배양조건 등을 최적화함으 로써 일부가 달성될 수 있으나 미생물이 생산물을 합성하는 능력에는 한 계가 있다. 따라서 미생물의 잠재적 (po te n ti al) 생산성을 조절하는 게놈 (g enome) 을 변화시킴으로써 잠재적 수율을 증가시켜야만 한다. 또한 변화 된 미생물의 증식요구성을 관찰하여 증가된 참재성을 충분히 발휘할 수 있는 조건을 제공해야 하고 니아가 균주개량을 위해 계속적인 유전적 변 화를 시도함으로써 균주의 증식요구성의 재평가가 수반되어야 한다. 유전 적 변희를 위해서는 (기) 자연변종의 선별, (L) 유도된 돌연변이주의 선 별, (디 재조합균주의 선별 등에 의해 이루어질 수 있다. 세포분열 때마. 다 일어날 수 있는 유전적 변화의 확률은 매우 낮으며, 그러한 분열이 수 없이 되풀이될 때 점차 이질성을 띠게 되는 것은 당연한 것이다. 미생물이 나타내는 이질성 (he t ero g ene ity)은 수율의 격감이라는 십각한 결과를 야 기시킬 수 있는데 이는 대개 변종들이 원래의 균주에 비해 생산성이 낮아 지기 때문이다. 그러나 새로운 산물의 개발 초기 단계에서 종종 관찰되는 변종들 중에는 생산성이 우수한 것들이 분리되기도 한다• 이러한 현상을
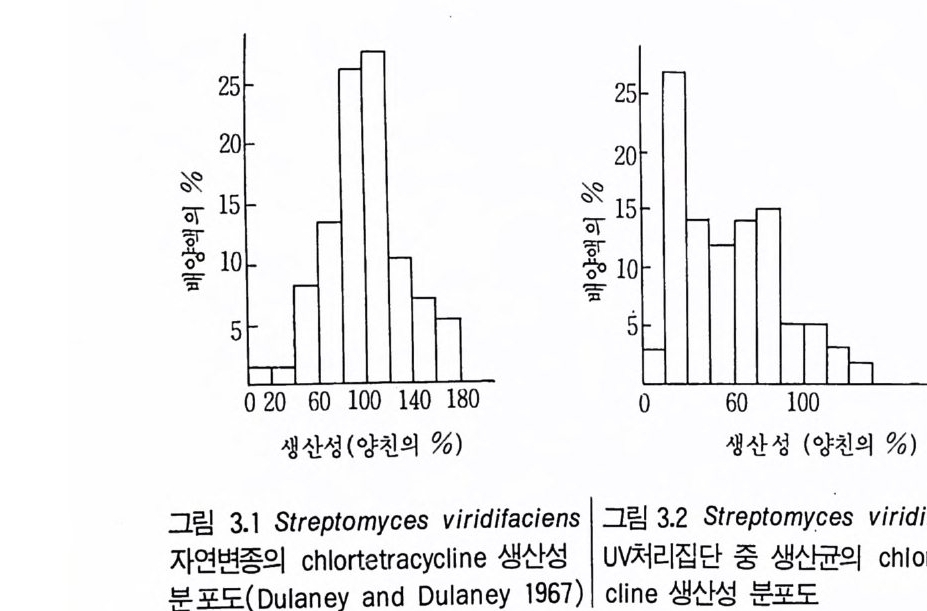
나타내는 것들은 균사체 형성균으로서 이형핵세포 (he t erokar y ons) 를 지 니는 분리균주 또는 단핵포자를 선별함으로써 우수한 생산자인 동형핵세포 (homokar y ons) 를 만동거내는 경우를 말한다. 그러나 이 현상은 동형핵세 포를 지니지 않는 단세포성 분리균주에서도 관찰되고 있다. 따라서 생산균 주를 주기적으로 도말하여 자손균주의 생산성에 대한 조사를 하는 것이 좋다. 이러한 과정은 관련 연구자가 높은 생산성과 연관된 형태적 특징들 에 익숙해질 수 있다는 이점을 가진다. 자연변종이 수율증가를 가져오기도 하지만 그러한 개량방법에 의존할 수만은 없으며 미생물개량의 기회를 증가시킬 수 있는 기술이 구사되어야 한다. Dulane y와 Dulane y (1967) 는 Str ep t om y ce s v i r i d if ac i en 회 자연변 종과 이를 자의선 처리한 후의 생존개체에서의 chlorte r racyc l in e 생산성 분포를 비교하였다. 그림 3 .1과 3.2 에서 알 수 있는 바와 같이 자의선 처 리가 된 생존개체의 대부분은 저급 생산자이지만 몇 균주들은 모균의 두 배 이상을 생산함을 알 수 있다.
 25201510 25201510
25201510 25201510
돌연변이 유발물질의 작용양상에 대해서는 Sermonti (1 969), Elander 와 Esp en shade(1976) 등이 언급한 바 있다. 유도된 돌연변이의 대다수가 원하는 산물의 수율에 미치지 못하지만 그림 3.2 에서 나타났듯이 소수의 변이주가 모균보다 높은 생산성을 보여주고 있다. 위와 같이 균주개발 계획에 의해서 10 個 l 이상의 수율증가를 달성시킬 수도 있다. 예를 들어 효소류와 같이 몇몇 유전자의 활성을 높임으로써 관 계되는 생산물의 수율을 증가시킬 수가 있으나 복집하고 고도로 조절된 생합성과정의 결과로 생기는 이차대사산물에서는 게놈에 다양한 변화가 있 을 때 비로소 높은 생산성 균주를 육종할 수 있게 되는 것이다. 또한 경비 효율적 공정을 위해서는 경우에 따라 발효시간이 짧은 균주, 불필요한 색 소를 생산하지 않는 균주, 산소요구량이 많지 않는 균주, 발효과정에 거품 을 많이 발생하지 않는 균주, 혹은 저렴한 기질을 대사할 수 있는 요건을 갖춘 균주 등을 분리하는 것도 바람직하다. 균주개량을 위한 가장 중요한 접근방법 중 하나가 재조합 DNA 기술을 구사함으로써 가능하다. 여러 생 물체의 유전자를 하나의 생물체로 모으면 생산량 증가뿐만 아니라 전혀 새로운 물질을 생산하게 될 가능성도 있다. 그러나 현존하는 공정의 개량에 더욱 새로운 유전적 기술을 적용함에 있어서 하나의 난점은 산업에서 널리 사용되는 균주들이 불행히도 충분한 양의 기본 유전정보가 알려진 생물체들이 아니러는 점이다. 기초연구와 산 업적 응용 사이에는 명백한 차이가 있다. 산업적으로 중요한 미생물의 유 전적 기본이 되는 생합성과 대사조절이 현재 쓰이고 있는 경험적인 방법 의 조합이 새로운 방법으로 교체되기 전에 먼저 이해되어야 한다. 몇 개의 산업회사들에 의해서 지난 1~ 킨간 기초지식과 산업적 응용 사이의 간격을 연결시키기 위한 노력들이 강구되어왔고 그 결과 균주개량사업의 효율성에 있어서 현저한 증가를 기대할 수 있게 되었다. 이 장에서 우리는 균주개량을 위한 기본적인 유전적 접근방법을 제시하 고 또한 이러한 접근방법들이 실제 어떻게 사용되는지를 알아보기로 한다.
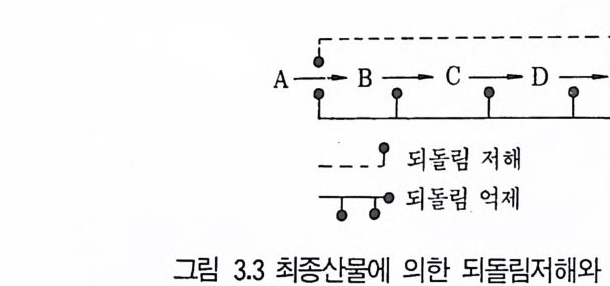
2 일차대사산물을 생성하는 유도 돌연변이주의 선별 일차대사산물을 축적하는 돌연변이주의 선별방법의 고찰에 앞서서 그들 의 생합성 조절 기작을 정확히 파악할 필요가 있다. 미생물에서 일차대사 산물의 수준은 되돌림조절계 (fee dback contr o l s y s t em) 에 의해 조절되 어전다. 여기에 포함되는 주요 조정방법으로는 되돌림저해 (fee dback inh i- b iti on) 와 되돌립억제 (fee dback re p ress i on) 가 있다. 되돌림저해는 생화 학 경로의 최종산물이 그 경로의 반응 중 하나(대개는 첫번째 반응)를 촉 매하는 효소활성을 저해하는 것으로 그 효소의 디른 자리 입체성 부위 (alloste r ic s it e) 에 최종산물이 결합함으로써 기질에 대한 효쇼호의 부칙을
 ‘?,- ---?- -----f ----f- -71
‘?,- ---?- -----f ----f- -71
방해하게 된다. 되돌림억제 (fee dback re p ress i on) 는 생화학 경로의 최종 산물(또는 최종산물의 파생물질 )이 그 경로의 한 반응(또는 몇 개의 반응 둘)을 촉매하는 효소(또는 효소들)의 합성을 막는 것으로서 최종산물의 파생물질이 게놈과 결합하여 전사과정을 저해하는 등의 유전자 수준에서의 조절을 말한다. 따라서 이 과정에서는 효소의 합성 자체가 억제되어전다. 되돌림억제와 저해는 생합성 경로의 조절에 협조적으로 작용하는대 저 해(in hi b iti on) 는 최종산물의 생합성을 차단하는 신속한 조절방법으로써, 억제 (re p ress i on) 는 과량의 효소가 생성되는 것을 차단하는 기작으로써 작용하게 된다. 분지하지 않은 경로 (unbranched p a t hwa y)의 조절은 대 개 최종산물의 저해작용에 민감한 과정에 있는 첫번째 효소와, 최종산물의 억제작용에 민감한 모든 효소의 합성여부에 의해 이루어전다(그립 3.3).
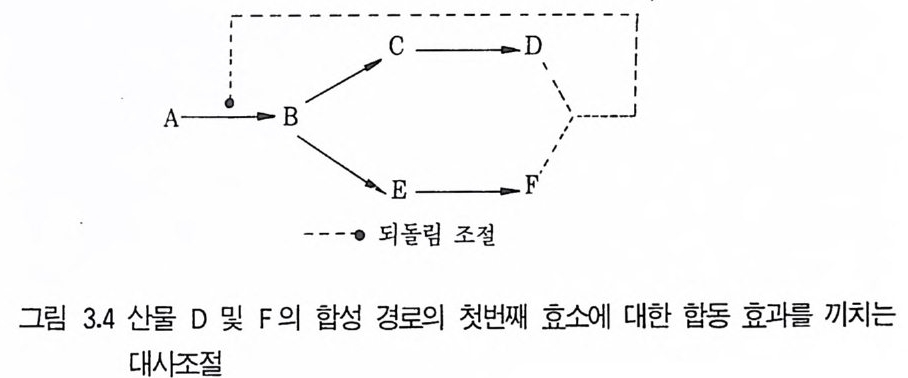
분지된 생합성 경로 (branched p a t hwa y)의 조절은 조금 더 복잡하다. 분지된 생합성 경로의 동일한 최종산물은 미생물에 있어서 거의 필요치 않은 물질이므로 하나의 최종산물이 생합성 경로의 일부를 제어함으로써 둘 이상의 최종산물에 영향을 끼치게 되고, 따라서 미생물은 제어에 참여 하지 않은 산물들의 손실로 대사과정에 어려움을 겪게 된다. 그러므로 분 지된 경로의 최종산물의 수준에 의해 세포에 필수적인 중간체의 손실이 일어나지 않도록 제어되는 기작들이 존재하고 있다. 이하의 기작들은 제어 의 효과에 기준을 둔 것으로 제어, 억제 또는 이들의 합동작용에 의해 이 루어전다. 합동 또는 다중 되돌림저해 (concerte d or multi va lent fee dback in- hib i t ion ) : 이 제어방법은 하나 이상의 최종산물에 의해 이루어지며, 이 경로의 첫번째 효소는 모든 최종산물이 과량으로 존재할 때만 억제되거나 저해된다(그림 3.4 ).
 lI --_---/--c-- -一----\---- ---,
lI --_---/--c-- -一----\---- ---,
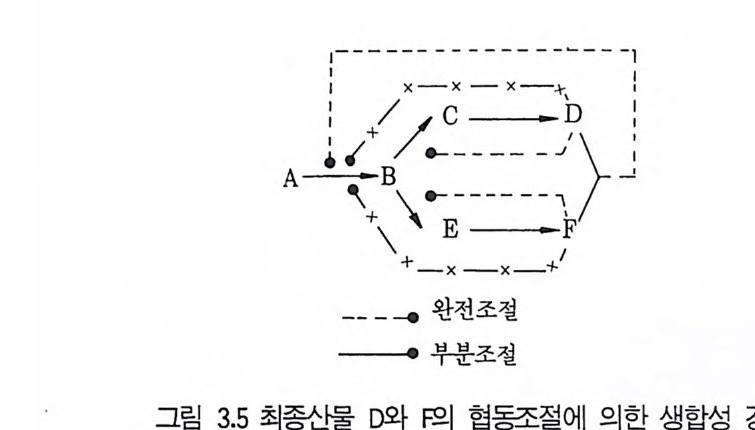
협동 되돌림조절 (co -0p era ti ve fee dback contr o l) : 이 방법은 각각의 최종산물이 독립적으로 서로 영향을 끼치는 약한 제어를 받는다는 점 의 에는 다중조절효소의 제어 (합동제어 )와 유사하다. 모든 최종산물이 과량으 로 있을 때 상승적 (sy n ergi st i c) 억제 또는 저해롤 받게 된다. 그림 3.5<> 1] 도식화되어 있는 이 방법은 하나의 산물이 과량으로 존재할 때 그 산물에 대한 분지점(괴정상의) 이후도 즉시 제어되는 효율적인 제어인 것으로 보
여전다. 따라서 최종산물 중의 하나의 저해작용에 의해 감소된 중간체의 흐름은 여전히 요구되고 있는 산물로 전환된다.
 도/,-:- - :--x_-— -\x- -—\ - -\x -_ -〈_-+ — 1 〉- - -」1!
도/,-:- - :--x_-— -\x- -—\ - -\x -_ -〈_-+ — 1 〉- - -」1!
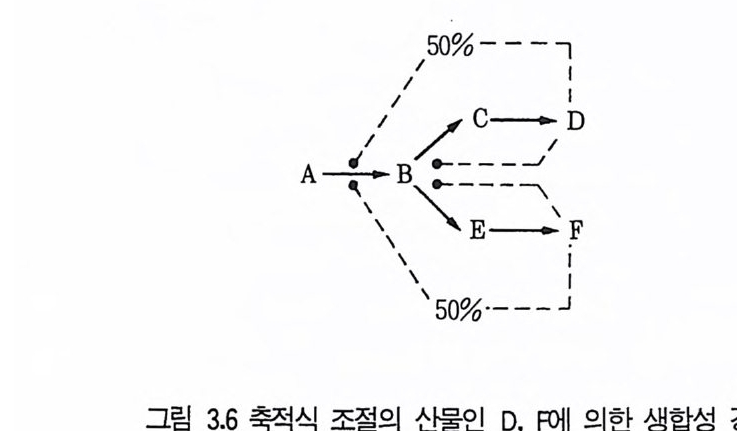
축적식 되돌림조절 (cumula ti ve fee dback cont ro l) : 합성 경로상의 최 종沮 ~1 각기 독립적으로 어떤 백분율로써 첫번째 효소를 저해한다. 그립 3.6 에서 D 와 F7} 독립적으로 50% 씩 첫번째 효소의 활성을 감소시킴으로 써 두 개의 산물 (D, F) 이 과량으로 있을 때 전체적으로 저해된다. 협동 되돌림조철에서처럼 각각의 최종산물은 공동 중간체인 E 가 분지한 후에 즉시 조절되어야 하며 이 합성 경로에서 방향을 전환하게 된다.
 50%--- 7
50%--- 7
순차적 되돌림조절 (se q uen ti al fee dback contr o l) : 합성 경로상의 최 종산물은 각기 생성물에 대한 분지점 이후에 즉시 효소를 제어한다. 그립 3.7 에서 D 는 B 가 C 로 전환되는 것을 저해하고 F 는 B 가 E 로 전환되는 것을 저해한다. D, F 또는 두 물질의 저해작용은 E 긱 축적을 야기하고 결국은 A7} B 로 전환되는 것을 저해하게 된다.
 , _______ 7
, _______ 7
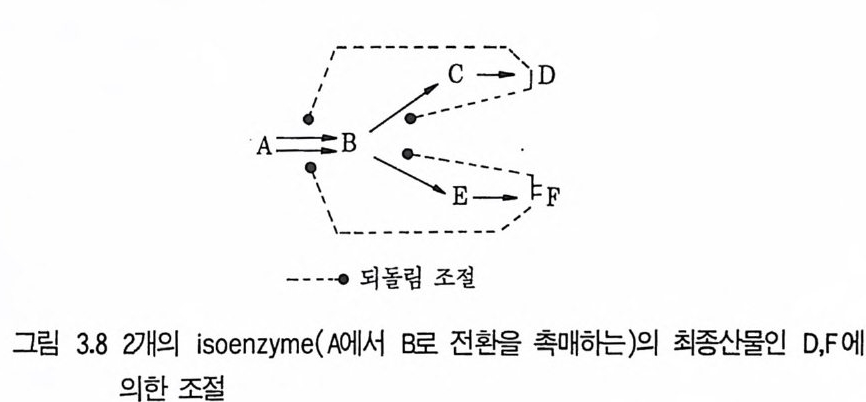
동위효소조절 (iso enzym e contr o l) : 동위효소란 같은 반응을 촉매하지 만 조절특성이 다른 효소를 말한다. 어떤 경로의 중요한 조절반왕기 하나 이상의 동위효소에 의해 촉매된다고 할 때 다른 동위효소들은 다른 최종 산물에 의해 제어될 것이다. 이러한 조절방법은 매우 효율적인 것으로 분 지점 이후에 즉시 조절되므로 감소된 중간체의 흐름은 과량의 산물로부터 전환되어전다(그림 3.8).
 I ____ -------\
I ____ -------\
미생물의 대사물질의 수준은 위에서 설명한 다양한 기작들에 의해서 조 절되고 있기 때문에 최종산물들은 증식에 요구되는 양 이상으로 합성되지 않는다. 그러나 이상적인 산업미생물은 증석에 요구되는 양보다 훨씬 많은 산물을 생산하여야 하므로 대사산물의 생성과정에서의 조절기작을 이해함 으로써 이 기작에 의해 생성이 제한되지 않도록 가장 유용한 산업미생물 의 청사전 (blue p r i n t)을 작성할 수 있게 되는 것이다. 여기서 요구되는 돌연변이주는 아래 세 가지 방법으로 변화시켜야 한다. 1. 세포막의 두과성을 변화시킴으로써 주효소 (ke y enz y mes) 를 조절하는 최 종入士물이 세포로부터 방출되도록 미생물을 변화시킨다. 2. 합성 경로상의 주효소 (ke y enz y mes) 를 조절하는 최종산물을 생산하지 못하도록 미생물을 변화시킨다. 3. 정상적인 조절대사산물이 저해나 억제기작을 나타낼 수 있는 수준으로 존 재해도 세포가 이를 인식하지 못하도록 미생물을- 변화시킨다. 2.1 두과성의 변화 (Mod ifi ca ti on of the per meabil it y ) 미생물의 두과성을 변화시킨 가장 좋은 예가 바이오딘 (b i o ti n) 요구주 이고 (K i ~osh it a et al., 1957a) Cory n ebacte r iu m g lu t am i cum 에 의한 글 루탐산(g lu t ama t e) 발효이다. 여기서 미생물의 투과성은 바이오틴의 양에 의해 변화를 일으킨다. 발효배지내 바이오틴의 수준을 5µg • dm- 3 이하로 공급하면 이 미생물은 글루탐산을 생성하나, 증식 최적농도의 바이오틴을 공급하면 낙산을 생성한다 (K i nosh it a and Nakay a ma, 1978). 결국 C. glu ta m i cu ~ 두과성은 배지의 조성에 의하여 조절되나 여기서 말하는 개 념의 균주개량의 예라고는 할 수 없다. 글루탐산 생산에서 투과성의 역할 에 대한 증명은 생산성을 높이기 위해 두과성의 유전적 변형이 가능함을 보여주었다. 따라서 이 단계에서는 바이오틴 제한 조건에 있어서의 글루탐 산 생산의 생리고찰과 관련된다.
바이오틴제한 조건하의 세포가 글루탐산에 대해 두과성이 증가되는 것 은 세포벽의 지방산과 인지질의 함량이 변화하는 것과 일치한다. 두과성을 조절하는 결정적 요인은 인지질이 결핍된 막의 합성으로 보여진다 (Nakao et al., 1973). 글루탐산발효에서 바이오틴의 역할은 배지내에 바이오틴의 제한된 수준 을 요구한다. 그래서 사탕수수 당밀을 탄소원으로 이용하고 바이오틴을 첨 가시키면 바이오틴 제한 이의의 수단에 의해 두과성의 변화에 의하여 극 복되어왔던 난점들이 드러나게 된다. 바이오틴JJ-화 배지를 사용한 대수증 식 기 동안 pol yo x y et h y le ne sorlit an mono-o le ate Tween 8~ 같은 페 니실린 또는 지방산 유도체를 포함시키면 세포의막의 투과성이 변화하게 되고 글루탐산을 방출하게 된다 (Uda g awa et al., 1962). 탄소원으로서 탄화수소를 이용한 글루탐산의 생성 또한 투과성의 조절 에서 난점을 나타낸다. 탄화수소의 이화과정에서는 바이오딘 제어 부위를 효율적으로 우회하여 지방산(fatty ac i d) 을 생성하게 된다 (Nakao 등, 1972). 생산균주의 투과성은 페니실린의 첨가에 의해 제어될 수 있으나 (Wang 등, 1979) 위 문제에 대한유전적 해결방법도 발견되었다. Nakao 등은(1 970) 인지질(p hos p hol ipi d) 합성이 글리세롤공급에 의해 제어되는 Cory n ebacte ri u m alkanol yti u 짜기 글리세롤요구, 영양요구성 돌연변이를 분 리하였다. 이 돌연변이는 0.01% 의 글리세롤 존재하에 n 파리핀에서 배양 하자 약 40g • dm - 3 의 글루탐산을 생산하였다 (Nakao 등, 1972). 따라서 글루탐산발효에서 바이오딘 제한시의 작용양상을 이해함으로써 생산균주의 정상적인 조절기작을 극복하는 방법으로 투과성의 유전적 변화를 이용할 수가있게 된다. 2.2 되돌림저해물질(fe edback inh ibi t or ) 또는 억제물질 (re p ressor) 을 생성하지 않는 돌연변이주의 분리 되돌립저해물질이나 여제물질을 생성하지 않는 돌연변이주는 합성 경로
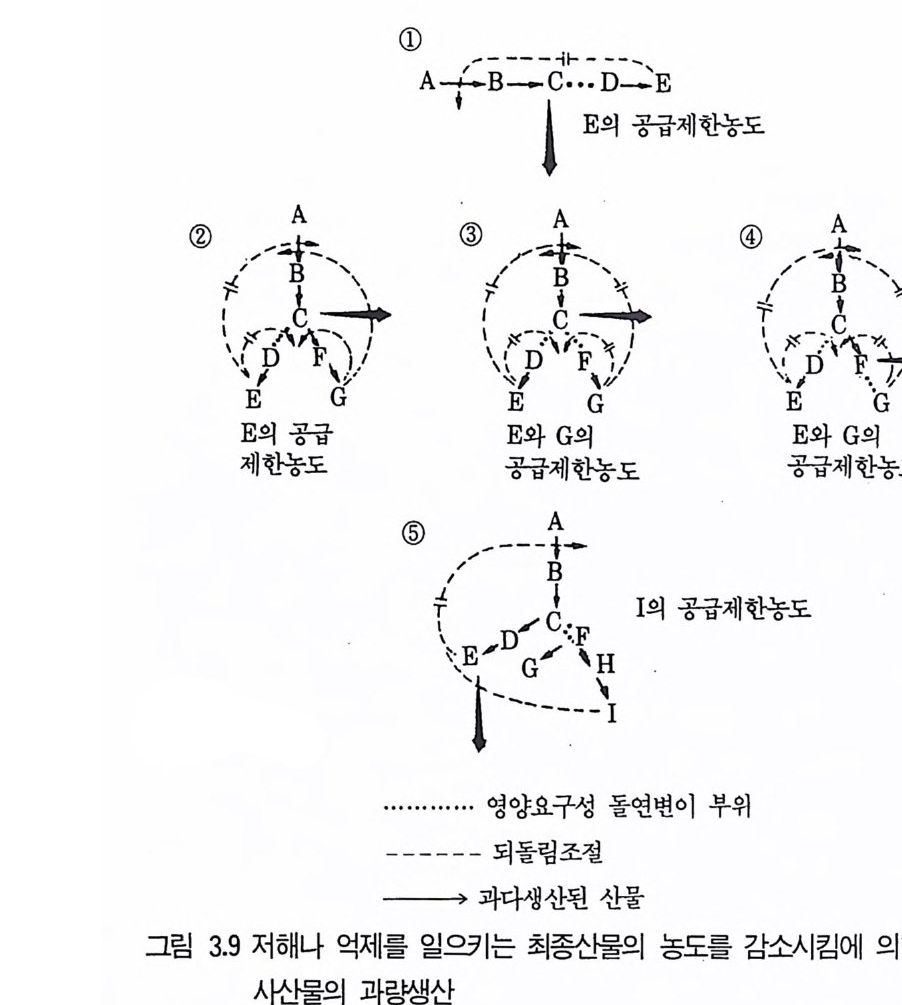
상의 중간물질 생산에 유용하게 사용된다. Dema i n(1972) 은 중간물질을 생산하는 가설적인 돌연변아주의 몇몇 청사전과 이들이 생합성 경로에서 口占들어내는 최종산물(그림 3. 9oJ]서 설명되고 있는 바와 같이 )을 제시하였 다.
 ®A 수' B-Cl· ·E• 의D -뜹E제 호冷도
®A 수' B-Cl· ·E• 의D -뜹E제 호冷도
위의 그림에서 제시된 돌연변이주들은 해당 경로상의 어떤 억제 또는 저해물질을 생성하지 못하므로 조철이 편중되게 일어난다. 그러나 조절요
소들은 증식에도 필수적 이 므로 증식은 허용하지만 정상적인 조절반응은 일 으킬 수 없을 만큼의 농도로 배지내에 첨가시켜야만 한다. 그립 3.9(1) 은 분지하지 않은 경로 (unbranched p a t hwa y)에서 경로상 의 첫번째 효소가 최종산물 E 에 의해 되돌림억제 또는 저해를 받는 제어 기작을 나타낸다. 그러나 이러한 경우의 미생물은 C 를 D 로 전환시키지 못하므로 E 에 대한 영양요구성을 나타낼 것이고 이때 만일 배지내에 증식 울 유지할 수는 있으나 억제나 저해를 일으키기에는 불충분한 양의 E 를 포함하고 있다면 이 대사조절은 C 가 축적되는 방향으로- 치우칠 것이다. 그림 3 .9(2) 는 분지된 경로 (branched p a t hwa y)에서 경로상의 첫번째 효소가 E 와 G 의 합동효과에 의해 합동저해 (concerte d i n hi b iti on) 를 받 는 제어기작이다. 이 돌연변이주는 C 를 D 로 전환시키지 못하므로 E 에 대 한 영양요구성을 나타내게 되고 결국은 첫번째 효소에 대한 합동조절을 할 수 없게 된다. 만일 여기에도 증식은 가능하나 저해를 나타내기는 불충 분한 양의 E 를 배지내 첨가시키면 C 가 F로 전환될 때 최종산물 G 의 저 해조절에 의해서 C 가 축적될 것이다. 그림 3.9(3) 에 나타난 예도 그림 {. 9(2) 와 유사한 것으로 차이는 이중 영양요구주이며 E 가 G 모두를 공급해 야 한다는 점이다. 그림 3.9(4) 도 F 와 G 사이에서 발생하여 G 의 생성을 차단하는 또 하나의 이중 돌연변이를 보여주고 있으며 결과적으로 F7} 축 적될 것이다. 그림 3.9(5) 는 경로상의 첫번째 효소가 E 가 I 의 합동효과에 의해 되돌 립저해(fe edback i nh i b iti on) 로 조절되는 분지된 경로를 나타내며 결과적 으로 하나의 최종산물이 축적됨을 알 수 있다. 이 돌연변이주는 C 를 F로 전환시키지 못함으로 해서 I 와 G 새 대한 영양요구성을 나타내므로 증식에 필요한 최소량을 배지내 첨가시키면 최종산물 E 가 축적될 것이다. 위에서 고찰한 가설적인 예들은 모두 영양요구성 돌연변이주들로 적당 한 환경하에서 최종샨풍기나 중간물질을 비교적 고농도로 축적하게 된다. 따라서 영양요구성 변이주를 선별하는 것은 생산성이 높은 균주의 선별이 라고 할 수 있으며 그림 3.9(1) 과 (2) 의 C 나 D 사이처럼 정확한 위치에
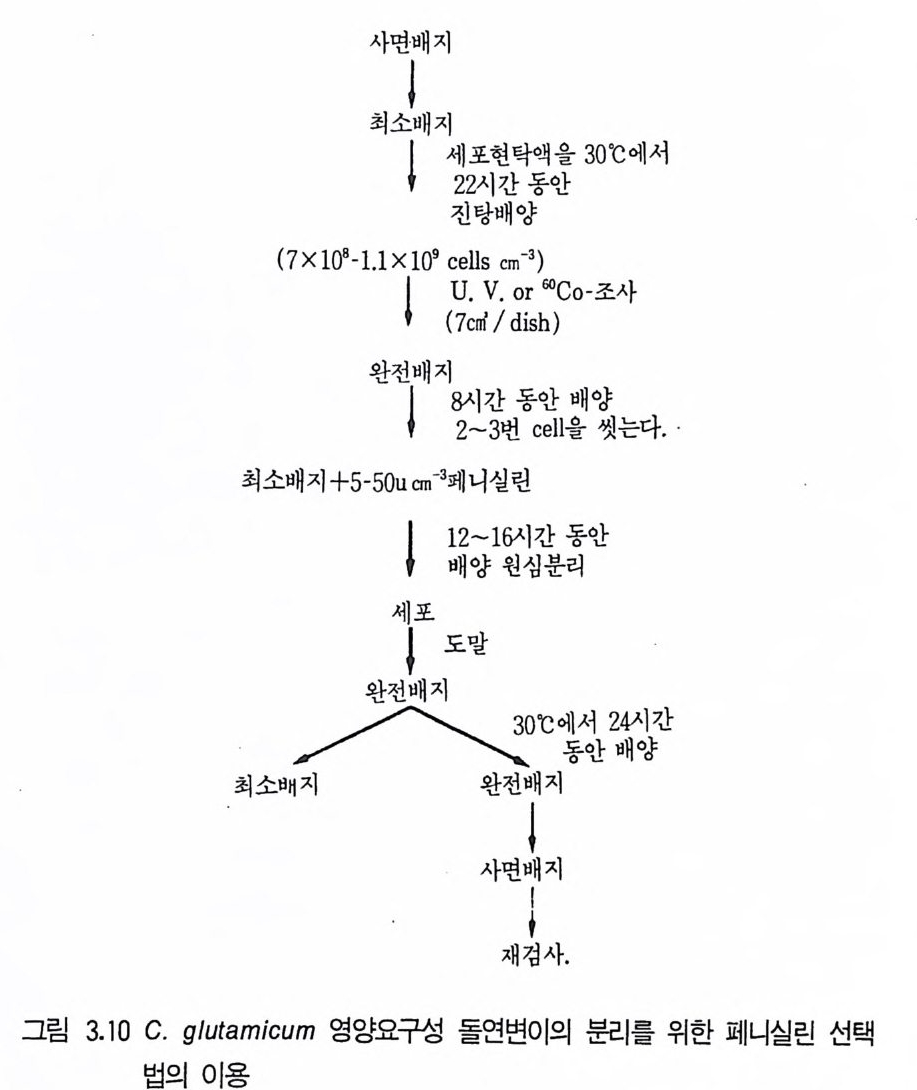
영양요구성에 대한 변이가 일어나야 한다. 영양요구주를 얻는 일은 높은 생산성을 지닌 균주를 찾는 것보다 좀더 간단한 작업이므로, 가장 좋은 접 근방법은 돌연변이 유발 후 생존개체로부터 적당한 영양요구-주를 선별하고 이어서 선별된 영양요구주의 생산성을 탐색하는 과정을 계획하는 것이다. 영양요구성 돌연변이주의 분리 : 영양요구성 변이의 획득에 가장 일반적 으로 이용되는 방법은 어떤 형태의 집적배양의 이용 또는 시각적으로 변 이주를 선별하는 기술이다. 죽 항생물질로서 야생주를 감소시켜 영양요구 성 변이주를 농축하는 방법이다. 집적배양 (enr i chmen t) 과정의 선택은 원영양성 세포에는 부가적인 효과를 나타내지만 영양요구주에는 무해한 조 건을 부여하는 원리를 기초로 한다. 그러한 조전들은 영양요구주만을 생존 하게 하는 항생물질에 노출시킴으로써 얻어질 수 있다. 이때는 최소배지 (mini m al med i um) 를 이용해야 한다. 저해물질로서 페니실린을 이용한 집적배양 (enr i chmen t) 기술이 Davis (1 949) 에 의해 개발되었다. 돌연변이 유발처리 후 생존세포를 완전배지 에서 일단 배양하고 원심분리하여 회수하고, 세척, 페니실린을 포함한 최 소배지내에 재현탁시킨다. 이때 증식하는 원영양성 세포들만이 페니실린에 민감하므로 증식하지 않는 영양요구주는 살아남게 된다. 이 세포들을 원심 분리하여 회수하고 페니실린 제거를 위해 세척한 후 영양요구주의 증식이 가능한 영양배지에 재현탁한다. 영양요구주는 고체배지상에서 순수하게 분 리할 수 있다. 분리된 영향요구주의 성질은 이른바 완전배지라고 불리는 배지를 고안함으로써 결정할 수 있다. 죽 만약 최소배지에 요구물질을 첨 가한다면 결과적으로 첨가물질에 대한 영양요구성인 변이주를 분리할 수 있는 그러한 배지성분을 의미한다. 글루탐산 생산균주인 C. g lu t am i cum 의 영양요구성 돌연변이를 분리한 과정은 그립 3 .1며 도식화되어 있다. 포자생성균의 경우 포자 자체는 어떤 화합물에 대해 내성을 지니므로 최소배지상에서 변이가 유발된 포지를 배양하면 원영양주만이 발아하게 되 고 이어서 적당한 화합물로 포자액을 처리하면 포자상태로 남아 있는 영
양요구주를 제외한 것들은 사멸하게 된다. 이를 다시 완전배지에 전이시켜 (저해제 등을 세척하여 제거한 후) 영양요구성 포자를 분리하게 된다. Gan j u 와 l y en gar (1 968) 는 Penic i ll i u m chry so g en um, Str ep t om y ce s aur- eofa c ie n s, S. oliv a ceus9 .} Bacil lu s sub ti l 려 포터 대히여 sodiu m pen - t achloro p hena t邊 사용하는 이러한 형태의 기술을 개발하였다.
 사최면소ll배배 지지세 22포 시현간탁동액안을 30 'c에서
사최면소ll배배 지지세 22포 시현간탁동액안을 30 'c에서
사상균의 영양요구성과 원영양성 포자의 기계적 분리에는 〈여과 집적 배양법 (filt r a ti on enric h ment me t hod) 〉이 도입되었다 (Ca t ches i de, 19 54). 액상의 최소배지에 변이가 유발된 포자를 접종하고 수시간 동안 진당 배양하면 영양요구주를 제의한 원영양주들이 발아하게 된다. 이 배양액을 . 적당한 sin t er ed gla ss 여과기로 여과하면 발아한 포자들은· 남아 있게 되 고 걷러진 액에는 영양요구성 포지들이 존재하게 된다. 영양요구주의 시각적 선별은 대상집락 (colon y)을 완전배지와 최소배지 상에 상호 노출시킴으로써 가능하다. 완전배지상에서는 출현하지만 최소배 지에서는 출현하지 않는 집락은 영양요구성이라 할 수 있다. 위의 선별은
었으나 이런 돌 연변이 주는 독립적으로 자신의 합성을 조절 하는 산물을 얻 는 데는 적합하지 못하다. 그림 3 .1 1 에 제시한 가설적인 예를 보면 최종산 물 D 는 이 경로의 첫번째 효소에 대해 되돌림저해 (fee dback inh ib i t ion ) 를 함으로써 스스로 지신의 합성을 조절하게 된다.
 ;--- ---------- -- --- -- --------- -- ------ -- - --- - --- -- ----,
;--- ---------- -- --- -- --------- -- ------ -- - --- - --- -- ----,
중간산물 F를 다량 생산하고자 하는 경우에는 P 에 대해 영양요구성 (Auxo t ro ph i c 인) 돌연변이를 분리해 F 에서 P7} 만들어지는 단계를 차단 해야 한다. 그러나 P 를 다량 생산하고자 할 때는 영양요구성 돌연변이주 를 만드는 것은 무의미하며 이때는 P7} 첫번째 효소를 저해하는 수준으로 존재해도 이를 감지하지 못하도록 미생물을 변화시켜야 한다. 조절요소들 을 감지하지 못하는 그러한 변화된 돌연변이주는 원칙적으로 다음 두 가 지 기술에 의해 얻어지게 된다. 1. 유사물질 (analo g ue) 에 내성을 지닌 돌연변이주의 분리. 2. 복귀돌연변이주 (rever t an t)의 분리. 유사물질이란 어떤 화합물에 대해 구조상 매우 유사한 화합물을 말한다. 아미노산과 누클레오티드의 유사물질은 여러 가지 기작으로 인해 흔히 독 성을 나타낸다. 유사물질을 거대분자의 생합성 과정에 이용하여 세포구성 성분이 결핍되도록 할 수 있다. 어떤 조건에서 유사물질은 자연산물 대신 도입시키는 것이 아니라 그의 조절 특성을 모방하여 생합성을 방해한다. 예를 들어 그림 3 .1 1 에 제시한 경로에서 생산물 P는 첫번째 효소에 대해 되돌림저해롤 하고 있다. 만약(생합성 경로상에서 F를 대치할 수는 없으
나) P 의 유사물질인 P*7 } p와 동일한 방법으로 첫 번째 효소 를 저 해한다 면 P 예 의해 P 의 생합성이 저해되고, 따라서 이 균 주 의 증식이 억제되는 결과를 야기한다. 그 유샤물질의 독성효과에 대해 내성을 지닌 돌 연변이주를 분리할 수 있으며, 유사물질이 독성을 나타내는 부위가 자연산물의 조절특성을 모방 하는 경우라면 그 돌연변이주는 유사물질과 구조가 유사한 특정 화합물을 과잉 생산하게 될 것이다. P*7 } p의 조절기능을 모방함으로써 독성을 나 타내는 P의 생합성 예를 재검토해보면 유사물질에 의해 . 첫번째 효소가 더 이상 저해되지 않으므로 P* 존재하에서도 증식할 수 있는 돌연변이가 분 리될 수 있다. 내성돌연변이주의 변형된 효소는 유사물질에 의한 저해에만 저항성이 있는 것이 아니라 P의 조절효과에 대해서도 내성을 나타내므로 결국 P의 생성을 저해하지 않게 된다. 만약 이 조절계 (con t rol sy st e m ) 가 효소합성을 억제하는 경우리면 내성돌연변이주는 유사물질의 존재를 인 식하지 않는 효소합성 장치를 갖도록 변화될 것이다. 그러나 돌연변이주의 내성부위는 조절계의 변화에 의한 것이 아니다. 예를 들어 유사물질을 분 해할 수 있는 돌연변이주는 최종산물을 과량 합성하지 못한다. 따라서 유 사물질 내성돌연변이주는 유사물질이 갖는 아래와 같은 유사성에 대응해서 최종산물을 과잉 생성할 것으로 기대할 수 있다. 1. 유사물질이 독성을 나타내는 것은 자연산물의 조절특성을 모방하기 때문 0l 다. 2. 내성돌연변이주의 내성부위는 최종산물에 의한 조절부위이다. 내성돌연변이의 분리는 변이처리 후의 생존개체를 적당한 농도의 유사 물질에 노출시키고 출현한 집락 (colon y)을 분리함으로써 이루어진다. Ser- mon ti (1969) 는 유사물질의 적당한 농도를 결정하는 방법을 언급한 바 있 다. 독성을 나탸개는 유사물질이 다양한 농도로 함유된 디수의 고체편평배 지상에 미생물을 (10 도 109 세포수) 접종하고 수일간 배양한다. 이때 매우
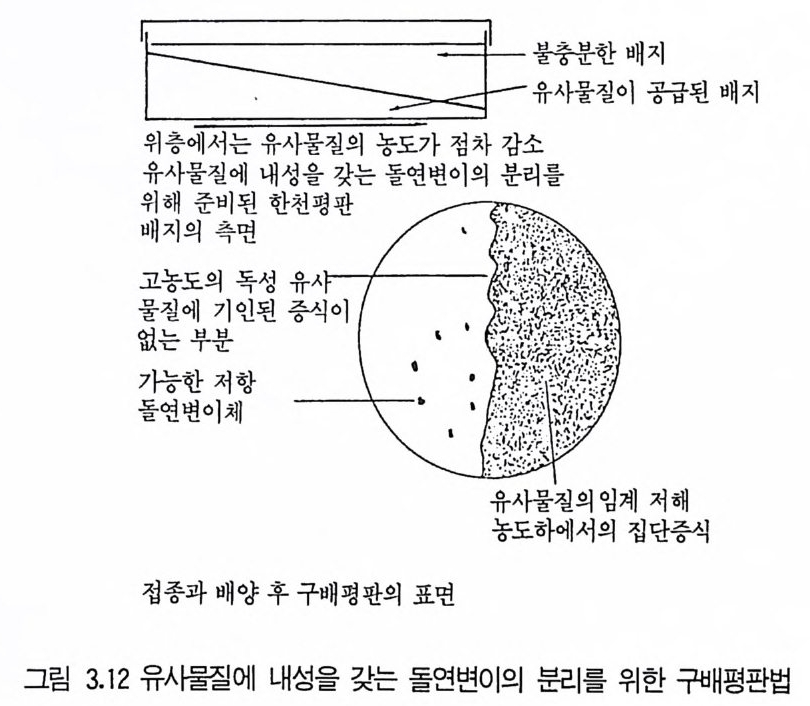
소수의 집락만이 증식하거나 완전히 증식이 저해되는 유사물질의 최저농도 를 결정할 수 있다. 그 후 변이처리 후의 생존개체들을 고체배지상에서 결 정된 농도의 유사물질로 처리하면 유사물질 존재하에서 출현한 집락들은 내성돌연변이일 것이다. Sz y bals ki (1952) 는 하나의 편평배지내에 어떤 범위의 유사물질의 농도 를 첨가시켜, 변이처리 후의 생존개체를 노출시키는 이른바 구매평판법 (gr adie n t pla te t echn iq ue) 을 고안하였다 ; 유시물질을 함유한 한천배지 를 페트리 집시상에 약간 기울여 어떤 각도에 고정시켜 굳힌다. 한천이 고 정된 후 유사물질을 함유하지 않은 배지를 한 충 덮고 바닥에 평행이 되 도록 굳힌다. 유사물질은 위충의 배지로 확산되어 하나의 편평배지내에 유 사물질의 농도구배가 형성될 것이다. 이때 변이처리 후의 생존개체를 배지 상에 도말하고 배양하면 그림 3 .1 2 에 나타난 것처럼 집단 증식지역 (유사물 질의 농도가 낮은 부분에 겹쳐서 증식하는 지역을 말함) 이상에서 나타나
 -— ――――>二〔麟: 0? ;된 배지
-— ――――>二〔麟: 0? ;된 배지
는 집락은 유사물질 내성돌연변이라고 판단할 수 있다. 어떤 방법이든지 유사물질 -내성돌연변이를 분리하는 경우, 유사물질 존 재여부에 따라 유사물잘에 감수성이 있는 것을 대조구로 아용하여 분리한 변이주가 지닌 내성이 분명한가를 확인해야만 한다. 그 후 이 내성분리주 가 원하는 화합물을 생성하는가 조사해야·하는데 이때는 그 화합물을 필 요로하는 세균(i nd i ca t or st ra i n) 을 이용한다. San 짝 Sh ii o(1970) 는 Brevib a cte r iu m fl avum 의 리신 유사물질 -내성 변이주를 리신생산에 이용한 연구를 한 바 있다. 리신합성의 주된 조절은 리신과 트레오닌에 의한 asp ar to k in a s~l 합 동되돌림저해 (concerte d fee dback i nh i b iti on) 이다. Sano9 .} Sh iiCi근 S-(2 ― am i noe t h y l)c y s t e i ne(AEC) 가 트레오닌이 존재할 때는 B. fla- vum 의 증식을 완전히 저해하지만 트레오닌이 없을 경우는- 부분적으로만 저해한다고 밝혔다. 또한 AECS 斗 트레오닌에 의한 저해는 리신이 첨가됨 으로써 역전될 수 있다는 것이다. 이러한 증거는 AEC 의 독성이 asp a r- t o ki nas 려 합동되돌림저해에서 리신의 효과를 모방함에서 기 인한다는 것 을 나타낸다. AEC ―내성변이주는 변이처리 후 생존개체를 AEC 와 트레 오닌 각 lm g /cm3 를 함유한 최소고체배지상에 도말함으로써 분리된다. 대디수의 내성변이주는 리신을 축적하여 최고 30 g /l를 생성하였다. 이 리 신 생산균주의 관찰로부터 이들의 as p ar t ok i nas~ 근 리신과 트레오닌의 합동저해 (concerte d i n hi b iti on) 에 대한 감도가 낮아져 있음을 볼 수 있 다. 제어요소에 대한 인식이 변형된 돌연변이룰 분리하는 데 이용되는 두번 째 방법은 복귀돌연변이주 (rever t an t mu t an t)의 분리이다. 영양요구성 변이는 변이인 모균(p aren t)의 표현형으로 복귀된다. 그림 3 .1 1 의 가설적 경로에서 P7} 첫번째 효소 (a) 를 되돌림저해함으로써 자신의 생성을 저해 하는 부분을 고려할 때 효소 떼} 생산하지 않는 변이주는 P 에 대한 영양 요구성을 나타내게 되는 것이다. 그러나 돌연변이주의 복귀돌연변이주는 呼 다량 생산하게 된다. 효소 a 의 생성과 관련된 좌위(l oc i)에 두 개의
변이가 일어난 역돌연변이는 원래의 원영양주의 효소오片근 다른 효소를 합 성하며 이는 P에 의한 조절을 감지하지 못한다. 복귀돌연변이는 자발적으 로 일어나거나 유발반도를 증가시키는 돌연변이 유발물질을 이용하기도 한 다. 이는 복귀돌연변이주만이 증식할 수 있는 배지 (위의 예로서는 P7} 결 여된 배지)상에 도말을 반복함으로써 얻어질 수 있다. Sh ii따 Sano(1969) 는 B. f lauu 짜긱 원영양원 돌연변이를 이용한 리신 생산을 연구하였다. 이들은 호모세린 탈수소효소 (homoser i ne dehy dr o- g enase) 가 결핍된 변이주로부터 원영양성 복귀돌연변아주를 분리하였는데 여기서 얻은 역돌연변이주는 작은 집락을 형성하는 균주들로서 23 g /L 에 이르는 리신을 생성하였다. 리신의 과다생산은 이 복귀돌연변이에서의 호 모세린 탈수소효소의 수준이 매우 낮기 때문에 야기된 것으로 증식에는 충분하지만, 저해 또는 억제의 기작을 일으키기에는 불충분한 양의 트레오 닌과 메티오닌을 합성하는 것으로 추정된다. 일차대사산물을 생산하는 균주의 개량계획은 하나의 선별기술에만 의존 할 수 없는 것이며, 대부분 자연변종의 선별과 다양한 수단에 의한 유도둘 연변이 선별을 포함, 많은 방법들을 통해 수행된다. 2.4 효소의 합성이 우량한 유도돌연변이주의 선별 미생물에 의해서 만들어지는 여러 효소의 수준은 어떤 대사조절 형태 아래에 있게 되고 효소의 높은 생산성에 °도 달하려면 대사조절이 변화되어 야만 한다. 한 효소를 많이 만들어내는 돌연변아주의 선별에 도움을 줄 수 있는 방법들이 개발되어왔으나 이 방법들을 고려하기 전에 효소합성을 조 절하는 메커니즘에 대해 고려해볼 필요가 있다. 산업적으로 중요한 효소는 일차대사의 생합성 반응을- 촉매하는 것과 이화반응을- 촉매하는 것으로 대 체로 분류될 수 있으며 두 범주는 보통 다른 조절 체계하에 있다. 다음 내 용은 각 범주의 조절방법과 조절체계가 변화된 돌연변이주를 선별하는 데 사용되는 방법을 간단하게 기술하고 있다•
일차대사의 생합성 효소 : 생합성 효소의 합성 조절은 되 돌림 억제 (rep - ress i on) 에 의해 주로 조절되고 이것은 앞 장에서 일차대사의 생합성에서 논의되었다. 그러므로 생합성 효소를 과도하게 만들어내는 돌 연변이주의 선별은 억제물질 (re p ressor) 을 만들지 않거나 인식하지 못하는 돌연변이 주의 분리를 의미한다. 영양요구성, 구조유사물질 (analo g ue) 내성 및 복귀 돌연변이주를 선별하면 과잉 생산주를 분리할 수가 있다. 이화 효소 (ca t abol i c enzy m es) : 이화효소들은 다음의 한두 가지 또는 세 가지 기전에 의해 조절된다. 1. 유도 : 효소는 단지 유도물질이라는 화합물의 존재에서만 만들어지며 유도 물질은 보통 효소의 기질이다. 2. 되돌림억제 : 효소의 합성은 효소활성의 산물(또는 산물과 밀접하게 관련 된 화합물)에 의해 억제된다. 3. 대사물 (ca t abo lit e) 억제 : 효소의 합성은 미생물이 즉시 이용할 수 있는 탄소원에서 빨리 자랄 때 억제된다. 효소생산시 위 조절체계의 해로운 효과는 배양환경을 조작함으로써 감 소시킬 수 있다. 즉 배지는 효소의 유도물질을 포함해야 하고 억제물질이 나 즉시 이용할 수 있는 탄소원은 포함하지 말아야 한다. 그러나 또한 효 소합성의 조절기능이 변화된 돌연변이주를 분리한다면 가능하게 될 것이며 유도물질이 존해하지 않고 억제물질이 있을 때 효소를 생성하는 돌연변이 주의 선별에 적용될 수 있는 여러 기술이 개발되어 있다. 유도물질의 부재시에 정상적으로 유도효소를 만들어내는 돌연변이주를 구성적 (consti tut i ve ) 돌연변이주라고 하며 야생형보다 돌연변이주에 더 유리하도록 배양조건을 조제함으로써 분리할 수 있다. Dema i n(1971) 은 구성적 돌연변이주의 분리에 사용되는 다음 기술들을 열거하고 있다• 1. 구성적 돌연변이주는 제한 기질로서 유도물질을 포함하는 연속배양 (che-
mos t a t)에서 세균집단을 증식시킴으로써 분리할 수 있다. 연속배양에서 제한 기질은 종종 유도에 대한 수준 이하로 매우 낮은 농도이다. 그러므 로 집딘에 존재하는 구성형 돌연변이주는 유도형보다 우선적으로 선별된 다. Nov i ck 와 Hor i uch(1969) 는 이 방법에 의해 탄소원으로 유당을 사 용하여 /J-g alac t os i das 떼 대한 E. col i의 구성형 둘연변이주를 선별하였 다. 또 S i k yt a 와 K y s li k(1981) 도 유당제한 연속배양에 의해 仕꿈타 ac t os i dase 에 대한 E. col i의 구성적 돌연변이주를 분리하였다. 2. 유도물질을 갖는 배지와 갖지 않는 배지를 미생물 집단이 순환하도록 하 면 구성형이 배양, 집적된다. 유도물질을 갖는 배지에 들어가면 유도형은 유도시간이 지연되기 때문에 구성형이 우세하게 된다 (Cohen-Baz i r e2t Jol it 1953). 3. 유도물질로는 적당치 않은 기질을 배지의 필수요소로 사용하면 그 결과 구성적 돌연변이주가 집적된다. Jac ob 2} Monod (1 961) 는 탄소원으로 ph eny l fi-g ala ct os i d 遷 사용해 B -g ala ct os i das 려 대해 구성적인 돌연 변이주를 분리하였고 Clarke(1974) 는 탄소원으로서 숙신산 (Succ i na t e) 과 유일한 질소원으로서 포름아마이드(fo rmam i de) 를 포함하는 배지에서 Pseudomonas aer 땡i nosa 를 배양함으로써 alip h ati c am i das 려 대해 구 성적 인 돌연변이주를 분리했는데 포름아마이드는 alip h ati c am ida se91 좋은 기질이나 유도물질로는 적당치 않다. S i k yt a 와 K y s li k(1981) 은 충 분한 락트산 나트륨 (sod i um lac t a t e) 과 유일한 질소원으로서 제한된 양 의 페닐아세틸 글루탐산{p hen y lace ty l glu ta m i c acid : 효소의 충분치 못한 유도물질 )을 포함하는 연속배양에서 E. col i를 배양함으로써 pen i - cill in am i dase 에 대한 구성적 돌연변이주를 분리하였다. 4. 구성적 돌연변이주는 효소의 유도물질과 유도저해물질의 존재하에서 세균 집단을 배양함으로써 선별되어질 수 있다. 5. 고체배지 위에서 구성적 돌연변이주를 감별하는 데 매우 유용한 기술은 유도물질로는 작용하지 않는 발색기질을 이용하는 것이다. Demain (1 971) 은 탄소원으로 글리세롤을 포함하는 고체배지에 돌연변이 처리가 된 자손세포(p ro g en y¾) 도말하고, 형성된 집락위에 o-ni tro p h eny l-P -D- g alac t os i d 톄 뿌립으로써 8 -g alac t os i das 려 대해 구성적인 돌연변 이주를 검출하였다. 구성적 돌연변이주는 기질을 분해하여 노란색의 o 니·
이트로페놀 (o- nit ro p henol) 을 방 출 하며 그 결과 구성적인 집 락들 이 염색 된다. 억제물질의 존재하에서 대사효소를 만들어내는 돌연변이주 또한 분리할 수 있다. 이화효소가 감지할 수 있는 두 가지 형의 억제로는 효소촉매반응 의 산물(또는 관련산물)에 의한 되돌림억제와 즉시 이용할 수 있는 탄소 원에서 빨리 증식할 때 일어나는 대사산물억제 (cata b olit e re p ress i on) 의 형태가 있다• 이화효소가 결핍된 돌연변이주의 복귀주 선별은 만족할 만한 결과를 얻을 수 있으나 효소의 되돌립억제 효과에 대한 내성을 선별하는 것은 어렵다. 어떤 효소의 대사산물억제 (cata b olit e re p ress i on) 에 대한 내성돌연변 이주의 분리에 다음의 몇몇 기술이 사용되어왔다. 1. 효소가 결핍된 돌연변이주의 복귀주 (rever t an t s) 를 검색하면 대사산물 억제 (cata b oli te re p ress i on) 에 대한 감수성이 변화된 돌연변이주를 분 리할 수 있다 . B -g alac t os i das 려 대사산물 억제를 받지 않는 돌연변이주 는 유당-분해력이 없는 돌연변이주의 복귀주로서 분리된다. Sm yt h 와 Chark(1972) 는 P. aer ugi nos 려 am i dase 결손 돌연변이 주 의 복귀주로부 터 am i das 려 대사산물억제에 내성이 있는 돌연변이주를 분리하였다. 2. 질소를 함유하는 기질을 분해하는 효소의 대사산물억제에 내성돌연변이주 , 는 탄소원으로 대사산물 억제물질 (cata b olit e re p ressor) 을, 유일한 질소 원으로는 효소의 기질을 포함하는 고체배지에서 집단을 배양함으로써 얻 어질 수 있다. Sik y ta 등 (1982) 은 제한 질소원으로서 D 세린 (D -s er i ne) 과 충분한 포도당을 포함하는 연속배양 (chemos t a t)에서 E .. c ol i를 배양 함으로써 serin e dea mi nas 팩 대사산물억제에 저항성있는 돌연변이주를 분리하였다. 3. 연속배양의 선택압 (sele cti ve p ressure) 은 효소의 기질과 배지성분으로 대사산물 억제물질을 둘 다 갖는 연속배양에서 미생물을 배양함으로써 대 사산뭉걱제 내성돌연변이주의 선별에 이용될 수 있다. 두 기질을 다 이용 할 수 있는 미생물이 연속배양 여건하 경쟁에서 유리하므로 선별된다.
유도물질과 억제물질에 대한 반응이 달라전 돌연변이주의 분리기술에 대한 위의 설명은 학문적 연구에서 얻은 예를 내포하고 있으나 산업적으 로 중요한 효소의 생산조절에 대한 많은 지식을 갖고 이 기술을 더 폭넓 게 적용하게 되었다. 한 세균의 효소의 생산은 그 효소를 암호화하고 있는 유전자의 복사수 를 증가시킴으로써 증가한다. 3 이차대사산물의 생산수율이 우량한 돌연변이주의 분리 지금까지의 논의는 선별 절차의 구상을 할 수 있게끔 생합성과 조절이 충분히 이해된 경로에 대한 돌연변이주의 분리에 대한 것이었다. 이차대사 산물의 생합성은 일차대사산물에 비해 잘 알려져 있지 않고 이차대사산물 을 합성하게 하는 미생물의 생산성을 제한하는 기작에 대해서는 거의 알 려져 있지 않다. 그러므로 특정 조절 돌연변이주를 분리하는 것은 극도로 . 어려우며 우량균주를 우세하게 해주는 편리한 선별방법을 사용하지 못하고 있는 실정하에서도 돌연변이 처리 후 생존균에 대해 월등한 생산성을 갖 는 것을 가려내야만 했으며 실제 우량균주 선별에 대한 무작위선별이란 경험적 방법이 표 3 .1에서 예를 든 것처럼 (Riv i e r e, 1977) 항생물질의 생 산울 증가시키는 메 아주 효과적임이 증명되어왔다.
표 3.1 연간 항생물질 생산의 양상 (Al i khan i an, 1962 과 Riv ie r e, 1977) Ini tial yield at Imp ro ved yield s Imp ro ved yield s tim ed ofd is c overy obt ai n e d in the in France, 1972 Ant ibi o t i c (units cm-3) USSR (units cm-3) (units cm-3) Penic il l in 20 ( 1943) 8.000 ( 1955) 12,000 ~ 15,000 Str e pt om y ci n 50 (1945) 5.000 (19 55) 12,000~ 15,000 Cholote t r a -200 (19 48) 4.000 (1959) 12,000~ 15,000 cyc l in e
Oxy tet r a - 400 (1950) 6,000 ( 1959) cyc l in e Eryt hr omy ci n 100 (19 55) 2.000 ( 1961 ) 3,000
그러나 균주 개발계획의 경험적 측면을 줄이고 선별방법에 대해 더욱 합리적인 접근을 하려는 시도가 나타났다. 이전 시도는 경험적 기술과 더 욱 계획된 선별방법의 이용을 의미한다. 균주개량에 대한 경험적인 접근은 미생물의 돌연변이 처리와 그 후 생 존균 중 생산성이 향상된 것을 가리는 것을 의미하는데 생존균 선택의 평 가는 풀라스크롤 진탕하며 수행하는 데 시간과 인력 두 측면에서 비용이 많이 드는 방법이다. Fan ti n i(l 975) 에 따르면 항생물질 생산 우량균주 분 리를 위한 계획을 고안하는 데 발생하는 두 가지 문제는 L 돌연변이 처리 후 생존균으로부터 얼마나 많은 집락이 시험용으로 분리되 어야만 하는가? 2. 어떤 집락이 분리되어야만 하는가? 첫번째 질문의 대답에서 Fan tini는 시험되기 위해 분리되는 집락의 수 는 인력, 배양기, 전당기의 공간, 시간의 실제적 제한요소에 의해 결정된다 고 주장하였다. 그러나 Dav i es(1964) 는 통계적 접근이 균주 개발계획에 서 물질적 자원의 효과적인 이용에 대한 가치 있는 지침을 줄 수 있다고 논증했다. Dav i es 는 200 개의 전당기 공간이용과 오차 변화의 실제적 결과 와 돌연변이주 사이에서 일어나기 쉬운 수율의 분포에 근거하여 돌연변이 와 검색계획의 컴퓨터 모형을 만들었다. Dav i es는 돌연변이주의 대부분이 생산성에 있어 크게 향상되기보다는 소폭 증가를 갖게 되므로 큰 증가를 얻으려는 목적으로 많은 수를 검색하기보다는 소폭 증가를 얻으려는 목적 으로 적은 수를 검색하는 것이 더 알맞다고 가정했다. 이런 접근방식이 갖 는 주요 난접은 소폭 증가를 결정하는 데 포함되는 오차로서 이것은 검색
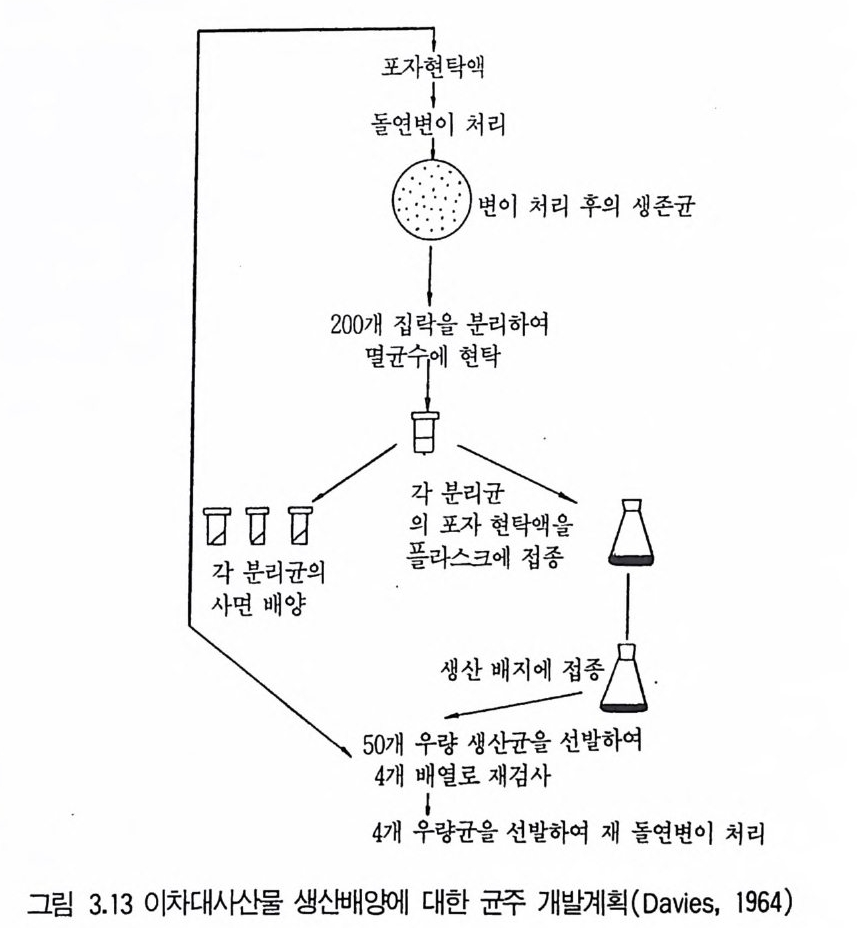
시험의 반복과 더 많은 설비의 이용을 의미한다. Dav i es 는 검색계획 반복의 장점을 연구하는 데 컴퓨터 모형을 사용하 여 마침내 짜계 조작의 이용을 제안하였는데, 돌연변이주를 일단계에서 한 개씩 실험해보고 우수한 생산균은 이단계에서 4 배열로 실험해본다. Dav i es 는 실험오차가 적고 유용한 형의 발생빈도가 높다면 한 단계 검색 울 채택할 수 있고 실험오차가 높고 유용한 형의 발생빈도가 낮다면 세 단계 검색을 채택할 수 있지만 두 단계 조작이 광범위한 조건에서 적당하 다고 결론내렸다. Dav i es 의 제안에 기초한 검색계획은 그림 3. 13 에서 볼 수있다.
 포자현I 탁액
포자현I 탁액
Fan tini의 두번째 질문(어떤 집락이 분리되어야만 하는가?)에 대한 대 답은 이차대사산물에서는 아주 어렵고 Dav i es 의 계획에서는 집락이 무작 위로 선택된다. 다수의 연구자에 의해 변화된 모양에 따른 집락의 선별이 고려되었으나 이것은 바람직하지 못한 방법으로 나타났다. Elander(1 9 66) 는 형태적 변이주가 우수한 생산균일지라도 생산울 증가시키기 위해 상당 한 발효기술을 요구하기 때문에 정상적인 모양의 균주를 분리하는 것이 더 유리하다고 했다. 또한 Al i khan i an(1962) 은 항생물질을 생산하는 acti - nom y ce t es 의 형태돌연변이주의 대부분이 하위의 생산균주였음을 말하였 다. 간소화된 방법의 기본은 생산되는 항생물질에 민감한 시험균주가 있는 고체배지 위에 돌연변이 집락이 자라도록 하는 것이다. 항생물질의 정도는 도포된 시험균주의 억제 정도에 의해 평가된다. 이 체계는 항생물질을 낮 은 수준으로 만들어내는 균주에 적용하는 것은 . 간단하지만 넓은 억제 범 위를 만들어내는 고생산자를 가려내기 위해서는 수정해야만 한다. 또한 우 수한 생산균이 시험균으로 오염되는 것을 막기 위해 어떤 체계가 고안되 어야만한다. Dulane y와 Dulaney( 1967) 는 chlor t e t rac y cl i n 례「 만들어내는 돌연변 이주의 분리에 중층법 (overlay t echn iq ues) 을 사용하였다. 돌연변이 처리 된 포자는 페트리 접시의 한천배지에서 6 일 동안 배양하고 그 다음 멸균 된 셀로판 조각을 덮는다. 그 위에 시험균을 포함하는 한천을 덮어 깔고 평판을 배양시킨다. 셀로판에 의해 돌연변이주 집락이 오염되는 것을 막을 수 있고 저지환의 크기는 기초충의 깊이, 도말했을 때 집락의 연령, 덮어 깐 깊이, 배양온도에 의해 조절될 수 있다. 이 체계는 돌연변이를 일으키 지 않은 균주의 단일집락은 저지환을 만들어내지 않지만 인접한 집락 두 개에 의해서는 저지환이 만들어지도록 먼저 조정된다. 실제에 있어 저지환 의 크기는 덮어 깐 깊이에 의해 조절된다. Dulane y와 Dulane y는 무작위 선택과 액체배지에서 실험해보는 것보다 중충법 (overlay t echn iq ues) 에 의해 다수의 원하는 표현형을 훨씬 많이 얻었다. Ich ika wa(1 9 71) 등은 aga r piec e me t hod라 는 소형화된 방법을 이용
하여 Str ep t om y ce s s p.에 의해 kasug am y ci n 생산이 증가된 것을 가려냈 다. 집락간의 방해작용을 막기 위하여 돌연변이 처리된 포자를 한천의 마 개 위에서 자라게 한 다음 시험균이 접종되어 있는 검정 한천 평판 위에 놓고 항생물질의 수준을 저지환의 크기에 의해 결정했다. 배지 개선작업과 위의 방법을 조합함으로써 생산성을 1()l ll 증가시킬 수 있었다. Ichik a wa 의 방법을 Di tch burn(1 9 74) 등이 변형하여 페니실린을 향상된 수준으로 합성하는 Aspe rgi llu s nid u lans 돌연변이주를 분리하였다. A. n i dulans 에 의한 페니실린 생산 수준은 P. ch 짱 so g enum 에 비해 매우 낮으며 위의 방 법을 상업적으로 이용하기 위해서는 상당히 변화되어야만 했다. Ball 과 McGonagl e ( 1978) 은 P. ch ry so g enum 의 고생산 균주 (6,000 un it s/cm 까지 생산)의 페니실린 생산검정에 적용할 수 있는 간소화된 방법을 개발하였다. 이들은 방법을 최적화하는 결정적인 요소로서 고체배 지의 고안에 중점을 두었다. 이들은 한천고체배지에서 집락의 증식은 같은 배지성분의 액내 배양시 미생물의 증식에서처럼 그렇게 배지를 변화시키지 는 않는다고 말하였다. 돌연변이 처리된 포자를 평판당 10~2~] 락이 나 타나도록 영양제한배지가 든 페트리 접시의 표면에 도말한다. 평판의 배양 시간은 제시하지 않았으나 집릭이 정확한 측정에 알맞는 크기가 되었을 때 p enic i ll i nas 혜[- O .l 6u nit s/cm- 3 로 포함玲片(저지환의 크기를 제한하 기 위해) B. sub ti l i펴 저온 멸균된 포자 현탁액을 평판 표면에 도말한 후 평판을 18~2 41-]간 배양한 다음 저지환을 조사했다• 적당한 집락은 sodiu m p e ni c i ll i n과 스트렙토마이신 (s t re pt om y c i n) 황산염이 든 영양 한천배지 위에서 배양해 B. subti li ~ 오염을 막았다. 이 기술의 이용으로 洞의 기능원이 沙狀월 동안에 자의선 조사된 포자집단에서 15,000 생존균주 를 세밀히 조사할 수가 있었다. 간소화된 방법의 주요 단점은 고체배지에서 나타났던 생산성이 액체배 양시 나타나지 않고, 역으로 더 중요한 점은 고체배지에서 활성을 보이지 않던 집락이 액체배양에서 높은 생산성을 보일 수도 있다는 점이다. 이런 한계에도 불구하고 위의 연구자들은 이 간소화된 방법이 상당한 장점을
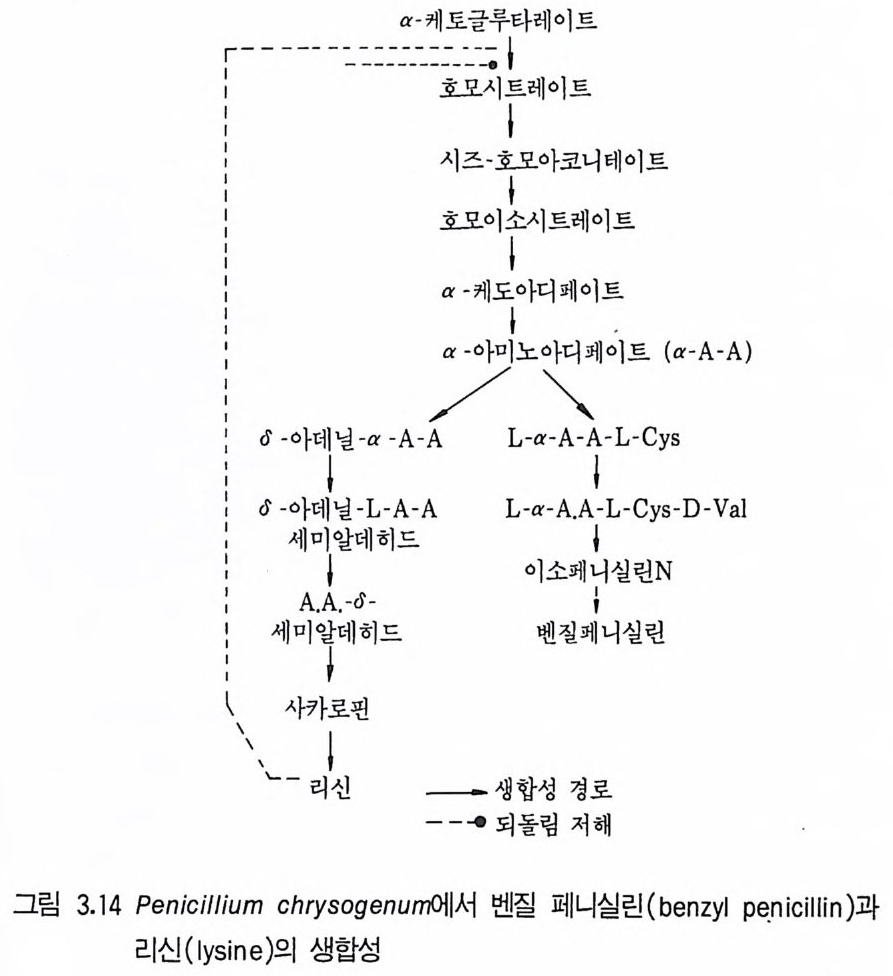
갖고 있음을 증명하였고, Ba11 (1 978) 은 전통적 인 전탕 -플라스크 검색계 획보다 2 ()lJ脂의 능률 증가를 가져 왔다고 말하였다. Dema i n(1973) 은 영양요구 돌연변이는 여전히 196 9i.1에 사용되는 생산 균주의 특칭이라고 말하였다. 그러므로 무작위 선별에 의해 분리되고 이차 대사물을 과량 생산하는 일부 균주들은 계획된 선별방법에 의해 분리되고 일차대사산물을 과량 생산하는 균주의 경우와 비슷한 방법으로 변화된 것 같다. 또 문헌에 의하면 우수한 일차대사산물 생산균 분리에 사용했던 방 법이 우수한 이차대사산물 생산균 분리에도 적용된 예를 보여준다. 경험에 의한 방법에는 영양요구주의 분리, 복귀주와 구조유사물 내성돌연변이주의 분리 등이 있다. 3.1 영양요구 돌연변이주의 분리 이차대사산물 생산균의 영양요구 돌연변이는 주로 낮은 수율의 생산균 주를 얻게 되지만 생산이 향상된 경우도 또한 보고되고 있다. 예를 들면 Ali kh ania n (1 9 59) 등은 5 해의 영양요구 돌연변이주의 테트라사이클린 생산능력을 연구하였는데 모두 정상적인 배지에서는 모균주보다 상당히 적 은 데트라사이클린을 생산하였다. 그러나 증식에 요구되는 물질을 공급하 면 한 돌연변이주는 모균주보다 월등히 높은 생산성을 나타냈다. 이차대사산물 수율의 해로운 효과에 대한 가장 간단한 설명은 영양요구 주는 최종생성물의 전구체 생합성이 막혔다는 것으로, 예를 들면 Pol-sin e lli ( 1965) 등은 악티노마이신 전구체 (이소류신, 발린 또는 트레오닌 ) 중 어느 하나를 요구하는 Str ep tom y ce s an ti b i o ti cu 려 영양요구주는 항생 물질의 저급 생산자임을 증명했다. 많은 이차대사산물은 또한 일차대사산물을 생성하는 분지된 (branched) 경로의 최종산물로 여겨진다. 그러므로 일차최종산물에 대한 영양요구성이 되는 돌연변이는 이차산물의 생산에도 영향을 준다. P. chry so g enum 에서 리신과 페니실린은 그림 3 .1 4 에서 보는 것처럼 a-am ino adip ic ac i d 까지
공통 생합성 경로를 갖는다. 이 생합성 경로는 Bonner(1947) 가 분리한 P.ch ry so g enum 의 리신 영양요구주의 25% 가 페니실린을 만들 수 없었다는 관찰을 설명해준다. 또한 페니실린 발효에서 리신의 역할을 알게 됨으로써 잠재적으로 우수한 페니실린 생산자로서 리신 영양요구주를 연구하게 된 것이다.
 r-- -- -- -- --:::a:-- :케:_토--글--루; i타 레 °l 트
r-- -- -- -- --:::a:-- :케:_토--글--루; i타 레 °l 트
Dema i n(l967) 은 리신이 페니실린 생합성을 저해한다는 것을 증명하였 다. 이런 현상에 대한 설명으로서는 리신에 의한 호모시트르산 합성효소
(homcit ra te s yn t hase) 의 저해 결과 페니실린 합성에 요구되는 a 아미노 아디프산(o: -am i noad ipi c ac i d) 이 고갈되기 때문이라고 생각된다 (Dem a i n과 Masurekar 1974). 3.2 내성돌연변이주의 분리 유사물질 내성 돌연변이주의 분리에 대해서는 이미 일차대사 분야에서 논의되었는데, 원리는 유사물질의 유해한 효과에 내성이 있는 돌연변이주 가 자연 대사산물의 조절 특칭과 같은 방식으로- 자연적 대사물질을 과잉 생산한디는 것이다. 이 접근법은 이차대사 분야에서도 적용될 수 있다. 1. 이차대사물질의 일차대사 전구체 유사물질에 내성 있는 돌연변이주를 분 리할수있다. • 2. 이차대사물의 되돌림효과에 내성 있는 돌연변이주를 분리할 수 있다. 3. 이차대사물질을 생산균주의 영양중식기(t ro phop hase) 에 가했을 때의 유 해효과에 대해 내성 있는 돌연변이주를 선별할 수 있다. 4. 이차대서물질의 전구체의 유해효과에 대해 내성 있는 돌연변이주를 분리 할수있다. (1) 이차대사물질의 일차대사 전구체 유사물질에 대한 내성돌연변이주 Elander (1971) 등은 항생물질 (py rroln it r i n) 을 과생산하는 Pseudo- monas aureo f ac i en 펴 돌연변이주의 분리에서 이 방법을 적용하였다. 트립 토판은 py rroln it r i n 의 전구체이며 생산을 촉진시키지만 산업공정에 첨가 제로 사용하기에는 비경제적이다. 그러므로 Elander(1971) 등은 이미 섣 명한 농도구배 평판법 (gra d ien t pla te t echn iq ue) 을 사용하여 트립토판 유사물질에 내성 있는 돌연변이를 분리하였다. 결과적으로 모균주보다 2~ 째의 항생물질을 생산하며 트립토판에 의한 되돌립저해에 내성이 있는 균 쥐 뿐]하였다. 생산성이 높아전 균주에 트립토판을 가해도 pyr-
rol i n tr i떼 더 많이 합성하지는 않는 것으로 보아 트립토판 공급은 더 이 상 제한요소가 아니며 균주는 항생물질 합성에 충분한 내부 트립토판을 합성하고 있다. (2) 이차대사물질의 되돌림효과에 내성 있는 돌연변이주 이차대사산물이 자신의 합성을 억제한다는 문헌은 많이 있다. Marti n (1978) 은 다음 예들을 인용하였다 : 클로람페니콜 (chloram phen i co l), au- rodox, cyc l ohexi m i de , sta p h y lo my ci n , ris t o m y cin, pur omy ci n , fun - gici d i n , cand ihe xin , my co p h enoli c ac i d 와 페니실린 등, 정확한 조절기 작은 명백하지 않으나 세포의 일반적 대사에 대해서가 아니라 이차대사산 물의 생합성에 대해서 특이적이다. 클로람페니콜에 의한 자신의 합성의 조철기작은 클로람페니콜에 의한 any la mi ne syn th e ase(choris m ic ac i d 에서 chloram p hen i co@.의 경로 에서 첫번째 효소)의 억제인 것으로 나타나 있다. Jo ne~ Vin i n g ( 19 76) 은 any !a mi ne s y n t heas 라 세포의 증식이나 클로람페니콜 경로의 다른 효소의 활성에는 아무런 영향을 주지 않는 항생물질의 농도인 lOOmg / dm-3 클로람페니콜에 의해 완전히 억제됨을 증명하였다. Mar ti n(1978) 은 이차대사산물 축적수준과 되돌림조절을 일으키는 수준 A }o l 에 상호관계의 몇 가지 예들을 제시하였는데 일부 이차대사산물의 수 율증가에 대한 제한요소는 최종산물에 의한 되돌림저해임을 의미한다. 이 차대사산물에 의한 되돌립저해에 대해 내성 있는 돌연변이주의 선별은 일 차대사 조절에 내성 있는 균주의 분리보다 더욱 어려운 작업이다. 이차대 사산물의 독성 있는 유사물질은 증식에 필수적인 화합물이 아니기 때문에 그 독성이 이차대사산물의 되돌림조절과 같은 기작에 의한 것은 아니다. 그러나 항생물질에 의한 되돌림저해에 내성 있는 돌연변이주의 검출은 전 술한 소형화 검색 (mini a t u r iz e d screenin g ) 방법과 유사한 고체배지 검 색법으로 행해질 수 있다. 이 방법은 억제작용을· 하는 수준으로 항생물질 울 함유하는 고체배지에 돌연변이 처리된 생존균을 배양하고 시험균으로
중충 (overla y)하여 우량생산균을 발견하도록 하였다. 이 방법의 난점은 원래 둘어 있던 항생물질 그 자체가 시험균의 발육을 억제한다는 점인데, 이 문제는 원래 배지에 들어 있는 것보다 더 많은 항생물질 수준에 의해 서만 저지환이 생성될 수 있게 중충 (overla y) 깊이 또는 시험균의 농도를 조절함으로써 극복될 수 있다. 그러나 이 방법은 상업적인 우수한 생산균 주의 선별에 반드시 만족할 만한 해결이 되지는 못하고 있다. 다론 접근방 법은 자연적 산물에 의한 되돌림조절을 모방하지만 항균성을 갖지 않는 항생물질의 유사물질을 이용히는 것이다. 대안은 원래 배지 안에 넣은 항 생물질보다 초과된 농도에서만 민감한 시험균의 돌연변이주를 이용하는 것 이다. 최종산물에 의한 되돌림 (fee dback) 조절이 생산성을 억제하는 데 중요한 역할을 한다고 밝혀질 경우 위와 같은 방법을 고안할 가치가 있다. (3) 영양중식기에서 이차대사물의 유해효과에 내성 있는 돌연변이주의 분리 이차대사물질이 영양중식기 (t ro p ho p hase) 에 존재할 때 이차대사물질을 만들거내는 세포에 대해 유해하다는 것이 많은 이차대사물질을 생산하는 미생물에 대해 증명되고 있다 (Dema i n, 1974). 그러므로 이차대사산물의 생산기 (i d i o p hase) 에서 미생물의 대사를 개시하는 것은 다른 말로 자가중 독 산물을 만들어내는 것처럼 보인다. 그러므로 어떤 경우에 있어서 증식 기에 이차대사물에 대한 내상이 높을수록 생산기에 생산성이 높아전다는 것이 증명되고 있다. Dolezil o va(1965) 등은 S. _ nourse i의 여러 균주에 의 한 n y st a ti n 의 생산수준이 증식기에서의 항생물질에 대한 균주의 내성과 관계되어 있다는 사실을 증명하였다• 즉 비생산 돌연변이주는 20unit s/ cm 헬 의 해 저 해되고 6,000 un its / cm- 3..을 만들어내는 모균주는 증식 기 에 2,000u nit s/cm 혀 의해 억제되며 15,000u nit s/cm- 별 만들어내는 돌연변이주는 20,000 un its / cm- 예도 내성이 있는 것으로 알려져 있다. 항생물질 내성과 생산성 사이의 관계에서 이용될 수 있는 점은 돌연변 이 처리 후 생존균을 높은 수준의 최종산물 존재하에서 배양할 때 고생산
돌연변이를 선별할 수 있다는 것이다. 높은 농도의 항생물질 존재시에 증 식을 할 수 있는 균주는 또한 생산기에서 일반적으로 높은 생산성을 나타 낼수있다. (4) 증식기에 유해한 전구체에 내성 있는 돌연변이주의 분리 발효배지에 첨가한 이차대사물질 전구체는 증식기에 있는 생산균주에 유해하다는 것이 증명되고 있다. 이런 현상의 예는 P. chry so g enu~ 기 페 니실린 발효에서 전구체로 사용되는 페닐아세트산의 유해효과를 들 수 있 다. 고농도 전구체에 견딜 수 있는 균주는 고농도의 최종산물을 합성할 수 있다는 것으로 최종산물의 생성결과 전구체의 유해효과가 해독된다는 것을 암시하고 있다. Pol y a 와 Ny iri ( 1 966) 는 P. chry so g e nu~ 페닐아세트산 내성 돌연변이주의 선별에서 이 가정을 적용하여 분리균의 7% 가 페니실 린 생성이 강화되었음을 밝혔다• 내성은 돌연변이주의 두괴성의 변화에 기인하든지 또는 전구체를 원하 는 최종산물과는 관계없이 해가 없는 대사물질로 분해하도록 하는 능력에 기인하는 경우도 있다. 3.3 복귀돌연변이주의 분리 일차대사산물의 선별에서 언급했던 바와 같이 돌연변이주는 그 모균의 표현형으로 복귀되기도 하지만 복귀체의 유전형은 원래 모균의 것과 반드 시 똑같이 되지는 않는다. 어떤 복귀영양요구주는 일차대사산물을 축적한 다는 것이 증명되었고 (Sh iio9-} Sano, 1969), 이런 시도는 이차대사산물을 과잉생산하는 돌연변이주를 분리하기 위한 기술에도 이용되고 있다. 1. 이차대사산물 생산에 영향을 주는 일차대사물질에 대해 영양요구적인 돌 연변이주의 복귀주 분리. 2. 이차대사산물을 생산하는 능력을 상실한 돌연변이주의 복귀주 분리.
(1) 이차대사물질 생산에 영향 을 주 는 일차대사물 질 에 대해 영양요구적 인 돌연변이주의 복귀주 분리 전에 언급된 바와 같이 이차대사산물에 대해 영양요구성 효고H t 설명하 기는 어렵고 어떤 것은 아직 규명되지 않은 교차경로 (cross- p a t hwa y) 현 상에 기인하며 또 어떤 것은 영양요구성과 관련된 다른 돌 연변이의 발현 에 기인하는 듯하다. 이와 같이 복귀돌연변이주는 다수의 방법, 즉 직접적 . 효과, 교차경로의 효과, 검출되는 복귀오柱근 다른 돌연변이에 기인한 효과 등으로 이차대사 경로에 영향을 준다. Dulane y와 Dulane y (1967) 는 각각 다섯 영양요구주에서 유도된 S. u i r i d ifa c i ens 의 독립영양 복귀주의 집단에 데트라사이클린 생산성을 연구 하였다. 우수한 생산균은 호모시스태인 (homoc y s t e i n) 영양요구주로부터 유래된 것 이의에도 모든 독립영양 복귀주 집단에서 얻어진다. 그러나 우 수 생산균의 발생빈도는 집단들 중 하나를 제의하고는 돌연변이 처리 후 생존균의 무작위 선별에 의해 얻어지는 빈도와 유사하다. (2) 이차대사산물을 만들어내는 능력을 상실한 돌연변이주의 복귀주 분리 비생산 균주의 복귀 결과 돌연변이주가 이차대사물질의 생산과 관련된 최소한 두 돌연변이를 겪기 때문에 고생산 돌연변이주를 검출해내는 경 우가 있다. Dulane y와 Dulane y (l967) 는 고체 생산배지 위에 S. uir i- d ifa c i en 회 비생산 균주의 돌연변이 자손을 도말하고 중층방법 (overlay ) 에 의해 우수한 데트라사이클린 생산균을 선별했다. 원래 모균주의 테트라 사이클린 생산 수율보다 역를 생산하는 돌연변이주를 분리하였다. 이 방 법에 내포된 주요 어려움은 고생산 균주의 비생산 돌연변이주는 극단적인 대사의 결핍 때문에 복귀될 수 없다는 점이다. 그럼에도 불구하고 복귀방 법은 정한한 중층 검색법을 구사하는 곳에서는 매우 가치가 높다.
4 산업미생물 개량을 위한 재조합 체계 넓은 의미에서 유전자 재조합 (recomb i ra ti on) 은 〈서로 다론 개체에 원 래 존재하는 유전자의 새로운 조합을 만드는 과정〉으로 정의하였다. 산업 적 균주의 개량을 위해 재조합 메커니즘을 이용히는 것은 돌연변이 기술 의 이용에 비하여 제한되고 있다 . 이는 산업미생물에 대한 기본적인 유전 학 지식이 부족하고 재조합 기술에 비하여 돌연변이 기술과 돌연변이주의 선별이 용이하기 때문이다. 그러나 Ponte c orvo9 -l- Sermon ti는 P. chr- y so g enum 에서의 준유성적 생활환(p arasexual c y cle) 을 통한 재조합을 페 니실린 수율 향상에 적용하게 하였고 st re pt om y ce t es 의 유전학에서의 많 은 발전은 산업적으로 중요한 그룹의 재조합 기술에 많은 발전을 가져왔 다. 또한 서로 다른 미생물군 사이의 유전 정보의 전달을 가능케 하여 재 조합 장벽을 국복하는 기술이 개발되어왔다. 4.1 진균류의 유성생식에 의한 재조합(p arasexual recombin a ti on in fun g i) 대부분 산업적으로 중요한 전균은 유성생식 단계가 알려져 있지 않으며 이러한 생물에서는 재조합을 성취하기가 어렵다. 그러나 Ponte c orvo (1953) 는 유성생식기관 밖에서나 혹은 유성생식기관의 부재하에서도 핵융 합과 유전자 분리가 일어날 수 있음을 밝혔다. 이러한 과정을 준유성적 생 활환이라 하며 불완전균류인 A. n ig er와 P. ch ry so g enum 뿐 아니라 유성전 균인 A. n i dulan 예서 증명되고 있다. 불완전균에서 일어나는 준유성적 재 조합을 위해 핵융합은 영양균사에서 이질 핵 사이에서 일어나야 한다. 그 러므로 재조합은 최소한 두 개의 다른 핵형, 즉 이형 다핵체 (he t eroka r y on) 를 가전 생물에서만 얻어진다. 다른 두 반수체 핵의 융합으로 생긴 이형 이배체 핵은 이배체 클론 (clone) 을 형성하고 드물게는 클론의 이배 체 핵은 비정상적 유사분열로 유사분열의 분리와 반수체나 이배체의 재조
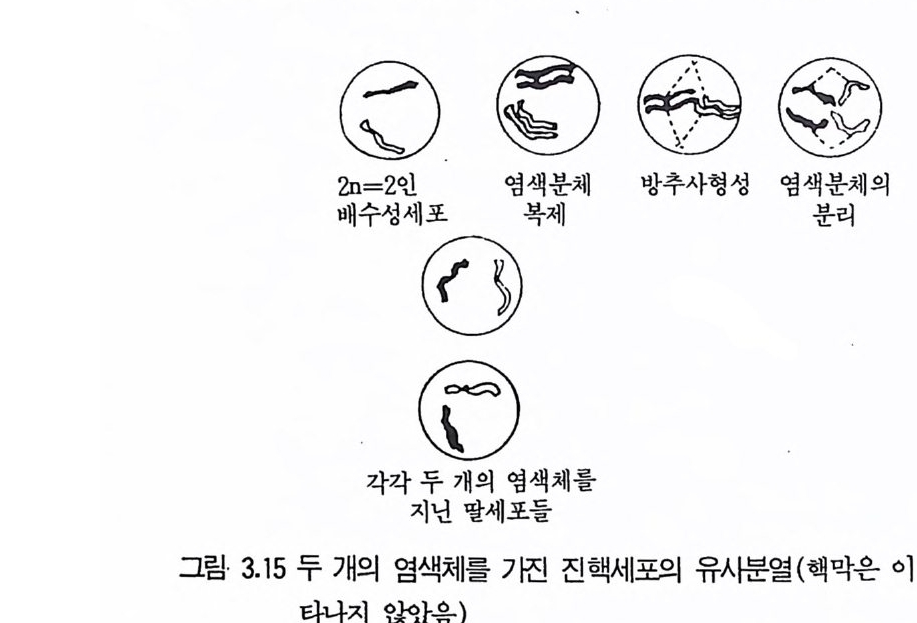
합클론을만들게 된다. 재조합 클론은 이형 다핵체에서 발현되지 않는 열성인자 를 노 출시 킴으 로써 검출할 수 있다. 재조합체를 분석하여 재조합체가 단 하나의 표지나 몇몇 연관된 표지로 분리된 것인지를 알 수 있고 분리체의 배양으로 초기 분리체보다 더 열성인 특징을 나타내는 클론을 성장시킬 수 있게 된다. 이 형집합 이배체의 성장중에 일어니는· 재조합 과정은 두 방법으로- 일어난다. 하나는 유사분열의 교차로서 이배체 재조합체를 만들며 또 하나는 반수체 화 (ha p lo i d i za ti on) 로서 반수체 재조합체를 만든다. 유사분열 교차는 비정상적 유사분열의 결과인데 이형접합 이배체 세포 의 정상 유사분열은 그림 3 .1 5 에 나와 있다• 유사분열 동안 상동영색체 각 쌍은 복제하여 두 쌍의 염색사 (chroma ti d) 를 만들고 한 쌍의 염색사는 다론 쌍의 염색사와 세포의 · 국으로 이동한다. 적도판을 따라 세포가 분열 하여 두 세포를 형성하고 두 세포 모두 염색체상의 모든 유전자에 대해 이형집합형이다. 상동염색체의 염색사간의 종적인 분리의 교환이 일어나는 유사분열 교차는 그림 3 .1 6 에서 볼 수 있다. 이 과정은 한 쌍의 염색체의
 :배2n수=성2 인세@ 포 :영복색 제분 체- 방추:사형성 s영색분분리체 의
:배2n수=성2 인세@ 포 :영복색 제분 체- 방추:사형성 s영색분분리체 의
 :2 n=2 인 : 영색분채 :t적:
:2 n=2 인 : 영색분채 :t적:
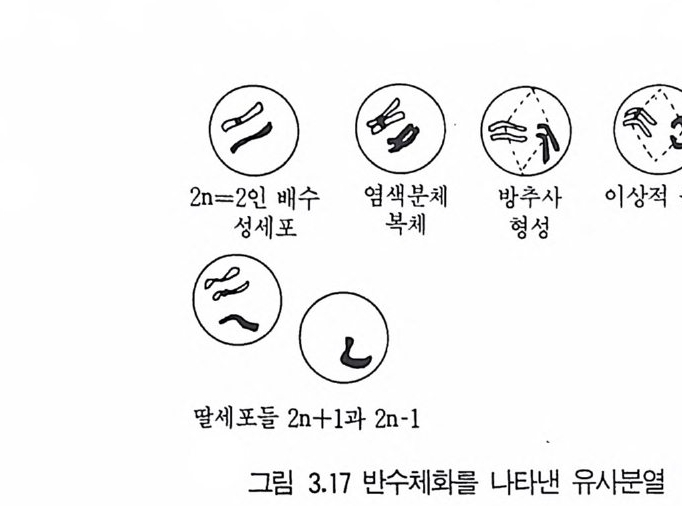
한 부분에 대해 상동인 딸핵을 형성하게 되며 그 부분에 포함된 열성 대 립인자를 발현시킨다. 그러므로 부분적 동형접합체 (homoz yg o t e) 로부터 생긴 클론은 재조합체가 되고 재조합체의 유사분열 교차는 더욱 열성인 대립인자를 발현시키게 된다. 반수체화 과정은 유사분열의 딸세포들간에 불균등한 염색사 분리를 일 으키는 과정이다. 그러므로 한 상동염색체쌍의 네 염색사 중에서, 셋은 한 극으로 이동하고 하냐는 다른 국으로 이동하여, 한 핵은 2h+l 염색체를 갖고 다른 핵은 2n-1 의 염색체를 갖게 된다. 2n ― 1 핵은 무작위로 하나씩 염색체를 잃게 되어 반수체 상태로 되려는 경향이 있다. 따라서, 결과적으 로 생긴 반수체 핵은 그 생물의 염색체와 상동인 임의 염색체 무작위로 조각을 갖게 된다. 이 과정이 그림 3 .1 7 에 나와 있다. 그러므로 준유성생식 과정의 주내용은 이핵체의 형성, 영양 핵융합과 재 조합체를 형성하는 유사분열의 교차나 반수체화라 할 수 있다. 실질적으로 이러한 과정의 발생과 검출은 영양요구성 유권자 표지를 이용함으로써 증 전시킬 수 있다. 교차한 양천은 다른 요구를 나타내게 되며 최소배지에서 쟈斗게 된다. 영양요구주는 전 배지로부터 증식에 필요한 성분을 지니고
 @2n=2 인 배수 영5색분체 S방추사 이5상적 분리
@2n=2 인 배수 영5색분체 S방추사 이5상적 분리
오기 때문에 매우 미미하게 자란다. 그러나 이핵체가 생기면 두 양친 사이 의 상호연계에 의해 빠르게 증식한다. 반수체 형성, 이형 다핵체에서의 영 양 핵융합의 빈도는 장뇌 (cam p hor) 나 자의선으로 처리함으로써 증가하며 유사분열 분리는 X 선, nit ro g en musta r d, p-flur op he ny la lanin e , 자의 선을 이용하면 증가한다 (Sermon ti, 1969). 산업적으로 중요한 전균에 대한 준유성적 생활환의 적용은 몇 가지 문 제가 있다 (Elander, 1980). 원하는 생산물의 합성에 있어서 이형 다핵체 의 선별을 위해 이용되는 영양요구성 표지의 영향이 주된 문제이다. 앞에 서 언급되었듯이 영향요구성 돌연변이는 이차대사산물 생산에 바람직스럽 지 못한 결과를 초래함이 관찰되었다. 분자포자의 색표지 (marker) 조차도 생산물 합성에 감소 효과를 보였다 (Elander, 1980). 적당한 표지가 이용 될 때라도 몇몇 산업적 진균의 이형 다핵체의 유도는 어려운 과정이며 특 수화된 기술이 이형 다핵체 형성의 확률을 증가시키도록 개발되어졌다. MacDonald 와 Hol t (1976) 는 이러한 기술에 대해 논한 바 있다. 이형 다 핵체 형성의 어려움을 줄이는 방법이 원형질체 융합인데 이 기술은 뒤에 서 설명하겠다. 소법적 전균에서 이형 핵접합체를 유도하기는 어려우나, 이러한 미생물
울 연구하는 데 두 가지 방법이 이용되어왔다. 생산성이 우량한 재 조 합체 를 분리하기 위해서뿐만 아니라 생산균주의 유전학 을 연구하기 위해 준유 성생식 과정이 이용될 수가 있는데 이 준유성생식 과정을 이용하여 생산 균의 기초유전학에 대해 얻어진 정보로는 염색체 수(또는 연관군), 특별한 염색체에 대해 생산물 합성에서의 중요한 유전자의 좌위, 염색체상의 중요 유전자의 지도작성 등이 포함된다. 페니실린 생산균주의 준유성적 생활환에 대한 연구는 페니실린 생성의 유전학에 대한 여러 정보를 제공하였다. 페니실린 생성균주인 P. chry - so g enum 과 A. nid u lanS i= 유전학적으로 잘 연구되어 페니실린의 생합성 연구에 대한 기준체계로 이용되어왔다. P. ch ry so g enum 에 대한 연구에서 MacDonald(1965) 등은 이 곰왕기가 筑 내지 4 개의 염색체를 갖는다고 보고하였고 Ball (1 973) 은 이 미생물에는 최소한 양 n 의 연관군이 있음을 입증하였다. Holt( 19 76) 등은 페니실린 비생성성 P. chry so g enum 의 돌연 변이주를 연구하여 페니실린 생성에 악영향을 주는 5 개의 유전자가 있으 며 그중 4 개는 한 염색체상에 존재함을 입증하였다. 유전적으로 더 잘 알 ’ 려진 A. n i dulans 에 대한 연구 결과, 페니실린 수율 증가를 암호화하는 3 유전자의 염색체상의 좌위를 밝혔으며 유성교차를 이용하여 이러한 유전자 지도를 작성하는 데 중요한 발전이 이루어졌다. 준유성생석 과정을 이용해 서 얻은 다른 중요 정보로는, 보다 많은 페니실린 생산에 관련된 몇몇 돌 연변이는 P. ch ry so g enum 에서 열성이라는 것인데 MacDonald 와 Holt (1976) 는 몇몇 우성돌연변이를 포함한 A. n i dulan Si.곤 페니실린 생산성이 높다는 사실을 제시하였다. 이러한 기초유전학 연구는 연구된 돌연변이의 생화학적 발현이 발견되고 유전학적 연구가 상세한 생화학적 연구와 연관 해서 행해져야만 비로소 전면적인 혜택이 성취되어진다는 것을 기억해야 한다. 우량균주의 육종에 준유성생식 과정을 응용해서 페니실린 생산 향상에 어느 정도 성공을 거두었다. Q ueener 와 Swartz ( 1979) 에 따르면 페니실 린 생성 우량균주를 육종하는 데 아래 세 요인이 크게 호제로 작용하였다.
1. 고수율로 미생물을 육종하기 위한 준 유성생식 과정 을 응용하는 미국 특 허 (Pon t ecorv 짝 Rop e r, 1958) 가 1975년 정월에 그 효력이 만료되었다 . 2. 최근에 와서는 돌연변이와 선별기술에 의한 페니실린의 수율을 증가시키 기가 더욱 어려워지고 있다. 3. Panlabs 사와 같은 회사는 페니실린 생산에 사용되는 P.chry so g en um 균주 를 수요자를 위해 만들어왔다. 그러므로 생산회사에 의해 사용되었던 균 주와는 다른 균주가 육종연구에 이용될 수 있게 되었다. 표 3.2는 유전적재조합이 이루어전 산업적 균주들을 보여준다. 다른 계 통을 지닌 모균주들로부터의 이형접합형 이배체들 (he t eroz yg o ti c dip - lo i ds) 이 우량 페니실린 생산균주를 육종하기 위한 시도에 사용되었는데 이배체 균주와 그들의 분리개체들 (se g reg an t s) 에 의해 생성된 페니실린의 양은 모균체의 생성량보다 그리 높지 않았다• 오직 반수체의 재조합체를 사용했을 때에만 항생물질 생산에 개량된 안정한 균주가 분리되었다.
표 3.2 재조합이 발견된 항생물질을 생산하는 진균류 균주 항생물질 재조합형 Aspe r gi llu s nid u lans Penic l li n G sexual, par asexual Cep h alospo riu m Cep h alosp o rin C pa rasexual acremoniu m Penic il lin N Emt er ic e llop si s Cep h alosp o rin C sexual, par asexual salmosyn n emata Penic i l lin N sexual Emeric e llop si s Cep h alosp o rin C ter rico la var. gla bra Penic illin G. 0. V pa rasexual Penic ll iu m chry so g en um Gris e ofu lv in Penic il l i u m patul um Patu l i n pa rasexual (Hop w ood arid Merric k , 1977)
4.2 방선균에서의 재조합 방법의 이용(t he ap plica ti on of recombi- nati on sys t e m in the acti no my ce te s ) 방선균 (ac ti nom y ce t es) 은 많은 종류의 항생물질 생산에 쓰이고 있는데 종전에는 균주개발에 있어서 돌연변이주의 유도와 단일집락 선별이 주로 사용되어왔다. 그러나 불완전 진균의 경우에서와 같이 재조합 기술이 우량 균주 육종에 가능케 되고 있다. Ho p wood 는 방선균의 산업적 균주 육종 에 세포융합을 이용하는 방법을 고려하였고, 발표 제한되고 있는 회사에서 도 이 기술의 성공적인 사례가 언급되고 있다. 접합 (conj u ga ti on) 은 한 세균세포에서 다른 세균세포로 세포간의 접촉 •. 울 통해 염색체 물질의 전달을 의미하는데 접합으로 생긴 집합체 (zyg o te ) 는 한 모균주로부터의 완전한 환상염색체와 다른 모균주 염색체 단편을 갖게 된다. 염색체 단편이 교차방법에 의해 환상의 염색체에 삽입되어 재 조합 염색체, 즉 다른 두 세포로부터 온 유전 정보를 갖는 염색체를 형성 한다. 접합은 드물게 일어나므로. 재조합체를 분리해내기 위해서는 양천세 포를 능가하는 재조합체 선별기술을 개발해야 한다. 이러한 이점은 양천에 다른 영양요구성 표지를 유도하여 부여시키고 최소배지에서 요구성을 확인 함으로써 얻을 수 있다. 이러한 방법으로 분리된 재조합체는 생성된 모든 재조합체를 모두 포함하고 있지는 않다. 그 이유는 양쪽 야생형 대립인자 를 모두 갖지 않은 재조합체는 선별되지 않기 때문이다. 그러므로 더욱 선 명한 재조합체를 얻기 위해서는 여러 다른 유전자표지의 재조합을 이용하 는것이 바람직하다. 접합은 ac ti nom y ce t es 에서 유전적 교환의 가장 보편적 형태인데(표 3. 3) 평균적으로 게놈의 5 여손의 l 이 수용세포로 전달되며 재조합의 빈도는 10 내 ~1 硏 정도이다. 성인자들이 세 str e p tom y ce te s (S. reti cu li, S. rim - osus, 그리고 S. coel i color) 에서 접합에 관여한다는 것이 밝혀졌다• 가장 잘 알려진 방선균인 S. coelic o lor fu <2) 에서 두 플라스미드가 알려져 있다. 이들은 메틸레노마이신 (me t h y lenom yci n) 합성에 관여하는 유전자들을
지니고 있는 분자량이 약 lOO x lO 떡 Sc p l 과 분자량이 약 18~ 20 x 10 6 의 Sc p 2 이며, 돌연변이형 Scp 2* 는 더 큰 재조합 빈도를 나타낸다.
표 3.3 Ac ti nom y ce t es 에서의 재조합 Str ep l o my ce s spp . S. coelic o lor (Acti no rhodin , Meth y le nomy c in ) S. achromog en es var. rubradir i s (Rubradir i n ) S. acrim y c in i S. aureofa c ie n s (Chlorte t r a cy cl in e ) S. bik i n i e n sis ( Zorbamy c in , Zorbonomy c in ) S. ery thr eus (Ery thr omy c in ) S. frad ia e (Neomy ci n ) S. gla ucescens S. gri s o fl av us S. grise us (St re p tom y ci n ) S. oliv a _ce u s S. r i mos 싹 (Oxy tet r a cy c li ne ) S. scabie s S. venezuelae ( Chloramp he ni c ol ) Nocardia spp . N. ery thr op o lis N. medit e r ranei (Rif am y cin) Mi cro monospo ra sp p. M. chalcea M. echin o spo ra M. pu rp u rea ( Genta m i ci n ) My c obacte r iu m smegm a ti s 1hermoacti no my c es vulga r is 생산되는 항체는 괄호속에 표시하였다. Thermoac ti nom y ces 에서 형질전환은 유전자 교환이 필수적이다. 다른 경우에는 접합 기작이 발견되지만 수정 인자 (fert i lity fa c t or) 는 대개 발견되지 않았다 .(Elander et al., 1977)
위의 기술로 분리한 재조합체는 생산성 증가에 대해서 조사하게 된다. 선조균주간 교배로 대립인자의 새로운 조합이 일어나고 결손돌연변이를 제 거하게 된다. 풀라스미드는 여러 방선균 항생물질의 합성에 관여한다는 것이 입증되 고 있다. 0kanash i (1979) 는 aureoth r ic i n , cep h amy ci n , chloramp he - nico l, holomy ci n , kanamy ci n , kasug am y ci n , meth y le nomy ci n A, oxy tet r a cy cl in e , pu romy ci n , str e p tom y ci n , tun im y ci n 생산에 풀라스 미드가 관여한다는 연구내용을 인용하고 있다. S. coel i colo 데서도 met- hyl e nomy ci n A 의 합성 에 관한 여러 구조 유전자가 풀라스미드에서 유래 된 것이라는 강력한 증거가 있다. 다른 항생물질의 합성에 풀라스미드가 관여하고 있디는 것은 그 합성의 조절이나 항생물질 생산균 자신의 항생 물질에 대한 내성에서도 추정된다. Cha t er(1979) 는 항생물질에 내성을 부여하는 풀라스미드의 소실이 항생물질을 합성하는 능력의 소실을 초래한 다는 몇 가지 예를 들고 있다. 방선균 항생물질 생성에 플리스미드가 관여하고 있다는 것은 풀라스미 드 조작에 의한 수율 증가의 방법을 예측하게 하는 것이다. 따라서 항생물 질의 합성능을 원래의 균주보다 산업적 생산에 더욱 안정한 균주에 전달 하는 가능성을 제시하고 있는 것이다. 항생물질의 합성 경로를 암호하고 있는 유전자의 복사체 수를 증가시킴으로써 모든 유전자가 증폭되어야 얻 어지기 때문에 매우 어려운 일이다. 4.3 원형질체 융합기술의 이용(t he ap plica ti on of pro to p la st fus - ion tec hn iqu es ) 원형질체는 세포벽이 없는 세포로서 고장액에서 세포벽을 분해하는 효 소를 작용시켜 얻을 수 있고 세균세포벽 분해에는 라이소자임 {lyso zym e ) 이 사용되고 균류에는 chit ina se 또는 cellulase7} 병용해서 사용된다. 세 포벽을 재생시키면 다시 정상세포로 증식할 수 있다• 융합하지 않는 균주
둘의 원형질체간의 세포융합 후 핵융합이 일어나고 결과로 융합된 원형 질 체는 세포벽을 합성하여 보통 세포로 증식한다. 원형 질 체 융합은 Str - ept om y ce s 속, Bacil lu s 속, 사싱균, 효모에서 증명되고 있다. 원형질체 융합은 다음 목적에 이용될 수 있다. 1. 유성생식 또는 준유성생식계들이 결핍되었거나 재조합 빈도가 너무 낮 은 균주들의 종내 재조합(i n t ras p ec ifi c recombin a ti on ). 2. 수식된 대사물질들을 생산할 수 있는 새로운 균주를 얻기 위한 종 간 잡종 (int e r sp ec if ic hy b rid i z a ti on ) 형성 . 3. DNA 클로닝 실험들 (DAN clonin g ex p er i men t s) 에 있어서 원형 질 체 형질전환(p ro t o p las t t rans fo rma ti on) 이나 트랜스펙션 (t rans fecti on) 의 시도. 원형질체 융합에 의한 사상균에서의 재조합 빈도는 영양요구성 표지를 유도하는 데 필요한 빈도와 바 슷 하다. 전균의 원형질체 융합은 종전 기술 로는 불가능했던 균주간의 이형 이핵체를 얻는 데 매우 좋은 방법이다. 이 상황은 P. chry so g enum 과 P. cya neofu lv um 사이의 이형 이핵세포를 얻는 데 성공하고 P. f luorop hen y lalan i n 러나 benomy l 처리 후 재조합체를 만 든 이배체 형성을 입증한 Peberdy (1 979) 등의 업적에 의해 설명된다 . 진균의 원형질체 융합기술 사용에 대한 입증은 ce p halos p or i n 을 생산하 는 C. acremon i um 에 관한 Haml y n 과 Ball(1979) 의 연구에 의해서도 제 시되고 있다. 이러한 연구들은 C. acremoniu m 균주들 사이의 핵융합을 얻 는 방법의 효율성을 원형질체 융합기술과 비교하고 있다. 융합된 원형질체 의 전자현미경적 실험에 의하면 1% 정도가 즉시 핵융합을 함을 지적하고 있다. Chan g (l982) 은 Penic i ll i u m ch rysog enu 짜긱 두 균주의 바람직한 성 질을 원형질체 융합을 이용하여 결합시킬 수 있었고, 집락 형태와 페니실 린 V를 생산하는 능력이 다론 두 균주로부터 원형질체를 융합시켜 100 개 의 안정된 집락 중에서 둘이 원하는 모양과 높은 페니실린 V 생산성을 나 타내었다.
산업적 방선균에서도 접합방법보다 원형 질체 융합방법이 특히 유용하며 원형질체 융합기술에서는 재조합에 전체 게놈의 참여가 더욱 그러하다. 또 한 Ho pwood(1979) 는 Str ep tom y ce s coelic o lor 원형질체의 융합 생성체로 부터의 매우 높은 재조합의 분리 기술을 발전시켰다. 원형질체를 자의선에 쬐어 융합 전에 99% 를 사멸시켰다. 낮은 재조합률 (1% )을 보이는 균주에 서 재조합이 1()II ~ 증가했고 교배에 대해 재조합 빈도가 배가 되어 20% 의 재조합체를 냈다고 주장했다. 산업적 균주에 이러한 재조합체의 수율이 가 능하다면 이 기술은 매우 가치 있는 것으로, 원형질체 융합체를 영양요구 성 표지 이용과 무작위 비율로 검색함으로써 재조합체를 선발할 수 있다. 원형질체 융합방법을 통한 종내재조합(i n t ras p ec ifi c recombin a ti on ) 은 Bacill u s 속과 같은 정합계를 갖지 못한 균주에서 널리 적용될 수 있고 그람음성균에서도 가능하다. 특히 유전자 교환에 성인자를 필요로 하지 않 으며 DNA 단편보다 게놈 전체의 전달, 통합이 가능하다. 종간잡종(i n t ers p ec ifi c h y br idi za ti on) 은 새롭거나 변형된 대사산물을 창조하기 위해서 생체내 조건에서 다른 두 종으로부터의 유전 정보의 결 합을 가져온다. 이 목적을 위한 원형질체 융합을 사용해서 여러 항생물질 생산균들에 시험되었다. 다음은 성공한 예들이다. Aspe rgi llu s nid u lans X A. rug ul osus ; A. nid u lans X A. fum i ga tu s ; Penic il l i u m chry so g en um X P. cya neofu l uum ; P. cya neofu l uum X P. cit- nin u m ; Saccharomy ce s cereuis ia e X S. dia s ta t i cu s ; Candid a trop i ca lis X S. fibu lig e ra. 이러한 경우에서 이형 다핵체가 형성되었고 유전적 재조합 이 이루어졌는데 s t rep t omy ce t e 려 종간교잠에서도 유사한 결과를 나타낸 다. 실패할 경우는 제한계와 변경계 (restr i c t i on and modif ica ti on sys - t ern) 의 작용과 생리적 불화합성 (ph ys i o l og ica l i ncom p a ti b ility)과 같은 게놈 비상동성 (ge nome nonhomolog y) 때문인 것으로 추정된다.
4.4 유전자 조작 기술의 이용(t he ap plica ti on of ge neti c manip u -lati on tec hniq u es ) 최근 in viv o 9 t in vit ro 기술을 이용하여 세균의 이종간 DNA 의 전 달이 가능해지고 있다. 즉 한 종에서 유래된 유전물질을 다른 종에 삽입시 키고 발현시킬 수 있게 된 것이다. In viv o 기술은 파지를 이용하여 한 세균의 염색체로부터 유전 정보를 취해 디른 세균에 감염함으로써 첫 숙주의 유전 정보를 전달하게 되고 두 번째 숙주에서 발현하게 된다. 풀리스미드는 넓은 범위의 그람(g ram) 음성 균 샤기에 이동하여 유용하지만, in viv o 기술이 벡터 (ve ct or) 가 한 세포 에서 유전 정보를 모아 다른 세포에 정보를 삽입하는 데 비해 in vit ro 기술은 인위적으로」 벡터에 유전 정보를 삽입시켜 carr i er 와 〈외래 ext ra > DNA를 수용세포에 삽입시킨다. 즉 DNA7} in vit ro 방법에 의해 벡터 에 삽입되기 때문에 DNA 원은 벡터의 숙주 생물에 제한되지 않는다. Ath e rto n (1 9 79) 등은 in vit ro 유전자 전달에 기본적으로 필요한 요건과 숙주세균에서 의래 DNA 의 발현에 필요한 것을 다음과 같이 열거하였다. 1. 숙주세포에 들어가 그 안에서 복제할 수 있는 〈벡터〉 DNA 분자. 벡터는 작고 준비가 쉽고 용이하여야 하며, 의래 DNA 의 삽입에 의해 필요 기능 이 파괴되지 않는 부위를 최소한 한 개는 포함해야 한다. 2. 벡터에 의래 유전정보를 절단하는 방법. 3. 벡터 /의래 DNA 재조합체를 숙주세포에 도입하고 선별히는 방법 . 주로 사용되는 성질은 약품내성, 면역, pla qu e 형성을 포함하며 삽입된 유전자 의 영양요구성 등이다. 4. 생성된 재조합체 집단으로부터 의래 유전자 산물을 분석하는 방법 . Old 와 Pr i mrose(1981) 는 세균에 새 유전물질을 도입하는 데 사용되는 벡터의 범위를 그의 저서에서 논하고 있다. 벡터로서는 대표적으로 풀라스
미드를 이용하는 방법과 파지를 이용하는 방법이 있어 그 특징을 여기에 서 설명하기로하겠다. (1) 플라스미드(p lasm i ds) 의 이용 풀라스미드는 환상으로서 염색체 의적인 자체 복제 DNA 분자인데(ci r- cular, ext ra chromosomal, self~r e p li c a ti ng DNA molecules) 분자량은 1.5 X 106~200 X 106 정도이다. 큰 풀라스미드와 작은 풀라스미드는 성질 이 다르며 큰 풀라스미드는 평균 65 x l06 의 분자량을 가지며 세균의 염색 체당 1~2 복사체 (co pi es) 를 갖고 집합시 전달될 수가 있다. 작은 플리스. 미드들은 약 5OOOJ 의 분자량과 세균의 염색체당 1()7 ~ 이상의 복사체를 지 · 니며 보통 전달성이 아니다. 플리스미드들은 다양한 세포기능을 수행하기 위한 암호를 지니고 있는데 디음과 같다. 1. 수정능력 (fer ti lit y ) : 접합을 통한 유전물질의 전달능력. 2. 항생물질 저항성 (anti bi o t i c resis t a n ce) : 하나 이상의 항생물질에 대한 저항성. 3. 중급속들에 대한 저항성 : Cd2+, Hg 2+ 4. 자의선에 대한 저항성. 5. 박테리오신 (bac t er i oc i ns) 의 생산 : 동종의 세포들을 억제 또는 죽일 수 있는물질생산. 6. 항생물질의 생산 : 특히 메틸레노마이신 (me t h y lenom y c i n) 과 클로람페니 콜 (chloram p hen i co l) 합성을 위한 암호를 지닌다. 7. 비정상적 탄소원의 이용 : 예를 들면 Pseudomonas 에 의한 장뇌 (cam- ph or), 옥탄 (Oc t ane) 과 Oc t anol의 분해• 8. 독성물질과 표면항원 (sur fa ce an tig en) 의 형성 : 예, 엔테로독신 (en t e rot ox i n) , 헤모라이신 (hemolys i n ) . 9. 식물체에서의 악성종양 유도(t umor ind ucti on ) : A gr obac t er i u 짜키 Tip- las mi d에 의한 크라운 골 종양 (crown gal l tum ors) 형성. 10. S tr ep t om y ce t e 쩌]서 포자의 형성에 관여.
풀라스미드는 세포의 유전물질에 의부 유전자 들을 첨가시킬 수 있다. 만 일 세균의 염색체에 이러한 의부 유전자의 상동영역 (homolog o us area) 이 없다면 교차중에 교환될 수는 없지만 플리 스 미드가 복제하는 동안은 유지될 수 있다. 산업균주 개발을 위해 이미 유전적 정보를 지니고 있는 자연 플라스미드를 사용할 수 있다. 또는 유전공학적 기술로 적절한 유전 자를 모아 새로운 플러스미드를 구축하는 데 사용할 수도 있다. 자연적으 로 발생하는 플라스미드가 사용되는 예는 Pseudomona~ 노 균주 (P . pu ti da , P. oleovorans 등)에서 찾아볼 수 있다 . 이들 플리스미드는 어떤 탄수화물 의 분해에서 각 단계를 수행하기 위한 암호를 지니고 있다(표 3.4 ). 서로 유사하나 함께 세포내에 안정하게 공존할 수 없는 두 풀라스미드를 비화 합성 (i ncom p a ti ble) 이라 하는데 여기에 적힌 대부분의 풀라스미드는 화 합성 (com p a ti ble) 이고 그럼으로써 다른 균주들의 분해대사능력 (cata - boli c ab i l ity)을 한 균주로 모아 조합할 수 있다. 한 Pseudomonas 종의 4 개의 디른 균주들로부터의 풀라스미드 정보가 함께 재조합된 예가 알려져 있고 그 균주는 수면에 유출된 기름(i l sp ills ) 분해에 사용하기 위해 육 종된 것이다.
표 3.4 Pseudomonas £1 cata b olic pla smi ds Plasm id Substa n ce Transfe r abil li t y Molecular deg rad ed Weig h t ( X l04 ) NAH Naph th a lene Conju g at i ve Not dete r m ine d SAL Salic y lic acid Conju g at i ve 40, 55 CAM Camp h or Conju g at i ve 150 OCT n-O c ta n e Not conju g at i ve Not dete r mi ne d XYL p-o r m-xy le ne Not conju g at i ve 10 TOL Toluene Conju g at i ve 75 (Chakrabarty , 1976)
여러 항생물질을 생산하는 s t rep t omy ce t e 쩌1 서 몇 가지 조철유전자들, 또
는 구조유전자가 풀리 스미 드에 위치한다는 증거도 있다(표 3.5 ). 풀라스미 드가 존재한다는 증거로서 acrid in e orang e, acrif lav in , eth idi u m bro- mide 또는 고온도 처리를 하면 특정 플라스미드가 제거된다는 cur i n g실 험에 근본적인 기반을 두고 있는데 처리 후 풀라스미드가 세포로부터 제 거된다는 것은 물리적 방법으로 알 수 있고 항생제 생산능력이 동시에 소 실된다. 그러나 풀라스미드에 영향을 주는 큐어링 약제 (cu i n g ag en t s) 는 염색체 DNA 에도 손상(결실, 염색체 절단 등)을 유발할 수 있으므로 이 방법에 의한 풀라스미드 관련여부의 증거를 제시하는 것은 불완전하다는 것을 기억해야한다.
표 3.5 S t re pt om y ce t es 에서 항생물질을 생산하는 데 관여하는 pla smi ds Mi cr oorga n is m Ant ibi o t i c Curin g Ag en t Plasmi d Prop er ti es, Molecular weig h t S. coelic o lor Meth y le nomy ci n UV ~100x 106 SCPl, Ferti lity factor S. rim osus Oxy tet r a cyc l in e AO, AF, PF S. bik i n ien sis Str e p tom y ci n AF, EB S. reti c u li Leucomy ci n EB 48Xl04 S. frad ia e Neomy ci n AO 55Xl06 (DOS syn th e sis ) S. rim osus subsp. Paromomy ci n AO pa romomy ci n u s S. hyg ro scop icu s Turim y ci n AO S. clauulig e rus Holomy ci n UV S. uenezuelae Chloramp h en ico l AF,T S. kasuga e nsis Kasug am y cin AF,T S. kasug a ensis _ Aureoth r ic i n AF,T 18Xl04 S. gri se us Str e p tom y cin AF ~30xl06 S. Kannamy ce ti cu s Kanamy ci n AF, AO, EB ~6.7x106 pS K:14X106
(DO S syn th e sis ) S. anti b1 0llcus Ac tino my ci n EB S. pa rvulu.s Acti no my ci n AF, NOV ll.2 X l06 pS LA2 S. Sp . 7434- A N Lankacid i n EB S. rib o sid i f icu s Rib o sta m y ci n AF 56xl01 pS RI S. ambofa c ie n s Sp ira my ci n AF AO 아크리딘 오렌지 ; AF 아크리플라빈 ; RF 프로풀라빈 : EB 에티디움 브로마이드 : T 증가된 온도 : NOV 노보바이오신 : UV 자외선 ; DOS 2- 디옥시스트랩트아민 (Chate r , 1978:Hop w ood, 1979, wit h addit ion s)
풀러스미드-암호화된 효소(p lasm i d -c oded enz y mes) 가 어떤 다단계 (mul ti-st a g e) 생합성 경로에서 속도제한 (ra t e lim i ting ) 요인이라면 염색 체당 플러스미드 복사체의 수를 증가시킴으로써 생산량 증가를 기대할 수 있을 것이다. 그래서 산업균주 개발에서 폴라스미드의 무비판적 사용은 성 공적이지 못할 것 같다. 더 기대할 수 있는 것은 유전공학에서 외래 유전 자 운반체, 죽 벡터 (ve ct or) 로 플라스미드를 사용하는 것이다. (2) 유전자공학의 방법 유전자공학(i n vit ro 재조합, 유전자 클로닝 혹은 유전자 조작)은 원핵 생물 혹은 진핵생물의 DNA 서열을 숙주생물에 넣어 클론화시키는 과정 인데 DNA 삽입은 형질전환성의 원형질체 혹은 CaCh 처리를 통해 com- p e t en t하게 만들어진 세포 (E. col 떠- 같은)에서 가능하다. 전달용 운반체 (vecto r )로서 플라스미드, • 용원성 파지, 혹은 코스미드 (cos mi d) 가 사용된다. 코스미드는 A 파지의 cos 부분을 포함하는 풀라스미 드인데 이러한 코스미드는 긴 염기서열의 의래 DNA 를 포함할 수 있는 것으로 세균성 파지 입지에 싸여 수용체인 E. col i내로 이동한다. 플리스. 미드가 가장 보편적인 운반체로서 이용되고 있는데, 가장 적당한 것은 특 정 제한효소 (res t r i c ti on endonuclease) 에 대해 하나의 인식부위 (recog ni- tion sit e) 만을 가지고 있는 작은 플러스미드이다. R fac to r s 의에도
Co!El 번이체가 종종 이용되는데 그 이유는 Chloram p hen i col 의 존재시에 도 증식하고 1,000 개 이상의 복사수의 풀라스미드를 가전 세포를 얻을 수 있기 때문이다. 이런 형의 세포는 염기서열 분석용 DNA 분리에 특히 유 용하다. 제한효소 (res tr i c ti on endonuclease) 는 DNA 를 절단하는 데 이용된다. 이러한 효소는 특별한 제한과 구조, 변형방법에 쓰이며 세포가 외래 DN A£부터 그 자신을 보호하려 할 때 원래 이용된 것이다. 제한효소.는 특정부위에서 보통 팔린드롬(p al i ndrome) 구조의 길이 4~11 누쿨레오티 드 부위에서 DNA 이중나선을 끊어낸다. 이들 효소에 따라 이중나선의 무딘 (blun t) 말단이나 짧고 접착성이 있는 단일 가닥의 접착성 (s ti ck y) 말단이 만들어전다. ( XanXth mo maIo nas ) CCCLG GG ( SerraStmi a a I CJC CGGG malvucearum GGGfC CC marcescens ) GGGCCfC 500 개 이상의 제한효소가 알려져 있고 그 수는 해마다 증가하고 있다. 의래 DNA 의 도입 (inc orpo rati on of for eig n DNA) 은 무딘 말단인가 접착성 말단의 단편인가에 따라 다르게 행해전다. 무딘 말단 단편의 경우 5 '말 단이 )L -e xonucleas 쵸: 분해하여 3'말 단을 ATPL 十 TTP로 서 말단 전 달효소(t erm i nal t rans fe rase) 의 작용으로 연장시킨다. 이러한 방법으로 말단의 p ol y -A나 pol y- T 배열이 생기게 된다. Poly- A 배열을 가전 한 사 슬이 po ly- T 배열을 가전 디른 사슬과 결합하여 잡종 플라스미드와 같은 환상구조를 이룬다. 접착성 말단의 경우 어떤 기원의 DNA 단편이든 동 일한 제한효소를 사용하는 이상 말단은 서로 결합하여 환상구조를 이룬다. 재조합된 DNA의 생성과정이 그립 3.21 에서 설명되고 있다. 클로닝에 적당한 DNA 획득 (ob t a ini n g DNA su itab le for clon ing )
: 적당한 DNA 서열을 선택하기 위해서 몇 가지 방법이 이용되고 있다.
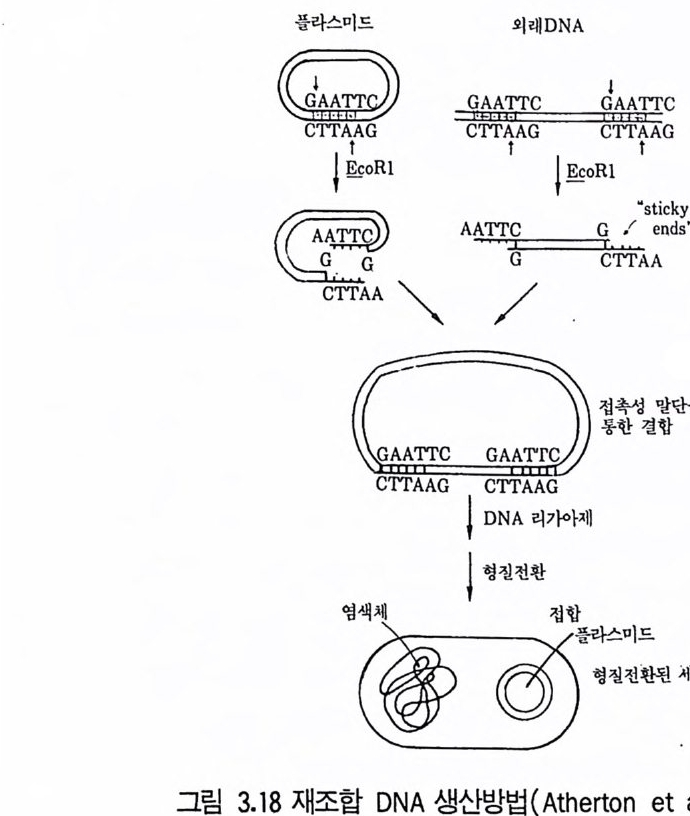 C‘풀 라G C스jT D T!lg A드!oA! R I \ AA/~ 의 래 DlN 回A oRGC1 T /T AsAet in cd k sy
C‘풀 라G C스jT D T!lg A드!oA! R I \ AA/~ 의 래 DlN 回A oRGC1 T /T AsAet in cd k sy
mone) 인 소마토스타틴 (soma t os t a ti n) 과 인슐린(i nsul i n) 의 A 와 B 사슬 의 유전자에 대한 인공유전자 합성에 쓰여졌고 이들 유전자가 대장균에서 클론화되었다. 또 달리 광범위하게 이용되는 방법은 상보적 DNA(cDNA) 의 생산인 데 한정된 mRNA( 풍부한 mRNA 를 가진 세포나 조직으로부터 )에서 역 전사효소 (reverse t ranscr ipt ase) 러는 효소를 이용하여 상보적인 DNA (cDNA) 로 전사된다. 이 방법은 E. col i에 쥐의 인슐린 유전자를 클로닝 하는데 쓰여졌는데 그 내용은 그림 3.19 oJ] 설명되어 있다.
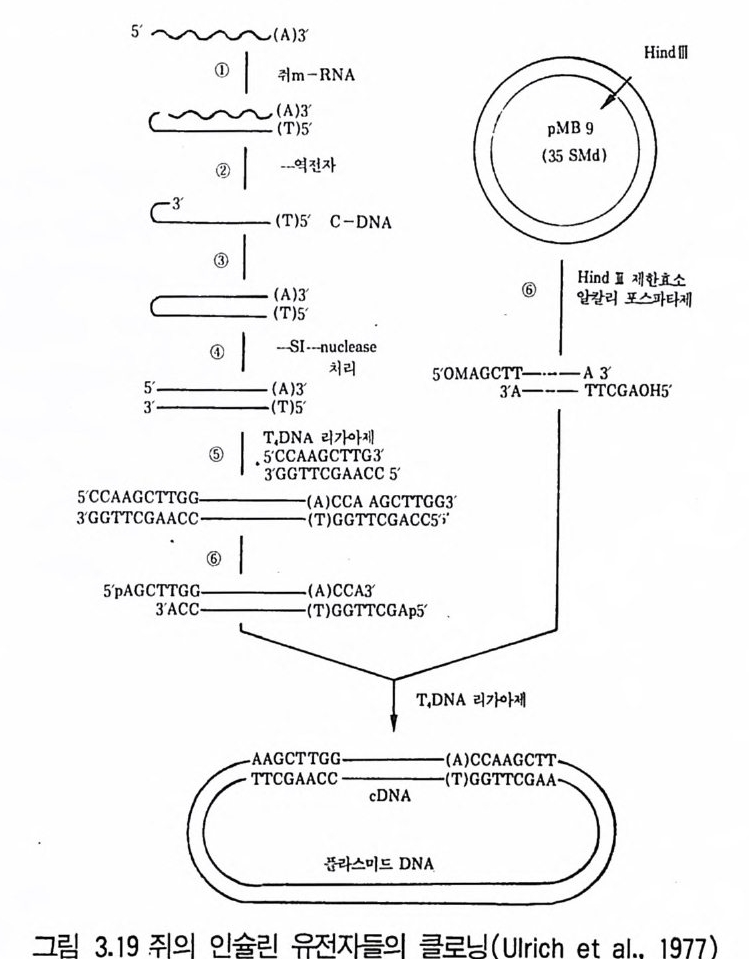 S' ~ (A)3'
S' ~ (A)3'
1. mRNA7} 쥐의 인 슐린 생성종양으로부터 분리되어 역전사효소에 의해서 cDNA .£ 전사된다. 동시에 역 전사효소 가 이 중가닥을 완성시키기 위한 개 시물질(p r i mer) 로 쓰이는 머리핀 구 조 (구부러진 부분 ) 를 생성한다. 2. RNA7} 알칼리 처리에 의해서 mRNA-cDNA 잡종 분자로부터 제거 된다 . 3. 단일가닥으로 된 cDNA7} 역전사효소에 의해 이중가닥으로 된다. 4. 머리핀 구조의 구부러진 부분이 S1 - mucleas 려 의해서 분해된다. 5. 제한 엔도뉴클레아제 Hin d III 가 인지하는 서열 을 포 함하고 있는 화학적으 로 합성된 뉴클레오티드 서열을 cDNA 의 양끝에 T 』 lig as 쵸i 연결한다. 6. H i ndIII 의 작용으로 유사하게 처리된 풀러스미드에 붙을- 수 있는 접착성 말단을만든다. 재조합 DNA의 발현 (Ex p ress i on of recombin a nt DNA) : 숙주생물 에서의 의래 DNA 의 발현은 주로 방법에 좌우된다. E. col i에서는 원핵생 물 DNA는 전사되고 단백질로 발현된다. Bac i llu 쩌]서 Bacil lu s 유전자의 클로닝은 어려움이 없이 행해지지만 Bacil lu s sub ti l i쩌]서 E. coli 유전자 의 발현은 성취되기 어렵다. E. col i에서의 Saccharomy ce s cereuis ia e 혹은 Neurospo ra crass 러 같은 하등한 진핵생물의 유전자 발현은 성공적으로. 이루어져왔지만 보다 복잡한 진핵생물의 경우에는 DNA 전사와 번역이 정확히 일어나지 않는다. 이러한 어려움은 적당한 조절신호를 가지고 있는 원핵생물의 유전자에 진핵생물의 유전자를 도입시킴으로써 극복될 수 있 고, 따라서 진핵생물의 DNA 발현이 가능하게 된다. 예로서 소마토스타틴 에서 처음으로- 성취되었는데, 이때 소마토스타틴 유전자가 플라스미드 pB R 322 에 위치한 lacto s e o p eron 에 도입되었으며 (그림 3.2 0 ) E. coli 세포에 의해 합성된 이 산물은 p-g alac t os i do -s oma t os t a tir:r이었다. 메티 오닌잔기에서 펩타이드를 끊는 cya n og en bromi de 처리에 의해 활성화 소마토스타틴이 in v it ro 에서 거대 단백질로부터 절단 분리되었다. 생성된 소마토스타틴의 수율은 플라스미드 복사수로부터 계산된 양의 1 0¾손의 1 이 지만 E. coli 발효의 간단함을 고려할 때 상대적으로 유리한 것이다 (100 g
의 E. coli 습균체량당 10m g의 소마토스타틴 단백질).
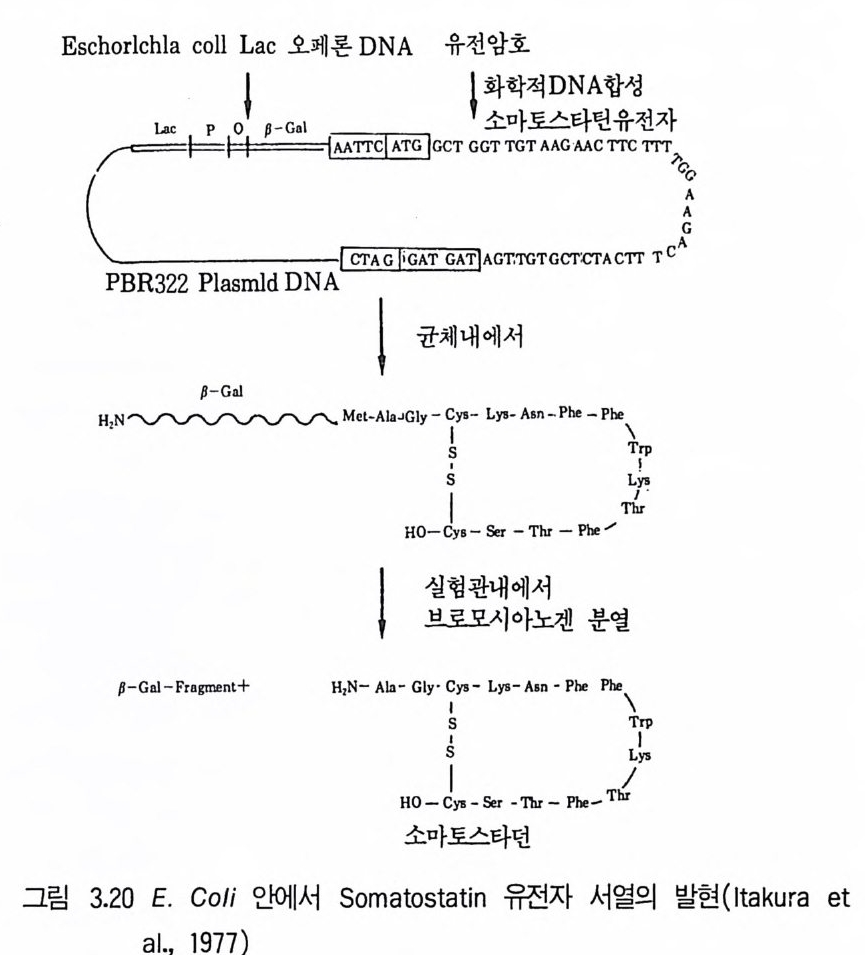 Es广chorlchla c一oll Lla c 오페三론 DNA GC유T전Gl 훑화암학호갑적 D已NA雲 합성뿐 %;
Es广chorlchla c一oll Lla c 오페三론 DNA GC유T전Gl 훑화암학호갑적 D已NA雲 합성뿐 %;
이와 같은 방법으로 인간의 인슐린 A와 B 사슬의 합성유전지를 pB R 32 껴 p-ga lacto s id a se 영역에 도입시켜 E. col i에서 각각 클론시켰다. 형 질전환된 세균이 각기 A 와 B 사슬을 합성하였고 두 가지 화합물을 혼합 시켜 활성화 인슐린이 개발되어 현재 Eli L i ll y회사에 의해서 시판되고 있 다. 다른 인슐린 생산방법으로 E. coli x1776 을 사용하는 것이 있다. 프리
프로인슐린 (Prep ro i nsul i n)-mRNA 의 상보적 DNA 복사체를 플라스미드 pB R 32 썩 페니실리나제 (Pen ici l li n a se) 유전자내로 클론시키는 것이다. Pen ici ll i n a se(24-182) —(G lyh -P ro i nsul i n(4-86) 인 Pen ici l li n a se- pro in s ulin 복합체가 세균에서 생성되었고 그 합성율이 세포당 약 10 여만 자였다. E. col i의 Pe ni c i ll i nas~ 근 원래 세포의 단백질로 분비되기 때문에 복합체는 세포 밖으로 분바되었고 인슐린 C 사슬로부터 Pen ici ll i n a se 잔 기를 절단 분리함으로써 활성 인슐린으로 전환시킬 수 있다. 원핵생물에서 진핵생물의 DNA 발현에 관련된 어려움을 극복하기 위해 진핵성 생물을 재조합된 DNA 의 숙주세포로 이용할 수도 있다. 클로닝 체제가 개발된 효모들이 유전학적으로 잘 이해되고 있기 때문에 이러한 연구에 상대적으로 적당하다. 생체 의 재조합의 응용 : 유전자 조작 기술을 통해서 진핵생물 유전자의 조절기작 연구와 원핵생물과 진핵생물 유전자의 염기서열 결정에 상당한 진보가 있었다. 진핵생물에는 mRNA 로 전사되어지는 암호화된 유전자 (exon) 와 mRNA 에는 나타나지 않는 염기쌍으로 된 암호화되지 않은 부 분(i n t ron) 이 있다. In t ron 을 in v it ro 에서 제의시키는 기술은 아직 앞으 로의 과제로 남겨져 있기 때문에 이를 극복하기 위해서 in vit ro 유전자 조작에서는 mRNA를 분리하여 사용하여 기술을 개발하고 있다. 이렇게 하여 사람의 유전자 산물을 미생물세포에서 생산시킬 수 있게 되고, 잘 확 립된 발효생산의 기술을 확립하는 또 하나의 분야를 개척하게 된 것이다. 유전자 조작을 통한 실제적 응용 (Prac ti cal ap plica ti on s) : 가능 분야 를 열거해보면 다음과 같다. 1. 주로 얻기 어려운 단백질의 대량생산. 몇몇 포유동물의 미량 단백질을 정 제된 형태로 다량 얻을 수 있다. 이런 것들에는 인간의 인슐린, HGH( 인 간성장 호르몬), 소의 성장 호르몬, 인터페론 등이 있으며 혈전증 치료제 urakin a se, 그리고 치즈 제조의 rennin 등을 대표적인 것으로 둘 수 있 다.
2. 헤파티티스/}, 인플루엔자 등 백신의 생산이 가능하다 . 3. 혈액응고 인자와 다른 펩티드 호르몬의 생산이 가능하고 혈병을 녹이기 위한 TPA(ti ss ue pla smi no g en a cti va t or) 에 관한 연구가 성공되고 있 다. 4. 유전병에 있어서의 유전자 결손에 대한 이해와 그러한 병에 대한 치료의 개발로, 소실된 효소를 보충하는 것을 들 수 있다. 5. 단백질, 연료에탄올, 글리세롤, 에틸렌 옥사이드, 에틸렌 굴리콜과 같은 유 기화합물의 생산에 대한 석유 의존도가 높은 현실에 있어서 B i omass 로 부터 나오는 폐기산물로부터의 전환을 통해서 대체 가능성이 있다. 6. 단일클론 항체 (monoclonal an ti bod i es) 는 특별한 단백질, 혹은 다른 분 자에 매우 특이하게 결합하는 것으로 인간이나 동물의 hyb r id o ma 세포 에 의해 생산된다 (h y br i doma ·s 는 무한정적으로 복제된 m y eloma 세포와 항체를 형성하는 세포의 융합에 의해서 만들어진다). 단일클론 항체는 전 단연구와 단백질 혼합물로부터 한 단백질을 정제하는 데 사용되는 것으로 감염성 질병에 대한 광범위한 임상적 사용도 가능하다. 보다 저렴한 공정 을 개발하기 위해서 항체성분을 암호화하고 있는 포유동물 유전자가 대장 균에서 클론되고 유전자산물들의 화학적 조합에 의해서 기능적 항체가 된 다. 7. 식물재배에 있어 바이러스나 제초제에 대한 내성, 내영성, 식물단백질에서 의 필수 아미노산의 바율 증가, 야자기름으로부터의 생산량 증가와 같은 문제점에 관한 연구가 진행되고 있다. 토양 세균의 플라스미드를 이용한 질소 고정유전자 (n if)의 전이나 식물로의 nif-유전자의 직접적 전이를 통 해서 질소비료의 사용을 감소시킬 수도 있을 것이다. Agr o bacte ri u m tum - e fa c i en 루부터의 Ti 풀라스미드와 Caulifl ow er mosaic vir u s 2} 같은 DNA 식물 바이러스가 식물유전자 운반체로서의 유용성에 대한 집중적 연구가진행되고 있다. 8. 오염 조절을 위한 특별한 생물분해성 균주가 개발되고 있다. 9. 하나의 생물체내에서 다른 생합성 경로의 유전자들을 결합함으로써 항생 물질과 같은 새롭거나 변형된 생산물을 얻는 것. 10. 생산균주에 이화효소 cata b olic enz y mes 를 도입시켜 저렴하게 물질을 분해할 수 있는 발효과정의 개선.
11. 경제적 발효방법의 효율화로 공정 비용 감소( 예 : 세균에서의 짧은 발효 시간). 12. 일차대사산물의 유전자 조작에서는 유전자 양의 증 가 를 통한 수율 증가 . 13. 생합성의 속도 결정단계를 암호화하고 있는 유전자의 시 험관 내 돌 연변이. 어떤 균주에 있어서 효과적 클로닝 체제가 이미 확립되어 있는 반면에 다른 균주의 경우는 적당한 클로닝 체제가 아직 개발중이거나 불가능한 상태에 있다. Bacil lu s sub ti l i려 경우 세포내 독성물질을 생성하지 않는 비병원성 균주로서 산업적으로 - 광범위하게 이용되기 때문에 숙주생물로서 유망하다. 그래서 이러한 생물을 위한 플리스미드 벡터가 개발되고 있다. 플라스미드 벡터와 파지 벡터를 지닌 클로닝 체제가 S t re pt om y ce 퍼]서도 이용이 가능하며 , 원형질체 융합기술에 기초를 둔 형질전환 방법이 Sac- charomy ce s cereu i s i ae 에서도 확립되어 있다. 오늘날 곰팡이에서도 적당한 벡터가 개발중에 있다. 염색체의 DNA 가 두 종류의 식물병원성 곰팡이에서 발견되었다 (Fusar i um ox y sp oruw 斗 Rhi- zocto n ia solani) . Fusar i u m..으로부터 DNA7} E. coli Kl2£ . 이전되어 플 라스미드로써 복제되었다. 폴라스미드 유사 DNA 의 존재가 ascomy ce te 곰팡이인 Podospo ra anse rii na 에서도 발견되었는데 이 경우는 현재 클로닝 연구에 사용될 수있다. 적당한 벡터가 없는 경우 리포종 (l ip osome) 에 DNA를 원형질체와 융 합함으로써 가능한데 높은 형질전환율이 S t re pt om y ces 에서 나타났으며 이런 기술이 디른 원핵생물과 진핵생물에서도 참재적으로 응용될 수 있다. 여기에서는 유전공학에 대한 몇 개의 가능성만을 기술하였다. 클로닝 방 법이 완벽해짐에 따라서 이러한 방법들은 산업미생물학의 모든 영역에서 보다 광범위한 범위로까지 적용될 것으로 기대하는 바 크다.
5 산물의 수율향상 이외의 균주개량 이 장의 앞 절은 산업균 주 에 의해 생산되는 대사산 물 의 수융 을 증가시 키는 방법을 알아보았다. 그러나 상업적 공정의 경제성이나 설계는 생산성 의의 마생물의 고유성 질 에 의해 영향을 받는다. 예를 들면, 대사산물을 매 우 높은 수 준 으로 생산하는 균주라도 생산성이 극도로 불안정하다거나 미 생물의 산소요구가 충족되지 않는다면 공정에 부적당하다. 그러므로 공정 에 영향을 미치는 생산균주의 성질은 상업적 성공에 중요하다. 따라서 자 연적 변이, 유도된 변이와 재조합체를 선별함으로써 얻어지는 생산균주의 성 질 을 변형시킬 필요기- 있다. 물론 변형된 균주가 원하는 생산성을 유지 하여 선별된 성질뿐 아니라 수율의 측정방법을 포함하는 것이 중요하다. 이 상황에 중요한 성질로는 균주 안정성, ph age 침입에 대한 저항, 용존 산소에 대한 반응, 배지 조성분의 허용, 거품의 생성, 원하지 않는 부산물 의 생산, 그리고 미생물의 형태적 유형 등이다. 5.1 안정한 균주의 선별 균주 유지와 발효 동안 생산균주의 높은 생산성을 유지하는 능력은 매 우 중요한 성질이다. 균주 보관 동안 수율의 저하는 유지 기술을 이용하여 피할 수 있지만 발효 동안의 생산성의 소실은 보다 어렵다. 산업균주의 생 산성 감소는 보통 고생산 모균보다 높은 증식을 갖는 저수율의 자연 복귀 주가 생기기 때문이므로 수율 저하는 빠르게 증식하는 낮은 생산자가 고 생산균주보다 우세한 fe dba t ch 나 연속배양과 같은 장기간 발효에서 특히 문제가 된다. 이런 상황은 상업적 아미노산 생산균주에서 나타나는데 그것 은 연속배양에 충분히 안전한 균주가 아니기 때문이다. Bu'Lock은 아미 노산 발효는 매우 안정한 균주의 개발을 필요로 하는데 연속발효를 이용 할 수 없다면 새로운 화학적 방법이나 고정화된 효소 과정과 경쟁할 수 없기 때문에 아미노산 발효의 미래는 의심스럽다고 주장하고 있다. 일차대
사산물을 과대생산하는 돌연변이주는 영양요구주, 혹은 유사체 내성돌연변 이주이거나, 복귀주인 경향이 있고 이런 돌연변이는 일차대사산물의 생산 을 조절하는 일반 기작을 제거시킨 것이다. 같은 표현형을 나타내는 하나 이상의 돌연변이를 도입하면 더욱 안정한 균주를 확보할 수 있는데 그 이 유는 모든 돌연변이는 균주가 생산성을 상실할 때까지 복귀되어야 하기 때문 0l 다. 호모세린과 트레오린을 모두 필요로 하는 Mi cro coccus g lu t am i cus 의 이 중 영양요구 돌연변이주를 선별하고 호모세린 요구주의 리신 생산성과 비 교해보면 이중 돌연변이주는 단독 영양요구주와 비교하여 리신을 두 배 더 생산하였고, 저생산성으로 되돌아가는 데 덜 민감하며, 연속배양으로 리신을 생산하는데 이중 영양요구주가 더 적당한 균주라는 것이 Wood- ru ff (l970) 에 의해 보고되고 있다. Naka y ama 는 리신 발효에서 균주 복귀돌연변이에 관해 디루었는데 60~8 81-]간 배양시 세포의 87% 가 복귀된 발효의 예를 제시하였다. 이런 복귀돌연변이주의 수준이 높다는 것은 호모세린 제한배양에서 단독 영양요 구주에 비교하여 복귀돌연변이주가 빠르게 증식했기 때문일 것이다. 이런 상황은 호모세린 제한요구주보다 빠르게 증석하는 복귀돌연변이주를 더 억 제하는 에리트로마이신과 같은 항생물질을 첨가함으로써 조절할 수 있다. 그러나 디중 유전자 표지 (marker) 를 갖는 돌연변이주를 이용하는 것이 더 좋은 해결방법인데 그 이유는 모든 표지가 복귀해야 하기 때문에 야생 형으로 되돌아가는 확률이 낮고 이는 일어나기도 매우 어렵기 때문이다. 5.2 감영저항성 균주의 선별 세균의 발효는 파지 침입에 의해 치명적인 영향을 받는다. 파지 오염을 줄이기 위한 가능한 방법은 발효조에서 분리한 파지에 내성을 갖는 세균 주를 선별하는 것이다. 발효에서 파지를 세포내에 지니게 되면 참재적인 용균성 파지 돌연변이주의 원천이 되기 때문에 분리된 내성균주가 용원성
이 아닌 것이 되어야 한다. 새 숙주 범위의 파지는 파지 돌연 변이주에 도 입될 가능성이 있기 때 문 에 파지 내성 돌연 변이의 이용이 파지 침입으로 부터의 면역이 확실히 된다는 보장은 없다. 야생 미생물을 사용한 발효의 감염은 다양한 항생물질 내성인 산업균주 롤 선별함으로써 더 쉽게 조절할 수 있다. 산업균주가 내성인 항생물질을 어느 정도의 오염을 조절하는 데 이용할 수 있다. 5.3 거품 없는 균주의 선별 발효 동안의 거품 생성에 의해 오염의 위험이 생길 뿐만 아니라 공기 배출을 통한 배양액 세포 및 산물의 손실이 생길 수 있다. 그러므로 거품 생성은 보통 화학적 또는 기계적 방법으로 조절할 수 있지만 거품 비생성 균주를 개발할 수 있다면 거품을 조절하기가 더 쉬워진다. 발효 초기에 생 기는 거품은 주로 배지의 조성성분에 기인되나 발효 말기의 거품은 보통 증식하는 미생물의 성질에 의하므로 후자의 경우만 균주선별로 조절할 수 있다. S r i mosu 폐 의한 옥시테트라사이클린 (Ox yt e t rac y cl i ne) 생산에서 거품 비생산 균주의 선별에서는 돌연변이보다는 재조합 방법을 이용하였고 s. r i mosus 의 두 균주 사이의 교배로 영양배지에서 거품을 만들지 않는 잡종 울 분리하였다 (M i ndl i n, 1961). 5.4 배지성분에 내성을 갖는 균주의 선별 산물생성에 필요한 배지성분이 미생물중식을 방해할 수 있으므로 배지 조성분에 대한 내성균주를 선별하는 경우도 있다. Pol y a 와 Ny iri ( 19 66) 는 페니실린의 전구체인 페닐아세트산이 높은 농도에서 미생물에 독성이 있어 이 물질에 내성이 있는 P. ch ry so g enum 의 돌연변이를 선별하는 데· 이 방법을 적용하였다. Alik h ania n (1959) 등은 높은 농도의 인(p hos-
p ha t e) 에 내성이 있는 옥시테트라사이 클 린 생산자인 S. rim osus 균주를 선별하였다. 옥수수 침출액 (CSL) 은 높은 농도에서 발효고H j 을 억제하는 인을 포함하기 때문에 높은 수준의 옥수수 침출액의 공급은 미생물의 질 소 요구를 충족시키지만 인의 저해현상을 초래한다. 그러므로 높은 수준의 인에 내성이 있는 균주를 선별하였고 높은 인의 농도에 의해 영향을 받지 않으면서 필요한 만큼의 옥수수 침출액을 포함하는 높은 탄수화물 배지에 서 증식할 수 있는 균주를 육종하였다. 5.5 형태학적 유용군의 선별 액내 배양에서 미생물의 형태는 종종 공정의 조작 용이성에 크게 영향 을 미친다. 사상균의 형태적 유형은 발효조의 통기와 발효액의 여과에 영 향을 주게 된다. 액내 배양에서의 곰팡이의 형태는 포자접종 방법이나 배 지에 의해 조절할 수 있지만 유전자형을 바꿈으로써 미생물의 형태에 영 향을줄수도있다. Barth o lomew(1977) 등이 선별한 P. chry so g enu 짜긱 균주는 배지의 점 성을 낮춤으로써 발효조의 산소전달 능력을 증가시켰다. 특별한 형태적 유 형의 균주를 육종하기 위해 재조합에 비하여 돌연변이의 선별 방식에 대 해서는 Bal l( l978) 에 의해 논의되었는데 많은 수의 돌연변이주가 선별되 어야 하기 때문에 재조합 기술이 더 유리하다고 주장하였다. 재조합 방법 에서는 상업균주와 원하는 형태의 균주 사이에 교배를 시켜 상대적으로 소수의 자손을 선별하게 된다. Haml yn과 Ball(1979) 은 Cep h alospo riu m acremoniu m 균주를 만드는 데 원형질체 융합을 적용하였다. 포자를 생성하지 않고 느리게 증식하는 균주와 그보다 Cep ha losp or in 울 時의 1 만을 생산하면서 포자를 형성하고 빠르게 증식하는 균주를 교 배시켜 양균주의 바람직한 특성을 나타내는 재조합체, 즉 포자를 형성하면 서 빠르게 증식하고 고수율인(양천보다 40% 의 항생물질을 더 생산하는) 균주를 선별하였다. 풍부하게 포자를 내는 균주의 능력은 접종균의 생장에
매우 유용한 특 성이 된다. 효모의 응집 (fl occula ti on) 은 세포가 덩어리가 되어 붙어버리는 것으로 서 효모가 배양액으로부터 분리된다. 그러므로 효모의 응집성은 형태적 특 성이라 할 수 있다. 응집현상이 맥주 발효에서 일어날 때 효모가 〈상충― 발효〉 효모라면 용기의 상부로 울라가고 〈바닥-발효〉 효모라면 용기의 바닥으로 떨어진다. 그러므로 효모의 응집성은 효모와 맥아즙의 접촉시간 과 맥주 정화의 용이성을 결정하게 된다. 많은 양조업에서 돌연변이주 선 별은 드물지만 자연적인 변이선별은 매우 보편적이다. 또한 맥주 발효에서 생산된 효모를 새 발효액에 접종하여 이용하는데 다른 발효산업에서는 이 러한 이용은 매우 드물다. 발효에서 생산된 효모를 주의깊게 선별하여 원 하는 정도의 응집성을 나타내는 균주를 선별할 수가 있다. 상충발효의 상 충으로 울라온 첫번째 세포나 바닥발효의 바닥으로 먼저 떨어전 세포들은 가장 응집성 강한 세포인 데 반해 분산된 세포들은 가장 미약한 응집성 세포인 것이다. 그러므로 중간 시간에 응집히는 세포를 선별함으로써 다음 접종을 위하여 가장 적절한 형태적 특성을 가진 자연변이주를 선별할 수 있다. 5.6 일부 발효산물의 제거와 신발효산물 생성균주의 육종 산업균주가 원하는 대사산물을 대량으로 생산하여도 필요치 않거나 추 출과정을 방해하는 대사산물을 생산할 수도 있다. 페니실린 생산균주에서 한 예로는 무색소 돌연변이주의 분리로 항생물질의 추출을 용이하게 하고 노란 색소인 chrys o g en ein 생산을 제거할 수 있게 되었다 (Backus, 1955). Dolezil o va( 1965) 등은 S. nourse i의 돌연변이주에 의한 . fu n gi c i d i n 을 고농도로 생산하지만 사이클로헥사마이드 (c y clohe ximi de) 를 생산하지 않 는 돌연변이주를 분리할 수 있었다. 자연환경으로부터 유용한 대사산물을 합성하는 미생물의 분리는 비싸고 힘든 과정이다. 그러므로 산업적으로 중
요한 물질을 생산하기 위해 다른 수단이 시도되어왔다. 그중에서 가장 성 공적인 방법은 반합성 과정으로서 미생물산물이 화학적으로- 변형된 예가 반합성 페니실린이다. 자연적 생성물의 전구체를 발효배지에 넣어줌으로써 최종산물을 증가시켰고 그 예가 페니실린 G 생산에서의 페닐아세트산의 A 냉이다. 자연적 생성물의 보통 전구체의 유사체의 주입으로 빈번하게 자 연적 생산물의 유사체가 생긴다. Hami ll( 1970) 등은 aureo f ac i en 회 배양 에서 5, 6 또는 7 의 자리가 치환된 트립토판을 Pseudomonas 항전균성 물 질인 py rroln itr i n 의 보통 전구체인 트립토판 대신으로 넣어주면 일련의 치환된 py rroln itr i n을 얻고 그중 몇몇은 항전균성 활성이 증진된다는 사 실을증명하였다. Na g aoka 와 Dema i n(1975) 은 〈돌연변이의 생합성〉으로 새로운 산물의 문기를 위한 이 기술을 기술하였고 선별된 돌연변이주를 〈i d i o t ro phs 〉라 하였다. 돌연변이적 생합성 기술은 네오마이신 (Neom y c i n) 과 같은 ami - nog ly c o sid e -ami no cy cl it ol 항생물질 외에도 macroIid e 항생물질, nov-obio c in 항생물질과 p-락탐 항생물질에 적용되었으며, 그 의에도 많은 새 로운 산물기 등정되었지만 197~ 빈까지는 생산수율아 낮기 때문에 상업적 으로 개발된 것은 없다. 그러나 이런 방법으로 선별된 돌연변이주를 이용 해서 생합성 경로롤 규명하는 데는 매우 유익한 것이 명백한 사실이다. 참고문헌 Abe, S.(1972) Muta n ts and the ir iso lati on , The Mi cro bia l Producti on of Ami no Acid s (Edit or s Yamada, K., Ki no shit a, S., Tsunoda, T. and Aid a , K.), pp. 39~66. Halste a d Press, New York. Alik h ania n , S. I.(1 962) ; Induced muta g e n esis in the selecti on of micr o-o r ga n ism s. Adu. Ap pl. Mi cro bio l. 4, 1~5. Alikh ania n , S. I., Mi nd lin , S. Z., Goldat, S. V. and Vlad imizo v, A. V. (1959) .. Geneti cs of orga n ism s pro ducin g tet r a cy cl in e s. Ann. N.
Y. Acad Sci 81, 914 . At he rto n . K. T., By ro m, D. and Dart, E.C. (19 79). Geneti c manip u -lati on for ind ustr i a l pro cesses. Soc. Gen. Mi cr o. Sy m p . 29, 379~ 406. Backus. M. P. and St au ff r, J. F. (19 55) The pro ducti on and selec- tion of a fam i ly of str a in s of Penic i l li u m chrys o g en um, My co log ia, 47, 429~463. Ball, C.(1973) The gen eti cs of Penic i l li u m chrys o g en urn. Prog . Ind. Mi cr o. 12, 47~72. Ball, C.( 1978) Geneti cs in the develop m ent of the pen ic i ll i n pro cess, In Anti bi o t i cs and Oth e r Secondary meta b olite s Bi os y n th e sis and Pro- ducti on (Edit ors Hut ter , R., Leis i n g er , T, Nuesch, J. and Wehrli n, W.), pp. 163~176. Academi c Press, London. Ball, C. and McGonag le , M. P. (1978) Develop m ent and evaluati on of a po te n cy ind ex screen for dete c ting mut an ts of P. chry so g en um havin g inc reased pe nic i ll in yiel ds. J. Ap pl. Bact. 45, 67~74. Barth o lomew, W. H. , Sheehan, B. T., Shu, P. and Sg uire s, R. W. ( 1977) Abstr a cts of the 174t h Nati on al Meeti ng of the Americ a n Chemi ca l Soc., Ch ica g o , Illin o is . Di vi s i o n of Mi cr obia l and Bi o- chemi ca l Technology , Abstr a ct number 37. Bonner, D.(1 9 47) St ud ie s on the bio s y nthe sis of pe n ici l lin, Arch. Bio c hem. 13, l. Catc h esid e , D. G.( 1954) Isolati on of nutr i t ion al mut an ts of Neu-rosp o ra crassa by filt r a ti on enric h ment. J. Gen Mi cr o. 11, 34~36. Chakrabarty , A. M. 1976. Plasm ids in Psedomonas, Ann. Rev. Genet. 10 ; 7~30. Chang , L.T., Terasaka, D.T. and Elander, R. P.(1982) Proto p la st fus io n in ind ustr i a l fun g i. Dev. Ind. Mi cr o 23, 21-29. Chate r , K. F.(1979) Some recent develop m ents in St re p tom y c es ge n-eKt.i csa. n dI nL aGseknien ti, csA .o f I .I)n, dpuspt.r ia 1 l2 3M— i 1c3r 3 o.o rgAa mn ies rmi cs a n (SEodc i. toMr si crS oebbieo kl ,o g0 y., Wash ing ton . Clarke. P. H. ( 1974) The evoluti on of enzym e s for the uti liza ti on of
novel substr a te s . Socie ty for General Mi cr obi ol og y Sy m p o si u m , 24. 183~218. Cohen,Bazir e , G. and Jol it , M. (19 53) Isolati on by selecti on of E. coli muta n t s wh ich spo nt an eously sy n th e siz e amy lo malto s e and fJ -ga lacto s id a se, Ann. Inst. Paste u r, 84, 937~945. Davie s , 0. L. ( 1964) Screenin g for inp ro ved mut an ts in anti bi o t i c research, Bio m etr ic s , 20, 576~591 . Davis , B. 0. (19 49) Nutr i t ion ally defi ci e n t bacte r ia l mut an t s iso - late d by pe n ici l lin, Proc. Natn . Acad. Sci. U.S.A 35, l~10. Demain , A.L. (19 67) Inhib i t ion of pe nic i l li n for mati on by lys in e , Archiv e s of Bi oc hemi str y and Bio p h ys i c s 67, 244~245. Demain , A.L. (1971) Overpr o ducti on of micr obia l meta b oli tes and enzy m es due to alte r ati on of reg u lati on Adv. Bio c hem. Eng . 1, 113~142. Demain , A. L. ( 1972) Cellular and envir o nmenta l fac to rs aff ec ti ng the sy nthe sis and excreti on of meta b olit es J. Ap pl. chem. Bi ot e c h. 22, 346~362. Demain , A. L.(1 973) Mut at i on and Produc tion of secondary met- aboli tes Adv. Ap pl. Mi cr o. 16, 177~202. Demain , A. L. (1974) How do anti bi o t i c pro ducin g orga nis m s avoid suic i d e ? Ann N. Y. Acad. sci. 235, 601~612. Demain . A. L. (1978) Producti on of nucleoti de s by mi cr oorga n ism s, In Pri',n a ry Products of Meta b olism Economi c Mi cr obio l og y, 2, 187~ 209 (Ed itor Rose, A. H). Academi c Press, London. Di tch burn, P., and MacDonald, K. D. (1974) Rap id screenin g for the iso lati on of mut an ts in A. nid u lans wi th inc reased Pen ici l lin yiel ds J. Ap pl. Bact. 37, 515~523. Dolezil o va, L. and Vanek, Z. (19 65) Cy c lohexim i de pro ducin g and fungici d in pro ducin g muta n ts of St re p ton y ce s noursei ; J. Gen Mi cr o. 39, 305~310 Dulaney, E. 1 and Dulaney, D.D. (1967) Mut an t po p u lati on s of Str - ept om y ce s vir i d i f aci e n s '!ran s, N. Y. Acad. Sci 29, 782~799. Blander. R. P. (1966) Two decades of str a in develop m ent in anti -
bio t i c- p r o ducin g mi cr o-o r ga n is m s Dev. Ind Mi cro . 7, 61~73. Elander, R. P. (19 80) New gen eti c app r oaches to ind ustr i a l ly im - po rta n t fun g i, Bio t e c h. Bio e ng . 22, Sup ple ment 1. 49~61 . Elander, R. P. and Espe n shade, M. A.(1 9 76) The role of mi cr obia l gen eti cs in ind ustr i a l micr obio l og y. In Industr ia l Mi cro bio lo g y (Edit ors Mi 'lle r, B. M. and Lit sk y . W. L.). pp. 192~256. McG- raw-Hi ll, New. York. Elander, R. P. and R. W. Vaug ha n, 1977. Geneti cs of ind ustr i a l mi c- roorga n ism s, Ann. Rep Ferment. Proc. 1 ; 1~40 Elander. R.P . and Gorman, M. (1971) Bi os y n t he sis of pyrr olni tri n • by analog ue resis t a n t mut an ts of Pseudomonas fluu orescens Fol, Mi cr obia l . 16, 157~5. Fanti ni , A. A. ( 1975) St ra in develop m ent , Meth o ds in Enzy m olog y, 43, 24~41 . Ganju , P. L. and Iye n g ar , M. R. S. (1968) An enric h ment tec hniq u e for iso lati on of aut ot r o p ic mi cr o-o r ga n ism s Hi nd usta n . Anti bi o t. Bull. 11, 12~21. Han ill, R. L. and Gorman, M. (1970) Meta b oli sm of try p top h an by seudomonas aureofa cien s Ap pl. Mi cr o. 19, 721~725 .. Hamlyn , P. F. and Ball, C. ( 1979) Recombin a ti on stu d ies with Cep - halosp o riu m acremon ium . In Geneti cs of Industr ia l Mi cro orga n is m s (Edit or s Sebek, O.K . and Laskin , A. I.), pp.18 5~191 . Americ a n Soc. for Mi cr obio l og y, Washin g ton . Holt, G. F. and MacDonald, K. D. ( 1976) The gen eti cs of muta n ts im p a ir e d in the bio s y n th e sis of pen i ci l li n . In Second Inte r nati on al Sy m p o siu m on the Genti cs of Industr ia l Mi cro -orga n is m s (Ed itor MacDonald, K.D .), pp 199~212. Academ ic Press, London. Hop w ood, D.A.(1979) The many fac es of recombin a ti on . In Geneti cs of Industr i a l Mi cr oorga n is m s (Ed itor s Sebek, O.K . and LaskiO :, A. I.). pp 1~9. Americ a n Soc. for Mi cr obio l og y, Washin g ton . Hop w ood, D. A. and M. J. Merric k , 1977. Geneti cs of anti bi o t i c pro ducti on Bacte r io l , Rev. 41, 595~635. Ich ika wa , T. and Ozaki, A. (1971) Imp ro vement of kasug am y cin
pro ducin g str a in by the aga r piec e meth o d and pro t ot r o p h met - hod. Folia Mi cr obi ol og ica , 16, 218~224. Itak ura, L., and Boy er , H. W. ( 1977) Exp re ssio n in E. coli of a che- mi ca lly syn th e siz e d gen es for the hormone somato s ta t i n. Scie n ce, 198, 1056~1063. Ja cob, F., and Monod, J. (19 61) On the reg u lati on of gen e acti vi t y. Coid Sp r in g Harbor Sy m p Qu ant, Bi ol . 26, 193~211 . Jo nes, A. and Vi ni n g , L. C. ( 1976) Bi os y n t he sis of chloramp h en ico l in str e p tom y ce s ; Ident ifica ti on of p-a m ino -L-ph eny la lanin e as a pro duct from the acti on of aryl a mi ne sy n th e ta s e on choris m i c acid . Can, J. Mi cro , 22, 237~224. Ki no shit a, S. and Nakoy a ma, K. ( 1978) Amino acid s . In Prim ary Products of Meta b olism . Economi c Mi cr obio l og y 2, 210~262. Aca- dem ic Press. London. Ki no shit a, S. and shi m ono, M. ( 1975) St ud ie s on the am ino acid fer menta t i on s, pa rt 1. Producti on of L- G lu. acid by vario u s mi c- roorga n ism s, J. Gen. Ap pl. Mi ro , 3, 193~205. Lederberg, J. and Lederberg, E. M. (19 52) Rep li c a pla ti ng and in- dire ct selecti on of bacte r ia l mut an ts , J. Bact. 63, 399~406. MacDonald, K.D. and Gi llet t , W.A.(1965) Hete r ozyg o us dip lo id s of Penic i ll i u m chry so p e num and the ir seg re g a ti on pa tt er ns. Genti ca , 36, 378~397. Marti n, J. F. ( 1978) Manip ul ati on of gen e exp re ssio n in the devel- op m ent of anti bio t i c pro ducti on . In Anti bi o t i cs and oth e r Secondary meta b olite s. Bi os y n th e sis and pro ducti on (Edit ors Hut ter, R. Lei- sin g er , T., Nuesch, J. and Wehrlin , w.) Academ ic Press, London. Mi nd lin , S. Z. and Mi kh ail o va, G. R. (1961) A new hy b rid str a in of an oxy tet r a cy cl in e pro ducin g orga nis m , Str e p tom y c es rim osus Ap pl. Mi cr o. 9, 349~353. Naga oka, K. and Dema in, A. L. (1975) Muta t i on al bio s yn th e sis of a new anti bi o t i c, str e p tom uti n A, by an idi o t r o p h of St re p tom y c es grise us, J. Anti bi o t , 28, 627~647. Nakao, Y. and Doi, M. (1970) Mi cr obia l pro ducti on of L-Glu acid
from n-pa raff in by gly c e rol auxot op h s, Ag r. Bio l , Chem 34, 1875. Nakao, Y. and Yamato dani, S. (19 73) Extr a cellular accumulati on of ph osp h olip ids , UDPN-acety lh exosami ne deriv a ti ve s and L-gl u t am i c acid by pe nic i l lin tre ate d Cory n ebacte r iu m alkanolyt icu m, Ag r. Bio l . Chem. 37, 2399~2404. Nakao, Y. and Doi M. (19 72) Mi cr obia l pro ducti on of L-gl u ta m i c acid by gly c erol auxot rp h s and pr oducti on of L-gl u t am i c acid fro- m n-p a raff ins . Ag ri . Bio l . Chem. 36, 490~496. Novic k , A. and Horiu c hi, T. (1961) Hy pe rpr oducti on of P-ga lac- tos id a se by E. coli. Cold Sp r in g Harbor Sy m p Qu ant Bio l . 26, 239~ 245. Okanis h i, M. and S, Nabeshim a, 1983. Basic tec hn iqu es for DNA clonin g and condit ion s req u ir e d for str e p tom y c ete s as a host. Jo ur. Anti bi o t i cs 36 ; 99~ 108. Old, R. W. and Prim rose, S. B (1981) Prin c ip le s of Gene Man ipu -lati on . An int r o ducti on to Geneti c En gine erin g 2nd edit ion . Blackwell, Oxfo r d. Pep e rdy , J. F. 1979. Fung al pr ot op la sts : Isolati on , reversio n , and fus - ion . Ann, Rev. Mi cr obio l . 33:21~39. Pep e rdy , J. F. 1980. Prot op la st fus io n -a too l for gen eti c manip u -lati on and breedin g in ind ustr i a l mi cr oorga n ism s, Enzy m e Mi cr ob. Technol. 2:23~29. Polsin e ll i, M. and Cif er ri, 0. (19 65) Relati on of bio c hem ica l mut- ati on s to acti no my c in sy n th e sis in St re p tom y c es anti bi o t i cu s. J. Gen. Mi cro 39, 239~246. Polya , K. and Ny iri, L. (1966) Abstr 9th Jut . Con gr . ,Vf icr obio l ., p. 172 . Ponte c orvo, G. P.A. and Rop e r, J. A. (19 58) Un ited Sta t e s Pate n t 2, 820, 742. Ponte c orvo, G. and Buft on , A.W.J. ( 1953) The ge neti cs of A. nid- ulans, Adv. Genti cs , 5, 141~238. Qu eener, S. and Swartz , R.(19 79) Penic i ll ins ; bio s y nthe ti c and sem- isy the ti c. In Economi c Mi cr obio l og y 3:Secondary Products Meta b -
olis m (Edit or Rose, A.H.), pp. 35~123. Academi c Press, London. Ri vi e r e, J. (19 77) Induste r ia l Ap pli c a ti on s of Mi cr obio l og y (Tra-nslato r s Moss, M.O. and Sm ith, J. E.). Surrey Univ e rsit y Press, London. Sano, K. and Shii o, I. ( 1970) M icr obia l Producti on of L-lys in e III -pr oducti on by muta n ts resis t a _nt to S-( L-ami no eth y l)-L -c ys te i n e . J. Gen. Ap pl. Mi cr o. 16, 373~391. Sermonti , G. (19 69) Geneti cs of Anti bi o t i c Producin g Orga n ism s Wi le y -I nte r scie n ce, London. Shib a i, H. and Hi ro se, Y.(1978) Purin e nucleosid e fer menta ti on s, Process Bio c hem. 13(11), 6~8. Sh iio, I. and Sano, K.(19 69) Mi cr obia l pro duc tion of L-lys in e II -Producti on by muta n ts sensit ive to th reonin e or meth io n ine J. Gen. Ap pl. Mi cr o, 15, 267~287. Sh iio, Sik y ta, B. and Ky s li k, P. (1981) Selecti on of Escheric h ia coli wi th an inc reased endoenzym e sy nthe sis in conti nu ous cultu re Adu, Bi ot e c h. 1, 215~220 (Ed itor s Moo-Young , M., Robin s on, C. W. and Vezin a , C.). Perga m on Press, Tornto . Smy th, P. F. and Clarke, P. H. ( 1972) Cata b olit e rep re ssio n of Pse-udomonas aerug ino sa arn ida se, J. Gen. Mi cr o. 73, ix. Szy b alsk i, W. ( 1952) Mi cr obia l selecti on . Part 1. Gradie n t Plate tec hn iqu e for stu dy of bacte r ia l resis t a n ce, Scie n ce 116, 46~48. Udag a wa, K., Abe, S. and Ki no sh ita, S. (1962) J. Ferment. 'Iec hnol. (Osaka) (Ja pa nese), 40, 614 Ullric h , A. and Goodman, H. M. ( 1977) Rat ins uln gen es : Constr u c- tion of pla sm ids conta i n ing the codon seq u ence. Scie n ce, 196, 1313~1319. Wang, D.I. C. and Li lly , M.D. (1979) Fermenta t i on and Enzy m e Technolog y, Wi le y - lnte r scie n ce, New. York. Woodru ff, H. B. and Jo hnson, M. (1970) U. S. Pate n t 3, 524, 797.
제條l- 발효공업에 사용되는 배지성분 1 서론 발효공정의 최적화를 위해서는 가장 적합한 배지를 연구, 확립해야 하고 그 배지는 어떤 기본적인 요구조건을 충족시킬 수 있어야 한다. 모든 균주 는 물, 에너지원, 탄소원, 질소원, 무기성분, 혹은 비타민과 호기성 균주에 는 산소를 공급해주어야 한다. 소규모에서 순수한 화합물을 함유하는 합성 배지를 고안해내기는 비교적 간단하지만 합성배지를 대규모의 공정에 사용 하는데는부적당하다. 대규모에서는 아래와 같은 기준을 되도록이면 많이 충족시킬 수 있는 배지를 만들기 위해 염가의 영양원이 사용되어야 한다. 1. 사용되는 기질의 그램당 생체량이나 최고수율의 산물을 생산해내야 한다. 2. 산물이나 생체량을 최대농도로 생산시켜야 한다. 3. 고속도로 산물 생장을 해야 한다. 4. 불필요 산물을 최소로 줄여야 한다. 5. 값이 싸고 질이 일정하고 연중 쉽게 입수할 수 있어야 한다. 6. 생성과정, 특히 통기, 교반, 추출, 정제, 폐기물 처리의 면에서 어려움을 최소화시켜야 한다.
탄소원으로서 사탕수수 , 당밀, 사탕무당, 곡물, 녹말, 포도당, 설탕 , 젖당, 그리고 질소원으로서 암모늄염, 요쇼:., 질산염, 옥수수 침출액 (corn ste e p liqu or), 콩가루 (so y bean meal), 그리고 도살장 폐기물과 발효 잔류물 등이 생산배지로서 위의 기준을 충족시키는 경우가 많다. 포자형성 (sp o ru- la ti on) 이나 접종(i nocula ti on) 배지를 선별하는 데 이용되는 기준은 따 로고려되어야한다. 가스_전이가 낮은 대형 발효조에 실험실적 배지를 적용시키는 것은 바 람직하지 못하다. 점성이 높은 배지는 교반 및 수송에 높은 동력을 소모하 게 되고 배지는 증직과 산물의 생산뿐만 아니라 p H 변화, 거품형성, 산화 _환원 전위균의 형태에 영향을 주게 된다. 또한 전구물질 또는 대사적 억 제물질을 배지에 첨가해주는 경우가 많다 (A i ba et al., 1973). 2 배지성분의 조제 (mediu m for mulati on ) 표 4 .1은 용액내 배양의 발효를 위한 표준배지의 성분을 나타내고 있으 나 이들 성분이 현재 사용되는 것 중에서 가장 좋은 배지임을 의미하는· 것은 아니다. 배지성분의 조제에 대한 조사는 실험적 과정, 시험공장 규모 의 개발, 제조공정에 필수적으로 거쳐야 할 단계인데, 배지의 성분구성은 세포 생체량과 대사물질의 생산에 필요한 기본적인 요구를 충족시키고 생 합성과 세포 유지에 필요한 에너지를 공급해줄 수 있어야 한다. 고려해야 할 것은 증식과 산물의 생산을 위한 디음과 같은 식이다. 탄에소너원지원과 +질소원+기 요구타조 건 _균 체량+산물 +C0 2 +H 2 0+ 열 이 식은 정량적으로 표현하여야 할 것이며 만약 성분의 소모량을 최소 화시킬 수 있다면 배지의 경제적 디자인에 중요한 의미를 지니게 될 것이다.
표 4.1 발효배지의 예 아밀러아제 (Underkofl er , 1966) 지베렐린산 (Calm and Nix o n, 1960) 콩가루 .1. 85 % Glucose monohy d rate 20g dm -3 효자모가분조해각된 양조 1.50 % NMHg S40N 40 3 llggdd mm --33 증류전조된 가용성물질 0.76% KH2P04 5gd m -3 FeSOi • 7H2 0 O.Olg dm -3 NZ- am i ne 0.65% MnS04 • 4H20 O.O lg d m -3 (효소적 카세인 가수분해물) 락토오즈 4.75% ZnS04 • 7H2 0 O.Olgd m - 3 Mg S0 4 • 7H20 0.04% Cu804 • SH2 0. 0.0lgd m -3 Hodag KG-1 소距 1] 0.05% 옥(건수조수된담 고근체액로 서) 7.5g dm -3 리보풀라빈 (Harned, 1969) 글루탐산 (Gore Reis m an and Gardner, 1968) 콩기름 20cm3dm-J 뚜당 270g dm -3 글리세롤 20cm3dm-3 NH4H2P04 2gd m - 3 포도당 20g dm -3 ( NH4 hH P04 2gd m -3 옥수수침출액 12cm3dm-J Ki8 0 4 2gd m -3 카세인 12g dm -J Mg S0 4 • 7HO 0.5g dm -J KH2 P0 4 lgd m -3 MnS04 • H20 0.04g dm -J FeS04 • 7H2 0 0.02 g dm -J Polyl y c o l 2,000 0.3g dm -J 비오딘 l2µg d m-3 페니실린 lµg d m-3 페니실린 (Perman, 1970) 포도당또는당 전체의 10% (연속주입에 의한) 옥수수 침출액 (CSL) 전체의 4~5% P(h연en속y주l a입 ce에t i c의 한 ac)i d 전체의 0.5 ~ 0.8%
거품방지제 전체의 0.5 % 산이나 알카리에 의한 pH 6.5 ~7.5% 주의 : 5 가지 배지에서의 구성성분은 우연히 서택된 것이 아니며 배지 조 성의 이론 적 근거는 이 장의 뒷부분에서 상세히 거론하겠다.
이렇게 해서 균체량의 일정량을 생산하는 데 필요한 최소량의 영양소량 을 계산할 수 있다. 균체량의 확실한 양을 아는 것은 요구산물의 수율 산 출과 필요한 기질의 농도를 산출하는 데 필요하다. 물론 모든 요소들을 정 확히각 제요한소한간다의는 균 것형은이 쉬유운지 일되이는 아배니양다액.에 서 균주의 구성요소(이것은 c, H, 0, N, S, P, Mg , K 를 포함해야 한다)에 관한 지식이 있어야 한다 (표 4.2). 미량원소(t race elements Fe, Zn, Cu, Mn, Co, Mo, B) 는 극소량만을 필요로 한다• Coone y (l981) 는 박테리아 세포에서 각 요소간 의 상대적인 농도의 분석과 일반적으로 사용되는 배양배지를 예시하였는데 P, K 와 갑은 몇몇 영양소는 종종 실질적으로 초과량을 요구한다. 그리고 Zn, C 퍄 제한된 효용성을 가지고 P 의 농도는 완충능을 증가시키는 많은 배지에서 증가시키는 데 이 점은 배지 디자인을 하는 데 특히 강조된다.
懿 (Car 二표 4 .2 세균 • 효:(모A i • :곰3팡a이l의, I원 (A소 ' 구i성~(o건a조l , 무I 게(L의 l e백~분y율:\): 갑i ba 수소( Hy d rog en ) 7 7 질소 (N it rog en) 12~15 . 7.5~11 7~10 인 (Phos phorus) 2.0~30 0.8~2.6 0.4 ~ 4.5 황 (Sul p hur) 0.2~1 .0 0.01~0.24 0.1 ~ 0.5 칼륨 (Pa t ass i um) 1.0 ~4.5 1.0~ 4.0 0.2~2.5 나트륨 (So di um) 0.5~1 .0 0.01~0.1 0.02~0.5
칼슘 (Calc i um) 0.01~1 .1 0.1 ~ 0 .3 0.1 ~1.4 마그네슘( Mag ne siu m ) 0.1 ~ 0.5 0.1 ~ 0.5 0.1 ~ 0.5 영 소 (Chlor i de) 0.5 철 (I ron) 0.02 ~ 0.2 0.01~0.5 0.1 ~ 0.2
미생물 중에는 특별한 영양소, 예를 들어 아미노산, 비타민, 누클레오티 드를 합성하지 못히는 것이 있다. 일단 특별한 성장인자가 밝혀지면 순수 화합물로서 또는 복합물의 성분으로서 적절한 양을 배지에 첨가할 수 있 다. 탄소기질은 생합성과 에너지 생성에서 이중의 역할을 한다. 호기상태에 서 탄소의 요구는 다음과 같은 세포 수율계수 (cellular yiel d coeff iei e n t Y) 로부터 산정된다. Y= 생산되는 세포건조물의 양 이용되는탄소기질의 양
표 4.3 C 톤 탄소기질에 대한 세균의 세포 수율계수 (Y) (Abbo tt와 Clamen, 1973) 기질 세포수율계수 메탄 (Me t han) 0.62 n-알 칸 ( n-Alkanes ) 1.03 메탄올( Meth a nol) 0.4 0 에탄올 (E t hano l) 0.68 아세 데이트( Aceta t e ) 0.34 말레이트( Maleate ) 0.3 6 포도당(당) ( Glucose ( madsses ) ) 0.51
이리하여 0. 禁 1 포도당을 Y 값으로 가지는 세균의 경우(이것은 l.Og g lucose 당 0.5g 세포를 나타낸다) 30gd r n-3 세포를 얻는 데 필요한 포도 당 양은 30I0.5=60 g dm -3 이 된다 이 배지는 또한 대략 3.0g dr n-3 N, lgd r n-3 P와 0.3 gdr n-3 躍 함유해야 한다. 산물을 생산하는 발효공정에서는 탄소원의 적절한 공급이 필수적이다. 다른 중요하게 요구되는 영앙소는 산소인데 배양에서 통기를 함으로써 공급된다. 배지의 디자인에 따라 배양시 산소 요구에 영향을 미치는데 배 양에서 탄소원을 감소시키면 많은 산소를 요구하게 된다. 3 물 물은 모든 발효배지의 주요 구성성분이고 많은 부수적인 역할에 요구된 다. 일정 성분을 함유한 깨끗한 물이 영구적인 수원으로부터 충분히 공급 되어야 한다. pH , 용해물, 바용해 잔사 등 몇몇 요소가 고려되어야 한다. 물의 무기성분은 양조에 매우 중요하며 담금과정에서 더욱 중요하다. 역 사적으로 양조장의 위치가 생산되는 맥주의 맛에 영향을 미쳐왔다. Ca804 의 농도가 높은 경수 (hard wa t er) 는 영국형 Burto n bit ter beer 와 Pil - son type lage n s 맥주에 더 좋고, 탄산울 많이 함유하는 물은 Sto u t ~ 같은 혹맥주에 더 좋은 것으로 되어 있다 (Hou g h et al. , 1971). 오늘날 양조장은 지역적인 수원에 의존하지 않고 마음에 드는 다른 형 의 맥주들을 생산하기 위해 물을 탈이온화하거나 영을 첨가하거나 p H를 조절하는 등 물을 처리하여 사용한다. 대규모 연속배양 SCP 공장에서는 물을 재순환시켜 사용한다. 영양수준을 적당히 조정하여 발효기 급수에서 물을 재이용하는 것은 가능하다 (To pi wala, 1978).
4 탄소원 (carbon sources) 4.1 일반적으로 사용되는 탄소원의 예 증식에 필요한 에너지는 배지 구성성분을 산화하거나 빛에서 온다. 대부 분의 균주는 화학합성 종속영양체 (chomohe t ero t ro p hs) 로서 가장 일반적 인 에너지원은 탄수화물, 지질, 단백질과 같은 탄소원이다. 일부 미생물은 탄소와 에너지원으로 메탄, 메탄을을 이용하기도 한다. 미생물 발효공정의 탄소원으로서는 탄수화물이 일반적으로 이용된다• 가장 광범위하게 이용되 는 탄수화물은 주로 옥수수, 전분 (s t arch) 이고 다른 곡류인 감자 카사바 (cassava) 도. 가루로 이용되고 있다. 전분은 약산(di lu t e ac i ds) 이나 효소 로서 쉽게 가수분해시켜 다양한 포도당 제품으로 만들 수 있다. · 산을 가수 분해시켜 만들어진 제품은 유독 부산물을 함유하는 경우가 있어 주의해야 한다. 보리알은 부분적으로 발아시켜 맥아를 만들 수 있는데 여기에는 전분 이의에도 다양한 종류의 당분 (su g ar) 을 함유한다(표 4.4 ). 맥아는 오랜 세월 동안 맥주 양조에 주요한 원료가- 되어 왔다.
표 4.4a 보리 맥아의 탄수화물 구성 (Harr i s, 1962) 서o T티 r 건조중량의 % sta r ch 58~60 sucrosP 3~5 reducmg sug ar s 3~4 oth e r sug ar s 2 hPmi ce llulose 6~8 cellulose 5
표 4.4b 맥아 추출물의 성분 서o口T 건조중량의 % Malto s e 52.2
Hexoses (glu cose, fruc to s e) 19.1 Sucrose 1.8 Dextr i n 15.0 Ot he r Carbohy d rate s 3.8 Ni tro ge n ous mate r ia l s N 4.6 Ash 1.5 Wate r conte n t 2.0 pH (10% soluti on )=5.5
설탕은 사탕수수와 사탕무에서 생산되는데 설탕을 결정시켜 생산한 후 나오는 폐당밀과 같이 매우 불순한 형태로 발효배지에서 이용된다(표 4.5).
표 4.5 사탕무 당밀과 사탕수수 당밀의 분석표 (전체 w/ v£1 백분율로 표시 ) • Dry matCt eorm p os it ion % 7s8umg~ oe8 rl a5s sbeese t 7su7mg~ ao8r l 4as csaesn e Sucrose 48.5 33.4 Ra ffino se 1.0 Invert sug ar 1.0 21. 2 Mi sc ellaneous orga nic mate r ia ls 20.7 19.6 N 0.2~2.8 0.4 ~1.5 P20 s 0.02~0.07 0.6~2.0 CaO 0.1 5 ~0.7 0.1 ~1.1 Mg O o.0l~0.1 0.03~0.1 K20 2.2~4.5 2.6 ~5.0 Si0 2 0.1 ~ 0.5 Al203 0.005~’ 0.06 Fez03 0.001~0.02 Ash 4~ 8 7~11
Thia m i ne µg/ 100g dry weig h t 130 830 Rib o fl av in 41 250 Py r id o xin e 540 650 Ni ac in a mi de 5100 2100 Pant ot h enic acid 130 2140 Folic acid 21 3.8 Bi ot i n 5.3 120 (Rh odes and Fletc h er, 1966 ; Imrie , 1969 )
배지조성에 젖당과 mi lk whey p owder 의 이용은 연속 유가공저에 이 용될 수 있으나 범위가 제한되어 있다. 그러나 유당은 균체 생산을 위한 기질로서 여전히 이용되고 있다 (Me y ra t h . and Bay er , 1979). 상업적인 식물성 기름(울리브, 옥수수, 목화씨, 아마씨, 콩 등)은 두 가 지 이유로 배지에 첨가되고 있는데 하나는 순수한 탄소원(주로 oleic , lin o leic , lin o len ic acid 등)으로서, 다른 목적은 계면활성제 (surfa c e ac 一 tive ag e nt )와 관련해서 소포제로 쓰인다.
표 4.6 옥수수 침출액의 부분적 분석치 (Rhodes and Fletc h er, 1966) 총 고체 (tot a l soli ds ) 51% w/v lac tic ac i d 의 산도 (ac i d ity) 15% w/v 유리 환원당(fr ee reducin g sug a rs) 5.6% w/v 가수분해 후의 유리 환원당 6.8% w/v 총질소 4% w/v 질소의 백분율로서의 아미노산 Alan ine 25 Arg inine 8 Gluta m i c acid 8 Leuc ine 6 Proli ne 5
Isoleucin e 3.5 Threonin e 3.5 Valin e 3.5 Pheny !a lanin e 2.0 Meth ion ine 1.0 Cy st e i n e 1.0 회분 (Ash) 1.25 % w/v 칼륨 (Po t ass i um) 20% w/v 인 (Phos phorus) 1.5% w/v 나트륨 (Sod i um) 0.3~1% 마그네슘 (Ma g nes i um) 0.003~0.3% 철 (Iron) 0.01~0.3% 구리 (Cop pe r) 0.01~0.03% 칼슘( Calciu m ) 아연 (Z i nc) 0.03~0.08% 납 (Lead) 은 (S i lver) 0.001 ~0.003% 크롬( Chrom ium ) B vit am i ne s Aneurin e 41~49 jig g-1 Bi ot i n 0.34~0.38 jig g-1 Calciu m pan ot ot h e nate 2 14.5~21. 5 jig g-1 Foli c acid 0.26~0.6 µg g-I Ni co ti na mi de 30~40 µg g-1 Ri bo fl av in e 3.9~4.7 jlg g-l N i ac i呼 Py rido xin e
옥수수 침출액 (표 4.6) 은 옥수수의 전분 추출 후의 부산물이다. 주로 질소원으로 이용되지만 젖산의 소량과 환원당이 복합한 다당류를 함유하고 있다. 콩가루와 같은 식물성 질소원도 탄수화물원으로 일부 대체
할 수 있고 백신의 생산에 이용되는 배지조성에서는 소알부민, NZ-<:as~ 같은 단백질도 탄소원으로 이용된다 (Van Hemert, 1974). 알코올류나 단순 유기산, 알칸과 같은 탄소함유 물질에도 관심이 높아지 고 있으나 가격면에서 불리한 형편이다. 다만 이들 화합물은 순수한 형태 로 얻어지기 때문에 차후의 회수와 정제과정을 쉽게 해주는 이점이 있다. 메탄, 메탄올, n-알 칸 (n - alkanes) 은 균체 생산울 위한 기질로 이용되고 있 는데 메탄올은 Meth y l o p h ilu s me t hy lo t rop hu 회 (ICI Ltd ) 단세포 단백질 생산을 위한 기질로 영국 ICI 에서 이용하고 있다. n~알 칸은 유기산, 아미 노산, 비타민 보조인자, 탄수화물, 핵산, 항생물질 , 효소, 단백질의 생산에 이용되고 있다 (Fuk ui와 Tanaka, 1980). 4.2 탄소원의 선택에 미치는 요인 산물기 탄소원의 직접적인 이화에 의해 생산되는 경우 발효공정에서의 주샨물은 탄소원의 선택에 의해 결정된다 (W hit aker, 1973 ; Moo-You-ng, 1977). 원료가 생산비용의 60~77% 를 차지하는 에탄올이나 단세포 단백질과 같은 발효에서는 산물의 판매가격이 탄소원의 비용에 의해 크게 좌우된다. 시트르산 공정의 경우와 같이 금속과 같은 불순물은 탄수화물원으로부터 이용되기 전에 제거되어야 한다 (Woodward, J, et al., 1949). 기질의 선택은 정부 규정 입법에 의해 영향을 받게 된다. 우리나라에서 도 당밀이나 카사바 등의 탄소원의 수입은 시대에 따라 정부 방침이 달라 질수있다. 스카치 맥아 위스키 (Scotc h malt wh i sk y)는 단지 보리 맥아, 물, 효 모로만만들어진다. 배지조제의 방법 중 특히 멸균공정은 개개의 발효공정에 대한 탄수화물 의 적부에 영향을 미친다. 많은 균주의 증식을 부분적으로 제한하는 갈변 물질을 형성하는 암모늄이온과 아미노산이 반응하기 때문에 당질은 별도로
멸균하는 것이 가장 좋다. 잔분은 멸균과정에서 열을 받았을 때 젤라딘화 되어 점질성 용액이 되는 결점이 있기 때문에 2% 이하의 농도에서만 변 함없이 사용할 수 있다 (Solomons, 1969). 4.3 산물생성에 대한 탄소원의 영향 탄소원이 대사되는 속도가 균체량이나 1, ~} 대사산물의 생성에 영향을 미칠 수 있다는 것이 알려지고 있다. 신속히 대사되는 당의 농도가 높음으 로써 증식이 빨라질 때 종종 이차대사의 생산성이 낮아지는 수가 있다. 이 러한 현상은 gri s e ofu lv in ( Rhodes, 1963), 페니실린 (P i r t et al., 1967), 시오마이신 (K i mura, 1967), 바시트라신 (We i nber g, 196 7 ), 악티노마이신 (Marshall et al., 1968) 의 항생물질 생산에서 알려지고 있다 . 한때 젖 당 과 길이 즉시 대사되지 않는 당을 사용함으로써 문제를 극복하 였 으나 지 금은 포도당이나 자당의 반연속적 또는 연속적 공급방법을 채택하고 있다. 5 질소원 5.1 일반적으로 이용되는 질소원 대부분의 산업균주는 무기질소 또는 유기질소를 이용할 수 있는데 무기 질소는 암모니아가스, 암모늄염, 또는 질산염 등을 공급하게 된다• 황산 암 모늄 (ammon i um sul p ha t e) 과 같은 암모늄염에서 암모늄이온이 이용되면 유리산이 생성되어 산성화되는 것이 상례이다. 반면에 암모니아기스와 질 산염은 일반적으로 알칼리화한다. 질산암모늄 (runmon i um n it ra t e) 은 우 선 암모니아가 이용되면 산성화쪽으로 기울게 되고 질산염의 이용은 억제 된다. 암모니아가 고갈되면 질산염이 질소원으로 이용되어 다시 알칼리쪽 으로 기울게 된다. 이 유형의 한 예의로는 Gib b erella fu j i kuro i의 대사가
있다 (Borrow et al., 1961, 1964). 질산염의 존재하에서 암모니아의 동화 는 pH 2.8~3. 떼서 여제된다. 질산염의 동호片근 계속되고 p H 가 증가된 후 비로소 암모니아 동화기작을 다시 시작할 수 있게 된다. 유기질소로서 는 아미노산, 단백질, 요소들이 공급된다. 많은 경우 유기질소가 공급될 때 증식은 더 빠르고 일부 균주에서는 아미노산울 요구하는 것도 있다. 순수 아미노산의 주요 산업적 요구로는 아미노산 생산에 이용되는 아미노산 요 구성 돌연변이주에 대해서는 계획적으로 첨가되어야 한다. 그러나 리신 생 산에서 순수한 아미노산을 이용하는 것은 너무 비싸기 때문에 콩가루 분 해물로부터 얻은 메티오닌과 트레오닌을 첨가하기도 한다 (Naka y ama, 1972 ). 화학적으로 성분이 확인된 아미노산은 채용으로 쓰이는 백신의 생산에 이용된다 (Rhodes and Fletc h er, 1966 : Van Hemert, 1974). 단백질성 질소원으로서는 일반적으로 욱수수 침출액, 콩가루, 콩, 땅콩가 루, 목화씨가루, 증류 폐액, 카세인 가수분해물, 도살장 폐기물, 생선가루, 효모 추출물 등을 이용하게 된다. 5.2 질소원의 선택에 미치는 요인 질산염을 알루미늄이온으로- 전환시키는 효소인 질산영 환원효소(ni tra te reduc t ase) 는 암모니아 존재 아래에서 억제된다는 조절 메커니즘이 알려지고 있다 (Brown 과 MacDonald, 1974). 이와 같은 이유 때문에 암 모니아나 암모늄이온이 질소원으로 선택된다. 곰팡이에서 연구된 바에 의 하면 암모늄이온이 아미노산 투과효소(p ermease) 에 의한 아미노산의 홉 수력을 억제한다는 것이다 (W hit aker, 1976). Aspe rgi llu s n i dulan 예서는 암모니아에 의해서 알칼리성과 중성 pro te a se7} 생산되고 있다 (Cohen, 1973). 따라서 혼합질소원을 쓸 때 각각의 질소 구성성분은 대사 조절에 영향을 주어 한 성분의 농도가 감소할 때까지 그 구성성분이 우선적으로 이용된다. 질소원은 발효 경과에도 영향을 미친다는 것이 알려지고 있다. 죽 항생
물질 생산은 질소원이 빠르게 이용될 때 억제된다. 예를 들어 대두박 (so y meal) 은 질소 영양분기 골고루 갖추어져 있기 때문에 폴리엔 (po lye n e) 항생물질의 생산에서 좋은 질소원으로 생각되고 있다. 주요 성분은 단백질 이고 인을 적게 함유하고 천천히 가수분해되는 것이 특징이다. 따라서 생 성기에서의 항생물질 생산에 알맞게, 영양증식기 (t ro p ho p hase) 에서는 적 당한 생리조건을 부여하게 되는 것이다. 즉 분해물질 저해현성이 일어나지 않기 때문이다. 지베렐린(gi bberell i n) 합성에서 배지 중의 질소원은 다른 종류의 지베렐린의 생성과 상대적 생성비율에 영향을 미치는 것으로 알려 지고 있다(J e ff er y s, 1970). 개발 연구시 선택된 최우량 질소원의 예를 표 4.7 에 나타내었다.
표 4.7 이차대사산물을 위한 가장 좋은 질소원 소邊 주요질소원 참고문헌 Penic il l in 옥수수 침출액 (Corn ste e p liq u or) Moy er and Cog h il l (1946) Bacif rac in 땅콩가루 Inskeep et al.( 19 51 ) Ri bo fl av in 젤라틴의 췌장 소화액 Malzahn et al. ( 1959 ) Novobio c in 증류 폐액 (Di st i ller 's solubles) Hoeksema and smi th (19 61) Rif am y ci n \ 약용 배지 (Pharmamedia ) Sensi and Thie m ann 콩가루 (So y bean meal) , (NHi ) zS04 (19 67) Gib b erell in 암모늄과 천연식물 질소원 Jef f er ys ( 1970) Polye n es 콩가루 (So y bean meal) Marti n and Mac Dan- iel (1 9 77)
5.3 유기 질소원 대규모 공정에서는 질소원으로 암모니아염, 요소 또는 암모니아를 사용 한다. 효과적으로 대사할 수 있는 질소원은 옥수수 침출액의 농축된 추출
물(약 4% 가 질소) 속에 알라닌, 아르기닌, 글루탐산, 이소류신, 트레오닌, 발린, 페닐알라닌, 메티오닌, 시스테인과 같은 여러 아미노산들이 포함되어 있다. 옥수수 침출액이 함유하는 당은 주로 락트산균에 의해 락트산 (9~ 20% )으로 전환되고 있다(표 4.6). 효모 추출액 (yea st ex t rac t s) 은 많은 미생물에 대해서 유용한 기질이 다. 이는 빵의 효모로부터 50~55°C 에서 자기분해를 통해 생산되거나 또 는 고농도의 염화나트륨 존재하에서 원형질 분리를 시켜 생산된다. 효모 추출물 속에는 아미노산들과 펩티드, 수용성 비타민, 그리고 탄수화물이 포함되어 있다. 효모세포의 글리코겐과 트레할로오스(t rehalose) 는 효모 추출뚱기 생산되는 동안 포도당으로 가수분해되는데 표 4. 淡는 이에 대한 전형적인 분석치를 나타내고 있다. 효모 추출물의 구성성분은 세포배양에 사용된 기질들이 일부 효모 추출물의 질에 영향을 주기 때문에 변화될 수 가있다.
표 4.8 효모 추출물(y eas t e xt rac t)의 주성분 Yeast extr a ct pro duced by means of Aut ol ys i s Plasmolys i s with NaCl Comp o sit ion (%) Dry matt er 70 80 Tota l nitro g en 8.8 7.4 Prote i n ( N X 6.25) 55 46 NaCl <1 18 Amino acid s (% of tot a l ) Alan ine 3.4 2.3 Amino buty ric acid 0.1 0.1 Argi nine 2.1 1.1 Asp ar agi ne 3.8 3.1
Cy st i ne 0.3 0.2 Glut am i c acid 7.2 5.1 Glyc i n e 1.6 1.6 Hi st i di n e 0.9 0.8 Isoleucin e 2.0 1.6 Leucin e 2.9 2.3 Ly si n e 3.2 2.9 Meth ion ine 0.5 0.5 Ornit hin e 0.3 0.9 Pheny! a lanin e 1.6 1.6 Pralin e 1.6 1.5 Serin e 1.9 1.5 Threonin e 1.9 1.4 Tyros in e 0.8 0.5 Vali ne 2.3 1.9 Vi tam in conte n t( ppm ) Th iam ine 20~30 10~75 Ri bo fl av in 50~70 50~70 Py rido xin e 25~35 20~30 Ni ac in a mi de 600 100 Panto t h e n ic acid 200 350 (Da ta from Ohly Inc., Hamburg)
펩돈 (Pe pt ones, 단백질 가수분해물)은 많은 미생물들에 의해 이용되고 있으나 산업적인 응용에는 가격이 비교적 비싸다. 펩톤의 원료로는 고기, 카세인, 젤라틴, 땅콩 씨앗, 콩가루, 목화 씨앗, 그리고 해바라기 씨앗 등이 入냉된다. 펩톤의 구성성분은 원료에 따라 다르다. 예를 들어 젤라틴으로 만든 펩돈은 프롤린과 히드록시프롤린이 풍부한 반면 황을 지닌 아미노산 은 거의 없다. 반면 젤라틴에서 뽑아낸 펩톤은 프롤린과 시스데인이 상당 한 비율을 차지하는 반면 리신은 결핍되어 있다• 식물체에서 뽑아낸 펩톤
(콩펩톤, 면실펩톤)은 탄수호稽이 많은 비율을 차지한다. 또한 표 4. 斜|서 보듯이 펩톤의 최종산물은 산 또는 효소적 가수분해 방식에 따라 영향을 받으며 특히 트립토판 함량에서 영향이 크다. 콩에서 콩기름을 추출하고 난 후의 잔사물인 대두박 (so y meal) 은 복합 기질이다. 이의 분석 결과를 보면 단백질 함량이 50%, 탄수화물 함량이 30%, 1% 의 지방찌꺼기, 그리고 1. 8% 의 레시틴 (le cit h i n) 으로 구성되어 있다.
표 4.9 펩톤의 조성분 N-Z- HY-Case® Soy Amine ® A Amine Pep ton e Sta r ti ng mate r ia l Casein Casein Soy meal Hy dr olyt ic meth o d Enzy m ati c Acid Enzy- mati c Comp o sit ion ( %) Wate r conte n t 4.8 3.5 4.0 Ash 5.8 39.7 14.0 Tota l nit ro g en 12.8 8.3 9.2 Amino nit ro ge n 6.7 6.4 1.8 NaCl 3.0 38.0 5.9 Carbohyd rate 29.0 Free Ami no acid s ( mg / g) Alan ine 16.8 14.1 3.3 Argi nine 30.2 5.0 1.1 Asp ar ti c acid 8.7 33.2 2.4 Cy st i ne 0.7 Gluta m i c acid 38.6 79.6 5.6 Glyc i n e 4.4 9.3 2.3 Hist i din e 13.3 4.6 1.1 Isoleucin e 29.9 10.7 2.8
Leucin e 71. 9 29.7 9.4 Ly si n e 61. 1 12.8 7.9 Meth i o n in e 22.7 11. 2 3.3 Pheny la lanin e 33. 0 9.7 3.7 Prolin e 7.4 34. 5 0.8 Serin e 28. 7 19.8 4.8 Threonin e 21. 5 13. 1 1.9 Tryp top h a n 8.6 0.0 5 1.6 Ty ro sin e 14.0 4.9 0.7 Vali ne 36.4 16.7 3.8 (Da ta from Sheff ield Chem. Co.)
6 무기영류(mi neral) 와 미량성분 배지에서 마그네슘, 인, 칼륨, 황, 칼슘, 염소는 필수원소인데 요구 농도 때문에 별개의 구성성분으로- 첨가되어야 한다. 코발트, 구리, 철, 망간, 몰 리브덴, 아연 등도 필수적이긴 하지만 보통 다른 주요 성분의 불순물로 존 재한다• 옥수수 침출액의 분석이 표 4. 個} 같으며 합성배지를 사용할 때 미량원소(mi nor elemen t s) 는 별도로 첨가되어야 한다. 보통 무기성분을 공급하는 상태와 농도의 범위는 표 4 .1여t 참조할 수 있다.
표 4.10 무기성분의 전형적인 농도 범위(g dm -3 ) 성 분 · 첨가범위 *KH2 P0 4 1.0 ~4.0 Mg S0 4 • 7H20 0.25~3.0 KCl 0.5~12.0 CaC03 5.0~17.0 FzS04 • 4H2 0 0.01~0.1 ZnS04 • 8H2 0 0.1 ~1.0
MnS04 • H20 0.01~0.1 CuS04 • 5H2 0 0.0 0 3~0.01 Na2M o O • 2H2 0 0.01~0.1
무기질의 농도는 발효과정에서 매우 중요한데 어떤 이차대사 과정은 무 기인산의 농도에 대해 영양중식 (ve g e t~ti ve gro wt h) 시기보다 내성의 범 위가 더 낮다. 무기인산의 농도는 바시트라산 (bac it rac i n), 시트르산 (c it ric acid , 표면배양), 에르고트 (er go t), 모노마이신 (monom y c i n), 노보비 신 (novob i c i n), 옥시테트라사이클린 (ox yt e t rac y cl i ne), 폴리엔(p ol y en es), 리파마이산 Y(rif am y ci n Y), 스트렙토마이신 (s t re pt om y c i n), 반코 마이신 (vancom y c i n), 비오마이신 (v i om y c i n) 의 생산에 영향을 미친다 (Sensi and Thie m an, 1967 ; Wein l erg, 1974). 그러나 Py ro lni tri n (Arim a et al., 1965), bic y cl omy ci n ( Mi yo shi et al., 1972), t証 op ep tin( Mi yai r i et al., 1970) 은 인산 농도가 높은 배지에서 잘 생산된 다. 두 모노마이신 항생물질은 인산이 O.l m M 또는 0 .4 mM 일 때 Str - ept om y ce s j ama i cens i폐 의해 선택적으로 생산된다 (Hall and Hassall, 1970). 망간, 철, 아연은 이차대사에서 가장 중요하다. 이차대사 체제에서 산물 의 수율은 주요 금속 (ke y me t al) 의 대수적인 농도에 따라 직선상으로 변 화하는데 이 직선관계는 세포 증식에 유해할 때는 적용되지 않는다. 최대 성장에 요구되는 것보다 더 많은 미량 금속의 농도에 의해 수율이 영향을 받는 일차, 이차 미생물 산물을 보면 표 4. 11 에서와 같다• 염소는 곰팡이의 대사에서 영양학적 역할이 뚜렷하지 않지만 호영성 세 균은필요하다. 천연 탄소원이나 질소원은 요구되는 비타민을 함유하는 경우가 많다. 비 타민이 결핍되었을 때 이 결핍울 제거하도록 하여야 하는데 만약 하나의 비타민이 요구될 때 값이 싼 다양한 비타민원을 다량 이용하는 것보다 순 수한 비타민을 첨가하는 것이 더 경제적일 수 있다는 것을 기억할 필요가
표 4.11 이차, 이차 대사산물에 영향을 미치는 미량 원소 소별 미량원소 참고문헌 Ba cit rac in Mn Wein b erg and Tonnis (19 66) Rib o fl av in I Fe • Co Hi ck ey ( 1945) Fe Tanner at al. (19 45) Prote a se Mn Mi zu sawa et al. ( 1966) Acti no my ci n Fe, Zn Katz et al. ( 1958) Chloramp he n ico l Fe, Zn Gallic c hio et al. ( 1958) Neomy ci n Fe, Zn Maju m der and Maju m der (19 65) Ci tric acid Fe, Mn, Zn Shu and Jo hnson (1948) Penic i l li n Fe, Zn, Cu Foste r et al. (19 43) Koff ler et al. ( 1947) Gris e ofu l vin I Zn I Grove ( 1967)
있다. 식초 생산에는 calciu m pan t ot h enat e (Beaman, 1967), 글루탐산 의 생산에는 바이오틴, 또한 어떤 생산균주에는 티아민을 요구한다 (K i n osh ita et al., 1972). 7 완충제 (bu ffers ) 적절한 생산성을 확보하려면 p H 조절이 매우 중요하다• 한 화힙물을· 완 충제로서 특별히 배지에 첨가할 수 있다. calciu m carbona t혜十 첨가함으 로써 pH 7.0 정도로 완충화시킬 수 있고 만약 p H 가 감소하면 탄산염이 분해되고 pH 7} 증가되면 미생물의 산 생산에 의해 중성화되어 수정된다. 배지의 한 성분인 인산염의 첨가도 또한 중요한 완충의 역할을 한다. 옥 수수 침출액과 같이 단백질, 펩티드, 아미노산에 의해 완충능이 제공되므
로 탄소원이나 질소원을 첨가하면 p H 조절의 토대가 된다. p H 는 또한 암 모니아, 수산화나트륨, 황산을 첨가함으로써 의적으로 조절할 수도 있다. 8 전구물질과 대사조절 대사조절물질 (meta b olic regu l ato r s) 및 소모제석을 유지시키기보다는 산물의 생산을 조절하는 것이 있다. 전구물질, 억제물질, 유도물질과 같은 첨가물은 발효과정을 조절하는 데 쓰인다. 8.1 전구물질 ( pre cursors ) 발효에 화학물질이 첨가되면 원하는 산물에 직접 도입될 수 있는 생물 전환반응이 있는데, 그 초기의 예로서는 페니실린의 수율을 증가시키는 발 효가 있다 (Mo y er and Cog hill, 1946, 1947). 다른 종류의 곁사슬도 페 니실린 분자에 도입시킬 수 있다. 다른 곁사슬 첨가의 가치는 옥수수 침출 액의 첨가가 페니실린의 수율을 20un it s/cm~에 서 100un it s/cm 3 로 증 가시킨다는 것이 인식되면서부터 처음으로 평가를 받게 된 것이다. 즉 벤 질페니실린 (benz y l pen ic i ll i n e ), 페니실린 G 를 산출하게끔 페니실린 분 자내로 우선 도입되는 페닐아민 (p heny la mi ne) 을 옥수수 침출액이 함유하 고 있다는 것이 발견되었다. 페니실린의 활성은 결사슬에 존재하고 제한요 소 O i m iti n g fa c t or) 는 결사슬의 합성이라는 것이 확립된 후부터는 배지 에 곁사슬 전구물질 (특히 ph eny la ceti c ac i d) 을 첨가하는 것이 실용화되 었다. Sm it h 와 B i de(1948) 는 배지에 페닐아세트산(p hen y lace ti c acid ) 과 그 유도체의 첨가가 페니실린 생산울 油店로 증가시킨다는 것을 밝혔다. 페닐아세트산은 현재도 페니실린 생산에서 가장 광범위하게 이용되는 전구 물질이다. 전구물질의 몇몇 예를 표 4 .1 2 에 나타냈다.
표 4.12 발효공정에 이용되는 전구물질 전구물질 소邊 균주 참고문헌 pl).ey l a ceti c acid Penic i ll in G Penic i ll i n Moy er and 와관련화합물 chry so g en um cog hi l l ( 1947) Phenoxy aceti c Penic i ll i n V Penic i ll i n Sop er et al. acid chlorid e chry so g en um (1948) *Prop ri o n ate chlorte t r a cy cl in e Str ep t om y ce s VanDy ck and de aureofa c ie n s Somer (19 52) Cy an id e s Gris e ofu lv in Penic il l i u n Rhodes et al. gri s eo fu lv in (1955) P-Iononones Ri bo fl av in Lacto b acil lu s Smi le y and bulga r ic u s sto n e (1955) a-Ami no Vi tam in B12 Prop ri o n o M~rvy n and Buty ri c acid bacte r iu m Smi th ( 1964) carote n oid s Str ep t om y ce s Rey es et al. SPP. (19 64) L-i so leucin e Phyc o my ce s Nakay am a blakesleeanus (19 72b) Bacil lu s subti lis 덕광은 타기술에 의한 것보다 높지 않다.
8.2 저해물질(inhi b it ors) 저해물질을 발효에 첨가하면 특정산물을 더 생산하거나 대사의 중간산 물이 축적되는 경우가 있다. 초기의 실례 중의 하나는 글리세롤의 미생물 적 생산이다. 글리세롤 생산은 아세트알데히드를 제거하여 에탄올 발효를 변경시킴으로 가능하다. 배양액에 소듐 바이설페이트 (so di um bis u lph it e) 를 첨가하면 아세트알데히드 바이설페이트 부가물 생성을 유도하게 된다•
C H:1 CH=O+Na + g o :1 一 CHi· C H < H O S0:1 N a+ 아세트알데히드가 NADH 최 재산화에 이용되지 않기 때문에 수소수용 체로서 그 위치는 해당 과정에서 생성된 디하이드로 아세톤 포스페이트에 의해 대치되는 것이다. 이 반응산물은 굴리세롤로 전환되는 gly c e rol-3- p hos p ha t eOl 다. 저해물질의 이용 예는 표 4 .1 3 에 정리되어 있다. 저해물질은 대부분의 경우 원하는 산물의 수율을 증가시키고 원하지 않는 산물의 수율을 감소 시키는데 효력이 있는 것이다• 저해물질은 또한 세포벽 구조에 영향울 주
표 4.13 발효에 이용되는 저해물질 소邊 저해물질 주요효과 균주 참고문헌 Glyc e rol Sodiu m Aceta l dehy de Saccharomy ce s Eoff et al. bis u lph it e 생산억제 cereui si e ae (1919) Tetr a cy c- Bromi de chlorote t r a cy c- Str ep tom y ce s Lep e ti t line li ne 형성억제 aureofa c ie n s (1957) Glut am i c Penic i ll i n 세포벽 두과성 Mi cr ococcus Ph illips and acid glu ta m i cu s Somerson (19 60) Cit ric acid 알칼리금속 oxalic acid Aspe rgi llu s Batt i /인산 2.0 억제 mg er (1967) 이하의 pH Valin e 다 oJ il- 다양한 저해물 Breuib a cte r iu m Uemura et 억제물질 질에 의한다 roseum al. ( 1972) 양한효과 Rif am y ci n Di-€thy l 다른 rifa m y ci n Nocardia Lancin i B borbit u- 류의 억제 medit err anei and Wi te rate (1973)
고 대사산물의 배설을 위한 두과력의 증가에 이용되는데, 가장 좋은 예로 는 글루탐산 생산에서의 페니실린과 계면활성제의 이용이다 (Ph i ll ip s and Somerson, 1960). 8.3 유도물질 ( ind ucers ) 샨법적 관심의 대상이 되는 대부분의 효소는 유도 가능하며 유도된 효 소는 보통효소의 기질이거나 구조적으로 연관된 화합물질로서 유도물질의 존재하에서만 합성된다. 따라서 특정한 유도물질이 다양한 미생물효소 배 지에 함유되어 있어야 한다. 광범위한 종설이 Dav i es 에 의해 정리되고 있 다(1 963). 불행히도 효소 제조업체들은 정보를 일반적인 용어로밖에 기술 할 수 없기 때문에 사용되는 유도물질에 대해 상세히 출판되고 있지 않다. 정확한 배지조제는 최적 수율을 울리는 데 분명히 중요하다. Prot ea se 생산에는 고농도의 단백질이 존재해야 하고 탄수화물은 과도하게 존재해서 는 안된다고 Auns t ru p (1974) 는 보고하고 있다.
표 4.14 공업적으로 중요한 효소 유도물질 효소 유도물질 균주 참고문헌 ex-Amy la se 전분 (s t arch) Aspe rgi llu s SPP. W ind is h and Mhatr e ( l965 ) Pullula-Malto s e Bacil lu s subti lis Wallenfe ls et nase Aerobacte r al. ( 1966) Pencil lin Pheny la ceti c aerog en es Carrin g ton ( 1971 ) acy la st acid Escheric h ia coli Keay ( l971) Prot ea se Vari ou s pro te i n s Bacil lu s SPP. Aunstr u p ( l974) Str ep t oc occus SPP. Reese( 1972) Cellulase Cellulose 'Irich oderma vir i d e Fog a rty and Pecti na se Pec ti n( 사과찌꺼기 , Aspe rgi llu s SPP. Ward(1 9 74) 감귤껍질)
탄수화물은 종종 이화 여제의 원인이 된다 (Dav i es, 1963 : Inami ne , Largo and Demain 1969 : Reese, 1972). 발효과정을 통해 낮은 농도를 유지하도록 탄수화물을 첨가함으로써 다양한 형태의 효소의 생산에 적정 조건을 달성해 온 것이다 (Dav i es, 1963 ; Kalabokia s , 1972 ; Reese, 1972). 유도물질의 색다론 응용으로는 수트랩토마이신 생산에서의 yea st man- nan 을 사용하는 것이다(I nam i ne, et al., 1969). 생산균주 Str ep tom y ce s gri s eu s- 2 mannos i dos t re pt om y c i n 을 스트렙토마기산으로 전환시키는 a -mannos i das 遷 생산하게끔 yea st mannan 에 의해 유도된다. 8.4 거품소포( anti foa ms ) 대부분의 미생물학적 과정에서 거품(fo am i n g) 형성이 문제가 된다. 일 반적인 원인은 배지의 단백질에 의한 것인데 이것은 공기와 배°뇽버의 접 촉면에 변성이 일어나고 즉시 파괴되지 않는 피막을 형성하는 것이다. 거 품형성은 자가분해롤 일으키고 나아가 세포 단백질의 방출을 일으켜서 거 품의 안정성을 증가시 배지로부터 세포를 소멸시키게 하는 경우도 있다. Hall et a l.(1 973) 은 발효에서의 거품형성에 57} 지 유형을 제시했다. 1. 거품형성은 발효과정을 동해 일정한 수준에서 지속된다. 2. 발효의 초기에는 거품형성이 일정하게 하강하고 후에 일정하게 지속된다. 3. 거품형성은 발효과정의 초기단계에서 약간 감소하고 나서 증가한다. 4. 발효는 처음에 낮은 거품형성에서 점차 증가한다. 5. 발효동안의 앞에서 말한 유형의 둘 도는 그 이상의 조합형인 더 복잡한 거품형성의 유형. 과도한 거품형성이 일어날 때 문제해결에 접근하는 두 가지 방법이 있 다 (Hall et al., 1973).
1. 복잡한 영양물질의 부분적 정제와 물리적인 변수(p H, 온도, 통기, 교반) 의 수정을 시도할 것.(거품이 배지의 구성성분 때문이고 대사 때문이 아 니라고 가정해서 이 영역에서의 제한된 작업만이 있을 뿐이다.) 2. 거품형성을 피할 수 없으면 소포제를 이용하여야 한다. 이 방법이 더 표 준적인 접근이다. 소포제는 표면활성제이며 거품의 표면장력을 감소시킨다. 소포제 자체는 안정된 거품을 형성할 수 없다 (Solomons, 1967). 이상적인 소포제는 다음과 같은 특성을 가져야 한다. 1. 거품에 대해 찰 반응하고 즉시 분산되어야 한다 . 2. 낮은 농도에서 작용해야 한다. 3. 새로운 거품형성을 방지하는데 오래 작용해야 한다. 4. 미생물에 비독성이어야 한다. 5. 인간과 동물에 대해 독성이 없어야 한다. 6. 산물의 추출에 어떤 문제를 야기하지 않아야 한다. 7. 조작하는 데 위험이 없어야 한다. 8. 값이 씨야한다. 9. 산소공급에 영향이 없어야 한다. 10. 가열 살균할 수 있어야 한다. 이와 같은 요구를 충족시키는 화합물은 다론 발효과정에서도 적용 가능한 것 으로알려지고있다. 1. 알코올류 ; ste a ryl and ocy l decanol. 2. 에스테르 (Es t ers) 3. 지방산과 . 그 유도체, 특히 목화씨 기름, 아마씨 기름, 콩기름, 울리브 기름 과 피마자유에 함유하는 gly c e rid s . 4. 실리콘류 5. Sulph o nate s 6. 기타 ; Alkate r ge C, oxazali ne , po lyp r op yle us gly c o l 등
이와 같은 소포제는 일반적으로 발효중 거품형성이 일어날 때 첨가된다. 많은 소포제는 낮은 용해성 때문에 돼지기름, 액체 파라민, 피마자유 등에 혼합하여 첨가하는데 때로는 발효과정에서 영향을 미친다 (Solomons, 1967). 불행히도 발효조절에 필요한 많은 소포제의 농도중가는 50% 정도에 이 르기까지 산소 이동률을 감소시킨다. 따라서 소포제의 첨가는 절대 최소량 이어야 한다 (Solomons and Perkin s , 1958 : Phil li p s et al., 1960 : Bull and Kemp e, 1971). 또박 산소이동이 소포제의 첨가에 의해 심하게 영향을 받는 경우라면 기계적인 거품 파쇄장치로 변경할 것도 고려하여야 한다. 참고문헌 Abbott . B.J. and Clamen, • A.(1 973) The relati on ship of substr a te , gro wt h rate and main t e n ance coeff ici e n t to sin g le cell pro te i n pro ducti on . Bi ot e c h. Bi oe ng . 15. 117~127. Aiba , S. and Mi llis, N.F.(1 9 73) Scale-up . In Bio c hemi ca l Eng ine ering (2nd edit ion ). pp. 195~217. Academ ic pre ss, New York. Arim a, K., Imanaka, H.(1965) St ud ie s on pyrr olnit rin , a ·ne w anti - bio t i c. 1. Isolati on of pyrr olni tri n . J. Anti bi o t ic s , ser A, 18, 201~ 204. Aunstr u p , K.( 1974) Industr i a l pro ducti on of pro te o lyt ic enzy m es. In Industr i a l Aspe cts of Bi oc hemi str y , Part A, pp. 23~46(Ed itor Sp e n-cer, B.). North Holland, Amste r dam. Beaman, R.G . (1 967) Vi ne ga r fer menta t i on . In Mi cro bia l Technolog y, pp. 344~359(Edit or Pepp le r, H.J. ). Rein b old, New York. Borrow, A., Brown, S., and Swait , J.C .(1964) The kin e ti cs of meta b -oli sm of Gi bb erella fuji kur oi in sti rre d cultu r e. Can. J. Mi cr obio l . 10. 407~444.
Borrow, A., Lio y d , P.B . and Ni xo n, I.S. (1 9 61 ) Meta b olis m of Gi b- berella fujiku roi in sti rr ed cultu re. Can. J. Mi cr ob i a l , 227~2 76 . Brown, C.M., and Meers, J.F .( 1974) Phy s io l og ica l asp e cts of mi - crobia l ino rga nic nit rog e n meta b oli sm . Adu. in Mi cr obia l Phy s. 11. 1~52. Bull, D.n. and Kemp e , L.L .(19 71) Infl ue nce of surfa c e acti ve age nts on oxy ge n absorp tion at the free int e r fa c e in a sti rr ed fer ment or , Bio t e c h, Bio e ng . 13. 529~547. Calam, C.T. and Ni zo n, I.S. (1960) Gi bb erellic acid , Briti sh Pate n t 839, 652. Carrin g ton , T.R. (1 971) The develop m ent of commercia l pro cesses for th e pro duc tion of 6-ami no p e nic i l la nic acid ( 6-A PA). Proc. Roy . Soc. London B. 179, 321~333. Cohen, B.L. (1 9 73) The neut ra l and alkalin e pro te a ses of Asp e rg i llu s nidu lans. J. Gen. Mi cr obia l. 77. 521 ~528. Cooney, C.L.(1981) Grow th of micr o--0 r ga nis m s. In Bio t e c hno lo gy , vol. 1. pp. 73~112(Edit ors Rehm, H.J. and Reed, G.). Verlag Chem ie, Wein h eim . Davie s , R.(1 963) Mi cr obia l ext ra cellular enzy m es, the ir Uses and Some fac to rs aff ec ti ng the ir for mati on . In Bi oc hemi st r y of Indus- trial Mi cr o-orga nis m s, pp. 68~150(Edit ors Rain b ow, C. and Rose, A.H ) . Academ ic Press, London. Eoff , J.R., Lin d er, W.V.(1 9 19) Producti on of gly c erin e from sug a r by fer ment at i on . Ind. En g. Chem. 11. 842~845. Fog a rty , W.M. and Ward, O.P.(1 9 74) Pecti na ses and pe cti c po l- ysa ccharid e s. Prog. Industr, Mi cr obio l , 13, 59~119. Foste r , J.W ., Woodruf f, H.B. (19 43) Mi cr obio l og ica l asp e ct s of pe n i- cil lin. 3. Produc tion of pe n ici l lin in subsurfa c e cultu res of Penic i l - lium not at u m, Bact. 46, 421~432. Fukui, S. and Tanaka, A.(1980) Producti on of usefu l comp o unds fro- m alkane media in Jap a n. Adu. Bi oc hem. Eng. 17, 1~35. Gallic ch io , V. and Got tlie b , D.(1958) The bio s y nthe sis of chi- oramp h enic a l. ill. Ef fec ts of mi cr onutr i e n ts on sy n th esis . My c -
olog ia, 50, 490~500. Gore, J.H ., Reis m an, H.B( 19 68 ) L-g l ut am i c acid by conti nu ous fer -ment at i on . U. S. Pate n t 3, 402, 102. Grove, J.F .( 1967) Gris e ofu lv in , In Anii bio t i cs , II , pp. 123~133( Edit or s Goltl ieb . p. and shaw, P.D.). Sp ri n g er -V erlag Berlin . Hall, M.J. and Bassali, C.H.(1 9 70) Producti on of the monomy c in s , novel dep s ip e p tide anti bi o t i cs , Ap pl. Mi cr obia l . 19. 109~112. Harned, R.L.(19 69) Ri bo fl av in e pro ducti on . U. S. Pa ten t 3, 475, 274. Harris , G.(1 9 62) The str u ctu ral chem ist r y of barley and malt. In Barley and Malt, Bio l og y, Bi oc hemi st r y and Technolog y, pp. 431 ~ 582(Edit or Cook, A.H.). Academi c Press, London. Hi ck ey, R.J.(19 45) The ina cti va ti on of iro n by 2,r-bip yr id i n e and its eff ec t on rib o fl av in e sy nthe sis by Clostr i d i u m aceto b uty li cu m. Arch. Bi oc h em. 8, 439~447. Hoeksema, H.an d Sm ith, C.G.(1961 ) Novobio c in . Prog. Industr. Mi c- robio l , 3, 91~139. Houg h , J.S ., Brig gs, D.E(1971) Maltin g and Brewin g Scie n ce, Chap ter 7. Chap m an and Hall, London. Imrie , F.K .E . 1969. Fermenta t i on media . Sug a r and molasses. Proc. Bio c hem. Ja nuary : 34~35. Inami ne , E., Lag o , B.D.( 1969) Reg u lati on of manosid a se, an enzy m e of stre p tom y c in bio s y n t he sis , In Fermenta t i on Advances, pp. 199~ 221 (E dit or Perlman, D.). Academ ic Press, New York. Inskeep, G.C., Bennett , R.E .(1 9 51 ) Bacit rac in , pro duct of bio c hem i- cal eng ine erin g . Ind.E n g. chem. 43, 1488~1498. Jef f er ys , E.G.(1 9 70) The gibb erellin fer menta t i on . adv. Ap pl. Mi c- robi ol . 13, 283-316. Katz , E., Pie n ta , P.(1958) The role of nutr i t ion in the syn the sis of acti no my c in . Ap pl. Mi cr obio l , 6, 236~241. Keay, L.( 19 71) Mi cr obia l pro te a ses. Process Bio c hem, 6(8), 17~21. Ki m ura, A. ( 1967) Bi oc hemi ca l stu die s on Str ep tom y ce s sio y a e nsis . II . Mechan ism of the inh ib i t or y eff ec t of glu cose on sio m y ci n for ma- tion . Ag r. Bi ol . chem.(Toky o ), 31, 845~852.
Ki no shit a, S. and Tanaka, K.(19 72) Glut ar nic acid in The Mi cr obia l Producti on of Ami no Acid s , pp. 263~324(Edit or s Yamada, K., Ki n- oshit a, S., Tsunoda, T. and Ai da , K.). Halste d Press-W ile y , New York. Koff ler , H., Knig h t, S.G.( 1947) The eff ec t of certa in mi ne ral ele-ments on te pro ducti on of pe nic i l lin in shake flas ks. J. Bact . 53, 115~123. Lancin i , G. and whit e, R.J.(19 73) Rif am y c in fer ment at i on stu d ie s . Process Bi oc hem, 8(7), 14~16. Lepe ti t, S.p. A .(1957) Bromote t r a cy cl in . Briti sh Pate n t 772, 149. Lil iy, V.G.(1965) The chem ica l envir o runent for gro wt h. 1. Media , macro-andmi cr onutr i e n ts . In The fun g i, Vol. 1, pp. 465 ~ 478 ( Edi -tor s Ai ns worth , G.C. and sussman, A.S.). Academ ic Press, New York. Maju m dar, M.K . and Maju m dar, S.K .(1 965) Ef fec ts of mi ne rals on neomy ci n pro ducti on by Str e p tom y ce s frad ia e . Ap pl. Mi cr obio l . 13. 190~193. Malzahn, R.C ., Phil lips, R.F. (1 9 59) Ri bo fl av in . U. S. Pate n t 2, 876, 169. Marshall, R., Redfi el d, B.,(1 968) Chang es in ph enoxazin o ne syn - the ta s e acti vi t y durin g the gro wt h cy cl e of St re p tom y ce s ant- ibi o t i cu s. Arch. Bi oc hem. Bi op h ys 123, 317~323. Marti n, J.F . and McDan iel , L.E.(1977) Producti on of po lye ne mac-roli de anti bi o t i cs . Adu. Ap pl. Mi cr obia l , 21, 1~52. Mervy n, L. and Sm ith, E.L.(1964) The bio c hem ist r y of vit am in B fer ment at i on , Rrog, Industr . Mi cr obia l , 5. 150~201 . Mey ra th , J.a nd Baye r , K.( 1979) Bi om ass from whey. In Economi c Mi cr obio l ogy , Vol. 4, pp. 207~269(Edit or Rose, A.H.). Academi c Press, London. Mi yairi , N., Mi yos h i, T.,(1970) St ud ie s on thi o p ep tin anti bi o t i es. 1. Characte r is t i cs of thi o p e p tin B. J. Anti bi o t i ~s , 23, 113~119. Mi yo shi, N., Mi yai k i, H.,(1972) Bi cy c lomy c in , a new anti bi o t i c. 1. Taxonomy , Isolati on and Charac ter iz a ti on . J. Anti bi o t i cs , 25, 269~275.
Mi zu sawa, K., Ichis h awa, E.( 1966) Prote o lyt ic enzym e of the th e- rmop h il ic St re p tom y c es [I . Identi fica ti on of the orga n is m and some condit ion s of pro t ea se for mati on , Ag ri c , Bio l . Chem (Toky o ), 30, 35~41. Moo-Young, M.( 1977) Economi cs of SCP pro ducti on . Process Bio - chem, 12(4), 6~10. Moy e r, A.J. and Cog h il l, R.D .(1 9 46) Penic i ll in X. The laborato r y scale pro ducti on of pe nic i l lin in submerge d cultu re by Penic i l lium nota t u m . Westl in g ( N RRL 832). J. Bact. 51, 73~93. Moy e r, A.J. and Cog h il l, R.D .(1 9 47) Penic i l lin X. The eff ec t of ph e-ny la ceti c acid on pe n ici l lin pro ducti on . J. Bact. 53, 329~341. Nakay a ma, K. ( 1972a) Ly s in e and dia m ino p im eli c acid . In '1he Mi - crobia l Producti on of Ami no Acid s , pp. 369~397(edit or s Yamada, K., Ki no shit a, S., Halste d Press-W ile y , New York. Nakay a ma, K.(1 9 72b) Mi cr o-0 r ga nis m s in am ino acid fer menta t i on . In Fermenta t i on Technolog Today, pp. 433~438(Ed itor Terui , G.). Socie t y of Fermenta t o n Technolog y, Ja p a n. Perlman, D.(1970) The evoluti on of pe nic i l lin manufa ctur in g pr o-cesses. In the Hi sto r y of Penic i ll i n Producti on , pp. 25~30(Ed itor Elder, A.L. ). Chem. Eng. Prog. Sy m p . Serie s , 60(100). Phil lips, K.L ., Roxburgh ,J. H .(1960) Ef fec t of anti foa m age nts on oxy ge n tra nsfe r in deep tan k fer ment at i on s. J. Bio c hem. Mi c- robio l . Thchnol. En g. 2, 81~91. Phil lips, Tand Somerson, N.L. (1 960). Gluta m i c acid . U. S. Pa ten t 3,080, 297. Pir t , S.J. and Rig h elato , R.C .(1 9 67) Ef fec t of grow t h rate on the sy n t he is of pe nic i ll in by Pen ici l lium chrys o g e num in batc h and chemosta t cultu res, Ap pl. Mi cr obio l 15, 1284~1290. Reese, E.T. ( 1972) Enzy m e pro ducti on from ins oluble substr a te s . Bio t e c hnol and Bi oe ng . Sy m p . 3. 43~62. Rey e s, P., Chic h este r , C.0.(1964) Mechan ism of B-io n one sti m u-lati on of carote n oid and ergo ste r ol bio s y n t he sis in Phy c omy c es blakesleeanus. Bio c him . Bio p h ys Acta , 90, 578~592.
Rhodes, A.(1 9 63) Gris e ofu lv in pro ducti on and bio s y n th e sis . Prag. lndustr. Mi cro bia l . 4, 165~ 187. Rhodes, A., and Fletc h er, D.L.(1 9 55 ) Imp ro vement s in or relati ng to the pro ducti on of the anti bi o t i c gri s e ofu lv in . Briti sh Pate n t 784, 618. Rhodes, A. and Fletc h er, D.L.(1 9 66) Prin c ip le s of Industr i a l Mi cr o- bio l og y Perga mon Press, Oxfo r d. Sensi, P. and Thie m ann, J.E .( 1967) Producti on of rif am y c in s . Prag. lndustr . Mi cro bia l , 6, 21 ~ 60. Shu, P. and Jo hnson, M.J. ( 1948) Inte r dep e ndence of mediu m con- sti tue nts in cit ric acid pro ducti on by submerge d fer ment at i on , J. Bact. 56, 577~585. Sm ile y , K.L. and St on e, L.(1955) Produc tion of rib o fl av in e by Ashby a gos syp ii, U.S. Pate n t 2,702, 265. Sm ith, E.L. and Bi de , A.E.(1948) Penic i l li n salts Bio c hem. J. 42, XVll~ XVIII. Solomons, G.L.(1967) Anti foa ms. Process Bi oc hem. 2(10), 47~48. Solomons, G.L.(1969) Mate r ia l s and Meth o ds in Fermenta t i on . Academi c Press London. Solomons, G.L. and Perki ns . M.(1 9 58) The measurement and mech- anis m of oxy ge n tra nsfe r in submerge d cultu r e. J. Ap pl. Chem. 8, 251~259. Sop e r, Q.F . and Jon es, R.G .(1948) Bi os y n t he sis of pe n ici l lins . vii. Oxy -a nd mercap toa ceti c acid s . J. Amer. Chem. SOC. 70, 2849~ 2855. Tanner, F.W., Voj no vic h , C.(1945) Ri bo fl av in pro duc tion by Can-did a spe cie s . Scie n ce (New York). 101, 180~181. Top iw ala, R.H. and Khosrovi, B.(1978) Wate r recy cl e in bio m ass pro ducti on pro cesses. Bi ot e c h, Bi oe ng . 20, 73~85. Uemura, T., Sug isa ki. 2.(1972) Valin e ..I n The Mi cr obia l Producti on of Ami no Acid s , pp. 339~368 (Edit ors Yamada, K., Ki no shit a, S.,) Halste d Press-Wi ley, New York. Underkofl er , L.A.(1 9 66) Producti on of commerci al enzym e s. In Enz-
ym es in Food Processin g . Chap ter 10(Edit or Reed, G). Academi c Press, New York. Van Dy c k, P. and DE Somer, P.(1 9 52) Producti on and ext ra cti on meth ods of aureomy c in . Anti bi o t i cs and Chemoth r apy 2, 184~198. Van Hemert, P.(1 9 74) Vaccin e pro ducti on as a unit pro cess. Prog. Industr . Mi cr obio l , 13. 151~271. Wallen fels , K., and Rached, J.R . (19 66) Pullulanase from Aerobac ter aerog en es. Bio c hem. Bio p h yo . Res. Commun. 22, 254~261. Wein b erg, E.D.(1 9 67) Bacit ra cin , gra mi ci d i n and tyro cid i n . In Ant- ibi o t i cs , Vol. 2, pp. 240~253(Edit ors Got tlie b , D. and Shaw, P.D.) Sp r in g er -V erlag, Berlin . Wein b erg, E.D.( 1974) Secondary meta b oli sm contr o l by tem p er atu re and ino rga nic ph osp h ate . Dev. Industr. Mi cr obio l , 15, 70~81. Wein b erg, E.D. and Tonnis , S.M.(1966) Acti on of chloramp h enic o l and its iso mers on secondary bio s y nthe sis pro cesses of Baci11 u s. Ap pl. Mi cr obio l . 14. 850~856. Whit ak er, A.(1 9 73) Fermenta t i on economi cs . Process Bi oc hem. 8(9), 23~26. Whit ak er, A.(1976) Amino acid tra nsp o rt int o fun g i : an essay . 'Ira- ns. Briti sh My c ol. Soc. 67. 365~376. Wi nd is h , W.W. and Mhatr e , N.S.(1 9 65) Mi cr obia l amy la ses adv. Ap pl. Mi _cr o bio l , 7, 273~304. Woodward, J.C ., Snell, R.L .(1949) Condit ion in g molasses and the like for th e pr oducti on of cit ric acid U.S. Pa ten t 2, 492~673.
제 5 장 발효방법 1 서론 미생물공학이란 미생물에 관한 인간의 지석을 공업적으로 응용하는 학 문으로서 미생물학자, 유전학자, 생화학자, 그리고 화학공학자 등에 의해서 달성될 수 있는 종합적인 학문이다. 미생물공학의 목적은 미생물체로부터 유용한 대사산물을 얻어내는 데 있다. 미생물공학은 두 가지 특칭적인 면, 죽 발효와 산물의 회수공정을 지닌다. 발효공정은 최적조건하에서 미생물을 배양하여 원하는 대사물질이 나 효소를 미생물로부터 생산하는 것이고 생산물 회수공정 (downstr e am p rocess i n g)은 미생물산물의 추출과 정제과정이 포함된다. 생물학 또는 생 화학적 산물 회수공정의 대부분의 기술은 순수한 화학적 공정, 죽 분리 • 증류 • 가열 • 냉각 • 건조와 같은 기술과 겹치는 부분이 많다. 다만 생화학 적 회수과정은 생물학적 산물이 화학적으로 불안정하다는 측면에서 화학적 인 회수과정과 크게 차이가 있다. 발효공정에서의 공학이라는 의미는 단지 생물학적인 공정을 조절하는 데 목적이 있으며 미생물이 이 공정에서는 관심의 주역이 되는 것이다. 따 라서 유전자 조작, 배양액의 최적화에 의한 대사 조절, 그리고 멸균공기의 공급 등의 모든 수단은 오직 목적으로 하는 산물을 생산시키기 위한 공정 인 것이다. 증식과 생산물 생성시의 대사과정을 더욱 정확히 이해하면 할
수록 경험적 경우보다 더 합리적으로 발효공정을 운용할 가능성은 더욱 커진다. 2 미생물의 증식 동력학 (gro wt h kin e ti cs of mi cr oorga n is m s) 발효방식에는 회분 (ba t ch) 발효, 연속 (con ti nuous) 발효, 그리고 fe d-ba t ch 식 발효가 있는데 생산물의 유형에 따라 발효방식을 선택할 수 가 있다. 우선 대규모 발효공정을 적절히 운용하고자 한다면 미생물의 증 식곡선에 대한 정확한 이해가 필요하다. 증식곡선은 연속공정에서보다는 회분식 공정에서 산물의 생산 시기에 지표로 중시된다 . 2.1 회분발효 (ba t ch fer menta t i on ) 회분발효는 하나의 폐쇄배양계로서 시간 T= ()ol]서 발효조내 멸균배양액 에 미생물을 접종시키고 최적생리적 조건하에서 배양을 전행시킨다. 발효 가 진행되는 동안 공기, 소포제, 그리고 p H 조절 물질 이의에는 아무것도 첨가하는 것이 없으며 배양액의 구성성분 균체의 농도, 그리고 대사물질의 농도는 세포들의 대사 결과 일반적으로 일정하게 변화한다. 멸균 배양액에 미생물을 접종하고 생리적인 조건하에서 배양하면 유도기 , 대수기, 정지기, 그리고 사멸기(그림 5.1 ) 등 전형적인 5 단계의 증식기가 관찰된다. 유도기(l ag pha se) :세포들을 새로운 배앙액으로 옮간 초기에는 비록 세포 무게는 변할 수 있어도 세포의 수는 아무런 증가가 없고 유도기 동 안 새로운 환경에 적응하게 된다. 새로운 배양액에 전이시킴으로써 세포들 에 대해 몇몇 변수가 변하게 된다. 예를 들면 p H 값의 변화, 배양액의 공급 증가, 증식 저해의 감소 등이 있을 수 있다. 새로운 영양분 수송계가 세포내에서 유도되어야 할 것이고
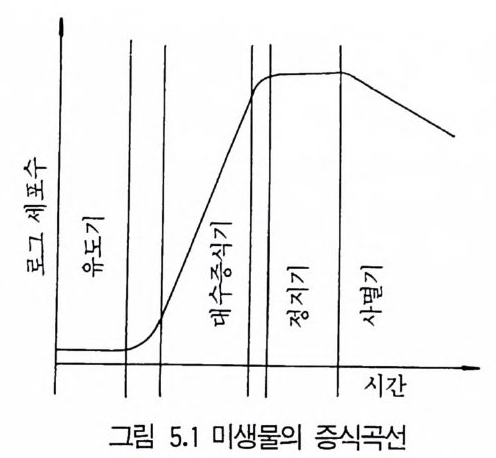 +
+
필수 보조인자들이 세포 의부에서 확산되고 일차대사를 수행하는 효소들도 새로운 조건에 맞게 조절되어야만 한다. 산업공정에서 유도기는 가능한 한 짧게 하는 것이 유리하며 이는 접종방법을 통해 단축시킬 수가 있다. 접종균의 생리적 조건은 유도기의 길이에 절대적인 요소인데 만약 접종 균으로 사용된 배양균기 대수기의 세포라면 지체현상은 일어나지 않을 것 이며, 따라서 증식은 즉시 가시된다. 그러나 양분 고갈로 증식이 중지된 배양균을 사용하면 새로운 배양액에 적응하기 위해 더욱 많은 시간이 필 요하게 된다. 종균의 농도 또한 유도기에 영향을 미친다. 적절한 배양과 접종의 전이가 일차 및 이차대사산물의 생산에 미치는 영향은 매우 크다. 비록 생산물 생성에 대한 조절작용이 완전히 이해되어 있지 않는 경우라도 전배양배지나 배양 조건들은 최적생산울 위해 고안할 필요가 있다. 하지만 생산물 생성에 대한 역학은 반드시 유도기의 길이에 관련되어 있는 것은 아니다. 대수기 (log ph ase) : 유도기가 끝날 무렵 세포들은 새로운 조건에 적응 하게 된다• 균체의 증식은 단위시간당 세포 수(효모와 세균) 또는 균체 사 상균의 정량적으로 배가 된다. 세미로그그래프 위에 시간에 대한 세포 수 또는 균체의 중량을 그려보면 일칙선을 얻게 되며, 따라서 〈대수기泥 k고 부르는것이다.
비록 세포가 기질을 흡수하고 대사산물을 분비함으로써 배양액을 변화 시키지만 대수기 동안의 증식속도는 일정하다. 중식속도는 과량의 기질이 존재하는 한 기질의 농도에 무관하다. 균체의 증식속도는 비중식속도 呼} 균체밀도 X( g /l) 에 연관되어 있으며 반면 세포 수의 증가속도는 µ와 세 포밀도 N(l/l) 에 연관되어 있어 대수기는 다음과 같은 식으로 나타낼 수 있다. ddtX =µ·X [1] -口:L\....T. ~dt =µ· N · [2] (t는 시간, 底근 시간당 비증식속도를 나타낸다) 비증식속도 底든 일반적으로 세 가지 변수에 대한 함수로 밝혀져 있는 데, 죽 제한 잔존 기질의 농도 s, 최대증식속도 µm, 그리고 기질이용 상수 K 루나타낼수있다. µ=Ks三+S [3] 이 식울 일반적으로 Monod식 이라 부르는데 상수 Ks 는 최대비중식속 도의 반이 얻어지는 점 (µ=0.5µm) 에서의 기질농도를 의미하고 균의 기질 에 대한 친화성을 나타내므로 Ks 는 효소반응론에서의 Mi ch aelis 상수에
상응한다. 몇 가지의 제한 기질들이 존재한다면 식 [3] 은 더욱 확대될 수 있다. µ=µmK, S(, ~I +K~. S. +. ' •…• • …+' 프K;호 S); /( \ —t,K느 )' [4] 모든 기질이 과량으로 존재할 경우, µ=m이 되며 배양균은 최대 증식속도에서 대수기에 있게 된다. 만약 한 종류의 기질이 모두 소모되고 다른 기질이 여전히 존재한다면 두번째 비중식속도가 µ1 인 두번째 기질의 대사 를 진행하는 두번째 대수기로 나타나게 된다. Ks 에 대한 값은 일반적으로 매우 낮다. 즉 E. col i에 있어서 포도당에 대해 측정해보면 1. 0m g /l 의 값이 측정된다 . 이러한 낮은 값들은 Ks 값에 상응하는 기질수준이 대수기 동안의 정상적인 회분발효에서는 얻어질 수 없음을 설명하고 있댜 대수기 말기에 존재하는 다량의 균체 때문에 기질 은 빠르게 소모되고, 따라서 기질농도가 Ks 값 근처에 있을 동안 경과시간 은 매우 짧으며, 결국 정지기에 빨리 도달하게 된다. 최대비중식속도 (max i mun spe c if ic gro wt h ra t es) 는 산업적으로 상당 히 중요하다. µrri은 생물에 따라 다르며 또한 발효조건에 따라 각기 다르 댜 몇 가지 균류에 대한 µm값 들이 표 5.l 에 나타나 있다. 여기서 비증식
표 5.1 굴루코오스를 사용한 일부 곰팡이류의 최대비증식속도 Orga n i sm T°C µm(h-i) Doubli ng tirn e(h) Aspe rgi llu s nig e r 30 0.20 3.4 6 Aspe r gi llu s nid u lans 20 0.090 7.72 25 0.1 4 8 4.68 30 0.215 3.23 37 0.360 1.96 Penic il l i u m chry so g en um 25 0.1 2 3 5.65 Mucor hie m alis 25 0.1 7 4.1 Fusarium auanaceum 25 0.1 8 3.8 Fusariu m gra mi ne arum 30 0.2 8 2.4 8 Vertic il l i u m aga rici n u m 25 0.24 2.9 Geotr ic h um candid u m 25 0.4 1 1.7 Geotr ic h um candid u m 30 0.61 1.1 Neurospo ra sito p h ila 30 0.4 0 1.73 (Anderson et al., 1975)
속도는 0.090~0.61h 기 사이로 다양하다. 어떤 균은 긴 사슬의 기질을 분해하기 위하여 추가 에너지를 필 요로 하 기 때문에 간단한 기질들에 대한 바증식속도는 긴 사슬의 분자의 경우에 바해 더욱 크게 된다. 표 5.2 에 나와 있는 한 예는 포도당, 말토오스(두 개의 포도당 단위 ), 그리고 말토트리오스(세 개의 포도당 단위 )에서 Fus- ariu m g ram i nearum 의 성 장을 나타내고 있다.
표 5.2 30 °C에서 Fusariu m g ram i nearum 의 배양시 포도당의 사슬길이에 최고증식속도 llm 에 미치는 영향 Substr a te Number of µm Doubli ng tim e glu cose un its (h) Glocose 1 0.28 2.4 8 Malto s e 2 0.22 3.1 5 Malto t r i o s e 3 0.1 8 3.85 (Anderson et al., 1975)
비록 적당한 기질이 배양액내에 존재하더라도 세포내 기질농도가 성장 이 빨라 감소될 때에는 비중석속도와 기질농도와의 관계를 나타내는 Monod 식은 실제적 인 것이 못 된다. 복잡한 배양맥을 사용할 때는 두 개의 대수기가 두번째 유도기에 의해 분리되어 나타나는 수가 있다. 이러한 과정을 이단중식 (d i aux y)이라 하는 데 기질 가운데 하나가 우선적으로 대사되기 때문에 나타난다. 기질 중 하 나가 다론 기질들의 분해작용을 억제하며, 타기질들에 대한 대사효소는 첫 번째 기질이 완전히 대사된 후에야 두번째 유도기 동안 비로소 유도된다. 정지기 (sta t i on ary pha se) : 정지기에는 균체가 최대치에 달하게 되는 데 기질이 대사되거나 혹은 독성물질들이 생성되자마자 증식은 둔화되거나 완전히 중단된다. 정지기 동안 세포의 성분은 변화할 수 있으나 균체의 무 게는 약간 증가되거나 · 그대로 유지된다. 세포가 용균됨으로 인해 새로운
기질(탄수호1-%, 단백질 등)들이 방출되며 이들은 생존하는 세포와 서서히 증식하기 위한 에너지원의 역할을 하게 된다. 정지기의 세포집단은 아직 대사작용이 활발하고 이차대사산물은 주로 이 시기에 생성된다. 생성되는 여러 가지 대사물이 바로 생물공학적인 측면에서 볼 때 커다란 관심사인 것이다. 사멸기 (death ph ase) : 이 시기에는 세포내에 잔여의 에너지들이 모두 소모된다. 시간 대 생존 세포 수를 세미로그그래프로 작성해 보면 일직선 울 얻을 수 있다. 이것은 곧 지수적인 속도로서 세포들이 죽어가고 있음을 의미하는 것이다. 정지기와 사멸기 사이의 시간적 길이는 사용되는 미생물과 사용되는 공 정에 따라 다르다. 상업적인 공정에서는 발효가 보통 대수기의 말기나 사 명기 직전에 끝나는 경우가 많다 (P i r t, 1975). 2.2 fed -batc h 배%뮤맹 Yosh i da (l 973) 는 회분발효시 배지성분을 연속적으로나 간헐적으로 공 급해주는 회분발효롤 페드-배치라 불렀다. 배치공정의 경우는 모든 기질 이 발효의 시작 전에 가해진다. 폐쇄계로서의 배치공정이 발전된 방법이 페드-배치 발효로서 이 공정은 페니실린과 같은 물질을 생산할 때 사용 되고 있다. 페드-배치 공정에서 기질은 발효를 전행시킴과 동시에 층가분 이 가해지게 된다. 죽 이차대사산물의 생성은 높은 농도의 포도당과 여러 단수화물 또는 질소화합물에 의해 대사억제를 받기 쉽다. 이러한 이유 때 문에 페드-배치 방법의 경우 최소성분의 영양액을 발효 시작시 적은 농 도로 가하며 생산과정 동안 필요한 영양분을 적은 양으로 계속 가하게 된 다. 이때 기질농도를 직접 발효과정 동안 연속적으로 축정하는 일은 통상 불가능하기 때문에 영양 공급과정을 조절하기 위해서 기본 기질들의 대사 와 관련 있는 간접적인 변수를 측정하게 된다. 예를 들어 유기산 생산의 경우 포도당 공급속도를 측정하기 위해 p H 값을 사용할 수 있으며 기준
삼투값을 지닌 발효에서 영양 공급은 배출공기의 p0 2 값 또는 CO2 함량 울 측정함으로써 조절할 수 있다. Wh it aker (1 980) 는 페드_배치 방식을 채용한 발효공정을 광범위하게 다루면서 종설을 발표하고 있다. 페드―배치 공정의 이점으로서는 첫째, 기질농도를 적절히 조절함으로써 잔존 기질농도를 항상 낮게 유지시킬 수 있어 신속히 대사되는 탄소원의 억제효과를 제거시킬 수 있다 . 둘째, 배지성분의 독성효과를 피할 수 있다. 셋째, 발효조의 통기효과를 향상시킬 수 있다. 2.3 연속발효 (con ti nuous fer menta t i on : Bazin , 1981) 회분의 배양과정에서 발효조에 새로운 배지를 첨가하게 되면 대수증식 기를 연장시킬 수 있다. 즉 새로운 배지가 일정한 속도로 유입하게 되고 증식용기내의 세균밀도는 처음 적응단계가 지나면 일정하게 유지된다. 용 기내의 세균은 배출구로부터 유출되는 분량만큼 대치되어 증식하게 되는 것이다. 연속배양 장치내의 세균 증식속도는 항상 하나의 영양소의 농도에 의해 제악되기 때문에 새로운 배지 첨가속도는 배양의 증식속도를 결정하 게 된다. 만일 새 배지가 적당한 속도로 연속적으로 공급된다면 일정한 상 태가 이루어질 것이고 균체 생성은 용기 의로의 세포 유출량과 균형을 이 루게 된다. 배지의 용기내로의 유입은 희석속도(di lu ti on rate , D) 가 용기의 크기 와 관계되기 때문에 다음 식이 성립된다. D=— VF [5] F는 유입속도(fl ow rate ) V는 용기의 용량 (volume) 따라서, D 는 unit h-1 로 표시할 수 있다.
일정시간에 대한 세포농도의 순변화는 디음 식으로 나타낼 수 있다. —ddxt= 증식-유출 혹은 —dt =µ X_DX [6] dx 따라서 ste a dy -stat e 상태에서는 세포밀도(농도)가 일정하며 一ddxt =O 따라A 1 µX=DX [7] µ=D [8] 이와 같이 ste a dy -stat e 상태에서 비증식속도는 희석속도 D 에 의해서 조절된다. 식 〔 3 ]인 µ=Ks+S~ 식 [이에 대입시키면 ddxt = x(' 」K르s+호S _D) [9] 한편 잔존 증식제한 기질농도의 순변화는 다음 식으로- 나타낼 수 있다. 뿔=기질 유입량-기질 유출량-세포 소비량 뿌dt =DSR-Ds- 」Y소 (K~s+s) [10 ] SR- 원래 기질농도
S ―잔존 기질농도 Y_ 수율요인(yi eld fac to r ) X ―균체농도 s~eady -s t at e 상태에서는 밍『와 :信떠 같고 따라서 식 [9] 와 [10] 을 정리하면 X=Y(Sn-8) [ll1][2] 5= Ks • D µm-D 여기서 X 는 s t ead y -s t a t e 의 세포농도, S 는 st ead y - s t a t e 의 잔존 기질 농도이다. 식 [12] 는 D 가 쩌} 조절하는 메커니즘을 설명하고 있다. 그림 5.2는 유속, 기질농도, 세포농도와 세포형성 속도간의 상호 연관성 울 나타내고 있다(p m=lh - 1, S=0.2g /l, Y=0.5).
 )gX 5 t二lO ,I -s·',。 - - , 51 )gX G
)gX 5 t二lO ,I -s·',。 - - , 51 )gX G
최대비증식속도는 최소발효조 용량과 최단시간내에 최대수윤을 얻고자 하는 산업공정에서 선택된다. Monod 모델은 낮거나 매우 높은 희석속도로 작동하는 연속발효에는 보통 적용되지 않는다. 제한기질로서 탄소를 사용하는 경우, 증식과 대사 유지를 위해 서로 다른 기질이 사용되기 때문에 Monod 모델은 낮은 희 석속도에서의 결과를 적절히 설명하지 못한다. 세포의 생존 유지를 위한 대사는 일정하며 비중식세포들의 일반 대사작용을 지탱하게 된다. 낮은 유 속에서의 첨가된 탄수화물은 증식이 아닌 세포 유지를 위해 주로 사용된 다. 반면 높은 유속에서는 첨가된 탄소 중 일부가 피루브산, 아세트산, 그 리고 트리카르복실산과 같은 산물로 불완전하게 산화되어 생산성이 감소된 다. 제한기질로서 질소를 사용하는 경우 다당류와 같은 저장물질이 낮은 유속에서 생성되어 그 결과 세포의 크기, 즉 균체무게가 증가하게 되는 것 01 다. 유속기 매우 낮거나 매우 높은 경우에서는 대사산물의 생산이 Monod 모델에 의해 잘 설명되지 않는다. 예를 들어 Penic il l i u m chry oo g enum 을 이용하여 페니실린을 생산하는 경우 최소성장률 이하에서는 페니실린의 생 산이 중지되며 이때는 분생포자들이 형성된다. 일정 유속으로 연속적 발효가 진행될 경우 ste a dy -stat e 조건이 존재하
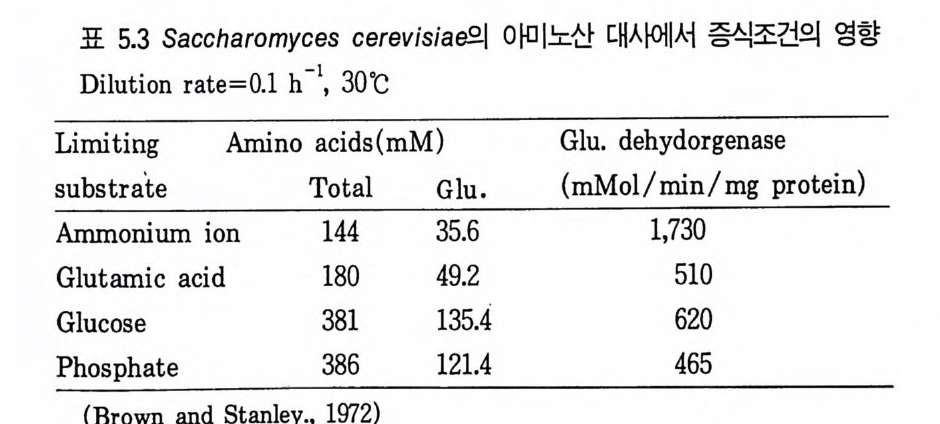 표 5.3 Saccharomy ce s cerev i s i a 팩 아미노산 대사에서 증식조건의 영향
표 5.3 Saccharomy ce s cerev i s i a 팩 아미노산 대사에서 증식조건의 영향
게 되며 기질함량 세포내 생화학적 반웅들-, 그리고 생산물 생성속도는 변 하지 않는다. 그러나 일정 유속하에서의 기질제한에 의한 대사에는 차이가 있다. 표 5. 앉본 Saccharomy ce s cerev i s i a 려서 아미노산과 글루탐산 털수소 효소에 대한 기질제한 효과를 나타내고 있다. 더욱이 산물 생성속도는 유속과 관련이 있으며 이것은 개개의 효소들뿐 만 아니라 일차와 이차대사산물의 분비에도 적용될 수 있다(그림 5.3). 산 물 생성시기 (i d i o p hase) 와 성장시기 (t ro p ho p hase) 가 분리된 경우 산물 생성은 최적혼합반응 기대에서 연속적으로 수행될 수가 없다. 따라서 이 경우 발효는 캐스케이드로서 일련의 발효조들을 사용한디든지 또는 체판에 의해 분리되어 있는 단일 반응실을 사용한 탑식반응기내에서 수행되어야만 한다.
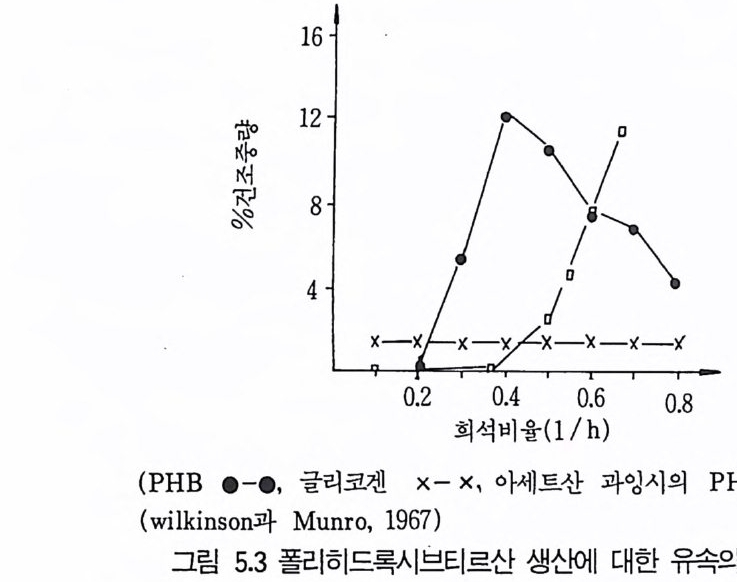 : 186
: 186
연속발효공정은 단세포 단백질, 항생물질, 유기용매, 그리고 종균배양의 생산과 셀룰로오스 분해를 목적으로 개발되어왔다. 한편 중간 시험공장들 이나 생산공장은 알칸류 c,- 화합물, 그리고 전분을 사용한 단세포 단백질 을 연속적으로 생산하기 위해 설치되고 있다. 연속발효를 이용한 산업공정에는 맥주글루코오스 이성화효소, 그리고 에
탄올 생산과 폐수 처리공정에서 적용되고 있다. 대사산물의 생산을 위해서 는 많은 발효공정이 실험실 규모에서는 연속공정을 잘 운용하고 있지만 실제로 산업적인 응용에서는 다음과 같은 몇 가지 이유 때문에 단지 몇몇 공정만이 유용할 뿐이다. 1. 많은 실험적 방법들은 단지 2 (}1.서지 20 ()1-]간 동안만 연속적으로 되지만 산 업적 응용에서의 번응계는 최소한 50 Qo1]서 l,OO CY-]간 동안 안정하게 유지 되어야 한다. 2. 소법적 규모에서는 오랜 시간 동안 멸균된 상태로 유지하는 것이 어렵다 . 3. 최대생산성을 얻기 위해서는 기질의 구성성분이 일정해야만 한다. 그러나 소법적 배양액둘의 구성성분은 변하기가 쉽다. 4. 고수율균주를 사용하였을 경우에는 역돌연변이주가 발생하여 이들의 연속 배양과정에서 생산균주에 비해 지나치게 증식할 수가 있다. (1) 다단계방식 (mult i-st a g e sys t e m s) 다단계 연속배양의 이점은 분리된 각 단계에서 다른 조건으로 배양이 수행된다는 점이다. 죽 여러 종류의 탄소원을 이용한 발효나 이차대사산물 생산에서는 이점이 될 수 있다. Harte ( 1967) 등은 Klebsie ll a aero g ene 를 포도당과 말토오스 함유배지 에서 증식시키면 포도당이 처음의 단계에서 이용되고 말토오스는 다음 단 계에서 이용된디는 사실을 제시하였다. 이단계방식을 채용했을 때 이단계 에서 제疾} 대사가 일어나며 그때의 증석속도는 일단계보다 훨씬 감소된 다. 그러나 연구에서나 산업계에서 다단계방식을 채용하는 경우는 그 복잡 성 때문에 매우 제한되어 있다. 다만 산업적 적용에는 연속주류발효에서 시도되고 있다. (2) 되돌림방식 (fee dback sys t e m ) 균체를 되돌려주는 연속배양방식에서는 발효조내의 균체가 간단한 연속 배양상태보다 높은 균체농도를 유지하도록 고안된 것인데 여기에는 다음과
같은 방법이 있다. 첫째는 유출액의 균체농도가 발효조의 균체농도보다 낮도록 연속배양상 태로부터의 균체유출을 제한하는 것이고, 둘째는 유출액을 균체 분리공정 울 거침으로써 농축된 균체를 중식 배양조로 되돌려주는 방법이 있다. 되돌립방식에 관해서는 P i r t(1 975) 의 종설을 참고할 수 있는데 이 방 식의 효과를 정리해보면 다음과 같다. 1. 발효조내의 균체농도를 증대시킬 수 있다. 2. 균체농도가 증대되면 단순 연속배양과 비교해서 잔존 기질농도가 감소하 게 된다 . 3. 균체 및 산물의 최대산출은 증가한다. 4. 한계 희석속도가 증대된다. 이와 같이 균체 되돌립방식은 양조공정이나 유출액 처리공정과 같은 매 우 희석된 기질 유출공정에서의 기질 이용성을 높일 수 있는 이점이 있다. 또한 균체를 되돌립으로써 농도를 변화시키는 혼합기질이 사용되는 체계에 서는 안정성을 개선시킬 수 있다. (3) 연속배양에서의 생산성 연속배양에서는 일정한 상태하에서 최적 희석속도로 작동할 때 생산성 (P) 은 일정하며 항상 최고치이기 때문에 다음과 같이 표현할 수 있다. P=D • X(g / l • h) D 는 유속, X 는 균체 (산물)농도 연속배양의 생산성을 장기간 수행하게 됨으로써 비생산적 시간은 최소 화되기 때문에 회분배양에 비해 크다. 따라서 회분배양에 비해 연속배양에 의한 균체의 생산성이 크며 발효기간을 통한 최대산출조건을 유지시킬 수
가 있고 장기 연속공정에서의 비생산기간은 무시할 수가 있다. 이론적으로 균체 이의의 산물 생산을 위한 발효에서도 회분발효에 비해 연속발효가 더 생산성이 높다고 할 수가 있다. 연속발효에서는 회분발효에 비해 용량 이 작아도 감은 효과를 낼 수 있기 때문에 건설장비 설치비 및 유지관리 비 또한 저렴하면서도 같은 생산성을 달성할 수가 있다 (Hos podk a, 1966). (4) 연속배양의 장단점 미생물균체를 생산하기 위해서 연속배양법은 매우 이상적이고 능률적이 라 할 수 있다. 균체 생산에서는 대사산물을 생산하는 경우에 비해 균주의 생산성 저하란 문제에 관해서는 크게 문제가 되지 않고 발효기술도 1960 년 이후 크게 발달하였다. 또한 새로운 ai r-l ift형 발효조도 SCP 생산용으 로설계되고 있다. 인류의 식량대체용 단백질이나 사료용 SCP 생산에 연속배양공정이 매우 유용하다는 것은 연속적 운전을 큰 변동없이 수행할 수 있고 따라서 자동 화가 가능하다는 점에 있다. 연속배양에서 증식속도는 희석속도(유입량)를 조절함으로써 세포농도, 기질농도, 산물농도 및 독성물질농도 등이 발효기간 중 계속 일정하기 때 문에 정상상태 (s t ead y -s t a t e) 의 발효 수행이 가능하다. 또한 연속배양에 서는 산소요구량, 냉긱공정, p H 조절도 일정하기 때문에 회분배양에 비해 조절이 간단하다. 배지조제 멸균공정에서, 회분배양에서는 노동력 소모형인 것이 단점이나 연속배양에서는 일정하면서도 연속적 방법을 채택할 수가 있다. 그러나 연속배양의 배양시간이 길고 연속적이므로 ·오염의 가능성과 일단 오염이 발생했을 때의 처리문제에 난점이 있다. 만일 오영균의 비증 식속도가 클 때는 용기내의 미생물은 전적으로 대치되어 버릴 우려가 있 는 것이다. 오염원은 발효의 선비와 같은 의부적 요인과 균주의 변화 등의 내부요인으로 구분해서 대처해야 한다. 균체 생산에서는 발효조건이 가장 효율적인 균주가 선별되어 살아남기
때문에 오히려 연속배양이 장점이 될 수 있으나 대사산물의 생산에서는 균주의 퇴화나 유전자 조작된 균주의 변종 가능성이 단점이 된다. 연속배 。阿 회분배양에 비해 많은 이점을 가지고 있음에도 불구하고 발효공업에 넓게 이용되고 있지 않는 것은 원래 회분방식 발효기· 경험적 성격을 띤 기술이라는 역사적 배경을 반영하고 있다. 그러나 최근에 와서 회분배양 장치를 사용해서 fed -batc h 배양을 채택한 결과 여러 가지 연속공정의 이 점이 나타나고 있는 것이다. 3 멸균 (s t er ili za ti on) 발효산물은 특정 미생물의 배양에 의해서 생산되므로 발효과정에 의부 미생물에 의해 오영되면 다음과 갈은 결과가 발생하게 된다. 1. 배지 중의 영양분이 오영균에 의해 소비되므로 생산성이 떨어전다 . 2. 연속발효인 경우 오영균의 증식속도가 빠를 때는 전 발효균이 오영균으로 대치되어 버린다. 3. 오영균에 의해서 최종산물의 성분이 달라전다. 4. 오 영균에 의해 생성된 산물로 산물의 분리 정제가 곤란해질 수 있다. 5. 오영균은 목적으로 하는 산물을 분해해 버리거나 구조를 변화시킬 수가 있다. 6. 파지에 의해 오염된 세균발효에서는 용균을 일으킬 수도 있다. 따라서 위와 같은 오염을 피하기 위해서 첫째 순수한 균을 종균으로 하 여 접종할 것이며, 둘째 배지와 발효조를 완전 멸균해야 하며, 셋째 발효 중 첨가하는 물질이나 공기를 완전 멸균하여 무균조건에서 발효를 계속해 야할것이다. 다만 위와 같은 멸균상태의 발효는 원리적으로는 적용되지만 발효조건
이 오염을 방지할 수 있는 환경이나 조건하에서는 오염을 방지하기 위한 범위나 조건은 완화될 수 있다. 즉 배지성분이 제한된 선택배지를 사용한 다거나 pH 범위가 오영방지에 유효한 조건하에서는 오염의 범위는 크게 완화될 수가 있다. 따라서 발효조의 멸균방법도 경우에 따라 완화될 수 있 는것이다. 3.1 배지의 멸균 배지의 멸균에는 열, 방사선 혹은 화학약품 등 치사인자를 이용해서 멸 균하거나 여과와 같은 물리학적 방법으로 멸균할 수가 있는데 일반적으로 발효배지의 멸균에는 수증기가 가장 보편적으로 사용되고 있다. 수증기로 인한 미생물의 치사율은 다음과 같은 식으로 나타낼 수 있다. -一ddNt— =k(No-N ' ) =kN N: 생존균수 No : 초기세포 수 /ml N' : (분)에 따른 사멸세균 수 k : 비사멸상수(사멸속도상수) t :멸균처리시간 t =O 일 때의 Nc4 t=t 1 일 때의 N 사이를 적분하면 kt= ln— NNo 혹 •은 1n— NN—o =-kt No/N 의 비는비활성화 인자가되고 :\ 는생존인자가된다. N N=V 의 1n 값은 설정기준치로서 멸균되어야 할 배지의 오염수준인 N~, 멸균되어야 할 기대수준인 N 에 관한 변수이다. 이상적인 곡선은 시간에 대해 생존균수가 지수적으로 감소되는 것이다.
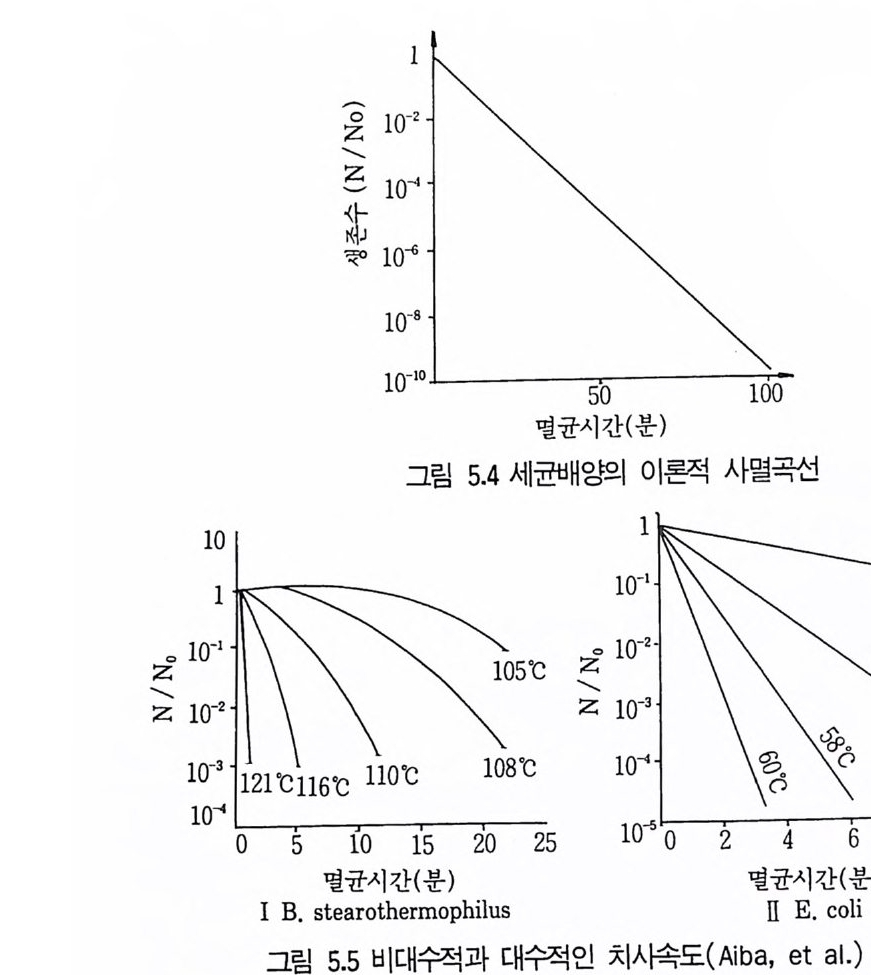 0N/N町)
0N/N町)
이 직선은 음의 기울기를 나타내며 이에 상응하는 사멸곡선은 54~60°C 에서 대장균의 영양세포들울 예로 하여 그림 5•~ p ar t II 에 나타나고 있 댜 실제로 이 곡선은 Bacil lu s s t earo t hermo p h i l 盛의 포자인 경우와 같이 항상 직선이 아니다(그림 5•~ pa rt I ). 이와 같이 비대수적인 사멸곡선 의 수학적인 모델이 개발되어왔다. 위의 식에서 K 는 비치사속도(반응속 도)를 나타내는 상수이다. 이것은 온도가 증가할 때 급증가하며 식을 이용 해서 실제로 미생물을 가지고 실험적으로 구할 수 있다. 반웅속도 상수는 온도가 일정할 때만 일정하게 되는 것이다. Arrheniu ~ 식에 의하면 온 도와 상수 K 는 다음과 갇은 관계가 존재한다.
dlnK .= E dt R • T 2 R은 물론 기체상수(J /Mol ° K) 이고 T 는 절대온도 ( O K), w.근 집단마 다 특이하게 갖는 상수, 즉 활성화에너지 (J /Mol) 이다. 만약 이 식으로부터 실험적으로 얻어진 lnK 값과 온도의 역수를 같이 그래프로 나타내면 직선이 나울 것이다. 이렇게 되면 우리가 원하는 온도 에서의 K 값을 계산할 수 있다. 아레니우스적인 상관관계는 단지 순수배지에서만 얻어질 수 있다. 멸균 되지 않은 용액 속에 보통 존재하는 개체집단은 일반적으로 열저항성을 지닌 균의 혼합배양물이다. 따라서 멸균속도는 두 종류의 미생물을 지닌 배잉액에서 볼 수 있듯이 직선을 나타내지 않고 곡선을 나타낸다. (1) 가열멸균 이 방법은 영양배지의 멸균에 가장 많이 사용되는 방법이다• 열에 의한 멸균방법은 여러 가지 요인들에 의해 영향을 받는다. 죽 존재하는 미생물 의 수와 형태, 배지의 조성, p H 가 들어 있는 입자들의 크기 등이다. 영양 세포들은 비교적 낮은 온도에서 재빨리 제거될 수 있지만 포자들은 121·c 의 온도까지 울라가야 파괴된다(그림 5.6).
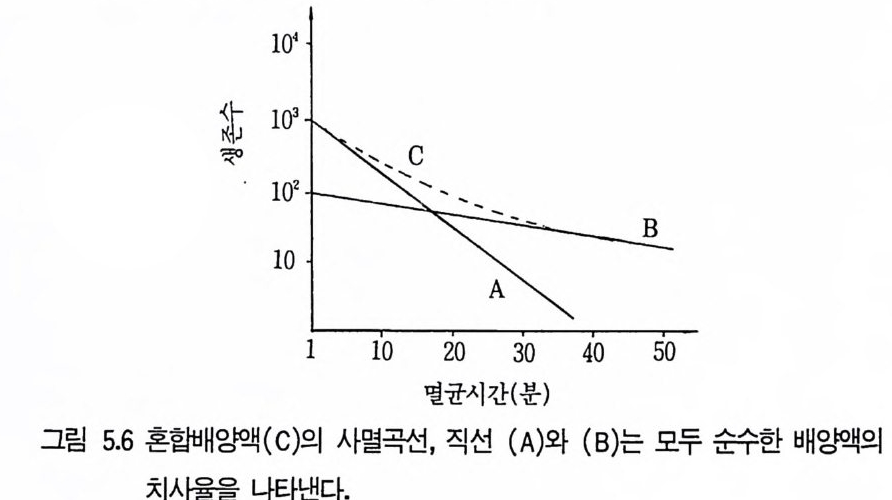 l04
l04
Bacil lu s s t earo t hermop h i lus 의 포자는 열에 대해 큰 저항성을 가지고 있 다. 따라서 이들은 여러 공정에서 사용될 멸균장치를 시험하기 위하여 쓰 인다. 표 5 .4는 온도와 K 값 사이의 관계 및 이 미생물에 대한 기준 설정 울 위한 자료를 제시하고 있다. 또 표 5.5 에 여러 미생물에 대한 멸균시간 과온도를나타내었다.
표 5.4 B.s t earo t hermo p h il u 해 있어 온도, K 값과 설정기준과의 관계 (Ric h ards, 1968) T (°C) k (min- t) V 100 0.019 101 0.025 0.044 102 0.032 0.076 103 。 •040 0.1 1 6 104 0.051 0.1 6 8 105 0.065 0.233 106 0.083 0.316 107 0.1 0 5 0.4 2 0 108 0.1 3 3 0.553 109 0.1 6 8 0.720 110 0.212 0.932 111 0.267 1.19 9 112 0.336 1.53 5 113 0.4 2 3 1.95 7 114 0.531 2.48 8 115 0.666 3.1 5 4 116 0.835 3.989 117 1.04 5 5.034 118 1.30 7 6.341 119 1.63 3 7.973 120 2.037 10.01 0
121 2.538 12.549 122 3.1 6 0 15.708 123 3.92 9 19.638 124 4.881 24.518 125 6.056 30.5 7 4 126 7.506 38.080 127 9.293 47.3 7 3 128 11. 49 4 58.867 129 14.200 73.067 130 17.524 90.591 ( V : Delfa c to r )
표 5.5 여러가지 개체집단의 멸균시간과 멸균온도 세포종류 Ste r ili za t ion Ste r ili za t ion time (min) tem p er atu r e ( ·c ) Vege t a t i ve cells 5~10 60 Fungu s spo res / yea st spo res 15 80 Str e pt om y ce s spo res 5~10 60~80 Bact er ia l spo res, gen eral 5 121 Bacil las ste a roth e rmop hilu s 15 121 의 Spo res
De i ndoer fe r(1959) 는 멸균의 설계기준으로서 Del fac t o 뎨 7 제시하였는 데 Del fa c t or(V) 는 다음과 같이 나타낼 수 있다. V =In뵤 Nt N<> i:-멸 균 전 생균수, N t는 松]간 멸균 후의 생균(포자)수, 예컨대 멸 균 전 생균 수는 1011, 멸균 후의 오염 위험 수는 l,OOQ ol] 1 개라 가정하면,
수N t치는는 1가0 _열3 이중므의로 vV, =멸l균n— 1l 최l0l l고~ 온 =도l에nl서0 1의1 = 3V 2 . 沙 및} 냉된다각.중 의De lV fa c값 t o의r 의 합 실계질가 된다. 따라서 Delfa c to r (V )는 가열온도와 가열시간에 따른 생균 수의 단 계적 감소 정도를 나타내는 값이 된다. (2) 물리적인 멸균 (A i ba et al., 1973) 원심분리, 이온교환수지를 이용한 흡착, 활성탄을 이용한 흡착 또는 여 과 등의 방법이 있다 여과는 실제로 사용할 수 있는 방법이다. 여과멸균 법은 열에 약하거나 변성되기 쉬운 영양성분을 멸균시키는 데 이용된다. 비타민, 항생물질 혹은 혈액 구성물질 등은 열에 약해서 여과방법에 의 해 제균시켜야 하는 물질의 예이다. 이러한 물질은 여과 전에 완전히 용해 시켜야 한다. 그렇지 않으면 이들은 미생물과 함께 걸러지게 된다. 여과의 단점은 첫째 어떤 배잉액의 성분이 여과물질에 흡수된디는 것, 둘째 높은 압력이 가해져야 하는데 이는 실제로 산업적인 측면에서 바람직하지 못한 것이다. 경제적으로 효율적인 방법은 배지의 조제에 사용될 물만을 여과시 키는 것이댜 예를 들어 스테로이드의 생물 전환공정에서 농축된 배양액은 열에 의해 발효조내에서 멸균되고 여과에 의한 멸균수로서 정상 농도로 희석시키는 것이다• (3) 물리 • 화학적 멸균방법 방사선방법은 식품공업에서 가끔 사용되나 발효산업에서는 쓰이지 않고 있댜 화학적 방법에는 비록 많은 화학적 살균제가 알려졌지만 그들은 영 양배지롤 멸균하는 데 사용되지 않는데 그 이유는 잔여 화학물질로부터 일어날 수 있는 발효균에 대한 억제 위험이 있기 때문이다. (4) 회분식 멸균 대부분의 배지는 121°C 의 발효조에서 멸균된다. 대략적인 멸균시간은
배지의 특 성과 발효조의 크기로 부 터 계산할 수 있고 발효용액뿐만 아니라 발효조의 부속품, 밸브 전 구까지도 멸균되어야 한다. 따라서 실질적인 멸균 시간은 계산된 수치보다 훨씬 길며 발효조에서 배양액에 대하여 실험적으 로 계산되어야 한다 . 멸균방법은 증기를 발효조 내부의 코일로 주입시키는 (간접멸균) 방법과 또 하나는 배양액 자체내로 증기를 주입시키는(직접멸 균) 방법이 있는데 이 경우에 증기 자체는 아무런 화학물질을 가지고 있 지 않고 순수하여야 한다. 산업적으로 사용하는 증기에는 사용된 부식방지 용 약품들이 들어 있는데 이들은 잠재적으로 독성을 나타낸다. 직접 증기 를 주입시키면 발효조내에서 액화되므로 멸균과정 동안에 액체의 용량이 증가하게 된다. 멸균온도가 l21 °C 에 도달하는 데 걸리는 시간은 증기의 유입과 발효조의 크기에 따라 다르다. 일단 적당한 온도에 도달하면 실제 멸균에 20~6~1 필요하고 그 후 한 시간 정도 냉각시키는 시간이 필요하게 된다• 만약 냉각하는 동안 얻어 전 더운 물이 다른 용도로 사용되지 않는다면 회분식 멸균은 에너지 낭비 형이 된다. 가열멸균의 다른 단점은 그림 5,7 에서 알 수 있듯이 가열해서
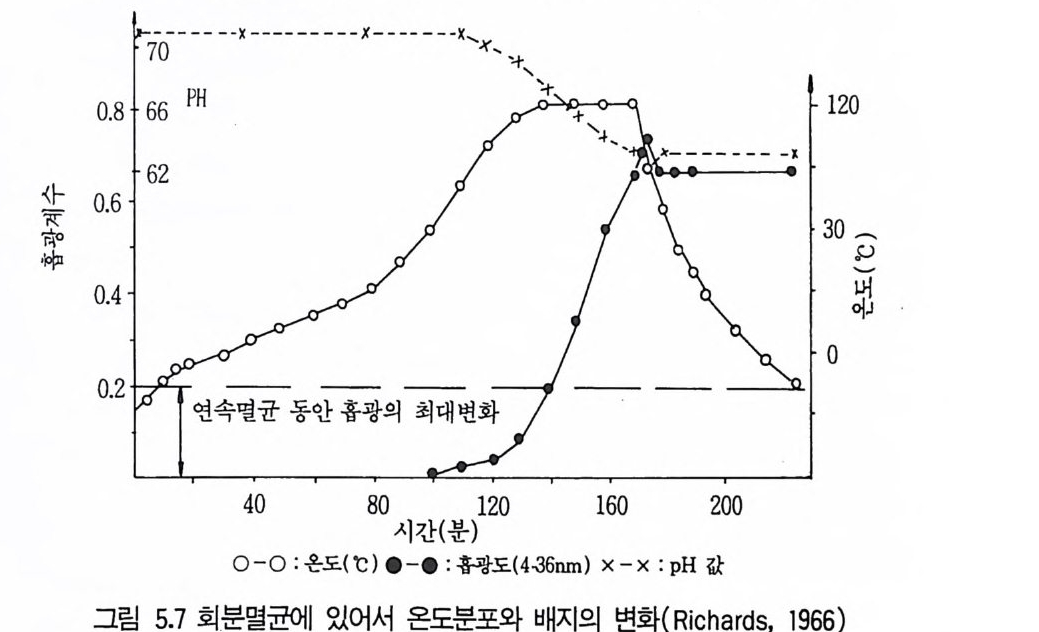 70 6- 6x x x’ x `
70 6- 6x x x’ x `
살균시키고 냉각시키는 과정에서 미생물의 멸균 이의에도 심지어 배앙맥까 지 변화시키게 된다. 캐러멜화와 메일라아드 반응(포도당의 아민화)의 결 과 탈색되고 p H 값이 변하게 된다. 비타민은 파괴되고 배양액도 질이 변하 게 된다. 배지의 회분식 멸균공정을 발효조내에서 멸균하는 방법과 멸균하기 위 한 멸균조를 별도로 설치하는 경우가 있는데 각각의 장단점이 있다. 죽 멸 균조를별도로설치하면 1. 동시 멸균함으로써 발효조의 청소, 발효시간이 절약된다. 2. 농축 멸균이 가능하고 멸균 후 희석은 발효조에서 멸균수로 행할 수 있 다. 3. 멸균중 점성도가 높아질 경우 동력에서 절약된다. 4. 고온에 의한 발효조의 부식을 줄일 수 있다. 그러나 단점으로는 1. 건설비의 증가 2 멸균배지액의 이송에 동력 및 조작의 복잡함을 수반하게 된다. 따라서 발효 규모에 따라 선택하게 되겠 으나 일반적으로 발효조내에서 멸균하는 쪽을 많이 택하고 있다. (5) 연속멸균 (R i chards, 1968) 배지가 파괴되고 높은 에너지가 소모되는 회분식 멸균의 단점은 연속멸 균방법을 사용하면 피할 수 있다. 연속멸균공정도 원리에서는 회분식 멸균 과 같이 멸균온도로 가열하는 단계, 멸균온도에서의 멸균시간 및 배지의 발효온도까지의 냉각시간 과정을 거치게 된다. 그 이유는 사멸속도와 온도 사이에는 대수적인 관계가 있고 이는 온도를 높여주면 생존균을 완전히 없애는 데 필요한 시간이 그만큼 줄어들 수가 있다. 회분식 멸균은 121.c 에서 30~6~ 손 동안 수행하는 것이 보통이나 연속멸균은 14o·c 에서 30~ 12~ 동안이면 수행하게 된다. 다만 연속멸균의 장점은 멸균온도를 가감 할 수 있다. 죽 멸균에 소요되는 시간을 감소시키면서 영양분 분해 정도를
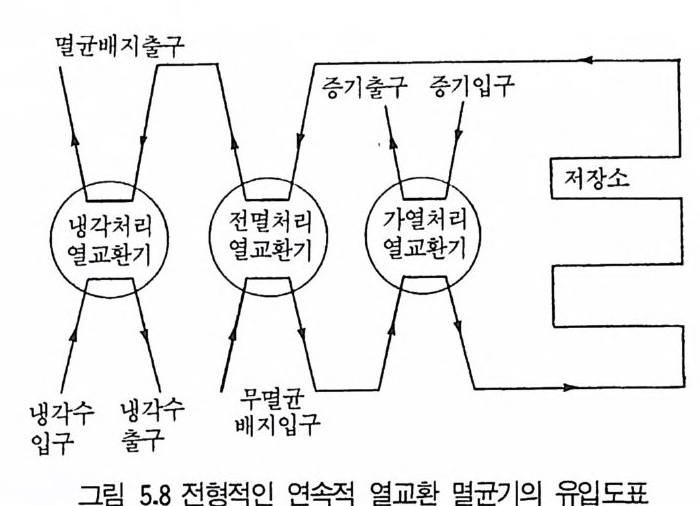 멸균배지 출 구
멸균배지 출 구
낮출 수 있다. 연속멸균방법은 두 가지로 나눌 수 있는데 그 하나는 연속 적 증기주입 및 냉각장치 (conti nu ous inj e c to r -fla s h cooler) 를 사용하는 방법과 연속적 열교환관 (con ti nuous pla te heat exchan g er) 을 사용하는 방법이다. 증기주입식 멸균방법은 증기를 배양액 속으로 직접 주입시키는 것이다. 온도는 짧은 시간내에 140 'C로 오르고 4~12 떠느 동안 유지된다. 증기는 응결되기 때문에 배 0~버 이 희석된다. 이것을 바로잡기 위해서 뜨거 운 용액은 팽창 밸브를 통해 전공 증발기로 빠져나가게 되고 전공 펌프롤 통해 제거된다. 이렇게 해서 멸균된 배양액은 냉각되어 원래의 농도로 되 돌아오게 된다. 이 방법의 단점은 배지의 점도를 변화시키고 열교환기를 사용하는 연속공정에서 첫번째 열교환기에 먼저 배양액을 보내어 20~30 초내에 90~120 °C 로 예열한다 . 그리고 나서 두번째 열교환기에서는 증기 에 의해 간접적으로- 멸균온도 (140'C) 로 가열한다. 파이프에서 이 온도로 30~120& . 동안 유지한 후 첫번째 열교환기로 가서 일차 냉각되고 세번째 열교환기로 가서 발효조의 온도까지 냉각된다. 냉각되는 단계는 20~3 祖느 에 불과하다. 그림 5.8, 5.9, 5 .10-t든 멸균되는 동안 배 0~버 의 온도 변화를 나타내는것이다.
 증기입구
증기입구
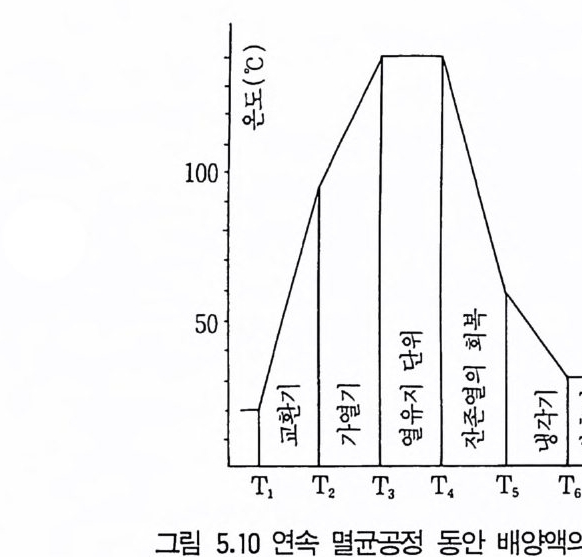 (
(
열교환기를 이용하는 공정에서는 투입되는 에너지의 90% 정도가· 회수 된다. 이 방법에서의 단점은 어떤 배양객에서는 첫번째 열교환기에서 멸균 된 뜨거운 배 OJ :i:!비과 새로 들어오는 찬 용액 사이의 온도차가 매우 크기 때문에 불용성의 염들(인산칼슘이나 옥살산킬슘)이 생기게 되는 것이다.
Banks(1979) 가 증기주입식 연속멸균방식의 장단점을 정리한 바에 의하 면 다음과같다. 장점 1. 고형분 현탁배지에 대해서 유리하다. 2. 설비투자가 저렴하다. 3. 청소관리가 쉽다. 4. 가열시간과 냉각시간이 짧다. 5. 고온증기의 이용효율이 높다. 단점 1. 가열 및 냉각시 거품이 발생할 수 있다. 2. 배지가 증기와 직접 접촉하므로 희석되거나 방부식제가 포함되지 않 는 증기를 사용해야 한다. 열을 가했을 때 점도를 가지게 되는 녹말이 포함된 용액은 연속멸균공 정을 시용하기가 어렵다. 실제의 멸균공정을 거치기 전에 산이나 amy la se 로 부분적인 가수분해를 하여 액화시켜야 한다. 더구나 배영팩 속에 녹지 않고 떠 있는 입자들이 있을 경우 연속공정에서 멸균시간을 짧게 하면 열 울 전체에 퍼지게 하는 데에는 불충분하다. 1mm 입자에 대한 가열시간은 1 초이고 1cm 입자들에 대해서는 l0 但 7} 소요된다. 따라서, 연속멸균공정에 서 입자의 크기는 1~2mm 로 제한해야 한다. 3.2 발효조의 멸균 (Cha i n, 1966) 배양액을 연속멸균방법이나 회분멸균공정에서 멸균조를 별도로 설치할 경우 발효조는 별도로 멸균배지를 넣기 전에 멸균해두어야 한다. 발효조를 멸균하기 위해서는 발효조 내부의 코일이나 재킷에 증기를 넣어 가열하거 나 직접 발효조 내부에 증기를 분사해서 공기 유출구를 제의한 모든 부분 울 멸균시켜야 한다. 증기압은 15 p s i에서 2W 손간 살균한 후 멸균공기를 발효조에 불어넣고 발효조 내부압을 가압상태로 해둘 필요기· 있다. 그렇지
않으면 냉각과 동시에 내부암이 감압되어 의부의 멸균되지 않는 공기가 유입되어 오염을 초래할 가능성이 생긴다. 3.3 공기의 멸균 호기발효에서는 상당량의 멸균공기를 연속적으로 공급해야 하는데 발효 조에 공급되는 공기는 반드시 멸균되어야 한다. 공기 중의 입자나 미생물 의 수는 공장의 위치와 공기의 운동, 공기에 대한 사전처리에 따라 달라전 다. 평균적으로 대기 속에는 lm' 당 10~100,000 개의 입자가 있으며 5~2, 00 伊回의 미생물이 들어 있다. 이들 중 50% 는 곰팡이의 포자이고 40% 는그람음성세균이다. 발효조는 일반적으로 0 .5~l. Ovvm( 공기부피 /액체의 부피 • 분)의 비율 로 통기하면서 작동한다. 통기의 비율이 lvvm 인 50m' 의 사용부피를 가전 발효조는 시간당 3,000m' 의 멸균공기를 필요로- 한다. 이러한 점에서 산업 미생물학에서 공기의 멸균은 매우 중요하다. 공기멸균에 유용한 방법에는 여과를 포함해서 가스의 주입, 오존, 가스세릭, 방사선, 자의선, 열과 같은 것이 있는데 산업적인 규모에서는 이들 중 여과법이 주로 사용되고 있다. 오렌 기간 동안 공기멸균은 공기를 전기적으로 가열한 망을 통과시키는 방법을 사용하였지만 전기료가 높기 때문에 여과법으로 대치되었다. 산업 적인 시스템에서 공기는 무균 여과된다. 여과에 의한 공기의 제균방법은 크게 두 가지로 나눌 수 있다. 죽 공기 중의 입자보다 작은 구멍을 공기가 통과함으로써 제균시키는 방법과 또 하나는 제거되어야 할 입자보다 큰 구멍을 통과하되 심층을 통과함으로써 결과적으로 제균되는 방법이 있다• 전자의 방법은 여과막이 파손되지 않는 한 제균율은 100% 가 된다. 후자 의 경우 솜, 유리솜, 강철솜 등의 섬유재료를 쓰게 되는데 섬유간 간격은 0.5 에서 l. 5µm 가 되므로 비록 심층여과해도 이론적으로는 절대적 세균이라 할 수 없다. 그럼에도 불구하고 산업적인 발효에서는 튼튼하면서도 가격이 싸고 낮은 압력으로 송풍할 수 있는 장점 때문에 섭유형 여과기를 사용하
는 경우가 많다. 유리솜으로 된 필터와 같은 순수 심층필터를 사용하여 물 리적인 효과와 연결시켜 입자들이 걸러지게 한다. 그림 5 .1 1 에서 볼 수 있 듯이 입자의 여과에는 관성의 효과 및 방해효과, 확산, 중력분리, 그리고 정전기적 흡착력 등이 이용된다. 주름진 막을 사용하는 새로운 카트리지 필터가 현재 매우 널리 사용되고 있다. 이러한 필터들의 장점은 유리솜이 나 활성탄소막대보다 크기가 작다는 것이다.
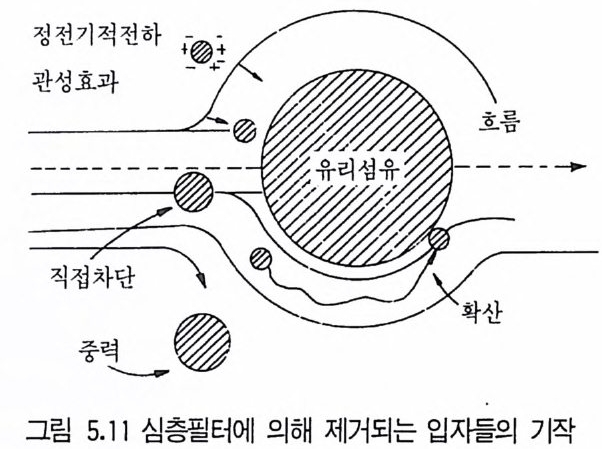 정 전기적 전하 델간
정 전기적 전하 델간
아 시스템을 작동하는 것은 매우 간단하고, 카트리지 설치와 사용될 필 터의 교환이 간단하다. 셀룰로오스 에스데르, po lys u lf on e 혹은 나일론으 로 된 박막필터들은 심층필터와 유사한 구조를 가지지만 이들은 막구조롤 가지므로 절대적인 필터의 효과를 가진다. 최근 절대여과효율을 울릴 수 있는 발효산업용 여과기가 개발되고 있다. 예를 들어 pol yt et r a f luo ro eth y le ne 카트리지 여과기가 있는데 막공폭이 0.2µm 균일막공으로 되어 있다. 이 여과막은 증기멸균이 가능하다 (Sm it h, 1981). 그립 5 .1 2는 나가고 들어오는 출입공기에 대한 필터장치가 발효조에 부 착된 것을 나타내는 것이다. 오늘날 설치되고 있는 대부분의 여과시스템에 서의 단점은 아직도 산업적으로 쓸 수 있는 박테리오 파지에 대한 완전한 필터가 없다는것이다.
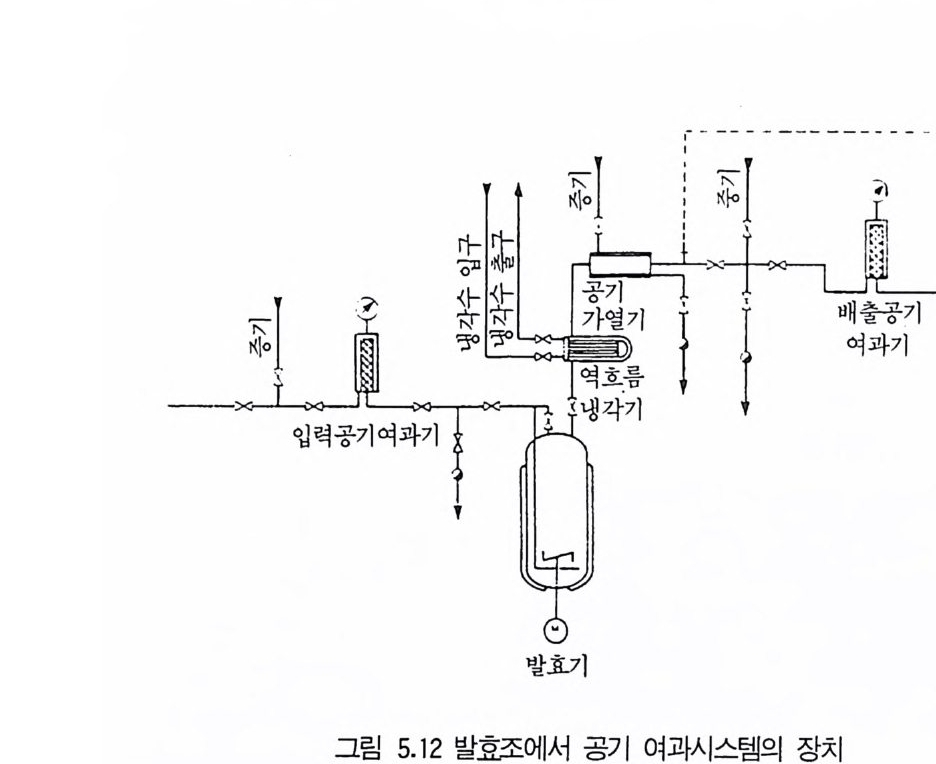 ,- 千
,- 千
4 미생물 접종 대규모의 산업적 발효공정을 효율적으로 수행하기 위해서는 큰 규모의 발효조에 미세한 세균을 직접 첩종하는 것이 아니라 단계적으로 미생물을 확대 배양하여 접종하게 된다. 접종하게 될 배양액이 갖추어야 할 조건으로서는 첫째, 종균배양이 순수 하고 활발한 증식상태에 있는 것으로서 접종 후 유도기를 최대한 단축시 킬 수 있어야 한다. 둘째, 접종량이 배양액에 대해 적당량이어야 한다. 셋 째, 형태학적으로나 유전학적으로 생산능력이 있는 균주의 특성을 지니고 있어야한다 . 일반적으로 종균배양에 사용되는 배지성분은 본 배양에 쓰이는 발효배
지오柱근 다르다. 종균배양에는 본 배양에 사용될 종균의 건강한 증식과 생 산성에 중점을 둔 배지성분을 사용하고 발효배지는 영양성분뿐 아니라 최 대의 산물 생산에 필요한 성분이 고려되어야 한다. 따라서 종균배지성분과 생산배지성분은 별도로 연구 개발되어야 하는 것이 성공적인 발효를 위한 중요 사항 중의 하나이다. 다만 주의할 점은 종균배양에 사용할 배지성분 과 본 발효 배양의 배지성분이 기본적으로는 유사해야만 새로운 배지에 이전시켰을 때 적응시간을 단축할 수 있고 유도기를 최소화시킬 수가 있 다. 종균배양의 배지성분의 특징은 발효배지에 비해 탄소원과 질소원의 함 량이 낮거나 배양시간이 짧기 때문에 조절되고 있는 것이 일반적이다. 종 균배양은 사면배지로부터 이양하여 충분한 균체가 증식할 때까지 시험관 및 삼각플라스크의 배양을 거쳐 본 배양에 들어갈 때까지도 한 단계 내지 혹은 세 단계의 발효조에서의 종균배양(본 발효의 발효조 크기에 따라)을 거치게 된다. 따라서 확대배양단계가 많을수록 오염의 위험이 따르기 때문 에 각별한 주의가 요구된다. 오염이나 생산성 저하현상을 확인하기 위해서 원래 종균배양을 수단계 수행하면서 소요되는 기간내에 소규모 진탕배양을 별도 병행하여 시료의 생산성을 조사할 필요기 소 있다• 각 단계의 종균이 순 수한지에 대한 오영균 조사도 단계마다 조사해야 한다. 4.1 효모의 접종 효모는 발효산업에서 가장 오랜 역사를 가전 미생물로서 맥주발효, 효모 균체의 생산 및 빵효모의 생산은 특히 효모이용 공업의 대표로 들 수 있 댜 맥주발효에서는 새로운 발효조에 대한 접종은 전번 발효에서 나온 효모 를 사용하는 것이 관례가 되고 있다. 이 경우 일어나는 위험성은 오영균의 유입과 균주의 퇴화를 둘 수 있는데 그 퇴화에는 응집도의 변화와 효모의 발효능의 감소현상이 가장 잘 일어나는 현상이다.
상면발효 를 채댁하는 경우는 다른 종 균용 효모 를 중 간 충 에서 회수한 효 모 (m i ddle sk i mm i n g s) 를 사용함으로써 위 험 성 을 최 소 화시킬 수 있다. 발효중 효모가 응집하여 표면에 뜨게 되는데 처음 뜨는 세 포 가 가장 응집 성이 있는 것이고 마지막에 뜨는 세포가 가장 응집성이 낮은 세포인 것이 다. 효모가 먼저 자라면 표면충(이 충이 가장 응집성이 강하고 오염되었을 가능성이 있는 효모임)은 제거하여 버리고 아래쪽 세균을 집균하여 디음 종균(pit c hi n g)으로 사용하는 것이다. 따라서 소위
식탱크 (1. 5 dm' 와 1 50 dm' ) 를 연 결 한 것 이다. 작은 증식탱 크 에 맥아즙을 채 우고 멸균한 뒤 냉각 후 통 기하면서 풀 라스크 배양액으로 접 종 하고 3~4 일 배양 후 다른 증식 조 로 이 송 시키는 것이다 . 3~4 일 배양 후 lOOOdm' 발효조로 옮기게 된다. 이 방법은 순수배양을 할 수 있다는 장점도 있으나 연속배양 후에 일어날 수 있는 균 주 의 퇴화 위험도 있다는 점에 유의해야 한다. 빵효모의 생산도 종균을 접종한 후 몇 단계 증식을 거쳐 행해진다 . 생산공정은 엄밀한 무균상태에서 행하는 것은 아니지만 초 기 종균접종 에서는 오영을 방지하기 위하여 순수배양을 하게 된다. Reed(1973) 의 방 법에 의하면 5 단계 중 처음 두 단계는 무균적으로 조작하여 증식시키고 나머지 단계는 개방증식 조 에서 수행하고 있다. 죽 처음 두 단계는 밀폐식 아며 통 기를 하지 않고 영양분도 공급하지 않는다. Rosen(1977) 의 방법 에서 는 첫 단계 배양에서 통 기방법 을 채택하고 있다. 4.2 세균의 접종 세균의 종균접종도 그 목적은 다음 단계의 확대배양에서 유도기를 단축 시키기 위해 활성이 강한 배양세균을 접종하는 데 있다. 유도기가 길다는 것은 시간적 낭비일 뿐 아니라 거기에 따른 배지성분의 낭비도 또한 초래 하게 된다. 유도기 기간은 접종량과 생리적 상태에 영향을 받게 되는데 (Mey ra th , 1972) 보통 접종량은 3~10% 가 통례이다. 그리고 접종은 세 균증식기 중 대수증식기에 있는 대사 활동이 활발한 배양을 사용한다 . 특 히 포자생성균은 대수증식기 후기에 포자가 형성되기 때문에 주의를 요하 며 포자의 함유량이 높은 배양액을 접종하게 되면 다음 발효의 유도기가 길어지게 된다 . 내열성 단백질 분해효소 생산에는 대수증식기에 있는 Bacil l u~ 5% 접종하는 방법을 검토한 예가 있고 (Kea y, 1972), Under Kofl er (1 9 76) 는 세균효소 생산에서 종균배양에서 사용한 것과 동일한 배지를 생산배지
에 사용하고 증식이 왕성한 종균을 대량 접종함으로써 유도기를 최소로 단축시킬 수 있음을 확인하고 있다. 산업적으로 중요한 방선균은 무성포자를 생성하기 때문에 종균접종시에 는 포자현탄액을 사용하는 경우가 많다. 포자는 한천배지에서 생성시켜 고 농도 포자를 얻게 되는데 Sta r k(1961) 등은 배지를 굳히는 데 쓰이는 한 천 자체가 증식이나 포자 형성을 저해하는 효과가 있기 때문에 이러한 유 해물질을 제거하기 위해 한천을 물로 세척함으로써 유해효과가 감소된다는 사실을 지적하고 있다. 곰핑이에서는 pel let 형성은 포자 형성에 영향이 크나 방선균에서는 pel let 형성이 포자 형성에 크게 영향이 없는 것으로 알려지고 있다 (W i ll i ams, 1974). 또한 Law t on(1984) 은 접종시 포자농도 와 배지성분 등에 의해서 방선균의 형태학적 pel let 모양이 달라진다는 것 울 지적하고 있다. 4.3 진균류의 접종 산업적으로 주요한 전균류는 대부분 무성생식으로 포자를 형성할 수 있 으므로 종균접종에는 포자현탁액을 일반적으로- 사용한다. 종균접종용으로 포자를 고농도로 생성시키기 위해서 대략 세가지 방법이 있다. 첫째 방법 은 한천고체배지에서 포자를 형성시키는 기술인데 Parker(1950) 는 한천 배지에서 포지를 형성시키기 위해 표면적을 넓히는 roll-bo tt le7] 술을 고 안하였다. 즉 3% 한천배지 300cm를 ldm' 원통형 병에서 멸균하여 45°c 로 냉각한 후 회전기에서 돌리면 한천배지는 원통형 병의 내벽에서 굳게 된다. 여기에 포자현탁액으로 접종한 후 24°C 에서 약 1 주간 정지 배양하 면 되는데 최대한의 면적을 활용하여 간편하게 포자를 생산할 수 있다• 두 번째 방법은 곡물입자를 사용함으로써 넓은 표면에서 포자를 생산하는 기 술이다. 이 기술은 우리나라 등 주로 동양에서 발달한 발효 기술이라 할 수 있는데 곡물로는 밀기울, 보리, 쌀, 분쇄 옥수수, 감자 등이 사용된다 . 이 경우 포자 형성은 멸균 전 첨가하는 수분의 양에 특히 영향을 받으므
로 적절히 조절해야 하며 포자 형성중의 실내 습도가 중요한데 일반적으 로 습도를 높여야 한다 (Vez i na, 1975). Asp e rgi llu s9 -} Pen i c i ll i u 짜기 대량 포자 형성에 관한 연구가 Sans i n g(1 973) 에 의해 행해져 있고, Vezin a (19 68) 둥은 Phy co my ce te s , Ascomy ce te s , Dente r omy ce te s 및 Basid i o - my ce t es 의 포자 형성의 효율에 관해 고찰하고 있다. 세번째 방법은 액내 배양에 의한 포자 형성 기술이 있는데 이 경우 적당한 배지성분을 사용하 면 액내 배양에서도 포자를 유효하게 생성시킬 수가 있다. Rhodes(1957) 등은 산업적인 gri s e ofu lv in 발효의 종균접종을 위해 Penic i li u m p a t ulum 의 포자 형성능을 조사하였는데 질소원의 공급을 0.05 에서 0.1 % w / v 로 제한하면서 통기를 잘 조절해야 한다고 하였다. 즉 통 기량과 질소원을 줄이는 것이 포자 형성의 유도에 필요하다는 것이다. 다 음 방법으로 영양균사체를 접종종균으로 이용하는 경우도 있다. 이 경우는· 무성포자를 왕성하게 생성시키지 않는 경우에 서용하는 방법의 하나의 예 가된다. Hansen(1967) 에 의하면 지베렐린 생산에서 먼저 긴 시험관 (25 xl50 mm )에 po ta t o dext ro se 한천배지를 넣어 24°c 에서 일주일간 배양한다. 그 후 배양물을 채취해서 9dm' 용기에 액체배지 (glu cose 2%, Mg S0 4 • 7H2 0, 0.3 %, NH4Cl 0.3%, KH2P04 0.3 %) 4dm' 에 접종한다. 이것을 28°C 에서 7 51-]간 통기 배양하여 lOOdm' 종균배양조에 접종하게 된다. 액 내 배양에 의해 배양할 때 균사체이기 때문에 균일한 접종이 곤란할 때는 균사를 유화기 등으로 단편화시켜서 접종시키는 방법도 있다 (Wor g en, 1968). 특히 사상균을 액내 배양할 때 생기는 형태도 산업적인 발효수율에 크게 영향을 끼치게 되는데 곰핑이의 배양형태를 결정하는 것은 주로 배 지성분과 포자접종시 포자의 농도가 주요한 요인이 된다. 포자농도가 높을 수록 생육이 분산된 형태를 나타나게 된다. 페니실린 생산에서의 P. chry so g enum 의 적절한 배양형태는 섬유상(fi la men t ous) 이고 (S mit h, 1980), 시트르산 생산에서의 A. n ig er의 형태는 입자형 (p elle t s) 인 경우이다 (Clark, 1966).
5 발효공정과 발효조 5.1 발효공정 발효산물 생산울 위한 발효공정의 전반적인 단계는 첫째 종균의 보존 관리, 둘째 종균의 증식, 셋째 발효 전 배양단계, 넷째 발효 생산단계로 나 눌수있다. (1) I 단계 : 종균의 보존(p reserva ti on) 생산균주의 장기간에 걸친 보존은 실제적인 발효를 위해서 꼭 필요한 조처로서 균주는 일정 주기로 옮겨줌으로써 생존은 물론 그들의 생산물을 생성하는 능력도 보존되어야 한다. 생산력이 높은 균주들은 균주 선별과정 동안에 일차대사에 손싱을 받기 쉽고 이러한 균주는 연속적인 이식과정 동안 자연돌연변이의 결과로 종종 퇴화되는 경우가 있다. 보존의 목적은 세포분열 없이 가능한 한 오랫동안 균주를 유지시키는 것이다. 주균주들은 灰! 동안 1 번 이상 배양되어서는 안 되며 매사용시 활 성도를 반드시 검사해야 한다• 균주에 따라서는 선별과정을 주기적으로 해 야만 하는 것도 있다. 주균주들로부터 활성균주를 선별해내는 것이다. 활 성균주들은 오염성과 산물 생산능력을 검사한 후 사용될 때까지 보존 관 리해야 한다. 또 각 균주들마다 각 공정에 따라 최적의 보존방법을 개발해 야만 한다. 보존방법의 상세한 것은 제 2 장에서 언급한 바와 같다. (2) II 단계 : 종균배양 (seed cultu r e) 보존된 미생물은 액체배지에서 진당배양하거나 또는 포자 형성이 필요 할 때는 고체배지에서 재생시킨다. 배지, 배양온도와 같은 배양의 초기에 사용되는 조건은 균종에 따라 다르겠으나 동결전조한 균은 일주일 전후 배양하고 냉동보관한 세균은 1~5 일, 곰팡이는 1~7 일이면 성장하기 시작 하는 것을 관찰할 수 있다. •
소규모 발효조를 위한 종균을 얻기 위해서는 많은 풀리·스크를 써서 진 탕배양한다. 접종하기 위해 포자와 배지를 합한 전체배지는 트윈(t ween) 8 떠 같은 계면활성제를 써서 잘 섞어주고 발효조로 옮겨준다. 종균의 적당한 배양은 그 후에 있을 최종 생산공정의 규모에 매우 중요 한 관건이 된다. 종균배양할 때 관여된 유도 및 억제현상도 생산율에 영향 을미칠 수 있다. (3) m 단계 : 전배양(p recul t ure ; Mey ra th et al., 1972) 대규모 발효조에 필요한 충분한 종배양을 공급하기 위해서 전배양을 해 야 한다. 만약 본발효 생산에 너무 소량의 종배양을 사용하여 시작한다면 성칭이 지연되고 산물의 생성속도가 만족스럽지 못하게 된다. 생산발효의 최적종균농도에 따라 전배양의 단계수가 결정된다. • 다음과 같은 종균농도로 일반적으로 접종된다. 죽 세균은 0.1~0.3%, 방선균은 5~10%, 곰팡이는 5~10%, 포자현탁액은 1 Xl05/ l 배양객 등 이다. 때로는 생산물 생성을 유도하기 위하여 종균배양의 마지막 단계에서 생산배지가사용된다. (4) N 단계 : 생산발효 발효에 따라 여러 크기의 반응조가 쓰인다. 정밀 발효산물 생산에는 l~20m' 의 발효가 쓰이나 항생물질 생산에는 보통 40~150m' 의 발효조가 쓰이고 효소 생산에는 100m3 이싱이 쓰이며 아미노산 생산에는 450m' 발 효조가 쓰이기도 한다. 생산용 영양배지는 사용되는 성분들뿐만 아니라 어 떻게 영양배지가 조제되는가 하는 것도 중요하다. 최적화시켜야 하는 요건 은다음과같다. 1. 성분물질의 조성, 질, 탄소/질소의 비율, 불순물, 각 발효조간의 차이 등. 2. 성분물질의 현탁액의 등급, 멸균 전후의 p H 값, 전체 배양맥의 성분이나 개개의 구성물질에 대한 멸균과정의 영향.
3. 접종 전의 온도 및 통기율의 증 가에 의한 멸균 배양성분의 변화. 발효공정 중 가장 중요한 변수요인은 온도의 관리와 발효액의 용존산소 의 조절이다. 온도발효는 중온균의 범위 20~45°c 나 고온균의 범위 45° c 이상에서 행해지는데 최대증식과 최적의 발효생산을 위해서는 적당한 온도를 조사 결정해야 한다. 어떤 발효에서는 증식시키기 위해 온도를 높였다가 생산기 의 초기에서 온도를 낮추기도 한다. 온도가 얼마나 중요한가를 보여주는 한 예로는 페니실린 아실라아제 발효에서 최적온도 1 °C 만 높여줄 경우 생 산율은 20% 나 낮아전다. 통기와 교반 : 통기의 일차 목적은 대사에 필요한 산소를 공급하는 것으 로 통기율은 보통 0.25~l. Ov vm(a ir volume/lig u id volume mi nu te ) 의 법위에 있다• 통기율은- 필요한 Oz9 -l 양에 따라 조정하게 된다. 발효조내 압력은 오염을 최소로 줄이기 위해 0.2~0.5bar 의 가압이 사 용된댜 큰 발효조에서는 수압도 고려해야만 한다. 왜냐하면 이것이 배양 액 속에서 0 퍼 COz 9-l 용해에 영향을 미치게 된다. 교반은 미생물세포를 영양배지에 균일하게 현탁시키고 통기가 충분한 교반을 통해서 산소흡수율을 높이게 되는데 통기와 교반의 효율을 높이기 위해서 구조적으로는 임펠러 baff le 및 s p ar g er 로 구성된다. 5.2 발효조 설계의 기본 산업적 발효공정에서 대규모 발효조를 사용한 초기대상은 제 1 차 대전시 (1914~1918) 아세돈의 심층배양에 의한 발효 생산과 193 ()!;1대 유럽에서 의 압착효모의 생산이었다. 그 의의 194 01;:祖]까지의 주된 발효산물 생산은 주로 에탄올, 글리세롤, 아세트산, 시트르산 등의 유기산과 효소류를- 들 수 있다. 194 ()1,반대 이후 페니실린의 발효 생산에서 본격적인 발효조가 건설되 었는데 (194 :M), 이때의 규모는 54,000dm'(12,0007. ]l런)였고 교반방법과
통기방법에 대한 기술적인 검토가 시작되었다고 할 수 있다 (Has ti n g s, 1971). 발효조 설계시 고려되어야 할 기능적 측 면에서의 기본은 미생물을 증식 시키기 위해 충족되어야 할 환경을 조절하는 것이다. 그리고 미생물 증식 에 따른 목적산물을 효율있게 생산시키기 위해서는 다음에 열거하는 몇 가지 조건을 갖추어야 한다. 즉 1. 발효조는 무균조작에 의해 필요한 기간 동안 가동되어야 한다. 2. 미생물의 증식과 대사산물의 생성을 충족시킬 수 있게 통기 및 교반을 할 수 있어야 하며 이때의 동력 소비는 최소화시킬 필요가 있다. 3. 발효조건에 맞는 온도와 p H 조철이 가능해야 한다. 4. 발효조 설계시 집균, 시료채취, 청소관리 및 운전을 용이하게 할 수 있도 록고려해야한다. 5. 발효조의 크기를 발효 생산량, 공간 및 공정 전체와 조화되도록 설계해야 하며 경제적인 재료를 사용하여야 한다. 산업적인 발효조는 호기성 발효가 주축을 이루고 있으며 가장 많이 채 택되고 있는 형태는 원통형으로서 밑바닥에 공기분산 유입구 (s p ar g er) 가 장치되면서 위쪽에 교반장치가 부착된 것이다(그림 5.13 , 5.14). 발효조의
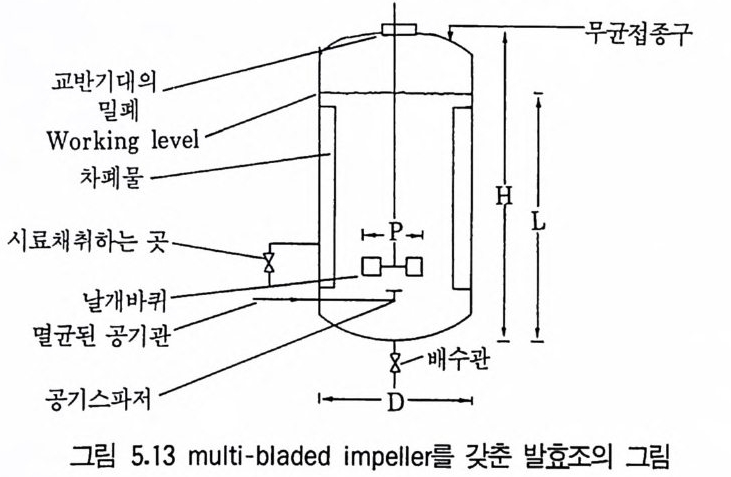 무균접종구
무균접종구
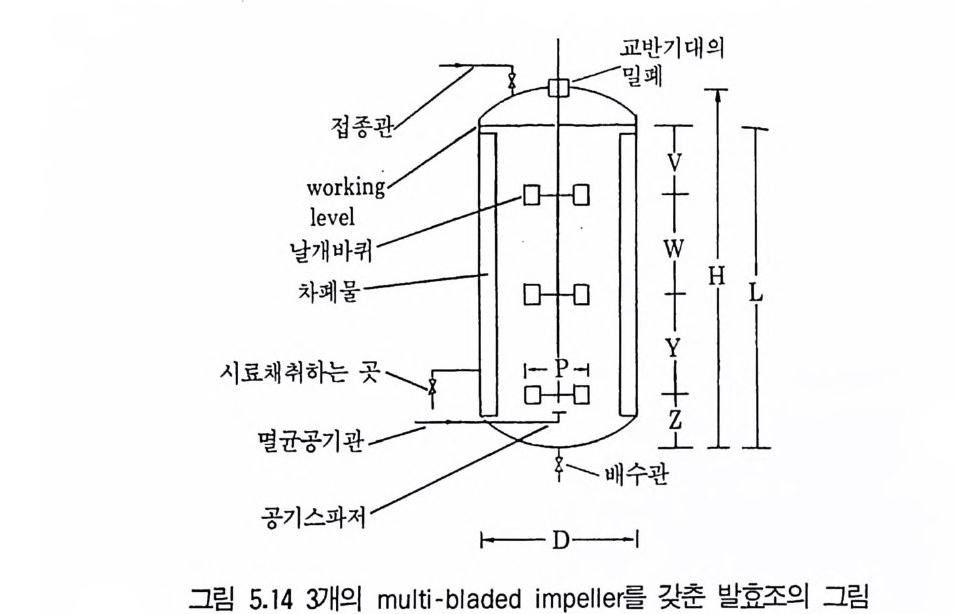 / 밀교폐반기 대 의―
/ 밀교폐반기 대 의―
크기는 ll 에서 30 여론 이싱에 달하는 것까지 다양하다. 무균 조작이 필수적인 발효조는 증기멸균을 하기 때문에 이 조건에 충 족할 수 있게 재료를 택해야 한다. 소형 발효조 (1~30l 규모)의 경우 원 통에는 유리나 스테인리스를 사용하면 표면처리 방부에 편리하다. pilo t 규모와 공장 규모의 발효조는 가압살균이나 부식, 독성성분을 고려하여 재 료를 택하게 되는데 요즈음은 스데인리스를 사용하거나 유리나 페놀릭 에 폭시 (ph enoli c epo xy ) 재료로 피막을 입혀 부식을 방지하고 있다. 발효조 제작에서 유의해야 할 문제 가운데 온도조절이 있다. 미생물 증식에서 나 오는 대사열이나 기계적인 교반 결과 나오는 열이 과량이거나 발효온도에 비해 모자랄 때는 온도를 조절해야 한다. 실험실에서는 온도조절용 수조를 사용할 수 있으나 대규모 발효조에서는 냉각용 혹은 가열용 피통(j acke t) 울 장치하거나 내부코일을 가설하여 온도조절을 하는데 500l 정도까지는 피통을 장치하나 대규모 발효조에서는 내부코일을 가설하여 온도를 조절한 다. 정확한 온도조절에 대한 검토는 R i chards (1 968) 의 책자를 참조할 수 가있다.
5.3 발효조 본체 순수 배양을 통한 발효를 수행하는 데는 발효조를 멸균할 수 있는 재질 로서 발효조를 제작하여야 한다. 실험실 규모의 발효조 (30l 정도까지 )는 유리제 발효조가 내용물이 투시되고 부식이나 용출되는 물질이 없어 편리 하나 lOl 정도가 되면 취급상의 파손 등의 우려 때문에 스데인리스 스틸 제가 흔히 쓰인다. pilo t 규모나 그 이상의 발효조 규모에서도 가압살균이 나 부식성 그리고 독성물질의 용출에 대한 발효조· 재료에 대한 적합성에 관한 Solomons(1969) 의 보고가 있다. 산업적 규모의 발효조도 스데인리 스 스틸로 만들거나 부식을 방지하기 위해 때로는 유리나 페놀릭 에폭시 (ph enolic e p ox y)로 철재내부를 입힌 발효조가 있다 (Irv i n g 1968). 오염 에 대한 우려가 없는 경우에는 목재 혹은 풀라스틱이나 콘크리트를 사용 하는 경우가 있다 (S t eel and Mi ller, 1970). 페니실린 발효에서는 철제 발효조에서도 1 Z1,빈 이상 불편없이 계속 가동 한 보고가 있다 (Walker and Holdsworth , 1958). 발효조 건조시 발효조의 두께는 규모에 따라 증가되어야 하는데 300~ 40~ 용량의 경우, 용기 양쪽은 7mm 후판을 사용하고 싱하부는 10mm 후 판을 사용하여 반구형으로 제작하는 것이 상례이다. 발효조의 설계 건조시 온도조절을 위한 설비에 유의해야 한다. 미생물대사와 기계적인 교반작용 에 의해 발열이 일어니는데 이를 냉각하가 위해 소규모 발효조는 온도조 절 수소에 넣어 조절할 수 있으나 대규모 발효조에서는 내부에 냉각 혹은 가열용 코일을 장치하거나 혹은 500l 정도의 발효조는 재킷을 의부에 붙 여서 냉각수를 순환시킨다 (M ii ller and Ki es li ch , 1966). R i chards(1968) 는 발효과정에서 냉긱수와 온도조절에 필요한 냉각 표 면적자의 관계를 검토하고 있다.
6 통기 (aera ti on) 와 교반 (a git a ti on) 대부분의 발효공정은 호기적이기 때문에 산소를 포함한 공기의 공급이 필요하다. 산소는 미생물대사에서 가장 중요한 가스상태의 기질이고 이산 화탄소는 기체상태의 대사산물이다. 예를 들어 포도당 (C 6 H1 2 0 6 ) 한 몰을 완전 산화시켜서 물과 탄산가스를 발생시키는 데는 텨薛 1 산소분자가 소 요된다. 이때 양쪽 화합물 모두가 수용액 중에 용해되어 있어야만 미생물 이 이용될 수 있고 산소는 포도당에 비해 6,00 0¾의 일이 용해될 뿐이다 (포화料 샨묘는 10 mg dm-3 임 ). 따라서 포도당을 완전 산화시키는 데 필요한 산소를 배지에 한 번에 공급하기는 불가능하지만, 그러나 미생물이 산소를 한번에 모두 요구하는 것이 아니므로 미생물의 요구를 충족시킬 수 있는 속도로 증식과정에 산소롤 공급하면 된다. 산업적 발효공정에서의 산소요구는 보통 통기를 하거나 배양액을 교반 해줌으로써 충족시킬 수 있다. 그러나 발효의 생산성은 산소이용성에 의해 제한되기 때문에 산소공급의 효율성에 영향을 주는 여러 가지 요인을 잘 검토하는 일은 매우 중요한 사항이다. 미생물균체 생산에 소요되는 산소요구량과 세포증식 후 세포 의로의 대 사산물을 산출시키기 위한 산소요구량은 다르다. 즉 대사산물의 생성량은 배지 중에 용존되어 있는 산소의 농도에 좌우되는 경우가 많다. 6.1 임계산소농도 (cr iti cal oxy ge n concentr a ti on ) 임계산소농도란 장애없이 호흡할 수 있는 비산소흡수율 (s p ec ifi c oxy - gen up tak e rate , Q oz) 의 값을 나타내기 위한 용어이다• 비산소 흡수율은 시간당 건조세포의 그램당 소비되는 산소의 m몰 로 나타내는 것인데 이것 은 M i chae li s-Men t en 유형으로 나타난다(그림 5.1 5 ). 그림 5 .1 5 에서 알 수 있듯이 비산소의 흡수속도는 용존산소농도가 일정수준 C cr iti cal 까지 는 증가하지만 그 이상에서는 증가하지 않는다. 몇몇 미생물의 임계산소농
도의 예가 표 (5.6) 에 나타나 있다. 따라서 최대균체 생산은 임계농도보다 높은 용존산소농도를 유지시킴으로써 그 균의 최대의 비산소요구량을 충족 시켜서 달성한다. 만일 용존샨소농도가 임계농도 이하로 떨어지게 되면 그 미생물의 대사는 일부 방해받게 된다.
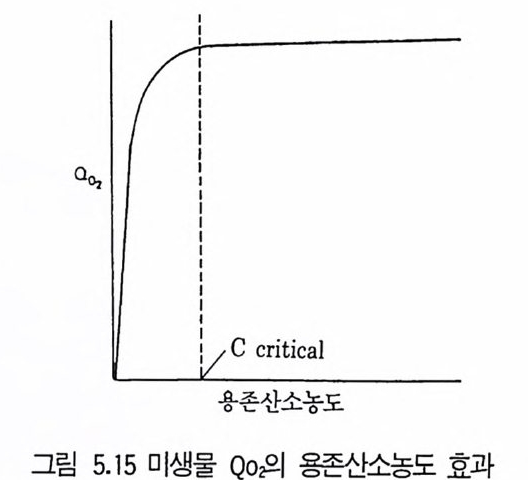 Q0,
Q0,
표 5.6 몇몇 미생물의 임계용존산소의 정도 Crit ica l diss olved Orga n i sm Temp er atu r e oxy ge n concentr a ti on (m moles dm- 3) Azoto b acte r sp. 30 0.018 Escherich ia coli 37 0.008 Saccharomy ce s sp. 30 0.004 Penic i ll i u m chry so g en um 24 0.022
H i ros 러 Shib a i( 1 980) 등은 Brevib a cte r iu m fl avum 에 의한 아미노산 생합성시, 대사경로가 같은 아미노산족의 생산과 용존산소농도와의 관계를 조사하여 홍미로운 관찰을 하였다. 죽 B .fl avum 에 대한 임계용존산소농도
는 O.Olm g dm -3로 서 이 값은 산소충족도(t he deg re e of oxy ge n sati s- fa c ti on) 를 l. 臨로 하여 산소공급의 범위를 조사하였다. 여러 아미노산 생산에 대한 산소충족도의 영향이 그립 5 .1 6 에 나타나 있다. 그림 5 .1 6 에 나타난 바와 같이 글루탐산과 아스팔트산족 아미노산 (TCA 회로의 대사산 물) 생산은 산소충족도 1.0 이하에서는 저하되는 결과를 초래하고 있으나 페닐알라닌, 발린 및 류신(해당과정중의 대사산물)의 최적생산은 산소충족 도가 각각 0.55, 0.60 및 0.85 이었다. 이 결과로 산소 과잉상태에서는 TCA 회로 산물의 생산이 효율적으로 되고 한편 산소 제한조건하에서는 포 도당의 해당 과정에 있는 대사산물이 효율적으로 생합성된다는 것을 의미 한다.
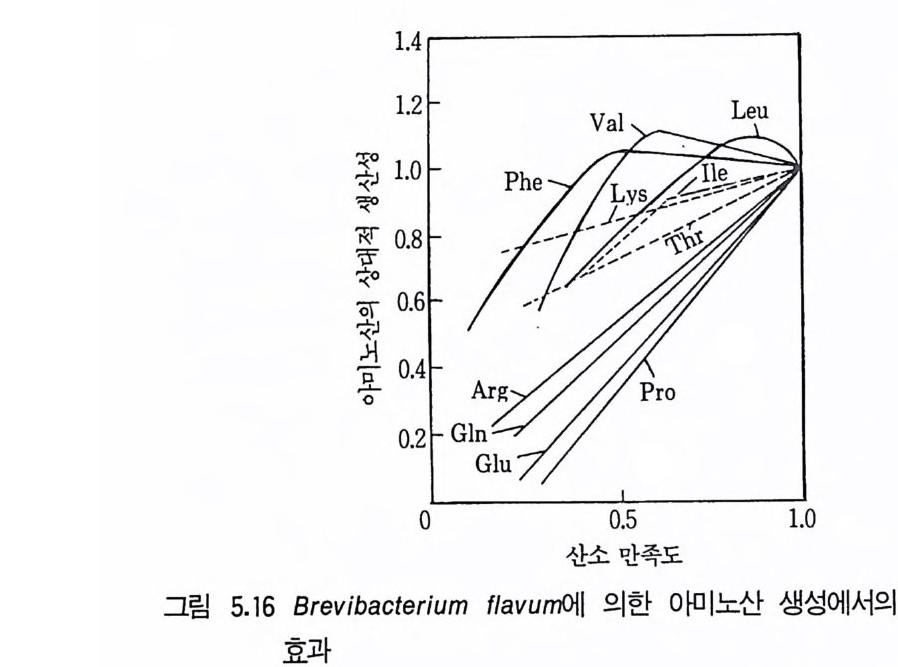 1.4
1.4
발효에서의 산소요구성은 주로 미생물 균체량과 그 증식속도에 관련되 는 호흡활성에 의해서 좌우된다. 따라서 배지의 초기농도를 제한하여 발효 조내의 균체농도를 적정농도로 유지시킬 수 있고, 한편 일부 영양성분을
공급 조절함으로써 증식속도 즉 호흡률을- 조절할 수 있다. 6.2 산소공급 (ox ygen su pp l y)과 산소 전달 (ox yg en tra nsfe r ) 산소공급은 보통 공기의 상태로 미생물 배양액에 공급된다. 이때 배양설 비와 규모에 따라 공급방법이 달라진다. 즉 50~100cm 정도의 실험실 규 모일 때는 진탕배양 (shake flas k t echn iq ue) 으로 통기하게 되고 ldm3 규모 이상의 발효조나 시험공장(pil o t scale) 규모 이상이 되면 통기교반 울 하게 되는데, 교반을 하지 않고 통기만 하는 발효조도 설계되고 있다. 산소가 미생물기질로서 요구될 때에는 발효에서 제한요소(li m iti n g fac - t or) 가 된다. 산소는 물에 대해 용해도가 0.3mMO 료서 낮기 때문에 2o ·c 에서 겨우 9 pp m만 이 녹게 된다. 배지에서는 다른 구성성분의 영향을 받아 최대산소함량은 순수한 물에서보다 더 낮게 된다. 산소는 기포로부터 개개의 세포로 전달되기 때문에 여러 가지의 독립적 인 부분 저항들을 극복해야만 한다. 즉 그림 5 .1 7 의 (1) 기체의 막의 저 항, (2) 기포와 액체 사이의 침투, (3) 경계면으로부터 액체까지의 전달,
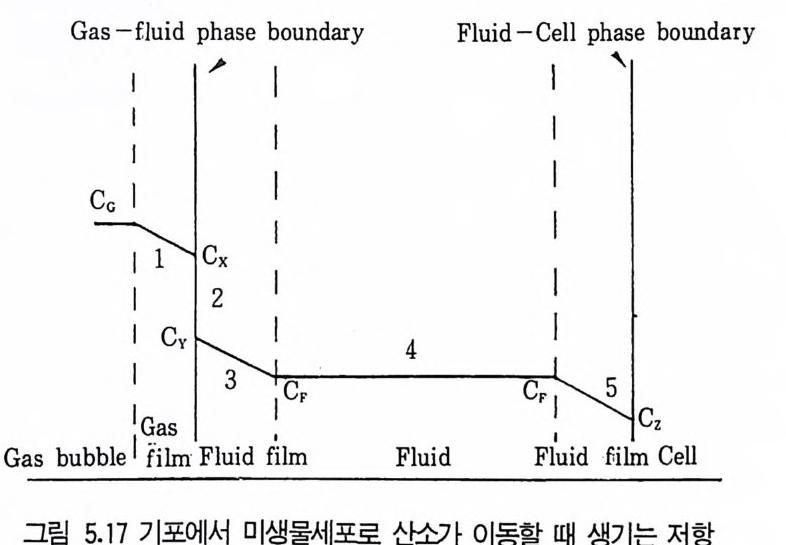 Gas-fl ui d ph ase boundary Fluid -C ell ph`a se boundary
Gas-fl ui d ph ase boundary Fluid -C ell ph`a se boundary
(4) 배양액내에서의 이동, (5) 세포의 표면으로의 전달 등이다. 세균이나 효모와 같이 단세포로 된 생물을 이용해서 발효시킬 때 기체의 전달속도 룰 조절하는 가장 중요한 요인은 기포와 액체 사이의 상경계면에서의 저 항 0] 다. 기포 근처의 미생물세포들은 상경계면을 통해 직접 산소를 흡수하여 이 러한 세포에 대한 기체의 전달속도는 증가될 것이다. 세포가 응집되거나 과립상으로 되면 산소전달의 제한요소가 된다. 기포로부터 액체상으로의 산소전달속도 (ox ygen tra nsfe r ra t e) 는 다음과 같이 특정지어질 수 있다. dCdtL = KLa.( C *-CL) [6.1 ] 무dt = 幹전달속도로서 일정시간의 산소농도의 변화 (m moles 0 2 /lh) 로 나타낸다(t는 시간). KL= 기체 • 액체상 경계면에서의 전달계수 (cm /h) a= 액체 용량에 대한 기체 /액체의 비교한 면적 (cm' /c m) KL • a= 용적 산소전달계수 (h - 1) C* =상경계면에서 용존산소의 포화농도 (m moles/l) CL= 배 0~석 의 용존산소농도 (moles /Q) OTR= 산소전달속도 (m M Oz /l • h) KL는 기체로부터 액체로의 산소전달에 대한 저항의 역수로 생각할 수 있고 C*-CL은 이 저항에 대한 추전력으로. 생각할 수 있는데 발효에서 KL3 !t a 양쪽을 측정하기란 매우 어렵다. 따라서 이 두 가지를 합쳐서 KL 료 하거 용적전달계수 (volume t r i c tra nsfe r coe ffi c i en t)로 시간에 대한 단위 (h-1) 가 된다. 즉 용적전달계수는 발효의 통기용량의 측정치로서 KLa7} 크면 그 발효조의 통기능력이 높음을 의미한다. 용존산소의 공급과 미생물의 용존산소요구간의 균형은 배양액내의 용존 산소농도에 반영된다. 만일 발효조의 KL ~근 미생물의 산소요구가 충족되
지 않는 경우라면 용존산소농도는 임계농도 (Ccr it) 이하로 저하하게 되고 만일 KLa 이 미생물의 산소요구를 쉽게 충족하는 경우라면 용존산소농도 는 Ccr i요다 크게 되고 포화농도의 70~80% 정도 높아진다. 이와 같이 발효조의 KL~ 산물생성을 위한 최적산소농도가 발효기간중 용액에 유지 될 수 있는 조건이어야 한다. 6.3 산소흡수율 KL a 값 측정 발효조의 KL a값 을 측정하는 것은 통기효율을 확립하고 산소공급시 가 변운전효과를 정하기 위해서도 필수적인 것으로서 KLa 값을 측정하는 방 법으로 네 가지가 제안되고 있다• ( 1 ) Sulph it e meth o d Coop e r(1944) 등에 의한 아황산산화법 (the sulph it e oxid a ti on tec h- niq ue) 으로서 아황산염 용액의 산화에 의해 통기한 용기내의 산소전달속 도를 측정하는 방법으로서, 이 방법은 용존산소의 농도를 측정하지 않고 아황산염 (NazS03) 의 황산염으로 전환하는 속도에 의한 것이다. 반응속도 는 산소가 용액내로 들어가게 되면 아황산의 산화에 의해 즉시 소비되므 로 아황산 산화속도는 산소전달속도 (OTR) 와 동일하다. Cu2+ 혹은 Co2+ [NlNI 2m aa+zS;SON0 33; ++ : L :1 3+/20H 0 二 220 ~ . 一225NNm a2;N;a 2N aa1zS+4HS0S 〕004 4 비산화 아황산염은 요오드(i o di ne) 액과 반응시켜 잔존 요오드를 so- dium thi osu lf a t e 로 적정한다.
(2) 가스처리방법 (ga ssin g -o ut meth o d) 가스처리방법은 통기 및 교반시의 용존산소농도의 증가를 측정해가는 방법으로서 Cv} C* 에 접근하게 되면 추진력 (C* ―Q)은 감소하게 되므로 OTR은 통기의 기간에 따라 감소하게 된다. 이 방법 중에서 정적인 방법 (sta t i c me t hod) 을 처음 발표한 것은 W i se(1951) 로서 질소가스로 액체 롤 처리하여 용액의 산소농도를 최저화시킨 후, 탄산소화된 액체를 통기 교반하면서 용존샨소의 증가를 용존산소전극(di ssolved oxy ge n p robe) 으 로 측정한다. 식 [6 .1]에서 다음 식을 얻게 된다. In(c·-cL) = -KLot [6.2] In(C*-CL) 의 도면을 시간에 대해 그리면 경사 -KL a 의 직선을 그림 6 .1과 같이 그릴 수 있다. (3) 동력학적 방법 가스처리방법 중 또 다른 방법은 Ta g uch i와 Hum p hre y (1966) 에 의해 제안된 것으로서 통기 전에 산소수준을 저하시키는 배양액의 호흡활성을 이용한 것이다. 회분발효에서 실제 용존산소농도 CL은 통기를 중단시킨 후에 CL의 감소속도를 측정함으로써 알 수 있다. 따라서 산소전달계수 (KL • a) 를 알 수 있게 한다• 다음의 식은 현재의 산소농도 변화를 나타낸 것 0] 다. ddCt L =KL • a • (C*-CL)m -Q0 2 • X 園] 묘. CL= 土KL • a . (' d후t +Q 0 2 • X) m+C* . [6.4 ] m= 생물 반웅기의 평균값 동기를 중단한 후에 발효액 속의 산소농도가 감소하는 것을 시간별로
측정해보면 -Qo z • X의 기울기를 가지는 직선으로 나타난다(그림 5.1 8 ). 이 직선의 기울기는 용적산소 전달계수 KL • a 의 역수와 같다. 이 방법의 장점은 발효조의 효율은 실질적으로 평가할 수 있는 발효기간중에 측정할 수 있고 단지 하나의 변수만이 계산되어진다는 것이다. 이 방법의 단점은 그 결과가 정확하지 않디는 것이다. 왜냐하면 산소 전극반웅의 시간이 길 고 발효조 상층부분의 공간으로부터 산소가 전달되기 때문이다. 따라서 질 소로 기체를 교환시켜주는 것이 필요한 것이다. 어떤 경우에는 발효조에서 의 정확한 측정이 가능하지 않아서 CL값 이 매우 낮게 나타날 때도 있다. 또한 통기가 약간씩 중단될 때마다 생산량이 감소되는데 이 현상은 아세 트산 발효에서 찾아볼 수 있다.
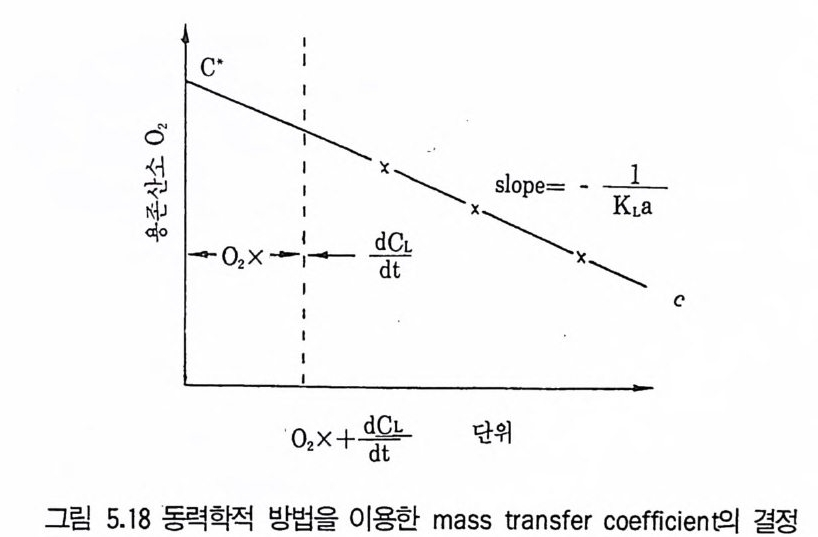 c·
c·
(4) 용적산소 전달속도를 직접 측정하는 방법 산소전달을 직접 측정하는 방법이 가장 정확한 방법이다. 하지만 이 방 법을 채택하는 데는 매우 정밀한 분석과 많은 시간이 필요하게 된다. 이 방법에서는 유입되고 방출되는 공기 중의 산소함유량이 산소전달속도를 결 정하기 위해서 측정된다. 산소흡수량을 정확히 측정하기 위해서는 온도와
압력이 일정하게 유지되는 상태에서 유입되고 방출되는 공기 중의 산소함 량의 차를 통기속도 (aera ti on ra t e) 에 곱하여 결정할 수 있다. 공기 중의 산소함량은 그들의 상자성체성인 특성가 mass s p ec t rome t e 례 7 이용해서 목]하고 정확하게 알아낼 수 있다• 또한 다른 기체들의 방해도 받지 않는 다. Q(Y i n- Yout) = OTR [6. 5] Q=통기율 Y i n= 홉인되는 공기 중의 산소함량 You t=방출되는 공기 중의 산소함량 (5) 미생물의 증식 측정을 통한 산소전달속도 (OTR) 의 측정 산소의 소요량은 열역학적인 고찰을 통해서 계산할 수 있다. 만약 하나 의 탄소로 된 기질이 한 생물체에 의해서 이산화탄소와 물, 그리고 암모니 아로 산화된다고 가정한다면 호기적 상태에서 산소요구량 C 는 생산된 건 조균체 lg¾ 기준으로- 계산된다. C= 一YAs 맹 [6.6] C= 산소요구량/생물체의 건조중량 (mM • Oz /g 균체 건조중량) A=l g의 기질을 CO2, H20 , NH 로 산화시키는 데 필요한 산소의 양 B=l g의 균체를 CO2 , H 20 , NH 로 산화시키는 데 필요한 산소의 양 Ys= 균체수율/기질 (g/g) A 값은 기질의 이론적인 산화로부터 계산된다. 庄값을 알아내기 위해서는 균체가 분석되어야 한다(효모에서 ; B=934ml • O z/g건량). 효모와 세균 에 있어서 여러 가지 기질에 대한 세포수율 (Ys) 의 몇 가지 예를 표에 나
타내었다. 또 산소의 요구량에 대한 실험적인 값들을 표에 나타내었다 . 이 값들은 요구되는 총량을 나타내므로 발효하는 동안에 필요로 하는 산소의 。於 l] 대한 정보는 주지 못한다. 시간당 배양에 요구되는 산소의 양을 결정 하기 위해서는 비중식 속도(µh - 1), 균체 X(g /l), 또 l g의 산소를 필요로 하는 세포의 그램수로 나타낸 Yo(g /g) 등을 알아야 한다. OTR=µ·XYK·o ~ [6.7] K= 보정치 • 31. 3 gm M• 0022 기질에 대한 균체수율, Yo=g • 세포/g • 산소를 알아내기 위해 다음의 식을이용한다. _!_=16( 2C+H/2-O +으 __ 上+소-__l[_ Yo Ys,M 1600 600 933 200 ) [6.8] C, H, 0= 기질에 있는 탄소, 수소, 산소의 원자량 C', H ' , O ', N ' =생물질에서의 탄소, 수소, 산소의 백분율 M= 기질의 분자량
표 5.7 여러 기질에 대해 얻어진 세포수율 Substr a te YsBacte r ia YsYeast Aceta t e 0.36 0.37 Glyc e rol 0.51 Glucose 0.51 0.50 Meth a nol 0.40 Et ha nol 0.68 Alkanes 1.03 1.00 Meth a ne 0.62 Abbot t and Clamen(1 9 73).
표 5.8 몇몇 미생물의 산소요구량 Mi cr oorga n i sm Substr a te (ml 02 / g요 d구r소yB w 二e량i g h t) Aerobacte r aerog en es Glucose-NHJ 515 Escherich ia coli Glucose-NHJ 400 Pen. chry so g en um Glucose-N H J 410 Sacch. cerevis ia e Molasses 500 Sacch. cereuis ia e Molasses 420~590 Sacch. cereuis i a e Molasses 430~550 Rhodoto r ula glu ti ni s Glucose-pe p t on e 510 Candid a util is Glucose-pe p t on e 550 Candid a util is Glucose-u rea 460 Candid a uti lis Glucose-p e p t on e 480 (Bronn, 1966)
6.4 발효조내의 KL • a 값에 영향을 미치는 요소 여러 가지 요소가 발효조내의 KL • a 치에 영향을 미치는데 그중에서도 공기의 유속, 교반의 정도, 소포제의 첨가 여부, 배양액의 유동성 (rhe- olo gy)이 득히 관계가 깊다. 발효조의 운전 규모가 커지면 소규모 발효조 에서 조사한 최적 KL • a치 를 대규모 발효에서도 이용하는 것이 중요하다. 규모가 다른 발효조에서 동일 KL • a 치를 달성시키기 위해서는 운전조건을 변화시켜야 한다. 운전변수와 KL • a간 의 상관관계를 정량화시킴으로써 특 정 KL • a 치를 달성시키기 위한 운전조건을 예측할 수가 있다. 공기의 유 속이 KL • a 에 미치는 영향을 보면 매우 높은 공기유속일 때는 매우 낮은 산소전달률을 초래하게 되는데 그 이유는 공기유속이 높은 곳에서는 임팰 러가 가스상(g as p hase) 에서 회전하게 되는 현상이 생기기 때문이다. 그 결과 가스의 용액내로의 전달을 돕지 못하게 된다. 한편 교반의 정도는 발효조내의 산소전달효율에 크게 영향을 미친다.
Banks (1 977) 은 교반작용이 산소전달에 미치는 효과에 대해 다음과 같이 말하고있다. 1. 배양 3겨 내 공기를 작은 기포형태로 분산시켜 산소전달의 면적을 증가시킨 · 다. 2. 공기의 기포가 액체로부터 빠져나가는 시간이 지연된다. 3. 기포의 합체를 방지한다. 4. 배°뇽비내에 난기류를 발생시켜 가스/액체 접촉면에서의 액체막의 두께를 감소시킨다. 교반의 정도는 발효조 내용물을 교반하는 데 소모되는 동력의 양을 측 정하여 알 수 있다. 동력의 소모(교반)와 KL • a치 를 연관시키려는 연구가 Coop e r(1 9 44), Ri ch ards(1961) 과 St ee l 및 Maxon(1962) 에 의해 연 구되었다• 발효액의 유동성은 KL • a 값과 교반 정도간의 상호관계에 현저한 영향 울 미친다. 발효액은 배지성분과 미생물이 증식하고 있는 배 0~내 으로 되어 있어 발효의 종류에 따라 유동 특성도 다르고 발효기간중에도 배양액의 유동성은 달라진다. 배지의 점성과 유동성에 따른 산소흡수율에 관해서는 Tuffil려 P i nho(1970) 의 Str ep t om y ce s aureo fa c i en 려 배양액에 관한 연 구가 있고 Banks (1 977) 는 단세포와 균사체 배 0~버 간의 산소흡수 양상의 챠기에 대하여 연구하였다 .. 참고문헌 Aiba , S., Hump h rey, A.E .(1 9 73) Bio c hemi ca l eng ine erin g, 2nd edit ion . Academi c Press, New York. Anderson, C. J. Long ton , C.(1975) The gro wt h of micr ofu n g i on car-bohy d rate s , pp. 314~329. In : Tannenbaum, S.R. and D.I.C Wang (eds), Sin g l e cell pro te i n uol. II . MIT Press, Cambrid g e , MA.
Banks, G.T.(1977) Aerati on of moulds and str e p tom y ce te cultu re flu- ids . Top ics in Enzy m e and • Fermenta tion Bio t e c hnolog y, 1, 72~ 110 (Ed itor , Wi se man, A.), Ellis Horwood, Chic h este r . Banks, G.T.( 1979) Scale-u p of fer ment at i on pro cesses. Top ics in En- zym e and Fermenta t i on Bio t e c hnolog y, 3. 170~266(Edit ior Wi se man, A.). Ell is Horwood, Ch ich este r . Brown, C.M. and 8.0. St an ley, 1972. Envir o runent -m edia t e d chang es in the celular conte n t of the
Hospo dka, J.(19 66) Industr i a l ap plica ti on s of conti nu ous fer men- tat i on . In Theoreti ca l and Meth o dolog ica l Basis of Conti nu ous Cultu r e of Mi cr oorga n is m s, pp. 493~645(Edit or s Malek, I. and Fencl 2.) Academi c Press, New York. Irvin g , G.M.(1968) Constr u cti on for brewerie s . Chem. eng . (N ew Yor- k), 75(14), 100, 102~104. Keay, L., Moseley, M.H.(1 9 72) Producti on and iso lati on of micr obia l pro te a ses. Bio t e c h. Bi oe ng . sym p . 3, 63~92. Lawt on , P., Wh itak er, A.(1 9 84) A stu d y on gro ss morph olog y of act- ino my ce te s in shake flas ks. Presente d at the Socie ty for General Mi cr obio l ogy meeti ng , Readin g Uniu e rsit y, Ja nuary 1984. Meyr ath , J. and Suchanek, G.(1972) Inoculati on tec hn iqu es eff ec t s due to qu ality and qua nti ty of ino culum. In Meth o ds in Mi cr o- bio l og y, Vol. 7B, pp. 159~209(Edit ors Norris , J.R. and Ri bb ons, D.W.). Academi c Press. London. Muller, R. and Ki es li ch , K.(1966) Technolog y of the micr obio l og ica l pre p a rati on of orga nic substa n ces. An gw ante Chem. (I nte r nati on al edit ion ), 5, 653~662. Parker, A. ( 1950) Asep tic tec hn iqu e in ind ustr i a l scale fer menta t i on . In Recent Advances in the Fermenta tion Industr ie s . Roy a l Insti tut e of chemi st r y , London. Pir t , S.J. (19 75) Prin c ip le s of Mi cr obe and Cell culti va ti on . Bla-ckwell, Oxfo r d. Reed, G. and Pep ple r, H.J. ( 1973) In Yeast Technolog y, pp. 664~668. Avi, Westp o rt. Rhodes, A., Crosse, R., Fergu s on, T.P. and Fletc h er ; D.L.(1957) Im- pro vements in or relati ng to the pro duc tion of the anti bio t i c gri - seofu lv in . Briti sh Pate n t 784. 618. Ri ch ards, J.W .(1 9 61) St u die s in aerati on and ag itat i on , Prog. Ind. Mi cr o. 3, 143~172. Ri ch ards, J.W .(1966) Fermente r mash ste r ili s a ti on . Proc Bi oc hem. 1(1) , 41~46. Rchards, J.W . ( 1968) Intr o ducti on to Industr ia l Ste r ili s a ti on . Academ ic
Press, London. Ri ch ards, J.W .(1 9 68) Desig n and Op e rati on of asep tic fer mente r s. In Intr o ducti on to Industr ia l Ste r ili z a t ion , pp. 107~ 122. Academi c Press, London. Roessler, J.G .(1968) Yeast manege ment in the brewery, Part. II , Yeast handlin g and tre atm ent, Brew, . Dig es t, 43(9), 94, 96, 98, 102, 115. Rosen, K.(1 9 77) Producti on of bakers ye ast. Process Bio c hem. 12(3). 10~12. Sansin g , G.A. and Cie g l e m, A.( 1973) Mass pr op a g a ti on of con idi a from several Asp e rgi llus and Pen ici ll ium spe cie s . Ap pl. Mi cr obio l . 26, 830~831. Sm ith, S.R. L. (1981) Some asp ec ts of ICI 's sin g le cell pro te i n pro cess. In Mi cr obia l Growt h on G. Comp o unds, pp. 342~348(Edit or Dalto n , H. ) Hey d en, London. Sm ith, G.M. and Calam, C.T.(1980) Varia t i on s in ino cula and the ir inf l ue nce on the pro ducti vi t y of anti bi o t i c fer ment a ti on s. Bio - tec hnol. Lette r s, 2(6), 261~266. Sta r k, W.M. and Sm ith, R.L. (1 9 61) The ery thr omy ci n ferm enta t i on Proc, pp. 76~79. Solomons, G.L.(1 9 69) Mate r ia l s and Meth o ds in Fermenta t i on . Academ ic Press, London. Ste e l, R. and Mi lle r, T.L.(1970) Fermente r desig n , Adv. Ap pl. Mi c- robi ol . 12, 153~188. Tagu c hi, H. and . Mi yam ot o, S.( 1966) Power req uire ment in non-Newt on ia n fer menta t i on broth . Bio t e c h .. Bi oe ng . 8, 43~54. Thorne, R.S. W.(1970) Pure yea st cultu res in brewi ng . Process Bi o- chem, 5(4), 15~22. 'Tuffile, C.M. and Pin h o, F.(1970) Dete r mi na ti on of oxy ge n tra nsfe r coeff ici e n ts in vis c ous str e p tom y c ete fer menta ti on s. Bio t e c h. Bio - eng . 12, 849 국 87 1. Underkofl er , L.A.(1976) Mi cr obia l enzym e s. In Industr ia l Mi cr obio l ogy , pp. 128~164(Ed itor s Mi ller, B.M. and Li tsk y , W.). McGraw- H ill,
New York. Vezin a , C., sehg al , S.N.(1 9 68 ) ''T r ansfo r mati on of orga n ic comp o unds by fun g al sp o res. Adv. Ap pl. M i cr obia l . 10, 221~268 . Vezin a , C. and Sin g h , K. (1 975) Transfo r mati on of orga n ic comp o unds by fun g a l sp o res In The Fi la mento u s Fun gi, Vol. 1. pp. 158~192 (Edit or s Smi th, J.E . and Berry, D.R .). Arnold, London. Walker, J.A.H , and Holdsworth , H.(1958) Eq u ip m ent desig n . In Bio - chemi ca l Eng ine erig , pp. 223~273(Edit or Ste e l. R.) Heyw o od. Lon-don. Whit ak er, A.(1 9 80) Fed-b a tc h cultu re. Proc. Bi oc hem, 15(4), 10~15. Wi lk in s on, J.F . and A.L.S. Munro. 1967. The inf l ue nce of gro w th- lim - iting condit ion s on the syn th e sis of po ssib l e carbon and energy sto r age po lym ers in Bacil lu s mega ter iu m , pp. 173~184. In : Powell, E.0. , C.G.T. Evans, R.E . Str a ng e, and D.W. Temp es t (e ds.), Mi - crobia l ph yc io l og y and conti nu ous cultu r e. HMSO, London. Wi lli a m s, S.T., Ent w i st l e , S(1 9 74) The morph olog y of str - ep tom y ce te s grow i ng in media used for commercia l pro ducti on of anti bi o t i cs . Mi cr obio s . 11. 47 ~60. Wi se , W. S. ( 1 951) The measurement of the aerati on of cultu r e med ia. J.G en, Mi cr ob. 5. 167~177. Worga n, J.T . ( 1968) Cultu re of the hig h er fun g i. Prog. Ind. Mi cr o. 8, 73~139. Yoshid a , F., Yamane, T.( 1973) Fed-batc h hy d rocarbon fer menta t i on s wit h colloid a l emulsio n fee d. Bio t e c h.Bi oe n g. 15. 257~270.
제懿l- 발효산물의 회수 1 서론 공업적 인 발효공정 중에서 가장 중요한 부분의 하나는 발효산물의 회수 와 정제이다. 대부분의 경우 생산물은 전체 발효액에 비해 매우 적은 정도 이며 그것을 싱업적 규모로 회수하기 위해서는 많은 정제과정이 필요하다. 많은 과정들이 생산물회수에 이용되는데 그것은 원래의 물질, 원래의 농 도, 생물학적 생산물의 안정성 그리고 최종산물에 요구되는 순도에 달려 있다. 여기서는 가장 중요한 생화학적 정제과정에 대해서만 설명하겠다. 원하는 산물은 세포 그 자체이거나(단세포성 단백질 생산처럼 ) 세포내 혹은 세포 의의 몇몇 대사산물인데 세포내 대사산물(i n t racellular me t abo lit e) 의 예로는 핵산, 비타민, 효소, 그리고 몇몇 항생물질들(시소 마이신, 그리세오풀반 )이 있다. 세포 의 대사산물 (ex t racellular me t abol it e) 로는 아미노산, 시트르산, 알코올, 효소류(아밀라아제와 단백질 분해효소)와 항생물질들(페니실린, 스트렙토마이신)이 있다. 때로는 생산물이 세포와 배양액 양쪽에 존재한다 (폴라보마이신, 리보풀라빈). 정제의 첫 단계는 배양맥으로부터 균체와 불용성의 영양물질을 분리하 는것이다. 여과(fi l t ra ti on) 혹은 침전 (sed i men t a ti on) 에 의해 배양액에서 세포
를 분리할 수 있으며, 대량 여과를 위해서는 드럼여과가 흔히 사용되며 여 과재료(주로 천이나 세밀한 망사)는 회전하는 드럼 주위에 감싸둔다. 드럼 이 움직임에 따라 발효액은 여과되어, 두명한 액체가 고체로부터 분리된 다. 여과효율은 규조토 같은 여과조제를 사용함으로써 증대시킬 수 있다. 침전은 주로 대규모 원심분리법으로. 행하며 그 결과 크림 같은 고체상 이 남는다. 세포내 물질을 분리할 때는 세포들을 화학적, 물리적 혹은 생물학적인 방법으로 파괴해야만 한다(그림 6.1 ).
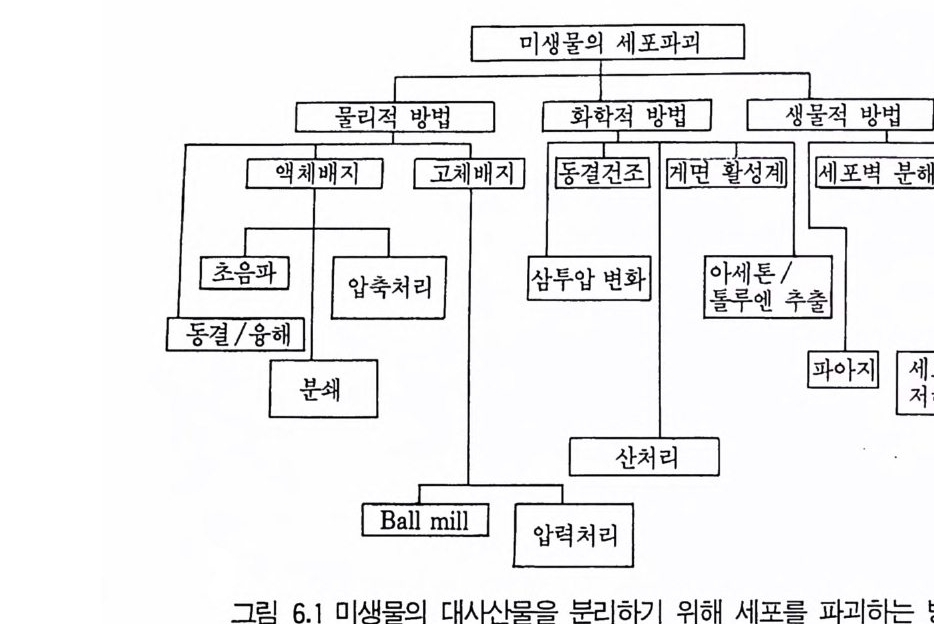 미생물의 세포파괴
미생물의 세포파괴
표 6.1 발효의 마지막 단계에서 대사산물의 농도 대사산물 수율(g/l) Vit arnin B12 0.06 Ri bo fl av in 0.1 ~ 7 Ant ibio t i cs 0.2~30 Amino acid s 2~100
만약 산을 사용한다면 생산물은 시소마이신 (s i som y c i n) 의 경우처럼 산 에 내성이 있어야만 한다. 초음파가 일반적으로 세포를 파괴하는 데 효과적이긴 하지만 많은 양의 에너지가 필요하고 비교적 비용이 많이 들기 때문에 공업적인 규모에서는 부적합하다. 그림 6.2는 최고 560bar 까지 압력을 울릴 수 있는 특별한 밸브를 가지 고 세포현탁액을 파쇄했을 때 효모세포로부터 방출된 단백질 양을 나타내 고있다.
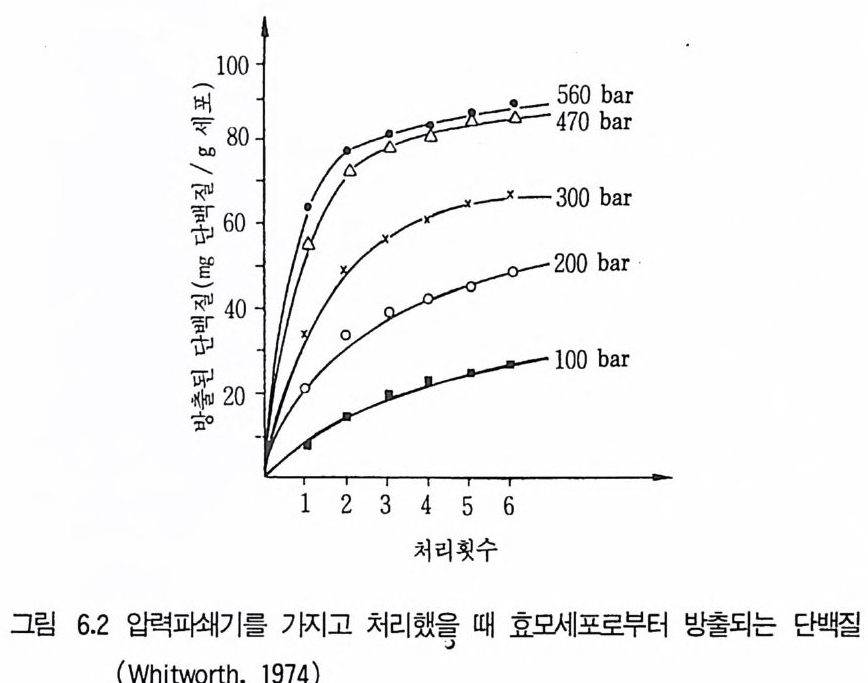 1 00
1 00
발효산물들은 항상 저농도로 발효액내에 존재한다. 그래서 초기단계에 농축과정 (concentr a ti on p rocess) 이 필요하게 된다. 한 예로 novobio c in 과정에서 이 항생물질을 여과된 발효액으로부터 이온교환체에 의해 흡수하 거나 배 0~예 으로부터 직접 흡수시킨다.
농축과정은 항상 정제과정과 연관시켜 이루어져야 한다. 그러므로 업 H 의 과정을 서로 분리시키는 것은 비합리적이다. 그림 6. 梵 7 일반적으로 사용하는 여러 가지 농 축 과정을 간단히 설명하고 있 으며 이것을 다양한 크기의 입자들이 분리되는 원리에 따라 배열하였 다.
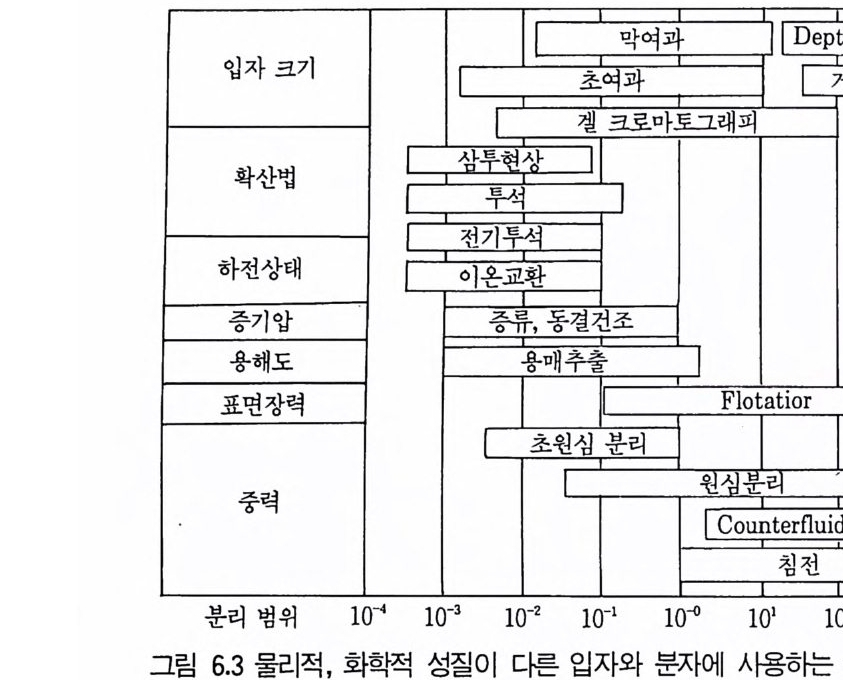 입자크기
입자크기
2 단위조작 (un it op e rati on ) 여러 가지 단위조작을 고려한디는 것은 생화학적 공학에서 일반적인 것 으로 단위조작이란 것은 여러 가지 발효과정에서 적용될 수 있는 특별한 종류의 과정을말한다.
2.1 추출 (ex t rac ti on) 대사산물을 분리 농축하기 위해서 사용하는 가장 중요한 방법은 프로판 울 혹은 부틸 아세테이트 같은 혼합되지 않는 용매로서 호기질성 물질을 추출하는 방법이다. 이렇게 추출된 물질은 제灰}계에서 수용액상으로 옮겨 진다. 용매를 가지고 추출하는 방법의 이점은 대규모 발효공정에서 빠르게 수행할 수 있다는 것이다. 한 예로 페니실린은 두 번의 용매 추출과정을 거쳐 903 :. 동안에 수용액 상으로 옮겨진다 . 이러한 신속한 추출공정은 생성물이 불안정할 경우에 특 히 중요하다. 2.2 크로마토그래피 방법 (chromato g rap hic meth o ds) 많은 발효과정 중에서 크로마토그래피의 기술은 비교적 저농도의 대사 산물을 분리 정제하는 데 이용된다. 크로마토그래피는 액체가 칼럼을 통과할 때 각기 다른 용질들의 이동과 분리의 원리에 따르는 발효산물의 정제에 널리 사용된다. 용질이 칼럼상에 무]하게 흡착되는 기작에 의하여 그 기술은 다음과 같이 구분할 수 있고 발효 산물의 종류에 따라 적절히 사용된다. 1. 흡착 크로마토그래피 (ads -o r pti on chromato g r a ph y ). 2. 이온교환 크로마토그래피 (ion -e x change chromato g r a ph y ). 3. 겔여과 크로마토그래피 (ge l-f il tra ti on chromato g r a ph y ). 4. 천화성 크로마토그래피 (affini t y chromato g r a ph y ) 조료마트래피 기술은 많은 발효 생산물의 마지막 정제단계에도 역시 O] 용된다.
(1) 흡착 크로마토그래피 (adsorp tion chromato g ra p h y ) 흡착 크로마토그래피는 주로 약한 Van der waals 힘에 의해 고체상에 서 결합하는 것을 말한다. 이 경우 칼럼을 채우는· 데 사용하는 물질들로는 무기흡착제(활성탄소, 산화알루미늄, 수산화알루미늄, 산화마그네슘, 실리카 겔)와 유기 다공성 수지가 있다. 디 히이드로스트렙토마이신 (d i -h y dro-s t re pt om y c i n) 은 활성탄 칼럼을 사용하여 여과액으로부터 추출할 수 있다. 그리고 나서 이것은 메타올성 영산에 의해 용출되고 다음 단계에서 정제된다 (Nakazawa et al. , 1960). 활성탄은 액체를 맑게 하기 위하여 색소를 제거하는 데 이용된다. 페니 실린을 포함한 용매는 색소와 다른 설순물들을 제거하기 위하여 0.25~0. 5% 의 활성탄으로 처리된다 (S y lves t er 와 Cog hi l l, 1954). 다공성 흡착제 (~aero-po rous adsorban t s) 도 역시 실험적으로 사용되 고있다. 최초의 합성유기 다공성 흡착제인 AmberIit e XAD 수지는 Rohm 과 Haas 에 의해 1965 년에 생산되었다. 이 수지는 바극성에서부터 고도로 극 성을 띠는 것까지 다양한 표면극성을 나타내며 어떠한 이온기능기 (ion ic fun cti on al g rou p s) 는 가지지 않는다. Voser (1 982) 는 이들의 가장 홍미있는 응용분야는 친수성 발효산물들 울 분리하는 것이라고 했다. 예컨대 이러한 수지들이 cep ha losp o rin C (산성아미노산), Ce foti am( 염기성 아미노산), desfe r rio x ami ne B( 염기 성 hy d ro-xam ic am ino aci d) , p arame t hasone( 중성 스테로이드)들의 회수를 위해 이들 수지를 이용한 예가 있다. (2) 이온교환(i on exchang e) 이온교환이란 고체 구조에 어떤 반응기의 변화를 동반하지 않으면서 고 체상과 액체상 사이에서의 이온의 가역적 교환으로 정의한다. 유기 이온교환수지의 경우 주요한 구성성분은 개개의 수지에 그것의 양
이온 또는 음이온적 성질을 부여하는 반응기에 부착되는 div i n y l sty re ne 중합체로되어 있다. 양이온적 이온교환수지는 보통 술폰산 (sul p hon i c acid ) , 카르복실산 (carboxy li c acid ) , 또는 포스폰산(p hos p hon i c ac i d) 을 활성기로 포함한 다. 음기온적 이온교환수지는 일반적으로 疾} 아민 (am i ne), 4 차 아민 (am ine ) 또는 4 차 암모늄 (ammon i um) 을 활성기로 가진다. 특별한 목적에 적 합한 수지의 성질은 구슬 크기 (bead siz e ), 구멍 크기 (po re siz e ), 확산 속도(diffu s i on rate ) , 수지용량 (res i n cap ac it y), 반응기의 범위 (rang e of reacti ve g rou p s) 와 대체하기 전까지의 수지의 수명과 같은 다양한 요 인들에 의존한다. 약산 양이온적 이온교환수지는 스트렙토마이신, 네오마이신과 이들과 유 사한 항생물질의 분리 정제에 이용되기도 한다. 스트렙토마이신의 회수과정에서 수집된 여과액을 염형태인 Amberlit e IRC 5 빠 같은 약간 양이온적 이온교환수지의 칼럼에 넣으면 스트렙토마 이신은 칼럼에 흡수되며 염이온으로 세척되어 나오게 된다. R-COO' N a++ str e p tom y ci n (수지 ) ➔ R —CO O 'st r e p tom y ci n + NaOH (수지) 용출속도는 시간당 10~3Qi lB 용량으로 하고 수지충은 물로 세척한 후, 흡착된 스트렙토마이신은 희석된 영산으로 용출시킨다. R-COO 'str e p tom y ci n + +HCI (수지 ) ➔ R ― COOR+s t re pt om y c i n+ • Cl' (수지)
천천히 용출시킴으로써 최소용량의 용출액을 이용하여 스트렙토마이신의 회수효율을 가장 높일 수 있다. 한 단계 공정으로도 항생물질을 10() lJI 이상 농축하고 정제할 수 있다. 수지칼럼은 적당한 양의 NaOH 울 천천히 통과시키고 이어 과다한 Na이 온을 제거하기 위하여 증류수로 세척함으로써 Na 형태로 재생된다. R-COOH+NaOH 一 R-COO ' Na++H 2 0 (수지) (수지) 수지는 l g스트렙토마이신/g二지 (res i n) 의 용량을 가지며 상업적으로.는 수지를 완전히 재생시키는 것은 그 용량이 감소하므로 비경제적이다. 실제로 세 개 중 하나는 용출되고 재생되는 동안에 연속적으로 업 n 의 칼럼에서 여과액을 취하게 된다• 첫째 칼럼이 포화되면 용출시키고 재생시 키며 그동안에 셋째 칼럼은 작동하게 한다. 다른 항생물질들의 분리에 대한 자세한 것은 Wein s te i n and Wag- man (l 978) 의 논문을 참조한다. (3) 겔여과(g el filtr a ti on ) 겔여과는 분자의 크기에 따라 분리하는 것이다• 작은 분자는 큰 분자보 다 훨씬 빠르게 겔에 확산하며 겔의 구멍에 모두 침투하여 들어가게 된다. 일단 용출이 시작되면 겔의 공간에 남아 있던 큰 분자들이 먼저 용출된 다는 원리에 의한다. 일찍이 이 방법은 상업적으로 비록 소규모이기는 하 지만 백신 (vacc i nes) 의 정제에 적용되었다 (La t ham et al., 1967). 100,l- 명 정도가 복용할 수 있는 양의 파상풍 (Te t anus) 과 디프테리아 배양액을 10 떠 13 dm3 칼럼에 통과시키고 이어서 G-20~ 13dm3 칼럼을 통과시 켜 정제하였다. 용출 완충액 Na2HP04 제거를 위해 압력 투석을 하여 l()ll~로 농축함으 로써 상당히 순수한 분획제품을 이 방법으로 생산했다.
(4) 천호남 크로마토그래피 (aff ini t y chromato g ra p h y ) 친화성 크로마토그래피는 많은 응용성을 지닌 잠재적인 분리 기술로서 대부분의 생물학적 분지를 그들의 기능이나 화학적 구조에 따라 분리 정 제하는 데 이용할 수 있다 (Scou t en, ed., 1981). 이 기술은 효소-기질, 효쇼:―저해제(i n hi b it or), 항원-항체와 같은 생 물학적 물질간의 고도의 특이 상호작용에 의한 결합 및 분리를 원리로 하 고 있다. 정제하려는 분지들은 비가용성 지지체 (ma tr i x) 에 고정화된 결합 물질 (lig and) 에 특이하게 흡착된다. 리간드는 물리적 흡착이나 화학적 공 유결합에 의해서 기질 (ma tr i x) 에 부착되고 있다. 화학적 방법이 선호되고 있다• Pora t h(1974) 와 Yang and Tsao(1982) 둘이 방법과 결합방법 (coup li n g p rocedures) 을 고찰 설명하고 있다. 결합방법에는 겔과 과립의 기질을 위하여 cya n og en brom ide , bis - oxir a nes, d i saz i r i d i nes 와 pe rio d ate s 등을 사용해서 개발되고 있다. 흔히 기질물질로 사용되는 47} 지 중합체로는 한천 (a g arose), 셀룰로 오스 (cellulose, 덱즈드로 오 ~(dex t rose) 와 폴리아크릴아미드(p ol y acr y- lam i de) 가 있다. cy an og en bro mi d 료서 활성화한 한천은 아미노 리간드 의 결합용 지지체로 사용되는 가장 보편적인 것 중의 하나로서 이들 방법 에 의해 활성물질의 수천 배의 회수율로 정제할 수도 있다• 친화성 크로마토그래피는 원래 단백질의 분리 정제와 특히 효소에만 이 용되었으며 그 후 효소 저해제, 항체와 인터페론을 위한 대규모 적용 (Jan son and Hedmen, 1982) 과 핵산 세포내 소기관, 세포성 물질 등 소 규모 응용법 (Yan g and Tsao, 1982) 이 개발되었다• (5) 연속 크로마토그래피 (conti nu ous chromato g r a p h y ) 연속적 효소 분리의 개념이 잘 정립되어 있지만 (Dunn ill and Lil ly , 1972), 가장 발달이 지연된 분야가 이 연속 크로마토그래피라 할 수 있다. Fox(1 9 69) 등은 이러한 목적하에 연속유가칼럼 (conti nu ous fed col- umn) 을 개빌하였다(그립 6.4 )
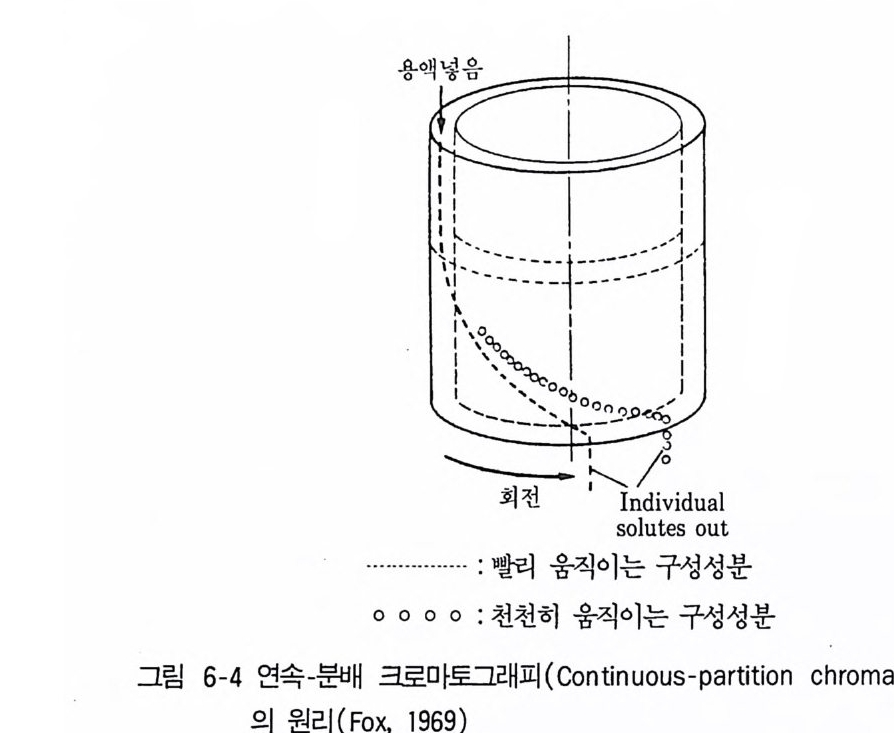 IIIII1IkI I1)'_ll
IIIII1IkI I1)'_ll
이 장치는 기저판에 고정된 두 개의 동심의 원통형 부분으로 구성되어 있다. 둘 사이의 간격(1 cm 넓이)은 2.58dm 3 의 총칼럼 용량의 적당한 수지 나 겔로 채워져 있다. 칼럼 공간 아래의 기저판 주변에 있는 연속적인 구 멍은 수집관 (collec ti n g vessels) 으로 이어진다. 이 칼럼장치는 천천히 움 직이는 회전대 (0.4 ~ 2.0rpm ) 위에서 돌아가게 되어 있다. 분리하려는 혼 합물은 칼럼과 같은 속도로 회전하는 주입관에 의해서 칼럼 속에 공급된 다 . 반면 용충객은 칼럼의 전체 주변에 고르게 넣어진다. 혼합물의 성분들 은 그 구성성분의 특유성질에 따라 다른 일련의 나선상 경로로 분리된다. 이 방법으로 만족할 만한 분리와 회수를 할 수 있지만 용출액의 소모와 생산량 속도가 일정치 않아 대규모 방법으로는 적합하지 않다 (N i cholas and Fox, 1969 ; Du nnill and Lil ly , 1972). 그러나 대규모 추출에 적합 한 연속분리장치를 개발한다면 크로마토그래피 분리의 이용이 상당히 편리 하게 될 것이다.
(6) 분배 크로마토그래피 (dis t r i b u ti on chromato g r a ph y) 물은 주로 칼럼 속에서 기질에 흡착되고 용출되는 액체는 그냥 통과된 댜 분자들은 두 종류의 용매에 대한 친화성에 따라 두 종류의 액상(p ha se) J..j-o l 에서 스스로 분배되는 것이 원리이다. 2. 3 농축 ( concentr a ti on ) ( 1) 증발 ( evapo rati on ) 증발은 중요한 단위조작으로서 낮은 농도의 대사산물을 결정화하거나 침전시키기 전에 침전막 혹은 박충증발기에서 감압 농축시킨다. (2) 한의여과 (ul tr afi l t ra ti on), 투석 (d i al y s i s) 분자의 혼합물을 분리하기 위해서 막사용 공정은 막의 유형과 그 방법 에 따라 구별할 수 있는데 두석은 좀더 작은 분자를 분리하는 데 쓰이며 농도구배는 반투막에서 행해전다. 막을 통해 확산되는 분자는 두석물질과 함께 제거된다• 한의여과공정은 고분자의 용질을 남기고 저분자의 용질이나 용매는 가 ’ 압하에서 미세한 공간을 이루는 막을 통과시켜 분리하는 것으로서, 50() oll 서부터 500,00077回 범위의 분자량을 분리시키는 각종 미세막이 있다. 단 백질, 효소, 호르몬, 바이러스, 세균 등 거대분자의 분리에 쓰이며 대규모 이용의 상세한 것은 Lacey (1 972) 및 Coo p er(1983) 의 문헌에 싱술되어 있다• (3) 결정화 (cr y st all i za ti on) 와 침전(p rec ipit a ti on) 증발이나 저온 결정화과정은 대사산물을 농축해서 정제하는 마지막 공 정 0] 다. 시트르산 생산에서는 여과역을 Ca(OH) 료- 처리한 후 불용성 칼슘시트 레이트 (cal ci um c it ra t e) 로 침전시켜 활성탄을 이용해 정제한다 (Sodeck, 1981).
(4) 건조 (dr yi n g) 미생물 균체나 발효산물의 건조과정은 제조공정의 마지막 단계의 공정 으로서 탈수와 열감수성 물질을 제거하여 저장하거나 운송비를 줄이고 취 급하기 쉽게 하는 것이 목적이다. 많은 건조공정이 있는데 여기에는 대류전조기(분무건조기, 회전전조기, 드럼건조기 등)와 접촉성 건조기(박충전조기, 용기건조기)가 있다. 세번째 종류로는 작은 규모의 과정 (즉 효소 혹은 항생물질의 정제 )에 주로 사용 하는 동결전조기가 있다. 3 수율 회수의 손실은 공정중에서 그 물질의 감수성과 정제단계의 수에 따라 달라전다. 표 6.2는 전형적인 수율의 손실을 나타내고 있다. 따라서 세포내 효소의 경우 산물회수 연구에서 가장 큰 어려움이 있다. · 생산비용(발효와 정제를 합해서) 중 정제과정에 드는 비용의 백분율은 20% 정도여야 하나 몇몇 세포내 대사산물의 경우는 90% 에 이른다.
표 6.2 전형적인 발효고정에서의 회수손실 발효산물 회수손실(%) 단세포단백질 5 항생물질 20~50 세포의 효소 10 세포내 효소 90
표 6. 党 7 글루탐산 정제에서 회수방법을 최적화할 수 있는 범위를 나타 내는실험치이다.
수율은 단지 하나의 요인에 불 과한데 그 이유는 화학약품과 기계의 비 용 그리고 인전비를 전 체적 계산에서 고려해야만 하기 때 문 이다.
표 6.3 글루탐산의 정제공정의 수율 고0 처0 직접 결정화 공 정 수융 % 음기온공정수 융 % oJ .:,達공 정 수 융 % 배양액 100 배양 액 100 배양액 100 Filt r a ti on 90 Fil tra ti on 90 Filt ra ti on 90 pH 7.5~ 8 .0 pH 7.5~ 8 .0 pH 7.5 ~8 .0 공 정 단 계 Filt r a te e va po r at i on 98 Adsorbti on to anio n 5 Adsorbti on to cati on exchange r 95 exchang er 98 pH adju s tm ent Eluti on wit h acid 98 Eluti on wit h base 95 Crys r alline acid 73 Crys t a l lin e acid 90 Crys t a l lin e Na salt 88 Crys t a l li ne Na salt 93 Crys t a l li ne Na salt 93 샤용하는 3 equ iv a lents of acid 3 equ i v a le nts of acid 3 equ iv a lents of acid 화 학 약품 1 equ i v a lent of NaO H 3 equ i v a lents of NaOH 2 equ iv a lents of NaOH 총 수 율 56.6 70.0 78 (Wolf, 197 4)
참고문헌 Coop er , A.R .(e d.). 1980. Ult ra fi ltr a ti on membranese and app li ca ti on s. Pie - num Press. New York. Dunn ill, P. and Lil ly, M.D.(1 9 72) Conti nu ous enzym e iso lati on . Bio t e c h. Bio e ng sym p 3, 97~113. Fox, J.B . , Calhoun, R.C . and EcLINTON, W.J. (1 969) Conti nu ous chromato gr a ph y app a ratu s. I. J. Chromato g . 43, 48~54. Jan son, J.C . and Hedman, P.(1982) Large - s c ale chromato g r a p h y of pro te i n s . Adu. Bi oc hem. Eng. 25, 43~99. Lacey, R.E. and Loeb, S.(1972) Indnstri a l Processin g wit h Membranes. Wi ley - I nte r scie n ce, New York. Lath am, W.C., Mi ch elsen, C.B. and EosALL, G.(1967) Prep a rati ve pro -
cedu_re for the pu rif ica ti on of tox oid s by gel filt r a ti on . Ap pl. Mi cro bia l . 15, 616~621 . Nakazawa, K, Shib a ta , M., Tanabe, K. and Yamamot o, H.(1960) Di-h y d rostr e p tom y c in . U.S. pa te n t 2, 931, 756. Ni ch olas, R.A . and Fox, J.B .(1 9 69) Conti nu ous chromato g ra p h y ap -pa ratu s. II .Ap pli c a ti on . J. Chromato g . 43, 61~65. Porath , J.( 1974) Affini t y tec hn iqu es-General meth ods and coup ling pro cedures. In Meth o ds in Enzy m ology , Vol. 34, pp. 13~30(Edi- tor s Ja koby , W.B. and Wi lc hek, M.). Academi c Press, New York. Scoute n , W.H.(ed). 1981. Af fini t y chromato g r a p h y. Bios electi ve adsorp - tion on ine rt matr i x e s. J.W iley and Sons, New York. Sodeck, G., Modl, J., Komi ne k, J. and Salzbrunn, G.(1981) Pro-ducti on of cit ric acid accordin g to the submerge d fer menta t i on . Process, Bi oc hem. 16(6), 9~11 . Sy lv este r , J.C . and Cog hill, R.D .(1954) The pe nic i l li n fer ment a ti on . In Industr i a l Fermenta t i on s, Vol. 2, pp. 219~263(Edit ors Und- 'er kofl er , L.A. and Hi ck ey, R.J.) Chemi ca l Publi sh in g Co., New York. Voser, W.(1982) Isolati on of hy d rop h il ic fer ment a ti on pro dut s by adsorp tion chromato g r a ph y . J. Chem. Tech. Bio t e c hnol. 32, 109~ 118. Wein o t ei n , M.J. and Wag m an, G.H.(1978) Anti bi o t i cs ; Isolati on , sep - arati on and pu rif ica ti on . Elseie r , Amste r dam. W血 wor t h, D.A.(1974). Assessment of an ind ustr i a l homog e niz e r for pro te i n and enzy me solubil i z a ti on from sp e nt brewery ye ast . Comp t. Rend. 'Irau . Lab. Carlsberg. 40 : 19~32. Wolf , F.J. 1974. Outl in e for fer menta t i on tec hnology , MIT, Cambrid g e, MA. Yang , C.M. and Tsao, G.T.(1982) Affini t y chromato g ra p h y . Adu. Bio c hem. Eng . 15, 19~42.
제 7 장 미생물이 생산하는 유기용매와 연료 1 서론 Pas t eur(1861) 는 협기성 세균이 당을 부탄올 (bu t anol) 과 아세톤 같은 유기용매로 발효한다는 사실을 알게 되었고 We i ~man (1 915) 은 산업적 규 모로 이들 용매를 생산하는 데 공헌을 하였다. 제疾} 세계대전 후기에는 석유화학산물의 비용이 저렴하여 식물성 당원 료의 미생물학적 생산에는 거의 관심을 기울이지 않았었다. 197 0¼빈대 중반 이후 석유와 천연가스가 고갈되면서 이들 유기용매의 발효생산에 다시 주 목하게 되었다. 지구상에서 생산되는 식물성 물질은 연간 180xl0 9톤 이 되는데 그중 단 지 l~2% 가 동물과 인간의 영양공급으로 이용되고 10% 가 에너지와 섬유 생산에 이용된다. 식물성 탄수화물로부터 유기용매의 발효 생산비용을- 효과적으로 하기 위한 요구조건은 다음과 같다. 1. 원료의 저수송비. 2. 고분자원료(목질, 셀룰로오스, 헤미셀룰로오스, 전분)를 유용한 단당이나 이당으로 전환시키는 데 드는 저비용. 3. 각기 다른 기질을 분해하고 그것들을 유용한- 대사산물로 전환시키기 위한
혼합된 배양물의 사용. 4. 냉각비용이 절익되고 높은 전환율을 나타내며 오영의 위험이 적은 고온성 균주의 사용. 5. 통기를 위해서는 높은 에너지가 필요하므로 형기적 과정이 유리하다. 6. 계속적인 공정으로 당화 및 발효할 수 있는 방법 (lnloes, 1983). 7. 회수와 농축에 드는 저비용 등. 2 에 탄올 ( eth a nol) 수천년 동안 에탄을을 생산하여 인간이 소비해왔는데 적어도 천년 전부 터 증류방법에 의해 농축된 알코올 주류 를 만들 수 있었다. 화학적 원료로 사용되는 에탄올은 몇 년 동안은 에틸렌의 분해적 수화에 의해 주로 화학 적 방법으로- 얻어왔다. 오늘날 에너지 고갈 문제에 있어서 발효에 의한 에탄올의 생성이 1980 년대에 이르러 다시 그 중요성이 부각되었다. 농지면적이 넓은 나라, 죽 브라질, 남아프리카, 미국과 같은 나라에서는 자당과 전분 같은 탄수화물 로부터 에탄올의 생산울 하는 연구가 진행되고 있다. 이같은 연구의 목적 은 에탄올을 지동차 원료로 사용하고자 하는 것이고 어떤 나라에서는 에 탄올로부터 에틸렌과 디론 석유화학물질을 생산하고자 하는 것이다. 1980 년대에 브라질에서는 석유수입의 20% 를 사탕수수에서 생산해낸 에탄올로 대치해오고있다. 2.1 에탄을의 생합성 (bio s yn th e sis of eth a nol) 효모와 박테리아는 에탄올 생산에 사용되고 있다• Saccharomy ce s cer- evis ia ~ 가장 많이 사용되는 효모이고 Kluy ve romy ce s fra g ilis £ 역시 사 용되고·있다.
호기적 조건하에서는 당 농도가 높울 때 Saccharomy ce s cereu i s i a~ 근 잘 자란다. 그러나 알코올의 생산량은 거의 없다. 형기적 조건하에서는 증식 은 느리나 분해 과정으로부터 피루브산이 피루브산 탈탄산효소 (P y ruva t e decarbox y lase) 에 의해 아세트알데히드 (Ace t aldeh y de) 와 이산화탄소로 분해된다(그림 7.1 ). 그러고 나면 에탄올이 알코올탈수소효소 (Alcohol de- h ydro g enase) 의 환원작용에 의해 아세트알데히드 (ace t aldeh y de) 로부터 생산된다. 티아민 피로인산 포도당 • 피루브산 Mg 뉴 아세트알데히드 +co2 해당작용 피르브산 탈탄산효소 l 알콜탈쓴나소 NADH2 Eth a nol 그림 7.1 에탄올의 생합성 에탄올 생산을 위한 회분방식 (ba t ch s y s t em) 은 형기조건이 너무 일찍 시작되면 좋은 전환율을 얻기 위한 균체밀도가 충분히 높지 않아서 최대 생체량을 얻기 위해서는 호기적으로 시작되어야 한다. 강제적인 호기조건 은 생산량 손실을 피하기 위해 짧은 시간에 행하는 것이 좋다. 회분방식에 비해 연속적인 과정에서는 적당한 효모성장과 에탄올의 생성이 당의 제한 (〈 l g /l) 과 소호기적 환경 (0.2~5mg Odg dry substa n ce. h) 아래에서 수행되어진다. 에탄올은 고농도에선 저해적이며 효모의 알코올 저항성은 에탄올의 생 성을 높이는 데 중요 요인이 된다. 각기 다른 균주에서의 에탄올 저항성은 상당히 다양하다. 일반적으로 5% 에탄올에서 증식이 그치게 된다 (vol- ume eth a nol in volume wate r =vv). 그리고 생산율은 6~10%(vv) 에서 거의 0 까지 감소한다. 당밀을 사용 하면 (12% 자당, weig h t per volume wate r =wv), 자당은 일반적으로
3 이간 동안에 6% ( vv) 에탄올로 전환된다. 15% 발효성 당을 함유하는 목질 가수분해물들은 8~9% 에탄올로 전환된다. 최종산물에 의해 받는 저해작용을 막기 위한 한 방법은 탄수화물의 사 용량을 제한하는 것이다. 다른 방법은 계속적인 진공 증류에 의해 발효 동 안 생성되는 에탄올을 제거해주는 것이다. 180k g의 곡물로부터 100k g의 전분을 얻을 수 있는데 질량수지에 입각한 91% 의 수율인 5 1. 7k g의 에탄올을 생산할 수 있다. 에너지 측면에서 보면, 1,700me g a j oule(M J)의 전분으로부터 단지 1,400M J의 에탄올 수 ~l 유지되고 그 에너지 전환율은 79% 정도이다. 2.2 에탄을 생산공정 (eth a nol pro ducti on pro cess) 에탄올은 세 단계를 거쳐 생산되는데 각 단계마다 최적상태가 유지되어 야 한다. 죽 ® 영임l:o거의 준비, ® 발효, ® 에탄올의 증류. 그림 7.2 에
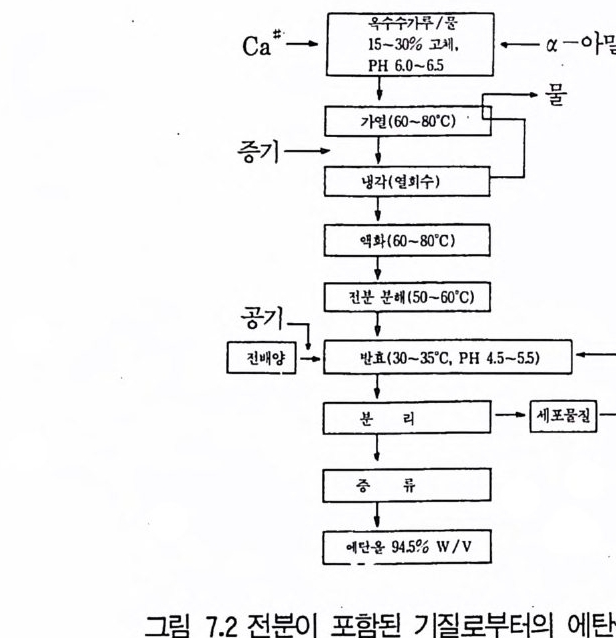 Ca g 一 __ a - 아밀라아제
Ca g 一 __ a - 아밀라아제
서는 옥수수가루로부터 에탄올이 생성되는 단계를 나타내고 있다. (1) 배 0~버 의 조제 (Prep a rati on of the nutr i e n t soluti on ) 세 종류의 기질이 에탄을 발효에 사용된다. ® 전분이 포함된 뿌리 • 줄 기나 곡물, ® 사팅수수나 사탕무로부터의 즙이나 당밀, ® 목재 당화액, 유장 (m i lk whe y)으로부터의 알코올의 생산도 실험되고 있지만 아직 상업 적으로 생산되지 못하고 있다. 가장 중요한 뿌리 전분은 열대식물인 Manih o t esculeen t~료부터 얻어지 는데 카사바(녹말), 마니오크 또는 타피오카 등이다. 브라질에서는 이런 산물기 매년 28 x l0 6 톤이 수확된다. Saccharomy ce s cerevis ia e -E - 전분 분해효소가 없기 때문에 전분을 가수 분해하여야만 한다. 우선 뿌리를 (20~35% 전분과 1.2% 단백질 포함) 파 쇄하여 짜서 말린다. 가압상태에서 전분을 끓여 액화시킨 다음 효소분해시 킨다. 미생물에서 얻은 셀룰로오스 (cellulose) 를 분해하는 효소를 첨가하여 카사바죽의 환원당 비율을 증가시킬 수 있다. 아시아지역에서 사용하는 전분질 곡물은 주로 쌀이고 미국에서는 주로 옥수수이지만 어떤 지역에서는 기장도 사용한다. 유럽에서는 감자나 그 밖 의 곡물도 사용한다. 곡식은 모두 사용할 수 있으나 옥수수의 경우는 대강 빵은 것을, 죽 옥수수알을 수시간 동안 40~5o·c 의 물에 담가 침지시켜 액화시킨 것을 사용한다. 처옵 증기분사 (15o·c, 혀손)를 통한 연속적인 액화 당화과정 후 전공 냉 각과정이 현재의 공정에 사용된다. 물 침지 후 생기는 정성도를 감소시키 기 위해 가열하기 전에 a 이밀라아제 (a-am y lase) 를 첨가하게 된다. 포도 당생성을 위해서는 가열냉각 후에 글루코아밀라아제 (g lucoam y lase) 와 a- 아밀라아제를 가해준다. 1 톤의 전분에는 1l 의 a 아밀라아제와 3.5 Q의 글 루코아밀라아제를 첨가하게 된다. 설탕 결정화 후의 부산물인 당밀은 오늘날 에탄을의 원료로 흔히 사용 되지만 가축사료나 다론 발효에 사용하는 것이 더 유리하기 때문에 앞으
로는 이용이 어려워지게 될 것으로 추정된다. 사탕수수의 경우 그 즙은 압 착방법으로 얻어지는데 사탕수수 줄기로부터 설탕을 짜낸 후의 찌꺼기를 바가스 (ba g asse) 라 한다. 부산물인 사탕수수 바가스의 약 80% 는 증류과 정에서의 연료로 이용된다. 나머지의 20% 는 화학적 가수분해 후 다시 발 효시킬 수있다. 목질은 에탄올의 상업적 생산에는 아직 사용되지 않고 있으나 이용 가 능한 목질 폐기물이 풍부하기 때문에 셀룰리아제로 가수분해시킨 목질계의 직접 발효는 매우 중요한 과제이다. 당화에는 Clostr id i u m t hermocelluw 斗 C. t hermosaccharol yti cu 짜긱 혼합 배양객이 사용되기도 하는데 이들에 의해 헤미셀룰로오스 (He mi cellulose) 와 셀룰로오스가 단당(육탄당과 오탄당)으로 분해되고 이들 단당류는 직 집 에탄올로 발효된다. 아황산 폐액은 또 다른 당원료라 할 수 있다. 침엽 수로부터 종이를 생산하는 동안 나오는 폐액으로서 발효 가능한 육탄당을 함유한다. 낙엽수로부터 아황산 폐액은 육탄당보다 오히려 오탄당형의 당 이 많이 있기 때문에 상업적으로 이용성이 낮다. (2) 발효공정 (ferm enta t i on ; Dellweg, 1979) 연속발효공장에 대해 최근 수년 동안 거론되어왔지만 계속 가동된 것은 단지 소수에 불과하다. 발효영양액은 디암모늄 포스페이트 (d i ammon i um p hos p ha t e) 를 첨가한 당밀이다. p H 는 황산으로 初}지 조절한 후 살균한 다. 발효온도는 35°c 이고 효모생산량은 lO g /l 이다. 발효 후 원심분리로서 효모 균체를 분리하여 다시 처음 발효조로 되돌려보낸다. 10. 앙]간 후 첫 번째 발효조의 생산수율은 l% 의 잔당과 6.1 % (vv) 알코올농도이고 두번 째 발효조에는 0.1 % 잔당과 8.4 % (vv) 알코올이 생산된다. 회분발효 (ba t ch fer menati on ) 방식이 아직 에탄올 생산에 가장 많이 채용되고 있다. 생산은 전분 가수분해물 (20% 건조중량)이나 당밀을 기질 로 하고 접종량(균체밀도 3 xl0 6 /ml) 은 3% 가 보통이다. l V- l 간내에 Saccharomy ce S i: 1 리터당 10~20g 건조균체량과 10%(vv) 에탄올을 생
산한다. 양질의 당밀을 이용하면 최대수율이 이론상 95% 에 달한다. 표 1 에서는 셀룰로오스 분해물을 사용하여 회분발효로 발효시킬 때 세포농도 와 발효시간과의 관계를 나타내고 있다. 증류하기 전에 원심분리나 침전법 으로균체는분리한다.
표 7.1 발효속도와 균체농도의 관계 균체농도 g/ l I 12%(v/v) 에탄을을 생성하는 데 요구되는 시간 21.4 I 7 23.6 I 6 27.2 I 5 (Ghose and Ty ag i, 1979)
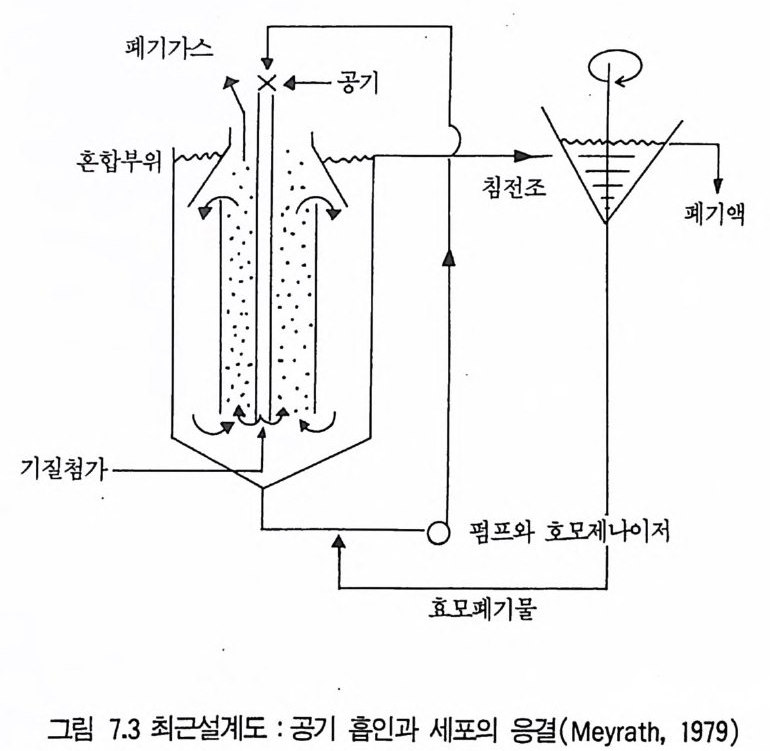 폐기가스 l\ |曺 | I l
폐기가스 l\ |曺 | I l
2.3 에탄을 발효의 에너지 수지 (energy balance of the eth a nol) 에탄올은 주로 연료와 에너지원으로서 생산되어지기 때문에 전체 과정 의 에너지 수지는 그 경제적 가치를 결정하게 된다. 각종 기질로부터 에탄 울 생산공정의 각 단계에 요구되는 에너지를 요약하면 표 7. 疾} 같다. 생산물 회수단계, 에탄을 증류단계가 전체 과정 중 가장 에너지가 많이 요구되는 단계이다. 그렇기 때문에 증류단계에 있어서의 공정개선은 발효 자체의 개선보다 전체 공정을 성공시키는 데 더욱 중요한 역할을 하게 된다.
표 7.2 무수 알코올을 생성하는 데 필요한 에너지 (순수 알코올 리터당 MJ ) 기질 공정단계 I 사탕무 入}팅수수 전분질 원료 분해/가수분해 회분 4~5 7~8 연속 2 사탕수수가루 1.1~1.5 :I 크슨- 0.8~l 2~3 발효 회분 0.06 0.06 0.06 연속 0.1 0.1 0.1 증류 단일관계 10~13 10~13 10~13 최적화 공정 5~7 5~7 5~7 고ox o 1 재래식 16 13 19 최적화공정 7 7 8 (Mi ss elhorn, 1979)
만약 생산된 에탄올의 에너지 수율이 여러 단계 공정의 총에너지 입력
과 상관관계가 있다면, 사실상 적정 수지나 혹은· 순에너지 손실 여부를 발 견할 수가 있다. 죽 모든 공정단계를 최적상태로 유지하는 것이 중요하다 는 것을 강조하고 있는 것이다. 이윤이 매우 낮기 때문에 정밀 화학물질이 나 항생물질의 경우보다는 에너지원의 생산을 위해서 최적조건을 유지하는 것이 경제적으로 매우 중요하다. 3 아세톤 및 부탄올 (Has ti n g s, 1977) Pas t eur 는 최초로 세균에 의한 부탄올의 생산을 관찰했었고 제 1 차 세 계대전에는 합성고무를 만들기 위한 부타디엔 (bu t ad i ene) 을 얻기 위해 미생물학적 공정이 개발되었는데 그 당시 Chaim We i sma 血은 아세톤 • 부탄울 • 에탄을을 생산하기 위해 Clostr id i u m aceto b uty li cu m 발효의 연구 를 수행하고 있었다. 제 1 차 세계대전중에는 폭발성의 TNT('.f rin itro - tol uene) 생산에 사용되는 아세톤에 대한 관심으로 기울어졌다. 그러나 전 쟁이 끝나자 부탄올은nit rocellulose lac q uer 의 생산에 주로 사용되어 그 중요성은 한충 더 커졌다. 제疾} 세계대전 후에는 석유를 원료로 하는 방 법이 발효방법에 대치되었고 20m' 용량 이하의 발효조를 가진 대부분의 공 장이 문을 닫게 되었다. 그러나 이 정도의 공장일지라도 정치적, 경제적, 혹은 기후적 조건이 적당한 대만이나 남미와 같은 나라에서는 오늘날까지 여전히 가동되고있다. 부티르산 (bu ty r i c aci d) , 부탄올, 아세톤 이소프로판을(i so p ro p anol) 이 전분, 당밀, 자당, 목질 가수분해물, 5탄 당으로부터 Clos t r i d i u 짜긱 발효로 제조할 수 있다 (Oun i ne, 1983). 발효공정에서 각각의 생산물의 상대적 비 율은 사용된 균주와 · 발효조건에 좌우된다. 발효산물에 따라 세 가지 발효 유형으로분류된다.
1. 아세톤-부탄올 발효 (Clos t r i dum aceto b uty li cu m) 2. 부탄올-이소프로판을 발효 (Clos t r i d i um buty li cu m) 3. 부티르산 -아세트산 발효 (Clos t r i d i um buty ri c u m) 3.1 생합성 그림 7 .4에서 주요 발효산물의 생합성 경로를 알 수 있다• 여기에 언급 되는 부탄을은 모두 n 부탄올 (n-bu t anol) 이다.
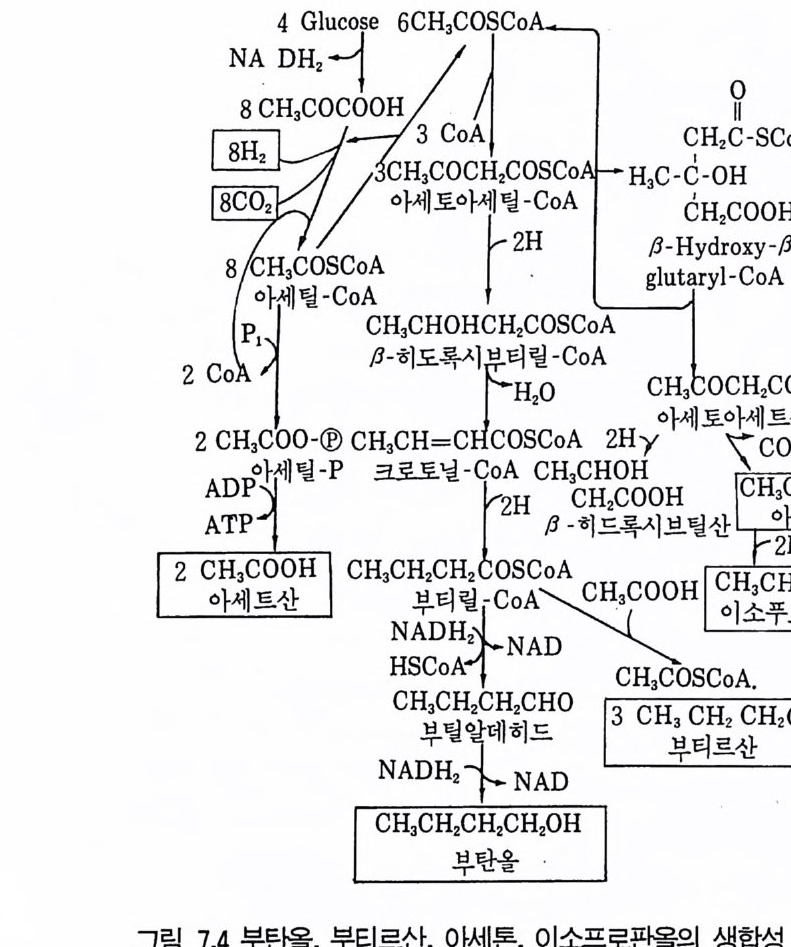 『
『
분자상태의 수소와 이산화탄소도 동시에 생성된다. 더욱이 아세트알데히 드의 환원으로 에탄을이 생산될 수도 있다. 이 미생물은 포도당에서 피루 브산으로의 전환단계에서 2 분자의 ATP 를 내고 이것이 아세트산이 생산되 지 않았을 때 방출되는 총에너지가 된다. 아세톤-부탄올 발효만이 경제적 관심의 대상이 되었었는데 균주와 발 효조건에 따라 산물이 매우 다양하기 때문에 생합성 조절은 균주에 따라 다양하고 에탄올과 같은 원하지 않는 부생산물의 생성을 최소화하여야 한 다. 상업적 발효에서는 최고 6~7% 농도의 발효성 당을 첨가할 수 있는데 그 이유는 당의 약 30% 가 산물로 전환되며 형성된 유기용매는 2% 이상 의 농도가 되면 이들 미생물에 독성을 나타내기 때문이다. p H 가 너무 낮 아지는 것을 막기 위해서 옥수려二 침출액과 같은 유기질소원을 암모늄 이 온과 함께 사용하기도 한다. 3.2 생산공정 (Walto n , 1979) 남아프리카에서 아직까지 사용중인 아세톤-부탄올 생산공장에서는 Clostr id i u m ace t obu ty l i cu 짜 1 균주 보관를 포자상태로 3~ 동안 모래 속 에 저장하고 있다. 포자의 생산과 종균의 준비는 매우 중요하다. 생산발효 조에 1 : 3,000 정도의 낮은 접종비로 접종이 되지만 몇 단계에 걸친 접종 은 다음과 감은 이점을 갖는다. 즉 오염에 대한 저항성의 증대, 발효시간 의 단축, 생산수율의 증대, 발효성, 당 농도의 증대 등이다. 멸균 후 발효조는(1 2x90m') CO 키스로 치환하고 접종 전후의 발효조 내용물도 CO 를 공급하면서 교반시킨다. 발효용 기본원료는 당밀과 옥수 수 침출액으로서 시발조건은 34°c, 5.8~6.~ p H 에서 발효시킨다. 3 6J-]간의 발효기간 중 다음 세 가지 상태를 거치게 된다(그립 7.5). 1. 처음 1 8'\]간 동안은 아세트산과 부티르산 생성으로 인해 p H 가 5. 初}지
떨어진다. 2. 다음 1 81-]간 동안은 이러한 산들이 아세톤과 부탄올로 대사되기 때문에 p H 가 올라간다. 과다량의 NADH, iJ} 존재하게 되면 세포는 부티르산을 흡수하겨 그것을 부탄울로 환원시키게 된다. 3. 다음 단계에서는 증식과 유기용매 생산이 중단되고 p H 는 5. 또료 일정하게 유지된다. 그때 산물은 회수된다.
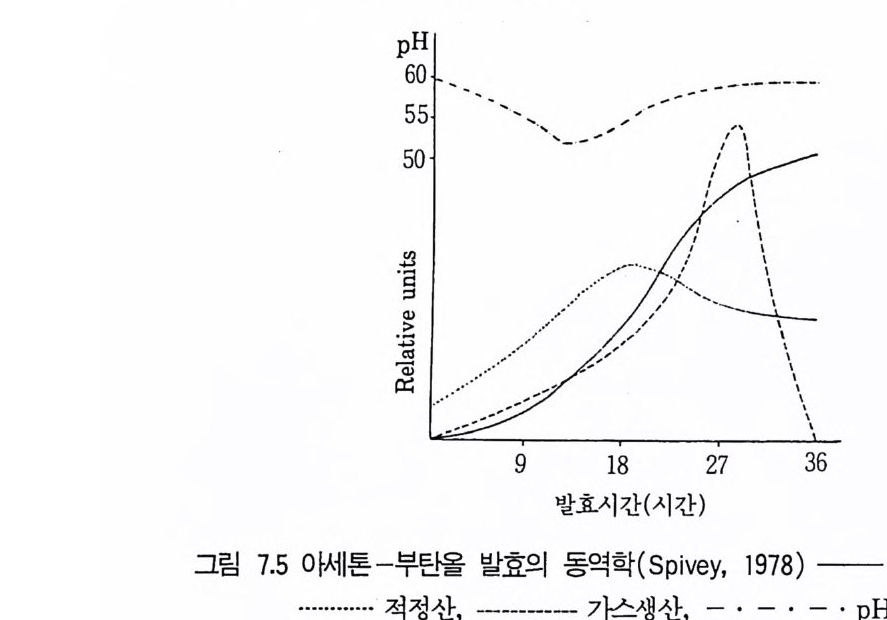 p H050
p H050
박테리오파지와 젖산균에 의한 오염이 문제이기 때문에 완전한 멸균이 필요하다. 표 7• 沃븐 발효성 당 5.8 뎃냇 7 포함한 90m' 발효조의 전형적인 수율량을 나타내고 있다.
표 7.3 90m' 용량의 발효기로부터의 생산 소邊 전환된 당의 % 생산량 ·부탄올 1,053 kg 아세톤 30( 비율 6:3:1) 526kg 에탄올 175kg
이산화탄소 50 2 2,900kg 수소 117kg (Sp ive y , 1978)
발효 동안 생산된 co 눈· 회수되어 액체 C0 2 나 드라이 아이스로 전환 되고 아세톤, 부탄을, 에탄올은 연속증류와 분류과정을 통해 회수되어진다. 증류 후에 남은 잔사는 말려서 가축사료로 이용할 수 있다. 공정을 더 효율화시키기 위해서는 활성탄에 대한 흡착이나 역삼두를 통해 유기용매를 동시 제거하는 연속적인 공정, 유기용매에 대한 저항성이 강한 균주의 선 별, 또는 고정화 세포사용 등의 개발을 통해서 가능하다. 4 글리세롤(g l y cerol) 글리세롤은 폭발성 물질의 생산원료로 사용되기 때문에 두 차례의 세계
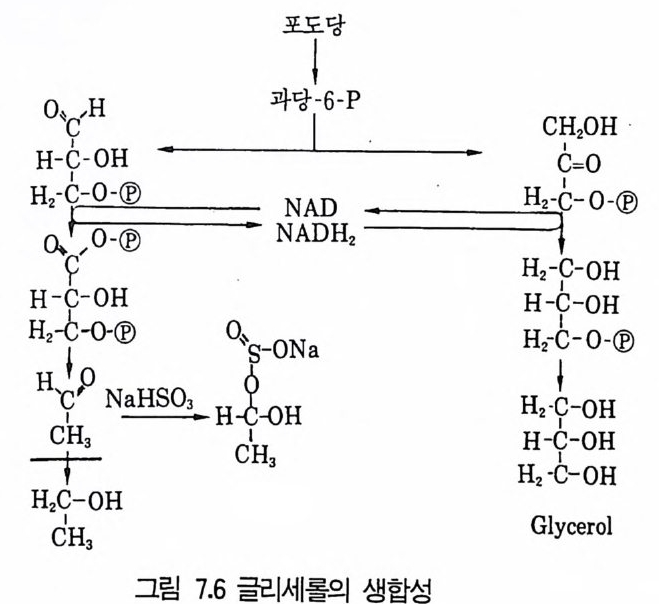 0`¢ , H 과포당도l -당6 - P CH20H
0`¢ , H 과포당도l -당6 - P CH20H
대전 동안 미생물학적 방법으로 생산되었으나 오늘날 이러한 방법은 더 이상 싱업적 가치가 없다. 그러나 글리세롤 발효는 발효 조 건을 변형시킴으 로써 산물을 변화시킬 수 있으므로 이론적 홍미를 끌고 있다. 글리세롤은 알코올 발효중 에탄올과 함께 효모에 의해 생성된다. 일반적 으로 글리세롤의 생성량은 소량이나 발효과정의 균형을 변화시킴으로써 글 리세롤의 생성량을 크게 증가시킬 수 있다. 에탄올 발효의 중간산물은 아 세트알데히드인데 만약 sodiu m d i su lfit여t 첨가하면 aceta l dehy de -s u l- fite 복합체가 생성된다. 보통 해당 작용의 첫단계에서 생성되는 NADH2 는 아세트알데히드에 의해 재산화되어 에탄을을- 생성하지만 아세트알데히 드를 이 su lfit~합체로써 제거하면 NADH~ 글리세르알데히드 포스페 이트 탈수소효소(g l y ceraldeh y de ph osph ate deh y dro g enase) 가 디히드 록시아세톤 포스페이트 (d i h y drox y ace t one phos p ha t e) 를 글리세롤 포스 페이트(g l y cerol p hos p ha t e) 로 환원시키는 데 이용된다. 아세트알데히드 두 분자가 아세트산과 에탄올로 전환되면서 글리세롤 농도는 알칼리 Na2- HPO 를 첨가하며 높아진다. 글리세롤의 공정은 다음과 같다. C6H 1 20 6 一 C3H 8 0 3 + C 02+ C 2H 4 Q 부산탉기 생성되기 때문에 1,000 rri' 용량의 발효조에서 2~3 일간 발효시 킬 때 수율은 사용한 당의 20~30% 를 결코 넘지 못한다. 삼투저항이 있 는 효모가 글리세롤 발효에 가장 적합하고 Saccharomy ce s rouxii , Tor- ulop_ s is ma q nol i ae와 Pich ia fari n o sa7} 흔히 사용되는 균주들이다 . 글리세롤 생산에 대한 홍미있는 공정이 최근 이스라엘에서 개발되었는 데 호영성 조류인 Dunalie ll a salin ~ 사용한 것이다. 이 조류는 주로 고 염성 호수나 고영농도의 환경에 의해 야기되는 삼두암울 유지하기 위한 세포내 용질로서 글리세롤을 합성하는 것이다. 의부의 영농도가 높을수록 세포내의 글리세롤 농도가 높아진다. 그러나 영농도가 갑자기 감소하면 과
다의 글리세롤이 조류세포로부터 분비되어 나오게 된다. 글리세롤 생산공정의 고영농도 함유배지에서 최초로 광합성적으로 조류 가 배양되었다. 성장이 완전히 끝난 후 세포를 농축하여 저영배지에 옮기 면 저영배지에서 짧은 시간 동안 배양하는데 상당히 농축된 형태로 글리 세롤이 분비되고 이를 정제할 수 있다. 5 수소가스 수소분지는 연소하면 물이 되므로 깨끗하고 재생 가능한 미래의 연료라 할 수 있다. 석유가격이나 자원의 유한성 때문에 장기적 안목에서 수소가 스의 생산방법의 개발은 계속되고 있다• 수소는 ® 화학적 방법, ® 전기 화학적 방법, ® 석유 혹은 석탄가공 부선물로의 방법, ® 미생물에 의한 방법으로 생산할 수 있는데, 생물학적 생산방법은 물이나 탄수화물로부터 가능하므로 재생성 자원으로부터 높은 에너지롤 요하지 않고 생산할 수 있는 이점을 지니고 있다• 三Fd(red)〉 nitro g en ase 82HNH+ 3 H2 N2 생물학적 수소생산 : 분자상태의 수소를 생합성하는 데 관여하는 효소는 수소화효소 (h y dro g enase) 나 질소화효소(nit ro g enase) 이다. 수소화효소는 2H 나 2e 노—沮 2 編 촉매藍 프이며 질책후는 8H+ + N2 +8 e- ― ➔ 2NH 3 +H2, 죽 N 룔 NH 료 전환시켜 세포에 저장하는 과정에서 수소를 발생케 하는 것이다. 수소화효소와는 달리 수소를 비가역적으로 생 성하고 0제 의해 매우 저해롤 받게 된다 .• 그 리고 전자는 페레독신(fe r redox i n) 에 의해 공급받게 된다.
많은 종류의 생물이 수소를 생성하는데 이하 대표적안 것은 설명하겠다. 5.1 조류 (al g ae) 와 Cy an obacte r ia 수소생성 조류에서 많이 연구된 것은 Chlamy d omanas, Scenedesmus, Chlorella 그리고 Sp iru lin a 등이다(표 7.4 ).
표 .7.4 최근에 보고된 조류에 의해 생성되는 수소 Alga e Produc tion of H2 Lig h t Durati on Refe r ence Ch/amy do monas 6.92 mo! / mo! 100W/m2 3.5 h GFELLER and rein h ardti i glu cose GIBBS( l98 4) C. rein h ardti i 660 µLImg chl'1 30 µE/m2 Is > 50 h APARICIO et al.( 19 85) C. rein h ardti i 302 µmo llmg cw• 1 2 00 W/m2 160 h REEVES and GRE- ENBAUM( 1985) Scenedesmus 44 µmo l I mg ch] al 8.2W/m2 5 h ROSENKRANS obliq u ns et al. (19 83) C. rein h ardti i 1.5 µmo l/cir . wt. dark 12 h MIURA et al. (1982) chi a l =chlorop h yl l
이들 조류는 광합성 생물로서 수소화효소 (h ydro g enase) 작용으로 수소 가 생성되는데 빛에 노출되면 수소생성이 촉진되나 강한 빛은 오히려 저 해한다 (Bo t he, 1982). Cy a nobacte r ia ( blue gre en al g ae) 는 산소발생형 광합성을 하여 두 개 의 관계를 갖는 원핵생물이다. 수소생성은 조류의 경우와 유사하나 다만 일차적으로는 질소고정 (nitro g e nas~ 작용)을 통해 수소를 생성한다. Cy an obacte r 중 이질세포 (he t eroc y s t)는 N2 제한시 산소 비발생형 광합 성을 하고 질소 고정과정에서 수소를 발생한다•
표 7.5 Cya n obacte r ia 2.I 수소생성속도에 관한 보고 Cy an obacte ri a Producti on of Hy dr og en Refe r ence Hete ro cys t o u s Nit ro g en Fix in g Nosloc link ia 22 mL/mg dr.wt ./h KUMAR( 19 86) Anabaena cyli nd ric a 1.91 runol/mg dr.wt ./m i n KUMAZAWA and MITSUI (19 85) Anabaena cylind ric a 집 µmol/mg dr.wt ./h LACZKO (19 86) Non-hete ro cys t o u s Nit ro g en Fix in g Oscil la t or ia sp. 260 µmol/mg chl/h PHLIPS and MITSUI (1986) Oscil la t or ia sp. 5 to 6 µmol/mg chl/h PHLIPS and MITSUI(1 9 83) Non-n itro g en Fix i n g Syn e chococcus 0.05 to 1.38 µmol/mg chl /h HOWARTH and CODD (19 85) chi = chlorop h yl l
그러나 광조사하에서 수소는 수소화효소 (h y dro genase) 작용에 의해서 발생하는 것으로 알려지고 있다 (Laczko, 1986). Cy an obacte r ia 7 ~ 수소 를 생성하는 데 대한 환경요인의 영향에 대해선 충분히 규명되어 있지 않 으나 최근 연구에 의하면 배양시간, 온도, 광도 등이 중요한 것으로 알려 지고 있다 (Ph lip s and Mi tsu i, 1983). 5.2 산소 비발생형 광합성 세균의 수소생성 여기에 해당하는 세균에는 홍색비유황세균 (A t h i orhodaceae, . Rho- dosp iri l lac eae), 홍색유황세균 (Chroma ti aceae, Th ior hodaceae) 그리고 녹색유황세균 (Chlorob i aceae) 이 있는데 이들은 전자공여체로 설파이드 (sulf ide ), 황, 티오설페이트(t h i osu lf a t e) 와 유기화합물을 이용하여 0 邊 생성하지 않고 광합성을 한다. 또한 이들 세균은 CO 2나 유기물을 탄소원 으로 이용하기 때문에 폐수처리와 연관시켜 수소를 생산할 수 있다는 이 점을 지니고 있다. 광합성 세균은 유기화합물을 이용할 수 있을 뿐 아니라 懿생성 속 중에서도 조류나 c y anobac t er i타i다 높고 비광합성 세균에
비해서도 기질당 있]지 3tln 수소생성량이 높기 때문에 가장 유리한 입장 에 있다 (Hallenbeck, 1983).
표 7.6 광합성 세균에 의한 수소생성속도에 대한 보고 Bacte r ia Producti on Durati on Refe r ence Rhodop se udomonas 책 mL/g dr. 5 to 7 day s MARGARITIS and sph aeroid e s wt. V:O GRINETZ (19 83) Rhcoadpo spu slae utad m onas 60 dtro. 1w30t . µ/ Lh/ mg H(1I9L 7L7)M ER and GEST Rhodospi ril lu m 힉 113 mL/g MIYAKE et al. ( 1982) rubrum dr.wt ./ h
광합성 세균은 광조사하에서나 암소에서나 수소를 생성할 수 있는데 그 기작은 아직 명확하지 않다• 수소는 수소화효소 (h ydro g enase) 와 질소화 효소(nit ro genase) 의 양효소에 의해 생성되는데 광합성 세균은 주로 질소 화효소(nit rogenase) 에 의해 생성된다 (M iy ake. 1982). 죽 질소원의 종류 에 따라 크게 좌우되는데 N2 , 아 미노산, 소량의 암모늄 존재하에서는 수소 가 생성되나 고농도의 암모늄 나이트레이트(nit ra t e), 우레아 글루타민 (urea glu t am ine ) 및 아스파라긴 (as p ara gi ne) 존재하에서는 그 생성이 크게 저해된다 (Kondra ti eva, 1983). 영양성분이나 환경요인이 Rhodos- piri llu 떠 hodo p seudomona 려 질소화효소 활성에 영향을 미치는데 그 내 용은 어느 정도 Yoch 에 의해 검토되고 있다 (Yoch, 1980). 5.3 형기성 세균의 수소생성 Chemotr o p h 중 수소를 생성할 수 있는 것은 Azo t obac t er의 몇몇 종 을 제의하면 주로 형기성 세균들이다. 이들 형기성 세균 중 대표적인 것 이 Clostr id i u m 속과 대칭균이다. Clos tri d i쩌 l 수소생성은 pyru uate ferr e- doxin ox i doreduc t as 폐 반응으로기 생성반응계는 다음과 같다 (Huan g et al., 1985).
pyru vate -+ CoA+2 Fd(ox)— -ac ety l CoA+2Fd(red)+C02 2H++2Fd ( red) 一 2Fd( ox) +2H2 NADH2 +2 Fd(ox)-NAD+2Fd(red) Souts c hek(1984) 일파는 협기적 오니로부터 고온성 수소생성균인 Ace- tom i cro biu m flau i du m-1끌 분리하였는데 이 균은 60°C 에서 lmol 의 포도당
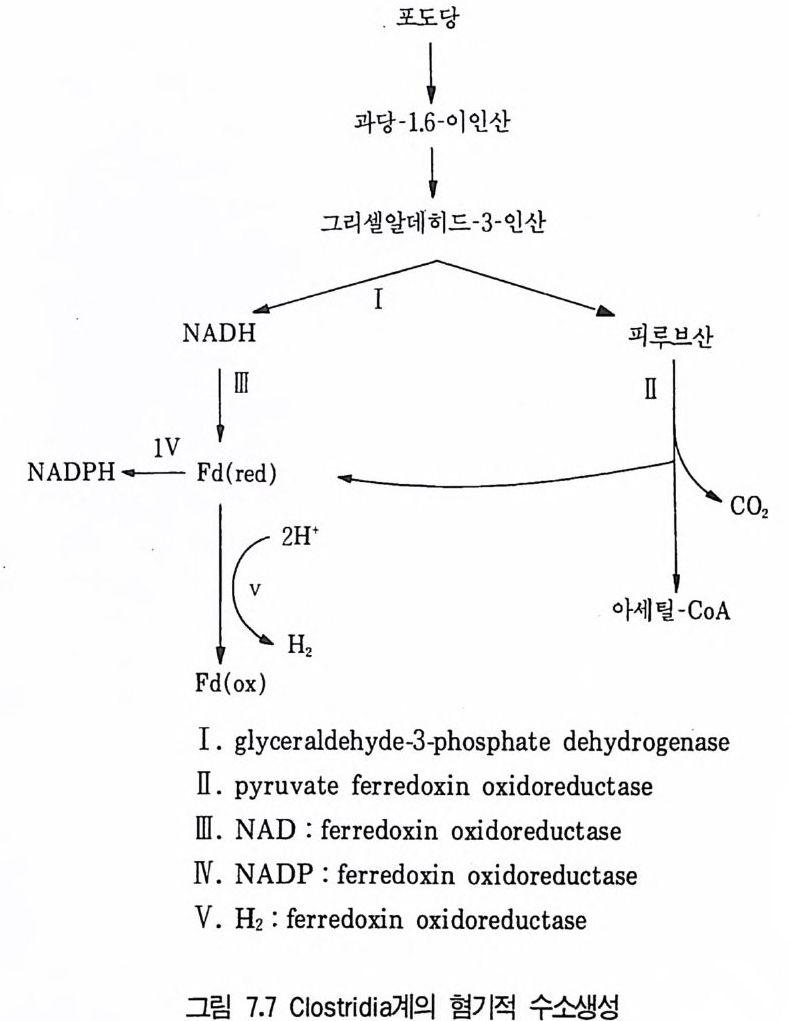 포도i당
포도i당
으로부터 4mol 의 수소를 생성하였다. 그중 2mol 은 피루브산(py ruva t e) 의 산화를 거쳐 페레독신(fe rredox i n) 으로부터 발생하고 또 2mol 은 浪} 당의 산화를 거치는 동안 NADH 로부터 유래함이 밝혀지고 있다. 대칭균계의 수소생성은 피루브산이 피루브산_포름산 분해효소(py r uvate for mate l y ase) 에 의해 포름산(fo rma t e) 으로 분해되고 다시 포름 샨기 포름산 탈수소효소(fo rma t e deh y dro genase) 와 수소화효소 (h y dro g enase) 에 의해 co~ H 로 분해될 때 생성된다. py ruva t e+CoA 一 -ace ty l CoA+fo r mate
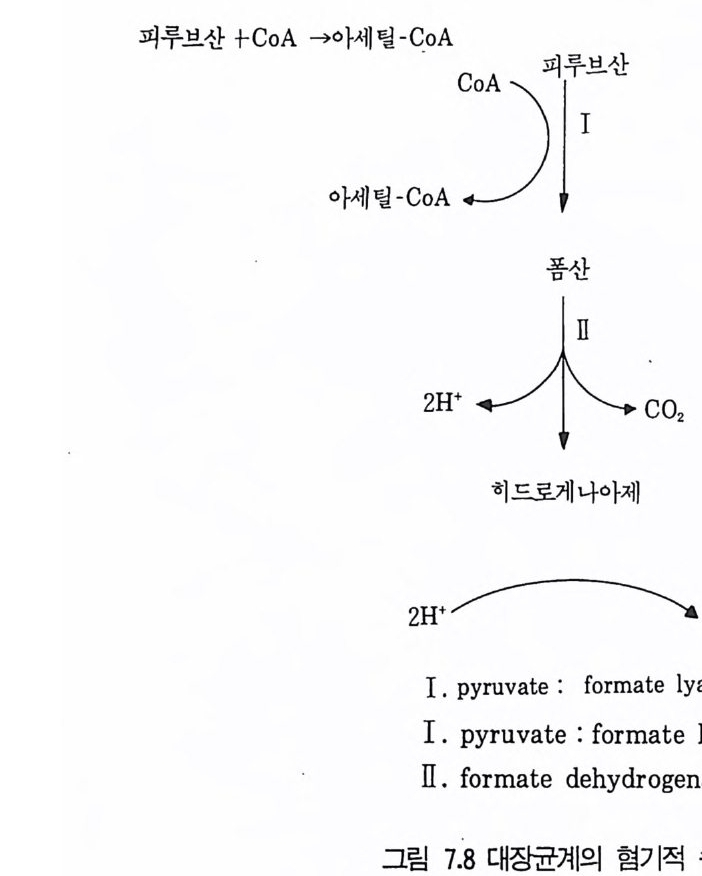 피루브산 +CoA ➔ 아세틸 -CoA
피루브산 +CoA ➔ 아세틸 -CoA
이와 같이 clos t r i d i um 과 E. col i계의 효소계는 다르다 즉 포름산 탈 수소효소를 clostr i d i u m p as t eur i anum 의 수소화효소와 혼 합하여도 수소생 성은 일어나지 않는다 (Huan g et al. , 1985). 춥卜고문헌 Both e , 51(1 9 82) Hy d rog en Producti on by alga e,(in New '!ren ds in Research and Ut iliz a ti on of Solar Energy thr ou gh Bio l og ic a l Sy st e m s) H.Mi sl in , eds, pp 65~70 Bi rk hauser Verlag, Basel. Dellweg, H.( 1979) New asp e cts in eth anol pro ducti on , pp. 35~42. In : Dechema Monog ra p h ie n , vol. 83. Verlag Chemi e, Wein b eim . Ghose,TK . and R.D . Ty a g i(1 979) Rap id eth a nol fer menta t i on of cellulose hy d rolys ate 1, Batc h versus conti nu ous sys te m s. Bio - tec hnol. Bio e ng . 21 : 1187~1400. Hasti ng s. J.J.H . 1977. Aceto ne-buty l alcohol fer menta t i on , pp. 3145. In : Rose, A.H.(ed.) . Prim ary pr oducts of meta b olism . Academ ic Pre- ss,London. Huang , S.D., Secor, C.K., Ascio n e, R. and Zweig , R.M (l985). Int. J. Hy d rog en Energ. 10, 227. Inloes, D.S., D.P. Tayl o r, S.N. 1983. Et ha nol pro duc tion by Saccharo-my c es cerevis i a e im mobil ize d in hollow-fib e r membrane bio - reacto rs. Ap pl. Enuir , Mi cr obio l . 46 : 246~278. Kondrati ev a, E.N ., and Gog o to v, I.N .(1 9 83) Producti on of molecular hy d rog e n in mi cr oorga n ism s. Adu. Bi oc hem. Eng, Bio t e c hnol. 28, 139~191. Laczko, I.( 1985) Phys i o l . Plant 67, 634. Meyr ath , J. 1979. The ALCO-FLOC sys te m , a conti nu ous and re- liab le meth od for the manufa c ure of eth a nol at extr e mely high pro ducti vi t y, pp. 107-116. In : Dellweg, H.(ed.), 4th Sy m p . 'lec- hnis c he Mi kr obio l og ie. Verlag Versuchs-und Lehransta l t fur Sp i- rit us fa b rik ati on , Berlin . Mi ss elhorn, K. 19 79 Et h anol pro ducti on under energy -effici e n t con-
dition s. St an d der Technik , pp. 47-5 5 . In : Dellweg, H.(ed.). 4th Sy m p . 'Iec hnis ch e Mi cro bio l og ie. Verlag Versuchsund Lehransta l t fur . Sp iri t us fa b rik a ti on , Berlin . Mi ya ke, J., Tomi zu ka, N. and Kami ba y a shi, A.(1982), J. Ferment. 露 hnol. 60, 199. Ounin e , K., H. Peti tde mang e, G. Raval, and R.G ay. 1983. aceto n e-buta n ol pro rlucti on from pe nt os es by Clostr id i u m aceto b uty li c u m. Bio t e c hnol. Lett er s 5 : 605~610. Phlip s, E.J., and Mi tsu i, A,(1983). app l. Envir o n. Mi cr obia l . 45, 1212. Sp ive y, M.J. 1978. The aceto ne/buta n ol/eth a nol fer ment a ti on . Pro-c. Bi oc hem. 13 : 2~4.25. Walto n , M.T. and j_L .Marti n. 1979. Producti on of but an ol-a c eto n e by fer menta t i on , pp. 187~209. In : Pep ple r, H.J. and D. Per-Iman(eds.), Mi cr obia l tec hnolog y, vol. 1. Academi c Press, New Yor- k. Yoch, D.C., and Cant u, M:(1 9 80). J. Bacte r ia l . 142-8 9 9.
제窮}유기산 발효 1 서론 유기산은 식품공업에 있어서 첨가제와 화학원료로서 폭넓게 사용되고 있다. 대부분의 유기산생성은 발효과정을 통해 행해지는데 TCA 회로의 모 든 산은 미생물학적으로- 다량 생산할 수 있다. 이타콘산처럼 크렙스 (Kre bs) 회로에서 간접적으로 유도되는 산도 생산할 수 있고 그 의 유기산은 포도당에서 직접 만들거나(예 : 글루콘산) 피루브산이나 에탄올에서부터 최종산물로 생성된다(예 : 젖산, 아세트산). 전체적으로 발효에 의해 제조 되는 시트르산의 생산을 제의하고는 긱종 유기산을 생성하는 데 있어서 미생물학적인 면과 화학적 과정이 경쟁적인 위치에 있다. 어떤 산(젖산, 아세트산)의 생산은 미생물학적 방법과 화학적 방법이 동시에 사용되고 있다. a-케 토글루탐산 (cx-ke t og lu t ar i c acid ) , 말산 (mal i c ac i d) 의 발효과 정은 수요가 적어 상업적으로 이용하지 않고 있다. 표 &1은 미생물학적으 . 로 생산되고 있거나 공정이 개발된 산을 열거해두었다. 이 장에서는 상업 적으로 관심있는 중요한 과정만 언급하겠다. 2 시트르산 (c it r i c acid ) 시트르산은 1 양 1) 기말 이래 식물성 천연물질로 알려져 왔으며 189:M 이
래로 곰핑이에 의해 생산되고 있다. 192 '.N_에 이 유기산생산을 위한 첫번 째 발효가 표면배양방법을 사용하여 시작되었고 깊은 발효조를 사용한 발 효는 193 ()11대에 시작되었다. 남아메리카와 멕시코에서는 덜 익은 레몬 (7~9% 시트르산을 함유한 레몬)에서 시트르산을 추출해내는 작은 공장 이 있지만 오늘날 시트르산의 세계적 생산의 99% 이상이 미생물학적으로 생산된다. 시트르산이 미생물학적으로 생산되는 양은 다음과 같다.
표 8.1 유기산생성의 실질적인 미생물공정 유기산 균주 상업적 기질 공정 수 율 산물의 참 고 생산 이용 Fuma ri c Rhiz ipu s sp. , Glucose 3 일 33'C 65 수지 Rhodes et al., acid 195 9, 196 2 Candid a 생산 n-Alkane 7 일 30'C 84 Furukawa et al., 1970a Prop ion ic Prop ion i- 생산 Lacto s e 8~12 일 60 古}료 Allen et al., 1964 acid bacte r iu m Glucose 30C 살균제 Sta r ch Ri vi e r e, 1977 Malic Leuconosto c 비생산 Fumaric 2 이간 99 음식 Furukawa et al., acid breuis , acid 1970b Candid a n-Alkane 72 Sato et al. , 1977 a:-k et o Candid a 비생산 n-A lkane 4 0'-]간 67 Rose, 1978 glu ta r ic Aerobacte r Gluta m ic 46 aci d acid 5-keto Aceto b acte r 생산 Glucose 5~6 일 85 L-T a rta r ic Kheshg i et al., glu conic subo.x yd ans acid 1954 acid 2-k e to - Serrat ia 생산 Glucose 1 이간 95 Isoascorbic Mi se nheim er glu conic mercescens 100 aci d et al. , 1965 aci d Sh ina ga wa et al., 1976 모든 공정이 현재 상업 생산되고 있는 것은 아니다.
1929 5,00 여 1953 50,00 여 1976 200,00 여 1979 220,00 여 발효과정은 표면배양 혹은 부피가 200m' 이상되는 발효기에서 행해지고 있다. 시트르산은 시트르산_수화물 (c it r i c ac i d-1-h y dra t e) 이나 무수시트 르산으로 시판된다. 대부분 시트르산(전체의 60% )은 식품과 음료공업에 쓰이는데 과일주스나 과일주스 추출액, 사탕, 아이스크립과 마멀레이드 (잼 )의 향미는 시트르산의 첨가로 증가된다. 제약공업 (전체 사용의 10% )에서 철의 원료로 철 시트레이트(i ron cit- ra t e) 를 사용하며 혈액보존, 정제, 연고와 화장품의 제조에 시트르산울 보 존제로 사용한다. 화학공업(전체 사용의 25% )에서 시트르산은 연화제, 소 포제, 또는 방직물 처리에 사용된다. 금속공업에서 순수금속은 금속 시트 레이트 형태로 생산된다. 시트르산은 폴리포스페이트와 대치될 수 있기 때문에 세제공업에 많이 사용된다. 폴리포스페이트 함유세제는 어떤 지역에서는 금지되고 있으며 폴리포스페이트는 시트르산으로 완전히 대치되고 있다. 2.1 시트르산 생산균주 많은 균주가 일차대사산물로서 시트르산울 분비한다. 예로는 Aspe r gi l- lus nig e r, A. wenti i, A. clauatu s , Penic il l i u m lute u m, P. citr inu m, Mu- car pirif o rm i s, Paecil om y ce s diu a ri ca tu m , Cit rom y ce s pfeff e ri a n us, Can- did a gu il li er m ondii , Saccharomy co p si s lip o lyt ica , 'Irich oderma • uiri d e , Arth r obacte r p ara ffi ne 盛와 Cory n ebacte r iu m s p가 있다. 그러나 Aspe r- gillu s n ig er의 돌연변이주와 Aspe rgi llu s wen tii에 밀집하게 ,연관된 균주만 이 싱업적 생산에 이용되고 있다 . Penic i ll i u m 균주와 비교해서 Aspe rgi lli
는 단위시간당 더 많은 시트르산을 생산한다. 따라서 옥살산, 이소시트르 산과 글루쿈산과 같은 원하지 않는 부산물의 생성은 이들 돌연변이주에서 는 효과적으로 억제할 수 있다. 2.2 생합성 시트르산 (2-h y drox yp ro p ane-l, 2, 3,-tr i c a rboxy li c ac i d) 은 일차대사 산물이며 TCA 회로에서 생성된다. 포도당은 시트르산 생산을 위해 사용되 는 주요 탄소원이고 사용된 포도당의 80% 는 Embden-Mey e rhof- P ar- nas(EMP) 경로를 통해 분해된다. 피루브산이 아세틸코에이 (acety l- CoA) 의 생성으로 탈탄산될 때 아세데이트 잔기는 TCA 회로로 들어간다. 고유상(i d i o p hase) 에서는 크렙스 회로의 모든 효소는 a 케토글루타르산 탈수소효소 (a-ke t og lu t ara t e deh y dro g enase) 를 제의하고 발현되며 , 시트 르산 합성효소 (s y n t hase) 의 활성은 시트르산 생산 동안 여러 가지 요인 에 의해 증가되는 반면 아코니타아제 (aco nit ase) 와 이소시트르산 탈수소 효소(i soc it ra t e dehy d rog en ase) 같은 시트르산을 분해하는 효소의 활성 은 영양중식상(t ro p ho p hase) 에서는 그들의 활성을 비교할 때 현저하게 줄어든다. 포도당은 펜토오스 포스페이트(p en t ose ph osp h ate ) 회로를 통해서도 분해되는데 5 탄당은 시트르산 생산에 사용될 수도 있다. 펜토오스 포스페 이트 회로의 효소가 Asp e rgi llu s nig er 에서 검출되고 있다 (Szczodrak, 1981). As p er gill us 에서 검출되는 첫 보충대사효소 (ana p lero ti c enzym e ) 는 피루브산(py ruva t e) 과 co 邊 ATP 존재하에서 옥살아세트산, 무기인 산과 ADP 로 전환시키는 피루브산 탄산효소(py ruva t e carboxy la se) (그 림 8 .1에서 반응 4) 이다. 이 반응효소는 M g표와 K 미온을 요구하는데 아세틸코에이 (acety l- CoA) 는 반응게 관여하지 않는다. 따라서 피루브산 탄산효소 (P y ruva t e carbo xy lase) 는 시트르산 생산의 주효소이다.
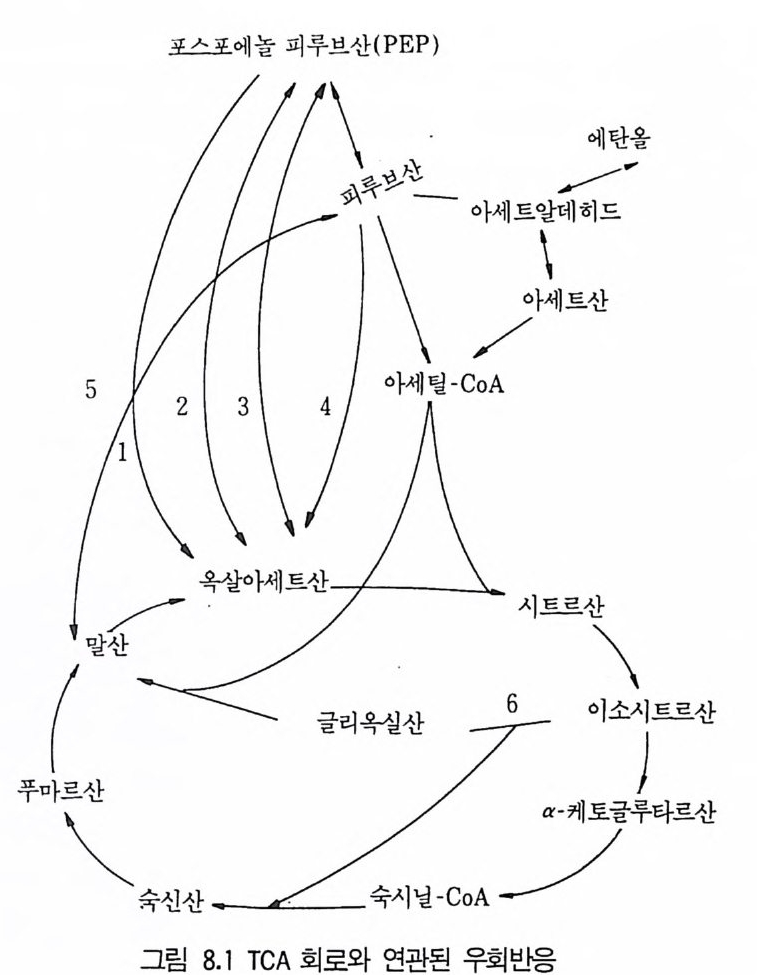 포스포 에 놀 피루브산 (PEP)
포스포 에 놀 피루브산 (PEP)
두번째 보충대사반응 (ana p lero ti c se q uence) 으로서 ADP 의 존재하에 서 PEP 와 CO 를 옥상가세트산과 ATP 로 전환시키는 포스포에놀 피루브 산 카르복시키나아제 (ph osp h oenol pyru vate carbox yki nase) 가 있다. 이 효소는 M g++, Mn + +와 K+ 혹은 NH4+ 울 요구한다. 아세데이트나 노르말 - 알칸 (n-allcanes) (C g -C zi)과 같은 지방족 화합물이 탄소원으로 사용되며 Asp e rgi llu s nig er 에서 검출되는 浪볜 보충대사반 응은 포도당이 없을 때 글리옥실산(g l yox y la t e) 회로(그림 8 .1에서 반응
6) 가 작동해서 iso cit ra te lya s e7} 유도되고 말산 합성효소 (mala t e sy n- t hase) 가 생성된다. 만일 포도당이 첨가되면 이소시트르산(i soc it ra t e) 이 부분적으로 활성하더라도 글리옥실산(g l yoxy la t e) 회로는 억제된다. 2.3 수율(yi elds) 영양중식기 (t ro phop hase) 에서 첨가된 포도당의 일부는 균사의 생산에 쓰여지며 호흡을 통해 co 료- 전환된다. 고유상(i d i o p hase) 에서는 포도당 의 잔여물은 유기산으로 전환되며 이 기간에 호흡을 통한 미량의 손실이 있다. 표 8.2는 각종 공정에서의 시트르산 수율을 표시한다.
표 &2 각종 발효공정에서의 시트르산 수율 균주 원료뭉질 (Sucrose%) 공 2J 실제수운 이론적 최대수윤 아론적인 원료물질 탄소원 kg . % /k g탄소원 최대수융(%) A. nige r Beet molasses (50%) 표면 42(kg %) 84(kg %) 61.4 68.4 A. nige r Beet molasses (50%) 액내 41 82 61.4 66.8 A. nige r Beet molasses (54%) 액내 46 85 66.3 69.4 Yeast n-Alkane 액내 165 82 247.0 66.8 Yeast Meth a nol 액내 40 45 109.4 36.6 Yeast Eth a nol 액내 60 48.4 145.8 41.1 (Sie b ert and Schulz, 1979)
이론적인 수율은 설탕 100 g당 시트르산 수화물 123g 혹은 무수시트르 산 112 g인데 영양중식상에서 일부 이용되기 때문에 수율은 약간 밑돌게 된다. 2.4 영양배지 (nutr i e n t media ) 시트르산 생산에 사용되는 배지는 수년 동안의 산업공정을 통한 경험으 로 완전히 개발되고 있다•
(1 ) 탄수화물원 ( carbohy d rate source ) 발효 동안 15내 지 25 % 당 용액이 전환된다. 각종 당자원 물질이 탄소원 으로 쓰여지는데 예컨대 감자녹말, 녹말가수분해물, 당화녹말에서 니~ 포 도당 시럽, 사탕수수 시럽, 사팅수수당밀, 사탕무당밀, 각종 정제단계의 자 당을들수있다. 녹말을 사용할 경우 곰핑이에서 생산하거나 별도로 첨가한 아밀라아제 에 의해 녹말은 당으로 가수분해된다. 가수분해물이나 시럽을 사용할 때는 침전제나 양이온 교환제로 전처리하여 앙이온을 제거시켜야 한다. 금속제 거 당밀은 살균하기 전 일반적으로 calciu m hexac yano fe rra t죠i 처리하 거나 양이온 교환제를 사용한다. Hexac y ano fe rra t e 의 일차적 효과는 금 속침전을 생기게 하는 것이지만 금속복합체 형성에 요구되는 hexacy an o- fe rra t읊 초과 첨가하게 되면 시트르산 생산량을 증가시키므로 발효에서 의 직접적인 영향을 나타낸 연구도 있다. 생산균주는 사용되는 탄소원에 따라 최적화된다. 한 가지 탄수화물원에 적합한 생산균주는 다른 탄수화물원을 사용하게 되면 일반적으로 수율이 실질적으로감소한다. 당밀원을 시트르산 생산에 사용할 경우는 당밀의 품질을 평가하는 분석 방법이 없으므로 예비 발효시험을 해야 한다. 시발물질로 당밀을 사용하는 회사는 당밀이 생산에 사용되기 전에 전처리와 30m' 발효 모델에서 배양 배지롤 만들어 최적화해야 한다. (2) 미량원소(t race elements ) 시트르산 발효에서 미량원소의 역할에 대한 본격적인 연구는 194 0\:祖] 에 시작되었고 계속적인 분석방법이 개량, 향상되어왔다. 구리, 망간, 마그 네슘, 철, 아연과 몰리브덴은 최적생산을 위해 미량이 필요하지만 최적농 도가 초과되면 독성효과를 나타낸다. 철의 역할은 특히 중요하다. 최적중식에는 높은 철농도를 요구하는 반면 아코니타아제 (aco nit ase) 를 위한 보조인자와 비교해볼 때 시트르산 최대
생산에는 0.05~0.5p pm 정도가 요구된다. 최적철 농도 (o pti mal iro n concen t ra ti on) 는 사용된 원료물질에 의존한다. 예를 들면 순수자당에는 철 0.2 pp m 이 증식 최적농도인 반면에 전화딩이나 전분의 가수분해물이 원료일 경우는 철 0.2 pp m 이 첨가되면 원료용액의 철 함유량이 높기 때문 에 산의 생성이 없이 증식만 일어난다. 아연, 철, 망간과 구리 같은 중금속 에 대한 균주의 감도는 온도가 낮아짐에 따라 감소한다. 더욱이 구리는 철 의 억제 효과를 회복시켜준다(표 8.3).
표 8.3 시트르산 생산의 8pp m FeJ + 저해에 대한 구리의 회복 효과 구리(pp m) 시트르산 %수율 。 5.0 42.0 10.0 40.0 20.0 72.4 40.0 67.5 80.0 69.2 100.0 81. 1 (Schweig e r, 1961 )
영양용액의 성분과 더불어(자당함유량, 금속-영농도와 인과 질소농도) 배지의 p H도 수율에 영향을 준다• 대사물질 생성기에서 p H 는 옥살산과 글루콘산 생성을 억제하기 위해 3 이하이어야만 하지만 영양증식기의 pH 는 일반적으로 5 에서 시작된다. 영양중식기에서 처음 4 8'-]간 동안 p H 는 암모늄이온의 대사결과로 3.0 아래로 떨어전다. 액내 배양에서 수율의 효 과적 조절을 위해 영양중식기와 고유기는 성장이 중지되는 그 아래로 pH 가 낮아지는 것으로서 구분된다. 낮은 pH 7} 주는 또 다른 장점은 오염의 위험성을 줄일 수 있다는 것이 다. 낮은 pITTl-oJ]서는 Pen i c i ll i urw 가 y eas t만이 오염될 수 있기 때문에 특 히 표면발효에서는 오염의 빈도가 중요한 경제적 요인이 된다.
2.5 생산공정 (pro ducti on pro cesses) 시트르산은 표면배양과 액내배양 양쪽 공정에 의해 생산되고 있다. 표면 배양공정은 사용된 배지의 상태에 따라 고체와 액체로 나누어진다. 액내배 %방정의 두 가지 유형에는 교반발효기 (s ti rred fe rmen t ers) 와 공기보급 (ai rl ift)형 발효조가 있다(그림 8.2).
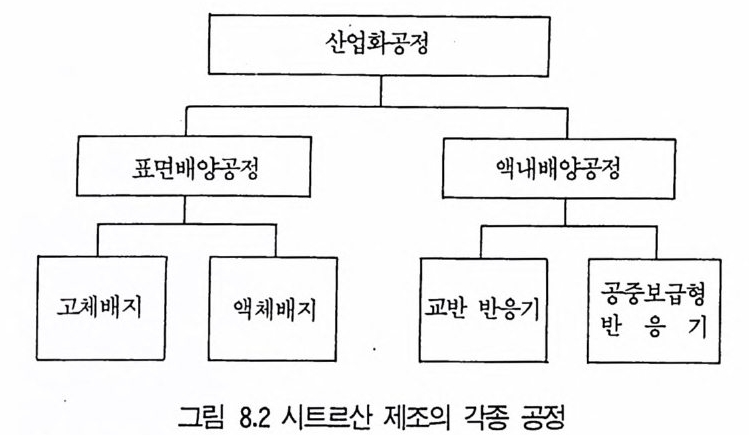 산업화공정
산업화공정
고체배양배지를 사용하는 표면배양공정은 소규모 공장에서만 사용되며 연간 최대 5,00 여탄끌 생산하지만 다른 세 가지 방법이 채용되고 있다. 생 산형태의 선택에는 여러 요인이 영향을 주는데 투자지본, 에너지, 인력과 숙련기술에 드는 비용과 공정제어 등 기술의 여부가 요인이 된다. (1) 종균생산(p roduc ti on of ino culum) 시트르산 생산에 종균으로 사용되는 것은 포자현탁액이다. 포자는 고체 배지에서 25°c , 10~14 일을 배양하여 생성시칸다. 생산된 포자의 생존능력 은 매우 중요하다. 액내발효조에 접종할 때는 포자는 전발효조에서 발아를 유도한다• 15% 자당을 포함한 당밀 영양용액을 종균발효조에 사용하여 균 사의 형성을 유도하기 위해 시안화물을 첨가하면 증식은 잘 진행되지만
이 낮고 냉각 시스뎀에서의 에너지 비용이 낮으며 기술이 쉽기 때문에 아 직까지 사용되고 있다. 그러나 파이프 쟁반과 벽을 청소하는 데 드는 인력 이 필요하기 때문에 노동력비는 대형 발효조공정보다 사실상 비싸다. • 표면배양공정에서 당은 사탕수수당밀울 대신해서 사탕무당밀을 사용한 다 . 최근 방식에서는 배지의 연속멸균방법이 채택되고 있다. 그림 8. 党 전형적인 발효공정도를 나타내고 있다. 살균된 영양용액은 자距}으로 분주계기를 통해 쟁반으로 흘러간다. 접종은 30~40 °c 의 배양 상자에서 건조된 포자를 퍼뜨리거나 (2~5 x l07 포자/ m' ) 포자현틱액을 뿌 린다.
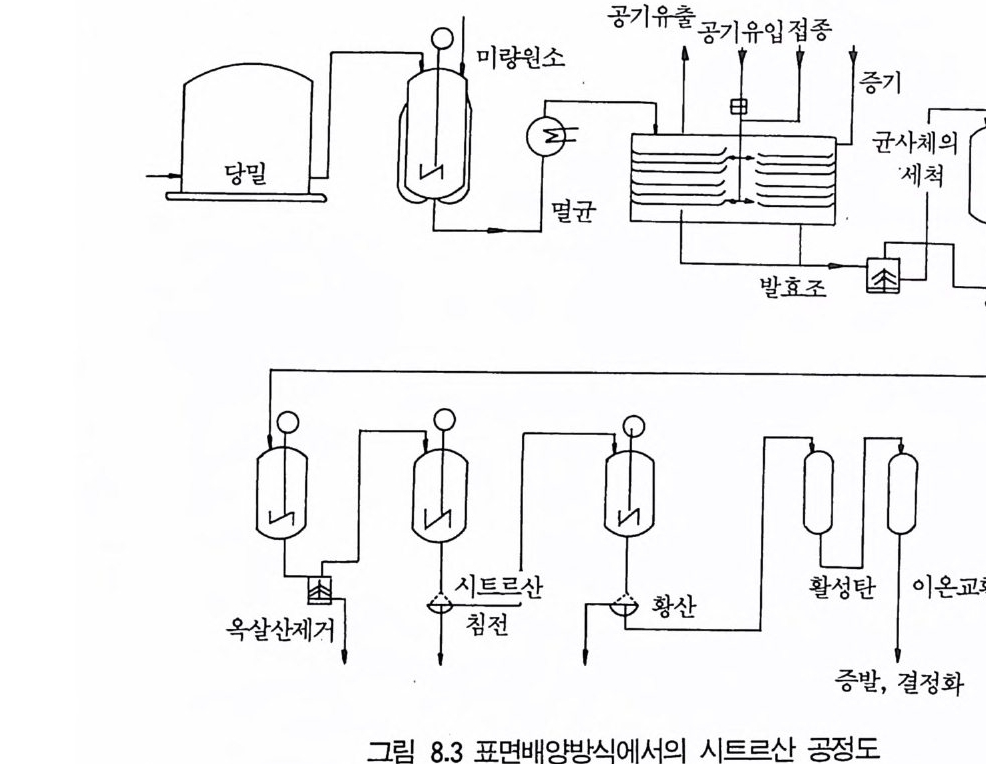 발효조
발효조
발효 동안의 온도는 공기흐름장치에 의해 30°C 로 일정하게 유지시키고 공기중의 co 가 10% 이상으로 증가되면 시트르산 생산율이 떨어지기 때
· 생산발효에서의 시트르산 수율은 낮아진다. 포자는 32 °C 에서 발아하며 24 시간 안에 지름이 0.2~0.5mm 인 과립을 형성하고 p H 는 4. 또녁i 떨어전다. 이러한 과립은 생산발효조의 접종에 사용한다. 생산발효조에서의 전환속도 와 효율은 포자와 과립이 형성되는 양상에 크게 좌우된다. (2) 표면배양공정 (surfa c e pro cesses) 고체기질을 사용하는 표면배양공정은 배양배지로 밀기울이나 감미, 감자 전분 생산에서 나오는 잔사를 사용한다. 이 방식에서의 A. n ig e riJ:9,는 다 른 공정에 비해 미량원소에 대해서는 그렇게 예민하지가 않다. 밀기울의 p H 는 살균 전에 4~誌i 낮추고 살균 후 배지에다 포자를 접종시키고 3~ 5cm 두께로 쟁반에 펼쳐 28 °C 에서 배양시킨다. 곰팡이는 자신의 amy la se 로 녹말을 가수분해하기는 하지만 a-am y las 예t 첨가함으로써 성장이 증가 된다. 고체의 표면배양공정에서는 5~8 일 배양 후에 뜨거운 물로 전체 용 액을추출해내게 된다. 액체의 영양용액을 사용히는 표면배양공정은 가장 오래된 생산방법인데 세계 전체 시트르산의 20% 를 이 방법으로 생산한다. 이 공정은 두자비용
표 8.4 표면배양계서의 영양용액의 구성성분 (Schu_lt z ) 기질 g/ l 기질 자당 160~200 ca. 320~400g 당밀 NH4N03 1.6 ~3.2 당밀이 요구되지 않는다. CaHiP 0 4 0.3~1 .0 Mg S0 4 • 7H20 0.2~0.5 당밀이 요구되지 않는다. ZnS04 0.01~0.01 Calciu m hexacya n ofe r rate 0.4 ~ 2.0
문 l 통]나 가스교환이 중요하다. 접종 후 2 41- l 간 이내에 발아된 포자 는 영양용액의 표면에 균사의 얇은 막을 형성한다. 암모늄이온 흡수결과로 배 °0택 의 p H 는 1. 5~2. 但녁i 떨어진다. 그림 8 .4는 처음 6 (Y-]간 동안의 발효과정을 나타내고 있다. 3 伊 l 간 후 고유상(i d i o p hase) 이 시작된다. 너 무 과량의 철이 들어 있으면 옥살산이 생산되고 노란 색소가 생성되어 후 에 회수공정을 방해한다. 완전히 성장한 균자가 영양용액에서 두껍게 돌돌 말린 흰막으로 떠다니게 된다. 증발을 통해 온도는 일정하게 유지되지만 배양액은 원래 용량의 30~40% 를 상실하게 되고 발효는 8~14 일 후에 중지시킨다.
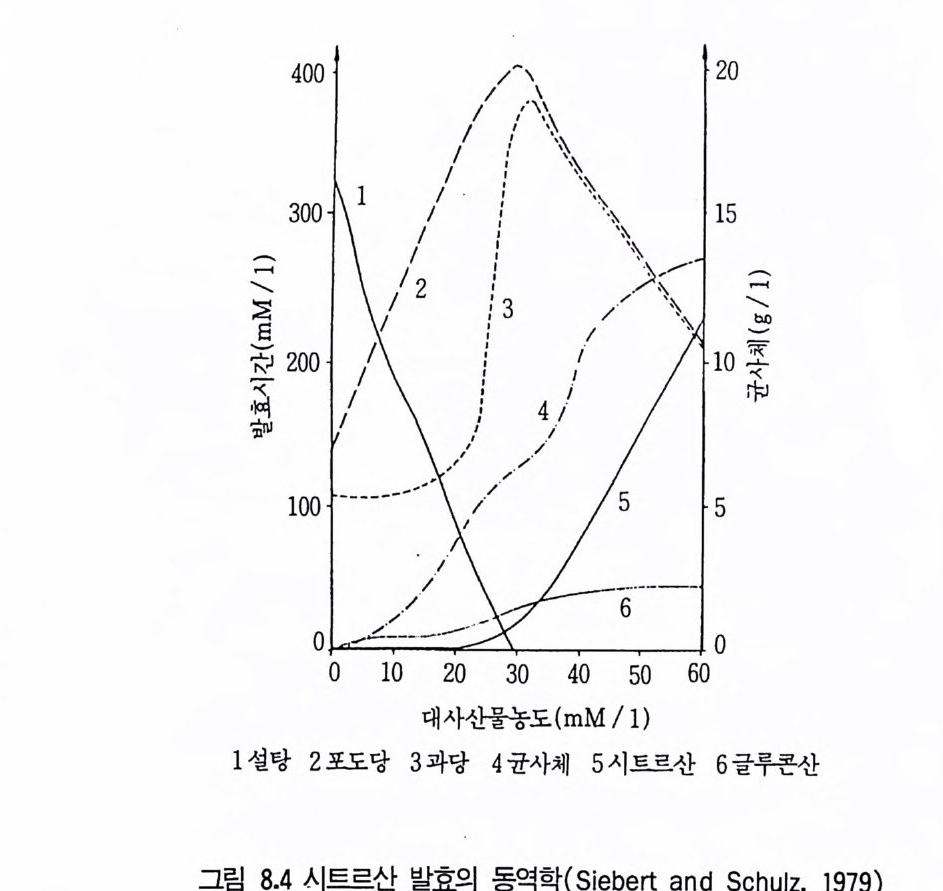 400 /// I /','~ ,’.\, \' ’,,\`\ ''\,, `3 ,/ 420 /
400 /// I /','~ ,’.\, \' ’,,\`\ ''\,, `3 ,/ 420 /
액체영양용액을 사용한 표면배양공정에서의 수율은 하루에 발효 표면적 m' 당 시트르산 수화물 (c itr i c acid monohy d rate ) 1. 2~ 1. 5k g이다. 발열 량은 생산된 시트르산당 12,500K J이다 . 회수 동안 균사와 영양용액은 용기에서 제거되는데 그 부피 때문에 주 의해서 세척해야 한다. 어떤 경우에는 세포의 시트르산 수율을 높이기 위 해 기계적 압착방법이 사용된다. (3) 액내배양공정 (submerge d pro cesses) 세계적인 시트르산의 공급의 80% 가 액내배양공정에 의해 생산된다. 액 내배양공정은 시간이 오래 걸리더라도 25% 의 전체 두자비가 낮고 노동력 비가 낮은 장점이 있다. 단점은 높은 에너지 비용과 고도로 숙련된 인력을 필요로 하는 복잡한 제어기술을 요구한다는 점이다. 액내배양공정에서의 생산에 중요한 세 가지 요소는 다음과 감다. ® 발효조를 만들기 위해 사용된 재료의 질, ® 균사구조, ® 산소공급이다 (Sodeck, 1981). 시트르산을 생산키 위한 발효조는 내산성이거나 스테인리스 스틸로 만 들어져야 한다. 1~ 일 k] 의 p H 값에서 철제 발효조 벽으로부터의 중금속 은 시트르산의 생성을 저해한다. 작은 발효조 (lOOl 까지 )에서는 스테인리 스 스틸 발효조는 표면/부피의 비율이 크기 때문에 풀라스틱 피막을 입혀 야 한다. 대형 발효조에서는 스테인리스 스틸울 사용한다면 피막의 입힘은 필요없다. 영양중식기 동안의 액내배양에서 형성된 균사체의 구조는 성공적인 생 산공정을 결정적으로 좌우하게 된다. 균사체가 풀어지고 제한된 가지와 클 라미도스포어 (chlam y dos p ore) 가 없는 사상체로 되면 고유상에서 시트르 산이 거의 생산되지 않는다. 최대생산율을 나타내는 균사체는 작은 과립체 룰 구성하는 것이다. 배지 중의 구리에 대한 철의 비율이 균사체 구조를 결정한다. Aspe rgi ll u~ 유전적으로 불안정하기 때문에 최소수의 전배양단 계만 허용되며 어떤 경우에 생산발효조는 직접 포자접종을 한다 . Aspe r gi llu s nig e rE 비교적 적은 산소요구성이지만 산소부족에 대해서는
민감하다. 전체 발효기간을 통해 포화치의 20~25% 최소산소농도가 요구 된다. 산소공급을 잠시라도 중단하면 생산이 줄어든다. 깊은 발효조에서의 통기속도는 산생성기간을 통해서 0.2~1 용량/부피 /분 (vvm) 이다. 낮은 점성도 때문에 교반이 필요없으므로 어떤 공장에서는 교반발효기가 사용되 기도 하지만 공기보급형(ai r- lift) 발효기가 채택될 수 있다. 시트르산 생산에 이용되는 대부분의 발효조는 120~220m' 의 크기로 만 들어진다. 액내배양 체제는 표면배양 체제보다 배지성분과 당밀구성 변화 에 있어서 덜 민감하므로 액내배양방식이 더 재현성 있게 가동될 수 있다. 액내배양발효에서는 거품이 생기는 문제가 있다. 발효조 부피의 G 크기 의 거품 소실이 공기보급(ai r-l ift)형과 교반 • 발효기 모두에 필요하다. 라 드유 같은 소포재를 일정 간격으로 첨가하고 기계적인 소포장치를 사용한 다. 아직까지 시트르산 생산에 연속발효를 달성시키지 못하고 있는데 과립 형성의 복잡성과 고유상에서의 조절 필요성은 다단계 방식의 발효에 의해 서만 충족될 수 있다. 그렇지만 미생물학적 문제나 살균에 대한 문제가 해 결된다 해도 경제적인 이유로 연속발효방식은 일반적으로 현실적이지 못하 다. (4) 알칸 -자화 미생물의 시트르산 생산 (c it r i c acid pro ducti on wi th alkane-uti lizin g mi cr oorga n is m s) 효모와 세균을 이용하며 C9~CZl 탄화수소에서 시트르산 생산의 여러 방법이 보고되고 있다. 우량 효모로서는 Candid a lip o ly tica 7} 있는데 회 분식 발효, 반연속 혹은 연속발효로 행해전다. 탄수화물발효와 비교해볼 때 수율은 탄화수소에서 더 높지만(1.4 5g 시트르산/g 파라핀) 일칸의 용 해성이 낮고 이소시트르산 생산량이 증가해서 나중에 시트르산에서 분리시 켜야 하는 어려움이 있다(표 8.5). 어떤 경우에는 이소시트르산의 비율이 시트르산 분량의 50% 를 차지한다. 그림 8. 얹근 회분식 발효와 반연속발효 에 의한 탄화수소로부터의 시트르산 생산울 나타내고 있다.
표 8.5 기질에 따른 시트르산과 이소시트르산 생산 기질 시트르산 g/ l 이소시트르산 g/ l 이소시트르산 g/ l Glyc e rol 125.5 11. 4 8.3 Glucose 89.4 7.0 7.3 n-Paraff in 92.0 49.0 34.8 (Treto n et al., 1978)
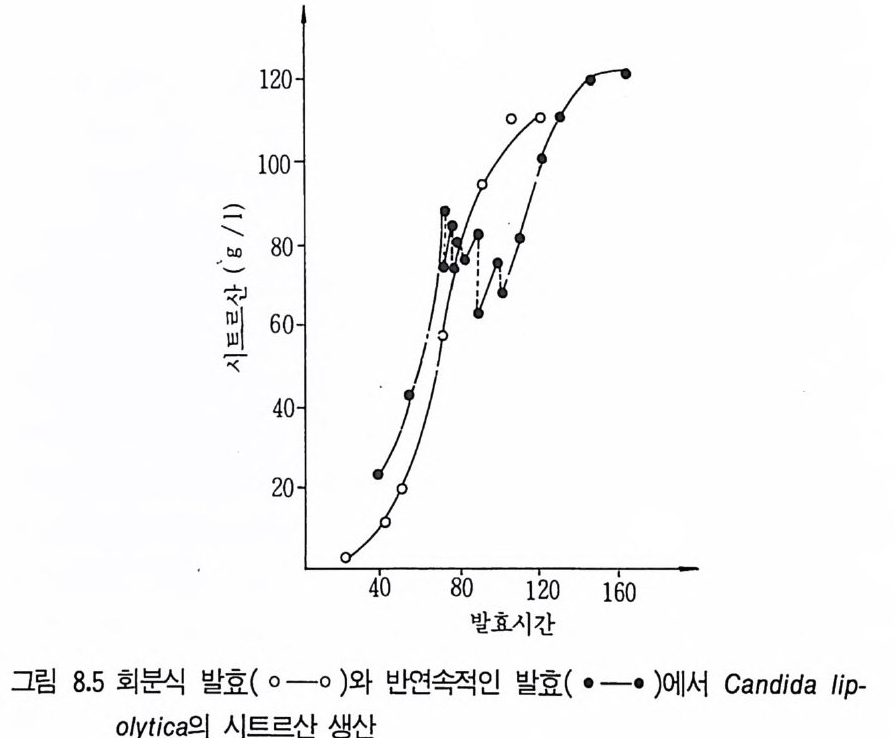 120
120
2.6 산물 회수공정 (pro duct recovery) 옥살산이 불충분한 발효조절에 의해 부산물로 생성되면 낮은 p H 에서 옥살산 칼슘 (calc i um oxala t e) 으로 침전시키고, 시트르산은 모노칼슘 (monocalc i um) 으로서 용액에 남게 된다. 그때 액체로부터 균사와 침전된
옥살산 칼슘 (cal ci um oxala t e) 을 분리하는 데 회전여과기나 원십분리기가 A 냄된다. pH 7.2 士 0. 22-} 70~90 ·C에서 시트르산은 침전되고 그것은 회전 여과기에 의해 분리시켜서 건조시킨다. 어떤 경우에는 시트르산에 황산을 첨가하여 용해시키고 황산칼슘 (calc i um sul fat e) 로 침전시켜 순수해전 것 울 사용한다. 연속적인 회수단계는 활성탄 처리, 양이온과 음이온의 교환 처리, 시트르산 혹은 시트르산 수화물(cit r i c aci d monoh y dra t e) 로의 결 정화과정을 거친다. 40°C 이상에서 시트르산은 무수물로, 그리고 36.5 °C 이하에서는 수화물 (monoh y dra t e) 로 결정화된다• 생산물의 순도는 사용되는 목적에 따라 다르다. 식품에 첨 가되는 시트르 산은 산업적 목적에 서용되는 것보다 더 순수해야 한다• 3 글루콘산(g lucon i c acid ) 글루콘산(g luco ni c ac i d) 은 금속, 피혁 및 식품공업에 사용된다. 글루콘 산나트륨 (so di um g lucona t e) 은 세제에서 분리제로 사용되며 &glu cono-lacto ne2 베이킹 파우더 첨가제로, 글루콘산 칼슘 (calc i ~m g lucona t e) 은 의약에 사용된다. 많은 미생물의 포도당 산화효소(g lucose ox i dase) 에 의 해 포도당으로부터 글루콘산이 생산되는데 (그림 8.6), 이때 FADH 제서
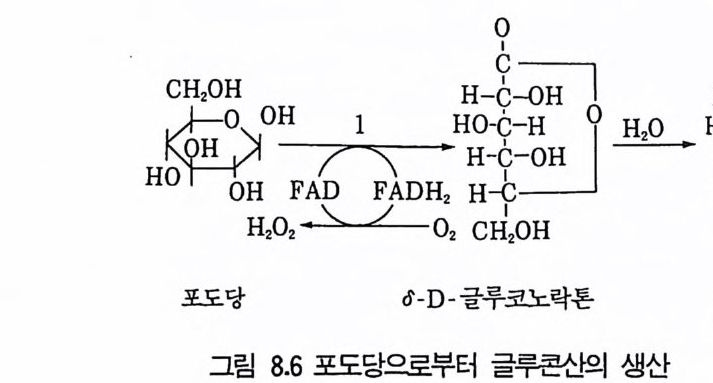 HCH:2 0HHo 0 H二 l H HHOH- 二-:cC 교-H」 口° 一H2 0 HH麟OC- 心0¢0 --갈 OH H H
HCH:2 0HHo 0 H二 l H HHOH- 二-:cC 교-H」 口° 一H2 0 HH麟OC- 心0¢0 --갈 OH H H
수소가 산소로 전달되면서 과산화수소 (H 2 0 2 ) 가 생성되고 이어서 cata l ase 에 의해 물로분해된다. 18801 ;1 Bou t roux 는 Ace t obac t e r:가 포도당으로부터 글루콘산을 생성하 는 것을 발견하였고 1911 년에 Alsber g는 Pseudomona 려 글루콘산의 생 산개 대 해 언급했고, Penic i ll i u m lu t eum - p u rp uro g enum 을 사용한 표면배 양공정에 의한 생산이 192~ 에 시작되었다. 이 공정에서의 수율은 이론값 의 80~87% 였다. 오늘날은 Asp e rgi llu s n ig e 려· 세균 Aceto b acte r suboxy da ns-을 사용한 액내배양공정만이 채택되고 있으며 이 방법으로 글루콘산, 글루콘산염, 그 리고 포도당 산화효소(g lucose ox i dase) 가 제조되고 있다. 글루콘산 생산 조건은 잘 연구되어 있는데도 상업적으로 쓰여지지 않는 미생물에는 Pen- icil l u m, Scop u lariop s i s , Gona tob otr ys, Endom y cop s i의 Pullularia 등의 진균류와 세균 Vi br i o 및 Pseudomona 이} 있다. 고정화 세포나 고정화 포도당 산화효소(g lucose ox i dase) 의 방법도 검 토되고 있다. 고수율을 얻기 위한 미생물학적 방법과 화학적인 방법이 경 쟁적인 위치에 있다. 생산방법 : 이 발효에서 결정적인 변수는 포도당의 양과 산소의 공급이 다. 글루콘산 칼슘을 생산할 때 글루콘산 칼슘의 용해성이 낮기 때문에 기 질로서 13~15% 이상의 포도당을 첨가해서는 안 된다 (30°c 에서 4g /l). 기질농도가 높으면 높은 수준으로 글루콘산 칼슘을 만들기 때문에 자연히 결정화되어 정제를 어렵게 한다. 붕선영을 첨가함으로써 침전의 생성을 억 제할 수 있고 고농도발효가 가능하게 된다. 글루콘산 나트륨(용해성 396 9 I Q )의 생산에서는 28~30% 정도 높은 포도당농도를 사용할 수 있다. 발효는 높은 통기율 (1~ l. 5vvm) 로 28~30°c 에서 3 6]간 전행한다. 용 기내의 압력이 울라감에 따라 산소의 용해도와 글루콘산 생산량이 증가한 다(표 8.6). 오늘날 상업적 수율은 90~95% 에 달한다.
표 8.6 굴루콘산 생산과 압력과의 상관관계 압력 (bar) 중량당 수율 1 42.5 3 80.4 4 82.4 5 81. 3 6 86.l (May et al., 1934)
4 아세트산 (aceti c acid ) 발효 아세트산 발효는 오랜 세월 동안 알코올 함유액을 자연정지배양으로 행 하여졌는대 187 興 Hansen은 아세트산 발효의 미생물로서 아세트산균을 처음 분리하였다. 청량음료로 희석된 식초를 사용한 로마안이나 그리스인 둘은 포도주를 공기 중에 방치함으로써 식초를 생산했었다 . 식초는 중세까 지는 단지 지역적인 소비용으로 생산되었는데 처음 공업적으로 제조된 식 초는 납작한 통에서 생산되었다. 이 과정은 진행이 느리고 세균의 막이 포 도주의 표면에 퍼지곤 했다. l 양1 ] 기에 좀더 신속한 표면배양발효가 개발되 었다. 그중의 하나가 tri c k lin g gen erato r 공정으로 오늘날까지 사용되고 있다. 194 91;1에 시작된 액내배양공정이 개발되어 tri c k li ng g enera t or 와 액내배양 발효기 양쪽 모두가 세계적으로 사용되고 있는데 좋은 향기 때 문에 오래된 방법이지만 아직까지 사용되고 있다. 액내배양방법은 독일의 H. Fr i n g s 회사에 의해 급속도로 향상되었다. 아세트산은 여러 발효세균에 의해 생산되지만 특별한 종류인 아세트산 세균군만이 상업적으로 이용되고 있다• 아세트산 세균은 두 속 Glu- conobac t er와 Ace t obac t e r.로 나누거지는데 첫번째 군은 에탄올을 아세트산 으로만 산화시키며 두번째 군은 에탄을을 아세트산으로 산화시킨 후 다시 COi2 } H20 가 되도록 산화시킨다. Aceto b acte r4 r-균 은 그람음성균, 내산성
이고 주모성 편모를 가진다(또는 비운동성이다). 산업적 균 주 로는 Ace- tob acte r aceti , A. pa st e u ria n u. s 또는 A. pe roxid a ns 등기다 . Glu- conobac t e 속 균주는 괴산화성 세균은 아니며 옥모성 편모를 갖거나 (3~8 옥모성 편모) 혹은 비운동성이다. Gluconobacte r ox y dans( 형식적으로 Aceto m onas ox y dans) 와 여러 아종기 상업적으로 사용되고 있다 . 접종시 순수하더라도 특히 표면배양공정에서는 오염에 의한 혼합배양이 나타난다 . A. xyl i n u~ 과량의 점액을 형성하기 때문에 사용할 수 없지만 수백 종 에 달하는 Ace t obac t e 라 Gluconobac t e f.가 생산에 사용되고 있다. 4.1 아세트산 생합성 아세트산 생산은 진정한 발효라기보다는 불완전한 산화과정이다. 왜냐하 면 생산된 환원력이 산소로 전달되기 때문이다. 에탄올로부터의 첫번째 산 화단계에서는 NAD- 나 NADP- 의존성 알코올 탈수소효소 (alcohol de- h ydro g enase) 에 의해 아세트알데히드 (ace t aldeh y de) 로 전환되고 그때 아세트알데히드 수화물 (ace t aldeh y de h y dra t e) 로 수화된다. 두번째 산화 에서는 아세트알데히드 탈수소효소 (ace t aldeh y de deh y dro g enase) 에 의 해 아세트산이 된다(그림 8.7).
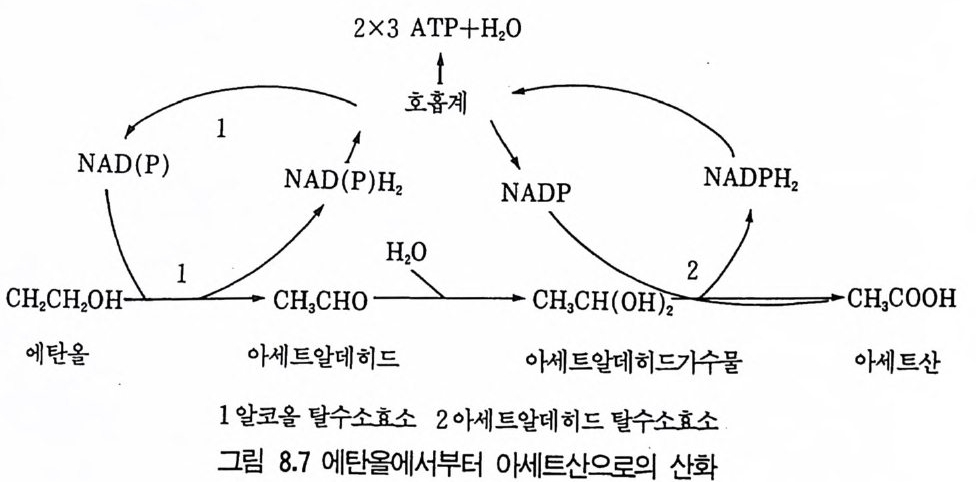 2X 3 ATP+H2 0
2X 3 ATP+H2 0
산화과정에서 에탄올 lM 에서 아세트산 1M 이 생산된다• 12%(v/v) 알코올 1l에 서 12.4 % (w/v) 아세트산 U가 생산된다. 최적생산에는 충분한 산소가 요구되며 그것은 호흡사슬을 통해 환원된 다. 생산된 아세트산은 lM 당 6ATP7} 생산된다. 충분한 산소가 공급될 수 없을 때 높은 아세트산과 에탄을의 농도에서 세포는 죽게 된다. 즉 에 탄을을 첨가한 5% 아세트산의 농도에서 (2 분 통기를 중단한 후에) 세균의 34% 는 죽는 반면 에탄을을 첨가한 12% 아세트산의 전체 농도에서는 단 10~20 it: 후에 같은 앙이 죽게 된다. Ace t obac t e 려 최적성장에는 아세트산과 에탄을이 모두 있어야 한다. 에 탄올의 공급은 필수적이며 용액에 0.2%(v/v) 보다 낮을 때 치사율은 증 가한다. 그렇지만 최대에탄올의 함량은 보통 공정에서 5% 를 초과할 수 없 다. 오늘갈 고수율의 균주는 13~14% 의 아세트산을 생산한다. 4.2 식초 생산 (Greensh i elds, 1978) 포도주, 유장, 맥아, 사이다 같은 알코올 농도가 낮은 시발물질은 완전한 영양용액의 조제에 추가적인 성분을 필요로- 하지 않는다. 그렇지만 감자 알코올, 에틸 알코올이 사용될 때는 최적생산을 얻기 위해 영양성분이 첨 가되어야 한다(표 8.7). 액내발효에서 영양성분의 농도는 생체량의 증가
표 8.7 아세트산 발효의 첨가물 Gram/m3 영양臼 표면배양공정 액내배양공정 곡물 가수분해물로부터의 당 용액 200 1000 Ammon ium pho sph ate 96 480 Magn e siu m sul fat e 24 120 Calciu m cit ra te 24 120 Calciu m pan to t h e nate 0.24 1.2
때문에 5 배가 높아야 한다. 종균접종은 순수배양하거나 회분발효조에서 나 온식초로할수있다 . 표면공정 침수공정의 결과 대신에 아직까지 tri c k lin g g enera t or 가 식 초 생산에 널리 사용된다(그립 8.8) . (1) 표면배양공정 (surfa c e pro cesses) 식초 생산에서 액내배양방식의 성공에도 불구하고 tri c k lin g gen erato r 는 특히 가정용 식초를 만드는 데에 아직까지 널리 사용되고 있다(그립 8. 8). 목재 생체반응기 (b i oreac t or) 는 최대부피가 60m' 인 것이 있고 너도밤 나무의 목재 대팻밥으로 채워진다. 원료물질은 표면에 분무하면 아세트산 균을 포함하고 있는 대팻밥을 통해 바닥에 있는 용기로 뚝뚝 떨어지게 되 는데 그곳에서 부분적으로 전환된 용액은 냉각하며 위로 울려 재순환시킨 다.
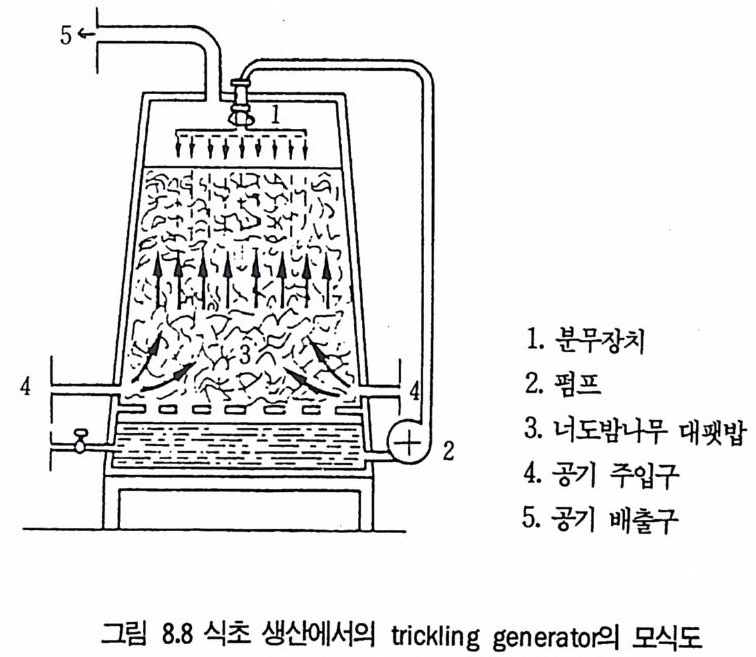 1. 분무장치
1. 분무장치
첨가된 알코올의 88~9r f/o7 Ht ri c k li ng gen erato r 공정에서 ) 아세트산 으로 전환된다. 나머지 알코올은 일차대사에 쓰여지거나 폐기공기로 빠져 나간다. 발효조 윗부분의 온도는 29 °C 이고 아랫부분은 35°C 이다. 이 과정 에서 12% 아세트산 생산에 필요한 시간은 약 3 일 걸린다. (2) 액내배양공정 (submerge d ·pr o cesses) 전체적으로 알코올 농도가 낮은 과일주와 같은 담금액이 액내배양공정 에 사용되었는데 그런 저수율공정에서 통기는 결정적 요인이 아니지만 오 늘날의 50m' 용량으로 13% 아세트산을 생산하는 고수율공정에서는 통기 가 엄격하게 조절되어야 한다. 그림 8. 伊] 발효조는 디른 생물반응기와 비
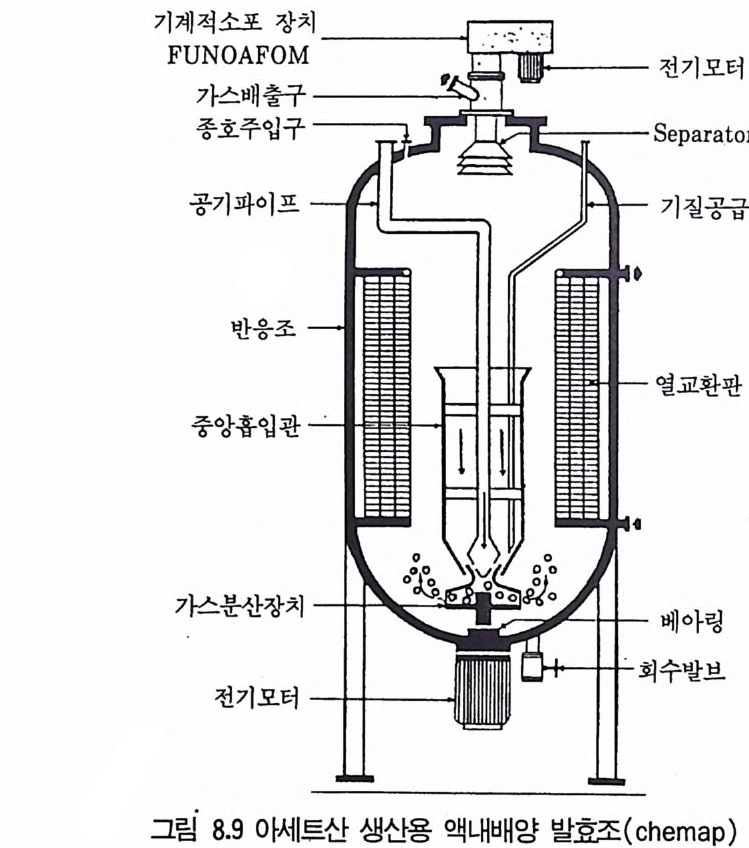 기계적소포 장치
기계적소포 장치
슷한데 스데인리스 스틸제로서 바닥에서 교반된다. 통기장치는 발효조의 윗부분에 있는 파이프를 통해 아래쪽으로 들어가는 공기흡입 회전자로 만 울가져 있댜 열교환기는 온도를 조절하며 대개 기계적 소포장치가 설치되 어야 한다. 발효조건은 디음과 같다. 발효온도 3o·c 통기속도 3~4wh 회전속도 1,500 rpm 압력 0 오늘날 13% 아세트산의 가정용 식초는 반연속적이며 완전자동공정으로 생산되고 있다. 35A] 간마다 영양용액의 50~60% 가 새로운 딤금액으로 치 환된다• 4o ·c 에서 98% 의 수율을 울리는 완전연속적 공정이 개발되고 있 다. 액내배양공정은 m' 당 생산속도(p roduc ti on ra t e) 가 표면배양공정보다 l 떼 높으며 tri c k lin g gen erato r 공정보다도 약 5% 가 높다. 다른 장점 은 생산량당 두자비용이 낮고 공장부지에서 20% 만이 설비에 요구되며 단 시간에 다른 담금액으로 치환할 수 있는 능력과 완전자동조철로 인전비가 낮은것이다. (3) 회수 (recover y) 액내배양공정에서 얻은 아세트산은 세균의 혼탁 때문에 여과해야 한다. 터과와 여과조제가 일반적으로 사용되고 있으며 최종산물의 탈색시에는 K i Fe(CN)s) 을 이용할 수 있다. 5 젖산발효(l ac ti c aci d) 유기산 중에서 미생물학적으로 처음 생산된 것은 젖산으로서 188 ()1;1이
었다. 오늘날 젖산 생산의 화학적인 방법은 생물학적 공정과 같은 비용이 들어서 매우 경쟁적이다. 젖산세균은 한 분자의 포도당으로부터 두 분자의 젖산을 생성하는 호모 (Homo) 형 발효균과 한 분자의 포도당으로부터 한 분자의 젖산과 한 분자의 에탄올 및 한 분자의 co 遷- 생성하거나 젖산과 아세트산, 만니톨 (mann it o l) 등을 생성하는 헤데로 (He t ero) 형 젖산발효 균이 있다. 따라서 Leuconosto c mesentr o id e~ 같은 헤 테로형 젖산균은 산업적 목적에는 적당하지 않다. 포도당에서 젖산으로의 생합성은 gly c e raldehy de -3-ph osp h ate , 1,3-d i- P -g l y cera t러 피루브산을 통해 진행된다. 글리세르알데히드 포스페이트 (gly c e raldehy de p hosp ha t e) 가 산화될 때 생성되는 환원력은 NAD 의 존성, 젖산 탈수소효소(l ac t a t e deh ydro g enase) 에 의해 피루브산으로 전 달되며 입체, 이성질체적으로 L(+ )나 D( 一) 젖산으로- 환원된다(그림 8. 10).
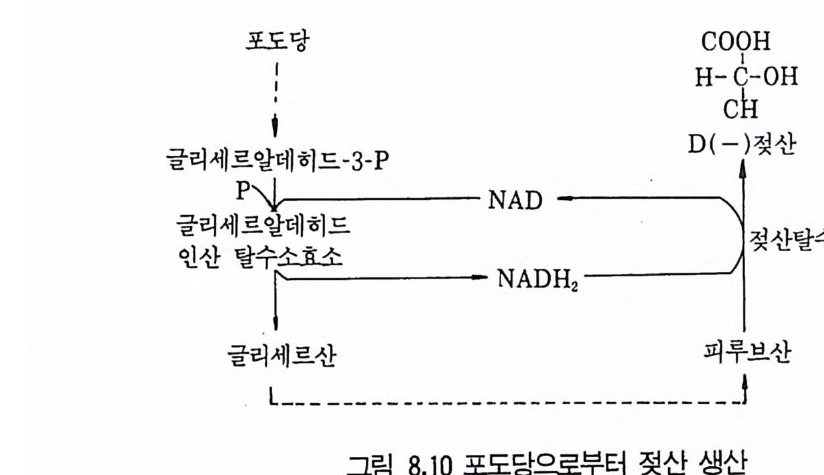 포도당 COOH COOH
포도당 COOH COOH
포도당으로 생산할 때 이론적 수율의 90% 이상이 확실하게 실질적으로 생산된다. 사용 미생물은 기질로 포도당을 생산할 때 Lacto b acil lu s ·de lbrueckii , 유장을 사용할 때 Lacto b acil lu s bulga r ic u s, 아황산 폐액을 사용할 때는
Lacto b acil lu s pen to s us7} 이용된다. 이들 미생물은 절대적인 형기성이기보 다는 통성형기성이므로 발효조를 완전히 무산소상태에서 진행시킬 필요는 없다. 그렇지만 소량의 산소가 있으면 과산화수소가 생성된다. 발효배지는 12~13% 포도당과 (NH4) 2 HPO i 0.25%) 를 첨가하고 비타 민 B 를 포함해야 한다. 젖산발효는 목재나 스테인리스로 만든 25~120m' 발효조에서 교반하면서 6.3~6. 話~ pH 7} 조절되면 포도당은 7 언 l 간내에 젖산으로 전환된다. 젖산은 미생물학적 인 과정을 통해 20,00() 0:j 톤이 넘게 매년 생산된다. L(+ )젖산만이 상업적으로 생산된다. 젖산은 청량음료나 방부제로서 식품에 널리 사용되고 그 밖에 피혁가공에서의 탈회, 직물의 세탁에도 쓰이며 폴리아크릴산, 에스터 합성원료로 사용된다. 6 코지산 (ko ji c acid ) 190 연 Sait o7 } 쌀 Koji 추출객에서 염화철로 보라색을 나타내는 결정 울 얻어 1924 년에 결정화한 유기산이다. 코지산 (5-h y drox y - 2-h ydrox y me t h y l -4-py rone) 은 플라스틱 산업에서 기본재료로 상업적으로 소량 사용되고 살균제, 방미제의 원료로도 약간 사 용되고 있다. 오랫동안 포도당의 직접발효에 의해 생산되었다. Aspe r gi llu s fl auu 라 A.ory za eol] 의해 포도당에서 70~90% 의 수울기 얻어진다(그림 8.11). 이 산은 또한 피루브산, 글리세롤, 아세트산이나 에탄올에서도 생산
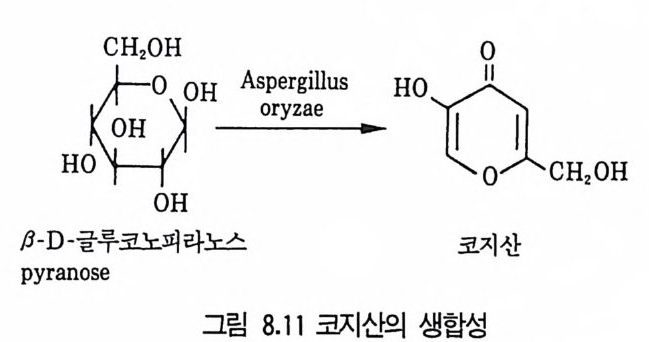 o110°
o110°
할 수 있다. 포도당을 사용한 공정은 시트르산과 이타콘산(it acon i c acid ) 공정과 매우 비슷하다. 어떤 균주에서는 교반이나 통기와 같은 발효변수를 바꿈에 따라 시트르산이나 이타콘산의 생산으로부터 koji c ac i d 의 생산으 로전환되기도한다. 7 이타콘산(it acon i c acid ) 발효 1929\ 1 K i nos hit a 는 매실식초에서 분리한 Aspe rgi llu s itac onic u s7} 자 당배지에서 이타콘산을 대사산물로 생성함을 밝혔다. 이어서 곧 Rais tr i c k 도 A. terr eus 균주가 또한 이타콘산을 분비한다는 것을 발견했다. 두 균 주의 돌연변이주는 오늘날 산업적인 생산에 사용되고 있다. 현재 서유럽에서 두 곳, 미국, 소련과 일본 각각 한 곳에서 이타콘산을
 HO -C H-CCOH
HO -C H-CCOH
생산하는 산업적인 업체가 있다. 이티콘산은 폴리에 스 터 수지의 원료로서 중요하고, 이타콘산의 디에스터 중합에 의하거나 이타콘산과 글리콜류의 에스터의 혼합물은 스티렌 등과 공중합하여 우수한 풀라스틱이나 수지가 제조된다 . 따라서 이들 에스터 및 다량체는 제지산업의 접착제로 사용되며 또한 이티콘산과 고분자 알코올의 디에스터는 염화비닐수지의 가소제로 쓰 이기도한다. 이타콘산은 TCA 회로의 경로를 거쳐 탈탄산울 통해 시스이코니트산 (cis- a c onit ic a ci d) 으로부터 생산된다. 시스이코니트산 탈탄산효소 (c i s acon itic aci d decarbox y lase) 는 정제되었고 특징이 밝혀져 있다. 다른 생성합성 경로, 즉 시트라말산 (c it rarnal i c aci d) , 시트라코닌산(cit raconic ac i d) 과 이타탈탄산(it a t ar t ar i c ac i d) 을 통해 피루브산에서도 또한 이타콘산이 생성된다. 불 필 요한 부산물인 숙신산 (succ i n i c ac i d) 과 이타타르타르산(it a t ar t a ric ac i d) 이 이타콘산에서 생산된다(그림 8.1 3 ). 칼슘은 이타콘산울 억제 하므로 칼슘의 첨가는 이터콘산 생산수율을 증가시킨다.
 CcHII —2 CO OH 이타콘산산화효소 HO— CHC|I2 0— H COO H
CcHII —2 CO OH 이타콘산산화효소 HO— CHC|I2 0— H COO H
A: ter reus- 2 현재 회분식 액내배양공정에서만 쓰여진다. 15% 자당용액 에서 이타콘산으로의 전환은 이론적 수율의 78% 에 도달할 수 있다•
참고문헌 Allen, S.H.G., R.W . Kellermey er , R.L. Stj er nholm, and H.G. Wood, 1964. Purif ica ti on and pro p e rti es of enzy m es inv olved in the pro - pion ic acid fer menta t i on . J. Bacte r ia l . 87 : 171~187. Alsberg, C.L. 1911 . The for mati on of D-gl u conic acid by Bacte r iu m savasta n oi( S ch mith) . J. Bio l . chem. 9 : 1~7. Furukawa, T., T. Nakahara, and K. Yamada, 1970a. St ud ie s on the uti lisa ti on of hy d rocarbons by micr oorga n ism s. XIX. In flue nce of several fac to r s on fum aric acid pro ducti on from n-pa raff in by Can- did a hyd rocarbofu m aric a . Ag r. Bio l . Chem. 34 : 1402~ 1406. Furukawa, T., T. Nakahara, and K. Yamada. 1970b. St ud ie s on the uti lisa ti on of hy d roc~rbons by micr oorga nis m s. XX. Conversio n of fum aric acid to 1-malic acid by the associa t i on of tw o kin d s of yea sts . Agr. Bi ol . Chem. 34 : 1833~838. Gledh ill, W.E ., I.D . Hi ll. and P.H. Hodson. 1973. Ci tra te pro ducti on from hy d rocarbons by use of a nonste r ile , sem ico nti nu ous cell rec- ycl e sys t e m . Bio t e c hnol. Bio e ng . 15 : 963~972. GreReonsseh, ieAl d.sH, .(Red.N.) ., E19c7o8n.o mi Ac cmetii c cro baico il do g y :, Vvio nle. g a1 r. , Pprpim. a1ry2 1p~r1o 8d6u.c tsI n o f: meta b olis m . Academi c Press, London. Kheshg i, S., H.R. Roberts , and W. Bucek. 1954. St ud ie s on the pro -ducti on of 5-keto g l u con ic acid by Aceto b acte r suboxy d ans. Ap pl. Mi cr obio l . 2 : 183~ 190. May, O.E ., H.T. Herric k , A.J. Moy er , and P.A .W ells. 1934. Gluconic acid pro ducti on by submerge d mould gro wt hs under inc reased air pre ssure. Ind.E n g. Chem. 26 : 575~578. Mi se nheim er, T.J., R.F. Anderson, A.A. Lago d a, and D.D. Ty le r. 1965. Producti on of 2-keto g l u con ic acid by Serrati a· marcescens. Ap pl. Mi cr obia l . 13 : 393~396. Rhodes, R.A ., A.J. Moy er , M.L. Schm ith, and S.E. Kelley. 1959. Pro-ducti on of fum ari c aci d by Rh izo p u s arrhi zu s. Ap pl. Mi cr obia l 7 : 74~80.
Rhodes, RA., A.A. Lag o da, T.J. Mi se nheim er, M.L. Schmi th, RF. Anderson, and RW. Jac kson. 1962. Produc tion of fum aric acid in 20-lit er -fe rm ente r s. Ap pl. Mi cr obio l . 10 : 9~ 15. Ri vi e r e, J.( ed.). 1977. Industr ia l app li c a ti on s of mi cr obio lo g y. Surrey Un ive rsit y Press, London. Rose, A.H. 1978. Producti on and ind ustr i a l im p o rta n ce of pr im ary pro ducts of mi cr obia l meta b olis m , pp. 1~30. In : Rose, A.H. (e d.), Prim ary pro ducts of meta b olism . Academ ic Press, New York. Sato , M., T. Nakahara, and Y. Mi no da. 1977. L-m alic acid pro -ducti on from n-pa raff ins by Candid a brump tii IFO- -07 31 . Ag r. Bia l . Chem. 41 : 967~973. Schulz, G. and H. Rauch, 1975. Ci tron ensaure( Cit ric aci d) , pp. 626~ 636. In : Ullmanns Encyk lop a die der tec hnis c hen Chemi e., vol. 9. Schweig e r, L.B. 196 1. Producti on of cit ric acid by ferm enta tion . U.S. Pat- ent 2,970,084. Sh ina g aw a, E., T. Chiy o nobu, 0. Adachi, and M. Amey a ma. 1976. Dist r i b u ti on and solubil i z a ti on of pa rti cu late glu conate dehy d ro- gen ase and pa rti cu late 2-keto g l u conate dehy d roge n ase in aceti c acid bact er ia . Ag r. Bi ol . chem. 40 : 475~483. Sodeck, G., J. Modi, J. Kom ine k, and W. Salzbrunn. 1981 . Pro-ducti on of cit ric acid accordin g to the submerge d fer menta t i on pro cess. Proc. Bio c hem. 16 : 9~11. Sie b ert, D. and G. Schulz, 1979. Ci tric acid pro ducti on by fer men- tat i on . Inte r n. Mi cr obio l . Food Ind. Cong r. , Paris . Szczodark, J. 1981 . Bi os y nthe sis of citri c acid in relati on to the ac- tivi t y of selecte d enzym e s of the Krebs cyc l e in Aspe rgi llu s nig e r my ce li um . Europ . J. Ap pl. M i cr obio l . Bio t e c hnol. 13 : 107~112. Treto n , B., M.-T. Le Dall, and H. Heslot. 1979. Excreti on of cit ric and iso cit ric acid s by the yea st Saccharomy co p si s lipo lyt ica . Eur-
op. J. Ap pl. Mi cr obio l . Bi ot e c hnol. 6 : 67~77.제 9 장 아미노산 (am i no acid ) 발효 1 서론 아미노산은 단백질을 구성하는 기본 화합물로서 동물이 필요로. 하는 영 양학적으로 매우 중요한 물질이다. 190 婦 일본에서는 Ikeda 에 의해 미역의 맛성분이 글루탐산이라는 것이 밝혀졌고 그 후 바로 밀의 글루텐과 콩단백질의 산 가수분해 산물에서 글 루탐산 나트뮴 (sod i um g lu t ama t e) 을 상업적으로 생산하게 되었다. 1957 년에는 Cory n ebacte r iu m g lu t am i cu 짜니 배°뇽버 에서 L 글루탐산 (L -g lu tam i c ac i d) 이 산물로서 발견되었고 그 후 이 균주는 글루탐산 나트뮴 (sod ium g lu t ama t e) 의 중요 생산원이 되었다. 이러한 개발은 일본의 발 효산업을 크게 자국하게 되었고 누쿨레오티드뿐 아니라 아미노산 생산의 발효공정은 일본이 거의 독점하여 개발하게 되었다. 17 개의 중요한 공장 중 1 양 n 가 동남아시아(일본, 한국, 대만)에 있는데 대표적 인 일본의 회사로서는 Aji no moto Co., Ky ow a Hakko Kog yo Co 가 있고 한국의 대표적 생산회사로서는 미원(주)와 제일제당을 들 수 있다. 구미지역에서의 글루탐산염 생산업체로서는 Sta u ff er 화학회사와 Orsan S. A 가 있다. L- 리신 (L-l y s i ne) 의 잘 알려진 제조회사는 Eur- olys i n e Co. (프랑스)이고, L 이스파르산 (L-as p ar ti c a ci d) 의 제조회사로 서는 두 개의 프랑스 회사인 Orsan S. A. 와 Phone Poulen S. A.를 들
수있다. -1 981 년에는 세계의 생화학적 아미노산의 생산량은 3&1 J- 향J 톤이었고 그중 3 책 돈이 글루탐산 나트륨 (sod i um g lu t ama t e) 이고 4 만 톤은 L- 리신 (L-l y s i ne) 이었다. 198 ()1;j도의 거래액은 17 억 달러로 추정된다. 지금 까지 경제적으로 생산되지 못했던 아미노산의 생산이 유전공학적안 방법으 로 개발된다면 198 ()1;jtl1말에는 50% 의 증가가 기대되고 있다. 2 아미노산의 용도 아미노산 발효의 궁극적 목적은 인류 식량의 단백질 공급의 절대량을 증가시키는 데 기여하는 것이다 .' 물론 개개의 아미노산은 각각 독자적인 가치가 있어 각기 다른 의의를 가질 수도 있다. 아미노산은 식품공업에서는 식품첨가물로서 의약품에서 그리고 화학공업 의 원료물질로 폭넓게 이용되고 있다. 식품공업에서는 아미노산이 맛을 증 가시키기 위해 사용된다. 글루탐산 나트륨 (sod i um g lu t ama t e) 의 중미효 과에 대해서는 이미 언급한 바 있는데 아스파탐 나트뮴 (sod i um asp - ar t a t e) 과 DL -알 라닌 (DL-alan i ne) 도 감칠맛을 내기 위해 과일 주스에 첨가하고, 글리신(g l y s i ne) 은 감미료 첨가식품에 넣어주기도 한다. L 시스 테인 (L -cy s t e i n) 은 빵을 굽는 동안에 빵의 질을 증가시키고 과일 주스에 는 항산화제 (an ti o xi dan t)로서 작용한다. L - 히스티딘 (L-h i s ti d i ne) 과 결 합된 L 트립토판 (L- t r ypt o p han) 은 항산화제로 이용되고 분말우유가 상하 는 것을 방지하여준다. L 페닐알라닌 (L- p hen y lala ni ne) 과 아스파르트산 (L-asp a rti c ac i d) 의 에스데르 (es t er) 화합물인 아스파탐 (As p ar t ame) 은 음료수에 저칼로리 감미료로 사용된다. 배합사료는 콩단백질 이의에 필수 아미노산 중 특히 L- 리신 (L-l y s i ne) 이 부족하여 트립토판(t r ypt o p han) 과 함께 첨가의 주요성이 강조되고 있다. 식물성 단백질은 · 주로 L-리 신 (L-l y s i ne), L 페티오닌 (L-me t h i o ni ne),
L-트 레오닌 (L-t hreon i ne), L-트 립토판 (L- tr ypt o phan) 과 같은 필수아미 노산이 부족하다. 표 9 .1은 몇 가지 식료품과 사료의 리신 (L y s i ne) 함량 표이다. 일본에서는 리신을 빵에 첨가하고 디른 나러에서는 메티오닌 (me t h i on i ne) 을 콩식품에 넣어서 맛을 증가시키고 있다. L- 리신 (L-l y s i ne) 과 DL 페티오닌 (DL-me thi on i ne) 은 사료의 질을 향상시키기 위해 사용되고 L-트 레오닌 (L- t hreon i ne) 과 L-트 립토판 (L- tr ypt o p han) 을 음 식에 첨가하는 방법이 개발중이다. 제양 1] 계에서의 식량부족의 관점에서 볼 때 필수아미노산을 함유한 식물성 단백질에 대한 필요성이 계속 증가하는 추세이다. 의약품계에서는 아미노산울 수술 후의 치료제에 이용하고 있다.
표 9.1 식료품과 사료의 L- 리신 함량 Food/fe e d Lys i n e Food/fe e d Ly si n e conte n t( % ) conte n t( %) Corn 0.21 Soy meal 2.90 Oats 0.50 Dry yea st 3.4 0 Barley 0.4 0 Skim mi lk pow der 2:so Wheat 0.60 Meat- m e al 2.60
화학공겁에서는 아미노산이 풀리알라닌(p ol y ala ni ne) 섬유와 리신 아이 소시아네이트(ly s i ne iso cy a nate ) , 수지 같은 중합체의 대량 생산용 원료 물질로 이용되며 p ol y -r-me t h y l g lu t ama tei'근 합성피혁제조에서 표면처리 에 사용된다. 그리고 몇 가지 아미노산의 N 이실 (N-ac y l) 화 아미노산은 화장품의 제조에 이용되고 있으며 계면활성물질로서도 이용되는데 독성, 자극성이 낮아 좋은 첨가제가 된다. 3 생산방법 ( Hir o se et . al. , •1 979, Nakay am a, 1979) 발효공정은 글리신(g l yci ne), L 시스테인 (L-<: y st e i ne) 과 L 시스틴 (L
c y s ti ne) 을 제의한 모든 아미노산에서 개발되었지만 모두가 상업적으로 채용되고 있는 것은 아니다. 아미노산의 상업적인 제조에는 세 가지의 경 쟁적 방법이 있다. 1. 단백질의 가수분해물에서 아미노산을 추출하는 방법. 이 방법은 L 시 스 테 인 (L -cy s t e i ne), L- 티로신 (L- ty ros i ne) 생산에 사용된다. 2. 화학적 합성방법. 글리신(g l y c i ne), DL-알 라닌 (DL - alan i ne), DL 페티오 닌 ( DL-me t h i on i ne) 과 DL-트 립토판( DL-t r y p top h an) 등. 3. 미생물을 이용하는 방법. 미생물학적 생산방법에는 세 가지 접근법이 있다. 첫째는 포도당, 과당, 당밀, 전분가수분해물, n-알 칸 (n-alkanes), 에탄올, 글리세롤(g l y cero l), 아 세데이트, 프로피오네이트(p ro pi ona t e) 와 같은 다양한 탄소원을 사용하여 아미노산을 직접 발효하는 방법이다. 원료물질로 메탄을을- · 사용한 발효는 기질값이 저렴하기 때문에 광범위하게 연구되고 있지만 생산수율이 낮아 상업적으로 아직 채용되고 있지 않다. 두번째 접근방법은 생합성 과정을 통해서 값싼 중간산물을 전환하는 것 이다. 글리신(g l y c i ne) 을 예로 들자면 Cory n ebacte r iu m g ly c i nop h i lum 을 이용하여 L 세린 (L -s er i ne) 으로 전환할 수 있다 (16 g/l). 세번째 접근방법은 효소나 고정화 세포를 사용하여 L- 알라닌, L ..0比적파 르트산, L-DOPA(dih y d roxy ph eny la n ine ), L -트 립토판과 L-티 로신을 생 산하는것이다. 유전공학적 방법 (ge neti ca lly eng ine ered s t ra i ns) 으로 육종된 균주를 이용하는 접근방법이 점차 증가하고 있는데 다음과 같은 아미노산 생산에 대장균을 이용한 유전자 글로닝법이 개발되고 있다. 즉 L-글 루탐산, L- 리 신, L 페닐알라닌, L-트 레오닌, L-발 린, L-히 스티딘, L 세린, L 이르기닌, L 페티오닌, L-트 립토판, L-프 롤린 등이다. 아미노산 우량 생성균주 (Cor yne bacte r iu m g lu t am i cum) 를 이용하여 상업적 재조합 DNA 방법에서 숙주
로서 대장균을 대치할 만한 클로닝 체계가 연구중이다 (A i da et al., 1986). L-리 신은 현재 효소법에 의해서도 대량 생산되고 있다. 시클로산 (C y cl ohexane) 이 비교적 염가인 것을 이용하여 a-am i no-s-<:a p rolac t am 을 경 유해서 리신의 합성효소 병용법이 개발되었다. 이때 생성하는 D-ami no ca p rola ct am 을 라세미화하는 효소생성균으로서는 Achromobacte r aba 례검 또 L-am ino ca p rolac t a m-을 L- 리신으로 가수분해하는 효소생성균으로서 Cry ptoc occus lauren ti카 있어 이들 두 균을 동시에 작용시키면 DL-am i- noca p rolac t am 에서 100% 가까운 수율로서 L- 리신을 생산할 수 있다 (Fukumura, 1976, Nakaya m a, 1978).
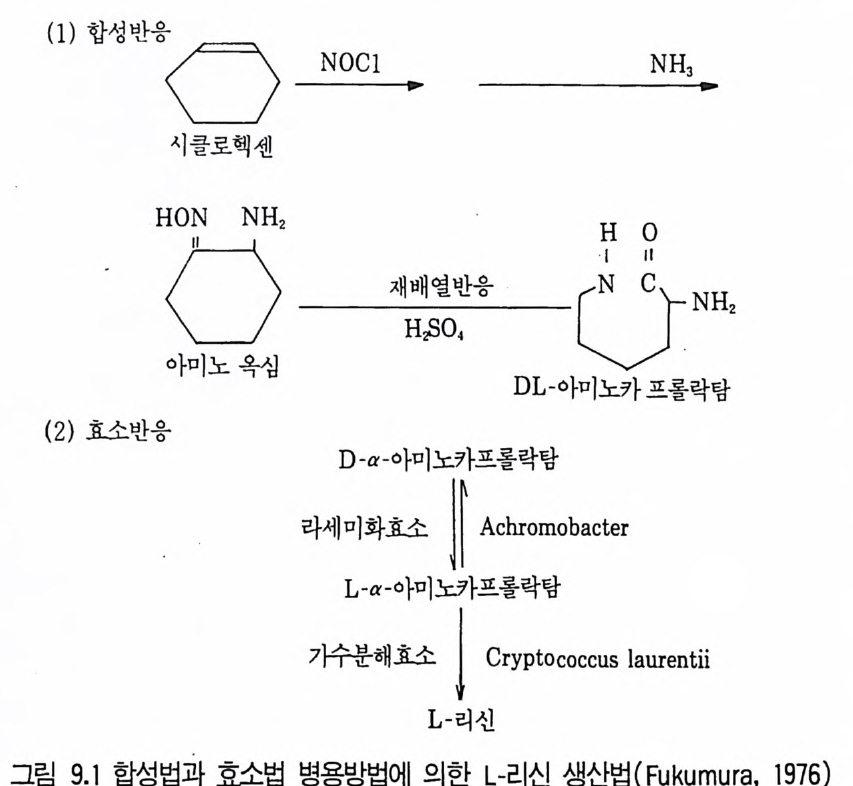 (1) 합성반응O 二
(1) 합성반응O 二
광학적으로 활성인 알라닌, 메티오닌, 페닐알라닌, 트립토판, 발린의 L형
은 이와 감은 방법을 통해 실험실 규모로 생성되고 있으며 산업적으로 아 미노아실화 효소 (am i n o ac y lase) 를 고정화히는 방법이 개발되고 있다 . 표 9.2 는 현재 생산되는 아미노산울 나타내고 있다.
표 9.2 세계적으로 생산되는 아미노산 생산과정과 그 이용범위 Am ino acid 연간 생산량 생산과정 적용 L-Alanin e 10~50 효소법(고정화) 중미효과 (Flaver enhancer) DL-A l an ine 150~200 합성법 증미효과(음료수 생산) L-Argi ni n e 200~300 발효법,추출법 첨가제 (Inf u s io n s), 치료(간 질 환) L-Asp ar ti c acid 500~1,000 효소법 치료,증마효과 L-Asp ar agi ne 10~50 발효법,추출법 치료 L-C ys te i ne 100~200 추출법 탕 생산 (Bread pro ducti on ), 항산화제, 기 관지 치 료 L-G lutam ic acid 320,000 발효법 증미효과 L-G l uta r n ine 500 발효법 궤양치료 Glyc i n e 5,000~6,000 합성법 감미료 (swee t ener) L-Hi sti d ine 200 발효법,추출법 궤양치료 L-I so le u ci ne 150 발효법 첨가물 질 L-Leucin e 150 추출법,발효법 첨가물 질 L-L y s i n e 40,000 발효법,효소법 사료첨가물질 DL-Meth ion i ne 70,000 합성법 사료첨 7H 뭐 L-O r ni thine 50 닙갈효법 간치료 L-Pheny la lanin e 50~100 합성법,발효법 첨가물질, 치료 L-Prol in e 100 발효법 첨가물질 L-S er in e 40 발효법 화 2持 뭄멉 L-Threon ine 160 발효법 사료의 첨가물질 L-Tryp top h an 200 합성법,발효법 첨가물질 L-'I'y ro s i n e 50~100 추출법, 고정화효소법 첨가물질, L-DO P A 합성을 위한전구물질 L-Vali ne 150 발효법,합성법 첨가물질
4 아미노산 생산균주의 새로운 개량방법 글루탐산을 분비하는 미생물이 자연계에서 쉽게 분리되었다 해도 디론 아미노산을 분비하는 자연균주를 얻기는 쉽지 않다. 광범위한 조사를 통해 OJ'2.}닌 (DL - alan i ne) 과 L-발 린 (L-va li ne) 을 분비하는 균주만을 분리했을 랸 l 다. 그림 9.2 는 아미노산에 대한 생화학 경로를 나타낸다.
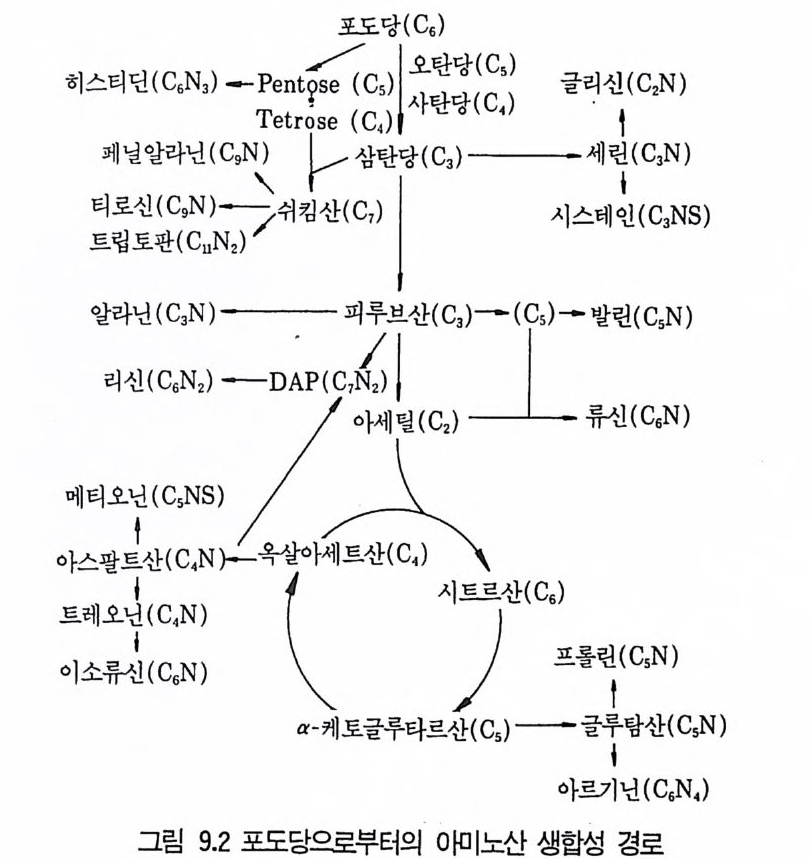 〉당 (C 6 )
〉당 (C 6 )
자연에서의 분리균주는 이들 아미노산울 미량 분비할 뿐인데 그 이유는 세포대사에서 생성을 조절하기 때문이다. 균주의 개발을 통해서 제어조철 을 제거하는 두 가지 방법이 있다.
첫째는 reg ul ato r y e ff ec t or 나 core p ressor 를 더 이상 생성할 수 없는 영양요구성 돌연변이주 (auxo t ro phi c mu t an t s) 를 사용해서 생합성 경로 에서 차단된 바로 앞 단계의 중간대사산물을 분비하도록 하는 것이다. 두 번째 방법은 제어 돌연변이주 (re g ula t or y mu t an t s) 를 사용하는 것으로 서 예를 들면 생합성 경로의 최종산물이 과다하게 생성된다면 되돌림 (fee - dback) 에 민감하지 않은 주요 효소를 내는 돌연변이주를 항대사산물-내성 균주나 혹은 영양요구성 균주에서의 복귀주집단으로부터 분리해내는 방법 이다. 아미노산을 과다하게 생산하는 돌연변이 균주는 양쪽 방법을 함께 구사해서 분리하고 있다.
표 9.3 아미노산을 생산하는 유용균주 아미노산 사용균주 유전적 특 징 급,,_0 탄소원 DL-Alani ne Mi cro bacleriu m ArgH x' 60 Glucose ammonia p h ilu m L-A l anin e Str ep lo my ce s wil d type 9 Glucose coelic o lor 3-19 L-Argi ni n e Breuib a cte ri u m Cua-TA' 35 Glucose flau um 26 Aceta t e L-Gluta m ic Cory n ebncte ri u m Wi ld type >100 Glucose aci d glu ta m i cu m Breuib a cte ri u m 98 Aceta t e flau um Arth ro bacte r 82 n-A lkanes par a/fin e u s L-G l ut am ine Cory n ebacete ri u m wil d type of 40 Glucese, wi th glu ta m i cu m glu t am i c acid hig h bio t i n and pro ducer NH4Cl conte n t L-H i s t i di n e B. flav um TA 『 SM'E t h 『 ABTr 10 Glucose L-lsoleucin e B. flau um AHV'OMT' 15 Glucose
L-Leucin e Brevi ba clenum Ile- M et -T A ' 28 Glucose lacto fe r m enlum L-Ly si n e C. glu ta m i cu m Hom -Le u- A EC' 39 Glucose B. flau um FAl-30 AEC' 57 Glucose B. fauu m Hom ka ky T hre - 75 Aceta t e L-Meth i o n in e C. glu ta m i cum Thr-Eth 'M etH x ' 2 Glucose KY 9276 26 Glucose L-0 r ni thi n e C. glu ta m i cum Arg L-Pheny la lanin e C. glu ta m i cum Ty r - PFr 'PA P' 9 Glucose L-Prolin e B. flau um Ile -SG -D HP + 29 Glucose L-Threonin e B. flau um Met -A HV' 18 Glucose 27 Aceta t e E. coli K-12 Increased gen e cop y 55 Sucrose number L-Tryp top h a n C. g/u ta m i cum Phe- T y r- SMT'TrpH x' 12 Glucose Px-115-97 6FT 『 4MT 『 PF P 『 PAPr Ty rH x'PheHx' L-Ty ro sin e C. glu ta m i cum Phe- PF PrPAPrPATr 18 Glucose Pr-20 Ty rH xr L-Valin e Breuib a cte iu m TAr 31 Glucose /aclofe rm enlum No. 487 Resis t a n c e : ABT 2-Ami no benzth i a z ole ; AEC S-( P-Ami no eth y l)-L - e y st e i n e : AHV a-Ami no -P-hy dr oxy va le ri c acid : ArgH x Arg ini n e hyd r oxamate : DHP 3. 4-Dehy d rop ro lin e :Et h Et hi o n in e : 6FT 6-Fluorotr y p top h a n ; MetH x Meth i o n in e hy dr oxamate : 4MT 4-Meth y l t r y p top h an ; 5 MT 5-M eth y l t r p t op h an : OMT 0-M eth y lt h r eonin e : PAP p-A m ino -p he ny la lan ine ; PAT p-A mi no t y ro sin e ; PFP p-F luovop h eny la lanin e : PheHx Pheny la lanin e hy d rox amate : SG Sulfa gu anid i n e : SM selenometh i o n in e : TA 2-Thia z olalanin e ; Ty rH x Tyro sin e hyd roxamate ; TrpH x Trpt op h an hy d roxamate (Hi ro se, 1979)
표 9.4 효소적인 아미노산 생산에 사용되는 균주 o ):o]노산 효소 효소 ul04 수 효융 생산균주 (g/ Q) (%) L-Alan ine Asp ar ta t e Pse ud omonas L-A s p ar ta t ~ 268 100 decarboxy la se dacunhae L-A l an i net C O2 L-Asp a r- Asp a rta se Escheric h ia Fumarate +NH4 560 99 tic acid coli -+L-A s p a rti c aci d L-C ys te i n e Cy stei n e des- Aerobacler P-Chloro-L - a la nin e + 49 89 ulfu yd rase aerog en es NazS --+L-Cy s te i n e +NaCl+NaOH LDOPA Ty ros in e Erwi ni a Py ro cate c hol+Py r - 59 95 {L-3 ,4 ph enol lya se herbic o la uvate + NH4 +•- > Dihy d roxy ph eny la lan ine ) L-D OPA+H2 0 L-Ly si n e D-Ar nino Ach- DL-A m i- 100 cap ro lacta m romobacte r nocap ro lac ta m + H2 0 racemase, abae -L-L y si n e L-Ami no - Cry ptoc occu. s capr o lacta r n laurenti i 100 hyd rolase L-Pheny l D- 5- Benzy l Fla- DL- 5- Benzyl h y - 50 100 alan ine uobacte r iu m dant oi n + 2 H 2 0 ➔ hyd anto i n am1- L-Pheny la lanin e + racemase nog en es C02+NH4+ L-5 - Benzy l hy d anto i n hy d rolase N-C a rbamoy l- L ph eny la lan ine hy d rolase L-Tryp to- Try- Prote u s Indole+Py ru vate + 63 98 ph an ptop h anase rellge r i NH ◄ + ->L-Tryp top h an+H20 (Hi ro se and Okada, 1979)
여러 가지 탄소원을 사용한 생산방법이 각각 다른 생산균 주 에 의해서 개발되었다. 이 표에서는 공개된 가장 높은 수율의 방법만을 나타낸 것이 고 실제 산업적 수율은 상당히 높은 것으로 추정되고 있다. 5 아미노산 생산공정 조절 아미노산 발효는 최고 450m' 의 회분발효조에서 2~4 일 걸리는데 연속공 정방법이 개발되었지만 상업적으로는 아직 실용화되지 못하고 있다. Bacte r io p h ag e7 } 강겸되면 생산에 막대한 손실을 가져오므로 파지 내 성돌연변이주(p ha ge resis t a n t mu t an t)와 파지 증석을 억제하는 화학약 제가 사용될 수도 있다. 순수배양의 지속성 유지를 위한 연구도 관심의 대 상기 되고 있다. 영양용액의 멸균은 보통 연속적으로 행해지고 있다. 발효공정 동안의 높은 당소모율관 높은 호흡작용 때문에 산소요구량이 증가한다. 개별적인 공정의 적정 통기율은 균주, 기질, 생합성 경로에 따라 좌우된다. 발효공정은 28~38°C 사이에서 행해져야 하므로 과다한 열의 발생은 동시에 냉각시켜야 한다. p H 는 공정에 따라 6.8~8.0 사이에서 유 지된다. 때로는 암모니아가 p H 조절에 사용되는데 동시에 질소원으로서도 이용되기도 한다. 글루탐산 발효공정에서의 통기속도, 온도, p H 와 소포제 의 양과 같은 기준치는 모두 자동적으로- 조절되고 경우에 따라서는 컴퓨 터로조절되기도한다. 발효공정 종료시 세포물질을 분리하기 위해 원심분리를 한다. 아미노산 은 산성화 후 등전점에서의 침전, 이온교환 크로마토그래피, 전기두석 혹 은 유기용매에 의한 추출방법 등을 통해 회수한다. 6 각종 아미노산의 생산 아미노산의 요구가 증가하는 추세인데 L- 리신 (L-l y s i ne) 과 DL 페티오
닌 (DL - me t h i on i ne) 은 사료첨가제로서 경제적으로 생산이 가능한 반면, L-트 레오닌 (L- t hreon i ne) 은 기존의 과정으로는 수윤이 낮기 때문에 아직 충족되지 못하고 있다. 그러나 최근 소련에서 E.coli 균 주를 이용한 재조합 DNA 기술로 L-트 레오닌 (L- t hreon i ne) 을 약 55 g /l롤 생산하는 데 성공 하였다. 또한 일본의 3 개 회사에서도 L-트 립토판 (L- t r ypt o p han) 을 경제 적으로 생산하는 공정이 개발되었다. 세계 요구량은 연간 3 만 톤으로 추정 된다 (Showa Denko K.K ., Aji no mot o Co., Ky od a Shir y o Co.). Ls글 루탐산 (L- g lu t am i c acid ) , L- 리신 (L-l y s i ne) 과 L-트 립토판 (L tr ypt o p han) 을 생산하는 공정은 중요하므로 아래에서 자세히 설명하겠다. 6.1 L-글 루탐산 (L- g lu t am i c acid ) 발효 (1) 사용균주 (A i da, 1986) L-글 루탐산은 화학적으로도 생산할 수 있지만 주로 미생물을 이용하는 방법이 사용되고 있다. 화학적 합성에 의한 DL-글 루탐산 (DL- g lu t am i c ac i d) 은 라세미체의 혼합물이기 때문에 직접적인 발효공정이 일본에서 개 발되었다. 세균, 방선균, 효모, 곰팡이 등 다양한 범위에서 L s글 루탐산이 생 산된디는 것을 밝혔는데 195 7¼빈에 Cory n ebacte r iu m glu ta m i cu m=Mi c- rococcus glu ta m i cu s< >1 분리되어 Ky ow a Hakko 회사는 이 균주를 글루탐 산을 산업적으로 생산하는 데 이용하였다. 30g / l 이싱을 생산하는 균주로 서 Breuib a cte r iu m lacto f e rm entu m , Breufl au um, Mi cro bacte r iu m , Amm- onia p h il u m, Breu. diu a ric a tu m 등이 알려지고 있다. 이들 글루탐산의 생 산균주는 형태적, 생리적으로 C. g lu t am i cu 따라 유사하다• 그들은 보통 그 량競꾼]고 포자를 형성하지 않으며 운동성이 없다. 더욱이 모든 글루탐 산 생산균주는 모두 생육에 b i o ti n 을 필요로 하고, a 케토글루탐산 탈수 삭 (a-ke t o glu ta r ate deh y dro g enase) 의 활성이 없거나 낮으며, 글루 탐산 탈수소효소(g lu t ama t e dehy dro g enase) 의 활성은 증가된다. 또한 어떤 Breu i bac t er i u mi-斗 Cory n ebacte r iu m 돌연변이주는 이소시트르산 분해
효소(i soc it ra t e lya se) 활성이 매우 낮다. 자연분리 균주가 30 g /l 의 양 울 생산하는 것과는 대조적 생산유전자를 운반하는 재조합 pla smi c@.. 형 질전환된 대장균은 lOg / l 정도로 생산하는 것이 현실정이다. (2) 글루탐산의 발효 메커니즘 글루탐산의 생합성 메커니즘을 간단히 설명하면 포도당은 해당 경로 (EMP) 와 펜토노스 포스페이트(p en t ose- p hos p ha t e) 경로를 통해 피루 브산으로 대사되고 탄산가스몰 고정하여 acid 7 } 되거나 혹은 아세틸코에 이 (ace ty l - CoA) 를 거쳐 각각 TCA 회로로 들어간다. 글루탐산울 생산하 는 데는 EMP 경로가 주로 이용된다. 글루탐산의 주요 전구체는 a 케토글 루타르산이고 이 a- 케토글루타르산은 시트르산 (c it ra t e) 과 이소시트르산 (i soc it ra t e) 을 통해서 TCA 회로에서 생성되며 유리 NH t이온과 함께 환원적인 아민화 과정을 통해 Ls글 루탐산으로 전환된다(그림 9.3). 마지막 단계는 NADP에 의존하는 글루탐산 탈수소효소(g lua t ama t e deh y dro genase) 에 의해 촉매된다. 이 단계에서 요구되는 NADPHn =-이 소시트레이트 털수소효소(i soc it ra t e deh y dro g enase) 에 의해 촉매되는 이소시트레이트로부터 a- 케토글루타르산으로의 산화적 탈탄산 과정에서 공 급되고 이 NADP 는 a- 케토글루타레이트의 환원적 아민화 과정에 의해 재 생산된다. 글루탐산 생산에 산업적으로 이용되는 균주는 a- 케토글루타르산 탈탄산 효소 (a-ke t og lu t ara t e dehy dro g enase) 에서 제어를 받는다. NH4+ 이온이 。` 산화 。탄 1 소소 Al 무+二 二 케 토評 타 르 산+암 모 니 움 .
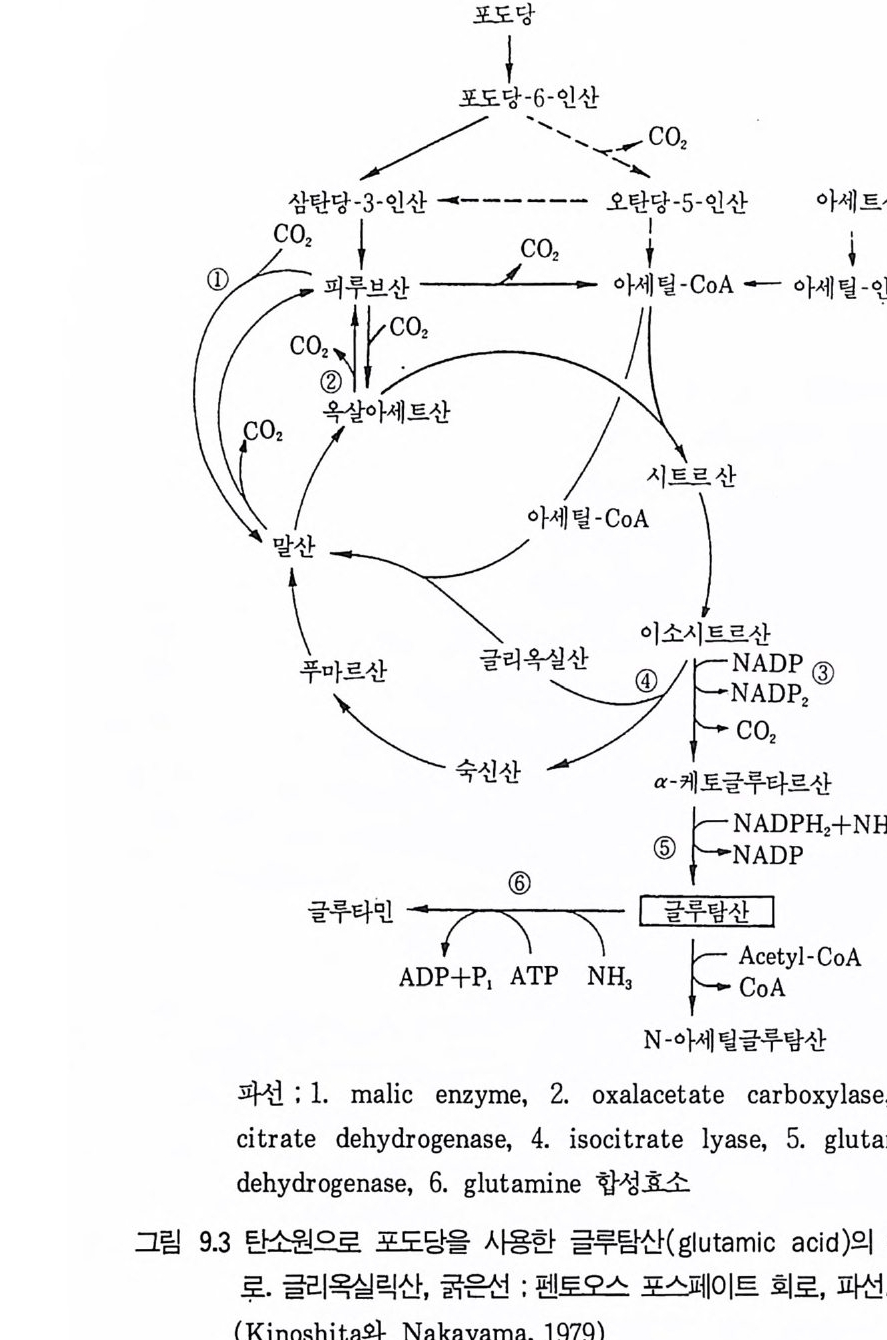 포도l당
포도l당
없으면 TCA 회로가 방해받기 때문에 a- 케토글루타르산이 축 적된다. 그러 므로 효율적인 보충대사 (ana p lero ti c) 경로를 위해 다른 세포내 반응에 필요한 TCA 회로의 중간물질을 공급할 필요가 있다. 생합성 경로에 대한 연구에는 방사선 표시화합물을 이용하는데 14C 0 2 존재하에서 글루탐산을 생성하는 데는 글루탐산의 a-카 르복실(a. -<:arbox y 1) 기가 방사선으로 표지 된다. 옥살로아세트산 탄산효소 (oxaloace t a t e carbox y lase) 와 NADP 의 존성 말산효소는 co 교정에 관여하고 말산효소는 피루브산울 말산으로의 탄산화를 촉매한다(그림 9.3). 이들 ana p lero ti c 경로는 C4 디카르복시산 (dic a rboxy li c ac i d) 을 함유하는 TCA 회로를 이루게 되는데, 말산은 옥 살로아세트산을 거쳐 시트르산과 이소시트르산으로 전환되고 이어서 글루 탐산 형성의 중간물질로 제공되거나 혹은 글리옥살산 회로로 들어가게 된 다. 특히 탄소원으로 아세데이트를 사용할 경우 C. g lu t am i cum 에서는 에 너지 획득과 중간물질의 생성은 주로 글리옥살산 회로를 통해 이루어진다. 그러므로 숙신산과 글리옥실산울 생성하는 이소시트레이트 분해효소(i so cit ra te l y ase) 의 촉매반응과(최적증식을 위해 필요함), 중요 전구물질인 a- 케토글루타르산으로 향하는 이소시트르산 탈수소효소(i soc it ra t e de- hyd r oge n ase) 반응 사이에는 경쟁관계가 있다. 포도당과 아세테이트에서 글루탐산울 생성하는 반응은 다음과 같다. CsH 1 20 s + N H3 + 1 .5 02 ― ➔ CsH 9 0 4 N +C02+ 3 H20 3C2 H4 02+ N H3 + 1 .5 02 一 CsH 9 Q 4 N +C02+ 3 H2 0 포도당 1 mol 타 아세트산 3 mole 에서 각각 1 mol 려 글루탐산아 생산 된다. Resti ng eel 邊 이용한 실험에 의하면 실제적인 전환율은 . 50~70 mole %인데 수율감소의 일부는 말산효소의 가역반응과 옥살아세트산에서 CO 로의 탈탄산화에 기인한다.
(3) 글루탐산 생산과 막투과성 과다한 양의 글루탐산의 생산분비는 세포의 두과성에 좌우되는데 글루 탐산 생산세균의 막투과성을 증가시키기 위해서 여러 가지 방법이 쓰이고 있다.죽 1. 비오틴을 결핍시킨다. 2. 올레인산 요구성 균주에서 울레인산을 결핍시킨다. 3. 포화지방산이나 지방산 유도체를 첨가한다. 4. 페니실린을 첨가한다. 5. 글리세롤 요구성 균주에서 글리세롤을 결핍시킨다. 글루탐산을 생산하는 모든 균주는 지방산 생합성에 필수적 조효소안 바 이오틴을 증식에 필요로 한다. 바이오틴의 농도가 5µg / l 이상으로 존재하 면 울레인산 합성이 증가해서 세포막의 인지질 함량이 높아진다. 인지질 함량기 높은 세포는 글루탐산을 분비할 수 없고 글루탐산이 25~35µg / mg 건조균체가 될 때까지 세포내에 축적되어 되돌림저해작용으로 생합성이 억 제된다. 반면에 바이오틴이 결핍된 배지에서는 인지질 합성이 감소되어 포 화지방산과 불포화지방산의 비율이 변화하여 막에 손상을 일으킨다. 이러 한 조건하에서 세포내 글루탐산이 분비된다. 지방산합성의 첫단계인 아세틸코에이에서 말로닐 코에이 (malony l- CoA) 로의 전환을 촉매하는 바이오틴 함유 아세틸코에이 탄산효소 (ace ty l-CoA carbox y lase) 가 지방산 생합성에 관여하는데 포화지방산 (C1 6 ― C1 8 ) 은 이 아세틸코에이된산효소를 억제한다. 그러므로 울레인산 요구주나 포화지방 산을 첨가한 균주는 인지질 함량이 낮은 세포막을 합성한다. 이러한 균주 는 b i o ti n 이 존재하는데도 L-글 루탐산울 분비한다. 대수증식기에 페니실린 을 첨가하면 bio t i n 존재하에서도 글루탐산 분바가 현저히 촉진된다. 페니 실린은, 발효조에 접종 8~l V.]간 후에 과량의 바이오틴을 함유한 배지에 첨가하는데 페니실린 농도를 ml 당 5~30 QtJ-위로 택하면 세균의 증식속도 는 바이오딘의 함량이 낮은 배지에서의 증식 속도에 상응하는 수준으로 감소된다.
심법적으로는 페니실린이나 포화지방산을 사용함으로써 사탕수수당밀이 나 사탕무당밀과 같은 값이 저렴한 배지성분을 사용할 수 있게 되었는데, 그렇지 않았다면 이들 당밀은 바이오틴 을 많이 함유하고 있으므로 이용하 지 못했을 것이다. 글루탐산 생산에 대한 세포 투고 R상 의 역할을 발견할 수 있었가 때문에 중요 아미노산을 산업적으로 생산하는 데 크게 기여하게 된것이다. (4) 생산의 조건 최적배양 조건하에서 글루탐산 생산균주는 첨가한 탄소원의 50 ~60 % 를 L-글 루탐산으로 전환한다. 발효 조건이 적합하지 못해서 글루탐산 수율이 낮을 때는 균체량이 증가하고 락트산, 숙신산, a- 케토글루타르산, 글루타민 과 N 아세틸글루타민 (N-ace ty l g lu t a mi ne) 이 나타난다. 글루탐산 발효에 영향을 미치는 요인을 살펴보면 아래와 같다. 페니실린 (/3-la cta m 항생물질) (3) UDP-N- 아세틸 핵소스아민 유도체 , ,포도당 지방 \, 4? /스글리-세`롤 !/, ` 아세틸 -CoA 二=二츠 glu cose 티아민(시〉산 2- 옥소글루타르산 글루탐산 인지질합성의 제어와 글루탐산의 분비 (Nakao, 1972)
탄소원 : 여러 가지 탄수화물이 발효공정에서 탄소원으로 이용되는데 단 당류로서는 포도당과 설탕이 주로 이용되고 과당, 맥아당, 자일로오 A 도 이용된다. 미정제 탄수화물원으로는 사탕수수당밀과 사탕무당밀이 가장 많 이 이용되고 전분 가수분해물로 쓰인다. 당밀은 바이오틴 함량이 높기 때 문에(수수당밀 k g당 0.4 ~1.2m g , 무당밀 k g당 0.02~0.08mg ) 페니실린이나 지방산을 첨가해주어야 한다. 유럽에서는 사탕무당밀이 주로 쓰이고, 다른 여러 나라에서는 사팅수수당밀이 주로 이용된다 . 일본에서는 아세트산이 가격이 저렴하여 많이 사용되나 사탕무당밀과 함께 이용되기도 한다. 메탄올, 에탄올, 아세트알데히드 또는 n- 알칸 (n-alkane) 을 사용하는 방 법도 개발되고 있으나 이들 공정의 가격효용성은 주로 석유값에 의존한다 (그림 9.4 ). 그림 9. 隣} 그림 9. 斑든 탄소원으로 포도당과 아세데이트 그리
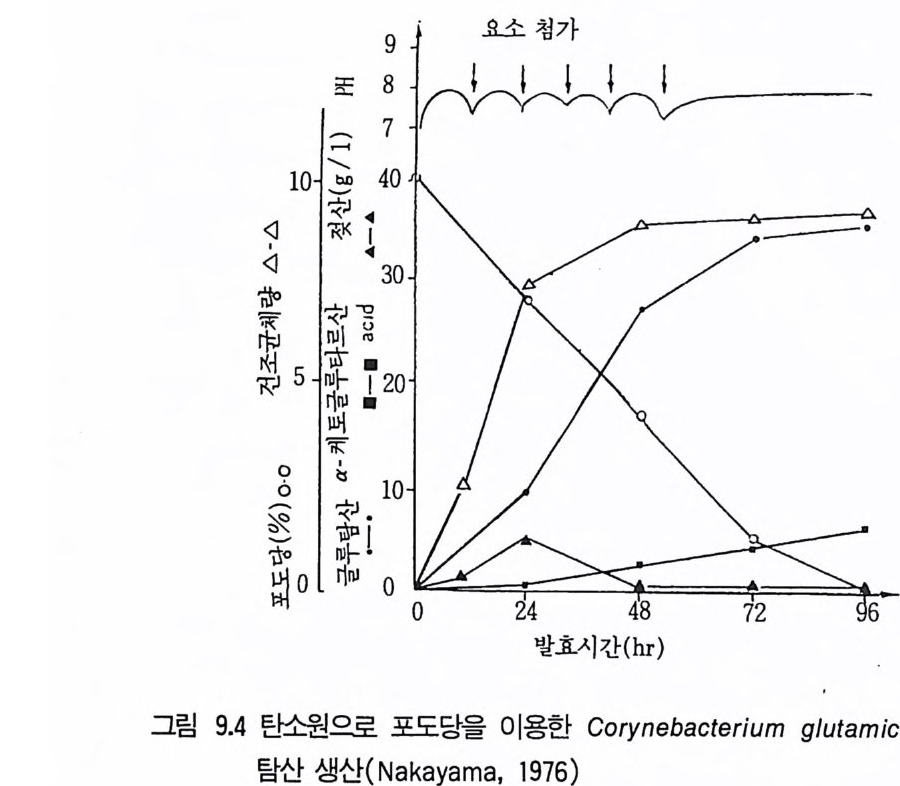 기 프첨가
기 프첨가
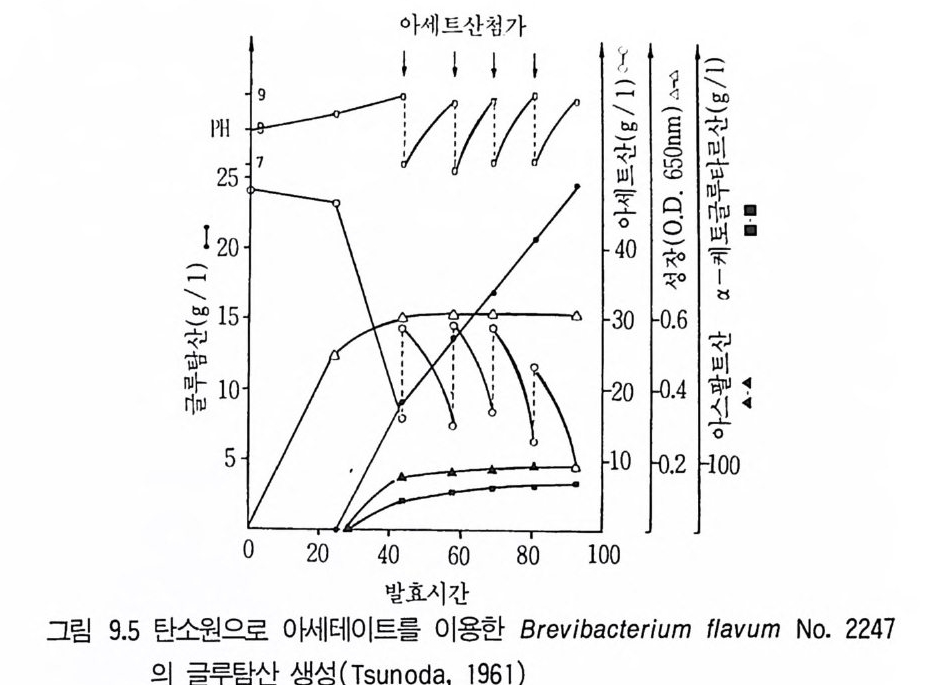 아세트산첩가
아세트산첩가
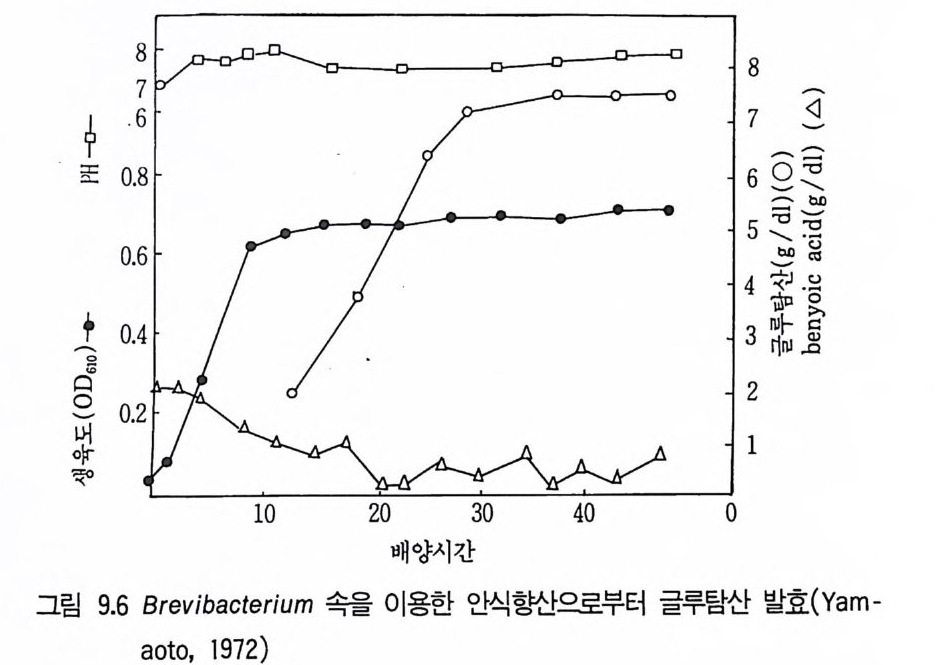 876 8
876 8
고 benzoic ac i d 를 사용한 전형적인 발효과정이다. 질소원 : 암모늄영과 더불어 가스나 수용액 상태의 암모니아를 질소원으 로 사용할 수 있다. 글루탐산의 산업적 생산에서는 암모니아를 첨가하면 p H 도 조절되고 암모니아의 독성도 제거된다. 글루탐산을 생산하는 대부분 의 세균은 Urease 활성을 가지므로- 우레아가 질소원으로 이용되기도 한 다. 산성 p H 범위에서 암모니아를 과잉공급하면 글루탐산 대신 글루타민이 생산되고 암모니아 공급이 부족하면 2-o x og lu t ar ic acid 7 } 생성되어 소위 발효전환이란 현상이 나타난다. 성장요소 : 최적 바이오틴 농도는 사용된 탄소원에 좌우되는데 10 % 의 포도당이 함유된 배지에서는 바이오틴 농도가 5µ g /l 이고 포도당 농도가 낮아지면 상대적으로 낮아진다. 아세트산의 경우 0.2-l µg/l 이 소요된다. 균주 중에는 추가 성장요소로 시스테인 (L -cy s t e i n) 을 요구한다. 알칸을 함유한 배지에는 티아민의 공급이 필수이다. 아세트산을 탄소원으로 한 Breu. thi o g e n it al is D 24 8it주에서는 저농도의 Cu 이온 첨가에 의해 글루 탐산 생성이 촉진되는 경우도 있는데 이 현상은 호흡계에 영향을 미치는 것으로추정되고 있다. 0 2공 급 : 글루탐산 생성률은 Kd 값이 3.5 X10-6 mole • 02 /a tm .mi n. m1 일 때 가장 높다. 산소의 농도는 적절하게 유지되어야 하는데, 산소가 부족하면 락트산과 숙신산이 분비되고, 반면에 산소의 양이 많으면 성장이 억제되고 a 케토글루타르산이 생산된다. 두 경우 모두 글루탐산 생산을 저 하시킨다. (5) 생산공정 (pro ducti on pro cesses) Breuib a cte r iu m div a ri ca tu m (NRRL B-231) 의 포도당을 이용한 발효는 다음과같다. 종배양 : 포도당 40g, K2HP04 l.Og , Mg S 04 • 7H20 0.5g , 효모엑기스 l.Og , 우레아 8g, 물 ll ; 35°C 에서 1 61-]간 배양•
본배양 : 포도당 121g : 암모늄 아세테이 트 (ammon i um aceta t e ) :Jg , 당밀 6g, KH2 PO i 1.2g , K,S 0 1 1.2g , Mg SO ., 6 g, FeSO~ • 7H~ O 6 ppm , MnSOi • H2 0 6 ppm , 소포제 Hodag K- 69 0.1 m l, 물 1l, 접종량 6%. 발효 초기 0.65ml/l 의 울레산울 첨가하는 데 p H 를 암모니아로 8 . 5 로 고정시키면 발효과정 동안에 7. 誌i 자동조절되며, 배양 개시 1 4-A]간 후에 온도는 32~33°C 에서 38°c 로 증가한다. 또한 포도당대사가 0.5~2% 로 낮 아전 뒤에는 발효가 완료될 때까지 포도당을 첨가해준다. 평균 리터당 160 g을 첨가하게 되고 통기는 조절하여 배기가스내 gas 의 CO ,함 량이 4. 5vol% 를 넘지 않아야 한다 . 글루탐산의 함량은 시간마다 분석되는데 대체 로 30~3 터간 후에는 약 lOO g /l의 수율로 생성되면서 발효가 끝난다. 만일 전분 가수분해 당밀 대신 포도당을 사용한다면 글루탐산 수율은 36 시간 후에는 94 g /l 가 된다. 여러 가지 탄소원을 이용한 글루탐산 수율이 표 9.5 에 나와 있다.
표 9.5 각종 탄소원을 사용한 굴루탐산 생산수율 탄소원 균주 Yie l d(g / Q ) Sug ar beet molasses C. glu ta m i cu m >100 Glucose+Ammoniu m aceta t e Breuib a cte r iu m diu a ric a tu m 100 Aceta t e B. flau um 98 Eth a nol Breuib a cte r iu m sp. 136 59 n-Alkanes Arth r obacte r pa ra[(in e us 62 Cory ne bacte r iu m 84 hyd r ocarboclastu s 72 Benzoic acid C. alkanolyt icu m ( Gl y cero 「 ) 80 Breuib a cte r iu m sp.
(6) 글루탐산 생산균 육종 동향 현재는 글루탐산울 다량 축적할 수 있는 상태이기 때문에 생산균을 육
종개량하는 것은 쉽지 않다. 그러나 실제 변이주가 유도되어 그 제법에 관 한 특허가 신청되고 있는 것도 사실이다. 특히 최근에는 재조합 DNA 기 술의 응용 이 시도되고 있는 것이 특징이다. 변이주로서는 울레산 요구주 (T. Kanzaki, 1967), 페니실린 내성주 (Kobaya s h i, 1971), 중키세린 요구주 (Nakao, 1970) 그리고 아데닌 요구 주 (Tanaka, 1965) 를 이용하거나 바이오틴의 영향을 받지 않는 온도감수 성 변이주의 이용이 시도되고 있다 (Momose, 1978). 한편 재조합 DNA 기술을 이용하는 시도로서 Pares 등 (Pares, 1974, Jof r e, 1979) 은 Cit ro bacte r int e rm ediu m C 리 글루탐산 분비 등이 높은 빈도로 전달되는 것과 글루탐산 분비에 염색체의 DNA 가 관여한다는 추 정을 하여 글루탐산 생산균의 숙주―벡터계 확립에 노력이 경주되고 있다. 특히 Breuib a cte r iu m loc t ofe rmen t um 에서 pla smi d7 } 분리되어 대장균의 pB R 322 혹은 Bac i llu 려 pU B 11~ 回 shutt le 벡 터를 구축하여 숙주 ―벡터계가 개발되고 있다 (M i wa, 1985). 그리고 C. g lu t am i cum 에서 용 원파지를 분리하여 DNA 의 형질도입방법도 확립되고 있다 (Ka t suma ta, 1983, Kats u mata 1984). 재조합 p las mi d 를 구축한 각종 결과도 나오고 있다 (Oza ki, 1984. Tsuch ida , 1976). 또한 원형질 융합법을 이용하여 재 조합체도 획득하고 있다 (Kaneko, 1979). 이상 간단히 살펴본 바와 같이, 유전자 조작의 가능성에 대한 기술이 점 차 개발되어 재조합 DNA 기술을 어떻게 미생물 육종에 결부시키느냐 하 는 문제는 특정 아미노산 발효뿐만 아니라 발효공업전반에 걸친 과제로 등장되고있다. 6.2 L- 리신 발효 리신은 인간과 동물의 영양에 필수적인 아미노산이다. 식물성 단백질에 는 소량이 함유되어 있어 그 질을 높이기 위해 수요가 매우 크다. 오늘날 L- 리신은 미생물을 이용한 방법만으로 생산되고 있으며 또 다양한 방법이
개발되고 있다. 리신의 생산기술은 아미노산 생합성의 대사제어를 인공적으로 제거하여, 목적으로 하는 아미노산을 축적시키는 생합성 조절 메커니즘 생산균의 육 종개 대해서 많은 연구가 행해지고 있다. 1985 년 리신의 세계생산량은 발 효법 (직접발효법과 전구체안 dia m i no p im eli c ac i d) 으로 약 74,00 闇 E, DL-ami no lac t am 을 원료로 한 효소법으로 약 4,00 混찌 생산된 것으로 추정되고 있다. (1) 리신 생합성 경로와 대사조절 Di am i no p im elic ac i d(DAP) 의 경로 : E.coli ( ATCC 13002) 의 이중 영양요구 돌연변이주(ly s i ne 과 h i s ti d i ne) 는 당밀배지에서 DAP 를 19~ 24 g /l 의 수율로 생산하는데, 이어서 세포를 포함한 전발효용액을 35°c 에 서 Aerobacte r aeroge n es(ATCC 12409) 와 함께 배양하면 2 也 l 간 후에는 DAP7} 리신으로 탈탄산화된다. 이 발효공정의 한 가지 복잡한 문제는 생 성되는 DAP는 meso 형과 LL 형의 혼합물인데 meso-DAPoJ< >] L- 리신으 로 탈탄산화되므로 LL-DAP 를 탈탄산 단계 전에 라세미화에 의해 meso 형으로 전환시켜야 한다는 것이다. DL-'J.c ami no ca p rolac t am 의 전환 : DL-ami no ca p rolac t am 이 L- 리 신으로 효소전환되는 과정은 그림 9.7 과 같다 (Fukumura, 1976). 10% 의 DL-ami no ca p rolac t am 용액 (pH 8.0) 을 0.1%(w/v) 의 아세톤으로 탈수 한 ·.Cr yptoc occus Lauren tii와 Achromobacte r obae 의 세포에 첨가하면 40°C 로 2 이간 후에는 99.8% 의 효율로 전환되어 리신이 생성된다. 직접발효법에 의한 리신 생산 : L- 리신의 공업에 세계적으로 널리 사용 되는 방법은 직접발효법과 합성중간체의 효소전환법인데 먼저 직접발효법 에 대해 설명하겠다. 직접발효법에 의한 리신 생산에는 Co ry nebac t er i u m:라 Breuib a cte r iu m 속 세균의 돌연변이주를 사용하고 있다. 호모세린 (Homoser i ne) 요구주나 메티오닌 및 트레오닌 이중 요구성
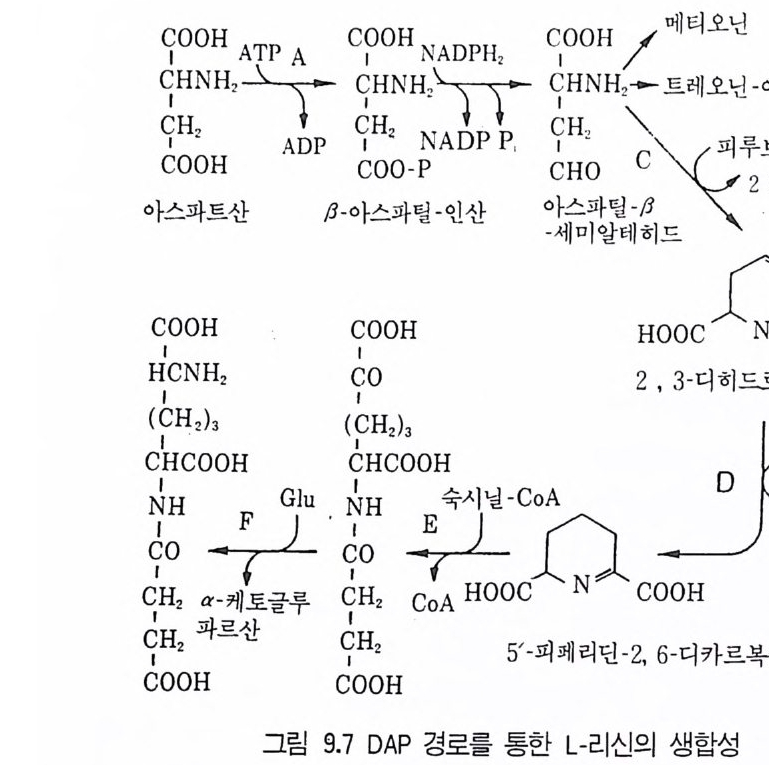 아『1~0:0=H; )A二 ',I 'P A /3 - Co:~~:O~2 H}N- H P틸工訂N - A 인D 산PH , °C『\i°;H oON: H 麟 H 2/: IC 트메:티레오\닌\\ :i 2 :0 요
아『1~0:0=H; )A二 ',I 'P A /3 - Co:~~:O~2 H}N- H P틸工訂N - A 인D 산PH , °C『\i°;H oON: H 麟 H 2/: IC 트메:티레오\닌\\ :i 2 :0 요
균주, 그 의에 리신을 고생산균주로서 리신 유사체인 S-(/3 - anin o eth y l) -L -cy st e i ne(AEC) 에 대한 내성주도 육종되었다. 감수성 균주도 리신 생 산용으로 육종되었는데 그 예로는 트레오닌이나 메티오닌 감수성이 육종되 었고 이 균은 호모세린 탈탄산효소 (Homoser i ne deh y dro g enase) 의 활성 이 야생주의 1/300] 다. 리신을 분비하는 중요한 균주는 표 9.7 에서 정리 하였다. 발효가 수행되는 동안에 발열량아 많기 때문에 냉긱수· 절약을 위 해 고온균의 육종도 필요한 대상이다. Candid a pe ric u losa, Saccharomy ce s cerevis i a e 또는 Saccharomy cop s is lip o lyt ica 같은 효모도 리신 생산의 연구대상이 되고 있는데 건조 중량의 20% 정도로 세포내에 리신이 축적된다. 그렇지만 리신을 배지로 분비하지 못하므로 산업적으로 이용되지 못하고 있다. 리신 생합성과 대사조절 : 리신은 DAP 경로나 amino adip ic acid 경로
를 통해서 미생물과 합성되지만 한 균주는 이들 중 한 경로에 의해서만 가능하다. 세균, 방선균, cya n obacte r ia , ph yc o my ce te s, 원생동물은 DAP 경 로를 이용하고, ascom y ce t es 와 basid i o m y ce te s , 그리고 몇몇 ph y - com y ce t e 러 진핵조류 (eucar y o ti c al g ae) 는 ami no adip ic aci d 경로를 이용한다 (Sh ii o, 1974). 세균의 DAP 경로를 통해서 생합성되는 과정은 그림 9.7 에 있다. 두 개 체가 같은 경로를 이용한다고 해도 이 과정이 조절되는 방식이 서로 다른 데 그림 9.8 에서는 대장균과 Brevib a cte r iu m lac t o f ermen t um 의 예를 들어 비교하였다. 대장균에서는 세 가지의 뚜렷한 조절기전이 있는데 다음과 같 다. 1. L 에티오닌이나 L-트 레오닌에 의해 억제되는 호모세린 탈수소효소
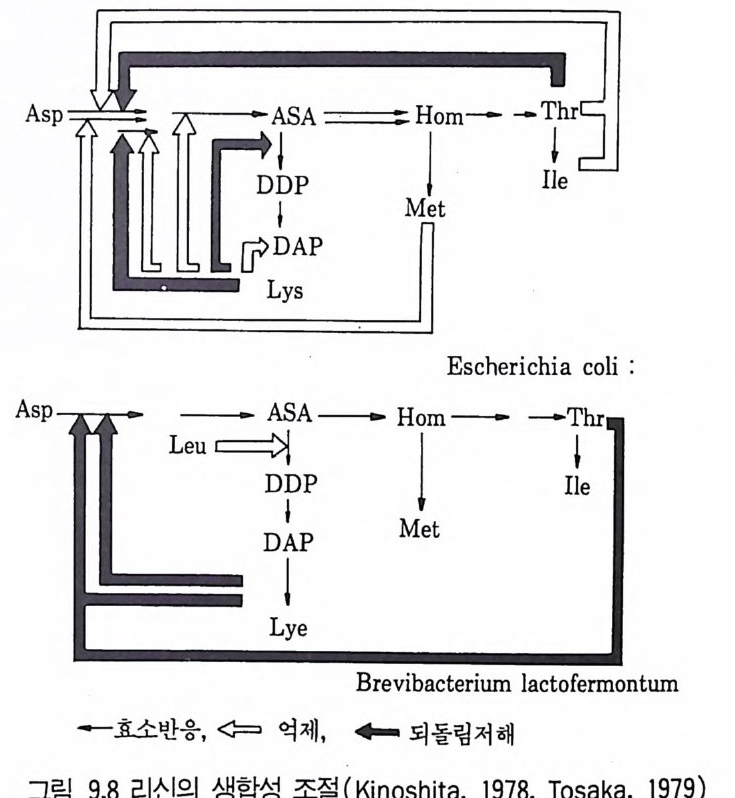 As p:::;;;;一一. ~ASA —~ Hj om-- TIhtr
As p:::;;;;一一. ~ASA —~ Hj om-- TIhtr
(homoserin e deh y dro g enase) 에 두 i soenz y m 리 존 재한다. 2. As p ar t ok i nase 에는 세 가지 iso enzy m eOl 있는데 하나는 L 에티오 닌에 의해 억제되고 두번째는 L -트 레오닌에 의한 되 돌 림저해가 추가 되어서 Ls트 레오닌과 L 이소류신에 의한 다중억제와 세번째는 L- 리 신에 의한 억제와 되돌림저해를 나타내는 경우이다. 3. 리신 생합성에서의 첫번째 특이한 효소인 dih y d rodip ico lin a te 합성 효소는 L- 리신에 의해 되돌림저해를 받는다. L- 리신을 과잉생산하기 위해 이들 세 가지 효소반응에 대하여 조절 메 커니즘을 제거해야 한다. 대칭균에 비해서 Cory n ebacte r iu m glu ta m i cu m(Nakay am a, 1972) 이나 Brevib a cte r iu m flav um 같은 균주의 생합성 경로 조절대사는 훨씬 간단하다. 이 경우 하나의 asp a rto k in as~ 하나의 호모세린 탈수소효 소 (horn oserin e deh y dro g enase) 만이 있는데 as p ar t ok i nas~ 근 표 9. 停 l 실험자 료에서 알 수 있듯이 Ls트 레오닌과 L - 리신에 의한 되돌림저해를 통해 조 절된다.
표 9.6 aspa r t ok in a se 활성에 대한 각종 아미노산의 영향 아미노산 첨가 상대적 B. flav um (10 µmol/ml each, L-fo r m) asp a rto k in a se acti vi t y(% ) C. glu ta m i cu m( Homoserin e - ) Contr o l 100 100 Threonin e 123 99 Ly si n e 94 80 Homosorin e 94 102 Meth ion ine 109 102 ·Th reonin e +Ly si n e 52 44 Homoserin e +Ly si n e 95 74 Threonin e +Meth i o n ine 129 114 (Nakaya m a, 1972)
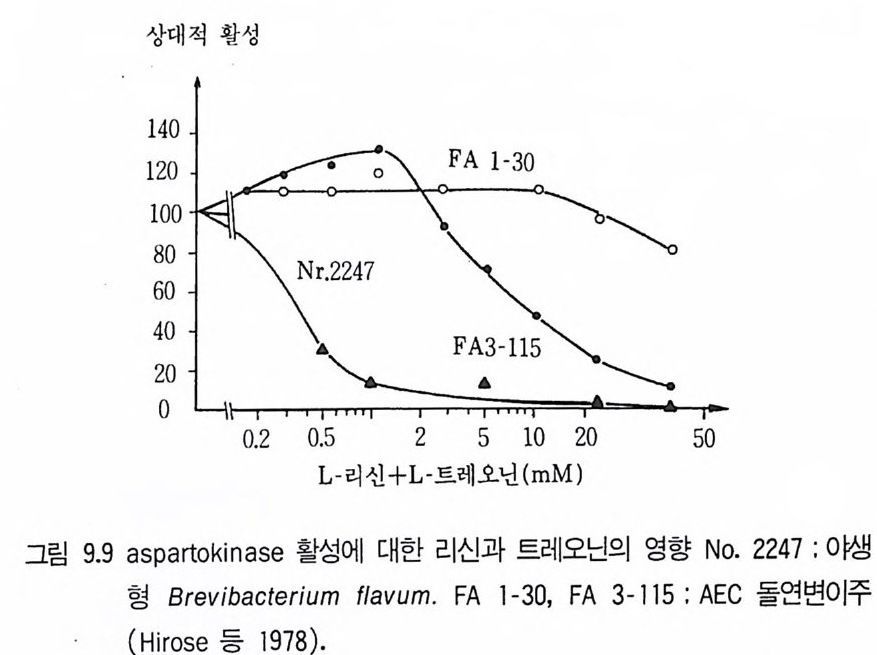 상대 적 활 성
상대 적 활 성
두 미생물 균주 모두 L-트 레오닌에 의한 되돌림저해와 L 페티오닌에 의 한 억제에 의해서 호모세린 탈수소효소를 조절한다. 야생형에서 아스파르 트산 세미알데히드 (as p ar t a t e sem i aldeh y de) 에서 L- 리신까지의 합성과 정은 제어조절 없이 이루어지므로 우량 리신 생산균주는 다음의 세 가지 돌연변이주형으로 분류된다. 1. 호모세린 영양요구성 균주의 경우 , 아스파르트산 세미알데히드에서 트레오 닌으로의 전환이 감소된다. 세포내에 트레오닌 함량이 적기 때문에 리신 생산의 증가에도 불구하고 as p ar t ok i nas 려 여러 되돌림저해는 일어나지 않는다. 2. 호모세린 탈수소효소가 트레오닌에 의한 되돌림저해에 과민한 돌연변이주 에서도 똑같은 효과를 볼 수 있다 . 3. 야생형과 비교해서 AEC 내성돌연변이주의 as p ar t o ki nas ei근 다중 되돌 림저해에 대해 민감하지 않다(그립 9.9).
트레오닌으로의 전환아 되돌립조절로 인해 억제되기 때문에 과다한 아 스파르트산 세미알데히드가 리신 생합성으로- 향하게 된다. 이러한 간단한 조절체계를 통해 리신 생성능이 높은 균주가 몇 가지 돌연변이 단계를 거 쳐 개발될 수 있는 것이다. L-리 신 분비는 눕동수송을 통해 이루어지며 어떤 균주에서는 cadaver- i n~ 로의 탈탄산으로 인해 리신이 손실되는데 이러한 분해는 Cor- y nebac t er i um 이나 Brevib a cte r iu m 균주에서는 일어나지 않는다. (2) 리신의 발효 생산조전 산업적인 생산에서는 탄소원으로 당밀이 주로 사용된다. 아세데이트, 에 탄올, 알칸 등도 사용된다. 질소원으로.는 암모니아 가스와 암모늄염이 사 용된다. 생산균주가 urease 활성을 가진다면 Urea. £ 사용할 수 있다. L- 호모세린이나 L-트 레오닌과 L 페티오닌 같은 성장요소를 첨가해야 하고 콩단백 가수분해물이나 값싼 단백질원이 많이 사용된다. 배지의 바이오틴 함량은 리신 최적생산을 위해 30µg / l 이상이어야 한다. 사탕수수당밀의 바이오틴 함량은 매우 높은 편인데, 만일 사탕무당밀아나 전분 가수분해물 울 사용할 때는 바이오틴을 더 첨가해야 한다. 표 9.7은 여러 가지 탄소원 과 유전적 특칭을 가진 균주로부터의 리신 생산량을 나타내고 있다. 육종한 리신 생산균에 대한 배양조건을 검토한 후 시험공장 규모로- 확 대 배양한다. Breu. lac t o f ermen t u 짜기 리신 생산균은 실험실에서 다음 조 성을 가전 발효배지에서 배양한다. 즉 포도당 130g /l , KH~ PO ., lg/ l , Mg S0 1 • 7H2 0 0.4 g/ l, FeSO. • 7H2 0 2mg / l, (NH 」 )~o 」 25g /l , DL- 양判 0.35g /l , 비오딘 500µg / l, 티아민 • HCl 200µg / l 니코틴아마이드 0.5mg /l , soy meal hy dr olys a te 15ml/l, pH 7.0. 발효는 소형 시험관, Erlenmeye r flas k, 소형 발효조 배양의 순으로 확대 배양하고 온도 32°C 에서 30~7 이간 배양한다. 소형 발효조를 사용하여 리신 발효를 수행한 결과, 4 V-]간 후 L- 리신 HC 툐. 60g /l 생산된다 (Tosaka, 1986).
표 9.7 각종 탄소원을 함유한 배지에서의 리신 생산 탄소원 균 주 유전적 특 성 기,, 、 국 。 f (g/ Q ) Glucose C. glu ta m i cu m Hom- L eu 34 Glucose C. glu ta m 1cum Hom -L eu- A EC' 39 Glucose B. flau um Thr-, Met 34 Glucose B. lacto f e rm enlum AEC'Ala- , C CL' ML' 60 Glucose B. flau um F 1-30 AECr 57 Aceta t e B. flav um Hom kaky T hr - 75 Et ha nol B. lacto f e rm entu m AEC 『 66 n-Alkanes(C,i - C 짜 Nocardia AECr 29 alranogl u ti no sa
최적의 배양조건은 사용하는 원료, 미생물에 따라 다르다. 공업 규모의 리신 생산은 탄소원으로서 전분당화액이나 당밀을 사용하고 고농도 리신 축적을 위해 배양 도중에 당질의 공급이 행해지는데, Sh i v i nka(1980) 에 의하면 자당농도가 12% 이상이면 리신 생성이 저해되고 5% 이하로 당농 도를 유지하는 것이 고수율을 울리기 위해 중요하다고 보고 있다. p H 는 암모니아 가스를 공급하여 배양중 6 . 5~7.5 로 유지하고 첨가한 암모니아나 암모늄은 질소원으로 이용된다. 통기교반은 고수율에 매우 주요한 요인으 로서 최대의 리신 생산은 균의 호흡이 충분할 때 가능하고, 산소전극예 의 해 PL~O.Ola t m 이 되게 조절할 때 만족할 만한 발효 성적을 거둘 수 있 다. 즉 리신 생산에 최적의 산소충족률 (Yab/KrM) 은 1.()0]며 0.3 이하 에서는 젖산이 생성하기 시작한다. 6.3 L- 트립토판 (L- t r ypt o p han) 의 발효 생산 트립토판은 화학합성법이나 화학적으로 합성한 중간산물의 발효적 혹은 · 효소적 전환을 통해 생산된다. 트립토판 생합성의 조절 메커니즘은 복잡하
여 최근에 이르러 완전한 발효공정이 개발되었다. (1) 중간산물의 발효 전환 완전한 화학합성방법 이외에 중간산물의 발효전환방법도 L-트 립토판을 샨법적으로 생산하는 데 이용된다. 가장 중요한 방법이 표 9.8 에 나타나 있댜
표 9.8 전구체를 전환하는 방법에 의한 트립토판 생산 균주 전구체 사용량(g/ Q ) 수율(g/ Q ) Hansenula Anth r an ili c acid 4.2 5.7 anomala Bacil lu s subti lis Anth ranil ic acid 5.0 5.5 (Anth r anil a te - ) Candid a uti lis Anth ran ilic acid 4.2 6.4 Clauic ep s pu rp ur ea Indole 1.3 1.5 Escheric h ia coli Indole+DL-S er in e 3.0 5.2 Bacil lu s subti lis Indole 6.0 10.4 (MT') (MT' : resis t a n t to meth y lt r y ptop h an) (Terui, 1972 : Ki no shit a and Nakay a ma, 1978)
전분가수분해 산물이나 당밀을탄소원으로 사용하고 sug ar / NH1N03- 용액을 첨가하여 배양 후에는 an t hran i la t혀춘 첨가한다. (2) 트립토판의 효소적 생산방법 표 9. 快근 L-트 립토판의 효소적 생산방법이다. 이 방법은 화학합성에 의해 유도된 히단토인 (h y dan t o i n) 화합물의 라 세미 혼합물을 분리하거나 중간산물을 생물학적으로 사용하여 트립토판 합 성효소를 포함한 연속적 공정으로 개발되었는데, 재조합 DNA 기술로서
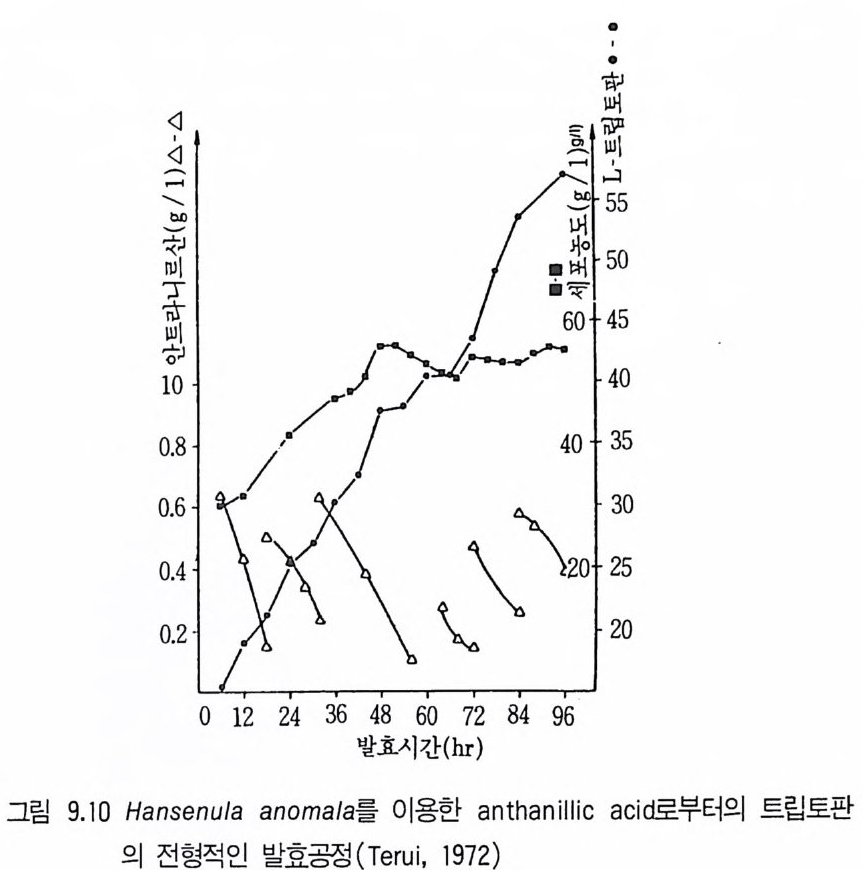 ••’
••’
표 .9.9 L- 트립토판 생산을 위한 효소학적 방법 (Sh ii o, 1986) Enzy m e Orga n is m Reacti on D-Tryp top h an hy da nt oi n recemase Flauobacte r iu m DL-Tryp top h an hy d ant oi n + H2 0 --+ L-Tryp top h an hy d ant ion hy d rolase ami no ge n es L-Tryp top h an+C02+ NH3 N-C a rbamoy l- 1-tr y p top h an hyd r olase Tryp top h anase Prote u s rellge r i Indole+Py ru vate +NH:1 ➔ L-Try ptop h an+H2 0 Indole+L-S e ri ne ➔ L-T r yp top h an+H2 0 Tryp top ha n sy n th e ase Escheric h ia coli lndole+L-S e rin e ➔ L-Try ptop h an+H2 0
대장군기 트립토판 합성효소 활성을 23Q li~ 증가시켰다. 이 효소의 추출물 에 인돌(i ndole) 과 세린 (ser i ne) 을 첨가하면 트립토판이 78g / l 생산되면 서 97~100% 의 전환율을 갖게 되나 수율이 너무 높아서 트립토판의 일부 가 침전하게 된다. (3) 직접발효공정 (Shii o, 1986) 위에서 언급한 공정은 비싼 재료를 필요로 한다. 그러나 경제적 인 탄소 원을 사용한 직접발효를 통해 트립토판을 생산하기 위한 연구가 진행중이 다. 표 9.lQ .g-트 립토판을 분바하는 균주와 유전학적 특성을 나타낸 것이 다.
표 9.10 포도당의 직접발효법에 의한 트립토관을 생산하는 돌연변이주 균주 유전학적 특성 수율(g/ Q ) Bacil lu s subti lis 5FT', Arg -o r Leu- 6.2 Breuib a cte r iu m flau um 5FT', PFP' Phe -T ry - 10.5 Cory n ebacte r iu m Phe -T y r -SMT' 12 glu ta m i cu m Tr p Hx 『 6FT' 4MT' PFP 『 Px-115-97 PAPr Ty rH x'PheHx' Resis t a n ce : 5FT 5-flu o rotr y ptop h an : PFP p-fluo ro-ph eny la lanin e : 5MT 5-meth y lt r y p o to p h an : TrpH x Try : 6FT 6-flu o rot ry ptop h an : 4MT 4-m e th l tr y p r op h an : PAP p-a m ino p h eny la anin e : Ty rH x Ty ros in e hy d roxamate :. P heHx Pheny la lanin e hy d roxamate . Auxotr o p h y : Arg arg inine : Leu leucin e : Phe Pheny la lanin e .
그림 9 .1 1 의 트립토판 생합성 경로는 많은 미생물에서 발견되고 있으며 각각의 균주에서는 조절상의 상당한 차이가 있다. 예를 들자면 Cory n ebacte r iu m g lu t am i cum 에서는 트립토판 생합성이 DAHP 합성효소와 ant h ranil a te 합성효소의 활성에 의해 조절된다. ery-
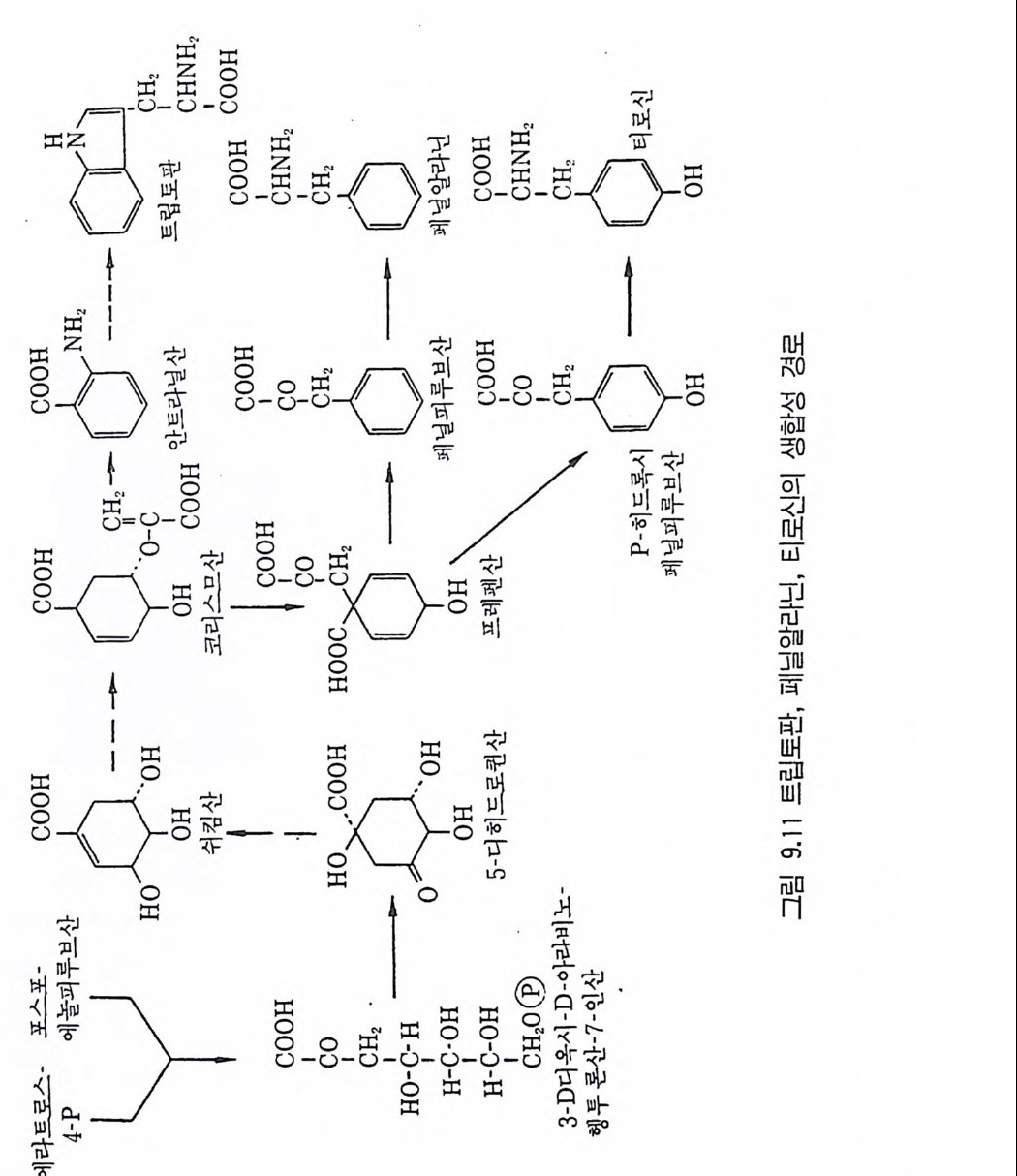 —:[ooe— 广HeH :〈一DN凡o CIC c 산凡 _〉- o C2H\H H판토트 I립 OH 2HNCHO。 H 산I HOH OC三 산lH]C'cICCH0 H O 晶0 o臨 0P 宁1닐 皇比O〈' — 一길 〉O산브 퀸 》 IoC꾹1Ho1 I年 백떠 :CH __ o 〈 시신로' 3 산 O O OH H로 경 성의합생 신로티 1.1 ,닌9닐페판토 : O
—:[ooe— 广HeH :〈一DN凡o CIC c 산凡 _〉- o C2H\H H판토트 I립 OH 2HNCHO。 H 산I HOH OC三 산lH]C'cICCH0 H O 晶0 o臨 0P 宁1닐 皇比O〈' — 一길 〉O산브 퀸 》 IoC꾹1Ho1 I年 백떠 :CH __ o 〈 시신로' 3 산 O O OH H로 경 성의합생 신로티 1.1 ,닌9닐페판토 : O
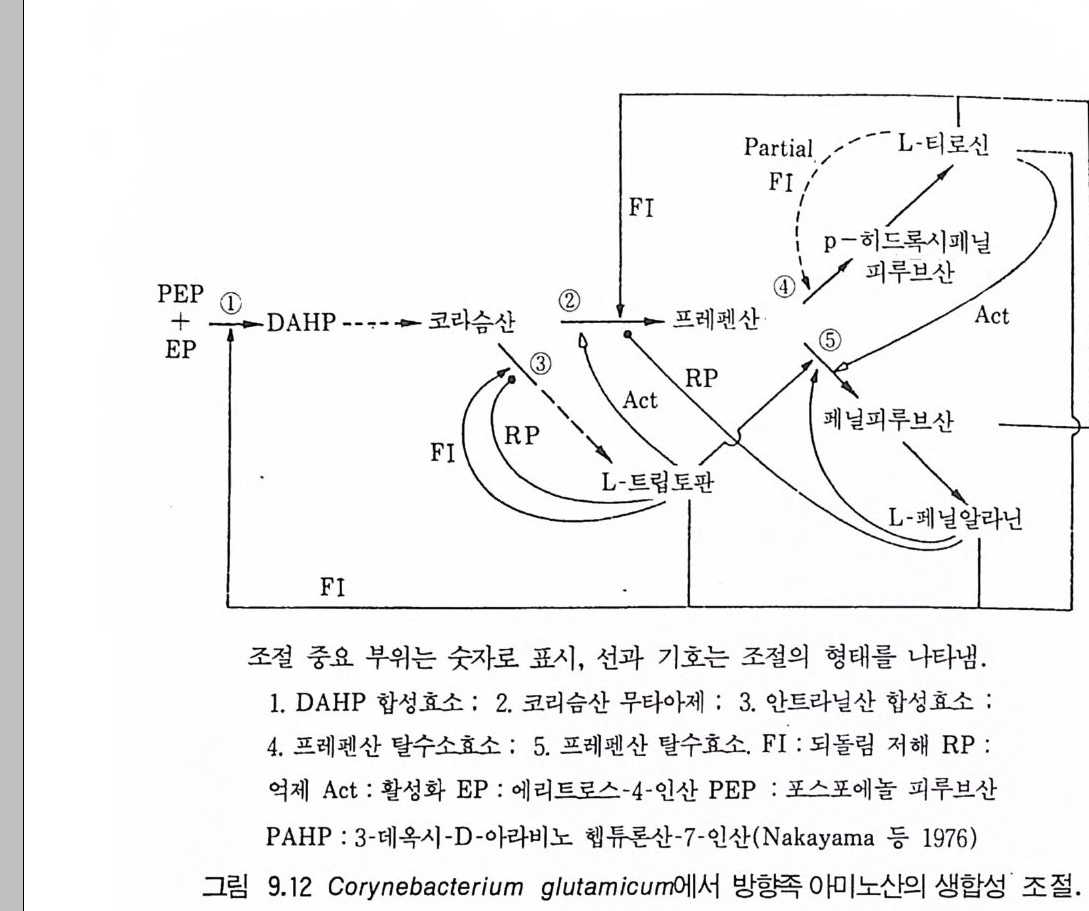 +pEpE P® _f D A H P \ ® \ F[pal
+pEpE P® _f D A H P \ ® \ F[pal
t hrose -4 -P 와 pho sp h oenol py ruva t려 축함을 촉매하는 DAHP 합성효 소는 페닐알라닌과 티로신에 의한 합동 되돌림저해를 나타내는데 트립토판 은 저해롤 증가시켜 세 가지 아미노산이 모두 존재하는 하에서는 DAH- P 합성효소 활성이 90% 까지 억제된다. 합성경로 분기점 이후의 트립토판 생합성 경로의 첫번째 효소인 anth r anil a te 합성효소는 Ls트 립토판에 의 한 되돌림저해와 억제를 나타낸다. C.g lu ta m i cu m Px-115-97 의 DAHP 합 성효소는 페닐알라닌과 티로신에 의한 조절에 매우 민감하다. 조절 메커니 즘의 효과뿐 아니라 생합성 사슬의 개개의 효소 활성에 의해서도 최대 생 산량이 결정된다. 조철기전과 효소의 비활성을 바꿈으로써 수율 증가가 기 대된다.
참고문헌 Aid a , H. et al. : Ami no acid Fermenta t i on , 197. P( 1986) . Fukumura, T. : Ag ri . Bi ol . Chem. 41. 1321(1976). Hagi no , H. : Ag ri . Bi ol . Chem. 39. 345(1 9 75). Hi ro se, Y. and H. Okada, M icr obia l pro duc tion of ami no acid s , pp. 211~240. In : Pep ple r, H.J and D. Perlman(eds), Mi cr obia l tec h- nolog y, vol. I, 2nd edit ion . Academi c Press, New York(1979). J. Jo fr e and R. Pares : J. Bacte r io l ., 138. 721 .(1 979). H. Kaneko and K. Sakag uc h i ; Ag ri c . Bi ol . Chem. 43. 1007( 1979) . J. Kanzaki and H. Fukuda ; Ag ri c . Bi ol . Chem., 31. 1307(1 9 67). Kats u mata , R : 『 昭和 5 緖度 日本 農藝化學會 要旨 』 . p. 332(1 9 83). R.K ats u mata and A Furuy a : Ag ri c Bi ol . Chem., 48. 2597(1 9 84). Ki no shit a, S. and Nakay a ma, K. Ami no acid s , pp. 209~261 . In : Rose, A.H.(ed.), Economi c mi cr obio l ogy , vol. 2, Academ ic Press, London ( 1978) . K. Kobay a shi and T. Shir o : Ag ri c . Bi ol . Chem., 35. 1241(1 9 71). K. Mi w a and K. Sano : Gene, 39. 281 (1 985). H. Momose and T. Takag : Ag ri c . Bi ol . Chem., 42. 1911(1978). Y. Nakao and M.Doi : Ag ri c . Bi ol . chem. , 34. 1875.(1970). Nakao Y. and M. Doi : Ag ri c . Bi ol . Chem., 36. 490(1972). Nakay a ma, K. Ly s in e and dia m i no p im elic acid , pp. 369~397. In ; Yamada, K., S. Ki no shit a, T. Tsunoda, and K. Ai da (eds.), The mi - crobia l Producti on of ami no acid s . Kodansha, Toky o (1972). Nakay am a, K. J. Ferment, 'Jec h., 56. 425(1978). Nakay a ma, K. Ami no acid ferm enta t i on s. In ; Cong re s int e r nati on al mi cr obio l og ie et ind ustr i e alim ent ai r e , Paris ( 19 79) . Nakay a ma, K., K. Araki, H. Hag ino , H. Kase, and H. Yosh ida , Amino acid • fer ment a ti on usin g reg u lato r y mut an ts of Cor- yn ebacte r iu m glu ta m i cu m, pp. 437~449. In : Macdonald, K.D .(ed.), 2nd Int. Sy m p . Genet. Indust. Mi cr oorg( G IM 74) Academi c Press, London(1976). A.Ozak i and Furuy a : Ag ri c . Bi ol , Chem., 48, 2597(1984).
R.P ares and J.Ja fr e : J.B a cte r io l ., 119. 9(1 9 74). Shii o, I : Ami no acid Fermenta t i on (Ai da ed) P. 349. Kakkai sup a n Cente r , Toky o. Sh iio, I : J. Ferment. 'Iec hnol. 52, 63(1 9 74). J. Shvin k a, U. Vi es t u rs and M. Rukli sh a : Bi ot e c hnol, Bi oe n g., 22, 897 (1980). Sano, K. and J. Shii o. 1971. Mi cr obia l pro ducti on of L-lys in e . N. Selecti on of lys i n e -pr o ducin g muta n ts from Brevib a cte r iu m flav um by dete c ti ng thr eon ine sensit ivit y on halo-fo r mi ng meth od. J. Gen. Ap pl. Mi cro bia l . 17 : 97~113. Tanaka, K., Ki no sh ita, S. : Ami no Acid and Nucleic Acid . 11. 106 (1965). Terui, G. Tryp top h an, pp. 515~531 . In Yamada. K., s. Ki no shit a, T. Tsunoda and K. Ai da (eds.), The mi cr obia l pro ducti on of ami no acid s . Kodansha. Toky o (1 9 72). Terui, (19 72) Ki no shit a and Nakay a ma(1978). Tosaka. 0 : Ag ri . Bi ol . Chem., 43. 1513(1979). Tosaka, H : Amino acid Fermenta t i on (Ai da , ed). Ly s in ferm enta t i on , p. 284. Kakkai Sup pa n Cente r , Toky o (1986). 土田 O : 『特開昭 』 56~82096(1976). 土田隆康 ; 『特開昭 』 56~117795(1 9 76). 土田隆康 中森茂, 百潮春生 ; 『 特開昭 』 56~148295. 土田隆康 中森茂, 百潮春生 ; 『 特開昭 』 56~148296. Yamamoto M. et al. : 『 圖孝工學 艦志 』 50. 876. 884(1972). Tsunda, T., I. Sh iio and K. Mi tsu g i, Bacte r ia l for mati on of L-- gl u- tam ic acid from aceti c aci d in the grow i ng cultu re mediu m .(l) cultu ral condit ion s. J. Gen. Ap pl. Mi cr obio l ., 7 : 18~29(1961).
제 10 장 누클래오티드, 누클레오시드 및 그 관련 물질 1 서론 미생물이 생성하는 누쿨레오시드와 누쿨레오티드는 음식에 맛을 내는 데 널리 사용되고 있다. 중미제 (fl avor -e nhancers) 의 사용은 처음에 일본 에서 발전되었고, 전세계적으로 서용하고 있다. 17 세기초 이래로 일본은 음식에 맛을 내기 위하여 여러가지 물질(곰핑이, 전어물, 해초류 등)을 사 용하여왔다. 190 8\민과 191 3\:遠 이노신산염과 L 글루탐산이 물질의 맛을 내는 성분으로 밝혀졌다. 연구가 진척됨에 따라 디론 몇 가지 성분인 퓨린 계열의 리보누클레오시드 -5 ' - 일인산염이 증미효과가 있는 것으로 밝혀졌다. 효과의 순으로 나열해보면, 구아닌산(g uan y li c aci d) (5'- G MP), 이노신산 (5'- IM P), 크산틴 (xanth y li c acid ) (5-XMP) 문]다. 5 디옥시리보누클레 오티드 (5 ' -d eox y r i bonucleo ti des), 누클레오시드와 피리미딘 누클레오티 드와 같이 5 ' -AMP 와 2 ’와 3’ 이성체 (i somer) 는 증미효과가 없는 물질이 다. 효모 RNA 를 효소로 가수분해하여 5' - IMP 와 5'-GM~ 룹 생산하는 과 정은 195 興에 일본에서 개발되었으며, 1961 년에 상품화되었다. 누클레오 티드 생산에 대한 직접발효과정의 개발로 증미 특성과 5 '- IMP 와 5' -GMP 의 나트뮴 염간의 상승효과 (s y ner gi sm) 의 발견은 또 다른 연구업 적이었다. 누클레오티드계 조미성분인 ~nosin i c ac i d 의 국내 개발은 1972
년 (Bae 등)에 처음 성공하였고 이 직접발효방법은 제일제당(주)에서 공 업화에 성공함으로써 1 97 ()1,빈대 중반 이후 상업적 생산이 시작되었다. 한끼 의 식사에 소비되는 조미료의 양은 0 .1 ~0.2 g인데 여기에는 글루탐산 나트 뮴 (sod i um g lu t ama t e) 과 혼합되어 첨가된 1. 5~2.0 % 의 5 ' -GMP 와 8~ 12% 의 5 ' -IMP 가 함유되어 있다. 이렇게 식품공업에 사용되는 것과 더불어 누클레오티드와 누클레오시드 그리고 이와 관련된 물질들은 의약품의 원료로도 연구되고 있다. 퓨린 유 사체 (8-azag u an ine , 6-merca pt o p ur i ne) 의 항생물질로서의 효과가 검사 되고 있는데, 특히 암의 화학치료요법제로서 연구되고 있다. 9-[J- D-arab i- no fu ranos y laden i n 쑥 인간의 수포진 (herps sim p le x and herps zos- t er) 에 대하여 효과적이다. 2 핵산의 생합성 조절 핵산계 증미성분으로서 대표적인 것은 5 ' -IMP 와 5 ' -GMP 인데 그 구조 는 그림 10 .1에 있는 바와 같다. 퓨린 -5' -리보누클레오티드의 생합성은 리보오스 -5- 인산 (r i bose-5- p hos p ha t e) 과 ATP로 부터 형성되는 5' -포스포리보실피로포스페이트 (5'- p ho-
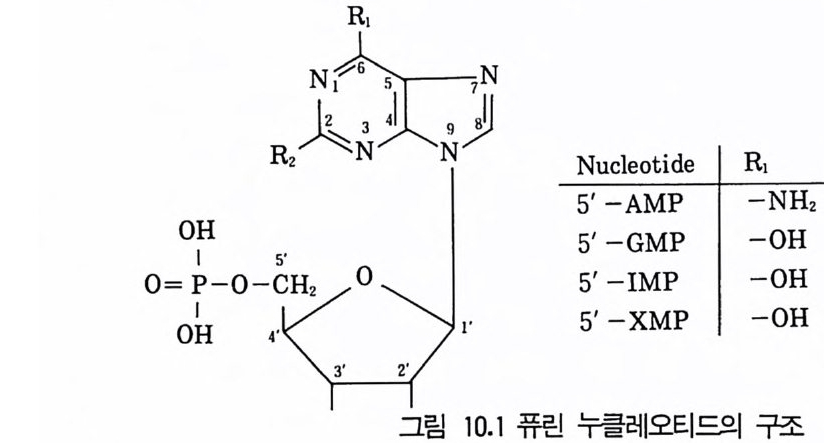 R2 \ Nucleoti de R1 R2
R2 \ Nucleoti de R1 R2
표 10.1 누클레오티드, 누클레오시드 및 관련 물질의 이용가능성 물질 이용분야 5 '-IM P 증미제 ( Flavor enhancer ) 5'- G MP 증마제 ( Flavor enh ancer) Inosin e 심장병 (Heart ail m ents ) ATP 근위축증 (Muscular dy st r o p h y ) CDP-Cholin e 뇌일혈 (S t roke) FAD 간이나 신장병 (Li ve r or Ki dn ey dis e ases) NAD 간이나 신장병 (Li ve r or Ki dn ey dis e ases) Adenin e 백혈병 (Leukop en ia ) Adenosin e 혈관계 결함 (Coromar yde fi c i enc i es) ,협심증 (an gina p ec t or i s) ,동맥경화증 (ar t er i oscleros i s), 고 혈압 (h ig h blood pre ssure) 5'-AMP 순환계 장애 (Ci rc ulati on Problems), 류머티즘 (rheumati sm ) cAMP 당뇨병 (Asth m a), 천식 (Diab ate s ), 암치료요법 (Cancer the rap y), 생화학적 시약 (B i oche mi cal reage n t) Oroti c acid 간장병 ( Liv e r dis e ases ) 6-Azaurid i n e 암의 화학치료요법 (Cancer chemo-th e rap y) (Yamada, 1977)
sp h orib o sy lp y ro p h osp h ate , PRPP) 에서부터 시작되어 몇 단계의 반응 울 거쳐 이노신산 (5 '- IMP) 이 생성되며, 5'-IMP 는 5'- A MP, 5 ' -XMP 와 5 '- GMP 의 전구체가 된다. AMP 생합성은 아데닐숙신산분해효소 (aden yi succin a te l y ase) 의 작용을 포함하며 (그림 10.291 M 단계 ), 이 효소는 H 단계에서 AICARP의 생합성 반응을 촉매하는 이중기능의 효소 (b if uncti on al enz y me) 이다. 한편 IMP 는 XMP 로 산화된 후 (N 반응), 반응 어 거쳐 GMP7~ 생합성된다. 야생형 세균의 퓨린 누클레오티드의 생성과정에서 AMN GMP의 생
성이 과잉일 때는 되돌림조절에 의해서 반응이 억제되든 것이 상례이다 (D. E. At ki n s on et al., 1967).
 ;’: --------• 안PPRRttA P P ABc PFGPGRRAAAPRRP===5= '55 - -5'PP- -hPhP oh ohsosopspsh php oh o h ro -o irb/-3i o b-es Do x y-s-l y grD lll b y- Nocrsi'i n -by Foal a mso ymr im l dpi neyy e lr o:g : lp y hc o i ns pa mh aitdee ::
;’: --------• 안PPRRttA P P ABc PFGPGRRAAAPRRP===5= '55 - -5'PP- -hPhP oh ohsosopspsh php oh o h ro -o irb/-3i o b-es Do x y-s-l y grD lll b y- Nocrsi'i n -by Foal a mso ymr im l dpi neyy e lr o:g : lp y hc o i ns pa mh aitdee ::
특정 대사물질 생산에서는 조절기작이 부분적으로 제거되어야만 한다, 한 가지 접근법은 영양요구성 돌연변이룰 분리하여 필요로 하는 최종산물 울 성장한계농도로 첨가하는 방법인데, 그 결과 되돌림저해 및 억제가 발 생하지 않도록 하는 것이다. 또 다른 접근법은 퓨린 유사체에 저항성을 갖
는 돌연변이주를 분리하는 것이다. Bacil lu s sub ti l i5'°1 l 는 GMP와 AMP 합성의 조절에 몇가지 특색이 있다. AMP 와 GMP의 선구체인 IMP 는 주로 GMP 로 전환된다. 왜냐하면 이 생합성 경로의 IMP 탈수소효소가 아데닐숙신산 (aden y lsucc i na t e) 합성효소보다 10~3 ()llfl나 더 큰 활성을 갖고 있기 때문이다. 퓨린 누클레오티드의 생합성 조절을 보면 IMP 탈수 소효소의 되돌림저해와 억제는 GMP 와 XMP 에 의해 일어나는데, 죽 이 경로의 마지막 효소인 GMP 합성효소는 GMP 에 의해 거의 영향을 받지 않기 때문이다. 이러한 조건하에서 AMP 의 생성이 증가하게 된다. AMP 합성은 제 1 효소(fi rs t common enz y me) 인 PRPP 아미도 전이효소의 되 돌림저해에 의하여 주로 조절된다. GMP 의 조절 효과는 상대적으로 낮은 편이며 예를 들면 PRPP 아미도 전이효소는 0.2mM 의 AM Pt-十 2mM의 GMP 에 의해 50% 저해된다. AMP 생합성 효소인 아데닐숙신산 합성효 소 (Sh ii o, 1979) 와 아데닐숙신산 분해효소는 AMP 에 의해 조절된다. 따 라서 AMP 에 대한 영양요구성 돌연변이주나 AMP 와 GMP 모두에 대한 영양요구성 돌연변이주는 이노신(i nos i ne) 을 축적하게 된다. 이때 아데닐 숙신산 합성효소의 활성이 결핍된 AMP 요구주는 소량의 아데노신 (ade nos i ne) 을 첨가해주어야 하며 AMP와 GMP 에 대한 이중 영양요구성 돌 연변이주는 소량의 아데노신과 구아노신(g uanos i ne) 을 첨가해주어야 한 다. 한편, GMP 의 유사물질인 8 아자구가닌 (8-aza g ua ni ne) 에 내성을 나 타내는 돌연변이주는 구아닌울 축적하게 된다. 3 조미성분 5 ' -IMP 와 5'-GMP 의 생산 누駒]오티드를 생산하는 데는 여러 가지 방법이 있다. 1. 핵산을 분해하는 방법 a. 미생물의 효소를 이용한 효모 RNA의 가수분해(실용화).
b. 세포내 효소로 세포의 RNA 를 분해한 뒤 5' -모 노누 쿨 레오티드 (5 ' -mononucleo ti de) 를 분비하도록 하는 방법 . c. 효모 RNA 를 누클레오시드로 화학적으로 가수분해시켜서 화학적으 로 인산화(실용화). 2. 최종산물에 의한 조절이 제거되어져 누클레오티드 생합성에서 결함을 • 갖는 돌연변이주를 사용하여 칙접발효로 얻는 방법 . a. 발효로써 누클레오시드를 대량 생산하여 화학적으로 인산화(실용 화). b. 발효를 통한 5' -누 클레오티드의 직접 대량 생산법(실용화). c. 누駒 l 오시드의 염기를 5' -누클레오티드로 미생물학적인 전환. 3.1 RNA 의 효소 가수분해에 의한 5 ' -IMP 와 5 ' -GMP 의 생산 RNA 의 분해는 5 ' -누클레오티드를 상업적으로 생산하는 데 이용한 최초 의 방법이었다. 1975년 까지 일본에서 5' -누클레오티드를 50% 만드는 데 이 방법이 사용되었다. 다음과 같은 여러 단계로 RNA 를 분해한다. ® 높은 RNA 함량을 지 닌 효모세포의 배양, ® 세포물질에서 RNA 추출, @ RNA 가수분해에 사용될 효소의 생산, ® 효소를 이용하여 RNA 분해, @ 5' - AMP 에서 5' -IMP 의 생산과 5'-GMP 의 분리 및 정재 (1) RN.A 생산 (RNA pre p a rati on ) 핵산의 함랑은 각 미생물에 따라 다양하다. 세포내 RNA 는 5% 의 mRNA(messenge r RNA), 10~15% 의 tR NA(tr a nsfe r RNA), 75~ 85% 의 rRNA(rib o somal RNA) 로 구성되어 있다. 효모는 상대적으로 DNA 의 함량이 낮기 때문에 가장 좋은 RNA 공급원이 되고 있다. 가장 일반적으로 사용되는 효모는 Candid a u ti l i히며 , 그 다음으로는 Sac- charomy ce s cereuis ia e 7} 이용되고 있다. 효모세포의 높은 RNA 함량은 대
수駒 초]에 특히 배지에 탄소/ 질 소율이 낮을 때 나타난다 (O g a ta, 1963). 효모발효는 일반적으로 아황산폐기울이나 당밀을 이용한 공중보급 (air - lift ) 발효조에서 연속적으로 행해지는데 당밀로 배양할 경우 RNA 향呼 아연이온 (0.25 pp m) 과 인 (0 .1 5 % ) 을 첨가함으로써 증가된다. 이러한 과정을 통하여 생산되는 생체량은 35 g dm - ~ 기며 10% (아황산폐 기물의 경우) ~15%(molasse 의 경우)의 RNA7} 함유되어 있다. 세포가 문, 전조된 후 RNA는 뜨거운 영기성 식염 (5~20% NaCl, 8h, 100°C ) 으로 추출된다. 세포 잔사를 제거한 후 RNA는 HCl 이나 에탄올을 넣어 침전시킨 후 건조시킨다. 분자량이 10,000~15,00~ 범위로 RNA 함량 70~90% 가 되는 조 RNA 제품이 준비되면 효소도 분해과정에 직접 이용 할수있다. (2) RNA 의 효소적 가수분해 (enzym ati c hyd r olys i s )
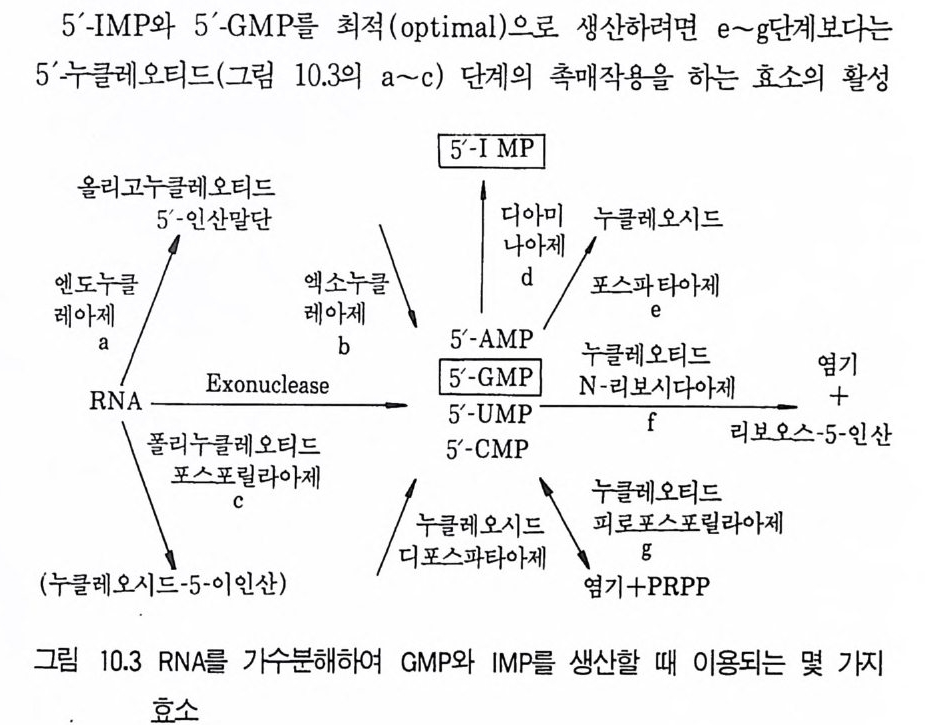 5 '二 -5 '누 -R\I클N'MA레P 오 와雲.티 드5E (' :-x그oC麟 G n림Mu.c P 麟.le. 를1a.~0 s.e 筑 ~최적 ~1a \(~o pc 1t):i巨 m단로al계\판) 으의] 로 \촉 \매생N二-작산 리보용하시려을t:j리면 -하o H는eI ~ 0 효 g소:단의계 5염 보+기활다 인 성산는
5 '二 -5 '누 -R\I클N'MA레P 오 와雲.티 드5E (' :-x그oC麟 G n림Mu.c P 麟.le. 를1a.~0 s.e 筑 ~최적 ~1a \(~o pc 1t):i巨 m단로al계\판) 으의] 로 \촉 \매생N二-작산 리보용하시려을t:j리면 -하o H는eI ~ 0 효 g소:단의계 5염 보+기활다 인 성산는
이 높은 세포를 사용해야 하는데, 그것은 불필요한 물질의 생산을 막기 위 해서이다. Penic il l i u m c it r i num 과 Str ep t om y ce s aureu i!f.근 이에 적합한 효 소를 함유하고 있기 때문에 공업적 수준의 효소적 RNA 가수분해에서는 대부분 이 두 미생물을 이용하고 있다. 한 가지 방법은 Penic il li u m c it r i num 의 nuclease P, 을 가수분해에 이 용하는 것이다 (Kun i naka, 1959). P. c it r i num 의 색소결핍형 돌연변이주 를 30 °C 에서 5 일간 밀기울에서 배양한다. 이 추출액 에는 폴리누클레오티드 ( pol yn u cleoti de )의 3 '-5 '-포스포디 에 스테르 ( 3 '-5 '-p h osp h adie s te r ) 결합 과 모노누클레오티드와 울리고누클레오티드의 3 ' 위치의 3'- 푸人푸꾸_누에스 테르 (3 ' - p hos p homonoes t er) 결합을 분해하는 열에 안정한 핵산 가수분 해효소 R 이 함유되어 있고 분자량 44,00 ()0]다 (Fu ji no t o et al., 1964). 3' -누클레오티드를 만드는 불필요한 p hos p homonoes t erase 의 활성은 열처 리로써 완전히 실활된다. 최적온도가 45°C 인 남아 있는 탈인산 가수분해효 소(p hos p ha t ase) 의 활성 효과를 제거하기 위하여, 2% RNA 용액을 핵 산 가수분해효소 (nuclease) P1 의 적정온도인 65 °c 에서 pH 5. 偉] 조건으 로 4hr. 동안 가수분해시킨다. 이 과정에서 5'- G MP, 5'- A MP, 5'- C MP 와 5'-UMP7} 생성된다. 5'-AMP는 Aspe rgi llu s ory zae 의 adeny l dea- mi nas 쩍 의해 탈아미노되어 5 ' -IMP 로 전환된다. 핵산 가수분해효소 R 을 고정화하여 반응시키는 과정도 알려져 있다. 이 러한 효소적 가수분해로 형성된 5' -누클레오티드는 음이온교환 크로마토그 래피에 의하여 분리된다. 또 다른 방법은 Str ep tom y ce s aureu 려서 추출된 핵산 내부 (endo) 및 핵산 의부 가수분해효소 (exonuclease) 의 혼합물로 가수분해하는 것이다 (Omura, 1961). 즉 모든 5'-AMP는 이 세균의 AMP 탈아미노효소에 의 해 5'-IMP 로 탕가미노되기 때문이다. 연구자들은 적당한 돌연변이체를 선 별함으로써 S. aureu 예서 생성되는 효소혼합물 속의 5'-nucleo ti das 惑} 비특이성 알칼리 탈인산 가수분해효소 (alkal i ne p hos p ha t ase) 의 양을 감 소시키려는 노력을 하고 있다. 표 10.2 는 야생형과 비교되는 서로·디른 돌
연변이주의 효소 활 성 을 나타내고 있다.
표 10.2 S. aureus 돌연변이주와 야생형의 효소 생산 비교 St ra in Endonu- Ex onu- AMP 5'- N u cl e o - Alkali ne clea se clease dea m i na se tiJa se ph osp h ata s e Wi ld ty p e 100 100 100 100 100 K-1 310 180 110 160 20 A-5 400 210 150 180 10 S-S 100 80 100 60 10
A-5 돌연변이 주 는 탈인산 가수분해효소의 활성이 뚜렷이 저해되어 있는 최고의 돌연변이주이다. 핵산 내부 가수분해효소의 생산은 전분 가수분해 물 3% , 콩가루 2%, 옥수수 추출액 1% , 그 의 약간의 유안과 M g4김을 함유하는 배지에서 28° C , 3 也]간 동안 진탕배양 (K d =2.72 x 10 一 5 g • Mol- • 02 /atm • min • ml) 함으로써 생산한다 (Yoneda, 1964). 분자량은 16, 000, 등전점은 pH 10.0, 최적작용 p H 는 7.0, 온도는 40 ,C이다. Str - ept om y ce s aur e u 려 6m' 발효의 전형적인 변화 양상이 그림 10 .4에 나타나 있다. S. aureu s 7} 생산하는 효소 중에서 5 ' -누쿨레오티드 가수분해효소 (5' -nucleo ti dase) 의 활성이 매우 높기 때문에 RNA 가수분해는 순차적 가 수분해 조건의 변경하에서 작용시키고 0.5~1 .0% RNA 용액을 pH 7.2 ~8.5 범위에서 42~65°C 1 伊]간 반응으로 가수분해시킨다. 5 ' -GMP 와 5 ' -IMP 의 정제는 활성탄소에 흡착시켜 우선 분리한 후 이 온교환 크로마토그래피 후에 메탄올로 각 부위를 침전시키는 과정을 통하 여 행해진다. (3) RNA의 화학적 가수분해와 5 '- IMP 와 5 ' -GMP의 생산 알칼리성 조건 (NaOH 혹은 암모니아액 )하에서 RNA를 화학적으로 가 수분해하면, 5' -누클레오티드가 직접 생성되지 않고 2', 3 ' 시이클릭 포스포
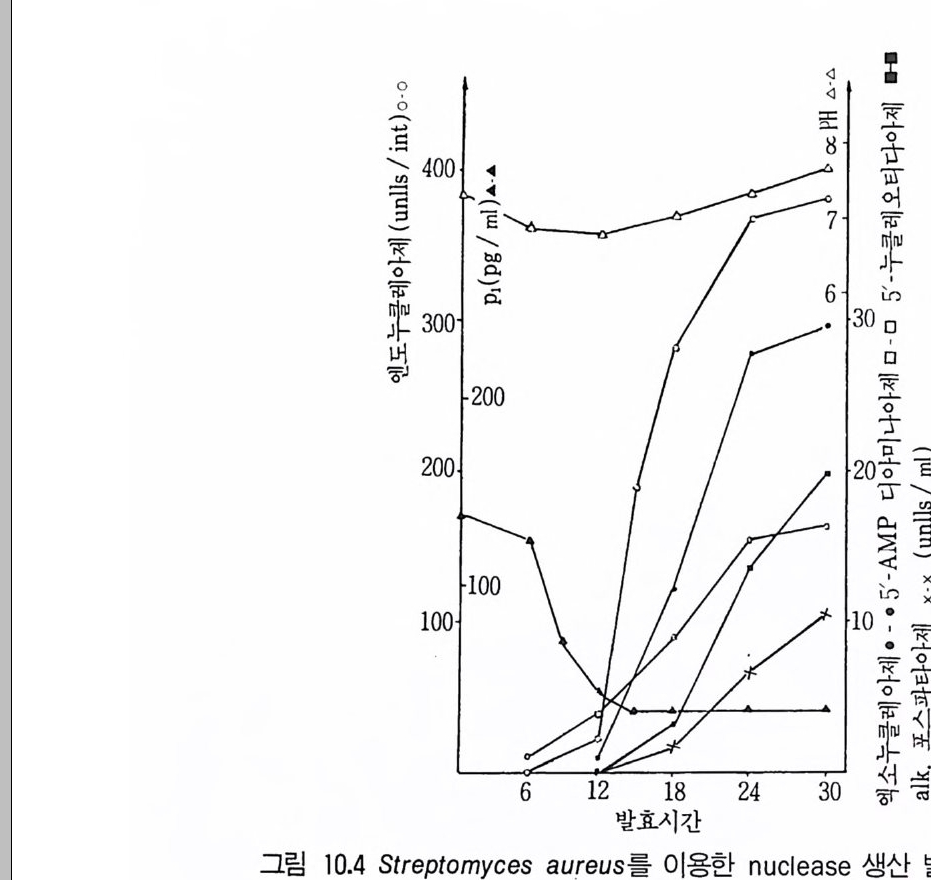 O'0
O'0
디에스데르 (2', 3'- cy c lic p hos p hod i es t er) 를 통하여 2 ' -누쿨레오티드와 3' -누쿨레오티드가 생성된다 (Boulan g er et al., 1951). 그러나 수산화칼슘 (pH 5.0~6.0) 에서 3~ 4'- 1 간 동안 130 °c 의 열을 처리함으로써 RNA 부터 누駒]오시드가 대량 생성된다. 아데노신을 이노신으로 탈아미노시킨 후 누駒]오시드를 인산화제인 쿨로로인산(p hos p hor y l chlor i de) 으로 반응 시켜 5'-IMP 와 5'-GMP 로 화학적인 인산화를 시킬 수 있다. 3.2 직접발효법에 의한 5'-IMP 생산 5'-IMP 는 여러 가지 방법에 의하여 발효적으로 생산될 수 있다.
l. 이노신을 발효 생산한 후 화 학 적 인산 호 H t 통 하여 5' - J MP 를 만든다(실용 화). 2. 직접 5 ' -IMP 를 발효 생산시킨다(실용화) . 3. 아데노신이나 5 ' -AMP 를 발효적으로 생산한 후 화학적 혹은 효소적으로 5 ' -IMP 로 전환시킨다. 4. 화학적으로 합성된 하이포크산틴 (h yp oxan t h i ne) 을 미생물이 이용하여 5' -IMP 로 전환시킨다. (1) 이노신의 발효 생산 세포막은 누클레오티드에 대하여는 두과성이 없지만 탈인산화된 유도체 나 누쿨레오시드에 대하여는 투과성이다. 세포가 5 ' -IMP 를 합성함에도 불 구하고 그것은 세포막을 통하여 분비되지 못하지만 세포에 의해 탈인산화 되면 분비될 수 있기 때문에 이노신은 배지에 축적될 수 있다. Bacil lu s sub ti li s 의 경우에는 PRPP 아미도 전이효소에 대한 AMP와 ADP 의 . 조 절 효과 때문에 세포의 아데닌 누쿨레오티드의 함량은 IMP 를 생산하는 데 있어서 낮은 농도로 유지되어야만 한다. 이것은 AMP 생합성에서의 차단을 통해 성취될 수 있다 (SAMP 합성효소를 제거 ). 누쿨레오티드 가 수분해효소 활성의 저하, IMP 탈수소효소의 결핍, 혹은 5' -누쿨레오티드 가수분해효소 활성의 증가 등은 이노신의 축적에 좋은 조건이 된다. 이노 신을 생성히는 미생물은 아데닌 요구주로서 Bacil lu s, Breuib a cte r iu m , Cory n ebacte r iu m , Str ep tom y ce s, Saccharom y ces4r 이 며 , Bacil lu s subti lis , Breuib a cte r iu m ammonia g e n es, Mi cro bacte r iu w l} 같은 균주들은 표 10.3 에서와 같이 상업적인 생산울 위해 개발되어왔다. Bac i llus 의 전형적인 발효과정에서 탄소원으로 전분 가수분해물이 가장 일반적으로 사용되고 있으나 포도당도 사용될 수 있다. 건조효모와 조 RNA는 아데닌원으로 배지에 공급되고 히스티딘은 Bac i llu 예 균주에 매 우 효과적이다. 암모니아는 p H의 조절과 질소원의 공급, 두 가지 목적으 로 첨가된다. 최적 p H 범위는 6.0~6.2 이며 최적온도는 30~34°C 이다. 최
표 10.3 이노신산 발효에 이용되는 돌연변이주 돌연변 01 주 유전 특성 lnosin e 생산 (g/ l) Bacil lu s subti lis St ra in No. 2 Ade 0.21 B-4 Ade-Hi s 4.4 6 c-30 Ade- H is- T y r- 10.5 RDA-16 Ade-Trp - R ed- D ea- 18.0 8AGr Brevib a cte r iu m ammonia g e n es KY 13714 Ade-6 M G' Gua- 13.6 KY 13761 Ade - 6MG'6MTP 『 Gua - 30.0 Mi cr obacte r iu m sp. No. 250 B i o-6MP 『 8AG MSOr6TGr 35.0 Auxot ro p h y :A de Aden ine : Bio Bio t i n: Gua Guanin e :Hi s Hi st i di n e : Ty r Ty ro sin e : Trp try p top h an : Red- GMP reducta s e is absent : Dea-A MP deami na se is absent. Resis t a n ce : 8AG 8-Azag u an ine ; 6MG 6-Mercap -tog u an ine ; 6MTP 6-Meth y lt h iop u rin e : MSO Meth i o n in e sulf ox id e ; 6TG-Thio g u an ine ; 6MP 6-Mercap top u rin e (Furuy a, in Og a ta et al., 1976)
대이노신 축적은 Kd=5.8~7.0 X10-6g • Mol • 02 /a tm • min • ml 의 산 • 소전달속도 (ox yg en tra nsfe r coe ffi c i en t)로서 얻어질 수 있다. 동시에 배지의 이산화탄소 함량은 낮아야 한다. Breuib a cte r iu m ammon i a g ene 려 이노신 발효 추세가 그림 10.5 에 설명되어 있다. pH 11 에서 이노신은 배양액으로부터 침전, 여과, 결정화된다. 이노신의 화학적 인산화는 PCb에 트리알킬포스페이트(t r i alk y l p hos p ha t e) 를 사 용하여 수행한다. 불필요한 2'(3')5' -포스포디에스데르 (2'(3')5'- p hos p ho-
d i es t er) 의 함링은 10% 이하로 감소시킬 수 있으며, 이러한 조건하에서 5' -모노에스테르 (5 ' -monoes t er) 의 함량은 90% 이다 (Sh i ba i, 19 78). (2) 5 ' -IMP 의 직접발효 생산 5'-IMP 의 직접발효를 위한 돌연변이주는 다음과 같은 특성을 지녀야 한다.
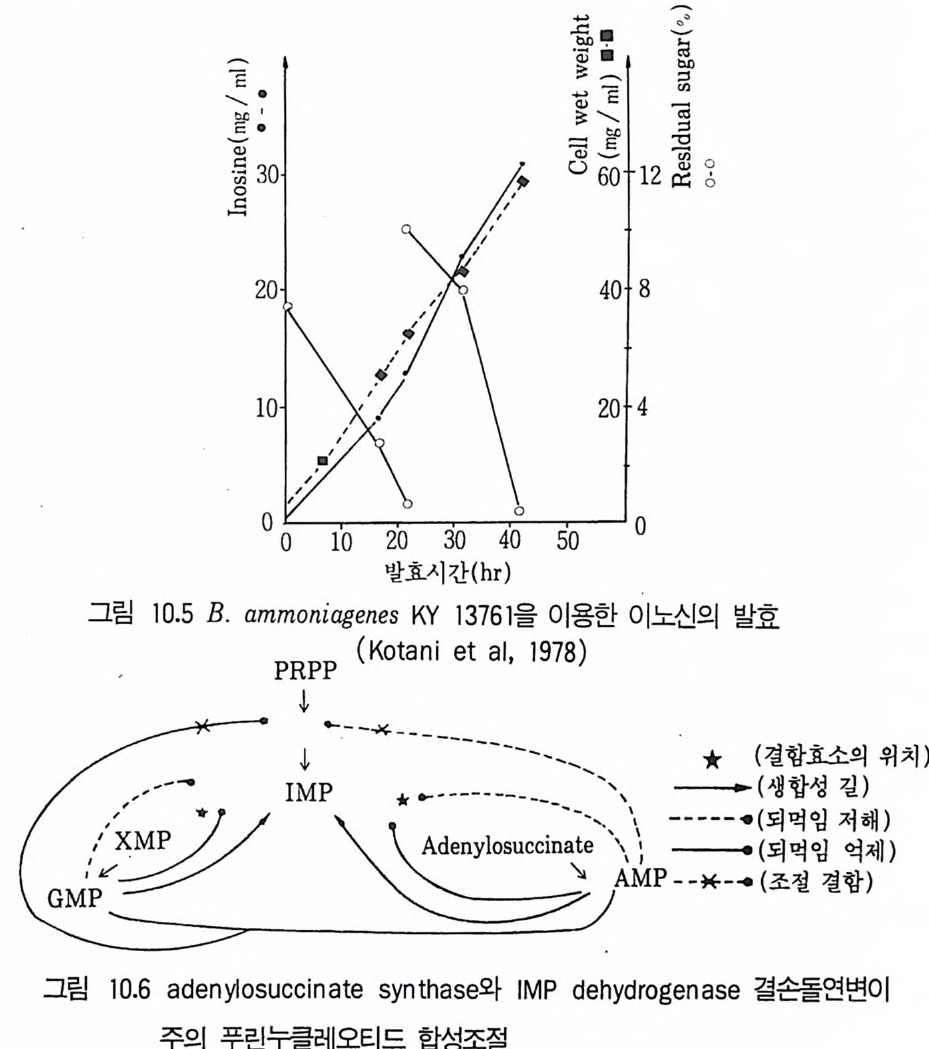 lltuliUl :/(Ul i!S O• U。' • 3 AI-a-1A1동3 .E( 8I.E) 6I , F01 2 ~ sn()o0넓1 1m o0,p 1saH
lltuliUl :/(Ul i!S O• U。' • 3 AI-a-1A1동3 .E( 8I.E) 6I , F01 2 ~ sn()o0넓1 1m o0,p 1saH
1. PRPP 아미노 전달효 소 (am i no tra nsfe r ase ) 수준에서 AMP 의 조절을 제거하기 위한 SAMP 합성효소의 결여. 2. 5'- IM P 분해효소의 낮은 활성 . 3. 5 ' -IMP 가 분비되도록 세포막의 투과성 증가. 누]오티드 가수분해효소의 활성이 저하된 돌연변이주가 이노신을 생 성하는 B. subti lis 중에서 처음 분리되었다. 이 돌연변이주는 아데닌 존재 궁려서는 자라지만 AM 醫回]서는 자라지 못하며 누클레오티드 분해력이 0 芹 낮다. 누클레오티드 가수분해효소 활성에 대한 더 많은 저해는 돌연 변이주 A-1-25 에서 얻었으며, 다른 5'- I MP 생산균주와 함께 표 10 .4에 나타나 있다. 5 ' -IMP 는 공업적으로는 Breuib a cte r iu m ammon i a g ene 폐 의 해 생산되고 있다. IMP 의 축적이 Mn2 + 에 의해 영향을 받지 않는 투과성 있는 돌연변이를 분리한 것은 중요한 진보였다. Mn 2+ 에 예민한 돌연변이 주 KY 720~ KY 13102는 배지 속의 최적 Mn 2+ 함량기 0.01~0.02mg /l 이기 때문에 고농도에서는 IMP 생산이 감소된다 (Furu y a, A., 1968,
표 10.4 5 ' -IMP 를 생성하는 미생물들 돌연변이주 유전적 특성 5'-IMP 산출량(g/l) B. subti lis Ade- N uc- 0.6 A-1-25 Cory ne bacte r iu m Ade-6MP' 2.0 glu ta m i cu m Brevib a cte ri u m ammonin g e n es KY 7208 Ade KY 13102 Ade 5.0 KY 13105 Ade- M n2+ 12.8 ins ensit ive 19 Ade-Aden ine -req uiri n g : Nuc-N ucleoti da se-n e ga t i ve : 6MP 6-Mercap top u rin e -resis t a n t.
1982). 그립 10.7 은 두 돌연변이주의 IMP 축적 관계를 설명하고 있다. KY 13102 균주로 발효시키면 첫 2~3 일간 계속 하이포크산틴이 생산 되지만 IMP 축적이 시작되면서 감소하게 된다(그림 10.8). 제한요소로 Mn 2+ 를 이용하면 투과성이 저하된 비정상적인 세포가 형성된다. 즉 세포
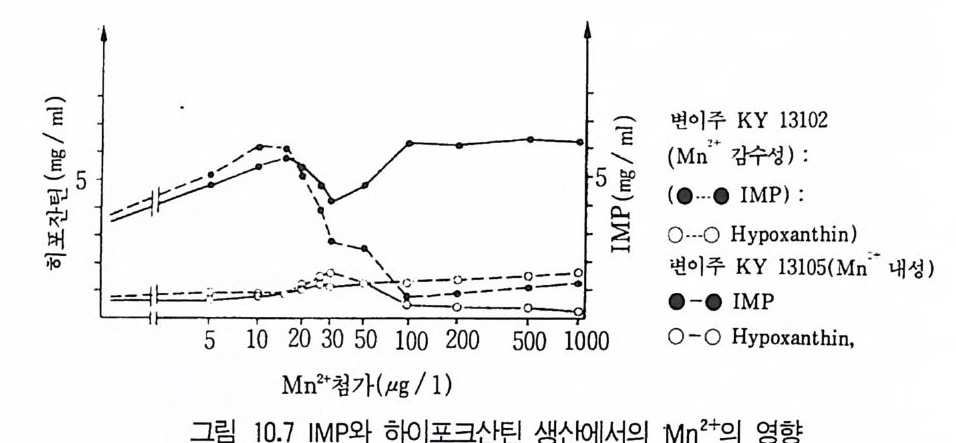 변이주 KY 13102
변이주 KY 13102
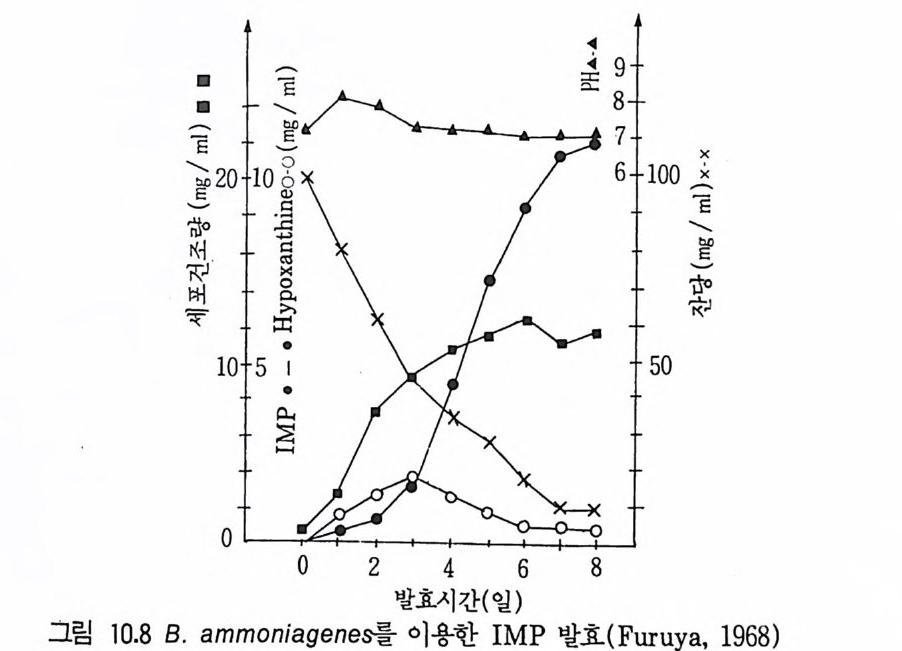 .. (IW/llE) 으{’◄ 9876
.. (IW/llE) 으{’◄ 9876
밖에서 5 ' -IMP 로 인산화될 수 있는 하이포크산틴을 분비하게 된다. 더욱 이 5 ' -IMP 는 뒤이어 일어나는 발효로 새로이 (de nova) 합성되고 배양액 으로 직접 분비된다. 균주개발로 IMP 생산은 20~27 g /l 로 증가되면서 하이포크산틴은 미량만을 생성하는 돌연변이주가 육종되고 있다. B. ammon i ag enes 의 발효에서는 인과 Mg S O~ 농도를 각각 1% 및 2% 정도로 유지하는 것이 중요하다. Mn2+ 비감수성 B. ammon i a g enes 의 배양액 조성은 일반적으로 다음과 같다(g//). KH2PO 』 10.0 : K2HP01 10.0 : Mg SO i • 7H2 0 10.0 : CaC} z • 2H2 0 0.1 : FeSOi • 7H2 0 0.01 : urea 6.0 : cys t e i n 0.02 : th ia m i ne 0.0 5 : nic o t ini c acid 0.05 : Ca pa nto t h enate 0.01 : bio t i n 3 X 10-5 ; MnCL • 4H2 0 0.001 : adenin e 0.04 : glu cose 100.0 : pH 8.3 3.3 5'-GMP 의 발효 생산 야생형 균주는 PRPP 아미도 전이효소, IMP 탈수소효소, GMP 합성 효소 수준에서 대사조절이 되기 때문에 5'- G MP7} 다량 분비되는 것은 드물다. 더욱이 5'-GMP는 5 ' -누클레오티드 가수분해효소나 nucleosid a se 에 의해 분해되어질 수도 있고 GMP 환원효소에 의해 IMP 로 전환될 수 도 있다. 그렇기 때문에 다양한 생산법이 개발되고 있다. 1. AICAR 를 발효한 후 5 ' -GMP 로 화학적 전환시키는 방법(실용화). 2. 구아노신울 마생물 생산한 후 5 ' -GMP 로 화학적 인산화시키는 방법 (실용 화). 3. 크산틴 (Xan thi ne) 이나 5 ' -XMP를 발효적으로 생산하고 5'-GMP 로 효 소전환시키는방법. 4. 5 '-G MP 의 직접발효법 . (1) AICAR 로부터 5'-GMP 생산 AICAR는 5'-GM P-i룬 생산하기 위한 출발물질로서 싱업적으로 생산되
며 퓨린 유도체의 화학적 합성에 대한 출발물질로 이용되 는 5-am i no -4 - im i da zole carboxam i de(AICA) 의 효소적 생산 에 필요 한 중간물 질 로서도 入냄된다. B. subti lis IAM 152 3, B. meg a te r iu m 1AM 124 쩍 Bre- vib a cte r iu m f lavum 은 AICAR 생산균주로서 이들의 퓨린 요구주는 AIC- AR 생성에 중요한 역할을 하며, Ki no sh ita 등 (1967) 은 B. meg a te r iu m No. 366(ATCC 15117) 의 퓨린 요구주가 배지 중에 AICAR 룰 다량 축 적하는 것을 발견하여 공업적 생산에 이용하고 있다. 최적의 발효조건하에 서 이러한 균주들은 80 g /l 의 포도당으로부터 16g / l AICAR 를 생산한다. 이 균주들이 AICAR 를 축적하는 데 적합하게 하는 유전적 특성으로는 ® 균주는 퓨린 요구성이고 AICARP 를 FAICARP( 그림 10.2 참조)로 전환시키는 AICARP fo rm y l t rans f erase 반응이 차단되고 @ AICA-rib - ose 의 가수분해를 일으키는 활성이 없고 @ PRPP 아미노 전달효소를 비 롯한 AICAR 생합성을 촉매하는 효소들이 세포내 퓨린 누클레오티드에 의해 저해 또는 억제되지 않을 것. @ AICAR 분해능이 없을 것 등을 둘 수있다. B. mega te r iu m ATCC 15117 돌연변이주를 사용할 때 탄소원으로는 전 분가수분해물이 이용되며 전체 AICAR 합성의 50% 는 포도당대사가 끝난 후에 일어난다. 최대로 AICAR 을 생성하려면 배지 속에 전조효모나 효모 RNA 와 같은 퓨린 공급원이 최적수준보다 약간 낮은 농도로 함유되어야 하고 적정 KH2 P0 4 농도는 35~40m g /d@서 이때 인산의 과잉첨가는 역 효과를 초래한다. 콩단백질의 가수분해물과 NH4Cl 을 질소원으로 이용하 고 금속염 ( Mg 80 4 • 7H2 0, Fe804 • 7H20, Mn804 • H20 ) 등도 이용한 다. 암모니아가스는 질소원으로서 그리고 p H 조철에 사용된다. B. mega te r iu m 발효 동안의 AICAR 수율은 포자 형성의 과정에 의해 영향받는데, 포자 형성시에는 AICAR 의 생성이 현저히 감소된다. 포자 형 성은 대수기 말기에 부티르산 (bu ty r i c ac i d) 과 계면활성제, 항생제의 첨 가나 산소의 공급을 감소시킴으로써 억제할 수 있다. 발효를 시작한 후 8~1 앙]간 동안 충분한 공기 공급을 하면 포자가 형성되어 AICAR 의 생
소비 저하된다. 그러나 특히 이 기간 동안에 산소의 공급을 적정수준보다 약간 낮추면 포자 형성이 억제되어 AICAR 의 생성이 증가하게 된다. 마지막 단계는 AICAR 를 5 ' -GMP 로 화학적 전환을 시키는 것이다. 생 성된 AICARP 는 탈인산화된 AICAR 형태로서 발효배지로 분비된다. AICAR 의 분리는 몇 단계의 정제단계를 거쳐 90% 수확률로 완성될 수 있다. 5 ' -GMP 로 전환시키기 위하여 AICAR 는 우선 몇단계의 화학적인 과정을 거쳐 구아노산으로 전환시킨 후에 인산화시켜야 하는데 이 방법은 Yamasak i (1967) 에 의해 개발된 것이다. (2) 발효에 의한 구아노신 생산 5'-GMP 생산에 있어서 저렴한 생산공정은 발효에 의해 구아노신을 생 산하고 화학적으로 인산화시키는 것이다. 구아노신을 분비하는` 균주들은 다음과 같은 성질을 갖고 있어야 한다. 1. SAMP 합성효소 결핍 및 GMP 환원효소가 결핍될 것. 2. 누클레오시드 가수분해효소 활성과 nucleosid e ph osp h oryl a se7} 결핍되 어 있을것. -3 . PRPP 아미노전달효소, IMP 탈수소효소, GMP 합성효소와 같은 GMP 생합성효소들이 대사제어에서 벗어날 것. 구아노신을 분비할 수 있는 미생물둘로는 Bacil lu s subti lis , B. pu m- ilu s, B. lich enif orm i s, Cory n ebacte r iu m pe tro p h il u m, C. gua nofa c ie n s, Str ep tom y ce s grise us 등이 있으며 B.sub ti l i s 의 돌연변이주는 이노신 생산 균주이기도 하며 상업적인 생산에 주로 이용되고 있다(표 10.5). IMP 달은효소는 5 ' -GMP 에 의해 조절된다. B. sub ti l i s 의 Ade- Red-퓨 린 유사체 8-aza g ua ni ne 에 저항성 돌연변이주는 GMP 환원효소 활성의 감소뿐만 아니라 원래 균주보다 세 배나 높은 IMP 탈수소효소 활성을 지닌다. B. sub ti l i펴 ps ci co fu r anin e 3 ll- decoy ini n e 3 ll- 같은 핵산
계 항생제에 저항성 돌연변이 주 에 있어서 GMP 합성효소의 활성은 현저 하게 증가된 반면 GMP 에 의한 조절은 완전히 제거되었다. 돌연변이주 MG-1 의 높은 구아노신 생산은 다음의 몇 가지 요인에 의한다. 아데닌 영 양요구성, GMP 환원효소의 결여, GMP 에 의한 되돌림 조절의 결여, IMP 양군―요파 GMP 합성효소 활성의 증가 (Doma i n, 1978) 이다.
표 10.5 구아노신을 분비하는 Bacil lu s sub ti li s 계 돌연변이주 돌연변이주 유전적 특성 구아노신 생산(g/l) B. subti lis AJ 1993 Ad- , Red- , 8AG 4.3 No. 30-12 Ad- T rp - R ed 5 8 AXr MG-1 Ade- H i s- . Red- , 16 MSO' , P si Dec' 표 10.3 참조 . Resis t a n ce : SAX. 8-azaxanth ine Psi. Psic o fu r anin e (GMP 합성 저해제 ) Dec. Decoy ini n e(GMP 합성 저해제) (Furay a , 1976)
3.4 아데노신과 아데닌 누쿨레오티드의 생산 아데노신과 아데닌 누클레오티드의 생산은 의학적으로 중요한 아데닌 유도체의 합성에 이 물질을 출발물질로서 사용하기 때문에 의의를 갖는다. Haneda(1971) 등은 아데노신 생산울 위해서 Bacil lu s subti lis 돌연변 이주 P 53-18(Hi s- T hr- X an-8 AX') 를 분리하였다. 이 균주는 아데노 신 달가미노효소, GMP 환원효소, IMP 탈수표소에 있어서 차단접을 갖는다. 최적의 발효조건하에서는 l6 g /l 의 아데노신이 축적하는데 그 전 형적인 발효양상이 그림 10.9ol] 나타나 있다. 아데노신 트리포스페이트 (Adenosin e tri p h osp h ate , ATP) 는 아데닌이나 5'-AMP의 인산화를 통 해 아세톤으로 건조시킨 빵효모를 이용하여 얻을 수 있다.
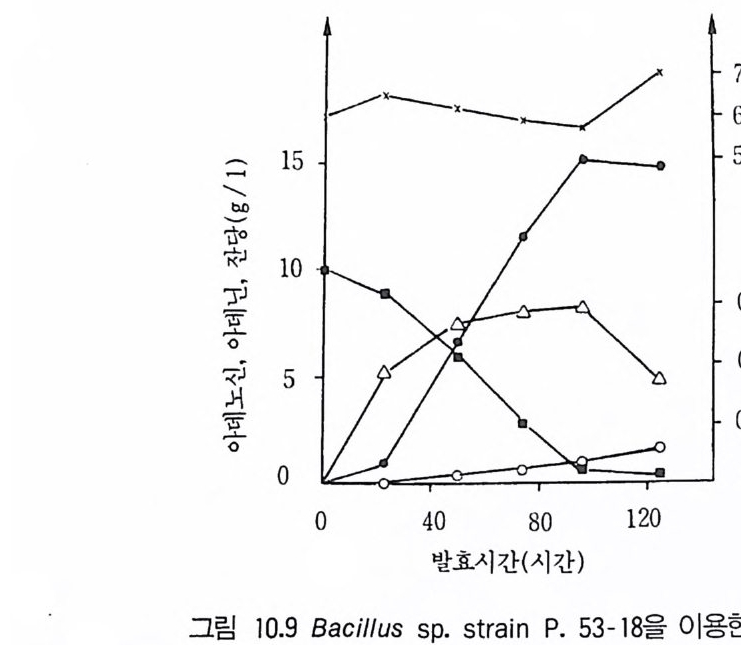 765
765
이 과정에서 아데노신 l g은 1. 6 g의 ATP 나트륨영으로 전환된다. Bre- vib a cte r iu m am 따 on iag enes로 아데노신 유도체로서 1. 57 g Il 의 ATP, 1. 59 g /l 의 ADP, 2 .1 6 g /l 의 AMP7} 생산된다. 환상 아데노신 -3', 5 냐나푸人페이트 (C y cl i c adenosin e -3', 5 '-monoph - os p ha t e)(cAMP) 는 다른 공정으로 미생물 생산이 가능하지만 현재 수율 로는 상품화하기에는 너무 낮다. 포도당 0.3%, 5'-AMP, 그리고 적당한 영이 있는 배지에서 30°C 로 4 앙]간 .11 ic ro bacte r i11 1 11 균주 205-M-32를 키 우면 8.6 g /l 의 cAMP 를 생산할 수 있다. 3.5 누클레오티드 관련 물질의 발효 생산 누클레오티드 관련 물질의 생성은 그러한 물질의 성품시장이 제한되어 있음에도 불구하고 의학적 목적으로 일본에서 발효 생산되고 있다(표 10.1 참조). 이 과정의 생산량과 생산균주는 표 10.6 에 나열되어 있다.
표 10.6 핵산 관련 물질의 발효 생산 소낼 균주 Yi el d(g /l ) FAD Sarcin a lute a 1 NAD Breuib a cte r iu m ammonia g e n es 1.9 Coenzy m e A Breuib a cte r iu m ammonia g e n es 2 IFO 12071 Oroti c acid Arth r obacte r pa raff ine us 20 CDP-c h olin e Saccharomy ce s carlsberge n sis 17 (Og at a et al., 1976 : Hir o se at al., 1979)
Pseudomonas fl uorescen 遷 사용하여 DNA 를 생산하는 것과 B. amm- on i ag ene 로 누클레오시드 울리고포스페이트 (nucleos i de oli go p h osp h ate ) (ppG p ~ ppp G pp)를 생산하기 위한 공정이 개발되어왔으나 이들 공정 의 어느 것도 상업적으로는 생산되지 않고 있다. 춥卜고문헌 At kins on. D. E. and L. Fall : J. Bi ol . chem., 242. 3241 (19 67). Aok i R et al. J. Gen. Ap pl. Mi cr obia l ., p. 387(1963). Bae, M. & K. J. Lee : Kor. J of Mi cro bio l og y. Vol. 10, No. 3, 109 (1972). Boulange r . P. and J. Mont ev il ; Bull. Soc. Chem. Bi ol ., 33, 784(1951) 33, 191 ( 1951 ) . Demain , A. L. Producti on of nucleoti de s by micr oorga nism s, pp. 187~208. In : Rose. A. H. (ed), Prim ary pro ducts of meta b olism , Vol. 2. Academ ic Press, London(1 9 78) . Fuji mo t o. M., Ag r. Bi ol . Chem., 33. 1517(1969). Furuy a, A., S. Abe and S. Ki no sh ita. Producti on of nucleic acid - re7 late d substa n ces by fer menta t i ve pro cesses. XIX. Accumulati on of 5'-in o sin ic acid by a muta n t of Breuib a cte r iu m ammonia g e n es.
Ap pl. Mi cro bia l ., 16 ; 981~987(1 9 68). Furuy a, A. S. Abe and S. Ki no shit a. Producti on of nucleic acid - re-late d substa n ces by fer ment at i ve pro cesses. XX X N. Accumulati on of ino sin e by a muta n t of Breuib a cte r iu m ammonia g e n es. Ap pl. Mi cro bia l ., 20 ; 263~270(1970). Furuy a, A. and S. Teshib a . Producti on of 5'- IM P by mut an ts of Bre- uib a cte r iu m ammonia g e n es, pp. 259~263. In ; Ikeda. Y. and T. Bep - pu( eds). 1982. Geneti cs of ind ustr ia l mi cr oorga n is m s. Kodansha Ltd., oky o( 1982). . Haneda, K., A. Hi ra no. R. Kodair a , and S. Ohuchi. Accumulati on of nucleic acid - relate d substa n ces by mi cr oorga n is m s. II . Producti on of adenosin e by muta n ts deriv e d from Bacil lus sp. Ag r. Bi ol. Chem. , 3 5 ; 1906~1912(1 9 71). Og a ta , K eta l ; Mi cr obia l pro ducti on of nucleic acid relate d substa n -ces, Kodansha Lt d. , Toky o. (1976)._ Kunin a ka A. Bull: Ag r. Chem. Soc. Ja p ., 23. 239(1 9 59). Ki no shit a K. et al. Bi ot e c h and Bi oe ng ., 9. 329(1967). Og at a . K. Ami no acid and Nucleic acid 8.1 (19 63). Kota n i, Y.K . et al ; Inosin e accumulati on by mut an ts of Brevib a cte r i- um ammon iag e n es. Ag r Bi ol. Chem. 42, 399( 1978). Omura. 『일본 특허공보』. 1961~16630. Sh iio I. et al. J. Bi oc hem. 69. 339(1 9 71). Sh iba i H., Enei, H. and Hi ro se. Y. Purin e nucleosid e fer ment at i on s. Process Bi oc hem., 13(11). 6:.....8(1978). Yamada, K. 1977. Bi oe ng ine en ing rep o rt. Recent advances in ind us- tri a l fer menta t i on in Jap an . Bio t e c hnol. Bi oe n g., 19 ; 1563~1621. Yoneda M. J. Bio c hem. , 55. 475(1964). Yamazaki . A. et al. J. Org. Chem., 32. 1825(1967).
제 11 장 미생물효소의 생산 1 서론 공업적으로 생산된 최초의 효소는 곰핑이에서 분리해낸 amy la se tak - ad i as t ase 로서 미국에서는 1894 년에 이미 이 효소를 소화제로 사용하였 다. 191 5년 Ott o Ro e hm 은 〈모든 의류에 적용 가능한 트립신 효소 첨가 세탁법 只t 발표하여 특허를 얻었다. 196 9t;빈에 이르러서는 모든 세탁용 세 제의 8 0 % 에 pro te a se7} 첨가되었다. 이 의에도 pro te a se, lipa se, amy - lase, pec ti na se, ox i doreduc t ase( 산화환원효소) 같은 효소들이 실험적으 로 세제공업에서 이용되었다. 1971 년 세계 생산직 근로자들과 소비자들 사이에서 알레르기 증세가 발 생하여 세제에 pro te a st½ 첨가하는 율이 급격히 감소되었다. 그 후 마이 크로캡슐화 (m i croenca p sula ti on) 와 갑은 특별한 기술이 개발되어 근로자 와 소비자에게 위험이 없고 문제를 야기시키지 않는 pro te a se 제제가 생 산되기 시작하였다. 오늘날 유럽에서 사용되는 세탁용 세제 중 80~90 % 가 pro te a st½ 함 유하고 있다. 전분에서 포도당을 생산하는 데 쓰이는 amy la s~ amy - lo g lucos i das 려 개발로 인해 효소는 새로이 산업적으로 이용되기 시작하 였다. 또한 197 {)1,빈 이후 과당(fr uc t ose) 생산을 위한 glu cose iso merase 샤분] 보편화되었다. 미생물 레닌 (renn i n) 은 두번째 중요한 효소로 1965
범 도위의서건상하조 안에정성/활성 0 006475 10101 9 000 80… ……tiiytg lsbiaptamr nmoue gny titicatipova er mmu一 tip ti s s mutmfOaiem:;=oa x0m%;um:8 온정
적최0 3 의소되효 용는 'Cp 0meT2 tnamufc.era ru 11.1 로으업 적표산 이CE 소효명 균산생 번류호분piitdroceAgni n aAs. e r3e4..1 .23 ii rlM. iM itoba cm.h3en.ee34e6nr2. prtie ulttlNaii23B4. sa.so4be. r3.esun p Tfki iaiAelntim na4oehorBi4re3e14ss.l.2 .c nl. piir Atfleknaiil.o .l4 e . B 3omnn.e14lrscsahi24Ie ygyln- araF3u.a szmaAela 1.2. oe ygiigAsnAdaesmr ceoolu. l3 3.2.1. ytiisBelbmal3ss a2-..a u 1.1.ailBe『cta yitBf arila. iceaiBslaehm -asncln2n3.eo .1.1 gluesallPnau, nee3leobKa sre 1 .41.2. ggp-eaniacuullagn Fs3 Aer9 3 .n2.. 1. g-pitBacatilu lareilca3n se. 31.ssub72B.. pyitrg- Aesza3 soac22adlo3... e1.a -Ptgigioclafai K.ead3 s2rals2s3 .. .1 yg B esloaocXalu5 .ns 5..1.3sea『emosi igpi :BysluresA :Al yl caB ulu : moK sreulK cse M rocuM: nzitfiitp l'armi y'ynot ebn eddcehnosc mesee ooh rsea1-4 21
HP 소범효 의 위는정조상건하에성의 활안/서성정 2 8 4 6pH 01 广·…·………… ••••••••••···••·•··•·••·•••·••·•·· ............. ........... ………………·……………………… ....:-::--: :… yiilbmuats. .. …mtirtopgn ae .1 21로용 산업으적이되생산균 주ammala nmi /peg rrug Almisse moii e cruheM aB uulslsitic bsli /liBcole osimun1h isfcr nBcs la ifihormiuesllci loygire srlpsuAeza ulligines sprAegr liti cualssilubsB linslifoBr miiuhccaesl gllaseeoriel abKs een l/gnigipse usrA er illcBa ltiusis sub gAresp u/ryoizales moresuyiufir lgaceylsK ligirinpsseg ulAe r llicaBf sudi soisstau gcusulila/aco aBns yitiutca eog mumtipa nr 표 CE분번류호 .. 3.1243 .332.4.6 3443.2.. .2 .443.4 4 3.421..1 34.42.1 .1 .2. 13.23 .31. .2.31 1. 21 31...14 .32.1. 3.93.2 1. .3237.1. .3 2.32.1 3 ..232.1 4 4..3.1 1.1 4..31.7 3..35.3. .15一 ID효 명소pPe sni p todrcAeas inei Mlai cirbo nteenr ptaetenu Nlaerorsi plrkonieAtes enlaa i pakAenl lroetinas ei yes-laam a: y,sea- alm yase-alam esla aym-a: Plasu enllauug-nal/sclae luna -gacl/es a-otg/lclaa edsis /asa tog-idseclal nooxdansoMeema ii cua soeGl esoxdi racU sei ysooslXe eraise m년 이후 치 즈 생산에서 송 아지 레닌 대용으 로 사용되고 있다. 197 ?1,빈에 이르러서의 전세계적 효소 총 매싱액 은 1 억 5 0 0 만 달러이었고 1 9 81 년에는 4 억 달러에 달했으며 1 985 년말에 이르러서는 6 억 달러에 달한 것으로 추 정되고 있다. 현재 상업적으로 생산되고 있는 효소들은 다음과 같 다. 1. 공업용 효소 : amy la se, pro t ea se , cata l ase, 이성화효소(i somerase,) pen ic i l li n acy la se. 2. 분석용 효소 : glu cose oxid a se, gal acto s e oxid a se, alcohol dehy d ro- gen ase, hexokin a se murami da se, choleste r ol oxid a se. 3. 의약용 효소 : asp a rag ina se, pro t ea se, lip a ses, str e p tok in a se. 효소의 양을 근거로 보면 산업적으로 쓰이는 효소가 가장 중요하다 (1 년 에 약 l,20~). 분석용이거나 임상(의약)용 효소가 시험공장(pi lo tp lan t) 크기의 발효조에서 생산되는 것에 비해 공업용 효소는 1 2 0m ' 의 발효조에 서 생산된다. 모든 생물이 잠재적으로는 유용효소의 생산자가 될 수 있지만 실제 동 물과 석물조직에서 효소를 추출할 수 있는 수는 제한되고 있으며 아에 비 해 미생물은 짧은 기간내에 대량 배양할 수 있는 이점이 있기 때문에 상 업적 원료로서 가능성이 가장 크다. 생물계의 효소원을 간추려 보면 다음 과같다. l. 식물효소 : 대표적인 p ro t ease 인 파파인(p a p a i n) , bromelain 및 fici n 이 있고 대두에서 나오는 Iipo xy ge nase7} 있다. 대부분의 식물성 효소는 천급수쿠 생산되지만 최근에는 안정제 첨가에 의한 액체형으로 생산되 고 있다. 식물의 재배는 조건이나 기간, 기온에 제한이 있기 때문에 이 둘 효소의 공급은 장기간의 사업으로 행해지므로 국가 정책이 뒷받침되 어야 할 특칭이 있다. 2. 동물효소 : 대표적인 것으로 췌장 트립신과 I ipas 혜t 들 수 있고 송아지 위에서 나오는 renne t가 있다. 이들 효소는 가축 산물이기 때문에 수요 률 충족시키지 못하는 경향이므로 점차 미생물효소로대치되고 있다.
3. 미생 물효소 : 미생 물효소 의 생산이 접차 중 가하고 있는 것은 사실이지만 식품가공에 사용되는 효소는 인가를 얻기 위한 제한이 있기 때문에 사 용되고 있는 미생 물 의 종류는 제한되고 있다. 대부분의 미생물효소는 대략 11 종의 곰핑이, 浜 등의 세균과 4 종류의 효모에 의해 주로 생산되고 있는 것이 현실이다. 효소 이용의 전망은 다음의 분야 개발로 인해 점차 밝아지고 있다. 1. 미생물유전학의 발전, 즉 유전자 조작에 의해 높은 수율을 얻을 수 있다 . 2. 발효조건의 최적화 : 효소 생산 유도, 값싼 영양물질 사용, 배지 조성분의 최적이용. 3. 새로운 세포분쇄법 개발로 세포로부터 효소를 추출. 4. 이온교환 크로마토그래피, molecular-s iev e 크로마토그래피, 친화성 (af- fini t y) 크로마토그래피, 침전법과 같은 현대적 정제과정 개발. 효소의 고정화와 이의 재순환 공정 개발 : 일정 양의 기질을 전환시키는 데 필요한 효소의 양은 상대적으로 크게 감소하게 된다(그림 ll.l). `
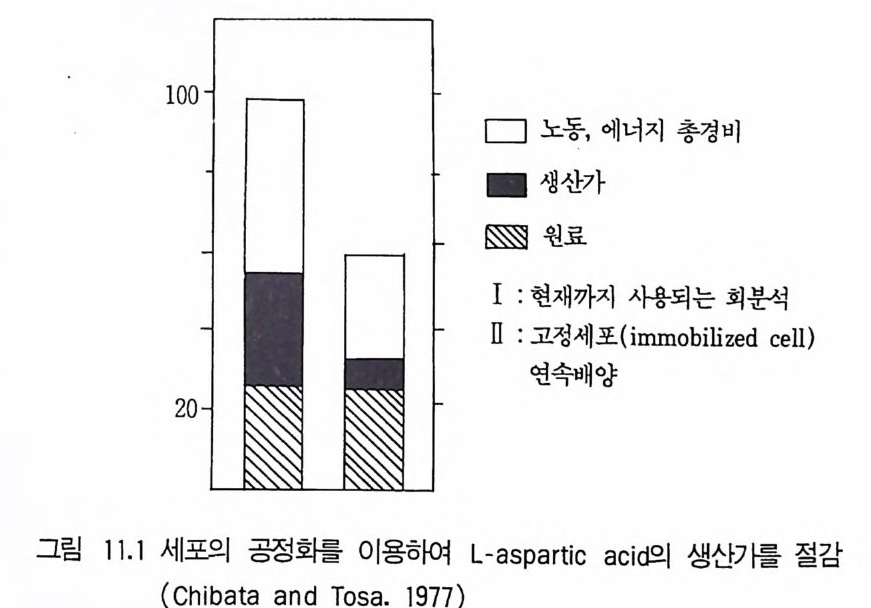 100
100
특수반응기내에서의 연속적인 효소 생산 연속조작을 할 경우, 소규모의 기구을 사용함으로써 새롭게 체제에 두자되는 비용을 국소화시킬 수 있다. 2 전분 가수분해 포도당 중합체인 전분은 가장 널리 이용할 수 있는 식물성 다당류이다. Amy la s~ 전분을 가수분해하는 효소이며 주로 식품공업에서의 감미료 생산에 사용된다. 전분을 amy la se & 가수분해시키면 먼저 호정 (dextr i n ) 이라고 불리는 짧은 사슬의 중합체가 얻어지고 그 다음으로 이당류인 맥 아당 (mal t ose), 최종적으로 포도당이 얻어진다. 포도당은 이성체인 과당보 다 당도가 떨어지므로, glu cose i someras 려운 사용하여 포도당을 과당으로 전흰시킨다. 과당을 이용한 시판용 감미료는 현재 널리 사용되고 있는 설 탕 (sucrose) 보다 경제적이며 제조면에서 이점이 있다. 전분의 당화과정에 서 중요한 효소로는 1-amy la se, fl-am y la se, glu coamy la se, glu cose iso - merase, pu llulanase, i someras 라 있다. 그림 1 1. 2 는 전분에서 이들 효 소의 작용기작을 나타내고 있다.
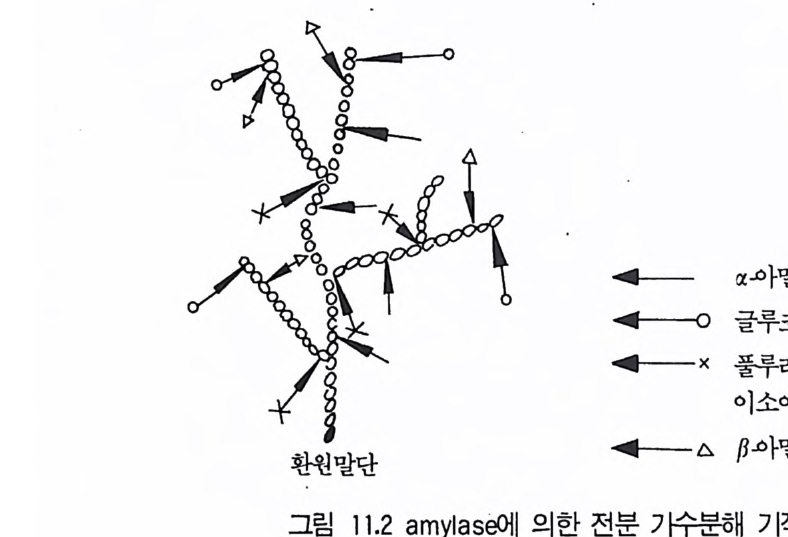 빼 a 아밀라아제
빼 a 아밀라아제
식품공업에서 전분의 가수분해물은 사탕, 제빵, 통조림재품 , 냉동석품을 제조할 때 첨가제로 이용된다. 이때 쓰이는 시럽에는 맥아당이나 포도당 (당화 이후의 ), 과당(이성화 이후)이 함유되어 있가도 하다. 전분 가수분 해물은 맛과 당미, 식품 감촉에 영향을 미찬다. 가수분해물을 생산하기 위 해서는 전분을 먼저 65~ g o·c 에서 풀 상태로 전환시키는데 이 과정중에 20% 용액의 점성이 3,000cen tip o i se 까지 증가한다 .1 2 0~14o ·c 에서 pH 1. 8~2. 懿로. 산처리를 하거나 a-am y las 쵸 1 처리하면 다음 단계에서 전분 이 액화된다. 또 다른 액화방법으로는 산/효소 혼합액화법이 있다. 산처리 법의 단점으로는 일반적으로 포도당 수율이 낮고, 정제비용이 많이 들며, 가수분해물의 질이 저하될 위험이 있는 데다가 장치의 부식 우려 등을 들 수 있다. 그러므로, 일반적으로 산처리법 대신 효소에 의한 액화법이 사용
 옥수수 전분 (40% W/V)
옥수수 전분 (40% W/V)
된다. 용액이 풀로 전환되기 전에 ll0 °C 에서 B. sub ti li s 의 'Y. -am y las 혜卜 첨가하여 액화시킨다. A. n ig er 나 A. ory z aeol] 서부터 나온 'Y. -am y las 여卜 이용할 때는, 이 공정이 55 °C 에서 행하여지며 다른 효소의 첨가가 없이도 맥아당과 malt ot r i o s e 혼합물이 얻어질 때까지 계속 가수분해시킨다. 었 -amy la se½ 이용하여 액화된 전분용액은 중간 정제단계를 거치지 않고도 pH 4.0~5.0, 55~60 °C 에서 g lucoam y lase 에 의해 당화될 수 있다. Pul- luf a nase 나 i soam y las 죠 1,4 결합 의의 결합을 분해하기 위해 이 단계에 첨가될 수 있다. 2.1 ':/.-amy la se :x- amy la se( l,4 a.-gl ucan-gl u canohy d rolase, E.C. 3.2 . l )는 a~l,4 - Glu- cosid e 결합울 가수분해하는 균체 의 (extr a cellular) 효소이다. 이 효소는 분자내로 침투하여 기질을 분해하는 endoenz y me 이다 . 'Y.- 1,6-gl u cosid e 결 합은 이 효소에 의해 끊어지지 않으며 :x- amy la se-9 -l 작용을- 저해하지도 않는다. a.-arriy las ei:근 많은 세균과 곰핑이에 의해 만들어지며, 전분 액화 능력과 당화 효과, 최적 pH , 최적온도, 안정성에 따라 액화형 (liq u efy ing ) '.X- amy la se2 } 당화형 (saccharog en i c) a. -am y las 료 분류된다. 당화형 am y las ei:곤 유리 (fr ee) 당을 만들며, 반면에 전분 액화형 amy - las 눈 전분 중합체를 분해할 뿐 유리당을 생산하지는 않는다. 많은 미생 물동기 여러 종의 a. -am y las 혜t 만든다. :x - am y las 읊 만드는 세균은 Bacil lu s subti lis , B. cereus, B. amy - loliq u efa c ie n s, B. lich enif orm i s, B. ste a roth e rmop h il u s 등 많은 Bacil lu s 속 세균과 Lacto b acil lu s, Mi cro coccus, Pseudomomas, Arth r obacte r, Esc- heric h ia , Prote u s, 'Iher momonospo ra, Serra ti a 속 등이다. 당화형 :x- amy - las 릅 생산하는 매우 비슷한 세 가지 균주는 B. subti lis marburrg, B. subti lis var. amy lo saccharati cu s, B. na tt o 이다. B. am y lol iq ue fa c i en 려
균 주 는 엑화 형 'Y. - am y la s 톄 7 생산 한다 는 점 에서 위 의 셋 과 다 르 다 . 이 효 소가 액화 형 또 는 당 화 형 방 식으로 작 용하는 정 도는 기 질 농도에 따라 결 정된다. 몇몇 'Y.- amy la se 생성 곰 팡 이는 Asp e rg i l lu s ory za e , Asp. nig e r 이의에 Pen i c i lli u m'속 , End o m y ce 흡 , C e p halos p o r i u m'속 , Muco ~ , Cand i d~ 두, Ne uro sp o ra 속 , Rh i zop u~ 에서 찾가볼 수 있 다. 각 a-am y lase 의 분자량 은 매우 유사하다(표 11. 3 ).
표 11. 3 C론· 미생물에서 ..얻 어 진 몇몇 'J. -am y las 莘 1 분자량 미생 물 분자량( X1 0' ) Aspe r g il l u s ory za e 51 ~5 2 Asp. nig e r 58~ 6 1 Baci ll u s acid o c a ldariu s 68 B. am y lo li g u efa c ie n s 49 B. sub til i s 20~100 The rm o m o no s p o ra currua t a 62
이 효소들의 효소단백질 중 상당량이 티로신과 트립토판으로 이루어져 있으며 대부분 안정제로 Ca 2+ 울 필요로. 한다. }am y las ei근 Bacil lu s amy lo li qu efa c ie n s, Bacil lu s lich enif orm i s, Aspe rgi llu s o ry z a 려 의 해 주 로 생산되고 있으며 Bacil lu s am y las~ 근 Asp e rgi llu s am y lasd 다 훨씬 더 광범위하게 사용되고 있다. 이들 두 효소의 가장 중요한 응용분야는 t 포도당, 과당, 맥아당 생산울 위한 전분의 액화, @ 제분, ® 알코올 제조 시 맥아를 당화하기 전에 전분 액화, ® 제빵에서 발효성 탄수화물의 비율 증가, ® 양조에서 액화 및 곡물의 발효성을 증대시켜 맥주 특성을 개선, ® 제지에서 전분의 액화, @ 방직에서 연속적 호발, ® 사료산업에서는 가금, 송아지 사육용, 효소 처리된 보리의 이용율 개선, @ 제당에서는 사 탕수수즙의 전분을 분해하여 즙의 여과성을 증대, ® 세제에서는 전분으로
더럽혀진 세탁물의 세정력 증대, 식기 세칙용 세제의 첨가물 등이다. 2.2 세균 ex-amy la se 생산 세균의 amy la se 생산은 정상 세포의 단백질 합성기구의 기능과 관련되 어 있으며, 이것은 항생물질 첨가 실험의 결과로 밝혀졌다. 만일 B. sub- tilis 7 t ~-am y las 톄 생산할 때 이 균주의 단백질 합성을 저해하는 특정 항생물질을 처리하면, 균체 증식과 amy la se 생산이 모두 중단된다 (Ter ui, 1973). 세포내 효소의 mRNA(E. col i에서는 약 2분 간 안정 )와 바교해서 세포 외 가수분해효소를 생산하기 위한 mRNA 는 생존시간이 매우 길다. RNA 합성을 억제하기 위해 am y las 례卜 생산하는 배양액에 악티노마이산 D(acti no my ci n D) 를 첨가하면 3~ 후에 RNA 합성과 증식은 모두 중 단되나 amy la se 생산은 계속된·다 (Ter ui, 1973). 공업적인 a-amy la se 생 산은 아직 회분식 (batc h ) 발효에만 의존하고 있다. 많은 생산균주들의 효 소 생산속도는 지수 증식에는 매우 낮다가, 증식속도가 감소되고 포자 형 성이 시작되기 직전이 되면 증가하는· 경향이 있다 (Teru i, 1973).
표 11.4 전분 가수분해 효소류와 생산균주 생산 미생물 효소 lUB number Bacte r ia Bacil lu s celeus P-amy la se 3.2.1. 2 iso -a m y la se 3.2.1. 68 B. lich enif orm i s ex-amy la se 3.2.1. 1 B. meg at e r iu m P-amy la se 3.2.1. 2 B. subti lis ex-amy la se 3.2.1.1 P-amy la se 3.2.1. 2 Endo-P-g l ucanase 3.2.1. 6
Fung i Asp . nig e r 1.- amy la se 3.2.1. 1 Glucoamy la se 3.2 .1 . 3 Asp. ory za e ':J.- amy la se Glucomy la se Endo-p- glu canase Penic i ll i u m emersonii Endo-fi-g lu canase 3.2.1 .6 Rhiz o p u s arrhiz u s Rhiz o p u s delemar Glucoamy la se 3.2.1. 3 :x- amy la se 3.2.1. 1 Glucoamy la se 3.2.1 .3 Rhiz o p u s niu e us Endo-p- glu canase 3.2.1. 6 Rhiz o p u s ory za e Glucoamy la se 3.2.1. 3 ::x- amy la se 3.2.1 .1 'Irich oderma reesei Glucoamy la se 3.2.1. 3
요 -am y las 려 생산은 여러 유전자에 의해 조절되며 이러한 유전자들의 특성은 아직 부분적으로만 규명되어 있다. 단일단계 돌연변이는 2~7 배 수 율이 증가되는 반면, 5 단계에 걸쳐 얻어진 돌연변이체는 야생균주보다 약 25 따 수융기 증가된다. 전분은 거대분자이므로 세포에 의해 흡수될 수 없 기 때문에 었 -am y lase 합성을 할 때 유도물질로 작용할 수 없다. 이 경우 소량의 효소성분이 생산되어 배지에 분비되면 이 효소성분이 전분에 작용 하여 저분자량의 유도물질울 생산한다. 이화물질 억제 (cata b olit e re p ress i on) 는 대다수의 균체 의 효소 생산 에서 중요하다. 포도당은 다른 기질과 비교하여 증식을 증진시키나 amy - lase 생산에는 가장 부적합하다. 탄수화물을 제한요인으로 사용하여 연속 발효시킬 경우, 세포 증식은 :<-amy la se 생산에 반비례한다. 과량의 포도당
과 함께 질소 (N) 를 제한요인으로 쓰면 미량의 am y lase 만이 생산된다. amy la se 분자가 매우 크고 친수성이므로 단순 확산에 의해서는 분비되지 않을 것 같다. 즉 효소 분비 에 대한 가장 적 절한 가설은
2.4 glu coamy la se g lucoam y lase( o. -1,4 - g lucan- g lucoh y drolase) 는 전분의 비환원성 말단 (nonreducin g end) 에서부터 포도당 단위로 잘라준다. 맥아당은 매우 느 린 속도로 분해되며, 반면 분기된 다당류내의 1,6 결합은 공격을 받지 않 는다. 그러므로 glu coamy la se 작용에 의한 최종산물은 포도당. 맥아당. 한 계 덱스트린(호정 )이 된다. glu coamy la se 생산에 이용되는 미생물은 As- per gi llu s nig e r, A. ory za e, Rhiz o p u s niu e us 등 주로 곰핌비류이다(표 11.4 ). 사용되는 균주는 A. n ig er와 R. n i ueus 의 돌연변이주이다. 오늘날 g lucoam y lase 의 공업적 발효는 거의 용량이 150m' 에 이르는 액 내배양기에서 생산된다. 과당 시럽 생산에서의 g lucoam y lase 의 이용이 증 가되고 있으므로 액체나 고체의 표면배양을 이용하는 소규모 시설은 비경 제적이다. 그러나 유전자 연구에서는 액침배양에서보다 표면배양할 때 수 율이 더 높은 변종이 자주 분리되고 있다(표 11. 5) .
표 11.5 Rhiz o p u s f ormosaehs i휘 몇몇 변이주의 g lucoam y las 쑥於산 액내 배양 표면 배양(액 체 ) I 표면 배양(고체 ) 균주 (unit s/ 100ml) (unit s/ 100ml) (unit s/ 100ml ) R 13-5 295 2745 I 858 RR 1133-—5 95 91 1549951 33076878 12312620 R 13-59136 4432 7425 5120 (Lin , 1972)
하나의 균주에 의해 여러 가지 glu coamy la se i soenz y rne 이 생산되기도 하는데 이런 효소들은 발효과정중에 변형되는 것 같다. 전분이나 호정 (dex t r i n) 은 효소 생산울 유도하며 효소 생산을 위한 영양액은 일반적으 로 전분을 주로 포함한다. 포도당, 글루타민산, 락토오스는 이화물질 억제
(cata b olit e re p ress i on) 를 유 발 시킨다. 발효기간은 균주 에 따라 3~5 일 정도로 다양하며 발효온도는 28~ 3 5°c 정도이다. g lucoam y lase 에 덧붙여 rx-am y las 죠 동일한 발효공정에서 생산될 수 있다. A. n ig e 뮬- 이용한 glu coamy la se 생산에서는 접종에 사용되는 포 자의 질 이 효소 수율에 영 향을 준다. 맥아 추출물이 든 배지처럼 영양분이 풍부한 한천배지에서 포 자를 생성시키면 새 배지로 옮길 때마다 포자 생성속도는 감소하지 않지 만 glu coamy la se 생성율은 감소한다. 원래 효소 활성의 5 0 % 만이 생산되 지만, 隣 정도 옮긴 경우 접종포자가 최소영양분을 포함한 배지 (Czape k Dox) 에서 만들어질 때는 효소의 생성율이 일정하게 유지되나 포자 생성 률은감소한다 . 2.5 1,6- 글리코시드(g l y cos i de) 결합을 분해하는 효소 a-l,6 결합을 가수분해함으로써 아밀로펙틴 (am y lo p ec ti n) 의 곁사슬을 잘라낼 수 있는 효소는 공업적으로 중요한 위치를 차지하고 있다. 이러한 효소들은 두 가지로 분류된다. 즉 1. Pullulanas~ i soam y las 펙 강] 아밀로펙틴에 직접 영향을 주는 효소 2. 효소에 의해 기질을 변화시킨 후에 간접적인 영향을 주는 효소 Pullulanas 러 i soam y las 눈 아밀로펙틴을 가수분해한다. 더욱이 Pul- lularia pu llulans 곰팡기에서부터 얻어지는 a- g lucan 인 풀루란(p ullulan) 은 p ullulanas 려 의 해 분해된다. 후자의 경우 i soam y lase 에 의 해서는 분 해되지 않는다. 표 11.&g - P-am y las 려 의한 전분 가수분해에 미치는 pu llulanase9 -l 영향을나타내고있다. 대수기의 말기에 Aerobacte r aerog en es ATCC 1505~ 든 배지에 pu l-
lulanas 遷 분비한다. 유도성 균주를 사용할 때는 종전엔 탄소원으로 맥아 당기나 풀루란을 사용하였으나 근래엔 일반적으로 구조 돌 연변이주를 사용 한다. 또 회분식 발효법과 연속배양과정 둘 다 이용되고 있다. Aerobacte r aerog en es 외에 디른 몇몇 pu llulase 생산균주로는 Bacil lu s po lym y x a, Pseudomonas saccharop h ila , Str ep t oc occus. sp. , Str e p tom y ce s sp. 동기 있다. Isoamy la se 생산균주 중에서 Pseudomonas amy lo deramosa7~ 가장 중 요한 균주이며, 그 밖에 Ag ro bacte r iu m , Envin i a , Sta p h yl o coccus, Ser- rati a, Nocardia , Bacil lu s, Pedio c occus, Lacto b acil lu s, Leuconosto c 동] 있다.
표 11.6 Pullulanase 와 fl - am ylase 에 의한 10% 감자 전분의 전환(:x -am y lase 로 전처리시) 과정 형태 맥%아당 포%도당 malto% t r i o s e 덱스O//트0 린 25 unit s P -am y lase/ 전분(g) 65.5 1.1 3.5 29.9 ; 45°C 1 衍]간 10 unit s Pullulonase + 25 un its P-am y lase/ 전분(g) 90.5 0.4 1.2 7.9 : 45·c 1 61-]간 I ( Hay as hib a ra, 1970 )
3 Glucose 1somerase ( Marshall, 1957 ) Glucose iso merase(D-gl u cose ke t o i somerase) 는 포도당을 과당으로 이성화(i somer i za ti on) 시킨다. 이 반응은 가역적이며 포도당과 과당의 혼 합물기 만들어지고, 사용된 효소와 온도 등의 반응조건에 따라 조성비가 결정된다. 이 효소는 설탕 가격이 전분 가격에 비해 상승되었기 때문에 상
업적으로 가치를 지니게 되 었 다. 현재 서방세계에서의 일인당 연간 설탕 소비율은 50k g이다. 포도당과 과당 혼 합물인 과당즙은 1 98 01-;빈 마국에서 감미료 수요의 30 % 에 달했다 . 독일의 과당 생산규모는 10,000~20,00 0-e른 (연간)으로 추정된다 . 전분은 산이나 효소 가수분해에 의해 포도당으로 전 환될 수 있다. 전분 가수분해의 장점은 밀, 옥수수, 카사바, 감자 등 부패 하지 않는 물질을 재료로서 사용할 수 있다는 것이며 직접적인 설탕 생산 에 쓰이는 사탕무는 단지 연간 약 100 일 정도밖에 아용할 수 없다. 포도당은 설탕 (sucrose) 의 70~75 % 의 감미도를 가지나, 가장 단맛이 강한 단당류인 ,8 -o- fr uc t o py ranos e-f픈 설탕보다 감미도가 沙壯나 더 강하 다. 그러므로 과당 제조공장은 상당히 가치가 있다. 과당은 생화학적으로 설탕이나 전분에서부터 얻어질 수 있고 또한 화학적으로는 알칼리성 조건 하에 고온에서 포도당으로부터 만들어질 수도 있다 . 그러나 화학적 방법에 서는 체내에서 대사될 수 없는 psi c o se 같은 부산물이 형성되기 때문에 (그림 11.5 ) 식품공업에서는 과당의 화학적 생산법을 채택하지 않고 있다. 오늘날 이용되고 있는 포도당 이성화효소(g lucose i somerase) 는 실질적 으로 D-포 도당뿐 아니라 D- 리보오스에 대해서도 부가적으로 작용하는. D- 자일로오스 이성화효소 (D-x y lose- i somerase) 이다 . 사용되는 포도당 이성 화효소는 다음과 같은 기준을 갖추어야 한다. 죽 부반응을 피하기 위한 낮 은 최적 pH , 높은 특이적 활성 능력, 높은 최적온도의 조건이 그것이다. 그 의에 어느 정도 다론 glu cose iso merase 활성을 지닌 디른 세균들 로서 , Escherich ia int e r media , E. freu dii , Aerobacte r aerog en es 등이 있 다. 실질적으로 이들 세균에 의해 생산되는 효소는 glu c9se ph osp h ate 전분(밀, 옥수수, 감자) ➔ 가수분해 (효소적 , 산) 一 포도당 glu cose iso - merase ➔ 포도당 : 과당 (60 : 40) iso sy ru p 그림 11.4 과당을 포함한 시럽 생산을 위한 생화학적 방법
D - 포 도당 CCI H- O~ OH H CCI H= ,O O H HOHH- H-C\CC IcIII --- /O0 OH H H HOHH- -_ CCIICC |II _ H - O01 0HHH 一 HHH - -- CCIC CIII -H -一O O~O OHHHH H-CCI H- ,O O \H H HO-CCC’lI H=-,OH O H D-ps i c o se H 一 C_OH I H-C-OH l CH~ O H D- 과당 그림 11. 5 포도당의 화학적 이성화에 의한 과당 생산
표 11. 7 Glucose iso merase lUB number(S.3.1. 5 ) 생산균주 pH tem p ( ·c ) Acti no p la nes mi ss ourie n sis 7.5 60 Arth r obacte r sp. Bacil lu s coa gu lans 8~8.5 60 Str ep tom y ce s albus 7 75 Str ep tom y ce s oli uac eus Str ep tom y ce s oliv o chromog en es 8 63
i someras 러다. 그러나 이둘 효소가 최고활성을 갖게 되는 데 필요한 비 소 (As) 는 석품산업에서 사용할 수 없으므로 이들 균을 공업적으로는 샤용 하지 않고 있다.
3.1 Bac ill us 의 glu cose iso merase Novo 산업은 상업적 용도로 B. coag ulans 에서부터 포도당 이성화효소 를 개발하였다. 이러한 고정화 효소공정 (im mobil iz e d enzy m e pro cess) 은 오늘날 미국, 유럽, 일본, 한국에 있는 많은 공장에서 적용되고 있다. 여기서의 포도당 이성화효소란 주로 자일로오스 이성화효소이기 때문에 모 든 야생균주에 의해 효소 생산을 유도할 때, 자일로오스j} 첨가되어야 한 다. 그러나 자일로요~} 매우 고가이므로 자일로오스를 포함하고 있는 자 일란 (x y lan) 이나 밀기울로 대치되고 있다 . 구조 돌연변이체 (consti tut i ve mu t an t s) 도 분리되어 있다. 이화물질 억제작용은 포도당 이성화효소 생산 을 조철한다. 즉 포도당이 회분식 발효공정이나 연속발효공정 모두에서 억 제물질로 작용한다. 회분식 공정에서 B. coag ulan Si근 대수기 동안에는 효 소를 생성하지 않는다. 배지의 포도.당 함량이 고갈되면 증식은 정지된다. 그 다음 전형적인 d i aux y기에서는 배지내에 존재하는 이차탄소원이 대사 되고 효소 생산이 시작된다. 효소 활성은 2 4J-]간 배양 후에 최고로 나타난 다. 코발트 (Co) 와 마그네슘 (M g)은 야생균주에서 효소 생산울 최고로 높이 기 위한 필수조건이지만 Co 없이도 최적의 효소역가를 나타낼 수 있는 돌연변이주가 분리되었다. 효모 추출물이나 옥수수 침출액 (corn ste e p liq uor) 은 질소원으로 이용될 수 있다. 질소원의 선택이 수율에 있어 극히 중요하므로 각각의 공정에서 질소농도는 최적조건으로 맞추어져야 한다. 포도당 이성화효소 생산울 위한 질소원을 선택히는· 데는 신중을 기하여 ’ 선택하여야한다. 3.2 S t re pt om y ces 의 포도당 이성화효소 Stre p t om y ce s 균주로부터 나온 포도당 이성화효소는 오늘날 회분식 발효 공정 (batc h p rocess) 에서만 생산된다. 자일로오스나 코발트 (Co) 를 필요
로 하지 않는 돌연변이주도 발견되었다. 많은 생산균주의 최적온도는 30°C 生]고 최접 p H 는 pH 8.5 정도의 영기성이다. Mi les 연구소에서 특허받은 변종인 Str ep tom y ce s oliu a ceus NRRL 358M : pH 8. 와 60~70 °C 에서 포도당 이성화효소를 생산한다. 한편 Takasaki 등의 경우는 pH 8.59 -1- 80'C 부근에서 과당 생성량이 최대치에 달하고 있다.
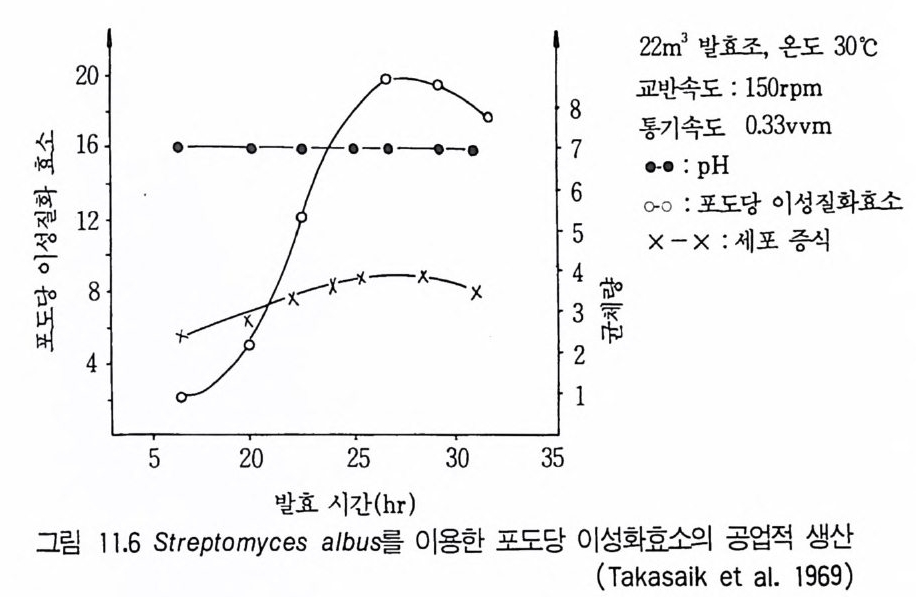 寄~섭어< :o 1162 •_p. ._\. 8675 교통20•x2-반•m기0 -:3속속: px 포발도도H 도 효: : 당세1조05.포 3 0이3온 rv증p성v도r 식nm 질 3화0효·c 소
寄~섭어< :o 1162 •_p. ._\. 8675 교통20•x2-반•m기0 -:3속속: px 포발도도H 도 효: : 당세1조05.포 3 0이3온 rv증p성v도r 식nm 질 3화0효·c 소
3.3 포도당 이성화효소의 고정화(i mmob ili za ti on) 포도당에서 과당을 생산하기 위한 공업적 공정은 효소의 고정화공정이 개발된 후에야 가능해졌는데 그 이유는 효소 고정화공정에서는 동일한 효 소를 여러 번 사용할 수 있기 때문이다. 포도당 이성화효소는 대부분 균주 의 세포내에서 형성되므로, 많은 공업적 공정이 고정화세포를 가지고 행해 지고 있다. Novo 회사에서는 B. coa g ulan 펴 세포현탁액을 교차 결합시 키기 위해 글루타르알데히드(g lu t araldeh y de) 를 사용한다. 교차 결합된 물질은 지름이 0.3~ 1. 0mm 인 작은 과립으로 가공되어 일련
의 연결된 생체반응기에서 연속적으로- 쓰이게 된다. 그림 1 1.7에는 하루에 10 昞의 과당을 생산해낼 수 있는 용량 2.2111' 인 세 개의 반응장치가 두 줄로 이어전 공정이다. 포도당 성분이 93~96% 함유된 전조중량의 40~ 45% 의 포도당 즙 (s y ru p)을 사용한다. 용액은 이성화공정 동안 일어나게 되는 효소의 활성 저하를 막기 위해 먼저 여과, 활성탄 처리, 이온교환 등 으로 정제되어야 한다. M g '+ 이 활성화 물질로 첨가되며 반응은 pH 8.5, 온도 60~65 °c 에서 행하여진다.
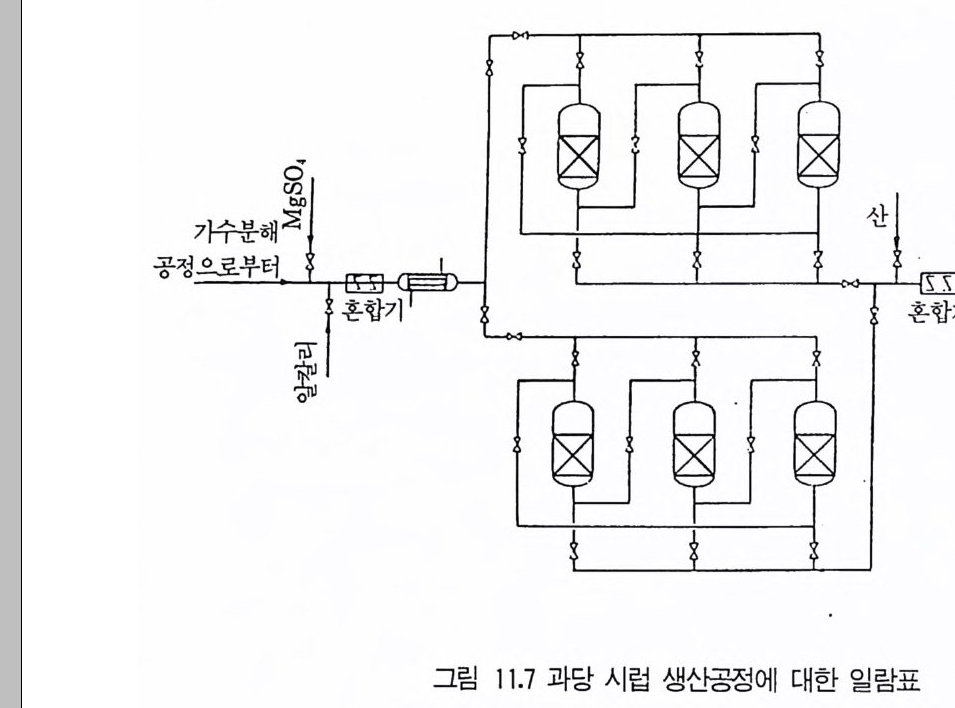 o『
o『
이성화 반응에 소요되는 시간은 0.8~ 心]간이다. 동일한 전환 (c q nver sio n ) 온도에서 회분식 공정 (batc h p rocess) 과 비교할 때 연속공정에서 는 반응시간이 회분식의 20% 정도가 소요되며 용적이 4% 정도인 반응기 를 가지고도 상당히 좋은 산물을 얻을 수 있다(표 11.8 ) .
표 1 i.8 과당 생산에서의 회분법과 연속법 비교 Paramete r s 회분식 공 정 연속전환 공 정 생 물 반응기 용적 75Q m :I 30m ~ 효소소모량 1 7 ~ 2 여 l 아론 Mg SO , • 7H ~ O 소모량 4 . 惡 2 . 2 톤 CoSO 』 • 7H ~O 소모량 2 . 2톤 。 색체 형성 (OD 42 0 nm) 0.05~0.1 0 0~0.02 Psic o se 생성률 0.1 % 0.1 % 정제 탄소처리, 양이온의 탄소처리 음.o l 온교환 7l (Zit tan et al., 197 5)
회수공정에서는 전환된 용액을 먼저 산성화시킨 후 염과 착색물질을 제 거하기 위해 활성탄과 이온교환 수지를 통과시칸다 . 과당 시럽은 이어 약 70 % 용액이 될 때까지 농축시킨 후(건조중량 기준) 식품공업에서는 이러 한 형태로 그대로 이용된다. 2 당류와 3 당류가 포도당 이성화효소에 의해 전환되지 않기 때문에 산물의 조성은 일반적으로 다음과 같다(표 11. 9)
표 11. 9 포도당이원화 효소에 의한 과당 생산에서의 산물의 조성 산물의 조성( % ) 과당(fr uc t ose) 42% 건조중량 포도당 ( glu cose ) 53% 전조중량 올리고당 (ol ig osacchar i de) 5% 건조중량 Psic o se 0.1 % 건조중량 회분 (ash) O.os..:...0.1 % 건조중량 염료가 (d y e value) 0.003 pH 4~5
Escheric h ia coli ATCC 9637 과 Serrati a marcescens ATCC 6(}3 ll- Erwi ni a caro t ouor 려 변종만이 이용된다. 3% 옥수수 침출액, 0.6% 초산
나트륨, 0.2% 황산암모늄이 든 pH 7.09 .l 배지가 적합하며 아때 반응기의 용적은 8cm까 지도 사용가능하다. 16~4 伊 l 간 발효공정 동안 Q 공급이 매 우중요하다.
표 11. 1 0 28'c 소형 발효조에서의 Erwi ni a aro i dea 책 I 의한 L-asp- ara gi nas 핵 생산 차폐장치 교반속도 (r p m) 세포전조중량 L-asp ar gi na se 통풍속도 (vvm) (Baff le) (I mp el ler spe e d ) (g/ 10 1 ) (unit s/ g) 0.5 300 14 960 1.0 + 300 16 580 1.5 + 300 18 340 2.0 + 300 18 230 (Pete r son and Cie g le r, 1969)
발효공정 말기에 이르면 세포는 파괴되어 세포내 효소를 방출한다. 효소 는 인체내에 주사되기 때문에 모든 결정화 과정중에 정제되어야만 한다. 4 Prote a se amy la se 다음으로 중요한 공업 효소는 p ro t eas 쵸i 세제공업과 낙농공 업에서 가장 많이 이용되고, 다른 분야로는 의약품공업, 피혁공업, 단백질 가수분해물질의 생산, 석품공업, 필름공업, 폐기물 처리 등을 둘 수 있다 (Berg, 1976). Prote a se- 2- 심법적으로 세균과 곰팡이에서 생산된다. 이 두 경우의 중요한 차이점은 p ro t ease 의 최적 p H 조건이다. 시판되는 pro - tea se- 2-양 갈리성, 중성, 산성으로 나눌 수 있다. 알칼리성 많은 세균과 곰팡기가 알칼리성 p ro t eas 예卜 분비한다. 가장 중요한 생 磁뱀주로는 B. lich enif orm i s, B. amy lo liq u efa c ie n s, B. cereus, B. meg-
ate r iu m , B. subti lis 같은 Bac i llu~ 과 S. fra dia e , S. gri s e us, S. rec/us 같은 Str ep tom y c e~, 그리고 Aspe r gi llu s nig e r, A. soja e , A. o ry zae 과 같은 곰핑이를 둘 수 있다. 세제에 이용되는 효소는 주로 Bacil lu s 균주에 서 얻어지는 p ro t ease(bac ill o p e pti dase) 이다. 가장 잘 알려진 pro te a se 는 B. li chen if orm i째서 얻은 Subti lis i n Carlsber g와 B. l iq uef ac i en 쩌 서 얻은 Subti lis i n BPN 이다. 이들 효소는 분자내 활성 부위에 ser i ne 이 있고, EDTA 에 의해서는 저 해되지 않지만 DFP(dii so p ro p yl fl uoro p hos p ha t e) 에 의해서는 저해된 다. 이러한 형태의 p ro t eas~ 근 세제용 효소로 사용될 만한 여러 특징을 지니고 있다. 이 효소는 알칼리성 조건하에서 안정하므로, 더 나은 생산균 주를 찾기 위한 선별과정에는 강한 알칼리성 배지를 이용한다. 발효 생산 : 생산균주는 동결전조된 상태나 액체질소하에서 보관한다. 초 기 증식은 30~37°C 의 소형 발효조에서 플라스크 진탕배양을 하여 행한 다. 효소 생산에는 40~100m' 발효조가 사용된다. 세포 의 pro t ea se 생산 성은 주로 배지조성에 의해 조절된다. 질소함유물질에 의해 pro t ea se 생 산이 억제되므로, 회분공정 (fed -batc h p rocess) 을 써서 배지의 암모늄이 온과 아미노산 농도를 낮게 유지시켜준다. 연속공정도 제시되고 있으나 상 업적으로는 이용되지 않는다. 일반적으로 가장 높은 p ro t ease 역가를 얻기 위해 산소분압이 높아야 한다. 통기속도는 lvvm 이며 세균에 따라 발효시 간은 48~7 V.]간으로 다양하다. 건조효소 분말을 흡입할 경우, 알레르기 반응을 유발할 수 있기 때문에 pro t e as~ 세제 첨가 전에 특수한 형태로 가공되어져야 한다. 즉 효소 농축액이 미세 캡슐화된 형태로 시판되고 있다. 적절한 캡슐 제품을 만들 기 위해 효소의 현탁물을 폴리에틸렌 글리콜(p ol y e t h y lene gly c o l) 같은 소수성 물질과 함께 50~70°C 에서 녹여 작은 입자로 가공한다. 이러한 고 형화된 구상입자는 세제에 직접 첨가되어도 무해하다. 앞으로 섬유상 중합 체(fi brous p ol y mer) 로 효소를 고정화시키는 연구도 계속되고 있다. 중성 p ro t eas~근 세균과 곰팡이 모두에서 분비된다. 생산하는 균주는
Bacil lu s subti lis , B. cereus, B. mega te r iu m , Pseu dom onas aerug ino sa, Str ep t om y ce s gri se us, Aspe rg i llu s 01y za e , A. soja e , Peric u laria ory za e 등이다. 중성 p ro t easei근 상대적으로- 불안정하며, 최대 활성을 내기 위해 서는 Zn 이 첨가되어야 하고, 안정제로 Ca '+ 이 필요하다. 효소~ 활성 p H영 역이 매우 좁으며, 온도 증가시 효소 안정성도 매우 낮아진다. 즉 370c 에 서 활성 10 伊모료 할 때 50'C 에서 한 시간 후에는 30% , 60 °c 에서는 80% 이상의 활성이 실활하게 된다. 중성 p ro t easei근 또한 알칼리성 pro te a se 에 의해 빨리 불활성화된다. 이러한 약점· 때문에 중성 p ro t eas 탸근 산업적 으로 적용할 때 제한울 받지만 피혁공업과 제과, 빵, 롤케익을 만드는 식 품공업에서 약간 쓰이고 있다. 산 Aj 치즈 생산에 주로 이용되는 곰팡이에서 얻어지는 renn i n 유사 pro te a se 가 여기에 포함된다. 또한 포유류의 펩신과 유사한 다른 산성 pro te a se.5 :. 시판중에 있다. 이러한 효소의 최적 p H 는 2~3 이다. 대부분의 산성 pro - te as~ 의약품에 쓰이며 Aspe rgi llu s 균주에서 얻어지는 것은 빵을 구울 때 밀 단백질인 글루텐 (whea t g lu t en) 을 분해하기 위해 사용된다. 5 Rennin 옛날에는 치즈 생산을 위해 우유 속에 자연적으로 존재하는 미생물을 우유 카세인에 작용시킴으로써 옹유시켰다. 이러한 미생물들은 유기산 중 주로 젖산을 생산하며, 이 젖산은 p H 를 카세인의 등전점까지 낮추고 유장 (whe y)에서부터 쉽게 분리할 수 있게 카세인을 응고시켜 자연 침전시킨 다. 웅유 생산의 또 다른 방법으로는 영석법이 있으나 거의 이용되지 않고 있으며, 세번째 방법은 열침전법인데 이 방법은 몇몇 공정에서만 이용될 뿐이다. 네번째 방법은 우유 응집효소인 renn i n 을 첨가하는 것으로 오래 전부터 알려져왔고 오늘날까지 가장 많이 이용되고 있다.
현대식 처리과정에서는 s t ar t er 믈 첨가하여 젖당을 젖산으로 바꾸고 p H 를 저하시킨다. 가장 보편적으로 이용되는 균주는 Str ep t oc occus lacti s, S. cremoris , S. the rmo ph il us , Lacto b acil lu s helue tic u s, L. bulga ric u s 등 이다. 균주 선택은 원하는 커드의 구조와 풍미, 발효과정중의 최소가스생 산량, 박테리오파지에 대한 감수성이 낮고 산 (a ci d) 생산량 등에 따라 좌 우된다. R enne t 는 우유 응집효소로서 오랫동안 이용되어왔으나 우유로 사 육된 생후 3 ~4 주가 된 송아지의 4 번째 위로부터 얻은 추출물이기 때문에 공급에 어려운 점이 있다. Rennet 정제한 효소를 rennin , chy ma se, chy m osin ( EC 3 .4 .23. 4) 이라 부른다. 치즈 생산량이 증가되고( 1974 년 전 세계적으로 6 백만 톤이 생산됨 ) 공급난 때문에 196 {)1,빈대 이후, 미생물에 서 renn i n 을 얻기 위한 연구가 집중적으로 진행되었다. 효소 생산체계는 다음 조건을 만족시켜야 한다. 1. 가수분해하지 않고 카세인을 응고시킬 것. 2. 치즈의 향과 구조가 양호할 것 . 3. 불쾌한 냄새를 방지하기 위해 lip a se 활성이 낮을 것. 4. 무독성일 것. 5. 숙성과정에서 쓴맛이 증가하는 것을 방지하기 위해 단백분해력이 낮 을것 많은 곰팡이와 세균이 rennin 생산균주로 분리되어 위의 특성들이 시험 되었는데 가장 중요한 생산균주는 다음과 같은 속이 알려져 있다. Ale- alig e nes, Bacil lu s, Cory n ebacte r iu m , Lacto b acil lu s, Pseudomonas, Ser- rati a, Str ep toc occus, Str ep tom y ce s 등이다. Bac i llu 씁 균주 (B. subti lis , B. po lym y x a, B. mesen t er i cus) 도 시판되고 있으나 상업적으로 성공하지 는 못했다. 우유 응집효소를 생산하는 곰팡이로는 다음의 속들이 알려지고 있다. Aspe rgi llu s, Candid a , Corio l us, Endoth i a , Enth o mop h th o ra, lrp - ex, Mucor, Penic il l i u m , Rhiz o p u s, Scleroti um , Thrulop si s 문]다• 전세
계적으로 rennin 생산에는 이 중 세 가지 곰팡이가 이용되고 있다. Mucor pus il lu s var. L i nd t ➔ 고체표면배양 Endoth ia p aras iti ca ➔ 액내배양 Mucor m i eche i려내배양 Mucor pu sil l u~ 아직 액내배양법에 의해서는 배양할 수 없으며 교반 식 반응조 (s ti rred b i oreac t or) 를 이용할 때도 표면배양공정에서 얻어지 는 rennin 활성의 약 반 정도이다. 더욱이 액내발효공정에서는 pro te a se 와 lipa se 같은 2 차 부산물이 나타나므로 고순도로 청제하지 않으면 이룰 효소제로 직접 사용할 수 없다. 최초로 상품화되어 시판된 renn i n은 Endoth i a p aras iti ca 에 의해 생산 된 것으로, 196?1 1 첫선을 보였다. 이 효소는 산성 p ro t eas 쵸~ pH 4.0~ 5.5 에서 안정되고 분자량이 34,000~37,50 ()o]다. 몇몇 Mucor m i ehe i균주는 매우 유용한 · renn i n 을 생 산하는데 이 효소는 pH 4.5 근처에서 안정하고, 분자량이 38,000~41,80 ()o]다. 미생물에 의해 생산되는 renn i n 은 실제로 온도에 대해 안정하므로 침전 이후에도 커드내 에서 활성상태로 남아 나중에 유해한 단백분해를 일으킨다. 그러므로. 송아 지의 renn i n 을 미생물에 유전자 조작하려는 연구가 진행되었다. 그 결과 송아지의 p rorenn i n 에서 얻어전 상보적인 DNA(cDNA) 가 성공적으로 E. col i내에서 발현되어, 최초로 미생물에 의한 송아지 rennin 효소를 상 업적으로 생산할 수 있게 되었다. 미생물 renne t에 관해서는 Ste r nberg ( 1975) 의 종설이 있다. 6 Penic i ll in acyl a se
의약품에 이용되는 많은 p e ni c illi n 계 항생제가 페니실린의 B- 락탐({] -lacta m ) 고리구조에 연결된 아실 잔기 (ac y l res i due) 를 화학적으로 전환시켜 반합성적으로 생산된다. 화학적 전환에서의 출 발물 질 은 페니실린의 아실화되지 않은 티아 졸 리딘 8- 락탐(t h i azol i d i ne - P - lac t am) 고리구조, 즉 6 아미노 페니실린산 (6-am i no pen ic i ll an ic aci d, 6-A P A, 그림 1 1. 8) 이다.
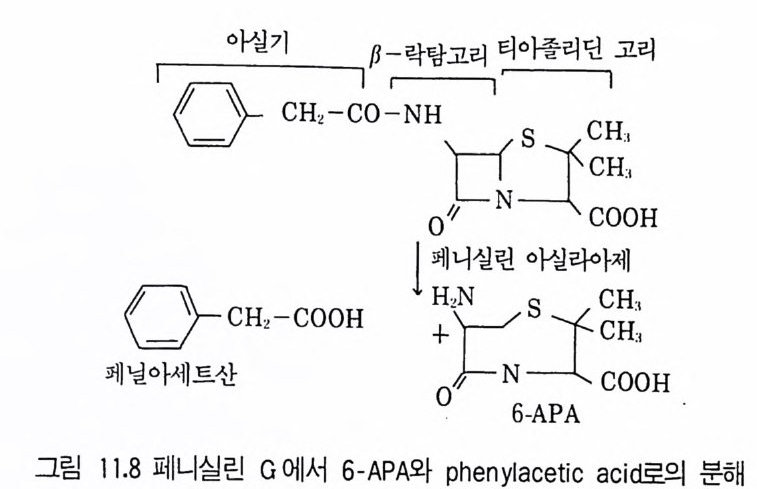 三0 많 기 0o -二- 락탐고리 티아三 종 리딘 H고H' , 리
三0 많 기 0o -二- 락탐고리 티아三 종 리딘 H고H' , 리
전구체인 페닐아세트산이 첨가되지 않은 배지에서 자라는 Penic il l i u m ch ryso g enum 은 6 - APA 를 저농도로 분비한다. 기본 고리구조의 합성공정은 오늘날 비용이 너무 많이 들어 싱업적으로 이용되지 못하고 있다. 미생물 이 생산한 페니실린 G 게 pen i ci ll i n ac y las 대 7 처리하면 아실 (ac y l) 곁 샤釣 절단되어 6 - APA 로 된다. 이때 효소에 의해 8-락 탐(/l -lac t am) 고 리가 파괴되지 않아야 한다 . 그러므로 pen i ci ll i n ac y las ei근 반합성 페니 실린 생산에 상업적으로 이용된다 (H iip er, 1973, Kaufm ann, 1959). ( 1 ) Pen icilli n ac y lase 의 유형 Peni ci ll in ac y las 눈 효모, 곰팡이, 세균에 의해 생산되며 다음의 두 가 지 형태로세분된다. Funga l type acy la se : 펜옥시메틸 페니실린(p heno xy me t h y l pen ic i l-
!i n) 을 분해하나, 벤질페니실린(페니실린 G) 에 대해서 는 덜 효과적으로 작 용한다. 이러한 acy la se 생산균주로는 Pe ni c i l li u m sp. , P. chry so g en um, Aspe rgi llu s, Ochraceus, Tric h op h to n me nt a g ro p h yt es , Ep ide rmop h y ton floc cosum, Cep h alospo riu m sp. , Fusariu m sem i tec tu m 등이 알려져 있다 곰팡기는 이의에 세균속의 Str ep tom y ce s lauendulae 도 이런 형태의 acy - las 릅 생산한다. 페니실린 V 뿐만 아니라 페니실린 K(hep tyl pc ), dih - yd ro pc F(p e nty l p c) 와 다수의 합성 페니실린도 분해된다 . 이러한 acy - las 完 보통 세포 의 효소이며 최적 p H 는 10, 최적온도는 50°C 이다. Bacte r ia l type II acy la se : Aerobacte r , Alcalig e nes, Bordete l la, Cel- lulomonas, Cory n ebacte r iu m , Erwi ni a , Escheric h ia , Flauobacte r iu m , Mi cro coccus, Nocardia , Prote u s, Pseudomonas, Salmonella, Sarcin a , Xanth o monas 문] 여기에 속한다. 최적온도는 4o·c 이고 최적 p H 는 誌i fun g al ac y las 蟲다 낮은 최적 p H 범위를 갖는다. 각종 미생물의 pe n ici l lin ac y las~ 근 기질 특이성이 다르며 그것은 6-APA 에 의해서가 아니라 아실 부분의 성질에 따라 결정된다. 많은 N 이 실 아미노산 (N-ac y 1 ami no acid ) 곁서슬이 분해되나 페닐아세트산 잔기 가가장 빨리 제거된다. (2) 세균성 (Pen ici l li n acy la se) E. col i에서부터 나온 pe n ici l lin ac y las 탸근 주로 6-APA 를 생산하는 데 사용된다. E. coli ATCC 111059 -} E. coli ATCC 9637 의 돌연변이주가 주로 쓰이고 있다. 세포내 acy la se 생산은 야생형 균주에 페닐아세트산울 첨가하면 유도된다. 포도당은 효소 생산을 억제하므로 배지내의 포도당 농 도를 낮추어야 한다. 효소 생산속도는 0 붑압에 의해서도 크게 영향을 받 는다. E. col i는 형기적 조건하에서도 증식은 가능하나 효소 수율이 낮아 진다. 또 통기속도가 너무 클 때에도 효소 생산이 억제된다. pH 7. 伊] 2% 욱坪 침출액이 효과적이며 접종(i noculum) 은 l 앙]간 전 배양시킨 종균의 025% 로 한다. 효소 형성을 유도하기 위해 24°c 에서 앙]간 발효
시킨 뒤 멸균 암모늄 페닐아세트산 (ammon i um ph eny la ceta t e ) 1% 용 액을 한 시간 간격으로 1 :1/]간 동안 가해준다. 세포는 2 ()ll ll 로 농축시켜 가압분쇄기 (pre ssure dis i n t e g r a to r : 500kg /cm압 력 )를 이용하여 유리시킨다. 이렇게 하여 얻어전 조효소제는 계속하 여 관례적인 방법으로 정제된다. 상업적 생산시 효소 수율은 배지의 조건을 최적화하고 전형적인 조작기 술을 이용하여 개선되어지고 있다. DNA 재조합기술로 수율이 더 높아질 것으로 기대되어지고 있다. 예를 들어 고복사형 풀라스미드(p lasm i d) 에 pen i ci ll i n acy la se 유전자를 대장균 (ATCC 11105) 에 clon i n g시킴으로써 비유도발효의 효소 생성율이 28tt l] 증가하고, 유도발효에서는 6 배 더 증가 한 균주가 얻어졌다 (Me y er, 1979). 페니실린 G 게서 6-APA 를 생산하는 데는 세 가지 방법이 상업적으로 이용되고 있다. 순수한 화학적 방법으로는 페니실린 G 를 일련의 단계를 거쳐 N-im i no meth o xy pen ic i ll i n es t er 로 바꾸어, 그것을 다시 액체 암 모니아를 이용하여 6-APA 로 가수분해하는 방법이 있다. 미생물을 이용한 다른 두 가지 방법은 효소 전환에 이용되는데 한 방법에서는 세균체를 이 용하고 다른 방법으로는 담체 결합된 (carr i er-bound) pen i ci ll in acy la se 를이용한다. 효소적 분해공정 : 원래의 공정에서는 세포에 결합된 (cell-bound) pen i- cill in ac y las 瑾 이용한다. 과거에는 E. coli 균체를 pH 8, 37° C 회분공 정시 조효소용액으로 직접 페니실린 G 액에 첨가하는 방법을 이용했으나 오늘날에는 담체에 결합된 (carr i er-bound) pe ni ci ll in acy la se 공정을 광 범위하게 이용함으로써 매년 수백 톤의 6-APA7} 생산되고 있다. 이 공정 의 이점으로는 재순환에 의해 pen i ci ll i n ac y las ei순 보존할 수 있고, 6-APA 의 순도가 더 높고, 부반응으로 인한 손실이 더 적다는 점을 들 수 있다. 세포 전체를 고정시키기 위한 처리과정에서 acy la m ide 단량체 (monomer) 가 세포와 중합체를 이룬다. 그러나 정제 pe ni ci ll in acy la se 롤 고정시키는 방법이 더 널리 쓰인다. 그중 한 방법은 E. col i에서 얻은
pen i ci ll i n ac y las 례- 중합체 (p ol y mer) 와 함께 공유 절합시켜 불용성으로 만드는 법이다. 페니실린 (100,000 unit s/m e) 기질과 효소가 pen ic i ll i n acy la se 1 unit 당 기질 5 X 10 un it s 의 바율로 이용될 때 &l 간 동안 38°C , pH 7.8 에서 정량적으로 분해될 수 있다(1 670 Inte n ati on al uni- ts= lmg 페니실린 G). 효소 1 un it란 1 분내에 1JL M ole 페니실린 G 를 37 °c 에서 6 - APA 와 페닐아세트산으로 가수분해하는 활성을 의미한다. 이 방법을 쓰면 이론 수율 87% 정도이며, 순도가 97% 가 되는 6-APA 를 회 수할수있다. (3) Cep h alospo rin acy la se 세팔로스포린 (ce p halos p or i n) 은 페니실린과 유사하긴 하지만 다른 /3- 락탐 고리를 가진 항생물질이다. 반합성 세팔로스포린도 페니실린과 유사 한 방법으로 생산된다. 미생물을 이용한 방법은 수율이 낮기 때문에, 과거 에는 합성을 위해 필요한 고리구조를 만들기 위해 곁사슬인 L-'J .- ami . noadip ic a ci d 를 화학적으로 분해하였다 . 그러나 오늘날에는 미생물을 이 용하여 세팔로스포린 C 를 7-acy l 곁사슬과 7-ami no cep h alosp o ran ic aci- d(7-ACA) 로 분해하는 과정이 이용된다. 35% 세팔로스포린 C 용액은 Pseudomonas p u ti d 러 밀접하게 관련된 Pseudomonas s p.에서 얻은 효소 를 쓰면 7 시간내에 분해된다 (Moss, 1977 ). 7 기타 미생물효소 7.1 L-Asp ar agi na se L-Asp ar agi na se(L-Asp a ragi ne am i doh y drolase) 는 백혈병과 임파종 치료에서 항종양제 (an tit umor g en t)로 이용된다. 이 효소를 사용하는 원 리는다음과갇다.
항종양제에 종 양세포의 대사에는 L .b}스파라긴 (L - as para gi ne) 이 필요하 며 이 아스파라긴은 as p ara gi nase 에 의해 asp ar ti c ac i d 와 암모늄이온으 로 분해되므로 악성 종양세포를 파괴할 수 있다. 이 효소 .는 여러 세균에 의해 생산되지만 산업적 생산에는 Escheric h ia coli ATCC 9637, Ser- rati a marcescens ATC 6 떠 Erwi ni a caro t ouora 의 돌연변이주가 이용된 다. 3% 옥수수 침출액, 0.6% 초산나트륨, 0.2% 황산암모늄이 든 pH 7.0 의 배지가 적합하며 16~40Al 간 발효공정 동안 Q 공급이 매우 중요하다.
표 11. 1 1 소형 발효조에서 Erwi ni a aro i dea 혜를 이용한 L-aspa r agi n ase9 .I 생산 • 차B폐a장ff l치e 세포(g건/ 조10중1) 량 I L-a(supn air tasg /m g a) se 통풍속도 (vvm) 0.5 14 960 1.0 + 16 580 1.5 + 18 340 2.0 + 18 230 (Pete r so n and Cie g le r, 196 9 ) 주 :28 °C 배양. 교반속도 : 3 00 rpm
발효공정 말기에 이르면 세포는 파괴되어 세포내 효소를 방출한다. 효소 는 인체내에 주사되기 때문에 모든 결정화 과정중에 순수하게 정제되어야 만한다. 7.2 Pecti na se Pec tina se 제제에는 분자내 다른 위치에서 펙턴을 분해하는 효소가 적 어도 67}지 가 있다. 펙틴의 기본 구조는 C(- 1,4 -l in k ed gal actu r onic acid 이며 그중 카르복실기 (carboxy l g rou p)의 75% 정도가 메탄올에 의해 에
스테르화될 수 있다. Pecti n as~ 펙틴(p ec ti n) 분자에서의 공격 위치에 따라 분류된다. Meth y l es t er 는 p ec ti nes t erase 에 의해 분해되고, 펙틴 사슬의 글리코시드(g l y cos i de) 결합은 endo- p ol yg alac t uonase 나 exo~ p ol yg alac t uronase 에 의한 가수분해에 의해 분해된다. 다른 분해방법은 세균의 endop ec t at e l y ase 나 곰팡이의 exo 요t endo- p ec ti nl y ase( 그림 1 1. 9) 에 의한 t ransel i m i na ti on 이다 . 전분(밀, 옥수수, 감자) ➔ 가수분해(효소적, 산) ➔ 포도당 ➔ (포도당 이성질화효소) ➔ 포도당 : 과당 ~60 : 40 이소시럽
COOH COOH COOH ___ COOH 忍 ~o~。 /모/〈〉;~ o OH OH OH OH 풀리갈락두로나 0 넨 三°COOH詩 〈CO〕OH 0펙 /틴二。: C;OO~H H 円COO°H /0CO:OC 尸HJ 二C『OOC° 比 /一 仁coo\c 比 巳C0거0CH03 펙틴리아제 0H OH 그림 11. 9 Polyg a lactu r onaseOII 의한 가수분해와 pec ta t e lyas e, pec ti n lya- seOII 의한 tr ansel i m i na ti on 을 통해 펙틴내의 굴리코시드 결합을 분해.
여러 회사가 Aspe rgi llu s n iger나 A. wen tii를 이용하여 곰팡이의 pee - ti nas 遷 생산하고 있으며, 한 발효공정만이 Rhiz o p u s¾ 이용한다. 표면배 。料 액침배양이 모두 이용된다. p ec ti nas~ 즌 다른 곰팡이에서뿐 아니라 세균, 원생동물(p ro t ozoa), 곤충, 고등식물에서도 발견된다. 이 효소는 주 로 점도를 감소시키고, 혼탁물질을 제거시킴으로써, 과일 주스를 맑게 하 기 위해 사용된다.
7.3 Lip a se Lip a se(g ly c e rol este r h y drolase) 는 지방(g l y cerol es t er) 을 글리세 롤(g l y cerol), 알코올, 지방산으로 분해한다. Lip a sei ::- 모두 세포 의 효소인데 산업적으로 이용되고 있는 균주는 Asp er gi llu s, Mucor, Rh i zo p u 어 Candid a 동기다. 대다수의 경우, 효소 생 샨은 기름 (o i l) 과 지방 첨가에 의해 유도될 수 있다. 그러나 지방이 li- pas e 생산에 아무런 영양도 미치지 않는 경우도 몇 가지 있고 Penic i l- lium ro q ue f or ti에서는 지방이 실제로 효소 생산을 억제한다. 다양한 · 최적 pH , 최적온도, 기질 특이성을 지닌 lip a se7} 주로 생산되고 있다. 세균 li- p ase 의 최적 p H 는 중성이거나 약알칼리성이지만 곰팡이가 생산한 lip a se 에서는 최적 p H 가 중성 혹은 약산성이다. 두 부류 모두 최적온도는 일반 적으로 30~35°c 부근이다(표 11. 12). l ip ase 의 상업적 용도는 제한되어 있어, 췌장 l ip as 어둔 보충하기 위한 소화효소로서 주로 시판되고 이 효소 둘은 낙농산업에서도 약간 쓰여지고 있다. 유리지방산이 치즈의 냄새와 맛 울 결정하며 치즈의 숙성과정이 우유내에 존재하는 미생물 lip ase 에 의해
표 11. 1 2 여러 미생물에 의한 lipa se£ ! 온도와 pH 최적조건 미생물 최적 pH 최적온도 Penic il l i u m chry so g en um 6.2~6.8 37 Pseudomonas fra gi 7.0~7.2 32 Rhiz op us delemar 5.6 35 Aspe r gi llu s nig e r 5.6 35 Penic il l i u m rog ue fo r ti 8.0 37 Sta p h y l o coccus aureus 8.5 45 Geotr ic h um candid u m 8.2 37 Achromobacte r lip o lyt icu m 7.0 37 (Shahani , 1975)
영향을 받기 때문에 오늘날은 Mi cro coccus9 -} Lac t obac i llus 에서 얻은 Ii- p as 라 치즈 제조에 이용된다. 7.4 Lacta s e Lacta s ec p-g alac t uron i dase 라고도 불리 며 유당을 포도당과 갈락토오 즈로 분해한다. 이 효소는 세균과 효모에서는 세포내 효소이나, 많은 곰팡 이에서는 세포 의로 분비된다. 상업적으로 관심이 있는 lac t as ei근 Aspe r gi llu s 01 y zae 와 A. n ige 데서 얻은 것과 Kluy ue romy ce s lacti s, K. fra g ilis , Torula Cremoris 등 효모에 서부터 얻고 있다. 효모는 액침배양에서 배양되나 Asp ergi llu~ 근 30°C 의 밀기울 표면에서 배양되며 최적 p H 는 산성 (2.5~4.5) 이고 최적활성온도는 55 °C 이다. 일반 적으로 효소 생산을 유도하기 위해 젖당이 첨가된다. La ct as 탸근 유당 과 민성 (lacto s e-in t o l erance : 보통 lacta s e 결핍에 기인)일 경우에 소화효소 로 이용되고 때로는 영양 가치를 증진시키기 위한 사료 첨가물로도 이용 된다. 낙농산업에서는 우유의 유당을 분해하고 유장 (whe y)를 처리하기 위 해 lac t as 혀t 사용한다. 8 효소의 안정화와 고정화 일반적으로 정제효소는 오래 보관하면 그 활성을 잃게 된다. 천연효소는 화학적, 물리적, 생물학적 요인에 의해 불활성화되기 쉽고 보관하거나 사 용 도중에도 불활성화된다. 그러므로 생산 비용이 높은 효소는 안정화시킬 필요가 있다. 효소는 다양한 조건하에서도 활성을 수개월간 유지할 만큼 안정해야 이상적이고 그 안정화를 위해 효소를 담체가 되는 물질에 고정 화시키는 것이다. 나아가서 각종 상업적 처리공정 중에서도 효소를 계속
되풀이 사용할 수 있도록 효소를 고정화시키는 것이 가능해야 한다. 효소 의 안정성을 획득하는 네 가지 기본 방법이 있다. 8.1 가용성 효소의 안정화 경우에 따라 효소를 고정할 수가 없어서 반드시 가용성 형태로 이용해 야 하는 것도 있다. 액체세제나 전단 시약, 사료 첨가물로 쓰이는 효소가 그 예이다. 이러한 경우 가용성 효소의 보존기간을 연장하기 위해 효소를 안정시킬 필요가 있다. 가용성 효소의 안정화는 첨가제나 화학적 변형 조 작에 의해 이루어진다. 이것은 효소의 용해도를 감소시키지 않고도 물리화 학적 약품에 대해서 효소 안정성을 증가시켜준다. 안정화된 효소는 성공적 으로 저장될 수는 있지만 여전히 가용성이므로 사용 후 재순환시킬 수 없 다. 안정화법은 다음과 같다. 기질 안정화 : 효소의 활성 부위는 효소의 특이한 작용을 위해 필요하며, 이 부위는 기질 첨가에 의해 안정시킬 수 있다. 예를 들어 1J. -am y las ei근 전분을 첨가하면 안정되며, 포도당 이성화효소는 포도당을 첨가하면 열에 의한 손상으로부터 안정화된다. 반면에 기질이 첨가되면 효소 활성이 저하 되는 피루브산 탈수소효소 같은 효소도 있다. 용매 안정화 (solven t sta b il iz a ti on ) : 효소는 용매 첨가에 의해서도 안 정화될 수 있다. 효소 중 고농도 용매에서는 변질될 수 있으나 저농도 용 매에서는 상당히 안정되어지는 것이 있다. 그림 l l.1Qol 1 는 benzyl a lcohol deh y dro g enas 려 대한 용매의 안정화 효과를 예로 도시하였다. 영 (sal t)에 의한 안정화 : Ca, Cu, Fe, Mn, Mo, Zn 같은 양이온은 금 속성 효소의 안정성과 활성에 영향을 준다. 예를 들어 Ca 1+. 은 Bacil lu s caldol yti cuSol] 서 얻어전 a-am y las 려 ~} 구조와 p ro t eas 례: 안정시키는 것을돕는다. 중합체 (po lym er) 첨가에 의한 안정화 : 젤라틴(g ela ti n) , 알부민 (albu min) , 지방성 알코올(fatty alcohol) 또는 폴리에틸렌 글리콜(p ol y e t h y l-
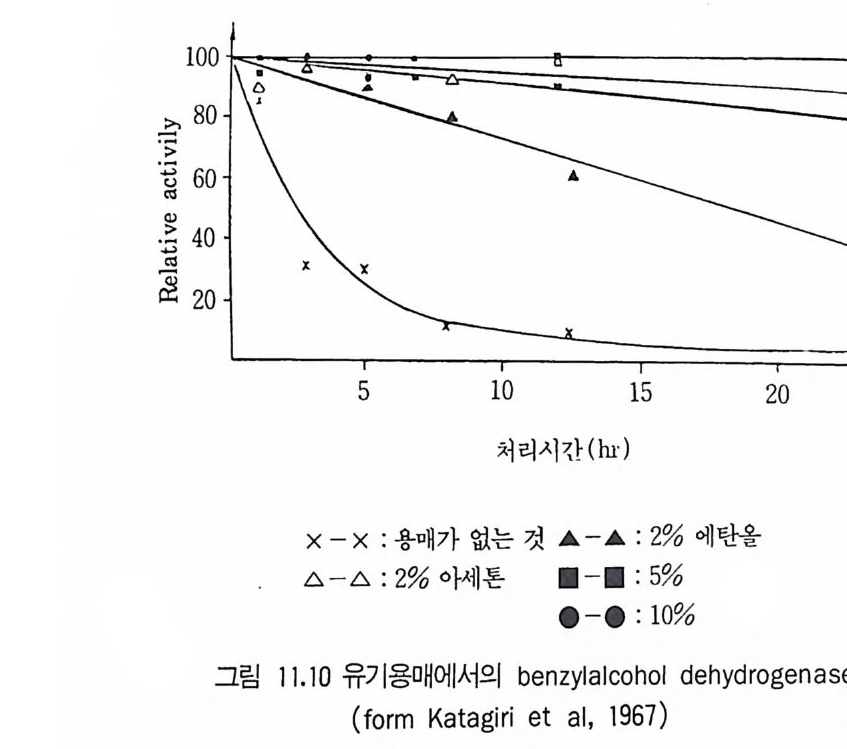 l 0080604020
l 0080604020
ene gly c o l) 같은 중합체에 의해 효소의 열 안정성이 증가될 수 있다. 화학적 수단에 의한 안정화 : 가용성 담체에 효소를 결합시키는 방법 의 에도, 효소는 용해도 저하 없이 화학적 변형에 의해 안정화될 수 있다. 하 나의 방법은 폴리티로실(p ol yty ros y l) 이나 폴리글리실(p ol yg l y c y l) 효소 생산에서와 같이 폴리아미노(p ol y am i no) 곁사슬 (s i de cha i n) 을 갖는 효 소를 만드는 방법이다. 다른 방법은 아세틸 (ace tyl), 포르밀(fo rrriyl), 프 로피오닐(p ro pi on y l), 숙시닐 (succ i n y l) 기를 이용하여 아실화시키는 것이 다. 혈액내 as p ara gi nas ei:근 아실회에 의 해 상당히 보호될 수 있다. 8.2 고정화(i mmob i l i za ti on) 에 의한 안정화 효소를 다른 효소나 담체에 결합시킬 때는 효소분자의 활성 부위의 3 차
구조를 변화시키지 않고 이루어져야 한다. 고정호臼豆정 결과, 기잘 특 이성 이나 반응 특 이성이 상실되어서도 안 된다. 고정화 처리에 알맞은 효소분 자 내의 기능기 (fun cti on al g rou p)로는 적당한 아미노산내의 유리 'l., {J, Y-카 르복실(:1., fi, Y-<:arbox y l) 기, ':J., '아미노('l., fi -am i no) 기, 페닐(p he n y l) 기, 히드록실 (h y drox y l) 기, 설피드릴 (sul fhy dr y l) 기, 이미다졸(i m i dazole) 기 등이 있다. 사용된 작용기들은 효소 활성에 치명적인 것아어서 는안된다. 위에서 언급한 바와 같이 효소의 고정에는 세 가지 방법이 있다(그림 11. 11)
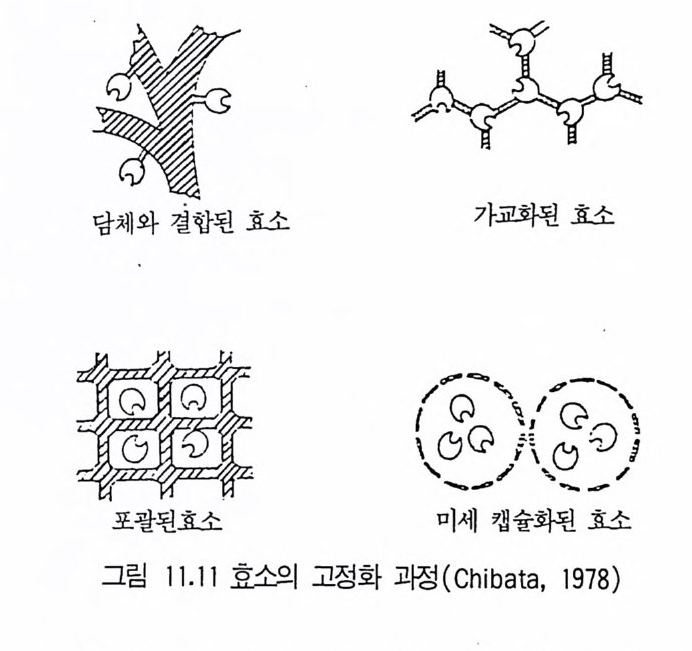 多:
多:
(1) 효소분자를 교차결합(중합)시킴으로써 안정화시키는 법(가교법) (Brown, 1976) 효소 활성이 영향을 받지 않는 방법으로 글루타르알데히드와 중합체를 써서 서로 교차결합될 수 있다. 이런 효소는 더 이상 가용성이 아니므로 계속 되풀이 사용할 수 있다.
글루타르알데히드는 일반적으로 이용되는 중 합 제로서 그림 1 1.1 2 에는 이 화합물이 sc hif~김기 형성에서 어떻게 효소의 아미노기와 반응하는가물 나 타낸다.
 N- 효소 -N=CH 一(CH 2 } 3 -CH
N- 효소 -N=CH 一(CH 2 } 3 -CH
:x- Amy la se, chy m ot ry p s in , rib o nuclease, ami no acy la se, 알코올 탈 수소효소 (alcohol deh y dro genase) 는 모두 글루타르알데히드에 의해 중합 된다. 다른 교차결합제 (cross-lin k ing a g en t)로는 hexameth y le nedii so - cya n ate 7 } 있는데 이것은 펩티드 결합을 이루므로 효소와 반응한다(그림 11. 13 ).
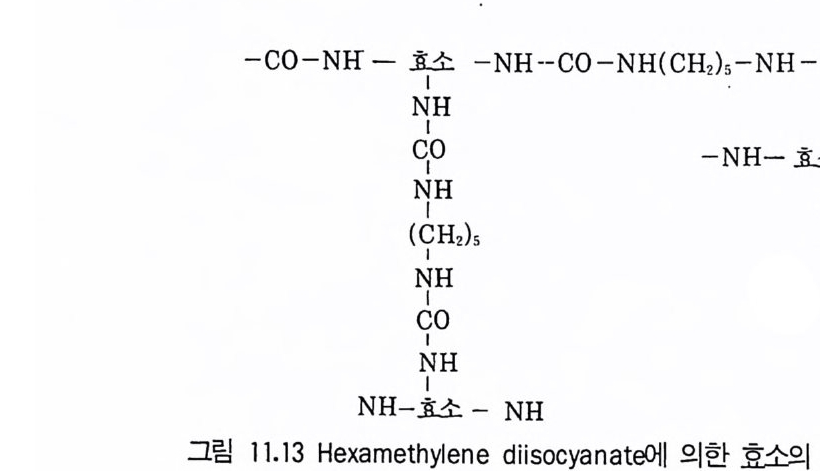 c。 N H __NHH--co _NH(CH 2 )5 _ NH _co
c。 N H __NHH--co _NH(CH 2 )5 _ NH _co
(2) 담체와 결합된 효소 (carr i er-bound en zy m e) 효소를 홉착, 이온결합 또는 공유결합을 통해 운반체에 절합시키는 것은 효소고정법 중 가장 ' 오래된 방법이며, 상업적으로 가장 널리 사용되고 있 다. 담체의 구조, 기능결합 위치 (fun cti on al bin d in g s it e) 의 형태, 소수 성기에 대한 친수성기의 비율, 입자 크기, 표면용적비는 각각의 효소와 궁 국적인 상업적 용도에 적합해야만 한다. 흡착 (adsor pti on) 에 의한 결합은 단백질에 가장 손상을 적게 주고, 구 조 변형도 가장 적 게 일어난다. 이 방법으로 쉽게 고정화할 수 있으며 다 양한 효소들에게 적용할 수 있고 대부분 경우 담체의 재생이 가능하다. 그 러나 결합력이 약하디는 단점이 있어, 반응기 (b i 9reac t or) 에서의 온도변 화에 의해 담체에서 효소가 빠져나갈 수가 있으므로 활성이 떨어진다. 유 기적 담체와 무기적 담체 둘 다 흡착과정에 적용될 수 있고 표 11.1 3 에 여러 형태가 나열되어 있다.
표 11.13 효소 과정을 위한 흡착 담체 운반체 형태 담체 사용효소 무기질 Alumi ni u m oxid e Glucoamy la se Bento n it e Inverta s e Glass Lip a se Ca pho sp h ate gel Asp a rta se 유기질 활성탄 Glucose oxid a se :x- amy la se P-amy la se Glucoamy la se Inverta s e 전분 :x- amy la se Tannin ami no hexy l Glucose iso merase Cellulose Amino acy la se
이온교환기(i on exchan g er) 도 효소 담체로 이용할 수 있으며 이온 결 합에 의해 효소가 담체에 부착된다. 이 방법은 부분적으로 흡착법과 중복 된다. 이온결합은 p H 와 이온의 강도가 변할 때 담체에서부터 효소가 손실 될 수 있다는 단점에도 불구하고 활성 저하가 낮고 고정화조작이 용이하 다. 시판되는 다양한 이온교환기들이 담체로 사용될 수 있다. 공유결합 (covalen t bond i n g)에 의한 고정은 강한 결합력을 갖는 장점 을 갖고 있다. 이 방법에서는 단백질내 하나 또는 그 이상의 아미노산 곁 A 冷이 담체에 공유결합하도록 변형된다. 공유결합된 효소제는 값도 비싸 고, 활성 중심부위의 아미노산이 반응에 관련될 우려가 있어 공정이 어렵 다. 공유결합은 상업적으로 가장 널리 이용되는 방법이다. 사용되는 공유 결합의 종류에는 알킬 (alk y l) 화 BrCN 활성화 탄수화물과의 iso urea 결 합 형성뿐 아니라 펩티드 결합과 dia z o 결합도 포함된다. 효소결합이 일어 나기 위해서는 담체의 기능기가 활성화되어야 한다. 효소단백질의 1 차 아 미노기를 써서 펩티드 결합을 형성할 때는 담체의 카르복실 (carbox y l) 기 가 아지드 (az i de) 나 안히드라이드 (anh y dr i de) 유도체를 생성하여 활성화 될 수 있다. 공유결합의 예는 그림 1 1.1 4 에 카르복시메틸 셀룰로오스의 경 우를들어 나타내었다.
Cellulose-0 ― CH2-COO~ 讐 Cellulose -0 -CH2 -C OO-CHJ ~ Cellulose -0 -CH2 -C O -N H -N H2 ~. HCl Cellulose-0-CHz-CO-N J도 Cellulose-0-CH2-CO-NH-Enz y me 그림 11. 14 카르복시메틸 셀룰로오즈 (carbox y me thy lcellulose) 를 이용한 효소 의 고정
CM 셀룰로오二는 먼저 메틸에스데르 (me t h y les t er) 로 전환되고 이어
히드라전 (h y draz i ne) 으로 처리된다. 얻어지는 하드라지드 (h y draz i de) 는 아질산 나트륨 (NaN0 2 ) 과 반응하고 그에 상당하는 아지드 (az i de) 유도체 가 만들어져서 효소의 아미노 (am i no) 기와 반응한다 . (3) 효소의 포괄법 (encap su lati on ) 효소가 물리적으로 겔 미세 캡슐이나 섬유성 중합체내에 포괄될 때, 거 기에는 효소분자가 씻겨나갈 수 없을 정도로 매우 작으면서도 분자량이 적은 기질이나 산물이 장벽을 통과해 방해없이 확산할 수 있을 정도의 구 멍이 있어야만 한다. 불행히도 포괄된 효소는 제조시 상당한 비율의 손실 이 있을 수 있지만 최종산물은 매우 안정한다• 겔 포괄(g el enclosure) : 효소를 에워싸는 데는 폴리아크릴아미드(p ol yac ry la mi de ), 폴리비닐 알코콜(p ol y v i n y l alcohol) 이나 전분같이 교차 결합된 불용성 중합체를 사용할 수 있다. 가장 널리 이용되는 방법은 폴리 아크릴아미드 겔내에 집어넣는 방법이다(그림 11. 15 ).
CIO — NH 2 NI H2 -C O -CH2 -C cH,o-NC_HHC2 -C_ HH- CH2 -C H-CH2 -C CHI-OCN_HH2C -C H - _ H2 I NH NH NH2 I I —CH 2 -CC OHI -CH2 -C H-CNHH2 -2 C- CIHO -CH2 -CC OIH -CH2 -C CHOI - CO-NH- 그림 11.15 폴리아크릴아미드 겔내로의 효소 포괄
표 11. 1 4 고정화 효소와 담체에 결합된 효소의 실용화 認 | 소규모 생산 1 대량 생산 Penic il l in acy la se X Glucose iso merase X Amino acy la se X Lact as e X Hy da nto i n a se X Glucoamy la se X Inverta s e X Fumarase X (Buchholz, 1982)
아크릴아미드와 효소는 수분내 실온에서 교차결합 화합물 NN' - meth y le ne bis a cryl a mi de , 개시물질 Na- p ersul fat e 와 촉진제 8 검i me t h y l ami no p ro pi o nit r i le 에 의해 g e 묘. 중합된다. 그러고 나서 g e 분 절 단되어 이용된다. 미세 캡슐 (m i croca p sule) 화 : 미세 캡슐 제제를 이용하여 효소를 고정 화시킬 때의 장점은 유리 (fr ee) 효소나 유리세포를 번두과성 중합체막에 의 해 둘러쌀 수 있다는 점이다. 비수용성 유기상 (or g an i c p hase) 에 현탁되 어 있는 수용성 효소의 입자 표면에서 중합반응이 일어남으로써 생산이 이루어진다. 미세 캡슐제로 된 효소는 아직 상업적으로 이용된 예는 없으 나 앞으로 임상적 용도와 분석용도로 유망한 것으로 보인다 . 섬유상 중합체내에서의 고정화 : 이 효소 고정법은 미세 캡슐을 이용한 방법과 유사하다. 효소 수용액과 소수성 (wate r -im mi sc ib l e) 유기용매의 유탁액 (emuls i on) 을 침전조(p rec ipit a ti on ba t h) 로 내보내면 섬유상 중 합체가 형성되어 효소를 고정화하게 된다. 셀룰로오스 트리아세테이트 (cellulose t r i ace t a t e) 와 그 의 셀룰로오스 유도체가 적절한 중합체로 이 용되고있다. 세포에 고정된 효소의 산업적 응용 : 효소 활성을 지닌 모든 세포는 효
소처럼 비 슷 한 방법에 의해 고정호祠! 수 있다. 고정 화 효소세 포 계 를 이용 하면 몇몇 장점이 있다. 생산 품 회수 와 정 제에 시간이 적게 걸 리므로 비용 울 절 감하게 된다 . 만약 효 소 활 성에 보조인자 (co fac t or) 가 필 요하면 이 보 조 인자는 이마 세포내에 공존 하고 있 을 수 있다. 더 나아가 여러 효소의 협동작용 을 필 요로 하는 반응도 수 행 될 수 있다. 그러나 단접범위한 연구 에도 불구하고 소수의 고 정 화 효소세 포 계만이 상업적 생산에 이용되고 있 울 뿐이다( Cheet ha m, 198 0 ). 참고문헌 Aunstr u p , K., 0, Andresen, 1979. Produc tion of micr obia l enzym e s, pp. 281 ~309. In : Pep ple r, H. J. and D. Perlman(eds.), Mi cro bia l tec hnology , Vol. 1. academ ic Press, New _Yo rk. Berg, M., A. Boeck, 1976. Enzy m e als waschm ittel komp o nente (Enz- yme s in dete r ge n ts ) , pp. 55~178. In : Henkel and cie( eds.), Was- chmi tte lc hem i e. Hi ithig Verlag, Heid e lberg. Brown, G. B. 1976 ....C h em ica lly agg r eg ra te d enzym e s, pp. 263~280. In : Mosbach, K.(e d.), Meth o ds in enz ym olog y, vol. 44, Imm-obil ize d enzy m es. Academi c Press, New York. Buchholz, K. 1982. Reacti on eng ine erin g pa ramete r s for im mobil ize d bio c ata l ys t s . Adv. Bi oc hem. eng ., 24 : 39~71. C~eeth a m, P.S.J. 1980. Develop m ents in • the im mobil isa ti on of mi- crobia l cells and the ir ap plica ti on s, pp. 189~238. In : Wi se man, A(ed.) , Top ics in enzy m e and ferm enta tion bio t e c hnology , vol. 4. Ell is Horwood Lt d. , Ch ich este r . Ch iba ta , L. 1978. Immobil iz e d enz ym es. Jo hn Wi ley and sons, New York. Ch iba ta , L. and T. Tosa. 197 7. Transfo r mati on s of orga n ic com- po unds by im mobil ize d mi cr obia l cells, pp. 1~27. In : Perlman, D. (ed.), Advances in app l. mi cro bio l ., A cademi c Press, New York.
Chib a ta , L., T. Tosa and T. Sato , 1979. Use of im mobil iz e d cell sys - ter ns to pre p ar e fine chemi ca ls. pp. 433~461 . In : Pepp le r, H. J. and D. Perlman(eds.), Mi cr obia l tec hnolog y, vol. 2. academi c Press, New York. Fog a rty , W. M. and C. T. Kelley. 1979. St ar ch-< leg r a din g enzy m es of micr obia l orig in. Part 1. Di st r i b u t ion and charact er is t i cs , pp. 89~150. In ; Bull, M. J( ed.), Progr e ss in ind ustr i a l mi cr obio l ogy . Elsevie r Scie n ti fic Pub!. Co., Amste r dam. Glym ph , J. L. and F. J. stu t ze nberge r . 1977. Producti on , pu rif i- cati on , and Characte r iz a ti on of a-amy la se from Thermomonosp o ra curvata . Ap pl. Envir o n. Mi cr obio l ., 34 : 391~397. Hay a shib a ra, 1970. Techniq u e for pro ducin g hig h ly pu re malto s e. Ger- man Pa ten t 1, 935, 760. Heit ma nn; P. and D. Mey e r. 1981. Sp ec ia l uses for mi cr obia l pro - tea ses. Acta Bi ot e c hno!og ica 1 : 377~386. Hup e r, F. 1973a. Techniq u e • for the pro ducti on of 6-ami no pen - ici l lan ic acid by the enzy m ati c breakdown of pe nic i l lin. German Pate n t 2, 157, 970. Hi ipe r, F. 1973b. Carrie r -bound pen ici l lin acy la ses. German Pa ten t 2, 157, 972. Kau fm ann, W., K. Bauer an_d H. A. Of fe. 1959. Enzy m ati c pro.- cedures for the pro ducti on of 6-ami no pen ici l la n ic acid . German Pate n t l, 149, 361 . Kata g iri, M., S. Takemori, K. Nakazawa, 1967. Benzy la lcohol de-hy d rog en ase, a new alcohol dehy d rog en ase from Pseudomonas sp. Bio c hem Bi op h ys . Acta . 139 ; 173~176. Lin . C.F, 1972. Producti on of glu coamy la se by a tem p e rat u re-sensi- tive muta n t of Rhir o p u s form osaensis R 13~5 and its p ro p e rti es, pp. 327~332. In : Terui, G.(ed.), Fermenta t i on tec hnology tod ay, Yamada-Kami , Osaka. Marshall, R. 0. and E. R. Kovi, 1957. Enzy m ati c conversio n of D- glu cose to D-fr uc to s e.'.' Scie n ce 125 ; 648~649. May er , H., J. Coll ins . and F. Wag ne r, 1979. Clonin g of the pe n i-
cill i n G acy la se gen e of Escheric h ia coli . ATCC 11105 on mu!- tico p y pla smi ds , pp. 459~470. In ; Ti m mi s, K. N. and A. Pu- hler ( eds. ) . Plasmi ds of medic a l, envir o nmenta l , and commercia l imp o rta n ce. Elsevie r / North Holland Bi om edic a l Press. Moss, M. 0. 1977. Enzy m i c alte r ati on s of pe n ici l lins and cep - halosp o rin s , pp. 110~131. In ; Wi se man, A(ed.), Tap ics in en- zym e and ferm enta t i on tec hnology , vol. 1. El lis Horwood, Ch i- cheste r . Novo Industr i e s . 1977. Produc tion of high -pu rit y glu cose sy rup s. U. S. Pate n t 4, 017, 363. Pete r son, R. E. and A. Cie g l e r, 1969. L-A s p a rag ina se pr oducti on by Erwi ni a aroid e ae. Ap pl. Mi cr obio l ., 18 ; 64~67. Shahani, K. M. 1975. Lip a ses and este r ases, pp. 181~217, In ; Reed, G.(ed.), Enzy m es in foo d pro cessin g . Academ ic Press, New York. Takasaki, Y., and Kanbay a shi, 1969. Str ep tom y ce s glu cose iso -merase, pp. 561~589. In ; Perlman, D.(ed.) , Fermenta t i on adv- ances. Academi c Press, New York. Terui , G. 1973. Ki ne ti cs of hy d rolase pro ducti on by mic- roorga n ism s, pp. 377~395. In ; Ste r bacek, 2. (ed.), Mi cro bia l eng ine erin g , Butt erw orth s , London. Up ton , M. E. and W. M. Fog a rty , 1977. Producti on and pu rif i- cati on of th ermosta b le amy la se and pro t ea se of The- rmomonospo ra uir i d i s , Ap pl. Enuir on m. Mi cr obio l ., 33 ; 59~64. Zit tan , L., P. B. Poulsen, and S. H. Hem ming se n. 1975. Swe-etz y m e-a new im mobil ize d glu cose iso merase. Di e sta r ke 27 ; 336~241.
제 12 장 비타민 (Vi tam i ns ) 1 서론 비타민은 대중적인 약으로서 대량 소비되고 있는데 대부분의 비타민은 화학합성으로 생산되고 있다. 티아민, 리보풀라빈, 엽산, 판토텐산, 피리독살, 비타민 B 12 등의 비타민 은 미생물을 이용하여 생산할 수 있으며 그 의에 비타민 합성에서 일정 단계는 미생물을 이용하여 수행할 수 있는데 예컨대 아스코르빈산 생산시 D -소 르비톨 (D-sorb it ol) 을 L -- 수근 님 ~(L -s orbose) 로 산화하는 과정에 서는 Aceto b acte r suboxy d ans( 15.4 단락)이 이용된다. 비타민 D~ 전구 비타민인 에르고스테롤 (er g os t erol) 은 Saccharom y ces 의 여러 효모주에서 세포중량당 0.1% ~10% 농도로 존재하며 효모-는 양질의 단백질과 풍부한 비타민을 함유하고 있으므로 영양제로서의 이용이 확대되고 있다. 비오틴의 미생물 생산은 상세히 연구되고 있지만 아직 경제성에 문제가 있다. 현재 리보플라빈과 비타민 Bl2 생산에서만 발효 생산에 경제성이 있 다. f)-카로틴 (f)-c aro t ene) 의 미생물을 이용한 생산은 화학합성법보다 비 용이 더 들지만 원료물질의 가격이 싱승함에 따라 발효공정은 보다 경제 성이 있는 공정으로 부상되고 있다. 이와 같이 비타민은 대증약으로서뿐 아니라 균체성분과 함께 사료의 영양강화용으로 사용되는 범위가 넓어지고 있기 때문에 사료공업의 발달에 따라 균체 비타민의 생산에 대한 관십이
높아지고 있다. 미생물 을 이용한 몇몇 비타민의 생산방법을 다음 단락에서 설명하겠다. 2 리보플라빈(비타민 B2 ) 2.1 분포 및 경제적 의의 리보풀라빈(l a ct o fl av i n 또는 비타민 B 료로 도 불린다)은 l93: 31 d Kuhn 과 Gy o rgy , Wagn e r..J a uregg 등게 의해 유장에서 처음으로 분리되었고 1935 년 Kuhn 과 Karrer 등기 이 물질을 합성함으로써 구조가 확성되었 다. 리보풀라빈은 우유에서 유리된 상태로 존재하지만 간, 심장, 신장, 달 걀 등에서는 보결분자단으로 FMN(fla v in mononucleo ti de) 이나 FAD (flav in aden ine d i nucleo ti de) 를 가전 풀라보 단백 질 (fl avo p ro t e i n) 로 존재한다. 리보풀라빈이 결핍된 백서는 성장 저해와 피부염, 시력 저하를- 일으킨 다. 리보풀라빈 결핍증 (ar i bo fl av i nos i s) 은 리보풀라빈 결핍으로 생기는 일종의 피부영 증상으로 1 일 1m g의 리보풀라빈을 두여함으로써 치료할 수 있다. 미국에서는 티아민 및 니코틴산과 더불어 리보플라민도 밀가루에 첨 가하여 비타민 강화 빵을 만드는 데 사용된다. 리보풀라빈은 세균, 효모, 곰팡이 등 많은 미생물에 의해 생합성된다. 리 보풀라빈 생산에 이용되는 고수율의 균주들이 표 12.l 에 수록되어 있다. 그러나 수록된 두 종류의 자낭균류 중에서 처음에는 Eremoth e ciu m ash- b yii를 사용하였지만(생산량 2 g/ l) 194 6¼빈 이후에 유전적으로 안정한 Ashby a g ossy pii를 이용한 공정이 소개되었다. 생산량이 많음에도 불구하 고 화학합성법과의 경쟁이 어려워 197 0¼:!대 후반에는 미생물 발효법에 의 해 리보플라빈을 생산하는 회사는 단지 Merck & Co. Inc. (미국)뿐이다. FMN 와 FAD 의 의약용 용도가 증가함에 따라 Breuib a cte r iu m amm-
onia g e n es 등 세균에 아데닌에 FMN 을 첨가 발효시켜 FAD 를 생산시킨 후 합성법에 의한 리보풀라빈을 제조하는 공정에도 관심이 모아지고 있다.
표 12.1 리보플라빈을 생성하는 균주와 생합성시 철분의 영향 균주 리보플라빈 생합성시 생산량 (m g/ Q) 철분의 영향 (m g/ e ) Clostr id i m aceto b uty li cu m 97 • l~3 My co bacte r iu m smegm ati s 58 영향없음. My co candid a ribo fl av in a 200 영향없음. Candid a flar eri 567 0.04~0.06 Eremoth e ciu m ashby ii 2480 영향없음. Ashby a gos syp ii 6420 영향없음. (Perlman, 1979)
2.2 구조와 생합성 리보플라빈은 프데리딘(pt er i d i ne) 고리가 벤젠 (benzene) 고리에 축합 된 알록사전 (alloxaz i ne) 유도체이다. 곁사슬은 리비톨 (r i b it ol) 유도체인 C s- p ol y h y drox y기로 되어 있다. 리보풀라빈 (6, 7-d im eth y l- 9-(D-l'-rib - ityl)-i soalloxaz i ne) 의 구조는 그림 12 .1에 나타나 있다. 이소알록사전
二데리딘고二리 〔H o 1 · 멘 H-c2·- 0 H H-C3·- 0 H H-c ◄ · -oH H295·-oH 그림 12.1 리보풀라빈의 구조
(iso alloxazin e ) 고리는 가역적인 산화환원제로 작용한다. 그림 12.2 에 나타낸 생합성 경로는 주로 효모 및 Ashby a gos syp ii 행한 실험을 기초로 가정한 것이다. Eremoth e ciu m ashb yii와 A. g os sypii에 의 한 리보풀라빈의 과잉생산은 철분에 의해 영향을 받지 않지만 clos t r i d i a 와 후에 의해 리보풀라빈을 생산할 때는 매우 낮은 농도의 철분에 의해서 도 생산이 저해된다. 철분-풀라보 단백질이 리보플라빈 합성의 억제제로서 작용하는 것으로 추정된다 E. ashb yii와 A. g ossy pii에 의한 과잉생산은 구성적인 리보풀라반합성효소에 의해 설명할 수 있다.
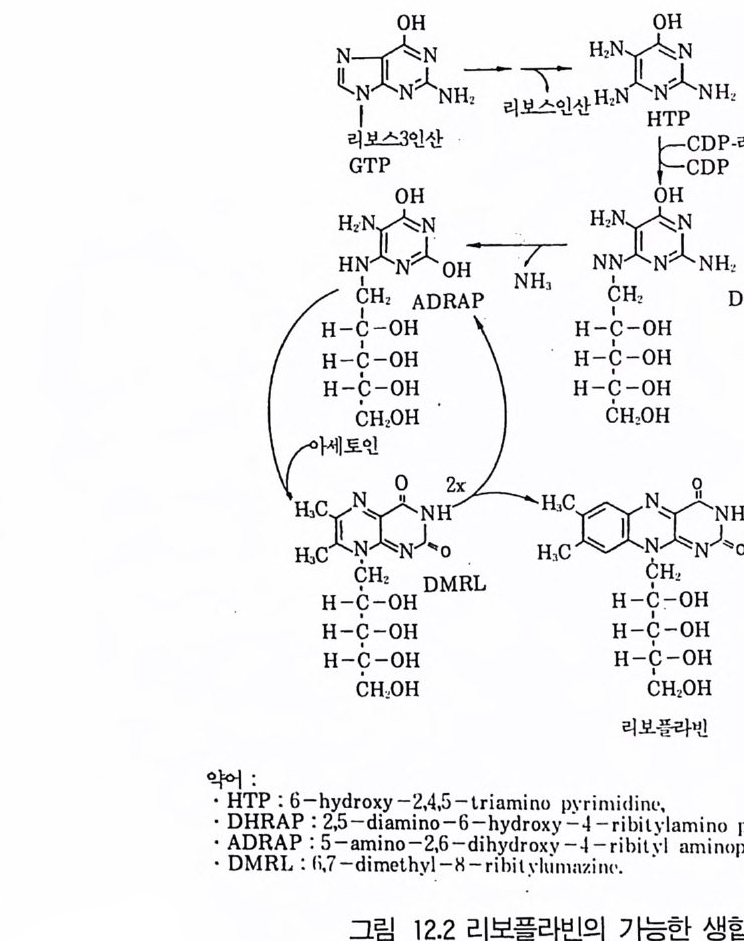 [二OH N H二 그 :H2 ::OHT N H
[二OH N H二 그 :H2 ::OHT N H
2.3 생산방법 현재 발효에 의한 생산은 Ashby a gos syp ii NRRL Y-10 56 에 의해 수 행되고 있다. 균주를 개량함으로써 최적조건하에서 7g / l 이상의 고수율을 얻고 있다. 처음에는 포도당과 옥수수 침출액을 포함한 배지를 발효공정에 사용하였다. 서당과 맥아당도 적당한 탄소원이 된다. 지방질을 에너지원으 로 사용하였을 때 수율은 현저히 증가하였다. 현재 리보플라빈 생산의 기 본 배지 (옥수수 침출액 2.25%, 시판펩론 3.5%, 콩기름 4.5%) 에 다양한 펩론 글라이신 증류폐액 또는 효모 추출액 등을 첨가함으로써 리보플라반 의 생산을 더욱 증진시킬 수 있다. 배지를 철저히 멸균하는 것이 생산량을 높이는 데 중요하며 24~4 앙]간 증식시킨 활발한 배양종균을 소량 (0.75~ 2%) 접종한다. 28°C 에서 0.3vvm 속도로 통기시키며 7 일 동안 발효시킨다. 기포를 제거시키기 위해서 먼저 실리콘 소포제를 첨가해주고, 나중에 콩기 름을 첨가해주는데 이 콩기름은 대사되기도 한다. 리보풀라빈은 발효액 중에서 균사체에 결합되어 있거나 용액 중에 유리 된 채로 존재한다. 결합되어 있는 리보플라빈은 열처리 (1 시간 12o·c) 에 의해 세포로부터 유리되고 균사체는 분리 제거한다. 그런 다음 리보플라빈 울더 정제한다. 지방족 탄화수소 (C 10- C1 8 ) 를 탄소원으로 하여 Pic h ia g u i ll i ermond ii를 이용해서 리보풀라빈을 생산한 보고가 있지만 (La g o, 1981), 수율에 관한 정보는 보고되지 않았다. Pich ia m i s 예t 이용했을 때 n 책사데칸 (n-hex adecane) 옥수수 침출액 요소를 함유한 배지에서 5lm g /l 의 리보플라빈이 생산된다. 3 비타민 B12 3.1 분포 및 경제적 의의 192 61;1에 G. R. M i no t과 W. B. Mur p h y는 간 추출距 l 사람의 악성
빈혈을 치료한디는 사실을 발견하여 1934 년에 노벨 의 학상을 받았다. E. L. R i cke 와 L. Sm it底 독자적으로 간 추출물에서 비타민 B12 결정을 분 리해냈다. 후에 이것이 동물 단백인자 (APF) 와 같은 물질임이 밝혀졌다. 비타민 B1 2 ( 시아노코발라민)는 자연계에서 미생물에 의해서만 합성된다(예 를 들면 간에 lpp m ). 조직으로부터 분리된 물질이 시아노코발라민이라 하더라도 세포내에서는 닌 주 , 수 형태 (adenosyl 또는 meth y lc obalami ne ) 로 존재하기 때문에 시아노코발라민은 생산물 회수단계까지 나타나지 않는 다. 동距鬪 필요한 바타민 B1 는 사료를 섭취하거나 장내 미생물에 의해 생산된 비타민 B1 2 를 홉수함으로써 충당된다. 그러나 사람은 대장내의 미 생물에 의해 합성된 비타민 B1 2 를 소화시키지 못하므로 단지 음식물로부터 비타민 Bl 2 를 얻을 수 있다. 하수처리장의 활성오니는 4~10mg B1 2 /k 겁t 함유하지만 이 원료로부터 비타민 B1 2 를 분리하는 데는 다양한 B12 동족체를 분리하는 문제 때문에 비용이 많이 든다. 화학합성법도 7~ 계의 반응과정을 거치므로 비실용적 이다. 초기에 비타민 B 1 눈 - 스트렙토마이신 (s t re pt om y c i n,) 클로람페니콜 (chloramp he nic o l) 또는네오마이신 (neom y c i n) 등의 항생물질을 생산하 는 스트렙토마이신 발효공정의 부산물로 약 lm g/Q의 수율로 상업적 생산 울 했다. 현재 상업적인 생산은 전적으로 균주 개량에 의한 발효공정에 의 해 수행된다. 비타민 B1 를 생산하는 주요 회서들은 다음과 같다. Far- mital ia S.P.A. (이태리 ), Glaxo Lab, L t d. (영국), Merck & Co., Inc. (미국), Rh8ne Poulenc S. A. (프랑스), Rous.sel UCLAF( 프랑스), G. Ric h te r Pharmaceuti ca l Co. 와 C hi no i n( 헝가리 ) . 현재 비타민 B 려 연간 세계적인 생산량은 약 10,000k g으로 추정된다. 약 3,500kg 시아노코 발라민, 2000kg 하이드록소코발아민 hy d roxocobalam in, 1000kg 조효소 (coenzym e) B1~ 소량의 메틸코발라민 (me t h y lcobalam i n) 을 제약회사 들이 사용하고 있다. 나머지는 동물 사료회사들이 사용하고 있다. 돼지와 가금의 사료에는 1톤 당 10~15 mg의 비타민 B1 2를 첨가하는데 이것은 식물 성 단백질에 비타민 B;& 보강함으로써 동물성 단백질로 전환할 수 있기
때문 01 다. 3.2 생합성 비타민 B 려 기본 구조인 corr i펴본 포르피린 환(p or p h yri n ri n g)과는 달리 A 와 D 고리 사이에 메텐 (me t hene) 가교가 없는 테트라피롤(t e t rapy rr ole) 고리로 되어 있 다. 코바마이드 (cobam i de) (그림 12. 契] 구조 식 참고)에 들어 있는 리보오스의 C - 1 은 헤데로사이클 염기인 5, 6 디메
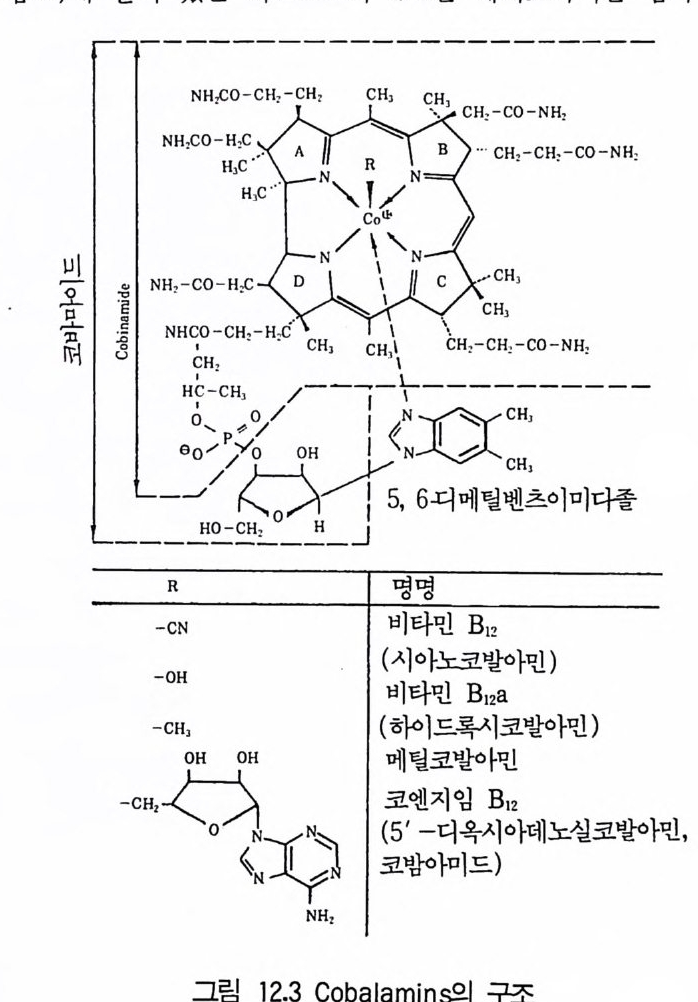 NH *C N0\`:C< >CH *- C :-CN: co - NH
NH *C N0\`:C< >CH *- C :-CN: co - NH
틸벤즈이미다졸 (5, 6 -di me t h y lbenz i m i dazole) 에 결합하고 이 화합물은 다시 최종산물인 시아노코발라민의 CN 옆에 붙은 코발트에 결합한다. 다 론 헤데로사이클 염기 퓨린(p ur i ne) 또는 치환된 벤즈이미디졸 (ben z i .m i dazol) 을 가진 비타민 恥 동족체들은 미생물에 의해서 자연적으로 생산되거나 이러한 물질들을 배지에 첨가한 후에 생산된다. 그러나 척추동 물에서 비타민 B1 동족체들은 5, 6 디메틸벤즈이미다졸 화합물에 비해 생 물학적 효과가 적다. 퓨린 염기를 가진 비타민 B12 동족체가 사람에게 효 과가 없다는 사실은 주목할 만하다. 비타민 B1 려 생합성은 우로포르피리 노겐 (uro p or p h y r i no g en) ill 형성 단계까지 포르피린과 클로로필 (chloro p h y ll) 의 생합성과 동일한 과정으로 그림 12 .4에 나타내었다. 우로포르피 리노겐 ill를 corrin 고리로 전환하는 과정은 아직 완전히 알려지지 않고 있다.
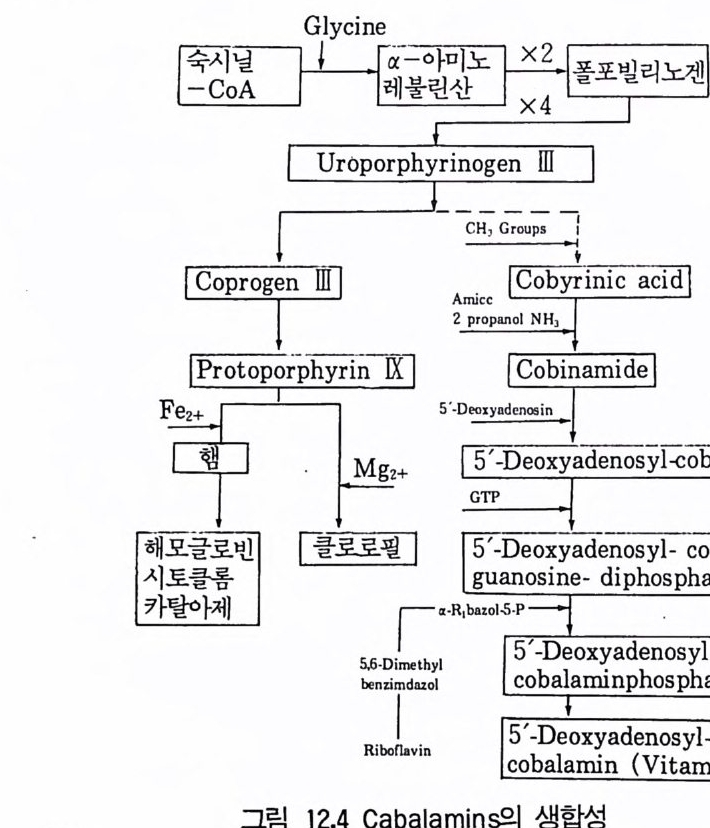 Glyc i n e
Glyc i n e
3.3 비타민 B12 생산 비타민 B1~ 발효공정의 대부분은 탄소원으로써 포도당을 사용한다. 몇 가지 생산균주의 B12 생산량은 다음과 같다. Bacil lu s meg at e r iu m (0.4 5 mg / !) , Buty r i b a cte r iu m rettg e ri ( 5mg / l) , ·str ep t om y ce s oliu a ceus( 3.3mg / l) , Mi cr omonospo ra sp. (l l.5 m g / l), Klebsie l la pn eumonia e (0.2 m g / l) : 가장 생산량이 높은 것은 Prop ion ib a cte r iu m fre udenreic h ii (l9m g /l ), Pro- pion ib a cte r iu m shermanii (23 mg /Q1 , Pseudomonas denit rif i ca ns(60mg /Q : 사탕수수당밀에서 )이다. ( 1) Prop i on i bac t er i a 의 발효공정 Prop ion ib a cte r i u m fre udenreic h ii ATCC 6207 와 P. shermanii ATCC 13673 및 이들의 돌연변이주는 코발트 (10~lOOm g /l) 를 첨가하는 灰}계 공정에 사용되는데 먼저 형기 단계 (2~4 일 )에서는 5' 디옥시아데노실코빈 아미드 (5 ' -
비타민 B 1 2를 생산하는 Pseudomonad 중에서 Pseudomonas denit rif i - cans7t 가장 생산성이 높은 종이다. 이 공정은 일단계로 수행되며 전체 발 효과정 동안 생산된다. 코발트와 S.6 디메틸벤즈이미다졸은 배지 중에 첨가 해야 한다. Be t a i n 려 첨가는 생산량을 증가시키는 것으로- 알려져 있으며 저렴한 베타인 (be t a i ne) 원료로 사탕무당밀이 사용된다. 이 화합물의 작 용 양식은 밝혀지지 않았지만 생합성과정을 활성화시키거나 막투과성을 증 가시키는 것으로 추정된다. 그림 12. 翁 1 공정은 가장 저렴한 생산공정 중
접종물의 저장 : 분유에서 동결견조한다 . 디슈니M도트B모로24나피36스컨 스 배1 Q지 AE로 rle r사un면e배ye 지r fl만 as듬k 에 배 1양50 :m9e6 h 28'C 배지 B, 배양 :72h, 28'C 진당배양 5Q 발효조에 3.3Q 배지 C 120 ,C에서 접종물의 배양 7 얹은 멸균 접종물 :150 빠 전배양, 배양 : 90h 전배양 29,C :420rpm 교반 ;lvvm 통기 생산배양 배지 A(g / Q ) 사탕무우당밀 60 : Yeast extr a ct l:N- Z-Am ine l : (NH ◄l 2 HPO ◄ 2:M g So ◄ 7H20 l: MnSo ◄ • H20 0.2:ZnSo ◄ • 7H20 O.OZ:Na 2 MoO ◄ ZH20 0.005:Ag ar 25: 증류수 ; p H 7.4 배지 B{g / Q ) aga r 제의한 배지 A 배지 C(g / Q ) 사탕무우당필 100:Yeast extr a ck Z:(NIL)2 HPO ◄ 5:M g So ◄ • 7H20 3:MnSo 』 • H20 0.2:Co(No 奭 6H2 0 0.1 8 8:5,6-Di ne th y l - benzim i da zol 0.025:ZnSo4 7H20 0.02:Na2 Mo04 2H2 0 0.005; 런 수:p H 7.4 그림 12.5 Pseudomonas den it r ifi can 혜: 이용한 비 E 뻔 81 최 실험실 규모의 생산공정
의 하나이다. 1 21,반 동안의 균주 개량 결과 이 공정의 생산량은 0.6m g /l 에 서 60mg / l 로 증가되 었다. 지난 1()1 ,1 동안, 다양한 알코올과 탄화수소를 비타민 B1 최 생산기질로 사용할 수 있는지에 대한 연구가 여러 균주를 대상으로 하여 진행되어왔 다(표 12.2). 그 결과 탄화수소와 고급 알코올을 이용한 비타민 B1 2 발효 는 수율이 적었지만 메탄올을 이용한 발효는 수율이 상당히 높았다.
표 12.2 탄소원으로서 alcohols 과 탄수화물을 이용한 비타민 8 12 생성 균주 탄소원 비타민 B12 수율 (m g/ Q ) Bacte r ia from acti va te d sludg e Meth anol 0.3 ~1.2% (w/ v) 35 Meth a nobacte n um soehn g em i Meth anol 0.8% (w/v) 8.0 Meth a nobacil lu s omehansk1 Met h anol 0.8% (w/v) 8.8 Prota m i no bacte r ruber Meth anol 1.2% (w/v) 2.5 Bacte r i um FM -02 T Meth anol fed -batc h cultu re 0.4 ~1.38 % (v/v) 2.6 Art hr obacte r sp. Isop ro p an ol, fed -batc h cultu re 1.1 Art hr obacte r hya l in u s Isop ro p an ol 1% (v/v) 0.5 6 Nocardia MT 2003 1,2-p r o p an edio l 5% (w/v) 0.78 Klebsie l la sp. 101 Et h anol 2% (v/v) 0.0 2 1,2-Prop an edio l 2% (v/v) 0.06 Meth anol 2% (v/v) 0.1 6 Meth anol, fed -batc h cultu re 0.5% (v/v) 1.3 Pseudomonas sp. A TCC 14718 Et h anol 1% (v/v) 0.05 1,2-pr o p an edio l 2% (v/v) 0.1 2 Meth anol 2% (v/v) 0.1 6 Meth anol fed -batc h cultu re 0.7~0.8% (v/v) 3.2 Str a in XF Meth anol 2% (v/v) 0.2 3
Pse u do m o na s ova/i s N-Decane 1O'(} (V /V ) 0.08 Pse u do m o na s aureof a c ie n s n-Dode can e 1% (v/ v) 0.04 No ca rdw gar dneri n-H e xadec ane 2% (v/ v) 4.5 혼합배양 Cor rn e ba clenum sp. and n-A l kanes 10% (w/v) 2.3 Rho do p s e u d o m o na s sph eroid e s ( Florent and Ni ne t, 1979 : Kam iku bo et al., 1978)
4 /3-카로틴 4.1 분포 및 경제적 의의 카로티노이드는 카로틴 (caro t ene) 와 크산토필 (xan t ho p h y ll) 을 포함하 는 용어로서 오로지 식물과 미생물에 의해서만 생성되며, 식물조직과 동물 조직에서 발견된다. p-카로틴 (pro vit am i n A) 은 내장의 점막에서 비타민 A 로 전환되며 간에 팔미트산(p alm it a t e) 에 스데르로서 저장된다. 사람에 게 있어서 비타민 A 의 결핍 (1 일 요구량 1. 5~2m g)은 야맹증과 피부 및 점막의 변화를 일으킨다. 특히 무코폴리사카리드 (muco p ol y sacchar i de) 의 정상적인 생합성에 필수적이다. 197 ()ld대 후반에 p카로틴의 수요는 연간 27 톤이었으며 주로 식용색소 로 사용되었다. 비타민 A 전구체에 대한 수요는 매우 낮다. 비타민 A 전구 체의 활성을 갖지 않는 리코펜 (l y co p ene) 이나 크산토필 같은 카로티노이 드는 식용색소나(예를 들면 마가린, 치즈, 달걀로 만든 식품) 닭고기나 난 황의 빛깔을 좋게 하기 위해 사료 첨가제로 사용되며 (cit rin a xanth ine 연 간 3~~) 소량은 화장품공업에서 경구용 t ann i n g제 (canth axanth in e ) 로 사용되는데 크산토필은 식물성분을 추출하여 얻을 수 있다. 카로티노이 드는 많은 미생물에 의해 생산되지만 현재 발효공정의 수율은 저렴한 화
학합성법과 경쟁이 안 되므로 발효에 의한 생산은 경제성이 없다. 그렇지 만 미생물학적 과정에서 수율이 상승하거나 화학합성법에서 원료물질의 단 가가 높아지면 발효법에 의해 카로티노이드를 생산하는 것이 더 경제적일 수도있다. 4.2 생합성 카로티노이드는 고도로 불포화된 이소프렌(i so p rene) 유도체이다. 자연 에 존재하는 카로티노이드는 &n 의 이소프렌 잔기로 구성된 테트라테르피 노이드(t e t ra t er p eno i d) 이다. 오늘날 자연 중에 40 眞은 이상의 카로티노이 드 화합몽기 존재하는 것으로 알려져 '있다. 그림 12.6 에는 미생물에 의해 생성되는 몇 종의 카로티노이드 구조가 나와 있다. p이오논 (P- i onone)
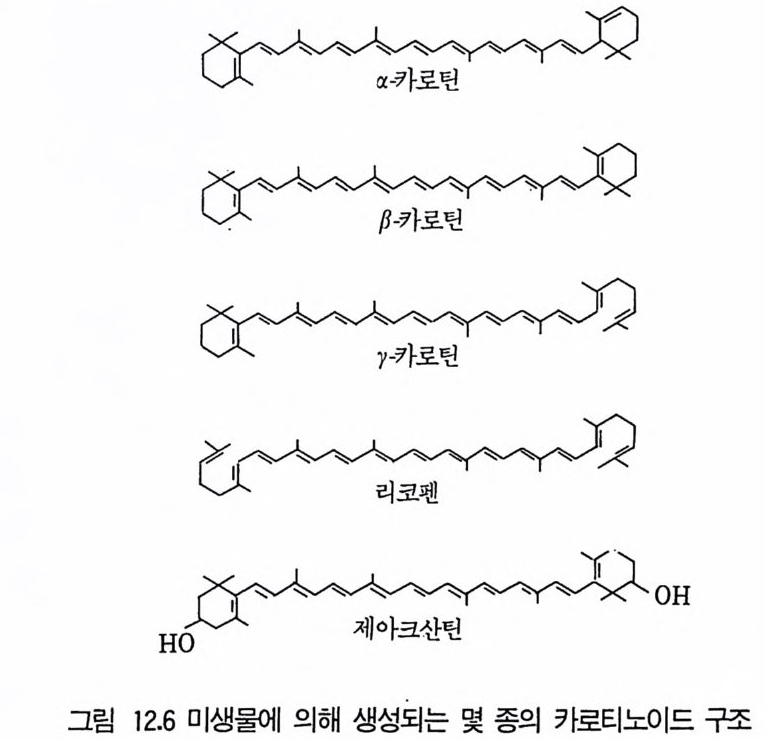 OH
OH
구조 (P-카 로딘 분자의 양말단에 있는 고리구조)를 가전 화합물만이 비타 민 A 전구체로써 활성을 갖는다. 따라서 p-카로틴으로부터 2 분자의 비타민 A7} 생성된다• a 와 Y-카 로틴은 각각 하나의 p이오논(/3-i onone) 고리를 가졌으므로 한 분자의 비타민 A 를 생성한다. 伯-카로틴의 생합성은 주로 식물과 곰팡이에서 연구되었으며 그림 12 . 7 에 나타난 것처럼 이소프렌 단위로 생합성된다. p-카로틴과 관련된 카로티노
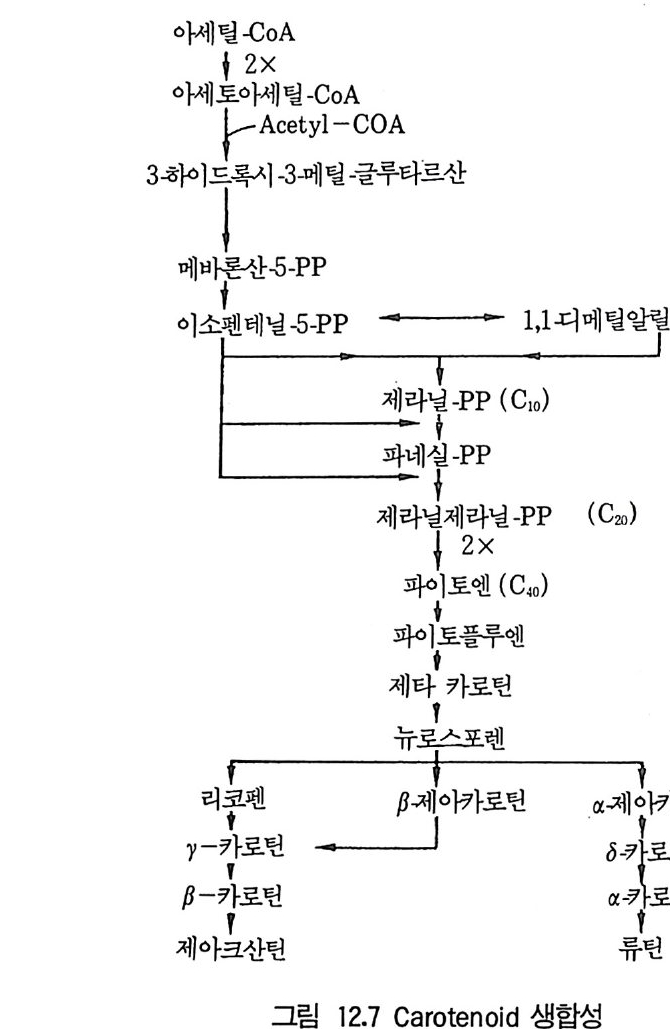 아이메세바소틸l론펜ttr-산 테2C- AX 닐 o5c A e -- tP5y P-lP - PC O-A 1,1 디메틸알릴 -PP
아이메세바소틸l론펜ttr-산 테2C- AX 닐 o5c A e -- tP5y P-lP - PC O-A 1,1 디메틸알릴 -PP
이드는 주로 곰핑이와 조류에 의해 생성되지만 크산토필은 세균과 조류에 의해 생성된다. 4.3 /J-카로틴의 생산공정 Blakeslea t r i sp ora 를 이용한 생 산아 가장 수율이 높다. 이 미생 물이 집 합포자를 형성할 때 카로틴이 생산된다는 사실은 공정개발에 의의를 지니 고 있다. (+)와 (-)균주의 양배양을 혼합했을 때 (-)균주에서 카로틴 생산이 현저히 증가한다. 밀접하게 관련된 물질들의 혼합물인 트리스포린 산(t r i s p or i c ac i d) (그림 12.8) 에 의해서 생산이 유도된다. 트리스포린산
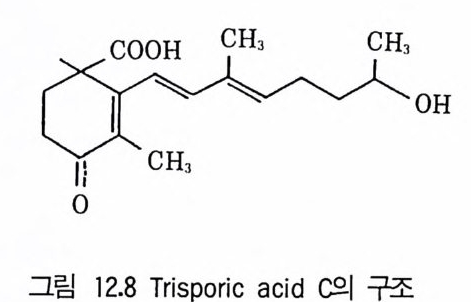 COOH ~H3 CHJ
COOH ~H3 CHJ
은 p-카로틴의 전구체는 아니지만 (+)-g amone( 성호르몬)으로써 작용하 는데 이들은 표지실험 결과에 의하면 8-카 로틴으로부터 생합성에 의해 유 래된다• (+)와、 ( ―.)균주의 혼합물을 액침배양하며 p-카로틴을 생산한다 (그림 12.9). 두 균주의 혼합비율은 동일할 필요는 없고 ( —) 균주가 p-카 로틴을 생산하므로 ( —) 균주가 과량으로 존재해야 한다• 또 다른 p-카로 틴 합성의 활성제는 p이오논과 혼합시킨 이소니아지드(i son i az i d) 이다. p이오논 단독으로는 생산균주에게 유해하지만 식물유와 함께 첨가하면 카로틴 생산을 촉진한다. p이오논 자체는 카로틴속으로 통합되지 않고 테 르핀(t er p enes) 과 사이클로핵산 (c y clohexane), 사이클로헥사논 (c y clohex-
~one) 이들의 트리메틸 (tri m et hy l) 유도체 등으로 바뀐다. 정제 등유를 배지 중에 첨가하면 생산량은 두배로 된다. 이들 물질이 카로딘 생합성 효 소를 유도하는 데 관여하는지 또는 투과성을 변화시켜서 지용성 카로티노 이드를 분비하여 최종산물에 의한 생합성 경로의 저해를 막는지에 대해서 는 아직 규명되지 않았다.
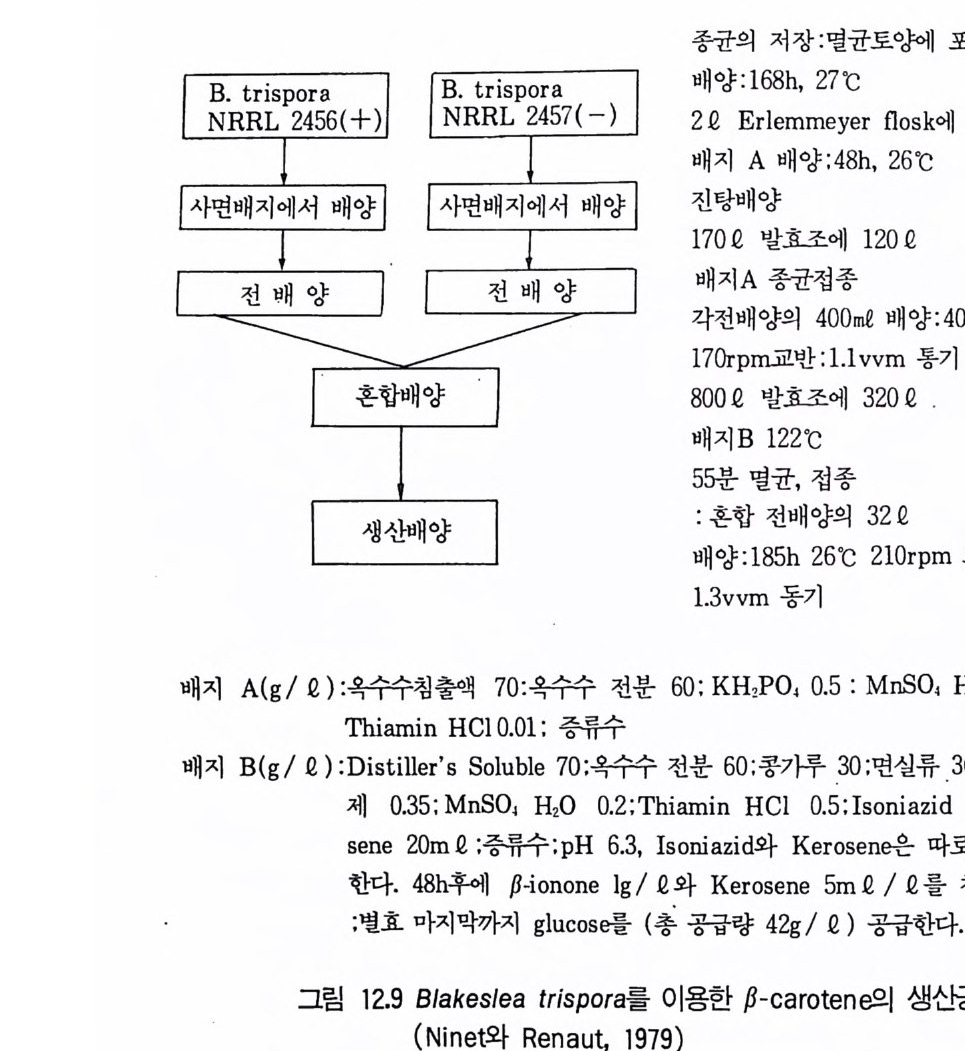 종균의 저장 : 멸균토양에 포자상태
종균의 저장 : 멸균토양에 포자상태
표 12.3 몇 종의 Carote n oid s 생산공정 Carote n oid 균주 배지성분 발효기간 T., `o£ (일) (mg / ( ) p-Ca rote n e Blakes /e a tns po ra NRRL 그립 12 .9 참조 8 3,00( ) 2456(+) 과 NRRL 2457(- ) 혼합배양 Lyc o p en e Stre p to m y ce s chresto m y ce ti cu s 전분, 콩가루, ( NH i ) cSO 』 6 500 subsp. rubescens Blakes/ea tns po ra NRRL 목화씨가루, 옥수수가루, 면 5 400 2895(+) 와 NRRL 2896( -) 실유 柏시간 후에 tri - 혼합배양 eth y l a m ine 첨가 (Caro t e- noid Cy cl iz a to n 억제 ) qo.)% Canote - My co bacte ri u m phl ei 사탕무당밀, Urea: 빛에 노출 7 300 noid s 혼합물 S. chresto m y ce ti cu s 포도당, Yeast ext ra st 5 500 Yeast sug ar , eth a nol or alkenes <5 (Ni ne t and Renaut, 197 9)
세포내에서 p-카로틴의 안정성이 낮기 때문에 발효공정중에 항산화제를 첨가할 필요가 있다. 카로티노이드가 풍부한 균사체는 사료 첨가물로 직접 이용할 수 있다. 晉한 p-카로틴을 얻기 위해서는 균사체를 제거하고 탈수시킨 후(예를 몽 메탄올로) meth y le ne chlorid e (75~92% 수득률)로 추출하여 얻은 조생산물을정제한다. 참고문헌 Demaio , A. L. 1972, Rib o fl av in oversy nthe sis , Ann Reu. Mi cr obia l . 26 : 369~388. Ka miku bo, T., M. Hay as h i, N. Ni sh io and S. Naga i , 1978. Ut i-
liza ti on of non-s u ga r sources for vit am i n B12 pro ducti on . Ap pl. Envir o n. Mi cro bia l . 35 : 971~973. Lag o, B. D. and L. Kap la n. 1981 . Vi tam i n ferm enta t i on s ; B 2 and B12, pp. 241~246. In ; Moo-Young , M.(ed). Advances in bio - tec hnolog y, Vol. III . Perga m on Press, Toront o. Ni ne t, L. and J. Renaut. 1979. Carote n oid s , pp. 529~544. In ; Pep- ple r, H. J. and D. Perlman(eds.), Mi cro bia l tec hnology , vol. I , 2nd edit ion . Academi c Press, New York. Perlman, D. 1979.-M i cro bia l pro cess for rib o fl av in pro ducti on . pp. 521~527. In ; Pep ple r, H. J. and D. Perlman(eds), Mi cro bia l tec hnology , . vol. I, 2nd edit ion . Academi c Press, New York.
제 13 장 항생물질 1 서론 항생물질은 다른 미생물의 증식과정을 저해하는 이차대사산물이다• 증식저해의 가장 잘 알려진 예는 192~ Alexander Fle mi n g에 의해 관찰된 것인데 이때 페트리 접시상의 S t a p h y lococcus 의 증식이 오영된 Penic il l i u m no t a t um 에 의해 저해된 것이다. 오염된 이 곰팡이가 항생물질 인 페니실린(p enic i ll i n) 을 생성한 것이다. 疾} 세계대전 동안 부상 감염 을 치료하는 화학요법제에 대한 요구가 페니실린 생산공정을 발전시켰고, 항생물질 (an ti b i o ti cs) 연구시대가 시작된 것이다. 이것이 오늘날 산업미생물의 가장 중요한 영역으로 자리잡게 되었고 모 든 국가에서는 집중적인 연구계획으로 항생물질의 발견이 계속 증가되고 있다• 196 짜에는 51 峰려 항생물질이 알려졌고 1974 년에는 4,0761 은, 그리고 해마다 약 20(} 종의 새로운 항균성 화합물이 발견되어져 왔고 1984년 에는 7,00()0 :j 종의 항생물질들이 알려져 있는데 적어도 그중 91종 은 발효에 의 해 상업적으로 생산되고 있다. 클로람페니콜 (chloram p hen i col) 과 피롤니트린(py rro lnit r i n) 은 원래 미생물 생산물로서 발견되었지만, 현재는 화학적인 방법으로만 생산되고 있다. 전세계적 항생물질 생산은 198Q ltl 한해 동안 추정되는 총판매고가
42 억 딜러였다. 미국에서만도 해마다 총판매고는 10 억 달러이고, 세팔로스 포린 (ce p halos p or i n) 을 선두로 해서 그 뒤를 암피실린 (am pi c il li n), 데트 라사이클린(t e t rac y cl i ne) 이 뒤따르고 있다. 사료 첨가용 항생물질은 해마 다 10 倍 달러의 세계시장을 가지고 있는 것으로 추정되고 있다. 1.1 항생물질을 생산하는 미생물집단 세균, 방선균, 곰팡이에 의해 생산되는 항생물질의 분포는 표 13 .l에 나 타나 있다. 곰팡이의 경우 Asp er gi lla ceae. 2} Mon i li ales 에 의해 생산된 항생물질만이 실제로 중요하며 Bas i d i om y ce t es 에서 분리된 화합물은 실 제로 사용되지 않고 있다. 그중 페니실린, 세팔로스포린 C, 그리세오펄빈, fus id i c ac i d 만이 임상적으로 중요하다.
표 13.1 미생물에 의해 생산되는 항생물질의 수분포 Type of pro ducin g orga n i sm Ap pro x im ate number Percenta g e Bacte r ia 950 9 Acti no my ce te s 4600 143 Fung i 1600 15 All micr oorga n ism s 7150 67 Lic h ens 100 1 Alga e 250 2 Hig h er pla nts 2500 23 Anim al orga n i sm s 700 7 All 'high er' orga n is m s 3550 33 Tota l 10700 100 (Berdy, ,] .. 1 984)
세균의 경우 항생물질을 생산하는 많은 종이 있는데 가장 다양한 것은 Acti no my ce te s , 특히 St re p tom y ce s 속게서 발견되고 있다. 또 하나의 중요한 군은 펩티드계 항생물질인데, 이는 Bacil lu s 속의 세균에서 생산된
다. 최근에 다수의 새로운 화합물이 다른 분류군에서도 분리되고 있다(제 2 장 참고). 생성하는 균주에 대한 항생물질의 중요성은 아직 불명확한 상태 이나 그 역할에 관해서는 Barabas7} 논하고 있다. 1.2 항생물질의 분류 항생물질은 항균범위, 작용기작, 생산균주, 생합성방법, 화학구조에 따라 분류할 수 있다. 각 분류 방식에는 몇몇 중복되는 부분도 있는데 표 13.2 는 단순히 화학구조에 따른 분류표이다. 이 장에서는 주로 경제성이 있는 중요한 화합물만 다루기로 하겠다.
표 13.2 화학구조에 따른 항생물질 분류 1. 탄수화물 함유 항생물질 Pure sug ar s (Noji rim y cin) Amino g ly c o sid e s (St re p tom y ci n ) Orth o somy ci n s (Everni no m ici n ) N-Glyc o sid e s (St re p tom y cin) c-G l yc o sid e s ( Vancomy ci n ) Glyc o lip ids ( Moenomy ci n ) 2. Macrocy cli c lac t on 폐 Macrolid e anti bi o t i cs ( Eryt hr omy ci n ) Polye n e anti bi o t i cs ( Candic i d in) Ansamy cins (Ri fam y ci n ) Macrote r tr o li de s ( Tetr a nact i n) 3. Qu in o nes 관련 항생물질 Tetr a cy cl in e s (Tetr a cy cl in e ) Anth r acy cl in e s (Adria m y cin) Nap h th o q uino nes ( Acti no rhod in)
Benzoq u in o nes (M itom y ci n ) 4. 아미노산과 펩티드계 항생물질 Amino acid deriv a ti ve s ( Cy cl oseri n e ) P-Lact am ant ibi o t i cs ( Penic i l li n ) Pep tide anti bi o t i cs ( Bacit ra cin ) Chromop ep tide s ( Acti no my c in s ) Dep si p e p tide s (Valin o my ci n ) Chelate - fo r mi ng pep tide s (Bleomy ci n s ) 5. 질소함유 He t er i c y chl i께 항생물질 Nuclesid e anti bi o t i cs (Polyo x in s ) 6. 산소함유 He t eroc y cl i폐 항생물질 Polye t h e r anti bi o t i cs (Monensin ) 7. Alic y cl ic 유도체 Cy cl oalkane deriv a ti ve s ( Cy cl ohexim i de ) Ste r oid ant ibi o t i cs ( Fusid i e acid ) 8. Aromati c 항생물질 Benzene deriv a ti ve s ( Cholr amp h eni c ol ) Condensed aromati c anti bi o t i cs ( Gris e ofu lv in ) Aromati c eth e r (Novobio c in ) 9. Alip h ati c 항생물절 Comp o unds conta ini n g ( Fosfo m y ci n s ) pho sp h orous (Berdy, 1974) ( ) : 대표적 안 항생물질
1.3 항생물질의 이용분야 화학요법제 : 항생물질은 병원성 미생물 퇴치 의약용으로 필수적인 위치 를 차지하고 있는데 많은 미생물에 대해 항균 범위가 광범위한 것과 제한 된 범위의 미생물에만 활성이 있는 좁은 항균 범위를 지닌 것이 있다. 어
떤 항생물질은 다음과 감은 다론 용도를 지니고 있다. 항암 항생물질 : 이러한 항생물질은 임상적으로 cyt os ta t i c 약제로 사용 된다(표 13.3 참고). 이러한 항생물질은 어떤 종류의 종양 치료에는 효과 적이다.
표 13.3 항생물질의 종류와 용도 • 주요 항암 항생물질 항생물질 종류 생산균주 Acti no my c in C1, C3 Chromop e p tide S. anti bi o t i cu s Adria m y ci n Anth r acy cl in e S. pe uceti us Daunomy ci n Anth r acy cl in e S. pe uceti us Chromomy ci n AJ C-Glyc o sid e S. gri se us Mi thr amy ci n C-gl y c o sid e S. pli ca tu s S. argi lla ceus, S. atr o oliu a ceus Mi tom y ci n C Benzoq u in o ne S. caespi tos us Bleomy ci n A2, B 2 Glyc op e p tide S. uerti cil l u s Neocar zi n ost a ti n Pep tide S. carzin o sta t i cu s
• 직물질병에 쓰이는 항생물질 항생물질(화학적 유형) 생산균주 Blasti cid i n S ( Nudleosid e ) S. gri se ochromog en es Polyo x in (Nucleosid e ) S. cacaoi uar. asoersis Prumy ci n (Nucleosid e ) S. Kaga w aensis Cy c lohexir nide (Am ino acid ) S. gri se us Kasug am y c in (Ar nino g ly c osid e ) S. Kasug ae nsis Valid a my c in ( Ar nino g ly c osid e ) S. hyg ro scop icu s uar. lim oneus Tertr a nacti n( Macrote r tr o li de ) S. flau eolus
식물병에 쓰이는 항생물질 : 항생물질은 식물질병조절에서 합성화학물질 보다 더 유용하다. 죽 항생물질은 저농도에서 선택적으로 적용할 수 있고 온혈동물과 천적에는 유독성이 적으며 보통 토양 미생물에 의해 쉽게 분 해된다. 처음에는 의약적으로 유용한 항생물질이 식물에 사용되었지만 현 재는 전적으로 식물에만 작용되는 항생물질이 발견되고 있다(표 13 .4참고).
표 13. 4 상업적으로 생산되는 펩티드계 항생물질 항생물질 생산균주 작용 적용:임상치료 Amp h omy c in Str ep tom y ce s canus G+ Bac itra cin Bacil lu s lic h enif orm i s G+ (G - ) Cap re orny c in S. cap re olus My Gram icidi n A B. breuis G+ Gram ici d i n S (J) B. brev is G+ Polym yx in B B. po lym y x a G- Tyrot h ric i n B. brevis G+ (bacit rac in - ty ro- cid in comp le x) Tyroc id i n B. breuis G+ Vi om y cin S. flo rid a e My 적용:사료첨가 Bacit rac in B. lic h enif or m is G+ (G - ) Sio m y c in S. sio y a ensis G+ Thiop e p tin S. tat e y a mensis G+ Thios t r e p ton S. azureus G+ 적용:식품보존 Ni si n St re p toc occus cremoris G+ • G+ :그람양성세균 (Perlman, 1979) • G- :그람양성세균 • My : my co bacte r ia .
식품 방부제로서의 항생물질 : 각 나라에서는 식품의 보존제로서 항생물 질 사용량을 정부가 규제하고 있다. 이용할 수 있는 화합물은 다음과 같 다. 1. Pim aric i n : 식품표면에 적용되는 살진규제 . 2. 티로신(ty los i n) : Bacil lu s 포자에 대해 효과적. nis i n , Clos t r i d i a 에 대해 효과적. 둘 다 통조림 산업에 사용. 3. chlorote t r a cy cl in e : 얼음 속에 5pp m 농도로 침투시키거나 침지액에 첨 가함으로써 생선, 육류, 가금육류의 신선도 유지에 사용. 동물 성장촉진제와 가축 질병의 치료에 사용되는 항생물질 : 만일 항생 물질을 치료농도 이하(1 ~lOm g /k g 사료)로 첨가한다면 그 동물 사료는 동물의 소화계에 효과적으로- 작용하여 체중 증가가 촉진될 수도 있다. 이 러한 성장촉진의 원인은 위 장관의 rni cro fl ora 의 변화에 의한 것인데 처음 에는 다량의 항생물질, 죽 페니실린, 데트라사이클린, 에리트로마이신 (er y thr omy ci n ) , 바시트라신 (bacit rac in ) , 스트렙토마이신 (str e p tom y ci n ) 같은 것이 사료에 첨가되었으나 그런 일반 항생물질의 사용 증가가 항생 물질에 대한 내성을 급속도로 증가시키는 위험을 조장했기 때문에 인체 의약품과 동물 사료에서 같은 항생물질을 사용하지 못하도록 정부 규제로 설정했다. 사료 목적으로만 사용되는 새세대 항생물질들은 표 13.52 -} 같다. 가축 질병의 치료에서도 항생물질의 사용이 규제되고 있다. 가축 질병에 서만 사용되는 항생물질은 hyg r omy ci n B, thi o s tr e p tin, · t ylo sin , coc-cid i o s ta t i c ag en ts , monensin , lasalocid , sali no my ci n 등기 있다. 생화학과 분자생물학 연구에 쓰이는 항생물질 : 선택적 저해제로서 항생 물질의 사용은 DNA복 제, 전사, 단백질 번역, 세포벽 합성, 물질대사 같은 세포 기능을 이해하는 데 중요한 기여를 했다. 이 영역에서 항생물질의 사 용은 저해제로서 또한 유전자 표지를 부여하고 내성유전자 도입에 의한 유전자 조작에 특히 널리 사용되고 있다.
표 13.5 동물 사료에 사용되는 항생물질 항생물질 분류 생산균주 Enduraci di n Pep tide 항생물질 S. fun g icid i c u s Mi ka my ci n Pep tide 항생물질 S, mi tak aensis Sio m y ci n Pep tide 항생물질 S. sio y a e nsis Th iop ep tin Pep tide 항생물질 S. tat e y a m eusis Th ios tr e p ton Pep tide 항생물질 S. azureus Vi rg iniam y ci n Pep tide 항생물질 S. uir g i ni a e Macarbomy ci n Phosp h o gly c o lip id S. ph aeochromog en es Moenomy ci n Phosp h o gly c o lip id S. bambergi en sis Qu ebemy ci n Phosp h o gly c o lip id S. vir i d a ns Ty lo sin Macrolid e S. frad ia e Mocim y ci n Hete r ocy cl ic 화합물 S. ramocis s im us (Perlma n, 1979)
1.4 항생물질 연구의 목적 196 떠 이전에는 새로 분리된 항생물질의 약 5% 가 치료 목적으로 사용 되었다. 그 후 새로운 항생물질이 대략 일정한 비율로 발견되었으나 시장 에 실제로 나온 새로운 항생물질의 비율은 1961~1965 년에는 2.6% 에서 1966~1971 년에는 l% 로 감소했다. 이것은 주로 개발과 임상시험에 드는 비용이 증가했기 때문이며, 치료용으로 확실히 쓰일 수 있는 화합물만을 생산하기 때문이다. 이미 알려진 많은 화합물들을 고려해볼 때 새로운 항생물질에 대한 연 구가 계속 수행되어야 하는지는 의문점이 제기되나 연구되어야 할 이유는 다음과같다. 1. 많은 경우 자연 그대로의 항생물질의 특징은 치료에 적합하지 않다. 따라 서 독성을 감소시킴과 함께 더 강한 활성, 부작용의 감소, 항균 범위의 확
대, 병원균에 대한 선택성의 증대, 약물학적 특 성의 향상 등의 개선이 요 구된다. 의학적 혹은 비의학적이거나 농업적 모든 영역에 광범위하게 사 용가능한 항생물질은 없다. 2. 화학요법이 시작된 이래 내성균주들의 수가 증가되어 다중내성과 교차내 성이 발생될 수 있다. 만일 한 항생물질에 내성이 생기면 그 내성은 동시 에 같은 유형의 작용기작을 가진 다른 항생물질에 대해서도 생기게 된다. 현재 내성문제를 극복하는 유일한 선택은 새로운 항생물질의 발견이다. 개량된 항생물질은 화학적 또는 유전학적 방법을 통하여 알려진 화합물을 구조 수정함으로써 얻어질 수도 있다. 그러나 전적으로 새로운 기본구조를 가전 항생물질은 오직 선별, 특히 새로운 시험방법을 사용함으로써, 그리 고 새로운 미생물집단을 연구함으로써 기대할 수 있다. 2 /3-락탐({J -lac t am) 계 항생물질 페니실린, 세팔로스포린 (ce p halos p or i ns), 세파마이신 (ce p ham y c i ns) 은 독특한 구조를 가전 펩티드계 항생물질이며 지난 몇 년간 반합성 화합물 질과 monocy cl ic P-lacta m s, clavams, carhape nems 같은 또 다른 자연 형태의 p-락탐환 구조가 분리되었다(A ck i, 1980, Demain , 1980). 2.1 페니실린 페니실린은 192~ Fle mi n g에 의해 발견되었다 Ox fo rd 에서 Flore y와 Chain 등의 연구팀이 194 ()l;:젼 Fenic i ll i u m no t a t u 짜긱 표면배양에서 페 니실린을 분리해내었고 페니실린의 최초 임상시험은 1941 년에 실시되었다. 페니실린은 많은 곰팡이, 특히 Pen i c illi um 속과 Asp ergi llu~ 예 의해 생성 되는데 천연 페니실린은 수많은 그람양성세균에 대해 효과가 있으며 산에 봉간정하고 P-lac t amases 로 P- 락탐환을 절단함으로써 불활성화된다. 페니
실린은 독성이 낮아 다량의 페니실린을 두여할 수 있으나 일부 환자는 알 레르기 반응을 나타낸다 (0.5~2%). /J-락탐 항생물질은 세균의 세포벽 (pe p tido g ly c a n) 합성에 특이한 저해 제로서 펩티도글리칸(p e pti do g l y can) 사슬의 중합을 촉매하는 tra nspe p - ti dase 와 D-alani ne carboxy pe p tida se 부위에 작용한다. 이 항생물질은 증식히는 세포는 죽이지만 휴지세포는 죽이지 않는 특칭을 지니는데, 이는 증식하는 세포만이 새로운 세포벽을 합성하기 때문이다. (1) 화학구조 (chem i cal str u ctu r e) 페니실린의 기본 구조는 6 아미노페니실린산 (6-am i no pen i c i llan i c acid , 6-APA) 으로 티아졸리딘 (t h i azol i d i ne) 환과 축합된 p-락탐환으로 구성되 어 있다. 6-APA는 떠치에 그림 13 .1과 같이 여러 아실 (ac y])기를 지닌 다. 만일 페니실린 수효가 측쇄 전구체의 첨가없이 실행된다면 천연 페니 실린이 생산된다. 이 혼합물로부터 벤질페니실린 (benz y l p en i c illi n) 만이 치료용으로 유용하며 다른 화합물들은 분리 정제단계에서 제거되어야 한 다. 발효는 측쇄 전구체를 가함으로써 목적하는 페니실린을 효율적으로 생 성할 수 있다• 10 ()7}지 이상의 생합성 페니실린이 이 방식으로 생산되어왔 다. 그러나 싱업적 공정에서는 페니실린 -G, 페니실린 -V 가 주로 생산되어 왔다. 반합성 페니실린을 생산하기 위해 페니실린 G 를 화학적 또는 효소 적으로 분해하여 6-APA 를 생성시키고, 6-APA 에서 화학적으로 다론 페니 실린 유도체를 만든다• 2 ()7}지 이상의 반합성 페니실린이 상업적으로 생산 되고있다. (2) 생합성조절 페니실린의 p-락탐 티아졸리딘 (P-lac t am t h i azol i d i ne) 환은 L 시스데인 (L -cy st e i n) 과 L- 발린 (1-va li ne) 으로 구성된다. 생합성은 L 시스테인, 1- 발린, 1-cx-am ino adip ic ac i d(L-cx-AAA) 로 구성된 트리펩티드에 의해서 비리보솜 (nonr i bosomal) 과정으로 생성된다. 트리펩티드 고리화의 첫번째
R 『’II NHH 三 1 CH3C H 3 0 / 4 ••• C000 (N a© , K@ ) H p_락탐환 티아졸리딘 환 I 아실잔기 | 6 아미노페니실린산 명칭 N- 아실잔기 R. 자연 페니실린 벤질페니실린 (페니실린 G) OcH2- c o-cH3 -c o- • 2- 펜텐닐 페니실린 (페니실린 F) CH3 -C H2 -C H=CH-CH2 - co- • n( 페- 니아실밀린 페 D니i실hy린 d ro F) CH 3 (CH 2 ) ◄ -co n- 헵틸 페니실린 (페니실린 K) CH3 (C H2 )6 - c o- · P(-페 하니이실린드 록X시) 벤질페니실린 HO-( 〉 -CH 2 一 CO- 데니실린 N( 시네마틴 B)D-4- 00 0C-CH-(CH2)3-CO- 아미노 -4- 카르복시 -n- 부틸페 사H 3 D 니실린 。 • 이소페니실린 N (L-4- 아미노 - 00 0C-CH-(CH2 )3 -CO- 4- 카르복시 -n- 부틸페니실린) 油 · 메틸페니실린 생합성 페니실린 • 벤질페니실린(p en -G) :산 불 안정성, P-lacta m ase 감그수람入음j 성 세균에 낮은역가 . O—C페H닐 아2 세C O트 산 • 유페:산사녹 시안한정메특성틸성, 페페니니실실린린( pG e 와n- V) 0—0-페C녹 시H 아2세- C 트O산 • 알沼릴르멀]캅토성메 틸감 소페 니실린(p en -0) 1 H2C양=립C H멀-C캅H토2 -아S 세-C트H산2 -C O-
반합성 페니실린 ·:프산로 안피정실성린. P-lacta m ase 감수성 O 。 _H 12 CcH - _C cHo:I _ ·(··(산특메옥카독안히티사르히정 실실벤p그성린린니s람e 실up음d린-o성:m락세광타o균n범메a)s이위 스 a 劑e감ru수g성i n o sa) O0—C-H三\NCl -HHC2 - COD (0 C—- - Co H) J : 산 안정성. P-lacta m ase 저항성 :산 안정성. P-la c ta m ase 저항성 · 암피실린:광범위 항균력 산 안정성 . 경구투약시 효과감소 C00° N a0 p-락타메이스 감수성 그림 13.1 자연 페니실린, 주요 생합성 페니실린, 여러 반합성 페니실린의 구조 (Qu eener, 1970)
산물로 분리되는 것은 이소페니실린(i so p en i c i l li n) N 이지만 이 중간물질 까지의 생화학 반응은 밝혀지지 않고 있다. 벤질페니실린은 1-rJ.- AAA 대 신 활성화된 ph enyl a ceti c ac i追i 교환시켜 생성시킬 수 있다(그림 13. 2). 6-APA는 생합성의 중간산물은 아니며 측쇄 전구체의 결여된 물질이 다. 페니실린 생합성에는 몇몇 제어 기작이 알려져 있다. 아미노산인 리신 (ly s i ne) 은 1-rJ. -amin oadip ic ac i d 를 포함하는 경로에서부터 합성되고 따 라서 페니실린과 리신은 공통분지 (common branched) 생합성 경로롤 공 유한다. 리신은 1-a - AAA 합성에 관여하는 효소인 호모시트르산 합성효소
(homocit ra te s y n t hase) 의 최종산물 저해제이므로 페니실린 합성을 저 해한다. 만일, L-a-AAA7} 결핍되면 페니실린은 합성될 수 없지만, 소량의 L-a-AAA7} 첨가되면 페니실린 합성을 촉진한다. 리신에 의한 호모시트르 산 합성효소 저해는 페니실린 형성의 · 저해보다 더 적으므로 추가적인 제 어과정이 가정된다(그림 13.2, Marti n, 1979).
IX- 케토글루타르산 + 아세틸 _CoA r- . _ . _ . ―--기-동형시트르산합성효소 :’i11} 시동스형동_이형동소시형IlI시트 아트르코르산니산 트 산 최종산물저해 1X- 케토I아 디프산 a- 아미노아디프산 억제 (a.- AA) ,--------7-\ 一 b- 아데닐 -a/ .1- AAL_I ,L-.,a-/.~-< A ~AA -AL--LC-Cy sy s -D-Val 8- 아데닐-a. -AA I \ L.. 1굿- 리세b신핀미--세A알 미-A데/ 알 --히데b-드-히- 드 - -i...|!II L-cx페\- 닐A\ 아A세-\G틸 A -A6SA AS (이소페니실린 N) 벤질페니실린 그림 13.2 Penic i l/ ium chrys o g en um 균주에서 L- 리신에 의한 페니실린 생합 성 제어 (Mart in, 1979)
(3) 균주 개발 Flem i n 터 분리한 균의 페니실린 생산은 약 2 IU/ml 였 다. 최근 공정수 율은 약 85,000u nit /ml 의 역가를 지닌 페니실린이 생산되며, 이것은 0. 0012 g /l로 부터 약 50 g /l 까지 증가함으로써 균 주 개량계획의 중요성을 보여준다. 초기의 균주 개량은 194 :31
빈형 임펠러가 사용된다(1 20~150r p m). 일부 생산회사들은 Waldhof 발 효조나 공중보급 발효조를 사용하는데 이것은 낮은 점성을 지닌 돌연변이 균판]만 가능하다. 배양 최적온도 범위는 25~27°C 시이이며 페니실린 생산의 전형적 공정도는 그립 13.3 에 있다. 접종은 동결전조된 포자롤 사 용한다. 수율이 높은 균주들은 역가의 보존을 위해 취급상 주의해야 한다. 묘퓸도와(최적 5xl03/ m l) 소균주의 형성은 수율에 필수적 요건이 된 다. 최적 페니실린 생산율에 도달하려면 p elle t은 느슨한 형태로 성정해야 한다.
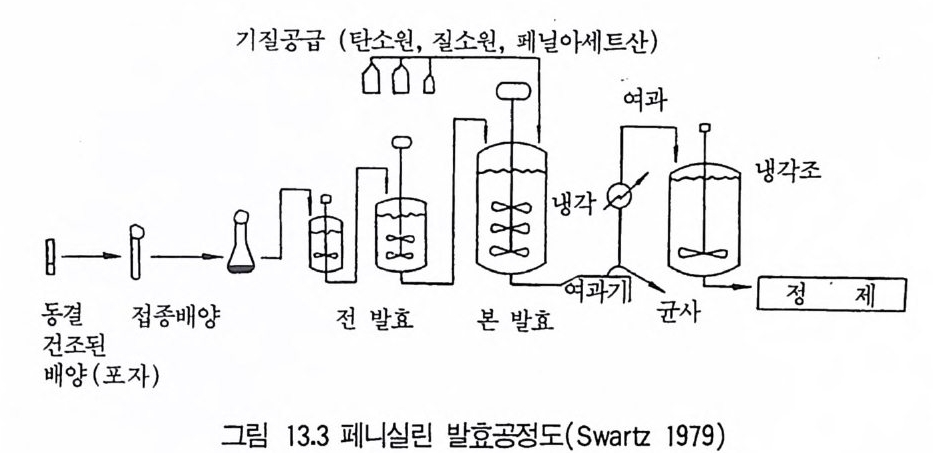 二건조된 』」기 질 공 급凰 (탄소三원, 질소」원,二 페1 균닐 아세트二산· 여)과 二工]
二건조된 』」기 질 공 급凰 (탄소三원, 질소」원,二 페1 균닐 아세트二산· 여)과 二工]
증식의 몇몇 성장단계 후에 생산배양에 들어가게 되는데 성장기는 약 4 이간 동안이고 배가 시기는 앙]간인데 이 기간 동안 균체 생산이 대부 분 형성된다(그림 13.4 참고)• 배양에 있어서 점도의 증가가 산소전달을 방해하므로- 산소공급은 중요 하다• 이는 발효조의 설계, 또는 점도를 감소시키는 변이주를 사용함으로 써 해결할수 있다• 전형적 인 Fed-batc h 배양배지는 균주에 따라 다르나 보통 다음과 같은 배지 구성으로 되어 있다.
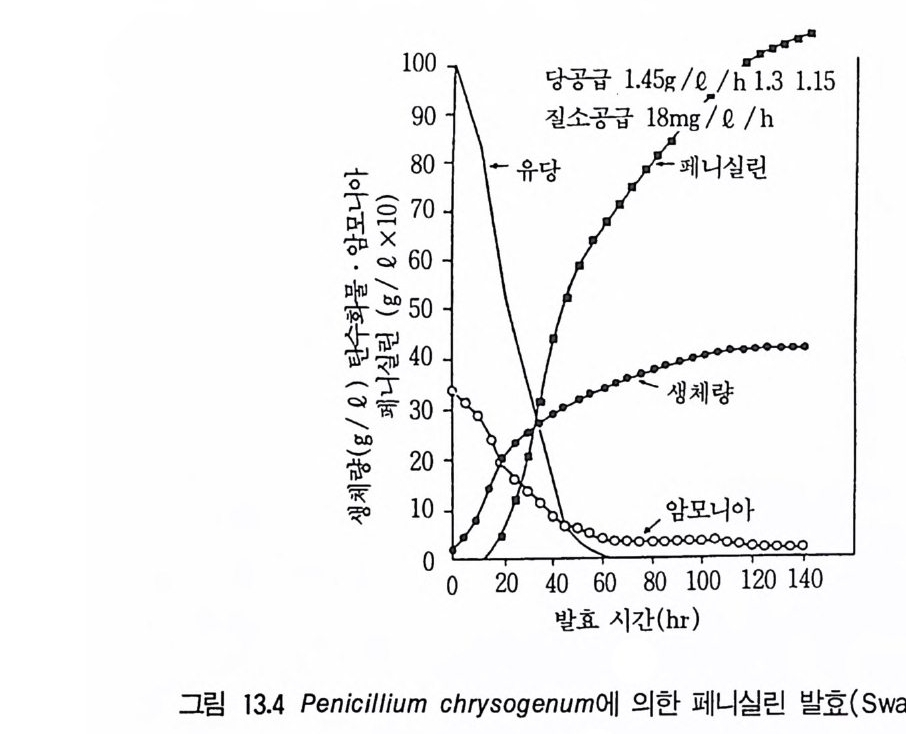 100 당공급 1.45 g /Q,,_. I h/ 1 .3 1.15
100 당공급 1.45 g /Q,,_. I h/ 1 .3 1.15
1. 옥수수 침출액 (건조중량 4~5%) 2. 대두, 효모추출액, 유장 등 추가 질소원 3. 유당등의 탄소원 4. 여러 완충용객 p H 는 6. SoJ]서 일정하게 유지된다. 페닐아세트산이나 펜옥시 아세트산(p henoxy aceti c ac i d) 은 전구체로 서 일정하게 공급된다(전체의 0.5~0.8). 공정 중 포도당이나 당밀을 공급 하는 것도 결과가 좋다(전체의 10%). 포도당과 초산을 가함으로써 25% 생산량 증가가 보고되었다(J ensen, 1981). 이들 Fed-batc h 배앙에서 중요한 변수는 당이용율과 산소공급률이다• 페니실린의 연속발효생산이 시도되었으나 생산균주의 불안정성으로 인하여
R~ 三to; CH , -R , '-락탐 환 디하이드로티아전 환 분 류 R, II R, 7스-모 아라이닉노산세 (7판 -로 A CA) -NH , -0 -C O - C H, -H 자인세안로스보린스 -co 세만로스포린 -C I -0- C O-CH ., -I I 내아세인내 . -키르 ((:IH, ), -0 - C O-NII, -H 바오인 •I 판로스보린 C (D) CIH -NH , ?_에목시세안보 coo 。 -0 - C O-CH, -O CH1 스모린 C 세피아이신 A -oco - C - C HOSOo,H ~O CH, 세파아이신 B oco- c -C HO OH -O CH, 0I- CH, 세파마이신 C -0 - C O-NH, -O CH, 반 합성 세안로스보린 Ccp h alot in Q cHH, ';N 0 -0 - CO -C H , .H Ccp ha le, in OyN lOtH · H -H 그림 13.5 세파로스포린 C • 세파마이신과 반합성 세파로스포린의 구조
다. 7 -ACA는 항판격이 없지만 N 이실화에 의해 항균력이 회복되므로 부 분합성 세팔로스포린의 중요 원료가 되며 미생물학적으로도 직접 7-ACA 룰조제할수있다. (1) 생합성 (Treic h ler, 1978) 벤질페니실린의 경우에서처럼 cep h alosp o rin 생합성의 첫번째 단계는 & (a - ami n oa dipyl} -L -cy st e i n y l-D -va li n 합포료부터 이소페니실린 N 까지 계
속된다(그립 13.6 참고). 고리화 활성이 Cep h alospo riu m acremon i u 짜나 cell- fr e 예에서 발견되었지만 효소들에 대한 자료는 없다. 다음 단계에서
L-a-ALALAD+_L t트 一리 C 펩y s타+L이-드V al t 이소페니i실 린 N (L 국 -A라AA세-메A이PA스) (페D니 굽실 _린A ANA —AP A) (D) H it F의se 한2+ ,환 아형스성코 르촉브진산 , ATP 에 a_AAA ―0 \亡 k~CH J COOH 데아세톡시세팔로스포린 C 더 Fe2+ · °무브산, a- 케토 글루타르 (D) H 산s에 의해 촉진된 탈산소효소 a_AAA_ON二 二\ CH2 0H COOH 데아세틸세팔로스포린 C :nr>CH 36 c-CoA (D) H s CH2 0 CO CHJ a_AAA-N 丁二〈 COOH 세팔로스포린 C 그림 13.6 Ceph a/ospo riu m acremon i u ni.랸隨 의한 세팔로스포린 생합성 (Treic h lev. 1978)
봉간정한 racemase 작용을 거쳐 L-a-AAA 결사슬에서 D 형으로의 전환 에 의해 페니실린 N 이 생성된다. 페니실린 N 의 고리확장에 의해 dea-ceto x y ce ph alosp o rin C 가 생성되고 산화와 아세틸화 acety la ti on 후 세 팔로스포린 C 로 전환된다. 페니실린과는 달리 D-a-AAA 부분은 전구체를 가하므로 변형시킬 수는 없다• 세팔로스포린 생성은 탄수화물, 이화물질 억제와 인산조절의 영향을 받 으며 저농도의 리신을 첨가하면 세팔로스포린 생성이 촉진되고 과량의 리 신에 의하여 생긴 저해는 DL-a-AAA를 첨가함으로써 극복될 수 있다 (Mehta et al., 1979). 메티오닌은 C. acremaniu m 균주에서는 세팔로스포린 합성을 촉진하지 만 Str ep t om y ce s 균주에서는 촉진하지 않는다. (2) 균주 개발과 발효 생산 균주 개발은 돌연변이, 선택, 준유성생식(p arasexual) 기술을 사용하여 원래 Bratz u 균주인 C. acremoniu m CMI 49137 돌연변이주는 황화합물 에 저항성이 있기 때문에 분리되는데, 세팔로스포린 생성을 증가시키거나 메티오닌과 마찬가지로 무기황산을 이용한다. C. acremon i um 에서 준유성 적 재조합(p arasexual recomb i na ti on) 이 일어나기는 어렵다. 왜냐하면 균사의 격실은 거의 항상 단핵이므로 융합실험에서 다른 균주들의 원형질 체를 사용함으로써 반수체 재조합체가 분리되며 세팔로스포린 C 생성이 40% 증가함을 나타낸다. 세팔로스포린 O 기 고생산균주에 의한 역가는 약 30 g /l이 다 (KAIST Rep o rt, 1989). 세팔로스포린의 발효는 페니실린 발효와 비슷하다. 옥수수 침출액, 서당, 포도당, 초산암모늄의 복합배지가 시용되고 발효온도는 25~28·C , p H는 7. ()ol]서 실행된다. 주요 증식기 (9 ()A]간까지 )에서는 높은 통기율이 필요하 지만 생산기 (90~16 ()A]간) 동안은 0 최 소비가 급격히 감소한다. 세팔렉 신 (ce p hale xi n) 은 페니실린 V와 G로 부터 화학적으로 직접 생산할 수도
있다 (chame tte et al., 1971). 2.3 새로운 p-락탐계 항생물질 페니실린 세팔로스포린 C 串즌 구조가 다른 새로운 p-락탐계 항생물질에 대한 폭넓은 연구가 진행되고 있다(그림 13.7 참고). 이는 광범위한 항생 물질이나 P-la c ta r nase 저해제로서의 활성이 있으므로 반합성 유도체와 갇 은 이둘 새로운 화합물가 치료에 유용하게 쓰일 가능성이 기대된다.
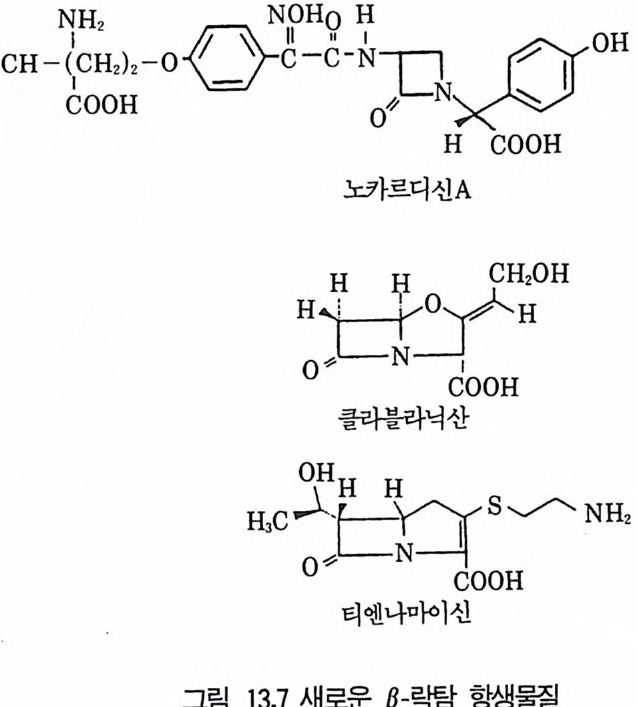 CH -1 CH。 三0 2 ;-Oo?\ 三 OH
CH -1 CH。 三0 2 ;-Oo?\ 三 OH
(1 ) Nocardic i n s Nocard ici퍼 Nocardia unif orm i s sub sp. tsu ya m anensis 2} Str - ept om y ce s alcalop h il u s sp. no 대서 생성된 monocyc l ic P-lac t ams 인데
(Aoki et al., 1976), nocardic i n A 는 그람음성세균에 대해 주로 효과적 이며 펩티도글리칸(p epti do g l y can) 생합성계의 저해작용이 있다. (2) . Clavulanic acid Clavulanic ac i d 는 p-락탐옥사졸리딘 (P - lac t am -0 xazo li d i ne) 환 구조인 데 이는 Stre p to~ y ce s clavulig en us 균주에 의해 세팔로스포린과 함께 생 산된다 (umezawa et al., 1973). Clavulanic ac i d 는 항균적으로 그 효과 가 미약하지만 0.1 µg/ ml 이하의 농도에서 광범위의 P-lac t amases 를 저 해한다. 이 저해는 비가역적이다. P-lacta m ase 감수성 페니실린과 세팔로 스포린을 동시 투여함으로써 p-락탐 항생물질에 저항성이 있는 세균에 대 해 항생물질의 활성을 현저하게 증가시킨다. (3) Th ien amy ci n s T hi enam y c i諺 보통 g-락탐피롤린 (P-lac t am- py rro li ne) 환 구조를 가 지고 있다. 매우 비슷한 구조를 한 일련의 카바페넴 (carba p enems) 계에서 첫번째인 t h i enam y c in-f는 197 料에 Str ep tom y ce s Catt ley a 배양에서 분 리되었다 (Kahan, J. S. • et al. , 1979). T hi enam y c i n 은 P-lacta m ase 저 해제로 작용하고 Pseudomanas aeru gi nosa 를 포함하여 그람양성세균과 그 람음성세균에 대한 광범위 항생물질로서 작용하며, 이 화합물은 극도로 불 안정하지만 합성유도체의 발달로 인하여 안정성을 향상시키려는 시도가 행 해지고 있다. 3 아미노산과 펩티드계 항생물질 이 부류의 항생물질에는 사이클로세린 (c y closer i ne), 아자세린 (azase rin e ) 같은 아미노산 유도체 , 이미 다룬 p-락탐계 항생물질, 크로모펩티드 (chromo pepti de) 계 항생물질, 뎁시펩티드 (de p s ip e pti de) 계 항생물질, 선
상 또는 환상 펩티드계 항생물질이 있다 (Z i mmer, 1979). 3.1 D- 사이클로세린 (D-cy cl oserin e ) D -4 -am i no-3- i soxazo li don 인 사이클로세린은(그림 13. 8A 참고) 합성
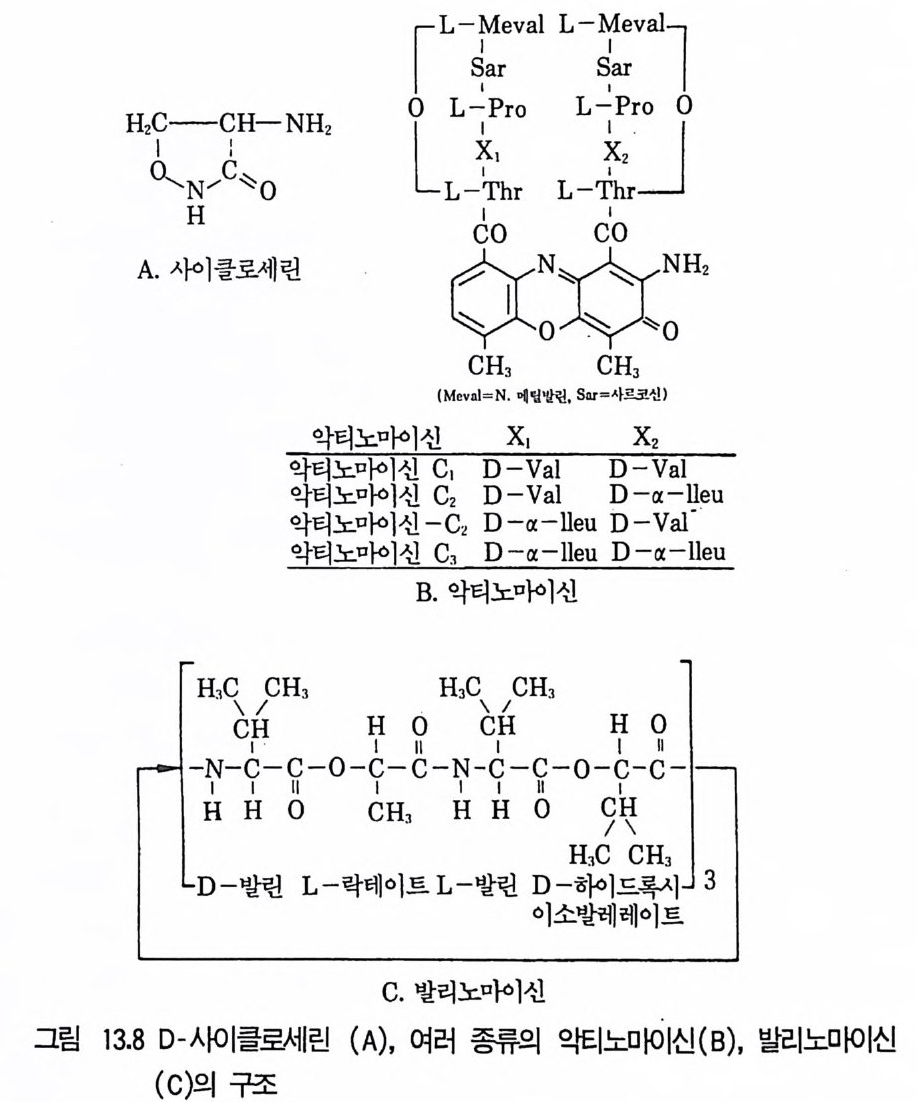 L广L仁-~ t:r,e va l L:L --i~:; vjaHll 2
L广L仁-~ t:r,e va l L:L --i~:; vjaHll 2
햐겨 생산되거나 Str ep t om y ce s orchid a ceus, S. lavendulae, S. gar - yph alus, 또는 S. roseochromo g enes 의 배양에 의해 생산된다. D 시이클로 세린은 펩티도글리칸의 D 세린 생성에 작용하는 alan ine racemase½ 저 해함으로써 세포벽 합성을 저해한다• 사이클로세린은 My co bacte r iu m tu- berculos i예 특히 효과적이고 iso nic o ti ni c acid h ydraz i de(INH) 와 rif- amp ici n 또는 스트렙토마이신 (s t re pt om y c i n) 과 함께 조제되어 결핵 치 료에 사용된다• 3.2 Chromo p e pti de 계 항생물질 이 부류는 악티노마이신 (ac ti nom yci n) 을 포함하는데(그림 13.8 B 참 고) 악티노마이신은 매우 비슷한 물질의 혼합물로서 특히 Str ep t om y ce s an ti b i o ti c 국 S. chry so mallu.s oll 의해 생산된다. A, B, Ci, C2 i-C z, C:i, D, Fi, Zo- 乙 등의 악티노마이신은 ph enoxazone-c h romop h ore(acti no - c i n) 을 가지고 있는데, 그것은 업 n 의 펜타펩티드 락톤(p en t a p e pti de lac- t ones) 에 결합되어 있다. 이 두 가지 락돈(l ac t ones) 은 아미노산 배열이 다양하고 발효액에 다른 아미노산을 가함으로써 307} 지의 악티노마이신이 생합성된다. 3-hy d roxy -4-m eth y la nth r an ilic acid 2 분자로부터 악티노신 (ac ti no c i n) 의 생성이 펜옥사진 합성효소(p henoxaz i ne s ynt hase) 에 의해 촉매 된다. 이 효소는 성장기로 전환한 후에만 생성되고 포도당에 의한 현저한 이화대사 산물 제어를 나타낸다. 악티노마이신의 펜옥사존(p henoxazone) 환은 DNA 의 5I-T-G-C-A-3I 회문구조에서 G-C 쌍에 끼여들어감으로써 DNA 의존성 RNA 중합효소 (RNA- p ol ymerases) 를 저해한다. 악티노마이신은 매우 유독하여 간과 신 장장애를 유빌하지만 암 치료에는 효과적이다. 암화학요법에 사용되는 가 장 중요한 악티노마이신은 닥티노마이신 (dac ti nom yci n, acti no my ci n C1) 이다.
3.3 De p s ip e pti de 계 항생물질 De p s ip e pti d 예에서는 그 소단위이체 (아미노산, hy d roxy ac i d) 는 보 통 es t er 와 acid ami de 결합이 번갈아가면서 이어진다. 바리노마이신 (vali no my ci n ) (그림 13.8 C 참고)은 St rep tom y ce s fu lu i ss i mus 에 의해 생 성된 c y clododecade p s ipti de 인데 이는 경제적 중요성은 없지만 uncoup - ling ox ida t ive ph osp h ory la t ion 시약으로서 생화학적 연구에 이용된다. 그것은 K+ 이온의 선택적 결합으로 인하여 K 운반물질로서 유용하다. V i r gini am y c i n 군의 항생물질도 또한 dep si p ep tide 구조를 가지고 있 으며, 구조적으로 다른 macrocy cl i c lac t on~(A 형과 B 형)의 혼합물로 구성되어 있다 그림 13. 얌든 vir g ini am y ci n S(B 형 )의 구조이다.
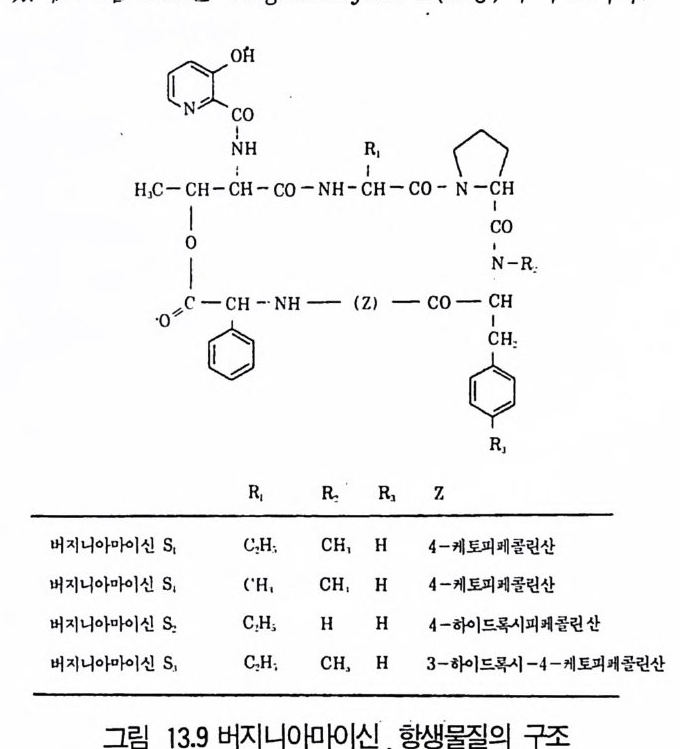 0·e\ x-N;?:HH -(Z)F - [c广
0·e\ x-N;?:HH -(Z)F - [c广
V i r gini am y c i n 계 항생물질들은 그람양성세균에 효과적이고 가금류, 돼 지, 송아지의 성장촉진제로서 널리 사용된다. 이들 중 17개 종류가 상업적
으로 생산되는데 그중 중요한 것은 mi kam yci n 과 v i r gi n i am y c in:이며 Str ep tom y ce s mi tak aensis 또는 S. v i rg i n i a 려 의해 생산된다. 3.4 선상과 환상의 pe p tide l-ll 항생물질 (Lard y, 1967)
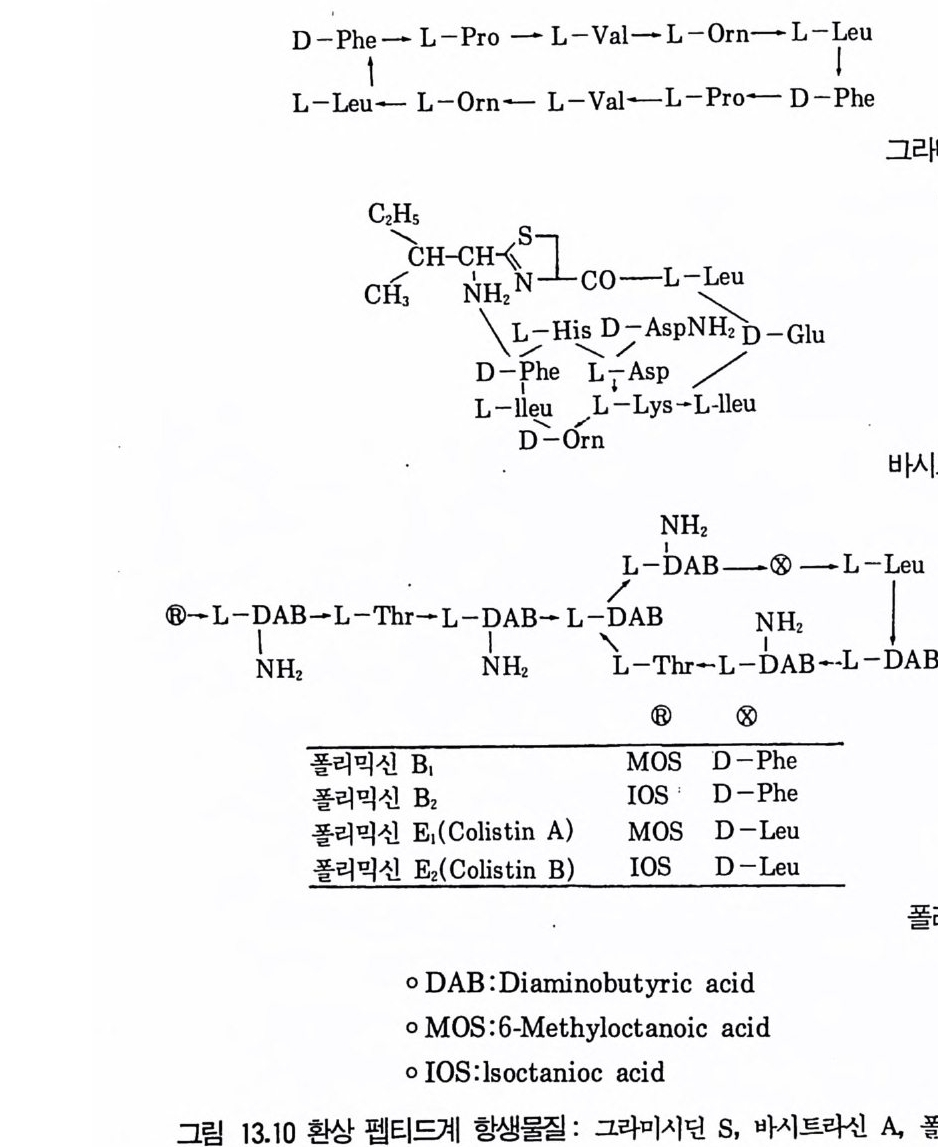 D-Phel 一 L- P ro 一 L - Val-L - Orn 一 L - LIe u
D-Phel 一 L- P ro 一 L - Val-L - Orn 一 L - LIe u
Bacil lu s 속에 의해 생성된 대다수의 항생물 질 은 펩티드계이며, Str - ep t omy ce 예 의해서도 생산된다. 몇몇 펩티드계 항생물질은 선상이지만 (g ram i c i d i n 계 ), 대부밝즌 환상화합물인데 아미노산만을 함유하거나 아미 노산 이의에 다른 구성성분을 포함한다(그립 13.1 0 참고)• Bac i ll i u 폐 의 해 생성된 펩티드계 항생물질은 포자 형성 개시기에서 형성되고 포자 형 성 과정에서 조절역할을 하는 것 같다. 펩티드계 항생물질의 치료상 적용은 그 독성 때문에 제한되어 있으나 그라미시던(g ram i c i d i ns), 선상그라미시던 (l i near gra m icid i n s ), 티로시 딘(ty ro ci d i n), 바시트라신은 부상, 화상, 피부이식 등 국소적으로 사용된 다. Polym i xi~ 그람음성병원균 (Pseudomonas 포함)에 의한 감염에 사용 되고 v i om y c i n 과 ca p reom y c i~본 결핵 치료에 사용된다. 3.5 바시트라신 (bac it rac i n : Joh nson, 1945) 바시트라신은 펩티드 항생물질 중 경제적으로 가장 중요한 국소적 항생 물질이며 동물 사료에 성장촉진제로서도 사용된다• 사료공급시 바시트라신 은 Zn 또는 Mn염으로서, 리그린바시트라신 {lign in - bacit rac in ) 혼합물 로서, bacit rac in meth y le ne d i s ali c y la t료서 공급되며 전세계 바시트라 신 총생산량은 197~ 텨 50~ 겨 이르는 것으로 추정되었다. B. lich eni- form i s 의 여러 균주가 바시트라신 A, A', B, C, D, E, F, Fi, F2, F:i, G 의 혼합물로 생성된다. 바시트라신 A 가 주요소(약 70% )이고 가장 큰 생 물학적 활성을 가지며 BL 괴. 4D ..o}미노산으로 구성된 dedeca p e pti de 이 고 사이클릭 헥사펩티드 (c y cl i c hexa p e pti de) 와 티아졸린(thi azo li ne) 환 구조를 모두 포함한다(그림 3.1 0 ). 바시트라신은 펩티도글리칸 생합성에서 세균 세포벽의 형성을 저해한다. 이는 C5 .5-is op re ny l pyro p h osph ate 7 } C5. 5-iso p re ny l p has p ha t료 가는 탈인산화를 억제한다 (S t one, 1971).
펩티드 항생물질의 생합성은 단백질 합성 장치가 관여하지는 않고 대신 다효소 혼합물에서 일어난다. 이러한 비리보솜성 펩티드 합성과정은 th i- o t em p la t e7] 작기라 하며 여기에 gra mi ci d i n S, tyro cid i n , lin e ar gra - micidi n s , bacit rac in 등이 해당된다. Bacit rac in syn th e ta s e 소단위체 A.B. C 로 구성되며 그 분자량은 각각 200,000, 210,000, 380,00 ()o]다. 바시 트라신 생산공정은 그림 13 .1 1 과 같다. 이 공정의 수율은 약 9g /l로 균주 개발과 적정배지를 통해서 증가된 것이다(J ohnson et al., 1945, Wri- nch, 1957). 고정화된 세포를 사용하며, bac it rac i n 을 생성하는 연속배양 과정이 개발되고있다•
접종 보존 ; 사면한천 혹은 멸균토양에 포자현탁 지\... 타0 배18양- 2 .V- l, 간 : 42X00lmQl 트삼립각톤 풀 혹라은스 크펩에톤 배양액 37°C pre fe 전r m배en양t조e r ((전 80 0발 Q효 ) 조) : 전당배양과동일 8] 간 37'c 생산본전 배 발배양효양조조조 (’’9 ( 03,000000통3대 7QQ기수° C) ) 증 배식양 ;l l :: 대대((NN두두IILL 5)5)%%z2 sS,, oO서서 ◄◄ 당0당0..2 2%2%1..,24, %% CC aaCCOOJJ 00.2.2%% 정 P3()A]간 37C a: 제약용 ~n- 뷰탄올로 추출. 유기충을 완충객으로 재추출. 히수층눕축, 이온교환 크 라아토그라피 b: 동물사료용~전체 발효액을 분무 건조 그림 13.11 B. /ich enif or mi s 균주에 의한 바시트라신 생산공정도 (Perlman, 1979)
3.6 Bleomy ci n Str ep t om y ce s uer ti c i llu 려 배 0~식 으로부터 구리 를 함유하는 청색물질이 발견되어 p hleom y c i n 이라 했는데 그람양성 및 음성균에 유효하며 항종양 작용을 나타냈다 (Maeda et al., 1956. Ikekawa et al., 1964). 이어서 1966 ',1 p hleom y c i n 과 유사한 bleom y c i ns 은 Str ep t om y ce s uer ti c i llu 펴 배양버으로부터 Cu( II ) 혼합물로서 분리되었다 (Umezawa et al., 1966). 嗣코펩티드(g l y co p e pti de) 는 상피암에 항암물질을 나타내고 bleomy ci n A 와 B~ 혼합물로서 판매된다. Bleomy ci n A~ 아민부인 3-am ino p ro - pyl d i me t h y lsu lf on i um 을 배 0~석 에 첨가하면 bleomy ci n A i만 선택적 으로 생산되고 다른 bleom yci곱접 생산이 억제된다 (Fu ji, 1973). 4 탄수화물계 항생물질 단수화물계 항생물질은 치료용으로 중요한 amino g ly c o sid e s, orth o so- m y c i n 러 여러 당유도체를 포함한다. 4.1 Gly cos i de 와 당유도체 Noj i r i m y c i n( 그림 13.1 2 A) 은 Sarcin a lu t ea 와 Xanth o monas ory- za eit에 대 해 항균력 이 있고 a 와 p-glu cosid a ses2 } am y las 려 대한 높은 저해력이 있기 때문에 관심의 대상이 되고 있다. Vancomy ci n. ?:- Str ep t om y ce s ol i en t al i예 의해 생산되는 글리코펩티드 (gl y co p e pti de) 계 광범위 항생물질인데 이 것은 amino suga r vancos- amine , 2 P-hy d roxy c hlorty ro sin e 부분, 3-ph eny lg ly c i n e 유도체 , N- meth y l leucin e , asp a rti c acid .£. 구성된다 (Rey nold, 1961). Van- com y c i퍼 그람양성세균의 세포벽 합성을 저해하며 (Ni et r o et al.,
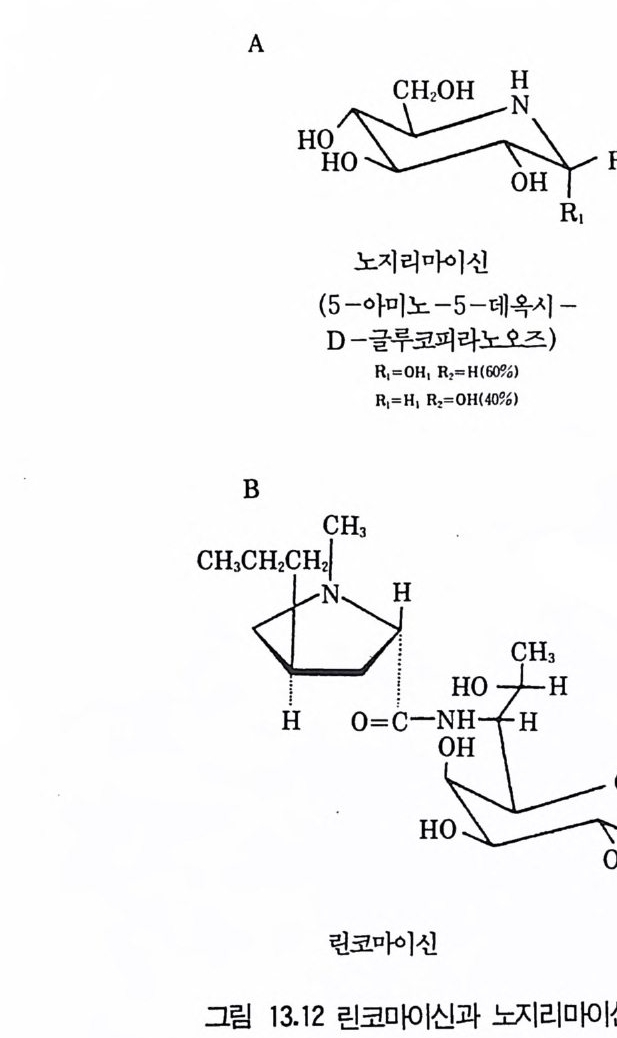 A
A
1971), 특히 S t ap hy lococc i에 효과적이지만 사람에게는 부작용이 있으므로 다른 항생물질에 저항성이 있는 병원균에 대한 감염치료에, 또는 페니실린 에 과민성이 있는 환자에게만 사용된다. Vancom y c i n 에 대한 저항성은 치 료시 아직 발견되고 있지 않았다. Li ncom y c in(그립 13 .1 2) 은 Str. li nonens i폐 의해 생산된다 (Herr, 1962). Sta p h y l o coccus 감염치료에 사용되며 약한 부작용만 관찰하고 치료
문J- 내성이 빠르게 얻어진다. Clin d amy ci n (7-c h lor-7-d e oxy -l in - com y c i n) 은 약물적 특성이 향상된 반합성 유도체인데 이는 linc omy ci n 에 첨가되어 판매된다. 단백 질 합성에서 리보소음 (r i bosome) 의 A 결합 回에 대한 ami no acy l t RNA 의 결합은 li ncom y c i n 에 의해 저해되는데 켈은 펩티딜기 전달효소(p e pti d y l t rans fe rase) 를 저해한다 (Scoln i c k, 1989). Moenomy ci ~ 내성 플라스미드를 함유하는 그람음성세균과 그람양성 세균에 대해 활성을 나타내는 p hos p ho g l y col ipi d 이다. Moenomy cin A 와 관련 항생물질인 macarbomy ci n , q uelem y c in{든 동물 사료 첨가제의 용도로 판매된다. 이들 항생물질의 작용점은 펩티도글리칸 생합성에서 인 지질 중간체 lip id- p p -M ur NAC(-Gle NAC)- p en t a 쳅티드가 폴리머 (p ol y mer) 화하는 중합반응을 tra nsgl y c o sy la ti on 반응게 영향을 끼치므 로 세균 세포벽 합성을 저해한다 (N i e t ro, 1971). 5 아미노글리코시드 (am i no g l y cos i de) 계 항생물질 아미노글리코시드계 항생물질은 o lig osacchar i d 하 1 물질로서 스트렙토 마이신, 가나마이신, 겐타마이신, 네오마이신 등이 대표적인 것이다(그림 13.1 3 ). 이들은 항산균, 포도상구균, 그람음성균 등에 강한 살균작용을 나 타내며, 연쇄구균, 폐렴구균 및 형기성균에는 효과가 낮다. 반합성 세팔로 스포린은 그람음성세균 감염에 널리 사용되기는 하지만, 십각한 감염에서 는 ami no g l y cos i des 가 종종 사용된다. 스트렙토마이신과 dih y d rostr e p tom y ci ~ 광범위 항생물질이며 주로 결핵 치료에 사용되며 염색체 돌연변이에 의해 내성이 빠르게 전달될 수 있으므로 내성균에 유효한 새로운 아미노글리코시드계 항생물질의 연구 개 발이 왕성하게 추전되고 있다.
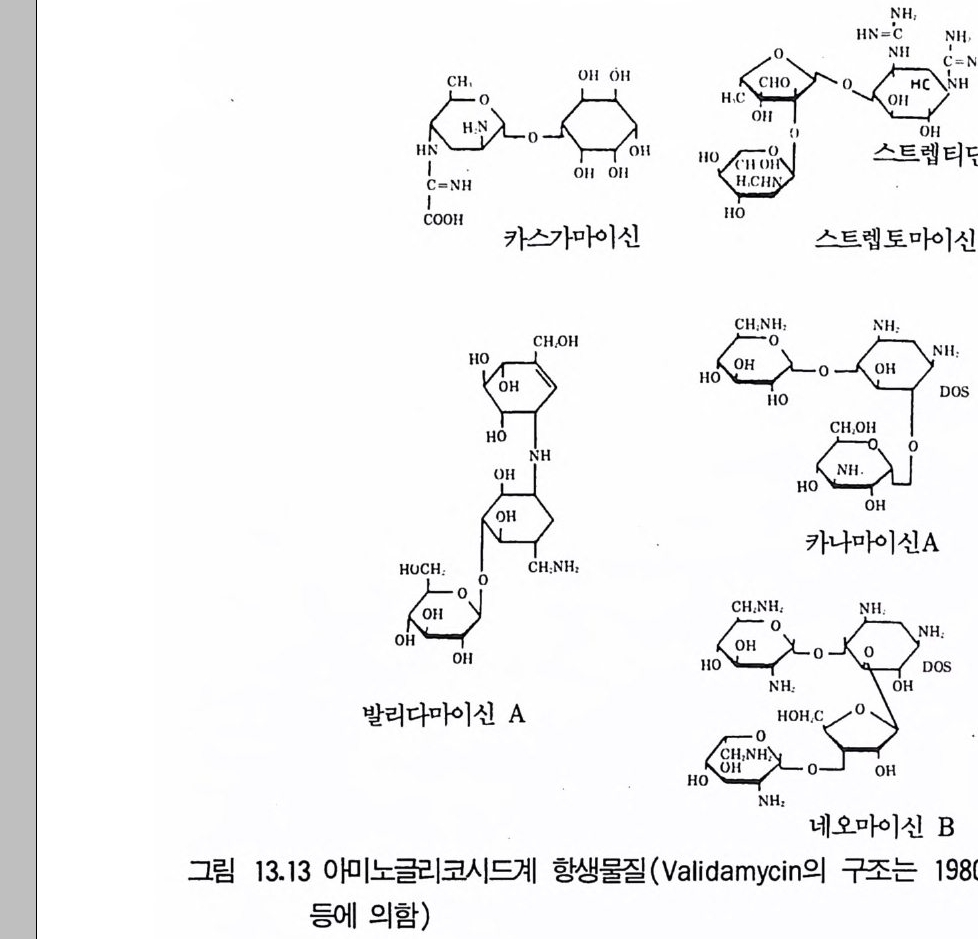 I1尸 。 딘 H 습출N스= 펜C 트 렙티\R\H 딘 N, II
I1尸 。 딘 H 습출N스= 펜C 트 렙티\R\H 딘 N, II
모든 아미노글리코시드 항생물질은 부작용으로 신장의 장애와 난청현상 을 유발하며 내성전개에 덧붙여서 불활성화시키는 효소 생성 p las mi d 에 의한 내성이 알려져 있다. 검색사업의 결과로서 fo r tirni c i ns 의 새로운 군 이 발견되었으며 특히 아미노글리코시드 내성세균에 대해 광범위한 활성을 지닌 p seudod i sacchar i de s;i처다. 가나마이신 유도체인 arnika cin (1 - N-L (-)-r-am ino -a-hy d roxy b ut_y n ylk anamy ci n A), bekanamy ci n ( 2:am i- no-2'- d e oxy k anamy ci n B), dib e kacin ( 3', 4 '-d ide oxy k ana rnici n B) 와 ne tihni c i n(1-N -tit h y ls i so rnici n) 은 불활성화 효소에 부분적으로 저항성
이 있는 반합성 화합물로서 이들 화합물은 임상적으로 이용되며 인체 치 료에 유용한 항생물질들 이의에도 kasu g am y c i n 과 val i dam y c in{든 벼의 도열병과 문고병에 중요한 항생물 질 로서 농약용으로 사용된다. (1) 아미노글리코시드 항생물질의 작용기작 아미노글리코시드는 단백질 합성계 , 특히 reborn 려]의 mRNA 의 기능 킹녕I 를 일으키는 저해제이다. 스트렙토마이신은 30S 소단위체와 결합하며 (Si, S4, S,2 } 결합 )(schre i ner, 1974) 스트렙토마이신의 감수성, 내성을 지배하는 리보솜 (r i bosoma l) S1 2 에 영향을 주며 단백질 합성의 개시반응 즉 30S 개시복합체 (ini t iat i on comp le x) 형성을 저해하게 된다 (Oku yam a A et al., 1971). 리보솜 단백질 (r i bosomal pro te i n ) S1 놈 아미노 야실(ami noac y l t RNA) 과 fM e t-t RNA 의 결합으로 A -sit려 구성요소 로서 활성이 있다. 2 검 eoxy s t re pt am i n e½ 함유하는 항생물질은 pep - ti d y l- t RNA 의 이동을 저해한다. 아미노글리코시드는 또한 세균의 세포막 에 손상을 유발시켜서 그 세포로부터 낮은 분자량 세포 성분의 손실을 초 래한다. (2) 아미노글리코시드의 생합성과 제어 (Walker, 1979) 방사선 동위원소 실험에서 밝혀진 바에 의하면 포도당은 시험된 모든 아미노글리코시드(ami no g l y cos i de) 항생물질의 소단위체 (sub unit)의 전 구체이고 일부 효소 반응이 밝혀졌지만 어떤 아미노글리코시드 항생물질의 정확한 생합성은 아직 밝혀지지 않았다. 스토렙토마이신 생합성 중 str - e ptidi n 峰 생성하기 위해서 두 개의 평행 번응사슬이 가설되었고 거기에 서 두 개의 구아니딘 잔기가 아미노 전달효소 (am i no t rans fe rase) 에 의해 서 계속 도입된다. S t re pt os 혁근 4-ke t o -6-d eox yg lucose -d TD~ 를 통해서 생성되며 이어서 deh y dros t re pt ose -d TDP는 st re pti d i ne -6 -P와 연결된 다. N-meth y 1- L-gl u cosami ne i:-메 틸 (me t h y l) 기 공여체로서 메티오닌과 함께 글루코사민-6 -P( g lucos ami ne -6 -P) 로부터 생산된다. DOS 아미노글
표 13.5 주요 아미노글리코시드계 아미노사이클로헥시놀 부분에 따른 분류 (산업적으로 생산되는 항생 물질 의 생산균주, 항균범위, 적용에 대해 기록) 군항생물 질 생산균주 항균범위 적용 SI tS ret rpe t pid tia nm e i ne 유도St체r e p tom y ci n Str ep t om y ce s G+ G - M y Human the rap y sANtcr- Dte ipn i mta am em ti h in ny e e l( -)N , SDtopim hec yy t dci nir noo sm tyr ec pi n - C gSSSr... i sfshepluau emvs c oti pad b eu rissl bii sc u s 하G+= G - M y aHH(nPuute m mngiaaco innn l ol icttnohh• cree cerrsi aa)i s pp t y y • Bluensomy ci n (S.b lu ensis ) Il 2-Deoxy st r e p tam i ne (DOS) 유도체 AN(P. es4oe,~u5dy-D oci t i ns e ut 군~b s- ti t uPNt eaed ro omD~y OocmSin ys c i B~ , C SS. ;firma do siua es fon ns GG+~ GG -- HHuummaann tthhee rraapp y y Rsaic bco hsatra im d e y sc)i n 군 LRIi iv, b i od I slo tma ym ciy n cs i nA , B pSSa.. r orliimub ioo d smui dsy ic f i inc uu s s PGGr+ + . :•o GG t o --z o a HHuummaann tthhee rraapp yy (Pseudot ri s a - Buti ro sin s (Bacil lu s corclil a ns) ccharid e s) BK.a n4a,6m-Dy cisi un b 군sti tuKt ead n aDmOy Sc i n s S. kanamy ce ti cu s G+' G - M y Human the rap y TAo, bBr,a mCy ci n S. ten ebrariu s G+ G - Human the rap y S( =elNdoembyr acmi n sy ci n fac( Sto . r l w6f) u n ensis ) Genta micin 군 G1C, ei, 2n ,t Ca 31m,. , i5c Ci n2 s pMoi r car opmuo rpnou sr-e a G+G- Human the rap y M. echin o spo ra Sag amici n = (M. saga m i en sis , etc . ) SGiesn ot am miciciin n C2b M.in j oe nsis G+ G - Human the rap y Verdami ci n (M. gri s e a) tCu. t eM d o nDoOsSub sti - HD ey sgtro o m my y cci i nn s B S(S. . h ryig mro o f~a ocp ie inc su) s wGo+ rGm - sF mVeetde ir c iin n ae r y A, B, C Ap ra my ci n (=Nebramy ci n - ( S. ten ebrariu s ) fac to r 5)
~ Forti m i ci n M. oliu o aste r - G+ G - Human the rap y 윤 osp o ra Sannamy ci n s (S. san nanensi s sp. n ou .) A, B Sp o raric i n s A, B (Saccharop o lys p o ra hir su ta subsp . kohensis Ista m y ci n s A, B (S. tenj i ma rie n sis nou.s p . ) ~ Valid a my ci n s S. hyg ro scop icu s G •G F Plant pa th o log y amino cy cl ohexanoK] a유su도g체 am y ci n Sua.kr .a s luimg a o ennesniss i s G+ • G - F Plant pr th o log y a. • 하 : 그람양성세균에 대한 항균효과 • G :그람음성세균에 대한 항균효과 My : m y cobac t er i a 에 대한 항균효과 • F : 항곰팡기 항생물질 b. Di h y dros t re pt om y c i n 은 s t re pt om y c i n 의 화학적 감소에 의해 생산된다. c. S t re pt om yci n 은 amino cy cl it ol 부분 가지나 아미노당은 갖지 않는다 .(Berdg 1974, Rein h art and Str o shane, 1976, Perlman, 1979)
리코시드( DOS-a m ino g ly c o sid e s )에서 (표 13.5) 2 -
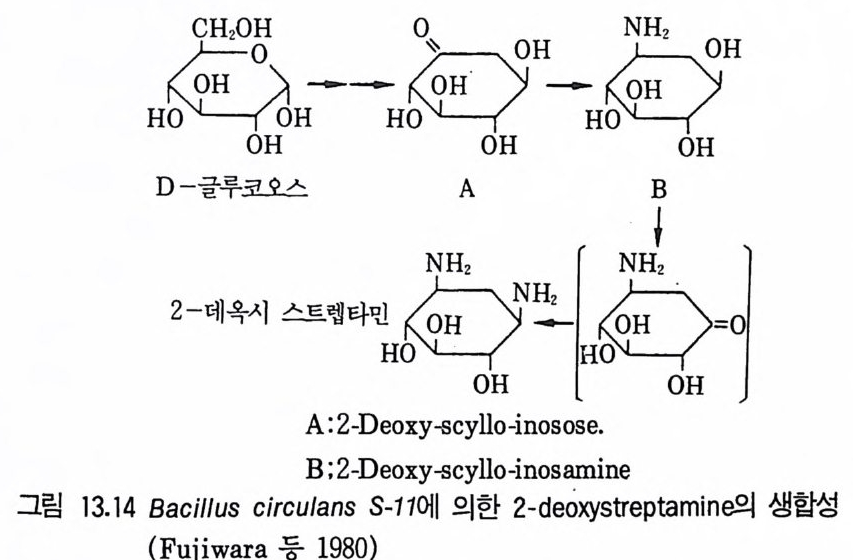 H〈 H -- -H 尸 H-H:H
H〈 H -- -H 尸 H-H:H
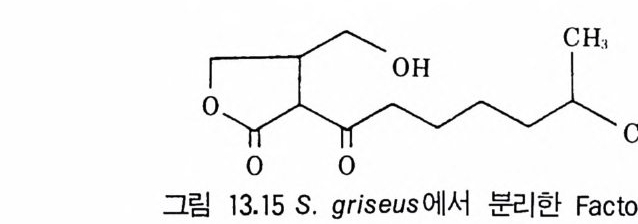 CH,
CH,
토마이신 합성과 포자생성 동안 그들의 능력을 상실하고 amidino t ra ns- fer ase 수준은 동시에 낮아짐으로써 fac to r A는 유도과정에 관여한다. 배 양 초기에 순수한 화합물 l µg을 fac to r A - 돌연변이주에 가하면 스트렙토 마이신 lg 생성이 유도되므로 fac to r A 는 전구체가 아니다. 질소조절, 탄 수화물조절과 무기인산의 조절은 또한 아미노글리코시드 생합성에 영향을 미친다. (3) 균주 개발 균주 개발계획은 모든 산업적으로 생산되는 아미노글리코시드 항생물질 의 수율 증가를 위해 중요하다. 스트렙토마이신 생산 수율은 균주 개발기술에 의해 초기 100~200µg /ml 에서부터 약 l5 mg /m 까지 증가되었으며 현재 생산량은 많은 경우에 서 알려진 값보다 훨씬 높다. 돌연변이와 단세포 검색법이 균주 개발에 사용되는 보편적 방법이다. 재 조합(접합과 원형질체 융합)이 사용되는 몇몇 경우도 있다. Kas- u g am yci n의 균주 개발이 전형적인 예이다.
최적산소공급은 통기율 0.5~ l. Ovvm 이고 중성 p H 에서 28~30 °C 에서 발 효된다. 전분이나 덱스트린 (dex tr i n) 을 포함하는 포도당이 탄소원으로 사 왕탄다. 원래 항생물질 bu ti ros i퍼븐 탄소원으로서 글리세롤로만 생성될 수 있는데 이는 포도당에 대한 대사물억제 (cata b olit e rep re ssio n ) 때문이 다. 그러나 대사물조절 (cata b olit e reg ula ti on) 에 무관한 돌 연변이주의 분 리로서 포도당 사용이 가능하게 되었다. 대두(콩)는 대사가 느리므로 아미노글리코시드 생성에서 이상적인 질소 원이고 NaC l( l~3 g /l) 은 스트렙토마이신, 네오마이신, 가나마이신 발효 에 첨가해야 한다 . gen ta m i ci n , sis o mi ci n , for ti mici n A 의 생성은 Co 狂 첨가에 의해 촉진되고, Co 2 + 는 생합성 동안 메틸 (me t h y l) 화 단계에서 활 성이 있다. 아미노글리코시드 발효과정은 특히 buti ro sin 발효에서 (그림 13.1 6 ) 증
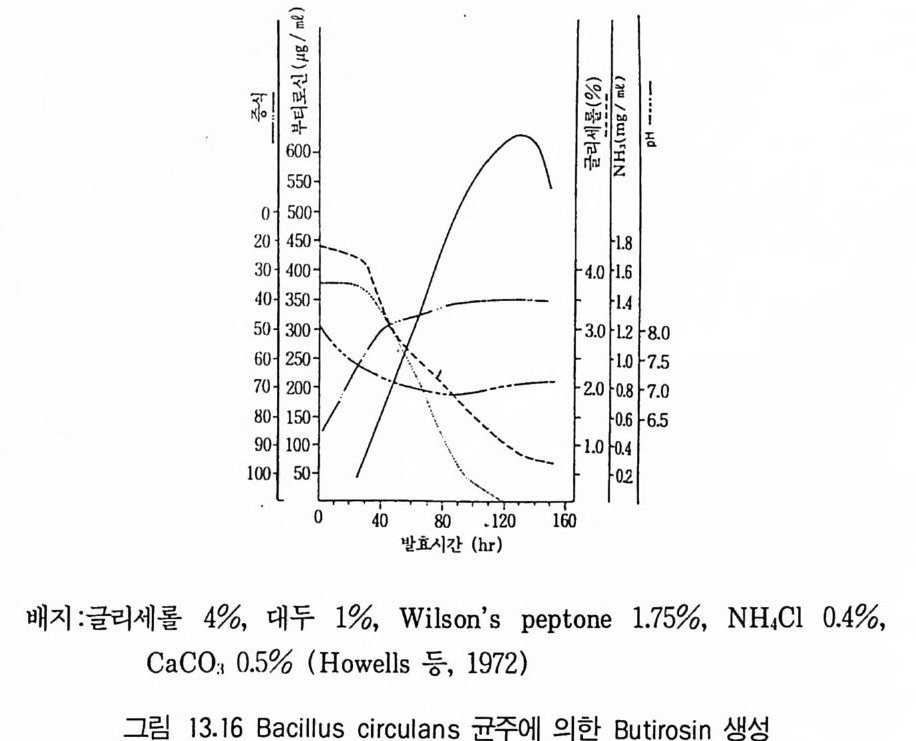 얻lg
얻lg
식기와 생성기를 가전 전형적인 이차대사 발효이다. 대부분의 아미노글리코시드 항생물질은 배설되고 나서 배양 상정액으로 부터 이온교환수지 칼럼에 흡수됨으로써 분리된다. gen ta m i ci n , sis - om ici n , for ti m i ci n 같은 세포내 아미노글리코시드는 우선 H:S O & 사용 햐겨 pH 2~2. 또료 산성화시킴으로써 추출시킨다. 6 Macrocy cl i c l acto n e 계 항생물질 마크로리드 (macrol i des), 폴리엔(p ol y enes), 안사마이신 (ansam y c i n) 이 이 군에 속한다. 이 부류에 속하는 항생물질은 메틸 (meth y l) 곁사슬을 가전 다원화 락톤(l ac t on) 또는 폴리엔(p ol y ene) 이라 하는 4~7 개의 공 역 이중결합을 가진 다원환 락톤을 지니고 있기 때문에 Woodward 에 의 해 마크로리드 (M i cro li de) 라 명명되었다. 이들은 방선균 또는 Mi cr omo- nos p ora 에 의해 주로 생산되고 실용적인 항생물질이 많이 포함되어 있다. 폴리엔 항생물질은 진균 효모 원생동물에 항균력을 나타내고 마크로리드계 는 그림양성균을 발육저지한다. 6.1 마크로리드 항생물질 마크로리드계는 소수성이고 보통 염기성 화합물이며 아글리콘 (a g l y con) 으로서 12, 14, 16 원고리 구조의 마크로리드에 디메틸아미노슈가(di me- thy la m ino sug ar )가 한 몰식 12 원고리는 隣] 자리에 , 1~ 1~! 고리 구조 에서는 책 자리에 결합하고 있으며 중성 마크로리드는 디메틸아미노슈가 롤 갖지 않는 것이 특칭이다. Meth y m y ci n , neometh y m y ci n -€:-구 조적으 . 로 가장 간단하고 기본적인 것으로서 meth y m y ci n -€:-아 글리콘으로 met- hno li d 러 아미노당인 desosa mi n 혀끝 가지며, 이 계통의 항생물질로는 최 초로 구조가 결정된 것이다.
피크로마이신 (pi krom y c i n) 은 처음 발견된 마크로리드 항생물질이고 에 리트로마이신 (er yt hrom y c i n) 및 B 형, C 형의 구조가 유사한데 생합성도 상관관계가 있는 것으로 해명되고 있다.
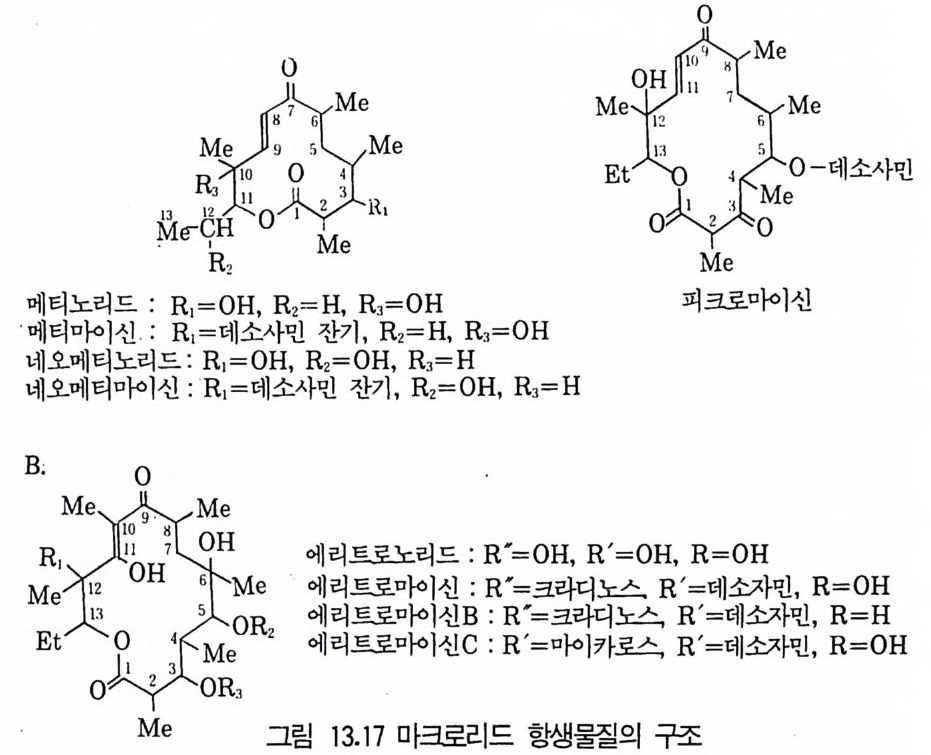 。
。
마크로리드는 그람양성세균, 특히 s t ap h y lococc 떠- d ip h t hero i d 폐 매우 효괴적이며 페니실린 내성균에 사용된다. 아글리콘과 당부분 (mo i e ti es) 은 항균력에 모두 필요하다. 마크로리드계 항생물질은 치료 사용시 내성이 빨리 생기고 각 항생물질 사이에 교차내성도 나타난다. 모든 마크로리드 항생물질은 단백질 합성의 저해제이고 세균 리보솜 (r i bosomes) 의 50S 부단위에 결합하여 펩티드 전 달효소(p e pti d y l t rans fe rase) 반응을 저해한다 (Tanaka, 1971). 에리트로 먀기신 (er yt hrom y c i n) 은 리보솜의 P s it쵸부터 탈아세틸화된 t RNA 의
표 13.7 상업적으로 생산되는 마크로리드계 항생물질 Macrolid e 항생물질 생산균 주 항균범위 적 용 Carbomy ci n A Str ep t om y ce s G+ Was markete d for several halste di i Years but dis co nti nu ed due to ine ff ec ti ve ness Eryt hr omy ci n S. ery thr eus G+ Human the rapy , fee d addit ive Jos amy ci n S. narbonensis v ar. G+ Human the rap y ( = Leucomy ci n A:1) jos amy ce ti cu s Leucomy ci n s A1, -A 9 S. kita sa loensis G+ Human the rapy ( =Kit as arny ci n s ) Oleandomy ci n S. ant ibio ti c u s G+ Human the rap y S. oliv oc hromog enu s Spi ra my cin s , I, Il , 冊 S. ambofa ci e ns G+ Human the rapy Ty lo sin S. frad ia e G+ Feed addit ive , foo d S. hyg ros cop icus My co pre servati ve Plasmas
신장요소 (elon ga ti on fac to r G,· E F • G) 의존성 유리를 저해하는 것으로 알려져 있다. (1) 생합성과 제어 마크로리드계의 아금리콘 부분 (m~ i e ty)은 프로피온산(p ro pi ona t e) 소 단위체 또는 아세트산 (ace t a t e) 과 프로피온산 소단위체의 결합형이거나 때로는 부티르산 (bu ty ra t e) 과 그 관련 화합물이 결합되어 만들어진다. 제 일 먼저 널리 연구된 마크로리드계 중의 하니는· 에리트로마이신인데 이 에리트로마이신의 생합성은 항생물질 생합성능이 저해된 Str ep t om y ce s ery thr eus 돌연변이주를 이용한 방법과 방사선 동위원소 실험에 의해 연구 되었다. 지방산 합성과 유사하게 에리트로노리드 (er yt hronol i de) 생성은 프로피오닐 코에이 (p ro pi on y l -C oA) 로부터 시작되어 2 페틸말로닐 코에이
(2-meth y lm alony l- CoA) 礎자가 축합된다 (B i rch, 1958. Woodward, 1957. Bi rc h, 1960). 이 폴리케티드(p ol y ke ti de) 합성은 락톤 합성효소 (lac to n e s yn t hase) 라 하는 다효소계에서 일어나고 락톤 합성효소는 S. e ryt hreu 뢰 지방산 합성효소와 매우 비슷하다. 아글리콘으로의 고리화 후 최초의 화합물인 6 데옥시 에리트로리드 B(6 검 eox y ery thr onoli de B) 를 분리할 수 있으며 나머지 글리코실레이션 (gly c o sy la ti on ) 단계는 그림 13 .1 8 에 도시되어 있다. 마크로리드 티로신의 생합성은 긴 사슬 지방산에 의해 촉전된다. 포도당 은 지방산 대사와 티로신 생성을 아세틸-코에이 결핍울 야기시켜 저해한 다. 에리트로마이신 생합성은 인산을 포함한 여러 수준에서 조절된다. 예를 들어 에리트로리드 B 는 자신의 생성 6 대옥시에리트로리드 E 라 락톤 합 성효소의 활성을 저해한다. 에리트로마이신 A 에 의한 t ransme t h y las 려 최종산물 저해가 관찰되며, 이 효소는 생합성 과정의 마지막 단계로서 m y carose 에서 clad i nos 쵸의 메틸 (me t h y l) 화를 촉매한다• 산업적 생성에 사용되는 고생산균주에서 이 조절은 배제되어 있다. 프로 판을(p ro p anol) 0.2~0.5% 가 S. e ryt hreu 펴 발효액에 가해질 때 acety l- CoA -c arbox y las 려 합성을 유도하고 에리트로마이신 생산에서 100% 증 가를초래한다. 6.2 폴리엔(p ol y ene) 항진균 항생물질 폴리엔 항생물질은 방선균에 의해 생산되며, 곰핑이, 효모, 원생동물에 대해서 항균력을 나타낸다. 3~7 개의 공액 이중결합을 가전 26 에서 284 원 락톤환으로 구성되어 있다. 발색단 길이에 의존하여 공액 이중결합의 수에 따라 트리엔(t r i enes), 테트라엔(t e t raenes), 펜타엔(pe n t aenes), 헥사엔 (hexaenes), 헵타엔 (he p aenes) 으로 분류되며 보통 많은 폴리엔은 다원환 락톤에 amino sug ar (my c osam ine 또는 p eros ami ne) 를 포함
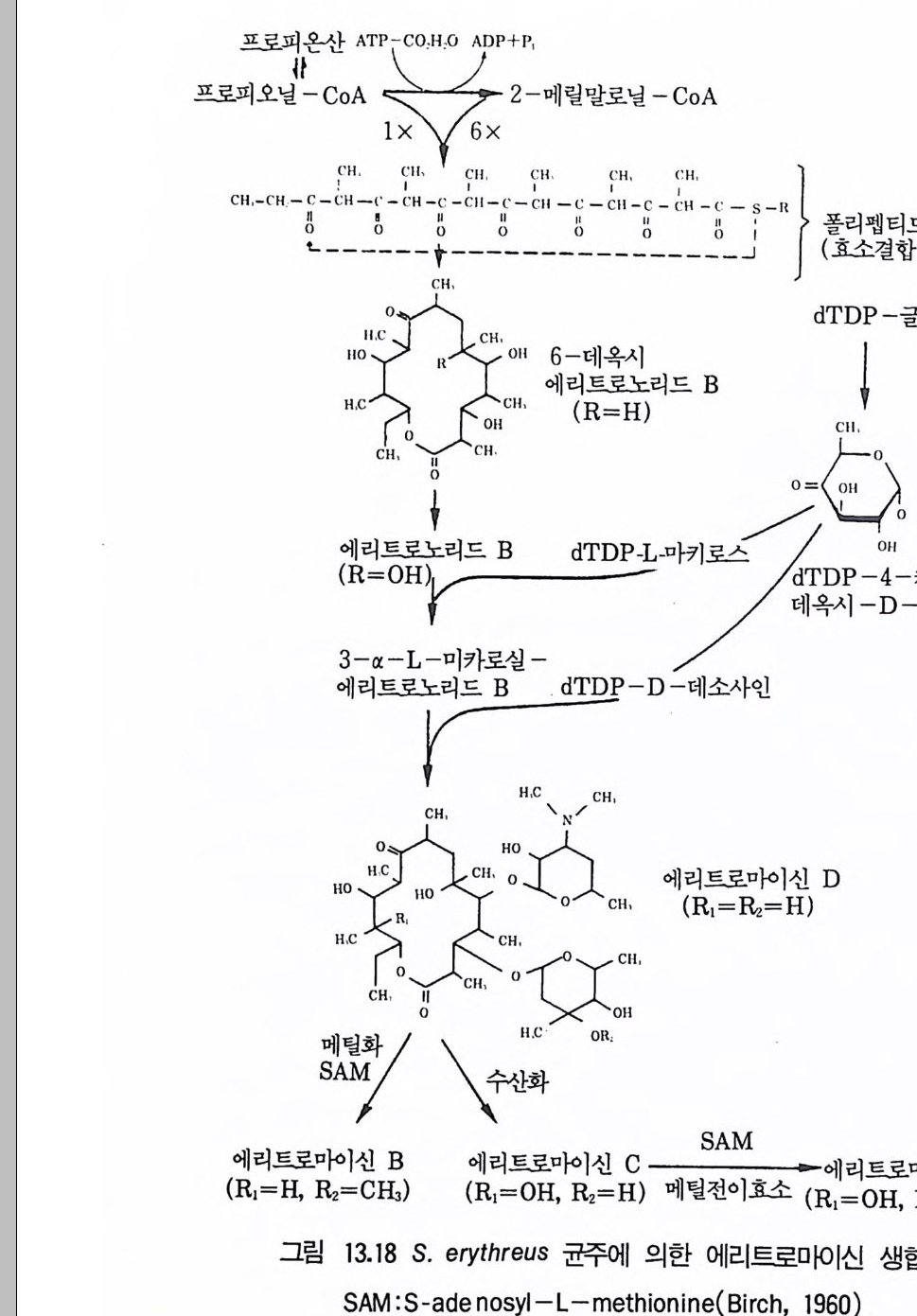 [[t
[[t
표 13.8 상업적으로 생산되는 폴리엔 마크로리드계 항생물질 항생물질 생산균 주 Polyc n c 형태 적 용 Arnp ho t er ic in B Str ep t om y ce s nod o s us Hcp tac ne, M F, His t o p l a smosis Cnndic id in B S. gn se u s Hep tae ne, M, AAP F, Prosta t e hyp e rtr o p h y Candid i n S. vir i d o fl av us Hep tae ne, M F Fili pin S. filip i ne nsis Met hy l p e n ta e ne F Fung im y ci n ( =Perim y ci n ) S. coelic o lor var. ami no ph i lu s Hep tae ne, P, MAAP F Hamy ci n S. pn mp ri n a Hep ra ene, M, AAP F Levorin s S. leuons Hep tae ne, M, AAP F, pro sta t e hyp er tr o p h y My co hep tin Str ep to u eti cil l i u m Hep tae ne, M F my co hep tini c u m, S. netr op si s Nys t a t i n Ai, A2, A :i S, noursei Trtr a ene, M F, Candid a alb1cans;slig h tl y tox ic Pim a ric i n S, nata le nsis Tetr a ene, M F. Food pre servati ve Tric h omy ci n A, B S. hachij oe nsis Hep tae ne, M, AAP F, 'lrich omonos uag ina lis M=My co sam ine : AAP=P-Ami no aceto ph enone : P=Perosami ne : MAAP=N- Meth y l- p- ami no aceto p h enone : F=Anti fun g a l acti vi t y.( Marti n, 1977, 1979b : Perlman, 1979)
한다. 트리엔(t r i ene) 계로는 트리엔의 수종이 알려져 있는데 트리엔은 항세균, 항효모 작용 의에 항종양성을 나타내기도 한다 (Aszalos, 1968). 테트라엔 (t e t raene) 계는 4 개의 공액 이중결합을 가지므로 앙 n 의 특유한 자의선 흡수 290, 303, 310, 319mw 나타낸다. 대표적인 것으로는 니스 타틴 (N y st a ti n( f, fu n gi c i d i n) 이 있다. 펜타엔(p en t aene) 계는 57n 의 공액 이중결합이 있어 320, 335, 350, 354m 쩌 자의선 흡수를 나타낸다. 이들 중 St. fi l ipi nens i예서 생산된 filipi n 의 구조는 그립 13.l gi!} 같다 (Dhar, 1964).
헵타엔 (he pt aene) 계는 7 개의 공액 이중결합을 가지며 자의선 흡수대는 358~360, 378~380, 397~403mµ 부단 1] 극대치를 나타낸다. 대표적인 것으로 Amp ho t er ic i n B 가 있다 (Mechl i nsk i, 1970). 9 파지 이상의 풀리엔이 주로 s t rep t omy ce t e ss.넥-터 분리되었는데 폴리 엔은 감수성 진핵생물의 막 스테롤 (s t erol) 에 영향을 미쳐서 막 투과성에
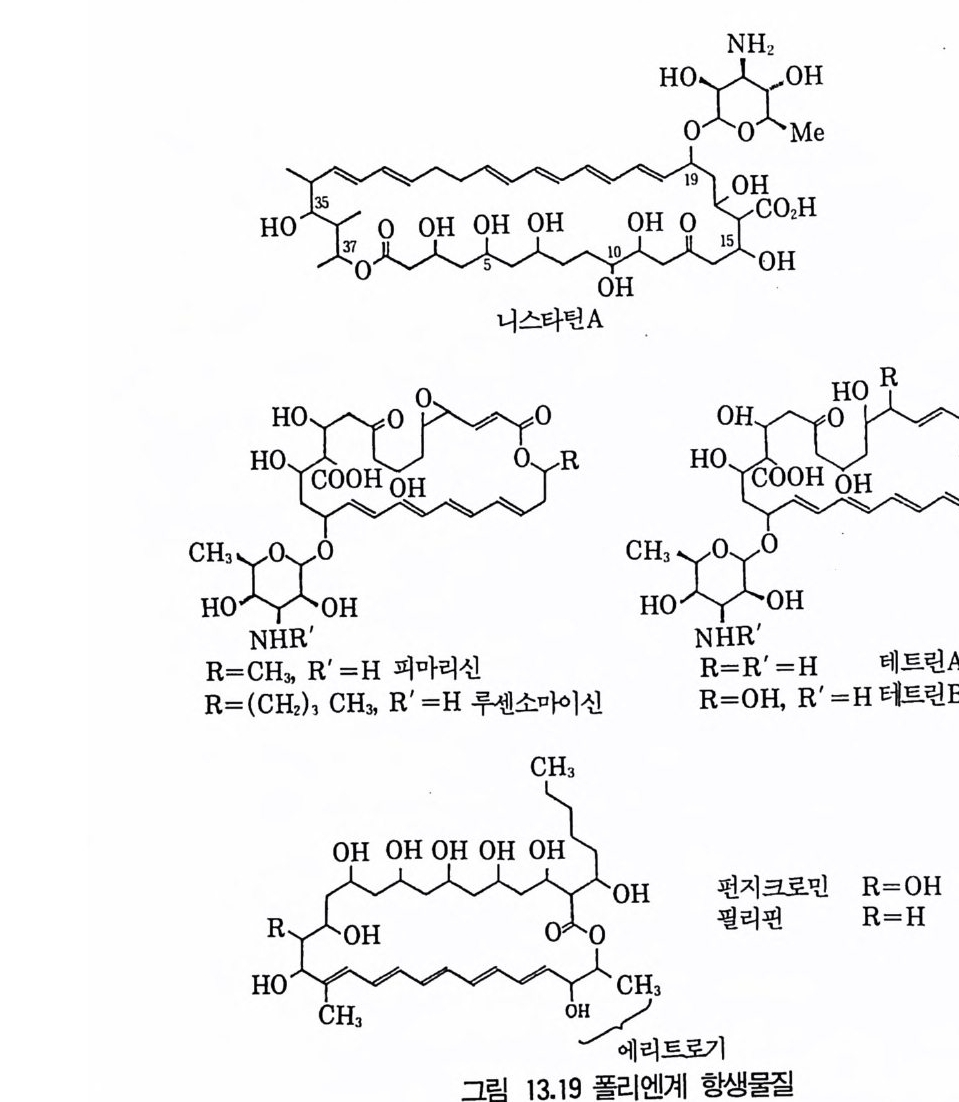 HOO근 OHMe
HOO근 OHMe
변화를 유발한다 (Weh e r, 1965). 몇 몇 폴 리엔은 상대적으로 유독하지만 (ne p hro 또는 hep a to t o x ic ) 더 좋 은 항곰팡이 항생 물질 이 없으므로 국소 적 용도로 널리 사용되고 있다. 폴리엔은 빛과 열에 민감하므로 식물 질병에는 적합하지 않다. 표 13.8 은 상업적으로 생산되는 풀리엔이다. (1) 생합성과 생산 마크로리드처럼 폴리엔 항생물질은 폴리케티드 생합성 과정을 통해서 Cz 2} C 3 un it로부터 생성된다. 방향족 폴리엔 중에서 p-a m ino aceto p h e- non 펴 N-meth y l- p - a m ino ace t o p henon 려 전구체인 p-a mi no benzoy l CoA7} 폴리케티드 중합의 출발점으로서 작용하~큰 듯하다. 포도당은 보통 폴리엔 생산에 있어서 가장 좋은 탄소원이고 이화물질 억제 (cata b olit e re p ress i on) 는 포도당의 요구농도에서 (candic i d i n 7~9, 6%) 일어나므로 포도당을 사용한 대부분의 발효는 연속배양법을 이용한 다. candic i d i n 생성시기는 포도딩을 가해줌으로써 300~ 포료 연장될 수 있다 (Mar ti n, 1976b). 아세데이트, 프로피오네이트(p ro pi ona t e), 말로네 이트 (malona t e), n~프 로판을 (n-p ro p anol) 의 첨가한 폴리엔 생산을 촉진 하고 so ym eal 이나 so yp e pt one 이 질소원으로 사용된다. 폴리엔의 최대생성을 위해서는 통기조절이 필수적이다. 증식기 동안 필 요한 산소전이율이 0.8m mole Oz /l • min 정도이나 정지기 동안 02 농 도는 포화의 40% 를 초과해서는 안 된다. 폴리엔은 수용성이 아니므로 세포의 표면이나 배지에 결정체나 미소입 자로서 축적하고 이로부터 폴리엔은 용매로 추출할 수 있다. 6.3 안사마이신 (ansam yci ns, rifa m y ci n s ) 먀기신은 방향족 발색단을 가전 마크로락탐 (macrolac t am) 계 항생물질 인데 지방족 폴리케티드 유도체가 소위
결합되어 있다(그립 13.20 참고). 안사마이신은 그 발색단에 의해 구별된 다. g eldnam y c i n 이나 ansa mitoc in 같은 벤젠환을 가전 화합물들은 주로 진핵생물에 작용하고, 반면 나프탈렌 (na p h t halene) 구조를 가진 화합물들 은 세균에 유효하다. 후자에는 rifa m y ci n s , halomy cins , str e p tov aric i - ns 이 있다. CH3 CH, CH3 亡OIHN sV|HN H 에음 성의세해균 에생는성 리된효파다과C마H 가(이S3 e신그 없n` 림0s다B i ,. 1 13R.92 i50f 9 a리).m 파 y 약c□ i I 퍼OI끈 신2 0C 다7HB}른지, J S ,항 각S생V기.1°1~물 〔 의广11 °二O 질다 구과른조 교r차 if내a m성 y을 c i n 이나 H 。 Rif am y ci ~ 그람양성세균과 my cobac t e ri a 에는 매우 효과적이나 그람 탸서지 않으며 Str ep t om y ce s (현재는 Nocardia .£. 분류됨 ) medit er ra-n e i Nocarid a 돌연변이주의 배 0~예 으로부터 분리되었고 rifa m y cin 생성에 관 한 몇몇 유전자 조작작업이 실행되었다. 야생균주는 주로 rifa m y cin BS 斗 소량의 rif am y ci n 혼합체 (A, C, D, E) 를 생성한다. 이 혼합체의 생성은 sod ium diet h y l barait ura te 첨가에 의해 억제될 수 있으며 이 화합물 의 전구체는 rif am y ci n S( 또는 SV) 인데 rif am y ci n SV를 배설하는 돌연 변이주도분리되었다.
Rif am p ici ~ rifa m y ci n SV 로부터 유도된 반합성 화합풍기고 결핵 치 료에 사용되며 동물의 RNA 중합효소에는 작용하지 않으나 세균의 RNA 중합효소의 특별한 저해제이다 (Har t mann, 1967). 이는 중합효소의 f]소 단위에 결합하고 고등생물의 RNA 중합효소는 영향을 받지 않는다. 7 데트라사이클린(t e t rac y cl i ne) 계 항생물질 7.1 데트라서이클린계 데트라사이클린은 의약적으로 중요한 항생물질이다. Chlorte t r a cy cl in e 은 Str ep tom y ce s aureo f ac i ens 의 배양버에서 1945 년에 분리되었고 tet - racy cl in e chlor t e t rac y cl i ne 의 탈할로겐화에 의해 처음 제조되었으나 S. uir id i f ac ie n s 배양에서도 역시 발견되었다. 현재 각종 테트라사이클린 혼합 물들을 생산하는 약 2 0¾의 방선균이 알려져 있다(표 13.9).
표 13.9 테트라사이클린을 생산하는 Str ep t om y ce s 균주 균주 생산물. S. albofl av us CTC, TC, OTC, acti no my ci n S. anti bi o t ic u s OTC,TC S. aureofa c ie n s CTC,TC S. aureus TC S. califo rn ic u s TC, acti no my ci n S. cellulosae OTC, acti no my ci n S. feof a c ie n s TC S. flav eolus OTC, TC acti no my ci n S. flav us CTC, TC, OTC, acti no my ci n S. lusita n us CTC,TC
S. pa rous OTC, TC, acti no my ci n S. pla te n sis OTC S. rim osus OTC, TC, rim ocid i n S. saya maensis TC, CTC S. vendarge n sis OTC, veng ac id e S. vir id i f aci e n s CTC,TC •cTC7 갑 hlor t e t rac y cl i ne, TC tet r a cy cl in e : OTC oxy -tet r a cyc lin e (Perlm 빡 1979)
데트라서이클린의 기본 구조는 nap h th acen~ 체계로 구성된다. 그림 13.21 은 몇몇 치료용으로 중요한 화합물의 구조이다. 현재 발효로 생산된 데트라사이클린 @回 반합성 유도체들이 시판되고 있다.
:Hi RJ R ;2 R1 HH2 C\ N[IC H3 2 데트라사이크린 I R1 R, RJ R4 생산균주 테트라사 °l 크린 H OH CH, H S. 베au지re )o f또a c는 i e ns쿨( 로 영르화데 ~트l라 없사이는크 린의 화학적 변형운 동해서 7- 쿨(로아르우데레트오라마이사신이)크 린 H OH CH, C I I S. aureofa c t en s 5- 옥(데시라데아트이라신사) 이크린 OH OH CH, H S. rim osus 6- 대뻔에틸신 구 (-데쿤크로로르°테서트신라) | H OH H Cl S. n+u저re해of재n c ien s -6데- 데트옥라시사 -이5크-린 하 ( 독이시드사록 이시크 린) IOH H CH H 반합성 7- 디메털아미노 -6- 데메틸데 I H H H N(CH, ), 반합성 트6라- 사대이옥크시린 - 6(-미 데노에사틸이 -크6린 ) IOH ` =C、H一, H 반합성 크게릴렌 _5- 하이드록시데트라 사이크린 (메타사기크린) 그림 13.21 주요 의약용으로 중요한 테트라사이클린 구조
테트라사이클린은 ric k ett sia s , my co p la smas, lep tos p ira s, sp iro che tes , chlam yd i as 뿐만 아니라 그림양성세균과 그람음성세균에 대해 효과 적인 광범위 항생물질이다. 다른 데트라사이클린간에 현저한 교차내성이 있다. 테트라사이클린계와 B- 락탐계는 현재 가장 널리 사용되는 항생물질이고 chloro t e t rac y cl i ne 과 oxy tet r a cy cl in e - €:- 인체와 가축용 의약품으로 사용되며 많은 나러에서 가 금과 돼지 생육에서 영양공급으로 널리 사용되기도 하고 몇몇 나라에서는 물고기, 육류, 가금 사육에도 사용된다. 테트라사이클린은 단백질 합성 저해제이며 그 작용 부위는 30S 리보솜 이고 리보솜의 A 측에 아미노아실-t RNA(am i noac y l- t RNA) 의 실합이 저 해된다. (1) 생합성과 생산 Chlor t e t rac y cl i n 하 oxy tet r a cy cl in f f ll s t rep t omy ce t e 여 의해 생성 되는 주된 데트라사이클린 물질이고 데트라사이클린 그 자체는 미량 성분 이다. 그러나 chlorin a ti on 반응기 저해된 S. aureofa c ie n s 돌연변이주의 주요 생성물은 테트라사이클린이다. Chlor t e t rac y cl i ne 생합성 과정은 그 립 13.229 -} 같고, 沙 H 의 부분으로 세분화될 수 있다. 즉 ® 해당과정을 거 쳐 아세틸-코에이로 된 후, ® Ace ty l-CoA -c arbox y lase 에 의해 아세틸 코에이가 말로닐-코에이로 전환되고, 말론아모일-코에이 (Malonamoy l- Co A) 로 아미노기 전달(t ransam i na ti on) 후 말론아모일-코에이는 anth r a-cene s y n t has 려 결합되어 喆 L자 의 말로닐-코에이와 축합된다. 데트라사이클린 생산과 탄수화물 대사 사이에는 명확한 상관관계가 있 다. 고생산균주는 저생산균주보다 해당작용(g l y col y s i s) 률이 더 낮다. 해당 작용 저해제인 벤질티오시안산 (benz y l t h i oc y ana t e) 0.5~3 µg /ml 의 첨가 로 chlorte t r a cy cl in e 생산이 50% 증가한다. 동시에 펜토오스 인산 경 로(p en t ose p hos p ha t e c y cle) 의 역가가 증가한다. S. aureofa ci e n s 유전학 에 대한 연구에 의하면 30U l-지 이상의 유전자가 chlorte t r a cy cl in e 생
雷『一C :: [C:2H _ bCo:교 」; g:0:S_H _HE: ( 言H 2 ° 피루브산--아세틸 _CoA 말로닐_ CoA -H2C :0\\\말\로E닐 _C:oA, .:] oo:H °0: 广 ::-N: 2 C노HJ 고부리화 :C言H3 亭 °CHONHT :CH3二 :OHNH 2 HS 一 E OH OH OH OH -- -- -.H20 ® OH OH OH OH 二三二CH3 二OH °C:NNAH드 D ~A D二H2 C亨H3 〉0 COOHNH 2 OH O OH OH. ©0H O OH O H二 @ 三 oH OH : bC 0HO bO HN:22®三 3 0H OH :O \o\ ONH 2 二® 二COIH H 3OC 0Ho N(o C H3c )0二2 N H一NA D 뿐 D®P仁 C0IH H 3Cb 二 O oHH OHNb二 ( CH3)2 a, 6-m e th y lp r e te t r a m ide ; b, 4-Hy d rox y-6m eth y lp r e tet r a m ide ; c, 6-D e ox ytet r a m ide gre en ; d, 4-0 x y a nhy d rochlorte t r a cy cl i ne : e, Ahhy dr ochlorte t r a cy cl i ne : f, Dehy d rochlorte t r a cy cl in e ; g, Chlovte t r a cy cl i ne ; I, Acety l- C ~ A carboxy la se ; II , Pho- sph o enolpy ruv ate carboxy la se 그림 13.22 (SV. anauekre o등f,a c ie1 n9 7~1 ,균· 주H o에s t의a l e한k 클등,로 1르9테79트) 라사이클린 생합성
합성에 관여하는 것으로 알려지고 있다. 이로 인해 생합성과 제어에 대한 지식의 결핍으로 균주 개발의 논리적 접근이 불가능하였다. 이제까지는 모 든 고생산균주 개발은 경험적인 돌연변이 유발에 의해 행하여졌다. 자의선 또는 X선 , eth y le neim i ne 처리를 함께 사용하여, S. aur- eo f ac i en 러 S. r i mosu 遷 사용한 최다수의 고생산균주를 유발했다. 혼성화 (h y br i d i za ti on) 는 생산율을 증가시키지는 못하고 있지만 돌연변 이와 함께 작용하여 균주 변이성을 증가시켰으며 또한 원형질 융합도 가 능한 기술로 등장하고 있다. 그림 13.23 에서와 감이 야생균주인 S. rim osus(ATCC 10970) 에 대한 유전자 지도가 작성되었다. 이 지도는 유전학적으로 잘 알려진 Str - ep t om y ces 인 S. coel i color의 지도와 유사점을 가지고 있다. Oxy tet r a -
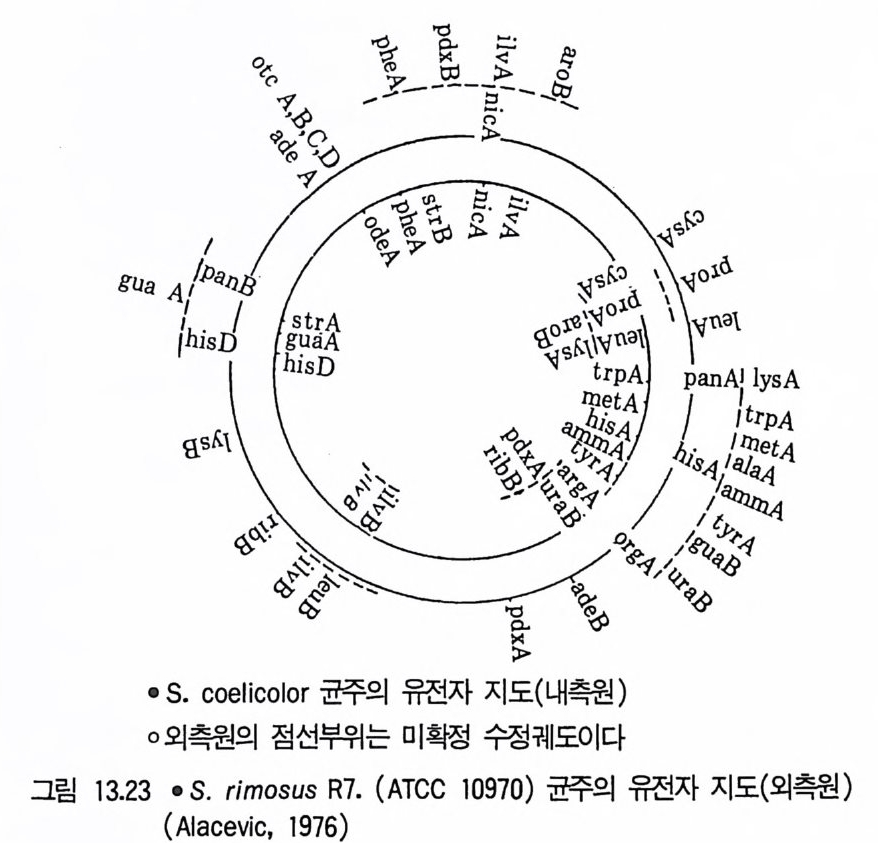 -닿/7 pg一B ic1 Anli> Al -RoBl
-닿/7 pg一B ic1 Anli> Al -RoBl
cy cl in e 생합성 첫단계에 대한 유전자는 S. rim osus 염색체의 좁은 영역에 서 rib BS 斗 Cy s D 사이에 위치한다. Anh y dro t e t rac y cl i ne 에서부터 oxy - t e t rac y c li n~ 로의 단계에 대한 유전인자는 pro A 와 ade A 사이의 썩i 째 clus t er 에 위치한다. 지금까지의 연구 결과에 의하면 테트라사이클린 생합성에는 풀라스미드가 관여하는 것으로 알려지고 있다. 데트라사이클린 생산은 150,0001 용량의 교반 발효조에서 행해지는데
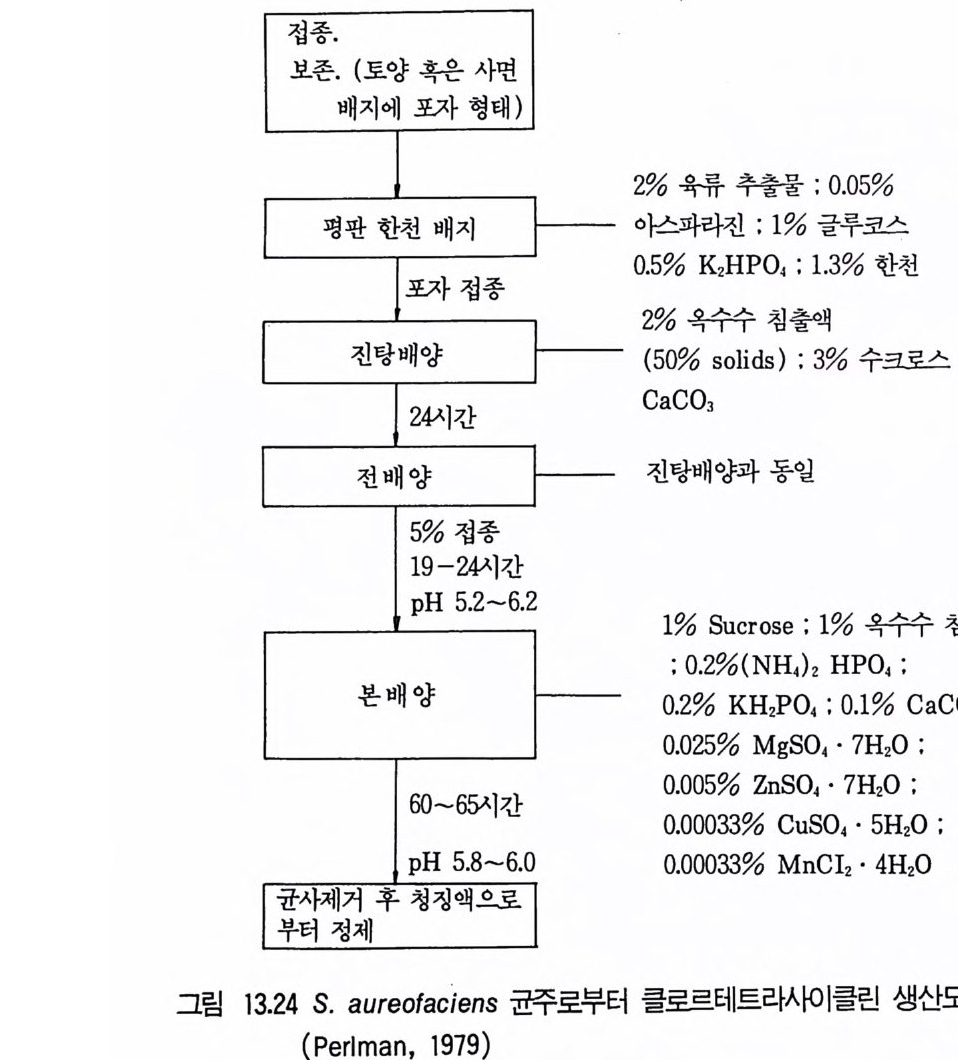 접종.
접종.
chlorte t r a cy cl in e 생산에 대한 전형적인 공정이 그림 13.24 에 나와 있 다. 포도딩이 사용되면 계속적인 첨가가 필요하며 전분이 부수적 탄소원으 로 사용될 수 있다. 인산억제로 인하여 테트라사이클린 발효는 인산 제한 과 함께 행해진다. 최대수율을 얻기 위해서는 최적의 산소공급이 중요한데 특히 발효의 처음 몇 시간 (6~l V- l 간)이 중요하다. 통상 통기율은 lvvm 이다. 산소를 많이 함유한 공기가 사용되면 수율 증가가 초래된다. 8 푸린 및 피리미단 관련 항생물질 195()1 1 Cordg ce p ts mil it a r is7 } 생산하는 Bacil lu s 속에 항균력을 나타내 는 cord g ce pin:이 분리된 이후 (Cun ni n g ham, 1950) 누클레오시드 유사구 조를 가전 항생물질들이 약 507} 지가 알려져 있다. 이들 중 대표적인 것으 로 식물의 항곰팡이 항생제로 사용되는 Str ep t om y ce s grise ochromoge n es7} 생성하는 po lyo x in ( Isono, 1965) 이 있다. p ol y ox i n( 그림 13.25 A) 은 키
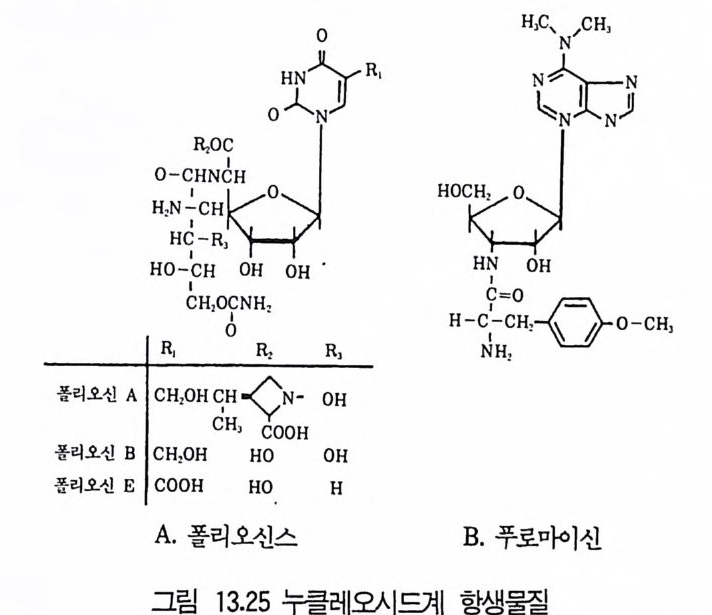 OH丈 ~ O R, H댜,C , _Nj C갑H,
OH丈 ~ O R, H댜,C , _Nj C갑H,
틴 합성요소 (ch iti n syn th a se) 경쟁적 저해에 의해서 곰핑이 세포벽의 키틴 부분으로의 N - ace ty l-o- g lucosam i ne 의 결합을 저해한다. S. allon ig e r.가 생성하는 퓨로마이신(p urom y c i n : Waller, 1953) 은 단 백질 생합성에서 리보솜의 기능을 연구하는 데 널리 이용되지만 임상적 중요성은 없다. 퓨로마이신은 t -RNA 의 아미노아실 말단과 유사하다. 원 핵생물과 진핵생물 모두에서 퓨로마이신은 리보솜의 A 부위에 결합하여 신장하는 폴리펩티드 사슬에 옮겨져서 중합(p ol y mer i za ti on) 과정을 차 단한다. 9 방향족 항생물질 분자내에 방향족 고리를 가진 물질로서 클로람페니콜 (chloram p hen i col) , gri s e ofu l vin , novob i oc i n 이 공업적으로 생산되고 있으며 각 화합물 의 생화합물의 생합성은 상당히 다르다. 9.1 클로람페니콜 클로람페니콜(그림 13.26) 은 Str ep t om y ce s venezuelas, S. ph aeochromo- gen es var. chloromy ce ti cu s, S. om iy aens i러 다른 stre p tom y ce te s 균주에 의해 생산되나 현재 합성법에 의해 생산되고 있다. D-(-) - t hreo 체만이 항 균 활성을 나타내는데 그람양성세균, 그람음성세균, acti no my ce te s, ric - kett si a s , chlamy d i a 폐 작용하는 광범위 항생물질이다 (Ehr li ch, 1947). 쿨 로람페니콜은 특히 골수손상등 중요한 부작용을 유발하지만 치료를 주의깊 게 하면 독성의 위험이 감소될 수 있으며, 체내 장기의 분포성이 양호하며 이질균에 매우 유효하다. 다만 내성균의 발생이 용이하며 이는 유전적으로 플러스미드에 의하며 구조내 수산기의 아세틸화효소 생성에 의해서 클로람 페니콜이 불활성화되는 것이다.
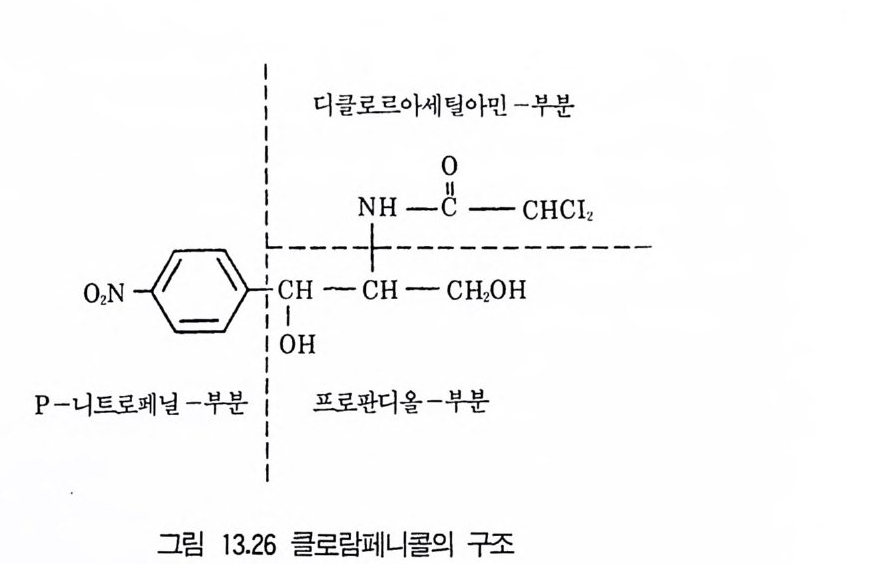 _II
_II
클로람페니콜은 70S 리보솜의 50S 소단위체에 특별히 결합하고 pep- tidy le 전이반응을 차단한다 (N i erhaus, 1973). 9.2 Gris e ofu lv in Gr i seo fu lv i諺 Penic il l i u m gri se ofu lu um, P. p u tu lum5 斗 Penic in l liu m j anczewsk ii에 의해 생산된다 (O xf ord, 1939) (그립 13.27). Gris e ofu l vi n 은 chit ino us 세포벽을 가진 곰팡이에만 작용하는 정균적 항생물질이다.
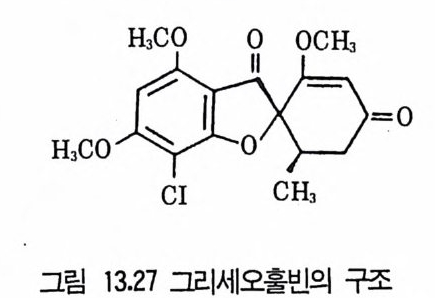 HJC O 0CH3
HJC O 0CH3
사립에게는 Gris e ofu lv in 이 곰팡이의 피부감염 (dermato m y c oses) 치료에 이용된다. Gr i seo fu lv i n 은 Botr y t is, Alte r naria so/an i에 기인한 잎 질 병에 널리 사용된다. Gr i seo fu lv i n 은 많은 곰핑이의 형태에 영향을 미치 고 100~1,000 pp m 의 농도에서 균사의 특징적인
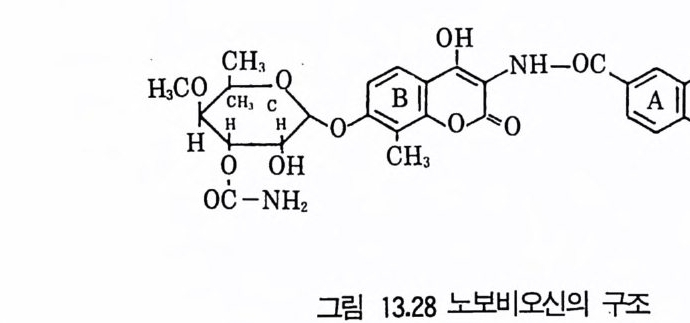 OH
OH
다. Novob i oc i n 은 그람양성세균, 특 히 포도상구균 s t ap h y lococc i에 효과적 이고 그람음성 men ing ococc 따 임균g onococc i 에 효과적이며 , 또한 Hae- mop h i lu 화 몇몇 Pro t eu 예도 균주에 효과적이다 (Hoeksem a, 1956). Novob i oc i n 은 다른 항생물질들과 교차내성을 나타내지는 않지만 병원균 은 내성이 나타나기 때문에 의약적 용도에 대한 단점이 되고 있다. Nov- ob i oc i諦 DNA복 제 동안 DNA 선회효소 (DNA gyr ase) 의 특별한 저 해제로 작용하며 DNA 복제를 저해한다 (Geller t M, 1976). Coumarin 모핵의 생합성은 방향족 대사를 거친다. L 티로신이 고리 A 와 고리 B 로 통합되고 고리g근 포도당으로부터 우려]한다 (Wal t on, 1961). 10 기타 상업적으로 생산되는 항생물질 10.l Fusid i c acid 스테로이드 (S t ero i d) 항생물질 중 fus id i c acid 만이 (그림 13.29) 치료 용으로 중요하다. Fusid i u m cocc i neu 짜니 배 0~버 으로부터 분리되는 (God-
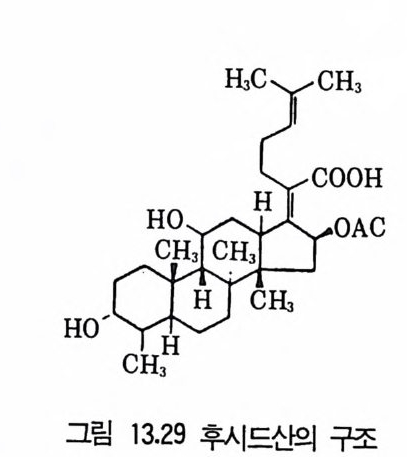 그림 13.29 후시드산의 구조
그림 13.29 후시드산의 구조
tfred sen, 1962) 이 화합물은 세균의 단백질 합성 동안 리보솜의 전위과 정 (t ransloca ti on) 을 저해한다. Fusid i c ac i&근 Sta p h yl o cocci 등 그람양 성균 감염 치료에 특별한 용도를 가지고 있다• 10.2 Polye t h e r 항생물질 이 항생물질은 그람양성균 및 곰핑이에 유효하나 독성이 강하다. 다수의 t e t rah y dro py ran 과 t e t r af ura 며t 함유하는 항생물질로서 p ol y e t her 라 불린다. Monens i n( 그림 13 -3 0) 는 상업적으로 가장 중요한 군의 화합풍기 고 5 아세트산 (ace t a t e), 4 프로피온산(p ro pi ona t e), 3 부티르산 (bu ty r ate ) 단위로 구성된다. 생물학적 또는 인공막을 통하여 l7} 혹은 沙} 양 이온을 운반하는 능력이 있으므로 이 항생물질은 i ono p hor 로 분류된다. 。’ CHc H3 。H 그림 13.30 모넨신의 구조 J
s i싱&업부터적 으생로산 생된산 m되o는ne n이s in군 , 의S . 항la생sa물l i e질ns에 i는폐 S의t해r ep t 생o三m 산y 된ce s lcaisn an laomciod ne e,n -S. albu 예 의해 생산된 sa li _ nom y c i n 이 있다. Sali no my ci n 생산량 60g /l가 o지ba방ct산e r을 i a , 함곰유팡한기 와배 C지oc에c 서i d i a{얻 p어 ro진 t 다oz.oa )P 에o l y대 e t해 h e r활i근성 이그 람있양다성.세 균Po,ly e Mt Yh eC r- 항생물질 중 monens in-t든 Coccid i o s es¾ 막기 위 해 가금 사료에 첨가되기 도 한다(약 lOOp pm 정도).10.3 M it om y c i n 계 1956 \'! Str ep t om y ce s caesp it osu 예 의 해 생산된 mit om yci퍼본 벤조퀴 논 (benzo qu i nones) 이다. 보라색의 이 항종양 항생물질은 그람양성, 음성 및 항상성균에 강한 항균력을 나타낸다 (Ha t a, 1956) (그림 13.31). Ery- t hrose 와 피루브산은 메틸 벤조퀴논의 전구체가 된다. Mi tom y ci n 앉즌
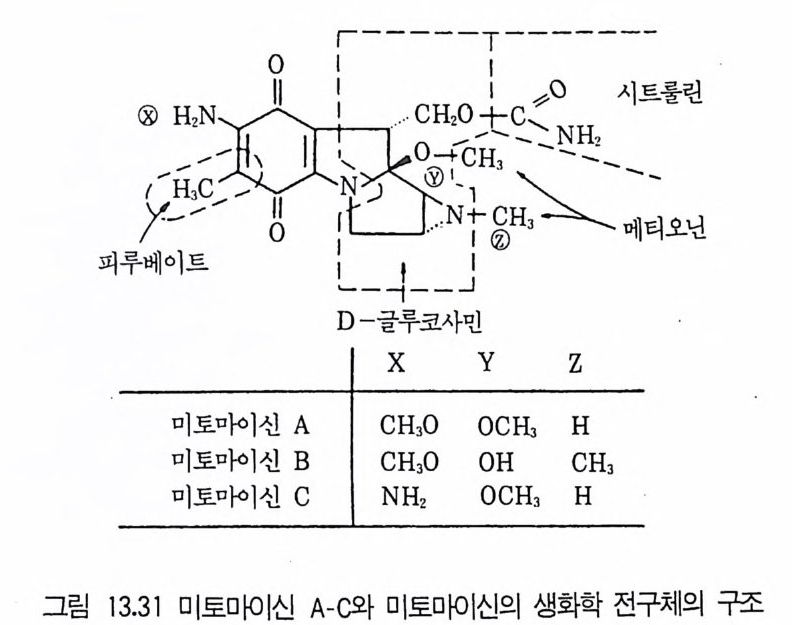 OII 〈广 ___ H一N子1 h-:H으:- -`-A-머 -;: 룰오:
OII 〈广 ___ H一N子1 h-:H으:- -`-A-머 -;: 룰오:
암에 매우 효과적이나 상대적으로 유독하다• M it om y c i퍼끈 이중나선 DNA 와 점·국 DNA 복제를 저해하는 교차결합을 유발한다. 독성이 감소 된 여러 유도체가 개발되고 있고 항종양제로서 임상적으로 사용된다.
춥卜고문헌 Alacevic M. 1976. Recent aduances in stre p tom y ce s rim osus gen eti cb . pp. 513~519 Allsop , A, P. J. Normansell and G. Holt, 1981 . Bi oc hemi ca l gen eti cs of P-lacta m pro ducti on 2nd Europ . Cong r. Bi ot e c hnol, Eastb o urne, Eng la nd. Abstr a cts of commu nica ti on s, p. 232. Aok i H. and M. lmanaka : J.A nti bi o t i cs 29. 492( 1976). Aok i H. and M. Okuhara, 1980. Natu r al P-lacta m ant ibi o t i cs . Ann. Reu. Mi cro bia l. 34 ; 159~ 181 Aszalos A and B. Berk ; J. Anti bi o t i cs 21. 611(1968). Ball, C. 1978. Geneti co in the develop m ent of the pe nic i l lin pro cess, pp. 165~176. In ; Hut ter , R, T. Leis i n g e r, J. N'uesch, and W. Wehrli (e ds), Federati on Europ. Mi cr obia l . Soc. Sy m p . No. 5. Aca-dem ic Press, London. Berdy , J. 1984. Recent develop m ent s of anti bi o t i c research and classif ica ti on of anti bi o t i cs accordin g to chemi ca l str u ctu re. Adu. Ap pl. Mi cr obia l 28 ; 309~406. Berdy, J. 1974. Recent develop m ent s of anti bio t i c research and classif ica ti on of anti bi o t i cs accordin g to chemi ca l str u ctu re. Adu Ap pl. Mi cro bia l. 18 ; 309~406. Bi rc h A. J. and H. J. Smi th ; J. Chem. Soc 360(1 9 58). Bir c h A. J. and H. Sm ith ; J. Chem, Soc 365(1958). Bi rc h A. J. Chem and Ind, 1245(1 9 60). Chauvett e R.R et al ; J. Org Chem 36. 1259 ( 1971 ) . Cunn ing ha m K.G . et al ; Natu r e 166. 949(1950). Davie s J.E : Geneti cs of Ind M icr oorg( l 982)(Proceedin g of IVt h Intl Sy mpo ) 103. Dhar M. L and M.C Wh iting ; J. Chem Soc 842(1964). Demam, A.L 1980 P-Lacta m anti bi o t i cs , p. 10 In ; VI th Int, Fer- men t, Sy m p . and VIth Int. Sym p. on Yeasts . London, Onta r io , Can-ada. Dj er assi C. J. Am. Chem Soc 78. 6390(1 9 56).
Ehrlic h . J. Scie n ce 106. 417(1 9 47). Fuj i i A and H. Umezawa : J Anti bi o t i cs 26. 396(1 9 73). Fuji wa ra, T, Y, Takahashi, K. Mats u mot o. and E. Kondo. 1980. Iso- lati on of an int e r media t e of 2 검 eox y s t re pt am i ne bio s y n th e sis from a muta n t of Bacil lus cir cu lans. J. Anti bi o t . 33 : 824~829. Gellert M : Proc. Natl . Acad Sci 73. 4474(1976). Goltf red sen. W. 0 and L. Ty br in g : Natu r e, 193, 987(1 9 62). Gris e bach, H. 1978. Bi os y n t he sis of sug a r comp o nents of anti bi o t i c substa n ces. Adu. Carbohy d r. Chem. Bi oc hem. 35 : 81~126. Hartm ann G. et al ; Bi oc him Bi op h ys . Acta . 145. 843(1967). Hara T. and T Hoshi : J. Anti bi o t 9A 141 (19 56). Herr R.R and M.E. Bergy : Anti m i cr ob Ag chemoth 560(1 9 62). Hoeksema H. and G.F. Crum ; Anti bi o t , chemoth 6. 143(1956). Hota l ek, 2. M Blumauerova and Z Vanek 1974. Geneti c Problems of the bio s y n th e sis of tet r a cy cl in e anti bi o t i cs pp. 13~67 In ; Chose T.K.A Fi ec hte r and N. Blakebrough ( eds). Advances in bio c hemi ca l eng ine erin g. v~l. 3. Sp r in g er . Verlag. Berlin Hosta l ek, 2 Blumauerova and Z . Vanek. 1979. Tetr a cyc lin e anti bi o t i cs . pp. 293~354. Howello, J.D , L.E . Anderson, G.L. and J. Ehrli ch . 1972. Buti ro sin , a new ami no g ly c o sid e anti bi o t i c comp le x. Bacte r ia l orig rin and some mi cr obio l og ica l stu d ie s . Anti mi c r ob Ag en ts Chemoth e r. 2 : 79~83. Isolati on of an int e r med iat e of 2-d e ox ys tr e p tam ine bio s y the sis from a mut an t of Bacil lus cir c ulans J. Anti bi o t . 33 ; 824~829. Isono, K. et al ; Ag r. Bio l Chem 29. 848(1965). Jen sen, E.B, R. Ni el sen, and C. Emborg. 1981 . The influe nce of ace- tic acid on pe nic illin pro ducti on . Europ. J. Ap pl. Mi co rbio l . Bio - tec hnol. 13 : 29~33. Jo hnson B. A and F. Meleney : Scie n ce 102. 376(1945). Kahan J. S. et al ; J. Anti bi o t i cs 32. 1(1979). L~rdy H. A. et al : Fed. Proc ; 26. 1355(1 9 67). Maeda K and H. Umezawa : J. An tibi o t. 9A. 82(1956). Marti n J.F . 1977 Bi os y nthe sis of po lye n e macroli de anti bi o t i cs ,
Ann Reu. Mi cr obia l . 31 : 13~38. Marti n, J.F . 1979 a Nonp o lye ne macroli de anti bi o t i cs . pp. 239~291. In ; Rose A. H ( ed ) , Economi c mi cr obio l ogy vol. 3. Secondary pro ducts of meta b il is m . Academi c Press. London. Marti n, J. F. 1979 b. Polye n e macrolid e anti bi o t i cs, pp. 355~387. Marti n, J. F. J.M Lueng o, and J.R. Vi llan ueva. 1979. Bi oc hemi ca l gen eti cs of the {1- lacta m anti bi o t i c bio s y n th e sis , pp. 83~89. In : Sebek, O.K . and A.I. Laskin . (eds), Geneti cs of ind ustr ia l mi c- roorga n is m s(GIM 78). Amer. Soc. Mi cr obio l , Washin g ton , D.C. Mechli ns ki, W. and G. Avit ab il e ; 'letra hed Lett 387. 3(1 9 70). Mehta , R.J. and C.H. Nash. 1979. Ly s in e sti m ulati on of cep - halosp o rin C syn th e sis in Cep h alosp o riu m acremoniu m . Europ. J. Ap pl. Mi cr obio l . Bi ot e c hnol 8 ; 177~182. Morin , R.B and M. Gorman(eds). 1982. Chemi str y and bio l ogy of {1- lac- tam anti bi o t i cs ; Volume 1, Penic i ll i n s and cep h alospo rin s : Volume 2, Non tra dit ion al {1- lacta m anti bi o t i cs ; Volume 3, Bi oc hem ist n y , Aca- dem ic Press, New York. Newt on , G.G.F. 1954. Bio c hem J. 58. 103(1954). Newt on , G.G.F & E.P. Abraham Natu r e 175, 548(1955). Ni er haus, D. Proc Na t. Acad Sci. 70. 2224(1973). Ni et o , M.J. L , I. Garcia - Acha, and J.F . Marti n. 1981 . Penic i l lin pro -ducti on by recombin a nt str a in s of Pen ici l line chrys o g e num obt- aine d by fus io n of pro t op la sts . pp. 57~61. In ; Moo-Young , M. (ed), Advances in bio tec hnolog y, vol. 血 Perga mon Press, Toronto . Ni et r o , M. and H. R. Perkin s ; Bi oc hem J. 123. 773. 798(1971). Okuy a ma , A. and _T. Ki no shit a ; Bio c hem Bi op h yo . Res Comm 43. 196 (i97 1). Oxfq rd , A. E and P. Sim onart ; Bio c hem J. 33. 240(1939). Perlman, D. 1979. Mi cr obia l Producti on of anti bi o t i cs. pp. 241~ 280, In ; Pep ple r, H.J and D. Perlman(eds), Mi cr obia l tec hnolog y, vol. I. 2nd edit ion , Academ ic Press. New York. Pie p e rsberg, W. ; Bio l ogy of Acti no my ce te s 88. 869(1 9 88). Proc of VDlt h I ntl . Sy mp. on Bi ol of Acti no my ce te s (J a p. sci soc
Press Toky o ). Qu eener, S.and R. Schwartz 1979. Penic i l li n s : Bi os y n th e ti c and Sem- isy nthe ti c, pp. 35~122. In : Rose, A.H(ed), Economi c mi cro bio b og y. vol 3. Secondary pro ducts of meta b io l i om . Academi c Press, Lon-
don. Rey n old, P.E : Bio c hem, Bi op h ys . Acta . 52.4 0 3( 1961 ) . Ri ne hart, K.L. Jr. and R.M St ro shane, 1976. Bi os y nthe sis of am i- nocy cl it ol anti bi o t i cs, J. Anti bi o t . 29 : 319~353. Schrein e r G : J. Mol. Bi ol . 81. 71( 19 74). Scolnic k E and M. Ni re nberg : Proc, Na t Acad Sei, 61. 768(1968). Sensi, P. and R Ballott a : Anti bi o t Ann. 262(1959~1960). Suami , T.S Og aw a and N. Chid a , 1980. The revis e d str u ctu r e of val- ida my ci n A. J. Anti bi o t 33 : 98~99. Swarts , R.W . 1979. The use of economi c analys i s of pen ici l lin G manufa c tu n ing costs if esta b li sh in g pnior it ies for fer ment at i on pro cess im p ro vement Ann. Rep . Fenn. Proc. 3 ; 75~110. Sto n e K.J. and J.I. Str o mi ng e r : Proc. Nat. Acad. Sci. 68. 3223.(1971). Takeuch i S et al : J. Anti bi o t. llA. 1(1 958). Tanaka T : FEB. S. Lett er 13. 65(1 9 71). Treic h ler. H.J, M.Li er sch. and J. Nu·eroch. 1978. Geneti cs and bio - chemi st r y of cep ha losp om in bio s y n t he sis , pp. 177~199. In : Hu· · tter. R. T. Leis i n g er , J. Nuesch, and W. Wehrli (e ds). Anti bi o t i cs and oth e r secondary meta b io i t es Federati on Europ . Mi cro bio l. Soc. Sy m p . No. 5. Academ ic Press, London. Uanek. Z. J. Cudlin , M. Blumauerova, and Z. Hosta l ek 1971. How many gen es are req ui r e d for the sy nt h e sis of chlorte t r a cy cl i ne : Folia Mi cr obio l 16 : 225~240 . Umezaw. et al. 1966. Umezawa, H. eta l ; J. Anti bio t i cs 26. 51( 1 973). Walker, J.B . 1979. On the develop m ent of enzym ic pa th w ay s for the bio s y nthe sis of am ino cy cl i tol anti bi o t i es and oth e r idiol it es Fol- ia Mi cr obio l. 24 : 286~291. Waller, C.W. and J. H Wi llam s : J. Am Chem Soc, 75. 2025(1953).Walto n, R. B and H. B Wood ruff . Deuelop m ent in Industr ial Mi cr ob, ple num pre ss 3. 370(1961). Weber M.M and S.C Ki ns ky : J. Bact. 89. 306(1965). Woodward R.B : An gre w. Chim 69. 50(1 9 57). Wrin c h D : Natu r e. 179. 536(1 9 57). Zim mer, T.L. 0. Froy sh ov. and S. G. Laland, 1979. Pep tide ant- ibi o t i cs , pp. 123~150. In : Rose, A. H.(ed), Economi c mi cr obio l ogy . vol. 3. Secondany pro duts of meta b olis m . Academi c Press. Lon-don.
제 1 炫} 미생물이 생산하는 유용물질 1 생리활성물질 생리활성물질이란 어떤 화합물을 생물에 주었을 때 어떠한 반응을 - 나타 내는 것으로 정의할 수 있다. 생물은 기온, 빛 등 의부환경에 의해 지배되고 있는데 그 밖에 생리현상 의 발현에 관여하는 내성생리활성물질이 있고 또한 다른 생물이 생산하는 생리활성물질에 의해 자극을 받는 것이 있다. 그 대상도 인간을 포함시켜 고등동물, 곤충, 식물, 미생물 등 모든 생물에 걸쳐 광범위하다 . 미생물이 생성하는 생리활성물질 1. 생장 촉 전물질, 생장억제물질 2. 길항작용물질, 항생물질, 항균물질, 형오물질 3. 생식억제물질 4. 식물호르몬 5. 식물생장 조절물질 6. 유독성분 1.1 식물병원균이 생성하는 독소 식물병원 미생물에는 세균, 사싱균, 바이러스 및 방선균 등 여러 미생물
이 있는데 그 중 사상균이 가장 많다. 식물병과 관련하여 1981 년까지 발 전된 독소(p h yt o xi c com p ounds) 는 15 峰쩨 달하며 계속 새로운 것이 발견되고있다. 독소에는 균의 침입에 대응해서 숙주식물이 생성하는 대사산물이 독소 가 되는 경우와 균이 직접 생성하는 독소가 있다. 또한 식물과 병원균 사 아에는 일정한 상관관계가 있어 숙주 특이적 독소와 숙주 비특이 독소가 있다.
표 14.1 식물병원세균과 그 생성 독소 균명 병명 독소 문헌 Ag ro bacte r iu m 근두종°성경 6-(3-m e th y- 2 -b u te n y l 5 tum efa c ie n s (쌍자영식물) amino ) pu rin e IAA Cory n ebacte r iu m 알팔파 위축세균형 당단백질 5 mi ch ig an ense pv. minis cihd iig o as nu men se 토마토궤양병 당단백질 55 Erwi ni a 화入J-병 고분자당 amy lo uora (사과, 배) (아미노포린) Pseudomonas rye g r a ss coronati ne 1.2 syri n a ga e pv. 줄기 마름병 P. astryor p in u g r pae u rpeav . 커피 줄기 마름병 tab to x in e 3 grac ae 담배°接뻥 pv. tab aci P. syr in g ae pv. 콩coronati ne 1.2 P. glsyy cr i i nn ge a a e pv. 복숭아 궤양병 syr m go m y cm 3 Rhsiyz roi bnigu ame 콩근류형성 rhi zo bit ox in 3 Jap o n icu m
코로나딘 (corona ti ne)(1, 2) 는 독보리속 목초 (r y e g rass) 에 침입하는 P.coronafa c ie n s ver. a t rop urea 에 의해 생성되는 독소로서 병반형성이 우 산 (corona) 모양의 남갈색 반점을 나타낸다. 이 균을 감자절편에 접종하 면 뚜렷한 비대현상 (h yp er t ro pi e res p onse) 을 나타내며 이를 생물검정에 사용할 수 있다. 이 독소는 P. syr in a ge pv. g l y c i nea 에 의해 콩과식물에 서도 생성되며 제초제 2,4-D 보다 강한 생육저해를 나타낸다. (3) 페세울로독신 ( ph aseolot ox in ) ( 3,4) 은 P. syr in g a e pv . p haseol i cola 에 의해 콩과식물에 생성되는 독소로서 이 식물 병원균의 배양물로부터 2종 의 독소가 분리되고 있다. 그 주성분은 N-ph osp h osulfa n y l ornit yl ala-ny l homoar gi n i n 리며 부성분은 주성분의 알라닌 잔기가 세린 잔기로 치 환된 2 세린 파세울로독신 (2 -s er i ne p haseolo t ox i ne) 이다. 탑톡신(t ab t o xi ne) 은 담배야화병균인 P. syri n g a e pv . t abac i에서 생성 된 독소인데, 후에 pv . corona f ac i ens나 pv . g raca 려서도 생성된다는 서실 이 밝처지고 있다. 。 II NH-P(OH) -O-S04N H 2 I (CH2 )3 H2 NI - CH-CO —ala -hoarg 주 : hoarg ; homoargi ni n e 그림 14.1 pha sedoto x in e 식물병원균 중 사상균은 식물 중에 감수성 품종에 발병하나 저항성 품 종에는 침해하지 않는 득칭이 있어 이들 병원균과 숙주와의 상호관계를
이해하려는 경향이 관심의 초점이 되고 있다. 그중 Helmi nt h o spo riu m 속 균과 Alte r naria 속 균에서는 숙주 특이적 독소가 발견되어 그 생리활성의 특이성에 관심이 집중되고 있다.
표 14.2 몇몇 주요 숙주 특이적 독소 독소명 균명 숙주식물 및 병명 문헌 HS-to x in e Helmi nt h o sp o riu m 사탕슈켜二 안정병 5. 6 HMT-to x in e sHa.c cmhaaryi d is 옥수수 깨무늬 잎 마름병 I 7 HC-to x in e H. carbonum 옥수수 north ern 8 leaf sp o t HV-to x in e H. vic t o r ia e 연맥 vic t o ria blig h t 3 AL-to x in e Alte r naria 토마토줄기 궤양병 9 alte r na ta sp. lyc o p e rsic i
한편, 숙주 특이적 독소가 아닌 즉 숙주 비특이적 독소로서 생리활성물 질을 생성하는 병원균도 디수 존재하며 그 개발 응용면에서의 관심도 주 목되고 있다 (3. 10). 식물병균과 숙주식물은 일정한 기생관계가 존재하며 품종간의 특이적 저항성은 식물의 유전자 대 병원균의 유전자 수준에서 설명할 수 있다. 물 질 수준에서 식물에는 균에 대한 물리적 장벽과 식물 고유의 항균물질이 나 피토 알렉신(p h yt o allex i n) 에 의해 나타나는 저항반응이 존재하며, 병균에는 대응 전화의 과정에서 획득한 숙주 특이 독소의 생성이 나타나 면서 식물세포에서 유도 저항성 물질의 생성이 억제되고 이어 발병을 일 으키는 것으로 이해되고 있다. 1.2 지베델린 지베렐린은 1938 td 벼의 키다리병균 (G i bberella fuji rur oi or Fusariu m
mon i l if orm) 의 대사산물로서 벼를 신장시키는 물질로 처음 분리된 것으로 서 오늘날까지 6~ 려 지베렐린이 알려지게 된 식물 호르몬의 일종이다. 영국의 ICI 연구진은 G. f uj i kuro i의 배양액으로부터 식물의 신장 활성 물질을 분리하여 이를 지베렐린산(gi bberel li c ac i d) 이라 명명하였다 (Curti s, 1954). 이어 S t odola 는 위의 균배양액으로부터 두 종류의 지베 렐린 활성물질을 분리하여 그것을 지베렐린 A 와 X 라 명명하게 되었다 (St od ola, 1955). 그리고 Sumi ki 등은 지베렐린을 메틸화하여 潟류의 지베렐린 메틸에스터 Ai, A2, A 를 분리하였는데 (Takahaski , 1955) 비교 검토한 결과 A1 과 A, 지베렐린산과 X 는 A 왼 동일물질이며 Az i:-새 로운 것으로 밝혀졌다. 이후 대사조절 등의 연구를 통해 수많은 새로운 지베렐 린이 분리되고, 이 진균 이의에도 카사바에 기생하는 Sph aceloma man- i ho ti colarr 으로부터 GA 가 분리됨으로써 Gib b erella 이의의 곰핑이로부터 지베렐린이 생산됨이 밝혀졌고 미생물기원 지베렐린은 2 또문 1l 이르고 있 다. (1) 지베펠린의 생합성 지베렐린은 많은 종류의 식물과 생산균인 G. f uj i kuro i에서 분리되고 동 정되었으며 그 생리작용도 연구되고 있는데 그 생합성 연구도 미생물과 식물 (Wes t et al., 1965. Graebe, 1974) 에서 모두 연구되고 있는 것이 특징 o] 다. 지베렐린의 생합성은 일반적 디테르핀(dit er p ene) 의 경우와 같은 경로 로 전행된다. 죽 이소피레노이드 단위 (iso p re noid u nit)는 메발론산 (mevalon ic ac i d) 에서 탈탄산과 인산화를 거쳐 이소펜테닐 피로인산(i so pen te n y l pyr o p hos p ha t e) 이 합성되고 제라닐 피로인산(g eran y l pyr- o p hos ph a t e) 과 제라닐제레닐 피로인산(g eran y l ger eny l pyro p ho sph a te ) 이 합성되는 경로까지는 st er 이 합성 경로와 동일하다 (L y nen, 1960, 1959). 야성 오이 (Echin o c ys tis macroca rpa) 의 미숙종자의 배유조칙 효소계에
의해 ATP 와 Mn2+ 존재하에서 메발론산 (me v alona t e) 이 트랜 스 제라닐 제레닐 피로인산으로 전환되며 (U pp er, 1967), 또한 (-) - kauren-19-al 과 (-)-kauren-1 9 -o ic acid .£ 전환된다 (Den ni s, 1967). (-)-ka ureneOl 지 베렐린의 전구물질이라는 직접적인 증거는 Fusariu m monil if o rm eol 14C - kauren 대 지베렐린 A에 도입한디는 Cross(1964) 의 실험에 의해서 증 명되었다. 또한 F. mon il i fo rm 려서는 한 종류의 지베렐린만을 생성하지 않고 그 변이주들은 AI, A1, A4, A7, & 등 여러 종류를 생성하며 (Sp e- cto r , 1968) 상호전환할 수 있음을 밝혔다. (2) 지베벨린류의 생산과 분리 Fusariu m mon i l ifo rm 려 의한 지배렐린의 종류나 수율은 사용하는 균 주나 배지성분 및 배양조건에 의해 좌우된다. 영국의 ICI 에서는 변형 Rou li n~Tho m:배지 (포도당 40g , ammon iw n tar tr a te 9.5g , KH2 P0 4 2.0g , KzS04 0.6g , Mg S 04 • 7H2 0 0.2g , 미량성 분 1.0m l 물 ll, pH 5.5) (Bria n , 1946. Borrow, 1955) 에서 25 °C 로 18 일간 심부배양을 하여 200 m g /l의 수율로 지베렐린 A 를 생산하였으며 그 후 배양조건을 개량하여 500m g /l의 수율을 올린 것으로 보고되고 있 다 (Br it, pat ; 838,082 (19 60), 850,018(1 9 60) ). 2 세포 외 다당류 다당류는 상업적으로 유화제, 식품, 의약품, 그리고 공업적 산물의 부형 제, 안정화제 등에 사용된다. 또한 원유 회수과정에서 기름표면을 깅하게 하기 위해 액체내에서 중합물질로서도 이용된다. 식물성 다당류(전분, algi na te , 한천)는 여러 해 동안 사용되어왔으나 미생물 다당류는 약 196 0l:;:回 이후에야 광범위하게 사용되고 있다. 생산가 격 때문에 상업적으로 - 이용되는 미생물 다당류는 세포 의 다당류에 제한 되고있다.
알지네이트는 해초에서 상업적으로 생산되어왔지만 미래에는 아조트박터 가 이용될 전망이고 알지네이트와 잔탄, 우론산 · (uron i c acid ) 잔기를 가 전 음이온성 다당류이다. 포도당으로부터 포도당원산을 거쳐 만들어지고 GDP 판노오즈 (man nose) ―➔ GDP-만 우론산 (mannuro ni c acid ) 등의 전환과정으로 전행된 다. 세포막과 세포 밖을 통한 단당류의 수송은 C-55 이소피레노이드 알코 울인산(i so p reno i d alchohol p hos pha t e) 과 함께 결합한 후에 이루어전 다. 현재 세포 밖에서 생합성되는 과정에 대해서는 거의 알려진 것이 없고 세포 의 다당류 분자의 자세한 구조도 거의 알려져 있지 않다.
표 14.3 상업적으로 사용되는 미생물의 다당류 다당류 구조 균주 Xanth an -Glc 1 !4 Glc Xanth o monas camp e str i s 규 a Mann 6-0Ac f: 8 • GlcA 가 8 Mann 4,6-0Py ruv ate Algi na te _4 D-MannA 1 l4D Pseudomonas aeru 양' nosa, -MannA 1-: -4 L-GulA 1 ➔a 4L Azoto b acte r vin el andii GluA Curdlan -Glc 1l3 Glc- Alcalig en es Sclero -Glc /l3 G lc- Sxleroti um glu canic u m,
glu can f 6p1G glu canic u m, l c SS.. droellfpsh i ii n i i , Pullulan - 6 (Glc 1 :(:1::.. 4• G-·lc :a: . Pullularia pu llulans 4 Glc) 1 - Dextr a n -Glc 1 :a:’. 6 Glc- Acet o b acte r sp. , s1e v-e ra4l c1o m-p o2 u,1n d-s 3 and LSLteeruu epcc oot nnoooc ossttcooc ccu sd memexsutertn aa tnn e sir c o ui md e, s , Gle=Glucose, Mann=Mannose, GlcA=Glucuronic acid , MannA=Man- nuronic acid , GulA=Guluron ic acid Ac=Aceta t e
잔탄 (xan t han) 은 Xanth o monas camp es tri예 의해 생성되며 상업적으 로 이용되는 첫번째 이형 다당류이다. 195 01;:撲텨 만들어져서, 1964년 에 시판되었다.
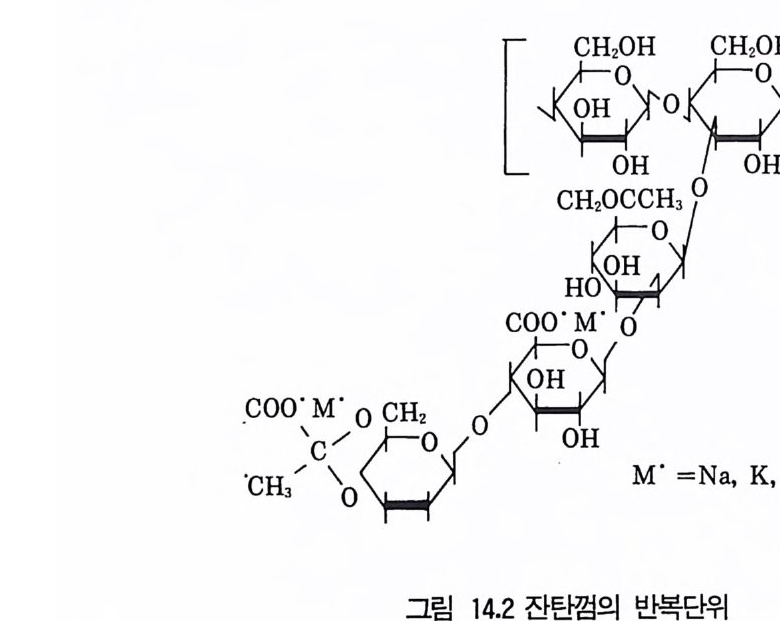 >OQo
>OQo
잔탄의 기본적인 반복단위는 포도당, 만노즈, 글루쿠론산, 아세테이트, 피루브산을 포함하는 5 탄당으로 구성되어 있다. 잔탄을 생성하는 균주는 안정하지 못하고 크고 작은 집락을 형성하며 작은 집락은 질이 낮고 생산 량도낮다. 상업적인 생산을 하기 위한 영양성분으로는 2.4 % 탄수화물(포도당, 자 당, 옥수수 전분 가수분해물), 0.05~0.1 % 질소(효모 추출액, 펩톤, 질산 암모늄 혹은 요소) 그리고 pH 7. 어t 조절하기 위한 영으로 구성된다. 점 성은 대수 증식기 동안 증가하기 시작해서 정지기까지 계속된다. 대량 배양에서 점성도는 20~30,000 c p (cen tip o i se) 까지 될 수 있으나 점성도가 10,000cp 이상으로 되면 기술적인 문제를 야기시킬 수도 있다. 샤용하는 탄수화물의 무게당 생성되는 잔탄의 무게에 대한 효율성은 70~ 80% 이고 수율은 20~30 g /l 이다. 생산물의 회수는 배양액을 제거하는 과 정에서 이소프로파놀(i so p ro p ano l) 혹은 메탄울을 가지고 다당류를 침전 시키면 된다. 그리고 침전된 잔탄은 건조시키면 된다.
표 14.4 탄수화물의 양을 제한하였을 때와 과잉상태일 때의 다당류 생산 산물 균주 탄소원 제한 질소원 제한 Cells(g /l) Polys a ccharid e Cells(g /l) Polys a ccharid e Xanth a n Xanth o monas 1.1 2.7 1.6 7.0 camp es tr is Algi na te Azoto b acte r 1.3 2.2 1.5 2.0 uin e landii Algi na te Pseudomonas 1.5 5.8 1.3 8.9 aerug ino sa (Pace and Righ elato , 1980)
알지네이트 (al gi na t e) 는 갈조류의 세포벽 성분으로 분자량은 38,000~ 200,00 떠 물질로서 Pseudomonas aerug ino sa- 2} Azoto b acte r u i neland ii는
업 n 의 우론산, 만우론산, 글루쿠론산(g lucuro ni c ac i d) 으로부터 알지네이 트를 생성한다. 제한된 양의 탄소 혹은 질소하에서 더 잘 생성되며 그 중 질소의 양이 제한되었을 때 더 높게 생산된다. Sclerog lu can(Comp ere , 1981) 은 Scleroti um glu canic u m, S. delph in i i , S. rolfsi i , 그리고 Heloti um s p.에 의해서 생성되며 주로 P-1, 3,으 로 연 결되어 있고 경우에 따라 p-6, 1~글 루코시드 결합으로, 연결된 포도당 단 위를갖는다당류이다. 위의 미생물들은 가수분해된 lign ocellulose 기질에서 자란다. Sclero- g lue 훑 식품 생산에도 사용되며, 步} 석유 회수과정에서도 사용된다. Scleroti um rolf s i카 질산의 양이 제한된 상태에서 포도당을 이용해 성 장하면서 Sclero g lucan 을 생성하는 상태를 나타내고 있다.
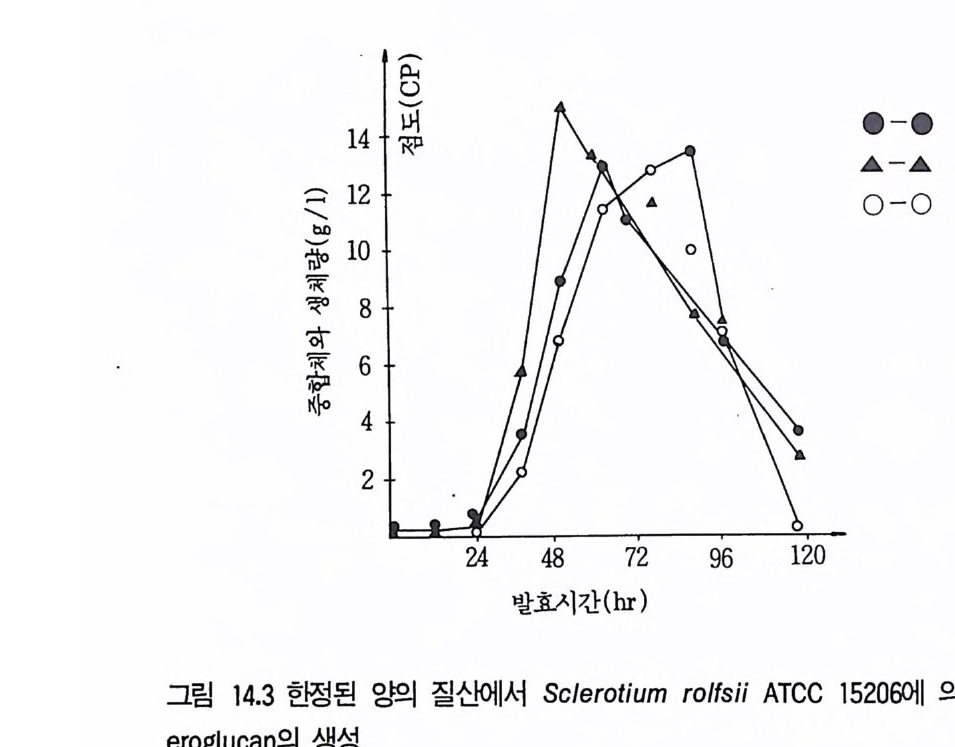 14 ()3守버 •_•
14 ()3守버 •_•
Sclerogl u can 생산(발효, 정제 그리고 효소적으로 가능한 절단)은 생산 조건이 최적화되면 경제적으로 가능한 공정이다. 풀루란 (Pullulan) 은 IJ.- 1, 4 와 약간의 IJ.- 1, 6-글 루코시드 결합을 가전 글루간(g lucan) 으로 곰팡이인 Aureobasid i u m pu llulans (Pullularia p ullulans) 에 의해 생산되며 5% 포 도당용액에서 5 일간 배양하면 70% 의 효율을 나타낸다 (Ca tl e y, 1979). Pullulanas 햐 세균에 의해 생성된다. 풀루란 형성을 위한 생리학적인 연구는 많이 이루어져왔으며 그림 14.4 은 풀루란 생성의 발효 동력학을 나타내고 있다.
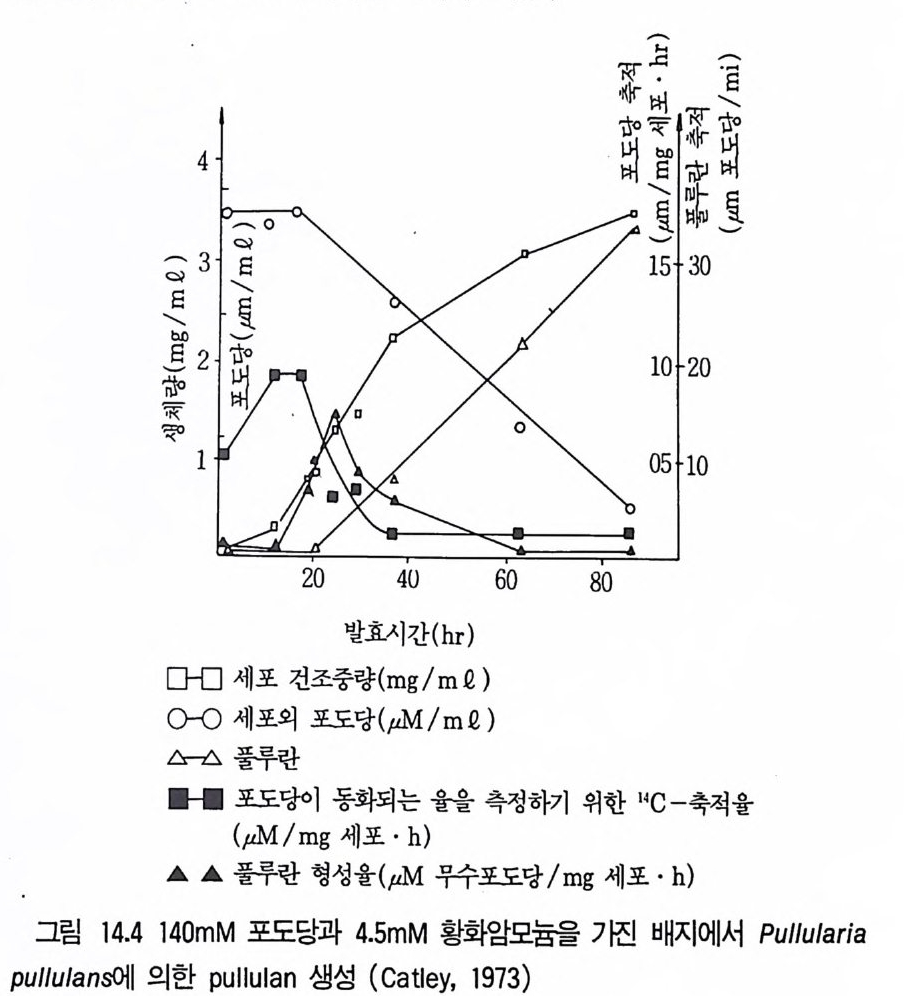 홍 ^뵤버 . =\ E
홍 ^뵤버 . =\ E
덱스트란 (dex t ran) 은 혈장의 효력 중전제 (ex t ender) 로서 중요하며, 또 한 식품 생산에도 사용된다. 이것들은 15,000~50,000 정도의 분자량을 갖 는 복합체이다. 대부분은 1,6-글 루코시드 결합을 갖는 글루칸이다. 그러나 몇몇 덱스트란은 1,2-, 1,3-, 1,4- 글루코시드 결합을 갖는다(J eanes, 1978). 다당체인 덱스트란은 t ransg lucos i dase 인 dex tra nsucrase 효소에 의해 생성되며, 이 효소는 자당 g lucose- fr uc t os i de 에 작용해서 포도당 단위들 을 덱스트란으로 중합하고 과당을 방출한다. 이 효소는 젖산균인 Leu- conasto c mesen t ero i de 띄 여러 균주에 의해 생성되는데 시판 덱스트란 생 성은 무기인산과 유기질소원을 가진 배지에서 L. mesente r oid e s½ 가지고 회분배양으로 생산된다. 알코올 침전을 통해 얻어지는 천연의 덱스트란은(분자량 500,000) 산으 로 가수분해되어 원하는 크기의 덱스트란(분자량 40,000~60,000) 을 얻어 결과적으로 에탄올 침전에 의해 회수되고 건조된다. 배잉액 속에 남아 있 는 과당은 회수가 가능하다. 참고문헌 Borrow, A. et al. ; J. Sci . Food, Ag r. B, 340 (1955). Bott ini, A. T. ; Tut r ahedron Lett , 22, 2719, 2723 ( 1981 ) . Bri a n, P.W ; '!ran s Brit, My co l. soc, 29, 173 (19 48). Cat l ey, B. J., The rat e of elalorati on of t he ext r acelluar pol ys a ccha- ri d e, pul lulan, duri n g gro w th of Pullulan ia pu llulans. J. Gen. Mi c- robi o l, 78 ; 33~38(1973). Cat l ey, B. J., Pullulan syn t h esi s by Aureoeasi d i u m pu llulans, pp. 67~84. In ; Berkeley, R.C .W, G.W Gooday, and P.C Ellwood(eds), Mi crobi a l pol ys a cchari d es and po lys a ccharases, Academ ic Press. Lon-don(1 9 79).
Comp e re, A. L. and W.L. Grif fith ; Sclerog lu can bio p o ly m er pro -ducti on , pro p e rti es , and economi cs , pp. 441~446. In:Moo-Young , M. (ed), Advances in bio t e c hnolog y, vol. ID. Perga mon Press. Tor- not o (1981). Cross, B.E . : J. Chem Soc 1964, 295 (19 64). Denn is D. T. & West. C. A. : J.B i ol .Chem, 242, 3293(1967). Durbin , R. D. : Toxin s in Plant Di se ase, Academ ic pr ess Inc. New Yor-k(1981 ). Frie n d, J. ; Bio c hemi ca l Aspe cts of Plant- P a rasite Relat ion ship s, Academ ic Press, London(1976). Je anes, A.R . ; Dextr a n bil liog ra ph y . U.S. dep t. Ag ri c . Res. Seru. Mi sc . Puhl. 1355(1 9 78). Kawano F. ; Chemi ctc y and Bio l ogy , 19, 208(1981). Lie s ch J.M .;'I etra hedron ·Le tt , 38, 45(1982). Mi tch el, R.E . ;Phys io l , Plant Pa th. , 19. 227(1981). Pace, G.W. and R.C Righ elato ; Producti on of extr a cellular micr oli al pol ys a ccharid e s, Adu. Bio c hem. Eng . 15 ; 41~70(1980). Sahamura, S ; J. Ag r. Chem. 55. 607(1981). Sahamura : Chemi str y and Bio lo g y, 14. 78(1976). Str o bel, G. A. ; Ann. Rev. Mi cro bia l , 31. 205(1977). Up pe r C. D & West. C. A. ; J. Bio l . Chem., 242. 3285(1967). Wood R.K.S ; Phyt ot o x in s in pla nt Dis e ase, Academi c Press, London (1972).
제 15 장 미생물의 물질전환 l 서론 미생물은 다양한 유기화힙물을 화학적으로 변화시킬 수 있는 능력을 가 지고 있다. 이러한 변화를 미생물학적 물질전환(mi crob i al tra nsfo r ma- tion s) 또는 생물학적 전환 (b i oconvers i ons) 이라고 한다. 이러한 효소학 적 반응을 통해 기질은 대사되어지고, 어떤 경우에서는 에너지 수지와는 무관하게 전환이 이루어지기도 한다. 일반적으로 산업공정에서는 화학합성 또는 생물학적 전환이 있는데 다음과 같은 몇 가지 이유 때문에 생물학적 전환이 바람직하다. 1. 기질 특이성 (substr a te spe c i fici t y) : 일반적으로 한 효소에 의해 하나의 반응단계만이 촉매된다. 2. 부위 특이성 (sit e spe c i ficit y, reg ios p ec if icit y) : 분자내에 한 종류의 기 능기가 여러 개 있더라도 한 특정 부위만이 작용을 받는다 . 3. 입체 특이성 (ste r eospe c if icit y) : 반응물질로 라세미 혼합물을 사용해도 한 종류의 이성체만이 전환된다. 또 한 효소반응의 결과로 비대칭 중심이 나타나면 반응산물은 대개 광학활성을 보이게 된다. 4. 반응조건 (reac ti on condit ion s) : 효소반응은 전환시에 온화한 조건을 유
지하므로 민감한 기질을 파괴하지 않는다. 또한 적당한 효소계를 가지는 한 미생물을 이용하여 발효과정, 또는 다른 여러 미생물을 이용하여 단계 적인 전환과정으로 여러 반응을 연결시킬 수도 있다. 이 반웅들은 주로 물에서 이루어지므로 환경오영을 덜 일으킨다. 2 생물학적 전환반응의 종류 가장 중요한 미생물적 물질전환반응은 표 15 .1과 같다 (K i esl i ch, 1976).
표 15.1 각종 생물 전환 반응 산화 Oxid a ti on s • Hy d roxyT la rtyi op nt op h an ~B.subti lis 5-Hy d roxy -try p top h an • Ep o xy da 1ti. 7o-n 0 c t a die n e --P-s=oeul:e.d:o:ov.m:o:.ro:a:nn:a-ss 7 .8-Ep o xy -l -octe n e • -C H-CH 의G la탈uc수in e ~Fusariu m solani Dide hy d rog la ucin e • Alip h ati c 결사슬의 산화에 의한 Aldehy d e, Keto ne, Carbox y l 기의 형성 nb-eDnzoedneec y l -.N..o.:c.a.r:d.i.a: : .s.p: Pheny l aceti c acid •• 알방킬붉 (A l고kyI리- l)P의 h결 en산n사\y슬 l\。- 의·N \o산ca7화r~d적iah 분opo해a c ae· 2-nHyy d r\o x\y\ p\h \en\y l a ceti c acid dodecane Naph th a lene
•치환기의 산화적 분해 Oxid a ti ve deam ina ti on , N- C1 13 demeth y la ti on , 0-C H 3 -d e me- thy la ti on Cunnin gh amella blakes le an a 10.11-Di m eth o xy -a p or ph in e ~ATCC 9245 Isoap oc odein e • He t ero fu n cti on 려 산화 (아미노기를 니트로기로, N-o x id e s 와 sulph oxid e s9 -l 형성 ) 2-Ami no -4 - alky l- im ida zole ~ 2 Nit ro -4 - alky l- im i- dazole 환원 ( Reducti on ) •카르복실기의 환원 Benzaldehyd e c=Se-rae=cuc=i hs~a= rao=em --y .c e Bs enzyl alcohol • He t ero f un cti on 려 환원(특히 -N02) Ni trop en ta - c h lorbenzol -aSutrr eepo ft ~oa mc iye cn es s Penta c hloranil ine 가수분해 반응 (H y drol yti c reacti on s) •두 탄소 사이의 이중결합의 수화 s . 叫 reo f ac i ens Anhy d rote t r a cyc l in e .A.T.C.C:. .1:07.6.2: ..:: Tetr a cy cl in e • 카르복실산 에스테르 의 가수분해 My co bacte r iu m d, 1-Menth y l laureate ph lei I-Menth o l •N 유도체들의 가수분해 。 R-C N 득PH9.0 RR --CiCi -ONOHH2
축합( Con den sa tion s ) • 인산화 Str e p tom y cin ~쯔므 Str e p tom y ci n - P •N-글 리코시6-드Az a결u합rac il ~ E. coli ATCC6 10798 -Az auracil ri b o sid e •O 글리코시드 결합 Beauueria sulfu re scens Meth y lg lu co- R1 =R2 =CH3 -CO- ATCC 7159; pyran osid e •N 이실화 derir v ati ve 6-APS Kluy ue ra + • ..c.i.t:r :o.:p .. h: :i.l.a . Amp ici ll in D-Pheny l- g l yc i n e meth y l este r
특히 산화반응이 산업공정에서 유용하며 그 밖에 이성질화, 환원, 가수 분해, 축합반응 또한 산업적으로 응용된다. 3 생물학적 전환공정 유기화합물의 미생물학적 물질전환에 포자, 증식 미생물, 휴면세포효소, 고정화세포 또는 고정화효소 등을 이용할 수 있다. 균체를 이용하는 공정에서 사용될 균주는 적당한 배지에서 배양하여 적 당한 증식 (6~24 시간) 후에는 농축된 기질용액을 첨가하게 된다. 이 과 정은 많은 양의 접종을 한 후 즉시 기질용액에 트윈 (Tween) 이나 독성이 낮은 용매(에탄올, 아세톤, 디메틸_포름아마이드, 디메틸술폭시드) 같은 유화제를 첨가하여 잘 녹지 않는 화합물을 용해시키기도 한다. 낮은 용해
도로 인해 첨가 기 질 의 양을 제한해야 하는 스 데로이드 전환에서는 비록 어떤 경우에는 30 g /l 가 전환될 수 있으나 보통 0.1 ~ lOg / l 배지의 기질 농도에서 행하게 된다. 용매의 농도는 사용되는 배지 l 당 5 ~15m Q.가 사용 된다. 어떤 스데로이드 전환에서는 기질은 미세한 결정형으로- 첨가하여 전환되기도 한다. 쉽게 용해되는 기질의 생물학적 전환 (b i o t rans fo rma ti on) 은 상당히 높은 기질 농도에서도 진행될 수 있다. 전환 시간은 반응의 종류, 기질의 농도, 사용되는 미생물에 달려 있다. 세균을 이용한 산화와 탈수반응이 몇 시간 동안에 이루어지는 데 반해, 효 모 특히 곰팡이에 의한 전환은 며칠이 걸리기도 한다. 대부분 미생물을 이 용한 가수분해반응은 몇 시간 안에 완결된다. 대규모의 물질전환반응은 멸균상태하의 통기 교반 발효조내에서 이루어 지며 전환과정은 크로마토그래피나 분광학적으로- 추적된다. 공정은 최대생 산량에 도달했을 때 종결된다. 또 오염은 원하는 반응을 억제하고 불필요 한 부산물의 생성을 야기시키거나 또는 전체 기질을 분해하므로 멸균 조 작이 필요하다. 첨가된 기질에 의한 효소의 유도가 필요하지 않을 때는 휴면세포를 사 용할 수 있다. 휴면세포는 기질에 의해 생장억제가 되지 않는 중요한 이점 이 있다. 세포의 높은 밀도는 생산성을 높이는 동시에 오염의 위험을 감소 시킨다. 이러한 종류의 어떤 공정에서는 고정화세포(i mmob ili zed cells) 가사용되고있다• 무세포 효소 추출액은 원하지 않는 부차적 반응이나, 분해를 피해야 할 생물학적 물질전환공정에 이용된다. 그러나 담체와 결합한 고정화효소 (carrie r -bound im mobil ize d enz ym es) 의 사용은 연속적인 공정 전개를 가능하게 할 수 있다. 고정화 세균세포나 고정화 효소의 사용은 증가추세 에 있다. 단일단계 또는 다단계 반응을 촉매하는 고정화 세균세포는 현재 o P-:파르트산과 말산의 상업적 생산에 이용되고 있다. 생물학적 물질전환 의 몇몇 공정에서, 예를 둘어 페니실린 아실라아제(p e nic illi n ac y lase) 와 포도당 이성질화 효소(g lucose i somerase) 와 같은 고정화 효소의 사용이
실용화되고 있다 (Ch i ba t a . 1977). 물질전환반응의 최종산물은 대개 세포 밖에 용해되거나 현탁된 상태로 존재한다. 세균이나 효모는 일반적으로 분리되지 않으나 곰팡이 균사는 여 과] 의해 분리된다. 모든 경우에서 반응생성물의 대부분이 세포에 흡착된 상태로 있을 수 있으므로 분리된 세포물질은 물이나 유기용매로 되풀이하 여 세척해야 한다. 회수는 생성물의 용해도에 의존하며 칼슘염에 의한 침 전, 이온교환제에 흡착, 적당한 용매나 휘발성 물질에 의한 추출, 배양액으 로부터의 직접적인 증류에 의해 이루어진다. 생물학적 물질전환에 대한 상당히 많은 예가 소개되어왔지만 겨우 몇몇 공정만이 산업적으로 이용되고 있다. 몇몇 공정은 생산량이 낮거나 또 경 제성이 아주 낮기 때문에 앞으로는 고정화 세포나 효소를 이용하여 좀더 경제적이고 새로운 기술을 통한 광범위한 응용이 기대되고 있다. 특정한 공정을 위한 유전적으로 최적화된 균주의 개발도 기대되고 있다. 4 스테로이드와 스테롤의 전환(t rans fo rma ti on of ste r oid s and ste r ols) 천연적으로 생성되는 스테로이드 (s t ero i ds) 는 호르몬 성질을 가지고 있 다. 죽 부신피질 호르몬(g lucocor ti co i ds, mi ne ral corti co id s ), 안드로겐 (androg en s), 에스트로겐 (es t ro g ens), 프로게스테론(p ro g es t erone) 과 같 은 호르몬이 그 예이다(그림 15.1 ). 에스트로겐, 프로게스테론과 안드로겐은 임상학적으로 사용되며, 프로게 스데론과 에스트로겐 유도체들은 피임약으로 사용된다. 더욱이 스테로이드 는 전정제, 항종양제로 사용되며, 가축병 치료에도 이용되고 있다• 글루코 르티코이드(g lucor ti co i des) 는 임상학적으로 광범위하게 이용되는 유용한 화합물기다. 코르티손 (Cor ti sone) 은 특히 소영작용으로 류머티스성 관절 영과 피부 질병에 유용하게 이용된다. 특히 코르티솔 또는 코르티손 분자
글부미루신네피코랄o질코코의르코르 티:티르호코=티코르이이손몬드 드 O CH2 0OH O0[안t tH H c2 0H: 더]H : 근0 티 후 :임 테 H\ 2론 °0H 0
\二〉H 데스토스테론 에게스탁로三겐 亡。0H 三 ::0 3 :Ol:06H I0X, \ o프로•게스~테론 그림 15.1 자연에서 생성되는 스테로이드 호르몬의 구조의 A 링 구조에서 1,2 이중결합을 형성함으로써 소염 효과가 상당히 증가 될 수 있다. 불소와 메틸기의 첨가로 l6a-hy dr ox y-9 a-flu o rop re d niso lo- ne(tr i a m c ino lone), 또는 6a-me t h y l p red ni solone(medrol) 과 강기 환원 형 mine ral corti co id 활성을 가지는 화합물을 만들 수 있다. 물질전환방 법을 통해 1-me t h y l- /J,. 1-andros t enolon 러 강기 남성 호르몬 효과가 감소
된 스데로이드들도 개발되고 있다. 4.1 스테로이드 전환의 종류 스데로이드 분자는 몇 개의 바대칭 중심을 가지고 있어 전적인 합성은 매우 어렵다. 과거의 화학공정으로는 31 개의 분리된 반응단계를 거쳐 615 g의 데옥시콜린산으로부터 l g의 코르티손 아세데이트를 산출했었다. 근 래의 화학공정은 훨씬 간단해졌으며 여러 생산공정에서 기질로서 데옥시콜 린산이 사용되고있다. 프로게스테론의 11a 숙캇}화 (lla-h y drox y la ti on) 에 대한 예비연구에 의 하면 미생물을 이용하여 스데로이드 핵내의 특정 위치에 입체 특이적으로 산소를 도입할 수 있는 가능성을 지적하고 있다. 현재 이러한 번응에 대한 연구가 잘 진행되어 코르티손의 값싸고 효율적인 생산이 가능하다. 11 번째 의 탄소 위치에 있는 산소원자는 코르티손의 소염 효과에 필수적이다• 현 재 스테로이드 분자의 거의 모든 위치는 디른 종류의 미생물 균주를 이용 하여 특이적으로 수산화시킬 수 있으며, 물질전환반응의 종류는 동물조직 에서 수행되는 반응의 종류보다 훨씬 많다(그립 15.2). 미생물학적 수화반 옹은 고도의 특이한 monoo xyg enase 에 의해 수행되며, 예로는 l1a 또는 llp-h y d rox yla se, 17a-hyd r oxy la se, 21-h y droxy las 혀문 둘 수 있다.
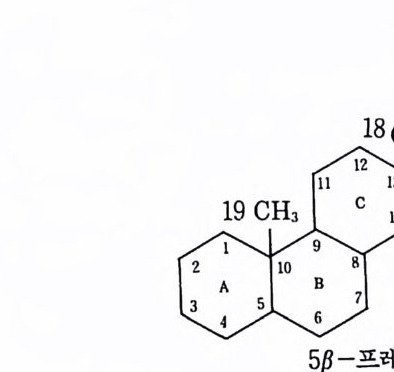 21 CHJ
21 CHJ
미생 물 동 물조직 la 7a • 15a la 15a 2l/aJ 79a, 1156pa 22ap 16a 17a 23ffJ3 1l0lap 1167Pa 66pa 1189 55/aJ 112lfaJ 1189 117pa 21 6{1 12{3 21 12a 14a 그림 15.2 동물조직과 미생물의 스테로이드 수산화반응의 비교(li zuk a, 198 1 )
표 15.2 스테로이드의 미생물학적 전환반응의 종류 A. 산화 Conversio n of secondary alcohols to keto n es Int ro ducti on of pri m ary hy d roxy l gro up s int o the st.e r oid sid e chain Intr o ducti on of secondary hy d roxy l gro up s int o the basic ste r - oid fram ework Intr o ducti on of ter ti ar y hy d roxy l gro up s int o the basic ste r - oid fram ework Dehy d rati on of rin g A in po sit ion s 1(2) and 4(5) Aromati za ti on of rin g A Oxid a ti on of the meth y le ne gro up to the keto gro up Sp litting of the sid e cha in of pre g na ne at C-17 durin g pro -ducti on of a keto n e Sp litting of the sid e cha in of pre g na ne at C-17 and op e~ in g of rin g D durin g pro ducti on of tes to l olacto n e
Sp litting of the ste r oid sid e chain durin g prc ducti on of a car- boxy ! gro up Sp litting of the sid e chain of pre g na ne at C-17 durin g pro -ducti on of a secondary alcohol Producti on of ep ox id e s Decarboxy la ti on of acid s B. 환원 Reducti on of keto n es to secondary alcohols Reducti on of aldehy de s to pri m ary alcohols Hy d rati on of double bonds in pos it ion 1(2) in rin g A Hy dr ati on of double bonds in pos it ion 4(5) in rin g A and 5 (6) in rin g B Eli mina ti on of secondary alcohols C. 가수분해 Sap on if ica ti on of ste r oid este r s D. 에스데르 생산 Acety la ti on (Sebek and Perlman, 1979)
4.2 경제적으로 중요한 스테로이드 전환 근래에 와서 화학적 방법과 미생물학적 방법을 조합시켜 생산한 수천 가지 스데로이드의 임상학적 효과가 시험되어왔다. 이같은 조합에 의해 합 성되는 전형적인 예로는 d i os g en i n 으로부터 Reic h ste i n ' s· substa n ce S 를 경유하여 생산되는 코르티손 (cor ti sone) 과 1-d e hy d ro 유도체들이 있 다. 표 15.3에 제시되어 있는 미생물적 반응과정은 경제적 중요성이 매우 크다. 더욱이 프로게스데론(p ro g es t erone) 이 C J9스페로이드로 전환되는 반응은 테스토스데론과 에스트로겐 생산에 산업적으로. 이용되며 A 환의 미
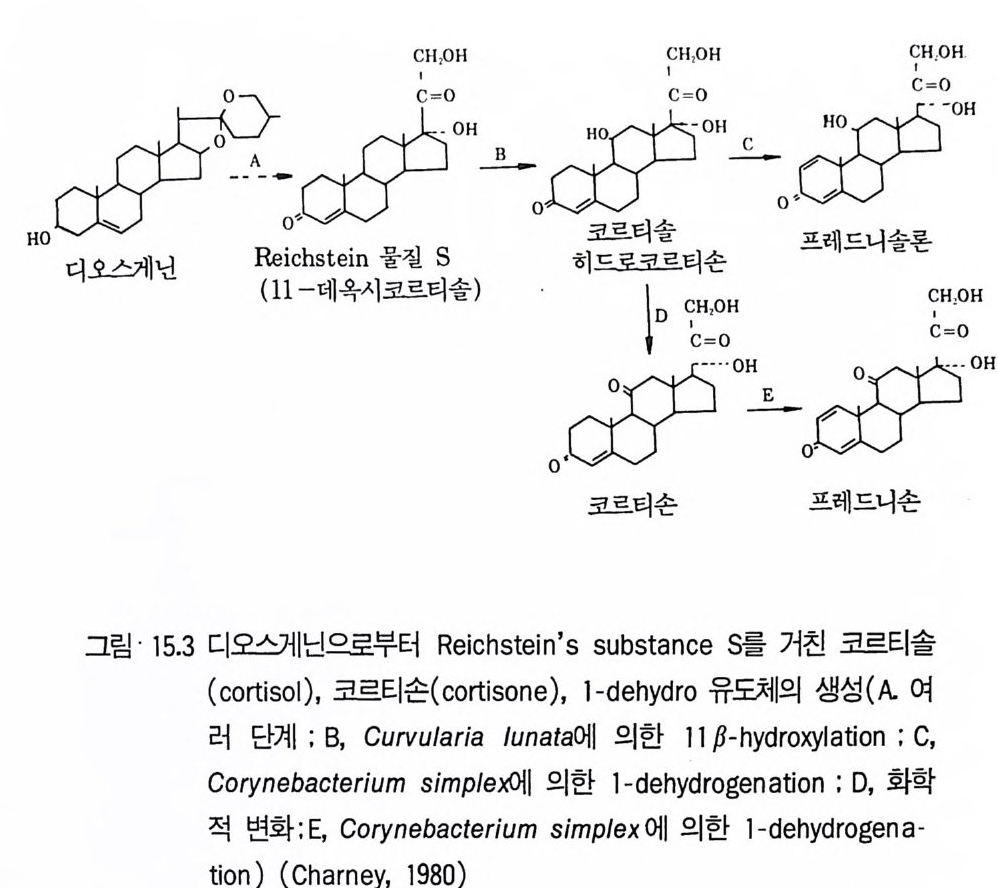 °二六- o 广C1H , 0° 0H H 드广C1 H, 0° 0H H 느。 广fH0° H 0H
°二六- o 广C1H , 0° 0H H 드广C1 H, 0° 0H H 느。 广fH0° H 0H
생물학적 탈수반응은 에스트로겐 생산에 사용된다. 이러한 생물적 전환을 위한 몇 가지 조건들이 표 15 .4에서 제시되어 있다. 스데로이드 전환은 회 분 발효조에서 주로 이루어지며, 공정에서는 고정화 세포나 효소가 사용된 다. 고정화 세포나 효소의 사용은 오염의 위험을 줄일 수 있고 생산물의 회 수가 간단하며 전환시간이 단축되고 기질의 농도를 증가시킬 수 있다는 이점이 있다. 대부분의 스데로이드 기질들은 용해도가 매우 낮기 때문에 물불용성 용매 시스템이 개발되었으며 Nocardia rhodochrou 려 고정화 세 포를 이용한 테스토스테론 전환에서 볼 수 있다.
13.5 표업산적인 테이스로환정공 드전 기―一질 수i물산gio rMHc빈nr amso제조 사회 yotHa-HytgPrdios reax y norleoneg-llycop-H rdotorx sreeneo ipRiohzigusnpncajr hnopsUynam Co -s pty HpCyinottoxroa-minHldeCno ro soliautruorClaifPlza arenu I .,nc tiBsGr-aeds co y1y-HirFrtl6txooi9udo-aono rcoals-laF9rul-oo16-a-tptorSRyeqec.sm.i Eua Sbb n,n soSxdi scrgoeosLeeroonmhlrbiedLa tee orreaos tyhyciorxdorl so yte~Dhgiti1droeCoionrlsnaors ndoe-P nolettrbAripeocahelsg r ix .mnc rhSCpero lrT-D dii iionedenlb opteSifiymofs naxapjpohU ya nnm oC niyIDt -h ,adre otgoPresetytne-De-1rotseodrh e_oncaoloyiCapocdrnl norRq..EinuS abb d Sons iir olaccdaiis eitipnlhc dg tans ipiSde-pn gitcils h attSitnseoitordnAl-iroodnedas n,eyt, Mpericbaoc.s um.DGrlenea.S a d Co. ynday-h 9or / dtrodnaxrodijennose ittoM muur pjCpn ohy:oU amno g.i(sto f.451F eetcrus rre)u ttms nau Di/3iyi- (, 11= ldodneh )12-4yg-p 71,xordianre )2 0(ne3-eend -o rrhriil=oldenyh21 ,lPy-dli-<4,-1·roxid4yyh)217(,,1p-1xrod생re-0)(217,git의산-3neeran(p enytm-a6ro-ilhdeeno ensol aekeb(SreP ndalm )9791 ,n)체들전구
표 15.4 여러 가지 스테롤과 스테로이드 전환의 작용조건 번호 기질 소邊 수율 (w 미생물 배지 반응조전 eigh t % ) (균주) 1 Proge s te r one 1-Dlaech tyo nd er o te s to l o- 50 Cyrl aind di cr oic co a lrap o n a 72 h, 25°C 2 Proge s te ro ne 1.4- Androsta d ie n e- 85 Fusariu m solani b 96 h, 25'C 3,17-d ion e 3 Proge s te r one lfo -H y dr oxy- 4-pr e- 11 Stre p t om y ce s C 72 h, 25'C gne ne 3,20-< lion e aureus 4 4-Androste - lla-Hy dr oxy -4- 25 Rhiz op us arrhiz us d 96 h, 28'c ne 3,17-d ion e androste n e- 3 ,1 7 검i one 5 Prog es te r one ll-<1.- Hy dr oxy - 90 Asp er gi llu s e 72 h, 28'C pro ge s te r one ochraceus 6 Hy dr ocorti - Prednis o lone 93 Arth ro bacte r f 120 h, 28'C sone sim p l e x Pseudo- crys t a ll i ne fer menta t i on 7 Choleste r ol 1,4 - Androsta d ie n e- 90 Arth ro bacte r g 44 h, 30'C 3,17-< lion e sim p l e x +chelati ng age n ts 8 p-Sitos te r ol 9ri-H y dro xy 4- and- Data My co bacte ri u m h 336 h, 30'C Choleste r ol roste ne 3 ,1 7 겁i one unavail ab le fort u i tu m muta n t wit h Stig m aste r ol block in brea k Camp es te ro l down of s te - eroid nucleus
표 15.421 배지류 a. 3g Corn ste e p liqu or (dry weig h t) , 3g NH4H2P04, 2.5g CaCO:i , 2.2g soy bean oil, 0.5g pro ge s te r one, dis t i lled H20 to 1 l, pH 7.0.
b. 15g Pep ton e, 6ml corn ste e p liq u or, 50g glu cose, dis t i lle d H2 0 to 1 l, pH 6.0 ; 0.25g pro g es te r one- g. 4 硏간 후에 첨가. c. 2.2g Soy bean oil, 15g soy meal, 10g glu cose, 2.5g CaC0:1, 25g pro - ges te r one, dis t i lied H2 0 to 1 l. d. 20g Pep ton e, 5ml corn ste e p liq u or, 50g glu cose, tap wate r to 1 l, pH 5.5~5.9;0.25 g androste n dio n~ 27 시간 후게 첨가. . e. Edam in, glu cose, corn ste e p liqu or : 20g pro g es te r one- g. 미세하게 부 수고 0.01% Tween 8 어 현탁해서 18~2~] 간 후에 첨가 f. 5g Pep ton e, 5g corn ste e p liq u or, 5g glu cose ; dis t i lled H2 0 1 l ; pH 7.0 ; 1~50% 미세하게 부순 hy d rocorti so n~ e t hanol 에 녹여 2 41-]간 후 배양액에 첨가. g. 10g Corn ste e p liq u or, 2g meat extr a ct, 5g glu cose, 0.5g K2HP04, dis t i lled H2 0 1 l ; pH 7.0 : choleste r ol (lg) 2 ()1-]간 후에 첨가(물에 분 산시켜) ;0.8 mM a a'-di pyri d y l( an iro n chelati ng ag en t)을 에탄距] 녹여 2 6'\]간 후에 첨가. h. 10g Glyc e rol, 8.4 g Na2HP04, 4.5 g KH2P04, 2g NH4Cl, tra ce ele-ments ; dis t i lled H20 1 l ; lg soy meal 과 10g sit os te r ol 첨가. (Sebek and Perlman, 1979) 4.3 스테롤 (s t ero l) 곁사슬의 미생물적 분해 스테로이드에 대한 수요 증가로 멕시코산 y am뿌 리 (Di os corea com- p os it a) 나 남아프리키산 식물인 'Iest u d in a ria sy lva ti c 죠료부터 얻어지는 dios ge n in 화합물 같은 생물적 전환을 위한 스데로이드 원료가 부족하게 되었다. 따라서 원가가 싼 스데롤인 동물의 콜레스데롤, 식물의 f3시토스 테롤과 스티그마스테롤 이용에 대한 집중적인 연구가 Arim a 연구실 팀인 저자들에 의하여 행해져 후에 공업화되었다. 이러한 연구의 목적은 스데로이드 핵의 분해 없이 지방 족 사슬을
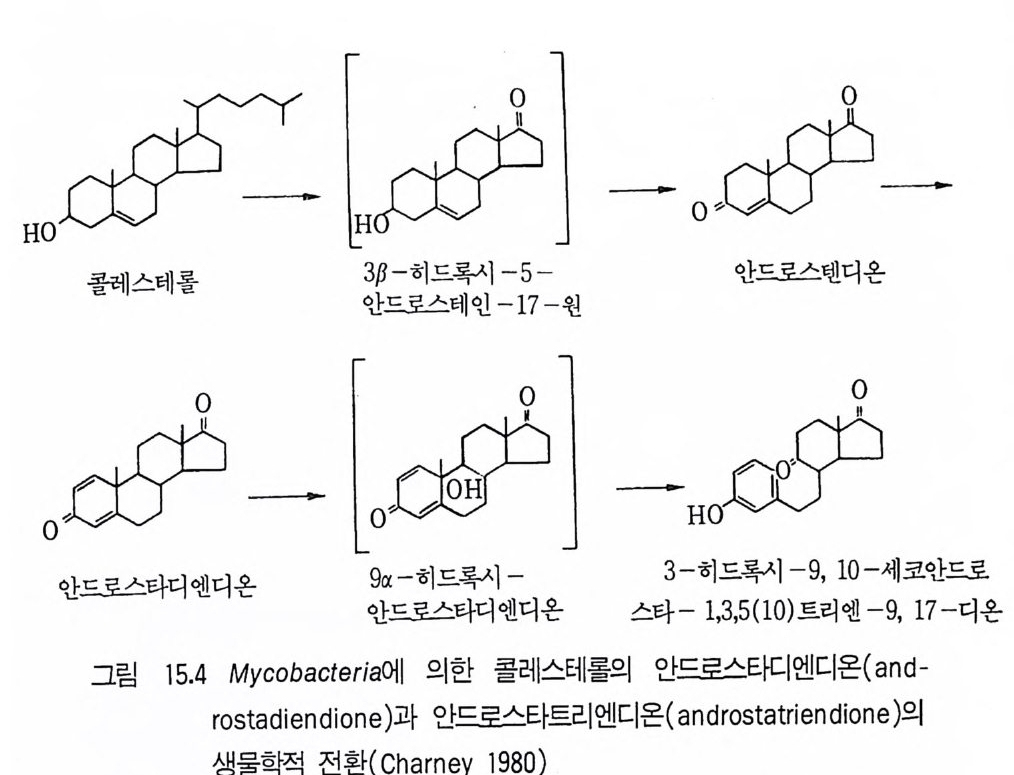 HO 二〉. O II _o ’ 广一O
HO 二〉. O II _o ’ 广一O
선택적으로 제거하는 데 있다. 그러나 기질로서 콜레스테롤을 사용 할 때 균들은 스테롤을 COi2 .} H 2 0 로 완전히 분해하게 된다. C-1( 2) 될수소화 (deh y dro g ena ti on) 와 9a 수산화 (h y droxy la ti on) 은 스테로이드 핵을 분해하기 위한 도화선이다. 그림 15 .4에서 보듯이 콜레스테롤로부터 고리가 열리면서 분해산물인 3-hy d rox y-9 .1 0 -s e coandrosta t r i e n e-9, 17-d ion eOl 생성되며 이 과정에서 두 가지 유용한 중간산물인 안드로스텐 디온 (andros t end i one) 과 안드로스타디엔디온 (andros t a di en di one) 이 생 성된다. 모핵 구조를 분해하지 않고 스데로이드 모핵을 변경시키기 위해서 는 몇 가지 유용한 방법들이 있다. 1. 분해반응을 기질의 화학적 변형에 의해 억제할 수 있다 (S i h et al, 1968). • 2. 저해제의 존재하에서 전환을 일으킨다• 이때 저해제로는 C-1( 2) -d e h-
y dro g ena ti on 이나 9a 수산화를 저 해하는 Fe2+ , Cu 2+ 와 킬레이트하는 화합물 또는 Fe 2+ 를 대치할 수 있는 27 }-0 l 온, 설프하이드릴 (sul fhy dr y l) 기를 차단할 수 있는 Ni 2+ , Co2+ , Pb2+ 같은 물질들이 사용된 다 (Ar i ma et. al., 1968, 1969). 3. C- 1(2) -탈수소효소와 9- 쩌찬화효소가 비활성인 돌연변이주를 사용할 수 있다. 콜레스테롤, 스티그마스데롤 (s tig mas t erol), p시토스데롤(p -5it os t erol) 을 전환시켜 주산물로 안드로스텐디온 (andros t end i one) 과 부산물로 안드로스타디엔디온 (andros t ad i ened i one) 을 만드는 My c- obacte r iu m 돌연변이주가 분리되었으며 이들 돌연변이주를 사용할 경우 이같은 후자의 산물에 있어서 더 이상의 분해는 일어나지 않는다 (Kra ych y, 1972, Marsheck, 1972). 위에서 언급된 공정의 몇 가지는 산업적으로 사용되어지고 있다. (표 15.4 예. 7 과 8). 5 비스테로이드계 화합물의 물질전환 스데로이드 전환 이의에도 알칸, 지방고리족, 방향족 이질고리화합물, 테 르펜, 알칼로이드의 미생물적 전환이 기술되고 있다. 지베렐린, 카로티노이 드와 캄퍼 (cam p hor) 를 기질로 할 경우는 분해반응이 우세해서 미생물학 적 전환은 조절하기 어렵다. 분해반응이 저해된 돌연변이주를 분리하기 위 한 시도는 성공하지 못하고 있다. 알칼로이드의 생물적 전환 같은 경우는· 반응 ~l 너무 낮게 나타나므로 산업적인 공정에 부적당하다. 초산균을 이 용한 글리세롤의 디히드록시아세톤 (d i h y drox y ace t one) 으로의 전환 등 몇 몇 전환반응은 경제적으로 중요한데 널리 알려진 반응 중에서 몇 가지 경 제적으로 중요한 생물학적 전환에 대해 언급하기로 하겠다. 5.1 L-Ascorbic acid ( vit am i n C) 그림 15. 요]서 보듯이 L 이소구근닌산 (L-ascorb i c acid ) 생산공정은 몇
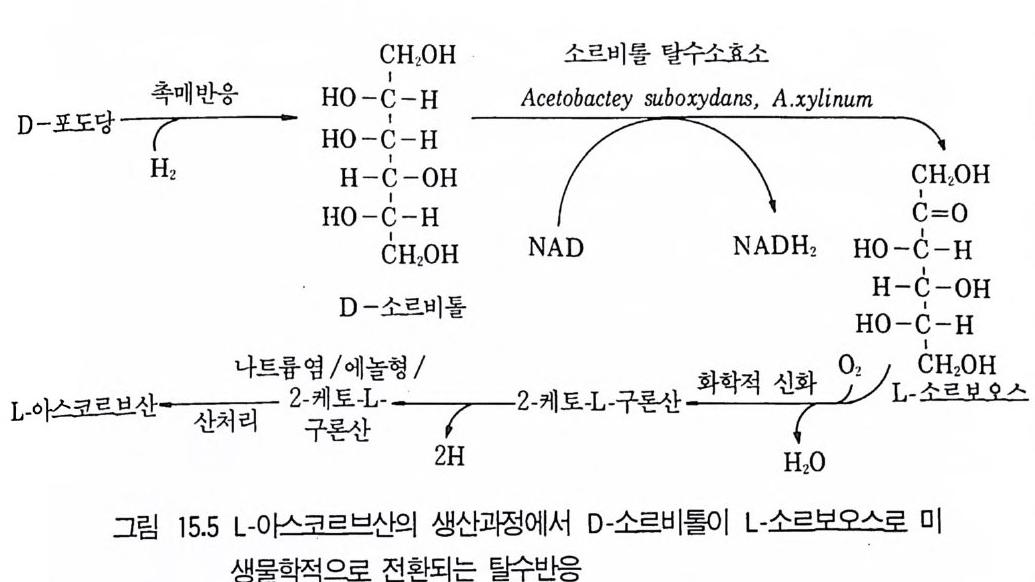 L-0 戶르브산H촉2매 - 반칼응나 詞트륨 2-영칼 HHH /ODHOO에-- -놀--CC C-CC소C형lIIl HH-—르 -- _O/,2HHH O 비0HH H7 톨 — 터ANceA토t/o소D b a르L c -t바e 구 y 롤 s런u탈b上o수x\화y소― d학a 효 n―N적s소,A ― DA신了H.x화 y2 一 l i no u夕 Hm,Hi H / OOL ----CCC\C CCI모I’ II H =-H--OO적2HH2 0 0 HH 오 H 스
L-0 戶르브산H촉2매 - 반칼응나 詞트륨 2-영칼 HHH /ODHOO에-- -놀--CC C-CC소C형lIIl HH-—르 -- _O/,2HHH O 비0HH H7 톨 — 터ANceA토t/o소D b a르L c -t바e 구 y 롤 s런u탈b上o수x\화y소― d학a 효 n―N적s소,A ― DA신了H.x화 y2 一 l i no u夕 Hm,Hi H / OOL ----CCC\C CCI모I’ II H =-H--OO적2HH2 0 0 HH 오 H 스
가지 화학공정과 한 가지 미생물적 전환으로 구성되어 있다. 이 공정에 의 해 세계적으로 생산되는 아소구근닌산은 연간 35,00~l 달한다. D 소르 비톨 (D 용 orb it ol) 이 L-수 근 님 22:: (L 용 orbose) 로 산화되는 단계는 통기와 교반이 되는 Aceto b acte r subox y da ns<게 의해 액내 배양으로 행해진다. 소 르비톨은 0.5% 효모 추출액이나 옥수수 침출액을 포함하는 영양배지에 초 기농도가 20% 되게 첨가한다. 전환은 약 2 心]간 후에 완결되며 소르비톨 농도가 높을수록 전환시간은 길어진다. 오늘날 이 공정은 두 단계에서 연 속적으로 이루어지며, 폴리아크릴아미드로 고정된 세포가 사용되기도 한다. L-수 근 닙 ¢ A 가 2 케토 -L-글 로닌산 (2-ke t o-1- gu lo ni c ac i d) 으로 산화되 는 과정 또한 미생물에 의해 수행될 수 있으나 화학적 전환이 좀더 비용 울 경제적으로 절감하기 때문에 이 방법이 선택되어 이용되고 있다. 5.2 프로스타그란단 (Pros t ag land i ns) 프로스타그란딘은 조직 호르몬으로 작용하는 c~] 불포화지방산이다. 이들은 다양한 생리적 활성으로 인해 의학적 중요성이 증가하고 있으며
가장 중요한 프로스타그란딘인 PGEi, PGE2, P GF1, PGF 놈 불포화지방 산인 아라키돈산 (arach i don i c ac i d) 으로부터 곰팡이를 이용한 미생물학적 전환에 의해 생산될 수 있다. 이 물질의 효율적 전환방법의 개발이 기대되 고있는실정이다.
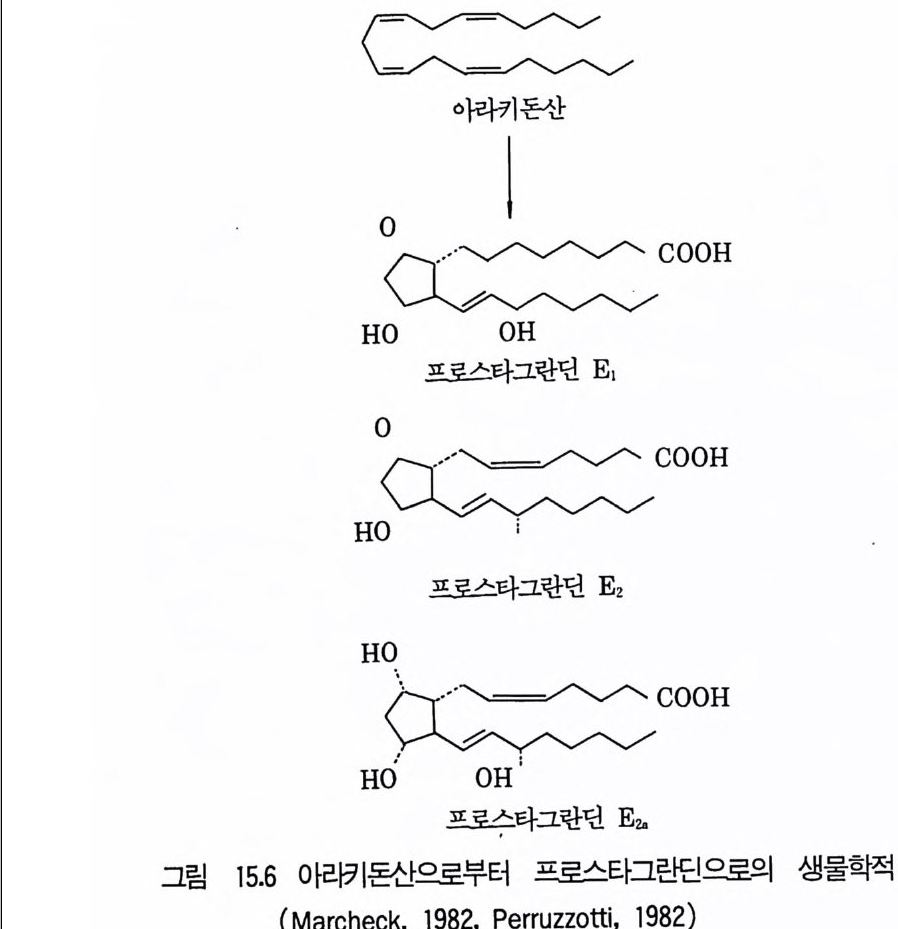 二。 아라키I돈 산
二。 아라키I돈 산
6 항생물질의 전환 항생물질의 탐색과정 이의에도 근래의 연구는 이미 존재하는· 화합물을 미생물적으로 전환시켜 새롭고 개량된 항생물질을 생산해내는 데 집중되고
있다. 전환의 목적은 효과의 개선, 독성의 감소, 광범위한 항생물질, 경구 홉수력의 중전, 내성균 발생이나 알레르기 효과가 감소된 물질의 개발에 있다. 대부분의 경우 물질전환의 결과는 항생물질의 부분적 또는 완전한 불활성을 유발한다. 따라서 많은 생물학적 전환이 시도되어지며 변형된 산 물이 바람직한 성질을 나타내는 것을 찾아내기 위해 그들 산물을 분석해 야한다. 많은 가능한 반응의 전형적인 몇 가지 예를 들어보겠다. 간접적 물질전환 : 배지에 저해제나 변형된 전구체를 첨가하여 생합성 경로를 조철하여 변형된 항생물질을 합성할 수g 있다. 예를 들어 시스-4페 틸프롤린의 존재하에서 Str ep t om y ce s p arvulu Si곤 이 프롤린을 프롤린 유사 물로 대치, 沙}지 새로운 악티노마이신 K 1 c2l- K 2 쇄 7 생산한다. 또한 특별 한 항생물질의 합성과정이 억제된 돌연변아를 사용할 때 새로운 화합물이 발견된다. 예를 들어 r i bos t arn y c i n( 그림 15.7) 은 네오마이신 (neomy ci n )
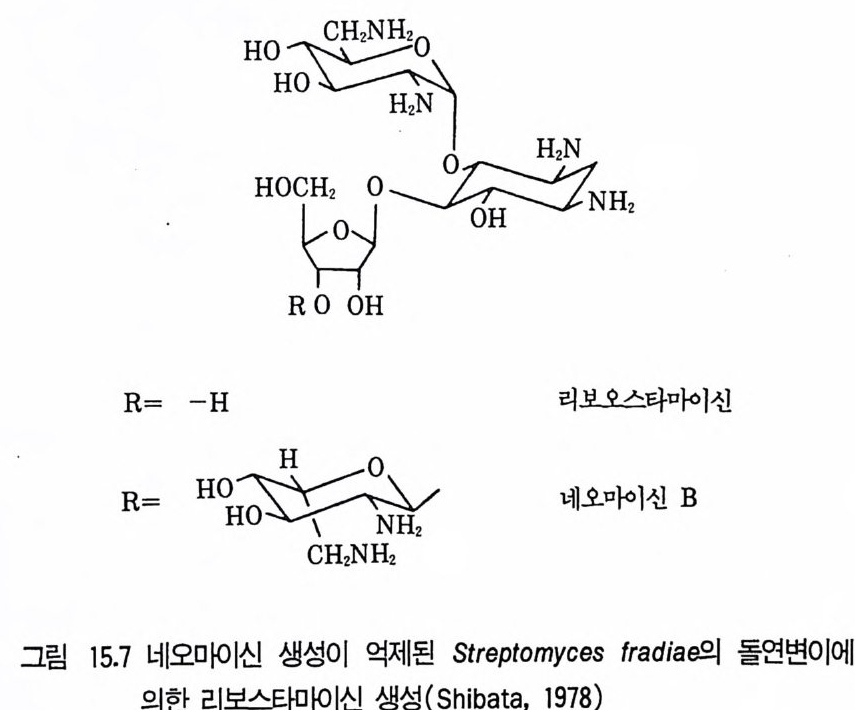 RO OH
RO OH
을 생산하는 균주인 S. f rad i ae 의 돌연변이주가 네오마이신을 생합성할 때 축적된다. 돌연변이주를 이용하여 합성 (muta t i on al s y n t hes i s) 한 개선된 항생물질이 알려지고 있으나 아직 상업적 생산에 이용되고 있는 것은 없 다. 직접적 전환 : 아실화반응 (ac y la ti on) 은 다양한 항생물질 생산에 이용되 고 있다. 대부분의 경우 불활성의 화합물이 생산되나 Bacil lu s meg at e r iu m IFO 12108 에 의해 lankacid in 0 나 메틸부티르산 (me t h y lbu ty ra t e) 으로
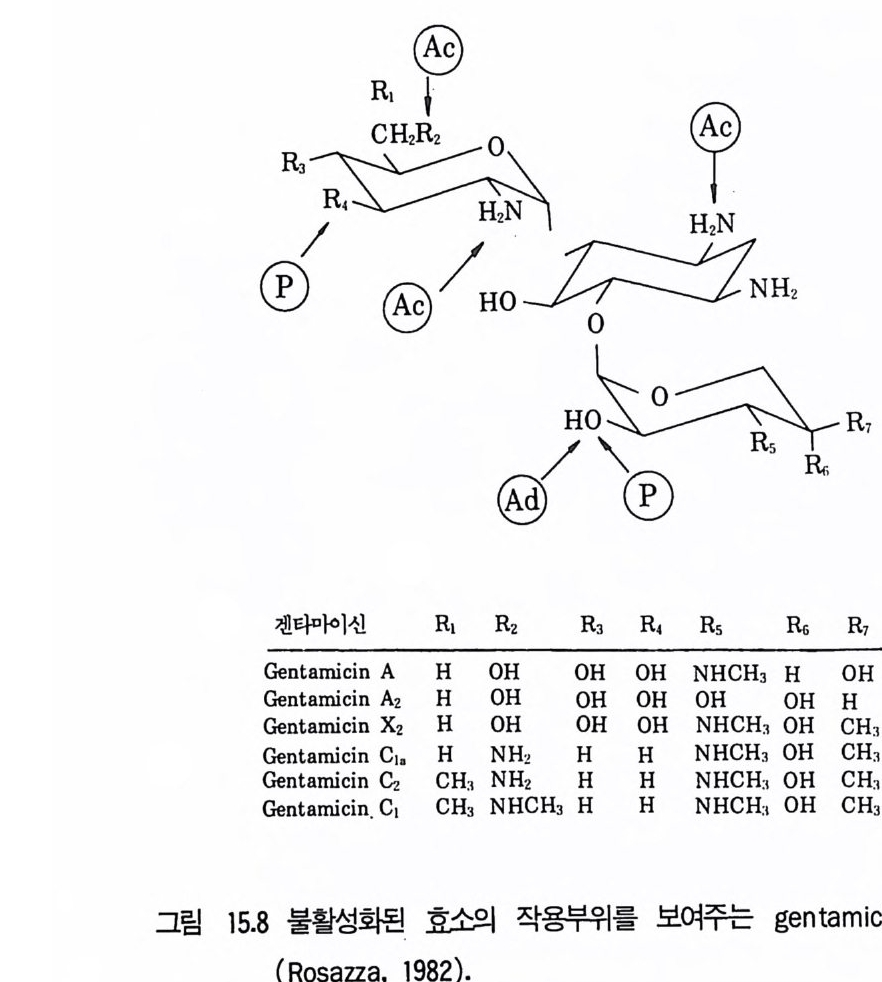 @
@
부터 생성된 생물학적 전환산물인 lankac i d i n - C-14-bu ty ra t e 의 경우는 독성이 낮고 항미생물학적 활성이 개선된 산물이 얻어진다. 탈아실화반웅 은 특히 마크로리드 항생물질 생산에 이용된다. 생물학적인 활성이 적은 탈아실화된 산물은 반합성 화합물의 생성을 위해 사용될 수 있다. 디른 p hos p ho t rans fe rases 에 의한 인산화와 aden y l t rans fe rases 에 의한 아데 닐화 (aden y la ti on) 는 주로 아미노글리코시드를 불활성화시칸다. 아세틸화 (acety la ti on ), 인산화, 아데닐화 (aden y la ti on) 는 아미노글리코시드 세균 내성을 개발하는 데 중요한 일차적인 반응이다. 距-락탐계 항생물질 (P-lac t am an ti b i o ti cs) 에서 가수분해의 반응은 특히 중요하다(그립 15.9). P-lac t amases 가 페니실린과 세팔로스포린 (ce p halo s p or i n) 에 있는 락톤 고리를 가수분해해서 항생물질을 불활성화한다. p-락 탐 항생물질에 대한 세균의 내성은 주로 이 반응에 의해 유도된다. 다른 한편, 페니실린이 pen i ci ll in ac y lases 에 의해 6 오}미노페니실린산 (6- ami-
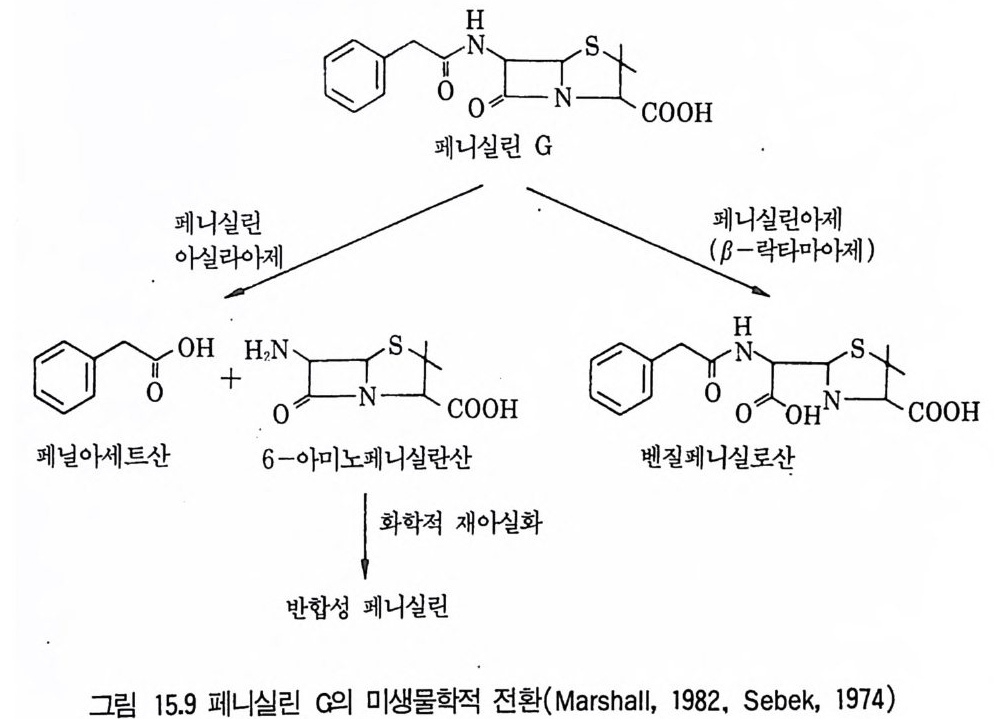 :〔二~ COOH
:〔二~ COOH
nop en ic i l la n ic ac i d) 으로 분해되는 것은 경제적으로 아주 중요하다. 왜냐 하면 암피실린 (am pi c i ll i n) 이나 아목실린 (amox i c i ll i n) 의 재합성을 촉매 하는 acy la ses7} 이론적으로는 가수분해효소와 결합해서 두 단계의 합성 과정을 구성하기 때문이다. 그러나 이 공정의 싱업적 적용에 대한 데이터 는아직 없다. 또 다른 미생물학적 전환반응에는 nabom y c i n 에서 pi crom y c i n 으로의 수산화를들수있다. 7 살충제의 물질전환 지금까지 상업적으로- 유용한 화합물의 생산을 위한 미생물학적 물질전 환에 대해 논의해왔다. 상업적으로 중요한 화합물 중의 한 분류인 살충제 분해를 일으키는 전환으로 화제를 돌리겠다. 식물의 질병과 해충조절을 위 한 약품은 인류의 생존을 위해 필요하다. 현재 세계수확량의 1/ 決폰 해충 에 의해 손실되며 또 다른 1/ 決든 화학적 조절 약품의 사용이 없다면 손 실될 것이다• 말라리아, 발진티푸스, 콜레라, 발진열 같은 전염병은 급격히 감소하였고 질병을 옮기는 곤충 매개체를 조절함으로써 완전히 제거되고 있다. 그러나 화합물의 난분해성은 환경에 대해 부정적인 영향을 끼친다. 환경에서의 난분해성 문제는 DDT, 린단 (l i ndane), 딜드린 (d i eldr i n) 같은 염화탄화수소 살충제에서 심하다. DDT 의 사용은- 질병의 조절에서는 주목할 만한 성공을 거두었으나 이 화합물은 분해되지 않고 미생물에 축 적이 먹이사슬에 유입된다. 197 ()1,1대 초반 이래로 DDT 의 사용이 제한되 었고, 독물학적으로나 환경적으로 안전한 약품 제조어} 대한 연구가 행해져 왔다. 이러한 상황에서 미생물학적 전환은 새로운 활성물질의 생산이 아니라 환경을 최대한으로 해독하기 위한 방법으로 관심이 높아지게 되었는데 이 것은 자연에서는 정상적으로 일어나지 않는 기질의 효소학적 전환을 말한
다. 이들 물 질 전환을 위한 많은 미생 물 효소들 이 유도되어야 함 을 의미한 다. 살충제의 제거는 다양한 기작을 통해 이루어진다. 탄소원으로서 살충제 (pes ti cid e s as carbon sources ) : 살충제가 미생 물의 증식과 에너지 생산울 위한 기질로서 사용될 수 있다. 제초제인 달라 폰 (dala p on) 의 예로서 Arth r obacte r s p는 염화지방산을 산화적으로 탈할 로겐화해서 피루브산으로 전환할 수 있다( Clarke, 1980) . 상호 물질대사 (come t abol i sm) : 상호 물질대사에서 미생물은 전환반응 으로부터 에너지를 얻지 않으며 증식을 위해서 또 다른 기질을 요구한다• 그러므로 상호 물질대사는 분자를 약간만 변형시켜 독성을 감소시키거나 증가시키게 된다. 상호 물질대사의 예는 표 15.5 에서 보여주고 있다.
표 15.5 살충제의 상호 물질대사 기 질 전환산물 미생물 Chio r benzil a te 4.4 '-D i ch lorbenzop h enone Rhodoto ru la grac il is (eth y l - 4, 4'- d i- chlorobenzil a te ) Chloroneb 2.5-D ich lor-4 - Fusarium sp. ( l,4-< lich loro-2 ,5 meth o xy ph enol dim eth o xy benzene) DDT p.p '-Dich lor- Aerobacte r aerog en es dip h eny lm eth a ne p,p '-D i ch lorodi- p-C hlorph e ny l aceta t e Hy dr og en omonas sp. phe ny lm eth a ne 2,4,5-T r ic h loro 3SD ich lorcate c hol Brevib a cte ri u m sp. phe noxy ac et a te
3,5-Di ch lor 3.5-Di ch lor-2- Achromobacte r sp. cate c hol hy dr oxy mu con ic- acid semi al dehy de (Bollag, 1974)
탈할로겐화 또는 산화적 탈할로겐화반응은 중요한 상호 물질대사반응으 로(그림 15.1 0 ) 살충제 분자를 그 이상의 분해가 가능하도록 만들어준다. chlordecone, hexachlorocy cl op e nt ad ie n e 유도체 같은 일부 화합물들은 훌륭한 살충 효과를 갖지만 그것들의 복잡한 구조와 심한 할로겐화 때문 에 미생물에 의해 쉽게 분해되지 않는다.
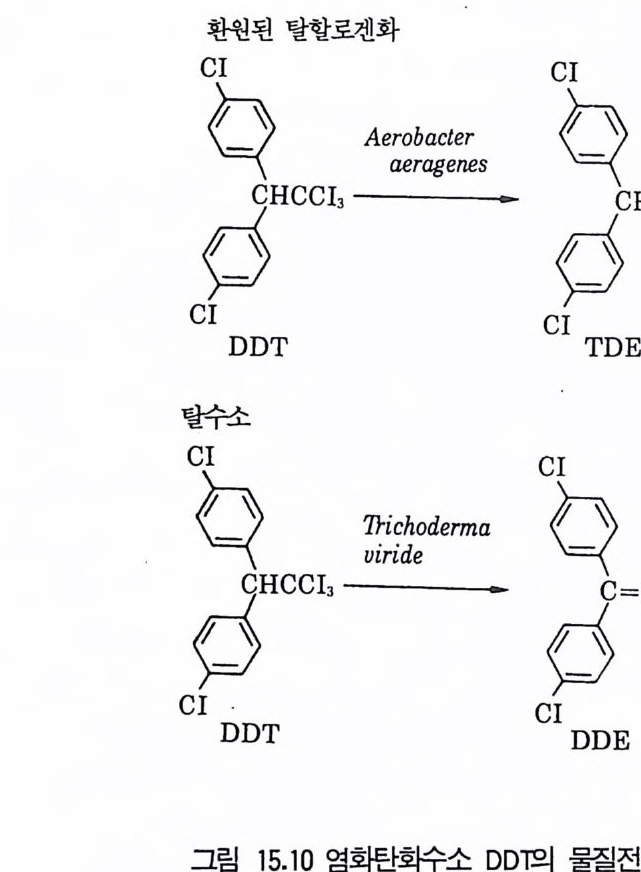 환원된 탈할로겐화
환원된 탈할로겐화
결합체 형성 : 살충제나 분해산물이 아미노산, 탄 수화물 과 같이 자연에 존재하는 화합물과 결합하여 일시적으로- 해 독 이 된다. 즉 독성 화합물은 어느 때이든 다시 방출되어질 수 있다. 그림 15 .1 1 는 dit hio c arbomate 살균제의 전환을 보여준다.
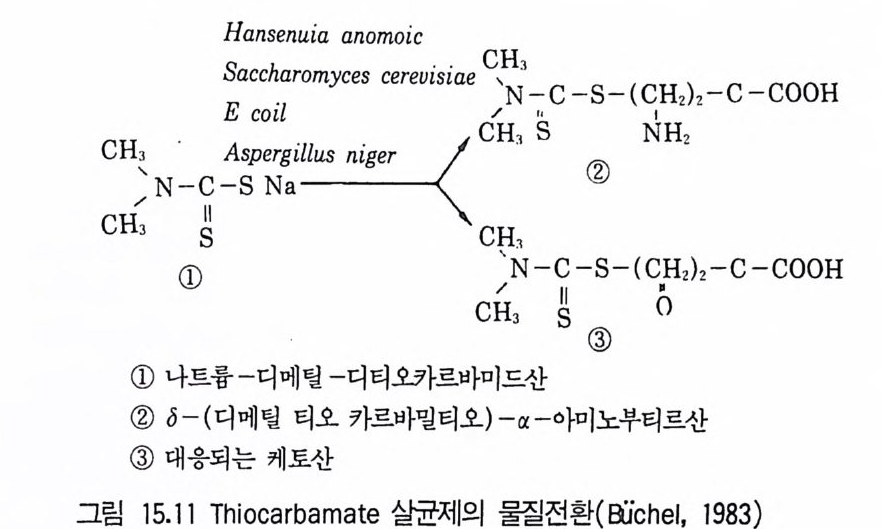 Hansen u ia anomoic
Hansen u ia anomoic
살충제의 축적 (accumulati on of pes ti cid e s) : 미생물이 살충제를 흡수 하였을 때 일시적으로 환경의 해독이 이루어진다. 해양 미생물과 플랑크론 이 DDT를 흡수하여 10 데의 계수로 농축된 것이 밝혀져왔다. 이들 미생 물동기 해양동물에게 먹히면 DDT는 지방조직에 저장되어 더욱 큰 농축 계수에 이르게 된다. 결국 먹이사슬을 거침으로써 화합물은 높은 수준까지 축적된다. 환경정화에서의 커다란 전전은 유전공학적 방법의 응용을 통해서 기대 되어진다. 제초제 2.4 .5 -T(2,4,5-tr i c h lorph enoxy aceti c a ci d) 의 경우 유전적으로 변형된 Pseudomonas cep a ci~ 사용하며 1 주일 동안에 1, 000~2,000 ppm 농도의 98% 이상까지 분해할 수 있다. 이것은 어떤 환 경적 오염물질의 분해에 특이하게 적용되어질 수 있는 〈맞춤된〉 미생물 균주의 생산을 위한 첫 걸음이다.
쵸卜고문헌 Arim a, K., Tamura, G, Naga s awa. M. and Bae, M. 1968 U.S . Pate n t 3388. 642. Arim a, K, Naga s awa. M, Bae, M. and Tamura, G., 1969 Ag ri c . Bio l . Chem. 33. 1636. Bae Moo (19 74), 10 KIST Rep o rt Bs. J. 37-562- 6 . Bollag, J.- M, (1982), Mi cr obia l meta b oli sm of pe sti ci d e s, pp. 125~ 168. In :J.P .Rosazza(ed). Mi cr obia l tra nsfo rm ati on s of bio a cti ue com- po unds vol. II . CRC Press, Boca Rato n . Buchel, K. H. (1983), Chemi str y of pe sti ci d e s, Jo hn Wi le y & Son, New York. Charney, W. and H. Herzog (1980), Mi cr obia l tra nsfo r mati on s of ste - roid s , 2nd edit ion . Academ ic Press, New York. Ch iba ta , I. and T. Tosa (19 77), Transfo r mati on of orga n ic com- po unds by im mobil ize d mi cr obia l cells. Adu. Ap pl. Mi cr obio l . 22;l~27. Clarke, P.H. (1980), Mi cr obio l og y and po lluti on :th e bio d eg ra dati on of natu ral and sy nthe ti c orga nic comp o unds. Phil . 1rans.R . Soc. Lond. B 290:355~367. Fuku i, S. S., A. Ahmed, T. Omata , and A. Tanaka (19 80), Bi o- conversio n of lipo p h il ic comp o unds in non-aq u eous solvent. Ef fec t of gel hy d rop h obic i t y on div e rse conversio n s of tes to s te r one by g el 군 n t ra pp ed Nocard ia rhodochrous cells. Europ. J.A p pl. Mi c- robio l . Bio te c hnol. 10 : 289~301 . Iizu ka, H. and A. Nait o (1981), Mi cr obia l conversio n of ste r oid s and alkaloid s , Un ive rsit y of Toky o Press, Sp r in g er -Verlag, Berlin . J. Overhoff U.S . Pate n t 2, 467. 422(Ap r 19.1 9 49). Ki es li ch , K. (1976), Mi cr obia l tra nsfo rm ati on s of non-ste ro id cyc l ic com- po unds. Georg Th iem e Verlag, St ut t ga rt. Ki es li ch , K. (1978), Mi cr obia l tra nsfo r mati on s-t y pe reacti on s, pp. 57~85. In:H 'ut t er, R., T. Leis i n g er , J.N ·uesch, and W.Wehrli (e ds), An tibi o t ic s and oth e r secondary meta b olite s . Federati on Europ . Mi c-
robio l . Soc.Sy m p . No.5. Academi c Press, London. Ki es lic h , K. (19 82), Practi ca l app li c a ti on s of mi cr obia l tra - nsfo r mati on s in the sy n th e sis of natu ral comp o uds or analog u es, pp. 311~324 In : Krump ha nzl, V., B. Sik y ta, and Z. Vanek(eds). Overpr o ducti on of mic ro bia l pro ducts . Academi c pre ss, London. Kray ch y , S. et al, 1972, U.S Pate n t, 3, 684, 657. Leuchte n berge r , W., A. F. Buecknann, M-R . Kula, R.W i ch mann, and C. Wandrey (1981), Enzy m ati c syn th e sis wi th cofa ctor -reg e ner-ati on . 2nd Europ. Cong r. Bi ot e c hnol., Eastb o urne, En gla nd. Abstr a cts of communic a t ion s, p. 47. Leuenberge r , H.G.W. (1978), Mi cr obia l tra nsfo r mati on s-s o me ap p- lica ti on s in natu ral pro dut chemi st r y , pp.8 7~100. In:H 'ut t er, R., T. Leis i n g er , J. N'uesch and W.Wehrli( e ds.), Anti bio t i cs and oth e r secondary meta b olite s . Federati on Europ . Mi cr obio l . Soc. Sy rop. No. 5. Academ ic Press, London. Marshall, V.P. and P.F.W ile y (1982), Mi cr obia l tra nsfo r mati on s of anti bi o t i cs , pp. 45~80. In :Rosazza, J.P .(ed.), Mi cr obia l tra - nsfo rm ati on s of bio a cti ue comp o unds, vol. 1. CRC Press, Boca Rato n . Marsheck,W.J. Kray ch y S. Mur R.D . (1972), Ap pl. Mi cr obio l , 23, 72. Marsheck, W. J. and M.Mi yan o (1982), Mi cr obio l og ica l bio - conversio n of pro sta g la ndin s , pp. 1~19. In:Bull, M.J. ( ed.). Prog- ress in ind ustr i a l mi cr obio l og y, vol. 16. Elsevie r Scie n ti fic Publi sh in g Comp a ny , Amste r dam. Paul Rump f : Chem. Abst 54. 3229 (19 60). Peruzzott i, G. P. (1982), Mi cr obia l tra nsfo r mati on s of pro -sta g l a ndin s , pp. 109~126. In:Rosazza, J.P . (ed). Mi cr obia l tra- nsfo rm ati on s of bio a cti ue conp o unds, vol. I. CRC, Boca Rato n . Rosazza, J.P .(ed). (1982), Mi cr obia l tra nsfo rm ati on s of bio a cti ve com- po unds. Vol II CRC Press, Boca Rato n . Sebek, 0.K. (1974), Mi cr obia l conversio n of anti bio t i cs. Lloy d ia 37:115~133. Sebek, O.K . and K. Ki es li ch , 1977, Mi cr obia l tra nsfo r mati on s of or- gan ic comp o unds. Ann. Rep. Ferm Proc.1 : 267~297.
Sebek, O.K . and D. Perlman, 1979, M icr obia l tra nsfo r mati on of ste - roid s and ste r ols, pp. 483~496. In : Pep ple r, H. J. a nd D. Perlman (eds.), Mi cr obia l tec hnolog y, vol. l. Academi c Press, New York. Sh iba ta , M. and M. Uy ed a (19 78), Mi cr obia l tra nsfo r mati on s of ant- ibi o t i cs . Ann. Rep. Ferm. Proc. 2:267~303. Sib , C. I,T ai H.H. and Lee S.S. 1968 : Bio c hemi st ry 7, 769~808.
제 16 장 단세포 단백질 1 서론 〈단세포 단백질 (SCP) 〉이라는 용어는 오늘날 식량이나 사료 첨가물로 이용되는 미생물 균체를 일컫는데 일반적으로 분리된 세포 단백질 혹은 총 세포물질을 SCP(sin g le cell p ro t e i n) 라고 부른다. 동물체와 식물체는 주요 식량원이지만 미생물도 치즈, 식초, 버섯, 요구 르트 효모, 청녹조류와 같은 산물로 적은 양이나마 식용으로 쓰이고 있다. 부족한 세계 식량공급과 미생물 세포의 높은 단백질 함량을 고려하여 볼 때 발효조에서 생산되는 균체를 이용하는 것은 관례적인 식량보급에 이상 적인 영양보충이 될 것이다. 단세포 단백질은 비타민, 단백질, 지질의 함량이 높고, 모든 필수아미노 산이 완전하게 함유되어 있기 때문에 영양적인 가치가 크다. 그러나 많은 나라에서 주요 식량원으로 미생물을 이용하는 데는 심리적인 장애가 있다. 아래 항목들은 안정성에 대한 심리적인 장애를 유발하는 요인이 되고 있 다. L 높은 핵산농도(조류에서 4~6%, 박테리아에서 10~16%, 효모에서 6~ 10%, 곰팡가에서 2.5~6% )는 건강을 해칠 수 있다. 2. 독성물질이나 발암물질이 미생물의 증식기질(홀수의 탄화수소, 곁가지의
탄화수소, 다환식 방향 족 화합 물 )로부터 흡 입 될 수 있고 미생 물 자신이 독성물 질 을 생산할 가능성이 높다. 3. 소화관개서 미생 물 세 포 가 느리게 소 화되 므로 소 화 불 량과 미지의 반응을 일으킬 우려가 있다. 식량으로써 미생물의 이용은 비록 회의적이지만 인간에 의해 소 비되는 가축의 사료 SCP 를 통해 간접적으로 인간 영양에 중요한 역할을 담당할 것으로 생각된다. 생산원가는 가축용 SCP 의 궁극적인 위 치 를 결 정 하는 데 하나의 요소가 된다. SCP 는 콩이나 생선과 같은 천연 단백질원과 경쟁하 게 되는데 SCP 의 가격은 이용방법에 따라 다양하다. 예를 들면 인간을 위한 SCP 는 높게 정제된 생산물을 이용하기 때문에 l()ll ~ 정도가 비싸다. 현재 SCP 생산을 위한 연구에 이용되는 물질은 알칸, 메탄, 메탄올 , 셀룰 로오스 및 이들 폐기물이다. 2 알칸 (alkanes) 으로부터 SCP 의 생산 (Fuku i, 1981) 긴사슬 알칸은 많은 효모와 몇몇 곰팡이 (예를 들면, Mucorale~ Mon- i li ales) 와 몇몇 세균에 의해 분해된다. 아래 효모의 종류는 · SCP 생산을 위해 널리 연구되고 있다 : Candid a trop i ca lis, Candid a oleop h il a , Sac- charomy co p s is lip o lyt ica 알칸을 이용하는 데 있어서 단점은 알칸이 쉽게 용해되지 않는다는 것이다. 세포들이 교반날개가 달린 생체반응기나 air- lift형 발효조기에서 증식하는 동안 l~lOOµ m 크기를 가전 큰 알칸 방울 이 형성되어 부유상태로 있게 된다. 알칸의 용해도(용해도 10-4 ~ 10-9 v /v) 가 낮기 때문에 알칸에서의 미생물의 높은 증식속도는 물에 용해된 알칸 의 수송에 의해서만으로는 설명할 수 없다 : 디른 흡수 기작이 존 재할 것 이다. 세포들은 불용성 알칸을 0.01~0.5 µm의 작은 방울로 전환시키는 유 화물질을 형성하는 것 같다. 그러면 알칸 분자는 수동확산에 따라 세포벽
을 통하여 세포막에 이른다. 알칸에서 성장한 세포는 지질이 풍부하고, 이 런 지질은 세포막을 통한 알칸 전이에 어떤 역할을 하는 것으로 생각된다. 2.1 건사슬 알칸의 이화작용 알칸 분해에는 말단산화와 준말단산화의 두 가지 경로가 있다 (Re run, 1981). 말단산화에서는 1 차 알코올과 알데히드의 중간단계를 거쳐 상응하 는 모노카르복실산 (mono -c arbox y l i e ac i d) 이 생산된댜 말단산화 후의 분해는 일반적으로 l 산화에 의해 아세틸-5L에이가 생성된다. 말단산화는 세균이나 효모의 물질대사에서 중요한 경로이다. 어떤 경우에는 w 신감화에 의해 분자의 양끝에서 말단산화가 일어남에 따라 디카르복실산(di-c ar-
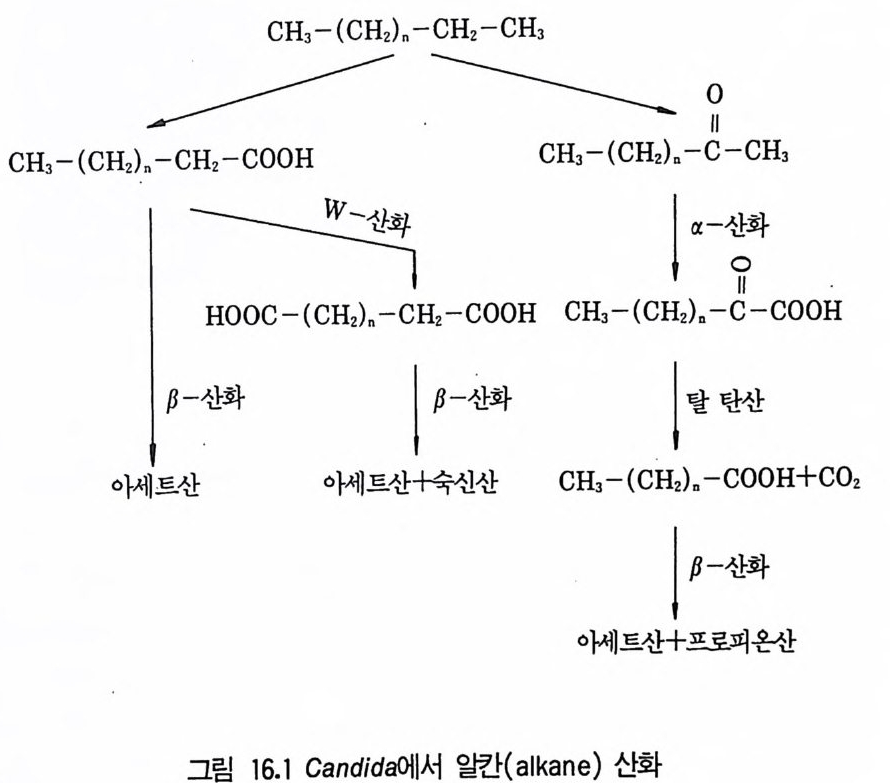 CHa -(C H2 )n- - -C -H三-2H--OC-OO-CC--OH(-HCa- H--2(-C) -H . -一2 ) Cn H-.C- 2 H--C2 -O--CO HH- aC- HC-aH--J( -—C (-HC-2H).2-)C。I.I - -C운C- HCaO OH
CHa -(C H2 )n- - -C -H三-2H--OC-OO-CC--OH(-HCa- H--2(-C) -H . -一2 ) Cn H-.C- 2 H--C2 -O--CO HH- aC- HC-aH--J( -—C (-HC-2H).2-)C。I.I - -C운C- HCaO OH
boxy lic ac i d) 이 생산되고 이것은 化산화에 의해 아세트산과 숙신산 (sue c i na t e) 후 7e타 전다. 말단산화의 효소적 기작은 아직 완전히 밝혀지지 않고있다. 준말단산화에서는 2 차 알코울을 거쳐 케톤 (ke t one) 이 생산된다. 이 반 응은 C2 자리에서 일어나거나 분자의 내부, 예를 들면 C·1, C 4, C 5, C ,, 자 리에서 일어난다. 내부산화는 C2 자리에서 일어나는 것이 아닌 준말단산화 를 일컫는다. 미생물은 탄소원자를 준말단산화방식으로 분해하는 특이성을 보인다. ~} 알코올의 그 이상의 분해는 다양한 과정을 거친다. 탈탄산과 정을 수반하는 Cand i da 에는 a 산화와 p산화가 일어나고, 그리고 este r - as 려 의해 분해되어 es t er 로 전환되기도 한다. Este r ase 작용의 산물인 산과 알코올은 계속해서 대사되어진다. 2.2 효모를 이용한 대규모 SCP 생산 두 가지 석유 산물이 원료물질로 이용될 수 있다. 1. 연료용 기름으로 알려진 가스오일로서 10~25%C1s~c30 알칸을 포함한다. 2.C10~C13 알칸이나 cl3~C11 알칸 구분을 분자분리막을 이용해서 가스오일 로부터 분리하여 이용한다. 1973~1975 년 프랑스의 Cap Lavera 에서 Candid a t rop i cal i혜卜 가지고 비멸균 연속시스템 (16,000 t ons/ 년)으로 가스오일 공정이 실험되었다. Gran g emou t h 에서 Saccharomy co p si s l ip ol yti ca( 전에는 Candid a lip- olyt ica . £ 불렸다)를 이용하여 n-알 칸을 함유한 300m3 생체반웅기에서 무 균적으로 배양시켜 연간 4,000 ton s SCP 를 수년간 생산했다. 3tll의 1, 000m3 발효기를 가지고 alkane 공정으로 연간 100,000 t ons 을 생산하는 완전한 공장이 Sard i n i a 에 설립되었으나 그 후에 정치적 이유로 작동이 중단되었다. 알칸 공정에 관해서는 Forbes(1979) 의 보고가 있다.
3 C1 화합물로부터 SCP 의 생산 3.1 메탄 자화세균 풍부한 천연가스의 주요 성분인 메탄 (me t hane) 은 SCP 생산의 에너지 원으로 기대되고 있다. 메탄은 매우 순수한 가스로 얻을 수 있으나 높은 탄화수소외는 대조적으로 쉽게 액화되지 않는다. 또한 수송이 어렵고 폭발 의 위험 때문에 메탄을 취급할 때 매우 안전한 방법으로 다루어야 한다. 메탄을 산화시키는 세균은 obli ga te meth y lo t ro p h s. £. 분류되는데 이 부 류는 단지 C1 기질 메탄, 메탄올, 메틸아민 (me t h y lam i ne), 포름알테히드 (form aldehy de ), 또는 포름산(fo rma t e) 에서만 자란다. 메탄을 자화하는 효모는 아직 분리되지 않았고 비교적 소수의 메탄 자화세균만이 동정되고 있다. 이런 세균에는 Meth y l o monas meth a nic a , Meth y l o coccus cap- sulatu s , Meth y l o vib r io soehn ge nii , Meth a nomonas marga r ita e %ol 있고 아직 분류되지 않은 것도 있다 (Haber, 1983). 메탄 산화효소 (me t hane o~ yg enase) 가 메탄을 메탄올로 산화시키며 , 메탄을이 대사된다. CH4+02+ X H2 ➔ CH3 0H +H2 0+ X 산화 결과 메탄올이 축적되면 세균의 증식이 저해된다. 아미노산, 당 또 는 아세테이트 같은 일차대사산물도 역시 증식과 메탄 산화를 저해한다. 0.4g / l 건량의 Meth y l o coccus cap sula t u 遷 이용하여 1.00 ~1 .03 g 건량 / g 메탄의 SCP 를 얻을 수 있다. 메탄올은 메탄으로부터 화학적으로 생산되고 취급하기 쉽기 때문에 C1 기질을 이용하는 공정에서 원료물질로 이용가능성이 가장 높다 (Harwood, 1972).
3.2 메탄을 발효 현재 단세포 단백질 생산을 위해 메탄올은 가장 중요한 물질이다. 메탄 울은 합성가스, 천연가스, 메탄, 석유, 석탄으로부터 얻을 수 있고 목재도 이론적으로 메탄올 생산을 위한 원료물질로 이용될 수 있다. 세균, 효모, 곰lf}
표 16.1 단세포 단백질의 구성(%) 알 7J 메탄올 pro te i n Mi lk 효모 박테리움 iso late 곰팡이 조류 콩 pow der 조단백질 60.0 80 91 31. 7 72.6 45.0 34.0 지방 9.0 9.5 o.5 4.9 7.3 1.8 1.0 핵산 5.0 15 1.0 무기염 6.0 9.5 3.5 2.0 4.7 6.0 8.0 아미노산 54 65 102 40 수분 4.5 2.8 4.0 13.5 3.6 12.0 5.0
표 i6.2 메탄울게서 자라는 미생물 1. Obig a te meth y lo t ro p h ic bacte r ia Meth y l o bacte r Meth y l o cys t is Meth y l o coccus Meth y l o sin u s Meth y l o monas 2. Faculta t i ve meth y lo t ro p h ic orga n i sm s a. 세균 Arth r obacte r Prota m i no bacte r Bacil lu s Pseudomonas Hy ph omi cro biu m Rhodop se udomonas Klebsie ll a Stre p tom y ce s Mi cro coccus Vib r io b. 효모 Candid a bio d in i Pic h ia hap lo p h il a Candid a pa raps ilo s is Pich ia lin d nerii Hansenula caps u lat a Pich ia pa sto r is Hansenula henric i i 1brulop si s gla brata Hansenula min u ta 1brulops i s meth a nolouescens Hansenula nonfe rm enta n s 1brulops is meth a nosorbosa Hansenula wic k erhami i 1brulop si s molisc hia n a 1brulop si s memodendra C. 곰팡이 Glio c ladiu m delin q u e scens Paecilo m y ce s uario t i '.lrich oderma lign orum (Sa hm, 1979)
표 16.3 다양한 메탄올 이용자들의 최대비증식속도 미생물 µma x(h - I) Pseudomonas rosea (ICI ) 0.38~0.50 Prota m i no bacte r ruber 0.1 0 Pseudomonas exto r qu e ns 0.1 8 Meth y l o monas meth a nolic a 0.53 Pseudomonas B45 0.1 9 8 Kloeckera sp. 2201 0.075 Hansenula po lym orph a 0.22 Thrulop si s gla brata 0.1 1 (Braunegg , 1975)
(1) 메탄을 산화 (Haber, 1983) 메탄을은 세균에 의해 아래 중간단계를 거쳐 co 료- 산화된다. CH30 H —~ HCHO 一 HCOOH 一 CO2 포름알데히드로의 첫단계는 비특이적 메탄올 탈수소효소를 요구한다. 효모는 FAD 를 포함하는 비특이적 메탄올 산화효소를 이용해서 메탄올 울 산화한다. 메탄울은 또한 유도성 cata las~ per oxid a se 활성으로서 H 2 0 제 의해서도 산화되는데 이런 H2 0z i =- 메탄올 산화효소에 의해 생산 되어진다. 다음 단계는 포름알데히드 산화인데 이것은 세균에서 몇몇 효소에 의해 수행된다. ·환원형 glu ta t h i o n e(GSH) 존재하에서 NAD 의존성 포름알데히드 탈수 소효소에 의한 포름알데히드의 포름산으로의 전환인데 이 반응은 효모에서 일어난다.
HCHO+NAD+H 2 0 으한 ;HCOOH+NADH 2 이 산화과정에서 기질의 mole 당 2~3 ATP7} 획득된다. 마지막 단계인 포름산의 산화는 모든 메탄을 이용하는 미생물에서 공통 적 반응이다. 포름산 산화는 NAD 의존 포름산 탈수소효소가 관여하고 기 질 mole 당 3 ATP 를 생산한다. HCOOH+NAD ~ C02+ N ADH2 몇몇 메탄을만을 이용하는 세균(예를 들면 Meth y l o monas Ml5) 에서는 포름알데히드 탈수소효소와 포름산 탈수소효소는 발견되지 않았다. 대신 이런 생물들은 pho sph o g lu conate 경로 (그림 16.2) 에 의해 포름알데히드 를 산화한다 (Sahm, 1979).
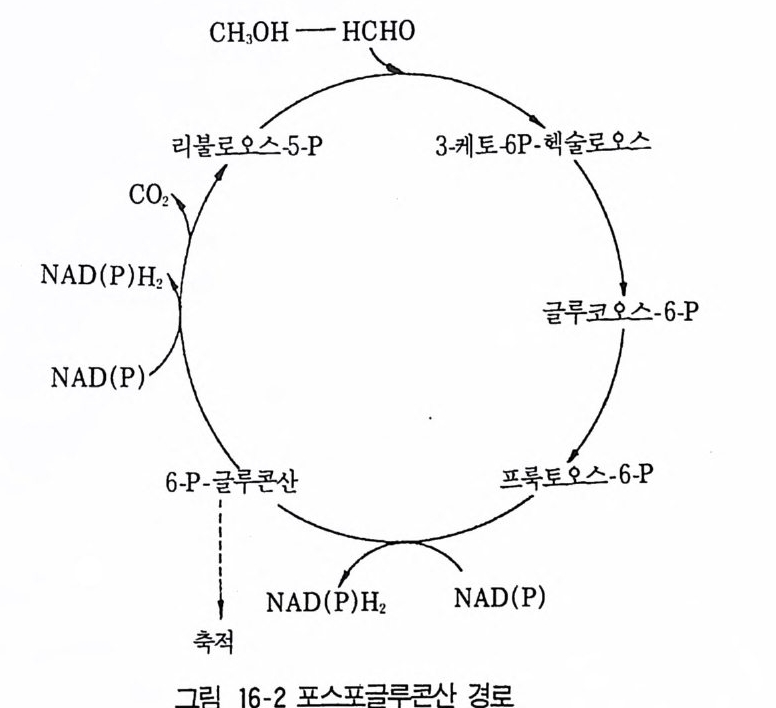 리CH 3 0H불 一 HC〈HO 二\
리CH 3 0H불 一 HC〈HO 二\
(2) 메탄을 산화균의 탄소자화 메탄올에서 자라는 세균은 피루브산(py ruva t e) 같은 일차대사산물로 공급하기 위해 C 분자를 생산하게 된다. C1 - 분해에 대한 37} 지 명확한 경 로가 밝혀져 있다 (Sahm, 1979). 1. co 논 리불로오스 (r i bulose) 이인산〈 Calv i n 〉 회로를 통해 광합성 생물 에 동화된다. 2. 포름알데히드는 리불로오스일인산 회로(Q uay le c y cle) 에서 hexulose pho sph ate s y n t hase(HUPS) 의 촉매에 의해 rib u lose-5 -P 와 축함한다 (그립 16.3). 3-keto - 6 - P-h e xulosel} fr uc t ose-6-P로 이성화된 후에 dih - yd rox ya ceto n e-P7} 해당과정을 통해서 생산되거나 Entn e r-Doudoroff 경로를 통해 피루브산이 생산된다. 리불로오스-5 -P 는 tr? f lSk eto l ase.2 .J- tra nsaldolase 과정을 통해 리불로오스.일인산 회로에서 재생된다. 이 회 로의 주요 효소인 HUP 決근 일부 구성요소이면서 메탄올에 의해 부분적으 로 유도되기도 하는데 포름알데히드에 의해 억제된다. 3. 세린 경로에서의 포름알데히드와 글리신의 농축은 serin e tra nshy d ro- xy me t h y lase( 그립 16 .4)의 작용에 의해 일어난다.
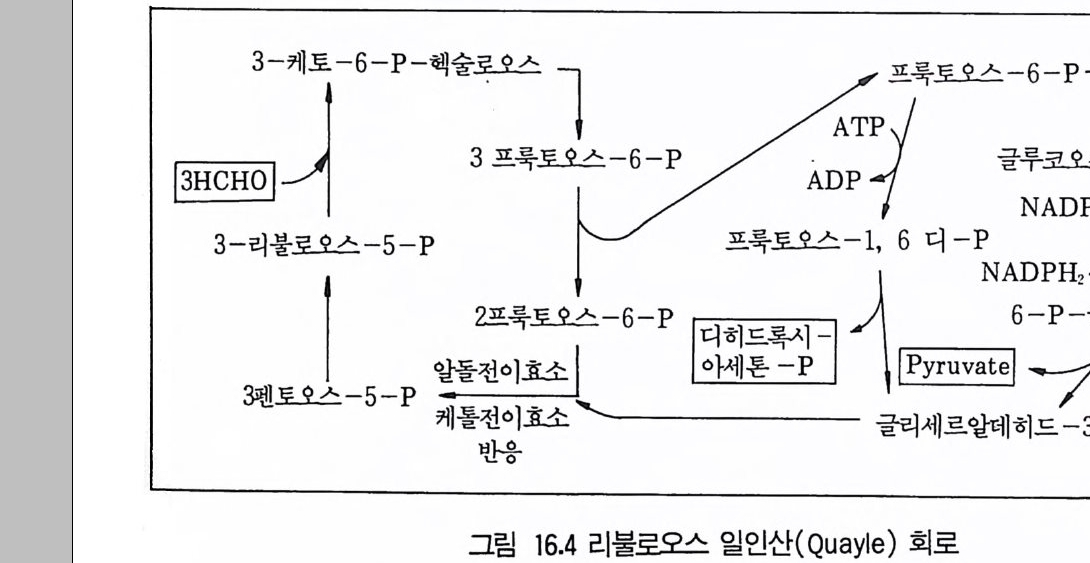 言3-亭 리3」-불 케무로토오I -스 -6 --55P---P 헥 케P톨술~3타전빈 후프 이드냥스후효 록소니 스-i - -66--PP 디아세프 히톤드룩 활 訂Da/AA 三\〔N 길\_\「 P근||i6 」'L P
言3-亭 리3」-불 케무로토오I -스 -6 --55P---P 헥 케P톨술~3타전빈 후프 이드냥스후효 록소니 스-i - -66--PP 디아세프 히톤드룩 활 訂Da/AA 三\〔N 길\_\「 P근||i6 」'L P
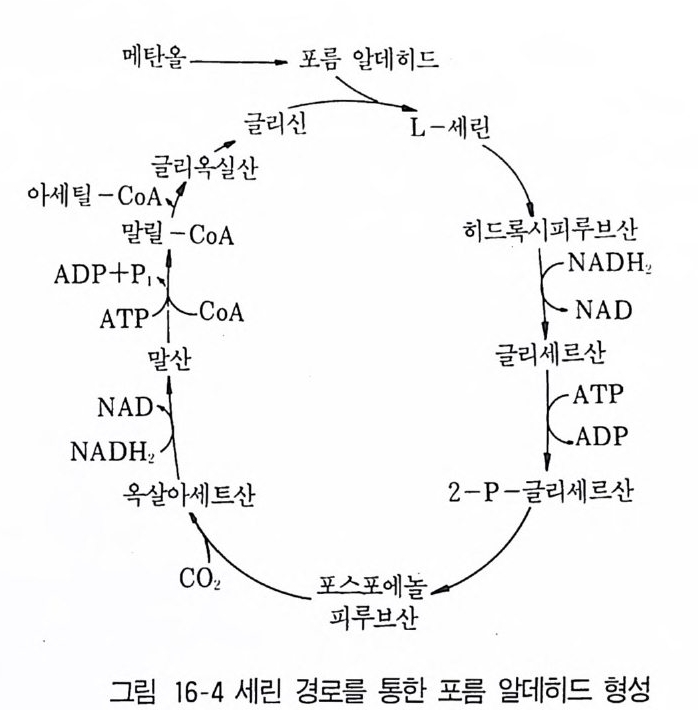 메 탄올 L 포름 알 데히 드
메 탄올 L 포름 알 데히 드
리불로오스일인산 회로와 아주 유사한 경로인 dihy dr oxy ac eto n e 회로 가 효모에서 발견되고 있다. 표 16 .4는 다양한 단일 탄소화합물을 이용하는 세균과 효모에 대한 이 론적인 수율 계수를 나타내고 있다. 이 표에서 보면 리불로오스일인산 경 로를 이용하는 세균의 수율이 가장 좋은 것임을 알 수 있다.
표 16.4 메탄올에서 자라는 미생물들의 수율 미생물 경로 수율 ( g cell dry weig h t / g meth a nol) a. Bacte r ia (세균) Pseudomonas C RMP 0.54 • P.meth y lo tr o p h us RMP 0.53
Meth y l o monas meth a lonic a RMP 0.4 9 Pseudomonas AM 1 SER 0.30 Pseudomonas M 27 SER 0.4 1 Pseudomonas rosea SER 0.4 1 b. Yeas t s( 효모) Candid a boid i n i DA 0.32 Habse 血 la po lym orp h a DA 0.38 RMP : Rib u lose monop ho sp ha te cyc l e, SER : Serin e pat h w ay, DA : Dihy d r oxy ac eto n e cyc l e (Sa hm, 1979)
(3) 생산공정 영국의 ICI는 연속적인 메탄올 발효로 SCP 의 공업적 생산을 처음으로 성공시킨 회사이다. 그들은 생산성에 영향을 미치는 02, C O2 , 메 탄올 농도 와 발효조의 표면과 바닥 시이의 압력 차이의 효과를 연구하였다. 공중보 급형과 loop reac t or 형을 결부시킨 〈 ICI 형 발효조났근 그림 16.5 에 나타
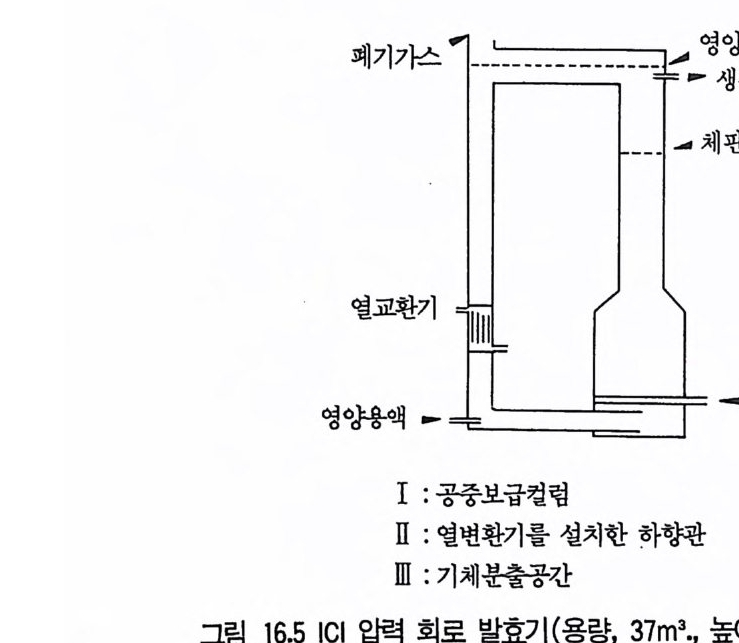 폐기가스 기 --I-- · - · ------ 一士” 영양분 표면
폐기가스 기 --I-- · - · ------ 一士” 영양분 표면
나 있는 바와 갇다. 연간 1,000 t ons 의 능력을 지니는 실험공장은 pH 6. 5~6.9, 34~37°C 에서 가동되고 있다. 산업적 SCP 생산을 위해 이용되는 미생물은 ICI 에 의해 분리된 메탄올 발효균인 Pseudomonas met- h y lo t ro p h 磁 l 며 생리적 유전자 조작을 통해 개량된 것이다(표 16.5) (Gow, 1975).
표 16.5 메탄을게서 자라는 Pseudomonas me t h y lo t ro p h 혜t 위한 ICI 발효 고정의 최대활용 조단백질 83% ➔ 85% 정제 단백질 59% ➔ 64% 세포전량 4 ➔ 30g / l µma z 0.38 h-1 ➔ 0.5 h-1 (Gow et al., 1975)
생산물 회수과정에서 영양액은 여과에 의해 정화되고 세포는 분사 건조 된다. 이런 실험 연구 결과를 기초로 ICI 는 197 9¼빈에 연간 50,000~70,000 t ons 의 생산력을 가전 발효기로서 배양을 정확하게 수행할 수 있었다. 이 런 연속공정을 기술적으로 해결하기 위해 100 일 동안 시험 가동되었다. 또 다른 SCP 생산공정이 독일 화학회사 Farbwerke Hoechs t에서 40m3 의 관형 루프 반응기 (tub ular loop reac t or) 를 이용하여 개발되고 있다. 원래의 화학적 공정은 메탄올―제한시스템이었지만 후에는 질소_제한 시스템으로써 가동되었다. 원래 사용된 세균균주는 NH 동회·가 업 n 의 비효 율적 방식으로 일어났었지만 유전공학을 이용해서 대장균으로부터 더 효과 적 인 글루탐산 탈수소효소체계를 Pseudomonas ne t hy lo t rop hu 펴 GOG- AT 돌연변이주에 전이시킬 수 있게 되었고 오늘날 상업적 생산에서 이용 되고있다.
Gluta m i ne -Keto a cid Transami na se ( GOGAT) rx-Ket og l u rate + NAD ( P ) H+Glu t am i ne — ➔ 2 Glut am ate + NAD ( P) Gluta m i ne syn th e t as e Gluta m ate + NH3 +A TP— ~ Gluta m i ne +ADP+Pi 4 셀룰루 Q人쿠부터 SCP 의 생산 (Rolz, 1982) 오늘날 천연 섬유질자원은 폐목발효 알코올의 생산원료뿐만 아니라 단 세포 단백질 생산울 위한 원료물질로서 각굉을- 받고 있다 (Bae, 1974, Ghose, 1978). 지구상에는 셀룰로오스가 풍부하기는 하지만 보통 리그닌, 헤미셀룰로오스, 전분, 단백질, 염 (표 16.6) 같은 물질과 혼합하여 존재한 댜 그러므로 셀룰로오스를 발효 가능한 당으로 분해하기 위해 전처리해 하는데 전처리에는 효소적 (cellulase) 또는 화학적 (acid h y drol y s i s) 인
표 16.6 cellulosic substr a te s < ll 구성 셀룰로오스 Hemi cellulose 리그닌 % % % 나무 Ang ios pe r ms 40~55 24~40 18~25 나무 Gy m osp er ms 45~50 25~35 25~35 풀 25~40 25~50 10~30 나뭇잎 15~20 80~85 신문 40~55 25~40 18~30 종이 제조로부터 나오는 폐기물 60~80 20~30 2~10
방법이 있다. 셀룰로오스의 가수분해에는 cellalase¾ 이용하는데 celluia s e 는 세균 Cellulomona 회- Ac ti onomy ce t e 려- 곰팡기 '1rich oderma, Penic i l- lium , 'Iherm oascus, Sp o rotr i chum, 그리고 Humi co la 등에서 생산된다. '1rich oderma reesei (T, vir i d e ), T. konin g i i, 그리고 Sp o rotr ic h um
p ulverulen t um 에 대해서 많은 연구가 진행되고 있다 (Andreo tli, 1978). cellulas 눈 적어도 37} 지의 효소로 구성된 효소 복합체이다. 1. Endo-p- 1,4 -glu canase, 이는 endocellulase, carboxy me th y l cellulase (CMCase), 또는 C, cellulas 료도 불린다. 2. Exo-P- 1, 4-gl u canase, 이는 cellobio h y dr olase, avic e lase, 또는 C1 cellulas 쵸도 불린다. C1 cellulase- E- T. v i r i d 邊 가지고 발효시키는 동안 효소 단백질의 80% 를 차지한다. 3. P-1,4-gl u cosid a se, 또는 cellobia s e, 이런 cellobio s e 분해효소의 세 포의 분리농도는 낮은데 T.u i u i de 의 경우 다량의 효소를 세포내에 갖 고있다. cellulase 연구의 현황 : 'lrich oderma uiu i d e QM 9414 를 이용한 eel- lulase 생산방법이 연구되어왔지만 수율은 아직까지 비교적 낮다. p H 조건 효과, 접종 시기 , 배양액 첨가물 등이 연구된 바에 의하면 (Ny st r o m, 1976, 1978) 최대생산량은 14 QJ.]간 성장 후 3o•c 에서 달성되고 그림 16.6
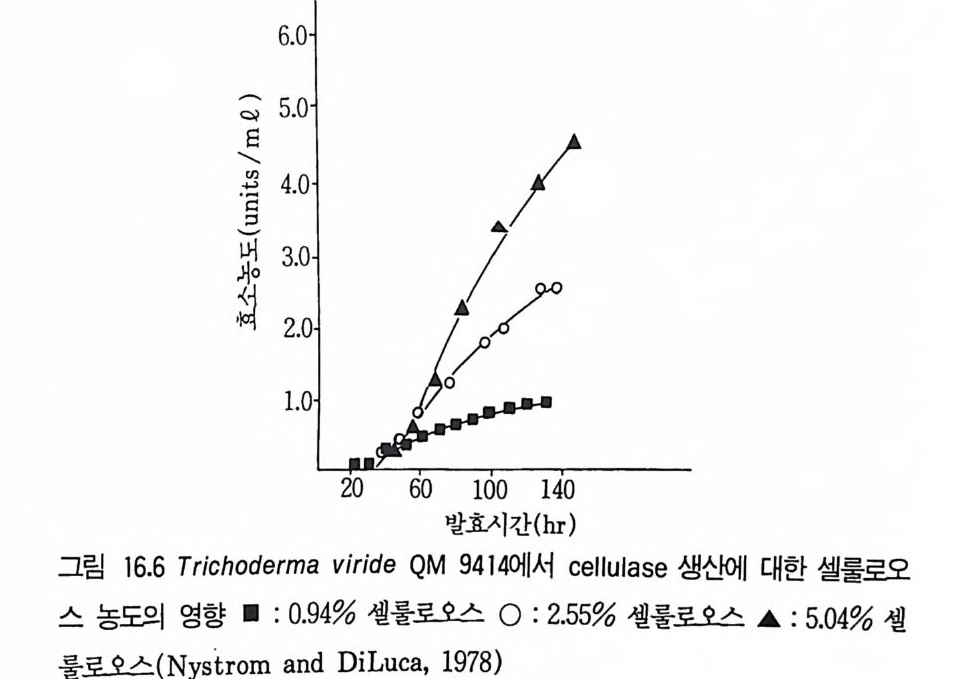 6.0
6.0
에서 보는 바와 걷이 생산량은 셀룰로오스 농도와 관련된다. 실험공장 실 험을 기초로 해서 cellulas 태산과 이 효소를 이용한 셀룰로오~수로부터 당 의 생산에 대한 생산가 산정을 하면 생산가격은 정제된 효소용액 1 리터당 0.11$, 천연 배양용액 1 리터당 0.011$9 -J 시세에 있다• 셀룰로오스를 발효성 당으로 만드는데 필요한 생산가격은 셀룰로오즈 분해의 공정에 의존하며 분해당 k g당 0.037~0 .4 89$ 이다. 198 0\:텨 설탕의 국제 시장가격에 비추 어볼 때 가격이 높다. 분명히 SCP 생산 자체가 상당한 생산가격이 들기 때문에 SCP 생산울 위한 기질로서 높은 가격의 당을 이용하는 것은 아직 실용적 가치가 없디는 것을 의미한다. 셀룰루 인선쿠부터 경제적으로 SCP 를 생산하기 전에 먼저 cellulase 생산 수율에 큰 증가를 보여야 하며 그 내용은 더 값싼 p re -s accar ifi ca ti on 용 목재섬유질 처리방법이 개발되어야 하며 에너지 철약방법이 공정 전체를 통해 개발되어야 한다. 5 페수로부터 SCP 의 생산 현재 가정 폐수는 대규모 SCP 생산에 부적당하지만 미래에는 메탄 생 샨게서 매우 중요하게 될 것이다 (17 장 혀길). 지금까지는 섬유질 가공, coff ee 생산, 전분 생산, 그리고 식품 가공으로부터 나오는 산업 폐수가 SCP 생산에 이용되어왔다. 제지와 섬유소 생산으로부터 나오는 황화 폐수 (sulf at e waste liq uors) 는 효모의 생산에 광범위하게 이용되어왔는데 그 이유는 많은 양의 일관된 이용성, 적은 투자비와 생산비, 기질에서 높은 성칭률을 가지는 생물의 이용이 가능하였기 때문이다. 황화 폐수에서 증식하기에 적당한 미생물은 Candid a uti lis , C. tro - pica lis, Chaeto m i um cellulolyt icu m, 그리고 Paecil o my ce s uar i o t카 있다. 연속공정은 껴의 360m3 발효기를 가지고 행해전다. 시간당 0.2 희석율 에서 Paec i lomy ce 邊 사용했을 때 SCP 생산량은 2.7~2.8 kg /m 3 • h 였 다.
Candid a u ti l i邊 이용한 연속공정에서는 식품가공 공장으로.부터 나오는 폐수를 이용하였는데 25 굶 발효기는 최대기간인 3. 덮 R 월에 걸쳐서 33°C p H4 에서 120~150m3 폐수로부터 하루에 1~1 .5 t ons 의 건조효모를 생산 했다 (Dav y, 1981). 참고문헌 Andreott i, R. E., M.Mandels and C. Roche. 1978 Proc. Bio c onuersio n Sym p. II T Delhi pp. 249~267. Bae. M et al., 1974. Kor. J .A p pl. Mi cro bio l and Bio e ng . 79~829. Braunegg , G. 1975. pp. 218~234. J. Arbeit sta g u ng Bio te c hnolog ie in Ost- erreic h . Dalto n , H. (ed.) (1981), Mi cro bia l gro wt h on C1 comp un ds Hey de n, London. Davy , C.A.E., et al. (1981), pp. 343~350. In:Moo-Yong, M.(ed.), Advances in bio t e c hnolog y vol. III . Perga m on Press, Toronto . Fie c hte r , A.(ed.). 1981 . Bio e nergy . _Ad v. Bio c hem. En g. vol. 20. Spr - ing e r -Verlag, Berlin . Forbes, A.D. 1979. The tec hnolog y of sin g l e cell pro te i n pro - ducti on from n-alkanes Int Mi cr obia l. and Food Cong r. Paris. Fuku i, S. and A. Tanaka 1981 . Meta b oli sm of alkanes by yea - sts Adv. Bio c hem, En g, 19:217~237. Ghose, T.K (ed). 1978, Bio c onversio n of cellulosic substa n ces int o en- erg y, chemi ca ls and mic r obia l pro te i n Thomson Press, Farid a bad. Gow, J.S ., et al., 1975. pp.3 70~384. In:Tannenbawn, S.R. and D. I. C Wang (eds.), Sin g l e cell pro te i n vol. II . MIT Press, Cam- brid g e , MA. . Haber, C.L., et al, 1983. Meth y l o t ro p hic bacte r ia : bio c hem ist r y , dive rsit y, and gen eti cs. Scie n ce 221:1147~1153.
Harwood, J.H . and S.J. P ir t . 1972 Qu ant itat i ve asp e cts of gro wt h of the meth a ne oxi di z i n g bacte r iu m Meth y lo coccus cap s ulatu s on meth a ne in shake flas ks and cont inu ous chemosta t cul- tu re J. Ap pl. Bacte r ia l . 35:597~607. Ny s tr o m, J.M . and A.L.Allen. 1976. Pil o t scale inv esti ga ti on s and econom ics of cellulase pr oducti on . Bio t e c hnol. Bio e ng . Sy m p . 6 : 55~74. Ny s tr o m, J.M . and P.H.Di Lu ca. 1978. Enhanced pro ducti on of Tric h oderma cell 따 as · e on hig h levels of cellulose in submerge d cultu res. Proc. Bio c on-uersio n Sy m p . II T Delhi , pp. 293~304. Prave, P., et al., 1978. Bi ot e c hnolog ica l pr oducti on of new kin d s of foo ds and fee d pp. 18~50. In:BMFT(ed.), Bi ot e c hnolog ie. Umschau Verlag, Frank fur t. Puhar, E., I. Lorencez, and A. Fie c hte r . 1983. Infl ue nce of pa r- tial pre ssure of oxy ge n and carbon dio x i de on Meth y l o monas clara in conti nu ous cultu re. Ap pl. Mi cr obia l . Bi ot e c hnol. 18 : 131 ~ 140. Rehm, H.J. a nd I.Re if f. 1981 . Mechanis m s and occurrence of mi - crobia l oxi da ti on of long -ch ain alkanes. Adu. Bi oc hem. En g. 19 : 175~ 215. Rolz, C.and A.Hump h rey. 1982. Mi cr obia l bio m ass from ren-ewables:Revie w of alte r nati ve s. Adu. Bi oc hem. Eng. 21:1~53. Romants c huk, H. et al., 1978. Op e rati on al exp e rie n ces of firs t full scale Pek ilo SCP-m ill ap plica ti on . Proc. Bi oc hem. 13:16~17.29. Sahm, H. 1979. Producti on of SCP by meth anol uti lizin g mic- roorga nism s. Int. M i cr obia l .and Food Ind. Cong r. , Paris . Sen ior , P.J. and J.W i nd ass. 1980. The ICI sin g l e cell pr ote i n pro cess pp. 97~101. In : Verbraeck, A.(ed.), 13th Int. TNO Confe r - ence. TNO, The Hag ue . Sm ith, A.J. and D. S. Hoare. 1977 • Sp e cia l i st ph oto t r o p h s, lit- hotr o p h s and meth y lo tr o p h s : a unit y among a dive rsit y of pro caryo t e s ? Bacte r io l. Reu.4 1 : 419~448.
Str u b,A.,P. charti er, and G. Schleser(eds.). 1983. Energy from bio - mass Ap plied Scie n ce Publish ers, London. Uhde -GmbH. 1979. Plant for the pro ducti on of bio p r o te in Lo II 5,19, 150079.
제 17 장 페수 처리의 새로운 방법 1 서론 도시화된 나라에서 거대한 양의 산업 및 가정용 폐기물이 생물학적으로 처리되고 있다. 현재, 폐기물은 우선 전통적이며 호기성인 활성오니법으로 처리되는데 표면통기방법에 의하거나(그림 17.1 ), 통기법으로 산소를 공급 햐겨 처리한다. 또 다른 형태의 호기적 처리방법 (여과장치 ; 똑똑 떨어지게
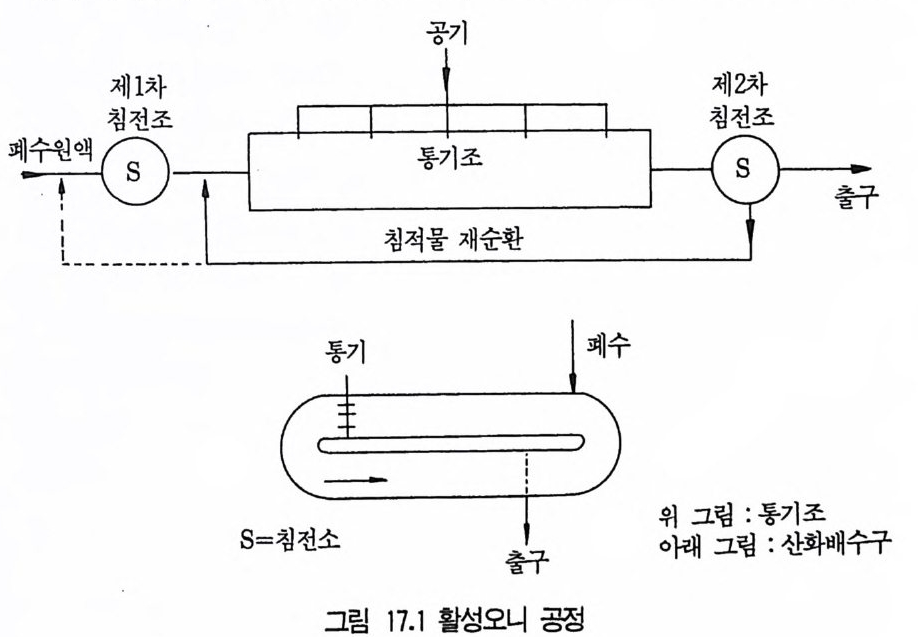 공기
공기
하는 것)으로서, 자갈이나 모래충을 사용하여 배지 위에서 자라고 있는 생 물들의 포상표면에 폐수를 똑똑 떨어지게 하여 폐기물 속의 유기화합물을 산화시킨다. 다론 처리방법으로서 형기성 분해가 사용되는데, 때로는 폐액 울 직접 이용하거나 혹은 호기적 처리과정의 침전으로부터 얻은 고체물질 (오니)을 종종 사용한다(그림 17.2).
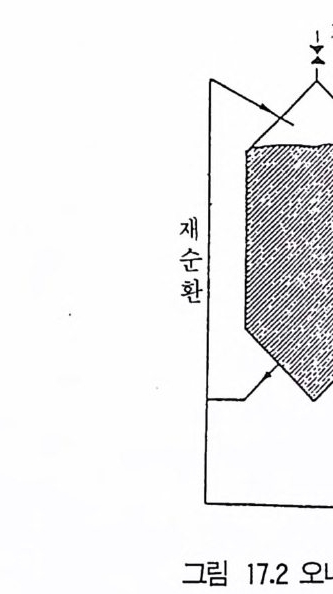 z1 가 스 제거
z1 가 스 제거
호기적 방법은 다음과 같은 불리한 점을 가지고 있다. 즉, 개방 구조는 공정관리에 제한이 있고, 생물집단의 제어 곤란, 악취 방출로 인한 환경오 염, 그리고 안개 생성들이 문제점을 가지고 있다. 이 장에서는 폐수 폐기물 처리의 효율을 증가시키기 위한 잠재성을 지 닌 네 가지의 새로운 처리과정을 검토해보려고 한다. 2 처리공정을 위한 스터아터 배양 전통적인 폐수 처리는 폐수 처리 시스템에서 자연발생한 미생물들을 사
용하는데, 이때 수반되는 생물 들을 최적화시키는 시도는 고려되고 있지 않 다. 폐수 처리과정의 효율을 증가시키기 위한 잠재성을 지닌 접근방법은 특수 폐수 처리과정을 위해 특별히 선택된 미생물군을 이 시스템에 접종 하는 것이다. 식품발효에서 사용한 것에 비유하여 그런 생물군을 〈스타아 터 (종균) 배양〉이라 부른다. 비록 이 스타아터 배양을 가정용 폐수 처리에 서 사용하는 것을 볼 수도 있으나 이들 종균배양물은 특수산업용 폐기물 처리나 혹은 잘못 흘린 산업적 화합물 처리에 더 유용하게 쓰인다. 그런 폐기물은 일반 처리공정으로 들어갈 수 없는데, 왜냐하면 그 독성과 생물 적 난분해성 때문에 적응치 못한 생물들에게 심각한 해를 주게 되기 때문 이다. 이 종균배양을 이용하는 또 디론 방법은 폐수 처리공정이 폐쇄된 후 일반적으로 요구되는 처리 개시기간을 단축시키는 데에 있다. 이 시스템이 충분히 재가동할 수 있게 하기 위해서는 최적의 박테리아 혼합배양이 회 복되어야 한다. 죽 보통 1 주 동안의 배양 강화과정이 요구된다. 종균배양 은 처리 개시기간을 단축시킬 수 있다. 미국에서는 낙농산업의 것과 유사 한 스타아터 배양이 개발되었으며, 이 배양은 탱크 청소, 도관 청소, 도시 정화공정의 개시, 그리고 폐수내의 특수물질 분해 등과 같은 폐수 처리에 서 다양한 특수g g에 적용되고 있다. 냉한지에서 분리한 박테리아는 0~15 °C 의 영생지에서 알칸과 방향족 화 합물을 분해시킨다. 이들은 해양에서 기름 누출을 분해시키는 데 유용하 다. 또한 DDT, 염소처리된 디페놀 (d ip henol), 그리고 페놀(p heno l) 등 을 대사시키는 혼합배양 균주 혹은 높은 프로데아제, 리파아제, 셀룰라아 제 활성을 지니는 혼합배양 균주가 시판되고 있다. 만약 p H 족 5.0 혹은 측 9.0o1l 서의 성장과 같은 특수하게 작용하는 조건을 원한다면 선택된 집적배 양을 통해 충족될 수 있다. 특허를 얻어낸 과정으로서는 옥탄 (oc t ane), 자일렌 (x y lene), 메타자일 렌 (me t ax y lene), 캄퍼 (cam p hor) 등 분해를 위한 풀라스미드를 지닌 Pseudomonas pu tid a 7} 개발되어 있다 (Chakrabar ty, 1974). 또한 스타아 터배양은 동물 배설물의 냄새를 제거하는 데에도 사용되어왔다.
197 純 미국에서는 이 스타아터 배%快l....법으로 언버 ~4 백만 달러의 매상 울 올린다고 하지만 참재적인 총가치는 2 억 달러로 추정된다. 20 개 공장에 서 10rn 3%량의 배양 용기에서 멸균상태로 혼합배양이나 단일배양 등을 생산하였다. 이런 사용된 배양 조건들은 세포들이 충분하게 유도되기 위해 서 어떻게 배양이 사용되는지에 의해 결정된다. 이 분야에서의 연구는 아 직 초기단계에 있으며 각 화합물의 분해에 관한 과학적 연구가 계속 전행 되고 있으나 실제적인 적용은 아직 널리 확대되지 못하고 있다 . 3 호기적 페수 처리 -공기보급형 공정 (aerobic sewage tre atm ent, air lift pro cess ) 활성오니법에 의한 전통적인 호기적 폐수처리의 불리한 점으로서는 산 소전달의 효율이 낮으며 설바장치에 큰 공간을 필요로 하는 것이다. 이 과 정은 산소유입과 산소이용을 향상시키기 위해 공정이 개발되어 효율이 향 상되고 있다. 이들 시스템은 루프형 도관반응조와 ai rl ift형 발효조를 사용 한다. 영국의 화학회사 ICI 는 땅 밑바닥으로 l0 伯]터를 넣을 수 있는 loo p형 도관반응조를 사용한다. 두 독일회사인 Ba y er(b i o t ower) 와 Uhde/Hoe- chst( b io h i gh reac t or) 들은 높이 30m 의 생체반응조 (b i o-reac t or) 를 건 설하였다. Unde/Hoechs t반응조는 원형 침전대야를 생물반응조의 꼭대기 가장자리의 둘레에 설치해둔다. 이런 유형의 활성오니 발효조의 용적은 산 소전달효율을 상당히 좋게 해준다. 표 17 .l에서 이런 형태의 여러 활성오 니 시스템의 성능 자료를 보여주고 있다. Hoechst 시스템은 혼합을 촉진시키는 조절관을 가지고 있다. Ba y er 의 bio t o w er 공정은 두 개로 구성된 노즐이 주입기로 연결되어 있는데 이 주 입기에 의해서 액 유출의 운동에너지가 마치 물 분사 펌프와 유사한 방식
표 17.1 활성오니 시스템 (Uhde/ Hoechs t)의 자료 물 깊이 (m) 4 8 20 산소포화( g0 z / m3 ) 13 17 28 산소수율(%) 8~15 15~30 40~60 요구공가량 (Nm 3 /K g 02) 42~23 23~11 9~6 에너지특이적 산소유입 2~2.5 2.5~3 3~3.5 (kg OdKWh) 생체반응조의 직경 (m) 18 13 8 1000 硏 용량을 위한 반응조 250 125 50 표면적 (m2)
으로 공기를 작은 기포로 분산시키는 데 이용되고 있다(그림 17.3). 이들 주입기는 탑반응조의 밑바닥에 4 개의 주입기더미로 설치되어 있다 (1 주입 기 /1~2m2 밑바닥 표면).
 그림 17.3 Baye r 주입기 (Zlokam i k, 1979)
그림 17.3 Baye r 주입기 (Zlokam i k, 1979)
4 순수산소의 통기 순수한 산소로 하는 활성오니 처리장치의 통기 조작이 미국과 독일에서 시도되어왔다. 목적은 산소전달의 효율을 증가시키는 것인데 이유는 전통 적 정화조의 처리 용량과 미생물집단의 규모가 용존산소의 낮은 용해도에 의해서 제한되어왔기 때문이다. 순수산소는 공기에서의 산소분압이 4. 別 H 인데, 그래서 순수산소를 사용 한 통기가 활성오니 시스템의 산소 함량을 현저히 증가시킨다. 그러한 시 스템에서 용존산소는 90~95% 이용되며, 가스누출(전통적 통기의 l%) 은 악취를 제거하기 위해 밀폐 시스템에서 화학적으로 또는 열처리로써 계속 처리될 수 있다. 산소를 사용한 공정에서의 처리 능력을 높이는 것은 결국 더 작은 통기 탱크와 더 작은 침전용기의 사용을- 가능케 한다. 생성된 오니의 양이 더욱 감소되기 때문에 디음 단계의 처리를 위한 설치 비용 또한 감소된다. 부정 적 측면으로는 자본 두자가 많고, 설비가 더 복집하고, 처리과정의 변수에 대한 세심한 조절이 필요하며, 고도로 훈련된 기술자가 필요하다는 점을 들수있다. 현재 몇몇 회사에서는 순수산소를 사용히는 상업적 처리설비를 시장에 내놓고 있다. Unox 시스템이 그런 예의 하나이다. 첫번째 통기단계는 업 H 의 채널로 되어 있는데 각각 1,500,750,730m 3 용량을 가진 앙 H 의 생체반응 조가 폭포처럼 배열되어 연결되어 있다(그림 17.4 ). 첫번째 생체반응조(활 성오니조)에서는 공기 분리장치로부터 온 순수산소를 주입기를 통해 밀어 넣어 주는 것이다. 이 단계에서 유기성을 분해할 수 있는 물질은 90~ 93% 가 제거된다. 생성된 co 논· 잔여 산소와 함께 모아져 1,ooo·c 에서 처 리된다. 두번째 단계(침전조)에서는 누적된 오니가 활성오니조로 되돌아온 다. 이 폐수는 두번째 처리단계를 통해 홀러나오는데 그 결과 쉽게 분해되 지 않는 물질을 제거하게 된다(그림 17.5).
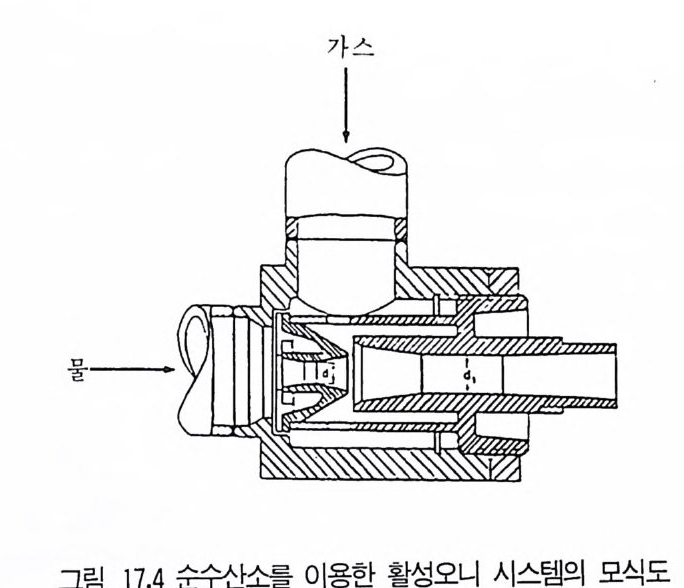 7 `스L'.
7 `스L'.
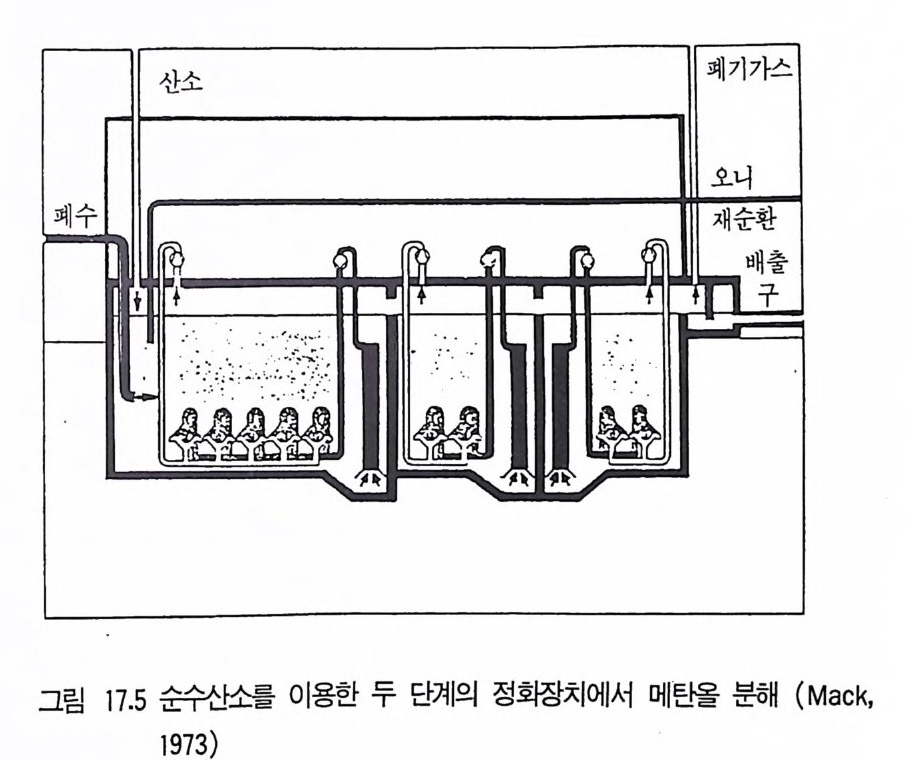 산소 폐—기가스
산소 폐—기가스
5 메탄생산 메탄 혹은 천연가스는 유기물질의 협기적 분해에 의해 생긴 미생물적 샨탉》]다. rne t hano g enes i s 는 유기성 폐액 처리에서 널리 사용되고 있는 공정으로, 우선 메탄가스는 비용해성이기 때문에 이 처리 시스템으로부터 쉽게 제거될 수 있다. 이 메탄은 연료이므로 이 처리 시스템에서 생성된 메탄은 에너지원으로 사용될 수 있댜 어떤 농업적인 여건에서는 생성된 메탄이 중요한 에너지원 (b i o g as) 이며 처리과정의 주요 목표는 메탄 생산 의 최대화이다. 그러나 대부분의 폐기물 처리 시스템에서는 바록 메탄이 연료로 사용되기는 하지만 주요 목적은 에너지원으로서의 메탄 생산이 아 니라 그 환경에서 안정하게 처리될 수 있는 오니의 안정화에 있는 것이다. 그러한 시스템에서는 메탄 생산공정의 최적화에는 별로 관심이 경주되어오 지 않았다. 서유럽의 27 531j]수 처리 시스템의 한 연구에서 보면 생성된 가 스의 75% 가 처리공장 자체내에서 에너지원으로 사용되고 있지만 생성된 메탄의 일부만이 다른 사용자에 보급되고 있다. 메탄 생성 박테리아는 특유한 생물군을 이루는데 이 생물군은 협기적 먹이사슬에서 유기물질의 분해라는 점에 최종적 및 주요 연관을 두고 있 다. 메탄 생성 박테리아는 메탄 생성을 위해 제한된 기질만을 이용할 수 있는데 이는 아세트산, 메탄올, 포름신·(fo rma t e), H2+ 0 2 등이다. 폐기물 처리 시스템에서는 약 75% 메탄이 아세트산에서 유래되며, 나머지의 대부 분은 H 2 +co 로부터 생성된다. 형기적 분해과정의 출발 물질은 섬유질, 전분, 지방, 단백질과 감은 복합중합체로서 그들 중 어느 것도 메탄 생성 박테리아가 이용할 수 없다. 메탄 생성 박테리아는 기질의 초기분해와 아 세트산, H2+CO~ 생산을 위해서 디론 협기적 발효 미생물들에 의존하 고있다. 비록 폐기물 처리를 위한 rneth a nog en esis 7 } 순수한 경험에 의한 과정 이었다 할지라도 아마 미래에는 조작변수가 최적화된 충분한 생물공학적 공정으로 전환될 것이다. 여기 몇 가지 가능한 발전이 있다.
1. 미국에서는 메탄 생성의 생체 자원은 수서히야신 스에 의해 얻어지는데 이 식물은 열대, 아열대 운하나 수로에서 자란다. 최저조건하에서 매일 1 헥타 르당 식물 전량 2 돈이 생산되며 이론상 800m~ bio g a s 7} 산출된다. 2. 인도의 어느 한 시골마을게서는 작고 비싸지 않은 설비들이 만둘어졌었는 데 이는 소거름을 bio g a t l 전환시키고 있 다(약 k g건량당 200[ gas ). 3. 혼합배양에 의한 메탄 생성은 충분히 규명되어 있지 않을 뿐 아니라 최적 화되어 있지도 않다. 통성 형기성균은 고분자 중합체 (지방, 탄수화물, 단 백질 )를 단일체 (아미노산, 굴리세롤, 지방산, 포도당)로 가수분해하게 된 다. 그 다음 다른 형기성균에 의해서 ® 저급지방산(아세트산, 프로피온 산, 부티르산), ® 알코올, CO2 , @ 수소의 생산이 이어진다. 폐수 처리 시스템에서 이 단계의 분해과정을 폐기물 액화단계라 한다 . 메탄 생성이 가능한 미생물군은 제한되어 있는데 반해 대다수의 미생물은 초기 분해반 응을수행할수있다. 4. 생산된 b i o g a 려 조성이나 양은 기질과 온도에 관련이 있다(표 17.3). 협 기적 폐기물 분해과정에서 유기물 전량 k g당 600l 이상의 메탄이 생산된 다. 메탄의 함량비는 60~70%, co 는 25~30%, 그리고 나머지는 H2, N 2 이다. 이에 따르는 변수의 최적화가 기대되는데 즉 사용 균주, 메탄 생 성속도, 온도, 폐기물 기질의 공급속도 등이다. 또한 기질의 분해속도를 높힐 수 있는 전처리공정의 개발에 의해 공정 개량이 가능하게 될 것임에 도의심의 여지가없다. 5. 폐기물 처리 시스템에서 다음과 같은 방침에 따라 집중적 개량이 기대된 다. 죽 각 단계를 최적화하기 위해 공정의 여러 단계에 수반되는 미생물 집단의 물리적 분리, 이미 통기폐수 처리공정에서 행해전 바와 같은 다단 계 처리공정의 적용, 온도의 최적화, 반응조에서 교반방법의 개선 등이다 . 이 책에서 전개시켜온 대규모 발효의 원리는 메탄 생성공정에 상당한 경제적인 면과 사회적 이익을 가져디주면서 쉽게 응용시킬 수 있음은 명백한것 같다.
세번째 처리단계 후에 정화된 폐수는 정화수의 흐름으로 이어지게 된다. 표 17.2 에서 Unox 공정을 사용한 운전 특성을 보여준다.
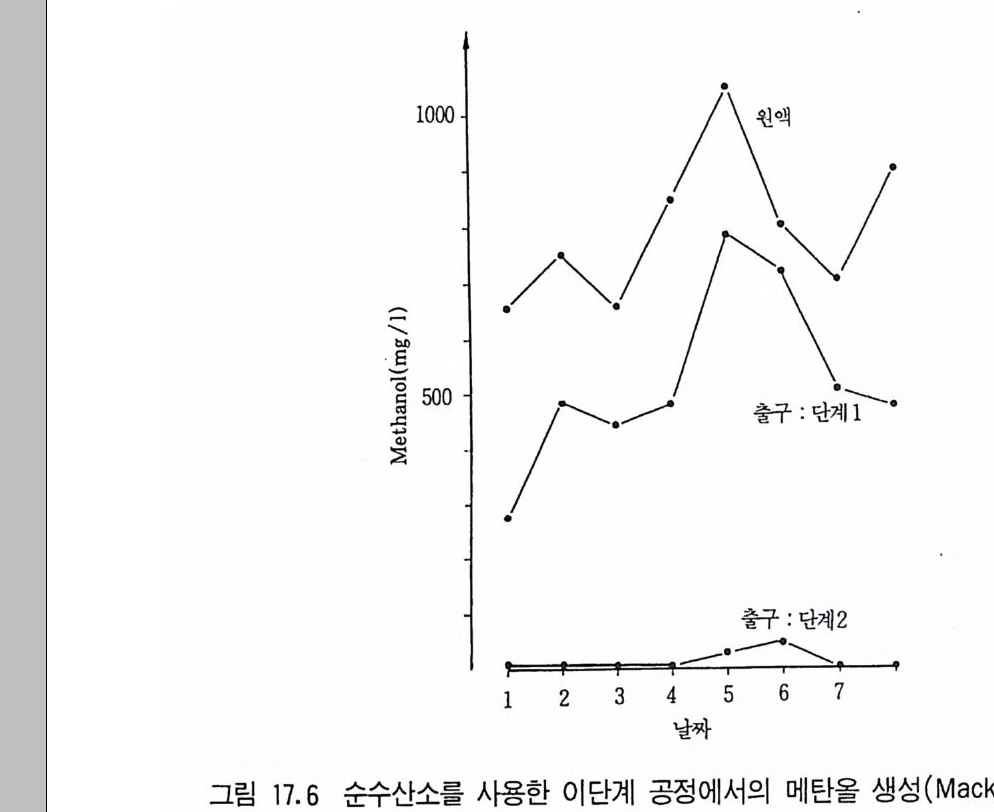 1000 /\~ .
1000 /\~ .
표 17.2 순수산소를 이용한 Unox 정화공정의 재료 폐수량 20,000m3 / day 화학적 산소요구 61 ton s / day (COD) -분해능력 생물적 산소요구 34 to ns/day (BDD)s- 분해능력 산소유입 활성단계 l 51 to ns/day 활성단계 2 7 to ns/day
부포1 활성단계 1 6200m3 활성단계 2 3200m3 중간단계 정화 4400m3 마지막정화 4800m3 요구되는시간 활성단계 1 7.5 h 활성단계 2 3.8 h 중간정화 5.3 h 마지막정화 5.8 h 분해활성 활성단계 l max. 80% COD max. 93% BODs 활성단계 2 max. 7% COD, tot a l 87% max. 5% BODs , tot a l 98% 오니 적재 활성단계 l 0.7 kg BODs/kg dry weig h t • d 활성단계 2 0.2 kg BODs / kg dry weig h t • d 공간필요성 활성단계 l 5.6 kg BODs /m 3 • d 활성단계 2 0.8 kg BODs /m 3 • d 초과오니 25% of the BODs load
참고문헌 Chakrabarty , A. 1974. U.S.pa te n t 3,813,316. Grasner, L. L. 1979. Mi cr oorga n ism s for waste tre atm ent pp.2 11~ 222. In:Pepp le r, H. J. and D. Perlman(eds.), Mi cr obia l tec hnolog y vol. II . Academ ic Press, New York. Kandler, 0. 1979. Op timiza ti on of the bio g a s pro cess usin g th e-rmop hilic micr oorga n ism s pp.1 9~31 . BMFT(ed.), Bi ok oversio n . 2nd BMF T-St a t u sse mi na r • Lemke, J. R. and K. Mack. 1978. Bi os ta t u s of anaerobic sludge sta - bil iza ti on pp.17 9~188. 4th Sy m p . 'lec hnis c he Mi kr obio l og ie, Berlin . Magr u der, G. C. and J. L. Gaddy. 1981. Producti on of far m energy fro m bio m ass pp.2 69~274. In:Moo-Young, M(ed.), Advances in bio - tec hnolog y vol. ill. Perga mon Press, Toronto . Mack, K. 1973 Bi ol og ica l tre atm ent 'of sewage with oxg ye n. Was-ser, Ru ft und Betr i e b . 17:108~111. Ohta , Y. and M. Ikeda. 1981 Rap id mi cr obia l deodoriz a ti on of agr i- cultu ral and anim al waste s pp.6 21~626. In:Moo-Young, M.(ed.), Advances in bio tec hnolog y vol. II .Perga m on Press, Toronto . p·o p e l, F. 1976 'lex tb o ok for sewage tre atm ent and wate r pu rifi ca ti on Deu- tsc her Fachschrif ten -verlag, Main z . Sta t i sch es Ja hrbuch, 1980. Verlag W. Kohlhammer, St u tt ga rt. Tayl o r, G. T. 1982. The meth a nog en ic bacte r ia pp.2 31~329. In:Bull, M. J. (ed.). Progr es s in ind ustr i a l mi cr obio l og y vol 16. Elsevie r Scie n ti fic pu blis h in g Comp a ny , Amste r dam. Wi nk ler, M. A. and A.Thomas. 1978. Bi ol og ica l tre atm ent of agu eous waste s pp. 200~279, In:Wi se man A.(ed.), Top ics in enzy m e and fer menta tion bio t e c hnolog y Ell is Horwood, Ch ich este r . Zeik u s, J. G. 1977. The bio l og y of meth a nog en ic bacte r ia . Bacte r ia l . Rev. 41 :514~541. Zlokarn ik, M. 1979. Eff icien cy of op tim i ze d inj e c to rs for the oxy ge n demand of .bio l og ica l sewage tre atm ent sys te m s. Verf ah enste c hnik 13:601~604.
제 1 礎 광물자원 회수기술 1 서론 리칭 (leach i n g)이란 미생물을 사용하여 광석이 함유된 암석에서 금속 울 용해시켜 내는 공정이다. 현재 많은 광석들이 금속함유량이 적기 때문에 화학적 방법으로 경제적으로 처리하지 못하고 있다. 많은 양의 저급광석이 고급광석의 분리과정에서 부산물로 나오게 되는데 일반적으 로 폐기물로 버려지고 있다. 전세계에 걸쳐 전형적인 화학적 방법에 의해서 적당하게 정제될 수는 없지만 리칭에 의해 가공 •• 처리될 수 있는 저급의 구리광석은 막대한 양이 있다. 그 밖에 회수할 수 있는 니켈, 납, 아연 광석도 상당한 양이 있다. 처음 리칭공정은 산성갱내 수중에 설치되어 있는 펌프나 도관에서 일어 나는 과정에서 발견되었다. 그것은 저급의 광석으로부터 금속을 회수하기 위해 개발되어왔고 많은 급속들을 오늘날 금속 황화물이나 다른 광석으로 부터 추출해내기 위해 리칭방법을 사용하고 있다. 죽 구리, 코발트, 몰리브 덴, 카드뮴, 비소, 니켈, 타이타늄, 우리늄과 같은 금속에서 황산과 Fe3+용 액을 가지고 산화 환원반응에 의해 암석으로부터 추출해낼 수 있다 (Bos eker, 1982) . 삼법적 응용예는 구리와 우라늄을 미생물을 사용하여 생산하고 있으나 실험실과 실험공장의 결과를 실제적인 현장조건으로 도입하려 할 때 어려
움이 있다 (Bosecker, 1980. 1982). 2 미생물학적 리칭의 원리 미생물학적 리칭에 일반적으로 사용되는 두 세균은 Thio b acil lu s thi- oox i dan 의 T fe rroox i dan 이며 그 밖에 사용되는 것은 다음과 같다 . Thi- ob_a ci l lu s concreti uo rus, Pseudomonas flu orescens, P. pu tid a , Achromo- bacte r, Bacill u s lich enif orm i s, B. cereus, B. lute u s, B. po lym y xa , B. meg a t er i u m:s.斗 고온성 세균인 Thio b acil lu s the rmop h ili c a , Thermoth r ix thio p a rus, Thio b acil lu s THl 과 Sulfol o bus acid o caldariu s 등이다( Kelly, 1979). 종속영양세균은 아직 사용되고 있지 않으나 그 방법은 미생물학적 으로 생산된 유기산과 킬레이트와 염의 형성으로 금속을 광석에서 추출해 내는 방법이 그 원리가 된다. Thio b acil lu s fe rroox i dans 는 가장 널리 연구된 세균 (Thoma, 1979, 1982) 인데, 독립영양군이고 호기성이며 CO2 고정으로 유일하게 생합성에 필요한 탄소원을 확보할 수 있는 세균으로서 F e2+ 를 Fe 3+ 로 산화시키거나 황분자와 환원된 황화합물을 황산염으로 산화시켜 에너지를 얻는다. 4FeS04+2Hz804+02 一 2Fe2(S04)3+ZH20 [1] 28 나 302+ZH20 一 2Hz804 @] 2Fe8z+702+ZH20 ― ➔ 2FeS04+2Hz804 떠 불용성인 황을 황산으로 산화시키는 것은 1hio b acil lu s t h i oox i dan 쩌 l 의 해서도 진행되는데 〔 3 〕식에서 볼 때, 철은 직접적 세균의 리칭과정을 통해 용해된다. 단지 미생물에 의해 수행되는 이 리칭과정 이의에도 미생물이 없을 때 서서히 반응이 일어나는 것도 있는데 예를 들면, 황철광의 산화롤 둘 수 있다. 황철광은 많은 광석과 결합하여 발견되는 혼한 암석의 광물이
며 철이온에 의해 황철광이 산화하는 것은 다음 식과 같 다. FeSz+Fez( S 04) 3 ― ➔ 3 FeS04+2S0 印 이 과정을 거쳐 형성되는 황도 @〕식에서와 같이 재산화된다 . 실험에서는 항상 T t h i oox i dans 와 T ferr ooxid a ns 혼합배양하에서 행하 는데 50 리터 규모의 시험공장에서의 리칭은 세포와 리청되는 물질의 재순 환과정으로 연속적으로 수행되며 (Sanmug as underam, 1981), 여과기에 매우 작은 입자로 만든 광석을 넣어 적당한 조건하에서 배양액을 전당시 키면서 실험실에서 행하지만 실제 적용실험에서는 이러한 조건하의 생산은 비용이 많이 둘기 때문에 실용적이지 못하다. 3 미생물 리칭의 공정과 현실 세 가지 방법이 실제적으로 적용되고 있다(그림 18.1 ). 1. 사면 리칭 (Slop e leachin g ) : 미세하게 분쇄된 광석울 산중턱 아래에 쌓 아 큰 더미가 되게 하고 그 위에 1h i obac i llu 遷 - 혼합한 물을 계속 뿌려 준다. 그 물을 밑바닥에서 모아 금속을 추출하고 산화용 못에서 세균을 재생한 후 다시 사용한다. 2. 적재리칭 (Heap leachin g ) : 광석을 커다란 더미로 쌓고 사면 리칭과 같 이 처리한다. 3. 원 위치 리칭 (In- s itu leachin g ) : 1hio b acil lu s7~ 혼합된 물을 뚫어 놓은 통로를 통해 지상에 원래의 위치 그대로 남아 있는, 추출되지 않은 광석 까지 펌프하여 보낸다. 대부분의 경우, 암석에 대한 투과도는 처음에 암석 을 폭파시킨 후의 표면에서는 증가된다. 산성수는 암석을 통해 스며나와 서 펌프되어온 밑바닥의 파전 곳에서 모아지고 광물들이 추출된 후 그 물
은 세균을 재생한 후 다시 사용된다.
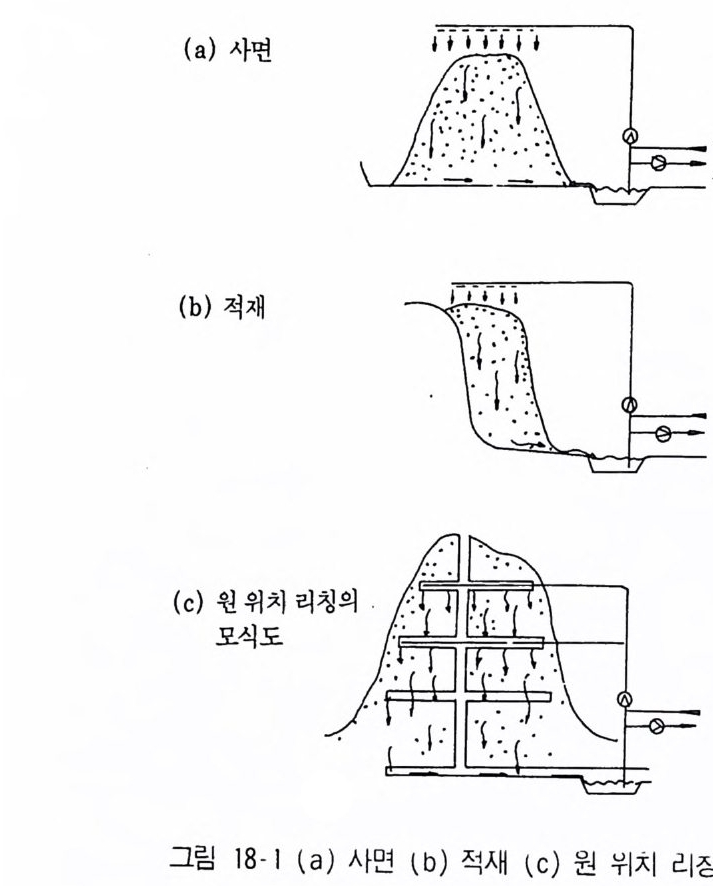 (a) 사면 I••t I II I I
(a) 사면 I••t I II I I
(1) 구리 리칭 (Cop pe r leach ing ) 만약 휘동광, · 황동굉이나 코벨라이트 (covell it e) 가 구리 생산에 사용될 때는 몇몇 금속도 함께 발견된다. 예를 들어 황동광은 26% 구리 , 25.9% 철, , 2.5% - 아연과 33% 황을 포함한다. 황동광은 다음과 같이 산화된다. 2CuFeS2+s11202+HzS04 _ ➔ 2CuS04+Fe2(S04h+H20 〔미 코벨라이트는 황산구리로 산화된다.
CuS+Z02 一 Cu804 [6] 구리 리칭공장은 다년간 전세계에서 널리 가동되어왔고 일반적으로 단 순한 적재 리청공정으로 행하여지지만 때때로 적재와 위치 리칭을 함께 샤용하기도 한다. 리칭용액 (황산과 Fe 3+ 용액 )은, 미생물의 배양액을 공급 하고 용해된 구리를 용출해낸다. 즉 용액은 광석더미 위에 뿌려지고, 구리 가 풍부한 액이 모아지는 낮은 평지까지 암석더미를 통해 여과된다. 구리 를 함유한 용액을 분리하여 (0.6 g/l) 구리를 침전시키고 물은 p H 를 '2ll} 지 재조절한 뒤 다시 사용한다 (Kell y. 1979). 구리를 미생물학적 리청으 로 얻는 방법을 널리 사용하는 나라는 미국, 오스트레일리아, 일본 등이다. (2) 우라늄 리칭 (Urani um leach ing ) 미생물적 리칭에 의한 우라늄 리칭과정은 경제적으로 매우 중요하다. 1 톤의 우라늄을 얻기 위해 l,00~ 達] 우라늄 광석을 처리해야 하므로 원위 치 미생물적 리칭이 좋은 방법으로 인정되고 있다. 그것은 막대한 양의 이러한 물질의 수송비를 줄일 수 있기 때문이다. 齊 떼공정에서는 불용성의 47} 우리늄을 가열 황산과 Fe3 + 용액으 로 산화시켜서 가용성의 67} 황산 우리늄을 만든다. U02+ F ez( S 04h 一 ➔ UOzSQ 4+ 2 Fe804 [7] 황산철과 황산은 T fe rroox i dan 폐 의해 우라늄 광석내에서 황철광으로 부터 생산할수 있다. 2FeSz+H20 + 7.5 0 2 一 Fe2(S04) 3 +HiS 0 4 [8] 황철광 반응은 Fe3+ 리칭용액의 일차생산과정을 위해 사용된다. 시험공 장은 하수처리에 사용하는 삼투여과상과 유사한, 표면반응기로서 가동된다.
최적의 우라늄 리칭조건은 pH l .5~ 3.5, 온도는 35°c , 그리고 흡입되는 공기에는 0.2% co 가 있어야 한다. 상업적 공정에서 용해된 우라늄은 t r i bu ty l p hos p ha t e 와 같은 용기용매 롤 가지로 리청용매로부터 추출해내고 우리늄.은 용기용매로부터 계속 침전 이 된다. 이온교환기를 가지고 우라닐 (uran yl) 이온을 흡착시키는 방법도 또 다른 가능성을 가진다. 추출 후 수계에 남아 있는 유기용매는 미생물계 의 재사용시 독성문제를 일으킬 수 있다. 원위치 리칭은 암석에 대한 투과도가 낮고 뚫어놓은 통로가 반드시 영 00回 내과 산소의 충분한 공급을 광석 깊숙히 들어갈 수 있도록 해주지 못하 는 단점이 있다. 이러한 상황에서는 우라늄 리칭으로 아직까지 싱업적으로 사용되고 있는 방법은 적재 리칭방법이다. 우라늄 리칭을 하고 있는 지역은 미국, 캐나다, 님이프리카 등이다. 춥卜고문헌 Boseker, K. 1980. Mi cr obia l leach ing -u se of bacte r ia for the bene- fica ti on of meta l ores. Forum Mi kro bio l. 2:98~103. Bosecker, K. 1982. Mi kro bie ll e Lang u ng ( Leachin g ) pp 535~553. In:Pra- ve et al.(eds.), Handbuch der Bi ot e c bnolog ie Akademi sc he Ver-lags g e s ellschaft , Wi es baden, Ebner, H. G. 1977. Meta l extr a cti on from ind ustr i a l waste wi th Thi- obacil li pp. 217~222. In:Schwartz , W.(ed), Con fere nce Bacte r ia l Leach ing . Verlag Chem ie, Wein h eim . Kelly, D. P., P. R. Norris and C. L. Brie r ley. 1979. Mi cr obio l og ica l meth o ds for the ext ra cti on and recovery of meta l s, pp. 263~308. In:Bull,A.T.,D.C.Ellwood, and C Ratl e dg e( eds.), Mi cr obia l tec h- nology :C urrent sta te, futu re pro spe cts Cambrid g e Un ive rsit y Press, Cambrid g e .
Sanrnug as underam, V., D. W. Duncan and R. M. R. Branio n . 1981 . Novel reacto r confi gu rati on for small scale Mi cr obio lo g ica l leach- ing , pp. 595~600. In:Moo-yo n g , M.(ed.) Advances in bio te c hnolog y vol. l.Pe rga m on Press.Toronto . Torma, A.E. 1977. The role of Th iob acil lus fer rooxi da ns in hyd - rometa l lurgi ca l pro cesses. Adv. Bio c hem. Eng . 6 : 1~ 37 . . Torma, A.E. and K. Bosecker, 1982. Bact er ia l leachin g pp.7 7~118. In : Bull,M.T.(ed). Progr e ss in ind ustr ia l mic ro bio lo g y Vol. 16. Els- evie r Scie n ti fic Publi sh i ng Comp an y , Amste r dam.
제 19 장 발효공정의 수지계산과 경제성 1 발효산물의 경제성 미생물에 의해 생산되는 산물이 소비자에 이용되려면 그 제품이 경제적 으로 시장성을 지녀야 한다. 제품의 시장성을 유지하기 위해서는 소비자가 원하는 제품으로, 공급에 있어서는 생산성이 높고 가격이 같은 성질의 제 품이나 국제적인 가격에 비해 경쟁력이 있어야 하는데 먼저 그 제품생산 에 대한 생산원가를 검토해야 한다• 생산원가를 낮추기 위해서는 미생물 사업이란 특수성에 비추어 고려해야 할 문제점을 몇 가지 검토하기로 하 겠다. 1. 생산하는 주체가 미생물이기 때문에 사용하는 미생물 균주가 목적으로 하 는 산물을 고수율로 생산하는 균주이어야 한다. 2. 생산원료 (raw mate r ia l s) 죽 기질원료가 가능한 저렴하여야 한다• 따라 서 대체원료의 가능성을 항상 검토하여야 한다• 3. 발효 생산공정 죽 희분식이냐 연속식이냐의 고수율을 위한 발효장치의 유 형, 발효조건의 확립, 회수 • 경제공정의 합리화 등을 검토해야 한다. 4. 발효장치 및 부대시설이 적정하여야 한다. 생산규모에 맞는 시설을 산정하 고(fi xed cost) 동력 (u tliti es) 이나 열의 손실을 최소화시켜야 한다. 5. 노동력 (labour) 을 절감할 수 있고 관리를 신속 효율화할 수 있는 자동시 설의 설치 검토 등이 있어야 한다.
위와 같은 기준은 개개의 산물의 성질에 따라 다르기 때문에 각각의 발 효공정에 대해 산정해야 한다. 대부분의 발효공업에서는 각 단계에서 발생하는 부산물도 많고 소비되 는 열에너지, 냉각수도 매우 막대한 양이며 폐액 등이 대량으로 나오게 되 므로 이들을 재활용하거나 공해가 발생되지 않도록 폐기전에 처리하여야 한다. 이러한 발효폐액 처리에 관한 종설로는 Pa p e(l977) 의 책자를 참고 할수있다.
표 19.1 생산비의 구성원가 백분율 소묶 Aceti c Cit ric Cit ric Beer Alcohol Aci d acid ' acid t Norpr o te in SCP Penic i ll i n Pratt en Rig h elato Pap e schie rh olt S chie r holt Mog re n Anon. Swartz 구성항목 (l 암 1) (19 80) ( 1'!17 ) (l
2 산업균주와 균주개량에 의한 경제성 향상 발효공정에 사용되는 미생물균주는 통상 토양에서 분리한 균주를 서용 하는데 균주 분리작업은 시간과 노력을 매우 요하는 작업으로서 유용균주 가 발견된다는 보장이 없는 작업이다. 예를 들면, 항생물질 생산균주의 분 리작업에서 Eli L i ll y사는 l ()ld간에 4QP J- 주의 균주를 검색하여 겨우 羽든
류의 새로운 항생물질 생산균주를 발전할 수가 있었다 (Nelson, 1961). 한편 발효유형이나 사용할 발효균주의 종류가 정해져 있을 때의 검색방 법은 상대적으로 단순하다. 목적이 뚜렷하지 않는 광범위한 검색공정에서 는 검색방법을 여러 각도로 고안해야 한다. 예컨대 단세포 단백질 생산균 의 경우라면 냉각문제를 해결하기 위해 5o·c 정도의 고온에서 증식하고 사료성분에 필요한 메티오닐 (meth i o n l) 함량이 높은 단백질 생산균이면서 집균이 쉬운 대형세포나 섬유상 세포를 검색하는 편이 좋다 (Hum p hre y 1977). 일단 목적으로 하는 균주를 토양이나 자연계에서 분리하여도 일반 적으로 그 균주가 산업공정에 사용하기에는 생산 수율이 낮다. 따라서 사 용균주의 생산수율을 향상시키는 것은 제품가격에 크게 영향을 미치므로 균주개량과 함께 배양조건을 검토해서 생산수율을 향상시키는 작업이 우선 필수적이다. 균주개량에서 이룩한 예로는 페니실린 생산에 194 ()1,빈대 ml 당 10 따위 이하였던 것이 197 6\1에는 ml 당 51,00 派持위까지 수율을 향상시킨 것이다(Q ueener et al., 1979). 이 과정에서 소요된 시간이나 비용은 매 우 크기 때문에 일반적으로 돌연변이나 단일균주 분리시험에 지출할 예산 은 생산규모에 따라 그 범위를 산정해야 할 것이다. 3 발효장치 및 발효원료의 경제성 이론적으로 보면 장치의 규모가 크면 경제성이 높은 것으로 나타나지만 장치의 조작 규모를 결정하기에 앞서 고려해야 할 제한적 조건이 있다. 즉 그 조건은 냉각, 통기, 발효조의 구조 및 건설방법에 관한 것이다. 여기서 중요한 것은 발효조의 용량은 r3(r은 발효조의 지름)에 비례하는 데 반해 표면적 증가는 규에 비례하는 것이다. 따라서 용량 증대의 결과 여기에 대 한 표면적의 감소를 초래하므로 냉각의 효율성이 감소하게 되는 것이다. 그 결과 일정 온도를 유지해야 할 때 내부 냉각장치를 증가시켜야 할 것 이고 발효조 교반장치와도 연관이 발생한다.
발효공정에서 산소요구성에 따라 발효조의 규모에 제한울 받게 된다. 단 세포 단백질 생산에서는 두자 규모와 작동비용을 고려해서 산소공급의 효 융기 높고 구조가 단순한 발효조를 설계하는 추세인데 Schu g erl (1 978) 이 산출한 바에 의하면 메탄올로부터 연간 10 만톤의 단세포 단백질을 생산할 경우 공장에 대한 두자가 생산비의 20% 를 차지하는 것으로 계산하고 있 다. 그중 20~25% 가 발효조 시설인데 그 중 발효조가 5~10%, 교반기와
표 19.2 발효공장의 투자비 내역 (a) Penic illin pla nt, esti m ate d for five 225,000-< lm3 fer mente r s wi th ancil lar y equ i p m ent (Swartz , 1979) (% of tot a l ) 공정정비 23.6 Insta l lati on 5.2 Insulati on 1.9 Instr u ments 2.7 Pip ing 11.8 Elect ri c a l 15.8 건물 11. 3 동력 21. 3 토 ~1 2.4 연구실장비 3.8 Sp ar e par ts 0.5 (b) Norpr o te i n pla nt (Morgr e n, 1979) (% of tot a l ) 원료저장 10 Media pre pa r ati on and uti lities 17 Fermenta t i on 41 Cell. r ecovery and dryi ng 22 산물저장 10
(c) ICL Ltd. Sin g l e -c e ll Prote i n pla nt (Smi th, 1980) (% of tot a l ) 원료 3 저장 ·포장 12 Off -si t e servic e s 161114919124 On-sit e s ervic e s 발효 압착 탈수 건조 발효액처리
통기장치에 5~10%, 냉각장치에 10~15% 가 소요되며, 동력, 물, 통기, 그리고 기타 보조물에 생산비의 10% 가 더 추가로 소요된다. 따라서 발효 조 투자비가 약 4~5% 이고 작동비가 10% 이므로 발효조의 유형이 전생산 비의 15% 범위내에서 영향을 주게 된다. 만일 이 경우 t ower 형 발효조를 채택하면 동력과 냉각주의 절감으로 인해 운전비가 절감된다• 단세포 단백질 생산공장의 수명은 10~15 년 정도이나 (Hamer, 1979), 아세본부탄올의 경우 25 년된 발효조도 사용되고 있다 (Sp ive y , 1978). 발효 생산에서 발효배지의 여러 성분의 비용은 (표 12 .l)에 나타난 바 와 같이 전체 생산비의 38~73% 를 차지하므로 매우 큰 비중을 차지한다. 보통 유기탄소원이 가장 많은 비용을 차지하는데 그것이 지역적으로나 계 절적으로 생산되는 원료라면 그 원료 확보와 보관에 많은 두자가 소요된 다 (Ra t led g e, 1977). 기질원료의 저장, 처리, 혼합에도 경비가 소요되나 그것이 분말이라면 굳어지거나 덩어리가 되지 않게 건조상태에서 보관되어 야 하며 액체상태의 배지성분이라면 농도에 따라 응고, 응집을 방지하거나 혹은 온도를 높일 때 분해가 되지 않도록 보관되어야 한다 (Corbe tt, 1980). 탄소원은 배지성분 중 가장 큰 비중을 차지하는 성분이므로 탄소원을
다른 종류의 탄소원으로- 대체시키는 시도도 가능하겠으나 원료대체시 수반 되는 통기량이나 교반속도의 변화도 고려해야 한다. 폐당밀, 곡류의 전분 질이 가장 보편적 탄소원이지만 석유가격이 저령할 때는 탄화수소, 메탄, 메탄을이 대체 가능한 탄소원이 될 수 있고 또한, 장차 천연가스나 농산 폐기물, 도시 폐기물도 사료단백질 생산 등에는 탄소원이 될 가능성을 지 니고 있다. 다만 이들 폐기물은 실제 .불순물, 수분함량에 의한 운반비 문 제, 그리고 지역적 혹은 계절적 산출량의 변동으로 많은 제약을 받게 된 다. SCP 생산에서 배지원료 중 무기영은 배지비용 중 4~14% 정도이므로 그렇게 크지는 않으나 인산염은 다른 종류의 설순금속의 함량이 낮은 것 울 사용해야 하므로 비료용 인산염보다 보통 비싼 편이다 (Coone y et al., 1977). 4 발효공정의 관리와 수지 호기성 발효에서는 대량의 멸균공기의 공급은 필수적인데 이에 필요한 공기를 가열해서 멸균하는 것도 가능하지만 그것은 바용이 매우 소요되는 방법이다. 압축기에 의한 공기 멸균방법도 여러 측면에서 검토되고 있다 (Sta r k, 1950). 오늘날에는 공기의 여과방법이 공기멸균에 상용되고 있다. 소요비용은 그 크가나 규모에 따라 다르지만 주로 횡단면적에 따라 다르며 가동비용 은 여과재료의 종류와 여과기에 대한 압력에 주로 좌우된다. 이 경우 거친 입자로부터 미세입자까지롤 단계적으로 제거하는 단계적 제거방식을 채택함으로써 고가의 미세여과 여과막의 수면을 연장시키는 방 법이 효과적이다. 공기의 공급과 함께 초기발효에서는 일정한 환경조건을 부여하기 위하 여 교반도 필요하게 된다. 그러나 아세톤부·탄올 발효나 에탄올 발효와 같
이 공기의 공급을 요하지 않는 발효에서는 접종 직후를 제의하고는 교반 은 필요없으므로 생산비에서 그만큼 경제적이다. 산소요구가 큰 발효에서 는 통기의 환경을 균일하게 하기 위하여 교반해야 하므로 이런 경우 여기 에 소요되는 경비는 전생산비의 1. 9% 에 달한다 (R y u, 1977). 발효공정에서 가열이나 냉각공정은 없는 편이 이상적이긴 하지만 그것 은 불가능에 가까운 것이어서 그러한 공정은 최소화시키는 것이 소망스러 운 것이다 n 알칸에서 SCP 를 생산할 때 냉각장치비를 감소시키기 위해서 는 공중보급형 발효조를 사용하거나 (Schu g erl, 1978), 증식온도가 높은 내열성 균주를 사용하기도 한다. 5 발효산물의 회수와 수지 발효산물에는 저가이면서 대용량 산물과 고가 저용량 산물로 구분될 수 있는데 전자의 개념에 속하는 산물로는 유기용매, 유기산, 단세포 단백질 등이 포함되고 이 제품은 화학 합성법에 의해 생산되는 제품과 경쟁관계 에 있다. 다만 화학구조가 복잡한 제품의 경우와 화학적으로. 불안전한 제 품은 예의이다. 일반적으로 미생물공정은 복잡한 화학구조를 한 물질에서 는 경제적으로 매우 유리하며 합성에 많은 공정을 요하거나 온도에 불안 정한 산물에서는 미생물 공정이 상대적으로 유리하다. 이러한 산물의 대표 적인 것이 항생물질, 스데로이드호르몬, 아미노산류 및 비타민류로서 이들 은 고가 저용량 산물로서 정밀한 화학제품인 것이다. 시장성을 고려할 때 는 현재의 상태 및 잠재적 시장성 그리고 그 산물의 수요 증가의 규모도 추정할필요가있다. 발효산물이나 균체는 발효액 중에 존재하고 있으므로 이들을 회수하여 이용할 수 있는 상태로 정제하여야 하는데 이 과정은 수율에 크게 영향을 준다. 죽, 각 단계의 회수 정제공정의 회수율과 그 과정에 소요되는 에너 지와 관리비 그리고 산물의 회수에 사용되는 회수방법의 선택이 크게 좌
우하게 된다. A t k i nson(1983) 에 의하면 인산(p o t ass i um) 영을 만들 때까지 시트르 산 생산에서는 8% 의 수율 감소가 일어나고 페니실린 G 생산에서는 4% 의 수율 감소가 일어난다고 한다. 따라서 시설비 두자와 운전비 절하도 중 요하지만 소위 downs t ream 의 공정에서도 비용이 절감되도록 하는 여러 시도가매우중요하다. 효卜고문헌 Atk ins on, B. and Mavit un a, F. Bio c hemi ca l En gine erin g and Bio - tec hnology Handbook Chapt er 12, pp.8 90~931. Macmi lla n, London. 1983. Cooney, C.L. and Marig u ch i, N. An assessment of sin g l e cell pro te i n from meth a nol-g r own yea st. In Sin g l e cell Prote in from Renewable and non-Renewable Resources, Bio t e c h. Bio e ng , Sym p 7, 65~76. Corbett , K. Prepa r ati on , ste r ili za ti on and desig n of media . In Fun- gal Bio t e c hnolig y Brit My co l. Soc. Sym p . 3, pp.2 5~41 (E dit ors Smi - th, J., Berry, D. R. and Kris t i an sen, B.). Academi c Press, Lon- don. 1980. Hamer, G. Bio m ass from nat ur al gas . In Mi cr obio l Biom ass Econ- omi c Mi cr obio l og y, Vol 4, pp. 315~360 (Edit or Rose, A.H.). Aca- dem ic Press, London. Hump h rey, A.E., Moreir a , A., Arm ige r, W. and Zabn isk ie , D. In Sin - gle Cell Prote i n from ~enewable and Non-Renewable Resources, Bio t e c h Bio en g Sym p . 7, 45~64. 1977. Morga n , H. : SCP from meth a nol, -the Norpr o te i n pro cess. Proc. Bio c hem. 14(3) 2~7( 1979) Nelson , T.C. Muta t i on and Plant Breedin g p. 331, Pwbl, No. 891. Nat Acad, Sci. N a t. Res. Council , Wash ing ton . 1961 .
Pape , M. The comp et i tion betw een mi cr obia l and chemi ca l pro cesses for the manufa c tu r e of basic chemi ca ls and int e r media t e s . In Mi - crobia l Energy Conuersio n pp. 510~530. (Edit ors schlegc l , H.G. and Barnea, J.) .Perga m onPress, Oxfo r d. 1977. Pratt en , C, F., : Economi cs of Scale in Manafa c tu r in g lndustr y . Dep t. of Ap pl. Economi cs, Vol 28, Univ , Press Cambrid g e . Qu eener, S. and Swartz , R.W . Pen ici ll ins , bio s y nt h e ti c and sem- isy n th e ti c. In Secondary Prodncts of Meta lo bis m , Economi c Mi cro - bio lo g y Vol. 3, pp.3 5~122 (Edit or Rose, A.H.). Academi c Press, London. Ratl e dg e, C, Fermenta t i on substr a te s , Ann. Rep. Fenn. Processes, 1. 49~71. 1977. Ry n,D .Y. and Oldshue, J.Y . A reassessment of mi xin g cost in- fer menta t i o·n pro cesses, Bio t e c h, Bio e ng . 19, 621~629. 1977. Schug er l, K, Lucke, J., Lehmann, J.a nd Wagn e r, F. Ap plica ti on of tow er bio r eacto r s in cell mass pro ducti on . Adu. Bio c hem. Bio en g . 8., 63~13l. Smi th, S. R. ; Sin g l e cell pro te i n . Phil . '!ran s. Roy . Soc.(London) B 290, 341~354(1980) Spi ve y , M.J. The aceto ne/buta n ol /eth a nol fer menta t i on . Proc Bio - chem, 13(11), 2~4, 25. Sta r k.W.H. and Pohler, G.M. Ste r ile air for ind ustr i a l fer - menta t i on s. Ind. Eng. Chem, 42, 1789~1792. 1950. Swartz , R. W. ; The use of economi c analys i s of pen i cil l in G manu- fac tu r in g costs in esta b lis h in g pri o r i ties for ferm enta t i on pro cess im p ro vement. Ann. Rep. Ferm, Processes. vol. 3 75~110(1979).
찾 0~ 보 71
A AICAR for my lt r a nsfe r ase 325 AICAR 324, 325 Arrheniu s 식 166 DL- al an ine 274, 276 DL- cx - am i no capr o lacta m 277, 295 D- al an ine carboxy pe p tida se 404 L-:- a sp a rti c acid 273, 274 L- as p a rag ina se 360 L- as p a ragi ne 361 L- cx - am i no adip ic acid 360 acety l CoA 285 acety la ti on 493 acti na rnin e 428 acti no my ci n 398, 417, 418 ac tno rhodin 397 acy l resid u e 356 acy la ti on 493 adenosin e tri p h osph ate ( ATP) 327 adenosin e 313 adeny l succi na te lya s e 311 adeny lt r a nsfe r ase 493 adria m y cin 397, 399 adsorp tion chromato g r a ph y 212 affini t y chromato g r a p h y 215 albu min 365 alcohol dehy dr og en ase 223, 334 algi na te 465, 467 alkalin e pho sp h ata s e 316 alloste r ic sit e 4 8
alloxazin e 379 ami di n o t ra nsfe r ase 430 ami ka cin 426 ami no acy la se 278 ammoniu m ph eny la ceta t e 359 amoxic i l lin 494 amp ho my ci n 400 amp ho te r ic i n B 437, 438 amp icil lin 396, 476, 494 amy la se tak adia s ta s e 331 amy la se 331, 333, 336, 338 amy lo g lu cosid a se 331 amy lo p ec ti n 344 analog ue 59, 64 androg en 478 androsta d ie n dio n e 487, 488 androste n d ion e 487 anhy dr ote t r a cy cl i ne 446, 475 ansamy ci n 397, 432, 439, 440 ansamy toc i n 440 anth r acene syn tha se 443 anth r acy cl i ne s 397 anth r anil a te 302 anti bi o t i c resis t a n ce 91 anti bi o t i cs 21 anti tum orge n t 360 ascorbic acid 488 aspa rag ina se 334 aspa rta m e 업 4 aspa rti c acid 361 aspa rto k ina se 298, 299 auxo t ro ph i c( 영양요구성 ) 59
avic e lase 515 azauracil 476 p-a m i no benzoy l CoA 439 5'-A MP 309 , 311, 313, 316 6-ami no pe ni cil l an ic acid 357, 494 7-a m i no cep h alospo ranic aci d 360 8-a z agu a nin e 313 a-a m y la se 225, 336, 337, 339, 341 p-am y la se 336, 342 B baci tra ci n 400, 401, 421, 422 bact er ia l type II acy la se 358 bacte r io c in s 91 batc h fer menta t i on 266 batc h pro cess 348, 350 batc h sys t e m 223 bekanamy cin 426 benzaldehy de 475 benzim i da zol 384 benzoq ui n o nes 398 benzy al cohol dehy dr og en ase 365 benzyl p e nic i ll in 404 bio c oversio n 473 bio g a s 530, 531 bio r eacto r 524 bio t i n 284, 288 bio t r a nsfo r mati on 477 blasti cid in S 399 bleomy ci n A2, A3 399, 423 blunt 95
bromelanin 334 buti ro sin 431 P- la cta m 33 P-l a cta m ase 33 P- 1. 4 -g l u cosid e 515 c L- cy s t e i n 274, 276 camp es te r ol 486 candic i d i n 397, 437, 439 cap re omy cin 400, 421 carboxy m eth y l cellulase 515 carot en e 388 cata b olic enzy m es 64, 101 cata b olit e rep re ssio n 68, 341 , 344 cata l ase 333 cellobia s e 515 cellobio h y dr olase 515 cellular yield coeff ici e n t Y 119 cellulase 514, 515 cellulose tri a c eta t e 372 centi po is e 467 cep ha lexin 414 cep ha lospo r in 360, 396, 411, 415-416, 493 cep ha my ci n 403 characte r iz a ti on tes t 41 chemohete r otr o p h 121 chemosta t 64 chlomomy cin A3 399
chlomop ep tide s 398 chloramp he nic o l 75, 382, 395, 398, 448 chlordecone 496 chlorte t r a cyc l in e 401, 441- 44 4, 447 choleste r ol oxid a se 334 cholranil in e 475 chy m ase 355 chy m osin 355 clavulanic acid 416 clin d amy ci n 425 cobalam in 385 cobami de 383 coccis t a t i c age n t 401 cometa b ois m 495 com p a ti ble( 화합성 )pla smi d 92 comp le x media 35 concerte d or multi va lent fee dback inh ibi t ion 49, 55, 62 conj u ga t i on 85 consti tut i ve muta n ts 348 consti tut i ve 64 conti nu ous chromato g r a ph y 215 conti nu ous inj e c to r -f la s h cooler 173 conti nu ous pla te heat exchang er 173 cordg ce p in 447 corn ste e p liqu or 22, 348 coronati ne 461 corrin 383 corti so ne 478, 482
cosmi d 94 coumarin 451 co- op e rati ve fee dback cont ro l 49 cryo p r o te c ti ve age n t 40, 42 crys t a l liz a ti on 217 cumulati ve fee dback contr o l 50 curdlan 465 curin g age n ts 93 cx cellulase 515 cya n obact er ia 236 cya n ocobalam in 385 cyc l ic adenosin e -3', 5'- monp ho sp ha te ( cAMP) 328 cyc l ohexim i de 75, 398, 399 cyc l oserin e 398, 417 5'-CMP 316 D DFP 353 dacti no mucin (Acti no my ci n Cl) 417, 418 daunumy ci n 399 deaceto x y ce p h alospo r in C 414 death ph ase 155 delf act o r 169 dep si p e p tide s 398 dext ra n 466, 470 dext ra nsucrase 470 dex tri n 336, 343 dial ys i s 217 diam i no p im eli c acid ( DAP) 295, 297
dia u xy 154, 348 dibe kacin 426 die l drin 494 dih y d r op st r e p tom y cin 425 dilu ti on rate 156 dim eth o xy apo r ph ine 475 ddiiso ts rg ie bn u itn i o4n8 2 ,c h4r8o6m ato g r a ph y 217 dit erp e n e 463 dodecyl benzene 474 double via l meth o d 40 2-d e oxy st r e p tam ine 429 5'-de oxy ribo nucleoti de s 309 p-d i me th y l a m ino pro p ion itri le 372 E EMP 285 Enbden-Meye r hof- P arnas{EMP) 경로 246 endo, exo-pe c ti nl ya s e 362 endocellulase 515 endoenzym e 338 endop ec ta t e lya s e 362 endop ol yg a lactu r onase 362 endo-p- 1.4- gl u canase 515 enduraci di n 402 ente r oto x in 91 enzym es 23 epo x y da ti on 474 eryt hr omy cin 397, 401, 433- 43 6 estr o ge n 478
everni no mi ci n 397 exon 100 exop ol yg a lactu r onase 362 exo- P- 1 . 4 -g l u canase 515 exte n den 470 ext ra cellular meta b oli te 207 F B- D - fr uc to p y ra nose 346 FAD 378 FMN 378 fac ulta t i ve meth y l o tr o p h 506, 507 fatty alcohol 365 fed -batc h pro cess 353 fee dback inh ib i t ion 48, 55, 59 fee dback repr e ssio n 48, 64 fee dback sys t e m 161 ferm enta t i on 16, 226 fibr ous pol ym e r 353 ficin 334 filipin 437 filtr a ti on enric h ment meth o d 58 flav op ro te i n 378 fl occula ti on( 응집 ) 107 foa m ing 139 for tim icin 426, 429, 431, 432 fos fo m y ci n 398 free ze drye r 39 fun ga l type acy la se 357 fus id ic acid 396, 398, 451, 452
G gas sin g out meth o d 196 gel ati n 365 gel dnamy ci n 440 gel -f il tra ti on chromato g r a ph y 214 gen ome nonhomdog y 89 gen ta m y cin gro up 428 ger any l pyro p ho sph ate 463 ger any lg e r eny l pyro p ho sph a te 463 gibb erelli c acid 463 gla ucin e 474 glu can 466, 469 glu coamy la se iso enzym e 343 glu coamy la se 225, 336, 338, 343 glu cocorti co id 478 glu conic acid 258 glu cose iso merase 331, 477 glu cose oxid a se 334 glu cose pho sph a te iso merase 347 glu cose- fr uc to s id e 470 glu curon ic. a cid 468 glu ta m ate dehy dr og en ase 285 glu ta m ic acid 273, 284 glu ta r aldehy de 349 gly c e rol 233, 234, 235 gly c ine 274, 276 gly c o li pids 397 gly c o sid e 362 gly o x y la te 회로 248 gra di en t pla te tec hn iqu e 61, 74 gra m icidi n A 400
( line ar ) 421, 422 S(J) 400, 420- 42 2 gri s e ofu lv in 396, 398, 448, 449, 450 gua nosin e 313 gua ny lic aci d (5 '-GM P) 309, 311, 313, 316 a.- gl u can 344 fi-g a la ct ur onid a se 336, 345, 346, 364 H halomy cin 440 hcxulose pho sph a te syn t h a se 510 heap leach ing 535 hemolys i n 91 hep tae ne 438 hexameth y l e nedii s o cy an ate 368 hexok ina se muram ida se 쩌 hist i di n e 274 homocit ra te syn tha se 407 homoserin e dehy dr oge n ase 63, 296, 298 byb r id o ma 101 hyd a nto i n 302 hyd r azin e 371 hyd r oxy la ti on 474 hyg ro my cin 401, 428 hyp o xanth i n e 319, 323, 324 N-im in o meth o xy pen i cil l in este r
359 idi o p h a se 25, 160 im mobil ize d cell 474 im mobil ize d enzy m e pro cess 348 inc omp a ti ble pla smi d 92 int r a cellular meta b olit e 2 07 int r o n 100 in- sifu leachin g 535 ion -exchange chromato g r a ph y 212 iso amy la se 344 iso ap o codein e 477 iso cit ra te dehy dr oge n ase 286, 287 iso c itra te lya s e 285, 287 iso enzy m e contr o l 51 iso merase 333, 336, 338 iso meriz a ti on 345 iso nia z id 391 iso pe n i cil l in 406 iso pe n te n y l pyrop h osph ate 463 iso p re noid alchohol ph osph ate 465 iso p ro p an ol 467 5'-IMP 309, 311, 316, 321, 322 P-io n one 390 J jos aroy ci n 434 K kanamy cin 426 kanamy ci n grou p 428
kasuga m y ci n 399, 426, 427, 429, 430 key meta l 133 cx- ke to g l u t am ate dehy d roge n ase 285 L L-lys i n e 273, 274, 277, 294 lacta s e 364 lacto n e syn th a se 435 lacto s e ope r on 98 lankacid i n e C 492 lasalocid e 402, 452 laureate 475 leucomy ci n Al-A9 434 leukaemomy ci n 33 lign ocellulose 468 lim i ting fac to r 193 linc omy ci n 424, 425 lind ane 494 lipa se 334, 363 lipo some 102 lipo xyg e nase 334 liqu efy ing 338 log ph ase 150 log pha se 24, 151 pply--cl! oaa cpc tteaan mme a3s38e586 ,4 0439,3 416 M
L- m eth io n in e 274, 275, 276 maxim um spe c if ic gro wt h rate 153 Monod 식 152 multi -st a g e sys te m 161 NN '-m eth y le ne bis a cryl a mi de 372 macarbomy ci n 402, 425 macrocy cl ic lacto n e 397 macrot et r o li de s 397 macro- po r ous adsorbants 212 main t e n ance mediu m 34 malto s e 336 malto t r i o s e 338 mannan oxid a se 139 mannose 465 mannuronic acid 465 medrol 479 ment ho l 475 meth ane oxy ge nase 505 meth y lb uty ra te 492 meth y le ne chlorid e 393 meth y le ste r 370 meth y myc in 432, 433 mevalonic acid 463 mi cr ocap su lati on 331 micr ocap su le 372 mi ka my ci n 402, 420 mine ral corti co id 478 mi nim al media 35 mithr amy c in 399 mi tom y c in A-C 399, 453 mitom y cin 398, 453 moc im y cin 402
moenomy ci n 397, 425 monensin 398, 452 monoclonal anti bo die s 101 mucop ol ys a ccharid e 388 7- m eth o xy cep ha losp o rin s 411 N Na-pe r sulf ate 372 nabomy ci n 494 nap ftho q ui n o nes 397 nap h th a lene 474 neocarzin o sta t i n 399 neometh y m y ci n 432 , 433 neomy cin B 426 neomy ci n gro up 428 neomy cin 382, 491 neti lmici n 426 nisi n 400 nitra te reducta s e 127 nocard ici n 415 noji rim y ci n 397, 423, 424 novobio c in 448, 451 nucleosid e olig o p ho sp ha te 329 nutr i e n t gel ati n 37 ny s ta ti n A 437, 438 5'-nucleoti da se 316, 317 。 obli ga te meth y lt r o p h 505, 506 octa d ie n e 474
orth o somy ci n s 397 overlay tec hniq u es (중충법 ) 70, 78 oxaloaceta t e carboxy la se 287 oxy ge n tra nsfe r rate 194 oxy tet r a cy cl in 442, 443, 445, 446 2-o x og lu ta r ic aci d 292 P C5- po l yh y dr oxy 379 DL- ph e ny la lanin e 274 pB R 322, 294 pU B 110, 294 pal i nd rome 95 pal m itat e 388 pap a i n 334 pec ti na se 361, 362 pec ti ne ste r ase 362 pen i cil l in acy la se 334, 357, 358, 359, 477, 493 pen i cil l in 395, 398, 401, 403- 40 6, 411 pen ta e ne 437 pen to s e pho sph a te pat h w ay 285 pep t on e 130 per mease 127 pha seoloto x in 461 • phe noxazi ne syn tha se 418 phe noxym e th y l pen i cil l in 357 phe ny l aceti c acid 135 phe ny la ceti c aci d 474 phe ny la m i ne 135 phl eomy ci n 423
pho sp ho enol pyru vate 306 pho sph o g lu conate pat h w ay 509 pho sph o ryl chlorid e 318 pho sp ho tr a nsfe r ase 493 ph y to allexin 462 picr omy ci n 494 piko my ci n 433 pilot p la nt 334 pim aric i n 401, 437, 438 pla smi d 91 pla smi d- co ded enzym e s 94 pol ya c ryl a mi de 371 pol ya l anin e 275 pol ya m i no 366 pol ye n e 435 pol ye t h e r 398, 452 pol ye t h y le ne gly c o l 353, 365 pol yg ly c y l 366 pol ym yx in B 400 pol ym y xi n 420, 421 pol yo x in 398, 399, 447 pol yt yro sy l 366 pol yv i n y l alcohol 371 pre cip itat i on 217 pre cultu r e 185 pri m ary meta b oli tes 24 pri m er 98 pro g es te r one 478, 482 pro sta g l a nd in 489 pro te a se 333, 334, 352 pro to p l a st fus io n 30 pro vit am in A 388
pru my ci n 399 psi c o se 346 pter id i n e 379 pu llalan 466, 469 pul lulanase 336, 338, 344, 469 pur omy cin 75, 448 pyrr olnit rin 395 pytox ic comp o und 460 5'-ph o sph o rib o syl pyro p ho sph a te (PRPP) ami no tra nsfe r ase 322 5'-p ho sp ho rib o syl pyro p ho sph a te (PRPP) 311 Q qua y le cyc l e 510 que bemy ci n 402, 425 qui n o nes 397 R RNA 314 recog ni t ion sit e 94 recombin a ti on 78, 89 reg ios p ec if icit y 473 rennet 334 rennin 354, 356 rep li ca ti on 58 rep re ssor 64 resti ng cell 287 restr i c t i on endonuclease 94, 95 reverta n t 59, 62
rib o se-5 - p h o sph a te 310 rib o sta m y ci n gro up 428 rib o sta m y ci n 491 rifa m y ci n 397, 440 s D- so rbit ol 377, 489 1- so rbose 377, 489 saccharoge n i c 338 salicy l i c acid 474 sandw ich 기술 58 sclero 465 sclerogl u can 468, 469 screenin g 30 secondary meta b oli te 24, 25 seed cultu r e 184 selecti ve pre ssure 66 sequ e nti al fee dback contr o l 51 serin e tra nshyd r oxy m eth y l a se 510 sio m y ci n 400, 402 sis o my cin 431- 43 2 slop e leach ing 535 sod ium aspa r ta t e 업 4 sod ium glu ta m ate 霜 310 soli no my ci n 401, 452 soy meal 131 spe c if ic oxy ge n up tak e rate 190 sta p h y lo my ci n 75 sta t i on ary ph ase 24, 155 ste r eospe cificit y 473 ste r oid 478, 486
ste r ol 478 s ti ck y말단 95 sti gm aste r ol 486, 488 str a in desig n ati on 34 str e p tidi n e 427- 42 8 str e p tok in a se 334 str e p tom y ci n 21, 382, 397, 401, 426, ~27, 476 str e p tov aric i n 40C submerge d pro cesses 264 sulf at e waste 516 sulph it e meth o d 195 surfa c e anti ge n 91 psu-srif at oc es tep rr oo lc e4s8s6e, s 48286 3 T L-tr y p top h an 274, 275, 276, 284, 301 TCA 285 tab to x i ne 461 tal ap on 495 ter mi na l tra nsfe r ase 95 tet r a cy cl in e 396, 397, 401, 441, 442 tet r a ene 437 tet r a fu r an 452 tet r a hy dr op yran 452 tet r a nacti n 397, 399 tet r a py rr ole 383 tet r a te r pe n oid 389 thi a z oli dine -p- la cta m 357 thi e n amy cin 416
thi e n e 437 thi o c arbamate 497 thi o p e p tin 400, 401 thi o s tr e p ton 400, 401, 402 . thr eonin e 275, 284 tol erance tes t 42 tra ce elements 118 tra nseli m i na ti on 362 tra nsfe r schedule 35 tra nsfo r mati on 473 tra nsgl u cosid a se 470 tra nsgl y c o sy la ti on 425 tra nspe p tida se 404 tri a l ky l phl sp h ate 320 tri a m cin o lone 479 tri s p o ric acid 391 tro p ho p ha se 24, 128, 160 try p top h an 474 tum or ind ucti on 91 tw een 476 tylo sin 401, 402, 434 tyro cid i n 400, 421, 422 tyro sin e 276 tyro th r ic i n 400 2, 4, 5-tr i c h lorph enoxy aceti c aci d 497 u Unox sys t e m 526, 528 ul t ra filt ra ti on( 한의여과) 217 uronic aci d 465
5' -U MP 316 v valid a my ci n A 426, 427, 429 valin o my ci n 397, 399, 419, 417 vancomy ci n 397, 419, 423, 424 via b il ity tes t 36 vio m y ci n 399, 421 vir g ini a m y ci n 402 v1rg1 v ia m y ci n gro up 399, 419, 420, 424 volumetr i c tra nsfe r coeff ici e n t 194 w wheat glu t en 354 whey 354 x D- x y lo se- is o merase 346 xanth a n gum 24, 25 xanth a n 465 xanth o p h y ll 388 xanth y li c acid ( S' -XMP) 309, 313 xy la n 348 Y ye ast extr a ct 129 yea st mannan 139
배 무 동경대학교 대학원 미생물학 전공(박사) 한국 미생물학회 회장 역임 현재 이화여자대학교 생물과학과 교수 교육부 유전공학 연구 평가위원 저서 『 과학대사전 』 (식물편, 미생뭉의 세계 ) 『 미생물학 』 , 『 생명공학 용어집 』 (공동연구) 外 다수의 논문과 번역서가 있음 산업 U| 생물학 대우학술총서 • 자연과학 76 찍은날 19921d 1 월 1OOJ 펴낸날 1992 년 1 월 2OOJ 지은이 배 무 펴낸이 朴孟浩 펴낸곳 (주) 民音社 출판등록 1966. 5. 19 제 l-14t i. 우편대체번호 010041-3 1 --0 5 23282 은행지로번호 3007783 135-1 20 서울 강남구 신사동 506 강남출판문화센터 515-2003~5( 편집부) 515-2 0 00~2( 영업부) 515-2101, 2007( 팩시밀리 ) 값 20,00~ 」 © 배 무, 1992 萊변과학, 미생물 KDC/475 ISBN 89-374- 00 03-0 94500
대우학술총서 자연과학 | 소랍자와 게이지 48 리이만 기하학 박 을 용 상호작용 김진의 49 群표현론 박 승안 2 동력학특론 이병호 50 비선형 편미분 방정식론 3 질소고정 송승달 하기식 4 相轉移와 임계현상 김두철 51 생체막 김형만 5 촉 매 작용 진종식 52 수리분 류학 고철환 6 외스바우어 분광학 옥항남 53 찰스 다윈 정용재 7 극미량원소의 영양 승정자 54 금속부식 박용수 8 수소화 붕소와 55 양자광학 이 상수 유기 붕소화합물 윤능인 56 효소반응 속도론 서정헌 9 항생물질의 전합성 57 화성암 성인론 이민성 강석구 .58 확률론 구자홍 10 국소적 형 태의 Atiy a h- Sin g e r 59 분자 분광학 소현수 지표이론 지동표 60 벡터속 이론 양재현 11 Mucop ol y sacchar i des 의 61 곤충신경생리학 부경생 생화학 및 생물리학 박준우 62 에너지띠이론 모혜정 12 천체물리 학 홍승수 63 수학기초론 김상문 13 프로스타굴라딘 합성 김성각 64 신경과학 박찬웅 • 김승업 14 천연물화학 연구법 우원식 65 SCH 부호와 Reed- 15 脂防營養 김숙회 Solomon 부호 이만영 16 결정화 유리 김병호 66 양자전기역학 김영덕 17 고분자의 화학반응 조의환 67 군환론 박재결 18 과학혁명 김영식 68 대수기하학 조영현 19 한국지질론 장기홍 69 양자장이론 이재형 20 정보이론 한영열 70 해양오염과 생태계 21 원자핵반응론 정운혁 심재형 22 파괴역학 김상철 71 비기체 연소합성 (SHS) 23 분자궤도이론 이익춘 ~ 칠현 24 반응속도론 정경훈 72 크로마토그래피 이대운 25 미분위상수학 이현구 73 곤충의 사회행동 주종길 26 磁器共鳴방법 조성호 74 동위원소 지질학 김규한 27 플라스마 물리학과 핵융합 75 X 선 결정학 金 洋 최덕 인 76 산업미생물학 ·사 무 28 천문관측과 분석 이시우 乃 석탄에너지 변환기술 김상돈 30 해양微古生物學 백광호 31 편미분 방정식론 김종식 32 대통일이론 조광섭 33 금속전자계의 다체이론 김덕주 34 액정중합체 진정일 35 복합재료 권숙인 36 단백질 생합성 박인원 37 한국의 광물종 김수진 38 일반상대론 이철훈 39 레이저 광산란 분광학 김종진 40 복소다양체론 김상문 41 疾學的 연구방법 김일순 42 핵구조물리학 민동펄 43 후리에 해석과 의미분 작용소김도한 44 한국의 고생물 이하영 45 질량분석학 김명수 4476 생급체변에론너 박지대 현주 층노