
金洋 부산대학교 화학공학과 (공 학사 ) , 부산대학교 대학원 화학공학과 (공 학 석사 ) 미국 Univ e rsity of Hawaii 대학원 화학과 ( 이학 박사 ) 눌원 문화상, 부산시 문화상 및 대한화학회 학술 진보상을 수상 현재 부산대학교 자연대 화학과 교수 저서 『 현대생활과 화학 』 『 일반화학 실험 』 역서 『 물리화학 ( Cas t e ll a n ) 』 『 물리화학 ( Barrow ) 』 『 생명과학을위한 물리화학 (Barrow ) 』 『일반화학 (Br own 과 LeMa y ) 』 『 최신 일반화학 ( Ko t z 와 Purcell ) 』 논문 Selec ti ve Reducti on at the Sin g l e - C rys ta l Surfa c e of All Mobil e Catio n s in Zeolite A 외 다수
X- 선 결정학 
 x- 선 결정학
x- 선 결정학
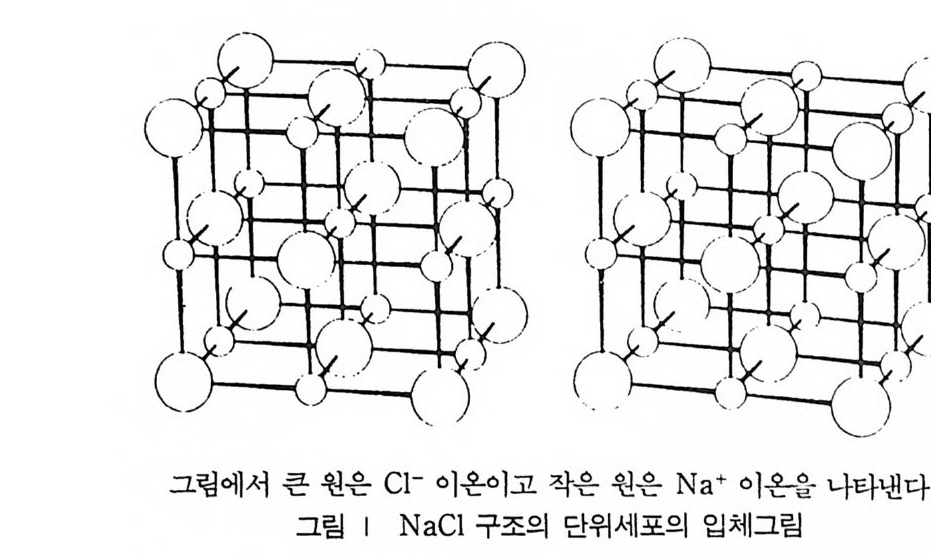
책 머리에 1912 년 독일의 물 리학자인 러우에 (Max von Laue) 는, 결정은 규칙적인 간격을 가지는 원자로 만들어져 있기 때문에 X- 선을 회 절할 수 있다고 제안한 후, 황산구리 결정과 사진 전판을 X_ 선이 지나가는 통로에 두어 사진 전판에 생기는 회절반점으로 결정에 의 한 X- 선의 회절현상을 실험적으로 증명할 수 있었다. 그 후 브래 그 (W. L. Bra gg)는 결정에 의한 X 선의 회절현상을 이용하여 간 단한 실험에 의해 NaCl 의 구조를 밝힐 수 있었고, NaCl 구조를 갖고 있는 KCl, KBr 과 KI 의 구조도 밝혔다. 이렇듯 간단한 구조 에서 시작하여 오늘날에는 고속 컴퓨터의 도움으로 복잡한 단백질 의 구조까지 X- 선 회절법을 이용하여 3 차원적 구조를 알아낼 수 있다. X 선 결정학은 결정학 그 자체가 하나의 훌륭한 학문 분야를 이 루어, 많은 사람들이 결정학을 연구하는 데 일생을 바쳤다. 그리하 여 X 선 회절과 결정학을 연구함으로써 노벨상을 받은 학자로도 물리학에서 1901 년에 빌헬름 뢴트겐 (W il helm C. Roentg e n), 1914 년에 막스 폰 라우에 (Max von Laue) , 1915 년에 브래그 경 부자 (Sir Wi lli a m H. Bragg 와 Wi lliam L. Brag g) , 193 저에 클 린돈 데이비슨 (C li n t on J. Dav i sson) 과 죠지 톰슨 경 (Sir George P. Thomson) 이 그리고 화학에서 피터 디바이 (Pe t er J. Deby e ), 1954 년에 라이너스 폴링 (Linu s C. Pauli ng ) , 1962 년에 막스 퍼루
츠 (Max F. Peru t z) 와 죤 켄드류(J ohn C. Kendrew), 1964 년에 도로시 크로풋 핫킨 (Doroth y Crawf oo t Hodg k in ) , 1976 년에 윌리 엄 립스콤 (Wi lliam N. Lips comb) , 1982 년에 아론 클 룩 (Aaron Klu g)이, 1985 년에 헐버트 하우프트만 (Herber t A. Hau pt man) 과 제롬 칼레 (Je rome Karle) 가 받았으며, 의학에서 1962 년에 제임스 왓슨(J ames D. Wat~ o n), 프란시스 크릭 (Franc i s H. C. Cr i ck) 과 와 모리스 윌킨스 (Mauric e H. F. Wi lk in s ) 가 있다. 또 결정학은 하나의 작은 학문적 도구로서 수학. 물 리학. 화학. 광물학, 생물학, 의학, 약학. 섬유학. 금속학 등 여러 분야에서 많 이 이용된다. 이 책의 목적은 X- 선 결정학에 관한 지식이 없는 독자에게 대칭 조작에서 시작하여 점군, 평면군, 공간군에 대해 소개하고 X - 선의 물리적 성질과 X- 선의 회절이론, X- 선 회절법으로 구조를 결정하 는 기본적 개념과 방법을 설명하며 아울러 X- 선 회절에 의한 화학 분석법을 소개하는 데 있다. 따라서 이 책은 대학 3, 4 학년이나 대학원 과정에서 화학, 물리학, 지질학, 금속학, 섬유학, 의학, 약 학 분야의 X- 선 결정학에 대한 기초적 교재로서도 사용할 수 있 을 것이다. 이 책을 펴내는 데 있어 원고의 교정과 타자 등 여러가지 면에서 도움을 준 부산대학교 화학과 물리화학 교실의 송승환, 이현도, 정 미숙, 고광락, 장세복 군과 나의 아내에게 깊은 사의를 표하며 또 재정적 지원을 해준 대우재단에 감사를 드린다. 1991 년 9 월 金 洋
X- 선 결정학
차례 책 머리에 5 제 1 장 결정의 기하학( I ) 1 서론 13 2 결정상태 15 3 결정축 15 4 Miller 지수 16 5 격자의 방향과 형 21 6 대칭요소 23 7 결정의 분류 27 8 결정계와 결정족 31 연습문제 33 제 2 장 결정의 기하학 (II) 1 서론 37 2 격자 37 3 격자의 선택 39 4 3 차원 격자 42 5 공간군 대칭 47 6 평면군 507 공간군의 유도와 명명법 56
연습문제 59제 3 장 결정구조 l 서론 61 2 금속의 구조 62 1) 면심 입방격자 구조 • 62 2) 체심 입방격자 구조 • 65 3) 육방 조밀쌓임 구조 (P63 / mmc) 67 3 다른 원소의 구조 69 1) 다이아몬드 (Fd3m) • 69 2) 흑연 (P63/ mmc) • 69 4 몇 가지 화합물의 구조 70 5 고용체 (solid solution ) 72 연습문제 74 제 4 장 X- 선의 성질 1 서론 77 2 전자파로서의 X- 선 78 3 X- 선의 발생과 연속 스펙트럼 80 4 특성 스펙트럼 83 5 X 선의 흡수 87 6 X- 선 필터 92 7 X- 선의 발생 94 1) 기체관 • 95 2) 필라멘트관 • 95 8 X- 선의 검출 991) 사전필름 • 99
2) 형광 스크린 • 100 3) 계수기 • 101 연습문제 101 제 5 장 회절( I ) 1 서론 103 2 Bragg의 법칙 104 3 역격자 (reciprocal lattice) 113 4 역격자와 X- 선 회절과의 관계 118 5 Laue 의 회절조건 119 6 X- 선 회절 실험장치 122 1) 분말법 • 122 2) 분말 회절장치 • 128 3) Laue 법 • 130 4) 움직이는 결정과 움직이는 필름법 • 131 5) Weissenberg 법 • 134 6) 4 축 단결정 회절장치 • 136 연습문제 138 제 6 장 회절 (II) 1 서론 141 2 전자에 의한 산란 142 3 원자에 의한 산란 145 4 단위세포에 의한 산란 151 5 이상적 결정에 의한 X- 선의 회절 157 6 회절강도의 표현 1631) Lorentz 인자 • 164
2) 결정에 의한 X- 선의 흡수 • 169 3) 온도 인자 • 172 4) 다중도 인자 • 175 7 적분강도의 표현식 176 연습문제 177 제 7 장 결정구조의 해석 1 서론 179 2 구조인자의 계산 180 3 공간군의 결정 188 4 회절의 대칭 188 5 Friedel 법칙 190 6 Fourier 방법 192 7 이상적 결정의 구조결정의 개요 196 8 이상분산과 그 영향 199 9 Patterson 함수 203 10 Harker 선과 면 209 11 중원자법 210 12 직접법 214 13 동형 치환법과 단백질 구조결정 226 14 이상분산과 원자의 절대배열 233 연습문제 242 제 8 장 시험구조의 정밀화 1 서론 245 2 Fourier 법 2453 최소자승법 249
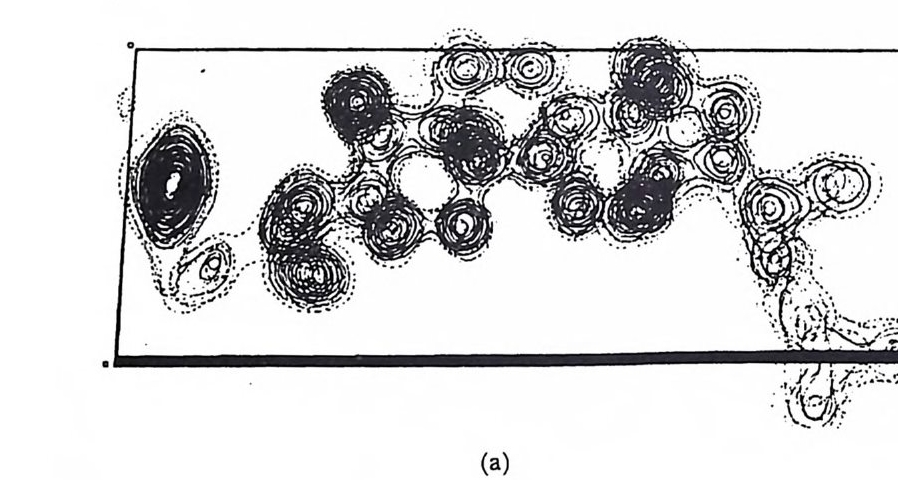
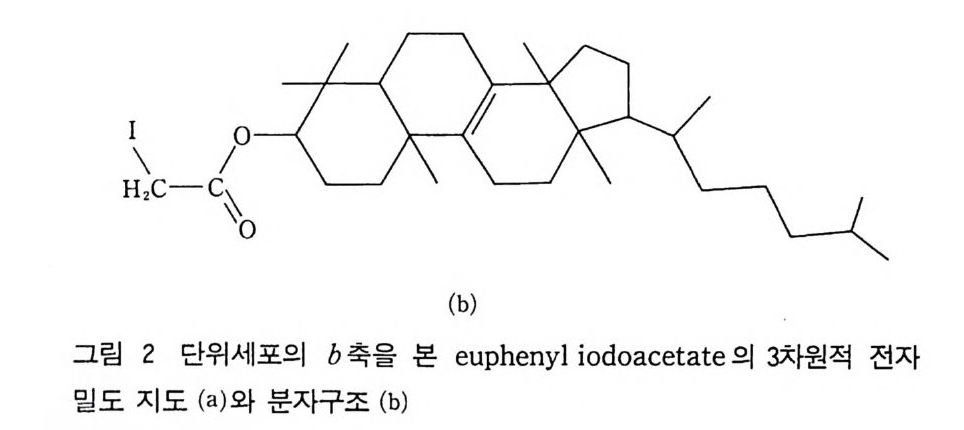
4 결정구조 해석의 개요 252 연습문제 254 제 9 장 X- 선 분말회절법에 의한 화학분석 1 서론 255 2 X - 선 회절패턴 256 3 분말 X - 선 회절무늬의 강도 계산 261 4 정성분석 265 1) Hanawalt 법 • 266 2) Fink 법 • 267 3) 정성분석 실험절차 • 267 4) 정성분석의 예 • 268 5 정량분석 273 1) 외부 표준법 • 275 2) 직접 비교법 • 276 3) 내부 표준법 • 281 연습문제 284 부록 1 물리적 상수와 환산 인자 289 2 결정구조 데이터 291 3 질량 흡수계수와 밀도 295 4 분말법에서 사용되는 다중도 인자 300 5 원자 및 이온의 X- 선 산란 인자 301 연습문제 해답 305 참고문헌 313 찾아보기 323제 1 장 결정의 기하학( I ) 1 서론 결정학은 천연에 존재하는 결정, 특히 광물결정을 알아내고 분 류하고 표기함으로써 광물학의 한 분야로서 시작하였다. x- 선 결 정학은 1912 년 결정에 의해 x- 선을 회철시킬 수 있음을 발견하여 시작된 비교적 새로운 학문의 한 분야이다. 그립 l 은 이와 같이 새로운 X 선 결정학적 방법으로 그 구조가 처음 결정된 결정 중 하나인 NaCl 결정구조의 3 차원적 그립을 보여주고 있다. 오늘날 에는 X- 선 회절법으로 결정의 내부 구조를 알아내고 공간에서 실 제 원자가 어떻게 배열되어 있는가를 알아낼 수 있다. 그립 2-(a) 는 eup h eny l iod oaceta t e (C32Hs3I0 2 ) 의 3 차원적 전자밀도의 등 고선 지도를 보여주고 있으며 이 구조에서 수소 원자는 X- 선에 의 한 산란력이 적어서 나타나 있지 않다. 전자밀도의 최대치를 가지 는 곳에 중심 원자를 두면 그림 2_(b 뫼- 같은 분자모델을 얻을 수 있다. 요요드 원자는 전자수가 가장 많아서 분자내의 타원자에 비 해 X- 선 산란력이 크고그림의 왼쪽끝에 윤곽선이 가장전한곳 에 표시할수 있다.
 •• )
•• )
탄소와 산소는 그림 오른쪽 측쇄를 제의하고는 대략 비 슷 한 윤곽 선 밀도로 표시된다. 이 오른쪽 끝의 원자들은 열전동이 크므로 전 자밀도가 뚜렷하지 못하고 분자내의 타원자에 비해 약하게 보인 다. 오늘날에는 단백질, 의약품, 금속합금, 광물, 핵산과 같은 더 복잡한 분자도 X- 선 결정학적 방법으로 연구하고 있다 .
 ....
....
 H\ 2c— c/\ 0'
H\ 2c— c/\ 0'
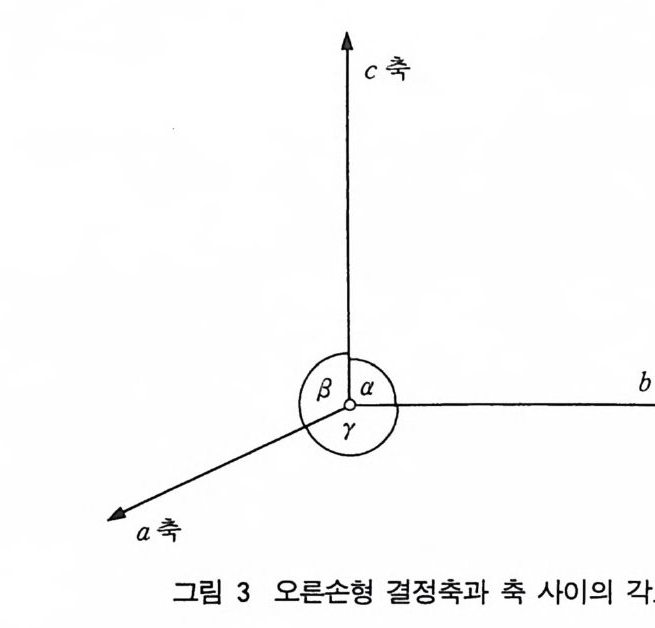
2 결정 상태 고체 물질의 대부분은 결정이다. 결정에서는 결정체를 구성하는 원자, 이온, 분자들이 규칙성을 가지고 주기적으로 배열하고 있 다. 이 규칙성은 당연히 의형을 반영하여 잘 발달된 결정에서는 광 택을 가전 평면으로 된 결정을 이룬다. 유리나 석영은 육안으로 비 슷하게 보이나 석영은 결정체이고 유리는 비결정체 혹은 무정형 물 질이다. 유리는 매우 짧은 거리에, 죽 2, 3 원자 단위에 걸쳐서만 규칙을 보이는 과냉각된 액체로 생각할 수 있다. 결정 (c ry s t al) 이 란 말은 얼음(i ce) 을 뜻하는 희랍어에서 유래한 말이며 석영을 나 타내는 말로 옛날부터 사용되어 왔다. 결정체 물질은 3 차원의 규 칙성과 평면으로 둘러싸여 있는 면을 가진다. 3 결정축 결결정정에서을 설주명요하 방기향 에위 해평서행는하 게3 개 의a, 표b,준 c축 을축 을택 하선택여한야다 .한다 .이 죽세 개의 축은 보통 서로 같은 평면에 있지 않다. 나중에 설명하겠지만
이 축의 방향은 결정의 대칭성과 긴밀한 관계가 있으며 어떤 경우 에는 축 사이의 각이 90°보 다 큰 사각 축 ( 斜 角軸 : obliq u e axis ) 을 택해야 한다. 그립 3 에서 +b 축과 +c 축은 종이 평면 안에 있고 a 축은 앞쪽으로 향하고 있다. a-b-c 쪽으로 돌면 오른쪽으로 도는나사운동이 된다. a 축과마주보는각을 a, 그리고 b 축, c 축과 마주보는 각을 각각 /3, r 로 택한다.
 C 국스
C 국스
4 Mi ller 지수 1~] 기 중엽, 결정의 연구에서 AbbeHaue y는 결정은 주기적 으로 반복되는 조그만한 블록 (block) 으로 이루어져 있다고 생각했 다. 이리하여 유리지수 (ra ti onal ind ice s), 죽 유리수 평면과 결정 축의 교점은 a/h, b/k, c/l 의 비로 표시할 수 있다(여기서 h,k, l 은 영을 포힘하는 정수이다). 이러한 생각은 19 세기에 둘어와서
W. H. Mi ll er 에 의하여 체계화되고 평면을 나타내는 세 개의 정 수에 그의 이름을 붙여 표시하였다. 결정축의 상대적 길이가 정해 지면 3 개의 M ill er 지수는 다음과 같이 정해진다. (1) 결정의 대칭성을 내포하는 3 개의 결정학적 표준축을 선택해 야 하며 3 개의 결정학적 축과 만나는 평면의 절편을 구한다. (2) 절편의 역수를 구한다. (3) 분수 값이 나오면 최소공배수를 곱해 정수화한다. 위의 절 차 를 설명하기 위하여 그림 4 와 같이 단면이 만나고 a 축과 평행인 평면을 생각하자. 그립의 A 평면은 원점에서 c 축으 로 1/ 2, b 축으로 2 의 거리에서 만난다. a 축과는 평행이므로 무 한대에서 a 축과 만난다고 할 수 있다. a b C 1 단계 oo 2 1/2 2 단계 1/o o 1/2 2 3 단계 。 1 4 따라서 이 평면의 지수는 (014) 이다. 비교하기 위하여 B 에 대 해 생각하면 디음 관계를 얻을 수 있다. a8 b11cll l1 1 단계 2 단계 00 3 단계 따라서 이 평면의 Mi ller 지수는 (Oll) 이다. 표준축을 택함에 있어 다음 사항을 알 수 있다. 첫째, 표준축은 결정의 대칭성에 따라 선택하므로 서로 칙각이.되지 않을 수 있다. 둘째, 세 축으로의 단위 길이도 일정하지 않다. 축과 단위 길이를 선택하는 일이 임의적인 것으로 생각되나 실제 여러 면(fa ce) 에
의미 있는 지수를 부여하려면 분명한 축이 선택된다. 평면의 지수 lz, k, l 은 항상 유리수이다. 이것은 유리지수의 법칙 (Law of Rati on al Ind i ces) 으로 알려져 있고 결정학에서 중요 한 법칙 중 하나이다. 실제로 결정면의 지수는 항상 정수이고 보통 존재하는 면은 작은 정수로 표시할 수 있다.
 c
c
평면 (hkl) 의 다른 의미는 a 축을 h 부분으로, b 축을 k 부분 으로, c 축을 l 부분으로 자르는 평면을 의미한다. 그러면 평면과 축과 실제 만나는 절편은 a/h, b/k, c/l 가 된다. 만약 평면이 축의 음의 방향을 지나면 이 축에 상당하는 지수는 음이고 Mi ller 지수의 숫자 위에 줄을 그어 표시한다. 두 지수의 부호가 서로 반대면 이 두 평면은 평행이고 원점에서 반대편에 놓여 있다. 예컨대 (210) 와 (2Io) 는 서로 반대편에 놓여 있다. (nh nk nl ) 평면은 (hkl) 평면과 평행이고 그 간격은 (hkl) 평면의 1/n 을 가진다. 같은 평면이 두 개의 다른 평면 모 임에 포함될 수도 있다. (210) 평면의 모임은 (420) 평면에 속할
수 있다. 죽 (210) 평면은 (420) 평면도 된다. 육방정계에서는 세 개의 대칭적으로 대등한 축 a 가 120° 떨어져 있다(육방정계에서 단위 세포는 두 축 a1 과 a2, 그리고 이것과 직각인 c 축으로 정해진다. 그림 5 참조). c 축으로 내려다보면 그림 5 와 같 이 된다. 대칭 때문에 이러한 평면이 6 개 있다. ° 육방정계의 평면의 지수는 특히 Mi ller -Bravais 지수라고 부른 다. 지수 i는 a3 축과 만나는 절편의 역수이고 (hk i l) 로 표시한 다. 그립 5 에서 A 평면은 c 축과 평행이고 a1 과는 一 1 이고, a2 와는 평행이며, a3 와는 +1 과 만난다. 따라서 이 평면의 육방정 계 지수는 (1010) 이다. a1 a2 a3 C 1 단계 -1 00 1 00 2 단계 —1 。 1 。 3 단계 필요없다
albl/ \\\ \ A\ /\/I / \/ / / 120 )-12-\ \ \ \ /\Ifa 2 \ \ 126 \ \ \ \ __. ____ 一_j I I I I a1 그림 5 육방정계에서 사용하는 M iller -Bravais 지수
a1 과 a2 가 만나는 평면의 절편은 a3 축과 만나는 철편으로 결정 하므로 i 값은 h 와 k 값의 함수로 표시할 수 있다. 죽 h+k=-i
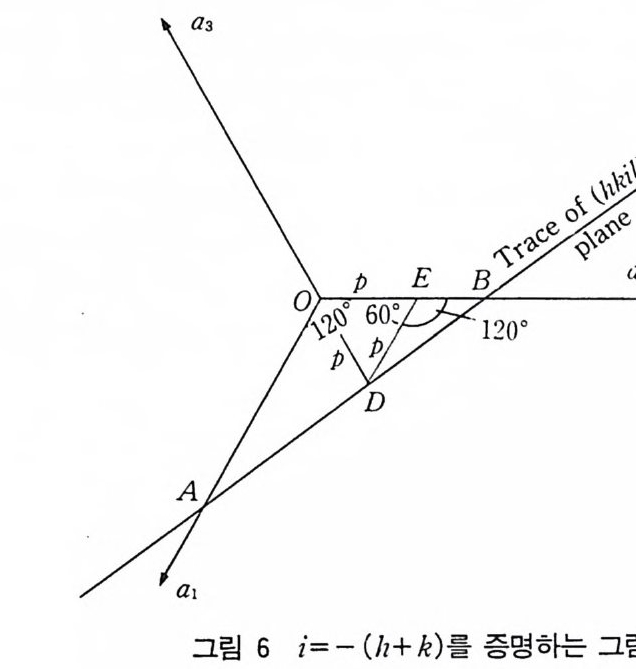
로 표시된다. 그립 6 을 이용하여 이 관계식을 증명할 수 있다.
 a3
a3
그림에서 Mi ller 지수의 정의로부터 OA=a/h OB=b/k (hk i l) 의 a3 축과 만나는 접은 D 이고 OD 의 길이는 p이다. DE 는 AO 와 평행이며, OD 는 각 AOB 를 이등분한다. LAOD=60° ODE 는 정삼각형이고, OD=OE=DE=P 삼각형 EBD 와 OBA 는 닮은 삼각형이다. 따라서
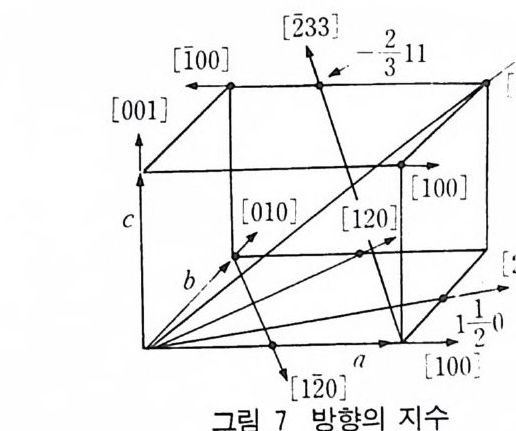
EB! E D= OBI O A= (bl k) I ( al h ) 그러나 EB=b/k — p (bl k -p) I P = (bl k) I ( al h ) 혹 은 p= ab/ (ak+ bh) 육방정계에서는 6 회 회전축을 가지고 있으며 따라서 a=b=u 이다. 또 , p =_ a / i이다. 그러므로 i =一 (h + k) 이다. 5 격자의 방향 (d ir ec ti on) 과 형 (型 : for m) 직선의 방향 (d i rec ti on) 은 원점을 지나고 그 직선과 평행인 선을 그려 나타낼 수 있다. 지금 직선이 단위세포의 원점을 지나고 좌표 u, v, w 울 지난다고 하자 ( u , v, w 는 정수이지 않아도 좋으며 이 선은 2u 2v 2w, 3u 3v 3w , ……도 지나간다). 이것을 큰 괄호 (squ are bracke t)로 표시하고 〔 uv i 파 를 이 직선의 방향이라고 한 다. uvw 의 값은 항상 최소공배수를 곱하여 작은 정수로 표시할 수 있다. 죽 [1/2 1/2 나 , 〔 11 인 [ 224 〕는 같은 방향으로 나타내며 [112] 가 가장 좋은 표시범이다. 대칭으로 관계지 어지는 방향들은 방향형 (dir e c tion of form ) 이라 부른다. 예컨대, 입방체의 4 개의 대각선 방향 [111]' 目 11], [ii l] 과 〔 111] 를 방향형 〈 111 〉로 표시할 수 있다. 또 단순 정방 격 지에서는 [10 0], 〔 Io 이 , [01 0], [01 이를 묶는 방향형 〈 100 〉와 [00 미 및 〔 oo IJ를 묶는 <00 1}. g.벡 터 길이가 다르므로 묶어서 같은 방향형으로 표시할 수 없다.
 [00 1 ] [i• o o ]A ' /r/1 l 1-..
[00 1 ] [i• o o ]A ' /r/1 l 1-..
 (a)
(a)
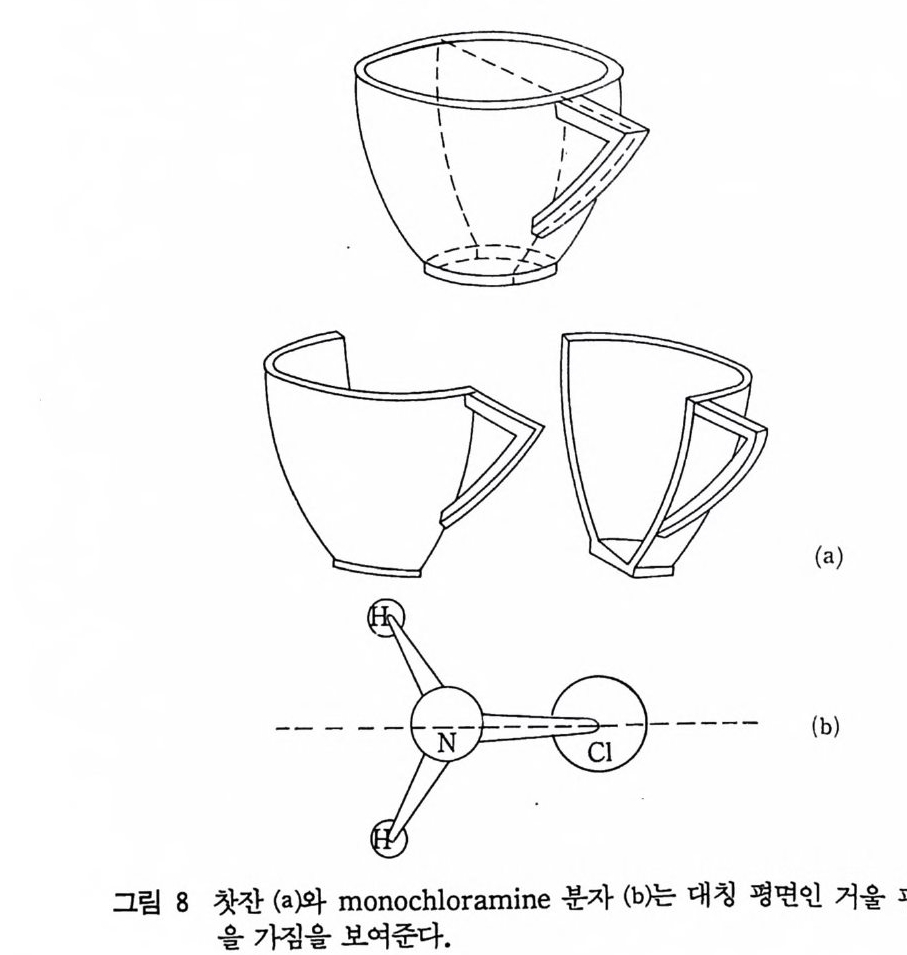
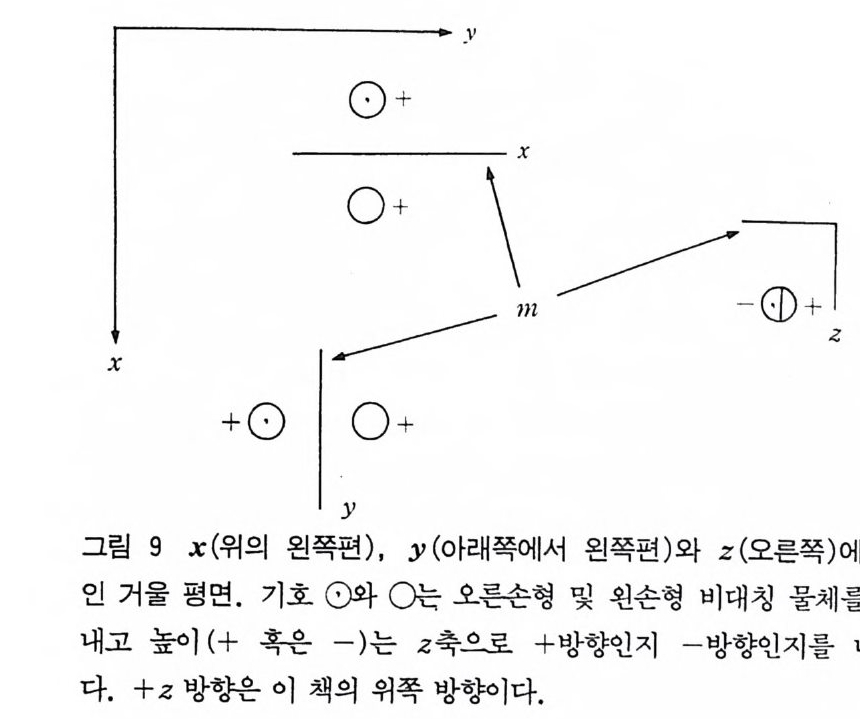
6 대칭 요소 물체 는 평면을 통하여 반사시키든지 (이 조작을 錦映〔 re fl ec ti o 미이 라고도 함), 어떤 축을 따라서 회전 (ro t a ti on) 하든지, 어떤 점을 통하여 반전 (i nvers i on) 하든지 혹은 이러한 조작 몇 개를 조합하여 처음 물 체와 구별할 수 없는 상태가 되면 그 물체는 조작전 물체와 조작후 물 체가 동위되었다고 하고 이러한 조작을 대칭 조작 (sym me tr y ope rati on ) 이라고 한다. 또, 물 체의 한 조각에 적절한 대칭 조작을 시켜 그 물체 전체를 만들 수 있다. 예컨대 그림 8- ( a 째서 찻잔의 손잡이를 지나고 반 울 쪼개는 것이 가능하다면 나머지 반조각은 다론 반조각의 거울상 (mi rr or im age ) 이 될 수 있다. Mo~ochlorami n e 분자 (그림 8- ( b ) )도 이런 종류의 대칭을 가지고 있다. 아러한 대칭평면을 거울평 면 (m i rror p lane) 이라 부르고 결정학에서 많이 사용하는 Hermann-Mau gui n 의 표기법으로는 거울평면을 m 으로 표기한다. 분광학에서 사용하는 오래된 표기법인 Schoenfl ies 표기법으로 는 주축 (Pr i n cip al ax i s) 에 대해 수평인지 수직인지 혹은 대각선 인지에 따라 이 거울평면을 h, V 혹은 d 로 표기한다 . 결정학에서는 관습적으로 x, y 및 z 축 방향으로 반복되는 단위 세포의 길이를 a, b, c 로 표기한다. 일반적으로 x 축, y축은 종 이 평면내에 두고 x 축의 +방향은 이 페이지의 아래쪽 방향이고 y축에 대해서는 수직일 필요는 없다. y축은 수평으로 오른쪽 이 +방향이다. z 의 +방향은 종이 위쪽 방향이고 x y평면에 대해 꼭 수칙일 핀요는 없다(그립 9). 비대칭적 단위의 표시에서 원내 쉼표( , )가 있으면 그 물 체의 거울상을 표시하고 이러한 표시는 오른손형 (r ig h t handed) 혹은 왼손형 (lef t handed) 물질을 표시 한다. 왼손형 단위와 오른손형 단위는 투사하면 서로 겹쳐질 수 있고 원
 -\'
-\'
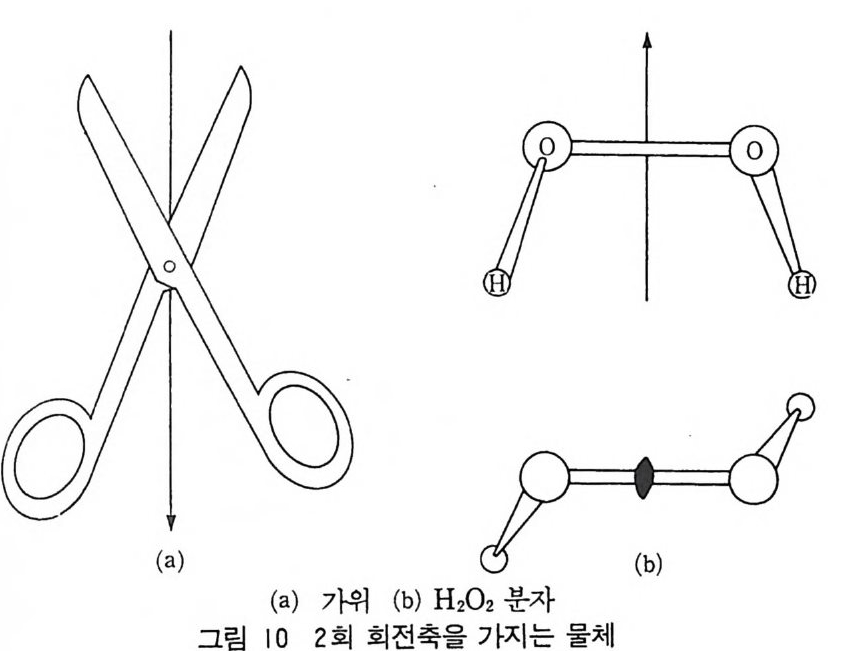
을 이등분하고 이등분한 한쪽편 단위에 쉼표를 써서 표 시한 다. 높이는 +나 _로 표시하여 이 책의 위쪽을 +z , 아래쪽 울 ― z 로 표시한다. 그림 10 의 가위는 2 회 회전축을 가지고 있으며 가위의 반쪽은 그림 10 의 선을 축으로 하고 180° 회전하면 다른 반쪽이 된다. 회 전 대칭을 가지는 물체는 혼하지 않다. 과산화수소는 2 회 회전축 울 가진다. 튜울립은 꽃의 줄기를 축으로 하여 3 회 회전축을 가진 다. 일반적으로 n 회 회전축을 가지는 물체는 축에 따라 360° 만큼 회전해도 그 물체는 동위가 된다. 죽 n 회 회전축을 가지는 물체는 n 번 회전시키면 본래의 위치로 돌아온다. 물체를 대칭축에 따라 완전히 회전시키는 과정중 n 위치가 동일한 모양을 가진다. 회전 축을 표시하는 기호는 완전히 회전하기 위해 반복해야 하는 수로 표시한다. 죽 Hermann-M aug u in 의 표기법으로는 1, 2, 3,
.••. •• 않 브로 표시하고 이에 대응하는 Schoenfl ies 표기법은 C1, c2 , C3 … … 요이다. 개개의 분자는 5 회 회전축 (5) 를 가질 수 있으나 장거리로 정렬하면 5 회 회전축의 대칭성을 가질 수 없다. 그립 11 은 이러한 것을 설명해 주고 있다.
 (a)
(a)
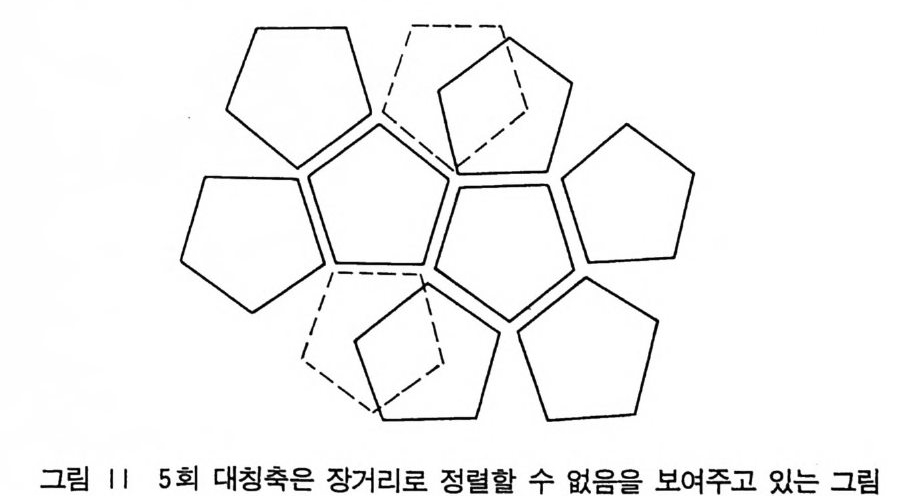 그림 | I 5 회 대칭축은 장거리로 정렬할 수 없음을 보여주고 있는 그림
그림 | I 5 회 대칭축은 장거리로 정렬할 수 없음을 보여주고 있는 그림
표 l 은 결정학에서 사용하는 Hermann- Ma ug u in 표기법 에 의 한 결정 표기법과 Schoenfl ies 표기법 및 결정학 에서 사용하는 기 호롤표시하였다.
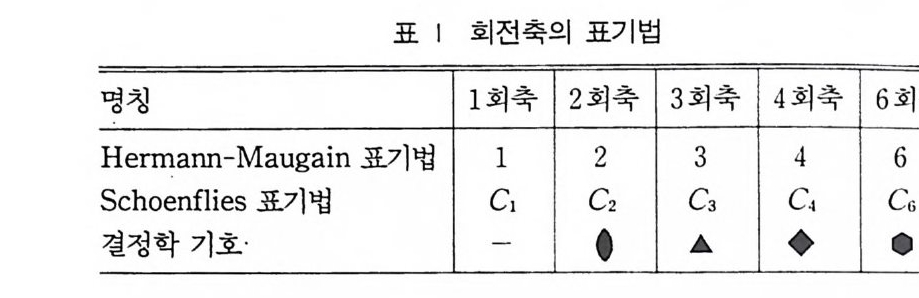 표 I 회전축의 표기법
표 I 회전축의 표기법
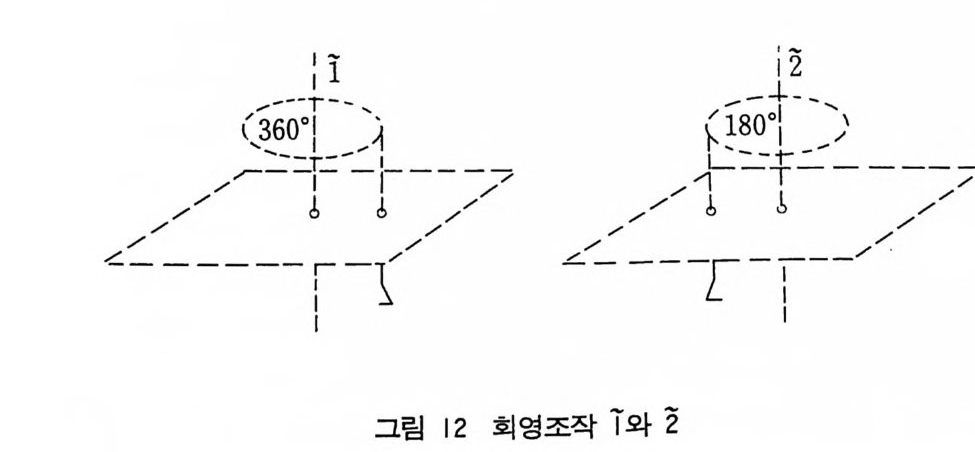
광의의 회전축(i m p ro p er rota t i on ax i s) 은 왼손형 물체 를 오른손 형 물체로 바꾸거나 오른손형 물체를 왼손형 물체로 바꾼다. 회전 조작과 경영 (j鄧央)조작이 합치면 이 합성조작을 회영 (roto r efl ec - ti on) 조작이라고 부르고 대응하는 회전조작 위에 tild e 를 붙여 I, 2, 3 등으로 표시한다• I 에 대해 설명하면 그림 12 와 같이 물체 (여기서는 7) 를 360° 회전하면 변하지 않고 제자리로 돌아오고 이 것을 다시 평면에 대해 거울상으로 구하면 된다. 따라서 I 조작은 평면을 통해 반사하는 것과 같은 조작이므로, 죽 거울상의 반사와
 < ___/_;(_:3-:6-_-0:-°.-! lTj.「 -l.- -~-`= : - 〈디_ ――一/_ 주- _/ _지ir 二-l_8--0-° I구!1'-f! 二~2- - _-` _>― , ,, .— —— 7
< ___/_;(_:3-:6-_-0:-°.-! lTj.「 -l.- -~-`= : - 〈디_ ――一/_ 주- _/ _지ir 二-l_8--0-° I구!1'-f! 二~2- - _-` _>― , ,, .— —— 7
같으므로 문자 m 으로 표시할 수 있다. 같은 방법으로 ? 조작은 180° 롤 회전한 후 거울상으로 구하면 되고 이는 그립 12 에서 알 수있다. 회전조작과 반전조작을 합한 대칭조작굴 회반 (ro t o i nvers i on) 조 작이라고 한다. 따라서 회반축은 두 조작의 합성조작이며 회전축 조작이나 반전조작은 아니다. 5 개의 결정학적으로 중요한 회반축 을 그립 14 의 아래쪽에 보여주고 있다. 회반축은 해당되는 회전축 위에 선 (bar) 을 그어 표시한다. 예컨대 3 회 회반축은 5 로 표시하 고 3- 바아(t hree bar) 라고 읽는다. 5 개의 회영축과 5 개의 회반축 울 비교하면, 표 2 와 갇이 몇가지 조작은 서로 같다. 표 2 에는 이 들 대등한 조작에서 관례로 결정학에서 사용하는 표기법을 나타내 고있다.
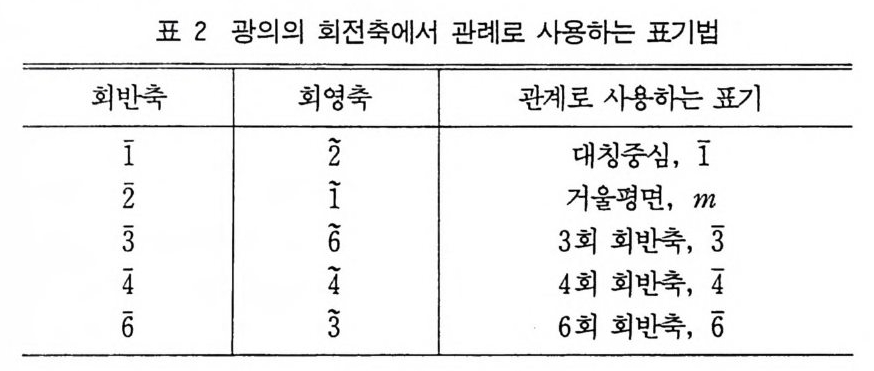 표 2 광의의 희전축에서 관례로 사용하는 표기법
표 2 광의의 희전축에서 관례로 사용하는 표기법
7 결정의 분류 결정의 의형은 그 대칭성을 나타낸다. 옛날의 결정학자는 자연 에 존재하는 결정, 특히 광물을 수집하여 그 형태를 연구 조사하여 결정이 가지는 대칭요소를 결정하였다. 더욱 더 많은 결정을 검토 함에 따라 의형은 달라도 이들 중 어떤 것은 서로 같은 대칭요소를 가짐을 알게 되고 동일한 결정족 (cry st a l class) 에 속하도록 분류할
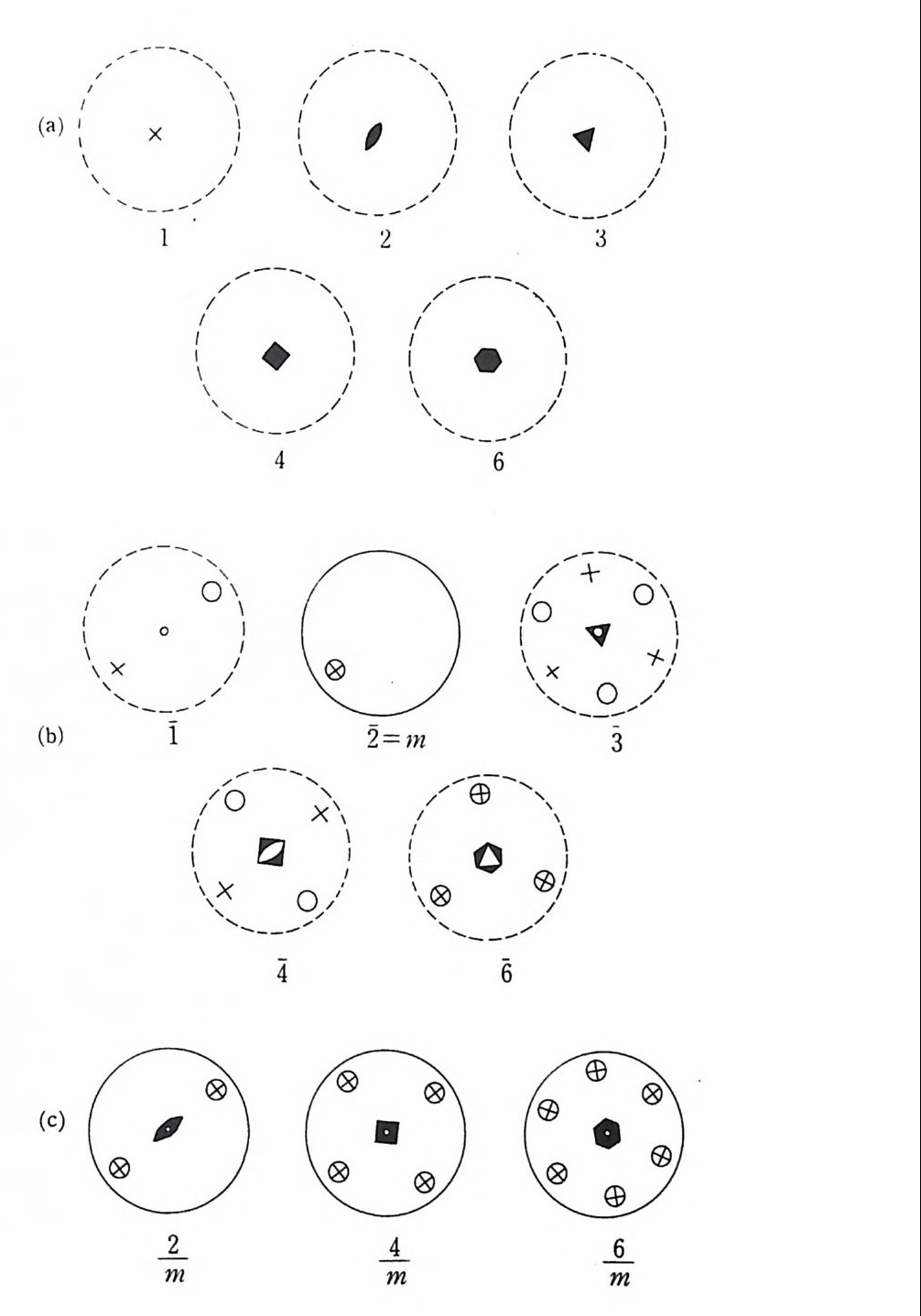
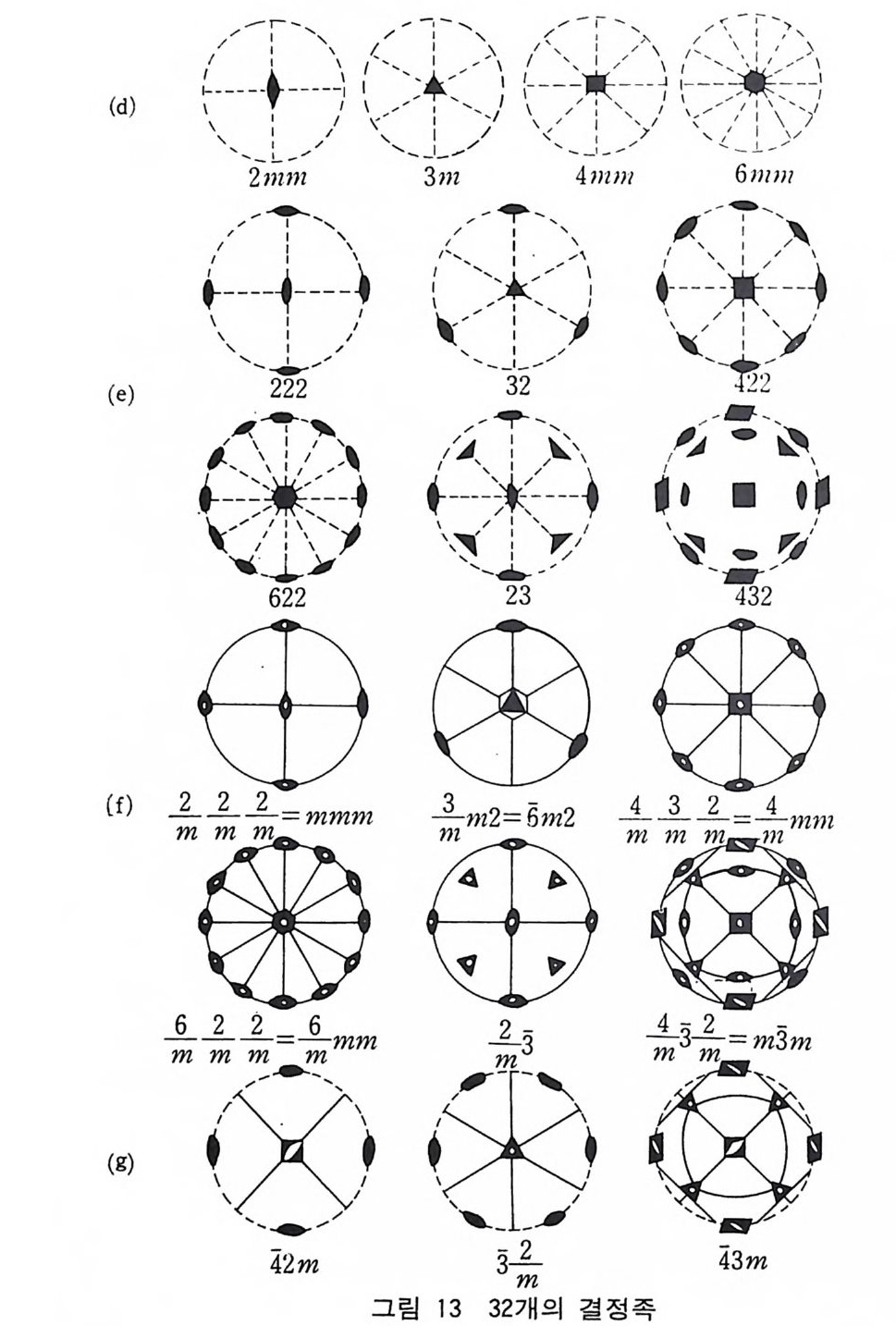
수 있었다. 또 이들 결정족 중 어떤 것은 어떤 대칭요소 를 공동으 로 가침을 알 수 있었고 이러한 결정족을 모아서 결정계 (crys t a l sys t e m ) 라 불렀다. 공간에서 임의의 점 주위로의 대칭은 점군(p o i n t g rou p)이라 부 르는 대칭요소의 모임으로 나타낼 수 있다. 결정에서는 전술한 다 섯 개의 회전 (pro p e r ro t a ti on) 축과 광의의 회전 (im p ro p e r rota - ti on) 축을 조합하여 구성된다. 이러한 가능한 모든 조합을 체계적 으로 얻으려면 먼저 각각의 5 개의 회전축(1, 2, 3, 4, 6) 과 5 개 의 회반축(i, 2, 5, i, 5) 이 점군을 이루며 이것 을 그림 13 - (a 퍼 } 13-(b 셰 나타내었다. 회전축의 직각 방향에 거울평면을 합치면 그 점군은 1/m, 2/m, 3/m, 4/m 및 6 /m 으로 써서 표시할 수 있 다. 이 조작을 행하면 이 중 1 /m=m= ?가 되고 3/m=6 이 되므 로 이것은 새로운 점군에 속하지 않는다. 따라서 이 조작으로 2/m , 4/m 및 6/m 만 새로운접군을만들어 준다. 2 개의 대칭조작 울 행하면 제 3 의 대칭조작이 생기는 수가 있다. 이 새로 생긴 대 칭조작, 죽 여기서 짝수의 회전축과 이 축에 수직되는 위치에 거울 평면을 합치면 대칭중심 (cente r of sym m etr y ) 이 생기고 이것을 대 칭 표시의 중앙에 흰점으로 표시하여 나타낸다(그립 13- (c ) ). 거울 평면을 회전축에 나란히 둘 수도 있다. 이 경우 생기는 제 3 의 대칭요소는 거울평면이고 이 거울평면도 회전축과 나란한 방 향에 있다. 이러한 조작으로 생기는 점군은 2mm, 3m, 4mm, 6mm 이다. lm=m 과 같으므로 새로운 점군을 만든다고 할 수 없 으므로 제외한다(그림 13-(d)). 점군 3m 는 3mm 으로 표시하지 않 는다. 이것은 대칭조직 3 이 m 과 결합하면 거울평면 사이의 각도 는 129°/2=60° 가 되고 이 각도는 거울평면 m 을 3 회 회전축으로 조작하면 생기고 이 평면을 2 개의 대칭조작에 의해 생기는 새로운 제 3 의 대칭원소인 평면이라 불 수 없으므로 3mm 으로는 표시하 지 않는다.
 (a) \I\ I \ / \ / `/ 一― _-X_ 一_ -`/` `/ '/ \ I\ I\, i \I\/ I\ / \-/- -_- _'-_ - ~,`,. ,\/ / \ I \I } I./ .\ /’ / \// `뺄}- `.l`l -\\/\ ` /.I 3_///l
(a) \I\ I \ / \ / `/ 一― _-X_ 一_ -`/` `/ '/ \ I\ I\, i \I\/ I\ / \-/- -_- _'-_ - ~,`,. ,\/ / \ I \I } I./ .\ /’ / \// `뺄}- `.l`l -\\/\ ` /.I 3_///l
 도I// - O「- -\---I I, I..` /\ /: *_/i`\/ '/ \I {I- / _( _ :二/ 東 二/ `> _-, 1 (_,〈 _`:조 :,* \ [:〈 二' -\ -\
도I// - O「- -\---I I, I..` /\ /: *_/i`\/ '/ \I {I- / _( _ :二/ 東 二/ `> _-, 1 (_,〈 _`:조 :,* \ [:〈 二' -\ -\
회전축둘을 서로 공동되는 점에서 직교시킴으로써 222, 32(2), 422, 622, 23, 432 의 6 개의 점군을 얻을 수 있다. 그림 13-(e) 점 군 32 는 322 로 표기하지 않는다. 이 이유는 2 개의 2 회 회전축은 60° 간격으로 서로 떨어져 있으나 이것은 2 회 회전축을 120° 회전 시켜 (3 회 회전조작) 얻는 것과 동일한 2 회 회전축이 되기 때문이 다. 이러한 점에서 422 조작과는 구별된다. 2 개의 2 회 회전축을 90° 회전시키면 (C4) 이들은 각각 45° 씩 떨어져 있고 상호 구별되 는 2 회 회전축이기 때문이다. 회전축 R(R=2, 3, 4 및 6) 과 2 회 회전축이 결합하고 2 회 회전 축 하나는 거울 평면에 나란히, 또 하나는 수직이 되도록 하면, 즉 두 개의 거울 평면 (m) 은 서로 직각이 되므로 2 회 회전축은 이들 평면의 교점상에 놓이게 된다. 그러면 6 개의 점군 _ml___ml__m2 _ ' ¾m2, ¾¾¾, 占겁¾, ¾3 및 占吐;이 생긴다. ~m m2 는 im上m로 표시하지 않는다(그림 13-(f) ). 이것은 3 회 회 전축과 나란한 거울평면이 2 회 회전축과는 수직이 아니기 때문이다. 회반축 5 와 4 를 회전축과 결합시키면 42m, 3 으m_ 및 43m 을 얻 을 수 있고 (그림 13- (g )) 이들 점군으로써 결정족 (cr y s t al class) 에 속하는 3 양 R 의 점군을모두만들수있다(그림 13). 8 결정계와 결정족 결정을 회전축과 반전축을 중심으로 분류할 수 있다. 결정은 표 3 과 같이 특성적 대칭요소를 기준으로 하여 일곱 가지의 계로 나 눌 수 있다. 특성적 대칭요소는 결정을 분류하는 데 그 계가 갖추 는 최소의 대칭요소이다. 따라서 주어진 결정은 그 계의 특성적 대
칭요소 이상의 대칭요소를 가질 수도 있다. 결정의 접군(결정족)도 결정계와 함께 표 3 에 나타내었다. 대칭요소는 단위세포의 모양을 결정하므로 32 개의 결정족은 일 곱 개의 결정계로 분류할 수 있다. 만약 결정이 대칭을 갖지 않거 나(점군 1) 대칭중심만 갖고 있으면 단위세포는 어떠한 모양도 가 질 수 있다. 세 각도 (a, /3, r) 도 제한이 없다. 이때 이 결정계는 삼사(t r i cl i n ic) 정계이다. 단사정계 결정은 한쪽 방향에는 2 회 회전축을 가전다 (2, 111(= 2) 및 2/m. 여기서 2/m 의 뜻은 2 회 회전축과 이것의 수직방향에 거울 평면이 있다는 뜻이다). 하나의 결정학적 축은 2 회 회전축과 평행
 표 3 결정계와 최저 대칭요소 및 결정족
표 3 결정계와 최저 대칭요소 및 결정족
인 방향으로 취하고 나머지 두 개의 축은 2 와 수직 방향에 있다. 단사정계의 단위세포는 두 개의 직각을 가지는 평행육면체가 되고
또 다른 하나의 각도는 명시되어야 한다. 2 회 회전축보다 더 큰 대칭성을 가지면 단위세포의 모양에 더욱 더 큰 영향을 준다. 삼방정계, 정방정계, 육방정계는 각각 하나의 3 회 회전축, 4 회 회전축, 6 회 회전축을 가진다. 이들 대칭축은 결정학적인 축에 평행으로 되게 잡고 이것은 c 축으로 취한다. 나 머지 두 개의 축은 c 축에 수직이고 서로 같다. 접군의 기호는 특 성적인 c 축 (un iq ue axis ) 성질을 먼저 나타내고 거울평면은 이 축 과 수직이 되도록 /m 으로 나타낸다. 하나 혹은 그 이상의 기호를 그 다음에 표기하기도 하며 특성적인 c 축과 수직이 되는 다른 방 향에서의 대칭성을 나타낸다. 예컨대 42m 은 4 회 회반축과 4 회 회반축에 수칙 방향에는 2 회 회전축이 있고 2 회 회전축 사이의 각 을 거울평면 (m) 이 2 등분한다. 가장 대칭성이 큰 것은 입방정계이나 3 개의 결정학적 축은 서로 직교하며 대등 (e q u i valen t)하다. 단위세포내 몸체 대각선 방향으 로 제 2 의 3 회 회전축이 있다. 점군의 표시는 먼저 결정학적 축의 대칭성을 표시하고 그 다음에는 필수적인 3 회 회전축을 쓰고 마지 막으로 단위세포의 면 대각선에 평행되는 방향의 대칭성을 적어 표 시한다. 표 3 은 결정계와 결정족과 특성적인 최저 대칭요소를 표 시하고 있다. 단사정계에 있어서는 다른 결정계와 달리 결정학적 특성적인 축을 b 축으로 잡는다. 이것은 역사적인 이유 때문에 이 렇게 정한다. 즉 특성적인 축의 대칭성이 2 회 회전축보다 큰 회전 축을 가지면 모두 c 축을 특성적인 축으로 정한다. 연습문제 L 교점이 다음과 같은 평면의 Mi ller 지수를 구하라. (a) a, -b /2, lie. (b) 2a, b/3, c/2.
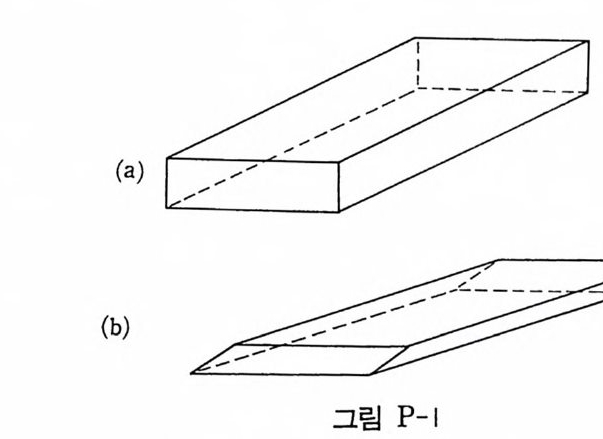
((ce)) IIl laa,, l-ib ,b -/4,c .c /3. ((df)) -a, a—/4b,, b3/c 2/, 4 —. c/ 3 . 2. 성냥각을 취하고 다음 경우를 생각하여 답하라. (a) 라벨을 무시하면 어떤 접군에 속하느냐? (그림 P1- a ) (b) 대각선 방향으로 납작하게 만들면 (그립 P 1-b ) 어떤 점군에 속하느냐?
 (a)
(a)
3. 아래 그립 (P-2) 을 면밀히 조사한 후 존재하는 대칭요소를 모두 나열하라. 올바른 결정족과 결정계를 써라.
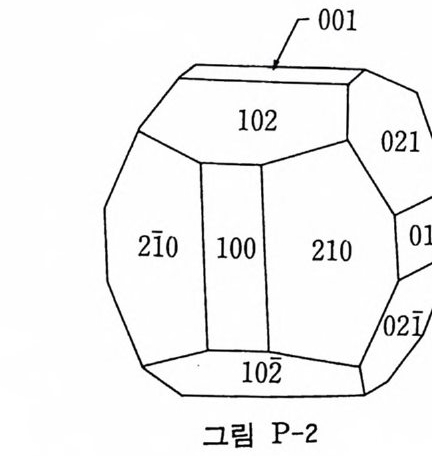 그림 P-2
그림 P-2
4. 육방 프리즘에서 축을 명시한 후, 다음 평면과 방향을 표시하 라. (1210) , (1012) , (1011) , 〔 11 이 , [111 ] , [021] 5. 본문의 그립 14 와 같이 5 회 회반축 (5) 과 8 회 회반축 (8) 의 조 작을그려라. 6. 2 와 2 와 90 으로 서로 놓이면 이 합성조작은 어떤 점군이 생기 게 하느냐? 7. 입방정계 단위세포에서 방향 [111], [10 이, 〔 11 이, [122] 를 그 려라.
제 2 장 결정의 기하학 (II) 1 서론 이 장에서는 결정 물질의 내부 구조를 연구하여 결정의 기하학에 대해 생각하고자 한다. 결정은 3 차원에서 주기적 특성을 가지고 있다. 원자 모임은 대칭조작을 반복하여 결정을 만들 수 있고 공간 군의 대칭성을 이룬다. 공간군의 패턴은 그 간단한 형으로 결정학 적 점군대칭을 가지는 무늬 (mo ti O 를 격자 이동시켜 얻을 수 있다. 2 격자 모든 결정은 기하학적 기본으로 격자를 가전다. 격자는 모든 점 이 다른 점과 같은 주위환경을 가지는 규칙적으로 무한히 많이 정 렬된 점으로 되어 있다. 이러한 표현은 1 차원, 2 차원, 3 차원 공 간에서 모두 적용된다. 격자는 3 개의 기본되는 반복단위, 죽 평행 이동 벡터 a, b 및 c 로 표현할 수 있다. 격자내의 어떤 접을 원점 으로 선택하고 다른 점까지의 벡터 r 은 디음 식으로 나타낼 수 있다; r=ua+vb+wc (2-1) 여기서 u, v, w 는 양수, 음수 혹은 영이고 격자점의 좌표를 나
타낸다. 그림 1-(a) 에서 점을 b 만큼 계속 이동시키면 반복되는 무한대의 직선형의 점의 열을 만들 수 있다. 이러한 점의 이동 b 와 다른 방 향으로의 평행이동 a 와 결합하면 그림 1-(b) 와 같은 2 차원 격자, 혹은 평면격자를 얻을 수 있다. 이 2 차원 격자를 그물이라 부른 다. 그립 1 에서 선을 그린 것은 편리상 격자점을 쉽게 알게 하기 위한것이다.
 • • b .. • • • • • - )'축
• • b .. • • • • • - )'축
그물은 대칭성을 보여준다. 격자를 대표하여 나타내 주는 부분이 단위세포(unit cell) 이고 벡터 a 와 b 로 나타낼 수 있다. 이러한 단 위세포를 나란히 무한하게 많이 쌓으면 그물이 된다. 단위세포가 a f b 이고 r=90° 이면 각 격자점의 대칭은 2mm 이 다. 이러한그물은 칙사각형 격자 (rec t an gu lar la tti ~e) 에속한다(그림 2). 그립 3 의 그림은 a f b 이고 r t 120° 이다. 이러한 그물은 사방형 (obli qu e) 그물인 것 같으나 주의 깊게 관찰하면 각 점은 2 mm 대 칭성을 가진다. 따라서 이 그물도직사각형 격자로 분류할 수 있다. 그리고 단위세포당 하나의 격자접을 포함하면 이러한 세포를 단순
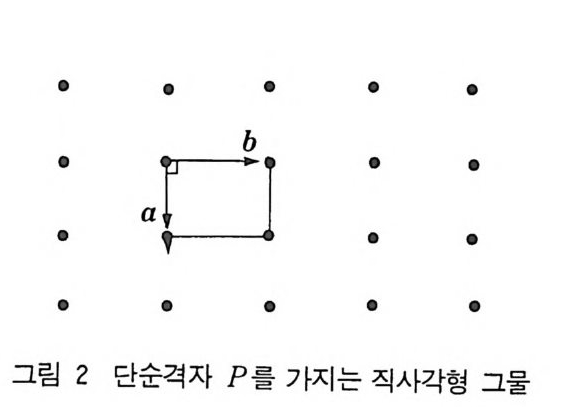 • • • • •
• • • • •
세포(p r i m iti ve cell) 라 부른다. 단위세포내의 각 격자점은 이웃하 는 단위세포 4 개와 공유하고 있다. 그림 3 에서 백터 a 와 b 를 선택하면 저면심 격자 (base cente r ed unit cell) 를 가질 수 있다. 이러한 단위격자는 단위세포당 2 개의 격자점을가진다. 평면 격자에 제 3 의 평행이동 벡터 c 를 결합하면 공간격자, 죽 3 차원 격자의 열을 만들 수 있다. 3 차원 격자에 대해서는 이 장에 서 다시 자세히 디루겠다.
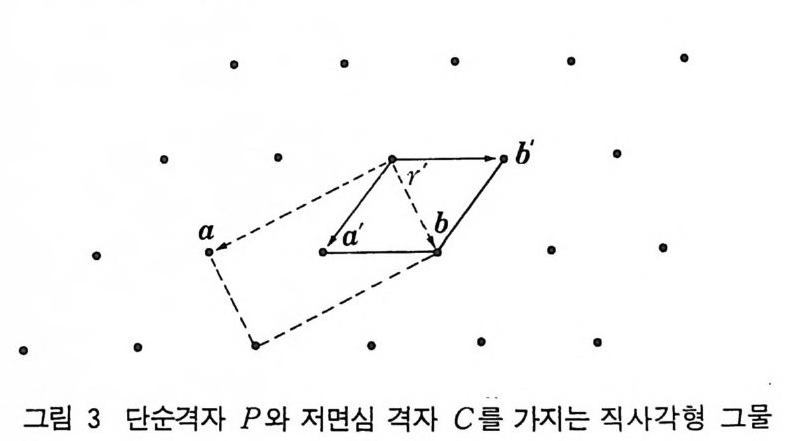 • • • • •
• • • • •
3 격자의 선택 2 개의 나란하지 않은 평행이동은 평면격자를 만들고 3 개의 나란
하지 않는 평행이동은 공간격지를· 만든다. 평면격자에서는 평행하 지 않는 벡터 2 개를 어떻게 선택해야 하는가, 공간격지에서는 어 떤 3 개의 나란하지 않는 벡터를 선택해야 하는지가 문제가 된다. 실제 이러한 평행이동 벡터를 선택하는 방법은 무한히 많고 임의적 이다. 그림 4 는 평면격자를 보여주고 있고 몇 가지 다른 종류의 단위세포를 선택한 것을 보여주고 있다. t1, & 혹은 t3, {4 와 이동 벡터쌍을 선택하면 단순격자가 된다. 왜냐하면 이 경우에는 전술한 바와 같이 각각의 단위세포에는 하나의 격자점이 포함되기 때문이 다. 그러나 t5 와 氐료 단위세포를 정의하면 각각의 모서리에 공유함 으로써 포함되는 하나의 격자점 이의에 세포 중앙에 하나의 격자점 이 포함되고 이 경우 복합세포 (mul tip le cell) 라고 부른다. 이러한 종류의 세포는 여러 가지가 있는데 단위세포당 포함되는 격자점이 2 개이면 이중세포 (double cell) 이고, 3 개이면 삼중세포(t r ip le cell) 라고부른다.
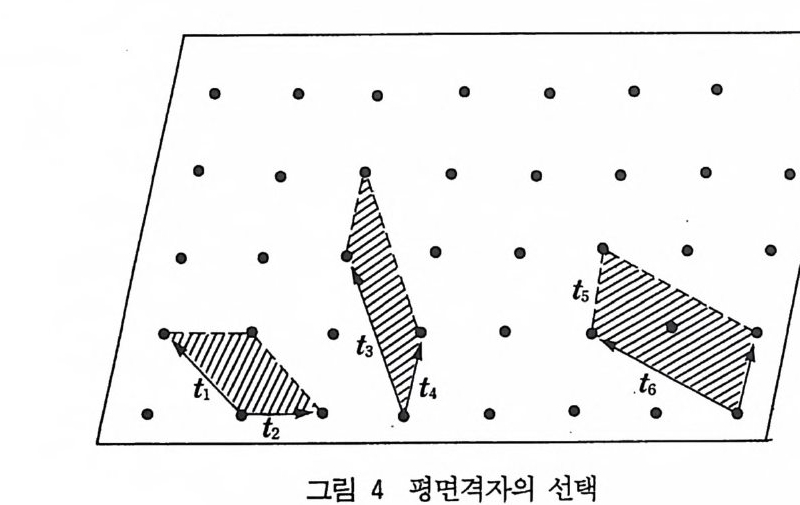 • • • • • • •
• • • • • • •
단순세포나 복합세포가 격자의 단위세포로 선택할 수 있다. 단위 세포라고 부르는 것은 전체 격자를 축의 길이를 이용하여 단위세포
를 반복함으로써 모두 얻을 수 있기 때문이다. 그러나 단위세포를 선택하는 데는 국제적으로 결정학에서 구하는 관습이 있다. 되도록 이면 가장 적은 반복단위를 선택해야 한다. 즉 복합세포보다 단순 세포를 선택해야 하고 축으로 서용하는 벡터는 격자내의 중요한 대 칭방향과 나란하거나 혹은 일치하도록 정한다. 그리고 축 사이의 각 도는 가능하면 g o o 에 가까운 각도가 되도록 택한다. 그림 3 의 단위세포의 선택에서는 단순세포는 격자의 대칭성을 명확히 나타 내지 않으나 이중세포인 중심을 가진 세포는 벡터 a 와 b 는 그물 에서 거울대칭 ( m) 을 가지므로 이중세포를 택하는 것이 좋다. 표 1 은 이차원 격지 를 요약한 것이다.
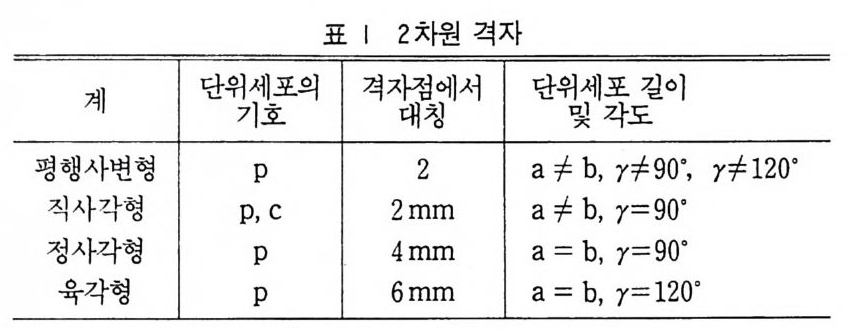 표 I 2 차원 격자
표 I 2 차원 격자
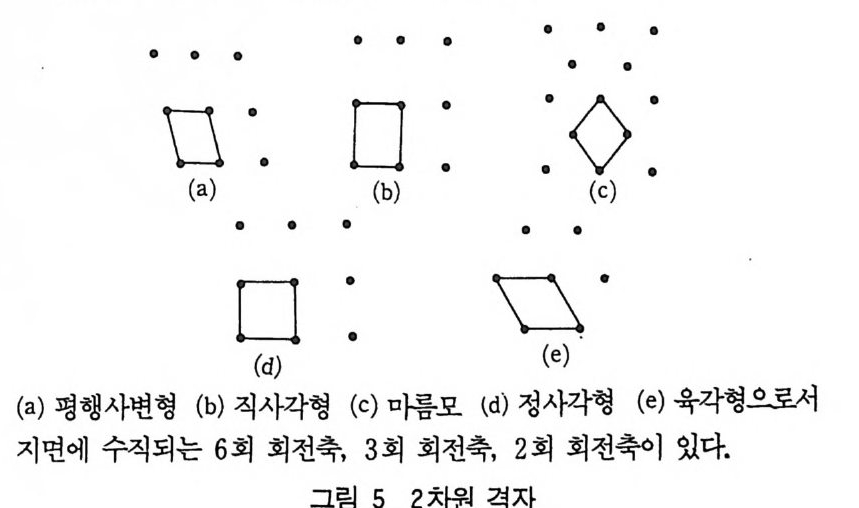
이것을 그림으로 나타내면 그림 5 와 같다.
 • •®巳 ••□ •• • •:• □ ® • •• •D • •• ••. • •◊2 • •• •
• •®巳 ••□ •• • •:• □ ® • •• •D • •• ••. • •◊2 • •• •
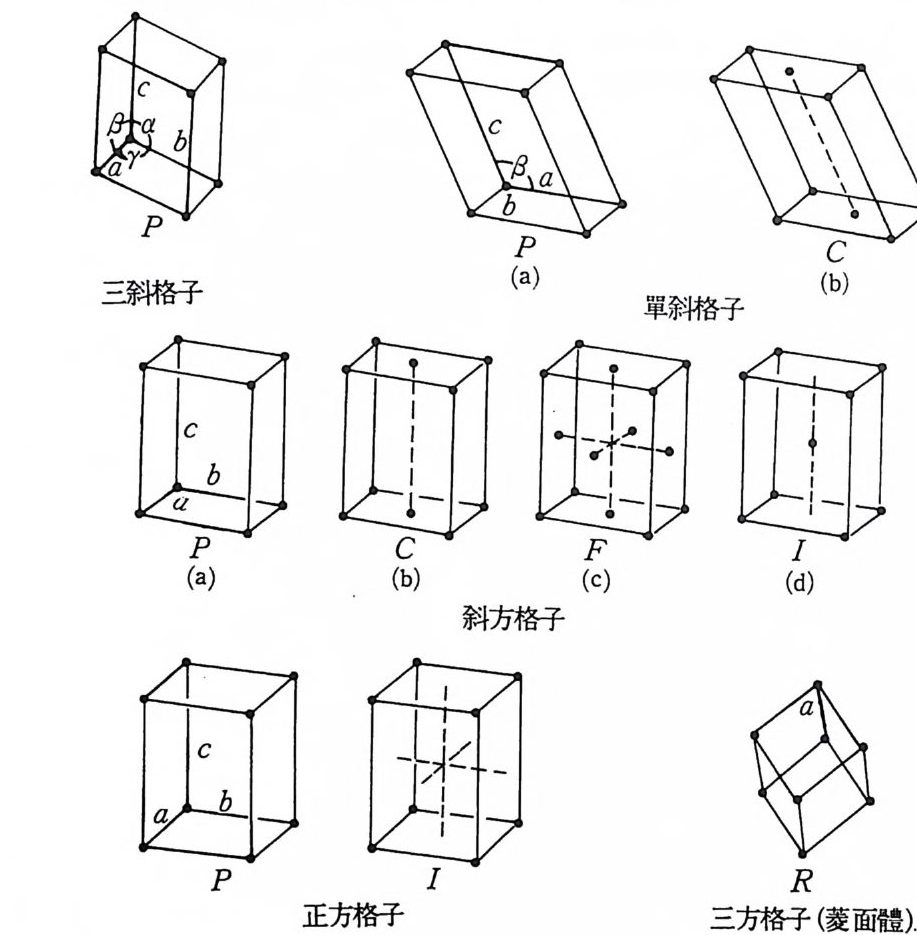
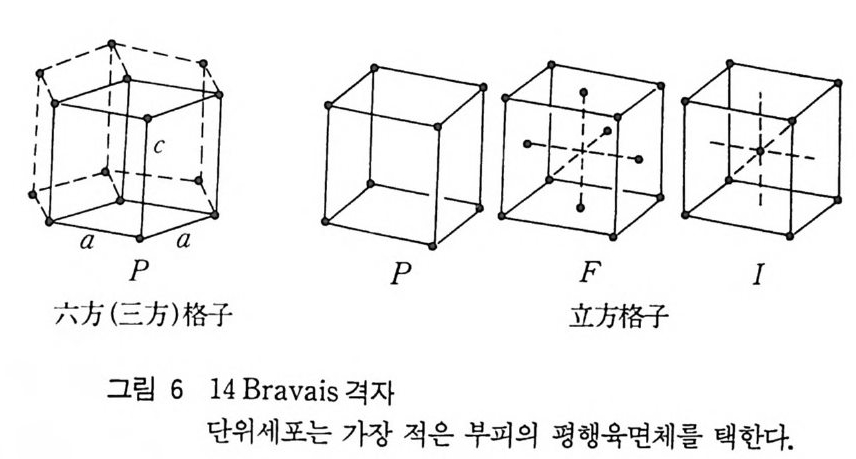
4 3 차원 격자 3 차원 격자 혹은 Bravais 격자는 그물을 규칙적으로 쌓아 생긴 다. 7 가지 결정계에는 그림 6 에서와 같이 14 가지 방법이 있다. 각 격자는 동일 평면에 있지 않는 3 개의 벡터 a, b, C 에 의해 결 정되는 단위세포로 표시되고 관습에 따라서 이들 벡터는 가장 작은 부피가 되는 평행사변형으로서 격자내의 중요한 대칭방향과 일치 하도록 하는 단위세포를 선택한다. 3 차원에서 단위세포로서 가질 수 있는 형과 그 명명법은 표 2 에 나타내었다.
 책셔 單斜 格 子
책셔 單斜 格 子
 _,.../i\———
_,.../i\———
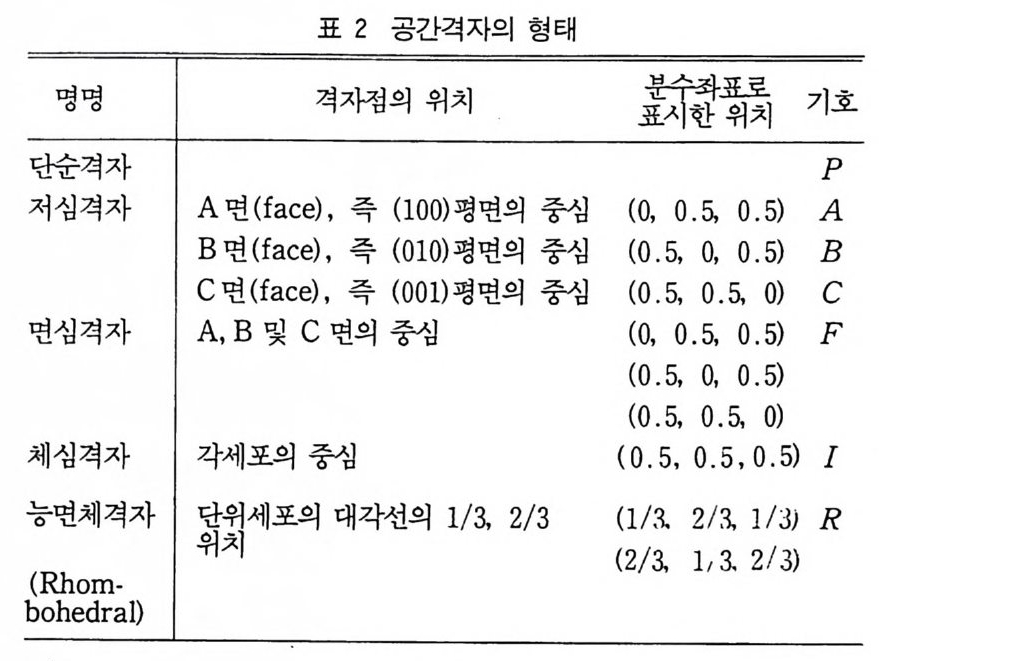 표 2 공간격자의 형태
표 2 공간격자의 형태
삼사(三斜)격자 회전축도 없고 거울평면도 없다. 그러나 대칭중심 (i)는 있을 수 있다. a=/=b=/=c 이고 a=/= /3=I= r =I= 90°( 혹은 120°) 인 단위세포는 단순 세포 (P) , 죽 단위세포 부피당 하나의 격자점이 된다.
단사격자 단사격자는 y축 (b 축)에 나란한 방향에 2 혹은 2 가 있다. 관습 적 단위세포는 a-f -b i- c 이고 a= r= 90°, /3# 90, 120° 이다. 그립 7 은 단사격자의 입체그림이고 8 개의 단위격자를 그림에서 보여주 고 있으며 관습에 따라 /3 *90° 이다. 단사격자는 Bravais 단위세 포형으로 P 와 C 가 있다. A 면에 중심을 둔 단위세포는 C 면 중심 단사정계 단위세포와 같다. 이는 b 축의 선택은 대칭에 의해 결정되지만 a 축과 c 축은 서로 교환이 가능하기 때문이다.
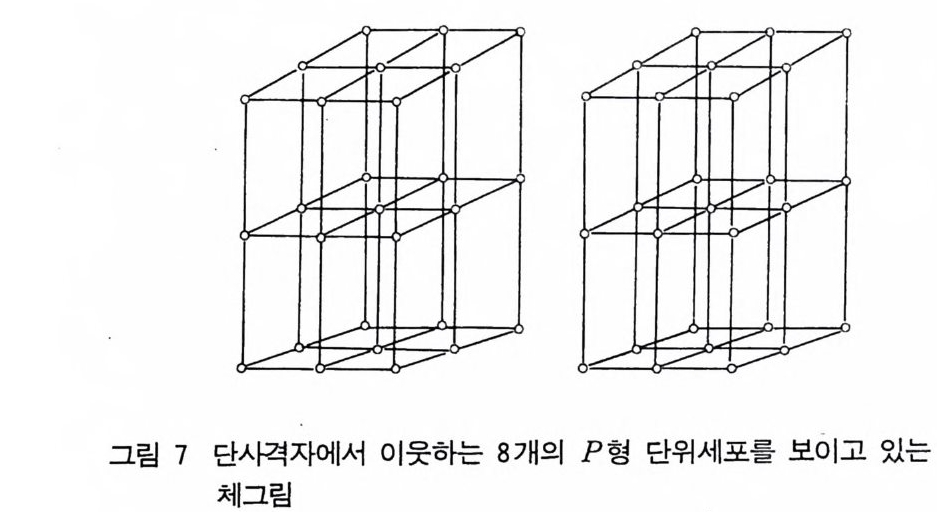 그림 7 단사격자에서 이웃하는 8 개의 P 형 단위세포를 보이고 있는 입
그림 7 단사격자에서 이웃하는 8 개의 P 형 단위세포를 보이고 있는 입
B 면 중심 단사정계는 있을 수 없다. B 면 중심으로 선택을 하 면 그 크기가 1/2 이 되는 단순 단사정계가 생기기 때문이다(그립 8) . 이 경우 새로운 단순 단사정계 (P 형)의 단위세포 상수는 (a', !J' 및 c') 다 음과 같다. a'= a, b'= b, c'= a/2+ c/2 /3가 둔각이 아니면 c'=-a/2+c/2 로 대등한 변화를 시키면
/3 ' 는 둔각이 된다(그립 8). c' 은 ab 평면에 놓이고 a= r'=90° 이고 /3= 120° 이다. 비슷한 방법으로 I= F= C 가 됨을 그림 9 와 10 에 서 알수있다.
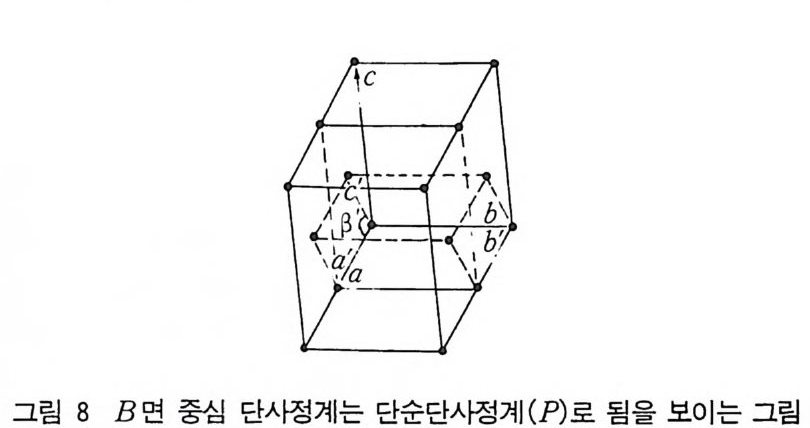 그림 8 B 면 중심 단사정계는 단순단人陸계 (P) 로 됨을 보이는 그림
그림 8 B 면 중심 단사정계는 단순단人陸계 (P) 로 됨을 보이는 그림
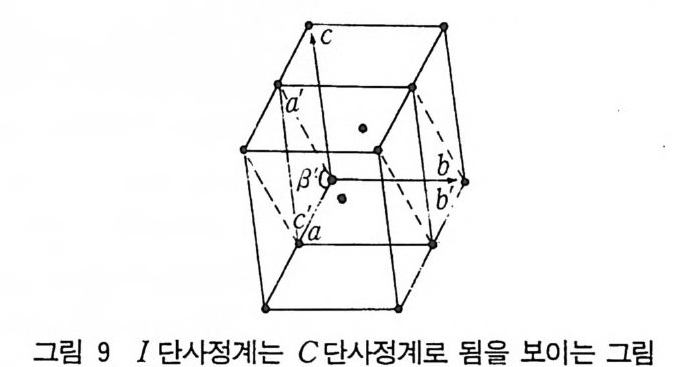 그림 9 I 단사정계는 C 단사정계로 됨을 보이는 그림
그림 9 I 단사정계는 C 단사정계로 됨을 보이는 그림
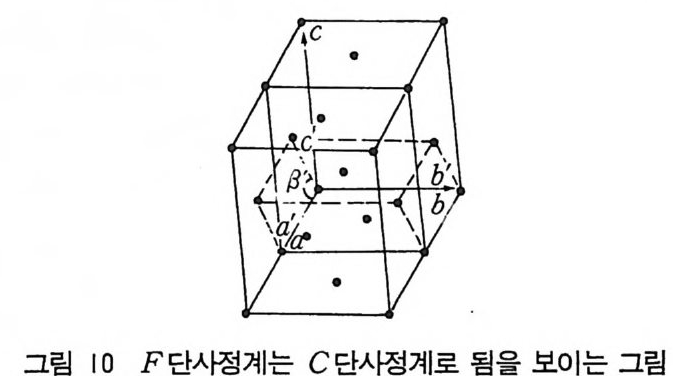 그림 10 F 단사정계는 C 단사정계로 됨을 보이는 그림
그림 10 F 단사정계는 C 단사정계로 됨을 보이는 그림
人提방격자 단사정계의 Bravais 격자에 대하여 자세히 기술하였으므로 다른 격자계에 대해서는 어떻게 하여 이러한 Bravais 격자만 허용되는 지 설명할 필요가 없을 것이다. 사방격자는 서로 수직이 되는 2 회 회전축 (2 혹은 ?)을 세 개 가지는 특성이 있고 단위세포 벡터는 이 러한 대칭축에 일치하도록 나란하게 택한다. 사방격자에서는 a= I b =l c 이고 a= /3= r=90° 이어야 한다. 사방격자에서논 P, C, I, F Bravais 격자계만 허용된다. 이때 다음 사항을· 유의해야 한다. (1) 선택한 Bravais 격자는 올바른 격자인가 ? (2) 대칭의 변화는 없는가? (3) , 대칭의 변화가 있다면 새로운 격자를 나타내는 단위세포는 올 바르게 선택했는가? 정방정계 정방정계에 있어서는 z 축에 따라서 4 나 4 가 있는 특성이 있다. 단위세포싱수는 a=b=/=c 이고 a= /3= r=90° 이다. P 와 1 계가 허 용되고 C 와 F 는 각각 P 와 I로 바뀐다. 그립 11 은 C 중심 정방 정계 격자는 구 크기가 1/2 이 되는 단순 P 정방정계 격자로 전환 됨을보여준다.
 a)--a
a)--a
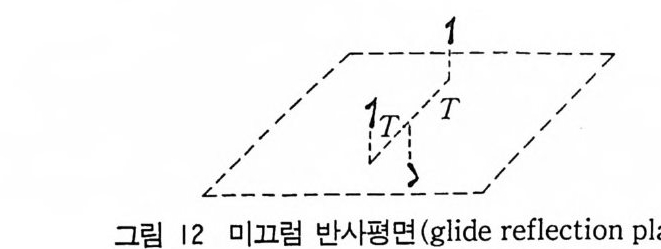
입방정겨 I 입방정계 대칭은 입방체의 중심을 지나는 네 개의 대각선 방향, 즉 <11 1> 방 향으로 각각 하나의 3 회 회전축(혹은 3) 이 있는 특성이 있다. 또 방향족 〈 100 〉 로는 2 회 회전축이 있으며 Bravais 격자 종 류로는 P, I 및 F 가 있다. 육방정계와삼방정계 육방정계에서는 격자의 c 축을 따라서 6 회 회전축이 있으며 격 자심냐는 a= b -/=c, a=/ 3=9 0°, r=120° 이나 단순격자만 있다. 삼방정계 격자에서는 Bravais 격자로 단순 P 격자와 능면체 R 이 있다. 삼방정계 격자상수는 능면체에서는 a=b=c 이고 a= /3=y #90 ° 이다. 그러나 단순 삼방정계에서는 a=b-/=c, a=/3 = 90°, r= 120° 이다. 5 공간군 대칭 제 1 장에서 두 개의 대칭요소가 결합하면 새로운 대칭요소가 생 기는 것을 설명하였다. 이제 하나의 대칭요소와 두 개의 병진(竝 進)운동이 결합하면 평면군(다음 절에 이에 대해 설명하겠다)에서 새 로운 대칭요소를 준다. 이 새로운 대칭요소가 나선축 (screw axis ) 과 미끄럼 반사평면(映進面 : glide refl ec ti on p lane) 이다. 거울반사와 병전운동을 혼성 결합하면 미끄럼 반사(gli de re fl ec ti on) 가 생기는데, 이는 아래 그립 (그립 12) 을 보면 쉽게 알 수 있다. 그림에서 7 자를 격자축에 따라 1/2 만큼 병전운동한 후 거울상 반사를 한다. 만약 a 축을 따라서 미끄럼 운동을 하고 송 a 또병 이동한 후 거울상 반사를 하는 것은 a 영전면이다. 영진 면의 종류와 조작을 표 3 에 나타내었다. 이와 비슷하게 대각선 방
 /----- 1广 __ ----7
/----- 1广 __ ----7
 표 3 가능한 영진면
표 3 가능한 영진면
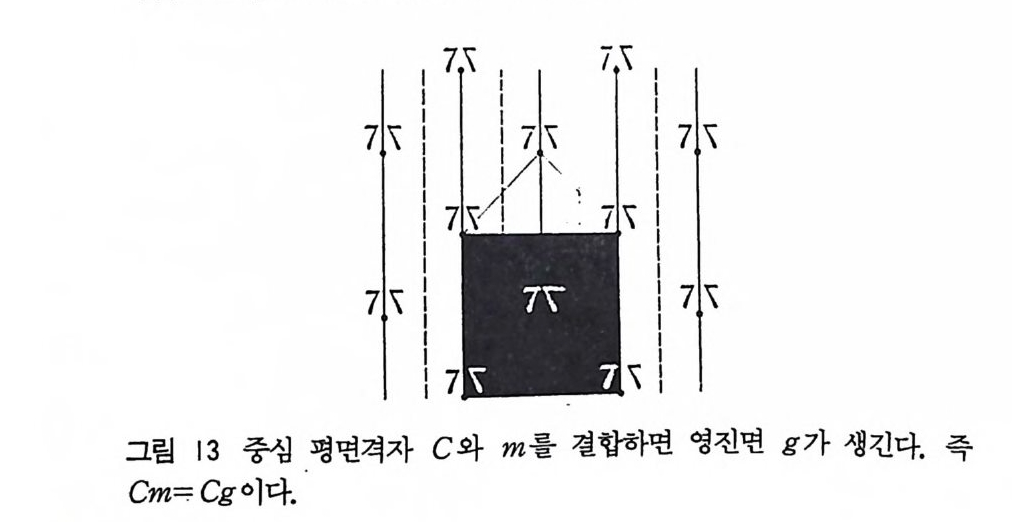
향의 영진은 T=l/2a+1/2b 혹은 1/2b+1/2c 등으로 이동하고 거울상 반사를 하면 된다. 단위세포 중심에 격자접을 가지고 또 거 울평면(기호는 m 이고 그림에서 실선 -으로 표시)이 있으면 미끄럼 반사 대칭요소가 생긴다(기호는 g이고 그림에서 기호는 _ _이다). 이것은 그림 13 을 보면 쉽게 알 수 있다.
 -' \ILIIIIII`I T`
-' \ILIIIIII`I T`
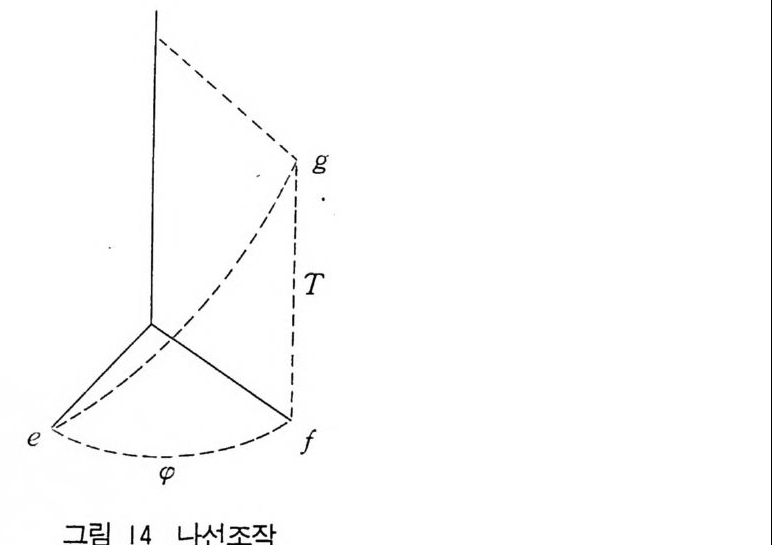
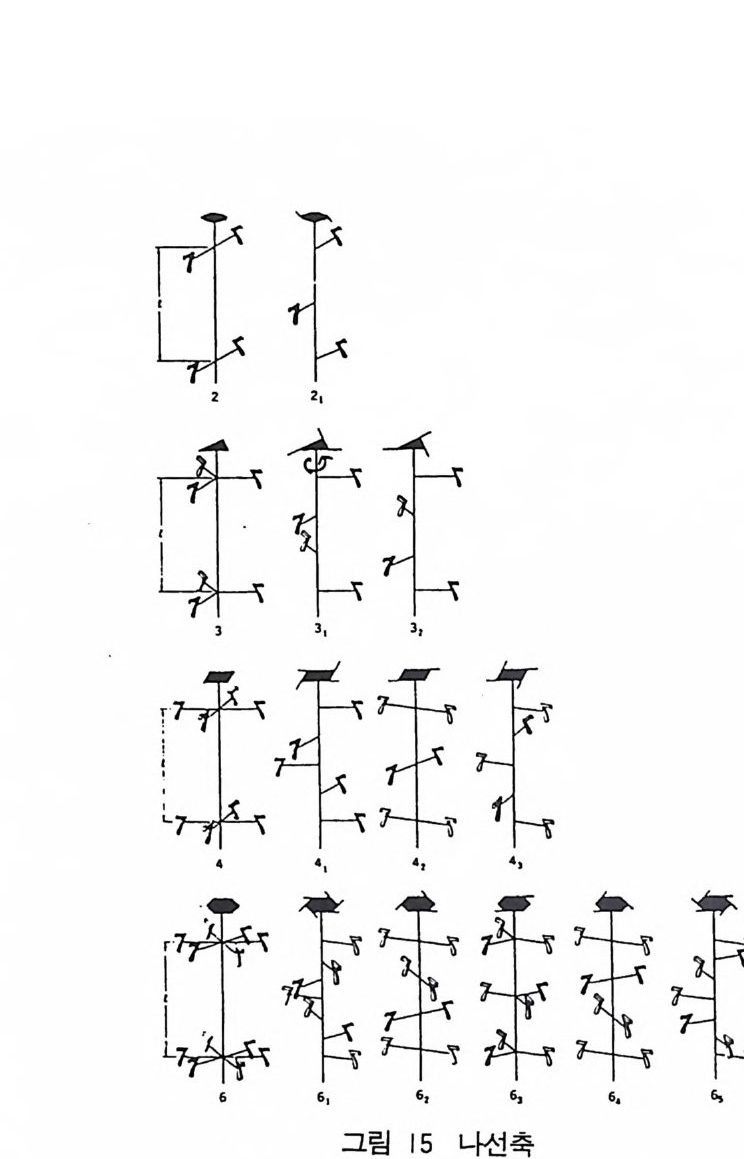
회전축과 병전조직을 합하면 나선축이 된다. 그림 14 에서 e 의 7 자를 각도 ¢만큼 회전하면 f의 7 이 되고 다시 병진운동 T 에
 \\ /
\\ /
f의f 의 f의 7 에서 g의 7 로 이동하였다. 결국 나선운동에 의하여 e 의 7 에서 g의 7 로 이동한 것이다. 이때 회전축은 격자의 병전운 동하는 방향과 나란하다. 각도 이만큼 n 회 회전 후 나선축을 따라 T 만큼 병진 이동한다. 일반적으로 나선축은 nm(n>m) 로 표시한 다. 이것은 축 주위로 360°/n 회전하고 축을 따라서 m i n 만큼 병 진이동한다는 뜻이다. 그림 15 에서 11 개의 나선축을 보이고 있고 결과로 생기는 물체 (여기에서는 7) 의 모양을 보이고 있다. 그림에서 알 수 있는 바와 같이 31 과 32, 41 과 43, 62 와 64, 61 과 6s 는 동일하다. 나선운동의 방향만 다르다. 따라서 이들 쌍은 거울상체 (enanti om orph ) 이고 각각의 축은 우선성 축 혹은 좌선성 축으로 구별할 수 있다(관습적으로 오른손형 축〔rig h t -handed axis ] 은 나선 운동이 축을 따라 위로 볼 때·시계방향으로 운동하는 축이다). 32 개의 점군에 공간격자와 영진면 및 나선축을
 : rd
: rd
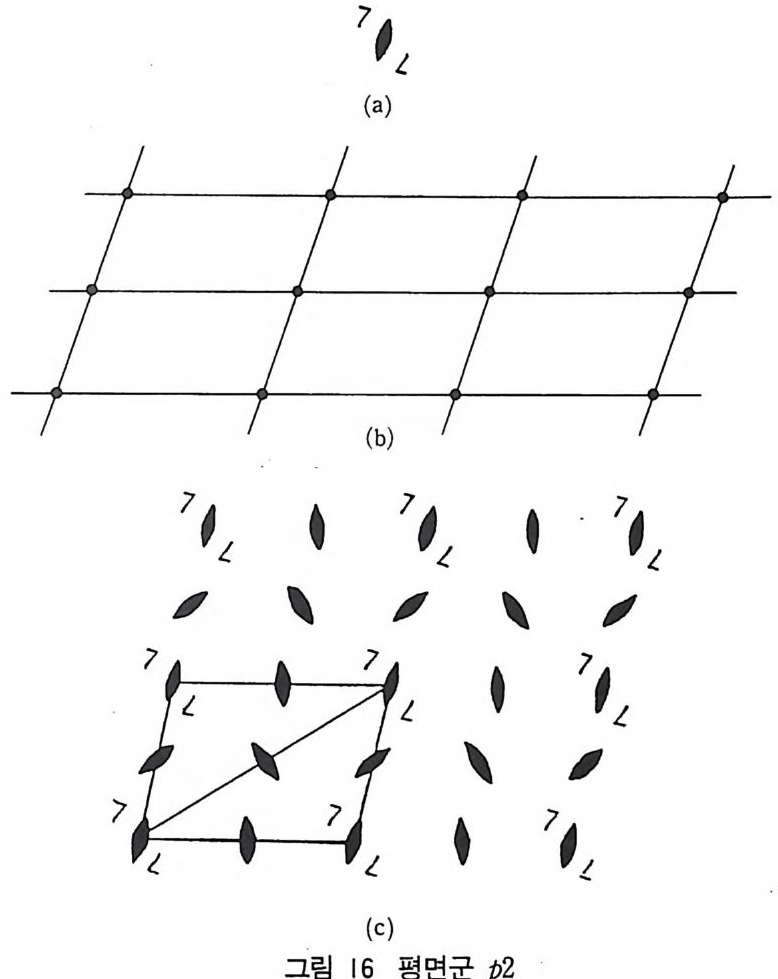
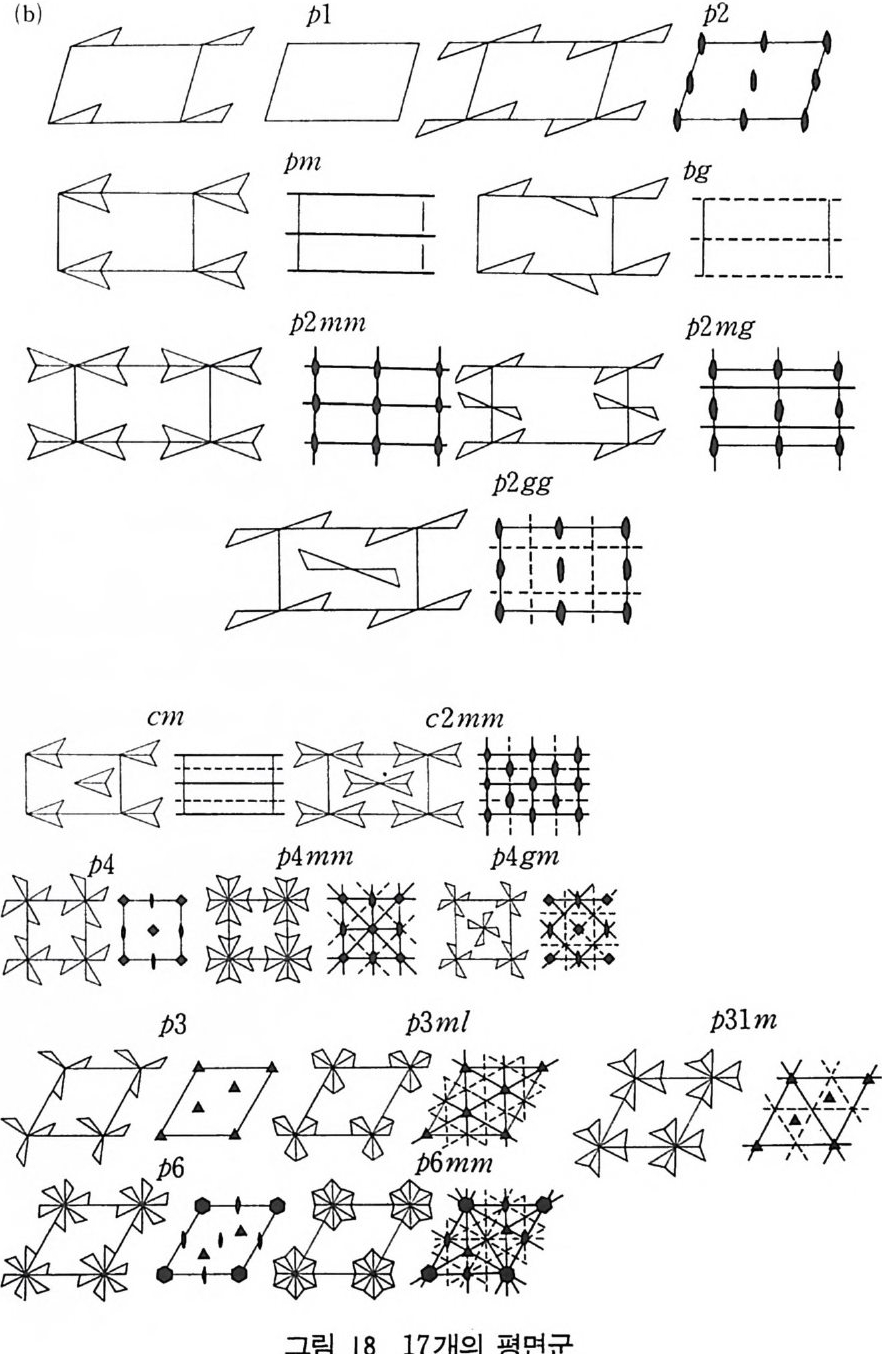
230 개의 공간군을 얻을 수 있다. 공간군에 앞서 먼저 평면군에 대 해 생각해 보자. 6 평면군 이차원적 공간군, 죽 평면군에서 모두 17 개가 있고 그림 16 과 갇은 단순 사면(斜面) 그물을 생각해 보자. 이러한 그물은 평면에 서 무한히 연속되는 단순 격자로 원점은 어느 격자에서도 선택할
수 있다. 그림 16-(a 펴- 같은 2 회 회전축을 그린 무늬를 배치하고 사각그립에 정리하면 그림 16-(c~ 같이 또 다른 2 회 회전축을 각 무늬 사이에서 찾을 수 있다. 죽 새로 생긴 2 회 회전축은 분수 좌 표로 각 단위세포의 0, 1/2 ; 1/2, 0 ; 1/2, 1/2 에 있다. 이러한 평면군은 p 2 이다.
 7,4
7,4
(a) 2 회 회전축을 가지는 무늬 (b) 둔각을 가지는 평행사변형 그물 (c) P2 평면군을 가전 무늬의 그물망
그림 17 에는 단위세포내 대칭에 관련 되 는 위 치 와 분수좌표 를 보 이고 있다. 공간군 대칭에서 얻 을 수 있 는 위 치 의 최 대 수는 일반적 인 대등위치(g eneral eq u iv a lent p os iti o n) 이 고 jJ 2 평면군 에 서는 일 반적인 대등위치의 좌표는 x, .1/ 와 굿 ` § 이다. .f' Ii 는 1-. r , 1 - y 를 뜻한다. 평면군 표시에서 처음의 숫자 는 대 등점 의 좌표 숫자이 고 그 디 ~ 휴 문자는 W y cko ff표시이고 그 다음은 각 위치 의 대청성 운 나타 내
 。。
。。
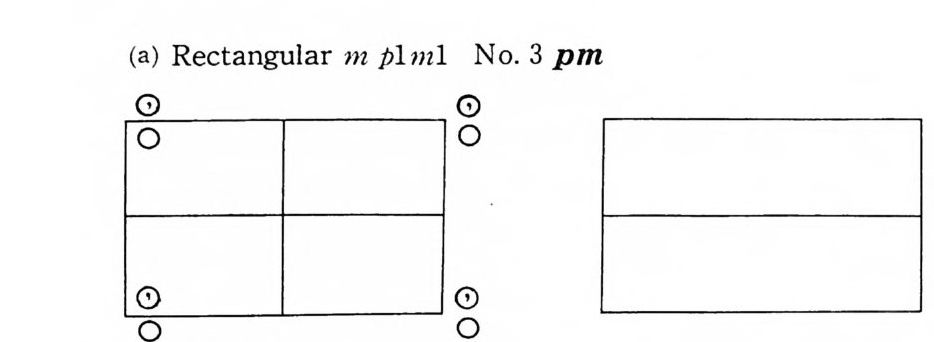
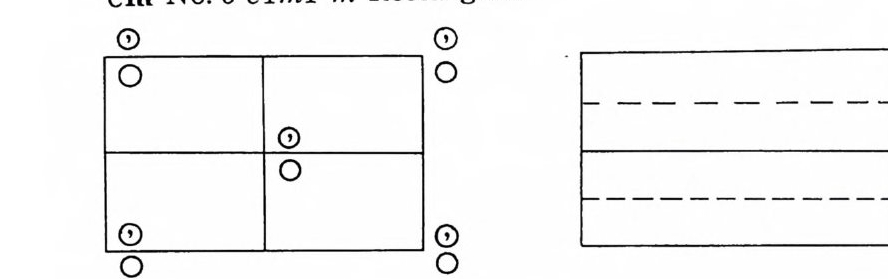
고 마지막 숫자는 분수 좌표이다. p2 평면군에서 W y cko ff표기 법, (a) , (b) , (c) , ( d ) 는 2 회 회전축을 가지고 있고 이러한 위치가 네 개 있다. 이러한 위치를 특별한 위치 (s p e ci al p os iti on) 라고 부 른다. 일반적인 위치 (gen eral p os iti on) 는 대칭성이 1 인데 비해 특 별한 위치에는 더 높은 결정학적 점군 대칭성을 가진다. 직사각형 모양의 평면군에 대해 생각하자. 이러한 평면군은 점군 m 과 2mm 이 포함되고 p단위세포와 c 단위세포가 있으며 먼저 평면군 p m 과 cm 에 대해 생각하자. 그림 18 에서 x 축은 이 책 종이의 아래쪽 방향을 택하여 정하고 y축은 가로 질러서 정하며 양의 방향은 오른쪽 방향이다. p m 평면군에서는 원점에는 m 대칭 이 있고 일반적인 대등위치는 두 개 있으며 m 대칭을 가지는 두 개의 특별한 위치가 있다. 평면군 cm 은 몇 가지 새로운 특칭이 있다. 좌표 (0, 0 ; 1/2, 1 / 2) 를 머리에 표기해 놓고 있다• 이것은 아래에 표시한 좌표에 (0, 0) 과 (1/ 2, 1 / 2) 로 이동하면 모든 좌표를 얻을 수 있다는 뜻이 다. 그러면 일반적인 좌표(g eneral po sit ion ) x, y와 료 y는 다 음과 같이 된다. 즉 x, y ; 로, y ; x+1/2 ; y+ 1/2 ; 1/2-x, 1 / 2+ y가 된다. 거리 1/2 ― x 는 a 축을 따라 원점에서 1/2 만큼 이동하고 난 후 x 만큼 빼 주어야 한다. c 중심 단위세포에 m 대칭 울 결합하면 미끄럼 반사평면(기호로 g이고 그림에서 -__ -로 표시) 이 생긴다. 특별위치가 p m 평면군에는 2 조가 있지만 cm 평면군에는 1 조가 있다. 그러나 머리에 표시해둔 좌표를 고려하면 이 1 조에서 아래 와 같이 두 개의 좌표를 얻을 수 있다. 0, y ; 1/2, 1/2+y 그림 18 에는 17 개의 평면군에 대한 그림을 Inte r nati on al Tables for X-ray Cry st a ll og r aph y, Vol. I 에 의하여 표시하였다.
 (aO) KR)e cta ng ula r nz pl ml oNoo. 3 pm
(aO) KR)e cta ng ula r nz pl ml oNoo. 3 pm
Orig in on m Number of po sit ion s, Wy c koff nota ti on , and po in t s ym metr y Coordin a te s of equ iv a lent po sit ion s Condit ion s lim it ing po ssib l e refl ec ti on s 2 c 1 x, y ; x, y, General: No condit ion s 1 b m T1• y, Sp e cia l : No condit ion s 1 a m 0, y cm No. 5 c1ml m Recta ng ula r
 o。 o。 ,_ _______ _
o。 o。 ,_ _______ _
Orig in on m Number of po sit ion s, Wy c koff nota t i on , and po in t sym n etr y Coordi na te s of eq u iv a lent po sit ion s Condit ion s lim i ting po ssib l e refl ec ti on s (0, 0; 랑, ½)+ 4 b I x, y ; x, y, General: hk ; h+k=2n 2am o,y. Sp e ci al : as above only (~)Inte r nati on al Tables ]or X-ray Cry st a ll og r ap hy , Vol. I 에서 발췌 (b) 17 개의 공간군을 무늬를 넣어 평면군의 대칭성을 나타냄
 ( b l 二\二ftJ
( b l 二\二ftJ
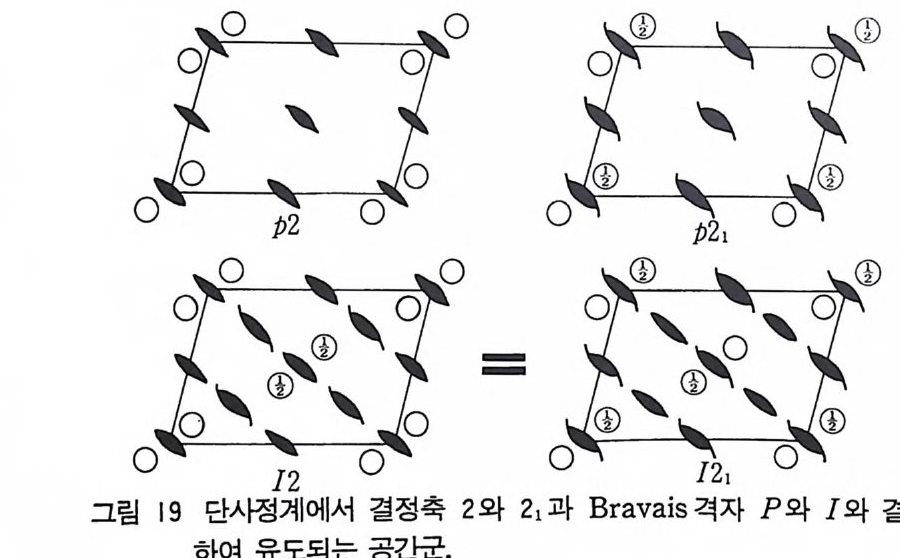
7 공간군의 유도와 명명법 230 개의 공간군 모두를 어떻게 하여 얻을 수 있는가 를 설명하는 것은 복잡하므로 간단한 예를 들어 설명하겠다. 삼사정계에 있어서 는 2 개의 공간군 Pl 과 P i만 있다. 단사정계에 있어서는 세 개의 결정족(2, m 및 2 / m) 과 두 개의 Bravais 격자 형태 (P 와 C) 가 있 으며 이들울 고려하여 공간군을 유도해야 한다. 2 와 2 과 두 개의 격자형 P 와 I 를 결합하면 어떻게 되는가 생각하자 . 그림 19 는 네 개의 가능한 조합 P2, P2I, I2 및 121 에 대해 c 축 을 따라 본 그림을 나타내고 있다. 평면 위쪽의 물체가 놓아는 위치 를 원내에 분수 숫자로 표시하였다. I2 와 121 는 원점만 다르나 같은 공간군 에 속함을 알 수 있다. 따라서 결정족 2 에서 세 개의 공간군을 얻 울수있다. 국제적으로 통용하는 공간군 기호는 계가 내포하고 있는 대칭요 소를 나타내는 약어로써 표시한다. 대칭요소의 표시는 점군에서 사 용하는 것과 다르다. 중요한 하나의 차이점으로, 공간군에서는 대
 P2 -- P21
P2 -- P21
칭요소가 세 개의 결정축에 대해 어떻게 대칭을 가지는가를 나타낸 다. 삼사정계에서는 이것은 중요하지 않다. 그러나 다른 결정계에 서는 이러한 법칙에 따른다. 그러나 전례가 임의로 만들어져서 모 든 결정계에 대해 일관성 있게 통일되는 표시법이 없다. 단사정계에서는 기본되는 축을 c 축으로 정하는가, b 축으로 정 하는가 하는 문제가 있다. 화학에서는 보통 b 축을 기본축으로 정 한다. 그러면 주어전 공간군이 기호에서 abc 로 표시한다면 P2 에 공간군에 대한 기호는 c 축을 기본축으로 정하면 P112 가 되고 b 축을 기본축으로 정할 경우 P121 이 되며 P112 의 의미는 단순 단 사정계로서 a 축으로의 대칭이 1 이고 b 축으로의 대칭이 1 이고 c 축으로의 대칭이 2 회 회전축이 있다는 뜻이 된다. 단사정계에는 Brava i s 격자형으로는 단순 P 형과 C 형 두 가지가 있고 13 개의 공간군이 여기에 속한다. 각각 두 가지 종류의 기본축에 따라 표시 되어 있다. 사방정계에서는 대칭에 대한 명명법은 단사정계와 같이 축에 따 라 abc 순서로 표시한다 . 기본축은 c 축으로 정하며 Pmm2 의 경 우 Bravais 격자형이 단순정계 (P) 이며 a 축으로 m( 거울면)이 있 고 b 축으로도 거울면이 있고 c 축으로 2 회 회전축이 있음을 뜻한 다. 그러나 Pmna 와 Pnma 의 총괄적인 완전한 표시는 P—m 2_ _ 2n 요a 와• F 쇼n 요m소 -a 로서 이것도 사방정계로서 a, b, C 축을 따라 대칭성이 Pmna 의 경우 각각 2/m , 2/n 및 21/a 가 있음을- 뜻한 다. Brava i s 격자형으로는 P, C, F, I 형이 있고 59 개의 공간군 이 있다. 정방정계에서는 c 축에 4 회 회전축이 있다. Bravais 격자형으로 P 와 I 가 있고 대칭요소를 나열하는 순서는 c 축, a 축과 방향, [11 이으로의 대칭성을 나타낸다. 예컨대 공간군 P4m2 의 경우 단
순 사방정계이고 기본축 c 축으로 대칭 4 가 있고 두 개의 a 축 (a 축과 b 축은 대등함)은 거울면 (m) 과 나란하고 〔 11 이 방향으로 대 칭 2 가 있음을 뜻한다. 정방정계에서 Bravais 격자형으로는 단순 (P) 와 I 형 두 가지가 있고 모두 68 개의 공간군이 있다. 삼방정계에는 Brava i s 격자형으로 단순 (P) 형과 능면체 (R) 형 두 가지가 있고 25 개의 공간군이 있으며, 육방정계에는 단순 (P) 형과 27 개의 공간군이 여기에 속한다. 단순 삼방정계와 육방정계 의 명명법은 c 축울 기본축으로 정하고 a1=a2 이므로 명명법은 정 방정계와 같은 의미를 갖는다. 입방정계에서는 모든 결정축은 대등 하다 (a=b=c, a=/3 =r =90). 공간군의 표시에는 먼저 Bravais 격자형의 표시가 오고, 그 후 a 축 방향의 대칭, 〔 11 니 방향의 대 칭, 〔 11 이 방향의 대칭의 순서로 표시한다. 〔 11 니 방향에서는 입방 정계에서는 반드시 3 이나 5 가 있으며, 중간 위치에 3 이나 3 가 오는 것으로 육방정계의 공간군과 구별된다. Bravais 격자형으로 는 P, F, I 가 있고 모두 36 개의 공간군이 입방정계에 포함된다. 공간군 기호와 점군 사이의 관계에서 결정계를 알 수 있다. 공간 군 기호를 보고 이것이 속하는 점군을 알아야 한다. 여기서는 예를 들어서 생각해 보자. P21/c-2 1/c-2 /c-2/ m- 단사정계 Ibca-m mm-사 방정계 P41212-422- 정방정계 F43c-4 3m-입 방정계 공간군 기호에서 대칭적 특성도 생각해 보자. P21/c : 단순 단사정계 ; 屈r° l 유일축이면 c- 미끄럼 평면 ..l b ; 21IIb, 중심 대칭형 공간군 Ibca : 체십 사방정계 ; b- 미끄럼 평면..l a ; c- 미끄럼 평면..l b,
a- 미끄럼 평면 1- c ?41212 : 단순 정방정계 41/ /C ; 21 // a 와 b ; a 축과 b 축의 45° 방향에 2 가 있다. 즉 2 /I [ll O] F43c : 면심 입방정계 ; 41 / (a, b 및 c 축) ; 3/I [lll] ; c- 미끄럼 평면 나 llO ] 연습문제 1. (i) a= b, r = 90 ' 안 그물망과 (ii) a= b, r=120' 인 그물망이 있 다. (a) 각 격자점의 대칭을 구하라. (b) 이 그물망이 속하는 2 차원적 결정 계 (tw o-dim ensio n al sys - ter n) 이름을 써라. 2. a-:/=b-:/=c, a-:/=( 3- :/=90° ,=90 ° 는 이사정계 (d i cl ini cs y s t em) 라 할 수 있고 이것은 하나의 새로운 결정계가 될 수 있는가? 이에 대 한이유를써라. 3. ( 공a) 간어군미 점P군2(/cp,P acraen2 t1 p, oCin m t cgmr o , uP p4)2과1 c결, 정P6계3를22 와써라 .Pa 3 에 대하여 (b) 공간군 기호의 의미를 각각 써라. 4. 다음 평면군과 공간군의 대칭요소오와 대등위치를 보여라. (a) Pm (b) P2/m (c) Pg 5. 다음 결정족 중에서 대칭중심을 가지는 것은 어느 것이냐? (a) 4 (b) 4 (c) 4mm (d) 4 2m
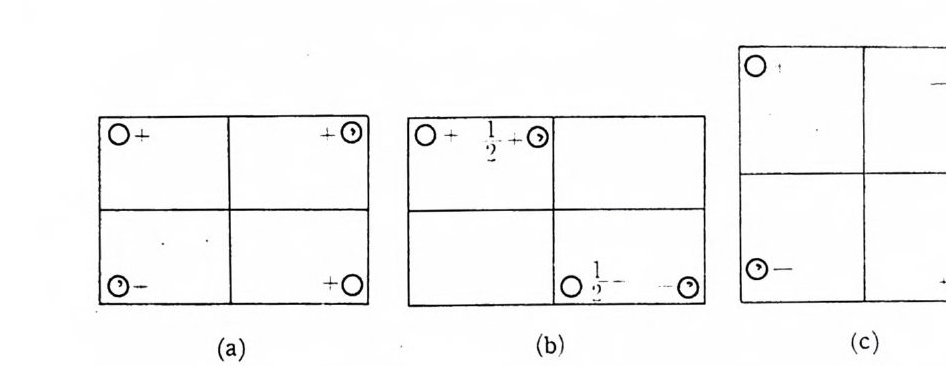
(e) 422 (f) _m!_ mm (g) 4/ m 6. 다음 그림은 단위세포내의 한 se t의 대등위치 볼 보이고 있다. 결정계와 공간군을 써라.
 O , -O
O , -O
제 3 장 결정 구조 1 서론 결정내 원자의 상대적 위치는 X- 선, 전자, 혹은 중성자를 사용 한 회절 스펙트럼의 상대적 강도를 측정하여 알아낼 수 있다. x -선은 전자나 중성자에 비하여 X- 선으로 얻은 회절파의 강도가 결 정의 완벽함에는 그렇게 크게 영향을 받지 않으므로 더욱 유용하 다. 결정구조는 단위세포내의 원자의 상대적 위치로 설명할 수 있 다. 원자와 화합물로 이루어진 결정에서 화학결합에 관여하지 않는 외각 전자의 전하분포는 대략 구형 대칭이고 따라서 원자로 이루어 전 결정구조를 생각하면 결정구조는 동일크기의 구로서 이루어져 있다고 생각할 수 있고 혹은 화합물이 다른 원자가 쌓여져 만들어 져 있으면 다른 크기의 구조로서 이루어져 있다고 생각할 수 있다. 안정한 원소나 대부분의 간단한 화합물의 결정구조는 이미 결정 하였다. 이 장에서는 다수의 구조를 원찬의 상대적 위치의 기하학 적 특성을 강조하면서 설명하겠다. 원소의 구조와 간단한 화합물의 구조를 이 장에서 주로 설명하겠다. 많은 경우 화합물이나 원소는 한 개 이상의 구조를 가지며 각 구조는 주어진 온도나 압력 영역에 서 열역학적으로 안전한 형으로 존재한다. 이 경우 이들 원소들을 동소체 (allo t ro p e) 라 하고 화합물은 여러 가지 형 (po lym o rp h ous)
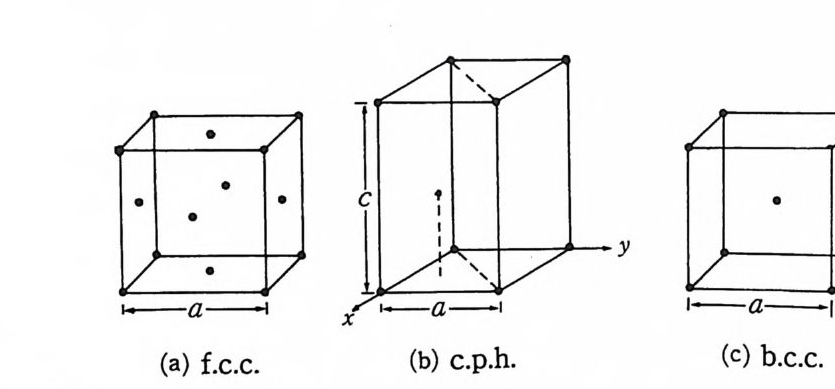
을 갖는다고 한다. 화합물의 결정구조 를 설명할 때 MX 형으로 표 시할 것이며, 이때 M 은 금속이온이나 원자를 뜻하며 X 는 전기음 성도가 큰 원자, 죽 0, F, Cl 등을 뜻한다. 결정구조는 격자의 원 점에서 격자내 원자의 좌표를 나타내어 설명할 수 있다. 2 금속의 구조 대다수의 원소는 금속이나 마그네슘, 인듐(i nd i um), 주석, 수 은, 우라늄, 플루토늄 등 몇 개의 금속원소를 제의하고는 세 가지 구조 중 하나, 죽 면심입방, 육방조밀충전 혹은 체심입방 중 하나 의 구조를가지고있다. 1) 면심입방격자 구조 (Fm3m) 귀금속 (Cu, Ag , Au), 높은 원자가를 갖는 금속 (Al 과 Pb), 후반 기 전이원소 (Co, Ni , Rh, Pd, Ir, P t) , 불활성기체 (Ne, Ar, Kr, X e) 는 이러한 구조롤 하고 있다. 그림 1-(aK: = 면심입방격자의 구조를 보여주고 있다. 단위세포당 4 개의 원자가 포함되고 단위세포에서 원자의 좌표는 (0, 0, 0), (1/2, 1/2, 0), (1/2, 0, 1/2) 및 (0, 1/2, 1/2) 이다. 각 원자는 가장 가까운 이웃에 12 개의 원자
 y
y
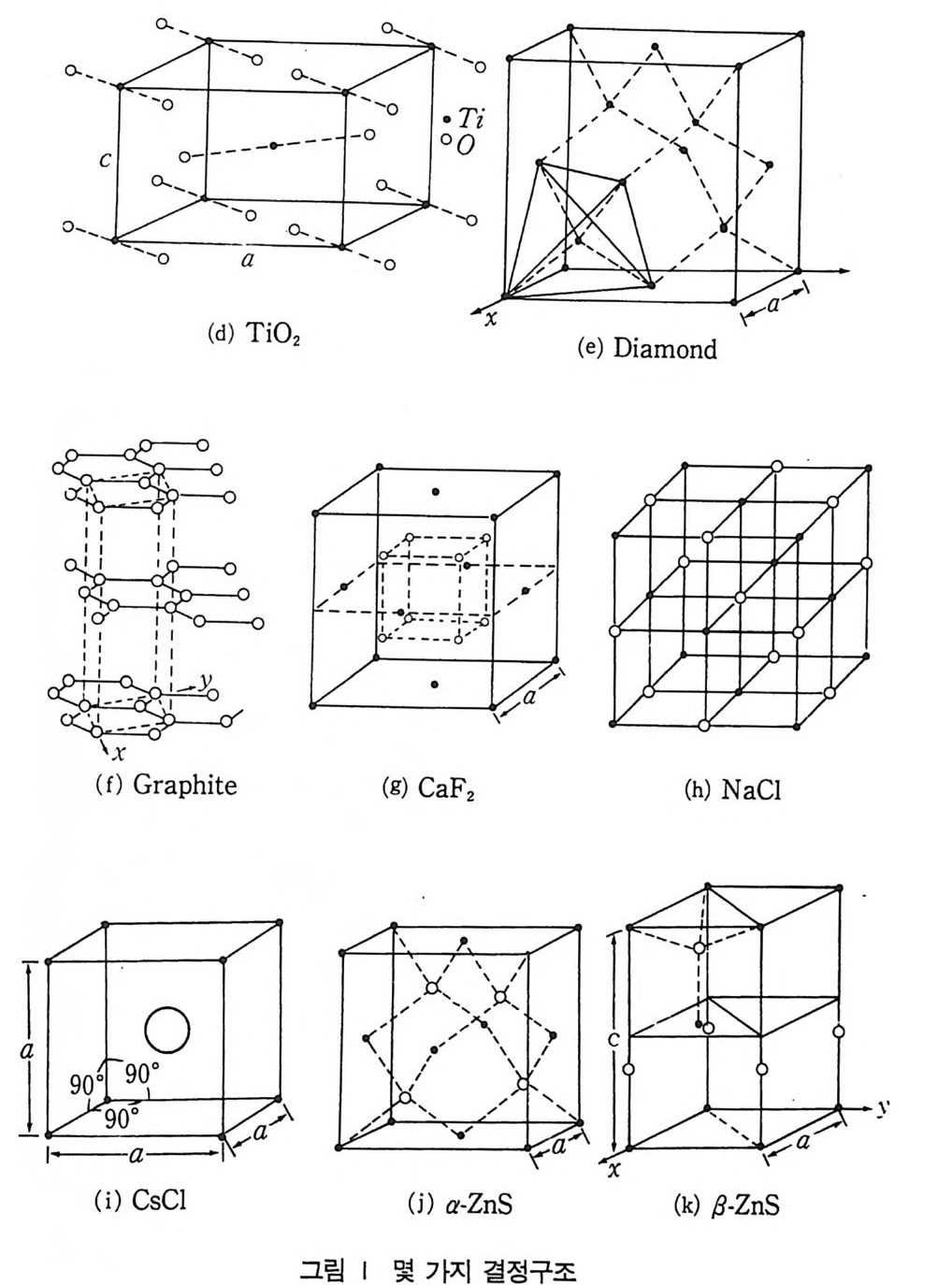 00`- `_` c ````°oo` - o--'`-- ``_Toa -) . .. -oo ..-..`_ - ~ ==--`0-`` o0o . . .` -•-o0oT i / / ,’ y` / ,/\/스\X,/`' If\,,V``/'`? /`/ak \ / / `\L
00`- `_` c ````°oo` - o--'`-- ``_Toa -) . .. -oo ..-..`_ - ~ ==--`0-`` o0o . . .` -•-o0oT i / / ,’ y` / ,/\/스\X,/`' If\,,V``/'`? /`/ak \ / / `\L
롤 가지고 있고 단위세포상수를 a 라고 나타내면 이들 원자간 거리는 /Z a/2 이다. 따라서 배위수는 12 이다. 구의 반경이 R= a/(2/2 ) 이면 충전 비율(p ack i n g frac ti on ) 이 0 . 74 이며 이 값 은 같은 크기의 구조로써 채울 수 있는 가장 큰 값이다. 격자내 방 향형
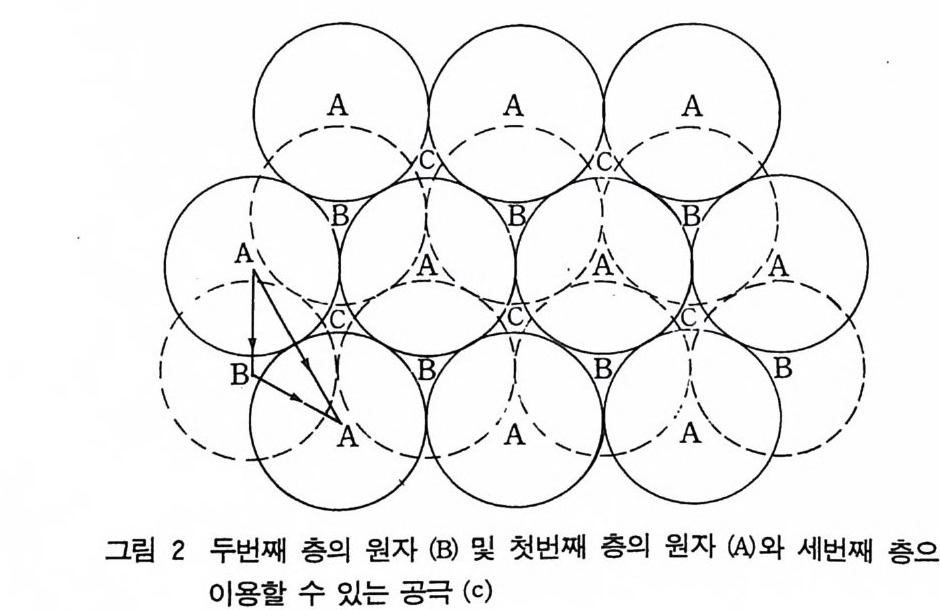 그림 2 두번째 충의 원자 (B) 및 첫번째 충의 원자 囚와 세번째 충으로
그림 2 두번째 충의 원자 (B) 및 첫번째 충의 원자 囚와 세번째 충으로
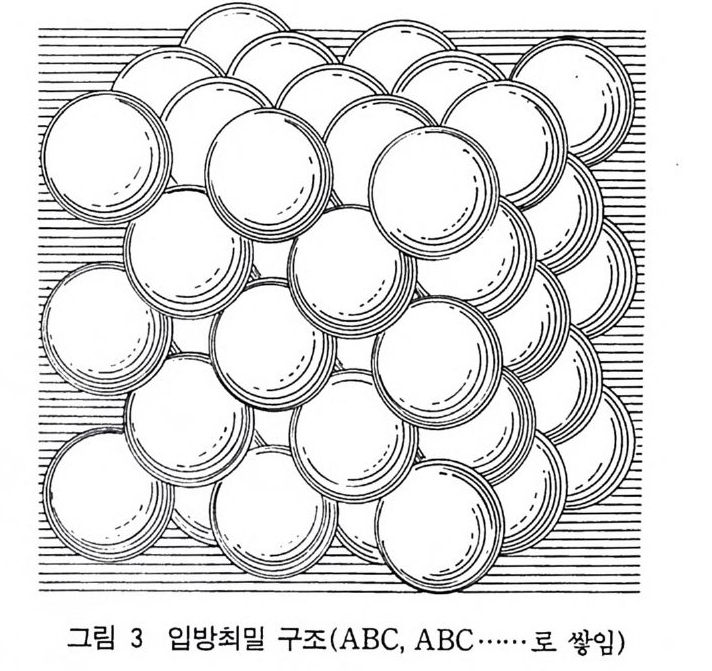 그림 3 입방최밀 구조 (ABC, ABC·· … · 로 쌓임)
그림 3 입방최밀 구조 (ABC, ABC·· … · 로 쌓임)
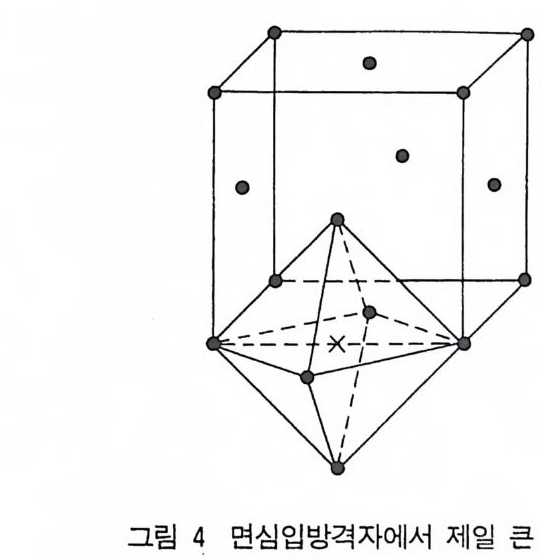
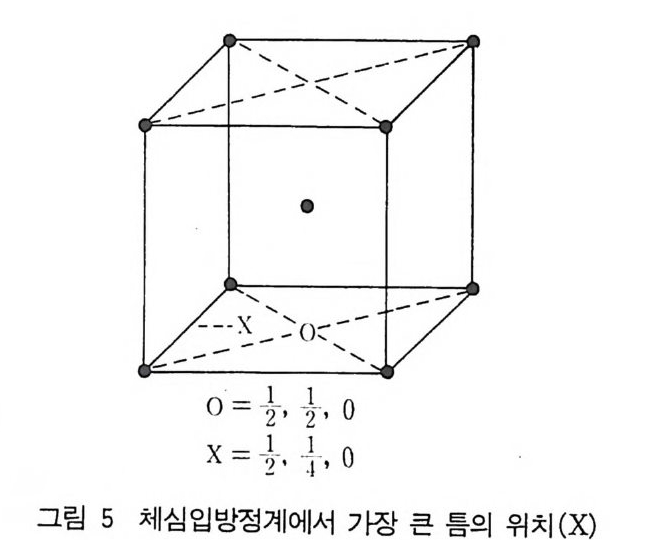
다. 같은 결정구조로써 다르게 쌓는 방법은 ACBACBACB …… 가있다. 면심입방 결정에서 임의의 원자에 대해 가장 가까운 이웃은 윤 ( = 2R) 거리에 있는 12 개의 원자가 있고 그 디음으로 가까운 이웃은 거리 a(=2 ./2 R) 에 있는 6 개 원자이고 세번째로 가까운 이웃은 24 의 ./[3f}J a(=2 ./3 R) 이고 네번째의 가까운 이웃은 譯 a(=4R) 거리의 12 개가 있다. 단위세포내의 가장 큰 톰의 좌 표는 (1/2, 1/2, 1/2) 와 이와 대등한 위치인 (0, 1/2, 0 ; 0, 0, 1/2, 1/2, 0, 0) 에 있다(그림 4). 2) 체심입방격자(I m3m) 실온에서 알칼리 금속인 Li, Na, K, Rb, Cs 과 어떤 온도 범위에 서 전이원소인 V, Cr, Nb, Mo, W, Fe, Ti, Zr 등이 체심입방 구조
 •
•
를 하고 있다(그립 1-(c)). 체심입방격자에서는 원자 하니는· 각 격 자점에 있다. 따라서 원자좌표는 (0, 0, 0) 와 (1/ 2, 1/2 , 1 / 2) 이 다(그림 1-(c)). 한 원자는 <[a거 리에 가장 가까운 8 개의 이웃 을 가진다 (a 는 격자 상수기다). 원자가 같은 크기의 구조로서 반경 이 R=/ 3a /4 이면 8 개의 <11 1> 방 향, 죽 체대각선 방향은 최밀충 진 구조를 가지며 충전 비율은 1C /3 / 8=0.68 이다. 두번째 가까운 이웃은 4R//3 (= a) 거리의 6 개가 있고 세번째 가까운 이웃은- 12 개로 그 거리는 4R/ /W짧아고 이 구조에서는 최밀충전된 구 조를 가지는 평면은 없다. 같은 크기의 구조로 되어 있으면 가장 큰 툼은(1 /2, 1/4, 0) 위치와 이 위치의 대등위치에 있다. 두번째 큰 톰은 (1/2, 1/2, 0) 위치와 그 대등위치에 있다(그림 5). 위와 같은 위치는 단위세포당 6 개 있다(입방체의 면의 중심에서 6 X l/2 과 입방체 모서리의 중간점에 12X1/4=3). CsCl( 그림 1- (i))의 Bravais 격자형은 무엇인가 ? 그립에서 보 면 단위세포당 두 개의 원자를 가지고 있다(고체상태에서는 완전히
 ` `
` `
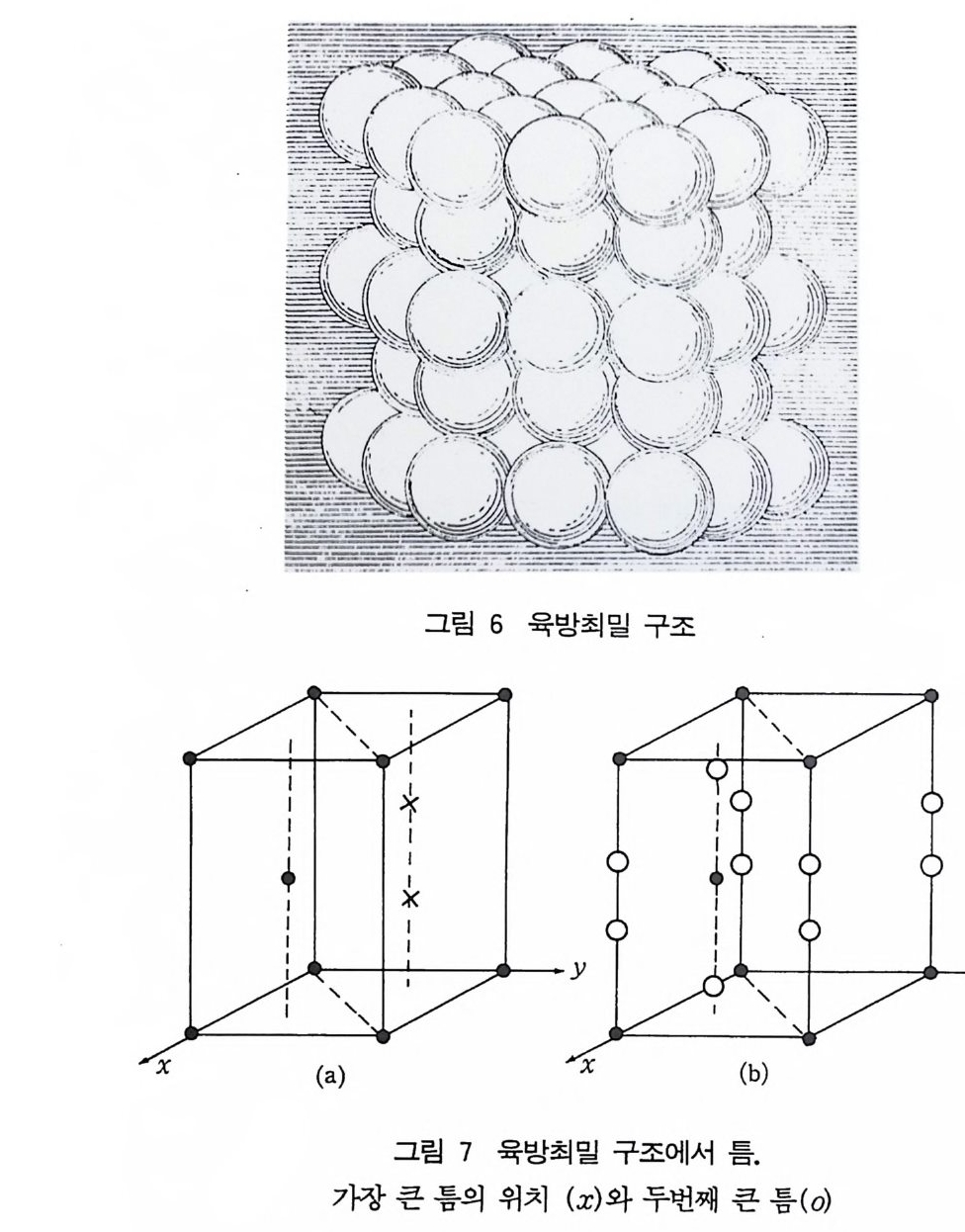
이온화되므로 실제는 두 개의 이온이다). 죽 Cs+ 이은은· (0, 0, 0) 위 치에 Cl- 이 온은 (1/ 2, 1/2 , 1/2 ) 위치에 있다. 두 이온 사이에는 체심입방 구조 이동에 관계가 있으나 (Cs + ~위치를 (1/2, 1/2, 1/2) 만 큼 이동시킴) 체심입방격자 구조는 아니다. 우리는 (0, 0, 0) 위치 의 Cs+ 이온과 (1/ 2, 1/2 , 1/2 ) 위치의 c1-이 온은 격자점 (0, 0, 0) 에 관련시켜 위치한다고 생각해도 좋다. 따라서 단순입방격자 구 조 를 가지며 각 원자에 대한 배위수는 8 이고 가장 가까운 이웃은 ~(a 는 격자坪)의 거리에 있다. 이러한 구조를 갖는 다른 화 합물에는 CsBr, Csl, CuBr, CuZn, Ag C d, A g M g이 있으며 FeAl 도 이러한 구조를 갖는다. 3) 육방조밀 쌓임 구조 (close pac ked hexago n al, 공 조꾼은 P 훑 -me) Mg전 , 이Zn원 소및인 C 스d 칸그듐리,고 티대탄,부 분이의트 륨희, 토지류르 코원늄소 는및 육2 방가최 원밀소 인구 조B롤e, 하고 있다(그림 6). 육방최밀 구조에서는 단위세포당 두 개의 원 자, 죽 (0, 0, 0) 와 (2/3, 1/3, 1/2) 에 원자가 있다(그림 7). 6 회
 i―l 一 \ \ ― 누\ I_I-그i X 죠림I_I_ iI. _6-_· X 육I—I방—— —최一i 밀- t:구 \[.\f>i―_―:一_ 조 \『\ _ 一一―一 l 〉--t-―冒―푸――二―-言――戶〔I ·\i_ 二
i―l 一 \ \ ― 누\ I_I-그i X 죠림I_I_ iI. _6-_· X 육I—I방—— —최一i 밀- t:구 \[.\f>i―_―:一_ 조 \『\ _ 一一―一 l 〉--t-―冒―푸――二―-言――戶〔I ·\i_ 二
회전축은 없지만 단위세포의 원점에 z 축에 나란한 위치인 O; 0, z 위치에 63 축이 있다. 그림 2 에서와 같이 같은 크기의 구를 ABAB··… · 형 이나 ACAC· ·… · 형(그림 2 참조)으로 쌓음으로써
얻을 수 있다. 각 구는 12 개의 가까운 이웃이 있고 축 길이의 비 c/ a =/( 幻 硏 =1.633 이다. 그러나 실제 금속 원자만 이상적인 구 에서 약간 벗어난 타원형이어서 c / a 의 비가 금속에 따라 1.5 (Be 의 경우)에서 1. 89(Cd 의 경우)의 비가 된다. c / a=/@ 刀 Y 이면 가 장 큰 톰은 그 좌표가 (1 /3, 2/3 , 1 / 4) 과 (1/ 3, 2/3 , 4 / 3) 의 위치 에 있다 ( 그림 7). 3 다른 원소의 구조 1) 다이아몬드(공간군은 Fd3m) 실리콘, 게르마늄, a 쿠꾹4 (실온 이하에서 안정한 형임)과 고온 고 압에서 안정한 결정성의 탄소 , 죽 다이아몬드 등의 구조는 그림 1 에 있다. Bravais 격자는 면심입방격자이며 단위세포당 8 개의 탄 소 원자가 있으며 그 위치는 (0, 0, 0), (0, 1/2, 1/2), (1/2, 0, 1/2) , (1/ 2, 1/2 , 0) , (1/ 4, 1/4 , 1/4 ) , (1/4, 3/4, 3/4) , (3/4, 1/4 , 3/4 ) , (3/ 4, 3/4 , 1/ 4) 에 있다. 즉 이 위치는 (0, 0, 0) 위치 와 (1/ 4, 1/4 , 1/4 ) 위치에 각각 면심이동한 것과 같다. 각각의 탄소의 가장 가까운 이웃 탄소수는 4 개(죽 배위수가 4 임)이고 사면 체의 모서리에 13a/4 거리에 각각 있다. a-ZnS 도 다이아몬드와 비슷한 구조를 구조를 하고 있으나(그림 1-( j )) 이 구조에서는 (0, 0, 0) , (0, 1/2, 1/2) , (1/2, 0, 1/2) , (1/2, 1/2, 0) 에는 유황이온이 위치하고 (1/4, 1/4, 1/4), (1/4, 3/4, 3/4), (3/4, 1/4, 3/4) 및 (3/4, 3/4, 1/4) 위치에는 아연 이온이 위치한다. 2) 흑연 (P63/mmc) 실온에서 탄소의 안정한 구조는 흑연이다(그림 1). 흑연은 육방
정계를 가지며 단위 세포당 4 개의 탄소를 (0, 0, 0), (0, 0, 1/2 ) , (1/ 3 , 2/3 , 0) 와 (2/3 , 1/3 , 1/2 ) 위치에 가지고 있고 실온 에서는 c=6.7A 이고 a=2.46A 이며 c l a=2.72 로서 비교적 큰 값이다. 이 구조는 육각형 판상 원자군을 계속 z 축을 따라서 쌓아 만들 수 있으나 쌓는 모양은 ABABAB·· · … 혹은 ACACAC······ 형이다. 여기서 A, B 및 C 는 육각형의 구석에 배열되는 원소의 시트 (shee t)를 말한다. 이들 충은 서로 멀리 떨어져 있고 (3.354A), van der Waals 힘으로만 결합되어 있다. 충간 의 결합 이 약하므로 흑연은 쉽게 쪼갤 수 있고 따라서 윤활제로 사용할 수 있는이유가된다. 4 몇 가지 화합물의 구조 MX 형, 죽 NaCl 분자는 2 개의 다른 종류의 원자가 격자점에 위치한다. 예컨대 M 이 (0, 0, 0) 위치에 있으면 X 는 (0, 0, 1 / 2) 에 있다(그림 1). 총괄해 보면 NaCl 의 단위세포에서 8 개의 이온, 죽 . 4 개의 NaCl 이 다음 위치에 포함된다. 4 Na+ : (0, 0, 0), (1/2, 1/2, 0), (1/2, O, 1/2) 및 (0, 1/2 , 1/2) 4 c1-: (1/2, 1/2, 1/2), (o, o, 1/2), (o, 1/2, o) 및 (1/2, 0, 0) N 갑 이온은 분명히 면심입방격자의 구조를 하며 c1 - 이온 (1/2, 1/2, 1/2) 에 면심 이동 ((O, 0, 0), (1/2, 1/2, 0), (1/2, 0, 1/2), 및 (0, 1/2, 1/2) )을 하면 위의 Cl- 이온 모두를 얻을 수 있다. 따 라서 NaCl 의 Brava i s 격자는 면심입방격자이다. 각 원자는 배위 수가 6 이며 이웃 원자는 정팔면체의 각각의 꼭지점에 위치한다. 각각의 (111) 격자평면은 이중 시트 (shee t)를 이룬 원자들로 되어
있고 각 시트는 한 종류만의 원자가 등변 삼각형 그물의 마디점에 배열된다. 하나의 원자종의 시트를 희랍어로 표시하고 디론· 종류의 시트를 로마자로 표시하면 [11 1] 방향의 원자가 쌓인 모양은 ArB aC /3 ArBaC /3··…·로 나타낼 수 있다. 원자들의 시트 사이의 간 격은 a / 13(a = 격자상수)가 된다. NaCl 구조의 공간군은 Fm3m 이다. 섬아연광 (a - ZnS) 의 구조는 면심입방 구조 (F43m) 를 갖는다. 이 구 조를 갖는 다른 화합물의 예는 Be, Zn, Cd, Hg 및 Cu 의 황화 물, 셀렌화물 (selen i de), 텔루즈화물(t ellur i de), Cu 의 할로겐 화 합 물, A g l 이다. 격자는 면심입방격자이다. 한 종류는 (0, 0, 0) 와 면심입방 이동 위치에 다른 종류는 (1/ 4, 1/4 , 1 / 4) 과 면심입 방 이동 위치에 있다. 즉 s2 - 는 (0, 0, 0), (1/ 2, 1/2, 0), (1/2, 0, 1/2 ) 및 (0, 1/2, 1/2 ) 에 , Zn2 + 는 (1/ 4, 1/4 , 1/4) , (3/ 4, 3/ 4, 1/4 ) , (3/ 4 , 1/4 , 3/4 ) 및 (1/ 4, 3/4 , 3 / 4) 에 위치한다. 따라서 다이아몬드 구조와 아주 유사하다. 각 종류의 원자는 f.c . c. 격 자의 제일 큰 틈에 놓인다고 생각해도 좋다. 각 원자의 배위수 는 4 이고 한 종류의 원자의 제일 가까운 이웃은 정규적 사면체의 꼭지점에 놓이고 그 거리는 13a / 4 이다. /3 - ZnS 는 섬유아연석 (,vurtz i t e) 구조 (P63mc) 를 하고 있다(그림 1). 이 격자 구조는 육방정계로서 한 종류의 원자는 (0, 0, 0,) 와 (2/3, 1/3, 1/2) 에 놓이고 다론 종류의 원자는 (0, 0, u) 와 (2/3, 1/3, u+1/2) 에 놓인다. 여기서 z( 값은 3/8=0.375 에 가까운 값 이다. 그림 7-(b 께서 보면 이 구조와 육방조밀 구조의 관계를 알 수 있다. 각 원자는 다른 종류의 원자 4 개와 4 면체형으로 배위된다. f . c.c 구조의 사면체 틈이 다른 종류의 원자로 채워지면 CaF2 (fluo rite : 형석)의 구조가 된다. 이 격자구조는 면심입방격자로서 한 원자, 즉 예컨대 Ca 는 (0, 0, 0) 와 (0, 1/2, 1/2), (1/2, 0, 1/2), (1/2, 1/2, 0) 와 F 는 (1/4, 1/4, 1/4) 과 (1/4, 3/4, 1/4)
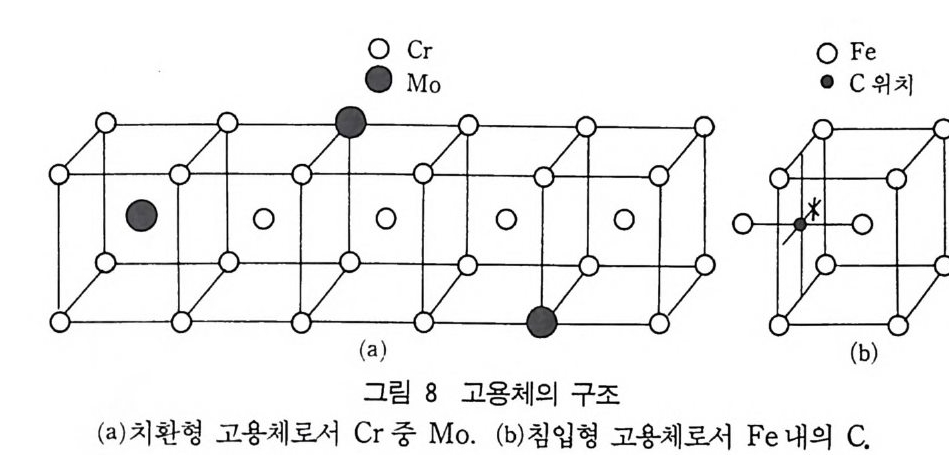
과 이에 대등한 다른 격자점에 놓인다. 단위세포당 화학식 CaF 2 가 4 개 존재한다(그림 1). Ca2+ 배위수는 가장 가까운 이웃인 F- 가 입방체의 각 모서리에 위치하므로 8 이다. F- 는 단순 입방정계의 격자점에 놓인다. F 는 이웃에 4 개의 Ca2+ 이온이 있고 이들 Ca2+ 이온은 정사면체로 놓인다. CaF2 를 제의하고 AX 2 의 일반적 구조는 Ti 0 2 구조(금홍석, ruti le, P42/mmm) 이다. 때때로 이 구조를 주석석 ( 朱錫石 : Sn02) 구조라고 부른다. Ti , Sn, Sb, W , Mn, V, Nb, Ta, Ge 의 이산화 물과 M g, Zn, Co, N i과 Fe 의 불소화물은 이러한 구조 를 하고 있 다(그림 1). 격자는 단순입방격자로서 c /a =0.65 이다. T i원자는 (0, 0, 0) 와 (1/2, 1/2, 1/2) 에 놓이고 산소 원자는 士 (u, u, 0) 와 土 (u+1/2, 1/2-u, 1/2) 이고 여기서 u 는 대략 0.3 이다. 단 위세포당 화학식 T i 02 가 2 개 포함된다(그림 1). 각각의 T i는 6 개의 0 원자에 둘러싸이고 0 원자는 약간 어긋난 팔면체를 이룬다. 5 고용체 (soli d s oluti on ) 많은 순수한 금속은 다른 종류의 다량의 원소와 함께 녹아서 고 용체를 만든다. 고용체에는 2 가지 중요한 형의 고용체가 있다. 치 환형과 침입형이다. 치환형 고용체에서는 용질 원자가 용매 원자와 치환한다. 침입형 고용체에서는 용질 원자가 용매 격자내의 틈에 침입하여 들어간다. 이들 구조의 재미있는 특징은 용질 원자는 다 소 무질서하게 분포된다. 예컨대 크롬 중에 몰리브덴이 10% 포함 되는 고용체에서 원래 크롬은 체심입방 구조를 하고 있는데 몰리브 덴은 입방체의 체심이나 모서리에 무질서하게 불규칙적으로 배열 된다. 결정의 조그마한 부분을- 그림 8 에서 보여주고 있다. 그림에서 5 개의 단위세포를 연결하였고 29 개의 원자가 있고 그 중 3 개는 Mo 원자이다. 따라서 Mo 이 약 10% 이상 포함되어 있
 0 Cr 0 Fe
0 Cr 0 Fe
고 따라서 다음 5 개의 단위세포에는 Mo 이 조금 적게 포함될 것 이다. 이러한 구조는 정규적 결정학적 법칙에 따르지 않는다. 평균 적으로 볼 때 이 구조는 체심입방 구조이고 실험적으로는 BCC 격 자에 해당하는 X- 선 회절효과를 나타낸다• 이러한 것은 놀라운 현 상은 아니다. 왜냐하면 결정을 검토하는 데 사용하는 X- 선 빔 (beam) 은 단위세포의 크기에 비해 너무 커서 한꺼번에 수백만 개 의 단위세포를 관측하여 구조의 평균치를 얻게 되는 것이다. 이러 한 점은 침입형 고용체에는 적용될 수 있다. 이 경우에는 용질 원 소가 소량 있어서 용매 격자에 크게 영향을 주지 않고 비틀지 않는 경우에 해당된다. a- 철에 탄소가 들어가 있는 고용체인 Ferr it e 는 이것의 좋은 예이다. 그림 8- ( b) 에서 격자에는 두 가지 톰이 있다. (1/2, 0, 1/2) 위치의 〈 O 〉으로 표시한 톰과 (1/4, 0, 1/2) 위치의 〈 X 〉로 표시한 톰과 이것들과 대등한 위치에 있는 톰이 있다. 실험결 과에 의하면 탄소는 (1/2, 0, 1/2) 위치와 이것과 대등한 위치에 위치한다. 그러나 평균적으로 보면 완전히 질서 있는 격자는 무질 서한 격자보다 낮은 대칭을 가지고 큰 격자칫수를 가전다. 따라서 초격자 (su p erla tti ce) 라고 부른다. 약 500 개의 단위세포 중 한 개 정도에 탄소 원자가 위치한다. 고용체에는 또 다른 형의 고용체가 있으며 이것은 장거리 질서를
가지는 고용체이다. 위에서 언급한 바와 같이 치환형의 고용체는 용매의 격자점에 용매 원자가 다소 무질서하게 분포되어 있다. 그 러나 어떤 고용체에서는 고온에서 침입형 고용체에서와 같이 용질 원자가 무질서하게 분포되어 있으나 저온으로- 냉각하면 용질분자 가 질서 있게 주기적으로 정열된다. 이러한 고용체는 질서 있고 초 격자 (su p erla tti ce) 를 가진다. 합금인 AuCu3 가 그 예이다. 고온에 서 구리와 금은 면심입방격자 위치에 위치하고 구리 원자는 면 중 심위치에 위치한다. 질서가 있는 고용체는 화합물과 비슷하다. 한 종류 원자는 격자 위치의 한 종류에 위치하고 다른- 종류의 원자는 다른위치에 위치한다. 연습문제 1. CaHg C l3 분자는 입방정계의 구조를 하고 있고 다음 좌표에 CaHg C 13 분자가 있다. Hg 1/2 1/2 1/2 Cs 。 。 。 Cl 1/2 1/2 。 。 1/2 1/2 1/2 。 1/2 단위세포당 분자수는 몇 개나 있으며 한 변의 길이가 0.554nm 이면 가장 가까운 Cl-Cl 길이와 H g -Cl 의 길이를 구하라. 결정 의 밀도를계산하라. 2. H g S 는 육방정계를 하고 있고 c=0.950run 이고 a=0.417nm 이다. 다음 좌표에 다음 원소가 위치한다.
Hg O O 0 S 1/2 0 1/2 0 0 1/3 -1/2 一 1/2 5/6 0 0 2/3 。 1/2 1/6 1010 평면에서 H g -S 의 거리를 구하라. 3. Al 과 Pb 는 체심입방격자의 구조를 하고 있고 단위세포 상수 a 는 각각 0 . 4046nm 와 0.4920nm 이다. Al-Al 의 거리와 Pb - Pb 의 거리와 Al 과 Pb 의 밀도를 계산하라. 4. 철과 텅스텐은 체심입방 구조를 하고 있고 단위세포 싱수는 각 각 0. 28 79nm 와 0.4920nm 이다. 원자간 거리와 밀도를 계산하 라. 5. 최밀육방정계 구조에서 cla= l. 633 임을 보이시오. 6. HCP 구조 ( cl a= l. 633), 면심입방 구조, 체심입방 구조에 대해 원자가 점유하는 공간의 퍼센트를 각각 계산하라. 7. 정방정계에서는 c 면 중심 정방정계는 없다. 그 이유를· 써라. 8. 반경 500 p m 의 구형 분자가 (a) 면심입방격자의 구조와 (b) 체심 입방 구조를 하고 있다면 각 경우에서 입방격자 한 변의 길이를 구하라.
제 4 장 X- 선의 성질 l 서론 19 세기 후반 많은 저명한 물리학자들은- 물리 세계의 성질을 모 두 본질적으로 이해할 수 있어서 이제 더 정확한 데이터를 얻는 것 만 남아 있다고 생각했다. 그러나 그 후 약 20 년 동안 새로운 많 은 것을 발견하여 이러한 생각을 버려야 했다. 이러한 새로운 발견 은 라디오파 (Her tz, 1887) ; 불활성 원소 (Ramsa y , Ray le ig h 및 Travers, 1895~98) ; X 선 (Roen tg en , 1895) ; 전자 (Thomson , 1897) ; 방사선 (Becq u erel, 1896 ; Curie , 1898) ; 양자론 (Planck, 1900 ; Ein - ste i n , 1905) ; 상대성 이론 (E i ns t e i n, 1906) 및 우주선 (Hess, 1910) 등의 발견이다. 독일의 물리학자인 Roen tg en 의 X- 선의 발견은 위의 어느 발견 에 못지않게 중요하다. 발견 당시에는 그 성질을 알 수 없었기 때 문] x- 선이라 불렀다. 그러나 자연과학, 공학, 의학에서 X- 선의 무한한 중요성을 그 후 곧 알게 되었다. X- 선은 발견 후 곧 의 학과 공업에서 투과 사전법 (Rad iog rap h y ), X 一 선 형광 두시법 (Fluoroscop }') 등의 여러 방법으로 사용되었고 오늘날 널리 쓰이 는 X- 선 회절법, X 선 분광법 등은 그 후 신빙성 있는 X- 선 관 과 X 선 발생장치, 전자 감지장치와 같은 X- 선 강도를 읽어내는
장치가 상업적으로 일반화됨에 따라 더욱 널리 사용하게 되었다. Mosele y는 1923 년에 정성적, 정량적 X- 선 분광 분석의 기초 를 확립하였고 1912 년에 Laue, Frie d ric h 및 Kn ippi n g은 결정에 의하여 X- 선이 회절됨을 보였다. 이리하여 결정학자들은 원자를 기초로 하여 결정체를 연구하기 시작하였고 결정의 대칭과 아름다 움의 원인이 되는 결정내 원자의 규칙적 배열과 원자가 서로 결합 하는 방법을 연구하는 수단으로 X- 선이 사용되었다. 각각의 단위 세포는 전 결정체에 걸쳐서 같은 대칭성을 가짐을 알게 되었다. 점 군의 이론이 개개의 단위세포에 응용되었다. 사전 필름상의 회절반 점의 배열을 조사하여 회절반점의 계통적 소멸에 주의를 기울여서 결정을 32 개의 결정족에서 시작하여 230 개의 공간군으로 분류할 수 있게 되었다. X 선 필름상의 회철반점 사이의 위치와 거리를 측정하여 평면사 이의 거리를 계산할 수 있게 되었다. 회절반점의 강도의 차이에 주 의를 기울여 Four i er 급수의 이론을 도입하여 결정학자들은 단위 세포내 원자의 위치를 알 수 있게 되었다. 2 전자파로서 X- 선 x- 선은 빛이나 자의선과 같이 전자파이다. x- 선과 동반하는 자 기장은 X- 선 회절에는 아무런 역할이 없다. 따라서 X- 선은 X- 선 회절을 생각함에 있어 파의 진행 방향에 수칙되는 평면에서 진동하 는 자기장으로 생각해도 좋을 것이다. x- 선 파장은 일반적으로 O.lA 과 lOOA 사이에 놓여 있다. 따라서 X- 선은 전자파 스펙트 럼에서 감마선과 자의선 영역 사이에 놓여 있다(그림 1). 또 빛의 속도로 진행한다. x- 선은 파동과 같은 성질을 가지며 이것은 회절 현상을 이해하는 데 중요하다. 그립 2 는 단일평면내에 진동하는 X 선을 보여주고 있다. x- 선을 해변의 파도와 갇이 끊임없이 바
 110043 7 I 라디오파
110043 7 I 라디오파
 전기장
전기장
다 쪽에서 연속적으로 진행에 오는 파도로 생각하는 것이 X - 선을 이해하는 데 도움이 될 것이다. X 선 회절에 사용하는 X- 선은 파장이 0.5~2.5 A 사이에 있는 파장을 사용한다. x- 선 빔 (beam) 과 같은 전자파는 에너지를 가지 고 있고 파의 운동 방향에 수직 방향에서 단위면적당 에너지가 흐 르는 속도를 강도 (D 라고 한다. 강도의 평균값은 X - 선 파의 전폭 의 제곱에 비례하고 절대단위로 표시하면 강도는 J oule / m 2/ sec 로 측정하나 이 측정은 매우 어렵고 거의 이루어지지 못하고 있다. 따 라서 X- 선 강도의 측정은 임의적 단위로 상대적인 값으로 나타낸 다. 전자파를 고전역학의 이론으로는 파동이라 생각하지만 양자론 에 의하면 양자 또는 광자라고 하는 입자의 흐름이라 생각할 수 있 다. 광자 한 개의 에너지 (E) 는 lw 이다. 여기서 h 는 Planck 상수로 6.62x 1 0-34 J oule•sec 이고 J/는 진동수이다. 파장과 전동 수는 다음 식과 같은 관계가 있다. -1= cl11 (4-1) 여기서 c 는 빛의 속도로 3.O X 108m/sec 이다. 3 X- 선의 발생과 연속 스펙트럼 x- 선은 전공 상태에서 충분히 큰 운동에너지를 가전 전기를 띤 입자가 급격히 감속할 때 발생한다. 전자가 이 목적에 보통 사용되 고 X- 선이 발생되는 X- 선 관에는 전자를 발생시키는 필라멘트와 2 개의 전극을 가지고 있다. 전국에는 수만 볼트의 전압이 걸리고 음극에서 발생하는 전자는 양극, 죽 금속 타겟(t ar g e t)에 매우 고 속으로 충돌한다. 충돌시에 X- 선이 발생하고 모든 방향으로 방출 된다. 충돌시 전자의 운동에너지는 다음 식으로 표시된다. KE= eV= I/2 mv2 (4-2)
어기서 e 는 전자의 하전 (1.6 X 10-31 coulomb) 이고 V 는양극에 걸린 전압이고 v 는 전자의 속도 (m / sec) 이고 m 은 전자의 질량 (9. l1 X l0-3 1 k g)이다. 타겟에서 나온 x- 선을 분석해보면 여러 가지 종류의 파장의 혼 합물로 구성되고 x- 선 관에 걸어둔 전압의 크기에 따라 발생되는 X 선의 파장과 강도가 다르다. x- 선 강도는 어떤 파장에서는 영 이 되고 이 파장을 단파장 한계 (short waveleng th lim i t) 라고 부른 다. 강도는 파장이 커짐에 따라 급속히 증가하여 최대값에 이르고 그 후 감소한다. 장파장 쪽에는 뚜렷한 한계값이 없다. x- 선 관의 전압의 크기가 증가함에 따라 강도의 최대값은 짧은 파장 쪽으로 이동한다. 그림 3 의 완만한 곡선으로 나타낸 복사선을 연속 복사 선 (conti nu ous radia t i on ) 혹은 백색 복사선 (whit e r adia t i on ) 이라 부른다. 백색 복사선은 전자가 급속한 감속에서 생긴다는 뜻에서
6 5 (
寄守 F 宅훈3 버 1군 F2 Y, Xl 。。 1.0 2.0 3.0 파장 (A) 그림 3 X 선관에 걸어준 전압의 함수로서 MoX 선 팬세서 얻은 X 선 스펙트럼제동된 복사선 (bremss t rahlun g혹은 brakin g rad i a ti on) 이라 부른 다. 연속 복사선은 전자가 금속 타겟울 때릴 때 급속히 일어나서 생 기는데 감속된 전자는 에너지를 방출한다. 어떤 전자는 금속 타겟 울 한 번 때리고 정지하여 모든 에너지롤 방출한다. 또 어떤 전자 는 타겟의 원자와 여러 번 충돌하고 연속으로 운동에너지 를 상실하 면서 잃는다. 한 번 충돌하고 정지하는 전자는 최대의 광자에너지, 즉 최소의 파장을 가전 X_ 선을 준다. 이러한 전자는 모든 에너지 를 광자에너지로 바꾸므로 다음과 같이 쓸 수 있다. eV= hllmax Asw1=Ami n =c/llmax= he/e V Aswl= (6 . 626(1 X. 6 100-23X4) 1(02- 1.9 9}9 8V X 108) mete r Asw1=¥(A) (4-3) 위의 식으로 단파장 한계 (A) 를 X- 선 관에 걸어준 전압의 크기 에서 구할 수 있다. 전자가 한 번 충돌로 완전히 정지하지 않고 여 러 번 충돌한 후 정지하면 그 속도는 접차로 감속되고 에너지 (e V ) 의 일부가 복사선으로 방출되고 생성되는 X- 선 광자는 hv 보다 적 은 진동수를 가지고 Aswl 보다 긴 파장을 가전다. 따라서 이러한 원 리에 의하여 Aswl 에서 긴 파장을 가진, 각종 파장을 가진 X- 선을 얻을 수 있어 그림 3 과 같은 연속 스펙트럼을 얻을 수 있다. 그림 3 에서 보면 X- 선 관의 전압이 증가할수록 초당 생성되는 광자의 수와 광자의 평균 에너지가 증가하므로 곡선은 더 높이 왼쪽으로 이동한다. 초당 방출하는 X_ 선 에너지는 타겟의 원자번호 Z 와 X -선 관 전류 i의 함수이나 타겟의 전류 i는 타겟울 때리는 초당 전자수를 나타낸다고 볼 수 있다. 따라서 총 x - 선의 강도는 다음 식으로나타낼수있다.
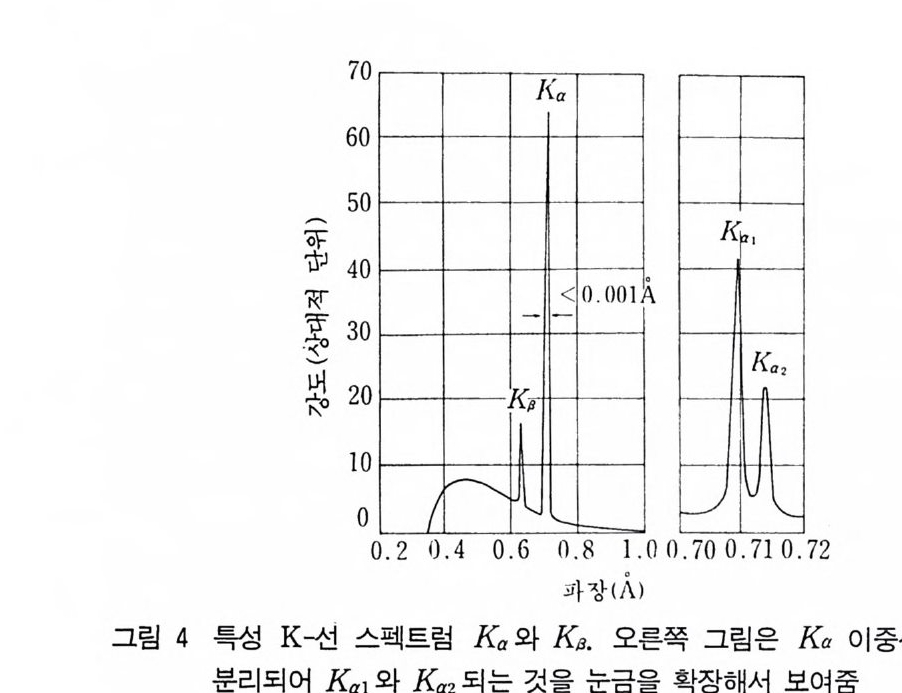
lcant .sp e c1 rum = A izv m (4- 4) 여기서 A 는 비례상수이고 m 은 상수로서 그 값은 2 에 가까운 값이다. 위의 식에서 알 수 있는 바와 같이 큰 강도의 백색 X- 선 이 필요하면 원자번호가 큰 타겟으로 만든 X- 선 관과 X - 선 전압 울 크게 해야 한다. 타겟의 재질은 X- 선 강도에 영향을 주나 연속 스펙트 럼의 파장의 분포에는 영향을 주지 않는다. 4 특성 스펙트럼 X 선 관의 전압이 금속 타겟의 특성값인 어떤 전압보다 높아지 면 어떤 파장에서 연속 스펙트럼상에 뾰족하고 X- 선 강도가 최대 가 되는 피크(p eak) 가 나타난다. 이들 피크는 매우 좁고 그 파장 은 금속 타겟에 따라 독특한 값을 가지므로 특성 X- 선이라 부른 다. 특 성 X- 선은 K, L, M 등과 같은 여러 가지의 계열로 나타 난다. 타겟울 때리는 전자가 K 껍질 (shell) 내의 전자를 떼내고 이 때 생긴 K 껍질의 빈 공간은 더 높은 에너지를 가지는 L, M, N 껍질에 있는 전자가 채우고 에너지 차이는 X- 선 광자의 형으로 방 출된다. L, M …… 껍질에서의 전자가 K껍질의 빈 공간을 채울 경우 Ka, KP 특성 X- 선아라 부른다(그립 4). 원자의 K, L, M ...... 껍질은 원자의 종류에 따라 일정한 에너지를 가지므로 이들 특성 X 선은 일정한 에너지, 죽 일정한 진동수를 갖는다. 여러 가 지 껍질 사이의 에너지 차이는 원자의 원자번호에 비례한다. 따라 서 Mo( 원자번호 =42) 의 특성 X- 선의 파장(A =O . 71073 A) 은 Cu (원자번호 =29) 의 특성 X- 선의 파장 (11= 1. 542 A) 보다 짧다. 터켓 울 때리는 전자가 타겟 원자의 L 껍질의 전자를 떼내고 이때 생긴 L 껍질의 전자의 빈 공간을 M, N… … 전자가 채울 경우 Lp, La 특성 X 선이라부른다.
 70 00
70 00
Mo 의 L 특성 X- 선의 파장은 대략 5A 이다. x- 선 회절 실험에 서는 K 특성 X - 선만 유용하고, L M …… 특성 X - 선은 사용하지 않는다. 이것은 이들이 긴 파장을 가지므로 작은 에너지를 가지고 또 아주 쉽게 흡수되며 결정내 깊이 침투할 수 없기 때문이다. K 특성 X- 선에는 여러 개의 선이 있고 보통 3 개가 쉽게 관찰된다. 이들은 Kai, Ka2, Kp 1 이라 부르고 Mo 타겟에 대해서 이들의 값 은다음과같다. Kai : 11=0.70930 A( 강도가 대단히 강함) K따 : 11=0·.71359 A( 강털} 강함) K81 : 11 =0 . 632288 A (강뚜 ~) KaI 과 Ka2’ 는 퍄상버 서로 가깝게 붙어 있어서 각각 다른 피크 로 보통 분리되지 않지만 분리되면 이중선 (double t)이라 부르고 분 리되지 않으면 Ka 선이라 부른다. 비슷하게 Kf J I 은 하첨자 1 을 빼 고 Kf J선이라 부른다. Ka, 은 Ka2 보다 대략 그 강도가 2 배이다.
또 Ka1 I K111 의 강도의 비는 원자번호에 따라 다르지만 보통 약 5/ 1 이다. Ka I 과 Ka2 의 파장의 차이에 대해 양자론을 도입하여 생각해보 자. 주 양자수 n 은 1, 2, 3·… • • 의 값을 가지고 n=1 일 때 K 껍 질이라 하고 n=2 일 때 L 껍질, n=3 일 때 M 껍질……이라고 한다. 부 양자수 l 은 0, 1, 2······(n ― 1) 까지의 값을 가질 수 있 고 궤도의 각 운동탓을 결정하는 양자수이다. 자기 양자수 m1 (m1= 0, 士 1, 土 2 …… 土 l) 은 자기장에서 전자궤도의 방향을 나 타낸다. 스핀 양자수 ms(ms= 士 1/2) 는 스핀 방향의 배향을 나타 낸다. 각 전자에 할당되는 특별한 양자수는 가장 낮은 에너지롤 갖 는 부껍질이 먼저 채워지고 원자내 하나의 전자는 동일한 네 개의 양지수를 가질 수 없다는 Paul i의 배타원리 (Pau li exclusio n p r i nc ip le) 에 따라 결정된다. 원자 스펙트럼을 생각할 때는 스핀의 자기 모멘트와 전자의 궤도운동 사이의 상호 작용이 다전자 원자의 에너지에 주는 영향을 생각해야 한다. 스핀과 궤도 사이의 상호 작 용에 주는 영향의 결과를 간단히 쓰면 두 개의 양자수, 죽 j =l 土 J ns 와 +j 와 —j 사이의 정수적으로- 간격을 가진 값 양자수 m 을 정의하여 생각함이 좋다. 가장 낮은 에너지 상태의 이러한 분포를 표 1 에 나타내었다. 원자의 총 각운동량은 개개 전자의 궤도와 스 핀 모멘트를 벡터로 합하여 결정하는데, 두 가지 방법이 있다. H. N. Russell 과 F. A. Saunders 가 사용한 방법에 따르면 모든 스핀 벡터는 합하여 합성 벡터 S 가 되고 궤도 벡터는 합하여 L 이 되고 두합성 벡터 S 와 L 의 합은원자의 합성 벡터 J가된다. 다른방 법에서는 jj결합 (cou pli n g)이라고 부르는데 각 전자의 j벡터를 먼 저 계산하고 벡터합을 구하여 합 J를 구한다. 이러한 두 계산법은 분광학에서 한 상태에서 다른 상태로 전이(t rans iti on) 할 때 생기는 최종 각운동량 값을 계산하면 약간 서로 다른 값을 준다. 그러나 Russell-Saunder 가 사용한 방법이나 jj결합이나 전자를 모두 가
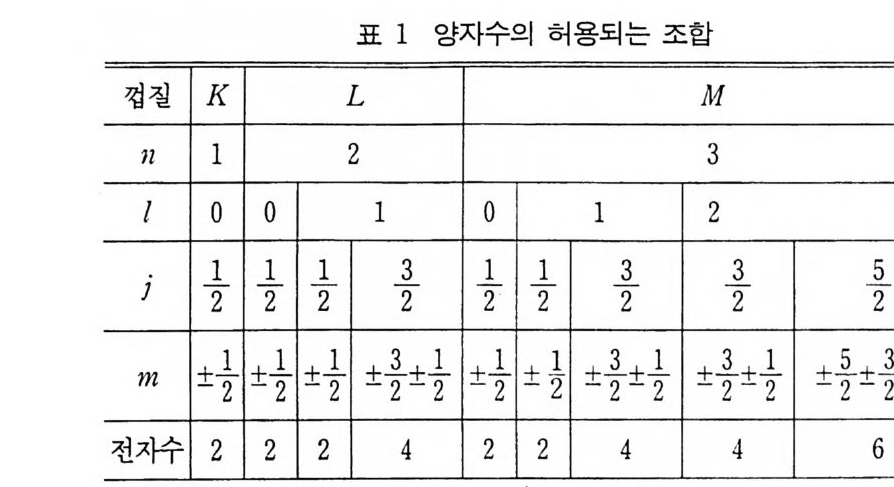 표 1 양자수의 허용되는 조합
표 1 양자수의 허용되는 조합
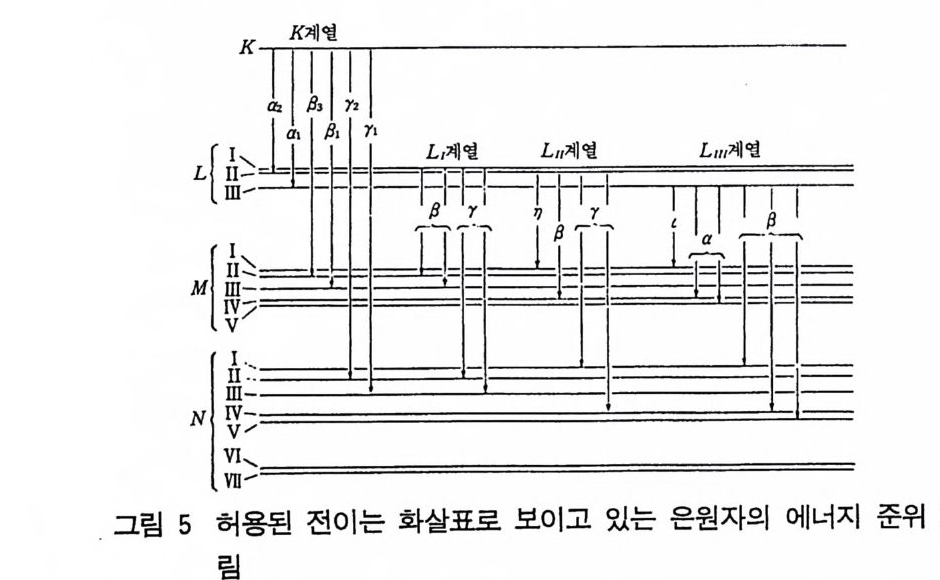
지는 원자의 각운동량 값은 하나의 내부껍질 전자 를 제거한 후 계 산할 때의 J값과는 다르다. 실제로는 원자의 양자상태를 잃어버린 전자(전자와 충돌에 의하여 떨어져나간 전자 를 뜻함)의 양자수·로써 나 타냄이 편리하다. 이 방법에 따라 은 (A g)원자가 가질 수 있는 양 자 상태의 상대적 에너지 상태를 나타내면 그림 5 와 같다. 아래로 내려온 수직 화살표는 전이를 관찰할 수 있는 허용되는 전이이다 .
 \:'
\:'
한 상태에서 다른 상태로 전이될 때 허용된 전이의 양자수의 변화 는다음과같다. 스 l = 土 1 6 j= O 혹은 土 1 (4-5) 5 X- 선의 흡수 X 선 빔 (beam) 이 물질을 통과할 때 통과한 빔은 물질내 존재하 는 전자에 의해 모든 방향으로 X- 선을 산란시키므로 약화된다. 약 화된 정도를 추정하기 위하여 물질 g m 당 n 개의 전자를 포함하고 빔에 수직으로 된 방향에 단면적이 1cm 히고 두께가 x 인 물체를 x- 선이 통과한다고 생각하자. 이 물체의 부피 dV 는 다음과 같다. dV= lX lX dx= dx cm3 (4-6) 물체의 밀도가 p이면 이 조각은 모두 np dx 개의 전자를 가지 고 있다. 이 조각에 의해 산란되므로, 통과되는 X - 선 빔의 강도의 감소 dl 는 다음 식으로 나타낼 수 있다. dl= -Iae np dx (4-7) • 음의 부호는 X- 선의 빔의 강도가 감소된 것을 뜻한다. 야는 전 자산란 계수이고 적분하면 다음과 같다. J dl/I= 규
여 기 서
 4X 10- B
4X 10- B
40 단위에서 330 단위로 파장이 1. 39 에서 1. 37 로 변함에 따라 변 한다. 이것은 파장이 1. 38 을 지나면서 통과하는 X- 선의 강도가 갑자기 감소함을 뜻한다. 이 뾰족한 끝을 흡수끝 (abso rpti on ed ge ) 이라 부른다. 이 급격한 흡수의 변화는 물질의 원자에 의하여 특성 x- 선의 발생과 관련된 에너지의 감소에 기인한다. 흡수계수는 파장에 따라 대략 다음 관계식에 따라 변한다. µm=K泣 (4-12) 여기서 K 는 상수이고 곡선의 각각의 가지에 대해 틀리는 값을 가지고 Z 는 X- 선을 흡수하는 물체의 원자번호이다. 짧은 파장의 x- 선은 매우 침두성이 크므로 단단하다 (hard) 라고 하고 이와 반대 로 파장이 길면 X- 선은 쉽게 홉수되고 이러한 X- 선을 부드러운
(soft ) X- 선이라 부른다. 물질은 X 선을 두 가지 방법으로 흡수한다. 산란에 의해 흡수가 일어나기도 하고 원자내 전자의 전이에 의한 전흡수(t rue absorp- ti on) 가 일어나기도 한다. 원자에 의한 X- 선의 산란은 많은 방법 에서 공기 중 먼지에 의한 가시광선의 흡수가 유사한다. 전자가 원 자에서 K 껍질의 전자를 떼낼 수 있고 K 특성 X- 선을 방출할 수 있다. 이때 떨어져나온 전자를 광전자(p ho t oelec t ron) 라 부 르고 발 생하는 X- 선을 형광 X 선(fl uorescen t X-ra y)이라고 부 른 다. K 껍질의 전자를 떼내기 위해서는 입사 광양자의 에너지 가 어떤 값 Wk 보다 커야 한다. 죽 파장이 어떤 값보다 적어야 한다. 따라서 Wk= hvk= he/Ak (4 -13 ) 여기서 l/ k 와 Ak 는 K 흡수끝의 진동수와 파장이다. 그림 7 에서
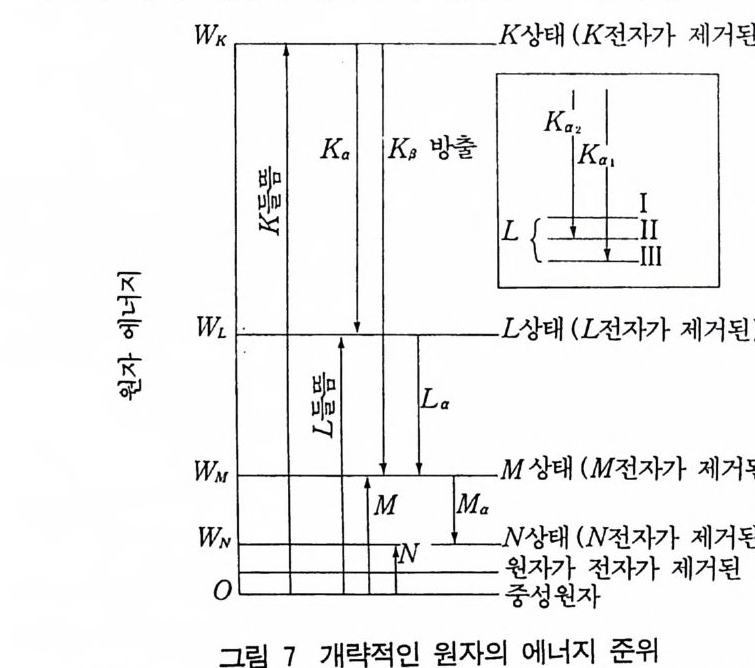 WK K상 태 (K 전 자가 제거된)
WK K상 태 (K 전 자가 제거된)
들뜨는 과정과 방출과정은 화살표로 나타내었다. 위쪽 오른편의 그림 은 L 상태의 미세 구조를 보여주고 있다.
알 수 있는 것처럼 특성 방출선의 파장을 계산할 수 . 있다. 죽 두 상태 사이의 에너지의 차이는 hv 와 같으며 u 는 하나의 상태에서 다른 상태로 전자가 전이될 때 방출하는 복사선의 진동수이다. Ka1 의 특성 X- 선을 생각하면 원자의 L 준위, 죽 L1, Lu 및 LIII 가 서로 가깝게 붙어 있다. Ka i의 방출은 K-Lm 전이에 기인 한다. 이 Ka1 의 전동수 Llha, 은 다음 관계식에서 구할 수 있다. 加 ha1 = wh_ WLI/I 加 k a,=h )) k _加血 1/ A ha= 1/A,,-1 /ALIII (4- 1 4) 여기서 하첨자 K와 Lm 는 각각의 흡수끝을 뜻하고 하첨자 Ka i은 X- 선 방출선을 뜻한다. 들뜬 전압도 (4-3) 식과 비슷하게 계산할 수 있다. K 복사선을 얻기 위해서는 타겟을 때리는 전자의 에너지는 Wk 의 에너지를 가져야 한다. Wk= eV i= hvk= he/A1r vk=hc/eAk Vi= 12390/Ak 여기서 Vk 는 K 껍질의 전자를 둘뜨게 할 수 있는 전압이고 Ak 는 K 흡수끝의 파장 (A) 이다. Au g er 효과 K 껍질의 전자가 없는 원자는 K 복사선을 낼 수 있으나 항상 그 렇지는 않다. K 껍질에 전자의 빈 공간이 있으면 이온화된 높은 에너지 상태가 된다. 과잉의 에너지를 잃고 정상 상태로 돌아오는 데 두가지 방법이 있다. (1) K 복샤인을 방출한다. (2) K 껍질의 전자내 빈 공간에 에너지가 더 큰 전자, 예컨대
Lu 전자가 채워지고 Ka 방출선은 내지 않고 에너지 차이에 의해 다른 껍질의 전자, 예컨대 Lm 전자를 떼낸다. 이때 떨어져나온 전자를 Au g er 전자라고 하고 Au g er 전자의 운동에너지의 크기는 K 와 LII 준위의 에너지 차와 관계가 있고 이러한 Au g er 과정을 KLuLm Au g er 과정이라 한다. Au g er 과정은 중요하지 않는 것 이 아니다. 원자번호가 31 번(갈륨 , Ga) 보다 큰 원소에 대해서는 x- 선을 방출하기보다 Au g er 전자를 낼 경향이 더 크다. Au g er 과 정이 일어날 확률 (1 ― Wk) 은 형광수율(如사에서 구할 수 있다. Wk( 형광수율, fluo rescence yiel d) K 복땐을 방출하는 원자의 수 -K 껍질에 전자의 빈 공간을 갖는 원자의 수 Au g er 전자와 같이 에너지가 별로 크지 않은 전자는 고체내로 깊숙히 침투해 들어갈 수 없다. 고체시료내 원자에서 방 출 되는 Au g er 전자는 원자가 표면에 lOA 내에 위치하지 않는 한 시료에 서 밖으로 나갈 수 없다. 달아날 수 있는 전자는 본래의 원자의 에 너지 준위의 차에 상당하는 운동에너지롤 가진다. 이 운동에너지는 측정할 수 있고 이 에너지값에서 표면충의 화학 분석을 할 수 있어 서 촉매, 부식, 표면에 있는 불순물의 분리 등의 연구에 Au g er 분 광학은이용될수있다. 6 X- 선 필터 X 선 관(t ube) 에서 방출되는 X 선 스펙트럼은 연속 X- 선과 함 께 타겟 금속의 특성에 따른 예리하게 뾰족한 특성 X_ 선을 방출한 다. 대개의 X 선 회절 실험은 실제적으로 단색광 빔을 필요로 하 므로 가장 강도가 큰 K(l 선만 남겨놓고 그 나머지의 X- 선, 죽 KB 선과 연속 X 선을 제거할 수 있는 필터가 필요하다. K 흡수끝
가까이의 흡수곡선이 쇠톱 이빨 모양인 것을 생각하여 K 흡수끝이 사용하려고 하는 X 선 성분보다 약간 적은 파장을 갖는 원소를 선 택하여 필터로 사용하는 것이 필요하다(그립 8). 그림 8 의 c 에서 보는 바와 같이 이 원소의 금속박(foi l) 형의 X- 선 필터를 넣어서 필요한 파장보다 짧은 파장(예컨대 Kp 등)을 강하게 흡수하고 필요 한 성분은 상대적으로 비교적 적게 홉수케 하는 것이 가능하다. 이 러한 필터는 식 (1 0) 에 따라 스펙트럼의 어떤 영역의 X- 선 강도를 줄이나 이 영역의 X- 선 강도를 모두 흡수하지는 - 않는다. 필터를 선택하는 편리한 법칙은 Ka 성분을 K, 성분의 강도에 비 해 대략 1 : 600 의 비율로 그 강도를 감소시키는 필터를 선택하여 사용한다. 보통 관습적으로 사용하는 X 국 1 관의 필터의 성분원소 를 표 2 에 나타내었다. 표 2 에 언급한 필터는 a 성분의 상대적 강도를 크게 하나 /3성 분의 강도를 완전히 제거하지는 못한다. 이런 경우 X- 선 빔은 여 과했다고는 하나 단색 X- 선은 아니다. 그러나 실질적인 단색광은 두 개의 필터를 사용하여 얻을 수 있다. 예컨대 Mo 타겟에서 나온
 표 2 X- 선관의 파장과 알맞은 필터
표 2 X- 선관의 파장과 알맞은 필터
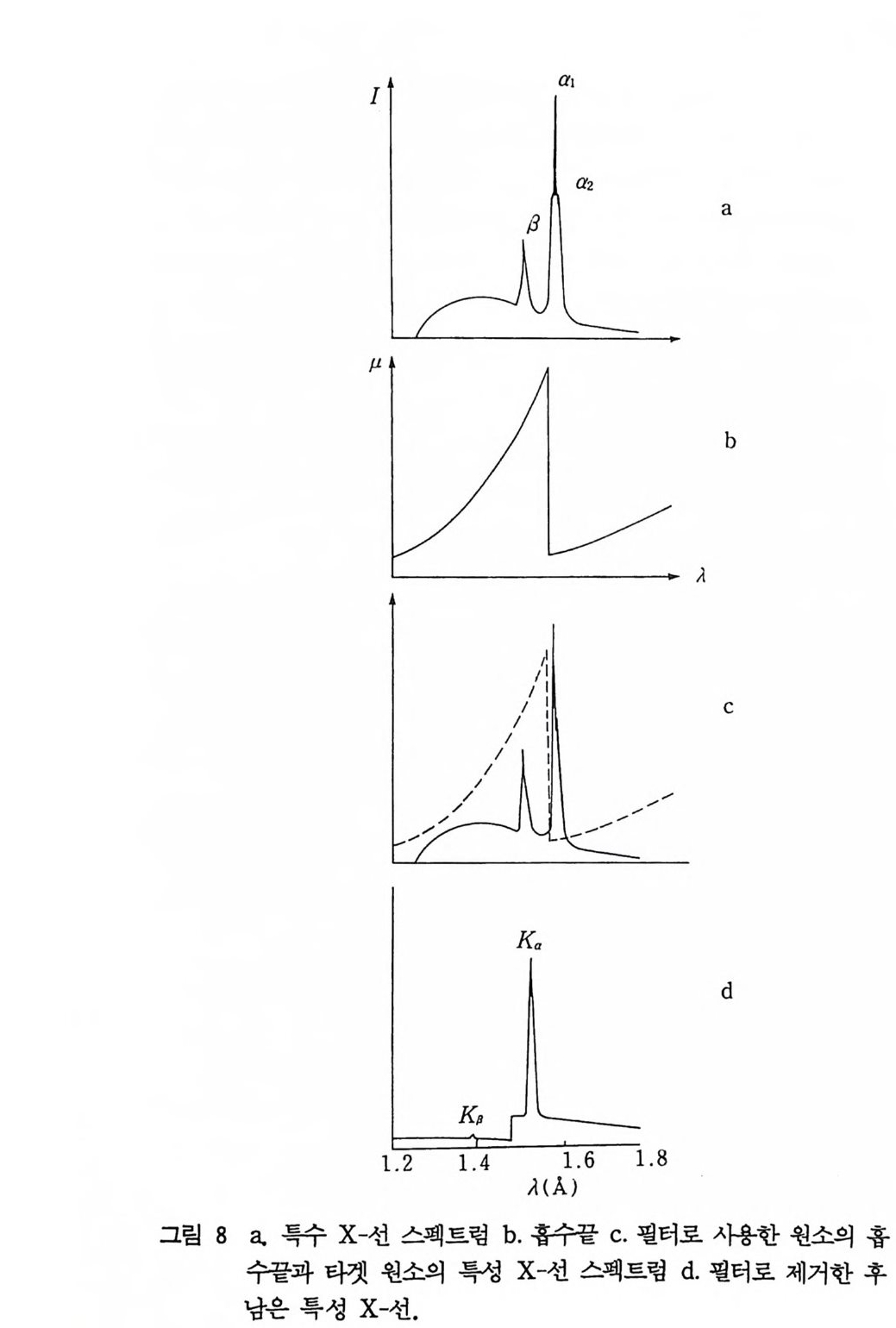 I a1
I a1
x- 선의 빔을 지르코늄 필터에 통과시키면 지르코늄 (Zr) 필터는 0.6874A 이하의 파장을 가지는 X- 선을 강하게 흡수하고 Mo 의 K 려 (0.71073A) 을 남긴다. 그후 이트륨 (Y) 필터를 통과시키면 0 . 7255A 보다 적은 X- 선을 가장 강하게 흡수하고 이 두 필터의 두께를 조정하면 연속 x - 선의 짧은 파장 쪽을 서로 균일하게 흡수 한다. 이러한 필터를 균형 필터 (balanced filt er) 라고 부른다. 이러 한 방법으로 측정한 X- 선의 강도는 두 흡수끝 사이의 영역에 놓여 있는 X- 선만 남고, 즉 Mo Ka 선의 강도만 남게 된다. 7 X- 선의 발생 전술한 바와 같이 에너지가 큰 고속의 전자 빔이 타겟울 때리고 감속될 때 X- 선이 발생한다. x- 선관은 (a) 전자의 발생장치 (b) 고 전압을 줄 수 있는 장치 (c) 금속 타겟울 반드시 갖추어야 한다. 또 대부분의 전자의 운동에너지는 타겟에서 열로 바뀌므로 고온에서 녹는 것을 방지하도록 물로써 냉각해야 한다. x- 선 관에는 (a) 기 체관(거의 오늘날에는 사용 안함) (b) 필라멘트관의 두 종류가 있다. 1) 기체관(t ube) 1895 년 W ilhe lm Conrad Roen tg en 은 기체관을 사용하여 X -선을 발견하였다. 이 기체관은 이제는 구식이므로 사용하지 않는 다. 기체관내에 공기의 압력이 아주 낮으면 무거운 기체는 음극을 때린다. 음극에 도달하면 이온은 음극의 표면에서 전자를 떼낸다. 이 전자 음극선은 양극을 향해 가속된다. Roen tg en 은 음극선이 진공된 관의 유리벽을 때릴 때 내는 빛, 죽 형광에 홍미가 있었다. Roen tg en 은 기체관을 종이로 덮어 형광을 희미하게 하고 관에서 먼 거리에 바륨 시안화백금 스크린을 두고 찬란하게 빛나게 하였으
 /I//
/I//
며, 그는 보이지 않는 복사선이 관의 공기를 통해 옆의 스크린을 빛나게 한다고 하였는데 이것을 X- 선이라 불렀다. 기체관은 많이 개선되었지만 이제는 사용하지 않는다. 큰 결점은 기체관의 전압은 기체 X- 선 관내의 기체 압력을 변화시켜야만 가 능하다는 것이다. 이러한 결점은 전자발생 장치로 뜨거운 필라멘트 를 사용함으로써 극복되었다. 2) 필라멘트관 1913 년 Cooli dg e 가 처음으로 발견하였다. 필라멘트관은 진공 으로 된 유리관의 한쪽 끝에는 양극이 다른 끝에는 음극이 있으며, 음극은 텅스텐 필라멘트로 되어 있고 양극은 물로 냉각시킨 구리덩 어리로 되어 있는데 희망하는 금속 타겟이 한쪽 끝에 삽입되어 있 다. 그립 9 는 필라멘트관의 내부구조를 보여주고 있다. 고전압 변 압기의 도선의 한자락은 필라멘트와 연결되어 있고 다른 자락은 어 스 (ear t h) 와 연결된다. 타겟은 냉각수와 접촉됨으로써 자동적으로 어스 (ear th)된다. 필라멘트는 약 3~3.5Am p의 필라멘트전류로 가열되고 전자가 방출된다. 이 전자는 약 50KV 의 고전압으로 가 속되고 타겟에 충돌한다. 필라멘트 주위에는 필라멘트가 갖는 고전 압으로 유지되어 있는 작은 금속 컵이 있고 이것은 전자를 반발하 고 타겟의 좁은 영역, 죽 초점으로 전자를 집중시킨다. x- 선은 초 점에서 모든 방향으로 방출되고 X- 선 관내의 두세 개의 Be 창문을 통해 X - 선 관 밖으로 방출된다. x- 선 튜브(t ube) 의 전압은 고전 압 변압기의 전압을 조정하는 자동변압기로 조정된다. 볼트메타는 입력되는 전압을 나타내나 출력 전압을 나타내도록 조정할 수도 있 다. 밀리암미터 (m illi amme t er) 는 X- 선 튜브의 전류, 즉 필라멘트 에서 타겟으로 흐르는 전류의 흐름을 나타낸다. 전류는 보통 10~30mA 의 크기이고 필라멘트 가변저항기로 조종한다. 가변저 항기는 필라멘트 변압기의 출력 전압을 조종하고 이 출력 전압은
필라멘트의 전류, 필라멘트의 온도와 일초당 방출하는 전자의 수를 결정한다. 필라멘트 튜브에는 밀봉된 튜브와 교환할 수 (demoun t able) 있는 튜브의 두 가지 종류가 있다. 밀봉된 튜브는 공장에서 튜브를 진공 하고 밀봉한 것이다. 조작하기 편리하고 듀브내를 고전공으로 만들 필요가 없다. 그러나 가격이 비싸고 튜브의 수명이 필라멘트의 수 명으로 결정된다. 교환할 수 있는 튜브는 오늘날에는 특수한 목적 에만 사용되고 필라멘트와 타겟은 교환 가능하다. 죽 타버린 필라 멘트와 타겟을 교환할 수 있으나 조작중에 연속적으로 전공을 유지 해야 하므로 고전공을 얻기 위하여 확산 펌프와 기계 펌프가 모두 필요하다. 기체튜브는 조작하기는 어려우나 타겟이 다른 금속으로 오염되지 않으므로 순수한 X- 선 복사선을 얻을 수 있다. 필라멘트 튜브에서는 때때로 필라멘트에서 텅스텐이 증발하여 타겟에 달라 붙 고그러면텅스턴 (W) 이타겟의특성 X- 선뿐만아니라, 텅 스 턴의 L
 전자
전자
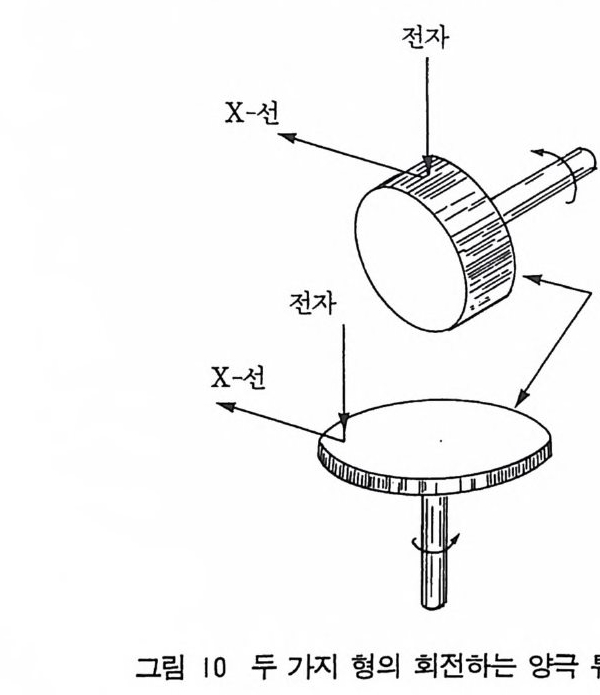
선울 방출하는 수가 있다 ( W 의 L 야기 전압은 10,200Vol t이다). x- 선 튜브의 초점의 모양과 크기는 가장 중요한 특성 중 하나이 다. 타겟의 조그마한 면적내에 전자의 에너지를 집중시켜 큰 강도 의 X 선을 얻는다. 필라멘트 튜브는 선 모양(실제는 직사각형 모 양)의 초점을 얻기 위해 필라멘트를 나선형으로 감는다. 모든 X -선 튜브는 튜브에 손성을 주지 않고 견딜 수 있는 최고의 전압, 전류의 한계값이 있다. 이 한계는 어떤 튜브 전압에서 최고로 허용 되는 튜브 전류로 표시된다. 어떤 X - 선 듀브는 양극을 회전시킬 수 있다. x_ 선 튜브는 X - 선을 생산하는 데는 그 효율이 보통 1% 이하이다. 또 결정에 의 한 X - 선의 회절은 이 값보다는 훨씬 적다. 따라서 회절된 X- 선 빔의 강도는 매우 낮다. 따라서 사진 필름상의 회절 패턴을 얻기 위해서는 여러 시간을 X- 선에 노출시켜야 한다. 이러한 문제를 해 결하려면 X- 선 발생원의 강도를 크게 해주어야 한다. 이러한 문제 룰 해결할 수 있는 한 가지 방법은 회전할 수 있는 양극을 가지는 튜브를 만드는 것이다. 즉 양극을 계속 회전시키면 항상 신선한 타 겟 (fres h t ar g e t)을 주고 따라서 양극을 크게 가열시키지 않고 큰 동력을 걸 수 있다. 그림 10 에서는 회전하는 양극을 가지는 X- 선 듀브의 두 가지 형을 보여주고 있다. 여기에서는 양극 타겟울 연결 하고 있는 축대가 움직이고 고정된 초점을 가지는 튜브보다 5~10 배 정도 큰 동력으로 가동시킬 수 있어서 투과 사진법에서 X- 선 노출시간을 훨씬 작게 할 수 있다. 8 X- 선의 검출 x- 선 빔을 검출할 수 있는 주요한 방법으로 사진 필름, 형광스 크린, 계수기 (Coun t er) 의 3 가지 유형이 있다.
1) 사진 필름 역사적으로 보면 Roen tg en 은 음극 튜브 가까이 바륨 백금 시안 아이드 (bar i um p la ti noc yni de) 로 덮은 스크린으로 X - 선을 검출하 였다. 3 가지 유형의 X- 선 검출기 중에서 사전 필름은 영구적인 기록을 준다. 다른 검출기는 X- 선에 대해 빛이나 전기의 펄스 (Pulse) 를 주고 이 펄스는 X- 선이 지나가면 사라진다. 물론 다음 실험을 위하여 이 펄스를 기록할 수 있다. 사진 필름은 X - 선 회절 실험에서 2 가지 중요한 이점이 있다. 사진 필름은 필름상의 어떤 점을 지나가는 X- 선의 수를 나타낼 뿐만 아니라 여러 가지 크기로 회절된 빔이 공간에서 상대적으로 어떻게 배열되는가도 나타낸다. 필름의 또 다른 이점은 영구적 기록을 얻을 수 있고 검토하기 쉬 우며 크기가 작아서 저장하기 쉽다는 데 있다. x - 선 회절 실험의 사진기록 장치는 보통 사용하는 다론 기록형보다 가격도 저렴하다. 큰 결점은 상대적으로 정확성이 떨어지고 X- 선 강도 측정에서 감 도 (sens itivity)가 낮다. 또 X- 선의 강도를 필름에서 절대적 눈금 으로 측정할 수 없다. 그러나 필름의 좋은 점은 많은 응용에서 단 점을 훨씬 능가하여 훌륭한 장치를 갖춘 실험실에서도 필름법은 널 리 쓰이고 있다. 필름에서 상(i ma g e) 은 사진의 유탁액 중의 Ag B r 알맹이가 X- 선 광자가 지나갈 때 이온화하여 적당한 현상액으로 환원하여 유리된 은으로 바뀜으로써 된다. A g Br 알맹이로 필름의 양쪽에 덮으므로 X- 선 광자와 작용하는 확률을 2 배로 증가시키는 것이 가능하다. 따라서 이중으로 A g Br 로 덮은 필름은 노출을 적 게 해도 되고 회절 실험에서 가장 많이 사용된다. 이중으로 덮은 필름은 결점이 있는데 X- 선 빔이 첫번째 충에서는 두번째 총보다 침투에 따른 흡수가 감소함으로써 더욱 심하게 검게 된다. x- 선 빔이 비스듬한 각도로 입사하면 형성된 상은 균일하게 검 게 되지 않는다. x- 선 빔 위치가 비스듬한 각도로 입사할 경우 정
확히 측정을 해야 하며 양면으로 덮여진 필름은 쓰지 않는 것이 좋 으며 한 면만 덮은 필름은 노출시간을 길게 해야 한다. 최근에 매 우 빨리 현상하는 방법이 E. H. Land 에 의해 고안되었다. 이것의 현상과정은 보통의 폴라로이드 카메리에서 포함하고 있다. x- 선 회절 스펙트럼의 현상은 노출이 완결된 후 10 초 만에 완결된다• 현재는 평평한 나무판자 모양의 카메라 카세트만 있으나 현상이 대 단히 빠르고 간편하여 많이 쓰이고 있다. 2) 형광 스크린 형광 스크린은 마분지 위에 소량의 니켈을 함유한 황화아연의 얇 은 충으로 만든다. x - 선의 작용으로 이 화합물은 가시광선 영역에 서 형광을 나타낸다. 즉 노란색을 낸다. 대개의 회절 빔은 너무 약 해서 이러한 방법으로는 검출할 수 없다. 따라서 형광 스크린은 X 선 회절 장치와 같은 기계를 조정할 때 1 차 빔을 알아내는 데 사 용한다. 3) 계수기 계수기는 X- 선을 펄스전류로 바꾸는 정치이고 단위시간당 펄스 전류의 수는 계수기에 들어오는 X- 선의 강도에 비례한다. 세 가지 종류의 계수기, 즉 비례 계수기, GM(Geig e r-Muller) 계수기, 섬 광 (sc i n till a ti on) 계수기가 현재 널리 사용되고 있다. 연습문제 1. Cr Ka X 선에 의한 공기의 질량 흡수계수와 선 흡수계수를 계산하라. 단 공기는 무게비로 80% 의 질소와 20% 의 산소로 되
어 있고 공기의 밀도는 1. 29 X 10 - 3 g / cm3 이고 Cr Ka X 선에 의한 질소의 질량 흡수계수는 24.42cm2 / g m 이고 산소의 질량 흡수계수는 37 .10 cm2/gm 이다. 2. Cu 의 K 껍질의 전자를 들뜨게 할 수 있는 전압을 계산하라. 단 K 의 Ak edg e = 1. 38059A 이다. 3. Mo 의 Lm 흡수끝의 파장을 구하여라 . 단, Mo 의 Ak=0.61978A 이고 Aka,=O.70930A 이다. 4. N i의 밀도는 8.91 g m / cm3 이다. N i의 Cu Ka X 선에 의한 질 량 흡수계수는 48.83cm 2/ g m 이다. 본래의 강도의 1 / 2 로 Cu Ka X- 선의 강도를 감소시키는 N i필터의 두께를 계산하여라. 5. Cu Ka1 X 선의 파장을 계산하라. 단, 구리의 K 흡수끝의 파장 은 1. 3 8059A 이고 Lm 흡수끝의 파장은 13 . 288A 이다. 6. X- 선 필름의 감도는 사홍하는 X- 선 파장에 대해 필름의 Ag B r 의 질량 흡수계수에 비례한다. 그러면 Cu Ka X- 선과 Mo Ka x- 선에 대한 필름의 감도의 비를 계산하라. 7. MoKa 선과 CuKa 선의 파장은 각각 0 . 71073A 과 1.54 184A 이다. 이둘 X 선 빔의 전동수와 에너지를 구하라.
제 5 장 회절 (I) l 서론 x- 선의 성질과 결정의 기하학을 이미 공부했으므로 이제 이 두 가지 를 결부하여 이들이 서로 작용할 때 생기는 X- 선의 회절 현상 에 대해 생각하자. 오랫동안 광물학자와 결정학자는 결정에 대한 지식을 쌓고 결정의 면간의 각도, 화학분석, 결정의 물리적 성질 등을 측 정하였다. 그러나 결정의 내부 구조에 대한 지식은 거의 없 었으나, 결정은 원자나 분자를 주기적으로 반복시켜 만둘 수 있다 고 추정하였다. 또 X- 선은 전자파로서 파장이 대략 1~2A 이 된 다고 생긱하였다. 회절의 현상은 찰 이해되었고 가시광선이 g ra ti n g에 의해 회절되는 것처럼 회철은 파의 파장이 산란점 사이 의 반복 거리와 같은 치수를 갖는다면 파가 규칙적으로 간격을 가 지는 산란체와 만나면 회철 현상이 일어난다. 이러한 것이 독일의 물리학자인 von Laue 가 1912 년에 이러한 문제에 대해 생각할 때 그때까지 알고 있는 지식 수준이었다. 규칙적인 간격을 가전 원자 로 이루어지면 X- 선이 전자파로 파장이 결정내 원자간 거리와 같 다면 결정내 원자는 이러한 생각 아래 이 가설이 맞는지를 실험하 였다. 황산구리의 결정을 X- 선 빔 통로내에 두고 회절 빔이 있으 면 기록할 수 있도록 사진 건판을 두었다. 이 같은 시도는 성공적
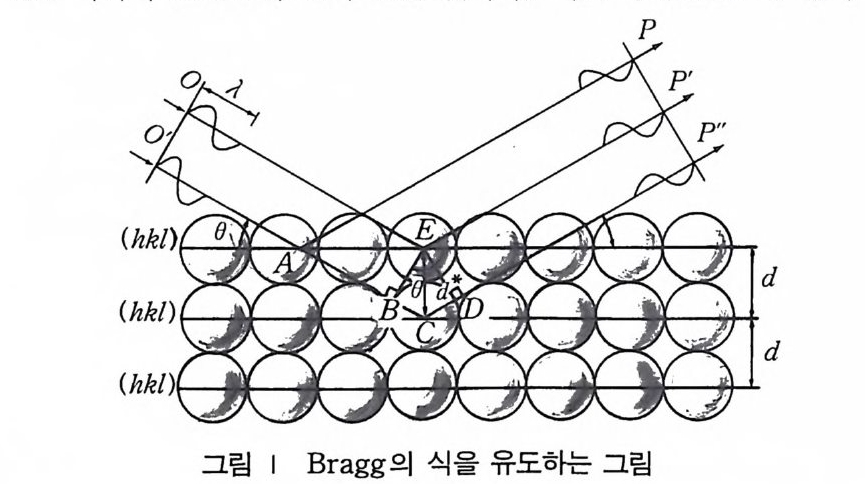
으로 달성되었고 사진 전판에 회절 무늬가 나타나므로 X 것 1 은 결 정으로 회절됨울 증명할 수 있었다. 영국의 물리학자인 W. H. Brag g(l86 2~ 1942) 와 그의 아들인 W.L. Bra gg (1890~1971) 는 Laue 의 실험에 깊은 홍미를 느꼈고 W. L. Bra gg는 1912 년 Laue 의 실험을 성공적으로 해석하고 von Laue 가 생각한 것보다 더 간단한 수식으로 회절 조전을 표현 하였다. 또 X 선 회절 무늬로써 결정 구조를 해석하려고 시도하여 NaCl 형의 구조를 가전 NaCl, KCI, KBr, KI 등의 구조를 해석하 였다. 2 Bragg 의 법칙 Roen tg en 이 X 선을 발견한 후 물리학자들아 X- 선을 더 잘 알 수 없었던 것은 X- 선 강도와 에너지를 연관시킬 수 없었기 때문이 다. Planck 가설 E=hv=h c/ 11 로 Bra gg는 X- 선이 반사하는 각 도와 X- 선의 파장 A 사이의 관계를 구하려 했다. 결정이 주기적으 로 반복되는 나란한 원자의 평면으로 되어 있다면 결정 구조는 평 면을 따라서 보면 그림 l 과 같을 것이다. 서로 평행인 X 국 1 빔이
 P
P
결정과 0 각도로 부딪친다고 하자. x- 선은 파도와 같이 취급할 수 있고 입사 빔은 공통적인 파의 정면, 죽 모든 입사 빔은 서로 위상(p hase) 이 맞다. 위상이 맞는 것은 파가 서로 작용함을 이해 하는 근본이 된다. 이것은 그림 2 를 보면 알 수 있다. 그립 2 에서는 동일한 파장과 동일한 전폭을 가지는 두 파를 더 할 때 무엇이 일어나는가를 보인 예이다. 각각의 예에서 두 개의 각각 다른 파를 왼쪽에 보아고 이것의 합의 합성파를 오른쪽에 보· 이고 있다. 그림 2 에서 (b), (c}i =-위 상의 차가 서로 다르다. 파의
 ( a ) 三 합성파 ,.
( a ) 三 합성파 ,.
위상 (Phase) 은 임의의 점에 대한 꼭지점의 위치이다. 이 위치는 보통 파장의 분수로써 표시하고 이 분수를 360° 혹은 27[ 라디안 (rad i an) 을 곱하여 위상을 각으로써 표현할 수 있다. 죽 위상의 차 이가 (1/4 )/t이면 1/4X360=90° 혹은 7[ / 2 라디안이다. 임의파의 위상은 파가 이동함에 따라 시간에 따라 변하지만 동일한 속도와 파장을 가지는 두 파의 위상은 시간에는 무관하다. 합성파는 동일 한 파장 A 를 가지고 합성파의 강도 I 는 전폭 A 의 제곱에 비례한 다. 그림 2-(a 제서는 파의 위상의 차가 없다. 죽 영이다. 이 경우 완전히 보강 간섭이 일어나고 두 파는 위상이 맞는다(i n p hase) 라 고 한다. 원래의 파의 진폭이 1 이면 합성파의 진폭은 2 이고 강도 는 4 이다. 그림 2-(b 세서는 위상의 차가 A / 4 이다. 부분적인 보강이 일어 나고 합성파의 진폭은 1. 4 가 되고 강도는 2 이다. 그림 2 -( c 제서 는 위상의 차는 -1/ 2 이다. 이 두 파는 완전히 위상이 벗어나고 (ou t of ph ase) 상쇄간섭이 일어나서 합성파는 없다. 죽 합성파의 전폭 이 영이고 강도도 영이다. 그림 1 에서 X- 선파 OE 와 0'A 는 평면 (hkl) 에 각도 O 를 이루 면서 EP' 와 AP 로 산란한다. 경로 길이 OEP' 와 O'AP 는 서로 같고 따라서 PP' 에 같은 위상을 가지고 도착한다. 이것이 결정내 의 한 평면으로 위상에 맞게 산란하는 조건이다. 아래쪽의 결정 평 면충에 대해 어떤 제한을 주는지 입사 X- 선 O'C 와 산란하는 X -선 CP 를 생각하자. EB' 는 파의 정면 00' 와 평행이고 비슷하 게 ED 는 P'P 와 평행이다. 총 경로 길이 O'CP 는 OEP' 와는 다음 길이 (스)만큼 길다. 6.= BCD=2BC=2dsin 0 두번째 평면에 의한 산란 X- 선인 O'CP' 가 PP'P 에서 첫번째 평면에 의해 산란된 O'AP 와 OEP'가 서로 위상이 맞으려면 경로
의 차 스 는 파의 진동수의 정수배 nA( 여기서 n=l, 2, 3 ··· …)가 되 어야 한다 . 따라서 결정내에서 규칙적인 간격을 가지는 나란한 평 면에 의해 산란되는 X- 선이 위상이 맞으려면 다음 조건이 만족되 어야한다. 쩌 = 2ds i n 0 (5-1) (여기서 n= l, 2, 3 …… ) 이 관계식은 W. L. Bra gg가 유도한 식이고 Bra gg식이라 부른 다. 이 식은 회절이 일어니는 기본 조건식이다. n 은 회절의 차수 라 부른다. n= l 일 때는 1 차 반사라고 부르고 OEP ' 가 O'CP 는 1 A 만큼의 경로의 차가 있다. x - 선이 산란되는 양상에는 두 가지가 있다. (1) 일원자 기체와 같이 공간에서 무질서하게 원자가 배열된다. 이때 산란은 모든 방향으로 일어나나 약하다. 산란강도는 더해진다. (2) 완전한 결정체에서와 같이 원자가 공간에서 주기적으로 배열 된다. 가) 몇몇 방향에서는 Bra gg법칙이 만족되고 산란은 강하고 이것을 회절이라 하고 진폭은 보강된다. 나) 대개의 방향에서는 Bra gg법칙이 만족되지 않고 산란 X -선이 서로 상쇄되므로 산란이 일어나지 않는다. 결정에 의한 X- 선의 회절과 가시광선의 거울에 의한 반사는 모 두 입사각과 반사각이 갇으므로 비슷한 현상같이 보인다. 또 원자 의 평면은 X- 선을 반사하는 작은 거울처럼 생각할 수 있는 것처럼 보이나 회절과 반사는 세 가지 면에서 근본적으로 다르다. (1) 결정에 의해 회절된 빔은 입사 X_ 선 빔의 경로에 놓여 있는 결정내 모든 원자에 의해 산란된 X- 선으로 이루어지나 가시광선의 반사는 얇은 표면충에서만 일어난다. (2) 단색 x- 선의 회절은 Bra gg법칙을 만족하는 어떤 특별한 입
사각을 가진 X- 선만으로 일어나나 가시광선의 반사는 입사각에 관 계없이 항상 일어난다 (3) 좋은 거울에 의한 가시광선의 반사는 거의 100% 의 효율이 있으나 산란된 X- 선 빔의 강도는 입사 빔의 강도에 비해서는 아주 적다. 이러한 차이에도 불구하고 회절 평면이나 회절 빔이라는 말대신 보통 반사 평면, 반사 빔이라는 말을 쓴다. 따라서 반사라는 말은 실제 회철이라는 뜻을 암암리에 의미한다. 요약하면 회절은 다수의 원자가 서로 침여하는 산란 현상이다. 원자는 격자상에서 주기적으 로 배열되므로 원자들 사이에 산란된 X- 선은 서로 일정한 위상 (p hase) 의 관계를 가지고 대부분의 방향에서는 상쇄 간섭이 일어 나고 몇몇 방향에서만 보강 간섭이 일어난다. 전술한 바와 같이 회절은 X- 선의 파장이 산란 중심 사이의 반복 거리, 죽 원자간 거리의 크기와 치수가 비슷할 때 일어난다• 이것 은 Brag g 법칙에서도 알 수 있다. 즉, sin 0 의 값은 1 보다 적다. 따라서 Bra gg법칙에서 까 /2d=s i n 0< 1 (5-2) 죽 ntl는 2d 보다는 적다. 또 n 의 가장 작은 값은 1 이므로 tl,< 2d 이어야 한다. 대개의 결정 평면에서 d 는 3A 정도의 크기이다. 따라서 A 는 6A 보다는 작아야 한다. 자의선 복사선의 파장은 500A 범위이므로 결정은 자의선 복사선을 회절시킬 수 없다. 또 A 가 너무 작으면 회절 각도는 너무 작아서 쉽게 측정할 수 없다. Bra gg법칙은 다음 식으로 표시할 수 있다. J= 2(d/n) ·sin B (5-3) A 의 계수가 1 이므로 평면간 간격이 A 의 계수가 n 일 때의 1/n 인 실제 이러한 평면이 있든지 혹은 가상적인 평면이든지간에 이러
한 평면에서 얻은 1 차 반사로서 생각할 수 있다. 이 식은 대단히 편리하다. 여기서 가상적인 평면(fictiti ous p lane) 이라고 한 것은 평면이 격자접을 지나가지 않기 때문이다. 전술한 2 장에서 알 수 있는 바와 같이 평면 간격 d100 는 d200 의 2 배이다. 일반적으로- dhkl 는 dnh nk nl 의 n 배이다 (M ill er 지수의 정 의에서 (nh nk nl) 평면은 (hkl) 평면과 평행이고, 평면 간격은 (nh nk nl) 평면은 (hkl) 평면의 l /n 이다). 죽, dhk1= n• dnh nk nl (5-4) 따라서 nA= 2dhkl sin 0 A= 2(dhki/ n) •sin 0 (5-5) A=2dnh nk n1·sin 0 (5 一 6) 위의 식에 의하면 (hkl) 평면에서 얻은 n 차 반사는 (nh nknl) 평 면에서 얻은 1 차 반사로서 생각할 수 있고 이때 평면간 거리는 dnh nk n1= dhki ln 이 된다. 일반적으로 결정학에서는 n 을 생략하여 표시한다. 즉, 11=2dhk1sin 0 혹은 11=2dsin ehkl (5-7) (5-6) 식과 (5-7) 은 동일한 식이나 n 을 생략하여 표시한 것이다. Bra gg가 Bra gg분광기로 단결정에서 나온 X- 선의 스펙트럼을 연구할 때 평면 간격 (d) 도 X- 선의 파장 (A) 도 몰랐다. 이러한 문 제를 극복하기 위해 W. L. Bra gg는 소금 (NaCl) 의 결정을 깎아서 평면 (100), (110) 과 (111) 평면에서 반사를 얻도록 결정을 배열하
였다. 이러한 결정에서 얻은 개략적 회절 강도는 그림 3 과 같다.
 버 기
버 기
그림에서 (111) 회절 강도는 다른 것과 달리 강도가 교대로 약해 졌다 강해졌다 한다. 이것은 (111) 평면에 따라 원자의 종류가 다른 것이 교대로 배열되어 있음을 암시해 주고 있다. 각각 (111) 평면에 서 한 종류의 원소는 상에 맞게 정렬되고 다론 종류의 원소는 싱에 맞게 정렬되어 있지 않다. 그림 4 의 NaCl 의 구조는 이미 W. L. Bra gg에 의해 제안되었으며 Bra gg는 x- 선 실험으로 실험적으 로 증명하였다. (100), (110) 과 (111) 평면에서 얻은 회철 반서에 대해 sin 8 의 값을 Bra gg식에 대입하면 다음 식을 얻는다.
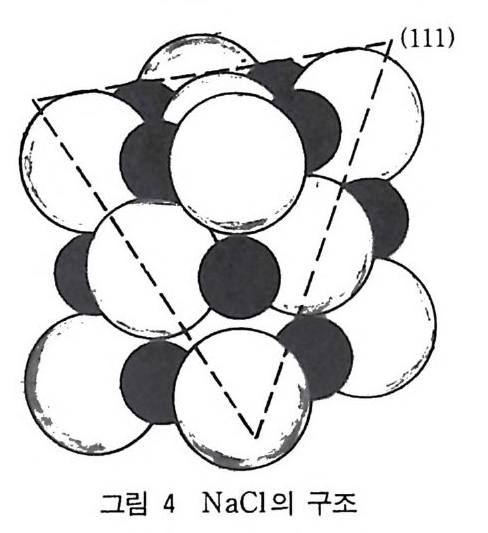 그림 4 NaCl 의 구조
그림 4 NaCl 의 구조
n1=2d1oo(O.126) n2= 2duo(O .178) n3= 2 du1 (0 . 109) (5-8) 입방정계 격자에서 dIOo= 譯 dIIO ’ dIOo= 譯 dm d110= (M,) d111 (5-9) 위의 관계식을 대입하고 A 를 소거하면 다음 관계식을 얻는다. 뚜duo= - ((0O ..112768) )nn2l -=v 譯 ' 뿌n2 =끄 (5-10) 따라서 n1=n2 이다. (5-11) 또
年= (O .l09) nl =譯 du1 -( 0 .126) n3 따라서 n1=2na (5-12) 위의 식을 동시에 만족시키려면 n,=2, n2=2 이고 113 = 1 이 되 어야 한다. 이것은 관측한 반사는 실제 (200), (220), (111) 평면에 서 얻은 반사임을 뜻한다. 따라서 그림 3 의 위의 두 개의 그립에 서 할당한 평면은 (100) 가 아니고 (200) 이며 (110) 가 아니고 (220) 임을 뜻한다. 또 NaCl 의 면심입방 격지를 가짐을 알 수 있 다. 결정 구조가 결정되면 NaCl 의 밀도에서 단위세포의 격자 상 수 a 를 쉽게 다음과 같이 계산해낼 수 있다. 밀도(p)=麟 결정에 대해서는 다음과 같이 쓸 수 있다. 밀도= 단위단세위포세내포 원의자 부의피 무 게 (5-13) p= I:AV/ N (5-14) 여기서 p는 밀도(gm /cm3) 이고 ~A= 단위세포내 모든 원자의 무게이고 N 은 Avo g adro 수이고 v 는 단위세포의 부피이다. p= ~vNA =- (6 . 02257X~ 10A23 ) v'x 10-24 = l.660V4 I 2~A (5-15) 여기서 v'는 단위세포의 부피 (A3) 이다. 그런데 NaCl 의 실험식 량은 58.45amu 이고 NaCl 결정의 밀도는 2.15 g m/cm3 이다. 또
단위세포에는 네 개의 NaCl 이 포함된다. 따라서 2 .15 (g m/cm 이 = 1 . 66042 (a538 . 45 X 4) a=5.6 5 2A 그리고 a 드 (2d200) 3 이다. dzoo= 2 . 8260A 여기서 그때까지 알 수 없었던 X- 선의 파장을 계산할 수 있다. t1= 2 d2oosin 0=2dzoo(0. 12 6) = 2(2 . 8260) (0 .12 6) A =0 .7125 A 따라서 Mo 복사선의 Ka 선의 파장이 O.7125A 임을 알 수 있었 다. 이 값이 최초로 결정한 X- 선 파장이다. 참고로 정확한 Mo Ka 선의 파장은 O.71073A 이다. 3 역 격 자 (Rec ipr ocal latt ice ) 실제 결정은 3 처원이다. x- 선 회절 무늬에서 보는 역격자도 3 차원이다. 역격자는 실제 결정격자와 서로 간단하게 관련지어진다. 회절 반점이 공간에서 배열된 것을 측정하여 단위세포의 치수와 역 격자뇌 모양을 계산할 수 있다. 여기서 실제 결정격자의 모양과 단 위세포를 계산할 수 있다. Bra gg법칙은 다음 식으로 표시할 수 있다. s i n0= 뿐》 sin e 는 결정격자에서 평면간 거리인 d 에 반비례한다. d 값이 크면 회절 무늬가 압축되고 d 가 작으면 확장된다. s i ne 와 1/d
은 비례한다. 역격자는 1 / d 값을 기초로 하고 있다. 역격자 세포 를 정의하는 세 개의 벡터를 a*, b* 및 c* 로 표시한다. a* 는 실 제 세포를 나타내는 벡터 b 와 c 에 수직이고 b* 는 a 와 c 에 수직 이다. c* 는 a 와 b 에 수직이 되어야 한다. 역격자점을 정하기 위 해서는 다음과 같은 방법으로 정한다. (1) 공통되는 원점에서 각 평면에 수직선을 그린다. a* 는 b 축과 c 축에 수직인 벡터를 그리고 b * 는 a 축에 수직인 벡터이다. (2) 원점에서 1/dhkl 과 같은 거리에 점을 찍는다. 이것이 역격자 점 d*(hkl) 이다. 그림 5-(a) 2 단사정계의 실제의 격자이고 그림 (b) 2 이에 대응 되는 역격자이다.
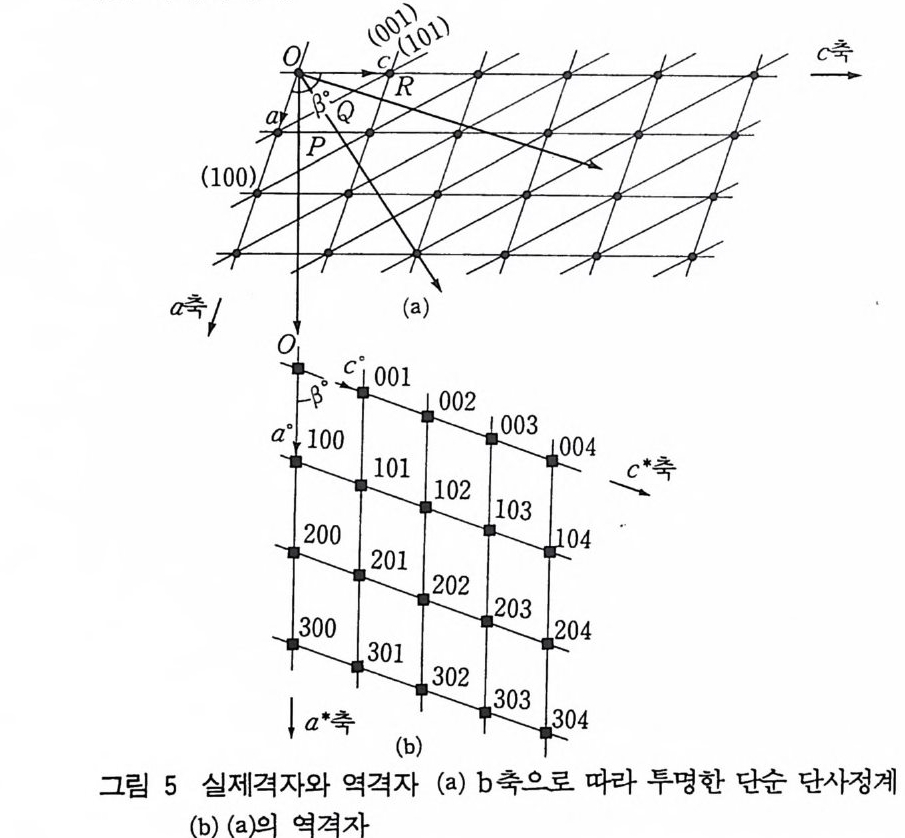 邊
邊
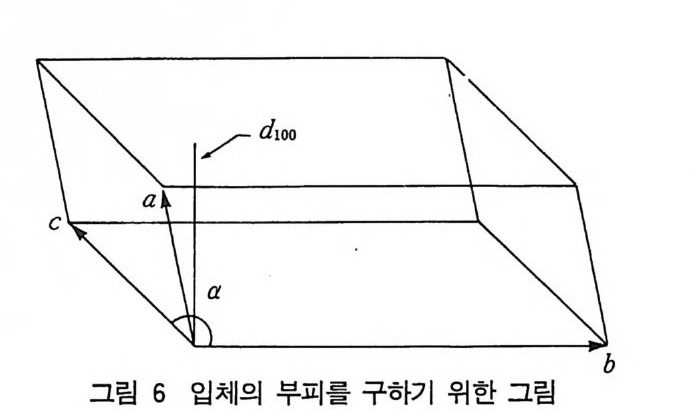
단계 2 에서 다음 관계식이 성립한다. d*(hkl) =K-J - (5-16) dhkl 여기서 K 는 역격자를 구성하는 데 사용한 척도 인자 (scale fa c t or) 이다. 평면간의 거리를 생각하면 d100=2d200=3d300… … 이 다. 따라서 d*(lOO)=½ d*(200)=½ d*(300)= ……이다. 역격자에 대해 수학적으로 생각해 보자. 그림 6 과 같은 입체물 의 부피를구해 보자. v = ( b, c 평 면의 면적 ) • 높이 = ( b • c) sin (1. d100= ( b x c) • d100 一d1l 00 •n• =~a *밑=면V~ 적 = bVx c bXc (밀면적) ·-a;cos(d10 려-: a 사이의 각도) = a· b(bX xc c) (5-17) 여기서 벡터 대수학에서 평면에 수직되는 것을 단위벡터 n 으로 나타내었다. 같은 방법으로
 _,,,,,-d 100
_,,,,,-d 100
b*= a· c(bx xa c) (5-18) c*= a·a(bx xb c ) 역격자와 실격자 벡터의 관계에서 다음 식을 얻을 수 있다. a*· b=O a• ·c =O b*·c=O b*• a=O c*· a=O c• • b=O (5- 1 9) a*·a=l b*· b=l c*· c=l v*· v=l 일반적으로 역격자 공간에 다음 관계식이 성립한다. d*(hkl) = ha* + kb* + le* 이것은 원접에서 역공간의 점 hkl 까지의 거리이다. 이 관계식은 그립 6 울 보면 쉽게 알 수 있다. 또 d*(hkl) • d*(hkl) = d*2(hkl) =h2a* 2+ k2b*2+ !2c * 2 +2klb* c *cos a* +2lhc* a * co s (J* + 2hka* b*cos r* = 1/dhkl· l/dhkl cos 0 =l/dhkl (5-20) 입방정계, 사방정계 및 정방정계에서는 a* = / 3*= r*=90° 따라 A1 1/dhkl= h2a*2+ k2b*2+ l2c*2 (5-21) 이다. 입방정계에서는
a*2= b*2= c*2= 1/a2 d2 ( hkl) = a2/ ( h 도 섬+ l2) (5-22) 다른 결정계에 대해 정리하면 표 1 과 같이 쓸 수 있다. 육방정계에서는 a*=b*= t= c*, a*= /3 *=90 ° 이고 r*=60 ° 이다. 따라서 1/ d hk/= (h2+ hk+ k아 a*2+ !2c *2 (5-23) 이다. 그 밖의 결정계에 대해서 표 l 에 수록하였다.
 표 I 7 결정계에 대한 d*(hkl) 과 d(hkl) 의 표현식
표 I 7 결정계에 대한 d*(hkl) 과 d(hkl) 의 표현식
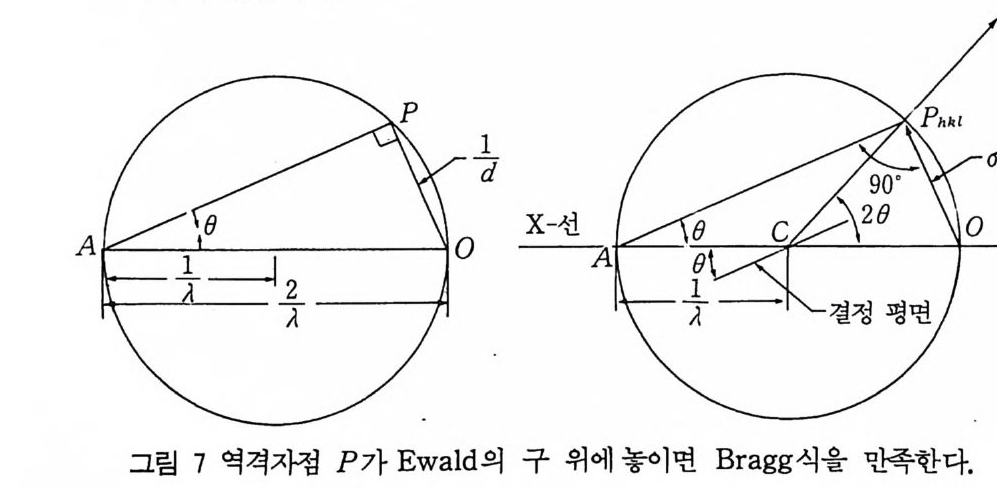
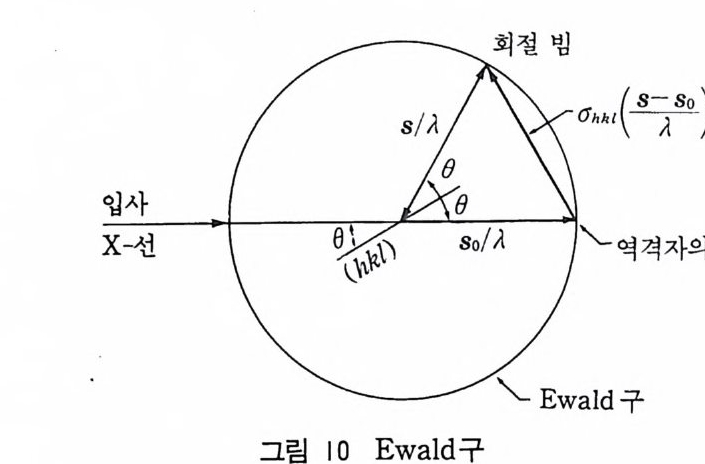
4 역격자와 X- 선 회절과의 관계 역격자를 써서 결정과 평면 사이의 기하학적 관계식을 비교적 간 단히 나타낼 수 있고 이것은 X - 선 회절 현상을 취급하는 데 매우 유용하다. Bra gg법칙이 만족하여야 X- 선 회절이 일어나고 회절 각도 Bhkl 로 Bra gg식을 다음과 같이 나타낼 수 있다. sin 0h1, 1 = (11/2) /dhk1= (1/ d h1, 1 ) I (2/ 11 ) (5- 2 4 ) 위의 식에 의하면 원의 중심을 지나는 삼각형을 그리면 원 둘 레 위 의 각은 g o· 이다. 그러면 지름이 2 / 11 이고 수선은 l / d11kl 이 된다. 1/dhk t = · d*(hkl) 이므로 그림 7 과 같이 그릴 수 있다. 수평 직 경 AO 는 입사하는 X- 선의 방향을 나타낸다. 乙 PAO 는 Brag g 각 0 가 되고 원의 중점은 C 이다. OP 는 결정평면에 수직아 되고 그 길이는 d*(hkl) 아다. 또 乙 OCP=2L OAP =2 0 이다. 그림 7 에서 다음을알수있다. (1) 결정은 원의 중심 c 에 놓여 있고 원의 지름은 2 / 11 이다. (2) X- 선 빔이 결정을 통과한 후 원을 떠나는 점 O 는 결정의 역 격자의 원점이다.
 1d 6hl
1d 6hl
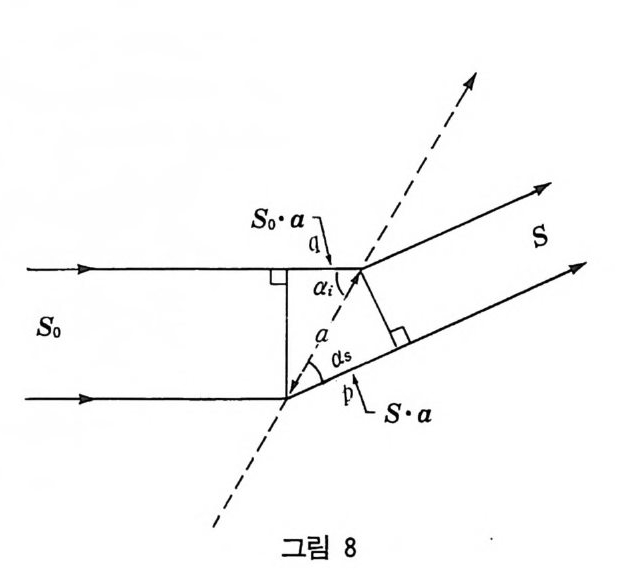
(3) 역격자점이 원주 (3 차원에서는 구) 위에 놓이면 Bra gg법칙이 만족되고 회절된 X - 선 빔은 역격자점을 지나간다. (4) X - 선 회절은 원 위에 역격자점이 놓일 때 (3 차원에서는 구) 일 어나고 이 구를 Ewald 구 혹은 반사의 구 (s p here of re fl ec ti on) 이 라 부른다. 역격자는 Ewald 구를 써서 X - 선 회절 실험을 설명할 수 있다. 회절은 역격자점이 반사의 구와 만날 때 일어나고 회절된 빔은 교점을 지나고 회철된 X- 선 빔의 사진 기록은 역격자를 기록 하고 역격자의 개념은 회절을 이해하고 해석하는 데 꼭 필요하다. 5 Laue 의 회절조건 그림 8 과 같이 주기적인 원자의 열을 생긱하코. 원자간 간격을 a 라 하고 입사 X - 선 방향의 단위벡터는 So 이고 원자의 열에 의해 산란된 X- 선 방향의 단위벡터를 S 라고 하자. 그림 8 의 두 X- 선 의 경로의 차는 서로 위상에 맞으려면 파장이 정수배가 되어야 한 다.
 I
I
경로의 차=p_q =rA (5-25) 여기서 r 은 정수(― oo< r
 • • • • • • • • •
• • • • • • • • •
a· (ha*+ kb*+ le*) = r 따라서 r=h 이다. (5-29) 같은 방법으로 s=k 이고 t =l 이다. 그러면 Laue 의 식은 다음 식으로 변형된다. a· (s— So) = htl b·(s ― So)= 臥 c· (s-So ) = ltl (5-30) 세 개의 서로 갇은 평면에 놓여지지 않은 3 차원적 주기적인 원 자열의 a, b, c 가 상에 맞게 산란되려면 위의 식 (5-30) 이 동시 에 만족되어야 한다. 죽 (5-30) 의 세 개의 식이 동시에 만족하면, 죽 세 개의 원추가 서로 만나면 하나의 칙선이 되므로 회절된 X -선 빔은 다만 하나의 허용된 방향을 갖는다.
6 X- 선 회절 실험장치 x- 선 사진법은 보통 단결정을 사용하는 것과 분말을 사용하는 것이 있고 상세한 결정구조 해석을 알고자 하면 잘 만들어전 단결 정이 있어야 하고 회절 데이터는 적절한 사진법 중 하나를 사용하 여 수집하거나 혹은 단결정 회절 장치를 써서 회절 데이터를 수집 한다. 그러나 화합물의 특성을 X- 선 패턴에서 알고자 하면 소량의 미세한 분말 물질을 취하여 분말 사진법이나 분말 X - 선 회절 장치 롤 써서 확인하면 된다. 구조 해석에서는 분말법은 별로 많이 쓰이 지 않는다. 단결정 X- 선 회절법으로 결정계, 단위세포 상수를 알 수 있고 단위세포내에 들어 있는 화학종의 수와 공간군을- 결정할 수있다.
 (Jh k/ (두터
(Jh k/ (두터
1) 분말법 X 선 분말 회절법은 1916 년 독일의 Deb y e 와 Scherrer 그리고 1917 년 미국의 Hull 이 각각 독립적으로 고안하였다. 이 분말법은 가장 일반적으로 많이 사용하는 회절 방법이고 적절히 사용하면 많 은 구조적 정보를 얻을 수 있다. 근본적으로 이 방법은 분말시료를
단색 X - 선으로 회절시키는 것이다. 단색광 이란 타겟 물질의 K -야기전위 이상의 전압으로 가동시켜 X- 선 튜브에서 필터를 사용 하여 강한 K 특성 성분을 얻어서 사용함을 뜻하고 분말 이라함은 실질적으로는 분말을 결합제 (b i nder) 로 쓰거 나 하여 다결정 (po lyc rys t a l lin e fo rm) 을 서로 결합시킨 실질적이고 물리적인 분말 울 뜻한다. 분말법에는 시료와 필름의 상대적인 위치로 세 가지의 방법을구별할수있다. (1) Deby e -Scherrer 방법 : 실린더의 표면에 필름이 있고 실린더 의 축중심 위치에 시료가 있다. (2) 집중 사전법 (Focus i n g법) : 필름, 시료, x- 선 원이 모두 각 각 실린더의 표면상에 있다. (3) 핀호울 사전법 : 납작한 사진필름은 입사 X - 선 빔에 대해 수 직 방향으로 두고 시료에서 편리한 거리에 둔다. 여러가지 분말 카메라가 회절 장치에 대해 경쟁적으로 사용되나 회절 장치는 회절선의 위치와 강도를 동시에 빨리 측정할 수 있다. 카메라는 회절 장치에 비해 싸다. 사진법은 일반적으로 느리고 선 강도를 측정하려면 많은 시간을 들여 측정해야 한다. 전형적인 Deb y e-Scherrer 카메라를 그림 11 에 나타내었다. Deb y e-Scherrer 카메라는 햇빛이 들어오지 않도록 만든 뚜껑을 가진 원통형 방울 가지고 있어서 입사 X- 선이 coll i ma t or 를 지나 가게 하고 통과하는 빔을 정지시키는 빔 스탑 (beam s t o p)과 내부 카메라 원주에 장착된 필름을 잡아 주는 장치와 회전하는 시료 홀 더 (holder) 로 만들어져 있다. 카메라 직경은 5cm 에서 20cm 까지 있고 직경이 클수록 필름 상에 쌍을 이룬 선들이 잘 분리된다. 분광학에서 분해능은 A/ 스 A 로 표시된다. 여기서 스 A 는 두 개 파장 사이의 차이를 나타내고 A 는 평균값이다. 여기에서는 거의 같은 평면간 간격을 가전 평면에 서 얻은 회절선을 분리하는 능력이다. 죽 d/ 6. d 이다. 필름상에서
 그림 I I Deby e -Scherrer 카메 라 뚜껑을 벗겨 놓았음 .
그림 I I Deby e -Scherrer 카메 라 뚜껑을 벗겨 놓았음 .
 x- 선 s
x- 선 s
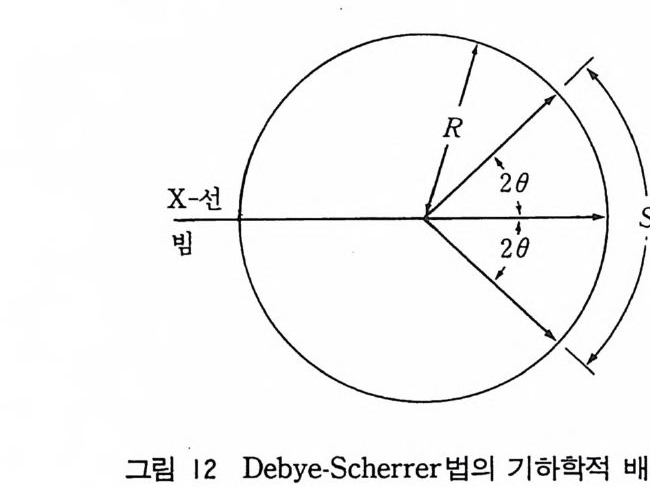
쌍을 이룬 호의 길이를 S 라고 하자. 그립 12 에서 S=R·40 f:::.S =R•f::: .4 0 (5-31 ) 여기서 R 은 카메라의 반경이다. 거의 비슷한 평면 간격을 가전
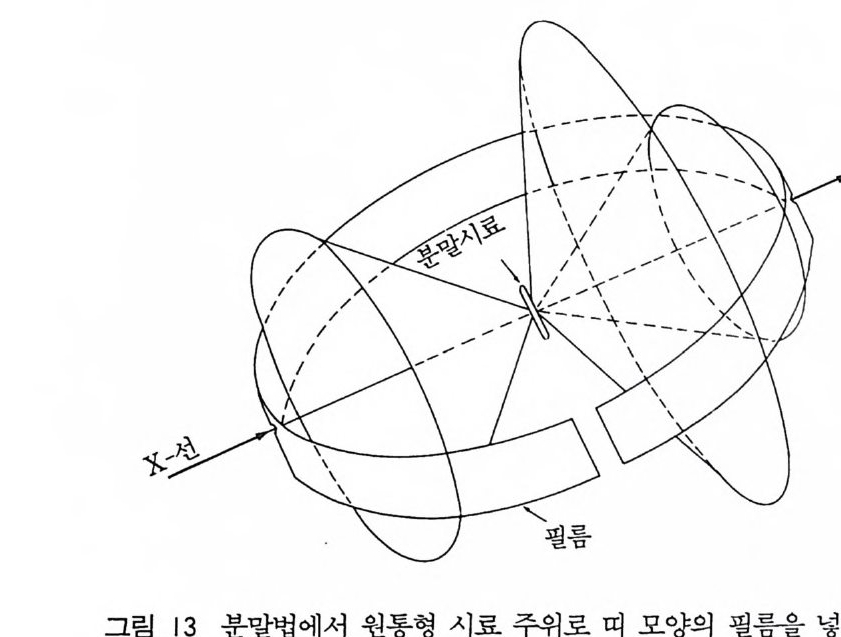
두 조의 평면이 두 개의 회절 빔 사이를 작은 각도 640 로 나누고 있다. (5-31) 식을 보면 주어전 640 값에 대해 필름상에서 쌍을 이룬 두 호 사이의 거리는 카메라의 반경 R이 클수록 크다. 분해 능은 Bra gg식을 d 와 0 에 대해 미분하여 얻을 수 있다. 11=2d sin () 0=2dd sin ()+2 d cos () d() d()/dd= (-1/d) (sin ()/cos ()) (5-32) = (-1/d) ta n () 여기서 필기체 소문자 d 는 미분을 나타내고 평면간 거리는 d 로표시하였다. 그러나 d0=dS/4R 따라서 dS/dd=— (4 R/d) ta n 0 분해능= d/ 6. d= 一 (4R/6. S )ta n 0 (5-33) 여기서 d 는 두 조의 평면간의 평균거리이고 6. d 는 그 간격의 차이이다. 위의 식 (5-33) 에 의하면 분해능은 카메라의 반경이 커 지면 커진다. 분말법에서 관측한 실험치의 해석 방법은 어떤 실험 배열을 사용 했는가에 따라 다르다. 그림 13 과 같은 사전 필름의 배열을 가졌 다고 하자. 그림에서 볼 수 있는 바와 같이 X- 선 빔이 들어가서 필름에 나오는 점 중간 위치에 필름이 찰라져 있다` 이런 모양은 M. S t rauman i s 와 A. Lev i ns 가 고안한 방법인데 다음의 이접이 있다. 죽 필름 조각 하나로 o· 에서 g o· 까지 총 회철기록을- 정확히 얻을 수 있다. A. J. C. W il son 은 필름이 갈라전 위치가 정확히
 `II ` 一 一 一一
`II ` 一 一 一一
중간 지점에 있을 필요가 없다고 했으며 결정이 작은 0 값에서만 반사 반점을 줄 경우는 전면 반사 영역에 필름이 갈라진 곳에 두면 좋다고했다. 필름에서 평면간 간격을 얻으려면 각각의 반사에 대해 상에 쌍을 이룬 호 (ar c) 사이의 거리 (s) 에서 계산해야 한다. 필름상의 한 쌍 의 호 사이의 거리를 특별한 필름 측정 장치를 써서 측정하면 편리 하다(그립 14). 그림 14 에서 회절각 O 와 측정한 호의 길이 S 사이의 관계를 다 음식과같이 알수있다. 40=5/R 0=S/4R rad = (180/1r) • (1/4R) S deg (5-34) R 은 카메라의 반경이므로 괄호 안의 값은 일정한 값이다. S 와
 101-·· 。 a
101-·· 。 a
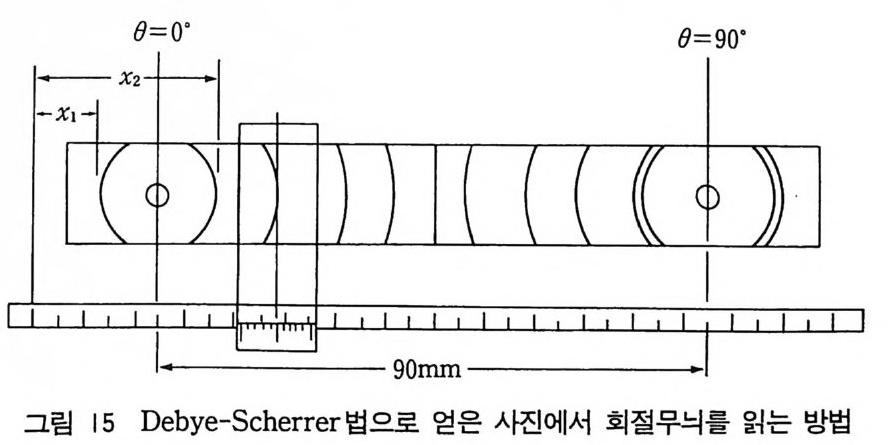
R 은 보통 m illi me t er 단위로 측정한다. 그림 15 에서 S=x 2 -x1 이다. R 이 57.26mm 일 때는 0=0 과 0=90° 사이의 간격은 90 mm 이다 ( R 이 11 4 . 6mm 일 때는 0=0 파 0= 9 0° 사이의 간격은 180 mm 이다). 만약 이 간격이 P% 만큼 틀리면 S 값에 대해 Sx P / 100 만큼 더해 주어야 한다. 이 수정한 호의 길이룰 표해서 S' 으로 표시한 난 밀에 기재한다. R 이 180/mnm( 죽 57 . 26mm) 이면 수 정한 호의 길이 S' 는 다음과 같다. 0= (180/ 7f나 /4· 7r/l80) S'= S'I4 deg (5- 35 )
 0=0° 0=90·
0=0° 0=90·
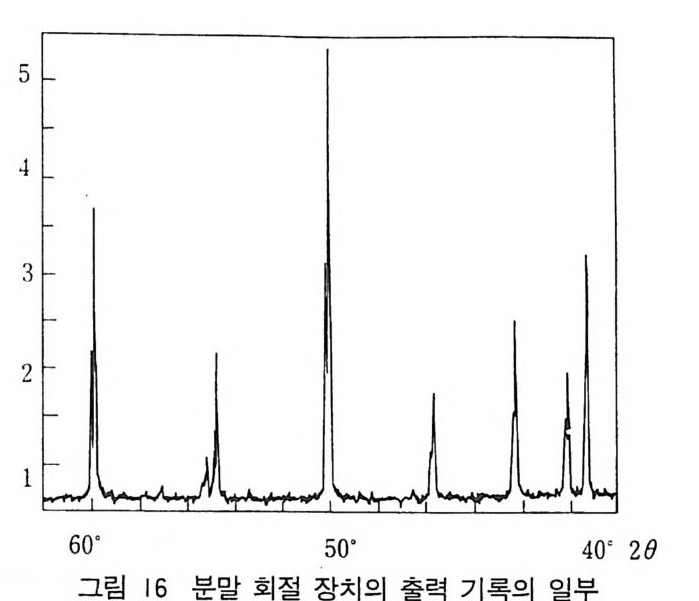
위의 식에서 보면 카메라의 반경이 180/ 元 =57.26mm 이면 계산 이 편리하고 회절각이 바로 m illi me t er 눈금과 같다. 2) 분말 회절장치 (dif frac to m ete r ) Deb y e-Scherrer 카메라법은 간단하고 모든 회절 반점을 동시에 기록할 수 있는 이점이 있으나 회절 빔을 정량적으로- 정확히 측정 하기 어렵다. 분말 회절 장치는 20 의 조그마한 범위에 걸쳐 반사 의 위치를 측정해야 한다면 빠른 시간내에 실험을 마칠 수 있는 이 점이 있다. 그러나 전자적으로 회절 강도를 측정한다면 훨씬 좋을 것이다. ‘이러한 목적으로 보통 많이 쓰는 검출기 (de t ec t or) 는 섬광 계수기 (sci nt i llat i on counte r ) 이고 이것은 X- 선 광자물 흡수할 때 마다 섬광을 방출하는 얇은 결정판(보통 Tl 불순물기 들어 있는 NaI 결정)으로 되어 있다. 섬광 계수기의 출력은 더욱 증폭되고 X- 선 광자가 도착하는 율을 기록지에 기록한다. 검출기가 Bra gg각도에 따라 계속 움직이면 회절 패턴이 20 각도로 보정된 기록지에 그림 16 과 같은 피크를 기록할 수 있다. 이렇게 하여 여러 가지 반서를 사전 필름에서와 감이 한꺼번에는 기록 못하지만 연속적으로 기록 도할도 수 중있가다.시 킬또 수적 당있다한. 시그간 내원에리 는회 절그 림실 험1을7-( a끝) 내에 기나 타위내한었 회다.절 강x -선은 이 책의 종이의 수직 방향에서 원통형 표면 위에 얇은 충의 분말시료 S 에 쪼여지고 회절 X- 선은 F 에 모여진다. 이러한 조건은 모든 X- 선이 시료충에 대해 같은 각도를 만들고
 표 I I De y be-Scherrer 법으로 0 률 구하는 고멍을 나타내는 표
표 I I De y be-Scherrer 법으로 0 률 구하는 고멍을 나타내는 표
 5
5
 P
P
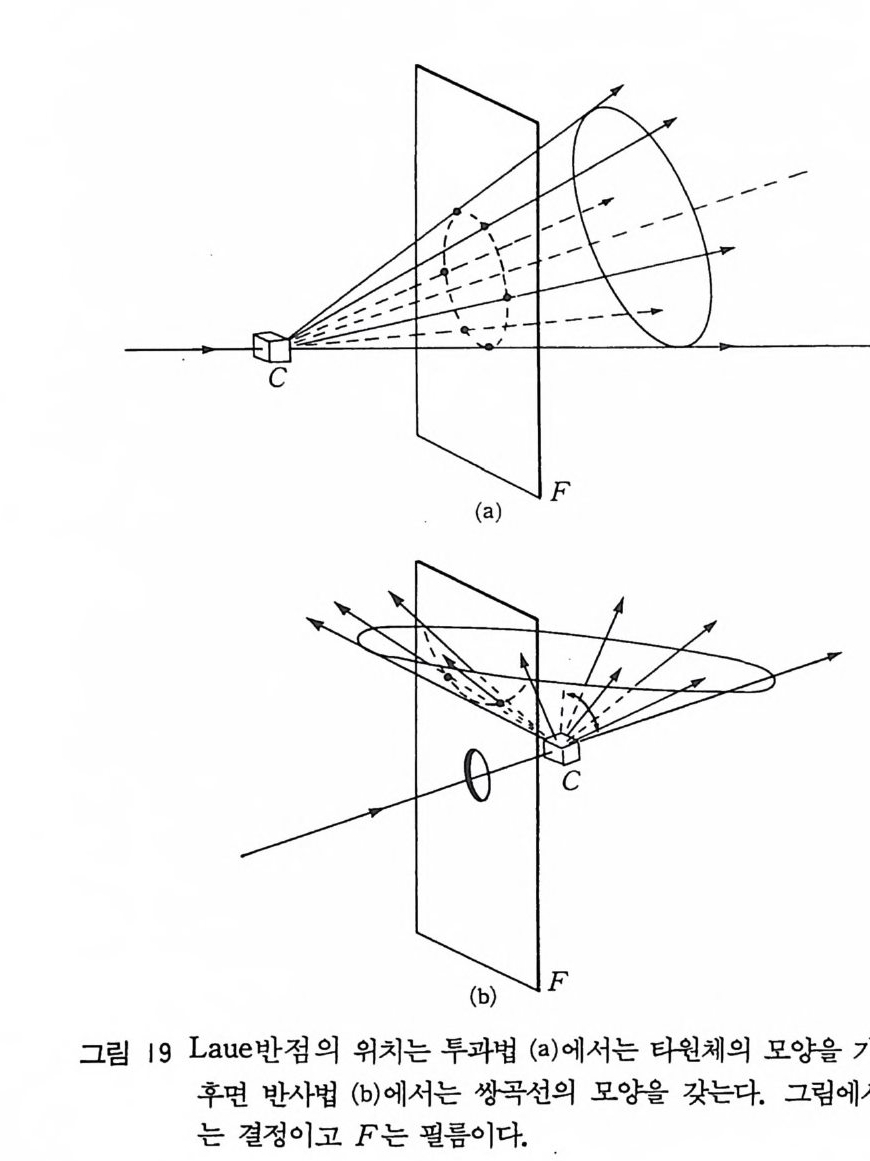
있음을 의미하고 만약 이 각도가 시료 표면에 평행으로 놓여 있는 한벌의 평면에 대한 Bra gg각도 0 라면 반사 X - 선은 F 로 집중된 다. 검출기 D 는 섬광 계수기로 되어 있고 슬릿 뒤에 있다. S 가 큰 반경의 원통상의 일부에만 놓여 있고 S 가 평면 모양이면 X - 선 은 일반적으로 정확히 F 에 집중시킬 수 있다. O 를 바꾸기 위해 S 를 회전시킬 수 있고 F 에 슬릿이 있고 검출기가 S 의 중심에서 선회하는 축위에 놓여 있으면 검출기는 2 배나 빨리 회전하고 대칭 적으로 X- 선을 집중시키는 조건은 몇 도에서 100 ° 까지의 20 의 모 든 각도에 걸쳐 유지된다. 분말시료는 유리나 도자기 혹은 금속판 안의 홈 위쪽이 열려 있 는 곳에 분말을 충전시켜 만들 수 있다. 또는 분말을 아세톤으로 반죽을 만들어서 현미경용 슬라이드 위에 반죽을 펴고 아세톤을 증 발시키면 분말은 유리 표면에 적당히 붙어 있어서 분말시료로 사용 할수있다. 3) Laue 법 Laue 법은 최초로 Laue 가 사용한 실험법으로 X- 선은 모든 가 능한 파장을 가지는 백색 X- 선(혹은 연속 X 선)을 사용하고 이 X -선은 고정되어 있는 단결정에 쪼이도록 한다. 결정은 X- 선 빔을 회절하고 결정의 내부구조를 나타내는 아름다운 회절 반점을 나타 낸다. Bra gg식을 이용하여 실험 결괴를 이해할 수 있다. 결정은 X 선 빔에 대해 고정되어 있다. 결정의 d 값이 고정될 뿐만 아니 라 0 값도 고정된다. 따라서 변할 수 있는 값은 정수 n 과 파장 A 이다. 따라서 Laue 회절 사전에서는 어떤 파장값을 가전 1 차 반사 와 파장의 방 A 값을 가전 2 차 반사와 §A 값을 가진 3 차 반사 등 이 관찰된다. 단결정에서 얻은 Laue 사전은 결정 평면의 스테레오 두영이다. Laue 방법에는 X- 선 원, 결정과 필름의 상대적 위치에
따라 두 가지 방법이 있다. 각 방법에서 모두 사진 필름의 평평하 게 입사 빔에 대해 수직 방향으로 둔다. 투과 Laue 법은(그림 18) 필름은 결정 뒤에 두고 X- 선 빔은 결정 전면에서 진행하여 결정을 회절시키도록 한다. 이 방법에서는 회절 빔온 결정을 부분적으로 두과하기 때문에 투과 Laue 법 (tra nsmi ss io n Laue me t hod) 이라고 부른다. 후면 반사 Laue 법은 사진 필름을 결정과 X- 선 원 사이 에 두고 입사 X - 선 빔은 필름내의 구멍을 통과하여 후면 방향으로 회절된 빔이 기록된다. 필름상의 반점은 그림 19 와 같이 어떤 곡 선상에 놓여진다. 이 곡선은 투과 패턴에서는 타원형 모양이고 후 면 반사 패턴에서는 쌍곡선이다. 필름상의 반점의 위치는 투과나 후면 반사 모두 입사 빔에 대해 결정의 배치를 나타낸다. 결정이 어느 정도 구부러져 있거나 비틀어져 있으면 회절 반점은 찌그러져 있거나 희미하게 된다. 따라서 Laue 법은 결정의 방위를 결정하거 나 결정의 질을 알아내는 데 시용할· 수 있다. 4) 움직이는 결정과 움직이는 필름법 회전 결정법 Laue 법에서는 연속 복사선을 사용하고 결정과 필름은 고정된 위치에 있다. 그러나 회전 결정법에는 단색광 X- 선을 사용하고 단 결정은 회전하고 필름은 고정된다.
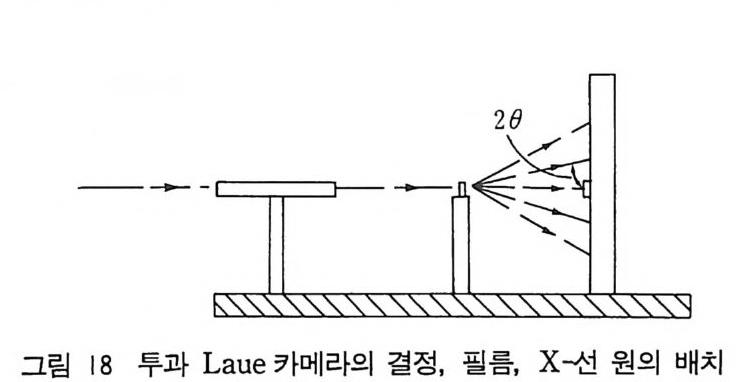 20
20
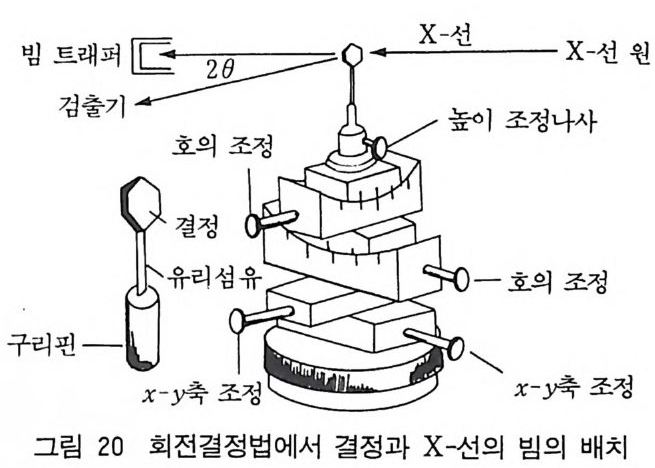
한 변의 길이가 대략 0 . 1~2mm 의 단결정을 유리 섬유 위에 붙 이고 이 유리 섬유는 다시 고니오메타 머리 위에 붙인다. 결정의 방위를 조정하여 결정의 결정학적 축(실질적으로 결정의 주축) 주위 로 회전되도록 한다(그림 20).
 c
c
 빔트래퍼 X 선 X 선원
빔트래퍼 X 선 X 선원
 결정 회전축
결정 회전축
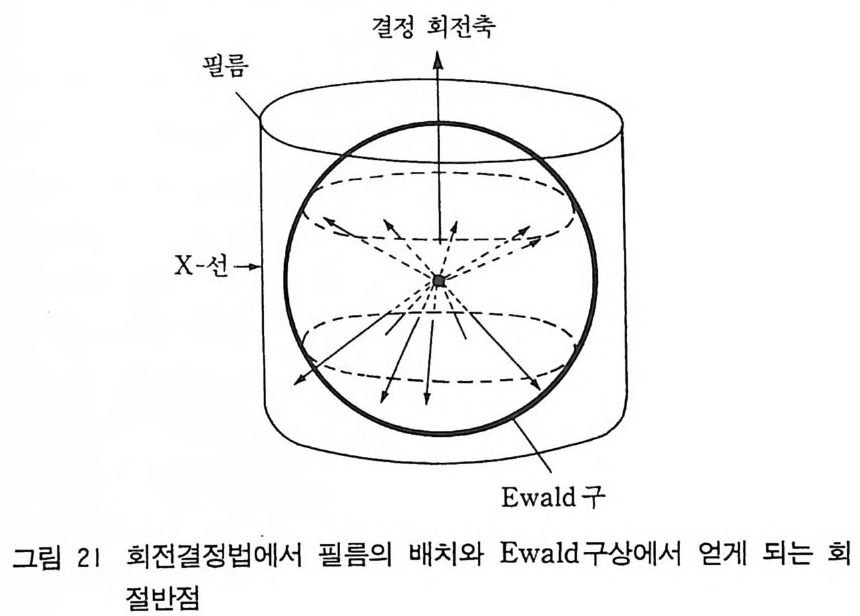
콜리메이터를 통과한 단색 X- 선은 결정의 회전축에 수직 방향으 로 입사시킨다. 그림 21 에서 보듯이 필름은 회전축 주위로 원통형 으로 놓아서 회절 반점을 기록한다. 결정내의 여러 평면은 X- 선 빔을 반사하고 결정이 회전됨에 따라 각각의 평면이 회절 위치에 오게 된다. 죽 Bra gg식이 만족된다. 회전축이 결정의 c 축이라
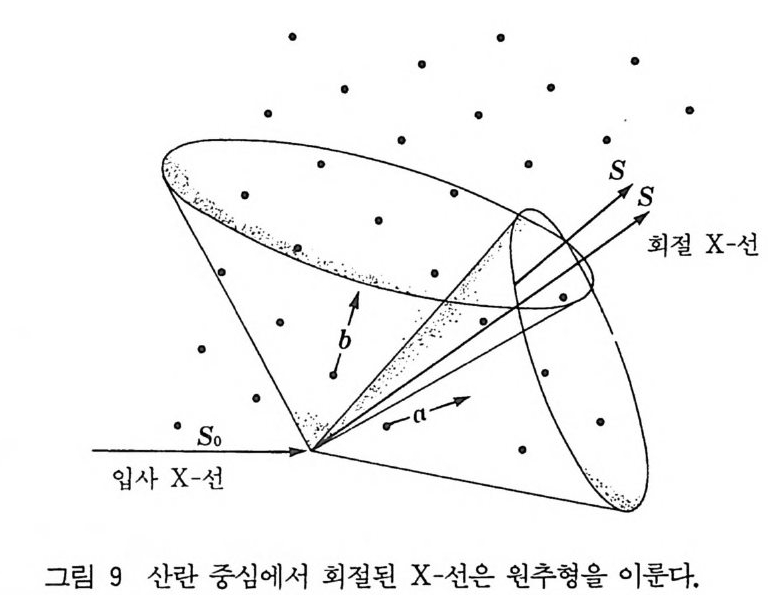
하자. 같은 [지수를 갖는 모든 (hkl) 평면은 같은 원뿔 (cone) 의 표 면에 반사 반점을 나타낸다(원뿔의 꼭지각은 Laue 식에 만족됨). 회절 사진을 보면 결정에서 모은 개개의 회절 반점은 필름에 직 선을 이룬다. 선 사이의 간격에서 결정의 회전축의 길이룰 계산할 수 있다. 필름상의 반점이 만든 패턴의 대칭에서 단위 세포의 대칭 성을알수있다. 5) Weis s enberg 법 We i ssenber g법은 회전법을 발전시킨 법이다. 전형적 인 Weis s enberg 카메라를 그림 22 에서 개략적으로 보여주고 있다. 홈이 있는 원통형 스크린이 결정과 필름 사이에 놓여 있고 원통형 스크린은 결정의 회전축 주위에 같은 축 상에 놓여 있어서 사전 필 름상에 한 개의 회절선 원뿔만이 나타나도록 되어 있다(그림 23). 사전 데이터를 수집할 동안 결정은 약 180° 회전하고 동시에 필 름 홀더 (holder) 는 회전축에 평행하게 회전축을 따라서 진동하면서 병전운동을 한다. 이렇게 하는 동안 스크린은 정지되어 있고 한 충
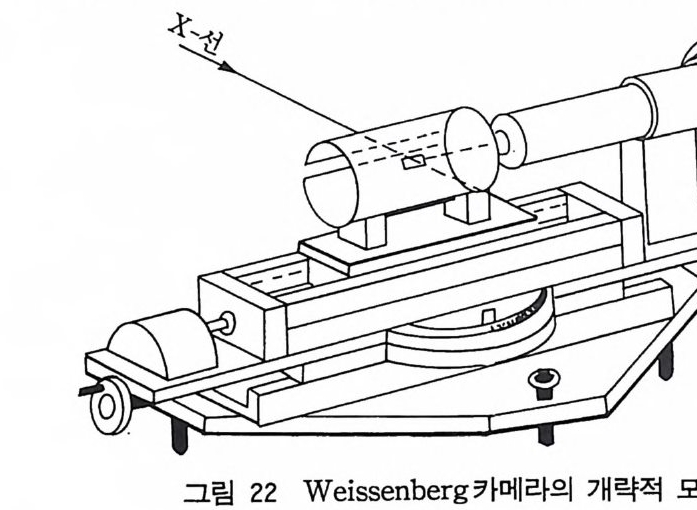 그림 22 We i ssenber g카메라의 개략적 모양
그림 22 We i ssenber g카메라의 개략적 모양
 x - 선 ,/--/./ I I,平 l\ l 1l\- ,- --'- s
x - 선 ,/--/./ I I,平 l\ l 1l\- ,- --'- s
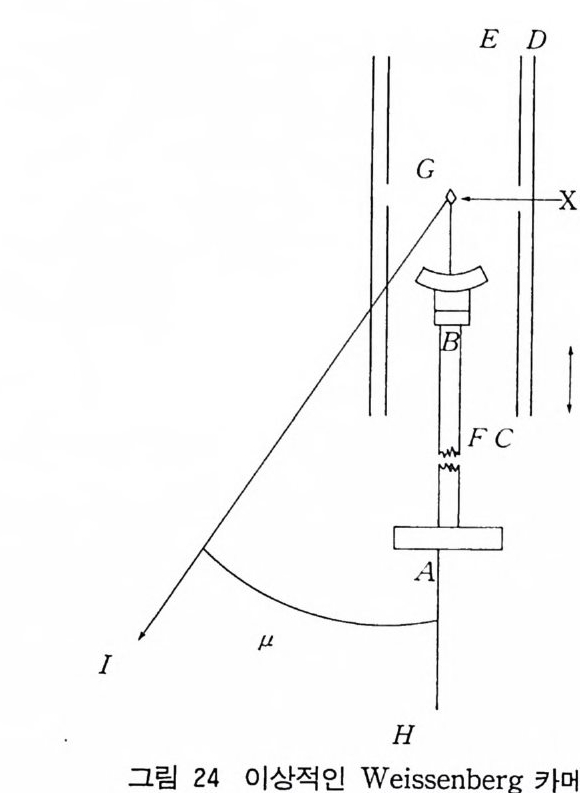
의 데이터만 수집된다. 결정의 회전과 필름 홀더의 병전운동은 보 통 기어로써 조종되고 1· 회전은 2mm 이동과 같다. 그림 24 는 이상적인 Weis s enberg 카메라를 보여주고 있다. 이 방법으로 얻은 데이터를 이해하려면 결정의 역격자를 생각해 야 한다. 결정에 의한 회절된 X- 선 회절선의 원뿔은 결정축이 a 축 주위로 회전하면 한 조의 평면, 죽 nkl 에 의해 나타난다(여기 서 n 은 정수임). 각 충선상의 각점은 결정내의 한 조의 평면, 예컨 대 평면형 {001} 에 의해 생성된다. 이것은 역격자에서 하나의 반점 으로 나타난다. 각 충선은 필름상에 2 차원적 역격자 그림을 투영 한것이다. We i ssenber g카메라의 스크린은 움직 일 수 있고 반사의 충선은 하나씩 하나씩 따로따로 얻을 수 있다• 사진에서 결정축과 축 사이 의 각도를 알 수 있고 또 계통적으로 관측되지 않은 반사의 M ill er 지수를 알아내어 단위 세포의 공간군과 대칭을 알아낼 수 있다. We i ssenber g카메라는 가창 많이 사용되는 X- 선 카메라이 고 과거 40 년 동안 결정구조를 알기 위해 회절 강도를 얻는 데 사 용해왔다.
 E D
E D
(1) 결정의 축 주위로 미리 정하여 조정해 둔 각도만큼 진동한다. (2) 필름 홀더 CD 는 미리 정하여 조정해 둔 거리만큼 CD 를 따 라서 전동할수있다. (3) 스크린 EF 는 데이터 수집중에는 정지해 있으나 필름에 또 다른 회절 원추를 찍으려고 할 때는 EF 를 따라 이동할 수 있다. (4) 높은 충선의 데이터를 수집할 때는 장치의 축은 µ만큼 전동 한다. 죽 GH 는 GI 까지 이동할 수 있다. 6) 4 축 단결정 회절 장치 We i ssenber g법은 X- 선 필름을 사용하여 회절을 기록한다. 이 방법을 보정하여 Ge ig er 계수기나 다른 전자 계수기에 각각의 회
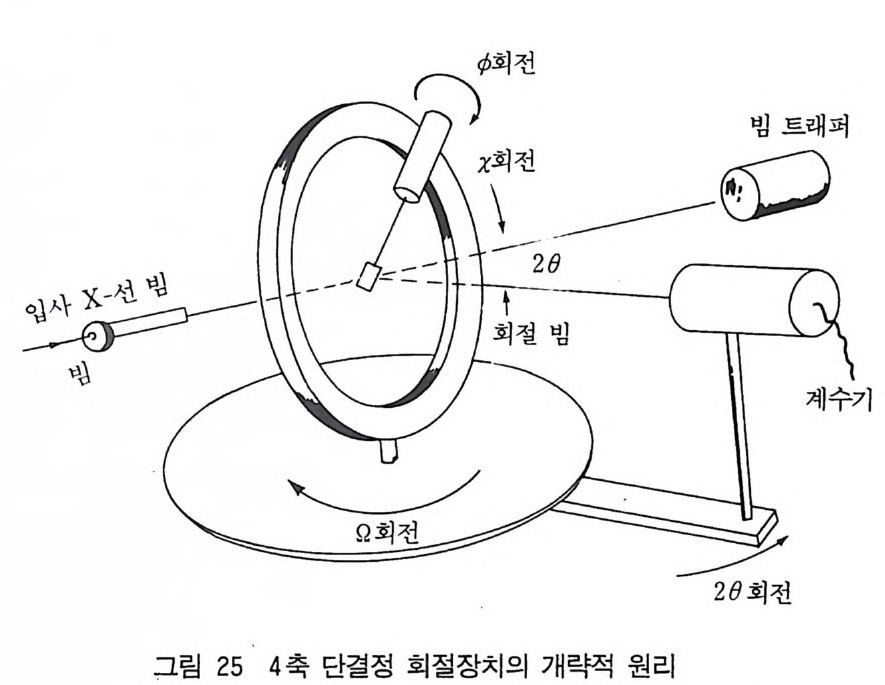
절 반점을 찾아내게 하고 기록하게 할 수 있다. 이제 컴퓨터가 회 절 장치를 조정하게 할 수 있어서 결정을 X- 선 빔 속에 있게 하면 회절 장치는 단위 세포의 크기를 측정하고 정밀화시킨 후 미리 정 해둔 최대의 0 각도까지의 모든 반사점을 기록하고 hkl 과 반점 강 도와 각 반사의 측정오차까지 기록한다. 그립 24 는 4 축 단결정 회 절 장치의 개략적인 기하학적 배치를 보여주고 있다.
 -28 빔트래퍼
-28 빔트래퍼
자동 X 선 회절 장치는 단결정에서 일분간에 하나의 속도로 반 사를 측정하면 보통 결정 구조는 며칠 사이에 수집할 수 있다. 유 능한 결정학자는 현대 컴퓨터의 도움으로 100 개의 원자(수소의 수 는 계산하지 않고)를 가지는 분자의 상세한 구조는 2~3 주 내에 완 결할 수 있다(시료 파괴 화학적 방법에서는 이것을 알려면 여러 달 혹 은 여러 해가 걸린다). 필요한 것은 약 한 변의 길이 0.2~0.3mm 의 입방체 모양의 결정이다.
연습문제 1. (CHa)2S02( 분자량 = 94.13) 는 사방정계로서 단위세포당 네 개의 분자가 있고 a=O.736nm, b=0.804nm, c=O.734nm 이다. 이 결정의 밀도를 계산하라. 2. 구리 타겟에서 얻은 특성 X- 선의 파장은 1.54 A 이다. NaCl 결 정 (a=5 . 63A) 에서 얻을 수 있는 처음 여섯 개의 반사에 대한 Bra gg각을 계산하라. (힌트 : NaCl 은 면심입방 격자이고 hkl 가 모두 짝수이거나 모두 홀 수일 때만 회절 강도를 얻을 수 있다.) 3. T i O 는 NaCl 형의 구조를 가진다. 밀도가 5536k g m - 3 이면 단 위세포의 한 변의 길이 (a) 를 구하라. 4. CaF 눅 면심입방 격자를 가지며 (111) 반사는 파장 0.1542run 인 X- 선을 사용하여 fJ =14.18 ° (s i n0=0 . 245 ' 이고 cos0= 0 . 970°) 에서 얻을 수 있다. (a) 단위 세포의 한 변의 길이를 계산하라. (b) 결정의 밀도를 계산하라. 5. 단위 세포 파라미터는 다음과 같다. a=5A, b=lOA, c= 15A, a=/3 = 90° 및 r=120· 이다. (a) 역격자 파라미터 a*, b*, c*, a*, /3*, r* 를 구하라. (b) 실제의 단위세포와 역격자 단위세포의 부피를 구하라. (c) (321) 평면 사이의 간격을 구하라. (d) Cu Ka (A=l. 54A) 를 사용하였다면 (321) 반사의 Bra gg각도 (2()) 를 구하라.
6. Te t raborane 은 단사정계를 가지고 a=0. 86 8nm, b=l .01 4 nm , c= 0 . 578nm 이고 /3 =105. g · 이다. a 축 c 축을 보이는 그 림을 그리고 (101) 평면을 보여라. 그림을 기초로 하여 (101) 평 면간의 간격을구하라. 7. Zn 의 분말의 회절 무늬를 Cu Ka X- 선을 사용하여 Deby e- Scherrer 카메라 (57.3mm 의 직경)로써 얻었다. (a) M ill er 지수 1 1. 0 와 10.3 회절선을 분해하는 데 필요한 분해 능 (resolv i ng p ower) 을 계산하라. (b) 이 두 회절선을 분리하는 데 필요한 카메라의 분해능을 구하 라(선폭〔 li ne w i d t비은 0 . 03cm 라고 가정하라). (c) 이 선들을 분리하는 데 필요한 카메라의 최소지름은 얼마인 가.
제 6 장 회절(II) l 서론 단위세포내 원자의 위치는 X- 선의 회절 강도에 영향을 주나 회 절되는 빔의 방향에는 영향을 주지 않는다. 그림 1 은 단위세포당 같은 종류의 원자를 두 개 가지는 사방정계의 구조를 보여주고 있 는데, 왼쪽 그림은 저심 사방정계이고 오른쪽 그림은 체심 사방정 계이다. 왼쪽 그림의 원자 하나를 c / 2 만큼 이동하면 오른쪽 그림의 구 조를 얻을수있다. 그림 2 에 보인 (001) 평면에서 얻는 반사를 생각하면 그림 2-(a) 의 저심 격자에서는 특정한 A 와 0 값에서 Brag g 법칙이 만족된 다. 이것은 선 1’ 과 2’ 의 경로차가 1A 이고 l’ 과 2' 는 위상이 맞아서 그립에서 보여준 방향에서 회철이 일어난다. 이와 비슷하게 그림 2-(b 펴 체심 격자에서 1’ 과 2’ 는 위상이 맞고 경로의 차는 1A 이 다. 그러나 (001) 평면 사이에 하나의 원자 평면이 있고 l’ 과 3' 의 경로의 차 DEF 는 ABC 의 1/2, 죽 A/2 의 차이가 있다. 따라서 l ’ 과 3’은 완전히 위상이 벗어나고 반사 X- 선의 강도는 서로 상쇄 된다. 이와 비슷하게 그 다음 평면에서 나온 4' 선은 2' 선을 상쇄한 다 (4' 선은 그림 2-(b )ol]는 표시되어 있지 않다). 이와 같은 방법으로 체심 입방격자에서는 (001) 반사는 없음을 알 수 있다.
 Q
Q
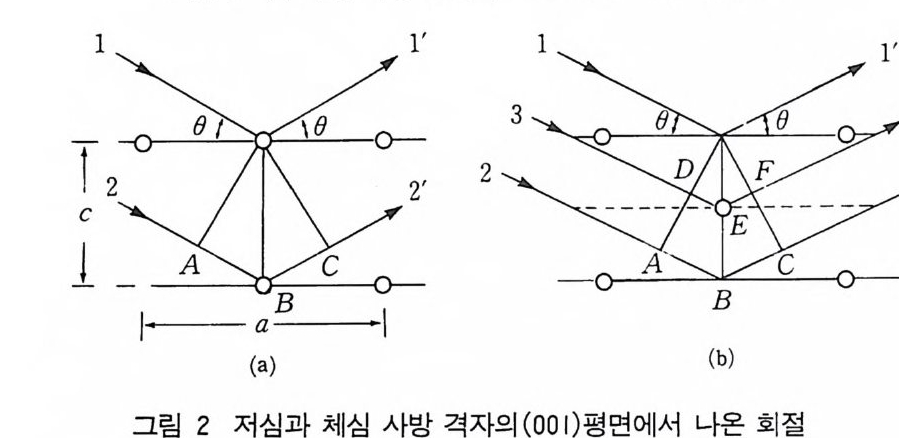 l l'
l l'
이러한 예는 단위세포내의 원자의 간단한 배열이 반사 강도를 완 전히 없앨 수 있음을 보여준다. 그러나 일반적으로 회절 빔의 강도 는 원자의 위치의 변화에 따라 영은 아니지만 변한다. 원자 위치와 회절 강도 사이의 정확한 관계를 얻는 것이 이 장의 목적이다. 그 러나 이 문제에는 많은 변수가 포함되므로 복잡하다. 우리는 한 단 계 한 단계 진행하여 먼저 하나의 전자에 의한 산란, 원자에 의한 산란, 또 단위세포내의 모든 원자에 의한 산란 등으로 생각해 보 .A}. 2 전자에 의한 산란 x- 선 빔은 전자파의 특성울 가지며 특성은 전기장의 영향을 받
으며 전기장의 강도는 빔내의 임의의 점에서 시간에 대해 s i ne 함 수로 변한다. 전기장은 전자와 같은 전하를 띠는 입자에 힘을 작용 하므로 X - 선 밤의 진동하는 전자는 운동중에 가속도 되고 감속도 되면서 전자파를 발생한다. 이런 의미에서 전자는 X- 선을 산란하 며 산란된 빔은 입사 빔의 작용 아래 전자에 의해 방출하는 빔이 다. 산란된 빔의 파장과 전동수가 입사 빔의 파장과 진동수와 같으 면 간섭성 산란 (coheren t sca tt e ri n g)이라 한다. X 선은 전자에 의해 모든 방향으로 산란하고 산란한 빔의 강도 는 산란각과 관계가 있으며 점 P 에서 산란 X- 선의 강도는 다음 식으로표현할수있다. Ip= I。 (µ 0/ 41r) 2(e4/ m 2r2) (1+cos2 2 0) /2 (6-1) 이 식은 단일전자에 의한 X- 선 빔의 산란에 관한 Thomson 식 이다. 여기서 Io 는 입사 범의 강도이고 %는 41rX 10-1 m Kg C 크 이고 r 은 전자에서 P 점까지의 거리이고 전자의 전하가 e 이고 전 자의 질량이 m 이다. Thomson 식은 입사 빔의 절대강도로서 산란 빔의 절대강도의 관계를 주며 이들 절대값은 측정하거나 계산하기에 어려우므로 상 대적인 값을 얻을 수 있다. 마지막 항인 (1+cos220)1/2 를 편광 인자(p olar i za ti on fa c t or) 라고 한다. 이 항은 입사 빔이 편극화되 지 않기 때문에 포함된 항이다. Thomson 식에 의하면 산란 강도 는 산란 전자에서의 거리의 제곱의 역으로 감소하며 입사 빔의 직 각 방향에서보다 전면이나 후면 방향에서 더 크다. 또 산란 강도의 크기가 한 /m2 에 비례하므로 보통 원자핵의 질량은 전자의 10 대이 며 전하는 10 배 정도밖에 안되므로 원자핵의 산란은 전자에 의한 산란에 비해 무시할 수 있을 정도로 작다. 따라서 X- 선의 산란 강 도의 기여는 거의 전자에 의함을 알 수 있다. 전자가 X- 선을 산란하는 또 다른 방법이 있다. 이것을
Com pt on 효과라고 한다. 이것은 X_ 선이 헐겁게 결합된 전자나 자유 전자에 충돌할 때 생긴다. 이 효과는 입사 빔을 파의 운동이 아니고 X 선 양자나 광자의 흐름으로 각 광자의 에너지를 h v 1 으로 생각하면 이해할 수 있다. 이러한 광자가 헐겁게 결합한 전자를 때 리면 이러한 충돌은 두 개의 당구공이 충돌할 때와 같이 탄성적이 다. 전자는 충돌 후 옆으로 가고 광자는 20 각으로 비껴간다(그림 3). 입사 광자의 에너지 일부는 전자에 운동에너지 를 제공하므로 충돌 후 광자의 에너지 hv2 는 충돌 전 에너지 ltU 1 보다 적다. 산란 복사선의 파장 A2 는 입사 빔의 파장 A1 보다 약간 크고 다음 식에 따라그크기가변한다. 611(A .) = 112-111= 0 . 0486 sin 2 。 (6- 2 ) 파장의 크기는 산란각의 함수이고 그 변화량은 전면 산란에서는 영이고 후면 산란에서는 0.05A 이다. 이렇게 산란한 복사선을 Comp ton 수정 복사선 (Comp ton mod ified radia t i on ) 이 라 하고 이 러한 복사선의 위상은 입사 X_ 선 빔의 위상과는 일정한 관계가 성 립되지 않고 이 때문에 비간섭성 복사선 (inc oherent radia t i on ) 이 라고 부른다. 이 복사선은 그 위상이 입사 빔과는 무질서하게 관계되어 간섭 효과를 주지 않으므로 x- 선 회절에는 관여하지 않는다. Comp ton 수정 산란은 없앨 수 없으며 회절 패턴의 배경을 검게 하는나쁜 영향을준다.
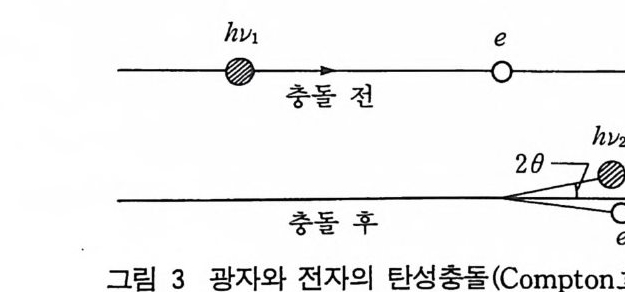 h111 e
h111 e
3 원자에 의한 산란 개개의 전자는 입사하는 X- 선을 Thomson 식에 따라 산란한다• 원자내 전자가 z 개 있으면 총산란 크기는 z 배로 산란할 것으로 기대된다. 산란이 전면에서 일어나면 (20=0) 이러한 사실은 옳다. 왜냐하면 원자내 모든 전자에 의해 산란되는 파는 위상들이 일치하 고 파의 전폭은 바로 더해진다. 디른 방향에서 산란이 일어나면 이러한 사실은 옳지 않다. 원자 내 전자는 공간에서 여러 가지 디른 위치에 있고 틀리는 원자 사이 에 산란되는 파 사이의 위상은 서로 틀린다. 따라서 부분적으로 상 쇄간섭이 일어난다. 이리하여 총산란파의 진폭은 산란각이 커짐에 따라감소한다. 원자 산란 인자 (a t om ic scatt er in g fac to r ) f는 주어전 방향에서 임의의 원자의 산란 효율을 설명하는 데 사용된다. /= 하나원의자 전에자 의에해 의 산해란 산되란는되 파는의 파 전의폭 진 (E폭a) ( Ee) (6- 3 ) f의 최대값은 Z 이고 모든 전자의 산란파가 서로 위상이 맞을 때 산란 인자의 크기이다. 산란 인자가 산란 각도에 어떻게 관계하는가를 알려면 원자내 전 자의 실제 분포를 생각해야 한다. 이 분포가 구대칭이고 전하 밀도 p (r) 로 설명할 수 있다고 생각하자. 원자내 부피 요소 dv 내에 포 함된 전하의 양 (dq )은 다음 식으로 표시된다. dq =pd V (6-4) 이 부피 요소에 의해 산란된 파의 전폭 dE~ 같은 방향에 있는 하나의 전자에 의해 산란되는 파의 전폭의 비는 이들 전하 사이의 비와같다.
dEal E e = dq / e= pd V/ e (6-5) 지금 입사 X- 선의 방향과 산란 X- 선의 방향의 단위 벡터를 각 각 So, S 로 표시하자. 원자내의 각 점에서의 전자가 산란될 때 경 로의 차를 생긱하자. 원자 산란 인자는 부피 요소의 위치 벡터 r 에 대해 입사 빔의 배치에 관한 위상 인자를 사용하여 수학적으로 처리하는 것이 편리하다. df= pd VI e ·exp (i¢) (6 一 6) 여기서 函근 위상 인자(p hase fac t or) 이다. 그림 4 에서 경로의 차=p― q= r cos as-r cos a; 6 1t== rr•· S(S-— r&· S) 。/=A r· (S-S(c 。)y c le(c) m) (6- 7)
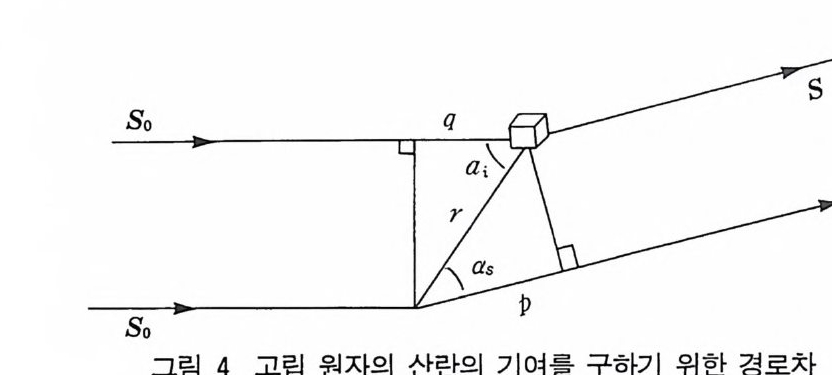 s 。
s 。
라디안으로표시하면 나 =27r 식 =21rr•(S-S 。 )/11 (radia n ) (6-8) df =파e 꼬 ex p(i¢) dV =뿐 ex 짜무 (S-S 。) • r) dV (6-9)
여기서 지수항은 원자내 다른 위치 사이의 위상의 관계를 나타낸 다. 원자내 전자에 대한 총산란 기여는 총부피에 대해 적분하면 얻을 수 있다. 전하 밀도는 구형 대칭이라 생각할 수 있으므로 구형 좌 표계 (sph eric a l coordin a te s s y s t em) 를 사용하여 계산하는 것이 편 리하다. 구형 좌표계에서 부피 요소는 환상고리의 반경이 rsin < p , 폭이 rdcp, 두께가 dr 이다. 따라서
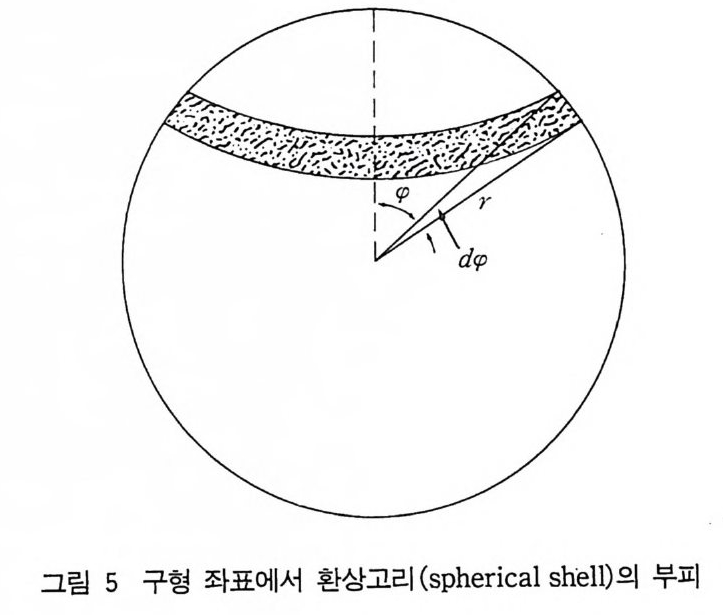 그림 5 구형 좌표에서 환상고리 (s p her i cal shell) 의 부피
그림 5 구형 좌표에서 환상고리 (s p her i cal shell) 의 부피
dV=2 記 s i n
이다. 여기서 | s-s 。 l= 2 sin 0 이고 이 관계는 그립 10 에서 쉽게 알수있다. 그러면 f= l/e1:rT:==O~~ . I1 :'1'P':= = l0:C p ( r) exp (ikr cos rp) 2 記 sin rpd rp d r (6-12) 여기서 K= 47r sin 0/A 이다. ’에 대해 적분하면 디음 식을 얻을 수 있다. 1。r rexp ( ikr cos q;) sin 랴 = l/ ikr [ex p ( ikr cos q;) 詩 = 2/kr(eik r— e -ik r) /2 i =2 sin kr/kr (6-13) (6-13) 식을 (6-12) 식에 대입하면 다음 관계식을 얻을 수 있다. f= (41r/e)J ~r2 p ( r) sin krIkr dr (6-14) 。 원자 산란 인자는 (6-14) 식에서 원자의 전하 밀도 p (r) 을 알면 계산할 수 있다. 위의 식은 전하 분포가 구형 대칭이고 X- 선 에너 지가 원자의 흡수단 가까이 있지 않을 때만 성립된다. 전하 밀도를 양자역학을 이용하여 계산하자. 양자역학에 의하면 전자는 일정한 궤도에 있고 원자에 대해서는 Schroed i n g er 방정식 의 해인 파동 함수 ¢로써 설명할 수 있다. 또 불확정성 원리에 의 해 전자는 공간내의 어디에 있는가하는 위치를 정확히 이야기할 수 없고 주어전 점에서 전자를 찾을 확률로써 이야기한다. Max Born 은 1926 년 부피요소 dV 내에서 전자를 찾을 확률은 rp2 dV 와 비례하고 ¢2 은 공간에서 전자를 찾을 수 있는 일종의 평균 확 률 밀도라 하였다. 우리는 전하 밀도를 e I ¢ 12으 로 나타낼 수 있 다. 수소 원자에 대해서는 Schroed i n g er 방정식은 정확히 풀 수
있다. 바닥상태에서 ipH = 1 / /( 교국)· e- rt a . (6-15) 여기서 an 는 0.53A 이고 수소원자의 Bohr 반경이다. 그러면 확 률밀도는 I ¢H l2=e- zr ia •/( 1 raB3) (6-16) 이고 p (r) = el r/J l2 이다. 따라서 수소의 원자 산란 인자는 다음과 같다. IH==~4K J f oO~O 'r 二 r1era-s2Jr i a뿌 s skinr dr (6-1
kr dr 7) 적분표에서 다음과 같다. fOO xe ~ax sin bx dx=2 ab/(a2+ b2) 2 (6-18) 。 따라서 !H= 1/[l+ (ask/2) 기 2 = 1/[l+ (21raa sin 8/A) 기 2 (6-19) 여기서 K= 41r sin ()/,1 이다. (6-19) 식에 원자 산란 인자는 sin ()/A 의 함수이다. 결정에서 sin ()I,1 = 1/2 dhkl 이므로 산란 인자는 각각의 결정 평면에서는 일 정한 값을 가지고 실제 파장의 크기와는 무관계하다. R.M . J ames 와 G.W. Br i ndle y는 1931 년 많은 원자와 이몬] 대해 원자 산란 인자를 계산하였다. 그 후 몇 가지 수정법도 제안 하였고 초기에는 너무 어렵다고 생각한 무거운 원소의 원자 산란인자도 계산하였다. 이에 대한 자세한 계산법과 결과는 Inte r n a- tion al Tablesf or X- ra y C1y st a l log ra p hy 제 3 권에서 찾아볼 수 있다. 부록 5 에 여러 가지 종류의 원자와 이온에 대해 sin 0/ 11 값 으로 f 값을 표시하였다. 그림 4 는 모두 10 개의 전자를 가지는 한 개의 중성 원자에 대해 f와 sin 0 I 11 를 그린 그림이다. 핵의 하 전이 증가하면 전자는 핵에 더 가깝게 당겨지고 산란 곡선은 원자 를 점으로 생각한 산란 곡선인 수평선에서 작게 벗어난다. 이 그림 에서 최의각 전자는 헐겁게 결합되는 전자로서 산란 각도가 작 을 때 총산란값에 크게 기여함을 알 수 있다. 죽 임의의 전자에서 K 전자인 내부껍질 전자는 모든 각도에서 기여하고 의각 전자인 L 전자는 산란 각도가 커짐에 따라 K 각 전자보다 산란에 기여함이
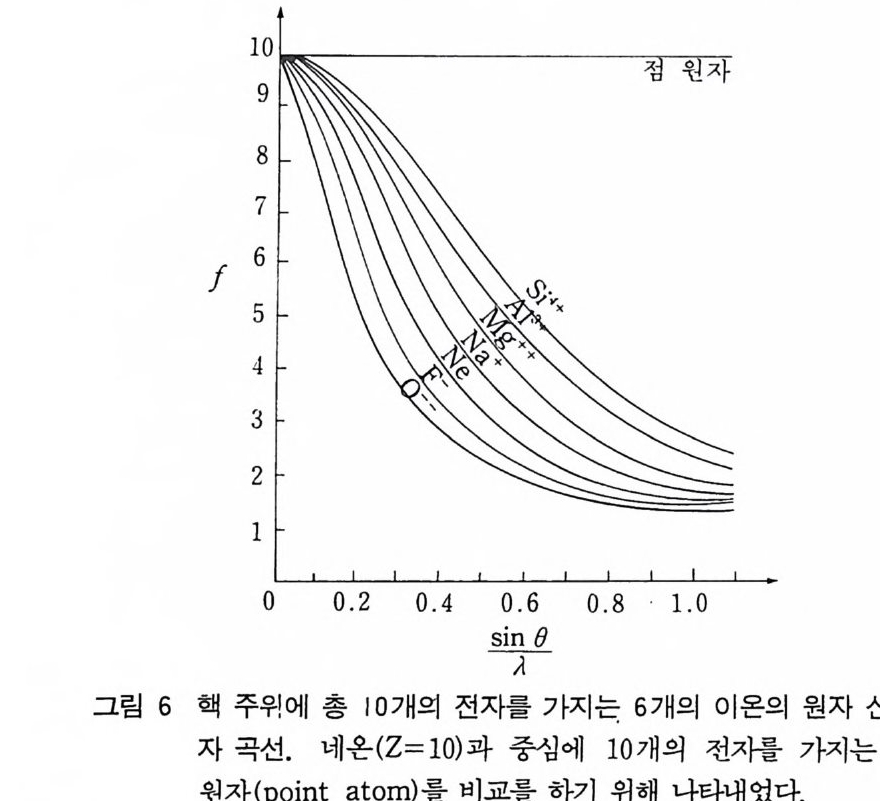 1。 987654321
1。 987654321
적어진댜 원자가 전자는 산란각이 작고 각도에서만 주로 기여함을 뜻한다. 원자나 분자에서 원자나 전자는 보통 구형 대칭으로 분포 하지 않으며 이웃 원자와 화학결합 방향으로 편재하고 있다. 무거 운 원자의 산란에서 의각 전자는 기여함이 적어서 X- 선 회절에서 의각 전자가 구형 대칭이 아니라도 무시할 수 있다. 4 단위세포에 의한 산란 회절되는 빔 강도에 대한 표현식을 얻으려면 간섭성 산란 (coherent sca tt er i n g)에 관해 생각해야 하고 고립 원자가 아니고 결정을 만드는 모든 원자에 대해 고려해야 한다. 원자가 공간에서 주기적 모양으로 배열되어 있다는 사실은 산란되는 X- 선은 어떤 특정한 방향을 생각해 주어야 한다. 이러한 일련의 회절 빔을 생각 하자. 이 빔의 방향은 Bra gg법칙에 의해 결정된다. Bra gg법칙 이 만족되지 않으면 회절되는 빔은 없다. Brag g 법칙이 만족되더 라도 6 장 1 절에서 논한 바와 같이 때로는 특정한 원자 배열 때문 에 회절이 일어나지 않을 수도 있다. Bra gg법칙이 만족하고 결정에 의해 회철되는 범의 강도를 원자 의 위치의 함수로 구해 보자. 결정은 기본적인 단위세포의 반복이 므로 하나의 단위세포내 원자의 배열이 회절 강도에 어떤 영향을 주는지를 생각해 보자. 이 문제를 원점에 있는 원자에 의해 산란되 는 파와 X 축 방향의 어떤 위치에 있는 다른 원자에 의해 산란되는 파의 위상의 차이를 생각하여 구해 보자. 문제를 간단히 하기 위해 편의상 그림 7 의 사방정계 단위세포를 생각하자. 원점에 A 원자가 있고 (hOO) 평면에서 회절이 일어난다고 하자. 이 평면에 대해서는 Bra gg법칙이 만족하고 선 2’ 과 선 1' 사이의 경로의 차를 82 ; 1, 이 라 하자. 그러면 다음 식이 성립한다.
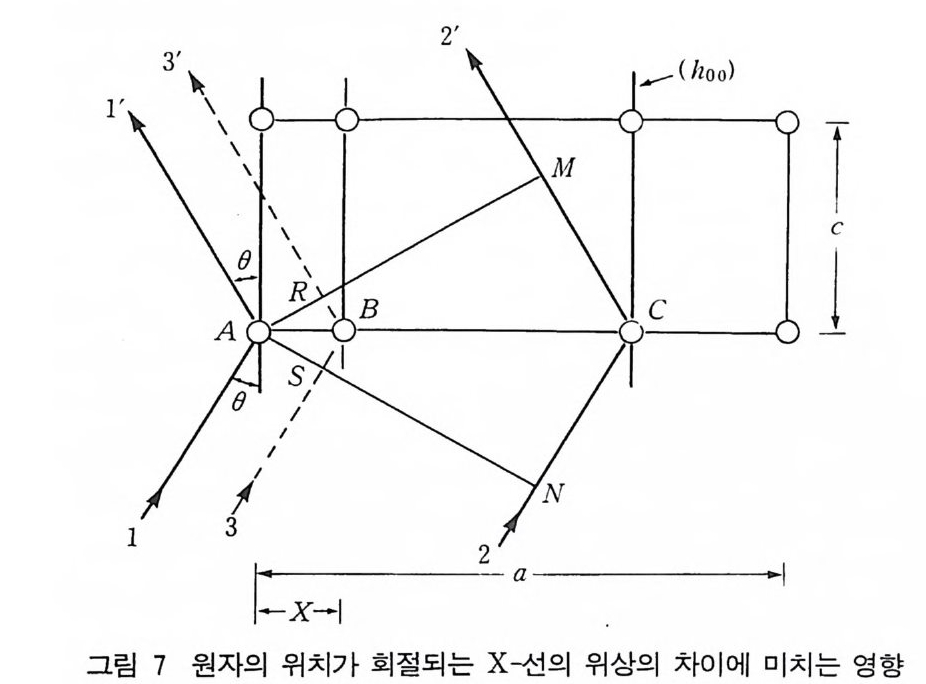 2'
2'
82,1,= MCN= 2 dho 。 sin 0= ,-l (6-20) Mi ller 지수의 정의에서 다음 식을 얻을 수 있다. dhoo=AC= a/h (6-21) A 에서 거리 X 위치에 있는 원자 B 에 의해 이 반사는 어떠한 영향을 받는가? 산란 X- 선 3' 과 1' 사이의 경로의 차 8안 1 는 A 보 다는 작고 간단한 비례 관계식에서 다음 식을 얻을 수 있다. 83' l'= RBS=AB/AC(A) =-dtii r (A) = hXA /a (6-22) 위상의 차이는 파장으로도 나타낼 수 있는 것과 갈이 각도로도 나타낼 수 있다. 두 산란 X- 선이 파장 1A 만큼 차이가 나면 360° 혹은 27C 라디안이 차이가 있다고 말할 수 있다. 지금 경로의 차가
8 이면 라디안으로 나타낸 위상의 차이는 다음과 같이 쓸 수 있다. ¢= (8/ A )21r (6- 23 ) 그러면 B 원자에 의해 산란된 파와 A 원자에 의해 산란된 파 사 이의 위상의 차이는 다음과 같이 나타낼 수 있다. ¢3'1'= 83,1 ,/ -1 ( 21r) = 21rhXI a (6-24) 지금 B 원자의 위치를 분수 좌표로 표시하고 X/a=x 로 표시하 자. 그러면 ¢3 , 1,=2 처t X (6-25) 이러한 방법을 3 차원으로 확대하자. B 원자의 실제 좌표는 X, Y, Z 이고 이것은 XI a =x, YIb=y , Z/x=z 로써 분수 좌표 x, y, z 로 표시하자. 그러면 hkl 반사에 대해 원자 B 에 의해 산 란된 파와 원점에 있는 원자 A 에 의해 산란된 파 사이의 차이는 다음과같이쓸수있고 ¢=27r(hx+ky + lz) (6-26) 이것이 임의의 모양을 갖는 단위세포에 적용할 수 있는 관계식이 다. 두 개의 파를 비교할 때 두 개의 파는 위상이 다를 수 있을 뿐만 아니라 원점에 있는 원자와 X 위치에 있는 원자 B 가 종류가 다르 면 진폭도 다를 수 있다. 이 경우 이 파의 전폭은 단일 전자에 의 해 산란된 파에 대한 적당한 값 f, 죽 원자 산란 인자로서 주어전 다. 이제 문제는 위상이 다르고 전폭이 다른 여러 가지 파를 합하 여 합성파를 얻는 것이다. 죽 원점에 있는 원자를 포함하여 단위세 포내 모든 원자에 의해 산란된 파의 진폭과 위상을 고려하여 합성 파를구해야한다. 그림 8 과 같은 두 파는 전기장의 강도를 시간 t함수로 그린 것
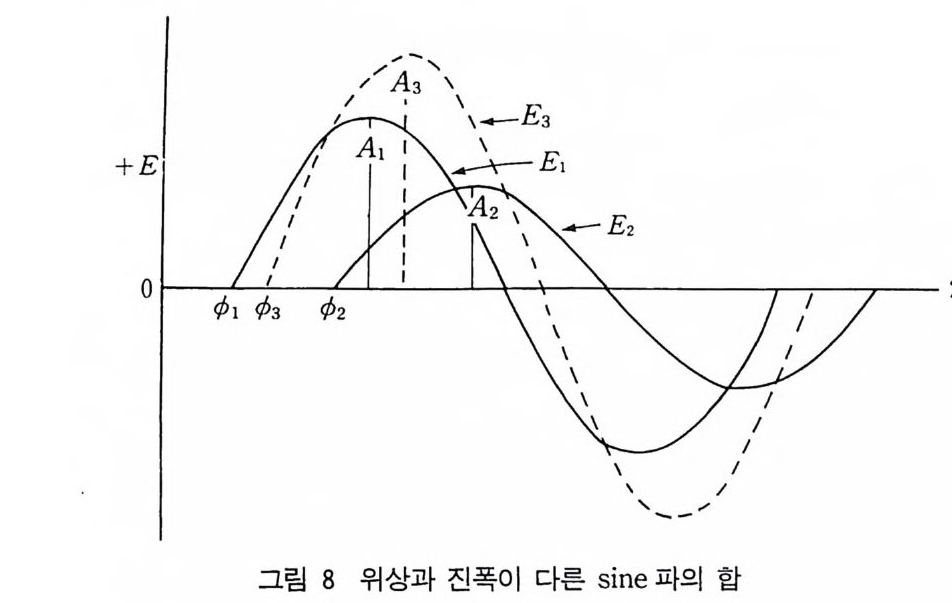 / /A/.' _3 ` `\ \
/ /A/.' _3 ` `\ \
이며 전기장의 강도는 다음 식으로 표시할 수 있다. E1=A1 sin ( 27rvt— 십 (6-27) E2=A i sin ( 27rvt -십 (6- 28 ) 여기서 이 두 파는 동일한 전동수 , 죽 동일한 파장을 가지나 전 폭 (A) 과 위상(¢)이 다르다. 점선의 그림은 두 파의 합을 나타낸 것이다. 그림 9 는 각 성분파를 길이는 파의 진폭과 같고 x 축으로 기울어전 각도는 위상각과 같이하여 파를 벡터로 나타낸 것이다.
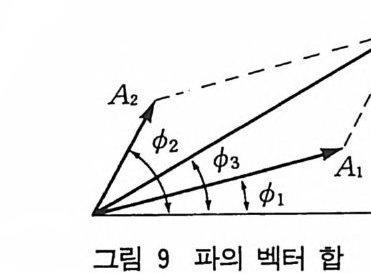 그림 9 파의 벡터 합
그림 9 파의 벡터 합
합성파의 진폭과 위상은 평행사변형 법칙으로 벡터를 합하여 간 단히 구할 수 있다. 또 파의 강도는 전폭의 제곱에 비례한다. 파를 복소수를 표시하여 전폭의 제곱은 복소수에 공액복소수를 곱하여 얻을수 있다. 츠-1 IA exp (i¢) l2= A exp (i¢) A* ex p (- i강) =I A l2 단위세포내의 각각의 원자에서 산란되는 파의 합을 구하는 문제 를 생각해 보자. 각 산란파의 전폭은 원자 산란 인자 f로써 풀 수 있고 각 평면 (hkl) 에서 나온 산란파의 위상은 원자의 좌표와 hkl 로써 표 현할 수 있다. 산란파를 복소수로 생각하여 다음과 같이 쓸 수있다. A exp (i¢)=f exp ( 21ri_( h x+ky + lz)) (6-29) 단위세포내 모든 원자에 의해 산란된 합성파를 구조 인자 (str u ctu re fac to r ) 라고 부르고 구조 인자는 원자의 배 열, 죽 각 원 자의 좌표는 산란파에 어떤 영향을 주는가를 나타낸다. 구조 인자 는 개개 원자에 의해 산란된 모든 파를 모두 합하면 구할 수 있다. 단위세포가 분수 좌표 X1Y1Z1 , X2Y 2Z2, XaY 따를 가지는 원자 1, 2, 3·· ·… , N 을 포함하고 있고 각 원자의 산란 인자를 fh f2, f3, … ••• 라고 하면 hkl 반사에 대한 구조 인자는 다음과 갇이 쓸 수 있다. Fhkt= !1 ex p (2 따 (hx1+ ky 1 + lz1) ) +/2 ex p (2 따 (hx2+ ky2 + lz2)) +/a exp (2 1ri( h xa+ kya + lza)) + …… = ~n In exp 2 m( hxn+ ky n + lzn) I = ~nI In exp( i
여기서 합은 단위 세포내 모든 N 원자에 걸쳐 걸쳐 행한다. 합 성파는 Arga nd 그림에서도 쉽게 구할 수 있다. F=/1 exp i¢1 +/2 exp i
 허수 축
허수 축
전폭으로 나타낸 합성파의 진폭을 준다. 원자 산란인자 I 와 같이 IFI 는진폭의 비로써 정의된다. IF|= 단위세포내 모든 원자에 의해 산란된 파의 전폭 하나의 전자로 산란된 파의 전폭 다음 절에서 알 수 있는 바와 같이 Bra gg법칙에서 예측되는 어 떤 방향에서 단위세포내 모든 원자에 의해 산란되는 빔의 강도는 IF I~ 죽 합성 빔의 전폭의 제곱에 비례한다. 따라서 (6-30) 식은 원자의 위치를 알면 hkl 반사의 강도를 계산할 수 있으므로 X- 선 결정학에서 매우 중요한 관계식이다. 5 이상적 결정에 의한 X- 선의 회절 빔의단면적이측정하려는결정의 단면적보다큰단색광의 X- 선빔
을 써서 결정에 쪼인다고 생각하자. 빔이 평행 X - 선으로 되어 있 고 그림 11 과 같은 공통적인 진행 방향의 파의 면을 갖는다고 하 자. 입사 빔의 단위벡터를 So 라고 하고 산란되는 빔의 방향에서 단위벡터를 S 라고 하자. 결정내 어떤 원자의 위치를 원점에서 시작하여 표시하자. R 값 =m,a+m2b+ m2c+ rn (6- 3 7) 여기서 m1, m2, m3 는 원점에서부터 m 번째 단위세포까지 a 축, b 축 및 c 축으로의 각각 거리이고 rn 는 우리가 생각하는 단위 세 포에서 그 원점에서 n 번째 원자까지의 거리이다. 11 번째 원자내 전자는 적합한 원자 산란 인자 fn 에 의해 입사하는 X - 선을 산란 한다. x- 선이 단위벡터 방향 쪽으로 주기적 원자열에 의해 서로 간섭하면서 어떻게 산란하는가를 알려면 점 P에 도착하기까지 여 러 가지 산란 X- 선의 경로의 차를 알아야 한다.
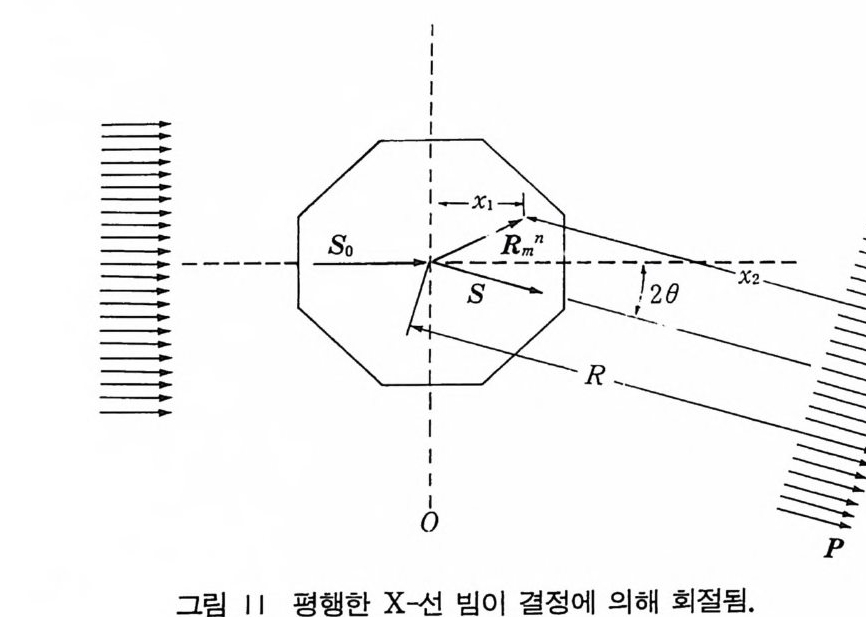 •.►.•••’••..•..’.•’•.’• 그 -림-- -|l- 평 행한 X 선二_I _빔_이_ 결정에 의해 회절됨.
•.►.•••’••..•..’.•’•.’• 그 -림-- -|l- 평 행한 X 선二_I _빔_이_ 결정에 의해 회절됨.
입사하는 단색광의 X- 선의 파장이 A 이고 결정의 원점에서 입사 하는 X 선은 공통적인 파의 전면을 가진다면 벡터 Rmn 끝에 놓여 있는 원자에 도달하면 x1 거리만큼 파는 이동해야 하고 이 점에서 전기장의 값은 디음과 같다. c0 = Eo exp (2 7ri( f • t -풍) ) (6-38) 여기서 Eo 는 입사 빔의 전기장의 전폭이다. 원자는 S 방향으로 입사 빔을 산란시키고 고려하려는 원자에서 功 거리에 있는 P 점 에 도착할 때는 전기장의 강도는 디음과 같다. c p=fn (e2E 。 / mc2R) exp 2J ri(c /11· t-(1/1 1) (xi+ x2)) (6-39) 여기서 e 와 m 은 각각 전자의 하전과 질량이고 c 는 빛의 속도 이고 fn 는 원자의 산란 인자이다. 점 0 의 원점에서 측정 장치가 있는 P 까지 산란한 X- 선은 모두 x1+x2 만큼 여행해야 한다. 그 리고 X1=Rmn•S 。 X2=R_Rmn·S x1+ x2= R— (S— s 。) • Rmn (6-40) 그러면 이것을 (6-38) 식에 대입하면 다음 식을 얻는다. ep = e2Eo/(mc2R) • Un) •exp [21 ri( ( c/A)t 一 1/A(R 一 (S-So) ·R 십))〕 (6-41 ) 모든 원자에 의하여 산란되는 전기장의 크기를 구하려면 단위 세 포내에 포함된 n 원자에 걷쳐 합하여야 하며 또 결정내의 모든 단 위 세포에서 그 기여를 구하려면 m1 m2 ms 에 걸쳐 합해야 한다. 모든 결정 전체에 의해 산란된 파에 의하여 점 P 에서 감지되는 순 간적인 전기장의 세기는 다음과 같다.
cp = e2Eo/ ( mc2R) ~n ~m1 ~m2 ~ms In exp [2 7ri ( ( c/ 11 ) t-RI ,1 + (S-So) /11· ( rn + m1a+ ni2b + mac))] (6-42) 九 mI, m2, m 폐 의존하는 항으로 분리하고 역격자와 구조 인 자에 관한 표현을 생각하면 다음과 갇다 . Fhkl= ~n In exp [2 7 fi(h xn+ ky n + I%) ] d*(hkl) = (S— &) /A= ha*+kb* + le* 그리고 rn=Xna+Ynb+ZnC 로 표현할 수 있다. 여기서 Xn , Yn, Zn 는 각각 a, b, C 축으로의 분율 좌표이다. 그러면 다음 식을 얻을 수 있다. d*(hkl) • rn= (S-S 。) /A· rn =hxn+kyn + lzn 구조 인자는 다음과 같이 표현할 수 있다. Fhkl= ~n In exp [( 27ri/ A ) • (S— &) • r 』 (6-43) (6-43) 식을 (6-42) 식에 대입하고 정리하여 쓰면 다음과 같이 된다. cp = :潟 e(무 )(c t -R)F 흡 e(2n: 1 /.\)(S-So)•m1 a 2: e(2n: t!.l)( S-So)• mz b 2: e(2ir 1/ .l) ( S-So)•m3C (6-44) m’z m3 (6-43) 식의 합을 계산하려면 결정의 모양을 평행사변형이라 생 각하자. 결정의 변의 길이는 각 변에 있는 단위세포수와 M1a, M2b. Mac 와 같다. 그러면 총단위 세포의 수는 M=MXM2XM3 이다.
m1=M1-l ~ e(2rc,t A) ( S-S o) • m t a = eo+ e(21Ct / A )( 5-S o)•l a + m,=0 + e(2rr :1 /A ) (S-So)•2a+ …… + e(2 rr: 1 / A)(S - So)•(M 터 )a (6-45) (6-44) 식은 다음 형의 식과 같다. MML =~! oI arMM = a+' ar+' ar2? +, …… +' arM...,-_1, = a(rr M —-1 )a (6-46) 따라서 (6- 4 6) 식을 이용하여 계산하면 (6-44) 식은 다음과 같 이 된다. C p = me2c2ER 。 e 뚜A (C t -R) Fz; ,~ e2무 1t i s-So1)· a —1 e무 (S-So h lf, b_l eT2t r(iS -So)•M , c_1 e뚜 ( 5 - So)• 드 1 e 무 (S-So)•c ― l (6-46) 우리가 계산하고자 하는 양은 관측점에 도착하는 X- 선 빔의 강 도 Ip 이다. 이 강도는 전자장의 진폭의 제곱에 비례한다. E/= I cp l2= cp X cp * (6-48) 그리고 ]p= (c/87 r) •E/·(l+cos220)/2 이므로 (6-44) 식에 공 액 복소수 값을 곱하는 것이 필요하다. 따라서 e iM X-l e-iM X -l = e° 一 e iM X_ e -i M X+ 1 e ix -I X e-iX -I eo_ e iX_ e-+ 1 44 s sini n2 2( 1(1/2/2) )• M•xx (6-49)
의 관계식에서 P 점에서의 X- 선 산란 강도는 다음과 같다. s i n 맛 (S ― &) ·M,a sin 2 - f(S -So) ·M2b Ip = IOF2 s i n 망 (S 一 &) • a s i n 멋 (S 一 &) • b s i n2 子 (S ―&) •M3C sin 2 - f(S— & ) • c (6-50) 여기서 Io= e4I 。 (1+cos2 20) /2m2c2R2 이다. sin 2 Mx/sin % 를 그리면 그림 12 와 같다.
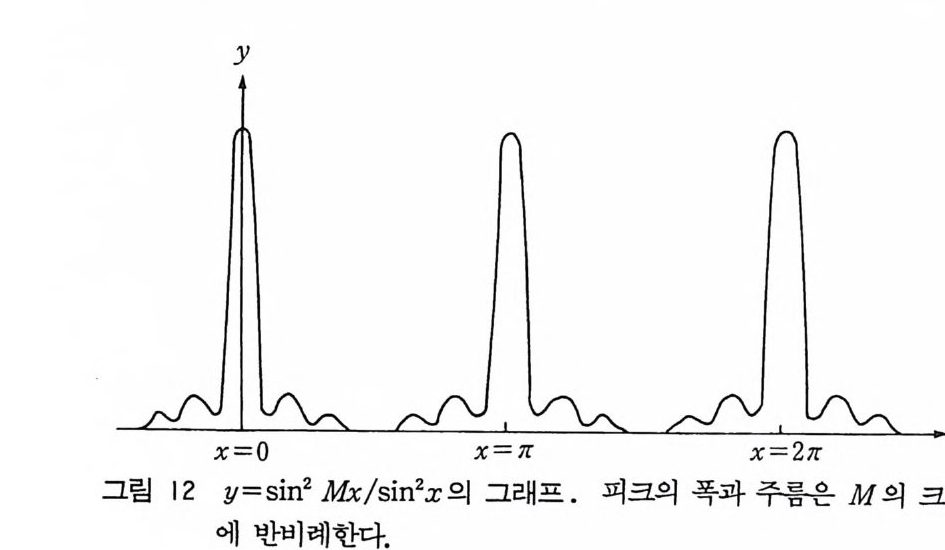 y
y
이 그립은 x= q 7r( 여기서 q는 임의의 정수임)점 이의는 거의 그 값이 영이고 영이 아닌 경우의 최대값은 M 히다. 그런데 lxi -mo( s i굽 M1x/sin 2 x) = M i2갔 /x2= M12 이다. 따라서 x=7r/,1• (S-S 。) .a= q 7r 이어야 그 값의 최대값은 M12 이된다.
그 이의의 값은 영에 가깝다. 죽 (S-S 。) • a= hA (S-S 。) • b= 臥 (S-S 。) • c= !A (6-51) 가 동시에 성립해야 Jp가 영이 아닌 값을 가질 수 있다(여기서 h, k, l 은 영을 포함한 양, 음의 정수이다). (6-51) 식은 Laue 의 식이 며 hkl 은 반사 평면의 M ill er 지수이다. 죽 세 개의 Laue 의 석이 동시에 성립해야 점 P 에 도달하는 산란 X- 선은 그 강도가 영이 아닌 값을 가질 수 있다. 피크에서 Ip= IOF2M12M22M32 그리고 M1M2M: r2 결정내 단위세포의 수이다. 이것을 M 으로 표시하면 디음 식을 얻을 수 있다. Ip= IOF2M2 (6-52) (6-52) 식에 의하면 P 점에 도달하는 산란 X- 선의 강도는 결정 내 단위세포의 총수의 제곱에 비례하고 구조 인자의 제곱에 비례한 다. 그리고 구조 인자는 단위 세포내에 원자가 어떻게 배열되는가 에 따라 그 크기가 다르다. 6 회절 강도의 표현 x- 선 회절 강도에서 얻을 수 있는 가장 중요한 양은 관측한 구 조 인자 F 。 (hkl) 이다. 전절에서 알 수 있는 바와 같이 구조 인자 는 실험에서 관찰한 회철 강도 (I。 (hkl) )의 크기와 다음 식의 관계
가있다. I。 (hkl) ex: I F.。 (hkl) 12 혹은 I。 (hk l) = c(hkl) I F.。 (hkl) 12 (6-53) 여기서 c(hkl) 은 평면 hkl, Lorentz 인자, 편국 인자, 흡수· 보 정, 온도 상태와 같은 실험 조건에 관계되는 몇 가지의 기하학적, 물리적 요인을 합하여 나타낸 인자를 의미한다. 단위세포내 원자의 위치를 알면 구조 인자는 계산할 수 있다. 더 욱이 구조 인자는 전자밀도 지도를 계산하는 데 사용되고(다음 장 에 설명할 것임) 이 전자밀도 지도에서 원자의 위치를 결정할 수 있 다. 따라서 식 (6-53) 은 X- 선 구조 해석에서 기본이 된다. 실험적 인 양 I。 (hkl) 은 |F 。 (hk l) I 을 통해 구조와 관계되는 결정학자가 원자의 좌표로써 구조를 알아낼 수 있는 정보를 제공할 수 있음을 보여준다. 1) Lorentz 인자 Lorentz 인자는 회절 실험 방법에 따라 Lorentz 인자를 구하는 표현식이 다르다. 입사 X- 선의 각도의 퍼짐, 파장의 퍼짐, 시료 방위의 배향성이 영향을 주는 인자이다. Lorentz 인자와 편광 인· 자를 합쳐 Lorentz 편광 인자 (P=(1+cos220)/2) 라고 하며 모두 삼각함수의 각도의 함수이다• 분말법에서 Lorentz 편광인자는 디음과 같다. LP= (1+cos220) /(s i n 내 cosfJ ) (6-54) 회전 단결정법, 진동 결정사전법 (oscil lat i on meth o d) 및 Wei. ssenber g법 (단결정을 사용하여 적도충선과 단색광 X 국 1 을 사용)에서
LP 인자는 다음과 같다. LP= (1+cos220)/sin 20 (6-55) Laue 법에서는 LP 인자의 표현식은 디음과 같다. LP= (1+cos228) /2s i n 내 (6-56) 여기에서는 하나의 예로 분말법에서 사용되는 Lorentz 인자를 구해 보자. 그림 13-(a 펴· 같이 평행으로 조사되는 단색광의 X- 선 의 빔을 생긱하고 결정은 점 0 에서 균일한 각속도로 회전하며 반 사 평면 중 어떤 것은 결정 표면에 나란하면서 Brag g 법칙이 만족 하면 이때 그 각을 0B 라고 하자. Brag g 각도에서 약간 벗어나도 강도는 제법 크다. 따라서 20 때 강도의 크기는 그림 13-(b 펴- 같 다. 결정이 Bra gg각에서 회전하면서 얻은 회절 범으로 사진건판 이나 계수관에서 얻어서 회절 빔의 총에너지를 측정할 수 있다. 이 에너지가 반사의 적분 강도이고 그립 11-(b 펴 곡선 아랫부분의 면 적과 같다• 적분 강도는 최대 강도보다 홍미로운데 이것은 최대 강
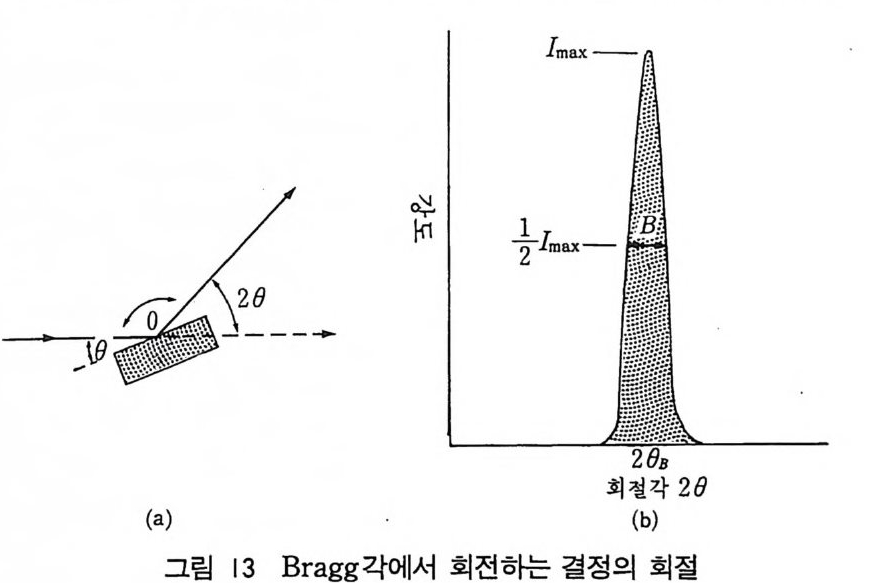 Jh7 2l— Img
Jh7 2l— Img
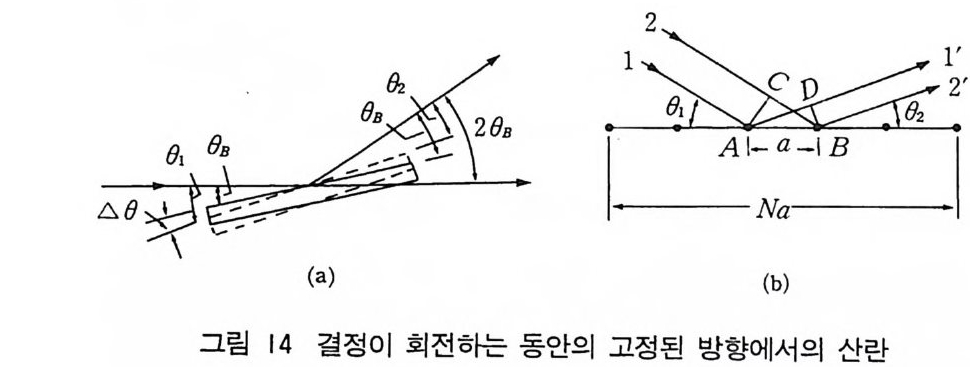 2
2
도는 시료의 특성을 나타내지만 적분 강도는 실험 기구를 약간 조 정해도 영향을 받기 때문이다. 더욱이 회절선의 강도를 육안으로 비교해 볼 때 육안으로 검토하는 것은 최대 강도보다 선의 적분 강 도이다. 반사의 적분 강도는 다른 변수가 고정되어도 0 유] 특별한 값에 관련이 있다. 이것을 회절 곡선의 두 가지 측면으로 생각할 수 있다. 그것은 최대 강도와 폭이다. 반사 평면이 입사 범과 0B 각도로 만나면 Bra gg법칙은 정확히 만족되고 20B 방향으로 회절 되는 강도는 최고가 된다. 입사각이 0B 에서 약간 벗어나면 이 방 향에서는 에너지는 약간 회절된다. 결정이 Bra gg긱에서 회전함에 따라 20B 방향에서 회절되는 총 에너지는 그림 13-(b 펴 Im ax-으로 주어지고' 따라서 lmax 의 값은 20B 방향으로 회절되는 에너지가 큰 결정이 회전하는 각의 범위에 관계한다. 그림 14-(a 제서 점선은 Brag g 각에서 6. 0 만큼 조금 벗어나서 회전하는 결정의 위치를 보여주고 있다. 이 경우 입사각 과 회절각은 반사평면에 대하여 같지 않고, 죽 입사각은 0B+ 스 8 가 되고 반사각은 0B ―6. 0 이다. 원자 치수로 확대해 보인 것이 그 림 14-(b) 이다. 여기서 원자의 하나의 평면에 대해 생각하자• a 는 평면내 원자 간격이고 Na 는 그 평면의 총길이이다. 이웃 원자에 의해 산란된 선 1’ 과 선 2 ’ 의 경로의 차는 다음과 같다.
81'2'= AD- C B =a cos 02-acos 01 = a[cos(0s— L::,,0 ) ― cos(0 計책)〕 즈 2a 스 0 sin 0 B 평면의 양끝의 원자에 의해 산란된 선 사이의 경로의 차는 N81'2' 이다. 이 두끝 원자에 의해 산란된 선은 1A 만큼 위상이 틀리면 회 절된 강도는 영이다. 그러면 영의 회절된 강도를 갖는 조건은 다음 과같다. 2Nat::, .0 sin 0s= ,1 따라서 책= 2Na Asi n Bs (6-57) (6- 5 7) 식은 제법 큰 에너지가 2(J B 방향으로 회전될 때 결정의 회전 최대 각 범위이다. Imax 는 이 범위에 관계가 있고 따라서 Imax는 1/sin 0B 에 비 례한다. 따라서 Imax는 낮은 산란 각도에서는 크고 후면 반사 영역에서는 적다. 회절 곡선의 폭은 이와 반대로 28g } 크면 크다. 또 최대 반폭 B(half- m axim um bread t h) 는 1/cos 0B 에 비례한다. 반사의 적분 강도는 회절 곡선 아래쪽의 면적과 같고 따라서 이 값은 Imax B 에 비례한다. 이것은 (1/sin (Ja ) (1/cos 0 이, 죽 1/s i n20B 에 비례한 다. 결정이 Bra gg각 부근에서 회전하면 반사의 적분 강도는 2(JB 의 중간 크기보다 2(J g} 크거나 작은 값에서 크다 분말법에는 또 다른 기하학적 요소가 있다. 어떤 특별한 Brag g 각에서 회절의 적분 강도는 그 Bra gg각도와 그 각도 가까이에 배 열된 결정의 숫자에 비례한다. 이 수는 결정이 완전히 무질서하게 배열될 경우일정하지 않다. 그림 15 는 점 0 에 있는 분말시료 주
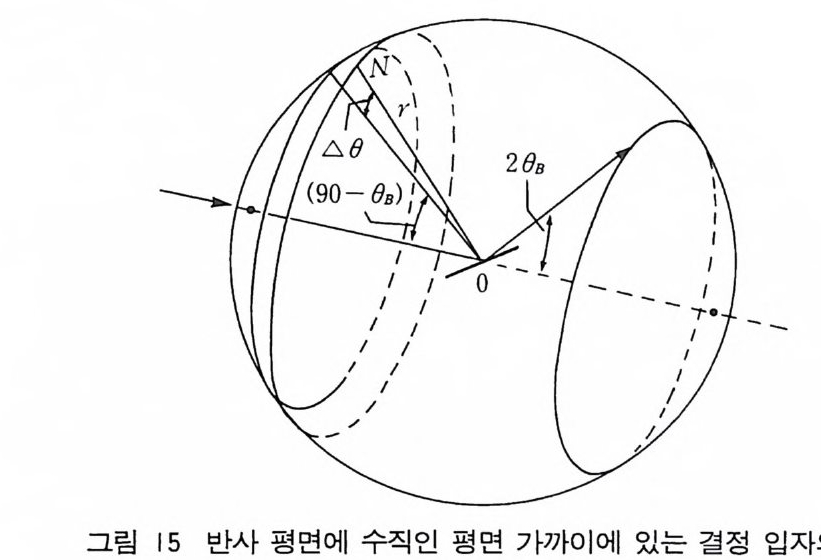 그림 15 반사 평면에 수직인 평면 가까이에 있는 결정 입자의 수
그림 15 반사 평면에 수직인 평면 가까이에 있는 결정 입자의 수
위를 그린 것이고 그림에서 보인 특별한 /'ik l 반사에서 ON 은 분 말내의 결정에서 이 평면군에 수직이다. 반사가 제법 큰 Bra gg각 부근의 각도 범위를 6. 0 라고 하자. 구의 표면에 띠의 폭이 R6 .0 에 놓여 있는 결정이 이것에 기여한다. 이 수 스 N 는 그림 15 에서 보듯이 전체 결정 입자수 N 에 대한 비율은 다음과 같다. 6.N IN= r6 .0 • 2Jr r sin ( 90— @ /4Jr r 2= 스 0 cos OB/2 (6-58) 죽, 반사하기 쉽도록 배열된 결정수는 cos OB 에 비례하고 후면 반사 (20s=180°) 에서 반사는 거의 없음을 알 수 있다. 상대적 강도를 평가할 때는 임의의 원추의 총회절 에너지와 비교 하지 않고 하나의 회절선의 단위길이당 적분 강도와 다른 것과 서 로 비교해야 한다. 예컨대 Deby e -Scherrer 방법에서 (그림 16) 회 절선 길이는 2Jr R sin 20s 이다(여기서 R 은 카메라의 반경임). 따라 서 단위길이당 상대강도는 1/sin 20s 에 비례한다.
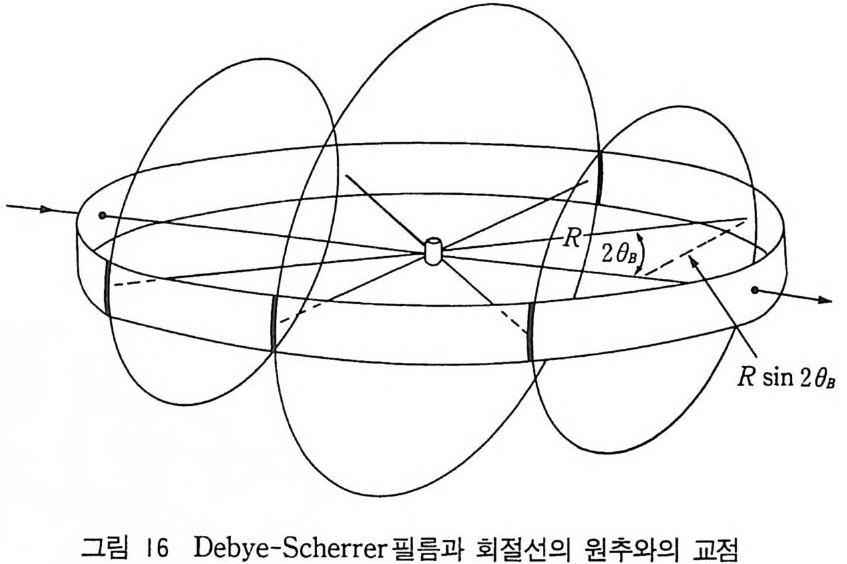 그림 16 Deb y e-Scherrer 필릅과 회절선의 원추와의 교점
그림 16 Deb y e-Scherrer 필릅과 회절선의 원추와의 교점
강도 계산에서 위에서 설명한 세 가지 기하학적 관계를 합하면 Lorentz 인자는 다음과 같다. 여기서 Bra gg각을 의미하는 B 를 없애고표시하면 Lorentz 인자= (1/ sin 2 0) • (cos 0) • (1/sin 2 0) = cos 0/sin 2 2 0 = l/4 s i n 내 cos 0 (6-59) Loentz 인자와 편극 인자 1/2(1+cos220) 와 결합하고 싱수인 1/8 을 생략하면 Lorentz 편국 인자는 다음과 같다. LP 인자= (1+cos220)/(sin 2 0 cos 0) (6-54) 이 값을 0 의 함수로 그리면 그림 17 과 같고 LP 인자는 중간각도 인 45· 에서 최하이고 전면이나 후면에서는 가장 큼울 알 수 있다. 2) 결정에 의한 X 국接의 홉수 그립 18 에 보인 바와 같이 입사 X- 선과 회철 X- 선이 단결정을
투과할 때 흡수하여 그 강도가 감소한다. 결정내에 미소 체적 dV 에 의해 회절된 X- 선은 결정에 입사하여 dV 에 도달할 때까지 거 리를 x, 또 회절한 X- 선이 결정내를 나갈 때까지 x' 의 거리를 통 과한다면 회절 X- 선 강도는 다음 식에 보인 인자만큼 감소한다. A= Jv exp( — EV4 x+x1) dV (6-60)
 50
50
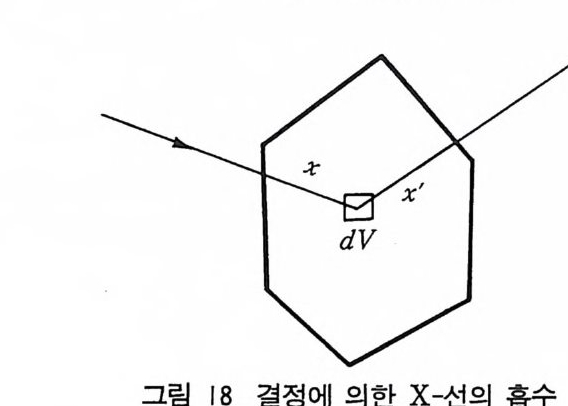 그림 18 결정에 의한 X- 선의 홉수
그림 18 결정에 의한 X- 선의 홉수
여기서 µ는 결정의 선형 흡수계수이고 dV 는 결정내의 미분소 의 부피이며 A 는 흡수 인자라고 부른다. 여기서 적분은 결정 전 체의 흡수의 영향이므로 결정 전체에 걸쳐서 한다. 그립 19 에 보 이는 바와같이 장방형의 단면을 가지는 결정에 따라 A 는 방향에 현저한 변화를 보인다. 따라서 정밀한 강도 측정에는 흡수 보정을 해야한다.
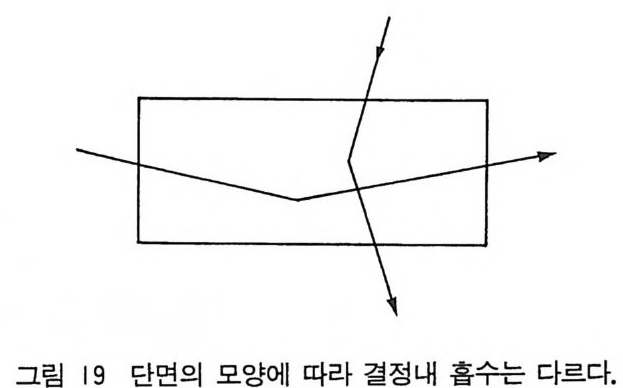 그림 19 단면의 모양에 따라 결정내 흡수는 다르다.
그림 19 단면의 모양에 따라 결정내 흡수는 다르다.
결정이 구상이나 원통형일 경우 A 는 쉽게 계산할 수 있고 이 결 과는 Inte r nati on al Tables for X-ray Cry st a l loga p h y 2 권 에 수록되어 있다. A 값은 µ의 크기에 관계가 있고 µ가 적으면 이 보정을 무시할 수 있다. 예컨대 결정이 반경 r 의 구상일 때 µr< 1. 0 이면 흡수 보정을 무시할 수 있다. 주어진 결정에서 회철된 X- 선의 강도는 그 부피에 비례한다. 죽, 시료내 존재하는 물질의 양에 바례한다. 따라서 가능하면 큰 결정을 선택하면 좋다. 그러나 X- 선 흡수 때문에 회절의 두께에는 제한이 있다. 두께가 커지면 결정을 지나는 회절 빔의 강도가 감소 한다. 최적 두께(t o Pt)는 선형 홉수계수의 함수이고 다음 식으로 주 어진다.
t。 P t =2/µ (6- 61 ) 대개의 유기화합물의 결정은 Cu Ka 단색 X- 선에서 µ< lO cm- 1 이다. 따라서 이들 유기화합물 결정의 최적 두께는 0 . 2cm이다. 흡수계수는(흡수단에서 제외하고) 원자번호가 커지면 급격히 증가한 다. 따라서 요드 결정은 µ=1450cm-1 이고 따라서 최적 두께는 단지 0.0014cm 이다. 한편 흡수는 파장이 짧아지면 적어진다. Mo Ka 선에서 유기화합물의 흡수계수는 대략 lcm - 1 미만이고 결 정성 요드는 183 cm-1 이다. 최적 크기 이하의 결정에 대해서도 여러 가지 반사에 대해 결정 내로 X 선이 지나가는 길이가 다르면 심각한 문제가 생길 수 있 다. 결정의 모양을 정확히 알면 컴퓨터 프로그래밍을 써서 흡수 보 정을 할 수 있으나 계산은 복잡하고 시간이 많이 걸리고 흔히 정확 하지도 않다. 따라서 적절한 크기의 결정을 선택하고 최적 실험조 건을설정해야한다. 3) 온도 인자 온도의 변화에 따른 X- 선의 강도의 영향을 생각해 보자. 전술한 바와 같이 sin 0/A 가 커지면 원자의 산란력이 떨어진다. 이것은 핵 주위의 전자구름의 크기에 관계가 있고 주어진 전자수에서 이 구름이 커지면 산란 효력은 더 빨리 떨어진다. 보통의 산란 인자 곡선은 정지 상태의 원자에서 전자의 분포를 기본으로 하고 있다. 그러나 실제 결정내 원자는 그 정지점 (rest po in t ) 주위로 항상 전 동하고 있다. 이 전동의 크기는 온도와 원자의 질량과 공유결합이 나 혹은 다른 화학결합으로 얼마나 단단히 결합되었는가에 달려 있 다. 일반적으로 온도가 높아지면 전동도 커진다. 열전동은 전자구 름을 더 큰 부피로 퍼지게 하고 실제 원자의 산란력을 이상척으로 정지하고 있는 모델보다 더 빨리 떨어지게 한다. 산란력의 감소는
다음 식으로 표현할 수 있다. /= /o exp ( -B(sin2 0)I,12 (6-62) 여기서 B 는 등방성 온도 인자(i so t ro pi c tem p e ratu r e fa c t or) 를 나타내고 B 는 원자 진동의 평균 제곱 진폭( U2 : mean squ are amp li tu d e of v i bra ti on) 과 다음 관계식으로 나타낼 수 있다. B=8 군 U2 (6-63) 표 1 은 B(A 아, U2(A 아과 평균 자승근 진폭 (rmsA) 사이의 값을나타내었다. 가끔 보게 되는 가장 작은 rms 진폭은 0. 05 A 이며 대개 유기 구조에서 실온에서 B 값은 3 에서 lOA 사이에 있다. 따라서 결합 길이를 논할 때는 B 값에 유의해야 한다. 그림 20 은 탄소의 원자 산란 인자가 sin 0/11 와 B 값에 따라 어떻게 변하는가를 보여주고 있다. 실제 결정내 원자는 이방성 열전동 운동울 한다. (6-62) 식을 이 방성 열전동의 경우로 확장시킬 수 있으며 총괄적 등방성 온도 인 자 T 는 다음 식으로 표현할 수 있다. T=exp ( -B(sin 0/11)2) =exp ( -Bl4(2sin 0I11)2) =ex p (-B/4(1/dhkl) 아 (6-64)
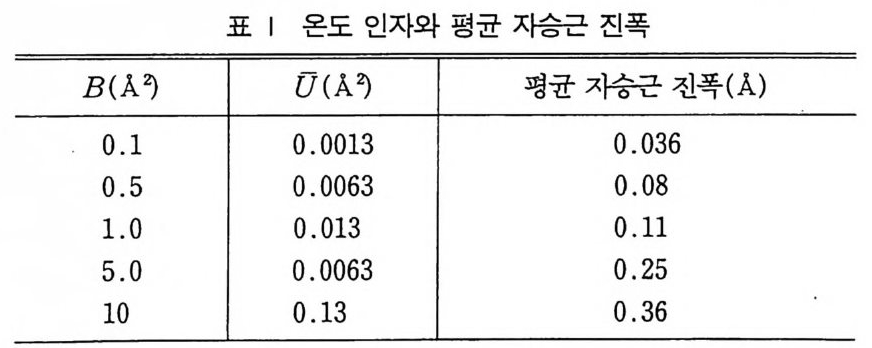 표 | 온도인자와평균자승근진폭
표 | 온도인자와평균자승근진폭
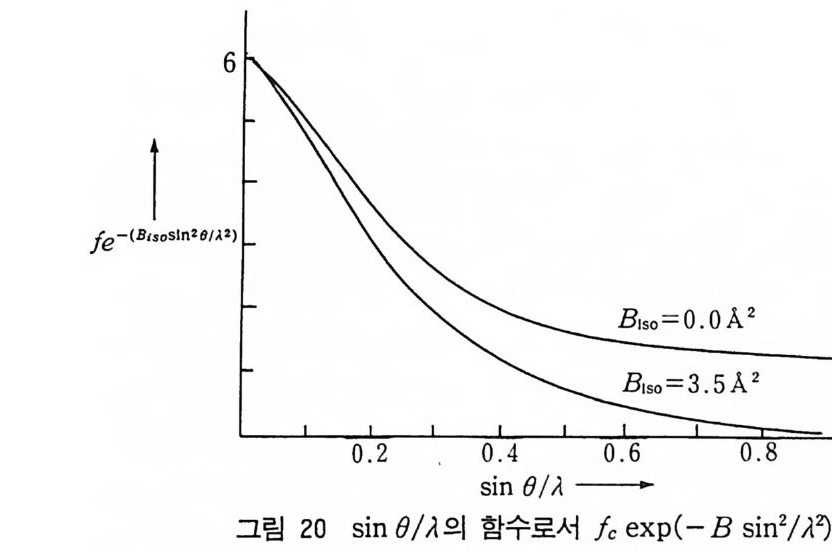 6
6
그리고 (l/d hkl)2=d*(hkl) •d•(lzkl) = (ha*+ kb*+ le*) • (ha*+ kb*+ le*) = h2a*2+ k2b*2+ l2e*2+ 2klb* e*cos a* + 2lhe*a*cos /3* +2hka* b*cos r* 따라A 1 T=exp [- B/4(h2a•2+k2b*2+ !2c *2+2klb*c*cos a* +2lhc*a*cos /3나 2hka*b*cos r*)J (6-65) 또 T 는 이방성 온도 파라미터 (/3iJ)로 표시하면 다음과 같이 쓸 수있다. T=exp [-(/3 1 1h2+ /32 2k2+ /33 3[2+2/3 1 2hk +2/3 2 3kl+2/3 1 3hl)] (6-66) 식 (6-65) 와 식 (6- 66 ) 을 비교하면 이방성 온도 파라미터는 다 음과같다.
f3u =Ba*2/4 ; /3z z=Bb*2/4 ; /33 3=Bc*2/4 ; f31 2=Ba*b*·cosr*/2 ; f32 3=Bb*c*·cosa*/2 ; f31 3= Ba*c* ·cos /3* /2 (6-67) /3IJ 대신에 각 원자의 전동을 나타내는 대칭적 ten sor Uu 파라 미터를 써서 온도의 영향을 나타낼 수 있다. T=ex p [-2 군( U11h2a*2+ U22k2b*2+ u33l2C•2+ 2 U12hka* b*cos r*+2 U13hlc*a*cos /3* +2 U23k/b* c*cos a*)] (6-68) 4) 다중도 인자 분말 시료에서는 어떤 결정은 (100) 평면에서 산란되도록 배열되 고 또 어떤 결정은 다른 평면에서 산란되도록 배열된다. 입방정계 결정을 예로 들면 (001), (010), (100), (100), •( 010), (001) 평면 에서 산란된 x- 선은 동일한 d 간격을 가지므로 이들 평면에서 회 절된 빔은 동일한 원추의 일부를- 만든다. 또 (111) 평면을 생각하면 (111), (111), (111 ), (ill), (111 ), (ITl), (111), (lIT) 은 또 동일한 d 간격을 가전다. 따라서 (111) 평면이 반사에 맞도록 배열 된 확률은 (100) 평면이 반사에 맞도록 배열된 확률의 4/3 배이다. 따라서 다른 모든 것이 동일하다면 (111) 반사의 강도는 (100) 강 도의 4/3 배이어야 한다. 동일한 평면에 기여하는 평면의 상대적인 수를 동일한 평면 간격 을 가지는 다른 평면의 수로써 정의하면 다중도 인자 (P) 라고 부른 다. 따라서 입방체 결정에서 {100} 평면형의 다중도 인자는 6 이고 {111} 평면형의 다중도 인자는 8 이다. 다중도 인자 P 는 결정계에 따라 다르다. 정방형 결정에서는 (100) 평면과 (001) 평면은 갇은 평면 간격을 가지지 않는다. {100}
평면형의 P 값은 4 이고 {001} 평면형의 디중도는 2 이다. 5 적분 강도의 표현식 앞 절에서 논한 강도에 영향을 주는 여러가지 요인과 강도와의 관계식을생각해 보자. Deby e -Scherrer Camera I=IFl2P(l+cos220)/(sin 2 0 • cos 0)A(0) T (6- 6 9) 여기서 I 는 상대적분 강도(임의의 단위), F 는 구조 인자, P 는 다중도 인자이고 O 는 Bra gg각이다. 삼각함수의 항은 Lorentz 편극 인자이다. A(0) 는 흡수 인자이고 T 는 온도 인자이다. 분말 패턴에서 이웃에 있는 선 사이에는 A(0) 와 T 를 무시해도 대략 성립한다. 분말회절장치 흡수 인자는 O 와는 무관하고 따라서 상대강도 계산에서 포함시 키지 않아도된다. I= I F l2P[l+ (cos220/sin 2 0 cos 0)] T (6- 7 0) 진동 및 회전회절 단결정 회전 회절법에서 상대적 적분 강도 I 는 근사적으로 다음· 과같이 표현할수 있다. /= IF r 12( 1+ cos2 20) /(sin 20) ·A(0) (6- 71 ) 여기서 | FT P은 온도의 영향을 고려한 구조 인자의 제곱이다. 흡수계수는 전술한 바와 같이 µ값이 적거나 작은 원통형이나 작 은 구형 결정에서 µR 값이 적으면 포함시키지 않아도 된다. 실험 에서 실제 관측되는 hk[ 회철 반접의 총 산란 강도 E 는 다음 식으
로표현할수 있다. E=K·lo/w· I F 津· (1+cos2 2(j )/ (sin 2(j ) ·A· V• c (6-72) 여기서 Io 는 입사 x- 선 빔의 강도이고 c 는 결정의 회전하는 각 속도이다. K 는 전자에 의한 복사선의 산란, 전자의 질량 (m), 전 자의 하전 (e)' 기본적 전자상수 (co=8.85416 X 10-12 far ad/mete r ), 전자 복사선의 속도 (c)' 결정의 부피내에 있는 단위세포 총수 (N), 입사복사선의 파장 (A) 등을 고려한 기본적 물리적 상수를 고 려한 인자이고 K= 〔터 (47rcomc2)]2N2A3 으로 표시된다. V 는 결 정의 부피이고 e 는 일차 및 이차 소멸효과를 고려한 보정상수이 다. 비이상적 결정내 파의 파괴적 간섭으로 입사하는 빔의 강도가 약화하는 것을 보정하는 값으로 보통 중요하지 않아 생략한다. 연습문제 L 다음과 같은 구조를 가지는 가상적인 원자를 생각하자. (a) 단위세포당 0, 0, 0 ; 1/2, 1/2, 0 위치에 두 원자를 가지는 저심 정방정계 세포 A 에서 a=2A, c=3A 이다. (b) 0, 0, 0 위치에 하나의 원자를 가지는 단순 정방정계의 세포 B 에서 각 원자에 대한 구조 인자 계산식을 간단히 하라. Cu Ka 선을 샤용할 경우 처음 네 개의 20 위치를 구하라. 2. Cu 금속은 면심 입방정계를 하고 있고 격자상수 a=3.615 A 이 다. 부록을참고하고
(a) Fu1 과 F331 을 구하라. (b) Cu Ka X 선을 사용하여 실험하였다. Lorentz 분극값은 각 각 얼마인가. (111) 반사와 (331) 반사의 다중도 값을 구하라. (c) (111) 반사와 (331) 반사에 대해 Deby e -Scherrer 사진에서 상대적 강도를 비교하라.
제 7 장 결정 구조의 해석 l 서론 1913 년 W. L. Bra gg가 NaCl 의 구조를 결정한 이래 수만 개 의 유기, 무기 결정의 구조가 결정되었다. 이러한 광대한 지식은 고체물리학, 생물과학, 결정화학 분야에서 기본적으로 ·중요하다. 왜냐하면 물질의 구조를 완전히 알기 전에는 물질의 성질을 완전히 이해할 수 없으며, 구조는 물질의 성질을 결정하기 때문이다. 금속 학에서는 결정구조는 소성변형, 합금형성 및 상변화와 갇은 현상을 이해하려면 필수적으로 알아야 한다. 새로운 물질은 항상 합성되고 또 과거에 합성된 많은 물질의 구 조도 아직 꾸근口쿠 구조를 결정히는 것은 끊임없이 진행되고 있 다. 결정구조는 다양하게 복잡하다. 간단한 구조는 몇 시간내에 그 구조를 알 수 있고 더 복잡한 것은 여러 달, 여러 해가 걸린다. 특 히, 단백질 구조는 복잡하여 어떤 단백질은 구조 해석이 어려워 아 직도 모르고 있다. 복잡한 구조는 복잡한 해석 방법이 필요하다. 구조 해석에 대해서 자세히 쓰기는 이 한 권의 책으로 어렵다. 알지 못하는 : 구조의 결정은 다음과 같은 근본 원칙에 따라 결정 된다. (1) 단위세포의 모양과 크기는 회절선의 위치에 의해 결정된다.
(2) 단위세포내의 원자의 갯수는 단위세포의 모양과 크기, 결정의 화학조성과 밀도에서 계산할 수 있다. (3) 마지막으로 단위세포내 원자의 위치는 회절선의 상대적 강도 에서 알아낼수있다. 위의 3 단계가 모두 완결되어야 구조결정은 완성될 수 있다. 그 러나 제 3 단계는 일반적으로 복잡하여 많은 결정은 1, 2 단계는 마 쳤으나 제 3 단계를 못마친 상태에 있다. 그러나 단위세포의 모양과 크기는 알고 단위세포내의 원자의 위치를 알지 못해도 1, 2 단계에 서 얻은 지식이 큰 응용성을 가지는 경우가 있다. 2 구조 인자의 계산 제 6 장에서 논의한 바와 같이 구조 인자는 다음과 같이 쓸 수 있 다. Fhk1= ~N fnex p (2 1ri( h xn+ ky,, + lzn)) (6-30) n=1 여기서 fn 은 n 원자에 대한 원자 산란 인자이고 이 원자의 단위 세포내의 분수 좌표는 (XnYnZn) 이나 여기서 합은 단위세포내의 모 든 원자에 대해 행한다. 따라서 단위세포내에 있는 여러 원자의 산 란 인자의 크기와 좌표만 알면 구조 인자를 계산할 수 있다. 예를 들어보자 (a) 간단한 면심정계의 구조를 가지는 세포는 대등점 0, 0, 0 ; 1/2, 1/2, 0 ; 1/2, 0, 1/2 ; 0, 1/2, 1/2 에 같은 종류의 원자가 놓여 있다. 그러면 구조 인자의 표현식은 다음과 같이 된다. Fhkz=/(exp (21riO ) +exp (1 ri( h + k)) +exp (1 ri( h + l)) + exp (1 ri( k + l)) (7-1)
=4/ : 이때는 h, k, l 이 모두 짝수거나 흘수이다. 즉 h, k, l 가 섞여 있지 않다. Fhu = O : 이때는 h, k, l 이 각각 짝수, 흘수, 짝수거나 홀수, 찍수, 홀수이다. 죽 h, k, l 이 섞여 있다. (b) 가장 간단한 격자형으로 단위세포의 원점에 하나의 원자가 있는 경우의 구조 인자를 계산해 보자. 그러면 Fhkt= Iexp (2 1ri( h xn+ ky n + lzn)) =f (7-2) 따라서 F 는 h, k, l 에 무관하고 모든 반사에 대해 같다. (c) 저심 단위세포에 대해 생각하자. 단위세포내에 같은 종류의 원소가 (0, 0, 0) 와 (1/ 2, 1/ 2, 0) 에 있다. 그러면 Fhk t= fex p (2 TCi 0) +/ exp (2 TCi (h /2+ k/2)) =J+fex p (T Ci (h + k)) =/(1+ exp (T Ci (h + k) )) (7-3) 이 표현식은 공액 복소수를 곱하지 않아도 계산할 수 있다. (h+k) 는 항상 정수이므로 F 값은 실수가 되고 복소수는 아니다. h 와 k 가 둘다 짝수이거나 흘수이면 h 와 k 의 합은 짝수이고 exp (1r i (h+k)) 는 l 이 된다. 그러면 Fhk1=2 f이다. 또 한편으로 h 와 k 가 하나는 짝수이고 하나는 홀수이면 그 합은 홀수이고 exp (T Ci (h+k)) 는 ― 1 이다. 그러면 F=O 이다. 이 경우에 l 지수의 값은 구조 인자 계산에서 영향이 없다. 예컨대 111, 112, 113, • 021, 022, 023 은 모두 같은 F 값, 2 f를 가지고 있다. 또 011, 012, 013, 101, 102 는 F 값이 영이다. (d) 체심 단위세포를 가지는 구조에 대해 구조 인자를 계산해 보자. 이러한 단위세포는 같은 종류의 원자가 0, 0, 0 ; 1/2, 1/2, 1/2 에 위치한다고 생각할 수 있다. 그러면 F 는 디음과 같이 계산 할수있다.
Fhk1=Iexp ( 21ri0 ) +Iexp (2 1ri( lz / 2 +k/2 + I/2 ) ) =/(l+ ex p(처 (h+k+ l))) (7-4) h+k+ l= 짝수이면 Fhk1=2/ h+k+l= 홀수이면 Fhk1=0 이다. 우리는 제 5 장 2 절에서 단위 세포의 기하학적 구조를 생각할 때 저심 세포에서 001 반사는 관찰되고 체심 세포에서는 관찰 안된다 고 했다. 이 결과는 구조 인자의 계산 결과와 찰 일치된다. 여기서 우리는 단위세포의 모양에 대해서는 언급하지 않았다. 예 컨대 예를 든 (d) 의 단순 단위세포가 어느 계에 속하는 단순 세포 인가는 언급하지 않았고 또 좌표도 분수 좌표를 사용했다. 즉 구조 인자는 단위세포의 모양과 크기에는 관계가 없다. 예컨대 어떠한 체심정계 세포도, 죽 입방정계냐, 정방정계냐, 사방정계냐에 관계 없이 h+k+l= 홀수일 때 회철 반사는 관측되지 않는다. 따라서 물질의 Brava i s 격자형은 회절 패턴과 긴밀한 관계를 가지고 있 다. 이것을 표 1 과 같이 간단히 요약할 수 있다. (e) 이제 NaCl 의 구조에 대해서 생각하·자. NaCl 은 면심입방 격자로서 NaCl 의 두 종류의 원자는 다음 위치에 있다 (NaCl 의 공
 표 | Bravais 격자의 소멸규칙
표 | Bravais 격자의 소멸규칙
간군은 Fm3m 이다). Na : 0, 0, 0 ; 1/2, 1/ 2, 0 ; 1/2, 0, 1/2 ; 0, 1/2, 1/2 Cl : 1/ 2, _ 1/2 , 1/ 2 ; 0, 0, 1/ 2 ; 0, 1/2, O ; 1/2, 0, 0 Na 원자의 위치는 면심 이동위치와 관련되고 Cl 원자의 위치도 면심이동 위치에 있다. 따라서 공통적인 항을 묶어내면 구조 인자 의 계산이 간단히 된다. Fhk1 = /Na 目 + exp ( 1ri( h + k) ) +exp ( 1ri( h + l) ) +exp ( 1ri (k + l) ) ]+ / c1 exp ( 1ri (h + k+ l) ) [l+ exp ( -1ri( h + k) ) + exp( — 1ri( h + l) ) +e xp (— 1ri( k + [) )] (7-5) 이다. 그리고 ex p (n1r i )=ex p( 一 n1r i)이므로 Fhk/ 은 다음 식과 같이 간단히 쓸수 있다. Fhk1 = [/Na+lei e xp (1 ri( h + k+ l))] [l+exp (1 ri( h + k)) + exp (1 ri( h + l)) +exp 1 ri( k + l)] h, k, l 이 모두 짝수거나 홀수로서 h, k, l 의 합이 짝수면 Fhk1=4(/Na+f a) h, k, l 의 합이 홀수면 Fhk1=4(/Na-fc 1) h, k, l 이 짝수, 홀수가 섞 여 있으면 Fhk1= 0 (7-6) (f) 이제 CsCl 의 결정 구조에 대해 생각하자. CsCI 는 단위 세 포당 2 원자(하나의 실험식 단위)를 가지는 단순 입방격자이다. 공간 군이 Pm3m 으로서 두 원자는 다음 위치에 위치한다. Cs 는 0, 0, 0 에 위치하고 Cl 은 1/2, 1/2, 1/2 에 위치한다. 그러면 Fhk1=f cs exp (21riO ) +fc1ex p (1 ri( h +k+ l)) =!cs+lc1exp (1 ri( h + k+ l) )
h+k+ l=2n 이면 Fhk1=fc s +f c1 h+k+ l=2n+ l 이면 Fhk1 = f cs -fc 1 (7-7) 따라서 CsCl 이 만약 체심격자라면 h+k+l=2n+I 일 때는 반 시를 관측할 수 없다. 그러나 CsCl 는 단순격자이므로 h+k+l= 2n+l 일 때 관측된다. 따라서 계통적인 소멸만을 관찰하여 어떤 Brava i s 격자인가 쉽게 알 수 있다. (g) 조밀 육방정계 결정의 구조 인자를 계산해 보자. 같은 종류 의 두 원자가 0, 0, 0 와 1/3, 2/3, 1 / 2 에 위치한다. Fhk1=/exp (2rci0 ) +fexp (2 rci( h / 3 +2k/ 3 + //2 ) ) =/[1+exp (2 rci( ( h+2k) /3 + l/2 )) ] 여기서 (h+2k)/3+l/2=g 라고 두면 Fhk1=f ( l+exp (2 rcig ) ) g는 1/3, 2/3, 5/6 와 같은 분수값이다. X- 선의 회절 강도는 IFl2 에 비례하므로 |F|2 울구해 보자. I Fhkl |2=/ 2( 1+exp (2 rcig )) (1+exp ( -2mg )) =/2( 2+exp (2 rcig )+ exp ( -2rcig )) 그런데 exp (ix)+ exp (-ix)= 2cos x 이므로 I Fhkl 12=/ 2( 2+2 cos 2rcg ) =/2(2 +2(2 cos2rcg - l)) =/2(4 cos2rcg) =4/2 c os2rc ((h+2k)/3+ (l/2) ) (7-8) h+2k 가 3 의 배수이고 l 이 홀수이면 cos rc((h+2k)/3+ 송) =O 따라서 | Fhkl 12= 0 따라서 1, 1, 1 ; 1, 1, 3 ; 2, 2, 1 ; 2, 2, 3 과 같은 반사는
관찰할수없다. 또 h+2k 가 3 의 배수이고 l 이 짝수이면 ((h+2k)/3+'l /2 ) = n (7-9) 여기서 n 은정수이다 . COS2J rn = 土 1 이므로 COS2J rn = 1 이다. h, k, l 의 가능한 모든 값을 생각하고 결과를 요약하면 다음과 같다 . 3hm+2 k l― 麟。 333mmm 土士 11 ii군f34 f/2 2 있을(h) 경결우정 이원 자b가 축 에x , 수Y, 직z인 에 미있끄군으럼면 평면반(드gl시i dex ,p lya n ez)+ lc/ 를2 에 가도지 원고 자가 존재하게 된다. 그러면 ’ Fhkz=f n[ e x p ( 21ri( h x+k y + lz) ) +exp ( 21ri( h x— k y + l (z+l/2))] =In ex p (2 저 (hx+ lz)) [ex p (2 1rik y ) + exp ( -21rik y+ 7ril ) ] Fhkz=f n exp ( 21ri( h x+ lz)) [e xp ( 21rik y )+ (exp (— 21rik y ) ) (exp ( ml ))] . (7-10) 만약 k=O 이면, 죽 h·l 반사에 대해 다음 관계식을 얻을 수 있 다. Fhoi= fnex p 2 7ri’ ( hx+ lz) (l+e xp 7r il ) (7-11) l=2n 이면 Fhol=2/nexp m '(hx+ lz)
l=2n+I 이면 Fho1=0 죽 hOl 반사에서 l 이 홀수일 때 X- 선 반사 강도는 관측할 수 없다. (i) 마지막으로 결정의 c 축에 평행하게 2 회 나선축 (21) 이 있으 면 하나의 원자가 x, Y, z 에 있으면 다른 원자는 x, y, z + I / 2 에 존재한다. 그러면 Fhkl 은 다음과 같다. Fhk1=f n[ exp (2 TCi (h x+ ky + lz)) +ex p (2 처(― lzx-ky + l =I(nz +ex l/p2 ()2 T))C]i l z ) [e xp (2 TCi (/ zx+ky ))+ exp ( 2m.(— hx-ky + l/2) ) ] 여기서 h 와 k 가 모두 영이면 Foo1=f ne xp (2 TCi lz (l+exp m l)) l=2n 이면 Foo1=2f ne xp 2T Ci lz l=2n+l 이면 Foo1=0 따라서 OOl 반사에서 l 이 홀수인 반사는 관찰할 수 없다. 일반적으로 Brava i s 격자에 의한 소멸칙은 hkl 반사에 나타나고 미끄럼 평면에 의한 소멸칙은 hkO, hOl, Okl 형 반사에 나타나고 hOO, OkO, OOl 반사에는 나선축에 의한 소멸칙이 나타난다. 종합하 면표 2 와같다.
 표 2 나선축과 미끄럼 평면에 의한 소멸칙
표 2 나선축과 미끄럼 평면에 의한 소멸칙
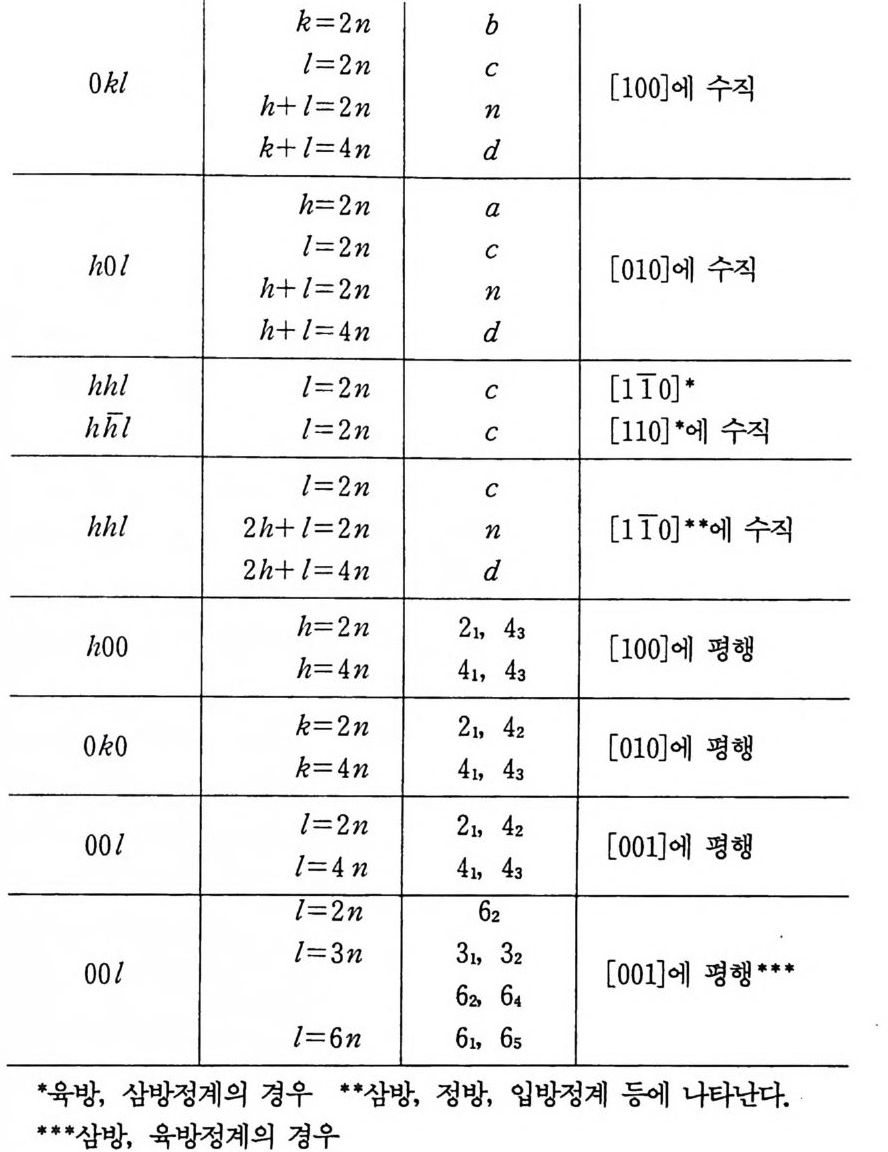 k=2n b
k=2n b
3 공간군의 결정 계통적 소멸을 나타낸, 표 1 과 2 를 검토하여 X- 선 회절 반사 강도에서 Bravais 격자형과 나선축이 있는지 혹은 미끄럼 평면이 있는지 알아낼 수 있다. 그러나 모든 hk[ 반사를 검토해야 정확한 공간군을 판단할 수 있다. 때로 부분적인 데이터에 기초하여 예컨 대 hkO, hOl 혹은 0kl 등만 조사해 보고 공간군을 결정하여 툴 리 게 판단할수있다. (1) 보다 일반적인 형의 반사가 소멸되면 이 반사에 포함되는 특 별한 형의 반사에도 자동적으로 소멸칙이 존재하게 된다. 죽 체심 격자에서 h+k+ l= 홀수에서 소멸되면 lzOO 반사는 h 가 홀수이면 소멸됨이 자동적으로 의미하게 된다 . 따라서 a 축에 평행한 2 리 있는지 없는지 결정하는 기준에는 이것이 이용될 수 없다• (2) 표 1, 2 에 열거한 것 이의의 반사가 있으면 이에 해당하는 대칭요소가 이 결정에는 없음을 의미한다. 이 사실로 다른 종류의 대칭이 있음을 알아내는 데 사용할 수 없다. 예컨대 k 가 홀수에서 0kl 반사가 관측되며 이것은 단지 b 미끄럼 평면이 없음을 의미한 다. 이것으로 다른 대칭, 죽 거울평면에 평행한 다른 대칭요소가 있는지 없는지는 알 수 없다. 4 회절의 대칭 다른 방법으로 어떤 대칭요소가 있는지 없는지 알 수도 있다. 단 결정의 역격자에서 강도 분포를 검토하여 그 결정에 존재하는 특별 한 대칭요소가 있는지 없는지 알 수 있다. 결정의 a 축과 b 축에 평행한 거울평면은 단위세포내의 점 xyz 에 대해 이것은 대칭의 대 동점 xy z 와 관계가 지어진다. 이것은 구조 인자 |Fhkll=IFhkl| 가
되도록 한다. 따라서 hkl 과 hk[ 은 같은 반사 강도를 가진다. 회 전축에도 동일한 관계를 적용할 수 있다. c 축에 평행한 4 회 회전 축이 있으면 |Fhk1I=IF-;; 』 =|R 비 =|F 죠 11 이 성립하게 된다. 이 와 비슷하게 결정에 대칭 중심이 있으면 |FhkI|=|F57| 이 성립하 게 된다. 이상 분산이 무시할 정도로 적으면 대칭중심이 없는 결정 에서도 |Fhk1I 와 |Fh,; 기를 구별할 수 없다는 사실을 유의해야 한 다. 대개의 회절 실험에서 이와 같은 대칭중심의 도입을 결정학에 서는 Frie d el 법칙이라 한다. 결정에 대칭중심이 있는지 없는지 알면 공간군 결정 문제는 상당 히 쉬워진다. 때때로 이 문제는 대칭에 관계하는 결정학적 성질을 조사하여 알아낼 수 있다. 결정의 형(形)에서 올바른 점군대칭을 알아내는 것이다. 불행히도 이것은 결정이 잘 발달된 표면을 가지 지 않으면 알 수 없다. 결정이 대칭중심을 가지지 않을 때 가지는 전기적 성질이 압전성 (堅電性 : P i ezoelec t r ic)과 초전성 (魚電性 : Py roe lectr i c ; 결정의 일부, 가열했을 때 표면에 전하가 나타나는 성질) 이 있는가를 조사하는 것이다. 이러한 특성이 있으면 대칭중심이 없음이 확실하나 그러나 이러한 성질이 없다고 해서 대칭중심이 있 다고는 단정할 수 없다. 때때로 이러한 효과는 너무 적어서 사용하 는 측정기기의 감도 범위 밖에 있기 때문이다. 다행히도 이러한 문제를 해결하는 데 x- 선 회절 강도를 이용할 수 있다. 원자의 흡수단에 가까운 에너지를 가지는 X- 선을 사용하 면 이상 분산 효과는 이상 산란체와 그 밖의 원자 사이에 위상의 지연 (Phase la g)을 일으킨다. 대칭중심 구조를 가지면 이 효과는 그 원자의 기여의 크기를 바꾸어 준다. 그러나 비대칭 구조에서는 hkl 과 EET 반사 쌍의 회절 강도의 상대적 크기률 분산에 의해 바꾸어 준다. 따라서 결정의 대칭중심이 존재하는지는 적철한 X -선 빔을 쬐어서 Frie d el 법칙이 위반되는지롤 관찰하여 알 수 있 다. • 이러한 실험은 쉽게 사용할 수 있는 X- 선 듀브가 있는지에 달
려 있으나 생각보다는 간단하고 쉽다. 결정의 단색화 장치로서 X -선 파장을 선택하고 조그마한 회절 강도처를 측정할 수 있는 아온 화 측정 장치가 있으면 이것은 특히 쉽다. 실제로 X- 선 회절 강도 그 자체가 결정의 대칭성의 존재를 반영 한다. 회철 강도의 크기는 결정내에 존재하는 대칭에 의해 원자의 열에 제한받기 때문이다. 대칭중심 구조를 가진 결정에서는 구조 인자의 평균 크기와 평균 회철 강도의 비는 0.785 인 데 비해 비대 칭 중심구조를 갖는 결정은 0.637 이라고 W i lson 은 유도하였다. 실제에 있어서는 모호한 원인 때문에 두 이상적 값의 중간값을 가 진다. 5 Fried el 법칙 같은 조(組)의 평면의 서로 반대편 대동위치의 회절 강도는 같 다. 죽, Ihkl=I;;;-l 이다. 이것이 Frie d el 법칙이고 이것은 다음과 같이 간단히 증명할 수 있다. 구조인자는 복소수이므로 다음과 같 이쓸수있다. Fhkz= 2:f;ex p (2 元i (hx1+ ky1 + lz1) ) 조 짜 os 21r(hxJ + ky j+ lzi) + i sin 2 1r (hx.서 -ky 1 + lz1) ) ] =Ahkl+ iBh kl 여기서 Ahk1=~f ;co s(2J r( hxj+ kyJ+ lzj)) 그리고 Bhkl=~/j s i n(27r(hx;+ky ;+다)이다. 또 합성파의 위상은 다음과 같다. ahkt= tan -1 (Bhkt! Ah kt) F죠 7 =~/;exp (2 7ri( - hxrkYrlzJ) ) = ~/Jc os(27r(hx;+ ky i+ lzj) ) - i~/J sin (2 7ri ( hx;+ ky ;+ lz;) )
= Ahkl 一 iBh kl 계산에서는 | F l 와 위상각 a 는 보통 이들 식에서 계산할 수 있 다. 따라서 Ahkt= Ai; ;;l Bhkl=-Bhkl Fhk1= Ahk1+ iBh kl F訂 ;1=Ahkl ―iB hkl Ihkl OC Fhkl • F· hkl= (Ahkl+ iBh kl) ' (Ahk1-iB h kl) I 訂 ;locF; ;石· F*;=;; A;1 h = k(/A+hBkhl—k i/B h kl) (Ahk1+ iBh kl) = A2hkt + B2hkl 따라서 Ihkl= l;;; ;7 Frie del 법칙은 Fhk1= F.죠 7 을 요구하지 않고 | FhkI1=|F; ;;;기을 요구한다. 그림 1 에서 이러한 반사에 대해 위상의 그림을 보이고 있으며
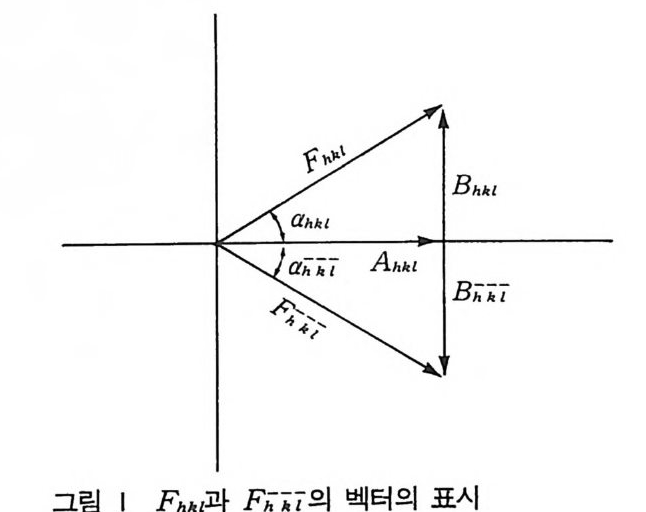 Bhkl
Bhkl
일반적으로 다음 관계식이 성립한다. ahkl=— a hkl 6 Fourie r 방법 어떤 잘 행동하는 함수 (well-behaved fu nc ti on) 는 적절한 삼각함 수의 합, 즉 Fourie r 함수라고 부르는 함수로 나타낼 수 있다. 전자밀도 함수는 cosin e 함수로 된 Fourie r 급수로도 표시할 수 있다. 그림 2 에서 나타낸 열은 적절한 대칭성을 가지고 있으므로戶 따라서 이러한 전자밀도는 cos i ne 의 함수로서 다음과 같이 나타낼 수있다.
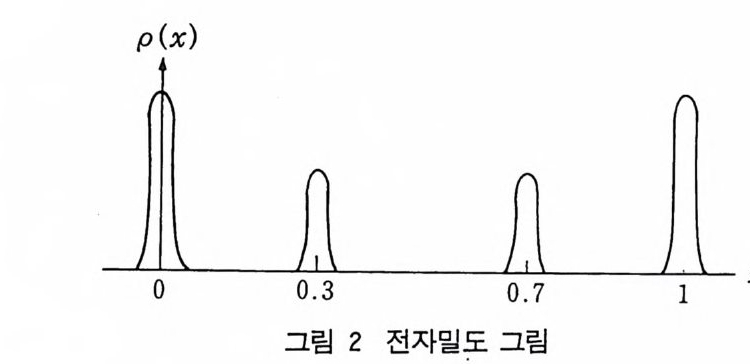 p( x)
p( x)
p( x)=~ An cos2 Jr n( 건X <7- 12) 여기서 변수 n 은 영을 포함한 음, 양의 정수이고 X 는 a 축상 의 거리이다. 계수를 적절히 선택함으로써 피크의 분포를 나타낼 수 있다. 계수는 함수 p (x) 의 Four i er 급수의 직교성 (o rth o g ona lity)을 이용하여 구할 수 있다. 죽 양변에 cos21Cm(X/a) dx 를 곱하고 이동 주기 a 에 걸쳐 적분하면 된다.
a ~p(x ) ~os27rm(X/a) dx = I:An J ! cos 2mz(X/a) cos 27rm(X/a) dx (7-13) 오른편 식의 적분항을 계산하면 다음과 같다. 1: cos 27rn(XIa) cos 27rm(X/a) dx= 1/2 f~ cos 27r (n+ m) (X/a) dx+ I/2 ,Ca cos 27r(n— m) (X/a) dx 봅 (7-14) 따라위서의 적n=분—은 m 주 이기거함나수 의n =적+분m으 일로 때한만 주을기 제에의 걸하쳐고 는적 분영이을다 .한다 또. 11= 土 m 에서의 적분값은 a 이다• 그러면 £_p(x ) cos 27rm(X/a) dx= a/2(A-m+A 깁 봅 A-m=Am 라고 두면 cos i ne 계수는 다음과 같다. Am= l/a ,C_a p( x) cos 27rm(X/a) dx (7-15) 움 더 일반적인 대칭에서 Four i er 급수는 지수를 써서 표시할 수 있다. 실제 결정의 3 차원적 전자밀도는 다음과 같이 쓸 수 있다. p( xyz ) = In: I-ocmo:o Ip: Anm p e xp (2 7ri (n (x/a) + m(y / b) +p(z /c) ) (7-16) 여기서 Anm p는 결정해야 할 계수이다.
구조인자는 아래와 같이 표시할 수 있다. Fhk1= ~fnex p ( 2m(h(x/ a )+ k(y / b ) + l (z/ c ) ) n 구조인자를 전자밀도로써 표시하면 아래와 같이 쓸 수 있다. Fhk1=j jjp(x y z ) exp (2m . (h (x / a) + k(y / b ) + l (z/ c ) ) dxdy d z (7- 1 7) 그리고 x=ax', y =b y'및 z=cz' 로 두자. 그러면 fdv= i adx i bdy icdz = abc11dx'i 1dy 'i1dz' = V11dx'11dy '1 1dz' 이다. 따라서 Fhkl= V 「o 1o1 1o1 p (xy z ) exp { 2m (h(x/a) + k(y / b) + l(z/c)}dx' dy ' dz' = V 「O 「./0 f./0 1 죠n 효-OmO ~p Anm p ex p {21C i (n(x/a) + m(y / b) +p(z /c) }exp {2 1Ci (h (x/a) + k(y / b) + l(z/c)}dx' dy 'd z' = V 「o f./0 1 f./0 12n _초mOO ~p Anm p ex p {21C i (nx'+ my '+ Pz') } exp {2 1Ci (h x'+ky '+ lz')}dx' dy ' dz' =V 효n 효-oomoo ~pA nmP-.1/ 01 1./01 l.101 ex p {21C i (h+ n) x'} exp {2 1C(k+ m) y'} exp {2 1Ci (/+p) z'}dx' dy ' dz' (7-18)
위의 주기함수에 관한 적분은 n=-h, m=-k, l=- p가 아니 면 영이다. 따라서 Fhk 1= VAhk1J 1J 1J 1 dx' d y ' dz ' (7-19) = VA 函 따라서 Ah k t = Anmp = Fhk1/ V 이다. 그러면 전자밀도함수 p (x yz ) 는 다음과 같이 쓸 수 있다. p( xyz ) =— 1V ~n ~°h~° FI hk1exp { -21ri( h x/a+ ky / b+ lz/c) } (7-20) (7-20) 식에서 좌표는 분율좌표로 x/a, y/ b, z/c 로 나타내었 다. 따라서 x, Y, z 는 37H 의 결정학적 축을 따라 측정한 거리이 다. 합은 hkl 의 모든 양수 및 음수에 걸쳐 행한다. 따라서 3 차원 적 역격자 공간 전체를 걸쳐 회절 강도의 분포를 계산해야 한다. (7- 20 ) 식에 단위세포내 어떤 점 (x/a, y/ b, z/c) 에서의 전자밀도 는 주어진 분율좌표 (x i a, y/b , z/c J에 대해 모든 hkl 값, 죽 모든 관찰한 반사에 걸쳐서 (7-20) 식의 합산울 수행함으로써 결정할 수 있다. 이러한 합산은 그 좌표가 지정되는 단위세포내의 여러 위치 에 대해 행할 수 있다. 따라서 여러 점에서 전자밀도를 결정함으로 써 전자밀도 그림을 그려 전자밀도가 큰 위치에 그 크기에 대응하 는 원자가 존재한다고 생각할 수 있다. Fhkl 의 부호가 결정되지 않음은 실험적으로 측정한 값이 X- 선 회절 빔의 세기이지 진폭이 아니라는 사실에 기인하며 이것은 매우 골치 덩어리인 것으로 밝혀졌으며 이러한 문제에도 불구하고 (7-20) 식을 사용할 수 있는 여러 방법이 제안되었다. 하나의 접근 방법은 단위세포내 분자의 근사적 모양이나 근사적 위치를 얻도록
하는 방법에 좌우된다. 예컨대 어떤 분자는 높은 산란 확률을 가져 위치를 밝혀낼 수 있는 하나의 무거운 원자를 포함하기 때문에 그 분자의 나머지 부분의 복잡성을 처음에는 무시한다. 그러면 가장 중요한 구조 인자의 부호는 측정할 수 있다. 이들 몇몇 구조 인자 의 값을 (7-20) 식에 대입하면 근사적인 전자밀도 그림을 그릴 수 있다. 그리고 나서 더 많은 구조 인자의 부호를 (7-17) 식을 사용 하여 알아낼 수 있다. 이러한 방법으로 더 많은 반사에서 얻은 정 보를 이용하여 구조를 점점 구체화시켜 가면서 상세한 구조를 얻을 때까지 계속한다. 구조 인자의 식 (6- 30 ) 과 전자밀도의 식 (7-20) 을 비교해 보면 대단히 유사하다. (7-20) 식은 역격자 공간으로 나 타낸 구조인자로 표시한 실제 공간에서의 전자밀도에 관한 식이다. 죽 전자밀도는 구조 인자를 Fourie r 변환으로 나타내었고 구조 인 자에 관한 식은 전자밀도를 Fourie r 변환으로 나타낸 식이다. 그 렇다고 하여 두 식이 동일한 식이라는 뜻은 아니다. 전자밀도에 관 한 식은 음의 지수항을 가졌고 구조 인자에 관한 식은 양의 지수항 을가졌다. 7 이상적 결정의 구조결정의 개요 결정구조를 결정하는 기본 식을 이용하여 예를 둘어 생각해 보 자. 주기(단위세포의 길이)가 lOA 인 가상적인 1 차원 구조를 생각 하고 Cu Ka 선 (A= l. 5418A) 과 Bra gg식을 적용하여 h 를 -12 에 서 +12 까지의 25 개의 값을 얻었다. 표 3 의 값은 탄소원자가 x=l.833A 위치와 8.167A 위치에 있 는 구조에 대한 회절선에 대한 h 와 sin 0 의 값과 구조 인자 Fh 의 값이다. 이 위치는 주기적인 성질 때문에 원자가 +1.833A 과 - 1.83 3A 에 있다고 표현할 수 있다. 죽 구조는 중심 대칭형이다. 구조인자 식을 생각해 보자.
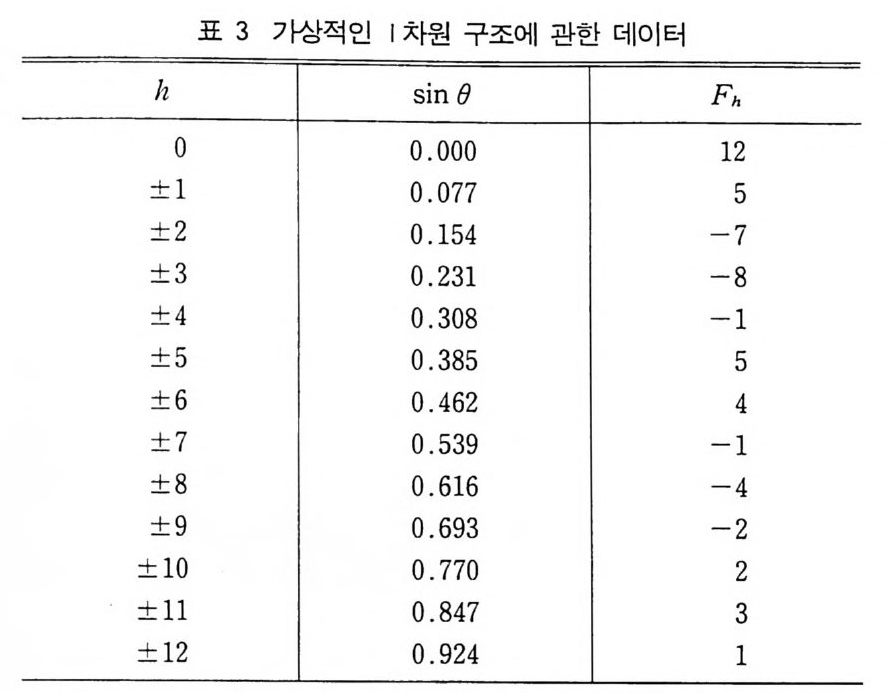 표 3 가상적인 1 차원 구조에 관한 데이터
표 3 가상적인 1 차원 구조에 관한 데이터
2 Fh= j~= l fiexp (2 1rih x i) 정/J cos 21rhxi+ i sin 21rhx』 (7-21) 그리고 Xc2= —Xc1 이면 Fh =/c[co s 2 처Z Xc1+cos 21rh(-Xc1) + i sin 2 처 ZXc1+ i sin 2 짜 (-xc1) 〕 = 2/c COS 21rhxc1 (7-22) 중심 대칭형의 구조에서 허수부의 항은 Xc2=-xc1 의 구조적 특 성 때문에 s i n(-x) =一 s i nx 이므로 제거된다. 일반적으로 중심 대칭 구조에서는 허수항은 서로 제거되고 구조 인자는 cosin e 항의 합으로 표시할 수 있고 각각의 중심 대칭쌍의 cos i ne 항에 2 를 곱 하여 다른쪽 편의 위치에 있는 원자분의 기여를 생각해 주면 된다.
죽
~leis i n 21rhx=0 (7-23) 또 t ana=O 이므로 a=O 이거나 r 이다. 이 두 개의 위상각 (ph ase an g le) 은 F 크기에 (+)나 (키부호에 할당한다. 표 3 의 Fh 칸은 (7-22) 식에서 계산한 값에 위상도 생각하여 측정한 진폭 이다. 실험적으로 측정한 것은 강도이고 강도에서 진폭이 계산된 다. 그러나 일반적으로 위상은 관찰하는 것이 불가능하다. 이러한 정보의 부족은 위상각 문제를 일으킨다. 전자밀도를 계산해 보자. 전자밀도를 나타내는 1 차원 Fourie r 급수를 쓰자. p( x) =1/L ~Fh ex p(一 2 Jri hx) (7-24) h 중심 대칭형 구조에서 구조 인자 표현식과 같이 간단히 쓸 수 있다. p(x ) = 1/L -~nn F h[cos 21rhx— i s in 21rhx] (7-22) 식에서 Fh=Fi: 이다. 따라서 p(x ) = 1/L[~--n1F h[(cos 21rhx+ i sin 21rhx) + Fa+ 幻있 (cos 21rhx —i s in 21rhx) ] 1 = 1/ 互 Fa+ ~n1 Fh (cos 2 처 hx+ i sin 2 처 hx) + 幻갓 cos 2 챠h xj ― i sin 2 챠h x) ] 1 = 1/L[Fo+ 2~n Fhcos 21rhx] (7-25) 1 표 3 의 Fh 칸의 구조 인자 값을 대입하면 임의의 점 x 에서의 전 자밀도를 나타내는 급수의 식을 준다.p( x)= 1/10[12+ 2(5) cos 27rx 一 2(7) cos 2 짜 2x) -2(8) cos 2 짜 3x) +…… +2(1 ) cos 27r( l2x )] (7-26) 표 4 에는 x=0.00, 0.02,… …, 0.24 의 값을 가질 때의 2Fhcos 27rhx 의 값을 포함한 13 개 항의 값을 계산한 것이다. x=0 . 24 까 지 계산하면 원자가 있는 부분의 전자밀도의 거동을 충분히 알 수 있고 원자가 있는 위치는 전자밀도와 Fourie r 급수에서 구한 값을 그립 3 에 나타내었다. 8 이상 분산과 그 영향 구조 인자 계산에서 원자 산란 인자 IJ 를 실수라고 가정하였다. 보통 사용할 때 실수값을 가지는 것은 사실이며 입사 X- 선의 진동 수가 원자의 흡수 전동수와 크게 다르다는 가정 아래 계산한 것이 다. 이 사실은 가벼운 원자와 X- 선 회절에서 보통 사용하는 복사
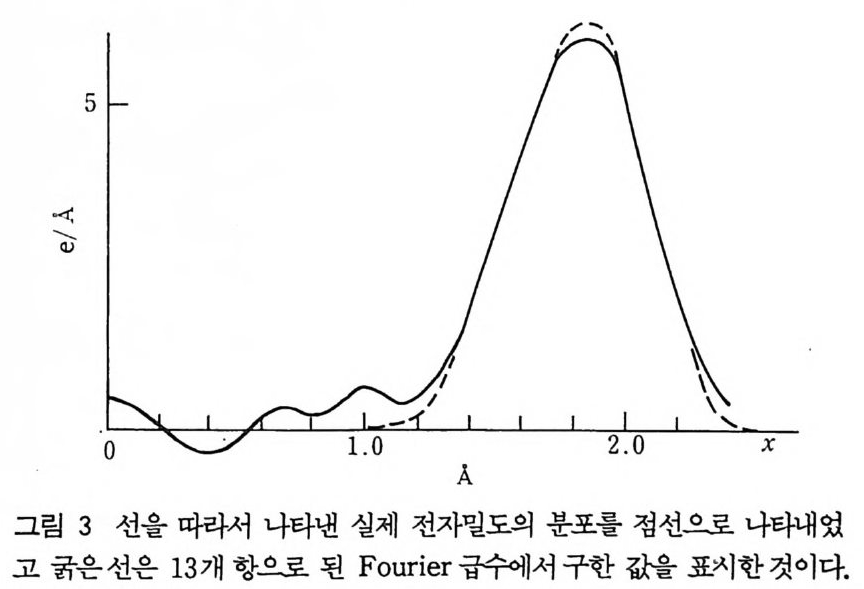 5
5
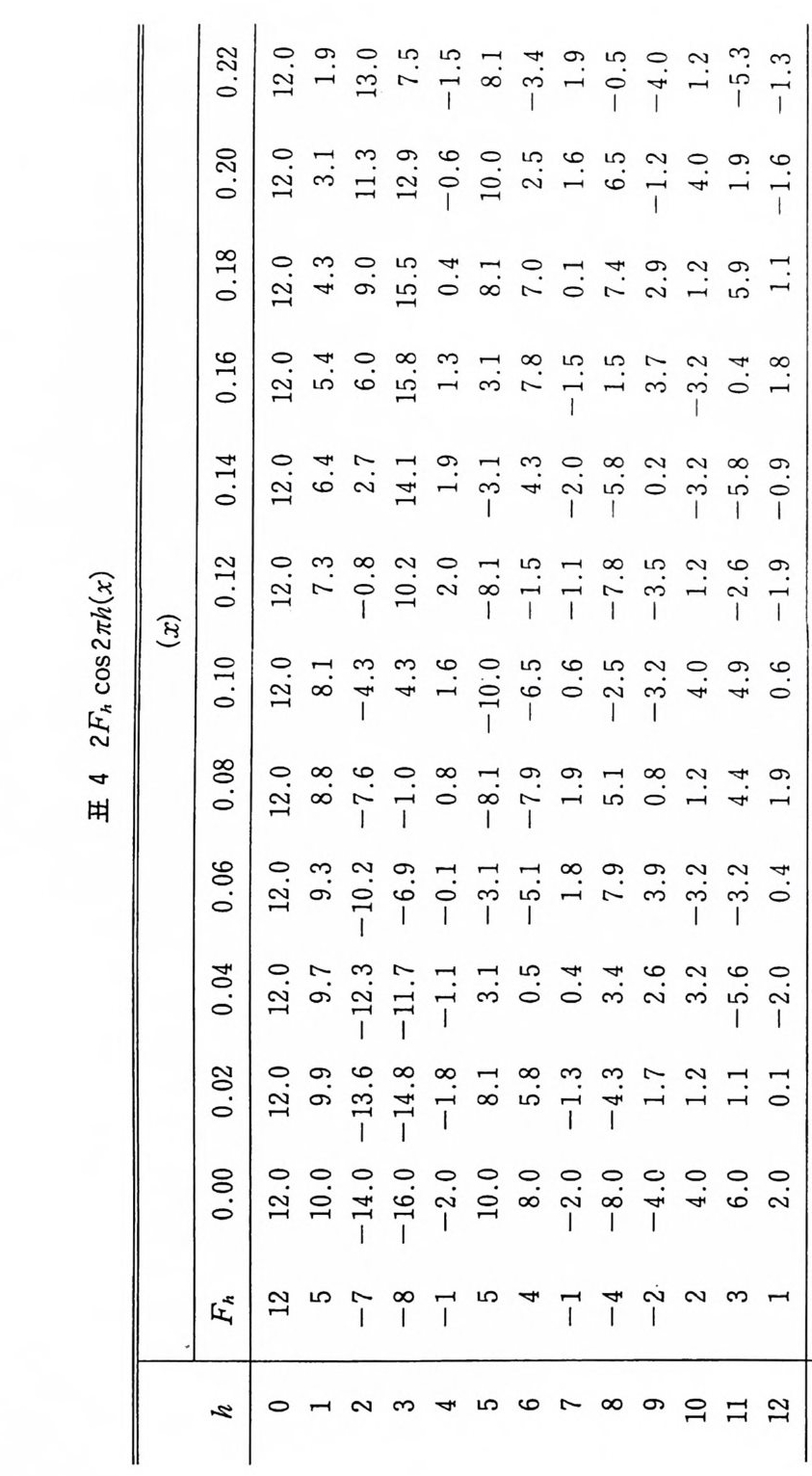 220. 2.1 0 9 1. 31 .07 .5 5 —1. .18 3 4.— 9 1. 0.- 5 -0 .42 1. 5-.3 3 1-. 3.0
220. 2.1 0 9 1. 31 .07 .5 5 —1. .18 3 4.— 9 1. 0.- 5 -0 .42 1. 5-.3 3 1-. 3.0
빔의 진동수가 흡수 진동수와 거의 같고 그 흡수끝에 관련되는 전 자에 의해 산란될 때 이상 위상변화 (anomalous ph ase chan g e) 가 일어난다. 이 영향을 이상 산란 (anomalous scatt er in g ) 혹은 이상 분산 (anomalous d i s p ers i on) 이라 하고 산란 인자를 다음과 같이 복 소수 로표현하게 한다. f =I計 6./'+ i6./=/ '+ i6./ (7- 27 ) 여기서 fo 는 정상산란 인자이고 ^ f ' 는 실수로서의 수정항(보통 음수임)이고 스f'’는 허수 부분이다. 그림 4-(a) 는 원점에 원자가 있을때 비이상적으로 산란하 는 파에 대한 복소수 산란의 영향을 보 이고 있다. 그림 4-(b) 와 (c) 는 이상 산란체가 단위세포 주위에 움직임에 따라 위상각이 변하여도 f'와 Af 사이의 관계는 그대로 변하지 않고 있음을 보여주고 있다.
 < — If ' 一|D>A`. f'f ' I- · -8 f;; Aj
< — If ' 一|D>A`. f'f ' I- · -8 f;; Aj
표 5 를 보면 산란효과의 크기를 알 수 있다. 여기서 주어진 원 자와 X- 선에서 스/'와 6/ 의 값을 보여주고있다. X- 선 복사선 의 파장이 크면 이 효과의 크기도 커짐을 알 수 있다. 그림 5 에서 Cu Ka 복사선을 샤용할 때 구리 (Cu) 부근의 원자에 대해 스/'와 6/' 의 변화를 보여주고 있다.
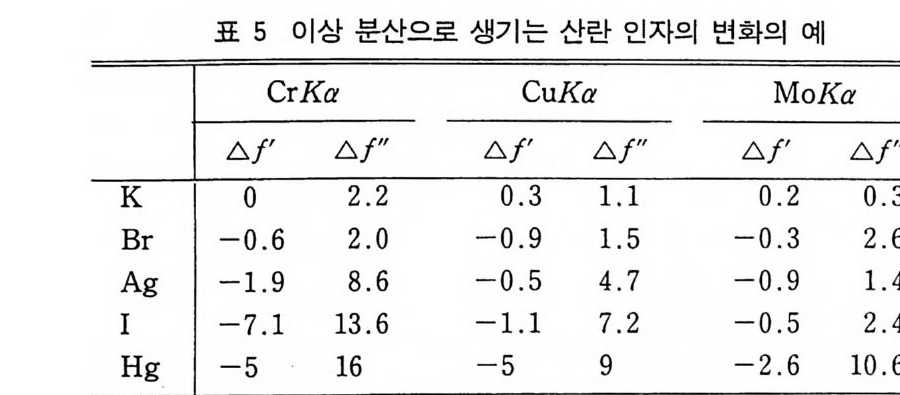 표 5 이상 분산으로 생기는 산란 인자의 번화의 예
표 5 이상 분산으로 생기는 산란 인자의 번화의 예
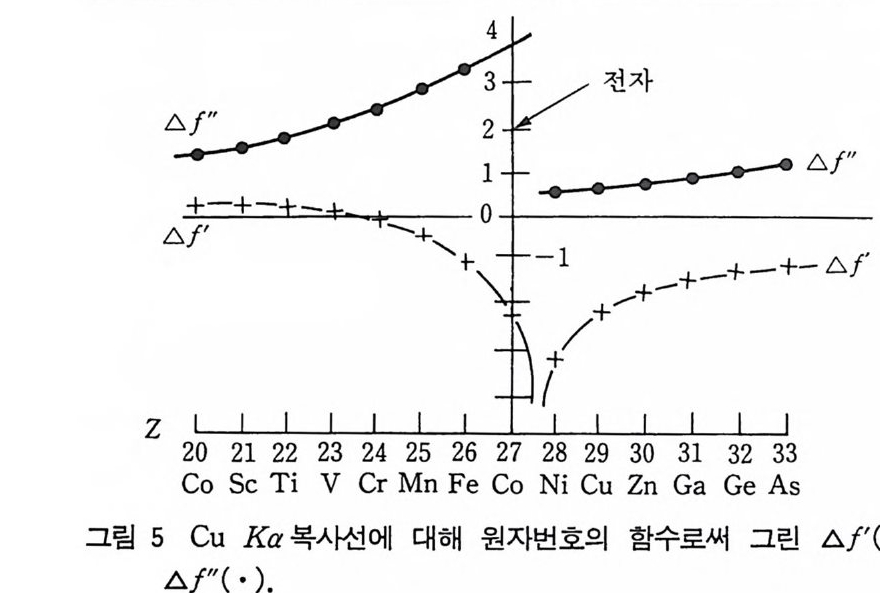 전자
전자
이상 산란에서 생기는 스f ' 와 스f의 수정항은 원자의 내부 전 지에 주로 영향을 받으므로 sin e 와는 거의 무관하다. 그러나 주어 전 원자에 대해 산란효과는 낮은 sin e 값보다 높은 sin e 에서 비 교적 크다. 따라서 sin 0/tl= O에 서 (6/collco) cuxa= 3 . 6/24 . s 이고 sin 0/A=0 . 6 에서 이 비율은 3.6/7.8 로서 약 3 배가 커진다. 그립 6 은 sin 0/A 의 함수로서 fc o+ 스f&=fC o 와 fCo , 스危값을 나타내 고있다.
9 Patt er son 함수 측정한 적분 강도에서 전자밀도를 바로 얻을 수 없으므로 강도 F2 에서 Four i er 급수를 적용하여 어떤 유용한 정보를 얻을 수 있 는 가가 문제가 된다. A. L. Pa tt erson 은 구조결정에서 전자밀도 향만큼은 유용하지 않지만 큰 가치가 있는 다른 형의 함수를 고 안하여 이 문제에 해답을 주었다. 1 차원 결정에 대해 Pa tt erson 함수를 도입하는 것이 편리하다. Patt er son 함수는 다음과 같이 표현할 수 있다. P(X ) = l/ 기pa (x) p( x+X ) dx (7-28)
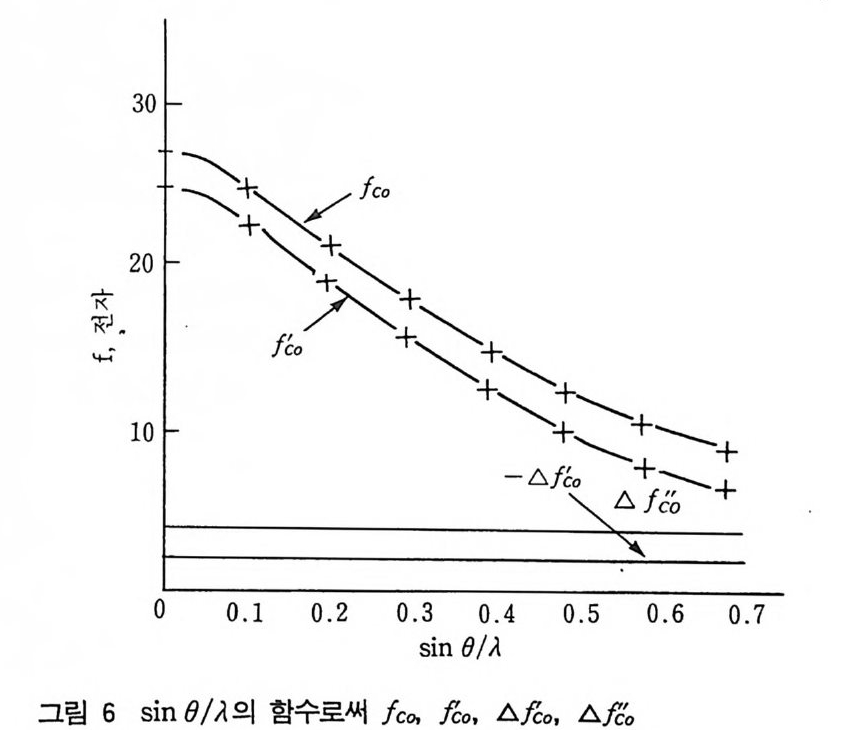 30
30
여기서 X 는 a 축에 따라서 측정한 x 의 값이다. 전자밀도에 대 한 (7-20) 식의 1 차원에서의 표현식을 (7-28) 식에 대입하면 다음 식을얻을수있다. P(X) = 1/a J!2 1;a 짝n Fnex p (-2TC i n(x/a)) 1/ a ~n’F ;,exp (-2TCi n '(x+X )/a ) dx =1/a 露 FnF.:ex p (-2TC i n'(X / a)) J! exp n n' (-2TCi (n +n')x dx (7-29) (7-29) 식의 적분값은 n= ―짜가 아닌 한 영이다. 11=_n' 일 때 그 적분값은 a 이다. 또 Fn,=F-n=F*n 이므로 (7-29) 식은 다음과 같이 간단히 표현할 수 있다. P(X) = 1/a2~F/exp( 2 TCi n( X/a)) n =l/a2~F/cos21rn(X/a)) (7-30) n 급수의 합은 _00 에서 +00 까지 취하므로 sin e 항은 서로 쌍으로 나타나서 제거할 수 있다. (7-30) 식의 Four i er 급수의 특칭은 실 험적으로 측정할 수 있는 구조인자의 진폭을 제곱하고 있다. 물리 적 의미를 알기 위해 그림 7 을 보자. 위의 두 그림은 p (x) 와 X =0.2 만큼 이동하여 그린 그림이다. 세번째 그림은 p( x)p ( x+O. 2) =P'(X=O. 2) 이다. Pat ter son 피크의 폭은 전자밀도 피크의 합과 같으므로 X=0.2 士 0.1 의 범위를 보여준다. 마지막 그림은 완전한 1 차원 Pat ter son 함수를 보여 준다. 제일 위쪽 그림은 비대칭적 1 차원 전자밀도는 PA, PB, Pc 의 밀 도를 가지는 세 개의 최대값을 가진다. 그 아래 그림은 X=0.2 만 선에 대해서는 성립하나 무거운 원자에 대해서는 옳지 않다. 입사
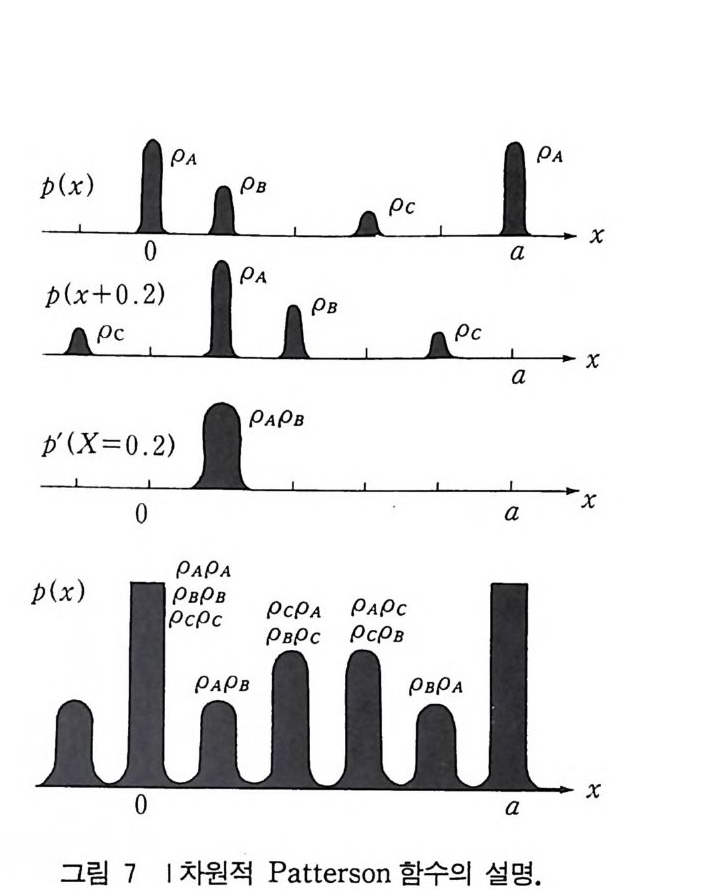 pp(九 PB Ia
pp(九 PB Ia
큼 위의 전자밀도를 이동한 것이다. 이것이 (7-28) 식의 p( x+X ) 의 의미이다. 이 두 함수의 곱이 a 축일 때 각각의 접 x 에서 이루 어지면 이 함수 중 하나이거나 두 함수 중 다론 하나가 x=x+ X=0. 2 가까이룰 제의하고 영이 된다. 따라서 P'(x)=p ( x)p ( x+ 0.2) 는 X=0.2 에서 하나의 최대값만 가지고 그 총밀도는 두 개의 겹치는 전자밀도 pA , p유] 곱과 같다. 이와 유사하게 X 를 0 과 1 사이의 모든 값을 허용하면 그림 7 의 맨 위쪽의 전자밀도에 분포 에서 피크 상호간의 거리에 해당하는 X 값마다 P(X) 의 피크가 생긴다. 원래의 함수가 세 개의 피크를 가지므로 Pat ter son 함수 는 3X3=9 개의 피크롤 가진다. 그 중 세 개는 원자가 그 자신 겹 침에 상당하고 (X=O) 따라서 그림 7 의 맨 아래 그림처럼 원점에
놓인다. 따라서 Patt er son 함수는 전자밀도 함수의 모든 원자간 거리마다 정확히 피크가 있다. Patt er son 함수를 체계적으로 해석 하여 이 피크를 알아낼 수 있다. 3 차원 Patt er son 함수는 다음과 같이 쓸 수 있다. P(XYZ) =1/ V2~ 후oo 합 Flk t cos27r(hX+kY+ !Z) h k l (7-31) 여기서 Fhkl= I Fhkil 2= Fhk 려?;; ;7 이고 X, Y, Z 는 a, b, c 축에 따라 나타낸 분율좌표로 다음과 같이 표시된다. X=x-x' ZY==zy —— zy' ' 여기서 점 x, y, z 와 점 x', y', z' 에 단위세포내 원자가 있는 분율좌표°]다. 흔히 Patt er son 함수의 두영을 다음 함수의 형으로 원한다. P(XY ) =쟈꾸 ~Fhk/cos 21r(hX+ kY) (7-32) 여기서 A 는 투영한 단위 세포의 면적이다. Patt er soi;i 함수를 구조 해석에 이용하는 방법을 예를 들어 설명하자. P2 공간군에 속하고 그림 8 과 갇이 단위세포내에 세 개의 원자 AI, BI, B2 를 가질 경우의 전자밀도의 투영을 생각해 보자. 전자밀도에서 Patt er son 함수를 어떻게 도식적으로 구하는가를 보여주기 위해 그립 8 에서 이웃하는 네 개의 단위세포를 보여주고 있다. Patt er son 지도 (ma p)는 공통되는 원점에서 그려 원자간의 벡터의 끝부분 위치에 피크롤 가지고 있다. P(X Y)에서 최대값을 알아내는 방법은 전자밀도상의 각각 원자의 위치에 단위세포의 원
고내한점다었을 .다최 .계종그 속 림전P적 a자8으t t밀 의e 로r 도s 삼 o놓피n각아 크지형보의도의고 는 얼 열 단마그에위는림 세대 어해포10떤 내 과이 의곳 러 같에다한다서. 른결 는 이과원 한 를자그 의번그립 림에위이 서치상9 를에 나각 나주각타의목타나
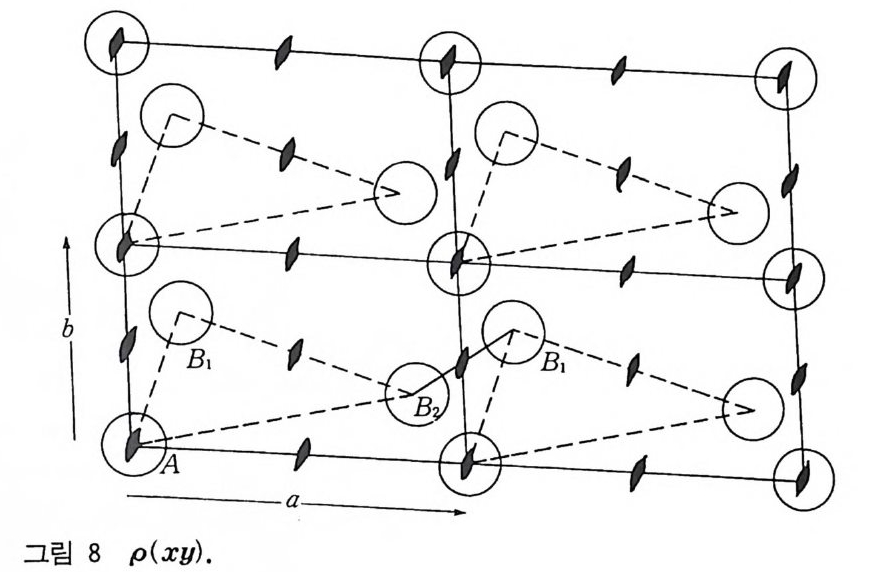 \b ----,_------- ```1-`-``-
\b ----,_------- ```1-`-``-
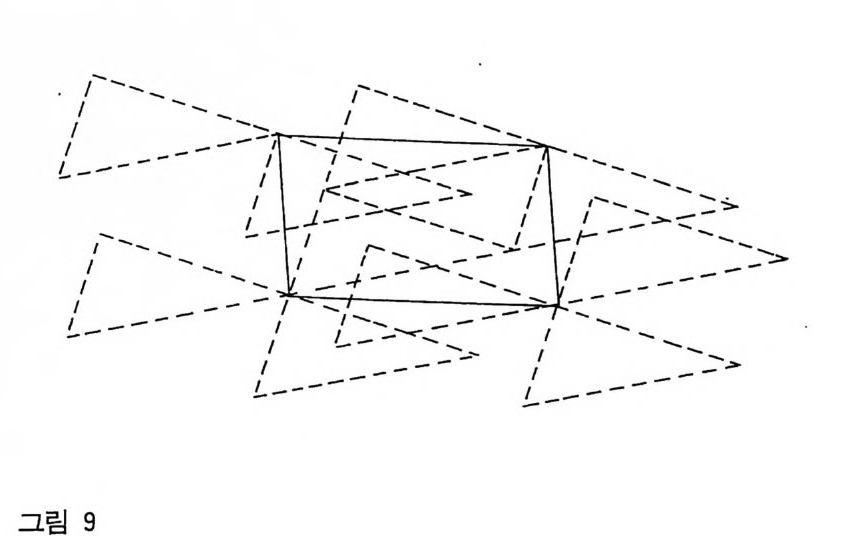 LI ll -,-------- - - - ---ll- ’ \, ' l, I- 'Il/ /,lV-- l-- l---{---4L`V-`/- l` l-- l -Al-{ - -l ---l l- -
LI ll -,-------- - - - ---ll- ’ \, ' l, I- 'Il/ /,lV-- l-- l---{---4L`V-`/- l` l-- l -Al-{ - -l ---l l- -
원형의 등고선은 그 위치에서 중복되어 나타난 전자밀도 피크의 수 이다. 이제 단독 피크, 이중 피크 및 심증 피크로써 Patt er son 피 크롤 구별할 수 있다. 전자밀도에 N 개의 피크가 있으면 원점에 N 개 피크가 중복되어 나타나고 세포내의 다른 위치에 N2-N 개 의 피크가 분포한다. 이것이 실제 Patt er son 법의 큰 결점이다. 더욱이 Patt er son 함수의 각각 피크의 부피의 크기는 해당되는 쌍 의 전자밀도의 부피의 곱에 비례한다. 원자번호가 Z1, Z2 인 두 원 자가 단위세포에 있으면 이 두 원자에 상당하는 벡터 지도상의 피 크의 부피는 Z1 • Z2 전자수를 가전다. Patt er son 함수는 중심 대칭 형이라 벡터 지도상의 모든 점은 대칭 중심에 의해 비슷한 다른 점 과관계가지어진다. 무거운 원자를 가지는 결정에 대해 Patt er son 합성을 계산하면 벡터 지도상의 최대점은 무거운 원자와 무거운 원자의 벡터를 나타 내고 이것은 다른 피크보다 훨씬 크다. 다른 큰 피크가 작은 피크 와 중첩함에 따라 나타낼 수 있다. 예컨대 공간군 PI 를 생각하고 단위 세포당 2 개의 비대칭 단위 가 있고 이것의 대등위치의 좌표가 x, y, z ; 굿, y, 芝이고 각
 ·b
·b
대등 위치에 무거운 원자가 위치한다면 벡터 지도에서 최대점의 좌 표는 무거운 원자 사이의 벡터가 될 것이고 이것은 (x, y, z)— (굿, y, z)=2x, 2y, 2z 일 것이다. 그러면 X=2x, Y=2y, Z=2z 가 되고 단위 세포내에 무거운 원자의 좌표는 Patt er son 지 도에서 큰 피크의 좌표의 각각 1 /2 일 것이다. 그림 11 에는 이러한 단위세포와 이 단위세포에 대응하는 벡터 공간을 보여주고 렀다.
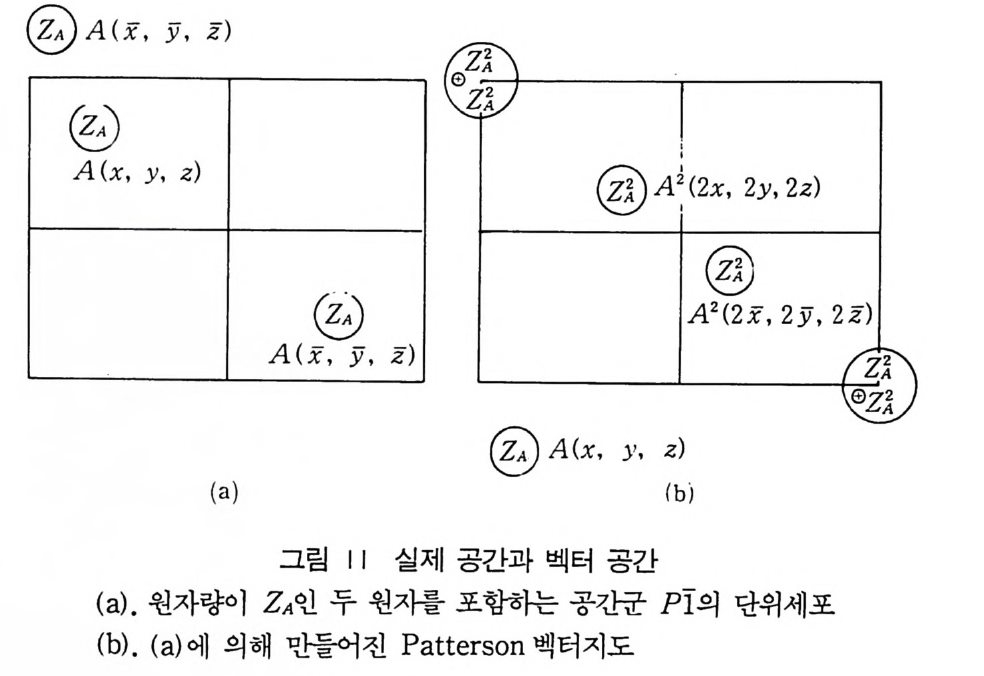 @A( 굿, Y, z)
@A( 굿, Y, z)
10 Harker 선과 면 결정이 대칭축이나 대칭평면을 가지면 단위세포의 벡터 표시에 서 어떤 평면이나 선은 단위세포내 원자의 좌표를 결정하는 중요한 정보를 포함하고 있다. 예컨대 (1) 단위세포가 단위세포의 b 축에 평행하여 2 회 회전축을 가지 면 x, Y, z 에 위치하는 원자에 대해 료 y, z 위치에 대칭과 관련
있는 원자가 있다. 그러면 벡터 지도에서 최대가 X=Z x, Y=O, Z=2z( 죽 두 조의 좌표의 차이에 상당함)에 나타난다. Y = O 에서 b 축에 수직되게 취한 벡터 공간면은 모두 이러한 최대를 포함한다. 단위세포내 원자의 x 와 z 의 위치는 최대의 좌표에 2 로 나누어서 간단히 얻을수있다. (2) b 축에 평행하게 2 회 나선축이 있으면 대등 원소는 x, y, z 와 瓦 y+ l/2, 芝에 있다. 이에 대응하는 벡터는 벡터 공간 X= 2x, Y=l/2, Z=2z 에 있다. 나선축에의 원자의 벡터 거리는 이 러한 면에서 찾을 수 있다. 이 피크에서 x, z 좌표를 정할 수 있 다. 하나의 원자가 y 좌표 1 / 4 에 있으면 다른 원자는. y 좌표 3/4 에 있다. (3) 삼사정계로서 중심대칭 공간군 PI 에서는 대동점아 x, y, z 와 료 y, 芝에 원자가 있고 이에 대응하는 벡터는 X= 2 x , Y= 2y, Z=2z 에 있다. 따라서 대칭중심인 원점에 대해 원자의 위치 x, y, z 를 쉽게 찾을 수 있다. (4) b 축과 수직 방향에 c 미끄럼 평면이 있고 원자는 x, y, z 에 있으면 반드시 x, y, z+l / 2 에도 원자가 있다. 벡터 공간에서 최 대점은 X=O, Y=2y , Z=l/2 에 있다. 11 중원자법 Patt er son 함수를 그린 그림을 벡터 지도라고 부르고 Patt er - son 힘수는 단위세포의 모양과 크기로써 공간을 채운 3 차원 그리 드(gri d) 내의 각 점 x, y, z 로써 평가한다. 벡터 지도에는 위상에 대한 정보는 필요없다. 왜냐하면 | Fhk1l2 은 위상(p hase) 과는 무관 하기 때문이다. 3 차원 지도에서 개개 원자간 작용이 피크의 높이 에 기여하는 것은 벡터 한쪽변 원자 번호수 Z i 와 다른쪽 원자의 원자 번호수 (Z;) 의 곱 Z i Z제 비례한다. 무거운 원자의 위치는 Patt er son 지도를 해석하여 알아낼 수 있
다. 그림 12 는 비타민 B1 러 유도체로서 그 분자식이 C.sHs101.Ns C0Cl•C3Hs0·3H20 인 화합물이 Pa tt erson 투영이고 이 화합물은 공간군 P212121 에 속한다. Patt er son 지도에는 많은 다른 피크가 있지만 cobalt- c obalt 피크가 다른 어떤 것보다 무거워서 이것이 Patt er son 지도를 지배한다고 생각할 수 있다. 중원자법은 전 구 조 에 대한 각각의 회절 빔의 위상각이 무거운 원자의 위상에 의하 여 무거운 원자로써 결정된다고 생각한다. 비타민 B12 에는 cobalt 가 한 개, 염소 원자가 하나 있고 탄소, 질소, 산소 원자가 모두 약 7 0 여 개 있다. 전자밀도에 대한 근사로서 cobal t원자로써 위 상이 결정된다고 생각한다. Co, Cl, 0, N, C 와 H의 원자번호는 각각 27, 17, 8, 7, 6 과 1 이다. Patt er son 지도에서 기대되는 근 사적이고 상대적인 피크 높이는 다음과 같다. Co-Co : 27 X 27= 729 Co-Cl : 27X 17=459 Cl-Cl : 17X 17=289 Co-0 : 27X 8 =216 Co-C : 27X 6 = 162 0-0 : 8X 8 =64 H-H : lX l =1 따라서 Pa tt erson 지도는 Co- C o, Co-Cl 벡터에 의해 지배될 것 으로 기대된다. Patt er son 합성에서 중원자 피크의 좌표는 단위 세포내 대등 위치의 좌표를 서로 빼어 구할 수 있다. P2121 읽 공간 군에서 대등 위치는 다음과 같다. (1) x, y, z (2) 1/2-x, -y, z+1/2 (3) -x, y+ 1/2, 1/2— z (4) x+l/2, 1/2-y, -z
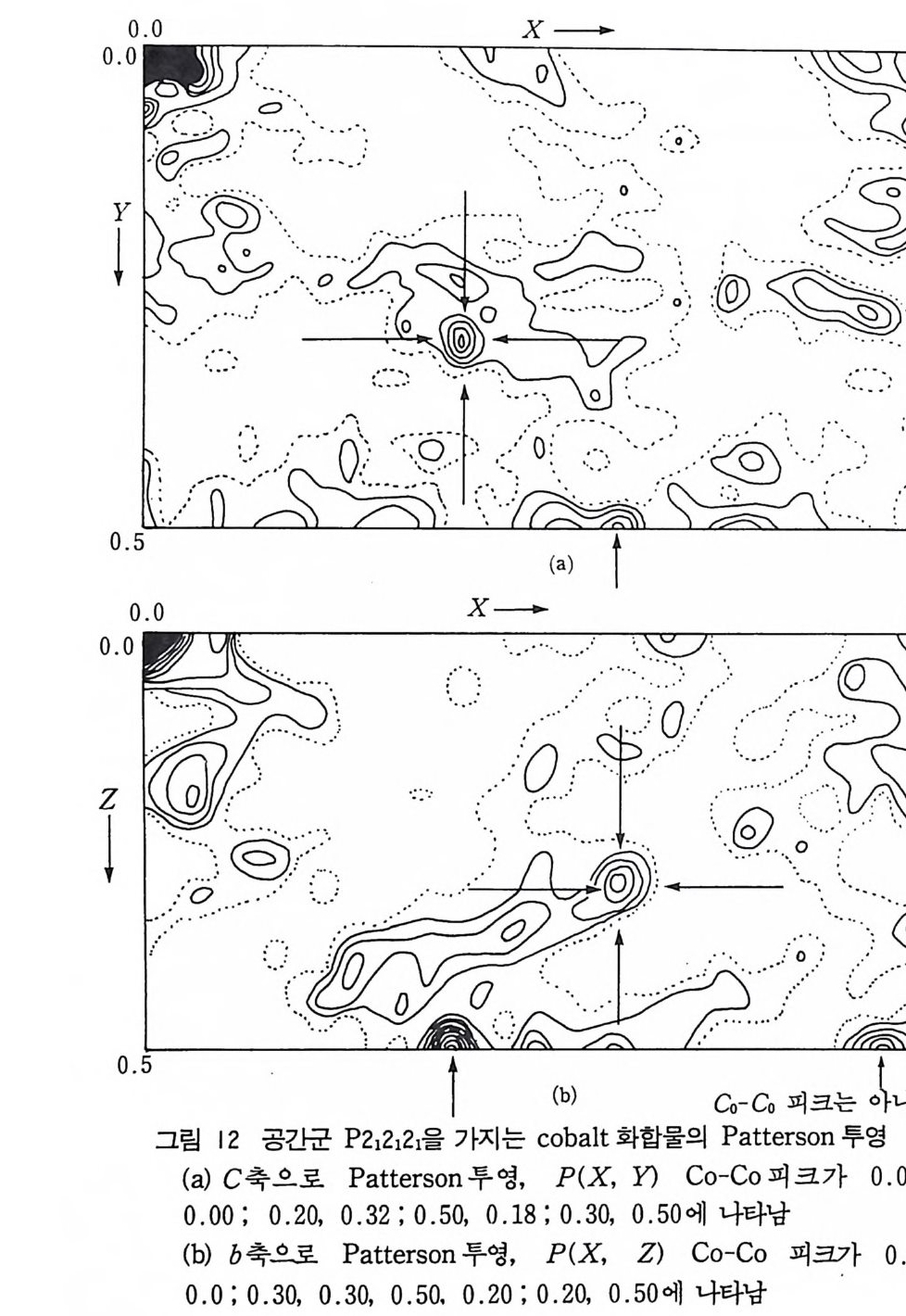 0.0 x-
0.0 x-
여러 위치의 좌표에서 차를 구하면 대칭에 관련되는 원자 사이의 원자간 벡터는 다음과 같이 구할 수 있다. XX= =Ol ,/ 2 —Y =2Ox, , YZ==O— 2(y위, 치Z 1 =에l서/2 위 (치위 치1 ) 2 에서 위치 1) X=-2x, Y=l/2 , Z=l/2 — 2 z (위치 3 에서 위치 1) X=l/2 , Y=l/2 -2y, Z=-2z (위치 4 에서 위치 1) 다른 위치 사이의 벡터, 예컨대 2 에서 3, 혹은 3 에서 4 는 위에 서 구한 벡터와 같거나 2 회 회전축이나 원점에서 대칭 중심 등에 의해 관련된다. 모든 Pa tt erson 지도는 중심 대칭형이다. 이 결정 에 대한 실제 Patt er son 지도는 다음 위치를 찾을 수 있다. X y z 。。 。 土 0.2 土 0.32 0.5 土 0.3 0.5 士 0.3 0.5 士 0.18 士 0.2 여기서부터 x=0.15, y= 0.16, z=0.10 에 Co 원자가 위치함을 알 수 있다. 중원자법의 결정은 중원자는 원자번호가 충분히 커서 벡터 분포를 지배해야 하고 또 X- 선 산란도 반드시 지배해야 한 다. 따라서 가벼운 원자는 측정 반사강도에 그 기여가 적기 때문에 어떤 정밀화법으로도 아주 정확히는 위치를 알아낼 수 없다. 따라 서 무거운 원자가 포함 안된 화합물에서는 직접법으로 그 구조를 알아내야한다. Patt er son 지도의 어려운 접은 N 개의 개개의 원자에 대해 단위 세포에서 N2 원자간 · 벡터 피크가 있고 이 피크 중 N 개는 원접에 놓이고 벡터 지도는 중심 대칭형이므로(벡터 BA 는 벡터 AB 와 서 로 반대 방향가] 같은 크기를 가지고 있는) 총 (N2;N) 의 독립적 피
크가 있다. 예컨대 N=20 이면 (20X19)/2=190 개의 피크가 있 다. 따라서 단백질과 같은 큰 분자를 갖는 결정에 대해서는 큰 원 자번호를 갖는 원자 사이의 작용으로 생기는 피크를 제의하고는 해 석할수없다. 1 2 직 접 법 (Di re ct Meth o d) 칙집법에서 반사 강도가 구조적 정보를 포함하고 있으면 실제 결 구정조의 에전서자는밀 도한는 원 음자수가는 x , 될Y ,수 z 없위다치는에 사있실으을면 이-용x한, 다 -.y ,중 —심z 대위 칭치 에 대등 원자가 존재한다. 원점에 대칭 중심이 있으면 각 구조인자는 그 위상이 0 혹은 180° 의 각도에 위상을 가전다. 그래서 cos = cosO=l 혹은 cos 180=-1 이고 sin =O 이다. |Flcos = F=+IF| 혹은 -IF I 이다 (6-32 식을 참조). 만약 어떤 구조에서 N 개의 반사가 관찰되었 다면 N 개의 독립적 구조인자의 부호를 감안하여 모든 관측 가능 한 조합을 하면 2N 개의 전자밀도를 계산할 수 있다. 따라서 2N 지 도 중 하나가 올바론 지도를 나타낸다. 따라서 어느 전자밀도가 올 바론가를 말하기는 어렵다. 20 개의 반사가 관찰되었다고 해도 일 백만 개 아상의 전자밀도 지도를 계산할 수 있다 (220=1,048'576). 더구나 대개 관심을 가지고 풀려고 하는 구조는 대개 1,000~10,000 개의 반사를 가진다. 구조 인자의 전폭이 큰 반사 는 올바른 구조에 상당하는 위상으로 계산하면 전자밀도 지도에 큰 영향을 주고 처음에는 매우 높은 전폭을 가전 항만 고려하여 근사 적인 지도를 구한다. 그러나 10 개 반사만 가져도 가능한 지도의 수는 1,024 개이고 시행오차범으로 계산하기에는 너무 많은 수이 다. 비대칭구조에서는 위상각은 oo~360° 사이의 어느 각이고 10 개의 반사에 대해서 올바르게 가지는 지도만 해도 무한히 많이 계
산해야한다. 그러나 다행하게도 여러 가지 반사의 위상 사이의 관계를 구할 수 있다. 이 관계는 전자밀도는 결코 음일 수 없다는 사실에서 얻 을 수 있고 또 원자가 있는 위치에서 대략 구형인 피크를 제의하고 는 전자밀도는 영에 가깝다는 사실에 기인한다. x- 선 회절패턴의 강도는 위상이 전자밀도가 +값이 되는 값을 가지므로 위상에 대한 정보를 가지고 있다. 중심 대칭구조에서 위상각이 o· 이거나 180° 이 므로 cos =土 l 이고 sin <1> = 0 이므로 구조 인자의 부호를 말할 수 있다• 이 항은 전자밀도가 | F I cos 와 | F I sin 의 항을 가 지고 있고 이 경우 |Fl 와 - |F| 울 가전다. 이러한 관계는 구조 인자와 부호 사이에서 찾을 수 있다. 임의의 반사에 대한 상대적인 위상의 관계는 그림 13 에 설명하 고 있다. 중심 대칭구조를 가지는 결정에서 F1oo7l- 크 다고 생각하 자. F10 가 +부호(상의 각도 o ·) 이면 이 반사를 사용하여 계산한 전자밀도 지도는 X=O 에서 피크가 나타나고 X=l/2 에서 구멍 (hole) 이 있다. 그러나 F1oo7l- 음 의 부호를 가지면 피크는 X= l/2 에 있고 구멍은 X= O에 있다. 이 반사가 강하다는 사실은 F1oo7l- 부호가 어떠하든지간에 전자밀도 지도에서 피크는 X=O 이나 X= 1/2 에 있어야 한다. F200 을 생각해보면 0 이나 1/2 에 피크가 있음 은 F20u i= F10 려 부호에는 관계없이 +부호를 가짐을 암시한다. 따라서 F10o7l- 강 하면 F2ou i= F10 려 부호에는 관계없이 +이다. 전자밀도는 항상 양이라는 원리는 3 차원으로 확장시킬 수 있다. 다음식이 널리 사용된다. s(hi. k1, /1)S(h2, k2, /0 ::::: s(h 급 -h2, k1+k2, f1+ 10 (7-33) 여기서 S 는 부호 (s ign)를 뜻하고 (hi. k1, /1), (h2, k2, !0 와 (h1+ h2, k1+ k2, l1+ lJ 는 모두 강도가 큰 반사이다. 위의 관계식
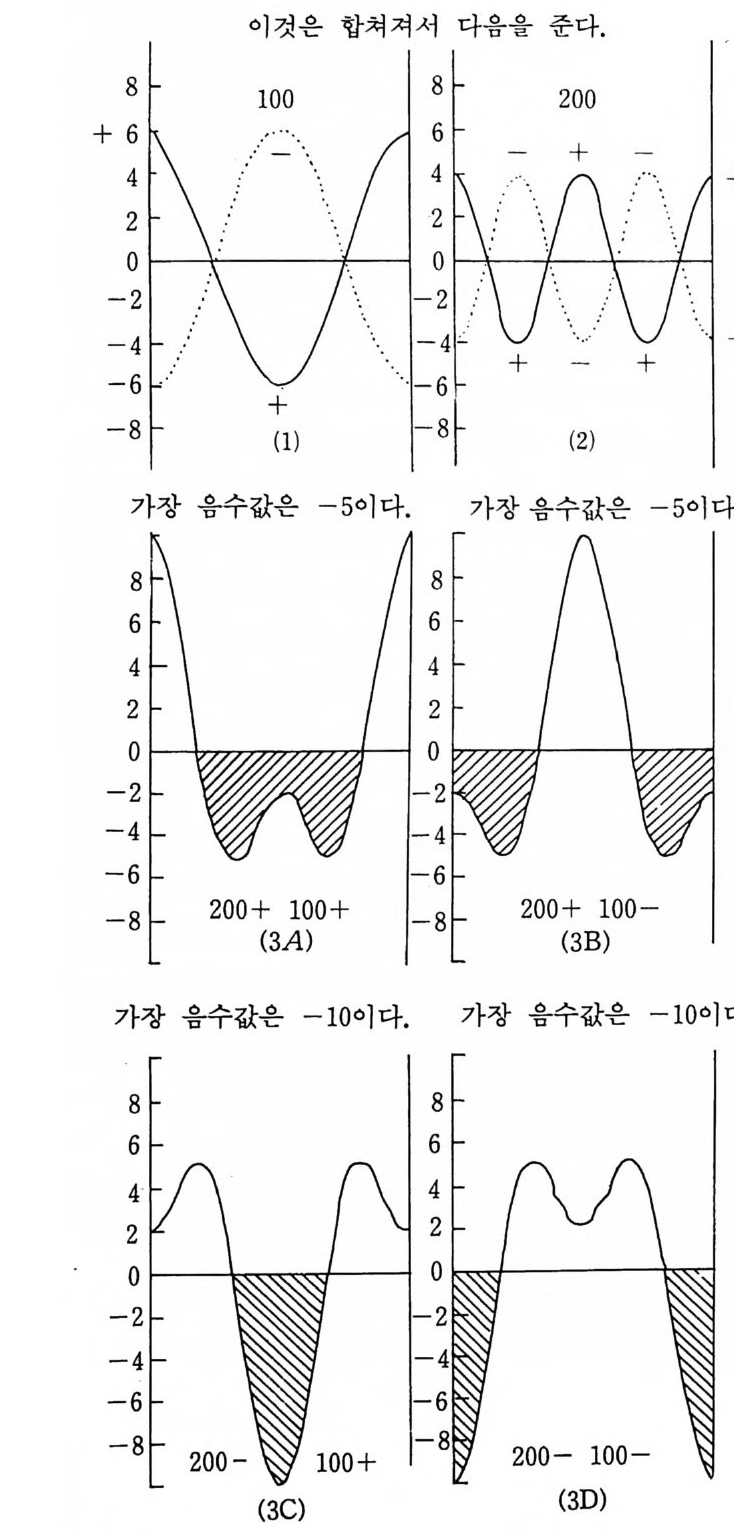 이 것 은 합쳐 져서 다음 을 준다.
이 것 은 합쳐 져서 다음 을 준다.
그림 |3 해석적 방법으로 부호 결정 중심 대칭형 구조에서 구조 인자 (Fhkl) 의 위상각은 o· 이거나 180° 이다. 하나의 구조 인자를 기초로 한 전자밀도 지도를(밀도파) F10 라 F200 에 대해 보여주고 있다. 일반적으로 중심대칭형 구조에 서 Fhkl 이 크면 그 부호가 어떠하든간에 F2h2k2[ 도 크면 F2h2k2 려 부호는 양 (o · 의 각도)일 가능성이 크다. (1) F100 에 대한 가능한 경우 ; 굵은 선 _F 는 양이고 위상은 o· 이 다 ; 점선 …··· F 는 음이고 위상은 180° 이다. (2) F200 에 대한 가능한 경우 ; 굵은 선에서 F 는 양이고 위상은 o· 이 다. 점선은 F 는 음이고 위상은 180° 이다. (3) (1)과 (2) 의 파를 조합하여 합천 네 가지 경우에는 F200 의 위상이 l80 ° 이면, 죽 F 가 음일 경우 F10 려- 파를 합치면 큰 음의 값을 얻 는다 (C, D). 전자밀도의 음의 면적에 빗금을 쳤음. 이 전자밀도 지도에서 원자의 위치 (X) 는 다음과 갇이 생각해낼 수 있다. 3A 에서 X= O, 3B 에서 X= l/2, 3 C, 3D 에서 X= l/4 과 3/4 이 다. 그러나 마지막 두 그립은 음의 값을 가전 골이 깊어서 제의시 킨다. 따라서 F2 。志- 양이고 X=O 이거나 1/2 이다. 은는 정~확을 한 써 식서이 표라시고하 였하다기.보 다위는의 통식계의 적특인별 한확률 경이우고로 서따 라서 =보다 s(2h00) ~[ s(hOO) 〕 2~ 十 (7-34) 인 관계식이 우리가 검토한 해석적인 해석과 찰 일치한다. 실제로는 위상을 결정하는 해석적 방법은 규격화한 구조 인자, 죽 산란각 2 0 가 커침에 따라 개개의 산란 인자 f가 떨어지는 것 울 보정한 구조 인자 F 의 값에 대해 시행한다. 규격화한 구조 인 자 E 는 구조 인자 F 와 〔 2 f』 1/2의 비율이다*. 여기서 합은 단위세포내의 모든 원자에 걸쳐 합한다. 총괄적인 진동 인자 (overall vibr ati on fac t or) 와 반사의 (hkl) 값에 적절한 sin 0/A 값도 고려한다. 죽
2f i= 고 (fi°) exp (一 2 B s i n 내 /A 아 이 합은 구조가 같은 종류의 원자로 무작위하게 되어 있다면 sin 0/A 값에서 모든 | F l2 의 측정한 근자승 평균값 (roo t -mean squ are value) 을 나타낸다. 이러한 F 값의 사용은 각 원자가 점으로 된 원 자(p o i n t a t om) 라고 생긱하는 것과 같다. 화합물의 회철패턴에서 E 값 (E 값의 분포)을 해석하면 F 값의 경 우와 같이 구조가 중심 대칭형인가 아닌가를 알 수 있다. 예컨대 E 의 평균값이 중심 대칭구조에서는 0.798 이고 중심 대칭구조가 아니면 0 . 886 이다. IFI 값에 표가 준비되면 보통 E 값을 크기가 감소하는 순서로 정렬시키고 가장 강한 10% 정도를 가지고 작업한다. (7-33) 식에 표시한 것과 같이 이를 지수가 (7-33) 식에 의해 서로 관계되는 세 개의 반사군을 정한 후 3 자간의 곱, 즉 [E (h, k, !), E(h', k', l'), E(h+h', k.+ k ', l+l')] 을 컴퓨터를 사용하여 계산한다. 세 개의 곱에서 세 개의 반사의 각각은 높은 E 값을 가지므로 이들 부 호 (s ign)의 곱은 양일 것이다. 이러한 목록을 2 홉-라고 부른다. 확률식에서 합이 사용되므로 2 라는 말이 사용된다• 각각 씽울 이 룬 E(hkl) 과 E(2h , 2k, 2l) 의 부호는 중심 대칭구조에서는 양일 것이다. 이들 부호 사이의 관계에 확률을 생각하는 것이 중요하다. Sa yr e 의 방정식에서 다음의 3 자간의 곱이 양일 확률을 다음과 같이 얻을수있다. P+= 1/2+1/2 t anh(N 당| E 硏, £h',k',1', Eh-h',k-k', 1-1'1 ) = 1/2+ 1/2 ta nh(N-1'21 EHEKEH-xl ) (7-36) 여기서 N 은 단위세포내에 있는 원자수이고 H=h , k, l 이고 K= h', k', l’ 이다.
이러한 함수의 형은 다음과 같다. f(x ) = l/2+ 1/2 tan h x 이 함수의 그립은 그립 14 와 같다.
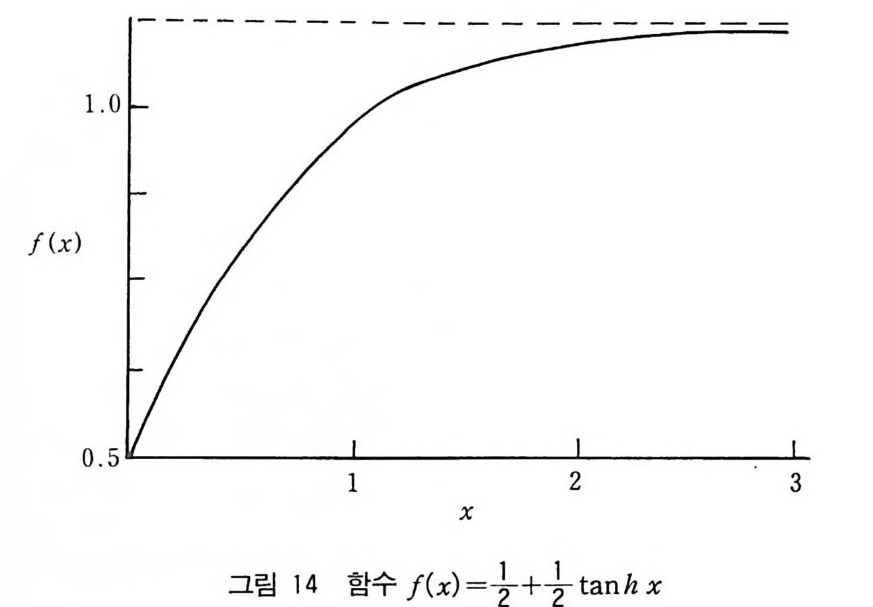 1.0
1.0
tan h x= (ex-e- 하 /(ex+ e- 히 H=(h, k, l), K=(h', k', l '), 그리고 H+K=(h+h', k+ k', l+ l') 이다. E(hkl) 이 양일 확률은 다음과 같다. P+= 1/2+ 1/2 tan h(N-1'2 1 E 까 ~EKEn-KI ) (7-37) 여기서 합은 K= (h', k', l ') 의 모든 값에 대해 행한다. 이 함수는 N=50 이고 |EHEKEH-K1=8 이면 x=8/Js o=l.13
이다. 그리고 부호의 곱이 양일 확률은 그림 14 에서 보면 90% 이 다. 이제 직접법 (dire ct me t hod) 에 의하여 중심 대칭형 구조를 결정 하는 방법울 예를 들어 설명하겠다. 3 개 곱(t r ip le produc t s) 을 나 타낸 목록이 준비되고 중심 대칭형 구조에 대한 이들 부호를 구하 려면 처음 몇 개의 부호를 선택해야 한다. 처음에 3 차원에서 많은 중심 대칭형 공간군에 대해 3 개의 반사의 부호를 선택한다. 이러 한 선택은 몇 개의 대등 위치 중 어느 것을 단위세포의 원점으로 사용해야 하는가를 결정한다. 이러한 선택은 구조를 바꾸지는 않는 다. 3 개의 원점을 정하는 반사 (or igi n- fi x i n g re fl ec ti on) 에 대해 임 의적인 부호를 부여한다(이 세 개는 3 자 곱은 아니어야 한다). 이 세 개는 개개 지수의 짝수 혹은 홀수에 대해서는 서로 달라야 한다. h, k, l 은 모두 짝수가 되지 않아야 한다. 예컨대 원점을 고정하 는 반사로서 임의로 세 개를 선택하자. 죽 F(3 3 1) (홀수 홀수 훌 수) F(9 6 7) (홀수 짝수 홀수)와 F(13 1 4) (홀수 홀수 짝수)에 대 해 먼저 임의적으로 부호를 선택한다 (Fhk 을 편의상 F(hkl) 로 표시 하여 나타내었다). 지금 구조 인자에 관한 일반식에서 중심 대칭구조에 적용할 수 있는 식을 유도해 보자. 그러면 F(hkl) = ~fjex p 21 Ci (h xj+ ky j+ lzj) =A'(hkl) + iB '(hkl) (7-38) 여기서 A'(hkl) = ~fjco s 21C(hxj+ ky j+ lzj) 그리고 B'(hkl) =~fjsin 2 1C(hxj+ kyj + lzj) 단위세포당 N 개의 원자를 갖는 중심 대칭구조에서 원점의 좌표 롤 단위세포의 대칭 중심으로 잡으면 대칭 중심에 원자가 있다고 생각하면 단위세포당 N/2 원자가 각각 대칭적으로 놓일 것이다.
죽 Xj , yJ, zJ 에 있는 원자는 祐 5 검j에 있는 원자와 중심 대칭 으로 놓일 것이다. 그러면 A'(hkl) =2 f』 cos 2n(hxj+ kyj + lzj) +cos 2n(-hxj- ky j-l zj)] = 22 :hc os 2n(hxj+ ky j+ lzj) B'(hkl) =2:/』 s i n 2n(hxj+ ky j+ lzj) +sin 2n(-hxj- ky j-lZ j) ] (7-39) 그러면 공간군 P2,/c 에 속하는 화합물 2-keto -3-eth o xy -bu ty raldeh y de-b i s( t h i osem ic arbazone) 에 대해 생각하자. 이 공 간군은 중심 대칭형 공간군이고 Inte r nati on al Tablesf or X-ray Cr yst a l log ra ph y , Vo l. 1 에서 일반적인 대등 위치는 다음과 같음을 요약할수있다. 土 {x, y, z ; x, 1/2— Y , l/2+z} 따라서 일반적인 대등 위치에 관한 좌표를 구조 인자 식에 대입 하면 다음식을얻는다. B(hkl) =O A(hkl) =2{cos21r(hx+ky + lz) +cos21r(hx 一 ky + lz+ 강 (k+ l) } (7-40) = 4cos 21r (hx+ lz+41 (k+ l) ) cos 21r (ky - 41 (k+ l) ) k+l=2n 이면 A(hkl) = 4cos21r(hx+lz)cos21rky (7-41) k+l=2n+l 이면 A(hkl) =-4sin 2 1r(hx+ lz)sin 2 ;r ky (7-42)
따라서 디음 관계 식을 얻을 수 있다. | F(hkl) 1= I F( EET) |= | F(l1EI) |= | F( Ek T) | (7-43) 또 부호에 대해서는 다음 두 가지 가능성이 있다. k+l=2n 이면 s(hkl) = s(hkl) = s(hkl) = s(hkT ) (7-44) k+l=2n+l 이면 s(hkl) = sUi k T )=- s(hkl) = -s ( hk T) (7- 45 ) 그리고 (7-33) 식에서 s(h+h', k+k'. l+l') ~s(/i, k, l)s (h', k', l') (7-46) h k l E 원점을 고정하기 위해 임의로 부호를 §3 63 17 33..7245++ ] 선(택이들한 다부.호 중 하나나 뗀 것울 -로 표시 13 1 4 2.92+ 하면 원점이 다르게 표시됨) h k l E 사용한관계 계부산호한 참고 12 0 0 4 . 35 ( 6 0 0 ) ( 6 0 0 ) + ( + ) ( + ) = ( — ) —2—252 6 ((132301o))((12 35 1144)) ++? (- ) =+++++ ==++ 6 010444258 302429 2228 6 a 아칙 결정하지 못 한부호를우선 a 로표시한다. 18 4 2 2 . 92 (12 0 0 ) ( 6 4 2 ) a + a= a
9 7 3 2.07 (331)(642) a +a=a 2 홍 6 1 2.30 (TTI 4)(97 3) -a -(+a)=-a 19 3 2 2.84 (3 3 1) (苑 6 1) —a +(-a) =-a (詩 14) (6 42) —( +a)=-a 7 3 2 2.1 4 (120 0) (19 3 2) 一 a +(— a)=— a 25 1 。 2.03 (18 4 2 ) ( 7 3 ? ) —a a(— a )=- ( 6 4 2 ) ( 19 3 2 ) a(-a)=— 결국 다른 반사의 부호도 a 로써 표시할 수 있다. a 의 부호는 아마 +일 것이다. E 거도의 계산에서 어떤 반사는 ―부호를 가져야 한다. 모든 부 호가 +이면 원접에 큰 피크롤 가지며 복잡한 구조에서는 이러한 경우가 드물다. E_ 지도에서 모든 부호가 양이면 Pa tt erson 함수 와유사하게 된다. 위와 같이 세 개의 곱의 목록에서 시작하여 여러 가지 E 에 대 해 그 부호를 이해할 수 있게 결정할 수 있다. 어려운 문제가 생기 면 디론 한 조의 원점을 고정하는 반사를 선택해야 한다. 위의 예 와 같이 반사의 부호를 결정해야 한다. 이러한 조작을 기호 붙이기 (sym bolic addit ion ) 라고 한다. 나중에는 더 약한 반사에 대한 세 개의 곱도 포함시켜 부호를 결정한다. 전술한 예와 같이 a, b 와 같은 부호를 할당함으로써 비합리적인 것을 최소로 할 수 있다. 이 러한 방법으로 강도가 강한 반사의 대부분의 부호(예컨대 |El> 1. 5) 는 별 어려움 없이 보통 결정할 수 있다. 마지막 단계에서는 전자밀도를 F 값에서가 아니고 E 값에서 계 산한 전자밀도 지도인 E 지도를 계산한다(이렇게 하면 원자는 점원 자〔p o i n t a t om) 로 되어 원자의 위치는 예리하여 나타난다). 모든 것이 잘 되면 구조는 이 지도에서 분명히 알 수 있을 것이다. 때때로 구 조의 일부분만 이러한 해석 방법으로 알 수 있다. 이 때에는 연속
적인 전자밀도 지도나 전자밀도의 차의 지도 (d iff erence electr o n dens ity ma p)에서 그 나머지는 알 수 있다. 어떤 경우예는 분자의 일반적 배치나 연결은 알아낼 수 있으나 단위세포내 위치는 부분집 합 중 얼마의 부호가 틀려서 옳지 않는 경우가 있다. 이러한 문제 는 원자간 거리를 계산해 보면 결합 안되는 원자 사이의 거리가 불 합리하게 너무 가깝게 되어 쉽게 알 수 있다. 이런 경우 부호를 다 시 붙여서 원점을 정하는 반사 (or igi n fixi n g re fl ec ti on) 를 다시 선 택하여 계산울 앞에서와 같이 다시 반복해야 한다. 중심 대칭이 아닌 결정구조에서는 위상각의 근사적 값을 알아내 기 위해 다음 식이 사용된다. (/)H~< (/ )H-K+( /)K> K (7-47) 여기서 H=h , k, l, K=h', k', l’ 이고 O 는 구조 인자의 위상 각이고 괄호 <〉 는 K 의 모든 값에 대해 평균값을 의미한다. 또 여 기서 H=( K) +(H-K) 이다. 디음의 t an g en t식을 사용하여 중 심 대칭형이 아닌 구조의 위상을 계산하고 정밀화시키는 데 널리 사용된다. t an fP H 척| Exl I EH-Kl sin ( fP K + {T)H -K) 간/〈 I E 찌 | EH-Kl cos( 仇計 0H_K) >K (7-48) 중심 대칭이 아닌 구조의 확률 함수는 다음과 같다. P( {T)미 =ex p曰 x cos({T )y-fPK -” 띠 /rr exp (4x cosy ) dr (7-49) 여기서 x=7 넛 |EHEKEH-K| 이고 r 는 변수를 표시한다. 중심 대칭구조와 비중심 대칭구조의 직접법은 고속 컴퓨터에 사용할 수 있도록 프로그래밍되어 있다. 직접법에 사용하는 식은 정확한 관계
식보다는 확률에 대한 식이고 원점으로 정하는· 반사와 부호를 할당 한 위상이 디수의 강도가 큰 반사의 위상을 결정하는 데 만족스럽 도록 초기단계에 주의를 하고 그후 더 많은 반사의 상을 결정하면 직접법을 서용하는 것은 아주 성공적이다. 많은 구조에서 관측한 반사의 단지 5~10% 의 반사만을 사용하여 계산한 E- 지도에서 근 사적이나 올바른 구조를 알아낼 수 있다. 일반적으로 직접법으로 정밀화시킬 수 있는 구조를 얻을 수 있 다. 그러나 직접법에는 여러 가지 문제가 생길 수 있다. 죽 부정확 하게 계산한 E 값을 사용하거나 원점을 정하는- 반사룰 잘못 선택 하였거나 반사의 세 개의 곱을 너무 적게 선택하였거나 어떤 부호 는 원하는 것보다 낮은 확률을 가지거나 계산한 부호에서 너무 양 수가 많아서 원점에 중원자가 없는데도 원점이 큰 피크가 있거나 한다. 이러한 문제는 경험과 주의를 기울여서 시행하여 극복할 수 있다. 직접법으로 구조를 해석하는 단계를 요약하면 다음과 같다. (I) E 값이 그 크기가 감소하는 순서로 목록을 만들고 가장 큰 10% 정도로써 작업을 한다. (2) £값의 통계적 분포를 해석하여 구조가 중심 대칭형인가 비 중심 대칭형인가를 결정한다. 이 방법은 반사의 계통적 소멸에서 공간군을 결정하는 것이 특히 중요하다. (3) 가장 높은 E 값 사이의 세 개의 곱을 구하고, (4) 원점을 정하는 반사를 선택하고, (5) 세 개의 곱과 확률 식을 써서 되도록이면 많은 E 값의 위상 이나부호를결정하다. (6) E- 지도를 계산하고 지도의 피크에서 구조를 결정한다. 이러한 모든 단계는 컴퓨터 프로그래밍을 써서 시행할 수 있다.
13 동형 치 환법 (iso morph ous rep la cement) 과 단백 질 구조 결정 한쌍의 동형 결정 혹은 일련의 동형 결정을 찾-0l-낼 수 있으면 해 석적 방법이 부적당한 복잡한 구조에 대해 위상각(p hase an g le) 을 결정하는 강력한 방법이다. 이 방법은 지금까지 결정한 대부분의 단백질 구조 해석의 기본이 된다. 동형 결정은 본질적으로 같은 세포 크기와 원자 배치 를 가지고 있고 단위 세포내에 존재하는 원자 하나 혹은 두 개만 다르다. 명 반은 일련의 동형 결정의 잘 알려진 예이다. Pota s h 명반 (KAI(S04) 2 ·12H20) 은 무색의 팔면체로 성장하지만 Chrome 명반 (KCr(SO 나 • 12H20) 은 Pota s h 명반과 같은 모양과 구조를 가진 전한 자주 빛 결정이다. Chrome 명반에서 Cr(II) 원자는 Pota s h 명반에서 Al(III) 원자와 같은 단위 세포내 위치를 차지한다. 실제 Pota sh 명 반 속에 Chrome 명반을 매달고 결정을 성장시키면 무색의 물질에 둘러싸인 검은 자주색 중심을 가진 팔면체 결정이 된다. 일반적으로 하나의 원소가 다른 원소로 치환된 동형 물질의 쌍은 치환된 원자의 크기가 바뀌면 구조의 변화가 일어나기 때문에 작은 단위세포를 갖는 결정을 찾아보기 힘들다. 큰 단위세포를 가전 것 도 연구하려는 화합물에 대한 동형 물질의 쌍을 만들려면 인내완 슬기로움이 필요하다. Peru t z 와 Kendrew 는 단백질인 헤모글로 빈과 마이오글로빈 (M y o g lob i n) 의 유도체로 동형 물질의 유도체를 찾아보았다. 단백질의 결정에 염이나 중원자의 화합물이 단백질 결 정의 분자 사이의 채널에 침투해 들어가는 것이 가능하다. 단백질 은 결정화될 수 있고 단백질 분자가 중원자 화합물과 반응하면 분 자 구조가 약간 비틀어지는 것을 알았다. 단위세포의 치수는 약 0.5% 이하로 차이가 낮으며 회절 강도의 패턴에도 차이가 있었다. 사실 단백질 분자를 다룰 경우 분자의 여러 곳에 중원자의 유도
체로 치환된 것을 얻으면 좋다. Patt er son 지도를 계산하고 중원 자의 위치를 각각의 유도체에 대해 찾은 뒤 한 결정에서 다론 결정 으로 회절 강도의 변화를 적절히 고려하여 반사의 위상을 계산함이 가능하다. 단백질과 같은 복잡한 결정은 104~105 개의 반사를 각각 다른 결정 물질 네 개 정도에 걸쳐 측정하고 이들 결정에 대해 상 호 바교하려면 많은 노력이 필요하다. 동형 단백질 유도체를 만드 는 기술은 계속 발전되고 경험이 축적되고 있다. 많은 단백질의 구 조는 이러한 방법으로 성공적으로 연구되고 있다. 중심 대칭구조를 가지는 동형 치환구조에 대해 관찰한 구조 인자 를 생각하면 다음과 같이 쑬 수 있다. Fr=FM+ F R (7-50) 여기서 M은 치환된 원자 혹은 치환된 원자의 무리를 뜻하고 R 은 구조의 나머지 부분을 뜻한다. M 의 위치룰 알면 FA( 도 알 수 있다. 두 개의 동형 결정에 대해 연구하면 치환해 둘어간 것을 제 의한 구조의 나머지 부분은 각각 같다. 따라서 하나의 결정에 대해 Fr=FM+FR 다른 결정에 대해서 다음과 같이 쓸 수 있다. Fr '=F M' +F R (7-51) 실험에서 얻은 데이터는 측정한 강도 |F 거와 |F 기이다. FM 과 FM’는 Patt er son 지도의 해석에서 구한 M 과 M' 위치에서 계산할 수 있다. F#} FT’ 의 부호는 다음 표에서 설명한 것과 같이 결정 할수있다. 예 컨대 Oll 반사에서 FRb 과 FK 의 Patt er son 지도에는 얻은 위 치에 계산한 값에서 그 차이는 대략 +33 이다. Rb 염 의 FT 값은 은 그 실험치가 土 16 이고 칼륨 영의 E 는 士 20 이다. 따라서
 h k l RIbF 염가 |KFT 영'I 금FR속b원-FK자 에(알서고 계있산는) 물Rb의 화부합호 물K의 화부합호
h k l RIbF 염가 |KFT 영'I 금FR속b원-FK자 에(알서고 계있산는) 물Rb의 화부합호 물K의 화부합호
(FRb-FK)=+36 이므로 FRb 이 +16 이고 FK 이 一 20 이 되어야 가 능하다. 또 013 반사에서 계산한 값 (FRb-F사 는 一 59 이고 FRb 의 실험치는 士 132 이고 FK 는 土 78 이다. 이 차이값이 _5 9 이므로 FRb 는 -132 이고 FK 는 ― 78 이면 실험치의 차이는 _54 이다. 어 떤 경우에는 그 위상의 부호가 모호하며 이 경우에는 생략한다. 비중심 대칭구조에서는 위상각은 o· 에서 360 ° 사이의 각도를 가질 수 있으므로 위상의 결정은 복잡하다. 단백질은 비대칭성 때문에 결정화하여 비대칭 공간군에 속하게 된다. 단백질에 중금속 원자가 치환되면 치환 안된 단백질과 중금속이 치환된 단백질은 동형태성 (i somor p h i sm) 이다. 덩치가 큰 무거운 원자가 치환되면 그 때문에 구조의 다론 부분이 구조 이동이 크다. 때문에 효소의 활성 위치에 이러한 구조 이동이 있으면 곤란하다. 위상각을 결정하려면 적어도 두 쌍의 동형 화합물이 필요하다. 무거운 원자의 위치를 Patt er son 지도에서 알 수 있으면 무거운 원자의 구조 인자 FH 와 위상각 a lfi근 각각 유도체에 대해 알 수 있다(여기서 H= 무거운 원 자). 그립 15-(a) 에서 Fp 쩌즌 단백질에 무거운 원자의 유도체가 치 환된 구조인자이고 Fp 는 단백질만의 구조인자이다. 그림 15-(a) 에
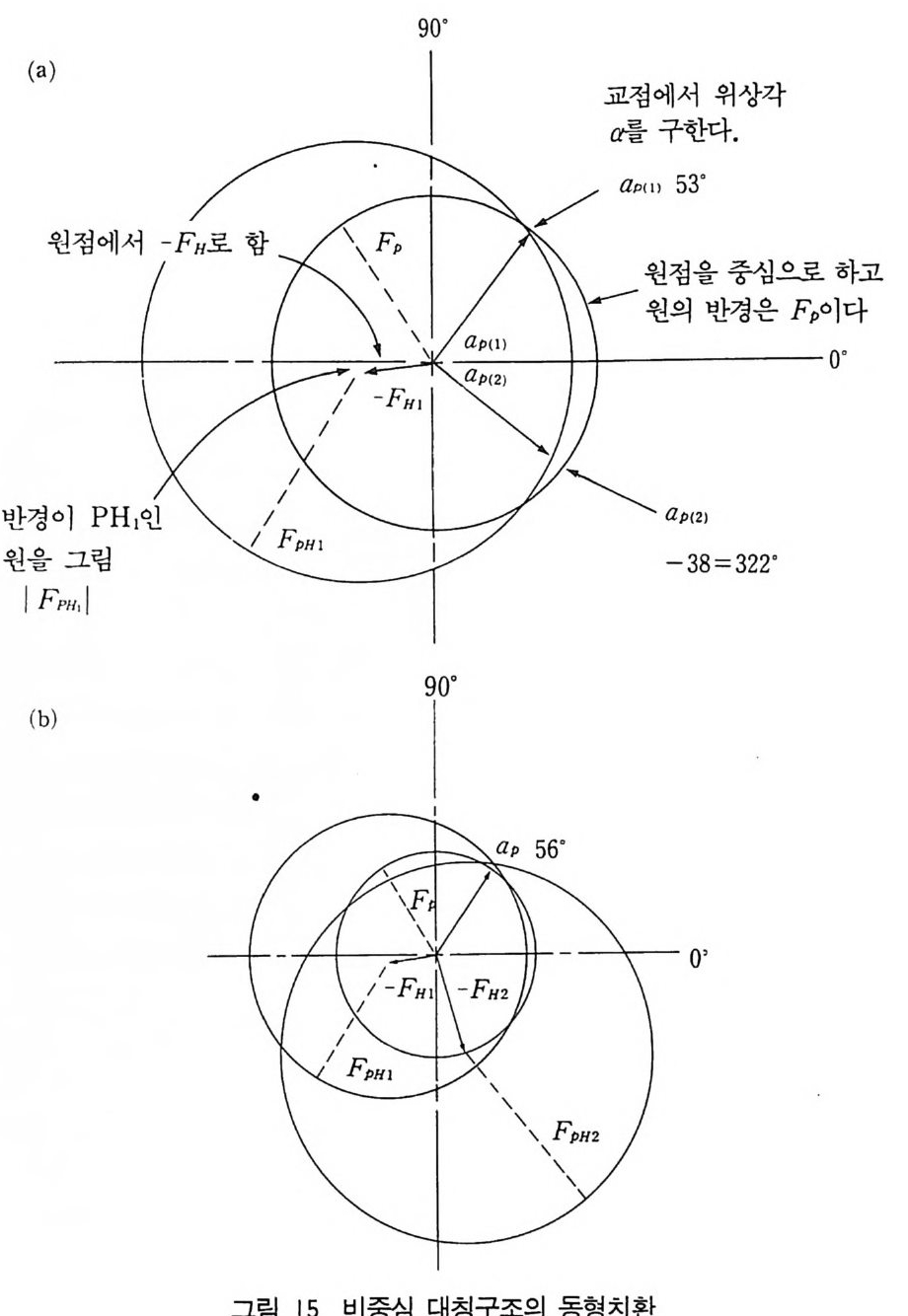 (a)
(a)
서는 단백질의 위상각을 그림을 써서 결정한다. 두 개의 단백질 유 도체 PH 와 PH 제서 단백질에 대한 두 개의 가능한 위상각을 보 여주고 있다. 그림 15 一 (a) 에서 PH 겨 대해서 대략 53 ° 와 322 ° 이 고, 그림 15-(b) 에서는 56 ° 와 155 ° 이다. 따라서 이 특별한 회절 빔 의 유리 단백질의 위상각을 추정하는 이러한 과정을 각각의 회절 빔에 대해 반복하여 행해야 하고 보통 유리 단백질 이의의 두 개의 중원자 유도체에 대해 연구해야만 위성을 정확히 결정할 수 있다. 단백질 구조를 결정하려면 단백질의 결정화, 중원자 유도체의 제 조, 원래의 단백질과 그것의 중원자 유도체의 회절 패턴의 측 정, 중원자 위치와 결정, 위상각의 결정 (그립 15- (b) ) ) , 원래의 단백질 데이터와 동형 치환에서 얻은 위상각에서 전자밀도 지도의 계산 등 의 단계를 거친다. 전자밀도는 이미 알려진 po lyp e p tide 연쇄의 기하학적 구조를 이용하여 단백질의 골격을 전자밀도 지도에서 추 적한다. 이전에는 이 작업은 모델을 이용하여, 공과 막대기를 이용 한 모델과 전자밀도 지도가 상호 겹치도록 하여 육안으로 바교하여 이루어졌으나 오늘날 전자밀도의 해석은 컴퓨터 그래픽 (comp u te r gr a phi cs) 을 이용하여 이루어진다. 단백질 결정에서 구조 인자 |F거 를 가지고 회절된 빔 hkl 의 위 상 (ap )은 그림 15 를 이용하여 결정할 수 있다. 그림 15 에서 Fp = FPH — FH 가 성립함을 알 수 있다. 그림 (15) 의 (a) 는 하나의 중원자 유도체가 만들어졌고 이 중원자 유도체의 hkl 반사에 대한 구조 인 자가 | FPHI | 이다• 반경 I FP I 로써 원을 그리고, Pat ter son 지도에 서 중원자의 위치를 결정하고 중원자의 구조 인자의 전폭 (IFHI| )과위 상 (am) 을 알 수 있다. 위상각 aHI( 죽 -am+180° 에서 -FHI 을 구한다. ), 길이 |FHII, 그리고 이 벡터의 끝에 중심을 두고 반경이 IFPm| 인 원을 그린다. 반경 IFP| 인 원과 두 점에서 만나고 두 개 의 가능한 위상각 야(I ) 과 aP(2) 를 구한다. Cos i ne 의 법칙과 그림에서 위상각을 구할 수도 있다.
따 = a 計 cos-1 (FPH2— Fp 드 FH2) /2FPF싸 = aH 土 a' (7- 5 2) 그 립 15 의 ( b ) 에서 두 개 혹은 두 개 이상의 중원자 치환체가 있 으 면 ( a ) 에서 설 명한 과정을 반복한다. 운이 좋 으면 원래의 단백질에 대해 하나의 위상의 값 을 얻을 수도 있다. 두번째 유도체에 대해서 ( a ) 경 우의 두 배의 부함뚜 피할 수 있다. 이 방법은 |F시 , IFPml 과 | FP / 12 1 의 정 확 한 측 정이 중요하고 원래의 단백질에 중원자를 넣 은 것 이외에 는 다 른 영향이 없다는 가정이 필요하다. 위상각의 정 확성 을 증 가시키기 위해 또 다른 유도체가 때때로 필요하다. 단백질 구조를 해석하려면 많은 양의 일이 필요하므로 처음에는 낮은 산란각에서 관찰한 회절 패턴의 일부로써 일을 시작한다. 낮 은 산란각에서 동형 물질을 사용하는 방법은 효과적이다. 그 이유 는 치환으로 생기는 위치의 차이는 낮은 산란각에서는 높은 산란각 보다 영향이 적다. 그러나 이 말은 처음에는 분리능이 좋지 않아 상세한 구조는 전자밀도 지도에 정확히 나타나지 않음을 뜻한다. 그림 16 에서는 주어진 구조의 모양이 분리능이 개선됨에 따라 변 화하는 모양을 보여주고 있다. x- 선 회절법에서 산란각에 따른 분리능이 변화하는 것은 보통의 현미경에서 상의 분리와 비슷하다. 현미경으로 물체를 관찰할 때 산란하는 복사선의 일부가 싱을 만들지 않고 도망가면 형성된 상은 산란 물체를 완전히 나타내지 못한다. 특히 미세한 부분은 분리해 내지 못한다. 이와 유사하게 X- 선에서 일반적으로 많이 사용하는 파장으로 비교적 작은 산란 각도만으로써 회절 패턴을 얻으면 여기 서 만든 상의 분리는 낮다. 더욱이 분해능은 전 패턴을 관찰한다 해도 사용한 파장으로 제한울 받는다. 산란된 복사선으로 상을 만 드는 과정에서 사용한 파장보다 더 적은 상세한 것은 구별해내지 못한다. 그러나 다행하게도 보통 우리가 사용하는 X- 선으로 원자
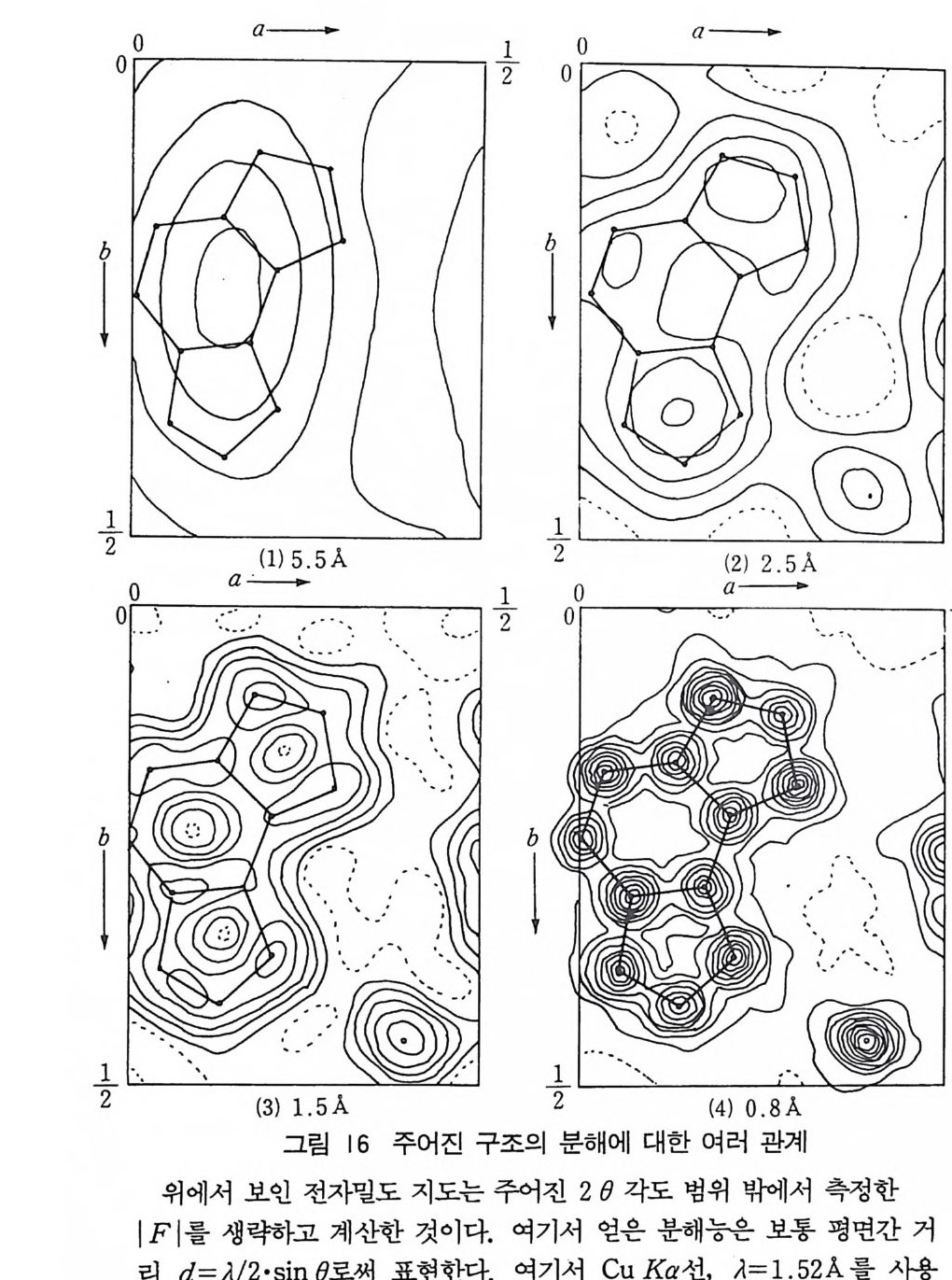 a • 2—1 。 。 a • 12—
a • 2—1 。 。 a • 12—
d 최대각도 계산에 포함된 반사의 상대적 수 (1) 5. 5A 16° 7 (2) 2. 5 36 27 (3) 1.5 62 71 (4) 0 . 8 162 264 각 각 지도에서 주어진 데이터에서 얻은 실제 구조의 윤곽은 겹쳐져 있 다. 단계 (1)은 보통 단백질 구조결정에서 경험하는 전형적인 경우이다. 단계 ( 2 ) 와 (3) 도 일반적으로 단백질 구조에서도 가능하다. 그러나 단계 ( 4 ) 는 Cu Ka 선으로서 분자량이 적은 좋은 결정에서만 얻을 수 있다. 간 거리는 3 차원에서 분리해낼 수 있다. 따라서 분리한 원자의 위 치를 측정할 수 있고 상세한 분자의 기하학적 모양을 아주 정확히 계산해낼 수 있다. 14 이상 분산(異常分散, anomalous d i s p ers i on) 과 원자의 절 대 배 열 (absolute confi gura ti on ) Tarta ric ac id 분자의 화학식과 3 차원적 구조는 보통 많이 사용 하는 X- 선 회절법으로 결정할 수 있지만 원자의 철대 배열에 대해 때로는 모호한 점이 있다. 철대 배열에 대한 정보는 보통 측정하는 결정의 회절 패턴에는 포함되지 않는다. 비대칭 탄소원자의 치환체 도 알고 분자의 상세한 3 차원적 기하학적 구조는 알아도 두 개의 거울상 이성체 (enanti om er) 중 어느 것이 3 차원적 분자의 구조를 나타내는지는 알 수 없다(그립 17). 분자의 절대 배열을 결정하는 수단으로서 X- 선 결정학적 방법을 서용할 수 있다. 이 방법은 X- 선에 대한 원자의 흡수계수를 입사 x- 선의 파장에 대해 그리면 불연속선을 보인다. 이 불연속선이 제 4 장 5 절에서 언급한 바와 같이 흡수끝이다. 흡수끝의 파장에서나 흡수끝 가까운 파장에서 X- 선 에너지는 전 자를 더 높은 에너지의 양자 상태로 들뜨게 하거나 원지에서 전자
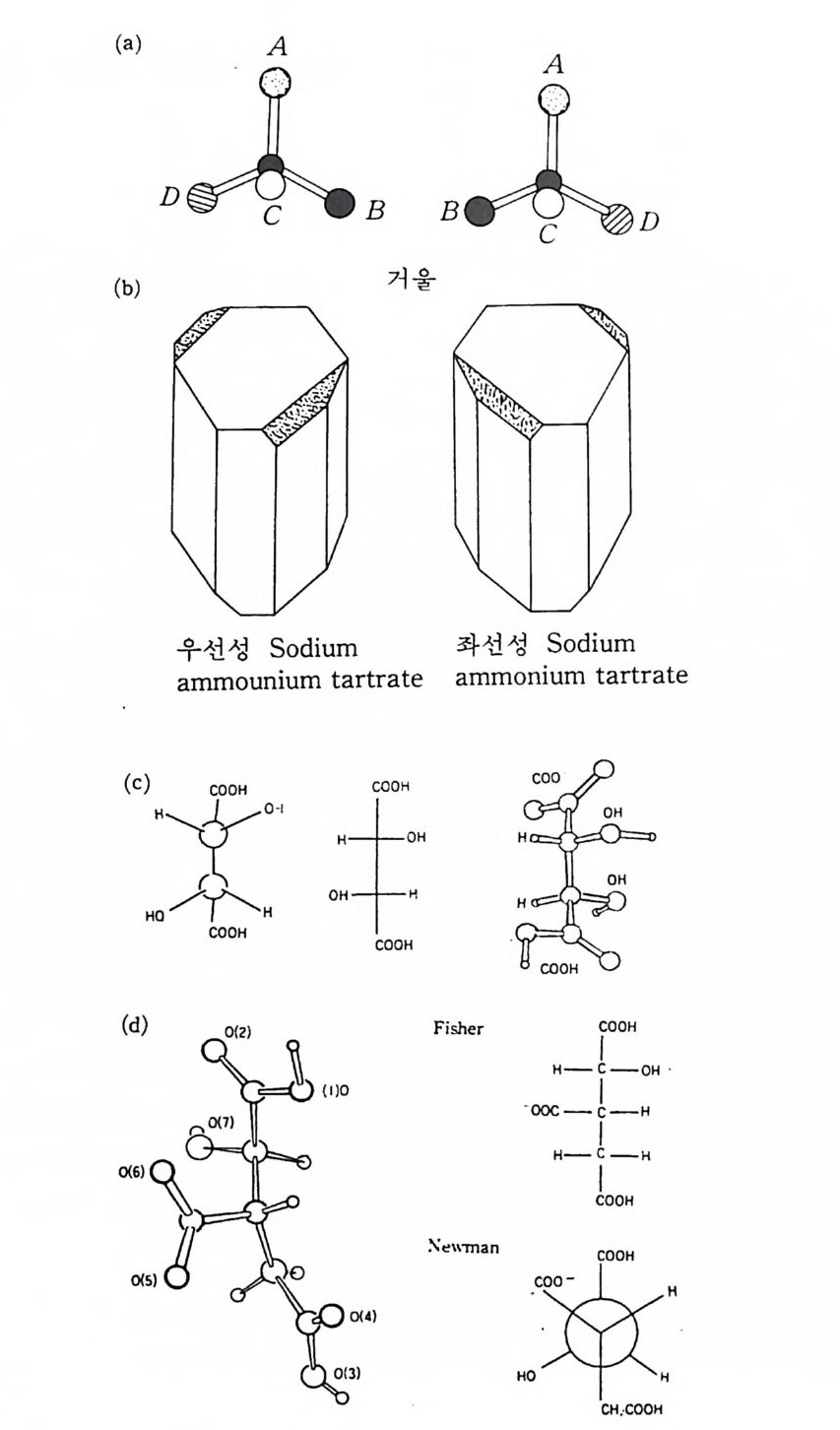 (a) D~A B B. lD
(a) D~A B B. lD
그림 17 절대 배열 (a) 4 면체 탄소에 붙어 있는 A, B, C 및 D 가 모두 다른 원소면 거울 면에 대해 서로 두 개의 chir a l 이성체가 있다. (b) sodiu m ammoniu m tar tr a te 결정의 반면상 결정 (半面像 結 11911) 의모양 (c) (+) tar ta r ic a ci d 의 절대 배열. 실제 구조(오른쪽)에서 네 개의 탄소 원자는 zig -z ag 모양을 하고 있다. 왼쪽 그림은 Fis c her 석으 로서 수직의 탄소쇄는 평면을 나타낸다. 가운데 그립과 왼쪽 그림 에서 실제 구조와 바교할 때 위쪽에 대해 아래쪽 반은 180° 회전하 였다. 이것은 형태에서 영향을 주나 분자의 절대 구조에는 영향을 주지 않는다. c 의 왼쪽에 설명한 tar ta r ic a ci d 의 형태는 이 분자 의 가능한 형태이나 결정에 실제 존재하는 형태인 오른쪽 것보다 결합이 서로 eclip s e 되므로- 높은 에너지를 갖는다. (d) (+)iso cit ric 산의 K 영의 절대 구조. Fis c her 와 Newman 식을 동시에 나타내었다. 이 거울상 대칭 물질의 정확한 표시는 lR: 2s -l- hyd roxy -1, 2, 3 Prop a netr i c r boxy la te 이다. 를 떼낼 수 있을 만큼 충분한 에너지를 갖는다. 이것은 산란에서 위상의 변화를 준다. (7-27) 식에서와 같이 원자의 산란인자(f, . )는 복소수로써 다음과 같이 표시할 수 있다. fi = /,.0+ 6//+ i6 / /' (7-27) 여기서 f?는 X- 선에 대해 보통 산란하는 원자의 산란 인자이고 A f,. ’는 보통 음수로서 실수항의 교정항이고 스f, . ”는 fi o 와 스fi’에 대해 복소수 평면에서 반시계 방향으로 90° 회전한 허수 성분의 교 정이다. 그리고 스f,’와 스f,.”는 입사 X- 선의 파장에 따라 변하고 이 파장이 흡수끝 가까이 있으면 스f, · '’은 가장 큰 값을 갖는다. 구조내의 원자가 사용한 X- 선을 어느 정도 흡수하면 이 흡수 때 문게 그 원자에 의해 산란되는 X- 선은 구조내 다른 원자에 의해 산란되는 X- 선의 위상과 비교하면 위상 변화가 일어난다. 죽 복사
선은 짧은 순간 전행을 늦추는 결과와 동일하다. 이러한 위상각은 그림 18 에서 알 수 있는 바와 같이 산란한 빔이 여행하는 경로의 변화를 주는 것과 동일하다. 따라서 경로가 달라지면 X- 선 강도의 변화가 일어난다. 이러한 영향은 중원자가 포함되는 결정과 사용한 x- 선의 파장과 어떤 원자의 흡수끝의 서로 가까우며 특히 현저히 나타난다. 이러한 이상 분산 (anomalous d i s p ers i on) 이나 이상 산란 (anomalous scatt er in g ) 이 없으면 지수 h, k, l 을 갖는 반사 강도 와 지수 Ji, k, T 를 갖는 반사 강도가 동일하나(이것이 7 장 5 절에 서 언급한 Frie d el 법칙이다) 이상 산란이 있으면 이 두 반사 강도는 이상 산란을 하는 원자의 흡수에 의해 상변화가 경로의 차가 있으 므로다르다. 강도의 차이는 f,의 복소수항 때문이라고 생각할 수 있고 따라서 F(hkl) 의 절대값과 F(-h, -k, -l) 의 절대값이 서로 다르기 때 문이다(그림 19). 산란되는 X- 선 빔의 경로의 차에 대한 이상 산란의 영향을 생각 해보면 여기서 보통의 경로의 차 2P 에서 이상 산란체는 경로의 차 q만큼 다르게 된다(그립 18). 결정에 이상 산란이 있으면 f는 다 음과같이쓸수있다. f=f°+6./'+ it:::,f 그리고 A'= GU+6 ./1 +A B'= H(/+ 6./1 + B (7-53) 로 두자. 여기서 G 와 H 는 이상 산란체이고 A, B 는 이상 산란 성이 없는구조의 나머지 부분이다. 그러면 F(hkl) = (A'+ iG L :::.f'') + i(B '+ iH L :::.f'') = (A'-H6 ./) + i(B '+ GL :::.f) (7-54)
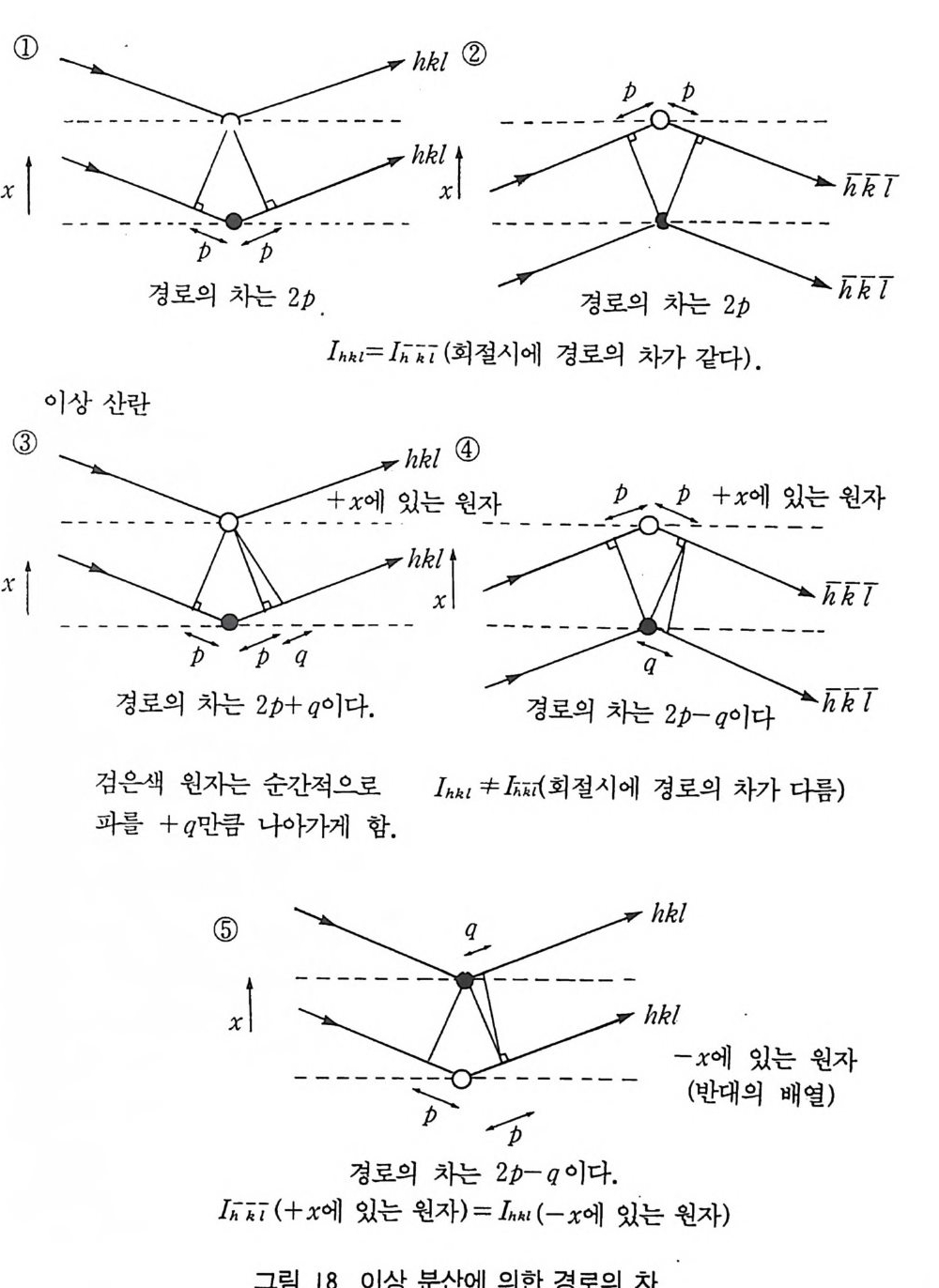 ®
®
I F(hkl) 12= (A'-H6/) 2+ (B' + G6 /) 2 (7- 5 5) 이와비슷하게 F( iikT ) = (A' + iG 6f ) —i(B '+ i H 나') = (A'+ H6J ) 규 (B' 一 G6 /) (7- 56 ) I F( iik T ) l2= (A'+ H6/) 2+ (B'-G 6 /) 2 (7- 5 7) 따라서 다음 식이 성립한다.
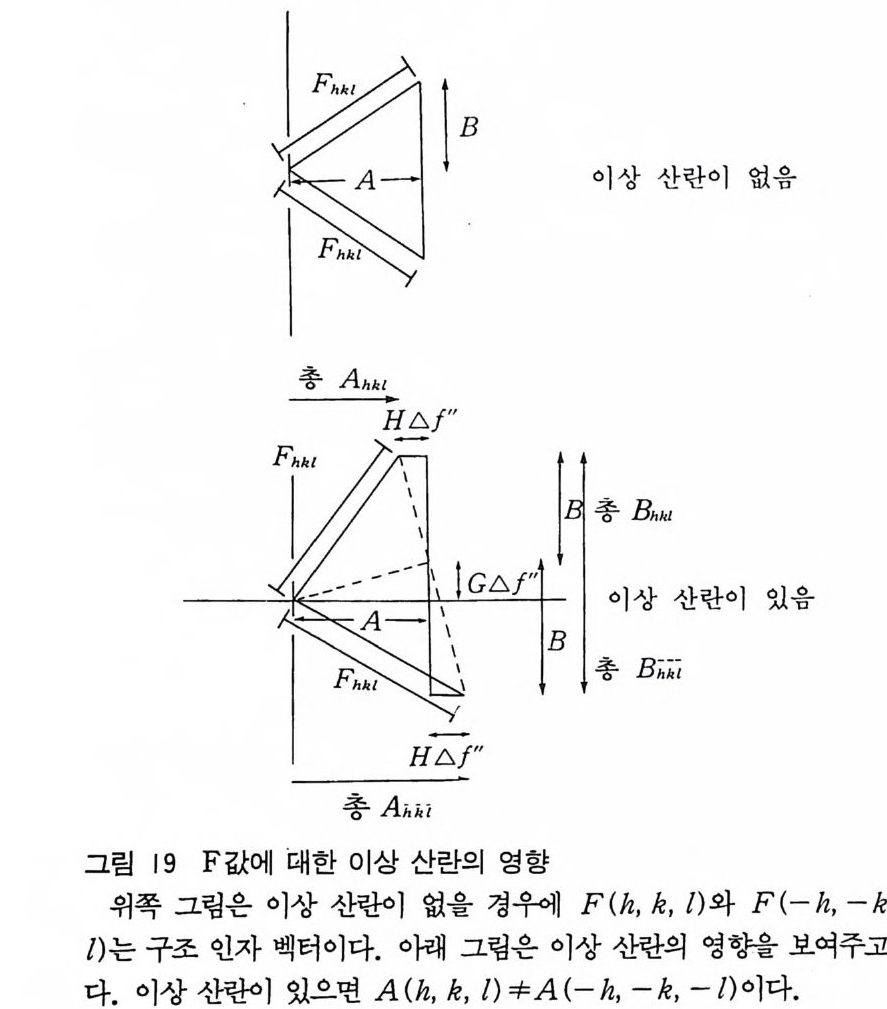 이상 산란이 없음
이상 산란이 없음
I F(hkl) 12— | F ( hkl) 12=46/(B'G-A'H) (7-58) 따라서 입사 X- 선이 구조내 어떤 원자의 흡수끝 가까이 있는 파 장을 가지면 |F(hkl) I 은 |F(EET) I 와 다르다. 그러나 보통 조 건 아래에서는 X- 선 복사선은 흡수선에서 멀리 떨어져 있어서 이 두 양은 서로 같다. 이 두 개의 Frie d el 쌍의 반사에 대한 I F l2 의 차이의 크기는 입사 복사선이 흡수끝에 얼마나 가까이에 있는가에 달려 있는 스f와 구조에서 이상 산란체와 그 밖의 부분의 위치 파라미터의 함수이다. 주어진 거울대칭 이성체에 대한 | F(hkl) 12 과 | F( hkT ) 12의 차 이룰 (7-58) 식을 써서 계산하는 것이 가능하고 또 이들 구조 인자 의 측정값과 계산에 사용한 모델 화합물의 절대 배열과 관련시킬 수 있다. 실제 반사의 지수는 h, k, l 이 우선계가 되도록 할당시 킬 수 있고 hkl 과 EET 에 대한 |Fl2 의 값을 측정하고 이들 차이 의 크기와 부호는 4 6 /(B ' G ― A ' H) 의 계산치와 비교한다. G 와 A ' 는 cosin e 향을 가지고 계산하려는 모델 화합물의 〈 handness 넹 바꿔도 이들은 부호가 바뀌지 않는다. 그러나 B' 과 H 는 sine 항 이므로 모델 화합물내의 모든 원자의 좌표의 부호가 거꾸로 되면 B ' 와 H ' 의 부호는 바뀐다. 따라서 |F(hkl) |드 |F(EET) |2과 (B ' G-A'H) 가 반대부호를 갖는다면 모델 화합물의 x, Y, z 의 값은 一 x, -y, 一 z 로 바꾸어서 올바른 모델을 갖도록 해야 한다. 이러한 것을 예를 들어 생각하자. Pota s siu m dih y d rog e n i so cit ra t e 결정에서 다섯 쌍의 반사 hkl 과 EET 의 |Fl 값을 chrom i um 복사선으로 측정하여 비교해보면 구조내에 K 미온이 있기 때문에 이상 분산을 나타냄울 알 수 있다. 이 데아터에서 이 상 분산의 효과가 충분히 커서 시료의 절대 배열을 쉽게 결정할 수 있다. 여기서 |Fe! 값은 그립 17-(d) 에서 나타낸 dih y d rog e n iso c itrat e 이온의 절대 구조에서 계산한 것이다. 거울쌍 대칭형에
서는 hkl 와 EET 에 해당되는 값이 반대로 될 것이다. h k l IF 겨 IFcl —ll —33 -11 2129.. 90 1293.72 -11 -33 —22 260..47 260..06 -11 —33 —33 2206..37 2205..07 4 5 2 7.2 7.0 -4 • -5 -2 2.5 2.7 7 —1 2 9.2 9.0 -7 1 _2 13.1 12.9 전자밀도 계산에서 이상 분산의 효과는 Acta Cr yst a l log r ap hi c a 16(1963), p .1255 에서 A. L. Pa tt erson 이 논했다. 그는 F 값을 교정하는 방법을 설명하였다. | F± 12=2A 821 +(A BA 프d +(8 B 선Bd )참 -)2 ( A(J8d2 2 (A+ BBdd2—) +B A d) (7-59) 여기서 A 와 B 는 보통 산란하는 원자의 구조 인자이고 Ad 와 B 초 이상 산란하는 원자이고 6 는 |F(hkl) I 의 값에는 +1, IF (EET) I 에서는 ― 1 이고 &=^jd / jd 이고 f2 = b.f: ;I fd 이다. 그러 면 두 양은 다음과 같이 정의된다. S=1/2{ I F+ 12+I F-12}=A2+B2+201 (AAd+BBd) D=·+l /2( o{f I+ F o 니 n드(A| ~F+-1B2~}=) — 20 2(ABd-BAd) ((77--6 601 )) 따라서 hkl 과 EET 의 반사쌍의 평균 강도의 (7-60) 식으로 계 산할 수 있고 그 차이는 (7-61) 식으로 계산할 수 있다. D의 부호
가 툴리면 구조모델은 툴리는 절대배열을 갖는다. 전자밀도 지도를 계산하는 데 사용되어야 할 항은 다음과 같다. I F lo={S-281(AAd+BBd) 一 (812+ 참) (Ai + Bd2 )} (7-62) 따라서 정확한 전자밀도 지도가 필요하면 구조에서 회절 대이터 는 원자의 흡수끝에서 먼 것을 측정하는· 것이 좋다. 홉수끝 가까이 에서 측정 한 데이터를 절대 구조를 결정하는 데 사용할 수 있다. 즉 이상 분산으로 절대 배열을 결정하는 방법을 요약하여 말하 면, 결정내 원자는 사용한 X- 선을 상당량 흡수할 경우 이 원자에 의해 산란하는 X- 선의 위상은 갇은 위치의 X- 선을 흡수하지 않는 원자에 의해 산란하는 X- 선의 위상에 비해 위상의 변화가 있다. 이러한 홉수에 의한 위상의 변화는 이상 산란을 일으키고 비중심 대칭구조에 대해 I F(hkl) 12 과 | F( iikT ) 12 의 차의 값이 이상 산 란이 없을 경우에는 없으나 이상 산란이 있을 경우 이 두 양의 값 의 차가 있다. 분자구조가 하나의 거울상 이성체가 존재하면 | F (hkl) |드 | F( iikT ) 12 의 계산값과 측정값의 부호를 비교하여 절대 배열을결정할수있다. 연습문제 1. Deby e -Scherrer 카메라로 Cu Ka X- 선으로 InSb 에 대한 회 철 패턴을 얻었다. 이 물질은 ZnS 구조를 가지고 있고 격자상수 는 6.48A 이다. 처음 두 개의 회절선의 지수는 무엇이며, 이 두 개 선의 적분 강도의 비를 구하여라. 2. (a) 공간군 P2 의 일반위치는 x, y, z ; x, y, 之이다. (b) 공간 군 P2/m 의 일반위치는 x, Y, Z ; x, y, 효 ; x, Y, z 와 x,
ji' z 이다. Patt er son ma p의 Vecto r 지도에서 피크 위치를 구 하라. 그리고 Harker 면의 위치를 구하라. 3. 다음 반사는 공간군 PI 에 속하는 물질의 반사로 매우 큰 규격 화된 구조 인자 |El 값을 가진다. 처음 세 개의 구조 인자~ 원 점을 선택함에 따라 임의로 부호를 붙였다. 세 개 사이의 곱의 관계를 써서 나머지의 구조 인자의 부호를 붙여라. hkl 507 232 716 211 413 241 !El 2.4 2.6 3.1 2.5 2.0 2.6 s + + + 4. Bis d ip h eny lm eth yld is e lenid e , (C 晶) 2CHSe2 (C6H 깊 走 단사 정계에 속하고 a=18.72A, b=5.7 7 3A, c=12.5 97A 이고 /3= 125.4 7°이다. 단위세포 부피 (Ve)=1107 . lA3 이고 밀도 (Dm)=1.49 g cm-3 이다. 또 분자량은 492.4 이다. x- 선 반사조
 @ ? 1/X2 숙
@ ? 1/X2 숙
전은 hkl 반사에 대해 h+ k= Zn 이다. Patt er nson 면 P(X, 0, Z) 에 대한 지도는 그림 p -1 과 같다. 이 분자는 노란색 침상 결정을 하고 있고 바늘 방향의 축 주위로 찍은 진동 사전에서 이 분자는 거울평면 m 을 가짐을 알 수 있었고 영충 (zero lay e r ) Weis s enberg 사진과 위쪽 충의 Weis s enberg 사전에서 이 분자 는 2 회 회전축을 가침을 알 수 있었다. (a) 단위세포당 몇 분자를 포함하느냐? (b) 공간군을 결정하라. (c) Se 의 위치를 중원자법으로 결정하라 . 5. Cup r ous chlorid e azometh a ne com p lex(CH2Cl2C2H2N 시를 c 축으로 Patt er son 투영한 그림 p -2 는 아래와 같다. 공간군은 PI 로써 단위세포당 한 분자가 있다. 가능한 대로 완전히 결정구 조를해석하라.
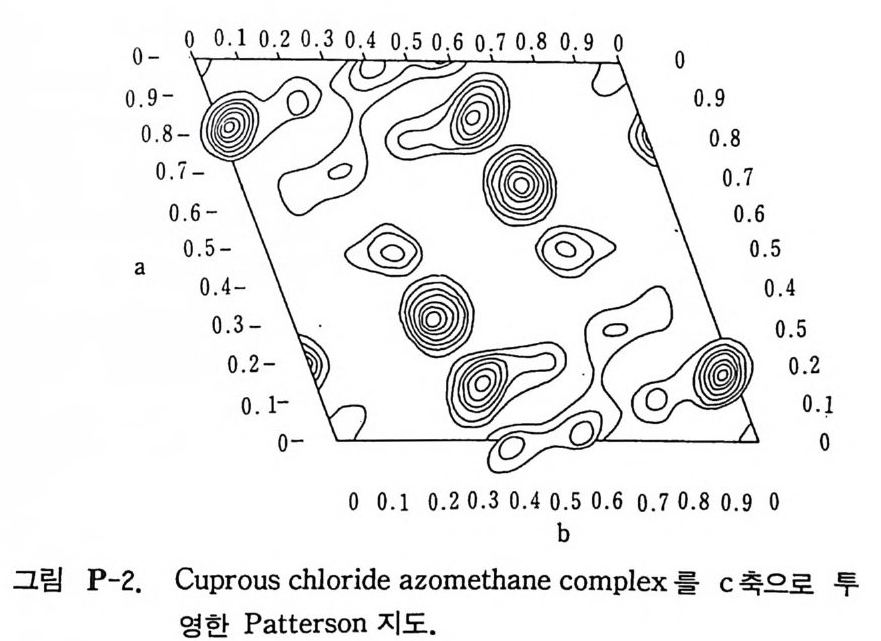 0- Q o._ 1 o._2 o._ 3 o.4 o.s o.6 0.1 o.s o. 9 o 。
0- Q o._ 1 o._2 o._ 3 o.4 o.s o.6 0.1 o.s o. 9 o 。
제 8 장 시험 구조의 정밀화 1 서론 대부분의 원자에 대한 대략의 위치가 결정되면 구조의 정밀화가 시작된다. 이 과정에서는 관측한 구조 인자의 진폭과 제안한 구조 에서 계산한 구조 인자의 진폭이 가능한 한 찰 일치하도록 원자의 파라미터는 체계적으로 바꾸어진다. 정밀화 기법에는 Four i er 합 성법을 포함한 정밀화 기법과 최소 자승법이 있고 이 두 방법은 거 의 대등한 방법이다. 실험 관측과 관련된 weig h ti ng 방법에서 주 로 다르고 조작하는 방법에서 차가 있다. 정밀화되는 파라미터가 한 단계 계산에서 다음 단계의 계산으로 옮길 때 추정 오차 (esti m ate d error) 가 거의 없는 단계로 구조가 수령할 때까지에는 수많은 정밀화 단계가 필요하다. 2 Fourie r 법 전술한 바와 같이 Four i er 법은 원자 중 얼마를 발견한 후, 죽 처음에 하나나 몇 개의 무거운 원자를 찾아낸 후거나 구조의 상당 부분을 찾아낸 후, 구조의 다른 부분을 찾는 데 사용한다. Four- i er 법은 시험 구조를 정밀화할 수도 있고, 전에 찾지 못한 낮은 산
란력을 가지는 원자를 찾는 데 사용할 수 있다. 구조에서 대부분의 원자의 근사적 위치를 알면 계산한 위상각은 거의 옳다. 측정한 구 조 인자의 전폭과 계산한 위상각으로써 계산한 근사적인 전자밀도 는 위상각을 계산하는 데 사용한 시험한 구조와 올바른 구조를 혼 합하여 포함하고 있다. 시험 구조가 올바른 구조의 원소 대부분을 포함하고 있으면 계산한 전자밀도 지도는 시험한 구조에서 원자 위 치 가까이에 피크를 나타내고 있을 뿐만 아니라 시험 구조에서 생 략하였으나 실제는 존재하는 다른 위치의 원자도 나타낸다. 반대로 시험 구조에서 원자가 올바르게 선덱하지 못했으면 전자밀도 지도 에서 이에 대응하는 피크는 보다 정상적인 것보다 훨씬 낮은 피크 로 나타난다. Fourie r 전자밀도 지도에의 계산에 넣은 원자의 정 확한 위치에 가까이 있으나 정확한 위치로 넣지 못하면 전자밀도 지도에서 이에 해당하는 피크는 넣은 위치에서 올바른 위치로 비뚤 어져서 나타난다. 중심 대칭형 구조에서는 위상각은 0 니. 180 ° 이고 구조에서 약간 의 오차는 대개의 위상각에는 크게 영향을 미치지 않는다. 따라서 측정한 |F| 값과 계산한 위상각으로 계산한 지도는 모델이 약간 틀려도 거의 옳다. 그러나 비중심 대칭 구조에서는 위상각은 0 ° 에 서 360 자이의 각도를 가질 수 있으므로 대개의 계산한 위상은 약 간의 오차가 있을 수 있고 계산한 전자밀도 지도는 중심 대칭 구조 보다 위성을 계산하는 데 사용한 모델 방향으로 더욱 치우치게 된다. 일반적으로 대개의 시험 구조의 구성원을 알면 정규적인 전자밀 도 지도 대신 전자밀도의 차의 지도를 계산한다. 차의 지도에서 계 산하는 계수는 (IFo| ― |Fe| )이고 위상각은 시험 구조에서 계산한 위상각을 사용한다. 따라서 Four i er 의 차의 지도는 관찰한 구조 인자와 계산한 구조 인자의 차를 근거로 한 지도이다. 전자밀도의 차의 지도에서는 양의 영역은 시험 구조에서 이 영역에 전자를 충 분히 넣지 않았음을 뜻한다. 음의 영역은 시험 구조에서 이 영역에
너무 많은 전자를 포함시켰음을 뜻한다. 예컨대 너무 높은 원자번 호를 가진 원자를 포함시키면 해당하는 위치에 음의 영역의 구멍이 나타난다. 수소원자는 보통 모든 무거운 원자를 포함시킨 시험 구 조에서 계산한 전자밀도의 차의 지도에서 찾을 수 있다. 그림 1 에 는 전자밀도 차의 지도를 파라미터를 정밀화하는 데 사용할 수 있 는 예를 보이고 있다. 원자를 정확한 위치 가까이에 포함시켰으나 정확한 위치에 포함시키지 않았을 경우 포함시킨 위치는 음의 영역 에 놓여지고 올바른 위치의 방향은 양의 영역으로 나타난다. 원자 롤 올바른 위치로 아동시켜야 할 양( 最 )은 음의 영역과 양의 영역 사이의 등고선의 기울기로써 표시된다 . 어떤 원자가 시험 구조에서 빠져 있으면 빠져 있는 위치에 피크로 나타난다(물론 전자밀도 지도 를 계산하는 데 사용한 위상각이 대략 옳다고 가정하자). 온·.£ 인자의 지수값이 계산한 시험 구조에서 너무 적게 표시되면 원자가 너무 집중되어 있다고 가정한 것과 감으므로, 죽 전자를 실제보다 너무 적은 부피내로 제한시켰으므로 원자가 있는 위치에 음의 구멍이 나 타난다. 반대로 열 진동 파라미터를 시험 구조에서 너무 크게 잡으 면 피크가 나타난다. 원자가 이방성으로 전동하는데 등방성으로 전 동하는 것으로 시험 구조에 계산했으면 원자가 많이 진동하는 방향 으로 피크가 나타나고 적게 진동하는 방향으로는 음의 구멍이 나타 난다. Fourie r 정밀화 과정이 고속 컴퓨터에서는 자동조작으로 수행될 수도 있다. 그러나 최소 자승 정밀화법보다는 사용되지 않는다. 최 소 자승 정밀화법은 컴퓨터로 사용하기 편리하고 실험 측정치의 신 빙성에 대한비중을두는방법이 통계학적으로볼때 더 합리적이다. 구조 결정이 훌륭히 수행되고 정밀화 작업이 끝나면 전자밀도의 차의 지도에 피크가 없이 평평해야 한다. |Fol 와 |Fcl 는 서로 찰 맞아야 하고 따라서 오차지수 값 R 은 낮아야 한다. (|F나 -|Fcl) 값이 크면 전자밀도의 차의 지도에 피크나 음의 구멍이 있고 이것
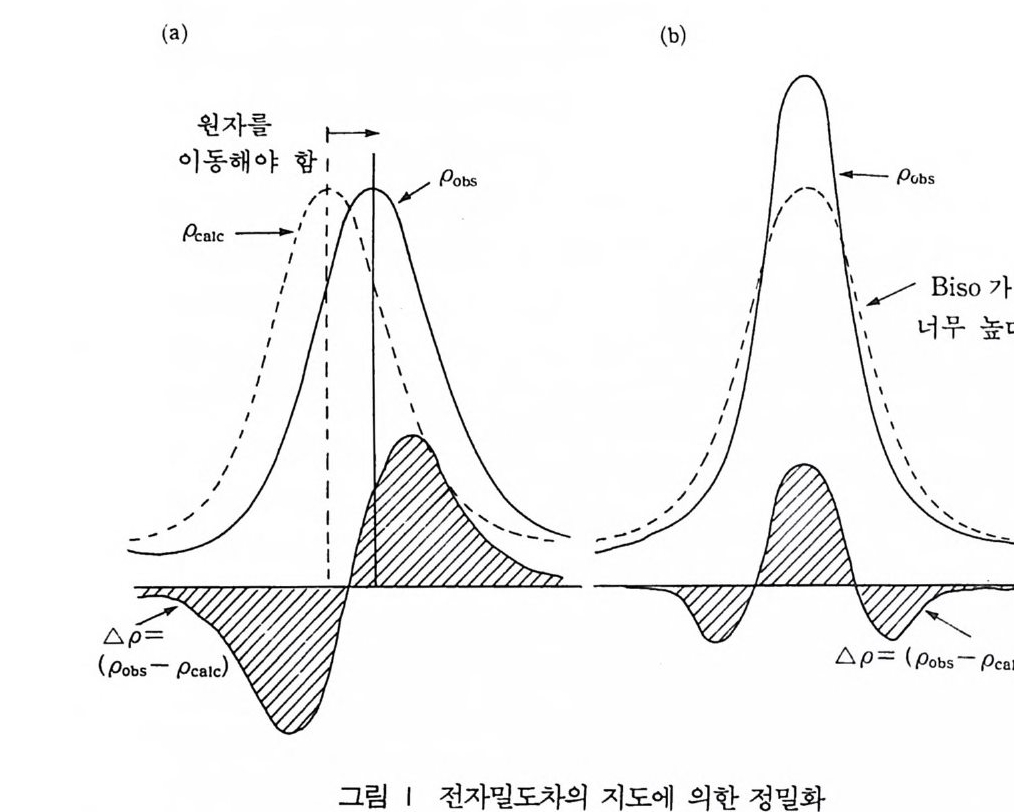 (a) (b)
(a) (b)
전자밀도 차의 지도는 원자의 위치와 온도인자를 정밀화하는 데 이용 할 수 있다. 차의 지도에서 피크(양의 전자밀도가 있는 영역)는 모델에서 피크가 있는 위치에 전자밀도를 충분히 포함시키지 않았음을 뜻한다. 반 대로 음의 구멍은 그 반대를 뜻한다. (a) 원자 위치에서 오차가 있을 경우 : pt c 에서 나타난 피크는 구조 인자 계산에서 사용한 근사적인 위치를 나타내고 Pob s 에서 나타난 피크 는 정확한 위치에 더 가깝다. 따라서 실제 원자 위치는 차의 지도에서 양의 피크 방향으로 옮겨야 한다. (b) 원자의 온도 인자에서 오차가 있음 : 지도를 만들 때 온도 인자의 지수를 너무 크게 사용하면 원자의 위치에 음의 전자밀도로 둘러싸인 양 의 피크로 나타난다. 죽 B 값을 감소시켜야 한다.
은 구조에 오차가 있음을 뜻한다. 따라서 구조해석이 끝나면 전자 밀도의 차의 지도를 계산하고 피크가 있는지 없는지 세밀히 관찰해 야한다. 3 최소 자승법 최소 자승법은 1806 년 Le g endre 가 처음 사용한, 결정할 파라 미터보다 더 많은 측정수가 있을 때 가정한 모델이 실험 데이터에 얼마나 잘 일치하는지를 알아내는 실험적 방법이다. 가정한 모델의 최상의 파라미터는 실험값과 유도한 파라미터로써 계산한 값의 차 이 를 제곱하여 합한 것을 최소화하여 얻는다. 하나의 측정치가 다 른 측 정치보다 더 정확할 경우 정확한 측정치를 정확지 못한 측정 치보다 계산에서 비중 (we ig h t)을 두게 할 수 있다. 이 비중은 각 각의 측 정에서 정확성에 역바례로 할당한다(실제는 보통 추정 표준 오차〔 es ti ma t ed sta n dard dev i a ti o 미의 제곱에 반비례하게 한다). 최 소 자승법은 측정한 회절 강도를 계산한 회절 강도에 맞추는 문제 에 확장하여 사용하였다. 이 방법은 문제점이 약간 있지만 구조를 정밀화시키는 방법으로서 지난 30 여 년 동안 가장 많이 사용해 왔 다(문제점은 최소 자승법 이론이 데이터에서 실험오차는 정규분포로 분 포되어 있다는 가정 아래 행한다. 죽 Gauss 오차곡선에 따른다고 생각 한다. 이러한 가정은 대부분- 데이터에 대해서는 검토하지 않는다. 관측 에 정밀도에 대한 비중을 두는 것은 이러한 문제를 어느 정도 완화시킨 다). 최소 자승법은 데이터를 직선에 맞추는 것과 같이 측정 데이 터를 가정한 모델에 근거로 두고 계산한 데이터에 맞춘다. .6.F =IFoI-I Fi니를 측정한 구조 인자와 계산한 구조 인자의 차라고 하면 |F。 (hk/)I 의 실험값의 표준편차를 〔 w(hkl)] 令로 표 시하면 오차이론에 의하면 시험모델의 최선의 파라미터는 다음 양 의 최소값에 상당한다‘
Q=I:w (hkl) [!:::: .I F(hkl) |]2 (8 一 1) 여기서 합은 모든 반사에 걸쳐 행한다. |Fc l 에 대한 식을 해석 할 때 파라미터가 약간 변하는 영향도 고려한다. 이 변화는 위의 (8-1) 식의 항을 최소로 되게 한다. 두 개의 파라미터가 있는 직선 에 맞추는 일도 많은 계산을해야 하고 결정구조 계산에서는 많은 파라미터가 포함되므로 최소 자승법 계산은 고속이고 많은 기억 용 량이 있는 컴퓨터를 사용해서 수행해야 한다. Q량을 최소화하는 데 사용해서 변수는 실험치에 대한 총괄척도 인자 (overall scale fac to r ), 원자의 위치 파라미터(각 원자에 대해 x, y 및 z)' 온도 인자의 지수항으로 전동 파라미터 (진동은 일반적으로 타원체 모양으 로 진동한다고 생각할 수 있다. 따라서 이방성 온도 인자일 경우 각 원 자에 대해 /3n , /322 , /333, /312 , /31 3 및 /323 의 6 개까지의 파라미터가 필요 하다)이다. 때때로 구조에서 무질서함이 있을 경우 점유 인자 (occup a ncy fac to r ) (0 에서 1 까지 변하고 다른 원자의 점유인자와 상 관관계가 있을 수 있다)도 각 원자에 대해 정밀화해야 한다. 일반적 인 경우 N 개의 독립적 원자를 가진 경우 정밀화해야 할 파라미터 의 총수는 (9N+l) 이거나 점유 인자를 포함해야 할 경우에는 9N+1 보다 파라미터 수가 많아질 경우가 있다. 때로는 각 원자의 대칭적 특성 때문에 원자의 파라미터와 열전동 파라미터 각각 사이 가 서로 같게 해야 할 경우(/3ii=/3jj 혹은 /3,.J= Bik , Xi =y,., Xi =y,= Z i등등……)가있다. 이 경우는정밀화해야할파라미터 수가감소 하게 된다. 정밀화해야 할 파라미터의 수가 P 이면 (8-1) 식을 최 소화하는데 이들 각각 파라미터에 대한 Q의 미분값을 영으로 두 어야 한다. Q의 미분값은 쉽게 계산할 수 있다. 따라서 P 개의 독립적 연립 방정식을 풀어야 한다. 적어도 P 개의 파라미터를 정 의하려면 P 개의 설험 측정치가 필요하다. 그러나 실제로 측정치 는 보통 상당량의 실험 불확실성을 포함하므로 측정수 m 은 정밀
화시켜야 할 변수 P 보다 상당한 배수로 많아야 정확한 결과가 기 대된다. 대개의 경우 3 차원 X- 선 데이터의 경우 m/ p (m l P 를 과잉으로 결정해야할 비율〔 overde t erm i na ti on ra ti이이라 부름)는 5~ 10 의 범위에 있다. 불행하게도 (8- 1 ) 식을 각각의 변수에 대해 미분하여 구한 식은 삼각 향수와 지수함수를 포함한다. 그러나 간단히 최소 자승법에 적용하려면 선형 방정식이 필요하다. 만약 합리적인 시험 구조(t r i al s t ruc t ure) 를 얻었으면 파라미터 그 자체보다 변수를 시험 파라미터에서 이동시 키는 일련의 선형 방정식을 얻을 수 있다. 이것은 시험 파라미터를 Ta y lor 함수로 전개함으로써 가능하다. 이 경우 1 차 미분항을 두 고 2 차, 3 차 미분항은 무시하고 한다. 6. IFc l= aFc/ a x1•6 .x1 +a l Fc l!a Y 1'6Y1+ …… + a IFe IIab33,n·6 .b3 3,n (8-2) 이 가정의 정당성은 시험 구조가 올바른 구조에 얼마나 접근하는 가에 달려 있다. 이 가정이 정당하지 못하면 (8-2) 식은 정확하지 못하고 최소 자승법 계산은 올바른 해에 해당하는 최소값으로 접근 하지 않고 틀리는 해의 최소값으로 수령한다. 따라서 최소 자승 정 밀화 과정의 성공 여부는 시험 구조가 올바른 것, 죽 합리적인 위 상각을 가진 구조 인자의 데이터가 있느냐 없느냐에 달려 있다. 최소 자승 방정식이 선형이라 가정을 했으므로 정밀화 단계가 수 령하려면 몇 회 계산을 해야 한다. 근사적으로 올바른 구조의 차의 함수가 되는 2 차 이상의 미분항을 무시했기 때문에 최소 자승 방 정식이 선형이라는 가정은 올바른 해에 접근할수록 타당하게 된다. 최소 자승법에서 사용한 모델이 옳지 못하거나 부분적으로 틀리 거나 하면 이 모델이 옳지 못하거나 부분적으로 틀린 증거가 항상 있게 된다. 죽 오차지수 R 은 납득할 수 있는 값으로 떨어지지 않 으며 파라미터에서 이상함을 볼 수 있다. 톨리는 원자가 초기의 시
험 구조에 잘못하여 포함되어 있으면 이 원자는 화학적으로 불합리 한 위치로, 예컨대 다른 원자에 너무 가까운 위치로 옮겨지거나 온 도 인자의 크기가 보통의 올바른 원자의 온도 인자의 크기에 비해 너무 커져서 납득할 수 없게 된다. 이 큰 온도 인자의 크기는 물리 적으로는 대단히 큰 진동진폭에 해당된다. 즉 시험 구조에 가정한 위치에 실제 구조에는 원자가 없다는 것이 확실하게 된다. 최소 자승 정밀화 과정이 완결된 단계에서 전자밀도 차의 Four i er 지도를 계산하는 것이 현명하다. 설험오차 범위내에서 피 크가 없고 평평하고 거의 영이면 최소 자승법에서 구한 해는 합리 적인 해이다. 그렇지 못하면 차의 Four i er 지도의 피크는 구조 인 자 계산에서 포함시키지 않는 가벼운 원자에 해당되는 피크가 아닌 다른 피크가 있으면 최소 자승법 계산은 처음 가정한 구조가 옳지 않음이 분명하고 새로운 근사 구조를 구하여 정밀화 계산을 다시 해야한다. 4 결정구조 해석의 개요 x- 선 회절법으로 결정구조를 해석하는 단계는 다음과 같이 요약 할수있다. (1) 적합한 단결정을 얻거나 성장시킨다――이 단계는 어떤 경우 는 어렵고 따분한 단계이다. 이상적인 결정의 크기는 대략 칙경 0.2~0.3mm 이다. (2) 단위세포의 치수와 공간군을 결정한다. 단위세포의 치수는 기 록한 회절 패턴의 위치, 간격을 측정하여 결정할 수 있다. 공간군 은 회절 패턴의 대칭과 계통적 소멸에서 구할 수 있다. (3) 결정의 밀도를 부유법 등의 방법으로 측정한다. 단위세포당 함량과 분자의 실험식량을 계산한다.
(4) 구조결정을 진행할 것인지 안할 것인지를 결정한다. 구조결정 울 하려면 많은 노력을 두자해야 할지 모르고 또 구조를 못풀 경우 도 있다. 따라서 풀려는 구조가 홍미가 있는가 또 결정은 단결정이 아니고 복결정은 아닌지 동을 회절 패턴을 보고 결정해야 한다. 단 결 정이 아니면 다른 결정을 구해야 한다. (5) 회절 데이터 를 수집한다. 4 축 단결정 회절 장치로 회절 데이 터 를 수집하거나 X 갓 ! 사진법을 이용하여 회철 패턴을 얻는다. 회 절 강도는 육안으로 측정하든지 계수기나 밀도계를 써서 측정한 다. 회절 강도를구조인자 |Fl 로바꾸기 위하여 여러 가지 기하학 적 인자를 곱하거나 평균을 구하거나 해야 한다. 이러한 데이터를 수집하는 데 걸리는 시간은 사용할 수 있는 장치와 경험 등에 달려 있는데 하루나 이틀 때로는 일주일에서 이삼 주일 걸린다. 이후의 데이터 처리는 컴퓨터를 사용하여 행한다. (6) 시험구조와 대략의 위상을 구하도록 한다. 보통 방법은 적철 한 컴퓨터 프로그래밍을 써서 직접법으로 풀든지 3 차원적 Patt er son 지도를 써서 중원자법으로 중원자의 위치를 구한다. (7) 만족스러운 구조는 화학적으로 합리적이고 측정한 구조 인자 (Fo) 와 계산한 구조 인자 (I Fe |)가 찰 일치해야 한다. 따라서 최속 자승법으로 구조를 정밀화시켜야 하고 전자밀도 차의 지도를 보고 시험구조의 위치 및 열적 인자가 합리적인지 또 발견하지 않은 다 른 피크가 있는지 검토해야 한다. 최종 전자밀도의 차의 지도는 평 평하고 피크가 없고 오차 인자 R 값은 합리적으로 낮아야 한다. 또 최종 구조는 화학적으로 합리적이어야 한다. 죽 이상한 결합길이나 각도, 분자간 거리가 없어야 한다. 결합 안된 분자간 거리가 짧아 서는 안된다. 분자의 기하학적 배치, 충전 등에 이상이 없어야 한 다. (8) 광학적으로 활성이 있는 물질을 성공적으로 구조 해석을 하면 구조의 절대 배열을 결정할 수도 있다.
연습문제 1. (a) 어떤 화합물은 15 개의 원소로 구성되고 각각 원소의 위치 (x, y, z) 와 이방성 열적 파라미터, 점유수二 모두를 정밀화 작업 울 하였다면 척도 인자 (scale fa c t or) 를 포함한 총 파라미터수는 몇 개이냐, 관찰한 독립적인 반사 (I>3 CJ (D) 가 모두 1150 개라면 과잉으로 결정해야 할 비율 (overde t erm i na ti on ra ti o) 은 얼마인 가? (b) 위의 (a )ol]서 점유수 인자는 각각 원자에 대해 모두 1 개로 고 정되어 있다. 또 열적 인자는 등방성 열적인자로써 정밀화하였 다. 이 경우에는 총 파라미터수는 몇 개이며 과잉으로 결정해야 할비율은 얼마인가? (c) (b 펴 경우 15 개의 원자 중 하나는 위치 파라미터를 대칭성 때문에 원자 좌표를 X, X, X 로 정밀화시켰다. 이 경우 총 변수 의 수는 몇 개이며 과잉으로 결정해야 할 비율은 벌마인가? 2. 어떤 염소 화합물은 단위세포당 4 분자가 포함하고 사방정계를 하고 있고 a=7.210(4) A, b=l0.43(1) A 및 c=15.22(2) A 이다. 그리고 염소 원자의 좌표는 디음과 같다. 1/4, y, z ; 3/4, y, z ; 1/4, 송+y, ½+z ; 3/4, ½-y, ½+z 여기서 y= 0.140(2) z=0.000(2) 이다. 가장 짧은 Cl… … Cl 거 리와 이 거리의 추정 표준편차 (es ti ma t ed sta n dard dev i a ti on) 를 구궁}라.
제 9 장 X-선 분말회절법에 의한화학분석 l 서론 물질은 순수한 상태에 있든지 혼합물의 구성원으로 존재하든지 간에 항상 특성적인 회절 패턴이 있다. 이 사실로부터 X_ 선 회절 법을 화학 분석에 사용할 수 있음을 알 수 있다. 정성 분석은 그 물질의 패턴을 확인함으로써 이루어질 수 있다. 혼합물에서 한 물 질의 회절선의 강도는 시료내에서 그 물질의 함량에 비례하므로 정 량분석도가능하다. X 선 회절의 이점은 성분 화학원소로써가 아니라 화합물로써 그 물질의 존재를 확인할 수 있는 데 있다. 예컨대 시료가 화합물 A g Cl 를 포함하면 X 선 회절법은 A g Cl 의 존재를 확인할 수 있 다. 그러나 보통 많은 분석법은 A g와 Cl 원소의 존재만 확인한다. 회절 분석의 응용은 같은 물질의 여러 가지 동소체를 구별할 수 있 는데 있다. 예컨대 고체 석영 (S i 02) 은 무정형 S i 02 와 여섯 가지 다른 종류의 결정체가 있는데 X- 선 회절 패턴은 이 일곱 개의 형 이 모두 다르다. 따라서 회철 분석은 원소의 화학적 결합 상태를 알고자 할 때 유용하다. X- 선 회절법은 광물, 점토, 내화물, 합 금, 부식 생성물, 공장의 먼지와 같은 물질도 분석할 수 있다. 보 통 다른 화학적 분석과 비교하여 X- 선 희철법은 훨씬 빠르고국 소
량의 시료만 필요하고 또 비파괴적 방법이다. 2 X- 선 회절 패턴 물질의 X 선 분말 회절 패턴은 물질에 따라 독특한 패턴을 주고 물질을 확인하는 지문과 같은 역할을 한다. 입방체 결정의 회절선은 s i n 내가 다음 식을 만족하는 회절선을 준다. 이 식은 (5-21) 식과 Bra gg식에서 얻을 수 있다. h2s+i nk 22 8+ [2 = sins 2 8 =EA7 (9-1) s=h 탸닫 +P은 항상 정수이고 112 I4a2은 임의의 하나의 패턴에 대해서는 일정한 값을 가지므로 입방체 물질의 패턴에 지수롤 붙이 는 문제는 일련의 정수 s 를 찾으면 된다. 관측한 s i n20 의 값을 s 값으로 나누면 일정한 값이 된다. s 값은 구조 인자 계산 결과에서 얻은 표 1 을 보면 쉽게 구할 수 있다. s 값으로 가능한 수는 디음 과같다. 단순 입방정계 : 1, 2, 3, 4, 5, 6, 8, 9, 10, 11; 12, 13, 14, 16 체심 입방정계 : 2, 4, 6, 8, 10, 12, 14, 16 면심 입방정계 : 3, 4, 8, 11, 12, 16 다이아몬드 입방체 : 3, 8, 11, 16 X 선 분말 회절 패턴의 지수를 붙이고 입방체의 격자를 붙이는 방법을 예를 들어서 생각해 보자. 이 예에서는 CuKa 복사선을 사용하여 여덟 개의 회절선을 얻었다. 여덟 개의 회절선의 s i n 냉 값은 표 1 에 나타내었다. s i n20 값을 s 값으로 나누어서 일정한 값 을 얻으려면 s 값은 결정할 수 있고 이 일정한 값에서 단위세포 길
이 a 와 hkl 값을 쉽게 계산할 수 있다. a 값의 계통적인 오차는 표 l 에서 0 가 커지면 감소한다. 따라서 격자상수 a 값을 가장 높 은 0 의 회절선 값인 여덟번째 선의 값 3. 62 A . 이라 결정할 수 있 다.
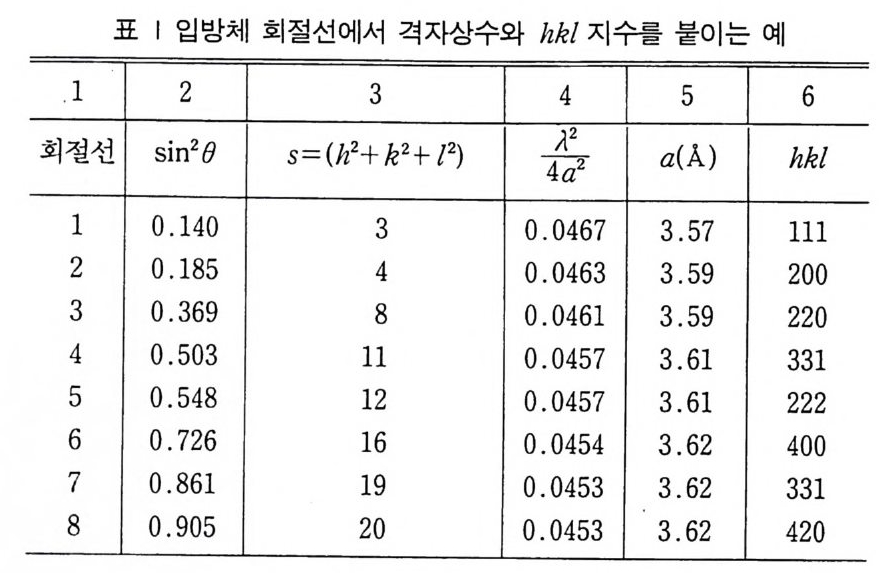 표 | 입방체 회절선에서 격자상수와 hkl 지수를 붙이는 예
표 | 입방체 회절선에서 격자상수와 hkl 지수를 붙이는 예
회절선을 관찰하여 어떤 회절선이 측정되고 어떤 회절선이 측정 안되는지를 파악함으로써 Bravais 격자형을 결정할 수 있다. 표 1 울 보면 모든 회절선의 지수는 홀수, 짝수가 섞여 있는 것을 알 수 있고 지수가 섞여 있지 않은 100, 110 선은 빠져 있음을 알 수 있 다. 표 1 에서 관측되거나 관측 안되는 반사와 Brava i s 격자의 관 계에서 표 1 의 입방체는 면심 입방격자임을 알 수 있다. 입방체의 x- 선 분말 회절선의 패턴은 쉽게 입방체가 아닌 것도 구별할 수 있다. 입방체가 아닌 결정은 훨씬 많은 선을 가지고 있다. 더욱이 Bravais 격자형은 그림 1 과 같이 구별 가능하다. 단순 입방정계는 체심 입방정계나 면심 입방정계에 비해 훨씬 많은 회절선을 가전 다. 면심 입방정계는 하나의 선이 존재한 후 잇달아서 두 개의 회
절선이 있고 다시 하나가 있고 또 두 개의 회절선이 있고 하는 유 형의 패턴을가전다. 정방정계의 분말 회절 패턴에 대해 생각해 보자. 정방정계에서 평면간의 간격 d 는 두 개의 미지 파라미터 a 와 c 를 포함하고 있 다.
 입방체
입방체
l/d 드 Ui2 + k2)/a2+ z2;c2 (9-2) 따라서 l/d 드 1/a2 〔 h 프 k 도/2/ (c/a) 가 혹은 2log d= 2log a-log [ (h2+ k2)+ /2( c/a )2] (9-3) 정방정계의 두 평면에 대해 (9-3) 식을 쓰고 두 식의 차를 구하 면 다음과같다. 2log d1-2log d2=-log [ (hi2 + 軒)+ 112/( c/ a) 기 +log [(hi+ 尉)+ ll/(c/a) 기 (9-4) (9-4) 식에 의하면 어떤 두 평면에 대해 2lo g d 값의 차이는 a 에 는 무관하고 c/a 의 비와 각 평면의 지수 hkl 에만 의존한다. 이 사실을 Hull 과 Dave y가 사용하여 정방형 결정의 회절 패턴을 정 하는 데 사용하는 도식법을 고안하였다. Hull 과 Dave y그림은 그림 2 에서 보여주고 있다. 먼저 어떤 특정한 hkl 평면에 대해 〔( h 탸 k2)+l2/(c/a) 기과 c/a 를 세미로 그 (sem i log) 종이에 그린다. 다른 평면 지수를 가지나 평면 사이 의 간격이 같은 것, 예컨대 (100) 와 (010) 는 그림상에 같은 곡선 으로 나타내며 이 둘 중 하나의 지수로 표시되며 여기서는 (100) 로 표시되어 있다. l=O 인 곡선은 c/a 축에 평행인 직선으로 나타나 있다. 도표와 눈금은 다음 방법으로 지수를 붙인다. 회절 패턴의 각 선 에 상당하는 평면의 d 값을 연필로 표시하자. 그림 2 의 1 위치에 d 눈금의 값을 옆으로 놓아두고 측정한 d 값을 연필로 표시하자. 그림 2 의 1 위치의 종이조각 위에 표시한 모든 점이 각각 Hull-Daver y도표의 곡선과 모두 일치하는 장소를 찾는다. 그림
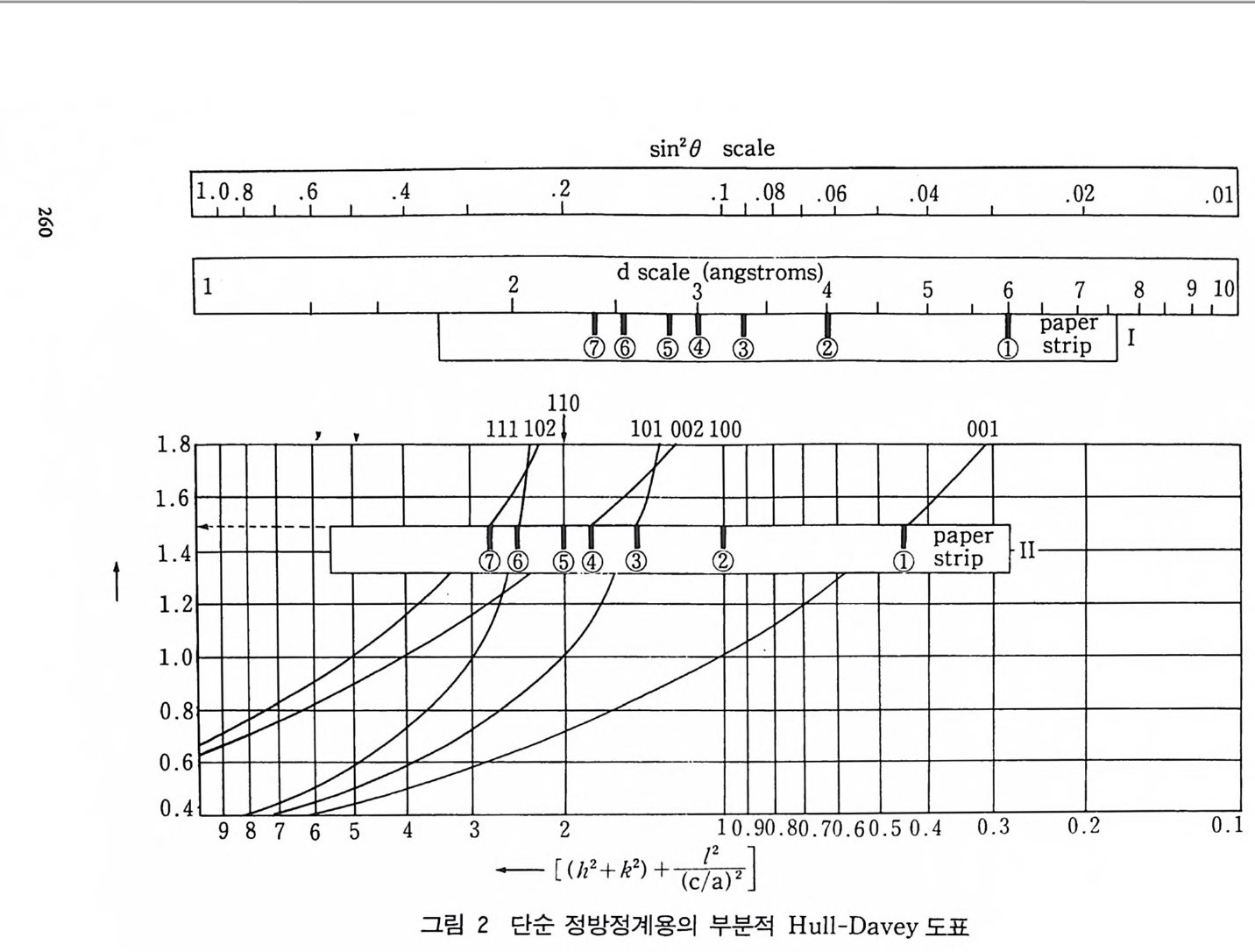 4 4
4 4
2 의 II 의 위치와 횡축의 c/a 값을 구한다. 예에서 c/a= l. 5 이 다. 또 패턴의 첫번째 선은 001 선이고 두번째는 101 선이다. 모든 선을 이러한 방법으로 지수를 붙이면 큰 각을 가지는 d 값에서 (9_2) 식의 연립방정식을 풀어서 a 와 c 를 구한다. 이 값에서 그래 프에서 구한 c / a 값보다 더 정확한 c/a 비를 구할 수 있다. 3 분말 X- 선 회절 무늬의 강도 계산 Deb y e-Scherrer 카메라로써 회절 무늬를 측정할 때 회절 강도 는 전술한 6 장에서 나타낸 바와 같이 근사적으로 디움 식으로 표 시할수있다. I= I F 12P[(l+ cos2 2 0)/(sin 2 2 0 cos 0)] (9-5) 여기서 I 는 상대적 적분강도 F 는구조 인자이며 p는디중도 O 는 Bra gg각도이다. (9-5) 식을 이용하여 Cu Ka 복사선으로 Cu 의 회절 패턴을 Deby e -Scherrer 카메라로써 측정할 때 예상되는 회절선의 상대적 강도와 위치를 구해 보자. Cu 는 면심 입방격자이므로 hkl 이 섞이 지 않는 지수, 죽 111, 200, 220, 311, 222, 400, 331, 420 …… 일 때는 회철 무늬를 가질 것으로 예상되고 구조 인자는 제 7 장에 서와 같이 F=4 fc u 일 것이고 hkl 이 혼합될 경우 구조 인자 F 는 영이다. 측정한 회철 강도와 계산한 강도 사이는 서로 잘 부합된다. 여기 서 다중도 P 는 회절선 강도의 중요한 조절 역할을 함을 알 수 있 다. |Fl2 과 Lorentz 편광 인자는 0 값에 따라 서서히 변한다. 그
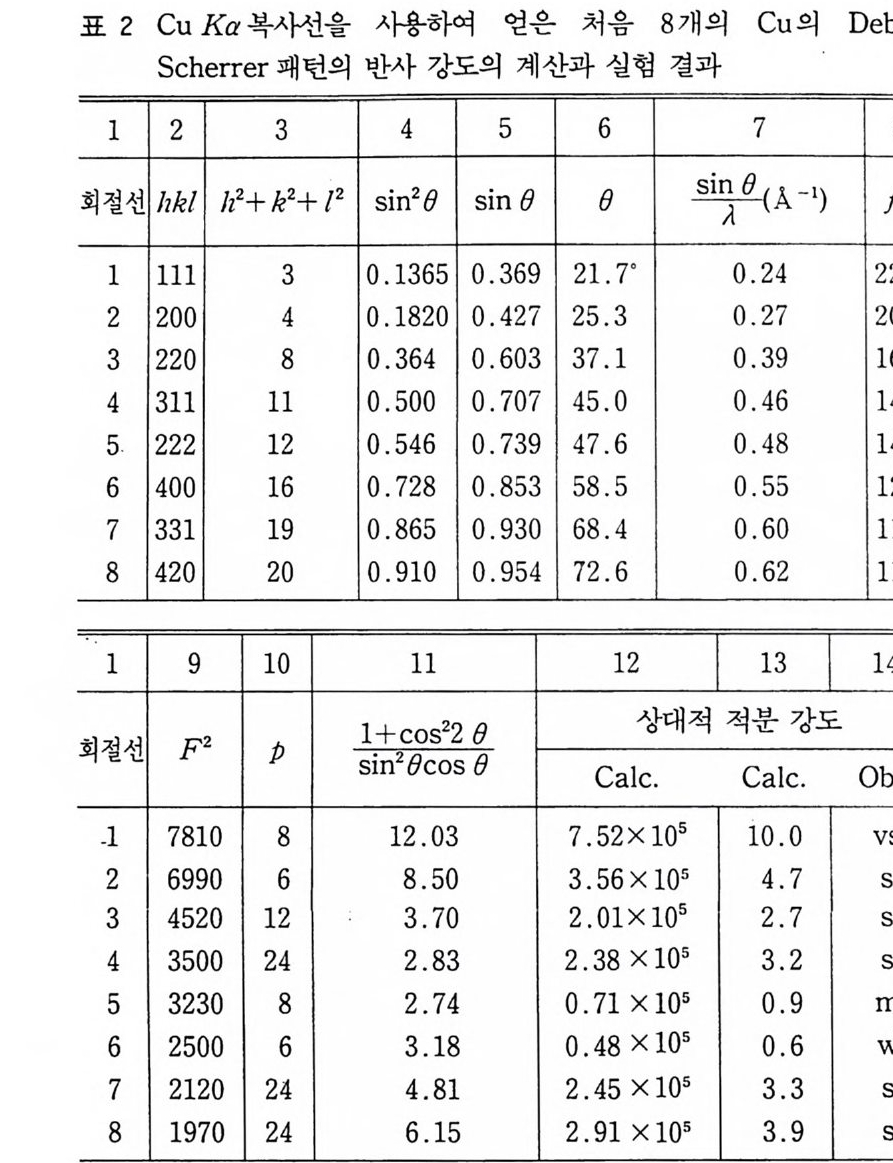 표 2 Cu Ka 복사선을 사용하여 얻은 처음 8 개의 Cu 의 Deby e -
표 2 Cu Ka 복사선을 사용하여 얻은 처음 8 개의 Cu 의 Deby e -
4 번째 세로줄 : 입방체 결정에 대해 s i n 냉 값은 다음과 같다. sin 2 8 =,~12 ( h2+ k2+ z2) 여기서 사용한 Cu Ka 선의 파장= 1. 542A 이고 구리의 단위세포 상수 a=3. 61 5A 이다. 따라서 (111) 반사에 대해
아 / 4a2) (l유 나 ?2+ /2) = [l.54 22/(4X 3 .61 52)] X 3=0 .1365 이고 이 값 이 (lll) 반사에 대한 s i n28 이다. 6 번째 세로줄 : Loren t z- 편광인자와 sin 0/11 계산에 필요함. 8 번째 세로줄 : 부록 5 에서 얻을 수 있다. 9 번째 세로줄 : F2= 16/cu2 에서 구할 수 있다. 10 번째 세로줄 : 부록 4 에서 얻을수 있다• ll 번째 세로줄 : 이 값은 (9-5) 식에 의해 9, 10, ll 번째 세로줄 값을 서로 곱하여 얻을 수 있다. 13 번째 세로줄 : 가장 강도가 센 반사인 (lll) 반사를 10 으로 두고 상 대적으로 구한 반사 강도이다. 14 번째 세로줄 : 측정 한 강도임. VS = 대단히 강하다, s= 강하다, m= 중간 정도의 강도다. t v= 약한 강도다. 러나 P 값에 따라서 I 값은 매우 불규칙하게 된다. 좀 더 복잡한 예, 죽 ZnS 를 예를 들어 X- 선 회절선의 강도와 위치 를 계산해 보자. ZnS 는 입방정계에 속하고 격자 파라미터는 5.41 A 이다. Cu Ka 복사선을 사용하여 얻은 처음 6 개의 Deby e - Scherrer 패턴의 상대적 강도를 계산해 보자. ZnS 는 단위세포당 네 개의 황원자를 가지고 있고 다음 위치에 위치한다. Zn : (1/4, 1/4, 1/4; 1/4, 3/4, 3/4; 3/4, 3/4, 1/4; 3/4, 1/4, 3/4) S : (0, 0, O; 0. 1/2, 1/2; 1/2, 0, 1/2; 1/2, 1/2, 0) 따라서 ZnS 의 구조는 면심 입방정계이다. ZnS 의 구조 인자를 계산하면 다음 결과를 얻을 수 있다. h, k, l 가 혼합된 지수를 가 지면 구조 인자는 영이다. h, k, l 이 혼합되지 않는 지수, 죽 모 두 찍수거나 모두 홀수이면 F= 산fs + fz n exp (7ri( h+k+l )/2 )] (9-6)
x- 선의 회절 강도는 |Fl2 에 비례하므로 |Fl2 울구해 보자• I F 12=16 伊+fz n exp (7ri( h + k+ l)/2 ) ][ I s + f zn exp (-7ri (h+ k+ l)/2 ) ] =4[//+ f z/ +2/sfz ,, COS (7r(h+k+ l)/2 ) ] (9-7) 따라서 h+k+l=Z n+ l 이면, |Fl 2 =l6[// + /감 ] (9-8) h+ k+ l=2(2n+ 1) 이면, | F 12= 16 岳― /~ , .]2 (9- 9) h+k+l=2·2n 이면, |F12 = 16[/s+ fz 군 (9-10) 반사 강도를 계산하면 표 3 과 같다.
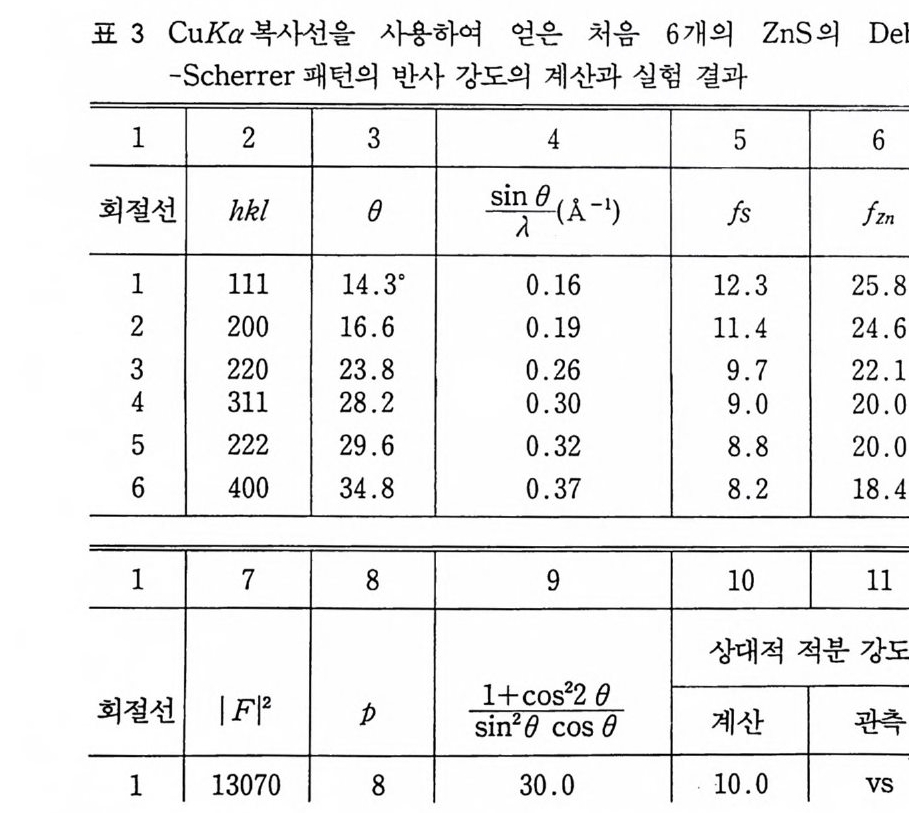 표 3 CuKa 복사선을 사용하여 얻은 처음 6 개의 ZnS 의 Deby e
표 3 CuKa 복사선을 사용하여 얻은 처음 6 개의 ZnS 의 Deby e
 2 2790 6 21. 7 1. 2 w
2 2790 6 21. 7 1. 2 w
3 번째 세로줄 : 입방체 결정이므로 (111) 반사에 대해 O 는 디음과 같 이 계산할수 있다. sin 2 0 = 112 (h 2+ k 댜 /2)/ 4 a2= 1. 5 422( 1 2 + 12+ l2)/4 ( 5 . 41)2 =0 .0 6 093 따라서 s i n0=0. 24 68 이고 0 = 1 4. 30 이다. 5 번째 및 6 번째 세로줄 : 부록 5 에서 구할 수 있다. 7 번째 세로줄 : (9- 8) , (9- 9) , (9-10) 식을 사용하여 구할 수 있다. ( 111 ) 반사에 대해서는 (9 - 8) 식을 사용하여 계산할 수 있고 (220) 반사 는 (9-10) 식을 사용하여 계산할 수 있다. 10 번째 줄과 11 번째 세로줄 : 계산한 회절 강도와 측정한 강도는 상호 잘 일치한다. |Fl 2 과 P 는 0 의 변화예 따라 불규칙하게 변화하므로 계산한 회절 강도는 0 의 변화에 따라 불규칙하게 변한다. 분말법에서 툴 리는 M ill er 지수를 가지는 두 세트의 평면은 필름에 같은 점에서 반사할 수 있다. 예컨대 입방정계에서 평면 (411) 과 평면 (330) 는 (h2 + k2+ 12) 값이 같아서 같은 평면 간격을 가지고 있다. 또 정방정 계에서 평면 (501) 과 평면 (431) 는 같은 (h 2 +k 2)과 F 를 가전다. 따 라서 같은 평면 간격을 가진다. 이 경우에는 각 반사의 강도를 따로따 • 로 계산하여야 하고 이 두 개의 반사는 틀리는 중첩도와 구조 인자를 가지므로 각각 강도를 합쳐서 회절선의 총강도를 구해야 한다. 4 정성 분석 물질의 회절 패턴은 그 물질의 특성으로서 물질을 확인할 수 있 는 지문(fi n g er pr in t ) 역할을 할 수 있다. 우리가 많은 물질의 회
절 패턴을 가지고 있으면 미지 시료의 회절 패턴을 얻어서 우리가 가지고 있는 다른 많은 물질의 회절 패턴과 미지 시료의 회절 패턴 과 비교하여 미지 물질을 확인할 수 있다. 그러면 우리가 가지고 있는 패턴은 상당히 많아야 하겠다. 필요한 것은 알려질 물질을 계 통적으로 분류하여 미지 시료의 회절 패턴과 같은 것을 빨리 찾아 야 하겠다. 이러한 계통적 방법은 1936 년 Hanawal t가 고안하였 다. 분말 패턴은 회절 무늬의 20 위치와 상대적 회절 강도 I 로써 특징지을 수 있다. 회절 무늬의 각도의 위치는 사용한 파장에 따라 다르므로 보다 기본적인 양은 평면 사이의 거리 d 이다. 따라서 Hanawal t는 회철 패턴을 회절선의 각 I 와 d 로 나타내기로 하였 다. 또 알려진 패턴에서 d 값이 감소하는 순서로 정리하였고 분말 회절 패턴은 Hanawalt, R i nn 과 Frevel 이 처음에 1,000 여 종의 물질을 분류하여 정리하였고 그 후 1941 년에서 1969 년까지 Americ a n Socie t y for the Testi ng Mate ria l (ASTM) 에서 새로 운 회절패턴을 모아서 분류하였다. 1969 년 이후엔 Joi n t Commi t- tee on Powder Di ffrac ti on Sta n dard (J CPDS) 에서 미국, 캐나 다, 영국, 불란서 등의 학회의 도움으로 이러한 업무를 관장하였고 1981 년까지 30,000 여 개의 회절 패턴을 분류 정리하였고 매년 약 2,000 개의 패턴이 첨가된다. 이들 물질로는 원소, 합금, 무기물 질, 광물, 유기물질, 유기금속물질 등이 있다. 1) Hanawalt 법 Hanawal t는 회절 강도가 가장 강한 세 개의 회절선의 d 값을 d1, d2, d 로 표시하고 이들의 상대적 강도도 같이 표시하여 미지 시료의 패턴과 표준 물질의 패턴을 비교하여 미지 시료의 성분을 알아낼수있다. 전형적인 J CPDS 카드를 표 4 에 나타내었다. 이 카드는 유기 부 분, 무기 부문으로 분류되어 있다.
2) Fin k 법 데이터 파일을 찾는 F i nk 법은 강도보다는 d 값에 의존한다. 이 방법은 원래 전자회절 패턴에 사용하려고 고안되었고 여기서 관측 한 선의 강도는 항상 구조와 직접 관련되지 않으므로 확인하기 위 한 신빙성 있는 방법은 아니나 F i nk 법으로 찾는 방법을 기록한 책은 무기물질만 수록되어 있고 각 물질에 대해 여덟 개의 강한 회 절선이 기록되어 있다. 3) 정성 분석 실험 절차 미지 시료의 확인은 회절 패턴을 얻는 데에서 시작된다. 시료는 미세한 알맹이로 만들어야 한다. 상대적인 선 강도는 어느 정도 사 용한 파장에 의존한다. 관측한 패턴을 틀리는 파장으로 만들어진 데이터 파일의 패턴과 비교해야 함에 유의해야 한다. 파일의 대부분 패턴은 Fe 화합물을 제의하고는 Cu Ka 복사선을 써서 만들었다. 패턴은 Deby e -S cherrer 카메라나 회절 장치나 기타 다른 방법 울 써서 기록할 것이다. 여기서 다시 선 강도는 사용한 장치에 따 라 다름에 유의해야 한다. Deby e -Scherrer 패턴에서는 회절 장치 (d iffr ac t ome t er) 에서보다 흡수 효과 때문에 높은 각도의 회절선의 강도를 낮은 각도에 비해 크게 한다(회절 장치에서는 흡수 인자는 0 각에 무관하다). 미지시료의 패턴을 얻은 후 패턴상의 각선의 d 값을 계산한다. 상대적 회절선의 강도는 보통 육안으로 검토하여 얻는데 가장 강한 선을 100 으로 두고 가장 약한 것은 10 혹은 5 로 두고 추정한다. 실험적으로 얻은 d 와 1/11 값의 표를 얻으면 미지 시료는 다음 순서로확인할수있다. (I) 수치 색인집에서 적절한 d1 그룹을 찾고 (2) 두번째 큰 강도인 d~ 과 맞추도록 책의 d 값의 두번째 값을
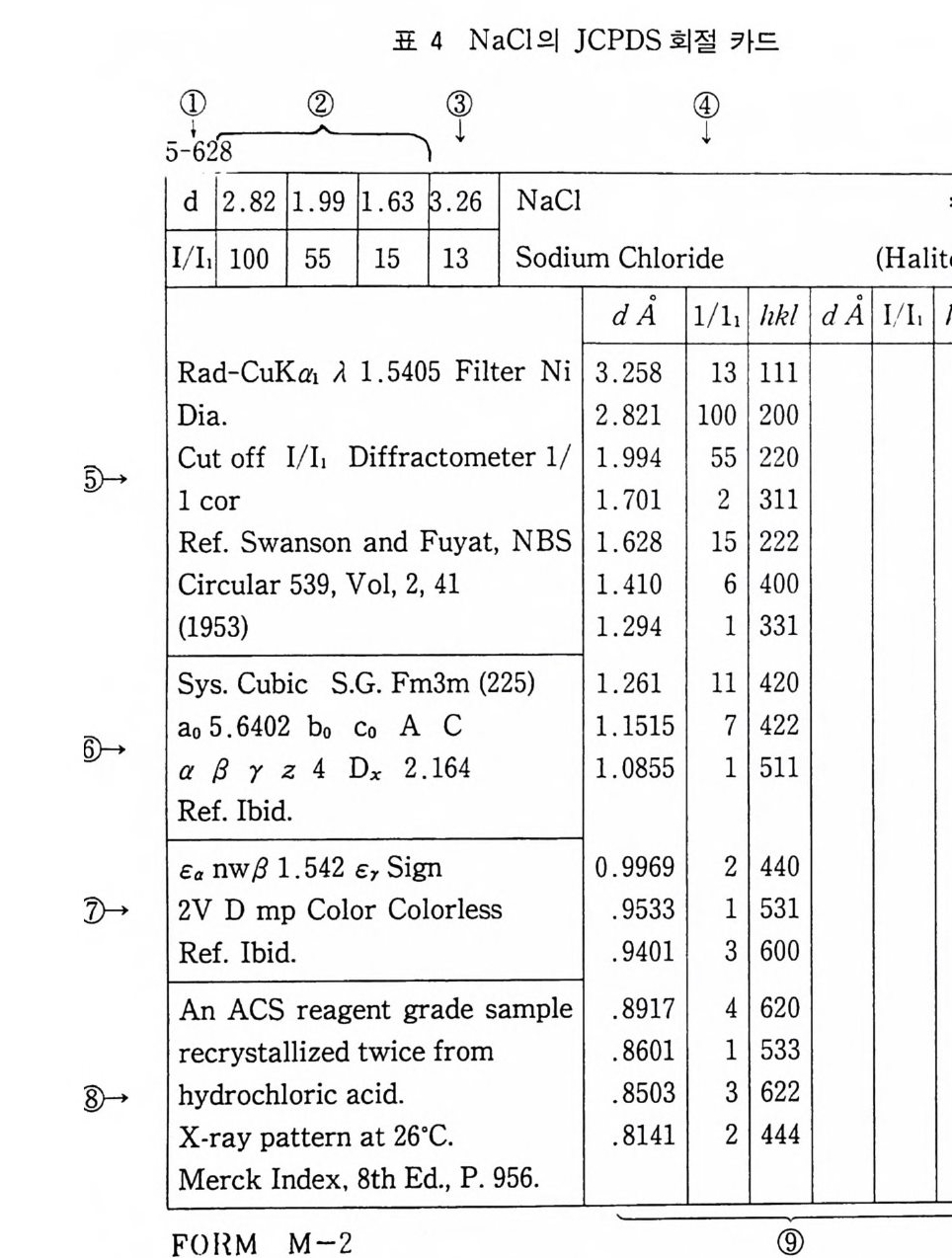 표 4 NaCl 의 JC PDS 회절 카드
표 4 NaCl 의 JC PDS 회절 카드
카드에 나타나 있는 것은 ®파일번호 ®세 개의 가장 강한 회절선 ® 가장 낮은각도의 선 ®화학식과물질 이름 ®사용한회철법 ®결정
학적 데이터 ® 광학적 데이터 ®시료에 관한 데이터 ®회절 패턴 강 도는 가장 강한 선에 대한 강도의 퍼센트로 나타나 있다. 대개의 카드 는 카드의 위쪽 오른쪽 구석에 데이터의 질을 표시하는 기호가 있다. * (질이 좋은 데이타) i(지수를 붙인 선이 있고 강도는 신빙성이 있다) c( 계산할 패턴이다) o( 신빙성이 적다). 물질은 알파벳 순으로 목록되 어 있다. 읽고 비교해 본다. 실험치와 책의 값을 비교함에 있어 두 값에 각 각 士 0.01 A 의 오차는 허용해도 좋다. (3) di, d2, d값 을 비교한 후 표의 상대적 강도를 비교해 보라. (4) 상대적 강도 I/11 과 d 값이 서로 잘 맞으면 미지 시료의 정성 분석은끝난것이다. 4) 정성 분석의 예 (a) 단일물질의 정성 분석 미지 시료가 혼합물이 아니면 분석은 간단하고, 예컨대 표 5 를 미지 시료의 d 값과 강도라고 하자. 이 데이터는 Cu Ka 로써 Deb y e-Scherrer 카메라를 써서 얻었다. 선의 강도를 육안으로 측 정하여 결정하였다. di, d2, d~ 실험치는 각각 2.82, 1.99 , 1.63 A 이다. J CPDS 카드집의 색인에서 d1 값이 2.84-2.80 A 그 룹에서 d2=1 .99 A 를 가지는 물질은 열일곱 개 있으나 열일곱 개 중 네 개가 d1=2.82 A 이었다. 이 4 개의 데이타를표 6 에 나타내 었다. 이 네 개 중 NaCl 만 d3=1 .63 A 이다. 또 이 물질의 강도가 강한 3 개의 회절선의 강도는 미지 시료의 실험치가 찰 일치함을 알 수 있다. 따라서 파일 번호 5 - 628 에 보면 NaCl 의 패턴과 미 지 시료의 패턴이 거의 일치하여 NaCl 이라고 확인할 수 있었다. 단지 상이접은 다음과 같다.
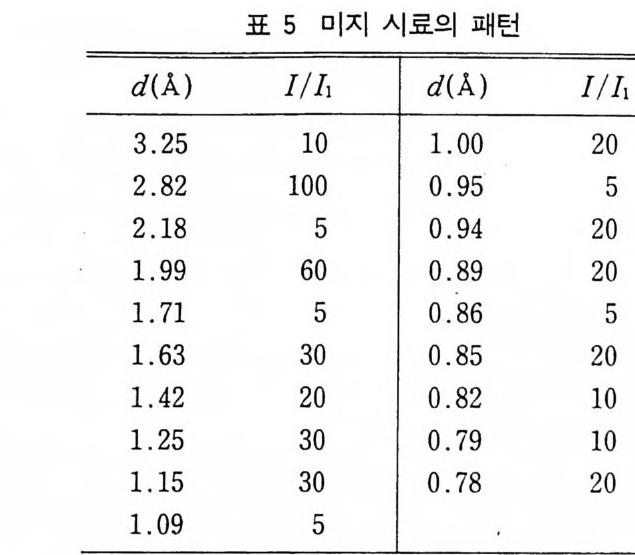 표 5 미지 시료의 패턴
표 5 미지 시료의 패턴
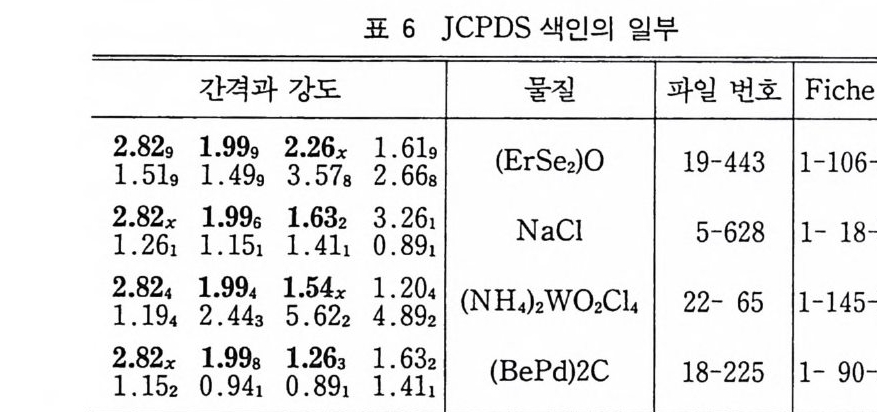 표 6 JC PDS 색인의 일부
표 6 JC PDS 색인의 일부
세 개의 회절 강도가 큰 d 값은 고딕체로 씌어 있다. (1) 파일 카드에 없는 d=2.18A 을 관찰하였다. 이것은 필터 로부터 제거 못한 CuKa 에 의한 220 반사임을 (iz!) sin 2 0p = sin 2 0a 관계식에서 (iz!)=l. 2 이므로 이 식에 만족함으로써 알 수 있었다. (2) 331 선 (d= l. 294 A) 이 카드에는 있는데 관찰하지 못했다.
그러나 이것은 강도가 낮은 반사였다. (3) d=0 . 79 와 0.78A 이 실험에는 관찰되었으나 파일에는 없 었다. 이것은 711-511 과 640 선으로 지수를 붙일 수 있는 회절선 이나 이것은 표준 카드의 444 선 다음에 있는 회절선으로 표준 카 드에서 명시하지 않은 것아 분명하다. (4) 다섯번째 회절선 이후에 Deby e -Scherrer 패턴이 회절 장치 로써 얻은 파일의 회절선보다 강도가 강했다. 이 차이는 흡수 효과 때문이라 생각된다. 이러한 차이를 이젠 이해할 수 있기 때문에 시 료는 NaCl 이라고 결론지을 수 있다. (b) 혼합물의 정성 분석 혼합물의 분석은 복잡하나 불가능한 것은 아니다. 표 7 의 미지 시료의 회절 패턴은 Cu Ka 복사선을 써서 회절 장치로서 얻었다. 세 개의 강한 강도를 가지는 d 값은 d1=2.09A, d2=2_.47A 및 d3= l .80 A 이다. 수치 색인표에서 2.09 와 2.0A 사이의 d1 그룹 에 속하는 d 값을 검토하여 d2 값이 2 . 47A 인 것울 보면 미지 시료 의 세 개의 d 값과 맞는 것은 찾아볼 수 없다. 이것은 미지 시료가 혼합물임을 암시한다. 가장 강한 d 선, d1=2.09A 과 두번째 강한 d 선, d2=2 , 47A 이 서로 다른 물질의 d 값이라고 생각하면, 죽 d1=2.09A 이고 d2=l .80 A 이 한 물질의 d 값이라면 파일번호 4-0836 의 구리 (Cu) 의 세 개의 d 값과 잘 일치한다. 죽 미지시료 의 패턴은 표 7 에 별표(*)를 붙인 것과 Cu 인 d 값과 찰 일치한 다. 한 물질이 Cu 이고 디론 회절선의 d 값에 해당하는 물질을 찾아 야겠다. 표 9 는 Cu 의 d 값을 뺀 나머지 부분의 d 값이고 가장 강 한 강도를 가진 d 값을 100 으로 만들기 위해 규격화 인자 1. 39 를 곱하였다. 다시 수치 색인표에서 보면 이 물질은 표 8 의 Cu20 의 패턴과 잘 일치한다. 죽 미지 시료는 Cu 와 Cu20 의 혼합물이다.
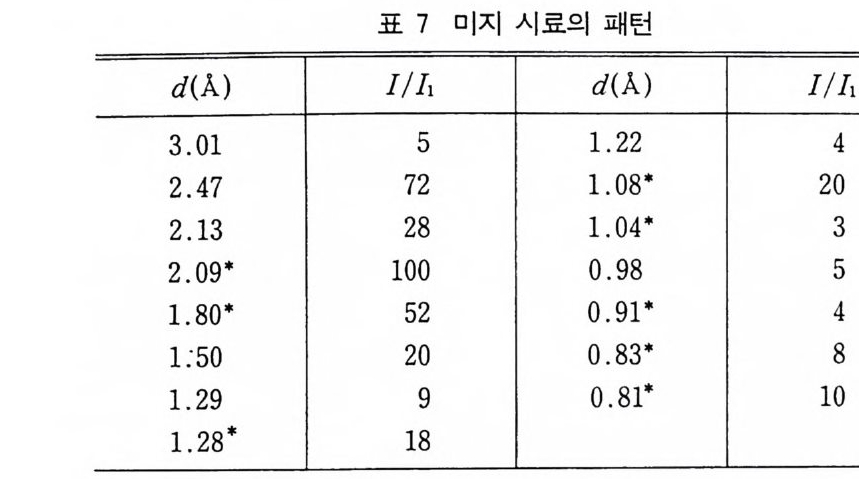 표 7 미지 시료의 패턴
표 7 미지 시료의 패턴
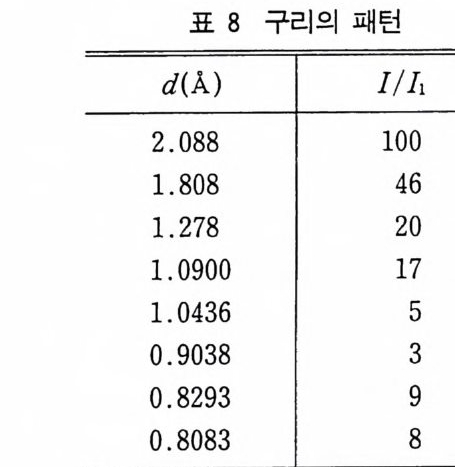 표 8 구리의 패턴
표 8 구리의 패턴
 표 9 미지 시료의 나머지 부분의 패턴과 Cu20 의 패턴
표 9 미지 시료의 나머지 부분의 패턴과 Cu20 의 패턴
 1.743 1
1.743 1
혼합물의 분석은 하나의 물질의 d 값과 다른 물질의 d 값이 서로 겹쳐지면 분석하기가 복잡하고 어려워진다. 특히 중복되는 선이 미지 시료의 가장 강한 선 세 개 중 하나일 때 해석하기가 더욱 어렵다. 일반적 해석법으로 d 값의 일부분이 일치할 경우 하나의 물질에 대해 잠정적으로 확인해 두고 다른 물 질을찾아야한다. 오늘날에서 미지 시료의 회절 패턴과 일치하는 데이터 파일상의 회절 패턴을 컴퓨터를 이용하여 찾을 수 있다. 미지 시료에 포함된 물질이 두 가지 이상이면 손으로 찾는 것은 어렵고 시간이 많이 소 모되므로 컴퓨터로 찾는 것이 효과적이다. J ohnson 과 Vand 가 For t ran 으로 쓴 프로그래밍은 혼합물에 여섯 가지 포함된 미지 시료는 2 분 이내에 찾을 수 있다. 5 정량 분석 x- 선 회절을 이용하여 정량 분석을 하는 것은 혼합물에서 어떤 특정 성분의 회철 패턴의 강도는 혼합물에서 그 물질의 농도에 비 례한다는 사실에 근거를 두고 있다. 회철 강도는 혼합물의 흡수계 수에 따라 다르고, 또 흡수계수는 농도에 따라서 다르므로 회절 강
도와 농도 사이의 관계는 일반적으로 직선 관계는 아니다. 회절 강도와 농도 사이의 관계를 알려면 분말 시료에 의하여 회 절되는 강도의 기본식을 생긱해야 한다. 이 식의 형은 카메라를 사 용했느냐 회절 장치를 사용했느냐에 따라 다르다. 여기서는 회절 장치의 경우를- 생각한다. 단일 성분으로 된 분말 시료에서 얻는 회 절 강도의 정확한 표현식은 다음과 같다. I=UoAA3/321rr)[(µ 。 /4 갑(강 / m 泊 l / V 기 (9-11) [I F 12P(l+ cos22 8)/( s in 2 0•cos0)]( e-2 M /2 µ) 여기서 Io 는 입사 빔의 강도(J oule·sec-1•m - 1), A 는 입사 빔의 단면적 (m2), A 는 입사 빔의 파장 (m), r 은 회절 장치의 원의 반 경 (m), e 는 전자의 하전 (C), m 은 전자의 질량 (k g), µo 는 4;r X 10-1mkg /C 2, V 는 단위세포의 부피 (m3), F 는 구조 인자, P 는 다중도 인자, O 는 Bra gg각도이고 e - 2M 는 온도 인자이고 µ는 선형 흡수계수이고 홉수 인자로서는 1/(2 씨이다. (9-11) 식은 무 질서하게 배열된 결정 알맹이로 되어 있고 평평한 판상(fl a t pla te ) 형 두께롤 가전 다결정질 시료에 적용된다. F, P, 0 를 포함하는 두번째 중괄호 안의 항은 Deby e -Scherrer 패턴에 적용한 근사식 (9-4) 식이다. 이 식은 특별한 경우, 두 물질 a, (J를 포함하는 혼 합물을 분석한다고 하자. a 물질에 대해 (9-11) 식을 쓰면 I 는 Ia 로 표시하고 혼합물에서 a 의 부피 분율 Ca 로 곱해야 한다. 또 µ 는 µm( 혼합물의 선형 흡수계수)로 바꾸어 표시해야 한다. 새로 간단히 표시한 식에서 모든 인자는 싱수이고 요와 µm 등 울 제의하고는 농도에는 무관하다. 그러면 Ia=K1Calµm (9-12) 여기서 K1 은 상수이고 I가 미지수이므로 K1 은 모른다. 그러나
어떤 표준 물질의 강도에 대해 Ia 는 소거할 수 있다. 따라서 a 의 농도는 이 비율에서 구할 수 있다. 회절법에 의한 정량 분석에는 표준이 되는 회절선의 이용 방법에 따라세 가지 방법이 있다. 죽 (1) 의부 표준법 (exte r nal sta ndard meth o d) (2) 직 접 비교법 (dir e ct comp a ris o n meth o d) (3) 내부 표준법 (int e r nal sta n dard meth o d) 1) 외부 표준법 두 물질 a 와 8 의 부피 분율이 각각 Ca, C p이며 무게 분율은 각각 Wa, WFJ 이고 밀도를 각각 pa , pp로 표시하면 혼합물의 질량 흡수계수는 디음과 갇이 쓸 수 있다. !P-m= w-a, (P~a )I + w p• \ (PP리 (9-13) 부피가 1 인 혼합물을 생각하자. 그러면 무게는 p m 이고 a 성분이 함유된 무게는 WaPm 이고 a 성분이 부피는 WaPm/Pa 이고 이 값은 Ca 와 같다. 그러면 (9-13) 식은 다음과 같다. µm= Caµa+ Cp µp= C 라 a+ (1-Ca) µp= Ca 나-µg) +µfl (9-12) 식에서 Ix= Ca (µKa1-µCap ) + µp (9-14) 9-14 식에서 두 성분 a, /3의 선형 흡수계수와 어떤 성분 a 의 부피 분율에서 8 성분의 회절 강도를 구할 수 있다. (9-14) 식을 혼 합물의 무게를 1 로 두고 무게를 기준으로 표현할 수도 있다. a 성 분의 부피는쓰P노a 이고 8 성분의 부피는 W p/pp이다. 그러면
Ca= Wa/pW a a+/p w ap /pp = Wa/p a +W (a1/—p aW a ) /p p Wa (1/PaW-1a//Ppap ) + 1/PP (9-15) (9-14) 식과 (9-15) 식에서 다음 식을 구할 수 있다. Ia= Pa[Wa(µa/PaK 一I Wµpa/ pp) + µp_/ pp] (9-16) 순수한 a 성분이 있을 경우 (9-12) 식에서 다음 식을 얻을 수 있다. Jap = K1/µa (9-17) 여기서 하첨자 P 는 순수한(p ure) 성분이란 뜻에서 표기한 것이 다. f뇨ap = - Wa(µa/PWaa— 區µ /fJp/p ap)) + µp—/p fJ (9-18) (9-18) 식에서 두 성분 혼합물에 대해 각각 성분의 질량 흡수계 수를 알면 혼합물 중 a 성분은 X 숫 1 회절 강도와 성분만 있을 때 의 회절 강도를 구하고 그 비롤 계산하여 그 성분의 함량 Wa 을 정 량 분석할 수 있다. 질량 흡수계수를 모르면 알고 있는 조성의 혼 합물에서 질량곡선을 그릴 수 있다. 순수한 a 성분을 표준 물질로 쓸 수 있는 동일한 조건 아래 Ia 와 la p를 측정해야 한다. 2) 직접 비교법 혼합물에서 성분을 정량하고자 하는 물질을 표준 상태로 쓰지 않 고 다른 물질을 표준 물질로 써서 정량한다. 직접 바교법은 다결정 성 덩어리 물질에 적용 가능하므로 금속학 분야에서 응용 가치가 크다. Averbach 와 Cohen 이 이 방법을 발전시켰으며 이 측정 방
법, 그 자체는 아주 일반적이지만 강철 가운데 aus t en it e 의 함량 을 측정하는 데 많이 사용된다. 강철을 단단하게 하려면 두 가지 조작아 필요하다. (1) 고온으로 가열하여 auste n it e 라 고 부르는 균일한 면심 입방 격자의 고용체를 만든다. (2) Aus t en it e 를 실온에서 물속으로 집어넣어 단단하고 준안정 한 상태인 체심 정방형 고용체인 mar t ens it e 로 바꾼다. 실제로 담금질한 강철 속에는 녹지 않은 탄화물이 포함되며 이러 한 미완성된 변형 때문에 실온에서도 aus t en it e 가 얼마간 포함된 다 . 강철 속에 aus t en it e 가 포함되면 보통 나쁜 영향을 주나 때로 는 좋 은 영향을 준다. 따라서 aus t en it e 의 정확한 함량을 결정하 는 것이 중요하고, aus t en it e 의 함량이 크면 정량적 현미경 검사 가 만족스러운 결과를 준다. 그러나 강철에서 15% auste n it e 함 량 범위에서는 꽤 정확하게 auste n it e 함 량을 결정할 수 있다. 강철에 두 개의 물질 mar t ens it e 와 auste n it e 가 함유되 었다고 생각하자. 여기서 문제는 혼합 중에서 화학적 성분은 같으나 결정 구조가 디론 혼합물의 조성을 결정하는 것이다. 의부 표준법은 이 문제에서는 사용할 수 없다. 그 이유는 순수한 aus t en it e 를 만들 수 없고 또 미지 시료 중 aus t en it e 와 같은 화학적 성분을 갖는 auste n it e 함 량을 아는 표준 물질도 만들 수 없다. 따라서 다음 방 법으로 진행한다. (9-11) 식에서 다음으로 두자. K2= UoA ...l 3/32rcr)[(µ 。 /4 갑(강 /m2)] R = (l/ v2) [| F l2P(l + cos22 0)/(sin 2 0 • cos 0))Je -2 M (9-19) 그러면 (9-11) 식은 다음과 같이 쓸 수 있다. l=K2R/2µ (9-20)
여기서 K눈 회절되는 물질의 양이나 종류에는 무관한 상수이고 R 은 그 물질의 종류와 O 와 hkl 값에 관계되는 값이다. Aus t en it e 를 하첨자 r 로 mar t ens it e 를 하첨자 a 로 표시하자. 각각 물질의 특별한회절선에 대해 (9-20) 식은 다음과 같이 쓸 수 있다. /7= K2R7C7/2µm 그리고 fa = K2RaCa/2µm 위의 두식을나누면 上Ia 一 = RRa7CCar (9- 21 ) Ra, Rr 을 계산하여 Ir/Ia 의 비를 측정함으로써 G/ 요의 값을 얻을 수 있다 (R 값을 계산하려면 결정구조와 격자 파라미터에 대한 지 식이 필요하다). Cr/Ca 의 비가 결정되면 Cr+Ca=l 이므로 G 의 값을 알아낼 수 있다. 죽 ma rt ens it e 선의 적분 강도 회절선과 aus t en it e 적분 강도 회절선을 직접 비교하여 강철 가운데 auste n it e 의 함량을 알아낼 수 있다. auste n it e- marte n sit e 선 의 몇 개의 쌍을 서로 비교하여 몇 가지의 auste n it e 함량을 얻을 수 있다. 강철이 제 3 의 성분, 예 컨대 Fe3C(ceme 0:tit e) 를 함유하면 회절 에 의해서나 혹은 정량적 현미경 시험법으로 cemen tit e 의 함량을 알아낼 수 있다. cemen tit e 의 회철 강도 Ic 를 측정하고 Re 를 계 산하고 Cr/Cc 를 비율에 대한 식 (9-21) 식을 쓸 수 있고 Cr+ Ca+Cc=l 이므로 C7 값을 알아낼 수 있다. 측정할 회절선을 선택할 때에는 다른 성분의 회철선과 너무 가까
이 있거나 중첩되는 회절선은 피해야 한다. 그림 3 은 1% 의 탄소 를 함유한 강철에서 C1 Ka X 선을 사용할 경우 aus t en it e 와
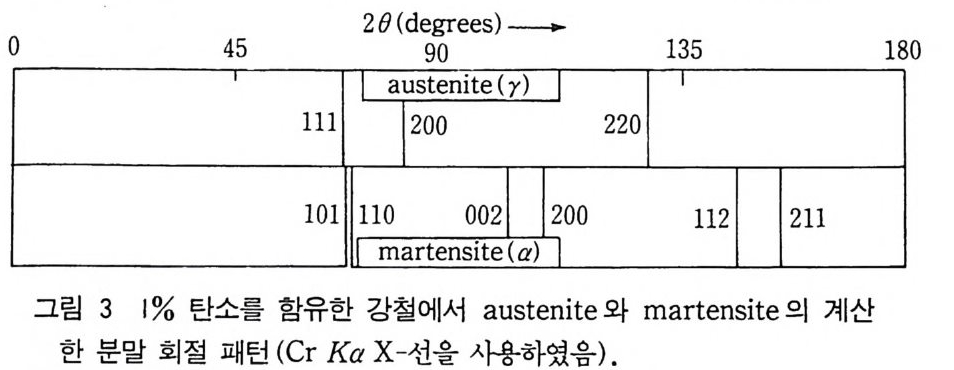 2 0 (deg ree s) —>
2 0 (deg ree s) —>
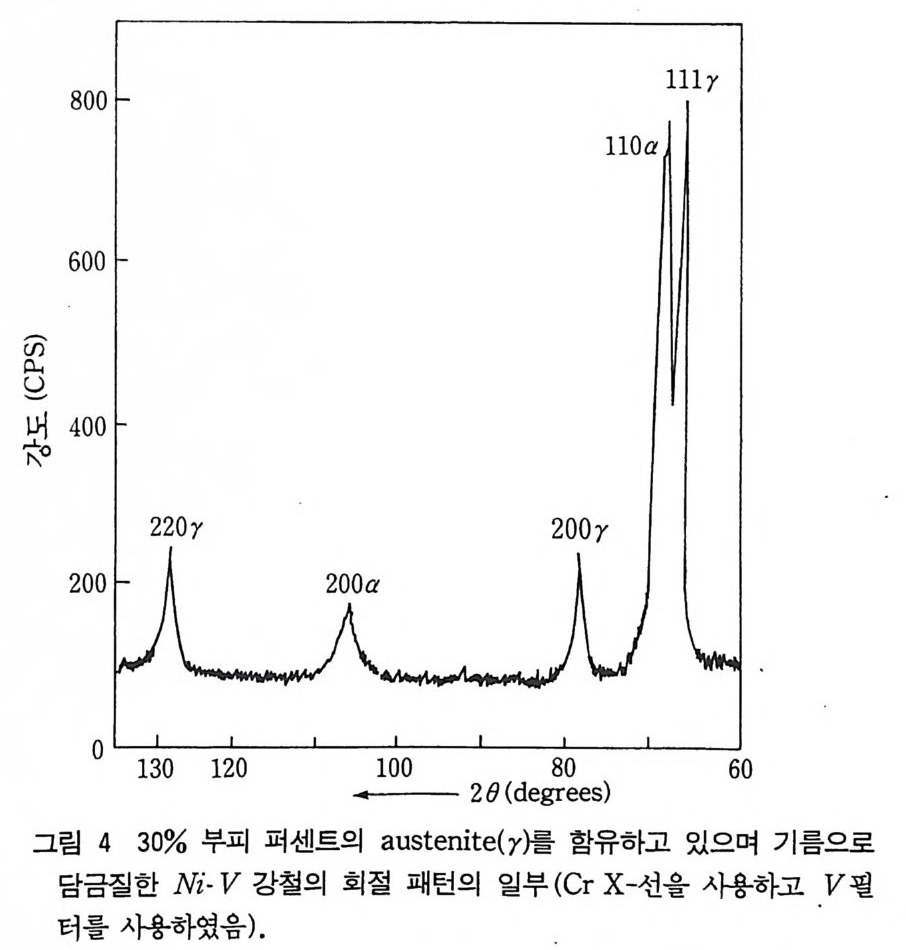 800 111-y
800 111-y
mar t ens it e 의 계산한 회절 패턴이다. 강한 aus t en it e 의 111 회절 선은 mar t ens it e 의 101 과 110 회절선과 너무 가까이 있다. 따라 서 적절한 aus t en it e 회절선은 200 와 220 이고 mar t ens it e 의 이중 선인 002-200 와 112-211 과 비교할 수 있다. 이 이중선은 marte n sit e 단 위세포가 정방형 세포이므로 생기는데 이들 회절선 은 폭이 넓으므로 보통 각각의 선으로 분리되지 않는다. 분리 안되 는 mar t ens it e 회절선은 입방체격자의 회절선처럼 이름을 붙여 002-200 이중선을 200 선이라 부른다. 탄화물이 상당량 존재하면 탄화물의 회절선과 mar t ens it e( 하첨 자 a 로 표시)나 aus t en it e( 하첨자 r 로 표시)의 회절선과 중첩될 수 있어서 측정하는 데 어려움이 따른다. Purn i n 과 R i dal 은 Fe3C 와 여섯 가지의 탄화물 합금의 회절선과 중첩되지 않는 a 선과 7 선을 조사하여 명시하였다. Cr Ka 와 Mo Ka 는 회철 패턴상의 회절수를 많게 하여 더 많 은 측정할 수 있는 회절선 쌍을 준다. 특별한 회절선은 R 값을 계산할 때에는 여러 가지 인자를 염두 에 두어야 한다. 단위세포 부피 V 는 측정한 격자상수에서 계산할 수 있고 이 격자상수는 탄소와 합금 함량에 따라 다르다. Ma rt ens it e 의 이중선이 분리되지 않으면 mar t ens it e 의 구조 인 자와 다중도는 체심입방 격자를 기초로 하여 계산할 수 있다. 이 경우에 이중선의 두 선의 적분 강도를 모두 합쳐서 계산되고 이 크 기는 실험적으로 분리 안된 이중선의 적분 강도를 측정한 것과 갇 다. 회철선의 강도를 측정할 때에는 최대 강도가 아닌 적분 강도를 측정해야 한다. 회절선의 모양은 시료의 알맹이 크기와 미세한 변 형에 따라 다르다. 회절선의 모양의 변화는 적분 강도의 크기에는 영향을 주지 않으며 최대 강도의 값은 무의미하다. 소량 함유된 aus t en it e 의 결정에서 X- 선 법의 감도는 배경
(back g round) 의 강도에 크게 영향을 받는다. 배경이 적으면 auste n it e 회 절선을 쉽게 측정할 수 있다. 필터를 사용한 X 국 1 으 로는 최소 감지 함량은 auste n it e 부 피 함량으로 약 2% 정도이고 결정 T_누 더로메이터를 사용한 X- 선으로 약 0.2 % aus t en it e 도 감지할수있다. 3) 내부 표준법 이 방법에서는 결정하려는 성분의 회절선은 표준 물질을 시료와 섞어서 얻은 회절선과 비교한다. 물론 이때 혼합한 표준 물질의 비 율은 미리 알아야 한다. 따라서 내부 표준법은 시료가 분말일 때만 7 뜹하다. 지금 A, B, C, ……성분으로 된 혼합 물질 중 A 의 양을 결정 하고자 한다고 하자. 원래의 알고 있는 양의 시료에 표준 물질 S 롤 섞어서 새로운 혼합 물질을 만든다. CA 를 원래의 혼합 물질 중 A 성분의 부피 분율이라 하고 CA’ 를 표준 물질 S 를 섞은 후 A 성분의 부피 분율이라고 하자. 또 G 를 새로운 혼합 물질 중 표준 물질의 부피 분율이라고 하자. 성분 A의 특별한 회철선의 강도를 (9-12) 식에 의해 표현하면 디음과 같이 쓸 수 있다. JA =K3C//µm (9-22) 표준 물질의 특별한 회절선에 대해 회절 강도의 표현식을 쓰면 Is=K4Cslµm (9-23) (9-22) 식을 (9-24) 식으로 나누면 다음과 같이 쓸 수 있다. IA/Is=KaCA'/K4Cs 여기서 µm 은 혼합물과 미지 시료의 선 흡수계수이고 제거된다. 그리고 다수의 성분에 대해 A 성분의 부피 분율은 다음과 같이 표 현할수있다.
CWAA'!PA'+ =WB'!P~’B + … … + Ws/Ps 그리고 Cs'= WA ,/ pA + wB ,W/ PsB/P+s …… + Ws/Ps 따라서 CCAs' = wPA'AWPss (9-24) WA 는 혼합물 조성에서 일정하게 유지하면 다음 식을 얻을 수 있다. IA/Is=K中 ' (9-25) 원래의 혼합물 중 A 의 무게 분율과 새로운 혼합물 중 A 의 무 게 분율 사이의 관계 식에서 다음 식을 얻는다. WA'= WA (l-ws) 그러면 IA/Is=K5WA (9-26) 미지 농도의 성분 A 의 회절선의 강도와 표준 물질 S 의 회절 강도의 비는 원래의 시료 가운데 A 의 무게 분율 WA 와 직선 관계 가 된다. 일정한 농도를 갖는 적절한 표준 물질을 함유하고 있는 농도를 알고었는 A 를 함유한 일련의 혼합물게서 검량 곡선을 그 릴 수 있다. 검량 곡선이 준비되면 혼합물 가운데 A 의 농도는 IAII려 비에서 간단히 구할 수 있다. 내부 표준방법은 공장 먼지 가운데 석영의 함량울 구하는 방법에 널리 사용되어 왔다. 이 분석 법에서 형석 (CaF2) 은 내부 표준물질로 적합하다. 그림 5 는 농도를 알고 있는 석영과 탄산칼슘의 혼합물에서 CaF2 의 무게 분율을 각 혼합물에서 0.2 로 되게 하고 검량 곡선을 만든 것이다. 이 검량
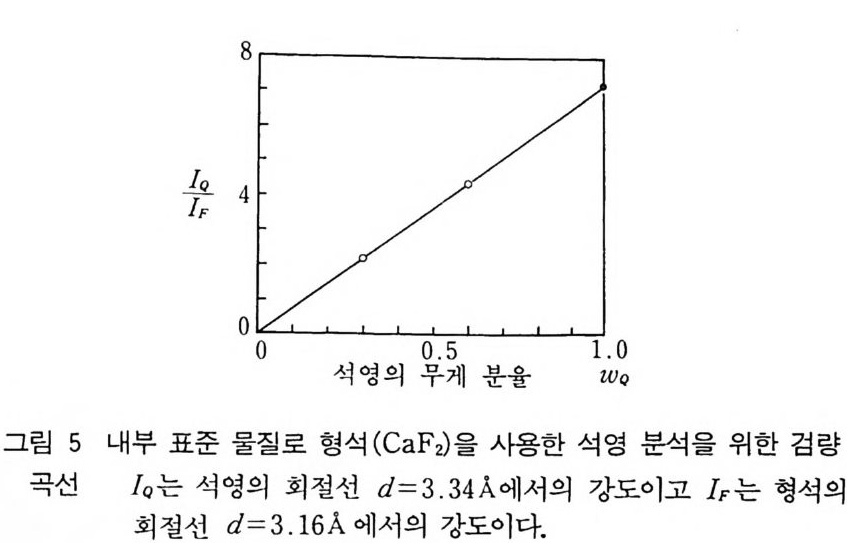 8
8
곡선은 원점을 지나는 곡선이다. Bums t ed 는 이 방법으로 먼지 가운데 석영의 양을 결정하였다. 엄격히 말하면 (9-26) 식은 적분 강도에 대해 성립하는 식이다. 그러나 먼지 가운데 석영의 농도는 최대 농도를 간단히 측정하여도 만족스러울 정도로 정확히 측정 가능하다. 그러나 이 경우에는 회 절선의 모양이 각 시료에 대해 대개 일정한 모양을 갖기 때문에 만 족스러운 결과를 얻을 수 있을 것이다. 죽, 적분 강도와 최대 강도 사이에는 일정한 비례 관계가 성립하고 회절 패턴은 동일한 실험 조건 아래 시행하면 최대 강도로도 만족스러운 결과를 얻을 수 있 다. 그러나 시료 가운데 입자의 크기가 너무 적고 틀리면 회절선의 선폭이 커지고 시료의 조성에 따라 최대 강도가 다르므로 아주 틀 리는 결과를줄수 있다. 내부 표준법은 시멘트의 분석, 접토 광물의 분석 등에도 많이 사 용된다.
연습문제 1. Cu Ka X - 선 을 사용하여 다음과 같 이 Al 분말 무 늬의 s i n 내 값 을얻었다. 0 .1118, 0 .14 87, 0 . 294 0, 0 . 403 0. 0 . 4:190 . 0. 58 30, 0.6 9 10, 0. 72 7 0 , 0.87 20, 0.9 82 0 회절선의 지수 를 붙이고 격자상수 를 구하라 . 2. 다음은 미지 시료의 d 값과 I / L 값 이 다. .J C P D S 분만 회정 파일 울 써서 이 미지 시료 를 확 인하여 라 . d(A ) I/I I d(A ) I,' k dt A ) I/1 1 3. 66 50 1. 46 10 1. 06 10 3.17 100 1. 42 50 1. 01 10 2. 24 80 1. 31 30 0. 96 10 1. 91 40 1.23 10 0.85 10 1.83 30 1.12 10 1.60 20 1.08 10 3. 다음은 미지 시료의 d 값과 I / I1 값이다. J CPDS 분말 회 절 파일 울 써서 이 미지 시료를 확인하여라. d(A) l/I1 d(A ) 1/1 1 d(A) 1/1 1 5.85 60 2. 08 10 1. 47 20 3. 05 30 1.95 20 1.42 10 2.53 100 1.80 60 1.14 20 2. 32 10 1.73 20 1.04 10 4. 다음은 미지 시료의 d 값과 III1 값이다. J CPDS 분말 회절 파
일을 써서 이 미지 시료를 확인하여라 . d(A) 1/11 d(A .) I/II d(A) 1/11 2.40 50 1.25 20 0.85 10 2.09 50 1.20 10 0.81 20 2. 03 100 1.06 20 0.79 20 1.75 40 1. 02 10 1. 47 30 0.92 10 1. 26 10 5. E l-g은 미지 시 료 의 d 값과 I / I1 값이다 . J CPDS 분말 회절 파 일옹 써서 이 미지 시료 를 확인하여라. d(A ) I/ II d(A ) 1/ 11 d(A .) 1/11 3.02 100 2.11 10 1.46 10 2.7 9 10 1.90 20 1.17 10 2.52 10 1.65 10 ~.31 30 1.62 10
부록 1 물리적 상수와 환산 인자 2 결정구조 데이터 3 질량흡수계수와 밀도 4 분말법에서 사용되는 다중도 인자 5 원자 및 이온의 X- 선 산란 인자
부록 1. 물리적 상수와 환산 인자 환산인자 긴 이 Ang s tr o m 단위 lA = 10-8 c m= 10-1 nm mICron l µ= 10- 4 cm= 1 µm ’:l 도 gram mer per cc 1 ge m- 3= 10 k gm것 압니 atm os p h e re 1 atm = 1. 0133 bar= 101 . 33 kNm-2 ba r 1 bar= 105 Nm- 2 에너 지 crg 1 er g =10 구J calorie l cal= 4 .18 4J = 41. 84 bar cm3 ele c tr o n volt 1 eV= l. 6 021 X 10-19 J = 23 . 061 kcalmoJe -1 엔트로피 entr o p y 단위 1 e.u . = 1 cal deg -1 mole-1 = 4 . 184 JK -1m0Je -1 상수 :r =-:L 141 5 9 ir-1 =0.31831 1 =0 .01745 radia n 1 radia n = 57 . 296' L' :: :: 2 . 71828 In 10= 2 . 30259 log 10 e= 0 . 43429 Planck 's 상수 /z= 6.6256X 10-2· e rgs = 6 . 6256 X 10-3~ Js Avo g adro 수 N= 6 . 02252 X 1023 mo le-1 Boltz m ann 상수 k= 1. 3805X 10-16 erg deg -1 = 1. 3805 X 10-23 JK- 1 기체 상수 R= kN= l. 9872 cal deg - 1 mo 1e -1 = 8 . 314J K -1 mole-1 전자의 질량 m=0. 91 1X l0-27g
양자의 하전 e= 4 . 8030 X 10- 10 e.s.u . = l.60 2X 10- 19 C 빛의속도 c=2 .9979x 1010cm s- 1 =2.9979X 108 m s- 1
부록 2. 결정구조 데이터 원소의 결정구조, 원자간 거리 및 실온에서 이온 반경은 다음과 같 다. 야온 반경은 반대부호 를 가지는 이웃 이온의 수, 죽 배위수에 따라 다 로 다. 위의 표 의 이온 반경은 배위수 6 을 가지는 이온을 기준으로 하였 댜 배위수가 4 이면 반경은 약 7% 작아지고 배위수가 8 이면 약 3% 커 지고 배위수가 12 이면 6% 정도 커진다.
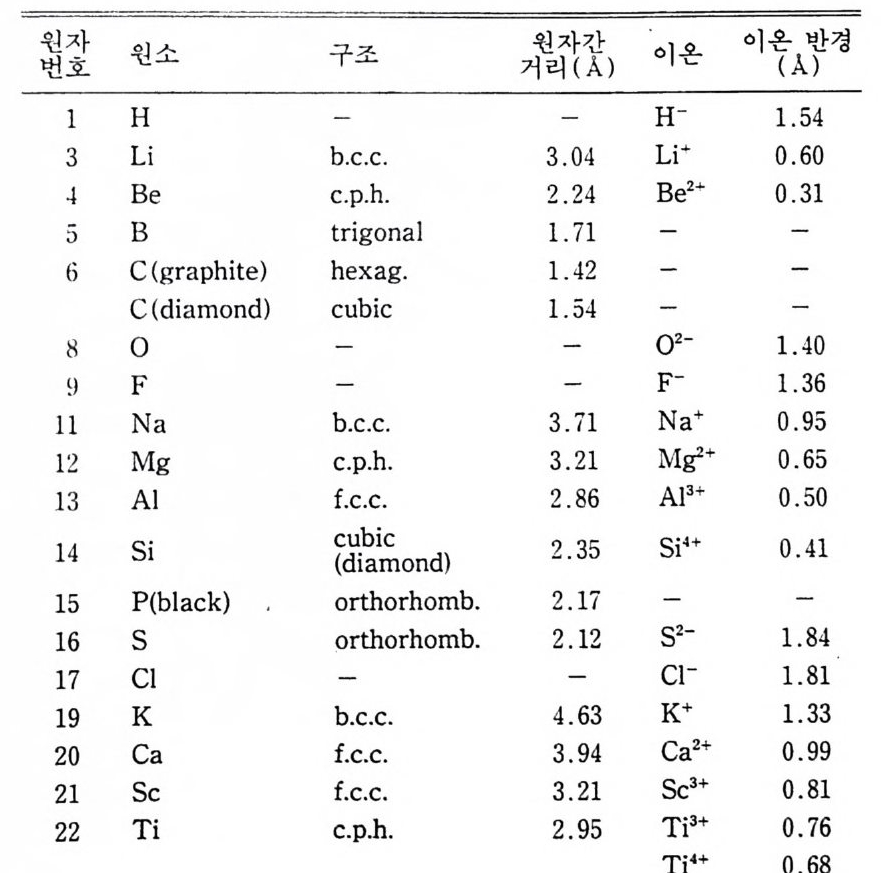 鬪 원소 구조 거원 리자( A간) 이온 이온(( A반 )) 경
鬪 원소 구조 거원 리자( A간) 이온 이온(( A반 )) 경
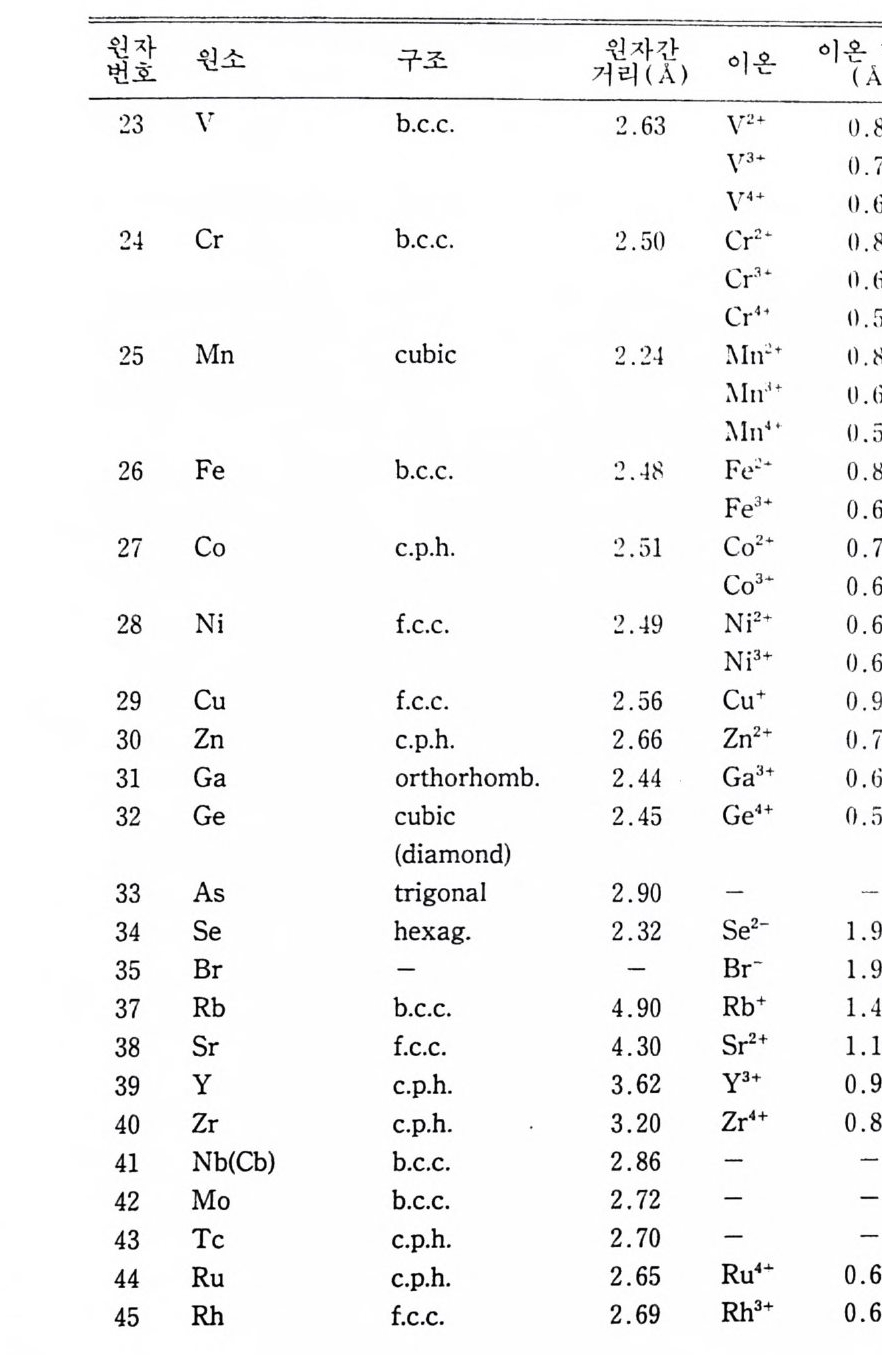 麟 원소 구조 거원리자 ( 간A ) 이온 이온(( A 반) )겅
麟 원소 구조 거원리자 ( 간A ) 이온 이온(( A 반) )겅
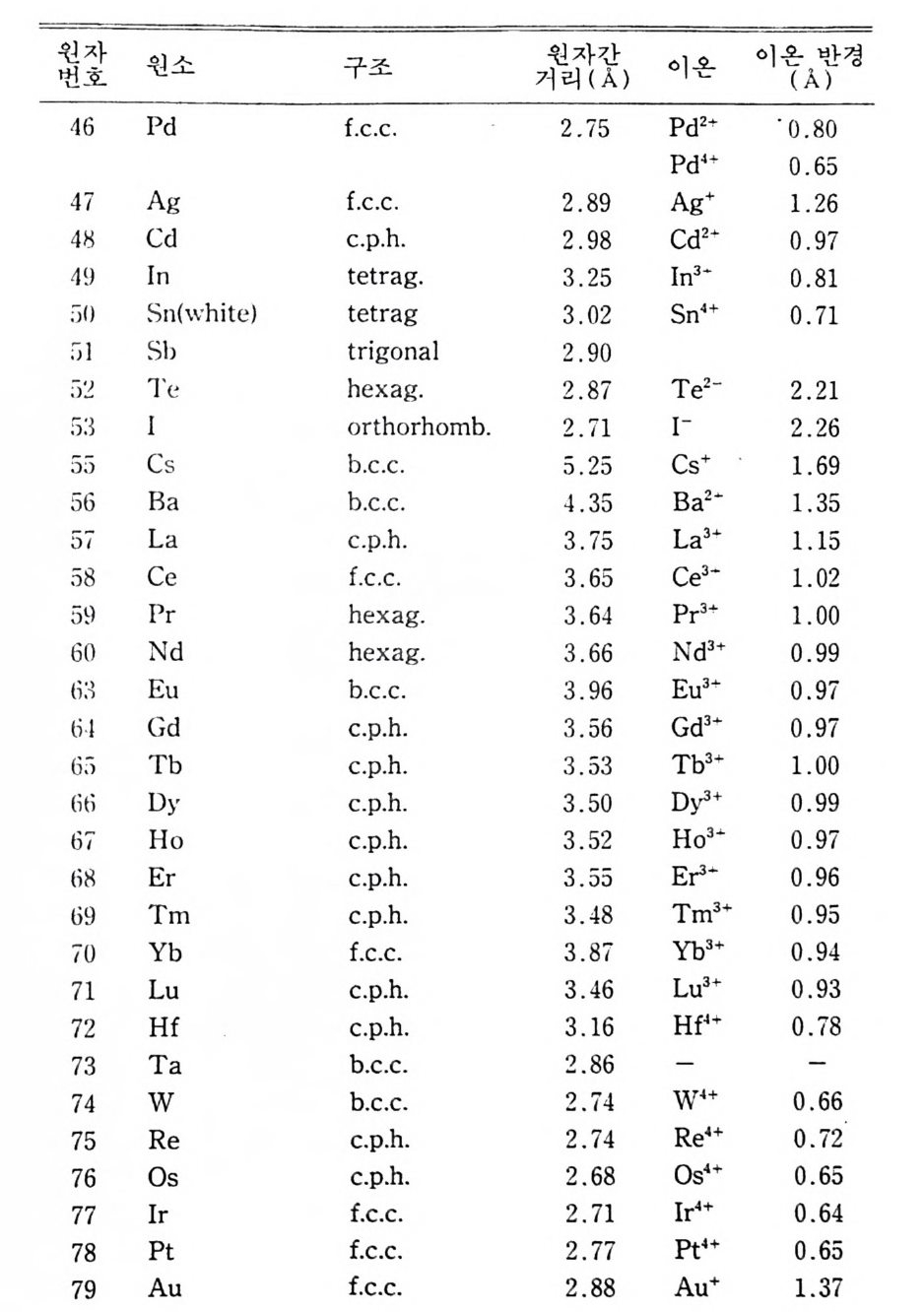 원번호자 원소 구 조 거원 리자( A간 ) 이온 이온(( A반 ) )경
원번호자 원소 구 조 거원 리자( A간 ) 이온 이온(( A반 ) )경
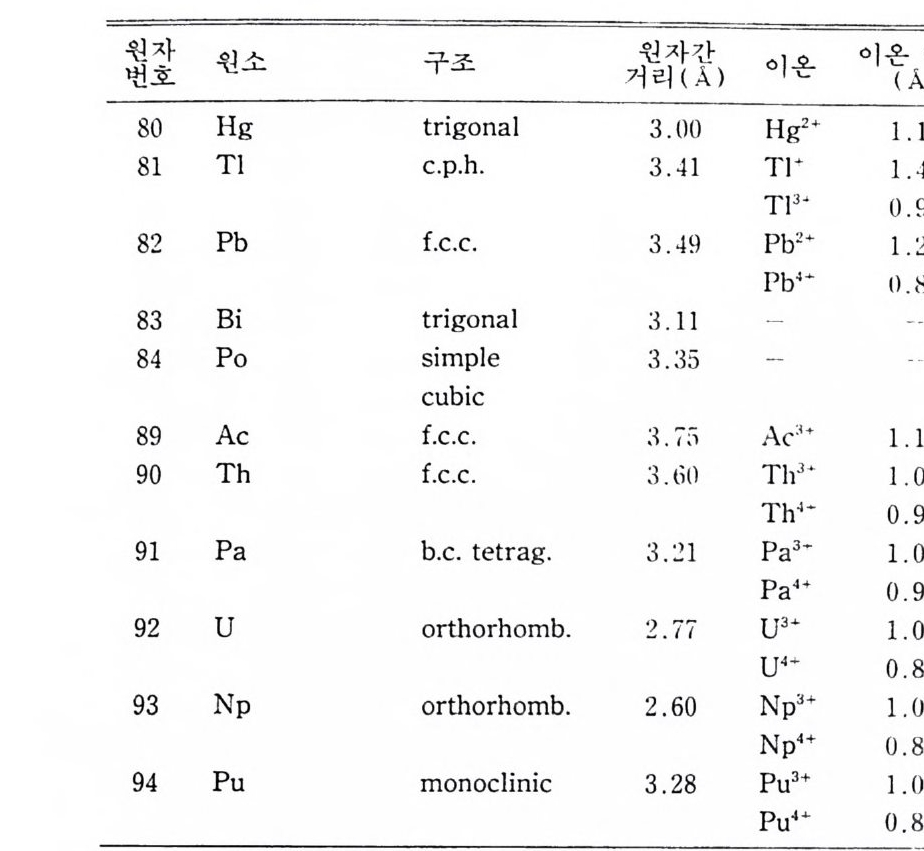 麟 원소 구조 거원 리자(A간 ) 이온 이온(( A 반) )경
麟 원소 구조 거원 리자(A간 ) 이온 이온(( A 반) )경
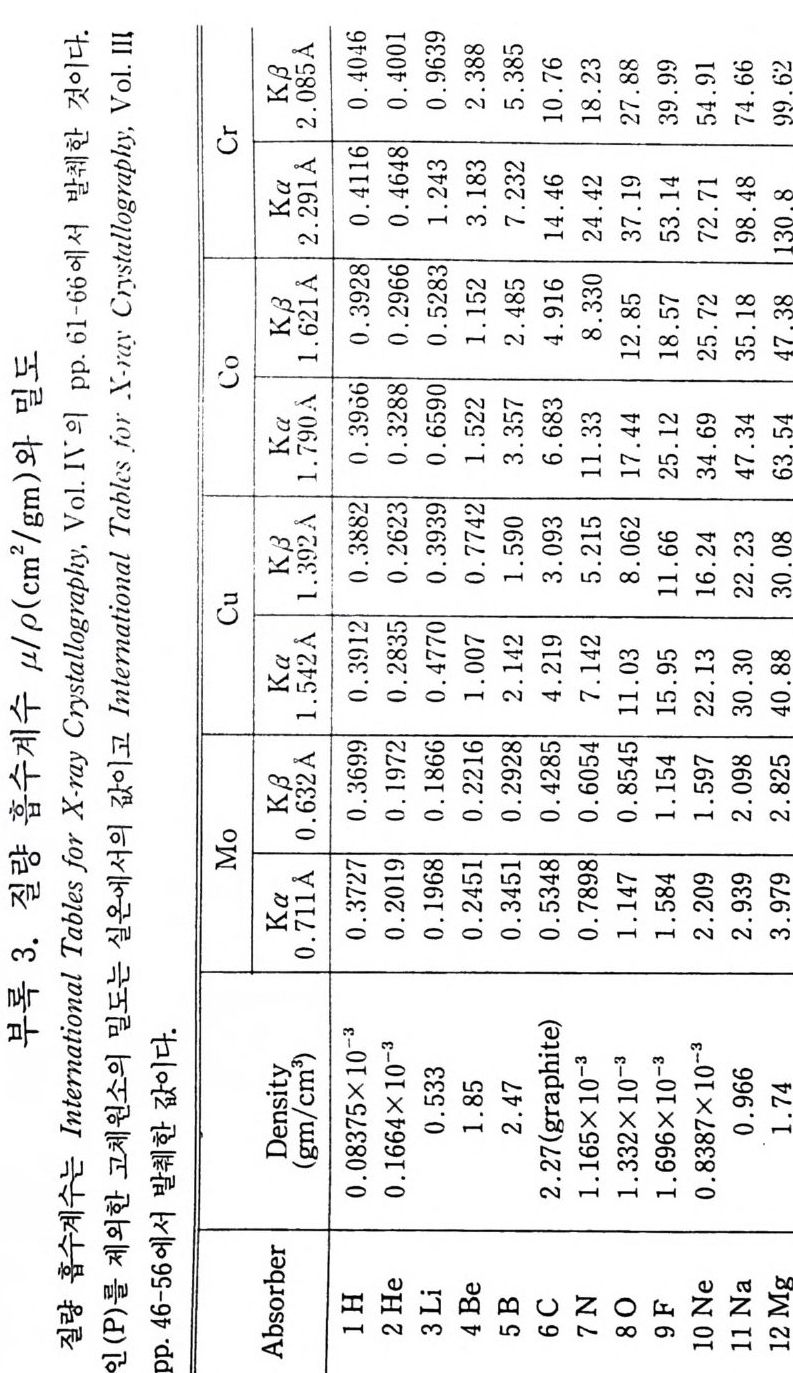 . 3록부 량질2I 도 ( 계흡/수cp와m)f밀수.Jmg pfgtlTnera-onyrl,raoCInba aXyes ozt aaVpyr.l lol,psit 계질l.흡수 량수는 \-61에의서6'6I 발이다 .췌한 것 pfrXa-etanrsToabllarl t ounie oas1lgVI,yt l ryCazlyo 고밀서 한를실) P제체l원.l소인의온는 도( 의!에고의 값 이 p.p 에서-54 66다이췌 발값.한 .. rCoM `C Lou gbrr eAosbKK K a3a/KaK K aK /K3/3 tny mec1>Ds/3i50.28 A11A 7.0A.67A 09 0232 122A.95 1 A6 .2.9 2 3 4l1AAg(m1 . .1 HlX8 304 07.45060. 7909376. 302.0.638496 19.1.3 60.3200 81283.9 2001 김 eH2 -X360 601 1 4.9 01000 14.20..2 7 109604 .48..02 8303.5062 2238982.0 66 0 39.1860.09 9618 66 3. 3.30.5i L774 300930 .8 3.2400 59.1.6035 92 e 4B4 520.12 16220. 883. 8750. 22.517 2453 128170.01 .3 .11. B5 1504.3 72 4..5 2857290..323 8.3595 213224 l 7..0584.2 C6 4830.5pa.2 h 85 420. 72) t(ei6.709 912.340 .1316r 9.464 83.4.g616 10 65 1X-3.1N7 54600. 988. 70.3 42.1783 .3 1112032 53.248..42 1 5 01 X3233 -08 5485.0 741 .8 183 0.11.72 50..891284 .7.43117.612 X966 F9 415 458.195 .91593 .976 .1l1.514182 .3.1.1. 5265 01 김 X878.0 759.1 920.23 -310.91N0 1 3 .122e 45 24.61 2 .17529 2.6.7743 993.2 a.61 106 .303 8409.N2 7 23.226.9 80 .148534 .8.39476 M28 .40 582.2 89971.3 08.03.62 994 7g8 4 0..51 363 8.374.1
. 3록부 량질2I 도 ( 계흡/수cp와m)f밀수.Jmg pfgtlTnera-onyrl,raoCInba aXyes ozt aaVpyr.l lol,psit 계질l.흡수 량수는 \-61에의서6'6I 발이다 .췌한 것 pfrXa-etanrsToabllarl t ounie oas1lgVI,yt l ryCazlyo 고밀서 한를실) P제체l원.l소인의온는 도( 의!에고의 값 이 p.p 에서-54 66다이췌 발값.한 .. rCoM `C Lou gbrr eAosbKK K a3a/KaK K aK /K3/3 tny mec1>Ds/3i50.28 A11A 7.0A.67A 09 0232 122A.95 1 A6 .2.9 2 3 4l1AAg(m1 . .1 HlX8 304 07.45060. 7909376. 302.0.638496 19.1.3 60.3200 81283.9 2001 김 eH2 -X360 601 1 4.9 01000 14.20..2 7 109604 .48..02 8303.5062 2238982.0 66 0 39.1860.09 9618 66 3. 3.30.5i L774 300930 .8 3.2400 59.1.6035 92 e 4B4 520.12 16220. 883. 8750. 22.517 2453 128170.01 .3 .11. B5 1504.3 72 4..5 2857290..323 8.3595 213224 l 7..0584.2 C6 4830.5pa.2 h 85 420. 72) t(ei6.709 912.340 .1316r 9.464 83.4.g616 10 65 1X-3.1N7 54600. 988. 70.3 42.1783 .3 1112032 53.248..42 1 5 01 X3233 -08 5485.0 741 .8 183 0.11.72 50..891284 .7.43117.612 X966 F9 415 458.195 .91593 .976 .1l1.514182 .3.1.1. 5265 01 김 X878.0 759.1 920.23 -310.91N0 1 3 .122e 45 24.61 2 .17529 2.6.7743 993.2 a.61 106 .303 8409.N2 7 23.226.9 80 .148534 .8.39476 M28 .40 582.2 89971.3 08.03.62 994 7g8 4 0..51 363 8.374.1
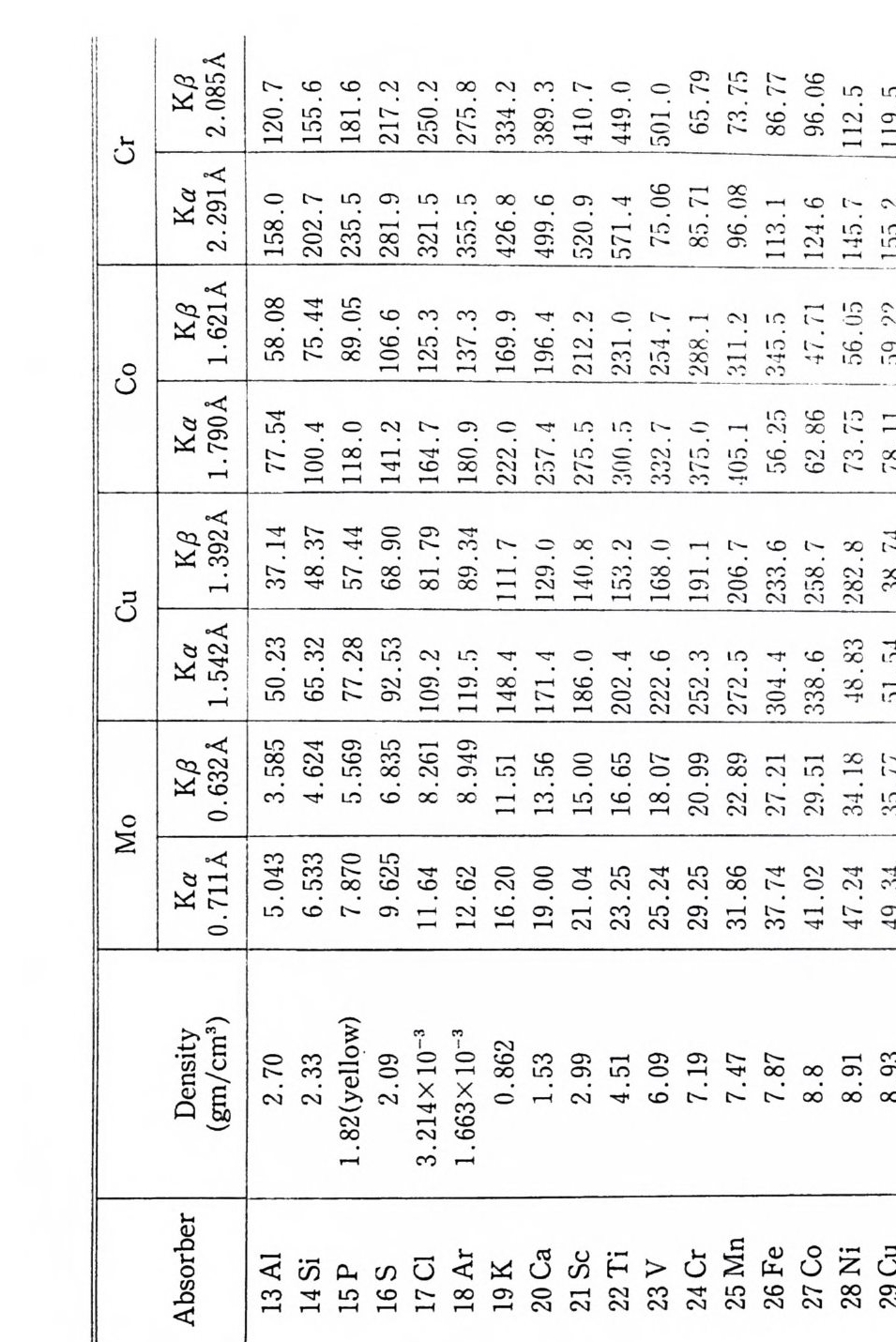
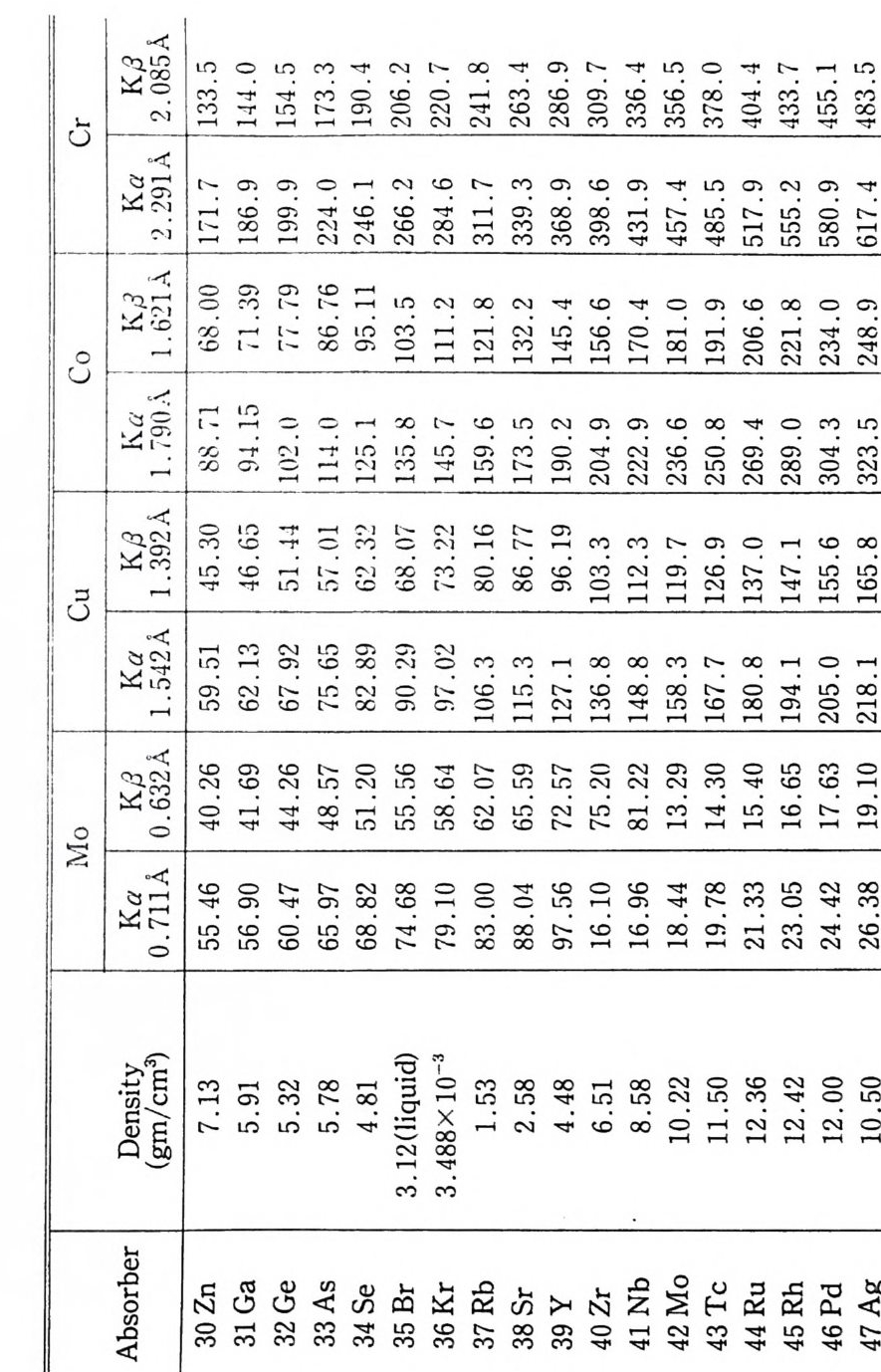

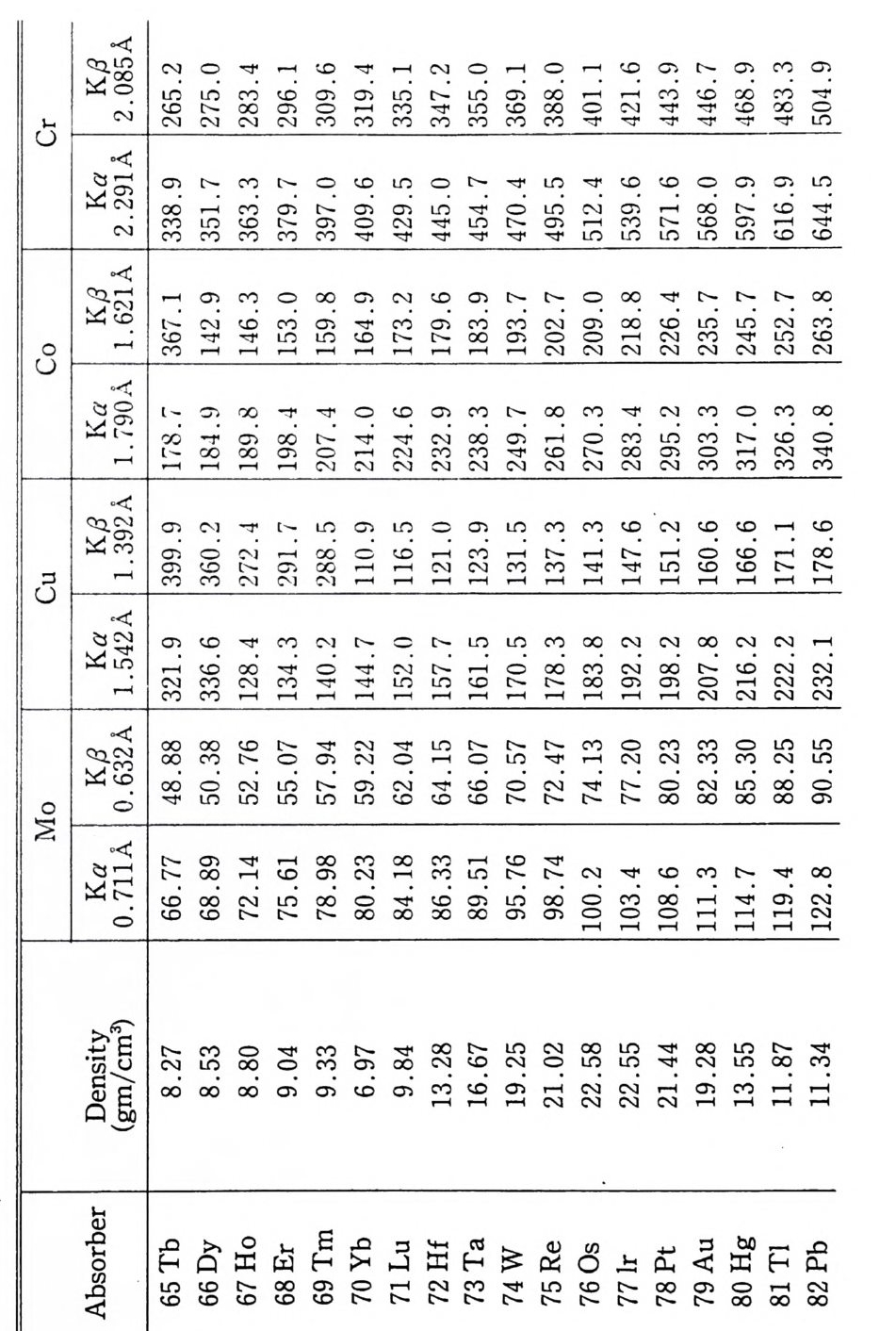 L」 j :악l4f0'Ng«) 。‘。ln J J pζl: r:N、>n . NF。'<:。 3!'e ‘~、 。“ J 。。、'ζM。 <〉 :、!。C..' η... 、 .M r~MU。 1→ Mr。M‘ - jMTζU:':l>n< 1:a‘~p 녁、! 。'0ζ: '。0:> <ζ..F『:. ;... !F 。‘'P 『J σ?「 f 、3,''r‘ 「p'、 :T!。c''U、' 。S': !?'。숫Ml。 '1 Q「ζlf ~')l
L」 j :악l4f0'Ng«) 。‘。ln J J pζl: r:N、>n . NF。'<:。 3!'e ‘~、 。“ J 。。、'ζM。 <〉 :、!。C..' η... 、 .M r~MU。 1→ Mr。M‘ - jMTζU:':l>n< 1:a‘~p 녁、! 。'0ζ: '。0:> <ζ..F『:. ;... !F 。‘'P 『J σ?「 f 、3,''r‘ 「p'、 :T!。c''U、' 。S': !?'。숫Ml。 '1 Q「ζlf ~')l
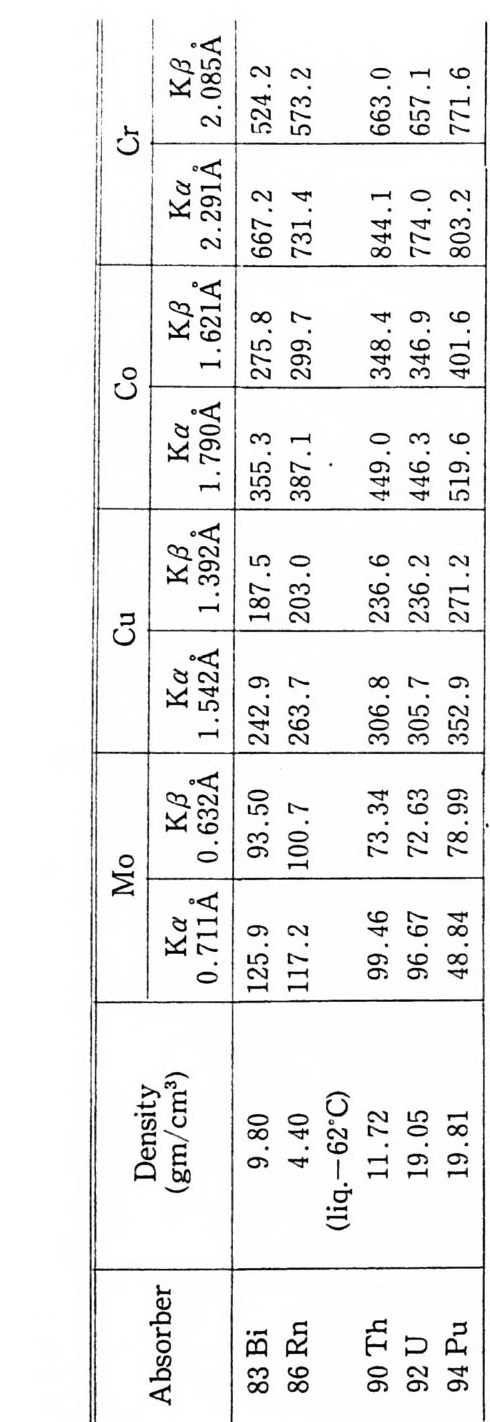 -- C rKa K J .(A. 2921A0 28。.5 2 .54626 27.357.23 7 41. 164.4 .3086 7 .165 0.477 3 08.7761 2.
-- C rKa K J .(A. 2921A0 28。.5 2 .54626 27.357.23 7 41. 164.4 .3086 7 .165 0.477 3 08.7761 2.
부록 4. 분말법에서 사용되는 다중도 인자 입방 정 계 hkl hhl Oki Okk hhh 001 石옳 24 짜 12 8 6 육방 정계 와 hk·l hh·I Ok·l hk·O hh·O Ok·O 00·1 능면체 짜 표 E E 6 6 2 정방정계 hkl hhl Oki hkO hhO OkO 001 蔣* 8 8 硏 4 4 2 사방 정 계 hkl Oki hOI hkO hOO OkO 001 8 4 4 4 2 2 2 단사정계 hkl hOI OkO 4 2 2 삼사정계 hkl 2 * 이 값 은 보통의 다중도 인자이다. 어떤 결정에서는 이러한 지수를 갖는 평면 은 같 은 평면 간격을 가지나 들리는 구조 인자를 갖는 두 가지 평면족윤 포 함한다. 이 때 각 평면족은 위의 값의 1/2 이 된다.

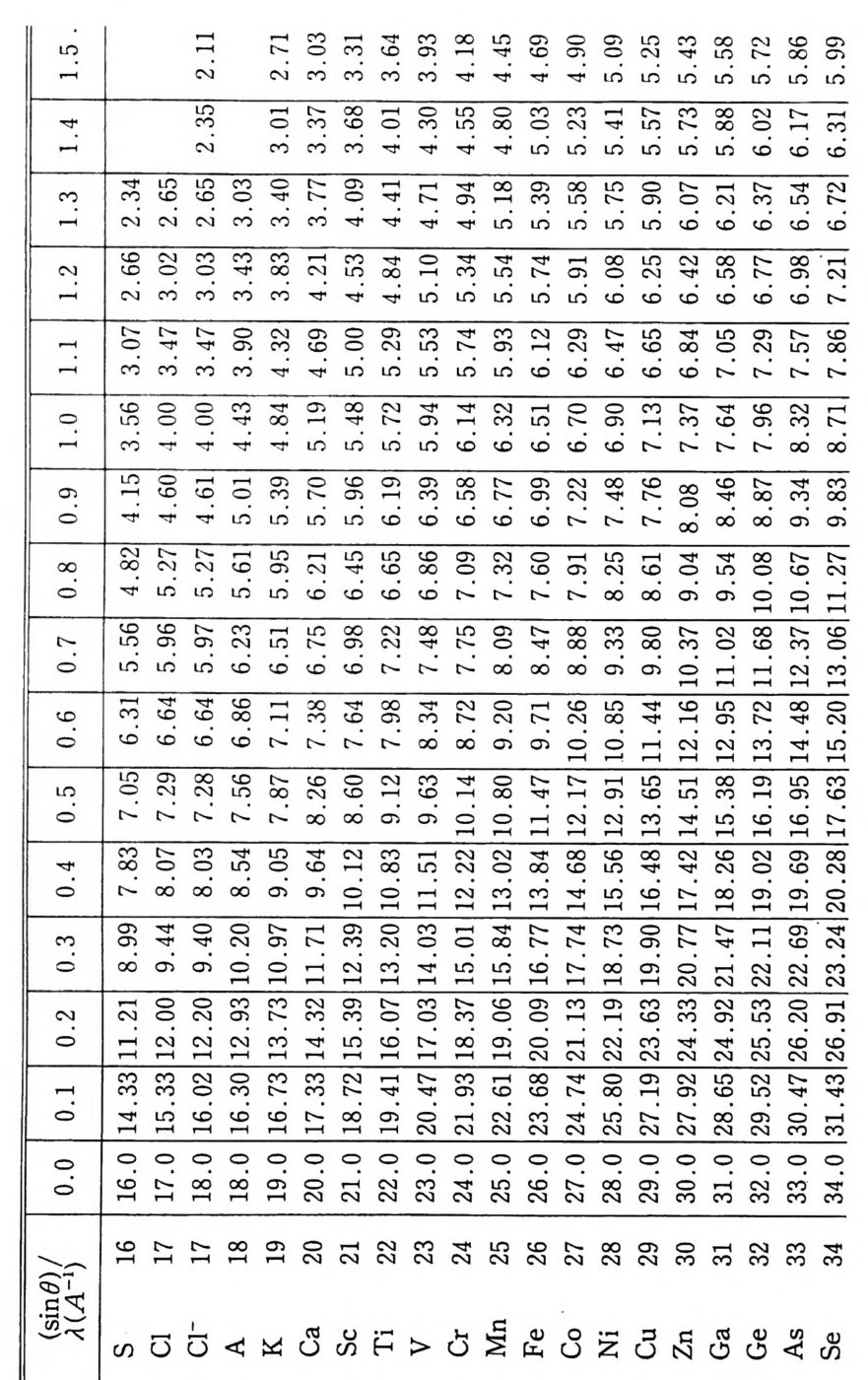 .51. 12.1 71. 2.033 331. 3 .64933. 18 .4 54. 4 694. 904.5.09 25.5 3 45. 5 5.85 2.7 5.68 59.9
.51. 12.1 71. 2.033 331. 3 .64933. 18 .4 54. 4 694. 904.5.09 25.5 3 45. 5 5.85 2.7 5.68 59.9
 .5.600. 07. 80 9.0 0 1 23 1.4 .15.111... 1 1 8.72591 1..7391 1 13.8.1401 1.9 98 .4.5721 956. 6. 511 66. 1 8.284. 156.74 4 .15214071.9 9 6.6871..16 9 .872. 6 70316 . .6053815.1 4714.9 142.1.6 166 809..51.5144. 88 8 37.5 .699 591 1.6.4 181 9643. 193.0.2 715. 109 9.996 4148..9 708. 42 .7 .6 791.137. 681 4.4 1593112 3 81.2.4.103 487 38.4.9 08.807.5 73. 20.497 15..192549 8.2911.0110 710.3 90 ..89 8668.3 7. 67 .02899 814.5.46. 1447 1820 13113.. 140.3 91.10 33.684 1..2 80 6 025914 9..106 1 42 1373.6.0.1259 3.11.1.45 10 46.9 .9289 8.2 1 22.2619.6.1047 .1158 21 1154..5 5 6.14 7.78 104 9.1 9.925 8.5 2 8.23.6 20161. 629 . 1712 2413. 1574.10 .1 5.0121 .1119.4 928.8 6.4322.702 7 18.1. 584161.363. 19924.4 6 5 . 411 6501. 8.7909 9. 02 8.48 228 .9180724. 142.5 15.012 ..81128 .711 807.1.37 .07 901 1 427.0 .51 8295 .5217 424. 1855.19 .1.131112 1.121. 9 7.301.64 9 2.4.2 235242 .020 .9917 814. 1286.16 .513.12 1 5.11 64.96 .62901 3 .02. 062 .5202 5.17 6.1.5 18 .913 .812 81.2 .01011 .1 66 .2 .6328 12.9 1146 .l2 7.1 .:~ .213. 11.21 31.510 :i. 1 2 .72 62 .124196 7.1.4 .7140 6.1.15.21 .51 3 61 .810. 1 .742 9.7219 1.2215. 6 .1.9 . I0 8.1 .813 8.21 1091. . 11j .325 5.8220 .622 .4 S 8.1 .-115 86.1 l.31 .21 13.221. 1-1
.5.600. 07. 80 9.0 0 1 23 1.4 .15.111... 1 1 8.72591 1..7391 1 13.8.1401 1.9 98 .4.5721 956. 6. 511 66. 1 8.284. 156.74 4 .15214071.9 9 6.6871..16 9 .872. 6 70316 . .6053815.1 4714.9 142.1.6 166 809..51.5144. 88 8 37.5 .699 591 1.6.4 181 9643. 193.0.2 715. 109 9.996 4148..9 708. 42 .7 .6 791.137. 681 4.4 1593112 3 81.2.4.103 487 38.4.9 08.807.5 73. 20.497 15..192549 8.2911.0110 710.3 90 ..89 8668.3 7. 67 .02899 814.5.46. 1447 1820 13113.. 140.3 91.10 33.684 1..2 80 6 025914 9..106 1 42 1373.6.0.1259 3.11.1.45 10 46.9 .9289 8.2 1 22.2619.6.1047 .1158 21 1154..5 5 6.14 7.78 104 9.1 9.925 8.5 2 8.23.6 20161. 629 . 1712 2413. 1574.10 .1 5.0121 .1119.4 928.8 6.4322.702 7 18.1. 584161.363. 19924.4 6 5 . 411 6501. 8.7909 9. 02 8.48 228 .9180724. 142.5 15.012 ..81128 .711 807.1.37 .07 901 1 427.0 .51 8295 .5217 424. 1855.19 .1.131112 1.121. 9 7.301.64 9 2.4.2 235242 .020 .9917 814. 1286.16 .513.12 1 5.11 64.96 .62901 3 .02. 062 .5202 5.17 6.1.5 18 .913 .812 81.2 .01011 .1 66 .2 .6328 12.9 1146 .l2 7.1 .:~ .213. 11.21 31.510 :i. 1 2 .72 62 .124196 7.1.4 .7140 6.1.15.21 .51 3 61 .810. 1 .742 9.7219 1.2215. 6 .1.9 . I0 8.1 .813 8.21 1091. . 11j .325 5.8220 .622 .4 S 8.1 .-115 86.1 l.31 .21 13.221. 1-1
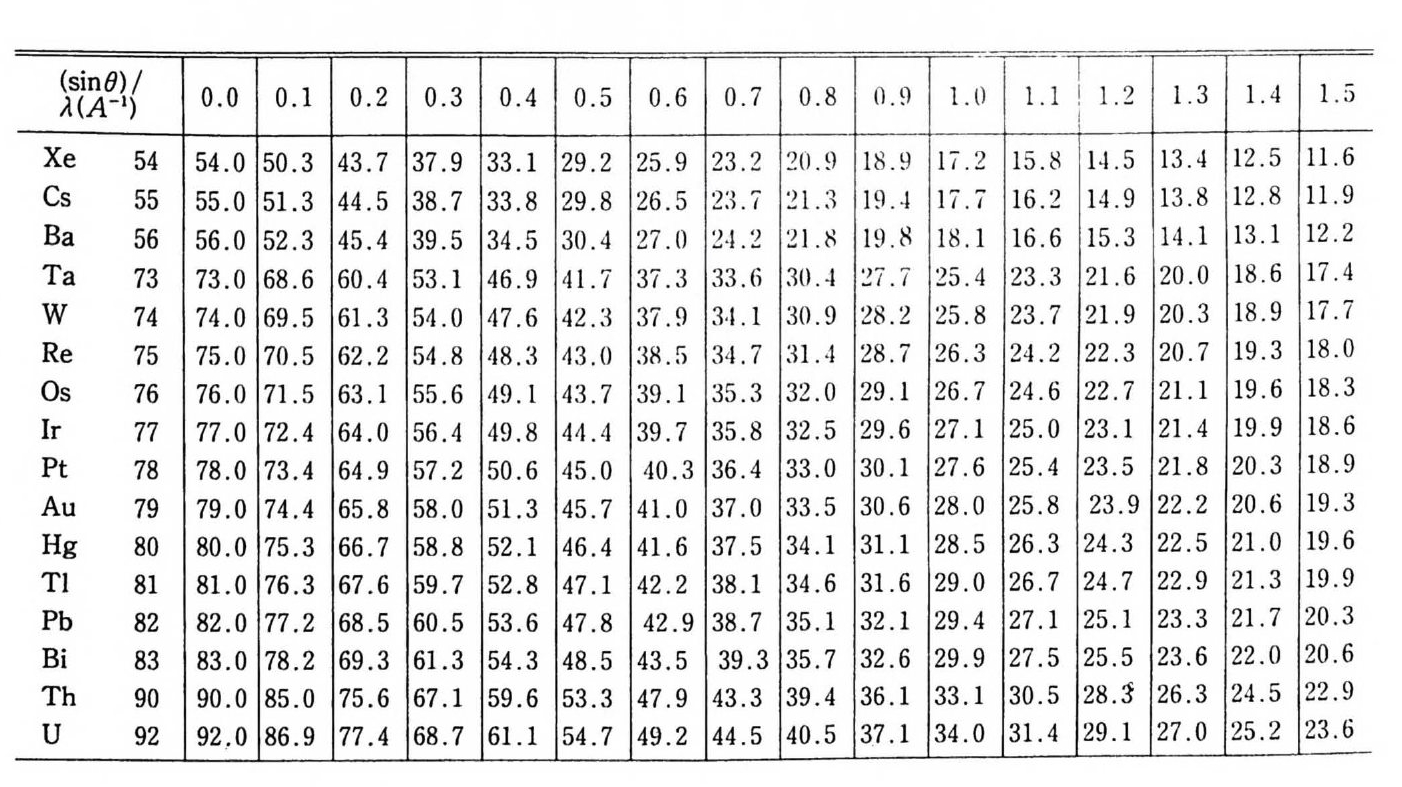 ,(HsinAO-)1)/ 0.00.1 0.20.3 0.4 0.5 0.6 0.70.8 0.9 1.0 1.1-- Iir 1. -2 1. 3 1.4 1.5
,(HsinAO-)1)/ 0.00.1 0.20.3 0.4 0.5 0.6 0.70.8 0.9 1.0 1.1-- Iir 1. -2 1. 3 1.4 1.5
연습문제 해답 제 l 장 1. (a) (120), (b) (164) , (c)(OOI ), (d) (334), (e) (043), (f) (42 3) 2. (a) mmm, (b) 2/m 3. 4 개 3, 3 개의 2, 3 개의 112 , 1 개의 T, 결정족 =(2 / m)3, 결정계 = 입 방정계 6. 2m 제 2 장 1. (a) (i) 4mm (ii ) 6mm (b) (i)정사각형 (sq ua re) ( ii ) 6 각형 (hexag o nal) 2. 대칭성이 I 보다 크게 되지 않는다. Y=90° 가 되는 삼사정계에 속하므 로 새로운 결정계는 될 수 없다. 3. (a) P(2/c) --. 2/m 단사정계 Pca21-+ mm2 사방정계 Cmcm-+mmm 사방정계 P421c-+ 42m 정방정계 P6a22-+ 622 육방정계 Pa3-+ m3 입방정계 (b) P2/c- 단순 단사정계이고 c_ 미끄럼 평면上 b, 2/ Ib Pca21-단 순 사방정계 c- 미끄럼 평면.l a 21 축/I c a- 미끄럼 평면.l b Cmcm-c 면 중심 사방정계 m. la,, C- 미끄럼 평면.l b m 평면上 c
P421C- > 단순 사방정계 4 /I c, 211 1 a 와 b CJ _ (110) 와 (110) P6322 一 단순 육방정계 6 춤 II c 2/la , b 와 u 2 가 (0001 ) 평면에서 a, b, C 축과 30° 를 이룬다. Pa3 -> 단순 입방정계 a- 미끄럼 평면J_ C b ~ 미끄럼 평면J_ a c- 미끄럼 평면 J_ b 3/I [11 1], [ 11 1], 〔 11 나 및 詞 5. (f)와 (g) 6. ( a) 사방정계 Pmm2 (b) 단사정계 P21/ C (c) 정방정계 P4 제 3 장 1. 단위세포당 1 분자가 포함되고 Cl-Cl 의 거리 =0.392 nm H g - Cl 의 거리 =0.277 nm 밀도= 4 . 266 gr/c m3 2. 0.2612nm 3. 원자간 거 리 ( nm) 밀도(g /cm 3) Al O.2861 2.705 Pb O. 3477 11. 56 6. HCP 의 충전율= 0 . 7402 면심 입방구조의 충전율 =0.74 체심 입방구조의 충전율 =0.68
s. (a) a= 1414 . 2 pm (b) a= 1154 . 7 pm 제 4 장 1. (µ/ p) air = 26 . 97cm2 /gr µair = 3 . 47X 10-2 c m- 1 2. Vx=8982 volt 3. Aun=4. 91 A 4. 1. 59 X 10-3cm 5. Axa,= l. 54072A 6. Cu Ka : Mo Ka=3.488 : 1 7. (a) Mo 의 경우게서 v= 4 . 22 X l018 sec-1 E=2.79X 1 0-s erg (b) Cu 의 경우 11= 1.945x 1018s e c~1 E= l. 29X 10-8e r g 제 5 장 I. p= I. 44 gr/c m 3 3. a= 4 . 248 X 10-8cm 4. (a) a= 5 . 450 X 10-8 c m (b) p= 3 . 204 gr/c m3 5. ( i ) a*=0.231 A-1 b*=0.115 A-1 c*=0.067A-i a•= /3*= go· , r* = 6o· (ii) V=650 A3 V·=1 .54 X10-3 A-3
(iii) dm= 1. 20 A (iv) 20=80', 4' 제 6 장 l. (a) 저심 정방정계에서 F= fex p ( 2ni( O + O+O)) +fex p ( 2ni( h /2+ k/2)) =J (l+e xp (n i( h + k)) h, k 가 혼합되면 F=O lL k 가 혼합되지 않으면 F= 2/ Cu Ka 의 파장 = 1. 54178 A sin 2 0 = (/z 탸 k 아 112/ 4 a 토 /21 12/4 c2 회절선 lz k I 20 1 0 0 1 29.78' 2 0 0 2 61.85' 3 1 1 0 66. 06 ' 4 1 1 1 74 .11 ° (b) 단순 입방정계에서 F=fe x p (2 1ri( O )) =I 회절선 h k l 28 1 0 0 1 29. 78° 2 1 0 0 45. 34 ° 3 0 1 1 55. 20 ° 4 0 0 2 61 . 85 2. Cu 는 면심 입방격자이고 h, k, l 이 혼합되면 F=O h, k, l 이 모두 짝수나 홀수면 F= 4fc u 입방체 결정에서 sin 2 8= (h2+ k2+ l 아 A2/4a2 (a) Fm에 대해 8=21. 7 : /cu=22.1
F111 = 4fc u = 88 . 4 F3 31 에 대해 0=45.O ' : fcu =14.8 F331=59.2 (b) LP= ( l + cos22 0) /si n 2 0 cos 0 (lll) 반사에 대한 LP=l2. 03 (331) 반사에 대한 LP= 2.83 (lll) 의 다중도 =8 (3ll) 의 다중도 =24 (c) 상대적 강도 Im/ f3 1 1= 10/ 3 . 2 제 7 장 1. (a) 111 과 200 (b) 1111 : 1200= 1942 : 1 2. (a) 벡터는 士 (2x, 0, 2z) Harker 면은 (x, 0, z) (b) 벡터는 土 (2x, 0, 2z) double weig h t type 1 土 (0, 2y, 0) double weig h t type 2 士 (2x, 2y, 2z) double weig h t type 3 士 (2x, 2y, 2z) double weig h t type 4 Harker 면 : (x, 0, z) 3. S(413) = S(241) S( 홍 11)=+ 4. (a) Z=2 (b) 가능한 공간군은 Cm , CZ, C2/m 이나 화학적 대칭성, Pat- t ersonma p의 특성의 조사에서 정확한 공간군이 C2 임을 판별할 수있다. (c) Se ; 0.0 6 7, 0, 0.0 2 2
Se' ; —0 . 067, 0, 一 0 . 022 5. Cu 원자의 좌표를 x, y라 하고 Cl 의 좌표를 x', Y’ 라 하자. Cu 의 원자번호는 29 이고 Cl 의 원자번호는 17 이다. 그러면 다음의 피크가 있을 것이다 . • 단일무게 (sin g le weig h t) 로서 Cu-Cu 는 2x, 2 y위치에 있고 무게 는 841 이다. • 단일무게로서 Cl - Cl 는 2x', 2 y'위치에 있고 무게는 289 이다. • 단일무게로서 Cu - Cl 은 x+ x ', y + y'위치에 있고 무게는 986 이 다. • 이중무게로서 Cu - Cl 은 x-x', y-y'위치에 있고 무게는 986 이 다. Patt er son 지도 물 검토하면 x=0 .074, y= 0 . 19 3 x'= 0 . 249, y'= 0 .14 3 이다. 제 8 장 I. (a) 총 변수수= 151 과잉으로 결정해야 할 비율 =1150 / 151=7.6 (b) 총 변수수 =61 과잉으로 결정해야 할 비율 =1150 / 61=18.9 (c) 총 변수수 =59 과잉으로 결정해야 할 바율 =1150 / 59=19.5 2. 가장 가까운 거리는 1/4, y, z 와 3/4 , y, z 사이의 거리이고 간 (Cl … Cl) = a2/4+ 4 y양 d(Cl ••• Cl) =4. 64 [2d ·a( d)]2= [2aa(a) I4]2+ 〔 8 y 2ba(b) 〕탸 〔 8 y b2a( y)〕%]다 . 따라서 a(d) = O.026A
제 9 장 1. lll, 200, 220, 3ll, 222 , 400, 331, 420, 422 와 51 1( 3ll) 이다. a=4.05A 2. BaS 3. FeCh 4. N i와 N i O 의 혼합물임 5. NaN03
참고문헌 일반적인 참고 문헌 아래의 책은 이 책을 집필할 때 참고한 책으로서 X- 선 결정학을 공부 하는 데 도움이 될 것이다. 1. L. V. Azaroff , Elements of X-ra y Cry st a ll og ra ph y , Mcg raw -Hi ll, 1968 ; 여러 가지 실험적 기술을 포함한 상세한 물리적 이론을 다룬 좋 은책임. 2 . L. V. Azaroff and M. L. Burge r, The Powder Meth o d in X-ra y Cry st a ll og ra ph y , McGraw-Hi ll, 1958 : 분말법에 대해서는 권위 있 는책임. 3. M. F. C. Ladd and R. A. Palmer, Str u ctu re Dete r mi na tio n by X-ra y Cry st a ll og ra ph y , 2nd Ed., Plenum, 1985 ; 많은 예제를 다룬 휼륭한 책임. 실제적인 문제도 많이 다루었음. 그립도 휼륭한 4. B. D. Cull ity, Elements of X-ray Diffrac ti on , 2nd ed., Add iso n-Wesley, 1978 : X- 선 회철, 각종 실험방법, 분광법과 그 웅용을 X -선 회철기기에 대해 상세히 다루었음. 5. J. D. Dunitz, X-ra y Analys is and the Str u ctu re of Orga n ic Molecules, Cornell Un ive rsit y Press, 1979 ; 이 책의 처음 300 페이 지에서는 현대 구조 결정학에 대해 상세히 설명함. 이 책은 화학지에 게 준 일련의 강좌에 기초하여 만들었음. 이 책의 뒷부분에서는 결정 구조와 화학, 록히 유기화학에 이용할 수 있는 부분에 대해 논함.
6. J. P. Glusker and K. N. Trueblood, C1y s ta l Str u ctu r e Analys i s : A Pn·me r, 2 nd ed., Oxfo r d Univ e rsit y Press, 1985 : 구조결정에 x- 선 회절이 어떻게 이용될 수 있는가를 수학은 별로 쓰지 않고 쉽 고 분명하게 기술하였음. 7. B. K. Vanis h te i n , Modem C1y st a l log ra ph y , I. Sy m me t, y of Cry st a ls . Meth o ds of Stn t c fu r al Chemi st, y , Sp ri n g e r-Verlag, 1981 . B. K. Vanis h te i n , V. M. Frid k in , and V. L. Inenboom, Modem Cry st a ll og ra ph y , II. Str u ctu r e of C1y s ta ls , S p ri n g e r-Verlag , 1982; 제 1 권에서는 결정학 책보다 더 깊이 현대 결정학에 대해 다움. 결장 의 현미경적 특성에 관한 장이 휼륭하고 회절에 관한 동력학적인 장 과 비결정질 물체에 의한 회절에 관한 장이 있고 분말 회절과 전자 회철에 대해 다루었고 제 2 권은 X- 선 회절 연구에 대한 구조적 결과 에 대해 다루었다. s. G. H. Sto u t and L. H. Jen sen, X-ra y Str u c tur e De te r mi na ti on . A Prati ca l Guid e , 2nd Ed., The Macmi llan Comp a ny, 1989 ; 이 책 은 결정학의 실험적 방법에 대한 상세한 교과서임. 즉 이 책은 결정 학은 어떻게 이루어지는가를 다루고 있는 휼륭한 책임. 9. P. Lug e r, Modern Analys i s on Sin g le Cry st a ls , W . De Gruy ter , 1980 ; 이 책의 첫 부분은 수학적 방법에 대해 다루고 X- 선 데이터 수집에 대해 그림과 더불어 기술하고 있으며 대칭과 결정구조의 해석 과 정밀화에 대해 예를 들어서 기술하고 있다. 10. T. L. Blundell and L. N. Joh nson, Prote i n Cry st a ll og ra ph y , Academi c. P ress, 1976 ; 일반적인 X- 선 결정학을 취급하고 있는 단 백질 구조결정의 가장 정통적인 책임. 단백질의 결정화와 무거운 원 소의 유도체와 분자 치환체 제조에 대한 논함. 11. R. Ste a dmam, Cry st a ll og ra ph y , Van Nostr a nd, 1982 ; 이 책 은 구조, 격자, 평면 및 결정의 기하학, 원자의 좌표, 분말 사전, 역격 자, 전자 회절에 관한 문제집. 12. L. S. Dent Glasser, Cry st a ll og ra ph y and Its Ap pli ca ti on , Van
Nostr a nd, 1977 ; 분말법에 관해 자세히 씌어 있고 광학 결정학에 대 해서도취급하고있다. 13. D. E. Sand, Intr o ducti on to Cry st a ll og r aph y, Benzami n, 1975 ; 대 칭과 결정 구조에 대해 다루고 있는 소책자. 대학 학부 학생용임. 14. A. I. Ki tai g o rodskii , Molecular Cry st a ls and Molecules, Aca-demi c Press, 1973 ; 저자는 결정구조 해석의 결과에 대해 관심을 가 지고 결 정의 충전에 대해 다루고 있음. 격자에너지, 열역학적 개념, 유기 분 자의 형태에 대해서도 다룸. 15. H. Lip s on , Crys t a l s and X-ray s, Sp ri n g er -Verlag, 1970 ; 일반적 이며 간단히 기 술 한 책임. 너무 상세히 취급하지 않는 것을 원하는 독자 를 위해 쓴 책. 16. M. M. Woolfs o n, An Intr o ducti on to Cry st a ll og ra ph y, Cambri d- ge Univ e rsit y Press, 1970 ; 결정학을 다룬 휼륭한 교과서임. 17. K. C. Homes and D. M. Blow, The Use of X-ray Diffrac tio n in tlze Stu d y of Prote i n and Nucleic Ac id Str u ctu r e, Inte r scie n ce, Wi ley , 1966 ; X- 선 회절 현상과 X- 선 결정학의 응용계 대해 다룹. Fourie r 변환과 섬유 회절법에 대해서도 잘 다루고 있음. 18. M. J. Buerge r, X-ra y Cry st a l log r aph y, Kreig e r, 1980 ; 1942 년 판의 재판임. Weis s enberg 법에 대해 찰 다루고 있음. 19. C. W . Bunn, Chemi ca l Cry st a ll og ra ph y , An Intr o ducti on to Op tica l and X-ray Meth o ds, 2nd ed., Oxfo r d at the Clarendon Press, 1961 ; 이 책은 옛날의 결정학자가 사용한 방법에 대해 명확히 설명하고있다. 20. G. H. W. Mi lbu rn, X-ra y Cry st a ll og ra ph y , Butt er wort hs, 1973 ; 이 책은 X-ray 회절법으로 결정구조를 해석하는 기본 지식을 간단히 설명하고있다. 21 . U. W. Arndt and B. T. M. W illis, Sin g le Cry st a l Diffrac to m ete r , Cambrid g e Un ive rsit y Press, 1966 ; 회철 장치 사용에 관해 자세히 논함.
22. D. Sherwood, Crys t a l s, X-ra ys and Prote i n , Long ma n, 1976 : 이 책은 기본적인 X- 선 회절이론과 구조해석 방법과 단백질 결정학에 대해 자세히 디루고 있다. 23. H. P. Klug and L. E. Alexander, X -ra y Di ffrc1c tio n Proced u re, W iley , Inte r nati on al, 1974 ; X- 선 회절의 기본게념, 회 절 의 원리. 분말법, 분말법에 의한 정성, 정량 분석, 무정형 물질과 다 결 정 질 에 대한회절법을다룹 24. D. Mckie and C. Mckie , Essen ti als of C1y s ta l l og r a pl zy , Blac k -well, 1986 : X- 선 회절이론과 분말법, 단결정법, 구조해석 이 론 과 전자 현미경에 관해 취급한 휼륭한 책임• 25. Inte r nati on al Tables for X-ray Cry •s ta l log r a p h y , Vol. I, S ym me- try Groups , N. F. M. Henny and K. Nonsdale (Eds.), K y n och pre ss, 1952 : 이 책은 공간군, 점군, 평면군에 대해 데이터 를 포 함 하고 있 다. Vol. II , Math e mati ca l Tables, J. S. Kaspe r and K. Lons da le (Eds.), Ky no ch Press, 1959 : X- 선 결정학자가 필요한 일반적인 수 학정보를 포함. 죽 Matr i x , 대수, 군론, 벡터 해석, 텐서 해석 , Fouri er 급수, Fourie r 변환, 최소자승법, 통계학, 회 절 , 역 격자 와 직접격자의 기하학, 흡수 수정식을 설명하고 있다. Vol, III, Phys i c a l and Chemi ca l Tables, C . H. Gi llar y, G. D. Ri ec k and K. Lonsdale (Ed s.), Ky no ch Press, 1962 : 이 책에서는 X 선 구조결정에 필요한 대부분의 물리, 화학적 데이터를 포함. 죽 원자산 란인자 표, 비이상산란 수정, 흡수계수, x- 선 파장 , 및 원자반경 을 포함함. Vol. IV, Revis e d and Supp le men-t ary Tables to Vol. II and III, J. A. lbers and W. C. Hami lton (Eds.), Ky no ch pre ss, 1974 ; 제 2 권과 제 3 권의 내용을 수정함 것임. Vol. A, Sp ac e-Grou p Sym m etr y, T. Hahn and D. Reid e l, 1983 : 이 책은 제 1 권의 공간군에 관한 책의 개정판임.
26. 결정학 잡지 결정학 잡지에는 두 가지 주요한 국제 학술지가 있다. (1) Acta C ry s ta, llog rap h i ca 는 1983 년 세 가지 부분으로 나누어졌다. Secti on A: Foundati on s of Crys t a l log rap h y 결정학 분야의 기본적 발전에 관한 내용 Secti on B: Str u ctu r al Sc ien ce 자연과학의 여러 분야에서 구조 연구의 결과와 구조에 관한 정보의 평가 Secti on C: Crys t a l Str u ctu r e Dete r mi na ti on 결정구조 해석의 결과를 논함. (2) jo urnal of Ap plied Cry st a, ll og ra ph y 1968 년에 시작함. 27. J. D. H. Donnay and G. Donnay (eds.), Cry st a ,/ Data ,, Dete r - mi na ti ve Tables, 1963, Americ a n Crys t a l log rap hic Assoc iat i on Sp e cia l Monog rap h , No. 5, 2nd ed. ; 이 책은 구조가 결정된 회절 패턴의 확인에 사용될 수 있는 결정 단위세포의 치수, 밀도, 공간군 을 포함함, Vol. 1 과 2 의 3 판은 J. D. H. Donna y와 H: M. Ondik 가 편집자로서 발행하였다. Vol. 3 과 4 는 1979 년에 발행하였고 무 기, 유기 화학물 45 , 000 종을 포함하고 있다. 28. 0. Kennard, D. G. Wats o n, F. A. Allen, and S. M. Weeds (eds.), Molecular Str u ctu r es and Di m ens ion s, Bi bl iog r a ph y , Orga nic and Orga n ometa l lic Cry st a ,! Stn , ctu r e, 1970 ; 탄소를 포함하는 화합물 에 정보를 제공하고 해마다 발행됨. 각 장의 참고 문헌 제 1 장 및 제 2 장 결정의 기하학 29. Inte r nati on al Tables, 참고 문헌 25, Vol I 과 Vol. A.
30. F. C. Phil lips, An Intr o ducti on to Cry st a l log ra ph y , Long m ans, Green and Co., 1946. 7 가지 결정계와 공간군에 대해 자세히 기술하고 있다. 31. M. J. Buerge r, Elementa 1y C1y s ta l log r aph y , MIT Press, 1978. 32. F. A. Cott on , Chemi ca l Ap pli ca ti on of Group Theory , 3rd, Ed., W ile y, 1990. 33. J. D. Durit z, X-ra y Analys is and the Str u ctu r e of Orga nic Molecules (참고 문헌 5) , pp. 73-98. 공간군에 대해 자세히 설명. 가장 혼한 공간군인 ·Pl. P21/ c 와 P212121 을 예를 들어 설명함. 34. P. Lu g er( 참고 문헌 9), Chapt . 3, Crys ta l Sy m metr y , pp. 111 -175, W. de Gruy ter , 1980. 35. M. F. C. Ladd and R. A. Palmer, Str u ctu r e Dete n nin a ti on by X-ray Cry st a ll og ra ph y (참고 문헌 3) ` 제 1 장과 제 2 장, Crys ta l Geometr y 1 과 2, pp. 1-102. 36. C. P. Brock and E. C. Ling a fe l te r , fou r, Chem. Educ., 57, 552 (1980). 37. L. D. Azaroff , Element of X-ray Cry st a l log ra p hy (참고 문헌 2) ` 제 1 장, 2 장, 3 장 및 4 장, pp. 2-73. 제 3 장 결정구조 38. A. Kelly and G. W. Grouves, Cry st a ll og ra ph y and Cry st a l Defe c ts , 제 3 장, pp. 92-118, Addis o n-Wesley, 1980. 39 .. B . D. Cull ity, Element of X-ray D iffr ac tio ns( 참고 문헌 4), 제 2 장, pp. 47-59. 40. F. Donald Bloss, Cry st a ll og ra ph y and Cry st a l Chemi sty, An Intr o ducti on , 제 9 장, pp. 221-284, Holt, Rin e hart and W ins to n, Inc, 1971 . 41. J. V. Smi th, Geometr ica l and Str u ct ur al Cry st a ll og ra ph y , 제 5 장,
7 장 및 8 장, Joh n W ile y, 1982. 제 4 장 X- 선의 성질 42. B. D. Cull ity, Elements of X-ra y D iffr ac ti on( 참고 문헌 4), 제 l 장, pp. 3-31 . 43. L. D. Azaroff , Elements of X-ra y C ry sta llo g ra p hy (참고 문헌 2), 제 6 장, pp. 86-134. 44. N. J. Tay lo r, Vacuum Sc i. Technology , 6, 241 (1969). 45. M. Lain g , An Intr o ducti on to the Scop e, Pote n ti al and Ap pli ca - tion of X-ra y Analys i s , Univ e rsit y Cardif f Press, 1980. 46. T. F. J. Qu in n , X-ra ys , Electr o ns and Cry st a ll in e Mate r ia ls , Butt er Worth s , 1970. 제 5 장 회절(I) 47. P. B. Ewald, Ed.Fift y Years of X-ra y Di ffrac ti on , Inte r nati on al Unio n of Crys t a l log rap y _, 1962. 48 . A. Auth i e r , The Reci pr ocal Latt ice, Inte r nati on al Un ion of Crys t a l log ra p hy , 1980. 49. L. D. Azaroff , Element of X-ra y Diffr ac ti on( 참고 문헌 l), 제 7 장, pp. 136-154, pp. 461-482. 50. M. Lain g , An Intr o ducti on to the Sop e, Pote n tia l and Ap plica- tion of X-ra y Analy s is ( 참고 문헌 45). 제 6 장 회절 (II) 51 . B. E. Warren, Acta Cry st . A, 32, 897 (1976). 52. B. D. Cullity , Elements of X-ra y D iffr ac ti on( 참고 문헌 4), 제 4 장 pp. 107-145. 53. L. D. Azaroff , Elements of X-ray C rys ta llog ra p hy (참고문헌 1), 제 8 장, 제 9 장, pp. 155-228.
54. D. Sherwood, C1y st a ls , X-ra ys and Pro t e i ns( 참고 문헌 22), pp. 227-363. 제 7 장 결정구조의 해석 직접법 55. M. F. C. Ladd and R. A Palmer, The 01 y and Prac tice of Di re c t metl w ds in Cry st a ll og ra p hy , Plenum, 1980. 56. M. M. Woolfs o n, Di re ct meth o d in Cry •s ta / l og r a p lzy , Oxfo r d at the Clarendon Press, 1961 . 57. J. P. Glusker and K. N. Trueblood, C1J •s ta l Str u ctu r e A na(}'S is ( 참 고 문헌 6), 제 8 장, 제 9 장, 제 10 장, pp. 102-149. 58. G. H. Sto u t and L. H. Jen sen, X-ray Str u ctu r e D e ter mi na ti on . A Pract ica l Gu i de( 참고 문헌 8). pp. 248-278. 중원자법 59. T. L. Blundell and L. N. Jo hnson( 참고 문헌 10), pp. 183-239. 이 장에는 단백질의 중원자 유도체롤 만드는 법을 기술하고 있다. 60. J. D. Dun itz, X-ra y Analys i s and the Str u c tur e of Orga nic Molecules( 참고 문헌 5), 제 3 장, pp. 117-123. 동형 치환법 61. J. D. Du nitz. X-ra y Analys i s and Str u c tur e of Orga nic Mole- cute s, 제 3 장, pp. 123-129. 단백질의 위상각 결정법에 대해 상세히 취급하고 있다. 62. J. P. Glusker, (ed), Str u ctu r al Cry st a, ll og ra ph y in Chemi stry and Bi olo gy , pp. 92-116, Hutc h im son Ross, 1981 . 63. M. F. C. Ladd and R. A. Palmer, Str u c tur e Dete r mi na ti on by X-ray Cry st a. ll og ra ph y , 2nd Ed. (참고 문헌 3) , pp. 266-282. 64. J. P. Glusker and K. N. Trueblood, Cr yst a ,[ Str u c tur e Analys i s (참 고 문헌 6), pp. 127-132.
이상분산 65. J. P Glusker and K. N. Trueblood, Cry st a l Str u ctu r e Analys i s, (참고 문헌 6), 제 10 장, pp. 136-148. 66. J. D. Dunit z, X-ra y Analys i s and Str u ctu r e of Orga nic M olecules (참고 문헌 5), 제 3 장, pp. 129-148. 67. J. C . Phil lips and K. 0. Hodg so n, Acta Cry st a ll og rap h i c a , A36, 856- 86 4 (19 80). 68. D. H. Temp le to n , L. K. Temp le to n , J. C. Phil lips and K. 0. Hodg so n, Acta Cry st a ll og ra p hi c a , A36, 436-442 (1980). Fourie r 금수 69. H. Lips on and W . Cochvan, The Cry st a l lin e Sta t e , Vol. III, The Dete n nin a ti on of Cry st a l Str u ctu r e, 제 4 장. 구조인자 계산은 제 5 장, pp. 60-82, Fourie r 급수의 합은 pp. 83 -108 에 있음. 70 M. F. C. Ladd and R. A. Palmer, Str u ctu r e Dete r mi na ti on by X-ray Cry st a ll og ra p hy (참고 문헌 3), 제 6 장, pp. 213-230. 71. L. V. Azaroff , Element of X-ra y Cry st a l log ra ph y (참 고 문 헌 1) , pp. 302~306. 제 8 장 시험구조의 정밀화 72. G. H. Sto u t and L. H. Jen sen, X-ray Str u ctu re De te rm i na tio n( 참 고 문헌 8) . pp. 316-317, 358-378. 7_3. D. W. J. Cruic k shak, Least-S qu ares Refi nem ent of At om i c Paramete r s, pp. 187-1~7 in Ahmed, 1969. 74. J. D. Dunit z, X-ray Analys is and the Str u ctu re of Orga nic Molecules( 참고 문헌 5), pp. 185-190, 219-220, 391-392. 75. J. P. Glusker and K. N. Trueblood, Cry st a l Str u ctu re Analy sis(참 고 문헌 6), 제 11 장, pp. 151-165.
제 9 장 X- 선 분말 회절법에 의한 화학 분석 76. J. D. Hanawalt, H. W. Ri nn , and L. K. Frevel, I nd_- Eng . Chem. , Anal. Ed., 8, 244 (1936) 및 10, 457 (1938). 77. B. L. Avebach and M. Cohen, Trans. AIME, 176, 402 (1948). 78. L. E. Alexander and H. P. Klug , Anal. Chem., 20, 886 (19 48). 79. J. Durnin and K. A. Rid a l. J. Iron and St ee l Inst., 206, 66 (19 68). so. A. W. Hull and W. P. Davey, Phy s. Rev., 17, 547 (1921). 81. H. E. Bumste d , J. Amer. Industr u al Hy gien e Assoc • pp. 150. Ap ri l 1973. 82. B. D. Cull ity, Element of X-ra y Di ffrac t i on 2n d Ed. (참고 문헌 4) pp. 140-143, 324-343 및 397- 42 0.
찾아보기
거 간섭성 산란 14 3 격 자 37~4 7 격 자의 방향 21~22 결 정 15 결 정계 31~33 결 정 족 28 결정 축 15 계수기 101 공간군명명법 %~58 공간군의 결정 188 과잉으로결정해야할비율 251 광전자 90 구조인자 155, 180~187 구형 좌표계 147 균형 필터 94 기체관 95 기호붙이기 223 L 니선축 47 나선축과 미끄럼 평면의 소멸규칙 186 내부 표준법 275, 281 E: 다이아몬드 69 다중도인자 175~ 176
단사격자 44 단순세포 38 단위세포 38 단파장한계 81 대칭요소 23~27 대칭조작 23 Deb y e-Schrrer 법 123 Deb y e-Scherrer 카메라 176 동소체 . 61 동형 치환법 226 ~2 33 동형태성 228 등방성 온도인자 173~ 175 근 Laue 법 130 Laue 식 163 Lorentz 인자 164 □ 면심 입방격자구조 62~65 미끄럼 반사평면(영전면) 47~48 M ill er 지수 16 -19 M ill er-Brava i s 지수 19 -21 t::t 방향형 21 보강간섭 105 복합세포 40 분말법 122
Bra gg법칙 104~113 14 1 Bravais 격 자의 소멸규칙 182 비 간섭성복시선 144 人 4 축단결정 회절장치 136~13 7 사각축 16 사방격자 46 사방정계 141 삼방정계 47 삼사격자 43 삼중세포 40 삼처원격자 42 상쇄간섭 105 선흡수계수 88~90 Schoen fli es 표기법 24 。 Arga nd 그림 156 압전성 189 X 선필터 92 Nacl 구조 70 역격자 113~117 연속복지선 81~83 Au g er 전자 92 Au g er 효과 91~92 온도인자 172 와이젠베 르그 (We i senber g)법 134~ 136, 164
원자 산란인 자 14 5 , 180 외부표준법 275 원자의 절 대배 열 23 3~ 241 위상인자 14 6 유리지수 16 유리지수의 법칙 18 육방 조밀 쌓멍 구 조 67~ 69 육방정계 47 이방성 열전 동 운 동 17 3 이상위상변 화 20 1 이상결 정의 구 조결 정 196 이상분산 201 이상산란 20 1 Ewald 구 118~119 이중세포 40 입방정계 47 깃: 적분강도 262 전자파 78~80 점군 28 정량분석 273~283 정방정계 46 정성 분석 265~273 직접 비교법 275~276 직접법 214 -22 5 진동결정사진법 164 진흡수 90
질량산란계수 88 질량 흡수계수 88~90 집중사진법 123 云 체심 입방격자 141 체심 입방격자구조 65~67 초전성 189 최대 반폭 167 최소자승법 249 -25 2 치환형 고용체 72 침입형고용체 72 = Comp ton 수정복뗀 144 Comp ton 효과 144 E Thomson 식 143 특성스펙트럼 83~87 立 Patt er son 함수 203 평균확률밀도 148 평면군 49 -55
Four i er 방법 192~196, 245~249 Fourie r 함수 192 Frie d el 법칙 189 --1 92 핀호울사전법 123 필라멘트관 95 F i nk 법 267 -_O Hanawal t법 266 형광수율 92 형광스크린 100 회반조작 27 회영조작 26 회전 결정법 131 회전단결정법 164 회전축 26 회절의 대칭 188 흑연 69 흡수끝 89 흡수인자 171
金洋 부산대 학교 화학공학과(공학사) , 부산대학교 대 학원 화학공학과(공학 석사) 미국 Univ e rsit y of Hawaii 대학원 화학과(이학 박사) 눌원 문화상, 부산시 문화상 및 대한화학회 학술 진보상을 수상 현재 부산대학교 자연대 화학과 교수 저서 『 현대생활과 화학 』 『 일반화학 실험 』 역서 『 물리화학 (Cas t ellan) 』 『 물리화학 (Barrow) 』 『 생명과학을 위한 물리화 학 (Barrow) 』 r 일반화학 (Brown 과 LeMa y) 』 『 최신 일반화학 (Ko t z 와 Purcell) 』 노\.프..'T Selecti ve Reducti on at th e Sin g le -C r ys ta l Surfa c e of All Mobil e Ca- tion s in Zeoli te A' '외 총 98 편의 연구 논문을 발표 X- 선 결정학 대우학술총서 • 자연과학 75 찍은날 一 1991 년 9 월 16 일 펴낸날一 1991 년 9 월 2 5 일 지은이-金 洋 펴낸이 - 朴孟浩 펴낸곳一民 音 社 충 판등록 1966. 5. 19 제 1-1 42 호 우편대체번호 010041 -31 -0523282 은행지로번호 3007786 135-120 서울 강남구 신사동 506, 강남출판문화센터 515-2003~' (편집부) 515-2000~2( 영업부) 515;2007, 2101 (팩시밀리 ) © 金 洋, 1991 자연과학 • 결정 학 KDC/469. 29 Prin t e d in Seoul, Korea 값 10,000 원
대우학술총서 자연과학 I 소립자와게이지 48 리이만 기하학 박을룡 상호작용김진의 49 群표현론 박승안 2 동력학특론 이병호 50 바선형 편미분 방정식론 3 질소고정 송승달 하기식 4 相轉移와 임계현상 김두철 51 생체막 김형만 5 촉매작용 진종식 52 수리분류학 고철환 6 뫼 스 바 우어 분광학 옥항남 53 찰스 다 윈 정용재 7 국미량원소의 영양 승정자 54 금속부식 박용수 8 수소화 붕소와 55 양자광학 이 상수 유기 붕소화합물 윤능만 56 효소반응 속도론 서 정헌 9 항생물질의 전합성 57 화성암 성인론 이민성 강석 구 58 확률론 구자홍 1 0 국소적형태의 Aliya h-Sin g er 59 분자 분광학 소현수 지표이론 지동표 60 벡터숙 이론 양재현 11 Mucop ol y sacchar i des 의 이 곤충신경생리학 부경생 생화학 및 생물리학 박준우 62 에너지([|이론 모혜정 12 천체물리학 홍승수 63 수학기초론 김상문 13 프로스타굴라딘 합성 김성각 64 신경과학 박찬웅 • 김승업 14 천연물화학 연구법 우원식 65 BCH 부 호와 Reed- 15 脂防營養 김숙회 So l omon 부호 아만영 16 결정화 유리 김병호 66 양자전기역학 김영덕 17 고 분자의 화학반응 조의 환 67 군환론 박재 걸 18 과학혁명 김영식 68 대수기하학 조영현 19 한국지질론 장기홍 69 양자장이론 이재형 20 정보이론 한영열 70 해양오염과생태계 21 원자핵반응론 정운혁 심재형 22 파괴역학 김상철 7I 바기체 연소합성 ( SHS ) E:' 여철현
