 김규한
김규한  김규한
김규한
연세대학교 지 질 학 과 및 동대학원 졸 업 일 본 나고야대학 지구과학과 ( 이학박사 ) 미 국 캘 리포니아공과대학 ( CALTECH ) 방문연구교수 현재 이화여자대학교 과학교육과 교수 저서 『 대학지 구 과학 』 『 온천지 』 『 한국의 지질과 광물자원 』 등 峰 Mi ne ralogi c a l and S tab le iso t o p e stu dies of the Shin y e m i lead-z i n c ore dep os it s South Kore 검 외 다수
 동위원소 지질학
동위원소 지질학
 동위원소 지질학
동위원소 지질학
책 머리에 Big Ban g에 의하여 태양계가 형성된 이후 지구의 내의부에서는 탈 가스, 화산활동, 지진, 조산운동, 조륙운동, 변성작용, 풍화, 침식, 퇴적, 기후변동, 생물계의 변천 등과 같은 다양한 지질학적 사건과 현상들이 일어나고 있다. 지질학적 현상의 모든 과정은 시간과 공간상에서 일어나는 특칭을 가짐과 동시에 물질간에 일어나는 뭉리화학적 반응과 생물학적 과정 이 반복되는 물질과학의 특성을 가진다. 약 200 만 년 전 인류가 등장 하기 이전의 46 억 년 동안에 일어난 지질학적 현상을 해석. .하 기 위하 여 17 세기의 제임스 허튼의 동일과정설 (U niforrnit ar i a ni sm) 에서부터 1970 년대의 판구조론 (Pla t e t ec t on ic s) 에 이르기까지 중요한 지질학적 철학과 사상이 정립되었다. 지질학적 특성인 시공간에서 일어나는 지구물질간의 반응을 정량적 으로 체계화한 학문이 바로 지구화학 분야의 동위원소 지질학이다. 지구물질의 방사성동위원소를 이용하여 지질학적 과정의 시간 개념 을 설정하여 절대적인 지질 시대를 수립하였고, 안정동위원소를 이용 하여 지구물질의 기원과 물질간의 상호반응과 지질학적 과정의 물리 화학적 조건 등을 정량적으로 해석할 수 있게 되어 동위원소가 지구 화학 분야에 광범위하게 응용 연구되고 있다. 안정동위원소는 광상학, 암석학, 수문학, 환경과학 등의 여러 분야 에서 물질의 기원, 동위원소 지질온도계, 물-암석 상호반응 등의 물 질간의 상호반응, 마그마의 혼합과 동화, 물질의 순환 등의 연구에 이용되며 연, 니오디미움, 스트론튬 동위원소비롤 이용한 지구의 전
화 연구는 동위원소 지질학의 큰 성과 중의 하나이다. 그리고 방사성 동위원소는 암석의 절대연령 측정뿐만 아니라 암석의 열역사 해석 및 트레이서로도 이용되고 있다. 따라서 이 책은 (1) 동위원소와 질량분 석 (2) 안정동위원소 지질학 (3) 방사성 동위원소 지질학 (4) 지구의 진 화로 대분하여 기초적인 이론에서 응용에 이르기까지 국내의의 연구 결과의 실례를 들어 지질학적 과정의 이해를 돕고, 대학원 및 학부 강의 노트를 중심으로 학부 고학년 학생에서 대학원생 및 일반 연구 자들의 교재 및 참고서가 될 수 있도록 집필하는 데 노력하였다. 관련 연구의 참고문헌과 인용문헌을 단원 끝에 실었으므로 구체적 인 내용은 참고문헌을 이용할 수 있게 하였다. 1979 년 저자가 일본 나고야 대학 지구과학과(지구화학 연구실)에 유 학하면서 안정동위원소 분석의 기술 습득과 이론적인 공부가 시작되 었다. 그 후 미국 Calif orn ia Instit ut e of Technolo gy와 일본 도야마 대학 등에서 연구를 계속할 수 있게 되어 이 책을 집필하는 용기를 얻게 되었다. 안정동위원소 지구과학의 학문을 처음 지도하여 주신 나고야 대학 지구과학과의 中井信之 교수에게 이 책의 출판의 영광을 돌린다. 그리고 이 책이 출판될 수 있게 지원해 주신 대우재단에 감 사하며 원고정리 등에 협력하여 준 이화여자 대학교 교육대학원생 박 재경, 이진수, 김기식 양의 수고에 사의를 표한다. 1991 년 9 월 김규한
동위원소 지질학
차례 책 머리에 • 5 제 I 부 동위원소의 발견과 질량분석 l 동위원소의 발견과 이용 17 1-1 서언 • 17 1-2 동위원소의 발견 • 18 1-3 안정동위원소와 방사성동위원소 • 19 1-4 동위원소 지구과학의 연구내용 • 23 참고문헌 • 29 2 질량분석 35 2-1 서언 • 35 2-2 질량분석기의 개발 • 36 2-3 질량분석기의 종류 • 39 2-4 질량분석의 원리 • 41 참고문헌 • 45제 2 부 안정동위원소 지질학
3 안정동위원소 지구화학 49 3-1 서언 • 49 3-2 동위원소 분별작용 • 51 3-3 동위원소 분석용 시료준비 • 78 3-4 동위원소 표시법 • 89 3-5 안정동위원소의 지질학적 이용 • 92 3-6 동위원소 지질온도계 • 96 참고문헌 • 111 4 산소 및 수소 안정동위원소 122 4-1 서언 • 122 4-2 산소 및 수소 안정동위원소의 특성 • 123 4-3 수권과 대기권에서의 수소 및 산소 안정동위원소 • 128 4-4 암석권에서의 산소 및 수소 안정동위원소 • 165 참고문헌 • 233 5 탄소 안정동위원소 245 5-1 서언 • 245 5-2 탄산염암의 동위원소비 • 248 5-3 고수온 측정 및 고기후 연구 • 252 5-4 변성암에서의 탄소 동위원소 • 256 5-5 광상의 탄산염광물 • 261 5-6 화성기원의 탄소 • 266 5-7 선캠브리아기의 탄소 • 269 5-8 우리나라 탄산염암, 셰일, 무연탄 등의 탄소동위원소 성분 • 2715-9 탄소의 순환 • 273
참고문헌 • 276 6 황 동위원소 282 6-1 서언 • 282 6-2 광상의 황 동위원소 • 286 6-3 황 동위원소 지질온도계 • 287 6-4 광화용액 중의 황 동위원소비 변화 • 290 6-5 열수계에서의 황 동위원소 • 291 6-6 멜트-유체간의 동위원소 평형 • 298 6-7 유체-광물간의 동위원소 평형 • 301 6-8 저온에서의 동위원소 평형 • 304 6-9 열수광상의 황의 기원해석 • 307 6-10 광상황의 기원 결정법 • 313 6-11 우리나라의 금속광상의 황 동위원소 성분 • 315 6-12 황의 순환 • 320 참고문헌 • 324 7 질소 안정동위원소 329 7-1 서언 • 329 7-2 질소 동위원소의 분별 • 331 7-3 질소 동위원소의 이용 • 332 7-4 만 퇴적물의 기원 • 336 7-5 생태계의 물질순환 • 337 참고문헌 • 339제 3 부 방사성동위원소 지질학
8 방사성동위원소 지질학 345 8-1 서언 • 345 8-2 방사성붕괴와 연령측정원리 • 347 8-3 방사성동위원소의 붕괴계열 • 350 8-4 시료처리방법 • 356 8-5 동위원소비를 이용한 절대연령 측정법 • 362 8-6 방사성붕괴에 의한 결정손상을 이용한 측정법 • 416 8-7 절대연령 측정결과 해석의 문제점 • 428 참고문헌 • 430 제 4 부 지구의 진화 9 지구의 진화 439 9-1 서언 • 439 9-2 원소의 합성 • 440 9-3 운석의 동위원소 성분 • 443 9-4 우주연대 측정 • 446 9-5 단반감기 핵종을 이용한 연대측정 • 451 9-6 지구의 연령 • 453 9-7 연 동위원소 진화 • 459 9-8 지각물질의 연 동위원소비 • 462 9-9 해수의 스트론튬 동위원소 진화 • 470 9-10 지구 대기의 진화 • 475 9-11 니오디미움 동위원소와 지구의 진화 • 479참고문헌 • 512
10 환경동위원소와 오염 515 10-1 서언 • 515 10-2 물의 환경동위원소값의 변화 • 516 10-3 환경수의 오염 유형 • 517 10-4 방사성 폐기물 • 520 참고문헌 • 524 부록/ l 안정동위원소의 질량과 존재도 • 529 Il 자연방사성동위원소의 반감기와 붕괴형 • 532 Ill 인공방사성동위원소의 반감기와 붕괴형 • 537 IV 지질연대표 • 544 찾아보기 • 549 제 1 부 동위원소의 발견과 질량분석
제 1 부 동위원소의 발견과 질량분석
1 동위원소의 발견과 이용 1-1 서언 자연의 물질의 동위원소의 분포와 존재량을 분석하고 이를 이용하 여 자연계에서 일어나는 여러 가지 지질학적 현상을 해석하는 지질학 의 한 분야가 동위원소 지질학 (Iso t o p e Geolo gy)이다. 동위원소는 광 물학, 암석학, 고생물학, 광상학 등 지질학의 모든 분야에 광범위하 게 이용되고 있다. 암석의 절대연령 측정, 암석의 성인 연구, 물질의 기원, 물질의 형 성환경, 물질의 순환 등의 연구에 동위원소가 중요한 연구수단으로 이용되고 있으며 지각, 해양, 지구의 진화 연구와 우주의 진화 연구 에도 동위원소가 크게 기여하고 있다. 방사성동위원소의 반감기를 이용한 암석의 절대연령 측정과, 아르 곤 유실 등에 의한 마그마 冷却史 해석 등은 방사성동위원소 연구의 결실이다. 또한 안정동위원소비를 이용하여 물질의 기원을 규명하고 동위원소 의 분별을 이용하여 물질의 생성환경을 해석하는 연구방법은 지질학 의 어떤 기타의 연구 수단보다 유용함이 알려졌다. 연 동위 원소비 (201p b / 2o•Pb, 206Pb / 2o•Pb) , 니오디 미움 동위 원소비 (143Nd/144Nd) 와 스트론튬 동위원소비 (87Sr/86Sr) 분석에 의한 지구
물질의 진화 연구는 동위원소 지구과학의 놀라운 성과이다. 먼저 동위원소의 발견과 그의 일반적 특성에 대하여 알아본다. 1-2 동위원소의 발견 동위원소란 영국의 Sodd y가 처음 사용한 용어로 동일원소에 속하 는 원자나 원자핵 가운데 질량 수가 다른 원자나 원자핵을 同位元素 (Iso t o p e) 라 한다. 죽 원자번호는 같지만 핵 가운데 중성자 수가 다 론 원소를 말한다. 동위원소의 표시는 奴)처럼 표시한다. 여기서 16 은 질량 수, 8 은 원자번호를 가리킨다. 예를 들면 수소의 동위원소는 lH, fH( D), fH 의 세 종류가 알려 져 있고 , 탄소는 i2c, i3c, H4C 그리 고 산소는 십 60, FO, A80 의 세 종류가 알려 져 있다. 일반적으로 같은 원소의 동위원소들은 화학적 성질이 유사하지만, 수소의 떤 와 탄소의 14C 동위 원소는 12c, 1ac 나 1H, D 와는 핵의 안정 성과 화학적 성질에 큰 차이가 있다. 죽, 동위원소에는 핵종이 안정한 동위원소와 불안정한 동위원소가 있어 安定同位元素 (S t able i so t o p e) 와 放射性同位元 素 (Rad i o g en ic i so t o p e) 로 나누어진다. 위의 예에서는 수소의 3H 와 uc 는 방사성동 위원소이고 나머지는 모두 안정동위원소에 속한다. 방사성동위원소의 최초 발견은 요오드 (I) 가 230Th 과 같은 화학적 성질을 가침을 알아낸 것에서 시작하여 토륨, 악티늄, 우라늄 붕괴계 열에서처럼 많은 자연 방사성동위원소와 1,000 종 이상의 인공 방사성 동위원소가 알려져 있다. 한편 안정동위원소에 대하여서는 1912 년 Thomson 이 양극선 분석 에서 네온의 동위원소인 “Ne, 22Ne 을 발견하였고, As t on 이 확산법 에 의해 이들을 구분하는 데 성공함으로써 연구가 시작되었다. 중수소가 1932 년 Ure y에 의해 발견된 후 현재까지 300 여 안정동위
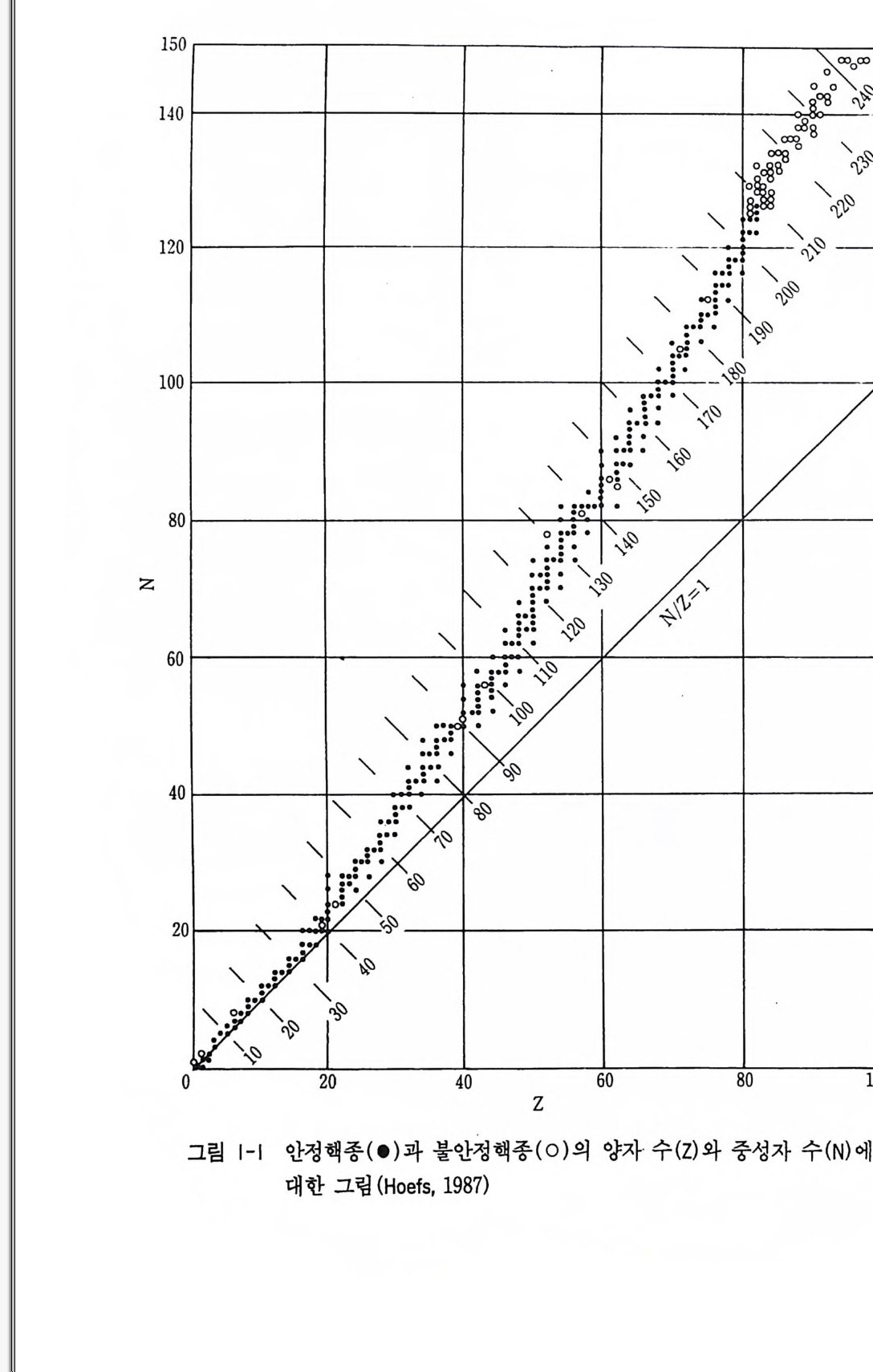
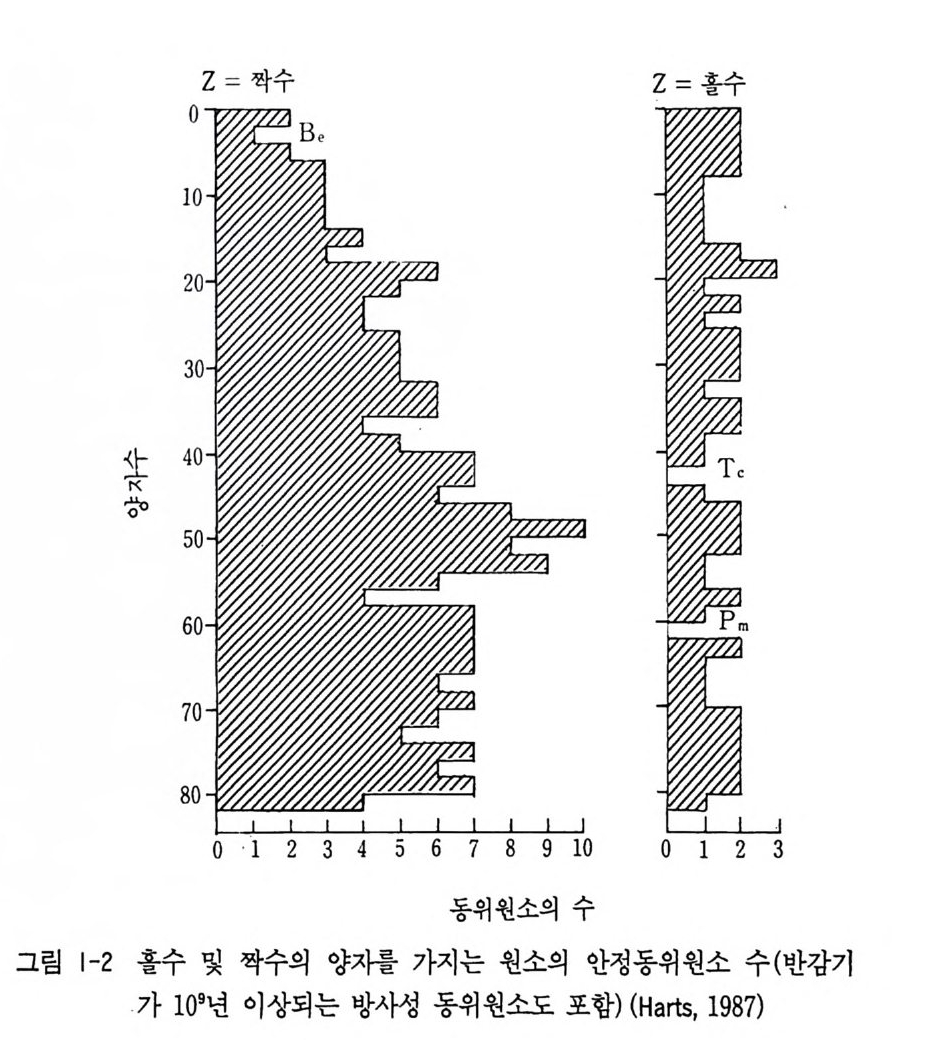
원소가 알려져 있다. 이 같은 동위원소의 분석은 질량분석기의 개발 에 의해 더욱 정밀측정이 가능해지고 있다. 1-3 안정동위원소와 방사성동위원소 안정동위원소의 ( 안정 〉 이란 의미는 방사성 붕괴 시간의 측정한계에 따른 상대적인 의미로 사용되고 있으며, 원자번호 1( 수소)에서 83( 비 스머스, B i)번까지 중 질량이 5 와 8 인 것을 제의한 모든 질량이 안정 핵종으로 되어 있다. 그중 21 원소만이 하나의 안정동위원소로 되어 있고, 그 의의 원소는 둘 이상의 동위원소의 혼합으로 구성되어 있 다. 동위원소의 존재비도 63Cu(69%), 65Cu(31% )인 것을 제의하면 거의 모두가 한 동위원소가 절대로 우세하고 여타 동위원소는 적은 양으로 존재하고 있다(부록 1 참고). 그리고 안정원소가 아닌 동위원 소는 모두 방사성동위원소들이다. 핵의 안정도는 대칭성과 오도-하킨스 법칙 (Oddo and Harkin s rule) 과 같은 규칙성을 가진다. 대칭성은 원자번호가 낮은 안정핵의 경우 질량 수와 중성자 수가 거의 같아 양자 (N) 와 중성자 (Z) 비가 거의 일 정한 것을 말한다(그림 1-1). 양자와 중성자가 20 이상인 안정핵에서는 N/Z 비가 항상 1 보다 크며 최대 1. 5 까지 이르기도 한다. 양전하로 된 양자는 Z 가 증가함에 따라 정전기적 쿨롱 반발이 급속히 증가한다. 핵이 안정하기 위해서 전기적으로 중성인 중성자가 양자와 더욱 빨리 결합하게 된다(그림 1-1) . 오도-하킨스 법칙은 양자와 중성자의 수가 홀수인가 짝수인가에 따 라 다음처 럼 Z / N비 가 짝수-짝수(1 60) , 짝수-홀수 (56) , 홀수-짝수 (50) , 홀수-홀수 (5) 로서 홀수의 양자 수보다 짝수의 양자 수가 안정 동위원소 핵종에 더 많다(표 1-1, 그립 1-2). 방사성동위원소는 자연 방사성동위원소와 인공 방사성동위원소로
 114500 :
114500 :
표 1-1 원자핵종의 유형과 산출반도수 Z-N 조합 안정핵종의 수 짝수 - 짝수 160 짝수 -홀수 56 홀수-짝수 50 홀수_홀수 5
 Z = 짝수 z= 홀수
Z = 짝수 z= 홀수
표 1-2 자연 방사성동위원소의 존재도 동위원소 존재도 (%) 반감기(년) 붕괴양식 안정산물 3H 10-1 3 12.33 g 3H e uc <1 0- 10 5 . 73 X 103 p- “N 4OK 0.0 1 167 1. 25 X1 09 EC '0Ar /3- '°Ca 50V 0.2 5 >4 X 1Q l6 EC SOTi f3- socr 87Rb 27. 83 46 4.88X l0 10 13- 87S r 113Cd 12. 3 9 X1 015 p- 1131n II5In 95. 7 5 X1 014 p- 11s sn 123Te 0.8 7 l.2X 1013 EC I23S b I38La 0.0 9 l.05 X l0 11 EC 13sB a 13- 138C e u2Ce 11. 1 >5 X 1 016 a 138Ba 10Nd 23. 9 2.1 X l 015 a 1,oc e 147Sm 15.0 l.06 X l011 a l43Nd I‘8S m 11.2 8 X1 015 a I“Nd 11IS4s629DGSymd 0013..20. 806 2l>. X11 1 XX0 11 l40Q 1l 46 aaa 1U1 ◄s S82 sGNmdd 176Lu 2.6 3.5 3 X1 01° p- l76Hf EC 176Yb 174Hf 0.1 7 2.0 X l015 a 11oy b 180Ta 0.012 >l.6X 1Q l3 EC lBOHf /3~ IBOW I87Re 62. 60 2 4 . 56 X 1010 /3- 1870s 2212293333D5812UPuPTt ah 090190..0.70 2 217 0334 9 374014. ..X247. 6 40 10 808031 XX8X1 Xll l000l09499 daaaa, , , {3g 1-3 - 222I800o&168pp OP bbbs 23 ◄ u 0.057 2.4 8 Xl05 d 230Th 7.2 5 X1 Q4 d 226Ra 1.62 2 X 103 d 21op b 22.26 d d: 딸원소, p-:베타붕괴, EC: 전자포획, a: 알파붕괴
분류된다(부록 2,3, 표 1-2 참고). 이 가운데 자연 방사성동위원소는 암석의 절대연령 측정에 이용되기 때문에 지질학에 대단히 중요하다. 방사성원소의 붕괴는 (1) 1 개의 a 입자 (me 핵) 붕괴 (2) 1 개의 8_ 입 자(음전자) 붕괴 (3) y선 방출 그리고 (4) 궤도전자 포착 (e.c. )의 형태 로 일어난다. Y 선 방출은 중핵에서의 경우에는 내부전환전자 (e 기 방출을 동반한 다. a 선, y선, 내부전환전자는 선스펙트럼 이고, /3선은 연속스펙트럼 이다. 일부 자연 방사성동위원소의 붕괴양식, 반감기 및 붕괴결과로 생긴 안정산물 등은 표 1-2 와 같다. 방사성 붕괴에 의해 주로 동위원소의 존재량이 변화하게 되며 안정 동위원소의 경우에는 주로 어떤 원소의 동위원소의 질량의 차이로 인 하여 물리화학적인 작은 변화에 의해 일어나는 同位元素分 ~1J (Iso t o p e fr ac ti ona ti on) 에 의해 자연물질에서 동위원소의 존재량 차이가 나타 난다. 이 같은 자연의 물질 중의 동위원소 존재량의 차이가 지구 내의부 에서 일어나는 지질학적 과정과 지질학적 현상의 해석에 대단히 중요 하다. 1-4 동위원소 지구과학의 연구내용 현재까지 약 1,700 여 핵종이 보고되고 있다. 동위원소는 핵화학, 분광학, 핵의학, 농학, 생물학 등의 자연과학의 여러 연구분야에서 많아 이용, 연구되고 있다. 특히 지구과학과 우주과학에 있어 동위원소는 지구 및 우주물질의 기원과 생성환경, 생성연대 그리고 지구 및 우주의 進化史 연구에 많 이 이용되고 있으며 그 결과 지질학 문제해결에 정량적으로 정밀도 높게 접근할 수 있는 놀라운 결실을 가져왔다. 동위원소는 앞에서 언급한 바와 같이 방사성동위원소와 안정동위원
소로 대분된다. 전자는 불안정한 핵종으로 된 원자로 반감기로 붕괴 하여 안정핵종으로 변하는 원소이다• 이때의 붕괴속도 관계 식 (dJ.V I dt = ― 11N) 에서 암석의 절대연령과 태양계 및 우 주 의 연령이 측정된다. 이처럼 지구연대학 및 우주연대학에 많이 이용되는 방사성 동위원소는 Rb- S r, K - A r, S m- N d, U-Th- P b, Ar-A r 등이 있다. 그 리고 1 , 000 여 종의 인공 방사성동위원소도 알려져 있으며 이 들 은 주 로 트레이서 (Tracer) 로 이용되고 있다. 한편 지구환경과학에서 많 이 이용되고 있는 수소, 산소, 탄소, 질소, 황과 같 은 안정 동 위원 소는 자연계 물질내에 안정핵종으로 존재한다. 현재 약 260 여 안정핵종이 보고되어 있다. 자 연계 물 질 은 동위원 소 교환반응과 갇은 화학적 과정, 증발 및 확산과 같은 물리적 과정 그 리고 박테리아 또는 광합성 작용과 같은 생물 학 적 과정에 의해 동위 원소 분별이 일어나 자연의 물질은 상이한 동위원소비를 가 지 게 된다• 이 사실에서 물질의 기원이나 생성환경, 물질의 순환, 고환경 ( 고기 후, 고온도 등)을 밝힐 수 있게 되었다. 지구과학에서 이들 동위원 소 를 이용한 연구의 내용과 최근 연구동향을 좀더 구체적으로 소 개하고 자한다. (1) 방사성동위원소의 연구내용 : 지구 및 우주연대학에 방사성동위 원소가 주로 이용되고 있다. 장반감기 방사성동위원소는 주로 지구 및 태양계 구성물질의 절대연령 측정에 이용될 뿐만 아니라 지각, 맨 틀의 진화, 우주의 진화 연구에도 크게 이용되고 있다. 그리고 단반 감기 동위원소는 주로 고고학 분야 및 젊은 지질시대의 물질의 연대 측정과 운석 등에서 소멸 핵종의 동위원소비 분석으로 태양계 형성 초기 물질의 同定에 이용되고 있다. 최근에는 방사성 핵종을 지구화 학적 트레이서로서 맨틀물질의 불균질성, 광상구의 구분, 맨틀에서 유래된 마그마에 지각물질의 혼합, 베니오프대에서 지각과 맨틀물질 의 순환, 범세계적인 해수의 혼합, 지구의 탈가스 (De g as) 등의 연구
에 관심이 집중되고 있다. 129I 와 26Al 과 같은 소멸핵종 (Ex ti nc t nucl i des) 은 운석내의 기타 지 구화학적 성분 연구와 함께 태양계 초기 기원물질 연구에 공헌하고 있다. 어떤 운석내에는 소멸핵종의 존재 증거가 확인되어 핵융합시차 간격 (Formati on int e r val) 결정과 태양계 형성초기의 가열과정 해석의 중요한 정보가 되고 있다. Rb- Sr , Sm-Nd 계에서 얻어진 아이소크론 (Isochron) 에서 물질형성 시의 연대가 얻어질 뿐만 아니라 부수적으로 얻어진 스트론튬의 초생 치 (87Sr / 86Sr), Sm-Nd 계에서 얻어진 Nd 동위원소비 (14 3Nd / 144Nd) 등에서 물질의 기원, 맨틀물질의 불균질성, 맨틀에서 지각의 진화사 등이 해석되고 있다. 특히 최근 지구연대학에 추가해 지구화학적 여 러 과정에서 트레이서로서의 응용에 대한 연구가 점증되고 있다 (B enne tt와 DePaolo, 1987 ; Wasserbur g와 DePaolo, 1979 ; Whit e, 1985 ; Hart 등, 1986 ; Tera 등, 1986 ; Alleg re 등, 1986, 1987) . Ar - Ar 법에서 절대연령이 얻어질 뿐만 아니라 아르곤 유실, 아르 곤 과다현상 등을 단계적 가열 실험방법으로 변성암의 변성시기 해석 과 화성암체의 냉각사 및 지각운동사 해석에까지 응용연구되고 있다 (Ber g er 와 York, 1981, Harr iso n, 1981, Nie l son 등, 1986) . E N d 와 (87Sr / 86Sr) 초생치에서 맨틀의 불균질성 해석, Pb 동위원 소 (201p b I 204Pb, 206Pb / 204Pb, 2osp b I 204Pb) 연구에 서 광상구의 구분 및 지각의 전화, 4He / 3He 바 분석연구에서 탈가스에 관한 모델이 제안 되고 있다. 방사성동위원소비 분석 이의에 휘션트랙법이나 전자스핀 공명법 등의 연령 측정법이 개발되었고 그 결과의 응용 및 해석에도 큰 성과가 얻어졌다. 그의 라돈 (222Rn) 측정 및 3He/4He 에 의한 지전 예지, 트리티 움, 14c 측정에 의한 수문학, 빙하학 연구, 우주선 생성핵종 측정에 의한 설빙학 연구, 화산암 중의 10Be 동위원소 측정에 의한 판구조론 검증 연구 등이 현재 수행되고 있는 주요 연구활동들이다.
(2) 안정동위원소의 연구내용 : 1960 년대 후반부터 산소 (180 / 160 ) , 탄소 (13 C / 12c) , 황 (“S / 32S) , 질소 (15N / l ◄ N) 등의 환경 동위 원소가 지 구과학에 이용되거 시작하여 최근에 와서는 이의 응용 분야도 방대하 며 연구 성과도 지대하다. 안정동위원소는 동위원소 교환반응과 반응속도론적 동위원소 효과 (Ki ne ti c iso to p i c effe c t) 에 의 해 동위 원소 분별 이 일 어 나 자연 계 물질 이 지질시대를 거쳐 각기 겪은 지질학적 과정에 의해 서로 다른 동위 원소바를 가지게 된다. 따라서 안정동위원소의 연구로 과거에 일어났 던 지질학적 과정변화, 환경변화 등의 地球 史를 해석할 수 있게 된 다. 따라서 안정동위원소는 광물학, 광상학, 암석학 , 고생물학, 수문학 등의 지질학의 많은 분야에서와 환경과학, 고고학 등에까지 광범위하 게 응용연구되고 있다. 특히 광상학 분야에서 동위원소의 응용연구의 성과가 지대하며 광 액의 기원, 동위원소 지질온도계, 금속광물 침전의 물리화학적 조건, 광화용액의 혼합의 정량적인 해석, 열수변질의 특칭, 광화작용의 기 구 및 성인 해석연구가 활발하게 이루어지고 있다. 반암동광상, 금은 광상, 스카른광상 등의 광화작용시 에 循環* (Mete o ric wate r ) 의 열수 계에 혼입으로 인한 금속광물의 침전기구 해석은 금세기의 동위원소 를 이용한 광상학 연구의 개가 중의 하나이다. 동위원소 분별정수가 온도의 함수이므로 공존 광물쌍을 아용한 동 위원소 평형온도 측정법이 통계역학적 이론과 실험연구로 많이 개발 되어 있다. 자연계의 모든 지질학적 과정에서 물의 역할은 대단히 중요하다. 특히 퇴적분지, 대수충, 열수계에서 일어나는 지질학적 과정에서 물 의 거동을 확인할 수 있고 물과 암석 상호작용을 정량화할 수 있다. 지열지역에서 물-암석 상호작용, 열수변질작용 등을 구체화할 수 있게 되었다. 최근에는 방사성동위원소비 분석결과와 안정동위원소비
분석을 동시에 실시하므로 마그마의 기원 등 암석 생성환경 연구에 큰 발전이 이루어졌다. 연대 측정과 동위원소 지질온도계 이용으로 나무의 나이데별로 셀 룰로오스를 추출하여 탄소, 수소 및 산소동위원소비를 분석하거나 선 캠브리아 시료의 처트 중의 인회석의 산소동위원소비 분석으로 젊은 지질시대에서 지구의 초기에 걸치는 해수온의 변동 등 지구환경 변화 사 연구를 시도하고 있다. 또 다른 동위원소 응용연구는 탄소 (013c) 및 질소 (01sN) 동위원소 비( 보분통의석 으나무로, 선쌀사, 시밀대과 인갇간은 의곡 식식류생)변은천 a의13 c 연값구의이 다범. 위식가물 — 중9~ -C136 식%물,, 이다. 그리고 질소 동위원소비 (ol5N) 도 대기 중에서 질소를 직접 동 화할 수 있는 레구민 식물 (Le gumi nes) 인 콩이나 완두 같은 것은 0%。 내외인 반면 밀이나 옥수수 같은 비레구민 식물 (Nonle gwni nous p lan ts ) 은 +9% o 내의로 동위원소바에 차이가 있다. 해양육식동물은 815N = +1 8%a, 813C = -12%a 내의의 값울 가진 다. 이같이 환경이나 식생이 다른 동식물은 각기 다른 동위원소비를 가지게 된다. 이런 점에 착안하여 연구된 다음과 같은 예가 있다. 페루의 중부 고원지역 고분에서 발굴된 인간의 뼈에서 콜라겐 (Colla g en) 을 추출, 이들 동위원소비롤 분석하므로 신석기시대 유럽 인들은 C3 식물을 주식으로 한 육성초식 또는 C3 초식을 주로 한 육식 동물(양, 사슴)을 주식으로 하였고 멕시코의 태후아칸 인디언은 C4 식 물을 주식으로 한 육성초식을 주로 하였음을 밝힐 수 있었다. 유럽인 둘이 정착하기 전 에스키모인들은 어류 등 해양 육식동물을 주식으 로 하였음이 동위원소비에서 밝혀지게 되었다 (DeN i ro (1 98 긴, DeN ir o 와 Hasto r f (l98 히 ) . 환경오염 연구로 대기의 가스 시료, 도시 및 농촌 지역의 나뭇잎의 황 동위원소비나 탄소 동위원소바 분석에서 인간활동에 의한 오염 등 의 연구도 수행되고 있다.
이 같은 연구활동은 Inte r nati on al Confe r ence on Geochronolog y, Cosmochronolog y and Isoto p e Geolog y 나 Inte r nati on al Sump o p- siu m on Wate r -Rock Inte r acti on 등의 국제 학회 에 서 나 Isoto p e Ge o- logy , Geochemi ca Cosmochmi ca Ac ta, Economi c Geolog y 등 과 기 타 지구과학 분야 전문 학술지에 다량 연구결과가 발표되고 있다. 국내에서도 연대 측정시설과 최근 안정동위원소 분석시설이 설치되 었다. 안정동위원소 분석연구는 이미 1979 년도부터 시작되어 기술습득 및 기본적인 연구가 다수 진행되어 오고 있다. 특히 우리나라의 온천, 지하수, 강수의 수소 및 산소 안정동위원소비 분석으로 우리나라 온 천수가 순환수 기원임이 밝혀졌고 지하수, 강수의 동위원소 분석에서 동위원소 값의 변화가 위도에 따른 영향보다 지형의 영향을 받고 있 음이 조사되었다. 그리고 스카론광화에도 순환수의 영향이 중요한 사 실임이 상동 중석광상의 동위원소 연구에서 밝혀졌다. 이의에 열수성 금은광상에 대한 동위원소 분석에서 열수성 금은광상의 금은광화작용 에 있어 순환수의 혼입이 대단히 중요함이 알려지게 되었다. 그 의 암석, 탄질물, 석탄 등의 동위원소비 분석, 석회암의 탄소 및 산소 안정동위원소비 분석연구에서 물질의 기원 및 퇴적환경이 해 석되었다. 1970 년도부터 시작된 방사성동위원소 분석에서 우리나라의 화성활 동의 시기가 밝혀져 중생대 쥬라기의 대보화강암류와 백악기의 불국 사화강암류의 절대연령이 다수 얻어졌으며 그 후 많은 연구자들에 의 해 연대 측칭연구가 실시되고 있다. 또한 1980 년대를 시작으로 안정 동위원소 분석연구도 지구과학 분야에 확대되어 연구가 활발히 수행 되고 있다. 지금까지 출판된 안정동위원소 및 방사성동위원소를 중심 으로 한 동위원소 지구화학 분야와 동위원소 지질학분야의 서적은 다 음과같다.
동위원소 지질학에 관한 참고문헌 Allegr e , C.J ., and G. Mi ch ard (1974) , Intr o ductz o n to geo chemi stry. D. Reid e l, Dordrecht, Holland, 142p . Arth u r, M., T.F . A nderson, I. R. Kap la n, J. Veiz e r, and L.S. Land(1983) , Sta b le iso to p e s in sedim enta ry geo log y. SEPM Short Course No. 10, SEPM, P. 0. Box 4756, Tulsa, OK , 74159. Barnes, H.L., ed. (1979), Geo che mi str y of hyd r oth e rmal ore depo s its . 2d ed. New York: Wi ley Inte r scie n ce. (This c ollecti on of b asic b y geo chemi sts at the leadin g edg e of research in ore-fo r mi ng sys t e m s has tw o long chap ter s, chapt er s 6 and 10, devote d to ligh t sta b le iso to p e s .) Bis h op , W.W. and ].A . Mi ller , eds. (19 72) , Calib r atzo n of homi no id evolutz o n. Scott ish Academi c Press, Edin b urgh , 487p . Bowen, R. (19 88) , Isoto p e s in the eart h scie n ces. E lsevie r Ap plied Scie n ce, London and New York, 647p . Brownlow, A.H . (19 79) , Geochemi stry Prenti ce Hall. Inc Eng le wood Cli ffs. N . ]., p. 4 98. Cahen, L., and N.]. Snell ing ( 19 66) , The geo chronology of equ a to r ia l Afr ica. North -H olland, Amste r dam, 195p . Cherdy nt s e v, V.V. (1969) , Uraniu m -234. Ato m i zd at, Moscow. Translate d by J. Schmorak. Israel Prog ram for Scie n ti fic T ranslati on s, Jer usalem, 1971, p. 234. Craig , H., S.L. Mi ller , and G.J . Wasserburg, eds. (19 64) , Isoto pic and cosmi c chemis try. North -H olland, Amste r dam, 553p . Currie, L.A. (1982) , Nuclear and clzemi ca l dati ng tec hniq u es; int e rp r eti ng the envir o nmenta l record. Ameri ca n Chem ica l Soc iet y , 516p . Dalry mple , G.B., and M.A. Lanph e re (19 69) , Pota ssium -argo n dati ng . Pri nc i ple s, tec hniq u es and app li ca tio n s to g eo chronology . W.H. Freeman, San Fran- cisc o, 258p . Doe, B.R. (1970) , Lead iso top e s. Spr i ng e r-Verlag, Berlin and Heid e lberg, 137p . Faul, H., ed. (19 54) , Nuclear geo log y. Joh n Wi le y, New York, 414p . Faul, H. (1966) , Ag es of rocks, plan ets and sta r s. McGraw-Hi ll, New York, p. 109. Faure, G., and J.L. Powell (19 72) , Str on ti um iso top e geo log y. Spr i n g e r -Verlag, Berlin and Heid e lberg. 188p .
Faure, G. (19 86) , Pn 1 1cip le s of Isoto p e Geolog y. ]ohn Wi ley & Sons. 589p . Ferronsky, V.I ., and Polyy ak ov, V.A . (19 82) , Envi ro 1 1me11ta l Iso to p e s i11 the Hy dr osp h ere. ]ohn Wi ley & Sons, 466p . Fleis c her, R.L., P.B. Pric e , and RM. Walker (1975) , Nuclear tra ck s in soli ds : Pri nc ip le s and app li ca ti on s. Univ e rsity of Cali forn ia , Berkeley, Los Ang el es, a nd London, 605p . Fritz , P., and J. C h. Fonte s , eds. (19 80) , Handbook of envir o nme nt a l iso to p e geo chemi stry ; Tlze ter restri al env ir o nme nt, vol. 1, Part A, Elsevie r Scie n ti fic Publish i ng Co., Amste r dam, Oxfo rd , and New York, 545p . Fritz , P., and J. C h. Fonte s , eds. (19 86) , Handbook of e11v ir o 1 1mc11t al iso to p (! geo chemis try, vol. 2, B. Elsevie r Scie n ti fic pub lis h in g Co. Amste r dam, Ox for d, and New York, 557p . Gat, J.R., and Gonfi an ti ni (1981 ) , Sta b le iso to p e lzy dr ology , De ut e r i um and oxy ge n-18 in the wate r cyc le. Inte r nati on al At om i c Energy Ag en cy, Vie n na. 337p . Geis s, ]., and E.D. Goldberg, eds. (1963) , Eart h scie n ce and mete o r itics. Nort h- Holland, Amste r dam, 312p . Geyh , M. A. (1980) , Ein f ii hn mg in die Meth o den der plzy si k a lisc l ze n und chemi s- chen Alt ers besti m mung . Wi ss enschaft lich e Buchg es ellschaft , D armsta d t, 276p . Ha milto n , E. I. (19 65) , Ap pli ed geo chronology . Academi c Press, London, 267p . Ha milto n , E. I., and RM. Farqu h ar, eds. (1968) , Radio m etr ic dati ng for geo lo- gists. Inte r sci en ce, London, 506p . Harland, W. B., A. Gib e rt Smit h, and B. Wi lco ck, eds. (19 64) , Tlze Plzane ro zoic time -scale. Qua rt . ]. Geo!. Soc. London 458p . Harland, W.B., E.H. Franci s, and P. Evans, eds. (19 71) , The Phane ro zoic time - scale. A supp le ment. Spe c . Pape r No. 5, Geo!. Soc. London, p. 356. Harland, W. B: , A.V . Cox, P.G. Llewellyn , C.A.G. Pic k to n , A.G . Smi th, and R. Walt er s (19 82) , A geo log ic time scale. Cambrid g e Univ e rsit y Press, 13lp. Harp er, C.T., ed. (19 73) , Geochronology : Radio m etr ic dati ng of rocks and min e rals. Dowden, Hutc h i nso n and Ross, Str ou dsburg, Pa., 469p . Hoefs , ]. (19 87) , Sta b le iso to p e geo chemis try. (3rd ed.) Spr i n ge r-Verlag, Berlin , Heid e lberg, and New York, p. 241 . Holmes, A. (1913) , The age of the eart h. Ha rpe r and Broth e rs, London, 194p .
Hurley, P.M . (1959) , How old is the Earth ? Doubleday, Garden Cit y, N.Y ., 160p . J섰g er, E., and J.C . Hunzik e r, eds. (1979) , Lectu r es in iso top e g eo log y. Spr i n g e r - Verlag, Berlin , Heid e lberg, and New York, 329p . Knop f, A., C. Schuchert, A.F. Kovari k, A. Holmes, and E.W . Brown (19 31) , The age of the Earth . N atl. Acad. Sci .-N atl. Res. Council, Bull., 80, 487p . Kulp, J. L ., ed. (1961) , Geochronology of rock syst e1 n s. N.Y. Acad. S ci. A nnals, 91, Art. 2, p p. 159-5 94 . Lib b y , W.F. (19 52) , Radio c arbon dati ng , Univ e rsity of Chic a go Press, 175p . Mahaney, W .C. , ed. (19 84) , Qzi a rtern ary dati ng metl wd s. E lsevie r , Amste r dam, p. 431 . Mamy ri n, B.A ., and I.N . Tolstik h i n (1984) , Heliu m iso top e s in natu r e. Elsevie r , Amste r dam, 274p . Moser, H., and W. Rauert (19 80) , lsoto p e iim eth o den in der Hy dr ologi e. Gebri .ide r Borntr a eg er , Berlin and Stu t tg a rt, 4 00p . Odin , G.S ., ed. (1982) , Numeri ca l dati ng in stra tig ra ph y , 2 vols., Joh n Wi ley , Chic h este r , U.K ., 1040p . Ozim a, M., and F.A . Podosek (1983) , Nobel gas geo chemi stry. Cambri dg e Univ e r- sity Press, 367p . Rankama, K. (19 54) , Iso to p e g eo lo g y. Perga m on Press, London, 535p . Rankama, K. (1963) , Prog re ss in iso top e g eo logy . Inte r sci en ce, London, 705p . Ric h ardson, S.M ., and H.Y . Jr. McSween (1989) , Geochemi stry Path w ays and proc esses. Prenti ce Hall, Eng le wood Cli ffs, New Jer sey, 488p . Robin s on, B. W ., ed. (1978) , Sta b le iso top e s in the eart h s cie n ces. Scie n ce Inf or ma- tion Div is io n , Dep t. Scie n ti fic and Industr ial Research, Bull. 220, P.O . 9741, Wellin g t on , New Zealand, 230p . . Romer, A. (1960) , The restle ss ato m . Doubleday and Co., G arden City , N.Y ., p. 198. Romer, A. (1971) , Radio c hemi stry and tlze disc o v ery of iso top e s. Dover, New York, 261p . Russell, RD., and R.M . Farqu h ar (19 60) , Lead iso top e s in geo logJ •. Inte r sci en ce, Joh n Wi ley , New York, 243p . Schaeff er , O.A ., and J. Zahrin ger , eds. (19 66) , Pota ssium arg o n dati ng . Spr in g e r- Verlag, New York, 234p . Schop f, J.W . , eds. (19 83) , Eart h 's earlies t bio s p h ere, ifs orig in and evoluti on . Prin c eto n Un ive rsity pre ss, P rin c eto n , New Jer sey, 543p .
Sto c kwell, C.H. (19 82) , Prop os als for time classifi cat i on and correla ti on of Precambnan • rocks and events in Canada and adja c en t areas of the Canadia n Shie ld . Part 1. A tim e classifi ca ti on of Precambria n rocks and events . Geo!. Surv. Canada, Pape r 80-19, 135p . Valley, J. W., Tayl o r, H.P., a nd O'Neil , J .R . , eds. ( 1986), Sta b le iso top e s in /ug h tem p er atu r e geo log ica l pro cesses, Revie w s in M i neralo 節' 16, Washin g t on , D.C., Mi ne ralog ica l Socie ty of Americ a . Van der Merwe, N.J . (1969) , The carbon-14 dati ng of iro n. Univ e rsity of Ch ica go Press, 1 37p . Weth e rill , W. (19 65) , Geochronology of Norlh Ame ,i ca . Natl. Acad. Sci. - N atl. Res. Council , Pub. 1276, p. 3 15. York, D., and R.M . Farqu har (1972) , The Earth ' s age a11d geo c hronology . Perga mon Press, Oxfo r d, 178p . Zeuner, F.E. (19 52) , Dati ng the pas t. Meth u en and Co., London, 3rd ed. 495p . 倉沃一 (19 70) , 同位體地質學, 弓 子 1 7-., 275p . 佐野博敏 • 富永健 (1978), 『 同位體&化學 』 , 廣川 苦 店, 298p . 小뺄稅 • 齋藤常正 (1982), 岩波講座 地球科學 6 r 地球年代母 』 , 岩波 音 店, 255p . 月 刊地球 (19 87) , r 同位體地球科學 J , 海洋出版株式 會 社 9 (10 ) pp. 544-614. 참고문헌 Alleg re, CJ ., Sta u dacher, T., and Sarda, P., 1 986-1987, Rare gas sys t e m ati cs : Formati on of the atm o sph e re, evoluti on and str u ctu r e of the eart h's mantl e. E a.rth Planet. Sci . Lett. 81: pp. 127-50. Armstr on g , R.L., 1971, Isoto p i c and chemic a l constr a in t s on models of magm a gen esis i n volca nic arcs. Ea.rth Planet. Sci . Lett. 12, pp. 137-42. Barreiro , B., and Clark, A.H ., 1984, Lead iso to p i c evid e nce for evoluti on ary chang es in magm a -crust int e r acti on , Centr a l Andes, south e rn Peru. Ea.rth Planet. Sci . Lett. 69, pp. 30-42. Barnes, H.L., e d. , 1979, Geochemi stry of hyd roth e rmal ore dep o sit s. 2nd ed. New York: Wi ley Inte r scie n ce. Bennett , V.C., and DePalo, D.J. , 1987, Prote r ozoic crusta l histo r y of t he weste r n Un ited Sta tes as dete r mi ne d by neody mium iso to p i c mapp ing . Geo!.
Soc. Am. Bull. 99, pp. 674-85. Berge r , G. W., and York, D., 1981, Geoth e rmometr y from '0Ar / 39Ar dati ng exp er im ents . Geochim . Cosmochim . Acta . 45, pp. 795-811 . Clay ton , R.N ., 1981, Isoto p i c the nnometry . In Thennodyn a mi cs of min e rals and melts, ed. Newt on . R.C ., Navrots k y, A., an d Wood, B.J. , 85-109. New York: Spr i n g e r Verlag. DeNi ro , M.J. , 1 981, Sta b le iso to p e and archaeolog y. Arner. Sci en ti st, 75, pp. -91. DeNi ro , M.j., and Hasto r f, C.A ., 1 985, Alte r ati on of 1 5N / 뺑 and 13( / 12C rati os of pla nt matt er durin g the int ia l sta g e s of dia g e n esis : Stu d ie s uti lizin g archaeolog ica l spe c im ens from Peru. Geochim . Cosmochim . Acta 49, pp. 97-115. Ellis , A .J., and Mahon, W. A.J., 1977, Geochemi stry and geo th e m w.l sys tem s. N ew York : Academi c Press. Faure, G ., 1 986, Pri nc i ple s of iso to pe geo log y. 2d. ed., New York: Joh n Wi ley and Sons. Gearin g , J. N., g ea rin g , P.J ., Rud nick , P.T., R eq ue io , A.G ., and Hurchi ns , M.J., 1984, Isoto p i c varia b il ity of orga n i c carbon in a phy t op l a nkto n -based tem p er ate estu a ry . Geochim . Cosmochim . Acta 48, pp. 1089-98. Harriso n, T. M., 1981, Di ffus io n of '0Ar in hornblende. Contr ib. Mi ne ral. Petr o l.,78, pp. 324-31 . Hart, S .R. : G erlach, D.C., and W 血 e, W.M., 1986, A pos sib l e Sr-Nd-Pb mantl e array and conseq ue nces for mantl e m ix i n g . Geoch im . Cosmochim . Acta 50, pp. 1551-57. Hatt or i, K., and Halas, S., 1982, Calculati on of oxyg e n iso to p e frac ti on ati on betw e en uraniu m dio x i de , urani um trio x id e , and wate r . Geochim . Cosmochim . Acta 46, pp. 1863-68. Hoefs , J., 1980, Sta b le iso top e geo chemi stry. 2d ed. New York: Spr inge r Verlag. Holser, W. T. and Kap la n, LR ., 1966, Isoto p e geo chem istr y of sedim enta ry Jag e r , E.s, ualfnad t eHs .u nzCihk eem r,. JG.Ce o.,l . 1l9,7 9p,p .L 9e3c-t1u 3r e5s. in iso top e geo log y. Berlin, spn nge r Verlag. Mats uhisa , Y., Goldsmi rh , J.R., and Clay ton , R.N ., 1979, Oxyg e n iso to p i c frac ti on ati on in the sys t e m qua rt z- albit e-a nort hite- wate r . Geochim . Cosmochim . Acta 43, pp. 1131-40.
My er s, J.D ., Marsh, B.D ., a nd Sin h a, A.K . , 1985, Str on ti um iso to p i c and selecte d trac e element varia t i on s betw een tw o Aleuti an volcanic cente r s (Adak and At ka ) : Imp li ca ti on s for the develop m ent of arc volcanic p lu mp b in g sys t e m s. Contr ib. Mi ne ral. Petr o l. 91, pp. 221-34. Nie ls on, D.L ., Evans, S.H . , and B.S ., 1986, Magm a tic , str u ctu r al, and hyd r oth e r- mal evoluti on of the Mi ne ral Mounta i n s int r us iv e comp le x, Uta h . Geo!. Soc. Amer Bull. 97, pp. 765-77. Tera, F., B orris, ]., S acks, I.S. , Klein , J., a nd Mi dd leto n , R., 1986, Se dim ent inc orp o rati on in isla nd-arc magm a s: Infe r ences from 10Be. Geochim . Cosmoclzim . Acta 50, pp. 535-50. Valley, ].W., Tayl o r, H.P., an d O'Neil, J.R., eds., 1986, Sta b le iso to p e s in hig h tem p era tu re geo log ica l pro cesses, Rev ie w s i11 Mi ne ralogy 16, Washin - gton , D.C.: Mi ne ralog ica l Socie t y of America . Wasserburg, G.J ., a nd EePaolo, D.] ., 1 979, Mo dels of earth stru c tu r e infer red from neodym ium and str on ti um iso to p i c abundances. Proc. Nat. Acad. 函 USA 76, pp. 3594-98. W 血e , W. M ., 1985, Sources of oceanic basalts : Radio g e n ic iso to p i c evi de nce. Geology 13, pp. 115-18. York, D., 1 966, Least-s qu a res fitting of a str ai g h t line . Can J Phys . 44 pp. 1079-86.
2 질량분석 2-1 서언 1886 년 음극선관 실험과정에서 골드스타인 (Golds t e i n) 은
성물질 원소의 동위원소비 분석으로 지구 구성물질의 기원, 성인과 생성 및 변천 환경연구에 그 중요성이 점점 증가하여 동위원소 지구 화학, 동위원소 지질학의 새로운 학문을 탄생시켰다. 2-2 질량분석기의 개발 질량분석장치는 독일과 영국에서 연구와 개발이 시작되었다. 독일의 물리학자인 골드스타인(1 886) 이 진공방전 실험중에 양극선 울 발견하고 이의 입자선의 정체를 확인하기 위해 편향장으로 전장과 자장을 이용하였다. 이 편향장에 의한 양극선 분석장치가 편향적 질량분석장치의 시초 이다. 본격적인 질량분석은 1907~1940 년경 영국의 톰슨과 그의 제자 인 아스톤에 의해 시작되었으며, 1910 년 파라볼라형 질량분석장치 (Parabola-ty pe mass s p ec tr o gr a p h) 가 제작되어 1912 년에는 네온 (Ne) 의 안정동위원소 20Ne 와 22Ne 를 발견하였다. 그 후 이들은 速度收束 質 量 分析器 (Velo city-fo cus i n g mass spe c tr o - mete r ) 를 완성 하여 1930 년대 까지 약 50 종 이 상의 안정 동위 원소를 발견 하였다. 이 분석방식은 편향장의 강도를 일정하게 해서 각각 다른 궤도를 통해 모아진 이온의 질량스펙트럼을 사전으로 현상해 스펙트럼의 검 은 정도를 측정하는 방법이다. 한편 영국의 뎀스터는 1918 년 방향수속 질량분석계 (Dire cti on fo c us- ing mass s p ec tr ome t er) 를 개발하여 영류룰 필라멘트에 부착 가열 증 발시킨 다음 열전자로 충격시켜 이온화하는 방법을 이용했다. 죽 이 것은 파라데이 상자의 위치를 고정해서 편향장의 강도를 변화시켜 동 일궤도를 통하게 해서 각각 다른 시간에 파레데이 상자에 입사한 m/e(m: 이온의 질량, e: 이온의 가수)가 다른 이온의 전기량을 연속 적으로 측정해 질량스펙트럼을 만들어 m/e 가 다른 이온량을 비교
결정하는 방법이다. 이 방법이 현재에 사용되고 있는 이온검출 방식의 질량분석법이다• 그 후 1935 년 이 중 수 속 질 량 분 석 기 (Double-fo c usin g mass s p ec t ro gr a ph y)가 완성되어 고체원소를 이온화시킬 수 있음과 동시에 多價이온을 이용하여 무거운 고체원소에서 m / e 가 작은 원자이온을 만들어 이중선 (double t)의 측정정도를 향상시켜 분해능을 30, 000~60, 000 까지 올렸다. 1950 년대 이후 진공기술의 향상과 함께 독일의 니어, 일본의 松田, 베인브리지, Matt au ch, 헤르조그 등이 분해능 100, 000~500, 000 의 이 중수속 질량분석계를 제작했다. 특히 니어는 편향각 180 ° 인 뎀스터형을 편향각 60 ° 의 대칭형 단수 속 질량분석계인 어어 〉 형 질량분석기를 제작하였다. 그 후 헤르조그 등에 의해 분해능 100, 000~500, 000 의 아중수속 질량분석기가 제작되
 사진 2-1 질량분석기와 시료자동주입장치
사진 2-1 질량분석기와 시료자동주입장치
었다. 이 질량분석계는 동위원소비를 직접 측정하기 위해 두 이온 빔울 동시에 검출 가능하게 제작되어 있다. 니어형 질량분석기를 이용 Ca, Ti, S, Ar, Sr, Ba, B, Ti, Hg , Ne, Kr, Rb, Xe, C, N, 0, K 등의 많은 원소의 동위원소비를 분석하였다. 그 후 McKi nn ey 의 (1950) 에 의해 니어형이 개조되어 DI H , 13C / 12c, 1so 1160, 34s 132s 등이 정 밀히 측정 될 수 있게 되 었으며 최 근에
 /\
/\
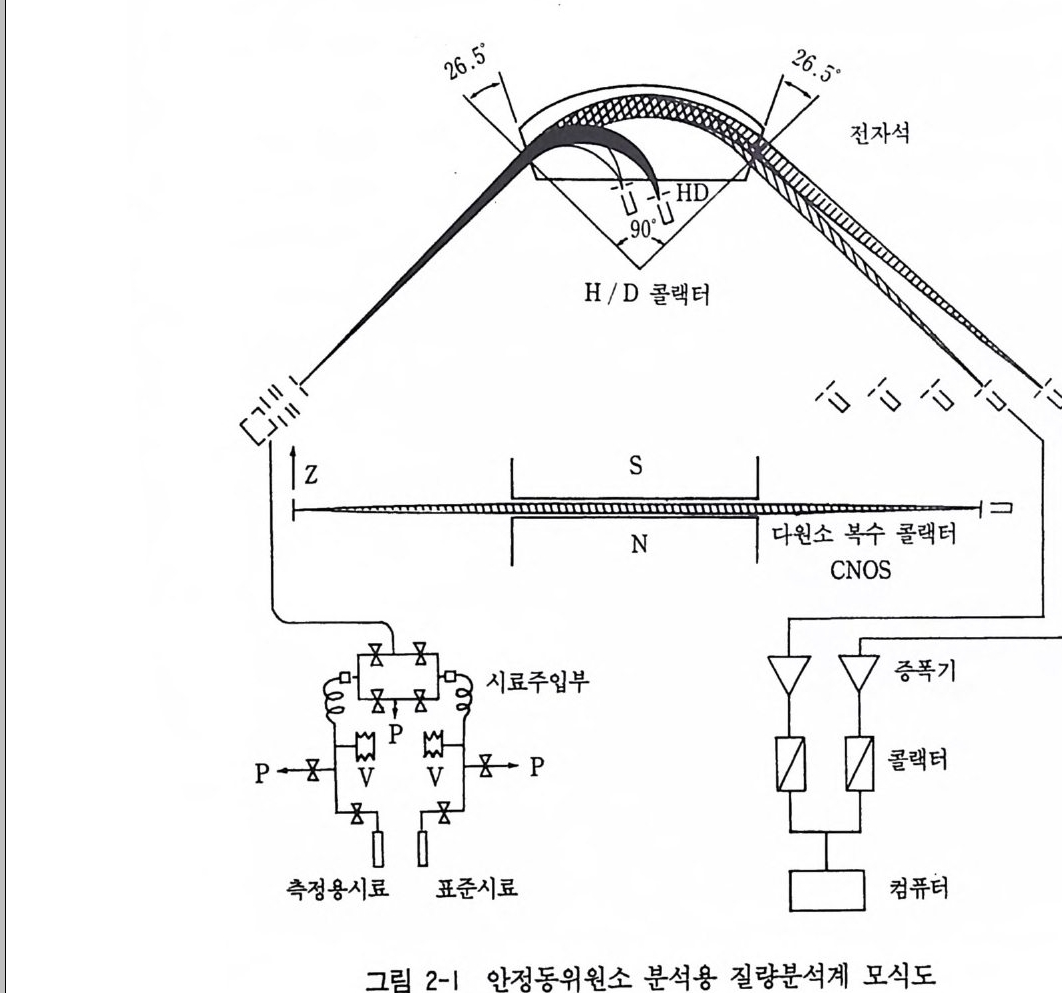
는 컴퓨터를 이용한 디지탈 자료수집 시스템이 부착되어 있고 일부 시료에 대해서는 시료처리에서 시료측정까지 자동화되어 있다(사진 2-1) . 이들은 H / D 와 CNOS( 탄소, 질소, 산소 , 황)의 동위원소 분석 겸용이 가능하다. MAT 251 의 이온광학시스템 (Ion opt ical s y s t em) 은 이온 빔을 26. 5' 각도에서 90 ° 의 자장내로 조사시켜 다원소 복수 콜렉 터 (MEMCO, multie le ment mul tic ollec t or) 나 CNOS 콜렉터로 측정하며 CNOS 이온 용 23 cm 의 편향반경을 가지고 있다• H/ D 측 정을 위한 H2 / H D 이온경로는 자석의 중앙부의 이은광 학시스템에서 튀어나온다(그립 2-1) . 2-3 질량분석기의 종류 지질학에 이용되는 질량분석기는 다음 7 가지 종류가 있다. 이들은 ® 스파크원 질량분석기 (Sp ar k source mass spe c tr om etr y) @ 가열 이 온화 질 량분석 기 (Thermal ion iz a ti on mas spe c tr o metr y) @ 가스용 질 량분석 기 (Gas source mass spe c tr om etr y) © 2 차 이 온 질 량 분석 기 (Secondary ion mass spe c tr om etr y) @ 프라즈마 질 량분석 기 (In- ducti ve ly coup le d pla sma mass spe c tr om etr y) @ 가속기 부착 질 량분석 기 (Accelerato r -based mass spe c tr om etr y) @ 레 이 저 질 량분석 기 (Laser mass spe c tr om etr y) 등이 다. 이들을 좀더 구체 적으로 설명 하면 다음 과같다. ® 스파크원 질량분석기는 지질학적 시료분석에 처음으로 많이 사 용되었던 것이다. 시료를 흑연과 같은 전기전도접합제와 섞어 압축해 서 전극으로 만든다. 시료전극과 계측전극 사이에 무선주파수 전기방 전을 시켜 이온화시킨다. 이 이온을 자석과 정전기 섹터로 된 이중수 속 질량분석계로 보내 측정한다. ® 가열 이온화 질량분석기는 시료를 탄탈륨 (Ta) 이나 레니움 (Re)
 7I
7I
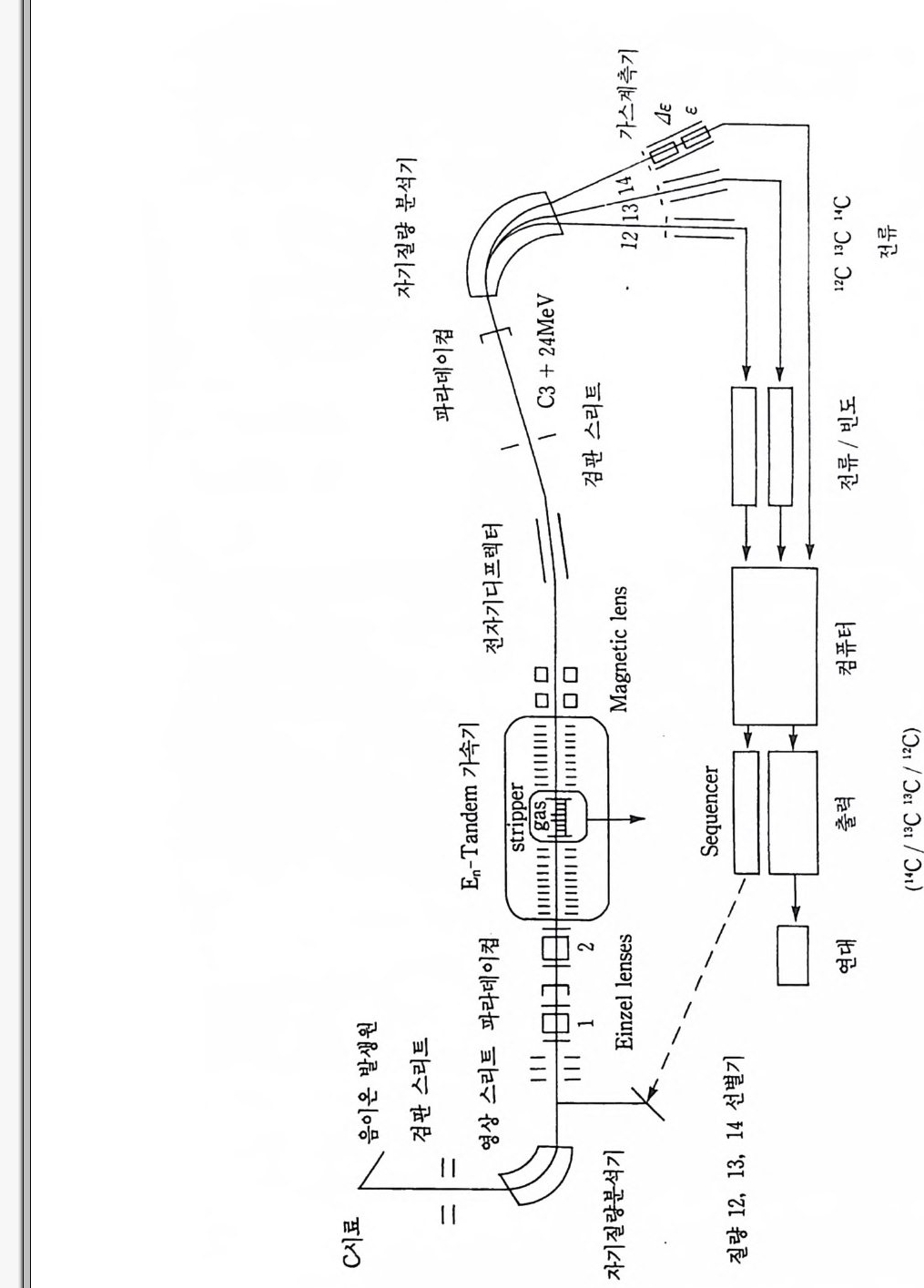
리본 위에 놓고 Rb I Sr 이나 Nd / Sm 과 같은 방사성원소의 상대적 존재비의 정밀분석이나 동위원소 희석분석 (Iso to p e dilu t i on anal y s i s) 을 하는 데 크게 응용된다. @ 가스용 질량분석기는 질량분석기 중에 가장 광범위하게 이용되 며 유기, 석유화학 산업에서 유기분자를 연구하는 데 이용된다. 그리 고 무기화학에서는 수소, 탄소, 질소, 산소, 황, 불활성 가스의 안정 동위원소비 분석에 이용된다. @ 2 차 이온 질량분석기는 박편에서 개개의 광물의 분석을 위해 마 이크로 빔을 사용하여 분석하는 것이며, 160-, Ar-, Cs + 와 같은 이온 빔을 시료에 조사한다. 이때 시료 표면에서 튀어나온 이차적 이온둘 을 질량분석계에서 분석하며 광물 중의 Ni, Sr, Pb 같은 미량성분의 동위원소비 분석에 이용된다• ® 프라즈마 질량분석기는 최근에 개발 응용된 것으로 이온원으로 Ar 프라즈마를 사용한 것이다. 시료중의 미량성분의 함량분석에 이 용된다. ® 가속기 질량분석기는 최근 “C 등의 방사성동위원소를 이용한 연대측정 등에 활용되는 가속기가 부착되어 있는 초감도 측정 질량분 석기이다(그림 2-2). 이 분석기의 장점은 저농도의 우주 방사성핵종 (IOBe, “C, 26Al, 36Cl, 1 미 등)의’ 극소량의 시료에 대하여도 정확도 높게 측정이 가능하다는 점이다. ® 레이저 질량분석기는 비유기화합물의 열에 의한 이온화와 증발 작용에 의해 일어나는 질량 식별효과를 이해하는 데 활용되었으며 10Be, 1291 와 같은 단반감기 방사성핵종 존재량의 측정 등에 이용되고 있다. 2-4 질량분석의 원리 질량분석계는 시료의 이온화를 가속시키는 이온원과 가속된 이온을
편형자장에 의해 질량별로 분리시키는 분석부와 분리된 이온을 검출 하는 측정계로 구성되어 있다. 질량이 m 이고 전하가 e 인 이온이 전 위차 V( 가속속도)로 작용할 때 요하는 에너지 E 는 다음과 갇다. E = eV = 1 / 2 mv2 (1) 여기서 v 는 이온의 속도이다. 동일한 전위차 V에 의해 가속되기 때문에 동일한 전하를 가지는 모든 이온은 동일한 운동 에너지를 가지고 이온원에서 빠져나간다. 그러나 질량이 다른 이온은 그의 속도가 다르다. 즉, v= 군 (2) 이온이 자장에 들어갈 때 다음 조건에 맞게 타원형으로 편향된다. HeV=~vr2 (3) 여기서 H 는 자장의 강도이며, r 은 자장이 통과하는 타원형의 반경 이다. 식 (1) 과 (3) 에서 v 를 소거하면 다음과 같이 된다. 享m= -旦 모m2亡 ' 쁘e -= 2旦v (4) 여기서 H 는 가우스 (Gauss) 로, r 은 cm 로, m 은 원자질량단위로, v 는 볼트로, 슌근 전자의 전하단위로 표시하면 위의 식은 다음과 같이 된다.
—me = 4.825X 1 0-s—H 모V (5) 위의 (5) 식에서 r 이나 H에 대한 해가 얻어진다. r = 143H95 근 !._ (6) 또는 H = 브隣〔군~ (7) 위 ( 7 ) 식 을 이 용하여 V = 10000 vol t에서 40c 강 이온이 분석 관 듀브 의 반경이 30.48cm 이면 질량분석기의 검출기로 들어갈 때의 자장을 계산할 수 있다. 40ca+ 이온의 전하는 e = 1 ecu(electr on ic charge unit)이고, 질량 m 이 39. 9626 amu 이므로 H = 944 g auss 가 얻어진다. (6) 식에서 가속전 압이나 자장은 질량 m, 전하 e 인 임의의 이온이 자석내에서 통로의 반경 r 을 통과할 때 조정될 수 있는 힘이다. 즉, H, V 가 정수라면 위의 식은 r oc .fm이 되어 이온이 분석관을 통과하는 반경은 질량의 제곱근에 비례한다. 따라서 가벼운 이온에 비해 질량이 큰 이온일수록 더 큰 반경으로 편향된다. 다시 말하면 CO2 의 경우 탄소는 동위원소가 12c, 13c, 14c 가 있고, 산소는 160, 170, 180 가 있어 이들의 조합 중 가벼운 12(16 Qt보다 13c1601so+ 의 무거운 CO2 가더 큰 원을 그리며 자석내를통과하게 된다. (4) 식에서 v, r 을 일정하게 하면 이온의 m/e 의 차이는 H 의 변화 로 나타나기 때문에 측정부에서 복식 콜렉터에 입사되고 있는 아온전 류의 강도비를 정밀히 측정할 수 있다. 시료의 질량분석을 위해 복식 시료도입부 (Inle t s y s t em) 에서 표준시료 가스와 미지의 측정시료 가스 를 일정한 시간 동안 전자식 교환발브를 통하여 번갈아 이온원으로 주입시켜 3~5 KV 가속에 의해 이온화시킨 후 편자장내로 통과시켜
복식 콜렉터에서 이온전류의 강도비를 측정하여 미지의 시료원소의 동위원소비를 측정한다. 참고문헌 Andersen, C.A ., a nd J.R . Hin t h o me (19 72) Ion mic r opr o be mass analyz e r. Sci en ce 175, pp. 853- 86 0. Arrien s, P .A., and W.Comp st o n (19 68) , A meth o d for iso to p i c rati o measure - ment by volta g e pea k s,vit ch in g , and its a pp li ca ti on wit h dig ital inp u t. Int. J. Mass Spe c tr o m. Ion Ph;'S., 1, pp. 471- 481 . Asto n , W. F. (19 19) , A pos it ive ray spe c tr o g rap h . Phil . M ag ., Ser. 6, 3 8, 707- 714 . Boelrij k, N.A. I.M . (19 68) , A gen eral fon nula for 'do uble' iso to p e dilu ti on analys i s. Che m . Geo!., 3, p p. 323-325. Broecker W. S., and V.M. Oversby (19 71) , Che mi ca l equ i li b r ia in the ea,1 /z . McGraw Hil l Book Co., 318p . Brown, L. (19 84) Ap pli ca ti on s of accelerato r mass spe c tr o metr y. Ann. Rev . Eart h Planet. S ci ., 12, pp. 39-59. Bowen, R. (19 88) , Isoto p e s in tlie Eart h Scie n c es . Elsevie r Ap pli ed Scie n ce London and New York, 647p . Comp st o n , w., Kinn y, P.D., Wi lliam s, LS. and Foste r , ].]., ( 1986), The age and loss behavi ou r of zirc ons from the Isua sup ra crusta l belt a s dete r mi ne d by ion micr op ro be: Eart h Planet. Sci. Lett. 80, pp. 71- 81 . Comp ston , W. , Wi lliam s, I.S. , and Meye r , C. (1984), U-Pb geo chronolog y of zirc ons from lunar brecci a 732,7 usin g a sensiti ve hig h mass-resoluti on ion micro p ro be. Proc. XIV Lunar Planet. Sci . Con£ ., ]. Geop h; 's. Res., 89 (Sup pl.) pp. B525-B534. Cummi ng , G.L. (19 73) , Propa g a t i on of e xpe r im enta l errors in lead iso to p e rati o measurements usin g the double spi ke meth o d. Chem. Geol., 11 , 157-165. Demp st e r , A.J. (1918) , A new meth o d of p os it ive ray analys i s. P hys . Rev., 11, pp. 316-325. Dodson, M.H. (19 70) , Sim plied equ a ti on s for double-spi ke d iso to p i c analys e s. Geochim . Cosmochim . Acta , 34, pp. 1241-1244.
Duckw o rth , H.E . (19 85) , Mass spe ctr o s cop y . Cambrid g e Univ e rsity Press, 206p . Faure, G., and J. L . Pow el l (1972) , Str o n tiu m iso top e geo lo gy . Spr i n g e r -Verlag, Berlin , H eid e lberg, and Ne w York, p. 1 88. Gale, N.H. (19 70) , A soluti on in closed form for lead iso to p i c analys i s u sin g a double spi ke . Chem . Geo ! ., 6 , p p. 305-310. Lit he rland, A.E. (19 79) , Dati ng meth o ds of Pleis to c ene dep os it s and the ir pro blems: T he pro mi se of ato m counti ng . G eosci . C anada, 6, p p. 80-82. Lithe rland, A.E . , A llen, K.W ., and Hall, E .T . (Ed s) , (1987), Ult ra -h ig h -sen si tz'v it y ma ss spe ctr o me try wit h accel er a to rs . The Roy al Socie t y , London, p. 1 72. Long, L.E . (19 66) , Isoto p e dilu t io n analys i s o f common and radio g e n i c stro n- tium usin g 8'S r-enric h ed spi ke . Eart h Planet. Sci. L et te rs , 1, p p. 289-292. McDowell, C .A . (19 63) , Mass spe ct ro me try . McGraw-Hil l, New York. McKi nn e y, C.R., J.M . , M cCrea, S. Ep st e i n , H .A . Allen, and H. C. Urey (19 50) , Imp ro vements in mass spe c tr om ete r s for the measurements of small dif fer ences in iso to p e abundance rati os . Rev . Sci. Instr u m. , 21, pp. 724- 73 0 Mi lne , G.W ., e d (1971) , Mass spe c tr om etr y: Techniq u es and app li ca ti on s. Wi ley Inte r scie n ce, New York, p. 5 21 . Mo ore, L.J., J. R. Moody , LL. , Barnes, J.W . , Grami ch , T.J., Murp h y, P.J. , Paul- sen , and W. R. Shie ld s (19 73) , Trace dete r mi na ti on of rubid ium and stro nti um in sili c a te gla ss sta n dard refe r ence mate r ial s . A nal. C hem., 45, pp. 2384- 23 87. Nie r , A.O . (1947) , A mass spe c tr om ete r for iso to p e and gas analys i s . R ev. Sci . Jns tr u m. , 1 8, pp. 398-411 . Nie r , A.O . (19 50a) , A redete r mi na ti on of the relati ve abundances of the iso - top e s of carbon, n itro g en , oxyg e n, argo n and pot a s siu m . Phys . R ev., 7 7, pp. 789-793. Nie r, A.O. (19 50b) , A redete r mi na ti on of the relativ e abundances of the iso - top e s of neon, kry pton , rubid ium , xenon, and mercu ry. Phys . R ev., 7 9, pp. 450-454. Purser, K.H ., C. J. R usso, R.B . Lieb ert , H.E . Gove, D. Elmore, R. Ferraro, AE . Lith e rland, R.P . Beukens, K.H . Chang, L. R. Kil ius , and H. W. Lee (1982) , The app li ca ti on of e lectr os ta t ic t an dems to ultr as ensit ive mass spe c tr o metr y and nuclear dati ng . In L. A. Currie , ed., Nuclear and chemi cal dati ng tec h niq u es: Inte rpre ti ng the envir o nmenta l record, 45
-74. Amer. Chem. Soc. Sym po siu m Serie s , No. p. 1 76, 516p . Russell, R .D . (19 71) , The sys t e m atic s of d ouble spi ki n g . ] . Geop/ zys. Res ., 76, pp. 4949-4955. Russell, R.D . (1977) , A soluti on in closed form for the iso to p i c dilu ti on analys i s of stro nti um . Chemi ca l Geology , 20, pp. 307-314. Schoeller, D. A., and M. Haye s (1975) , Comp u te r contr o lled ion counti ng iso to p e rati o mass spe c tr o mete r . AnalyH cal Che m is tr y , 47, pp. 408-41 5 . Sherrill, N.D ., and G.B. Dalry mple (19 79) , A comp u te r iz e d multic h annel data acqu is it i on and contr o l sys t e m for hig h -p re cis io n spe c tr o metr y . U.S. Geo!. S urvey Profe s sio n al Pape r 1129-A . . Sh imi z u , N., M. P. Semet, and C.J . Alleg re (1978) , Geochemi ca l app l ica ti on s of qua nti tat i ve ion -mi cro p ro be analys i s . Geocl1i1 11 . Cos111ocl1im . Ac ta, 42, pp. 1321-1334. Sta c ey, J.S ., E .E . Wi lso n, Z.E. Pete r man, and R. Terrazas (19 71) , Dig ital recordi ng of m ass spe c tr a in geo log ic stu d ie s . Can. ]. E art h Sci ., 8 , p p. 371-377. Sta c ey, J.S. , E.E. Wi lso n, and R. Terrazas (19 72) , Di gital recordin g of mass spe c tr a in geo log ic stu d ie s . Can. ]. Eart h Sci ., 9, pp. 824-834. Wasserburg, G.J., D.A . Papa n asta s sio u , E.V . Nenow, and C.A . Baum (19 69) , A pro g ram mable magn e tic field mass spe c tr o mete r wit h on-l in e data pro cessin g . Rev. Sci . b zstrn m. , 4 0, pp. 283-295.
 제 2 부 안정동위원소 지질학
제 2 부 안정동위원소 지질학
3 안정동위원소 지구화학 3-1 서언 자연에 존재하는 안정동위원소는 300 종이 넘는다. 주석 (Sn) 과 같 은 원소는 112sn 에서 124Sn 까지의 원소를 가지는 반면, Be, F, Na, Sc, Mn, Co 등과 같은 21 원소는 동위원소를 갖지 않는 단일원자(단일핵 종)로 구성되어 있다. 이들 동위원소의 존재량은 원소에 따라 크게 다르다. 이처럼 중성자의 차이가 있는 각각의 동위원소들은 원자의 질량이 다르게 된다. 예를 들면 산소의 경우 160, 170, 180 인 동위원소가 존 재한다. 탄소는 12c, 1ac, 14c 의 세 종류의 동위원소가 알려져 있으며 12c 와 13C 는 안정동위원소이며 “C 는 방사성동위원소이다. 납의 경 우 204Pb, 206Pb, 201p b, 2oap b 등의 동위 원소가 존재 한다. 방연석내의 납의 원자질량과 저어콘내의 납의 원자의 질량은 다르 다. 왜냐하면 저어콘내의 P ih즌 U, Th 와 같은 방사성동위원소의 봉 괴결과에 의해 생긴 것이 있기 때문이다. 그러나 산소의 경우에는 모 두가 안정동위원소임에도 불구하고 자연의 산소를 포함한 물질은 그 질량이 다르게 나타나고 있다. 그러면 자연계의 산소로 구성된 물질 은 왜 상이한 안정동위원소비롤 가지는 것일까? 그리고 안정동위원소를 이용한 연구가 왜 유용할까? 안정동위원소
를 이용하여 여러 지구과학적 문제를 해석하고 있는데 이는 반응속도 론적 동위원소 과정 (K i ne ti c iso to p i c p rocess) 이나 동위원소 평형분별 (Iso to p i c equ i li b r iu m frac ti on ati on ) 과정 에 의 해 가벼 운 동위 원소와 무 거운 동위원소간에 서로 분리가 일어나기 때문이다. 이 같은 동위원소 분리의 메커니즘을 이해함으로써 과거에 우주 및 지구에서 일어났던 지질학적 과정과 오늘날 자연환경에서 일어나고 있는 지질학적 과정을 이해하는 데 크게 도움이 될 것이다. 그래서 우리는 자연의 물질의 가벼운 동위원소와 무거운 동위원소 의 비를 측정하고 이들 동위원소비를 이용하여 자연환경에서 일어난 여러 과정의 경과과정과 환경을 해석하게 된다 . 지구과학에서 많이 이용되는 안정동위원소는 탄소 (1 3 C / 1 2 C), 산소 (l 8 0 / 1 6 0) , 수소 (DIH ), 황 (“S/32S) , 질소 ('SN / 14N) 등이다. 이들 동위원소의 특성을 요약해 보면 다음과 같다. ® 이들 원소는 모두 원자의 질량이 작다. 원자번호가 16 보다 큰 핵종들은 자연에서 동위원소 분별이 용이하게 일어나지 않는다. ® 이들 핵종의 가벼운 동위원소와 무거운 동위원소 사이에는 상대 적인 질량차가 비교적 크다. 예를 들면 수소의 경우가 가장 질 량차가 커서 면 (D) 는 가벼운 떤 질량의 두 배 정도나 된다. 그리고 황 은 34S 가 32S 보다 6.25% 무겁다. 동위원소 분별은 상대적인 질량에 따 라 일어나기 때문에 이 같은 사실은 대단히 중요하다. ® 위의 5 원소들은 자연에 존재량이 많아 지구의 구성물질의 주를 이루고 있다 . 특히 산소는 지각의 중량의 47%,, 체적의 92%, 를 차지하 고있다. ® 탄소, 질소, 황은 단일한 산화 상태 이상으로 존재하여 광범위 하고 다양한 산화-환원 조건에서도 이들이 물질계에 관여하고 있다. ® 5 원소 (CHONS) 들은 각각 이웃 원자들과 이온결합에서 공유결합 까지 다양한 결합을 하고 있다. 모든 조건이 동일한 경우에는 가벼운 동위원소와 무거운 동위원소간의 동위원소 분별은 결합 유형이 다르
고 결합 강도가 다른 相간에 분별이 최대가 된다. 마그네슘이나 알루 미늄과 같은 가벼운 원소들은 지구의 구성물질 중에 동일한 결합형으 로 결합되어 있기 때문에 동위원소 분별이 크지 않다. ® 탄소, 수소, 산소, 질소, 황 (CHONS) 원소들 중의 각 원소는 희소 동위원소의 존재도가 높은 동위원소의 존재도에 비해 대단히 낮 은 비율로 나타나므로 동위원소비 분석시에 높은 정밀도가 요구된다. 황, 산소, 수소, 질소, 탄소 등의 원소를 가진 물질의 각각의 원소 를 분리 추출하여 질량분석을 실시한 결과 물질이 각기 다른 비율의 동위원소로 되어 있음이 잘 알려졌다. 그러면 이와 같은 자연의 물질의 안정동위원소비가 다른 이유는 무 엇일까? 자연의 물질의 원소의 안정동위원소의 존재량의 차아가 지질학적 문제해석에 대단히 중요한 의미를 가지고 있다. 그래서 먼저 자연의 물질 중 원소의 동위원소 존재량의 변화에 주요 원인이 되는 자연에 서 일 어 나는 同位元 素 分JJ 1 J (Iso t op ic frac ti on at ion ) 이 론을 실 례 와 함께 구체적으로 소개한다. 3-2 동위원소의 분별작용 자연에서 일어나는 동위원소의 분별작용은 크게 화학적 과정, 물리 적 과정 그리고 생물학적 과정으로 나누어 생각할 수 있다. 이 중에 서 화학적 과정과 생물학적 과정이 자연물질 중의 원소의 동위원소 존재량의 변화를 일으키는 가장 중요한 원인이 되고 있다. 그리고 확 산과 증발과 같은 물리적 과정에 의해서도 동위원소의 존재비에 큰 변화가 일어나게 됨이 알려졌다. 1) 화학적 동위원소 평형분별 화학적 과정의 예로 화학적 동위원소 평형분별은 동위원소 교환반
응작용에 의해서 일어난다. 석영과 물 사이에 일어나는 산소 동위원 소 교환반응의 예를 들면 다음-:tj- 같다. 1 / 2 S i1 6 야 + H2180 = 1 / 2 S i 18 아 + H2160 위의 동위원소 교환반응의 평형정수 (K) 는 다음과 같이 표현된다. K = [Si1 8 02] [H 폰이 / [Si1 6 02] [H 2 18 이 상수 K 는 농도보다는 비로 측정된 값이기 때문에 흔히 다음과 갇 은 형태로 표시된다. K = [Si1 8 02 / S i 16 아] / [H/80 / H 폰이 다원자분자의 경우 평형상수 계산은 수학적으로 어려우며 여러 가 지 가정을 해야 된다. 따라서 계산값이 실험에서 얻어진 값과 잘 일 치하지 않는다. 평형상수 K 는 K = exp (-LJG I RT) 식에서 계산될 수 있다. 여 기서 4G 는 Gib b s 자유에너지의 변화를 의미하고 R 은 기체상수, T 는 절대온도이다. 이런 문제 때문에 Ure y (l947) 는 두 화합물의 두 동위 원소비 인 同位元素分別整數 (Fracti on ati on fac to r , a) 를 제 안했다. 죽
a = ((118800 // 1600 )) SHi20 02 01 다. 대부분의 동위원소 교환에서 a 와 K 의 관계는 a = K½ 이며, 이때 n 은 우리가 다루고 있는 분자 중의 최대로 교환 가능한 산소원자의수를 의미한다. 가장 단순한 동위원소 교환반응 (n = 1) 에서는 동위 원소 분별정수와 평형상수가 같다. n = l 이의의 경우에는 a 와 K 가 갇지 않다. a 의 값은 분자의 진동빈도 등에서 통계역학적으로 계산하거나 또 는 실험적으로 결정할 수가 있다. 위에서 K 가 온도의 함수이므로 a 도 온도의 함수이다. 따라서 Ure y는 일찍이 탄산염을 이용한 고수온을 동위원소 분석방 법으로 측정하였다. 유체포유물, 광물의 상전이온도, 광물조합 등에 서 그 광물들의 생성온도를 측정하는 방법을 地 質 溫 度計 (Geo th er mome t r y )라 한다. 이처럼 동위원소적으로 평형상태에 있는 공존하는 광물의 안정동위원소비 분석으로 그 광물의 생성온도를 측정하는 방 법을 同位元素 地 質溫度計 (I so t op e g oe th ermome try)라 한다. 동위원 소 지질온도계에 대해서는 뒷장에서 자세히 다루고자 한다. 2) 가 스 상의 동위 원소 분별 여기서 가스간에 일어나는 동위원소 평형분별작용(I so t o pi c equ i li b- riu m fr ac ti ona ti on) 의 특성을 이해하기 위해 구체적인 실례를 들어 보 자. 2 몰의 CO 가스와 1 몰의 02 가스가 평형상태에 있는 계를 생각 해 보자. 단 두 분자들간에 어떠한 화학반응도 일어나지 않고 02 의 동위원소 (1 원자에 500 개 존재)만이 두 분자간에서 동위원소 평형분배 가 일어났다고 가정하자. 이때 동위원소 분별정수 야근 다음과 같이 정의할 수 있다. (180 / 160) co a = (180 / 0) O2 • 이 계에서는 “O“O, “O180, 180l80, cl60, cl80 와 같은 5 동위원소종 이 존재하므로 분별정수는 다음과 같이 표현된다.
a = (2[0180 미 + [OL:?81]8 } / 協:』小] + [0160 미) 이둘 다섯 동위원소종의 농도는 다음과 같은 동위원소 교환반응 관 계에 있다. col6 + 018016 K=l col8 + 0016 01so1d + 016016 K=2 2016018 여기서 평형상수 K 는 다음과 같다. Kl = [[001168001 미6] [[Cc0o 미미 [0160 미 2 & = [ol80 미 [0160 미 활동도계수가 같은 것처럼(I'CQ 16 = I'CO) 두 동위원소종 사이에는 화 학적으로 동일하므로 수치 계산에서 퓨가시티 대 농도의 관계에서 나 오는 상수는 분모와 상쇄되기 때문에 퓨가시티 대신에 농도를 사용한 다. 이 관계에서 F[C 0 미 = KI [[00116800 미미 [0180 미 = 이 관계를 위의 a 에 대한 식에 대입하면
a = (2 / K2) (K[210 [(0[01Q6 미l60 Q 미디미 +[ /0 1f[06001 0미610)8 미 )+ [00 미 이 된다. 이것을 다시 표현하면 a = 2K1 2[01620[0)1 6+0 미(4 +/ K[20) 1(6[00 미16 0 미) 이 된다. 뒤에서 증명하겠지만 K 의 값은 모든 온도에서 4 가 된다. 따라서 CO 와 02 사이의 동위원소 반응에서 분별정수 a 는 평형상수의 두 배 와 같다 (a = 2K1). a 를 계산하기 위해서는 평형상수를 먼저 계산해야 된다. 열역학적 관계에서 위의 반응이 평형이기 때문에 반응물의 자유에너지와 생성 물의 자유에너지가 같다. LJG = 0 = Go••ou + G 따 18 一 Gcoucol6 - Gcol6 또 각 가스의 자유에너지는 G(T, P) = c·(T) + RT i n p로 표현 할수있다. 이 관계에서 4G° = -RTln Po16016p coI I Po11ouPco1& 이 된다. 동위원소 반응에서 존재하는 분자의 수는 변화하지 않으므로 다음
과 같이 분압은 농도로 직접 바꾸어 쓸 수 있다. 4G° = 一 RTln 醫隊가霧나 = —RT lnKI K1 에 대해 풀면 K1 = ex p(_舊) 이 된다. 동위원소종의 자유에너지를 결정하면 K 려 계산될 수 있다. 열역학 제 1 법칙에서 4G = 4H _ T4S 이다. 동위원소 교환반응에 서너또 는지 통 의체계 적변역의화학 에변4서E화 와가S 같=일아 어t야나 +지한 R다l않.n 으q따가므 라로얻서 어 엔진4탈G다피. =의 4여변E기 화—서 4TL HS1 는 S는 가 내엔된부트다에.로 피, E 는 에너지, T 는 절대온도, R 은 기체상수, q는 분배관수 를 의 미한다. 이리하여 TL1S = L1E + RTq oluon1 띠~ 'cou L1G0 = - RTln (~)r 가 얻어전다. 죽 평형상수는 다음과 같이 된다.
K,=(~t 여기서 T 는 평형상수 계산에 사용된 측정온도이며, 분배관수 (pa rt ition fun cti on s) 는 온도에 따라 변화한다. 분자의 에너지는 전기적 에너지 (electr o nic energy ), 병진운동 에너지 (tra nslati on energy ), 회전운동 에너지 (rota t i on al energy ), 진동운동 에 너 지 (vib r ati on al energy ) 등으로 표현된다. 총분배관수(q)는 q = Q 1ra n s 1!Q ro 1 Q vl b 이므로 병진운동, 회전운동, 진동운동 등에 의한 동위원소 분별을 각각 계산하여야 한다. 분자 (N) 는 식별이 불가능하므로 (N!) 삼 = \: 관계를 이용하여 계산한다. ® 병진운동 성분: 병진운동시의 분배관수는 Q1 rans = (~)v이다. 여기서 h 는 프랑크상수 (6.624 X 10- 2 1er g -sec ) 이며 m 은 질량, k 는 힘의 상수 (dy n e /cm) V 는 입방체의 체적 (a3) 이다. V 는각분자종간에 같기 때문에 (근 )lrans = (~) = (블) (二 :: )tran s = (~) = (룹) Ktr a ns = (붑 픕) = (景) = 1. 0126 이 된다. 병진운동 에너지 차가 동위원소 분별의 유일한 원인이었다면 무거 운 분자인 0 센서보다 가벼운 분자인 co 에 180 이 13%, 더 많이 포
함되어 있음을 의미한다. 병진운동에 의한 동위원소 분별은 온도와 무관하다. ® 희전운동 성분: 분배관수의 회전운동 성분은 qro l = 8 군µ『 kT 로 주어진다. 여기 서 µ는 AB 분자의 환산질량 (reduced mass) 으로 mmAA +• mmBB 이 며 d 는 원자간의 거리이다. 여기서 16018O 와 “O160 의 결합길이가 동일하기 때문에 (Qo노1 •0)1s /r ot = 上2 //JJ--0011 66Q0 1 1 88 ?1 (1166 Xx 1l68)) // ((1l66 ++ 1168)) _= 一1l 1187 이 된다. 회전운동시의 분배관수는 대칭인 분자가 비대칭인 분자의 1/2 이 므로 1 / 2 로 하였다. 또 co 에 대해서는 (Q노co 1)6 }r ot = 노/JcO-1 , =- ((1122 XX1 186)) // ((1l22 ++ 1168)) =- 꼬 20 따라서 Krot = 강풀픕 = 강불 = ½(0 .9916) 가 된다. 회전운동 에너지 차에 의해서만 동위원소 분별이 일어났다고 가정하 면 co 에서보다 02oJ l 180 이 8%, 더 많이 들어 있디는· 뜻이다. 이 경 우에도 동위원소 분별은 온도와 무관하다. ® 진동운동 성분: 전동운동시의 분배관수는 qvl b= l—e xp ~( — hTv / 2kT)
로 표현된다. 온도가 hv I k 보다 낮은 경우 분배관수는 대략 qvlb = e 기 틀)가 된다. 여 기 서 u 는 진동수 (vib r ati on al freq u e ncy) 이다. 이리하여 co 의 경우 진동운동 분배관수는 (~)vlb = exp [-걸 뉴 -(Ucol8-Vcol6)] 가된다. 02 의 경우 진동운동 분배관수는 (~tb = ex p [-훑( l/o 18018 - l/o1 60n)] 가된다. 위의 두 결과에서 Kvlb = exp {+ 畜[l/ co16 _ l/coI s) 一 (l/o16 018 -Uo160n)]} 가 얻어진다. 동위원소 분별은 일반적으로 수%만 일어나기 때문에 진동운동시의 동위원소 평형상수는 K조 1 + 훑~[ ( Vco1& - Vcou) -( vouo1s 一 Uo160n) ] 로 쓸 수 있다. 또 Ideal harmonic osc ill a t or 인 경우 v = 감w? 臼 다. 힘의 상수인 k 는 동위원소적으로 치환된 분자에서는 변화하지
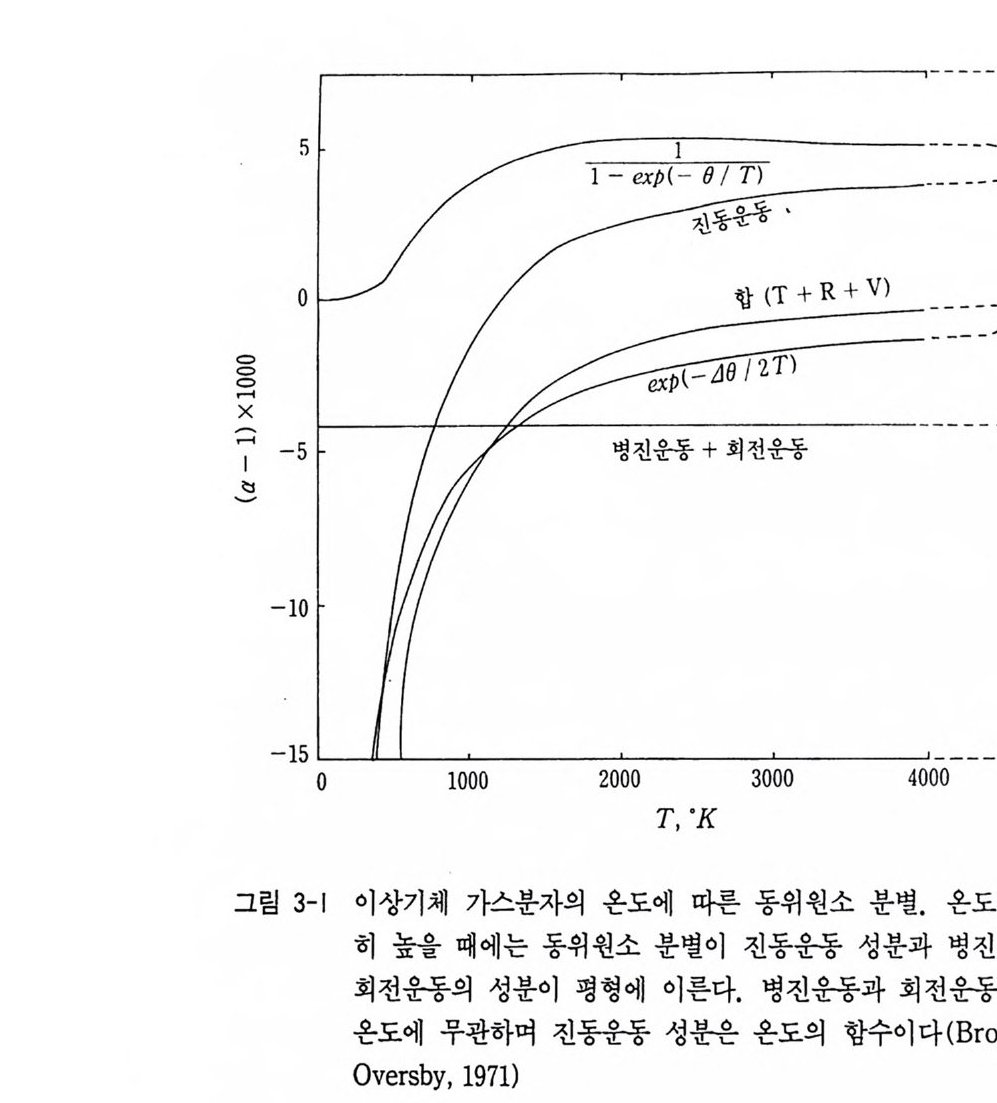
않으므로 llco1s = llco16 {if; = 層 llco16 I/Q1 6Q 1 8 = I/Q1 6Q 1 6 ,/ 乞言 = 譜 Vo18018 가 된다. 따라서 Kv1b 힉 + 훑[!l co•s (1 - 濬)- Uo16016 (l —澤 )] 힉 + 福h (0.0244vco•s - 0.0282vo,so1G) 가 얻어진다. 실험실에서 측정된 J/CQ I6 = 6.50Xl013sec-1, J/Q ISQ I S = 4.74Xl013sec-l 이고, hI2k = 2.4x10-11de g -sec 이므로 Kvt b = 1 + ~(15.86 -13.37) =l+ 5.9T7 6 관계가 얻어진다. 상온에서 동위원소 분별이 일어날 때에는 Kvtb = 1 + :亂쁜 = 1. 01992 가 된다. 진동에너지 모드의 차에 의해서만 동위원소 분별이 일어났다면 상 온에서 진동빈도가 더 높은 분자인 co 에 20%, 정도 더 많은 180 동 위원소가 포함되어 있음을 의미한다. 이 동위원소 분별은 온도 r 차 에 대략 0.06%, 증감한다. 상온에서 위의 모든 동위원소 분별정수는
a = 2K, = 2Ktr a nsKratK vlb = 1 . 024 가 된다. 그러므로 상온에서 평형 상태에 있는 CO 와 02 분자 사이에는 180 이 02 에서 보다 co 쪽에 24 % 더 들어 있게 된다. 앞에서 설명한 것처럼 동위원소 분별의 병진 운동 성분과 회전운동 성분은 온도에 무관하다. 그러나 진동운동 성분은 온도에 따라 변화한다. 저온에서 진동운동 성분은 온도에 반비례하게 변화한다. 따라서 온도가 증가하는 경우 분배 관수의 분모의 1 - exp (-hv / kt) 항이 대 단히 중요하게 된다. 평형상수 K 는 다음과 같이 주어진다. Kv 1b = exp {一 뚜 [1 —e xp ( 一 hVo160n / kT)][1 - exp( — hl.1c o16 / kT)] 2kT [l _ exp (_ hl.1o 16016 / kT)][1 _ exp (-h l.1c o1s / kT)] } 이때의 평형상수의 온도 의존성은 그림 3-1 과 같다. 1 —ex p (-h v I kT) 항은 절대온도 o · 에서는 0 이지만 2500K 부근 까지 점진적으로 증가하고 그 후에는 점차 감소한다. 온도가 무한히 높으면 전동운동에 의한 동위원소 분별은 병진운동에 의한 동위원소 분별과 회전운동에 따른 동위원소 분별과 균형을 유지하게 된다. 왜 병진운동과 진동운동의 결과로 co 에 180 이 농집되고 회전운동 의 결과로 02oJ l 180 이 더 농집되는가? 일반적으로 우주에서 180 농집은 엔트로피가 높은 쪽으로 일어나고 있는 사실이 틀림없음에도 불구하고 그 이유는 명확하지 못하다. 네 종류의 가스가 동일한 양으로 존재할 때 반응물 (180160 + cl60) 과 생성물 (16 Q 16 Q + c1so) 사이의 자유에너지 차를 계산할 수 있다. 이런 조건에서 생성물에 이용될 수 있는 병진운동 상태의 수는 생 성물의 질량의 3/2 배에 비례함을 알았다. 반응물의 경우도 같다. 반응물의 질량 (952) 산물이 생성물의 질량 (960) 산물보다 적을 경 우 생성물의 엔트로피는 반응물의 엔트로피보다 약간 크다 [(960 / 952)] .
 5 1 - exp (I- 二二二`::::.--
5 1 - exp (I- 二二二`::::.--
이런 조건에서는 CE0 + l80160 이 반응해서 C18O 와 “O16O 를 더 많이 만들어낸다. cl8O 와 “O“O 분자의 농도가 증가할 때 그들의 엔 트로피는 감소한다. 같은 식으로 생각하면 반응물의 엔트로피가 증가 하게 된다. 반응물과 생성물간의 엔트로피의 차이가 없어질 때까지 이 같은 변화가 계속 일어나 동위원소 평형에 이르게 된다.
3) 규산염 광물에서 동위 원소 분별 공존하는 고체 광물상 사이의 동위원소 분배는 전적으로 전동빈도 에 의해 지배를 받는다. 일반적으로 병진운동과 회전운동은 고체에서 는 일어나지 않는다. 규산염광물과 같은 고체내에서 원자는 상이한 진동빈도로 진동하기 때문에 대부분의 고체광물의 경우 이들 진동빈도의 정확한 스펙트럼 이 알려져 있지 않다. 이 때문에 정확한 분별정수는 계산할 수가 없고 대략적인 분별정수 는 각 고체상의 평균 진동빈도를 이용하여 계산하고 있다. 복잡한 산화물로 구성되어 있는 경우에는 그것을 구성하고 있는 산 화물의 합에 의하여 분별정수를 계산할 수 있다. 예를 들면 세니딘 (Sanid in e , KAS i 3 아)과 엔스타타이트 (Ens t a tite, M gS i 03) 간의 분별정수 를 계산하려면 lK20 + lAl203 + 6S i 02 의 합과 1Mg 0 + lS i 02 의 합 으로 가정하고 계산할 수 있다. Si0 2 —K2 0 상, Si0 2 -M gO상, Si0 2 一 Al2°3 상 등의 각각의 분 별정수가 알려져 있으면 분별정수의 전체합은 쉽게 계산할 수 있다. 임의의 온도에서 각각의 조암광물과 금속산화물에서 조암광물 전체의 분별정수를 계산할 수 있다. 예를 들면 함수광물과 탄산염광물을 제 의한 Na, K, Ca, Hg , Fe, Fe, Si, Al, Ti 산화물 등의 분별정수의 계 산 결과를 이용할 수 있다(표 3-1). 예를 들면 다음과 같은 반응식에서 AIO16 + SiO 1 8 = Al0l8 + Si0 1 6 분별정수 a 는 a = ((0108미 / 001”6)A)s1l--oO
= 1 一 奇[l/ s10•• (1 —/i :J;) —IIA 10•• (1 —/ 三)] 로 표현된다. 여기서 Jl,s10 16 = mms1s 1+·m om1o6, 6 이다. 그리고 u 의 값은 v = 伊거 에 서 아인슈타인 함수 (Ei ns te i n fun c- ti on) 를 알므로 계산이 된다. 0E 는 아인슈타인 온도이다. 몇 가지 산 화물에 대하여 이같이 계산된 값은 표 3-2 에 주어져 있다.
표 3-1 산화물과 석영간에 계산된 동위원소 분별계수 (Broecker 와 Oversby, 1971) 산화물 Cmp o Il en-,a tco aml / ·OKE, ls/ e1c0-113 /J-O,. 1-[i i; 흙 Xl -10 0占0 )+ X4 1oq0xtJz 0d c0 Si0 2 3.5 4 770 1.64 10. 2 0.036 47 。 Al20a 3.78 715 1.52 9.9 0.035 42 -5 MTig0 O2 44..53 28 558505 11..1238 129..6 0 00..004324 3421 —-165 Fe203 4.97 450 0.96 12.7 0.043 33 -14 CaO 5.12 420 0.89 11. 4 0.0 4 0 29 -18 FeO 5.2 5 375 0.80 12.7 0.013 27 -20 Na20 5.60 250 0.53 9.3 0.033 14 _33 K20 5.70 200 0.42 11. 4 0.0 4 0 13 -34 +상온 (300'K)
표 3-2 상온에서 석영과 주요 조암광물간에 계산된 동위원소 분별계수 釋 | 산화물성분 | ^겁 석영 Si0 2 0.0 규선석 Si0 2 + Al203 -3.0 남정석 Si0 2 + Al2 0 3 -3.0 알바이트 6Si0 2 + Alz03 + Na20 -3.0 정장석 6Si0 2 + Al203 + K20 -3.1 사장석 (알바이트 + 아놀사이트) -3.5 아놀사이트 4Si0 2 + 2Al203 + 2Ca0 -4.1 류사이트 4Si0 2 + Al20J + K20 -4.1 네펠린 2Si0 2 + Al203 + Na20 -6.0 파이로프 3Si0 2 + AI203 + 3Mg 0 -5.0 그로슈라라°]트 3Si0 2 + Al2 0 J + 3Ca0 -5.2 엔스타타이트 SiO z + Mg O -5.0 휘석 2Si0 2 + AI203 + CaO + Mg O -5.3 고토감람석 Si0 2 + 2Mg 0 -7 .5 철감람석 Si0 2 + 2Fe0 -1 0.0 루틸 Ti0 2 -6.0 티탄철석 Ti0 2 + FeO -10.7 적칠석 Fe20a -14.0 자철석 Fe203 + FeO -1 5. 5
l.1 16 과 l 一 〔µ》 o의 값에서 각 산화물에 180 이 농집되어 있는 경향 을 측정할 수 있다. 두 산화물간의 이 값의 차가 바로 평형정수의 값 이 된다. 상온에서 석영을 표준광물로 생각하면 석영에 대한 기타 산 화물에 180 의 평형부화 (E q u ili br i wn enr ic hmen t)의 값이 표의 마지막 난에서처럼 계산된다. 그 다음에 각 산화물의 합으로 표현되는 조암광물간의 동위원소 부 화의 값을 계산할 수 있다. 네펠린 (Ne p hel ine) 의 예를 들면 다음과 갇다.
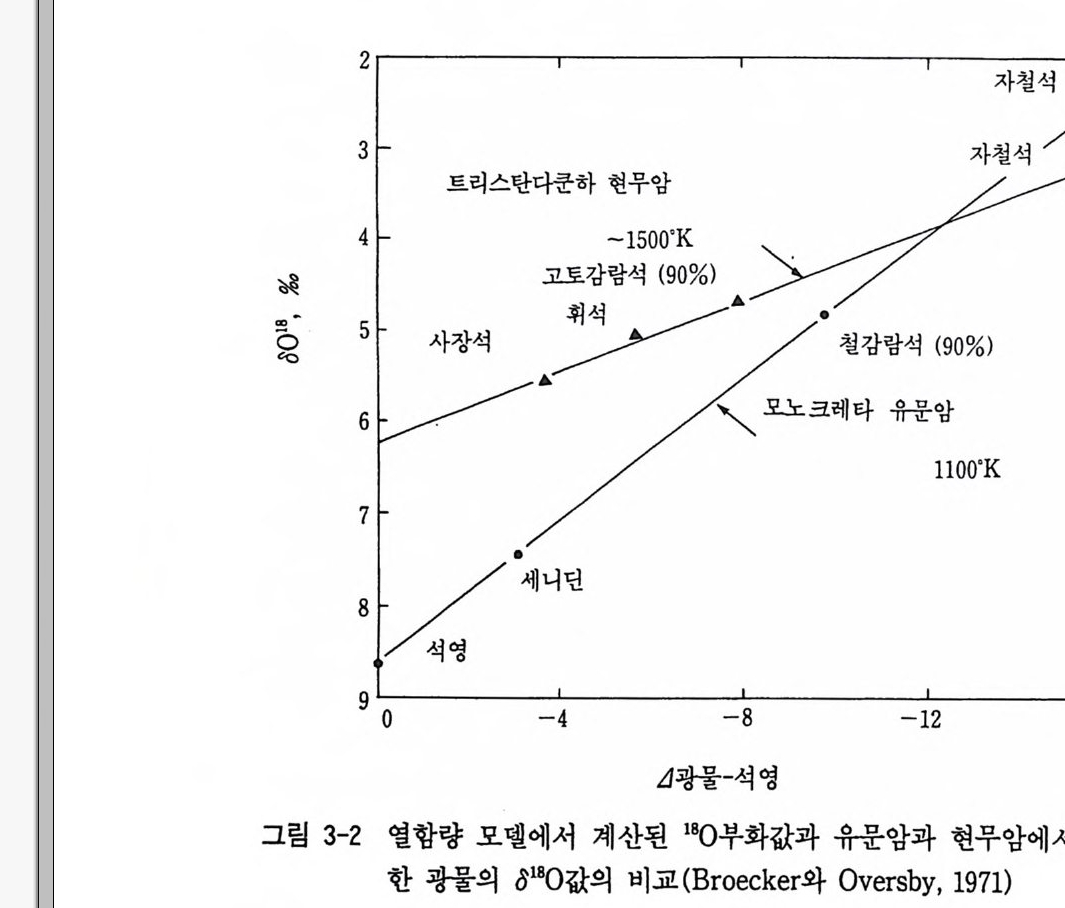
(Na2Al2S i◄ 야) = 2Si0 2 + Al203 + Na20 4 霜 = 강 4 器 + \끄뿐 + 강麟 0 = t(0) - t(5) — ½ (33) = --488= —6. 0 감은 방법으로 기타 광물에 대하여 계산한 값이 표 3-2 에 주어져 있다. 표에서 보면 조암광물 중에도 동위원소 평형에 있었을 경우에 는 동위원소 분별의 대소의 경향이 뚜렷이 나타난다. 죽 장석류, 석
 2
2
류석, 휘석류, 감람석, 티탄칠석, 자철석 순으로 나타나고 있다. Garl i ch 에 의 해 트리 스탄 다쿤하 (Trist a n Da Cunha) 의 현무암과 모 노크레 이 타 (Mono crate r s) 의 유문암의 실제 화성 암에 분석 된 동위 원 소의 성분은 위에서와 같이 계산에 의해서 얻은 값과 좋은 상관관계 에 있다(그립 3-2). 이 같은 상관관계는 이론과 실제가 일치함을 의 미한다. 따라서 화성암 중의 조암광물간의 동위원소 평형과 비평형을 식별할 수가 있다. 예를 들면 석영보다 장석의 동위원소값이 크다든가 또는 공존하는 조암광물 사이에 동위원소 분별값의 순서가 표 3-3 과 다르게 얻어질 때는 비록 그들 광물이 공존하고 있어도 동위원소간에 비평형에 있었 음을 가리킨다.
표 3-3 산소동위원소 교환평형하에서 나타나는 광물들의 동위원소값의 변화경향 광물 0180 값 1. 석영 (트리디마이트) 15. 0 2. 돌로마이트 14.2 3. 칼리장석, 알바이트 13. 0 4. 방해석 12.8 5. Na 가 많은 사장석 12. 5 6. Ca 가 많은 사장석 11. 5 7. 백운모, 파라고나이트 11. 3 8. 휘석, 사방휘석, 두휘석 10.5 9. 각섬석 (스펜, 로우소나이트) 10.0 言1801.8 0 감값람은석 ,모\ 두석 류이석론 적 (저인어 콘값,임 .인 회그석러)나 편암의 변성I도에 따 라 :값의9:. 5 차 이가 찰 나타난다. ( )속의 광물둘은 주광물보다는 부적절하다
이 같은 현상에서 광물정출 순서나 열수변질 등의 해석에 중요한 정보를 얻을 수 있다. 4) 동위원소 효과 원소의 질량 차로 인하여 생기는 물리화학적인 차이를 동위원소 효 과 (Isoto p ic eff ec t) 라 한다. 임의의 모든 원소의 동위원소는 그의 전자구조가 동일하기 때문에, 그들로 만들어진 화합물의 결합도 동일하다. 그러나 분자의 진동의 에너지 준위는 질량과 결합력에 의해 영향을 받기 때문에 동위원소 치환이 일어나 분자의 전동빈도에 변화를 일으킨다. 질량의 차는 병 진운동 (Transla ti onal mo ti on) 과 회전운동 (Ro t a ti onal mo ti on) 에도 영향 울준다. 따라서 물의 경우 180 을 많이 가지고 있는 분자와 적게 가지고 있 는 분자 사이에는 내부에너지, 열함량, 엔트로피 등과 같은 열역학적 특성이 다르다. 표 3-4 에서처럼 H2160, H2180, D 폰 0 등은 물리화학 적 특성이 서로 다르다. 동위원소 중의 한 원자를 다른 원자가 치환 했을 때 화학적 성질의 변화는 거의 나타나지 않는다. 그러나 중성자 가 하나 첨가되면 화학반응의 속도에는 큰 변화를 주게 된다. 죽 동 위원소의 치환으로 변화되는 분자의 특성은 정량적으로는 변화가 없
표 3-4 H20, D20, H2180 의 물리적 특성 Aok人T H2l6Q D/60 H2180 밀도 (20 ' C, gcm -3) 0.9979 1.10 51 1.1 1 06 최대밀도에서의 온도 (·C) 3.9 8 11. 24 4.3 0 용융점 (760 Torr, 'C) 0.0 0 3.81 0.28 비 등정 (760 Torr, C) 100.00 101. 42 100.14 증기 압 (lOO 'C, Torr) 760.00 721 .60 정 성 (2o·c , centi po is e ) 1.002 1.24 7 1.056
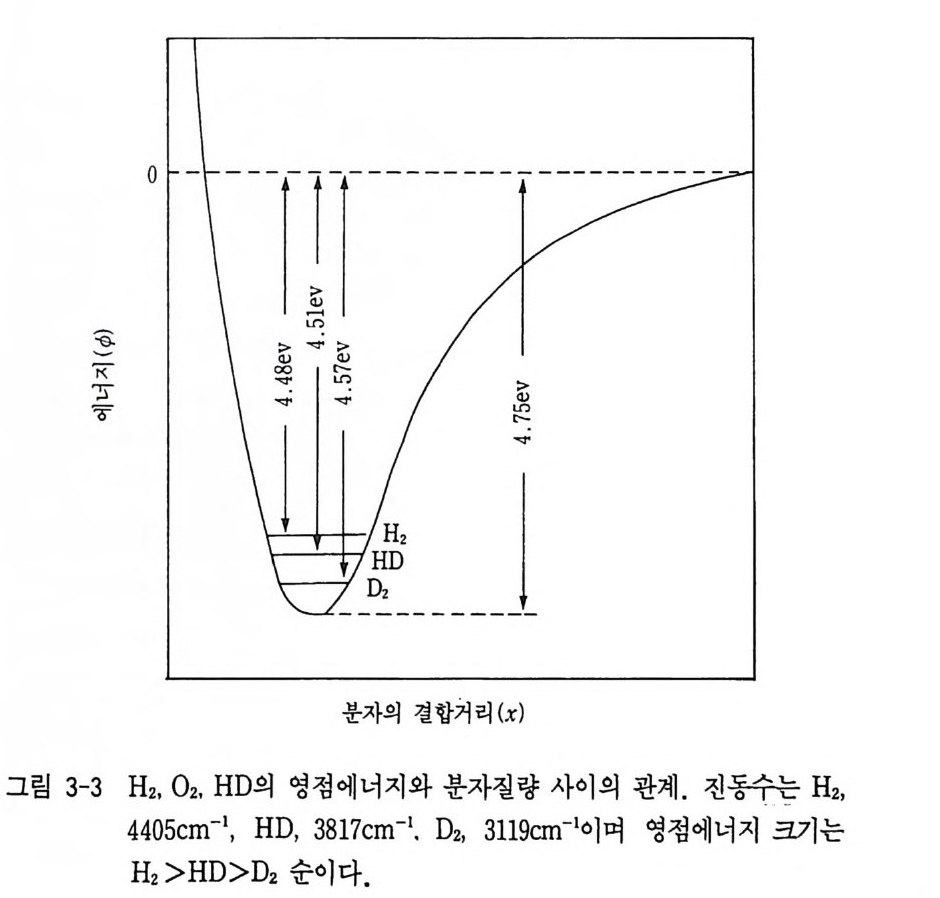
지만 정성적으로는 변화가 크다. 이들의 작은 차이가 공존하는 상 사이의 동위원소 평형분별을 일으 킨다. 동일한 원소의 두 동위원소 사이의 에너지 우물 (Ener gy well) 은 동일하지만, 가벼운 원자로 만들어전 분자의 영점에너지 (Zero poi n t energy ) 가 더 크다 (그림 3-3) . 양자역 학에서 진동자의 위 치 와 운 동량 사이의 불확정성 원리에 의해 위치에너지의 최소위치에서 정지 한 상태는 실현되지 않는다. 이런 상태가 이루어졌다고 가정했을 경 우의 에너지를 0 으로 하였을 때의 기저상태 에너지값을 영점에너지라 한다.
 。 l .A-3·• v0a0IV
。 l .A-3·• v0a0IV
그림 3-3 은 포텐셜에너지와 분자의 원자간 거리와의 관계로 나타낸 그림이다. 분자의 결합에너지 (¢)와 분자간의 거리 (x) 에서 - dd¢x = F( 힘)인 관계가 이원자분자(Di a t om ic molcule) 에서 ¢~0 일 때는 두 원자간에 화학결합이 이루어져 있음을 의미하고, ¢ > 0 인 경우 두 원 자는 분리되어 존재함을 의미한다. 여기서 에너지 우물이 비대칭인 이유는 견인포텐셜은 l/x 에 비례 하고 반발포텐셜은 1/Xn -l 에 비례하기 때문이다. 원자간의 평행거리가 증가할수록 포텐셜 에너지는 증가하고 고체는 팽창하게 된다. 두 원자로 된 분자의 결합의 진동에너지 E 는 E = (n + 1/ 2 )hv 여기서 n = 0, l, 2, 3… … 이다. h = 프랑크상수, v = 입자가 1 초 간에 진동하는 전동수이다. 온도가 낮으면 슈레 딩 거 방정 식 (Schrodin g e r equ a ti on ) , E = 着 /8me2 은 E = nhv = 릎汀 에서 절대 0 도에도 전동자가 에너지를 가지게 된다. 이 에너지 E 。 = 1/2hv 를 영점에너지라 한다. 한편 위의 식에서 전동수 v = 」21rV / Eµ 이다. 여기서 원자 A 를 질량 이 더 큰 A’ 로 바꾸어 놓으면 그때의 질량 µ'>µ가 되고 v'
울 보통 결합에너지에 대한 원자의 질량효과라고 하기도 한다. 5) 생물학적 과정에 의한 동위원소 분별 화학적 동위원소 평형분별작용예 비해 다음과 같은 비가역적 과정 울 보통 반응속도론적 동위원소 분별작용 (K i ne tic iso to p i c frac ti on a- ti on) 이라 한다. 황의 경우를 예로 들어본다. 32S04 뇨 H232S —(1) “S04 뇨+ H234S —(2) 위의 (1) , (2) 반응식에서 실험적으로 32s-o 결합과 “S-0 결합의 비 교에서 k1 / k2 = 2.2% 로 32so4 가 “so4 보다 반응속도가 2.2% 빠르다 (Harr i son 과 Thode, 1957) . 위의 반응은 보통 대단히 느리게 일어나지만 환원환경에서 Desulf o- vib n 'o d e su [fu ri ca1 is와 같은 황환원 박테 리 아의 촉매 역 할로 인 하여 반웅이 대단히 빨리 일어나고 있다. 이들 박데리아는 황산염이온의 산소를 분리시켜 H2S 를 우선적으로 만든다. 따라서 여기서 생긴 H2S 가 금속이온이나 비금속이온과 결합되어 침전될 경우 침전된 황화물 내의 황의 동위원소값이 크게 차이가 난다. 탄소에 있어서도 광합성 작용에 의해서 생성되는 유기기원의 분자 의 경우에 12c 가 13c 보다 더욱 빨리 농축된다. 즉 CO2 + H20 = [H CHO]+ 02 과 같은 광합성 반응에서 12C02 가 13c 아보다 반응속도가 빠르므로 이로 인해 생성된 유기물내에는 원료 탄산가스에서보다 가벼운 12c 이 더 많이 농축된다 (Cra ig, 1953). 유기 물 조각이 박테리아에 의해 산화될 때 만들어지는 물(H 20) 과 탄산가 스 (CO2) 에는 “O 이 180 보다 더 많이 농집된다. 이는 앞에서 설명한 것 처 럼 무거 운 동위 원소의 기 저 상태 전동수 (Ground sta t e vib r ati on fr e q uenc y)가 더 낮기 때문이다. 그립 3-3 에서처럼 무거운 동위원소로 된 분자가 가벼운 동위원소로 된 분자에 비해 위치에너지 우물
(Pote n ti al energy well) 의 바닥에 더 가깝기 때 문이 다. 즉 무거 운 동 위원소로 된 분자는 가벼운 동위원소로 된 분자에 비해 파괴시 더 많 은 에너지를 요하기 때문이다. 구체적으로 예를 들어보자. 가벼운 동위원소의 반응속도 (RL) 와 무거운 동위원소의 반응속도 (R 사의 비는 RRHL =_ eexxpp [[—- NN ((ee ——½½ lh 2v 미H) /I NNkkTT]] 11II = 11L \y fi !µi1:1: 이 므로 = exp [-훑 -(IIL - IIH)] 1f; = exp [-불 (1 -✓, 鬪 의 관계가 성립한다. 상온에서 아의 경우 계산해 보면 衍 = exp (_ (6.6X(;!-(?1:.:}\l;;{f.0 58 ) )츠 e-0 - 18~0.83 이 된다. 이는 16 야 원자를 가전 분자가 1so160 로 된 분자보다 반응 이 17%, 빠르게 일어난다는 의미이다. 6) 물리적 분별과정 물리적 동위원소 분별과정은 레이리 중류 (Ra y le ig h dis t il lat i on ) 과 정과 기체의 확산의 경우를 들 수 있다. 분자운동론에 의하면 기체가 확산될 경우 병전운동 확산속도는 v2 = 3kT I m 의 관계에 있다. 여기서 k = Bolzman 상수, T = 절 대온도, m 은 입자의 질량, I)는 병진운동 확산속도를 말한다. 입자
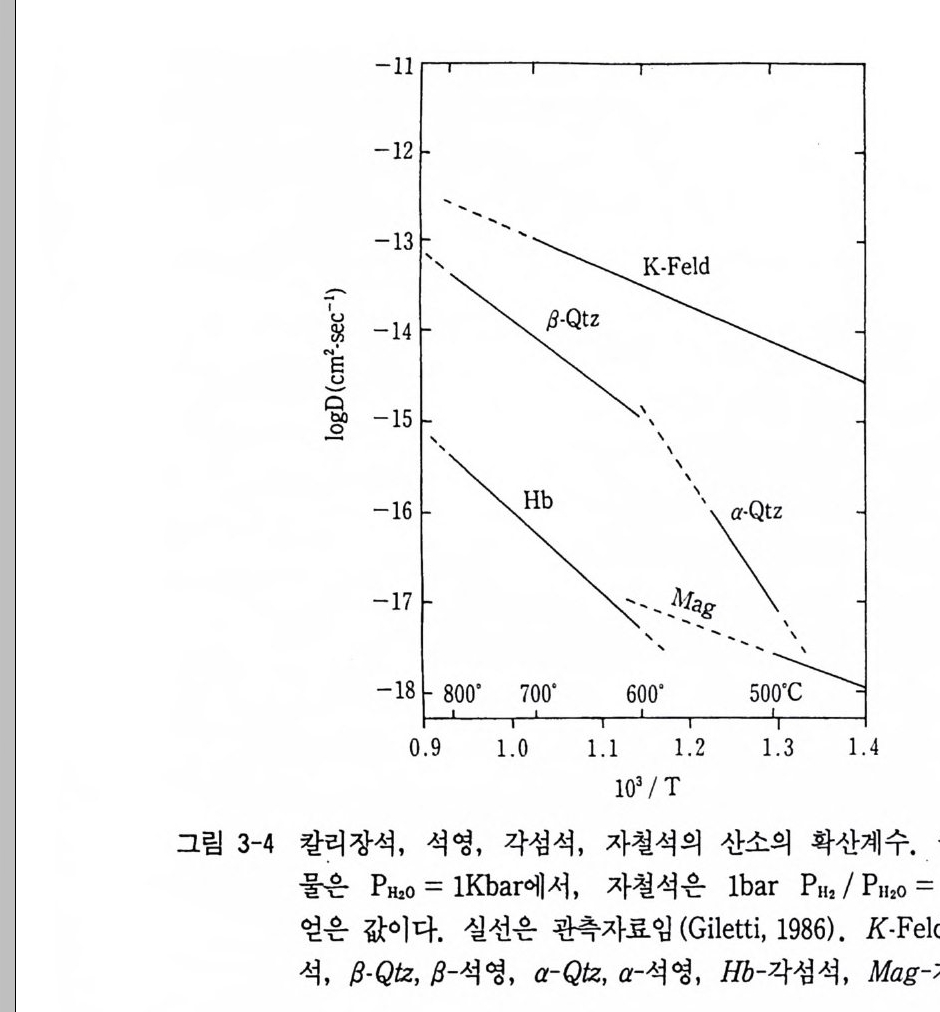
의 확산속도와 질량은 반비례한다. 기체의 동위원소 분자내에 상이한 동위원소를 1 (가벼운 동위원소)과 2 (무거운 동위원소)로 구별하면 동 위원소분자의 평균 병진운동 속도비는 ]:= ( 곱〔이 된다. 예를 들 면 수증기의 동위원소분자 H 詞 H 回 경우 :]= ( 릅 = 1.054 가 되어 m6o 분 자가 HP0 분자보다 5.4% 평균병진운동 속도가 크다. 물의 비평형 증발을 생각하면 액체표면의 H}6 가 빠르게 확산되어 기 상과 액상간에 평균치보다 큰 산소 동위원소 분별이 일어나게 된다. 따라서 질량이 다른 두 개의 동위원소로 된 기체분자가 있다면 질 량이 작은 동위원소가 질량이 큰 동위원소보다 빠른 속도로 확산된 다. 그 결과 기체의 확산 전후에 기체 중의 산소 동위원소 성분이 변 화된다. 고체상태 확산일 경우 체적확산도 고려되어야 한다. 주로 확산은 입자의 경계나 표면을 따라 쉽게 일어난다. 확산계수 (D iffus i on coeff i. cien t, D ) 는 보통 에너지 E 와 온도 사이에 다음과 같은 관계로 표현된 다. D = D 。(-jf) 여기서 R 은 기체상수, E 는 활동에너지, D. 는 온도에 무관한 값이다. 몇 종류의 광물의 산소 확산계수를 측정한 예를 들어 보자. 그림 3-4 에서 보면 6oo·c 에서 장석, 석영, 각섭석은 상당히 다른 확산계수 를 가진다. 이는 주어진 암석내에서 이들 광물의 산소가 다른 속도로 확산되었으며 상이한 온도에서 폐쇄계였음을 의미하고 있다. 열수환경하의 규산염광물내에서 산소의 확산은 낮은 활동에너지 (30 Kcal/mo!) 와, 비교적 높은 확산속도를 가지는 반면에 건조조건하에 서는 높은 활동에너지와 낮은 확산속도를 나타냄이 조사되었다. 확산 계수 결정은 산소 동위원소 지질온도 (G il e tti, 1986) 해석과 열수, 물 -암석 상호작용 연구 (G il e tti와 Yund, 1984) 등에 대단히 중요하다.
 -ll
-ll
레이리 증류 모델에 의하면 호수에서 물의 증발이 일어난다고 가정 하면 주로 가벼운 동위원소로 구성된 수증기가 먼저 증발하게 되어 상대적으로 호수에 남아 있는 물은 무거운 동위원소가 더욱 많이 농 축될 것이다. 이 런 증발 (Evap or ati on ) 또는 응축 (Condensa ti on) 효과에 의해서도 동위원소값이 달라진다. 이를 레이리 증류 모델로 생각해 보자. 수증기 중의 물분자 중
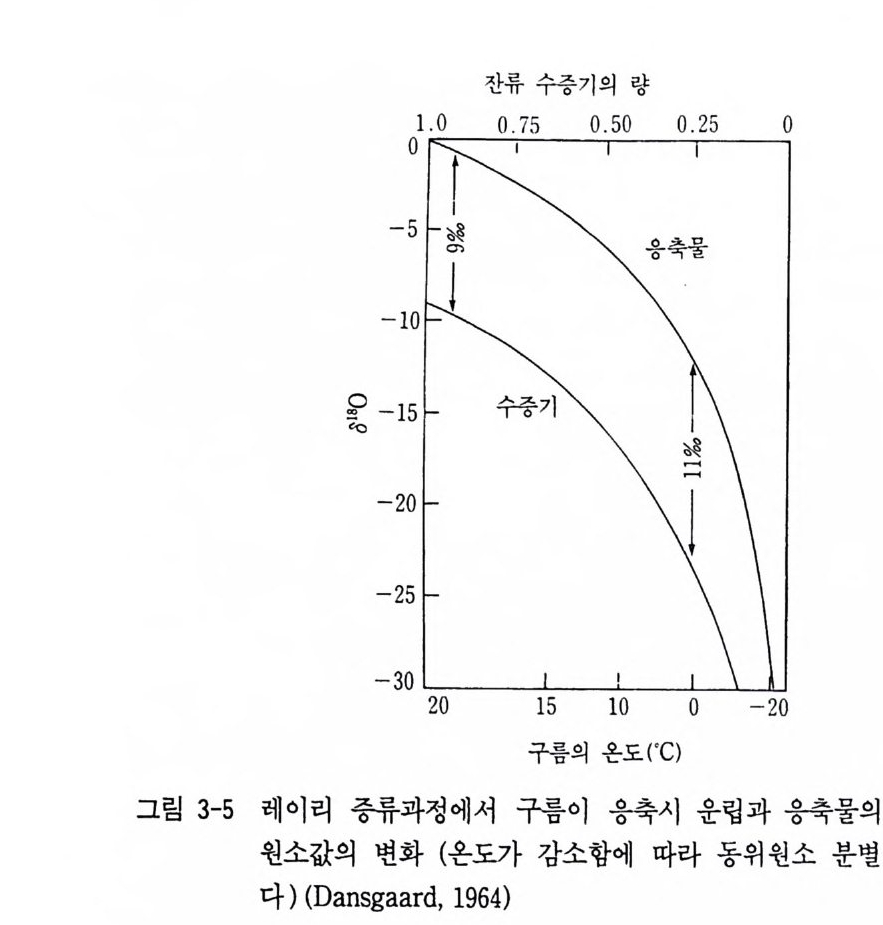
1so2H 를 포함한 것의 양을 A( 주요한 동위원소) 라 하고, 수증기 중의 물분자 중 160IH 를 포함한 것의 양을 B( 미량의 동위원소)라 하자. 이때 각각의 동위원소를 포함한 분자가 응축하는 비율은 각각의 분 자의 존재량에 비례한다. 죽 dA = kAA, dB = kaB 으로 표현할 수 있다. 여기서 kA, kB 는 각각 분자가 응축하는 반웅의 속도정수이다. kA/ka = a 와 연관시켜 생각할 수도 있다. 여기서 dB/ dA = a BlA 가 얻어지며 두 동위원소 중의 초기량에서 반응 후의 양까지 적분으로 표시하면 臼『= a\AA0 판 In 을 =aln i 욥=(信 이 된다. 양변을 A l A0 로 나누면 : / 1 。 = (것) a-I 가 된다. 동위 원소 종 B 는 A + B 합의 분률 (frac ti on ) 의 미 량에 지나지 않으므로 잔류물질 의 분률 f는 A/A0 와 같다. 따라서 BB0 I/ AAO -= fJ a- I B / AB0 - I BA O° 1A ° = fa- I - l 동위원소 성분의 천분율 표시에서 (BIA — Bo/Ao) / (Bo/Ao) • 103 이므로 a = 1ooo(r-1 - 1) 로 표현된다. 구름의 수증기의 산소 동위원소와 구름에서 만들어진 빗방울 사이 의 동위원소 분별이 바로 레이리 증류의 좋은 예이다. 빗방울에 l0% 180 이 농집되어 있다면 180 이 160 보다 1. 010 배 더 빨리 소모되었기 때문 0] 다. 8이 =는 —동1위0 0원0(소1 -분f 별° ·정OIO수) 을 a의 =미 한k1다80. I k160 = 1. 010 이며
 잔류 수증기 의 량
잔류 수증기 의 량
잔류 수증기내의 1so / 160 비의 감소 (De p le ti on) 는 구름에 남아 있는 원래의 수증기의 분류의 함수관계로 주어진다(그림 3-5) . 7) 화학성분과 결정구조에 따른 동위원소 성분변화 ®화학성분 광물의 동위원소 성분은 그 광물의 화학결합의 특성과 원자의 질량 에 따라 변화한다. 일반적으로 이온 포텐셜이 높고 원자의 질량이 작 은 이온의 결합으로 된 광물은 진동빈도가 높고 무거운 동위원소를 더 많이 함유하는 경향이 있다. 즉 180 가 많은 광물은 가장 강한 결
합의 산소로 되어 있고, 산소는 원자량이 작고 전하가 높은 양이온과 결합한다. 예를 들어 산소가 질량이 작고 전하가 높은 S i”와 결합한 석 영 (Si0 2 ) 과 원자질량이 크고 전하가 낮은 Fe2 + 와 결합한 자철석 (Fe J O ◄) 을 비교해 보면 후자보다 전자에 항상 무거운 산소의 동위원 소가 많이 있음을 알 수 있다. 석영에서 산소의 원자는 두 S i원자 사이에 대단히 강하게 결합되 어 있고, Si- 0 결합은 규산염광물 구조에서 가장 강하다. Al-0 결 합은 Si- 0 결합보다 길고 약하며 Al 과 S i의 원자량은 유사하다. 그 러므로 장석이 석영보다 항상 180/160 비가 낮고 칼슘질 사장석이 칼 리장석보다 180 / 160 비가 낮다. 일반적으로 함수 규산영광물을 제의하면 고차로 중합된 규산염광물 일수록 180 이 더 많이 농집되어 있는 경향이 있다(표 3-2). 그리고 탄산염광물의 경우 산소는 원자질량이 작고, 전하가 높은 C ” 와 결합하기 때문에 기타 광물에서보다 언제나 180 이 많이 들어 있다. Ca2+ 이온의 특성보다 C-0 결합의 특성에 더 크게 영향을 받 는다. 그러나 섬아연석 (ZnS) 과 방연석 (PbS) 울 비교해 보면 ZnS 쪽 이 PbS 에서보다 항상 “S 가 더 많이 들어 있어 질량효과 (Mass eff e- c t)에 큰 영향을 받고 있음을 알 수 있다. 탄산염광물의 경우 질량효과는 표 3-5 와 같다. 즉 CaC 아의 산소보 다는 언제나 PbC03 의 산소 쪽에 가벼운 산소가 농집된다.
표 3-5 탄산염광물-물 사이의 산소 동위원소 분별계수 (25 ' C) 탄산염광물 | l000lna | 양이온의 원자질량 CaC03 7.9 40.07 SrC03 7.4 87.63 CdC03 6.8 112.41 BaC03 6.2 137.37 PbC03 5.6 207. 20
®결정구조 일반적으로 광물결정이 밀착되게 결합되거나 질서도가 높은 구조를 가지는 광물일수록 무거운 동위원소가 더 많이 들어 있다. 예를 들면 다이아몬드와 흑연의 동질 이상 광물에서 Bo tti n g a(1969) 가 계산한 다이아몬드-흑연의 동위원소 분별은 o · c 에서 11. 5% : i, 1ooo · c 에서 0.4 %이었다. 그리고 25 ° C 에서 아라고나이트-방해석은 180 이 o.6 % ,, 13C 은 1.8%, 이었다 (Rob i nson 과 Clayt on , 1969). 안정동위원소 연구에서 함수광물이나 점토광물의 결정구조 를 연구 할 수도 있다. 예를 들면 He i nz i n g er (1 969) 에 의하면 50'C 이상과 50°C 이하에서, CuS04 • 5H20 에서 추출된 결정내에서 결합 특성이 다론 두 종류의 물을 구별해냈었다. 4 분자의 물의 산소는 Cu 이온과 결합되어 있고, 5 분자의 물의 산 소는 H 이온으로 결합되어 있어 후자가 전자에 비해 중수소가 57%, 더 들어 있음을 조사했다. 점토광물인 몬모리로나이트가 일라이트나 고령토에 비해 물과 점토광물 사이에 수소 및 산소의 교환률이 높은 사실은 O'Ne i l 과 Kharaka (1 976) 가 조사하였다. 이 같은 현상은 스멕타이트 광물내의 충간수의 존재와 관련이 있는 것으로 보여 점토광물의 충간수의 결정구조 연구에도 이용될 수 있으 리라본다. 그리고 Ultr a fi lter ati on 과정에 의해 점토광물에 무거운 동위원소 가 흡착되어 잔액에 가벼운 동위원소가 많아지는 과정도 동위원소 성 분변화의 원인 중 하나이다. 3-3 동위원소 분석용 시료준비 1) 물의 수소 및 산소 동위원소 측정을 위한 시료준비 물의 수소 동위원소비 (D/H) 측정을 위하여 물을 수소가스로 만 든 후 질량분석기에서 측정해야 한다. 현재 많이 사용하고 있는 방법
 ;==
;==
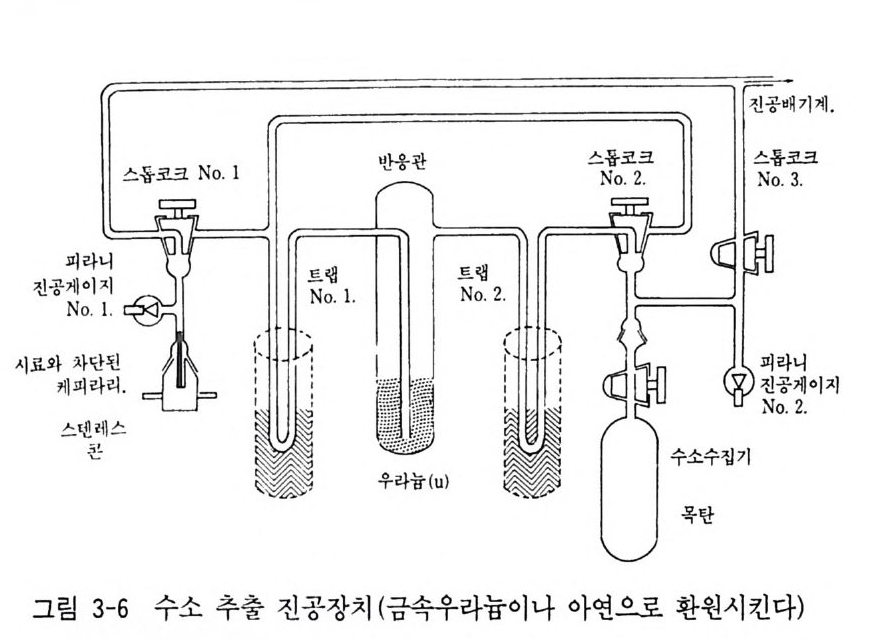
은 물의 환원법으로 금속 우라늄이 많이 이용되고 있으며 그 의 아연 도 이용된다. 사용되는 물의 시료의 양은 보통 5~10m g으로 적은 양 이므로 시료의 환원장치내에서의 공기 중의 물이나 기타 수증기와 동 위원소 교환의 혼합을 피해야 한다. 보통 사용되는 물의 환원장치는 위 의 그림 3-6 과 같다. 물시료는 전공장치내에서 금속 우라늄과 600 ' C 에서 환원시킨다. 이 때의 반응은 다음과 같다. 2H20 + U 享 U02 + 2H2 (금속우라늄 또는 아연) 이때 발생하는 수소가스를 데프라 펌프를 이용하여 수집한다. 현재 연구실에 따라서는 Bach s y s t em 을 이용 다량의 시료처리를 단시간에 하고 있는곳도 있다. 물시료 중의 산소 동위원소비 분석을 위하여 물과 이산화탄소간의
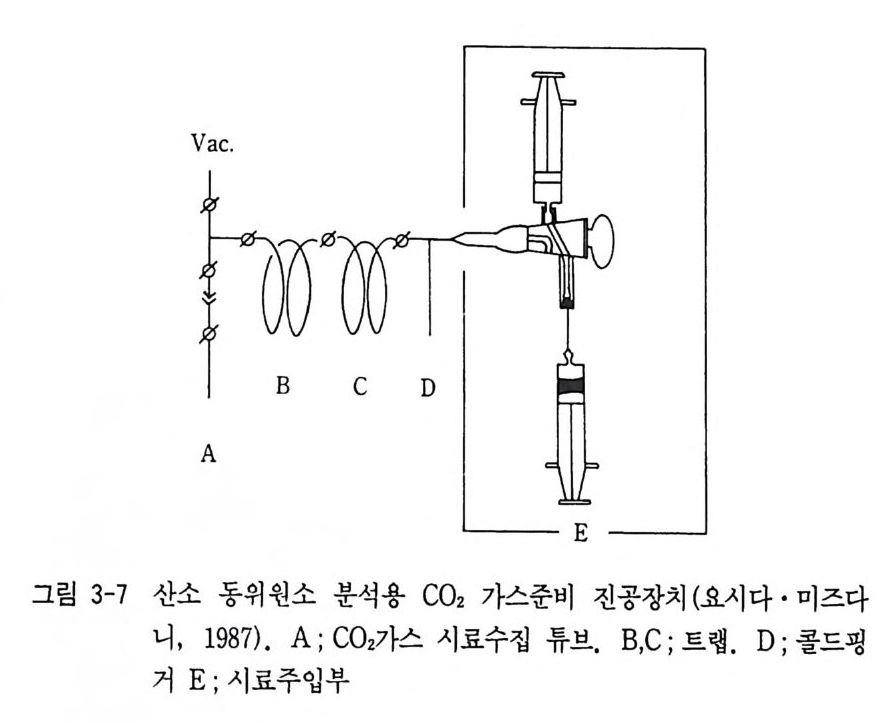
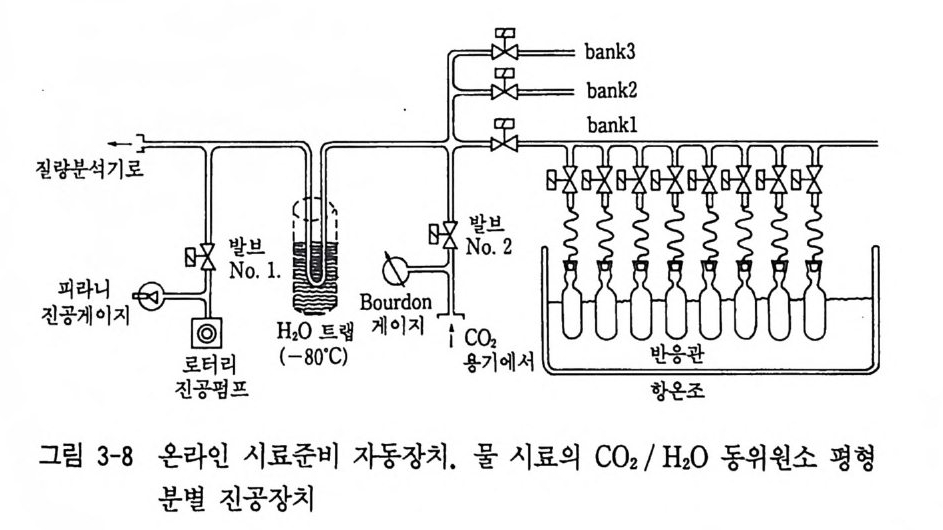
동위원소 교환법과 BrFs 을 이용하는 법, 수증기와 이산화탄소 환원 법 그리고 직접 측정하는 방법 등이 있다. 그 중 현재 물과 이산화탄 소의 교환법 이 가장 많이 이용되고 있다. 이 방법은 Cohn 과 Urey (19 38) , E p s t e i n 과 May ed a ( 1953) , Mats u bay a (19 71) 등이 구체 적 으 로 소개한 방법으로 물과 이산화탄소 사이에 25°C 에서 다음과 같은 동위원소 교환반응을 일으켜 평형에 이르게 한다. H2180 + 1 / 2 C1602 =K H/60 + 1 / 2C '80 2 동위원소 평형이 이루어지면 K=Hz180 ~I H216 며0 (18 C / 160) H20 = ~a( 180 / 160) CO2 관계가 성립한다. 앞에서 설명한 바와 같이 쩌큰 동위원소 분배계수 로서 온도의 함수이다. 보통 사용되는 시료수의 양은 l~2ml 이나 시 료처리장치의 개발로 더욱 적은 시료의 양으로도 가능하여졌다. 吉田 와 水谷 (1987) 에 의하여 물의 산소 동위원소비 측정시료 준비과정이 간략화되었다(그립 3-7). 죽, 대기압 아래에서 주사기와 같은 실린저 에 시료의 물을 6ml 를 넣고 다음에 CO2 를 7ml 넣은 후 25°C 항온조 에서 평형을 일으키고 CO2 를 추출 질량분석계에서 측정한다. 이 방 법은 자동화 전단계의 간략화된 방법으로 시간을 크게 절약해 준다. 이 같은 시료처리기구가 현재 자동화되어 시료처리에서 질량분석까 지 연속적으로 자동으로 이루어진 기구가 이용되고 있다(그림 3-8). 그리고 물의 산소를 정량적으로 이산화탄소로 변화시키는 방법으로
BrF5 를 이용해 다음과 같은 반응에서 CO2 를 얻기도 한다 (O ' Ne il 과 Eps t e i n , 1 966) .
 Vac.
Vac.
 질량분석기로
질량분석기로
H2 0 + BrFs = l / 2 02 + 2HF + Br F a C+02= CO2 이 방법은 물의 산소 동위원소비 를 직접 측정할 수 있고, 그 정도 도 물 - CO2 교환법과 비슷하나 시료처리시설에 금속제의 진공장치가 필요하며 위험한 BrFs 물질을 이용하여야 하는 단점이 있다. 다음에 설명하겠지만 규산염광물 중의 산소 동위원소바 분석을 위해 이 방법 으로 시료를 처리하고 있다. 그 의에 가열시킨 백금 필라멘트를 촉매로 하여 수증기와 이산화탄 소를 기상에서 동위원소 교환을 일으키는 방법 (Suzu o ki, 1 9 74) 이 있으 며, 이 방법은 미량의 시료에 대해서도 가능하다는 이점이 있다. 특 히 이 방법은 유체포유물의 동위원소 분석연구에 이용되고 있다. 2) 광물과 암석 중의 물의 추출 함수광물의 수소 동위원소 분리 : 점토광물이나 운모류, 각섬석류와 같은 함수광물의 수소 동위원소 분석을 위하여 시료 를 진공 중에서 고주파를 이용하여 가열 (1300~1600 ' C) 시켜 탈수된 물을 직접 우라늄 로에 유입시켜 수소가스를 만들어 수소 동위원소를 분석한다. 이때 일부 광물 중의 2 가의 철에 의해 환원된 수소를 만들기 때문 에 방전이 일어나 구리와 수소 사이에 동위원소 교환이 일어난다. 이 를 막기 위해 아래 그립 3-9 에서와 같이 이 수소를 700 ' C 로 가열한 산화동과 반응시켜 물로 바꾼 후 직접 탈수된 물과 함께 우라늄로에 서 환원시키는 방법을 Suzuok i와 E p s t e i n(1976) 이 이용했다. 보통 시 료주입 등의 작업은 시료에 수분의 혼염을 막기 위해 오산화인으로 건조시킨 전공상자내에서 실시한다. 점토광물은 충간수(흡착수)와 OH-이 온으로 존재하는 두 종류의 물이 존재하기 때문에 시료를 미 리 진공 중에서 100~250'C 가열해 충간수를 제거시킨 후 OH- 로 된 것만을분리추출한다.
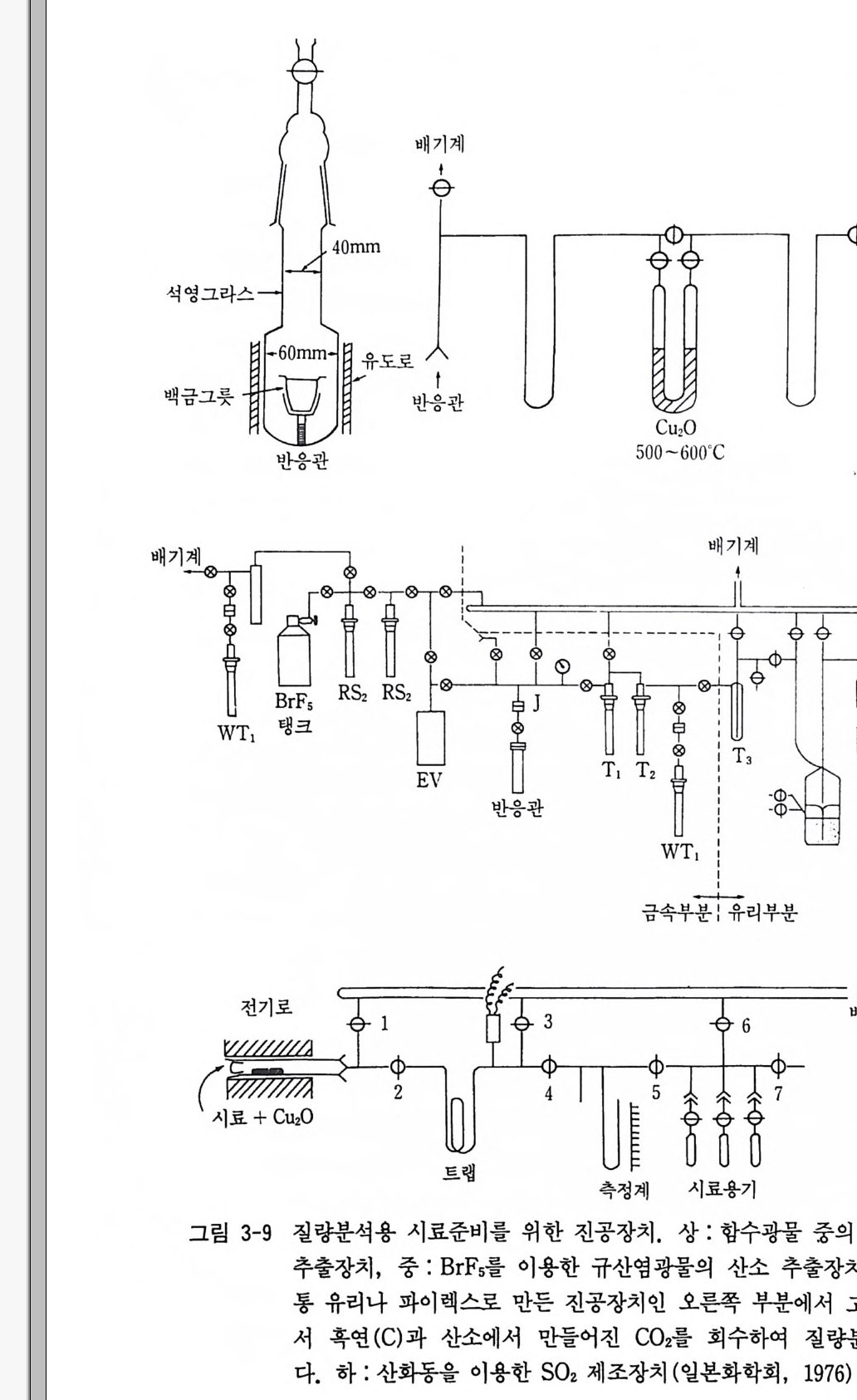
석고 등의 결정수는 전공 중에서 탈수온도까지 가열시켜 생긴 수증 기를 액체질소로 수집한 후 위에 설명한 물에서 사용하는 방법을 이 용, 수소 및 산소 동위원소 분석시료용 가스를 만들어 분석한다. 유체포유물 시료의 경우 진공 중에서 가열하는 방법과 진공 중에서 볼밀로 가루로 부수면서 포유물내의 물을 추출하는 방법아 있다. Roedder 의 (1963) 는 동관이나 스텐레스관 속에 광물시료를 넣고 진 공시킨 후 의부에서 압축기로 압축시켜 부수는 방법을 이용해 유체포 유물 중의 물을 추출했다. 이와 같은 방법은 금후 퇴적물 및 퇴적암 중에 포획된 가스의 성분 및 동위원소 성분분석용 시료를 준비할 때에도 이용할 수 있을 것이다. 3) 규산염광물 및 암석의 산소동위원소비 분석을 위한 시료처리 규산염광물 및 산화광물 그리고 암석의 산소 동위원소 분석을 위해 서는 규산염광물 중의 산소를 분리시켜 CO2 를 만들어야 되기 때문에 주로 〈 불소 〉 를 이용하는 방법을 사용하고 있다 (Ta y lor 와 Ep st e i n , 1962 : Cla yt on 과 Ep st e i n , 1958 : Cla yt on 과 May ed a, 1963) . 불소가스와 BrFs, BrF3 와 KHF 와 CoF3 의 혼합시 약 등을 사용하는데 , 이 중 불 소가스와 BrFs 가 가장 많이 사용되고 있다. 다음과 같이 규산염광물과 BrFs 를 500~650'C 의 반응관에서 반응 시켜 산소를 유리시킨다. Si0 2 + 2BrFs = S iF ◄ + 2BrFa + 02 KAlS i a 야 + 8BrFs = KF + AlFa + 3S iF ◄ + 40 + 8BrFa 이때 만들어전 산소는 700'C 에서 흑연과 반응시켜 CO2 를 만들어 질량분석기로 분석한다. 이 장치는 그림 3-9 와 사진 3-1 과 같다. 광물 및 암석의 분말시료를 20~25mg 반응관에 넣는다. 반응관은 불산이나 불소 가스를 쓰기 때문에 시료에서 산소를 추출하는 과정까
 배기 계
배기 계
 사진 3-1 규산염광물 및 암석의 산소 동위원소 분석을 위한 시료처리 진공
사진 3-1 규산염광물 및 암석의 산소 동위원소 분석을 위한 시료처리 진공
지는 니켈관 등 금속 전공장치가 필요하고 CO2 를 만드는 부분은 보 통의 유리나 파이렉스 전공장치를 이용한다. 반응관에 시료 를 넣을 때에는 공기 중의 수증기 혼입을 막기 위해 오산화인으로 건조된 진 공상자 속에서 작업을 한다. 시료를 넣은 반응관을 시료처리 전공장치에 부착시켜 배기시키고 난 후 2oo · c 에 2~3 시간 가열시켜 시료에 흡착된 수분이나 흡 착 가스 를 제거한다. 이때 함수광물인 경우는 광물 중의 물이 유실될 염려가 있으므로 주의해야 한다. 그리고 보통의 조암광물인 경우에는 BrFs 의 양은 반응에 필요한 양의 10 배 정도 넣고 전기로 속에서 550'C 내 의에서 12 시간 정도 반응시킨다. 반응온도는 광물의 종류에 따라 다 소 다르게 할 수 있다. 보통 감람석, 석류석, 휘석 등은 650'C 내의 에서 반응시킨다. 반웅이 끝난 후 액체질소로 과잉 BrFs 를 제거한 후 산소만을 700'C 분광분석용 흑연봉으로 보내어 CO2 를 만들어 이 CO 2 를 회수하여 질 량분석계로 측정한다. 이 실험에서는 불산이나 불소가스 를 사용하기 때문에 대단히 위험하므로 안전에 특별한 주의를 요한다. 4) 탄산염광물 및 탄산염암의 탄소 및 산소 동위원소 분석을 위한 시료처리 탄산염광물 및 탄산염암석은 시료의 C 아 가스에서 탄소 (13 C / 12C ) 와 산소 (180/“O) 의 비를 동시에 분석할 수 있다. 탄산영광물은 보 통 다음과 같이 인산으로 분해시킨다. 3CaC03 + 2H3PQ 4 = Ca3 (PQ 4 ) 2 + 3H20 + CO2 이때 사용되는 인산은 실험 결과 인산의 산소와 시료 중의 산소와 는 동위원소 교환이 거의 일어나지 않는다는 사실이 밝혀져 100% 인 산을 주로 사용하고 있다. 〈사자형의 반응관을 만들어 반응관의 한
끝에서 20~40m g의 분말시료를 먼저 넣고 다음 한쪽 관에는 100% 인산울 2ml 정도 넣은 후 진공실험장치에 부착, 배기시킨 후 25 ° C 에 서 반응시킨다. 탄산염광물은 보통 순수한 방해석 의에 방해석과 돌로마이트, 탄산 망간 등이 공존하거나 혼재하므로 반응시간에 의해 각각 이들 광물의 시료가스를 분리 수거할 수 있다. 순수한 방해석은 0.5~2 시간이면 반응이 종료된다. 그러나 돌로마이트는 3 일 정도, 탄산망간은 1 주일 이상이 걸린다. 순수한 시료의 CO2 가스만을 얻기 위해서는 드라이 아이스와 변성알콜을 혼합한 트랩을 사용해 수분(수증기)을 제거해야 한다. 반응에서 얻어진 CO2 시료가스에서 탄소와 산소 동위원소비를 질량분석기에서 동시에 측정하게 된다. 시료가 패류나 산호의 화석인 경우 유기물질기원의 물질을 제거해야 한다. 5) 유기기원의 탄소의 동위원소비 측정을 위한 시료처리 퇴적물내의 유기물질, 식물질과 석탄 등 유기기원의 탄소의 동위원 소비 측정을 위한 시료는 우선 유기기원 탄소 이의의 탄소는 화학처 리에서 제거시킨 후에 시료처리 진공장치에서 태워 CO2 를 만든다. 시료의 특성에 따라 시료의 양은 다르나 보통 5mg 정도의 시료를 CuO 와 950 ° C 에서 20~30 분 가열시켜 C 아를 만든다. 이때 시료 중의 CO2 이의의 S02, 수증기 등을 제거하기 위해 펜탄이나 시료와 CuO 와 은박편을 넣은 후 진공밀폐 후에 1ooo·c 전기로에서 C 아를 만들 기도한다. 실험실마다 약간씩 다론 방법으로 시료처리를 하고 있다. 6) 황화광물 • 황산염광물의 황 동위원소비 분석을 위한 시료처리 황 동위 원소 분석을 위 해서 황화광물은 보통 황산바륨 (BaS04) 으로 바꾸어 황화온 (Ag 2S ) 을 만든 후 C t12 0 와 800°C 에 태 워 S 아를 만들어 질량분석계에서 측정한다. 실험실마다 시료처리 방법에 다소 차이가
있다. 그리고 황화광물의 종류에 따라 처리방법이 약간 다르다. 여기 서는 저자가 실험시 사용했던 방법을 소개하겠다. Lung e meth o d ; 황철석, 유비칠석, 자류철석과 같은 황화광물 시 료는 시료분말 50~70m g을 바커에 담고 1 : 3 또는 3 : 1 비율의 HNO 파 HCI 시약을 넣고 Wate r ba t h 에서 증발 건조시킨다. 그 후 6N 의 HCI 을 20mg 넣고 증류수를 200ml 넣은 후 따뜻하게 한 후 10% 의 BaCl2 를 15ml 정도 사용하여 BaS04 를 침전시켜 여과시킨 후 태 워 BaSO 를 얻는다. 다음에 BaS04 는 동량의 흑연 (C) 과 섞 어 백 금 그릇에 넣은 다음 긴 석영관내에 장진하여 1 . ooo · c 에서 건식법에 의 해 다음과 같이 BaS 를 만든다. BaS04 + 2C 一 BaS + 2C02 이 시료를 여과시킴과 동시에 5% 의 질산은 (A g NOa) 을 20ml 정도 떨어뜨려 A g 2S 를 침전시킨다. 황화은광물은 흑연과 1, ooo·c 에 서 H2S 로 환원시 키 거 나 (Raft er 등, 1961), H-HaPOcHCl 환원제 용액에 의해 H2S 로 환원시킨 후 (Thode 등, 1961) 에 Ag 2 S---+ S02 로 변화를 시 키 는 Ag 2 S 산화법 과 BaS04 분 해법을 많은 실험실에서 쓰고 있다. V20 파 Si0 2 혼합물을 이용하여 황화광물과 황산영광물을 직접 S 아로 변화시키는 방법이 Yana gi sawa 와 Saka i (1983) 와 Ueda 와 Krouse(1986) 등의 실험에서 산소 동위원소비 값의 변화 없이 빠른 처리방법으로 황 동위원소 분석용 시료가 얻어짐이 소개되었다. 위의 몇몇 과정에서 얻어진 시료의 검은색 황산은은 시료처리 전공장치에 서 Cu20 와 800'C 에서 S 아를 만들어 질량분석계에서 분석한다(그림 3 선). 황화광물 중 섬아연석, 방연석 등은 산(H CI) 과 반응해서 황화 수소를 만들고 이것을 아래 예와 같이 착산카드뮴과 처리해서 CdS 를 얻은 후 질산은을 첨가하여 A g 2S 를 만든다.
ZnS + HCl 一 H2S + ZnClz H2S + Cd(CH 3 CO O) z 一 CdS + 2CH£00H CdS + 2Ag N Q 3 -- t Ag 2S + Cd (NQ 3 ) 2 시료에서 A g 2S 가 만들어지면 시료처리 진공장치에서 S02 를 얻는 방법은 위와 동일하다. 황화광물을 1,000'C 정도에서 그리고 CuO, V 요 또는 아 반응에서 직접 S02 를 얻는 방법도 이용되고 있고 (Aul t와 Kulp, 1959 ; Thode 등, 1961 ; Thode, 1963, 1970 ; Jen sen, 1967 ; Hoe fs, 1973), 최근에는 V20s 와 S i 02 와 섞어 직접 태우는 방법도 개 발되어 있다 (Ueda 와 Krouse, 1986). 7) 황산염광물의 산소 동위원소비 분석을 위한 시료처리 자연에서 산출되는 중정석, 석고 등과 같은 황산염광물과 해수나 온천수 중에 웅존하고 있는 so~- 이 온의 황 동위원소 분석을 위한 시료처리는 위에 설명한 방법과 동일하다. 그러나 이들의 산소 동위 원소 분석을 위한 시료 추출장치는 다르다. 시료는 다음 반응식에서 BaS04 + 2C = BaS + 2C02, CO 가 얻어진다. CO2 가스를 질량분 석기로 측정하는 방법이 있다. 그리고 온천수나 하천수 중의 sot 이온의 경우나 중정석, 석고 등은 황산바륨을 만든 후 다음과 같이 황산바륨을 진공장치내에서 환원시켜 CO2 를 만들어 질량분석기로 측 정한다. 황산바륨 10~15mg 시료와 그의 반 정도 양의 흑연을 잘 섞어서 환 원장치의 백금으로 만든 연소그릇에 넣고 진공내 가열장치에서 1,ooo·c 에 20 분간 환원시켜 이산화탄소를 얻는다. 3-4 동위원소 표시법 분석된 안정동위원소비의 표시방법은 표준시료에 대한 분석용 시료
에 포함되어 있는 동위원소비를 다음과 같이 천분율 편차로 표시한 다. 0 (%,) = ( 墨 -1 ) • 1000 여기서 R 은 시료와 표준시료의 13C / 12c , 180 / 0, D / H, 34S / 32s 등의 비이다. 산소와 수소의 표준시료는 표준평균해 수 SMOW (St an dard Mean Ocean Wa t er) 를 사용하며 하와이만의 해수 (1 8 0 / 160 = 0.0 0 19999, D I H = 0.00015744) 를 표준으로 하고 있다. V-SMOW 인 D / H = 0 . 00015595, 18 0 / 160 = 0 . 0020052 (Gon- fian ti ni, 1978) 가 사용되기도 한다. 탄소는 미국 남부 카로라이나 (South Caroli na ) 주의 백 악기 의 Pee Dee Formati on 중의 벨 렘 나이 트 (Belem nitel la amer ic ana)PDB 의 탄산칼슘 중의 탄소의 비 (13 C / 12c = 0.0112372) 를 표준으로 사용하고 있다. 그리고 황은 Cany o n Di ab lo 운석 중의 트로이라이트(tr o ilit e, FeS) CDT 의 황의 비 34S / 3 2s = 0.0 0 45(32S / 34S = 22.22) 를 표준으로 사용하고 있다. 분석된 동위원소비는 %로 표시되는데 물 (H 2 0) 을 예를 들면 수소 (IH, 2H) 와 산소 (16 (), 0, 180) 의 동위 원소의 조합으로 되 어 있다. 이 둘 조합에 따라 물분자는 질량수가 다르게 된다. SMOW 는 수소, 산소 모두 0%, 이다. 만일 물의 8180 값이 0 보다 큰 값이면 표준 해수에서보다 무거운 동위원소 (D, 1 8()등)가 상대적으 로 많이 농집되어 있음을 의미하고, 0 보다 적은 값이면 가벼운 동위 원소 (16 Q, IH 등)가 해수에서보다 상대적으로 많이 농집되어 있음을 의미한다. 예를 들면 물의 산소 동위원소값 (8180) 이 _ 8%, 이라면 해 수에서 보다 가벼운 동위원소가 많고 + 10% 이라면 해수에서보다 무 거운 동위원소가 많이 분배되어 있음을 말한다. 죽 동위원소값의 대
표 3-6 안정동위원 소 의 존재도와 표준시료 동위원소 존재량 표준시료 동위원소비 참고문헌 I2HH (D) 909. 0. 1985 45 5\ VSM-SOMWO W 22HH /I 11HH == 00 .. 00000011555579 5 CGorani fgi a(n 1 9ti 6n1i) ( 1978) 312Hc 98.* 88 8 Pee Dee 13C 112 c = o . 00112312 13c 1.11 12 for mati on “C * belemnit e (PDB) 14N 99. 63 4 Atm osph e ric 15N / 14N = 0 . 0036765 IIS6°N 9090... 037 536 796 nSViM-tS rOo M gWO en W 118800 /I 116600 == o0 .. 0000220o0o5s22 GCorani fgi a(n l 9ti6 n1i ) ( 1978) 110 31820s 950.. 20 0 4 Cany o n 떳 S / 32S = 0 . 0450451 33S 0.7 6 Dia b l o 떳; 4.2 2 tro il it e 36S 0.0 1 4 희 3가H스e : 0.0 0 014 Atm o sph e ric 3 He / 'He = 0 . 0000014C Lup ton and Craig (1975) 420HN e e 9(100. 04)8 Ahetl mi u om s ph e ric 21Ne / 20Ne = (1) Bott om ley et al. neon (1 ) 0 . 002980 (1984) 2221NN ee 90..22 75 0 22N e / 20Ne( 2 )= 0 . 002959 (2) Eberhardt et al. (1) 0 .10 219 (19 65) (2) 0.1020 36A r 0.337 Atm osph e ri c 36A r /'0Ar = 0 . 003384 Ste ig er and Jag e r argo n (1977) 38Ar 0.063 78842800AKKKrrrr 910901.... 23655402 773 Akrtym po tospn h e ri c 878820KKK rr r /// 88~44KKKrrr === 000. . . 200003269106078 7 Basfo r d et al. (19 73)
83Kr 11. 477 83Kr / 84Kr = 0 . 2013/i 114Kr 56.998 81264KX re 107. .3 099581 Atm o sph eri 81264KXr e/ / 8143K2rX e= = 0 .0 3 .0 050234 126Xe I O. 0887 I xenon • 1152367X e / 132Xe = 0 . 003 1122191Xxee 216..4931 9 131220890X X ee I/ 113322XXee == 00 .. 908731 36 113301X Xee 241.. 0272 1 113301XXee // 113322XXee == Oo.. 71 58 9104 I Basf o r d et al. ( 19 73) 1133s2 xXee 21680...884593 7 I1l ~36x Xee // 113322XXee == Q0 .. 33289749 134Xe *3H 와 14C 은 방사성동위원소로 상충대기권에서 계속적으로 생성되고 있음. SMOW (표준평균해수, Craig , 1961) V-SMOW (비엔나 -SMOW, 국제원자력기구, Gonfi an ti ni , 1978)
소는 표준시료의 동위원소값에 비해서 가벼운 동위원소나 무거운 동 위원소가 어느 쪽에 더 많이 분배되었는가를 가리키는 상대적인 척 도 인 것이다. 대부분 연구실에서 SMOW 롤 사용하고 있으나 PDB 를 사용하는 곳도 있다. 이들 두 가지는 0SMOW = 1.Q 3 Q8 6 0PDB + 30.86 관계식에서 서로 환 산할수 있다. 표준시료의 종류와 표준시료의 존재량은 표 3-6 과 같다. 비활성기 체 (Noble gas ) 가스도 같은 방법으로 이용되므로 참고로 표에 포함시 켰다. 3-5 안정동위원소의 지질학적 이용 현재 알려져 있는 약 300 여 종의 안정동위원소 중 지구과학에 가장
많이 이용되는 안정동위원소는 H, 0, C, S, N 등의 가벼운 원소들의 동위원소이다. 지구는 암석권 , 수권, 대기권, 생물권으로 나눌 수 있 다. 자연계에 있어서 각 권 사이에 광범위하게 동위원소 분별이 일어 나고 있다. 대기권의 수증기와 수권의 해수의 동위원소 교환반응이 일어나고 해수-탄산염, 해수-퇴적물 , 해수-암석, 지하수-광물(암석) 등 물질 상호간에 일어나는 동위원소 분별작용이 바로 지질학적 사건 의 중요한 문제해결의 단서가 되고 있다. 따라서 안정동위원소는 지 질학의 여러 분야에 가장 많이 이용되고 있는 것 중의 하나이다. 특 히 물질의 기원과 성인, 광상생성의 환경과 성인, 물질의 생성시의 물리화학적 조전해석, 환경연구, 고기후연구, 물질의 순환연구, 석유 자원탐사연구 등에 많이 이용되어 오고 있다. 광상학에 응용된 예는 아래 표 3-7 과 감다. 표에서와 갇이 황 동위원소는 안정동위원소가 광화용액 중의 황의 기원, 황의 이동, 광액의 침전온도, 금속의 기원 울 밝히는 데 이용되고 있다. 그리고 유체포유물의 수소 및 산소 동 위원소비 분석에서 광화열수용액의 기원, 순환수와 열수의 혼합과 광 물의 침전기구 등을 연구하는 데 이용되고 있다. Ure y(1 947) 는 처 음으로 해수와 탄산염 이온간의 아래 와 같은 동위 원소 평형을 이용하여 탄산염광물을 이용한 고온도 연구를 실시했다. C160 i-+ 3H/80 = C180 i-+ 3H2160 a = ((118800 // 116600)) CHO2°§ - = K} 평형상수 K 는 온도의 함수이므로 동위원소 분별정수 (a) 가 온도의 함수임을 이용하여 탄산염으로 구성된 유공충(Jo ram i nzf e ra) 등의 화석 의 산소 동위원소비 (8180) 를 측정, 고기후를 연구할 수 있게 되었 다. 물론 기후가 인간생활은 물론 지구상의 식량생산과 관련되어 있 으므로 우리 인간생활과 밀접하게 관련되어 있음은 두말할 필요가 없다.
표 3-7 안정동위 원소의 광상학에 응용 동위원소 해석 내용 응용 실례 1. 산소 (0180) 및 l) 광석광물 및 맥석광물 캐나다의 애뮤레트 광산의 애 및 수소 (8D) 동위 중의 유체포유물이나 맥석 뮤레트 A 광체 (Shepp a rd, 19 원소 광물의 oD, 0180 값에서 열 77 ; Tay lo r, 1979) . 상동중석 수광화용액의 기원과 순환광상, 무국금은광상등(Kim,K. 수의 혼입비율 해석 H. 등, 1988 ; 김규한 의. 1990 2) 동위원소 분별계수를 이용 캐나다의 함금석영맥 (Tay lo r, 한 광상형성온도 추정 1979). 2. 황 안정동위 1) 034s 값이 0%, 내의인 경우 오스트레일리아 북부 퀸스랜 원소(성명) 황의 기원이 마그마 기원 드에 있는 다이아네와 오케이 해석 광체 (Gre g or y와 Robin s on, 19 84). 황의 기원은 마그마 기원 이 우세함 2) ~s 값의 변화폭이 크고 오스트레일리아 퀸스랜드의 마 밋 S 가 부화된 경우 황의 기 운트아사 연, 아연 광체 중의 황 원은 생물학적 퇴적기원으 칠석 (Hoefs , 1980 ; Sm ith와 로 해 석 Croxfo rd , 1973) . 3) 황동위원소값의 변화경향 아일랜드의 타이나 (T ynag h) 에서 황의 이동을 해석 광산에서 단충을 따라 이동된 황 (Bo ast 등, 1981) . 4) 맛 S 가 부화된 황은 해수나 캐나다의 파인포인트광상의 황 증발 잔류암에서 유래 의 기 원 (Sasak i와 Krouse, 19 69). - 5) 광체간의 ~s 값 차이에서 오스트레일리아 퀸스랜드의 마 광체형성 과정의 차이를 해 운트이사 연, 아연, 동광체의 석 성인. 6) 동위원소 지질온도계로서 신예미, 삼보 광산(김규한, 19 광석 광물 침 전은도 추정 80, 1990) . 7) 동위원소자료의 체계적 분 아일랜드의 센트랄프레인에서 석연구에서 금속의 기원 해 의 금속의 기원 (Doe 와 Zart 석 man, 1979 ; Boast 등, 1981) .
고환경 연구의 일환으로 극소량의 시료에 대한 분석법의 개발에 힘 입어 미화석의 0180 분석, 남극빙하의 評 0 분석, 많은 수목의 셀룰 로스의 oD, 0180 분석, 처트 중의 인회석 등의 인산염광물의 0180 분석 등의 많은 연구가 진행중에 있다. 환경방제 (Envir o nmenta l pro te c ti on ) 연구로 환경오영원의 추적에도 동위원소가 이용된다. 해안의 물 중의 전탄소분석 (IC) 에 의해 자연 환경에서 생성된 탄소와 안간의 오염에 의해서 만들어진 탄소를 구별 할 수 있게 되었다. 대기와 해수 중의 SO t의 034S 분석으로 S 기원 과 황의 순환을 정량화할 수 있게 되었다. 예를 들면 비오영지역인 무인도, 공장지역 등의 대기 중의 S02 나 CO2 를 수집하거나 식물의 잎을 채취, S 를 축출하여 a34S 분석을 실 시하면 화석연료 등 인간활동에 의하여 오염된 지역과 동위원소비의 값이 차이가 있어 오염의 정도를 알아낼 수 있다. 하천수 중의 SO t의 샹 4s 분석에서 농약오염, 공장오염, 비오염 등의 황의 식별이 가능함과 동시에 하천의 주류와 지류간의 혼합비율 도 질량평형 계산에 의해서 정량적으로 추정할 수 있다. 수도수, 공업용수, 농업용수 등 수자원 연구에도 동위원소가 이용 된다. 지하수 시추공이나 지하수 양수장에서 물을 채취해 0180, oD 동위원소비를 분석하여 지하 대수충내에서의 지하수의 이동, 지하수 의 기원, 지하수의 수질, 지하수량의 평가 등에 응용하고 있다. 따라 서 안정 동위 원소 수문학 (Sta b le iso to p e hyd r olog y) 분야가 중요한 한 위치를 차지하고 있다.
Produc t labe lli n g으로도 이용되는데 예를 들면 o13C 값으로서 인공 산과 천연산의 바닐라를 구별할 수가 있다. 또 과줍, 쥬스 등에 첨가 된 물의 비율을 동위원소비로서 알아낼 수 있고 캠 시럽이 섞인 꿀울 식별하는 데도 이용되고 있다. 이처럼 안정동위원소의 응용연구가 다양하며 수권의 발달, 환경문 제, 열수변질, 광화용액의 기원과 침전조전연구, 멜트-유체-고제 상호작용, 물-암석 상호작용 등의 연구에는 안정동위원소 지구화학의 개념이나 자료 없이는 해석과 설명이 되지 않을 정도이다. 상온에서 형성된 물질의 동위원소 분석에서 물질의 기원규명과 물 질의 순환, 환경오염 등의 연구에 큰 성과를 얻었다• 한편 고온환경에서는 마그마 기원의 휘발성분의 트레이서, 동위원 소 분별작용, 물-암석 상호반응, 지각과 맨틀의 진화, 화성암, 변성 암, 광상학의 암석 및 광상의 성인 문제해결에도 안정동위원소의 이 용이 급증하고 있다. 그리고 달과 화성의 암석이나 운석 같은 우주물질기원 연구에도 많 이 이용되고 있다. 3-6 동위원소 지질온도계 안정동위원소 연구의 큰 성과 중의 하나가 동위원소 지질온도계의 실험 및 이론적 연구이다. 자연의 두 물질간에 다음과 같이 동위원소 교환반응이 일어나는 경우 앞장에서 설명한 것처럼 평형상수 K 는 보 통 아래와 갇이 표현된다. aA, + bB2 = aA2 + bB, K = (A2) a (BI) b = (A2 / Al) a (A,) a (B2) b - (B2 / B1) b 분배함수의 비 Q 2/ Q 1 과 비교하면 K = {$겁問 인 관계에 있다. 이 값은 보통 통계역학적인 방법이나 스펙트럼 자료에 의해 계산된다. 두 물질 A, B 간의 동위 원소 평 형 시 동위 원소 분별정 수(I so t o pic frac ti on ati on fac to r ) a 는 야 - B = RA / RB 로 정 의 되 며 이 를 8 로 표시 하면
aA - B=103 +~ 0 이 된다. 보통 a = K i 인 관계에 있으며 n 은 동위원소 교환이 일어난 원자 의 수를 말한다. CO 2 와 H 2 0 의 경우 K = a = M};:; 로 n = 1 인 경우이다. a 의 값은 보통 일정한 값을 가지며 보통 l.OOx 로 표현된다. 여기서 x 는 천분율로 나타낸 값으로 ZnS( 섬아연석)과 PbS( 방연석) 사이 에 2oo · c 에 서 a = 1. 0036 이 라면 방연석 보다 성 아연석 내 에 “S 가 3.6 % , 더 농집되어 있음을 의미한다. 평형상수는 K = exp( — 4G° / RT ) 관계 에 있고 Kl = (qA / qB) T 로 분배 함수로 표현된다. 진동 분 배함수는 온도에 따라 변화함을 앞장에서 설명했다. 따라서 공존하는 두 물질간의 동위원소 평형시 평형상수 a 는 온도의 함수로 a = 1. 0036 은 103 Ina = 3.6 %, 로 표현되며 이상기체인 경우 Ina 는 1 / T2 (고온 ) 과 1/ T ( 저온)의 비례관계로 변화한다. lOOOlna —1 / T의 곡선은 이론적인 계산이나 두 굉물씽. 또는 광 수물 용있액다간. 의 a실A- 8험 =에 憶서 얻=어 i진 : 동:畵위--원: 소이 며분 별1정03수ln에(l . O의O 해X)서 츠도 X 그이려므질로 lOOOlna 츠& —8B = 4A -B 로 표현되며 이 값은 안정동위원소 지구화학 에서 대단히 중요한 의미를 가진다. L1, a, lOOOlna 를 비교하면 표 3-8 과 같다. 그리고 실험에 의하여 실험실에서 떠춘 결정할 수도 있 다. 수소와 산소 동위원소에 대한 실험은 주로 광물분말 10~20m g과 물(보통 200m g)을 금이나 백금으로 된 캡슐에 넣고 진공밀봉한 후 압 력 은 보통 1 ~ 2Kbar 의 Confi ning pre ssure 조건의 보통실험 에 서 쓰 는 용기 (Hyd roth e nnal a pp ara t us) 에 넣은 후 온도를 변화시켜 가면서 동위원소 교환반응을 일으킨다. 석영과 물의 경우를 예를 들면 원래시료인 석영의 0180 는 + 10%,
표 3-8 L1, a, lOOOlna 의 비 교 8A 8e llA-8 aA-8 l0JI naA-B 1.00 。 1 1. 001 0.9995 10.00 。 10 1. 01 9.9 5 20.00 。 20 1. 02 19.8 0 10. 00 5.0 0 4.98 1. 00498 4.96 20.00 15.00 4.93 1.00493 4.91 30. 00 20.00 9.80 1.0 0980 9.76 30.00 10.00 19.80 1.01 980 19.6 1
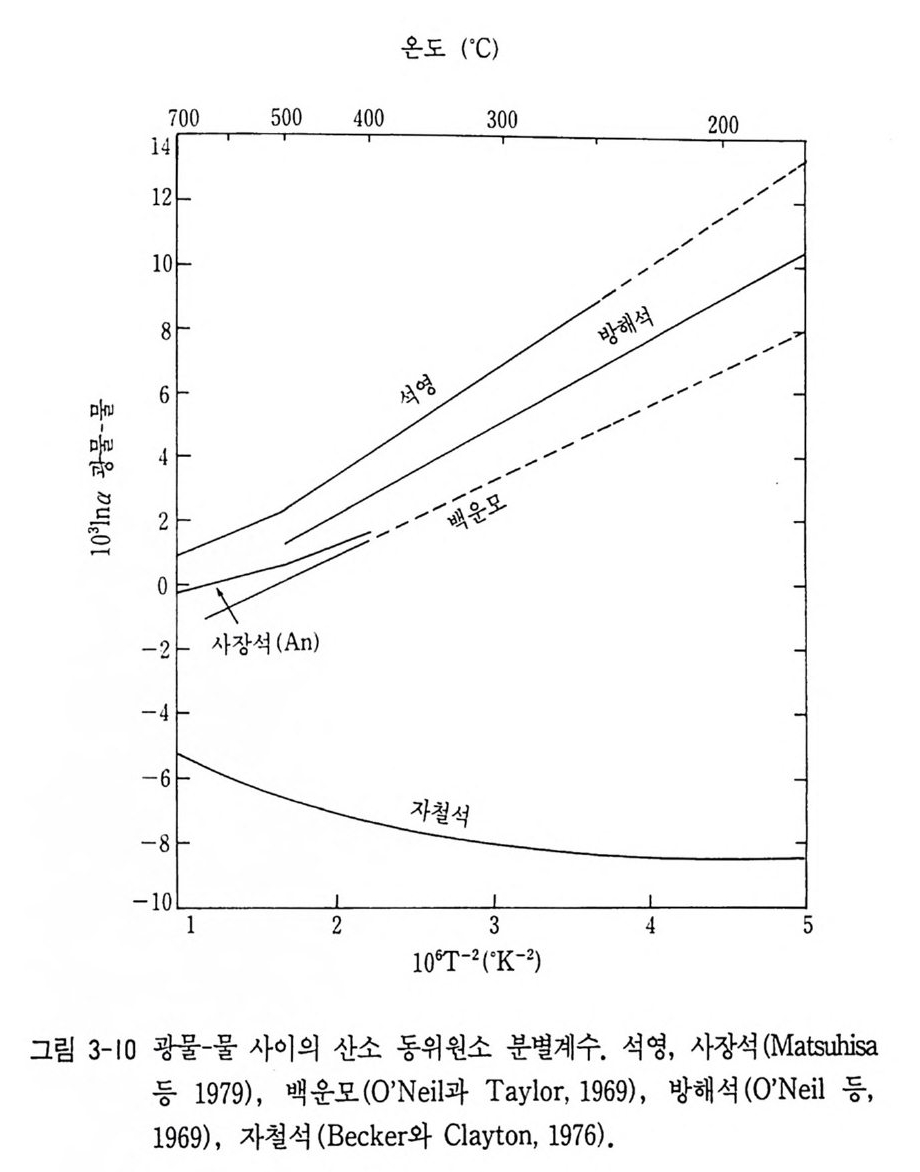
과 각각 —5, + 5, + 15%, 인 물을 500 ' C 에 서 교환반응을 일으킨다 면 L118 아 -u 의 초기값은 8180q 一 8180 roi료 정의되므로 각각 + 15, + 5, -5 가 된다. 50%, / 일 속도로 평형을 일으킨다면 약 1 주일 후에는 L1180 = 3.0 %인 값으로 평형이 이루어지게 될 것이다. L118 아 -m 값은 실제로 lOOOlna 를 사용한다. lOOOlna 와 T 에 대한 실험곡선이 많이 알려져 있다. 이와 같이 공존 광물쌍간의 동위원소 평형이 온도의 함수이므로 공존하고, 동위원소 평형에 있는 두 광물 의 동위원소비를 각각 분석하여 그들 광물의 침전시의 온도를 계산하 는 것을 동위원소 지질온도계라고 한다. 지질학적으로 주요한 여러 광물에 대한 많은 실험결과가 있으며 그 중 몇가지 예를 들어본다. 광물-물 사이의 산소 동위원소 분별계수는 그립 3-10 과 갇다. Mats u h isa 등 (1979) 에 의 하여 석 영 -물 사이 에 얻어 전 동위 원소 분 별계수는다음과 같다. lOOOlna석 영물= 2.05(106T-2) - 1.14 (500~soo·c 사이) lOOlna 석영불 = 3.34(1061 '-2 ) -3.31 (250~5oo·c 사이)
 온도 ('C )
온도 ('C )
공존하고 동위원소 평형에 도달해 있는 석영과 물의·산소 동위원소 비 분석으로 석영의 침전온도를 계산할 수 있다. 또한 석영맥의 석영 시료의 산소 동위원소 분석과 다론 지질온도계 에 의해 온도를 알면 석영이 침전할 때의 열수용액의 산소 동위원소
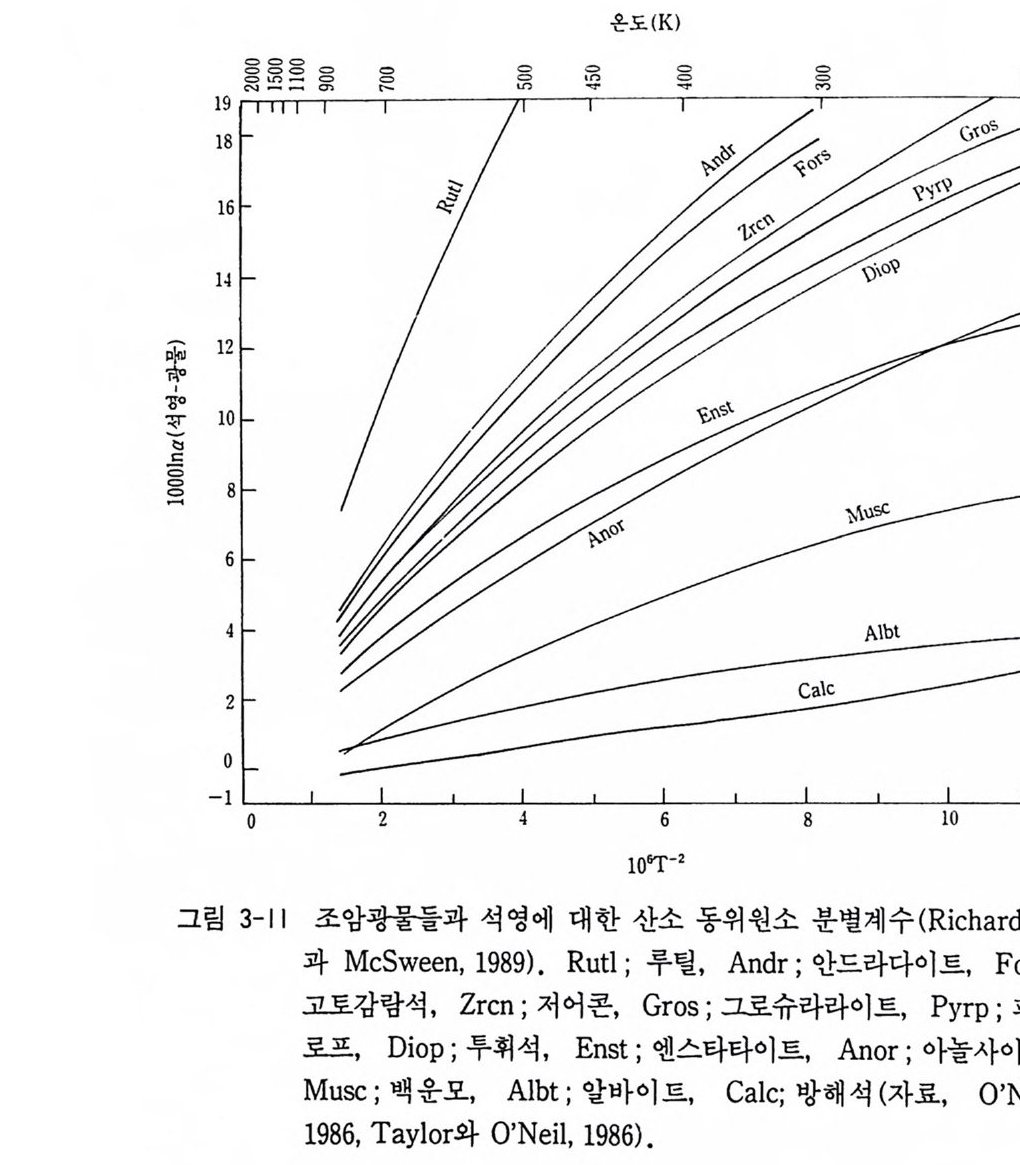
비 (81 8 0 距 o ) 를 계산할 수 있다. 이것은 열수광화용액의 기원과 상이 한 기원의 물의 혼합 등의 중요한 정보를 준다. 그림 3-11 은 석영과 기타 광물둘 사이에 얻어진 산소 동위원소 분 별계수를 나타낸 것이다. 석영과 기타 조암광물 사이에도 동위원소
 온도 ( K )
온도 ( K )
 T·c
T·c
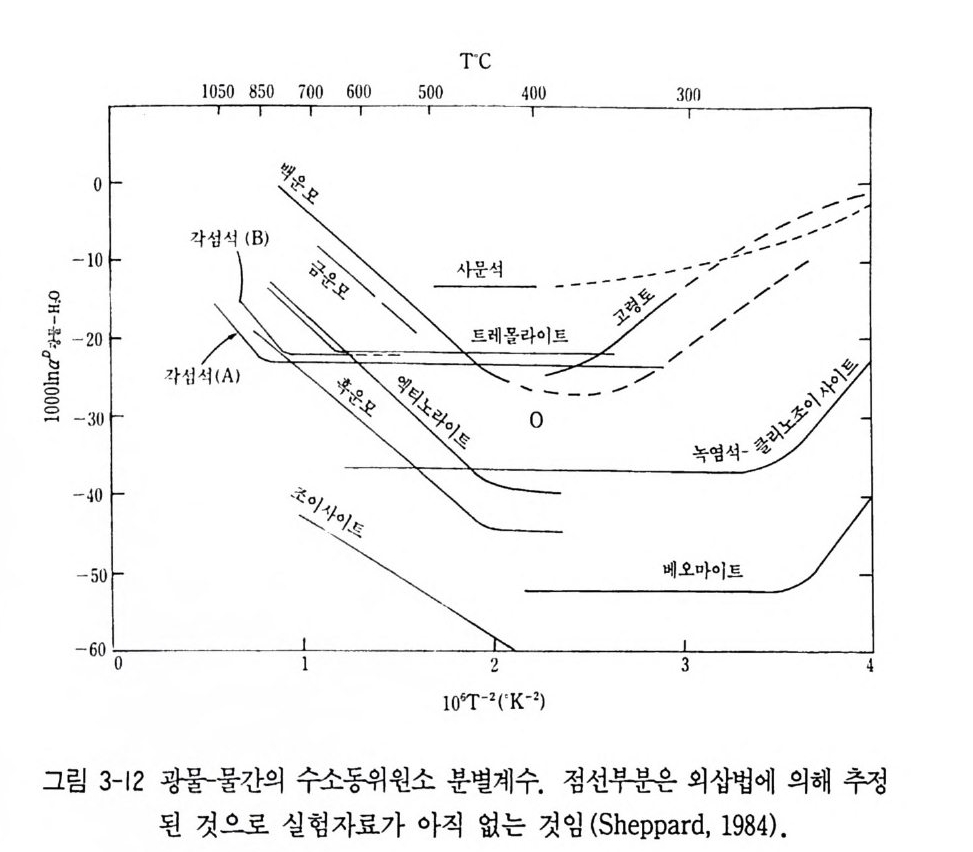
분별계수의 온도 의존성이 대단히 좋다. 산소의 경우는 실험결과가 많지만 수소의 경우는 비교적 적으며 수소 동위원소 분별계수의 온도 의존성은 불규칙하다(그림 3-12). soo·c 이하에서 각섬석 - 물의 동위원소 분별계수의 온도 의존성이 거의 나타나지 않고 운모류는 온도 의존성이 크다. 고령토와 백운모 등은 고온과 저온 환경에서 온도 의존성의 곡선의 기울기가 반대이다. Suzuok i와 Ep st e i n ( 1976) 에 의 해 얻 어 진 함수광물과 물 사이 의 동 위원소 분별계수는 다음과 같다. 1000 lna 백운 모 용- = -22 .1 ( 10 6T-2) + 19 .1
1000 Ina 표모 - 문 = _ 21. 3 (106T-2) - 2 . 8 1000 Ina 각섬석 웅 = —23 . 9 (10 6T- 2) + 7 . 9 이 같은 실험결과는 Fr i edman 과 O'Ne i l0977) 에 의해 종합되었으 며 O'Ne i l(1986) 에 의해 종합된 이론 및 실험자료는 표 3-9a 3-9b, 3-9c 와 같다.
표 3-9 a. 수소 동위원소 분별계수 실험자료 (O'Neil, 1986) Serpe n ti ne - Sakai and Tsuts u mi H20(s)-2 . SM I Ste w art (19 64) H20 (1978) NaCl Ep ido te - H20 Graham et al. (19 80) H3Q + .H 20 / Hein z in g e r and Westo n (1964a) Clin o zois it e - do I H20(v)-CH4 I Bott ing a (19 69a) H20 Zois it e -H 20 do H20(v)-H2 (g) Suess 0949) Suzuoki and Ep s te i n Bott ing a (19 60a) (19 76) Muscovit e- H 2 0I do CH4(g )- H2(g) Bott ing a (19 69a) Bio t it e- H 2 0 do Horib e and Craig (unp ub .) Chlori te-H zO I Graham et al. (in pre ss~ HzO(str u c.)- I Kuroda et al. ( 1982) H20(l ) Kaolin ite- H20 I Liu and Ep st e i n (19 80\ I Galley et a l. (19 72) Lambert and Ep s te i H20(l)- H 2S(g ) do (1980) Bruc ite- H20 I Sata k e and Mats u o H20(v)-rhy ol it Tay lo r and Westr i c h Trona-H200) IM {19a 8ts4 u) o et al. (19 72) m0Hel-t· H 20(l) H(1e9 i8n 5z )i n g e r and Westo n (1964b) H20(l )-H 20(v) j Merliv a t et al. (1963) Mi ra bil it e -H 20 Ste w art (1974) Ehhalt a nd Knott Borax-H20 Mats u o et al. (19 72) B(1o9t6t 5in) g a (1968a) I Gayl u ssite -H 20I do
Rennow (1970) Cop pe r-sulfa te-I Hein z in g e r (1969) H20 Majz o ub (19 71) Ste w art and Frie d man Cry st a l hyd r at Barrer and Denney (1975) s-H20 (1964) Kakiu c hi and Mats u o Gy ps um-H20 Fonte s and Gon fian ti ni H20(s)- H 2 0(v) IM (1e9 r7l 9i)v a t and Nie f (1967) M(19a6ts6 u) o et al. (1964) Hi{ g)- H 2 0(I) IR olsto n et al. (1976) H2 0(s)-H 2 00) I Westo n 0955) D20 ( s)-D 2 0 t v ) Mats u o et al. (1964) Po sey and smi th (1957)1~ ;.3-HzO-CH, HF- Kuhn and Thurkau 「 HCN-H2S- (19 58) I HCL- Merl iv a t and Nie f I Hz Ric h et et al. ( 197 7) (19 66) O'N eil (1968) Amason (19 69)
표 3 선 b. 산소 동위원소 분별계수 실험자료 (O'Neil, 1986) Qu artz - H ames magn e site - H 2 0I (19 82) Shir o and Sakai (19 72) Bott ing a and Jav oy Mg -c alcit e- I Taruta n i et al. (1969) (19 73) H20( H2 0) Becker and Clayt on H20(s)-H 2 0(1 ) I O'Neil (19 68) (19 76) Mats u his a et al. (1979) Westo n (1955) Anh ydr it e-Hz이 Lloy d (19 68) I H20-2 . 5M Ste w art (1975) NaCl Chib a et al. (1981) H20 ( g )· H20(g ) | Mats u o and Mats u baya Barite - H20 Robin s on and Kusa (1969) kabe (19 75)
Albit e- H 2 0 I O'Neil a nd Tayl o r I H20-H20(l) I Thornto n (19 62 ) (1967) Bott ing a and Jav oy OH'-H2 0( l ) do Mats u his a et al. (1979) Green and Taube (1963) Anorth ite- H20 I O'Neil a nd Tay lo r J co2(g )· D2 0 I Sta s chewski (1964) (1967) Bott ing a and Jav oy I CO2 (g ) .H20 I do (19 73) Mats u his a et al. (1979)j I O'N eil a nd Adami (19 69) Carbonate s - Nort hro p and Clay to Bott ing a and Craig H20 IO( 1'9N6e6i)l e t al. (19 69) B(1l9a6t9t n) e r 0973) Muscovit e- H 2 0I O'Neil a nd Tayl o r Horib e et al. (19 73) (1967) Bott ing a and Jav oy I O'Neil e t al. (1975) (19 73) Py rox ene-H20 I Matt he ws et al. (19 83) Bari a c et al. (19 80) Bott inga and Jav oy Brennin k meij er et al. (19 73) (1983) Garnet- H 20 I Tay lo r (1976) CO2(g )- C02(l) Groats et al. ( 1960) Try lo r and O'Neil CO2(g )C 02(aq) Vog el et al. (19 70) (19 77 ) Biot i te- H20 I Bert en rath Oi{ g)- 02(aq) Kroop n ic k and Craig and Frie d ric h sen Mi ra bil ite-H 20 (1972) (19 75) Bott ing a and Jav oy I Gy psu m-H20 I Ste w art (1964) (1973) Ruti le-H 20 I Addy and Gari ek I Fonte s (1963) (1974) Matt hew s (1972) H3Po~ lib e rad Gon fian ti ni and ed Matt hew s et al. (1979) CO2-C a rbonate Illite ·H . f) I Jam es and Baker I Rosenbaum and
Zois it e H 2° IM (1a9 7tt6 h) e ws et al. (1983) Shepp a rd (1986) Scheelite - HzO I Wesolowski and Oh~ Serie s of Ca 디 Golys h ev et al. (1981) moto (19 88) bonate s Powellite -H 2 0 I do C02·C 0 ·0CS· S03~ U02·U 0 3·H20 I Hatt or i and Halas (19 82) Magn e tit e· H20j Becker (19 71) NO-N20-S02 Berte n rach et al. NOz -0 2-H20 I Ric h et et al. (1977) (19 72) Bott ing a and Jav oy (19 73)
표 3-9 C. 황과 탄소 동위원소 분별계수 측정 실험자료 (O'Neil, 1986) HSOi -S -H2 S Oana and Ishik a wa Calcit e- HCOi Emric h et al. (19 70) (19 66) FeS zZ nS•P b S Groote n boer ( 1969) Rubin s on and Clayt on s (19 69) FeS2 Zn S-PbS Kaji w are et al. (1969) I Arago n it e- do HC03 S02- S -H2S I Grin e nko and Thode Arago n i te- do (19 70) Calci te FeS2-HSO, I Nakai (1970) Gay lu ssit e- I Mats u o et al. (19 72) ZnS-HS-PbS IS chill er et al. (19 70) ITCG 야rroa-np ah -i Ht e2 0 Mats u o et al. (19 72) FeS2-CuFeS2 Calcit e- Bott ing a (19 69a) FeS-Z n S-PbS I Kaji w ara and Krouse Dia m ond- I do FSe0S2-2S-P·Hb2SS-S ITS (1ah9loo7dm1e) o ents a(l1. 9(1791 7) 1) GCHOCra2Op(g i h )--i t(Cae Oq 2) -(!) IGM raoloi ntei n s eett aall.. ((1199 6697)) ZZnnSs--HPbSS-- PbS ICK ziy aom sua n(1sk9 7e3 )a nd Ry e IC O2(g ) IME ion or ikc he te t a l a. l.( 1(91794 7)0 )
E(1lc9 o74m) be and Hulsto n IC OJ ( aq )C 02( g) I Thode et al. (1965) PHbSSO-S, - S-H2S IRP 0uo9cb7hi5ne )sl ot na n(d1 9K73u)l lerud ICC O022·-CDHi a4m ond Bodtot ing a (1964) H2S(g) - H2S(aq ) IS (1h9a 7r0a)n et al. (19 74) CO2-Calcit e Baerts c hi (19 57) SOi{ g)- H2S(1 ) Sakai (19 57) Vog el ( 19 59) Thode et al. (197 7) North r op and Clay ton SOt (a q )· \ Sakai (19 68) I B(1o9 t6t 6in) g a (19 68b) H2 S(g ) s2--so2(g) do Emric h et al. (19 70) s2- -So z( g) do Grap hi t e- CH, Bott ing a (19 69a) SOt s2 Mi yo shi et al. (19 84) COi- th o leii te Jav oy et al. 0978) Bi2 s3 •S ° IB ente and Nie l son Smeerlite s of Car1 Golys h ev et al. (1981) (19 82) bonate s Serie s of Bachin s ki (1969) C02•0CS· Sulfid e s HCN-CS2 SO 3-SO 2-0 CS CH4-CO-CS I Ric h et (1977) CS2 CS-SrH2S I Ric h et et al. (1977)
이와 같은 실험 중 34 ~ 93°C 범위의 저온에서 석영-물 사이의 산소 동위원소 분별이 Kit a 등 (1985) 에 의해 열발전소의 지열수에 침전된 비정질 실리카와 물의 동위원소비 분석에서 1000lna = 3.52( l06T -2) -4.35 관계가 얻어져 속성작용이나 저온 열수작용시의 지질온도계 로서 이용 가능성이 높아졌다. 이처럼 지난 30 여 년간 고온에서 형성된 암석권의 암석, 광물 및 유체시료의 동위원소 분석자료에서 다음과 같은 특칭이 알려졌다. ® 온도와 동위원소 분별간에 좋은 상관관계가 얻어졌다.
® 온도가 증가함에 따라 동위원소분별이 감소하는 경향이 나타났다. ® 공존 광물상간에 동위원소의 농집에 있어 규칙성이 나타났다. ® 고온상간의 동위원소 평형은 분석 오차예 비해 큰 경향이 얻어 졌다. ® 자연의 많은 광물에 대하여 실험적으로 동위원소 평형실험이 이 루어져 있지 못하다. ® 동위원소 평형실험에 이용되는 시료는 순수한 광물이지만 자연 에서 산출되는 광물은 순수하지 못하여 불순광물이 온도에 미치는 영 향이 연구되어야 할 과제로 남아 있다. 동위원소 평형실험은 압력에 무관한 점과 상기 사실에서 안정동위원소를 이용한 고온 지질온도계 로 지금까지 개발된 지질온도계 중에서 이용도가 가장 높다. 따라서 이런 실험결과 측정된 수소, 탄소, 산소, 황의 동위원소 분 별은 광물, 지열지역의 하부 근원지의 온도추정, 변성암의 생성온도, 압력과 온도간의 관계해석 등에 광범위하게 응용되고 있다. 특히 지 질학적 유체나 조암광물의 평형분별작용을 이용하여 주어진 광물조합 이나 암석-유체, 암석-가스, 가스-유체들간에 동위원소 평형에 도달 한 것인지 아닌지, 냉각 동안이나 냉각 후의 저온의 지질학적 사건이 일어난 동안에 원래의 동위원소 성분이 보존되고 있는지 여부 등을 판별할 수 있다. 실험이나 이론으로 밝혀진 동위원소값의 대소 비교에서 그 평형의 판정은 동위원소값의 역전이 없고 지나치게 큰 동위원소 분별이 나타 나지 않으며 온도와 일관성 있게 동위원소비가 변화하고 있으면 서로 간에 평형에 있었다고 판정할 수 있다. 보통 화강암의 조암광물의 0180 동위원소비는 석영>장석>흑운모 >자철석 순으로 농집되어 있다. 동위원소 평형을 Jav oy 등 (1970) 은 iso th e rm me t hod 울 이용하여 그림으로 쉽 게 표현하고 있다. 103lnax-y = Ax-y ( l06T-2) + Bx-y
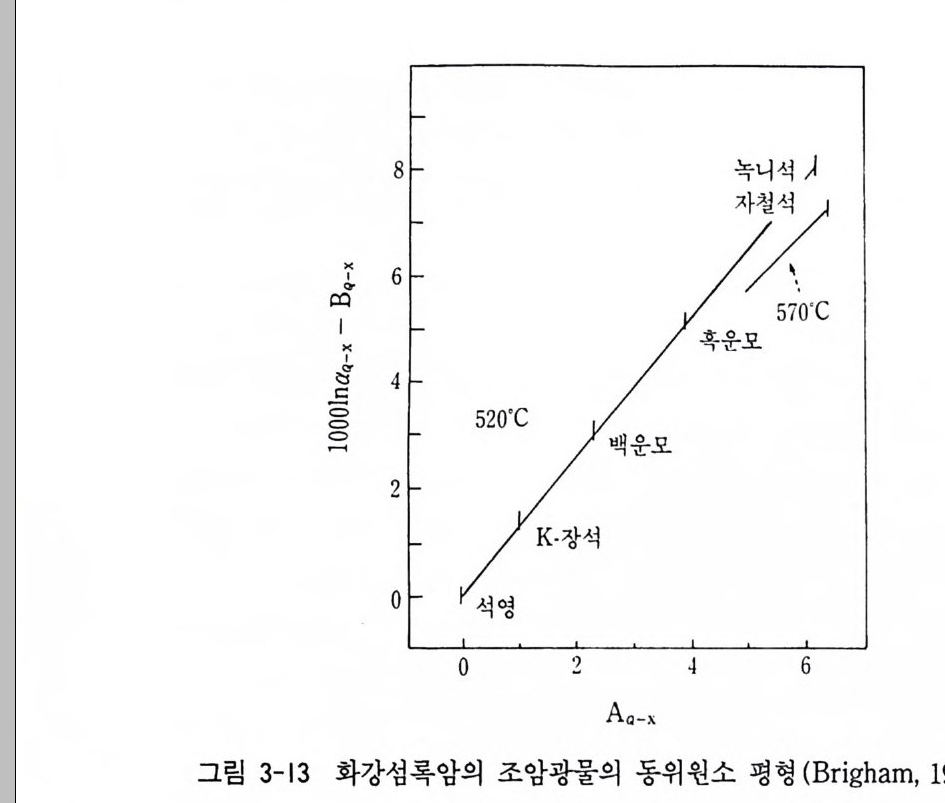 0g.VUI Ix O O'O4I8 혹 운 떼四/모 /5二c
0g.VUI Ix O O'O4I8 혹 운 떼四/모 /5二c
이 관계를 이용하여 화강섬록암에서 얻은 실례를 보면 그립 3-13 과 같다. 이 그림은 동위원소 평형 판별에 중요하다. 일반적으로 가장 이상적인 동위원소 지질온도계로 이용되려면 ® 공존하는 광물이 평형상태에서 형성되어야 하고 ® 광물상이 형성된 후에 동위원소 교환이 일어나지 않아야 한다. ® 동위원소 분별정수의 온도 의존성이 커야 하고 @ 자연에서의 동위원소 분별이 동위원소비 분석시의 실험 오차보 다 커야 한다. ® 그리고 순수한 광물상의 시료를 사용해야 한다. 예를 들면 석영-장석 쌍은 4180 값이 작고 온도에 변화가 적다. 특 히 장석은 결정 생성 후의 후열수용액에 의해 동위원소 교환을 쉽게 일으키기 때문에 지질온도계로 적절하지 못하다.
그러나 석영-자철석은 무거운 산소 동위원소로 된 석영과 가벼운 동위원소로 된 자철석의 경우 Becker 와 Clay ton 0976) 의 soo·c 이 상의분 석실 오험차커를브 에고서려 하L1면18 0 dL=1 148.08 I0 (d1T0 6=T 기 —로9 . 1지6 질(10온 6T도-3계) 으로로 양 호50하0°다C .에 서 ± TC, 800 ° C 에 서 土 1s·c , 11oo · c 에 서 士 38°C 정 도로 오차가 적으므로 조암광물 중에 공존하는 석영-자철석 쌍이 가장 온도에 민 감하여 지질온도계로서 유용하다. 공존하는 물질간의 동위원소값의 차이는 화학결합의 유형에 가장 크게 영향을 받으며 산화상태, 이온가, 원자질량, 전자배치 등에 따 라서도 영향을 받는다. 일반적으로 이온 포텐셜이 높고 원자량이 작은 이온과 결합된 것은 높은 진동빈도를 가지게 되고 계내에 자유에너지를 낮추기 위해 무거 운 동위원소와 우선적으로 결합하게 된다. 예를 들면 S i“인 석영은 언제나 180 이 많이 포함된 광물이고 Fe2+ 이온으로 된 자철석은 항상 180 이 결핍된 광물이다. 화성암과 변성암의 조암광물에서 석영-칼리장석-사장석 순으로 180 이 부화되 어 있는 규칙 성 이 Ta y lor 와 Ep st e i n (1962) 와 Garl i ch 와 E p s t e i n(1967) 에 의한 연구에서 나타났다. 이는 Si- 0 결합이 Al-0 결합에 의해 점진적으로 교대되기 때문이었다. 석류석광물의 그로슈 라라이트와 안드라다이트간에 일어난 1. 7 %o의 동위원소 분별은 Al-0 결합이 Fe-0 결합을 치환한 결과이다. Al 과 Fe 는 산화상태는 동일하지만 Al 과 Fe 사이에 원자량 차에 기인해 광물내의 전동빈도에 차이가 있기 때문인 것이다. 황화광물 중의 공존하는 ZnS 와 PbS 는 같은 관계로 ZnS 쪽이 PbS 쪽보다 34S 가 더 많이 농집되어 있게 된다. Suzuok i와 E p s t e i n(1976) 은 함수광물의 수소 동위원소 분석에서 함 수광물내의 팔면체 위치의 화학성분이 동위원소비의 변화원인이 됨을 제안했다.
4D( 협賤 옹 ) = 一 22 . 4 (10 6T-2) + 2XA1 - 4XMg - 68XFe 그리고 동위원소 교환시에 고체내에서 체적의 변화는 대단히 적으 므로 광물간에 동위원소 분별시 압력의 영향은 무시할 수 있는 정도 이다. 따라서 유체포유물에서는 측정된 균일화온도는 압력보정을 요하나 동위원소 지질온도계는 압력보정이 필요없다. 실험실간에 연구자간에 다소 동위원소 분별정수가 불일치하는 점도 있으나 현재 많은 실험결과와 이론적으로 계산된 결과와 다른 지질온 도계와의 비교에서 신뢰도가 높은 자료가 얻어짐으로써 지질온도계로 서 지질학적 문제해결에 유용한 수단으로 이용되고 있다. 동위원소 지질온도계를 이용하여 생성온도를 계산한 실례를 들어 보자. 미국 위스콘신 북동쪽에 있는 크랜돈 Zn-Cu 괴상 황화광상 (Crandon Zn-Cu massiv e sulfid e depo s it s) 은 안산암, 응회 암 등과 같은 중성 화산 암체내에 발달하고 있다. Munha 등 (1986) 은 이들 화산암 시료 를 채 취하여 변질작용을 받은 화산암의 구성광물인 석영, 사장석의 동위원 소비를 분석하여 광상 생성온도를 계산하고자 하였다. 우선 Mats u his a 등 (1979) 은 석영-물, 사장석-물간의 동위원소 분별 에서죽 석10영00-a 석장 영석 -A 봐간석의 = 동 (0위.7원4 소- 0분.9별A식n) 을X l 0얻6었T다- 2. — (0 . 43 -0.3 A n) 여기에서 T8180= 석 영 - 818[0 사장 석~ + o . 43 — o . 3An ] 가 계산된다. 이들이 채취한 시료는 광상에서 2km 떨어전 곳의 반상안산암과 녹니
석레피리옹회암이었다. 이 시료는 녹니석, 사문석, 녹영석 등의 열수 변질광물이 나타나 프로필릭 열수변질(p ro py l iti c al t era ti on) 을 받고 있었다. 사장석은 알바이트화 작용을 받았으며 장석은 AIlo,15 이었다. 안산암의 석영은 0180 = + 9.38%,, 사장석은 + 6.71%, 로 분석되 어 위의 식에 대입하여 T = 533 ° K(260 C) 가 얻어졌다. 웅회암에서 석영은 0180 = + 9.5 3 %,, 사장석은 0180 = + 6.44%, 이 얻어져 계산 된 온도는 T 는 503 ° K(230 ' C) 였다. 아 온도는 다른 지질온도계에서 얻은 240-310°C 범위내에 들어가고 있다. 이와 같은 동위원소 지질온 도계의 응용은 지질학의 여러 분야에 적용되며 화산가스나 지열지역 시료 중 CH4, CO2, H 2 0( 수증기), S02 등 사이에 이루어진 동위원소 평형을 이용하면 마그마 챔버내의 온도나 지열지역 리저버 (Reser voir ) 내의 온도나 압력 등을 알아낼 수도 있다. 참고문헌 Addy, S.K ., and Garlic k , G.D . (19 74) , Oxy ge n iso to p e frac ti on ati on betw een ruti le and wate r . Contr ib . Mi ne ral. Petr o l. 4 5, pp. 119-121. Amason, B. (19 69) , Eq ui li b r i w n consta n t for the frac ti on ati on of deute r iw n betw een ice and wate r . ]. Phys . C lzem. 73, p. 3491 . Bachin s ki, D.J. (19 69) Boad stre ng th and, sulfu r iso to p i c frac ti on ati on in coexis ti n g sulfid e s. Econ. Geol. 64, pp. 56~65. Barrer, R.M . , a nd Denny, A.F. (19 64) , Wate r in hyd r ate s , Pt. 1 of F racti on ati on of hyd r og en iso to p e s by cry st a l li za ti on of salt h yd rate s . ]. Chem. Soc. pp. 4677-4684. Becker, R.H., and Clay ton , R.N . (1976) , Oxy ge n iso to p e stu d y of a Precambria n iro n-fo r mati on , Hamersley Rang e, Weste r n Austr al ia . Geoclzim . Cosmochim . Acta . 40, pp. 1153-1165. Bente , K.b, eatnw d e eNn ie clos eexn,i s Ht in. g( 1 b9 i8s2m ) u, th Ei nx ip t ee r i(mB iei ,n Sta3 l) San isdo Sto upl ef u frr (aSc 0t) i o.n Eatair otn h sP tlua dn iee ts.
Sci. L ett. 59, pp. 18-20. Blatt ne r, P. (19 73) , Oxy ge n from liqu id s for iso to p i c analys i s, and a new dete r mi na ti on of aco,11,0 at 25C . Geocl1i1 11 . Cos 11 1ocl1i 111 . Ac ta . 3 i. p p. 269 1 -2693. Boast, A.M., Coleman, M. L., and Halls, C. (19 81) , Textu r al and sta b le iso to p i c evid e nce for the gen esis of the Ty na g h base meta l dep o si t. Irela nd, Econ, Geo!. 76, pp. 27-55. Bott ing a , Y. (1968) , Calculati on of frac ti on ati on fac to r s for carbon and oxy ge n exchange in the sys t e m calcit e- carbon dio x id e -wate r . ]. Phys . Che m . 72, pp. 800-803. Bott ing a , Y. (19 69) , Carbon iso to p e frac ti on ati on betw een gra p h it e. dia m ond. and carbon dio x id e . Earth Pla11e t. Sci . L e tt. 5 , pp. 301- 30 6. Bott ing a, Y., and Craig . H. (19 69) , ''O x y ge n iso to p i c frac ti on a ti on bet w een CO2 and wate r and the iso to p i c comp o sit ion of marin e atm osp h er i c CO2 . Ea i1h Planet. Sci . L e tt. 5 , pp. 285 -2 95. Bott ing a , Y., and Jav oy , M. (19 73) , Comments on oxy ge n iso to p e geo th e r- mometr y. Ea11h Planet . Sci. Le tt. 2 0. pp. 251-265. Bowen, R. (19 88) , Isoto p e in the ear th sci en c es , Elsevie r Ap pli ed Scie n ce. p. 6 47. Brig h am, R.H . (19 84) , K-fe l dspa r gen esis and sta b le iso to p e relati on s of the Papo ose Flat Pluto n , Iny o Mounta i n s , Califo rn ia Ph. D. Dis s e r ta t i on . Sta n fo rd Univ e rsity , Sta n fo r d, Cali forn ia . Brig h am, R.H ., and O'Neil, J.R. (19 85) , Genesis and evoluti on of wate r in tw o-mi ca plu to n : an hyd rog en iso to p e stu d y . Che m . Geo / . ,!9. pp. 159 -177. Chib a . H., Kusakabe, M., Hir a no, S., Mats u o, S., a nd Somi ya, S. (19 81) . Oxy ge n iso to p e frac ti on ati on fac to r s betw een anhy d rite and wate r from 100 to 550C . Eart h Planet. Sci . Lett. 53, pp. 55-62. Clayt on , RN. (1981) , Isoto p i c the rmometr y . In : Thermody1 1 a111i cs of Afine r a ls and Melts. R.C. Newt on , A. Navrots k y , and B.J . Wood, eds., Sp ri n g e r - Verlag, Berlin, pp. 85-109. Clayt on RN., O'Neil, J.R ., a nd Maye d a, T.K . (19 72) , Oxy ge n iso to p e frac ti on a- tion betw een qu art z and wate r . ]. Geop hy s . Res. 77, pp. 3057-3067. Craig , H (19 61a) , Isoto p i c varia t i on s in mete o ric w ate r s. S ci en ce, 133, pp. 1702 -1703. Crai g, H. (19 61b) , Sta n dard for repo rt ing concentr a ti on of deute r iw n and oxyg e n-18 in natu r al wate r s. Sci en ce, 133, pp. 1833-1834
Czamanske, G.K, and Ry e, R.O . (19 74) , Exp er im e nta ll y dete r mi ne d sulfu r iso to p e frac ti on ati on s betw een sph alerite and ga lena in the tem p er atu r e rang e 600' to z75 ·c. Econ. Geol. 6 9, pp. 17-25. Dansga a rd, W. (19 64) , Sta b le iso to p e s in pre cip itat i on . TellztS , 16, No. 4, pp. 436-468. Ehhalt, D.H . , and Knott , K . (19 65) , Kin e ti sc he Isoto p e n tr e nnung bei der Verdamp fun g von Wasser. Tel lz tS , 17, pp. 389-387. Elcombe, M.M., and Hulsto n , J.R . (1975) , Calculati on of sulfu r iso to p e frac ti on ati on betw een sph alerite and gal ena usin g latt ice dyn a mi cs. Earth Planet . S ci . L et t. 2 8, pp. 172-180. Eps t e i n , S., and T.K . May ed a (19 53) , Varia t i on of 180 conte n t of wate r s from natu r al sou rces. Geo c lzim . Cos m ochim . Acta . 4, 213-224. Faure, G. (198 6) , Prin c i p/. e s of Iso t o p e geo lo g y, 2nd ed. Joh n Wi ley & sons, p. 589 . Fonte s , J.C ., and Gon fian ti ni, R. (19 67) , Fracti on nement iso to p i qu e de l'hy d rog en e dans l'ea u de cris ta l lis a ti on du gypse . Acad. Sci. Comp tes Re nd ttS , 265 , pp. 4-6. Frie d man, I. and O'N e il , J .R . (197 7) , Comp ila ti on of s ta b le iso to p e frac ti on ati on fac to r s of geo chemi ca l int e r est. In : Data of Geochemi stry, 6th Ed. M. Fleis c her, e d., U .S . Gov. Prin t i ng Off ice , Washin g t on , D.C. Galley, M. R. , Mi lle r, A.I., Ath e rley, J.F ., and Mohn, M. (19 72) , GS pro cess ph; 'Si ca l pro p e rt ie s . Chalk Riv e r, Onta r io , Canada, At om i c Energy of Canada Lim i ted , ACEL-42 55 . Garlic k , G.D. and Ep st e i n , S. (1967) , Oxy ge n isto p e rati os in c oexis ti n g min e rals of regi on ally meta m orph osed rocks. Geo c him . Cosmochim . Acta . 31, pp. 181- 21 4. Golys h er, S.I ., Padalko, N.L, and Pechenkin , S.A . (19 81) , Fracti on ati on of sata b le oxy ge n and carbon iso to p e s in c arbonate s ys t e m s. Geochem. Int' !, 10, pp. 85-99. Gon fian ti ni, R., and Fonte s , J.C . (19 63) , Oxy ge n iso to p i c frac ti on ati on in the wate r of crys t a l li za ti on of gypsw n. Naft1 r e, 200, pp. 644-646. Gonfi an ti ni, R. (1978) , Sta n dards for sta b le iso to p e measurements in natu r al comp o unds. Natu re (London) , 271, pp. 534-536. Gonfi an ti ni, R. (19 84) , Advis o ry grou p meetin g on sta b le iso to p e refe r ence samp le s for geo chemi ca l and hyd rolog ica l inv estig a ti on s. Rep Dir e ct or General IAEA Vie n na.
Graham, C.M ., and Shepp a rd, S.M.F. (19 80) , Exp er im enta l hy d rog en iso to p e • stu d ie s ii : frac ti on ati on s in the sys t e m s epi do te - N aCI-H2 0 , epi do te - CaCI -H20 and ep ido te - s e awate r , a nd the hy d rog en iso to p e comp o sit io n s of natu r al epi do te s . Earth Plane /. Sci . L e tt. 4 9, pp. 237-251 . Green, M., and Taube, H. (19 63) , Isoto p ic frac ti on ati on in the OH 가-I 20 exchange reacti on . J Phys . Che m. 67, pp. 1565 . Greg o ry , P.W ., and Robin s on, B.W . (1984), Su lph ur iso to p e stu d ie s of the Mt . Molloy Di an ne and O.K . str a ti fon n sul ph id e dep o sit s. Ho dg k in s on Provin c e, Nor th Qu ee n sland, Austr a li a, Mi ne ralium De po s it a 19, pp. 36 -43. Greote n boer, J . a nd Schwarcz, H. P. (1969) , Exp e rim e n ta l l y de te r mi ne d sulfu r iso to p e frac ti on ati on s betw een sulfid e mi ne rals. Earth Plane /. S ci. Le tt. 7, pp. 162-166. Groote s , P.M. , Mook, W .G. , and Vog el , J.C . (1969) , Iso to p ic frac ti on a ti on betw een ga seous and condensed carbon dio x id e . Ze it. Plzys i k . 221 , pp, 257-273. Harriso n, A.G , Thode, H. G. (1957a) , Ki ne ti c iso to p e eff ec t in chemi ca l reduc- tion of sulph ate . Faraday Soc. Tra11S. 53, pp. 164 8-1651 Harriso n, AG., Thode, H.G. (19 57b) , Me chanis m of the bacte r ia l reducti on of sulph ate from iso to p e frac ti on ati on stu d ie s . F arad ay Soc. Trans. 54, pp. 84-92 Hatt or i, H. , and Halas, S. (19 82 ) , Calculati on of oxyg e n iso to p e frac ti o n ati on betw een uraniu m dio x id e , uraniu m tri o x id e and wate r . Geoclzim . Cosmochim . Acta . 46, pp. 1863~1868, Hein zing er , K. (1969) , Ein Wassersto f f iso to p iee ff ec t im CuSO ◄ • 5H20. Zei t. Natu rfors chung 24a, pp. 1502-1511 . Hein zinger , K. and Westo n , R.E . (19 64a) , Isoto p ic frac ti on ati on of hy d rog en betw e en wate r and the aqu eous hy dr og e n ion . ]. Phys . Che m . 68, 744 -751 Hein z in g er , K. (19 69) , Ein Wassersto f f iso to p iee ff ec t in CuSO. • 5H20 • Z. Natu r f ors ch 24, pp. 1502. Horib e , Y., Sh ige hara, K. and Takakuwa, Y. (19 73) , Isoto p ic sep a rati on fac to r of carbon dio x id e -wate r sys t e m and iso to p ic comp o sit ion of atm o - sph eric oxy ge n. J Geop hy s . Res. 78, pp. 2625-2629. Jam es, A.T. , and Baker, D.R . (19 76) , Oxyg e n iso to p e exchang e betw e en illite and wate r at 22·c . Geochim . Cosmochim . Acta . 40, pp. 235-239.
Jav oy , M. (19 77) , Sta b le iso to p e s and geo th e rmometr y. ] . Geo !. Soc. Lon:d on 133, pp. 609-636. Jav oy, M. , F ourcade, S., and Alleg re, C.J. (1970) , Graph ic a l meth o d for exami na ta i o n of 180 / 160 frac ti on ati on s in sili c a te rocks. E art h Planet. Sci . Lett . 1 0, pp. 12- 16 . Jav oy, M. , P in e au, F., a nd liy a ma, I.L. (1978) , Expe r im enta l dete r mi na ti on of the iso to p i c frac ti on ati on betw een ga seous CO2 and carbon dis s olved in tho leii tic magm a . Contr i b. Mi ne r a l. Petr o l. 6 7, pp. 35-39. Kakiu c hi, M ., and Mats u o , S . (19 79) , Dir e ct measurements of D / H and 180 / 16 0 frac ti on ati on fac to r s betw een vap o r and liqu id wate r in the tem p er - atu r e rang e from 10· to 40'C . Geo c h e m . ]. 13, pp. 307- 31 1 . Kaji w ara, Y., a nd Krause, H.R . (19 71) , Sulfu r iso to p e par t ition in g in meta l lic sulfid e sys t e m s. Canadia n ]. Earth Sci . 8 , pp. 1397-1408. Kim , K.H . , O .J. K im ., N. Nakai, and H.J. L ee (1988) , Sta b le iso to p e stu d ie s oft he Sarig d ong Tung st e n ore dep os it s. S outh Korea. Mi ni n g . Geo!. 38 (6) , 473- 48 7 . Kit a, I ., T agu c hi, S ., a nd Mats u bay a , 0 . (1985) , Oxy ge n iso to p e frac ti on ati on betw een amo rp h o us sili c a and wate r at 3 4- 9 3'C . Natu r e 314, pp. 83-84. Kiy o su, Y. (19 73 ) , Sulfu r iso to p e frac ti on ati on among sph alerite , ga lena and sulfid e ion s. Geo c he m . ]. 7, pp. 191-199. Kuhn, W. , a nd Thurkauf, M . (19 58) , Sep a rati on of i so to p e s by free zin g of w ate r and the dif fus io n consta n ts of d eute r iu m and oxy ge n-18 in i ce -Possib i li t y of the multip li ca ti on of sep a rati on on free zin g in a hair p i n counte r cur- rent app a rtu s . Helvet ic a Chim . Acta . 4 1, pp. 938-971 . Kuroda, Y ., Hariy a , Y ., Suzuoki, T ., a nd Mats u o, S. (1982) , D / H frac ti on ati on betw een wate r and the melts of qu art z, K -fe l dspa r , albit e and anort hite at hig h tem p e ratu r e and pre ssure. Geocl1em. ]. 16, pp. 73-78. Lambert , S. J., and Ep st e m , S. (19 80) , Sta b e iso to p e inr estig a ti on of an acti ve geo th e rmal sys t e m in Valles caldera, J em ez Mounta i n , New Mexic o . J. Volean. G eoth e rm. Res. 8, pp. 111-129 Liu, K.K., and Ep st e i n , S. (19 84) , The hyd rog en iso to p e frac ti on ati on betw een kaolin i t e and wate r -Isoto p e . Geoscz '. 2, pp. 335-350. Lloy d, R.M . (19 68) , Oxy ge n iso to p e behavio r in the sulfa te- wate r sys t e m . J Geop hy s . Res. 73, pp. 6099-6110. Majz o ub, M. (19 71) , Fracti on nement en oxyg e n-18 et en deute r iu m entr e l' eau et savape u r. J Chim . Phys . 6 3, pp. 563~568.
Malin i n , S.D., Krop o to v a, O.I ., and Grin e nko, V.A . (19 67) , Exp e rim enta l dete r mi na ti on of C13 exchang e consta n ts in C02(g ) -HCOJ ( sol' n) sys te m under hy d roth e rmal condit ion s. Geokhim i) ,a, 8, pp. 927-935 (in Rus- sia n ). Mats u his a , Y., Goldsmi th, J.R . , and Clay ton , R.N . (19 79) , Oxy ge n iso to p e frac ti on ati on in the sys te m qu artz - albit e- anorth i t e- wate r . Ge oc lzim . Cosmochim . Acta . 43, pp. 1131-1140. Mats u his a , Y., Goldsmi th, J.R., and Clay ton , R.N . (19 79) , Oxy ge n iso to p ic frac ti on ati on in the sys te m qu artz - albit e- a n ort hi t e- wate r . Ge oc / 1i1 11 . Cosmochim . Acta . 43, pp. 1131-40. Matt he ws, A. (19 72) , The crys ta l l iza ti on of anata s e and ruti le from amorph ous titan iu m dio x id e under hy d roth e rmal condit ion s. Am. Mi ne ral. 6 1, pp. 419-424. Matt he ws A., Beckin s ale, R.D ., Durham, J.J . , (19 79) , Oxy ge n iso to p e frac ti on a- tion s betw een ruti le and wate r and ge oth e rmometr y of me ta m orph ic eclog ites . Mi ne r a l. Mag. 43, pp. 405-413. Matt he ws, A., Goldsmi th, J.R . . and Clay ton , R.N . (1983a) , On the mechanis m s and kin e ti cs of oxy ge n iso to p e exchang e in qu artz and fel dsp a rs at elevate d tem p e ratu res and pr essures. Ge o/ . Soc. Ame rica Bull. 94, pp. 396-412. Matt he ws, A., Goldsmi th, J.R., and Clay ton , R.N . (19 83b) , Oxy ge n iso to p e frac ti on ati on s inv oiv i n g pyro xenes: the calib r ati on of mi ne ral-pa ir ge oth e rmomete r s. Geochim . Cosmoclzim . Acta . 47, pp. 631-644. Mats u o, S., Frie d man, I., and Smi th, G.I . (1972), Stu d ie s of Qu ate r nary salin e lakes: P t. I, Hy d rog e n iso to p e frac ti on ati on in sali ne mi ne rals. Geo- chim . Cosmoclzim . Acta . 36, pp. 427-435. Mats u o, S., Kuniy o shi, H. and Mi ya ke, Y. (1964), Vap o r pre ssure of ice conta i n - ing D20. Scie n ce, 145, pp. 1454-1455. Mats u o, S. and Mats u bay a, P. (1969), Vap o r pr esure of H2018ic e . Natu r e, 221, pp. 463-464. Merliv a t, L., Bott er , R., and Ni ef , G. (1963), Fracti on nement iso to p iqu e au cours de la dis t i llat i on de I'ea u. ]our. Chim . Phys . 2392, pp. 56-59. Merliv a t, L. and Ni ef , G. (1966), Fracti on netn e nt iso to p iqu e !ors des chang e- ments d'eta t soli de -vape u r et liq u id e -vape u r de d'eau des tem p er atu r es infer ie r es a 0°C. Tel/ us 19, pp. 122-127. Mi tzu tai , Y. , and Raft er , T.A. (1969), Oxy ge n iso to p ic comp o sit ion of sulph ate s :
Pt. 3 Oxy ge n iso to p e frac ti on ati on in the bis u lph a te ion -wate r sys t e m . Ne w Zealand ]. Sci . 12, pp. 54-59. Mi zu ta n i, Y. (19 71), An im p ro vement in the carbon-reducti on meth o d for the oxy ge n iso to p i c analys i s o f sulph a te s . G each, ]our. 5 , pp. 69-77. Miy o shi, T ., S akai, H ., and Chib a , H. (1984) , Exp er im e nta l stu d y of sulf ur iso to p e frac ti on ati on fac to r s betw een sulfa te and sulfid e in hig h tem p er - atu r e melts . G eo c h e m . ]. 18, pp. 75- 84 . Mook, W.G. , Bommerson, J.C . , a nd Sta v erman, W. H. (1974) , Carbon iso to p e frac ti on ati on betw een dis s olved bic a rbonate and gas eous carbon dio x - ide . E arth Planet . S ci . L et t. 2 2, pp. 169-176. Munha, J., B arrig a , F.J. A . S ., and Kerric h , R. (19 86) , Hi gh 0180 ore-fa n nin g flui d s in volcanic -h o st e d base meta l sulfid e dep os it s: G eolog ic, 180 / 160, and D / H evid e nce from the Iberia n Pyr i te belt; Crandon, Wi sc onsin ; and Blue Hil l, M ain e . E con. Geo ! . 81, pp. 530-52. North r op , D.A ., and Clay ton , R.N . (1966) , Oxyg e n iso to p e frac ti on ati on s in sys t e m s conta i n i n g dolomi te. ] . Geo!. 74, pp. 174-196. O'Neil, J .R . (1968) , Hy dr og en and oxy ge n iso to p e frac ti on ati on betw e en ice and wate r . ]. Phys . Che m . 72, pp. 3683-3684. O'Neil J .R . (19 86) , Theoreti ca l and Exp er im enta l aspe c ts o f iso to p i c frac ti on a- tion Valley et al., eds, Sta b le iso to p e s in hig h tem p er atu r e geo log ica l pro cesses. R ev ie w s in Mi ne r a log y 16, Mi ne ralog ica l Soc. Americ a . O'Neil , J .R . , and Adami , L.H . (1969) , The oxy ge n iso to p e par t ition fun cti on rati o of wate r and the stru ctu r e of liqu id w ate r . ] . Phys . C hem. 73, pp. 1553-1558. O'Neil, J.R . , Adami . L.H ., and Ep st e i n , S. (1975) , Revis e d value for the 018 frac t ion ati on betw een CO2 and wate r at 25'C . U.S. Geo!. Survey ]. Res. 3, pp. 623-624. O'Neil, J .R . , Clayt on , R.N ., and Maye d a, T.K . (19 69) , Oxyg e n iso to p e frac ti on a- tion in div a lent meta l carbonate s . ]. Chem. Phys . 5 1, pp. 5547-5558. O'Neil, J.R . , a nd Kharaka, Y.K . (1976) , Hy dr og en and oxyg e n iso to p e exchange reacti on s betw een clay min e rals and wate r . Geochim . Cosmochim . Acta . 40, pp. 241-246. O'Neil, J.R., and Tayl o r, H.P., Jr. (1967) , The oxyg e n iso to p e and cati on exchange chemi str y of feld spa r s. A m. Mi ne ral. 52, pp. 1414-1437. Posey, J.C ., and Smi th, H.A . (19 57) , The equ ili b r iu m dis tr ibu ti on of ligh t and heavy wate r s in a free zin g mix t u r e. Am. Chem. Soc. ] . 79, pp. 555-557.
Puchelt, H., and Kullerud, G. (19 70) , Sulfu r iso to p e frac ti on ati on in the Pb-S sys t e m . Ea1th Planet . S ci. Le tt. 7, pp. 301 . Rennow. M. (19 70) , Gleic h g ew i ch ts u nd kin e ti sc he Trennfa c to r en bei der Verdunstu n von Wasser, Ph. D. Dis s erta t i on . Phy si k a lisc hes Insti tut der Univ e rsita t Heid e lberg. Ric h ardson, S.M., a nd H. Y. JR McSween (19 89) , Geo che mi s/J y Path w a)'S and pro cesses, Prenti ce Hall, N .J. , p. 488. Ric h et, P., Bott ing a . Y ., and Jav oy, M. (19 77) , A revie w of hyd rog en , carbon, nit ro g en , oxy ge n, sulf ur, and chlorin e sta b le iso to p e frac ti on ati on among ga seous molecules.Re v. Ann. Earth Pla11e l. Sci . 5, PP- 65 - 11 0. Robin s on, B.W. (19 73) , Sulfu r iso to p i c equ il ib r iu m durin g sulfu r hyd rolys i s at hig h tem p e ratu r e. Eart h Planet . S ci . L e i/. 1 8, pp. 443-450. Rolsto n , J.H ., Harto g , J. den, and Butl e r, J.P . (19 76) , The deute r iu m iso to p e sepa rati on fac to r betw een hyd rog en and liqu id wate r . ]. Phys . Che m . 80, pp. 1064-1067. Rosenbaum, J., and Shepp a rd, S.M .S. (19 86) , An iso to p i c stu d y of sid e rite s , dolomi tes and ankerite s at hig h tem p er atu r es. Geo ch im . Cosmoclzim . Acta . 50, pp. 1147-1150 . .R ubin s on, M. , and Cla)rto n , R.N . (1969) , Carbon-13 frac ti on ati on betw een arag o nit e and calcit e. Geocl1im . Cosmoclzim . Acta . 33, pp. 997- 10 02. Saka i, H. (1957) , Fracti on ati on of sulfu r iso to p e s in natu r e. Geo cl zim . Cosmo- chim . Acta 12, pp. 150-169. Sakai, H. (19 68) , ''Isoto p i c pro p er t ies of sulfu r comp o unds in hyd roth e rmal pro cesses. Geoclzem. ]. 2, pp. 29-49. Sakai, H., and Tsuts u mi , M. (1978) , D / H frac ti on ati on fac to r s betw een ser- pen ti ne and wate r at 100' up to 5oo·c and 2000 bars wate r pre sure, and the D / H rati os of natu r al serpe n ti ne s. Earth Planet. S ci . Le tt. 4 0, pp. 231-242. Salomons, W. (19 71) , Isoto p e frac ti on ati on betw een ga lena and pyrite and betw e en pyrite and elementa l sulfu r. Eart h Planet. Sci . Lett. 11, pp. 236 -238. Sata k e, H., and Mats u o, S. (19 84) , Hy d rog en iso to p e fac to r betw een bruc ite and wate r in the tem p er atu r e rang e from 100· up to soo·c. Contr ib. Mi ne ral. P etr o l. 8 6, pp. 19-24. Sharan, Y., Galas, G., L ees, E., and Zhook, V. (1974) , Expe r im enta l dete r mi na - tion of the sulfu r iso to p e exchange equ il ibr iu m consta n t in the sys t e m
HS (g)- H2 (soluti on ) . 5th Nati on al Sym p os iu m in Sta b le Isoto p e Geochemi str y , Moscow, Prog ram -Pt. I, p. 31 (in Russia n ). Sharma, T., and Clayt on , R.N. (1965) , Measurement of 0 미 016 rati os of tot a l oxyg e n of carbonate s . G eochim . Cosmochim . Acta . 29, pp. 1347-1353. Shir o, Y., and Sakai, H. (1972), Calculati on of the reduced par tit ion fun cti on rati os of a-/3 - qu artz and calcit e. B ull. C hem. Soc. Jap a n , 045, pp. 2355 -2359. Shepp a rd, S.M.F. (1984), Isoto p i c geo th e rmometr y . In : Lag ac he M. (ed.) The nn ome tri e et barometr ie g eo log igu es. S oc Fr, Mi ne ral Cris t a l log r, pp. 349-412. Shepp a rd, S.F . M . , N i els en, R.L. , a nd Tayl o r, H.P . (1969) , Oxyg e n and hyd rog en iso to p e rati os of clay min e rals from por ph y r y cop pe r dep os it s. E con. Geo ! . 6 4, pp. 755-77 . Shepp a rd, S.F . M . (19 77), Identi fica ti on of the orig in of ore-fo r mi ng soluti on s by the use of sta b le iso to p e s . In : Vocanic pro cesses in ore gen esis. Geo!. Soc. London spe c . Publ. No 7, pp. 25~41 . Sim th , J,W ., and Croxfo rd , N.J .W . (1975), An iso to p i c inv estig a ti on of the envir o nment of dep os it ion of the McAr thu r min e ralis a ti on . Mi ne r. Dep o s ita 10 (4) , pp. 269-276. Sta s chewski, D. ( 1965 ) , Sta t is ti s c he Berechnung der 180-u nd 160-Gleic h g e- wic h ts v erte i lu ng in den Sys t e r nen CO2 / H20 und CO2 / D20 aus rnolekulspe c tr o skospi sc hen Date n . B er. Bunseng e. Phys . Chem. 69, pp. 426- 44 0. Ste w art, M. K., (19 74) , Hy d rog en and oxy ge n iso to p e frac ti on ati on durin g crys t a l liz a ti on of rnir a bil ite and ice . Geoclzim . Cosmoclzim . Acta . 38, pp. 167-17 2. Ste w art, M.K. , and Frie d man, I. (19 75) , Deute r iu m frac ti on ati on betw e en aqu eous salt s oluti on s and wate r vap or . J Geop lzy s. Res. 80, pp. 3812 -3818. Suzuoki, T., and Ep st e i n , S. (19 76) , Hy d rog en iso to p e frac ti on ati on betw een OH-bearin g min e rals and wate r . Geochim . Cosnio c him . Acta . 40, · pp. 1229-1240. Taruta n i, T., Clayt on , R.N ., and May ed a, T.K . (1969) , The eff ec t of pol ym o r- ph is m and magn e siu m substi tut i on on oxyg e n iso to p e frac ti on ati on bppe.t w 9 8ee7n-9 c9a6l.c iu m carbonate s and wate r . Geochim . Cosmochim . Acta . 33,
Tayl o r, B.E. , and O'Neil , J .R . (19 77) , Sta b le iso to p e stu d ie s of meta s omati c skarns and assoc iat e d meta m orph ic and igne ous rocks. O sgo od Moun- tai n s , Nevada. Contr ib. Mi ne ral. P etr o l. 63, pp. 1-49. Tayl o r, H.P. Jr ( 1979), Oxyg e n and hyd r og en iso to p e relati on ship s in hyd r oth e r- mal min e ral dep os it s. In : Geocl1emi sh J1 of lzy dr otl ze nn al ore dep o s its , 2nd ed. (ed., H.L. Barnes), Joh n Wi ley , London pp. 236-277. Tayl o r, H.P ., and S. Ep st e i n (1963), 018 / 016 rati os in rocks and coexis ti n g mi ne rals of the Skaerga ard Intr u sio n , East Greenland. f. Pet ro l., 4, pp. 51-74. Thode, H. G. (1970), Sulph ur iso to p e geo chemi st r y and frac ti on ati on betw een coexis ti n g sulph id e min e rals. Mi ne r a l Soc Am Spe c Pap. 3, p. 133. 'Th ode, H.G , Goodwi n, A. M. (1983), Furth e r sulfu r and carbon iso to p e stu d ie s of late Archean iro n-fo r mati on s of the Canadia n Shie ld and the rise of sulfa te reducin g bacte r ia . P rec a mbrian Res . 2 0, pp. 337-35 6. Thode, H. G., M onste r , ]., Dunfo r d, H. B. (1961), Sulph ur iso to p e geo chemi st r y . Geochim . Cosmochim . Ac ta. 2 5, pp. 159-174. Thode, H.G., Cragg , C.B., Hulsto n , J.R ., and Rees, C.E . (1971), Sulfu r iso to p e exchang e betw een sulfu r dio x id e and hyd r og en sulfid e . Geo c him . Cosmochim . Acta . 35, pp. 35-45. Thornto n , E.R. (1962), Solvent iso to p e eff ec ts in H2016 and H20 1 8. A m. Che m . Soc. f. 84, pp. 2474-2475. Tayl o r, H.P ., J r., and Ep stei n , S. (1966), Deute r iu m -hy d rog en rati os in coexis t- ing mi ne rals of meta m orph ic and igne ous rocks. [ab 타 Am. Geo p h i c s. Unio n Trans. 47, pp. 213. Ueda, A., and H.R. Krouse (1986), Di re ct conversio n of sulph id e and sulph a te min e rals to S02 for iso to p e analys e s. G each, fou r. 2 0, pp. 209- 21 2. Urey, H.C. (1947), The the rmodyn a mi c pro p e rtie s of iso to p i c substa n ces. J Chem. Soc. (London), p p. 562-581 . Valley, J.W ., T ayl o r, H.P., and O'Neil, J.R., eds. (1986) , Sta b le iso to p e s in hig h tem p er atu r e geo log ica l pro cesses. Revie w s in Mi ne ralogy 16, Washin - gton , D.C.: Min e ralog ica l Socie ty of Americ a . Vog el , J.C ., Groote s , P.M. and Mook, W.G. (1970), Isoto p i c frac ti on ati on betw een gas eous and dis so lved carbon dio x id e . Zeit . P hys i k, 230, pp. 225 -238. Wesolowski, D., and Ohrnoto , H. (1986), Calculate d oxy ge n iso to p e frac ti on ati on fac to r s betw e en wate r and the min e rals scheelit e and po well ite. E con.
Geo!. 81, pp. 471-477. Westo n , R.E., Jr. (19 55), Hy d rog en iso to p e frac ti on ati on betw e en ice and wate r . Geochim . Cosmochim . Acta . 8, pp. 281 . Yanagi sa wa, F., a nd Sakai, H . (1983), Prepa r ati on of S 02 for sulf ur iso to p e rati o measurements by the the rmal decomp os it ion of BaSO.-V20s-S-/ J2 mix t u r es. Anal. C hem. 55, pp. 985-987. Yoshid a , N., and Y. Mi zu ta n i (1986), Prepa r ati on of c arbon dio x id e for oxy ge n- 18 dete r mi na ti on of wate r by use of a pla stic s yr ing e . A nalyti ca l Chem. 58, pp. 1273-1275. 김규한, 中 -) H ;之 (1980), 「한국의 일부 금속광상의 유황 동위원소성분 및 동위 원소 지질온도에 관한 연구」, ( ( 지질학회지 }) 16(2), pp. 124-134 김규한, 김옥준, 장원선(1 990), 「우극 금은광상에 대한 유체포유물 및 안정동위 원소 분석연구」, (( 광산지질 )) 23( 1), pp. 1-9 日本化學合 (1976), 新tt 驗 化學 講 座, 『 宇宙地球化學 J , 丸善株式合社, p, 523.
4 산소 및 수소 안정동위원소 4-1 . 서언 수소, 산소, 탄소, 질소, 황 등의 경원소의 동위원소 중 산소와 수 소는 수권, 암석권, 생물권, 대기권의 가장 중요한 구성성분이다. 특히 수권, 대기권, 암석권의 물은 자연환경의 주요 구성성분이다. 산소는 규산염광물, 탄산염광물, 황산염광물 등의 조암광물의 주요 구성성분아며 대부분의 암석광물은 산소를 가지고 있으며 함수광물은 수소를 가지고 있다. 따라서 이들 물질의 산소와 수소 동위원소의 분포와 동위원소 분별 에서 이들 물질의 기원과 생성조건 해석의 주요한 정보를 얻을 수 있 다. 또한 이들 동위원소비는 여러 지질학적 과정의 트레이서로도 이 용되고 있다. 화성암, 변성암, 되적암의 암석성인 해석과 초생수와 순환수 등과 같은 상이한 기원의 물의 구별과 광화용액의 가원, 물 -암석 상호반응의 정량적 해석, 굉물의 평형과 비평형, 동위원소 지 질온도계 이용이 증가하고 있다. 암석의 산소동위원소비는 스트론튬 과 니오디미움 동위원소비와 함께 암석성인 해석에 많이 이용되고 있 다.
4-2 산소 및 수소 안정동위원`소의 특성 우주 초기의 구성원 소 가 주로 H 와 H~ 로 구성되어 있었으며 이 H 와 He 이 대폭발 (B ig Bang ) 이후 핵융합 과정에서 산소와 중수소, 탄소, 황 등 태양계의 여러 구성원소들이 형성된 후 이들 원소들의 존재량이 급증하였다. 자연계의 대다수의 물질은 산소와 수소를 함유 하고 있다. 물론 태양계 초기 구성물질인 운석에도 수소 및 산소는 여러 가지 형태로 다량 존재하고 있다. 산소와 수소는 결합하여 물 (H 2 0) 의 형태로 존재하기도 하고 규산염광물, 탄산염광물, 점토광물 등 많은 광물과 암석이 산소와의 화합물을 이루고 있다. 대기 중의 가스나 생물권의 식물과 동물 등도 산소와 수소를 그 구성성분으로 가지고 있다. 이 같은 지구상의 물질들은 그들이 형성된 환경이나 형 성 과정에 따라 각기 다른 수소 및 산소 안정동위원소비를 가진다. 그림에서와 같이 수소 동위원소비 (oD) 는 해수 약 0%,, 초생수 - 40 ~- 8 0% ,, 화성암 및 변성암 -5 0~-120%, 내의, 퇴적암
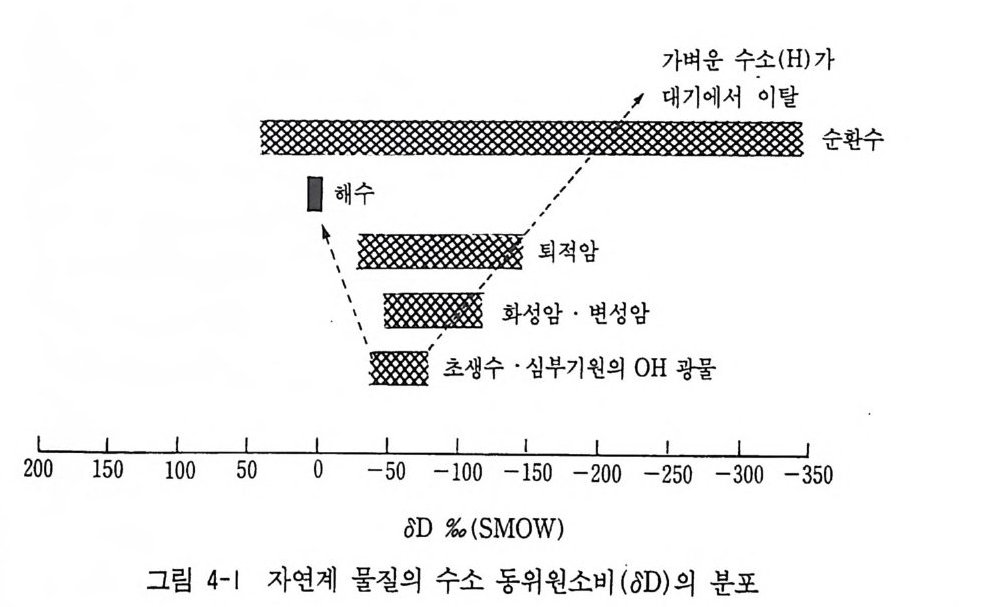 가벼운 수소(H)가
가벼운 수소(H)가
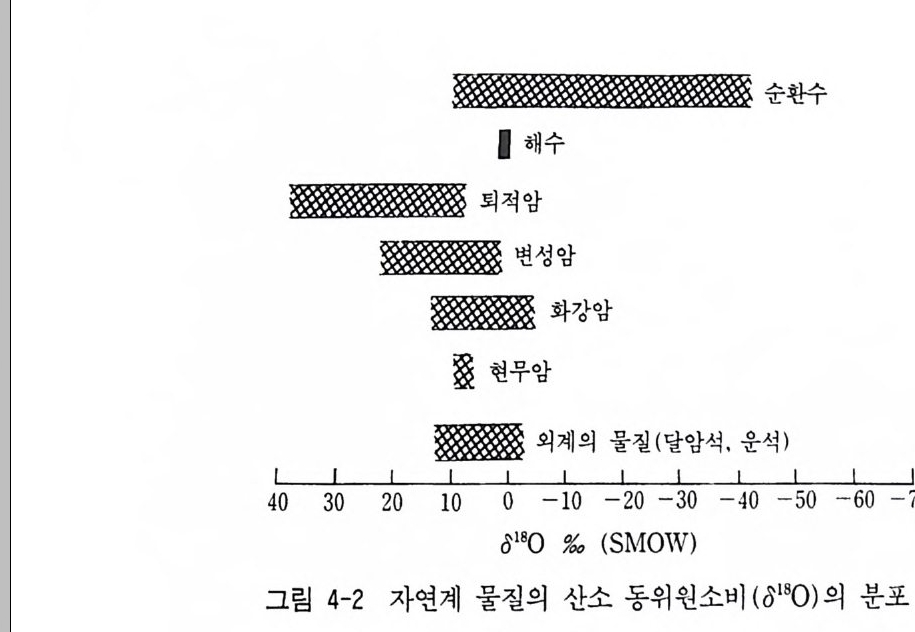 一순환수
一순환수
― 30~ ― 150%, 내의 그리고 순환수 +50~— 3 50% , 내의의 값의 범위를 가진다(그립 4-1). 그리고 산소의 경우 해수 0%,, 순환수 + 10~ -45% ,, 현무암 + 8:----9 %,, 퇴적암 + 40~+ 10 給 내의의 값을 가진다(그림 4-2). 동위원소비의 값을 보면 산소에 비해 수소의 값의 변화폭이 커 두 동위원소간에 상대적인 질량차가 큼을 알 수 있다. 수소는 H20, OH-, H2, CH ◄, CHO 동의 여러 형태로 존재하며 산소의 경우는 수소보다 더 많은 자연계 여러 물질의 주요 구성성분 이 되어 있어 지구 내의부에서 일어나는 중요한 여러 가지 지질학적 과정에 직접 · 간접으로 작용하고 있다. 따라서 수소 (D/ H) 및 산소 (180 / 160) 동위원소비 분석 연구가 자연계에서 일어나고 있는 지질학 적 과정과 환경 등을 규명하는 데 주요한 수단이 되고 있다. 1) 수소 동위원소 분별기구 수소의 동위원소 분별기구로는 ® 수증기압과 빙점차에 의한 분별
® 동위 원소 교환평 형 에 의 한 분별 @ Ultr a fi ltra ti on 등을 들 수 있 다. 빙점차보다 수증기압의 차 때문에 동위원소 분별이 더 크게 일어 난다, HDO 의 수증기 압아 H20 보다 약간 낮기 때문에 D 의 농도가 기상 보다 액상에 더 많이 농집된다. Bo tti n g a (1 969) 와 Ric h et 등(1 977) 이 가스상의 수소화합물의 동위원소 분별을 계산하였다. 그리고 광물-물 간의 수소동위원소 분별곡선이 Saka i와 Tsuts u mi (1 978), Suzuok i와 Eps t e i n ( 19 76) , Graham 등 (19 80 , 84 , 86) , Lambert 와 Ep st e i n ( 1 980) , Sa t ake 와 Mats u o(1 9 84), Shepp a rd(1 9 84) 등에 의해 얻어졌다. 수소 의 경우 동일군의 광물이라도 분별곡선의 변화가 심하다. 예를 들면 운모와 각섬석은 450~800°C 온도 범위내에서 1 / T 과 직선관계에 있 으나 녹영석, 트레몰라이트, 녹니석 등은 직선관계에 있지 않다(그림 3-12). 그리고 400°C 이하의 온도에서 물과 광물 사이에 수소 동위원 소 분별속도가 느리므로 아직 거의 알려져 있지 않다. 고령토의 경우 실험에서 O ' Ne il 과 Kharaka(1976) 은 200 ' C 에서 8 개월간 반응에서 30% 정도 수소 동위원소 교환이 일어났음을 알게 되었다. 그 후 L i u 와 Ep st e i n ( 1984) 이 200~35o•c 에서 실험한 결과는 400°C 이상 온도에서의 것과 비교해 곡선의 기울기가 반대로 나타났 다. Lamber t와 Ep st e i n ( 1980), Marumo 등(1 980) 의 천연시료 연구결 과와 종합해 보면 200'C 부근에서 동위원소 분별의 변곡점이 얻어지 게 된다. 이처럼 수소의 동위원소 분별의 복잡성은 일부 광물에서 수소가 여 러 결정격자 위치에 존재하기 때문이다. 0-H-0 결합과 동위원소 분 별간에 정량적인 관계가 성립한다. 즉 광물내에서 결합거리가 짧으면 짧울수록 광물은 IH 이 더욱 강하게 농집되는 결합효과 (Bond eff ec t) 가나타난다. 그 의 결정구조의 영향으로 M g-팔면체의 뒤틀립 구조가 D/H 분 별과 관계 있음이 Sa t ake 와 Mats u o (1984) 에 의 해 연구되 었다. 또한
고온에서는 수소 동위원소 교환속도가 산소에 비해 너무 빠르므로 동 위원소 평형 판정이 어렵다. 급속한 수소 이동은 S i -0 와 Al-0 결합 의 수화반응보다 빠르게 일어난다. Graham(1981) 은 수소를 포함한 유체가 존재하지 않는 경우 공존하는 함수광물 사이에 수소 동위원소 교환은 전혀 디론 기구로 진행된다고 보고하였다. 물이 존재할 때는 확산속도가 최소한 두 배 이상 크기 때문에 수소동위원소 교환반응에 서 함수광물에서 수소 확산시의 작용에너지를 정량적으로 결정할 수 있다고 했다. 앞장에서 설명한 것처럼 동위원소 교환평형에 의한 수 소 동위원소 분별은 온도 의존성이 있으므로 동위원소 지질온도계로 도 이용되어 속성작용, 변질작용, 광화작용, 화성작용, 변성작용 등 의 다양한 지질학적 과정에서 일어났던 온도를 추정하는 데 이용된 다. Ultr a fi lter ati on 과정에 의해 점토광물에 무거운 동위원소가 우선 적으로 흡착되 어 잔류수 중에 무거운 동위 원소가 농집 됨 을 Co p len 과 Hanshaw(1973) 가 지적했다. 이런 현상은 퇴적수 (Forma ti on wa t er) 의 동위원소 성분연구에 중요하다. 2) 산소 동위원소 분별기구 물의 경우 산소 동위원소 분별은 수소와 거의 평행한 관계를 가진 다. 그러나 수소에 비해 암석 광물내의 산소는 일관성 있게 동위원소 값이 변화한다. 왜냐하면 결정화학적 특칭인 결합강도나 질량효과 등 에 의해 공존하는 광물 사이에 l80 농도는 질서 있게 변화하고 있기 때문이다(표 3-2). 보통 규산영광물 중에도 고도로 중합된 광물일수록 180 이 더 많이 농집된다. 그러나 규산염광물 중의 OH 군은 예의이다. 180 이 많이 농집된 광물일수록 산소 결합력이 강하며 무거운 산소 는 질량이 작거나 이온의 전하가 큰 양이온과 결합하기 쉽다. 전자를 결합 강도효과라 하고 후자를 질량효과라고 부른다. 따라서
표 3-5 에서처럼 탄산염광물 중 CaC 아와 SrC03 를 비교하여도 질량이 87 . 63 인 SrCO 파 질량 40 . 07 인 CaCO 리 250 ' C 에서 동위원소 분별이 각각 7.4 와 7.9 로 CaC 아 쪽이 크다. S i와 Al 은 질량은 유사하지만 Si- 0 결합보다 Al-0 결합이 길고 약 하므로 석영이 장석보다 8180 값이 크고 알바이트가 아놀사이트보다 8180 값이 크다. K i e ff er(1982) 는 산소 동위원소 분별의 이론적 모 델 연구를 실시하였고, O'Neil 등 (1969), Cla yt on 등 (1972), Mats u - his a (l979) 등이 산소 함유광물의 동위원소 분별실험을 실시하였다. 그 결과는 표 4-1 과 같다.
표 4-1 실험에 의한 산소동위원소 분별정수 결정법 (Shepp a rd, 1984) 방법 1 계 1 바고 | 참고문헌 1. 방해석 - H 2 0 재결정작용 O'N e il e t al. (1969) 광물-유체간의 석영 -H 2 0 Clay ton et al. 2직. 접 동위원소 석 영-칼리 장석 1떠의 공타액 B(1l9a7t2t n) e r and Bir d 교환실험 Mats u his a et al. (1979) 광물-광물간의 엔스타타이트-현 lJ 야나 C 아를 거친 (1974) 칙접 동위원소 암마그마 동위 원소 교환 Muehlenbachs and 교환 실험 (1250~1500'C ) IKushir o (1974) 3. 석영 -H20 실리카겔로부터 합성 I Clay ton et al. 결정작용 백운모 -H 2 0 (1972) 겔그래스 제이다이트 -H20 O'Neil a nd Tayl o r (1969) Matt he ws et al. (19 83a) 4. 1 방해석 -H2° 아라고나이트-방해석 Clayt on (1959) 동질이상의 상전이 석영 -H20 크리스토바라이트- Mats u his a et al. 석영 (1979)
5합.성 법 알바이트 - H20 I_칼 . 리N장a 장석석 + + N KaCCl! O(1'N9 6e7i)l a nd Tayl o r 양이온교환법 복치환 백운모 -H20 | 파라고나이트 + KC O'Neil a nd Tayl o r 一 백운모 + NaCl (1969) 백운모 -H20 1 고령토 + KC! --> 백 O'Neil a nd Tayl o r 운모 + HCI 十 H20 (1969) 자철석 -H20 \ FeCOJ + H20 -> O'Neil a nd Clayt on Fe3 O. + CO2 + H2 (19 64) 자철석 -H20 J Fe20 J + H2 + H20 Berte n r ath et al. ----->F e30 4 + H20 (1973) 석영 -H20 I 규산염산성열수합성 Matt he ws and Beck (265~465'C ) ins ale ( 19 79) 석영-자철석 | 철감람석 + H20 _, Downs et al. (1981) 자철석 + 석영 + H 돌로마이트 -H 2 0 1방 해->석 둘 - >로M 마 g이-> 트 방 급。』 Matt he ws and Katz 석 (19 77 ) 액 재침전
대 부분 실험의 경우 동위원소 교환평형정수는 의삽법 (No rt hro p와 Clay ton , 1966) 과 3 동위 원소 교환법 (Matt he ws 등, 1983 ; Shepp a rd ; 1984) 을 이용하고 있다 . 수소에서와 같이 수증기압의 차에 의해서도 동위원소 분별이 일어 나며 광합성과 같은 생물학적 과정과 수화반응 등에 의해서도 동위원 소 분별이 일어난다. 4-3 수권과 대기권에서 의 수소 및 산소 안정동위원소 1) 강수의 동위원소 성분 물 (H20) 은 수소 안정동위원소 1H, D 와 산소 안정동위원소 “0, 110,
l80 사이에서 IH/60 , 1Hz110, IH2 1s o, HD16Q , HD110, HD1so , D2l6Q , D211 0 , D 2 1so 의 9 종류의 질량이 다른 물이 존재한다. 앞장에서 설명 한 것처럼 이같이 질량이 다른 물은 질량이 작은 동위원소로 결합된 물이 질량이 큰 동위원소로 결합된 물보다 진동빈도가 크다. 따라서 가벼운 동위원소로 된 물분자가 무거운 동위원소로 된 물분자보다 쉽 게 계내에서 빠져나간다. 예를 들면 호수나 해수에서 물이 증발하면 증발한 수증기는 가벼운 동위원소가 많아 이것이 응축되어 바를 만들 면 증발되기 전의 물보다는 가벼운 동위원소를 가지는 강수 (A tm os p he ric wate r ) 가 된다. 따라서 해수가 증발하여 만들어진 수증기단은 약 oD = -80 %,, 8180 = —9 % , 내의이다. 이 값은 물론 수증기단의 온도에 영향을 받 지만 수증기단은 항상 부의 동위원소값을 갖는다. 반대로 대기권에서 수증기단이 응축될 경우 비나 눈에는 무거운 동 위원소가 상대적으로 응축되기 쉬워, 응축 후 남은 수증기단은 점점 동위원소가 가벼운 것 만이 남게 되어 점점 가벼운 비를 내리게 한다. 이때 응축 후 남은 수증기의 동위원소비 (R) 와 응축 전 수증기 동위 원소비 (Ro ) 사이에는 다음과 같은 관계식이 성립한다. R = Rop a- l ) 여기서 f는 남은 수증기의 분률이고 a 는 동위원소 분별정수이다. 이 관계 식 울 레 이 리 증류 방정 식 (Ray le ig h dis t il lat i on equ a ti on ) 이 라 한다 . 초다기음의 예 제산에소서동 위좀원더소 구값체 (a적180으) 로이 살—펴9보. 자0%. 인 초기의 수증기단이 응 축하여 강우현상이 일어났다고 가정할 때 만일 50%, 75%, 90% 수 증기가 각각 응축했을 때 수증기단의 동위원소값은 얼마이겠는가? 또, 수증기단이 모두 응축하여 강우를 만들었을 때 전체 빗물의 동위 원소 성분값은 얼마이겠는가를 계산하여 보자(단, 이때의 a 액세 키 치 =
1. 0 092 라고 가정 하자) . 동위원소 표시법의 관계식에서 요R 。= f (a-(81180)) 。 =+ ~100 0 의 관계가 얻어진다. 50% 재응축한 경우 0180 = [(— 9.0%,) + 100 미 (0.5)0.0092 — 1000 = — 15.3%, 이 되고, 75%, 응축시 0180 = - 21.6%,, 90% 응축시 는 _ 29 . 8%, 이 된다. 수증기단이 계속적으로 응축될 때 빗물의 동위원소 성분은 a = RR 급•I; = 8101880 아 웅 기+ + 1 010000 0 으로 표현된다. 축면 시즉8 108810188 =어0 = —= —6 .a 22(%0o ,.1 98이%0 , 꿈 이되 고기 된,+다 1.705 0%0그) 러응一나 축10 시0전0 체이01 8강되0 수어= 의-5 0 동1%2위 .6응%원,축소, 이비90 는%된 다응질 의량 보하면존 법대칙 기이 의 성순립환하에여 의처 해음 형동 성위 된원 소순비환와수 (동M일e t하 eo다r i.c waC tr era) i 는g(l 986D1) 에= 8o18Q + 10 의 직선상에 도시된다(그림 4-3). 왜냐하면 25°C 에서 산소와 수소의 a 값(야와 %)이 각각 1.07 4, 1.0092 이므로 기울기가 약 8 이 얻어진다. 물의 동위원소 분별은 온도 에 크게 영향을 받기 때문에 강수의 동위원소 성분은 위도효과 (La ti- t ude eff ec t) , 고도효과 (Altit ud e effe c t) , 우량효과 (Amount effe c t) , 내 륙효 과 (Inland effe c t ) , 모세 관효과 (Cap illar y effe c t) 등의 영 향이 나타난다. 죽 저위도로 갈수록, 고도가 높을수록, 우량이 많을수록 동위원소값 은 작아전댜 내륙효과에 의하여 산소 동위원소비가 0%, 인 해수가 증
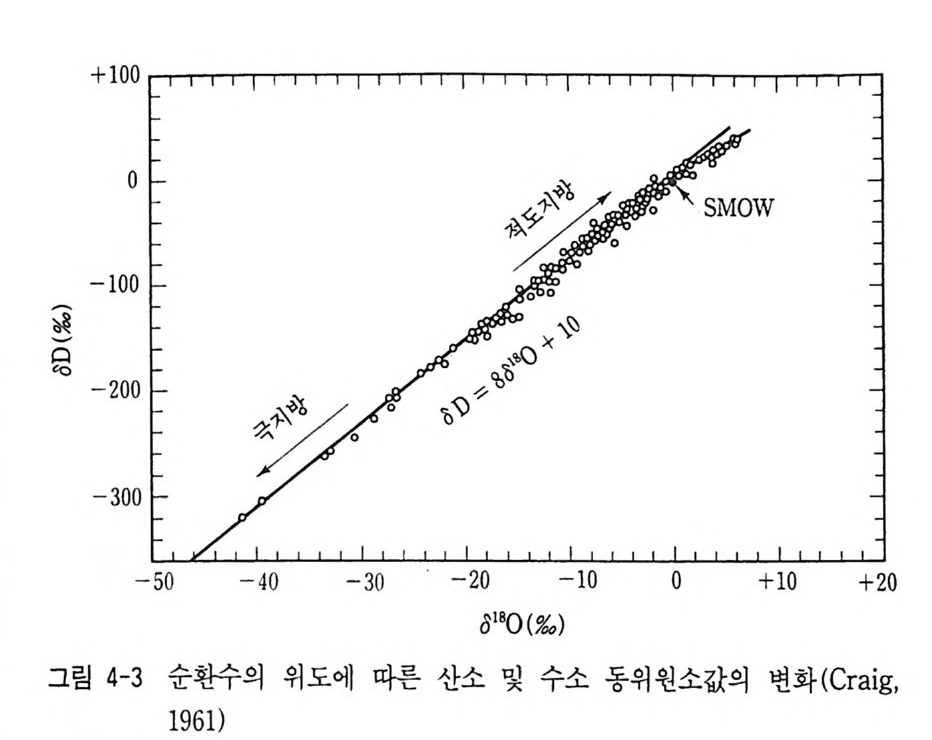 +100
+100
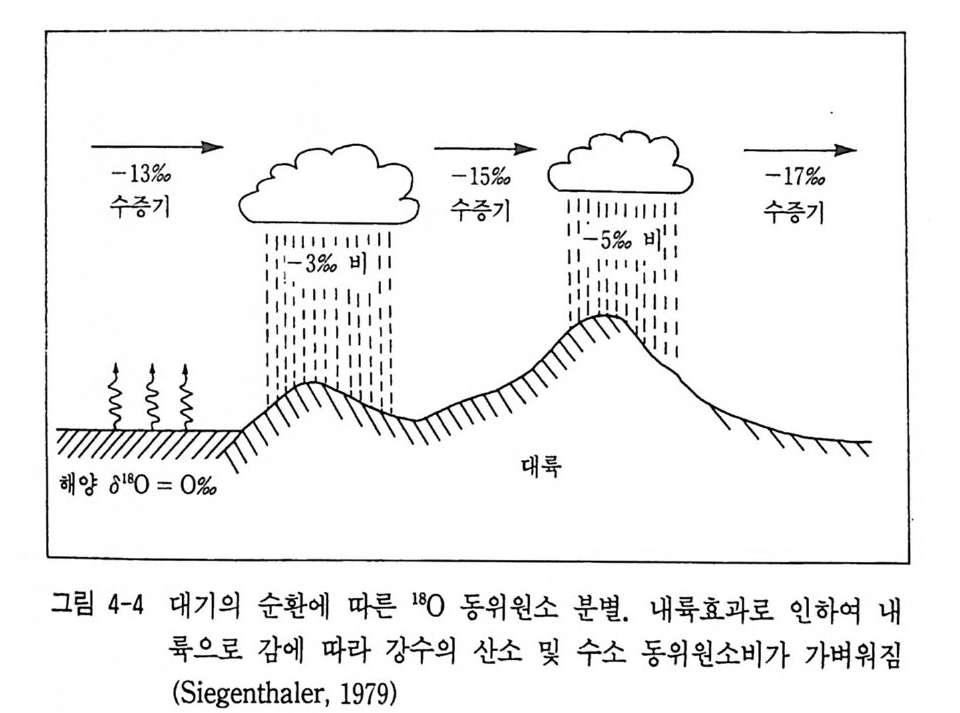 二11:Il: ::;1I1 :1':-:1;i 3氷!I1j 1!l%1111! 1:l1: : 1}II비I1! ::1! I!1IIJ!1 lII 三 ~二1I': 1!I: :- · 5PI~%l: II~ II, l II I.비': .1 1 1I1 Il 틀
二11:Il: ::;1I1 :1':-:1;i 3氷!I1j 1!l%1111! 1:l1: : 1}II비I1! ::1! I!1IIJ!1 lII 三 ~二1I': 1!I: :- · 5PI~%l: II~ II, l II I.비': .1 1 1I1 Il 틀
 .• • :04:.:.멀:.. 凡?
.• • :04:.:.멀:.. 凡?
발하여 수증기단을 형성한 후 대륙으로 이동하는 물의 순환 과정에서 수증기단에서 그림 4-4 에서와 같이 점점 가벼운 강수현상이 일어난 다. 전 세계의 강수의 산소 동위원소비의 분포는 그림 4-5 와 같이 적도 지방이 극지방에 비해 무거운 동위원소로 되어 있으며 위도효과에 의 해 위도에 거의 평행한 동위원소 등치선을 나타내고 있다. 그리고 북미의 경우 내륙효과 및 고도효과가 현저히 나타나고 있 다. 즉 록키 산맥과 아팔레치아 산맥에 의해 동위원소값의 등치선이
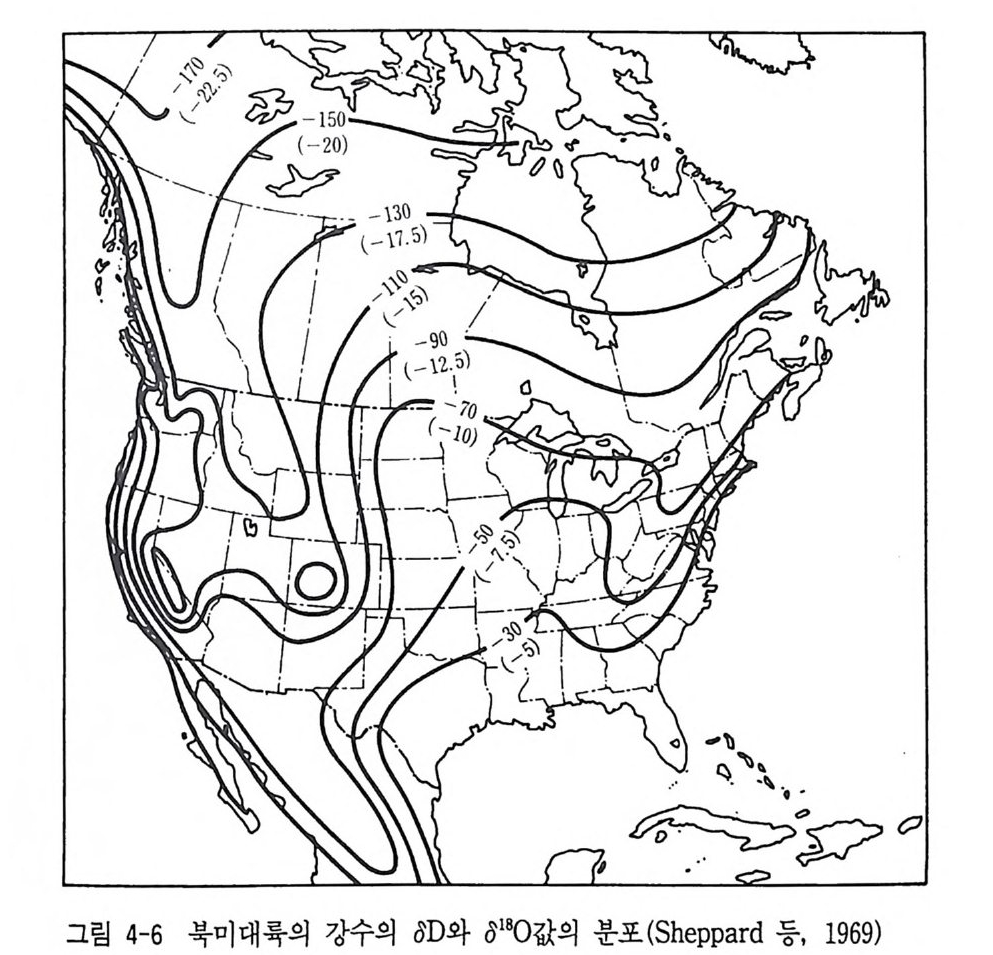 ,조°) 三^` ·` `乙 .. . 尹'
,조°) 三^` ·` `乙 .. . 尹'
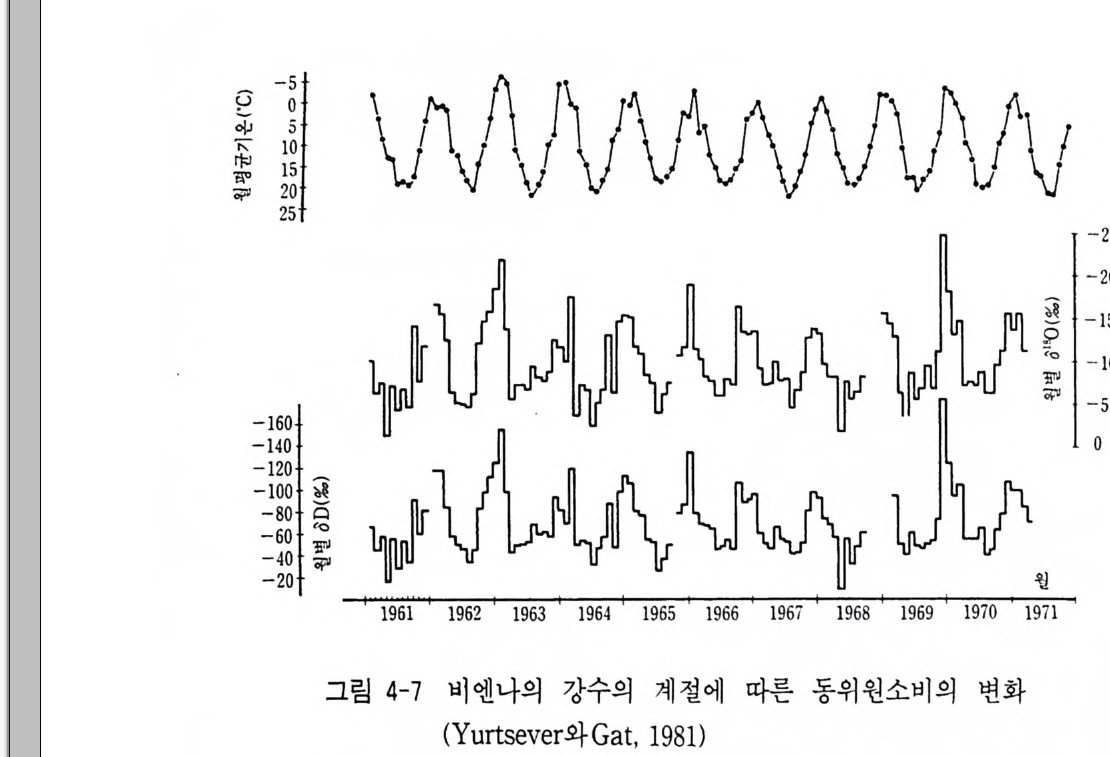 TB[L中.Jj)(Uo 50------一51 0152\02/51 P JV \ /\f\N V \/V
TB[L中.Jj)(Uo 50------一51 0152\02/51 P JV \ /\f\N V \/V
변화하고 있다(그림 4-6). 강수의 동위원소값은 온두효과 때문에 계절변화에 따라서 동위원소 값이 주기적으로 변화하고 있다. 월평균 기온과 수소 및 산소 동위원 소 성분변화는 조화적이고 주기적이다. 즉 여름에는 겨울에 비해서 동위원소값이 큰 강수현상이 일어나고 있다(그립 4-7). 2) 하천수의 동위원소 성분 하천수는 대부분 강수에 의한 것으로 지표수와 지하수로 구성된다. 지표수나 지 하수가 수계 에 주는 영 향은 하천분지 (Drain a g e basin ) 의 조건이나 기후에 따라 다르다. 하천의 물은 여러 기원의 물이 합쳐지 기 때문에 그의 동위원소 성분도 다양하다. 주로 지표수에 의해 공급되는 하천에서는 동위원소의 계절의 변화
가 나타나는 반면 단일기원의 지하수에서 유래되는 하천에서는 동위 원소값의 변화가 작다. 따라서 하천수의 동위원소 분석에서 물의 기 원과 양을 추정할 수 있게 된다. 특히 고전적인 수문학적 연구방법과 기타 화학분석을 실시하면 하천수를 지배하는 요소와 과정을 이해할 수 있게 된다. 중부 이탈리아의 터스케니 (Tuscan y) 지역에서와 갑이 소규모의 하 천수의 동위원소 분석 연구에서 특히 지표수가 우세한 하천에서는 여 름철에는 무거운 동위원소가 많이 농집되고 겨울철에는 가벼운 동위 원소가 많이 농집되는 계절의 변화가 현저히 나타나고 있다 (Gon fi na tini 등 , 1973) . 바바리 안 알프스 (Ba varia n Alps ) 의 레 인 베 취 (Lain b ach) 계 곡의 하천 에서도 여름철의 무거운 동위원소로 된 비와 겨울철의 가벼운 동위원 소로 된 비나 , 눈 녹은 물의 유입에 의해 사안 커브의 변화가 잘 나 타나고 있다 (Hermann 등, 1978). 우리나라의 한강의 하천수는 남한강 과 북한강이 합류하여 서해로 흘러 들어가는 동서 방향의 하천이다. 한강의 상류로 갈수록 태백산맥으로 향하게 되어 지형적으로 고도가 높아진다. 따라서 한강수의 동위원소 분석결과 (Naka i 등, 1981) 에서도 상류의 가벼운 동위원소로 된 물이 유입되므로 동측에서 서측으로 갈수록 수 소 및 산소 동위원소값이 점점 커지고 있다. 동위원소 분석에서 하천수의 증발현상도 쉽게 알 수 있다. 콜로라 도 수계에서 조사된 것처럼 고기 콜로라도 하천수 (0180 = -14.6%,, oD = - 11 .2%, ) 와 오늘날의 하천수 (0180 = 一 12. 1% ., oD = —9% ,) 의 화학성분 분석과 함께 동위원소 분석에서 하천수의 혼합을 정량적으 로 해석 가능하게 되었으며 분지의 지하수의 수문학적 사실을 알 수 있어 지하수의 부존지역의 규모, 저류시간등도추정 가능하게 되었다. 이처럼 환경동위원소 분석은 하천의 형성과 저류기구의 연구에 가 장 중요한 방법이 되고 있다. 그러나 수계마다 지질학적 수문학적 특
성의 차이가 있어 범세계적으로 하천의 비교연구에는 어려운 점이 있다. 3) 지하수 및 열수의 동위원소 성분 지하수의 특성과 기원연구 그리고 열수-암석간의 상호반응 등의 정 량적인 연구는 안정동위원소 응용연구 중에 가장 성공적으로 수행된 연구결과의 하나이다. 여기서 지하수는 크게 循環11' (Me t eor i c wate r ) , 古地下* (Paleowate r ) , 熱* (Geoth e ~al wate r ) 그리 고 Htb ' t 水 (Forma ti on wa t er) 로 구분할 수 있다. 순환수는 앞에서 설명한 것같이 강수 또는 지표면의 담수에서 유래 된 물로 보통 토양의 불포화대를 통해서 유입된다. 순환수의 동위원 소 성분은 온대기후 지역에서는 일반적으로 그 지역의 강수와 일치하 나 건조기후 지역의 지하수에는 강수에 비해 무거운 동위원소가 더욱 많이 농집되는 경우가 있다. 고지하수는 현재와는 다른 기후조건하에 존재했던 과거 지질시대의 순환수를 말한다. 14c 법에 의해 측정된 플라이스토세의 물은 고지하 수이지만 다른 기후 기간에서 유래한 젊은 물도 고지하수라고 정의할 수 있다. 지하수의 수온이 보통 25°C 이상인 경우 온천수라고 부른다. 온천 수의 수온의 법적 정의는 나라에 따라 다르다. 지하수는 수온이 80°C 이상 높아지면 물의 안정동위원소 성분은 원래의 물과 비교해 볼 때 많이 변화된다. 이런 조건을 우리는 열수조건이라 하며 이때에 존재 하는 물을 地熱7J( (Geoth e rmal wate r ) 라 한다. 원래의 해수가 퇴적물의 공국내에 간극수가 잔류된 것이든지 원래 의 물이 퇴적 후의 물의 이동으로 인해 후기의 물로 교대되었든지간 에 심부의 퇴적층내에 존재하는 함영수 지하수를 퇴적수라 한다. 이런 물은 흔히 거의 정체된 상태에 있기 때문에 물-암석 상호작용 이 지배적인 화학적 특성을 나타낸다. 이런 염수 (Br i nes) 는 유전 및 천연가스 퇴적과 밀접한 관계가 있기 때문에 대단히 홍미가 있으며
세계적으로 많이 연구되고 있다. 순환수 기원의 지하수는 그 지역의 강수의 평균 동위원소값과 비교 적 많이 일치한다. 그러나 건조기후 지역에서는 그렇지 않다. 지하수 의 동위원소 성분변화는 주로 지하수의 유입과정에 지배를 받는다. 그러나 물-암석 상호반응, 화석수와의 혼합 그리고 다른 기원의 물과 의 혼합 등도 고려할 수 있다. 유입과정에 의하여 지하수의 동위원소 성분변화가 일어난다. 일반 적으로 하천수나 강수의 동위원소 성분은 지리적 변화, 즉 위도효과 에 가장 크게 영향을 받는다. 지형과 그 지역의 기후에 의해 고도효 과의 강도가 다르다. 여름과 겨울 강수의 평균 동위원소비의 지하수 가 유입 저류지를 형성하며 지하수는 주위의 암석, 해수, 고지하수 및 지표수와의 혼합에 의해 동위원소비가 변화된다. 보통 고도효과에 의하여 評 0 은 0.15~0. 5% , I 100m 변화하고 oD 는 1-4%, / 100m 변 화하므로 지하수의 유입위치를 동위원소값으로 해석할 수 있다. 이의 좋은 실례를 중부 터키의 코냐 평원 (Kon ya p la in)에서 찾아볼 수 있 다 (Sen t urk 등, 1970) . d-excess 현상이 뚜렷한 지중해형 강수는 이 평야의 남부 타우루쓰: 산지에서 일어나 남부의 하천에서 평야로 유입되는 물은 북쪽에서 유 래되는 대륙형 물과는 동위원소적 특성이 현저히 다르게 나타나고 있다. 건조지역의 지하수는 그 지역의 강수의 동위원소 성분과 잘 일치하 지 않는다. 왜냐하면 증발에 의한 영향, 적은 강수량, 보존불량, 불 규칙한 강수현상 등 때문이다. 그래서 대부분 사막지역이나 건조지역 에서의 지하수는 그 지역에서부터 먼 곳에 위치한 산지에서 유래하거 나 (Sla yt er 와 Mabbut, 1 964) 과거 기후가 서늘한 시기에 유입된 물 (Munn ic h 와 Vog el , 1962) 이 나 화석 영수의 역 할이 크다. 이 러 한 수문학 적 시스템 연구는 온도가 지역에 따라 다르기 때문에 고전적인 수문 학적 연구방법으로는 어려움이 많다. 지하수의 염분도와 염분의 기원 과 염분의 방제가 지하수의 개발에 중요한 문제점 중의 하나이다.
증발잔류암 (Evap o rit e) 의 분해 나 표면증발에 영 분화 (Sa!i ni z a ti on ) 현상은 우리나라에서는 없지만 제주도와 같은 섬이나 해안지역에서 해수와의 혼합이나 화석수인 고지하수 (Paleowa t er) 와의 혼합에 의한 영분화 현상은 중요한 문제로 등장하고 있다. 그리고 최근에 비료나 산업폐기용수 등과 같은 인간활동기원 (An th ro p o g en i c source) 물이 해 결되어야 할 중요한 문제로 등장하고 있다. 예를 들면 동위원소 분석 연구에서 서울 근교의 난지도와 같은 쓰레기처리장 주변의 지표수, 지하수의 이동속도, 이동방향 등의 지하수 오염 문재해결에 중요한 정보를 얻을 수 있을 것이다. 지표에 노출된 암석과 반웅 등에 의해서도 동위원소교환이 일어나 물의 동위원소 성분의 변화가 나타난다. 증발잔류암의 분해 등에 의 해서는 8180 一 oD 의 변화가 거의 없으나 속성작용 과정에서 동위원 소교환은 특정지역 수계에서는 우세하게 일어나기도 한다. 화석영수, 퇴적수, 마그마수 및 광화용액 등은 화학성분, 미량성분, 동위원소 성분의 차이가 있으므로 이들 기원을 추정할 수 있다. 열수는 화산분출, 온천, 간헐천, 분기공, 지열지역 등지에서 지구 내부의 열원에 의해서 형성된다. 열수의 동위원소 연구는 지열에너지 자원개발에 있어서뿐만 아니라 지질현상 중에 중요한 속성작용, 변질 작용, 물-암석 상호작용과 열수광상 성인연구 등에 대단히 중요하다. 특히 동위원소비 분석으로 열수나 분기수의 물의 기원을 추정하며 H20, H2S, CO2, Hz, CH4, Nz, Ar 등 용존성분이 나 가스의 기 원 울 추정할 수 있다. 그리고 저류지층내의 물리적 상태추정과 열수기 원이 되고 있는 강수의 침두연대를 추정할 수 있다. 높은 엔탈피의 지열을 이용한 발전소가 게이저 (Geys e rs, 미국), 라 데렐로 (Larderello, 이탈리아), 와이라케이 (Wair a kei, 뉴질란드), 세로 프리에토 (Cerro Prie t o , 멕시코), 오다께 (Ot ak e, 일본) 등에 건설되어 있으며, 낮은 엔탈피의 지열지역인 헝가리에서는 저온열수를 농업에 이용하고 있으며 지열에 수반되는 특수화합물울 공업에 이용하기 위
해 회수하기도 한다. 지열지역의 열원은 아직 정확히 연구되어 있지 않으나 판구조에서 판과 판아 서로 만나는 판의 경계부에 주로 분포 하고 있어 최근에는 판구조론으로 이를 설명하고 있다. 그리고 열원은 주로 젊은 화성암의 관입지역이나 지하 증온률에 의 해 고온환경으로 해석되는 지하 심부지역으로 생각되고 있으며 이런 지역의 심부로 지하수가 순환할 때 이 열원에 의해 열수가 형성된다. 이 같은 지열계 (Geoth e nnal s y s t em) 를 이해하고 연구하는 데 지구화 학 특히 동위원소 지구화학이 크게 기여하고 있다. 특히 열수의 동위원소 성분과 화학성분 분석에서 열수의 기원, 저 류지역, 열수의 유동패턴에 대한 정보를 얻을 수 있고 지하온도를 추 정할 수 있다. 그리고 열전도, 냉수와의 혼합, 증기유실 등에 의해 열수가 지표로 이동하는 도중 냉각과정을 동위원소 및 화학성분의 변 화로 연구할 수 있다. 따라서 오늘날 지열지역 개발 및 탐사와 환경 보전을 위해 지열지역 열수나 증기, 메탄 용존 황산염 등의 산소, 수 소, 탄소, 황 등의 동위원소 분석방법을 많이 이용하고 있다. 위에서 설명한 것같이 지열수의 동위원소 성분은 시공간적으로 변 화하는데 그중 대표적인 원인은 다음과 같다. CD 1so ; 160 비가 다론 물이 서로 다른 비율로 혼합되므로 생기는 동위원소비의 변화 ® 여러 장소의 많은 암석들과 동위원소 교환반응의 정도가 다르므 로 일어나는 변화 ® 열수가 상승하는 동안 증기유실로 인한 동위원소비 변화 등을 들수있다. 열수계에서 물-암석 상호반응에 의한 동위원소비 변화가 현저하다. 풍암석 상호반응을 좀더 구체적으로 설명해 보자. 안정동위원소 연 구가 있기 전에는 고온 열수계의 물의 기원을 구별하기는 대단히 어 려웠다. 열수를 과거에는 일반적으로 마그마수 또는 초생수로 생각해 왔으나 Geo gu el(1953) 이 열역학적 연구에 의해 그리고 Cra ig (1963) 는
수소, 산소동위원소 연구에 의해 순환수 기원의 지열지역의 열수를 확인하였다. 그립 4-8 에서 보면 지열지역의 열수와 그 지역의 지하수 또는 지표 수 사이에는 동위원소값에 현저한 차이를 보이고 있다. 특히 산소의 경우 더욱 현저하다. 만약 이들 지역의 열수가 초생수와 그 지역 순 환수의 혼합으로 생겨났다면 혼합선상에 놓이는 관계가 얻어져야 할 것이다. 그림에서와 같이 열수의 산소 동위원소비가 그 지역의 지하수나 지 표수의 동위원소비보다 큰 쪽에 도시되고 있다. 이런 현상 을 산소편 이 (Oxy ge n shif t) 라고 하며 이 는 무거 운 산소 동위 원 소를 가지 는 암석 과 순환수가 서로 반응하여 동위원소가 재편성되었기 때문이다. 수소 와 동위원소 교환을 일으킬 수 있는 수소를 포함한 조암광물이 매우 적기 때문에 수소에는 거의 영향을 주지 않는다. 미국의 게이저, 솔
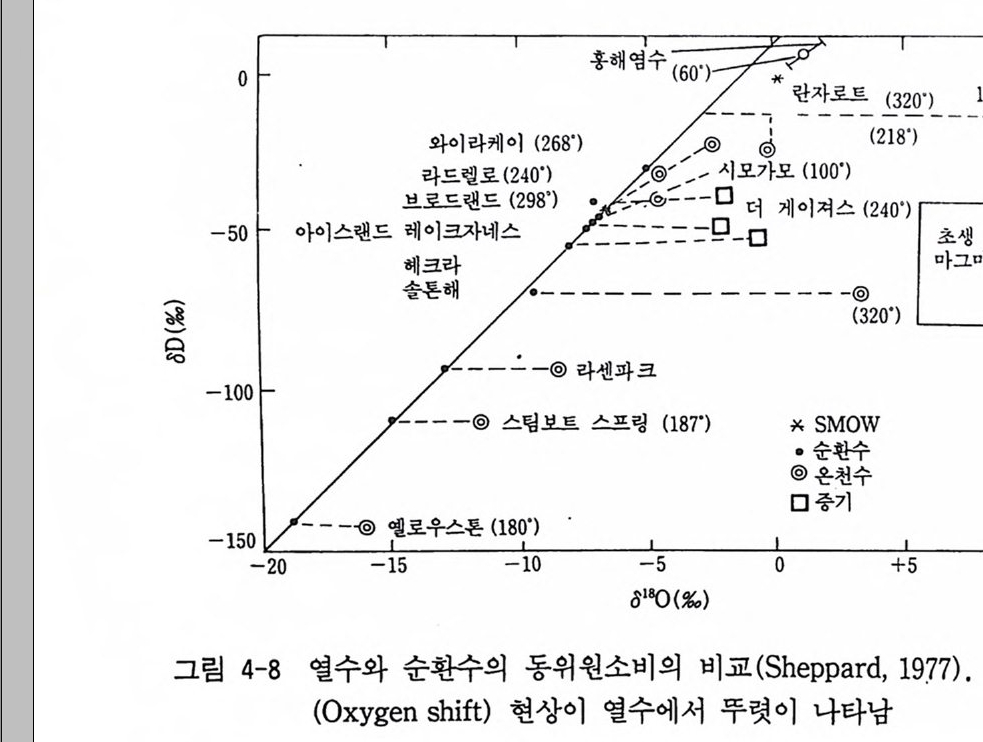 。 브로와드이랜라드케 이(2 98(2'6) 8 ')근 \\,,§®~- 1-~J,:* 1란-1자-:로 2- 트 -1 (224..( .1 0:.38 .':2: ) '. ). 0c . 기·_ __ 1-40 .7 •
。 브로와드이랜라드케 이(2 98(2'6) 8 ')근 \\,,§®~- 1-~J,:* 1란-1자-:로 2- 트 -1 (224..( .1 0:.38 .':2: ) '. ). 0c . 기·_ __ 1-40 .7 •
돈해 라센파크, , 스팀보트 스프링 등의 열수지역의 산소는 보통 0.5~15 %o까지 변화하며 와이라케이 (뉴질란드), 루쯔(콜롬비아) 등은 0.5 ~ 1.0% o 정도로 산소편이가 대단히 적다. 와이라케이의 경우 열수 변질을 받은 암석 (0180 = + 2.6~ + 5 . 2 %, )은 변질받지 않은 원암(단 산암, 유문암, 응회암)보다 3~ 衍 % 정도 1 8 0 이 결핍되어 있었고 열수 (0180 = -4 . 9 %, )와 동위원소 평형에 있는 경우의 값과 근사하다. 250 ' C 에 서 알카리 장석 과 물의 평 형 정 수가 7 . 2%o (O ' Ne il과 Tayl o r, 1967) 인 값 과 비교된다. 와이라케이 지역의 열수와 지하수의 동위원 소값이 유사한 원인은 지열지역의 열수의 기원이 그 지역의 지하수이 기 때문이거나 물-암 석 상호반응에서 물의 산소편이 현상은 물-암석 상호작용에 의 해 잘 설 명 되 었 다 (Cla y t on 과 Ste in e r, 1975) . 그러나 우리나라의 온천수의 동위원소비 분석에서는 위의 결과와 상반되는 결과가 얻어 졌 다(그림 4-9 ) . 척산 , 도고온천의 경우 그 지
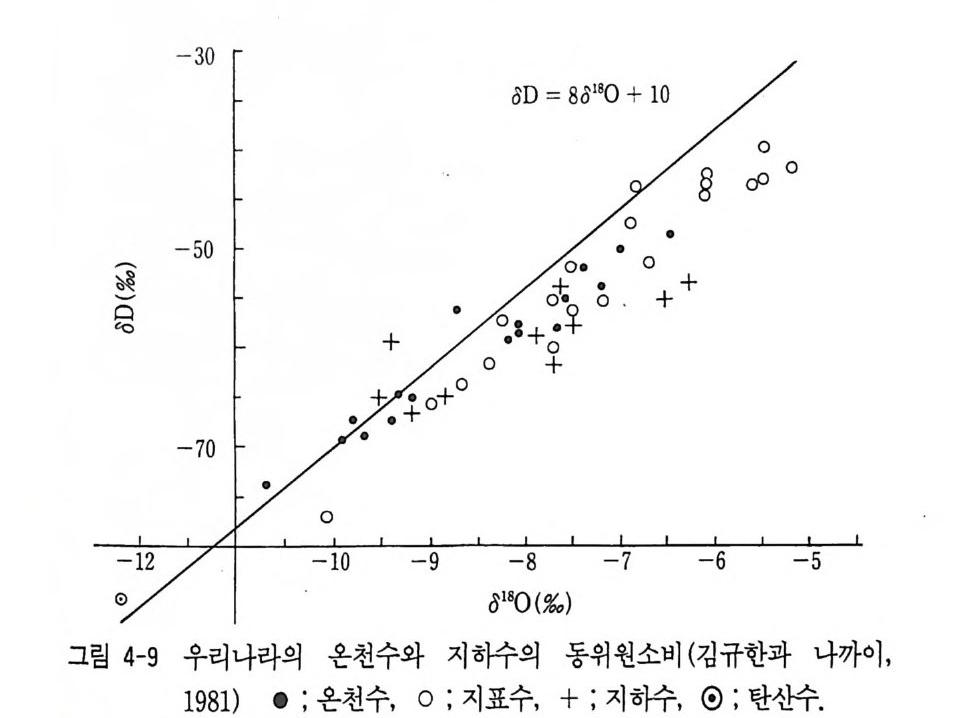 -30
-30
역의 지표수와 온천수의 동위원소 성분이 대단히 유사하고 그 의 지 역의 온천은 모두 온천지역의 열수의 동위원소 성분이 그 지역의 지 표수 또는 지하수의 동위원소 성분보다 가벼운 동위원소가 농집되어 있었다. 이런 사실로 우리나라의 온천은 온도가 40~60°C 내로 대단 히 낮은 편이고 열수의 저류시간이 짧아 물-암석 상호작용이 일어나 지 않는다는 재미있는 결과가 얻어졌다(김규한과 나까이, 1981 ). 특히 온천지역보다 지리적으로 북쪽이며 고도가 더 높은 지역에서 유래한 순환수가 유입되었음을 잘 나타내 주었다. 산성 온천수에서 8D 와 評 0 이 정의 관계를 나타내는 경우가 있다 (Craig , 1963 ; Gig ge nbach, 1978). 물론 이들 온천수의 기원은 순환수이 지만 순환수의 혼합의 영향을 나타내는 쪽으로 수렴하지 않은 결과가 얻어져 이룰 지하에서의 증발과 지표에서 증발에 의한 원인으로 다음 과 같이 설명하고 있다. G igg enbach(1971) 과 Truesdell(1977) 는 지하증발 과정을 다음 두 극단의 경우로 구별해서 설명하였다. ® 열수가 상승하는 동안 액상과 공존하고 지표에서만 분리되는 스 팀 ® 생성되자마자 계속적으로 없어지는 스팀 단일계 스팀 분리에서 잔류액의 함수 f는 엔탈피 평형에서 구할 수 있다. f = (Hs -Hw) / (Hs - HL) 여기서 H 는 초기 (증발 전)의 물의 엔탈피이고 HL 과 Hs i= 각각 분리시의 스팀과 액상의 엔탈피이 다.8 18O 와 8D 값의 도시 에서 기울기 S 는 S= ~깝 ::%\1 麟)0) 이 다. 여기서 80 는 초기의 동위원소 성분, e 는 증발에 의한 동위원소평 형 부화계수이다. 죽
a = l + E = R( 액) / R( 기) R = D / H 또는 180 / 160 이다. 22o·c 이상에서는 기울기 S 는 부(―)가 된다. 왜냐하면 22o·c 에서 는 ao< 1 , 든 D < O 이기 때문이다. 죽 180 함량이 증가하고 D 함량은 감소한다. 반대로 물의 임계온도인 374 ° C 까지는 a1so > 1 이다. 연속적으로 스팀이 분리되는 좀더 복잡한 경우는 아래의 식과 같은 비등온 레 이 리 증류과정 (Non-is o th e nnal Ray le ig h dis ti l at io n p rocess) 으 로 설명이 가능하다 (True s dell 등, 1977). ln 11000000 ++ B8LLO = \JHHLL O (lH /s a- 一H L1 ) dHL 단일스테이지 모델과 연속스팀분리 모델에서 최초와 최종온도가 150'C 이상 차이가 있다면 그 결과는 아주 다르다. 미국의 엘로우스톤 열수 (Truesdell 등, 1977), 칠레의 엘타티오 지열 지역 (G igg enbach, 1978) 에 대하여 지하증발에 의한 동위원소 성분변화 의 연구가 되어 있다. 표면증발에 의한 동위원소 성분변화에 대하여 G igg enbach (1 978) 의 연구에 의해 설명되고 있다. 그 의 지역에서는 열수와 차가운 지하수의 혼합에 대하여 동위원소 적 해석이 잘 이루어지고 있다. 동위원소 연구에 의해 자연수의 분류가 체계적으로 이루어졌다. 즉 위에서 설명한 순환수, 퇴적수 의에 해수, 화석수, 마그마수, 초생 수, 변성수, 열수, 유기기원의 물, 의계수 등으로 구분되고 있다(그 림 4-10).
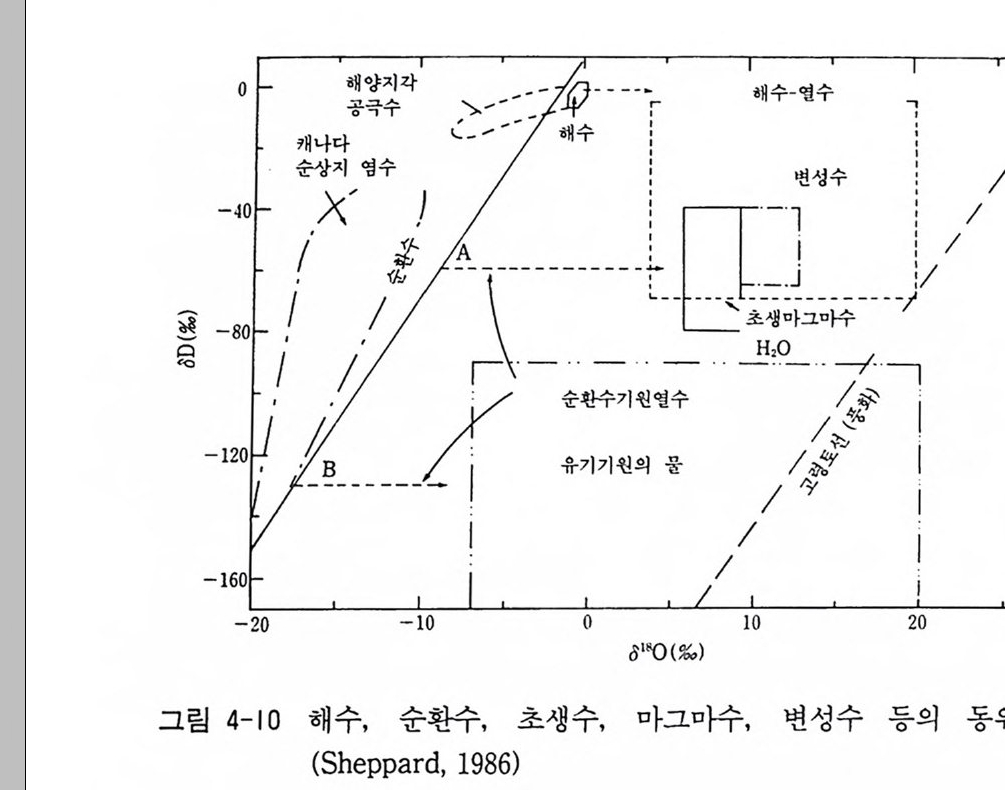 g)려G( -16-804。o _卜_'|I. o캐문///.. B X갭. i/,해공/ , /영양/국 수尸$수i ) , AI|〉 〔\一2\’〉t t約¢一呼紅- 回-뮤-― 가원 ~--·- - 의 원,';''I,1,i'L',』‘3 I 연 - ip -广\ / I 해》比一타l- 수/ - .O -p-1 Ir_i_/ i 변 연 성도 휴 수/싹 ~ 2:一수令今% 7기7II,I,'IIII':'L;l_ ..|_| . / / /
g)려G( -16-804。o _卜_'|I. o캐문///.. B X갭. i/,해공/ , /영양/국 수尸$수i ) , AI|〉 〔\一2\’〉t t約¢一呼紅- 回-뮤-― 가원 ~--·- - 의 원,';''I,1,i'L',』‘3 I 연 - ip -广\ / I 해》比一타l- 수/ - .O -p-1 Ir_i_/ i 변 연 성도 휴 수/싹 ~ 2:一수令今% 7기7II,I,'IIII':'L;l_ ..|_| . / / /
그림 4 - 10 에서와 같이 해수 (8D = 0%,, 8180 = 0% ,), 초생수 (o D = -4 0~— 80 %,, 8180 = 7~9%,)' 변성수 (8D = 0~— 70 % ,, 818 0 = 4~20%,) 등의 동위원소값이 현저하게 구별된다. 특히 종래에 거의 동의어로 사용되어 오던 마그마수와 초생수는 물의 궁극적인 기원에 관계없이 마그마와 평형상태에 있었던 물은 마그마수로 정의하고 초 생수는 수권에는 한 번도 표출된 바 없는 지구의 맨틀이나 핵에서 유 래하는 가상의 물을 말하며 지각-맨틀 상호작용, 판구조론에서 베니 오프대의 관의 침입과정의 설명에 중요하다. 4) 화석수와 퇴적수의 동위원소 성분 화석수 (Conna t e wa t er) 는 퇴적될 당시에 포획된 화석해수로 원래 동위 원소 성분은 고해수의 값과 같다. 그리고 퇴적수 (Forma ti on wate r)
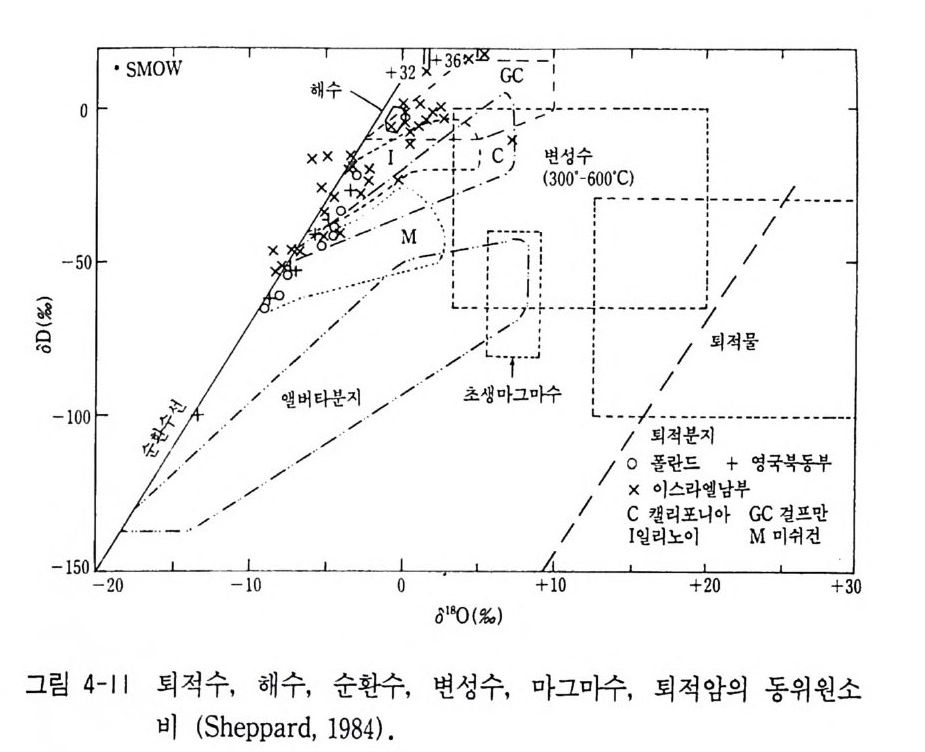 •SMOW 해수 +3 2) (, z- G-C- II
•SMOW 해수 +3 2) (, z- G-C- II
는 그 성인과 시대에 관계없이 퇴적암의 공국에 존재하는 물울 말한다. 몇몇 퇴적분지의 퇴적수의 동위원소 성분은 그림 4-11 과 같다. 이들 대부분의 퇴적수는 500m 와 3700m 심도에서 산출된 것이고 肝留岩이 오도뷔스기의 해성퇴적암이다. 5~30w t% 용존고형 물질을 가지는 염수이다(Hit chon 과 Fried man, 1969). Clay ton 등(1 966) 은 대부분 이 퇴적수는 해수기원이 아니고 순환수 기원이라고 밝혔다. 그러나 퇴적기원의 열수는 해수기원도 많이 있는 것으로 보고 있다. 화석수와 퇴적수는 대다수 “C 연령측정에 의하면 그 시대가 오래된 것으로 이들을 우리는 古 *(Paleowa t er) 라 부른다. 물론 앞의 지하수도 여기에 포함된다. 알제리아의 Chott -H odna 지역 의 지하수에서 고수가 명확히 구별되고 있다. 일반적으로 퇴적수의 8180 값은 온도와 영분도가 증가함에 따라 증가하고 있다. 많은 퇴적
분지의 시료는 oD 값도 온도나 0180 의 중가와 함께 증가하고 있으나 감소하는 경우도 있다 (She pp ard 과 Lang le y, 1984). 이는 비교적 제한된 용적의 열수에 있어서도 열수의 시대, 화학성 분 그리고 역사가 다르기 때문으로 해석된다. 미시시피 벨리형과 갇은 탄산영암을 모암으로 하는· Pb-Zn(F-Ba) 열수광상에서도 퇴적수 기원의 열수가 알려지고 있다 (Chare f과 She· ppa rd 1985, 1986) . 이 퇴적수가 마그마 관입시에 유입되어 열수용액이 될 수도 있다. 그 의에 비유기성 산화반응에 의해서도 물이 고수가 된 예도 있다. Manhe i m 과 Sa y les(l970) 은 멕시코만의 심부 시추코아에서 마이오 세 이후 해수나 해성퇴적물로 덮힌 암염돔에서 반영수를 발견하였다. 여기서 6 . 7%, 의 낮은 oD 값을 갖는 물은 다음과 같이 석고가 환원 되어 생긴 H2S 의 비유기적 산화반응에 의해 생성된 것이다. 3CaSO ◄ + C10H22 = 3H2S + C6H14 + 3CaC03 + CO2 + H20 sm-+ 3H2S = 4S0 + 2H20 + 2SH- 특히 퇴적수는 유전, 천연가스지역에서 많이 연구되고 있으며 유전 영수의 818O 와 8D, 염분도간의 관계에 대한 연구가 Clay ton 등 (1966) 에 의해 이루어졌다(그림 4-12). 그림 4-12 의 일리노이, 미쉬간, 알버타 등지의 유전의 염분도와 동 위원소 성분관계에서 절편이 염분도가 0 인 그 지역의 강수의 값과 잘 일치하고 있다. 유전염수가 낮은 중수소의 값을 가지기 위해서는 강수에 의해 충전 된 지하수가 유전 영수지역에 유입, 혼합되어야 할 것이다. 이처럼 유전영수 지 역의 수문시스템 (Hy dr olog ic sys t e m ) 연구에도 대 단히 중 요한 의의가 있다. 위에서 설명한 古 7k 는 일반적으로 저온에서 다음과 같은 반응이 전
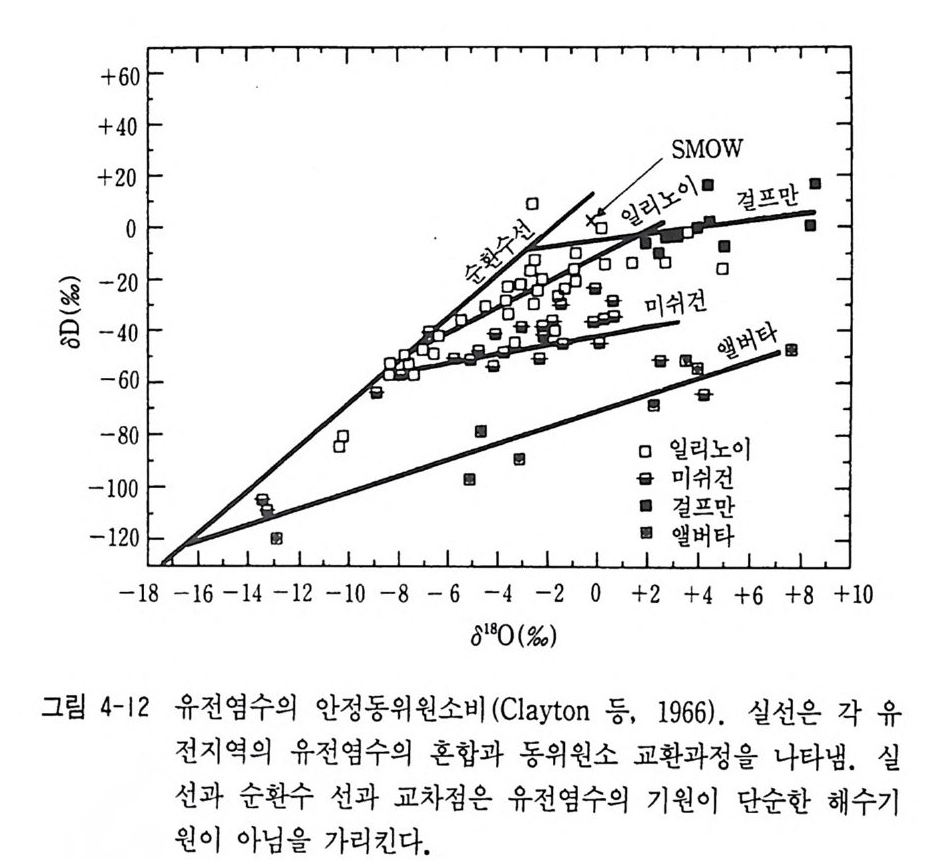 +60
+60
행되므로 고수문학 연구에 가치가 있다. ® 광물과의 교환반응에 의해 물의 함량의 변화는 없으나 180 의 함 량은증가한다. ® 점토와 불석과 갇은 새로운 자생광물 (Neo g en i c mi neral) 의 결정 화작용으로 인한 분류 때문에 D 의 함량은 증가하고 180 함량은 감소 한다. ® 유체와 교환반응에서 H2S, H 및 탄화수소와 같은 화합물의 수 소에 영향을 주어 물의 D 의 ·함량을 증가시키고 180 함량에는 변화를 주지 않는다. 예의로 다량의 CO2 와 교환이 일어나는 경우에는 물의 180 함량을 감소시키는 경우도 있다.
표 4-2 함수광물의 동위 원소 분별정수 굉땅 화학성분 a180 (25'C ) an (25'C ) 석고(gyp sum) CaSo.•2H20 1.0 0 4 0.985 미 라바 라이 트 (mi ra bil ite) Na S04 • lOH20 1. 0015 1.0 1 88 가이루사이 트 (ga yl u ssit e) Na2C03•CaC03•5H20 n.d. 0.987 트로나(t rona) Na2C 0 3• NaHCOJ . 2H 20 n.d. 0.9 2 0 보렉스 (borax) Na2B01· lOH20 n.d . 1.000 n.d, 측정되 지 않음.
© Ultr a fi lter ati on 현상으로 D 의 함량이 약간 감소되나 다른 원인 에 의한 변화와 구별이 어렵다. 상기의 현상으로 고수의 동위원소 성분이 변화된다. 함수광물이 용 액에서 침전되어 만들어질 때 결정작용의 물의 동위원소 성분은 원래 물의 동위원소 성분에 변화를 줄 것이다. 함수광물의 분별정수는 표 4-2 와 같다. . 이들의 분별정수가 온도에 무관하기 때문에 쉽게 원래의 물의 동위 원소 성분을 추정할 수 있다. 그러나 이들의 결정과 물 사이의 결합 에너지가 낮기 때문에 결정작용의 물과 침출된 물간에 동위원소 교환 이 일어나기 쉽다. 결정수의 동위원소 분석자료는 적지만 상부 마이 오세의 결정수가 조사되어 있다 (P i erre 와 Fonte s , 1978, 1979 ; Mat• suba y a 와 Sakai, 1973) . Savi n ( 1980) , Lawrence 와 Tayl o r (l971) , Sav i n 과 Ep st e i n ( 1970) 등이 암석의 풍화에 의해 형성된 광물의 동위원소 성분이 그 지역의 지하수의 동위원소 성분과 대단히 유사함을 확인하였다. 고령토, 깁사이트, 스멕타이트 등과 같은 광물의 동위원소 성분을 oD-0180 그립에 도시하면 순환수 선과 평행하게 나타난다. 이를 고 령 토 선 (Kaolin ite lin e ) 이 라 부른다. 동위원소 분별정수가 온도에 따라 변하고 결정수의 무거운 동위원
소 성분은 원래의 물과 온도 등에 따라 변하기 때문에 각 광물의 값 이 지하수의 값과 반드시 대비되지는 않는다. 그러나 점토광물과 그 지역의 순환수의 동위원소 성분이 대체적으로 대비된다. 즉 점토광물 의 동위원소 분석에서 고수를 추정할 수가 있고 점토광물 광상의 생 성환경과 생성과정을 해석할 수 있다. 5) 유기기원의 물의 동위원소 성분 유기기원의 물의 수소 동위원소비는 -9 0~-2 50%, 까지의 범위를 가진다 (She pp ard 와 Charef , 1 986). 유기기원의 물 (Or g an ic wa t er) 은 최 근에 정의된 것으로 유기물질, 비트민, 석탄, 케로겐, 석유, 유기기 원가스 등이 탈수화반응, 탈수소반웅, 산화, 교환반응 등과 같은 직 접적이거나 간접적인 변형과정에서 생기는 것이다. 예를 들면 O 케로겐이 속성작용에 의하여 다음과 갇이 탈수화 반 웅에 의해 물이 생성된다. (C20H2005) (케로겐 1)- (C20H100) (케로겐 2) + 5H20 ® 케로겐, 메탄 등이 변성작용 동안에 다음과 같이 산화되어 물이 생성된다. (C20H200) 케로겐 + 2( 야)一 --+20C (흑연) + 5H20 ® 퇴적물과 물이 접하면서 속성작용 초기에 신선한 유기물의 조각 이 반응해서 물이 생성되는 경우도 있다. @ 고변성도 지역에서 물이나 광물로 된 수소와 유기기원 수소나유 기기원 H, CH4 간에 수소 동위원소 교환반응을 들 수 있다. 최근 파나 스퀘아라, 튜니시아 등의 괴상연 광화작용과 기타 일부 텅스텐광 상에서 유기기원의 열수용액이 논의되고 있다 (She p ard 와 Charef, 1986).
6) 변성수의 동위원소 성분 변성수 (Me t amor p h ic wa t er) 의 동위원소 성분은 보통 변성암이나 변 성광물에서 계산에 의해 얻은 값이다 (Ta y lor, 1974 : Shep pa rd, 1976, 1981 ). 이 값은 oD = - 40~ - 100%,, 0180 = + 8~ + 26%, 범위이 다oD( 그=림 — 43-15 10). ~-변7성 0%현,, 무0암18이0 나= +해 양3지~각 +, 1 4%오,피 내오의라이이다트. 복그합림체 4등-1 은에 서와 같이 oD 값이 0%, 로 이어지는 것은 해양지각의 탈수화반응에 의 한것이다. 변성암은 암석의 종류나 고온에서 동위원소 분별정수값이 다르므로 180 / 160 비는 변화가 심 하다. 7) 동위 원소 지 질온도계 단원 3 에서 설명하였듯이 자연에 공존하는 한 종 이상의 동일한 동 위원소를 가지고 있는 어떤 화합물이라도 그둘간에 동위원소 평형에 있으면 동위원소 지질온도계로 이용될 수 있다. 여기서 수권에 공존 하는 동위원소 쌍을 이용한 지질온도계만을 간단히 소개한다. 흔히 고온지 열에 존재 하는 화합물은 H20 (증기 또는 스팀) , CO2, CH., H2, H2S, N2 등의 기체상의 주이며 이들 사이에는 다음과 갇 은 동위원소 교환반응이 일어난다. 12co2 + i acH ◄ = 1aco2 + 12cH. (반응시 간 > 5To.9, T = 3 쩡T_') CH3D + H20 = CH4 + HDO HD + CH. = H2CHsD cl6 야HD + + H H212800 == cHl26 °+18 H0 D+O H2“O
44- sO l6m- + H2180 = 上4 sl80 t + H216 0 (물이 탁월한 계 에 서 ) S16Q i- + H21s o = s16031so 2 一 + Hz160( 물이 탁월한계에서) (< l T) 위의 반응의 분별정수의 온도 의존성은 그림 4-13 과 같다. 지열지 역에서 동위원소 지질온도계는 물이 탁월한 계와 가스 등이 탁월한 계에 따라 위의 동위원소 분별식이 선택적으로 이용된다.
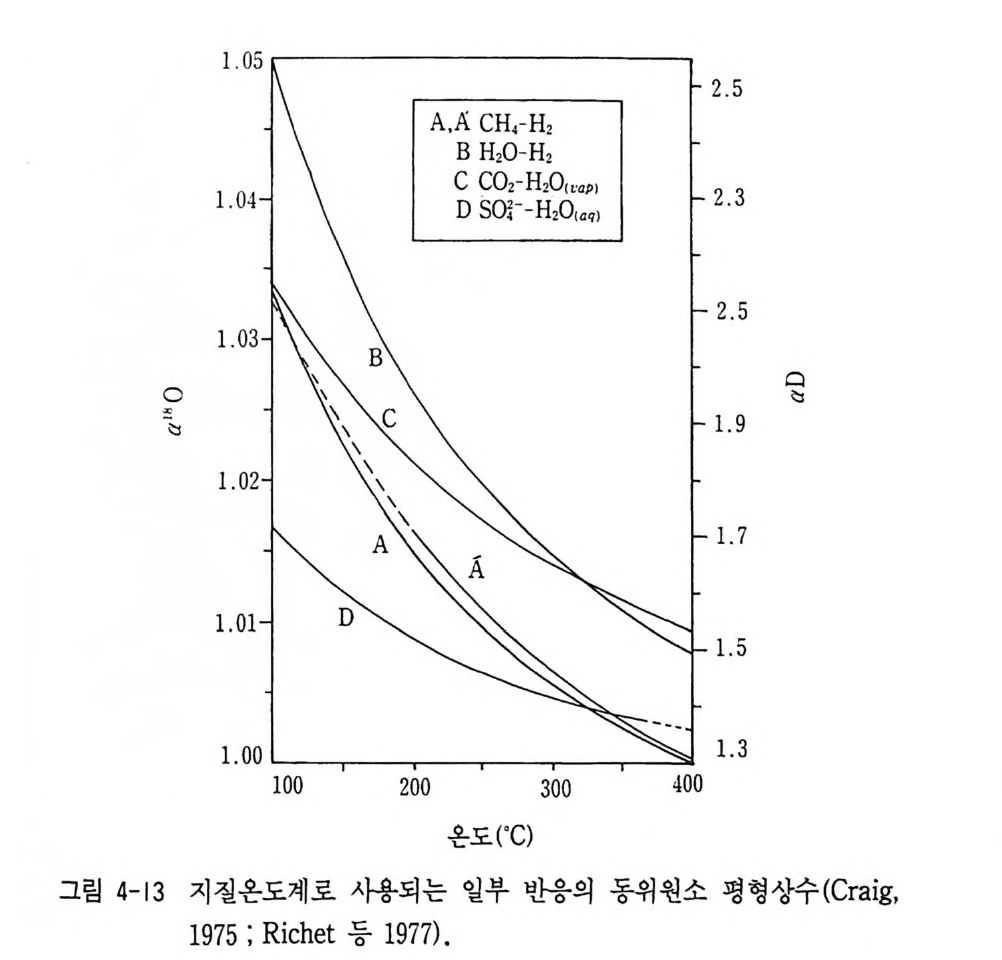 1 05
1 05
표 4-3 동위 원소 교환반웅의 반응시 간 (Hu lsto n , 1977) 동위원소 교환반웅 T~0 . 9( 년 ) 8 참고문헌 13CH.-12C02 >5 Hulsto n (19 73) S18 (),-H 2160 <1 300'C Lloy d (19 68) ~5200'C Hs1so.-H2 l6Q ~1 Hulsto n (19 73) HDO-H2
그러나 최근에는 표 4-3 에서처럼 CH4-H2 , H2 0- H2 , CO 2 -H20 가 실측치와 잘 일치하므로 많이 이용되고 있다. 가스가 탁월한 계에서 이들의 동위원소 분별식은 다음과 같다. CHrH2 ( Craig , 1975 ; Ric h et 등, 1977) 의 식 은 2oo·c 이 상에 유효하 며 1000 Ina = - 90 . 9 + 181 . 27 X l06T-2 -8 . 95 X 1012 / T4 의 관계 식 이 이용된다. 여기서 a = (D / H)cH4 / (D / Hh2 이며 T 는 절대온도 이다. C02-CH4 사이 에 는 1000 lnaco2- cH . = -9 . 01 + 15 . 301 X 103 / T + 2.361Xl06 / T2 식이 이용되며 이때 (13 C / 12C ) co2 aco2-CH4 = (13C / 12C)CH4 이다. 100-400° 떠 온도 범위에서 얻어전 H20( 수증기)와 H2(Ric h et 등, 1977) 사이의 식은 lOOOlna = -217.3 + 396.8X 103 / T + 11.76X 106 / T2 이다. 여기서 a = (D / H) H20 / (D / H) H2 이다(그립 4-14). 100~400° 떠 온도 범위에서 H20-C02 계의 산소동. 위원소 분포에서 이론적으로 계산된 식은 lOOOlna= -8.87+7.85x103/T+2.9 4
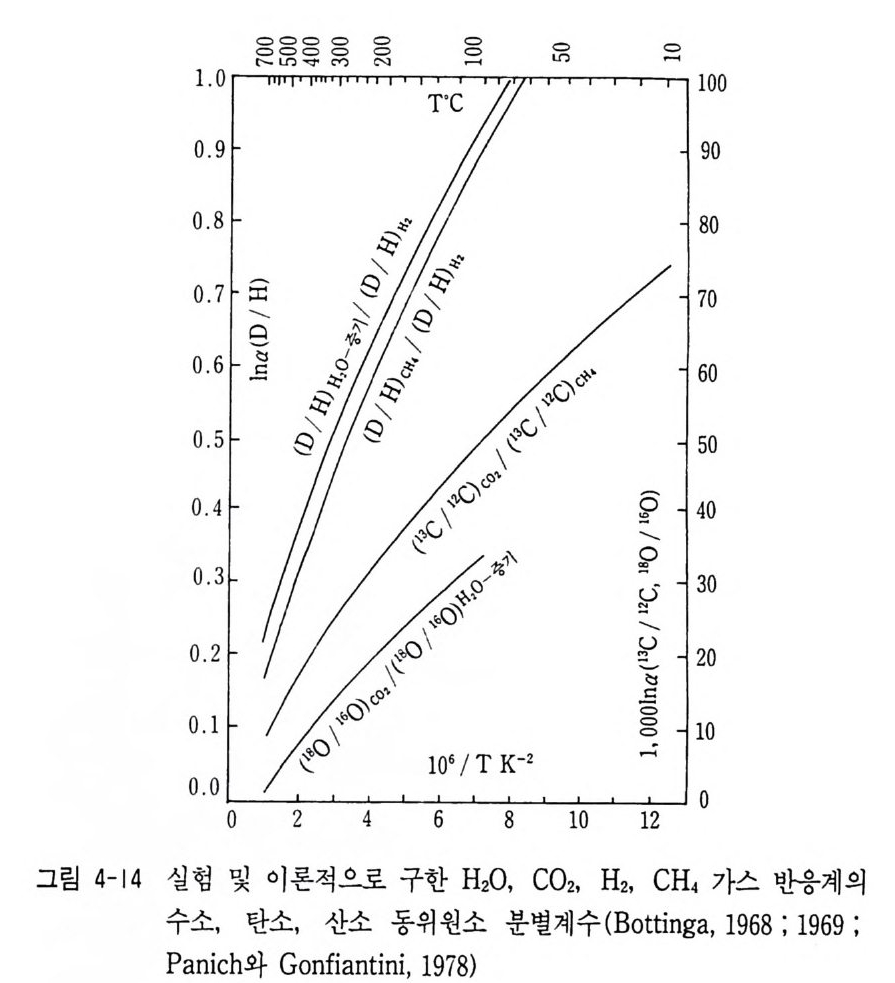 1.0 c응--응u , 응-r 응c ooz OOI OS :::: 100
1.0 c응--응u , 응-r 응c ooz OOI OS :::: 100
X l06 / T 비 다. 여 기 서 a = (1so ; 1so) co2 / (1so ; 1so) H20 이 다. 물이 우세한 계내에서 SO t -H20 간의 지질온도계는 Lloy d (1 9 68) 과 M i zu t an i와 Ra ft er(l969) 에 의해 실험적으로 다음과 같이 얻어 졌 다. OOOlna = 3 . 251 X 106 / T2 - 5 . 6 lOOOlna = 2 . 88 X l06 / T2 - 4 .1
여기서 a = (18 0 / 160)soi- / (180 / 160)1120 = = ~1000 + 0180oi. o) 이다. 위 식은 2oo · c 에서는 거의 일치하며 o,.;_3oo·c 내에서는 土 l0 ° C 의 차 이가 있다. 34-93'C 의 저온에서 고상인 비정질 석영과 물(열수) 사이 에 산소 동위원소 분별을 이용한 지질온도계는 lOOOlna = 3.52(l06T-2) - 4.35 이다 (K it a 등 , 1985). 저온에서 고상인 광물과 액상간에는 동 위원소 교환실험이 어려운데 이 같은 실험결과는 저온에서의 고상적! 상간의 동위원소 분별연구에 홍미있는 것이다. 8) 우리나라의 강수와 지하수의 동위원소 성분 남한의 순환수의 동위원소 성분은 018 0 = -s .2~ - 10.3%,, 8D = -3 9.5~ 一 72. 7% , 내의로 Cra ig (l961) 의 순환수선에 도시된다 (그림 4-15, 표 4-4) . 남한의 물의 동위원소 성분도 온도효과에 의한 위도효과, 고도효과, 내륙효과 등이 나타나고 있어 남쪽의 해운대 (0180 = -5.5 % ., oD = —39 .5%,) 에서 북쪽의 척산온천지역 (8180 = —9. 0 % ., oD = -62.3%.) 까지 감에 따라 위도 l.5° 변화에 산소는 3.5%,, 수소는 22 . 8%, 정도 변화하고 있다. 지형적으로 고도가 높은 지리산의 경우 저지대 구례지역 (8180 = -6 .4~, • 8D = -4 5~) 에서 지리산 천왕봉 (8180 = -9 .8~, SD = - 16.3~) 까지 고도차 약 1800m 에 산소는 3.4 % ,(0. 19 ~ I 100m) 변화 하 고 있다(김규한과 나까이, 1988). 이 같은 값의 변화는 보통 그 지역의 기후, 지형에 따라 다르다. 유럽지역에서 보통 산소는 0.1 5 ~o.5 %?I 100m, 수소는 1.5 ~ 4%, I 100m 까지 변 화한다 (Yu rt sever 와 Gat, 1981).
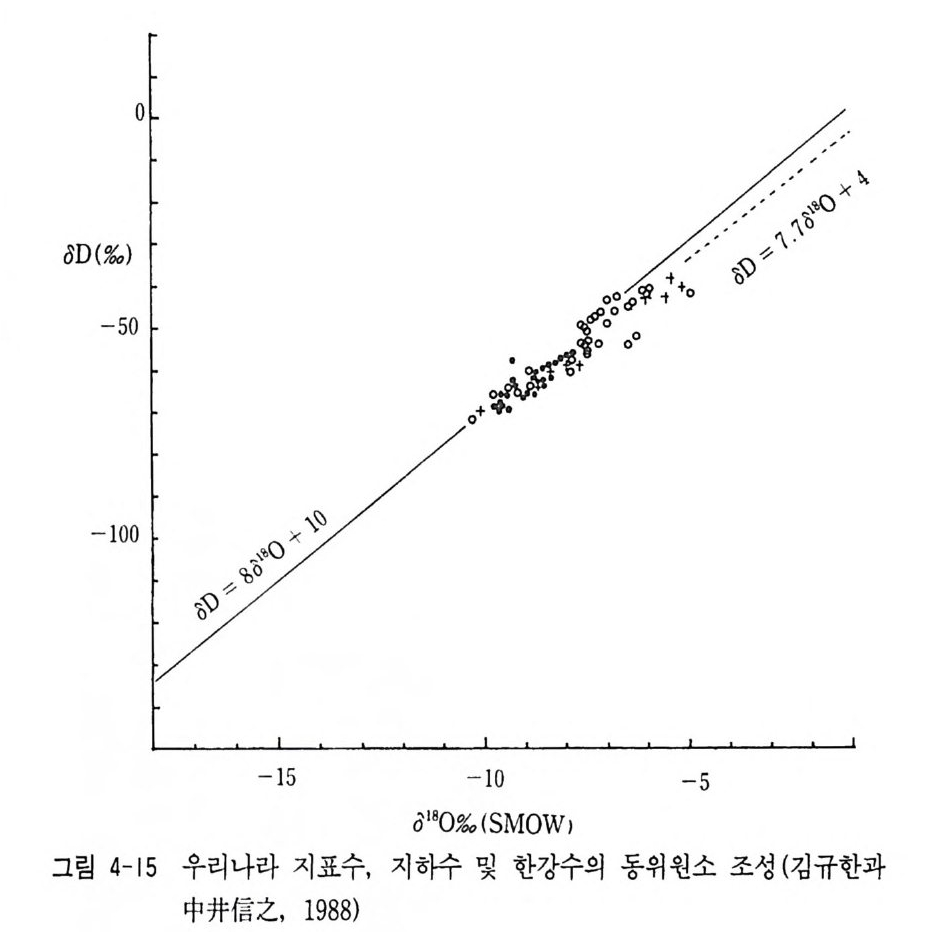 。
。
남한의 순환수의 산소 및 수소 동위원소비의 분포는 그림 4-16 과 같 다. 그림 4~16 에서와 같이 산소와 수소동위원소값이 위도에 의한 영 향보다 지형에 의한 고도의 영향을 크게 받음을 알 수 있다. 죽 태백산맥과 소백산맥 등의 지형의 영향이 크게 나타나고 있다. 한강수의 동위원소 분석결과 (M i zu t an i 등, 1980, Nakai 등, 1981) 에서 도 한강 상류인 북한강과 남한강 지역의 동위원소 성분이 현저한 차 이가 나타났으며 이들이 혼합된 하류의 서울지역의 한강수는 180 과 D 가 많은 물과의 혼합으로 인해 동위원소값이 점점 커지고 있다.
표 4-4 우리나라 지하수의 산소 및 수소 동위원소 성분 (김규한과 中井 信 之, 1988) 깁 1 위치 018 0 8D d PH 시료채취일 1 인천 -7.9 —58 . 9 4.3 7.5 G 21 Jul 80 2 부평은광산 -7.5 —5 6. 9 3.1 6.8 G 22 Oct 79 3 서울 연세대 -7 5 -5 1. 6 8.4 7.4 G 23 Oct 79 4 척산 -9.0 -6 2. 3 10. 3 7.1 S 31 Oct 79 5 오색 -1 0. 1 -7 0.7 10. 1 7.3 S 1 Nov 79 6 강릉 -7 .6 -54 .3 6.5 7.0 G 1 Nov 79 7 둔내 -7.9 -61. 3 1.9 6.9G 1 Nov 79 8 여주 -6.5 -50.5 1.5 6.7 G 6 Nov 79 9 이천 -7.2 -50.5 7.6 6.8 G 27 Oct 79 .10 제천 -6 .3 -53.2 -2 .8 7.lG 6 Nov 79 11 신예미광산 -9.4 -65.0 10. 2 6.8 G 5 Nov 79 12 연화(II)광산 -9 .2 -65.6 8.0 7.l G 29 Oct 79 13 장군광산 -8.9 -64.6 6.6 7.2G 15 Jul 80 14 덕구 -8 .7 -6 4. 1 5.5 7.8 S 19 Jul 80 15 운흥리 -9.0 -62.0 10. 0 -T Jul 81 16 소백산 -10.3 -72.7 9.7 7.5 G 4 Oct 82 17 수안보 -7.7 一 59.8 1.8 6.9 S 26 Oct 79 18 00 기;;x.- -7 .5 -5 7.3 2.7 -G 14 Jul 80 2109 백암 -—85.. 45 一 6 1. 7 5.5 7.0 S 30 Oct 79 오1... oO } -40.3 3.7 7.l S 24 Oct 79 21 덕산 -6.2 -42. 7 6.9 7.5 S 24 Oct 79 2223 도죽고암 휴게소 -—67 ..14 --4493..22 150..6 0 77..4l GS 24 OJcutl 7892 2245 대유성전 고속버스터미널 -—76..69 --5407..83 107..90 76..53 GS 26 OJcutl 8729 26 금강휴게소 -7.3 -48.4 10.0 7.lG Jul 82 27 부여 一 7 . 5 -52.0 8.0 7.lG Jul 82 28 추풍령 -5.0 -43.3 一 3 . 3 7.4 G 17 Jul 82 29 포항(운흥동) -7.7 -50.5 11. 1 7.0 30 Oc t 79 30 포항시 -7.2 -47.6 10.0 7.2G 17 Jul 82 31 전주시 진북동 -6.0 -42.2 5.8 7.7G 20 Jun 82
32 대구시 동인동 l 75726-59 84. 989 85665.12 5 2575.68G4 7079 06Ju56l 8162 8 32A 대구시 경대교 _-4 7.6 10. 0 7.7 S 18 Oct 81 3343 정지읍리 산 노고단 ____ --64 71.. 62 170.. 06 67..34 GG 2232 FJeubl 8822 35 지리산 천왕봉 -66.3 12. 1 6.3 G 26 Jul 82 36 부곡 -43.5 1.3 7.3G 29 Oct 79 37 마금산 _ -43.6 5.2 7.2 S 29 Oct 79 38 동래 _-41. 7 -0.1 6.8S 30 Oct 79 39 해운대 一_-3 9.5 4.5 6.8S 30 Oct 79 40 구례역 __ -45.0 6.2 7.3 G 23 Jul 82 41 진주시시의버스터미널 -4 9. 6 6.4 7.8 G 8 Jul 82 42 전남광주시의버스터미널 -44. 6 11.4 7.8 G 23 Feb 82 43 순천 I-4 5. 6 6.4 7.7G 23 Feb 82 44 남해 ll -42.1 6.7 7.8 G 8 Jan 82 45 제주시 -4 3.7 10.7 7.lG 5 Nov 79 G, 지하수 . s, 지표수. T, 열수.
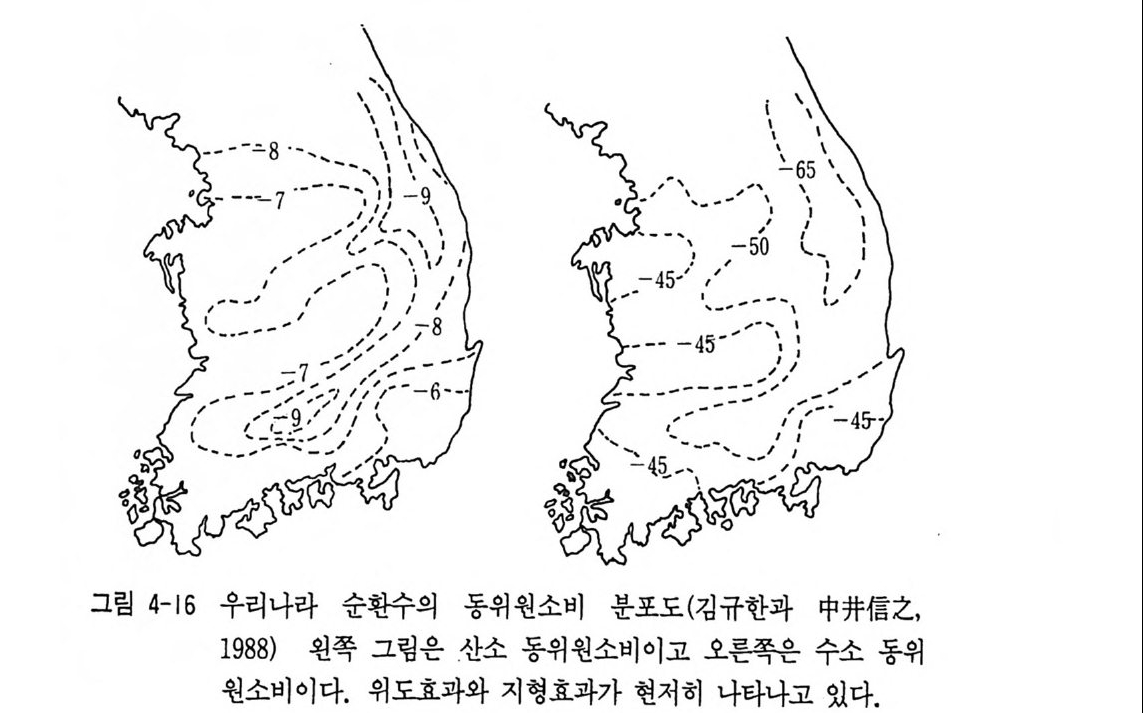 •\I / ~r-',`:I-,-.~-. - --- --·, -,,---근,. =I,- -러로 .I, 2-'-:, ,.,8一,-,z ,/,9. ·.` ,,,-1'- -’,적z,, .`,-.',,, ,, /.,/` - ,/ ;' ',-. -, ’.`/ I ,/. ,I~,.,`,', & I, I,,/`-,I ,,` . ., \ ,/,,,,` ’\ -). I`',‘`/ t,`\ / ,’;!I`,r ’'<. I- /I \-\ ,.、 ,,-.``’ : \·.,-I \ 9- 8 ' \6` , I II_' • ,- I -_,’ . . . -P`-’_`-`t-、,.- `~t-1t、- -?2:,tt ,`_- , : _2 ’-- ` ,`i`-5```4` I_0\\\ 5J,- 5/,\5I-,.`6' _-\``Ir,-4,,' -I_, : J}, /`.I ', ',',,I2,,I -/ ; I -:
•\I / ~r-',`:I-,-.~-. - --- --·, -,,---근,. =I,- -러로 .I, 2-'-:, ,.,8一,-,z ,/,9. ·.` ,,,-1'- -’,적z,, .`,-.',,, ,, /.,/` - ,/ ;' ',-. -, ’.`/ I ,/. ,I~,.,`,', & I, I,,/`-,I ,,` . ., \ ,/,,,,` ’\ -). I`',‘`/ t,`\ / ,’;!I`,r ’'<. I- /I \-\ ,.、 ,,-.``’ : \·.,-I \ 9- 8 ' \6` , I II_' • ,- I -_,’ . . . -P`-’_`-`t-、,.- `~t-1t、- -?2:,tt ,`_- , : _2 ’-- ` ,`i`-5```4` I_0\\\ 5J,- 5/,\5I-,.`6' _-\``Ir,-4,,' -I_, : J}, /`.I ', ',',,I2,,I -/ ; I -:
198 1. 6~1982.5 까지 서울의 강수 및 눈의 안정동위원소 성분 8180 == — l.0~ — 18.3%,, 8D = + 4.9 ~ — 14.1%, 로 넓은 변화폭을 나타내 고 있다(표 4-5).
표 4-5 우리나라 강수의 동위원소 성분 (김규한과 中井 信 之, 1988) 시번료호 시료채취일 채취장소 018 0 % , 8D% d PH 1 12 Jun 1981 서울 방배동 R -5.0 -32.9 7.1 4.5 2 1 Jul 1981 서울 이화여자대학 R -10.5 -75.3 8.7 6.3 3 25 Aug 1981 서울 이화여자대학 R —9 .7 -61. 7 15. 9 6.5 4 31 Aug 1981 서울 이화여자대학 R -8.8 -6 5. 0 5.4 6.5 5 24 Sep t 1981 서울 이화여자대학 R -18.3 -1 41 .1 5.0 6.4 6 18 Oct 1981 대구시 경북대학교 R -8.8 -43.3 21. 0 6.5 7 9 Nov 1981 서울 이화여자대학 S -10.6 -4 9. 3 30. 3 5.5 8 12 Nov 1981 서울 이화여자대학 R -13.8 -24.3 12. 7 6.3 9 15 Nov 1981 서울 이화여자대학 R -8.6 +2 .3 23.2 9.9 10 1 Dec 1981 서울 이화여자대학 S -12.5 -33.9 47. 3 5.5 10(A) 16 Dec 1981 서울 이화여자대학 S -9.4 -65.2 10. 0 4.7 1111143512 111144998 FFFDJeeeaebbnbc 11111999998888822221 서서서강강울울울원원 도도이이이 화화대화설 여여악여관자령자자산 대대대 학학학 SsSSs --1-1—-66611.....7580 6 —-——1 6+241 44426.....29870 212136790.....69 809 66465.....11087 16 4Mar1982 서울 이화여자대학 R -6.2 -24.1 25.5 4.7 17 15Mar1982 서울 이화여자대학 R -5.7 —3 5.0 10.6 6.5 18 30Mar1982 서울 이화여자대학 R -6.5 _4l.l 10.9 5.5 19 6 May 1982 서울 이화여자대학 R -6.0 -43.3 4.7 5.3 20 3 May- 19 82 서울 이화여자대학 R -7.7 -49.3 12. 3 6.5 21 13May l 982 서울 이화여자대학 R -2.7 -24.3 —2 .7 6.7 22 19May 1 982 서울 이화여자대학 R -1.0 +2.3 5.7 5.9 222354 3891 MJTaaann y 111 999888222 서제제 주울주도 도이 화여자대학 sRs ---466...301 --—413 073...395 -31100...5 11 446...461 d = 8D - 88180. R, 강수. s, 눈. *oD 값은 oD = 80180 + 10 식에서 계산된 값임.
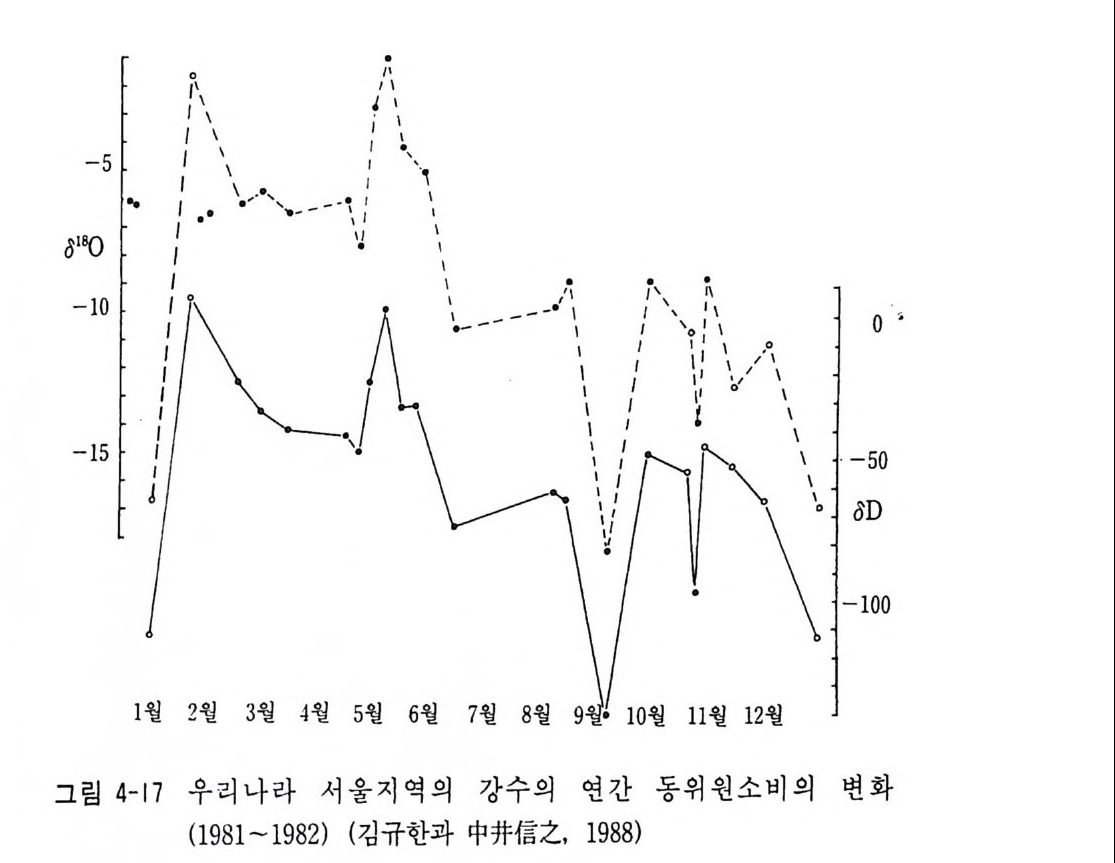 •III`
•III`
이 값들은 대다수 순환수 선에 도시되고 계절변화에 따라 동위원소 값이 변화하나 강수를 일으킨 기단의 종류에 영향을 받아 변화시기가 약간 전이되며 6 월경에 변화가 일어나고 있다(그림 4-17). 9) 한강수의 동위 원소 성분 변화 나까이 의 (1982) 에 의하여 한강유역의 생태계에 관한 환경동태 연 구 일환으로 한강의 수질변화에 관한 지구화학적 연구가 수행되었다. 1980 년 11 월과 1981 년 5 월, 2 차에 걸쳐 남한강과 북한강의 24 개소 에서 채취된 시료에 대하여 산소(성8()) 수소 (8D) 동위원소비 분석과 용존 sm- 의 황 동위원소비와 산소 동위원소비가 분석되었다.
남한강과 북한강은 수원지가 다르므로 상류에서 하류로 감에 따라 하천수의 산소와 수소 동위원소비의 변화가 뚜렷이 나타나고 있다(그 림 4-18).
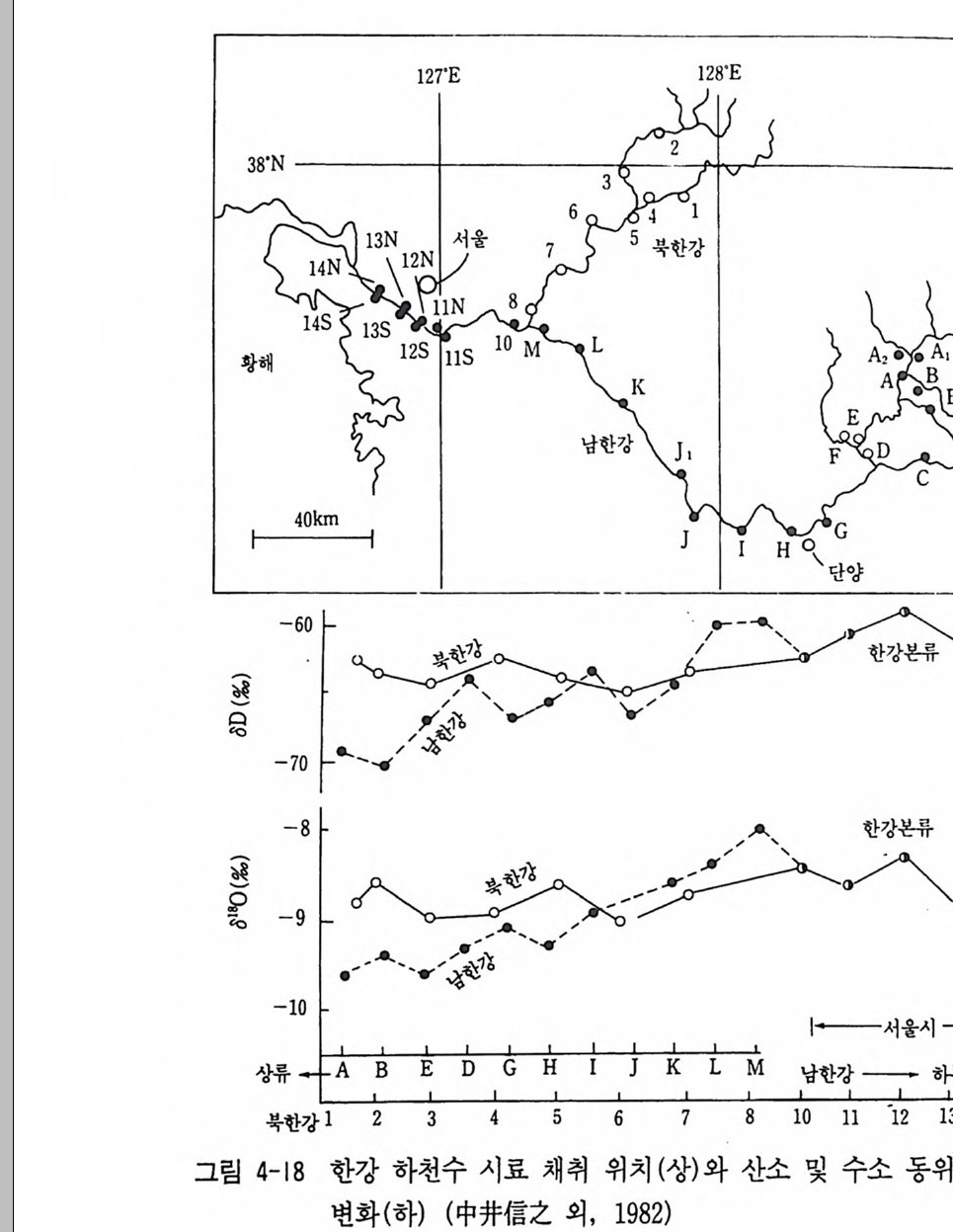 !27 'E 128 E
!27 'E 128 E
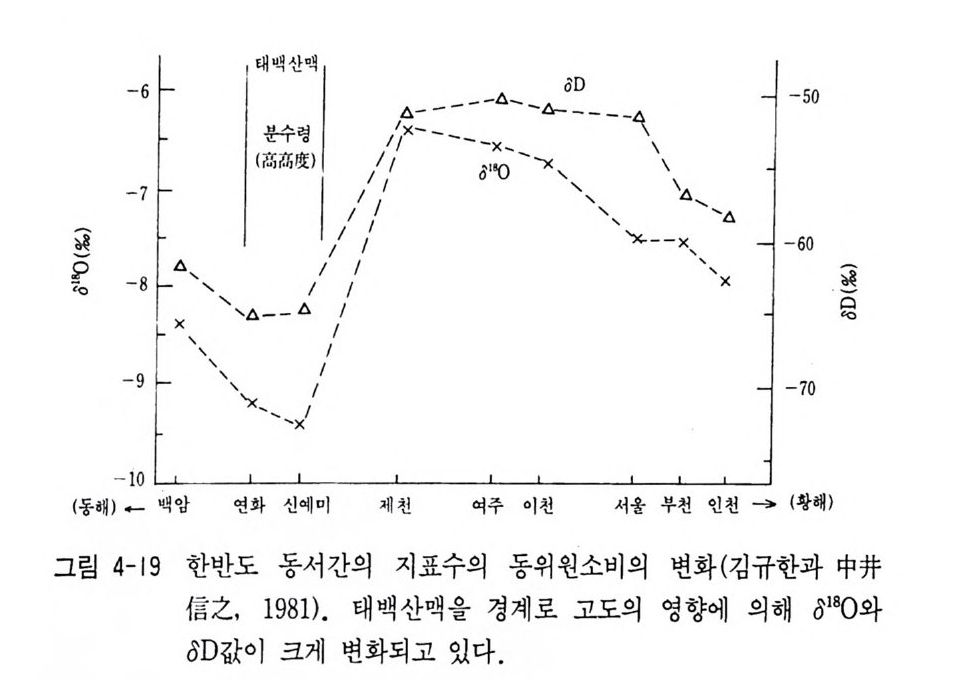 9P)~(려 ---786 소x \\ \\\`\' A \ 태璃」 一店백i X如팹령A/ / I1 /I// / I /,II'I I/ I/I IAX / - l -I- -I I섬 tl A Ll DI lF4\ `oD l \ l\_4\\\ \\ A-、- x `x`A` ` x -- 56 00 (려)gd
9P)~(려 ---786 소x \\ \\\`\' A \ 태璃」 一店백i X如팹령A/ / I1 /I// / I /,II'I I/ I/I IAX / - l -I- -I I섬 tl A Ll DI lF4\ `oD l \ l\_4\\\ \\ A-、- x `x`A` ` x -- 56 00 (려)gd
상류에서 남한강보다 북한강 유역 이 0180, oD 값이 적 어 가벼운 물이 존재하고 있음을 알 수 있다. 하류로 감에 따라 북한강은 변화 가 없으나 남한강은 변화가 심하다. 이 같은 원인은 한반도의 동서간 의 동위원소값의 변화에서 보여지듯이(그림 4-19) 남한강은 태백산맥 의 높은 위치의 가벼운 물을 수원으로 하고 있는 반면, 북한강은 고 도차가 별로 없는 수원지의 물이 유입되기 때문이다. 단양-양수리간 의 남한강의 물의 180 부화된 현상은 석회암과 황화물광상 분포와 같 은 부근 지질을 잘 반영하고 있다(나까이 의, 1982). 용존 HCO i의 농도도 북한강에 비하여 남한강이 현저하게 높게 나타나고 있어 이룰 잘 뒷받침해 주고 있다. 용존 황산염 (SO t)의 황과 산소 동위원소비 분석에서도 상류 (A, C 지 접); 84s = — 7~+ 11%,, 0180 = -2 ~ + 5%,, 중류지역 (G, 10 지점); r•s = + 3~ + 5 盆 8180 = 2 給, 서울시내를 포함한 하류한강 분류 지역 (llN, 14N 지점); r•s = + 3~ + 4%,, 0180 = + 5~ + 6%, 로
구분되고 있다. 상류에서는 탄광이나 텅스텐 등 금속광상의 황화광물에서 유입되기 때문에 동위원소값의 변화가 크다. 그러나 중류인 단양에서 서울에 이르기까지는 비교적 값의 변화가 적어 주위에서 새로운 공급원이 없 이 상류에서 유입된 기원이 혼합된 혼합물로 생각된다. 서울시내에 들어와서는 SO t의 황 동위원소는 일정하게 유지되나 산소 동위원소 는 변화되고 있어 생활하수에 의한 기여가 큰 것으로 나타나고 있다. 서울시내에서 들어와서는 그 의 인공오영의 영향으로 c1- , Na+, NHt 등의 함량이 크게 증가하고 있음이 조사되었다. 10) 우리 나라 온천수의 동위 원소 성분 우리나라의 온천은 60 개소로 알려져 있고 그 중 남한에서는 15 개소 가 알려져 있다. 온천의 온도는 황해도 마산온천이 102 · c 로 가장 높 으며 남한에서는 경남 영산에 있는 부곡온천이 67~70 ° C 로 가장 높 다. 대부분의 온천은 40~6o·c 내이며 25°C 내의의 온천도 있다. 온천은 대부분 화강암류의 분포와 밀접한 관련이 있다. 온천수의 기결과원 연0구180를 = 위 -해 6서. 5~온 천_ 수10와.7 %온 c,,천 o지D역 =의 - 지 3하9.수5~의 —동7위0 .7원%소, 를범 위분가석 한얻 어졌다(표 4-6), 온천수는 대부분 순환수 선 (Mete o ric wate r line ) 상에 도시 되 었으며 일반적으로 열수환경이나 지열지역에서 알려진 산소편이 현상은 나타 나지 않고 오히려 온천수의 동위원소값보다 그 지역의 지하수의 동위 원소값이 더 무거운 특징이 나타났다(그림 4-9), 이 같은 산소편이의 반대현상에서 남한의 온천수의 기원은 모두 순 환수 기원이며 온천수를 만든 지하수가 더욱 고위도에서 고도가 더 높은 지역에서 유입된 것으로 해석되었다(김규한과 나까이, 1981). 온천수의 동위원소 특칭은 위도효과와 지형의 효과를 잘 반영해 주 고 있다. 온천수의 동위원소 성분, PH, 화학성분 및 지리적인 분포
료시취채일 .O39 c71 t . c9 137O. t. .v.No17 9 c7. 7O9 2 .t .Oc7927 .t .62 cO 79t. .24Oc7 9t. .429Oc7 t. 4.cO 97 2 t. 42 Oc 97. t. 2.cO 976 t. 3Oc79 . 0 t. 30Oc79 .t . 30. Oc79 . t 92Oc 79 . .t 29 .Oc7 9 t. 30Oc7 . 9 t. 3Oc . 709 t. J8019u . l. 791oN ..v aNa1 1)k, i89 과mi 표수지 0O)s1(%. D%o( .) S(WW)O S(MO )M- 90.3.2 -6 .-09 -263. 11- .070-. 7 7·.- 2-5 05. -1 7.-5.65 -77. 一.895 -.24 7一61. -6 1.-32. 4 -. 164-3.2 5- 5.4-0.3 -6 .9 4-73. -8 .46 -1.7 -7 7.5 -0.5 5- .64 -35. .16-.4-36 5_ .5.53 -9 .25- 47. -1 .78- 6.-41 4.9- 5.-96 K비( Hp 7 .17 7.71 37.0 806 .8 6.8 05. 7 0 74. .0 47 0.7 7 5.0 6 .070 0.0 7 72. 6 5.17 8 .76 9 .76 70 .8.527
소원) 동의수지 표위◄(SO%,!성s- C(TD) 6+0 1. 8 .+2 21+ .9 . 3+1J 6+.5 5 5. + 5 7. +923. + 21.4+ 14.8+ 20.3+ 4.6+1 천수온와 역의천온지수천온 %)o(o8D섬(( ))%, OM SW)(WO(M)S3 -.9649-. -92. .651一 . 7-10.837一— -83.. 547 - 4.9.4·76- - 18.-5.29 - 5.68-4. 7— 5-3. 9 2.7-7 .7-58.0 -8.1-85.3 -- 967..0 9 6-7.2 — 9 .8-8 .7-5 5.9 85 -9.2-.9 7-5- 5.6.0 7- .42.1-5 7.5-5 -0.0 9.9--6 8.9 —.2-8 521 2. 4-6 표우나라리 Hp(C십 온·도)도( m) 08.3 300 8 5.638.0 308 056. 013.81 0. 2.8 50. 2083 2 490.8.0 04 84. 08028.7 2 04.30 72 6. .257 .55 002 084 9.508 .28 8. 84 0.02.208 9 .940 410 3.0 027.69 630-180 0 7.9.88 04527 0. .77552 5.5 0.5326 56.315 75. 00 0 .19 (.04) 0 ? 65 .7 위치 척 산설척산(악) 색오이 천 보안수 덕산 도고 온양유 성 백암 항포부 곡 산금마 대해운동 래 덕구오색산탄수하지*수에서 ® 백암형 온천 ® 온양형 온천 ® 해운대형 온천으로 분류되었다. 백암 온천형은 온천수의 동위원소 성분이 0180 = -9 .2 ~ _ 10. 6 %,, oD = -6 4.9~_ 73 . 8 앓이고 PH 는 8.1~9.4 이다. 한반도 중동 부에 분포하고 있는 오색, 척산, 덕구, 수안보 온천 등이 여기에 속 한다. 온양 온천형은 온천수의 동위원소 성분 0180 = -7 .2 ~ -8.3%,, oD = ― 53 . 9~_59 . 2%, 이며 약 알카리 내지 알카리성 온천이다. 온 천수 중의 Na+, c1-, sm-함 유량이 적고 F 이 많다. 한반도의 중서 부에해 운분대포 온하천는형 덕은산 ,한 반유성도, 동 이남천부 에온 천분 포등하이며 여0기18에0 =속 —한7다..0 ~_ 8 .7 % ,, PoDH == -65.505. ~5 ~7 ―.7 559 이 . 다9%., 로온 천가수장의 무용거존운성 분동 중위 원K소+ , 로 N a되+, 어C a2+있, ,으, c며i-, SOt 등의 함유량이 높으며 부곡, 포항, 해운대, 동래, 마금산 온천 등이 여기에 속한다. 온천수의 동위원소 특성에서 우리나라의 온천수는 모두 순환수 기 원이며 물-암석 상호반응이 거의 일어나지 않았거나 온천수를 만든 지하수가 지하수계에서 순환속도가 빨랐음을 추정할 수 있다. cl-p ar amete r (d = oD —8 0180) 값이 지 하수, 강수, 지 표수의 트레 이서 (tr acer) 로 함양원, 기단의 특성 및 지하수계 연구에 유용함이 연 구되었다. 우리나라의 경우 강수의 기단 특성 때문에 cl- p arame t er 값도 여름 -겨울에 따라 변화하고 있다. 일본의 경우 강수현상을 cl- p arame t er 로 구별하여 설명하고 있는데 동해안 쪽의 20
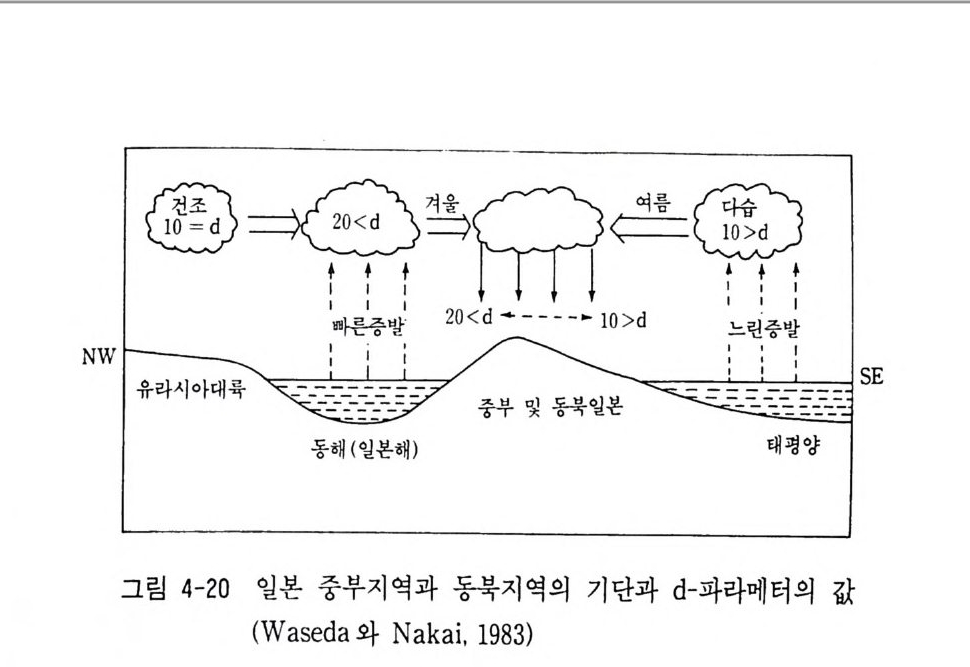 @ \ [ 二
@ \ [ 二
4-4 암석권에서의 산소 및 수소 안정동위원소 수권, 대기권, 생물권, 암석권의 각권 사이에 물질의 순환, 에너지 의 이동을 통하여 지 질학적 , 지구화학적 과정이 일어나고 있다. 특히 암석권내에서의 마그마의 형성, 속성작용, 변성작용을 통하여 이들 구성원소의 동위원 소 의 조성이 재분배되어 동위원소비를 트레이서로 이용한 물 질 의 기원 규명 , 지질학점 과정의 물리화학적 조건 해석 등 이 이루어지고 있다. 지질현상 중에 물-암석 상호반웅이 정량화되고 베니오프대에서의 물질의 혼합, 지각과 맨틀에서의 동위원소 성분의 진화가 설명되고 있다. 암석권의 대표적인 구성원인 화성암, 되적암, 변성암의 안정동위원소 특성은 다음과 같다. 1) 화성암의 안정동위원소 화성암은 화산암, 반심성암과 심성암으로 구분된다. 1960 년대 말부 터 암석 및 규산염광물의 산소 및 수소 동위원소비 분석이 암석성인 연구에 유용한 수단이 되고 있다. 화산 활동시에 유출되는 화산가스
의 동위원소 화학성분에서 마그마 챔버의 물리화학적 조건을 해석할 수도 있다. 화성암의 동위원소 성분은 마그마의 기원, 마그마의 혼 합, 주위물질에 의한 마그마의 동화 등 마그마의 성인과 광물의 정출 온도와 같은 생성환경 그리고 지각과 맨틀의 구성물질 등의 연구에 중요한 정보를 주고 있다. 먼저 주요한 화성암류의 동위원소 성분 분포를 다루고, 다음에 마 그마의 생성, 진화, 결정화 작용 동안의 산소 및 수소 동위원소 변화 를 일으키는 중요한 과정을 소개하고자 한다. 최근 점증되는 암석과 광물의 818O 와 oD 분석자료는 기타 미 량원소, REE, 지 화학적 , 암석 학적 자료와 함께 ® 중요한 화성암의 현상을 설명하는 최적의 지질 학적 상황을 규명하고 ® 특수한 암석학적 상황을 이해하고 ® 여러 다마양그한마 화의성 암동의위 원발소달 전성화분를은 설 8명18하0 는= 데— 2이~ 용 +되 1고6% ,있, 다 .oD = 一 200~ —30% , 정도로 변화폭이 크다. 그러면 이 같은 동위원소바의 변화는 왜 생기는 것일까? 마그마의 분화시 oD 와 a180 의 변화와 함께 화학성분, 미 량원소, 기타 동위원소 성분도 변화한다. 화성암연구에 산소 및 수소 안정동 위원소 응용연구가 화성암화 과정을 해석하는 데 크게 도움을 주고 있다. 화성암의 동위원소비의 다양성은 주로 이차적인 원인으로 생각 되고 있으며, 열수작용 영향, 저온의 수화반응 그리고 풍화와 같은 固相線 아래에서 일어나는 과정이 중요한 의미를 가지고 있다. 특히 화성암에 있어서의 고상선 아래에서 일어나는 과정의 복잡성과 중요 성을 인식하게 된 것이 안정동위원소 연구의 큰 성과이다. 화성암화 과정연구에서의 동위원소 응용의 이해를 돕기 위해 다음 과 같은 관점에서 다루어 보고자 한다. ® 화성암의 산소 및 수소 동위원소 성분 ® 원시기원 물질의 동위원소비
® 마그마 결정작용시 폐쇄계의 효과 ® 마그마 결정작용시 개방계의 효과 ® 물-암석 상호반웅 ® 스케어가아드 관입암체의 안정동위원소비 @ 산소 및 스트론튬 동위원소와 암석성인 ® 우리나라의 화성암류의 동위원소성분 ® 반암동광상에서의 산소 및 수소 동위원소비 ® 우리나라 금속광상의 동위원소 성분 (1) 화성암의 산소 및 수소동위원소 성분 화성 암의 산소 및 수소 동위 원소비 변화는 그림 4-21 과 4-22 와 같 다. 운석, 초염기성암과 화산암의 산소 동위원소 성분은 비교적 균일 하나 화강암 저반의 화강암류나 변성암류는 물-암석 상호반웅 등의 변질작용과 변성작용 등에 의해 동위원소값의 변화가 크다. 화성암울 구성하고 있는 조암광물 사이에 180 부화의 규칙성이 존 재한다. 죽 석영, 알카리장석, 사장석, 백운모, 아놀사이트, 휘석, 각섬석, 감람석, 혹운모, 자철석 등의 순으로 180 이 낮아진다 (Ep s t e i n 과 Tayl o r, 1961) . 이 같은 현상은 결정구조와 관련이 있으며 Si- 0 -Si (1 80 이 많고) Si -0-M g와 Si- 0 -Fe (2%. 정도 적은 180 롤 함유) Si- 0 -Al (4%. 정도 적 은 18O 를 가짐) 결정구조에 따라 180 의 부화 정도가 다르다 (Garl ic k, 1966 ; O'Ne il 과 Tayl o r, 1967). 따라서 화성암에서 S i 02 의 함량이 증가 할수록 암석의 01so 값이 증가하여 초염기성암(+ 5.4 ~ + 6 . 6%,) 에서 화강암, 페그마타이트(+ 7 ~ + 13%,) 에 이른다. 그립 4-21 과 4-22 에서 보면 지구상의 대부분의 화성암의 동위원소 성분이 0180 = + 5.5~ + ll% 와 oD = —5 0~ _ 95%, 의 분포를 가 진다. 이 범위 밖에 도시되는 시료는 화성암의 생성사나 형성과정이 다른 경우일 것이다.
 운석류
운석류
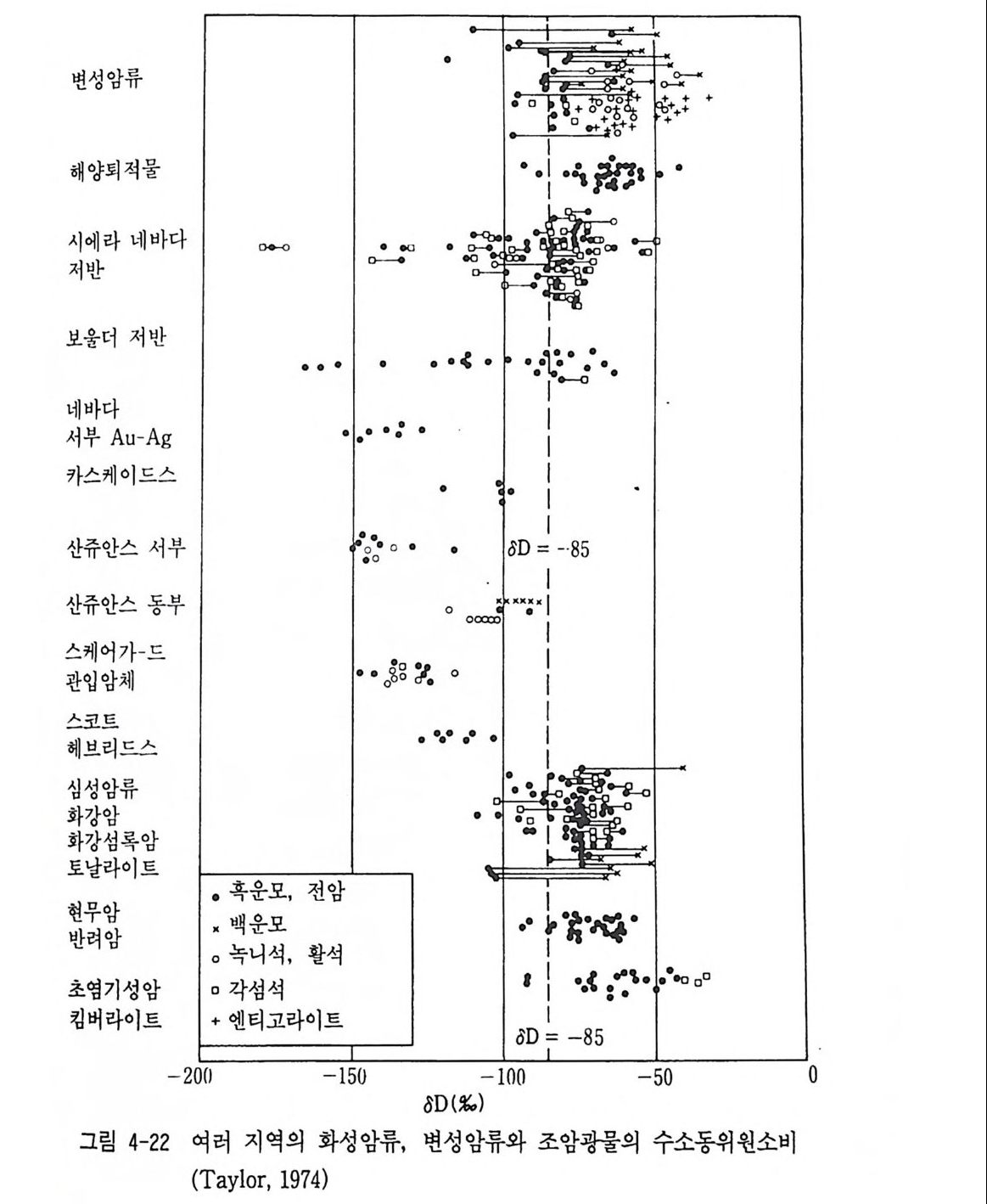 •
•
그리고 8D(-95 %,) 와 0180( < 5.0%, )의 값이 낮은 시료들은 주로 고 상선하의 순환수 기원의 열수변질을 받는 시료이다. Tayl o r 0977, 1978) 의 동위 원소 분석 자료를 보면 화강암질 암석 의 산소 동위원소 성분에 따라 ® 180 값이 보통인 화강암류 (8180 값이 6 %와 10%, 사이) ® 180 값이 높은 화강암류 (8180 값이 l0% 이상) @ 180 값이 낮은 화강암류 (0180 값이 6%, 이하)로 구분할 수 있다. 『 0 값이 6%, 에서 l0% 내 외 의 화강암류가 가장 많으며 이 중 6%, 부근의 180 이 결핍 되 어 8180 값이 낮은 화강암류는 대 륙지 각이 존재 하 지 않는 호상열도(예 : 과달케널 ‘Guadal canal’ 의 콜로우로 화강암 복합 체)에서 산출된 것이다 (Ch i vas 등, 1982). 이는 맨틀기원으로 생각된다. 하부 지각물질이 부분용융되어 형성된 화강암질 암석에서 도 성만 값이 낮다. 그리고 10%, 내의의 180 이 많이 함유된 화강암류는 퇴적 암이나 화산암 물질이 함유된 지각 물질이 부분용융된 것으로 보고 있다. 한편 8180 값이 l0% 이 상인 화강암류는 180 값이 높은 퇴 적 암이나 변성암류의 무 분 g . 산물일 것이다. 예를 들면 히말라야 지역의 화 강암류 (Blattn e r 등, 1983) , 스코틀랜드의 칼레 도니 아 화강암류 (Hallida y 등, 1980) 그리고 유럽 서부의 헤르시니안 화강암류 (M ic hard Vit rac 등, 1980) 등이 있다. 그러나 6%, 이하의 낮은 a1so 값을 가지는 화강암류는 현무암질 마 그마의 분화산물로 보기는 어렵다. 아마 그런 화강암류는 고상선 이 하 조건에서 180 이 결핍된 순환수 기원의 열수용액과 동위원소 교환 때문일 것이다. 물론 아이슬란드에서처럼 예의로 8180 가 낮은 마그마가 존재하기 도 한다. 이같이 180 이 결핍된 마그마에서 정출되거나 물이 우세한 계내에서 형성된 화강암 마그마에서 가능할 수도 있다• 아이슬란드 (Ha tt o ri와 Muehlenbachs, 1982), 네바다(Lip man 과 Fried man, 1975), 옐로우스톤 (H il dre th 등, 1984) 등에서 이 갇은 예가 관찰된다. 우리
나라의 경우 거제도의 화강암의 0180 값이 + 2.4%, 로 대단히 가벼운 값이 얻어졌다(김규한 등, 1990). 이는 거제도의 화강암질 마그마의 형성시 180 이 결핍된 순환수나 해수의 영향을 생각해 봉 수 있다. 일반적으로 1 8 0 이 결핍된 화강암 은 어느 경우에서나 마그마 챔버의 상부에서 180 이 결핍된 모암과의 반응에 의해 만들어질 수도 있다. 에크로자이트나 오피오라이트와 같은 열수변질을 받은 해양지각의 암석은 동위원 소 비에서 서로 유사성이 있다. 지금까 지 화성암의 산소 동위원소 분석연구에서 얻어진 일반적인 결과는 다음과 같 다. ® 해양지각에서의 대부분의 유문암질 흑요석은 현무암, 반려암, 섬장암, 안 산 암의 818 0 값과 유사하다. 이들은 고온에서 현무암질 또 는 안산암 질 마그마에서 분화된 시알지각의 용융물과는 다르다. 그러 나 대륙 내부에서 산출 되는 일부 혹요석은 대륙지각 물질과 동화되어 대륙지각 물 질 의 동위원소값과 유사한 높은 성한값을 갖는다. ® 심성암인 화강암류는 상응하는 화산암류에 비해 180 함량이 높 다. 왜냐하면 기원물질이 180 함량이 풍부한 퇴적암 성분을 함유하였 거나 저온에서 분화되었기 때문이다. ® S i 0 가 풍부한 분화물들의 81 8 0 값과 화산암 복합체의 화학성분 변화경향 사이에 상관관계가 존재한다. 1ao 이 . 높은 함량을 가지는 분 화산물들은 Fe/ M g 비가 낮아지는 경향이 있는 반면, 철질 반려암 분화는 180 이 결핍되는 경향으로 일어난다. 이때 산소 분압의 변화가 영향을 준 것 같다. 즉 초기에 자철석이 다량 정출되면 후기의 분화 산물에는 180 이 부화되고 Fe 가 결핍되기 때문이다. ® 180 이나 D 성분이 대단히 결핍된 화성암이 많이 관찰된다. 어 느 화성암이 결정될 때나 심성암이 냉각될 때에 가벼운 동위원소 성 분을 가지는 다량의 순환수와 동위원소 교환평형이 일어났기 때문이 다.
(2) 원시 기 원물질의 동위 원소비 원시 기원물질의 동위원소비를 조사하여 지구의 기원물질 및 심부 기원물질 해석연구에 응용하고 있다. 원시 기원물질 연구대상은 주로 콘드라이트와 인공위성을 통해 수집한 달의 암석 또는 토양 시료 등 이다. 원시기원 물질에 대한 산소 및 수소 동위원소비의 연구결과를 소개한다. 산소 동위원소 : 대폭발 (B ig Bang) 과정 후 우주의 원소가 수소나 헬륨에서 핵융합 과정에 의해 점점 무거운 원소가 만들어지게 되었 다. 태양계의 형성시 가벼운 원소의 동위원소의 존재도는 몇 가지의 물리화학적 과정에 의해 차이가 나타났다. 초기의 이런 과정은 저온 (T<50K) 에서 일어났으며 이로 인해 수소, 탄소, 질소 동위원소비에 큰 변화가 일어났다. 초기 태양계의 성운이 가열과정에 의해 증발 응 축이 일어나 Mg , Si 동위원소의 큰 분별을 일으키고 고체저장소와 기체저장소간에 대규모의 산소 동위원소 교환이 일어났다고 해석하였 다 (Clayt on , 1986) . 8110-i 1s o 분석에서 여러 종류의 운석의 산소 동위원소 성분과 지 구물질의 동위원소 분화선과 일치하나 CI, G,C3 탄소질 콘드라이트 등은 이와 일치하지 않아 초기 태양계의 기원물질이 균질하지 않았음 울 보여주고 있다. 그러나 지구와 달은 동일한 기원물질에서 형성되어 형성초기에 용 융과정과 균질화과정을 거쳤기 때문에 달의 8110 와 i1s o 동위원소비 는 지구의 상부멘틀의 동위원소 성분과 잘 일치하고 있다 (Cla yt on 등, 1976 ; Cla yt on 과 Maye d a, 1983 , 1984) . 오늘날 대양저 중앙해령 (MORB) 에서 형성되는 현무암은 산소 동위 원소비 (+ 5.7 士 0 . 3%,) 는 대단히 균일하다. 그리고 초염기성암도 균일 한 산소 동위원소값을 가져 지구의 상부맨틀의 8180 저장소는 대단히 균일한 값을 가지고 있었음을 말해 주고 있다. 또 달에 비해서 멘틀 의 8180 값은 변화가 다소 있는데 달에는 H20 가 없기 때문으로 생각
된다. 8180 값이 높은 퇴적암과 변성퇴적암울 포함하고 있는 대륙지 각의 평균 산소 동위원소값 (8'80 > + 7.5 % , , Sh i e th와 Schwarcz, 1977; Tayl o r, 1974) 과 비교하면 MORB 의 용암은 질량평형 계산에서 180 이 결핍되어 있음을 쉽게 알 수 있다. 지질시대에 따른 화성암의 8180 변화는 나타나지 않았다. 물론 오래된 암석은 변성 내지 변질을 받았 지만 초염기성암이나 콘드라이트 등의 분석결과를 고려하여 과거 지 질시대 중의 현무암질 마그마와 코마타이트질 초염기성 마그마의 동 위원소비 를 약 + 6.0 土 0 . 5 %, 로 추정하고 이 값을 기준으로 삼고 있다. 수소동위원소 : 지구 원시 기원물질의 D / H 비는 현재로서는 알 수 없다. 두 동위원소 사이에 퍼센트 질량차가 대단히 커서 물리화학적 과정에서 D/ H 동위원소 분별이 대단히 크게 일어난다. 운석의 경우 oD = —50 0~ + 9000%,(Yan g과 Eps t e i n , 1 983) 까지의 값을 가진다. 그러나 달은 형성초기 대부분의 휘발성분이 유실되었고 현재의 수소는 중수소 를 가지지 않는 주로 태양풍에서 유래한 것이기 때문에 달의 D/ H 자료는 별로 도움이 되지 못한다. 따라서 지구의 원시 D / H 바는 지구에서 해결되어야 할 것 같다. 오늘날 지구의 수소저장소인 수권의 oD 값은 —l0 % 정도이다. 기 타 지구의 수소는 규산영굉물- 중의 함수광물의 동위원소값이 8D = 一 40~ _ 9%, 이며 마그마 기원의 H20 값 (8D = 50~ -8 5%,) 도 이 범위에 들어간다. 따라서 현재 지구의 평균 D/H 비는 _5~ 一 20%, 정도일 것이다. 그러나 이 값이 지구의 기원물질의 값을 대표하지는 못한다. D 에 비해 상충대기에서 H의 장기적 유실이 일어나기 때문 에 질량평형 관계가 대단히 복잡하며 지질시대에 따라 수권에서의 D/H 비가 변화한다. 따라서 수권의 D/H 값은 언제나 _ 10%, 이 아 니다. 그래서 고해수의 D/H 값을 구하기 위해 노력하였지만 (Knau th과 Eps t e in , 1976) , 세 립 질의 함수광물은 쉽 게 동위 원소 교환 이 일어나 (O'Ne il과 Kharak, 1976) 수억년 지질시대 동안 보존되지 못 하므로 고해수의 D/H 값을 규명하는 데 어려움이 있다.
퇴적암 연구에서 지난 3 억 년 동안 해양의 oD 값이 크게 변화하지 않았다고 가정하면 시생대의 순환수와 오늘날의 순환수 그리고 시생 대의 순환수_열수 시스템에서 얻은 조립질 광물의 D/H 비는 서로 유사하였을 것으로 본다. 지구역사의 어느 시기에 있어서나 그 시기 의 순환수의 oD 값이 그 당시 해수의 D/H 비에 지배받기 때문에 이 사실은 대단히 중요하다. 그러면 원시 심부맨틀의 H20( - 70%. )와 전체지구의 값( 一 15~ _ 20%,) 의 차는 어떻게 설명할 것인가? 순환수 기원의 열수변질을 받은 경우 (-200 %,) 를 제의하면 기타 지 구의 화성암류, 퇴적암류, 변성암류, 오피오라이트 등 모든 암석이 oD = —40 ~ -95%, 의 범위에 들어간다. 서로 다른 종류의 암석들의 oD 값이 서로 중첩아 되는데 어떤 원인과 결과 때문일까? 이는 판구 조운동에 따른 해양저 확장으로 암석들간의 oD 값이 중첩된 것으로 설명할 수 있을 것이다. 베니오프대의 OH 함유 광물들은 해양퇴적물내에서 존재하였던 것 일 것이며 궁극적으로 이 함수광물에 의한 물은 베니오프대에 섭입 (subduct) 한 판이 뜨거워 지므로 탈수화반응에 의해 나오거 나 판이 용융될 때 만들어진 규산염 용액 속으로 흘러들어가 함몰될 수도 있 울것이다. 지질시대 중 어떤 원시 상부맨틀의 천수라도 다량의 베니오프대를 동해 유입된 물에 의해 압도당할 수 있을 것이다. 따라서 변성암 복합체내의 심부에 존재하는 해성퇴적암과 화산암류 의 재용융에 의하여 형성된 마그마의 D/H 비와 상부맨틀에서 직접 유래한 원시 마그마에 의해 형성된 마그마의 D/H 와 사이에는 동위 원소비의 차이가 없다 . 그런대 3He/4He 측정에서 일부 원시 가스가 지구의 맨틀에서 탈 가스됨을 나타내 주었다 (Cra ig과 Lup ton , 1976 ; Poreda 등, 1986 ; Kurz 등, 1982). 그러면 He 을 많이 가지는 맨틀 기원의 현무암에서 얻은
oD 값 —80 ~ _85%, (Poreda 등, 1986) 은 원시 기원의 D/ H 비일까? 이처럼 원래 D/H 의 값이 대단히 작은 사실과 현재 수권의 -10%, 의 동위원소 성분은 전 지구의 D / H 동위원소 분별결과나 초 기 휘발성분의 유실 때문일까? 지금까지의 연구결과로는 아직 원시 기원물질의 수소 동위원소비를 추정하기 어렵다. (3) 폐쇄계에서의 동위원소 분별 폐쇄계에서 동위원소 분별은 레이리 분별작용과 평형정출 작용의 과정을 생각해 볼 수 있다. 마그마의 분별정출 작용은 마그마에서 정 출된 광물이 계속적으로 제거되어 그때의 광물과 잔액의 성분차는 항 상 일정하다. 폐쇄계에서 이 관계를 적용하여 레이리 정출작용에 따 론 질량평형을 생각해 보자. 동위 원소 효과는 R / R 。 = IC - 1 으로 표현할 수 있다. 여기서 a 는 정출된 결정과 액 (멜트) 사이의 동위원소 분별정수이고 Ro 는 처음 액에서의 동위원소비, R 은 정출작용 동안의 어느 지점 f 에서의 액의 동위원소비이다. f는 잔액의 몰분율이다(죽 처음에는 1, 끝에는 0 이다). 8 의 정의로부터 1l ++ o80 /I l1000000 =- 1l000000 ++ 성8 = f(a -1) 8 엔트 = [oo 멜트 + 1000] (Ja- 1) — 1000 8 멜트 - 8 멜트 = 4 엔트 = (1000 + o0 면 트) [f(a- I) - l] 이 얻어진다. 죽 4 액( 델 트 ) 은 처음 액과 정출과정중의 임의의 어느 액과의 동위원 소값의 차이이다. 예를 들면 결정과 액간에 분별정수가 1. 001 인 경우 를 가정해 보자. 죽 결정에서 액에 180 이 더 많이 농축된 경우를 가
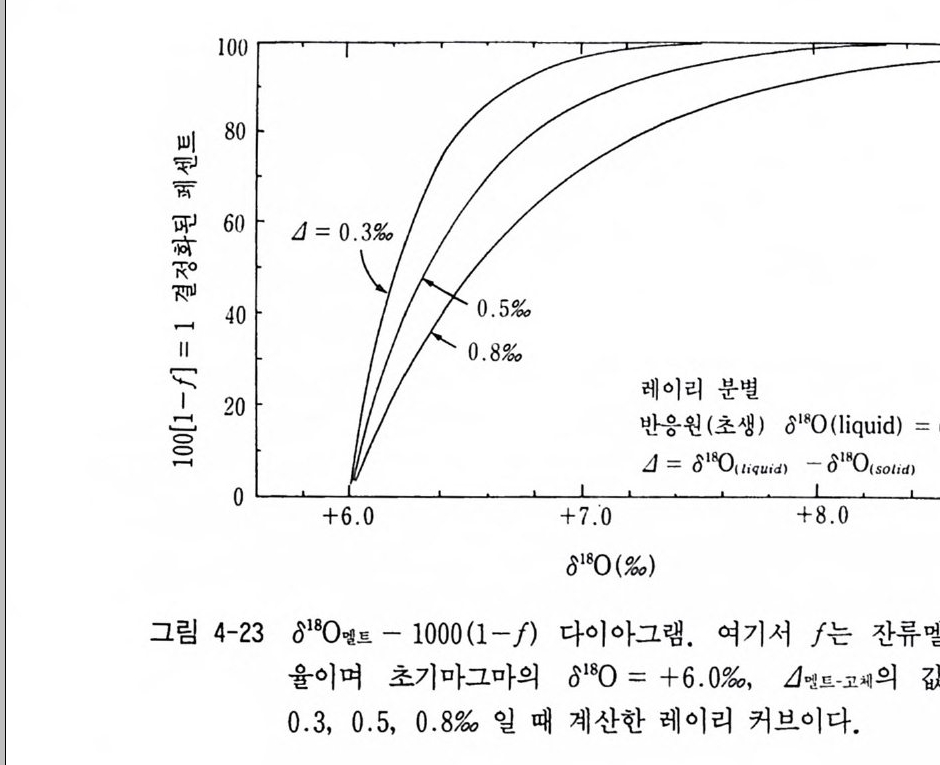 l00
l00
정하고 초기 현무암질 마그마 (0180 = + 6.0%,, f = 0.0 5 [%% 정출)) 가 연속적으로 중복되게 분별이 일어난다고 하자. 이때 각 95%, 단계 에서 8180 이 3%, 변하고 4 스테이지 후에 남은 액은 + 18%, 로 분별된 다. 그러나 실은 1. 001(% )의 값은 자연의 규산염액에는 너무 높은 값이다. 보다 근사한 값은 1. 0001 일 것이다. 이 경우 4 스테이지의 마 그마는 8180 이 1.8%, 이 될 것이다(그림 4-23). 한편 폐쇄계에서 평형정출 작용이 일어날 경우에는 레이리 효과와 다르다. 마그마 정출작용에 있어 결정과 액 사이에 1so/160 평형분 별 작용이 일어날 때, 마그마의 동위원소 성분은 각 온도에서 평형 4180 길겅적값, 결정과 액간의 고상 재평형 정도, 정출된 여러 광물의 상대적인 존재량 등에 영향을 받는다. 결정-액간에 얻어전 1so / 160 평형 실험자료가 적기 때문에 자연의
시료의 동위원소값 등을 이용하여 반정량적으로 검토하여 보았다. 예를 들면 화산분출시 화산성 유리질 물질과 공존하는 반정들은 급 냉된 것이므로 이들과 서서히 냉각된 심성암과는 크게 다를 것이다. 그림 4-24 에서처럼 저온에서 동위원소 평형을 일으킨 심성암류의 석영운모의 4180 값은 + 3.8 ~ + 8.5 %o이고, 화산회질 응회암의 경우 + 1.3 ~ + 3.2 %o로 8180 값이 작아서 심성암의 경우 순환수-열 수 용액이 존재하지 않는 곳에서도 계속적으로 고상선 아래에서 산소
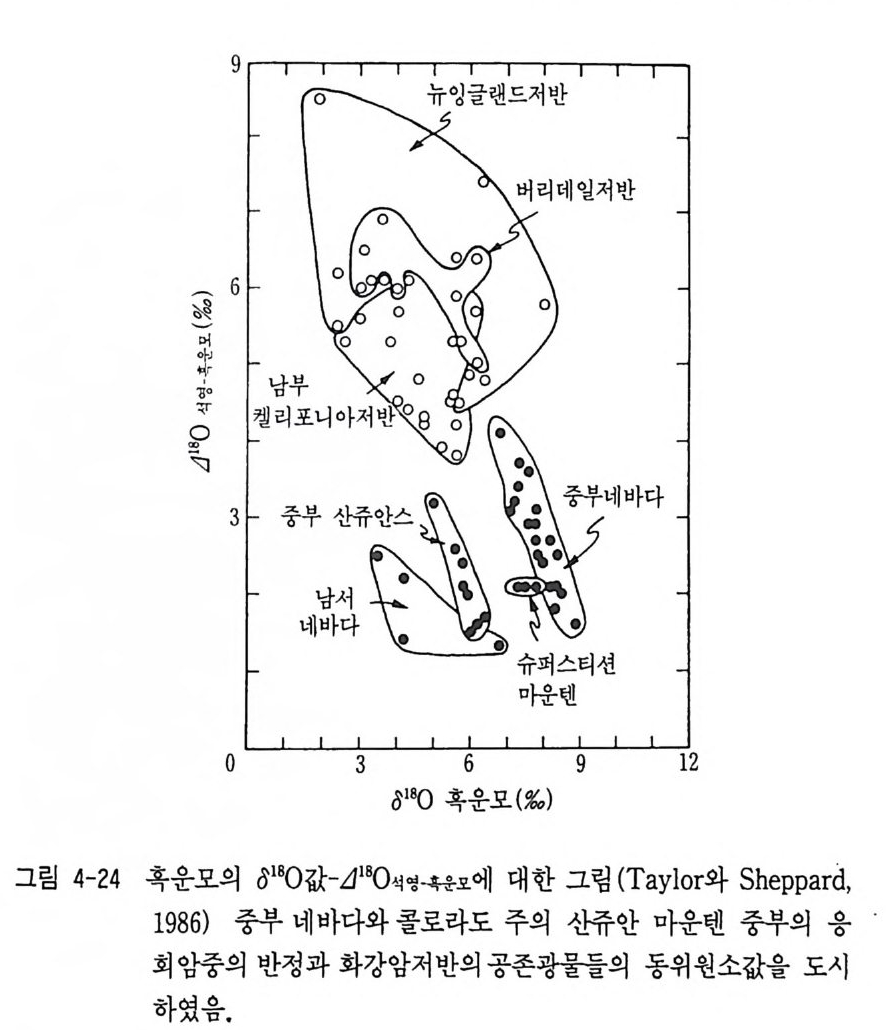 9
9
동위원소 교환아 일어났음을 잘 나타내 주고 있다. 이 그림에서 동위원소값들이 부 방향으로 나타나는 경사는 마그마 저장소로 인한 결과이다. 여러 화산암의 동위원소 분석자료에서 관찰 된 바에 의하면 조암광물에서 결정-액간의 lBQ / l6Q 분별이 보통 2%, 이하로 작고, 석영이 180 이 가장 높고, 자철석이 가장 낮다. 유 문암에서 액-사장석간의 4180 값은 + 0.1~ + 0.5 % , 정도로 변하며, 현무암에서는 -0.2~— 0.6 %, 정도로 변하고 있어 사장석의 성분변화 에 따라 성빈값이 변하고 있음을 알 수 있다. 따라서 석영 정출시에는 규산염 멜트의 180 결핍울 초래하고 자철 석, 각섬석, 흑운모 등의 정출은 공존하는 멜트의 180 를 항상 증가시 키는 결과가 된다. 이상에서 마그마의 8180 변화경향은 장석의 4180 값에 지배받는다 는 사실을 알 수 있다. S i 02 가 많은 광물에는 180 이 농집되기 때문에 마그마 챔버에 균일한 8180 값으로 동위원소 평형이 유지될 수만 있 다면 유문암질 마그마 멜트가 항상 현무암질 멜트에서 보다 180 이 많 이 농집될 것이 확실하다. 그러나 마그마 중에는 Si0 2 함량이 41~75w t%,까지 다르더라도 온 도가 goo ·c 이상이 되면 동위원소 성분은 1%, 이내의 변화밖에 일어 나지 않는다. (4) 개방계에서의 동위원소 분별 개방계에서는 물질과 에너지의 유입이 가능하므로 물질유입이 불가 능한 폐쇄계에서와는 동위원소 분별결과가 다르다. 개방계에서 일어나는 동위원소 분별과정의 한 예로 화성암체내에서 일어나는 동화작용의 영향을 들어 보자. 동화작용 (Ass imil a ti on) 은 현 무암질 마그마나 안산암질 마그마가 산성 지각물질을 포획하여 녹여 버립으로써 마그마가 화강암질로 되는 작용을 말하며 혼합작용 (Conta mina ti on ) 이 라 부르기도 한다.
Bowen(l928) 이 마그마의 분화시에 동화에 대하여 소개한 후 마그 마의 동화와 마그마의 혼합에다]하여 많이 검토하였다. 동화가 일어날 때 산소동위원소의 변화를 검토하기 위하여 Tayl o r (1980) 는 초기의 현무암질 마그마 (0180 = + 5.7%, )와 셰일 또는 편암 과 같은 모암 (0180 = 19%, )의 동화작용에 따른 분별정출 과정에서 일 어나는 산소 동위원소값의 변화를 조사하여 그림 4-25 에 나타냈다. 이들간의 질량평형 계산은 8 마그마츠 (oa-L1R) [1- f晶)]
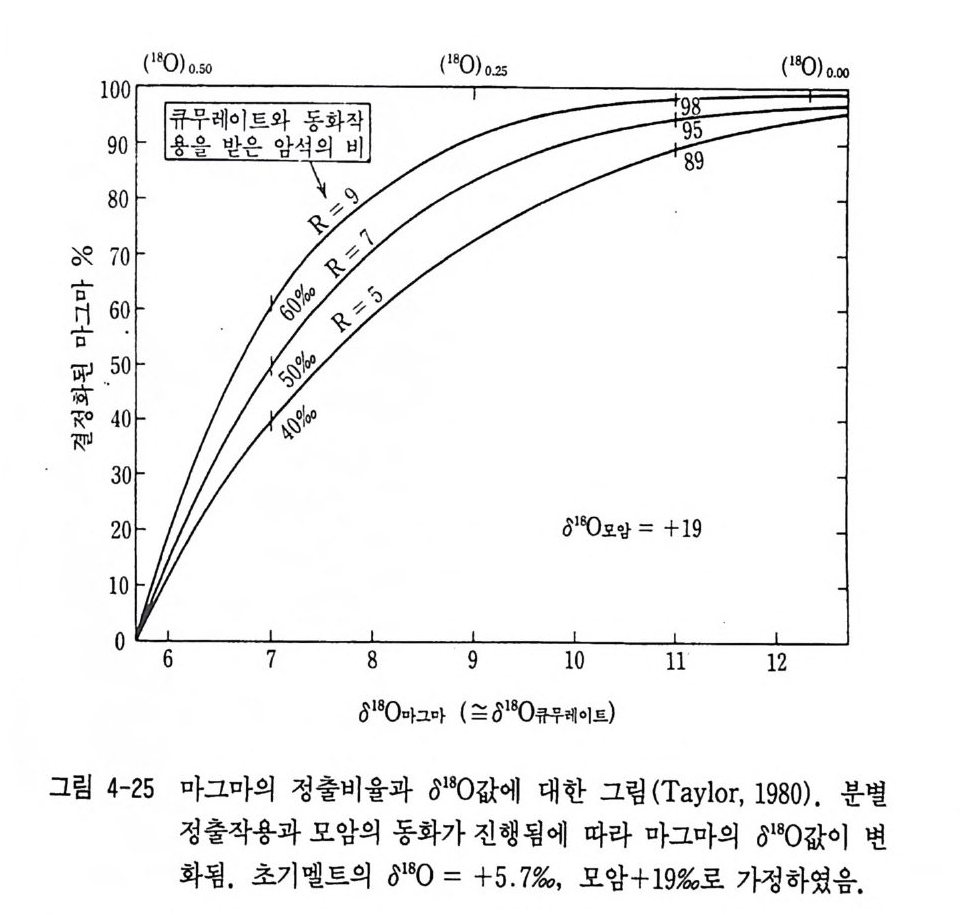 100 (1 8 0) 。 ’ so (' 8 0) 。 .25 (18 ()) 。 . 00
100 (1 8 0) 。 ’ so (' 8 0) 。 .25 (18 ()) 。 . 00
의 관계에서 계산이 된다. 여기서 8 값들은 모두 초기 01 8 0 마그아 값을 0 으로 한 값 (o o 마그아 = O) 에 서 표준화한 값이다. 8 마 그마 값은 동화작용과 분별정출작용 과정에의 임의의 스데이지에서의 마그마의 동위원소값이고 &는 동화된 모암의 동위원소값 (8180) 이다. R 은 동화된 암석과 큐무레이트 (Cumulla t e) 간 의 비이고 f는 임의의 스 테이지에서 잔류 멜트의 몰분율이다. 이처럼 동위원소 분석자료를 이용하면 동화과정과 혼합과정 을 동시 에 고려하여 정량적으로 설명할 수 있게 된다. 즉 마구마의 정 출 과정 에서 정출바, 그때의 큐무레이트나 마그마의 동위원소비 추 정 그리고 큐무레이트와 동화된 암석의 비 등을 정량적으로 계 산 추 정할 수 있 게 된다. (5) 물-암석 상호반응 Tayl o r (l974, 1977) 에 의 해 화성 암과 순환수 사이 에 상호반응이 연 구되기 시작하였다. 형성시기와 장소가 다른 여러 많은 화성암체의 산소 및 수소 동위원소값이 얻어졌다(그림 4-21 과 4-2 2 ) . 그리고 이들 암석의 전암의 동위원소비와 석영 , 장석 , 휘석 , 운모 류, 각섬석 등의 광물의 동위원소비도 동시에 분석되었다. 흑운모와 각섬석의 본래의 8D 값은 -50~-80 %, 로 대단히 변화가 적다. 이 값은 광역변성암, 해양퇴적물, 녹색암의 동위원소값과 유사 하다. 따라서 이들 화성암의 일차적인 물은 초생수가 아니고 하부지 각이 베니오프대에 섭입되어 탈수화반응이나 부분용융되어 생긴 것일 것이다. 다수의 화강암 저반의 천부 위치에서 고상선 아래에서의 동위원소 교환반응이 일어나는 동안에 국부적으로 낮은 8180 값을 갖게 되어 대규모의 순환수-열수의 대류시스템이 이루어지게 되었을 것이다. 순환수의 순환에 의한 8D 값의 저하는 K-Ar 연대측정 결과와 대비 되어 순환수-열수 순환시스템에서 Ar 유실이 일어났음을 가리켜 주
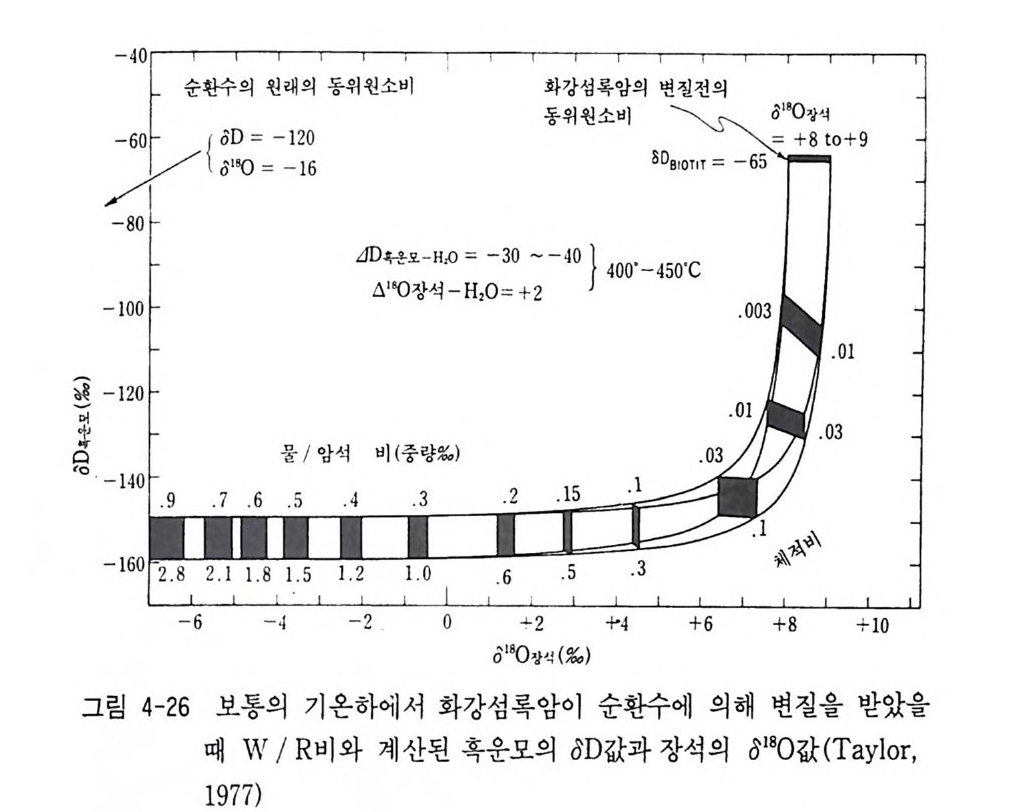 순환수의 원래의 동위원소비 화강섭록 암의 변질전의
순환수의 원래의 동위원소비 화강섭록 암의 변질전의
었다. 그림 4-26 은 대표적인 화강섬록암과 고위도 지역의 순환수 사이의 동위원소 교환을 물/암석 비의 함수로 표현한 것으로서 흑운모의 oD 와 장석의 0180 값의 변화를 나타낸 것이다. 물-암석간에 폐쇄계에서 동위원소교환이 일어날 경우 물과 암석의 비 (W/R) 에 따른 변화를 정량적으로 다음과 같이 계산할 수 있다. 『 = [ 』皮 (:-)4) ] [羅] 좀더 간단히 하면
RW: . .-_= oiW8 /-R( 」8 /iRR - L 1) 이 된다. 여기서 &W와 o i R 은 각각 동위원소 교환반응 전에 존재했던 액의 동위원소값과 암석의 동위원소값이다. 그리고 4 는 동위원소 분별정 수이며 W/R 은 암석과 액의 상대비율이다. 한편 개방계에서는 W/ R ope n = (Ci R / CiW ) In {(CiW / CiR ) (W / R) closed + 1} 의 관 계로 표현되며 좀더 간단히 하면 W I R ope n = In {(W / R) closed +1} 식으로 계산할 수 있다. 이 식을 이용하여 이론적으로 화강섬록 암이 400~450°C 의 순환수-열수용액에 의한 변질작용을 받아 동위원
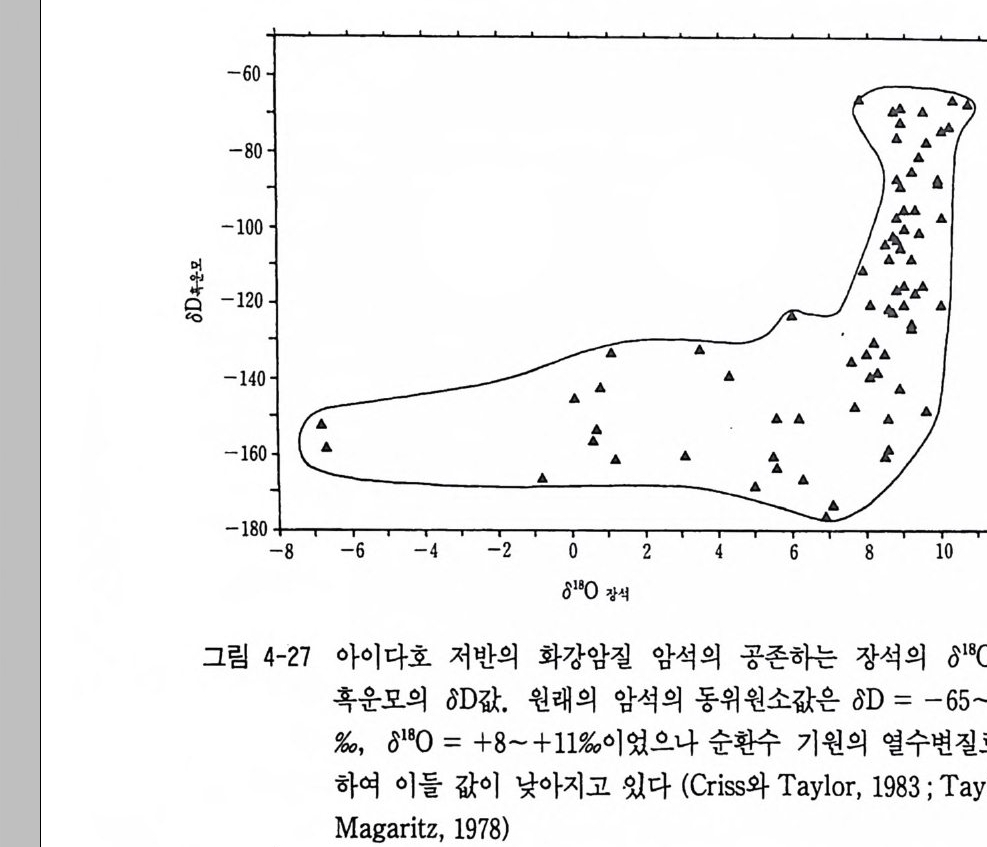 -60
-60
소 교환이 일어났다고 가정하였을 경우에 계산된 W / R 비와 흑운모 의 oD 와 장석 의 0180 값을 함께 도시 한 것 이 그림 4-27 이 다. 그림 4-26 과 4-27 에 서 보면 W / R 비 가 낮으면 암석 내 에 산소 동위 원소비의 변화에는 영향을 주지 못하나 수소의 동위원소비의 변화에 는 크게 영향을 준다. 즉 W / R 가 클 경우 암석의 0180 의 변화를 일으킨다. 이때 암석내 의 수소의 경우 이미 유체와 평형에 도달되어 있기 때문에 광물내의 수소의 동위원소비의 변화는 거의 없다. 이 같은 사실은 미국의 아이다호 저반의 화강암질 암석에서 흑운모 의 oD 와 공존하는 장 석 의 81 8 0 를 도시한 결과 그림 4-27 에서처럼 원 래의 동위원소 성분이 oD = -65~- 7 5%,, 0180 = +8~+11% 인 암 석이 순환수 - 영수 용액에 의한 변질작용을 받아 동위원소값이 점점 가벼워지는 경향으로 나타나고· 있다 (Cr i ss 와 Tayl o r, 1 983). 광산에서 의 광화작용에 수반되어 일어난 물 - 암석 상호작용에 따라 열수변질이 일어났을 때 이들 사이의 W / R 비의 추정과 광화용액의 기원을 해석 한 실례를 들어 보자. 페루의 산크리스토발 (San Cris to b al) 광체는 함혹중석 석영맥 광상 으로 고생대의 변성암류를 관입한 제 3 기 석영몬조니암과 밀접히 관계 되어 있다. Camp be ll 등 (19 84) 에 의 해 산소 및 수소 동위 원소 분석 및 광화작 용의 기원해석이 이루어졌다. 열수광화 작용시의 물-암석의 비를 계 산하기 위 해 앞에 서 정 의 한 Tayl o r (19 79) 의 다음과 같은 식 의 동위 원소 분석자료를 대입하여 계산하여 광화환경을 검토 해석하였다. 끄 = 8암 석 m-8 암석 ( I ) R - 8 문 ( i ) -(8 암 석 m-4) 여기 W 와 R 은 물과 암석에서 교환 가능한 산소 또는 수소의 원자
퍼센트이며 i와 f는 계내에서의 최초와 최후의 상태를 가리킨다. 위 식에서 물-암석 상호 동위원소 교환이 일어난 후 물의 8DII2o 와 8180H20 의 값을 다음과 같은 관계식에서 얻을 수 있다. 8 뭉 U) = w+WZ r 硏 + wZ+rZ r (8 암 석 (I)_4) 여기서 W, r 은 물과 암석의 원자비율 대신에 질량단위를 쓰고 물 과 암석에서 서로 다른 양으로 둘어 있는 산소나 수소를 환산한 값이 다. Z 는 물과 암석내의 산소나 수소의 양의 차이를 보정하기 위한 값이다. 즉 물은 89w t% 산소를 가지고 있고 화강암은 45w t%의 산 소를 가지고 있으므로 산소의 경우 Z 는 45 / 89( 약 0 . 5) 가 된다. 화강암을 분석한 결과 보통 물인 0.6 w t % 포함되므로 수소의 경우 Z 는 약 0.006 이 된다. 산크리스토발 광산지역에서 신선한 화강암의 동위 원소비는 8'80 = 7%, 와 8D = -70%, 이 다. 후기 저온에서 형성된 중정석내의 유체포유물의 물의 동위원소비는 8D = -14%, 와 8l80 = ― 20%, 이므로 이 것을 초기 순환수로 가정 하였다. 수소의 4 값은 흑운모-물의 동위 원소 분별식 (ll = 8D 묘·모 -8 恥 · = —21 .3X106- f-2 -2.8, Suzuok i와 Ep st e in , 1976) 에서 산소의 4 값은 사 장석 (An30) 과 물 (4 = 8180 사 강석 -8180 뭉 = 2.68X l 06T-2- 3 .53, O'Ne il과 Tayl o r, 1967) 의 동위 원소 분별을 이 용하여 400°C (673'K ) 온도에 서 계산하였다. 그 결과 W· / R 변화에 따른 8 문 (j)의 값의 변화관계를 그림으로 도 시하면 그림 4 - 28 과 같이 얻어진다 (Cam p bell 등, 1984). 그림 4-28 에서와 갇이 W/R 의 비가 높은 (>0.2 ) 환경에서 동위 원소 교환에 의해 생성된 열수용액은 산소 동위원소비의 편이만 나타 나고 W/R 비가 증가함에 따라 산소 동위원소비는 극소화되고 수소 동위원소비의 변화가 더욱 크게 나타난다.
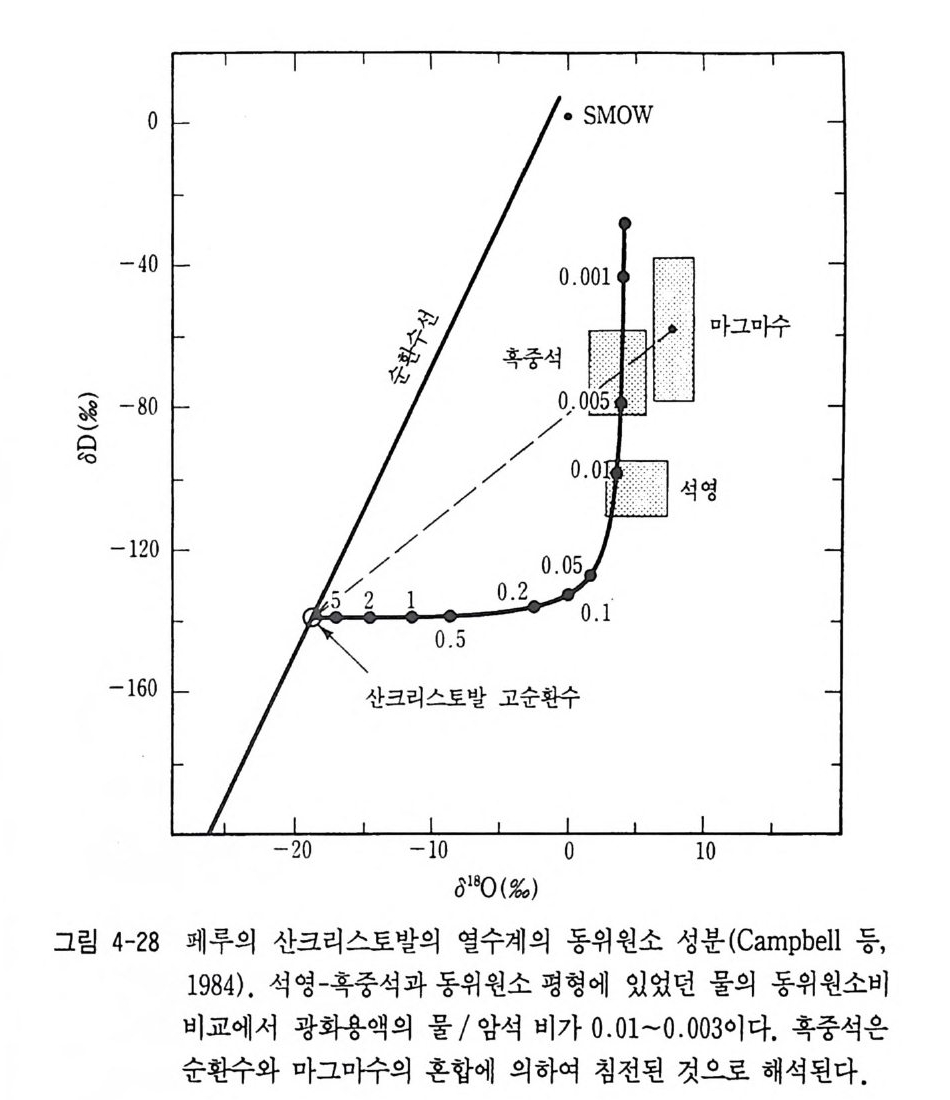 。 •SMOW
。 •SMOW
유체포유물의 동위원소값이나 혹중석-물, 석영-물 사이의 동위원소 분별에서 얻은 값을 이 그림에 도시하여 실제 이 광상의 W/R 비 를 추정한 결과 W/R~0.01~0.003 내의였으며 혹중석을 침전시킨 광화열수용액의 기원은 고순환수와 마그마수의 혼합으로 해석되 었다.
(6) 스케어가아드 관입암체의 안정동위원소바 그린랜드의 에오세의 스케어가아드 (Skaer g aard) 반려암 관입암체에 대한 안정동위원소 연구가 E p s t e i n 와 Talyo r (19 63), Ta y lor 와 Fo· reste r (19 79), Nor ton 등 (1979) 에 의해 이루어졌다. 선캠브리아기의 편마암울 관입한 70km2 면적의 스케어가아드 관입 암체는 소레아이트질 현무암 마그마의 분별정출 과정에 의해 후기 분 화산물에 Fe 가 많이 분배된 전형적인 관입암체로 알려져 있다 (Wa g er 와 Brown, 1967 ; McBim ey, 1975) . 스케 어 가아드 관입 암체 의 암 석은 중력분화에 의하여 큐무레이트 조직이 전형적으로 나타나며 리 드믹한 충상구조(호상구조)를 잘 나타내고 있다. 감람석이나 휘석같 이 무거운 광물은 충의 하부로 갈수록 증가하고 장석류는 상부로 갇 수록 증가한다. 관입암체의 2500m 충준을 통하여 광물성분의 변화와 조화적으로 화학성분도 규칙성 있게 변화하고 있다 (Wa g er, 1968). 스케어가아드 관입암체는 마그마의 특징적인 분화경향이 나타나 암 석학자들에게 대단히 홍마있을 뿐만 아니라 관입암체 주위의 급냉된 후기의 결정분화 산물 중에는 동이 많이 포함된 황화물이 불혼화액에 서 침전되어 광상학자들에게도 대단히 홍미가 있다. 조기에 정출된 감람석 중에 니켈이 많이 포함되어 있으며 함니켈황 화물 용융체에서 함니켈 황화굉물이 침전되어 정마그마성 광상연구의 주요 대상이 되고 있다. E p s t e i n 과 Ta y lor(1963) 에 의해 처음 산소 동위원소 분석연구가 이 루어졌으며 초기 분화산물에 비해 후기 분화산물의 0180 값이 3~4%, 낮은 이유를 레이리 분별과정으로 설명하였다. 그러나 그 후 Tayl o r (1968) 와 Tay lor 와 Foreste r (1979) 의 연구에 의 해 해 석 이 찰못되 었음 울 알게 되었다. 왜냐하면 스케어가아드 관입암체 전체가 순환수-열 수 과정에 의해 동위원소성분이 크게 변화되었기 때문이다. 즉 마그 마의스 케분어화가설아명드은 관81입80암 체연구의 로암는석 부의적 수절소하 다동는위 사원실소이비다 (.8 D) 는 —100 ~
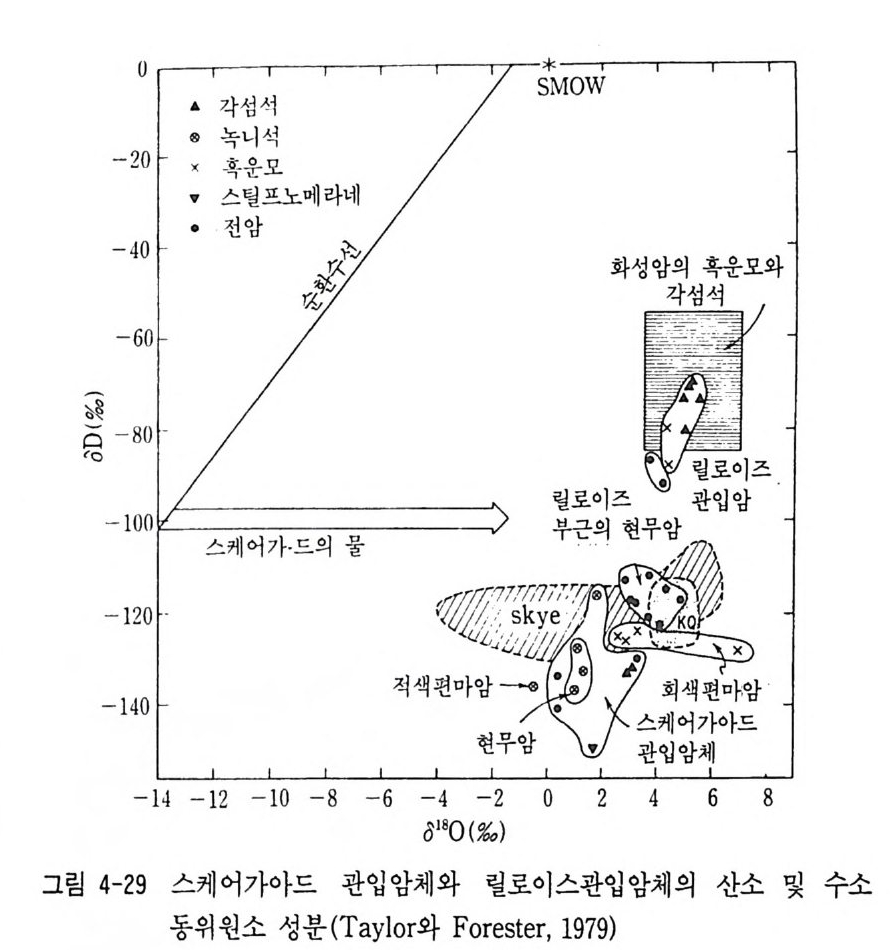 。 鼻 각섬석 S*M OW
。 鼻 각섬석 S*M OW
-145%, 로 대단히 낮은 값을 가진다. 이 역시 순환수-열수용액에 의 한 수소동위원소 교환의 결과이다(그림 4-29). 소량의 순환수는 선캠 브리아기의 기반암까지 순환하였으며 그 깊이에서 W/R 비는 0.05 보 다 낮았을 것이다. Nor t on 과 Tayl o r (19 79) 는 스케 어 가아드 관입 암체 의 동위 원소 자 료의 수치모델링을 시도하였다. 온도, 압력, 유속, 유체의 融;!f lj (플럭 스), 암석과 유체의 8180 값 등을 이용하여 2 차원 단면을 컴퓨터 시뮬 레이션을 실시하여 얻은 결과는 그림 4-30a 와 같으며 이는 관입암체
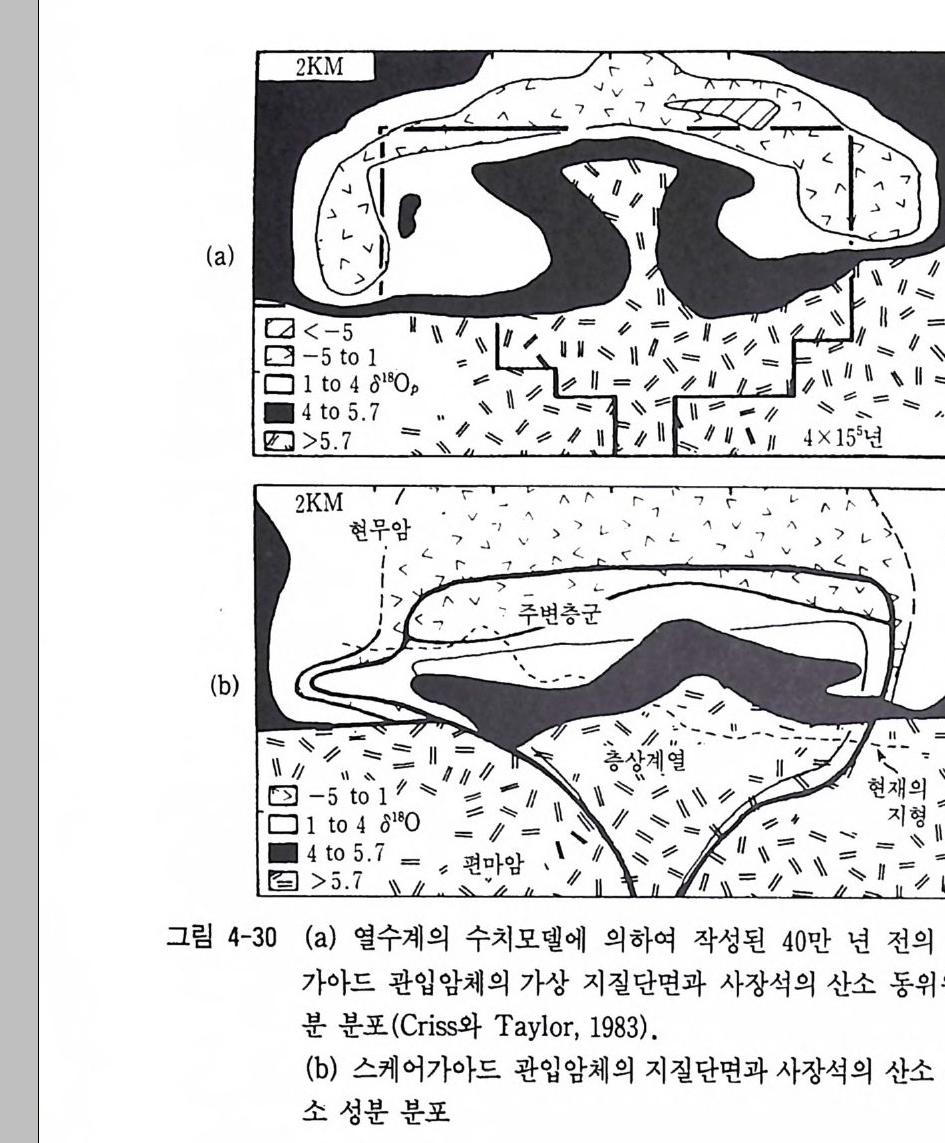 (a)
(a)
의 지질단면에서 보인 동위원소 등치선 (그립 4 - 30b) 과 잘 일치하고 있다. 이처럼 관입암체가 관입하기 직전에 대규모의 열수계가 그린랜드 동부의 암맥군 주위에 형성되었으며 마그마 자체내에서도 대류가 일
어나 큐무레이트 조직이 형성되었다. 사장석의 0180 값의 변화가 북서쪽에서 동남쪽으로 감에 따라 규칙 적으로 현저하게 변화하고 있다. 관입암체와 부정합 관계로 북서쪽에 분포하는 하부의 원암은 0180 사강 석 = 6.2 土 0 . 2 %o이었고 제 3 기충의 투수성이 큰 현무암질 용암으로 둘러 싸인 관입 암체 의 상부에 분포하는 암석 은 낮은 0180 ( = 2. 4% ,) 값을 나타내고 있다. 광역적인 부정합 경계면을 따라 투수성의 차이가 관입암체 주위의 열수계의 산소 동위원소 성분 패턴 형성에 크게 영향을 주었을 것이 다. 두수성이 큰 현무암에 대규모의 물이 순환하여 많은 물이 부정합 상부의 반려암 속으로 들어갔으며 부정합의 최하부에는 두수성이 낮 은 현무암을 통해야 하기 때문에 하부의 반려암 속으로는 소량의 물 이 침투하였을 것이다. (7) 산소 및 스트론튬 동위 원소와 암석성 인 다양한 지각물질의 산소 동위원소비와 스트론튬 동위원소비의 초생 치를 도시하면 그림 4-31 과 같다. 마그마의 기원암들의 동위원소비가 다르므로 이들 암석들이 부분용융되어 마그마를 형성하였을 때 마그 마 기원을 산소 동위원소비와 스트론튬 동위원소 초생치로써 추정할 수 있으며 동화작용-분별정출 작용에 의하여 일어난 기존 마그마의 혼염 (Conta m i na ti on ) 을 연구할 수 있다. 그림 4-31 에서와 같이 대표적인 지각구성 암석의 동위원소비의 분 포 특칭을 보면 퇴적암은 산소 동위원소비와 스트론튬 초생치의 값이 셰일과 이암에 비하여 변화가 크다. 산소 동위원소값은 +31%, 까지 큰 값울 가지기도 한다. 사암이 낮은 8180 값을 갖는 이유는 퇴적물 이 결정질 화성암 지역에서 유래하였기 때문으로 보인다. 셰일과 이암은 +13~+20%, 내의로 높은 값을 가진다. Rb 이 많이
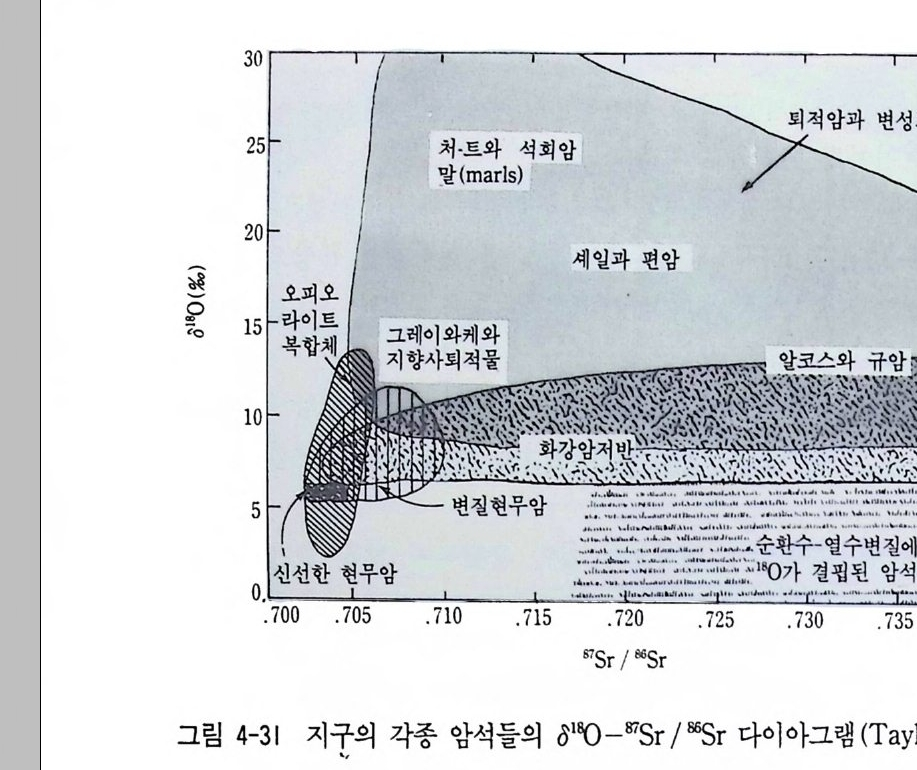 30
30
포함된 선캠브리아기 지역에서 유래된 퇴적암은 87S r 함량도 높게 나 타난다. 화강암 저반의 화강암류는 87Sr/86Sr 초생치의 변화는 크지만 018 0 값은 +1. 4~+6%, 로 퇴적암의 값에 비해 균질하다. 현무암이나 오피 오라이트 복합체는 스트론튬의 초생치나 산소 동위원소값이 낮고 균 질한 값을 가짐이 특칭이다. 그러므로 상부 맨틀물질은 CD MORB(8180 = +5 .7% ,, 18Sr /8 6S r = 0.702-0.7 0 3) 값에서와 같이 균질인 것과 @ MORB 보다 약간 높 은 8180 값과 “Sr / 86Sr = 0 . 704-0 . 710 인 알카리 감람석 현무암과 Si0 2 불포화 네팰린질 암석의 복합체 ® 에크로자이트 기원 (8 1 80 값이나 87 Sr/86Sr 값이 변화가 큼)으로 대표될 수 있다. 산소 동위원소값이 약 6%, 이하인 암석은 180 이 결핍된 순환수-열
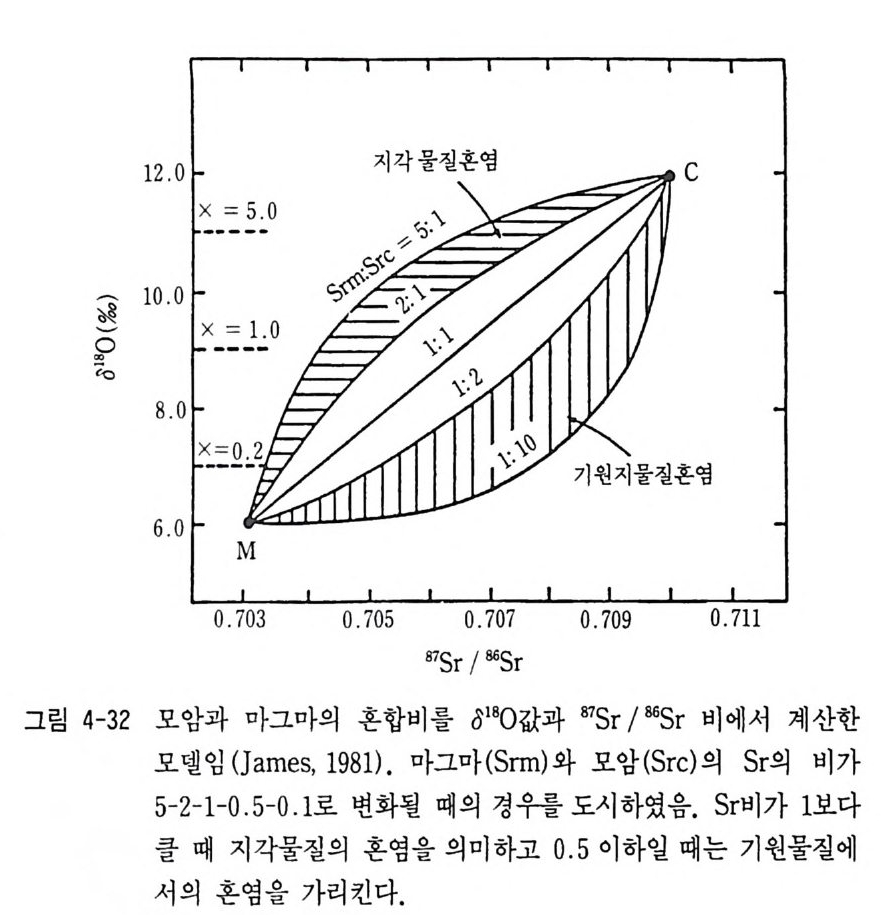 12. 0 I X = 5.0 c
12. 0 I X = 5.0 c
수 변질에 의해 형성된 암석이다. 그러므로 마그마와 모암과의 상호 반응 및 마그마를 만든 기원암을 추정하기 위하여 산소 동위원소비 (성한)와 스트론듐 동위원소비의 초생치 (87Sr/86Sr) 의 비교연구가 도 움이 되고 있다. 마그마와 모암의 혼합관계를 818O 와 87Sr / 86Sr 동위 원소비에서 모델화하면 그림 4-32 와 같다. 그림 4-32 에서 베니오프대에서 섭입되는 스라브물질과 멘툴물질의 혼합을 잘 설명할 수 있다. 두 기원물질이 혼합된 혼합물의 8180 값 은 직선관계를 나타낼 것이다. 마그마가 지각물질에 의해 혼염이 되 면 위로 볼록한 커브가 되고 기원물질의 혼영이 일어나면 아래로 볼
록한 커브가 된다. 예를 들면 스라브물질 (0180 = 12 %, )과 맨틀물질 (01 8 0 = 6 %, ) 이 l ·· 4 의 바로 섞인다면 이때 생긴 맨틀물질의 01 8 0 는 + 7 . 2 %, 이 퇴근것
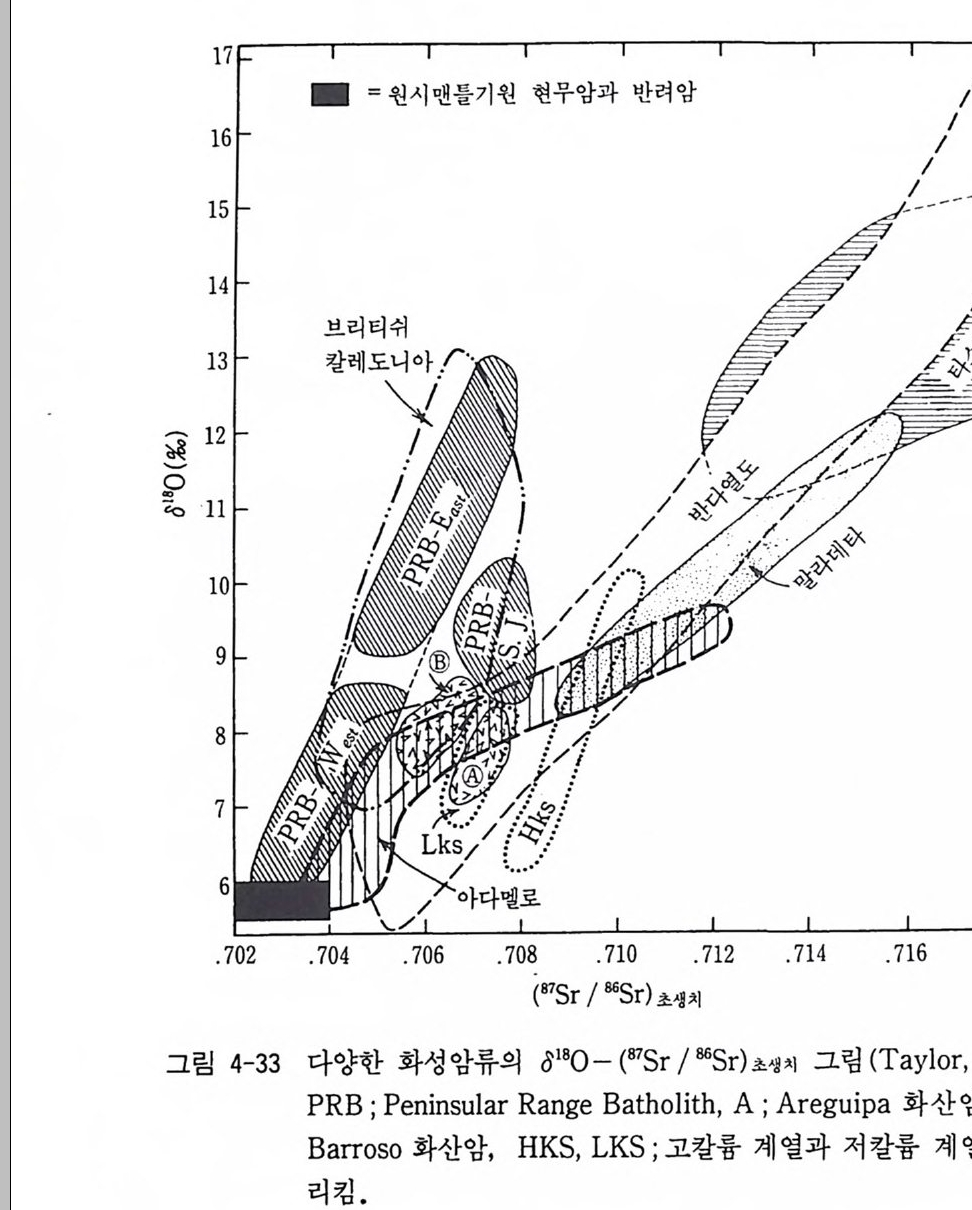 17 - =원시맨 불 기원 현무암과 반려암 / / / / \ \',.
17 - =원시맨 불 기원 현무암과 반려암 / / / / \ \',.
이다. 스라브원에서 유래한 성분의 혼입 때문에 맨틀물질내의 미량원소와 부분용융 산물의 87S r / 86S r 초생치와 부적합원소(i ncom p a ti ble element) 의 함량이 증가하게 될 것이고 맨틀의 a1 8 0 값에 의해 혼합커브는 밀 으로 볼록하게 될 것이다. 이 같은 실례는 그립 4-33 과 같다. 이 그 립에서 아다멜로 복합체는 지각물질의 동화의 경향을 나타내고 대부 분은 전형적인 맨 틀 기원이거나 MORB 쪽으로 경사되고 있는 특징이 나타나고 있다. 우리나라 화강암류와 관련성이 예상되는 중국대륙의 동남부의 원생 대-중생대 화강암류는 (87S r/ 86 S r)i = >0 .7 1 0, 018 0 = +9~+14%,, 0180 == -5 ~ + 1 7%,( 평균 내 . 6 %, ) 로 보고 되어 있다 (Zhan g 등, 1984 ; Xu 등 , 198 4). 그리 고 중생 대 의 1 8 0 와 87 Sr 이 많이 농집 된 화강암류는 W, Sn, Nb -Ta, HREE, U 광상과 밀접히 관련되고 있으며 지향사 퇴적물의 부 분용융 산물로 해석하고 있다. 호상열도인 일본열도의 경우 화산암의 a180 값이 화산전선을 경계로 81 8 0 평균 < + 6.5%, 와 8180 평균 > +6.5% 가 구분되고 있다 (Ma t suh i sa , 1979 ; Ma t suh i sa 와 Kurasawa, 1983). (8) 우리나라 화강암류의 동위 원소 성분 우리나라의 화강암류에 대한 동위원소 분석연구는 현재 수행중에 있으며 그 내용을 간단히 소개한다. 우리나라의 현생이언의 심성암류는 중생대의 대보화강암류(쥬라기 -백악기초)와 불국사화강암류(백악기말께 3 기초)로 대분된다(그림 4-34). 화산암류는 제주도와 울릉도 등 도서지역과 경상분지내에 주로 분포 하고있다. 김규한(1 990) 의 화강암류의 전암의 산소동위원소비 분석결과에 의 하면 0180 = +2.38~+ll . 0%, 로 Tal y or(l974) 의 심성암류의 값의 범위내에 든다. 이중 대보화강암류는 0180 = +4 . 97~+ll.0% 이고
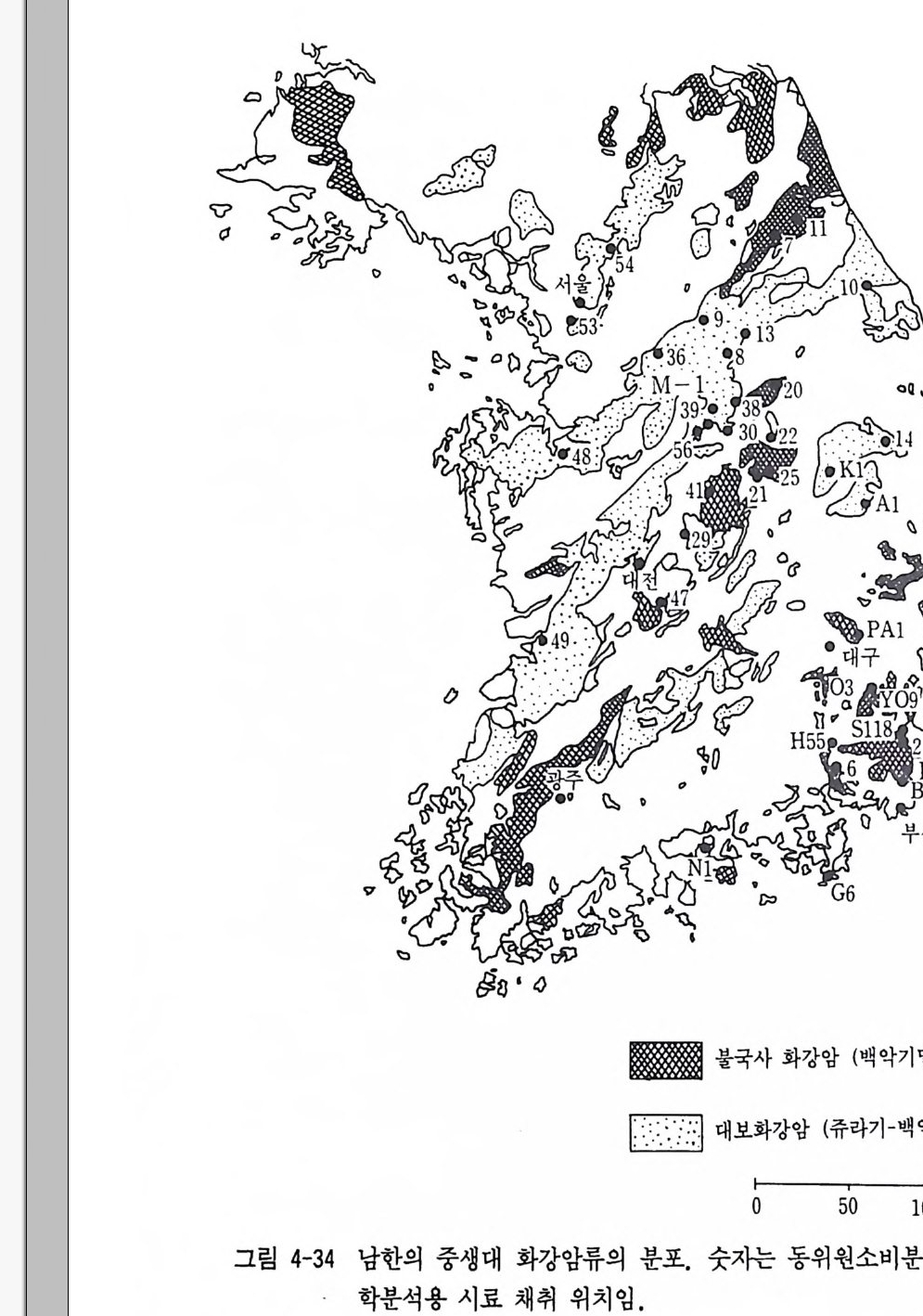 ’广1 :'v :4\3
’广1 :'v :4\3
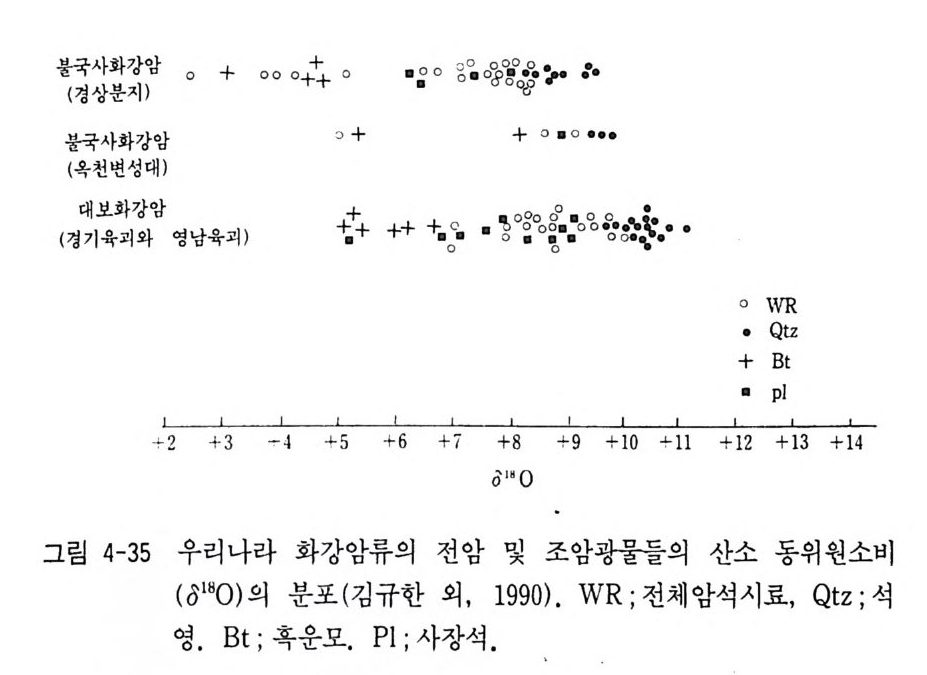 붕국사화강암 0 + oo o++ + o •~ o g 나°§~• t :.
붕국사화강암 0 + oo o++ + o •~ o g 나°§~• t :.
불국사 화강암류는 +2.38~+9.83%, 로 대보화강암류 쪽이 180 이 부 화되어 있다(그림 4-35). 조암광물 중 석영>장석>운모 순으로 0180 값이 변하며 이들 광물 간에 동위원소 평형이 인정되고 있다 조암광물 중 기타 물질과 동위원소 교환에 비교적 안정된 석영의 0180 값은 대보화강암 (+9.5~+11.10%, )과 불국사 화강암 (+3.73~ +9. 8 3%.) 간에 명 확한 차이 가 나타난다. 일본열도의 심성암류의 0180 값과 암석유형 구분에서 얻어진 결과 를 적용하여 보면 대보화강암류는 티탄철석계의 특칭을 나타내고 불 국사화강암류는 자철석계의 동위원소 경향을 나타내고 있다(그림 4-36). 또한 REE 함량에서도 이들 두 암군간에는 현저한 차이가 있어 이 둘 두 암군간의 마그마의 기원, 마그마의 분화과정 등에 차이가 있음 울 알 수 있다(김규한, 1990) .
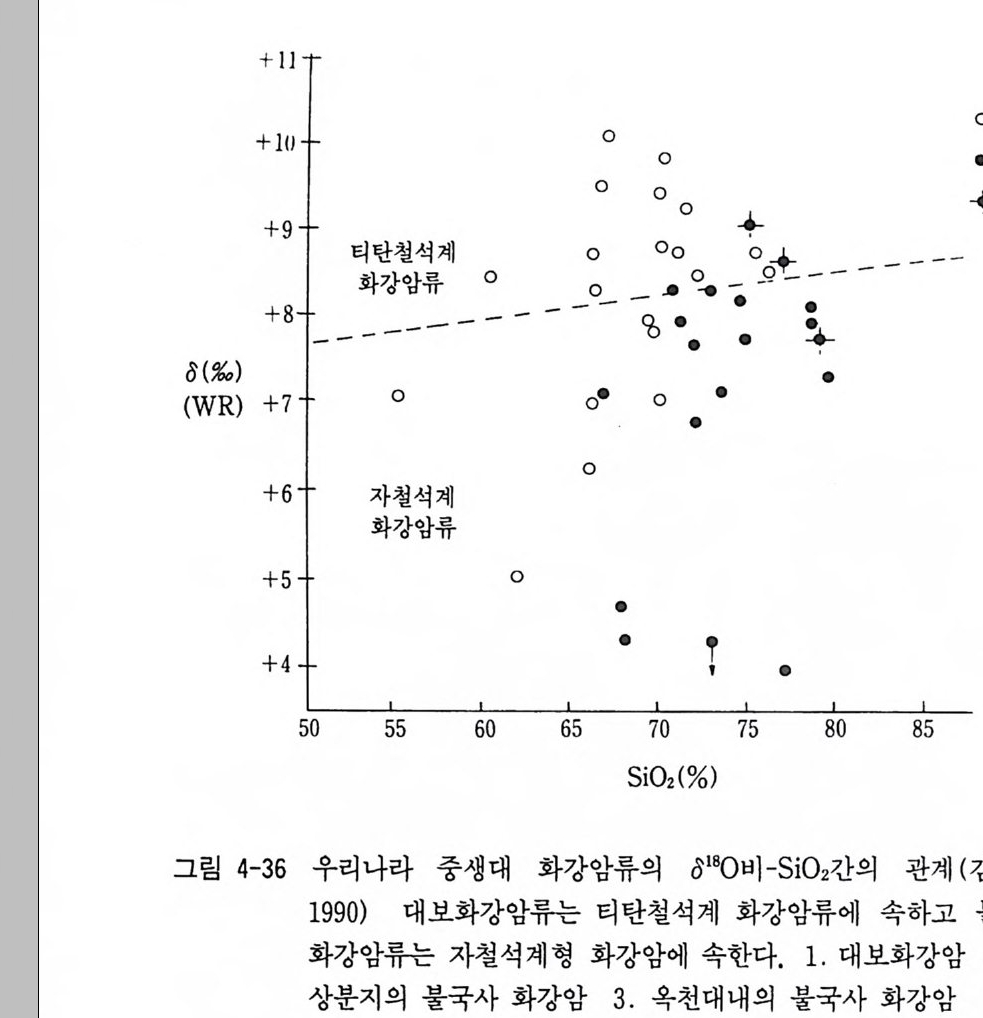 +1 1
+1 1
이 같은 동위원소비의 특징은 중국 동남부의 화강암류와 조화적으 로, 대보화강암은 중국의 t rans fo rma ti on 형과, 불국사 화강암류는 중국의 syn tex is 형과 대비되고 있어 동북아의 지구조 화산활동과 밀 접 한 관련성 이 나타났다(그립 4-37) . 그 외 제주도의 화산암은 0180 = +5.8%, 이고 울산 철산지역의 페 리도타이트 기원의 사문암은 0180 = +3.4~+6.8%, 으로 분석되었다 (김규한 의, 1990).
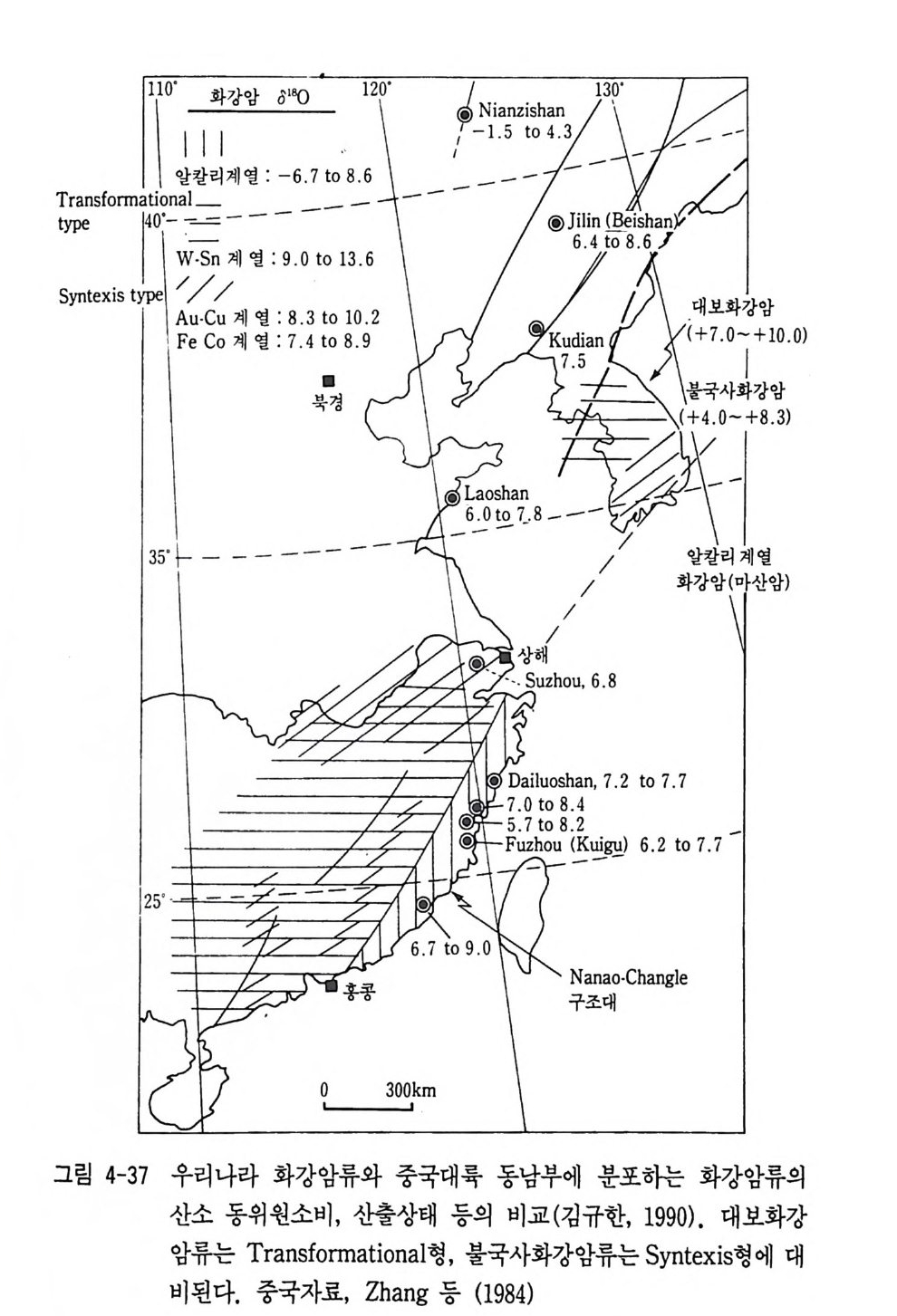 Ttyra Snp s e0I' fy S ntnnt eya 1.pb·0,x4一e n' . I0 — 알al1 ew/F1畑 一 ― 二呼nS/1 1화10 계 계-계강계열 암一열 열열:··.:: _一섬9 一347一6tootto l: 31088 一 .9l 20 。 ·6 8I¢/ 6 1N-12i.a 5n z tiso h 8序/A· 대알강 보-칼암 화-리p—강계t암연산 . 。,' _
Ttyra Snp s e0I' fy S ntnnt eya 1.pb·0,x4一e n' . I0 — 알al1 ew/F1畑 一 ― 二呼nS/1 1화10 계 계-계강계열 암一열 열열:··.:: _一섬9 一347一6tootto l: 31088 一 .9l 20 。 ·6 8I¢/ 6 1N-12i.a 5n z tiso h 8序/A· 대알강 보-칼암 화-리p—강계t암연산 . 。,' _
(9) 반암동 광상의 수소 및 산소 동위 원소바 반암동 광상 (Porp h y ry cop pe r dep os it s) 은 주로 환태 평 양 지 역 의 중 생대 이후의 신기 조산대에 많이 분포하고 있다. 최대 규모인 미국 유타주의 빙행과 남미의 추키카마타 등 다수의 광상이 알려져 있으며 동이 0.5% 내의의 저품위라도 규모가 크므로 광석의 대량처리에 의해 전세계 동광석량의 50% 를 생산하는 유용 광상으로개발되어 오고 있다. 광상은 칼크알카리암 계열의 화강암류와 섬록암-몬조니암-섬장암 계열에도 광염상(0 . 5% 내의의 Cu) 으로 나타나나 2 차 부화작용에의 2% 이상의 Cu 함량을 나타내기도 한다. 반암동 광상에서 나타나는 주요한 특징은 열수변질 작용이다. 열수 변질대가 동심원상으로 나타나며 일반적으로 중심에서 의측으로 감에 따라 칼륨 변질대(칼뮴장석, 흑운모, 백운모), 필릭 변질대(견운모, 석 영, 황철석), 점토화 변질대 (고령토, 몬모리로나이트), 프로필라이트화 변질대(녹니석, 녹영석, 방해석)로 분대된다. 동위원소 지질온도계에 의하여 얻어진 광상생성 온도는 중심부에서 600~1oo·c , 칼륨 변질대 400~600°C , 필릭 변질대 300~4oo · c 이다. 유체포유물 연구에서 추정 된 광상형성 심도는 1~2km 내의이다. 북미의 반암동 광상의 산소와 수소동위원소 연구에서 남부의 뉴멕 시코 주 산타리타에서 유타주의 빙행 크라이막스 북부의 몬타나 주의 뷰트광상에 이르면서 광액의 8D 값이 점점 작아침과 동시에 오늘날의 순환수의 변화경향과 잘 일치하고 있다(그림 4-38). 이 사실은 반암 동 광상의 광화작용시 열수용액에 순환수가 혼입되어 온도, PH 등 의 물리화학적 변화를 주어 금속광물의 침전을 일으켰음을 가리켜 주 고 있다. 이처럼 반암동 광상의 광화작용과 열수변질 작용에 순환수 가 기여한 중요한 사실이 동위원소비 분석에서 밝혀지게 되었다. 일반적으로 변질을 받지 않은 화강암류 중의 흑운모 칼리장석은 마 그마에서 초생적으로 정출한 評 O 와 8D 값을 가지고 있으며 변질대와 광체 주위의 견운모와 고령토 등은 순환수 혼입에 의해 동위원소 교
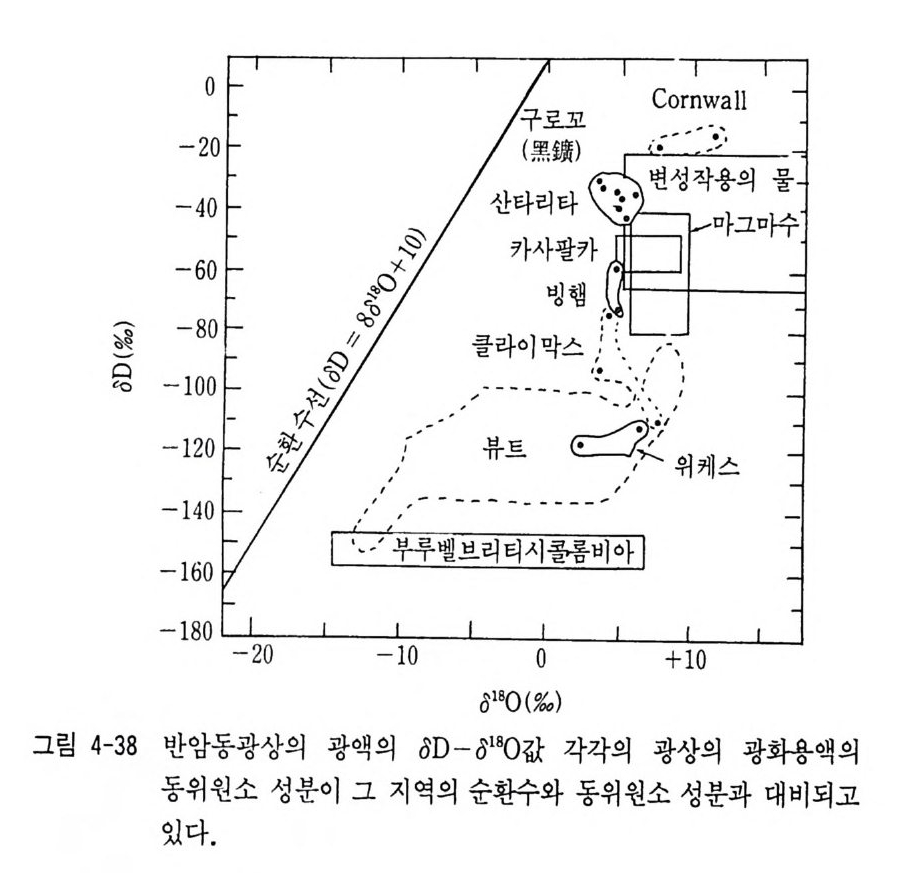 000000000
000000000
환을 일으킨 값을 나타내고 있다. 그림 4-39 에서 처 럼 반암동 광상에서 열수계의 모델은 정마그마형 열수모델과 순환수의 대류모델을 제시하고 있다 (M cMill an 과 Pante eley e r , 1980) . 정마그마형 열수계 모델에서는 화강암질 암체 내부의 PH2o>Peo 자i n i떄 p ressure 일 때 ten sile 스 트레스에 의해 파쇄대가 형성되고 비등현상이 일어나 화강암질 암석내에 잔류되기 어려운 금속원소들은 열수에 농 집되어 파쇄대내에 충전된다. 변질광물의 oD 와 評 0 분석 결과 칼륨 변질대에서는 마그마수가 우세하고 점토 변질대에서는 순환수가 우세하게 나타났다. 필릭 변질
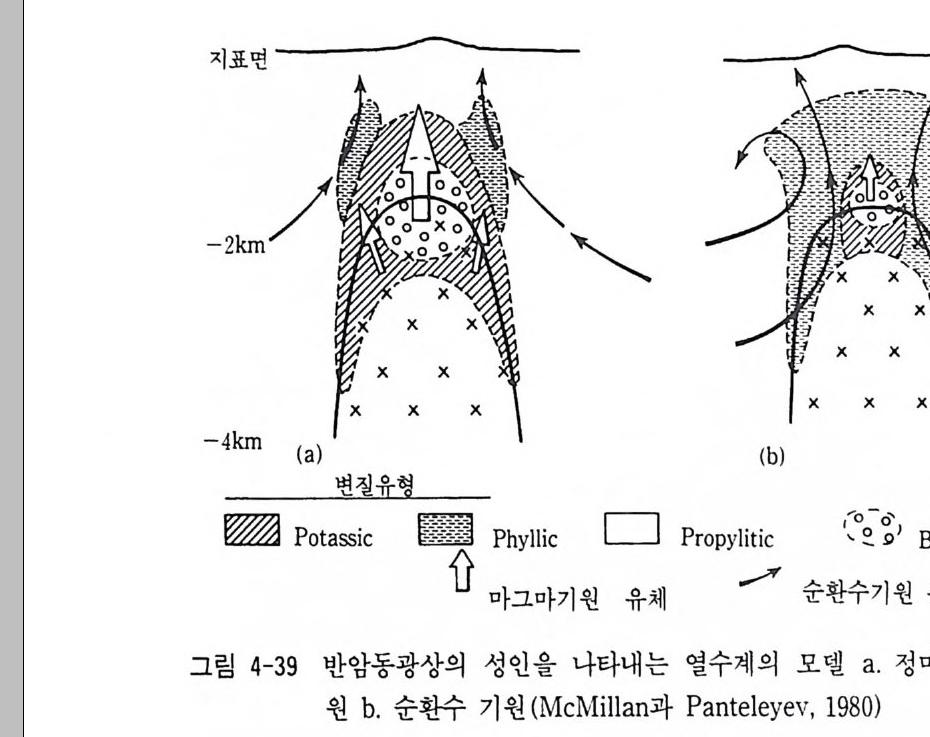 지표면
지표면
대에서는 마그마수와 순환수가 혼합 반응, Cu 농도가 상승하여 Cu -황화광물이 대량 침전하게 되었다. 동위원소 분석 연구에서 순환수 의 대류모델이 더욱 정량적으로 입증되었다. 우리나라에서도 경상남 도의 동점 광산, 일광 광산 등은 반암동 광상형으로 알려져 있다. 스카론 광상의 경우에도 스카른 광화시에 순환수의 혼입이 광물침 전에 크게 기여한 사실이 밝혀지게 되었다 (K i m, K.H . 등, 1988; Sh im a - zaki,1 9 89) . 그리고 광석에 공존하는 각 광물들의 포유물의 동위원소비 분석으 로 광화 스테이지별 광액의 기원이나 열수광화용액과 순환수의 혼입 비율 등도 정량적으로 연구할 수 있게 되었다. (10) 우리나라 금속광상의 산소 및 수소 동위 원소 성분 유용광물자원인 금, 은, 동, 연, 아연, 철, 망간, 텅스텐, 몰리브
덴, 주석, 창연 등의 금속광물들이 산성 화강암류와 밀접히 관련되어 산출된다. 주로 스카론형 광상, 열수광맥 광상, 열수교대 광상이다. 여기서는 동위원소 연구가 수행된 금은 광맥형 광상과 텅스텐, 몰 리브덴 스카론형에 대한 연구결과를 소개한다. 금은 광맥형 광상 : 금은 광맥형 광상은 천열수형, 한국형, 중열수 형 광상으로 구분된다 (So 등, 1988 ; Shelto n 등, 1988). 우리나라의 대부분의 금은 광상은 쥬라기와 백악기의 화성활동과 밀접하다. So 등(1 989) 에 의하면 250'C 이하에서 형성된 천열수형 광상은 주
표 4-7 우리 나라 금은광상의 특성 (So 등, 1988) 천 열수 형 한국형 중열수형 광화 시기 백악기말- 제 3 기 백악기초~말 쥬라기 생성 심도 <7 50 m 750~1500m >4 500m 모암 화강암, 화산암, 화강암, 변성암 화강편마암 퇴적암 , 변성암 지질 구 조 칼데라 화산중심부 화산중십부, 단충대 단층대 광석 광물 복합적이고 다단계의 단순다단계 단순 단일단계의 괴상 석영 및 방해석맥 석영맥 석영맥 황화광물 소량 황화광물 다량 수반 Au / A g비 1 : 10~1 : 200 1:3~2: 1 5 : 1~8 : 1 연수 변질 심하고 규화작용, 보통 규화작용 약함 , serici ti c pro p yli- argi llic, po ta s sic Serici ti c, a rgi lti c tic chloriti c pro p ylitic pro p h yl i ti c Au 광화유체 < 240'C , 낮은 CO2 225~300'C , 300~370'C 낮은 CO2 산소 동위원소비 -13.1 ~ -4.2 _l.7 ~ 5. 5 5.5 ~ 7.7 (성8() mo%) 광액침전 비등, 모암변질, 비등, 냉각 불혼화 메커니즘 회석작용
로 백악기와 제 3 기의 화강암류와 밀접한 관계가 있으며 Au / A g비 (1 :10~1:20) 와 다량의 황화광물과 복합적인 황화광물들이 수반되는 특칭이 있다. 그리고 4.5 k m 이상의 심도에서 형성된 중열수형 광상 은 쥬라기 대보화강암류와 밀접히 수반되며 Au / Ag 비는 5 : 1~8 : 1 이다. 생성온도는 300~370'C 내의이다. 한국형 광상은 백악기 화강 암류와 밀접히 수반되며 Au/A g비가 1:9~2:1 이다. 황화광물은 소 량 수반된다 (표 4-7). 맥석광물인 석영, 방해석 및 포유물의 수소 및 산소 동위원소 분석 에 의하면 0180 = +5 . 7~+14.0%, 의 범위의 값을 가지며 유체 포유 물의 수소의 동위원소값 (8D) 은 스테이지별 광물 종류에 따라 큰 차 이가 있다. 이들 동위원소값에서 동위원소 평형에 있었던 광화용액의 동위원소 성분을 계산하여 0D-0180 그림에 도시하면 그림 4-40 과 갑다. 이 그 립에서 보면 모암인 화강암류와 밀접한 관계를 가지는 열수용액이 순
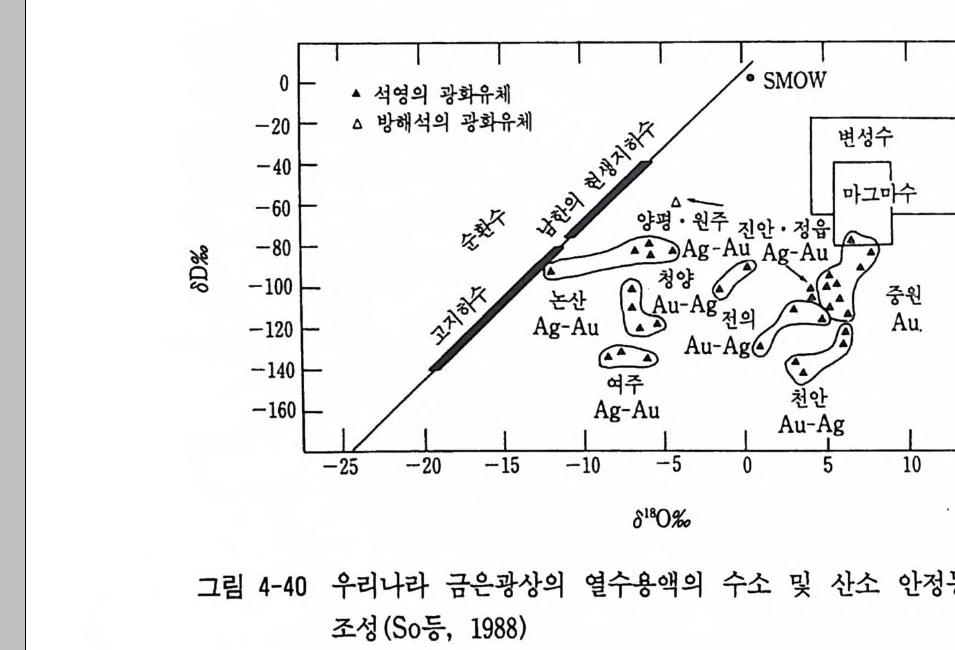 。 .. 석영의 광화유체 •SMOW
。 .. 석영의 광화유체 •SMOW
환수와의 혼합의 특징을 잘 나타내고 있다. 그러나 오늘날의 우리나라의 지하수의 동위원소비 (김규한· 나까이, 1981, 1988) 값과 비 교하여 보면 오늘날의 지 하수와 화강암류간에 산 소편 이 (Oxy ge n shif t) 로는 설 명 이 되 지 않는다. 이 같은 사실은 고지하수와의 동위원소 교환을 추정케 하며 상이한 W/R 비 때문으로 해석할 수도 있다. 청양, 전의, 천안 등지의 한국 형 광상은 천열수형 광상과 중열수형 광상의 중간 정도의 산소전이의 값을 나타낸다. 논산, 양평, 원주, 여주 등의 천열수형 광상은 물-암석 상호반응이 약하거나 W / R 비가 큰 경우이며 중열수형은 반대이다 (So 등, 1989).
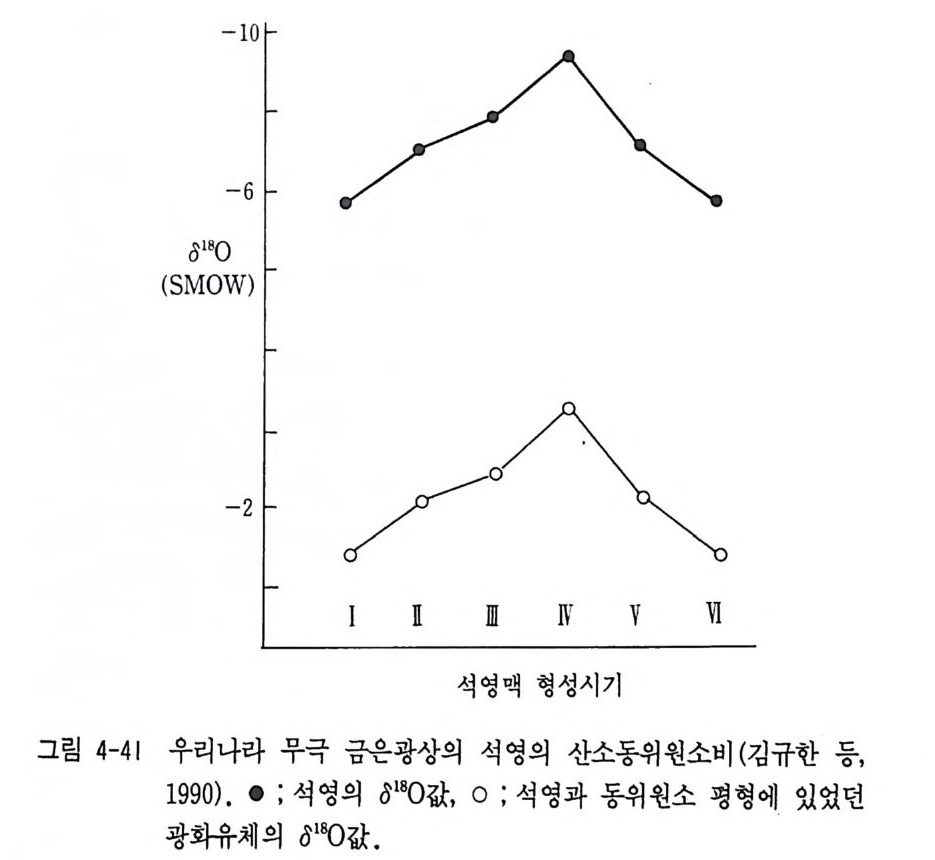 -1 0
-1 0
천열수 금은 광상의 대표적인 예로 무국광상의 각 스데이지별 석영 맥의 석영의 산소 동위원소비는 +5.7~+9.3%, 까지 변화하며(그림 소4-4비1) (81석80영H, o)침 는전 시—에3. 2 동~+위0원.4소% , 평1형80에 이 있결었핍던된 열순수환용수액의의 혼산합소이동 위추원정 된다(김규한 등, 1990). 각 스데이지간의 동위원소비의 변화는 열수용 액과 순환수의 혼입비율의 변화로 해석되고 순환수의 혼입에 따른 온 도저 하, H2S 양의 감소, PH, Cl 농도변화 등이 금-은 광물을 침 전시 킨 요인으로 해석되었다. 스카른형 텅스텐 몰리브덴 광상 : 세계적으로 유명하게 알려진 상동 중석광상은 태백산 광화대내에 분포하며 캠브로오도뷔스기의 풍촌 석 회암충 및 묘봉충과 상동화강암 (87 . 5m . y.)과의 접촉부에 발달하는 스 카론형 텅스텐 몰리브덴 광상이다 (Moon , 1983). 광화작용은 풍촌 석 회암충과 묘봉층에 협재된 석회암충을 선택적으로 교대하고 있으며 스카른 광물들이 광체의 주위에서 중심으로 감에 따라 규회석 - 석류석 -휘석대, 각섬석-운모대, 운모-석영대로 분대가 되며 중석과 몰리브 덴의 함량도 증가하여 운모석영대에는 wo3 가 2.0% 이상이다. 관계 화성암으로 생각되는 상동화강암의 전암 및 석영의 산소 동위 원소비는 각각 +10.1%, 과 +10 . 9%, 이다. 그리고 스카론 광체 중의 석영과 후기 석영맥의 석영의 산소 동위원소비는 +8.1~ + 19.6%, 까 지 변화하고 있다(Kim K.H . 등, 1988). 이들 동위원소비에서 계산된 열수광화용액의 산소 동위원소비 (018 0.i,o) 는 규희석-휘석-석류석대에서 각섬석-운모대, 운모-석영대로 감에 따 라 점점 감소하고 있다. 이 같은 현상은 열수광화용액과 순환수의 혼 합에 의한 것으로 해석되며 규희석-휘석-석류석대의 8180H20 는 상동 화강암과 유사하나 후기로 갈수록 온도가 낮아지고 스카른 광체내에 발달하는 후기의 석영맥의 석영은 8180tt 20 값도 변화가 심하고 18° 이 결핍되어 있다(그림 4-42). 그리고 각섭석, 흑운모, 백운모의 수소 동위원소비는 각각 —123 .6%,,
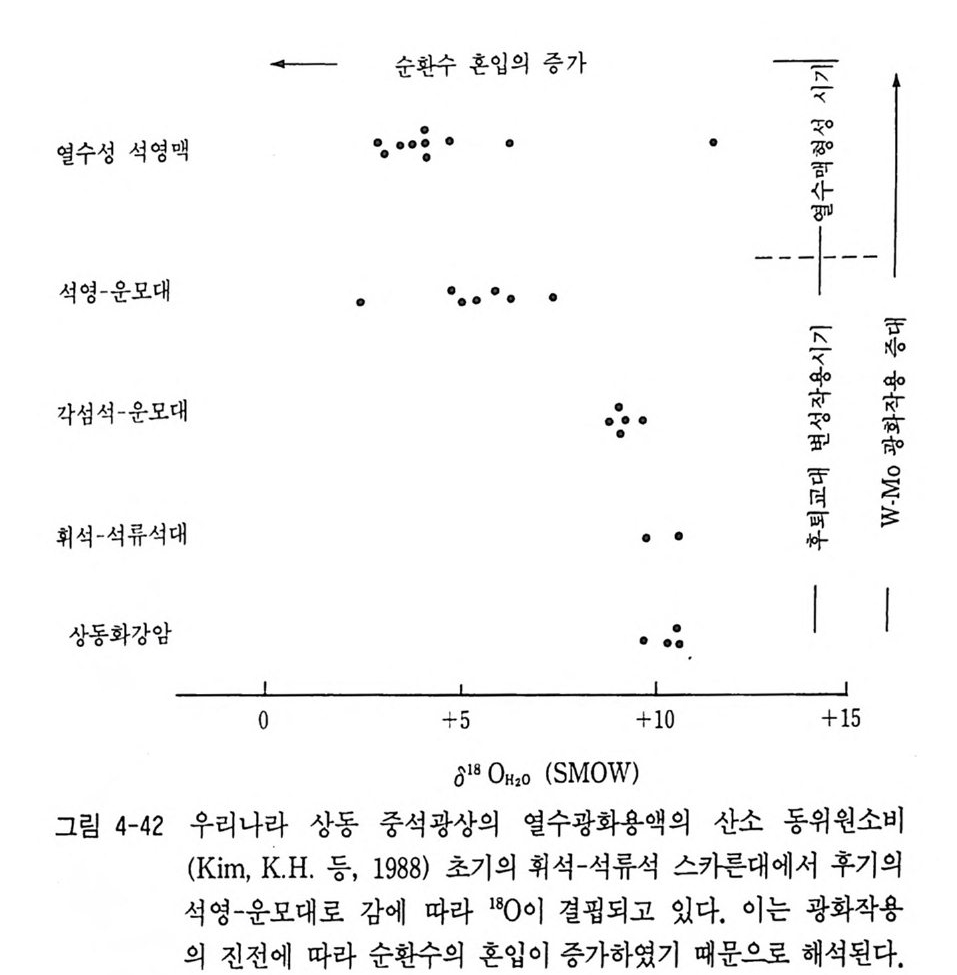 • 순환수 혼입의 증가 4i
• 순환수 혼입의 증가 4i
-85.3 % ,, -78.4%, 이며 여기서 얻어진 열수용액의 수소 동위원소비 는 Tayl o r (1979) 의 마그마 유체의 동위원소비의 범위에 들어가고 있 다. 동위원소 분석결과 해석에서 상동스카론 광상의 광상형성 모델이 제안되었다(그림 4-43). 기타 울진지역 석석페그마타이트 광상의 페그마타이트 중의 석영, 장석, 운모류의 산소 동위원소비는 +6.3~+12.9%, 이다(문상호, 1990). 그리고 그라이젠 I 기에서 그라이젠 II 기로 감에 따라 산소
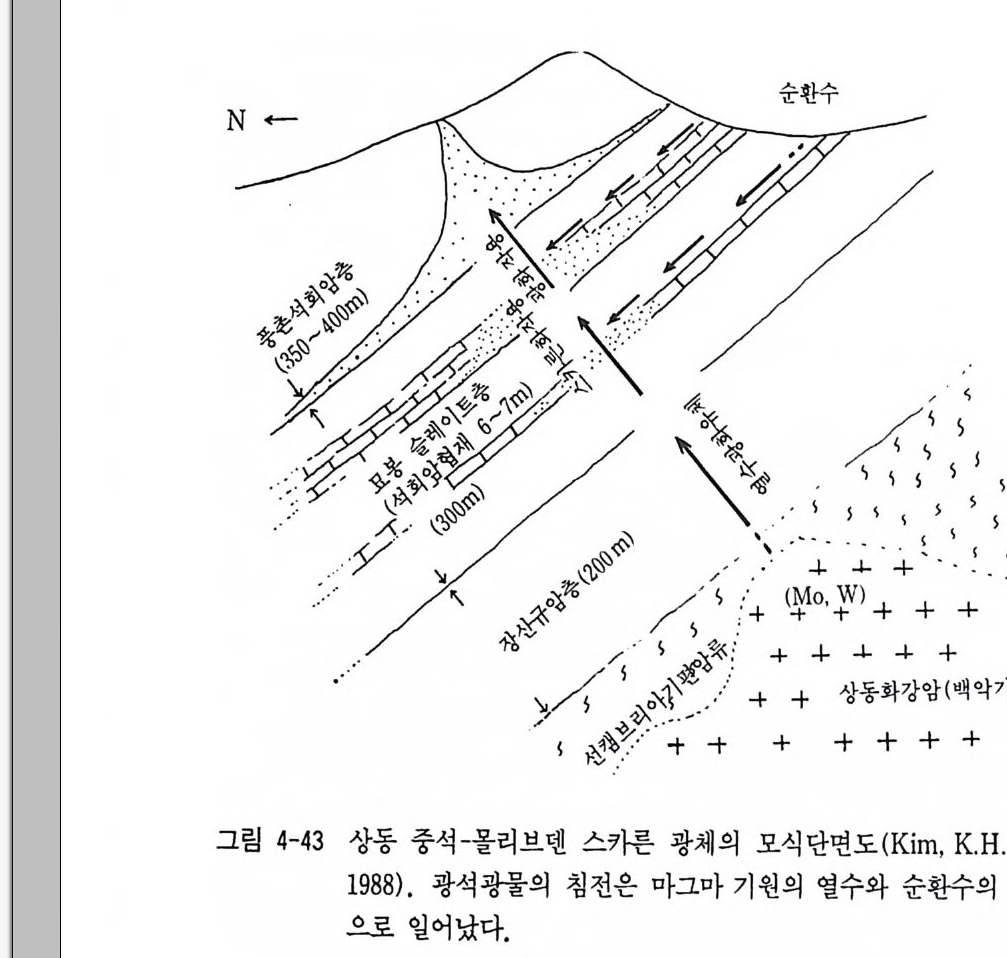 \\广s
\\广s
동위원소값이 증가하며 페그마타이트와도 값이 차이가 있다 . 이는 기 원이 다른 물이 유입된 것으로 해석된다. 페그마타이트내의 운모류는 마그마수의 범위에 도시되고 화강편마 암의 운모류는 카오리나이트 선상에 도시되어 페그마타이트와 편마암 의 변질작용시의 열수용액의 기원이 상이하였음이 추정된다. 순경 석 석페그마타이트의 석영의 산소 동위원소비는 +13.3~ + 15 . 2%, 로 18° 이 부화된 변성되적암류와의 동위원소 분별이 예상된다 (Kim S.Y . 과 Park N.Y ., 1 990) . 동위 원소 지 질온도계 에 의해 석 석그라이 젠 페그마
타이트와 석석페그마타이트는 각각 415 ' C 와 525 ' C 가 얻어졌다. 2) 퇴적암류의 동위원소 성분 퇴적암은 화성암, 변성암, 퇴적암이 풍화 침식 운반되어 물 속에서 나 지표환경에서 퇴적된 퇴적물이 속성작용을 받아서 만들어진 암석 이다. 퇴적암의 퇴적물의 구성광물에 따라, 그리고 퇴적환경과 퇴적암의 종류에 따라 동위원소값이 크게 변화하고 있다. 일반적으로 퇴적암의 동위원소 성분 018Q = +5~+44% o, oD = -3~-150 %o의 범위를 나타낸다. 쇄설성 퇴적암, 화학적 퇴적암 및 생물학적 퇴적암에 따라 동위원 소값이 크게 다르다. 왜냐하면 이들 사이에는 동위원소 분별과정이 다르기 때문이다. 일 찍 이 Urey (1 946) , McCrea (1 950) , Ep st e i n 등 (19 53) 은 탄산염 암 에 대한 동위원소 분석연구에서 탄산염암의 180 / 160 바가 탄산염광물 이 침전시에 온도에 따라 변화함을 이용하여 고해수온을 추정하였다. Cra ig (l965) 에 의하면 t = -0.07~1 .01 t'(t = 0 . 95) 과 같은 실제 성장온도 t와 계산된 t’의 고온도의 관계식이 얻어졌다(그립 4-44). t배 =양 1온7도.0와-4 .물5 -2 (o탄1산80염c— o동18 위0w원) +소0. 0분3(별0에18서0c ― 018 아 )2 의 온도 관계식이 얻어진다. 0180c 는 각질화석의 산소 동위원소비이고 0180 굵근 해수의 동위원소비이다. Wada 등 (1982) 은 화석시료의 CO2 가스 0.01cc 정도나 CaC03 4.5µg 정도의 소량의 시료라도 탄소 및 산소 동위원소 분석이 가능한 장치 를 개발하여 미화석을 이용한 고수온 등 고환경 연구에 응용하고 있 다. 위의 식을 이용하여 고수온을 계산할 때는 다음과 같은 가정이 필 요하다.
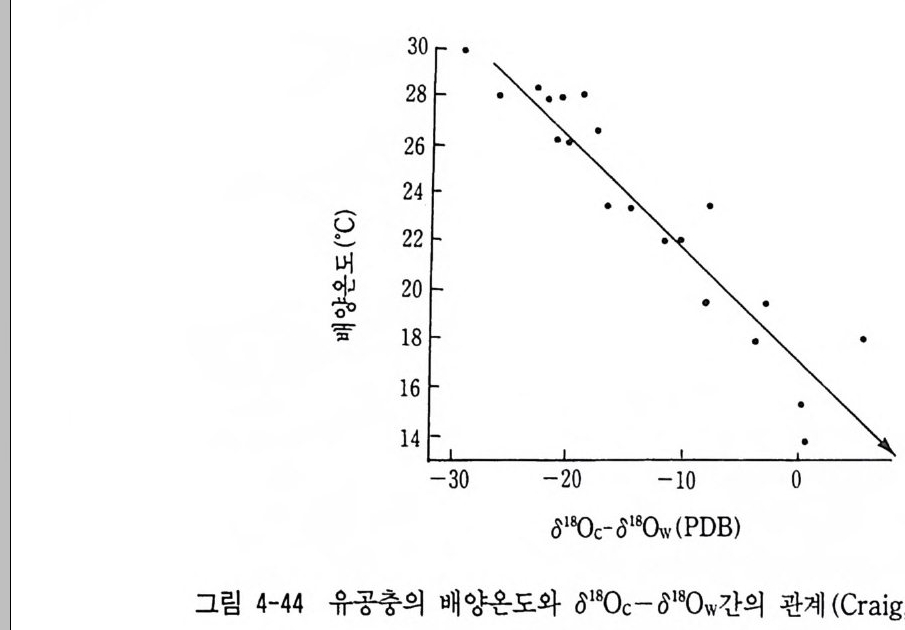 3028264 20864
3028264 20864
® 고해수의 동위원소 성분은 균질하였고 오늘날과 유사하였다. ® 이용되는 시료인 유기물 (mollusks 나 brachio p o d s 등)은 해수와 동 위원소 평형에 있는 방해석이나 아라고나이트로 이루어져 있어야 한다. 보통 echin o derms, aste r i od ea, o p h i uro i dea 와 c ri n c i d e a 는 이들이 퇴 적환경과 동위원소 평형에 있는 탄산영광물로 되어 있지 않다. ® 속성작용 동안에 재결정되거나 용해될 때 아라고나이트나 방해 석으로 된 껍질의 산소 동위원소 성분은 변화가 없어야 한다. Hend y와 W il son(1968) 은 뉴질랜드의 종유석의 산소 동위원소비를 분석하여 아래의 O'Neil 등 (1969) 의 방해석-물의 동위원소 분별식에 서 고기후 변동을 연구하였다. 8180 덴석 -8180 뭍 = 100 Ina 덴석 물 . = 2.7 8 (1 0 6T-2)-3.39 이 식을 이용하면 종유석의 침전시 온도를 계산할 수 있다. 예를 들면 일본의 오다끼 동굴의 종유석에서 얻어진 37,000 년간 온도(기
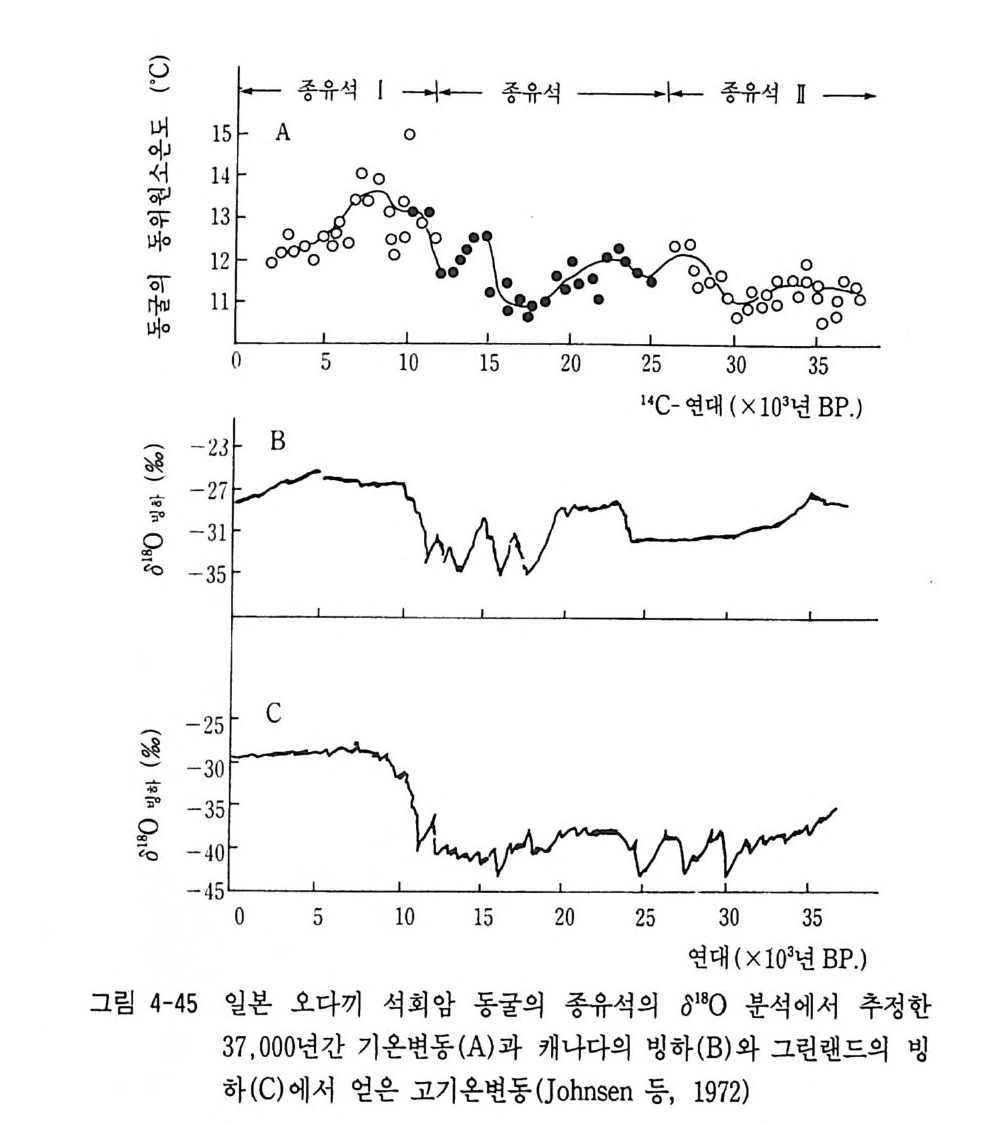 . 버3() 15— —l lA1 종 유 석l l ―。 니__ 종유 석 나__ 종유석 Il ___
. 버3() 15— —l lA1 종 유 석l l ―。 니__ 종유 석 나__ 종유석 Il ___
후) 변화는 캐나다, 그린랜드 등의 빙하의 8180 분석에서 얻은 기후 변동의 결과와 잘 대비되며 두 결과 모두 17000~18000BP 시기의 Wurm 빙 하기 를 잘 나타내 주고 있다(그림 4-45) . 이 같은 동위원소 지질온도계를 이용하여 제 4 기의 빙하기 , 간빙기 의 기후변동이 잘 연구되었다. 빙하기는 DSDP 에서 얻어진 시료 중
유공충의 산소 동위원소 성분이 해수온도의 변화와 빙하에 기인한 해 수의 동위원소 성분변화를 잘 반영해 주었다. 특히 저 서 성 유공충 (Benth o nic fora mi ni f era ) 과 부유성 유공충 (Pla· nkto n i c fora mi nifer a) 사이에 동위원소 성분변화는 저서성 유기물이 물 의 동위원소 성분의 영향을 더 받는다. 그리고 부유성 유공충의 01so 의 값은 물의 동위원소 성분과 온도의 영향을 받게 된다 ( Em i l i an i 와 Shackleto n , 1978) . 그림 4-46 의 태평양의 적도지역의 시료에서 얻은 결 과 로 1 4 0Ma 년 간 이들간에 대단히 유사한 변화경향을 나타내고 있어 동위원 소 의 변 동은 주로 적도지방의 표충수의 수온보다 물의 동위원 소 성분에 크게 지배받고 있음을 나타내 주고 있다.
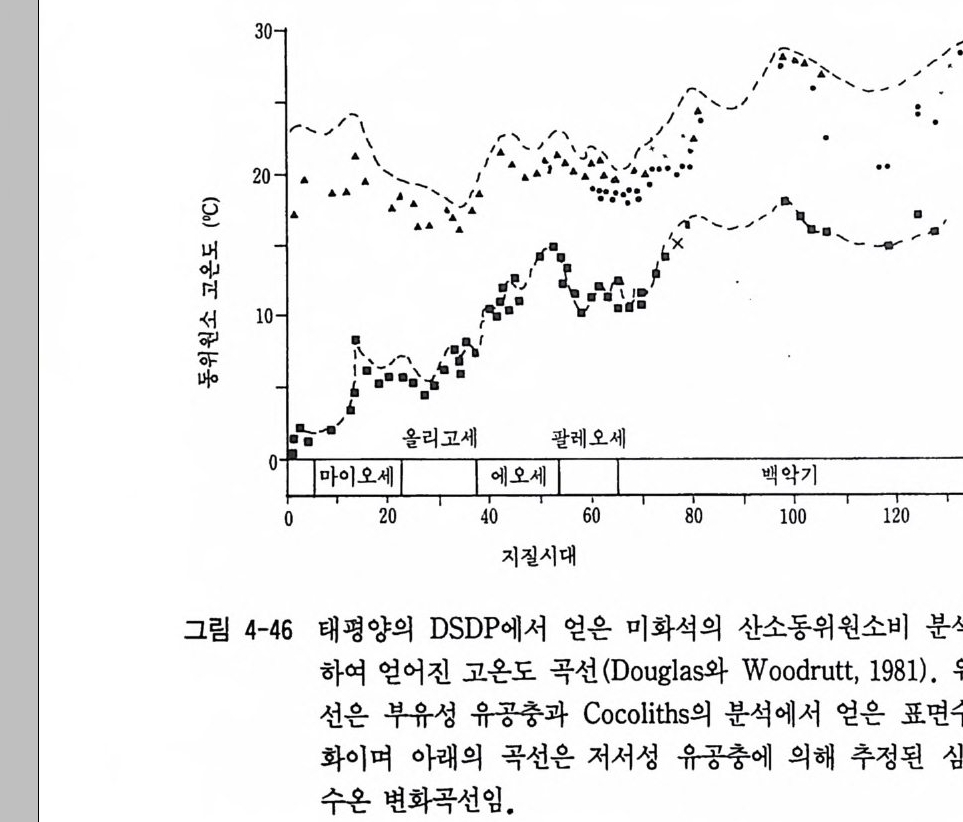 며앞()中231000 ^. .., ./- ·\·\ ' `..·` . .`. ` ~..., ~’ .'-{. ,.1 .: ~.. .•: , . `’.1 •'_. ' , ,•.. i••, - .남....•.. .-\.• :. . .-.. ^;. . .-,..., ,.../J . ., \ • ,. • ~,•/ x. 지 . .·r~• ; 、`` `一--, ✓ , -/ ,· .표`~ .\·.•- .. ` ,- ` _ - ..-..-, -’:• ,..• - . ,: , ,• 一. .
며앞()中231000 ^. .., ./- ·\·\ ' `..·` . .`. ` ~..., ~’ .'-{. ,.1 .: ~.. .•: , . `’.1 •'_. ' , ,•.. i••, - .남....•.. .-\.• :. . .-.. ^;. . .-,..., ,.../J . ., \ • ,. • ~,•/ x. 지 . .·r~• ; 、`` `一--, ✓ , -/ ,· .표`~ .\·.•- .. ` ,- ` _ - ..-..-, -’:• ,..• - . ,: , ,• 一. .
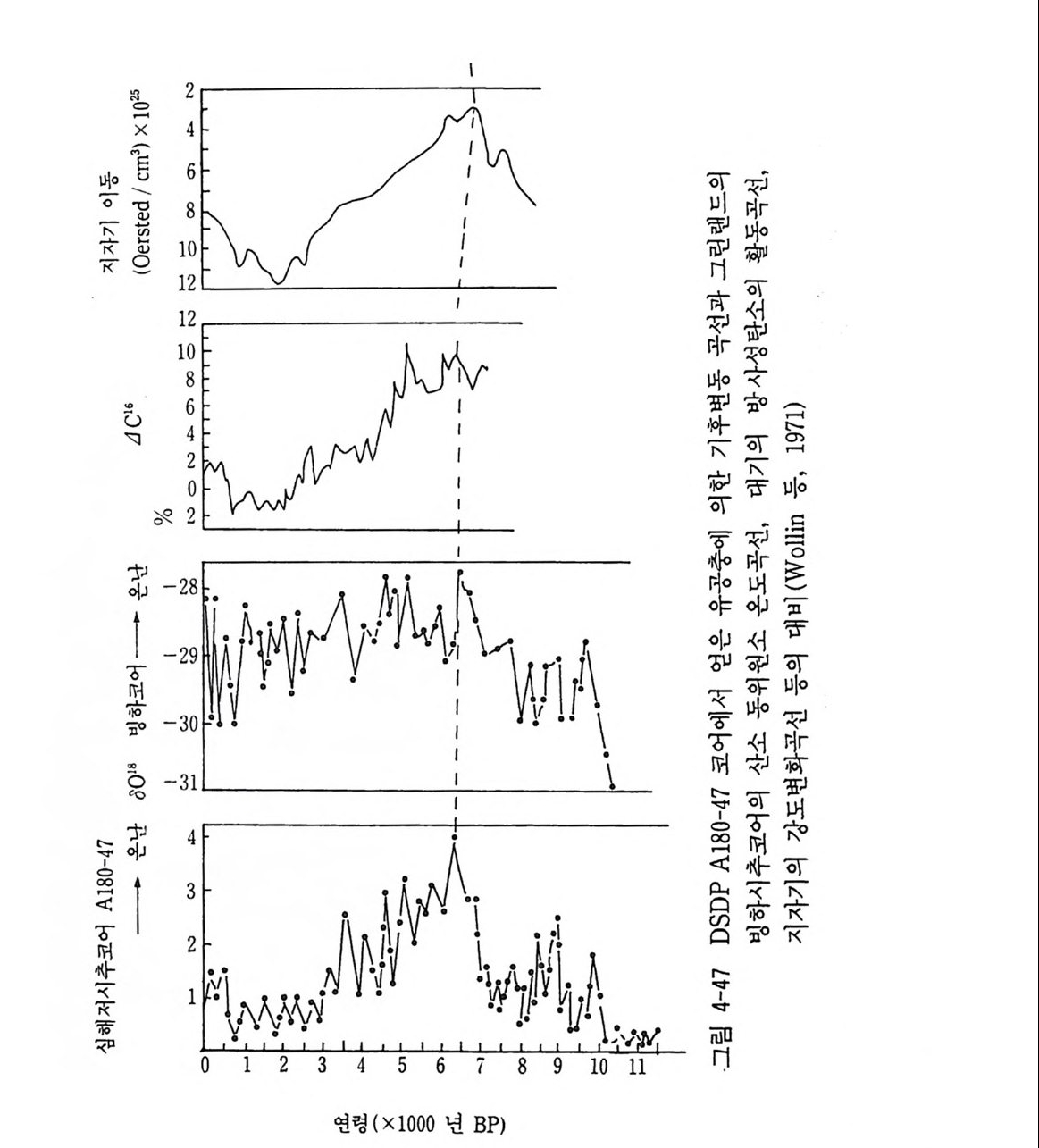
탄소 동위원소 성분변화도 저서성과 부유성간에 1~2%, 차이가 있 어 심층수가 표충수에 서 보다 H2CO i의 12c 가 1~ 2%, 더 농집 되 어 있 기 때문에 부유성 유공충보다 저서성 유공충에 1-2%, 더 농집되어 있 다. 일반적으로 백악기 중기 이후부터 이 지역의 해수는 냉각되어 가고 있으며 에오세와 올리고세~마이오세 중기에는 심한 해수온·변동을 나타내고 있다. 제 3 기의 심층수의 최고 온도는 14°C 정도이다. 현재 이 지역의 심층수의 수온은 l~2 ° C 이다. 이같이 급격한 온도 강화는 마이오세 중기 이후부터 일어나고 있는 범세계적인 기후변동을 잘 말 해 주고 있다. 이 시기가 바로 남국의 대규모 빙하작용 시기이다. Dansga ~ rd 등(1 973) 과 Wollin 등 (1971) 에 의해 빙하의 산소 동위 원소와 고기후가 연구되었다. 케이프 버르드섬 부근 심해저 퇴적암 시추코아에서 유공충을 통해 얻은 기후변화 곡선과 그린랜드의 빙하 시추코아의 산소 동위원소 분석결과를 비교하여 보아도 비교적 잘 일 치하고 있다. 특히 6500BP 경에 기후변동의 경계가 일치하고 있다(그 림 4-47). 수차례 반복되는 작은 기후변동은 태양방사의 변동과 과련이 있는 것으로 보여진다. 또한 대기중의 14C 농도와 지구자장 변화와도 잘 일치하고 있다. 죽 온난기에는 방사성탄소가 증가하고 지자장의 강도 는 감소하고 있다. Shackleto n 등 (1983) 은 탄소 동위원소비 분석에서 6500BP 경의 빙 하기의 대기에서 CO2 농도가 감소하였음을 지적하고 빙하 시추코아 에서 CO2 함량을 직접 측정하여 이룰 입증하였다. 되적암의 대표적인 몇 가지 종류와 점토광물의 동위원소 연구결과 를소개한다. (1) 석회암 석회암의 동위원소 성분변화에서 지질시대가 오래될수록 18Q /16Q
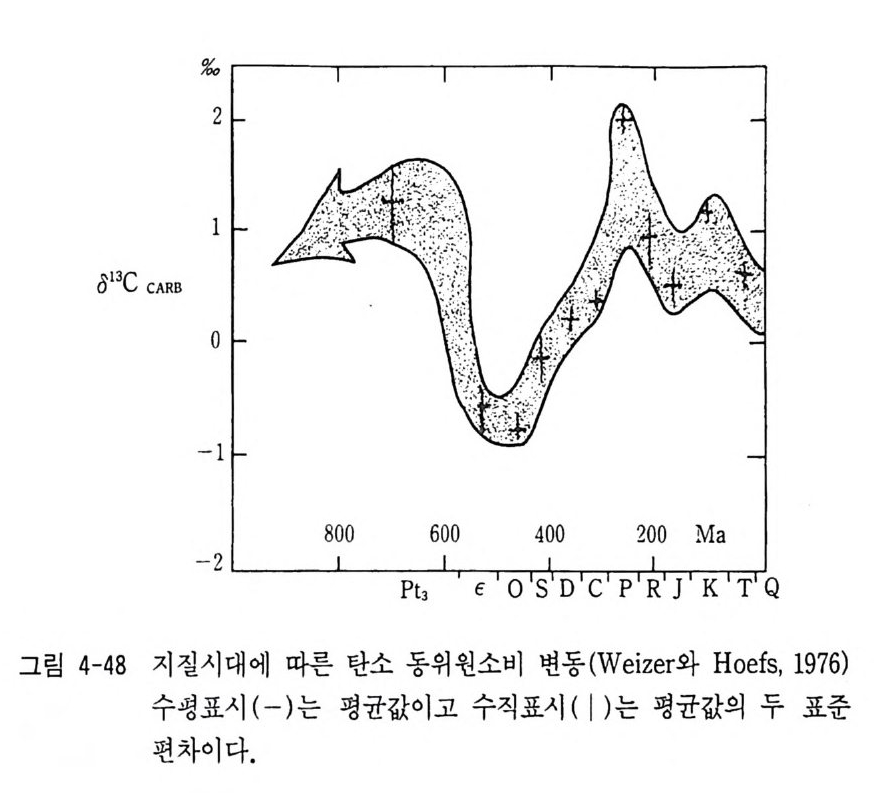 氐
氐
비 가 감소하는 경 향이 나타났다 (Ke ith와 Weber, 1 964 ; Ve i zer 와 Hoefs , 1976) . 이 같은 경향은 가벼운 동위원소로 된 순환수와 계속적인 퇴적 후 동위원소 평형 (po st- de p os it ion al equ i li br ia ti o n ) 반응 때문인 것으로 풀 이된다. 지질시대를 통하여 13c112c 의 비는 3~5%, 변화를 나타내고 있으 며 지질시대에 따른 변화경향 (Secular va ri a ti on) 은 그림 4-48 과 같다. 이같은 변화경향은 지질시대 중의 황산염의 황동위원소의 변화경향과 유사하게 나타나기도 한다. 석회암은 퇴적환경에 따라 담수환경에서 퇴적된 담수성 석회암과 해수환경에서 퇴적된 해성 석회암으로 구분된다. 이들의 퇴적환경의 차이로 인해 동위원소 성분에 차이가 나타난다(그립 4-49). 일반적으
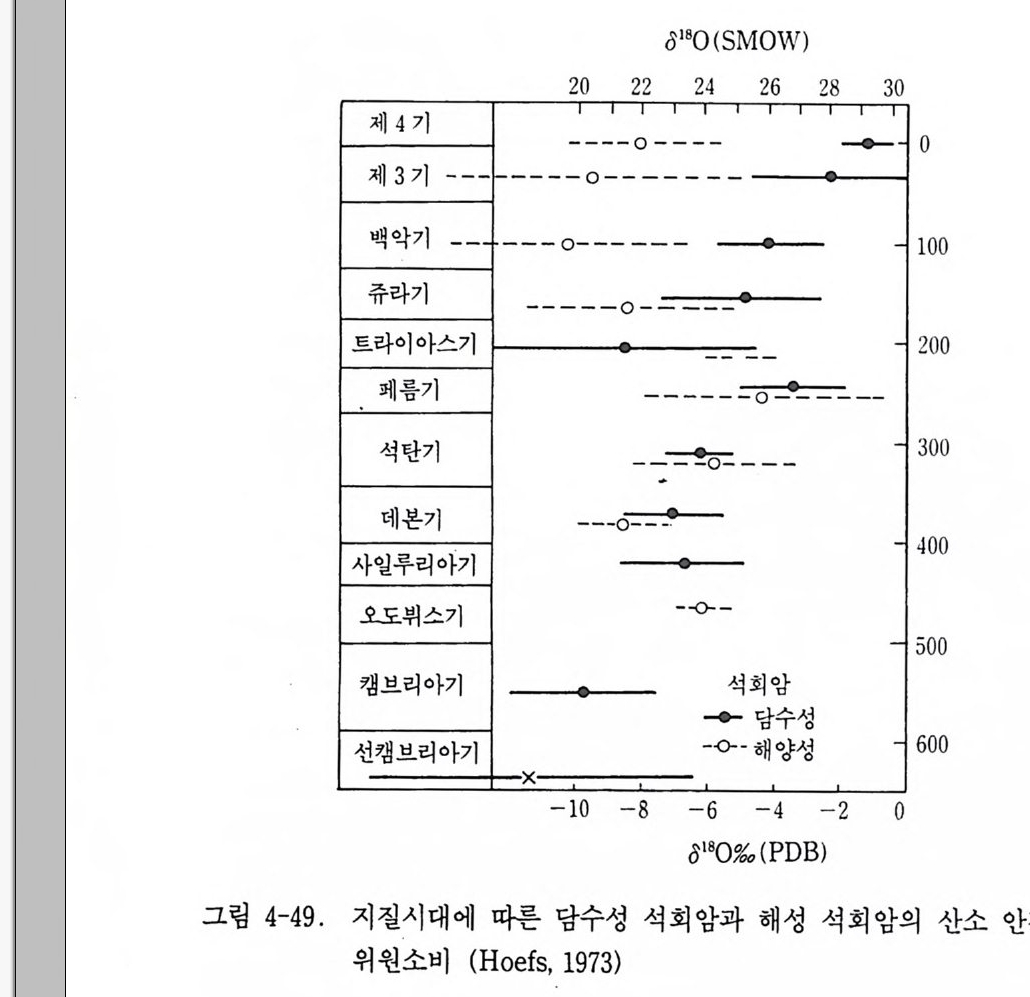 o180(SMO W )
o180(SMO W )
로 담수가 해수에 비해 180 이 결핍되어 있고 토양에서 유래된 유기기 원의 C 아의 영향을 많이 받기 때문에 담수성 석회암이 해성 석회암 에 비해 가벼운 동위원소로 되어 있고 변화폭도 크다 (Ke it h 와 Weber, 1964 ; Hoefs , 1973) . 동위원소 성분변화를 일으키는 근본적인 원인은 퇴적환경과 담수의 증발 정도이다. 예를 들면 증발이 심한 호수에서 퇴적된 탄산영암은 해성 석회암보다 0180 값이 더 클 뿐만 아니라 018(; 값도 크다 (Ro th e 와
Hoefs , 1977). 이는 대기와 표면수간의 CO2 동위원소 교환 때문일 것 이다. 계절변화에 따른 유기퇴적물의 종류의 변화에 따라 13c112c 비 의 변화가 일어난다 (McKenz i e, 1982). 담수성 완족류, 부족류, 달팽이 등의 화석으로 고수온 추정을 시도 하였으나 (Fr it z 와 Pop la wski, 1974 ; Yap p, 1979 ; Ma g ar it z 와 Heller, 1980 ; Abell, 1 986) 담수의 동위원소 성분은 변화가 심하고 증발에 의해 쉽 게 변하므로 정량적인 해석이 어려웠다. 그러나 달팽이의 경우 온대 가후 지역과 건조기후 지역 사이에 2%, 의 산소 동위원소비의 차이가 나타났다. 한편 해성 석회암은 伊 C = 0%, 내의가 많고 산소는 20~24%, 내의 가 많다. 물론 변질작용이나 변성작용에 의해 이 값들이 변화한다. 최근 석회암 자체보다 퇴적암의 고질물질로 사용된 시멘트 물질의 동위원소비가 속성작용의 과정을 해석하는 데 크게 기여하고 있다 (Hu dson, 1977 ; Dic k son 과 Coleman, 1980 ; Moldovany i 와 Lohmann, 1984 ; G i ven 과 Lohmann, 1981) . 탄소 동위원소비보다 산소 동위원소비가 속성작용 중 순환수나 해 수에 의한 영향을 잘 반영하여 주고 있다. 지표 부근의 속성작용에서 시멘트 물질의 동위원소비의 변화 경향이 뚜렷하연다• OIBC 변화는 식물기원의 토양에서 유래된 CO2 의 특칭이 퇴적암에 반영되고 있다. Beeunas 와 Knau t h(l985) 는 이와 같은 경향을 중부 아리조나 주의 메스칼석회암 (12 억년)에서 확인하고 선캠브리아기의 지표에 식물이 덮여 있었음을 주장하였다. D i ckson 과 Coleman(1980) 은 연속적인 속성작용의 시멘트 물질연구에서 초기 시멘트 물질에는 818O 와 018C 값이 크고 후기로 감에 따라 점진적으로 감소하는 경향을 밝혀냈다. 이 같은 사실을 온도상승과 매몰 속성과정 동안 공극수의 동위원소적 진화 때문으로 해석하였다. 또 818C 변화는 매몰 속성과정 동안 유기 기원의 CO2 의 증가로 해석하였다. 우리나라의 고생대 조선계의 · 석회 암의 동위원소비 분석에서 이들 석회암은 평균 o'3C = -1.1%,,
0180 = +16.0%, 으로 해성 석회암의 값의 범위를 나타내고 있다(김규 한, 1980), 광역변성작용에 의해 비변성 석회암에서 보다 8180 값이 작으며 변화폭이 크게 나타났다. 그리고 육성퇴적층인 경상계 지충 중의 탄산영암은 대석회암동의 석회암과 탄소 및 산소 동위원소값이 구별되어 해성 석회암과 다른 육성 석회암의 특칭을 나타냈다. 풍촌 석회암의 동위원소 분석으로 속성작용의 온도와 심도를 해석하였다 (박병권과 우경식, 1986). (2) 처어트 처어트는 저온에서 물과 석영 사이에 동위원소 분별정수가 크기 때 문에 보통 180/160 의 비가 높다. 탄산영암에서와 같이 여러 지질시 대의 처어트 시료분석에서 고해수의 동위원소 성분, 온도 그리고 속 성작용의 역사 등을 해석할 수 있다. 처어트는 광물성분이나 화학성 분 변화는 적지만 산소 동위원소 성분은 25%, 까지 변화한다. 퇴적암 의 심도가 깊어침에 따라 여러 종류의 실리카의 산소 동위원소비가 감소하는 경향이 밝혀졌다 (Knau th와 Ep st e in , 1975, Murata 등, 1977). 심도에 따른 이 a180 의 감소는 온도의 상승이나 가벼운 물과의 동 위원소 교환으로 인한 것으로 해석되었다. 처어트 중의 인회석이나 기타 인산염 광물원의 인산을 추출하여 산소 동위원소비를 분석하여 고수온 해석에 응용하고 있다. (3) 인산영광물 특히 P04 는 퇴적 후 비유기적 변화에 안정하므로 생물기원의 인회 석과 갇은 인산영광물의 산소 동위원소비는 퇴적환경 해석에 유용하 다. 인산염의 산소의 8180 값의 지질시대에 따른 변화는 신생대-현생 인산영암 (Phos p ho rit e) 은 25~20%,, 신생대와 중생대의 인산염암은 20~15%,, 고생대와 선캠브리아기의 것은 12.5%, 이하로 지질시대가
오래됨에 따라 8180 값이 작아진다. 퇴적 후 동위원소 교환 이의에 보통 지질시대에 따른 동위원소값 (81 8 0) 의 변화의 원인을 설명하는 방법에는 ® 지질시대에 따른 해수의 a180 값의 변화 ® 해수온의 변 화 ® 지질시대에 따른 인산영암충의 퇴적위치 등이 있다. 위의 그림 4-46 의 경향은 지질시대 동안에 해수의 a180 값이 일정 하였다고 가정하면 시대에 따라 해수온의 변동으로 해석할 수 있다. 이를 Lon gi nell i와 Nu ti (l973) 에 의한 o180(POt ) 지질온도계의 식 t = 111 .4 -4.3(op - ow) (여기서 t는 평균수온 ( ' C), 써 = 인산이온의 180 / 160 비, ow = 시료와 동위원소적으로 평형에 있었던 CO2 의 값임)을 이용하여 계산하면 고생대의 해수온이 약 40°C 였음을 알 수 있다. Knau t h 와 Ep stei n ( 19 75) 은 심 해 성 퇴 적 처 어 트와 캘 세 도니 에 포함 된 물을 분석하여 oD 값 - 57~ ― 86%, 를 얻었다. 이 물은 실리카내에 있는 수산기에서 유래된 것으로 밝혀졌다. 처어트 중의 인산염광물을 추출하여 8180 값을 분석한 선캠브리아 기에서 오늘날에 이르기까지의 해수온 변동에 관한 연구도 있다 (She mesh 등, 1983) . (4) 돌로마이트 돌로마이트의 지화학적 · 퇴적환경과 돌로마이트의 기원에 대해서는 아직 이론이 많다. 그러나 석회암의 돌로마이트화 작용 쪽으로 설명 이 진전되고는 있다. 안정동위원소비를 이용하여 돌로마이트의 형성환경에 대해 Matth ew s 와 Katz ( 1977) , Aharn 등 (19 77) , Land (19 80) , McKenzie ( 1984) 등이 많이 연구하였다. 돌로마이트는 과염분 해수환경이나 Subti da l 해수환경에서 퇴적되 고 있다. 그러나 돌로마이트의 동위원소 성분은 미지의 요인에 의해 크게 값 이 변화하고 있다. 화석 돌로마이트는 흔히 증발잔류암과 수반되며,
int e r tid a l 돌로마이트와 sup er ati da l 돌로마이트는 보통 기존 탄산염 의 치환에 의해 형성된 것이다. McKenz i e(1984) 는 페르시아만의 해안의 Sabkhas 의 돌로마이트화 작용 연구에서 아라고나이트와 M g겨J-해석이 돌로마이트 형성의 중 간과정 역할을 하고 있는 것으로 보았다. 염분도 스펙트럼에서는 순 환수와 해수의 혼합대에 형성되고 있었다 (Land , 1980). 이 같은 사실 은 선캠브리아기의 돌로마이트 퇴적과 조화적이다 (Tuck e r , 198 3) . 돌 로마이트의 속성작용과 기원해석을 할 때 동위원소 자료는 다음의 문 제점이 제기된다. ® 낮은 퇴적온도에서 물-돌로마이트간의 산소동위 원소 평형분별 계수결정이 불가능하다. ® 대규모의 마그네슘이 유입 되어야 하기 때문에 돌로마이트화 작용은 단순히 개방계에서 일어나 는 심것해으 로되적 한기 원것이의다 .돌 로마이트의 탄소 동위원소 성분은 —60 ~+ 2 0%, 로 변화가 큰 반면에 대륙 주변부나 Platf orm 돌로마이트는 ~2-+ 4 %, 의 값을 가진다. 심해성 돌로마이트 중 13C 이 결핍된 돌로마이트는 천해성의 유기물 기원에서 형성된 것아고 13c 부화된 돌로마이트는 심해수에 용존하고 있는 H2C03 가 메탄 형성과정의 환원반응에 의해 CO2 가 소실되어 메 탄이 형성되는 과정에서 심해에서 형성된 것이다. 박테리아 기원의 돌로마이트는 013C = -60-+21%, 의 값을 가진다 (Dewser, 1970). 돌 로마이트-방해석의 동위원소 분별실험에서 돌로마이트가 방해석보다 180 가 더 많이 포함됨이 밝혀졌으며 자연의 시료분석에서도 갇은 결 과가나타났다. 돌로마이트와 방해석간의 동위원소 분별이 작은 것은 탄산이온과 용액간에 산소 동위원소 교환반응 없이 CaC 아 격자내에 M, t+ 이온 이 확산되어 들어가는 돌로마이트화 작용시의 비평형으로 해석하였으 나 Ma tt hew 라 Ka t z(1977) 는 돌로마이트화 작용이 확산에 의하지 않고 용액 침전과정에 의해 일어남을 설명했다.
돌로마이트의 동위원소 성분변화 요인은 유기물질의 속성변질작용, 유기물질의 양, 퇴적속도, 지하중온률 등이 있다 (Kel t:s!나 Mc Kenzie, 1982). (5) 점토광물 해수나 담수와 암석간에 일어나는 화학적 풍화, 저온에서 일어나는 퇴적물의 속성작용 그리고 고온에서 열수용액에 의한 모암변잘에 의 해 점토광물이 생성된다. 동위원소 분석으로 이들 각 기원에 의해 만 들어진 점토광물을 구별할 수 있다 (Sav i n 과 Eps t e in , 1 970). 규산영광물의 화학적 풍화에 의해 형성된 점토광물의 수소 및 산소 동위원소 성분은 다음 사실에 의해 영향을 받는다. ® 점토광물 형성시 존재하였던 물 ® 물-정토 동위원소 교환 평형 정수 ® 온도 등아다. Yeh 와 Savin ( 1976), Sav i n 과 E p s t e i n(1970) 에 의해 몇몇 점토광물들과 물 사이의 평형정수가 얻어져 있다. 일반적으로 지구상의 토양은 0180 = +15~+25%, 와 oD = _30~ _ 100 %, 의 값을 가진다. 풍화시의 동위원소 성분은 모암보다 물의 영향을 더 많이 받기 때문에 김사이트(gi bbs it e) 가 많은 토양이 나 Al-Fe 수산화물이 많은 토양은 기타의 점토가 많은 토양에 비해 180 이 결핍되어 있다 (Lawrence 와 Tayl o r, 1972). 죽 풍화토양은 순환수의 동위원소 성분변화에 크게 영향을 받는다. 그림 4-50 에서와 같이 퇴적 점토광물의 oD 와 0180 동위원소 성분을 oD-a180 그립에 도시해 보면 oD = 80180+10 인 순환수의 동위원소 성분선과 평행하다. 죽 고령토 선, 몬모리로나이트 선과 순환수 선과 평행하며 이는 점 토광물 형성시의 기후조건을 잘 반영해 주고 있다. 고령 토-물간의 수소 동위 원소 평 형 상수는 L i u 와 Ep st e i n ( 1980) , Lambe rt와 E p s t e i n(1980) 의 실험에서, 산소는 Kullar 와 Anderson (1978) 에 의해 얻어졌으며 기타 점토광물에 대하여서도 고온실험 결 과로 저온까지 의삽법에 의해 알려진 온도, 기지, 물의 동위원소 성
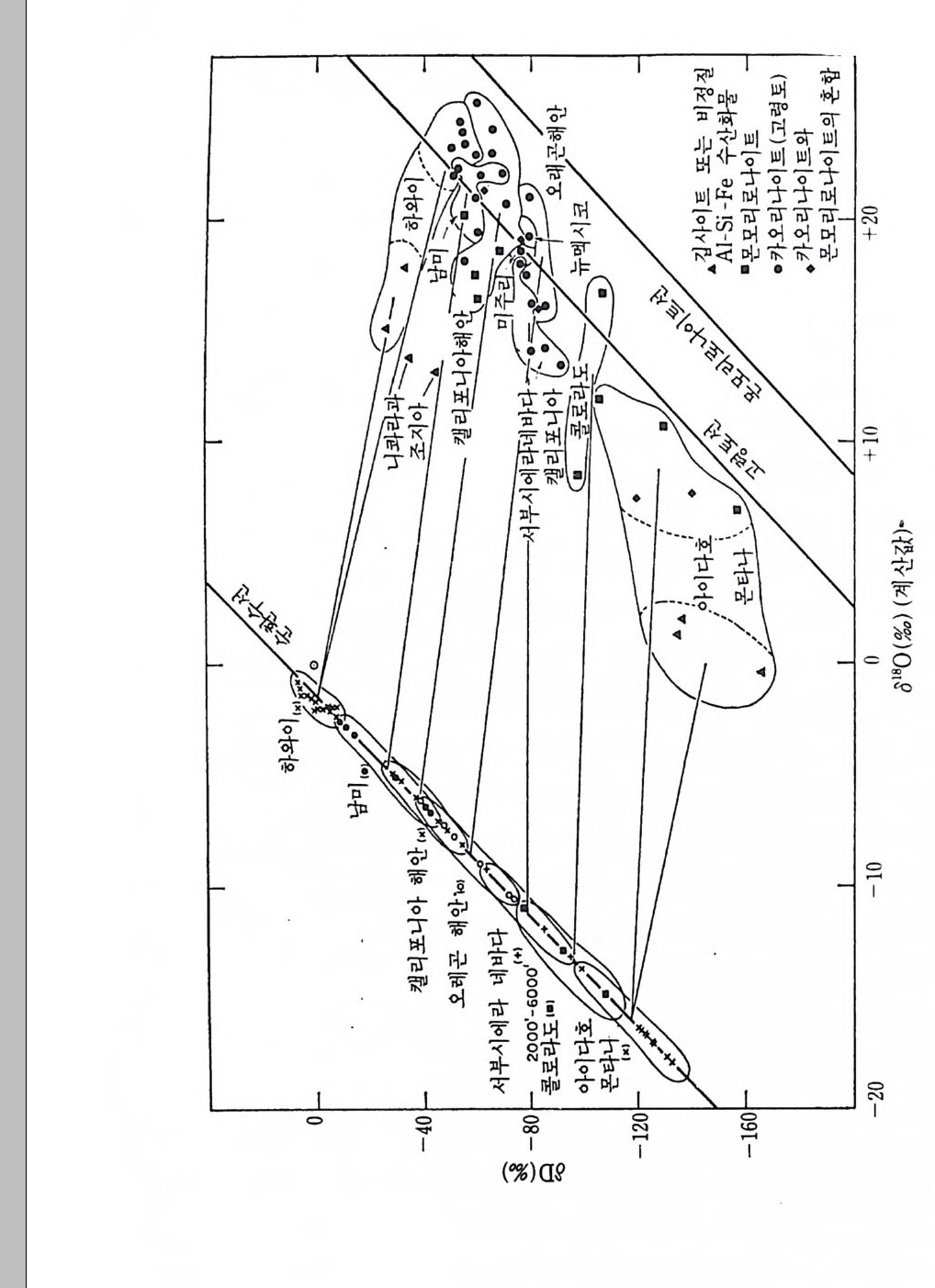 이 는트사E 비 정또그질ASF l--ei 수물화산 •·이리트몬나모로 나고리오카트•)(토이 령카·이 트나리와오 로리트 혼모이몬,합 나의 20+ y7ro1l) 1a,T9와ecner
이 는트사E 비 정또그질ASF l--ei 수물화산 •·이리트몬나모로 나고리오카트•)(토이 령카·이 트나리와오 로리트 혼모이몬,합 나의 20+ y7ro1l) 1a,T9와ecner
분에서 형성된 점토광물의 동위원소 성분비교에서 수정하여 사용할 수 있다. 일반적으로 Auth i g e nic 성분은 Detr i ta l 성분과 동위원소 성분에서 구별된다. 쇄섭성 광물 (de t r it al m i neral) 의 0180 값은 기원암의 값을 대표한다. Rex 등(1 969) 은 태평양 해저 퇴적물의 기원을 연구하기 위하여 퇴 적물 중의 석영의 동위원소바를 분석한 결과 동위원소비는 균일하며 석영의 81 8 0 값은 하와이의 토양과는 다름을 조사하였다. 풍성기원의 해저 퇴적물의 동위원소비는 균일하며 대륙권 먼지의 동위원소값과 유사하므로 이 풍성기원의 석영은 대륙에서 유래한 것 으로 해석되었다. 만일 Auth i g en ic 광물이 공국수와 동위원소 평형에 서 형성되었다면 원래의 동위원소 성분이 그대로 남아 있게 될 것이다. Yeh 와 Savin ( 1976) 은 점토광물과 해수간의 산소 동위 원소 교환평 형은 대단히 느리므로 쇄설성 0180 값은 광물 형성시의 환경을 반영 해 줄 수 있음을 입증했다. 이들은 수백만년된 해양되적물 중 0.1~0.5µm 크기와 이보다 더 조립질인 육성 점토광물은 원래의 산 소 동위원소 성분을 유지하고 있을 것으로 믿었다. 그러 나 Yeh 와 Ep st e i n 0 978) 과 Yeh (l98 0) 는 여 러 크기 의 점 토광물 에서 D/H 바를 측정한 결과 oD 값이 -33~ ― 72% 로 변화함을 조사 했다. 이 사실은 속성작용 동안에 점토광물의 동위원소 성분 변화는 일차 적으로 광물반응의 규모와 셰일의 탈수화반웅 말기에 스멕타이트 (Smec tit e) 에서 일라이트 (Ill it e) 로 변환됨으로써 일어나는 것으로 해 석했다. 양성자 교환기구에 의해 일어나는 수소 동위원소 교환반응에서 교 환속도는 용액의 PH 에 영향을 받게 된다 (O'Ne il과 Kharaka, 1976). 수소동위원소 교환반응 속도에 있어서 스멕타이트가 3~5 배 더 빠른 현상은 스멕타이트 결정구조내의 층간수의 존재가 결정적인 요인이라
고 보고 있다. 해양되적물은 주로 일라이트, 스멕타이트, 혼합총 접토, 녹니석, 고령토, 석영, 장석 등의 다양한 광물로 구성되어 있으므로 해양퇴적 물의 전암의 동위원소 성분 추정은 쉽지 않다. 해성 셰일은 현생 해 양퇴적물의 광물성분 및 화학성분과 대단히 유사하며 셰일의 동위원 소 성분은 +14 ~ +19%, 내의이다. Yeh 와 Sav i n(l977) 은 멕시코만의 시추에서 얻은 셰일의 산소 동위 원소 성분을 분석했다. 그 결과 세립질 점토광물이 조립질에 비해 1 8 0 이 많았고 점토광물 간의 비평형은 속정작용의 온도가 증가함에 따라 현저하지 못하였다. 점토광물의 입도별로 동위원소 성분 차이가 나타났다. 이는 상이한 입도의 점토광물간의 동위원소가 비평형 상태였음을 가리킨다. 그리 고 Yeh (l 980) 의 셰일의 동위원소 연구에 의하여 잔류 용액과 공극수 사이에 동위원소 분별이 크게 일어났음이 조사되었다. 그리고 셰일의 매몰속성작용 기간에 일어난 몬모리로나이트에서 일라이트로 변화가 후기 탈수화반웅의 가장 중요한 메커니즘임을 규명하였다. 우리나라 의 경우 문희수(1 986) 에 의한 제 3 기충에 배태된 벤토나이트의 동위원 소비 분석에서 점토광물의 형성 온도와 퇴적층후가 해석된 바 있다. 3) 변성암류의 동위원소 성분 변성암은 변성작용의 유형에 따라 광역변성작용과 접촉변성작용으 로 구분된다. 변성암은 화성암이나 퇴적암이 높은 온도와 압력하에 광물학적으로 재결정되어 변형된 것이다. 따라서 변성암의 산소 동위원소비 분석에서 ® 변성작용시 의부에 서 공급된 물을 연구할 수 있고 ® 변성작용 동안 변성광물간의 동위 원소적 평형 또는 비평형상태를 확인할 수 있으며 ® 변성작용시의 온도와 ® 유체-암석 상호반웅의 특성을 연구할 수 있다. , 공존하는 광물 사이의 평형은 광물조합에서 추정하지만 동위원소
분별을 이용하면 공존 광물간의 동위원소 평형 또는 비평형을 추정할 수 있다. 동위원소적 평형, 비평형에서 변성작용의 과정을 해석할 수 있다• 실험에서 얻어전 동위원소 지질온도계를 이용하면 변성작용시의 온 도를 추정할 수 있다. 만일 A, B, C 세 종류의 광물이 평형상태에서 형성되었고 또 그 후 평형이 보존되어 왔다면 세 광물 사이에 두 독립된 동위원소 분별빈 도와 일치온도 (Concordan t t em p era t ure) 가 얻어져야 할 것이다. 만약에 4A - B 와 4A - c 의 값을 도시 하면 4 값은 한 직 선 위 에 도시 되 어야 하며 이 직선은 기원암의 값을 가리키게 될 것이다 (Ta y lor , 1968 ; Schwarcz 등, 1970 ; Dein e s, 1977) . 세 광물상 중에 한 상이 만일 잔류광물상이거나 후퇴변성작용 동안 에 동위원소 평형이 이루어졌다면 불일치 온도(Di scordan tt em p era tu r e) 가 얻어지게 될 것이다. 이런 현상은 보통 후퇴변성작용 동안에 액상과의 반응 때문에 일어 나는 것으로 해석되고 있다. (1) 광역변성작용 광역변성작용에서 형성된 변성암 중 특히 니질기원암은 180 / 160 바 가 변성도가 증가함에 따라 감소하는 경향이 있다. 보통 저변성도의 니질기원암의 8180 는 셰일(1 5~18%, )의 값과 유사하나 편마암류는 6~10% 내이다. 이 같은 현상은 변성작용시 의부에서 계속적으로 물 이 공급되었기 때문으로 해석되고 있다. 다변성작용 지역에서 SD 와 8180 값의 분석으로 변성작용의 에피소드를 식별할 수 있다. 그러나 광역변성작용에 있어서 변성용액과 암석의 반응이 개방계에 서 일어나느냐 폐쇄계에서 일어나느냐에 따라 동위원소 분석결과의 해석이 전혀 달라진다. 만일 변성작용이 개방계에서 일어난다면 변성유체는 모든 암석과
반응해 균일화된 변성용액을 만들어야 될 것이다. 그러나 변성암들의 동위원소 분석결과 균일화된 변성용액은 아니었다. 그러면 폐쇄계에 서 의부에서 유입된 변성용액과 암석 사이에 변성작용이 일어난다면 진화된 변성유체가 폐쇄계내의 기타 암석과 반응 없이 그 지역의 변 성암에 영향을 주어 그 특성이 변성암내에 잔재해야 할 것이다. 전자의 경우 광역변성 작용시에 변성유체가 대류에 의해 순환되면 동위원소 성분이 균일화될 것이다. 그러나 변성유체의 이동특성과 변 성유체의 양의 다소에 의해서도 동위원소 성분은 변화할 것이다. Hoernes 와 Fr i edr i ch i sen (1 978) 은 헤르시니안의 전기-알파인 변성 작용시에는 대규모의 화성기원 및 되적기원의 편마암이 산소 동위원 소 평형에 있었고 이를 덮쳐 일어난 알파인 변성작용시에는 소규모의 동위원소 평형만 일어났음을 지적했다. 또 그들은 알파인 변성작용의 온도는 530 ° C 를 넘지 못했을 것이며 전기-알파인 변성작용은 600°C 이상이었을 것이라는 사실을 동위원소 분석연구에서 얻었다. (2) 접촉변성작용 화성암과 퇴적암은 산소 동위원소비가 현저하게 다르다. 따라서 접 촉변성작용시에 이들간의 동위원소 교환에 의한 동위원소비의 변화를 예상할 수 있게 된다. 모암과 관입암체 사이에 산소 동위원소 교환의 비율은 암석의 종류 에 따라 다르다. 접촉대의 폭은 관입암체의 크기, 온도, 고온 지속시 간, 유체의 존재유무에 따라 크기가 변화된다. 접촉대에서 동위원소 의 급격한 변화는 소규모의 동위원소 교환이 재결정 작용시 확산의 조철을 받으면서 고체 상태에서 일어났음을 의미한다. 접촉변성작용 의 경우도 광역변성작용시와 같이 접촉변성작용시에 계내로 의부에서 유입된 물과 접촉부위에서 두 암석간에 일어난 동위원소 평형, 모암 과 관입암체간에 동위원소 교환 범위 등을 추정할 수 있다.
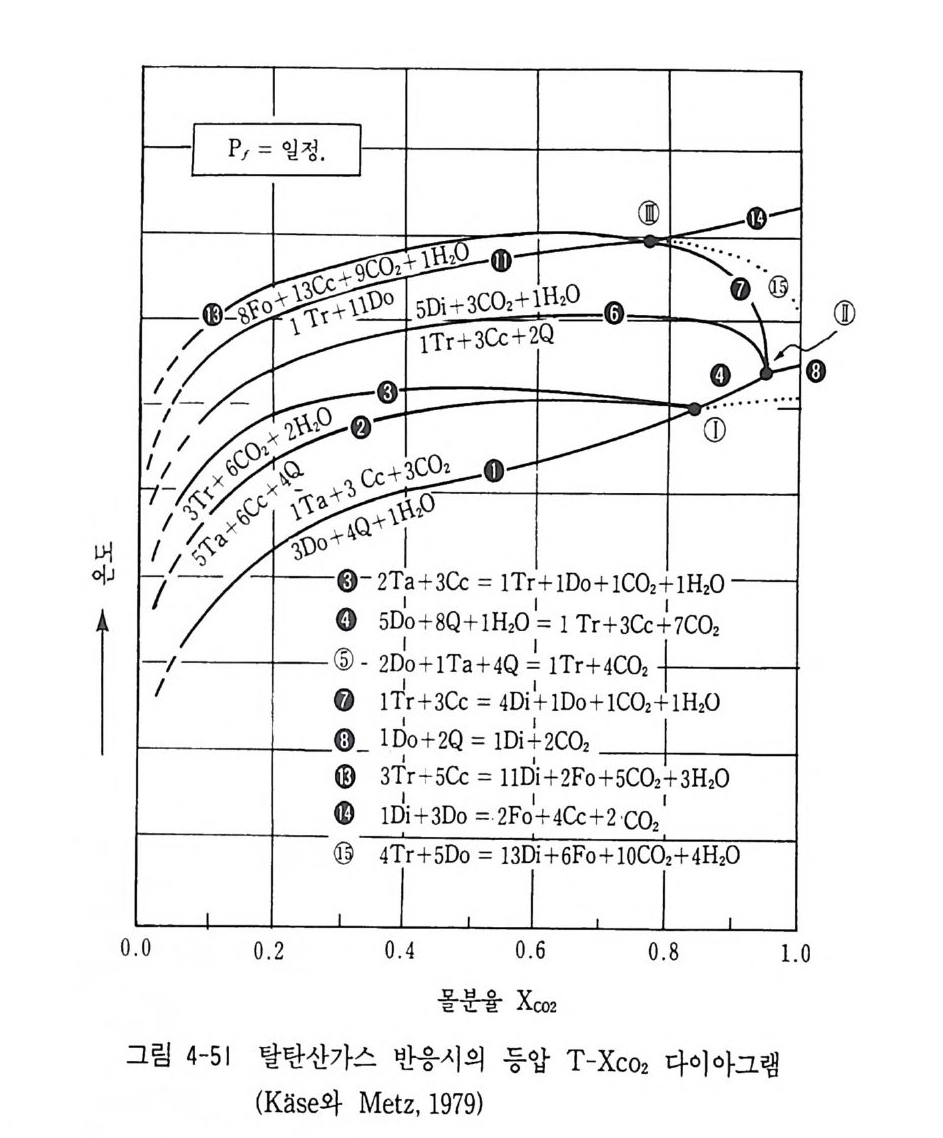 ®
®
탄산영암과 화성암 사이에 다양한 탈탄산가스 반응과 함께 스카론 贊아 형성되며 이들 광물 사이에이루어진 동위원소 평형에서 Xco2, 탄소 및 산소의 기원, 생성온도 등과 열수용액의 이동방향 등을 해석 할 수 있다(그림 4-51). 접촉대에서 산출되는 석회규산영암과 대리암은 변성도가 증가함에
따라 a180 값과 013C 값이 점점 작아진다. 그 이유로는 탈탄가스 작용 과 같은 휘 발작용 (Volati liz a ti on ) , 유체 의 침 부작용 (Inf i lter ati on ) 그리 고 P-T-X( 압력, 온도, 성분) 조건의 변화 등을 들수 있다. 과거에는 접촉변성작용이 진점됨에 따라 탈탄산가스 반응과정 (Decarbona ti on pro cess) 에 의 해 스카론 광물의 탄소와 산소는 동위 원소값이 점 점 작 아진다고 보았다. 그러나 자세한 연구에서 휘발작용에 의해 항상 무거운 동위원소가 결핍되는 쪽으로 변화는 일어나지만 동위원소값이 큰 전이를 일으키 는 원인은 의부에서 유입된 유체의 침투임이 밝혀졌다. 유체의 양이 많고 유체와 암석 사이에 동위원소값의 차가 크고 암석의 두수성이 클 때 유체의 유입에 따른 동위원소 효과는 최대가 될 것이다 (Valle y, 1986) . 접촉에서 돌로마이트와 석영이 반응해서 투휘석이 형성되는 아래와 같은 탈탄산가스 반응에서 다음과 같이 체적이 35% 나 감소하여 결과 적으로 공국률이 크게 증가한다. CaMg (C03) 2+ 2S i 02 一 ➔ CaM g SbO 計 2C02 돌로마이트 석영 두휘석 183g : 63cm3 120g : 4lcm3 215g : 67cm3 이렇게 공국률이 증가하면 특수성이 증가하여 지표수나 열수의 이 동이 용이해져 스카론화와 함께 금, 은, 동, 연, 아연, 텅스텐, 몰리 브덴늄과 같은 금속광물이 침전되기 좋은 환경이 되어 유용광상을 형 성하기도 한다. 접촉대의 유체의 압력이 정수압보다 낮을 때에 지표수가 접촉대로 유입이 되어 대량의 지표수와 동위원소 교환반응이 일어나게 되며 PH20<
지 침두하여 미그마타이트의 부분용융 작용에 관여한 사실이 지표수 가 가장 깊이 침투된 예로 보고되어 있다. 많은 스카른형 광상의 연구에서도 스카론 초기 단계에는 심성암류 에서 온 마그마수가 크게 기여하게 되나 스카론화 말기로 감에 따라 순환수의 기여가 점증함이 밝혀졌다. 우리나라의 신예미 광상 (K i m 와 Nakai, 1 980), 월악 광상 (So 등, 1983) , 상동중석 광상 (Ki m 등, 1988) 동에 서 화강암과의 접 촉대 의 탄 산영암내에 13c, 180 가 결핍되는 현상이 잘 나타나고 있다. 강원도 영월군 상동읍에 소재하는 고생대 석회암충과 신생대 상동 화강암 사이에 발달하는 상동중석 광상도 전형적인 스카른 광상이다. 스카론광물 및 석영의 동위원소 분석에서 동위원소 지질온도계 및 광 물조합을 이용하여 구한 생성온도에서 후퇴 교대 변성작용의 과정이 밝혀졌고 (K i m 등, 198 8), 후퇴 교대 변성작용의 말기로 감에 따라 순 환수가 크게 기여하였음이 산소 동위원소비에서 나타났다. 상동화강암과 스카른 광물의 동위원소바 분석에서 상동중석 스카론 의 형성에 기여한 열수교대 광화용액은 상동화강암에서 유래한 것으 로 해석되었다. 자세한 내용은 광상 단원에서 설명하겠다. 스카른형 광상인 몬타나 에 있는 엘크혼 광상과 캘리포니아에 있는 파인크리크 광상의 광화용 액도 마그마 기원으로 조사되었다 (Brown 등, 1985). (3) 변성유체의 기원 광역변성작용은 지각 심부에서 일어나는 반면 접촉변성작용은 l~2 km 심도의 지표 부근 접촉대 (Conta c t aureole) 에서 일어난다. 기존 암석이 고온, 고압 조건에서 재결정되거나 확산 등에 의해 새로운 변 성광물이 만들어진다. 변성작용 동안 기존 광물간의 탈수소반응에서 변성유체가 형성될 수도 있고 상부 맨틀이나 지각 심부에서 유래되는 마그마수가 변성유체가 될 수 있다. 그리고 지표에서 유래한 순환수
와 화석수 그리고 열곡대에서는 해수원의 변성유체 (W ic kham 과 Tayl o r, 1985) 도 존재 한다. 변성작용 동안 광물은 상기의 변성유체와 함께 공존하는 광물들이 재평형에 도달해 동위원소 성분에도 변화가 일어난다. 이때 두 가지 경우로 나누어 생각해 볼 수 있다. ® 기존 광물의 동위원소 성분이나 구조 및 암상에 무관하게 동위 원소 성분이 균질한 다량의 유체가 광범위하게 스며들어 변성광물들 과 평형에 이르는 경우. ® 세맥이나 파쇄대 또는 기타 구조선을 따라 유입된 유체가 광물 입자 사이에서 지역적으로 동위원소 평형이 이루어지는 경우. 특히 접촉대나 투수성이 큰 지층을 통하여 국부적으로 유체가 유입되어 광 물과 국부적으로 평형에 이르는 경우를 들 수 있다. 대부분의 c-o -H 동위원소 연구에서 유체가 구조선이나 두수성이 큰 지충을 따라 유입 됨 이 밝혀 졌다 (Rwnble 등, 1982 ; Graham 등, 1983 ; Valle y와 O' Neil, 1984 ; Bebou t와 Carlson, 1986) . Kerric k 등 (1984) 에 의하면 단총이나 파쇄대가 형성될 초기에는 물 -암석 비가 낮은 국부적으로 유입된 유체에서 지질구조가 발달 전전 됨에 따라 물/암석 비가 높은 변성수로 변화된다는 것이다. 그 후 지구조운동이 진행됨에 따라 탈수소반웅이나 탈탄산가스 반웅이 일어 나며 지역에 따라서는 탈황산가스 반응 등이 일어나게 된다. 휘발성분이 유리되는 반응은 암석, 광물 사이에 탈휘발 반응에 의 해 생긴 유체와 암석 사이에서만 일어나는 레이리 휘발과정이나 모든 유체가 연속적으로 진화되는 배취 휘발과정 (Batc h vola tili za ti on) 으로 구분할 수 있으며 자연에서 일어나는 반응은 위의 두 경우 중의 하나 일 것이다. 변성휘발 반응의 가장 대표적인 예는 탈수소 반응과 탈탄산가스 반 응이다. 탈수소 반응으로 인한 암석의 산소 동위원소 효과는 1%, 아 하로 작다. 그러나 온도효과가 중요하다. 400~500'C 이하에서 H20
는 암석에서보다 동위원소적으로 가볍고 탈수소 반응에서 180 부화가 일어날 것이다. 그리고 500'C 이상 온도에서 H20 의 산소는 무거우며 탈수소 반응에서 180 이 결핍될 것이다 . 따라서 변성반응에서 서로 상 쇄되어 탈수반응에 따른 동위원소 효과는 1%, 이하이다 (Valle y, 1986) . 그러나 산소와는 대조적으로 암석에 수소의 존재량이 대단히 적기 때문에 탈수소반응에 따른 수소 동위원소 효과는 대단히 크다. 고온 에서 유체의 동위원소 성분은 유체가 유래되거나 통과한 주위 암석의 동위원소 성분에 의해 버퍼 (Bu ff er) 되기 때문에 산소보다 수소가 유 체기원 구분에 유용하게 이용된다. 마그마수와 탈수소 반응에서 유래한 변성유체는 oD 로 구별이 어렵 지만 순환수나 화석수기원의 변성유체는 구별이 가능하다. 광물-물 사이의 동위원소 분별을 이용하면 변성광물의 동위원소 분 석자료와 온도에서 변성유체의 동위원소비를 계산할 수 있으며 이 값 으로 변성유체의 기원을 추정할 수 있게 된다. 그러나 수소는 확산속도가 빠르기 때문에 변성온도보다 훨씬 낮은 온도에서 동위원소 교환이 끝나 버릴 수가 있으므로 변성암 중의 함 수광물의 수소 동위원소 평형이 이루어지기 어렵다. 탄산염암의 변성작용에서는 탈탄산가스 반응이 대단히 중요하다. 탄산영암의 변성반응은 유체상 중의 H20ICO2 의 비에 따라 영향을 받으며 탄산염암에서는 C 아만 생성되기 때문에 대부분 탄산염암의 변성반응은 H20 유입 때문에 일어나는 것 같다. Rwnble 등(1 982) 과 Graham 등 (1983) 에 의하여 상평형과 동위원소 분석자료에서 녹색편 암상과 각섬석상의 변성탄산염암은 W/R 츠 l~5 정도의 물이 침투한 것으로 설명되었다. 암석과 반응할 물의 양은 실제로 암석을 통과한 물의 최소량을 가 리킨다. 이처럼 높은 W/R 비는 변성탄산염암에서만 가능하다. 이질암과 사질암 지층은 이들 암석들아 물이 많은 유체를 만들기
때문에 이를 적용하기 어려우며 더욱이 외부에서 유래된 물의 영향을 거론하기 어렵다. (4) 변성암의 형성온도 변성작용시의 온도는 변성광물조합을 이용한 상평형에서 추정하고 있다. 산소와 규산염광물조합을 이용한 산소 동위원소 지질온도계와 방해석-흑연 사이의 탄소 동위원소 분별을 이용한 동위원소 지질온도 계가 수립되고 있다. 산소 동위원소 지질온도계는 광물쌍에서의 산소의 확산 계수, 광물 입자의 크기, 암석, 유체상의 특성, 두수성, 냉각속도 등의 여러 요 소에 의해 영향을 받는다. 예를 들면 브라질의 Iron Q uadran g le 에서 석영-자철석의 산소 동 위원소 분별로 구한 온도가 구조 변형사와 밀접한 관련이 있었다 (Hoefs 등, 1982). 후에 일어난 변형운동이 철광석광화에 덮쳐 일어 나 저온의 동위원소 온도가 재설정되어 있었다. 즉 이들 암석내에 영 리구조가 많이 발달할수록 온도 저하가 더욱 크게 나타났다. 변성광물의 동위원소 지질온도계는 석영-루틸, 석영-석류석, 석영 -자철석, 석영-휘석(고온)과 석영-백운모, 석영-흑운모, 석영-장석, 석영-방해석 (저온) 등이 연구되어 있다. 저온에서는 동위원소 분별이 크나 저온에서는 동위원소 지질온도계 로 온도를 추정하기 어렵기 때문에 동위원소를 이용한 저변성도의 변 성온도 계산은 대단히 홍미있는 과제이다. 그러나 암석이 세립질이라서 광물분리가 어렵고 산소 동위원소 지 질온도계로 이용하기 위해서는 속성작용에 의해 만들어전 세립질 석 영과 일라이트/스멕타이트 혼합충이 매몰과정 동안 서로 평형에 있 었다는 가정을 필요로 한다. Es li n g er 와 Yeh(1986) 는 탄산염암과 셰일의 매몰변성작용 최고온도 를 160~250'C로 추정하였다. 이 온도는 암석학적 추정온도와도 잘
일치한다. 오스트레일리아의 해머스레이 레인지의 호상철광충에서 처어트와 철산화물의 매몰변성작용 온도는 270~310°C 였다(B ecker 와 O'Neil, 1969 ; Ma g ar it z 와 Tayl o r, 1 974 ; !k i n 와 Harman, 1983) . 엔티고라이트의 수소 및 산소 동위원소비는 녹니석의 동위원소값과 대단히 유사하며 엔티고라이트가 변성유체와 반응해서 생긴 것으로 추정되었다 (Ma g ar it z 와 Tayl o r, 1 974). 그리고 해양원 사문석은 대륙 의 오피오라이트 복합체에서 산출된 사문석보다 oD 값은 크고 8180 값 은 작게 나타나 가열된 해수가 해저 사문암화 과정에 작용한 것으로 해 석 하였 다 (Wenner 와 Tayl o r, 1973) . 변성암 중에 공존하는 방해석-흑연 광물쌍을 이용한 탄소 동위원소 지 질 온 도 계 는 Valley 와 O'Neil 0 981) 과 Wada 와 Suzuki ( 1983) , Mor i k iy o0984) 에 의해 연구되었다. Wada 와 Suzuk i (1983) 는 방해석-돌로마이트 솔버스 (Solvus) 지질온 도계에서 수정하였고 Valle y와 O'Ne i l(1981) 은 칼리장석-사장석과 자 칠석-티탄철석 지질온도계에서 수정하였으며 Mor i k iy o(1984) 는 변성 도 구분에서 변성광물조합에서 추정된 온도에서 보정하였다. 이들 각 온도계간에는 약간 차이가 있으며 500'C 이상에서는 사용 가능하나 그 이하 온도에서는 주의를 요한다. 물론 동일 변성대내에서 서로 다른 공존하는 변성광물쌍을 이용하 더라도 동위원소 평형온도는 같아야 할 것이다(그림 4-52). 즉 규선석대의 편암에서 석영-알카리장석 광물쌍, 석영-백운모 광 물쌍 석영-자철석 광물쌍에서 얻은 온도가 650'C 내의로 일치하여야 한다. 상이한 광물쌍을 이용하여 온도가 일치하였을 때 변성작용의 최고 온도로 인정할 수 있다. 만일 온도가 일치하지 않았을때는 광물간에 비평형이었음을 알 수 있게 된다. 비평형의 원인 중의 하나로 , 복합변성작용에 의해 중복되어 나타날
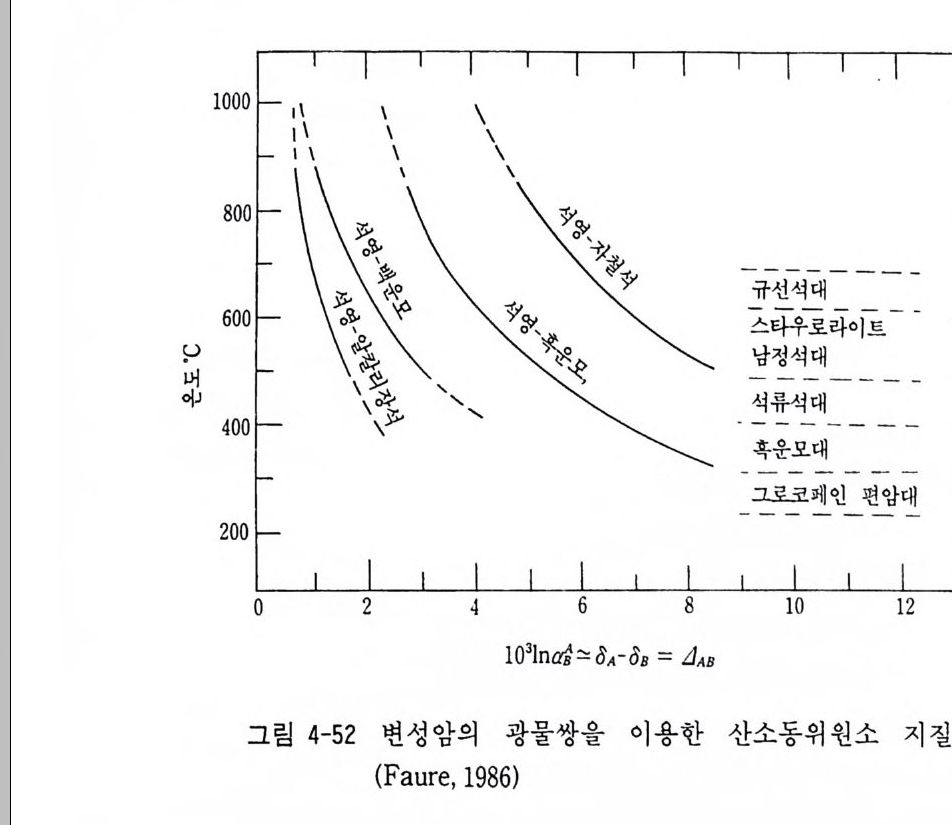 1000 r-\\ \\\ \\\\
1000 r-\\ \\\ \\\\
수도 있어 변성작용의 에피소드 해석의 중요한 정보를 줄 수도 있다. 우리나라의 옥천대의 창리층중에 협재된 대리암에서 방해석-흑연 지질온도계로 구한 변성온도가 380~430'C 였다. 이 온도는 변성광물 조합에서 추정한 온도와도 찰 일치하고 있다. 그리고 마전리 부근 화 강암과 접촉부에서는 500 'C로 높은 온도가 얻어졌다. 그리고 수산리 부근 조선계의 결정질 석회암에서 240 ' C 가 얻어져 옥천계의 변성온도가 조선계의 변성온도보다 높게 나타나 암석 광물 학적으로 알려진 변성도의 차이와도 조화적이다. 그러나 분석시료수 가 적고 연천계, 옥천계, 영남계 등 여러 지역의 변성암 복합체에서 많은 연구가 이루어지면 변성온도와 변성작용의 에피소드가 밝혀지게 될 것이다.
참고문헌 Abell, P. I. {1986), Oxy ge n iso to p e rati os in modern Afr ica n gas tr o p od shells : a data base for pal eoclim a to l og y. Chem. Geol. 5 8, pp. 183-193. Bebout, G.E., Carlson, W. D. (1986), Fluid evoluti on and tra nspo r t durin g meta m orph is m : evid e nce from the Llano Up li ft, Texas. C ontr i b. Mi n- era/. P et ro l. 9 2, pp. 518-529. Beeunas, M. A. , K nauth , L.P . (1985), Preserved sta b le iso to p i c sig na tu r e of subaerial dia g e n esis in the 1. 2 b.y ., Mescal Lime sto n e, Centr a l Ar- izo na. Imp lic a ti on s for the tim in g and develop m ent of a ter restr ia l pla nt cover. Geo!. Soc. Am. Bull, 96, pp. 737-745. Bott ing a , Y. {1969a), Calculate d frac ti on ati on fac to r s for carbon and hyd rog en iso to p e exchang e in the sys t e m calcit e- carbon dio x id e -g rap h it e- meth a ne-hy dr oge n - w a te r -vap o r. G eochim . Cosmochim . Acta . 33, pp. 49 -64. Bott ing a , Y. (19 69b) , Carbo n iso t o p e frac ti on ati on betw een grap h i t e, dia m nd and carbon dio x id e . Eart h plan e t. Set . Lett. 5, pp. 301-307 Brown. P.E ., Bowman, J.R ., Kelly, W.C. (1985), Petr o log ic and sta b le iso to p e constr a in t s on the source and evoluti on of skarn-fo rm i ng flui d s at Pin e Creek. Cali forn ia , Econ. Geo!. 80, pp. 72-95. Chiv a s, A.R . , A ndrew, A.S ., Sin h a A.K ., O'N e il, J.R . (1982), Geochemi str y of Pli oc ene -P leis to c ene oceanic arc plu to n ic comp le x, Guadalcanal. Natu r e (London), 300, pp. 139-143 . Clayt on , R.N . {1959), Oxy ge n iso to p e frac ti on ati on in the sys t e m calciu m carbonate - wate r . ]. Chem. Phys . 30, pp. 1246- 12 50. Clay ton , R. N. {1981), Isoto p i c the rmometr y. In : New ton , R.C , Navrots k y, A, Wood, B.J . ( eds.) Thennodyi zam i cs of mi ne rals and me lts . Sp ri n g e r , Berlin , Heid e lberg, New York, pp. 85-109. Clayt on , R. N., D eg en s, E.T. (1959), Use of carbon iso to p e analys e s of carbon- ate s for dif fere nti at in g fres hwate r and marin e sedim e nts . Bull. Am. Assoc. Petr ol . Geo!. 43, pp. 890-897. Clay ton , R.N ., Ep st e i n , S. {1958), The relati on ship betw een 018 / 016 rati os in coexis ti n g qu art z, carbonate and iro n oxid e s from vario u s geo log ical Clayt on , dRe.pN o .s , itMs .a y] e. d Gae,o T!. .K 6.6 , {p1p9.6 33)5, 2-T37h3e. use of bromi ne pen ta f lu o ri de in the
extr a cti on of oxy ge n from oxid e s and sili c a te s for iso to p i c analys i s. Geochim . Cos moclzim . Ac/a. 27, pp, 43-52. Clayt on , R.N ., May ed a, T.K. (1978), Geneti c relati on s bet w een iro n and sto n y mete o rite s . Earth Plane/ . S ci . Lel t. 4 0, pp. 168 -174. Clayt on , R.N ., Maye d a, T.K. (1983), Oxy ge n iso to p e s in eucrite s , shergo tt ites , nakhlite s and chassig nites . E arth Plane/ . S ci . Let /. 62, pp. 1-6 . Clayt on , R.N ., May ed a, T.K . (1984), The oxy ge n iso to p e record in Murchis o n and oth e r carbonaceous chondrite s . Eart h Plane /. S ci. Lei /. 6 7, pp. 151 -161. Clay ton , R.N ., Ste i n e r, A. (19 75), Oxy ge n iso to p e stu d ie s of the geo th e rmal sys t e m at W air a kei, New Zealand. Geochim . Cosmochim . Ac/a. 39, pp. 1179-1186. Clayt on , R. N., Fried man, I ., Graf, D .L. , May ed a, T. K., Meents , W. F., Shim p , N. F. (1966), The orig in of salin e for mati on wate r s. 1. Iso to p i c comp os i- tion . ]. Geop hy s . R es. 71, pp. 3869-3882. Clayt on , N., Muff er , L. J., P. Whit e (1968), Oxy ge n iso to p e stu d y of calcit e and sili ca te s of the Riv e r Branch No. 1 well, Salto n Sea Geoth e rmal Fie ld , Calif orn ia . Am. ]. Sci. 2 66, pp. 968-979. Clayt on , R. N., O'Neil, J. R ., Maye d a, T. K. (1972), Oxyg e n iso to p e exchang e betw e en qu artz and wate r . ]. Geop hy s . R es. 77, pp. 3057-3067. Craig , H., Lup ton , J. E. (1976), Prim o rdia l neon, heliu m and hyd r og en in o ceanic basalts . Eart h Plane/. Sci . L ett . 3 1, pp. 369-385. Craig , H., Boato , G., Whit e, D. E. (1956), Isoto p i c geo chemi str y of the rmal wate r s. Proc. 2nd Conf. Nucl. Process Geo!. Sett ing s , p. 29. Criss , R. E., Tayl o r, H. P. (1983), An 180 / 160 and D / H stu d y of Tertia r y hyd r oth e rmal sys t e m s in t he South e rn half of the Idaho bath o lit h. Geo !. Soc. Am. Bull. 9 4, pp. 640-653. Dein es , P. (1977), On the oxy ge n iso to p e dis tr ib u ti on among min e ral trip le ts i n igne ous and meta m orp h ic rocks. Geochim . Cosmochim . Ac/a. 41, pp. 1709-1730. Deuser, W. G. (1970), Extr em e 13C / 12C varia t i on s in Qu ate r nary dolomi tes from the conti ne nta l shelf . E art h Planet. Sci . L ette rs . 8, p p. 118-124. Doug la s, R. and Woodrutt , F. (1981), Deep sea benth i c for ami ni f era . In : C Eil ion i (ed.) The sea, Vol. 7. W i ley Inte r sci en ce Pub. N.Y. pp. 1233-1328. Emi lian i , C. (1978) , The cause of the ice age s . Eart h Planet. Sci . Lett. 37 :
349-354 Emi lia n i. C., Shacklet o n , N. J. (1974), The Brunhes epo c h : Isoto p i c pal eote m p er atu r es and geo chronology . Scie n ce, 183, pp. 511-514. Eps t e i n , S., May ed a, T. K. (1953), Varia t i on of 018 conte n t of wate r s from natu r al sources. Geo c hir n. Cosmochim . Acta . 4, pp. 213-224. Eps t e i n , S ., Tayl o r, H. 0 . (1970), 180 / 160, 30Si / 28Si, D / H and 13C / 12C stu d ie s of lunar rocks and min e rals. S ci en ce, 167, pp. 533-535. Eslin g e r , E . V., Yeh, H. W. (1986), Oxy ge n and hyd r og en iso to p e geo chemi str y of C reta c eous bento n it es and shales from the Dis tu r bed Belt. Monta n a. Geo c lzim . Cosmochim . Acta . 50, pp. 59-68. Fritz , P., P op la wski, S . (19 74), '1180 and 13C in the shells of fres hwate r molluses and the ir e nv ir o nment. Eart h Planet. S ci . L ett . 2 4, pp. 91-98. Giv e n, R. K., L ohmann, K. C. (19 85), Deriv a ti on of t he orig ina l iso to p i c c omp os i- tion of Permi an marin e cements . J Sed i m e nt . P etr ol . 55, pp. 430-439. Graham, D. W., Corliss , B . H., Bender, M . L., Keig \vin , L . D. (1981), Carbon and oxy ge n iso to p i c dis e q ui li b r iu m of r ecent deep -s ea benth ic f or ami nif e ra . Mar. Mic ro pa le onwl. 6 , p p. 483-497. Graham, C. M., Greig , K. M., Shepp a rd, S. M. F. Turi, B . (1983), Genesis and mobil it y of the H20 - C02 flui d pha se durin g reg ion al gree nschis t and epi do te amp h ib o lite facies meta m orph i sm : a pet r o log ica l and sta b le iso to p e stu d y in the Scott ish Dalradia n . J Geo!. Soc. (London) , 140, pp. 577-599. Graham, C. M., Harmon, R. S., Shep pa rd, S. M . F. (1984), Exp er im e nta l hyd r ?- . gen iso to p e stu d ie s : h yd r og en iso to p e exchange behveen arnp hi b o le and wate r . Am. Mi ne r a l. 69, pp. 128-138. Graham, C. M., Shepp a rd, S. M. F., H eato n , T. H. E. (19 80), Expe r im e nta l hyd r og en iso to p e - stu d ie s . I . Sys t e m ati cs of hyd r og en iso to p e frac ti on a- tion in the sys t e m s epi do te - H20, zois it e - H20 and AlO(OH)-H20. Geochim . Cosmochim . Acta . 44, pp. 353-364. Hoe fs, J. (1973), Ein Beit ra g zur Isoto p e n ge o chernie des Kohlensto f f s in mag- rnati sc hen Geste i n e n. Contr ib . Mi ne ral. Petr ol. 41, pp. 277-300. Hoefs , J . (1981), Isoto p i c comp o sit ion of the ocean-atm o sph eric sys t e m in the geo log ic pas t. In: O'Connell, R. J., Fy fe, W . S. (eds.) E volutz· o n of the eart h. Geody na rnic Series , vol. 5. Americ an Geop hy s . U n ion , Wash in- gton , D. C., pp. 100-119.
Hoefs , J., E mmermann, R. (1983), The oxy ge n iso to p e comp os i ti on of H ercyn ia n gran it es and pre -Hercy~ ian gne is s es from the Schwarzwald. S. W. Germany . Contr i b . Mi ne ral. P etr o l. 8 3, pp. 320-329. Hoe fs, J., Frey, M. (1976), The iso to p i c comp o sit ion of carbonaceous matt er in a meta m orp h ic pro fi le from the Swi ss Alps . Geochim . Cosmochim . Acta . 40, pp. 945-951 . Hoe fs, J ., Coolen, J. J. M., Touret, J. (19 81), The sulfu r and carbon iso to p e comp os it ion of scap ol ite - r ic h gran ulite s . C ontr i b . Mi ne r a l. P et ro l. 78, pp. 332-336. Hoe fs, J., Mi llier , G., Schuste r , A. K. (1982), Polym eta m orph ic relati on s in iro n ores from the Iron Qu adrang le , Brazil : T he correlati on of oxy ge n iso - top e varia t i on s wit h defo r mati on his t o r y . Contr i b . Mi ne r a l. P et ro l. 7 9, pp. 241-251. Hoemes, S., Frie d ric h sen, H.T . (19 78), Oxy ge n and hyd r og en iso to p e stu d y of the pol ym e ta m orph ic area of the Nort he rn Otz t a l -S t u b ai Alps (Ty rol ). Contr ib. Mi ne ral. P et ro l. 67, pp. 305-315. Hoernes, S., Frie d ric h sen, H. T. (1980), Oxy ge n and hyd r og en iso to p i c comp os i- tion of Alpi ne and Pre-Alpi ne mi ne rals of the Swi ss Ce nt r a l Alps . Contr i b . Mi ne ral. Petr o l. 7 2, pp. 19-32. Hudson, J. D. (1977), Sta b le iso to p e s and lim esto n e lith i f ica ti on . ]. Geo l. S oc. (London), 133, pp. 637-660. !kin , N. P., Harmon, R. S. (1983), A sta b le iso to p e stu d y of serpe n ti ni z a ti on and meta m orp h is m in the High land. Border suit e Scotl a nd, U.K . Geoclzim . Cosmochim . Acta . 47, pp. 153-167. Keith , M. L., Weber, J. N. (1964), Carbon and oxy ge n iso to p i c comp os it ion of selecte d lime sto n es and fos sils . Geochim . cosmochim . Ac ta. 28, pp. 1787 -1816. Kelt s, K., McKenzie , J. A. (1982), Di ag e n eti c dolomi te for mati on in Qu ate r - nary anoxic dia t o m aceous muds of DSDP Log 64, Gulf of Cali forn ia . Initi al Re p DSDP 64, pp. 553-569. Kerrick , R., Lato u r, T. E., Wi llm ore, L. (1984), Fluid par t icipa ti on in deep fau lt zones: evid e nce from geo log ica l, geo chemi cal and 180 / 160 relati on s. J Geop hy s . R es. 89, pp. 4331-4343. Knauth , L. P., E p st e i n , S. (1975), Hy d rog en and oxyg e n iso to p e rati os in sili ca from the JOI DES Deep Sea Drill ing Proje c t. Eart h Planet. S ci. Lett. 25,
pp. 1-10. Kim , K.H . and Nakai, N. (1981), A stu d y on hyd r og en , oxyg e n and sulfu r i(sJoa p toa pn )i c, 1ra5,t i p ops . o6f- 1 th6e. hot spr i n g wate r s in South Korea. Geochemi stry Kim , K.H ., O .J . Kim , N. Nakai, and H.J. Lee (19 88), Sta b le iso to p e stu d ie s of t he Sangd o ng tun g st a n ore dep os it s, South Korea. M i ni n g Geo!. 38 (6) , pp. 473-487. Lambert, S. J., E p st e i n , S. (1980), Sta b le iso to p e inv estig a tio n s of an acti ve geo th e rm al sys t e m in Valles Caldera, J em ez Mounta i n s , New Mexic o . ]. Vol c ano! Geoth e r m . Res . 8, pp. 111-129. Land, L. S. ( 19 80), The iso to p i c and tra ce element geo chemi str y ofd o lomi te: t he sta t e of the art. In: Conce pt s and models of dolomi tiza tio n . Soc. Econ. Paleo n to l . Mi n. S p ec . Publ. 28, pp. 87-llO. Law re nce, J. R ., Tayl o r , H . P. (197 2) , Hy dr og en and oxy ge n iso to p e sys t e m ati cs in weath e r i n g pro fi les . G eo c him . Cosm ochim . Acta . 36, pp. 1377-1393. Liu , K. K., Ep st e i n , S. (198 4), The hyd r og en iso to p e frac ti on ati on betw een kaolin i t e and wate r . Iso to p e Geosci . 2 , pp. 335-350. Long ine lli, A ., Nu ti , S . (19 73), Revis e d pho sph a te - wate r iso to p i c tem p er atu re sca le. E a11Jz Plane t. S ci . Le tt. 1 9, pp. 373-376. Maga r itz , M., Heller , J . (19 80), A desert mig rat io n ind ic a to r -o x yg e n iso to p i c comp os it ion of land sna il s hells. Paleog eo g r Paleoc lim ato l Paleoe col 32, pp. 153 -1 62. Mag ar itz , M. , T ayl o r, H. P. (1974), Oxy ge n and hyd r og en iso to p e stu d ie s of serpe n ti ni z a t i on in the Troodos oph io l ite comp le x, Cyp ru s. Eart h Planet . S ci. Le tt. 2 3, pp. 8-14. Mag ar itz , M. , T ayl o r, H . P. (1976), 18() / 160 and D / H along a 500km trav erse across the Coast Rang e bath o lith and its c ountr y rocks, Centr a l Briti sh Columbia . Can. ]. Earth Sci . 13, pp. 1514-1536. Mag ar itz , M . , T ayl o r, H. P. (1986), Oxy g en 18 / Oxy g en 16 and D / H stu d ie s of plu to n ic gran it ic and meta m orp hic rocks across the Cordil ler an bath - olith s of S outh e rn Brit ish Colwnbia . J Geop hy s . R es. 91, pp. 2193-2217. Marwno, K., Naga s awa, K ., Kuroda, Y. (1980), Mi ne ralog y and hyd r og en iso to p e geo chemi st r y of c lay min e rals in O hnwna geo th e rmal area, nort he aste r n Jap a n . Eart h Planet . Sci . L ett. 47, pp. 255-262. Mats u his a , Y. (1979), Oxy ge n iso to p i c comp os it ion s of v olcanic r ocks from the
east Jap a n isla nd arc s and the i r bea ri n g on pet r o g en esis . j . volc a11ic Geolh e rm Res . 5, pp. 271 -2 96. tlla ts u his a , Y., Goldsmi th, J. R ., Clay ton , R. N. (1979), Oxy ge n iso t o p e frac ti on a - tion in the sys t e m s qu artz - albit e- anorth i t e- w a te r . Geochim . Cosmo- chim . Acta . 43, pp. 113 1- 1140. Mats u o, S., F rie d man, I., Smi th, G. I. (1972), St ud ie s of Q u ate r nary sali ne lakes. I. Hy dr og en iso to p e frac ti on ati on in salin e min e rals. G eochim . Cosmo- chim . Acta . 3 6, pp. 427-435. Matt he ws, A., Beckin s ale, R. D. (1979), Oxy ge n iso to p e equ i li br ati on sys t e m - ati cs betw een qua rt z and wate r . Am. Mi ne ral 64, pp. 232- 24 0. Matt he ws, A., K atz , A. (1977), Oxy ge n iso t op e frac ti on ati on durin g the dolomi tiza ti on of c alciu m carbonate . Geocl1i1 11 . Acta . 4 1, pp. 143 1- 14 3 8. Matt he ws, A., Kolodny , Y. (1978), Oxy ge n iso to p e frac t i o n a ti o n in dec arbo na- tion meta m orph is m : the Mott le d Zone even t. Eart h P/a 11e t. Sci. Let t. 39, pp. 179-192. Matt hew s, A., Schli es te d t, M. (19 84 ), Evoluti on of t he bluesc h is t a nd gree nschis t facies rocks of Sif no s, Cy cl ades, Greece. A sta b le iso to p e stu d y of subducti on -relate d meta m orp h is m . Contr ib . Mi ne al. Pet ro l. 8 8, pp. 150 -163. Matt hew s, A., Goldsmi th, J. R., Clay ton , R. N. (1983a), Oxy ge n iso to p e frac ti on ati on inv olvin g pyro xenes: t he calib r ati on of mi ne r al- pa i r geo th e rmomete r s. Geoclzim . Cosmochim . Ac ta. 47, pp. 631-644. Mats u his a , Y. and Kurasawa, H. (1983), Oxyg e n and stro nti um iso to p i c characte r ist i c s of calc-alkalic volcanic rocks from the centr a l and weste r n Jap a n arcs. In : S. Aramaki and L Kushir o (eds.), A rc i·o l ca n- ism . ]. Volcanol-Geoth e rm Res. 1 8, pp. 483-510. Moldovanyi , E . P., Lohmann, K . C. (1984), Isoto p i c and pet r o g rap h ic record of ph reatic dia g e n esis : Lower Creta c eous Slig o and Cup ido for mati on s. ]. Sedim ent. Petr o l. 5 4, pp. 972-985. Moon, K.J. (1983), The gen esis o f the Sang do ng tun g st e n dep os it s, t he Rep ub lic of Korea, (unp ub .) D is se rt at i on Univ . of Tasmania . p. 366. Nort on , D., and H.P. Tayl o r, Jr. (19 79), Qu anti tat iv e sim ulati on of the hyd r oth er mal sys t e m s of c ry s ta ll iz in g mag ma s on the basis o f tran spo r t theo ry and oxyg en iso to p e data : An analys i s of the Skaerga a rd In- stru s io n .• ; ]. Petr ol. 20, pp. 421-486.
McKenzie , J. ( 19 84), Holocene dolomi tiza ti on of calciu m carbonate sedim e nts from the coasta l sabkhas of A bu dhabi, U .A .E. : A sta b le iso to p e stu d y . ]. Geo!. 89, pp. 185-198 McM illa n, W. J., and Pante le y ev , A. (1980), Ore dep os it models-1, Porph y r y cop pe r dep os it s. Geo s cie n ce, Canada, 7(2), pp. 52-63 Morik iy o , T . (19 84), Carbon iso to p i c stu d y on coexis ti n g calcit e and grap h i te i n the Ry ok e meta m orph i c rocks, nort he rn Kis o dis tr i c t , centr a l Jap a n . Contr ib . Min e ral. Pet ro l. 8 7, pp. 251-259 Muehlenbachs, K ., Kushir o , I. (19 74), Oxy ge n iso to p e exchang e and equ i li br iu m of s ili c a te s wit h CO2 or 02. Geop hy s . Lab. Yearb. 73, p. 232 Murata , K. J., Frie d man, I., Gleason, J. D. (1977), Oxyg e n iso to p e relati on s betw een dia g e n eti c sili c a min e rals in Monte r ey Shale, Temblor Rang e, Califo rn ia . A m. ]. Sci. 277, pp. 259-272 . North ro p , D . A., Clayt on , R. N. (1966), Oxy ge n iso to p e frac ti on ati on s in s ys t e m s conta i n i n g dolomi te. ]. Geo!. 7 4, pp. 174-196. O'N e il, J . R ., Clay ton , R. N. (19 64), Oxy ge n iso to p e the nnometr y. In : Craig , H., Mi lle r, S. L., Wasserburg, G. J. (eds.) Isoto p i c and cosmi c chemi stry. North Holland Pub!. Co., A mste r dam, pp. 157-168. O'N e il, J . R., Ep st e i n , S. (19 66), A meth o d for oxy ge n iso to p e analys i s of mil li g ram qua nti ties of w ate r and some of its app lica ti on s. ]. GeolJ h .}'S Res . 71, pp. 4955-4961. O'Neil, J. R ., Hay, R. L. (1973), 180 / 160 rati os in chert s associa t e d wit h the salin e lake dep os it s of East Afr ica . Eart h Planet. Sci. Lett. 19, pp. 257 -266 O'N eil, J. R., Kharaka, Y. K. (1976), Hy dr og en and oxyg e n iso to p e exchange reacti on s betw een clay min e rals and wate r . Geoclzim . Cosi no chim . Ac ta. 40, pp. 241-246. O'Neil, J. R ., Sil b erman, M. L. (19 74), Sta b le iso to p e relati on s in epi the nnal Au-Ag dep os it s. Econ. Geol. 69, pp. 902-909. O'Neil, J. R., Tayl o r, H. P. (1967), The oxy gen iso to p e and cati on exchang e chemi str y of fel dspa r s. Am. Mi ne ral 52, pp. 1414-1437. O'Neil, J. R., Tayl o r, H. P. (1969), Oxy ge n iso to p e equ ilibr iu m betw e en mus- covit e and wate r . ]. Geop hy s Res. 74, pp. 6012-6022. O'Neil, J. R., Clayt on , R. N., Maye d a, T . K. (1969), Oxyg e n iso to p e frac ti on ati on in div a lent meta l carbonate s . ]. Chem. Phys . 51, pp. 5547.
Panic h i, C., and Gonfi an ti ni , R. (19 78), Envir o nmenta l iso to p e s in geo th e mal stu d ie s . G eoth e nnic s, 6, pp. 143-161. Rex, R. W., Sye r s, J. K ., J ac kson, J. K., Clay ton , R. N. (19 69), Eolia n orig in of qu artz in soil s of Hawaii an Islands and in Pacif ic pel agi c sedim ents . Scie n c e 163, pp. 277-279. Ric h et, P., B ott ing a , Y., Jav oy, M. (1977), A revie w of H, C, N, 0, S, and Cl sta b le iso to p e frac ti on ati on among ga seous molecules. A111111 Rev Eart h Planet Sci . 5 , pp. 65-llO. Roth e, P., Hoe fs, J. (1977), Isoto p e n ge o chemi sc he Unte r suchung en an Kar- bonate n der Rie s -See-Sedim ente der Forschung sb ohrung Nordlin g e n 1973, Geol Bavari a 75, pp. 59-66. Rumble, D. Ill., Ferr y, J.M ., Hoerin g , T. C., Boucot, A. J. (19 82 ). Fluid flow durin g meta m orph is m at the Beaver Brook fos si l l ocality . Am. ]. Sci. 282, pp. 886-919. Sakai, H., Tsuts u mi , M. (1978), D / H frac ti on ati on fac to r s betw een serpe n ti ne and wate r at 100 to 500'C and 2000 bar wate r pre ssure and the D / H rati os of natu r al serp e nti ne s. Earth Plane t. Sci. L e tt. 4 0, pp. 231-242. Shackleto n , N. J., Hall, M. A. . Lin e , J., Shuxi, C. (19 83), Carbon iso to p e data in core Vl9-30 confi rm reduced carbon dio x id e concentr a ti on s in the ice age atm osph ere. N atu r e (London) 306, pp. 319-322. Shelto n , K.L., So, C.S., a nd Chang, J.S . (1988), Gold rich mes ot h e rmal vein dep o sit s o f the Rep ub li c of Korea. G eochemi ca l stu d ie s of the Jun g \\'o n gol d area. Econ. Geo!. Shepp a rd, S. M. F. (1984), Isoto p i c geo th e rmometr y. In : Lag ac he M (ed.) Thennometr ie e t b arometr ie g eo log iqu es. S oc. Fr. M i ne ral Cris t a l log r, pp. 349-412. So, C.S., and Shelto n . K.L . (1987a), Sta b le iso to p e and flui d inc lusio n stu d ie s of go ld-silv e r-bearin g hyd roth e rmal vein dep o sit s, Cheonan-Cheong ya ng- Nonsan min i n g dis tr i ct . Rep u blic of Korea. Cheonan area. Eco11. Geo!. 82, pp. 987-1000. So, C.S., a nd Shelto n , K.L. (1987b), Fluid inc lusio n and sta b le iso to p e stu d ie s of go ld-silv er-bearin g hyd roth e rmal vein dep o sits , Yeoju mi ni n g dis tr i c t , Rep ub lic of Korea. Econ. Geo!. 82, pp. 1309-1318. So, C.S ., Chi, S.J. , and Shelto n , K.L. (1987), Sta b le iso to p e and flui d inc lusio n stu d ie s of go ldsilv e r-bearin g vein dep o sit s. Cheonan-Cheong yan g -
Nonsan min i n g dis tr ic t, Rep ub lic of Korea. Nonsan area. Neues Jah rb. Mi ne ral. Abl10nd. 158, pp. 47-65. So, C.S ., C hi, S.]., Yu, J.S. , a nd Shelto n . K.L. (19 87b), The Jeo neui gol d-sil ve r min e . Rep ub lic of Korea: A geo chemi ca l stu d y . Mi ni n g Geo!. 3 7,pp . 313-322. So, C.S., S. J . Chi and S.H . Choi (1988), Geochemi ca l stu d ie s on Au-Ag hyd roth e r- mal vein dep os it s, Rep ul dic of Korea: J ina n-Je o ug eu p min e ralig ed Suzuoki, aTre.a, .E p] s. t eM i ni n, . SP. e(t1r 9. 7 E6 )c,o n.H Gy deor !o. g8e 3n , pispo. t o4 4p 9e - 4 fr7a 1c . ti on ati on betw een OH- bearin g min e rals and wate r . Geochim . Cosmochim . Acta . 40, pp. 1229 -12 4 0 . Tay lo r, H. P. (1968), The oxy ge n iso to p e geo chemi str y of igne ous rocks. Contr ib . Mi ne r a l. P et ro l. 1 9, pp. 1-71 . Tayl o r, H. P. (1974a), The app li ca ti on of oxy ge n and hyd r og en iso to p e stu d ie s to pro blems of h yd r oth e rmal alte r ati on and ore dep os it ion . Econ. Geo!. 69, pp. 843-88 3. Tayl o r, H. P. (1974b), Oxyg e n and hyd r og en iso to p e evid e nce for large - scale circ ulati on and int e r acti on betw een grou ndwate r s and igne ous int r u- sio n s wit h par tic u lar refe r ence to the San Jua n volcanic field , Color- ado. In : Geo c he m ic a l tra i zsp or t and kin e ti cs. Carnegi e Inst. Washi n- gton , 634, pp. 299-323. Tayl o r, H. P. (197 7), Wate r / rock int e r act ion s and the orig in of H20 in gran it ic bath o lit hs . ] . Geo!. S oc. 133, pp. 509-558. Tayl o r, H.P . (1978), Oxyg e n and hvdrog en iso to p e stu d ie s of plu to n ic gran it ic rocks. E arth Planet. Sci . Lett. 38, pp. 177-210. Tay lo r, H.P. (1980), The eff ec ts of assim i la ti on of countr y rocks by mag ma s on 180 / 160 and 87Sr / 87Sr sys t e m ati cs in igne ous rocks. Eart h Planet. Sci. Lett. 47, pp. 243-254. Tayl o r, H. P., E p st e i n , S. ( 1961), 180 / 160 rati os of f el dspa r s and qua rt z in zoned gran it ic peg m a ti tes . Geo!. Soc. Am. Spe c. Pap. 68, p. 183. Tayl o r, H. P., Ep st e i n , S. (1962), Relati on ship betw een 180 / 160 rati os in coexis t- ing mi ne rals of igne ous and meta m orph ic rocks, Part I : Prin ciple s and exp er im e nta l results . Bull. Geol. Soc. Am. 73, pp. 461-480. Tayl o r, H. P., Foreste r , R. W. (1979), An oxy ge n and hyd r og en iso to p e stu d y of the Skaerga ard int r us io n and its c ountr y rocks : a descri ption of a 55 M.
Y. old fos sil h yd r oth e rmal sys t e m . ]. Pet ro l. 2 0, pp. 355-419. Tayl o r, H. P., Sil v er, L. T. (1978), Oxy ge n iso to p e relati on ship s in plu to n ic igne ous rocks of the Penin s ular Rang es Bath o li th, so u th e m and Baja Calif orn ia . s hort pa pe r s of the 4th Inte r n Conf Geochronolog ,•, C osmo- chronolog y, Isoto p e Geology . U.S. Geolog ica l Survey Op en -Fil e Rep or t 78-701, pp. 423-426. Tayl o r, H.P . Jr., and Shepp a rd, S. M. F. (19 86) , Ign e ous rocks: I. Processes of iso to p i c frac ti on ati on and iso to p e sys t e m ati cs . In : Sta b le iso to p e s in hig h tem p era tu r e geo lo g ica l pro cesses, ed. J.W . Valley; H.P. Tayl o r Jr; J. R. O'Neil, 227-72. Revie w s in min e rology 16. Washin g t on , D.C.: Mi ne ral. Soc. of Americ a . Tucker, M. E. (1983), Di ag e n esis , geo chemi str y and orig in of a Precambria n dolomi te : The Beck spr i ng dolomi te of easte r n Calif orn ia . J Sedim ent Petr ol. 53, pp. 1097-1119. Urey, H. C. (1947), The the rmodyn a mi c pro p er t ies of iso to p i c substa n ces. J. Chem. Soc. 1947, p. 562. Valley, J. W . (1986) Sta b le iso to p e geo chemi str y of meta m orph ic rocks. In: Valley, J. W., Tayl o r, H. P., O'Neil, J. R. (1981) 13C / 12C exchang e betw een calcit e and grap h i te : a po ssib le the rmomete r in Grenvil le marbles. Geochim . Cosmoclzim . Acta . 45, pp. 411-419. Valley, J. W . , O'Neil, J. R. (1984), Fluid hete r oge n eit y durin g gran ulite facies meta m orph is m in the Adir o ndacks: s ta b le iso to p e evid e nce. Contr ib . Mi ne ral. Petr o l. 8 5, pp. 158-173. Veiz e r, ]., H oefs , J. ( 1976), The natu r e of 0 18 / 016 and C13 / C12 secular tre nds in sedim e nta r y carbonate rocks. Geochim . Cosmochim . Acta . 40, pp. 1387 -1395. Veiz e r, ]., H olser, W.T., Wi lgus, C. K. (1980), Correlati on of 13C / 12C and 34S / 32S secular varia t i on s. Geoclzir n. Cosrnochim . Acta . 4 4, pp. 579-587. Wada, H.,N. Nii tsu ma and T.Sait o (1982), Carbon and oxy ge n iso to p i c m easure- ments of ultr a- small samp le s, Geosci. ReJ )ts. Shiz u oka Univ . 7, pp. 35 -50. Wada, H., Suzuki, K. (1983), Carbon iso to p i c the rmometr y-c alib r ate d by dolomi te- calcit e solvus tem p er atu re s. Geochim . Cosmochim . Ac ta. 47, pp. 697-706. Wage r , L.R ., and Brown, G.M . (1967), Laye r ed ign eous rocks. San Franci sc o,
W.H. Freeman, p. 5 88. Wenner, D. B., T ayl o r, H . P. (1973), Oxy ge n and hyd r og en iso to p e stu d ie s of t he serpe n ti ni z a ti on of u ltr a mafi c rocks in oceanic e nvir o runents and conti - nenta l oph i o l ite comp le xes. Am. ]. Sci. 2 73, pp. 207-239. Wi ck ham, S.M ., Tayl o r, H. R. (1985), Sta b le iso to p e evid e nce for large - scale seawate r inf i ltra ti on in a -reg i on al meta m orph ic ter rane; the Trois Seig ne urs Massif , P y re nees, France. Contr ib. Min e ral. Petr o l. 91, pp. 122- 13 7. Wollin , G ., Erics on, D.B ., a nd Ry am , W.B.F. (1971), Mag ne tis m of t he eart h and clim ati c chang es . Earth Plane t. S ci . Lett. 1 2, pp. 175-183. Yang , J ., Eps t e i n , S . (1983), Inte r ste l lar orga n ic m att er in mete o rite s . G eochim Cosmochim . Acta . 47, pp. 219 9-2216. Yapp , C. J. (1979), Oxy ge n and carbon iso to p e measurements of l and snail shell carbonate . Geo ch im . Cosmochim . Acta . 43, pp. 629-635. Yeh, H. W. (1980), D / H rati os and late sta g e hyd rati on of s hales duri ng buria l. Geochim Cosmochim . A cta . 45, pp. 341-352. Yeh, H. W., Eps t e i n , S. (1978), Hy dr og en iso to p e exchang e betw een clay min e ra ls and seawate r . Geochim . Cosmoch i m . Acta . 42, pp. 140-143. Yeh, H. W. , E ps t e i n , S . (1981), Hy dr og en and carbon iso to p e s of p et ro leum and relate d orga n ic matt er. Geochim . Cosmochim . Acta . 45, pp. 753-762. Yeh, H. W. , S avin , S. M. (1976), The exte n t of o xy ge n iso to p e exchang e betw een clay min e rals and seawate r . Geochim . Cosmochim . Acta . 40, pp. 743 -748. Yeh, H. W. , Savin , S . M. (197 7), Mechanis m of buria l meta m orp h is m of argi l- laceous sedim ents . 3. 0 -i so to p e evid e nce. Geo/. Soc. Am. Bull. 8 8, pp. 1321- 13 30. Yurt se ver, Y. and J. R. Gat (1981), Atm o sph e ric wate r s in Sta b le iso to p e hyd r olog y. IAEA. Zhang , L., Guo, Y. and Qu , P. (1984), A stu d y on the oxyg e n iso to p e s of some Mesozoic gran it oi d s in s outh e aste r n Chin a . In : Geolog y of gra nite s and the ir meta ll og en eti c relatio n s. T. Xu and G. Tu, eds. Scie n ce Press Beij ing , Chin a , pp. 905-919. 김규한 (1980), 「한국 태백산 지역에 분포하는 고생대 석회암의 탄소와 산소 동 위원소에 관한 연구」, ((광산지질)} 13( 1), pp. 12 -27. 김규한 (1982), 동위원소의 지하수학에 응용, 《지질학회지》 18(3), 167-171.
김규한, 中井信之 (19 88), 「남한의 지하수 및 강수의 안정동위원소 조성」, (( 지질 학회지) ) 24-1, pp. 39-46. 김규한, 中井信之 (19 81), 「韓國(l) 溫泉 7k (1) 水菜 酸素及 u• 琉黃同佑묘t」, ( (地球 化學)) 15, pp. 6-16. 김규한, 박재경, 양종만, 吉田尙弘 (19 90), 「울산철광산의 탄산염암과 사문암의 성인」, ((지질학회지)) 26(5), pp. 407-417. 김규한 (19 90), 「남한의 중생대 화강암류의 안정동위원소 지구화학적 연구」 (한 국과학재단 연구보고). 中井信之 의 lOA (1982), 「漢江(韓國)及 u• 流域生態系 l:El t k 環境動態 (나써寸 h 基礎的 調査」, 卜 크 夕 財園硏究 助成 硏究報告 要約. 문상호 (19 90), 「울진지역의 석광화작용에 관한 연구」, 서울대학교 박사학위논 문, p. 1 84. 문희수 (19 86), 「제 3 기충에 배태된 벤토나이트의 산소 및 수소 동위원소 연구」, ((광산지 질)) 19, pp. 특 131-138.
5 탄소 안정동위원소 5-1 서언 탄소는 주로 대기권, 생물권, 수권, 암석권에 많이 존재하며 이를 각 권간에 4.5 년을 주기로 순환이 이루어지고 있다. 그러나 지구 내 부의 지각, 맨틀이나 핵에도 소량이 포함되어 있다. 자연에서 탄소는 산화 상태에 따라 C ' (흑연, 다이아몬드), C4-( 유기화합물), C”( 탄산염 암)로 다양하게 존재하며 주로 무기원탄소의 산화형 탄소화합물과 생 물권의 환원형 탄소화합물간에 동위원소 분별이 일어나고 있다. 탄소 동위 원소값은 탄산염 암의 +20%, 이 상에 서 메 탄의 _90%, 에 이르기까지 100%0 이상의 넓은 변화를 보인다(그림 5-1). 탄소 동위원소의 분별은 다른 동위원소에서와 마찬가지로 ® 식물 의 광합성시의 반응속도론적 동위원소효과(Ki ne ti c e ff ec t)와 ® 동위 원소 교환평 형 ® 크랙 킹 반응 (Crack i n g reacti on ) 과 확산과정 에 의한 동위원소 분별을 둘 수 있다. 광합성 (6CH2+6H20=C6H1206+602) 시 대기중(평균 813C=-7~) 의 co 제서 가벼운 12c 동위원소를 선택적으로 사용하여 형성된 유기물 에는 가벼운 12c 가 많이 농집되고, 남아 있는 CO2 중에는 I J C 가 상 대적으로 많아지게 된다. 효소 조절에 의해 광합성작용시에 생화학적 반응에서 일어나는 동
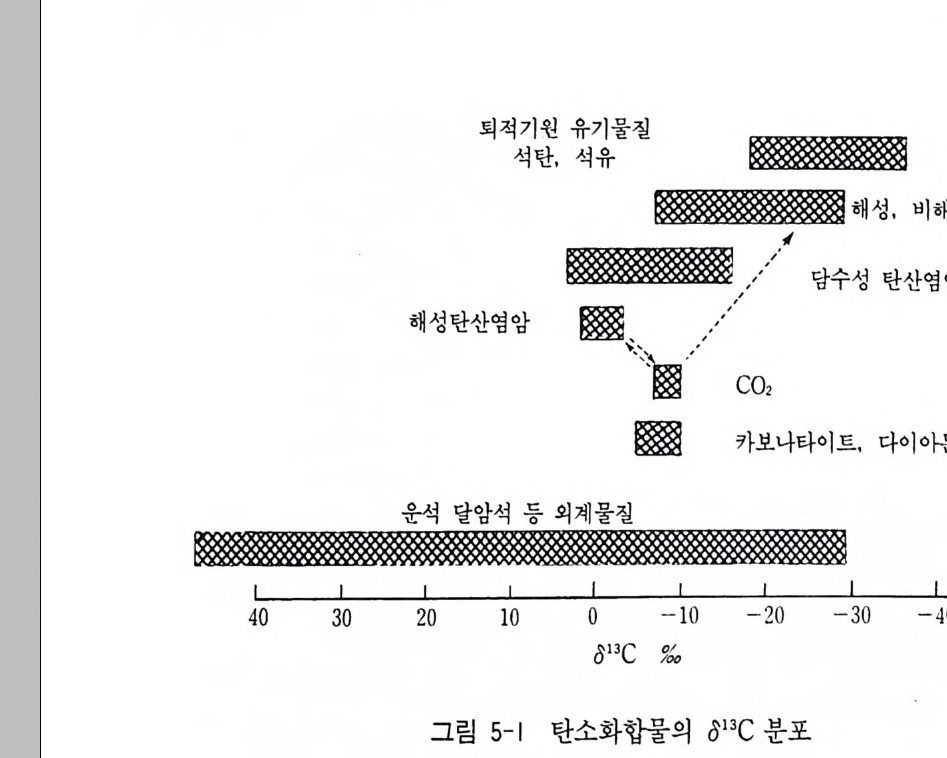 되적기원 유기물질 -해성-,« 비해성유 기물
되적기원 유기물질 -해성-,« 비해성유 기물
위원소 분별은 주로 반응속도론적 동위원소 효과 (K i ne ti c iso to p e e ffe c t)이다. 대표적인 반웅 예는 다음과 같다. C02 +r ib u lose-l, 5-bis p h o sph a te -—+ pho sph o g ly c e rate (C 3 식 물 alga e , cya m obacte r i a 등) C02/HCOi +pyruva te / ph o sph o enolpy ruv ate 一一 oxaloaceta t e ( C4 식물 ,CAM 식물 등) C3 식물은 3 개의 탄소화합물로 된 포스포그리세린산 (Phos p ho g l y cer ic a ci d) 이 무기영양성 물질대사과정에서 처음 만들어지는 식물을 말 하며 대다수의 나무와 쌀, 밀과 갇은 식물이 여기에 속한다. 4 개의 탄소화합물로 된 옥살착산 (Oxalacetic aci d) 이 무기 영 양성 물질대 사과
정에서 처음 만들어지는 옥 옥수수와 같은 식물을 C4 식물이라 한다. 그 리고 CAM 식물은 선인장과 같은 건조기후지역의 특수한 식물로 크라 술라시안산 (Crassulacean acid ) 신전대사룰 나타내는 무기영양성 물질 대사과정에서 만들어진 식물이다. 보통 C4 식물의 CO2 동화속도가 C3 식물보다 두 배 빠르다. 이 같 은 생물학적 탄소고정에 있어 동위원소 분별은 ® 의부 CO2 의 홉수 와 세포내 확산과정 과 ® 초기 CO2 _ 고정 (Carboxy la ti on ) 반응과정 에서 일어난다. 이 같은 2 단계 동위원소 분별 모델은 다음과 같다 (Park 과 Ep st e i n , 1960) . C02( e) =kk=ll C02( i) 一k3 R-COOH CO 2 (e) 와 C0 2( i)는 각각 내부 및 의부의 CO2 이고 k1, k2, k3 는 반응속도 정수이다 . 위 식과 같은 과정에서 동위원소 분별이 일어나 지만 실제는 더욱 복잡하다. 그러나 이들 두 과정이 동위원소 분별을 일으키는 가장 현저한 반 응속도 조절과정이다. 대다수의 식물이 C3 식물인데 이들의 탄소동위 원소 성분은 o13c= 一 23 ~ -34%。 (평균 -27%) 이며 C4 식물(옥수수) 은 -6 ~ -23%。 (평균 ― 13 %o)이다. 그리고 CAM 식물은 -11 ~ -33%, 범위를 나타낸다(그립 5-2). CaC03 와 CO2 (g ) 사이의 동위원소 교환평형은 13C02 (g) +H12co3( 액)-_ ➔ 12co2 (g) +H13co3( 액)식으로 일어나며 20 ° C 에서 평형상수는 7.6~8.8 이다. 여러 온도에서 계산 및 실험에 의해서 각 탄소 중의 탄소 동위원소 의 분별상수가 얻어져 있다. 생물권에서의 탄소 동위원소비의 분포를 보면 대부분은 C3 식물 및 C4 식물과 같은 육상식물은 탄소 동위원소비 013C=-2 . 4~-34% 이 며 현생 퇴적물 중의 유기물질은 -10~-30%, 정도이다.
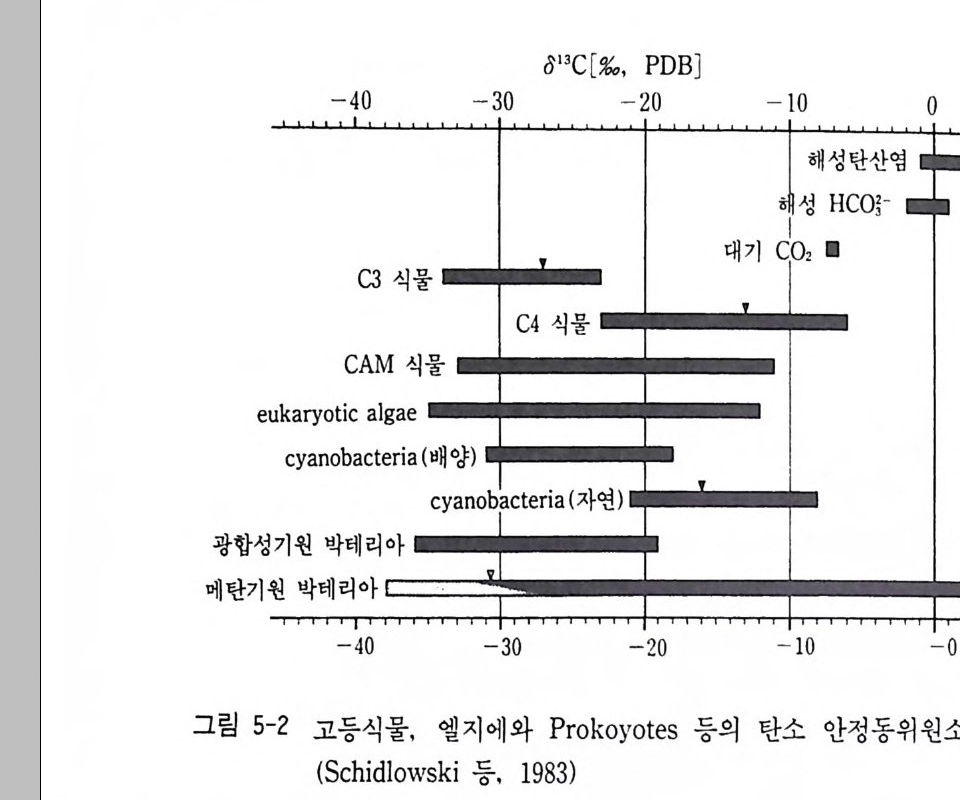 o'3C[%;,, PDB]
o'3C[%;,, PDB]
걸프만의 해저퇴적물의 탄소 동위원소비 분석에서 바다에서 육지로 감에 따라 _21 에서 _26% 까지 변화해 육상식물의 영향을 크게 받음 이 나타났다 (Sacke tt와 Thomp so n, 1963). 5-2 탄산영 암의 동위원소비 Ke ith와 Weber (19 64) 는 지 질시 대 에 따른 탄산영 암의 동위 원소 분 석자료에서 고생대 이후의 지질시대에 있어서 황 동위원소와 함께 시 대에 따른 변화 (Secular va ri a ti on) 를 보이고 있으며 황산염의 황 동위 원소의 시대별 변화와 상관성이 있는 것으로 해석하였다 (Ve i zer 와 Hoe· fs, 1976) . 그러나 Schi dl owski 등 (1983) 이 종합한 자료에 의 하면 선캠브리 아
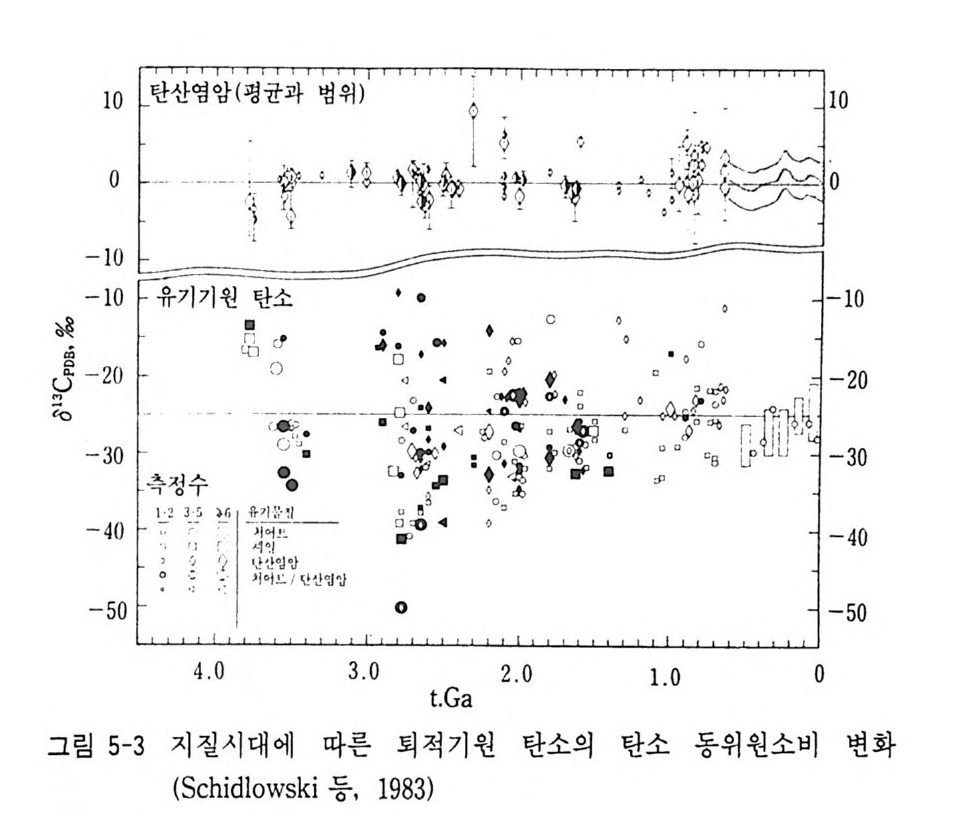 10 탄산영암(평남십-江 ,---- 口 『 ' 『 . · · 10
10 탄산영암(평남십-江 ,---- 口 『 ' 『 . · · 10
기 동안의 지질시대에 걸쳐서는 탄산염암의 어떤 특정한 탄소 동위원 소 변화특성을 찾아볼 수 없다. 선캠브리 아기의 탄산영 암에 13c 이 대 단이 많이 농집 되 어 +10%, 값 까지 가진다. 유기기원의 탄소에서 동위원소의 변화는 대단히 심하여 탄산영암의 동위원소 변화와 대조적이다(그림 5-3). 유기기원의 탄소에서 동위원소비가 다양하게 분산 도시되는 현상은 원래의 유기원탄소물질의 동위원소비의 다양성과 속성작용과 변성작 용에 의해 유기원 탄소의 탄소 동위원소비가 다양하게 변화된 것으로 보인다. 예를 들면 그립 5-4 에서처럼 변성도가 증가함에 따라 o13C 값 이 점점 증가하고 있다. 죽 퇴적암 중의 유기원탄소가 케로겐으로 변 하면서 메탄이 생성 유실되므로 “C 이 부화되기 때문이다 (Mck i rd y와 Powell, 1 974) .
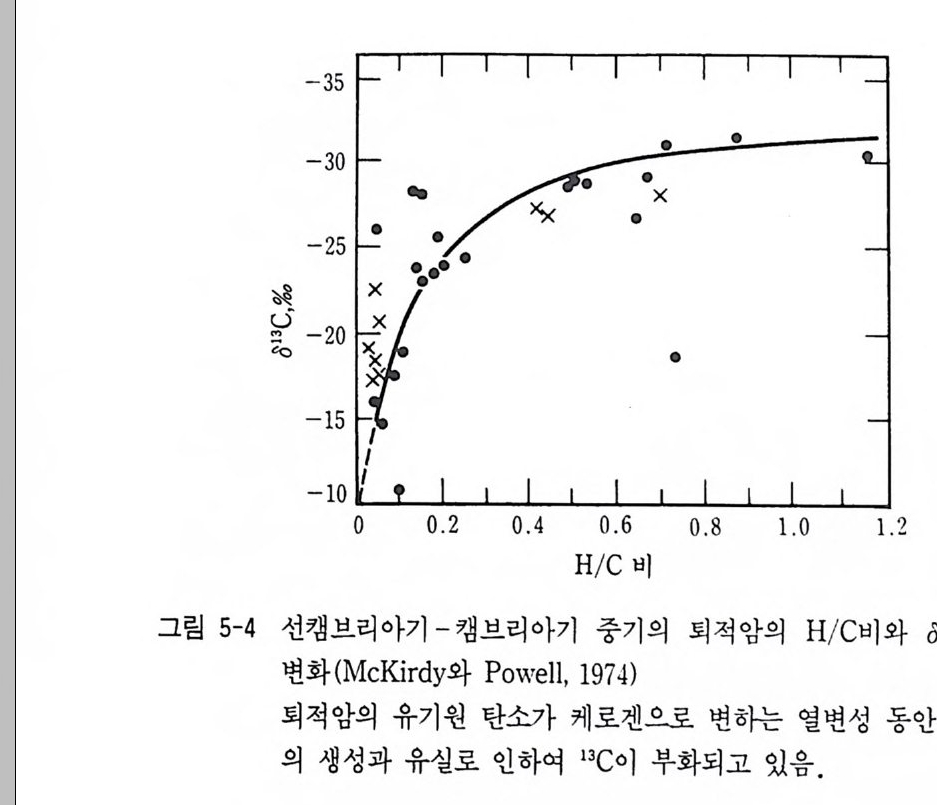 -35
-35
탄소 동위원소비는 해성 석회암은 +0.56 土 1.55%0 이고 담수성 석회 암은 -4 . 93 士 2 . 75%., 이 다 (Ke ith와 Weber, 1964) . 탄산염 암의 탄소 동 위 원소값은 보통 0 土 5%., 로 0% 가 보통이 다. 그러 나 속성 작용이나 변 성작용에 의해 가벼운 동위원소가 더 농집된다. 산소는 공극수나 해수 및 주위의 암석에 의해 속성 및 변성작용시 에 탄소보다 더욱 현저하게 동위원소값이 가벼워지며 그의 변화 폭도 크다. 탄산영암의 침전은 CO2(g) +H20+CaC03~Ca2++2HCO;( 액) 식에서 가열, 동요, 광합성에 의한 CO2 의 감소가 예상되는 천해 환 경에서 주로 일어난다. 해수나 담수에서 침전된 탄산염암의 동위원소 성분은 다음 몇 가지 요인에 의해 변화된다.
O 용액 중의 C02( g)나 HC03(a q)와 이와 평형상태에 있는 CO2 가스의 013c 값 ® 용존탄산아온과 CO 2 가스 사이의 온도에 따른 동위원소 분별 ® 수소이온 농도 및 기타 화학적 특성 등이다. 남한의 고생대 대석회암층군의 석회암에서도 속성작용 또는 광역변 성작용에 기인한 산소 동위원소값의 변화가 현저히 나타났다. 풍촌 석회암의 동위원소 분석연구에서 속성작용과 동위원소바 변화 롤 해석했고 속성작용시의 온도 (42.8~67. 4' C) 와 그 때의 심도 (1. 4~2.2km) 를 해석했다(박병권과 우경식, 1986).
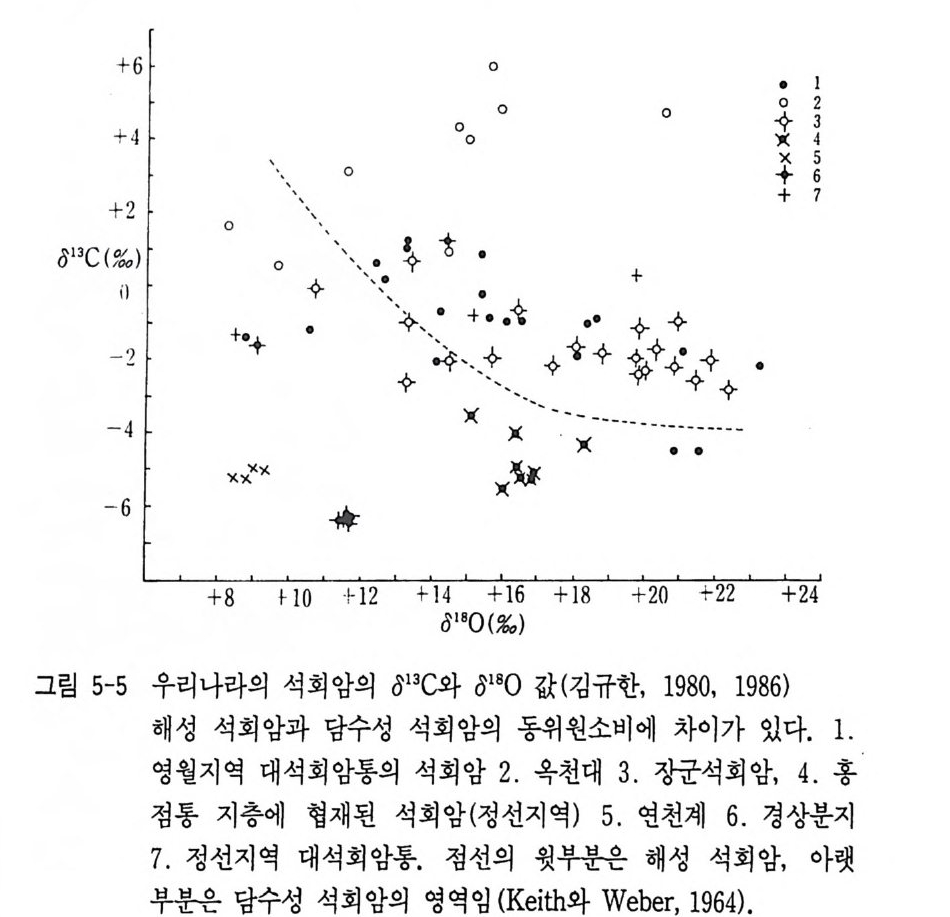 +6 。.°41x2x3+4+5 67
+6 。.°41x2x3+4+5 67
남한의 대석회암통의 석회암은 해성 석회암이었으며 경상계 지충 중의그 림석 회5-암5 에 노서듈 보은면 담 조수선성누기층원군의의 특 석징회을암 잘은 보a여13주c=었 다—(4.5그 림~ +5~1.53)%. ., (평균 -1.1% ..), 8180= +8.8 ~ +23.3%, (평균 + 16.0%..) 이지만 옥천습 곡대내의 석회암은 a13C=+5~16%, 로 대단히 무거운 동위원소가 농 집되어 있다. 이는 그림 5-3 에서 의국의 선캠브리아기의 탄산염암에 서 나타나는 경우와 대비된다. 미국 북동해안의 풀라이스토세 사충 중의 아라고나이트는 -23.1 ~ -6 0.6%, 로 기록되고 있다(H a th awa y와 Deg en s, 1969). 후자의 아라 고나이트의 C 의 기원은 메탄의 산화에 의해 異常的 으로 12c 가 농집 되었기 때문이며 13c 이 많이 포함된 전자는 해성기원으로 해석되고 있다. 5-3 고수온 측정 및 고기후 연구 Eps t e i n 등(1 951) 은 동위원소 분별식을 이용하여 완족류와 유공충 화석시료에서 고수온 측정을 적용하기 시작했다. 그러나 Donk0977) 과 Erez 와 Hon j o(1981) 의 연구에서 유공충 등은 동위원소 평형에 있 지 못한 결과를 얻었다. Erez 와 Luz (1 983) 는 이 문제해결을 위해 Globig e rin o id e s saccul if er 의 작은 개 체 의 배 양성 장 실험 에 서 50~ 90% 각질이 온도 14~3o·c 수온에 영향을 받으면서 퇴적되고 물의 동위원 소 성분에 영향을 받고 있음을 알게 되었다. 실제 유공층의 성장온도와 산소 동위원소 지질온도계에서 얻어진 유공충의 CaC03 형성온도 비교에서 유공충의 CaC03 가 동위 원소 평 형에서 침전되고 있음을 알게 되었다. 지질시대의 지층에서 산출되는 화석이나 심해저 퇴적물 중의 유공 충과 감은 화석의 산소 동위원소 분석을 통한 고생물학적 연구 의에도 십해저 퇴적물, 기수호 되적물, 종류석 등의 탄소 동위원소비와 C/N
비 분석으로 고기후 변동 연구가 수행되었다 (Naka i , 1975 ; Naka i와 Shi • rai, 1 978, 1984) . 일본의 비와 호의 200m 시추코어의 호수되적물의 탄소 동위원소비 와 유기물의 함량변화가 기후변동과 밀접하게 연관되었다(그립 5-6).
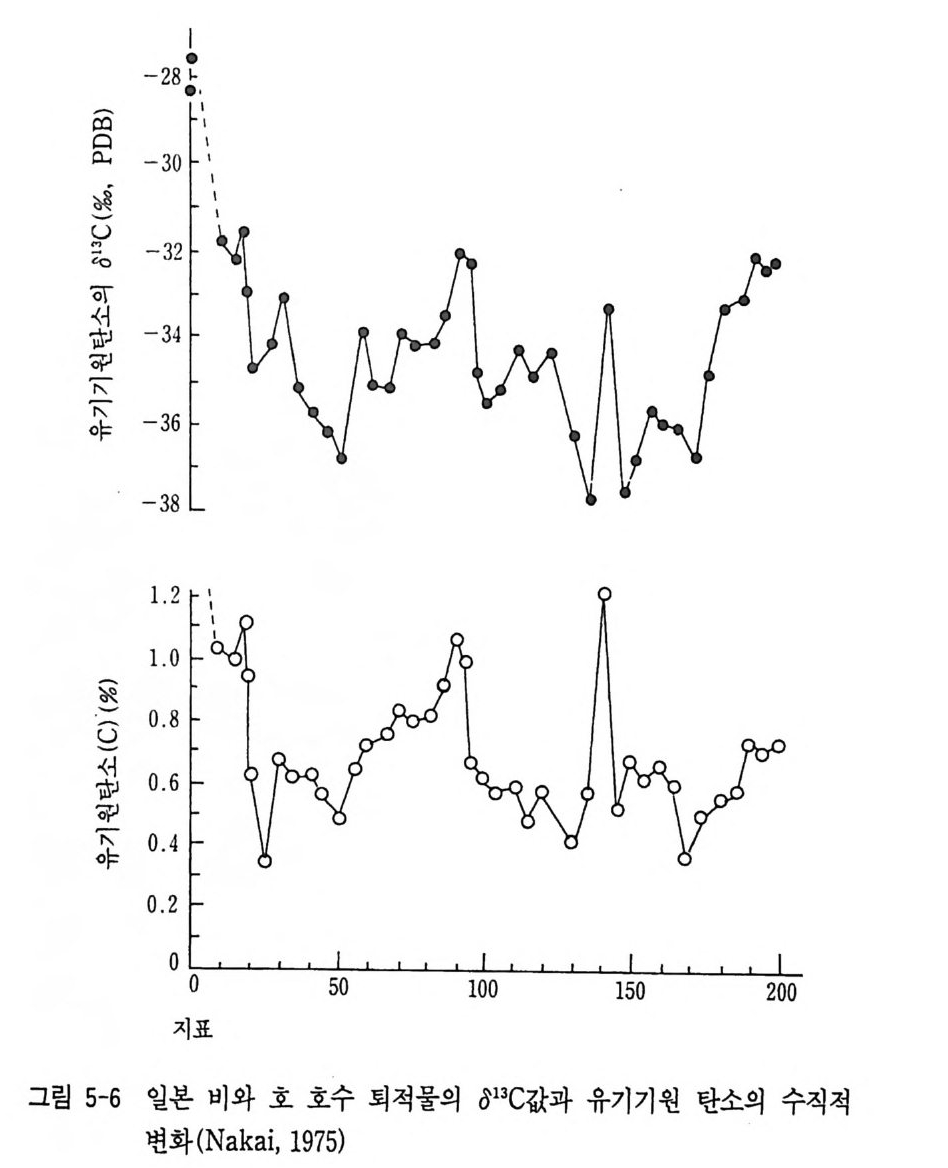 롭 --3280 ••I1•- I I I ’ I
롭 --3280 ••I1•- I I I ’ I
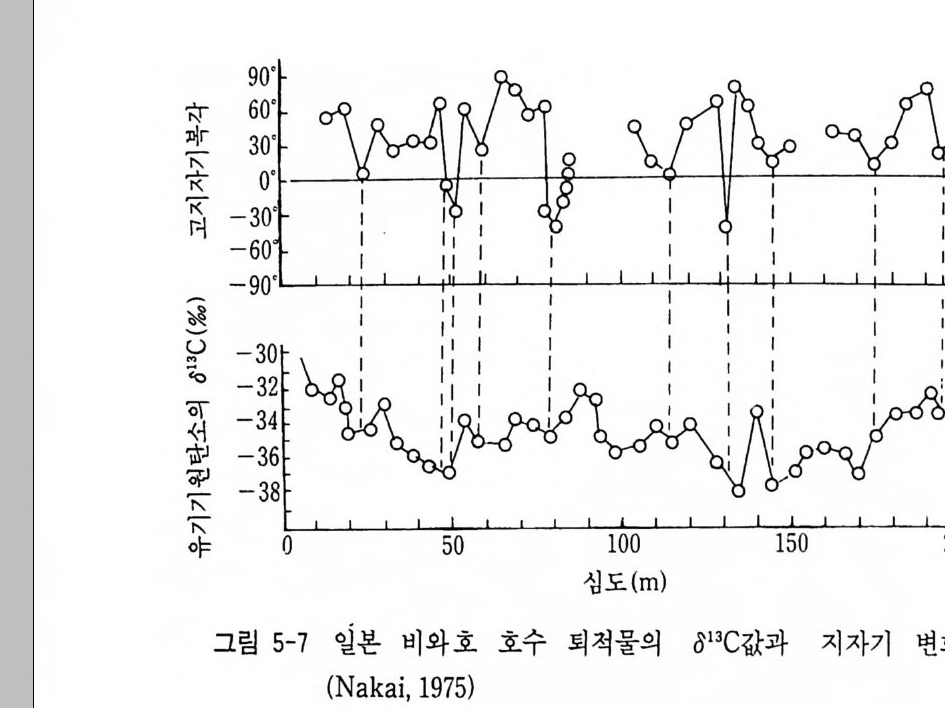 :도K 9300o·°'
:도K 9300o·°'
즉 온난한 기후시에는 한랭한 기후시에 바교해 플랑크톤과 같은 유 기물의 생산량이 높고 퇴적량도 많아 유기되적물에는 13c 가 더 많이 포함되어 있었다. 그리고 고지자기 자국 반전커브와 유기물의 o13C 와 도 조화적 이 었다(그림 5-7) . 일본의 하마나 항의 코어 퇴적물에서 o13C, AMS14C(Accelerato r mass s p ec tr ome t er) 연대 등을 분석하여 홀로세의 고기후 변동과 해수 면 변동을 연구하였다 (Naka i 등, 1987). 기수호 (Brack i sh lake) 란 고가후 변동으로 간빙기의 해수환경에서 빙기의 담수환경으로 퇴적환경의 변화를 수차 경험한 호수를 말한다. 일본에는 미가다 호 등 기수호가 대단히 많이 알려져 있으며 우리나 라에는 경포호, 화전포호, 영랑호 등이 여기에 해당된다. 기수호의 퇴적물에서 고기후 변동의 지질학적 기록을 찾아볼 수 있 게 되었다. 고생물학적, 되적학적 내용 의에 이들 퇴적물 중의 유기
물의 동위원소 분석법이 소개되고 있다. 기수호 퇴적물 중의 유기물 의 탄소 동위원소비와 C / N 비는 이들 퇴적물의 근원지가 육성기원인 가 해성기원인가에 1 차적으로 영향을 받고, 2 차적으로는 기후, 온도 변화에 따른 광합성의 영향에 따른 동위원소 분별에 의한 영향을 받 는다. 실제 퇴적물의 분석에서 온난기(간빙기)의 퇴적물 중의 유기물은 o13c 값이 크고 C / N 비가 낮으며 한랭기 (빙하기)에는 반대현상이 나 타났다. 일본의 하마나 항 퇴적물에서 고기후 변동에 따른 유기되적 물의 o13c 와 C / N 비의 변화가 뚜렷이 나타났다(그림 5-8). 이 결과에 서 6500BP 조몬기에 최대 해침이 일어났고 간빙기가 3500BP 까지 1,000~2,000 년간 지속되었음을 알게 되었다. 그리고 8000~8500BP 와 8000~7000BP 사이에는 해퇴가 일어났다. 유사한 결과가 나고야 항 퇴적물의 규조토 화석에 의한 방법과 013C, C/NBl 비교에서도 잘 입증되었다.
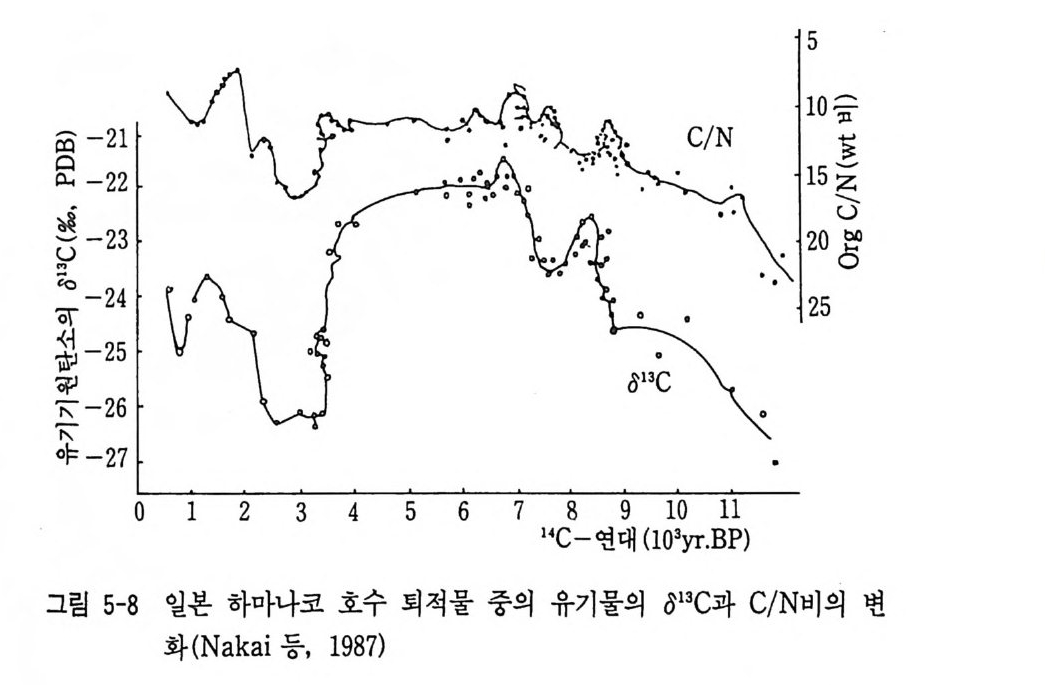 5
5
우리나라 동해안 기수호인 영랑호의 퇴적물 황철석 함량변화도 고 기후 변동과 밀접한 관련이 있었다(나까아, 198 0) . 5-4 변성암에서의 탄소 동위원소 석회암이 접촉변성작용이나 광역변성작용을 받으며 탈탄산가스반응 등에 의해 산소 및 탄소의 동위원소값이 변화한다. 변성암내의 방해석-돌로마이트 광물쌍의 탄소 및 산소 동위원소값 변화에 대 한 연구가 Schwarca (1966) , Sh i eh 와 Tay lo r (1969) , She- pp ard 와 Schwarca (1970) , Ry e 등 (19 76) , O'Ne i l 과 Ghent (19 75) 등에 의 해 연구되었다. 탄산염암의 변성반응 중 특히 탈탄산가스 반응과정과 동위원소값의 인화가 중요한데, 우선 몇 가지 탈탄산가스반응에 대한 등압 T·Xco2 그림은 앞장의 그림 4-51 과 같다. 이러한 반응에서 암석에서 탈 CO2 과정과 동위원소 효과가 밀접한 관련이 있다. 실례로 미국의 트랜돈석회암과 우리나라의 막동석회암, 파인크리크 의 텅스텐 스카론 광상 등이 있고, 그 의 의국의 많은 예는 표 5 - 1 과 같다. Ta y lor 와 O'Ne il (1977) 은 비변성석회암과 변성석회암 사이에 탈탄 산가스반응에 의해 8180 는 3%, 813C 는 5%o 정도 변화된다고 설명하 고있다. 이 와 같은 관계 롤 배 취 휘 발반응 (Batc h volati liza ti on ) 에 의 해 Brown 등 (19 85) 은 동위 원소 분별정 수 (Bott ing a , 1968) 와 레 이 리 분별 (Matth - ew 러 Kolodny, 1978) 을 이용하여 다음과 같이 개 방계 와 폐쇄 계 의 경 우에 13C 결핍올 계산하였다.
표 5-1 변성작용을 받는 818O 와 o13c 값의 변화 (Valley, 1986, So 등, 1983, Kim 등, 1980, 1988) . 광산 접목촉 (대km의) 압(k력b심ar도) 최(대'C온) 도 XC02 8(P“DC동B 위) 원8(소s1M8비0o w) 심성암 비고 상동 W-Mo 670 15 12 화강암 석회암, 스카 과0 사\.. 론, 후기영수 방해석 신예미 Pb· 550 4 7 화강섬록암 석회양 스카色 Zn-Cu 광산 열수성 방해석 월악 W-M 。 2.5 1~2.4 >4 00 11 15 화강암 석회암, 스카 광산 km T군 마운트로얄의 0.1 6 14 섬장암 석회암, 대리 트렌돈석회임 암, 방해석 메리스빌레 1-3 1 525 0.9 5 6 18 화강섬록암 대리암, 열수 (몬타나) 성탄산영광물 파인크리크 <2 600 <0 .2 5 14 22 석영몬조 대리앙 스카巳 W- 스茂 니암 석회규산염암 오스구-드 마
813Ccc-Xco, (설 3Ccc-co2) = 813C 계 (폐쇄계) Rl/R,.=Fa-1 (개방계) 8f_ &=l000 {F(a-1)-1} 여기서 R f과 R i는 반웅 전후의 13C/12C 비를 말하며 a 는 동위원소 분 별정수, F 는 암석내에 잔류하고 있는 탄소의 몰분률이다. 탈탄산가스 반응과정에 따른 동위원소값의 변화를 보여주는 구체적 인 예로 우리나라 상동 중석광상을 들어 보자. 상동 중석광상에서 풍 촌 석회암과 스카른 광체간에 탈탄산가스반응의 경향이 잘 나타나고 있다(그림 5-9). 개방계와 폐쇄계에서 위의 관계식을 이용하여 상동 중석광상의 모
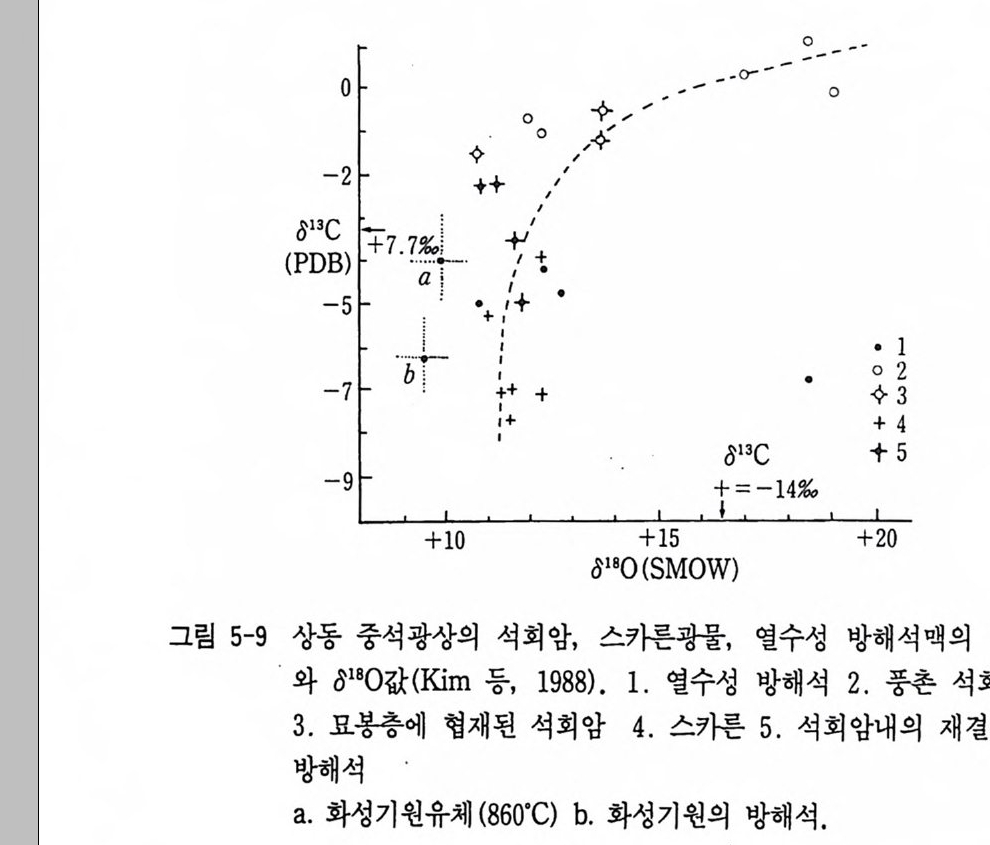 盆)---257。 「 , 7•.•b•7• 층· \ : ' 수t•. ++ '+’+ 꾸1,1 1O+ 0+I I, 1, , '/ 수수/+. / •/ _.o -- -。· 一 。- -· 04 + +'
盆)---257。 「 , 7•.•b•7• 층· \ : ' 수t•. ++ '+’+ 꾸1,1 1O+ 0+I I, 1, , '/ 수수/+. / •/ _.o -- -。· 一 。- -· 04 + +'
표 5-2 상동중석광 상 의 탄 산 영광 물 의 탈탄산가스반응 시 13 c 결 핍 (Ki m 등 , 1988) 계내의 폐쇄계내의 잔류방해석의 01 3 C 값 개방계내의 잔류방해석의 01 3 C 값 잔류탄소의 a13C= +o .6 013 C = -0.8 813C= +0 .6 013 C = -o.s 몰퍼센트 (풍촌석회암) ( 묘 봉충중의 석 회암) (타석회암) ( 묘봉 충중의 석 회암 ) 100 +0 .6 0 _ 。 . 80 + 0.6 0 - 0.8 0 90 +0.36 -1 .0 4 + 0.3 5 - 1.0 5 80 +0.12 -1.2 8 + 0.0 6 -1.3 3 60 -0 .3 6 -1 .7 6 -0.6 2 - 2.0 2 50 -0 .6 0 -2 .0 -1.0 6 -2.4 6 40 -0 .84 -2.2 4 - 1.60 —2 .9 9 30 -1.0 8 -2.4 8 -2.29 - 3.6 8 20 -1.32 -2 .7 2 -3.2 6 一 4.6 5 10 -1.5 6 一 2 . 96 -4.9 0 - 6.3 1 -1.7 8 -3 .1 8 -10.4 0 -11.7 8
암인 풍촌석회암(또는 묘몽충내에 협재된 석회암충)과 상동화강암의 접 촉부에서 탈탄산가스반응에 의한 13c 결핍울 계산하면 표 5-2 와 같다. Kim 등 (19 8 8) 에 의하면 상동 스카론 중에는 20% 내의의 방해석이 잔류되고 있다. 이 때의 계산된 813c 의 값은 스카른에서 측정된 값과 일치하지 않는다 . 이를 상동스카론내의 잔류 방해석의 탄소 (C) 의 기원이 풍촌석회암 의 탄소 의에 십부기원의 탄소가 추가되었기 때문인 것으로해석하였다. 실제 자연환경의 변성작용의 반응에서 C - 0-H 유체는 CH4 과 CO2 등이 존재하기 때문에 순수한 CO2 환경에서 일어나는 단순한 탈탄산 가스반응에서 기대되는 동위원소 효과와는 다 소 다르다 . 대부분 해성 석회암의 813 c 는 0% ., 내의이므로 이 석회암 의 탈탄산가스 반응시 생 성된 CO 2 는 보통 +3 ~ +5%.,(Bott ing a, 1968) 의 값을 나타낸다. 그러나 대부분 지열지역에서의 CO 2 는 -3 ~ _4%., 의 부의 값을 가 지므로 이 CO2 는 단순히 해성 석회암의 탈탄산가스 반응결과로 해석
하기는 힘들다. 광역변성작용에 의한 변성암에는 흑연과 방해석이 보통 대리암이나 기타 변성암류에 공존하고 있다. 앞장에서 언급한 바와 갇이 흑연-방해석의 탄소 동위원소 분별정수 (Bott ing a , 1969 ; Valle y와 O'Neil , 1 981 ; Wada 와 Suzuki, 1983 ; Morik i y o, 1984) 가 알려져 있다. 방해석과 흑연이 동위원소 분별계수의 온도 의 존성은 그림 5-10 과 같다. 직접 동위원소 분별실험은 어렵기 때문에 보통 기타 지질학적 자료와 함께 경험적인 온도계를 만들어 쓰고 있다. 이들의 동위원소 평형정수를 이용하여 계산된 우리나라 옥천습곡대 내의 창리층내에 • 협재된 대리암의 생성온도는 384~433 ' C( 김규한, 1986, 나기창 의, 1988) 로 변성광물 조합에서 추정되는 녹색편암상과 일치하고 있다. 변성암내의 대부분의 흑연은 퇴적암의 원유기물 기원의 물질에서
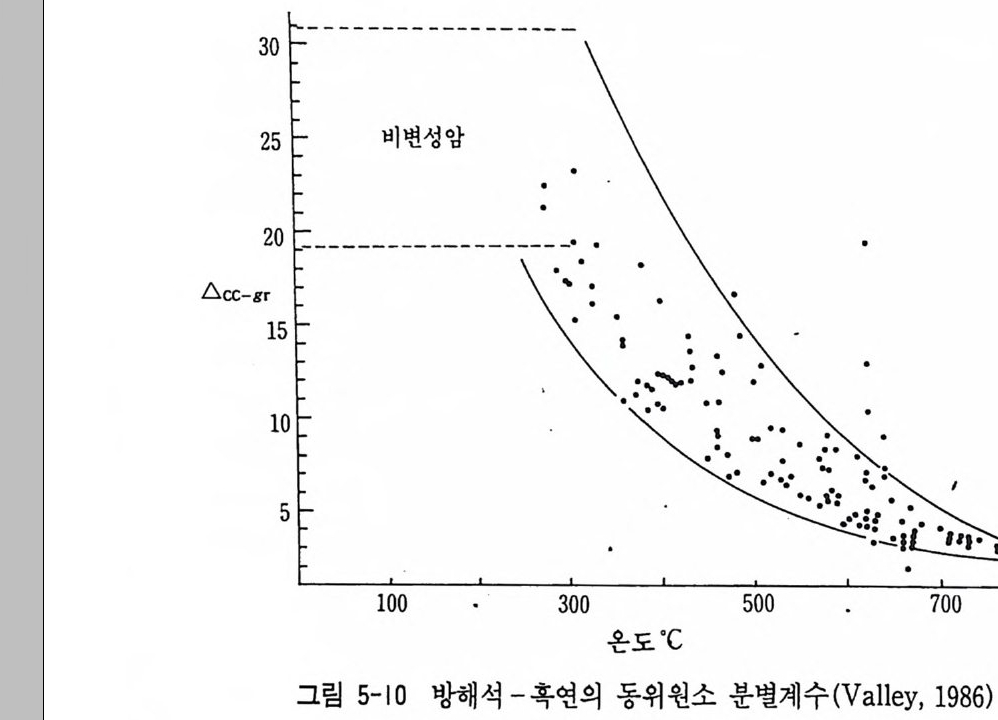 30
30
유래된 것이나 일부 대리암내의 흑연은 탄산염암 또는 C 아의 환원에 의해 생성된 것도 있어 흑연의 동위원소값이 -7%, 로 보고되었다. 우리나라 옥천습곡대 덕평지역의 탄질셰일 중의 유기기원의 흑연은 一 14.5 ~ 一 26 앎0 내의이다. 퇴적암의 8 1 3C o r g 과 813C c arb 의 연속성에서 적어도 35 억 년 전까지 무기 영 양성 생 명 형 태 (Auto t r o p hi c life for ms) 에 의 한 탄소고정 이 지구 의 탄소순환을 조정한 것으로 가정된다. 형태가 뚜렷한 화석산출이 거의 없는 선캠브리아기의 생물에 대한 연구로 탄소 동위원소 분석연 구가 유용하며 초기 지구의 탄소 순환에 서 무기 영 양성 (Auto t r op h y ) 의 가능성을 암시해 주고 있다. 그러나 동위원소 자료로는 광독립영양체 (Photo a uto t r o p hs ) 와 화학무기 영 양체 (Chemoauto t r o p hs ) 에 의 해 만들 어 진 유기 물과 형 기 성 및 호기 성 광독립 영 양체 (Anaerob i c 과 aerobic pho to a uto t r o p hs ) , Spa r k dis c harge syn the ses 등의 산물과 심 하게 변 성을 받은 생물기원의 탄소 등을 구별할 수 없으므로 해석의 한계접 이 있다. 그러나 이룰 다른 여러 자료와 종합하면 유기물의 진화의 최초의 단계를 밝히는 단서가 될 수도 있을 것이다. 5-5 광상의 탄산염광물 열수계에서 얻어지는 탄소의 기원은 보통 O 해성 석회암 기원의 탄소 (013C=O %i) @ 카보나타이트 (Carbona tit e) 나 킴버라이트(Kim ber lit e) 의 분석에서 얻어진 심부기원의 탄소 (013C=-5 ~ -8%) ® 퇴적 암내의 유기기원의 탄소 및 변성암 및 화성암내의 흑연 (013C=-20%,) 울 들 수 있다. 열수성 탄산염광물의 탄소의 동위원소 성분은 광화용액의 전탄소의 J l3C 뿐만 아니라 광화용액의 f。 2, PH, 온도, 이온강도 및 전탄소의 농도 (~C) 등에 크게 좌우된다 (Ohmo to, 1972 ; R y e 와 Ohmoto , 1974). 용존 탄소종은 CO2 (aq) , H2C03, HCO;-, cor, CH4 (aq) , CO,
cos 등 여러 종이 있는데 열수성 탄소의 기원 해석을 위하여서는 다음과 같이 013Crc 울 계 산해 야 한다. o13Crc=: (o13Cco,•Xco,) + (013CH, co ,•XH,C03) + (013CHc 03 •XHc o3) + ( o13Cco~-• Xco~-+ ( 013CCH 건 • XcH.) 여 기 서 Xi =m i/ m~C 이 다. 013CH2CO s (a q)를 기준으로 잡아 기타 탄소종의 동위원소값을 다음과 갇이 표현할 수 있다. 013C i = 013CH, Co l (aq ) + 석 여기서 S13C i는 i종의 탄소의 동위원소비, t::, i는 i종과 H2C03(aq ) 사이의 상대적인 동위원소 부화를 나타내는 항이다. 위의 두 관계식에서 813G=813c2e+A i _ [(6ttc o i · Xt tco i ) + ( 6 CO~-·XCO 訂 + (6 C H4 • xCH4) ] H2C03 (aq ) = H+ + HCOs HCOs=H+ + cor CH ◄ (aq ) + 202 = H2C03 (aq ) + H20 (1) 반응식에서 각 탄소종의 몰분율을 계산하면 XHcoi C= ' • 師 ·Y~HC03 X굶 = KH2Cco3· •( KH師C )023. • rrHco2C:0-3fa q,
xCH: = C ' \C;。 4 2 ) 2 가 된다. 위의 식에서 C'= 1+ ( ~aw ,)I (\ /H」co i근 ' aHK+H ' C/0C3O i )/ +' (K/0C2H4) 2 이다. 따라서 전탄소의 양에 대한 열수용액의 탄소종의 몰분율 (X i)은 용 액의 온도 (T), 산소 퓨가시티 (fo2 ), 수소이온농도 (PH), 이온강도 (I) 등의 함수이다. 따라서 o13Ci =f(o1 3C:i: c , T, fo2, PH, I) 의 관계에 있다. 산소 퓨가시티는 탄소종의 산화상태에 영향을 준다. 만일 산소 퓨 가시티가 10 기압 정도이면 대부분 탄소는 산화되므로 환원탄소종은 무시된다. 그러나 산소 퓨가시티가 낮으면 환원탄소종의 양이 증가하 고 이와 같은 환원탄소종은 12c 가 많기 때문에 이와 공존하고 있는 탄소종의 a13c 값은 현저히 적어진다. 또 fo 2 값 이 고정되었을 경우 산화된 탄소종의 a13c 값은 HC03 와 co~ - 의 양의 변화와 PH 변화에 따라 변화된다. 이처럼 광화용액 중 의 임 의 의 탄소종의 탄소 동위 원소값은 fo2 , PH, I, T, o13C :i: c 의 값에 의해 변화되기 때문에 이들을 함께 고려하여 그림을 그리면 (예, Rye 와 Ohmoto , 1 974) 열수광상 형성시의 환경이 해석된다(그림 5-11 ). 그림 5-11 에서 보면 캐나다의 에코베 이 (Echo Bay) 광상은 산소 퓨 가시티가 변화하는 환경에서 이루어졌고, 캘리포니아의 · 다윈 (Dar win) 광상은 PH 가 변화하는 환경, 그리고 아일랜드의 모굴 광산 (Mog ul Mi ne) 은 PH 및 산소 퓨가시티가 동시에 변화하는 환경에서 광상이 형성되었음을 알 수 있다. 그림 5-12 의 열수광상의 탄산염광물의 813C 값의 특징을 보면 탄산
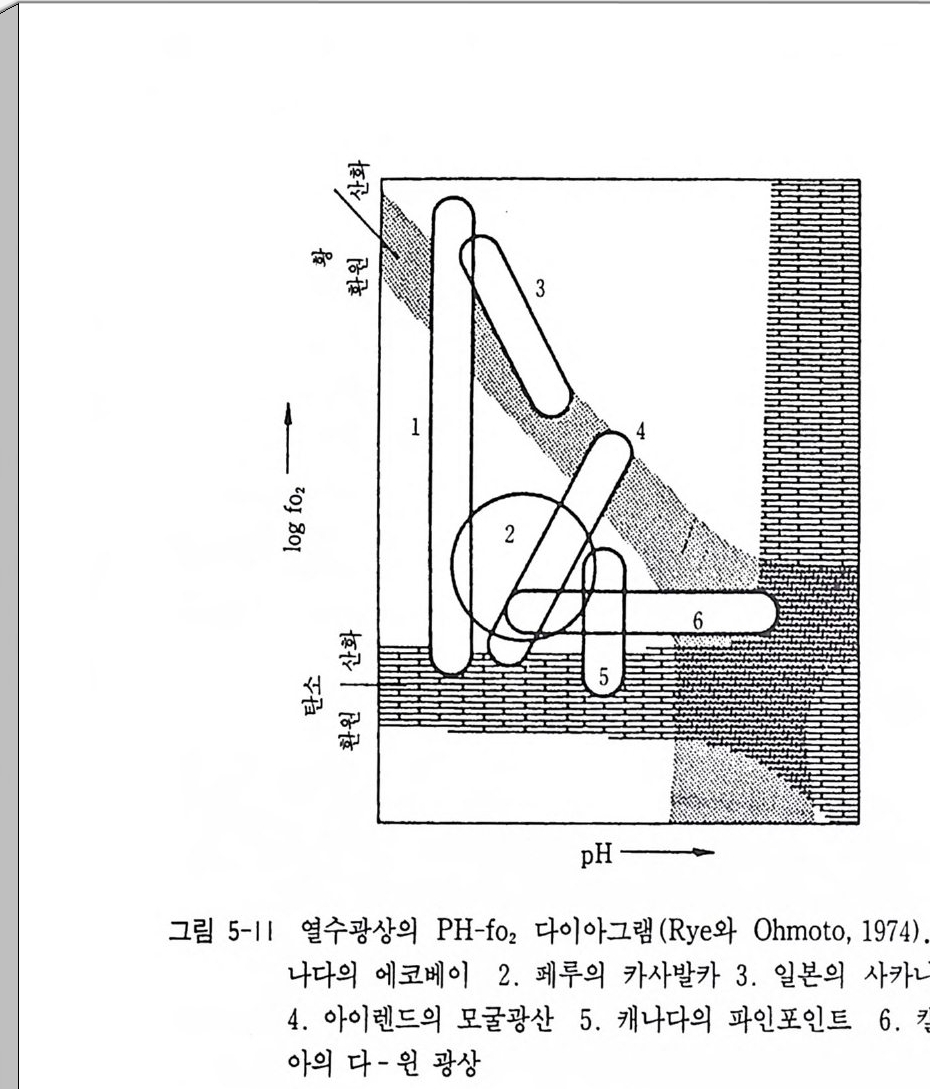 中古`
中古`
영광물이 생성시기에 따라 탄소 동위원소값이 변화하고 있다. 이와 같이 탄소 동위원소 값은 여러 가지 요인에 의해 변화하며 각 탄소종 의 존재비에 따라 다르므로 L! C02 의 813C 값을 계산하여 탄소의 기 원을 결정해야 한다. 파인 포인트 (P i ne Poin t) 광상, 부루벨 (Bluebe ll) 광상, 프로비덴시 아 (Pro vi denc i a) 광상 등의 광상의 탄산염광물의 813C 값은 초기에서 후기로 갈수록 13C 이 많이 농집되는 경향이 있다. 초기의 탄산염광물은 813C=-5 ~ -7 %o로 심부기원의 탄소의 값을
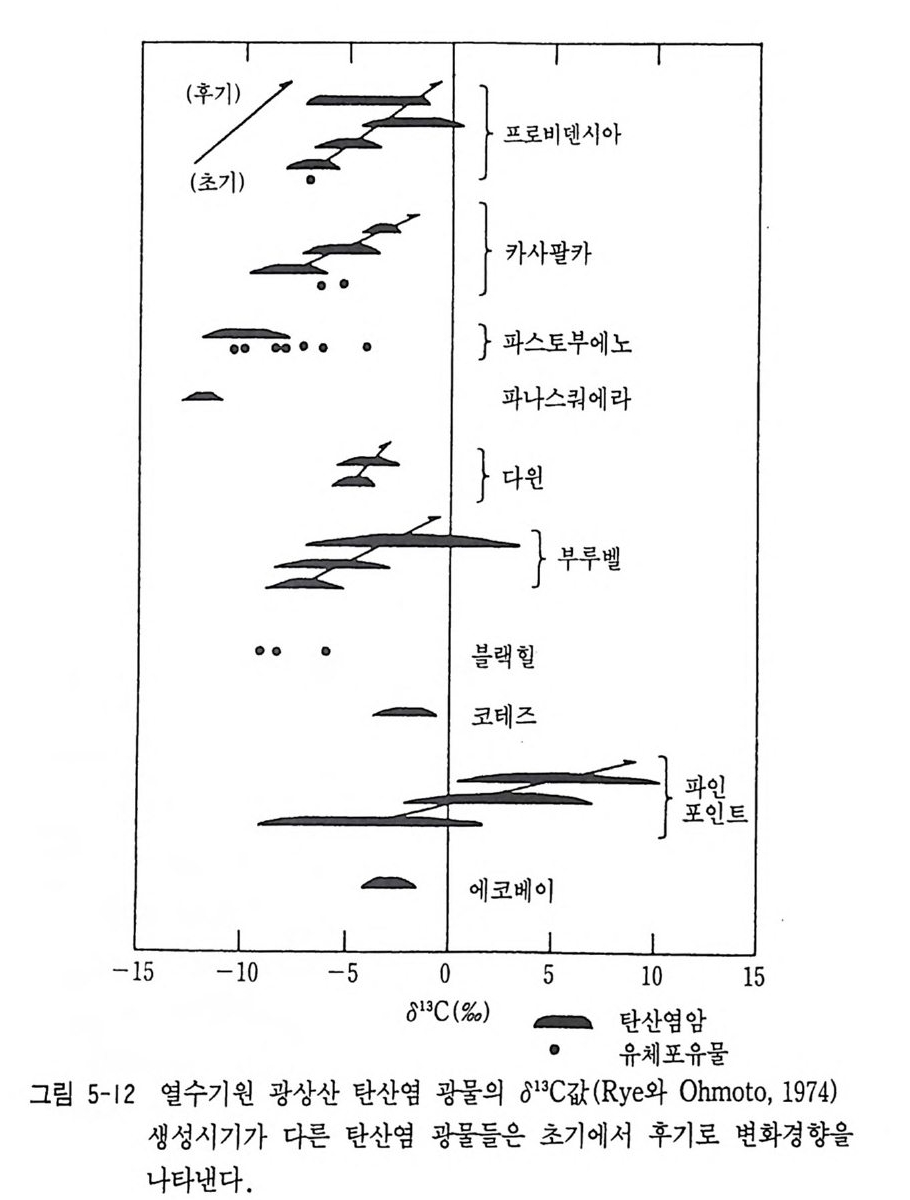 }무비덴시아
}무비덴시아
나타내지만 후기로 감에 따라 탄산영암 또는 유기기원의 탄소와의 혼 합에 의해 동위원소값이 변화하게 된다. 후기 탄산염광물의 주광화시 기의 탄산염광물의 동위원소값보다 무거워지는 이유는 O 광화용액의
냉각 ® 광화용액의 C0 z/ CH4 비의 감소 ® 기타 기원의 CO2 증가 등 으로 해석되고 있다. 열수성 탄산염광물의 산소 동위원소비로 광상생성온도나 원열수용 액의 산소 동위원소비를 결정할 수가 있다. 그러나 많은 연구에서 탄 소 동위원소연구는 탄산염굉물이 주광화작용의 후기에 보통 형성된 것이기 때문에 H, O, S 의 동위원소에서처럼 광범위하게 사용되지 못 하고있다. 5-6 화성기원의 탄소 카보나타이트 (Carbona tit e) 연구에서 013C 값이 —5 ~ _8%0 범위를 가지는 탄소는 마그마원 CO2, 초생수, 심부기원 또는 맨틀기원 CO2 로 제안되어 왔으며 (Tayl o r 등, 1967, Dein e s, 1973) 아 값을 가지는 탄 소를 보편적인 마그마의 특성으로 생각해 왔다(H o ef s , 1973 ; P i neau 와 J(aHvo oeyf,s , 19189373) ). , 이— 5값 . 5 %은., (O지h r각no의 t o 와평 R균y e,탄 19소79 ) 동과위도 원유소사의하 다값.인 —7 . 0 %., 기원마그마에 비해 13C 이 많은 CO2 와 마그마와 가스 사이에 동위 원소값의 변화가 적은 CO2 는 폐쇄계가 지배적인 CO2 탈가스 시스템 이었다고 추정할 수 있다. BAB (Arc-and back-arc basalt a ndesite -d ac ite associa t io n ) CO2 의 013C 가 MORB 의 현무암질 마그마의 o13c 보다 값의 변화폭이 크다. 화산가스의 013Cco2 와 화산 하부의 지각의 두께와 정의 상관관계가 나타난다. 이 관계에서 상승한 호상열도 마그마와 탄산영암이 점진적 으로 동화된 것으로 설명 하고 있으나 013Cco2 와 87Sr/86Sr 과의 상관성 은 나타나지 않았다 (Allard, 1983) . 3He/4He 비가 초생기원의 탄소를 인정하는 척도로 사용되고 있다. co 가 헬륨 (He) 과 동반자이기 때문에 헬륨과 013Cco2 관계에서 우리 는 탄소의 기원을 해석할 수 있다.
그림 5-13 에서처럼 He 열점인 하와이의 킬라우에와 아이슬랜드(크 라프라)의 CO2 는 a13c= —5.2 ~ _3.2%0 을 나타내며 이들 지역의 마 그마원 (또는 맨틀기원) CO2-He 가스는 환원된 퇴적기원의 C(o13C =一 28, 경향, 0) 와 해성 탄산염암의 C(813C=O, 경향, M) 과의 혼합 울 찰 나타내 주고 있다. MORB 유리질내의 기공의 C 아의 813C= _8. 0 ~ _4.3%0 로 폐쇄 계에서 CO2 가 탈가스된 것으로 보이며 013Cco, 는 C02 / H20 와 같아 감소하는 경향도 이와 일치한다. 또 현무암질 유리질 물질의 탄소 동 위원소 분석을 위하여 600'C 이상에서 축출한 고온형탄소(H TC) 와 600'C 이하에서 축출한 저온형탄소 (LTC) 의 동위원소비를 분석해 보면 각각 013CLTC = —22 .5 ~ ― 29.5%0 와 013CHrc=-11 ~ —3.5 % o 범위이다. 염기성 규장질 화성암에서도 이와 유사한 경향이 얻어졌다. 심성암 중의 흑연의 a13c 값은 대다수가 탄소질 변성 퇴적합의 동화에 의해 생성된 생물기원에 상응하였다. 카보나타이트는 흔히 알카리 성분이 많은 화성암과 밀접히 수반된다. 카보나타이트의 탄소 동위원소값 은 _2. 0 ~ _8.0% 이다. 그리고 킴버라이트의 다이아몬드의 o13C 값 은 _35 ~ +5%o 범위이며 주로 -5 ~ +2% o 이내이다. 아직 맨틀내 에서의 다이아몬드 생성기구가 명확하지 못하다. Ohmo t o 와 Kerr i ck (1 977) 에 의하면 CH4+C02=2C+2H20 반응에 서 다이아몬드가 생성될 수도 있으며 1500'C 부근에서도 CO2 와 CH4 사이에 동위원소 분별이 크기 때문에 동위원소값의 변화가 클 수 있 다고했다. 따라서 맨틀기원의 탄소의 동위원소값을 규정하는 것은 대단히 어 려운 일이다. 맨틀기원의 탄소의 동위원소값이 불균질한 이유는 G 원시지구의 탄소동위원소 불균질성 ® 지각-맨틀 상호작용 ® 판의 섭입시 유기기원의 탄소의 재순환 등으로 해석되고 있다. 보통 o13c =-5%, 을 맨틀기원으로 해석하고 있으나 사실은 지각기원의 것과 구 별이 불가능하다.
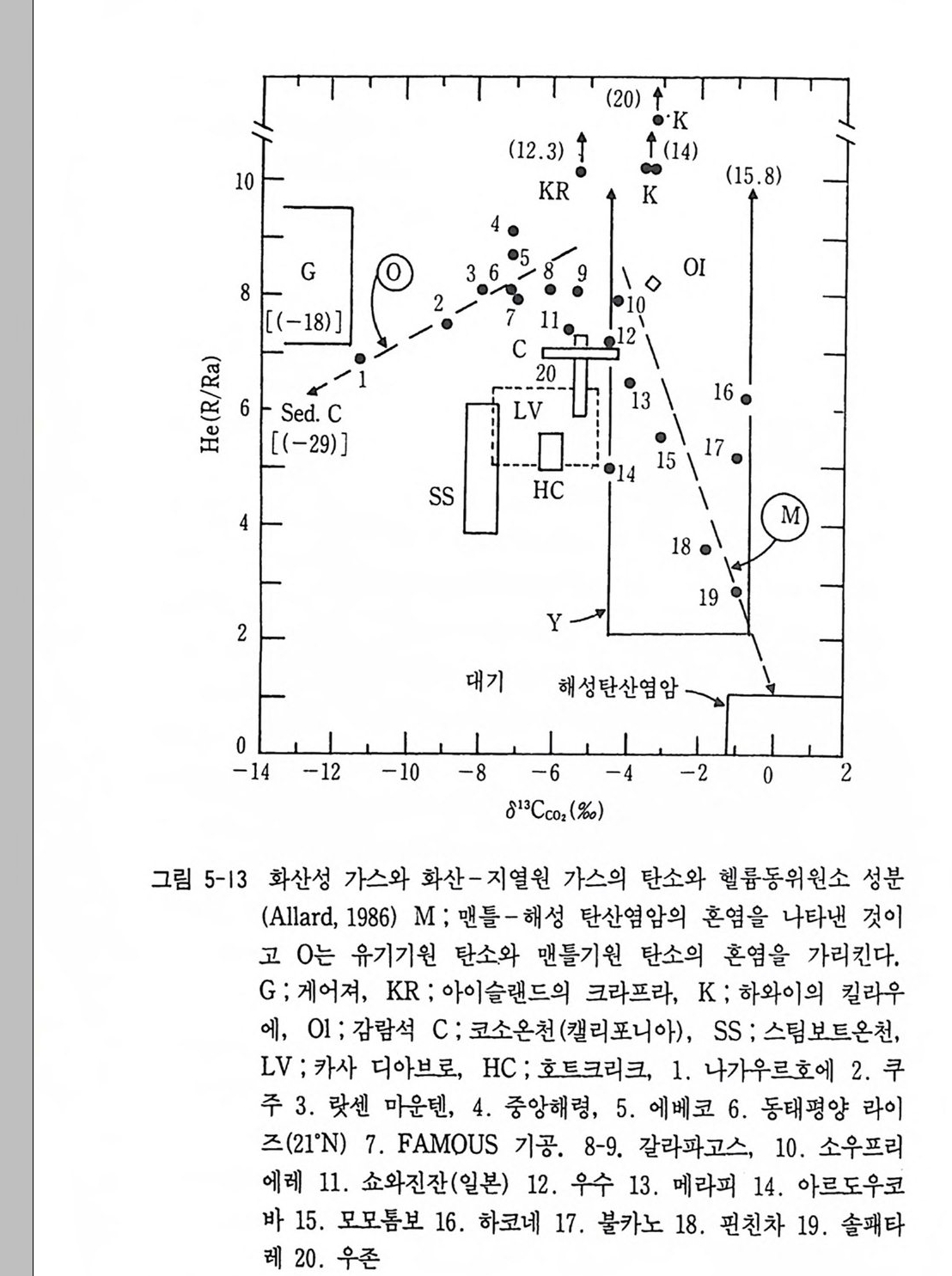 aH- 12140 4 G에(r A’, ; l 4l게a-0r1二de어Sr/1d82 , 져 사; H 1,감9 8람6-K6)1석 R0 M :C s 아; s ;맨- 이 코8틀니日 니니〔슬소 -0랜온1해천드3 -C성(6y의c해o 캘 ,~(성탄리~크)포탄산(. 21라二K-e 81〔CH 4니산염프 아염 라암),암의, -― 2 K혼、1 s염 ;s u하 을5;와 \0스 8 ‘’ ,이 나팀'• 의보 타 트l낸6온킬 1 천라것•,이우 \ `•
aH- 12140 4 G에(r A’, ; l 4l게a-0r1二de어Sr/1d82 , 져 사; H 1,감9 8람6-K6)1석 R0 M :C s 아; s ;맨- 이 코8틀니日 니니〔슬소 -0랜온1해천드3 -C성(6y의c해o 캘 ,~(성탄리~크)포탄산(. 21라二K-e 81〔CH 4니산염프 아염 라암),암의, -― 2 K혼、1 s염 ;s u하 을5;와 \0스 8 ‘’ ,이 나팀'• 의보 타 트l낸6온킬 1 천라것•,이우 \ `•
5-7 선캠브리아기의 탄소 선캠브리아기의 동위원소연구는 원시지구의 환경과 생명의 기원의 문제해결과 관련이 있어 대단히 홍미있다. 선캠브리아기의 연구는 주로 다음 분야에서 이루어지고 있다. O 청 록 해 조류와 박테 리 아와 같은 미 식물화석 발견 (Schop f, 1968) ® 생물기원물질의 분해산물로 추정되는 유기화합물의 복합체 추출 (Ord 등, 1965 ; Hoerin g, 1967) ® 현생되적물과 유사하게 12c 가 많은 환원성탄소연구 (Oehler et al, 1972) 등이다. McK i rd y와 Powell(1974) 는 오스트레일리아의 선캠브리아기_캠브 리아기 중부의 변성암의 변성도가 증가함에 따라 a13c 값이 커지는 관계를 H / C 비와 a1 3 c 관계에서 잘 설명하였다(그림 5-4). 이수아(I sua) 시기 (3. 8G a 전)에서 현재까지 지질시대별 탄산염암과 유기 기 원 탄소의 8 , 000 여 측정자료에서 청范값의 변화를 보면 앞에서 소개 한 그림 5 - 3 과 같다. 지난 800 Ma 동안 탄산염암의 3130 긱 값은 오도뷔스기에 최소 내 .8% 에서 페름기의 +2.0 %o까지 2.8% 정도로 뚜렷한 지질시대에 따른 동위원소 변화를 보이고 있다. 이 변화는 813Cor g와 석고와 같은 해성황산염이나 증발잔류암과도 밀접한 관련이 있다. 선캠브리아기의 경우는 자료 부족으로 변화 경 향을 잘 알 수 없으나 예상은 할 수 있다. 현저히 정의값을 나타내는 탄산염암은 폐쇄 또는 반폐쇄된 환경 때 문으로 해석되고 있다 (Loma gun d i effe c t, Sch idl owski 등, 1976). 부의 값을 나타내는 탄산염암은 생물원 CO2 의 기여를 의미하며 호 상 철광충 (Banded iro n fo rma ti on) 에서 잘 나타나고 있다 (Becker 와 Clay ton , 1972). 3.8Ga 의 이수아 탄산염암이 부로 전이된 현상은 변 성작용 때문이다.
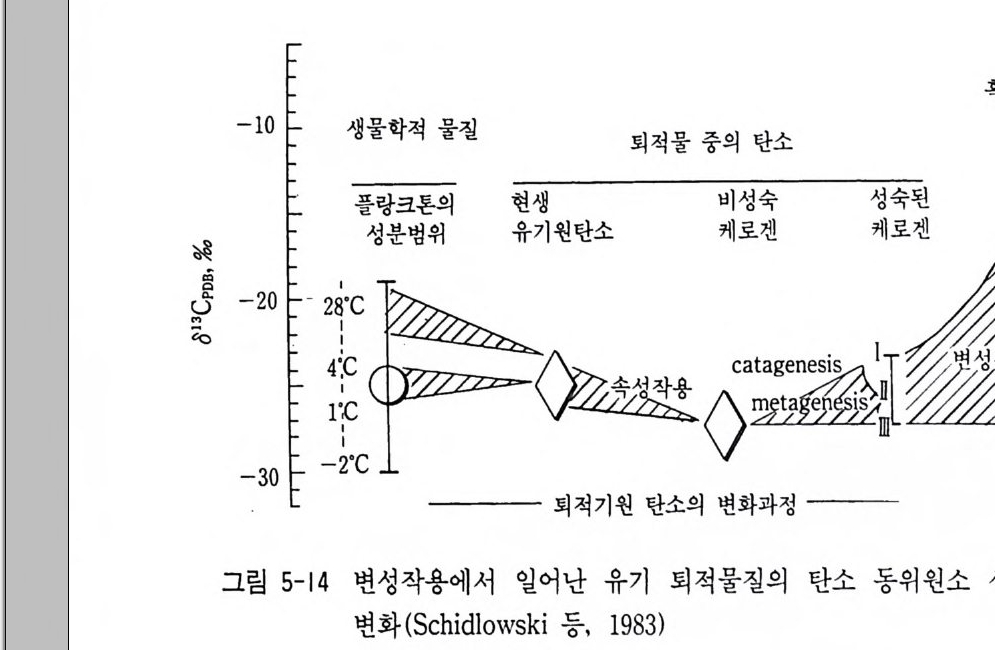 혹연`
혹연`
유기기원 탄소의 경우 동위원소값의 변화가 대단히 심하여 -10 ~ -50% 까지 변화하고 있다. 고생대 이후 지층의 유기물이 013c 은 -21 ~ -32%, 내의이다. 특히 무거운 동위원소를 갖는 케로겐은 흑연화작용의 여러 단계에 나타나며 H/C 가 0.1 인 심한 탈수산화반 웅의 특칭 이 나타난다 (그림 5-14) . 퇴적유기물의 속성작용과 변성작용과정에서 탄소 동위원소값은 점 점 무거워지고 있다(그림 5-14). 그런데 시생대 말의 케로겐 (2 .8 ~2 .5 Ga)-3 ~ -4%, 로 대단히 가벼운 값을 나타낸다. 이의 원인은 지금 까지 메탄으로밖에 설명하지 못하고 있다. 죽 다음 (1) (2) 식에서와 갇이 가벼운 동위원소를 갖는 메탄을 직접 이용하거나 (1) CH 一 ➔ fo rmaldehy de (H CHO) HCHO +ribu lose monop ho sph a te ---+ hexulose monop ho s- pha te
(2) CH4 一 form aldehyd e (HCHO) HCHO + gly c i n e --+ Serin e 또는 Cor g _-CH 4 _ 一 CO2_->Cor g과 같은 복합과정의 분별작용을 통하여 가능한 것으로 보고 있다. 13c 가 결핍된 co 라 CH 려 동위원소적으로 가벼운 세포를 만들어 가벼운 케로겐을 만들게 된다. 또 가벼운 메탄이 지층 중에서 확산에 의 하여 서 나 메 탄과 Pol ym e t han i za ti on 에 의 한 과정 도 생 각할 수 있 다. 이 처 럼 C o r g과 Ccarb 의 탄소 동위 원소값의 변화는 35 억 년 전부터 이미 지구상의 생물활동아 있었다는 증거가 된다. 5-8 우리나라의 탄산염암, 셰일, 무연탄 등의 탄소 동위원소 성분 우리나라의 탄산영암 및 석탄의 탄소 및 산소 동위원소비 분석연구 는(김규한 , 1980a, 198 0b , 198 5, 1986a,b, 1988 ; So 등, 1983 ; 박병권과 우 경식, 1986 ; 나기창 등, 198 8 ) 등에 의해 이루어쳤다. 고생대 대석회암 통의 석회암의 013C = -4.5 ~ + l. 3 %o( 평균 -1.1% .l. 0180= +8.8~ + 23 . 3 %o ( 평균 + 16 . 0 % )로 해성 석회암에 해당하였다. 그러나 경상퇴적분지의 의성지역 퇴적암 중의 석회암은 o13C= -6.3% o, 018 0= +11.7% 로 담수성 석회암에 해당되었다(그림 5-11). Ke it h 와 Weber (l96 4) 의 고생 대 의 해 성 석 회 암의 동위 원소값과 유 사하나 산소 동위원소비는 4~8% o 정도 180 이 결핍되어 있다. 이는 광역변성작용에 의하여 산소편이 현상이 일어난 것으로 보고 있다. 그러나 옥천변성대내의 일부 석회암(마전리층)과 덕산지역의 삼태 산층의 일부 석회암은 813C=+2.7 ~ +5.9 % o , 8180=+20.5 ~ +24.5 %o로 “C 부화가 異常的으로 나타나고 있다. 장군광상의 석회암과 탄산망간석의 탄소 및 산소 동위원소비는 각 각 813C=-2.6 ~ +0.1 %o(평균 -1.5% .), 8180=+10.9 ~ +21.9% o 과 813C=-4.2 ~ -6.3%( 평균 -5.3%.), 0180=-7.6 ~ ― 12 . 9%( 평
균 +10.7%.) 로서 탄산망간석을 침전시킨 탄소 및 산소가 모암과 동 일기원이 아님을 가르쳐 주었다. 우리나라의 석회암은 광역변성작용에 의하여 비변성석회암에 비하 여 813C=2.6% o 8180=6.2% o 정도 13C 과 180 동위원소 결핍현상이 나 타나고 있으며 접촉변성작용을 받은 지역은 탈탄산가스반응 등과 순 환수의 혼염에 의해 1sc 과 180 결핍현상이 현저히 나타나고 있다. So 등(1 983) 에 의하면 월악광산 지역의 접촉대에서 813C=11% o, 8180 = 15% o 동위 원소값의 차이 가 나타나고 있다. 박병권과 우경식(1 986) 에 의하여 풍촌 석회암충의 석회암이 지열에 의하여 동위원소값이 변화되었다고 가정할 때 속성작용시의 온도는 42.s·c~67. 4° C 이며 심도는 1. 4~2.2km 인 것으로 해석되었다. 우리나라 석탄의 탄소동위원소비는 -16.3 ~ -25.3%0 이었으며 혹
표 5-3 우리나라 석탄과 탄질셰일의 유기원탄소의 탄소동위원소비 (김규한, 1986) 1 경주-영탄일전( 포항) Lig nite 시료 J—l3 C25(% . 3o) 제지 질3 시기 대 2 충남(성주) Anth rac i te -22.8 중생대 43 경기(동두천) CCooaall ys hshaalele ,vith pla nt fos sil —-2233. .9 6 중중생생대대 56 문경(은성) CAonathl rsahca il tee -—2243. .48 중중생생대대 7 호남(화순) Coal shale -19.7 고생대 8 Anth rac it e -20.8 고생대 9 삼척(도계) Coaly shale -21. 9 고생대 10 Anth rac it e -21. 7 고생대 11 삼척(장성) Anth rac it e -23.1 고생대 12 Coal shale -23.9 고생대 13 정선(나전) Anth rac i te -21. 8 고생대 14 Anth rac it e -21. 2 고생대 15 영월(함백) Coal shale -23.1 고생대 16 Anth rac i te -23.6 고생대 17 영월(영월) Anth rac i te -23.5 고생대 18 7擇 Coal shale -19.7 고생대 (Ch ias to l it e bearin g ) 19 보은(진산) Coaly shale -16.3 고생대(?)
연화작용을 받은 석탄은 13c 이 부화되어 있었다(표 5-3). 그리고 옥 천변성대내의 함우라늄 탄질세일의 유기기원의 탄소는 o13C=-15.2 ~ -26.1%0 로 태백산 탄전지역의 고생대 탄질물의 동위원소값과 유 사하다. 흑연-방해석 동위원소 지질온도계를 이용하여 구한 창리층의 변성 퇴적암류의 변성온도는 384-433 ' C 로 녹색편암상에 해당되었으며 화강 암과의 접촉대에서는 508 ' C 가 얻어졌다(김규한, 1986 ; 나기창 등, 1988). 5-9 탄소의 순환 초기 지구의 대기권이나 수권은 분명히 산소가 없는 환경이었다. 죽 그 당시 지각에는 비산화형 유기물질이 바교적 풍부하였을 것이다. 그러나 언제 어떻게 일어나게 되었는지는 알 수 없으나 산소 광합 성작용이 선캠브리아기에 일어나기 시작했음이 고생물학 연구에서 나 타나고 있다. 유기지구화학 연구에서도 탄소의 생화학적 순환의 기록은 찾아내기 어려운 문제로 남아 있다. 그런데 유기퇴적물의 탄소동위원소값 (013C) 이 지금부터 28 억 년간에 크게 변화한 사실을 알 수 있다. 이 같은 사실은 선캠브리아기와 고생대 이후의 탄소 순환의 차이에 기인 하여 탄소 동위원소값의 변화와 산소 광합성작용의 기원 사이에 어떤 관련성이 존재할 것이라는 가정을 할 수 있게 되며 이런 가정하에서 탄소 동위원소 자료를 이용 탄소의 순환문제를 다루고자 한다. 즉 선캠브리아기의 유기되적물의 탄소 동위원소비의 변화는 탄소의 생화학적 순환과정 동안에 동위원소 분별 때문에 일어난 것이 아니겠 는가 하는 것이다. 대기-해양-퇴적물내에 저장된 산화 및 환원성 탄소는 6X1022g 정 도이 다 (Ju ng e 등, 1975) . 산화형탄소는 주로 석회암이나 돌로마이트와 같은 탄산염암으로 대
표되며 환원형 탄소는 케로겐, 생물원 및 유기탄소 복합체 등으로 대 표된다. 대기 _해양_퇴적물간의 탄소의 순환은 그립 5-15 과 같다. 그림에 서처럼 해양에서는 813C=O %i에 가까운 HCO; 가 지배적이며 생물권 의 탄소 (013C=-25%, )는 대기권의 C02(013C= - 7%, )와 해수 중의 HCO;(01 3 C=O%, )의 효소제어 반응속도론적 동위원소 효과에 의해 동 위원소값이 영향을 받는다.
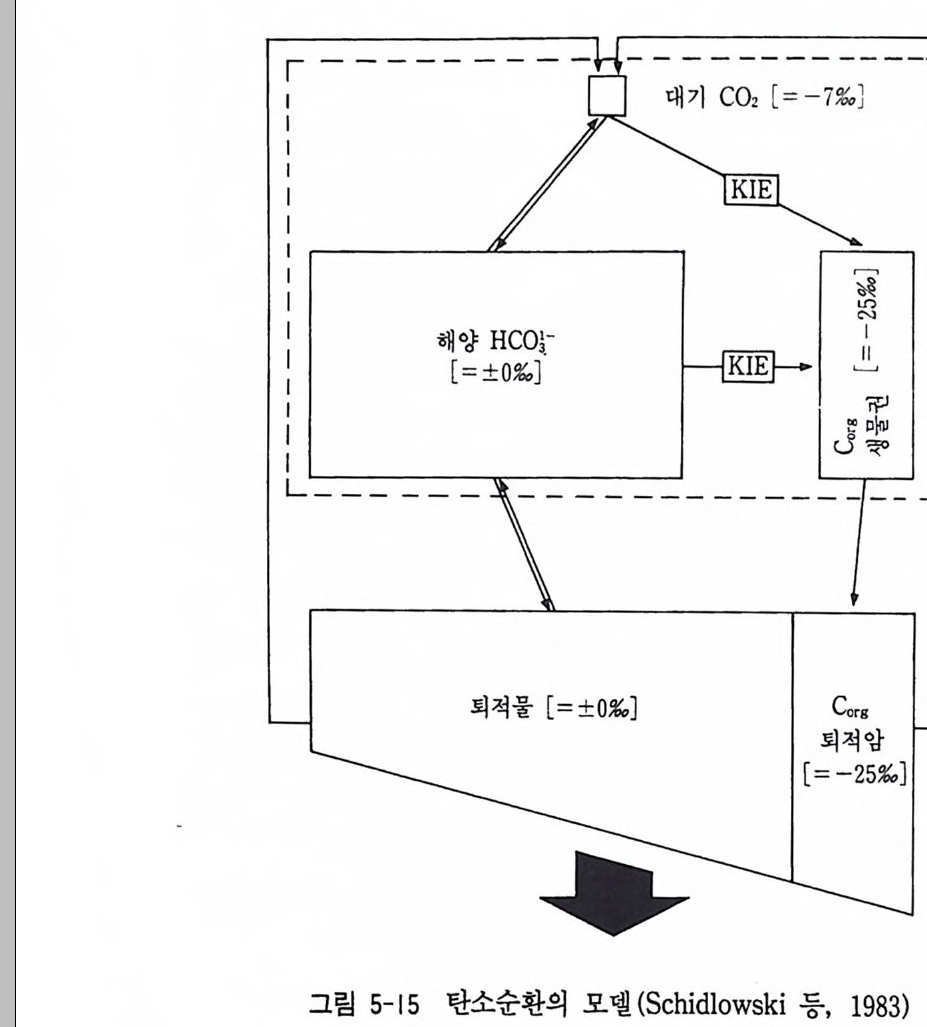 「 __一------g -----~- --~-- 7
「 __一------g -----~- --~-- 7
CO2-HCO i -co ~ 계내에서의 동위원소 분별은 평형분별이다. 주로 CO2 의 산화형의 탄소가 계에 유입되어 광합성과 같은 생물학 적 탄소고정 작용시에 동위원소 분별에 의해 무거운 동위원소와 가벼 운 동위원소가 선택적으로 유기물내에 축적이 된다. 12c 가 유기물질 에 우선 농집되므로 잔류 탄소에는 상대적으로 13c 가 농집된다. 탄소의 동위원소비가 _5%o 이고 무기원탄소와 유기원탄소 사이에 분별이 25%0 인 원래의 탄소 (Pr i ma ry carbon) 가 유입되었다고 가정한 다면 동위원소 값이 0 %o 에 가까운 해수의 HC03 의 o13c 값은 원래 유 입된 20 % 이 C o r g 으로 변한 것이 되어 Cor g / Ccarb~20 / 80 이 예상될 것 이다. 이 관계 를 동위원소 질량 평형 개념으로 생각하면 013 Cp r Jm = R o13C o r g + (1-R) 013 Cc arb 이 된다. 이때 R= C or g/ (C o rg+ C car b) =0.2 가 된다. 오늘날처럼 만약에 해양 HC03 저장소가 비교적 빠른 속도로 넘친 다면 위의 비와 같은 고정상태가 짧은 지질학적 시간내에서도 유지될 수 있을 것이다. HC03 가 co~- 로 침전될 때 동위원소 분별이 대단 히 적게 일어나기 때문에 계의 상태가 해양 HC03 에 의해 충분히 조 절될 수 있을 것이다. 탄소 동위원소비를 이용한 연구에 의하면 시생대 시기에 Calvi n c y cle 과 CO2 환원 메 탄 기 원의 박테 리 아와 수반된 탄소고정 작용과 같은 무기 영 양성 탄소고정 (Auto t r op h ic carbon fixa ti on ) 이 일어 났을 가능성이 있다. 선캠브리아의 호상철광충 연구에서 밝혀진 선캠브리아기의 고환경 처럼 탄소고정 과정 가운데 메탄이용 과정에서는 산소가 요구되므로 27~29 억 년 전에 산소 광합성작용이 일어났었을 가능성이 있다.
참고문헌 Allard, P. 0 983) , The orig in of hyd r og en , carbon, sulph u r, nit ro g en and rare gas es in volcanic exhalati on s: Evid e nce from iso to p e geo chemi str y , Chap ter 25 in : Foreca s ti ng volc anic events . H . Tazi e f f , a nd J.C S abroux- eds, Elsevi er , Amste r dam, pp. 337-3 8 6. Backer, R.H . , and RN. Clay ton (l97 2 ) , Carbon iso to p i c evid e nce for the orig in of a banded iro n-fo r mati on in W este r n Austr a lia . Geoch im . Cosm o ch im . Acta . 3 6, pp. 577-595. Belsky, T., a nd LR . Kap la n0970) , Lig h t hyd rocarbon gas es, C 13 , and orig in of orga n ic matt er in carbonaceous chondrite s . Geocl1i1 11 . Cosmocl1im . Acta . 3, pp. 257-278. Bott ing a , Y. ( 1 969a) , Carbon iso to p e frac ti on ati on betw een grap h ite , d ia m ond and carbon dio x id e . E arlh Planet . Sci . L e tte 13 . 5, pp. 301 -3 0 7. Bott ing a , Y. ( 1 969b) , Calculate d frac ti on ati on fac to r s for carbon and hyd r og en iso to p e exchange in the sys t e m calcit e- c a rbon dio x id e -g rap h ite , meth an e-hy dr og en -wate r vap or . Geo c l1im . Cos 11 zocl1i m. Acta . 33, pp. 49 -64. Craig , H. (1963) , The iso to p i c geo chemi str y of wate r and carbon in geo th e rmal areas. I n : Nuclea r Geology of Geotl ze rnzal Areas, pp. 17-5 3 . Spo leto , Sept . pp. 9-13, 1963. Craig , H., (1965) , The measurement of oxyg e n iso to p e s pal eote m p er atu r es. Proc. Spo l eto Con f. o n Sta b le Isoto p e s in Oceanog ra ph i c Stu d ie s and Paleote m p er atu re s, Ed. E. Tong ior gi , Vol. 3, pp. 3-24, Univ e rsity of Pis a . Dein e s, P., and D.P.Gold (1969) , The change in carbon and oxy ge n iso to p i c comp os it ion durin g conta c t meta m orp h is m of Trento n lim esto n e by the Mount Roy al plu to n . Geochim . Cos ,no chim . Acta . 33, pp. 421-4 24. Dein es , P., and D.P.G o ld0973) , The iso to p i c comp o siti on of carbonati te and kim berlit e carbonate s and the ir b eari ng on 塀 iso to p i c comp os it ion of deep- s eate d carbon. Geochim . Cosmochim . Ac ta. 3 7, pp. 1709-1733. Dein e s, P ., D. Lang muir, and R. S. H armon (19 74) , Sta b le carbon iso to p e rati os and the exis te n ce of a gas pha se in the evoluti on of carbonate grou nd wate r . Geochim . Cosmochim . Acta . 38, pp. 1147-1164. Dein e s, P. (19 80) , The iso to p i c comp os it ion of reduced orga n ic carbon. In P.
Fritz and J.C h . Fonte s , eds., Handbook of Envir o nmenta l Isoto p e Geo- chemi sh y, vol. IA, 329-406. Elsevie r , A mste r dam, p. 545. Eps t e i n , S., Buchsbaum, R., Lowensta m , H. A. and Urey, H.C., ( 1951) Carbonate - wate r iso to p i c tem p er atu r e scale. Bull. G eo!. Soc. Amer. 63, pp. 417-26. Erez, J., a nd Honjo , S. 0981) , Comp ar iso n of iso to p i c comp os it ion of pla n- kto n ic for ami ni fe r a in pla nkto n tow s, sedim ent tra ps and sedim e nts . Paleog eo g . Paleo clim at. P aleoe col. 33, pp. 129-56. Erez, J., and B. 0983) , Expe r im enta l pal eote m p er atu r e equ a ti on for pla n- kto n ic for ami nif e ra . Geochim . Cos, no c/z im . Acta . 47, 1025-31. Fried man, I., and J.R .O'Neil (l 977) , Comp ila ti on of s ta b le iso to p e frac ti on ati on fac to r s of geo chemi ca l int e r est. In M. Fleis c her, ed., Data of Geochemi stry, chap ter KK , U.S. Geo!. Surv. Prof. P ape r 440-KK, p. 12. and 49 figure s. Fritz , P . (1969) , The oxy ge n and carbon iso to p i c comp os it ion of carbonate s from the Pin e Poin t lead-zin c ore dep o sit s. Econ. Geo!. 64, pp. 733-742. Galim o v, E.M . , V .A . Kononova, and V.S. Prokhorov (1975) , Carbon iso to p i c comp os it ion in carbonati tes a·nd carbonati te like rocks (in connecti on wit h the source of carbonati te mate r ia l) . Geoclzemi stry Inte r natio n al, 11. pp. 503-510. Gearin g , J.N ., P.J. G earin g , D.T . Rud nick , A.G. Req ue jo , and M.J. Hutc h in s (1984) , Isoto p i c v aria b il it y of orga n ic carbon in a phy t op l a nkto n -based tem p er ate estu a ry. Geoclzim . Cos, no clzim . Acta . 48, pp. 1089-1098. Hath a way, J.C ., and E.T.D e g ~ ns (1969) , Meth a ne deri ve d marin e carbonate s of Pleis to c ene age . Scie n ce, 165, pp. 609-692. Hoe fs, J., and M. Schid lo wski (1967) , Carbon iso to p e comp os ti tion of car- bonaceous matt er from the Precambrian of t he Wi twa te r srand Sys t e m . Sci en ce, 155, pp. 1096-1097. Hoefs , J. (19 73) , Ein Beit rag zur Isotc ipe ng eo chemi e des Kohlensto f f s i n mag- mati sc hen Geste i n e n. Contr ib. Mi ne ral. Petro l. 41, pp. 277-300. Hoe fs, J. (1 980) , Sta b le iso top e geo chemi stry, second edit ion . Spr i n ge r-Verlag, New York, p. 208. Joh nson, S. J., Dansga a rd, W. , Clausen, H. B., Lang wa y, C. L. (1972) , Oxyg e n iso to p e pro fi les throu g h the Anta r cti ca and Greenland ice sheets .
Nahtr e (London) , 235, pp. 429-434. Jun g e, C ., M. Schid l owski, R. Eic h mann, and H. Pie t r e k (19 75) , Model calcula- tion s for the ter restr ia l carbon cy cl e : Carbon iso to p e ge ochemi st r y and evoluti on of ph ot os y n th e ti c oxy ge n. ]. Geop hy s . Re s. 80, pp. 4542-4552. Keith , M.L. , and J.N . Weber (19 64) , Isoto p ic comp o sit ion and envir o nmenta l classif ica ti on of selecte d lim esto n es and fos sils . Geoclzim . Cosmochim . Acta . 28, pp. 1787-1816. Kim , K.H . (19 86) , Orig in of mang an ese carbonate s in the Jan g gun mi ne , South Korea. J. K orean Inst. Mi ni n g Geo!. 1 9 (2) , pp. 109- 12 2 . Kim , K.H . and N. Nakai ( 19 80) , Carbon and oxy ge n iso to p e stu d ie s of the carbonate rocks from the Shin y em i zin c -lead ore dep o sit s, weste r n Taebaegs a n meta l log e n ic belt, K orea. ]. Ea,1/i Sci. Nag o y a Univ ., 28, pp. 57~74. Kim . K.H ., OJ .Kim , N. Nakai and H.].L e e (19 88 ) , Sta b le iso to p e stu d ie s of the Sangd ong Tung st e n ore dep o sit, South Korea. Mi ni n g Geo!. 38 (6) , pp. 473-487. McK ird y, D.M. , a nd T. G. Powell (1974) , Meta m orph ic alte r ati on of carbon iso to p i c comp o sit ion in ancie n t sedim enta r y orga nic matt er :N e w evi - dence from Austr al ia and South Af rica . Ge ol. 2, pp. 591~596. Morik i y o, Toshi ro (19 84) , Carbon iso to p ic stu d y on coexis t i ng calcit e and grap h i t e in the Ry o ke meta m orph ic rocks, north e rn Ki so ~ist r ic t , cen- tral Jap an . Contr b. Mi n Petr . v. 87, pp. 251-259. Nakai, N. (19 84) , Isoto p e stu d ie s, Rorie ed. in Lake Biw a Dr. W . Jun k Publish ers Dordrecht. Bosto n , Lancaste r . Oehler, D.Z.,J. W . Schop£ , and K. A. Kvenvolden 0972) Carbon iso to p ic stu d ie s of orga nic matt er in Precambria n rocks. Sc ien ce, 175, pp. 1246-1248. Ohmoto , H., (19 72) , Sy st e m ati cs of sulfu r and carbon iso to p es in hy d roth e rmal ore dep o sits . Econ. Geol. 6 7, pp. 551-578. Ohmoto , H., and Kerric k , D. (19 77) , Devolati lliza ti on equ i l ibr ia in grap hitic sys t e m s. Am. ]. Sci . 277, pp. 1013-1044. Ohmoto , H., and R.0 .R y e (19 79) , Isoto p es of sulfu r and carbon. In : H.L. Bain es , ed., Geochemi stry of hyd roth e rmal ore dep os its , second ed., 509-567. Joh n Wi le y, New York, p. 798.
Park, R ., and S. Eps t e in ( 1960) . Carbon iso to p e frac ti on ati on durin g pho to s yn t h - esis . Geocl1im . Cosmochim . Acta . 21. pp. 110-126. Pin e au, F., Jav oy, M. (1 983) , Ca rbon iso to p e s and concentr a ti on s in mid - ocean ridg e basalts . Earth Planet. S ci. L et t. 62, pp. 239-257. Pin e au, F., J av oy, M., Bott ing a , Y . (19 76) , 13C/ 12C rati os of rocks and inc lu- sio n s in pop p ing rocks of the Mi d-A t l an ti c Rid g e and the ir bearin g on the pro blem of iso t o p i c comp os it ion of deep- s ea te d carbon. Eart h Plane t. S ci. L ett. 29, pp. 413 -421. Rye , R .O ., and H. Ohmoto ( l97 4) , Su lfu r and carbon iso to p e s and ore gen esis . A Revie w . Econ. Geo/. 69, pp. 826-842. Rye , R. 0., Schuil in g , R. D., Rye , D. M., Jan sen, J. 8. H. (19 76) , Carbon, hyd r og en and oxyg e n iso to p e stu d ie s of the regi on al meta m orph ic comp le x at Naxos, Greece. Geo ch im . Cosmochim . Acta . 40, pp. 103 1- 1 0 49 . Sackett , W .M., and R.R . Thomp so n (1 96 3) , Isoto p i c o rga n ic c arbon comp os it ion of recent conti ne nta l deriv e d clastic sedim e nts of easte r n Gulf coast, Gulf of Mexic o . Bull. A mer. Ass. Pet ro l. Geo!. 47, pp. 525-531 . Schid lo wski, M ., J. M . Haye s , and LR. Kap la n (l983) , Isoto p i c inf e r ences of ancie n t bio c hemi str ie s :c arb on, sulfu r, hyd r og en , and nitr o g en . In : J.W . Schop f, ed., Eart h' s Earlies t Bio s p h er e:lts Ori gin and Evoluti on , 149-186. Schid lo wPskriin, cM et. o (n1 9 U8n4aiv) e, rsEitay r lPyr e astsm, Po srpinh ce ertico n o, x Ny. gJe. n levels : Constr ai n ts from Archaean pho to a uto t r o p hy . ]. Geo!. S oc. of London, 141 . Part 2, pp. 243-250. Schid lo wski, M. (1984b) , Orga n ic matt er in sedim e nta r y rocks: The· d ust we tre ad upo n was once aliv e . Terra Cog n ita , 4, pp. 45-49. Schop f, J.W . (19 68) , Mi cro fl or a of the Bit ter Spr i n g s Formati on , Late Precam- brian , Centr a l Austr a lia . ]. P aleo n to lo gy , 42, pp. 651-688. Schwarcz, H.P ( 1966) , Oxyg e n and carbon iso to p i c frac t ion ati on betw e en coexis ti n g meta m orph i c calcit e and dolomi te. J Geo!. 7 4, pp. 38-48. Schwarcz, H.P. (1969) , The sta b le iso to p e s of c arbon, In : K.H . Wedep oh l, ed., Handbook of Geochemi stry, vol Il/1 , Spr i ng e r -Verlag, New York. Shepp a rd, S.M.F.,and H.P.Schwarcz (1970) , Fracti on ati on of c arbon and oxyg e n iso to p e s and magn e siu m betw een coexis ti n g meta m orp h ic calcit e and dolomi te. Contr . M i ne ral. Petr o l. 2 6, pp. 161 -19 8.
Shie h , Y.N., and H.P . T a yl o r (1969) , Oxy ge n and carbon iso to p e stu d ie s of conta c t meta m orph is m of carbonate rocks. ]. Pe tr o l. 10, pp. 307-331. So. C. S., Ry e, D.M . an d Shelto n , K.L. 0983) , Carbon, hyd r og en , oxy ge n and sulf ur iso to p e and flui d inc lusio n stu d y of the Weolag tun g st e n - molyb d ermun dep o sit . Econ. Geol. 78, pp. 1551-1573. Shemesh,A., Y .K o lodny, and B. Luz (19 83) , Oxy ge n iso to p e varia t i on s in ph os- pha te of bio g e n ic apa ti tes , Il . Phosph orite rocks. Eart h Planet . S ci. Lette rs , 64, pp. 405-416. Valley, J.W ., O'Neil, J.R. (1981) , 13C/ 13 C exchange betw een calcit e a nd grap h it e: a po ssib l e the rmomete r in Grenv ille marbles. Geochim . Cosmochim . Acta . v. 45, pp. 411-419. Van Donk, J. (19 77) , 018 as a too l for mic r op al eonto l og ist s . In : Oce an ic Mi cro pa le onto lo gJ •, Ed. A.T . S. Ramsay, pp. 134 5 - 70 . Academi c Press, New York. Veiz e r, J., and J. Hoefs ( 1976) , The natu r e of 180 / 16 0 and C13 / C 12 secular tren ds in sedim enta r y carbonate rocks. Geoc /1im . Cos ,no clzim . Acta . 4 0, pp. 1387-1396. Wada, H., a nd K. Suzuki ( 19 83) , Carbon iso to p i c the rmometr y calib r ate d by dolomi te- calcit e solvus tem p er atu re s. Geoclzim . Cos, no chim . Acta . 47, pp. 697-706. Wendt, I. (19 68) , Fracti on ati on of carbon iso to p e s and its tem p er atu r e depe n dence in the sys t e m CO2-g as -CO2 in soluti on and HCO: i-C 02 in soluti on . Eart h Planet. Sci. L ett ers , 4, pp. 64-68. Whelan, T., .W. M. Sackett , and C.R. Benedic t ( 1973) , Enzym a ti c frac ti on ati on of carbon iso to p e s by pho sph oenop yruv ate carboxy la se from C, pla nts . Plant Ph ysiol. 51, pp. 1051-1054. 김규한(1 98 1). 「남한의 일부 석회암의 탄소 및 산소 동위원소비」, r 이화여대 한 국 생활과학연구원 논총 』 , pp. 133-142. 김규한 (1980), 「한국 태백산 지역에 분포하는 고생대 석회암의 탄소와 산소 동 위원소에 관한 연구」, {(광산지질)) 13( 1), pp. 21-27. 김규한(1 986). 「옥천 변성대내에 분포하는 우라늄광상의 동위원소 지구화학적 연구」, ((광산지질)), pp. 163-173. 나기창, 이동진, 김정택, 김규한 (1988), 「옥천층군의 변성 니질암내에 부존된 탄질물의 혹연화작용 및 안정동위원소에 관한 연구」, ((지질학회지)) 24,
pp. 199-212. 박병권, 우경식(1 986), 「중부캠브리아계 풍촌석회암충의 탄소 및 산소 동위원소 성분」 , (( 지질학회지 )) , 22(1), pp. 40-52.
6 황 동위원소 6-1 서언 황 동위원소 연구는 황의 순환, 지질시대를 통한 황 동위원소의 진 화 및 광상성인 해석을 위하여 지질학의 여러 분야에서 이루어지고 있다. 자연에 존재하는 물질 중의 황 동위원소비는 다음의 동위원소 분별 때문에 각기 다론 값의 범위를 가진다(그림 6-1 ) . 운석과 해양 현무암의 황 동위원소비는 대단히 유사하지만 화강암이나 변성암은
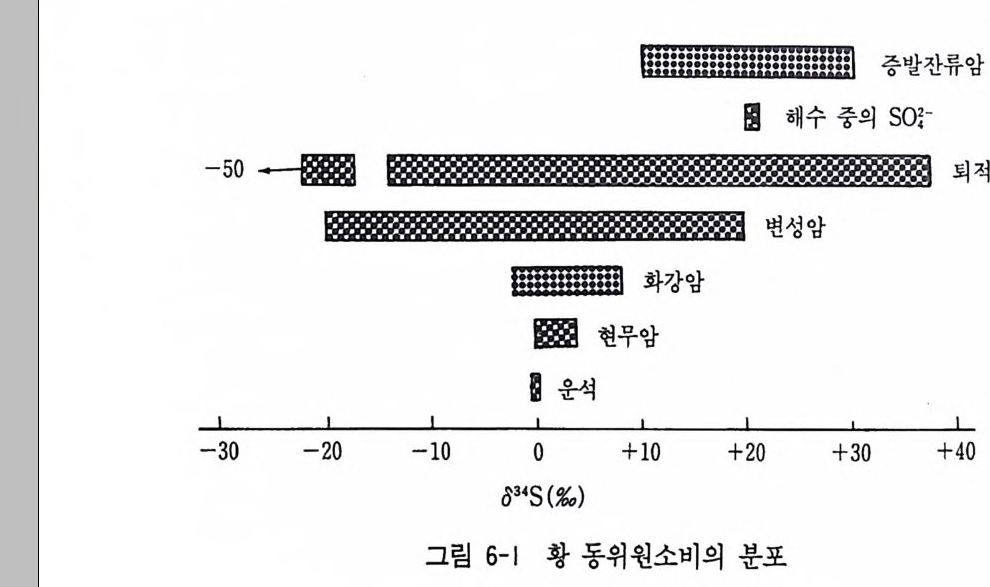 ::::;:::::;;ggg##iiii| 증발잔류암
::::;:::::;;ggg##iiii| 증발잔류암
o34s 값의 변화폭이 점점 커진다. 특히 퇴적암의 황은 생물학적 반응 속도론적 동위원소 분별 때문에 o34s 값이 +4 ~ -50% 까지 대단히 크게 변화하고 있다. 해수에 용존하고 있는 so~- 의 황 동위원소값 은 +20% o 내의로 일정하다. 석고와 무수석고와 같은 증발잔류암 중의 황산염의 황 동위원소비 는 과거 해수의 화석으로 취급될 수 있으며 지질시대 변화에 따른 지 구 전체의 산화환경 및 환원 등의 환경변동을 잘 반영하여 주고 있 다. 이들의 동위원소값의 차이는 시공간에서의 물질의 기원 및 생성조 건과 환경변동 해석에 대단히 유용하다. 황동위원소 변화에는 CD 反應速度論的 同位元素勅課와 ® 同位元素 交換反 應 울 들 수 있다. 앞장에서 언급한 것처럼 황산염광물 및 이온이 Desul fovi br i o 와 Desul fat omaculum 과 같은 황 환원박테리아에 의하여 가벼운 동위원 소가 많이 농집 된 H 2 S 를 만들게 된다. 황 환원박테리아는 아래 표 6-1 과 같이 비교적 환원환경에서만 안 정하다.
표 6-1 황산영 환원박테리아의 생존환경 (ZoBell, 1958) 요소 생존한계 EH + 350 ~ -500mv PH 4.2~10.4 온도 0~100°C 압력 1~1000 atm 영도
Goldhaber 와 Ka p lan(1974) 와 Schi dl owski( 1 983) 등에 의하면 황산 염이온은 아래와 같은 과정을 거쳐 H2S 로 된다.
SOJ -— ATI P APtS 一―I[l ― Fsooo~d- I-III H—2 s 여 기 서 ATP =A denosin e tri p h osph ate , APS = Adenosin e -5 -p h o- s p hosul fat e 이 다. 보통 실험실조건의 환경에서는 반응 Il 의 과정에서 s-o 결합이 파 괴되나 황산염이온 농도가 대단히 낮은 조건에서나 영양영류가 대단 히 많이 공존하는 환경에서는 반웅 I 의 과정으로 진행된다 (McCread y, 1975) . 그러나 자연환경에서는 반응속도가 대단히 느린 경우 황의 경신속 도 (Turnover ra t e) 가 아주 느리므로 반응 W 의 후퇴반응이 일어난다. 황산염에서 황화광물로 환원되는 자연의 특칭적인 두 가지의 환경 울 예를 들면 다음과 같다. (가) 흑해에서와 같이 개방계의 환경이며 정체되어 있는 물이 수직 적인 혼합이 별로 일어나지 않는 물은 환원성이 된다. 이런 환경은 H2S 가 대량 생산되어 독성이 되는 환경이 될 때까지 황산염 환원박테리아가 급속히 번식 성장하게 된다. 이때 H2S 의 S 는 “S 가 대단히 결핍되어 있어 여기서 침전된 황화광물의 황 동위원 소비는 적은 값을 가지게 된다. (나) 폐쇄계의 환경에서 황화광물의 침전이나 탈가스에 의해 계내 에서 H2S 가 계속적으로 제거되는 환경일 때 박테리아는 영양영류나 황산염이 다 없어질 때까지 황산염이온을 계속적으로 환원시킨다. 계 로부터 계속적으로 가벼운 황 동위원소의 축출이 일어나며 이때 레이 리 방정식과 같이 일어난다. 그 결과 황산염의 8“S 값은 황산염의 농도가 감소함에 따라 증가하게 되어 후기에 만들어진 H2S 도 역시 무거운 834S 값을 가지게 된다.
위와 같이 50°C 이하의 저온에서는 주로 박테리아의 활동에 의해 황 동위원소비의 값이 변화하나 250°C 이상의 열수환경에서는 4Fe+ 7H2S + So~- 一 4FeS2 + 4H20 + 6H+ 의 반응식에서처럼 Fe 와의 반응에서 황산영아온이 환원된다 (Ohmo t o 와 Ry e, 1 979) . 오늘날의 흑해, 발틱해, 캘리포니아 근해 등의 다양한 해저환경에 서 박테리아원 황산영의 환원과정을 거쳐서 형성된 동위원소 분별의 특칭은 ® 원래의 황산염의 동위원소값보다 부의 방향(가벼운)으로 동위원소 전이가 일어나고 ® 이들 동위원소값의 변화폭이 대단히 크 다는 점이다. 현생 퇴적분지에서 황 박테리아에 의한 환원으로 일어난 동위원소 분별 (그림 6-2 ) 과 페 름기 의 Ku pf ersch i e fe r 에 서 의 황 동위 원소값과 비 교해 보면 페름기의 황화광물 역시 넓은 o34s 값의 범위를 나타내어
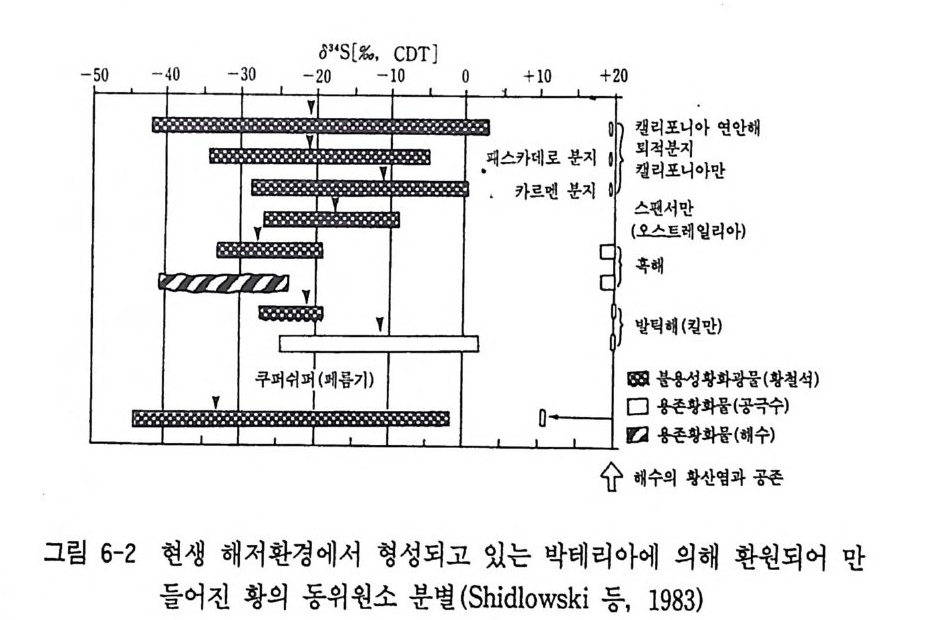 -5l 0 , -4I 0 I -3I 0 l -2l80 ' ‘S[l ., - 1C0 D T] +10 +20
-5l 0 , -4I 0 I -3I 0 l -2l80 ' ‘S[l ., - 1C0 D T] +10 +20
과거 퇴적분지에서도 생물기원의 동위원소 분별에 의한 황화광물의 경향을 잘 나타내 주고 있다. 6-2 광상의 황 동위원소 대부분의 금속광물은 황화광물로 산출되거나 황화광물과 밀접히 수 반된다. 광석에서든지 맥석에서든지 황화광물은 쉽게 발견할 수 있 다. 황동위원소비 (34s132s) 는 주로 광상형성의 fs2, T 등 물리 화학적 조건과 황의 궁극적 기원을 해석하여 광상의 성인해석을 하는 데 주 로 이용되어 왔다. 그래서 1960 년대 Jen sen(1957, 1967), Aul t와 Kulp (l 960), Gehlen (1965) 등은 운석이 o34S=o% 값을 가지며 화성기원의 황은 이 값과 유사하며 비교적 동위원소값의 범위가 좁으므로 주로 o 3 4S=O% 에 수 령된다고 보았다. 그러나 해수나 퇴적기원의 황산염에는 “S 가 많이 농집되어 지질시 대에 따라 다르지만 황 동위원소값이 +10 ~ + 30 %o까지 나타난다. 보통 되적기원 황화광물은 o34S=-70 ~ _70% 의 넓은 범위를 가지 며 “S 가 결핍되어 있음이 일반적이다(그림 6-1). 우리나라의 여 러 금속광상의 황화광물의 황 동위 원소비는 o34S= +2 ~+5 %o로 비교적 좁은 범위로 균질적안 동위원소 성분의 황을 가 지고 있다. 1960 년대에는 동위원소값의 범위로 황의 기원을 추정하였 다. 그러나 그 후 이론 및 실험적 연구 및 여러 유형의 광상의 동위 원소 연구에서 광물들이 황 동위원소비나 탄소 동위원소비의 값만으 로 단순하게 기원을 해석해서는 되지 않음을 알게 되었다. 앞장의 탄소의 경우처럼 황동위원소값은 열수계에서는 T, PH, fs2, I 등에 의해 크게 변화하게 된다. 이 문제에 대하여서는 후에 자세히 설명하겠다.
그러나 기타 자세한 지질학적 지구화학적 연구와 동위원소 분석자 료를 함께 종합검토하면 ® 광화작용의 온도 ® 광상형성시의 화학적 조건과 형성기구 해석 ® 광화 용액 중의 황의 기원 해석에 크게 도 움이 되어 이런 분야의 연구가 많이 이루어지고 있다. 6-3 황 동위원소 지질온도계 동위원소 지질온도계에 대하여는 앞에서 언급하였으므로 여기서는 황 동위원소를 이용한 지질온도계에 대하여 간단히 설명하겠다. 광석 중의 ZnS 나 PbS, 광화용액 중의 H2S 와 so~- 에서와 갇이 황 함유화합물 사이에 동위원소 평형이 이루어졌다면 이들 사이에는 Zn32S + Pb34S =Z n34S + Pb32S H34 S + 32SO!-= H 꾼 S + “S0:- 등의 관계가 얻어진다. 瞬 _.H 쵸 ((3“4SS//33 22SS) ) sHo2.S- = K 6.so i -- H 2s = 034Sso.-- o 34S 腦 =lOOO(a-1){1+~ 『} ::::,,:lOOO(a— 1 ) ::::,,:1000 Ina 평형상수 In K=- 6. G 0/ RT 이므로 a= f (T) 이다. 여러 종류의 황 화합물간의 평형분별정수 (a) 는 온도에 따라 변화 하기 때문에 지질온도계로 이용되고 있다. 평형조건하에서 황 화합물 사이에는 결합력과 질량차에 따른 동위원소 효과가 나타난다. 즉 결 합력이 강한 화합물일수록 무거운 동위원소가 농집된다.
질량이 작고 이온 포텐셜이 큰 화합물일수록 결합력이 강하다. 그리고 ZnS 와 PbS 사이에도 질량효과 때문에 평형상태에서는 언 제나 ZnS 에 PbS 보다 더 무거운 원소가 농집되는 경향이 있다. 따라
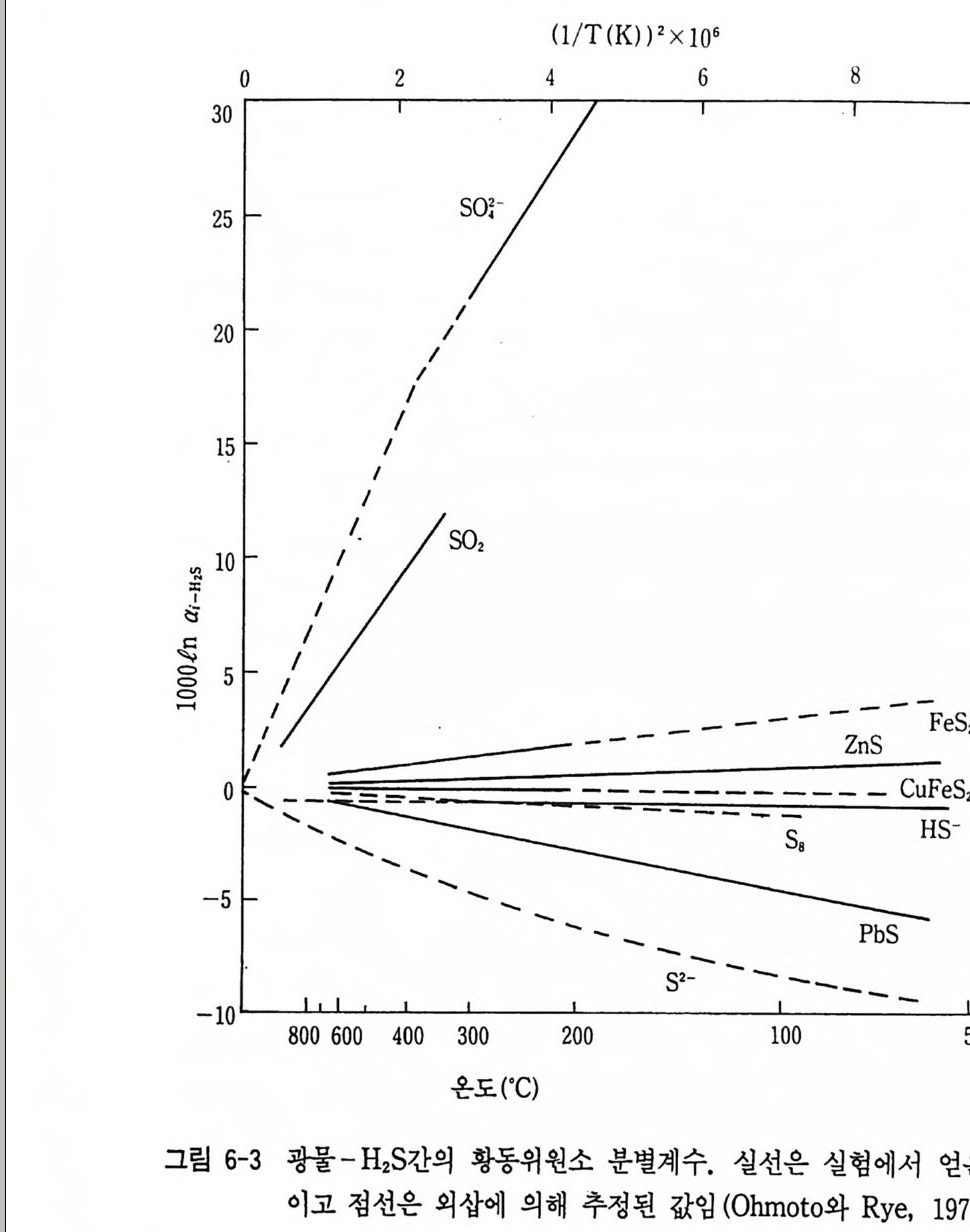 3。 o 2 4(1 / T (K))2X l 066 8 I(I
3。 o 2 4(1 / T (K))2X l 066 8 I(I
서 황철석 > 섬아연석 > 황동석 > 방연석 순으로 o3 ◄ s 값이 감소한다. 가 스나 용존 황종 사이에는 so~-> so ~-> S 02>sco>s-H2S-HS-> 훈 순으로 “S 가 농집된다. 여러 황화광물간의 동위원소 분별정수가 실험 및 이론적으로 연구 되어 있다(그림 6-3), 광상학에서 많이 이용되는 황동위원소 지질온도계는 표 6-2 와 같다. 지질온도계에 이용되는 광물시료는 (1) 공존하는 분석시료의 광물상간에는 동위원소 평형이 이루어져 있어야 하고 (2) 광물이 형성된 후에 광물상간에는 어떤 동위원소 교환도 일어나
표 6-2 황 동위 원소 지 질온도계 (Ohmo t o 와 Rye, 1979) 광물쌍 (Mi ne ral Pair ) 지(T질'K온) 도계의 식 (o3'SA-o3'Se) 오차 황산영광물-황동석 T 2.8 5 X l03 ( T > 4 。。 °C) ±25 ±5 (Sulfa tes -chalcop yrite) 스土 1)1 / 2 T ( L::,2 - . 630 土 X 0l 0. 53) 11 2 ( T < 35 。 .C) 土 10 土 5 황(S산ulf염a t광es물 -p- yr황ite철) 석 T= 2(t.:7, 6± X l)l0 13,2 ( T> 4 00'C) ±25 ±5 T (62- .616 士 X 0l .053) 1 12 ( T < 35 。 .C) 土 10 ±5 황(P철y r석i te --g 방a l 연en석a) T l.Ol +(0b ..) 0 411)2 X l03 土 25 士 20 섭(S 아p h연a l석er i(te 자 ( p류y철rr석h o )t -i t e방) 연석 T (0 . 85+(t0::, .) 0 13/2) X l03 土 20 土 25 -ga lena) 황(P철y r석ite--c 황 h a동lc석op yrite) T (0 . 67 土 601 ./ 024 ) X l03 土 35 士 40 황(섬철아석연-석자) 류(P철y r석it e- T (0 . 55+60. .1 0/2 4 ) Xl 03 士 40 土 55 pyrrh oti te (sph a lerite ) )
지 않아야 하며 (3) 실험시료가 순수한 성분의 광물상 시료를 이용하였으므로 분석 용으로 분리된 시료도 순수한 광물상이라야 한다. 그리고 유체포유물에 의한 방법이든지 기타 지질온도계와 비교하면 동위원소 평형 또는 비평형 해석에도 더욱 도움이 될 것이다. 6-4 광화용액 중의 황 동위원소비의 변화 열수광상에서의 황은 보통 황화광물이나 황산염광물로 존재하며, 이들 황은 주로 ® 화성기원이거나 ® 해수기원(퇴적암 기원) 등으로 대표된다. 화성기원 황은 직접 마그마용액에서 유래한 것이거나 화성암 중 황 을 포함한 광물에서 유래된 것이다. 해수기원의 황은 주로 so~- 형 태로나 황환원 박테리아에 의해 so~- ― -.H2S 된 후 황화광물로 침 전, 퇴적암지층에 존재하는 것이다. 따라서 동위원소 분별은 광화용액이 어떤 지질학적 과정을 거치느 냐에 따라 다르게 일어난다. 예를 들면 동위원소 분별은 ® 마그마에 서 광화용액으로 분리되는 동안이나 황화광물로 여과되는 동안에 일 어나기도 하며 ® 해수기원의 황산염광물의 환원과 같은 열수용액이 진화되는 과정에서 일어난다. 그리고 ® 열수용액이 냉각되는 과정이 나 광물의 침전 또는교대되는 과정 중에 동위원소 분별이 일어날 수 있 다. 이들 과정중에 동위원소적으로 평형에 이를 수도 있고 비평형상태 에 있울 수도 있으며 이들이 폐쇄계에서 일어날 수도 있으며 개방계 내에서 일어날 수도 있다. 따라서 열수광물 중의 o3'S 값은 열수용액의 지화학적 변화에 따라 달라진다. 그러므로 우리는 황 동위원소값을 지화학적으로 해석할 때 에는 그 광상의 지질이 대단히 중요함을 알게 된다.
6-5 열수계에서의 황 동위원소 열수용액 중에는 H2S, HS- , S2- , SO~-. HSO;., KSO;., NaSO;. 등과 같은 여러 종류의 유황종이 존재한다. 그러므로 광화용액 중의 황의 기원 해석을 위해서는 전황의 황 동 위원소비 (o34S i: s) 를 계산해야 된다. 앞의 탄소 동위원소에서와 같이 Ohmoto ( l97 2, 1974) 에 의 하여 o34S 값은 PH, T, fo2 , I 등 여 러 조건 에 의해 변화된다는 것이 밝혀졌다. 광화용액 중의 황동위원소는 여러 유황종의 동위원소의 합 (834S :i: s) 으로서 034S2: s = (034S H , S. XH, s) + (034SHs-.XHs-) + (o34Ss,-·Xs2-) + (o34& oi-'X soi- + (034S H s oi 'X Hs o.) + (o34SKsoi ' XKso.) + (o34SNaso i •X .시 aso.) 와 같이 표현된다. 여기서 Xi =1 ni/ m m~H2s + SmHs-+ =ms2- + ~mso~-+ mHso, + mKso, + mNaso1 이다. m 은 몰분율이다. 8“SH2s 값을 표준으로 잡으면 임 의의 i 종의 황 동위원소의 성분은 o34Si = 034SH2S+ 석 가 된다. 여 기 서 6i 는 i 종의 황화광물과 황화수 소간의 상대적인 동위원소 부화항이다. 위의 두 식 관계에서 o34Si = 034S I:S + 스 i_ [(I: :, Hs-·XHs-) + (t:, s2-•Xs 2-) + (6 soa-·Xsoa-) + (6Hso 건 .XHso i) + (6Ksoi• XKsoi) + (6Naso,•XNasoi) ]
가 얻어전다. 위의 S34S i를 계산하기 위해서는 다음과 같은 반응식에서 각 황화 광물 종의 몰분율을 계산해야 한다. H2S(a9i = H+ + HS- HS-=H++s2- 2H+ + SO!-= H2S(aq> + 202 HSO:. = H+ + SO!- KSO:. = K+ + SO!- NaSO:.=Na++SO!- 계산된 각각의 몰분율은 Xtt 2 s=l /C XHsCa-tt+ = Y~tts - Xs2-= KH2s •K HS_ • YH2S C (aH+ ) 2 Ys2 - Xso8-= C· 臨(f ao-2· )( a2H• Y+H)22S. Ysoa- X 函 C· 臨i (-f·oK2 )函 2' Y•Ha2HS •• YHsoI 도= (fo2 ) 2·mK++ YK+%s C· 臨 a-·KKSO t· (aH+) 2. YKso3 XNaSO, C• Ks(ofoi- 2) K 2fNfai N 책a • •• Y(aNaH• + •) Y2H• 2 YSN a 책 총 황의 양에 대한 용존황종의 몰분율 C 는 C=l+(는 )(1+ 는)+(白這:v)
(_YsoLa-+ K 函a.H +Y HSO, + Km 函K+ • 忘rK+ + 도mN·8+ • YYNNaas+o , ) 가된다. 따라서 Xi= f(T, fo2 , PH, I )이며 834Si= f(83 4Srs, T, fo2 , PH, I) 이다. 여기서 834S 1: s( 전황의 황동위원소값), T( 온도), fo 2( 산소 퓨가시티), I( 이온 강도, mK ♦ +mNa 令)를 말한다. 따라서 열수광화용액의 온도와 I 를 알고 834S 1: s 의 값을 가정 하면 Fe-S-0 계 에서 황화광물의 황 동위원소값의 변화와 산소 퓨가시티 (fo2 ), 그리고 PH 사이의 관계를 도시할 수 있어 광상형성의 물리화 학적 조건을 해석할 수 있게 된다. 예를 들면 250°C , I=1.0, 83'Srs=0%,,, S=0.l m ole/Kg 조건에서 Fe-Ba-02-S 계에서 황철석과 중정석, 황 동위원소비와 PH, fo2 사이 의 관계를 여라황종간에 얻어진 평형상수(표 6-3) 와 활동도 계수(표 6-4) 를 이 용하여 그리 면 그림 6-4 와 같다. Ohmo t o (1 972) 가 정량적으로 그린 ·이 그림에서 보면 834S=O%,, 의 광화용액에서 침전된 황철석은 fo 2 나 PH 의 조건에 따라 83'S 값이 +5 에서 -27%,, 까지 변화할 수가 있다. 죽 83•s 값은 PH 와 산소 퓨가 시티에 크게 영향을 받음을 알 수 있다. 특히 Ohmo t o 의 공헌은 광석 및 맥석 중에 공존하는 황화광물과 탄산염 광물의 동위원소바를 동시 예 검토하여 광화작용시의 fo 2 와 PH 동의 광화환경을 해석한 점이다. 그림 6-4 는 83'S i와 813C i는 등치선, Fe-S-0 광물의 안정도, 방해 석 -흑운모-백운모 (se ri c it e) 의 안정도와 fo2 -PH 관계를 복합해서 그린 것이다. 이 그립은 공존하는 탄산염광물과 황화광물의 동위원소 비의 변화와 산화상태를 찰 나타내 주고 있다. 여기저 PH 범위는 · 아래와 같은 고령토-백운모, 백운모-칼리장
표 6-3 황을 함유한 반.웅 계의 평형상수 (Ohmo t o, 1972) log K 반응식 150'C 200'C 250°C 300'C 350'C H2S (aq) :;::=H+ + HS- -6.7 2 -6.96 -7.3 5 -8.0 6 -9.0 a Hs-~H++s2- -10.6 2 一 9.57 -8.6 1 -7 .7 2 -6.9 a 2H ++ SO t :;: :::::=:H2S(aq ) +202 -79.3 1 -67.1 3 -57.1 0 -48.5 5 -4 1. 0 a HSOr=H+ + SO t -3.7 4 -4.4 9 -5 .4 1 -7 .0 6 -9.2 a KSO.~K+ + s o~- -1.60 —1.9 4 -2.4 -3.0 -4 .0 b H2S (aq) +伊습 H20 U) +½s2 20. 00 17. 53 15. 30 13. 60 12. 5 a FeS 는 FeS+ 강 S2 1-10.2 5 -8.48 -7.0 3 -5 .8 1 -4 . 7 9 a 3FeS2 + 202~ Fe304+ 3S2 40. 95 38.11 35. 81 33. 93 32. 36 a 2FeS 곱和근 Fe2 0 2 + 2S2 34.66 31. 72 29. 35 28.19 25.60 a 3FeS+20든 FelO ◄ +終 71. 76 63. 56 56. 91 51. 39 46 . 74 a 2Fe30. +t1D2·= =3Fe203 22.07 18.95 16. 44 14. 35 12 . 08 a BaS04~Baa + soi- -9.3 4 —9 .7 6 -10.3 4 -11.05 -11. 9 a 3KAISiJ O s+2H +:;== KAbSiJ 0 10 9.2 8.6 8.2 (OH )2 +6SiO a +2K+ (8.91) (8.49) (8. 12 ) (7 . 82) (7. 6) 2KA13Si3 01 o (OH) 2+2H + +3H20 (I) 7.9 6 7.04 6.2 0 5.4 4 4.9 ~3Al2Si2 0 (0Hl • + 2K+ a 는 3so · c 에서 의삽법으로 계산된 값이며 b 는 2oo · c 에서 의삽법으로 계산된 값임 . Helge s on (l96 9) .
석의 반응식에서 계산된 안정영역이다. 이때 온도에 따라 계산된 평 형상수값은 표 6 - 3 과 같다. 3KA1Si3 0 8 + 2H+ =K A1S i 3 어 (OH) 2+ 6Si0 2 + 2K+ 2KAlaSia 0 1o (OH) 2+ 2H+ + 3H20 U) =3 A1Si2 0 s (OH) 4+ zK+ 공존하는 탄산염광물과 황화광물의 B34S i와 a13C i의 값이 둘 다 변
표 6-4 용존화학종의 활동도계 수 (Ohmoto , 1972) log yi 용(S존p e이c i e온s )종 150'C 250'C 350'C l=l !=3 I = I I = 3 /=l 1=3 H2C02( ap ) , H2S, CH ◄ +0.0 8 +0 .2 3 +0.1 3 +0.27 +0.3 5 +0.5 8 K+. CJ- -0 .2 6 -0.2 1 -0.3 3 -0.3 1 -0.52 -0.49 OH- , HS- -0.2 3 -0.1 8 -0.3 0 -0.2 5 -0.4 5 -0.3 8 Na+, HC03, HSO, , -0.2 1 -0.1 3 -0.2 6 -0.20 -0.3 8 一 0 . 29 KSO, , NaSO, soi- _l .0 9 _l.2 0 -1. 44 -1. 62 -2.58 一 2.89 COJ - -1.01 -1.08 -1.33 -1.46 -2 .37 -2 .59 S2- , Bal+ -0.9 4 -0.9 9 -1.24 -1.33 -2.18 -2.34 Ca2+ -0 .83 -0.8 4 -1.08 -1.12 -1.88 -1.95 H+ -0.0 1 +0 .0 3 -0.0 9 +0.0 3 -0.0 6 +0.1 3 * Helge s on0967 , 1969) 와 Garrels and Chr i s t(1 965) 의 자료에 의해 계산된 값임.
화폭이 적거나 o3 4 S i는 변화폭이 크고 013Ci 값 이 균일할 때는 비교 적 높은 산화상태를 의미하고, o34S i은 균일하고 o13C i는 변화폭이 클 때는 비교적 낮은 산화상태를 나타낸다. 우리나라 신예미 연아연동광상의 동위원소 분석연구에서 서항광체 는 전자의 조건, 동항광체는 후자의 조건을 나타내어 서항광체의 광 화환경은 동항에 비해 높은 산화상태로 해석되었다(Ki m 과 Nakai, 1980) . 그림 6-4 에서 마그마멜트 (T=250 ' C, fo2 =10-37, PH=3) 를 가정하여 마그마원 광화용액이 세 가지 서로 다론 지질학적 조건으로 이동할 경우 o3•s 와 o13c 의 동위원소비의 값의 변화 패턴이 다르게 나타난 다. 만일 마그마원 광화용액이 A 쪽으로 PH 가 중성화되어 가는 과정에 서 침전된 경우는 화강암과 석회암이 접촉해 중성화되는 지질학적 현
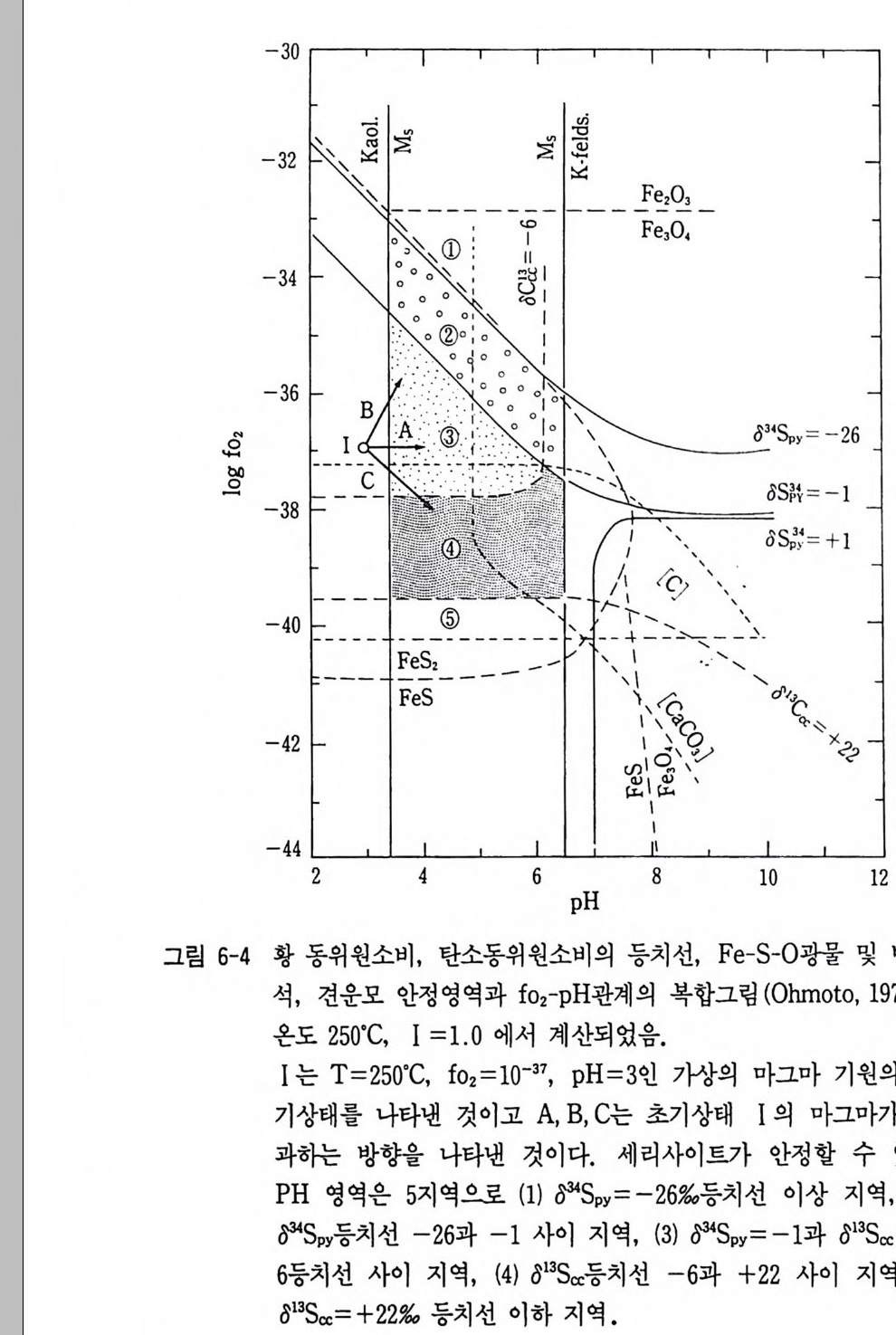 -30
-30
상으로 해석할 수 있다. 이때 광화작용 초기와 후기에 걸쳐 광화용액 에서 침전된 황화광물의 동위원소바는 황 동위원비, 834S 1: s( 균질)와 탄산염광물의 탄소 동위원소비, 813C 1: c( 균질)로 나타난다. 프로비덴 시 아 광상 (Sawkin s , 1964) 이 대 표적 인 예 이 다. B 경로는 A 와 같은 조건에서 fo 2 가 증가하는 경향으로 광화가 일어 났다고 보면 마그마원 광화용액이 적철석이나 자철석을 많이 함유하 는 모암과 반응하거나 산화된 순환수와 혼합되는 환경에서 침전된 것 으로 해석할 수 있다. 이때 탄산염광물은 813C 1: c( 균질)이고 834S 값은 후기로 갈수록 감소하게 된다. C 경로는 A 와 같은 조건에서 fo 2 가 감소하는 환경으로 마그마멜트 가 유색광물을 많이 함유하는 모암이었거나 모암이 유기원탄소나 혹 연을 많이 함유하는 경우이다. 탄산염광물의 o13c 값은 후기로 갈수록 값이 증가하게 된다. 일본의 구로꼬광상 유형의 하나인 사까나이(釋迎內) 제일광상에서 황화광물의 황 동위원소는 주로 +2 ~ +8 %o이며 광체의 하부에서 상부로 감에 따라 동위원소값이 가벼워지며 철_석영대의 황철석 은 -6 %o에 이 른다. 이 광상에 대 하여 온도 250°C, o34St s = + 20% o, ~S=O.OlM 에서 황철석의 동위원소비의 변화를 fo2 -PH 그림으로 도 시하고, PbS04, PbS, 고령토, 백운모, 칼리장석의 안정영역을 도시 한 것이 그림 6-5 이다. 834S 1: s 값을 +20 %o로 가정해서 작성된 fo2 -PH 그림에서 사까나 이 제일광상의 황철석이 초기에서 후기로 · 감에 따라 황동위원소값이 감소하는 경향과 그때의 각각의 동위원소값이 위 그립에서 +8, +3, -6 %o의 등치선의 변화경향과 찰 일치한다. 그러나 · 만일 전황의 동위 원소값을 마그마원으로 해석되는 o3•S=O %o로 가정하여 등치선을 그리면 각각 一 12, -17, -26% 이 되어 실측된 분석자료와 크게 차 이가난다. 따라서 구로꼬의 전황의 동위원소값 (8“S 리울 +20 %o로 가정함이
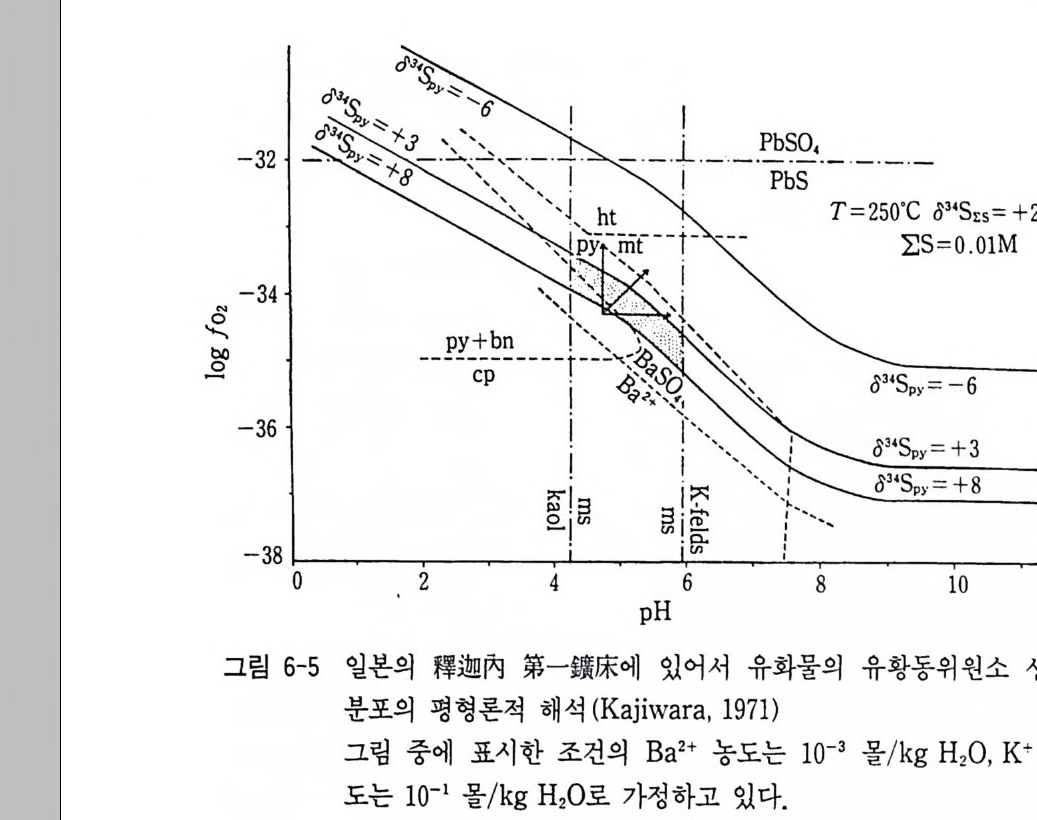 少춥
少춥
이상적임을 알 수 있다. 죽 이는 광화용액 중의 황의 기원이 해수에 유래하였다는 해석이 더욱 유력해진다. 열수광상의 황 동위원소값을 이와 같은 상평형론의 관점에서 설명하는 것이 가능한 것이 많지 않 으며 또 비평형 요소를 고려해야 설명되는 경우도 있다. 특히 2oo·c 이하의 저온형 광상이나 고온이라 하더라도 비교적 천 부에 짧은 시간에 침전된 광상의 경우에 그런 예가 많다. 6-6 멜트-유체간의 동위원소 평형 고온에서 멜트-유체간의 황종의 동위원소 평 형 (Melt-f l u id equ i li - bri a) 에 대해서 알아보자.
고온 (T > 400'C) 열수광화용액 중 용존하는 중요한 황종은 H2S 와 so 려다. 기타 여러 황종에 대한 열역학적 자료 검토에서 SO, S03, S2, Ss, Sa, SCO, H2SO ◄, H2S03 등과 같은 기타 황종은 이 같은 고온 조건에서는 H2S 와 S02 에 비해 거의 무시될 정도로 적다. 따라 서 열수용액의 황 동위원소값 (o34S 유 세 )은 간략하게 s34s 유세 = 034Stt ,s • Xtt ,s + 034Sso, •X so, = 034Stt ,s + !:::.so, (R/1 +R) (1) 로 생각할 수 있다. 여기서 XH2s(mH2s / mH2s+Il1so2) 는 용액내의 전황에 대한 H2S 의 몰 분율이다. 그리고 R 은 SO i/ H2S 의 몰비이고 스 so2 는 o34Sso,-o34SH,s 로 H2S 와 S02 와의 평형부화정수 (E q u ili b ri um enrich ment fa c t or) 이다. 유체와 멜트 중의 황 사이에 동위원소 평형이 얻어지고 멜트내에서 는 HS- 만 존재하는 경우 위의 식은 다음과 같이 된다. o34S 유 계 = o34S 멜 트 _ D..H s-+ 6so, (R/1 + R) (2) 여기서 6. Hs- 는 HS- 와 H2S 간의 평형부화정수이다. so 파 환원황종 사이에는 동위원소의 분별정수가 대단히 크기 때 문에 마그마 온도일지라도 위 식 (2) 의 마그마질 유체의 J 34S 값은 규 산염 마그마와는 전혀 다를 숙가 있으며, B34S 값은 유체내의 S02/H2S 의 비, 온도 그리고 유체의 분리지 마그마와 유체내의 질량비 등에 따라 변화한다. 고온에서 유체가 이상기체의 복합물과 유사하게 행동한다고 가정하 면, S02/H i S 의 몰비 R 은 T, P (전 유체 압력 ) , fo 2 의 함수로 다음과 같이 계산할 수 있다.
R= 쁘mH2드s ~XH2=s [[ffHso2 sJ / pp rr( (Y YsHo22s)) ]] Pr K' .r HY2H02' sX (Hf。2 20 )' 요2r s o2 (3) X i는 복합물 중 i종의 몰분율, YH20 는 Pr 와 T 조건하에 서 순수한 계내의 i종의 퓨가시티 계수이고 K 는 다음 반응식의 평형상수이다. H2s(g) +3 /2 02(g) =H 20(g) + so2(g) (4)
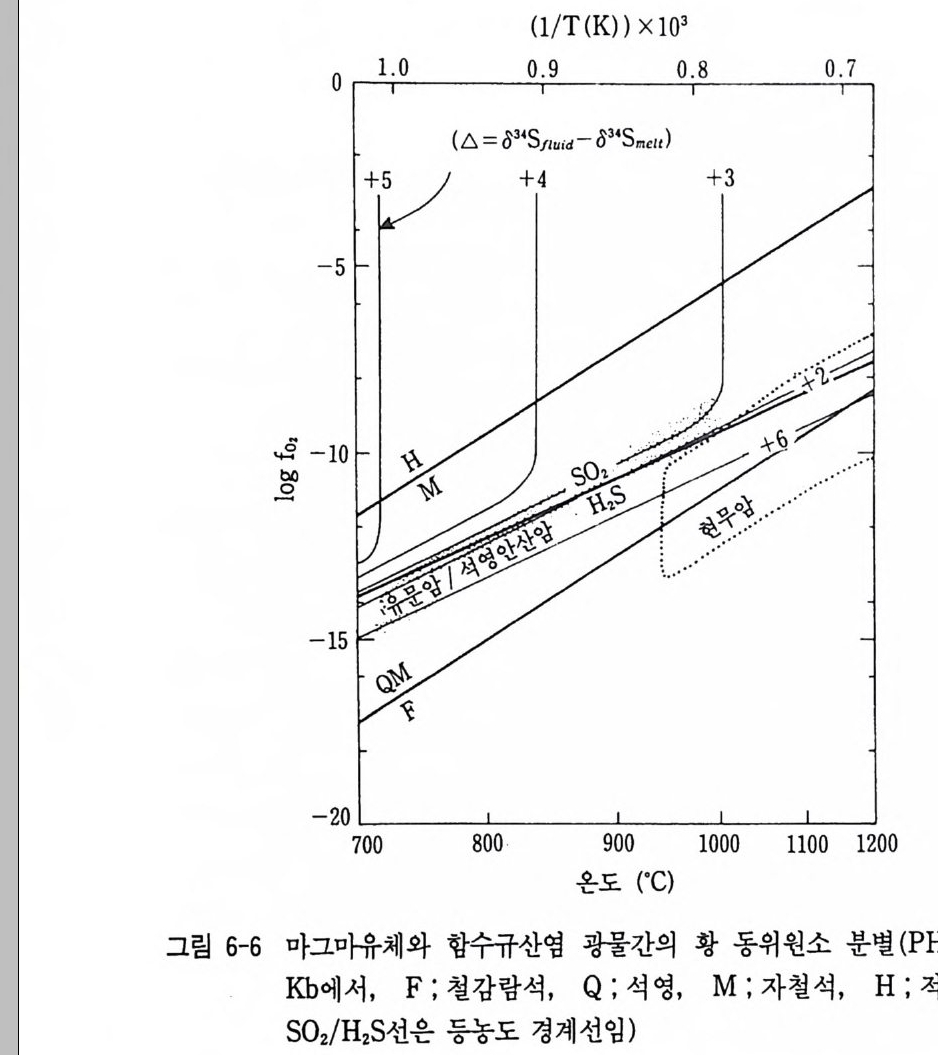 (1/T (K) ) X I03
(1/T (K) ) X I03
T 와 fo 2 의 함수로서 o 3 4s 멜트 에서 o 3 4s 유계 의 변화를 (2), (3) 식에서 계산할 수 있다. P.r~ PH 20=l Kb, XH 2 0 = 1 . 0 에서 계산한 것이 그림 6-6 이다. 이 그림에는 현무암질암, 유문암, 석영안산암내의 혹운모-각섬석 의 fo 2 - T 조건도 표시했다 (Ca rmi chael 등, 1974). P,·X tt 2 0 에 의해 S02 /H 2 S 경계선이 아동하고 o34 s 동치선도 낮은 fo2 쪽으로 이동될 것이다. 그러나 보통 광상형성과 관련된 열수용액 의 경우 고온에서 P 가 0.5~3Kb 범위를 벗어나지 않으며 XH 2 쇼i 0 . 8 이하는 되지 않을 것이다. 따라서 아런 Pr·Xtt 20 범위내에서는 fo2 -T 그림에서 S02 /H 2 0 경계와 o3.4 s 등치선이 +0.31og fo2 이상 변 하지는 않을 것이다. 그림 6 - 6 에서 고온 고압의 현무암질 마그마에서 유래된 마그마질 유체에는 H 2 S 가 우세한 반면, 화강암질 마그마에는 유체로 분리될 때의 멜트의 산화상태에 따라 H2S 또는 S0 2 가 많아짐을 알 수 있다. 6 구 유체 - 광물간의 동위원소 평형 유체 -광 물간의 동위원소 평형 (Fluid - m ine ral e q u ili b ri a) 에 대해서 알아보자. 400~800°C 온도 범위에서 위의 (2) 와 (3) 식을 이용하여 a3•s 유체어 1 서 034SH2S 값의 변화를 계산한 것아 그림 6-7 이다. 반암동 광상이나'접촉교대 광상, 스카론형 광상과 같은 고온형 광상의 산화 상태는 보통 자철석 -적칠석 버퍼 범위(황철석+적칠석 안정)에서 석 영 _자철석 - 철감람석 (Fa y a lit e) 버퍼(자류철석 안정) 영역 사이를 나 타낸다. 그런 fo2 조건에서 a3•SH2s 가 o34S 유체보다 10% 청도 낮은 값을 가지게 되며 열수용액 중의 T, fo 2 만의 변화(상 4S 유체 일정)에도 10% o 이 변화한다. 그림 6 - 7 은 고온형 광상에서 황화광물의 샹 4S 값이 변화한다 해서
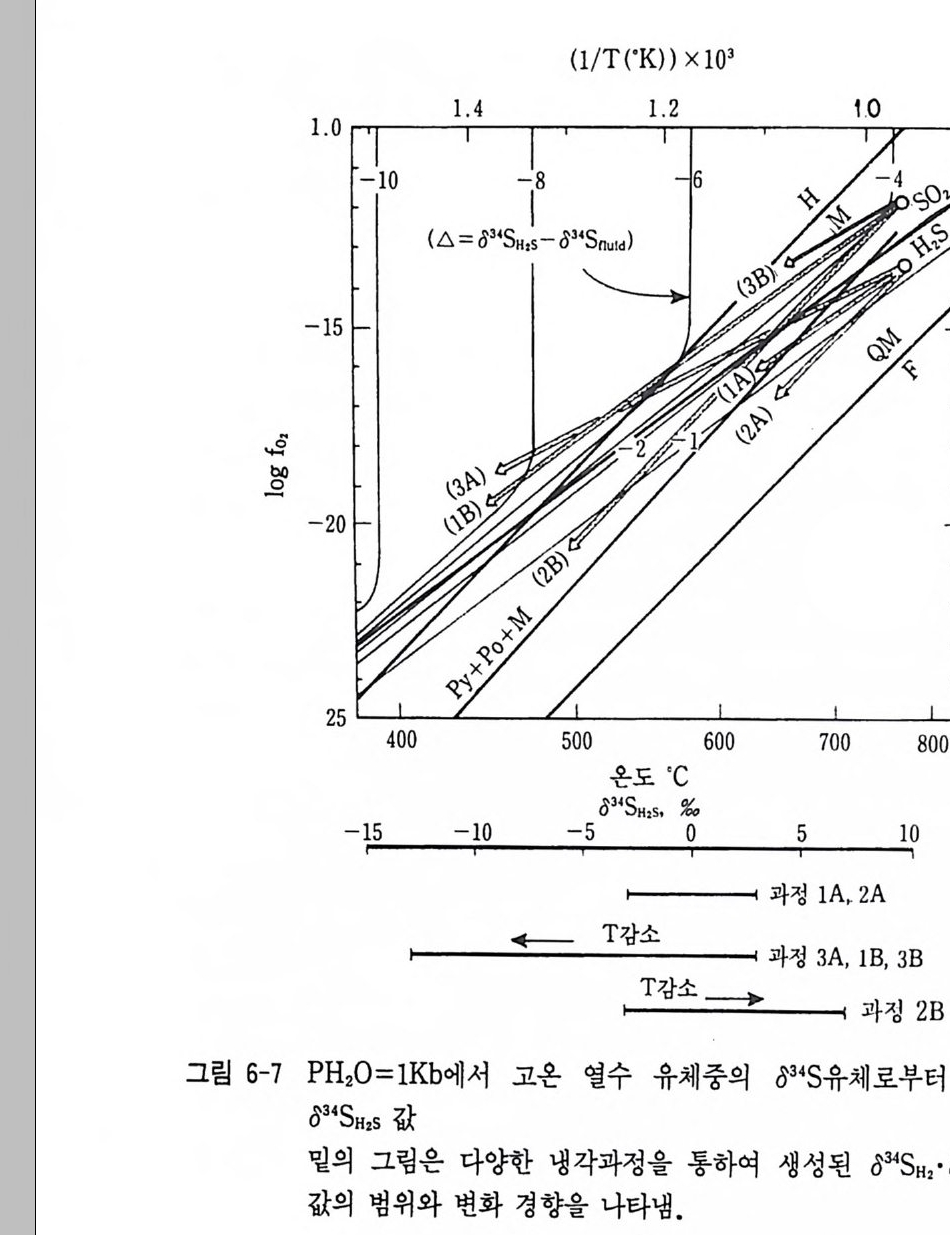 1/ T ('K) ) X 103
1/ T ('K) ) X 103
��T� ����D� ����İ. �(� ��� Ǵ��X� 8 S Ǵ�\���0� ���� 0���t� x�� ��� ��X�X� i� L�8�t�|� t��`� DՔ�� ���, 034S � 8�
나타내고 있다. 그림에서 마그마질 유체의 냉각 경로를 몇 가지 생각해 보자. 본원 마그마질 유체내의 황 중에 H2S 가 많은 경 우이 면서 1A 와 2A
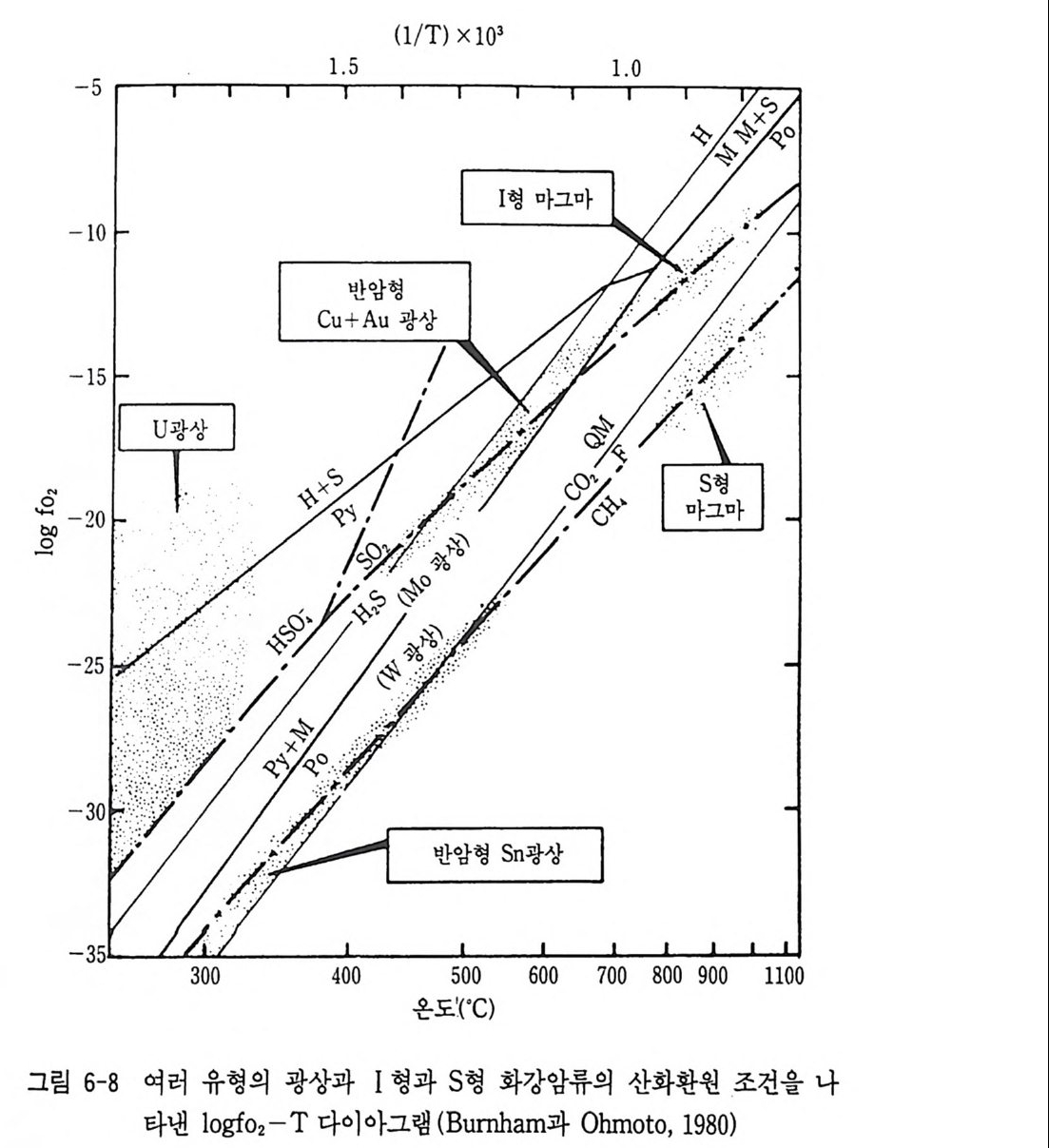 (1/ T) X l03
(1/ T) X l03
경로로 냉각될 때에는 034SH,S 의 변화가 없으며 8“S 유세 ~oa4s 멜 드 ~o 士 3%, 가 된다. 3A 경로는 대부분의 H2S 가 S02 화 되었을 때 8“S 腦값이 멜트의 샹 4S 값보다 10%, 작아진다. 그러므로 원래의 마그마멜트의 8“S 값이 0 土 83%, 이었더라도 냉각시 fo 2 조건에 따라 마그마멜트내의 황화수소 의 034SH2S 는 +3 ~ ― 13%, 까지 변화된다. 원래의 마그마질 유체 중 에 S02 가 많을 때 lB, 3B 경로로 냉각됨과 동시에 034SH2S 가 계속 증 가됨을 가리키고 있다. 400°C 에서는 멜트에서보다 유체 중의 H2S 가 4%, 더 높을 수도 있다. 어떤 광상에서 황 동위원소값이 비교적 균일한 값을 가진다면 산화 상태는 S02/H2S 경계 밀의 조건이거나 산화상태가 무변화한 조건이 었음을 가정 할 수 있게 된다. 반면에 8“S 값이 크게 변화한다면 fo2 가 S02/H2S 경계 부근이거나 또는 경계 위의 조건으로 볼 수 있다. 그의 fo 2 가 일정하거나 증가한 경우일 수도 있다. Ohmo t o (1 986) 의 Log fo 2-T 그림에서 I- 형 마그마와 S- 형 마그마간에 fo2 환경 그림에 서 전자가 더욱 높은 fo2 환경임을 알 수 있다(그립 6-8 ) . 그리고 반암동 광상, Mo 광상, W 광상, U 광상 사이에도 현저한 fo2 환경의 차이가 있음을 알 수 있다. 6-8 저온에서의 동위원소 평형 35o•c 이하의 저온과 저압(액상/기상의 경계) 조건에서 열수광화용 액 중의 황종은 위의 언급한 H2S 와 S02 와 갇은 이상기체의 혼합만 으로 생각할수 없다. 350~4oo·c 이하의 온도에서 HSO;-, NaSO;- 와 갇은 황산염의 산 화 황종이 우세하므로 4H20( g )+4S02(a q )=H q S(a g )+3H++3HS 야와 같은 반웅식을 생각할 수 있다. Naumov 등 (1974) 의 열역학적 자료에 의하면 35o·c 에서 log K=
-18.98 이고 300°C 에서 -13.76 이 된다. mso2(a q )=mEso4 2 - 에서 정확한 온도는 용액의 영농도 fH,O , ~s, fo2 , PH 등에 따라 달라진다. 350°C 이하의 저온의 광화용액 에서 중요하게 다루어 지는 용존 황종 은 H2 S, HS- , 황산염이온 (SO~-. HSO:;-, KSO:;-, NaSO,, CaS04) 등이 다. H2S 와 HS-사 이에 동위원소 분별이 작으므로 b. Hs-=O 으로 가정하 고 기타 모든 황산염들의 황동위원소값은 갇다고 가정하면 (1) 식에서 034SH,s = 034S 유체 一 6.so i- (R /1 + R') (5) 로 표현할 수 있다. 여기서 R' = ~sm -/ ~H 2 S 이다. R ' 의 값은 T, PH, fo2 , GK+, QN a+, Gca2 + 등의 함수로 아래 와 같은 반응식 에 서 K 값과 기 타 필요한 수치자료를 이용하면 계산될 수 있다. H2S
KSO:.=K+ +s m- NaSO:. = Na+ + sor CaS04(Bq ) = Ca2+ + so~- R' = { (fo당 • /H2S) (占+ KHS 어a ? ~Y H 책 + K 퍄또Y KS 야 + KNa:N.a;NaSOz + KcaS:Caso4 )}{ 도' 0H+2) (1 +~)} (6) 위의 (5) 식과 (6) 식에서 8“S 輯 관계를 log fo2 -PH 그림으로 그릴수도 있으며 여기에 광물의 안정영역도 그려 넣을 수 있다. 이 를 log ~sm-/~H2S-T 그림으로 그리면 그림 6-9 와 같다. 위 두 그림에서 열수용액 (광화용액)의 산화 환원 상태가 so~- /H 2 S 경계 부근에서 a34Si 값에 크게 변화를 줄 수 있음을 알 수 있다.
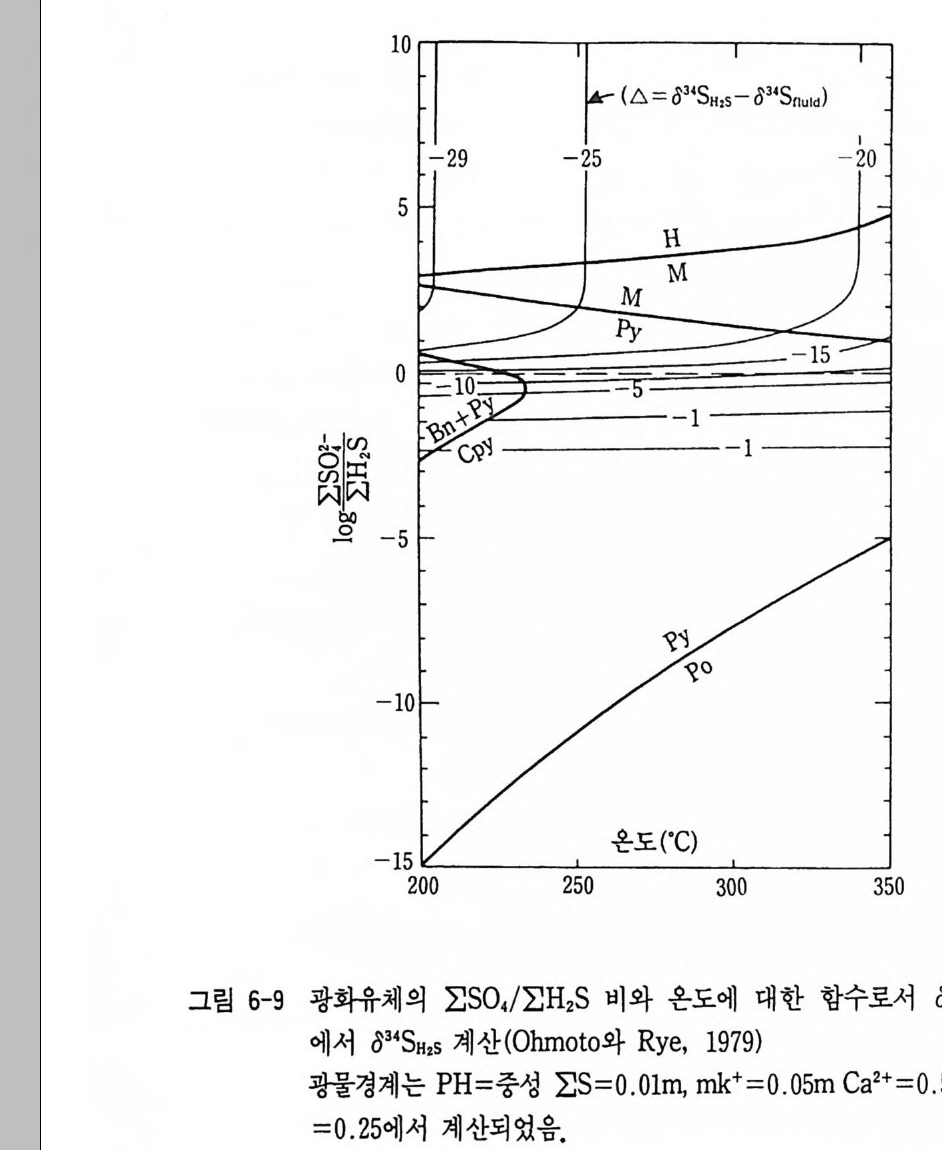 10
10
예 를 들면 약 250 ° C 의 so~- /H2 s 경 계 부근 지 역 에 서 so ~- / H2s 비 가 fo2 , 0.5 , PH 1, 단위 정도 증가하여도 황 동위원소비 o34 S i 값은 20%0 이상 변화한다. 그리고 자철석-적칠석과 평형에서 침전된 황화광물은 유체에서보 다 a34s 값이 훨씬 작다. f。 2 가 낮고 H2S 가 우세한 지역에서 황화광 물의 834S 값으로 유체의 동위원소값 (834S 유세 )을 계산하려면 T, PH, f。 2 aK * 등을 알아야 한다. 그러므로 광화환경의 시공간에 대한 a34s 광물의 값의 변화를 조사 하고 기타 지구화학적 자료와 비교분석하면 광화작용의 물리 화학적 조전 을 좀더 정량적으로 해석할 수가 있게 된다. 그림 6 - 9 에서 보면 834S 유 세 =- 3 ~ +7%o 인 마그마질 유체에서 황 철석과 섬아연석과 같 은 황화광물이 200°C 이상의 온도에서 침전될 경우 이들 광물의 동위원소값이 +8 %., 이상의 무거운 동위원소값을 가지기는 어려우나 ― 30 %0 까 지 가벼운 값을 가지기가 쉽다. 물론 증발잔류암과 퇴적암내에 포획된 화석수와 같은 해수기원의 황은 a34s 유 세 가 +1 0 ~ +30%0 값을 가질 수 있다. 따라서 그러한 광화용액의 SO t가 250°C 이상에서 평형을 유지하 면서 H 2 S(HS- )로 환원된다면 + 30%., 이나 -15%., 까지 낮은 값을 가 지는 황화광물이 침전될 수 있다. 6-9 열수광상의 황의 기원 해석 광상의 황의 기원은 맨틀(지구삼부기원)과 해수기원을 생각할 수 있 다. 황은 여러 지질학적 과정에서 순환하고 있다. 석고와 무수석고의 동위원소 성분과 여러 지질시대에 걸쳐 퇴적된 해성 황산염과 황화광 물 및 광상 황화광물의 동위원소 분석에서 황 동위원소의 지질시대에 따른 변화 (Secular va ri a ti on) 가 잘 나타나고 있다(그림 6-10). 그림에서 보면 과거 해수기원의 황산염광물은 평균 +17%., 이었으며
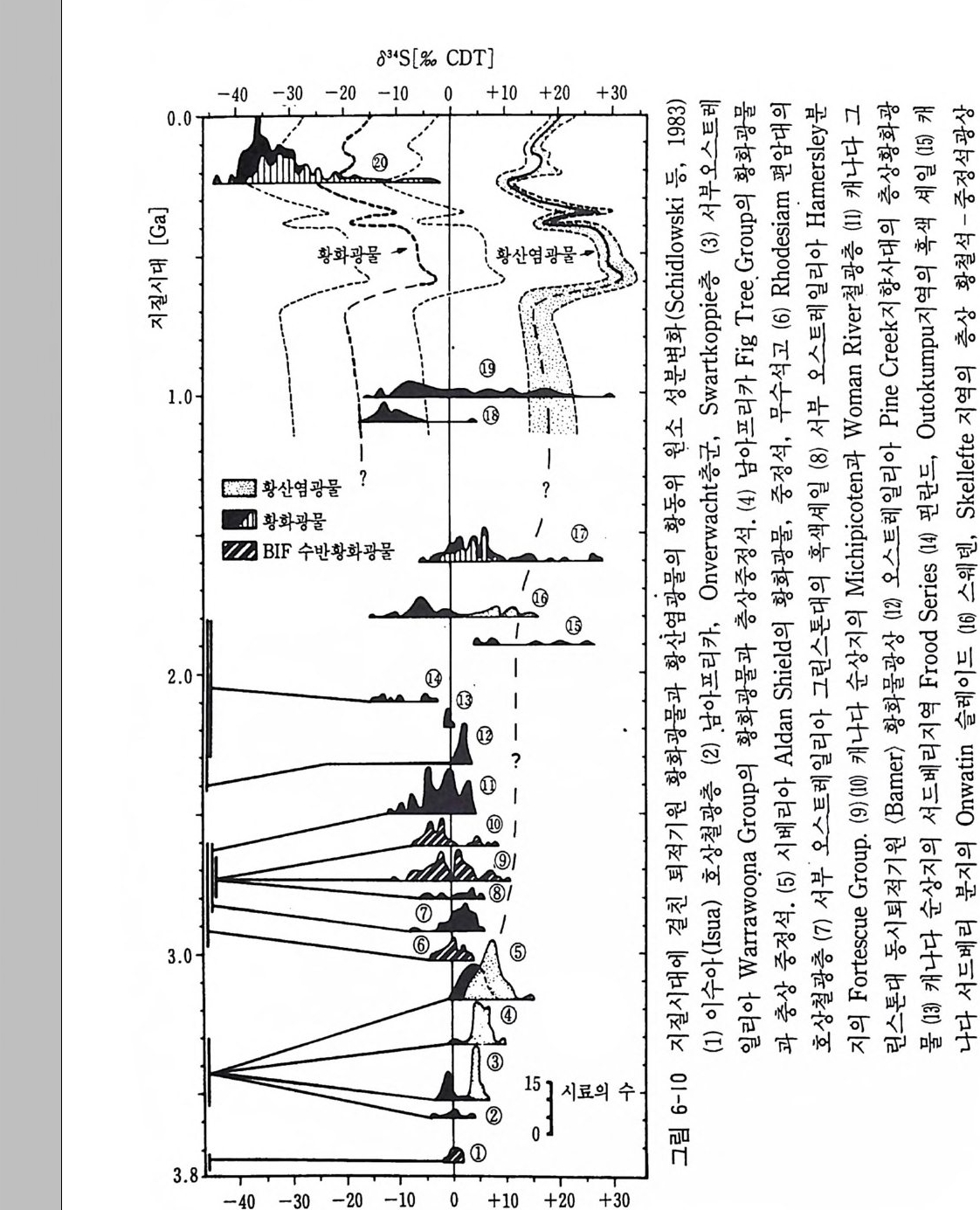 aG][대지 시질1.o. o02. 03. 004- E.ZUBn I쑤쑤 -3 0’ :A ',-\--〕--一二--一·\-一-中훌F쇼 +쑤엷I02 쑤·부 7 OI- 年얼曲 S [C ]TD% :.g 01+ `'-- - r `' V_&.'- —— -· _론1-\ -소:`.>r~ ` . , ._..0 2-+II I ©03+ 3)918기l분k 광물S황과광cs do (에위되산성물영소i,등의화황변걸 동친원 질w대화 지원 시i적h 황 -6림 ((3)1 ))(2 )aci부,트pev수O wao군Sh아kn프남오리et충아철sru상,서광 w호( I층r 스p충t레 카a 이 n.oo4 w aFrraWa() ig 아ere상의석rT정중o의광충화과 .광물 화 p물pG남oGr황황u 프리아u일. 카리 R) m(6a asnl5oe h d(dA)i편 ,광화중황대 il아의정h석중석 상리암 S베정,e시d무석 수충 과의 물고 8()트스7서r아 )(충광부철리분 e상서s셰일부 my레 a트대톤e스H스호일린 그 아의오리l흑일오 색 레 me an)o(uWroG eusoF9c. pc철i과p그rhvei M 의지상R순e 다나캐다 iJ(나c의충 in 광지t캐ot )II(r )O n rerneaBP광레트충k지스오 1e 상광r물화황의
aG][대지 시질1.o. o02. 03. 004- E.ZUBn I쑤쑤 -3 0’ :A ',-\--〕--一二--一·\-一-中훌F쇼 +쑤엷I02 쑤·부 7 OI- 年얼曲 S [C ]TD% :.g 01+ `'-- - r `' V_&.'- —— -· _론1-\ -소:`.>r~ ` . , ._..0 2-+II I ©03+ 3)918기l분k 광물S황과광cs do (에위되산성물영소i,등의화황변걸 동친원 질w대화 지원 시i적h 황 -6림 ((3)1 ))(2 )aci부,트pev수O wao군Sh아kn프남오리et충아철sru상,서광 w호( I층r 스p충t레 카a 이 n.oo4 w aFrraWa() ig 아ere상의석rT정중o의광충화과 .광물 화 p물pG남oGr황황u 프리아u일. 카리 R) m(6a asnl5oe h d(dA)i편 ,광화중황대 il아의정h석중석 상리암 S베정,e시d무석 수충 과의 물고 8()트스7서r아 )(충광부철리분 e상서s셰일부 my레 a트대톤e스H스호일린 그 아의오리l흑일오 색 레 me an)o(uWroG eusoF9c. pc철i과p그rhvei M 의지상R순e 다나캐다 iJ(나c의충 in 광지t캐ot )II(r )O n rerneaBP광레트충k지스오 1e 상광r물화황의
18 억 년 동안 + 10 ~ + 35 %o의 황 동위 원소값이 변동해 왔다. 선캠 브리아기의 황산염은 +3 ~ + 8%0 내의였다. 이들 황화광물은 유기물 또는 황환원 박테리아의 작용에 의해 황산 영이 환원되어 생물기원의 황화광물을 침전시키기도 하였다. 예를 들면 2CH20+so ~- +2H + ----+2H20+2C02+H2S 와 같은 E 응에서처럼 유기물에 의해 환원된 황화수소가 만들어진다. 이때 만들어진 황화수소는 퇴적물내에서 속성작용하는 동안 다음고 같이 황화광물을 침전시킨다. 2H2 S ( HS -) + Fe2 + 一 FeS2 + 2H2 또는 2Fe (OH) 3+ H 2 드 2Fe (OH) 2十 S + 2H20 Fe (OH) 2+ H2S - —, FeS + 2H20 FeS + S-一 ➔ FeS2 따라서 속성작용시에 형성된 황화광물의 양은 퇴적물내의 유기물질 의 양과 밀접한 관계를 갖는다. Berner (1 980) 는 해양되적물내의 황산염 기원의 황의 양과 잔류 유 기원탄소간의 상관관계 (S / C) 를 검토한 결과, 현생 퇴적물은 S/C 가 0.32 정도이며 지질시대를 통하여 S/C 의 값이 1~0.05 변화하였음을 조사하였다. W illi ams (1 978) 에 의하면 S/C>l 일 때는 속성작용에 의한 황화광 물의 침전은 거의 알어나지 않았다. 따라서 퇴적기원의 광상연구에서 는 S/C 값이 중요한 의미를 가지며, o34S 값은 ® 해수의 황산염의 a34s 값 ® 박테 리 아 작용에 따른 반웅속도론적 동위 원소 효과 ® 개 방계인가 폐쇄계인가에 따라 달라진다.
!:::,.SOt 황화광물은 SO!-황 화광물 사이의 비 가역 적 동위 원소 효과 의 영향을 받으므로 퇴적물 중 속성작용에서 형성된 황철석의 !:::,.SOt 황화광물값은 퇴적속도와도 관련이 깊다. 황철석의 수화반응에서도 다음과 같이 H2S 가 생성된다. 2FeS2+4H20=Fe203+4H2S+l/2 02 4FeS2 + 4H20 + 6H+ = 4Fe2+ + 7H2S + SO!- 위의 반응은 유기물질이나 Fe2 + 에 의체 산소가 소비되면 계속 일 어나며 온도가 증가함에 따라 H2S 의 양은 증가한다. 이때 만들어전 H2S 의 황 동위원소비는 원래의 황철석의 동위원소 비와 동일하다 (Ohmo t o 와 Ry e, 1979). 즉 황화광물이 산화되어 황산염 을 만들 때 샹 4S 값은 변화하지 않는다. 김규한과 나까이 (1981) 에 의하면 남한의 온천수 중의 so~ - 기원해석 에서 한강수 중의 so~- 의 동위원소값 ( + 2 ~ + 5%o) 과 여러 열수기원 금속광상의 황 동위원소값 (+2 ~ +5%.) 이 일치하여 한강수 중의 SO!- 의 황의 기원은 광상유황, 지각기원의 황임을 잘 말해 주고 있 다(그림 6-11). Red bed Cu 광상이나 미시시피 벨라형 광상 (MVT), 셰일형 광상 황화물 광상 (SHMS) 처럼 저온 퇴적기원의 광상의 경우 광화용액 중 의 H2S 와 금속이온의 총량의 다소에 따라 침전된 황화광물의 황 동 위원소값은 크게 달라진다. MVT 형 광상은 H2S<~ 쭙이기 때문에 비평형조건이 되어 침전된 공존 황화광물간의 동위원소비는 ,유 체의 H2S 의 동위원소비와 거의 같다.. 죽 o34SH,s ~ o34SsP ~ o34S811 .이 다. 그러나 H2S>~~ 인 SHMS 형 광상에서는 평형조건이 되어 o34SH2S~o34Ss p >o34S gn가 된다. 역으로 바평형광상은 H2S<~ 쭙임을 해석할수도 있다.
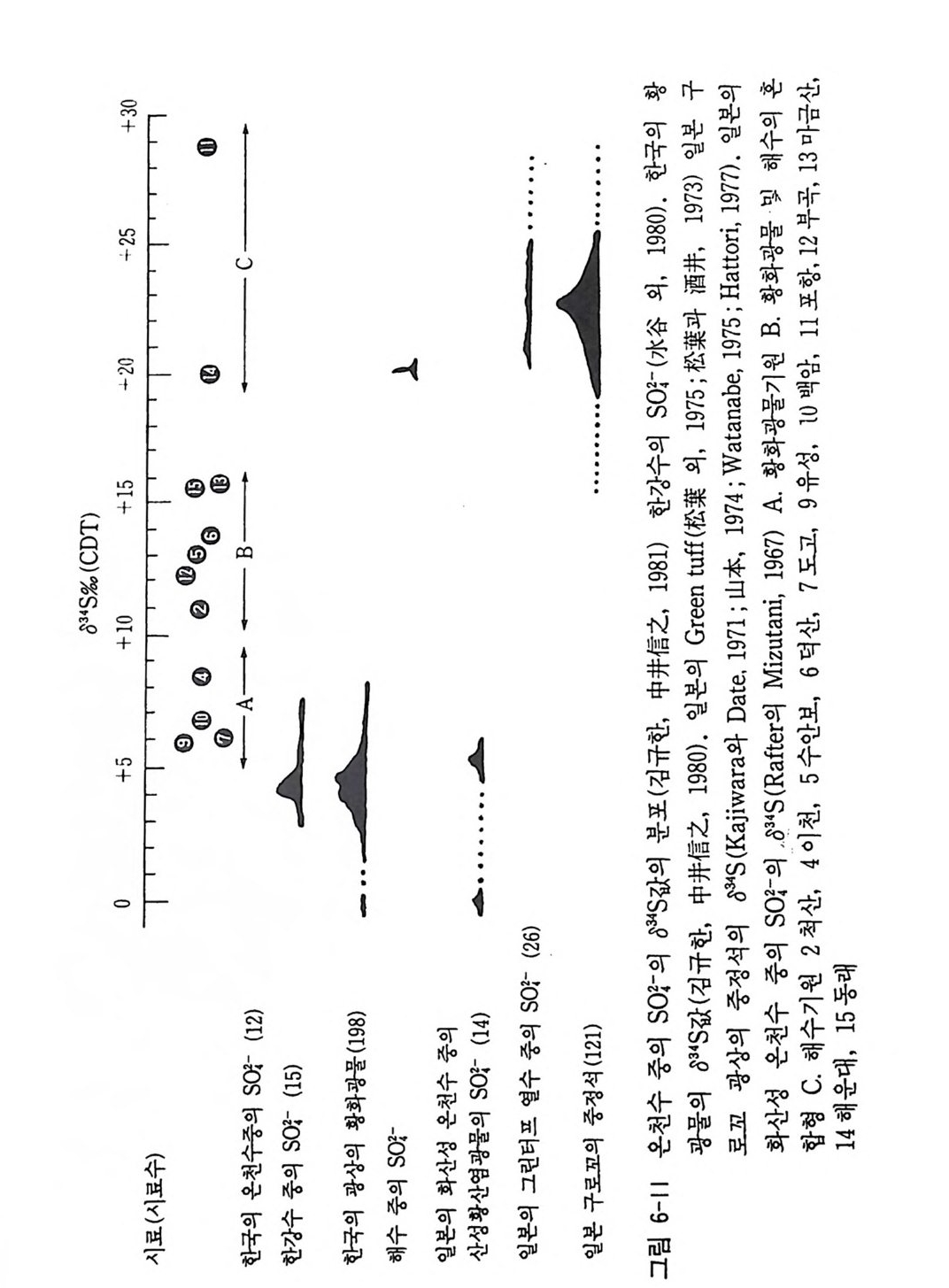
그러나 Ohmoto 0 985 , 1986) 에 의하여 l20°C 이상 고온의 셰일이 우세한 환경에서 만들어진 광화용액은 m H,s > m :i: ~> 10 -s m 이 되고 광화용액 의 온도가 12o·c 이 하이 거 나 프럽 계 (Pl umbin g sys t e m ) 내 에 황 철석이 부족한 경우에는 모암에서 황철석이 용리되거나 유기물질에 의해 황산염이 환원되거나 해서 mH 2s 가 추가되어야 함이 연구되었 다. 이런 경우 H2 S 부족으로 인해 광물침전시. mH ,s < 10- s m 이 되어 한 광물이 침전될 때 황 (S) 을 전부 소바하게 되어 침전된 황화광 물 의 동
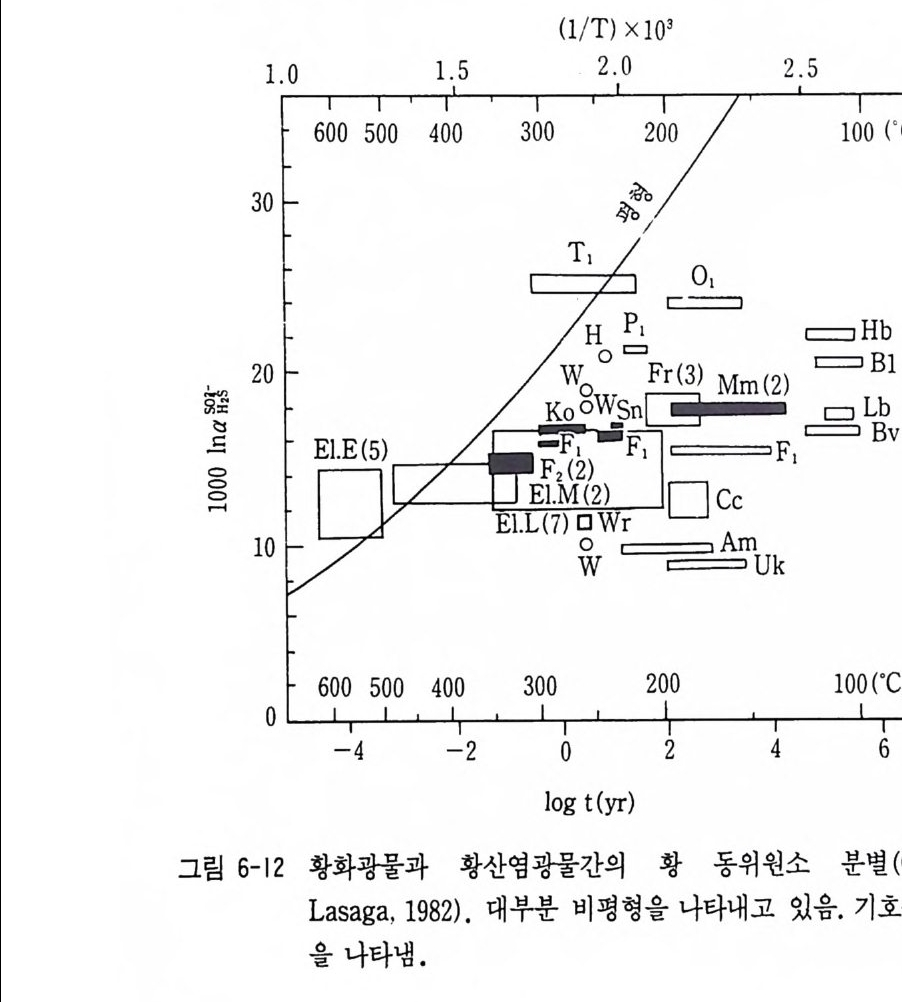 (1/ T ) X 103
(1/ T ) X 103
위 원소값은 834S :::: 834Szn 손 034SPbS 가 되 기 도 한다. 공존하는 황산염광물과 황화광물 사이의 동위원소 분별정수를 조사 해 보면 대부분 비평형이다(그립 6-12). Ohmo t o 와 Lasag a (1982) 는 황화물 -황 산염 의 분율 (Sulfid e -Sulfa te fr ac ti on) 이 평형분별정수보다 작기 때문에 이들 광상의 형성시에는 동위원소적으로 비평형상태에 있었음을 의미한다고 했다. 이 같은 비평형의 원인은 황산염과 퇴적지의 황산염원의 광화용액 의 혼합으로 생각할 수 있다. 즉
o34s 황 산입장문 = o34s 혼합왕산영 = 034Sso,- a • Xso4-a + 034Sso,-b• Xso,-b 예를들면 ® 동태평양 해령의 화산성 괴상 광상이나 일본의 구로꼬 광상과 같은 열수성 광화용액과 해수기원의 황산염용액의 혼합 ® 반암동광산에서와 같이 4H20+4S02---+H2S+3HS0:;-+3H+ 반 응석과 같은 S02 의 가수분해에 의해 생성된 것과의 혼합 @ MVT 형 광상의 후기 광화작용에서처럼 천부 지하수에 l0-5m 이상의 용존산소를 함유하므로 H2S 의 산화에 의해 생성된 S0:- 와 광화용액과 혼합 등을 들 수 있다. 6-10 광상황의 기원 결정법 위에 설명한 것처럼 저온이거나 금속함량에 비해 황의 양이 부족한 광화용액인 경우이거나 광화용액 중에 H2s, sor 가 평형에 이를 만 큼 충분한 긴 잔류시간을 가지지 못할 때 비평형이 된다. 이때는 H2 S 의 o34s 의 값이 바로 황화광물의 기 원을 대표하는 o34s 값이 된다. 퇴적물 중의 황철석의 수화반응에 의한 과정을 생각할 수 있다.그러나 H2S 나 SO t가 광화용액 중에 잔류기간이 길어 평형에 이 르게 되면 각 유황종의 834S 값은 광화용액 중의 유황종간의 ® 평형 분별정수 ® 유황종의 종류 @ o34Si: s 등에 따라 변화된다. 따라서 전 황의 동위원소 값 (o34S i: s) 을 계산해서 광화용액의 기원을 해석해야한다. o34Si: s = o34Sh2s • Xh2s + 03 4 S~ 。 4 • x§ 。 . = 034S~2 s • x~2s + o34S 隣 X §。 4 죽
034S:1: s = o34S H2s +L1 s 아 ~ H , s (R/ 1 + R) 여기서 R= 鴨이고 4s 야 - H , S 는 so~ - 와 H2 S 사이의 평형분별정수이다. 그림 6-13 에서처럼 F i eld 와 Gus t a f son (1 976) 은 칠레의 엘살바도르 반암동광상에서 공존한 황화광물과 황산염광물의 s3 4 s 와 4 사이의 상관관계를 찾았다. 죽 공존하는 두 광물 사이의 s34s- ,6,.황산영 釋琦 사 화강문 그림에서 o34Stt 2s = 034S I :s - D .so .-H2S (R/1 + R) 034Ssoi- = 034SI: s + D. so 터 -H 2 S (1/1+R) 1 차함수 관계가 위의 식의 관계와 일치하고 있다. 죽 기울기 R/l+R, 1/l+R 에서 우리는 R 의 값을 얻을 수 있고, 절편에서 샹 4s2s 값을 얻을 수 있어 이 값으로 광화용액 중의 황의 기원을 해석할 수가 있게 된다.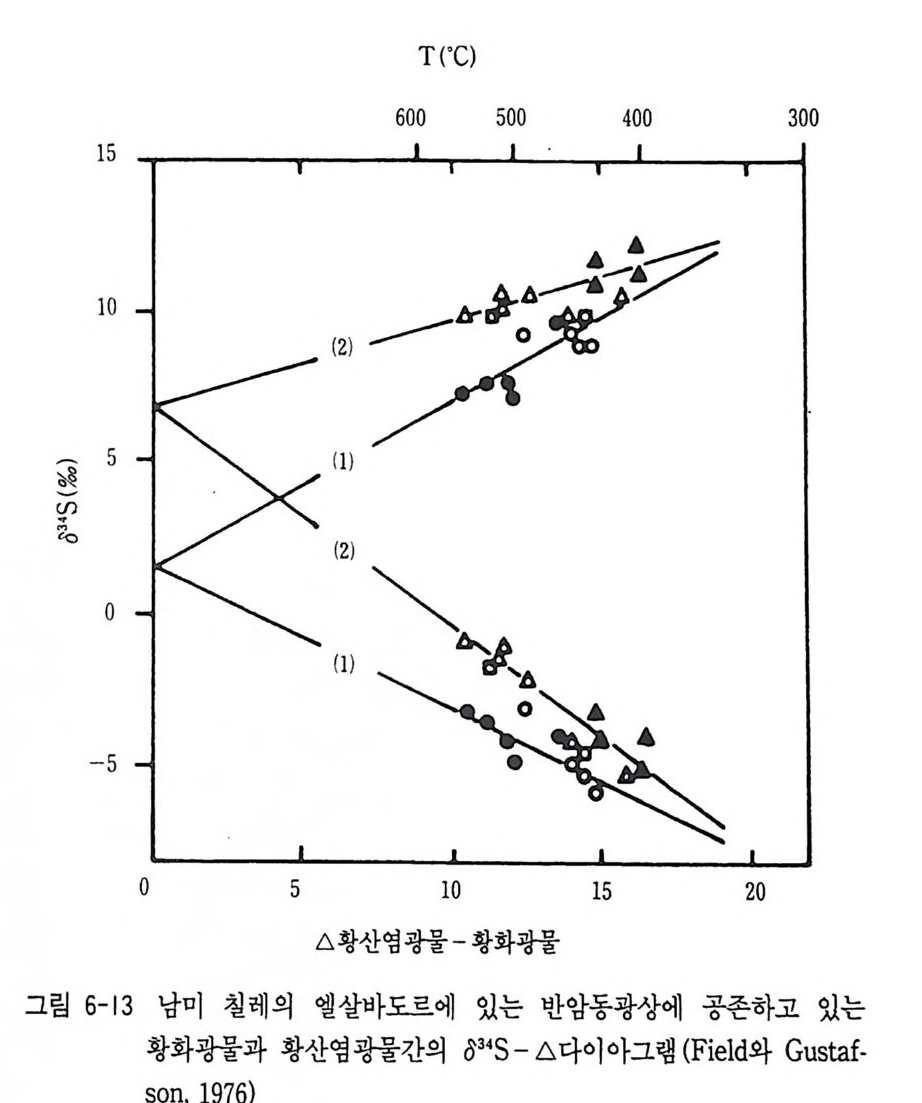 T('C )
T('C )
6-11 우리나라 금속광상의 황 동위원소 성분 우리나라 금속광상의 황화광물의 황동위원소바는 대체로 +2 ~ +7%, 범위로 비교적 균질한 황 동위원소 성분을 가진다(그림 6-14).
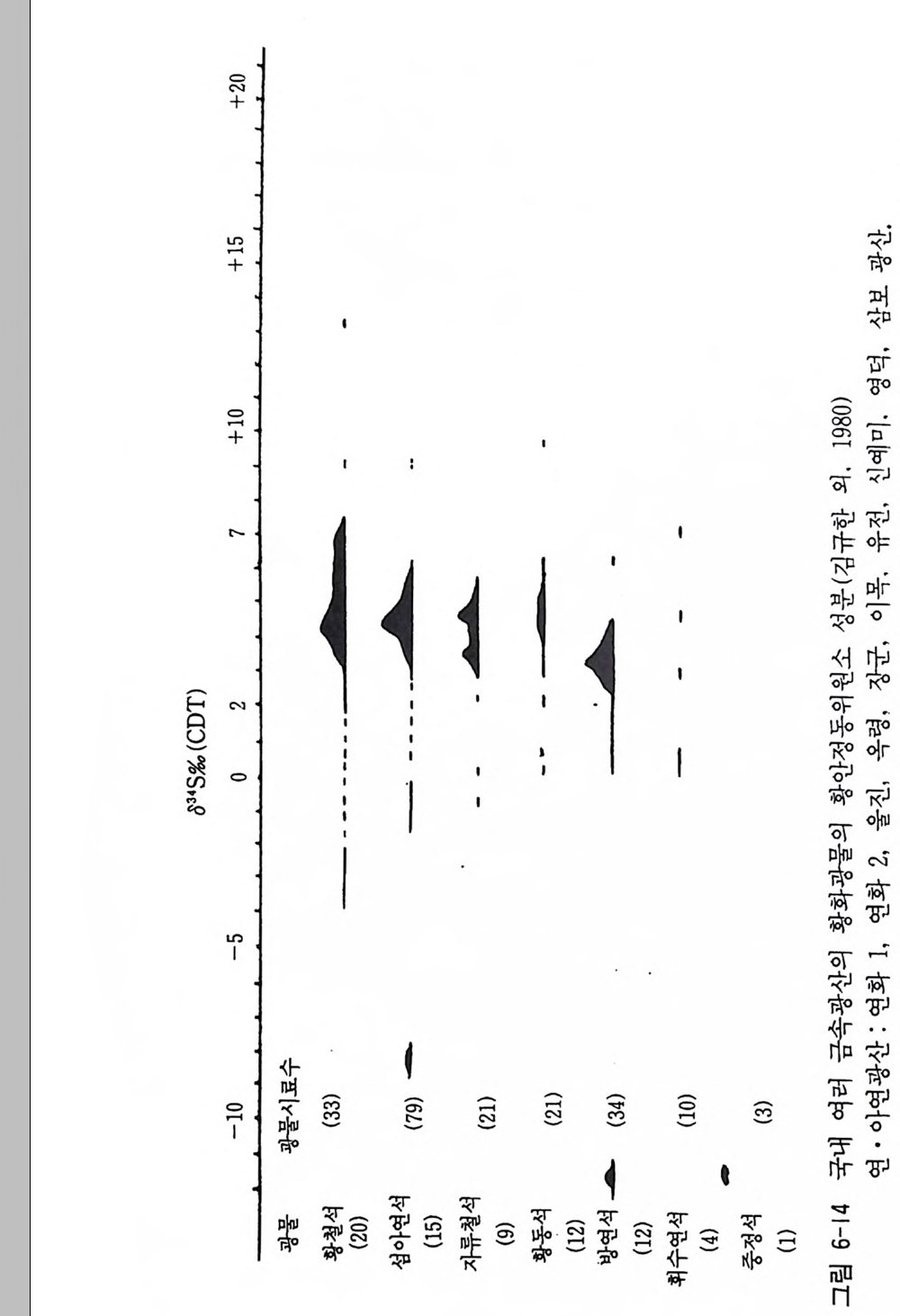 +20
+20
이처럼 우리나라의 텅 스 텐 - 몰리브덴 광상의 황 동위원소 성분은 일광 Cu- W 광상(키 . 6 ~ +0 .3 %0, So 와 Shelto n , 198 3) , 대화 ( + 2 .4 ~ +4.4% 0 . So 등, 198 3) , 월악 W - Mo 광상 ( + 3 . 0 ~ +7 .6% o. So 등, 1983), 쌍전 W 광상 ( + 2 . 5 ~ +5.2 % 0. Kim 등, 1988) 등이다. 텅스텐 -몰 리브덴 광상들의 황화광물의 034S= -1.7 ~ + 7 . 6% 이며 이들을 이용 계산한 034 S tt 2 s=- 1.7 ~ +6.1 %o를 가진다. 그러나 각 각의 광상에서 황 동위원소 성분은 대단히 균질적이다. 우리나라의 텅스텐 광상의 황 동위원소비는 일본의 자철석계 화강암류의 황 동위 원소 성분과 유사하다. 균질인 동위원소 성분을 가지는 황화광물들은 상이한 산화조건에서 화강암질멜트에서 분리되었을 것으로 추정하였 다 (Shel t on 등, 1986). 일광광상의 경우 황화광물의 o3 4 S 는 -1.6 ~ -0.3%0 로 대단히 균 질한 성분을 가지는 화성기원의 황으로 주위 백악기 되적암 기원의 황의 유입이 전혀 없다 (So 와 Shelto n , 1983). 연아연 동광상의 황동위원소 지질온도계를 이용하여 얻어진 광상생 성 온도는 제 1 연화 Pb-Zn 광상 470~540'C , 제 2 연화 Pb-Zn 광상 420' ~, 신예미 Pb-Zn-C u 광상 400~540'C , 장군 Pb-Z n ~C u 광상 340~420'C , 울진 W-Pb-Zn 광상 340'C , 삼보 Pb-Zn- 중정석 광상 200 ~ 250'C , 금장 Pb-Zn-Cu 광상 320'C , 옥령 Pb-Zn-Cu 광상 2so·c 이 며 (김규한과 나까이, 1980), 전주 1 Au-Ag 광상 245~270'C ( So 등, 1987) 등이다 . 그 중 삼보 광상에 대한 연구결과를 좀더 구체적으로 (김규한과 미즈다니, 1990) 소개한다. 삼보 연-아연-중정석 광상은 선캠브리아기 경기변성암 복합체의 흑운모편암 중에 발달하는 N 40-50' W 방향의 구조선을 따라 충전된 함 연, 아연, 중정석 석영맥 맥상 광상이다. 황산염 광물이 다량 공존하고 있는 삼보 Pb-Zn- 중정석 광상의 스데 이지 Il 의 황화광물과 황산염광물의 황동위원소비는 각각 -3.9 ~ -13 . 5%,, 과 +15. 7 ~ +17.2%,, 이다.
삼보광상의 황화광물과 황산영광물은 동위원소 평형에 가까우며 평 형온도는 213~291·c 가 얻어졌다. 이는 So 등 (1984) 과 J wa0989) 에 의해 얻어진 유체포 유물의 균일화 온도 155~335 ° C 와 110~260 ° C 와 도 조화적이다. 스테이지 Il 의 황화광물과 황산염광물의 황 동위원소비와 온도에서 구한 o34S1: s 값은 + 12 . 8% 이 며 ~H2S/~SO~-= 0 . 2 로 광화용액 은 마 그마 멜트에서 유래한 황산염이온 기원의 황이 우세한 특칭을 가진다 (그림 6-15). 황산염광물인 중정석의 산소 동위원소비 +2. 4 ~ +3 .9 %o와 o34S=
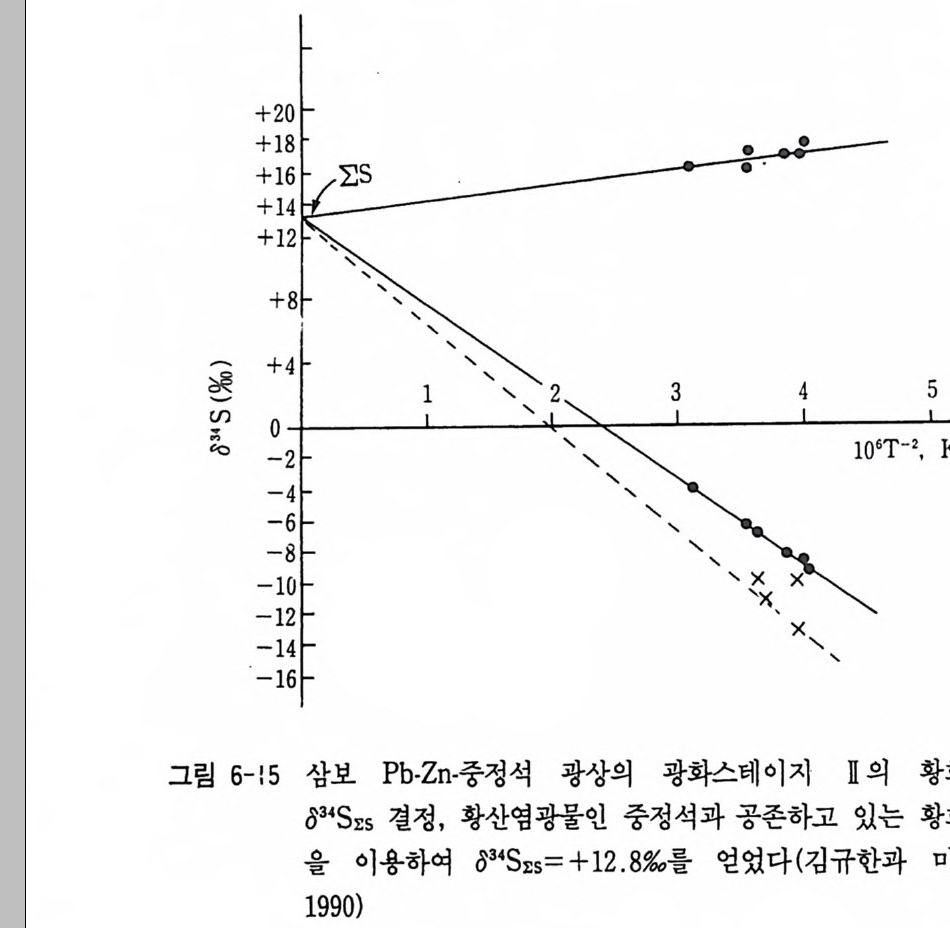 +2 0
+2 0
+15. 7 ~ + 17 . 2%() 로 대단히 균일하며, 해수기원인 일본의 구로꼬 광상이나 애팔래치아 마운텐과 로스베리 광산의 중정석의 값과도 크 게 다르다. 물론 해수기원의 so:- 의 값과도 다르다(그림 6-16). 공존하고 있는 중정석과 석영의 산소 동위원소비에서 이들과 평형상 태에 있었던 열수광화용액의 동위원소비를 계산하면 석영에서 계산된 0180H, O= 一1. 89 ~ + 0.94%a( 평균 ― 0.69 %,) 이고 증정석에서 계산된 0180H, O=— 4 .24 ~ —l .08%a. (평균 -2 .3 6%,) 로 서로 다르다. 이는 광
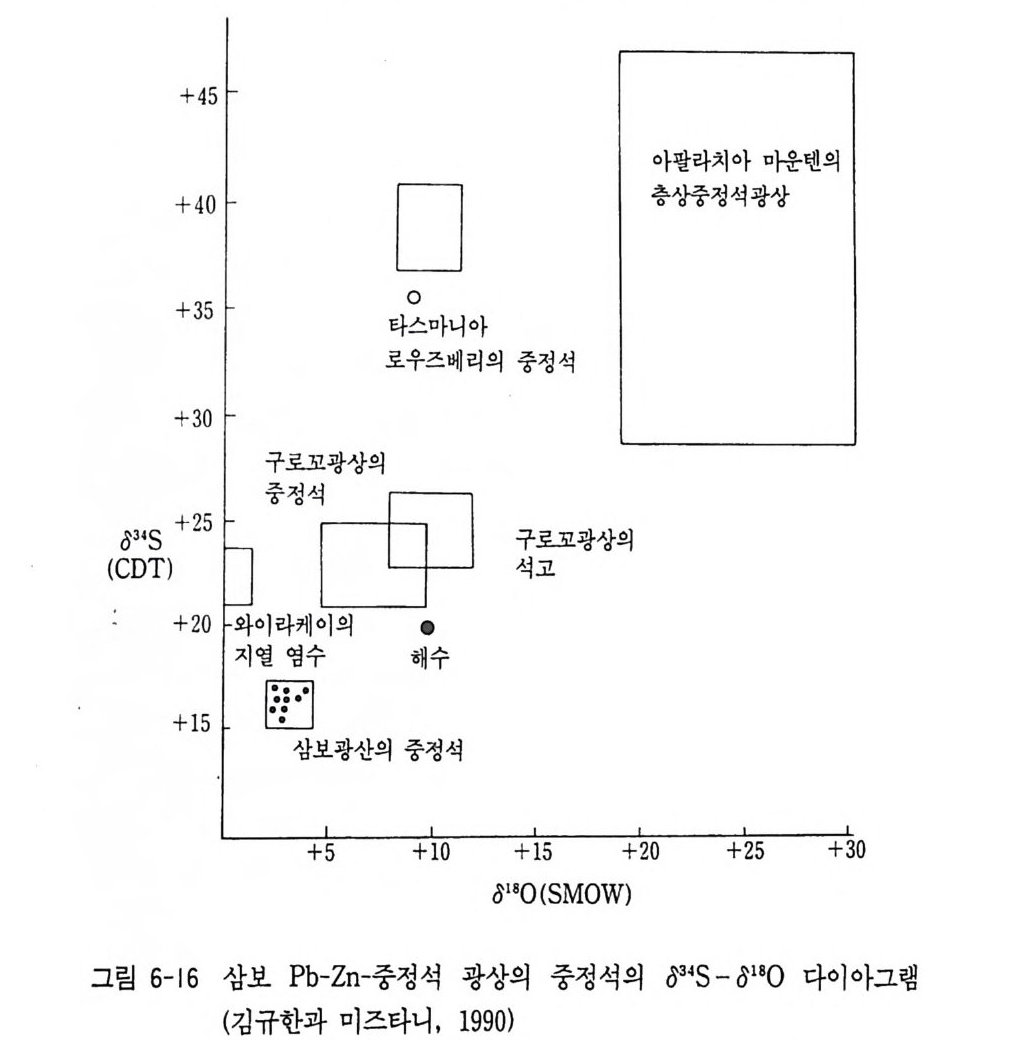 +45
+45
화용액 중의 산소의 기원이 달랐거나 마그마원 열수용액에 순환수와 혼입비율이 상이하였던 것으로 해석할 수 있다. 6-12 황의 순환 황은 퇴적 암 (4 .7/ 10 물), 해수 (3 . 9 / 10 몰), 대 기 (6.11 / 10 몰), 토양 (1 60/10 몰), 육상식물(1 9 / 10 몰)에 모두 들어 있다. 이들이 지질환경에 서 서로 순환하고 있다. 퇴적암내에서 황의 지구화학적 순환을 생각해 보자. 탄소의 지구화 학적 순환에서와 마찬가지로 황의 지구화학적 순환도 원시황 (Pri mo dia l sulfu r) 은 무거 운 동위 원소로 대 표되 는 산화형 과 주로 가벼 운 동위원소로 된 환원형의 황종으로 대분할 수 있다. 우선 해양 퇴적암계의 황의 순환을 모식적으로 가정하면 전체의 황은 1.33/ 10 22 g이고, 그 중 약 1 / 10 (1 ,3 / l021 g)이 의부 저장소에서 유래된다. 약 +20%o의 값을 가지는 해양 so~- 가 반응속도론적 동위원소 효 과 (KIE) 에 의하여 퇴적기원의 황화광물을 침전시킬 때에는 834S= ― 18 土 6 %o 가벼워지고 퇴적 황산염광물을 만들 때는 034S= +1 7 土 2 給로 평형분별이 일어난다. 퇴적기원의 황화물은 태양에너지 (hv) 에 의해 직접적 광합성작용이 나 간접적인 생물학적 산화작용에 의해 해양으로 되돌아간다. 원시황은 동위원소값이 8“S ::::: 0 %o (N 펴 sen, 1978 )이지만 박데리아의 작용에 의한 반응속도론적 동위원소 분별에 의하여 퇴적암내에서 만 들어지는 황화광물의 동위원소값은 현저하게 변화한다. 죽 박테리아기원의 H2S 가 퇴적물내에 존재하는 철이나 기타 금속 이온과 반응해서 황화광물을 침전시키므로 이 같은 생물학적 영향이 지각으로 계속 확산된다. 이 같은 황화광물의 동위원소 성분은 폐쇄된 간극수 환경에서는 레 이리 동위원소 분별작용의 영향을 받는다.
즉 가벼운 황이 황화광물에 우선적으로 농집되어 잔류 해성 황산염 광물에는 무거운 동위원소가 더 많이 집적된다. 퇴적기원 황화광물의 a34s 값이 변화가 다양한 것과 대조적으로 용 존 SO t이온은 그의 이동성과 해양에서의 빠른 혼합 때문에 잔류 황 산염의 a34s 값은 크게 변화하지 않는다. 따라서 해양 황산염의 평균값은 대체로 의부기원 황을 적분한 값을 의미할 것이므로 황산염의 동위원소값이 주어진 지질시대의 상태를 잘 반영해 중것이다. 해 양 황산염 의 잔류시 간을 20 Ma (H oIser 와 Kap la n, 1966) 이 라 가 정한다면, a34s 의 평균값에 의해 특칭지어지는 황의 정상상태 (St at i o- ary s t a t e) 가 지질시대를 통하여 빨리 수립되어야 할 것이다. 따라서 지질시대 동안에 황의 순환과정을 퇴적된 증발잔류암의 동 위원소 분석에서 연구할 수 있다. 탄소의 경우에서와 유사하게 834S 원시황 =Ro34S 황화 강문 + (1+ R) 034S 황산영장옹 (1) 의 관계로 생각할 수 있다. 평 균 퇴 적 기 원의 황화광물과 황산염 저 장소의 o3•s 값이 각각 +17%., 과 _18% 이며 동위원소 분별이 一 35%., 인 경우라면 여기서 R=S 황화왕인 (S 황화강문 +s 황산영광문) =0.5 이 되어 의부 황의 순환을 통하여 순환 되는 황이 환원형과 산화형으로 각각 반씩으로 분리됨을 알 수 있다. 지질시대를 통하여 황동위원소값의 변화는 그림 6-14 에서처럼 지난 600 Ma 동안에 034S 값이 크게 변화하고 있다. 최대값은 캠브리아기 의 +32% 에서 최소는 페름기의 +11 %o에 이른다. 페름기에 대규모 증발잔류암 형성시에는 낮은 034S 값을 나타내는 반면 고생대의 함황철석 셰일의 형성시에는 o3•s 값의 최대의 변화 패 턴을 나타내고 있다. 이처럼 해성 황산염의 834S 값의 변화원인은 위의 (1) 식에서처럼 퇴
적암내에 침적되는 산화형 황과 환원형 황의 비에 따라 변화하고 있 기 때문이다. 그림 6-17 에서 낮은 a 34 s 값을 나타내는 시기는 대량의 증발잔류암 형성시이며 퇴적원 황산염내에 대량의 산소가 존재하였던 시기로 이
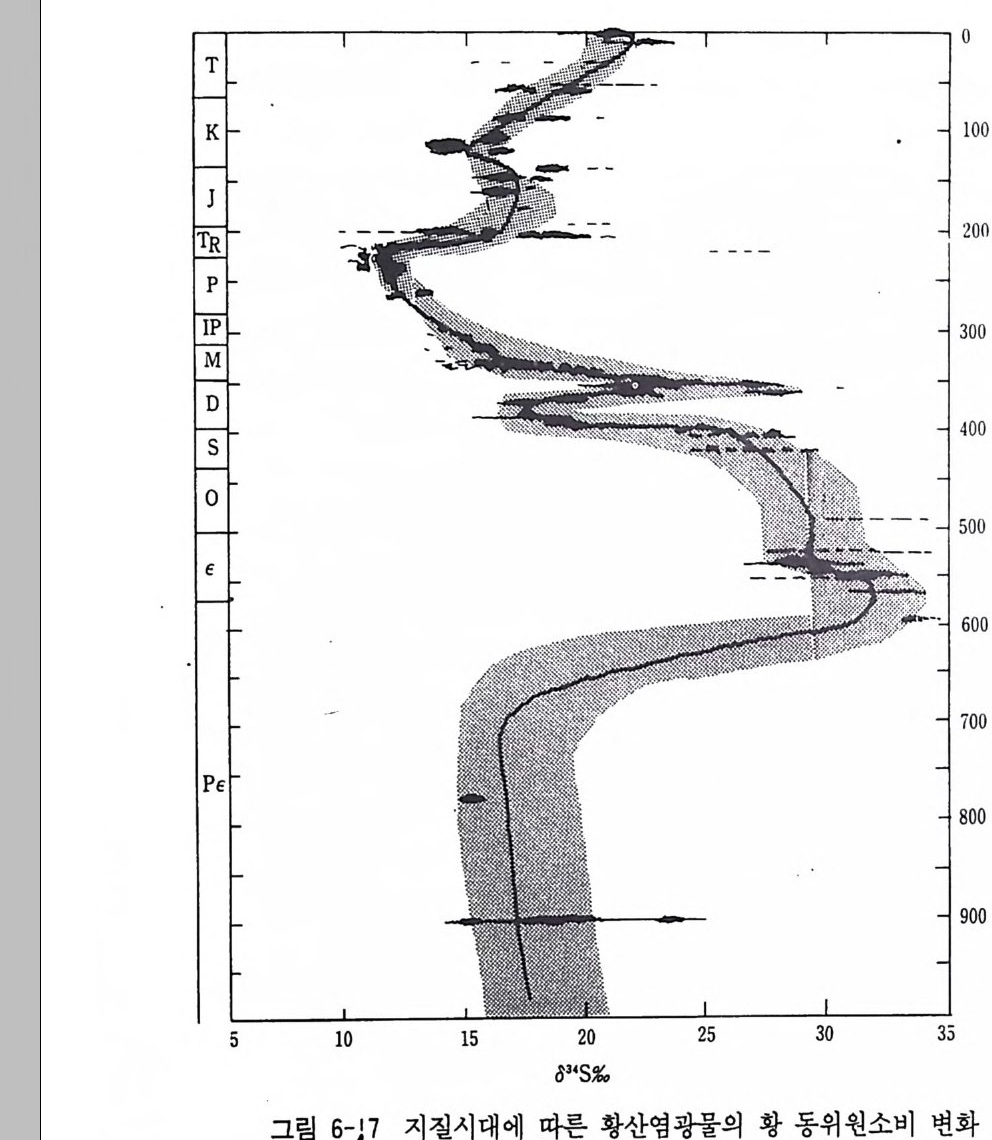 T 。
T 。
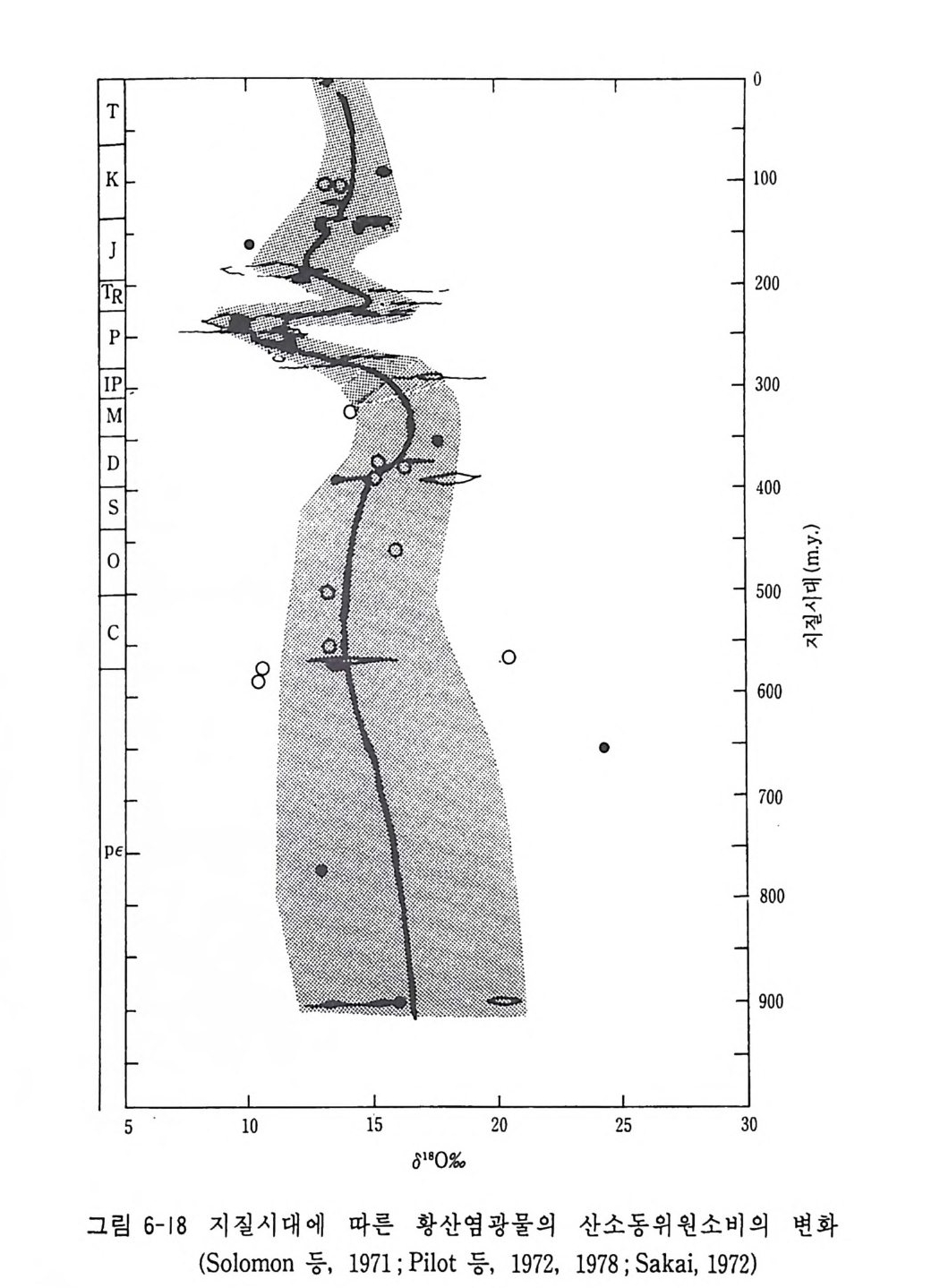 。
。
때 황산염과 결합된 산소의 동위원소값의 변동이 지구화학적 변수로 이용될 수 있다. 지질시대의 황산염광물의 산소 동위원소비 변화 경 향도 황의 경우와 유사하나 고생대의 변화 경향은 황과 크게 다르다 (그림 6-18). 산소의 순환이 탄소의 순환과 동일한 관계이기 때문에 황화물 / 황산 염비의 변화가 탄소동위원소값 변화에도 그대로 반영된다. 따라서 o13c 와 o3 ◄ s 사이에는 부의 상관관계가 얻어지는데 이런 관 계는 Veiz e r 등 (1980) 에 의해 분석 보고되었다. 참고문헌 Bemer,R. A . (1980) , Early Dia g e 11e sis : A Theo r eti c a l Ap pr oa c h . Prin c eto n Uni- versity Press, Prin c eto n , N.J ., p . 241 . Bemer,R. A. (19 85) , Sulfa te r educti on , orga ni c matt er decomp os it ion , and pyrite form ati on . Phil. Trans. R. Soc. Lond. A 315. pp. 25- 38 . Beth k e, C.M. (19 86) , Hy d rologi ~ constr a in t s on the ge nesis of the Up pe r Mi ss is s ip pi Valley mine ral ·dist r ict from Ilino is basin brin e s. Econ . Geo!. 81, pp. 233-249. Burnham, C.W. (1979) , Magm a s and hyd r oth e rmal flui d s . I n : Ge oc he 111 i st0 • of Hyd r oth e rmal Ore Dep o sits , 2nd ed ition . H.L. Barnes, ed., J . Wi le y and Sons, New York, pp. 71-136. Burnham, C.W . and Ohmoto , H. (19 80) , Late - sta g e pro cesses of fel sic mag- mati sm . Soc. Mi ni n g Geo!. Jap a n , Spe c ia l Issue 8, pp. 1-11. Cameron, E.M. (1983) , Genesis of Prote r ozoic iro n-fo rm ati on : Sulph ur iso to p e evi de nce. Geochim . Cosmochim . Acta . 47, pp. 1069-1074. Cameron, E.M. (19 82) , Sulph ate and sulph ate reducti on in early Precambria n oceans. Natu r e, 296, pp. 145-148. Cheney. , E.S. , and I.M . La ng e (19 67) , Evid e nce for sulfu r iz a ti on and the orig in of some Sudbury- type ores. Mi ne ralium Depo s ita , 2, pp. 80-94. Clayp o ol,G.E ., W.T.Holser, LR .K apl a n, H. Sakai, and I. Zak (19 80) , The age
curves of sulfu r and oxy ge n iso to p e s in m arin e sulfa te and the ir m utu a l int e r pr e ta t i on . Chem. Geol. 28, pp. 199-260. Fie ld , C. W., Gusta f s o n, L. B. (19 76) , Sulfu r iso to p e s in the por p h yr y cop pe r dep os it at El Salvador, Chil e. Econ. Geol. pp. 1533-1548. Kap la n, LR . (1983) , Sta b le iso to p e s of s ulfu r, nitr o g en and deute r iu m in recent marin e envir o runents . In : M.A. Art hu r, T .F . Anderson, LR. Kap la n, J. Veiz e r, and L.S. Land, eds., Sta b le Isoto p e s in Sedim enta ry Geolog y, 2-1 to 2-1 0 8, SEPM Short Course No. 10, P.O . B o x 4756, Tulsa, 0. K. Kaji w ara, Y., a nd H.R . Krouse (19 71 ) , Sulfu r iso to p e par tit ion in g in meta l lic sulfid e sys t e m s. Can. J. Ea1th Sci. 8, p p. 1397-1408. Kim ,K. H. ,and N.N a kai ( 19 82) , Sulfu r iso to p e comp os it ion and iso to p i c tem p er atu r es of the Shin y e m i lead-and zin c ore dep os it, weste r n Taebaegs a n meta ll og en ic belt, Korea. f ou r Kor. Inst. Mi nj n g Geol. 15 (3) , pp. 155- 16 6. Kim , K.H . and Y.Mi zu ta n i (1990) , Oxyg e n and sulf ur iso to p i c comp os it ion s of gu artz , barite and sulfid e min e rals from the Sambo Pb-Zn-Barite ore depo s it s s outh Korea (in pre p ar ati on ) . McCready, R.G .L ., LR .K apl a n, and G.A . Din ( l974) . Fracti on ati on of sulfu r iso to p e s by the yea st Saccharomy ce s cerevis ia e . Geochim . Cosmochim . Ac ta . 38, pp. 1239- 12 53. Monste r , J ., P .W .U.Ap pe l, H.G.Thode, M.Schid l owski, C.M . Ca nnic h ael, and D. . Brid g . va te r (1 979) , Sulfu r Isoto p e stu d ie s in early Archaean sedim ents from Isua, West Greenland : Imp lica ti on s to the anti qu ity of bacte r i al sulfa te reducti on . Geoclzim . Cosmoclzim . Acta . 43, pp. 405-413. Nakai, N., and M. L. Jen sen (19 64) , The kin e ti c iso to p e eff ec t in the bacte r i al reducti on and oxid a ti on of sulfu r. Geochim . Cosmochim . Acta . 28, pp. 1893-1912. Nie ls en, H. (19 74) , Isoto p e comp os it ion of the majo r contr ib u to r s to atm o - sph e ric s ulfu r. TellttS , 26, pp. 213-221 . Nie ls en, H. (1978) , Sulfu r iso to p e s in natu r e. In : K. H. Wedep o hl, ed., Hand- bo.o k of Geochemi stry, Spr i n g e r -Verlag, Berlin . Nie ls en, H. (19 79) , Sulfu r iso to p e s . In : E. Jag e r and JC .Hunzik e r, eds.: Lee- • tur es in Isoto p e Geology , 282-312. Spr i n g e r -Verlag, Berlin, p. 329. Ohmoto , oHre. (d1e9p72 o)s ,it s .S y E stc eo mn .a tGi ceso lo. f6 s7 u, lpfup .r 5a5n1d- 5c7a8r.b on iso to p e s in hyd r oth e rmal
Ohmoto , H., and R.0 .R y e (19 79) , Isoto p e s of sulfu r and carbon. In : H.L . Barnes, ed., Geoc /1e m is h )1 o f lzy dr oth e n n al ore d ep o s its , 2nd ed., 509 -56 7. Joh n Wi le y, New York, p. 798 . Ohmoto , H, Lasaga , A. C. ( 1 982) , Ki ne ti cs of r eacti on s betw een aqu eous sulfa tes and sulfid e s in hyd r oth e rmal sys t e m s. Geo c / 1in i . Cosm o ch im . Ac ta . 46. pp. 1727-1745. Ohmoto , H. and Ry e, R.O . ( 1974) , Hy d rog en and oxy ge n iso to p i c comp os it ion s of flui d inc lusio n s the Kuroko dep os it s, J ap a n . Eco n . Geo !. 6 9, p p. 947 -953. Ohmoto , H. (1985) , Thermodyn a mi c and kin e ti c evaluati on of the cause s of meta l rati on regu la riti es in low tem p er atu r e hyd roth e rmal dep o s it s. Geo!. S oc. Am. Abstr a cts wit h Prog 1'a m s, 17, p. 680. Ohmoto ,H . (1986) , Sy st e m ati cs of meta l rati os and sulf ur iso to p i c rati os in low-te m p er atu r e basemeta l dep os it s. Ter ra Cog n ita 6, pp. 134 - 1 3 5 . Ohmoto , H. (1986) , Sta b le iso to p e geo chemi st r y of ore dep os it s in Valley. et al eds. S ta b le iso to p e s in hig h tem p er atu r e geo log ica l pro cess e s. pp. 491 -559. Mi n. Soc. Americ a. Sakai, H . (19 57) , Fracti on ati on of sulfu r iso to p e in natu r e. Geo cl zi m . Cos m o- chim . Acta . 12, pp. 150-169. Sakai,. H . (1968) , Isoto p i c pro p er tie s of sulfu r comp o unds in hyd r oth e r m al pro cesses. Geoclzem. J 2, p p. 29-49. Sakai, H., A . Ueda, and C.W . Fi e ld ( 1978) , o3'S and concentr a ti on of sulfi de and sulf at e sulfu rs in some ocean-fl oo r basalts and serpe n ti ni t es . In : R.E . Zart ma n, ed., S hort pa pe r s of the Fourth Inte r nati on al Confe r ence. Geochronology , Cosmoclzronology and Isoto p e Geo lo gy . U.S. Geo!. Surv. Op en -Fil e Rep t. pp. 78-701, pp. 372- 37 4. Sakai, H., T .J. Casadevall, and J. G. Moore (1982) , Chemi str y and iso to p e rati os of sulfu r in basalts and volcanic gas es at Kil a uea volcano, Hawaii . Geochim . Cosmochim . Acta . 46, pp. 729-738. Sang st e r , D.F . (19 68) , Relati ve sulfu r iso to p e abundances of ancie n t seas and str at a b ound sulph id e dep os it s. Geo!. Assoc. Canada Proc. 19, pp. 79-91 . Sasaki, A., and S. Ishi ha ra (1979) , Sulfu r iso to p i c comp os it ion of t he magn e ti te- seri es and ilm enit e- serie s gran it oi d s in Jap a n . Contr ib . Mi ne ral. and Sawkin s ,P eFt.r] o.l ,. O68'N, pepil., 1 J0.7R -.1, 1a5n. d Thomp so n, J.M . (1979) , Fluid inc lusio n and
geo chemi ca l stu d ie s of vein go ld dep os it s, Bag uio dis t r ic t , P hil ip p ine s. Econ. Geo!. 7 4, pp. 1420-1434 . Schid lo wski, M., Hay es , J. M. , Kap la n, I. R.(1983), Isoto p i c inf e r ences of ancie n t bio - c h emi st r ie s : carbon, sulfu r , hyd r og en and nit ro g en . In : Schop f, J. W. (ed.) Eart h ' s e arlies t bios p h ere: Its orig in and evoluti on . Prin c eto n Univ . Press., p p. 149-186. So, C.S ., a nd Shelto n , K.L. 0983) , A sulfu r iso to p i c and flui d inc lusio n stu d y of the Cu-W- be arin g tou rmalin e breccia pipe , I lkwang min e , Rep u blic of Korea. E co n . Geo !. V . 78, pp. 326-332. So, C.S .,R ye , D.M ., and Shelto n , K.L. ( 1983) , Carbon, hyd r og en , oxy ge n, and sulfu r iso to p e and flui d inc lusio n stu d y of the Weolag tun g st e n - mo ly b d enum dep os it , R ep u blic of K orea, F luid his t o r ie s of m eta m orph ic and ore-fo r mi ng events . Econ. Geo!. V. 78, pp. 1551-1573. So,C .S ., Shelto n , K.L., a nd Ry e, D.M . (19 83 ) , Geolog ic, sulf ur iso to p i c, and flui d inc lusio n stu d y of the Ssang Jeo n tun g st e n min e , Rep ub lic of Korea. Eco 11 . Geo !. , V. 78, pp. 157- 16 3. So, C.S ., Shelto n , K.L., S eid e mann, D.E., and Skin n er, BJ . ( 19 83) , The Dae Hwa tun g st e n -molyb d enum min e , Rep u blic of Korea, A geo chemi ca l stu d(' Eco n , Ge o!. , V .7 8 , pp. 920-930. So, C.S .,S .J .C h i and S.H.Choi ( 1988) , Geochemi ca l stu d ie s on Au-Ag hyd r oth e r- mal vein dep os its , Rep u blic o f K orea, Jina n-Je o ng eu p min e raliz e d area. fou r, Mi u. Pet . Econ. Geo!. 83 (11) , pp. 449-471 . SO, C.,S .P ark, M.E., K L .Sh elto n and D.E Seid e mann(l984) , Geolog y and Geochemi st r y of the Sambo Pb-Zn dep o sit, Rep ub lic of Korea. Econ. Geo!. 7 9, pp. 656-670. Wi lliam s, N. (19 78) , Stu d ie s of the base meta l sulfid e dep o sits at McArth u r Riv e r, North em Temi tor y. Austr a lia, 11 The sulfid e -S and carbon-C relati on ship s of the concordant dep o sit s and the ir sig nifica nce. Econ. Geo!. 7 3, pp. 1005-1035. Zie r enberg, R. A., Shanks, W, C., Bis c hoff , J. L. (1984) , Massiv e sulfid e dep o sit at 2l' N, East Pacif ic Ris e , chemi ca l comp o sit ion , sta b le iso to p e s , and ph ase equ i li br ia . Bull. Geo!. S oc. Am. 95, pp. 922-929. Zobell. C. E. (1958) , Ecolog y of sulfa te- reducin g bacte r ia l . Prod-Mong r 22, 12. Jw a,Y.J. (1989) , Vein form ati on and min e rali za ti on of the Sambo Pb-Zn-Ba
dep os it ; South Korea. Mi ni n g Geo!. 39 (6) . pp. 383- 39 2. 김규한, 中井信之(1 980). 「한국의 일부 금속 광상의 유황 동위원소 성분 및 동 위원소 지질온도에 관한 연구」, (( 지질학회지 )) 16(2). pp. 124~ 13 4,
7 질소 안정동위원소 7-1 서언 질소는 원시 대기성분의 CH., H2, NH3', H20 와 함께 중요한 위 치를 차지하고 있으며 생물체내의 DNA 나 RNA 등의 핵산이나 고에 너지 화합물 NDA 등의 보효소 구성성분으로 생물계에 중요한 역할을 하고있다. 질소는 N 2 고정_생물권 ==NO;--N2 로 순환하고 있다. 따라서 생명활동과 물질순환 연구에 질소 안정동위원소가 이용되고 있다. 그러나 아직 질소 동위원소의 분별이나 응용연구가 다른 환경 동위원소에 비해 부진한 상태이다. 그러나 질소의 순환, 식물의 물질 신진대사 과정, 생명활동과 질소순환, 생명의 기원, 토양오염 등의 연구의 수단이 될 것이다. 질소는 “N(99.64%) 와 1 5N(0.36% )의 두 종류의 동위원소로 되어 있다. 동위원소비는 N2 가스로 측정하며 표준시료는 대기중의 질소가 이 용된다. 질소 동위원소의 표시는 a1sN =( 問/::記 -1)-1000 (%.,)
 .. & 10A0 8 0
.. & 10A0 8 0
으로 한다. 표준시료는 대기 (15N / UN=3676.5 士 8.1) 가 이용되고 있다. 자연물질의 o1sN 분포는 다양하며 해수 -5 ~ +9 %o, 해양퇴적물 + 2 ~ +15%o, 석유 석탄 천연가스 —12 ~ +18% 암석광물 一 18 ~ +30% o 그리고 달암석은 -40 ~ +100%0 까지 값의 변화 범위가 크다 (그림 7-1). 7-2 질소 동위 원소의 분별 생물권에서의 질소 동위원소 변화는 무기원질소의 동화, 질소고정, 질산화반응 (N it r ifi ca ti on) , 탈질산화반응(D en itrifi ca ti on) , 암모니 아화 반웅 (Arnon ifi ca ti on) 및 기타 질소 신진대사작용과 같은 생화학적 반 응에 의한 반응속도론적 동위원소 분별작용에 의하여 일어난다. • 질소의 생화학적 순환과정은 다음과 같다. O 질소 고정반응 : N 2( g )+ 3H 2 0( g )_2NH3( g)十 3/202( g) (a=l .00 0) ® 질산화반응 : NH3+3/2 0 2-HN02+H20 HN02 + 1/2 02 一 HN03 ® 탈질산화반응 N: HC tsH一12 0Ns0+22(4a/5= l.N 0004)3 +24/5 H+-— ~6C 02+42/5 H20+12/5N2 NO;- 一 N2(a= l. 02) 그리고 평형분별 반응으로 ® 암모니 아 휘 발반응 : NHt ~N H3(g> (a= l. 034, 25'C) ® 질소가스 용해 반응 : N2~N2c8> (a= l. 00085, O'C) 등의 반응과정이 있다. 그러나 질소 동위원소 분별에 관한 실험연구 는 많지 않다. 질소 안정동위원소는 주로 질소의 순환, 상이한 환경에서 질소의 침전과 질소의 기원해석 등의 연구에 이용되고 있다 (Kohle 등, 1971 ;
Edward, 1973 ; Pan g와 Nria g u , 1976 ; Yoshid a , 1988 등) . 석유나 케로겐 물질의 질소의 동위원소비로서 과거 지질시대에 생 물학적인 과정에 의해 질소 동위원소 분별이 일어났음을 추정하였으 나 분석자료가 적어 아직 어떤 생물학적 질소 이용 동안에 어떤 동위 원소 분별반응이 일어났는지는 알 수 없다. 고생대 이후 퇴적물의 OISN 바와 선캠브리아기 시료의 OISN 비가 유 사한 분포룰 나타내기 때문에 비교적 오랜 지질시대 전에 이미 생물 학적 질소순환이 일어났었음을 추정하고 있다. 7-3 질소동위원소의 이용 암석 광물학에서 질소동위원소의 응용보다는 토양오염 연구, 생태 계의 물질순환, 동물의 영양관계 평가 등의 응용연구가 더 활발하다. 이들의 연구내용을 간략히 소개한다. 변성암 중의 운모나 기타 규산염광물의 결정격자내에 암모니움 형 태로 질소가 고정되어 있고 유체 포유물내에 질소분자로 소량 존재하 기도 한다. 변성암의 변성도가 증가함에 따라 암모니움의 질소의 함량 과 질소 동위 원소값 (a1sN) 이 증가하는 경 향이 나타났다(H aendel 등, 1986). 이때 질소함량은 감소하고 a1sN 값은 증가하였다(그립 7-2). 북동 태평양 대륙봉 퇴적물의 질소 (a1sN) 및 탄소 (813C) 동위원소 비 분석에서 이들 지역 퇴적물이 비유기물인 NO;-, HCO;- 와 N2, co 플의 혼합을 추정할 수 있게 되었다(그림 7-3). 해양퇴적물의 동 위원소 분석에서 이처럼 해양되적물의 기원을 추정할 수 있고, 14c 연대측정과 함께 퇴적물의 퇴적속도를 연구할 수 있다. 그리고 질소 와 탄소의 동위원소를 이용하여 생명활동에 따른 물질순환을 연구할 수도 있다. 지구상의 상이한 생태계의 동식물의 시료의 질소와 탄소 의 동위원소비를 분석하여 a1sN 와 813C 관계를 도시하여 보면 그림 7-4 와 같다.
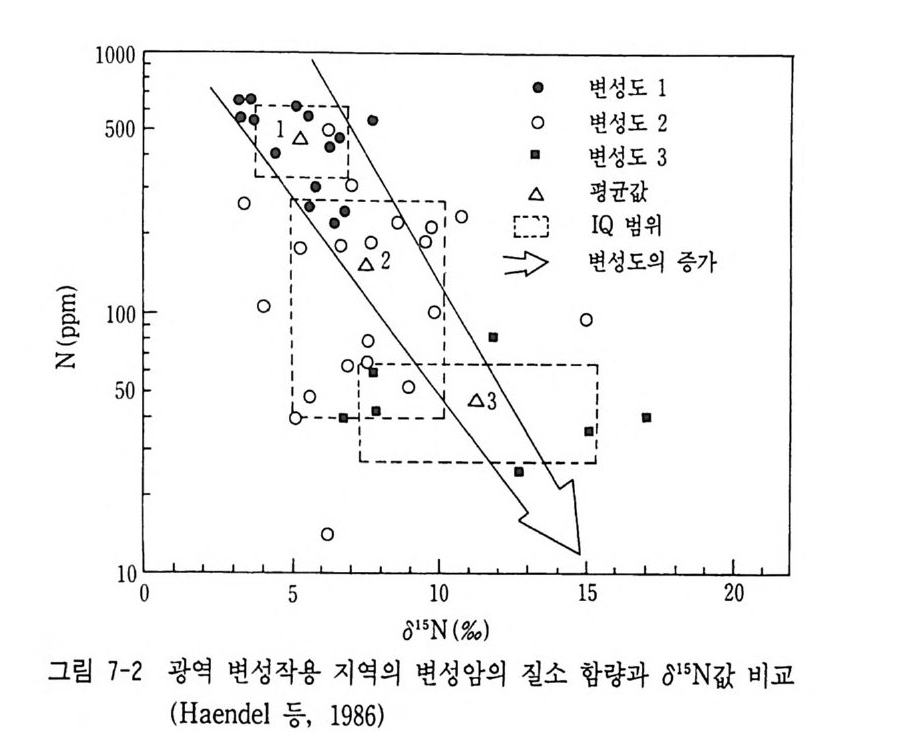 15000 00 니“\L 0 -.,_'• 占•0 · 변변평IQ성성균 범도도값위 32
15000 00 니“\L 0 -.,_'• 占•0 · 변변평IQ성성균 범도도값위 32
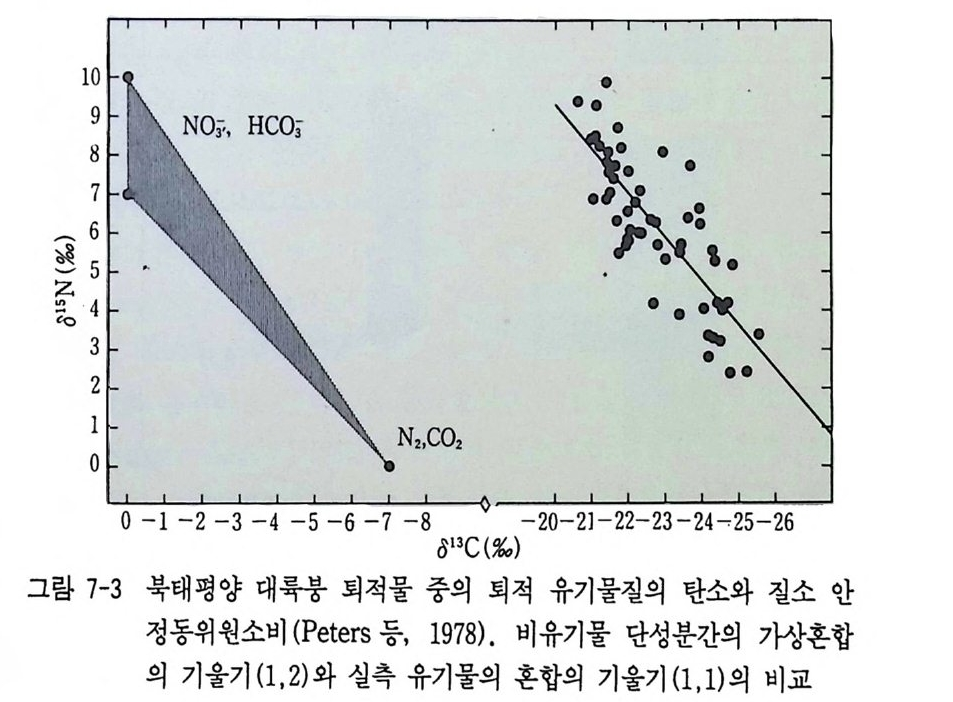 098765432 •IL
098765432 •IL
 :21.3% 二데 0. 14식釋〔〔;\
:21.3% 二데 0. 14식釋〔〔;\
식물의 815 N 값은 식물이 생육에 이용된 질소의 기원에 따라 구별된다. 질소고정으로 이루어진 계에서는 o1sN 값이 —2 ~ _0 %o이며 대기 중의 NH 3 나 N0 2 는 생성시의 동위원소 분별작용 때문에 815N 값이 麟 이하의 낮은 값을 가진다. 따라서 주로 강수와 질소고정에 의해 질소가 공급되는 산악지역의 산림은 815N 가 —2 ~ 0%,, 의 값을 가진다. 한편 토양 중의 무기형태의 질소는 NH3 의 증발 (a= l. 034) 이나 탈 질산화반응에 의해 815N 값이 5 ~ 6% 로 커지며 이들이 육상식물의 생육에 반영되어 C3 석물이나 C4 식물과 갇은 육상식물은 이의 영향 을 크게 받는다. 식물 중에 가장 높은 · 소 동위원소값을 가지는 것은 펭귄롯가리에 생육하는 녹조인 가와노리 (01 5 N= + 2 1. 3%) 이다. 왜냐하면 펭귄이 배 설한 뇨산이 토양 중에 분해되어 NH t가 되어 일부 가벼운 NH3 는 증발하고 남은 토양 중의 NH t에 박{가 농집되었기 때문이다. 가벼운 질소 동위원소값을 가지는 것은 남극의 드라이베리의 빙하 되적층인 모레인 중의 염수호에서 산출된 남조류에서 나타나는데, 이 지역에는 강설 중의 무기원질소의 015N 값이 _20%0 정도로 낮고 또 남조류가 호수 중의 N03 와 동화될 때 동위원소 분별정수가 1.03 크 기 때문으로 보고 있다. 또 C3 식물과 C4 식물은 815N 값은 유사하 나 o1 3 c 값이 현저히 다르다. 왜냐하면 중위도 해양이나 저위도 해양 지역에서는 식물 플랑크론 의 증식속도가 빨라서 광합성시 C 아의 흡수가 탄소 고정속도를 능가 하므로 육상식물보다 7%。 정도 높게 나타난다. 따라서 815N 값과 o13c 값의 동위원소 분석으로 동식물질의 기원을 해석할 수 있다. De Ni ro 와 Has t ro f (1985) 에 의하여 고분에서 발굴된 인간의 뼈에서 콜라겐을 추출하여 청 5N 값과 o13c 값을 분석함으로써 이들의 생식물 질의 근원을 밝힐 수 있게 되었다. 예를 들면 o15N=+l6 ~ +22% o, 013C=-18 ~ -8 %o의 값을 가지 는 에스키모인의 뼈는 이들이 어류 등 해양 육식동물을 주식으로 하
였기 때문이다. 그리고 815N= +17 ~ +IO%o, a13C= —22 ~ —18% 0 의 값을 가지는 신석기시대 유럽인들의 뼈에서 C3 식물을 주식으로 한 육성초식이나 C3 초식을 주로 한 육식동물을 주식으로 하였음을 추정할 수 있었다. 또한 성 5N= +7 ~ +11%.,, a13C= -7 ~ — 5% 의 값을 가지는 멕시코의 데후아칸 인디언의 뼈에서 C4 식물(옥수수, 사 탕수수 등)을 주식으로 하였음을 밝힐 수 있게 되었다. 이처럼 식물은 생육장소의 환경에 따라 다른 동위원소비롤 가지므 로 질소 및 탄소동위원소비가 이들을 구별하는 자료로 이용되어 생태 계의 물질순환을 연구할 수 있게 되어 고고학의 새로운 연구 분야로 등장하고 있다. 7-4 만 퇴적물의 기원 대륙봉, 만, 호수 퇴적물의 질소 및 탄소 동위원소비를 분석하여 육 상 유기물이 상기 퇴적지로 이동되는 과정이나 비율을 연구할 수 있다. 육상 고등식물과 위도차에 따른 퇴적물의 플랑크톤 중의 동위원소 비의 차이가 나기 때문에 이룰 트레이서로 이용할 수 있다. 예를 들면 Wada 등(1 887) 의 연구결과에 의하면 일본의 이와데현 (岩手県)의 오오스즈찌가와(大雄川) 수계 연구에서 산악지역에서 하천을 통해 유입되는 유기물은 815N=1.8% o, 813C= -26.5%o 이고 오오쯔찌 만(大雄灣)내의 식물 플랑크돈은 815N=6.3% o, 813C=-20.3%o 이었다. 만내에 분포하는 퇴적물은 장소에 따라 다론 동위원소비를 가지며 815N=0.72 813C+20.9 의 관계식을 나타내고 있다. 이는 상이한 두 기원의 유기물의 혼합을 의미하고 있다. 그래서 이들의 반영된 비율 울f라하면 f=-8- 대)양해-양 _8.육 8상 되기저원물물 질 XlOO
이 된다. 이 지역에 표충 퇴적물에 대하여 계산한 결과 만내에서 f =55 一 90% 이고 만입구에서 35% 가 얻어졌다 (Wada 등, 1987). 7-5 생태계의 물질순환 생태계에서는 끊임없이 물질순환이 일어나고 있다. 계내에서의 유 기물이 1 차 생산자에서 경과시간과 거리를 나타낸 영양단계 (Tro phic level, TL) 와 순환시간의 관계를 질소나 탄소동위 원소비를 분석 하여 연구하고 있다. 이들 동위원소비로 생물체의 구성 유기물의 기원, 식 생, 영양단계에 관한 정보를 얻을 수 있다. 왜냐하면 ® 식물의 1s N ;1 4N, 13c ; 12c 비는 생육환경, 질소동화의 물질대사계 의 차이와 CO2 고정계의 차아에 따라 다르며 ® 동물체의 13c 함량은 먹 이와 큰 변화가 없으므로 동물의 13c 함 량 변동을 유기물의 이동의 트레이서로 사용할 수 있으며 ® 동물 체내의 1sN 함량은 일정한 비율로 먹이의 1sN 함량보다 높 으며 동물의 ISN 함량은 식생이나 영양단계의 척도가 될 수 있기 때 문이다. Wada(l986) 에 의하면 먹이와 먹는 자 사이에 815N 값의 차 는 3.4 土 1%퍼 얻어졌다. 식물의 영양단계를 1 로 하고 식물을 먹는 동물을 2… … 으로 하면 815N (동물) =a {TL (동물) _ l} + 815N (식 물) 의 직선관계가 얻어진다. TL 값은 동물이 잡식일 경우에나 성장시에 식성이 변화할 경우에는 변화한다. 이것을 검증하기 위하여 생물종의 수도 적고 식성이 확실 한 동물이 많은 비교적 단순한 생태계로 되어 있는 남극 해상 생태계 를 택하여 동물의 s1sN 값과 TL 과의 관계를 얻은 것이 그림 7-5 이다.
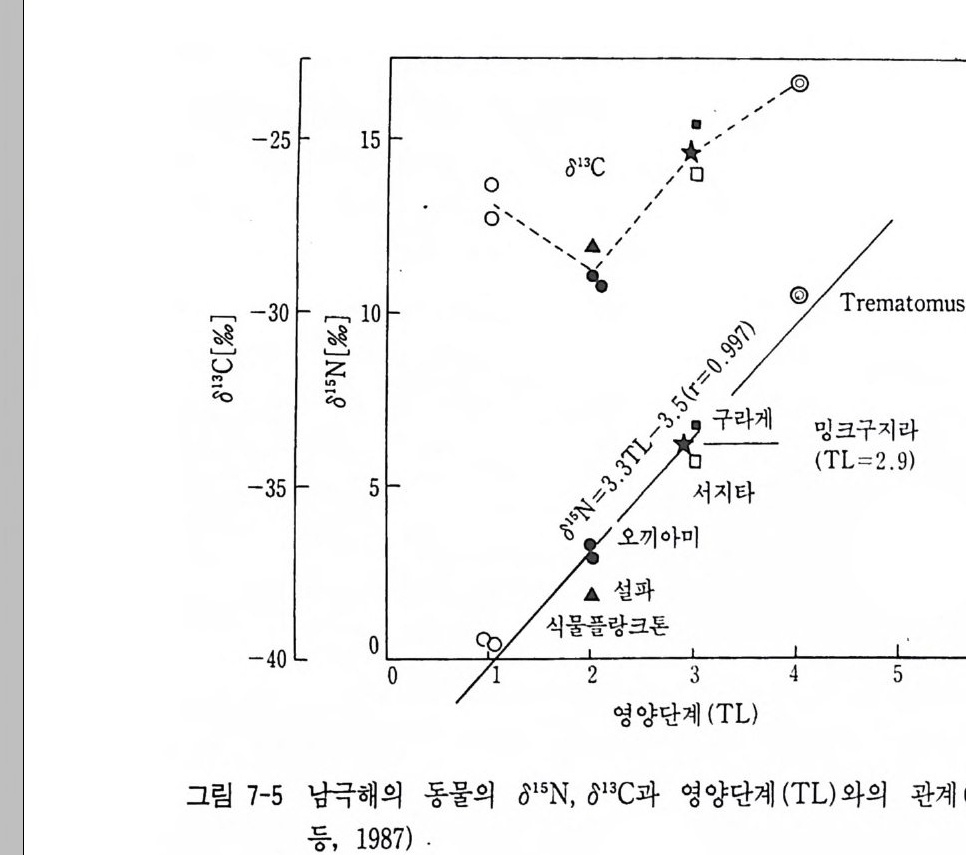 t 9 c3 _25 gsN15 o 8'3C 二/ 정. , /· /0 1 a\
t 9 c3 _25 gsN15 o 8'3C 二/ 정. , /· /0 1 a\
여기서 J ISN( 동물) =3.3(TL-1) ~0.2 가 얻어졌다. 남국 오끼아미를 주식으로 하는 밍크쿠자라 (TL 의 예상치 3 .0) 에 대 하여 a1sN 을 측정하고 이 식에서 TL 을 구한 결과 2.9 士 0.3 이 얻어 졌다. 식물 플랑크톤의 JIS N 값은 계절변화 때문에 위의 식을 일반화하 면 a1sN( 동물) =3.3(TL-1)-815N( 식물)로 표현할 수 있다. 이 관계 는 담수호에도 성립하였다. 그러나 여러 동물간의 지방질의 차가 크기 때문에 813C 값에 대하여 서는 특칭적인 변화가 얻어지지 않았다. 지방질 중의 “C 함량이 단백 질이나 당에 비해 6%o 낮은 것으로 알려져 있다 (Wada, 1968).
이 같은 동위원소 연구는 생태계의 생물종과 식성의 변화 등과 갇 은 물질의 거동을 화학으로 규명할 수 있음을 의미해 주고 있다 (Ha ny a, 1988) . 참고문헌 Becker, R.H . , a nd R.N . C la y ton (l977b), Ni trog e n iso to p e s in igne ous rocks. Eos, Trans. A mer. G eop hy s . Unio n , 58, p. 536. Becker, R.H ., and R.N .Clay ton (l977b), Ni trog e n iso to p e s in lunar soil s as a measure of cosmi c-r a y expo s ure and rego l it h histo r y. Proc. 8 th Lunar Sci. C onfe r ence, Geochim . Cosmochim . Acta . vol. 1, 3685-3704, Per- gam on Press, N ew York. DeNi ro , M.J ., a nd S.Ep st e i n ( 1981) , Inf lue nce of diet on the dis tr ibu ti on of nit ro g en iso to p e s in anim als. Geochim . Cosmochim . Acta . 45, pp. 341-351 . DeNi ro , M.J. , and C.A . H a sto r f (l9 85) , Alte r ati on of 15N/14N and 13C/12C rati os of pla nt matt er durin g the initial sta ge s of diag e n esis . S tu d ie s uti lizi n g archaeolog ica l spe c im ens from Peru. Geochi m . Cosmoch im. Acta . 49, pp. 97-115. DeNi ro , M. J. (1987) , Sta b le iso to p e and archaeolog y. Amer. Scie n ti st, 75182-91 . Edwards, A.P . (1973) , Isoto p i c trac er tec h niqu es for ide nti fica ti on of s ources of nitra te po lluti on . ] . Envir o n. Qual. 2, pp. 382-387. Haendel, D., M t ihle , K., Nit zs che, H. M., ·Sti eh l, G., W and, U. ( 1986) , Isoto p i c varia t i on s of the fixed nitrog e n in meta m orp hic rocks. Geochim . Cosmochim . Acta . 50, pp. 749-758. Kreit ler , C.W. (19 79) , Ni trog e n -is o to p e rati o stu dies of soil s a nd grou ndwate r nitr a te from alluvia l fan aqu i fe rs in Texas. ] . Hy dr olog y, 42, pp. 147-170. Leto l le, R. (19 80) , Ni trog e n -15 in the natu ral env iro nment. In : P.Fri tz and J. Ch. Fonte s , Handbook of Envir o nmenta l Isoto p e G eochemi stry, vol. lA,
pp. 407-434. Elsevi er , Amste r dam, 545p . Mari ot t i, A. (1984) , Natu r al 15N abundance measurements and atm o sph eric nitr og e n sta n dard cali br ati on . Naltm , 311, pp. 251 - 25 2 . Mart iot ti , A., C. Lancelot, a nd G. Bil len (1984) , Natu ra l iso to p i c comp os it ion of nit rog e n as a tra cer of orig in for suspe n ded orga n ic matt er in the Scheid t estu a ry . Geochim . Cos ,no chim . Acta . 48, pp. 549 - 55 5 . Min a g aw a, M. , and E.W ada (1984) , Ste p w is e enric h ment of 15N along foo d chain s , Furth e r evi de nce and the relati on betw e en o15 N and anim al age . Geochim . Cosmoc hi m . Acta . 48, pp. 1135-114 0. Pang, P.C ., and J.0 . N r ia g u (1 976) , Dist r ib u ti on and iso to p e comp o sit io n of nitrog e n in Bay of Qu in t e ( Lake Onta r i o ) sedim ents . Che m . Geo! . 18, pp. 93-105. Pang, P.C.,and J.O . Nr ia g u (19 77) , Isoto p i c varia t io n s of the nit ro g en in Lake Sup er i or . Geoclzim . Cosmochim . Acta . 41, pp. 811-814 . Pete r s, K .E .,Sweeney , R.E ., an d Kap la n, I.R. (19 78) , Correlati on of carbon and . nit or ge n sta b le iso to p e s and sedim enta r y orga n ic matt er . Lim nol, Oceo n og r. 23, pp. 687-692. Ross, P .J ., and E.A . M art in ( 19 72) , Rap id pro cedure for pre p ar in g ga s samp le s for nitrog e n -15 dete r mi na ti on . A1zalys t , 9 5, pp. 817- 82 2 . Sain o , T., and A.H a tt or i (1980) , 15N natu r al abundance in oceanic suspe n ded par t icu late matt er. Natu r e, 2 83, pp. 752-754. Shearer, G.,D.H.Kohl, and S.H . Ch ien (1978) , The nit ro g en -1 5 abundance in a wide varie ty of soil s. Soil S ci . Soc. Amer. ]. 4 2, 899p . Sweeney, R .E ., K .K. Liu , a nd I.R. Kapl a n(1 9 78), Oceanic nit rog e n iso to p e s ·a n d the ir u ses in dete n n ining the source of sedim enta r y nit ro g en . In : B.W . Robin s on, ed., S ta b le iso to p e s in earh sci en ce, Dep t. Sci . I nd. Res., New Zealand, Bull. 2 20, p. 9. Wada, E.,T. Kadonaga , and S. Mats u o (1975) , 15N abundance in nit ro g en of natu ral ly occu rring substa nc es and glo bal assessment of d en itrifica ti on from iso to p i c view po in t. Geoc he m. J 9, pp. 139- 14 8. Wada, E.,R. Irna izu m ian d, Y. Takai ( 1984) , Natu r al abundance of 15N in soil orga nic matt er with spe cial refe re nce to pad dy soil s in Jap a n . Bio g e o - chemi ca l im p lica ti on on the nit ro g e n cyc l e. Geochem ]. 18. pp. 109-123. -W ada, E.M . Te razaki , Y .Kabaya , and T.Nemoto ( 1987) , Deep -s ea. Res. 34,
pp. 829-841 . Yoshid a , N. ( 19 88) , 15N-dep le te d N2 gas a pro duct of n it rifica ti on . Natu r e 335, pp. 528-529. Yoshid a , N., Mats u o, S. (1983) , Ni tro g en iso to p e rati o of atm o sph e ric N20 as a key to the glo bal cyc l e of N20. G eochem. J 17, 231-239. 和田英太 M0986), 「生物界(I) “N, 13C (I)分布'각屈寸 5 總說」, Radio is o top e s 35, pp. 136-147. 半谷高久, 一國雅己, 石渡良志 和田英太郞 (1988)I 『 地球化學入門 』 , 丸善株式會 社, 2llp.
 제 3 부 방사성동위원소 지질학
제 3 부 방사성동위원소 지질학
8 방사성동위원소 지질학 8-1 서언 시간은 절대적 시간과 상대적 시간으로 나누어 생각할 수 있다. 지질연대표 등은 주로 화석이나 부정합과 지각변동 등 지질학적 큰 사건에 의해 구분된 것으로 주로 상대적 개념에서 수립되었다. 그러나 지질학적 모든 현상의 설명에 있어서 시간의 요소는 공간적 인 요소와 함께 대단히 중요하다. 특히 철대적 시간개념이 대단히 중 요하게 되었다. 지구의 시간개념을 처음 얘기한 사람은 고대 인도의 철학자로, 〈지 구는 영원하다〉라는 표현에서 시작되었으며, 중세 기독교인들은 지구 의 나이믈 4,004 년으로 예언한 바 있다. 절대적 시간 측정을 위해 졸리 (Jo ly, 1898) 는 해수의 염분도 측정에 서 9 , 000 만 년의 지구의 연령을 밝혀냈다. 지구의 냉각속도 (Kel vi n, 1897) 와 되적속도 등의 측정에 의해서도 지구의 나이를 측정하였다. 그러나 모두 지구의 연령인 46 억 년에 가까운 값을 얻지 못하였다. 1896 년 벡 쿼 렐 (Becqu e rel) 에 의 해 방사성 이 발견된 후 큐리 부부가 우라늄 광석 에서 두 가지 방사성 동위원소인 10Pa, Ra 을 분리하는 데 성공하였다 . 방사성 동위원소의 붕괴시 반감기를 이용하여 절대연령
측정이 가능해졌고 그 분석 정도도 대단히 높아졌다. 지질학에 많이 이용되는 장반감기 방사성 동위원소는 81Rb_87Sr, 40K- 4oAr, 238U, mu, 232Th-Pb , 141Sm-•43Nd 등이며 176 L u- 1 76 H f, 138La- 13ece, 1e1Re-1s10s, 등도 있다. 한편 단반감기 방사성 동위원소는 “C _l4N, 230Th 등이 있다(표 8-1 ) .
표 8-1 지질연대학에 이용되는 방사성동위원소의 종류와 측정 연령범위 A 반감기 연 령측정 모원소와 딸 모원소 /딸원소 붕괴 양식 (년 -1)• ( 년 ) 범위(년) 원소의 지각 측정대상뭉질 에서 존재량 2( 장3IU반I 감20기 'P핵b 종 〉 Ba+6P l(. I.5 535 61925x X1 10 0--•10 0 ) 4.sox 1 0• 10 '-To 00..2959228g g / g/ g P U b 나저이어트른 모우나라자 니이 트, 기타 납함유 감땅 'U/'0'P b 7a+4/3 9(9..78 24 1865 XX J 1 O0-- 1 0) 0.i l X 109 10' -To 00..02 017 52gg / g/ g P U b ” 'Th /’°‘ P b 6a+4 {3 4(4..9 9 8 4i7 5X X 10l Q-1- 1 I I ) 1.39 X 1010 10'- To 01..5002 0 gg // gg TPhb ” Rb/Sr fJ l.39 x 10-11 5.0 X 1010 10'- To 0.278g /g Rb 흑운모, 백운모 , (1. 42 X lQ- 1 1) 0.0 7 g /g S r 미 사장석. 전 암 '°K/Ar 전자포획 0.5 8 4 X 10-•• 1. 30 X1 0' 5 , 000-T o O. OOOlg /g K 흑운 모, 백운모, (0 . 581 x 10- 10 ) (tot a l ) 0.9 9 6g /g A r 각섬석, 전 암 K/Ca 8 4. 72x 10-•• (4 .96 2 X1 0- 10 ) 〈단반감기핵중〉 C/N /3 1.2 1 X 10 기 5,7 30 0-70,000 10-12g /gC 목단 목재, 토 0.9 9 6g /gN 탄, 곡식, 기타 탄소함유 물질 〈소멸핵종〉 Al Mg 9.6 o x 10-1 7.2 0 X 1 05 운석 . 기타 외계 물질 ,.'Pd '01Ag l.07 X 10 가 6.5 0 Xl06 12'I 12,Xe , 4.3ox10-• l.60 X 1 07 a‘Pu 131-‘Xe 8.SOX 10 내 8.20X 107 To 는 지구의 연령임
8-2 방사성 붕괴와 연령 측정원리 방사성 붕괴는 원자핵에서 방사성을 방출하며 원자번호가 다른 원 자로 변화되는 과정을 말한다. 비스머스(Bi)보다 원자번호가 큰 원소 는 모두 방사성을 가지며 탄소 (l4C) 처럼 원자번호가 작은 자연원소 중에 약한 방사능을 가진 것이 있다. 방사성 원소의 방사성 붕괴란 불안정한 핵이 더욱 안정하게 되기 위해 일어나는 작용이다. 방사성 동위원소의 붕괴는 a 붕괴, /3 붕괴 그리고 7 선 방사 등으로 일어난 다. a 입자는 2 개의 중성자와 2 개의 양자로 되어 있는 4He 원자의 핵 OHe) 이다. 이 입자는 a 붕괴 동안에 불안전한 핵에서 튀어나온다. 그 후 잔류핵(딸원자핵)은 원래의 것보다 불안정한 모핵에서보다 양 자를 둘 적게 가진다. ;『 U 一발 Th+a 의 반응식의 예에서처럼 모핵보다 원자번호가 2 단 위 낮아지고 질량은 4 단위 낮은 새로운 핵을 만든다. a 입자는 정의 전하를 가지며 통과하는 기체분자를 이온화시키는 능력이 있다. 두과 력 이 약하며 얇은 금속판을 통과하지 못한다. 어떤 방사성 핵종은 불안정한 모동위원소에 음전자를 방출하는 붕 괴를 한다. 즉 /3 붕괴 인데 핵의 질량은 변화하지 않지만 핵의 전하 는 한 단위 증가한다. /3 붕괴는 전자포획 방식의 붕괴이다. 예를 들 면 컴 Th_ ―댜마) +맑 Pa 과 같다. 그리고 여기된 원자핵에서 덜 여기된 상태로 될 때 방출되는 높은 에너지를 갖는 7 선은 거의 모든 방사성 물질에서 방출된다. r 선의 방출로 동위원소의 질량이나 전하에는 변화가 일어나지 않는다. r 선 은 X-선 보다 파장이 짧은 방사선으로 투과력 이 대 단히 강하여 8cm 의 납판도 통과한다. 원자핵 붕괴시에는 막대한 에너지가 방출된다. 이들 자연 방사성원소의 붕괴계열은 표 8-2 와 같다. 방사성 붕괴가 지수함수로 표현되며 (Ruth e rf or d, 1900) 방사성 붕괴
표 8-2 우라늄계 열의 방사성 동위원소의 붕괴계 열 (Russell 과 Farqu h ar, 1960) 235U 동위원소 붕괴유형 반감기 땅2 U a 0.713X 10 면 239\i T h /3 25.6 시간 239\Pa a 3.43 X l0 년 22;9A c 8 22 . 0 년 2297OTh a 18 . 6 시간 22&Ra a 1 1. 2 일 깝9 6Rn a 3.917 초 2iP o a 1.83 X 10 - 3 초 21&Pb 8 36.1 분 21813Bi a(99 . 7%) , /3 (0 . 3%) 2 . 16 분 2\1.Po a 0 . 52 초 20l1Tl /J 4.79 분 20s72Pb 안정 238u 239s2U a 4.50 X 10 년 239~Th 8 24.101 일 239\Pa /3 1.175 분 뱀 U a 2.4 7 5X l0 년 239打 Th a 8.0X10 년 22&Ra a 1,622.0 년 22;6Rn a 3.825 일 2,88,P o a 3.05 분 21842Pb {3 26.8 분 21&Bi a(0.04%), /3( 99.96%) 19 . 72 분 2184‘Po a 163. 7 µ초 21&Tl /3 1. 32 분 z1a°2 Pb /3 22.5 년 2le°3 B i fl 4 . 989 일 21~Po a 138 . 374 일 20862Pb 안정
232Th 239Hh a88aa 1. 39 X 1010 년 22888Ra 6 . 7 년 22889Ac 6.13 시간 229\Th 1. 90 년 22a\Ra 3.64 일 22806Rn a 54.53 초 2186,Po a 0 . 158 초 21822Pb 8 10.67 시간 21&Bi a(33. 7% ) , /3( 66. 3% ) 60 . 48 분 21&Po a 0.2 9 쵸 zoa8 1TI 8 3 . 1 분 20882Pb 안정
속도론에서 A— B 일차반응시 붕괴속도 K( 동위원소의 농도)는 _d.A/ d t =KA 로 표현될 수 있다. 시료 중의 방사성 동위원소 원자의 총수 (N) 가 시간이 지남에 따라 붕괴할 때 붕괴상수를 A 라 하면 위의 반 응속도론 관계식에서 dN/d t=― AN 의 관계로 표현할 수 있다. 이 식 에서 시간을 t=O 에서 t 까지 N 을 No 에서 N 까지의 구간에서 적분하 면 N=No e 一 u(No=N eu) 가 얻어진다. 붕괴속도론에서 원래의 동위원소가 붕괴되어 그 양이 반으로 되는 데 걸리는 시간을 반감기라 한다. 붕괴상수 A 와 반감기의 관계에서 t=나과 N=No/2 를 대입하면 l/2No=Noe-u 심 또는 냐 =ln 2/tl= 0 . 693 /A가 얻어진다. 또 t시간 동안 붕괴된 후의 시료와 모원자에서 동위원소의 원자수의 차이를 D( 딸원자, Daug h te r ato m ) (D=No-N) 라 하면 D=N(eAt - 1) t= l/tl l n(l+D/N) (1)
가 얻어진다. 붕괴가 진행될 때 계내에서의 딸원자는 D1=Do+D 로 표현되며, 이 때 D t는 딸원자의 총수이고 Do 는 초기 딸원자의 수, D 는 모원자가 붕괴시에 생성된 딸원자의 수이다. D=N(eu 一 1) 이므로 D t =D 。 +N(eu-1) 이 된다. 여기서 Dt, N 을 측정하면 광물과 암석의 절대연령이 얻어진다. 절대연령 측정용 시료는 보통 다음 조건이 구비되어 있어야 한다. ® 암석이나 광물은 모원소와 딸원소 모두가 폐쇄계에 있어야 한다. 죽 이들 핵종은 암석, 광물이 형성된 후에 원자를 얻지도 잃지도 않 아야 한다. @ Do 의 값은 현실적이어야 하고 D 가 Do 보다 훨씬 큰 경우에만 가능하다. ® 붕괴상수의 값이 정확히 알려져 있어야 한다. ® D 와 N 의 두 변수의 측정값이 정확하고 그 암석이나 광물의 대표 값이 될 수 있어야 한다. 동위원소를 이용한 절대연령과 지질학적 물질의 동위원소 역사를 다루는 지질학의 한 분야가 지질연대학 (Geochronolo gy)이다. 8-3 방사성동위원소의 붕괴 계 열 방사성동위원소가 붕괴되어 1 차, 2 차, 3 차 딸원소를 계속해서 만들 때 그때 딸원소들의 수를 각각 Ni, . N” .1'!3 라 하면 붕괴속도 식에 서 一 dN1/d t=tl 1N1 로 표현할 수 있다. 최초의 딸원소의 붕괴속도는 모원소가 붕괴될 때의 속도와 딸원소 자신이 붕괴될 때의 속도 차이다. 즉
뿔 =111 Ni -112M (1) 여기서 tl1 과 A2 는 각각 최초와 두번째 방사성 핵종의 붕괴상수이다. 시간 t가 지난 후 모원자의 수는 Ni = N? eH1 t)로 표현된다. 여 기서 N1 는 t =O 일 때 모원자의 수이다. 이 식을 (1)식에 대입하면 뿡 +A 晶 _A1N~ eH10=0 (2) 가 19되1어0 년 1 차Ba t선 em형a미n 이분 N방] 정_식 -N이2 一된一다. N 3_ …… _-N n 방사성 붕괴 계열의 일반식을 풀고 붕괴계열의 어느 한 멤버의 원자수를 N~= N~ =一 N g =o 인 조건을 만족하는 시간의 함수로서 Nn = C1 e(-At I ) + Ci e<- A2I) + …… + Cn eHnl) (3) cl = (A2 김)11 1( 서A3 길.. tt)n- 1• •N • ?( An 길) G= A 서 ··An-1N! (AI _A2) (A3 _A2) …( An_A2) C3 = (A1 김1)111 1(2AN2? 김) 로표현했다. 이 식은 임의의 시간의 붕괴계열과정 중의 어느 한 멤버의 원자수 를 결정하는 데 이용될 수 있다. 같은 방법으로 다음과 같은 식도 유 도될 수 있다. C1, C2, C3 를 (3) 식에 대입하면 M= 晶(A2 길N~ )e(H-Aait )) +1 (AA 1감A2)N~ (eA3H 감zt)) +1 (AA11 급t1 2 )N~ (eA2H 강st)) (4) 이 얻어진다.
만일 붕괴계열의 모원자가 붕괴시 처음에 딸원자를 만들고 최후에 안정동위원소로 된다고 하면 이때 두번째 딸원소는 안정하기 때문에 /1 3=0 이 된다. 따라서 위 (4) 식은 t1 3=O 일 때 다음과 같은 식으로 표 현된다. 隨? e(-AIt) _ AN? e(-A2t ) +Nf 凡= (A2 김) (AI_A2) M=N?(1+~ +~) (5) 이 식은 방사성원자 (N1), 방사성딸원자 (N2), 안정딸원자 (N3) 인 붕괴계열의 임의의 시간에 존재하는 원자의 수를 계산하는 식이다. 111<112 인 경우와 갇이 모원자가 딸원자보다 반감기가 대단히 긴 특수 한 경우에 (2) 식의 편미분 방정식은 凡= 112 A-1I 11 Nf (e( -A1 t) -e (-A2 t)) +Ng e( 야) (6) 으로풀린다. 이 식에서 처음 항은 모원자의 붕괴시 생긴 최초의 딸원자의 수이 고 두번째 항은 초기의 수 N g에서 남은 최초의 딸원소의 수를 의미 한다. 물론 초기에 존재했던 N~ 의 원자는 존재하지 않았을 것이므로 Ng =o 일 때 위 식은 凡 =AA2N-A~I (e 西)- e(-Azt) ) (7) 이 된다. A1
그러므로 t의 값이 큰 경우에는 凡二行 N!e(_AI t) 가 되어 N1 / N 계가 시간 t 가 증가함에 따라 일정한 값을 가지게 되어 보N2= - A 2/\-1A l =- 일c 처O 하게 된다. 따라서 이 붕괴계열은 방사성 붕괴평형에 이르게 된다. 238U, 235U , 231Th 의 반감기 가 각각 4 . 468 X1 09a, 7. 038 X1 08a, 1. 405 X 108 a 인 것처럼 자연에서는 모원소의 반감기가 딸원소의 반감기보 다 훨씬 긴 예도 있다. 따라서 이 경우에는 N1/N2=112/111, 111N1=112N2 로 표현할 수 있다. 따라서 붕괴계열의 장반감기 모원소와 단반감기 중간 딸원소 사이 에 시 간에 따른 평 형 (Secular equ i li br i um ) 이 성 립 되 어 t11 N1 =112N2 = t13 N3 =t1 ◄ N ◄ = … …-+ JnN n 이 된다. 이 감은 평형이 얻어진 곳에서·여러 불안정한 딸원소 중 임의의 딸 원자의 수는 Nn= 보An 으로표현될 수 있다.
딸원자의 적분비는 凰A2M = AA3 晶 凡 =A뚜4N=4 …… =1.000 이 된다. 시간변화에 따른 평형상태에서 방사성 붕괴계열의 최후에 안정방사 성 딸원자의 성장속도는 이 계열의 붕괴속도와 같다. 죽 D=N~_ 사_사…… _N11 이 되고 Nn= 꼬An 凡 =__AA_2l_ M , 凡 =__AA_3l_ N 1 , 등으로표현된다. 이것을 다시 표현하면 D=N~-N i(l -[ 王 … .. _虹 이 된다. A1!A2, A1 싸 등은 1 보다 훨씬 작은 값이므로 D=N~-N1 =N1eAi t- M
D=N1 (e' '1 -1) (8) 이 된다. 시간변화에 따른 평형 (Secular equ i li br i um ) 상태에 있어서 방사성 붕괴계열로 붕괴된 결과 축적된 방사성 딸원소의 수는 최초의 모원자 가 직접 붕괴하여 안정한 딸원자로 된 것으로 간주할 수 있기 때문에 일반적으로 붕괴시 딸원자의 양은 위의 식처럼 표현되고 있다. 지질학에 이용되는 방사성 동위원소는 대단히 많이 있다. 그중 여 기서는 우라늄 계열의 붕괴계열만을 소개한다(표 8-2). 23 8 U 는 a, 8 붕괴 를 거 쳐 안정 한 2o s p b 도 되 며 , 235U 는 201 p b 로, 23 2 Th 는 20 8 Pb 로 되어 안정해진다. 우라늄 계열에서 원자번호 83( 비스 머스)보다 큰 모든 원소는 방사성 동위원소로만 자연에서 산출되며 그 의의 자연 방사성동위원소는 모동위원소나 딸동위원소를 가지고 있다. 지질연대학에 가장 많이 이용되는 방사성동위원소의 특징을 요약하 면 표 8 ~ 1 과 같다 . 여 러 방사성 동위 원소 중에 서 “Rb - s1sr, 40K - 4DAr, 147Sm - 143Nd 법이 근년에 와서 많이 이용되며 특히 연대 측정은 물론 지각물질에 서의 미량원소의 이동과 지각에서의 원소의 혼염 등에 대하여 웅댕 연구되고 있다 (O'N i ons 등, 1977 ; Wasserburg 등, 1981). 이들 동위원소를 이용한 연대측정법에 대하여서는 뒤에서 자세히 다루겠다. 그리고 동위원소의 암석광물에서의 함량을 표 8-3 에 나타냈다. 표 8-3 에서와 같이 칼륨은 암석광물에 다량 포함되어 있으나 기타 원소 들은 그 존재량이 적다. 방사성 광물의 방사성 측정은 전기적인 방법이나 분광학적인 방법 으로 측정한다.
표 8-3 광물과 암석내의 방사성동위원소와 딸원소의 존재량(pp m) 암석.광물 u Th Pb Rb Sr K Sm Nd 콘드라이트 0.0 1 4 0.04 1. 2 2.8 11 860 l.3 7 4.41 현무암 0.8 2.7 4.5 30.0 470 8,500 8.07 41. 5 화강암 4.4 16. 0 20.0 170.0 290 33,000 8.2 2 43.5 셰일 3.8 12.0 20.0 140 .0 300 28,000 10.4 49.8 혹운모 20.0 25. 0 25.0 1,000.0 20 70,000 37.0 171. 5 백운모 20.0 25.0 25.0 700.0 80 70, 00 0 K- 장석 1.5 5.0 25. 0 500. 0 100 90,000 3.77 26.0 사장석 2.5 1.5 0.1 30.0 500 6,000 0.5~1 1.85 각섬석 15.0 25.0 7.0 10.0 150 3,000 6.03 17. 3 휘석 20.0 13.0 7.0 10.0 150 5,000 3.34 9.0 9 저어콘 2,500.0 2,000.0 100. 0 자료 Turek i an 과 Wede p oh l (l96 1) . Herrmann (l97 0) . Ro g ers 와 Adams (1969).
방사성측정 기본단위는 큐리 (C i)이다. 이는 초당 3.7oox 1 010 개의 방사성 핵종의 생성량을 말한다. 보통 mCi , µ Ci 등의 단위가 사용된 다. 전자기 방사능의 단위는 뢴트겐 (R) 이 사용된다. 8-4 시료처리 방법 실험적인 시료처리법은 너무 다양하므로 여기서는 · 간단히 소개한다. 시료의 연대측정을 위하여 Rb-Sr, S m-Nd, U-Pb-Th 동위원소를 이 용할 경우 이돌 방사성 동위원소 전량과 La, Ce, Nd, Sm, Eu, Gd, Dy , Er, Yb, Lu 등과 같은 희유원소 정량에는 동위원소 희석법 (Isoto - pe dilu ti on meth o d) 이 많이 이 용된다. 1) 우라늄(토륨) 시료준비법 연, 우라늄, 토륨, 스파이크(또는 트레이서라고도 함) 혼합용액을
이용한 동위원소 희석법의 원리를 간단히 소개하면 다음과 같다. 정량된 시료를 용해시킨 후 정확히 둘로 나누어 그중 하나에서 스 파이크 되지 않은 연광물 (Uns pi ked mine ral lead) 을 추출하여 고체용 질 량분석 기 로 정 확히 206Pb/ 2D 4 P b, 207Pb/ 20 4 P b, 208Pb / 2D4Pb 의 비 를 측정한다. 그리고 다른 한 시료는 2osp b, m u, 230Th 동위원소가 많이 들어 있는 정확히 알려진 양의 스파이크를 첨가한 후 질량분석 방법으 로 206P b/ 2D 8P b, mu;m u, 232 T h/2 3 0Th 등의 동위 원소비 를 측정 한다. 스 파이크된 시료용액내의 238U , mu, 232Th 의 그램분자수는 u2 38 = U\35 \ 二(238) S (_; 2(323\8\\) :\ l, 0235 = 1u372 3.88 ' Th23 2 = TM30 { 겁; \? A f _ ((昌汀 , 와 같다. 여기서 235Us 와 230Ths 은 스파이크로 사용된 동위원소의 양을 그램 분자로 나타낸 것이고 s 와 M 기호는 스파이크와 최종스파이크 혼합 물을 의미한다. 최종스파이크 용액에서의 연광물 (M i neral lead) 의 총 그램분자수는 Pb= 도#0!6 틀1-(( 二昌雲 : A fl ,
이 된다. 여기서 〈 m i n 〉은 광물을 의미하고 〈 a206 〉 은 Pb2os 의 광물 연의 몰분율 이다. 최종스파이크 용액내의 방사성 Pb2os 의 그램분자수는 #06= 1+ 를+틀+를 Pb206* =Pb (1'' ( 1-1 (206)[ ) 이 된다. 여기서 (206/204)c 는 보통연 (Common lead) 에서의 이들 동위원소비 롤 의미한다. Pb20 과 Pb20 도 위와 같은 식으로 표현되며 207, 208 만 바꾸어 넣으면 된다. 여기서 얻어전 207*/206* 비가 Pb-Pb 법에 이용된다. 2) 칼륨-아르곤 시료준비법 광물과 암석 중에는 많은 양의 칼륨 (K) 이 포함되어 있으며 많이 이용되는 광물은 흑운모, 백운모,· 각섬석, 전암 등이다(표 8-4 ) . 칼 륨은 동위원소가 3sK, 40K, 41K 이 있으며 이 중 전체 K 중의 40K 의 비율은 4°K ppm wt.% =K ppm wt.%/l . 22 x l0-4 이다. 칼륨의 분석 에는 주로 영광분석법이 이용되고 동위원소 희석법으로도 분석한다. 정량된 광물시료를 HF+NCI04 나 HF+H2S0 4 로 분해 후 증발전 조한 다음 HN03 +H20 로 희 석하여 염 광분석 법으로 분석한다. 40Ar 분석은 O 광물시료를 녹여 H20, CO2 와 같은 가스와 소량의 아 르곤 가스 등을 방출시킨다. ® 화학적 방법과 물리적 방법으로 순수 한 아르곤 가스가 되도록 한다. ® 융해된 광물에서 나온 방사성 기 원의 Ar 만을 정량한다. 시료의 용해는 Radi o- fr eq u e ncy i nduc ti on-hea ti n g법으로 광물을
표 8-4 K:-Ar 연령측정에 유용한 조암광물 암석 광물 화산암 심성암 변성암 퇴적암 장석류 Feldspa r s 세니딘 Sanid if l e ** 아놀소크레 이 스 Anorth o clase ** 사장석 Plagi oc lase ** 준장석류 Feldspa t h o id s 류사이트 Leucit e * 네펠린 Neph e lin e * * 운모류 Mic a s 혹운모 Bio t it e ** ** ** 견운모 Phlog op i te ** 백운모 Muscovit e ** ** 금운모 Lepi do lite 글로코니 Glaucony * 각섬석류 Amp hi b o le 각섬석 Hornblende ** ** ** 휘석류 P)rroxene ** ** ** 전암 Whole rock ** ** * 유용 * * 대단히 유용
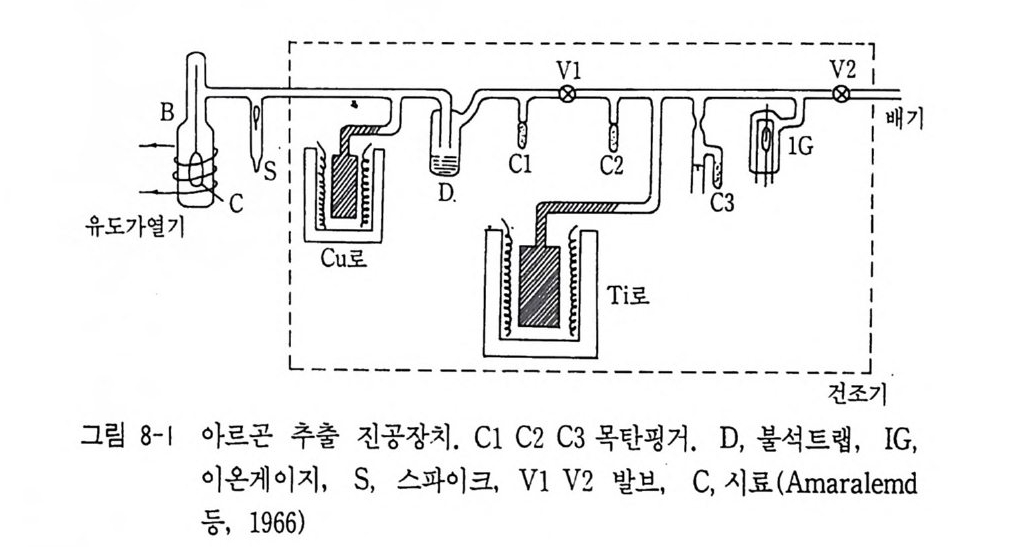 广- -- ---- -- ---- - ----_ _ ―---一 ----1
广- -- ---- -- ---- - ----_ _ ―---一 ----1
융해시킨다. 아르곤 정제시에 CO2 와 H20 는 액체질소와 같은 액화가스트랩으로 제거하고 산화시켜 CO 는 CO2 로 H2 는 H20 로 만들어 응축 제거 시 킨 다. 그리고 잔여 CO, N2, H2 는 고온의 티타늄로에서 반응시켜 제 거시킨다. 냉각 후에 티타늄로 속에 남은 소량의 H2 와 잔존하는 아 르곤 등은 먼저 아르곤을 차콜(목탄)에 흡착시킨 후에 H2 를 배기시 킨다(그림 8-1). 3) 방사성 아르곤의 측정 법 순수한 38Ar 로 된 스파이크롤 사용한 동위원소 희석법으로 광물에 서 방사성 ◄ oAr 을 추출하여 체적을 결정한다. 융해시에 일정량의 스 파이크가 방사성 아르곤과 대기의 아르곤의 혼합기체가 평형에 있는 진공계 속으로 흘러 들어온다. 정제한 후 융해 시스템으로부터 나온 이 스파이크된 아르곤을 가스 용 질량분석기로 정량한다. 방사성 “Ar 의 체적 (40 파)은 다음과 같이 계산한다. V§ 드기틀- (?\\ —[ 儒\―톱]\臺] ) (38) M (38) A 여기서 V 안는 스파이크된 38Ar 의 체적이고 M , S,A 기호는 각각 최종 혼합물의 아르곤, 스파이크된 아르곤 그리고 대기 중의 아르곤을 의 미한다. 대기 중의 아르곤의 오염의 비율은 (Ar40) ={(40) (36)/(36)A (40)m} 100% 이다. 국소량의 가스시료를 보통 이용하므로 융해 시스템이나 질량분석키는 초정밀 진공이 요구된다. 1 억 년 이상된 흑운모는 대기의 아르곤 오염이 16% 이하이나 젊은
현무암의 경우 50~90% 의 대기의 오염이 보고되어 있으므로 그의 영 향이 대단히 중요하다. 그 의에 K 분석은 X 선 형광분석법이나 중성자 여기 (Neutr o n acti• va ti on) 법을 이용하여 분석하며 Ar 역시 중성자 여기법으로 분석하 기도한다. 4) 루비듐-스트론튬의 시료준비법 스트론튬과 루비듐은 모든 암석에서 다량 포함되어 있다. 루비듐울 가지는 독자적인 광물은 존재하지 않지만 루비듐의 이온반경 U.48A) 과 칼륨의 이온반경(1. 33A) 이 유사하므로 칼륨이 포함된 광물에 미 량으로 수반된다. 주로 화성암과 변성암중의 혹운모, 백운모, 레피도 라이트 (Le pi dol it e) 와 칼리장석에 함량이 높다(표 8-3). Rb-Sr 측정법에서 86Sr, 87Rb 와 (“Sr/86Sr) p의 바는 동위원소 희석 법으로 분석 한다. Sr 과 Rb 의 스파이크롤 소량의 시료에 넣고 테프론 내에서 불산과 과염소산 두서너 방울을 첨가한 후 건조시켜 유기물질 을 파괴시킨다. 그 후 10 N HCl 을 첨가하여 증발 건조시키고 증류수로 탄탈륨 필 라멘트를 중심으로 모은 후 질량분석을 실시한다. 원심분리기에서 Rb 이 함유된 침전물은 HCl 로 용해시키고 또 다른 양이온 교환기구에서 질량분석을 위해 루바듐을 수집한다. 86Sr 이 많은 스파이크가 사용되었다면 86Sr 과 (“Sr/86Sr) p는 다음 과 같이 계산된다. (88) (88) Sr86=Sr 惡{ 萱__!f l (86) C (86) M ((SSrr8867)) p _= 面(8;6) +, 호Sr 뿐 ~(87-) +s(8W7)s -}
여기서 86Srs 은 스파이크로 첨가된 86Sr 의 수이고 ,l f ,S, C 는 각각 최종 혼합, 스파이크, Common 을 의미 한다. 한편 잔류하고 있는 스파이크 되지 않는 양을 분석하여 (“S r/8 6 Sr}p 값을 다음과 같이 표준화시킨다. M 은 질량분석에서 측정된 양을 의 미한다. 따라서 Sr 스파이크가 사용될 경우에는 스파이크된 시료용과 스파 이크되지 않은 시료용의 두 질량분석기가 필요하게 된다 . 8-5 동위원소비를 이용한 절대연령 측정법 1) 루비듐-스트론튬 측정법 루비듐은 원소 주기율표의 IA 족에 속하며 부드럽고 대단히 반응하 기 쉬운 백색의 알칼리 금속이다. 루비듐은 27 종의 동위원소가 있으 나 Nie r (19SO) 에 의 하면 85Rb (72 .15 %) 와 87Rb (27 . 85%) 의 두 동위 원 소가 알려 져 있고 85Rb/87Rb = 2 . 59 이 다. 그리 고 스트론튬의 동위 원소 는 “Sr(0.56%), 86Sr(9.86%), 87Sr(7.0 2 %), 88Sr(82.56%) 등이 있다. 챔 R b----+ nSr+{]-+v+ Q 관계식후 87Rb 이 붕괴되어 “Sr 이 되 며 붕괴상수는 4.987X1 Q -ll/ 년이며 반감기는 5.0X1010 년이다. 그리 고 D 는 반뉴트리노이고 Q는 붕괴에너지 (0.275 MeV) 이다. • (8) 식과 같은 앞장의 암석 철대연령 측정원리에서처럼 시료 중의 스트론튬 동 위원소는 87Sr=87Rb(e-1) 의 관계가 성립된다. 그런데 이 “Sr 의 양에는 “Rb 의 붕괴에서 생긴 “Sr 의에 물질내에 원래부터 존재하던 “Sr( 초생치)가 포함되어 있기 때문에 이것을 더 하면 s1sr (측정 치 ) = “Sri ( 초생 치 ) + “Rb (eu -1) 인 관계가 성립된다.
동위원소 존재량은 바의 측정어 정확히 측정될 수 있으므로 동위원 소비의 값으로 표현하면 틀 ) m =틀 ) , + (雪) (eu 一 1) 관계가 얻어진다. 여 기 서 (87S r/8 6 S r) ill을 Y 축으로, (87Rb/8 6S r) 을 X 축으로 잡으면 1 차함수식이 된다. 따라서 암석의 절대연령 (t) =1/, ,l In {1+ 기울기 (t an0) } 가 되어 기울기가 바로 연대가 되며 이 직선을 아이소크론 (Isochron) 이 라 부른다. 아이소크론은 York(l966) 와 Mckty re 등 (1966) 의 최소 자승법을 이 용하여 구한다. 즉 직선의 기울기 m 과 절편 b 는 ~XY-((~X)( 합 ))/N m=~ 드 (2X)2/N b= (짝 X) (짝 XY)-2 Y( 짝?) (~X)2-N(~X2) 에서 계산된다. 여기서 Y 는 87Sr/86Sr 비, X 는 87Rb/86Sr 을 의미하여 N 은 분석시료 수이다. 동일기원의 마그마에서 형성된 암석이나 광물은 직선의 아이 소크론이 얻어진다(그림 8-2 ) . 마그마에서 냉각결정화 시작시간(t =O) 은 동원마그마원의 화성암 시료에서는 87Sr /87 Sr 비가 동일하였다고 가 정 한다. 그러 나 암석시료 중의 87Sr/86Sr 비는 광물조성 에 따라 다르 다. 따라서 각 암석이나 광물의 동위원소값은 각각 —1 기 울기의 직 선을 따라 평행 이동되어 아이소크론상의 지점으로 이동된다. 암석과 광물이 루비듐과 스트론튬에 대하여 폐쇄계로 유지되었다면 아이소크 론 직선식을 만족시키게 된다.
 87
87
죽 형성시기가 같은 동일암체내의 장석, 운모 등의 광물과 전암 시 료를 채취하고 원암체의 (87Sr/86Sr),· 가 일정한 값을 가지고 시료광 물이 폐쇄계에서 Rb, Sr 의 이동이 없었을 경우에 한하여 (“Sr/ 86Sr) 나 81Rb/86Sr) 을 그림에 도시하면 각 시료의 값은 동일 직선상 에 도시된다. 이 그립에서 초생치 (87Sr/86Sr) i는 절편에서 얻어지며 이 값이 암 석성인 연구에 중요한 자료가 되고 있다. 그러나 시료가 동위원소적으로 폐쇄계에 있지 못하였거나 변성작용 이나 지각변동과 같은 지질학적 사건에 의해 동위원소의 값에 변화를 준 시료의 경우에는 광물시료와 전암시료에서 얻은 아이소크론이 일 치하지 않는다. 예를 들면 동일한 화강편마암 암체내의 서로 다론 가, 나, 다 세
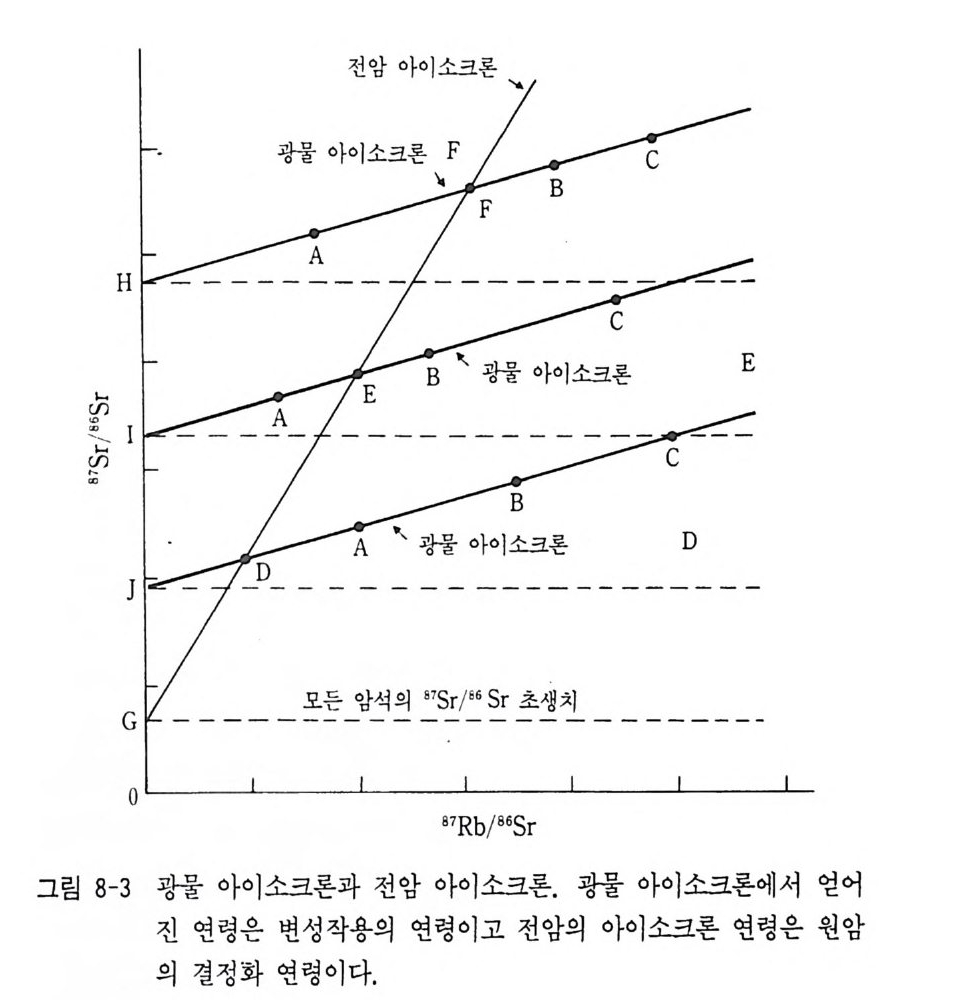 전암 아이소크론
전암 아이소크론
지역의 시료를 채취하여 전암과 분리된 광물에 대하여 87Sr/86Sr, 81Rb/86Sr 동위원소비를 분석하여 이들을 도시하면 그림 8-3 에서처럼 광물에서 얻어전 아이소크론인 광물 아이소크론 (M i neral i sochron) 과 전암에서 얻어진 전암 아이소크론 (Whole rock i sochron) 의 기울기가 다르게 얻어전다. 이 경우 전암 아이소크론은 암석의 원래의 결정화연령, 죽 화강암 의 관입시기이고 광물 아이소크론은 변성작용과 같은 지질학적 사건
에 의해 동위원소가 재분배된 사건의 연령을 의미한다. 즉 지각변동이나 변성작용과 같은 지질학적 사건시에 변성광물내의 동위원소가 광물격자내에서 이동되어 재분배되지만 계내의 전체 암석 내에 존재하는 동위원소의 양은 일정하기 때문이다. 이처럼 아이소크론에서 원암의 절대연령과 변성작용과 같은 지질학 적 사건의 연대가 얻어진다. 그러나 전암 아이소크론의 연령은 퇴적 물이 재결정화된 변성사건의 시대를 나타낼 수도 있다. 따라서 Rb -Sr 법은 비변성 퇴적암의 연령측정에도 적용될 수 있다. 퇴적암의 퇴적시에 형성된 해록석군 (Glaucon y), 칼리장석, 실바이트 등과 기타 점토광물들이 Rb/ Sr 함량을 많이 가지고 있으므로 방사성 Sr 양을 측정 가능한 정도를 가지고만 있으면 퇴적암의 퇴적 연령 측 정도 가능 하다. 글로코나이트질 운모, 글로코나이트질 스멕타이트 그리고 일라이트 질 점토광물 등과 갇은 퇴적 당시 형성된 광물도 연대측정에 이용될 수있다. 그러나 이들이 K20 가 6% 이하일 때는 불가능하다. 일라이트가 되 적 당시의 것인지 그 후 변형된 일라이트인지는 X- 선에 의해 구별하 여야한다. 따라서 점토가 많은 퇴적암 시료는 연령측정 전에 광물학적 연구가 선행되어야 한다• Mo rt on (1 985) 은 미국 텍사스의 데본기 말 우드포 드 (Woo df ord) 흑색 셰일 중의 점토 광물인 일라이트에서 아이소크론 연대 539 士 18Ma( 캠브리아기)를 얻었다. 이는 이 지층의 퇴적시기 (360~374Ma) 보다 오래된 연령이 얻어져 조립질 일라이트가 이동되어 온 퇴적공급지의 암석의 연령으로 해석 하였다. 여기서 쇄설성광물의 기원지 구별과 풍화 침식시의 저항도를 고려 하여 백운모, 일라이트, 칼리장석, 저어콘 등을 선택하여 이들이 포 함되었던 원래의 퇴적암에서 이들 광물을 이용하여 얻은 연대와 비교
검토해 볼 필요가 있다. Rb - Sr 법을 사용한 쇄설성 퇴적광물의 연령측정에는 다음 몇 가지 가정이 전제되어야 한다. O 퇴적광물이 풍화 침식 운반되는 퇴적과 정 동안에 Rb 과 Sr 은 폐쇄된 조건으로 유리되어 있어야 한다. ® 광 물입자는 속성작용이 일어나지 않아야 한다. @ 상이한 시대를 가지 는 기 원 암으로부터 온 광물의 87Sr/8 6 Sr 초생 치 가 유사하여 야 한다. 위와 갑은 모든 조건이 만족되기는 어렵지만 북미의 빙하퇴적물내 의 장석의 연대측정에 이 방법이 유용함이 입증되었다. 그리고 Kralik (19 82 ) 등은 비변성 선캠브리아기의 암석의 연령측정을 시도하였다. 전압 아이소크론에서 얻어진 초생치 (s1sr / B6Sr)' 는 암석성인론적으 로 중요한 의미 를 가지고 있으나 광물 아아소크론에서 얻어전 초생치 는 의미가 없다. 초생치 (87S r/8 6 S r)1 는 마그마의 기원이나 마그마의 혼합과 같은 암 석성인 해석에 유용하게 이용되고 있다. 화강암의 경우 현무암질 마그마의 분별정출작용 산물이거나 상부맨 틀이나 심부지각이 부분용융되어 생긴 것이라면 보통 87Sr/86Sr 의 초 생치가 작은 (보통 0.7 0 0~0.7 0 5) 반면 고기 시알질 물질기원 즉 지각 기원에서 유래된 화강암은 초생치가 큰 경향 (0.716~0.720) 이 있다. 따라서 이 초생치가 화강암질 마그마의 기원해석과 지각형성과정 및 지 각형 성 이 전의 역 사 (Crusta l pre hi st o r y ) 해 석 에 대 단히 중요하 다. 그림 8-4 에서처럼 많은 화강암의 분석치가 현무암 영역에 도시된 다. 이들 화강암질 마그마의 기원이 상부맨틀 물질의 무 분 g g이나 현무암질 마그마의 분화에 기인한 것으로 해석되며 (Faure 과 Powell, 1972), 87Sr/86Sr 비가 높은 지각물질의 혼입이 없었음을 의미하고 있 다. 한편 초생치가 높은 화강암들은 화강암이 형성되기 전에 존재했던 시알질 물질에서 유래했거나 이와 크게 관련이 있는 것으로 해석되고
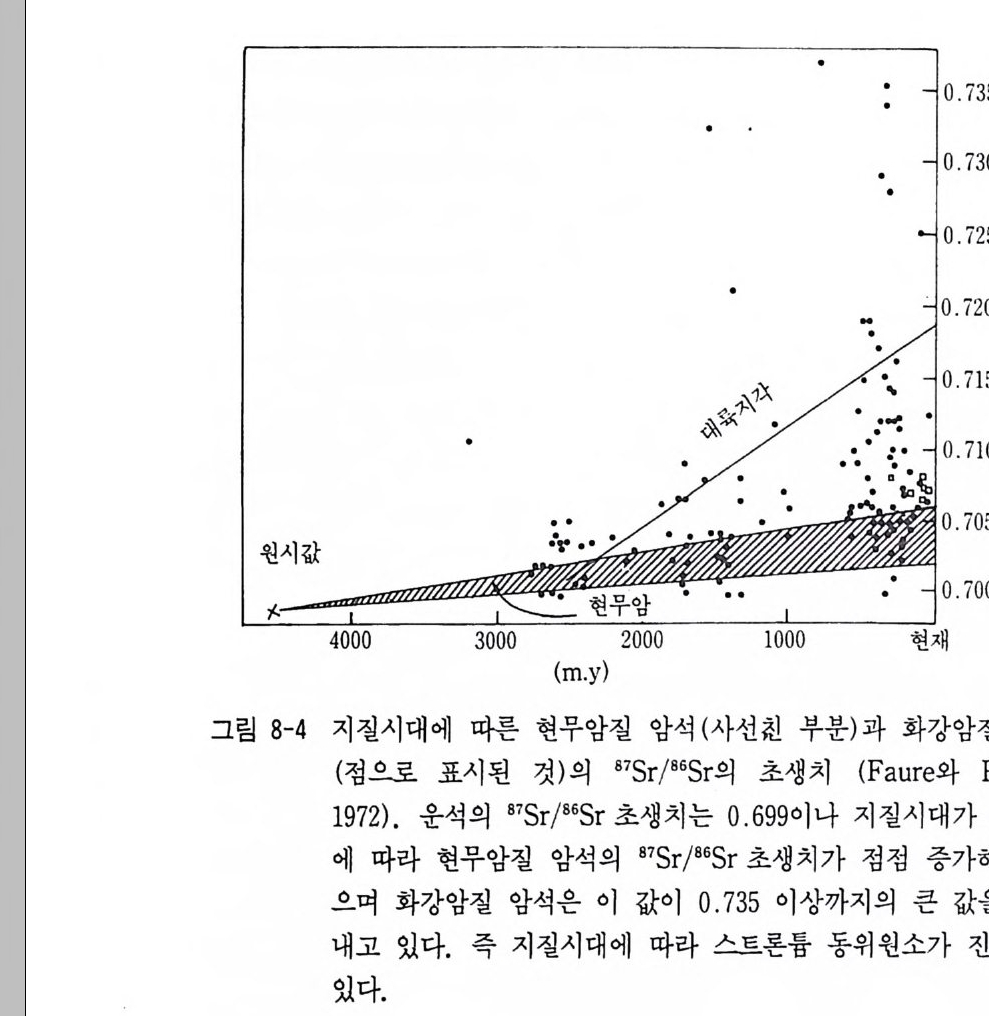 0.7 3 5
0.7 3 5
있다. 즉 마그마의 기원 해석에서 맨틀 기원인지 지각 또는 맨틀기원 의 마그마가 지각에서 동화와 혼합이 일어난 것인지 등을 해석하는 데 이용되고 있다. 또 다른 중요성은 상부맨틀에서 지각으로 진행된 스트론튬 동위원소의 진화이다. 그림 8 - 4 에서처럼 87Sr/86Sr 초생치는 원시 스트론튬(운석)의 0.699 에서 지질시대가 젊어침에 따라 현무암에서도 값이 증가하고 있다. 대륙지각의 값은 0.720 까지 크게 증가하고 있다.
Faure 과 Hurle y O96 3 ) 는 이들 대륙지각의 마그마가 상부맨틀에서 유래했기 때문으로 해석했댜 즉 지구의 지각은 맨틀에서 분화 전화 되었음을 의미한다. 2) 칼륨 - 아르곤 측정법 K- A r 측정법에 이용되는 광물은 운모 (7~9 % K 함유), 각섬석 (0. 1~ 1.5 % K 함유) , 칼리장석 (7~12 % K 함유), 사장석 (0.01~2 % K 함유), 휘석 (0~1 % K 함유), 해록석 (Glauconit e) (4~7% K 함유), 네펠 린 (Ne phe li ne) (3~7 % K 함유)과 화산암이나 슬레이트 등의 전암이 이 용된다(표 8-4). 칼륨 (K) 은 39K (93.08% ) , 4°K(0. 11 9% ) , 41K(6 . 91% )의 세 가지 동 위원소가 알려져 있고 그 중 “K 이 방사성 붕괴해서 “Ca(/3 붕괴)과 40Ar( 전자포착)이 만들어진다(표 8-5, 그립 8-5). 이때 붕괴상수는 사 =4 . 72 x 10-10(K - Ca). ;le= O,584x10-10(K-Ar) 이다. 4oca 은 자연물질에 많이 존재하기 때문에 “K - 40Ar 이 암석 연대측 정에 많이 이용된다. 그러나 “K- 4 °Ca 법도 개발되어 있다 (Marshall 과 Dep ao lo, 1982) .
표 8-5 칼륨, 아르곤, 칼슘동위 원소의 존재 량 ·동위원소 존재량(%) 동위원소 존재량(%) 칼륨 (Pota s siu m ) 칼슘 (Calciu m ) 39K 93. 25 81 '°Ca 96.941 ◄ OK 0.0 1 17 '2C a 0.647 K 6.7302 “Ca 0.1 3 5 아르곤 (Ar g on) “Ca 2.086 36Ar 0.337 '6Ca 0.004 38Ar 0.0 6 3 48Ca 0.187 •0Ar 99.600
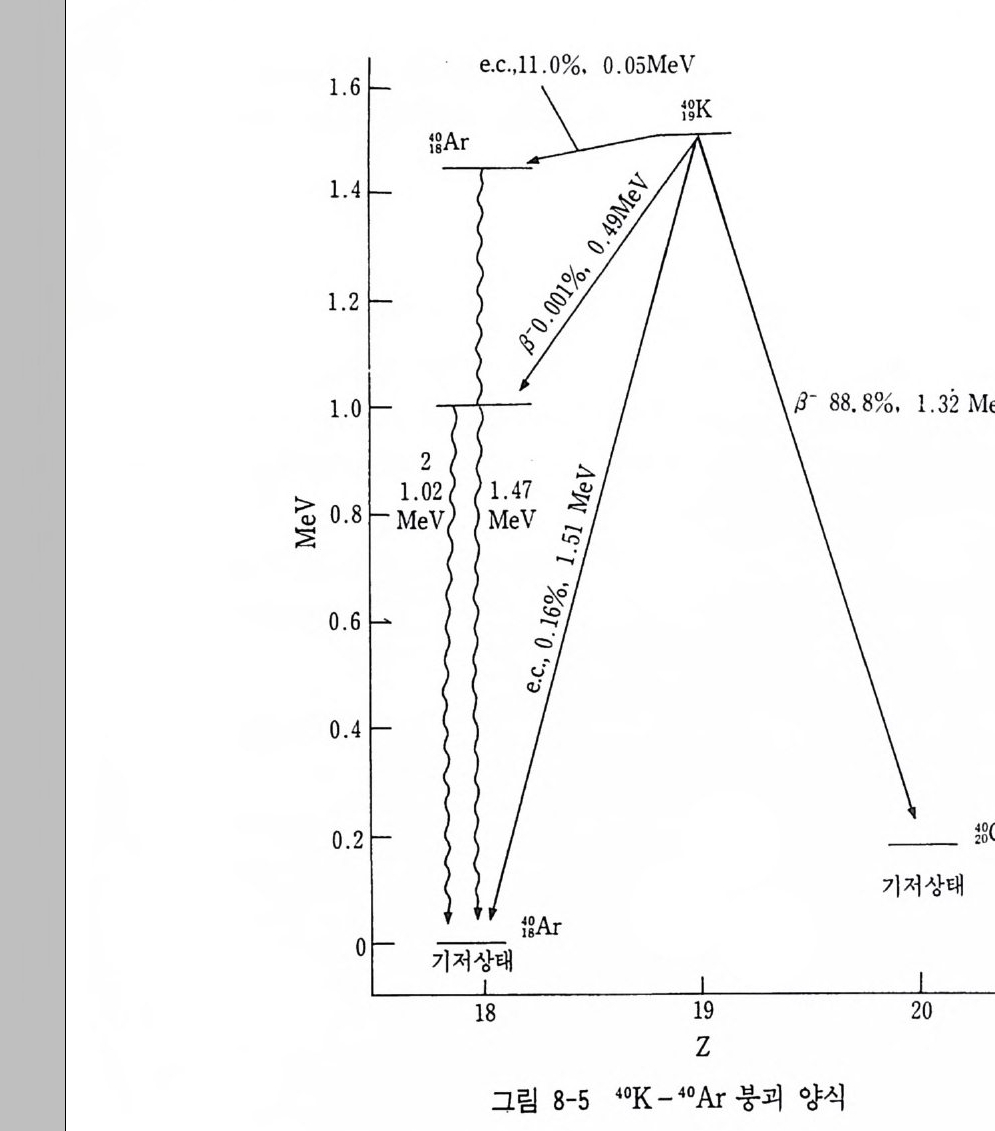 1.6 e.c ., 1 1. 0% . 0.0 5 MeV
1.6 e.c ., 1 1. 0% . 0.0 5 MeV
연령은 t= 급 ln[ 1 +( 모 e 멸] 에서 계산된다.
여기서 R=Ae / A g 이고 t\=t\ e+ 사이다 • 붕괴상수값을 대입하면 t=1.88 x 109 In(1+9.07 劑 이 된다 . 따라서 “K 와 “Ar 을 측정하면 연령이 계산된다 . K 을 직접 질량분석계로 결정할 수도 있고 4oK / 총 K 는 0 . 0119% 에 서 K 를 정량해서 “K 울 계산할 수 도 있다. 보통 오차는 土 2% 내의 이다 . 이 방법에서 일어날 수 있는 오차는 주로 시료에서의 Ar 유 실이다. K-Ar 법은 다음과 같은 장점 이 있다.
표 8-6 미국 몬타나 주의 보울다저반의 석영몬조니암의 K-Ar 일치연령 시료우]치 광물 (중K량20% ) (1동 0-위4100A 원몰r 소 / g ) (m연.령y. ) 크렌시의 케인쿼리 흑운모 A 8.74 9.42 71. 7± 2.3 (Kain Qu arry, Cla n cy) 흑운모 B 8.74 9.4 5 71.9 土 2.2 각섬석 A 0.4 5 6 0.503 73.3 土 2.5 각섬석 B 0.459 0.4 9 2 7 1. 4 土 2 . 5 홈스테이크 패스 혹운모 7.33 8.0 8 72 . 9 士 3.6 (Ho mesta k e Pass) 각섬석 0.550 0.589 7 1. 2 土 3.6 나인마일 스테 이 션 흑운모 9.0 0 9.84 72.7 土 3 . 0 (Ni ne - M ile Sta t i on ) 각섬석 A 0.600 0.691 76.5±2.4 、 각섬석 B 0.6 0 2 0.6 8 0 75. 0± 3.4 자료출처 : Til li ng , R. I., M. R. Klepp e r, and J. D. Ob ra d? vi ch , 196 8 .
® 많은 광물에서 K 가 다량 존재하며 ® 화산암, 슬레이트, 편암 은 물론 해록석 광물을 포함하는 퇴적암도 연령측정이 가능하며 ® 5 천 년에서 46 억 년까지의 넓은 연령범위의 시료에 대하여 측정이 가 등하다. ® 많은 광물에서 Rb 과 K 가 같이 산출되며 K~ A r 연대와 Rb-Sr 연대를 비교할 수 있다. 이 방법을 이용하여 측정한 연령의 예는 표 8-6 과 같다. 아르곤은 광물내에 화학적으로 결합되어 있지 않는 가스이기 때문 에 Ar 이 이탈되기 쉽다. 특히 변성작용시 온도상승으로 아르곤이 확 산될 수 있다. 그림 8-6 에 K-Ar 계와 Rb-Sr 계의 열적 영향을 나타냈다. 이 지역은 미국 콜로라도에 있는 엘도라 석영몬조니암 스목이 선캠
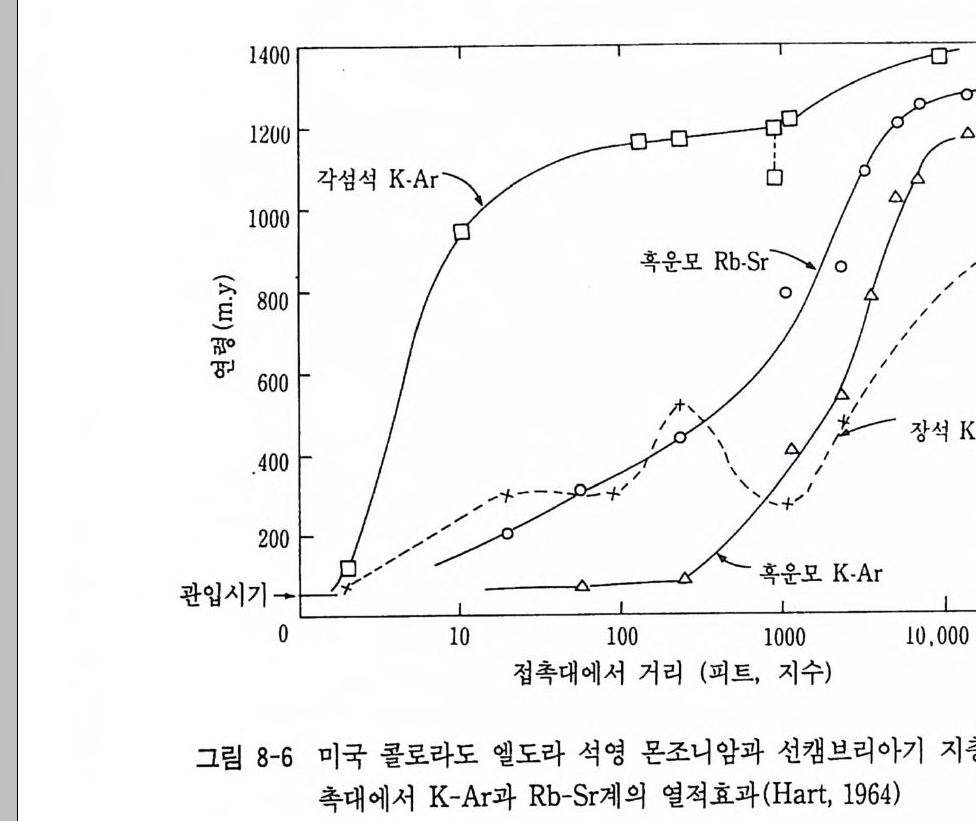 1400
1400
브리아기의 지충과 접하는 지역으로 접촉부에서 1,000 피트까지 거리 에서 혹운모의 연령이 크게 젊어진다. 그러나 각섬석은 그 변화가 비 교적 적어 접촉부에서 10 피트까지도 원래의 아르곤이 잔존하고 있다• 그림에서 보면 Rb-Sr 도 K-Ar 에서 처럼 열적 영향을 받고 있다. 그 러나 비교적 Ar 유실이 적은 광물이 각섬석이고 그 다음이 운모이며 칼리장석은 Ar 유실이 크다. 그러므로 기원암에서 지질학적(열적) 영향으로 일어난 Ar 유실과 획득을 구별하여 측정하는 기술이 개발되었다. 위에서 설명한 것처럼 측정용 시료는 시료가 형성될 때는 Ar 이 포 함되어 있지 않아야 하고 또 방사성 기원의 Ar 이 형성된 후에는 Ar 유실이 없이 보존되어 있어야 한다. 그러나 Ar 은 용융점 이하에서도 확산에 의해 쉽게 유실된다. 위의 그림 8-6 에서처럼 미국 콜로라도의 엘도라 석영, 몬조니암과 선캠브리아기의 아이다호 스프링충과의 접촉부에서 얻은 암석 중의 각섬석, 흑운모, 칼리장석 등을 분석한 결과에 의하면 접촉변성대에 서 온도의 상승으로 인하여 Ar 유실이 현저하게 일어났음이 입증되었다. 이 지역의 지층은 석영 -장석 -흑운모 편마암, 혹운모-석영 -장 석 편암과 각섬암으로 구성되어 있다. 연령측정에서 변성시기가 1,350~1400Ma 로 얻어졌고 관입암의 연 령은 약 55Ma 였다. 이들 접촉부에 소규모의 접촉 변성대가 형성되 어 있었으나 그림 8-6 에서처럼 변성광물의 K-Ar 의 연령측정 결과는 크게 영향을 받고 있다. 즉 접촉대에서 거리가 멀어짐에 따라 방사성 기원의 Ar 유실량에 현저한 차이가 있었고 광물종류에 따라 Ar 유실량이 차이가 나타났 다. 조립질 흑운모는 접촉대에서 약 30m 거리 밖에서는 방사성 Ar 이 전부 유실되었고 2,135m 까지 거리에서도 Ar 유실현상이 추적되 었다. 칼리장석은 접촉대에서 멀어짐에 따라 K-Ar 연령이 증가하였으며
6,860m 거리까지 Ar 유실현상이 나타났다. 그러나 각섬석은 방사성 Ar 의 보존상태가 좋아 접촉대에서 3m 거리 정도까지만 영향이 있었 고 그 이상의 거리에서는 급격히 Ar 유실이 감소하였댜 접촉대에서, 약 30m 떨어진 곳의 K-Ar 연령은 1,200Ma 이고 4 , 270m 거리에서는 1, 3 75Ma 이 었다. 위의 사실에서 접촉 변성작용으로 인하여 광물에서 Ar 유실이 규 칙성 있게 일어나고 있으며 동일한 물리화학적 조건에서도 혹운모보 다 각섬석이 Ar 보존상태가 대단히 좋다는 사실을 알 수 있다. 칼리 장석은 저온에서도 Ar 유실이 일어나므로 이 방법으로 측정시에는 주의를요한다. 동일지역의 시료에 대해 언제나 K-Ar 연령보다 Rb-Sr 연령이 큰 값이 얻어져 흑운모내에서는 Ar 보다 Sr 보존이 양호함을 의미하고 있 다. 접촉부분의 시료에 대하여 K-Ar 법으로 연령측정을 할 때는 주 의가 요구되며 적어도 4km 이상 거리에서라야 흑운모의 이용이 가능 할것이다. 따라서 측정대상 광물선택도 대단히 중요하다. 또 다른 주의를 요 하는 사실은 “Ar 이 많이 포함된 것 (40Ar excess) 이 다. Ozim a 등(1 983) 에 의하면 킴버라이트 중의 다이아몬드내에 excess 40Ar 현상을 조사하였다. 킴버라이트는 광역변성작용 동안에 높은 가스의 압력 때문에 Ar 이 다이아몬드내에 확산되어 들어가고 지각과 맨틀내에서 K- 함유 광물에서 탈가스되어 나오므로 인해 다이 아몬드내에 Ar 의 함량이 높아 이들을 연대측정에 이용하면 “Ar exces s.£. 인해 광물의 연령이 증가하는 결과가 얻어지게 될 것이다. 3) 아르곤-아르곤 측정법 •oAr-39Ar 법은 K-Ar 법과 유사하나 K 올 정량하는 대신 K 함유시 료를 원자로 속에서 열적 처리와 빠른 중성자를 조사시켜 39Ar 을 변 환시켜서 측정하는 것이 다르다. 중성자 조사시에 뀜 K(n, p) 겁Ar 의
반웅으로 일어나며 반감기는 269a 이다. M it chell (1 968) 와 Dallme y er(1969) 에 의하면 중성자 조사시에 방출 되는 아르곤 (39Ar) 은 39Ar=3 9K b .T J ¢( £)a(c)de 이다. 여기서 K 는 조사된 시료의 동위원소의 원자수이고, T 는 조사시 간, ¢(c) 는 에너지 c 에서의 중성자 플럭스 밀도 (Neu tr on flux dens ity)이고, 6(c) 는 에너지 e 를 가진 중성자에 대한 39K 의 포획단 면 (Cap tur e cross sec ti on) 이다. 4 0K 의 붕괴로 인해 시료내에 존재 하는 방사성 “ Ar 의 원자수는 40A r• 今 4°K (erp ( tlt) —1) 이 된다. t1 e 는 전자포획시에 붕괴상수이고 A 는 “K 의 전체 붕괴상수이다. 중성자 조사 후 시료의 “Ar* / 39Ar 의 비는 4309A Ar*r -=_ t itle .. 43°9KK .. 6.1T fe西xp) ( t6lt()c -)1dc 이 되며 여기서 J는 ]=i土 T f西 )a(c)dc 로 정의되며 이것을 위 식에 대입하면 4309AArr* =_ exp (AJt ) -1
이 된다. J의 값은 연대가 알려진 시료와 측정용 시료와 함께 조사시켜 구할 수가있다. 죽
]= e4xopA (rA *t/ m39 A)-rl 여기서 t m 은 플럭스 모니터 (Flux mon it or) 의 알려진 연대, “Ar*/ 39Ar 은 모니터에서 측정된 값이다. 그러면 연령은 떼 In( 寄 ·1+1) 에서 얻어진다. 정확한 연대가 알려져 있는 상이한 성분을 가지는 다수의 광물에 대해 Hux 모니터를 이용하였다. Hb3g r, MMH 6-1, LP-6, FY12a 와 같은 네 종류의 플럭스 모니터가 정밀한 K-Ar 측정에 이용되고 있다 (Rod di ck, 1983). 연령측정의 분석 오차는 다음과 같이 계산한다 (Dal rymp le 과 Lanp he re, 1971). (Jt= ]2tF2 2R (( (1J計++ F(JJJ)) 2I / 2 여기서 F=40Ar*/39Ar <11 와 6J 는 각각 퍼센트로 주어지는 F 와 J의 변화량이다. 그리고 t는 시료의 연령이다. 이때 측정한 연령은 전체 아르곤에서 얻어진 연령으로 시료에서40Ar 아 빠져나가거나 시료 속에 방사성 “Ar excess 가 없는 경우에는 지금까지 사용해 온 K-Ar 법과 같은 방법이다. 그러나 특정 시료내에 칼륨과 아르곤이 불균질하게 분포하기 때문 새 문제가 야기되는데, 이 방법은 아르곤의 비만을 측정하기 때문에 런 문제는 생기지 않는다. 됴 다른 한 방법은 단계적 가열방법 (Inc rementa l heati ng tec h niqu e) 一로서 시료내의 39K 의 알려진 시료.(fr ac ti on) 를 원자로내에서 빠른 중성자를 조사시켜 “Ar 으로 변환시킨다. 그리고 온도를 상승시키면 서 시료로부터 Ar 을 추출시킨다. 39Ar 의 전량과 방사성 “Ar 의 부분이 추출될 때 일련의 연령 스펙 트럼이 얻어진다. 따라서 “Ar / 39Ar 과 40K / 39K 의 비에서 암석의 연령 이 계산된다. 만일 지질학적 사건을 받지 않은 시료라면 “Ar/39Ar 의 비는 연속 적인 온도상승에서도 그 비에 변화가 없을 것이므로 낮은 온도단계에 서 얻은 연령과 높은 온도단계에서 얻은 연령이 동일할 것이다. 그러나 변성작용(재결정작용)시에 아르곤의 유출입이 일어났다면 각 단계의 연대는 다르게 나타날 것이다. 만일 문제의 시료가 처음 냉각 후 아르곤과 칼륨이 폐쇄계로 유지 되었다면 그때의 각 단계별로 얻은 연령은 일정해야 할 것이다. 그러 나 어떤 지질학적 사건에 의해 일부 방사성 아르곤이 유실되었다면 상이한 온도에서 추출된 “Ar/39Ar 비는 변화할 것이며 그때의 얻어 진 연령은 처음 냉각시간 이후의 연대가 될 것이다. 이런 현상을 Turner(1 9 68, 1969) 의 모델에 적용해서 변성작용 과정 에서 온도상승으로 인해 방사성 “Ar 이 부분적으로 유실된 K 함유광 물 입자의 “Ar*/39Ar 의 스펙트럼을 조사하기 위해 다음과 같은 모델 실험을 하였다. 암석 시료 중 변성사건 후 폐쇄계가 된 “Ar 의 부분유실이 일어난 광물입자를 택한다. 그런 시료 중 균일한 크기의 K 함유광물 입자를
단계적 가열법에 의해 분석하면 각각의 온도에서 추출된 “Ar•/3 9 Ar 의 비는 체계적으로 변화할 것이다. 가장 낮은 온도에서 주로 광물 표면에서 추출된 첫번째의 가스는 낮은 “Ar• / 39Ar l:l]를 가질 것이며 이는 변성사건 후 방사성 Ar 이 재축적되기 시작한 이후의 시간일 것 이다. 온도상승에 따라 계속적으로 얻은 가스는 Ar*/ 39 Ar 비가 계 속 증가하여 변성사건 과정에서 조금씩 조금씩 “Ar* 의 작은 양을 유
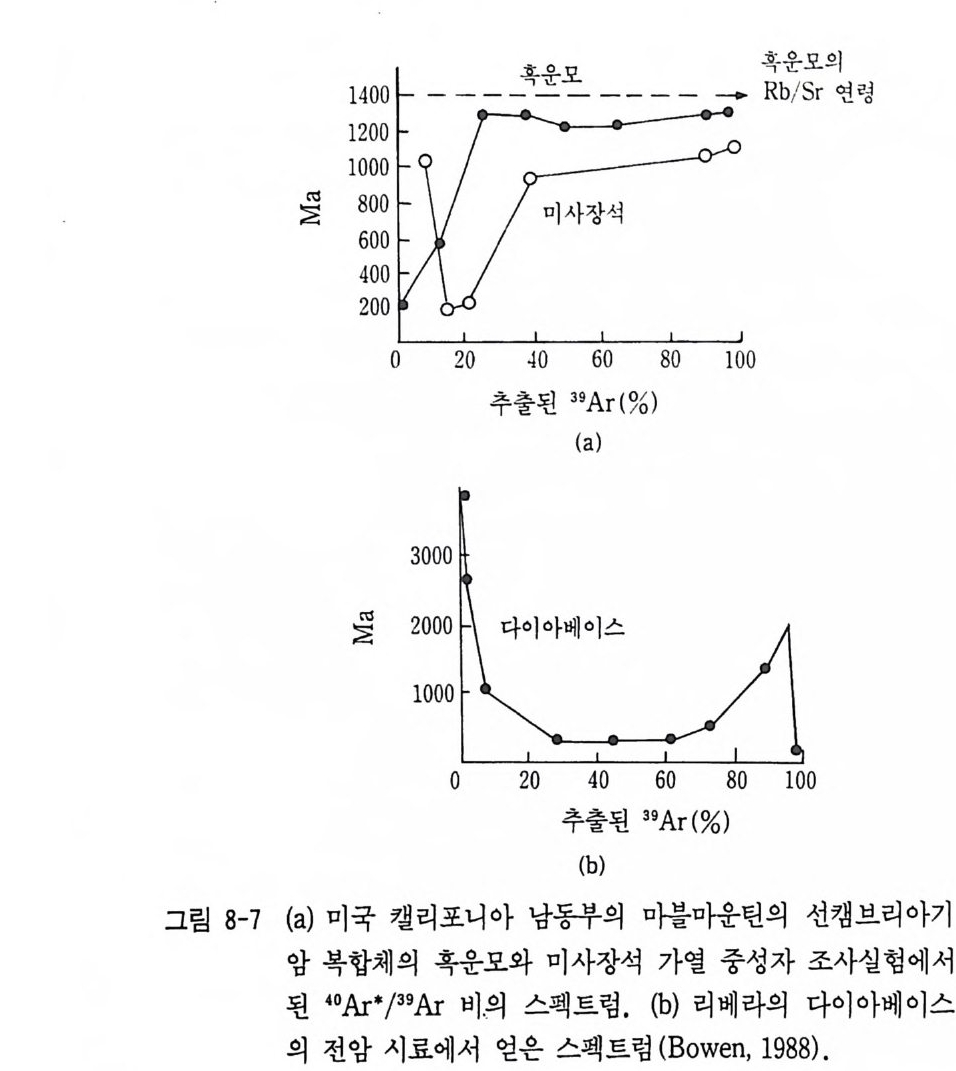 11240000 1 __•_ —.흑`—운 모— —- _ _____ _-.- : 흑Rb운/S모 r 의 연 령
11240000 1 __•_ —.흑`—운 모— —- _ _____ _-.- : 흑Rb운/S모 r 의 연 령
실한 부분의 위치수가 증가하면서 거기서 그때 나온 가스일 것 이다•. . 마지막에 방출된 “Ar* / 39Ar 비가 광물이 원래 냉각될 때를 대표하 는 시간에 가까운 값이 될 것이다. 따라서 광물의 단계적 온도상승 과정에서 저온에서 추출된 변성시기와 고온에서 추출된 초기 냉각시 기가 각각 얻어진다. 이것이 이 방법의 장점이다. Turner0969), Bo g ard 와 Hir sc h0980) 등은 석질운석과 충격변성 작용을 받은 운석시료 등과 달암석 (Dav i s, 1977) 그리고 변성지역의 암석광물 (Mar ti nez 등, 1984) 을 이 방법을 이용하여 측정하였다. 실례 를 들면 미국 캘리포니아 동남의 마블 마운틴 (Marble mounta in) 의 선캠브리아기의 기반암 복합체에서 혹운모와 미사장석의 단계적 가열을 통한 중성자 조사에서 얻은 “Ar* / 39Ar 에서 계산한 연령 스펙 트럼은 그림 8 -7 과 같다. 이 지역의 혹운모의 Rb-Sr 법 연령 1410 土 30Ma 이고 저어콘의 u . -Pb 연령은 1450Ma 이다. 그리고 보통 과거의 방법으로 측정한 혹운 모의 K - Ar 법으로 측정한 연령은 1152 土 30Ma 이고 미사장석은 992 土 26Ma 이었다. 그러나 그림에서처럼 흑운모의 고온가스 추출 연대는 1300Ma 가 얻어져 보통 방법보다 150Ma 더 오래된 연령이 얻어졌고 미사장석 은 심한 Ar 유실현상아 나타났다. 따라서 고온에서 추출된 Ar 가스 에 의한 연령은 결정화 연령 하한이 될 것이다. 또 다른 예로서, 알래스카의 녹색편암 중의 운모류와 각섬석을 550 °C 에서 50°C 간격으로 온도를 상승시 키 면서 얻은 39Ar 추출과 “Ar _39Ar 연령과의 관계는 그림 8-8 과 같다. 결정내부에서 유출되는 방사성 기원의 Ar 의 연령은 185m . y.이다 (S i sson 과 Onsto tt , 1986) . 凍結溫度 (Blockin g tem p er atu re) 가 변성 작용 의 최고온도에 해당될 것이므로 이 시기가 변성작용 시기로 보인다. 이의에도 Ar-excess 에 의한 연령도 이와 유사한 영향이 있으므로 해 석에 주의를 요한다.
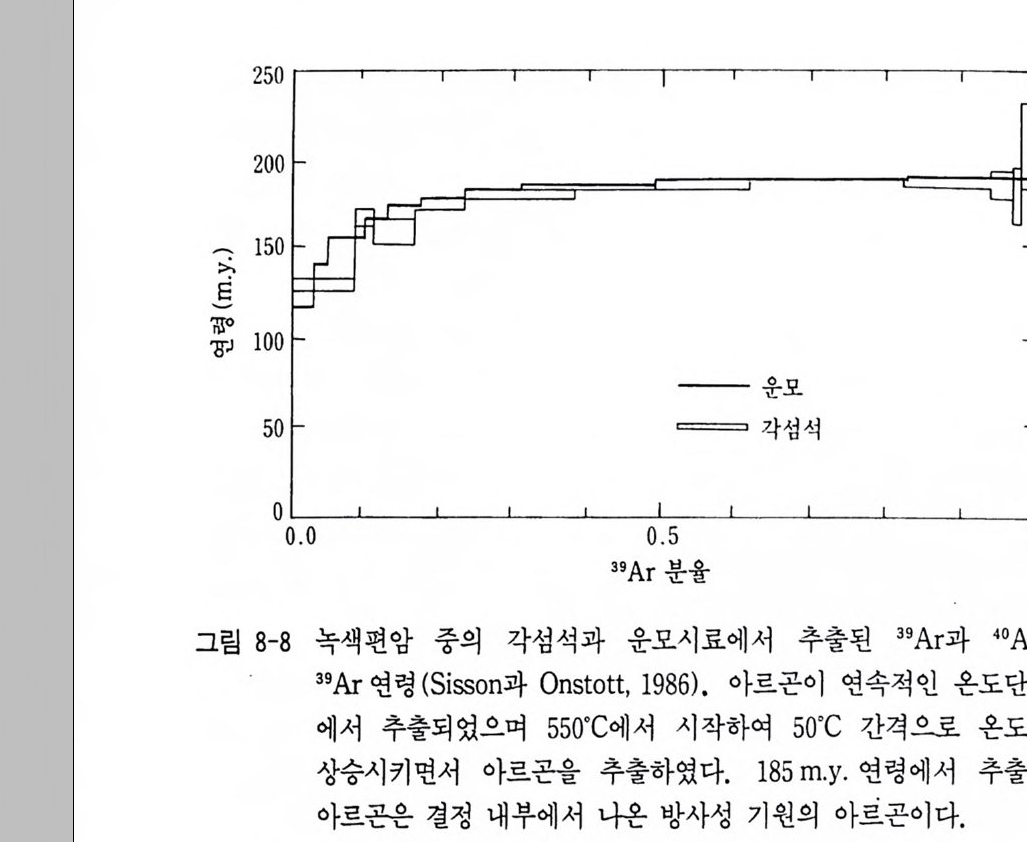 250
250
이처럼 “Ar/39Ar 의 연령은 Ar 유실이나 Ar-excess 영향이 있기 때 문에 광물의 산출상태에 따라 크게 달라진다. (1) 레이저를 이용한 아르곤 추출과 분석결과의 해석 원광물에 존재하는 Ar 가스의 추출을 위해 레이저 빔울 이용 개개 의 광물에서 Ar 가스를 추출하는 방법 이 개발되 기도 하였다 (Schae f fer, 1982) . 달암석 에 서 헬륨, 네 온, 아르곤의 산출상태 를 연구하기 위해 레이저를 이용하기 시작하였으며, 암석현미경과 연결된 장치에 서 광물입자에 레이저 빔을 쪼여 직접 Ar 가스를 추출, 액체질소 온 도에서 목탄으로 가스를 수집 하여 가스용 질량분석 계로 “Ar/39Ar 비 를 분석한다. York 등 (1981) 이 개발한 또 다른 방법은 빠른 중성자선을 조사했
던 0.5~1mm 직경의 광물입자를 아르곤 이온 레이저로 용해시키는 법 0] 다. 레이저를 이용하면 개개의 광물입자를 분석할 수 있으며 변질된 부 분을 분석에서 제거시킬 수도 있는 장점이 있다. 또한 시료의 양이 소량(마이크로그램)이어도 되며 칼륨, 아르곤의 보존에 있어 온도, 압 력, 변질의 영향을 줄일 수 있다. 또한 여러 시기의 복합각력암과 같 은 시료의 광물단체를 분리할 필요가 없다. Harr i son0981) 은 각섬석을 가열하여 여러 온도의 열수 조건에서 방사성 “Ar 이 광물내에 확산되는 실험을 실시하여 온도에 따른 “Ar 의 확산계수를 계산하였다. 그는 다음의 Fechti g-K albit ze r 식을 이 용하였다. D=D。 exp (— E/R T) 여기서 D 는 확산계수 (cm2 s 기, T(K) 는 온 도, Do 는 확산빈도를 나타내는 항 (cm2 s-1), E 는 가속에너지 (Kcal mole-1), R 은 가스상수(i .987cal deg -1 mo J e-1) 이다. 이것을 상용대 수로 표현하면 In D=ln D 。 -103 E / RT 로 직선식이 된다. 따라서 단계적 가열시 유출되는 아르곤으로부터 확산계수를 얻을 수있다. ln D 와 103 T 를 좌표축으로 잡으면 E=mR 이란 관계가 얻어진다. 각섬 석의 아르곤 확산계수를 경 험적으로 구하면 Do 가 0 . 024cm2 s-1 일 때 가속에너지 E=64.l 土 1 . 7 Kcal mole-1 가 얻어전다. 이 결과를 이용하여 이 광물이 80 µm 직경이 되는 閉鎖溫度 (Closure t em p era t ure) 는 578~49o · c 로 계산되며 다음의 Dodson 식을 이용하면 냉각속도는 soo·c Ma - 1 에서 5·c Ma-I 가 계산된다. Tc= ln( 『E『/R 儒. 2) 여기서 Tc 는 폐쇄온도이고 A 는 기하학적 항으로 타원형 입자는
55, 관동형 입자는 27 이다. dT / d t는 폐쇄온도에서 냉각속도이다. 각섬석의 폐쇄온도는 광물 크기가 커질수록, 냉각속도가 클수록 높 아지나 화학성분과는 무관하다. 몇 종류의 광물 폐쇄온도는 표 8-7 과 같다. 표 8-7 에서처럼 각섬 석, 혹운모, 칼리장석, 사장석, 미사장석 순으로 폐쇄온도가 감소하 고 있다. Ber g er 와 York (l 981) 는 캐나다의 온타리오 그랜빌 지역의 하리버 어돈 하이랜드(H al i bu rt on hig h lands) 에서 냉각속도가 975Ma 에서 20' C Ma-1 로 925Ma 에서 2'C Ma-1 로 700 Ma 에 0.3 'C Ma-1 속도로 접점 감소하고 있음이 조사되었다. 변성도의 연구에서 정암압 (L ith os t a ti c p ressure) 을 보정하여 온도가 700 ' C 였을 때 lOOOMa 에 21km 심도였음을 추정하였다. 또 냉각속도 곡선에서 lOOOMa 의 21km 심도에서 550Ma 의 4.3 km 심도로 약 37m Ma 의 속도로 융기하였음을 계산하였다. 이 같은 내용은 이 지역의 지질과 잘 일치하여 아르곤 동위원소 열 연대 (Iso to p e th ermochronome t er) 의 연구의 신빙성을 높혔다. 화산암 체의 냉각사의 해석에도 같은 방법을 적용할 수 있다. 이 방법을 이
표 8-7 냉각속도 5'C Ma-1 에서 구한 다양한 광물의 아르곤 확산속도에 의해 계산한 폐쇄온도 광물 폐쇄온도 입자크기(µ m) 각섬석 490 80 각섬석 685~53a 210~840 흑운모 373~21a 500~1410 K- 장석 230~18b 125~840 사장석 176~54a,b 125~250 미사장석 132~13 125~250 a . 신뢰할 수 있는 실험의 평균횟수 b. 냉 각속도를 0 .5'C Ma-1 로 가정
용하여 Nie l son 등 (198 6) 은 미국 유타의 신생대 화성암 복합체의 냉 각사를 해석했다. 즉 각섬 석 과 혹 운모의 K-Ar 연령은 각각 11. 8m. y . 과 10 . 8m. y. 이 고 아르곤 동결온도는 각각 5 2 0 ' C 와 275 ' C 였다. 그리고 저어콘과 인 회석의 휘션트랙 측정연령은 8 .3~8.9m. y과 8.1~9.1 m. y . 이며 트랙 의 출현온도는 7 5 ° C 와 1 25 ° C 였다. 이 결 과 를 이용하면 암체 형성시간의 변화에 따른 형성온도의 변화 를 도시할 수 있다(그림 8-9) . 이 그림에서 500 °C 이상에서부터 4 00 만 년 시간 간격 동안에 100°C 정도씩 온도가 냉각되었음을 알 수 있으며 , 빠른 냉각이 지각 심부에 서는 일어나지 않았으며 융기와 침식이 일어났었음을 알 수 있다• 지 하중온율은 30' K m - 1 로 가정하면 이 기간 동안에 0 . 6- 1. lmm / 년 속
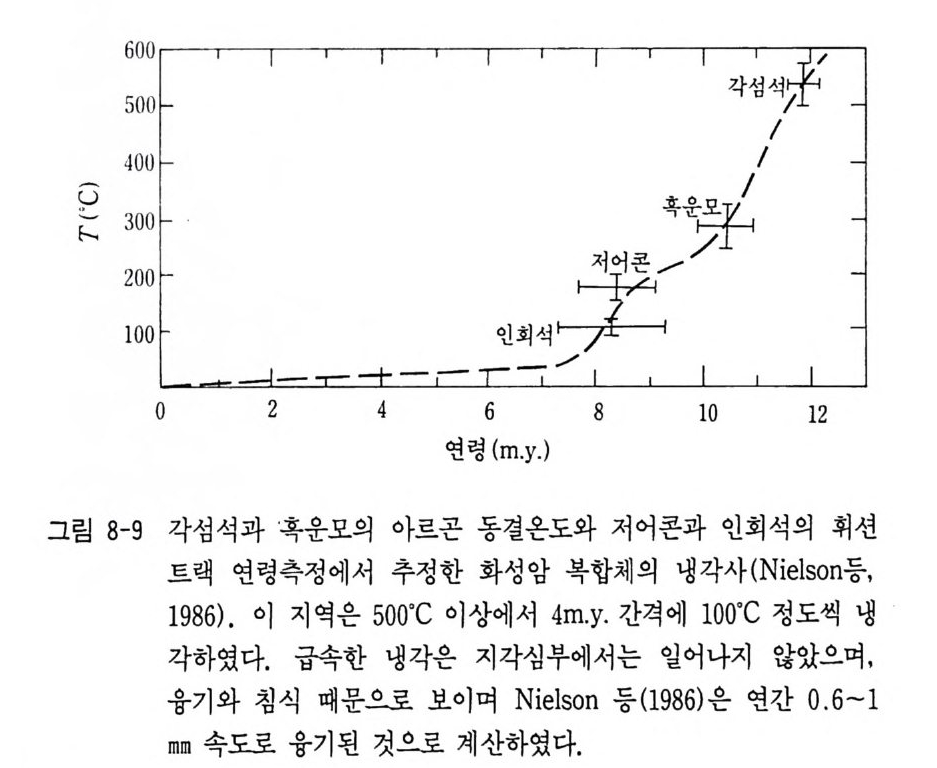 600, ’ 규,/
600, ’ 규,/
도로 융기가 일어난 것으로 계산된다. 4) 우라늄(토륨) -연 측정법 앞장에서 설명한 것처럼 우라늄 계열은 여러 단계의 붕괴를 거쳐 안정한 납으로 변한다. 238u 은 206Pb 으로, 235u 는 20 1 p b 로, 23 2 Th 는 20 8 Pb 로 각 각 변 하며 이 들의 자연에서 존재량은 각각 238U 99. 27 3 9 % ,, 235U o.12 0 4%0, 232 T h 100%, 이다. 추로 저어콘, 우라니나이트, 모나자이트와 기타 납 울 가전 광물들이 측정대상 광물이 된다. 우라늄 계열도 기본적으로 D=N(el1— 1 ) 식에서 다음과 같이 연령 과 관련된 식으로 표현된다. 206Pb= 238U (eA mt -1) 207 P b= 23S U (eAm t- 1) 208 Pb= 232 U (eA mt -1) 206Pb 측 정 치 = 2 06Pb 소생치 +23 8u (eA 23 —1) 220018 pP bb 축측정정치치 ==2 20018 pP bb 소초생생치치 ++2233520U ((eeAA2m3stt _—-11 )) 問) 측정치 =(二) 타치 +(국 )(eAm t -1) (1) 問) 축정치 =(二) 타치 +(국 )(e A 235 드 1) (2) (零) 측 정치 = (:曆) 터치 + (;옳) (eAmt _ l) (3) Rb-Sr 법에서와 같이 아이소크론에서 연령이 얻어진다. 그러나 일반적으로 U- P b 아이소크론은 적절하지 못한 경우가 많다.
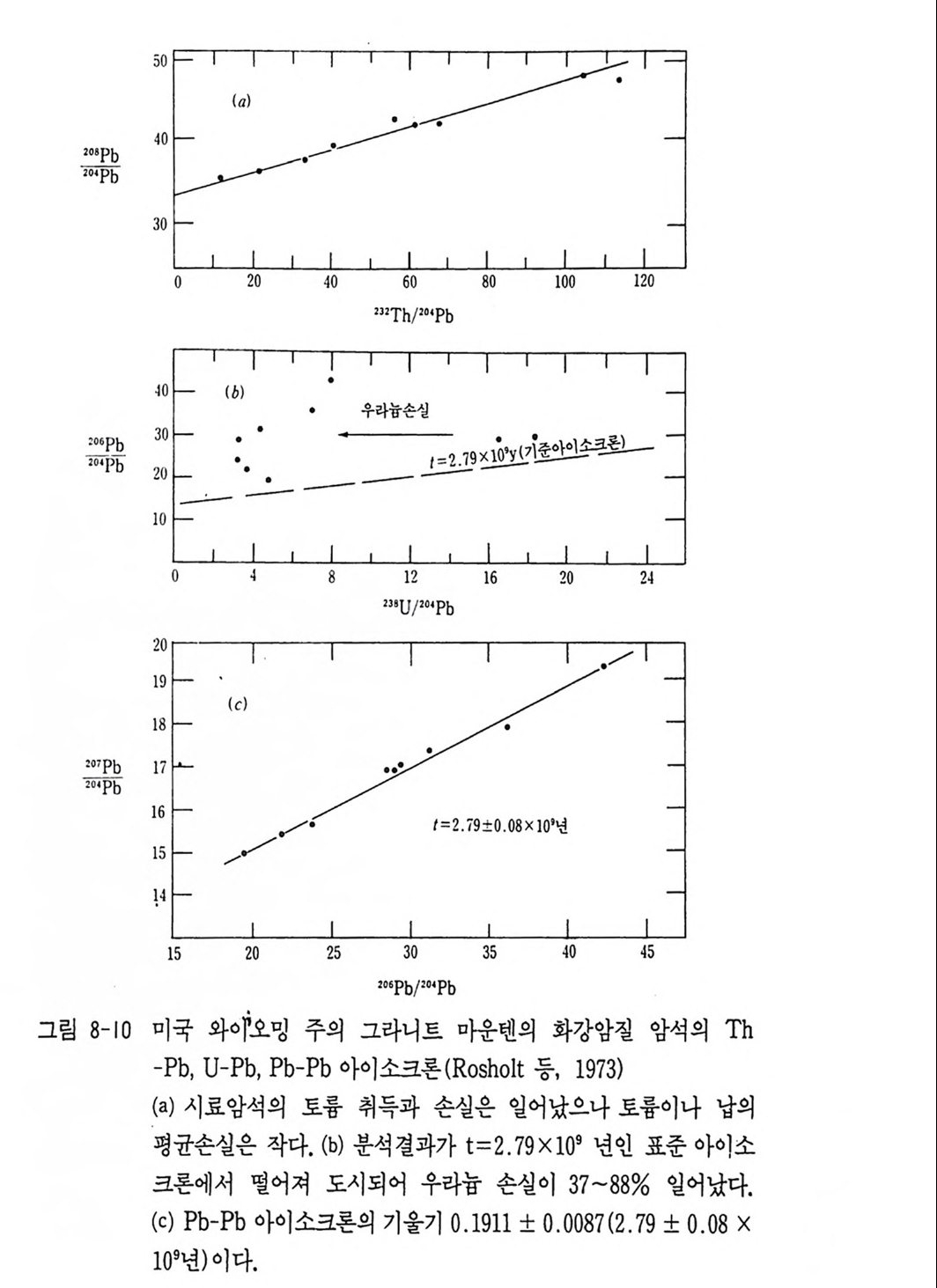 50, , I ' I 'I' /I '
50, , I ' I 'I' /I '
미국 와이오밍의 그라니트 마운틴 (Gran it e Moun t a i n) 의 화강암질 암석의 측정결과에서 암석의 화학적 풍화에 의해 우라늄이 현저하 게 유실되어 U-Ph 아이소크론은 부적절하게 나타났다. 그러나 Th- Pb 아이소크론과 Pb-Pb 아이소크론은 이의 영향이 바교적 적다(그 림 8-10). 동일 기원의 암석의 경우 U-Pb 계는 위의 ( 1 ) 식에서 ( 2 ) 식을 나누 므로 Pb 와 Pb 에 관한 수식으로만 표현되며, 이 식을 Pb-Pb 법 또는 207-206 법이라 하며 납의 동위원소비 분석만으로써 연령이 측 정된 다. 왜냐하면 시간 t 가 일정할 경우 이 식은 (20 7 Pb / 20 4Pb) i와 (2D6 P b / 204Pb) i인 한 점을 통과하는 직선들이 되기 때문이다. 이 조건은 (201 pb / 204Pb) 와 (206Pb/204Pb) 비가 기울기 m=l / 137 . 8(: ::: 二i)인 직선으로 도시되는 동일기원의 암석광물에서만 성립된다. 따라서 Pb- Pb 아이 소크론에서 연령이 얻어진다. Pb-Pb 법은 지질시대 동안 시료에서 Pb 가 존재하는 시료의 Pb 의 동위원소 비율에서 얻어지게 되므로 납의 유실(l ead loss) 의 영향을 가장 적게 받는다는 장점도 있다. 어떤 지질학적 사건에 의해 시료에서 납의 유실이 있는 경우에 는 U-Pb, Th-Pb 법의 연령은 참연령보다 젊게 얻어질 것이다. 따 라서 이것과 Pb-Pb 법과 바교함으로써 이 사실을 확인할 수 있게 된다. 납 유출입 이 일어나지 않은 시료라면 238u-206Pb, 235U-207P b , 232 Th- 2osp b, 201p b_ 2osp b 법으로 얻은 연령들은 모두 일치할 것이다. 이를 일치 연령 (Concordant ag e) 이 라 한다. 변성작용이나 동화작용, 지각변동과 같은 지질학적 사건으로 인해 납의 유출입이 있을 수 있다. 이로 인하여 둘 또는 둘 이상의 측정연 령이 일치하지 않을 때에는 불일치연령 (Disc ordant a g e) 이 얻어진다 (표 8-8).
표 8-8 우라늄 • 토륨 • 납 연령의 일치연령과 불일치연령 동위원소연령(년) 분석광물 시료위치 238u 23S u 232U 201 pb 亨亨亨亨 일치 연령 (Co nc ordant age s ) 사마스카이 트 (Samarskit e) Spr u ce Pin e , N.C ., 314 • 316 302 342 U.S.A . 저 어 콘 (Zi rc on) Wi tch i ta Mt s., 520 527 506 550 Okla., U.S .A . 저어콘 (Z i rcon) Cey lo n 540 544 538 555 피 치 브렌드 (Pit ch blende) Kata n g a , 575 595 630 Belgi an Cong o 우라니 나이트 (Uranin i te ) Romt ela nd, Nor- 890 892 900 920 way 두코라이트 (Thucol it e ) Wi tw ate r srand, 2 , 110 2 ,08 0 -2,0 7 0 South Afr ica 불일치연령 (Disc ordant age s ) 저어콘 (Z i rcon) Cap et o w n, South 330 356 · 238 530 Afr ica 저 어 콘 (Zir c on) Bearto o th Mt s. , 770 1,400 - 2,580 Mont. , U .S .A . 저 어 콘 (Zi rc on) Qu artz Creek, 930 1,1 3 0 515 1,540 Colo., U .S.A . 제노타임 (Xenoti m e) Uncomp a hg r e, 3,1 8 0 2,065 1,1 0 0 1,640 Colo., U .S.A. 육시 나이 트 (Eu xen ite) Wakefi eld , 620 710 550 1,0 0 0 Qu ebec, Canada 저어콘 (Z i rcon) Beartp o th Mt s. , 1,660 2,380 870 3,0 8 0 Mont. , U.S.A . 자료출처 : Hami lton , (1965)
(1) 콘코디아-디스코디아 다이아그램 206Pb*/238U=eAe t _l 와 207Pb/235U=eAs t -1 에서 동일한 연령을 가전 다면 붕괴 상수와 연령 에 서 206Pb/23su 와 201 p b/23su 를 축으로 잡으면
표 8-9 지질시대에 따른 eht— 1, eA 1_1 , 207P b/ 2 06P b 비의 수치계산결과 연령 f(1 09 년) e(Ai t ) -1 e(A2 1) - J (零)· 。 0.000 0 0.000 0 0.046 04 0.2 0.0 3 1 5 0.217 7 0.0 5 0 12 0.4 0.0 6 4 0 0 . 482 8 0 .05 4 71 0.6 0.0 9 7 5 0.8 05 6 0.0 5 9 92 0.8 0.1 3 2 1 1.19 8 7 0.0 6 5 81 1.0 0 .16 7 8 1. 677 4 0.0 7 2 50 1.2 0.2 04 6 2.2 6 0 3 0.080 12 1.4 0.242 6 2.970 1 0.088 79 1.6 0.281 7 3.834 4 0.098 72 1.8 0.3 2 2 1 4.886 9 0.110 00 2.0 0.363 8 6.168 5 0.1 2 2 98 2.2 0.406 7 7. 729 2 0.137 83 2.4 0.451 1 9.6 2 9 6 0.1 5 4 82 2.6 0.4 9 6 8 11.943 7 0.1 7 4 36 2.8 0.5 4 4 0 14.7 6 1 7 0.1 9 6 80 3.0 0.592 6 18.193 1 0.222 66 3.2 0.6 4 2 8 22. 37 1 6 0.2 5 2 41 3.4 0.694 6 27.459 7 0.286 72 3.6 0.7 4 8 0 33. 65 5 6 0.326 34 3.8 0.8 0 3 0 40. 20 0 4 0.3 72 12 4.0 0.8 5 9 9 50. 38 7 8 0.4 2 4 98 (零)·=굽터뿡邸국)
표 8-9 에서 계산된 수치로 도시하면 콘코디아 (Concord i a) 곡선이 얻 어진다(그림 8-11 ). 죽 결정화 초기에는 함우라늄 광물에 방사성 기원의 납은 전혀 포 함되시 않은 기원점에서부터 폐쇄계가 유지되었다면 시간이 지남에 따라 점진적으로 방사성기원의 납이 생성되어 포물선과 같은 콘코디 아 곡선이 얻어질 것이다.
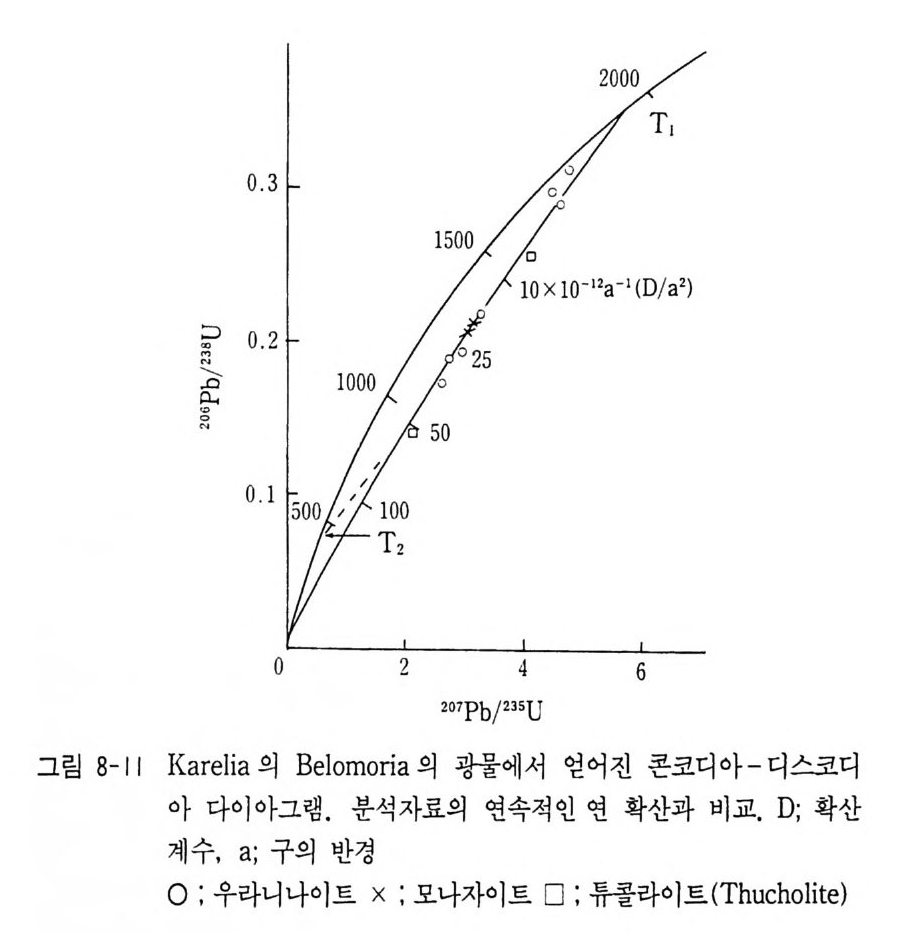 2000
2000
그러나 변성작용이나 풍화작용 등 지질학적 사건으로 인한 납 유실 이나 우라늄의 취득이 일어난다면 콘코디아 곡선상에 도시되지 않을 것이다. 예를 들면 그림 8-11 에서처럼 모나자이트 광물의 경우 시료내 에 2os p b/201 p b 비 가 일정 하기 때문에 콘코디 아 곡선 아래 에 직 선으로 도시된다. 이 직선과 콘코디아 곡선이 만나는 두 점 T1 과 T2 가 각각 얻어진다. 이때 T1 은 암석이 형성된 시기이고 T2 는 납 유실의 시기가. 된다.
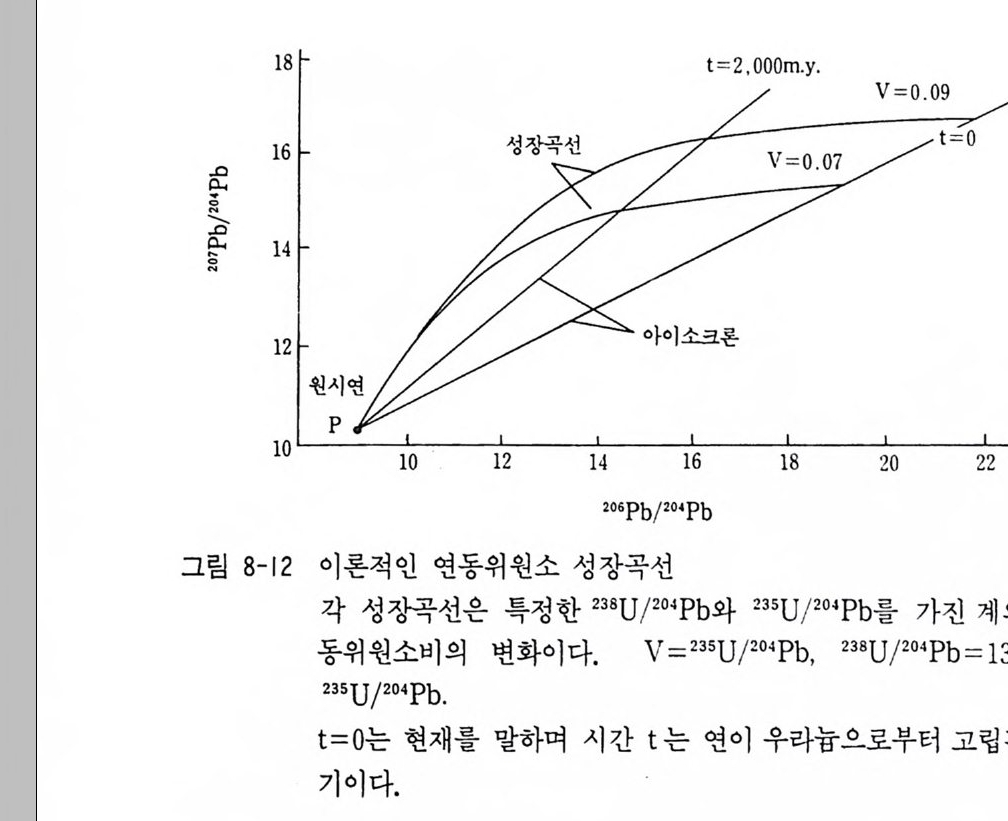 18 t = 2 , 000m.y.
18 t = 2 , 000m.y.
그림 8-12 에서처럼 원시 연 (P 점)에서 2000 m.y. 현재 (t =O) 로 움에 따라 연 동위원소비의 값은 점점 증가하고 있다. 이같이 시간에 따른 연 동위원소의 비의 증가를 나타낸 곡선을 연 동위 원소 성 장 곡선 (Lead iso to p e grow th curve) 이 라 한다. 위의 식 (1)’ 과 (2) '식에서 ((220076PPbb//220044PPbb)) tt -_ ((2200 76PPbb//22 00 44PPbb)) TT (국)현재 ::::::二 :::::: 의 관계가 얻어져 y =bo+A(x-ao) 인 1 차식의 관계가 얻어진다. 이때 ao=(禪 206P깁b T’ bo= (零 )T
이처럼 불일치하는 연령으로 나타나는 직선관계를 디스코디아 (D i scord i a) 라 부른다. 그런데 T 2 는 납 유실의 방식에 따라 지질학적 의미를 가질 수도 있고 가지지 않을 수도 있다. T2 에 대한 해석은 0 순간적 인 납의 유실 (Ep iso dic lead loss) (2)(2 ) 연속 확산에 의 한 납 의 유실 ® 팽 창 (Dila ta n cy) 모델 @ 화학적 풍화에 의 한 납의 유실 등이 제안되고 있다. 순간적 안 납 유실은 Cata n zaro (1963) 와 Weth e rill (1956) 등이 제 안 한 것으로 일정한 T 2 시기 에 납 유실이 한순간에 일어난 것으로 해석 한 것 이다. 그러나 이 해석은 젊은 연령을 가진 시료인 경우 납 유실 의 시기도 같이 젊어지는 관계가 얻어져 한 번 이상의 · 순간적인 납 유실이 일어난 경우의 시료는 해석이 불가능하다. 연 속확산 에 의한 납 유실은 그림에서처럼 납 유실이 긴 지질시대에 걸쳐 연속적으로 유출된 것 으로 해석하고 있다 (T i l t on , 1960). 이 경 우 T 2 는 지질학적으로 의미가 없어진다. T il t on 은 저어콘의 형성 역 사 를 통하여 연속 납 유실이 일정한 온도에서 일어났으며 D/ 강가 시 간의 변화에 따라 변화하지 않는다는 가정하에서 일어난 것으로 해석 하였다. 팽창모델은 Gold i ch 와 Mudre y (1972) 에 의해 제안되었다. 우라늄, 토륨과 연을 함유하고 있는 광물이 방사성 붕괴로 인하여 방사성 손 상 (Rad i a ti on dama g e) 을 받는다는 사실을 알게 되었다. 광물내에 U 과 Th 의 함량이 증가하고 지질시대가 증가함에 따라 손상 부분이 증 가하여 결정의 손상된 부위에 물이 유입된다. 이 물은 융기나 침식으 로 인해 광물에 압력이 제거되기 전까지는 광물내에 고착되어 있었으 나 저어콘이 팽창될 때 이 물이 용해된 방사성 납을 함께 유출시켰다 는 것이다. 따라서 방사성 납의 유출은 선캠브리야 순상지의 결정질 기반암체의 융기나 침식과 관계가 있다고 지적하였다. 화학적 풍화에 의 한 납의 유실은 Ste m 등(1 966) 에 의해 제 안되 었 으며 화학적 풍화로 인하여 모원소와 딸원소 사이의 비가 변화하였다
는 것이다. 미네소타의 모르돈 편마암으로부터풍풍화된 저어콘의 시료 를 연대측정한 결과 연령이 일치하지 않았으며, 207P b/ 20G p b 연령이 가장 오래된 연령으로 얻어졌고 풍화된 저어콘은 85 % 까지 방사성원 의 납이 유실되어 있었다. (2) 연 동위원소의 성장 안정동위원소인 204Pb 를 제의한 206Pb, 201p b , 2 o s p b 의 납 동위원소는 모두 우라늄계열의 광물이 붕괴로 형성된 안정동위원소이다. 이들 방사성기원의 납의 양은 시간이 경과함에 따라 그 양이 점점 증가하고 있다. 오늘날 시료 중의 납의 동위원소비를 (Pb/ Pb )t 그리 고 (U /Pb) p라 하고, 지구의 형성 당시의 납 동위원소의 비 (Pb/ Pb h 라 하면 우라늄광물이 시간에 따라 붕괴되어 생성된 납의 동위 권소 비 는
(~)t=(電 )T+( 국) 현재 (e• 2 3s T -e• 2os t) (ll' (무 )1= 二 )T+( 국) 현재 (e•2 3 sT_e •2ost) (2)' (零)t=(零 )T+(~) 현 재 (e•202T 一 e • 232 t) (3). 의 관계가 성립한다. (Pb/Pbh 의 값은 태양계의 형성초기의 물질을 대표하며 태양계 생 성 이래 우주공간에서 화학적으로 폐쇄계에 있었던 철운석내의 납 (銅 동위원소비는 생성 이래 거의 변화하지 않은 원시 연 (Pr i mord i al lead) 의 값이다. 원시 연으로 대표되는 Cany on Diab lo 철운석의 연 동위원소비는 각각 206Pb/204Pb = 9 . 307 , 201Pb/204Pb = 10 . 294 , 208Pb/2 ° 4Pb = 29 . 476 이 다.A = l37 .8e8A m(eTA 2 _3 8 eT'2 _ 3 5e1A 2381 ) (/ 23司BU 丁 ) 현재 = 137 .88 이다. 여기서 얻어지는 아이소크론은 원시연의 값인 (a 。, b 。)점을 지나며 T 와 t에 의해 기울기가 결정된다. 위 식에서 t =O 와 원시연의 값과 오늘날 암석광물내의 납인 현생연 (Modern lead) 동위원소 성분에서 지구의 형성연대를 계산할 수 있 다. 여기서 얻어진 지구의 연령계산 결과는 4,500~4,750rn. y.로 기타 동위원소 를 이용한 연령측정 결과와도 비교적 잘 일치하고 있다. 연 동위원소 성장은 지각물질의 전화를 찰 나타내 주는 것으로 연 동위원소 전화의 해석은 단일 스테이지 모델과 2 스테이지 모델 그리 고 다단계 모델 등이 있다. 이것은 뒷장에서 자세히 설명하기로 한 다. 5) 사마리움-니오디미움 측정법 사마리움 (Sm) 동위원소는 141Sm(15.0%), 148SmUl .2% ), 149Sm (13. 8% ) 이 있으며, 이의 방사성 붕괴로 생긴 니오디미움 (Nd) 동위 원소는 u3Nd, t44 N d, 14sNd 가 알려 져 있다. 이 중 141Sm 이 a 붕괴해서 143Nd 가 되며 이때 반감기는 1.06 X1011 년으로 대단히 길다. 1970 년대 초부터 가열 이온화 질량분석기 개발로 국소량의 동위원 소비 분석이 가능해졌으며, Sm-Nd 동위원소비 분석은 Lug ma ir 등 (1975), Ric h ard 등 (1976), O'Ni on s(1977), Wassserburg 등 (1981)I De p aolo 와 Wasserburg( 19 76) 등에 의해 본격적으로 시작되었다. 특히 Nd/Sm 동위 원소는 Rb/Sr 이 나 U (Th) /Pb 동위 원소보다 변 성작용에도 강한 특성을 가지고 있어 변성암의 원암의 연령측정에 대
단히 유용하다. 특히 Rb/ Sr 함량이 너무 적거나 너무 많아 연령측정에 부적합한 시료의 경우에 이 동위원소가 유용하게 이용될 수 있다. 암석광물의 사마리움과 니오디미움의 함량은 표 8-9 (a) 와 같다•
표 8-9 (a) 지구및 지구의 암석광물의 사마리움과 니오디미움의 평균함량 (Faure, 1986) 광물,암석 S(pmp m ) A(p,dp m ) 荒Sm (광물) 감람석 Q. 07 (1) (b) 0 . 36(1) 0 .19 사방휘석 3.3 4 (35) 9.09(34) 0.3 6 7 각섬석 6.0 3(3) 17. 3(2) 0.347 흑운모 37.0(2) 171 . 5 (2) 0.215 사장석 0.5 4 1(8) 1. 85 (9) 0.292 K· 장석 3.77(4) 26(3) 0.14 석류석 1.17 (15) 2 .17 (5) 0.539 인회석 223(2) 718(2) 0.311 모나자°]트 15, 000 (1) 88 , 000 (1) 0 .17 (화산암)코마타이트, 피크라이트 1.14 (15 ) 3.5 9 (15) 0.3 1 7 소레아이트(시생대) 1. 96 (23) 6.6 7 (23) 0.2 9 3 MORB 소레아이트 3.30(73) 10. 3( 78) 0.3 2 0 대륙 소레아이트 5.32(657) 24. 2( 657) 0.2 2 0 칼크-알칼리 현무암 6 . 07 (24) 32.6(25) 0.1 8 6 알칼리 현무암 8 .07 (65) 41. 5(62) 0 .194 조면암 14 .1 ( 8) 73 . 2 (8) 0.1 9 2 류사이트 현무암 15. 1( 29 ) 81. 4 (30) 0.1 8 5 안산암 3.90(28) 20.6(40) 0.189 석영안산암 5.05(32) · 24 . 9 (33) 0.202 유문암 4.65(10) 21. 6 (11) 0.2 1 5 (심성암)헤르즈버가이트 0.0025(2) 0.0085(2) 0 . 29 (4) 레저라이트 0.5 82 ( 19 ) 2.28(19) 0.2 5 5 페리도타이트
반려암 1.7 8 (52) 7.5 3 (56) 0.2 3 6 에크로자이트 2.61(5) 8.6 4 (5) 0.3 0 2 석영섬록암 4 .01 (9) 16.8(9) 0.2 3 8 몬조니암 5.31(10) 26.4(10) 0.200 화강섬록암 6.48(22) 29. 9( 22) 0.216 화강암 8.2 2 (587) 43.5(588) 0.188 그레뉴라이트 4.9 6 (16) 31. 8 (30) 0.156 섬장암 9.5 ( 8) 86. (8) o.1 1 네펠린섬장암 14.0(2) 75. 5( 2) 0.185 킴버라이트 8.0 8 (37) 66. 1( 37) 0.122 카보나타이트 38.7(47) 178 . 8 (47) 0.1 2 6 (퇴적암)해수 0 . 545 X 10- 6( 12) 2 . 58 X l0~6 (19 ) 0.2 1 1 셰일 10 . 4 (949) 49.8(949) 0.2 0 9 그레이와케 5.0 3 (6) 25. 5( 6) 0.197 사암 8.9 3 083) 39 . 4 (319) 0.2 2 7 석회암 2.0 3 025) 8.7 5 (125) 0. . 23 2 석인탄산 영암 3411 .(160 ( 22)) k 12248 .0 70(22)) 00..23646 ( 외암광석계물과의 fa 가: 많 P 은 유 에리이질 콘드 4811.. .23 277 (((722)40 )) 12444 8..4 .051 (((2724)0) ) 000..3.32 417 407 라이트 콘드라이트 0 .199 (41) 0. 햏 (39) 0.3 2 0 휘석-에이콘드라이트 0.69105) 1.91(15) 0.360 사장석-에이콘드라이트 0 . 507 (5) 1. 92 (5) 0.2 6 3 텍타이트(지구) 4 . 81 (16 ) 26 . 6 (16 ) 0.10 자료 출처 ; Herrmann(l979) 과 Faure(1 9 86)
뒤에 설명하겠지만 Hawkeswor th와 Cals t eren (1 983) 에 의해 시료 의 1 ◄ 3Nd/1 ◄◄ Nd 비와 87Sr/86Sr 비에 대한 그림에서 상부맨틀에서 미량 원소의 이동과 지각암석의 지구화학적인 혼염의 영향을 설명할 수 있 는 재미있는 연구결과를 얻었다.
그러나 이의 동위원소비의 분 석 은 가 타 동위원 소 에 비해 어렵다. 측정원리는 위의 기타 방법에서와 감 이 :::엷 =( ::麟 ), + : : ::問 (eu -1) 의 관계식이 성립한다. 여기서 얻어전 아이소크론에서 암석의 연령이 얻어진다. 예를 들면 아폴로 17 호가 채취한 현무암 시료의 분석 결 과 는 그림 8-13 과 같이 아이소크론 연령 3 . 7 土 0 . 0 7X 10 9 년과 (143Nd/ 1H Nd)i 값 이 0 . 50825 土 12 가 얻어졌다 . 이 방법은 Rb/Sr 에 비해 정밀측정이 가능하고 Rb / Sr 과 U / Pb 법의 측정자료와 비교할 수도 있다. 그리고 에이콘드라이트와 같이 Rb/ S r 의 함량이 적어 연대측정이 불가능한 시료라도 이 방법으로 가능하
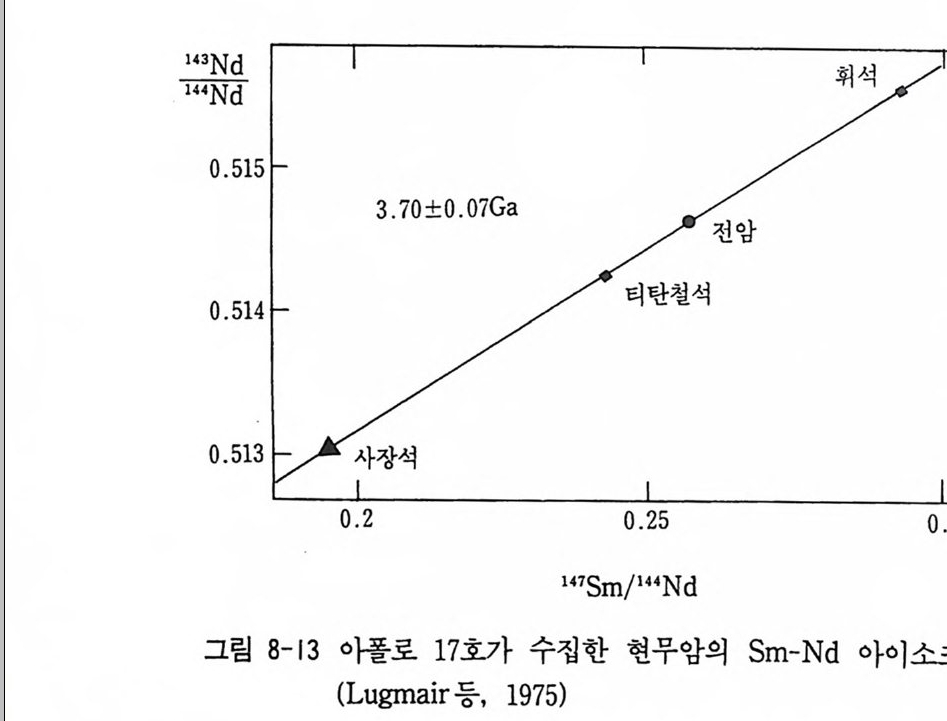 떄 휘 석
떄 휘 석
다. ( 1 43N d / 1 44 Nd ) 의 초 생치 가 태양계 물질의 진화, 특 히 지구물질의 진화 설명에 유용하게 이용되고 있다. 왜 냐하면 143 Nd / 144N d 은 Sm - Nd 의 화학적 유사성 에 서 맨틀과 지 각 의 분리라는 대규모의 분화현 상 설 명에 적합하기 때문이며, 88S r/8 6S r 은 지 각 물질과 멘틀물 질 의 혼합 해 석 에 유용하기 때문이다. (1 43N d / 144N d ) 와 (87 Sr / 86 Sr) 의 초생 치 를 도시한 그림에서 암석 성 인이 다른 여러 화 산암의 구분이 가능해지고 있다 ( 그림 8-14 ) .
 £OL
£OL
그림 8-14 에서 보면 중앙해령산 현무암 (MORB) 이 부의 경향을 나 타내고 있다. 호상열도와 판의 내부에 위치한 화산이나 대륙지각 물질의 구분이 가능해졌으며, 원퇴적지 퇴적물은 해수의 값으로 수령하고 해수-현 무암의 상호반응의 결과로 스트론듐 동위원소비의 변화가 현저하게 나타나고 있다. 해수 중에는 스트론튬 함량이 높으나 니오디미움의 함량은 대단히 낮기 때문에 변질된 해령저현무암에서 이 갇은 현상이 잘 나타난다. 해수 중의 많은 양의 Sr 과 Nd 는 육지에서 유입된 것이며 호상열도 의 암석에서 높은 87Sr/86Sr 비는 해수의 영향으로 결국 대륙기원의 스 트론튬의 순환을 의미하고 있다. 이 같은 비교는 동시기의 암석에 대 해서만 의미가 있으며 그 당시의 지구의 평균 동위원소비에 대하여 도시되어야 한다. 그래서 De p aolo 와 Wasserbur g(1 976) 는 t백만 년 전에 형성된 시 료의 초생치를 그 당시의 균일한 값의 유니폼리저버 (UR ; Unif orm reservoir ) 또는 콘드라이 트 유니 폼리 저 버 (CHUR ; Chondri tic unif orm reservo i r) 의 동위원소비와의 편차로 다음과 같이 표시하여 암석성인 등을 설명하였다. 瓚=[~ 1] X1 04 끊= [ 8:홍 r /I: 홍; ;:~-1] x 104 여기서 맨틀물질의 전화를 설명하기 위해 UR 과 맨틀물질의 동위 원소비를 CNd, csr 로 표시하고 비교적 젊은 화산암에 대하여 도시한 것이 그림 8-15 와 같다. 여기서 CNd=O( 운석을 기준으로 한 것임), csr=O(UR 을 기준으로 한 것임)은 지구의 평균성분에 근사한 값이다.
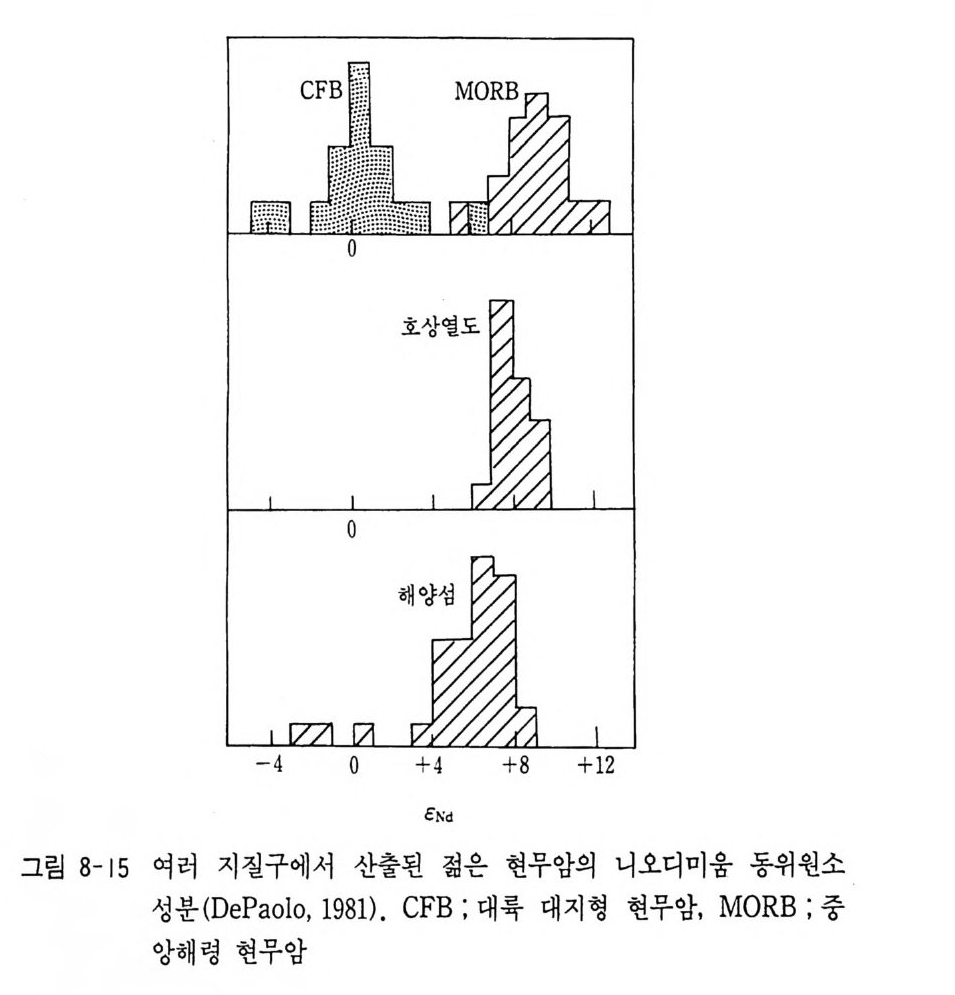 。
。
여기서 CNd, esr 자료가 직선 (eNd=- Q .37esr) 으로 배열되는데 이 를 맨틀배열 (Man t le-arra y)이라 부르고 있다. 이 갇은 배열에서 균질 인 원시맨틀 물질에서 마그마가 생성되어 점차적으로 지각을 형성하 였다는 연속 지각형성모델을 설정하기도 하였다. 그립 8-15 에서 보면 중앙해령 에서 동남하단으로 감에 따라 분포가 직선에서 벗어나 넓어전다. 이 같은 현상의 원인에 대하여 베니오프 대 쪽으로 섭입된 해저지각 때문이거나, 맨틀대류로 인하여 섭입된
대륙지각 또는 마그마의 상승시에 맨틀물질과 지 각 물 질 의 혼합 때문 일 것이라는 등의 여러 해석이 나오고 있다. 해양섬, 베니오프대, 대 륙 등과 같이 상이한 지구조 환경에서 형성된 젊은 현무암의 C N d 값 은 그림 8-15 와 같이 그 지역의 암석성인에 따라 다르다. (l) T 정晶 연령 T 陶 연령의 계산과 이에 대한 지질학적 해석이 De p alo 와 Wass-erburg ( l976) 과 McCulloch 와 Wasserburg (19 78) 에 의 해 이 루어 졌 다. 각 실험실간의 분석과정과 자료환산 방법이 달라서 원시 니오디미 움 동위원소의 비와 콘드라이트 리저버의 1 43 Nd / ' 44 Nd 비에 불 확실성 이 있다. Sm-Nd 법을 이용하여 연대를 측 정하기 를 원하 는 지질학자 둘은 동위원소 희석법에 의하여 Nd 과 Sm 의 농도 측 정에 사용된 스파 이크용액의 적절한 보정과 질량분석기에서 동위원소 분별의 질량의 조성울 보정하기 위하여 동위원소 분별법을 사용하여 보정하여야 한다. 캘 리 포니 아공대 (Califo rn ia Instit ute of Technolog y) 에 서 는 143 N d/ 144_N d 비를 150Nd/142Nd=0.2096 (J acobsen 과 Wassreburg, 19 8 0) 와 14s N d/ 142 N d= O .636151(Wasserburg 등, 1981) 로 보정하고 있다( 표 8 선 (b) ). 기타 실험실에서는 보정을 위하여 148Nd/144N d=0. 24 1578, 146 N d/ IHNd=O.7219 등을 사용하기도 한다. 1 4 6Nd/14 2 Nd = O . 636151 로 보
표 8-9(b) 현재의 콘드라이트 리저버 성분에 상응하는 니오디미움 동위원 소비 (Wasserbur g등, 1981) u2Nd 1•3N d 1“N d I“Nd 148Nd ISO N d 古 口 了 國 玉 國 (a) 1.138305 0.511847 0.348956 0.7 2 4 13 4 0.2 4 3075 0.2 3 8619 (b) 1.1 4 1827 0.5 1 2638 0.348417 0.7 2 19 0.2 4 1578 0.236418 (a)½,?:-1 80/160=0.00211, 1 7 0/160=0.000387 의 산소 동위원소비 를 가지고 있 는 Nd0+.2 } 146Nd/1 4 2Nd=0.636151 의 동위원소 분별로 보정한 현재의 CHUR (Chondriti c unif orm reservo ir-)의 니오디미움 동위원소비. (b~은. 146Nd/ 144Nd=O . 7219 로 다시 보정한 값임.
정한 콘드라이트 리저버의 l43N d / 144Nd 값은 0.511847 이며 146Nd/ 144Nd=O .72 19 로 보정하였을 143 Nd /1 44 N d 값은 0.512638 이 된다. T~ ~UR 연령이란 시료의 현재의 Sm / Nd 과 l43Nd/ 14 4Nd 비가 CHUR 의 l 43 Nd / 144Nd 비와 동일하였던 시기를 말한다. 이 연령은 I{HUR = I견 H UR _ ( Il44 雷 )。 (e AI _ 1) CHUR 로 표현된다. 여기서 I t H U R 는 과거의 특정 t 시기에서의 CHUR 의 143Nd/ '44 Nd 비 이며 I 은 H UR 는 현재의 CHUR 의 143Nd / '44Nd 비로서 0.512638 이다. (홀 )O 려질운석의 분석에 의한 CHUR 의 현재의 값은 CHUR 0.1967 이다. 어떤 특징시기 t 에서 CHUR 의 143Nd/1 44 Nd 의 비는 ItH U R= (H3Nd/l “N d) t 로 표현된다. 따라서 。 I8HUR_( 국) (e-1) CHUR =(접罰 -(국 ):(e-1) 가된다. 여기서 m 은 암석 (R) 에서 측정된 값이고 O 는 현재의 CHUR 에 해 당하는 값이다. 암석의 모델 연령은 위식은 t 에 대하여 푼 것으로
다음 식과 같다. t= +nl (二)〔m : U R+1l (l) 이 방법으로 측정된 연령은 측정하고자 하는 암석이 콘드라이트 저 장소에서 Nd 이 분리된 시기 이후에는 Sm / Nd 비가 변화되지 않았을 경우에만 지질학적으로 의미를 가진다. 이런 조건은 희유원소의 지화 학적 특성이 알칼리 금속과 알칼리토류 금속과 대단히 유사하므로 Rb 과 Sr 보다 Sm 과 Nd 이 더욱 적합하다. 일반적으로 지각의 암석의 Sm / Nd 비는 변성작용이나 침식 , 퇴적 과정에서 변화되지 않는다. 그러므로 위의 식으로 계산된 모델연령은 암석에서 Nd 이 지각에 채재한 시간으로 간주할 수 있다. 예를 들면 500Ma 전에 관입한 화강암 시료가 관입한 시기는 Y 점 이며 앞의 (1) 식에 따라 그 후 YZ 선을 따라 진화되었다. Y 점에서 143Nd/144Nd 비는 화강암의 니오디미움 동위원소 초생치로 동일 시기 의 CHUR 의 값보다 분명히 낮다. 만일 화강암 시료의 Sm/ N d 비가 그 기원지역의 비와 같았다고 가정한다면 500Ma 부터 기원지역에서 XY 선을 따라 진화한 것이 되어 CHUR 직선과 XY 직선의 교차점 X 점이 바로 T 성 ~UR 연령이 된다(그림 8-16). 이 T 정~UR 연령은 CHUR 내에서 단일스테이지와 현재의 값과 유사 한 Sm/Nd 비 범위내에서의 또 한 단계의 2 스테이지 진화모델 (Two-sta g e model) 을 가정하지 않을 수 없게 한다. 따라서 이 모델을 사용햐려면 2 스데이지 모델의 적용 가능성과 특 정 암석이 기원저역의 암석의 Sm/Nd 비와 같아야 한다는 전제조건이 필요하게 된다.
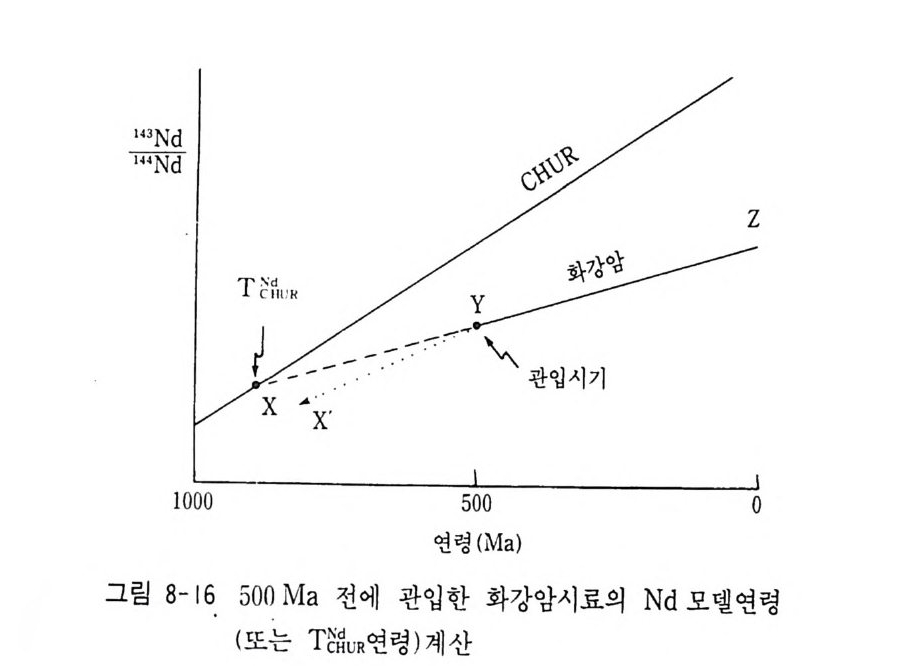 毒 ct` t
毒 ct` t
T 성 ~UR 연령에서 새로운 대륙지각의 형성, 고기 지각의 존재확인, 퇴적지의 기원, 테레인의 연대추정 등 대륙지각의 전화연구에 새로운 연구수단이 되고 있다. 이와 관련된 연구로 Nohda 와 Wasserbur g (1986) 는 일본해 부근의 시료의 스트론튬과 니오디움을 분석하여 마그마의 기원울 해석하였 다. 그린터프 지역의 화산암은 cN d= -0.9 ~ +5.7 이고 csr=14.1 ~ 16 .3 으로 지질시대에 따라 규칙적으로 멘틀 배열선에 도시되었다. 그리고 동위원소 성분의 전이가 일본해의 Back-arc 확장과 관계된 15 Ma 시기를 전후하여 확장 이전과 확장 이후의 지구조 발달과 관 련이 있는 것으로 해석했다. 전자의 화산압에는 동위원소가 부화되어 있고 후자는 결핍되어 있 었다. 유명한 구로꼬 광상도 이 전화의 범위내에 들어가며 대륙기원의 물 질이 기여된 경향을 나타낸다.
Palmer 와 Elderfie l d (19 85) 는 대 서 양 퇴 적 물 중의 유공충의 니 오디 미움 성분조사 연구에서 니오디미움의 해양에서 평균 정체시간이 행 성의 바다에서의 혼합 시간보다 짧고 함수 되적물과 해수의 143 N d/ I“Nd 비가 불균질함을 조사하였다. 그리고 대서양저의 퇴적물 유공충, 철망간 퇴적물 등의 니오디미움 동위원소 비에서 육성기원의 물질이 혼입되었다고 해석하였다 . 6) 레니움_오스미움 측정법 187 Re 이 f]붕괴로 1870s 이 되며 주로 구리나 몰리브덴과 같 은 황화 광물과 이리도스민 (Ir i dosm i ne) 과 같은 오스미움이 많이 함유된 광물 이 연령측정에 주로 이용된다. Rb-Sr, Sm- Nd, U-Pb, Lu-H f 측정법과 함께 맨틀의 분화, 대륙 지각의 부착설 등을 연구하는 데 이용된다. 그러나 반감기 결정이 어 렵고 、규 산영광물내에 오스미움의 함량이 낮은 단점 이 있다(표 8-10). Re 동위원소는 안정동위원소인 18 5 Re(37.398% )와 방사성동위원소 인 181Re(62 .60 2% )가 있다. 레니움은 다음과 같이 f] 붕괴로 오스미 움으로 변화된다. 18775Re~ 187760 s +g +;+Q 반감기는 4.5 6 土 O.llX10'0 년, 11= (1: 52 士 0.04) x1 0- 11 a-1·2 1 (Luck
표 8-10 암석 중의 레니움과 오스미움의 함량 암석 Re(pp b ) Os(pp b ) Re /O s 보통 콘드라이트 57 (30-80) 660(300-900) 0.086 철운석 2500(5-5000) 30000(7-50000) 0.0 8 3 달암석 0.002-2 0.0 2 -0. 9 페리도타이트 0.4 3 5.3 0.0 8 1 소레아이트질 현무암 0.84 0.03 28 화강암 0.6 0.0 6 10
와 Allegr e, 1 98 3) 이 다. 오스미움의 붕괴는 다음 식으로 표현된다. 認=(認),+국 (eA t -1) Rb - Sr 측정법에서와 같이 아이소크론이 얻어진다(그림 8-17). 간0 7 서- 이나 몰리브덴 함유광상의 생성연대 측정에 유용하다. 오스미움 함유광물의 동위원소 분석에서 맨틀에서 오스미움 동위원 소의 진화경향이 나타났다. 오스미움과 레니움이 태양계 초기의 균일 한 성분으로 지구와 운석에 존재하였음이 알려져 지구를 포함한 운석 의 기원이 다른 행성들과 동시에 형성되었음을 암시해 주었다. 표 8-10 에서처럼 화강암이나 초염기성암에서 레니움의 함량이 대단 히 유사함을 알 수 있다 . 이들 원소가 부분용융이나 분별정출작용 동
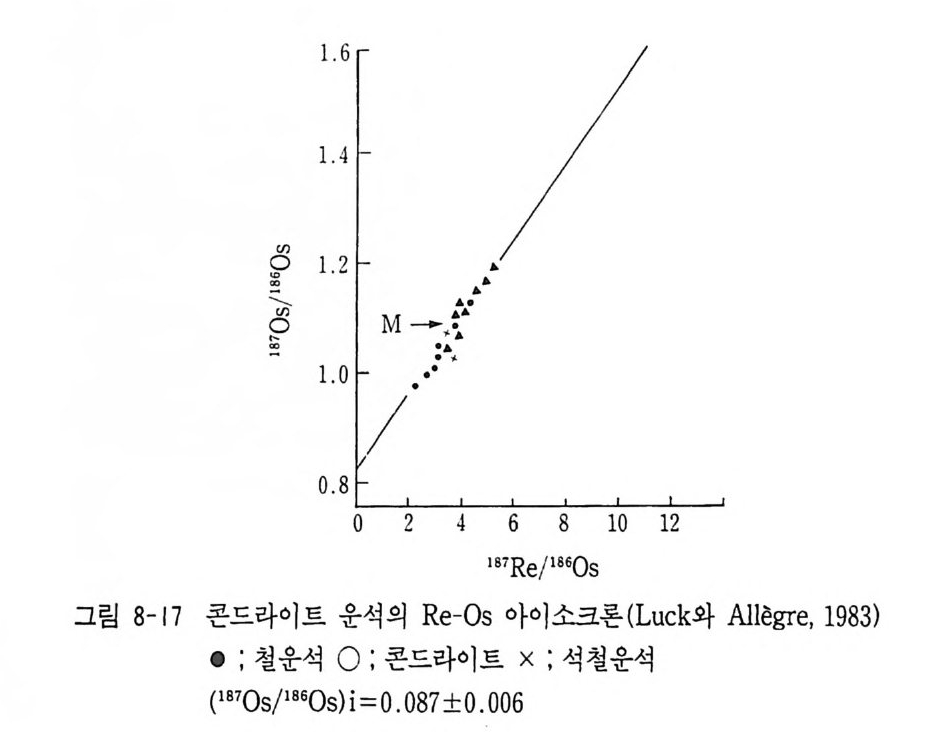 1.6
1.6
안에 많이 분해되지 않았음을 이 사실에서 알 수 있다. 죽 맨틀의 지 화학적 분화에 의해 레니움의 농도는 크게 변화하지 않았다. 그러나 오스미움은 초염기성암에 비해 화강암과 현무암에 결핍되어 있다. 따라서 소량의 맨틀 오스미움만이 지각에 전이되었음을 알 수 있다. 이처럼 Re/Os 바는 지질시대를 통하여 큰 변화가 없다. 그러나 지 각에서만은 높게 나타나므로 지각에서 마그마의 혼염의 주요한 지시 자가 될 수도 있다. 7) 루테티움-하프니움 측정법 Boud in 과 Deuts c h (19 70) , Owen 과 Faure (19 74) , Patc h ett 와 Tats u moto ( 19 80) 등에 의 해 178Lu 의 반감기 측정 과 광물에 서 하프니 움의 분리의 문제가 해결되므로 연령측정과 화성암의 기원해석에 유 용한 수단으로 등장하게 되었다. 루테티움 동위원소는 다음과 같이 /3 붕괴로 하프니움으로 변한다. 1776 , Lu 一 빠 11+ /3-+ D+Q 반감기는 3.53( 土 0.14) x1010 년 (Pa t che tt와 Tats u moto , 1980) 이고 붕 괴상수는 (1.96 土,Q .,08) X10-11 a-1 이다. 178Lu 이 방사성 붕괴를 하면 다음과 같이 176Hf 이 된다. 대{=(:脂+問輯 -(eA t -1) 여기서 얻어진 아이소크론에서 시간 t가 얻어진다. 화강암에서 루테티움과 하프니움의 분포가 불균질하기 때문에 지질 연대 재현성이 좋지 않다.
표 8-1 I 암석의 루테티움 (Lu) 과 하프니움(Hf) 함량 암석 Lu(pp m ) Hf( ppm ) Lu/ H f MORB(17) 0.447 2.408 0 .18 5 현우암 0.5 5 2.44 0.22 화강암 0.68 6.9 3 0.0 9 8 저어콘 (51) 23.65 11270.0 0 0.0 0 209 콘드라이트 (6) 0.0376 0.1 6 7 0.2 2 5 에이콘드라이트(1 2) 0.2 5 1 1.2 5 5 0.200 달 현우암 (7) 1.74 5 11. 75 0.148 달 암석 1.85 12. 7 0.1 5 ( ) 시료수
루테티움 함유광물은 저어콘, 혹운모, 인회석 등이며 모나자이트나 인산염에서처럼 REE 와 함께 수반되기도 한다(표 8-11). 스펜이나 인회석에 루테티움이 산출되고 저어콘내에 하프니움이 산출된다 . 현무암 마그마에서 화강암으로 진행되는 분화과정에서 평균 루테티 움의 함량은 변화가 없다. 루데티움과 하프니움은 사마리움과 니오디 움 동위원소와 지화학적으로 대단히 유사하다. 맨틀에서 유래한 현무 암질 마그마는 그 기원암보다 Lu / H f비가 보통 낮다. 물론 마그마의 유출 후 잔류 고체 중에는 하프니움이 결핍되어 용융 전의 본원 마그 마에서보다 Lu/ H f 바는 높다. 중앙해령 현무암 (MORB) 과 해양성의 현무암 (OIB) 의 i 16H f /111H f비 는 0 . 2828-0 . 2835 이 다. 이 들 시 료의 (11sHf /177 Hf ) 비 와 143Nd/144Nd 비 를 도시하면 정의 관계가 얻어지고 87Sr / 86Sr 비와 갇이 도시하면 부의 관계가 얻어진다(그림 8-18). 콘드라이트 리저버의 값 (176H f/17 7H f=O .28286, 87Sr/86Sr=O.7045, 143Nd/144Nd=0.5112638) 을 이 그림에 도시하면 그림 8-18 에서와 같이 영역별로 구분이 된다. 이 영역에 나타나는 화성암과 마그마기원의 지화학적 역사를 다음 분별정수 (f)로 표현할 수 있다.
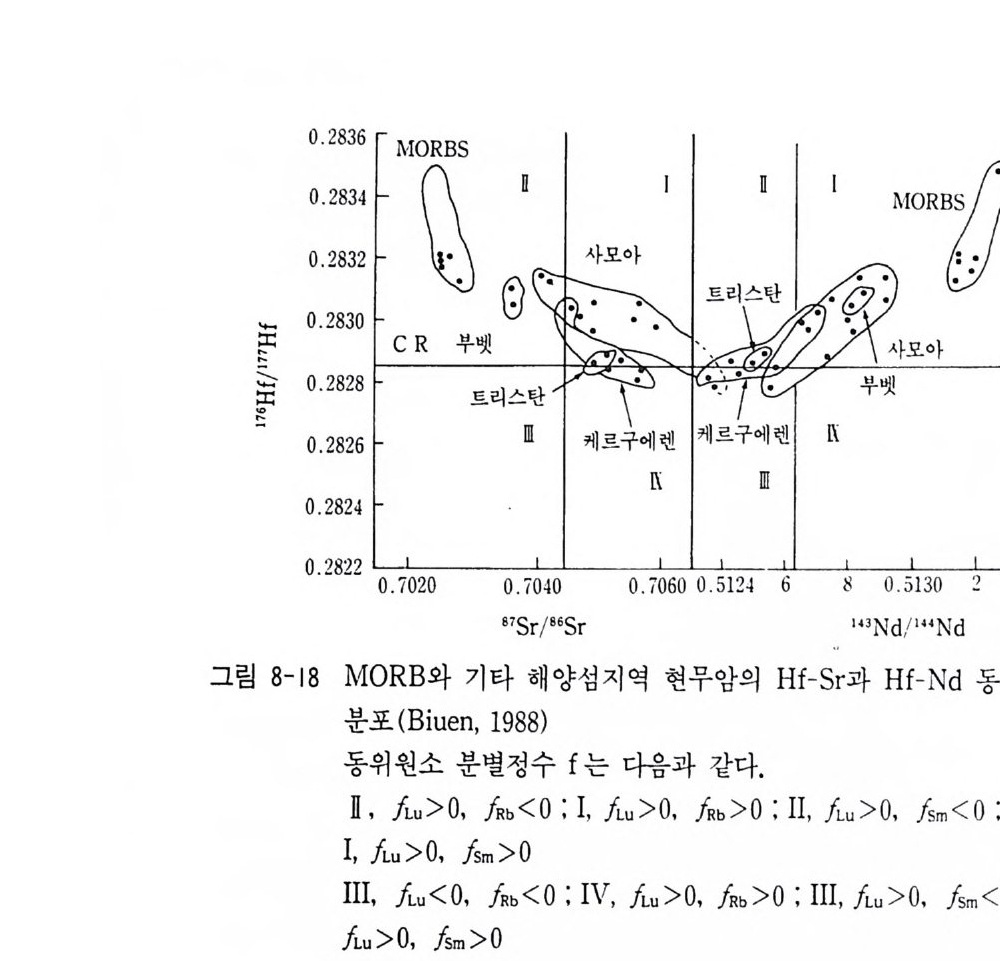 000...222 888 333 264 『u\ `n-’내 。 /
000...222 888 333 264 『u\ `n-’내 。 /
fLU = [i,;\言區 ] 여기서 mLu/1 1 1H f는 암석이나 마그마에서의 비이고 (17 6L u/ m H f) o 는 0 . 0334 로 콘드라이트 리저버의 값이다. 루테티움이 부화된 기원지역은 fu > O 이고 운석에 비해 루테티움이 결핍되고 하프니움이 부화된 기원지역은 fu < O 이 된다. 즉 이들 현무암의 기원마그마가 과거 Lu/ H f , S m/Nd 과 Rb/ Sr 비 가 상이한 기원에서 유래한 것임을 알 수 있다. 달 암석의 11sH f /1 11 H f 바는 0.2816-0.2834 로 중앙해령 현무암의
비보다 변화가 심하며 지구의 맨틀기원의 현우암보다 불균질하다. 그 러 나 달 암석 의 Lu/ H f 비 는 0 . 0985-0 . 1700 으로 낮고 균일한 값을 가 져 달과 지구의 지구화학적 해석에 새로운 변화를 요구하고 있다. 지질시대의 화강암류의 176Hf /l “ Hf 비의 초생치는 지질시대가 오래 됨에 따라 증가하며 콘드라이트 성분의 곡선 위에 도시되었다. 특히 30 억 년 정도 아주 오래된 암석은 이 곡선에 근접 도시되어 분별되지 않은 맨틀기원으로 해석되었고, 젊은 암석일수록 루테티움 부화와 하 프니움 결핍현상이 나타나 곡선에서 이탈되어 도시되어 분별작용이 있었던 기원으로 보였다. 석류석은 루테티움과 친화력이 강하기 때문에 이 효과가 석류석에 서 더 크게 나타날 것으로 보인다. 즉 루테티움이 멜트내에 들어가는 것을 막아 멘틀내의 여러 광물에 서보다 잔류 고체에 Lu/ H f 비가 증가하게 될 것이다. 13 개 시료의 에이콘드라이트의 아이소크론에서 얻어전 원시물질 의 E6 H f/1 7 7 Hf 동위원소비는 0.27978 土 0 . 00009(Pa t che tt와 Tats u rnoto , 1980) 이고 콘드라이트 운석의 Lu / H f비는 0.240 이며 Murchis o n 콘드 라이트는 0 . 0334 이다. 콘드라이트 리저버의 연대를 4.55Ga 로 가정하 면 현재 17 6 H f / 177H f비는 0.28286 이 된다. 니오디미움一사마리움 계 에서와 유사하게 지구의 광물과 암석의 하프니움 성장곡선을 다음 관 계식에서 얻을 수 있다. 강 (H f)는 현재의 하프니움 동위원소비와 비교된 것이고 당 (H f)은 176Hf /1 77Hf 비의 초생치를 근거로 과거의 것과 바교한 것이다. 강 (H f) =[ {:::갑[나問 1-x-1-lx04- 1 04 당 (H f) =[ {::::二區 (1 16H f /111H f)낡순시료가 형성된 후 붕괴된 시료의 초생치이고,
('76H f/ l77H f)나는 t 년 전의 콘드라이트 리저버의 비이다. 연령측정 관계식은 다음과 같은 대=(대 )l+~(eAl-1) 식에서 계산될 수 있다. 니오디미움은 모든 조암광물내에서 고루 발견되나 하프니움은 주로 저어콘의 격자내에서 Zr” 을 치환하여 산출된다. 니오디미움은 유동성이 크므로 마그마와 지각물질의 동화해석에 이 용될 수 있으나 하프니움은 그렇지 못하므로 암석성인 해석에 있어 . 활용도가 다르다. 그러나 니오디미움, 하프니움, 스트론튬 동위원소 는 모두 맨틀에서 일어나는 지구화학적 과정을 연구하는 데 크게 도 움이 된다. 8) 탄소 측정법 탄소 동위원소 (l ◄ c) 는 우주선에서 생긴 중성자와 질소 (l ◄ N) 가 상충 대기권에서 다음과 같은 반응에서 생성되고 붕괴된다. 1~N+Jn = 1\C+f tt, 1\C 一 141N+8 이때 생성된 방사성탄소는 산소와 결합하여 C 아를 만든다. 물론 이 C 야의 C 중에는 12c, 13c, 14c 가 포함되어 있다. 식물은 광합성 작 용에 의해 C 아를 이용하여 셀룰로스를 만든다. 따라서 식물이 살아 있을 때는 대기 중의 “C 아나 식물체 중의 14c 가 평형상태에 있게되 나 죽게 되면 평형이 깨져 그때부터 방사성탄소는 5730 土 30 년을 반감 기로 붕괴하기 시작한다. 시료의 연령은 t= -8,266 ln N/No 관계에 서 얻어진다. 여기서 N/No 는 대기와 시료 중의 을1 4C 농도의 바를 의
미한다. 실제로 Broecker 와 Olsen (l 961 ) 에 의해 제안된 연대는 t= *31og (~) 이다. 여기서 4=l4c _ 8:30 c 관계에 있고 LI=o14 C-( 2 013C + so)(1 + 麟) 이며 탄소동위원 소 비는 o13c = ( 』 二3 : :::료 -1) • 103 와 , 814C = (14C / 1 2 C ) 시료 -O . 95(“C / 1 2 C) 표준 시 료 0 . 95 (1 4C / 1 2 C) 표준시료 로 표현된다. 군 탄소 동위원소법에 이용될 수 있는 시료는 나무, 목탄 , 곡식 , 지하 수 등 탄소가 들어 있는 시료는 모두 가능하다. 또 반감기가 짧기 때 문에 7 만 년보다 젊은 시료에 대하여 유용하다. 따라서 고고학이나 제 4 기 지질학에서 많이 이용되고 있다. 제 4 기 지질학에 이용되는 방사성 동위원소들은 .1E 8-12 와 같다. 측정된 연령은 BP(Befo re Presen t)로 표시되고 1950 년을 기준연대로 하고있다. 이 방법은 젊은 연령의 시료에 대해서 유용하지만 대기 중의 탄소 의 함량이 과거나 현재나 변화가 없다는 가정이 필요하다. 그런데 오
표 8-12 제 4 기 지질학에 이용되는 방사성동위원소 동위원소 반감기 ( X 103 년) 방법 측정연령범위 대상 시료 l ◄ c 5.7 붕괴 50 유기물질 25 유기원 탄산염 230Th 75 저o 又o l- 0~200 유기원 탄산염 23'U 250 붕괴 50~100 산호 4He 서0 又0 \. 무한 부족류·산호 '0Ar 서0 ~0 1- 무한 화산성 물질 39Ar 서0 又0 ). 무한 화산성 물질
늘날 화석연료, 핵사용 등으로 대기 중의 CO2 가 증가하여 I4C 에도 다소 변화가 일어나고 있다. 가속기를 이용하여 극소량의 시료에 대하여서도 정밀한 연대측정이 가능하게 되었다. 최근 가속기를 이용하여 초고감도인 핵종을 정량할 수 있는 새로운 기술이 발표되어 14c, IOBe, 36Cl 측정이 용이해졌다. Nelson (19 77) 과 Nakai ( 19 89) , Nakamura 와 Nakai ( 19 89) 등에 의 해 Tandem Van Graaff 가속기를 이용한 l4C 연대측정 연구가 보고
표 s-13 14C 연령측정에 있어서 f3선계측법과 가속기 이용법의 비교 (Purser, 1979) . 시료의 연령 현 대 6 만 년 10 만 년 측정법 방사능 가속기. 방사능 가속기 방사능 가속기 시료사용량 lg
되어 있다. 가속기를 이용하면 다음과 같은 장점이 있다. ® 시료의 양이 종래 의 8 선 계측법보다 1/1 0 00 정도 적은 수 m g으로 가능하고 ® 측정 의 백그라운드의 걱정이 없으며 ® 측정에 요하는 시간아 짧고 ® l0 만 년까지 연대측정이 가능하다(표 8-13). 가속기 를 이용하여 14c 이 의 에 10Be 동위 원소를 측정 하여 해 양의 순 환속도, 해저되적물의 퇴적속도, 빙하의 연대 그리고 과거 백만 년간 우주선 강도의 시간에 따른 변동을 연구하고 있다. 그리고 36C ! 존재비를 측정하여 지하수 연령을 결정할 수 있다. 9) 트리티움 측정법 트리티움 (T) 은 수소 동위원소 중의 방사성동위원소로 대기권에서 질소와 우주선에 의해 만들어진 중성자와 다음과 같은 반응에서 만둘 어진다. 멉 N+an 一 ~H+12sC 물론 트리티움은 태양방사, 지구상에서의 입자의 가속·, 핵폭발과 중성자로에서도 만들어질 수 있다. 삼중수소는 /3 붕괴 에 의 해 헬륨으로 변한다 (出 H 쵸잉 He) . 트리티움의 자연발생 속도는 약 0.25 ato m cm-2 s-1 이다 (Lal 과 Suess, 1968) . 일단 형성된 트리티움은 빠른 속도로 물분자를 형성하여 l~10 년 동안 성층권 하부에 잔류된다. 후에 이들 분자는 대류권 하부로 들어 가 5 내지 20 일 간격으로 트리티움화된 강수가 되어 HTO 형태로 수 권에 들어간다. 트리티움은 과거 20~30 년간 대기 중에 존재하였던 물에 대하여 대단히 유용한 트레이서가 된다. H20 에 의해 희석되었기 때문에 트리티움의 농도가 대단히 낮으므
로 동위원소 분석시에는 농축처리를 실시한 후 방사성을 측정한다. 자연수 중의 트리티움의 함유량의 단위는 T.U.(Triti um un it s) 를 사용 하며, 1 T.U 는 수소원자 1018 에 대한 트리티움 원자 1 의 농도에 상 당하며 보통 실험실에서 측정하는 최저단위이다. 자연상태의 강수에서 3H 의 농도는 1~10 T.U . 이며 표면해수는 0.1~0.3 T.U. 이다. 강수에 의해 공급된 지표수나 지하수의 3H 농도 는 12.26 년을 반감기로 붕괴해 강수로써 공급되어진 연대 t로부터 e-u 에 비 례하여 감소한다. 그러나 1953~1962 년 사이에 핵실험 결과 인공적으로 생긴 3 H 가 대기중에 공급되어 대기와 자연수의 3H 농도는 10~1,000 배 증가하 였으며 현재 산업용 원자로에서도 계속적으로 소량은 방출되고 있 다. 대기 중의 트리티움 경시변화 : 온대지방의 대륙의 순환수 중에서는 우주방사선에 의해 약 10 T.U. 정도의 3H 가 생성된다. 이 값은 1953 년 이전 북반구의 강수에서 측정된 값이다. 1953 년 이후 핵실험 결과 강수 중의 떤 함유량은 증가하였으며, 1961~1962 년의 대규모 핵실 험 결과 1963 년 북반구에서는 10,000 T.U 에 달하였다. 그 후 핵실험 금지로 1968 년까지는 계속 감소했으며 1968 년 이후 거의 정지상태에 이르렀다. 핵폭발에 의하여 만들어전 트리티움은 대 부분 성층권에 축적되어 있어 그의 약 반은 매년 봄과 여름에 대류권 으로 이동되어 하계의 강수에 그 함량이 최대가 되고 동계에는 최소 가 되는 계절적 변화가 나타났다. 지역적안 차이도 커서 내륙지역에 비해 해양 및 연안지역에서는 낮 다. 그 이유는 해양에서는 대기 중에 수증기가 트리티움의 함유량이 적은 해수와 동위원소 교환이 일어나 HTO 가 흘러 들어오기 때문이 다. 이에 비하여 열대 및 남반구에서는 트리티움의 농도가 낮다. 대 부분 트리티움은 북반구에서 방출되어 주로 고위도 지역의 성층권에 서 대류권으로 이동하며 남반구의 해면이나 증기압이 높은 열대에사
는 씻겨 내려가 기타 지역보다 많이 희석된다. 지하수 중의 트리티움 : 강수의 트리티움 함유량은 지하수계에 첨가 되어져 지하수의 트리티움 추정에 이용된다. 식생아 있는 지역의 강 수는 생육기에 증산에 의해서 대기중으로 되돌아간다. 반전조지역에 서는 강수가 아주 작고 지하로 침투하기 전에 지표에서 증발된다. 지 하수 연구에 트리티움을 측정하면 지하수계의 함양지역의 정보가 얻 어진다. 상이한 기원의 물이 혼합되지 않은 경우라면 (1972 년 북반구 대륙에서) 다음 사항이 고려된다. (1) 수중의 농도가 3 T . U. 이하일 경우 : 20 년보다 젊은 물은 존재하 지 않음을 의미한다. 즉 지하수가 함양지역에서 시료 채취지점에 도 달하는 데 20 년 이상 시간이 경과하였음을 의미한다. (2) 트리티움 함유량이 2~20 T.U 일 때 : 소량의 핵실험에 의한 트 리티움이 존재하고 최초의 핵실험 (1 954~1961) 의 영향을 받은 것으로 해석된다. (3) 트리티움은 함유량이 20T.U . 이상일 경우 : 트리티움의 함유량이 많은 물은 분명히 최근의 것이다. 연간을 통해서 변동이 있으며 이것 은 함양지역의 강수의 변동에 관계되며 지하수로 유입이 빠르고 직접 적이며 이동에 걸린 시간은 연간의 피크의 이동거리에서 구할 수 있 다. 트리티움의 함유량이 20~200T.U. 로서 변동이 별로 없으면 대수충 중에서 젊은 물이 오래된 물과 혼합되어 있음을 의미한다. 그러나 지 하수의 저류층이 두터우면 함양시에 나타나는 이 같은 변동이 거의 나타나지 않게 된다. 이와 같은 지하수계는 지수관계적인 유출을 나 타내는 〈완전혼합 저류층〉으로 취급할 수가 있어 계내의 평균 채류기 간을 추정할 수가 있다. 우리나라 부산지역의 1980 년 강수의 트리티움 농도는 연평균 37.86 士 5 . 29T. R. (T . R. : T riti um ac tivity)이며 계절 변화에 따라 변화함 아 밝혀졌다(오재환, 1981).
8-6 방사성붕괴에 의한 결정손상을 이용한 측정법 광물내의 방사성동위원소의 붕괴시에 발생한 에너지에 의해 광물의 결정격자에 손상이 가서 결정면에 흔적 (Track) 이 나타난다. 이 같은 결정면의 흔적의 수는 시간의 함수로 표현될 수 있다. 이런 원리에 의해 최근 휘션트랙법 (Fis s io n tra ck dati ng ) , 전자스핀 공명법 (Electr o n spi n resonance), 열 루미네센스 (Thermolum i n esce nc e) 등으로 연대를 측정하고 있다. 1) 휘션트랙 측정법 위에 설명한 모든 방사성 동위원소의 연령 측정법은 질량분석기로 동위원소의 비를 측정해야 한다. 그러나 휘션트랙 연령 측정법은 질량 분석을 하지 않고 휘션트랙의 밀도를 현미경에서 정량하여 연령을 측 정하는 방법이다. 방사성원소가 핵분열시에 광물의 결정격자에 손상을 일으켜 그 혼 적이 생기는데 이를 휘션트랙이라 한다. 이 휘션트랙은 전자현미경이나 광학현미경에서 관찰할 수 있다. 화 학적으로 부식시키면 더욱 이들의 관찰이 용이하다(사전 8-1). 저어콘, 스펜과 같은 광물결정이나 혹요석 같은 유리질 물질에 열 중성자를 조사시켜 생기는 238U 의 유도핵분열에 의한 트랙의 밀도에 서 238U 의 함량을 구할 수 있다. 이 방법은 기타 방사성동위원소법으로 측정이 어려운 수천년 정도 의 젊은 연령의 화산암이나 수백만년의 암석까지도 가능하다. 주로 화산암이나 웅회암 중의 유리질 물질 등과 기타 저어콘과 스펜 등 광 물에서 이 휘션트랙울 관찰할 수 있다. 좀더 구체적으로 측정원리를 설명하면 다음과 같다. 만일 광물 입자내 에 238U 원자가 균등하게 분포되 어 있으면 t시 간 동안에 방사성 동위원소의 총 붕괴수는 D=23su(eu 一 1) 이 된다.
 (a) (b)
(a) (b)
여기서 D 는 붕괴사건의 수이고 23 민은 시료 lcm3 당 산출되는 방사 성동위원소의 원자수이며 Aa 는 238u 의 a 붕괴의 붕괴상수(1 . 55125 X l0- 1° a-I) 이 다. 238U 이 자발붕괴시 휘션트랙의 수는 Fs= (11t /1 1 a) ~ 38U(e ,l a t _l) 이 된다. 일부 휘션트랙들은 연마표면에서 사라져 보이지 않는 수도 있다. 이때는 부식실험 (E t ch i n g) 후에 휘션트랙 수를 정량하면 된다. 부식 실험에 사용되는 시약과 방법은 표 8-14 와 같다. 그러므로 광물표면의 자발붕괴 트랙의 면적밀도는 Ps= Fsq = U/ 11 a) 235U (exp (11 갑) -l) q 가된다. 여기서 q는 부식실험 후 출현되는 트랙의 비이다. 시료 1cm ' 당 열 조사에 의해 유도되는 238U 의 붕괴사건의 수 (F i)는 F i = 235U¢
표 8-14 휘션트랙 측정법에 사용되는 부식 시약과 부식 방법 광물 부식용시약 T('C ) 시간 인회석 (Ap at i te) Conc.HN03 5% HN03 25 10~30 초 녹염 석 (Ep ido te ) 6g NaOH+ 4 ml H20 159 150 분 (37.5M NaOH ) 백 운모 (Muscovit e) HF(48%). 20 20 분 스펜 (S p hene) Cone. HCI 90 30~90 분 !HF : 2HCI : 3HN03 : 6H20 20 6 분 화산유리 (Volcan ic g la ss) HF(24%) 25 1 분 저 어콘 (Zir co n) lOOM NaOH 270 1. 25 시간
의 밀도는 pl= Eq = 235U ¢6q 가 되고 위의 식을 아용하면 Psi P1 =MIla(exp (1 1at ) ― 1)/¢ 이 로 표현할 수 있다. 여 기 서 I 는 235U/238U 의 원자비 이 다. 따라서 연령방정식은 t =f 1n{ 1 + (:)({) ¢(J1} 로 표현될 수 있다. 여기서 Aa=1 .55 125X 1 0-10 a-I' 111=8.46X10-11 a-1, J=5 80.2X 10-2 4 cm', I = 1/1 3 7 . 88 의 값울 대 입 하면 t= 6.446X l0 9 ln(l +7. 715 X l0 니안 가된다. Ps i P 측정과 모니터로부터 중성자선(¢)을 측정하면 t가 얻어진다. t< 500 Ma 인 경우 이 방정식은 Ps / P i =11 ftl
내의이다. 이 방법에서 야기되는 측정 오차를 줄이기 위해 Hurfo rd 와 Green (1 982) 은 연령이 이미 알려진 광물에 대하여 휘션트랙 연령 울 보정하는 방법을 제시하였다. 보정요소 Z 를 Z=¢ (JI I t1 1 로 두어 미지의 시료의 연령방정식을 t 마 지 =\ln[1 + 信)미 지 ]ZA a 로 표현하였다. Z 의 값은 표준광물 시료와 미지의 광물 시료에 대하여 중성자 조 사 실험으로 구하였다. 그 다음 Z 는 표준시료에 유도된 트랙밀도와 자발붕괴에 의한 밀도의 바를 측정하므로 다음 식에서 계산하였다. z= ex p (Aa 垣 )-1 Aa( p s/ P, ) 표준 여기서 Z 의 값은 표준시료와 함께 조사되었던 미지의 시료의 연령 측정 계산에 이용된다. 만일 표준시료의 연령의 값이 238u 의 반감기 보다 적은 경우 eA t표 한 1 료 -1 은 A t표 준 시 료 로 넣어 생각할 수 있다. 따라 서 Z= t 표 준信)표준가 된다. 이때 미지시료의 휘션트랙 연령은 t미지=는 [1+ 麟益:군t표 준 ] 가된다. 이들을 사용한 몇몇 표준시료는 다음과 같다. ® 미국 콜로라도 산쥬안 마운틴의 휘시 캐넌 응회암 중의 저어콘 의 연령 (27. 9 士 0.7 M a)
® 미국 비숍 응회암의 저어콘 연령 (0.74 士 0 . 05Ma) ® 남아프리카 킴버라이트 파이프 중의 저어콘의 연령 (82 土 3Ma) 등이다. 그리 고 표준광물로 우라늄 함유 선량기 용 그래 스 (Dos i me t er gla s- ses) 를 보정하기 위해 다음과 같은 그래스내에 유도된 트랙의 밀도 (p d) 와 관련된 중성자선 사이에 ¢=B p d 의 관계를 이용하여 미지시료 의 연령측정을 위한 다음과 같은 연령식을 얻었다. t 미지 =±1n[1 + 信) 마지 信 )B p d (Jf] 여가서 B 는 보정상수이다. 이 식을 ,=1 뿐로 바꾸어 넣으면 t 미자 =±1n{1+ 信) 미지 } 가된다. 위의 식을 변형시켜 다음과 같이 (p s/P i)표 준 =A r/ Aa (e (Aa 垣) —1) /Bp dr ;J 信)표준= exp (}:;::) —l g= ex p (Aa t표준) —l Aa (ps /Pi) 표 준 Pd 로 표현할 수 있다. Green(l985) 은 제타방법을 저어콘 이의의 인회석과 스펜 광물에도
적용하였다. 휘션트랙이 상온에서는 긴 시간 동안 안정하나 온도가 상승할 때 감소함을 알게 되었다 : ·이에 근거 동일기원의 암석시료의 열적 역사 해석에 정보로 이용될 수 있게 되었다. 광물과 그래스간의 온도상승과 가열시간의 함수로 휘션트랙이 소멸하는 관계식이 다음과 같이 얻어졌다. t = A . e(u1 K T l 여 기서 t는 휘션트랙 의 밀도가 감소할 때 의 온도저 하 (An nea li ng ) 시간이고 A 는 상수, U 는 가속에너지이다. k 는 볼 쯔만 상 수 ( 8. 61 7 1 X 10-s evk-1) 이며 T 는 절대온도이다. 위 석에 상용대수 를 취하면 ln t= l n A+U/ kT 가 된다. ln t와 1/T 사이에는 기울기 U / k 인 정의 직선석이 얻어지고 y 축의 절 편 ln A 가 얻어진다. Naeser 와 Faul(1969) 는 화성암’과 변성암 중의 인회석, 스펜, 저어콘 등에서 휘션트랙의 수가 다른 속도로 감소함을 알게 되었다. 예를 들면 백만 년의 가열기간에 걸쳐 인회석은 약 50 ° C 에 서 휘 션 트랙이 없어지기 시작하고 약 175 ° C 에서 온도저하가 종료된 반면, 스 펜은 250'C 에서 흰션트랙이 사라지기 시작하여 420 ' C 에서 온도저하가 종료되었다. 따라서 안회석의 휘션트랙 연령이 어떤 조건에서는 주 기 적인 가열에 의해 재설정될 수 있다. 그러나 동일한 조건에서도 스펜의 경우는 그렇지 않았다. 동일 암석에서 수집한 상기의 두 광물의 시료의 휘션트랙 연령이 일치하는 경우(일치연령)라면 스펜은 빨리 냉각되었고 후에 재가열 과정이 없었음을 의미한다. 반면 불일치 연령이 얻어졌을 때, 즉 스펜 연령이 인회석 연령보다 오래되었을 때, 암석은 천천히 냉각되든가 인회석의 휘션트랙은 없어 지고 스펜에서는 없어지지 않을 정도의 온도로 재가열되든가를 의미
한다. 이처럼 인회석 광물은 암석의 냉각사 해석에 대단히 유용하다. 왜 냐하면 인회석은 운모와 공존하는 Rb-Sr 이나 K-Ar 지질연대계 (Geochronomete r ) 의 凍結溫度 (Bl ockin g tem p er atu r e) 보다 상당히 낮 은 온도에서만이 휘션트랙이 유지(잔존)될 수 있기 때문이다. 그림 8-19 는 몇몇 광물들의 냉각속도에 따른 閉鎖溫度 (Closin g tem p er a-
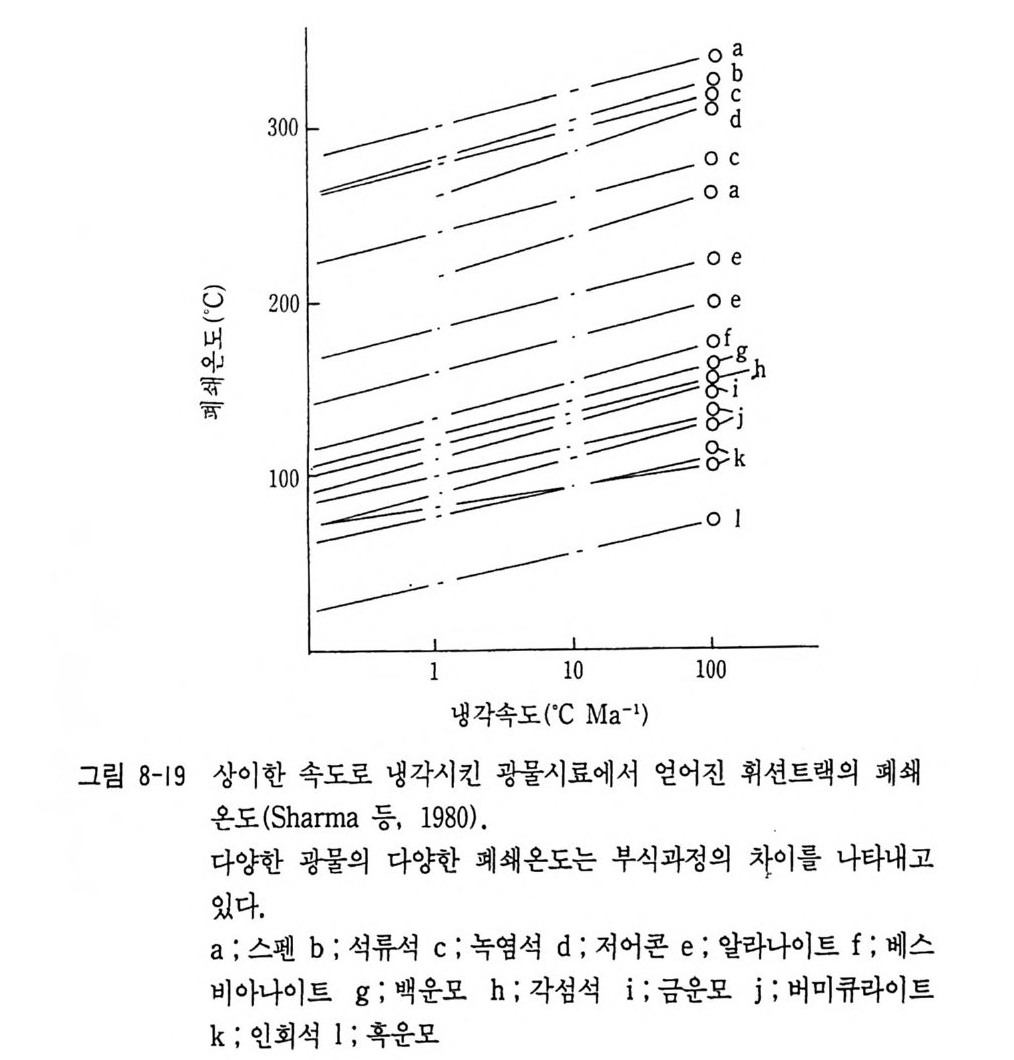 300 f-----~: 二 --- 三----- °§; ;
300 f-----~: 二 --- 三----- °§; ;
tur e) 를 나타낸 것 이 다. 여기서 폐쇄온도의 변화가 크며 폐쇄온도는 냉각속도가 빠를수록 증가함을 알 수 있다. 따라서 심성암이나 고변성도의 변성암의 광물 들은 형성온도가 그들의 폐쇄온도를 지나 버리는 연령이 나타난다. 그리고 인회석과 스펜 갇은 동일기원의 두 광물을 택할 경우 휘션트 랙 연령간의 차이는 스펜의 폐쇄온도에서 인회석의 폐쇄온도로 감소 하는 데 필요한 시간을 나타낼 수도 있다. 이와 같이 서로 다른 광물 울 사용하면 휘션트랙 연령측정과 폐쇄온도가 화성암과 변성암의 냉 각사를 재현시키는 데 응용할 수 있다. 그리고 휘션트랙 연령측정법을 지하중온률과 함께 고려하면 융기와 침식에 대한정보를 얻을 수도 있다. 예를 들면 남미 볼리비아 안데 스의 포토시 저반의 3 개의 인회석의 휘션트랙 연령이 평균 12. 5M a 이였고 이들 광물은 그 시기에 바로 폐쇄온도로 냉각된 것이었다 (Crou gh , 1983). 저반 자체의 연령은 211 Ma 이다. 따라서 평균 냉각 속도는 dT/dt= 95-10/12.5=6.8°C Ma 가 된다. 단, 4625m 고도에서 볼리비아의 안데스의 연평균 기온을 1o · c 로 가정하였다. 여기서 지하중온률은 2o · c~40 ° C/Km( 평균 30 C / km) 이므 로 평균 융기 또는 침식속도가 다음과 같이 계산된다. dx/dt = (dT/dt) / (dT/dx) = 6 . 8/30 = 0 . 226Krn Ma-1 T 는 온도 (°C), t는 휘션트랙이 보존된 이후의 연령 (Ma), x 는 표 면에서의 거리 (Km) 이다. 계산된 결과를 보면 기타의 신기 조산대에 비해 융기속도가 느리게 나타났다. 이처럼 휘션트랙 연령측정에서 암석의 냉각사, 지각운동사 등을 해석할 수 있다. 그러나 기타의 연령측정법에서와 마찬가지로 암석의 원래의 형성연 대와 그 후의 변성작용과 같은 열적 사건으로 중복되어 얻어진 연령
을 어떻게 구별하여 해석할 것인가가 지질연대학에 대두되는 중요한 문제 중의 하나로 남아 있다. 측정된 연령은 보통 본래의 연령과 중복된 사건의 중간연령이 얻어질 것이다. 후의 열적 사건을 받지 않은 원래의 형성연대를 가지는 암체 가 느린 냉각에서 이루어졌을 때는 위와 유사한 결과를 가져올수 있다. 위의 두 경우를 구별하는 방안이 350°C 이하에서 휘션트랙의 길이 분포를 조사하는 것이다. 왜냐하면 다음과 같은 휘션트랙의 특칭이 나타나기 때문이다. ® 모든 휘션트랙은 붕괴시의 에너지의 영향을 받으므로 대단히 일 정한 초 기의 길이를 가진다. @ 휘션트랙은 the rmal anneal i n g에 의해 길이가 점점 짧아진다. ® 각각 의 휘션트랙은 실제적으로 서로 다른 연령을 가지며 광물시 료의 전체 열역사 중의 광물마다 각기 다른 비율로 진행되었을 것이다. 따라서 복잡한 열역사를 가진 함우라늄 광물에는 휘션트랙의 길이 가 각기 다른 그룹들이 나타날 것이다. 그러므로 휘션트랙 연령과 함 께 휘션트랙의 길이의 분포는 지질시대에 따른 온도변화를 연구하는 데 중요한 가치가 있다. Gleadow 등 (1986) 이 오스트레일리아 동남부의 석유시추공에서 얻 은 인회석 시료의 bim odal 분포에서 2 단계의 열역사의 증거를 제시 하였다. 그리고 또 다른 응용연구의 하나로 Th iel 등(1 980) 은 남아프리카의 카아파발 지괴 (Kaapv a al cra t on) 의 함금-황철석 역암의 우라늄 분포 를 23 5U 휘션트랙법으로 연구하였다. 시료 중의 우라늄 우라니나이트 와 갑은 육성기원의 광물에서 bim odal 분포가 나타나 고화된 퇴적물 내에서 우라늄이 2 차에 걸쳐 반복 이동된 사실을 밝혔다. 2) 전자스핀 공명법 유전체 고체물질이 이온화된 방사성에 노출될 때 준안정성인 전자
가 발생한다. 이를 전자스핀 공명법 (ES R ; Electr o n spi n resonance ) 에 의해 검출할 수 있다. 보통 ESR 스펙트로메터로 측정할 수 있다. 이 방법은 Ikeya (1 9 75 ) 에 의해 종유석에 처음 시도되어 그 결과가 1978 년에 보고되었다. 이 방법은 표면 영향에 덜 민감하므로 연마방법이나 입자 크기에 따른 영향에 관계없이 문제의 전자를 가전 트랙의 농도 를 정밀히 측 정할 수 있으며 상온에서도 측정이 가능하다는 장점을 가지고 있다. 연대(t)는 전방사선량에 연간 방사선의 양을 나눈 값 으로 얻어전 다. 연간 방사선량은 우라늄, 토륨, 칼륨의 농도에서 구할 수 있고 Co 의 y 방사선 방사에 유도된 ESR 강도를 도시하므로 추정할 수 있다 . lke y a 와 M i k i(1 981) 는 인간과 동물의 뼈에서도 이 를 축 상하고 Sh i mokawa (1 984) 는 플라이스토세 화산암 중의 석영에서 측정하였 다. 그 후 Debuy st 등(1 984) 은 연간 방사성을 결정하지 않아도 되는 ESR 측정법을 개발하였다. 연간 방사성은 ESR 센터의 열안정도와 여 기서 얻을 수 있는 대응 방사성 (ED) 과 대비될 수 있다는 데에 착안 하여 상이한 열적안정도를 가지는 두 ESR 중심을 나타내므로 가능 하게 되었다. G rti n(1985) 는 이 방법을 아라고나이트 질 완족류 껍질 시료에 적용하였다. 그는 연령이 잘 측정된 아라고나이트 질 완족류의 껍질을 사용 g값이 2.0018 과 2 . 0014 인 ESR 중심을 선택하였다. 여 기서 g의 값은 ESR 강도 I 의 log I 값과 aneali ng 시간 사이의 좌표계 에서 얻어진 값이다. g=2.00 인 지역에 ESR 신호가 다섯 번 나타났다. 이때 g는 log I 와 냉각시간 (annea ling tim e) 간의 이 두 값은 y방사에 민감하였다. Annealin g 실험 결과 : CD g =2.001s 인 중심에서부터 전자가 재포획되는 과정은 2 차 비가 역과정이었고 @ g= 2.0007 ESR 시그널은 1 차 비가역과정으로 감소하였다. @ g =2.0014 의 종합피크에서는 g= 2.0007 시그널에서와 같은 속
도로 감소하였다. g= 2.0018 시그널은 anneal i n g시작시 감소하고 뾰 족한 피크가 알아볼 수 없을 때는 대단히 빨랐다. 이 지역에서 나머 지 시그널은 g =2.0007 에서와 같은 속도로 감소하였다. 불안정한 트 랩은 다음 방정식에 따라 전자를 축적시킨다. N=N 。 +k D 。 (1-e- t l r) 여기서 N 은 포획된 전자수이고 N 는 t =O 에서의 원자수이다. D 는 연간 방사성이고 k 는 방사성 감도이며 r 는 평균수명, t는 시간이다. 만약 N이 측정된 ESR 강도 I 에 바례한다면 I=I 。 +ED 。 r(l ― e- t i r) 로 쓸 수 있다. 여기서 E 는 ESR 의 강도이다. 만약 Io=O 이면 (ED) 1 ex E(I) 1 가 되어 (ED) =D 。 r(1-e- t / r) 로 간단히 된다. 이 모델은 (ED)1=f (r )1 의 일반식으로도 표현할 수 있다. 보통 g =2.0014 의 ESR 시그널과 관계된 중심은 측정연령 범위에 걸쳐 안정하다는 가정과 g =2.0018 인 중심에서 스핀의 밀도는 포화 수위보다 아주 낮다는 가정울 한다. 그리고 안정한 트랩 (g= 2.0014) 을 통하여 계산된 연령은 연령 =ED14/Do 가 되고 ED18 =D 。 r18 (1 —e-t /r l8) 로 표현할 수 있다. 여기서 t느 5 일 때 ED1s 은 1% 이하이므로 D 。::::: ED 니 T18 로 표현되어 연령 A 는 A=ED14r1s/ED1s 에서 얻어진다. 아 방법은 연령이 84,400 년인 아라고나이트질 완족류에 적용되었 다. 이처럼 비교적 젊은 연대의 시료에 적용되며 최근에는 ESR 측정
법이 활단충의 이동의 연구에 적용되고 있다 (Fukuch i 등, 1986). 8-7 절대연령측정 결과해석의 문제점 화성암체가 긴 시간에 걸친 냉각과정을 거치기 때문에 동일암체라 도 초기와 후기 사이의 절대연령의 범위가 대단히 넓다. 캐나다의 그 렌벌 지역 (Grenvil le Prov i nce) 의 순상지의 암석의 U- Pb , Rb- Sr , K -Ar 법에 의한 연령이 800~1200m.y. 범위까지 얻어졌다. 따라서 방사성 기원의 딸원소 산물이 결정화작용 직후 단시간에 결 정내에 보존되느냐 아니면 조산운동시 심부에서 형성된 암석에서처럼 딸원소가 완전히 고정 보존되는 온도까지 냉각되는 데 수백만년이 걸 리느냐가 중요한 문제점이 된다. 복잡한 순상지 지역의 지구조와 변성사를 시대적으로 연구할 때 이 같은 논쟁이 일어나게 된다. 예를 들면 그렌빌 지역의 순상지의 긴 연령이 몇 시기의 분명한 변성 에피소드의 영향 때문이라는 해석이 있는가 하면 몇 차례의 변성 에피소드 동안에 일어났을지라도 심부의 활동적인 조산대에서 긴 시간에 걸친 연속적인 딸원소의 확산이 일어 났을 경우에는 이돌 시기를 결정하기가 힘들다는 사실을 주장하는 학 자도있다. 오늘날 지질연대학에서는 느린 냉각설을 많이 받아들이고 있으며 조산대의 느린 냉각과 계속된 딸원소의 확산울 고려하고 있다. 느린 냉각 가설 (Slow-coo li n g hyp o th e sis) : 뉴질랜드의 운모편암의 지질시대가 그 지역의 지질조사에 의하여 약 150m. y.의 쥬라기의 변 성작용에 의해 형성된 것으로 조사되었다. 그러나 K-Ar 연령이 4~8 m. y로 얻어졌다. 이 편암은 최근 단층작용과 융기에 의해 노출되었다. Hurley 등 (1 962) 은 이 암체가 약 3km 심부에 100 m.y. 동안 매몰되어 있었으며 이때 편암은 약 lOO'C 의 온도하에 있어 운모에서 탈가스가 일어나기
에 충분한 온도에서 융기 후 온도가 하강하여 방사성 딸원소 동위원 소가 고정되었다고 보고 있다. 이렇게 본다면 얻어진 젊은 연령은 이 지역의 융기와 침식의 시기인 것이다. 유사한 결과가 스위스의 알프스 지역 변성암에서도 얻어졌다 (Armstr o ng 등, 1966). 몬트 로사 (Mon t e Rosa, 105m. y.)와 제브레일라 (Zervreil a, 335,345m .y.) 지역의 혹운모의 K-Ar 연령은 기존암석의 잔 류연령이고 그 외의 11~29m. y. 연령은 변성작용의 연령으로 해석되 었다. 넓은 연령 범위는 지리적으로 다른 지역에 분포하는 암체들의 융기 로 인한 냉각사의 차이 때문으로 해석된다. 그리고 백운모의 Rb-Sr 연령은 30m.y. 이전으로 얻어져 백운모의 연령이 흑운모의 연령보다 높은 것으로 밝혀졌다. 백운모가 흑운모보다 더 아르곤이나 스트론튬의 확산에 폐쇄적이기 때문이다. 일반적으로 광물에서 임의의 원소의 온도에 따른 확산은 D=D 。 e-E /R T 관계식에서 생각해 봉 수 있다. 여기서 D 는 광물내의 원 소의 확산계수이며, Do 는 광물이 갖는 고유특성의 확산상수이고, E 는 확산의 가속에너지, R 은 기체상수이다. 실험결과 확산 가속에너지가 백운모는 대단히 크며 흑운모는 낮다. 이처럼 운모류 중에 이 값의 변화가 다양하다, 즉 시료는 물리화학적 변화나 화학성분에 따른 근소한 변화에도 확산의 영향을 크게 받는 다. 예를 들면 E=40K Cal/ mo le 일 때 2TC 에서는 D=10-29D 。이지만 12TC 에서는 D=210-22D0 로 온도 1oo · c 상승에 확산계수는 2x101 차이 가나타난다. 이 사실에서 우리는 좁은 온도변화 범위에서도 광물이 계방계에서 폐쇄계로 전이가 일어날 수 있음을 알게 된다. 우리는 특정온도 이하에서 광물이 모든 아르곤원소를 보유하게 되
는 온도를 임 계 동결온도, CBT (Criti ca l bloc k in g tem p e ratu r e) 라고 하 는 개념을 도입할 수가 있다. 백운모는 K - Ar 의 C.B. T. 가 혹 운모의 그것보다 높다. 따라서 조산대나 변성대 내의 광물에 따른 방사성 절대연령이 차이 가 나타나는 것은 그 지역의 냉각에 수반된 각 광물의 C . B . T . 의 차 이 때문으로 볼 수 있다. 따라서 조산대지역의 냉 각 시의 동위원소 지 질시대의 시계는 지표 부근에서 제일 먼저 기록 될 것 이고 심 부 에서는 냉각이 느려 젊은 연대가 얻어지게 될 것이다. 참고문헌 Amaral,G., C ordani, U .G. , Kawashit a, K. and J.H . R e ~'11 o lds (19 6 6 ) , Geoch em . CoS1nochim . Acta . 30, p. 159. Armstr on g , R.L. (19 66) , K-Ar dati ng of p lu to n ic a nd vol canic r ocks in orog en ic belts. I n : Pota ssium Arg o n Dati ng , E d. D.A . Schaeff er and J. Z ahrin g e r . pp. 117-31 . Spr i n g e r -V e rlag . New York. p. 234 . Armstr on g , R.L. (1971) , Isoto p i c and chemi ca l constr a in t s o n models of m ag ma gen esis i n volcanic arcs. Eart h Planet . Sci . L et t. 12, pp. 137 -1 4 2 . Berge r , G.W ., and D.Y o rk (19 81) , Geoth e rmometr y from 40A r/39 A r dati ng exp erime nts . Geochim . Cosmochim . Acta . 45, pp. 795 -81 1 . Bog ar d, D.D. , a nd W.C.Hi rs ch (19 80) , 40Ar/39Ar dati ng , Ar dif fus io n pro p er tie s , and coolin g rate dete r mi na ti on s of severely shocked chondrite s . Geo- chem. Cosmochim . Acta . 44, pp. 1667-1682. Boud in, A., a nd S. Deuts c h (19 70) , Geochronolog y:R ecent develop m ent in the lute t i um -176/hafn ium -176 dati ng meth o d. Scie n ce, 168, pp. 1219-1220. Cata n zaro, E. J. (19 63) , Zir c on age s in south w este r n Mi nn esota . ]. Geop hy s . Res. 6 8, pp. 2045-2048. Croug h , S. T. (1983) , Ap at i te fiss io n -tr ac k dati ng _o f erosio n in the easte r n Andes, Boli via. Eart h Planet. Sci. L ett. 64, pp. 396-397.
Dallmey er , R.D ., Wrig h t, J.E ., Secor, D.T .J r. , and Snoke, A.W . 0986) , Charac- ter of the Alleg h ania n orog en y in the south e rn Ap pa lachia n s, Part II. Geochronolog ica l constr a in t s on the tec to n oth e rrnal evoluti on of the easte r n Pie d mont in South Carolin a . Geo!. Soc. of Amer. Bull. 9 7, pp. 1329-44. DePaolo, D. J. (1981b) , Trace element and iso to p i c effe c ts of combin e d wal- !rock assim i la ti on and frac ti on al crys t a l li za ti on . Eart h P lanet. S ci. Lett. Dallmeye 5r 3, , Rpp.D. .1 8(91 9-27092) ., '0Ar /3 9 Ar dati ng pri nc ip le s, tec hniq u es, and appli ca - tion s in o rog en ic t er ranes. In : E. Jag er and J.C . Hu nzik e r, eds., Lect ur es iso to p e g eo logy , pp. 77-104. Spr i n g e r -Verlag, Berlin , Heid e lberg, and New York, p. 329. Dalrym p le , G.B ., and M.A.Lanp he re (19 71 ) , ◄ 0Ar / 39Ar tec hniq u e of K/ A r dati ng : A comp ar iso n wit h the conventi on al tec hn iqu e. Eart h Planet. Sci. Let tm , 12. pp. 300-308. Davis , P .K . (19 77) , Ef fec ts of shock pre ssure on '0Ar/3 9 Ar radio m etr ic age dete r mi na ti on s. Geoclzem. Cosmochim . Acta . 41, pp. 195-205. Debuy st ·, R ., Deje h et, F ., Grun, R., Ap er s, D., and DeCannie r e, P . ( 19 84) , Possib i l- ity of ESR-dati ng wit ho ut dete r mi na ti on of the annual dose-rate . J . Radio n al. Chem . , Lett. 86, pp. 399-410, Budap es t. DePaolo, D.J ., and G.J. W asserburg (19 76a) , Nd iso to p i c vari at io n s and pet ro g en eti c models. Geop hy s . R es. Lett ers , 3, pp. 249-252. DePaolo, D.J ., and G.J .W asserburg (1976b) , Infe r ences about mag ma sources and mantl e stru ctu r e from varia t io n s of 143Nd / 14 ◄ Nd. Geop hy s . Res. Lett ers , 3, pp. 743-746. DePaolo, D.J. (19 81a) , Trace element and iso to p i c eff ec ts of combin e d wall rock assim il at i on and frac ti on al cry st a ll iz a ti on . Eart h Planet. Sci . Lette rs , 53, pp. 189-202. DePaolo, D.J (1981b) , A neodym ium and str on ti um iso to p i c stu d y of the Mesozoic calc-alkaline gran i tic bath o lit hs of the Sie r ra Nevada and Peni ns ular Rang es , Calif ornia. J Geop hy s . Research, 86, No. Bil, pp. 10470-10488. DePaolo, D.]. (1981c) , Neodym ium iso to p e s in the Colorado Front Rang e and crust- m antl e evoluti on in the Prote r ozoic . N atu re , 291, pp. 193-196. DePaolo, D.J. (1981d) , Nd iso to p i c stu d ie s : Some new per spe c ti ve s on Eart h
stru ctu r e and evoluti on . Eos, 62, No. 14, pp. 137- 14 0. DePaolo, D.] . (1981a) , Nd iso to p i c stu d ie s : Some new per spe c ti ve s on earth str u ctu r e and evoluti on . Eos 62, No. 14, pp. 137-140. (A luc id account of advances in iso to p e geo chemi st r y usin g Nd iso to p e s as tra cers.) Faure, G. (1986) , Pri nc i ple s of iso to p e geo log y. 2d ed. New York: Joh n Wi le y and Sons. Faure.G., H urley, P.M., and Fair b air n , H.W . 0963) , An esti m ate of the iso to p i c comp o sit ion of str o nti um in rocks of the Precambrian shie ld of North Americ a . J Geop lzy s. Res. 68, pp. 2323-2329. Faure, G., and J.L ,.Powell (1972) , Str o nti um iso to p e geo lo g y . Sp ri n g e r -Verlag, New York, p. 188. Fleis c her, R.L., Price , R.B.,a nd Walker, R.M . 0975) , Nuclea r tra cks in soli ds ., Pri nc ip le s and app li ca ti on s. B erkeley: Univ . of Califo rn ia Press. Fukuchi, T ., Im ai, N. and Shim okawa, K. (1986) , ESR dati ng of f au lt movement usin g vario u s defe c t centr e s in qua rt z: the case in the weste r n South Fossa Magn a , Jap a n . Ea ,1/z Planet . S ci . Le tt. 78, pp. 121 - 1 2 8. Gleadow, A.].W ., Duddy, LR ., Green, P. L. and Heg a rty , K.A . 0986) , Fis s io n trac k leng ths in the apa ti te annealin g zone and the int e r pr e ta t i on of mix e d age s . Eart h Planet. Sci . L ett. 78, pp. 245-254. Goldic h, S.S. and Mudrey, M.G.,J r. (19 72) , Dila ta n cy model for dis c ordant U-Pb zirc on age s . In: Cont. to R ecen t Geochemi str y and Analyti ca l Chemi str y , A.P. Vin o g rad ov Vol 血 1e , Ed. A. I. Tug a rin o v, pp. 415-418. Nauka Pub!. Off ice , M oscow, USSR . Green, P.F . (19 85) , Comp a riso n of zeta calib r ati on baselin e s for fiss io n -tr a ck dati ng of apa t i te, zirc on and sph e ne. Chem. Geol., Isoto p e Geo scie 11 ce Sectio n , 58, pp. 1-22. Grun, R. (19 85) , £SR -d atin g witho ut dete r mi na ti on of annual dose: a firs t app li ca ti on on dati ng mollusc shells. In: ESR Datz· n g and Dosim etr y, Eds. M. lkeya and T.Mi ki , pp. 115-123. Ionic s Publi sh in g Co., Toky o. Harr iso n, T.M. (19 81) , Dif fusi o n of '0Ar in hornblende. Contr ib. Mi ne ral. Petr ol. 78, pp. 324-331 . Hart , S.R. (1964) , The pet r ol og y and iso to p i c-m i ne ral age relati on s of a conta c t zone in the Front Ran ge , Colorado. J Geo!. 72, pp. 493-525. Hart , S.R. ,G erlach, D.C . ,and W 血 e, W.M. (1986) , A pos sib l e Sr-Nd-Pb mantl e
array and consequ e nces for mantl e mix i n g . G eochim . Cosmochim . Acta . 50, pp. 1551-1557. Hawkesworth , C.J., M. Hammi ll, A.R . G ledhil l, P. van Calste r en, and G.R o g er s (19 82) , Isoto p e and tra ce element evid e nce for late -s ta g e int r a -crusta l melti ng in the Hig h Andes. E arth Planet. S ci. L ett er s, 58, pp. 240- 25 4. Herrmann, A.G (1970) , Yt triu m and the lanth a nid e s. In : K.H . Wedepo h l, Handbook of Geochemi stry, Il (5) , pp. 57-718 to M, Spr i n g e r -Verlag, Berlin , Heid e berg. a nd New York. Hurfo rd , A.J. , and Green, P.F. (19 82) , A user's guide to fiss io n -tr ac k dati ng calib r ati on . E art h Planet. Sci. Lett. 59, pp. 343-354. Hurfo rd , A.] ., a nd Green, P.F. (1983) , The zeta age calib r ati on of f iss io n -tr a ck dati ng . Isoto p e Geoscie n c e. 1, pp. 258-317. Ikey a, M. (1 975) , Dati ng a sta l acti te by electr o n par amagn e tic resonance. Natu r e, 225, pp. 48-50. Ikeya , M.,T. Mi ki , a nd K. Tanaka (1982) , Dati ng of fau lts by electr o n spi n resonance on int r af a u lt mate r ia l. Sci en ce, 215, pp. 1392-1393. Kralik , M. (19 82) , Rb-Sr age dete r mi na ti on s on Precambrian carbonate rocks of the Carpe n ta r ia n McAr thu r Basin , Nort he rn Territo r ies , Austr al ia . Precambri an Res. 18, pp. 157-170. Lal, D., M uralli, A.V ., Raia n , R.S ., Tammane, A.S., Lorin , J.C .,and Pellas, P. (19 68) , Techniq u es for the pro p er revelati on and vie w ing of etc h - tra cks in mete o riti c a nd ter restr ial min e rals. Eart h P lanet. Sci . Lett. 5, pp. 11-119. Lang mu ir, C.H . ,R.D . Vocke, Jr., G.N. Ha nson, and S.R. H art (l 978), A gen eral mix i n g equ a ti on wit h app lica ti on s· of Iceland ic basalts. Eart h Planet. Sci. Lett er s, 37, pp. 380-392. Lop ez Mart ine z, M., York, D., Hall, C.M. , and Jan es, J.A . (19 ~4),_Oldest reliab le •0Ar/39Arag es for ter restr ial rocks:Barbertci~ n Mounta i n komati te. Natu r e, 307, pp. 352-354. Luck, J.M ., and G.J. A llegr e (1983) , 181 Re .l 81 0s sys t e m ati cs in mete o rite s and cosmolo 양 cal consequ e nces. Natu re , 302 , pp. 130-132. Marshall, B. D., and DePaolo, D.J. (1982) , Precis e age dete r mi na ti on s and pet ro g en eti c stu d ie s usin g the K/Ca meth o d. Geochim . Cosmoclzim Acta .46 , pp. 2537-2545.
Mi tch ell, J.G . (1968) , The argo n- '0/a r go n-39 meth o d for po ta s siu m -argo n age dete r mi na ti on . Geochim . CoS? n ochim . Acta . 32, pp. 781 -7 90. Mor ton , J.P . (1985) , Rb-Sr dati ng of d ia g e n esis a nd source age of c lays in U p pe r Devonia n black shale of Texas. Bull. Geo/. Soc. Ame r. 9 6, pp. 1043-1049. My er s, J.D .,M arsh, B.D ., an d Sin h a, A .K . (19 85) , Str o nti um iso to p i c and selecte d tra ce element varia t i on s betw een two leuti an volc anic cente r s (A dak and At ka ) : Imp li ca ti on s for the develpm ent of arc volcanic plu m bin g sys t e m s. C ontr ib . Min e ral. Pet ro l . 9 1, pp. 221 -2 3 4. Naeser, C.W . , and Faul, H. (19 69) , Fis s io n tra ck annealin g in apa tit e and sph e ne. J Geop hy s . Res . 74, pp. 705-710. Nakai, N., and T. Nakamurg (19 8 4) , Accele rato r mass spe c tr o me tr y of Natu r al-level 14C. Mass Ana/y e is, 32 (2) , pp. 211 - 219. Nie ls on, D.L . ,Evans, S .H . , an d Sib b ett , B .S . (1986) , Magm a tic , s tru ctu r al, and hyd r oth e rmal evoluti on of the Mi ne ral Mounta i n s int r u is iv e comp le x, Uta h . Geol. Soc. Amer. Bull. 9 7, pp. 765-777. Nie r , A .O . (19 50) , Phys , Rev. 77, p. 789. Nohda, S., and G.J .W asserburg (19 81) , Nd and Sr iso to p i c stu d y of volcanic rocks from Jap a n . Eart h P/a n et . S ci . L et te r s, 52, pp. 264-276. Nohda, S., and Wasserburg, G.J . ( 19 86) , Trends of Sr and Nd iso to p e s thro ug h tim e near the Jap a n Sea in nort he aste r n Jap a n . Eart h P/a n et. S ci. L et t. 78, pp. 157-167. O'Ni on s, R.K.,P .J. H ami lton , and N.M .Evensen (197 7) , Varia t i on s in 1'3N d / 4 Nd and 87Sr/8 6S r rati os in o ceanic basalts. Ea itlz Plane t. S ci . L e tte r s , 34, pp. 13-22. Ozim a , M. , and F.A . Podosek (19 83) , Noble gas geo chemi str y . Cambrid g e Univ e r- sity Press, p. 367. Ozim a , M.,S.Zashu, and 0. Nit os h (1983) , 3 H 티 4He rati o, n oble gas abundance and K-A r dati ng of diam onds. An att em p t to search for the r~cords of early ter restr ial hist o r y . Geochim . Cosmochim . Acta . 47, pp. 2217-2224. Owen, L.B. , and G.Faure (1974) , Sim u lt an eous dete r mi na ti on . of hafn ium and zirc o n ium in sili ca te rocks by iso to p e dilu ti on . Anal. Chem. 46, pp. 1323- 13 26. Rog er s J.J.W . , and IA. S. Adams (l969) , Thoriu m . In : K.H . Wedep oh l ed., Handbook of Geodie m i stry vol. Il ~5 Spr h g er , Verlag.
Papa n asta s sio u , D.A ., and G.J. W asserburg 0978) , Str o nti um iso to p i c anom- alie s in the Allende mete o rite . Geop hy s . Res. Let te rs , 5, pp. 595-598. Patc h ett , P .J ., and M.Tats u moto (19 80a) , A routi ne hig h -p re cis io n meth o d for Lu-H f iso to p e geo chemi str y and chronolog y. Contr ib . Mi ne ral. P et ro l. 75, pp. 263-2 6 8. Patc h ett , P.J ., and M. Ta ts u moto (1980b) , Lu-H f tot a l -rock iso chron for the eucrite mete o rite s . N atu r e, 288, pp. 571-574. Purser,K . H . 0979) , Dir e ct dete c ti on of 1'C and oth e r rare ato m s usin g aceler- ato r tec hniq u es. Tracer , 2, pp. 2-17 . Roddic k , J.C . 0983) , Hi gh pre cis io n int e r calib r ati on of '0Ar-39Ar sta n dards. Geoclzim . Cosmoclzim . Acta . 47, pp. 887-898. Schaef fe r , O .A . 0 982) , Laser mic ro p ro be argo n 39-argo n 40 dati ng of ind i- vid u al gra in s . In L.A . Currie , 139-148. Ame r. Chem, Soc., Sym p. Ser. 176, p. 516 . Sharma, Y.P ., Lal, N., Bal, K .D . , P arshad, R. and Nagp a ul, K.K. (19 80) , Closin g tem p er atu r es of d if fere nt fiss io n -t ra ck clocks. Contr i b . M i n. Petr o l. 72, pp. 335- 33 6. Shim okawa, K., N. Imai and H. Hir o ta ( l 9 8 4). Dati ng of a volcanic rock by electr o n spi n resonance. Isot o p e Geoscie n ce, 2, pp. 365-373. Sis so n, V.B ., and Onst o t t , T.C . (19 86) , Datin g bluesch ist meta m orp hism : A combin e d '0Ar /3 9 Ar and electr on mic r op ro be app ro ach. Geoclzim . Cos ,no chim . Acta . 50, pp. 211 1- 17 . Ste r n, T.W ., S .S . G oldic h , and M.F. Newell (1 966) , Ef fec ts o f w eath e rin g on the U-Pb age s of zirc on from the Mort on Gneis s , M i nn esota . Eart h Planet. Sci . L e tte rs , 1, pp. 369- 37 1 . Thie l, K. Saage r , R. and Muff , R . ( 1980) , U-f is s io n trac k mic ro mapp ing as a means to stu d y uraniu m mobil iza ti on pro cesses in Precambria n sedi- ments . Nucl . Instn n n. and Meth o ds. 173, pp. 223- 23 7. Til to n , G.R . (1960) , Volume dif fus io n as a mechanis m for dis c ordant lead age s . J Geop hy s . Res. 65, pp. 2933-2945. Tilton , G.R ., and B.A .Barreir o . (1980) , Orig in of lead in Andean calcalkalin e lavas, south er n Peru. Sci en ce, 210, pp. 1245-1247. Til to n , G.R. (1983) , Evoluti on of dep le te d mantl e:T he lead per spe c ti ve . Geo- chim . Cosmochim . Acta . 47, pp. 1191-1197. Turekia n , K.K., a nd K.H . Wedep o hl. (1961) , Di st r ibu ti on of the elements in
some majo r unit s of the Eart h' s c rust. Geo !. S oc. A m e r Bull., 72, pp. 175- 18 2. Turner, G. (1968) , The dis t ri b u ti on of po ta s siu m and argo n in chondrite s . In : L. H Ahrens, e d., 01-ig i n and dis tr ibu ti o11 of lite elem e nt s , pp. 387 -39 8 . Perga m on Press, London, p. 117 8. Turner, G. (1969) , Thermal his t o r ie s of mete o rite s by the 39A r/4 0A r meth o d. In : Me teo n 'te Res ea rch , p p. 407 - 41 7. R eid e l Publish in g Co., D ordrecht, p. 942 . Wasserburg, G.J ., and Dep ao lo, D.J. ( 1979) , Models of earth stru ctu r e inf e r r ed from neody mium and stro nti um iso to p i c a bundances. Proc. Na t. A cad . Sci . U SA 76, pp. 3594-3598. Wasserburg, G .J. ,S . B .Ja cobsen, D.J .D e Paolo, M . T.M c Culloch, a nd T.W e n ( l98 1 ) , Precis e dete r mi na ti on of Sm/ N d rati os , Sm and Nd iso to p i c abun- dances in sta n dard soluti on s. Geo c ltim . Cos m o c/ 1i1 11 . Ac ta , 45, pp. 2311- 23 23. Weth e rill , G.W . ,G. L. D av is, and C. Lee-Hu. (19 68) , Rb-Sr measurements on whole rocks and sep a rate d min e rals from the Baltim ore Gneis s, Mar- yla nd. Geol. Soc. Ame r. B ull, 79, pp. 757 -76 2 . Weth e rill , G .W . (1956) , Dis c ordant uraniu m - lea d age s . T rans. Ame r. Geop l tys. Unio n , 37, pp. 320- 32 6 . Weth e rill , G.W . (1963) , Disc ordant uraniu m -lead age s 一 Pt. 2, Dis c ordant age s resultin g from diff usi o n of lead and uraniu m . J.G e op hy s . R es ., 6 8, pp. 2957-2965. Weth e ril l, G.W. (19 66) , Radi oa cti ve decay consta n ts and energi es . I n : Hand- book of Phys i c a l Consta n ts , pp. 514-519, S.E. C larke, Jr. , e d. Geo!. Soc. Amer. M em. p. 95, 587. York, D. (19 66) , Least-s q u a res fitting of a str ai g h t line . Can. ]. Phys . 44, pp. 1079-1086. York, D. (19 67) , The best iso chron. E art h Planet. Sci . Lett er s, 2 , pp. 479-482. York, D. ( 1969) , Least-s qu a res fitting of a str ai g h t line wit h correlate d errors. Eart h P lanet. S ci. Lette rs , 5, pp. 320-324. York, D., C.M .Hall, Y.Y a nase, J.A. Hanes, and W.J. Keny on (19 81) , 40Ar/3 9 Ar dati ng of ter restr ial mine rals with a conti nu ous laser. Geop hy s . Res. Lette rs , 8, pp. 1136-1138. 오재환 (198 1), 「우수중의 Tr iti um 농도와 기단과의 상관관계연구」, 충남대 대학 원논문.
 제 4 부 지구의 진화
제 4 부 지구의 진화
9 지구의 진화 9-1 서언 150 억 년 전 우주의 대폭발 이후 끊임없이 우주의 물질은 전화되어 왔으며 태양계의 물질도 진화되어 오고 있다. 특히 지구의 물질은 운 석과 달리 화학적으로 분화되어 맨틀에서 지각으로 전화되었음이 연, 스트론튬, 니오디미움 등의 동위원소 연구에서 밝혀지기 시작했다. 지구 대기 역시 Tauri 단 계에 강한 태양풍에 의해 태양계 초기의 대기가 없어전 후 지구 내부에서 탈가스 (De g as) 에 의해 지구 . 초기에 는 환원형 대기에서 산화형 대기로 전화된 것으로 보고 있다. 전화의 원동력이 되는 에너지는 우라늄, 토륨, 칼륨 등의 방사성 붕괴에서 발생하는 에너지 (E 츠 1031) 와 지구의 형성과 전화과정을 통하여 해방되 어진 중력에너지를 들 수 있다. 죽 태양계 성운이 회전운동에 의해 분열되어 형성된 수많은 미행성 들이 빠른 속도로 상호충돌과 화합을 반복하는 과정에서 점차 지구와 같은 큰 행성으로 성장하였다고 가정해 보면 성장과정에서 질량이 증 대하여 지구의 자기중력도 증대하게 된다. 이 갇은 충돌에너지가 지열에너지로 지구에 축적되거나 우주공간에 방출되기도 한다. 지구형성 후 이런 에너지에 의해 지구내부의 물질 은 화학적으로 재분배되어 Fe, N i과 같은 무거운 원소는 지구 중심
으로 가벼운 규산염광물의 구성성분은 지각으로 집적되어 지구의 충 상구조를 만들게 되었다. 물론 판구조론 운동과 지질시대를 통하여 축적된 방사성 붕괴에너지에 의해 화산활동이나 조륙운동 등이 일어 나게 되었다. 이 장에서는 우주의 원소의 합성과 연, 스트론튬, 니오 디미움 등의 방사성 동위원소에 의한 지구물질의 진화를 살펴보기로 하겠다. 9-2 원소의 합성 아인슈타인의 일반 상대성이론을 이용한 우주의 모델은 우주는 무 한히 작은 체적으로 압축되어 있던 것이 어느 순간 갑자기 거대한 크 기로 되었음을 가리키고 있다. 천문학자들은 이 문제의 해답을 찾아 내기 시작했다. Gamow (l 948) 는 우주 초기 대단히 고온상태에서 평형상태에 있던 양자, 중성자, 전자, 뉴트리노 등의 소립자가 우주 팽창이 시작되어 온도가 낮아지므로 이들간의 평형이 깨어져 중성자의 일부는 8 붕괴 를 하고 양자는 중성자를 포획하여 중양자를 만드는 과정 이 반복되 어 연속적으로 무거운 원소가 합성되었다고 주장하였다. 이것을 이론화한 것이 1957 년에 제출된 B2FH(Burbid g e , Burbid g e , Fowler and Hoy le ) 이 론인 대 폭발설 (Big bang the ory) 이 다. 현존하는 모든 원소가 합성되는 데는 20 분 정도의 시간이 걸렸다고 보고 있다. 이 사실을 입증하는 놀라운 사실이 1965 년 전파 천문학자인 윌슨과 펜지아스에 의해 발견되었다. 그것은 우주에서 등방적으로 지구로 입 사되는 3°K 흑체방사파에 상당하는 전자파의 발견이다. 대폭발시 방 사된 뜨거운 빛이 우주팽창에 따라 토플러 효과 때문에 파장이 길어 져 현재 3°K 흑체 방사에 해 당하는 방사광이 되 어 빅 뱅 (Bi ng bang) 의 잔광으로 나타나고 있다는 것이다. 대폭발시에 만들어진 대부분의 원소는 빅뱅 과정에서 재분해되어
원자번호 6 번 이상의 원소는 빅뱅에서 만들어진 가벼운 원소가 별의 내부에서 수소와 헬륨이 핵융합 반응과정에서 C, Be, Mg 등을 만들 게 되었다. 그러나 Fe 보다 무거운 원자핵은 핵융합반응만으로는 불가능하여 He 핵융합과정에서 생긴 중성자를 포획하는 느린 중성자포획 반응이 일어나 점차 무거운 원자핵을 만들게 되었다. 이 과정은 바교적 느린 반응이므로 S- 과정 (Sfo w p rocess) 이라 한다. B i보다 무거운 원자핵을 만들기 위해서는 더 강한 중성자선의 조사가 요구되는데 초신성의 폭 발과정에서 가능하며 이때 일어나는 중성자 포획반응은 대단히 빠르 게 일어나므로 이를 R- 과정 (Rapi d p rocess) 이라 한다. 이 같은 과정에서 대부분의 원소가 만들어지지만 112sn 원자핵은 양자 포획반응에서 형성되므로 P- 과정에서 만들어진다. 빅뱅에서 만 둘어진 H, He 등 일부 경원소를 제의하면 모두 별의 내부에서 초신 성 폭발과 원자핵 반응에서 만들어진 것이다. 현재 태양계를 구성하고 있는 원소는 83 종 정도이고 그 중 수소 (H)와 헬륨(H e) 이 99.9% 를 차지하고 있다(표 9-1). 태양계 전체 구 성원소에서 보면 지구는 태양계 구성원소의 0.1% 에도 미치지 못하는 산소나 철, 마그네슘, 규소(비휘발성분) 등으로 되어 있다. 그럼에도 지구나 행성의 기원이나 진화를 논의하는 데는 이들 원소 의 상호작용이 중요하다. 태양계의 구성원소는 대부분 태양계 형성 이전에 만들어전 것이나 아르곤 (Ar) 과 같은 원소는 지구형성 후 지 구내부의 칼륨( ◄ oK) 이 붕괴하여 생긴 것이므로 초기 지구대기의 탈가 스 연구나 우라늄 동위원소와 함께 태양계 및 우주의 연령연구에 이 용되고 있다. 운석 에서 129I 나 244Pu 와 같은 단반감기 원소의 존재가 확인되 었 다. 방사성원소는 반감기의 배수의 시간이 경과하면 거의 소멸해 버린 다. 따라서 이 같은 원소를 만든 핵융합 반웅은 운석형성 직전에 일
표 9 기 태양계의 원소의 존재도 (Anders 와 Ebih a ra, 1982) 원소 존재도 원소 존재도 원소 존재도 원소 존재도 1H 2.7 2 Xl010 Ti 2400 Ru 1.86 Dy 0.398 He 2.18Xl09 V 295 Rh 0.3 4 4 Ho 0.0 8 75 Li 59.7 Cr 1.34 X 1 04 Pd 1. 39 Er 0.2 5 3 Be 0.7 8 Mn 9510 Ag 0.5 2 9 Tm 0.0386 B 24 Fe 9.0 0 X 1 05 Cd 1.59 70Y b 0.2 43 C 1.21 x w Co 2250 In 0.184 Lu 0.0369 N 2.48Xl06 Ni 4.93 X1 04 50Sn 3.82 Hf 0 .176 F。 2.0814X3 l07 3oC l,nu 1521640 STbe 04..39 51 2 wTa 00..10 32 726 10Ne 3.7 6 X l06 Ga 37. 8 I 0.9 0 Re 0.0507 Na 5 . 70 X1 04 Ge 118 Xe 4.3 5 Os 0.717 Mg 1. 075 X1 06 As 6.7 9 Cs 0.3 7 2 Ir 0.660 Al 8.4 9 X 104 Se 62. 1 Ba 4.36 Pt 1. 37 Si =106 Br 11.8 La 0.4 4 8 Au 0.186 P l.04 X l04 . Kr 45.3 Ce • 1.16 50H g 0.5 2 s 5.15X 105 Rb 7.0 9 Pr 0.1 7 4 Tl 0.184 Cl 5240 Sr 23. 8 60N d 0.8 36 Pb 3.1 5 Ar 1.04 X105 Y 4.64 Sm 0.261 Bi 0.144 21)CK a 6.13717X0 lQ 4 4oNl, rb 100..7 71 GEud 00..30 39 17 2 Tuh 00..00 03 930S Sc 33. 8 Mo 2.5 2 Tb 0.0589
어났음을 의미한다. 죽 태양계 물질을 만든 원소합성 반응의 끝과 태 양계 형성이 동시임을 의미하므로 단반감기 핵종이 존재하는 운석은 태양계 초기의 물질임을 알 수 있다. 우라늄 같은 원소는 100 억 년 이상되는 대단히 긴 반감기를 가지고 있다. 100 억 년 이전 수십억 년의 기간에 걸쳐 만들어졌음을 추정할 수 있다. 이같이 우주 물질의 우라늄이나 토륨과 같은 방사성동위원소의 반감기를 이용하여 우주의 연령을 측정하여 우주의 시간적 역사를 다 루는 분야가 우주연대 학 (Cosmochronolog y) 이 다.
9-3 운석의 동위원소 성분 1) 운석의 종류 태양계의 기원에 관한 많은 연구는 운석을 이용 연구하였다. 운석은 두 소행성 (As t ero i d) 이 궤도운동 중 충돌에 의해 생긴 파편 둘이 소행성 궤도와는 별도의 태양궤도에 진입 지구궤도와 접하여 지 구궤도에 들어온 질량 103g ~ 108g 정도의 물질이다. 운석 은 주로 규산염 광물로 구성 되 어 있는 석 질운석 (St on es) , 50% 씩 의 규산영 광물과 금속광물로 구성 된 석 철운석 (Sto n y iro ns) 그리고 98% 이상 금속으로 된 철운석으로 분류된다. 태양계 초기물질연구에 석질운석인 콘드라이트 (Chondr it e) 가 많이 이용된다. 콘드라이트는 밀리미터 크기의 둥근 감람석 , 휘석, 장석, 유리질 등 (Chondrule 이라 부름)의 콘드률로 된 운석을 말한다(사진 9-1 ) .
 사진 9-1 콘드라이트 중의 콘드를의 사진. 시료 길이 2cm 임.
사진 9-1 콘드라이트 중의 콘드를의 사진. 시료 길이 2cm 임.
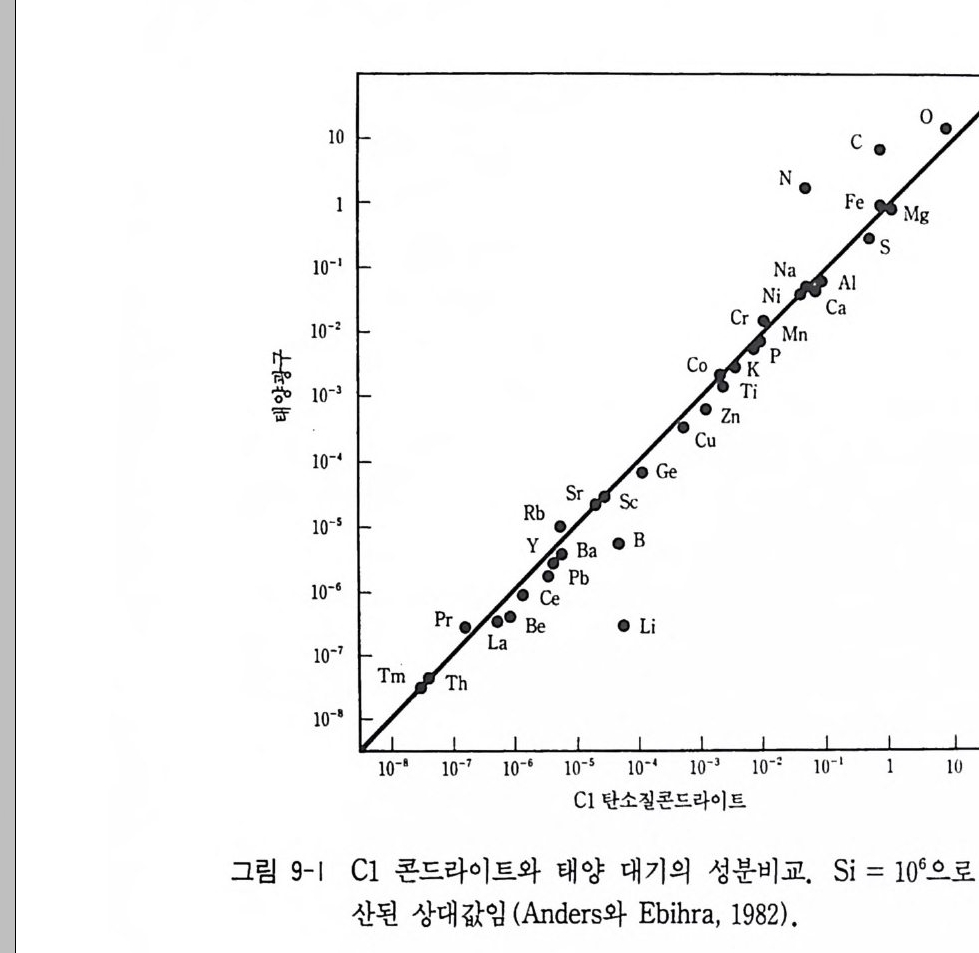 10
10
콘드라이트는 화학성분도 다양하며 암석기재도 다르다. 콘드라이트 는 철의 함량의 다소에 따라 세분하여 함량이 높은 데서부터 H, L, LL 군으로 분류한다. 탄소질 콘드라이트는 CI, CM, CO, CV 등으로 구분된다. CII (= Cl) 콘드라이트의 화학 성분은 태양코로나 중에서 관측된 원소조성과 상관성이 대단히 좋다(그림 9-1). 여기서 운석의 연구가 태양계의 성분연구에 유용함을 알 수 있다. 2) 운석의 동위원소 성분 운석의 동위원소 성분변화는 ® 동위원소 분별과정 ® 혼합 ® 방
사성붕괴 @ 우주선과의 상호작용 등에 의해 일어난다. 태양계 의부에서 만들어진 물질을 연구하는 데 동위원소가 어떻게 이용될 것인가? 콘드라이트 중 Ca, Al 이 많은 포유물은 응축이나 증발에 의해 형성된 것이며 초기 태양계 성운의 잔존물 중에서 가장 오래된 것으로 생각된다. U-Th-Pb 법의 연령측정 결과 4.55X109 년 이 얻어졌고 87Sr / 86Sr 초생치가 0.699 정도로 암석물질 중에 가장 낮은 값을 가진다. Ca, Al 이 많은 콘드라이트의 포유물의 산소 동위원소 성분의 분석 결과를 110I 160 와 180/ 16 Q의 축으로 도시하면(그림 9-2) 지구물질과 운석의 포유물 사이에는 동위원소 분별의 기울기가 다르다. 죽 지구 물질은 운석의 기울기의 1 / 2 이다. Ca, Al 이 많은 포유물은 보통의 태 양계 물질과 초신성 폭발시 형 성된 순수한 160 사이의 혼합선으로 해석하였다 (Cla yt on 등, 1973).
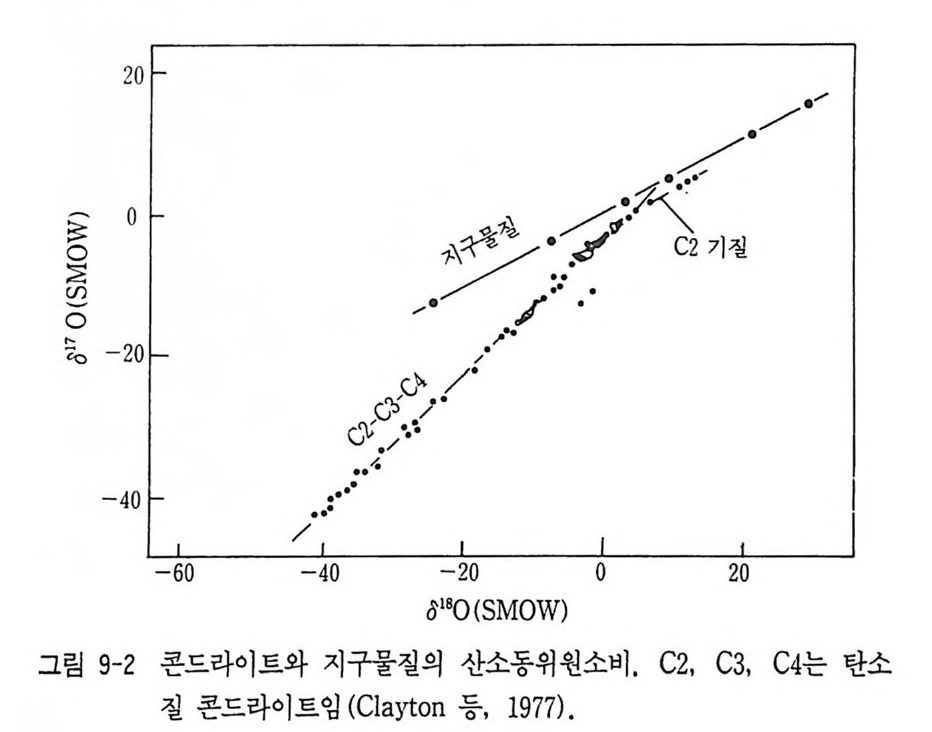 20 / •✓
20 / •✓
산소 동위원소 성분의 다양성에 비추어 다른 원소들의 동위원소 성 분에서도 다양하고 이상적인 성분이 예상되었다. 한 예로 소멸핵종의 과거 존재증거를 연구한 것이다. 콘드라이트의 포유물 중에 26M g의 많은 함량이 발견되 어 (Lee 등, 1977) 26Al 의 방사성 붕괴 를 가리 켜 주 었다. 26Al 의 반감기가 7.2 X l0 년인 점을 감안하면 이 방사성핵종은 핵 융합 직후 태양계 성운에서 형성되었음을 말해 준다. 160 과 같이 26A1 도 핵융합의 탄소폭발에서 만들어졌다. 이 갇은 동위원소의 산출은 초신성과 태양계 성운의 시간측정 척도 가된다. 9-4 우주연대 측정 우주연대학에 이용되는 핵종은 s_ 과정핵종, r- 과정핵종, p과정핵 종 등의 다양한 방사성 동위 원소들이다(표 9-2) .
표 9-2 우주연대학에 이용되고 있는 방사성핵종 (小 嶋 와 齊藤 , 1982) 핵종-+붕괴후 생성핵종 붕괴양식 반감기 (Ma) 비고 s 과정 핵종 81Kr 一 81Br EC 0.2 1 93Zr --+ “Nb p- 0.9 5 r 과정 기여 2osp b - 21l5'fl EC 15 176Lu 一 176Hf 8- 27,000 147Sm --+ 143Nd a 105,000 r 과정 기여 r 과정 핵종 233u --+ 209B i (a, g) 0.16 찍 u---+ 206p b (a, 13-) 0.25 248Cm -+ (門 Pu) a, SF 0.35 wp u --+ (238U) a, SF 0.3 9 236Np --+ 208Pb (a, f3- ) 1.3 237Np ---. 209Bi (a, 13-) 2.14 135Cs ➔ 135Ba f3- 2.3
따 )d _. 101Ag p- 6.5 s 과정 기여 182H f ._. 111..¥ .T /3- 9 247Cm -+ (효 U) (a, 13-) 15 1291 --+ 129X e g- 17 2J6 u --(2 32Th) a 24 244Pu --+ (232Th) (a, g), SF 82 235U --+ 201p b ( a, 1 3-) 703.8 238u --+ 206P b (a, p-) 4,468 232Th ---z o~P b ( a, 13-) 14 , 010 187R e 一 1870s 13- 43,000 “R b 一 87S r /J- 48,800 초중원소 (4 ) ? p과정 핵종 202p b --+ 202Hg EC 0.3 208B i 一 208P b EC 0.37 96T c --+ 9sR u 13- 1.5 1soG d _. (146Sm) a 1.8 91T c _. 91M o EC 2.6 14 汀 ` c---+ 1 막 Nd a 103 92N b __, 92zr EC ~100 138L a --+ 138B a, t3 8Ce EC,/3 - 150, 00 0 기타 60F e -> 60Ni g ~0.1 36C l 一 36A r f3- 0.3 26A l 一 26Mg /3\ EC 0.7 4 10Be -+ 10B 13- 1.5 53Mn -> 53Cr EC 3.7 40K --+ 40Ar, 40Ca 8\ EC, g 1,397
우주연대 계산에는 연속합성 모델과 순간합성 모델이 이용된다. 단위우주공간내에서 단위시간에 일어나는 임의의 핵종의 양의 변화 는
cJ!!..j/1 = -11,Nj ( t) + Pjp (t) (1)로 표현된다. 여기서 N i(t)는 핵종 i 의 시간 t 에서의 존재량 A i는 핵종 i 의 붕 괴정수 (안정핵종인 경우 ,,li = 0) pi는 원자핵융합과정시 핵종 i 의 생 성속도 p(t)는 시간 t에 있어서 원자핵합성이 일어나는 빈도이다. 위 식의 해는 Nl (to) = P,.exp ( _A,to ) \。~ exp (1 1; t)p(t) dt. (2) 이 된다. 안정핵종인 경우에는 N, (to) = P1\TP(t) dt (3) 。 이 된다. 태양계내의 핵종의 전량을 구하기 어려우므로 보통 핵종의 존재비 를 구한다. 임의의 시간 t에 있어 핵종 i와 핵종 j 의 존재비는 NN사晶 )) = iJP:· exp {-(A i-11;) to} f ~\r 。T: ee xxpp (( 1A1 J; rr ) ) pp (( r r )) ddtt (4) 로 표현된다. 태양계내 물질을 구성하는 원소의 동위원소의 성분은 대단히 균일 하다. 따라서 운석이나 지구암석 등 태양계 물질의 극히 일부분을 취 해도 그 동위원소 성분은 태양계를 대표한다고 볼 수 있다. 따라서 위 식의 우변은 측정이 가능한 양이다. 그리고 P j IP i는 원자핵 구조에 관한 경험법칙에서 이론적으로 추
정할 수 있다. 여기서 원소합성 반웅이 기간 T 사이에 전부 진행되었다고 가정하 는 소위 연속원소합성 모델을 생각해 보자. (1) 식은 P( t) = 일정 O~t < T (5) P( t) = O t> T 로 둔 것에 상당한다. 즉 별의 폭발빈도가 기간 T 에 걸쳐 동일하였다고 보면 좋을 것이 다. 이때 4, 5 식에서 원소합성이 종료시점 (t = T) 에서의 Nj I Ni 비는 役 )T = (%) exp {-(A J - A,) T} ~ (6) Ai 이 된다. 한편 원소합성 반응이 순간적으로 일어났다고 가정하면 순간적 합 성모델을 적용하면 p(t) = Ao( t- T) 가된다. 여기서 8 는 모델관수이고 A 는 반응강도정수이며 관측치와 비교하 기 위해 4 식을 이용하면 시점 t에 있어서의 값은 (N묘i) t = RReg xpp {{-_AMi (tt --TT ))} (7)
p(I) p(I) -45 . 5 억 년 1 원소합성 ( 1, -T) 一 l l 현,재 현재 。 T lo 。 / 。 (태양계의 시작) (a) (b) 그림 9-3 원소합성 반응의 모식도. (a) 연속합성 반웅 모델 (b) 순간적 합성반응모델. 이 된다. 시간축과 P( t)축을 잡아 연속합성 모델과 순간합성 모델을 모식적 으로 나타낸 것이 그림 9-3 이다. 그러면 연속원소합성 모델과 순간합성 모델을 이용하여 우주의 연 령을 계산해 보자. Ni = 238U, Nj = 235U 이라 놓으면 묘N,· = (235U / 238U) T = ((PP223385 // AA223385 )) 11_-eexx pp ( ( 키一 A 223358 TT)) (8) 으로표현된다. T 는 원소합성 종료시간으로 현재에서 45.5 억 년 전의 태양계 연령 이 된다. 지금부터 45 . 5 억 년 전 원소합성 반응이 종료된 시점의 P 23s / P238 의 값은 반이 론적으로 측정 된 P235 / P238 = 1. 42 를 취 한다. 이를 (8) 식에 대입하면 (2350 / 2380) r = (2350 / 2380) P X ~exp ( 4 . 55 x 109 X t12 39) = 0 . 3165 0.3165 = 1.42 X ~1. 55125 X 10-10 X ~1-(ex p키 ( -9 . . 58458152 5XX l100--101 0XX TT)) :. T 츠 8X10 년
::;;::I1 :; /l표 :9\-3 31우3주의: :연:령 : 。 〕(단위 I,: 三 Ma) I 三
이 계산된다. 따라서 U 을 만든 r- 과정의 원소합성 반응은 125.5 억 년까지 80 억 년의 기간에 걸쳐 연속되었다는 것이 된다. 같은 방법으로 순간적인 합성모델 식에서 계산하면 T = 6 .4X l09 년이 얻어져 64 억 년 전에 순간적으로 핵합성반응이 일어났음을 의미한다. U, Th, 1870 s, 8 7Rb 등에 의해 계산된 우주의 연령은 표 9-3 과 같다. 이 상에 서 보면 235u-2 3su-23 2 Th 의 경 우 연속합성 모델을 이 용하면 원소합성 시작에서 태양계 형성까지 (8.5 土 3) xl0 3Ma 걸렸다. 이 연령에서 우주의 연령을 계산하는 데는 빅뱅에서 최고 r - 과정 원소합성이 일어날 때까지의 시간을 추가해야 한다. 이는 은하전화 모델에서 2Xl 03M a 정도 (Tr i mble , 1975) 이므로 우주의 연령은 2+ (8 .5 土 3) + (4.6 土 0.1) ~ (15 士 3) X 10 3M a 가 얻어전다. 이 값은 허블정 수를 이용하여 구한 우주팽창연령 (17 土 2) x1 03Ma (Sand g e 와 Tam· mann, 1975) 나 구상성단의 연령에서 구한 (13 土 3) x 103Ma 와도 찰 일 치하고 있다. 9-5 단반감기 핵종을 이용한 연대측정 장반감기 핵종은 우주의 연령이나 원소합성 시기를 측정하는 데 이 용되지만 129I, 244Pu 과 107Pd 와 같은 단반감기 핵종은 태양계 형성 직 전의 원소의 합성에 관한 정보를 준다. 이 같은 단반감기 핵종은 방 사성 붕괴에 의해 태양계 형성 후 46 억 년 사이에 완전히 소멸되어
현재에는 붕괴결과로 생긴 딸원소밖에 조사되지 않는다. 1291 (반감 기 = 1. 7 X 10 년), 244Pu(8 . 2 X 10 년) 그리고 107Pd (6 . 5 X l0 년)와 같은 단수명 핵종을 소멸 핵 종 (Exti nc t nuclid e ) 이 라고도 한다. 운석 중의 1291 가 방사성 붕괴에 의해 형성된 129Xe* 이 운석에서 소 량이지만 측정되고 있다. 129Xe* = (1291) 。 여기서 (l291) *에 표시된 0 은 운석물질이 만들어진 시점을 나타내며 n 은 원소합성반웅 종료시점을 나타낸 기호이다. 원소합성 종료시점과 운석이 만들어진 시점 사이에는 (l29I) 。 = (l291) ne-m·l 과 같은 관계가 성립된다. ,11 29 (4.1 X 10 -s / 년)는 l29 I 의 붕괴상수이다. 위 식에서 J29X e* = (1 29!)ne- ,ll 29/ 으로 표현할 수 있다. 동위원소의 함량측정보다 동위원소비 측정이 측정 정도가 높으므로 ( 12 홉 )= (댜 )neA l29 t 로 표현된다. 여기서 (1291 / 121 1) n 의 값을 구하기가 어렵기 때문에 t의 절대치를 구하지 않고 상대치를 구한다. 예를 들면 `두 개의 운석시료 중 각각 운석의 시간을 t1, t2 이라 할 때 L1t = t 1- t 2 라 두면 다음과 같이 시 간의 상대 값 L1t 7} 얻어 진다. 129 129 Llt = t1- t2 = 六l n {( 麟 1/( 溫밥 실제에는 Bju r bole 콘드라이트 운석을 하나의 표준시료로 사용하
고 이 운석의 상대적인 형성연대의 편이를 구한다. 많은 운석에서 측 정한 결과 운석들이 3 , 000 만 년 이내의 짧은 기간 동안에 형성되었음 울 알 수 있게 되었다. 따라서 이 같은 핵종에서 태양계 형성 직전에 일어난 원소합성의 정보를 얻을 수가 있다. 9-6 지구의 연령 지구의 연령은 운석의 연대측정에서 얻어진 것으로 Rb-Sr 법과 Sm -Nd 법 등에서 측정된 결과는 (37 土 2) X l03Ma~(47 士 0.13) x· l03Ma 까지 나타난다(표 9 - 4 와 9-5 ) . 대 체 로 46 X 103Ma 가 많으므로 현재 46 억 년으로 보고 있다. 연 동 위원소법에 의해 얻어진 아이소크론 연령도 45 . 5 억 년(H ue y -Koh man, 19 7 3) 이 얻어져 Rb-Sr 법과도 일치하고 있다(그림 9-4). 스트론튬의 초생 치 (81S r / 86S r) ; = 0 . 698-0 . 703 까지 나타나지 만 0.699 - 0.700 값이 가장 많으므로 이 값을 지구의 초기물질의 스트론뮴 초생치로 간주하고 있다. 그러면 지구와 운석이 동시에 형성되었다는 증거는 무엇인가? 콘드라이트 중에서 앞절에서 소개한 방사성 핵종의 방사성 붕괴결 과로 생긴 129Xe * 의 발견이다 (Re yn olds, 1960). 129Xe* 는 129 I 가 방사성 붕괴되어 형성된 것이다. 이때 반감기는 17 Ma 이다. 태양계가 형성된 후에 태양계내의 129I 의 생성은 무시해도 좋다. 129I 는 모두 태양계 성운에서 원소합성 반응에서 만들어진 것으로 생 각해도 좋다. 129I 의 반감기가 짧기 때문에 태양계 역사 초기에 전부 붕괴해 버렸을 것이다. 운석 중에 포함되어 있는 소량의 129Xe 이 운 석 형성 후 운석내의 129I 가 방사성 붕괴되어 생긴 산물이라는 사실만 입증되면 그 운석은 태양계 초기단계에서 만들어진 시료가 될 수 있 게 된다.
표 9-4 운석 의 Rb-S r 연 대 운석의 종류 분류 연대 (103Ma ) (8; Sr / 86S r) 。 참고문헌 석질 운 석 a) 콘드라이트 Indurch I E4 I 4.5 6 土 0 . 1 5 0 . 7005 土 3 /Go p ar an & Weth e rill 0970) Tie sc h it z H3 4 . 6 3 土 0 . 06 0 . 6 9880 土 20 Min s te r e t a l. 0976) Guaren a H6 4 . 56 土 0 . 08 0 . 69995 土 1 5 Wa ss erb u r g cl al. (1969) Pea c e Riv e r L6 4. 56土 0 . 03 0. 69970 土 10 Gray et a l. (1973 ) Krahenberg LL5 4 . 70 土 0. 02 0 . 6989 土 5 Kem p & MUi ier (19 69) Oliv e n z a LL5 4. 63 土 0 .16 0.6994 ± l Sanz & Wasserb u r g 096 9) St Seve rn LL6 4. 55 土 0 . 09 0. 699 04 土 8 tlla nh e s el al. 0975) Allende C3 0. 69877 土 2( 0 . 69876) Gray et a l. 0973) Allende C3 0. 69 884 土 8(0 . 69877) Tats w no to et a l. 0 976) b) 에이콘드라이트 Nor to n County Aub 4.70 土 0 . 1 3 0.700 土 2 Bog a r d et a l. 09 67 ) Nort on County Aub 4.4 8 ±0.04 0 . 7005 土 4 Min s t er & All eg r e 0 976) Bis h op vi lle Aub 3.7 士 0 . 2 0 . 70 1 5 士 20 Com p st o n et a l. 0965) Juv in a s Euc 4 . 60 土 0 . 07 0 . 69 8 9 8 土 5 All eg r e et a l. 0 975 ) ~ereba Euc 4.18 ±0 .1 2 Min s t e r el a l. 0976) Sio u x County Euc 4.1 9 土 0 . 0 7 Min s t er el al. ( 19 76) lbit ira Euc 4.54 土 0 .20 Min s te r et a l. 0 976) Pasamonte Euc (3.4 ) 0 . 69893 土 3 Na kamu ra et a l. 0976) Nakhla Nak 1.3 7 土 0 .02 0 . 7 0 2 3 2 土 6 Pap an ast a s sio u & KNaap ko hel ata IHN oawk I 3 1..62 4 또 土 는0. 031. 9 0.70—25 4 土 3 WGPaaaplse as ene tra b sa utl r.ag s ( s1( 1i9 o97 u75 4) ) et al. (19 74 ) Ang ra dos Reis IAng | 0.6988 4 土 4 lwasserburg et a l. WC철o운eloe 석mk e의erro ao 규 S산ta염 ti o포n 유 물I ’ O Ohh I 4. 614 .土3 70 . 0 4 00 .. 76 9039 4 0 土 4 II SB(1au9n r7zn7 e )et tt &a l. W(1a9s 7s 0e)r burg
(19 67) Kodaik a nal Oh I 3.8 때 . 1 0 .713 土 2 0 Burnett & Wasserburg (19 67) 표 9~5 운석의 Sm-Nd 연대 1,3 운석 연대 (Ga) (내) , 참고문헌 〈 에이콘드라이트 〉 Juv in a s 4. 56 土 0 . 08 0.50677 土 10 Lug ma ir e t a l. (1976) Juv in a s 4.6 0 0.506616 土 2; Jac obsen and Wasserburg( l 980) Ang ra dos Reis 4. 5 5 土 0 . 04 0 . 50682 土 5 Lug ma ir a nd Mart i (19 77) Ang ra dop s Reis 4. 562 ± 0 .031 0. 5 06664 土 37 Jaco bsen and Wasserburg( 19 81) Pasamonte 4 . 5 8 土 0 . 12 0.5 06 81 土 14 Unruh et a l. (19 77 ) Moore County 4 . 60 土 0 . 03 0 . 50676 土 7 Nakamura et a l. (19 77 ) Moama 4 .5 8 土 0 .0 5 0 . 50684 土 8 Harnet et a l. 0978) 예 르고타이 트 (Shergo t ti tes ) > Nakhla 1.2 6 土 0. 0 7 0 . 51181 土 7 Nakamura et a l. (1982) Shergo t ty , Zag am i , 1.3 4 士 0 . 06 0 . 51020 土 10 Shi h et a l. (19 82) Allan Hil ls 7705 〈 콘드라이트 〉 Murchis o n, Allende 4.6 0 0.506609 土 8 Hamet et a l. (1978) Guarena, Peace Riv e r, St. Seve r in , a nd Juv in a s (achondrite ) *1 43 Nd / 144Nd 초생 치는 모두 6Nd / 1 ◄◄ Nd = 0. 7219 로 표준화하여 계 산하였다.
이 를 위 해 Je ffr e y -Re yn olds 은 운석 에 열중성 자를 조사시 켜 운석 중에 국소량 포함되 어 있는 I (門) 가 중성 자 조사에 의 해 1271 (n, p) 12a1 반웅이 일어나 128I 로 변하고 이는 다시 25 분 반감기로 l28x~ 로 변 하는 결과를 얻었다. 그러면 중성자 조사를 받은 운석 중에는 운석에 포함되어 있던 12axe 와 129Xe 와 실험적으로 만든 12axe* 이 존재하게 된다. 다음은 조
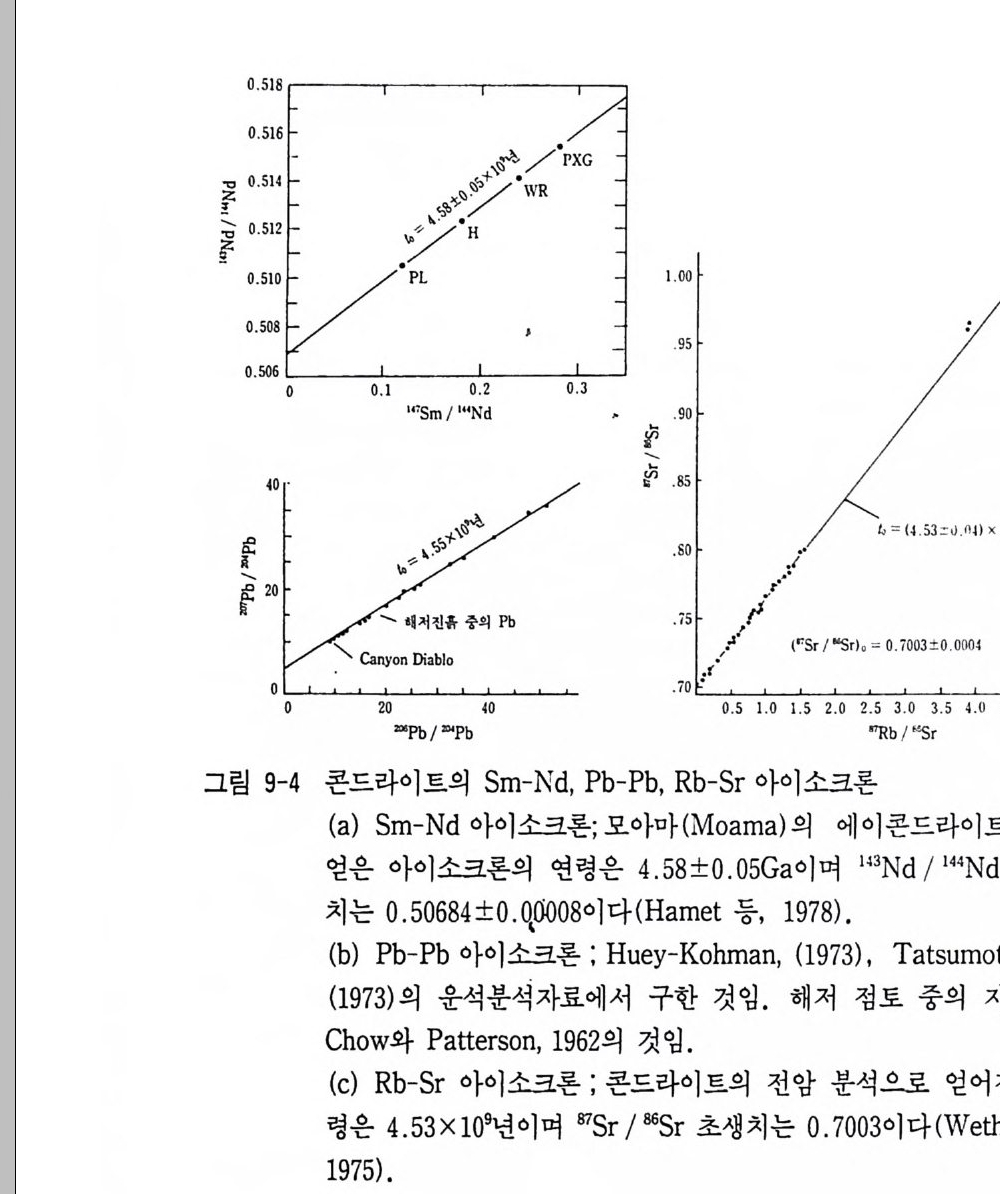 05 I8 5I5II I
05 I8 5I5II I
사시킨 시료에서 Xe 을 추출하여 단계적 가열에 의해 Xe 동위원소 를 추출한다(그립 9-5 a ). 추출된 Xe 동위원소 중에 129Xe/ 13oxe 과 iz sxe / 13oxe 의 값을 각각 X 축과 Y 축으로 하여 도시 하면 그림 9一 5b 와 같다. 두 동위원소비 사이에 좋은 상관관계가 나타난다. 이 상관관계
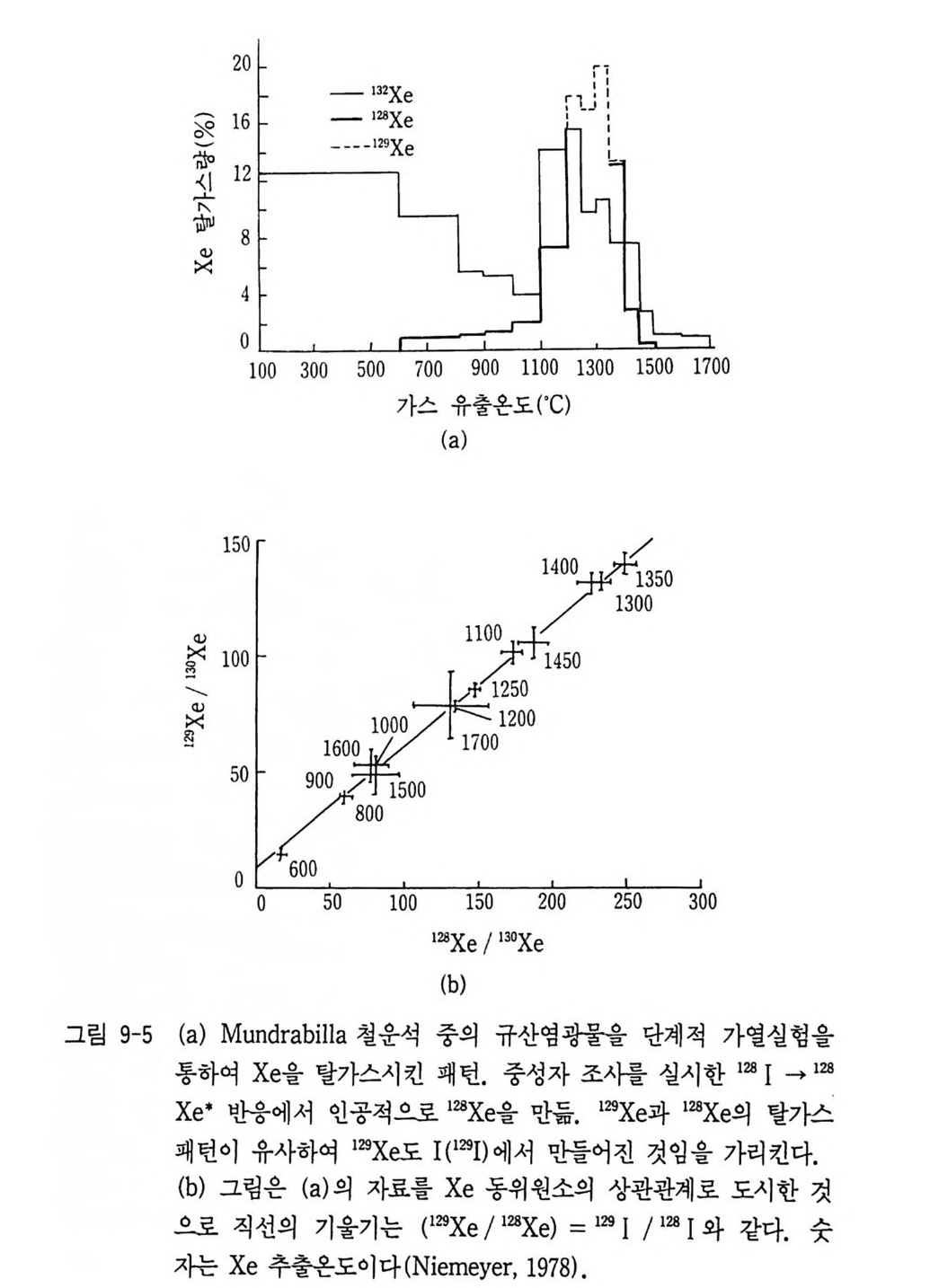 (201 612-—8 1l2382XX ee _'r l Jr ,_'‘IIII III'
(201 612-—8 1l2382XX ee _'r l Jr ,_'‘IIII III'
는 무엇을 의미하는 것일까? 운석 중의 128Xe 과 129Xe 동위원소는 1 29 I 의 방산성 붕괴결과로 생긴 것 (X~) 과 운석형성시 포획된 것 (Xe) 지 포함되어 있다. 따라서 國i29 X e = 國1 [(1 29 Xe) 。 + (12 9X e) *] 로 표현할수 있다. 이 식을 변형시키면 국 = 몫나 ((129Xe) 。 + ~ x {(12 8X e)-(1 28Xe) 。}} = {(〉)。 —(> )*(》 )。} + (>)*(: : : : 이 된다. 그림 9-6b 에 서 129Xe / i 30Xe 과 128Xe I 130Xe 사이 에 선 형 상 관관계가 나타난 사실에서 위식의 1 항과 2 항의 계수인 (12 9X e / 12sx e) * 값이 온도에 무관하게 일정함을 알 수 있다. 단계별로 가열하면 운석의 결정격자나 기질에 들어 있던 이들 각각 의 동위원소가 포획되어 있던 양식에 따라 상이한 방식으로 탈가스 될 것이다(그림 9-5 a). 그리고 그림 9-5b 에서 선형관계의 기울기가 O 이 아닌 점 (12 9X e*::\=O) 은 이 속에 떠 붕괴기원의 129Xe* 이 존재함을 의미해 주고 있다. 때문에 운석의 연령을 지구의 초기연령으로 간주하고 있다. 지구의 암석이 직접 운석연령에 상당하는 결과가 얻어지면 가장 이상적이지 만 지구의 암석은 판구조운동 등에 의한 물질의 순환과 화성활동 등 에 의해 끊임없이 분화되어 왔기 때문에 분화산물로 분화전의 연령을
추정하기가 현재로는 불가능하다. 지구상의 최고기의 암석은 그린랜 드 동부 이수아(I sua) 변성암으로 약 38 X l03Ma 이 얻어졌다 (Moor bath , 1977) . 그 후 오스트레일리아 동부의 암석 중에 포함된 저어콘의 연령이 42 x l0 3 Ma 으로 얻어졌다 (Com p s t on, 1986). 이수아 변성암은 원암이 퇴적암이므로 38 억 년보다는 더 고기의 암석임이 분명하므로 지구의 연령이 38 억 년 이상임은 인정할 수 있다. 9-7 연 동위 원소의 진화 앞 장에서 설명한 것처럼 운석의 연 동위원소가 비교적 균일한 값 (206 P b / 204P b = 9 . 307, 201P b / :zo.ip b = 10 . 294, 208Pb / 204Pb = 29 . 476) 을 가 지는 데 바하여 지구의 연 동위원소비는 아이소크론과 성장곡선에서 보는 바와 같이 변화되어 왔다. 지구가 운석과 동일한 물질에서 생성되었다고 가정하면 지구의 연 동위원소 비는 시간이 지남에 따라 원시연을 출발점으로 변화하게 된 다. 이 를 연 동위 원소 성 장 (Lead iso to p e grow th) 이 라 한다. 연동위 원소 성장은 단일 스데이지 연 성장곡선 (S i n g le sta g e lead iso to p e grow th curve) 과 다단계 연 성 장곡선 (Multi- s ta g e lead iso to p e grow th curve) 으로 나누어 설명할 수 있다. 1) 단일 스테이지 모델 지구와 운석의 구성물질이 균일하여 유사한 238U/204Pb 비를 가진다 고 가정하면 이때 우라늄의 붕괴로 인하여 지구와 운석 중의 연동위 원소비 인 206Pb I 204Pb 와 201p b I 204Pb 는 연대 와 함께 점 차 증가한다. 따라서 폐 쇄 계 로 가정 했을 때 201p b I 204Pb-206p b / 204Pb 의 그림 을 그 리면 46 억 년 전 원시연을 출발점으로 곡선이 그려진다 (그림 9-6a). 그림 9-6a 에서는 µ = 8.2 6 8, 9.646, 1 1. 024 인 경우에 모식적으로
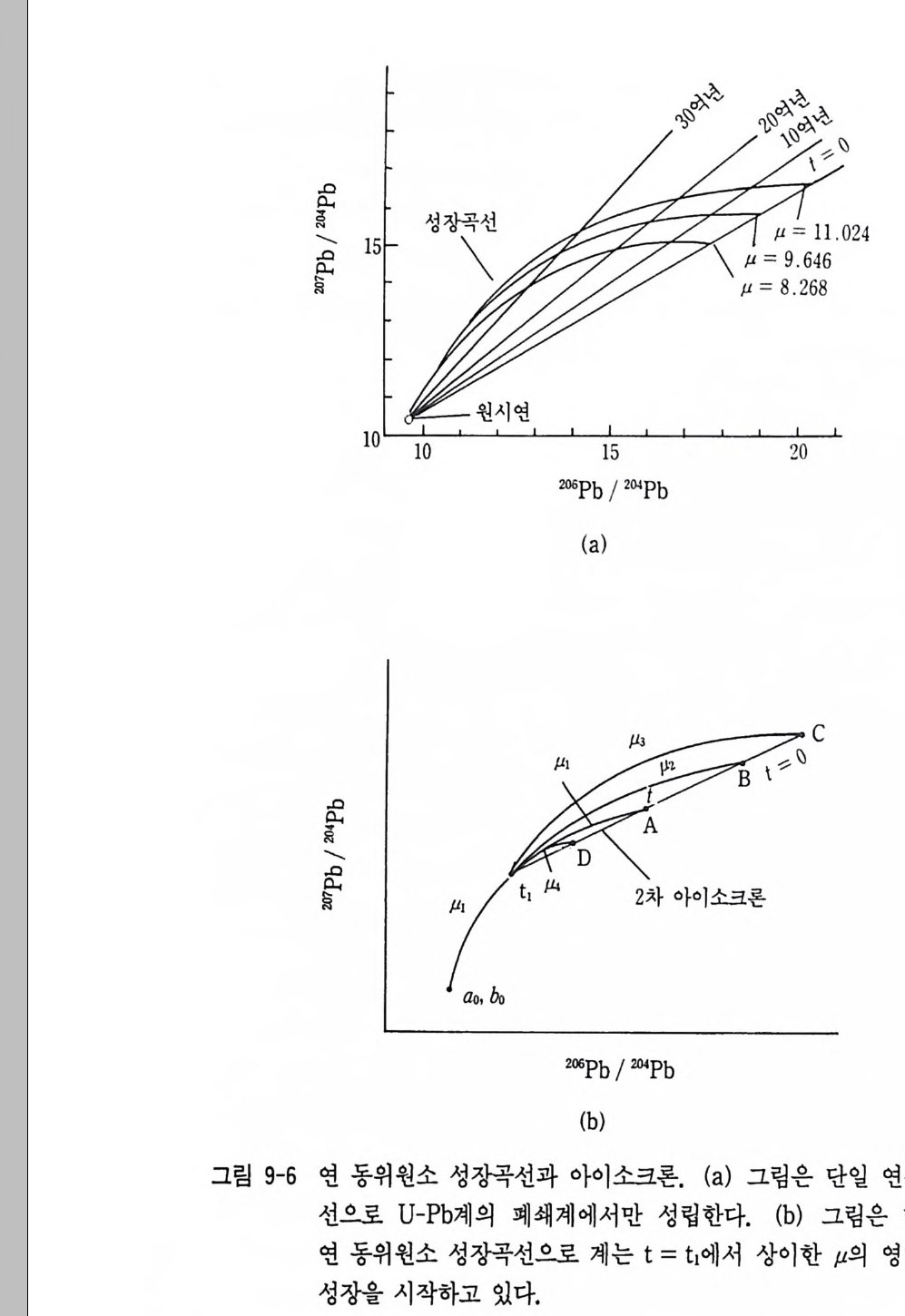 A%
A%
나타낸 것 이다. 이들 곡선을 단일 스 테이지 연동위원소 성장곡선이라 한다. 이때 다른 µ값을 가지는 계에서 성장한 연동위원소비는 동일 시점 에서는 직선상에 놓인다. 따라서 이 직선을 아이소크론이라 한다. 그 립에서 t = 0 (현재 ), 10 억 년 전 , 20 억 년 전, 30 억 년 전에 해당하 는 아이소크론을 표시하였다. ((220067PP bb // 220044PP bb)) 1I __ ((22006 7PP bb // 220044 PPbb)) 。。 = 1371 . 8 ee•A'IIO O 一_ 강e’AtI 이처럼 분명한 1 차석이 된다. 특히 t = 0 에 대한 아이소크론을 지구 연대선 (Geochron ) 이라 하며 이것은 운석의 연대에 대응된다. 스트 론튬과 니오디미움 등에서 보는 바와 같이 지구는 운석과 달리 지구 의 역사 를 통하여 화학적으로 진화되어 왔다. 따라서 연 동위원소는 지각이나 맨틀의 진화과정을 연구하는 수단이 되고 있다. 2) 2 스테이지 모델 만일 개방계에서 U, Pb 가 계의로 유출입이 일어나는 경우에는 2 스 테이지 또는 다단계 성장 모델로 설명해야 할 것이다. 여기서는 간단 한 2 스데이지 모델을 생각해 본다. 연동위원소가 to-+ t까지는 µ = µI, tI - + 0 (현재)까지는 µ = µ2 의 환경에 있었다면 이때 연 동위원소비는 t。 -+ t 1 까지는 µ = µ1 에 해당 하는 단일 스테이지 성장곡선상을 따르나 t = t 1 부터는 다른 성장곡 선을 따르게 된다 (그립 9-6b). 더욱이 t = t 1 에서 µ = µ2, µ3, /.4… ••• 의 몇 개의 다른 µ를 가지 는 계로 발전한 연 동위원소비를 생각해 보면 단일스데이지 성장의 경우와 같이 동일시점 t(t
칙선상에 놓이게 된다. 이 직선을 t 1 을 원점으로 하는 2 차 아이소크 론 (Secondary iso chron) 이 라 한다. 이때의 기울기는 l3}.8 (eA ’t 1- eA’ t) / (eMI_eAt ) 로표현되고 2 차 아이소크론의 기울기에서 2 스테이지 성장의 출발점의 t 1 을 구할 수가있다. 9-8 지각물질의 연 동위 원소비 1) 지각에서의 연 동위원소비 Sun 등(1 975) 의 해양 현무암의 연 동위원소비 분석결과는 그림 9-7 과같다 . 이 현무암 연대가 젊기 때문에 분출 후 연 동위원소비의 변화는 무 시될 정도이므로 이 값을 맨틀값으로 보아도 좋다. 그림에서 보면 분 석자료가 직선상에 배열되고 있다. 이는 상이한 동위원소비를 가지는 두 성분간의 혼합이나 2 스테이지 연 동위원소 성장에 기인할 것이다. 그러나 이 경우 2 스테이지 모델로 설명이 되지 않는 것은 지구연대선 을 중심으로 대칭되게 분포되지 않고 우측에 편중 도시된다는 점이 다. 이같이 지구연대선에서 편재 도시되는 이유는 ® 해양현무암을 만든 맨틀 중의 µ값이 연대와 함께 증가하였거나 ® 운석의 데이터 에서 정한 0 아이소크론이 지구에 적용되지 않는 등의 이유 때문일 것 이다. 화성활동의 결과로 생겨 마그마에 존재하고 있던 지각의 연의 일부 는 우라늄, 토륨 등 방사성 광물과 분리되어 동위원소 성장이 정지된
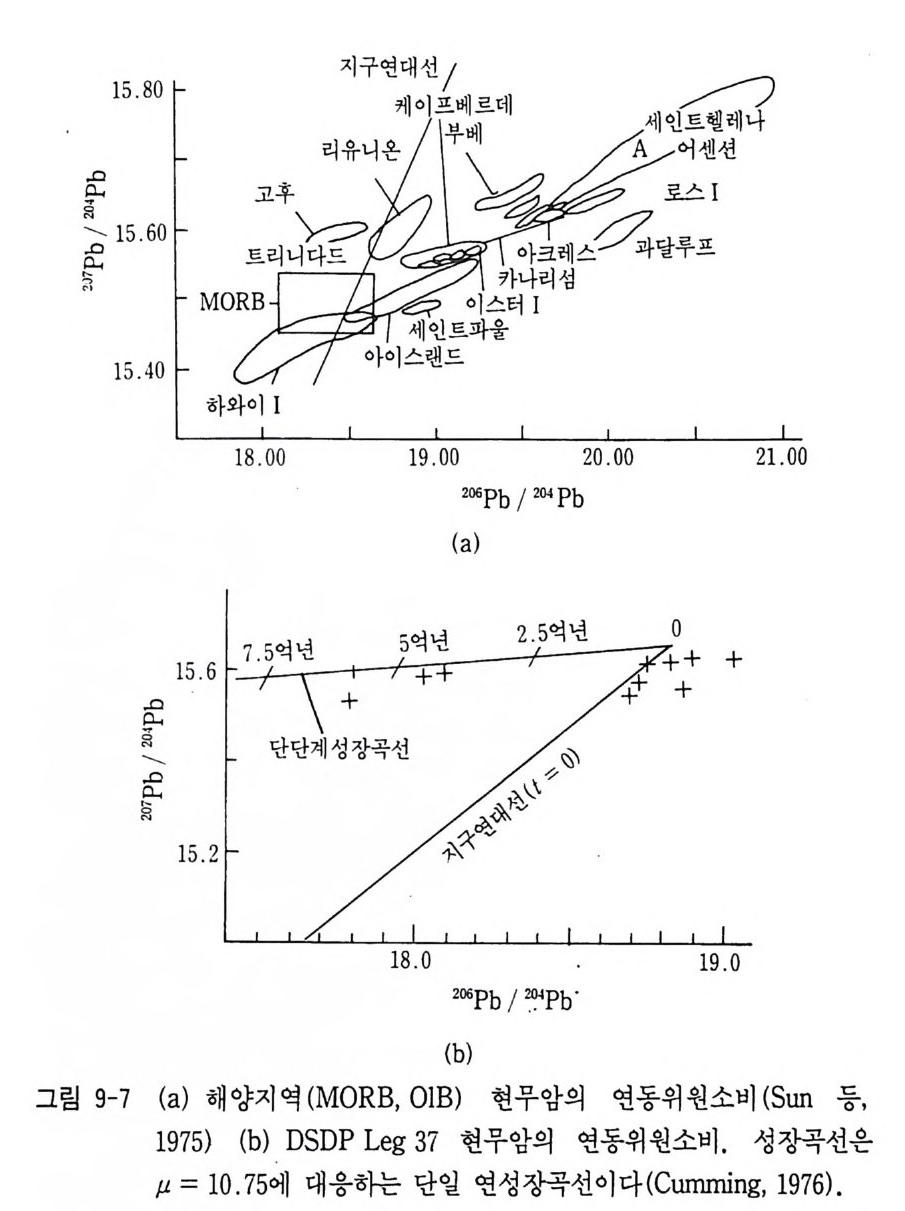 15. 80 지구 연케대 이 선프 / 베 르데
15. 80 지구 연케대 이 선프 / 베 르데
다. 이 같은 예는 광상의 연이나 칼리장석이 생성 당시 우라늄과 토 륨울 거의 가지고 있지 않았으므로 이 같은 물질을 시대별로 조사하 면 각 시대의 화성활동에 관여한 물질의 동위원소비롤 화석으로 취급
할 수 있게 된다. 지각형성시 만들어전 연은 우라늄, 토륨과 같이 지 각에 농축되지만 연의 농축 정도가 우라늄, 토륨보다 작을 것으로 예 상되므로 지각에 있어서 연 동위원소 성장속도는 맨틀보다 빠를 것으 로보인다. 그리고 화산암의 201 p b/204Pb 가 젊은 연대의 지각기원의 연에 비해 계통적으로 낮은 값을 가지는 사실이 조사되었다. 이 사실은 지구의 역사 초기에 맨틀과 지각의 UI P b 값에 차이가 있었음을 의미한다. 이 같은 연동위원소비는 지각의 화학적 전화를 추적하는 자료가 될 것이다. 2) 광상의 연 동위원소 진화 방연석과 연 함유광물은 광상형성의 시대가 젊울수록 동위원소적으 로 성장한 연을 포함하고 있다. 오스트레일리아의 브로큰힐 (Broken H ill)이나 캐나다의 스리비안 (Su ilivi an) 등 함연충상 황화물광상의 주 요 광체의 연 동위원소비는 대단히 균일하며 단일성장 곡선상과 대단 히 근사하나 그 모델과 완전히 합치되지 않고 계통적인 차이가 나타 나고있다. 이같이 단계적이고 연속적으로 계의 µ값이나 (J)값 (각각 현재값으 로 환산한 계의 238UI204Pb 와 232ThI2 여 Pb 비)을 증가시키는 모델로 잘 설명이 되는 것은 광상 연의 기원이 맨틀이라기보다 지각임을 가리키 고있다. 대규모 연광상은 다양한 지각물질이 관여한 지질과정에서 농집된 각 시대의 평균적인 지각 연을 나타낸다는 견해가 많다. 지구의 연 동위원소비는 지구조와 밀접한 관련이 있다. 지구 상충 부의 연의 리 저 버 (Reservoir ) 로서 상부대륙지 각, 하부대 륙지 각, 조산 대와 전지구의 프럼보 텍토닉스 (Plurnbo t ec t on ics) 에 의한 맨틀 연으 로 보면 이들 사이의 연 동위원소 값이 그림 9-8 에서처럼 서로 다르 다.
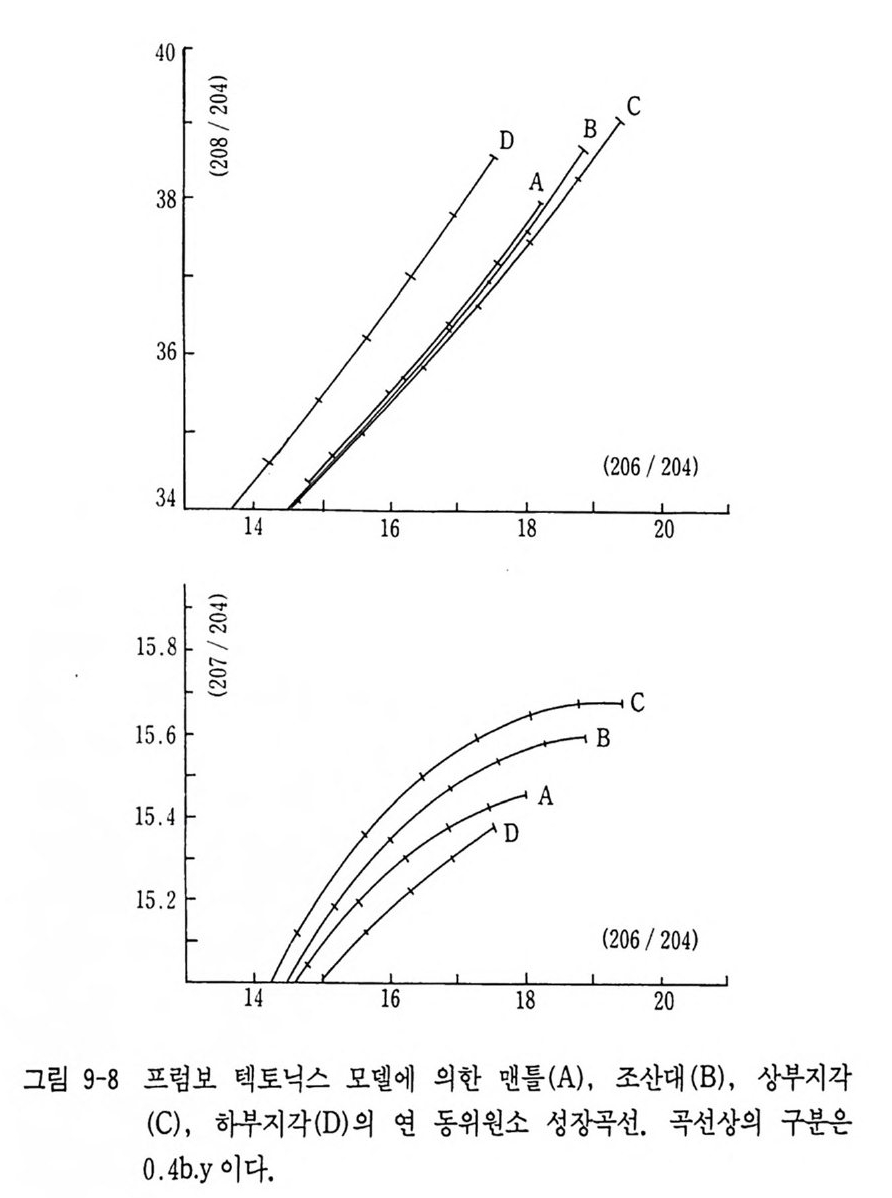 40
40
이 그림은 맨틀에서 40 억 년 전까지를 원시지각 (Pro t ocrus t)의 형성 시기, 그 이후 4 억 년 간격으로 현재까지 11 회의 대규모 조산운동이 있었다고 보고 각 리저버간의 물질의 이동, T-Th - Pb 의 분배 등을 수치모델로 시뮤레이션한 값이다.
중생대-제 3 기 화성암의 연동위원소바를 이용하여 Zartm an (19 74 ) 은 미국 서부지역의 광상구를 구분하였다(그립 9-9 ) . 그림에서 약 200m.y. 간격으로 연의 동위원소 성장이 나타나고 있 다. 이 지역에서 광상의 연의 동위원소 성장곡선은 화성암의 성장곡 선과 유사하다. 암석권에서 U; Th, Pb 의 분포를 보면 하부지각에는 우라늄이 연에 비해 결핍되어 있으나 상부지각은 우라늄이 부화되어 있다. 토륨의 경우에도 맨틀보다는 지각에 이들 원소들이 더 부화되어 있 다. 그림 9-9 의 미국 서부지역의 1 지역은 동위원소 성분의 변화는 심 하나 II, ill 지역에서보다 방사성이 적다. 1 지역에는 두꺼운 선캠브 리아 기반암이 깔려 있다. 연은 하부지각의 U / Pb 비가 낮아 우라늄 기원인 207Pb 와 206Pb 가 결핍되어 있는 기반암에서 유래하였을 것이 다. II 지역은 선캠브리아기 후기-고생대의 두꺼운 차지향사 퇴적물이 분포하고 기반암의 상부지각이 침식제거된 지역이다. 동위원소값의 좁은 범위를 나타내는 것은 상부지각 물질과 균질인 퇴적암의 혼합 때문으로 생각된다. 1Il 지역은 중생대-제 3 기의 완지향사 퇴적물로 구성되어 있다. 이 지역의 연은 해양지각과 멘툴해구의 퇴적물이 베니오프대로 침입되어 맨틀물질과 혼합된 물질의 기원에서 유래된 것으로 해석되어 지구조 적 블럭임을 가리키고 있다. 이 사실은 스트론튬 동위원소(Ki s t ler 와 Pete r man, 1978) 와 니오디미움 동위원소 (Benne tt와 DePaolo, 1987) 연 구에서도 입증되고 있다. 기원물질과 연 동위원소 연구에서 광상에서 금속성분이 추출된 심 도나 열수에 의해 이동된 통로 등을 해석하는 정보로 제공될 수 있을 것이다. 이 같은 연구는 광화작용의 과정 해석과 동시에 광상구 설정에 기 여하여 미래의 광상 탐사의 지침이 될 것이다.
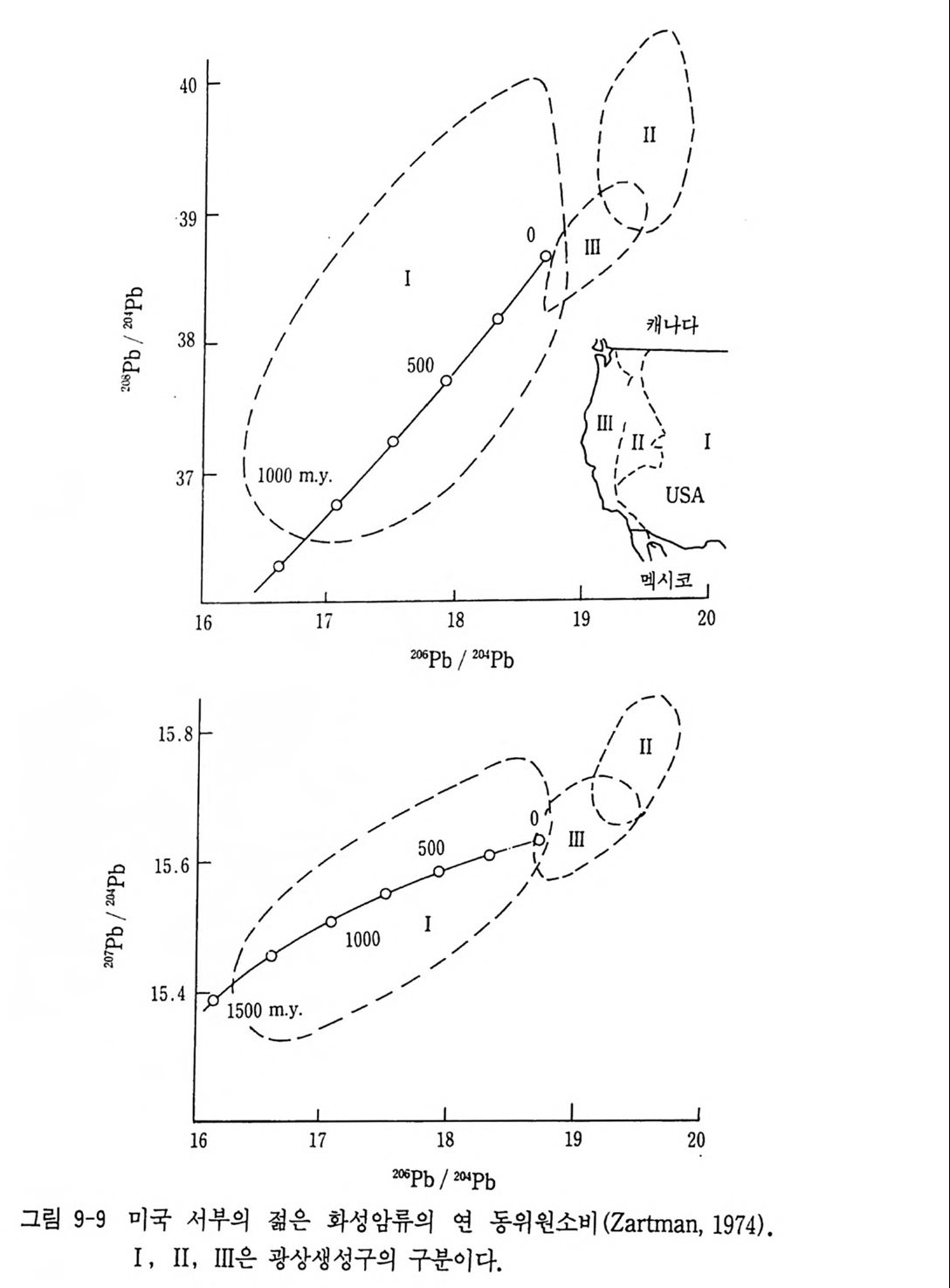 //\ ll\/7/
//\ ll\/7/
3) 우리나라의 연 동위원소 성분 한반도 30 개소의 광상 연 동위원소·분석연구 결과 (Sasak i, 1987) 를 요 약하면 다음과 같다. 연 동위 원소 분석 결과를 [2osp b / 204Pb] — [206Pb / 204Pb] 와 [201p b I 204Pb] _·[ 2o sp b / 204Pb] 그림에 도시하면 그림 9-10 과 같다. 그림 9-10 에서와 갑이 한반도의 연 동위원소는 광범위하게 분산 도 시됨과 동시에 직전상에 도시된다. 이 같은 사실은 한반도에는 선캠 브리아기에서 중생대 사이에 큰 지각변동 기간 동안에 기반암 중의 다양한 U-Th-Pb 계의 전화가 진행되었기 때문이며 직선상에 도시된 것은 2 차 아이소크론의 직선으로 볼 수 있다. 설명의 편의상 일본열도 제 3 기 광상연의 분석자료와 비교해 보자. 한반도의 연은 일본열도의 연에 비해 분산분포를 나타내는 특칭이 있 고 직선상에 도시된다. 그리고 광상연의 성장곡선 (Cumm i n g과 Rich ards, 1975) 보다 위쪽에 도시된다. 2 차 아이소크론의 일반석의 기 울기 S 는 S= l.88(~) 로 표현된다. 여기서 h 및 t 2 는 각각 모전화계(기원암)의 연령과 광화작용의 연대 를 나타내 며 A 과 A2 는 238U 과 23su 의 붕괴 상수이 다. t 2 를 백 악기 의 100m. y.로 가정해서 t 1 을 구해 보면 2.1 土 0.5b. y.가 얻어진다. 이 값 은 한반도 기반으로 널리 분포하는 선캠브리아기의 변성암류의 평균 연령 2.0 土 0.5b. y.와 잘 일치한다. 한반도의 광상연은 기본적으로 다양한 U-Th-Pb 계로 된 2.0b.y. 연령의 선캠브리아대 기반암 중에서 성장을 계속한 연이 중생대의 화 강암 및 이와 관련된 화성활동으로 인해 유출되어 각 지역의 광상으
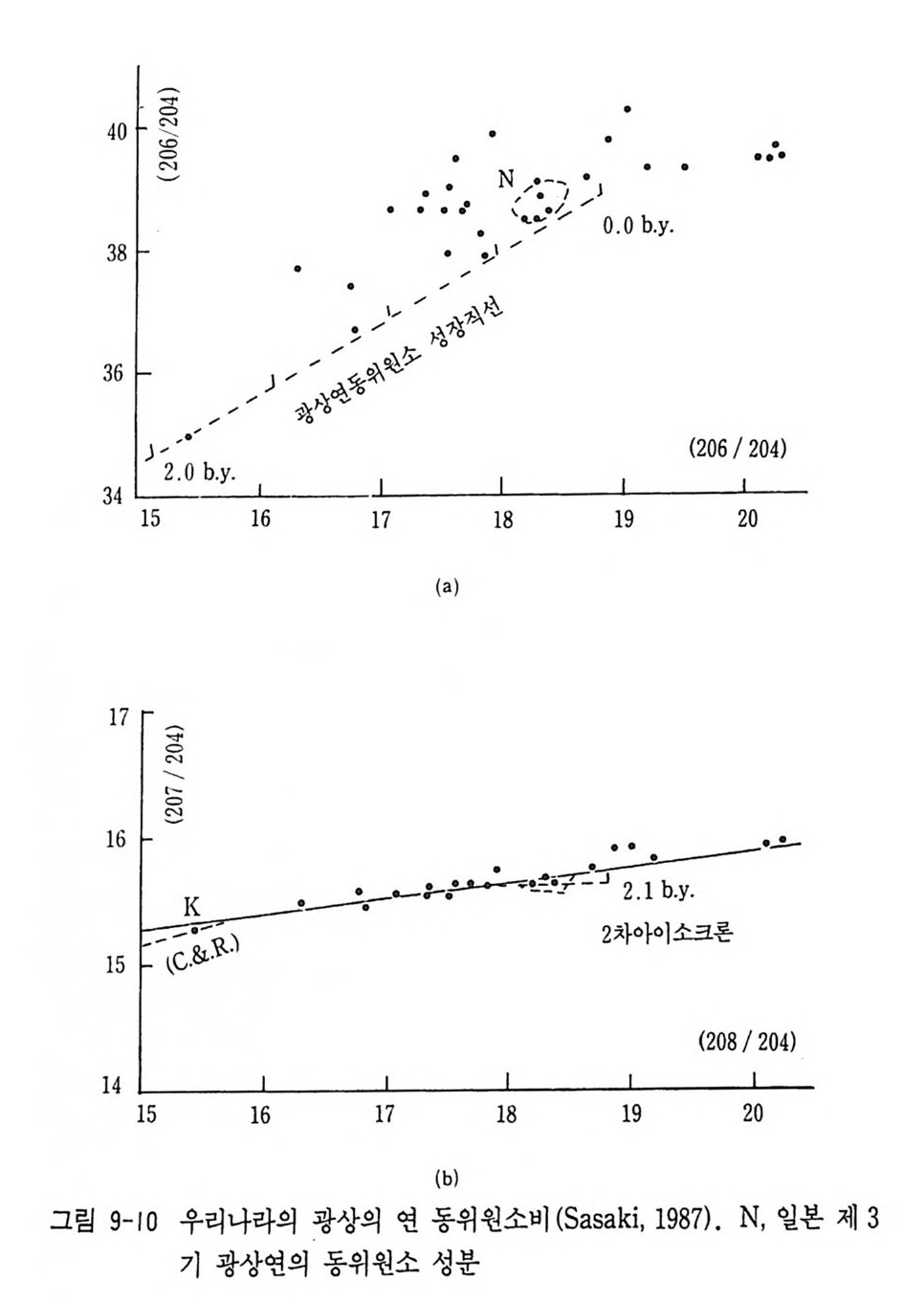 4。 .r 9)Z 0훌 • •· ••. •• . N',' -/~·.- •`v, /•) 。 . O b.y. ••.•
4。 .r 9)Z 0훌 • •· ••. •• . N',' -/~·.- •`v, /•) 。 . O b.y. ••.•
로 고정된 것으로 해석된다. 한반도의 연은 일본의 제 3 기의 연과 유사하게 광상연 성장선 위측 에 도시되며 평균지각의 값에 비해 Th / U 비 가 높은 환경에서 성장 하였다. 그러나 우라늄계의 연이 많은 것 (206 Pb / 2 여 Pb ~ l 9) 은 성장곡 선에 근접되게 도시되지만 아래쪽에 도시되는 것도 있다. Th / U 비 가 높은 환경으로는 그래뉴라이트상의 변성암이 산출되는 하부지 각 의 환경으로 볼 수 있다. 함경북도 검덕광산의 연 동위원소 분포 (K 점)는 독특하며 연령 1.8 b. y.의 성장선상에 도시된다. 광상은 마천령계의 석회암 충 에 수반되 는 연아연 충상광상이다. 그림 9-10 에서와 같 이 [201 p b / 204P b ]-[ 2 0s Pb / 204Pb] 그림 에 도시 하면 일본의 연 동위 원소 값 은 한반도의 연 동 위원소의 직선의 연장상에 놓인다. 이 같은 사 실 은 한반도와 일본의 연의 기원이 동일하지만 한반도에는 넓은 기반암 중에 다양한 U-Th -Pb 계의 진화가 선캠브리아기에서 중생대 사이에 일어난 대규모의 화성활동시에 일어났고 일본의 지각은 대륙연변 변동대의 덱토닉스를 대표하는 퇴적, 화성, 변성, 조산운동 등의 반복되는 환경에 있었기 때문이다. 일본의 연은 광화에 앞서 U - Th-Pb 계 에서의 혼합과 균질 화가 상당히 진행되었기 때문으로 해석되었다 (Sasak i , 1987 ). 9-9 해수의 스트론튬 동위원소의 진화 선캠브리아기의 탄산영암의 8 7 Sr/86Sr 비 분석에 의하면 원생대의 해양의 87Sr/86Sr 비는 25 억 년간 맨틀의 값과 유사하였으나 시생대 말에 와서 Sr 동위원소비가 증가하여 0.7090 에 이르게 되었다 (Ve i zer 등, 1983) . 현재 의 해 양의 해 수의 스트론튬 동위 원소바 (87S r / 86S r) 는 0.70906 土 0.00003 으로 대단히 균일하다. 일반적으로 해수의 Sr 동위 원소 성분의 기원은 ® 신기화산암류 ® 고기 대륙지각의 시알질암석 ® 현생이언의 해성 탄산염암울 들 수 있다.
그러므로 해수의 87 Sr / 86 Sr 비를 분석함으로 대륙이나 해양분지 주 위의 풍화된 암석의 종류와 유입량을 추정할 수가 있다• 즉 지질시대 에 따라 화학적 풍화를 받은 암석의 종류를 해양의 Sr 동위원소비의 변화에서 해석할 수 있다. 그러나 세부적으로 보면 해성 석회암, 돌 로마이트 등에서 분석한 Sr 동위원소비가 현생이언 지질시대 동안에 체계적으로 변화하고 있음이 조사되었다 (그림 9-lla). 현생이언 동안에 해수의 Sr 동위원소바의 변화에서 위에 주요한 세 가지 기원의 Sr 이 그 유입비를 달리하면서 해수에 유입된 사실을 해 석할 수 있다. 고생대 동안에 해수 중의 Sr 동위원소비의 변동은 최고 0.7091( 캠 브리아기말)에서 최저 0 . 7068( 페름기말)까지 이른다. 중생 대 트라이 아스기 중기 에 0 . 7077 에 서 쥬라기 말에 0 . 7068 까지 감 소하고 백악기말과 제 3 기에 증가하는 변동경향을 나타내고 있다. 이 같은 변동의 원인은 위에서 설명한 Sr 의 기원의 3 가지의 상이 한 암석분포 때문이다. 각기 다른 위치에 분포하는 해성 석회암 중의 Sr 에서 분석된 해양 의 Sr 동위원소비의 분석결과를 보면 전체적인 양으로 보면 대단히 균일한 성분을 가지고 있음을 알 수 있다. 그 이유는 해수의 짧은 혼 합시간 (10 년)에 비교하여 5 X 106 년의 긴 정체시간을 둘 수 있고 해수 중의 Sr 농도 (7.7µ g I g)가 하천수 중의 농도 (10 . 068µ g/ml) 보다 훨씬 높기 때문이다. Faure 등 (19 65) 의 모델 계 산식 은 (>)sw = (itv + ( >)ss + (>)AIm 과 같다. 여기서 (81Sr / 86Sr)sw = 해수 중에서의 비, (87Sr / 86Sr) v.S. M = 신기 화산암 (V), 고기시 알질암석 (S)' 해성 탄산염암 (M) 의
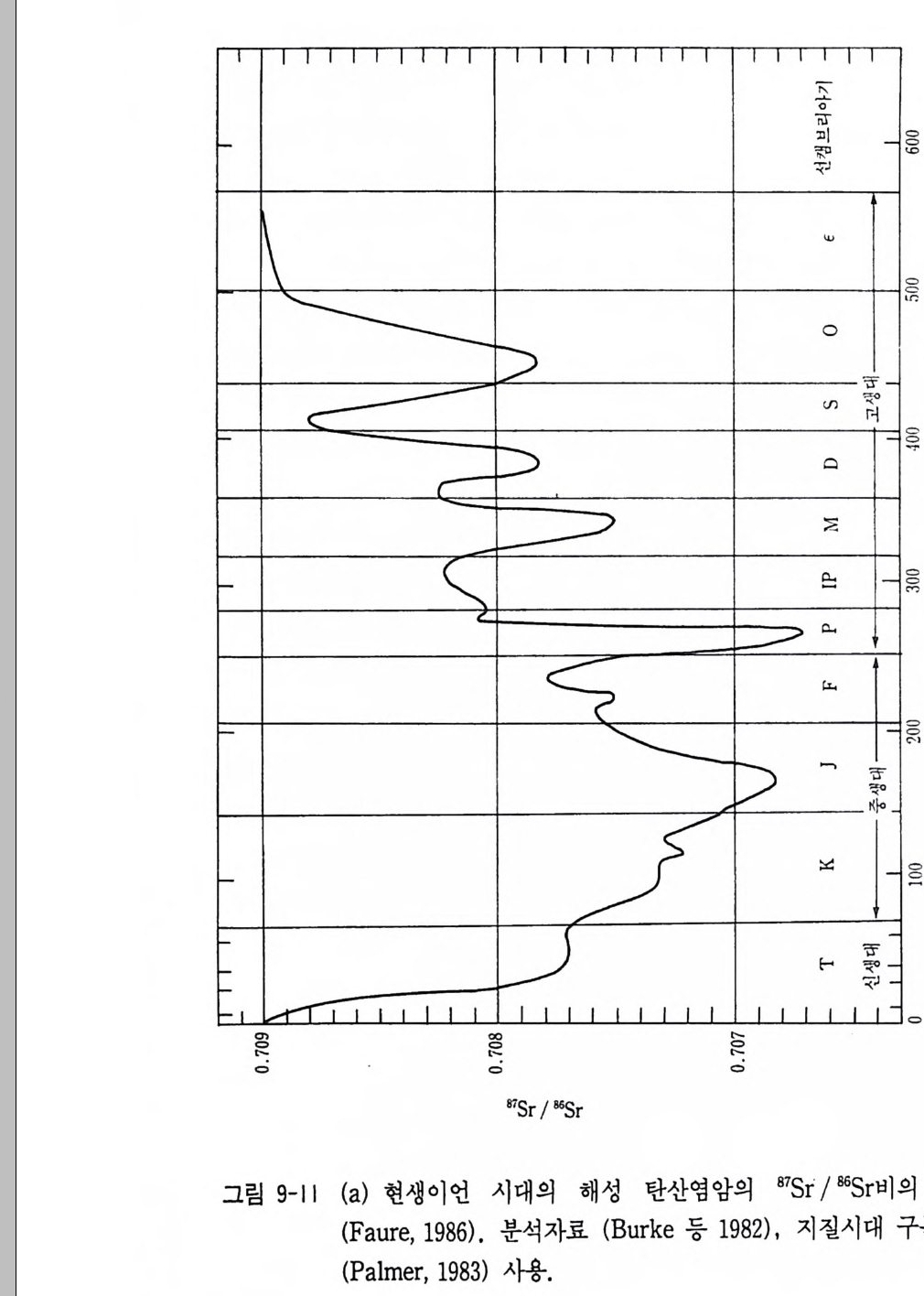 4l
4l
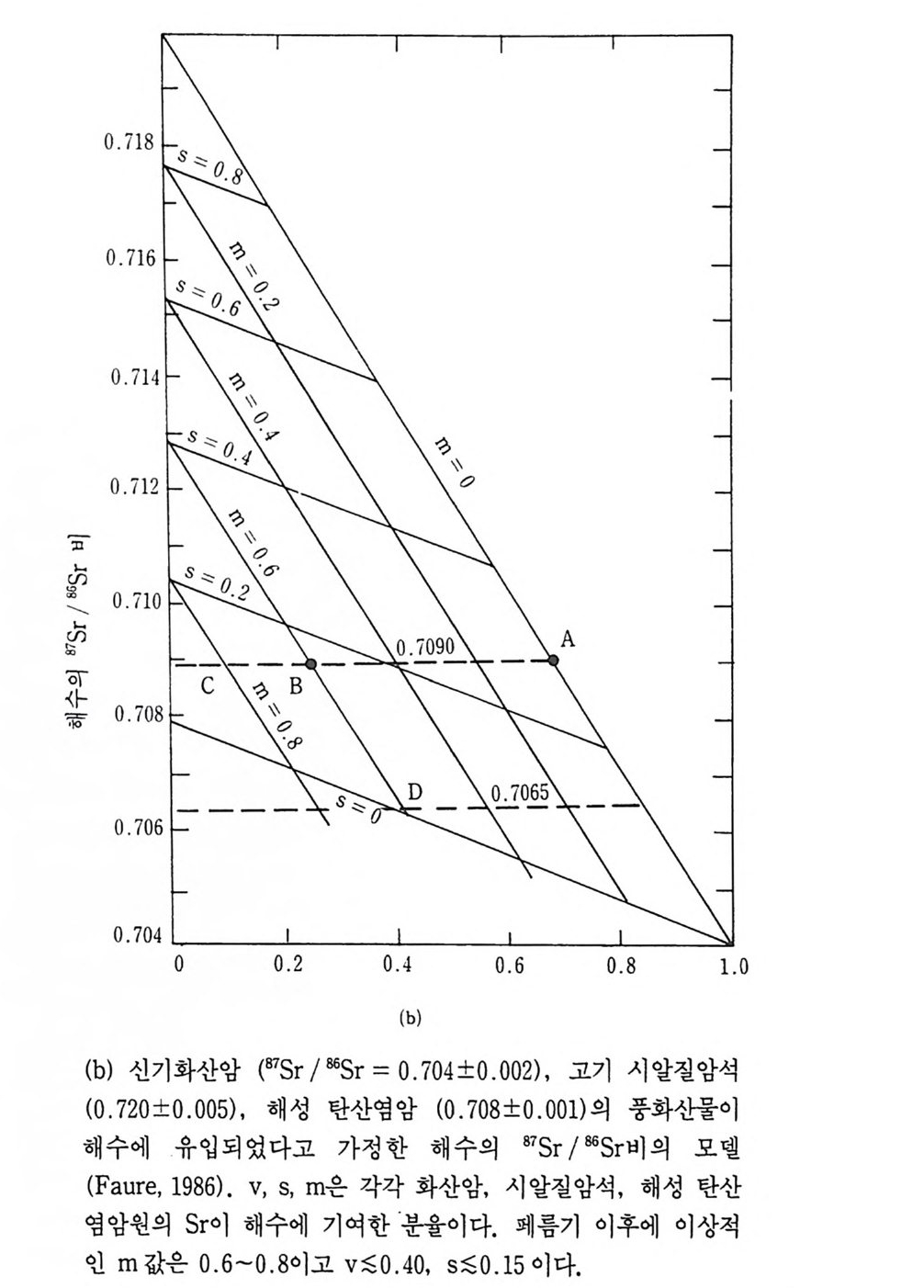 0.718
0.718
화학적 풍화에 의해 유입된 스트론튬의 동위원소비이며 v,s,m 은 각 각 화산암, 시알질암석, 탄산염암에 의해 유입된 해수의 스트론튬 동 위원소의 비율을 의미하며 이들 값은 O
동위원소비의 변동 경향도 유사하게 나타난다• 이처럼 해수에서의 동위원소 진화는 Sr, S, 0, C, Nd, Hf, Ca, Pb 등과 같은 원소의 동위원소 연구를 종합하면 퇴적암의 동위원소 변동 을 일으킨 지질학적, 지구물리학적 및 지구화학적 사건을 해석할 수 있을 것이다. 9-10 지구 대기의 진화 지구 대기의 총질량은 5 X 1021 g으로 지구질량 (6 X l027 g)에 비하면 근 소한 양이지만 인간을 포함한 지구상의 생물계에 대단히 중요하므로 지구 대기의 기원과 진화에 관한 연구는 대단히 관심도가 높다. 지구대기의 전화연구를 위해 He, Ne, Ar, K r, Xe 와 갇은 0 족 기체 (비활성기체)가스를 많이 이용한다. 지구형성시 지구에 포획된 0 족 기체가스(H e, Ne, Ar, K r, X e) 와 운석 중의 바활성 기체가스의 동위원 소비가 크게 달라 운석과 멘틀 등의 이들을 비교함으로써 지구 대기 의 기원과 대기의 형성과정을 연구하고 있다. Bowen (l 950) 은 지구의 암석 중의 S i양과 대기 중의 0 족 기체가스 양의 비 (0 족 기체가스 / S i)를 태양 중의 비와 비교한 결과 지구 대기 중의 0 족 기체가스가 태양 대기에 비해 대단히 결핍되어 있음을 조사 하였다. 이 사실에서 그는 지구 대기는 태양성분을 가지고 있던 원시 대기가스(원시태양계 성운가스)가 지표에 도달한 것이 아니고 지구 내 부에 포함되어 있던 가스가 지구 형성 후 탈가스에 의해 형성되었다 고 결론지었다. 지구대기가 이같이 탈가스에 의해 생성된 2 차 대기라고 한다면 지 구탄생시 둘러싸고 있던 1 차 대기인 태양계 성운이 없어져야 한다. 태양계 성운은 태양계 진화과정의 초기에 일어났다고 생각하는 태 양활동이 격렬하였던 시기 (TTaur i단계라고도 함)에 강한 태양풍에 의해 없어졌다고도 한다.
태양풍의 0 족 기체가스(태양형)와 운석의 0 족 기체가스(운석형)을 비교해 보면, 태양형은 헬륨이 3HeI 4He = 4 x 10 -4 이고 운석형은 헬 륨이 3He/ 4 He = 1.4 x 10-4 으로 현저히 다르다. 지구 내부에는 우라늄, 토륨과 같은 방사성 광물의 붕괴로 4He 생 성이 연속되어 지구 형성시 지구 내부에 포획되어 있던 헬륨에 첨가 되어 3HeI4He 비가 낮아지게 된다. 대륙지각은 우라늄 광물이 많이 함유되 어 있으므로 3He I 4He 비 가 낮다. 하와이섬의 열점 지역에는 He/ U , Th 의 농도비가 상대적으로 낮 기 때문에 높은 3HeI4He 비를 나타내고 있다.
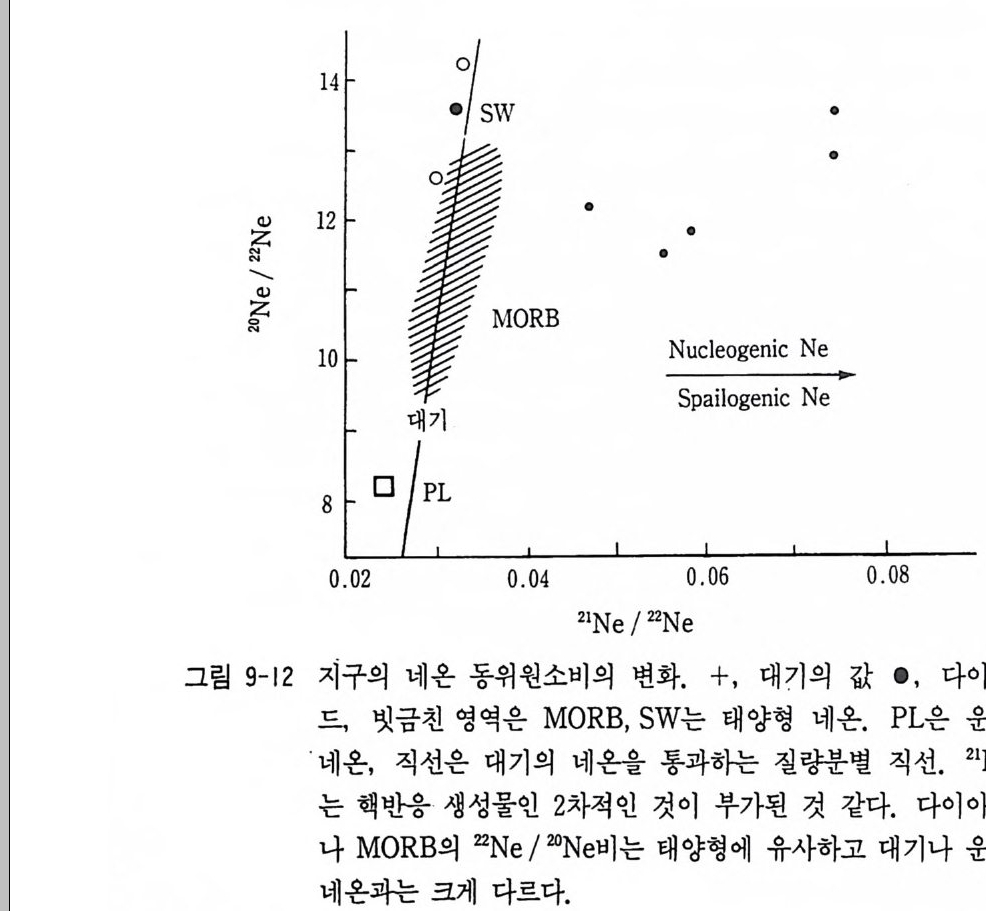 14 :'•
14 :'•
네 온의 동위 원소비 (20Ne / 22N e-21Ne / 22Ne) 를 도시 한 그립 에 서 대 기 중의 네온의 동위원소비는 태양형과 운석형의 중간에 도시된다(그림 9-1 2 ). 태양형은 20Ne I 22Ne 의 비가 13 . 6 이며 행성형은 8.2, 대기는 9.8 Ol 다. 맨틀과 대기의 네온 동위원소비가 크게 다른 사실이 알려졌다. 그 림에서처럼 다이아몬드나 중양해령의 20Ne I 22Ne 비에서 추정한 맨틀 네온 동위원소바는 태양형 네온의 비와 대단히 유사하다. 이는 맨틀 내에서 우라늄, 토륨의 붕괴에 의한 부산물인 21Ne 이 첨가되었기 때 문으로 생각된다(Ig arash i와 Oshim a , 1987). 한편 은하계 의 원소합성 반응에 의 한 아르곤은 40Ar I 36Ar~ 10-4 이 고 대기의 아르곤은 40Ar/ 36 Ar = 295 . 5 이며 맨틀의 아르곤은 300-25 , 000 의 범 위 로 변화가 크다. 이 같은 4o Ar I 36Ar 비의 차이에 근거하여 대기의 탈가스 모델 계산 을 해본 결과 대기의 대부분이 지구형성 후 수억 년 이내에 형성되었 음을 알게 되었다. 이처럼 지구의 0 족 기체가스의 동위원소비는 운석형 0 족 기체가스 와 크게 다르다. 원시태양계 성운가스는 동위원소적으로 불균질하였기 때문에 그립 9-13 에서 처럼 지구가 형성된 영역의 원시태양계 성운은 태양 그 자 체와 동일한 동위원소 성분을 가지는 가스로 되어 있었으며 지구는 이 성운가스를 지구 내부로 포획하여 성장한 것으로 보고 있다. 한편 휘발성 물질이 많은 운석은 태양에서 멀리 떨어전 장소에서 형성된 것으로 보인다. 왜냐하면 그 지역의 성운가스는 태양에서 멀리 떨어 져 있어 혼합에 의한 균질화가 불충분하기 때문에 동위원소적으로 불 균질한 상태로 남아 있게 되어 운석에는 산소, 마그네슘, 0 족 기체가 스 등의 동위원소가 불균질하게 나타나기 때문이다. 따라서 원시태양계는 동위원소적으로 불균질한 상태였다고 주장되
 I|I1-
I|I1-
고 있다. 지구 내부에서 탈가스에 의해 형성된 2 차 대기로 되어 있는 초기 지구의 대기는 주로 H, CH4, NH3, H20 등으로 되어 있는 환원형 대기였다. 이 같은 사실은 목성, 토성과 같은 거대 행성 연구에서 행 성의 크기가 클수록 초기 대기를 보존하기 쉽다는 사실에서 알 수 있 다. 그런데 목성과 토성의 대기연구에서 H, He, CH4, NH3, H20 등 존재량이 높게 나타나 이 사실을 잘 입증해 주고 있다. 초기의 환원 형 대기상태에서는 태양의 자의선이 지표까지 도달하였다. 이때 태양 자의선에 의한 수증기의 광분해에 의해 수소와 산소가 형성되었다. 수소분자는 우주공간으로 사라지고 산소는 다른 가스와 화합산화물을 만들기 시작하여 지구 대기는 점차 산화형 대기로 변하기 시작하였 다.
이 과정은 오래 지속되지 못하고 대기 상충의 02 는 자의선에 의해 02--+ o+o, 0 2+ 0-+03 의 과정으로 오존을 형성, 대기 중에 집적되 기 시작하였다. 이 오존층에 의해 자의선이 대기의 하층에 도달하지 못하게 되어 이때부터는 02 가 H20 의 광분해에 의해 형성되지 못하므로 아의 양 이
마그마의 생성에서 화성암에 이르기까지 부분용융, 분별정출 등의 복잡한 과정이 일어난다. 이런 과정 중에서 지화학적으로 다양한 변 화가 일어나기 때문에 화성암 중의 임의의 원소의 농도 또는 원소의 농도비를 측정하는 것만으로는 마그마의 생성 장소의 성질을 추정하 기에 불충분하다. 그런데 Nd, Sr 등과 같이 원자량이 큰 원소의 동위원소비는 기존 물질의 혼입이 없으면 화성암과 마그마가 형성된 장소에서 그 값이 일치하는 경향이 있으므로 이들 동위원소비에서 마그마의 직접적인 정보를 얻을수 있다. 더욱이 동위원소비와 함께 시간의 정보를 동시에 얻을 수 있는 장 점이 있기 때문에 과거 어느 특정한 시기의 맨틀의 성질을 해석할 수 있다. Sm - Nd 법의 또 다른 장점은 방사성 붕괴의 모원소와 딸원소가 모 두 희토류 원소라는 점이다. Rb-Sr, K -Ar 법은 모원소와 딸원소의 성질이 다르기 때문에 변성작용 등 지질학적 사건의 영향을 받음으로 오래된 암석의 연대측정에는 문제가 있다. 그러나 Sm-Nd 은 모원소와 딸원소 성질이 유사하기 때문에 변성작 용을 받아도 비교적 영향이 적은 장점이 있다 . 그러므로 Sm-Nd 모 델연령은 지각의 잔류연령 측정에 효과적이다. Sm-Nd 이 속하고 있는 희토류 원소는 서로 성질이 유사하지만 탄 타니드 수축효과로 이온반경이 원자번호와 함께 규칙적으로 변화하고 마그마내에서 이들은 고상-액상간의 분배계수가 다르다. 이 때문에 희토류 원소의 지구화학적 연구가 지구물질의 지구화학적 과정 해석 에 대단히 유용하다. 단점은 성질이 유사하기 때문에 모원소와 딸원소의 동위원소 분별 이 적고 또 l“Sm 의 반감기가 106Xl09 년으로 길고 동위원소비의 변 화가 적기 때문에 정도 높은 동위원소 측정이 필요하다는 점이다. 그 리고 탄산염광물과 알카리 화성암울 제의한 모든 암석에 함량이 10
ppm 이하로 대단히 낮다. 2) 니오디미움 동위원소 진화 니 오디 미 움 동위 원소비 (14 3Nd/ t4 4Nd) 와 초생 치 (14 3Nd / 144Nd) 는 지 구 초기에서 현재까지 지질시대가 젊어짐에 따라 점점 증가하고 있다. 지구형성 초기의 143Nd / 144Nd 초생치는 0.5084 에서 현재 0.5128 까 지 증가하였으며 부분용융 과정에서 마그마와 잔류고체 물질 중의 니
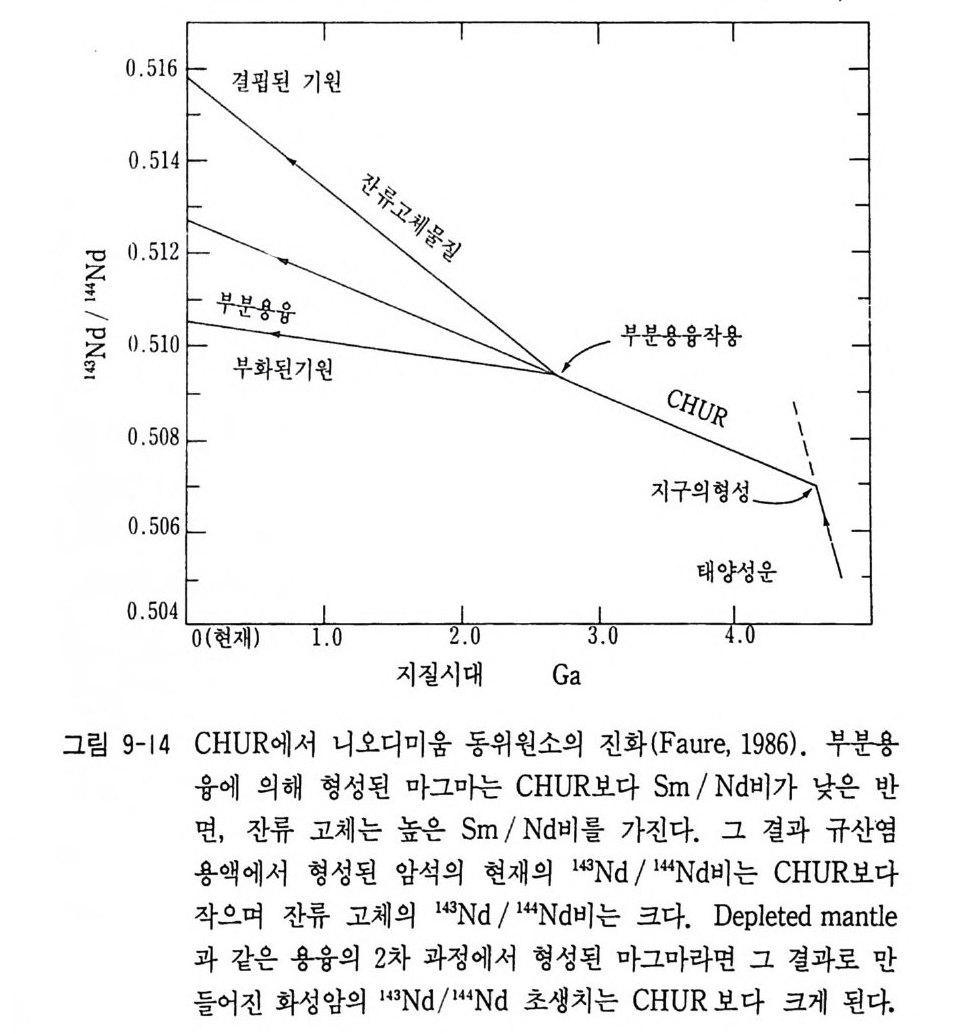 0.516
0.516
오디미움 동위원소비의 분배가 다르게 일어난다(그림 9-1 4 ). 이처럼 지구 전체의 니오디미움 동위원소바가 어떻게 진화하고 있는가를 아 는 것이 중요하다. U-Pb 계의 206Pb 는 238U 붕괴에 의해 생성되고 206p b I 204 Pb 의 전화 속도는 238U / 204Pb 에 비 례 한다. 초기 태 양계 의 성운 (Solar nebura) 중에서 는 U / Pb 의 비 가 작다. 성운이 응축할 때 우라늄은 연보다 응축온도가 높고 연은 지구가 성 운에서 집적될 때 증발에 의해 쉽게 없어지기 때문에 지구 전체의 U/Pb 비는 성운의 값보다 크게 된다. 지구의 핵이 형성될 때 연은 우라늄에 비해 핵으로 이동하기 쉽기 때문에 핵 이의의 규산염 부분의 U / Pb 비는 점차 증가한다. 맨틀의 부분융해에서 지각물질이 분화될 때에는 우라늄은 연보다 액상에 이동하기 쉽기 때문에 지각물질의 206p b I 2o ◄ p b 바의 진화는 맨틀에 비해 빠르게 일어난다. U/Pb 비는 응축과 집적시에나 핵형성시에 크게 변화하기 때문에 지구 전체의 연의 동위원소비의 진화는 측정이 어렵다. 이것이 연의 동위원소에 의한 지구진화 설명의 단점이다. Rb-Sr 계도 U-Pb 계에서와 유사한 단점이 있다. 그러나 니오디미 움은 이런 U-Pb, Rb-Sr 계의 단점울 보완하는 장점이 있다. 그림 9-14 는 Nd 동위원소 전화곡선이다. 여기서 횡축은 연대이고 종축은 1 ◄ 3Nd / 1 ◄ 4Nd 의 값이 다. U-Pb, Rb-Sr 계에서와는 달리 Sm-Nd 계는 모원소와 딸원소가 모 두 성운에서 동시에 응축되고 두 원소 모두가 천석원소이기 때문에 핵에 거의 포함되지 않는다. 이 때문에 그립 9-14 에서처럼 Sm / Nd 비는 성운에서 응축될 때나 핵 형성시 변화하지 않으므로 분석에서 추정한 성운의 Sm/Nd 비를 지구 전체의 값과 동일한 것으로 생각할 수 있다. J acobsen 과 Wasserbur g(1 980) 은 지구 전체로서의 니오디미움 동위
1원43소N비d I의 1 44N진d 화비 를를 많추이정 하측기정 하위여해 평 콘균드값라으이로트 1 43N운d석 / 의14 4NSdm = / 0 N . 5d1 1비84와7, 147 Sm / 144Nd = 0.1967 를 보고하였다. 앞에서 사마리움-니오디마움 연령측정법에서 설명하였듯이 지구전체의 니오디마움 동위원소비의 진화는 이 두 변수를 가진 가상의 물체 (CHUR) 의 전화와 동일하게 가정하면 과거 임의의 특정시기의 지구 전체의 니오디미움 동위원소 바를 구할 수가 있다. 따라서 암석의 니오디미움비물 검토하기 위한 표시법으로 입실론 함수 (C N d) 를 사용하고 있다. 희토류 원소 분배에서처럼 멘틀의 부분융해로 인해 고상-액상간에 원소분배가 일어날 때 액상에 분배되기 쉬운 원소를 不適合元素 (inc omp at ib le elemen t)라 부른다. 예를 들면 분배계수 D~l 인 것으로 K, Rb, Sr, Ba Zr, Th, LREE 등과 같은 천석원소나 LIL 원소가 여기 에 속한다 . 콘드라이트와 같은 분화되지 않은 맨틀이 부분융해되어 지각물질이 형성 분리되면 남아 있는 맨틀에는 희토류 원소의 농도가 감소한다. 이 같은 맨틀을 희토류 원소가 결핍된 맨틀 (de p le t ed man tl e) 이라 한 다. Nd 와 Sm 을 비교하면 Nd 는 더 쉽게 액상으로 이동하기 때문에 dep le te d man tl e 의 Sm / Nd 비 가 증가해 콘드라이트값보다 크게 된 다. 이 때문에 그림 9-14 에서의 CHUR 으로 표시된 것처럼 143Nd/ 144Nd 동위원소비의 진화속도는 CHUR 속도보다 크게 된다. 따라서 Nd 이 Sm / Nd 비가 CHUR 보다 큰 depl e te d 기원에서 온 것은 (CNd(T)) 로 표현하였을 때 정의값을 나타낸다. 이에 반해 지각물질의 Sm/Nd 비는 콘드라이트값보다 작으므로 CNd(T) 값은 부의 값을 나타낸다. 죽 맨틀에서 부분용융에 의해 형성 된 마그마는 CHUR 보다 Sm/Nd 비가 낮은 반면 잔류고체물질은
Sm / Nd 비 가 높다 (그림 9-14) . 니오디미움으로 처음 지구 전체의 동위원소비의 진화곡선이 확립되 었으므로 니오디미움은 지각과 맨틀이 상보적인 리저버 ( Re s enro i r) 임 이 확실해졌다. 시료의 C N d ( T)의 절대치의 크기, 즉 143Nd / 144 N d 비의 CHUR 에서 의 전이는 시료의 Sm / Nd 비와 CHUR 의 Sm / Nd 비의 차와 시료 가 CHUR 에서 분화된 후부터의 시점에서 결정된다 (Naka i , 198 7 ). 3) 멘틀물질의 불균질성 과 지 각과 맨틀의 진화 희토류 원소 중 사마리움과 니오디미움은 광물과 멜트에서 분배계 수가 다르기 때문에 지각과 맨틀에 상이한 분배 를 나타낸다. 즉 지각 에는 니오디미움이 맨틀에는 사마리움이 더 많이 분배되어 있다. 따 라서 사마리움의 방사성 붕괴 동안에 H3Nd / 1 Nd 의 바는 지 각 과 맨 틀내에서 변화된다. 맨틀내의 원래의 사마리움과 니오디미움은 콘드라이트 운석에서와 동일한 비로 존재하였다고 생각하고 있다. 앞에서 설명한 것과 감이 맨틀기원의 암석의 t43 N d / 1 44 Nd 과 동일 시기의 콘드라이트에서의 이 비 사이의 편차를 C N d 로 표시하고 이 값을 원시상태에서 니오디미움 동위원소가 진화한 정도의 척도로 사 용하고 있다. 만약 맨틀물질이 무 분 g 융되어 만들어진 현무암이라면 니오디미움 동위원소의 초생치는 용융시의 맨틀기원의 그 값과 같아야 할 것이 다. 해양성, 베니오프대, 대륙 등과 같이 상이한 지구조 환경에서 형 성된 젊은 현무암의 C N d 값은 그림 8-16 에서와 같이 그 지역의 암석 성인에 따라다르다. 죽 u3Nd/144Nd 비가 대륙지각의 값울 보충하는 높은 값을 가진다. 여기서 맨틀기원 지역의 해양현무암이 분화되고 나서 잃어진 물질 이 대륙을 형성한 것으로 추정하고 있다.
대륙지각 현무암과 소수의 해양성의 현무암의 C Nd 값은 0 에 가깝 다. 이는 맨틀기원 지역이 콘드라이트처럼 진화되었으나 미분화된 것 을 의미한다. 그러면 이들 자료가 의미하는 맨틀의 성질은 어떠하였 울까? Wasserbur g와 DePaolo (19 79) 는 이 감은 차이 를 총상 멘틀내 에 서 의 용융과정에 기인한 것으로 추정하였다.
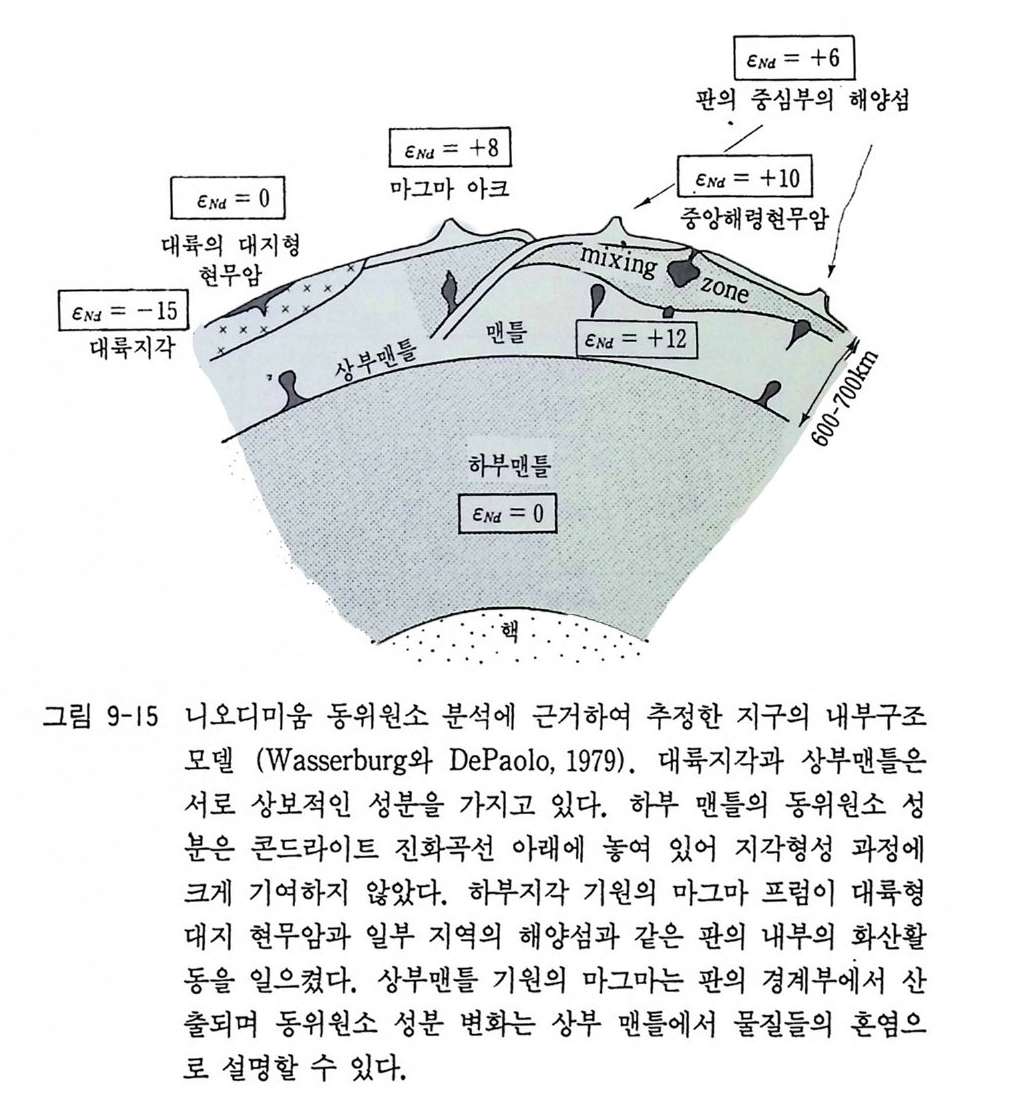 二J섭
二J섭
맨틀은 Sm 과 Nd 과 기타 부적합원소가 미분화된 하부맨틀과 정의 값을 가지는 고도로 분별작용을 받은 상부맨틀로 대분하였다. 하부멘틀은 형성 이래 원시상태로 그대로 유지된 곳이며 상부맨틀 은 베니오프대의 마그마질 아크에서 만들어진 대륙지각의 형성과 해 양지각의 섭입 (Subduc t)에 의해 계속적으로 물질이 순환되는 곳이다. 그리고 CN d 중간값을 가지는 그 의의 지구조 지역에서 산 출 되는 해양현무암은 두 맨틀 중의 물질의 혼합으로 볼 수 있다(그림 9-1 5 ) . 상부맨틀의 +12c N d 값은 대륙지각의 一 15c Nd 값과 균형을 이 룬 다. 대륙지각의 화강암질암의 l43Nd / 144Nd 과 87S r / 86S r 동위원소비는 해 령현무암에 비하여 대단히 변화가 심하다(그림 9-16). 그림 9 - 16 에서 보면 고생대 이후의 암석들은 143Nd / 144Nd > 0 . 511 8 이고 선캠브리아
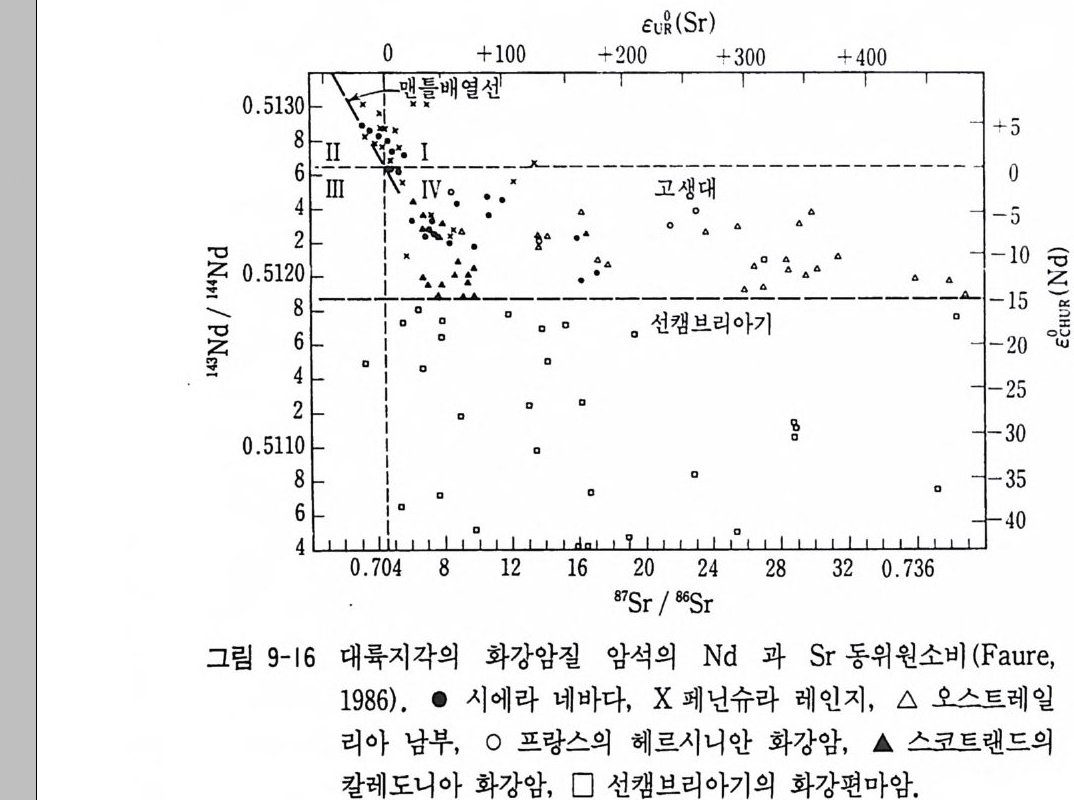 ~ : ::86 · -:IIII -I :- R난〔f0 · - j-IIV -;o- -\+-1_ -0翼0 - '--;--; +-2\-0 0-這 \-고- 생(\S-대r-)리 ----3〉0-0 }--\- -二-+ 4- _0- 0 _ -- 三--〕-1寸 :+:05 o'
~ : ::86 · -:IIII -I :- R난〔f0 · - j-IIV -;o- -\+-1_ -0翼0 - '--;--; +-2\-0 0-這 \-고- 생(\S-대r-)리 ----3〉0-0 }--\- -二-+ 4- _0- 0 _ -- 三--〕-1寸 :+:05 o'
기의 암석은 이보다 낮은 값을 가지며 분산되어 도시되고 있다. 87Sr / 86Sr 비 변화가 143Nd / 144Nd 보다 더 심 하게 변화하고 있다. 왜냐하면 화강암질 암석에 Sm / Nd 비보다 Rb/ S r 함량이 높고 변화 가 심하며 87Rb 의 붕괴속도가 14 1 sm 보다 빠르기 때문이다. 오스트레 일리아 동남부의 코스서우스코 (Kos ci usko) 저반의 화강암 류의 니오디미움과 스트론튬 동위원소 분석결과를 없펩 UR 一 c 益 도 표에 도시한 결과 I- 형 화강암류와 S- 형 화강암류가 모두 depl e te d 맨틀기원과 대륙지각기원 마그마의 동일한 혼합선상에 도시되었다(그 립 9-1 7 ). I- 형 화강암류는 20~80% 의 지각성분을 함유하고 있다. 그러나 실제로 이 암체에 대하여 화학성분 분석에 의한 혼합연구에서
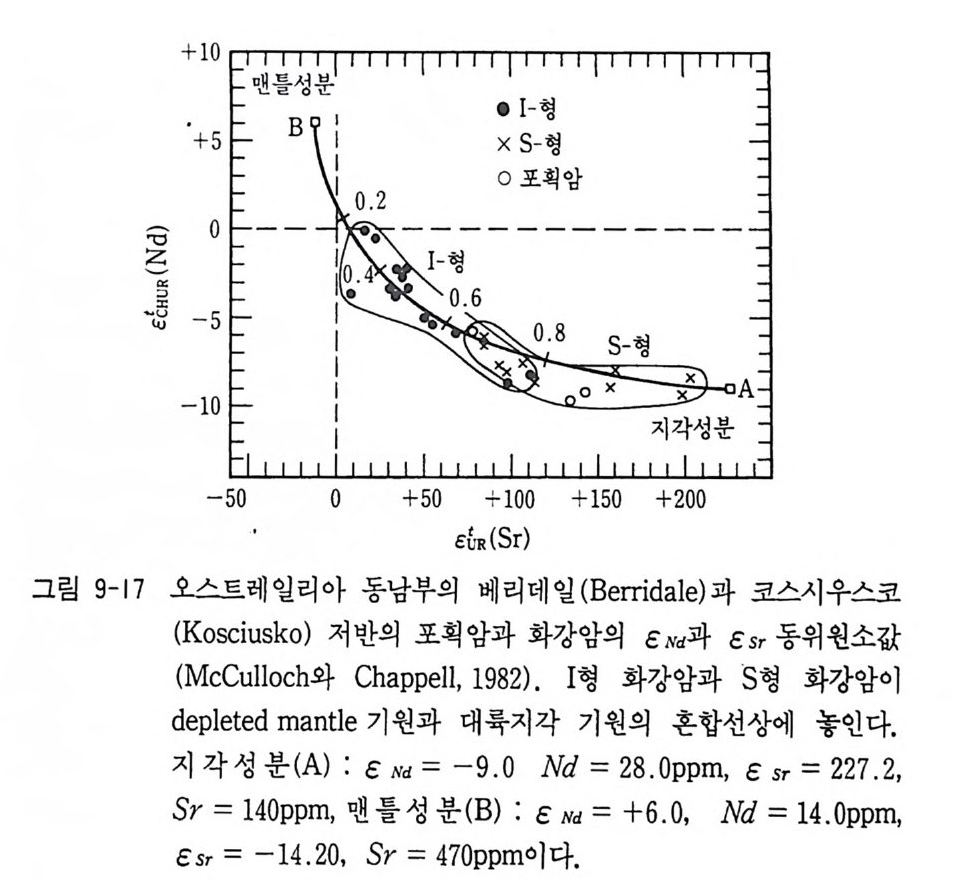 +1 0
+1 0
는 기원이 둘 이상인 화학적으로 불균질한 기원에서 유래하였음을 주 장하였다 (McCulloch 와 Chapp e l, 1982). 이와 유사하게 대륙지각의 질량을 알면 분화된 상부맨틀의 비율을 질량평형 계산에 의해 구할 수 있다. 대륙지각의 질량이 2 X 102 5 g이 며 니오디미움 함량이 상부 맨틀의 50 배이고 상부 맨틀의 질량은 100 X1 025 g이 된다. 이는 두께 600~700km 에 상당한다 . 이 심도는 지진파에 의해 알려 진 불연속면의 위치와도 잘 일치한다. 이런 사실에서 맨틀의 지진파 불연속면이 상전이 보다는 화학적 차이에 기인하는 것 으로 추정될 수 있다. 이 같은 견해가 옳다면 기타 동위원소 자료도 Sm-Nd 자료와 시교 될 수 있을 것이다. cS r 과 CPb 도 체계적으로 변화하여 Nd-Sr-Pb 맨틀 배열개념으로 발전시켜 생각해 볼 수도 있을 것 이다. 맨틀 분화연구에 의하면 미분화된 콘드라이트질 맨틀에서 대륙지각 으로 분화하므로 맨틀에서 부적합원소가 서서히 제거되어 현재의 중 앙해 령 현무암울 만들고 dep le te d man t le 로 진화했 다는 것 이 다. 홍미 있는 것은 지구의 맨틀의 50% 이상은 현재에도 미분화상태로 남아 있다는 결론이다. 또 대륙지각의 대부분은 25 억 년 이전에 형성되어 그 후 면적은 그다지 증가하지 않았다는 결론이다. 초기에 측정된 시생대 암석의 니오디미움 동위원소비 자료는 CHUR 곡선에 가까운 것이 많고 25 억 년 전경부터 여기서 이탈되는 것 이 나타나기 시작한다. Sr, Pb, Hf 동위원소비 연구에서도 시생대의 맨틀이 비교적 분화가 진전되어 있었음이 알려졌다. 예를 들면 Pachett 등은 Hf 동위원소 연구에서 28 억 년 전에 맨틀에는 이미 상당히 동위원소가 불균질하게 존재하여 현재 이 불균질한 동위원소비가 측정되고 있다. 시생대의 니오디미움 측정시료가 증가함에 따라 불균질성이 나타나 28 억 년 전 에 cNd(T ) = 3 의 맨틀이 존재하였음이 밝혀졌다. 이 결과는 시생대
초기에 현재의 중앙해령 현무암을 만들었던 dep le te d man t le 의 분화 가 시작되었음을 의미한다.측정된 암석시료의 c Nd( T) 값이 변화폭이 커 시생대의 맨틀도 불균질하였다는 것이다. Nelson 등 (1984) 은 약 17 억 년 전의 록키산맥의 녹색암의 동위원 소바 측정에서 c Nd(T ) = 6.5 를 얻었다. 이 시료는 도호를 만든 dep le te d man t le 에서 만들어진 것으로 생각되나 약 20 억 년간에 e Nd( T) 의 진화속도가 감소하였을 가능성을 시사하였다. CNd 의 전화속 도 를 저하시키는 기구로 대륙지각 물질 (C N d
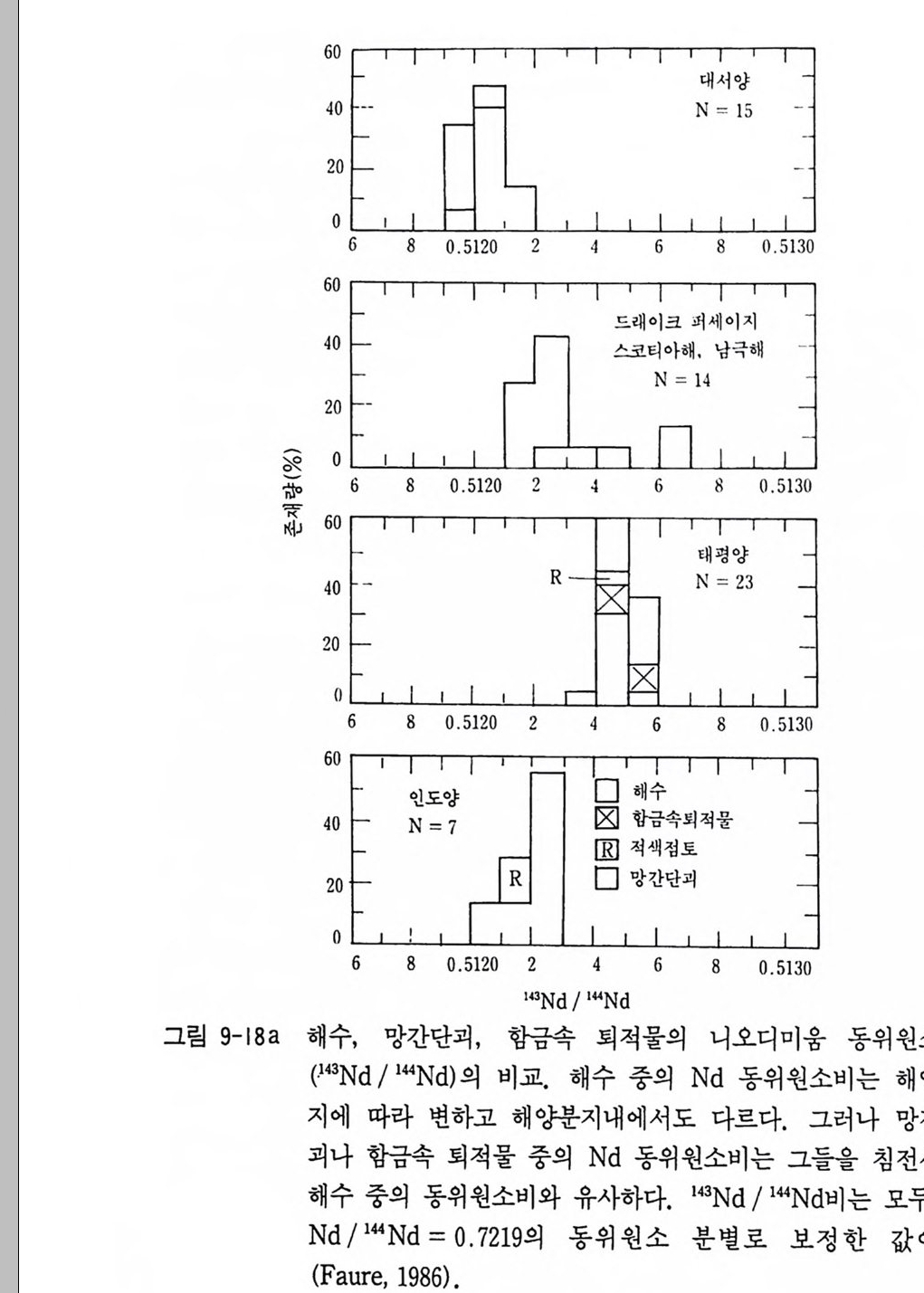 60
60
즉 대서양 주위에는 맨틀 저장고에서 분리된 후 화성활동 동안에 Nd 이 부화되 어 낮은 143Nd ; 144N d 비 를 가지 는 시 알질 성 분의 오래 된 암석이 분포하고 있는 반면에 태평양지역은 주위의 해양지각이 섭 입되는 과정에서 일어난 화산활동으로 143Nd; 144Nd 비가 높은 암석 울 만들게 되었다. 해양에서 Sm 과 Nd 의 정체시간이 약 300 년으로 짧기 때문에 혼합시간이 1,000 년 이상 걸리는 해양수는 혼합에 의하 여서는 Nd 동위원소비가 균일하게 되지 못하게 된다. 상이한 해수의 143N d ; 14 4 Nd 비의 차이를 이용하여 해수의 순환, 해수의 혼합을 해석 할 수 있다. 즉 니오디미움 동위원소비 분석으로 상이한 해수의 혼입 (mi xi n g ) 비율을 계산할 수도 있다. 예를 들면 남미의 남단에 있는 드라크 페 세 이 지 (Dr ake Passage ) 의 해수의 니오디 미움 동위 원소비는 태평양과 대서양 값의 중간값을 가지고 있었다 (P i e p ras 와 Wasserbur- g, 198 2). 그리고 이 지역 해수는 대서양에서 유래된 70% 의 남극해류 (Anta r cti c C ir cu mp ol ar Curren t)로 되어 있었음이 조사되었다. 심해저의 망간 노듈이나 해령 · 부근의 함금속 퇴적물과 M g-방해 석, 인회석 등의 니오디미움 동위원소비도 되적지역의 해수의 그 동 위원소비의 영향을 직접 받고 있다. 코노돈트 화석과 인회석과 방해석의 Nd 동위원소비 분석으로 해수 의 Nd 성분과 지질시대 사이의 관계 연구에서 해수의 Nd 동위원소 비는 선캠브리아기말에서 현재에 이르기까지 변화가 있었으나 변화폭 은 현재의 해수값의 범위내에 있었다 (Shaw 와 Wasserburg, 1984). 특 히 짧은 Nd 의 정체시간으로 인한 Nd 동위원소의 불균질 때문에 각 해양의 니오디미움 동위원소비가 각기 다르게 나타났다. 지질시대의 해양의 Nd 동위원소비의 다양성과 대륙의 이동과의 관 계도 검토될 수 있다. 중생대의 판게아 대륙에서 대륙이 분리된 이후 에 대서양과 태평양온 각기 분리되어 전화되었음이 니오디미움 동위 원소 연구에서 알려지게 되었다. 화산암의 Nd-Sr 동위 원소 분석에서 화산암과 해수와 반응으로 이
둘 동위원소값이 변화하고 있음이 연구되었다(J acobsen 과 Wasser- burg; 1979, McCulloch 등, 1980). 예를 들면 해양의 변질 현무암과 오피오라이트의 Nd 과 Sr 동위원소 분석결과에서 스트론튬 동위원소 비 (8 i Sr/86Sr) 가 증가하는 쪽으로 맨틀 배열선에서 떨어져 도시됨이 확인되었다. 이는 해수와 현무암 사이에 상호반웅으로 인하여 변질된 암석이기 때문이다. 해수와 암석간의 상호반응에 의한 동위원소 교환은 해수 / 암석의 비, 해수와 암석 중에 이들 동위원소의 농도에 영향을 받는다. 원소 X 의 동위원소비를 E , 동위원소 교환에 관계한 암석과 해수 의 양을 각각 R 과 W 라고 하면 다음과 같은 관계가 얻어진다. E {(XrR+XwW) = E ~XrR+ E ~X w w 여기서 Xr 과 Xw 는 각각 암석 (r) 과 해수 (w) 중의 X 원소의 농도이 다. i와 f는 반응 전(최초)과 반웅 후(최후)를 나타낸 것이다. 이것을 해수/ 암석비에 대해 표현하면 법=(~)(f) 가 되며、동위원소 교환 반응 후의 E 으로 표현하면 E{=Xr+X~w(WRI R) ) 가 얻어전다. 이 관계식을 이용하여 오피오라이트질 암석과 현무암이 해수에 의 해 변질된 증거를 그림 9-18b 에 도시 하였다.
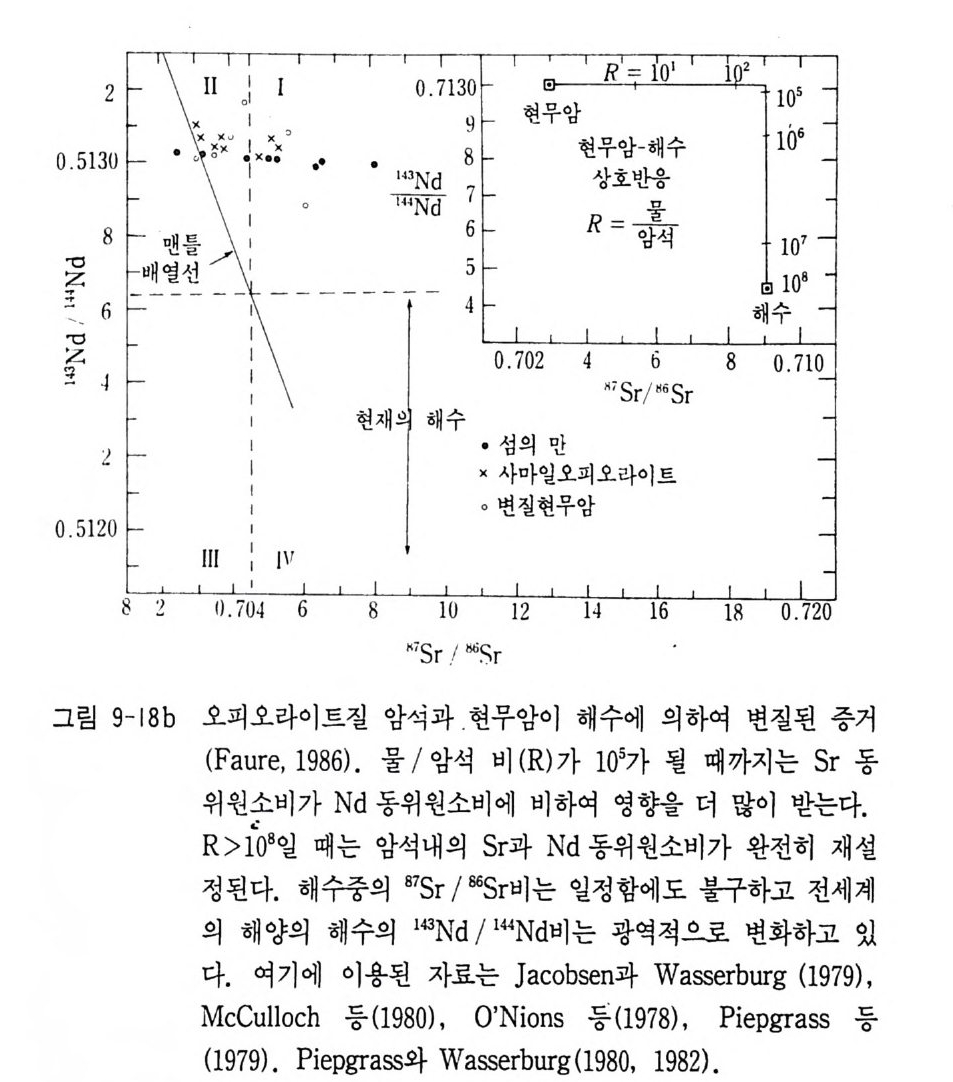 0.mC5NNppl-H 1 3 J802 —6u-열맨· ?선샤툴XV I- 0l ,/X_ 니x \ol1 l I-_·_II_IIl ·x ·-xI ’ - .. · I 국。d 71 d3 -0 3 094.7 0현8 2 무7암현6 4R상 무R= 호암'S =반훑-r /해6응i 0 1수 S r 18n2 싫011l000. °765 78 1 0
0.mC5NNppl-H 1 3 J802 —6u-열맨· ?선샤툴XV I- 0l ,/X_ 니x \ol1 l I-_·_II_IIl ·x ·-xI ’ - .. · I 국。d 71 d3 -0 3 094.7 0현8 2 무7암현6 4R상 무R= 호암'S =반훑-r /해6응i 0 1수 S r 18n2 싫011l000. °765 78 1 0
해양현무암과 해수의 값을 다음과 같이 가정하였을 때 위의 식을 이용하면 〈해양현무암〉 〈해수〉 143 I43 (鳩) = 0.51300 (색 )w = 0 . 51245
Ndr = 8.0p pm Ndw = 2 . 6 x 10-6p pm 87 87 틀 )T = 0.7 0 300 (출 )w = 0.70906 Srr = 120p pm Srw = 8.0p pm 그림 9-18b 에서와 같은 쌍곡선이 얻어져 W / R 비와의 관계가 얻 어진다. W / R 비가 10-104 으로 증가할 때 암석의 “S r / 86S r 비는 0.70300-0.70905 까지 변화하지만 143Nd / 144Nd 비는 거의 변화하지 않는다. 이는 해수 중에서 Sr 농도 (8 pp m) 에 비해 Nd 농도 ( 2.6X10-6 pp m) 가 대단히 낮기 때문이다. W/R 비가 105 이하일 때는 해양에서의 화산 암의 143Nd / t4 4Nd 바는 해수에 의해 크게 영향을 받는다. 그러나 W / R 비 가 105 이 상이 되 면 143Nd / l44Nd 도 변화하기 시 작한다. 이 런 조건에서는 암석 중의 스트론튬은 해수의 87Sr/86Sr 으로 완전히 재설 정된다 . W/R 비가 108 이 되면 마침내 암석 중의 143Nd/144Nd 비는 해수의 값에 이르게 된다. 5) 대륙 현무암의 니오디미움-스트론튬 동위원소비 많은 신기 화산암류들은 맨틀 배 열 (Mantl e array) 을 따라 Sr 과 Nd 동위원소비가 부의 상관성을 나타내고 있다. 이는 마그마가 상이한 Rb/ Sr, Sm/ Nd 비를 가지는 암석기원에서 형성되었음을 의미한다. 즉 143Nd / 144Nd 비는 MORB, OIB, 대륙대 지 형 현무암에 서 값이 다르다. 이 갇은 차이는 마그마 기원지의 물질의 연령이나 지화학사룰 해 석 하는 단서 가 될 수 있을 것이 다. MORB 는 UR (Chondrite reser- vo i r) 보다 Sm / Nd 비가 높고 Rb / Sr 비는 낮다. MORB 는 Rb 이나 LIL (Large ion lith o phi le) 이 상실된 지역으로 보 통 depl e te d 마그마 기원지역이다. 그러나 해양분지 밀의 맨틀에는 높은 Rb / Sr 비 와 낮은 Sm / Nd 비를 가지는
존재하고 있음이 알려졌다. 해양현무암 (OIB) 은 맨틀 배열선상에 놓이지만 MORB 에 바해 Sr 의 변화가 심하고 143Nd / 144Nd 비가 낮은 위치에 도시된다. 이는 해양 지각이나 대륙지각 물질의 혼입 때문으로 생각하고 있다. Faure (l 986) 는 다음과 같은 동위원소 부화 파라메터를 이용하여 대 륙 대지형 현무암을 구분하였다(그림 9-19). Is m = ~(l47)Sm / 홍l44Nd) H UR — l !Rb = ~(87R)b / 8입6Sr) R — l 1 상한은 fsm > O, f Rb > O 이며 II 상한은 fsm >O, f Rb
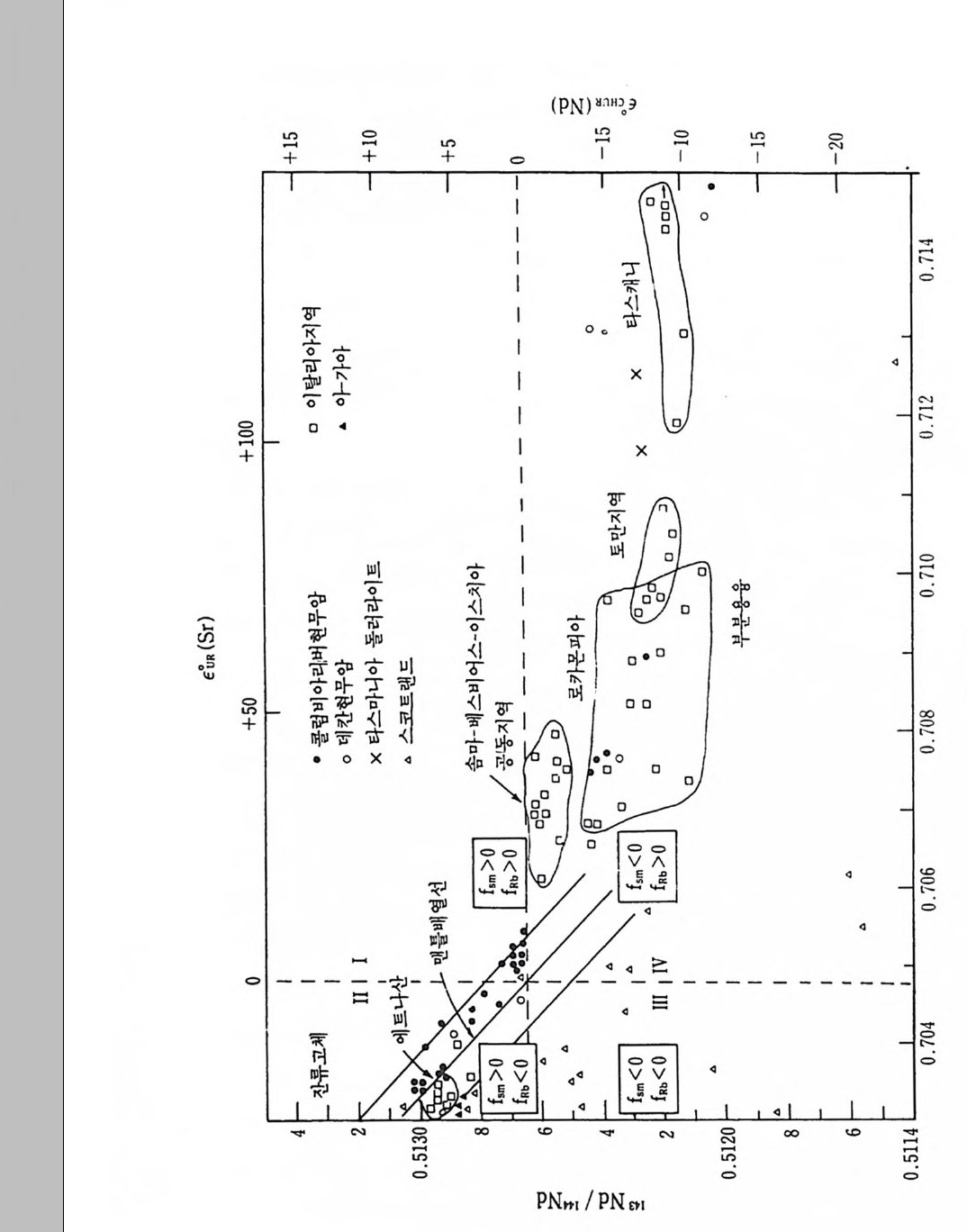 N)P!3
N)P!3
~) 마그마의 동화 마그마의 기원, 화성암의 기원, 상이한 마그마의 동화, 마그마와 모암 암석과의 동화 등의 연구에 니오디미움, 스트론튬, 연 동위원소 가 많이 이용되고 있다. 상승하는 마그마가 지각물질과 동화되어 동 위원소 성분이 변화되는 경우가 있다. 최근 니오디미움, 스트론튬 등 의 방사성 동위원소가 이 동화과정을 연구하는 데 많이 이용되고 있다. 해양 현무암들의 니오디미움과 스트론튬 동위원소비 분석에서 MORB 는 정의 E 선# U R 값을 가지며 부의 맨틀 배열을 잘 나타내고 있 다. 그리고 기타의 화산지역의 현무암들이 부의 맨틀 배열을 나타내 는 것 은 Rb / Sr 과 Sm / Nd 비가 다른 암석에서 마그마가 형성되었 기 때문으로 본다. 예를 들면 MORB 와 인도양의 케르구엘렌 (Ker gu elen) 섬 현무암질 암은 맨틀 배열선상에 위치하지만 MORB 에 비해 87Sr/86Sr 값이 높 코 143N d / 1 44 Nd 비가 낮은 값을 가진다(그림 9-20). 이 지역의 마그마 의 기원암에 해당하는 화성암은 Rb 이 많고 Sm 이 결핍되어 있었을 뿐만 아니라 Sr 과 Nd 의 동위원소 성분의 분배 차이가 현저하게 나타 날 만큼 지질시대가 오래되었음을 가리켜주고 있다. 이 갑은 동위원소비 분석에서 상이한 동위원소비를 가지는 각기 다 른 마그마원을 추정할 수 있고 이들 두 기원의 맨틀 배열선에서 마그 마의 혼합을 해석할 수도 있다. 혼합되지 않은 현무암이라면 87Sr/ 86 Sr 바가 맨틀 기원지역의 것과 동일할 것이다. 암석의 연령에 따라 다르 7 i는 하겠지만 보통 멘툴내 의 스트론튬에 바해 루바둠의 원래의 함량이 낮기 때문에 Rb/Sr 비 는 높다 . 그러므로 지각의 암석은 방사성 기원의 a1sr 을 더 많이 가 진다. 일반적으로 혼영되지 않은 현무암에 비해 혼염된 현무암이 낮은 143Nd / 144Nd 초생치를 가진다 . 지각의 연의 정확한 동위원소 성분을 예측하기는 어렵다. 그러나 만일 혼영현상이 확실한 혼염물질에서 연
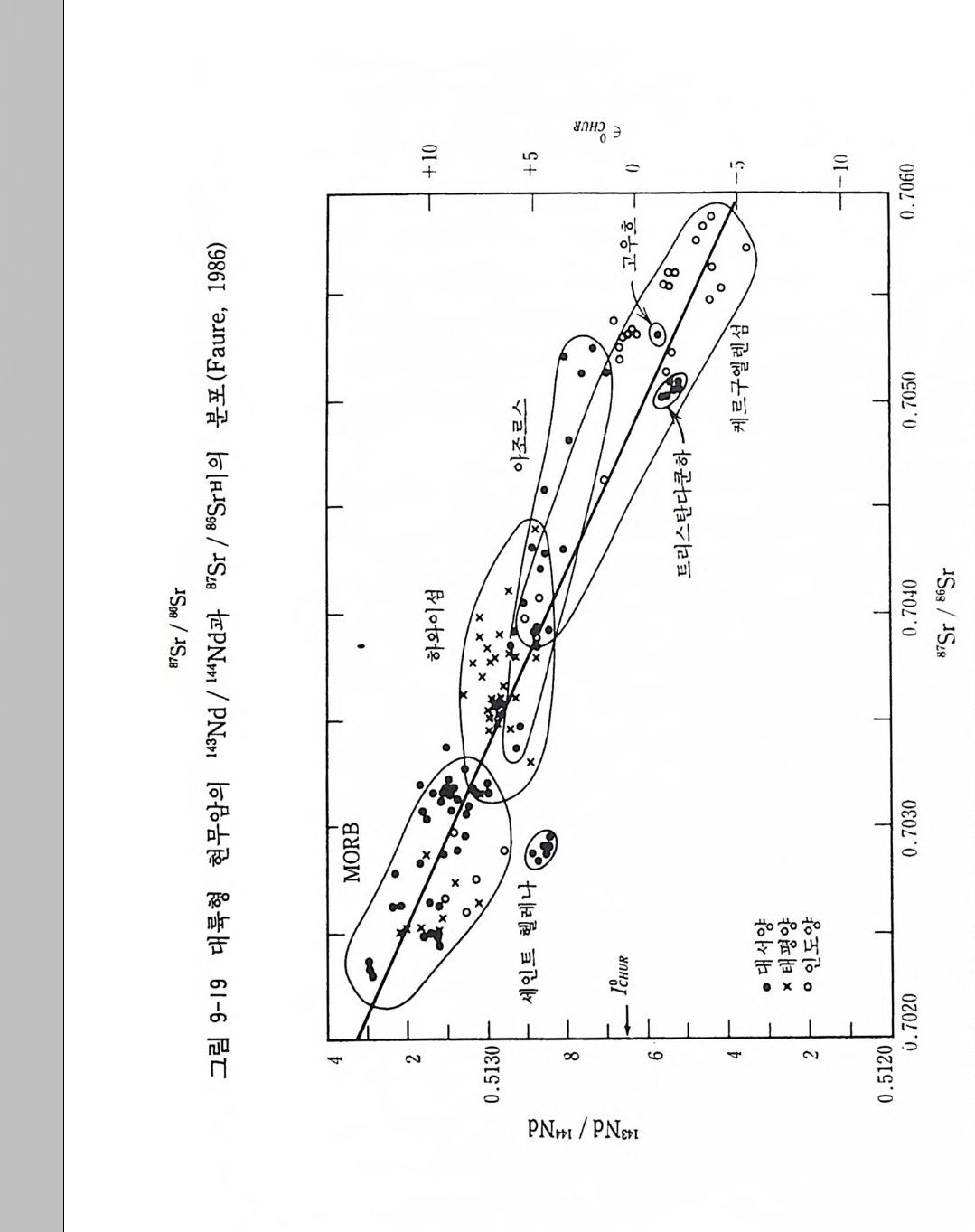
동위원소가 분석될 수 있다면 그의 혼염 영향을 추정할 수 있다. 화성암석학에서는 ® 맨틀 기원의 마그마와 상부 화강암질 지각 기 원의 마그마의 혼염 ® 맨틀 기원의 마그마와 지각 하부의 그래뉴라 이 트 (Granulite ) 원 마그마와 혼염 등을 생 각할 수 있다 (그림 9-21 ) . 이때 상이한 두 기원의 마그마의 혼염 비율을 다음과 같이 계산할 수 있다. 143 143 (14門3N 7d ) Af = (훑 )ANNddJ J ++ N(dB국(1- )f)B NdB(l- f)
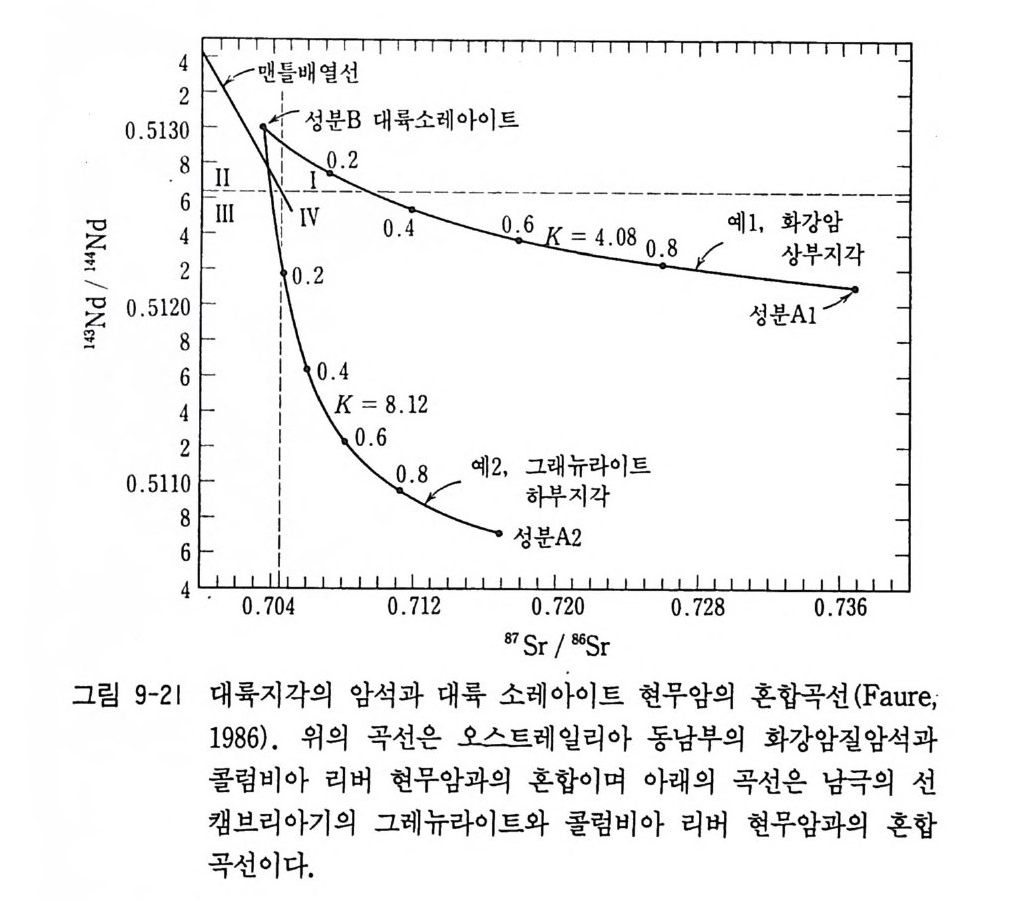 4208642
4208642
여기서 f는 혼염된 마그마에서 A 기원 마그마의 중량분률이다. 실 제로 자연계에서 동화는 복잡한 과정으로 일어난다. 동화의 해석에는 먼저 필요한 열원이 규명되어야 한다. 그러나 대부분의 마그마는 이 미 그의 액상 온도 이하에 있기 때문에 열원은 마그마 자체의 발열 결정작용으로 보아도 좋다. 따라서 동화작용이 일어날 때는 언제나 분별 정출작용이 동시에 일 어난다고 생각해도 좋다. Ta y lor (l 980) 와 DePaolo (1 981) 는 두 과정 울 경험한 마그마의 동위원소 성분변화의 모델 방정식을 유도하였다. 7) 화강암류의 성인 (1) 화강암류의 기원 화강암은 마그마가 심부에서 600~800'C 사이의 온도에 서 서서히 냉각 고결되어 만들어전 심성암류 중의 가장 전형적인 암석이다. 마그마의 기원해석은 현무암질 본원 마그마에서 현무암질 마그마, 안산암질 마그마, 유문암질 마그마로 분화되었다는 Bowen(1928) 의 분화 개념에서 시작된다. 오늘날에는 이들 마그마의 기원을 실험 암석학적 연구 결과와 판구 조론과 같은 지구조적 모델에 근거하여 ® 고온 고압의 맨틀에서 형 성되는 현무암질 마그마 ® 베니오프대 주위의 판의 섭입과 관련 부 분용융되어 형성된 안산암질 마그마 ® 화강암류의 용융실험에 근거 한 대륙 지각에서의 비교적 저온에서 부분용융된 화강암질 마그마로 구분하고 있다. 화강암질 마그마의 기원 역시 대륙지각 기원, 맨틀 기원 그리고 맨 툴 기원의 화강암질 마그마가 상승 도중 지각물질과 혼합 또는 분화 산물 또는, 화강암화작용 (Gr aniti za ti on) 등 여 러 모델이 제 안되고 있 다. 87SrI86Sr 의 초생치가 운석은 0.699~0.700 내로 대단히 균일한데 비하여 맨틀 기원의 현무암은 이 값에서 0.706 까지 변화하고 지각 기
원의 화강암류들은 0 . 735 까지 다양하게 변화하고 있다. 아에 근거하여 스트론튬의 초생치의 값의 비가 낮은 화강암은 맨틀 기원으로 초생치가 높은 화강암은 대륙지각 물질이 무 분 § 3 으로 인 한 지각 기원이거나 지각물질의 혼합 등으로 해석하여 왔다. Faure 와 Powell(1972) 은 130 여 화강암류의 스트론튬 동위원소비 분석에서 70 여 암석이 지각 기원임을 조사하였다. 미국 캘리포니아의 심성암류는 스트론튬 초생치가 맨틀의 초생치보 다 약간 높았으며 이 지역의 다양한 심성암류 중에 바교적 낮은 초생 치 를 가지는 암석의 기원을 대륙 주변부에 분포하는 화산암질 물질을 많이 함유한 퇴적암의 부분용융 산물로 해석했다(H urle y 등 ,1965). 또 다른 해석으로 그래뉴라이트 상의 변성상의 변성작용에 의한 루 비듐이 결핍된 하부 지각의 암석이나 맨틀 물질의 무 분 § §으로 87 Sr / 86 Sr 의 초생치가 낮은 값을 가지게 된 것으로 해석하였다. 또한 이들은 북미 판의 섭입으로 인해 해양저 퇴적물, 해저 현무암 상부 맨틀 물질 등이 혼합되어 이 지역의 가록 (Garlock) 단충의 북측 캘리포니아 저반의 암석이 동남쪽으로 감에 따라 “Sr/86Sr 초생치가 증가하고 산안드레스 단충의 동측 암석은 스트론튬 초생치가 0 . 7031~0.7082 로 변화하였다고 보는 견해도 있다 (K i s t ler 와 Pete r- man, 1978). 이 같은 사실에서 지질시대와 무관하게 스트론튬 초생치가 변화하 고 있으며 주로 지리적인 영향을 받고 있음을 알 수 있다. 죽 0.706 과 0.704 등치선을 나타내는 고생대 되적암 지층의 분포와 초염기성암과 광상의 분포, 고도, 중력이상 등의 영향으로 지각의 발 달사가 다르기 때문이다. 그리고 0.706 등치선을 나타내는 지역은 탄 산영암, 셰일, 사암, 화산암, 처어트 등의 분포지역이었다. 그리고 0.704 등치선은 중생대 화강암류의 동쪽 경계선을 가리키고 있으며 해양성 소레아이트와 알카리 현무암의 미량성분 농도도 이와 조화적 으로 나타났다.
선캠브리아기에서 트라이아스기의 퇴척암과 중생대 화강암류의 87Sr/86Sr 초생치와 화학성분의 대비에서 이 지역의 화강암질 마그마 는 지각의 영향을 크게 받았던 것으로 추정되고 있다. (2) 일본의 화강암류 일본의 80 개 의 심 성 암류(주로 화강암류와 반려 암류) 의 87Sr / 86Sr 초 생치는 중%나 L 조선을 경계로 일본의 동북부는 낮은 값 ( < O.706) 를 가 지고 서남 일본을 높은 값 ( > 0.706) 을 나타내고 있다(그림 9-22). 또한 이 값의 광역적인 변화경향은 부우게 중력 이상에서 추정한 지각의 두께와대비된다. 화강암류의 스트론뮴초생치는 0.7037~0.7124 까지 변하고 있으며 0.706 보다 작은 값을 갖는 화강암류는 지각물질 혼입이 적은 맨틀 기원이고 초생치가 이보다 높은 값을 가지는 화강 암류군은 심부기원 마그마에 지각물질이 혼입되었거나 대륙지각에서 형성된 마그마 기원으로 해석하였다. 그리고 화강암류의 87Sr/86Sr 초생치가 자철석계는 낮고 티탄철석 계는 높은 경향이 나타났다. 그리고 백악기-제 3 기 화강암류의 87Sr/ 86Sr 초생치와 ~4s 값은 부의 상관관계를 나타내고 있으며 낮은 스 트론듐의 초생치와 낮은 ~4s 값을 갖는 제 3 기 (Neo g ene) 의 화강암 질 마그마는 “S 가 많이 포함된 젊은 퇴적암과의 상호작용 때문으로 해석하였다. Ma t s uhi sa(1982) 의 110 개 화강암류 시료의 8180 동위원소비 분석 에서 지역별로 8180 값의 변화가 나타났다. 그리고 티탄칠석계 화강 암류는 산소동위원소비가 +8%, 이상으로 큰 값을 가져 자철석계 화 강암류와 구별되 었다 (그립 9-23) . S- 형의 티탄칠석 계 화강암류는 +12%, 까지 높은 값을 가지며 180 가 부화된 퇴적암이 관련되어 있음을 지적하였다. 그리고 기다가미 화강암류의 87Sr I 86Sr 초생 치 는 0 . 7042 ~0 . 7043 이고 ~4S 값이 1 ~ 2%, 로 제 4 기 칼크알카리 화산암의 값과 유사하였다. 한편 티탄철석계 화 강암류는 87Sr/86Sr 초생치가 히다카 대에서 0.704~0.706 에서 서남
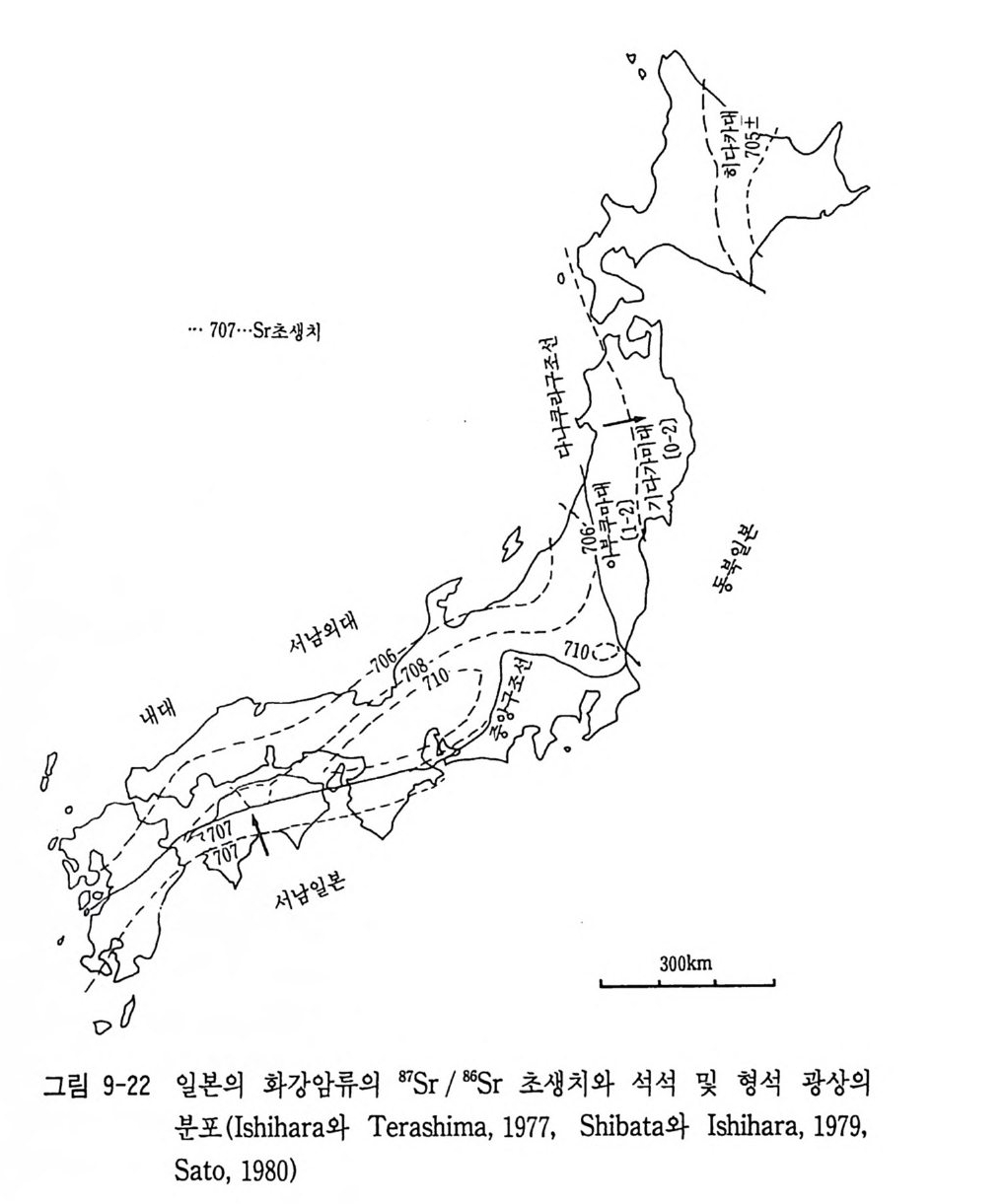 vC
vC
일본 내대를 거쳐 요께대와 산요대에 이르는 지역에서는 0.710 까지 크게 변화하고 있다. 8180-87Sr / 86Sr 초생치를 도시한 그립 에서 초생의 칼크알칼리 마그
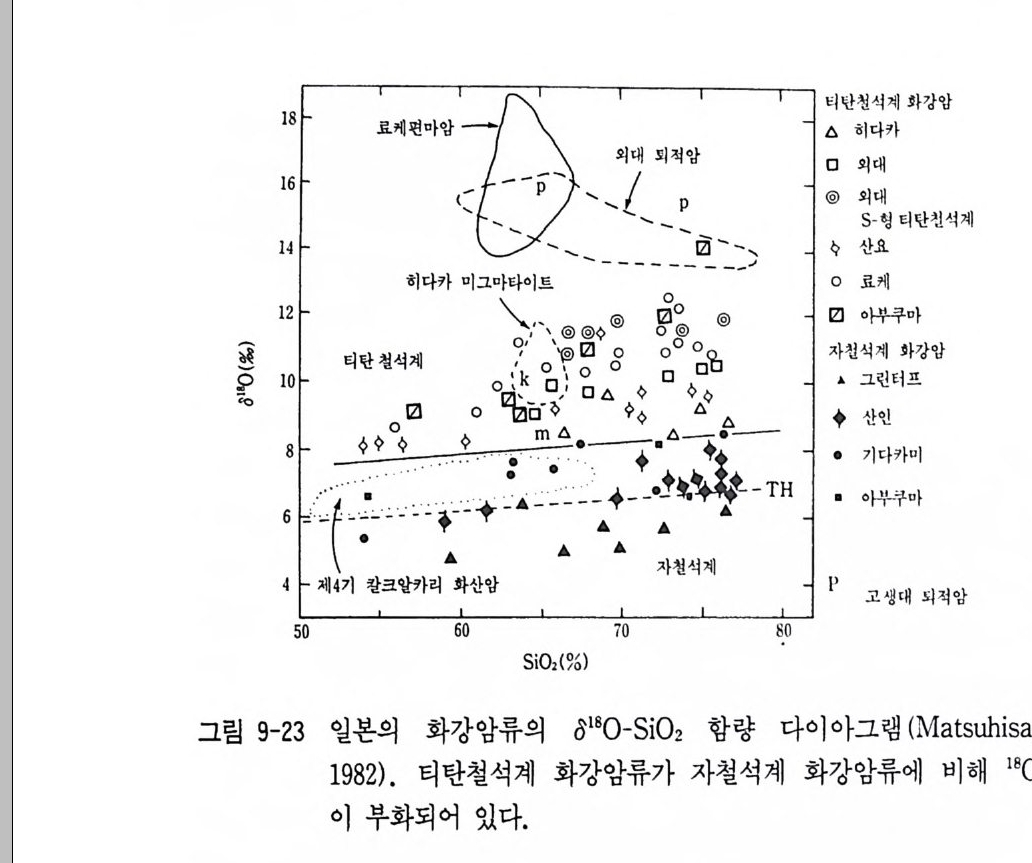 g낸 ()111I4 682 」-_,--, i -제 . 0\4.기 - 티i -· ,단. 칼- A8료철- 크L0i석케 宁.I편계Z히 - . 마다 回-~카` 」암 \o :A 一二S iO , ( %l ) `-l _ T~'l/-病 j ~--虹뗀 p ~l 석암 _ -IIZl계 IlI-、/ A티□©1I자b0令•2' 晶 난 ]신 히천석의산외그아료S산기고다삭 -대대계요런케부 안다생헝카 계 터 쿠 카대티 화마프미화 탄강 강외찬압적압석 암 계
g낸 ()111I4 682 」-_,--, i -제 . 0\4.기 - 티i -· ,단. 칼- A8료철- 크L0i석케 宁.I편계Z히 - . 마다 回-~카` 」암 \o :A 一二S iO , ( %l ) `-l _ T~'l/-病 j ~--虹뗀 p ~l 석암 _ -IIZl계 IlI-、/ A티□©1I자b0令•2' 晶 난 ]신 히천석의산외그아료S산기고다삭 -대대계요런케부 안다생헝카 계 터 쿠 카대티 화마프미화 탄강 강외찬압적압석 암 계
마와 변성되적암의 혼합의 영향이 나타나고 있다. (3) 우리나라 화강암류의 성인 우리나라의 화강암류는 관입시기에 따라 선캠브리아기에서 제 3 기까 지의 다양한 화강암류가 분포하고 있다. 그러나 가장 활발했던 화성 활동은 중생대에 쥬라기-백악기에 일어났으며 제 3 기까지 이어졌다. 따라서 여기서는 화강암류 중 중생대 쥬라기의 대보화강암류와 백 악기의 불국사화강암류에 대하여서만 소개한다. 대보화강암류는 한반 도 중부의 중국 방향으로 관입 분포하며 불국사화강암류는 주로 경상 되적분지내에 불규칙하게 관입 분포하고 있다. 이들 두 화강암류군을 비교하면 표 9-6 과 같다. 지구화학적 분석연구 결과가 많이 있지만 여기서는 이들 화강암류
표 9-6 우리나라 중생대 대보화강암류와 불국사화강암류의 비교(박과 김 , 198 2 ; Jin, 1986 ; Hong , 198 7 ; Kim , 1990 ; 김규한 의, 1990) 대보화강압류 1 불국사화강암류 관입시기 쥬라기 - 백악기초 백악기 말-제 3 기 초 산출상태 중국 방향으로 대상 관입 I 불규칙한 스목, 화산암류와 수반 저반암채 광물조성 I 칼리장석, 미사장석, I 칼리장석, 정장석, 혹운모 퍼사 이트, 복운모 화학성분 Si0 2 < 70 % Si0 2 > 70 % 산소동위원소 비 (0180) +9 .5 % o < o1 80 +9. % >8 180 자성특징 티탄 칠석계 자철석계 1 - S 형 1 형 ( S 형 ?) I 형 s;sr / 86Sr 초생 치 0.7 10 7- 0. 7 17 6 0. 7040-0 . 7070 광화작용 Au-Ag 열수광맥 광상 Cu- Zn - Pb 접 촉교대 또는 열수광맥 광상
에 대한 동위원소 분석연구 결과만 간단히 소개한다. 대보화강암류와 불국사화강암류의 전암 39 개 시료와 단체 분리된 석영, 사장석, 혹운모 등의 시료의 산소 동위원소 분석결과는 그림 4-35 와 같다. 남한의 중생대 화강암류의 산소 동위원소비는 8180 = +2.38~ + 11.10%0 로 Talyo r (1974) 의 화강암류 동위 원소값의 범 위 와 일치 하 고 있다. 그 중 대보화강암류는 S180 = +4.97~+11.10% 이고 불국 사화강암류는 8180 = +2.38~+9.83% 로 대보화강암류에 180 이 부화 되어 있다. 조암굉물 중 기타 물질과 동위원소 교환에 비교적 안정한 석영의 산소 동위원소비는 대보화강암 (+9.45~+ll.10 %o)과 불국사화강암 (+3.73~+9.83 %o)간에 명확하게 차이가 나타난다. 조암광물간에는 동위원소 평형에 있어 석영 >사장석 >흑운모 순으로 180 이 결핍되어 있다. 대보화강암류는 티탄철석계 화강암의 특칭을 가지고 불국사화
강암류는 자철석계화강암의 산소 동위원소의 특징을 나타내고 있다 (그림 4-36). Ji n(1988) 은 불국사화강암류는 칼크알칼리 계 열의 마그마에 서 섬 록 암상 알칼리화강암상으로 결정 분화한 산물로 해석하였고, Hong (1987) 은 쥬라기 화강암류와 선캠브리아기 화강암류는 S - 형 화강암류 이며 백악기 화강암류는 I- 형 화강암류으로 해석하였다. 표 9-6 과 표 9-7 에서와 같이 쥬라기의 화강암류는 87Sr /86 Sr 의 초생치가 0.7107~ 0 . 7176 이고 백악기 화강암류는 0 . 7040~0.7070 이다(박과 김, 1972;Ji n, 1986). a180 값, 87Sr / 86Sr 초생 치 , REE 분석 결 과 등울 고려 하면 대보화강암류는 지각물질의 부분용융 산물로, 불국사화강암류는 상부 맨틀 기원의 화강암질 마그마의 분별정출 산물로 해석된다(김규한 의, 1990).
표 9-7 우리나라 쥬라기 화강압류와 백악기 화강압류의 Rb-Sr 연령과 87Sr/8 6S r 초생 치 (Jin, 1986) (87S r / 86S r) 전압연령 (Ma) 초생치 참고문헌 〈쥬라기화강압류〉 서울화강암 160 土 10 0.712 Park0972) 황동화강암 167 0.7 10 4 K i m 과 Wend t(미발간) 진천화강압 19 4.1 土 18.3 0 . 7168 土 0.0009 Choo 등 (19 79) 청주화강암 146.3 土 2 . 8 0. 7129 土 0 . 0009 Choo 등 (19 79) 안동화강암 172 . 3 土 0 . 9 0 . 7126 土 0 . 0004 Choo 등 (1979) 춘천화강암 205 土 5 0 . 7151 土 0 . 0003 Jin 등(1 986) (백악기화강압류〉 마산화강암류 70 土 17 0.704 土 0.001 K i m 과 Wend t(미발간) 경상분지 100 0.705 Hurley 등 (1973) 유천화강암 75 . 5 土1.2 0 . 7070 土 0 . 0009 Ji n 과 Choo (l98 0) 창원화강암 118 .4士 7.3 0 . 7058 土 0 . 0004 Jin( 1 9 81) 일광화강암 125.0 土 15.5 0.7063 士 0 . 0006 Jin( l 98 1)
8) 동위원소비에서 본 맨틀의 구조 맨틀의 구조 연구에 해양성 현무암의 니오디미움 동위원소비를 이 용하였다. 앞에 설명한 것처럼 화성암에서 동위원소비는 맨틀의 직접 적인 정보를 주지만 기타 물질의 혼입에 의해 크게 영향을 받는 경우 가 많다. 대륙지각에서 용암이 분출할 경우 마그마는 두꺼운 지각을 통과하여 분출하게 되므로 주위의 지각뭄질이 혼입되기 쉽다. 해양현 무암은 이런 영향이 비교적 적기 때문에 맨틀연구에 적합하다. 앞에 서 설명한 것처럼 해양현무암의 니오디미움, 스트론튬 동위원소비 사 이에는 상관성이 발견되었고 dep le te d man t le 에 유래하는 중양해령 현무암과 콘드라이트질의 미분화 맨틀에서 유래하는 대륙의 대지 현 무암을 잇는 직선인 맨틀 배열선상에 분포하고 있다. 이 결과 Wasserburg 등 (1979) 은 2 층 구조의 맨틀을 제창했다(그림 9-2 1 ). 즉 상부 멘툴 물질은 대륙지각의 분화에 수반되어 부적합원소 의 농도가 감소된 dep le te d man t le 로 되 어 있으며 이 것 이 MORB 에 공급되고 있다는 것이다. 이에 대해 하부 맨틀은 미분화된 채로 남은 대지현무암 기원이다 . 2 층 혼합의 혼합선에서 맨틀 배열이 만들어진 다는 모델이다. 그러나 킴버라이트 중의 포유물이나 케르구엘렌 (Ker gu elen) 등의 일부 해양성의 현무암의 Nd-Sr 도상에서 enrich e d mantl e 영역에 도 시되는 시료가 나타났다. 그래서 모델변경을 시도하여 Zin d ler 등(1 982) 은 해 양성 현무암의 Nd, Sr, P b 동위원소비를 3 차원에 도시한 결과 이들이 동일 평면에 놓이는 사실에서 맨틀은 3 종류의 단성분으로 되어 있다고 결론지었다. 그러나 Wh it e(l985) 는 이 평면에서 벗어나 도시되는 시료가 또다 시 나타나 맨틀은 적어도 5 종류 이상의 단성분이 복합되어 있다고 주 장했다. 이런 사실에서 맨틀 성분의 불균질성이 잘 입증되었다. 맨틀 의 성충 구조는 동위원소 자료로 설명하기 곤란하였고 상부맨틀에서 수평방향의 불균질성이 분명하게 나타났다. 예를 들면 Ha rt(l984) 는
적도와 남위 60° 사이에 두팔 이상 (Du p al anomal y)이라 부르는 Pb, Sr 동위원소가 높은 영역이 있음을 보고하였다. 따라서 대륙지각과 해양지각 하부의 맨틀 간에도 차이가 있음을 제안하였다. Da vi s0982) 는 화학적으로 불균질한 물질의 덩어리가 혼합되어 섞 이지 않고 대류하는 모델을 제창하였다. 그들이 제창한 모델은 전 맨 틀에 걸친 대류를 가정하였으나 맨틀대류가 상부맨틀에서만 일어나는 지 전 맨틀에 걸쳐 일어나는지는 지진파의 650km 불연속면의 원인의 문제 규명과도 연계되어 금후 해결해야 될 중요한 연구과제로 남아 있다. 9) 되적암에서 본 대륙의 진화 세립질 육성기원 되적암의 Sm/Nd 비는 퇴적물 근원지의 화성암이 나 변성암의 비와 유사하다. 즉 풍화, 침식, 퇴적, 속성작용 등에 의 하여 퇴적물내의 Sm / Nd 비가 변화하지 않는다. 그러나 퇴적암의 Rb/Sr 비는 Rb 이 점토광물에 흡착되기 때문에 증가한다. 따라서 셰 일의 모델연령은 퇴적원암인 화성암이나 변성암의 연령과 유사하다. 그러므로 셰일의 Rb-Sr 모델연령은 퇴적연령에 근사하나 셰일의 Sm -Nd 모델연령은 퇴적연령울 상회한다. 지각에서 Sm/Nd 비가 지각 에서 일어나는 지질학적 사건에 의해 잘 변화되지 않으므로 퇴적암의 Sm-Nd 모델연령이 지각정체연령 (Crusta l resid e nce a g e) 으로 이용될 수 있게 되었다. 일반적으로 선캠브리아기와 고생대의 지각정체연령은 퇴적연령보다 오래되게 얻어지므로 셰일로 재되적되기 오래전에 CHUR 에서 분리 되어 순환된 지각물질임을 알 수 있다. 그러나 지각정체연령과 퇴적 연령의 차이는 퇴적시 젊은 화성암 퇴적물이 혼입되면 점점 줄어든 다. 순환된 고기지각은 약 20 억 년 정도 시기가 대단히 중요하며 화 산쇄설물이 조산운동지의 퇴적과정에 유입되었음이 많은 연구에서 조 사되었다. 어떤 시료의 니오디미움 동위원소비 (143Nd/144Nd), Sm/
Nd 비를 측정하면 그 시료의 니오디미움 동위원소비의 진화를 연구 할수 있다. 지각 구성물질의 대표가 되는 퇴적암에서도 주로 모델연대를 이용 하여 대륙의 진화를 연구할 수 있게 되었다. 모델연대란 다음과 같이 얻어진다. 시료가 CHUR 에서처럼 미분화된 맨틀에 얻어전 후 여러 지질 작 용에 의해 변화되었다고 가정하면 시료가 맨틀에서 분화된 연대는 과 거로 연장시킨 시료의 니오디미움 동위원소 진화곡선과 CHUR 의 니 오디미움 동위원소 진화곡선과 교차하는 점을 얻을 수 있다. 이 교차 점의 연대를 모델연대라고 한다(그림 9-24).
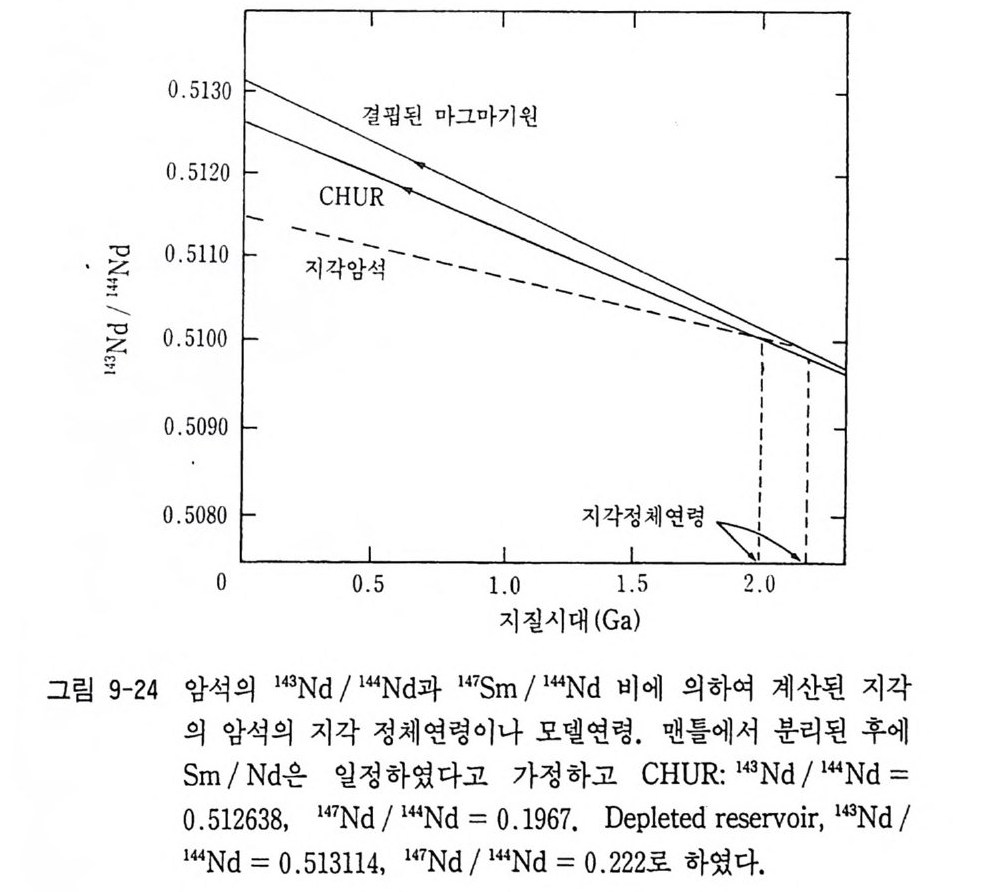 0.51 3 0
0.51 3 0
McCulloch 등(1 978) 은 캐 나다 순상지 의 평균 화학 성분을 나타내 는 여러 종류의 암석을 섞어 만든 복합시료의 Nd 모델연대를 구해 25~27 억 년을 얻었다. 또 스트론튬 연대도 이와 일치하는 결과를 얻 었다. 이들 연대는 캐나다 순상지의 평균연대를 나타내고 있는 것으 로 생각되나 이들 지역의 각각의 시료의 K-Ar 와 Rb--S r 연대가 잘 일치하여 이 지역의 대륙이 약 25 억 년 전에 형성된 것으로 보고 있다. 셰일은 여러 종류의 암석이 풍화된 입자가 퇴적된 것으로 주위의 상당히 넓은 지역의 암석을 평균적으로 채취한 시료로 생각할 수 있다. McCulloch 등 (1981) 이 얻은 오스트레일리아의 셰일의 니오디미움 모델연대와 기타 방법으로 측정한 결과는 일치하였으나 스트론튬 모 델연대는 연대가 젊게 나타났다. Sm-Nd 계는 풍화 퇴적과정에서 그 다지 변화되지 않는 반면 Rb-Sr 계는 크게 영향을 받고 있다. 니오디 미움 모델연대의 유용성이 인정되었으며 대륙지각을 형성한 암석은 미분화된 맨틀에서 된 것 이 아니고 분화된 dep le te d man t le 에 유래 한 것으로 연구되어 최근에 dep le te d man tl e 에서 분화한 모델연대 연구 가 진행되고 있다. 그리고 셰일 등의 니오디미움 모델연대와 퇴적연 대의 비교연구가 이루어지고 있다 (M i chaad 등, 1985). 일반적으로 셰 일의 퇴적연대와 모델연대는 일치한다. 그러나 앞에서 설명한 것처럼 셰일 형성보다 오래된 시대의 맨틀에 서 분화된 암석을 공급원으로 하는 셰일은 보통 모델연대가 퇴적연대 를 상회한다. 만일 대륙이 40 억 년 전에 형성되어 그 후 성장하지 않았다면 각 퇴적연대의 셰일의 모델연대도 40 억 년이 된다. 대륙이 만들어지고 난 후 맨틀로 재순환하면 모든 셰일의 퇴적연대는 모델연대와 일치할 것이다. 현재의 대륙의 전화는 이의 중간에 있지만 대륙의 성장속도 가 일정하였다면 균일성장(Unifo rm gr o wth)의 선상에 위치하게 되고 연속성장으로 성장속도가 시대와 함께 감소하면 연속성 장 (Con ti num grow th) 의 선상에 측정 점 이 분포하게 될 것 이다 (그림 9-25) .
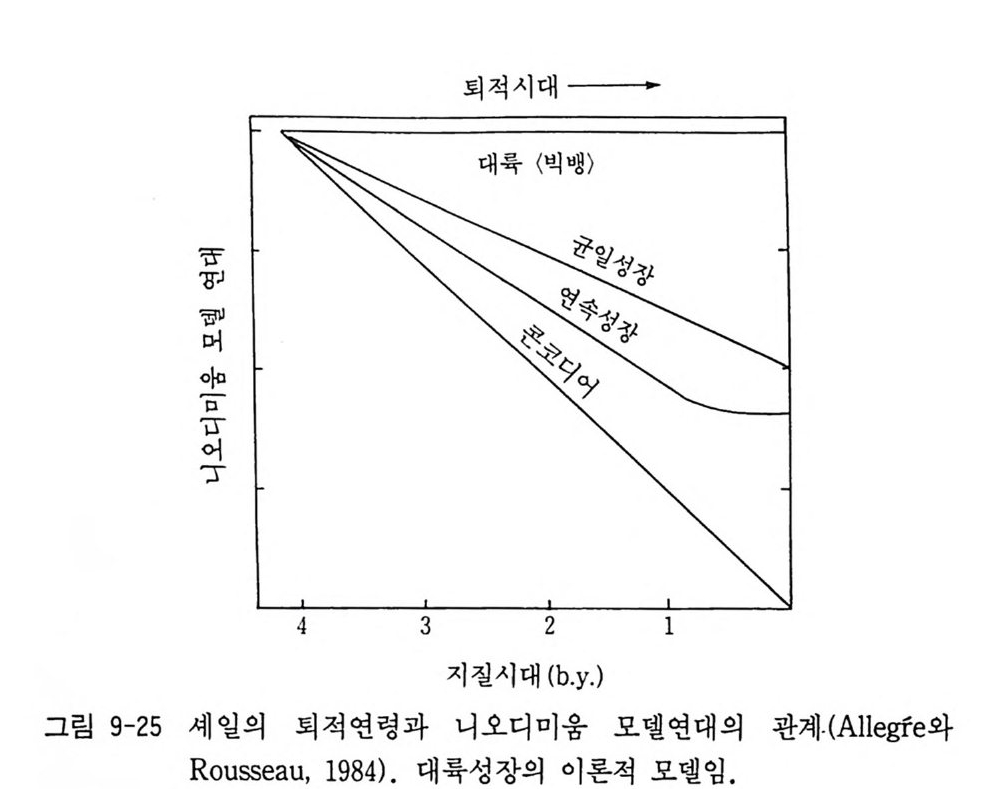 퇴적시대 ,.-
퇴적시대 ,.-
다양한 퇴적연대를 가지는 셰일의 니오디미움 모델연대를 조사해 보면 약 25 억 년 이전은 모델연대와 퇴적연대가 일치하고 있다. 이것 은 대륙의 암석이 맨틀내로 순환하는 속도가 빨랐음울 의미하고 있 다. 25 억 년 이후 모델연대는 퇴적연대보다 크게 된다. 그래서 선캠브리아기 이후에는 모델연대는 18 억 년 정도의 일정한 값을 가진다. 그 결과 대륙성장 속도가 감소하였다고 해석하는 경우 가 많다 (Nakai, 1987) .
참고문헌 Alleg re, C. ]., a nd D. Rousseau (1984), The grow t h of the conti ne nt thr oug h geo log ic t im e stu d ie d by Nd iso to p e analys i s o f s ha le. E a ,-t h Plane t. S ci . Let tm , 67, pp. 19-34. Anders, E . and M. Ebih a ra (1982), Solar-sy s t e m abunda nc es of the ele ments . Geoclzim . Cos m ocl zi m . Ac ta , 46, pp. 236 3 -23 8 0 . Bennett , V. C., and DePalo, D.J . (19 87 ) , Prote r zo i c crusta l his to r y of the weste r n Unit ed Sta t e s as dete r mi ne d by neody mi um iso to p i c map ping . Geo!. S oc. Am . Bull. 9 9, pp. 674 -68 5 . Clay ton , R.N ., N. Onuma & T. May ed a (19 76 ) , A class ifi ca ti on of me te o ri te s based on oxy g e n iso to p e s . E m- th Planet . S ci . Le tte ,- s , 30, pp. 10- 18 . Comp st o n , W. and R.T . Pid g e o n (1986), The age of ( a t iny par t o f) the Aust r a lia n conti ne nt. Nahtr e, 317, pp. 559- 56 0. Cummi ng , G.L. and J.R. Ric h ards (197 5) , Ore lead in the con t i no u s ly chang ing Eart h. Eart h Planet . S ci . L e ttm , 28, pp. 155-171 . Faure, G . and J.L . Pow e ll (1972), S tr o n h' um iso to p e g eo lo g y , Sp ri n g e r- V e rlag, N. Y., p. 188. Ganapa t h y, R. (1980), A majo r mete o rite im p ac t on the earth 65 mi llion yea r s ago : E v ide nce from the Creta c eous-Tert iar y boundary clay. Sci en ce, 209, pp. 921-923. Hart , S.Ra .r; r G ayer alancdh ,c oDn.Cs e.; q au ne dn cWesh ftoe ,r Wma. Mnt. l e(1 m9 8i6x)i ,n g .A Gpoeo ssci hbi l m e . SCr -o sNm d o 一c P hbi m m . aAnct tl ae 50, pp. 1551-1557. Hawkesworth , C.]., M. Ha m mill, A.R. Gledhil l, P . van Calste r en, and G. Rog er s (1982), Isoto p e and trac e element evi de nce for late - sta g e int r a -crusta l . meltin g in the High Andes. E art h Planet . Sci . L ette r s , 58, pp. 240 - 2 5 4 . Hong , Y.K . (19 87) , Geochemi ca l charact er ist i c s of Precambria n , Jur assic and Creta c eous gran i tes in Korea. f ou r. Kor. I nst. Mi ni n g Geo!. 20(1 ), p p. 35 -60. Jac obsen, S.B., and G.J . Wasserburg (1980), Sm-Nd iso to p i c evoluti on of chon- drites . Eart h Planet. S ci. L ett ers , 50, pp. 139- 15 5. Jin, M.S. (19 88) , Geochemi str y of the Creta c eous to early Tert iar y gran i tic rocks in South Korea Pant 2. Trace elements geo chemi str y. f ou r . G eo!. Soc. K orea, 24, Spe c . Issue, pp. 168~188.
Kis tl e r , R.W . and Z.E. Pete r man (197 8) , Reconstr u cti on of crusta l blocks of Califo rn ia on the basis of initia l stro nti um iso to p i c comp os it ion s of Mesozoic gran it ic rocks. U.S . Geo!. S urv . Prof Pape r , 1 07 1. p. 17. Lee, T, Papa n asta s sio u , D. and Wasserburg, G. J. ( 1977), Alumi nu m-26 in the early solar sys t e m fos sil or fue l. Astr op hy s i cs ]. 211, pp. 107-10. Mats uhisa , Y., A . Sasaki, K . Shib a ta and S. I shih a ra (1982) , Source div e rsity of the Jap a n ese gran it oi d s : An 0, S and Sr iso to p i c app r oach. 5 th Inte m a- tion al conf. G eo ch ron . Cosmochron. Isoto p e Geo!., Nik k o. McCulloc h , M.T ., and G.J . W ass e rburg (19 78), Sm-Nd and Rb-Sr chronolog y of conti ne nta l crust for mati on . S ci en c e, 200, pp. 1003-1011. McCulloc h , M. T., a nd W. Comp st o n (19 81), Sm-Nd age of Kambalda and Kano wn a gree n s to n es and hete r og en eit y in the Archaean mantl e . Natu r e , 294, pp. 322 -32 7 . Mc Culloch, M. T., and M.R . Perfit (19 81), 143N d / 141Nd, f!IS r / 86S r and trac t elements constr a in ts on the petrog e n esis of Aleuti an Island arc mag - mas. Ea 까 h Planet . S ci . Let te rs , 56, pp. 167-179. McCulloc h , M. T., a nd B.W . Chapp e ll (1982), Nd iso to p i c c haracte r ist i c s of S -and I-ty p e gran it es . Eart h Plane t. Sci. Let te rs , 58, pp. 51-64. Mi ch ard, A., P. Gurrie r , M. Soudant, a nd F. Albarede (1985), Nd iso to p e s in French Phanerozoic shales: e xte r nal vs. int e r nal aspe c ts of crusta l evo l uti on . Geochim . Cosmochim . Acta , 49,pp . 601-610. Moorbath , S. ( 1977), The oldest r ocks and the grow th of c onti ne nts . S ci. Amer., 236 , pp. 92-104. Nelso n , D.O . (1983), Imp lic a ti on s of oxyg e n-is o to p e data and trac e-element modelin g for a large scale mixi n g model for the Columbia R ive r Basalt. Geolog y, ll, p p. 248-251 . Nie m eye r , S. (19 78), I-Xe dati ng of s ili ca te and troi li t e from IAB iro n mete o r- ites . Geochim . Cosmochim . Acta , 43, pp. 834-860. Reyn o lds, J.H . (1960), Isoto p i c comp os it ion of pri m ordi al xenon. Phys . Rev. Lett er s , 4, pp. 351-354. Tayl o r, S .R. (1977), Island-arc models and the comp os it ion of the conti ne nta l . crust. In : Ewi ng Seri es Vol. 1, pp.3 2 5-335, Amer. Geop hy s . Un ion , Washi ngton D.C. Wasserburg, G. J., and DePaolo, D.J (1979) , Models of e art h stru c tu re infer red from neodym ium and str on ti um iso to p i c abundances. Proc. Nat. Acad.
Sci . USA 76, pp. 3594 -98 . Weth e rill , G. (19 75), Radio m etr ic chronolog y of the early solar sys t e m . Ann. Rev . Nuclea r Scie n c e , 25, pp. 283- 32 8. \Vhit e, W.M (1985), Sources of oceanic basalts : Radio g e n ic iso to p i c evid e nce. Geology 13, pp. ll5-18. York, D (19 66) , Least-s q u a res fitting of a str a ig h t line . C an. ]. Plzys . 4 4: 1079 -86. Zart ma n, R.E (19 74) , Lead iso to p i c pro v inc es in the Cordil le ra of the weste r n Un ited Sta t e s and the ir g eo log ic sig nifica nce. E con. Geo! . 69, pp. 792 -805. Zin d ler, A ., S.R. Hart and C. Brooks (1981), The Shabog am o Intr u s iv e suit e, Labrador: Sr and Nd iso to p i c e vi de nce for conta m i na te d mag ic magm a s in the Prote r ozoic . Earlh Planet . Sci . L e tte ,' S , 45, pp. 249 - 26 2 . 中井俊一(1 987), 「 Nd 同位 體 比力 6 見f려地球 (1)構造 之 進 化」, 《 月 刊地 球 》 10 號 , Vol. 9 (10) , pp. 573-578. 五十 蘭 丈二, 小 U島 秘(1 987), 「地球 希力次 同 位體 比」, 《 月刊地 球 》 10 號 , Vol9 (10 ) 1 pp. 561- 56 7. 小 鳩 秘 齋 藤常正 (1982) I 岩波 器座 地球 科學 6, r 地球 年 代 學 j , 岩波 晋 店 . p, 2 55. 佐夕木 昭(1 987), 「 鑛 床(1) 鈴 同位 體 比」, 《 月刊地球 》 10 號 , Vol. 9(1 0 ), pp. 579 -584. 김규한, 水谷義彦(1 990)I 「남한의 중생대 화강암류의 안정동위원소 지구화 학 적 연구」 (한국과학재단연구보고서). 박미령, 김규한(1 982)I 「남한에 분포하는 화강암류의 암석화학적 연구」, (( 지질 학회지}} 18(3), pp. 132-148.
10 환경동위원소와 오염 1-1 서언 환경수 중에 포함되어 있는 환경동위원소는 수소(1 H, 2H(D)), 탄소 (12 c, 13C ), 산소 ( “ O , 180 ) , 황(3 2S, 34S)' 질소 (l4N , 15N) 등의 안정동위 원소와 T, l 4 C 와 같은 방사성 기원의 동위원소가 있으며 이들 환경동 위원소가 최근 수문학 연구에 많이 이용되고 있다. 이들 환경동위원 소는 주로 지하수의 함양원, 지하수계 연구, 지하수의 기원, 지하수 의 이동(거동), 지하수의 함양속도, 지하수의 유래, 물수지 계산, 지 하수의 오영원 추적, 지하수의 연대측정, 지하수의 순환, 지하수와 하천수와의 관계, 지하수-해수의 혼합, 폐기물에 의한 지하수 오염연 구 등에 광범위하게 이용 연구되고 있다. 여러 환경동위원소 중 특히 물의 동위원소 분자는 9 종류가 있으며 그 중 H/60 (99. 73 %), HD160 (0.032%) 그리고 H/80 (0.20% )로 되 어있다. HD1so 와 H2180 는 모두 지 하수(육수) 중에 용존하고 있는 기타 용 존 화학성분보다 높은 농도로 포함되어 있으며, 물의 동위원소 분자 는 지하수에 용존하고 있는 기타 화학성분처럼 주위의 기타 물질과 반응해 변화하지 않으므로 물에서 D 와 180 의 존재량의 변화는 · 물의 거동 그 자체를 직접 반영하므로 물의 기원 연구에 유효하게 이용되
고 있다. 10-2 물의 환경동위원소값의 변화 여러 지질환경에 존재하는 물은 그 기원과 물이 겪은 지질환경의 변화 과정에 의해 각기 다른 동위원소값을 가진다. 이같이 동위원소 값의 변화요인이 환경오염 문제의 연구수단이 될 수 있다. 일반적으로 물의 동위원소값의 변화요인은 ® 서로 다른 기원의 물의 혼합 ® 증발에 의한 액상-기상의 상변화에 따른 동위원소 평형분별 ® 확산에 의한 반응속도론적 동위원소 효과 @ 물-암석 (또는 폐기물)과의 상호반웅 등을 들 수 있다. ®의 경우 함양지, 물의 기원 및 유래가 다른 물(특히 동위원소비가 상이한 물)의 혼합을 규명할 수 있고 그의 혼합비도 계산이 가능하다. 예를 들면 서로 다른 기원 A, B 의 물이 혼합된 경우 다음과 같은 물질평형 관계식에서 그 계산이 가능하다. 0180 = Ra180A + (l-R ) 0180B 이때 R= 같。 B 이다. 각기 서로 다론 물의 산소 OA 와 0B 관계로 해수와 담수의 혼합, 지표수와 지하수의 혼합, 강수와 지하수의 혼합 비율 추정과 물의 기 원을 해석할 수 있다. ® 의 경우 물의 기상과 액상간의 동위원소 분별시 동위원소 분별 정수는 a = Rt I Rv 이며 이때 R 은 1ao I 160, D I H 이다. 그리고 확산속도차에 의해서도 물의 동위원소 분자는 서로 다른 동 위원소비를 가지게 된다.
10-3 환경수의 오영 유형 하천수 및 지하수 오염 : 하천수의 화학성분은 유역환경(죽 분포하 는 암석, 토지이용 형태, 식생, 인간활동 등)에 의해 달라전다. 그리고 인공댐 등으로 인하여 변화하기도 한다 . 이 같은 하천수의 수질변화 는 주변의 생태계에 큰 변화를 준다. 中井 信 之 의 (1982) 의 연구내용을 참고하여 한강의 경우를 들어 본다. 하천유역이 주로 화강암질암과 편마암류로 구성된 북한강과 태백산 광화대내의 다수의 금속광상이 분포하는 남한강 유역과 남·북한강이 합류 서울시내로 유입되는 한강수의 동위원소 성분과 화학성분의 차 이점이 명확히 나타난다. 북한강에 비해 남한강이 Ca2+ , M 답\ HCOi , so~-농 도가 현저히 높아 탄산염암 및 금속황화물 광상의 다수 분포로 특징되는 유역의 지질환경을 잘 반영하고 있다 . 양수리와 팔당에서 합류 후 서울시내로 유입된 한강수 중에는 Na+, K+ , C l\ NH; 함유량이 인공오영에 의해 현저히 증가하고 있다(그 림 10- 1) . 용존 탄산염의 o13c 값은 서울시의 -7~-8%0,. 서울시내 —1 0.7%, 로 오염 에 의한 경 향이 현저하고 용존 so~- 의 o34s 값도 차이가 나타 났다. 용존 화학성분과 동위원소 성분 분석으로 하천수의 오염원을 해석 할수 있다. 예를 들면 한강이 하천수 중의 so~- 가 광산폐수, 농약, 비료 기타 공장폐수 등의 어디서 오염되었으며 그의 각각의 오염원의 비율도 정 량화할 수 있다. 이 같은 연구가 수행되면 오염에 의한 분쟁 등의 민원사항이 해결 될 수 있고 근원적으로 오염원의 예방책에도 크게 도움이 될 것이다. 광산에서 선광시약, 데이링 및 폐석 등에 의한 광산페수의 오염을
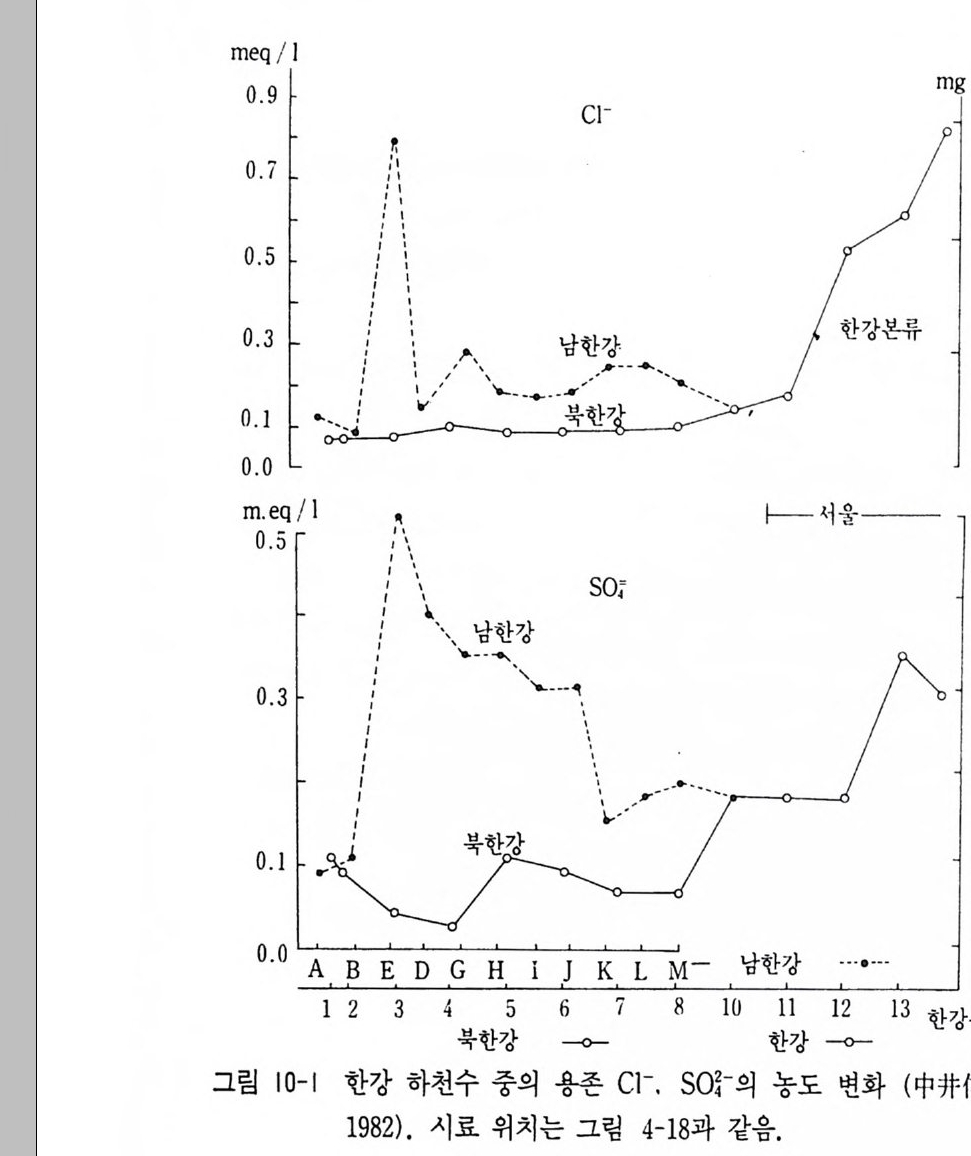 meq / 1
meq / 1
들 수 있다. 특히 폐석 중의 황화광물(황철석) 등은 산화에 의해 산 성화된 물이 농업이나 기타 생태계에 큰 영향을 주고 있다. 이 같은 오영은 황화광물의 산화에 의해 형성된 so~- 나 황산의 o34s 동위원 소비 분석에서 쉽게 확인할 수 있다. 생활하수에 의한 오염 : 인간활동에 의한 오염원은 주로 복합적인
요인에 의해 일어난다. 그러나 용존 화학종의 동위원소비, 즉 탄산의 탄소동위원소, 황산의 황동위원소비 등을 분석하여 그 근원을 추적할 수 있다. 목장 등 축산활동에 의한 오염도 점증하고 있다. 해수에 의한 오염 : 제주도나 해안지역의 지하수는 해수 침입으로 인한 담수의 오염이 일어나며 퇴적분지에서 퇴적수 (Forma ti on wate r ) 에 의한 오염 등을 생각할 수 있다 . 이와 갇은 혼입은 용존 화학성분 분석법에 의해 물의 산소 (8180), 수소 ( oD ) , 황 (o 34 S) 및 탄소 (a13C) 동위원소비 분석으로 쉽게 식별 할수있다. 제주도의 경우 지하수 0180 = -6.8%,, oD = -43.7%, 이다(김규한 과 나까이, 198 8). 그리고 해수는 각각 0% 이므로 이들의 혼합에 의해 지하수의 값은 좀더 무거운 값을 가지게 될 것이다. 그리고 해수 중 의 SO t 의 o34 S = +2 0%, 내의이고 우리나라의 보통 하천수의 so~- 의 o34 S = +3~+5 %o 이므로 이들의 혼합비율도 질량평형을 이용한 계산에서 규명이 가능하다. 산소 및 수소 안정동위원소비 분석은 집 수지와 지하수계 연구 및 상이한 기원의 물혼합 연구에 이용되며, 제 주도의 성산 , 대정지역 등의 영수 혼입에 의한 지하수 오염 등의 연 구에 효과적인 방법이 될 것이다. 안종성 의(1 984) 는 트리티움 분석 연구에서 제주시 지역의 지하수 오영은 염수 혼임보다 도시하수에 의한 오염을 지적한 바 있다. 댐수의 2 차 오염 : 남한강, 북한강 등에 다수의 댐이 건설되어 많은 하천수가 댐에서 장기간 저장된다. 이 같은 댐저에 홍수시 유입된 오 염물질이 댐 바닥에서 2 차적인 화학 변화를 일으켜 수질을 오염시키 기도한다. 핵 발전소 주위 의 오영 : 핵 발전소의 중수로 (m (n,r) , 3H) 에 냉각재 및 감속재로 사용하는 중수 (D20) 에 중성자 조사로 3H 이 생성되거나 핵연료 처리 시설에서 트리티움이 생성된다. 이때 만들어진 트리티움 이 강수에 의해 지하수계를 오염시킨다.
산업폐기물에 의한 지하수의 오염 : 난지도 쓰레기 처리장, 인공매 립지, 정화조 등에 의한 오영수의 지하수계에 유입으로 인한 오염이 미래의 지하수 오염원이 될 것이다. 우선 동위원소 및 화학분석법으 로 수계의 연구가 선행되어야 하고 이들로 인한 오염원의 추적은 위 에 설명한 방법과 유사하게 응용할 수 있다. 그리고 농약, 비료, 특수한 지충의 암석에 의한 지하수 오염 등도 상기와 같이 규명할 수 있다. 대기오염에 의한 지하수 오염 : 지하수는 우수의 일부이며 최근 인 류활동에 수반되는 배기가스원 및 화석연료의 연소로 심한 S02 등의 에어로졸 상태로 대기를 오염시켜 PH 가 5.6 이하인 산성바가 내리 고 있다. 특히 황화합물로 S02, H2S 에어로졸 상태의 황산 및 황 산 염이 존재한다. Jac obs Greenberg (1956) 에 의 하면 S02 가 여 름 280µg I m 으로 증가 하며 화석연료와 밀접한 관계가 있음이 조사되었다. 물론 황 이의에 Na, Mg , Ca, K 등의 금속원소도 에어로졸 형태로 존재 하고 있다. 강수 중의 so~ -의 황 동위 원소비 분석 에서 미국의 공업지역인 뉴해븐 지역 (8'34S = +5.06~+6.2 % 0) 그리고 지방도시인 피츠필드 지역 (8'34S = +3~+7.3 %o)과 비공업지역인 일본의 島 取, 秋 田지역 (8'34S =+12.1~+15.6%) 간에 현저하게 차이가 났다. 즉 이들 황이 해수기원이라면 +20% o 내의이어야 하나 현저히 32s 가 농집된 현상은 해수기원 이의의 황이 유입되었음을 명백히 나타내 여 주고 있다. 배기가스에 의해서도 대기 중의 S02 오염이 현저하다. 이 같은 오 염 강우가 지하수로 유입되어 일어나는 수질오영이나 토양오영도 공 업화, 도시화에 따라 점증하고 있는 것이다. 10-4 방사성 페기물 일반적으로 사암과 셰일과 같은 퇴적암이나 심해저 점토나 칼륨암
영내에는 방사성 원소의 함류량이 높다. 화강암류내에는 방사성 원소 의 농도가 높으며 보통 유라늄이 3pp m 내외로 함유되어 있고 토륨이 8.5 ~ 17pp m 정도 함유되어 있다. 우리나라의 옥천변성대내의 덕평-추부터널간에 분포하는 창리층중 의 흑색셰일이나 탄질셰일 중에도 우라늄의 함량이 높게 나타나고 있 다. 이처럼 자연환경에서도 자연방사성 광물이 존재하고 있다. 라듐 의 방사성 붕괴에 의해 형성된 226Rn 이 지하수 등에 다량 검출되기도 한다. 온천수에 소량의 Rn 은 방사성천으로 유용하나 다량의 라돈에 장기간 노출되면 폐암을 유발시키게 된다. 최근 화석연료의 고갈에 대비하여 개발된 대체에너지원으로 핵연료 에 의한 에너지를 얻기 위하여 핵발전소의 전설이 세계적으로 증가하 고 있다. 우리나라에서도 원자력 발전에 의한 전력 의존률이 높아지 고 있다(표 10- 1) . 그러나 제 2 차 세계대전시 일본 히로시마와 나가사 끼에 두하된 원폭의 피해를 잊울 수가 없다. 미국의 경우 1955 년 1986 년까지 탄광에서 약 6,879 명이 사망한 데 비해 핵발전소에서는 4 명만이 사망했다. 그러나 방사성은 누출되지 않았으나 1959 년 7 월 탄 타수산나 실험발전소에서 43 연료 원소 중 12 원소가 용융된 사건에서 1986 년 1 월 오크라호마에 있는 KerrMcGee 발전소에서 실린더의 우 라늄 핵사 플루오라이트의 부적절한 가열로 인해 한 명이 사망하고 100 여 명이 입원한 사건에 이르기까지 십여 차례 발생한 핵발전소의 사고의 실례가 있다. 더욱이 소련의 체르노빌 핵발전소의 사고로 인 한 체르노빌 구름에 의해 유럽의 방대한 지역의 대기나 우유, 채소 등에서 높은 양의 방사능이 검출되었다(표 10-2). Islam 과 Lin d g ren (19 86) 은 핵 발전소에 서 앞으로 t년 후에 발생 할 사고확률을 P(l,t) = £。0 .0. dr(l 다?-rt) r2T3e<-m2J = 1-(1 一t / T)-3
의 식으로 계산하였다. 여기서 r 은 폭발의 강도이고 반응로 연한울 T = 4 000 으로 하였다. 계산 결과에 의하면 금 후 10 년간 86 % 의 사고 확률이 예상되고 있다. 핵발전소의 사고나 핵발전소에서 발생하는 방사성 핵폐기물이 환경
표 10 기 1987 년 현재 세계 각국에서 가동중인 원자로(B o w er , 198 8) 국가 가동중인 원자로 전력 공급바 울 아르헨티나 2 23 벨기에 8 60 브라질 1 1 불가리아 4 32 캐나다 16 12 체코슬로바키아 5 15 핀란드 4 38 프랑스 40 65 FRG 18 30 GDR 5 12 항가리 2 5 인도 6 2 이탈리아 3 4 일본 33 27 네덜란드 2 6 파키스탄 1 2 남아프리카 4 18 호녁 4 18 스페인 8 24 스웨덴 12 42 스위스 6 34 태국 6 59 영국 33 19 소련 50 11 미국 98 16 유고슬라비아 1 5
표 10-2 소련의 체르노빌 원 자 력 발전소 사 고 이후 1986 년 5 월 2~5 일간 아이레에서 측 정된 대기와 강수에서의 방사성 핵종의 농도 방사능 핵종 대기( B중q m의 - 3)농 도 강수(B q중 lit 의r e -농1 ) 도 131I l~10 10~10000 1J2 T e-1 J2 I 1~10 10~10000 IO3R u 0.5 ~ 5 20~2000 106R u 0.3 ~ 3 10~1000 I“Cs 0.3~3 10~1000 137C s 0.5 ~ 5 20~2000 i,0 B a- 1• 0L a 0.3 ~ 3 10~1000
오염의 위험한 요인으로 등장하고 있다. 핵폐기물을 포함한 산업폐기 물이 1980 년대 미국에서는 5 , 700 만 돈이 발생하였으며 그중 3,2 0 0~ 50 ,0 0 0 개소는 산업폐기물 처리 시설을 갖추지 못한 시설이었다. 특 히 1 ,2 00~2 , 000 개소는 국민건강과 환경오염에 크게 영향을 미치는 곳이였다. 난지도에서와 같이 우리나라의 경우에도 산업폐기물에 의 한 환경오염 방제대책이 시급한 실정에 와 있다. 이와 같은 산업폐기 물이나 핵폐기물 처리대책을 각국에서는 강구하고 있다. 영국에서는 핵폐기물이나 산업폐기물의 처분장소를 ® 바다 쪽으로 경사한 내륙분지로 화산암이나 이암과 같은 두수성이 낮은 두꺼운 퇴 적층으로 구성된 되적분지 ® 퇴적층으로 덮인 투수성이 낮은 규암, 슬레이트, 이암, 화산암, 기타 결정질암석 등으로 구성된 기반암 지 역 ® 지형의 기복이 없는 단단한 암석으로 구성된 지역 @ 해수와 담수의 경계면이 낮게 위치하여 지하수가 안정하게 정체될 수 있는 지역인 작은 섬 등울 택하고 있다. 대부분 폐기물 기원의 오염물질이 지하수계로 유입 유동되어 인간 활동에 이용되는 지하수계에 유입이 되지 않는 지질학적 조건이 갖추 어전 지역을 최적지로 택하고 있다. 물론 지구조적으로도 안정된 지
역이라야 될 것이다. 그러므로 원자력 발전소 부지 선정 대상지역은 암염충이나 셰일충 과 같은 높은 불두수성의 암석지역, 지하수 유동이 적은 암석 , 수분 상태에서 방사성 핵종의 흡착력이 강한 암석, 그리고 화학적으로 안 정된 성분을 가지는 암석지역이 유용함을 알 수 있다. 지하수 유동에 의하여 방사성폐기물이 인간생활권으로 되돌아오는 것을 막기 위하여 수리지질학적인 연구가 필수적으로 요청된다. 지하에서 지하수의 유동특성, 방사성폐기물 기원의 핵종과 암석_지 하수간의 상호반웅 등이 정량적으로 연구되어야 하며 이 를 위하여 산 소 및 수소 안정동위원소 비분석 및 인공방사성동위원소의 트레이서 가 유용하게 이용되고 있다. 최근에는 인공방사성동위원소 추적자 그 자체가 환경오염원이 되기 때문에 미생물 추적자 (B i o t racer) 를개발 이용하고 있다. 예를 들면 자연환경에는 존재하지 않는 Bacil lus g lob igii와 같은 미 생물을 트레 이서로 이용 수문학 연구에 응용하고 있다. 참고문헌 Bowen, R. (1988), Isoto p e s in the Eart h Sci en ces. E lsevie r , Ap pli ed Sci en ce. pp. 541 -543. Chapm an, N. and McEwan, T. (1986), Geolog ica l soluti on s for nuclear waste s . New Sci entist, 28, pp. 36-40. Islam, S. and Lin dgren , K. (1986), How many reacto r accid e nts wil l the re be ? Natu re , 322, pp. 691-692. 中井信之外 lOA, (19 82), 「漢江(韓國)及 u• 流域生態系i :E it 5 環境動態i :0 月寸 5 基礎的調査」, 卜 3 夕財團硏究助成硏究報告要約. 中井信之 (1986) , 「地下水硏究^(T) 同位體利用」, 《 地學雜誌 》 , 95 (7) , pp. 15-22. 中井信之 竹內尹雄 (19 74) , r 雨(T)化學 & 大氣汚染」, 《 化學 》 29 (6) I pp. 418-426,
水谷義彦 (1986), 「水文*'=望圭札&諸問題一安定同位體 lk 文根」 《 I、 4 F 口口 〉 )) 16 (2) , pp. 74~82. 안종성, 한정상, 이정호, 정창조, 유장걷 (19 84), 「동위원소를 이용한 제주 지 역 수자원에 관한 연구」, 《 한국수문학회 지 》 17 (2) , pp. 72-79.
 부 록
부 록
부록 I 안정동위원소의 질량과 존재도 (Goldman, 1965, Wa p s tr a 와 Gove, 1971) 원소 질량 원자상대 원소 질량 원자상대 원소 질량 원자상대 빈도(%) 빈도(%) 빈도(%) 1H1 1.0 0 7825 99.985 16S36 35.96708 0.017 vC059 58 . 93319 100.00 IF 2.0 1 410 0.015 1£ l35 34.96885 75. 53 28 N ·I5 8 57.93534 67.8 2He3 3 . 01603 1.3 x 10-• I.,C l 37 36.96590 24. 47 28 N'I6 0 59.93078 26.2 ,H e' 4.00260 ~100.0 0 I 먀 곤 35 . 96755 0.34 2aNi 6l 60. 9..3 1 05 1.25 3L I'6 6.0 1 512 7.5 1& 곤 37.96273 0.06 28Ni 62 61. 92 834 3.6 6 1 LI·7 7.0 1600 92. 5 1sAr'0 39. 96 238 99. 60 28Ni ” 63. 92 796 1.16 ,Be9 9.01218 100 .00 19 K 39 38.9 6371 93. 08 29C U63 62 . 92959 69.1 sB 1 0 10.0 1294 18. 7 19K'0 39. 96 400 0.0119 29C U65 64 . 92779 30. 9 sB 11. 00931 81. 3 19 K 41 40. 96 183 6.9 1 값 n” 63. 92 914 48.89 .c1, 12. 00 000 98. 89 20Ca'0 39 . 96259 96. 96 싶 n” 65. 92 604 27.81 6cl3 13.0 0336 1.11 2!,C a'2 41. 95863 0.64 ~ n6 7 66. 92 713 4.11 ;N 14.0030 7 99. 63 5 20C a'3 42 . 95878 0.145 J,n6 8 67. 92 485 18.56 7N15 15 . 000ll 0.365 20Ca ~.95549 2.07 # n7 0 69. 92 533 0.6 2 .016 15. 99492 99.759 20C a46 45 . 95369 0.0033 31Ga69 68 . 92558 60.2 80 11 16. 99 913 0.037 20Ca'8 47 . 95253 0.185 31Ga71 70.92470 39. 8 .0 1s 17.99916 0.204 21 Sc4S 44.95592 100.0 0 32G e70 69.9242 5 20.55 9F 19 18.9 9840 100.0 0 22T i46 45.9 5 263 7.99 J2 Gen 71. 92 208 27. 37 ,0N e20 19 . 99244 90. 92 22Ti 47 46. 95 177 7.32 ,2G e73 72 . 92346 7.67 10Ne21 20 . 99385 0.257 22T i'8 47.94795 73.99 32G e 73.92118 36.7 4 10Ne22 21. 99138 8.82 22Ti '9 48.94787 5.46 32Ge10 75.92140 7.67 11Na23 22.98977 100 .00 22T iso 49.94478 5.25 33As75 74.92160 100. 00 12M 답' 23 . 98504 78.60 23V50 49. 94 716 0.2 4 ,.Se 73.92248 0.8 7 ,2Mi r 24 . 98584 10. 11 2lv51 50.94396 99. 76 머 Se 76 75. 91921 9.02 12M 균 25 . 98259 11.29 21C 곤 49.94605 4.31 34Se77 76.91991 7.58 13AIZ1 26.98154 100.00 u C 꼰 51.94051 83.76 :uS e78 77.91731 23. 52 14S i 28 27.97693 92. 18 2,C 곤 52.94065 9.55 34Se80 79.916 53 49.82 l ◄ S i 29 28. 97 650 4.71 z. C 손 53. 93 8 88 2.38 31Se82 81.91671 9.19 1,Si3 0 29.97377 3.12 25Mn55 54 . 93805 100.00 35B r;g 78. 91 833 50. 54 15 P31 30. 97 376 100. 00 ~e 더 53.93961 5.84 35B r81 80.91629 49.46 I6s32 31. 97 207 95.0 18 ~e56 55. 93 493 91. 68 &711 77.92 0 40 0.354 16S33 32.97146 0.750 2~e57 56.93539 2.1 9 하꾼 0 79.91638 2.27 l6S” 33. 96 787 4.21 5 26Fe58 57.93327 0.3 1 하 81. 91 348 11.56
부록 I (계속) 원소 질량 원자상대 원소 질량 원자상대 원소 질량 원자상대 빈도(%) 빈도( %) 반도( %) 하 r3 82. 91 413 11. 55 Pdl05 l04 . OO 沿 22.23 52T e126 125 . 9033 18. 71 하 83.91151 56. 90 ,sPd 106 105 . 90349 27.33 s2T e128 127 . 9045 31. 79 하군 85.91062 17.37 ,6Pd 圈 107.90389 26.71 s2T e130 129 . 9062 34.49 3;Rb 8 5 84.91180 72. 15 ,sPd110 109 . !Xl51 6 11.81 꼬 I12; 126.9045 100 .00 31Rb87 86 . 90919 27.85 ~1Ag 101 106 . 00509 51. 3 5 s.X e1u 123. 90 61 0.096 38S 촌 83.91343 0.55 .,Ag 10 9 108. 따 175 48.65 겁 Xe126 125 . 90~3 0.090 36S 곤 85.90928 9.87 ,sCd106 105 . 寧 1. 21 s.X e128 127 . 9035 1.9 1 9 38S r87 86.90889 7.02 ,aCd108 107 . 90419 0.8 8 s.X e129 128 . 9048 26.44 3SS r88 87.90563 82.5 ,8Cd110 109 . 90301 12. 39 s.X e130 129 . 9035 .j . 08 39Y89 88.9069 100.00 .aC d111 110.!X l41 9 12. 75 다 Xe131 130 . 9051 22.18 ‘g꼰 89. 90 471 51. 46 ,8C d112 111.90276 24.07 s.X e132 131. 9042 26.89 ,,;z.r91 90.90564 11.23 ,aCd113 112 . 90441 12.2 6 54Xe134 133 . 9054 10. 44 4 ,;z,곤 91.90504 17.11 .a C d11 ◄ 113.9 03 37 28.86 s.X e136 135 . 9072 8.87 4g ? 93.90632 17.40 48CdIIC 115.!X) -47 6 i.5 8 s;Cs133 132 . 9054 100. 00 必곤 95.90829 2.80 49In”3 112 .9041 4.23 56B a130 129 . 9063 0.101 ,iNb 93 92 . 90638 100.0 0 ,Jnl lS 114 .9039 95. 77 s6Ba132 131 . 9050 0.097 ◄ 2Mo92 91. 90681 15.86 soSn112 111 . 9048 0.95 s6Ba13- 1 133 . 9045 2.42 ,Mo94 93 . 90509 9.12 soSn114 113 . 9028 0.6 5 ssBa13 5 134 . 9057 6.5 9 ,zMo95 94 . 90584 15.70 soSn115 114 . 9034 0.3 4 s6Ba136 135 . 9046 7.81 ,zMo96 95 . 90467 16. 50 soSn116 115 . 9017 14.24 s6Ba137 136 . 9058 11. 32 ◄ 2Mo97 96 . 90602 9.45 soSn117 116 . 9030 7.57 s6Ba138 137 . 9052 71. 66 42Mo98 97 . 90541 23. 75 soSn118 117 . 9016 24. 01 s1La138 137 . 9072 0.089 .Mo lOO 99 . 90748 9.6 2 50Sn 119 118 . 9033 8.58 s1La139 138 . 9064 99.911 Ru96 95 . 90760 5.5 soSn120 119 . 9022 32. 97 ssCe136 135 . 9072 0.1 9 3 ..R u98 97. 90 529 1.9 soSn122 121. 9035 4.7 1 58Ce 璃 137 . 9060 0.250 44RU99 98.90594 12. 7 soSn12< 123 . 9053 5.98 saeeuo 139 . 9055 88. 48 «Ru100 99 . 90422 12.7 s1Sb121 120 . 9038 57.25 saCe142 141 . 9093 11. 07 Ru101 100. 寧 17.0 s1Sb123 122 . 9042 42.75 s9Pr141 140 . 9077 100. 00 ..R u102 101. 懿 31. 5 52Te1211 119 . 9040 0.089 60Nd1•2 141. 9078 27.09 ..Ru 1°' 103. 寧 18.7 52Te122 121. 9031 2.46 60Nd143 142 . 9099 12.14 .sRhlG 3 102. 綴 1 100.0 52Te123 122 . 9043 0.87 60Nd1~ 143 . 9101 23.83 .J>d1 02 101. 寧 l 0.9 6 s2Te124 123 . 9028 4.6 1 60Nd1 ◄ 5 144 . 9126 8.2 9 ~d1°' 103.00401 10.97 szTe125 124 . 9044 6.9 9 60Nd146 145 . 9132 17.26
부록 I (계속) 원소 질 량 ` 원자상대 원 소 질 량 원자상대 원소 질량 원자상대 빈도( % ) 빈도(%) 빈도(%) roN d 8 147 . 9169 5.7 4 ~r168 }67 . 9324 27.1 760s18 9 188 . 9582 16.1 00N d150 149 . 920 9 5.63 r,aEr '7 0 169 . 9355 14.9 76Q sl9 0 189 . 9585 26. 4 G2~ f fi14 4 143 .91 2 1 3 .16 69T m'ro 168 . 9342 100. 0 760s19 2 191. 9615 41. 0 62s m1 149 . 9149 15. 07 70Y b16 8 167 . 9339 0.1 4 nlr191 190.9609 38. 5 G2S m 8 147 .91 49 11. 27 10Y b 0 169 . 9348 3.0 3 까 rl93 192.9630 61. 5 G2S m 9 148 . 9172 13. 84 ,oYb171 170 . 9364 14. 31 78Pt 190 189 . 9600 0.0 1 2 62 Sm 園 149 .9 1 73 7.4 7 ;oY b11 2 171 . 9364 21. 82 1sPt 192 191 . 9611 0.7 8 62S m152 151 . 91 98 26. 6 3 ;oY b173 172 . 9382 16. 13 7 8P t 1 인 193 . 9627 32. 8 .2S m15' 153 . 922 2 22. 53 ;oY b174 173. 93 89 31. 84 nl't195 194 . 9648 33. 7 63E u151 150 . 9 1 99 47. 77 70Y b176 175 . 9426 12.73 n!'t'96 195 . 9650 25. 4 ~U153 152 .92 1 3 52.23 11L u115 174 .94 08 97. 4 18Pt 198 197 . 9679 7.2 ..G d15 2 151 . 919 8 0.20 11L u 6 175. 94 27 2.6 ~ul'll 196.9665 100. 0 o1G d,,. 153 . 920 9 2.1 5 nH f' 173.9401 0.1 9 soHg '96 195 . 9658 0.1 4 6 .,G d15 5 154 . 922 6 14. 73 12H fH6 175. 94 14 5.1 9 soHg 198 197 . 9667 10. 02 s.G d15 6 155 . 922 1 20. 4 7 12H f172 176 . 9432 18. 47 80Hg 199 198 . 9683 16. 84 ,;,G d15 7 156 . 9240 15. 6 8 nH f178 177 .9437 27.15 soHg 200 199 . 9683 23. 13 6,G d15 s 157 . 924 1 24.87 12H fi;g 178 . 9458 13.75 soHg 201 200 . 9703 13. 22 ,;,G d16 0 159 . 927 1 21. 90 12H f160 179 . 9466 35.22 soHi °2 201 . 9706 29.80 65T b159 158 . 925 4 100. 00 7JT a180 179.9476 0.0 1 2 60H 균 203 . 9735 6.85 GJ)}•lw 155 . 924 3 0.0 5 2 7JT a181 180 . 9480 100. 00 s1Tl203 202 . 9723 29. 50 ~}'158 157 . 924 4 0.0 9 0 1,W 160 179 . 9467 0.1 3 5 s1 Tl205 204 . 9744 70. 50 ..0y160 159 . 9252 2.2 9 1,W182 181 . 9482 26.4 82Pb 찍 203 . 9731 1.5 ~Y161 160 , 9270 18. 88 1,W183 1s2 . 9503 14.4 82Pb200 205 . 9745 23.6 ~Y162 161. 9268 25. 53 1,W1114 183.9510 30. 6 82Pbw 206. 97 59 22.6 ~y163 162 , 9288 24. 97 1,W186 1s5 . 9544 28. 4 82Pb208 207. 97 67 52.3 ~y161 163 , 9292 28. 18 75Re185 184 . 9530 37.07 83Bi 209 208 . 9804 100. 0 61 Ho165 164 . 9304 100. 00 75Re187 186 . 9558 62.93 90Th232 232.0381 100.0 ~r162 161. 9288 0.1 3 6 760s1111 183 . 9526 0.018 92l] 234 234.0 4 10 0.0058 ~f164 163 . 9292 1.56 1 6 Q뿐 185 . 9539 1.59 92U235 235. 04 39 0.7 2 0 ~r166 165.9303 33.4 76 0.뿐 186 . 9558 1.64 92lF' 238. 05 08 99.274 ~r157 166 . 9321 22.9 76( )slS 8 187 , 9559 13.3
부록 II 자연방사성동위원소의 반감기와 붕괴형 (理科年 表 , 1981) 원소 반감기 붕괴 분기비 방사선에너지 유형 (강도비) 1J<: 40 1.26 X1 01 ' /3- 89 1.31 4 c, r 11 1.46 0 23V50 6X l 015y c, Y 70 1.55 /3- 30 31R b 81 4. 8 X I01°)' g 100 0.274; r( 무) 491n11s 5.lX 1014y /3- 100 0.4 8 57La138 l.12 X lQ 1 1y E, r 1.4 3(10) g 0.2 1 Y 0.8 1 (6) S8Cel42 >5 . 1 X l01 꿉 a 100 1.5 60Nd1~ 2.4X l0 15y a 100 1.83 쇼 ;m147 l.05 X l0 11y a 2.2 3 71Lu176 2. 2 x 1Q1Dy f3- 0.43 7,e 0.2 0 2, 0.3 0 6 73Ta1so )5X l0 12 y 75Re187 4.3 X l Q1°y f]- 0.003 7ft 192 >101'y a 100 2.6 Ptl9 0 5.4 X l 0y a 100 3.18 80H 균 8.l m /3- 1.3 81Tl2D6 4.20m f3- 1.52 ; r( 무) P 배2 B 10.64h f1- 0. 3 5 (~88) , 0 . 59 (~12) y, e 0.2 3 860(80) {50% 다, 0.2 9 9(5) {~23% 다, 0.115(2), 0.1 7 6(1) P溫 26.8m {J- 0.6 7 , 1.03 7 0.053236, -0.24192, 0.2578, 0.2 9 522, 0.35199 • 4쿈 >2X 1011 \r a 3.0 0 B i溫 5.013d g 99 1.160 a 2x10 기 4.6 9 , 4.65, r( 무)
부록 II (계속) 원소 반감기 I 붕괴 1 분기비 I 방사선에너지 유형 (강도비) B i 談 2.1 5 m a 1 99. 68 I 6.622(84), 6.278(1 6 ) e 0.3 2 r I I O.3 5 1 B i 器 60. 60 m I 13- I 66. 3 I 2.2 5 3(~97), 2.1 5 , 0.7 2 , 0.8 3 , r I I 1. s1, 2 . 2 a I 33. 7 I 6.0 8 6(27), 6.0 4 7(70) r I I 0.0 4 0 B i 益t 199m 13- I 99 I 1.65 (~77), 3.17(~23) a I 0 . 02 I 5 . 512 (45) , 5 . 448 (55) , 0 . 6094 (4) , 1.12 (1. 6) , 1. 76 (1. 6) r Bi2 1s 7m f3- Tl 쳇& 4.79m f3- 1.44 r 0.8 9 7 Tl 뿐C ' 3.lm f3- 1.80 (4), 1.29 (3), 1.52 (2) (의) r 2 . 614 (10) , 0 . 511 (3) , 0 . 583 (9) , 0.8 6 (1) (의) Tl § 썹 1.3 2 m p:- II 909.0. 92 II 01..29 69 7 , 0.78, 1.1, 1.3, 2.36 n I 0.0 2 112 Pb 溫) 22 . oy I 13- 0.0 6 1 r,e 0.0 3 0, 0.0 4 3 PPbb2il&0 m 36(.단 l)m /3nr- II 1lU0U0 I 01..0366 5(9, 2)0 ,. 0 80 3.,5 3 0(6.4) 0(4의, ) 0.425, 0.487, 0.764, 0.8 2 9 Poi ~ 3.05m /3a- I o~.120202 I 6.002 다만 ~10-4s aaa 8.0 0 Af 16 3X 10- ◄ s 7.79 Af lB 1.3s 99 I 6.65(~6), 6.7 0 (~94)
부록 II (계속) 원소 반감기 붕괴 분기비 방사선에너지 유형 (강도비) 13- 0.1 At2 1 9 0.9m a 97 6.2 7 /3- 3 66 Rn2A 1n9 3.9 2 s a 100 6.813(82), 6.5 4 703), 6.4 1 9(5) Y 0.3 9 5(10), 0.2 6 8(11), 0.2 3 9, 0 .18 6. 0 .12 0 ( 의 ) Rn 窓 52s a 6.2 8 2(99. 7) , 5.7 4 0 r 0.5 4 2 Rn 꿈 3.8 2 5d a 5.48 2 r 1.510 B7Fr 器 22m 11- 1.15 a 6 X1 0-3 5.3 4 0 r, e 0 .05 0 (40) , 0.0 8 0(24), 0.2 2 ( ~ 3)' 0.31(~0.8 ) 88Ra fil: 11. 43 5d a 5 . 744 (9 .1) , 5 . 712 (53 . 7) , 5.600(26. 0) , 5.5 3 2(9.1), 5.4 7 2(3. 82 ) 84Po 福 138. 4d a 100 5 . 298 (99 . 9) r, e 0.802{0% 디 Po i!J:, 0.5 2 s a 7. 434 ( 99 ) , 6 . 88 ( 0 . 5 ) , 6 . 56 ( 0 . 5 ) r 0.56, 0.8 8 Po 꿈 0.3 0 4µ s a 100 8. 785 (10 0) Po~'c- 164µs a 7.680 Po~t 1.778ms a ~100 7.365 p- 5X 10-5 Po우& 0.1 4 5s a 6.7 7 4 Ra 쵸 1602y a 4.7 7 7(94. 2) , 4.591(5.7) r 0 . 186{~35% 디 (5. 7) , 0.260 Ra 꾼마 1 6.7y 8- 0.0 5 5; r( 무) 타\ .cm 21. 2y /3- 98.8 0.0 4 55 a 1.2 4.949(49), 4.937(36), 4.8 4 9(6)
부록 II( 계 속 ) 원 소 반감기 붕괴 분기비 방사선에너지 유형 (강도비) 2M2s8T h 2 6.1 3 h 13- 1.1 1(53), 0.4 5 (~13), 2.1 8 (~10), 1. 850 (9) , 0 . 640 (8) , 1. 700 (7) Y,e 0.9 6 , 0.9 0 8(25), 0.1 2 9, 0.058(70) h 짧A c 18 . l7d a 100 6 . 036 (23) , 5 .976(24) , 5. 755 (21) , 5.705(9) r,e 0.0 4 98(1 5 ), 0.2 3 5 , 0.2 5 6, 0.1 1 3, 0.1 0 04, 0.0 6 16 2R2d8Th 1.9 ly a 0.0 8 45(1. 6 ), 0.1 3 7, 0.1 6 9, 0.212 f 훈 8.0 X l0 4y a 100 4.685(76.3), 4.6 1 8(23. 4) y,e 0 . 068{98% 다, 0 .14 2, 0 .18 4 t앙 25. 52 h /3- 0.3 0 2(52), 0.218(20), 0.1 3 8(22), 0.0 9 (6) ,, e 0.1 6 7(2) , 0.122(2), 0.1 0 7(7), 0.0 8 5(100), 0.0 6 3(40), 0.0 5 9(40) 5.4 2 4(2. 3) Y 0.3 3 0(6.3), 0.2 6 8(15), 0 .15 4 (5) , 0 .14 8 ( 15) , 0 .14 4 (4) , 0 .12 2 (2) 2T2h 』X 3.6 4 d a 100 5.6 8 1(95), 5.440(4.9 ) r,g 0.24 1{ 12%e 가 . `h23 2 1.41 X 1 010y a 100 4.0 0 7(77), 3.9 4 8(23), 3.8 3 5 .Y 0.0 5 5 ` h 器 24. lO d 13- ~00 1.93 (66), 0.1 0 3(34) r, e 0.0 9 2 (1 5), 0.063(7), 0.0 2 9(7) a231 3.2 5 X 1 04y a 100 5.046(8.7), 5.0 1 8(23), 5.0 0 1 (28 ), 4.9 38(27), 4.7 2 4( 10 ) r,e 0.027, 0.102, 0.3 3 1 꿈 r 1.25m /3- 2.31 (96 ) r,e 1.0, 0.76 IT 0.63 92U 짧 2. 4 7X 10 낭 a 100 4.768(73), 4.718(27), 4.518(0.3 ) r, e 0.0 1 8, 0.053, 0.09, 0.1 2
부록 II( 계속) 원소 반감기 붕괴 분가비 방사선에너지 유형 (강도비) U 盤 7.13X l0~ a 4.394(62), 4 . 362 (12 ) , 4.3 6 8(6). ; 4.2 1 4(~6) Y 0.18, 0.37 U 뿐 4. 5 1 X l09y a 100 4.1 8 2(77), 4.1 3 5(23) r, e 0 . 048(99% 디
부록 Ill 인공방사성동위원소의 반감기와 붕괴형 (y년, d 일 , h 시, m 분, s 초, a, a 붕괴, 8, 8 붕괴, Y, 7 선, EC, 궤도전자포획, IT, 핵 이성체 전이) 핵종 반감기 붕괴유형과 에너지 oI1 I 12m 13-0.78 1H3 12.262y p-o .01 so; r( 무) 4Be7 53. 5d EC; r00.3 % ) 0.4773 Be10 I l. 5 X I06y I 13-0 . 555; r (무) GC14 I 5730y I 13-0 .155; r (무) 1N16 I 7.1 4 s I 13-10.40(28%), 4.3 9 (54%), 3.3 2(1 8 %); r6.10(100]' 7.1 0 (8) a01 9 I 29.ls {3- 4. 5( 30%). 2.9(70%); ro. 20 0( 10 0). 1.37 [ 67 ] · 0.112[ 4] 9f1 8 I 109 . 7m 13+ (9 7%) 0.649;EC(3%); r( 무) 11Na22 I 2 . 62y /3+ (9 0. 6% ) 0.5 4 , 1.83 ( );EC (9. 4% ); rl. 28 Na24 I 14 . 96h 13- 1. 39 4; rl. 37 (1 0 0), 2.75(102] 12M 균 9.4 5 m {3T 59(42%), 1.75 (58%); r0 .834 (7 아 1. 015 〔却 1~126 I 7.2X 1 05y {3+ (84%), 1.1 6; EC06%); r l. 84 (1 0 아 1. 10 〔다 2.9 4 (0. 4] Al28 I 2.31m 2.87; rl. 78 1iS i 31 I 2 . 62h {3T 471; rl. 26 (0 . 07%) 1sP3 2 I 14 . 28d /3-1. 711; r( 무) P33 I 24 .4d 13-0 . 249; r( 무) 16S 35 I 87 . 9d p-o .16 7; r( 무) 17Cl36 I 3 . 08 X1 05y {3- (98.3 % ) 0.714;EC(l. 7% ); r Cl38 I 37 . 29m p-4 .81(53%). 1.1 1(31%), 2.77(16%); rl. 60 (100], 2.15(130] '1sA r:r1 I 35 .ld EC; r( 무) A 곤 269y {3- 0 . 565; r Ar41 I 1.8 3 h {3-1.2 0(99+%), 2.4 8 (0.9%); rl. 29 19K42 I 12 . 36h p-3 .55(82%), 1.9 9(18%); rl. 53 , 0.32 Ca'1 I 1.1 x 105 y EC; r( 무) 20Ca'5 I 165d p-o . 254; r (무) Ca47 I 4.54d p-o .66(83%), 1.9 407%); rl. 31 (65 ), 0 . 83 〔탸
부록 m( 계속) 핵종 반감기 붕괴유형과 에너지 0 . 48 〔히 21Sc46 83.9d I go .3 5 7, 1.48(O.004%); 1 0.885, l.l19 22Ti s1 5.79m I 13-2.13(94.5%), 1.5 (5. 5% ); ,0.323, o . 928( 중) 0 . 605( 중) 23V48 162d I 13+(56%) 0.694;EC(44%); ,0.99 (1 0 叫 1.3 1(98], 2.%[ 2. 6] ~crSl 27.8d I EC; ,0.325(9%) Mn53 3.7 X l06y EC;r( 무) 려W n” 303d EC; !0.840 Mn56 2.576h p-2 . 86 (50%) , 1. 05 (30% ) , 0. 7; 재 . 845(100). 1. 81( 29 . 탸 2 .13(1 5 . 3] 2s fe55 2.60y EC; /3+; r( 무) Fes9 45. ld p-o .271(46%), 0.4 6 2(54%), 1.56 ; r1. 10 , 1.29 , 0.19 () Co57 270d EC; r0.014(9%), 0.122(87%), 0.13601% ) , 0.692(0. 14 %) T/C o58 71. 3d p+(l5% ) 0.472;EC(85%); r0. 81 Co60 5.2 6 3y p-o . 312, 1. 4 8 (미 ) ; r1. 17 28, 1. 3325 Co60m 10.47m p-(O . 28%) 1. 56; IT (99 + %) , rO . 0589 28Ni 63 92y p-0 .061 Ni6 5 2.564h p-0 .60(29%), 1.0 1(14%), 2.1 0 (57%); r0.37( 중), 1.10 , 1. 46 29CU64 12.88h p-( 39%) 0.5 7 1; p+ (l9% ) 0.6 5 7; EC(42%) ; rl. 35( 약) 3,; l,n6 5 57m /3- 0.897; r( 무) Zn69m 13.Sh IT, r0. 43 8 31Ca., 77.9h EC; /3+; r0 . 093, 0 .18 5, 0 . 296 Ga72 14.lh /3- 0 . 64 (42%) , 0 . 96 (31%) , 1. 51; rO . 630, 0 . 835, 2.20, 2.51 32Ge71 1l.4d I EC; r 따 s76 26 . 4h /3- 2 . 97 (50%) , 2 . 41( 31 %) , 1. 76 (16%) , 0 . 36; r0.561(10 이, 1.2 1@] , 0.65(9] As17 38 . 7h I 13-0 . 679; rO . 245, 0 . 525
부록 Ill( 계속) 핵종 | 반감기 1 붕괴유형과 에너지 uSe75 I l20 . 4d I EC; 8+; r 0 .l3 6, o . 269, o . 281, o . 405 36B r8 2 I 35. 34 h 1 p-o .4 4 4; r0.777[10 鬪 0. 55 3(78), 0 . 618 園), 1. 04 (35) . 1. 32 떠〕 , 0 . 698 [34 ] 36 K 폰 10 . 76y I p-o . 672; r0 . 52 J1 Rb 86 I 18. 66 d I f]T 78(~84% ) , 0.7 1 ; rl. 08 38 S 촌 64 . 0d I EC; r0 . 513 S 곤 52. 7d I p- 1. 4 63; r0. 91 3 Sr!l0 27. 7y I 13-0. 54 5; r 39y !l 0 64 . 0h I 13- 2 . 26; rl. 73 (미 ) Y91 58 . 8d I /30 . 33. 1. 54; rl. 19 (미 ) 40Z r 95 65. 5d I 13- 0. 3 6 5(43%), 0.396(55%); r0.235(NB96m), 0.722, 35d I0/ 3.-7 o5 .4 1 58, 0 . 93 (근) ; r0 . 753, 0 . 768 41N b 95 42M o 99 66.7h I 13-0 .4 4 5( 14 %), 0 . 87( 중), 1.2 3(85%); r0. 04 1 (23 0] ' 0.182, 0.74 1( 10 이, 0.7 8 0 43TC 9 7 2 . 6 X l06y I EC Tc99 2 .12 x 105y I 13-0 . 290; r (우) Tc99 m 6.04h I IT, r0. 00 21 . 0.1405, 0.142( 미) 41Ru97 2.88d I EC; rO. 11 , 0.2 1 6, 0.325 Ru103 39.5d I 13-0.227(~89%), 0.12(~7%), 0.6 8 ; r0.498, 0.610 Ru100 l.OOy /3- o . 0392; r 45Rhl05 35.88h /3- o.2s(~10%), 0.57(~90%); r0.315 4sP d109 13. 6h /3-1.02 ; rO . 31~0.77( 약) 47A g 110 24. 5s /3?. 24, 2.87; r0.66 (1副, 0.7 2 , 0.81, 0.8 8 , 0.9 4 (5) Ag llO m 255d p-(9 8%) 0.0 8 7, 0.5 3 0(43%); r0. 66 , 0.88 IT(~2%). r0.116 Ag lll 7.5d /3 ~0. 69 , 0.7 9 , 1.04 ; r0.24, 0.34 48Cd5 2 . 21d I p-o . 58 (42%) , 1.11 (58%) ; r0 . 49 血끽 , 0. 523 (43] Cdl15m 43d I 13-1 .61 (~98%); r0.49(1 이, 0.94(7 사, 1.3 0@] InIl4 72s I p-(98 %) 1.98 4(98%); r l. 30( 약); /3+ (0.004%) 0.4 0 ; EC(l. 9% ) In114m 50. 0d IIT(96.5%), r0.192;EC(3.5%); r0.556, 0.1 2 2
부록 m( 계속) 핵종 반감기 | 붕괴유형과 에너지 Inll6m 53. 99 m I /3- 0.60(21%), 0.8 7 (28%). 1.00 (51% ); r0. 40 6, 1.09 . 1. 27, 1. 49, 2 . 09 soSnll3 115d I EC; r0 . 255 (2% ) Sn121 27 . 5h /3- 0 . 383; r s1Sb122 2.80d /3- (97%) 1.4 0(63%). 1.9 7(30% ): r0.564[ 6 6), 0 . 69 繼 .4 ); /3 + (~0.01%) 0.5 7;E C(3. 0% ) ; r l. 14( 약) Sb1u 60 . 4d I p-o . 61 (49%) . 2 . 32 (21%) r0 . 603, 0 .122. 1. 69 Sb125 2.7 l y I p-o .13(29%), 0.30(45%) r0.43, 0.4 6 , o.60 52Tem 9.3 5 h I p-o . 6 9 5(99%); r0 .4 18 (1 0 이, 0.3 6 0(1 5 ]' 麟 15(11) Te129 68. 7m I /3T 45(7 1%), 0.9 9 05%), 0.2 9 00% ); r0.027, 0.21 . 0.48 Tel29m 34.ld I IT, r0. 10 6 Te132 77.7h /3- ~0.1(~40%), 0.2 2( ~60% ); r0.053, 0.231 SJ11 25 60.0d I EC; r0.035 Il28 24.99m I f]-( 93.6%) 1.13 , 1.6 706%), 2.12(76%); r0.4 5, 0.5 4 , 0.99; EC(6.4%); r0.7 5 I131 8.05d I /3- 0. 33 5(9.3%), 0.608(87.2 % ); r0. 18 , 0.2 84, 0.3 6 5(82%), 0.638 I132 2.26h I /3개 . 9, 1.16 , 1.53 , 2.2 1 ; r0.5 3 , o.67 떠), 0.7 8(7 5] ’ 0.96 54xe133 5.2 7 0d /3개 .347; r0.081 ssCs134 2.0 4 6y /3개 . 086(20%), 0.665(75%); r0.605 (1 0 야 0.7 96 [ 91 ] ’ 0.8 0 (1 8 ]. 麟 7 (1 3 〕 Cs137 30 . 0y /3- o . 514 (92%) , 1.18 (8%) ; r0 . 6616 (Ba 137m) 56Ba1J 1 12.0d I EC; r0 . 498 (1 0 이, 0.123(73), 0.216(55), 0.373[ 36 ] Ba133 7.2 y I EC; r0.355(100], 。節〔 34 〕, 鬪 8 〔 20) Bal33m 38 . 8h I IT, r0 . 0117, 0 . 2755 Ba139 82 . 9m /3- 0 . 82 (19 %) , 2 . 23 (66%) , 2 . 38 (15%) ; r0 .163, 1. 43 Ba140 12.8 0 d /3- o .48(25%), o.600%), o.9, 1.0 2(60%); r0.537@ ], 0 . 030(1 인, 0.16, 0.4 4 57LaIO 40.22h I /3- 0. 42 ( 16 %), 0.86(12%), 1.1 5(20), 1.36 (30%), 1.62 ( 14 %), 2.20(8%); r l. 60 (1 0 이, 8.8 2 @ ],
부록 Ill( 계 속) 핵종 반감기 붕괴유형과 에너지 0.49(4 인, 0.33[2 1 ] 58C e”I 32.5d I p-o . 4 3 5(70%), o.580(30%); r0.145 Ce 따 33h I 13- 1. 4 0(37 % ), 1.13(40%), 0.74; r0.2 9 4( 10 0), o . % 〔 2 이 , 0.67@ 띠, 0 .72 〔 2 끽 Ce144 285d I 13-0. 17 5(20% ) , o.2 4 0(8%), o.3 0 9(72%); r0. 03 4, 0.0 8 0, 0 . 133( 강) s9P r142 19. 2h I p-o . 6 4 (4%), 2.1 7 (96%); rl. 57 2 Pr143 13.5 9d I p-o . 9 3 2 ; r Pr144 17.27m /3개 .80( 중), 0 . 29( 중), 2.98(97.7%); r0.691( 강), 1. 49, 2. 18 60Nd l 47 11. ld I /3- o. 23 (16 %), o.3 8 08%), o.8 1 ( 66 %); r0.091 (29 ] ' 0.321(3 이, 0.533(1 3 ] N dl49 1.8h /3건 .95, 1.1, 1.5; rO .03 0~0. 65 0 61P mm 2 . 6y I 13-0 . 223; rO .12 1 Pm149 53 .lh /3-1. 05; rO . 285 62S mI S3 46. Sh /3개 .64(~38%), 0.7 0 (~40%) 0.8 0 (~22%); r0 . 070 〔파’ 0.103 〔 1 副 ~ Ul 52m 9.2 h I p-(7 5%) 0.5 5 , 1.55 , 1.88 ; r0.344(10 아 0.980(40], 1 . 32(10 이; 8 기약 )0.82; EC(25%); r0.122 〔쩌 0 〕, Eu 벼 16y I0 /3 . 8개7 .3 2 [53 (9 208]% . ) 0, . 9061 . 5(54 0( 030] ,% )1 ,. 420 [ .키 8 3이 (2 0%) ; rO .12, 0 . 72, 1.27 Eu1ss 1. 8lly I 13-0 .15 (80%) , 0 . 24 (20%) ; rO . 087, 0 .10 5 6lG dl53 242d I EC; rO . 069@] , 0 . 098 (100) , 0 .103 (100] Gdl59 18. 0h I p-o . 95(~80%), 0.6 0 (~20%); rO .36 4, 0.056 65Tbl60 72. ld /3~ 0. 3 0 , 0.4 6 , 0.5 6 (32%), 0.8 6 (30%), 1.71 ; rO.087(100), 。.3 。〔 200), 0.8 8 [ 20 0] ' 0 . 97 〔 26 。〕’ ss1JH)oy1l66 66 226.3.92hh II 1g 1.3 -1o18 . .(47 12 61, (아3o7 .%881.), ,2 7l .〔21副5.8; 4r(04.70%94)~; 1r.00 .2 0 8 血 5). 1.38 (1 0 ), 1. 54 〔인 ~rl69 9 . 6d I /3- o. 33; rO. 0084
부록 m( 계속) 핵종 반감기 1 붕괴유형과 에너지 Er111 7.5h I 13-0 . 55( 중), 1.05 (93%), 1. 43( 중) ; r0 . 308 〔 6 아 69Tm l34d I/0 3.- 2o9 .6 8 8따 (〕2,4 %0) ., 1102 . ( 916이8 ,(7 60%.1) 2; 4 r[0 8 .. 05 8)4 2 10Ybl75 4.2 d /3- 0. 07 (15%), 0.35(5%), 0.4 6 8(80% ) ; r0. 11 4[ 31 ] · 0.283@ ], 0.114(31), 0.283@ ], 0.3 % [ 10 0] 71Lu177 6.7 5 d I 13-0. 18 (7%), o.38(3%). o.497(90% ) ; ro.113(100] ' 0.208 〔 22 이 12Hf l75 70d I EC; r0.089(40), 0 . 343 (1 00 이, 0.4 3 3(1 6 ] Hf lBI 42.5d I 13-0. 40 , 0.4 0 8(93.5%); r0.13(7). 0.4 8 2(1 4 ] 73Ta182 115.ld /3- 0. 36 , 0.4 4 , 0.5 1 ; r0 . 068 園), 1.1 2 2(1 0 0] ' 1 . 222 園〕’ 1. 2 31 (50] nW185 75d I /3- o . 43; r w187 24.0h /3- 0.3400%), 0.63(70% ) . 1.33(20% ) ; r0. 13 6, 0.4 8 2, 0.6 8 6 75Re186 88.9h I /3-(92 %) 0.9 3 (22% ) , 1.0 7(70%); r0. 13 7, 0.627, 0 . 764; EC (8%) ; rO .12 3 ReI86 16.7h I 13-< l. 9( 중), 1.96 (20%), 2.12(79%); r0. 15 5, 0.6 3 3, 0.4 7 8, 0.931 760s191 15 . 0d I /3- o .14 3; r0 . 042, 0 .129 0s193 31. 5h /3개 .68(10%), 0.8 6 ( 12 %), 1.0 0(5%), 1.06 (33% ) , 1.14 (40%), r0. 07 3, 0.139, 0.251, 0.2 8 1 . 0.321 . 0.4 6 1, 0.558 nlr192 I 74.2d I p-(95 .5 % ) 0.6 7 ; r0.30 頭터, 0 . 317(10 이, 0 . 468 〔 6 사 EC(4.5%); r0.206, 0.4 8 5 Ir 며 | 17.4h I /3- 0.43(~8%), 0.98(10%), 1.91 ( 15 %), 2.2 4 (66%); r0.293[ 5) , 0 . 328@ 긴, 0.643(6), 0.937(2.9] ' 1. 1 織 .9 〕 1J' t197 I 18h I p-o . 468, 0.4 7 9, o.670; r0.077 園), 0.191 (3 .9]` 0.279(1) 7 먀 u196 1 183d I EC; r0 . 031, 0 . 099, 0 .129 Au196 I 2.967d /3- o. 29 , o.96, o.37; ro.412(100), o.6 7 6(1.3], 1. 09(1. 25]
부록 Ill( 계 속) 핵종 반감기 1 붕괴유형과 에너지 Au199 3.15d /3개 .460(6.4%), 0.302(69.3 % ), 0.2 5 1(24.3%); r0.050, 0.158, 0.2 0 8 Hg l91 65h I EC; r0. 07 7(18%), 0.191(2%), 0.2 6 8(0. 15 %) 80H g203 46.9d I p-0 .210; r0.279 81 Tl 如 3.8 l y I p-(~ 98%) 0.7 6 6;EC(~2%); r 93N p239 2.346 d 1/3 - 0.070 (20% ), 0. 3 27(35%), 0.382(21%), 0.439(16%); rO . 106(5 이, 0 . 2 짝 28), 0.2 7 8(31] 다 수 94P u239 2.4 4 X lO 'y I aS.149(72.5%), 5.1 3 4 0 6. 8% ), 5.09600.7%); rO . 0383 (1 3 이, 0 認。〔 320 〕. 。끄 O 〔 70), 0.207@ ], 0 . 34 〔幻’ 0 . 38(6 이, 0 . 42(40] 95A mUI 458y I a5. 43 9(12.8%), 5.48 2(85%); rO. 02 6, 0.0 5 96, 0.0 3 3, 0.0 55 96 Cm 2 』 2 162. 5d a5 . 965( 미), 6.066(26.3 % ), 6.110(73. 7% ); r0. 04 4 Cm2 4- l 17. 6y a5 .66 1( 미), 5.759(23.3%), 5.8 0 1(76.7%); ,0. 04 3, 0 .10 0 () , 0 .150 (중) 91B k24 3 4.6h a(0.15%) 6. 20 ( 17 ), 6.55(53). 6.72 〔 3 。 l ,0.0 4 2~0. 54 ; EC(99+ % ); ,o.74, 0.84, 0.96 Bk24 9 314d a(0.002%); r0.32; 13-(99+%); 0.1 1 48 9sC f32 2.646y a(97% ) 6.0 ( 15%), 6.12(82%); r0.0434, 0.100; 자발 핵분열 (3%)
부록 IV 지질연대표 지질시대 경계 Ma 대 (Era) 기 (Pennd) 세 (Ep o ch) 기 (Age) 1 2 3 제 4 기 홀로세 (Ho locene) 0.01 0.0 1 신생대 Qu ate r nary 풀라이스토세 Calabria n 1.8 2 2.0 1.6 Cenozoic Pleis t o c ene 신제 3 기 플라이오세 Pia c enzia n 3.4 Neoge ne Pli oc ene Zanclean 5-5 .5 5 .1 5.3 (Tert iar y } 마이오세 Messin i a n 6.5 Mi oc ene Tort on ia n 11. 3 11. 2 Serrav a ll ian 15.1 Lang hian 16.6 Burdi ga lia n 21 .8 Aq u it an ia n 23 24 .6 23. 7 고제 3 기 울리고세 Chatt ian 32.8 30.0 Paleog e ne Olig o cene Rup e lia n 34 38.0 36. 6 (Tert iar y ) 에오세 Priab onia n 42 .0 40 .0 Eocene Bart on ia n 43 .6 Lute t i an 50.5 52. 0 Yp re sia n 53 54. 9 57. 8 팔레오세 Thaneti an Paleocene (Seland ian ) 60.6 Unnamed (Seland ian ) 60. 2 63. 6 Dani an 65 65 66.4 중생대 백악기 후기 Maastr ich - 65 97.5 97. 5 Mesozoic Creta c eous tian 초기 Albia n 113 113 Ap tian 119 119 BHaarurtee mr i viaina n 112315 I112341
부록 W( 계속) 지질시대 경계 Ma 대 (Era) 기 (Pen·od) 세 (Ep oc h) 기 (A g e) 1 2 3 Valang inian 138 138 Berria s ia n 130 144 144 쥬라기 후기 Tit hon i an 150 152 Jur assic Kim merid - 156 156 gian Oxfo r dia n 150 163 163 중기 Callovia n 169 169 Bath o nia n 175 176 Bajo c ia n 181 183 Aaleni an 178 188 187 초기 Toarcia n 194 193 Plien sbachi an 200 198 Sin e muria n 206 204 Hett an g ian 204 213 208 트라이아스 후기 Noria n 225 225 기 Trias sic Cam ian 229 231 230 중기 Ladi ni a n 238 235 Anisia n 239 243 240 초기 Scy thian 245 248 245 고생대 페름기 후기 Tata r i an 253 253 Paleozoic Permi an Kaza nian Ufi mian 258 258 초기 Ku ngurian 263 263 Art ins kia n 268 268 Sakmarian Asseli an 290 286 286
부록 W( 계속) 지질시대 경계 Ma 대 (Era) 기 (Peri od ) 세 (Ep oc h) 기 (A g e) 1 2 3 후기석탄기 Gzelia n Pennsyl v ania n Kasim ovia n 296 (Late Car- Moscovia n bonif ero us) Bashkir ia n 320 320 ? 320 전기석탄기 Serp u khO \rian 333 333 Mi ss is s ip pian Vis e an 352 352 (Early Car- Toumais i a n 360 360 360 bonif ero us) 데본기 후기 Fammenia n 367 367 Devo nia n Frasnia n 375 374 374 중기 Giv e ti an 380 380 Eif eli a n 385 387 387 초기 Emsia n 394 394 Sie g e n ia n 401 401 Gedin n ia n 400 408 408 실루리아기 후기 Prid o li an 414 414 Silu r ian Ludlovia n 421 421 초기 Wenlockia n 428 428 Llandoveria n 418 438 438 오도뷔스기 후기 Ashg illian 448 448 Ordov ician Caradoci an 458 458 중기 Llandeli an 468 468 Llanvi rn ia n 478 478 초기 Arenig ian 488 488 Tremadoci a n 495 505 505 캠브리아기 후기 Tremp ea - leauan
부록 N( 계속) 지질시대 경계 Ma 대 (Era) 기 (Peri od ) 세 (Ep oc h) 기 (A g e) 1 2 3 Cambria n Franconia n Dresbachi an 523 523 중기 540 540 초기 530 590 570
2l 05연M0901대0 16 01I 이0E0o언 UYB0눈fn10 o II’ z P」 oPPL1? ?대 a』 ? t ~ (E0r代ka1)톱 五l 꾸 t RZlI 广 YBS tuuu쁘rr 기rzmPty(ei뜨aaa r紀ntni i o) n_d ~uYB I V Edariaa세E nc( pago世 r icaa) hnn VEadri ishntataPp기v e et A rner(u sn e gs期 una.ce o)mtba i £oab nor aradi nal nan d12m6135 100805630916國―5감 0eMa00 。s k s Huronia n H 0
3000 Y혼吉u AArr__az 2 UMB ES!Z R andia n Ran 009g繼뽀繼 4000 VA엿quJ r iri\ Sw Isuan I 寧寧霜ueHadean 盧 o d났t Hde 5000 I Pr참고문헌 1. Odin , G.S., D. Curry, N.H. Gale, and W.J. K ennedy (1 982), The Phanerozoic tim e scale in 1981 . In : G.S . Odin , ed., Numeii cal DaH11g in St,. al igr a ph y , vol 2, pp. 957-960. Joh n Wi le y, New York. 2 . Harland, W.B ., A.V . Cox, P.G . Llewellyn , C.A . Pic k to n , A.G . Smi th, and R. Walte r s (19 82), A geo log ic t ime scale. Cambrid g e Univ e rsity Press, p. 131 . 3. Palmer, A.R . (19 38), The decade of North Americ a n geo log y. 1983 geo log ic tim e scale. Geolog y, 11, pp. 505-504.
찾아보기
거 경신속도 284 고기후 25 3 고도효과 130 고령토선 219, 14 8 고수온 207 고지하수 136 광물 아이소크론 365 광상연의 성장곡선 468 광역변성작용 223 구로꼬 광상 297 그래뉴라이트 501 기수호 254 깁사이트 219, 148 L 난지도 523 납의 유실 386 딸원자 349 내륙효과 f30 냉각속도 345 느린 냉각가설 428 니오디미움 모델연대 510 C 다단계 연성장곡선 459 단계적 가열방법 377 단반감기핵종 451 단일스테이지 모델 459 대륙대 지 형 현무암 494
대보화강암 196 대폭발설 123, 440 돌로마이트 217 동결온도 383 동위원소 17 동위원소 분별 23, 51 동위원소 분별정수 52 동위원소 열연대 382 동위원소 지질온도계 53, 96 동위원소 평형분별 50 동위원소 희석법 357 동위원소 희석분석법 41 동화작용 178 디스코디아 390 2 레니움-오스미움 측정법 404 레이리 증류과정 72 루비듐-스트론튬 측정 법 362 루테 티움-하프니 움 측정 법 406 □ 마그마 멜트 304 마그마의 동화 497 마블마운틴 379 맨틀배 열 (Mantl e array) 399 모델연령 402 모세관 130 몬모리로나이트선 219 물-암석 상호반웅 180 미시시피 벨리형 광상 310
닌 반감기 349 반암동광상 198 방사성 손상 390 방사성동위원소 18, 346 방사성 폐기물 520 백암형 온천 164 변성수 150 병전운동 에너지 57 보동 연 358 부적합원소 483 불국사화강암 196, 504 불일치연령 386 불일치온도 223 붕괴계열 350 비와호 253 빙하기 254 人 사까나이 제 1 광상 297 사마리움 4 니오디미움 측정법 393 산소편이 140 산소퓨가시티 263 산크리스토발 열수계 185 산화형 대기 478 삼보광상 317 상동중석광상 204 석질운석 443 석철운석 443 석회암 212 소멸핵종 25, 452
소행성 443 속도지속 질량분석기 36 수화반응 310 순간적합성모델 449 순환수 130 슈레딩거 방정식 70 스케어가아드 관입암체 186 스트론튬 초생치 364 。 아르곤-아르곤 측정법 374 아이소크론 363 안정동위원소 19 안정동위원소 수문학 95 에어로졸 520 에피소드적인 납의 유실 390 연동위원소 성장곡선 392 연속합성반웅 449 열수 광화용액 304 열수계의 황동위원소 291 영양단계 337 영점에너지 ·7 0 오도와 하킨스 법칙 19 옥천대 232 온양형온천 164 와이라케이 138 우라늄(토륨)-연 측정법 384 우량효과 130 우주연대측정 446 우주연대학 442 운석 443
운석형 0 족기체가스 476 원소의 합성 440 원시지각 465 원시황 320 위도효과 130 유전영수 146 유체 구 광물간의 동위원소 평형 301 이단계 진화모델 402 이리도 스 민 404 이중지속 질 량분석기 37 이차 아이소크론 468 이차오염 519 일치연령 368 일치온도 223 임계동결온도 430 X 자철석계 화강암 195, 506 장군광상 271 전암 아이소크론 365 전자스핀 공명법 425 점토광물 219 접촉변성작용 224 중성자 여기법 361 중성자 프럭스밀도 375 중앙해 령 현무암 (MORB) 398 지각정체연령 508 지구대기의 진화 475 지구연대선 461 지구의 연령 453 지구의 진화 439
지열수 136 지질연대계 423 지질연대학 350 전동에너지 58 질량분석기 36 질량효과 77 질산화반웅 331 질소고정반웅 331 질소 동위원소 329 大 처어트 216 체르노빌 52l 구 카보나타이트 261 칼륨-아르곤 측정법 369 칼륨변질대 198 케로겐 332 콘드라이트 443 콘코디아곡선 388 콘코디 아-디스코디 아 다이아그램 387 킴버라이트 261 E 탄산망간석 271 탄산염암 248 탄소의 순환 273 탄소측정법 410 탈가스 439
탈질산화반응 331 탈탄산가스 반응과정 226 태양형 비활성가스 476 퇴적수 144 트리티움 측정법 413 티탄철석계 화강암 505 고 파인포인트 264 팽창모델 390 폐쇄온도 382 표준평균해수 (SMOW) 90 프럼보 렉토닉스 464 -_o 해록석군 369 해성석회암 250 해운대온천형 164 호상철광충 231, 269 혼합작용 178 화강암화 작용 500 화석수 144 환경동위원소 515 환원형 대기 478 활동도 계수 293 황 동위원소 분별계수 288 황 동위 원소 지 질온도계 287, 28~ 황 동위 원소비 분포 282 황산영광물 307, 308 황의 기원 307
황의 순환 32 0 황환원 박테리아 283 회전운동 에너지 58 휘발작용 226 휘션트랙법 41 6 흑연-방해석 동위원소 분별정수 260 혹연화 작용 272 a 붕괴 247 /3 붕괴 247 Y 붕괴 247 C Nd 398 B.P. 41 1 C3 식물 246, 335 C4 식물 247 CAM 식물 247 CHUR 398 I-~ 경 마그마 304 P- 과정 핵융합 441 PH- f야다이 아그램 263, 29 7 r- 과정 핵융합 441 Rb-Sr 아이소크론 456 Sm-Nd 아이소크론 456 s- 과정 핵융합 441 S- 형마그마 303, 304 T~~UR 연령 400 TU 414 UR 398
김규한 연세대학교 지질학과 및 동대학원 졸업 일본 나고야대학 지구과학과(이학박사) 미국 캘리포니 아공과대 학 (CALTEC H) 방문연구교수 . 현재 이화여자대학교 과학교육과 교수 ` 저서 때학지구과학 』 , 『 온천지 』 , 『 한국의 지질과 광물자원 』 등 논문 “ Mi ne ralog ica l and Sta b le iso to p e stu d ie s of the Shin y e m i lead-zin c ore dep os its South Korea” 의 다수 동위원소 지질학 대우학술총서 • 자연과학 74 1991 년 9 월 10 일 찍음 1991 년 9 월 20 일 펴냄 지은이·김규한 펴낸이·朴孟浩 펴낸곳•民音社 135-120 서울 강남구 신사동 506 강남출판문화센터 5 층 515-2000~2( 영업부) 515-2003~5( 편집부) 515-2007, 515-2101 (팩시밀리) 출판등록 1966.5 . 19. 제 1-142 호 우편대체번호 010041-31-0523282 은행지로번호 3007783 자연과학 지구화학 KDC/451 • 9 값 17,000 원 Pri nt e d in Seoul, Korea
대우학술총서 자연 과 학 I 소립자와게이지 48 리이만 기하학 박을용 상호작용 김진의 49 群표현론 박승안 2 동력학톡론 이병호 50 비선형 편미분 방정식론 3 질소고정 송승달 하기식 4 相轉移와 임계현상 김두칠 5| 생체막 김형만 5 촉 매 작용 진종식 52 수 리 분 류 학 고철환 6 외스바우어 분광학 옥향남 53 찰스 다 윈 정용재 7 극 미 량원소의 영양 승정자 54 금속부식 박용수 8 수소화 붕소와 55 양 자광학 이 상수 유기 붕소화합물 윤능민 56 효소반응 속도론 서 정헌 9 항생물질의 전합성 57 화성암 성인론 아민성 강석 구 58 확률론 구자홍 10 국소적형태의 Atiy a h-Si ng e r 59 분자 분광학 소현수 지표이론 지동표 60 벡터숙 이론 양재현 11 Mu cop ol y sacchar i des 의 61 곤충신경생리학 부경생 생화학 및 생물리학 박준우 62 에 너 지띠이론 모혜정 12 천체물리학 홍승수 63 수학기초론 김상문 13 프로스타글라딘 합성 김성각 64 신경과학 박찬웅 • 김승업 14 천연물화학 연구법 우원석 65 BC H 부호와 Re ed- 15 脂防營養 김 숙호} Solomon 부호 이 만영 16 결정화 유리 김병호 66 양자전기역학 김영덕 17 고분자의 화학반응 조의환 67 군환론 박재걸 ' 18 과학혁명 김영식 68 대수기하학 조영현 19 한국지질론 장기홍 69 양자장이론 이재형 20 정보이론 한영영 70 해양오염과 생태계 2| 원자핵반응론 정운혁 심재형 22 파괴역학 감상철 71 비가체 연소합성 ( SH S)
