

여철현 공주사범대학 화학과 졸업 ( 이학사 ) 연세대학교 대학원 석·박사과정 ( 이학석 · 박사 ) 이스라엘 We i zmann 연구소 연구원 (Po st— Docto r ) 프랑스 Bordeaux 제 1대 학 CNRS 고체화학연구소 연구원 일본 Osaka 대학, ISIR SANKEN 연구원 ( J SPS Fellow) 현재 연세대학교 이과대학 화학과 교수 및 자연과학연구소 초고온고압연구실 실장
비 기체 연소합성 (SHS) 
 비기체 연소합성 (SHS)
비기체 연소합성 (SHS)
책 머리에 내화성 화합물 또는 세라믹스는 높은 융점, 화학적 안정성, 높은 열과 전기전도도, 고경도 및 고파괴강도 등 물성이 특유하거나 금속 의 물성을 등가하므로 최근 그 응용 범위와 수요가 급증하는 경향을 보이고 있다. 이러한 내화성 화합물의 최첨단 합성방법에 해당하는 비 기 체 연소합성 법 (Gasless Combusti on Syn the sis ) , 고압 자체 연소소 결법 (High -Pressure Self-C ombusti on Sin t e r in g 또는 HPCS) 및 기체압력 연소소결법 (Gas-Pressure Combusti on Sin t e r in g) 등의 합성공정을 상술 하고자 한다. 이들 공정으로 정밀 요업소재의 합성 및 일반 기계산업 과 군수산업 발전에 대한 실용성과 전망을 밝힘으로써 물리학, 화학, 금속공학, 기계공학, 요업공학 및 전자공학 등에 관련된 과학 및 공 업기술 발전에 크게 도움이 될 것이다. 비기체 연소란 테르밋 (The rmit) 반응과 같이 고체혼합물을 접화시 키면 열과 빛을 발하는 격렬한 발열반응이다. 이 연소는 산소와의 결 합이 아닌 고체분말 자체들 사이의 발열반응에 해당한다. 그러므로 비기체 연소합성법은 종래의 내화성 합성기술과는 달리 부가적인 의 부적 가열과정 없이 고체원소 성분들의 자체 발열반웅열에 의하여 한 단계로 합성 및 소결이 동시에 완결되는 세라믹스 합성법이다. 이 연 소는 점화시킨 면에서 다른 면으로 연소파 (combus ti on wave) 가 자발 적 으로 진 행 하므 로 자체 전 파 고 온 합 성 (Self-P rop a ga tin g Hig h Temp e ratu re Syn the sis) 법 또는 간단히 SHS 라고도 한다. 비기체 연소합성법의 주된 장점은 낮은 제조시설 두자, 초고온 공 정온도, 에너지 절약, 빠르고 단순한 공정 및 불순한 반웅원료로부터 정제된 더욱 순수한 생산품을 얻을 수 있다는 것 등이다. 그러나 너
무 격렬하고 빠른 공정이므로 그 공정을 조절하기가 어렵다는 단점도 있다. 이 책에서는 좋은 합성의 선택, 반응온도, 상변화, 연소속도 및 연소 메커니즘의 예측에 도움을 주는 이론적인 분석 모델을 설명 한다. 비기체 연소합성법은 소련의 SHS 에 관한 연구개발 (R & D) 프 로 그 램 과 미 국 의 DARPA (Defe n ce Advanced Research Proje c ts Agen cy) 프로그램에 역점을 두어 기술하고, 고압 자체 연소소결법과 기체압력 연소 소결법은 일본의 연구개발 프로그램에 따라 설명하고 자한다. 복합 세라믹스와 착물 세라믹스의 제조, 비기체 연소합성법과 압력 의 결합, 원자로 연료합성 , 가벼운 군수품 생산, 세라믹스 코팅, 무 중력하에서 주물생성법에 의한 복합 세라믹스 제조 등 이 분야의 연 구개발은 거의 무한한 전망이 있다고 볼 수 있다. 그러한 의미에서 이 책은 재료과학 (Ma t e ri al S ci ence) 을 전공하는 대학원 석사과정 학 생들의 기초 교재로 적당하다고 생각한다. 물리학, 화학, 화학공학, 금속공학, 기계공학, 요업공학, 전자공학 등을 전공하는 많은 학생들 과 연구자들이 이 책울 통하여 본 첨단연구개발 분야를 이해하고 기 술개발에 박차를 가하여 훗날 과학과 산업기술 발전에 도움이 되기를 기대하는 바이다. 1991 년 5 월 여철현
비기체 연소합성 (SHS)
차례 책 머리에 • 5 제 1 장 서론 • 13 제 2 장 비기체 연소합성의 발달 2-1 비기체 연소합성법 또는 SHS 법 ―― 15 2-2 비기체 연소합성의 연역 ――21 2-3 비산화물 연소합성 ――24 2-4 비기체 연소합성의 점화방법 ―― 26 2-4-1 기체불꽃 점화법 • 26 2-4-2 전기방전 점화법 • 27 2-4-3 레이저 점화법 • 29 2-5 비기체 연소의 연소방식 ―― 34 2-5-1 정류상태 연소 • 35 2-5-2 진동 연소 • 36 2-5-3 스핀 연소 • 36 2-5-4 반복 연소 • 37 2-5-5 표면 연소 • 38 제 3 장 비기체 연소 생성물 3-1 표준생성물 ―― 393-2 분말 생성물 ―― 41
3-3 주물 생성물 ―― 44 3-3-1 열역학적인 측면 • 45 3-3-2 반응속도 • 46 3-3-3 발달상태 • 50 3-4 고성능 콤팩트 생성물 ―― 51 제 4 장 비기체 연소에 영향을 주는 변수 4-1 규소화물 합성의 공정변수 ―― 53 4-1-1 화학양론적 비 • 54 4-1-2 반응물 펠릿의 지름 • 55 4-1-3 반응물 펠릿의 밀도 • 56 4-1-4 반응물 분말의 입도 • 56 4-1-5 연소온도의 조절 • 57 4-1-6 규소 생성물 • 58 4-2 연소과정의 물리적 변수 ―― 58 4-3 연소조절 ―― 60 4-3-1 예열 • 60 4-3-2 생성물 희석 • 61 4-3-3 화학 활성제 • 62 4-4 비기체 연소의 정제효과 ―― 63 제 5 장 생성물의 고밀도화 5-1 화학로 ―― 65 5-2 기체 압력에 의한 고밀도화 ―― 68 5-3 기계적 압력에 의한 고밀도화 ―― 70 5-4 고밀도화 메커니즘 ―― 72 5-5 고열 프레스와 고열 등방압 프레스 ―― 74제 6 장 비기체 연소반응 현상학 6-1 관련된 연구 ―― 77
6-2 반응 파라미터 ―― 81 6-2-1 단열 반응온도 • 81 6-2-2 평형변환 • 86 6-2-3 열에너지 운반 • 87 6-2-4 루이스 수 • 90 6-2-5 열확산 방정식의 유도 • 90 6-3 물리 및 화학적 합성 데이터 ―― 96 6-4 질화알루미늄의 합성 ―― 99 6-4-1 열역학적 분석 • 100 6-4-2 반응 현상학 • 102 6-5 탄화티탄의 합성 (원소 반응) ―― 107 6-5-1 열역학적 분석 • 107 6-5-2 반응 현상학 • 109 6-6 탄화티탄의 합성 (산화물 반응) ―― 112 6-6-1 열역학적 분석 • 113 6-6-2 반응 현상학 • 115 6-7 TiB2 의 합성 (원소 반응) ―― 117 6-7-1 열역학적 분석 • 117 6-7-2 반응 현상학 • 119 6-8 TiB2 의 합성 (산화물 반응) ―― 122 6-8-1 열역학적 분석 • 122 6-8-2 반응 현상학 • 125 제 7 장 분석 모델화 • ―― 127 7-1 THERMLIST 128 7-2 COMBUST 1297-3 THERM ―― 132
7-4 모델화의 제언 ―― 135 제 8 장 고압 자체 연소소결 (HPCS) 법 8-1 HPCS 공정 ―― 137 8-2 HPCS법에 의한 단순 세라믹스의 제조 ―― 142 8-2-1 TiB2 콤팩트의 제조 • 142 8-2-2 TiC 콤팩트의 제조 • 145 8-2-3 SiC 콤팩트의 제조 • 149 8-3 소결 메커니즘 ―― 151 8-3-1 본성 체적변화 • 151 8-3-2 고압하에서 연소소결 메커니즘 • 153 8-4 HPCS법에 의한 복합 세라믹스의 제조 ―― 155 8-4-1 복합재료의 연구개발 • 155 8-4-2 TiB2 -TiC 콤팩트의 제조 • 159 8-4-3 TiB2 -SiC 콤팩 트의 제조 • 164 8-4-4 TiB2 -Al2O3 콤팩트의 제조 • 167 8-5 HPCS 공정의 응용 ―― 171 8-5-1 응용 범위 • 171 8-5-2 가압 연소용접 • 171 8-5-3 용접 생성물의 특성 • 174 8-6 새로운 가압 연소소결법 ―― 178 8-6-1 기체 압력 연소소결 • 178 8-6-2 질화 연소소결 • 183 제 9 장 비기체 연소합성법의 전망 9-1 역사적 배경 ―― 189 9-2 미래의 전망 ―― 192 9-3 최근의 발전 현황 ―― 196제 10 장 특성분석법
10-1 밀도측정 199―― 10-1-1 밀도 • 199 10-1-2 Archimedes법 • 201 10-1-3 복합 세라믹스 콤팩트의 이론밀도 • 205 10-2 X-선 결정구조 분석 ―― 207 10-2-1 X-선 분말회절 • 207 10-2-2 최신 X-선 분말기술과 그들의 응용 • 212 10-3 주사 전자현미경 (SEM) ―― 218 10-3-1 주사 전자현미경 • 218 10-3-2 분석의 한계 • 219 10-3-3 시료 준비 및 응용 • 221 10-4 경도측정 ―― 222 10 -4-1 경도시험의 종류 • 222 10-4-2 Vickers 경도 (Hv) • 223 10-5 파괴인성 (fracture toughness 또는 KIC) ―― 225 10-5-1 파괴인성에 관한 이론 • 225 10-5-2 파괴인성 측정식 • 227 10-5-3 KIC 측정 실례 • 231 10-6 꺾임 강도 (modulus of rupture 또는 M.O.R) ―― 234 부록 A 비기체 연소주조(캐스팅)의 공정과 생성물의 특징 • 237 부록 B 비기체 연소반응에 관하여 선택한 소련 모델의 요약 • 245 부록 C AIN, TiB2 및 TiC 합성에 관련된 열역학적 물성 • 255 부록 D 반응물과 생성물에 대한 기본 데이터 도표 • 259 부록 E 압력단위 환산표 • 283 참고문헌• 285 찾아보기 • 301제 1 장 서론 이 책에서는 1967 년부터 최근에 이르기까지 소련의 비기체 연소합 성법 또는 SHS 에 관한 연구개발 프로그램에 따라 성취된 내화성 세 라믹스 합성법을 다루게 된다. 미국의 SHS 에 관한 주된 연구개발 추 전은 DARPA(Defe n ce Advanced Research Proje c ts A g enc y)가 지원하 고, LLNL (Lawrence Liv e rmore Nati on al Laborato r y ) 과 Ceramate c 등 일곱 개의 연구실에서 진행되었다. SPC(Sy st e m Plann ing Corp o ra- tion ) 가 DARPA/LLNL 프로그램 에 따라 SHS 에 대 한 소련 논문 200 여 편을 리뷰 (rev i ew)! )한 것을 토대로 하여 내연성 화합물의 비기체 연소합성법을 설명하고자 한다. 일반적으로 연구되고 있는 소재들은 구조소재 (str uc tu ral mate r i al s) 의 범 주내 에서 세 라믹스 (cera mi cs) , 서 벳 (cermets ) 또는 금속간 화합 물(i n te rme t a lli c comp o unds) 등으로 분류된다. 제조하기가 약간 곤란 한 소재들이 많고 종래의 금속구조 소재들에 비해 가격상의 난점도 있다. 최근 비기체 연소합성법은 유일한 공정 단순성 때문에 종래의 세라 믹스 또는 분말야금(p owder meta l lurgy ) 공정 기술 대용으로 획 기 적 인 관심을 끌고 있다. 비기체 연소법의 확실한 이점은 낮은 공정비, 반 웅 생성에너지의 응용, 낮은 시설두자 및 고순도 생성물의 합성 등이 다. 합성반응시 강한 열에너지의 자체 생성으로 의부적인 가열과정의
필요성을 최소화하거나 완전히 제거할 수 있다. 이 특성이 발열 (exoth e rm ic) 과 자 체 전 파 (self-p ro p a g a ti ng ) 2> 및 자 체 지 속 (self- susta i n ing )3 ) 등과 같은 특이한 공정묘사를 기술하게 되었다. SHS 의 기본적 반웅 메커니즘의 이해는 내화성 생성물의 합성과 물 성에 대한 적합한 성분과 물리적 조건들을 결정하는 데 중요하다. 확 실히 기대되는 가능성은 생산품의 선택과 공정변수의 최적화의 조절 을 할 수 있게 되어 결국에는 산업적 응용시 생산가를 낮추는 효과를 성취하는 것이다. 연소 메커니즘의 상세하고 미시적인 설명이 유용하 겠지만 이는 비기체 연소공정의 성공적인 상업상 확장에 필요한 선행 조건은 아니다. 예로서 입자 크기나 밀도와 같이 더욱 거시적인 변수 들로부터 얻어지는 실험실 데이터는 반응을 조절하는 데 효율적으로 사용될 수 있다. 이 책에서는 비기체 연소합성의 이론과 실제를 모두 취급하게 된 다. 다시 말하면 연소과정의 성질 관찰로부터 시작해서 합성공정의 응용과 생성에 이르기까지 계속된다. 이들 고찰을 위하여 제시된 많 은 정보를 소련 문헌으로부터 얻을 수 있었던 것은, 비기체 연소공정 에 의한 소재합성 연구가 20 여 년간 소련에서 집중적인 발전을 이루 었기 때문이다. 책의 앞 부분에서는 비기체 연소합성법의 발달, 생성물 및 연소반 웅에 영향을 주는 변수에 관하여 설명하고, 중간 부분에서는 생성물 의 고밀도화, 연소반응의 현상학 및 해석 모델화 등을 취급한다. 마 지막 부분에서 SHS 와 압력기술을 결합시킨 공법에 해당하는 고압 연 소소결법 (HPCS), 기체압력 연소소결법, 비기체 연소합성법의 전망 및 생성물의 특성분석법을 다루게 된다.
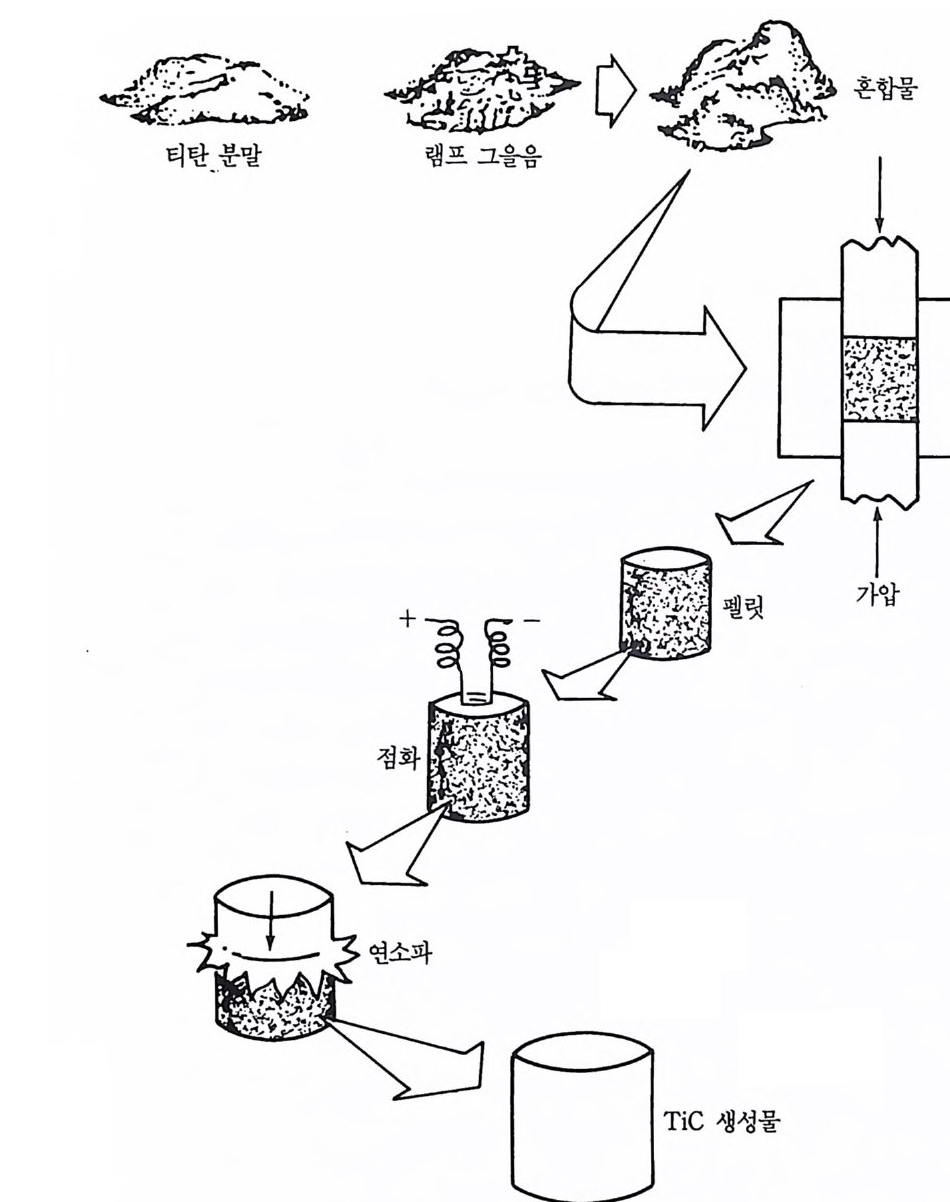
제 2 장 비기체 연소합성의 발달 2— 1 비기체 연소합성법 또는 SHS 법 바기체 연소합성법 또는 SHS 법의 한 가지 보기를 소개함으로써 이 공법의 성질을 설명하고자 한다. 비기체 연소합성법으로 내화성 물질 의 합성에 관한 간단한 공정개념은 그림 2.14) 에서 나타낸 바와 갇 다. 반응 전에 금속과 비금속 반응물질을 혼합하고 약하게 가압하여 펠릿(p elle t)을 만든다. 전기에너지의 순간방전으로 점화시키면 조성 물질인 T i와 C 사이의 열화학적 반응은 자체 유지되어 연소파 (combustio n wave) 는 펠릿을 통하여 전파되며 T i C 생성물을 만든다. 이상적인 이 생성물은 완전히 고밀도화되고 또 쉽게 사용할 수 있는 모양을 갖추어야 한다. 그 경우에 이 공정을 종래의 공정법들과 비교 해 볼 때 뚜렷한 장점은 의부적 가열이나 복잡한 공정장치들이 필요 없다는 것이다. 비기체 연소합성의 다른 특성은 극도로 높은 반응온도를 얻을 수 있다는 것이다. 이들 고온은 더 짧은 반응주기와 반웅완결에 도움이 된다. 고온으로 말미암아 의부적 가열이 필요 없게 될 때 훨씬 더 의 미가 있다. 실제로 Merzhanov5) 는 비기체 연소합성법으로 어떤 다른 공업적 연소과정보다 더 높은 온도를 얻을 수 있다고 주장하였다. 표
 _갔t之'. : 티· 소탄― · 분\말' •. 훑램프그絲又 숲國l
_갔t之'. : 티· 소탄― · 분\말' •. 훑램프그絲又 숲國l
그립 2.1 비기체 연소합성법의 한 가지 보기.
2.1 에 수록된 그의 자료에서 대부분의 비기체 연소합성 온도 범위와 그 최고 온도가 다른 공정의 온도를 능가함을 잘 알 수 있다. 종래의 공정들과 비교할 때 비기체 연소합성의 또 다른 특성은 연 소대 (combustio n zone) 의 국부화 (loc aliza ti on ) 이 다. 의 부의 가열이 필 요한 공정에서는 온도를 높이고 낮추는 것이 바기체 연소에서보다 상 당히 느리다. 반응, 가열 및 냉각에서 짧은 시간노출에 따른 가능한 장점은 마이크로 구조와 성질의 개선된 조절이며 주변 대기와 내포된 물질간의 의부적 오염을 감소시키는 것이다. 예를 들면 종래의 대부 분의 합성공정에서 기대되는 것과는 정반대로 비기체 연소 생성물은 출발물질보다 오히려 화학적으로 훨씬 더 순수하다고 소련의 비기체 연소합성 연구자들은 주장하였다. 표 2.1 공정별 연소온도. 고o 저o 생성물 연소온도 (°C) 탄화수소의 연소 불포화 탄화수소, 공장가스, 1300~1700 탄소그울음 가스-불꽃 합성 산화물 1000~2500 산화반응 산화물 600~900 송풍로공정 무쇠 1600~1900 금속 열반웅 공정 제일철합금과 다른 주요합금 2000~3000 비기체 연소합성 내화성 화합물 2500~4000 마지막으로 비기체 연소반웅의 뛰어난 특성은 뚜렷이 다른 성질과 다론 형태로 된 여러 가지 물질들을 하나의 기본적인 공정기술로 합 성할 수 있다는 다양성이다. 예를 들면 연구자들이 수많은 세라믹스, 금속간 화합물 및 서멧 (cenne t)을 이미 합성하였고, 그 기술기반은 의심할 여지없이 복합물의 합성과 점층화된 화합물의 소재에까지 확 장될 수 있다. 지금까지 많은 물질들이 덩어리와 분말 형태로 합성되 어 왔다 . 비기체 연소합성법을 더욱 응용하여 쉽게 볼 수 있는 또 다
른 가능성은 한 단계 조작으로 합성 반응과 동시 에 접 합(j unc ti on) 결합 (세라믹스와 세라믹스, 또는 금속과 세라믹스 결합)을 경할 수 있디는 것이다. 많은 다론 화합물을 생산할 수 있는 이 다양성은 다음과 같이 금속 (M) 과 비금속 (N) 조성들간의 일반적인 합성반응식으로 나타낼 수 있다. ~m aiM i + 짝n b j N j , P i= l i= I 금속분말 분말, 액체 또는 기체 고체 생성물 전형적으로 초기 소련의 연구에 있어서 M 원소는 주기율표에 있는 A 족의 전이금속이었으며, M 과 N 원소의 수는 처음에는 한 개씩이었 다. 5) 예를 들면 티탄과 탄소가 반응하여 탄화티탄을 형성한다. 후에 는 한 개의 M 원소와 두 개의 N 원소의 반응을 소련 연구원들이 조사 하였고(예로서 티탄이 탄소 및 질소와 반응하여 carbon it r i d 러문 생성함), 두 개의 M 과 한 개의 N 원소로 된 다른 화합물도 조사되었다(예를 둘 면 티 탄과 크롬이 붕소와 반응하여 d i bor i de 를 생 성 함) . 더 최근에는 소 련의 연구가들이 니오븀과 지르코늄이 carbon itri de 를 형성하는 반응 과 같이 두개의 M 과 두 개의 N 원소가 반응하는 더욱 복잡한 화합 물들을 연구해 왔다. 세라믹스 화합물의 착합성체를 생산하는 능력은 이런 물질들이 고 온 초가소성 (sup er p la stic ity) 을 나타낼 수 있고 주변 온도에 대 하여 기대하지 못한 높은 파괴강도 6) 를 나타낼 수도 있기 때문에 특히 홍 미를 끈다. 파괴강도가 높은 화합물인 착합성체의 비기체 연소합성은 두 가지 이유 때문에 홍미롭다. 그 첫째는 단순하고 빠른 합성이므로 낮은 생산가를 암시한다. 둘째는 비교적 높은 비율의 가열과 냉각이 파괴강도를 개선하는 데 하나의 필요조건이 될 수 있는 작은 결정 입 자 크기 와 분리 된 이중상 결합 (dup le x ph ase combin a ti on ) 을 유지 하는 데 도움이 된다.
비기체 연소합성이 금속열(산화-환원)반응 7 ) , 8) 과 결합된 다론 반웅 형태가 보고되어 있다. 한 전형적인 반응은 다음과 같다. MO 計 X ―一 MX 급 XkoI 이 경우 산화물 (MOm) 은 한 원소의 산화-환원제 (X) 와 반응하여 원 하는 내화성 생성물 (MXn) 과 부생성물 (XkOI) 을 형성하게 된다. 한 가 지 특별한 예는 산화몰리브덴이 붕소와 반응하여 붕소화몰리브덴 생 성물과 산화물에 붕소를 포함하는 슬래그 (sla g)를 형성한다. 다론 결 합된 과정들에서는 비금속 반응물 (N) 과 환원제 (R) 는 다음 반응에서 와 같이 원소들을 분리해서 반응에 가하였다. MOm+Nn+Rp ——~ MN1 + Rk01 비기체 연소공정들을 연구한 소련 연구가들에 의하여 이미 합성된 화합물의 수는 300 개 이상이라고 보고되었다. 이들 대부분은 금속간 (int e r rneta l l ic) 및 세라믹스 조성들을 가지고 있고 세라믹스형의 대부 분은 붕소화물, 탄화물, 질소화물 및 규소화물 등이다. 그 의에 그들 은 이런 물질들의 복합결합물을 합성하였고 몇 개의 서멧 (cerme t) 소 재도 생산하였다. 합성된 다른 세라믹스 화합물에는 게르만화물, 수 소화물, 인화물, 셀렌화물 및 황화물이 포함되어 있다. 또한 알루미 늄화물과 니켈화물도 생산되어 왔다. 표 2 . 2 에서 보는 바와 같이 비기체 연소반웅으로 합성된 여러 물질 의 응용성에 대한 소련 연구자들의 견해로 보아 예상되는 산업적 웅 용성이 매우 넓다고 본다. 붕소화물과 같이 비교적 견고하고 내화성 인 화합물과, 칼코겐화물 (chalco g e ni des) 과 같이 부드러운 물질이 있 는가 하면 탄화물같이 화학적 안정성이 대단히 높은 것과 수소화물과 같이 그 안정성이 더 낮은 것도 있어 물질 형태에 있어서 상당히 다 양성을보인다.
표 2.2 비기체 연소합성된 내화성 물질의 응용에 대한 소련의 견해. 으。 용 화합물 강합금 8 곱나 福갑 보호코팅 집기갑 윤활제 핵에너지 붕소화물 (Bor i des) X X X X X X 탄화물 (Carbid e s) X X X X X X g칼en 코 id겐e s화) 물 (Chalco- X X X 수소화물 (Hy dride s) X 금속간화합물 (lnte n neta l l ic X X comp ou nds) 질화물 (Ni tride s) X X X X X X 규소화물 (Sil icid e s) X X X a) 접합된 탄화물과 관련된 공구산업 생산품 지금까지 비기체 연소합성의 유리한 특성과 산업적 응용이 가능한 다양성을 살펴보았는데 이에 대한 필연적인 의문은 〈왜 비기체 연소 합성이 완전히 개발되지 못했는가〉 하는 것이다. 그것은 아마도 연소 과정을 조절하기 어렵다고 믿었기 때문일 것이다. 이와같이 새로운 소재합성을 위하여 기술개발을 할 때는 더 잘 이해할 수 있고 더 조 절하기 쉬운 기술에 역점을 두어야 했었다. 합성을 위한 비기체 연소 (고체상태)반응에 대한 관심은 로켓 추전연료로서 고체연료가 개발된 후에야 생겨났다 .9) , 10) 이 연소의 연구개발의 결과로, 소재합성에 비 기체 연소를 응용할 수 있는 가능성이 인식되었고, 그 후 20 년 이상 적어도 5 개국에서 다각도로 개발이 계속되어 왔다. 이러한 대부분의 개발노력은 기본적인 연소 메커니즘을 이해하는 것과 연소과정에 사 용된 물질의 열역학적 성질을 뒷받침하는 데 집중되었다. 비기체 연소합성에 있어서 소련의 연구개발이 가장 발전되어 있다. 소련의 연구방법은 관심 있는 물질에 대한 열역학적 반응 퍼텐셜을 예측하고 몇 가지 다른 연소방식의 반웅 메커니즘을 조사하여 특수한 내화성 화합물합성을 위한 공정개발에 그 정보를 응용하는 것이다.
내화성 물질과 다른 물질들의 화학적 성질이 폭넓게 변하므로 소련 연구자들은 각각 독특한 생성물 조성에 맞도록 공정조절을 개발시켜 왔다. 2— 2 비기체 연소합성의 연역 자체 전파 발열반응 11) 에 대한 기초적인 수학적 근거는 36 년 12) 이전 에 발전되었다. 한두 가지 예의는 있지만 13) 소련 화학물리연구소에서 1967 년에 Merzhanov 의 지시하에 연구를 착수하는 데 노력하기까지는 아 공정에 대하여 그렇게 큰 관심을 쏟지 않았다. 그 후 24 년간 이 노력은 적용범위가 집중적이며 광범위해져 갔다. 또 시간이 흐름에 따라 기초로부터 응용연구로 전환이 확실해지고 부수적으로 실제적인 생산활동 14) 에까지 이르게 되었다. 1972 년에 내화성 화합물 분말생성을 위한 실험설비가 그 화학물리 연구소에 설립되었고 1976 년까지는 30 개 이상의 다른 소련 연구기관 둘이 SHS 공정의 연구와 개발에 여러 가지 형태로 참여하였다. 그때 (1976 년)까지 200 개 이상의 소재들을 이 방법으로 합성하였고 적어도 그들 중 두 가지는 생산단계까지 도달하였다. 이규소화몰리브덴 (M0S i 2) 과 탄화티탄 (T i C) 은 상업적으로 생산되어 전자는 발열체 (heati ng elements ) 소재로 후자는 산업 상 다이 아몬드 대용품으로 각각 사용되었다. 더욱 최근의 소련 활동보고서 15) 는 SHS 로 제조된 소재의 총수가 이 제 300 개를 훨씬 넘는다고 지적했다. 이 공정으로 만든 소재들에는 전자소재, 금속 초전도체, 복합소재, 금속간 물질, 고체윤활제, 내화 성 물질 및 연마제 등이 포함되어 있다. 소련에서의 SHS 관련 연구 활동은, 이 공정에 대한 특수한 중요성의 결과로 국제적인 관심의 초 점이 되었다. 1984 년에는 SHS 공정이 소련에서 가장 중요한 과학성
취품 박물관인 Sta t e Reg ist r y of U.S .S .R. Inventi on s 에 들어갔다. 많은 산업체들은 열저항체 (heat resis t a n t) , 내화성 화합물 (re fr ac t or y com- po und) 및 다론 형태의 소재와 부품들을 제조하기 위하여 SHS 기술 개발에 지대한 관심을 쏟고 있다. 더욱이 SHS 기술을 기반으로 거의 실용단계에 있는 70 여 개의 특수장치 및 개발품이 연구되어 있다. 소련 이의의 나라에서는 현재까지 SHS 연구개발에는 그 활동이 아 주 미약할 따름이다 . 그렇지만 최근 몇 년간 다른 나라에서도 상당한 관심을 끌었고 연구개발 활동이 미국 , 일본 , 호주 및 폴란드에 의하 여 진전되고 있다 . 미국에서는 1981 년까지는 SHS 에 관한 연구개발 프로그램이 거의 생소한 것이었다. 1984-86 년까지의 2 년간 DARPA(Defe n se Advanced Reasearch Proje c ts Ag en cy) 프로그램 에 의 하여 비 기 체 연소합성 분야 의 연구개발 활동이 주로 시작되었다. 다시 말하면 서방 선진국 과학 자들까지도 이 현실적인 공정에 대하여 오랫동안 무지했고 미국에서 도 SHS 에 관심을 갖고 연구를 시작한 것은 불과 6, 7 년 전이다. 현 재 SHS 분야의 연구개발에 참여하고 있는 연구원과 연구기관의 수는 날로증가하고 있다. 일본에서의 SHS 에 관한 연구개발 16 ) 은 1984 년에 시작되었다. 그때 Osaka 대학 연구전이 SHS 와 고압기술을 응용하여 개발한 공정인 고 압 연소소결법 (High -Pressure Combusti on Sin t e r i ng 또는 HPCS) 으로 TiB 2 1 7), TiC I S) 및 SiC 1 9) 같은 내화성 세라믹스를 합성하고 동시에 고 밀도화하는 시범을 보였다. 이러한 새로운 고밀도화 공정의 성공은 큰 뉴스가 되었고 SHS 에 대한 광범위한 연구개발을 유도하게 되었다. 이제 적어도 5 개의 대학, 5 개의 국립연구소 및 8 개의 회사들이 여 러 가지 고성능 소재개발을 목표로 SHS 의 연구개발에 참여하고 있 다. 세라믹스 분말합성, 금속간 야금형성, 단순 세라믹스와 복합 세 라믹스의 형성과 동시경화, 세라믹스 코팅, 접합, 탄화물의 단결정 생장 등이 이들 예에 해당한다. 어떤 회사들은 그 SHS 또는 발열 합 성반응을 이용한 공정기술로 여러 가지 세라믹스 분말과 세라믹스 생
성물을 생산하고 있다. 한편 질소화물의 연소합성법에 관한 기초연구와 반웅분석은 Osaka 대학에서 수행되어왔다 .lOMPa 이하의 질소압력하에서 금속원소 분 말의 질소화 연소반응이 그 공정 이 며 TiN , NbN, ZrN, TaN, Si3 N . 및 AIN 의_ 고순도 질화물 분말이 합성되었다. 이 때 너무 높은 반 옹온도를 강하시켜 질소화를 완전하게 하며 녹은 금속입자들이 덩어 리지는 것을 방지하기 위하여 10~20% 범위의 적당량의 생성물질을 원료금속 분말에 미리 가한다. 반응분석은 고속 비디오, 2 색 파이로 미 터 및 광학 다중통로 분석 기 (op tica l multic h annel analyz e r) 를 사용 한 고압반응기 (auto c lave) 의 창을 통하여 실시 되 었다. Toky o Instit ut e of Technolog y 의 Odawara 교수와 그 공동연구자들 이 파이프 내면에 세라믹스-금속 복합충을 바르기 위하여 고안한 것 은 새로운 SHS 기술인 원심-데르밋 공정 20>(cen trifug al- th e rmit pro cess) 이다. 속이 빈 금속 파이프를 고속으로 돌리면서 3Fe30.+8A1-4A12 03+9Fe 삭 H=-3265K J와 같은 테르밋 반응을 일으켜 파이프내 표면 울 녹이고 반웅생성물로 복합체를 형성함으로써 세라믹스 코팅을 한 다. 5m 길이의 금속깃1 ] 라믹스 복합 파이프롤 그 원심-테르밋 공정으 로 생산할 수 있었고 그 기술은 Kubota Iron Work Co., L t d 로 이전되 었다. Nati on al Instit ute for Research in Inorga n i c Mate r i al s 에 서 는 질 이 좋 고 큰 TiC 단결정을 SHS 로 합성된 그 봉으로부터 제조하였다. Oh t a ni 2” 는 유동띠법 (floa ti ng zone me th od) 을 사용하여 진공에서 Ti 와 C 의 혼합분말봉을 점화시켜 생긴 TiC 다결정봉으로부터 큰 단결정을 생성시키는 데 성공하였다. 고순도 TiC 다결정 공급재료봉을 만들기 위하여 SHS 법을 사용함으로써 종래의 상품 TiC 분말로부터 제조한 단결정에 비교하면 더욱 완전한 단결정 생성을 할 수 있게 하였다. TiC 단결정은 효과적 인 장방출기 (field emitter ) 와 고온 SiC 반도체 기 질물질 (substr at e mate r ial ) 로 사용될 수 있다. 1986 년 Osaka 대 학의 ISIR-SANKEN 에서 Mi yam oto 와 공동연구자들은 HPCS 에 의한 TiB 2
-TiC , 22> TiB 2 -AI20s 및 TiB 2 -SiC 복합 세라믹스 콤팩트 제조를 최초 로 성공한 바도 있다. 이상에서 논한 바와같이 일본에서는 SHS 연구개발 16) 이 활발하게 발전되어 가고 있다. SHS 는 높은 열을 발생하는 빠르고 경제적인 공 정으로 특징지어지고 있다. 이 공정의 장점을 개발하기 위하여 기본 적인 연구는 물론 다른 공정과의 결합을 통하여 더 많은 아이디어가 특히 세라믹스와 금속분야의 소재 과학기술을 위한 여러 가지 새로운 공정을 유도해 낼 수 있을 것이라고 기대한다 .23) 호주의 연구에 대하 여는 5-2 절에서 간단히 소개될 것이다. 2— 3 비산화물 연소합성 표 2.3 에 수록된 바와갇이 여러 가지 합성법에 의하여 내화성 물질 들이 생산되어 왔다. 일반적으로 고체상태 반응합성은 이용할 수 있 는 공정이지만 고온로에서 장기간의 반응시간을 필요로 한다. 이때 유일한 연소합성법 또는 SHS 는 많은 고성능의 내화성 물질과 다른 물질들을 제조하는 데 간단하고 유효한 방법이다. 이 SHS 반웅은 출발물질들의 상태에 따라서 고체-고체계 (Ti +2 B--+ TiB 2 , Si+ C --+SiC 등)의 반응, 고체-액체계 (2T i +N2 (l )--+2T i N) 의 반 응 및 고체-기체계 (3S i +2N2( g )--+S i 3N ◄) 의 반웅의 세 가지 경우로 나 눌 수 있다. 그 첫번째 경우를 주로 비기체 연소라고 부르지만 둘째 와 셋째 경우들도 산소와의 연소반웅이 아니라는 면에서 비기체 연소 합성법에 포함시켜 취급하는 것이 상례다. 그 SHS 는 화합물을 형성 할 때 생기는 강한 발열반응이 2, 3 초 내에 냉압축된 반응물 (cold pre ssed reac tant)을 동해 자발적으로 전파될 수 있다는 데 기초를 두 고있다. 그립 2.2 는 그 연소반응을 모형도로 나타낸 것이다. 그 기발한
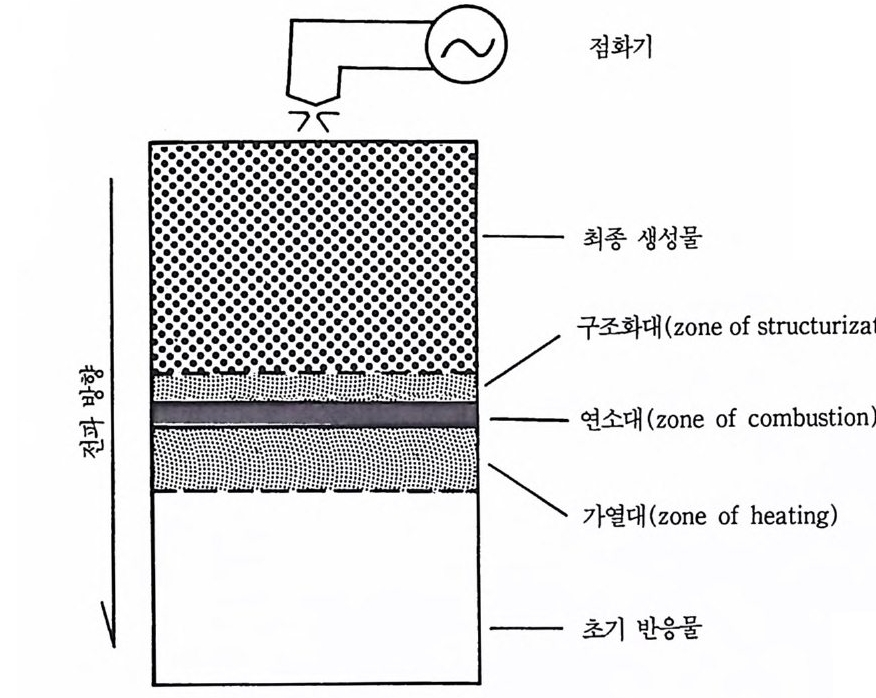
표 2. 3 TiB ,, TiC 및 SiC 분말을 제조하는 여러 가지 방법의 개요. 물질 방법 빈냥 TiB 2 17), 24) 원소들의 직접결합 Ti (s) + 2B (s)-.TiB 2 ( s) 금속화합물과 할로겐화 TiC I , (g) + 2BCI, + 5H2 (g) 붕소를 수소로 환원 --+TiB 2 ( s) + lOHCI (g) 금속산화물의 붕소 TiO , (s) +4B (s) 또는 --+TiB 2 ( s) + B20• (g) 탄화봉소와 탄소에 의한 환원 2Ti0 2 (s) +B,C(s) +3C(s) --+2Ti 8i(s) +4CO(g) 다른 금속둘을 사용한 환원 Ti0 2 (s) + B203 (s) + 5Mg ( s) 죠iB 2(s)+5M g0 TiC lB ),2 5) 원소들의 직접반응 Ti + C-.TiC 금속산화물을 환원기압에서 과잉탄 Ti0 , +3C-+TiC +CO 소로환원 금속염화물을 탄화물과 2TiC l , +CaC2+3H2 수소기체로 반응 ->2TiC +CaCl2+6HCI SiC 1 9),2 6)~ 2 8) 원소들의 직접반웅 Si+ C---SiC 금속산화물을 환원기압에서 과잉탄 SiO ,+C--+SiC 소로 환원 (Acheson 법) 할로겐화금속을수소와 4SiC I,+2C tH s+3H, 반응시켜 기상으로부터 침전 --+4SiC + l6HCI 열분해 반응 CH3SiC b-+SiC + 3HC1 SHS 의 모양은 반응물의 한 끝에서 시작한 뒤 자체 전파반응을 유지 하는 데 충분한 열이 방출된다는 것이다. 그 연소대는 최종 생성물을 생성하면서 원주형 시료축을 따라 전파된다 .19)
 戶 점화기
戶 점화기
그림 2.2 연소 진행앞면 (combus ti on fr on t)이 원주형 콤팩트를 따라 움직여 내 려가는 모형도.
2— 4 비기체 연소합성의 점화방법 2— 4— 1 기체불꽃 점화법 비기체 연소합성의 점화방법에는 기체불꽃(g as- fl ame or gas -to r ch) 법 , 전기 방전 (electr ic dis c harge ) 법 및 레 이 저 점 화 (las er ignition ) 법 등이 있다. 기체불꽃법은 다른 방법에 비하여 기체불꽃만 있으면 반
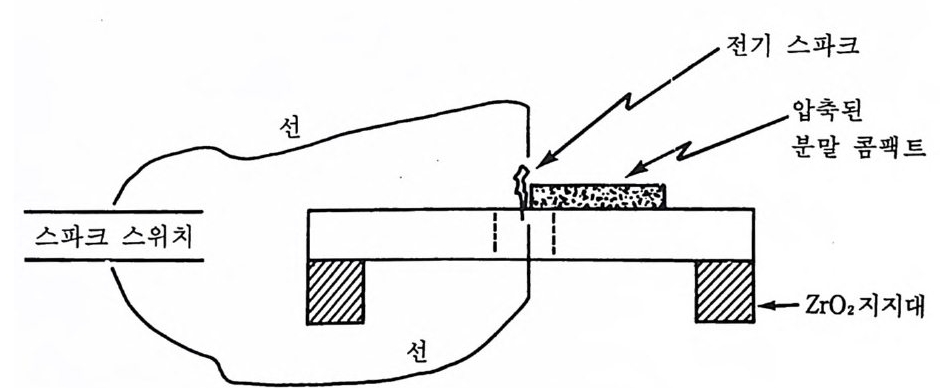
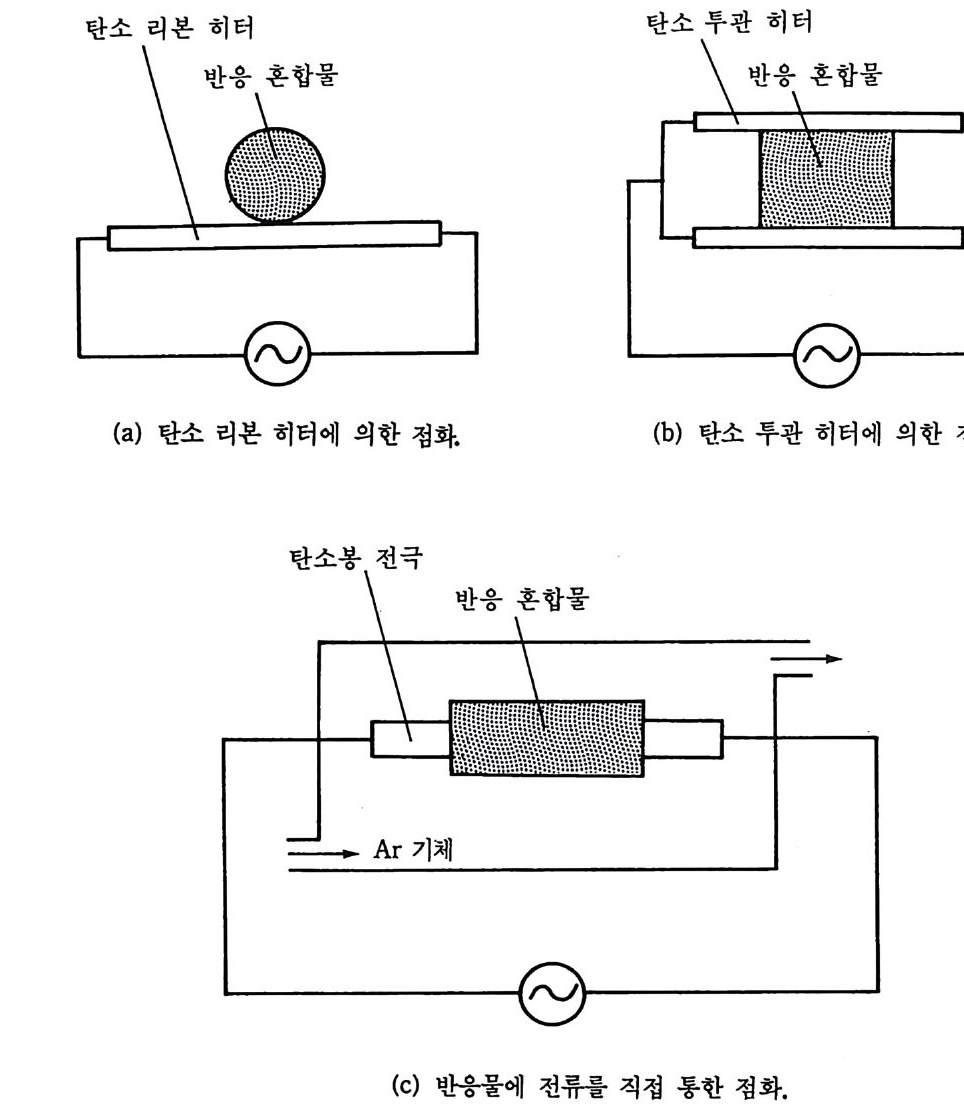
응 시료 펠릿에 불꽃의 초점을 맞추어 점화할 수 있으므로 매우 간편 하지만 발화점에 따라서 프로판 갓 산소, 아세틸렌-산소 및 수소-산소 토치들 중의 어느 한 가지 불꽃을 선택하여 사용하여야 한다. 대기 중에서 점화할 경우는 별 어려움이 없으나 연소 용기내에서 진공, 아 르곤 압력, 헬륨 압력 및 질소 압력 등에서 연소할 때의 점화법으로 는 적당치 못하다. 2— 4-2 전기 방전 점화법 전기 방전 점 화법 에는 반응하지 않은 콤팩트(gr een comp a ct) 의 한 부분에 전기 스파크 (elec tric al s p ark) 를 통하여 반응을 시작하는 점화 법 2 9) 인데 이 실험장치는 그림 2 . 3 에서 보는 바와 같다. 그립 2.4(a) 와 같이 압축된 반응물 펠릿을 탄소 리본히터 (carbon ribb on heate r ) 위에 놓고 한 끝에서 점화하거나, 그립 2.4(b) 와 같이 탄소 투관 히 터 (carbon sleeve heate r ) 안에서 큰 점화 면적을 갖고 열손실울 방지 하도록 점화하거나, 그림 2.4(c) 와 갇이 의부적인 탄소 히터에 의한 가열 대신 탄소봉 전극을 사용하여 반응물 자체에 칙접 전류를 통할 때 생성되는 열로 점화를 시키는 점화공정 30) 등이 있다. 이와같이 반
 팩트
팩트
그립 2·3 전기 스파크 접화도.
 탄소 리본 히터 탄소무관 히터
탄소 리본 히터 탄소무관 히터
그립 2,4 SHS 의 여러 가지 전기 접화법.
웅물에 전류를 직접 가하여 점화시에는 반옹물이 전기전도성인 경우 에 가능하고 그때 발생하는 열이 점화를 위한 가장 효과적인 열원이
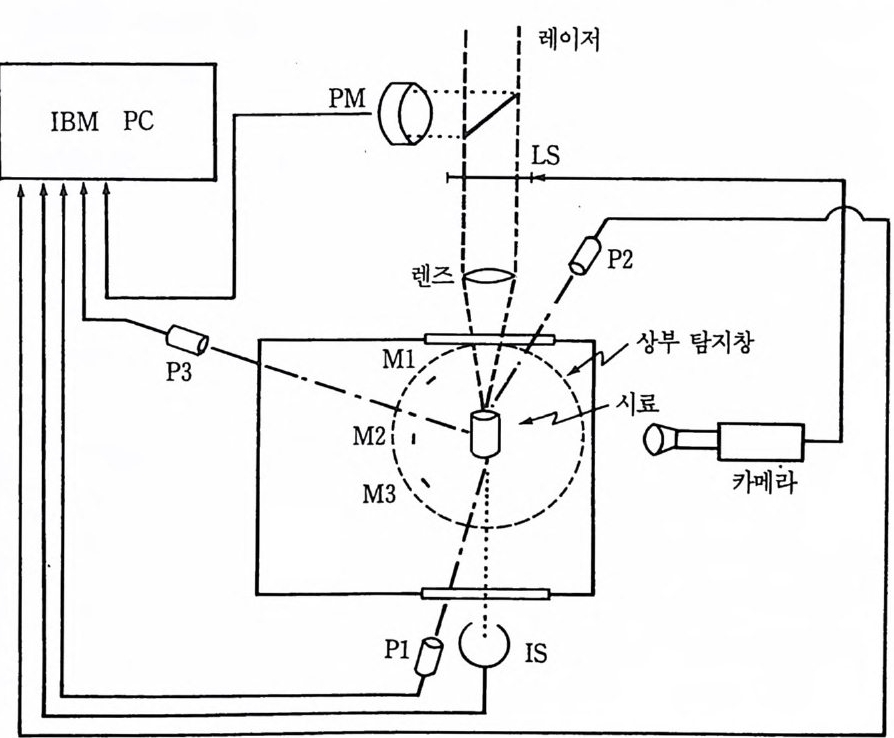
어야 한다. 이 실험에서는 Ar 기체로 채워진 용기내에서 반응물에 5 V 의 일정한 전압을 걸어서 연소한 예이다. 2— 4-3 레이저 점화법 여기에서는 레이저로 유도된 점화법을 SHS 에 적용시켜서 고속 사 진측정과 실제시간 광학 고온측정 (real-tim e opt ica l pyr ome try)을 결합 시킨 연구결과 31) 와 레아저를 사용한 테르밋의 점화연구 32) 의 일부를 설명하고자 한다. 그 첫번째 실험장치는 그립 2.5 에서 보는 바와 갇다. 레이저 셔터 (LS) 는 NAC 모델 E-10 고속 카메라(1 000 화면 /sec) 로 제동되었다.
 PM (D ....杉 !l ,巨 l 이저
PM (D ....杉 !l ,巨 l 이저
그립 2.5 레이저 접화 실험장치의 개요도.
Helio s HF-DF 레 이 저 (DF 모드, 3 . 8µm, 100 watt nom ina l pw r) 로부터 방사는 350mm 초접 길이의 CaF2 렌즈에 의하여 초점이 맞추어져 사 파이어 창을 통해 시료함에 들어가고 시료 펠릿의 앞표면에 닿도록 한다. 그 펠릿 앞표면에서 레이저 점 지름은 lmm 였다. 10-2to r r 에 가까운 전공 시료실은 10 t orr 의 Ar 압력으로 채워서 가열된 펠릿으로
 30 납/\./· /L.—. .1_. ....T _/ 림._.f / 二.|.\|,||. /.·l· ― ― .一.\ ._- —\_1\\. 진\\ . \M 공 .一L 1 창 튼 \.-저
30 납/\./· /L.—. .1_. ....T _/ 림._.f / 二.|.\|,||. /.·l· ― ― .一.\ ._- —\_1\\. 진\\ . \M 공 .一L 1 창 튼 \.-저
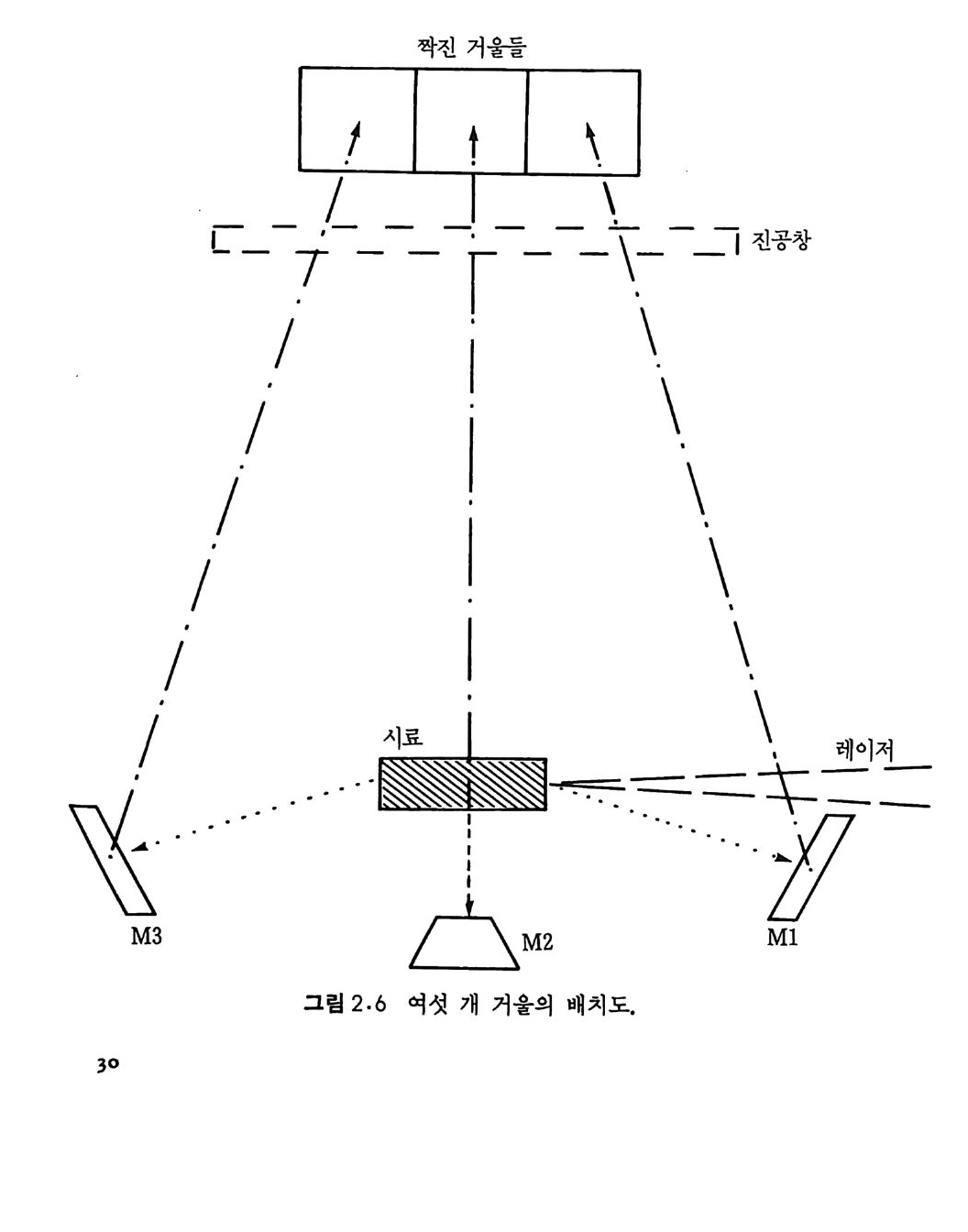
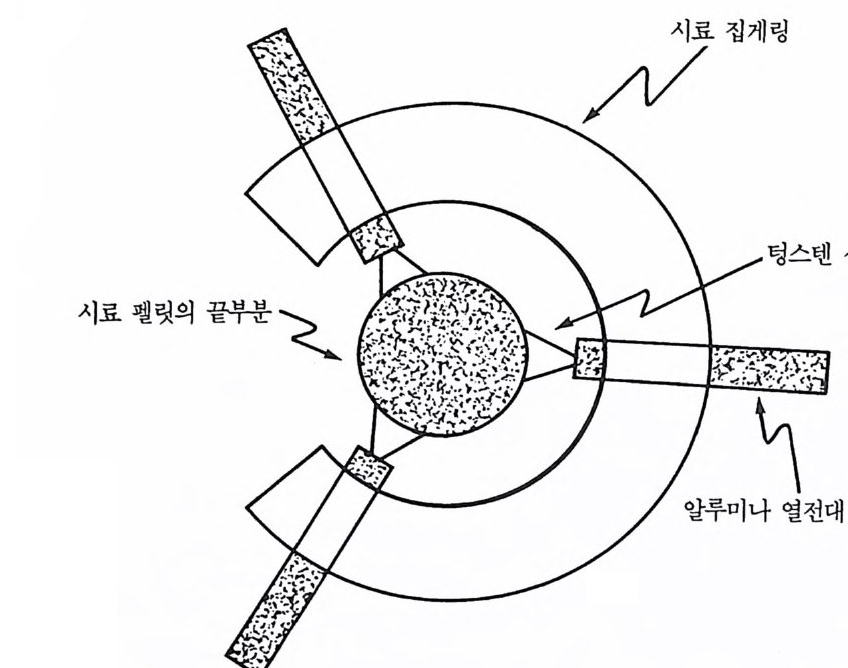
부터 증발된 물질에 의해 창이 오염되는 것을 최소화하도록 하였다. 시료 펠릿 앞표면, 옆표면 및 뒷표면의 사진촬영을 동시에 할 수 있 도록 그림 2.6 에서 보는 바와같이 여섯 개의 거울이 장치되어 있다. 시료함의 밀에 있는 세 개의 거울들 (M i, M2, M3) 은 펠릿의 상들을 시료함 밖에 있는 세 개의 짝전 거울들로 반사시켜 준다. 고속 카메 라는 짝전 거울둘로부터 그 상들을 잘 볼 수 있도록 적당한 장소에 위치시킨다. 카메라 광학의 축은 그림 2 . 6 에 그린 장치의 면에 수직 이 되게 위치시킨다. 펠릿의 앞면과 옆면을 보이는 거울둘은 고정시 키고 반면에 뒷면을 보는 거울은 다른 길이를 갖는 펠릿을 볼 수 있 도록 조절할 수 있다. 카메라 광학에서 장의 초점 깊이 (foc al dep t of fi eld) 는 40000 분의 1 인치였다. 분리된 영상 사진촬영과 함께 그립 2.5 에서와 같이 세 개의 고온온 도계는 펠릿의 앞, 옆 및 뒷표면의 온도측정에 사용되었다. IRCON 2 색 파이로미터 (P 1) 는 뒷표면을, 두 개의 열게이지 단색광 이극자 파 이로미터 (P2, P3) 는 앞면과 옆면을 각각 표적으로 하였다. 게르마늄 탐지기를 사용한 파이로미터 p 3 는 900K 이상의 정확한 온도측정을 할 수 있고 규소 탐지기를 사용한 파이로미터 P2 는 1900K 이상의 정 확한 온도측정을 할 수 있다. P2 파이로미터는 레이저 점을 중심으로 약 I.Imm 지름의 점 크기를 볼 수 있도록 초점을 맞추었다. 과학기 술 힘미터 (PM) 는 레이저력을 모니터하는 데 사용되고 적분영역 (IS) 레이저로 연소되어 통과한 거리를 결정하는 대 사용된다. 이들 전단 으로부터의 데이터는 IBM PC 컴퓨터로 얻어 저장한다. 컵퓨터에 의 한 데이터 획득은 레이저 셔터를 열기 500ms 전에 시작한다. 시료들은 I/I6 인치 지름 XI/8 인치 길이로부터 I/4 인치 지름 XI/2 인 치 길이까지의 크기를 갖는 원주형 펠릿들이었다• -325 메쉬의 분말 시 약의 화학양론적 혼합물로 된 펠 릿을 10000 또는 20000 p s i로 단일 축으로 압축하여 생성하였다. 시료 펠릿의 집게로 사용한 설치는 그 림 2.7 에서 보는 바와 같다. 고속 사진측정과 고온측정의 결과로 레아저 점화와 연소과정에 대
 ]시 료집게링
]시 료집게링
그림 2.7 시료 펠릿 집게의 개요도.
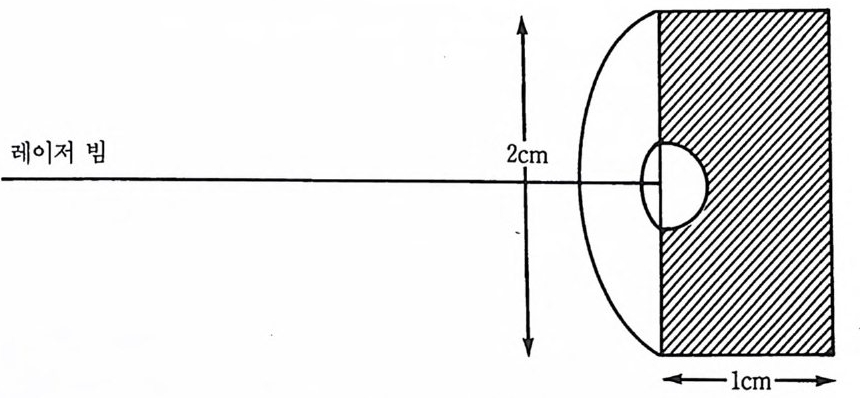
한 반응속도와 온도 데이터를 얻을 수 있게 분석되었다. 레이저 점화 는 직접적으로 일어나지 않으며 기대되는 바와같이 펠릿 표면에서 일 어나지도 않는다. 점화 유도주기가 나타나며 점화는 펠릿 안쪽에서 일어난다. 레이저를 펠릿 표면에 쪼이면 펠릿의 많은 부분이 점화를 일으키지 않은 채 가열되어 달아오론다. 그림 2.8 과 갇이 레이저 빔에 가열된 펠릿 체적은 반구 모양으로 보인다. 그 반구 밖의 차가운 펠릿 부분은 레이저 가열된 부분으로부 터 열을 전도하도록 열 싱크로 작용한다. 반구로부터의 열의 흐름속 도는 펠릿의 복잡한 열전도성에 의하여 조철되고 주위 열 싱크 온도 의 어떤 역함수로 정해진다. 그 열 싱크는 최종적으로 그 반구로부터 의 열전도속도가 레이저 가열속도와 같아지는 온도에 달한다. 부가적 인 레이저 가열은 점화를 하도록 반응물에 대하여 필요한 열에너지를
 ^
^
그림 2.8 레이저 빔에 가열된 펠릿의 반구형.
공급한다. 레이저 점 지름보다 더 큰 크기를 갖는 펠릿에 대하여 레이저 가열 된 체적으로부터 가열은 등방성이다. 그러나 펠릿에서 열전도도는 비 등방성임이 고속 사진촬영으로부터 명백하다. 펠릿의 지름에 대한 길 이의 비(f /d) 가 1 보다 크면 열흐름은 축방향이고 1 보다 작으면 방사 방향으로 나타났다. 예를 들면 f /d
론적 모델화 방법을 사용하여 일차원적이고 단열적인 형태에 대하여 결정되었다. 펠릿의 열-속도론적 상수와 열전도도는 그 모델로부터 연역될 수 있다. 전체 연소과정은 두 가지 다른 단계로 나누어지는 것을 알 수 있 다. 그 첫 단계에서는 시료 펠릿이 하나의 불활성체와 같이 작용하여 의부 열원으로 공급된 열로 단지 가열만 되어 뜨거운 충 (ho t la y er) 을 생성한다. 둘째 단계는 뜨거운 충내에서 화학반응에 의하여 조절된 다. 화학반응에 의하여 생성된 열로 그 반응의 자체-가속은 지속되는 연소를 일으키게 한다. 그 뜨거운 충에서 화학반응으로부터 공급된 열과 의부 열원으로부터 공급된 열이 같아지자마자 실제적으로 점화 가 시작된 것으로 가정할 수 있다. 발열 화학 반응속도에 따른 기본 적인 열흐름, 2 단계 과정 및 열-속도론적 모델화 등의 이론식들은 더 이상 논하지 않겠다. 전체 점화시간(tig)과 레이저의 입력 (q。)의 관계 는 t i g =A q。 -m 식에 따라 의존한다. A 는 상수이고, m 은 1. 20~ 1. 40 으 로서 q。 (watt ) 가 증가하면 tjg (µsec) 가 감소한다. 이상 논한 바와갇이 바기체 연소합성 또는 SHS 반응이 진행되는 조건들이 대기압, 진공, 여러 가지 기체압력, 금속증기압 및 역학적 압력 등에 따라서 기체불꽃 점화법, 전기방전 점화법 및 레이저 점화 법 중에서 적당한 점화법을 선택하여야 한다. 또한 반응물질의 종류 와 특성, 물리적 변수, 발열반응량 및 최종 생성물의 물성활용 등에 따른 최적 점화법 기술을 개발하여야 한다. 2-5 비기체 연소의 연소방식 (Combusti on Modes) 몇 가지 다른 방식의 연소파 전파들이 소련 연구자들에 의하여 관 찰되 어 왔다. 이들 연소방식은 정 류상태 (ste a dy sta te) 연소와 불안정 (unsta b le) 연소의 두 가지 일반적인 영역으로 구분할 수 있다. 정류
상태 연소에서는 연소파동이 점화 표면으로부터 반응물질을 통해 아 주 일정한 속도로 반응이 끝나는 반대 표면까지 진행한다. 불안정 연 소의 형태는 다양하게 변하며 일반적으로 합성과정에서 바람직하지 않기 때문에 널리 연구되지 않았다. 불안정 연소는 불균일한 조성과 밀도로, 불완전한 반응의 결과로 종종 일어난다. 대부분의 소련 연구 자들은 전동 (oscil lat i ng ) , 스핀 (spi n) , 반복 (repe a te d ) 및 표면 (sur- fac e) 연소 33~35) 의 네 가지 방식의 불안정 연소를 기술하였다. 이러한 불안정 연소방식은 일반적으로 그 계의 점화 한계점 근처에 서 일어나며 단열 연소반응이 일어날 수 있는 한계조건을 나타낸다. 합성과정에서 불안정 연소방식을 피하려고 한다면 불안정 연소방식에 달하는 조건들을 더욱 완전히 이해할 필요가 있다. 2— 5-1 정류상태 연소 (S t ead y -S t a t e Combusti on ) 기체 형태의 연소(표 2.1 참조)로부터 비기체 연소를 구별하는 한 가지 특성은 연소파동의 방향으로 질량이동 (mass tran sfe r) 이 거의 없 다는 점이다. 그 피동의 전파는 전파의 방향보다는 그 파동의 면으로 확산함에 의해 주로 조절된다. 이것은 비교적 넓고 천천히 움직이는 연소파가 되게 한다. 정류상태 연소는 보통 0.1~15cm/sec 범위의 전파속도를 가지고 점화점으로부터 일정한 속도로 움직이는 일차원적 파동모형으로 표시되어 왔다. 이 속도는 펠릿의 지름, 처음 혼합물의 물리적 특성, 연소 엔탈피 (combustio n enth a lpy ) 등과 감은 수많은 파 라미터에 의하여 영향을 받는다. 이들은 뒤에 다시 상당히 세밀하게 논의될 것이다.
2-5— 2 진동 연소 (Osc ill a ti n g Combusti on ) 불안정 연소방식으로 알려진 진동 연소는 한정할 수 있는 진동수와 일정한 평균 파속 (wave s p eed) 을 갖는 맥동하는 평면 연소파동이다. 평균 파속은 보통 lcm/ se c 이하로 10sec-1 보다 작은 전동수를 갖는다. 그 진동은 사전으로 기록하면 돕니 모양이고 이론적으로는 수학적 모델로 예측되어 왔다. 연소속도와 전동수는 처음 혼합물이 불활성 첨가물을 포함할 때 첨가물에 의한 희석도, 초기 압축밀도 및 콤팩트 펠릿 지름 등의 변동에 의하여 증가 또는 감소될 수 있으며, 연소반 웅시에 역학적인 압축에 의해서도 영향을 받게 될 것이다. 정류상태 연소로부터 진동 연소로의 변형은 다음 파라미터에 의해 조절된다고 이론적으로 보였다. 35) a= 9 .1 X 운Jsf!- (1-0 . 27 蓋) 여기서 Ep 는 평균 비열, Q는 단위질량당 발생열량, R 은 이상기 체상수, Tc 는 단열 연소온도 및 E 는 활성화 에너지 등이다. a 가 1 보다 작을 때에는 전동 연소방식으로 반응이 진행되고 a 가 l 보다 클 때에는 정류상태 방식으로 반응이 진행된다. 그 생성물은 보 통 따로따로 소결되어 박편 (wa fe r) 모양을 가전 총상구조를 하고 있 다. 이러한 충들은 일반적으로 쉽게 분리되고 그들의 두께는 맥동 전 동수(p ulsa ti on freq u ency) 에 달려 있다. 2— 5— 3 스 핀 연소 (Sp in Combusti on ) 회전 연소방식은 기체 연소에서 아주 일반적인 것이나 응축된 물질 의 비기체 연소에도 나타난 적이 있다. 콤팩트의 점화시에 작고 빛나
는 점이 시편의 원통 바깥 표면에 나타난다. 이 점은 원래의 위치로 부터 아직 타지 않은 부분의 바깥 면을 따라 나선 모양으로 움직인 다. 나선형의 회전으로부터 대응하는 자국을 따라서 점차 소실되는 밝은 자국을 뒤에 남기면서 움직안다. 이 운동은 보통 연소반응이 끝 날 때까지 lcm / sec 의 속도로 계속된다. 여러 개의 점들이 희미한 나선형 자국을 뒤에 남겨 놓고 동시에 같 거나 또는 다른 방향으로 선회하기도 한다. 회전 연소에 의한 표면충 의 두께는 약 2mm 이하이다. 초점은 압선 회전 때문에 생긴 가열된 충을 따라서만 안정된 방식으로 움직일 수 있다고 가정되어 왔다. 이 러한 충의 자국으로부터의 이탈은 증가되는 열의 손실 때문에 소화될 것이다. 2— 5— 4 반복 연소 (Re p ea t ed Combustio n ) 반복 연소는 새로운 물질에 첫번째 연소파동의 전파를 따라서 이미 타버린 물질을 통하여 두번째 연소파동의 통과로 이루어진다. 반복 연소는 정상과 급속의 두 가지 형태가 보고되었다. 급속 반복 연소 (fast r epe a te d combusti on ) 는 연소시 간이 시 약의 확 산시간보다 대단히 짧은 응축계에서 주로 일어난다. 시약의 일부분만 이 첫번째 파동의 통과로 반응한다. 연소대가 훨씬 더 광범위하고 연 소 속력이 첫번째 파동보다 더 느리기 때문에 두번째 파동은 체적 (volumetr ic) 반응으로 종종 나타나기도 한다. 정 상 반복 연소 (normal repe a te d combustio n ) 는 유사하지 만 파동속 도의 차이가 급속 반복 연소만큼 크지 않으며 일반적으로 금속-기체 계에서 일어난다. 예를 들면 질소-아르곤 대기 (PN,=60atm , PAr=l a tm)에서 하프늄 (Ha fni um) 의 연소시 1 차 파동속도는 0.7cm/sec 이고 2 차 파동속도는 0.4cm/sec 로 일어난다. 반복 연소 현상은 위와 아래 끝에서 동시에 점화되는 시료에서도
관찰되어 왔다. 두 개의 1 차 파동 진행앞면 (wave fr on t)들은 똑같은 속도로 서로를 향하여 움직인다. 충돌되는 지점에서 두 개의 엇갈리 는 2 차 파동의 진행앞면이 만들어지고 감속된 속도로 이미 타버린 물 질을 통해서 지나간다. 반복 연소 현상은 대기압, 시편의 밀도, 금속 반옹물질의 입자 크기 등에 의하여 영향을 받는다• 2-5-5 표면 연소 (S urf ace Combusti on ) 표면 연소는 바깥 표면을 따라서만 연소가 가능한 금속-기체계에서 일어난다. 시료 내부는 반응하지 않거나 표면 연소 진행앞면이 지나 간 다음에만 반응한다. 표면 연소를 일으키려는 제한 파라미터는 표 면 내부까지 기체를 투과시키는 것이다. 기체의 소모 때문에 반응대 (reacti on zone) 와 저 항 대 기 (resis t i ng atm o sp h ere) 사이 에 압력 차가 생 긴다. 표면 연소에서는 대기가 충분히 빨리 내부로 뚫고 들어갈 수 없어서 표면 반응과 똑같은 속도로 내부 반응이 일어날 수 없다.
제 3 장 비기체 연소 생성물 〈 보다 많은 다양한 응용을 위하여 비기체 연소합성으로 몇 가지 생 성물을 제조할 수 있다 〉 (표 2.2 참조)는 Merzhanov 의 발표 5) 에 더하여 현재 다수의 연구자들은 생성물들의 물리적 형태들 사이에서의 몇 가 지 차이점들을 주목하여 왔다. 세 가지 생성물 형태의 합성에 대한 특허권을 취득한 소련 공정들을 이 장에서 설명하고자 한다. 이 세 가지 생성물 형태는 일반적으로 표준형, 분말형, 그리고 주 물형으로 나누어지는데, 표준형은 원소조성의 분말 혼합물이 기본적 인 형태의 변화 없이 그 장소에서 생성물로 변화되는 것이고 주물형 은 생성물과 슬래그 (sla g)가 반웅중에 생성되고 또 동시에 분리되는 형태이다. 3— 1 표 준 생성물 소련 연구자들은 적어도 4 개국에서 비기체 연소합성으로 특허를 받 고 있다. 기본적 합성과정 기술은 미국 36) 과 소련 37) 양국에서 특허를 받고 있다. 이들 특허들에서 그들은 붕소화물, 탄소화물, 염소화물, 불소화물, 질화물, 인화물, 규소화물 및 황화물과 같은 단순 세라믹
스 화합물을 형성할 수 있는 금속 전이원소와의 반응들을 강조하고 있다. 특별한 점화 화합물 또는 비고체 반응물이 간혹 사용된 것을 제의하고는 그 공정은 일반적으로 그림 2 . 1 에서 설명한 조작순서를 따른다. 점화 화합물은 낮은 접화온도를 갖는 특별한 분말 혼합물이 므로 그 화합물은 점화표면 위에 놓여져 연소파의 개시를 쉽게 한다. 비고체 반응물들은 비금속성 원소들인데, 그중 기체 수소는 수소화물 화합물을 합성하는 데 사용되어 왔고, 기체 또는 액체 질소는 보통 질화물 화합물을 합성하는 데 사용되었다. 소련의 Merzhanov, Naib o rodenko 및 Maksim ov 등 4) 은 다른 소련 특허둘을 얻었거나 요청하고 있는데, 이들 각각은 유일한 공정의 적 용 또는 단일 혹은 비교적 소수의 생성물 조성들에 한정되어 있다. 이들 특허에는 붕소화물, 탄소화물, 질화물, 금속간물질(i n t er met~ llics ) 및 제일철합금(fe rroallo y) 등을 생성하는 합성과정이 포함 되어 있다. 다음 장에서 논의될 공정 적용은 예비 반응가열(열폭발), 화학적 활성제 의 사용, 화학로(th ermal blanketi ng ) 및 비 기 체 연소반 옹과 병행한 압력의 사용 등이 포함된다. 1977 년과 1978 년 사이에는 제강에 사용된 마스터 합금 (mas t er alloy) 화합물의 생성에 대한 특허들이 출허되었다. 미국 4) 에서는 이 들 물질들이 언제나 전기로에서 생성된 반면에 소련 연구자들은 비기 체 연소합성법을 생산가가 낮은 대용 합성법이라고 주장하였다. 공업적인 관점에서 볼 때 도구 부품 형태로의 응용성을 지니는 고 밀도 T i C 의 직접 합성 38) 은 상당히 중요하다. 충분히 고밀도화된 최 종 형태의 표준 생성물형을 직접 합성하는 데 성공하였다고 주장한 소련 논문에서 그 내용이나 또 다른 참고문헌을 발견할 수 앞었다. 이 특허 는 Dnepr o vskiy Hard Alloy s P lant 에서 최 근 출판물의 주제 였 던 티타늄 세라믹스 철단기 (cu tti n gt ool) 들을 생산하는 데 사용된 공 정을 잘 설명 39) 할 수 있다. 비기체 연소합성을 이용하여 공업적 발열체들 (M0S i 2) 의 생산에 관 한 특별한 발명 특허권은 아직 확인되지 않았지만 의미있는 공업적
성취 40) 로 소련 언론에서 발표된 바는 있다. 그렇지만 이들 발열체들 이 최종 형태로 전환된 것인지 결정할 증거는 기술적인 문헌에서 찾 아볼 수 없다. 비기체 연소합성의 공업적 사용에 관한 또 다른 소련 언론의 발표 는 니켈화티탄의 생산 41) 이다. 이 물질은 열적 감도가 필수적인 성질 인 형 상기 억 합금 (memory allo y)으로 사용되 어 왔다. 수백 킬로그램 의 니켈화티탄이 선, 판 및 관(t ube)42) 의 형태로 생산되어 왔다. 이 생 성물은 현재 소련 항공기에서 특히 연료와 공기의 통로(lin e) 분야에 많이 이용되고 있다. 비기체 연소합성의 공업적 응용에 관한 소련 참고문헌들을 몇 가지 더 열거하면 아래와 같다. i ) 흑연과 몰리브덴의 넓은 면적 용접 .43) ii) 부식성 매질을 다루는 데 사용되는 이중총 파이프의 결합 .43) iii) 발열반응열이 낡은 공업용 장치의 표면 수리에 반응열을 이용 할 수 있도록 하는 비 기체 연소전극들. 44) iv) 내화성 세라믹스충둘로 된 터빈 날개의 표면 코팅 .45) 금속-비금속 결합에 대하여 제한된 비기체 연소기술의 사용은 공업 적 공정들로 호기심을 돋우고 있다. 그 제안된 응용들이 낡은 산업장 치를 보수하는 데 확장될 때 중장비의 간단한 전장수리는 직접 방위 산업으로 응용될 수 있는 전망이 있다. 비기체 연소기술의 산업적 응용에 관한 연구둘이 최근 소련 언론 간행물에서 상당한 주목을 받고 있다는 사실은 그 연구개발 계획이 계속해서 예산지원을받을것임울예견하게 한다. 그리고미국은이러한 소련의 연구개발 계획에 특별한 관심을 갖고 계속 주시하고 있다. 3— 2 분 말 생성물 충분히 고밀도화된 합성 생성물을 만드는 것이 어렵다고 보아 소련
연구자들은 아마 세라믹스 분말을 공업적으로 이용하도록 깨닫게 되 었을 것이다. 적어도 그들의 기술적 문헌은 많은 화합물이 분말형 최 종 생성물로 의도되어 합성되어 왔음울 보여주고 있다. 소련의 기술논문과 언론 발표에서 가장 관심을 받고 있는 분말 생 성물은 탄화티탄이다. 이 합성공정에 대하여 Merzhanov 는 소련 46) 과
 접화 연결
접화 연결
그립 3. 1 Ti C 분말의 비기체 연소합성의 개요도.
미국 47) 양국의 특허를 받은 바 있다. 그립 3.1 의 도식은 재사용이 가 능한 용기내에서 20k g의 탄화티탄 분말을 어떻게 생산하는지를 보여 준다. 또 다른 소련 특허에서는 탄화지르코늄과 탄화티타늄 분말들의 생 성에 대한 공정 48) 이 설명되어 있다. 이 경우 금속성 반응원소의 수소 화물은 반응 혼합물 안에 있는 원소금속 및 램프 그울음과 결합한다. 수소화물의 성분은 반응온도를 조절하고 탄화물 생성물의 입자 크기 를 증가시키는 영향을 미치며 이때의 입자 크기는 3~25 µm라고 보고 되었다. 여 러 가지 참고문헌에서 탄화티 탄의 분말 생 성물은 연삭(gri nd i n g) 및 연마(p ol i sh i n g)하는 데 공업적으로 잘 사용된다고 43),49)~52) 보고되 었다. Baku 에 있는 새로운 분말야금 시험공장(pil o t p lan t)에서 이들 생성물을 생산하고 있다고 또 다른 언론에서 발표하였다 .53) 비록 생 산공정이 확인되지는 않았지만 이 설비를 이용한 다론 생성물은 탄화 붕소, 탄화질화티 탄 (titan iu m carbon itrid e ) 및 질화규소 등이 다. 그들 각 화합물들은 소련에서 비기체 연소합성으로 생산되고 있다. 비기체 연소합성에 의한 분말 생성물의 다른 공업적 이용은 다음과 같아 소련 문헌에 보고되어 있다. i ) 수소화 분말 생산의 특허가 출허되었다 (Nd, Sm, Sc, Ti 및 Y)?4) ii ) Annen ian SSR 의 과학원에서 차후에 분말로 분쇄 하는 많은 수 소화물을 성공적으로 생산하였다고 55) , 56) 보고하였다. iii) 비 기 체 연소합성으로 생산된 이봉소화티 탄 (T iB 2) 과 이규소화티 탄 (T i S i 2) 분말들이 티탄의 구조적 합금의 분산경화 밀어내기 (dis p e rsio n -harden extr us io n )5 7) 에 이 용되 었다. iv) 윤활제로서 황화물과 셀렌화물 분말들의 생산과 사용법이 또한 보고되 었다. 33),44),58),59) 미국의 S mith 60) 는 소련의 비기체 연소기술과 비슷한 공정으로 탄화 텅스텐 분말의 생산에 대한 특허롤 받았다• 그 미국 공정에서는 산화 철, 알루미늄 및 탄화칼슘과 혼합된 72 돈의 텅스텐을 60 분 이상 반웅
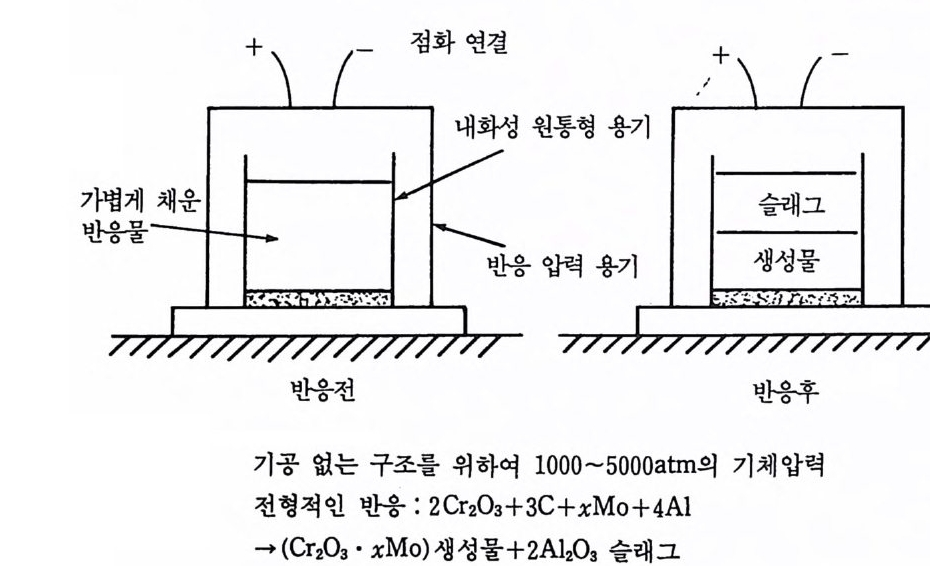
하여 22 돈의 탄화텅스텐 (WC) 을 생산하였다. 3— 3 주물 생성물 소련 연구자들이 비기체 연소합성으로 고밀도 생성물을 얻기 위해 연구한 방법 중의 하나는 액화법이다. 금속열과정 (rriet a l loth e rm ic pro cess) 61) 에 서 이용한 형 태 의 반응은 그립 3. 2 에 서 보는 바와같이 표준형 합성과 일치하고 있다. 일반적으로 원소반응물, 금속산화물 및 환원제를 혼합하여 반응 전 콤팩트 (gree n com p ac t)를 형 성 하도록 압력을 가한다. 점화 후 좁은 반응파동이 내용물을 따라서 진행된 뒤 에 주물 생성물 (cas t p roduc t)과 슬래그 (sla g)로 분리된 충을 형성한 다. 소련 공정설명 개요도에서 윗부분이 열리고 선도 긋지 않은 반응 용기가 사용된 것을 정확히 전술하지 않았다. 고열 등방압 프레스 (hot iso ta t ic pre ssin g 또는 HIP) 의 작동법 으로 내 용물을 밀폐 하는 다
 + _ 점화연결 +
+ _ 점화연결 +
그립 3.2 비기체 연소합성법을 수정한 주물 생성물의 개요도.
론 방법이 있다. 분명히 비기체 연소합성법으로 생산된 주물 생산물에 대한 첫번째 공식 발표는 연소공정에 관한 소련 전국회의 62) 에서 행하여졌다. 더 이전의 특허는 프랑스 8) 에서 얻었지만, 영국과 소련 63) 에서 그 공정 에 대한 소련 연구자들의 특허출허와 이 공식발표는 거의 동시에 행 해졌다. 비기체 연소합성 프로그램 64) 의 소련 지도자가 기술적 개관의 공정설명과 니켈화티탄을 생산하기 위한 참재적 활용을 토의한 뒤에 주물생성법이 개발되었다. 그 생성물에는 다음과 같은 것들이 포함되 어 있다. i ) 붕소화물 : MoB. ii ) 탄화물 : CraC2, Mo2C, VC, WC. iii) 질화물 : VN. iv) 규소화물 : NbSi2 , V3Si. v ) 금속간 화합물 : 니켈화티탄. vi) 착화합물 또는 서벳 (cermet) : (MoB 와 Ni) , (Cr2 야와 Mo), (T i C 와 Ni 를 포함하는 Mo2C) , (Ni 또는 Ni 와 M g를 포함하는 TiC 와 Cr203) , (Ni 또는 Ni 와 Mo 를 포함하는 TiC 와 Mo2C) , (VC 와 Co) , (VC 와 Ni) , (WC 와 Co) , (WC 와 Mn) . 3— 3— 1 열역학적 인 측면 이 과정은 환원제로서 하나는 알루미늄과 또 다른 것은 마그네슘을 사용할 때를 비교함으로써 보다 잘 알 수 있다. 소련 연구자들은 MoB 의 생성반응에서 환원제로 알루미늄과 마그네슘의 경우를 보고 하였다. 알루미늄을 환원제로 사용할 경우 화학양론적 반응식은 다음 과같다. 2Mo03 +B203+ 6Al __~ 2MoB + 3A} i03
열역학과 표준 화학사전을 이용하여 이 반응의 과잉 엔탈피 (excess en th al py ) 는 267.3kc a l/ mol 로 계산된다 . 마그네슘울 환원제로 사용하 여 MoB 를 생성하는 화학양 론 적 반응식은 다음과 같다. 2Mo0 吐 B203+ 9Mg ---> 2MoB+ 9Mg 0 이 반응은 315.8kca l/ mol 의 과잉 엔탈피를 방출한다. 마그네슘울 환원제로 사용하는 경우가 더 큰 과잉 엔탈피를 얻었지만 대부분의 반응 에서 환원제로 알루미늄을 선택하였다고 소련 문헌에 보고되었다. 반응온도는 모든 성분들의 녹는점보다 높아야 하고 반응을 시작하 는 데 충분한 에너지가 이용되어야 하기 때문에 금속열 방법에서는 높은 반응열이 필요하다. 반응 중에 8~30% 까지 변하는 열손실 63) 을 상쇄하기 위하여 실제 반응온도는 모든 성분의 녹는점보다 150 에서 200°C 이상이어야 한다. 이들 양을 계산하는 방법은 매우 복잡하므로 몇 가지 금속열반응에 대하여 널리 알려진 계산기술에 도전할 수 있 다. 예를 들면 소련에서 Ti C 서멧 (50% TiC +40% Cr3C2+10% N i)의 생산은 다섯 가지 초기 성분과 여러 가지 중간체상을 포함하고 있다. 더구나 휘발성 성분으로부터 많은 기체를 발생하는 경우 계산을 복잡 하게 할 뿐만 아니라 반웅폭발을 유발하는 원인이 될 수도 있다. 3-3-2 반응속도 금속열반응둘의 속도론에서는 연소분리와 응고상중 반응의 실상을 예상하고 최종 생성물의 특성을 예상하도록 고려되어야 한다 . 다음 논의는 실험적 관찰을 61) , 6 ◄) 기초로 한 반응속도론에 대한 소련 연구자 들의 견해롤나타낸다. 금속열반웅들은 정류상태 또는 불안정형으로 전행된다. 주어전 계 의 연소방식은 대기압 (P), 연소온도 (Tc), 환원제의 녹는점 (TT) 및
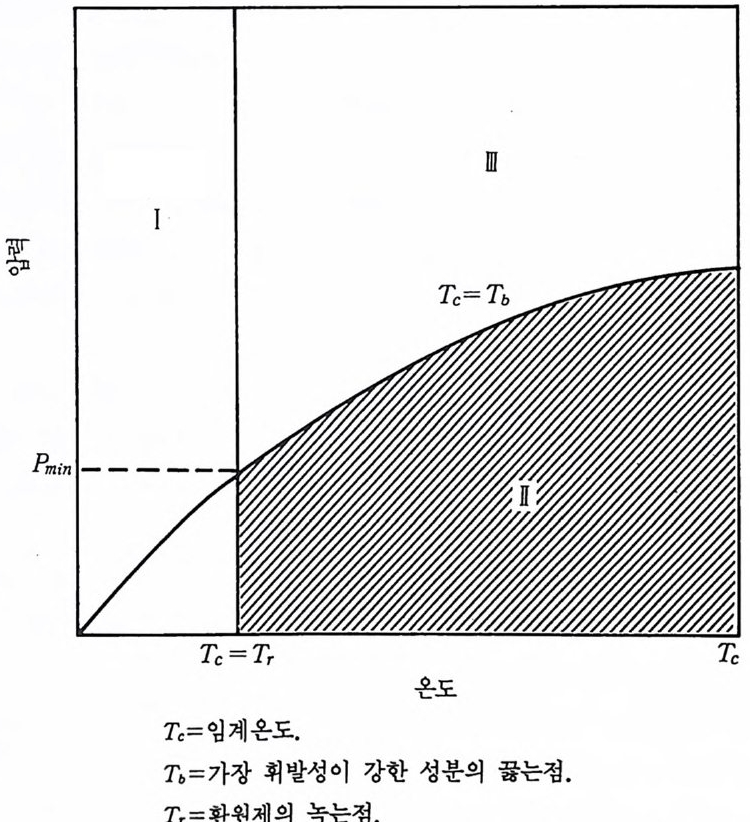
가장 휘발성이 큰 성분의 끓는점 (Tb) 에 의하여 영향을 받는다. 가장 휘발성이 큰 성분은 보통 환원제로 사용한 금속이거나 혹은 B203 이 다. 그림 3.3 에서 T, p도해의 I , Il 및 1l1 영역은 다음 변수에 의하 여 정의된다. I . Tc< Tr Il. Tc > Tr 및 Tc> T b fil. Tc> T r 및 Tc < Tb 영역 I 과 1Il 은 정류상태 연소영역이고 영역 I 는 불안정 연소영역
 Ill
Ill
그림 3,3 정류상태와 불안정 연소영역( I, Ill : 정류상태, n : 불안정).
이다. 불안정 연소영역에서 반응은 생성물의 강한 난사 (s t ron g sca tt er i n g)로 진행되거나 또는 곧 폭발에 달할 수도 있다. 연소파동의 속도는 반응속도 , 연소대 크기 및 반응이 일어나는 온 도를 나타내기 때문에 하나의 중요한 변수가 된다. 예를 들면 느린 연소파동은 비교적 느린 반웅속도와 계산된 연소온도보다 낮은 온도 에서 일어나는 많은 반응에서 한 넓은 연소대 (combusti on zone) 를 나 타낸댜 연소반응 속도론에 큰 영향을 미치는 다른 요인은 유효 열전 도도 (A) 이다. 일반적으로 고온반응 (Tc>2000°C) 에서 A 의 증가는 정 류상태 파동의 전파속도를 증가시킨다. 역으로 저온반응에서 A 의 증 가는 연소파동의 속도를 감소시키려는 경향이 있다. 이는 A 의 최적 값이 존재함을 나타내며 이 최적 A 값으로부터의 변화는 연소파동의 속도를 감소시킨다. 소련에서는 이 현상이 성분의 녹는 속도와 녹는 성분의 흐름에서 기인한다고 설명하였다. 반응물들이 서로 다른 용융온도를 갖는다면 액체물질은 낱알(gr a in) 의 표면을 따라 모세 분산 (cap illar y spr e adin g ) 또는 이 동 (migra- ti on) 으로 예비혼합이 일어난다. 비교적 낮은 온도 (1000~14oo·c) 에서 알루미늄 알갱이 (0 . 1~0 . 2mm) 에 대하여 알루미늄의 이동속도 59) 는 1.11 ~ l. 85cm/sec 에 달한다. 이 속도는 고온반응의 연소속도 범위내에 해당한다. 열전도에 대해 밀접한 관계가 있는 함수인 용융속도가 충분히 빠르면 반응은 이동속 도보다 더 빠르게 진행되는 것도 가능할 것이다. 낮은 반응온도 화학 종에 대하여 이동속도가 반응속도보다 빨라서 이동하는 성분이 많은 양의 열을 반응으로부터 제거할 수 있게 한다. 그러면 어떤 화학적 환원은 반응대 앞(p re - reac ti on zone) 의 낮은 온도에서도 일어 날 수 있 다. 열전도도의 증가는 이런 현상을 증가시키며 반응속도는 더욱 감 소시킨다. 이 방법으로 반응을 동결(q uench) 시키는 것도 가능하다. 연소온도 및 점화온도는 물론 반응속도도 촉매 또는 다른 첨가제들 의 첨가에 의하여 또한 많은 영향을 받을 수 있다. 이와 같은 첨가제 는 연소온도와 반응속도를 증가시키는 것과 점화온도, 연소온도 및
반응속도를 감소시키는 것의 두 가지 기본군으로 분류된다. NaN03, KCl03 및 Ba02 등의 테르밋 화합물들은 첫번째 군에 포함된다. A 를 증가시키므로 앞에서 말했듯이 반응속도에 영향을 미치는 화합물들에 는 불소화물과 염화물염 및 생석회가 포함된다. A 를 감소시키는 화 합물에는 불소화물염 (AIF3, Mg F 2, CaF2, NaCl) 들, 알칼리 및 알칼리토 금속 등이 포함된다. 반응속도를 증가시키는 다른 방법은 반응입자들의 접촉 면적을 최 대로 하는 것이다. 이 방법은 모든 화학종에 대하여 거의 같은 크기 의 마세한 낱알을 사용함으로써 이루어질 수 있다. 대기압력의 증가 (1 00~5000a tm)는 g값을 증가시키는 작용도 하지만 보다 중요한 것 은 높은 대기압은 휘발성 반응성분의 증발과 오염물질의 흡착을 방지 한다. 과잉량의 끓음 증발은 반응물의 양을 줄일 뿐만 아니라 반응을 방해하고 최종 생성물이 다공성(p ore) 의 성질을 갖게 한다. 높은 기 압은 매우 좋은 결과를 내므로 소련의 주물공정 합성에 사용되어 왔 다. 압력의 증가는 생성물의 수율과 반응속도를 증가시키고 또한 끓 음 증발량과 다공성을 감소시켜 주고 있다. 고속의 원심가속법이 다공성과 공동을 감소시키는 유사한 결과를 얻는 데 사용되어 왔다. 이 원심가속법의 사용은 생성물과 슬래그를 분리하는 데도 도움이 된다. 연소파동이 반응전 콤팩트{gr een comp a- c t)를 따라서 진행될 때 생성물은 어떤 한정된 시간주기 (Tm) 동안에 는 용융상태로 남아 있다. 만일 t o=O 초를 그 주물의 꼭대기에서 점 화가 일어나는 과정으로 정의한다면 그 반응은 한정된 시간주기 (Tc) 에 완결되도록 그 주물의 믿으로 진행된다. 완전히 분리가 일어나도 록 하기 위해서는 그 생성물이 응결되어 바닥에 가라앉아야 하므로 가장 위충에 점착하는 시간을 Ts 로 정의할 수도 있다. 그러므로 상 이 완전히 분리가 되려면 T.:-;;;Tm+Tc 의 조건이 만족되어야 한다. 그 러나 실제로는 Tc«Tm 이고, 산화물상은 내화성 화합물의 방울둘이 그것을 통해 움직이는 연속적 매질을 형성해야 한다. 원심가속법은 원하는 생성물의 수율을 감소시키는 불필요한 부수적
효과를 가지고 있다. 이러한 이유로 원심가속법은 Ts > Tm 인 그들 금 속열 조건에 대하여만 고려되어야 한다. 상분리에 대하여 고속 원심가속으로도. 임계 용기지름 (de) 이하에서 는 상분리를 성취하기가 어렵다고 보고되었다. d < 아인 경우 응결 (con g ela ti on) 이 상분리보다 빠르므로 연소생성물이 용융은 되지만 분 리되지 않은 덩어리를 형성한다. d > dc 인 경우 상분리가 응결보다 빠르므로 생성물과 슬래그는 선명하게 구분된 충으로 분리된다. de 의 크기는 원심가속의 증가 및 초기 온도의 증가에 따라 감소한다. 3— 3— 3 발달상태 소련에서 비기체 연소 주물 생성법의 발달상태는 소련의 보고된 여 러 특허둘 중에서 한 가지 결과를 재고기함으로써 가장 잘 알 수 있 다. 부록 A 의 표 형식으로 열거된 데이터는 넓은 조성범위의 생성물 (2 열)이 반웅산화물과 알루미늄 또는 마그네슘 환원제 (3 열)를 사용함 으로써 합성됨을 보여준다. 대기압력의 증가 또는 원심가속법 (5 열)을 사용할 때 기공 없는(p ore- fr ee) 생성물 (12 열) 이 형성된다는 것은 데 이터에 나타난 가장 중요한 주장이다. 다른 경우에서는 추가 데이터 없이 이 표의 상호관계를 이용하는 것은 어려울 것이다. 예를 들어 주어전 생성물의 밀도는 기공의 존재, 성분의 증발 또는 반웅완결성 의 차이에도 불구하고 대략적으로 일정한 값을 갖는다 (11 열). (6-9) 열에서 보는 바와같이 반응을 완결시키는 데에는 대기압력의 증가법이 원심가속법보다 효율적이다. 압력을 증가시키는 것이 원심 가속법에 비해 휘발성 기체의 방출을 더 잘 막을 수 있다는 것이 그 한 가지 이유이다. 이미 논의한 바와같이 이들 기체들은 반응물 증발 의 결과로 반응을 간섭한다. 이 표에서 상당히 홍미있는 다른 항목은 단순화합물(예 : Mo2C) 과 복합물(예 : T i C 와 Mo 2 C) 들이 합성된 것이 다. 경합금 (cemmen te d carbid e s, 예 : 90% WC 과 10% Mo 및 85% Cra
C2 과 15% Mo이 부록 A의 94 와 75 항목에 각각 보고되었다)과 금속간 화합물 6 5) 의 생산은 두 가지 모두 상업적으로 상당한 의미가 있다. 더욱 이론적 연구를 완벽하게 할 필요가 있을지라도 발전된 실제적 방법도 또한 중요하다. 고압(1 000~5000a t m) 또는 원심력(1 00~1500 g) 의 적당한 압력 (lOOa tm)하에서 고밀도 생성물의 생산이 인상적이지만 이들 금속열 공정들에 대한 반응 메커니즘의 이해는 아직 낮은 수준 에 머물러 있다. 소련 연구자들은 앞으로의 연구를 위해 다음과 같은 분야를 확인하고 있다. i ) 열과 열역학적 계산의 전보. ii ) 전체과정을 최적화하는 방법론의 개발. iii) 여러 가지 온도와 금속열 환원의 메커니즘과 반응속도론의 자 세한연구. iv) 기화되는 근원의 연구 및 발생된 기체와 승화체의 조성연구. v) 폭발될 수 있는 공정들의 확인. 3 一 4 고성능 콤팩트 생성물 일반적으로 내화성 화합물은 높은 융점과 성분 원소들의 낮은 자체 확산계수 때문에 소결되는 것이 어렵다. 30MPa 이하의 낮은 압력하 에서 전행되는 종래 소결방법 (conventi on al sin t e r in g me th od) 으로는 결 합제 없이 내화성 소재를 고밀도화하는 것은 불가능하다. 현재 일반 적인 고밀도화법은 산화물 또는 다른 적당한 원소들과 같은 첨가물의 존재하에서 정상소결과 고열-압력소결 (ho t-p ress s i n t e ring)하는 것이 다. 이들 첨가물들은 고밀도화에 중요한 역할을 하지만 그들은 자주 낱알경 계 (grai n boundary ) 에 제 2 상들을 생성 한다. 이들 제 2 상들은 고 온에서 역학적 및 열적 성질을 감퇴시킨다. 첨가제 없이 내화성 물질 을 고밀도화하는 유용한 방법은 고열-가압 (ho t-p ress ing )66) 으로 GPa
차수 및 고열 등방압 가압 (ho t iso sta t ic p ress i n g)으로 100~200MPa 차수 30) 고압을 가하는 것이다 . 첨가제 없이 고밀도화하는 것은 고온 세 기 (hig h tem p e ratu r e str en g th) 의 수행 뿐만 아니 라 자체 결 합된 난알 둘로 된 이상적인 내화성 세라믹스 소재의 특성을 정화하는 데도 의 미가 있다. 이와같이 비기체 연소합성 후 hot pre ssin g 또는 HIP 로 소 결시켜 고성능 내화성 생성물을 얻을 수 있다. 비 기 체 연소합성 (SHS) 과 역 학적 인 고압을 결합하여 GPa 차수의 압력이 가해전 상태에서 비기체 연소합성을 함으로써 생성반응과 동 시에 소결과정을 짧은 시간에 완료하는 고압 자체 연소소결법 (H ig h Pressure Self-C ombusti on Sin t e r i ng 또는 HPCS) 17),18),19),22) 으로 고성 능 콤팩트 생성물을 얻을 수도 있다. 한편 최신 공법에 해당하는 기체 -압력 연소소결법 (Gas-Pressure Combustio n Sin t e r i ng ) 16) 을 SHS 와 HIP 를 결합하여 고안한 바 있다. 이상 논한 바와같이 SHS 후에 소결시 키는 방법과 SHS 와 고압을 직접 결합시킨 방법을 통하여 상대밀도 (체적밀도/이론밀도)가 90% 이상인 고성능 콤팩트 생성물을 얻을 수 있다. 이들 방법의 상세한 설명과 실제 응용은 5 장, 9 장 및 10 장에서 다시 논의할 것이다.
제 4 장 비기체 연소에 영향을 주는 변수 소련 연구자들은 대부분의 경우 상업적 용도의 내화물 생산울 위하 여 그림 2.1 에 설명된 단순한 형태의 비기체 연소를 개선할 수 없었 다. 일련의 실험실 규모의 예비적 실험들은 각각의 가능한 생성물의 형태와 조성을 위한 특정 공정조건들을 결정하도록 수행되었다• 공정 개선에 대한 소련의 방법들을 이 장에서 재고하고자 한다. 그들은 모 두 다음과 같은 연소조절과 관련된다. i ) 연소활성화 : 이것의 목적은 반웅온도의 상승, 점화온도의 강 하, 불안정상태에서 안정상태의 연소방식으로 변화 또는 연소 속도의 증가등이다. ii ) 연소제동 : 이것의 목적은 반응온도의 강하, 연소속도의 감소 그렇지 않으면 불안정해질 생성물 조성의 해리를 방지하는 것 0] 다. 4— 1 규소화물 합성의 공정변수 규소화물 (s ilici des) 의 합성 에 관한 주된 소련의 연구 67) 는 많은 공정 변수들을 위에서 열거한 조철들과 관련시키는 것이다. 이들 공정개선
은 연소온도, 연소속도, 연소방식 등의 변화로 이루어진다. 규소화물 은 비기체 연소공정을 연구하는 데 바람직하다고 여겨지는 두 가지 유일한 특칭 때문에 실험 주제로 선택되었다. 첫째로, 규소화물은 상당히 낮은 단열 반응온도 (3000K 이하) 를 나 타내며 안정한 연소방식과 불안정한 연소방식의 양자는 규소화물 합 성으로 설명될 수 있다. 이에 반하여 모든 금속-탄소와 금속-질소계 둘 및 많은 금속-붕소 혼합물들은 3000~4500K 의 높은 온도에서 연 소한다. 둘째로, 실리콘 원자의 반지름이 크기 때문에 규소화물들은 틈새형 화합물의 범주에서 고려되지 않는다. 이들 실험의 바람직한 특칭은 광범위한 화학양론적 비를 갖는 비교적 많은 수의 규소화물(틈새형이 아닌)이 형성될 수 있다는 것이다. 4— 1— 1 화 학양론적 비 연소공정에 관한 화학양론의 영향이 세 가지 금속의 규소화물에 관 해서 표 4.1 에 요약되어 있다. 1 번에서는 연소 파라미터와 금속반응 표 4.1 규소화물의 연소합성에 대한 화학양론적 비의 영향. 1. 세 가지 금속원소의 규소화물에서 비금속 대 금속의 화학양론적 비에 따 라서 반웅온도 (Tad) 가 변한다• 1) Mo 이 증가하면 Tad7} 강하한다. 2) T i가 증가하면 Tad 가 상승한다. 3) Zr 이 증가하면 Tad7} 상승하고 최대 온도를 이룬 후 다시 강하한다. 2. 각 금속 조성의 수준이 실리콘 (S i)에 관하여 접전적으로 변하면 연소속 도는 증가하여 최대 온도에 달하고 다시 감소한다. 최대 온도에 대한 금 속 : S i의 화학양론적 비는 T i와 Zr 에 대하여는 약 1. 7 이고 Mo 에 대하여 는 1. 0 이다. 3. 대부분의 규소화티탄은 정류상태 연소방식으로 형성되지만 S i가 Mo 및 Zr 과의 모든 반응에서는 맥동하는 연소방식 (진동방식)이 관찰되었다.
물의 주기율표상에서의 위치 사이의 관계가 설명되어 있다. 참고문헌 (3) 에서 보고된 바와같이 생성물의 분자량이 감소함에 따라 연소는 강렬해지려고 한다. 또한 어떤 경우에는 연소가 너무 강렬하게 되면 생성물이 분해되는 경우가 있다. 반대로, 단열 연소반응은 국도로 낮은 연소 강도(Q /Tad) 에서는 불 가능하다. 낮은 강도의 한계에 대해서 소련 연구자들은 세 가지 규소 화물계의 단열 연소를 이루기 위한 최대 화학양론적 값을 표 4.2 와 같이 보고하였다. 표 4·2 화학양론적 비로 서 단열반응 한계. 규소화물계 비 (rat io) MZro — -SSi i 2.4 ( 112 : 5) Ti- S i 3 표 4.1 의 2 번과 3 번에서와 같이 금속과 규소의 화학양론적 비의 변 화는 연소속도와 안정성에 관계가 있을 수 있다. 정류상태 연소는 오 직 규소화티탄에서만 이루어진다. 최대 연소속도는 Mo- 화합물에 대 해서는 0.7cm/sec 이고 Zr- 화합물에 대해서는 3 . Scm/sec 이다. 4— 1— 2 반응물 펠릿의 지름 반응할 펠릿의 지름과 단열 연소 도달 사이의 관계는 각각 1.4 Si, 2Si, 2.4S i와 Mo 의 혼합물에 대하여 확립되었다. 이 세 가지 경우에 서 단열 연소에 대한 최소 지름 한계값(thr eshold) 은 약 20mm 이다. 모두 단일상 생성물을 형성하는 Ti+ 0.6 S i, Zr+ZSi 및 Mo+2S i에 대하여 반응 펠릿의 지름과 연소 안정도간의 관계를 확립하기 위하여 또 다른 실험이 계획되었다. 각 경우에 있어서 한계값 이하의 지름을
갖는 경우에는 연소가 불안정하고, 지름이 표 4.3 에서 보는 바와 같 은 한계값 지름에 가깝게 증가하면 연소속도는 증가한다. 이들 한계 값 근처에서 불안정한 연소방식이 안정한 연소방식으로 변화하고 연 소속도는 결국 점차적으로 일정해진다. 그 한계값 이하의 불안정 연 소에 대하여는 그 생성반응마저 불완전하게 된다. 표 4.3 정류상태 연소를 위한 한계값. 반웅 혼합물 a) 한계값 Mo+ZSi Zr+2Si Ti + 0.6Si 연소속도 (cm/sec) 0.7 1 3.5 반응물 펠릿 지름 (mm) 20 20 15 a) 모든 경우 반응 펠릿의 압축밀도는 이론밀도의 60~65% 였고 그 생성물의 조성은 단일상이었다. 4— 1-3 반응물 펠릿의 밀도 소련 연구자들은 반응물 펠릿의 지름을 20mm 로 일정하게 유지하 며 밀도를 변화시킬 때 이들 세 가지 연소계에 대한 유사한 관계를 보고하였다. 특정한 데이터가 보고되지 않았지만 한계밀도값 준위가 있어 그 아래에서는 아마도 연소가 안정하지 않거나, 일어나지 않는 것을 알 수 있다. 이들 한계값들은 이론밀도의 40~65% 범위 일 것이 라고 다른 소련 실험 데이터에 밝힌 바 있다. 4— 1- 4 반응물 분말의 입도 금속성 반응물의 입도는 연소공정에 상당한 영향을 미친다. 비금속
분말들은 일반적으로 마이크론 이하(l ow-m i cron) 와 초미세 (subm i- cron) 범위로 아주 미세하다. 소련 연구자들은 입자가 거칠수록, 입 자 크기 의 분별분포가 폭이 넓 을수록 (broad frac ti on al dis tr ibu ti on of siz e ) 연소속도는 감소되고 불완전한 반웅이 일어난다고 보고하였다. 규소화물 화합물에 대해서는 80µm 미만의 입자 크기가 적당하고 붕소화물과 탄소화물의 경우에는 더욱 거친 금속성 입자들도 아마 많 은 반응에 이용될 수 있을 것이다. 4- 1— 5 연소온도의 조절 연소온도를 강하시키기 위해 소련 연구자들이 광범위하게 사용한 방법은 생성물로 반응물을 희석시키는 것이다. 이것은 반웅속도를 늦 추거나 제동을 걸어서 종종 조밀하고 완전히 반응된 생성물을 얻는 데 도움을 준다. T i sS i 3 로 실험할 때 희석의 정도를 반응물의 0 에서 45% 까지 증가시키면 연소속도는 4 에서 0.7 c m/sec 까지 점차적으로 감소하게 된다. 30% 이상으로 희석된 경우에는 일반적인 정류상태 연소가 불안정한 연소로 되돌아간다. 여기서 상당히 낮은 단열 반응 온도를 갖는 반응 혼합물에서는 생성물로 희석되지 않은 경우에도 그 불안정한 연소가 기대될 수 있다. 역으로 연소온도는 200~600'C 로 출발물질을 예열시킴으로써 상승 시킨다 . 소련의 연구에서는 단일상 T i S i 2(Tad=1800K) 은 300~4oo·c 로 예열한 후 비기체 연소반응에 의하여 성공적으로 생성하였다고 보 고하였다. 그러나 본 연구실에서는 700C 까지 예열한 후에도 반응 혼 합물의 점화가 되지 않아 비기체 연소반응으로 T i S i 2 를 생성할 수 없 었다. 그래서 T i +2S i의 화학양론적 혼합물 펠릿 위에 T i +C 의 화학 양론적 혼합물의 얇은 펠릿을 올려놓고 점화시키면 일차적으로 비기 체 연소반응에 의하여 T i C 가 생성된다. T i C 생성 (Tad=3293K) 에 의 하여 발생되는 고열로 비기체 연소반응의 연속성이 이루어진다. 이와
갇이 예열 없이 이차적으로 비기체 연소반웅이 T i+ 2S i의 혼합물 펠 릿에도 진행되어 단일상 T i S i 2 를 생성하는 공법을 기술개발 23) 하였다. 4-1-6 규소 생성물 소련 연구자들은 M0Si2 , Tis S i3 , TiS i 2 등을 예 열의 도움으로 비 기 체 연소합성을 성공시켰다. 이들은 소련에서 고온로 발열체로서 상품으 로 이용된다. 규소화지르코늄 중에는 오직 ZrS i 2 만이 성공적으로 합 성되었다. 이 계의 다론 규소화물들은 연소 중 안정성이 없고, 그들 울 합성 하기 위 하여 생 성 물 희 석 (pro duct dilu ti on ) 이 필요하다. 4-2 연소과정의 물리적 변수 비기체 연소공정에 대한 세 가지 물리적 인자들인 반응물 펠릿의 지름과 밀도 및 반응물 입자 크기의 영향은 규소화합물의 합성에서도 이미 논의하였다. 연소역학과 물리적 인자간의 유사한 관계가 이 절 의 끝에 설명한 바와같이 소련 논문에 보고되었다. 특정 내용이 약간 변할지라도 물리적 특성과 연소역학간에는 다음 관계가 잘 일치된다. i ) 밀도 : 반응물 펠릿의 밀도 상승은 생성물 중에 미반웅물의 양 을 감소시키며 단열 반웅온도를 상승시킨다. 한 예 68) 를 들면 연소속도 증가는 반웅물 펠릿의 밀도가 약 55~60% 까지 증가 함에 따라 이루어진다고 보고하였다. 죽 이 최대 밀도 이상의 범위에서는 그 반대현상의 관계를 보인다. ii) 지름 : 반응물 펠릿 지름의 증가는 반응속도를 증가시키며 생성 물 중 미반응물의 양을 감소시키는 경향이 있다. iii) 금속성 분말 반응물의 입자 크기 : 금속성 입자의 크기가 거칠
면 거칠수록 반응속도를 감소시키며 미반응물의 양을 증가시키 고 단열 반응온도를 감소시키려는 경향이 있다. iv) 금속분말 반응물의 입자 크기 분포 : 보다 넓은 분율의 분말 분 포는 미반응물의 양을 증가시키려는 경향이 있다. v ) 반응 후의 냉 각 : 서 냉 (slow cooli ng ) 이 미 반응물의 양을 감소 시키려는 경향이 있다. 비기체 연소합성 화합물에 영향을 주는 물리적 인자를 조사한 실례 는 다음과 같다. i ) Hf, Mo, Nb, Ta, Ti 및 Zr 의 붕소 화합물들 69) : 반응물 펠릿의 지름, 반응물 펠릿의 밀도, 금속반응물의 입도, 냉각속도. ii ) TiC 1 0) : 반응물 펠릿의 지름, 반응물 펠릿의 밀도, 금속 반응 물의 입도, 반응물의 입자 분포. iii) TaC 및 Ta2C 1 1) : 반응물 펠릿의 지름, 반응물 펠릿의 밀도, 냉각속도. iv) TiC 1 2) : 비금속 반응물의 표면적, 비금속 반응물의 입도, 비 금속 반응물의 마이크로 구조 특성. v ) TiS i , T iS i 2 및 Tis S i3 73 ) : 금속반응물 입 도. vi) Nb-Al 및 Nb-G e 68> : 금속반응물 입도. 반응물 펠릿의 밀도. 위에 인용된 관계 의에 또 대부분의 물리적 성질이 연소방식에 영 향을 미친다는 것이다 . 연소를 빨리 전행시키거나 반응온도를 상승시 키는 물리적 인자들의 변화는 정류상태 연소를 유지하려고 한다. 어 떤 경우에 여 러 가지 물리적 성 질들의 한계 값(thr eshold value) 들은 정류상태 연소에서 불안정한 연소방식으로의 전이에 대한 값으로 보 고되었다. 참고문헌 (69) 에서 한계 연소속도는 물리적 인자들에 관련 되어 있다. ZrBr2 의 합성에서 반응물 펠릿의 상대밀도가 60% 인 경 우 그 한계속도는 완전히 단열된 구역에서 얻은 값의 0.65 배라고 보 고하였다. 불안정한 연소가 일어나고 있을 때 물리적 성질은 연소의 맥동 (pu lsin g ) 또는 전동수와 관계가 있다. 본래는 연소방식이 정류상태
연소가 아닌 모든 예에서 불완전한 반응과 생성물 성충(l a y er i n g : 가 변적 밀도 영역들)이 기대된다. 그 물리적 인자의 조사 실례의 i v) 에 인용된 참고문헌 (72) 에서 금 속성 입자보다는 비금속성 반응물의 특성이 더욱 연소변수들에 관계 가 있다고 다음과 같이 설명하였다. i ) 램프 그을음 입자 크기가 작을수록 반응속도와 반응완성도를 증가시키는 데 효과적이다. 이 관계는 물질의 추가분쇄로 분자 〈탄소연쇄〉를 추가로 붕괴시킨 결과이다. ii) 램프 그을음 표면적이 클수록 연소속도에 조금밖에 영향을 미 치지 않는다. iii) 램프 그울음 입자에 흡수된 기체는 합성 중 생성물 펠릿을 괭 창시킨다. 그 결과로 연소속도는 감소되고 미반응 물질의 양은 증가된다. iv) 탄소의 하소 (cal cini n g) 혹은 흑연화(gr a p h iti za ti on) 는 합성반응 울 촉진시키는 데 역효과적이다. 4— 3 연 소조절 비기체 연소합성법의 연소조절에는 여러 가지 변수와 요인들이 있 울 수 있지만 예열, 생성물 희석 및 화학 활성제 (chem ica l acti va ti ng a g en t)에 의한 연소조절만을 이곳에서 논의하고자 한다. 부분적으로 앞에 설명했거나 뒤에 설명하게 될 내용과 중복되는 경우도 있겠지만 개념을 확실히 이해하는 것은 대단히 중요하다. 4-3— 1 예열 〈열폭발(th ermal exp lo sio n )> 공정개선으로 소련 문헌에 알려진 한
공정기술 혁신은 보충 가열하는 것이다. 보통 이 용어는 반웅 동안에 높은 반응온도를 얻거나 반응 도중 녹게 하기 위하여 반응물을 예열 하는 것을 나타낸다. 참고문헌 (38) 에 의하면 생성물 (T i C 및 AlN i)의 융해는 자체 점 화 (sel f-igniti on) 온도에 도달할 때 까지 프로그램 된 단 계들을 거쳐 반응물 예형 (p re fo rm) 을 예열시킴으로써 이루어진다. 참고문헌 (67) 에서와 같이 규소화합물을 합성 할 때 상승된 반웅온도 는 200~6oo·c 로 예형(p re fo rm) 을 예열함으로써 얻어전다. 탄화탄탈 의 생성 74) 에서 예형을 4oo·c 로 예열함으로써 미반응물의 양이 12% 에 서 2% 로 감소되었다. 참고문헌 (68) 에서 금속간 알루미늄화물(i n t er meta l li c alum ini d e s) 의 예 열은 CrA13, M0Al2, TiA I 등의 비 기 체 연소에 서는 필요하지만 CoAl 과 NiA l 에서는 불필요하다. 알루미늄화구리의 합성 68) 에서 예형의 지름, 예형 밀도 및 예열온도간의 관계는 정류상 태 연소조건에 관하여 확립되었다. 일반적으로 450~54o•c 정도의 예 열이 필요한 것으로 알려졌다. 이 합성기술로 만들어진 알루미늄화구 리는 전기아크 재용융조작에서 전극으로 사용될 수 있다는 것이 이 참고문헌의 중요한 결론과 상업상의 관련성이다. 4— 3— 2 생성물 희석 (Product dil ut i on ) 비기체 연소반응의 강도를 감소시키거나 또는 제동을 걷기 위하여 원소반응물들울 어떤 생성물 물질과 혼합시킨다. MoB, NbB2, TaB2 및 ZrB2 의 합성에서 경험하였듯이 반응제동 (rea ti on brak ing)은 높은 단열 반응온도를 감소시킨다는 것을 참고문헌 75’ 에서 설명하였다. 이 예에서 여러 반웅 혼합물에 10~67% 의 생성물 첨가제는 약 50~10oo·c 의 단열 반응온도를 감소시킨다. Sark i s y an67) 과 Borov in- ska i a69) 는 연소속도의 감소와 연소방식에 대한 생성물 희석의 효과를 설명하였다. 규소화물 (Tis S i3 ) 과 붕소화물 (Hf B2 , NbB2 및 ZrB2) 의 합성 에 서 생
성물 희석이 증가함에 따라 연소속도는 점차적으로 감소하고, 어떤 점에서 그 연소방식은 불안정 연소방식 (auto - oscil lat o r y or auto - v i bra ti onal) 으쵸i 변한다. T i sS i 3 의 경우에 연소방식의 전이는 반응 혼 합물을 생성물로 30% 희석할 때 일어난다. 탄화탄탈의 합성 m) 에서 생성물 희석의 효과는 단열 반응온도의 감 소와 반응완결의 증가를 나타낸다. 유사하게, 탄화탄탈의 다른 실험 적 합성 1” 에서 반응 혼합물의 생성물 희석은 연소속도의 감소, 미반 응물의 증가 및 자동진동 연소 (auto - oscil lat o r y combusti on ) 의 진동수 감소를 일으칸다. 또 다론 생성물 희석실험 73) 에서 입도에 대한 필요조건은 T i sS i 3 의 합성에 인용되었다. T i와 Si 원소분말에 대한 크기는 45µm 이하이며 생성물 희석을 위한 필요한 크기는 63µm 이하이다. 이 경우 희석의 중량 퍼 센트가 20% 로 증가되 면 그 측정 된 온도는 24oo·c 에 서 l850°C 까지 선형관계로 떨어지고 연소속도는 3cm/sec 에서 0.5cm/sec 까지 유사한 관계로 떨어진다. 4-3-3 화학 활성제 비기체 연소반응의 조절을 위해서 화학 활성제의 사용은 소련 연구 자들이 다른 예에서 보고하였다. 한 예 76) 를 들면 활성제 (CaCl2, KMnO., NaF 및 NH.Cl04) 가 0.0005~0 . 003moles/ g -a t om 의 붕소수 준으로 사용된 붕소화물 (GeB, M0B2 및 Mo2B) 을 합성 하는 방법 이 특허를 받았다. 그 첨가제는 생성 화합물의 순도를 증가시킨다. 한 특별한 붕소화제 77l (magn e siu m po lyb orid e , 12%Mg 및 88%B) 는 Ti- C r 및 Zr-Cr 붕소화물을 합성하는 데 사용된다. 활성제는 연소속도를 감 소시켰으며 합성에서 얻어진 균일한 고용체의 조성영역을 확장시킨다.
4 一 4 비기체 연소의 정제효과 소련 연구자들은 비기체 연소합성 중 반응물을 정제시킨다고 보고 하였다. 예를 들면 T i sS i3 의 합성 중 두입한 출발물질의 금속 불순물 함량이 0 . 7% (6978 ppm ) 였으나 생 성 물에 서 는 0 . 05% (452 ppm ) 로, 죽 15 : 1 정도로 감소되었다는 것이다. 일반적으로 의부 가열이 필요한 종래의 공정에 있어서는 온도 상승시간, 소결시간 및 온도 강하시간 이 비기체 연소합성에서보다 대단히 길다. 반응과 가열 냉각에 있어 서 단시간 노출하는 큰 장점은 미세한 구조와 성질의 조절에 응용할 수 있을 뿐더러 주변 대기에 포함된 물질과의 오염을 감소시킨다는 점이다. 대부분의 재래식 공정과는 반대로 출발물질보다 오히려 화학 적 순도가 높은 생성물 23) 을 얻을 수 있다는 것이 비기체 연소합성의 장점 중 하나이다. 이것은 반응시 고온에서 불순물이 기화되고 반응 물 또는 생성물 중의 적어도 한 물질이 액화된 상태에서 연소파가 이 동하는 소결 메커니즘 (s i n t e ri n g mecha ni sm) 으로 띠정제 (zone refin - ing ) 7 8) 효과를 나타내기 때문안 것으로 설명할 수 있다.
제 5 장 생성물의 고밀도화 내화성 화합물의 합성을 위한 여러 가지 비기체 연소공정들의 개발 에 직면한 한 가지 주된 문제는 그 생성물을 완전히 고밀도화 (dens ifi ca ti on) 할 수 없다는 점이다. 만일 공정 조건들이 각 경우에 적합치 않으면 그 생성물은 다공성의 저밀도 물질이 될 것이다. 이 문제에 대한 명확한 해결은 필요한 추가 고밀도화를 얻기 위하여 간 단한 형의 비기체 연소와 압력을 결합시키는 것이다. 소련 연구자들 은 이러한 목적으로 많은 연구를 수행하였다. 이 장에서는 한편으로는 화학로 (che mi cal furn ace) 의 개 념 , 응용 및 고밀도화시 간접적인 영 향 등, 다른 한편으로는 원소반응물로부터 화 합물 합성시 압력응용의 방법, 이론 및 실험 등에 관하여 논하고자 한다. 5— 1 화학로 종래의 고밀도화법은 고온 전기로내에서 생성물질을 소결하는 방법 울 사용했다. 그러나 한정된 온도까지밖에는 발열체로 가열할 수 없 었다. 소련 연구자들이 더 높은 반응온도에 도달하기 위하여 사용한
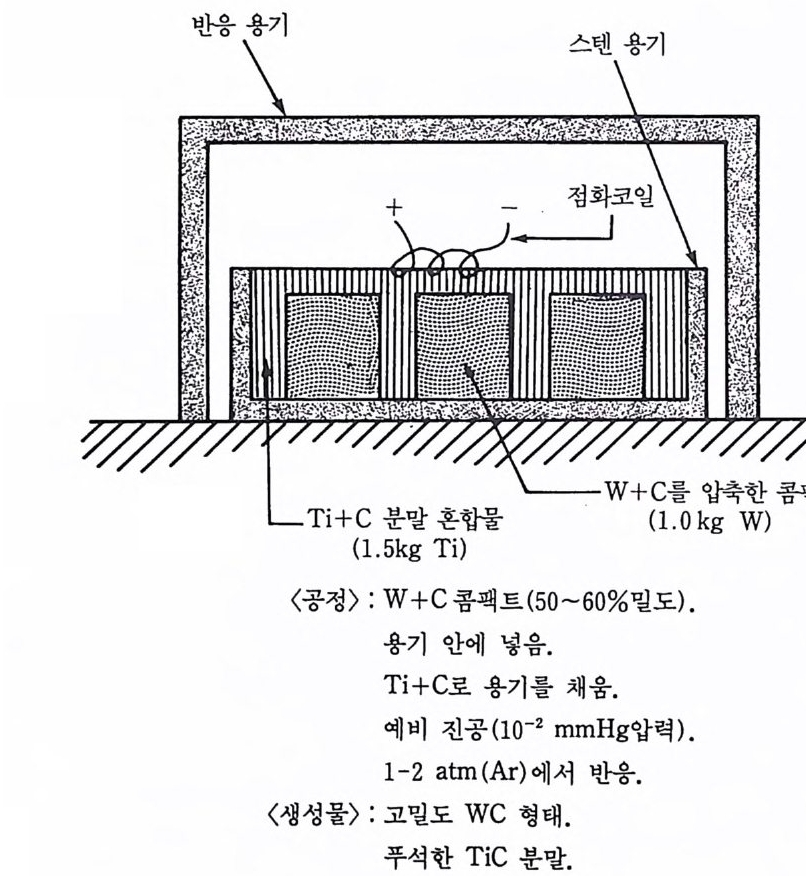
공정기술 혁신은 화학로의 개발이다. 이 노는 본래 낮은 단열 반응온 도를 갖는 반응물 예형 주위를 둘러싼 열덮개 (the rmal blanke t)이다. 이 열덮개는 필요한 생성물을 얻기 위한 반웅보다도 더 높은 온도에 서 진행하는 다른 비기체 연소반응을 이용하는 것이다. 그 발열반응 열이 공급되는 화학적 에너지에 의한 노(fu rnace) 이므로 그 열덮개 자체가 화학로 설계에 해당한다. 예롤 들면 티탄과 램프 그을음(l am p black) 의 느슨한 혼합물이 텅스 텐과 램프 그울음의 혼합물 예형 주위를 채우고 그림 5 . 1 에서 보는 바와같이 그 분말을 점화시키면 T i C 를 생성할 때 발생하는 발열반응
 반응용기
반응용기
그립 5.1 소련 〈화학로〉 제법의 개요도.
열은 아주 높은 온도에서나 가능한 W와 C 가 화합하여 WC 를 생성하 는 반응을 일으킬 수 있도록 고온으로 상승시키고 또 점화도 시킨다. 결과적으로 일차적인 바기체 연소의 화학로를 사용하여 초고온에서 나 가능한 이차적인 비기체 연소방법을 유도한 새로운 공법에 해당한 다. 이 경 우에 l ~ 1/2 시 간의 주기 로 서 냉 (slow cooli ng ) 이 바람직 하지 만 그 두 물질간의 상호 오염은 없었다. 그 결과로 얻은 무른 T i C 는 비교적 고밀도 생성물인 WC 로부터 손으로 눌러서 분리할 수 있다. MoB2, WB, WB2, Al ◄ C3, B ◄ C, Mo2C, NbC, SiC , VC 및 WC 와 같은 화 합물들이 이 기술로 생성될 수 있다고 주장한 소련 연구자들에게 소 련 특허 7 9) 가 출허되었다. 그 열덮개에는 보통 Ti 또는 Zr 과 붕소 또 는 램프 그울음의 혼합물이 포함되어 있었다. 그 덮개 혼합물과 생성 물 혼합물간의 질량비는 1 : 4~4 : 1 범위이어야 한다. 화학로 공정개선에 대한 한 가지 예를 들면, 생성물 Mo3S i에 대해 서는 Ti + 0.6Si, 57> TaC 와 Ta2C 에 대해서는 Ti+ C , H) Nb3Al 과 Nb3Ge 에 대해서는 N i +Al( 펠릿), 68) cuAl 과 Cu2Al 에 대해서는 T i +2B80) 들이 각각 열덮개 또는 화학로 (che mi cal f urnace) 로 사용되었다. 탄화탄탈 을 만들 때 화학로를 사용하여 얻어진 서냉속도는 반응완결을 이루는 장점으로 이용되었다. Nb 화합물의 경우 화학로 물질 N i +Al 은 생성 물과 대략 같은 온도에서 반응했다. 이때 그 화학로는 생성물을 위한 예형을 둘러싸고 있는 커다란 고리 모양 펠릿 형태로 사용하였다. 사 실상 화학로는 생성물의 반응 후 냉각을 길게 하도록 사용되었고 완 성된 반응과 단일상 생성물 및 고밀도화된 콤팩트를 얻는 데도 또한 효과적이다. 알루미늄화구리 생성물에 대해서는 T i+2B 가 캡슐로 된 덮개보다는 생성물을 위한 예형의 평평한 면 끝 위에 올려놓은 점화 정 (ignition tab let) 이 더 많이 사용되 었다.
5— 2 기체 압력에 의한 고밀도화 비기체 연소합성 중 생성물을 고밀도화하는 대부분의 연구는 반응 하는 동안 대기압, 역학적 압력 또는 양자 모두를 조철하는 것이 포 함되어 있다. 기체 질소나 수소로부터 질소화물과 수소화물을 생성할 때 높은 기압이 효율적으로 사용되지만 다른 조성의 비기체 연소 도 중 불활성 기체압력의 증가는 반응속도를 증가시키고 다공성을 감소 시킨다는 것을 소련 연구자들이 발견하였다. 비기체 연소 합성반응과 기계적 압축의 결합에 관한 호주의 연구 81),82) 가 유망한 결과로 주목되 어 왔다. 종래 소결에 대하여 새로운 반응 전 콤팩트(p recursor gree n comp a- c t)는 55~70% 범위의 상대밀도를 갖는다. 이 콤팩트는 대기압하에 서 역학적 가압 없이 계속 가열하는 동안에 더 조밀한 생성물을 형성 하도록 수축된다. 이 종래 소결법은 비기체 연소와 유사한데 이는 새 로운 반응 전 콤팩트가 비기체 연소를 시작하면 계속적으로 가열되기 때문이다. 그러나 비기체 연소에 포함된 반응속도론은 처음 콤팩트보 다 최종 생성물이 더 크고 많은 다공성 83),84) 으로 되게 한다. 다음 두 가지 현상이 이 기공 크기 증가의 이유로 가정되었다. i ) 부생성물 기체와 닫힌 기공 (closed p ore) 내에서 팽창하는 휘발 성 성분의 유출 .71) ii) 한 성분이 한 경계를 넘어서 다공성과 확대된 골격 구조가 생 기게 되는 또 다른 성분으로의 확산. 85),86) 그 확대 메커니즘은 연소파가 횡단해간 정지조절 부피 (s t a ti ona ry contr ol volwne) 를 상상함으로써 설명 할 수 있다. 최초의 콤팩트는 완 전히 고밀도화되지 않고 그 원소 성분들은 흡착기체, 흡수기체, 산화 물 및 다른 오염물 등을 포함한다• 이 조절 부피는 초기에는 대기압 의 비활성 분위기와 실온에서 존재한다. 확대는 반응 전대(p rereac tion zone) 가 조절 부피를 횡단함에 따라 시작되고, 더욱 휘발성이 강
한 불순물들은 끓어 증발하기 시작한다. 기체가 콤팩트 의부로 유출 되는 경로는 미소한 기공(p ore) 을 통해서 이루어지기 때문에 국부적 인 압력 구배 (pre ssure gr ed i en t)가 생기며 전체 압력 구배는 아마도 기화물질 내부 위치와 콤팩트 표면 사이에 생긴다. 이들 효과는 온도 를 상승시키고 기체를 팽창시키는 힘이 된다. 연소파가 그 조절 부피를 통하여 계속 지나가게 되면 확산 효과는 더욱 중요하게 된다. 간편하게 하기 위해 두 반응물 중 하나는 반응 전대 (pr ereacti on zone) 에서 녹고 계면간 확산은 녹은 성분을 더욱 내 화물 성분의 표면으로 이동시킨다고 가정하자. 녹은 성분은 입자 표 면에서 확산하기 시작하며, 온도가 충분히 높으면 발열반웅이 표면에 서 일어나 응축된 생성물을 얻는다. 그 녹아 있는 성분원소는 평형에 도달하거 나 또는 반응속도론 (reac ti on kin e ti cs ) 이 바람직 하지 못할 때 까지 생성물충을 통해서 계속 확산된다. 녹는 성분에 의해 비워진 자 리 로 둘러 싸여 생 성 물 입 자의 골격 구조 (skeleta l str uc tu re) 를 이 루게 되는 것이 이 과정의 결과이다. 그러므로 처음의 반웅 전 콤팩트 (gree n com pac t)보다 더욱 다공성일 것으로 기대된다. 이 예를 위해서는 한 비활성 분위기가 가정되었지만, 수소화물 37) 과 질소화물 87) 의 생성을 위해서는 비기체 연소가 활성 분위기에서 수행 되었다. 전형적으로 질소화물 생성공정은 50~lOOa tm의 질소 압력에 서 실시한다. 기체압력은 최초의 다공성뿐만 아니라 생성물의 균일도 (homo g ene ity)와 반응의 완결성에도 영향을 준다. 기체압력의 변화는 혼합조성에 영향을 줄 수도 있으므로 압력에만 칙접적으로 기인되는 반웅효과는 활성 분위기에 대하여 명료하게 이해할 수 없다. 그러나 비활성 기체의 압력 변화는 더욱 잘 설명할 수 있다. 예를 들면 다공성, 연소속도 및 반응완결도와 같은 생성물의 성질들이 비 활성 기체의 압력과 관계가 있다. 탄탈-탄소 혼합물에 관한 소련 연 구에서 연소속도와 상대밀도는 최대값 40a tm까지 기체압력 71) 에 비례 하여 증가하였다. 유사한 현상을 탄탈-붕소 혼합물의 연구 88) 에서도 볼 수 있었다. 여기서 연소속도 (u) 는 압력 (p)과 지수 (11) 간에 u=p
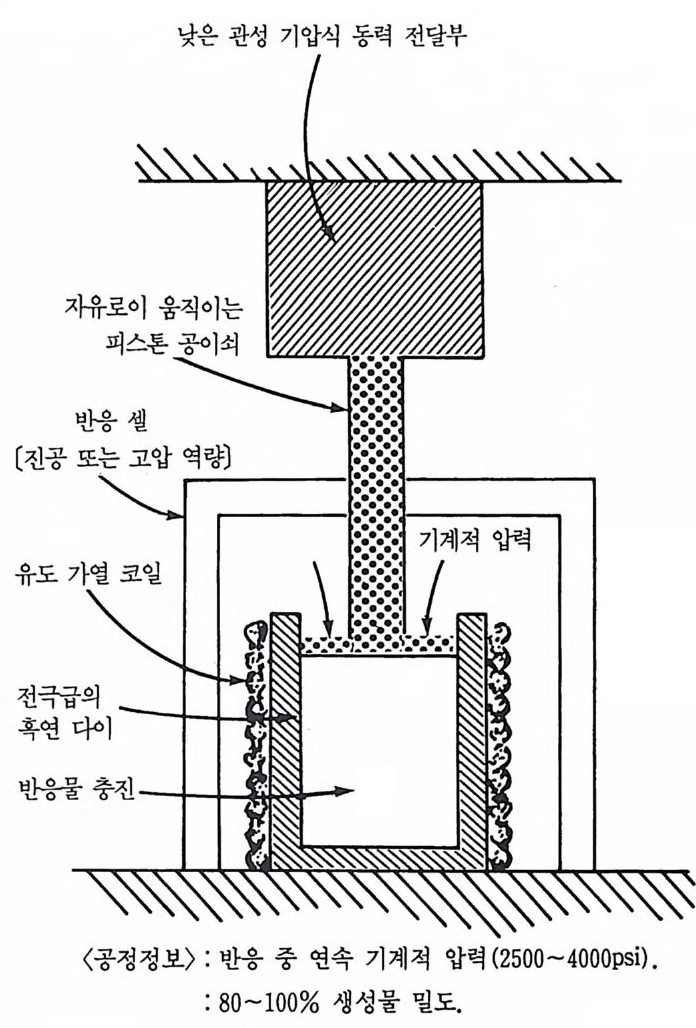
의 관계식을 따라 변한다고 보고하였다. 지수 v 는 물리적 성질의 함수이며 실험적으로 결정할 수 있다. 예 롤 들면 40µm 미만의 티탄 입자와 4µm 미만의 붕소 입자의 결합은 v=0.2 의 값을 갖는다. 이 계에서 연소속도는 lOatm 에서 최대값에 달한다. 이 최대 연소속도 역시 혼합물질들의 물리적 성질에 함수관 계가있다 . 탄탈-탄소 혼합물에서 길이가 늘어나지 않게 콤팩트의 끝들을 집게 로 조이고 실험을 실시하자, 그 결과 상대밀도와 연소속도가 모두 증 가하였다. 이때 밀도와 속도는 대기압의 변화에 관계없이 일정하였 다. 이것은 입자간 거리가 감소함에 따라 그 연소공정 자체는 더 격 렬하게 되는 것을 나타낸다. 더구나 밀도와 연소속도의 값이 기체압 력 포화값에서보다 더 크기 때문에 기체방출이 아닌 다른 메커니즘이 생성물 연장의 원인이 되어야만 한다. 한 가지 가능한 메커니즘은 앞 에서 논한 확산과정이다 . 5— 3 기 계적 압력에 의한 고밀도화 비기체 연소합성에서 얻어진 저밀도의 다공성 생성물과 그렇게 만 든 연소 메커니즘의 입장에서 보면 〈 왜 완전한 고밀도화를 얻기 위하 여 기계적 압력을 더욱 광범위하게 사용하지 않았는가 〉 하는 명확한 질문이 나올 수 있다. 이에 대한 부분적인 답변은 〈 적당한 압력장치 설계에 따르는 어려움이 많다 〉 는 점이다. 호주의 연구자들이 보인 것처럼 기계적으로 속박된 합성 시편은 2500~2400 p S i81 ). ” 의 하중으로 압축할 때 재 빨리 수축된다. 그림 5.2 에서 보는 바와같이 가압장치의 설계는 복잡하다. 대부분의 호주 연구는 A1203~M0S i2 와 같이 규소화물을 포함한 2 상 고용체에 집중되 어 있다. 규소화물은 상대밀도 99.5% 인 생성물을 얻을 수 있었고 붕
 낮은 관성 기압식 동력 전달부
낮은 관성 기압식 동력 전달부
그림 5.2 호주 반웅압축기의 모형도•
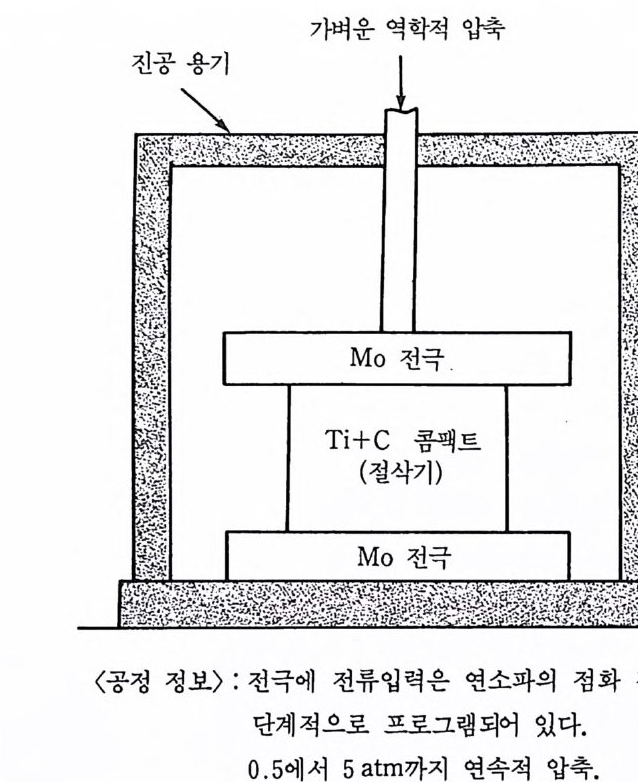
소화물의 경우는 95% 의 생성물을 얻었다. 소련의 방법 38) 은 그립 5 . 3 에서 보는 바와같이 몰리브덴 (Mo) 전극 사이에 Ti 분말과 램프 그울음 혼합물의 반응 전 콤팩트를 가압하는 것이다. 대기압과 기계적 압력 및 전기적 루과 (elec tri cal transmis- s i on) 가 고밀도화에 이용되었다. T i C 의 형태는 이론밀도의 96% 밀도
 가벼운 역학적 입축
가벼운 역학적 입축
그립 5,3 고밀도화를 촉진시키는 소련 압력장치의 개요도.
수준에서 절삭기 (cutt ing t ool) 의 형태로 생산되며 AlNi 3 또한 이 공 정 적용으로 얻어진 생산물로 보고하였다. 5— 4 고 밀도화 메커니즘 기계적 압력하의 고밀도화에서 시편 확장에 대한 주된 역메커니즘 은 소성흐름 (pla stic flow ) 과 난알간 미끄러 짐 (int e r gr an ular slip ) 이 다. 소성흐름에 필요한 최소 이상의 의부적 힘이 가해지면 낱알(gr a i n) 들 이 서로 흐른다. 이것은 난알간 공간을 감소시키며 따라서 연소속도
와 상대밀도를 증가시킨다. 난알간 미끄러짐은 각 성분과 중간체상 이 모두 녹지 않을 때 발생 한다. 큰 충 전단력 (shear forc e) 이 그 구 조내에서 생길 수 있으며 세라믹스 낱알들이 미끄러진다. 작은 낱알 크기는 미끄러 짐 메 커 니즘 (slip mechanis m ) 을 크게 돕는다. 대 단히 작 은 낱알 ( < 25µm) 로 된 2 상 화합물인 세라믹스 화합물은 비기체 연소 온도에 서 초소성 거 동 (sup er p la sti c behavio r ) s9>,90) 을 나타낸다. 기계적 압력과 대기압의 결합은 고밀도화에 유용하지만 출판된 정 보가 한정되어 있음을 알 수 있다 . 어떤 연구자들은 휘발성 불순물을 제거하기 위해 진공에서 시편을 압축하는 방법을 권장하였으나 이 방 법은 어떤 반응성분을 끓게 할 수도 있다. 기체 유출을 제거하는 다 른 방법으로는 알루미늄박 (Al- fl ake)82) 으로 시편을 둘러싸서 기체를 흡수시키는 방법이 있다. 그러한 방법은 실용성이 보다 적은 고압 결 합에 해당하지만 이 분야에서 최적의 해결책을 알아내기 위해 더욱 연구하는 것이 필요하다. 바기체 연소에서 대기압력과 기계적 압력의 효과를 설명하는 메커 니즘은 충분히 이해되지 않았다. 압력 특히 기계적 압력의 적용으로 생긴 생성물이 단지 가장 초보적인 방법으로 분석되었다. 압력효과를 수학적으로 모형화 (mode li n g)하려는 시도는 크기의 차수와 일차원적 형의 모형에 국한되어 있고 단지 연구되고 있는 득이한 시편에만 적 용된다. 일반적으로 비기체 연소의 압력적용 연구는 매우 정성적이고 사실상 경험적이다. 기본 메커니즘의 자세한 설명과 정량화는 확실한 이론과 유용한 분석모형을 발전시키는 데 필요하다. 예로서 비기체 생성물의 부피증가에 원인이 되는 메커니즘은 정량적으로 조사되지 않았다. 기체 방출과 확산이 생성물 팽창을 야기시킨다는 것은 긍정 적인 반면에 각 메커니즘에 기여하는 그 팽창의 분율(fr ac ti on) 은 주 어진 계에 대하여 예측할 수 없다. 팽창현상은 간단한 실험을 통하여 연구 및 측정될 수 있다. T i과 C 같은 주어진 혼합물의 두 가지 동일한 콤팩트를 제조할 수 있다. 첫째 콤팩트는 대기압하에서 반응하고 둘째 콤팩트는 고압(약 50atm )
에서 반응할 수 있다. 휘발성 기체 방출의 효과는 고압에서 최소로 되기 때문에 둘째 콤팩트의 부피증가는 주로 확산과정에 기인한다. 그 두 가지 체적중가의 비교는 기체의 방출과 확산 메커니즘에 대한 팽 창 기 여도의 상대 적 크기를 나타낸다. 기공구조 (po re stru ctu r e) 의 비교 또한 홍미를 느끼게 한다. 압력하에서 연소된 시편은 더 작고 더욱 균일하게 분포된 기공들을 갖는다. 생성물 팽창에 기여하는 기본적 연소 메커니즘의 지식은 생성물의 고밀도화에 대한 방법을 발전시키는 데 유용하다. 빠르게 작동하는 피스톤 공이쇠(p lun g er) 로 국단적인 기계적 압축을 얻는 현재의 방법 은 최적의 방법이 될 수는 없다. 더욱 적당한 방법의 발전은 연소반 응 속도와 메커니즘의 기본적인 연구를 통해서 촉전될 수 있다. 5— 5 고 열 프레스와 고열 등방압 프레스 고밀도화를 위하여 호주 81) , 82) 와 소련 38) 의 가압장치를 5 냉철에서 설 명한 바 있다. 최근 많이 사용하는 기계적 가압장치에는 냉 등방암 프레스 (Cold Isosta t i c Press 또는 CIP), 고열 프레스 (Ho t Press), 고열 등방암 프레스 (Ho t Isosta tic_P r ess 또는 HIP) 등이 있다. 입방모루 (cubic anv il) 66) 로 GPa 차수의 초고압을 이 용한 고열 프레 스 (Hot Press)91),92) 를 고압 고열 프레스 (HPHP) 라 하였으므로 압력의 크기 의에는 본질적으로 차이가 없다. HPHP 와 HIP 의 장점 30) 은 각각 다 음의 (1) ~(5) 와 (4)~(8) 에서 보는 바와 같다. (1) GPa 차수의 고압은 입자들의 분열, 재배치 및 소성흐름을 촉 전시켜서 그 소결공정을 활성화시킬 수 있으므로 출발물질들의 다공성 반웅 전 콤팩트(p orous gree n comp a ct) 가 거 의 이 론밀도 로고밀도화되게 한다. (2) HPHP 는 닫힌 반웅계에서 수행되므로 고온에서 생성물의 분해
룰 방지할 수 있다. (3) 다이 아몬드와 같이 상온에서 준안정 인 화합물을 고온-고압의 그들 안정범위에서 소결시킬 수 있다. (4) 첨 가제 를 가한 후 종래 의 고열 프레 성 (Hot Pressin g ) 또는 정 상소결할 때에 비하여 같거나 또는 낮은 온도조건에서 더 짧은 소결 지속시간에 첨가제 없이 소재를 거의 이론밀도까지 고밀 도화할 수 있다. (5) 더욱 짧은 소결 지속시간과 고압의 조건들은 확장된 난알 성장 (exagg e rate d grai n gr o wth)을 조절하므로 미세한 낱알로 된 마 이크로 구조를 갖는 세라믹스를 얻을 수 있다. (6) 거의 그물 모양 생성물은 등방압(i sos tati c p ressure) 을 적용함으 로써 소결될 수 있다. (7) 화합물의 분해나 증발은 종래의 고열 프레싱보다 한 차수(1 0 배 이상) 더 큰 고압을 적용함으로써 방지할 수 있다. (8) 역학적 강도와 같은 확실성으로 생긴 등방압을 적용시킴으로써 소재를 균일하게 소결시킬 수 있다. 이상과 같이 고밀도화에는 고압 고열 프레싱 (High Pressure Hot Pressin g ) 과 고열 등방압 프레 싱 (Hot Isosta t i c P ressin g ) 이 주로 사용 된댜 첨가물 없이 고압을 적용시켜 세라믹스를 고밀도화하여 고성능 (hig h per f or mance) 특성의 내화성 소재를 얻을 수 있다.
제 6 장 비기체 연소반응 현상학 이 장에서는 비기체 연소합성의 반응현상 (reac ti on p henomena) 을 분석하고 그 분석을 통해 관심있는 반웅거동의 과학적인 현상을 이해 하거나 참재력 있는 합성반응의 추정능력을 개발하는 데 목적이 있 다. 이들 추정능력은 반응속도, 국부 반응온도 및 상변환(p hase convers i on) 과 같은 반응변수들을 조절하거나 자체 유지 단열반웅 (self-s u sta i n i n g adia b atic reac ti on) 의 가능성을 확인 및 평가하는 데도 유용할 것이다. 그 분석은 합성반응 이론에 관련된 소련 연구자들의 재고찰로 시작하여, 합성반응 이론에 대한 SPC 확장이론까지 계속되 고, AIN, TiC 및 Ti B2 생산을 위한 합성반응의 고찰로 끝을 맺는다. 6— 1 관련된 연구 소련에서는 비기체 연소반응에 대한 연구가 초기에는 기본적으로 학술적인 성격을 띠었으나 세라믹스 물질의 생산에 응용된 이래로 자 체 전파 고온합성 (Self-p r o p a ga ti ng High Temp er atu re Syn the sis 또는 SHS) 의 개발에까지 그 연구가 급속히 확장되었다. 바기체 연소합성 에 대한 제조기술과 실험방법론 및 일반적인 특성은 앞 장에서 언급
되었으므로, 여기에서는 단지 그 이론만 재검토하기로 한다. 연소 진 행 앞면 (combus ti on fr on t)의 특성과 이동을 규정짓고, 물리적 상태의 결정과 그들의 안정도 조사 및 아마도 가장 중요하게는 어떤 열물리 상수(th ermo p hy s ic al cons t an t)를 예측하도록 분석 모델을 발전시키는 데 그 이론들이 사용된다. 소련 이론의 간단한 조사와 비기체 연소반 웅의 분석 모델화 (anal yti cal mode li n g)는 다음과 같다. SPC (Sy st e m Plannin g Corp o rati on ) 는 비 기 체 연소의 제 목으로 지 난 20 년간 출판된 200 개 이상의 소련 논문을 수집하여 검토하였다. 이들 논문들에 기 여한 200 명 이상의 소련 연구자들이 알려져 있는데 이들 과학자 중 가장 유명 한 사람은 A. G. Merzhanov, I. P. Borovin s kaia , S. K. Dolukhan ian , Yu. M. Maksim o 및 V. M. Shkir o 등이 다. 소련 에 서 는 비기체 연소공정에 관한 실험이 많은 연구실에서 수행되어 왔지만 전 체 계 획 은 Chemog o lovka 에 있는 Insti tut e of Chem ica l Phy si c s U. S. S. R. Academy of S ci ence 에서 수립 및 조절해 왔다. 소련 연구자들은 비기체 연소합성 반응의 분석 모델화에 상당한 노 력을 경주해 왔다. 일반적으로 논하면 이들 모델은 아래와 같이 확인 된 공정단순화 93) 로 특칭지어진다. i ) 연소파에서 온도의 장(fi eld of t em p era tu re) 은 일차원적이며 온 도는 연소파의 변위방향으로만 변한다. ii) 연소파의 변위방향으로 연소생성물의 확산이동은 존재하지 않 는다. iii) 연소시 열 방출속도는 균일반응에 대하여는 종래의 법칙으로 정의되는데 열 방출대에서 녹음이 분명치 않다. iv) 계의 밀도, 열 확산계수 및 열 용량 같은 물리적 파라미터들은 연소과정중에 변하지 않는다. 일련의 반응조건들이 각 모델에 대해서도 또한 가정되며 에너지 보 존과 열 확산식들은 주어전 반응에 대한 특성 조절체적 (characte r ist ic contr ol volume) 에 적용된다. 편미분방정식의 수치적분 (numer ic int e - gra ti on) 은 반응체적내에서 질량과 온도분포에 관한 식을 얻게 된다.
이 장에서 명백해졌듯이 이들 소련 모델들은 범위나 응용성이 극히 제한되어 있다. 예를 들면 거의 모든 비기체 합성반응은 생성물이나 반응물 혹은 그 둘 모두에서 상전이가 수반되는데 액체 또는 기체의 생성은 거의 확실히 연소파의 진행방향으로 질량이동 (mass tra nsfe r ) 이 일어난다. 실제 반응온도 영역에서 상전이가 수반되는 경우 열전 도도나 비열과 같은 대부분의 물리적 성질들은 광범위하게 변할 것이 다. 그 의에도 분체반응의 균일작용에 대한 가정은 모호한 것 같고 계의 열손실은 없다고 가정하였는데 이 열손실은 반응과 관련된 시료 의 형태와 두께를 한정하는 중요한 파라미터이므로 무시할 수 없다. 이들 문제는 다음 7 장의 SPC 모델에서 다시 논의될 것이다. 수많은 특수현상을 다룬 많은 소련 모델들이 재검토되었고 그중에 선택된 몇 가지를 부록 B93)~101) 에 요약하였다. 예를 들면 부록
한 점들이 단일 곡선상에 놓이므로 근본적으로 변하지 않는다. iii) 니켈과 알루미늄 반응에 대한 Tc 는 생성물인 NiA l 의 융점과 동일하다. 모델은 이들 데이터에 맞도록 발전되었고 그 모델로부터 그 반응에 대한 어떤 열역학적인 파라미터가 얻어진다. 이 모델은 연소속도가 생성물의 융점과 동일한 다른 계에까지 확장될 수 있다는 결론을 말 해주지만 포괄적인 모델을 개발하기 위한 시도는 볼 수 없었다. 제시 된 소련 모델도 상의 조건, 반응기하학 및 열적 성질에 관련된 특정 한 가정들하에서만 유용할 뿐 이들 가정들이 변하면 그 모델의 적용 성을 무효로 하고 한 조성의 상전이는 새롭거나 수정된 모델을 받아 들이는 것이 필요하다. 한 모델이 주어진 반응계획에 응용되기 전에 모델화되는 현상들을 알거나 가정되어야 한다. 그 조성들과 그들 상 조건의 확인, 그 조성들이 행하는 가능한 반응들, 그 가능한 반응위 치 및 그 모델 응용의 성질에 의존하는- 계의 부분적 기하학 등이 이 현상들에 포함된다. 소련 연구자들은 일반적으로 물리적 반응환경을 가정하고 이 환경 에서 질량과 에너지 전달현상의 모형을 만들었지만 어떻게 그 계가 주어전 상태에 달하는지 또는 언제 그 주어전 상태가 다른 상태로 전 이되는지는 명확하게 설명하지 않았다. 이 설명의 생략은 광범위한 반옹계들에 대하여 그들 모델을 쓸 수 없게 한다. 예를 들어 반응하는 고체의 구가 반응물 유체에 참겨 있는 모델은 구가 고체인 경우에만 적당하고, 그 구가 녹을 때는 그 모델아 무효 가 되어 또 다른 모델이 제시되어야 한다. 그러므로 주어진 반응환경 에 대한 모델의 선택은 계에 존재하는 상들과 상계면들의 본성, 질량 과 에너지 이동속도, 여러 가지 반웅들의 속도 및 그 의 고려할 점에 의하여 좌우된다. 소련 모델들의 한계성의 이해가 분명해지기 때문에, 관심있는 특수 반웅계의 상당히 엄격한 물리적 특칭 열거에 대한 필요성을 설명하고 이룰 위한 물리와 화학적 데이터를 필요로 한다. 연소 메커니즘의 기
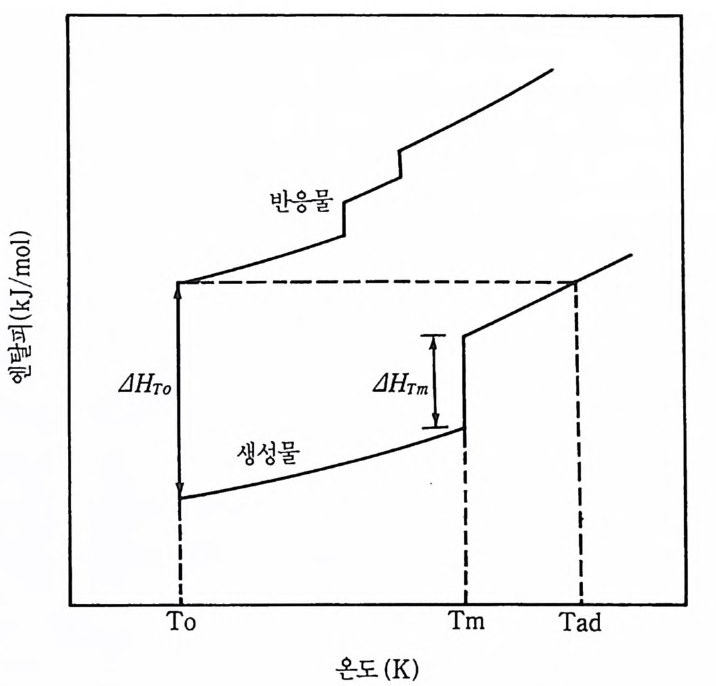
본 반응 파라미터는 SPC 의 연소분석의 다음 단계에서 확인 및 연구 되었다. 그들 파라미 터들을 고려한 후에 DARPA/ LL NL 프로그램 에서 표준 개발 생성물로 지명된 AIN, TiC 및 T iB 2 의 세 가지 화합물 합성을 연 구하기 위해 그 데이터들을 모았다. 6-2 반응 파라미터 6— 2-1 단열 반응온도 (Tad) 자체 전파 고온합성 (SHS) 반응의 단열 반응온도 (a di aba tic reacti on tem p er atu r e 또는 Tad) 는 발열반응에 의하여 방출되는 모든 열이 궁 국적으로 반응 용기내의 최종 내용물(생성물과 반응하지 않고 남아 있 는 반응물)의 온도를 올리는 데 사용된디는· 가정에서 계산되었다. 그 단열온도 (Tad) 는 이상적인 단열계에서 얻을 수 있는 생성물의 온도로 실제 연소온도의 최고 한계를 나타낸다. 반응의 발열도를 나 타내는 이 이론적 극한값 (Tad) 은 열용량, 생성 엔탈피 및 전이 엔탈 피 갇은 열역 학적 함수 11) , 30),103) 로부터 계 산할 수 있다. 단열온도의 계 산은 다음과 같은 기준에 따른다. i ) 만약 I::,. HJ (29 8) < L2:9m8 Cp ( s)dT (6.1 ) 이면 Tad< T군 ]고
A HJ (29 8) = J29T6 nd C p ( s)dT (6.2) 식으로 계산할 수 있다. 위에서 AH?(298) 은 298K 에서 표준 생성 엔탈피, C p(s) 는 고체상태 의 열용량 및 Tm 은 절대온도로 생성물질의 융점을 각각 나타낸다. ii) 만일 1929:8m Cp (s )dT< D..H J c29 8)
 ([OW
([OW
그림 6,l 온도변화에 따른 반응물과 생성물의 엔탈피 변화곡선.
시하였다. 위에 설명한 방법은 고체-고체 및 고체-기체 같은 다른 상 전이에 대해서도 연장해서 설명할 수 있다. 이들 식을 응용할 때 일 어나는 두 가지 곤란한 점 중의 첫째는 측정하고자 하는 각 온도 범 위에 대한 신빙성 있는 열용량 자료가 부족하고, 둘째는 초기 온도 (To) 와 기존 데이터 Tad 값간에 조정이 필요하다는 것이다. 죽 실험 의 초기 예열과 점화단계에서 계에 들어간 에너지를 모두 계산해야 한다. 첫번째 문제인 열용량 데이터는 필요한 온도 범위에서 취급하는 반 웅조성들에 대하여 찾을 수 있고, 이들 데이터의 신빙성은 모호하지 만 일반적으로 참고한 여러 자료 중에 잘 일치하는 좋은 값을 얻을 수있다. 두번째 문제는 계에 주입된 열에너지량을 측정하거나 계산하여 조
정할 수가 있다. 한 가지 방법은 필라멘트 혹은 의부 열원의 국부온 도가 한계 반응온도에 달할 때까지 반응이 일어나지 않고, 그때까지 열원은 멈춰진 것으로 가정하고 단열조건도 인정한다. 이것은 본질적 으로 열 추진원을 모델화한 것이다. 단열온도에 대한 SPC 근사법에서 사용된 방법은 단지 무의미한 의부 열량이 가해졌고 그 온도 To 는 298K 라고 가정 한다. 뜨거운 필라멘트롤 갑자기 콤팩트와 접촉하거나 혹은 테르밋 반응 같은 대단히 빠른 시발반응이 일어난 경우이다. 사실 그 반응은 처음 계의 온도 298K 에서 일어났고 반응 엔탈피와 똑갇은 열에너지량이 방출되었다. 그 반응용기의 내용물(1 00% 생성물)은 모든 가능한 에너 지(주입된 의부 열에너지와 반웅 엔탈피)가 흡수될 때까지 가열되는 것 으로 Tad 를 계산한다. 엔탈피는 경로에 무관한 상태함수이므로 이 방법론은 합리적이다. 표 6,I 화합물들의 연소합성에 대한 단열온도. 화합물 Tad(K) 화합물 Tad(K) TiB 2 3190 TiN 4900 ZrB 3310 ZrN 4900 NbB2 2400 Hf N 5100 TaB2 3370 NbN 3500 MoB 1800 TaN 3360 La& 2800 Si~ . 4300 B,C 1000 BN 3700 Al4C3 1200 AIN 2900 TiC 3210 Be3N• 3200 HfC 3900 Tis S b 2500 TaC 2700 Zr5Si3 2800 SiC 1800 NbSi2 1900 WC 1000 MoSi2 1900
질소화물, 황화물 및 수소화물과 갇이 휘발성인 상들에 대한 단열 온도의 계산은 정확하지 않으나, 선택한 화합물군의 단열온도의 예 둘 104) 은 표 6.1 에서 보는 바와 같다. 표에서와 같이 내화성 질화금 속 (me t al n itri des) 의 Tad 값은 극도로 높지만 실제 연소실험에서 Tad 는 열손실 때문에 좀처럼 얻어지지 않고 연소 진행앞면 (combus ti on fron t) 의 온도로 표기 된 것 이다. 주어전 물질의 합성을 자체 전파 고온 연소합성법으로 성취할 수
 7000
7000
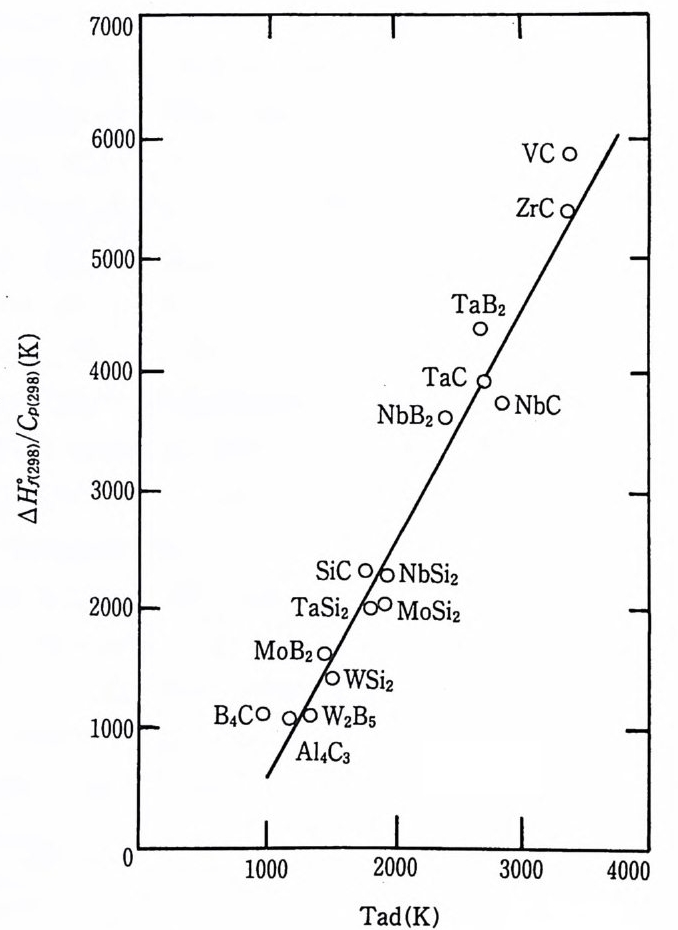
그림 6.2 AH?(298)/C p (298) 과 단열온도의 관계도.
있는지 없는지를 확인하기 위하여 반정량적인 방법이 사용되었다. 연 소반응은 Tad ~ 1800K'04) 가 되 지 않으면 자체 유지 또는 자체 전파가 불가능하다는 것이 경험적으로 알려져 왔다. 298K 에서 생성물의 표 준 생성열과 그 열용량의 비, 즉 A H?(298)/ CP(298) 을 Tad 에 대하여 그리면 높은 융점을 갖는 물질들의 경우 대략적인 직선관계를 보인 다. 단열온도가 생성물의 융점보다 더 낮은 경우에 위의 기준을 만족 시키는 물질들에 대한 이들 두 파라미터의 관계는 그림 6.2 와 같다. 이 그립에서 확인된 물질들에 관한 실험적 관찰로 A H}(298)/CP(298)< 2000 의 비를 갖는 것들은 의부적인 에너지를 가하지 않으면 자체 유 지 연소 진행앞면 (self -sus t a i n i n g combustio n fr on t s) 을 형성할 수 없다 고 하였다. 이와같이 이 값이 자체 유지 연소의 존재 여부에 대한 대 략적인 지침으로 사용될 수 있다. 6— 2-2 평형변환 평형변환 (e quili b ri um convers i on) 은 한 특별한 반응물이 생성물질로 화학변환된 물분율 을 나타내는데, 상들의 존재를 고려하면서 생성물 의 화학 퍼텐셜이 반응물의 화학 퍼텐셜과 평형을 이룰 때 생긴다. 화학 퍼텐셜이 조성뿐만 아니라 온도와 압력 두 변수의 함수이므로 평형변환도 온도와 압력의 함수이고 그 반응열에 의하여 변환과 관련 된다. 정반응도 역반응도 자발적으로 일어나지 않는, 죽 화학 퍼텐셜 . 의 변화가 영인 조건들을 계산하므로 평형변환이 결정된다. 반응자발성, 평형변환 및 단열 반웅온도 등은 상전이와 함께 그 반 웅현상을 설명하기 위한 가능한 열역학적 데이터를 사용함으로써 이 연구에서 제기능을 나타낸다. 계의 자발성, 단열 반응온도, 평형 변 환 및 다른 거시적 양둘이 산출되는 한 거시적 영차원의 분석이 첫째 로 고려되었다.
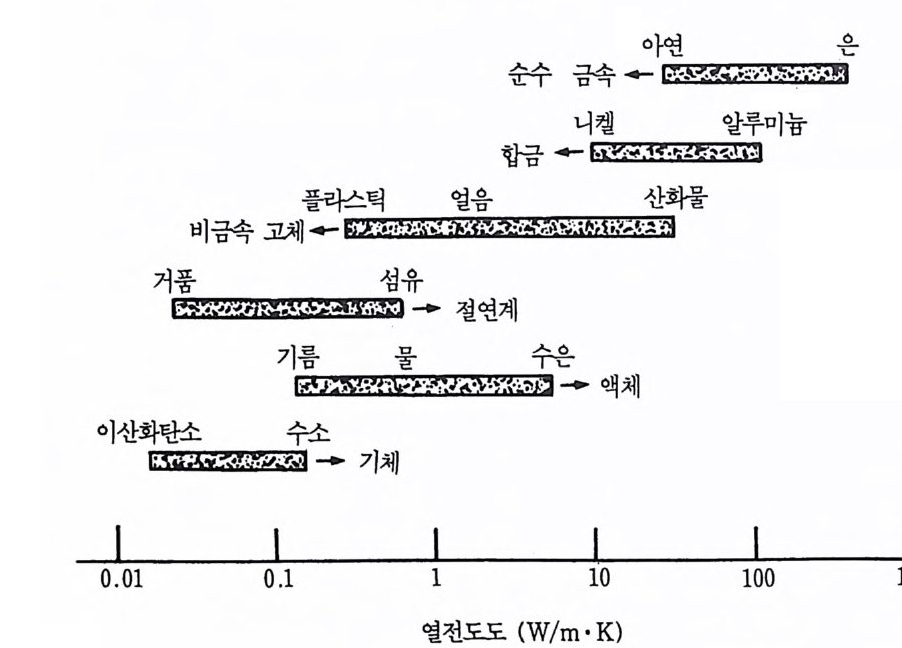
6— 2— 3 열에너지 운반 열에너지의 공간적 효용성은 비기체 연소공정에서 대단히 중요한 것이다. 상과 상의 계면조건, 물질확산성, 반응자발성, 평형변환 및 반응속도론은 모두 온도 의존성이므로 반응계내에서 에너지 운반은 유효한 정보를 줄 수 있을 뿐만 아니라 잘 알아야 한다. 열 에 너 지 의 운반에 대 한 추진 력 (dr ivi n g forc e) 은 온도 기 울기 (tem p e ratu re gr a(\ i en t)이다. 이 기본적 원리는 열전도의 푸리에 (Four i er) 법칙에 의하여 선형함수인 q=-'v (kT) 로 나타내었다. 여기 서 i는 하나의 벡터로써 열흐름이고, T 는 온도, k 는 비례상수인 열 전도도이 다. 열 확산도 (the rmal diffus iv ity 또는 a) 를 좋아하는 어 떤 저자는 열전도도 (k) 를 a=k/( p Cp )와 같이 다론 형태로 표현하였다• 여기서 p는 밀도, Cp 는 정압바열을 나타낸다. 한 물질의 열전도도는 그 물질의 조성, 상 및 온도의 함수이다. 일 반적으로 k 는 등방성 양(i so tr o pic q uan tity)으로 가정 한다는 것을 주 의하라. 죽 k 는 모든 세 공간방향에 대하여 똑같은 값을 갖는 것으 로 가정한다. 아 가정은 유체나 대부분의 균일 고체에 대해서는 타당 하지만 단순 입방결정이 아닌 고체들과 많은 불균일계들은 비등방 성 105) 이다. 주어진 순수한 고체물질에 대하여 열전도도는 온도 및 어쩌면 그 고체 결정상의 함수이다. 만약 그 고체가 다공성이면 열전도도는 틈 새 율 (void frac ti on ) , 기 공 크기 (po re siz e ) , 기 공벽 에 흡수되 거 나 또는 기공들을 채운 유체 및 열복사 등에 강력히 좌우된다. 이들 양들은 측정하거나 정확히 예측하는 것이 어렵기 때문에 열전도도 데이터는 경험적으로 결정된다. 어떤 경우는 순수한 금속에 대한 열전도도 데 이터가 전기전도도 데이터로부터 산출될 수 있는데, 이는 순수한 금 속에 대하여 전도성 전자들이 열에너지를 운반하는 주된 운반자 (princ i pa l carrie r ) 가 되 기 때 문이 다. 일반적으로 기체<<액체<<고체의 순서로 열전도도가 급증하는 경
향 106) 을 나타내는데 이는 그림 6 . 3 에서 보는 바와 같다. 한편, 고체 상태에서의 열전도도(열에너지 운반)는 자유전자와 격자진동파의 이동 에 관계가 있으며 k=ke+k1 로 나타낼 수가 있다. 여기서 ke 는 자유 전자에 의한 열에너지 이동항이고 k1 은 격자진동에 의한 열에너지 이 동항이다. 순수한 금속의 경우에는 열에너지 전이가 거의 자유전자의 이동에 기인되며 ke»k, 이고, 이때 ke 는 아래와 같이 나타낼 수가 있다. ke=—L PaeT = PLo+oPT' r (6.7) 여기서 Lo 는 로렌스 수 (Lorenz number), Po 는 전기비저항 (elec tric al resis t i vity), p 'r 는 고유비저항(i n t r i ns ic res i s ti v ity)을 나타낸다.
 순수 금속 --0}t 연·”; i구,실,'I,‘::지.':'; w!.` ‘下 。
순수 금속 --0}t 연·”; i구,실,'I,‘::지.':'; w!.` ‘下 。
그림 6.3 정상온도와 압력에서 여러 가지 상태의 물질에 대한 열전도도 범위.
 500
500
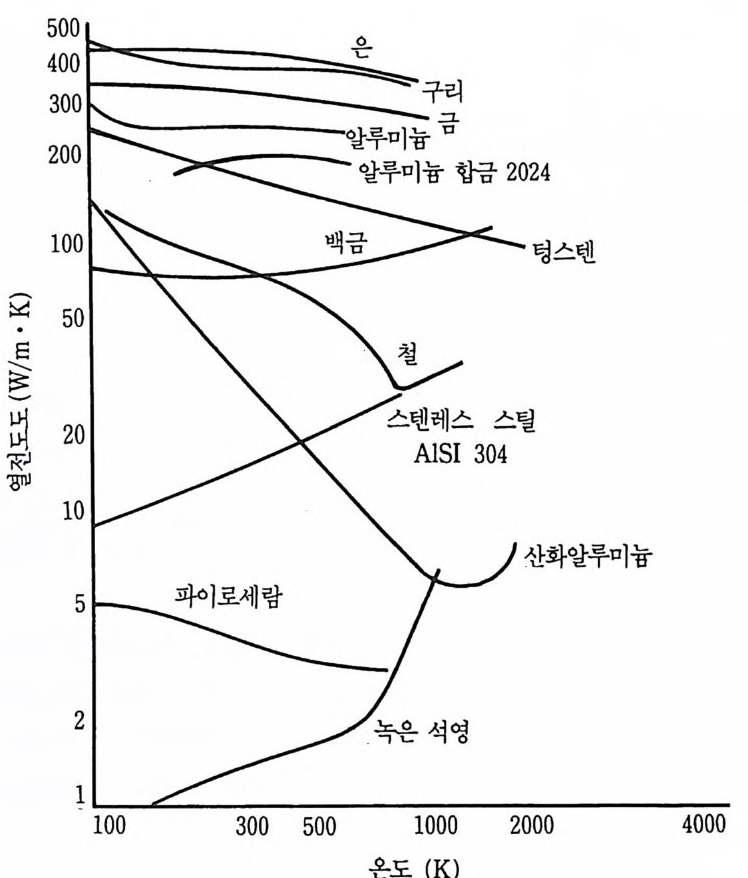
그립 6·4 선택된 고체 열전도도의 온도 의존성•
그러나 비금속 고체 (nonmeta llic so li d) 에서는 격자원자간의 상호작 용에 기인하는 격자진동이 있으므로 &항이 고려되어야 하는데 A 값 은 온도상승에 따라 중가하는 경향을 보인다. 그리고 합금의 경우 ke 값이 순수금속보다 작고 Pe 는 작아져 k 혼감을 무시할 수가 없게 된다. 죽 이 경우에는 온도상승에 따라 k 값이 증가한다. 각 금속의 온도에 따른 열전도도 (k) 값의 변화는 그립 6 .4에서 보는 바와 같다.
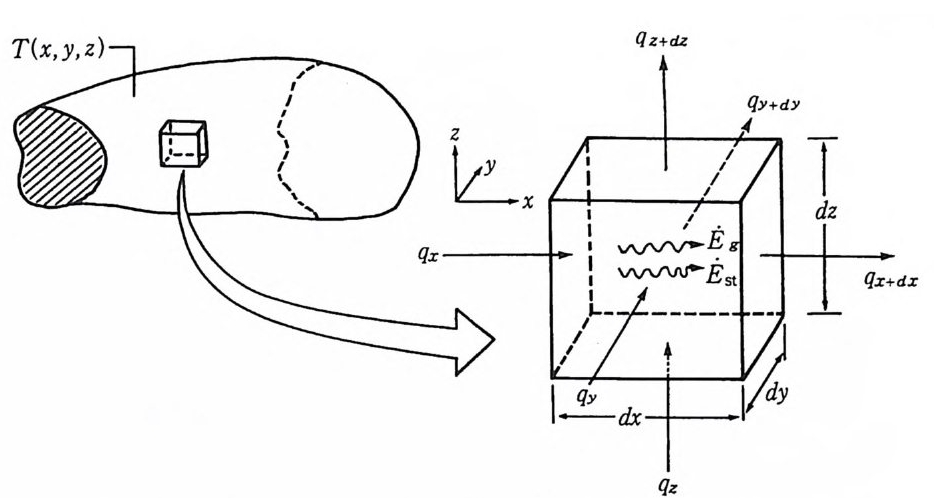
6-2 一 4 루이스 수 루이스 수 (Le wi s number 또는 L e ) 는 열확산과 물질확산 10 ” 의 상대 적인 비율을 나타내며 다음과 같이 정의한다. Le=—D a =-p-C- k=p D - (6.8 ) L e 가 1 보다 큰 값은 열에너지가 물질보다 더 빨리 확산되는 것을 나타낸다. 만약 Le 가 1 보다 대단히 큰 값 (L e» l) 이면 열확산은 물질 확산에 비하여 순간적으로 일어나므로 물질확산은 제한된 단계 (limitting s t e p)내에서만 고려할 필요가 있다. 또한 L e <<1 인 경우에도 그 역이 잘 성립한다. 열전도도 데이터는 넓은 온도 범위에서도 얻기 용이하나 질량확산 은 그 데이터가 부족하거나 얻기가 어렵다. 몇 가지 물질확산 데이터 가 알려져 있고 그들 상호관계는 선택된 온도 범위에서 L e 값들을 계 산하는 데 유용하겠지만 역시 물질확산 데이터의 이용도는 불확실하다. 6-2— 5 열확산 방정식의 유도 각 반응에 적합한 분석 모델을 제시하고자 할 때는 각 반응의 조건 을 명시해야 하고, 가정을 세워야 하며, 에너지나 질량이동에 있어서 는 각 반응에 대한 조절 부피 (con trol volume : 단위 부피)내의 질량 또 는 온도 분포식을 유도해야 한다. 이룰 위해 가장 간단한 판상 모델에서의 열확산 방정식을 유도해 보기로 하자. 먼저 온도 차이가 있는 동질 매체내에서 각 x y z 방향 에 대한 온도분포를 T( x y z) 라고 하면 그림 6.5 와 같이 나타낼 수 있다. 여기서 조절 부피를 따로 분리하여 이 단위 부피내에서의 에너
 Qz + d z
Qz + d z
그림 6.5 직교좌표에사 열전도 분석을 위한 미분 조절 부피 : dxdyd z .
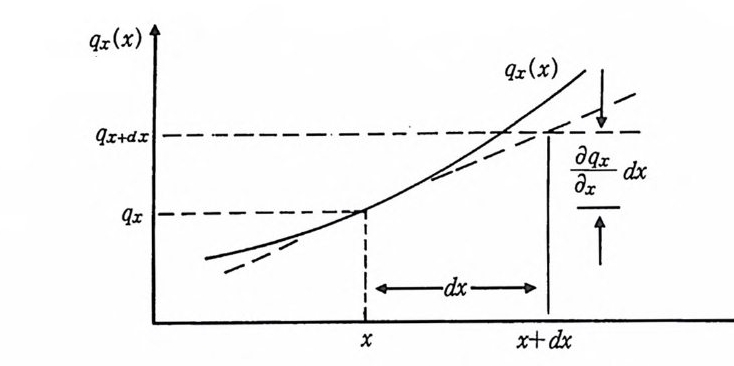
지 이동과정을 살펴보기로 하자. 각 조절 부피에 걸쳐 온도 기울기가 생성된다면 열은 각각의 조절 부피를 통과하면서 이동이 일어날 것이 다. 이때 조절 부피 속을 통과한 후의 열량을 qx +dX, qy+dJ! 및 q따쇼 라고 하면 이들의 열전도속도는 (6.9)~(6.11) 식으로 나타낼 수 있 다. Qx +dX= q x+ 붕 dx (6.9) qy+ dY= qy+흥 dy (6.10) qz+ dz= q z+ 총 dz (6.11) 여기서 1 차원적인 x 방향만 생각하면 x+dx 위치에서의 열 이동속도 의 x 성분 값은 x 위치 성분값에 dx 로 변한 열량의 합이므로 그립 6.6 에 나타낸 바와같이 거리 (x) 에 따른 열 이동속도의 변화를 나타낼 수 가있다.
 qqr,(+xd ), 1• --_ _________; :qz ( 「少」 / _dx
qqr,(+xd ), 1• --_ _________; :qz ( 「少」 / _dx
그립 6.6 열 이동속도의 변화를 거리의 함수로써 나타낸 설명도.
y ,z 방향에 대해서도 동일하므로 단열계내에서 반웅중에 생긴 열에 너지 생성항을 E g라 하고 반응 후에 최종적으로 계내에 남은 열에너 지 보존량항을 Es t라고 하면 이들은 각각 (6.12) 식과 (6.13) 식으로 나타낼 수가 있고 (6.14) 식을 쓸 수 있게 된다. Eg= qd xdyd z (615(2K)15( 3615 4 Est= p C플 dxdy dz .j)、 Est= E,n+ Eg 一 Eout 여기서
또 (6.9), (6.10) 및 (6.11) 식들로부터 (6.16) 을 얻는다. 홉모총 dy -홍 dz+ q dxdy dz= p C 폴 dxdy dz (6.16) 푸리 에 법 칙 (Fourie r 's law) 으로부터 qx = 一 kdyd .z;—aaTx— (6·17 ()618()619 ) qy = -k dxriz -caa:+Ty.: - · q z= -kdx d_릅 · 그리 고 각 열유속 성 분식 (heat flux comp on ent equ a ti on ) qx’’ = —k-8a -Tx- - ’_6·_2`0`,'_ __6` '2’·`1I'16L2 2 q%z’' = =_k王—a星z ,' ` 8T __ 으로부터 열확산 방정식 (heat diff usi o n e q ua ti on) 인 (6.23) 식을 얻을 수 있다. 占룹)+#룹)+占룹)+q=p C픕 {6.23) 이 열확산 방정식에서 보면 단위 부피내의 열에너지 보유량의 변화 속도는 각 단위 부피내로 유입되는 알짜전도 열량속도에 단위 부피당
의 열에너지 생성속도를 더한 것과 같다는 것을 알 수 있다. 이 식을 변형하면 아래의 (6.24) 식을 얻는다. 호ax2仁 1 호ay工 2 1+ d궁 호 구k= -上a 끄at (6.24) 여기서 a= ―p LC p 값, 죽 k 값이 커지면 그 매체내에서는 에너지가 축 적되기보다는 잘 전도되어 열량이 유출된다는 것을 의미한다. 이 식을 더 일반화시키면 정류상태에서는 단위 부피내의 에너지 측 정량이 일정{t::, £s1=0) 하므로 (6.25) 식과 같이 요약할 수 있다. 出룹)+嶽룹)+嶽룹)+ q =O (6.2 5 ) 이때 열이동이 x 방향으로만 일어나는 1 차원적 모델이라면 이 식은 (6.26) 식과 같이 더욱 간략해질 수 있다.
 qz + 쇼
qz + 쇼
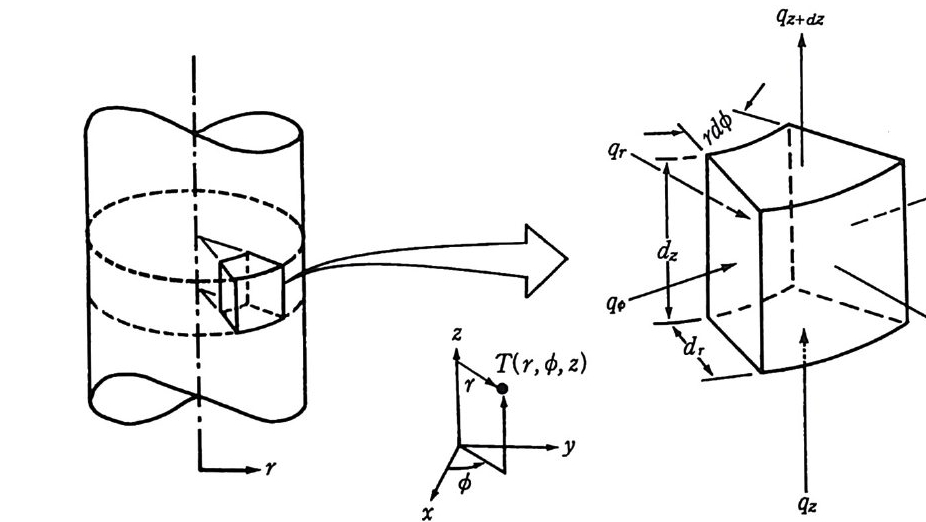
그림 6.7 원통형 좌표계 (r, t/J ,z) 에서 열전도 분석을 위한 미분 조절 부피 : dr • rdt/J • dz.
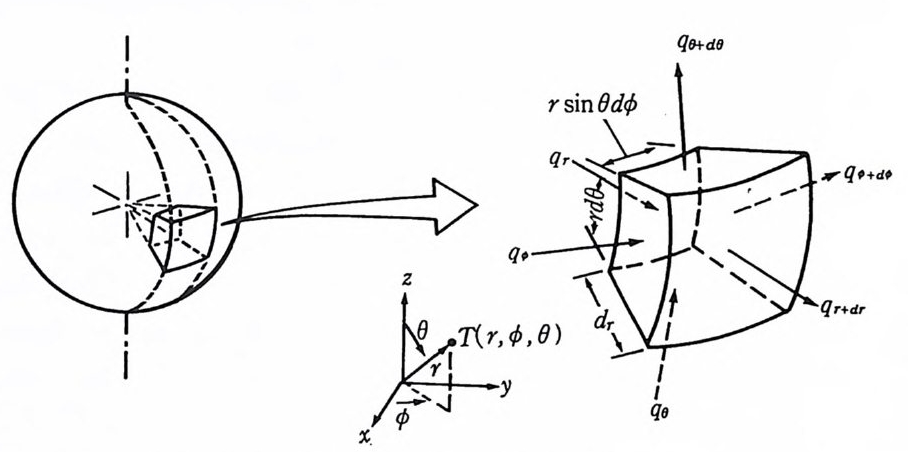
걸(틀 )=O (6.2 6 ) 죽 에너지 생성량이 없는 정류상태에서는 일정한 방향으로만 열이 동이 일어나며 열흐름 (hea t fl ux) 은 각 이동방향에 대하여 일정하다. (6.26) 식에서 dq x' '/dx=O 이 되는 것을 알 수 있다. 한편 그림 6.7 과 그림 6.8 에서 보는 바와같이 원통형이나 구형 좌 표계 (cy li n d eric al or sph eric a l coordi na te s ) 에 대 한 열확산방정 식 이 (6 . 27) 식과 (6.28) 식에 각각 표시되었다. 言 (k 룹)+訂훑(틀)+짊룹)+ q =p Cp 풍 (6.2 7 } 士蔚 (k 딩풍)+ 곱굽。 嶽물)+ 갑 n0 길 k s i n0 를)+ d =pC 플 (6.2 8 )
 q針 d8
q針 d8
그림 6. 8 구형 좌표계 (r,¢,0) 에서 열전도 분석을 위한 미분 조철 부피 : dr • rsin 8 d¢, • rdB.
열흐름 (heat flux ) q, 운동량흐름 (momentu m flux ) r 및 물질흐름 (mass flux ) m 은 각각 (6.29), (6.30) 및 (6 . 31) 식들로 표시되며 이 들 각 흐름을 대 류 (convecti on ) , 난류 (tur bulence) 및 확산 (dif fus io n ) 이라 명명한다. Convecti on (heat flux ) : q= kDT (6. 29) Turbulence (momentu m flux ) : t = µDv (6. 30) Diffus io n (mass flux ) : m=DDC (6.31) 이들은 흐름식도 갇은 형태로 표현될 뿐만 아니라 상호간에 연관시 킬 수 있는 유사성을 갖는 양둘이다. 6-3 물리 및 화학적 합성 데이터 소련 반응 모델의 리 뷰 (rev iew ) 와 그 후 Sy st e m Plannin g Corp o ra- tion (SPC) 의 조사보고에 의하면 다음과 같은 형 의 데 이터들이 반웅 현상학을 기술하는 데 중요한 것으로 예견된다. i ) 열역학적 데이터 : 열용량, 엔탈피, 엔트로피, 상전이 엔탈피. ii) 물리적 데이터 : 상전이 온도, 중기압, 용해도. iii) 화학 반응속도론적 데이터 : 열확산율, 물질확산율, 반응속도. 위 데이터 조사는 전면적인 문헌 리뷰 (rev i ew) 가 못 되고, 미국과 소련의 기술문헌에서 주로 볼 수 있고 쉽게 얻을 수 있는 핸드북이나 표에 집중되었다. 조사된 반응에서 관십있는 특수한 물질에 대하여 몇 가지 데이터들이 쉽게 얻어지지 않는 것은 예측한 바와 같다. 반웅 데이터 수집에서 주로 관심의 대상은 상조건(p hase cond i- tion ) , 반응대 (reacti on zone) 및 물질 분포 (mass distr ibu ti on ) 등이 다. 이들 양들은 응용 모델의 형태, 그들의 경계조건 (bounda ry condit ion )
및 그들의 타당성 범위들을 지시해 준다. 다음과 같은 다섯 가지 반 응에 대하여 중요한 온도 범위에서 이들 파라미터들을 정의하도록 돕 기 위해 데이터들을 찾았다. iii )) 탄질화화티알탄루(미원늄소 간: 2 A반l웅(s)) +: NT2i ((sg) ) +- -C-+(2gAr aIp Nh i(ts e)) — --+T iC (s) iii) 탄화티 탄 (산화물과 반웅) : 3Ti0 2 + 3C (grap h it e) + 4Al (s) 一 3TiC (s) + 2Al20 l s) iv) 이봉소화티탄(원소간 반응) : Ti (s ) +2B(s)------+TiB 2 (s) v ) 이 붕소화티 탄 (산화물과 반응) : 3Ti0 2 (s) + 6B(s)+ 4Al (s) 一 3TiB z(s) + 2Al20s(s) i )' ii) 및 iv) 반응에서 생성물은 원소 금속조성으로부터 생성되 고, iii)과 v) 반응에서는 주물생성에서 설명한 바와갇이 산화물로부 터 생성물이 형성된다. 산화물로부터 주물생성물 생성에 관하여 그 합성공법은 더욱 복잡하지만 그 재료물질값은 더욱 낮을 것으로 기대 된다 . 왜냐하면 원소 금속분말은 산화물형보다 대개는 값아 상당히 비싸기 때문이다. 위 반응을 위한 연소 메커니즘을 설명하기 위하여 다음과 같은 반 응조성들과 생성물들의 데이터가 필요하다 . • Al ·B ·C • Ti •AlN • B203 • N2 • TiB 2 • Al203 • TiC • Ti0 2 일반적으로 바람직한 형의 붕소와 탄소에 대한 데이터는 얻을 수가 없다. 우리들의 바람은 무정형 탄소 또는 그을음과 무정형 붕소에 관 한 데이터이지만 실제로 데이터들은 흑연이나 결정형 붕소에 대해서 만 쉽게 얻을 수 있다. 그 의에 특별히 AIN, B 및 C 에 관하여는 데 이터들의 차이가 나타나고 그들 일련의 데이터의 상대적인 질의 평가
가 불가능하다. 상업적으로 얻을 수 있는 물질의 순도는 또한 광범위 하게 변하고 분석적 연구에서도 불확정성이 개입될 것이다. 그 어려 움에 관하여 SPC 조사에서 사용한 가정들은 뒤에 소개될 것이다. 화학열역학적 데이터의 표에 대한 자료들은 앞의 SPC 기록 (document) 3) 에서 참조한 것 이고 그 이유 때문에 이 보고서 끝의 참 고문헌 목록에 되풀이하여 쓰지 않았다. 현행 연구를 위하여 사용된 많은 데이터는 금속 핸드북 108) 과 한 그룹의 열역학적 표 109) 들로부터 얻었지만 다른 참고문헌들 또한 정보로 사용되 었다. 110),111) 이 장의 6-4 절에서 6-8 절까지 특별 합성반응의 연구에 유용한 참고 문헌(1 08) 으로부터 선택한 데이터는 부록 C 에 수록하였다. 이미 연구한 다섯 가지 반웅의 온도들은 상당한 범위로 변하기 때 문에 반응하는 화학종들의 상변화와 비열변화는 단열 반응온도, 반응 에너지 등을 계산하는 데 고려되어야 한다. 따라서 몇 가지 기본 데 이터가 위에 수록된 11 가지 반응물과 생성물에 대하여 계산되고 또 도시되었다. 이들 계산의 결과는 부록 D 에 표시하였다. 참고문헌 (109) 의 표에서 원래 취한 온도 (T) 데이타에 대한 비열 (C p)의 그래 프를 그립 D-1~ 그림 D-11 에 도시하였다. 각 그립에는 화학종들의 상들, 각 상의 T 대 모델화된 C p의 식 및 그들 식으로부터 얻은 곡 선들이 포함되어 있다. 잠열 데이터와 결합된 그들 비열식들은 광범위한 온도에서 반응물 과 생성물의 화학종들에 대한 엔탈피, 엔트로피 및 Gib b s 자유에너 지롤 계산하는 식으로 발전시키는 데 사용되었다. 그들 식으로 계산 한 데이터가 부록 D 의 표 D-1~ 표 D-11 에 또한 수록되었다• 앞에서 확인된 각 다섯 가지 반웅은 반응계의 연소거동을 예측하 기 위하여 계산된 데이터를 사용하여 분석하였다. 열역학적 분석들은 반응자발성, 전체 반웅열, 단열 반응온도 및 각 반응에 대한 상들을 결정하는 데까지 진행되었다. 점화되어 연소한 각 계에 대하여 상조 건들과 확산의 역할, 흡착 등을 분석하기 위하여 반웅 현상학의 데이 터를 기억장치의 어드레스에 넣었다.
반응경로에 존재하는 상들과 상계면들의 대략적 설명은 비열과 잠 열 데이터에 기초를 두고 있다. 용해도와 속도론적 반응속도 데이터 는 주어진 계에서 물질 분포를 계산하기 위하여 분석되었고 이들 계 산으로부터 물질확산, 열확산 및 루이스 수와 같은 총계적 지표들은 어떤 단계나 위치에서 반웅이 일어나기 쉬운가를 결정하기 위하여 기 억장치의 어드레스에 넣었다. 각 반응에 대한 계속되는 고찰과 결정을 나타내는 데 사용한 서식 은 다음과 같다. i ) 일반적인 고려 : 반응물, 생성물, 초기 조건들. ii) 열역학적 분석 : 자발 반응온도, 단열 반응온도, 반응열, 평형 변환, 상들. iii) 반응현상학 : 반응계 환경 의 단계 적 분석 , 상조건들 등. 6-4 질화알루미늄의 합성 처음으로 다룬 반응은 다음 식과 같이 원소 알루미늄 금속과 질소 기체로부터 질화알루미늄을 생성하는 것이다. 2Al(s) + Ni{ g)----+ 2AIN(s) 이 반응에 대한 출발물질들은 고순도 알루미늄 금속입자 분말과 순 수한 질소기체라고 가정한다. 엄격한 측정을 하지 않는다면 그 알루 미늄 입자들은 공기에 노출된 모든 표면이 약 5mn 두께의 화학흡착 산화물충을 갖게 될 것이고 알루미늄 혹은 질소의 확산을 제한시키거 나 또는 열이동을 방해 함에 의하여 이 산화층은 그 반응역 학 (reac ti on mecha ni cs) 에 영향을 줄 수도 있다. 그 반웅 혼합물을 희석하거나 생 성물 상의 결정성장을 위한 핵 형성 자리를 제공하도록 질화알루미늄
입자들을 소량 가할 수도 있다. 6 ― 4 一 1 열역학적 분석 그 반응에 대 한 Gib b s 자유에 너 지 또는 화학 퍼 텐셜 (chem ica l pot e n ti al) 데이터는 표 6.2 에서 보는 바와같이 열역학적으로 정반응 은 낮은 온도에서 잘 일어나지만 역반응은 약 3100K 이상 온도에서 유리하게 일어난다. 온도증가에 따라 엔탈피는 최종에 가서는 감소하 게 되고 Gib b s 자유에너지는 단조롭게 증가하기 때문에 이 반응은 3100K 이상 온도에서는 엔트로피에 좌우된다는 것을 이들 데이터가 제시한다. 의부적으로 추가했거나 또는 반응 엔탈피의 인접대로부터 온 열은 최종 생성물의 온도를 상승시키지만 더 이상 변환에 대하여 는 기여할 수 없을 것이다. 이들 열역학은 자발성을 나타내지만 반응 속도론에 대하여는 아무것도 알 수가 없는고로 자발 반응온도의 고찰 은 결론적인 것이 아니다 . 표 6·2 질화알루미늄 합성의 자유에너지 값. 단열 반응온도 =2790K , AIN 상 : 67% 고체 및 33% 해리된 기체. T(K) t::i. H(cal/ mo l) t:. G(cal/ mo l) 300. 00 -152000.00 -1 37100. 00 400. 00 -152400. 00 —137 200. 00 500. 00 -152700. 00 -132100.00 600.00 -152900.00 -1 27000. 00 700.00 -153000.0 0 -121800.00 800. 00 -152500.00 -1 16800. 00 900. 00 -152500. 00 -111700. 00 1000.00 -157500.00 -1 06900. 00 1100.00 —157 500. 00 -101200.00
1200. 00 -157400 .00 -95600.00 1300.00 -157300. 00 -89980.00 1400. 00 -157300. 00 -84370.00 1500.00 -157200. 00 -78760. 00 1600.00 -157200. 00 -73160. 00 1700. 00 -157100. 00 -67550. 00 1800.00 -157200.00 -61980.00 1900. 00 -157200.00 -56370.00 2000.00 -157100. 00 -50770.00 2100.00 -157100. 00 -45170.00 2200.00 -157100.00 —395 80.00 2300. 00 -157000. 00 -33980.00 2400.00 -157000. 00 -28390.00 2500. 00 -156900.00 -22790.00 260 0. 00 -156900.00 -17200.00 2700. 00 -156900. 00 -11610.00 2800.00 -165.40 -17.9 5 2900. 00 —800 . 70 —23 .44 3000. 00 -1438. 00 -6.61 3100.00 -2078.00 32.43 3200. 00 -2721.00 92. 54 3300.0 0 —336 6. 00 173. 40 3400.00 -4 013. 00 274.50 3500. 00 -4662.00 395.00 일정한 온도에서 Gib b s 자유에너지는 다음 식으로 나타낸다. D.G =D .H -TD .S 6. H 는 취급한 전체 온도 범위에서 0 보다 작고 온도는 항상 양이므
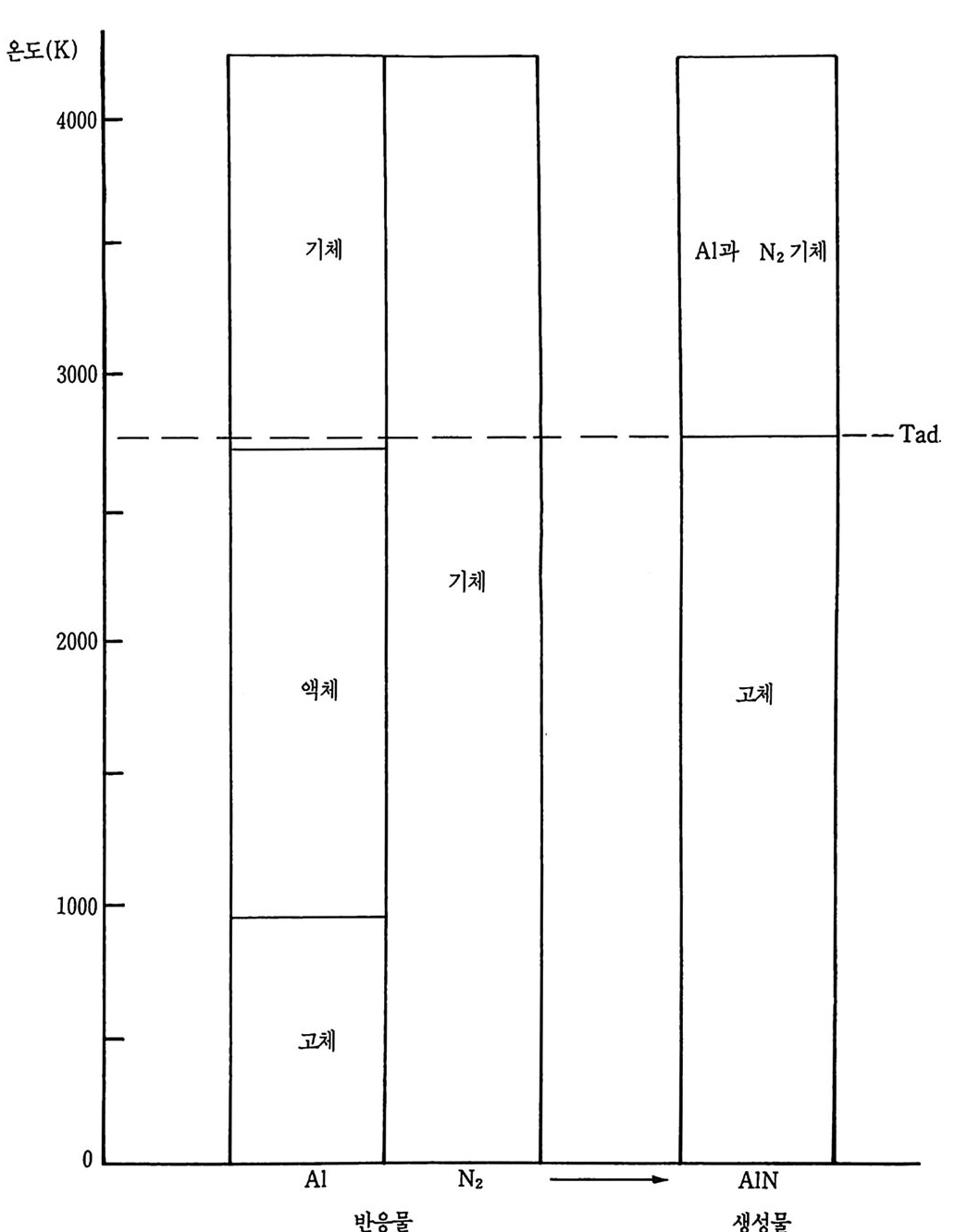
로 AG 가 양의 값을 가질 때 A S 항은 0 보다 작아야 한다. 이와같이 고도의 질서도가 있는 고상 질화알루미늄 생성물은 유체상 반응물들 특별히 큰 엔트로피를 갖는 질소보다 더 낮은 엔트로피를 갖는다. 단열 반응온도 2790K 는 참고문헌 (95) 에서 설명한 바와같이 참고문 헌(1 09) 의 데이터를 사용하여 이 반웅의 조성들의 엔탈피로부터 계산 할 수 있었다. 이 경우의 반응열은 1850ca ljg이다. 6_4— 2 반 응 현상학 AIN 합성반응에서 순수한 조성들의 상 데이터들은 그림 6 . 9 와 표 6.3 에서 보는 바와 같다. 관계된 첫번째 온도 범위는 298K 부터 933K 까지 연장된다. 298K 에서 알루미늄은 고체이고 질소는 기체이 다. 만약 질화알루미늄이 처음 반응물에 가해진다면 그것은 고체상으 로 있을 것이다. 이 초기 배열이 주어진다면 그림 6 . 10 에서 보는 바 와같이 알루미늄은 어떤 산화물충을 통하여 고체상태 분자확산에 의 하여 확산될 것이 기대된다. 유사하게 질소기체 분자들도 그 산화물 충 속으로 확산될 것이 기대된다. 그렇지만 처음에 기체질소는 그 산 화물 표면에 흡착되고 그 후에 내부로 확산된다. 그 이유는 흡착된 표면 농도가 형성되고 그것은 확산의 추전력으로 작용하는 농도 기울 기를 높이기 때문이다. 이 과정들 각각의 상대속도와 밀도 및 이들 조건과 이 온도 범위에 서 알루미늄과 질소의 반응성에 의존하여 질화알루미늄을 생성하는 반응은 때를 맞추어 많은 위치와 점에 일어날 수 있다. 만일 알루미 늄이 순수한 질소기체 환경에 있다면 질소기체는 그 입자들 표면에 흡착될 것이고 그 입자들 속에 있는 기공을 채울 것이다. 만약 반응 이 순수한 질소기체 환경에서 일어나지 않으면 흡착열역학에서 계산 할 수 있었듯이 질소분자들은 기체 불순물과 경쟁하여 흡착자리 (adsorp tion sit es ) 에 흡수될 것 이 다.
 온도 (K)
온도 (K)
그림 6·9 질화알루미늄 반웅의 상 데이터.
표 6·3 질화알루미늄 합성에서 순수한 조성들의 상 데이터. T(K) Al N2 AIN Al203 298:5 : T<933 s g s s T=933 s .... l g s s 933< T<2315 I g s s T=2315 l g s s .... 1 2315< T<2790 I g s I T=2790 l ..... g g 분해 I 2790 < T < 3253 g g I T=3253 g g 분해
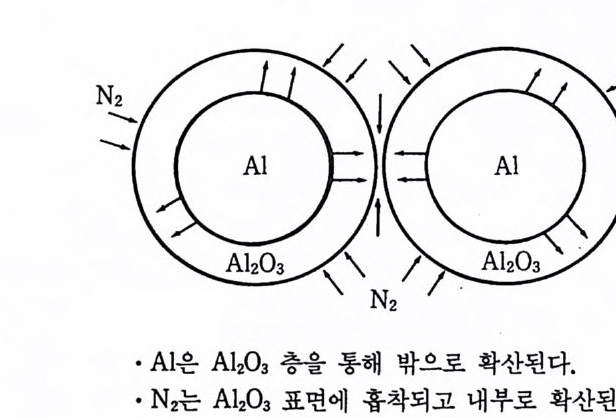 • Al 은 Al203 층을 통해 밖으로 확산된다.
• Al 은 Al203 층을 통해 밖으로 확산된다.
그림 6.10 알루미늄과 질소의 확산.
질소기체 분자가 알루미늄 또는 산화알루미늄 표면을 만나면 약간 은 흡착될 것이다. 이들 흡착된 질소분자들의 일부는 그 산화물충을 통하여 확산되며 알루미늄 원자들과 반응하여 고체 질화알루미늄을 형성하고 나머지는 흡착된 질소분자 본래대로 남아 있울 것이다. 그 변환은 새로운 흡착자리를 만들지만 기질 (subs tr a t e) 은 알루미늄보다 는 질화알루미늄이 될 것이다. 알루미늄 기질의 인접 자리들을 이용 할 수 없다면 이와같이 새로 흡착된 질소는 추가적인 반웅이 일어날
수 있기 전에 그 산화충에 더하여 불활성 생성물충을 통해 확산하여 야한다. 기체분자가 금속입자의 표면으로 확산이 일어나면 농도 기울기가 그 표면과 입자의 내부 사이에 생기는데 그 기울기는 입자 속으로 물 질확산의 추진력을 일으킨다. 기체조성이 고체입자로 확산되어 들어 가면 결합의 깨짐과 같은 의미있는 특수한 작용이 없다고 가정할 때 한 고용체가 형성되는데 그 고용체는 용융과 증발온도를 변화시킨다. 그런고로 그림 6.9 에서 보인 상 데이터는 반응에서 단지 상조건들의 근사값들이다. 반응하지 않은 질소가 알루미늄 기질 표면에 흡착되고 자유질소가 고체로 확산되어 들어갈 경우에 새로운 질소기체 분자는 빈 자리 (vacant s it e) 에 흡착될 것이고 본체 기체상 (bulk gas p hase) 으로부터 온 기체질소 분자들은 그 표면에 존재하는 질소필름으로 확산해 들어 간다• 관계된 두번째 온도 범위는 933K 와 2315K 사이에 해당하며 약 933K 에서 알루미늄 입자들은 녹는다. Al203 의 융점은 2315K 인데 이 것은 Al203 껍데기 안에 포함된 액체 Al 이 달아날 수 없음을 나타낸 다. 껍질충의 결함, 약 5nm 정도인 껍질의 얕은 깊이 및 온도가 상 승할 때 열 체적 팽창의 역학적인 힘 등 때문에 그 껍질은 작은 Al2 03 입자로 찰 파괴될 것이다. 녹을 때 Al 의 체적 팽창은 6.5% 이므 로 자유액체 Al 은 계 안에 나타날 것으로 기대된다. 녹은 Al 은 그 융점 부근에서 상당한 점성이 있다 (Al 의 접성도는 973~1023K 에서 1. 0~ 1. 2 센티포아제 (c p)이고, 25°C 에서 물의 점성도는 약 0.9cp 및 25°C 에서 수은의 점성도는 약 l.6c p이다). 그런고로 질소기체 가 입자간 톰새를 채우면 약간의 기체는 그 입자들이 액화될 때 포착 될 것이다. 이 점성 액체금속에 이와같이 포집된 기포들은 그곳에서 반응이 일어날 수 있는 표면을 만들 것이다. 또한 본체-기체 (bulk- g as) 와 본체-액체 (bulk- liq u i d) 상 계면에서 기체-액체 계면은 반 응 표면울 제공할 것이다. 액체 Al 과 N2 기체의 각 계면에서 질소는
분자확산에 의하여 액체 속으로 확산될 것이다. 질소가 알루미늄으로 흐름은 기체상의 질소농도와 액체 Al 에 질소의 물질확산율에 의존하 는데 이들 양들은 두 가지 모두 온도에 의존한다. 온도가 Al 의 녹는 온도 이상으로 상승하면 포집된 기체는 팽창할 것 이 며 본체 표면 (bulk surf ac e) 에 뜨게 된다. 그 온도 상승은 포집 된 기체 체적을 증가시키고 그 표면적을 증가시키며 그 밀도 또는 농도 롤 감소시킨다. 이둘 포집된 질소기포에 대한 부력의 근사치를 얻기 위하여 아르키메데스의 원리*가 사용되었다. 1~lOµm 크기 범위의 질소분자에 대 하여 부력은 최 소 10-9 d yn e 에 서 최고 10-6d yn e 까지 변 한다. 기포의 Rey no ld 수 (ReD) 는 1 보다 작기 때문에, 크리핑 운동 (creepi ng moti on ) 의 Sto ke 법 칙은 기포속도를 계 산할 수 있게 한다.
*PAi = Z.646-0.2sx10-4 T g/c m3, 여기서 T(K)108) PN,=P/RT= (1/ 82.05) y-i g /cm 인 힘 = (p.41 -PN,)g • V= [(2. 646-0.28Xl0-4T) -(1. 219 X 10-2 T 게 ] (980 . 7) [ (4/3) 7ry 3 ] lOOOK 에서 lOµm 기포에 대하여, F=~10-6dyn e s.
CD= 싶ReD _ -= l/2pF Du 2 A p 및;,_ nReeDu=- 쁘 µ싣 여기서 CD 는 저항계수, FD 는 부력, 쩌즌 밀도, u 는 기포 확산속도, A p는 기포의 단면적, µ는 액체의 점성, 그리고 D 는 액체충의 두께 룰 나타낸다. 이들 두 식을 결합하면 IOµm 와 Iµm 기포들에 대하여 각각 14 . 2cm/sec 와 1. 4cm/sec 의 속도를 얻는다. 이는 질소반응물의 주원천은 녹은 질소이며 액체 Al 에 질소의 용 해도가 고려할 만하다는 것을 제시한 것이다.
6 一 5 탄화티탄 (T i C) 의 합성 (원소 반응) T i C 를 생성하는 원소반응은 다음과 같이 쓸 수 있다. Ti (s ) +C (s) 一 ➔ TiC ( s) 이 연구와 관련된 소련 실험 5) 에서는 램프 그을음(l am p black) 을 사 용하였다. 램프 그을음에 대한 물리적 데이터를 쉽게 얻을 수 없으므 로 흑연(gr a phit e) 에 대한 데이터로 대용하였다. 램프 그울음 데이터 가 없어 비교의 기준이 없게 되므로 이 대용에 따른 오차는 알 수가 없다. 처음 반응물로 채운 것을 순수한 티탄분말과 순수한 탄소분말 인 것으로 추정하는 것이다. 6— 5-1 열역학적 분석 Ti C 합성반응에 대한 Gi bb s 자유에너지는 표 6.4 에 수록하였다. 유효한 데이터에 근거하여 Ia t m 압력에서 표준온도와 그 이상의 온 도에서 정반응은 자발적으로 일어나므로 반응속도론이 가장 중요하게 될 것이다. 열용량 데이터 95),109) 에 근거를 두면 단열 반응온도는 TiC 의 녹는 온도이기도 한 3290K 이다. 이 온도는 소련 계산치와 잘 일 표 6.4 Ti C 합성에 대한 Gib b s 자유에너지 값(원소반웅). 단열 반응온도 =3290K, T i C 상 : 76% 고체 및 24% 액체. T(K) t:,. H (cal/mo!) 6 G (cal/mo!) 300.00 -44010. 00 -43160. 00 400.00 -44010.00 -42880.00
500. 00 -43990. 00 —426 00. 00 600.00 -43930.00 —42 320.00 700.00 -43850.00 -42060.00 800. 00 -43780.00 -41810.00 900.00 -43720.00 -41570.00 1000. 00 -43700.00 -41330. 00 11210000..0000 -43930.0 0 ——4401 7 01500..0 000 -44960.00 1300.00 -44930.00 -40360.00 1400.00 -44900. 00 -40010. 00 1500.00 —448 90. 00 -39660.00 1600.00 -44880.00 -39320.00 1700.00 -44960.00 -39030. 00 1800.00 -44960.00 -38680.00 1900. 00 -44960.00 —383 30. 00 2000. 00 —49 360.00 -37860. 00 2100.00 -49340.00 -37290.00 2200.00 -49290. 00 -36710 .00 2300.00 -49230.00 -36140.00 2400.0 0 -49140.00 -35580.00 2500.00 —49 030. 00 -35020.00 2600.00 -48900.00 —34 460.00 2700.00 —487 50. 00 -33910.00 2800. 00 一 48570.00 -33360.00 2900.00 -48380.00 -32820.00 3000.00 -48170.00 —32 290.00 3100.00 一 47930.00 —31 760.00 3200.00 -47670. 00 -31240.00 3300.00 -30850.00 -30470.00 3400.00 —308 10. 00 —304 60. 00 3500.00 -30770.00 -30450. 00
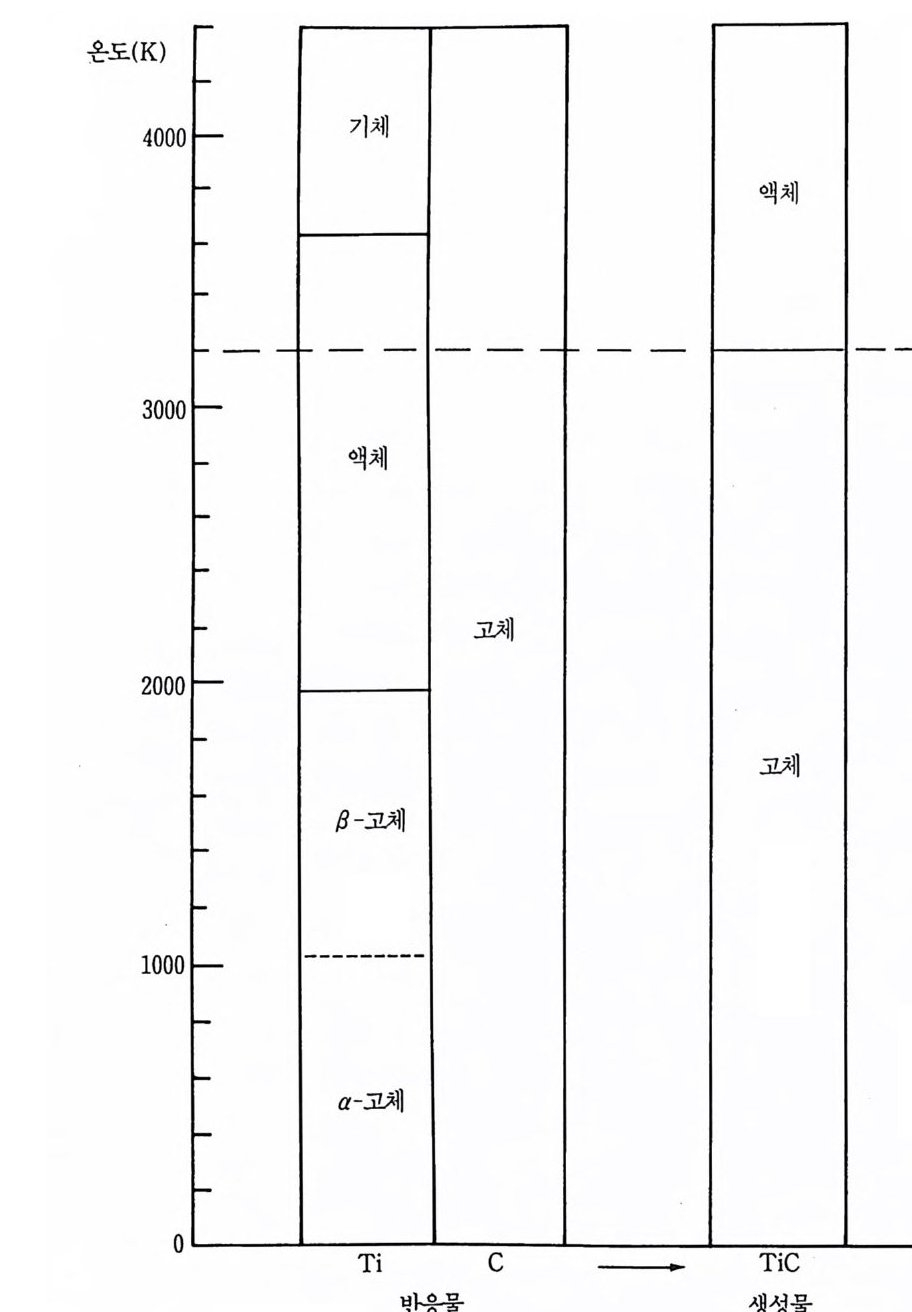
치하는데 이 연구 109) 에서 계산한 24% 액체 T i C 에 비교하여 소련 연 구에서는 33% 의 TiC 생성물이 액상(liq u i d p hase) 이라고 보고하였다. 똑갇은 열용량 데 이 터 에 의 하면 이 계 의 반응열은 약 730cal/ g이 된 다. 6-5— 2 반응 현상학 비기체 연소이론은 그 반응의 역학과 상당히 비슷한 것 갇다. 표 6.5 와 그림 6.11 에서 보는 바와같이 298~1933K 온도 범위에서 두 반응물질은 모두 고체이다. 단열 반응온도인 3290K 까지도 탄소는 고체로, 티탄은 액체로 그리고 탄화티탄은 고체로 세 가지 조성들 모 두가 여전히 응축상태이다. 특별히 여기서 생각한 온도에서 어떤 최 소 기체상이 그 응축된 상들과 평형을 이루고 있을 것으로 기대한다. 298~1933K 온도 범위에서 차게 한 반응 콤팩트와 틈새면 영역은 아마도 낮은 밀도의 기체상과 접촉되어 있을 것이다. 그 반응 용기가 전공 또는 비활성 기체환경으로 유지되지 않는다면 그 틈새 표면은 흡착된 기체를 포함할 것이다. 이갑은 계가 주어지면 다음과 같은 몇 표 6.5 원소형으로 TiC 합성에 대한 상 데이터. T(K) Ti C TiC 298-:1155 Sa s s 1155 sa~s, s s 1155~1933 s, s s 1933 s,. ... l s s 1933~3920 I s s 3290 I s s .... l 3290~3591 I s l 3591 l ..... g s 1
 온도 (K)
온도 (K)
그림 6-11 T i C 합성반응에 대한상 데이터(원소반웅).
가지 구역에서 반응이 일어난다. i ) 틈새들의 기체상에서. ii ) 틈새 표면에 있는 한 개의 고체 - 기체 계면이나 그 근처에서. iii) 고체-고체 접촉영역에서. 각각 이들 구역간 물질과 에너지의 상호이동은 그곳에서 일어날 수 있는 중요한 반응의 가능성을 평가하기 위해 고려되어야 한다. 이 고 려 대상에는 다음과 같은 많은 인자들이 있다. i ) 중기압, 승화에너지, 표면 장력. ii) 고체 , 액체 및 기체 상들에서 조성들의 확산성. iii) 흡착 데이터, 표면에너지. 고체 표면들이 접촉 또는 근접하지 않은 곳에서 물질의 운반현상은 그 반응물들이 본체 - 고체 (bulk-s o li d) 상을 떠나 기 체 상으로 들어가야 하는 필요성에 근거를 둔다. 거기서부터 그들은 다른 고체 반응물 입 자로 확산되고 이 반응입자들에 흡착되며 이 흡착자리에서 반응하거 나 반응이 일어날 때까지 그 입자로 확산해 들어간다 . 또한 반응이 그 기체상에서 일어날 수도 있다. 어느 한 경우에 이들 경과는 반응 분자들이 본체-고체상에서 기체상으로 변화하는 첫 단계로 제한되는 것 같다. 승화의 방해 지표는 평형 증기압, 승화에너지 및 표면 장력 에 의하여 결정된다. 기체상이 반응의 유력한 특칭인지 아닌지에 관계없이 고체_고체 입 자 접촉영역이나 또는 근처에서 확산이 중요하다. 전자현미경 척도로 고체반응물의 표면은 도저히 매끄럽지 못하지만 고체-고체 접촉점 또 는 표면들이 있을 것이다. 이들 접촉점에서 반응물질 A 가 물질 B 로, B 가 물질 A 로의 물질이동은 고체상 분자확산에 의하여 생길 것 이다. 이들 확산속도는 각각의 농도 기울기와 확산성에 의하여 조절 될 것이다. 만일 반응이 일어나면 이와같이 형성된 생성물충을 통하 여 반응물 분자들(이 경우는 금속원자들) 각각의 분자확산도 고려해야 한다. 접촉 부위 아주 근접한 부분에서 발열반응에 의한 온도상승과 이질
의 생성물과 반응물 분자들간의 상호확산으로 일어날 수 있는, 그 접 촉 부근의 반응물 분자의 소모와 밀도나 농도의 감소는 분자들을 고 체一본체상에서 접촉 부분으로 이동하도록 한다. 또 기체상에 들어가 는 접촉 부분에 아주 근접한 곳의 본체―상 반응물들은 그들이 흡착될 곳인 인접 입자 표면에 접촉하기 전에 기체상을 통해 짧은 거리를 확 산한다. 만일 이 거리가 기체상 분자의 평균자유행로의 차수라면 물 질확산의 장벽은 최소가 될 것이며 아마도 승화속도에 의하여 조절될 것이다. 응축상 조성의 평형 증기압은 그와 역학적 평형으로 존재하 는 기상반응물의 농도를 측정할 수 있게 하고 응축상과 기체상 계면 에 관하여 조성의 농도를 계산하는 방법을 나타낸다. 순수한 티탄의 녹는 온도에 가까워지면 티탄입자들은 아마도 티탄 용매와 탄소용질로 된 고용체로서 존재할 것이며 그 역도 성립한다• 만약 다른 조성들, 즉 열렸거나 진공되지 않은 계내에 있는 기체 또 는 탄소 의에 흡착된 기체가 있다면 그들은 또한 다성분 용액내의 용 질로서 그 입자들 안에 존재할 수도 있다. 용질분자들의 존재는 어떤 범위에서 티탄입자들의 녹는 온도를 변화시킬 것이다. 그렇지만 티탄 의 융점강하에 대한 데이터는 이 연구에서는 얻을 수가 없었다. 실질 적인 반응이 일어나기 전에 티탄 입자들이 녹는 한, 이 융점변화는 그렇게 중요한 것 같지 않다. 그렇지만 이 전이중에 반응이 크게 일 어난다면 반응이 일어나는 그 온도를 아는 것은 중요하다. 티탄입자들이 녹은 뒤에 탄소입자들은 티탄 액체로 둘러싸일 것이 다. 이 온도에서 티탄의 증발온도까지의 간격 약 1600K 에서는 반응 하는 구형입자들의 고전적 모델이 타당한 것으로 보인다. 6 一 6 탄화티 탄의 합성 (산화물 반응) 이 반응은 다음 경험식으로 보일 수 있는 바와같이 산화물 형태로
부터 탄화티탄을 생성하는 것을 나타낸다. 3Ti0 2 (s) + 3C (s) + 4Al(s) -一 3TiC (s) + 2Al203 알루미늄 분말은 환원제로 가하며 액체 슬래그(liq u i d sla g)로 반웅 생성물에서 나타난다. 초기 반응물들은 본래는 순수한 이산화티탄분말, 탄소분말 및 알루 미늄분말을 포함한 것으로 가정하고 가열하기 전에 찰 혼합한다. 앞 에서 말한 바와같이 램프 그울음에 대한 데이터는 이 연구에서 얻을 수 없으므로 고체탄소는 흑연으로 가정한다. 이 대용에 의하여 생간 불확정성은 또한 알 수가 없다. 6-6— 1 열역학적 분석 이 반응의 Gib b s 자유에너지 변화(1::,. G) 값은 표 6.6 에 수록하였 다. 상온에서 단열 반응온도까지 열역학적으로 정반응이 유리하다는 것을 이들 데이터가 나타낸다. 참고문헌 (109) 의 열용량 데이터로 계산한 단열 반응온도는 2317K 이고 이 분야의 소련 연구자들로부터 Tad 값은 이 반웅 95) 에 대하여 제시하지 않았으며, 위에 쓴 경험식에 대한 반응열은 665ca l/g이다. 표 6.6 산화물로부터 T i C 합성에 대한 자유에너지 값. 단열 반웅온도 =2317K, T i C 상 =100% 고체, Alz03=lOO% 액체. T(K) 6 H(cal/ mo l) t:,. G(cal/ mo l) 300.00 -255500.00 -247900.00 400. 00 -255900. 00 -245300. 00
500.00 -256100.00 -242600. 00 600.00 一 256500.00 -239900. 00 700.00 一 256500.00 -237100. 00 800. 00 -256500. 00 -234300. 00 900. 00 -256600.00 -231500.00 1000.00 -266700. 00 一 228200 . 00 111213000000...00 0000 --—222666777 567000000...00 0000 --—222212460 232000000...0 00000 1400.00 -267800.00 -212300.00 1500.00 -267900. 00 -208400.00 1600. 00 一 266700 . 00 -205400.00 11870000..0 000 --226666680000..0000 -—210918 800000..0 000 21900000..0000 --226666420000..0000 -—119940 240000..0000 22120000..0000 —-236154 920000..0000 --118860670000.. 0000 2300.00 -313900.00 -174700.00 2400.00 -258300. 00 -170400.00 2500. 00 -257800. 00 -166700.00 2600. 00 -257300.00 -163100.00 22870000..0 000 --253536770000..0 000 -—115592 550000..0000 2900.00 -532000.00 -139000.00 3000.00 -530200.00 -125400. 00 3100.00 -528300.00 -112000.00 33230000..0000 ~5—296247 0000..0 000 -91889447000.. 0000 33540000..0000 -—992241 1600..0000 120968500000..0 000
6-6-2 반응 현상학 표 6.7 과 그림 6 . 12 에서 보는 바와같이 세 가지 반응물질은 처음에 는 모두 고체상이다. 약 933K 로 가열할 때 알루미늄입자들은 녹는 다. 만일 화학양론적 양의 반응물들이 사용되면 액체 알루미늄은 933 K 에서는 반응 체적의 약 40% 및 2100K 에서는 약 43% 를 차지한다. 이와같이 약 933K 에서 2100K 까지의 온도 범위에서는 액체 Al 로 둘 러싸인 이산화티탄과 탄소의 고체입자들로 계를 이룰 것이다. 물질이동과 반옹에 대한 몇 가지 메커니즘들이 그 반응계가 아 온 도 범위에 있는 한 가능하다. i ) 입자들의 표면은 그들이 액상으로 짖게 되지 않고 확산 또는 반응도 일어나지 않도록 된다. ii) 탄소는 액상으로 확산되어 녹을 수 있고 이산화티탄의 입자 표 면까지 확산될 수 있다• 표 6.7 산화물로부터 TiC 합성에 대한 상 데이터. T(K) Ti0 2 C Al TiC Al203 298~933 s s s s s 933 s s s ..... 1 s s 933~2143 s s I s s 2143 s+->l s I s s 2143~2315 I s I s s 2315 I s I s s .... l 2315~2767 I s I s I 2767 I s 1-g s I 2767~3200 I s g s I 3200 분해 s g s I 3200~3253 Ti( g)/ 02(g) s g s I 3253 Ti( g)/ 02 (g) s g s 분해
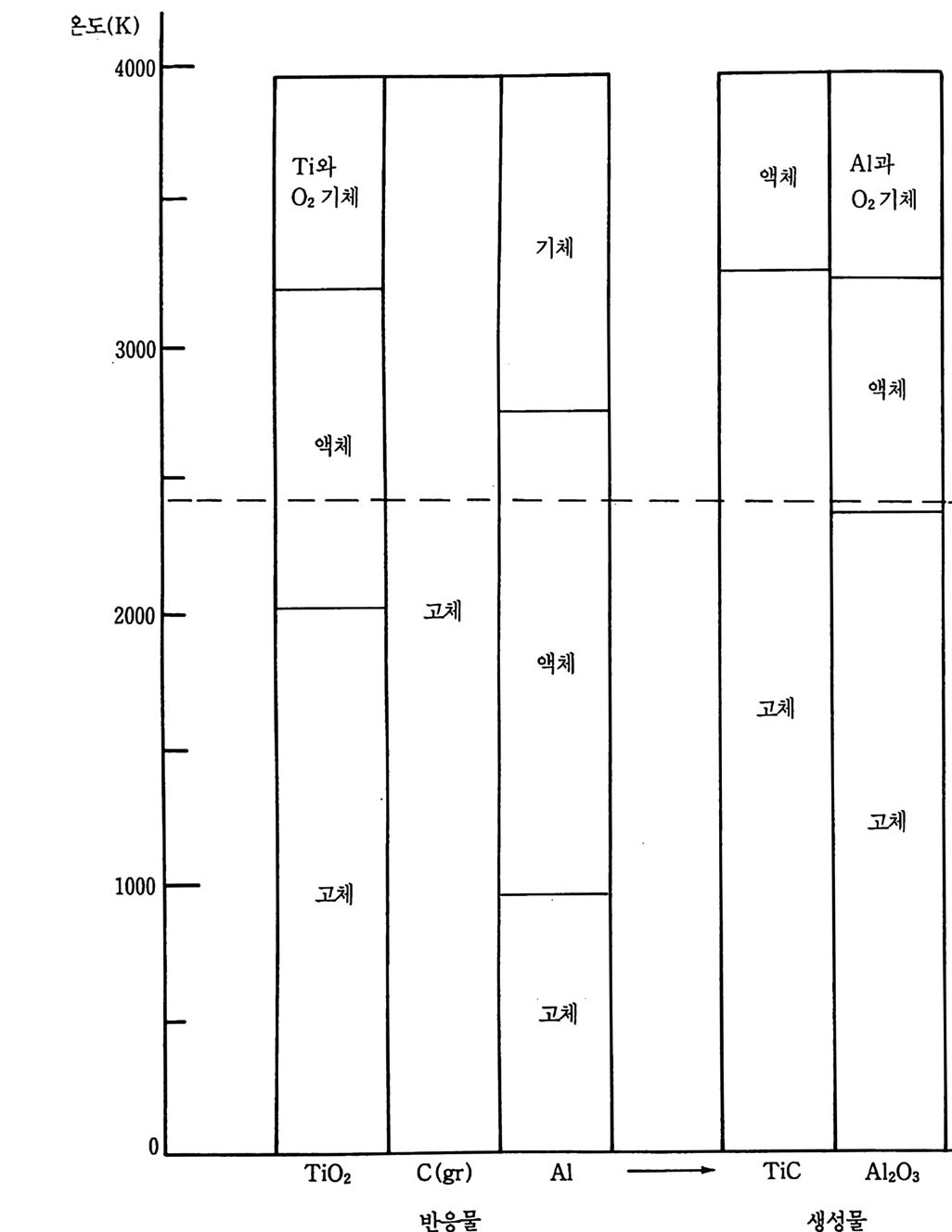 온도 (K)
온도 (K)
그림 6· l2 산화물로부터 TiC 합성반웅에 대한 상 데이터.
iii) 이산화티탄은 그 액상으로 확산해 들어가고 탄소입자 표면까지 확산된다. iv) 탄소와 이산화티탄은 그 액상으로 확산해 들어가고 상호확산할 수도 있다. 그들은 액상에서 하나 또는 두 입자 표면에서 반응 할 수도 있고 또는 전혀 반응하지 않을 수도 있다. 또한 그들 은 한 입자의 표면까지 확산하고, 거기에서 그 표면에 흡착되 고 확산되며 그리고 내부적으로 반응한다. v) 이산화티탄은 액체 Al 용매와 전기 화학반웅울 한다. 위의 마지막 메커니즘의 가능성은 이 반응에 대한 전기 화학 퍼텐 셜을 계산함으로써 평가할 수 있는 반면에 다른 메커니즘들의 가능성 은 그 정한 온도 범위에서 액체 Al 에 탄소와 T i 02 의 용해도를 계산 함으로써 조사할 수 있다. 6— 7 T iB 2 의 합성 (원소 반응) 아래 식에서 보는 바와같이 이 합성법은 T iB 2 를 생성하기 위하여 원소간의 반응을 나타낸다. Ti (s ) + 2B(s)-TiB i(s) 그 처음 반응물은 화학양론적 양의 티탄과 붕소분말들로 되어 있 다. 붕소에서는 결정형에 대하여만 데이터를 얻을 수 있으므로 결정 형 붕소로 가정한다. 6— 7— 1 열역학적 분석 온도의 함수로서 Gib b s 자유에너지 변화(/j_ G) 는 표 6.8 에 수록한
표 6 . 8 TiB 2 합성에 대한 자유에너지 값(원소반웅). 단열 반응온도 =3193K, T iB 2 상 =28% 액체 및 72% 고체 T(K) t::, H(cal/mol) !!. G(cal/ mo l) 300. 00 -66880. 00 -65060.00 400.00 -66870. 00 -64460.00 500.00 -66950.00 一 63850 . 00 600.00 一 67080.00 -63220. 00 700. 00 -67230.0 0 -62570.00 800. 00 -67390.00 -61890. 00 900.00 -67560.00 -61190. 00 1000. 00 -67850.00 -62920. 00 1100. 00 -68020.00 -62420. 00 1200.00 -69120.00 -61830. 00 1300.00 -69140.00 -61230. 00 1400.0 0 -69150.0 0 -60620.00 1500.00 -69150.00 -60010.00 1600. 00 -69150.00 -59400. 00 1700.00 —69 150.00 -58790.00 1800.00 -69220.00 -58160.00 1900.00 -69220.00 -57540. 00 22010000..0 000 --7733651800.. 00 00 -—556589 1700.. 00 00 2200.00 -73520.00 -55130. 00 2300. 00 —734 60. 00 -54300.00 2400.00 -73380.00 -53470. 00 2500.00 -84080.00 -52430. 00 2600. 00 -83970. 00 -51170.0 0 2700.00 -83850.0 0 -49910. 00 2800.00 -83720.00 -48660. 00 2900.00 -83580.00 -47410.00 3000. 00 -83440.00 -46160.00
3100.00 -83310.00 -44920.0 0 3200. 00 -58990.00 -45180.0 0 3300.00 -58700.00 -44760.00 3400. 00 -58410. 00 -44340.00 3500. 00 -58120.0 0 -43930.00 바와 같다. 이들 데이터는 열역학적으로 상온과 그 이상의 온도에서 정반응이 더 찰 일어남을 나타낸다. 가능한 데이터로부터 계산된 단열 반응온도 109) 는 3193K 이다. 이 값은 소련의 계 산값 95) 과 일치 한다. 이 단열 반응온도는 T i 02 의 녹는 온도와 같고 그 경 험 식 의 반응열은 960cal/ g이 다. 6-7— 2 반응 현상학 표 6.9 와 그립 6.13 에 표시된 바와 같이, 두 반응물은 298K 와 1 a t m 의 압력 에서 고체분말들이다. 그 반응물들은 1933K 부근까지 가 열될 때 그 티탄입자들은 녹기 시작한다. 완전히 녹을 때 티탄은 1950K 에서 반응 체적의 57%, 2450K 에서는 59% 로 될 것이다. 이 연구에 대한 자료는 주로 봉소에 대한 모순된 데이터 때문에 약 2450K 이상의 온도에서는 상당히 불확실하다. 모순된 값들은 결정형 붕소에 대하여 보고된 데이터가 알려져 왔고 오히려 더 필요한 무정 형 붕소에 대해서는 데이터가 알려지지 않았다. 미국 국립표준국 109) 은 붕소가 2450K 에서 녹고 3931K 에서 증발한다 고 보고하였다. 반면에 참고문헌 (107) 의 경우 붕소는 2573K 에서 녹 고 2823K108) 에서 증발한다고 제시하였다. 높은 온도에서 열용량이 제시되었기 때문에 참고문헌 (111) 으로부터 얻은 값들이 임의적으로 사용되 어왔다. 아마도 붕소는 2450K 와 2573K 사이 에서 녹을 것이다. 이 점에서 티탄과 붕소의 혼합도 또는 용해도가 결정되어야 한다.
표 6.9 원소반응으로 T iB 2 합성에 대한 상 데이터. T(K) Ti B TiB2 298~1155 Sa s s 1155~1940 Sa .... s, s s 1933 s,~l s s 1933~2450 I s s 2450 l s+-+1 s 2450~3193 I I s 3193 I I s ..... 1 3193~3591 I I I 3591 l. .... g I I 3591~3931 g I I 3931 g l .... g I 3931~4250 g g I 4250 g g 분해 이 용액과 평형을 이루고 있는 증기는 티탄, 붕소 및 그 계에 존재 하는 어떤 비활성 또는 다른 기체들로 되어 있을 것이다. T iB 2 는 기 체상태로는 찰 발견되지 않을 것이다. 만약 기체가 형성된다 할지라 도 그것은 고체침전으로 존재할 것이다. 그렇지만 만일 기체가 형성 된다면 그 용액은 T iB 2 의 용해도를 계산함으로써 이 가정을 시험해 불 수 있다. 즉 T iB 2 가 그 액체에 대단히 녹기 쉽다면 그것은 또한 기체상에도 있을 수 있다. 만약 약간의 변환이 그 액용체에서 생기지 않는다면 그 변환은 기 체상에서 일어날 수도 있다. 이것은 여러 압력에서 수율(yi eld) 을 분 석함으로써 시험해 볼 수 있다• 만약 그 반응이 기체상에서 일어난다 면 Le Cha t e li er-Braun 원리로 제시된 바와같이 압력이 높아질수록 변환을 증가시킬 것이다. 위에 보인 분석으로 T iB 2 를 생성하기 위하
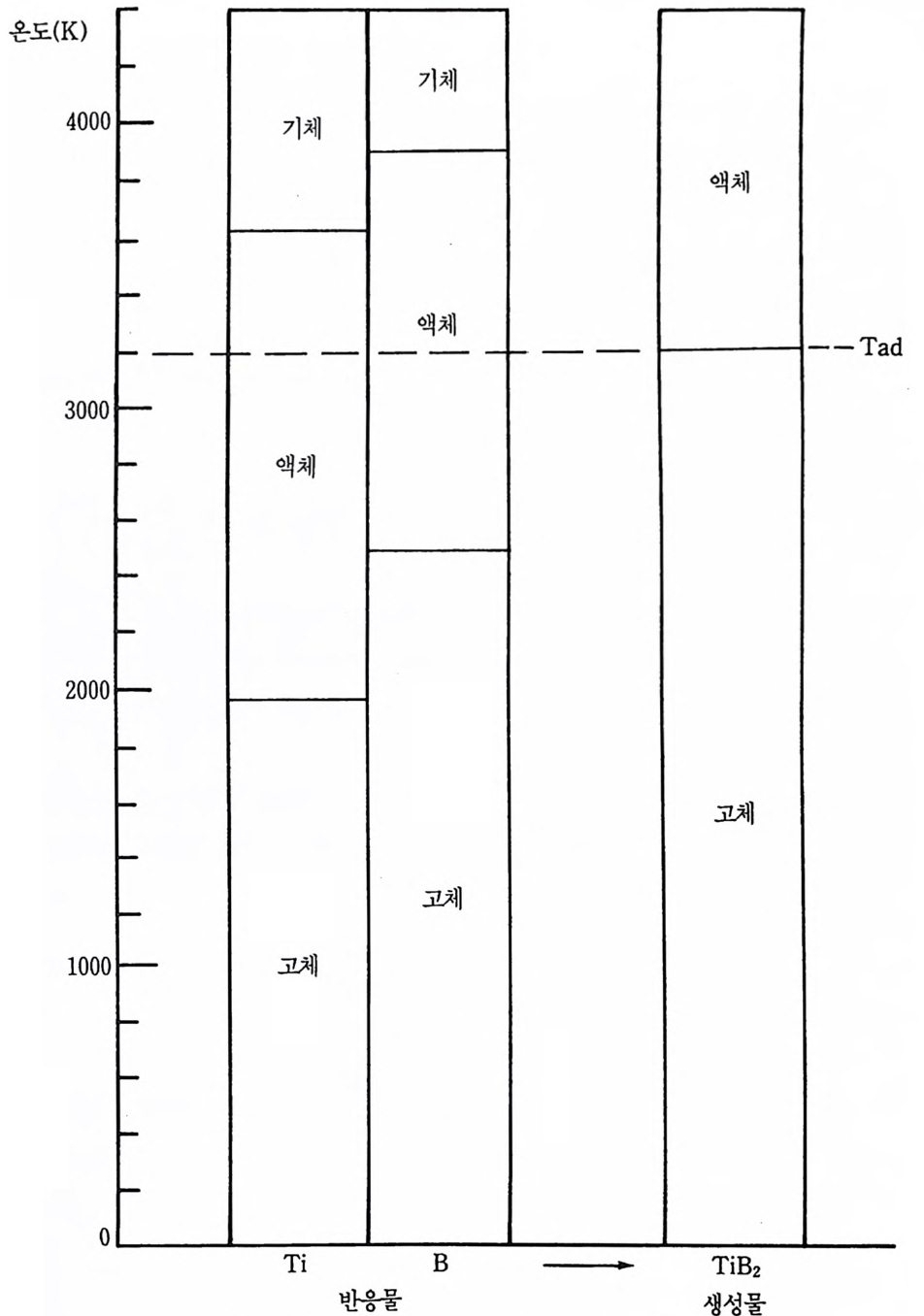 온도 (K)
온도 (K)
그립 6-13 TiB 2 합성반응에 대한 상 데이터 (원소반응)•
여 티탄과 붕소의 원소간 반응은 액체상태에서 일어나는 것 같으며 균일 반응 모델이 보장되는 것 갇다. 6— 8 T iB 2 합성 (산화물 반응) 이 반응은 다음 경 험식에서 보는 바와같이 T i 02 로부터 T iB 2 를 생 성하는 것을 나타낸다. 3Ti0 i( s)+ 6B(s)+4Al(s) ―一 3TiB 2 +2A12°3 앞의 원소간 반응에 의한 T iB 2 합성반응에서와 같이 붕소는 결정성 고체가 되도록 가정한다. 다루려는 온도 범위에서 무정형 붕소에 대 한 데이터가 알려지지 않아서 이 가정으로 생기는 불확정성은 알 수 가없다. 분석의 목적으로 처음 반응물은 화학양론적 양의 Ti0 2 결정분말과 결정성 붕소분말로 되었다고 가정한다. 이들 분말 또한 찰 혼합된 것 으로 가정한다. 6-8— 1 열 역학적 분석 온도함수로서 Gib b s 자유에너지 변화(/J. G) 는 표 6.10 에서 보는 바와 갇다. 이들 데이터는 상온으로부터 단열 반응온도까지는 정반웅 이 열역학적으로 바람직하다는 것을 나타낸다• 참고문헌 (107) 으로부 터 얻은 데이터를 사용하여 계산한 단열 반응온도는 2575K 이다 . 그 림 6.14 에서 보는 바와갇이 반응은 액체상태 Al2 야와 고체상태 TiB 2 로 일어난다. 그 단열 반웅온도에서 반응열은 785cal/ g이다.
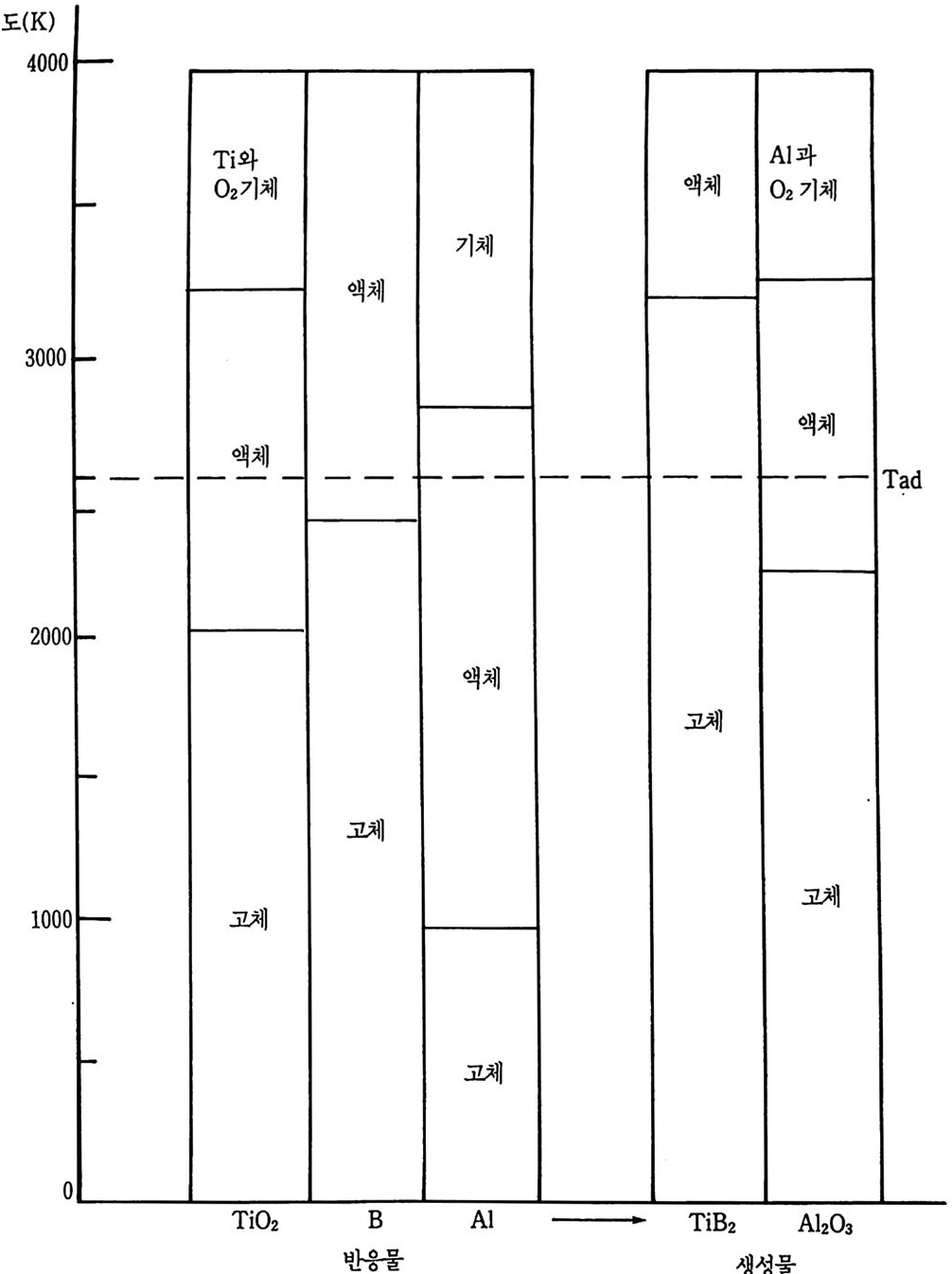 도 (K)
도 (K)
그림 6.l4 산화물로부터 T i B2 합성반웅에 대한 상 데이터.
표 6. 10 산화물로부터 T iB 2 합성에 대한 자유에너지 값 . 단열 반웅온도 =2527K, T iB 2 상 =100% 고체 , Ab03=100% 액체. T(K) 6. H (cal/ mo !) t, G(cal/mol) 543600000000....000 00000 —---333322224445 951900000000....0 0 000000 --——333310013620 6406 0 000 000 0....0 0000000 700. 00 -326600. 00 -298600.00 800. 00 -327400. 00 -294 60 0.00 900.00 -328100.0 0 -290400.00 1ll00000..0000 —-333399 270000.. 0000 一-2 28982390000..0000 1200.00 -340100.00 -283600. 00 1300.0 0 -340400. 00 -278900. 00 1400. 00 -340600. 00 -274100.00 1500.00 -340700. 00 -269400. 00 1600.00 一 339500.00 -265700. 00 1700.00 -339300. 00 一 261100 . 00 1800. 00 -339300. 00 -256400. 00 1900. 00 —339 100. 00 -251800. 00 2000. 00 -338900.00 -247200. 00 2100. 00 -338600. 00 -242700. 00 22230000..0000 -—338866 960000..0000 —-222396 100000..0 000 2400. 00 -331000. 00 -224100.00 22222679850000000000.....0000 000000 ----—333666663322397 050160000000000.....0 0 0 0 000000 -——-—21221181099273 8 075240000000000.....0000 000000 3000.0 0 -636000.00 -167100.00
3100. 00 -6 34400.00 -151500.00 3200. 00 -560300.00 -140300. 00 3300. 00 -176300.0 0 146600. 00 3400. 00 -175200.00 156300.0 0 3500. 00 -174200.00 166100 . 00 6 一 8 ― 2 반응 현상학 그림 6 . 14 와 표 6.11 에서 표시된 바와같이 298K 와 Iatm 압력하에 서 세 가지 반응물질은 모두 고체분말이다. 상온에서는 정반응이 열 역학적으로 바람칙하고 933K 에서 Al 은 녹는다. 약 933K~2143K 온 도범위에서 그 계는 액체 Al 로 둘러싸인 붕소와 Ti0 2 고체분말로 되 어 있다. 2143K 에서 T i아는 녹으므로 그 계는 약 2450K 온도까지 액체 Al 과 액체 T i 02 로 둘러싸인 붕소 고체분말로 되 어 있다. 2450K 이상 에서는 그 발견물들은 붕소의 불확실한 데이터 때문에 또한 불확실하 다. 붕소에 대 한 녹는 온도는 2400K 와 2753K 로 주어져 왔다. 3200K 이상의 높은 온도에서 T i 02 는 T i와 02 기체들로 분해될 것이다. B 는 액체상태로 될 것이고 Al 은 높은 온도에서 기체상으로 될 것이다. T iB 2 는 약 4250K 까지는 고체상으로 존재할 것이며 그 이하 온도 에서 기체상으로는 찰 보이지 않는다. 만약 기체상이 형성될지라도 T iB 2 는 한 고체 침전으로서 존재 할 것 이다. Al 은 933K 에서 녹지만 Al203 는 2318K 까지는 녹지 않는데 이는 Al2°3 껍질에 포함된 액체 Al 이 달아날 수 없게 된 것을 나타낸다. 그 껍질충에 있는 결함, 약 5mn 인 그 껍질의 얕은 깊이 및 온도상승시 열적 부피팽창에 의한 역 학적 힘 때문에 그 껍질은 쉽게 깨져서 작은 Al203 입자들로 된다. 녹을 때 Al 의 체적 팽창은 6.5% 이다. 이와같이 자유액체 Al 이 그 계안에 있게 될 것이 기대된다. 단열온도인 2527K 에서 T i B2 는
표 6.11 산화물로부터 T i B2 합성에 대한 상 데이터. T(K) Ti 0 2 B Al TiB 2 Al2°3 298~933 s s s s s 933 s s s ..... 1 s s 933~2143 s s I s s 2143 s ..... l s I s s 2143~2315 I s I s s 2315 I s I s s<-+l 2315~2450 I s I s I 2450 I s+-+l I s I 2450~2767 I I I s I 2767 I I 1-g s I 2767~3200 I I g s I 3200 해리 I g s I 3200~3253 I g s I 3253 I g s 해리 3253-3931 I g s 3931 l .... g g s 3931-4250 g g s 4250 g g 해리 100% 고체상으로 존재할 것이고 A12°3 는 100% 액체상으로 존재할 것이다. 3250K 이상의 고온에서는 Al2 아는 분해하고, 반면 T i B2 는 T i와 B 기체들로 분해하는 4250K 까지는 액체로 존재할 것이다.
제 7 장 분석 모델화 비기체 연소합성 반응의 모델화에 관한 SPC(Sy st e m Plannin g Corp o rati on ) 의 목표 4) 는 소련의 연구개 발과 현상학 연구의 결과에 관 한 앞의 기초 정보들을 통합하여 수적인 예측능력으로 처리하는 것이 다. 일반적인 모델들은 특수한 연소계의 작용을 설명하도록 만들 수 있다. 이러한 모델들은 다음과 같은 사항에 쓰려고 한 것이다. i ) 앞으로 실험할 반응계의 선택과 평가. ii) 반응 메커니즘과 반응속도론에 대한 이해. iii) 원하는 특성을 지닌 생성물을 얻기 위한 공정변수의 조절 . iv) 공정 확대를 위한 데이터와 상 관계의 결정 . 이상적인 모델은 반응물의 몰비, 희석도, 콤팩트의 형태, 주변 경 계 조건들과 같은 최소한의 입 력 (inp u t) 을 필요로 한다. 출력 (outp u t) 은 시간과 공간 좌표에 대한 함수로서의 온도, 연소파의 속력 및 반 응속도를 포함하여야 한다. 소련 모델(제 6 장, 부록 B 참조)은 농축상이나 액체금속-고체비금속 계와 같은 특수한 형태의 계에서 연소 작용을 예측하였다. 비록 이런 모델들이 제한된 범위의 정성적 작용을 예측하는 데는 유용하나 그들 출력은 종종 정량적인 결과와 잘 관련되어 있지 않은 경우도 있다. 소련 학자들에 의하여 제시된 이돌 가정과 제한은 더욱 실제적으로 확장되어야 한다. 예를 들면 열손실, 상변화 및 비-아레니우스
(non-Arrhen ius ) 열발생 항들이 포함되 어 야 할 것 이 다. 모델화에 대한 SPC 방법은 다음과 같은 두 경로를 따른다. i ) 소련 모델(부록 B) 의 연구와 재생. ii) 부가적이고 더욱 실제적인 제한성을 포함하도록 그들 초기 아 이디어의 확장. 이런 목표를 위하여 SPC 는 포트란 77 로 프로그램된 세 개의 분리 된 소프트웨 어 (THERMLIST, COMBUST 및 THERM) 패 키 지 를 개 발 하였는데 이 장에서는 이들에 대하여 설명하고자 한다. 7-1 THERMLlST 어떤 반웅계의 이상적인 열역학적 작용의 총체적 의미는 영차원적 열과 에너지 균형을 통하여 실현될 수 있다. THERMLIST4) 는 어떤 반응계에 대해서도 그와 갇은 균형을 수행한다. 제 6 장에서 설명한 바 와같이 비열은 표준 화학종에 대한 온도의 함수로서 모델화되었다. 그 결과식은 엔탈피와 엔트로피식들을 얻기 위해 경계조건인 잠열과 엔트로피 데이터로 적분되어전다. 이 모델에 대한 입력은 어떤 주어전 초기 온도에서 균형을 이룬 반 응물과 생성물의 몰량 (molar qu anti ty), 최고 온도 및 온도 구간이고 출력은 부록 D 의 표와 갇다. 여러 가지 반응물과 생성물에 대하여 불연속적인 온도에서 엔탈피, 엔트로피 및 Gib b s 자유에너지와 같은 열역학적 함수들이 수록되어 있다. 단열 반응온도가 계산되었고 그 온도에서 존재하는 생성물의 상도 수록되었다. THERMLIST 는 18 개 의 서브루틴 (subrou ti ne) 으로 되 어 있는 고도로 모듈화된 프로그램 (high ly modular pro g ram ) 이 다. 이 것은 Al, AlN, Ali 03, B, B2 야, C, N2, Ti, TiB 2 , TiC 및 T i 02 의 화학종들을 포함하 는 어떤 조합의 반응에서도 반응 데이터를 얻는 데 널리 사용될 수
있다. 위에 열거한 시료 이의에 추가 화학종에 대하여는 서브루틴 하 나와 프로그램 두 줄, 그리고 두 개의 입력 파일에 각 한 줄씩을 덧 붙여 쉽게 사용할 수 있다. 덧붙여진 서브루틴은 다른 11 개 화학종의 서브루틴과 매우 비슷한 포맷(fo rma t)을 가지며 부록 D 의 그림에서 보는 바와 같은 형태의 온도의존 엔탈피와 엔트로피 데이터 곡선 적 합도 (data curve fits) 를 포함할 수 있다. 7-2 COMBUST 현재까지 가장 빈도 높게 인용된 소련 모델은 부록 B 에서 설명한 일차원적인 전이 모델(t rans i en t model) 인 것 같다 . 이 모델로부터 정 류상태 연소(안정 연소)방식에서 불안정 연소방식으로의 전이에 대한 기준이 설정된다. 부록 B 에서 개요로 설명한 소련의 식들은 COMBUST4) 에서 재생된다. 그 모델은 적은 시간과 공간 단계들이 쓰여질 때 가장 유용하므로 분명하고도 반복적인 해석식이 선택되었다. 아레니우스 열생성항 (Arrheni us heat gen erati on t erm) 을 갖는 일차원적 전이 열확산식은 아래에서 보는 바와 같다. Cp ( T1m+:: T:m) = X( 福+~ + Qp • ¢( T, n) ¢( T, n) = k 。 e-E/RT':'(1-n ? 여기서 cp 는 정압열용량, T 는 온도, l::,,t는 시간변위, Ax 는 공간변 위, Qp는 열량, X는 열확산계수, ko 는 지수 앞자리 인자이며 첨자 m 은 현재 시간단계, i는 현재 공간단계를 나타낸다. 이 일차원적 모델에서는 한 경계 (onebounda ry)가 그 원통의 각 끝
부분에 존재하고 단열 경계조건들도 이들 각각의 끝부분마다 부과한 다. 균일한 초기 온도가 규정되고 첫번째 마디가 계속적 그리고 순간 적으로 접화온도로 상승한다. 이 모델은 점화 반응속도론을 무시하고 는 사용할 수 없으므로 점화온도를 입력한다. 이것은 계산상 인위적 으로 부과하는 것이다. 반응완결도 n 은 초기 온도에서 n=O, 단열온 도에서 n=l 을 갖는 현재, 초기 및 단열온도의 선형함수가 되도록 제한한다. 이 모델의 입력은 콤팩트 길이, 공간마디의 수, 총 연소시간, 시간 단계의 수, 점화온도, 단열온도, 몰당 열발생 및 평균 물성들이다. 이런 데이터로부터 각 마디의 온도와 반응완결도 (n) 는 표 7.1 에서 보는 바와같이 각 시간단계에서 출력이 된다. 표 7 . l SPC COMBUST 모델로부터의 부분적 데 이터 출력. COMPACT LENGTH (CM) ■ 5.0 00 NUMBER OF NODES ■ 5 COMBUSTION TIME (SEC) ■ 10.0 00 NUMBER OF TIME STEPS ■ 25 INITIAL TEMPERATURE (K) ■ 300.000 IGNITION TEMPERATURE (K) ■ 1000.000 COMBUSTION TEMPERATURE (K) • 2100.000 THERMAL CONDUCTIVITY (W/M f 2-K ) ■ 15.0 00 SPECIFIC HEAT (J/K G-K) ■ 300.000 DENSITY (KG/M t 3) ■ 2000.000 HEAT GENERATION (W/M t 3) ■ .900E+06 REACTION ORDER ■ 2 ACTIVATION ENERGY (N-M) ■ .200E-03 IDEAL GAS CONSTANT (N-M/K) ■ 2.000 ALPHA (M t 2/3) ■ .25 0 E-04 TIME 1 .00 SEC 12 T ■ 1000.0 0 NU ■ .00 T ■ 300.0 0 NU ■ .00
3 T ■ 300.0 0 NU ■ .00 4 T ■ 300.0 0 NU ■ .00 5 T ■ 300.0 0 NU ■ .00 TIMEl .40 SEC T ■ 2130.00 NU ■ .40 2 T ■ 370.0 0 NU ■ .00 3 T ■ 300.00 NU ■ .00 4 T ■ 300.0 0 NU ■ .00 5 T ■ 300.0 0 NU • .00 TIME1 .80 SEC 1 T ■ 2386.00 NU ■ .54 2 T ■ 539.0 0 NU ■ .00 3 T ■ 307.0 0 NU ■ .00 4 T ■ 300.0 0 NU ■ .00 5 T ■ 300.00 NU ■ .00 INTERMEDIATE DATA ARE NOT SHOWN TIME1 9.2 0 SEC T ■ 2178.5 7 NU ■ .91 2 T ■ 2054.3 9 NU ■ .89 3 T ■ 1778.8 3 NU ■ .83 4 T ■ 1474.4 5 NU ■ .54 5 T ■ 637.4 5 NU ■ .00 TIME1 9.6 0 SEC 1 T ■ 2175.5 8 NU ■ .91 2 T ■ 2053.4 3 NU ■ .90 3 T ■ 1811 .50 NU ■ .84 4 T ■ 1670.7 1 NU ■ .63 5 T ■ 721 .15 NU ■ .00 TIMEl 10.00 SEC 1 T ■ 2172.1 3 NU ■ .92 2 T ■ 2054.4 3 NU ■ .90 3 T ■ 1852.4 3 NU ■ .85 4 T ■ 1756.63 NU ■ .68 5 T ■ 816.1 0 NU ■ .00
7— 3 T HERM COMBUST 를 2 차원으로 확장하거나 또는 반응하는 계와 주위의 상호작용을 연구하는 것은 유용하므로 SPC 는 THERM4 } 이라 불리는 이차원적인 전이 열확산 모델을 개발하였다. 이 모델은 온도, 열, 대 류 및 모서리 마디를 따른 복사의 어떤 임의적 결합을 나타내는 임의 로 형태화한 대상에 대한 마디온도들을 도표로 나타낼 수 있게 한다. 표 7-2 SPC 모델 THERM 에 대한 출력 포맷 DENSITY (KG/M i 3) ■ 8933.000 SPECIFIC HEAT (J/ K G-C ) ■ 385.000 THERMAL DIFFUSMTY (M/S i 2) ■ .117E-03 TIME (SEC) ■ 5000.0 0 0 NUMBER OF TIME STEP ■ 10 SIZE OF TIME STEPS ■ 500.000 NODE SIZE (MM) ■ 100.000 OVERALL X DIMENSION (M) ■ 1.00 0 OVERALL Y DIMENSION (M) ■ 1.00 0 MAXIMUM TEMPERATURE ERROR ■ .010 TOTAL HEAT CHANGE (J) ■ .24 E+08 310.5 0 310.74 310.8 3 311 .11 311 .15 311 .25 311 .68 311.62 311.5 7 311.6 1 312.57 312.2 9 312.04 311.8 7 311.81 313.9 1 313.1 9 312.6 4 312.24 311 .96 311.7 9 315.0 2 314.09 313.3 3 312.72 312.2 3 311 .84 311 .57 316.0 4 315.0 1 314.1 0 313.3 2 312.6 2 312.0 0 311.5 1 311.1 8 317.1 0 316.0 2 315.00 314.0 7 313.1 6 312.2 4 311 .54 311 .05 310.72 318.2 2 317.1 0 316.0 3 314.9 9 313.86 312.4 9 311 .59 310.9 9 310.6 0 310.35
BOUNDARY T SUM .00 0 .00 0 .000 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .000 .00 0 .000 .000 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .000 .00 0 .000 .00 0 .00 0 .00 0 .000 .00 0 .000 .000 .00 0 .000 .000 .000 .000 .000 .000 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .000 .00 0 .000 .00 0 .000 .000 .00 0 .00 0 .00 0 .000 .00 0 .000 .00 0 .00 0 .00 0 .000 .000 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .00 0 BOUNDARY Q SUM .00 0 .00 0 .000 .00 0 .00 0 .000 .000 .00 0 .000 .00 0 .00 0 .000 .00 0 .00 0 .000 .000 .000 .00 0 .00 0 .00 0 .000 .00 0 .000 .00 0 .000 .000 .00 0 . 000 .00 0 .00 0 • .00 0 .00 0 .000 .00 0 .00 0 .000 .00 0 .000 .000 .00 0 .00 0 .000 .00 0 .00 0 .000 .000 .00 0 .00 0 .000 .000 5000.0 0 0 .000 .000 .000 .00 0 .00 0 .000 .000 .00 0 .000 5000.0 0 0 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .000 5000.0 00 .00 0 .00 0 .000 .000 .000 .00 0 .00 0 .00 0 .000 5000.000 .000 .000 .000 .00 0 .00 0 .000 .00 0 .00 0 .000 10000.0 0 0 5000.0 00 5000.000 5000.0 00 5000.000 .000 .000 .000 .000 .000 BOUNDARY Q SUM 6.1 2 4 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .00 0 .000 6.1 2 4 .00 0 .000 .00 0 .000 .00 0 .000 .00 0 .000 .000 6.1 2 4 .00 0 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .000 .00 0 6.1 2 4 .00 0 .00 0 .00 0 .000 .00 0 .00 0 .00 0 .000 .000 6.1 2 4 .000 .000 .000 .000 .000 .000 .00 0 .000 .00 0 .00 0 .000 .000 .000 .00 0 .00 0 .000 .00 0 .000 .000 .00 0 .00 0 .00 0 .00 0 .00 0 .000 .00 0 .000 .000 .000 .000 .00 0 .00 0 .00 0 .000 .000 .00 0 .00 0 .00 0 .00 0 .00 0 .00 0 .000 .000 .00 0 .00 0 .000 .00 0 .00 0 .000 .00 0 .00 0 .000 .00 0 .000 15.0 0 0 15.000 15.0 0 0 15.0 0 0 15.000
또한 이것은 판상형 물질(l am i na t ed ma t er i als) 을 모델화하는 것도 가 능하다. Crank-Ni co lson 반복해 석 식 (iter ate soluti on scheme) 이 사용되 었는데 이 모델에 대한 입력은 마디구조를 포함하는 파일 , 초기 온도 , 전체 시간, 시간단계의 수, 마디의 크기, 최대 허용 온도 오차, 물성 및 경계조건 등이다. 최종 시간에서 온도 분포, 임의로 선택된 경계조건 및 다른 입력 데이터는 표 7.2 에서 보는 바와같이 출력 (ou tp u t)으로 나타난다. 그 입력 파라미터와 전체 에너지 변화는 그 표에 첫번째로 수록되 어 있고, 마디온도 일람표와 경계조건들이 그 뒤에 이어서 기록되었 다. 이 경우 확산질량에 대하여 선택된 형태는 가로의 lm 밑변, lm 세로변 및 lm 깊이를 갖는 45° 의 쐐기 모양이다. 부가해서 단열 경 계조건은 직각삼각형의 빗변에 임의로 부과한다. 그 밀변의 오른쪽 반은 15W/M2-K 의 필름 계 수 (film coeff ici e n t) 를 갖는 300K 의 유체 로 서 임의로 냉각되는 반면 그 왼쪽 반은 5000W/M 떡 열유입 (hea t infl ux) 을 받는다. 두 가지 임의의 열 파라미터는 역시 세로변에 부과 된다. 위쪽 반은 300K 의 큰 흑체에 복사하며 아래쪽 반은 5000W/M 떡 열유입을 받는다. 이 쐐 기 모양내 에 서 마디 온도 (nodal tem p e ratu res ) 는 표 7 . 2 의 두번 째 절에서 보듯이 약 310~318K 에서 변한다. 온도 (T SUM), 열입력 (Q SUM) 및 필름입자(H SUM) 들에 대하여 경계조건들은 그 표의 셋 째, 넷째 및 다섯째 절에 각각 순서대로 인쇄되어 있다. 이 경우 온 도 경계조건은 부과되지 않았고 열입력 (heat i n p u t)은 위에서 설명한 것처럼 기록되었다. 복사 경계조건은 W/M2-K 단위인 필름 인자로써 선형화 및 기록되었다.
7-4 모델화의 제언 앞에서 설명한 모델 중 가장 홍미있는 것은 COMBUST 모델이다. 정량적 합성반응의 결과를 정확히 예측할 수 있는 어떤 모델이 있다 면 이는 연구비를 줄일 수 있을 뿐만 아니라 미래의 실험에 대한 기 초를 제공할 것이다. 현재 사용하는 COMBUST 모델에서 쉽게 알 수 있는 네 가지 결 점은 다음과 같다. i ) 단열반응이며 일차원적 반응이라고 가정한 것. ii ) 물성들이 일정하다고 가정한 것. iii) 상 변화가 없다고 가정한 것. iv) 아레니우스형의 열생성이라고 가정한 것. 이상의 가정에서 iii)과 i v) 의 가정들은 대부분의 비기체 연소합성 에 대하여 분명히 쓸모가 없음을 제 6 장의 논의에서 보인 바 있다. 반 응물이 생성물로 바뀌는 간단한 사실과 반응에서 대단히 큰 온도증가 가 있다는 것은 ii)의 가정도 매우 의심스럽게 한다는 것을 나타낸 다. 반응과 포위된 온도 사이의 큰 온도구배를 고려할 때 i )의 가정 도 역시 모호한 것 같다. 상 변화를 설명하는 더욱 실제적인 비-아레니우스 열발생 루틴 (rou ti ne) 은 COMBUST 와 THERMLIST 모델들의 부분들을 결합하여 짜넣을 수 있다 . 그 열확산식의 Qp • ¢(T, n) 항을 계의 엔탈피 변화 로부터 계산되는 더욱 실제적인 열발생항으로 대치하는 데 필요한 기 본적인 서브루틴들을 THERMLIST 는 포함하고 있다. 또한 반웅의 완결도가 엔탈피 변화의 칙접적인 함수이기 때문에 반웅차수에 대한 n 값은 알 필요가 없고 반웅완결과 열방출의 관계는 가정할 필요가 없다. 전체적인 물성의 변화는 반웅경로에 따른 반웅완결도와 온도 분포 의 함수이다. 반웅완결도는 계산할 수 있고 온도의존성 물성편차는
불연속적으로 곡선 적 합도 (curve fit) 를 그릴 수 있고 또 삽입 할 수 있다. 이것은 THERMLIST 에서 계산을 위하여 비열을 모델화하는 방법과유사하다. 주변으로 열이 손실되는 것을 설명하기 위하여 COMBUST 모델을 2 차원으로 확장시킬 수 있거나, 또는 열손실항을 일차원적 방식에 포 함시킬 수 있다. 2 차원적 모델이 더욱 신축성이 있으므로 아마도 이 것이 더 좋은 선택 (be tt ero pti on) 일 것이다. 임의적으로 형태화한 기 하학적으로 2 차원인 반응 모델을 설정하기 위하여 THERM 과 같은 모델은 COMBUST 로 통합될 수 있다. 연구 필수품들이 더욱 명료하게 정의될 때 그 밖의 다른 모델들이 고안될 수 있다. 예를 들면 금속에 세라믹스를 결합시키는 반응의 열 적 특성을 조사한 모델이 실행 가능한 것 같다. 그렇지만 이런 비법 적인 응용의 모델 개발은 간단한 반응 모델들의 정확성이 입증될 때 까지는 보류되어야 한다.
제 8 장 고압 자체 연소소결 (HPCS) 법 고밀도 세라믹스 제조를 위하여 새로운 간단하고 효과적인 소결공 법의 기술개발이 절실히 요구되어 온 것은 사실이다. 일반적으로 세 라믹스 제법은 먼저 분말울 합성하고 그 후 소결과정을 통하여 고밀 도화호性근 것이 종래의 방법이다. 이 복잡한 처리는 경우에 따라서는 오랜 기간이 걸릴 뿐만 아니라 고온에서 장시간 열처리하는 데 많은 에너지롤 소모하게 된다. 이와 같은 불편을 해결할 목적으로 일본 Osaka 대 학의 Y. Mi yam oto 교수와 M. Koiz u mi 교수 17),30) 는 고압 자체 연소소결 (High -Pressure Self -C ombusti on Sin t e r in g 또는 HPCS) 법 이란 새로운 공정을 기술개발하였다. 이제 이 HPCS 법에 수반되는 기술, 이론 및 고밀도 세라믹스 제조에 대한 응용 등에 대하여 이 장 에서 설명하고자 한다. 8— 1 H PCS 공정 HPCS 법은 그립 8 .1 에서 보는 바와같이 SHS 와 고압기술 (Ho t Press 또는 HIP) 을 결합시켜 새로 개발한 공법 30) 이다. 종래의 방법과 는 달리 이 HPCS 법은 짧은 시간 (2,3 초)에 반응 조성원소로부터 세
라믹스의 합성반응과 소결과정이 동시에 이루어져 고밀도의 고성능 세라믹스 콤팩트롤 얻을 수 있는 새로운 공법이다.
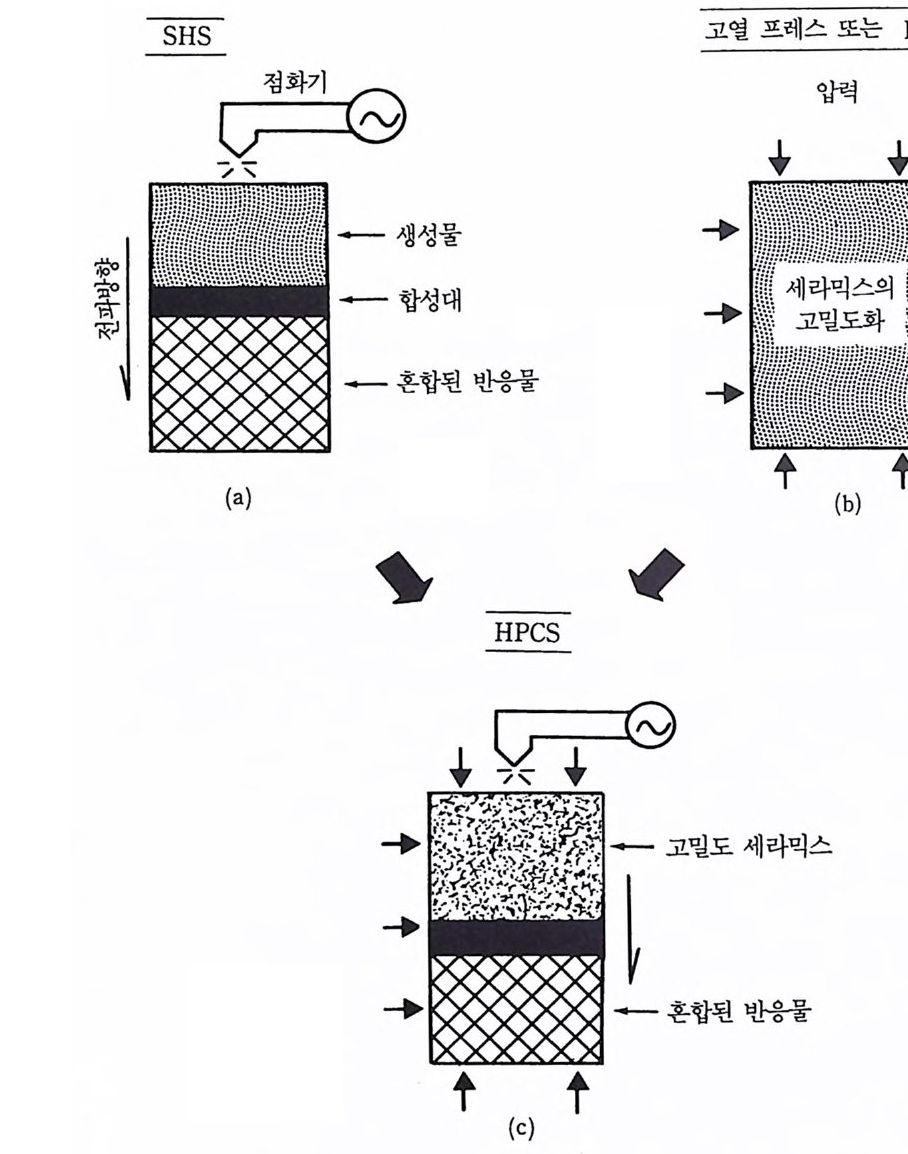 SHS 고열 프레스 또는 HIP
SHS 고열 프레스 또는 HIP
그립 s.1 SHS 와 고압기술을 결합하여 HPCS 법을 만드는 개요도.
HPCS 법 에서 고압기술은 고열 프레스 (Ho t Press) 나 고열 등방압 프레 스 (Hot Isosta t ic Press 또는 HIP) 를 쓰지 않고 입 방모루 (cubic anvil ) 66 률 사용하였다. 이 때 사용한 압력 셀 장치 (cell assembly) 19) 는 그림 8 . 2 에서 보는 바와 같다. HPCS 법에 사용한 고압 셀은 A 형과 B 형 이 있다. A 형 셀에 사용한 시료 펠릿의 지름 6mm 길이 9mm 이 며, B 형 셀의 경우는 지름 6mm 와 길이 6mm 이었다. A 형 셀에서는 흑연봉을 펠릿 반응물의 상부에 끼워 넣고 그것으로 전기 가열시켜 점화하는 데 사용한다. BN 두관 (sleeve) 과 BN 토막 은 파이로필라이트 셀(pyr op h yllit e cell) 로부터 오염을 방지하기 위하 여 끼워 넣는다. B 형 셀에서는 점화 전에 반응물 펠릿을 예열하기 위하여 탄소 두관을 끼워 넣는데 이것이 광범위한 점화면적을 갖는 점화기 역할을 한다. 반응물 펠릿은 탄소 두관에 직접 접촉되도록 중 심부에 끼워 넣는다. 파이로필라이트에 뚫린 구멍의 위와 아래 부분 은 몰리브덴 디스크 (Mo d i sk) 로 꼭맞게 닫는다. B 형 셀에서는 Mo 디스크가 전원과 탄소 무관을 연결하는 도선 역할도 한다.
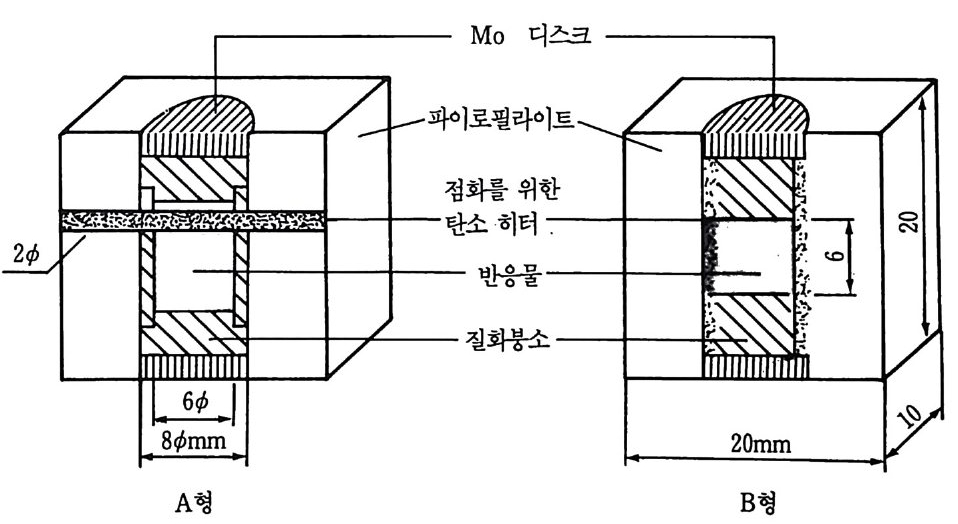 Mo 디스크
Mo 디스크
그립 8-2 HPCS 법에 사용한 셀 장치의 단면도.
반응물 펠릿 포함하는 셀을 입방모루 안에 넣고 서서히 증가하는 압력으로 3GPa 까지 가압한다. 가압된 시료에 연결된 점화 조절회로 를 통하여 A 형 셀에서는 탄소봉에 약 2.0 kVA(5V 와 400A) 및 B 형 셀에서는 탄소부관에 약 4.5 kVA(6.42V 와 700A) 의 전력을 각각 2 , 3 초 초 홀려서 점화시킨다. 탄소 히터의 온도는 순간적으로 거의 2300K 에 달할 것이며 이는 효과적으로 점화시키는 데 충분한 에너지를 공 급할 것이다. 또한 SHS 에 의한 많은 발열반웅열은 계의 온도를 더 욱 상승시키므로 의부의 부가적인 가열 없이 초고온 초고압하에서 생 성반응과 소결과정이 동시에 일어난다. 연소 처리가 끝난 후에 서서히 감소하는 압력으로 대기압까지 내린 후 생성된 고성능 세라믹스 콤팩트롤 얻는다. 이와같이 얻어전 최종 시료의 구조분석, 물리적 성질, 화학적 성질, 역학적 성질, 전기적 성질 등 모든 특성 규명이 뒤따라야 한다. 이러한 특성 규명에 대하 여는 제 IO 장에서 설명할 것이다. 한편 종래 소결법에 의한 고밀도 세라믹스 콤팩트 제조와 HPCS 법 을 비교 30) 하면 다음과 갇다. i ) 종래 소결법 : A+B 분말 혼합一성형一가열一분쇄一소결보조 제 첨가一첨가한 소결보조제 혼합一성형一소결一소결체. ii) HPCS 법 : A+B 분말 혼합一성형 -HPCS( 점화)공정一소결체. 위 두 공정에서 보는 바와같이 종래 소결법의 약 6 단계를 HPCS 공정 한 단계로 단순화할 수 있다. 이 공정의 비교는 그림 8.3 에서 보는 바와 같다. 이와같이 HPCS 공정을 사용하면 다음과 같은 장점 이 있다. i ) 공정의 단순화에 따른 생산설비 및 생산비 두자를 절감할 수 있다 . ii) SHS 에 의한 발열반응열을 직접 소결에 사용하므로 의부적인 고온소결로에 의한 가열이 필요없고 에너지도 철감된다. iii) 초고압과 초고온에서 아주 짧은 시간에 합성반응과 소결과정이 동시에 일어나므로 몇 시간 또는 며칠간 장기간 소결하는 불편
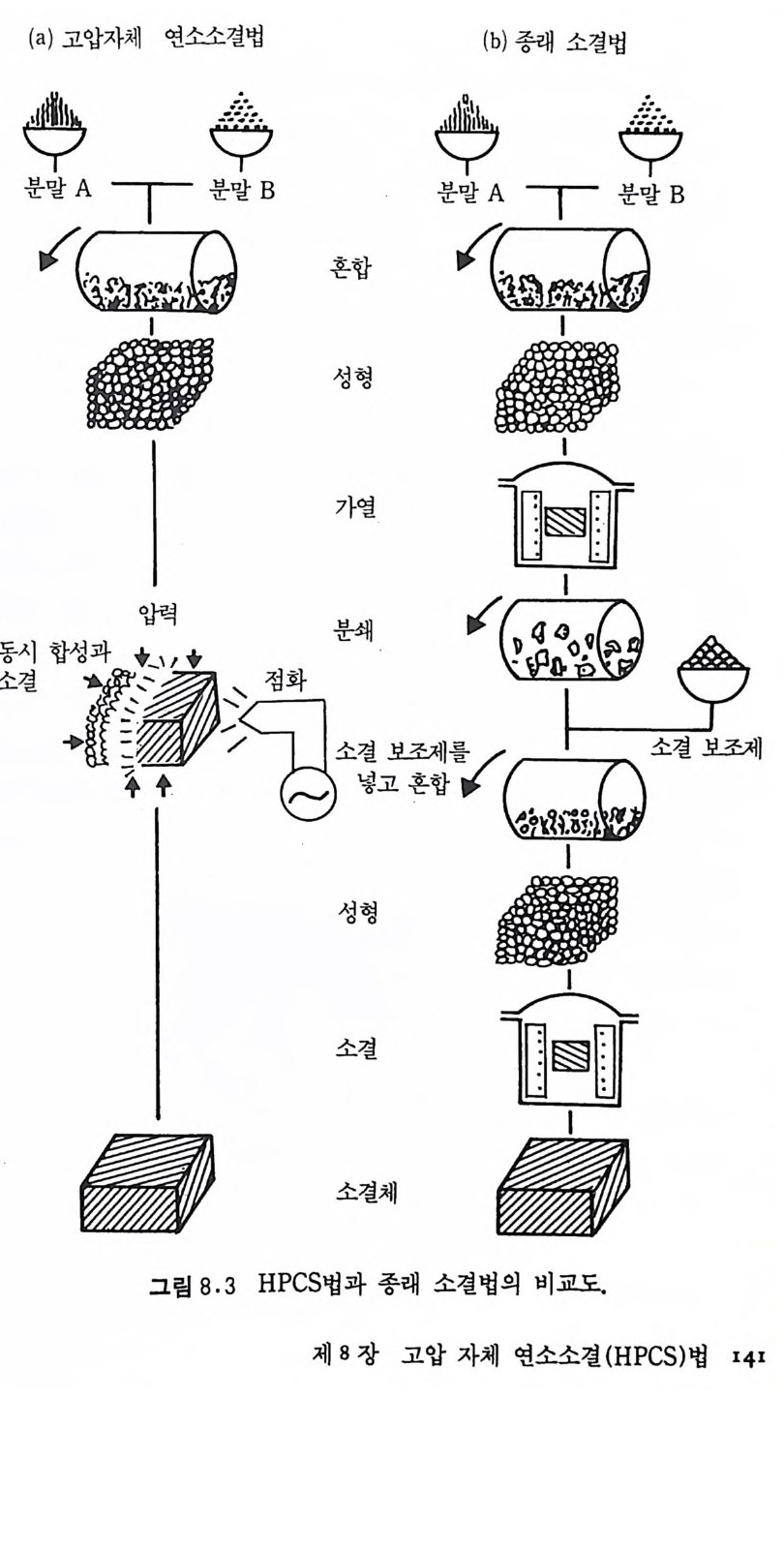 (a) 고압자체 연소소결법 (b) 종래 소결법
(a) 고압자체 연소소결법 (b) 종래 소결법
이 없다. iv) 종래 소결방법으로 소결제 없이 불가능한 공정을 가능한 공정 으로 하거나 더욱 고성능 세라믹스를 얻을 수 있다. v ) SHS 반응과 소결과정에서 적어도 한 원소 이상이 녹은 상태 이면 띠녹임 (zone mel ti n g)의 정제효과로 출발물질보다 고순도 생성물을 얻을 수 있다. 이상 설명한 것 이의에도 HPCS 의 공정을 특수한 세라믹스 제조에 맞도록 수정, 변형시키면 많은 장점이 있울 것으로 기대된다. 8— 2 HPCS 법에 의한 단순 세라믹스의 제조 8— 2— 1 TiB 2 콤팩트의 제조 (1) T iB려 HPCS 처 리 미세한 Ti 분말(입자 크기 <40 µm)과 무정형 B 의 몰비를 1 : 2 로 평 량하여 n- 핵산을 가하여 잘 섞고 진공, 건조시 킨다. 형틀 (mould)
 ?/
?/
그림 8,4 HPCS 실험 후 A 형 고압 셀의 단면도(가로선 =10mm).
에 넣어 압축 (hand p ress i n g)하여 지름 6mm, 길이 약 9mm 의 반응물 펠 릿 (reacta n t pel let) 혹은 예 형 펠 릿 (pre fo rm pel let) 을 만든다. 700°C 대기압하에서 약 2 시간 가열한 바 있는 파이로필라이트 셀(pyr op hy l lite cell) A 형에 HPCS 공정에서 설명한 바와같이 시료를 넣는다. HPCS 실험 후 셀 중심부에 고밀도의 화학양론적 TiB 2 콤팩트를 생 성하는데 그 셀의 단면도 17) 는 그립 8 .4에서 보는 바와 갇다. 3GPa 하에 서 2200K 로 TiB 2 분말을 한 시 간 동안 소결시 켰을 때 생기는 TiB 2 콤팩트의 밀도와 갇은 약 95% 의 상대밀도를 갖는 TiB 2 콤팩트 생성물을 얻었다. (2) Ti B2 콤팩 트의 특성 이와같이 생성된 Ti B2 콤팩트의 X 국] 회절분석은 육방정계의 상 만울 보여서 Ti 분말의 입자 크기에 무관하고 처음 반응물이 모두 화학양론적 화합물로 변했음을 알 수 있다. X- 선 마이크로 분석으로 아주 적은 양의 T i N 을 검출할 수 있었는데 이는 BN 두관이나 셀 안에 있는 공기 중 질소와 티탄이 결합하여 생성된 것 같다. T iB 2 의 이론밀도에 대한 상대밀도는 93~96% 였고 출발물질인 Ti 분말의 입 자 크기에 따라 거의 변하지 않는다. SEM 마이크로 그래프에 의한 Ti B2 콤팩트의 파열 및 연마된 표 면들의 전형적인 마이크로 구조는 그립 8.5 에서 보는 바와 같다. 약 5µm 의 균일한 낱알 크기 (grai n s i ze) 의 미세한 입자들이 굳게 자체 결합 (se lf -bonded) 되어 있다. 그립에서 보는 바와같이 소결체인 TiB 2 콤팩트의 낱알 크기는 Ti 분말의 입자 크기보다 작아졌음을 알 수 있다. 그 낱알 크기는 출발물질인 T i의 입자 크기에 그렇게 민감 하지 않은 것도 알 수 있다. 그 TiB 2 콤팩트의 마이크로 경도(mi crohardness) 는 상온에서 26 GPa 인데 이것은 3GPa 하에서 2200K 로 한 시간 동안 TiB 2 분말을 HPHP 로 제조한 소결체의 마이크로 경도값 18GPa 보다 더욱 큰 값 이다. 그림 8.6 에서 보는 바와같이 온도가 상승하면 마이크로 경도는 감
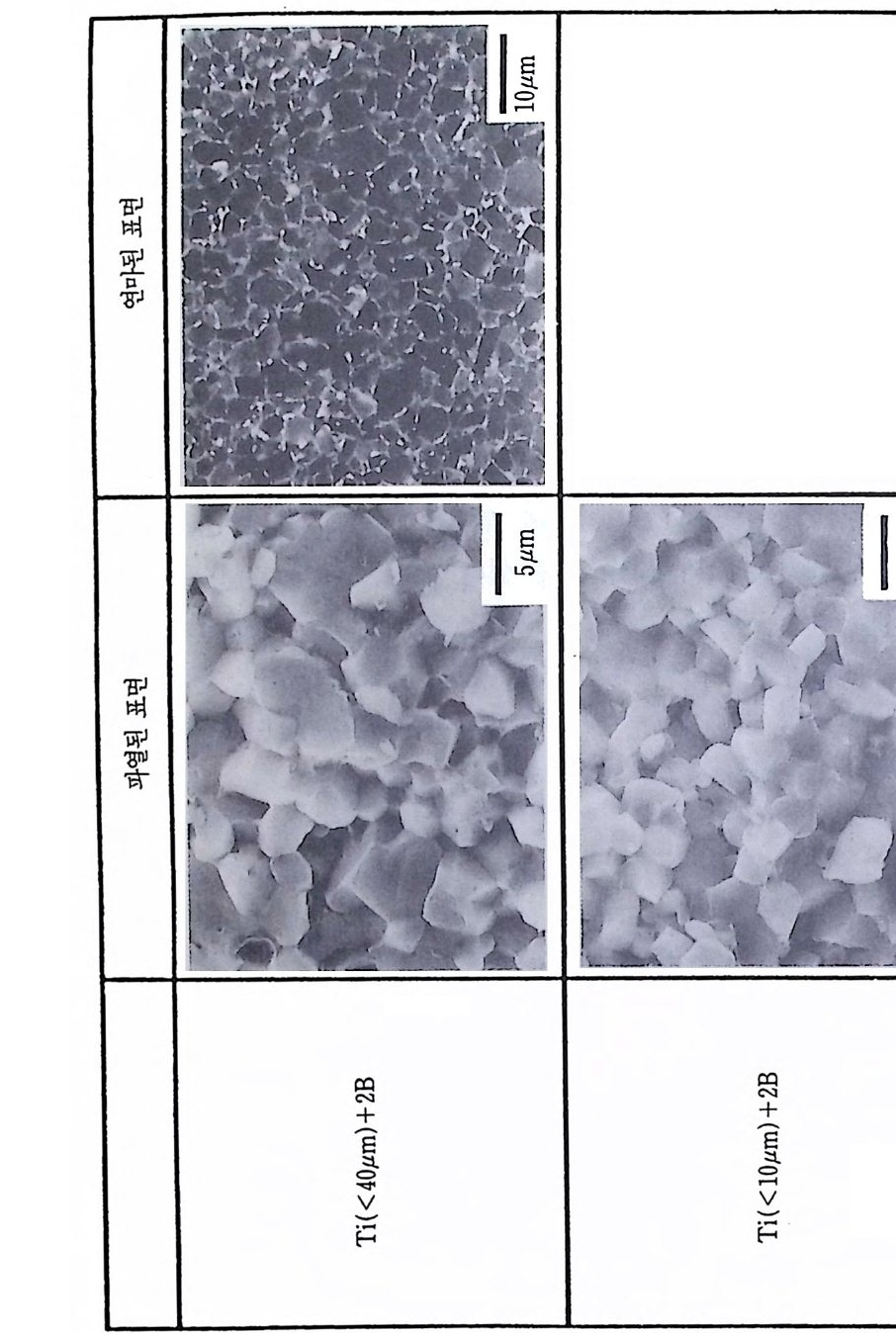
.프래그 로크이마 MES 는 내타나 를 조구 로크이마 의 트팩콤B2i T .8 5 립그
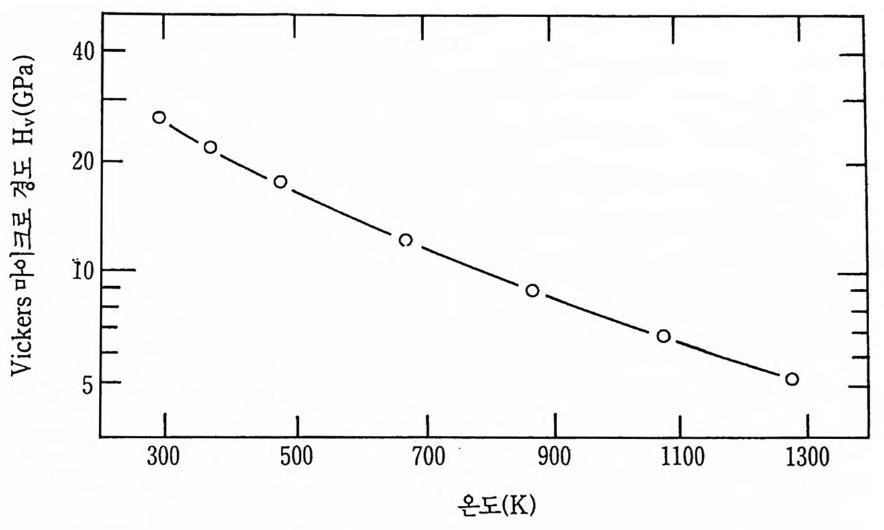 4oo2oI
4oo2oI
그림 8,6 HPCS 법으로 제조한 TiB 2 콤팩트에 대한 Vic k ers 마이크로 경도의 온도 의존성 (Ti 입자 크기 < 40µm)
소하지만 1273K 까지는 약 5GPa 울 유지함을 알 수 있다. 이 5GPa 은 고온에서 다른 TiB 2 세라믹스의 보고된 값 ll2) 보다 2 배나 더 큰 값에 해당한다. 8-2— 2 T iC 콤팩트의 제조 (1) T i C 의 HPCS 처리 HPCS 실험은 3GPa 의 압력하에서 A 형과 B 형의 고압 셀을 사용한 두 가지 점화법으로 진행되었다. A 형 셀에서 반웅물 펠릿이 점화되 면 연소반응은 전체 반응물을 통하여 전행되지만 그 생성물로 변환효 율은 72% 였다. 이 사실은 A 형 셀에서는 열손실에 따라 변환효율의 감소를 초래한다는 것을 나타낸다. 한편 연소반응성은 반웅물 펠릿 (또는 예형 펠릿)을 예열함으로써 상승되는 것을 예측할 수 있다. 이
것은 실험적으로 B 형 셀의 탄소 두관 히터 (carbon sleeve hea t er) 가 그 변환효율을 높이는 데 효과적일 것이다. A형 셀은 TiB 2 콤팩트 제조와 HPCS 공법에서 설명하였으므로 이곳에서는 B 형 셀을 사용 한 Ti C 콤팩트 제조를 설명하고자 한다. T i와 C 분말들에 n- 핵산울 가하여 잘 혼합한 후 전공, 건조시키는 데 이때 C 와 T i의 몰비 (C / T i)는 0.70~ 1. 10 으로 변화시킨다. 각 혼 합된 분말을 형툴 속에서 20MPa 로 가압하여 이론밀도의 약 50% 인 밀도로 지름 6mm 와 길이 6mm 의 펠릿을 만든다. 그 예형 펠릿은 B 형 HPCS 셀의 탄소 투관 히터에 직접 접촉하도록 끼워 넣고 HPCS 공정에 따라 가압, 점화, 감압 및 냉각의 HPCS 처리를 하여 고밀도 Ti C 세 라믹스를 제조 18) 한다. A 형 셀을 사용했을 경우, T i C 로 변환효율 72% 와 체적밀도 3.93 g /cm3 였지만 B 형 셀의 경우는 그 변환효율 99% 이상과 체적밀도 4 . 61 g /cm3 였다.
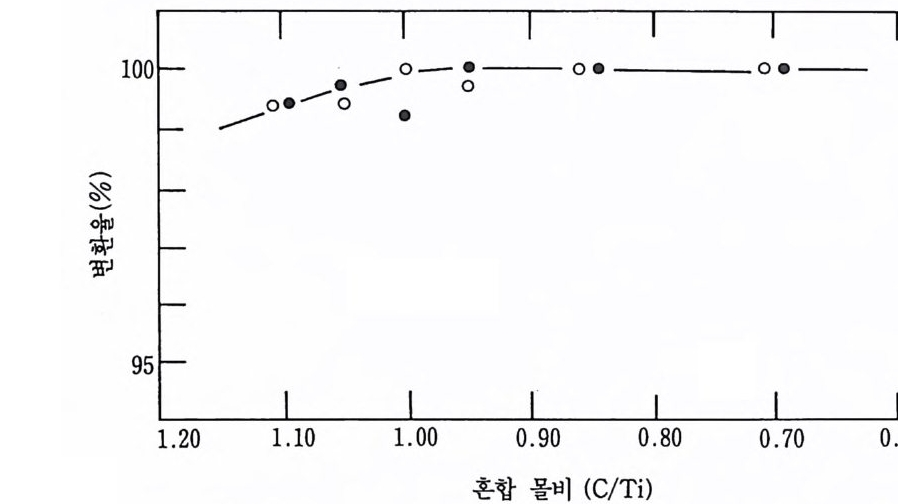 100 0-• 。• 。 •
100 0-• 。• 。 •
그립 8 . 7 T i와 C 분말들의 혼합 몰비 변화에 따른 TiC x 으로 변환효율 (• : Ti < 40µ rn, o: Ti
(2) Ti C 콤팩트의 특성 B 형 셀울 사용했을 경우 그 변환효율은 Ti 분말의 입자 크기에는 관계되지 않으나 조성원소들의 혼합된 몰비에는 관계가 있다. 그림 8 . 7 에서 보는 바와같이 0.7 0 ~C/Ti ~ O.95 범위의 여러 가지 혼합 몰 비를 갖는 반응물둘은 단일상이지만 T i Cx 의 비화학양론적 상으로 거 의 100% 변환한다. 그러나 그 혼합비가 0.95 를 넘으면 그 출발원소 들은 반응하지 않고 약간 남아 있게 된다. TiC x 중 T i Co.91 의 보고된 밀도 4 . 90 g /cm3 를 그 이론밀도로 택 하 였다. T i Cx 의 상대 밀도는 Ti 분말 입자 크기 에는 무관하고 C/Ti 혼 합 몰비에 관계가 있는데 그 최대 밀도는 이론밀도의 96% 를 넘는다. SEM 마이크로 그래프 분석결과 Ti C 낱알의 평균 지름은 Ti 분말 의 입자 크기의 감소에 따라 감소함을 관찰할 수 있었다. 그렇지만 T iB데서와 같이 출발물질 Ti 입자에 비하여 더 미세한 TiC 낱알의
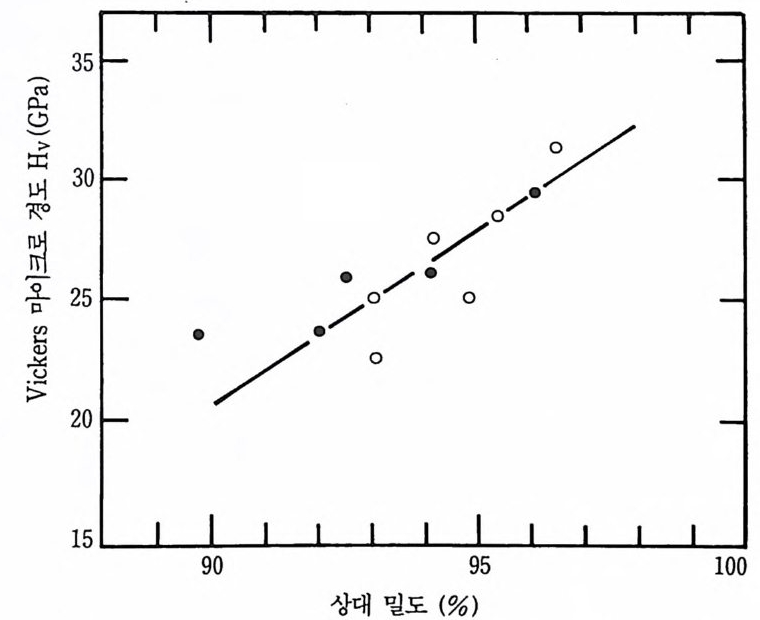 35302520
35302520
그림 8.8 Ti C x 콤팩트의 상온에서 마이크로 경도와 상대밀도간의 관계도 ( • : Ti <4 0.u m , o : Ti < lOµ m)
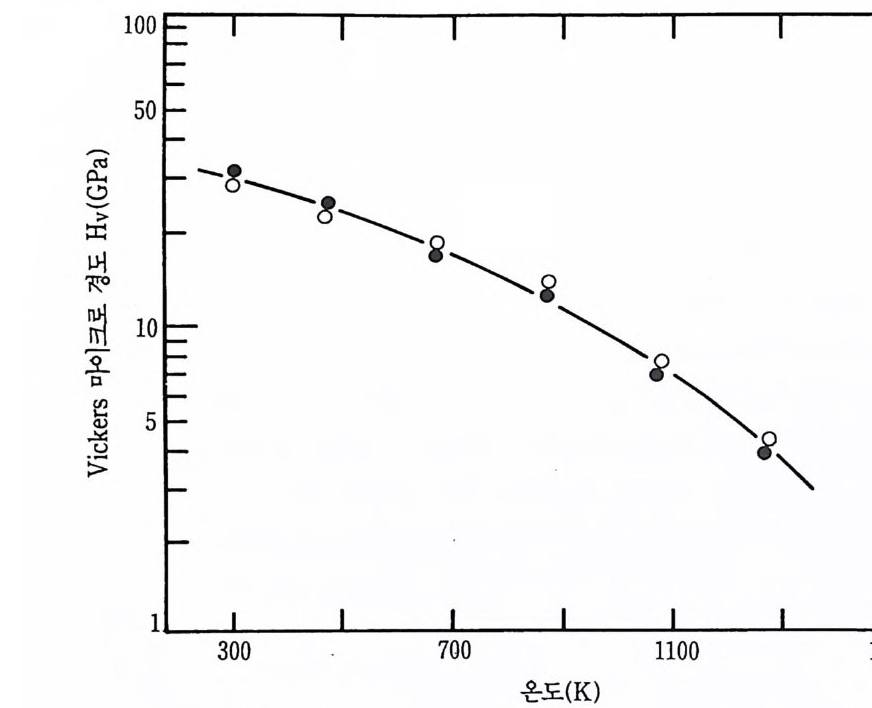 100
100
그림 8.9 T i C(•) 와 T i Co . ss( 이 콤팩트들에 대한 Vic k ers 마이크로 경도의 온 도 의존성•
생성은 관찰할 수 없었다. Vic k ers 마이크로 경도는 그림 8. 8 에서 보는 바와같이 상대밀도에 비례하여 증가함을 알 수 있다. 첨가제 없이 이론밀도를 갖는 Ti C 콤팩트의 마이크로 경도는 상온 에서 약 35GPa 인데 이것은 단결정에 대하여 보고된 값 113> 29GPa 보 다도 더 크다. T i C 와 T i C 。 ,85 에 대 한 Vic k ers 마이크로 경도의 온도 의존성은 그림 8.9 에서 보는 바와 같으며 상온에서 그 마이크로 경도 는 각각 31GPa 와 29GPa 이다. 온도가 상승함에 따라 두 화학종의 Vic k ers 마이크로 경도는 탄소 함량에 관계 없이 같은 경 향으로 서서 히 감소한다.
8— 2-3 SiC 콤팩트의 제조 (1) S i C 의 HPCS 처 리 조성원소들로부터 SiC 생성 30) 시 방출하는 열량은 상온에서 69kJ / mol 로 보고되 었는데 이 열량은 T iB 2 를 생성 할 때 방출하는 열 293 k J /mol 에 바 하면 대 단히 작다. SiC 생 성 시 단열온도 (Tad) 는 1850K 로 자체 전파 연소가 가능한 최저 단열온도 1800K(6-2-l 절 참조)보다 약간 높은 정도이다. 고압하에서는 원자 확산의 활성화 에너지마저 증가하기 때문에 HPCS 법에 의한 S i C 로 변환수율은 SHS 에 의한 수 율보다도 작은 것 같다. 실제로 반응물질이 3GPa 압력하에 A 형 셀에서 반응물 펠릿 한 끝 에 점화시키면 S i C 로 변환효율은 36% 로 감소된다. 초기 온도를 300 K 에서 1100K 까지 상승시키면 단열온도를 2500K 까지 상승시 킬 수 있 는데, 실험적으로 점화체로서는 물론 반응물 펠릿을 빠르고 균일하게 예열할 수 있는 B 형 셀의 탄소 두관 히터를 사용함으로써 수행할 수 있다. 평균 입자 크기 5µm 인 Si 분말과 C 분말에 n- 핵산을 가하여 찰 섞고 진공, 건조시킨다. 이때 Si : C 의 몰비를 1 : 1~1 : 1. 2 로 변화 시키며 , 변환효율의 영 향을 조사하기 위하여 lOµm 흑연과 25µ rn 무 정형 분말의 입자 크기를 갖는 두 가지 종류의 탄소가 사용되었다. 시료의 크기와 HPCS 처리 등은 앞의 소단원에서 설명한 바와 같다. 반응물들이 생성물로 생성된 변환효율 19>(S i C/(S i C+S i))은 각각 SHS( 대기압)법에서 64%, A 형 셀을 사용한 HPCS(3GPa) 법에서 36% 및 B 형 셀을 사용한 HPCS(3GPa) 법에서 96% 임을 보였다. (2) SiC 콤팩트의 특성 그립 8.10 에서 보는 바와같이 X- 선 회절분석의 결과는 소량의 a-S i C 를 포함하는 화학양론적 /3 -S i C 로 생성물을 이루고 있다는 것 울 나타내며 예리한 {3- SiC 피크는 입자들이 찰 결정화되었음을 나타 낸다.
/3 - S i C 는 2300K 이 하의 평 형 상태 에서 안정 화되는 낮은 온도형 이 라 고 일반적으로 말한다. 그렇지만 /3 -S i C 의 결정화는 S i C 의 승화―재 결정화 및 용융 Si 용매로부터 침전 114) 에 의하여 2300K 이상의 온도 에서까지 일어날 수 있다. 연소합성의 경우에, 실제 연소온도가 2300 K 를 넘더라도 용융 S i와 탄소의 반응에서 아주 빠른 결정화 때문에 /3 -S i C 는 준안정상으로 형 성 될 것 이 다. 출발물질 S i의 입자 크기가 감소하면 S i C 로 변환효율은 증가하는 데 입자 크기 O.lµm 의 Si 분말이 사용될 때 그 효율은 99 . 6% 에 달 한다. 반응물의 입자들이 미세할수록 입자간 접촉면적은 커지고 원소 둘의 확산행로는 감소된다. 그러나 상대밀도는 Si 입자 크기에 관계
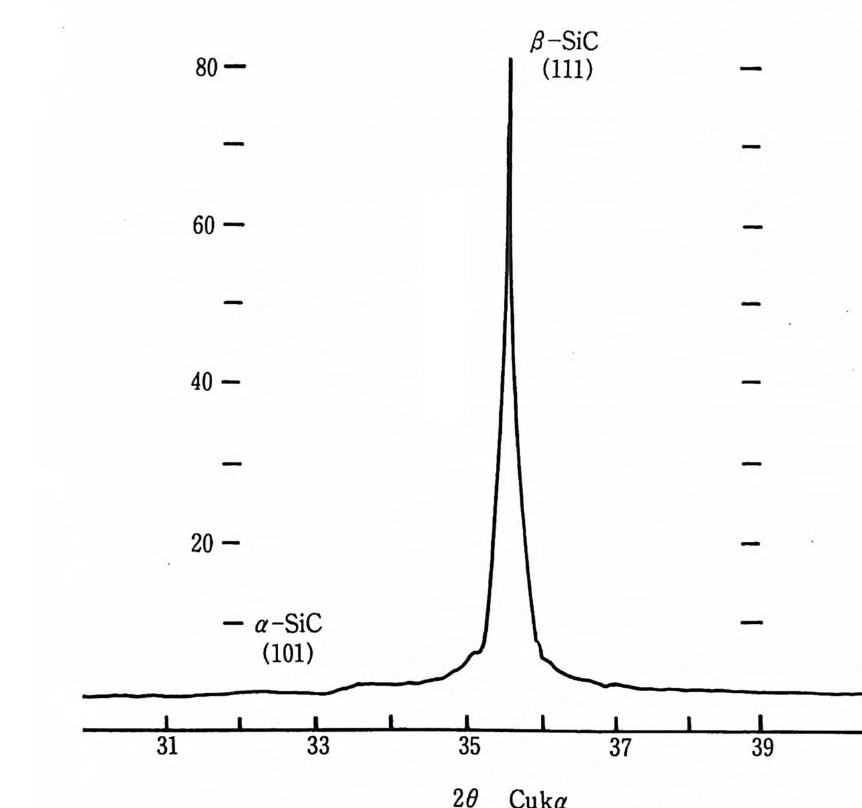 /i-S iC
/i-S iC
그립 a.10 HPCS 법으로 제조한 SiC 콤팩트의 대표적인 X - 선 회절 패턴.
없이 91~93% 범위에서 대략적으로 일정하다. SiC 콤팩트의 파열 표면의 마이크로 구조분석 30) 에서 출발물질 S i의 입자 크기를 5µm 에서 O . lµm 로 감소시키면 Si C 콤팩트의 낱알 크기 는 5µm 에서 lµm 로 감소되는데 이 사실은 반응물질의 입자 크기를 변화시켜 어느 정도 생성물의 낱알 크기를 조절할 수 있음을 보여준 다. HPCS 법에서 가열기간을 약간 길게 하면 부가적인 가열로 입자 간 소결이 증진되었음을 기대할 수 있다. 사실 가열기간을 2 초에서 10 초로 연장시킬 때 파열 패턴은 낱알간 (i n t er gr anular) 형에서 낱알관통(t ransgr anular) 형으로 변하였지만 난알 성장(gr a i n gro wth)은 관찰할 수 없었다. 10 초 동안 가열하면서 제조 된 SiC 콤팩트의 특성들은 표 8.1 에서 보는 바와 같다. SiC 콤팩트의 상대 밀도는 출발 Si 분말의 입자 크기나 가열시간에 무관하고 거의 같다. 그러나 SiC 콤팩트의 Vic k ers 마이크로 경도 (Hv) 와 파괴인성 (K(c) 은 더욱 미세한 SiC 분말을 사용함으로써 약간 개선되었음을 알 수 있다. 표 s . 1 3 GPa 에서 HPCS 법으로 10 초간 가열하여 제조한 SiC 콤팩트의 특성. 트-,.o서 Si (5 µm)+C Si (O .lµ m ) +C 상대밀도(%) 92.0 92. 8 Vic k ers 마이크로 경도 (GPa) 23 27 파괴 인성 (MN/m312 ) 4.3 4.5 8-3 소결 메커니즘 8— 3— 1 본 성 체적변화 비기체 연소합성 반응에 의하여 반응물에서 화합물로 변환될 때 계
의 체적변화를 일으킨다. 아주 실질적인 그 본성 체적변화(i n tri ns ic volume chan g e) 는 그 변환이 완료되었을 때 다음과 같은 식으로 설명 된다. X=~ 祐=〔급틀삶記/〔pi니 여기서 X 는 생성물과 반응물간의 본성 체적변화율, M 은 변하지 않을 것으로 가정한 계의 질량, pth p와 pth R 은 생성물질과 반응물 질의 이론밀도를 각각 나타낸다. 이 본성 체적변화는 표 8.2 에서 보 는 바와같이 Ti B2 , Ti C 및 S i C 의 경우 -20% 가 넘는 것으로 계산되 었다. 표 8,2 연소반웅 전후의 본성 체적변화. H'--냥 pth R(g/ c m3) pth P( g /cm 이 X(%) Ti +2 B- >T iB 2 3.5 4.5 -2 2 TSii ++ CC ---+>STiiC C 23..38 43..29 -—22 82 만일 연소반응 후에 시료 펠릿의 의형 (sha p e) 의 변화가 없다면 20% 이상의 다공성이 생성물질에 나타날 것이다. 실제 경우에 있어 서 반응물 펠릿의 밀도는 의성적으로 이론밀도보다 더 작으므로 이 다공성은 더욱 증가할 것이다. 그러므로 연소반응 중 다공성을 줄이 고 난알(gr a in)들을 결합시키기 위하여 압력이 필요하다. 한편, 단열 반웅온도와 그들의 융점 이 일치하는 T iB 2 와 T i C 의 HPCS 반웅들은 용융상 출현 (molte n ph ase app ea rance) 의 결과로 다공성 을 감소시 키 거 나 또는 제거시킬 것으로 기대된다. 사실상 T iB 2 와 T i C 의 상대밀도 둘은 용융상을 갖지 않는 S i C 의 상대밀도보다 더욱 크다. 이들 HPCS 반응은 생성물의 큰 체적 수축을 수반하는 빠른 반응
이다. 그러므로 압력 전달을 위한 매질의 신축성과 신뢰성은 생성물 의 고밀도화에 대한 중요한 요인 중의 하나이다. 이 연구에서 사용된 압력 전달을 위한 파이로필라이트(pyr o ph yllit e) 고체매질은 생성물을 고밀도화하는 데 효율적으로 작용하였다• 압력의 전달 메커니즘을 더 욱 개선한다면 더 낮은 압력에서라도 완전한 고밀도화를 얻을 수 있 을것이다 . 8— 3— 2 고 압하에서 연소소결 메커니즘 고압하에서 T iB 2 의 합성과 동시 소결에 관한 반응 메커니즘은 SEM 과 EPMA 관찰의 결과로 연구되었다. 그립 8 . 11 은 반응물내에 서 원소분말의 불균일 분포와 큰 입자들의 존재로부터 말미암아생기 며 Ti B2 콤팩트내의 미반응 영역에 있는 T i와 B 원소들의 마이크로 구조와 분포를 보인다. 2µm 이하의 입자 크기를 갖는 수많은 작은 Ti B2 결정이 SEM 사진의 흰색인 Ti 영역에 침전된다. 이 결과는 그림 8 . 12 에서 개략적으로 설명한 바와같이 T iB 2 의 HPCS 에 관한 반응 메커니즘을 설명하는 간단한 모델을 제시하여 준다. 연소대 (combusti on zone) 가 원주형 반응물 펠릿의 축을 따라 전행 할 때 연소대의 전진 앞면의 가까운 부근은 반응열의 열전도에 의하 여 예열될 것이고 반응 전에 Ti 입자들은 녹기 시작한다. 다음에 그 연소반응에서 B 원자들은 용융 Ti 입자들로 빠른 확산 때문에 Ti B2 의 많은 핵심생성은 용융업자들 안에서 시작된다. TiB 2 핵둘은 평균 크기가 5µm 까지 갑지기 자라고 이 계가 식을 때까지 고압하에서 서 로 유착한다. 결정의 핵심 생성―성장에 기초를 둔 이 모델은 TiB 2 콤팩트에서 낱알들이 원래 Ti 입자보다 HPCS 처리 후에 더 작아지 는 것도 또한 설명할 수 있다. 이에 반해서 더욱 미세한 낱알을 가전 그러한 결정화는 T i O 라 SiC 의 HPCS 에서는 관찰할 수 없었고 Ti C 또는 S i O 키 낱알들은 출발
 (a~ (b)
(a~ (b)
 (c)
(c)
그림 8. I I 티탄 (a) 과 붕소 (b) 에 대한 원 소분포의 X- 선상과 HPCS 로 제조된 TiB 2 콤팩트 (c) 내에 부분적으로 반응하지 않은 영역의 SEM 마이크로 그 래프.
원소인 Ti 또는 Si 입자들보다 그 크기가 크거나 또한 유사하였다• 그림 6.13, 그림 6.1 1 및 그립 8.13 에서 보는 바와같이 연소온도가 HPCS 의 단열온도에 접근하면 T iB 2 에 대한 T i와 B 두 원소는 반응 전에 녹지만 T i C 와 S i C 의 경우에 C 는 고체상태로 남아 있다. Ti -B 계의 연소반응에서와 같은 액체-액체상간의 원자확산은 T i -C 계 115) 와 같은 액체-고체상간의 원자확산과 S i -C 계와 같은 증기-고체상간의 원자확산보다 더욱 빠를 것이다. 원자의 이동도와 관련된 이들 확산 차이가 출발 분말 입자들과 비교하여 화합물의 더욱 미세한 결정화가
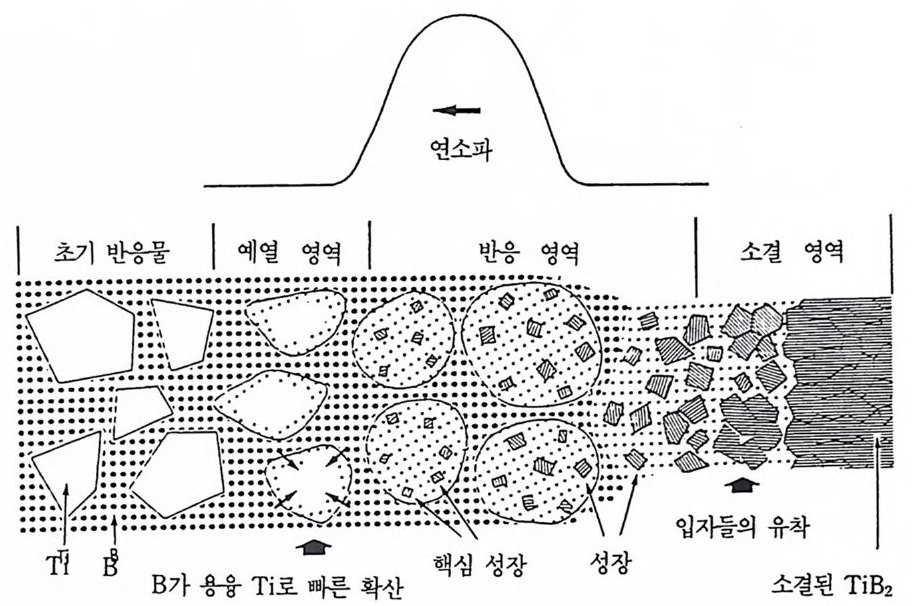 뀌 :〕二:;::三융B; 가:: ;@용二;:융gg \T;g: i:로:@ 장;빠판:른g;: 二:확:산·f· ::::i핵:십::: ·l성··장 ': •• l• -•·鬱 ·l` 성장瓚l l摩I 鬱: :소결'된역 T iB 2
뀌 :〕二:;::三융B; 가:: ;@용二;:융gg \T;g: i:로:@ 장;빠판:른g;: 二:확:산·f· ::::i핵:십::: ·l성··장 ': •• l• -•·鬱 ·l` 성장瓚l l摩I 鬱: :소결'된역 T iB 2
그림 8.l2 고압하에서 T iB려 합성과 동시소결의 반응 메커니즘에 대한 개요도•
일어날 수 있을지 또는 없을지를 결정하는 요인이 될 것이다. 8-4 HPCS 법에 의한 복합 세라믹스 제조 8-4-1 복합재료의 연구개발 1988 년 국내 의 한국 기 술자학술회 의 춘계 worksho p의 신소재 분 과의 과제는 복합재료의 제조 및 응용 116) 이었다. 주제 발표자들과 토 론 참가자들 및 방청 참가자들이 우리나라 복합재료의 연구개발에 관 한 많은 토의를 하였다. 주제 강연 제목은 전기재료용 복합재료, 고 온성 섬유강화 금속기 복합재료, 금속 복합재료, 열가소성 수지 복합
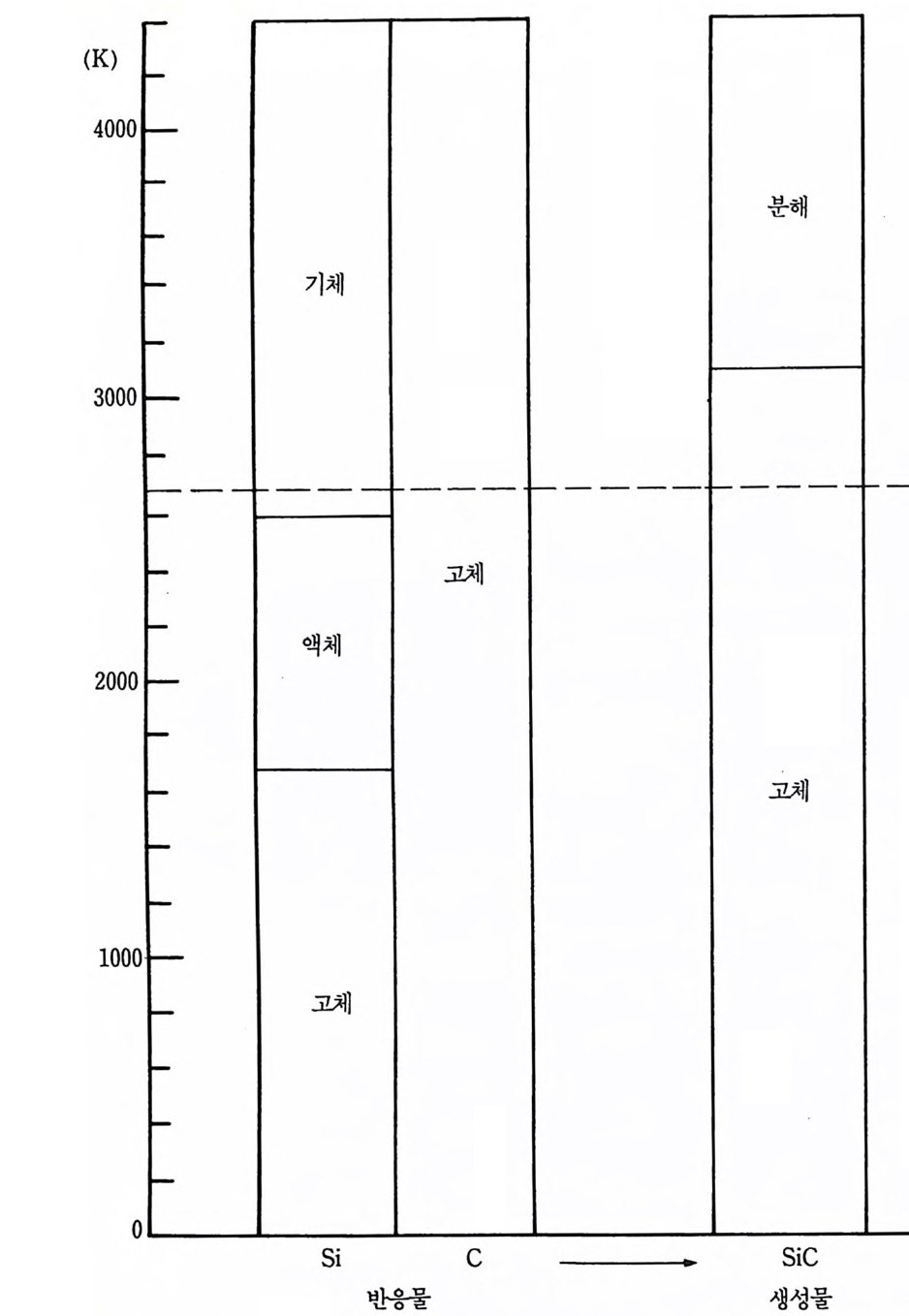 (K)
(K)
<� SiC ��1�<� ���� a.13 1300K\ � ���X�� HPCS ��<�\
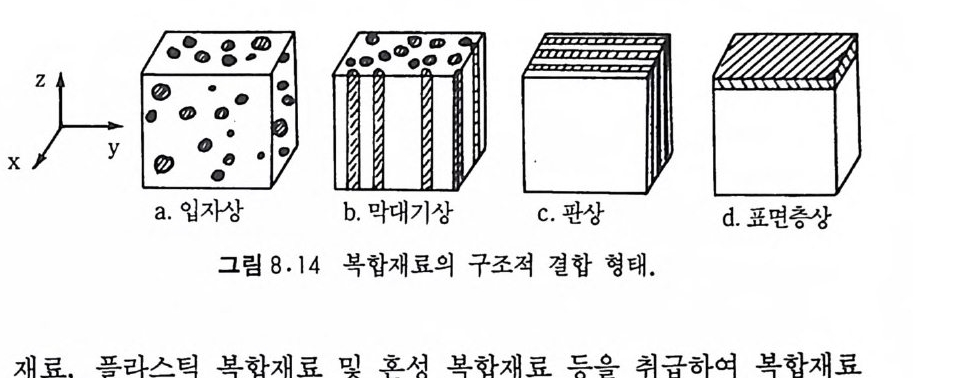 재x 료, 』풀라스틱 복a:합年재 료4 및//b 복 막 합 혼대재 성鬪 료기 의상복합구 재조 료 c . 결 등합판 「적 을상형 취테 급하여 복d합三 재료
재x 료, 』풀라스틱 복a:합年재 료4 및//b 복 막 합 혼대재 성鬪 료기 의상복합구 재조 료 c . 결 등합판 「적 을상형 취테 급하여 복d합三 재료
의 연구개발에 대한 획기적인 관심과 필요성을 강조하였다• 전기재료용 복합재료의 종류와 활용 116) 의 제목 으로 발표된 내용 중 에서 복합재료의 구성과 종류를 여기서 설명하고자 한다. 복합재료는 두 가지 이상의 상 또는 재료를 결합, 제조하여 밀도, 경도 (V i ckers hardness) , 파괴 인성 (frac tu r e tou g h ness) , 내 화성 , 화학적 안정 성 및 전기적 성질 등의 제반 특성이 개선된 고성능 신소재 제품생산에 사 용된다. 일반적으로 매트릭스 (ma tri x) 재료와 강화재 (rein for cement) 재료의 두 성분으로 구성되는 복합재료는 결합되는 물질의 구조적 형 태에 따라 그립 8.14 에서 보는 바와같이 구분된다. 그 구조적 형태에 따른 제품의 실례는 다음과 같다. i ) 입 자상 분산 : 경 금속 (hard meta l) , 서 멧 (cermet) , 침 윤재 료 (im p re gn a te d mate r i als ) . ii ) 섬 유상 강화재 료 : GRP, 강철 콘크리트 (ste e l concrete ) . 표 8 . 3 섬유상 강화제의 경우 , 재료의 결합. 매트릭스 섭 유 여] 세라믹스 금 속 금속성유로 강화된 유리 또는 콘크리트 금 속 세라믹스 탄소성유로 강화된 알루미늄 금 속 중합체 경섬유 (hard fi ber) 로 강화된 알루미늄 중합체 금 속 금속섬유로 강화된 고무 세라믹스 중합체 중합체로 결합된 콘크리트 중합체 세라믹스 유리로 강화된 중합체
iii) 적충된 판상(l am i na t ed sta c kin g ) : 합판, 안전유리. iv) 도금된 표면 : 부식 방지 및 내 마모성 도금. 이상과 같이 여러 가지 형태의 강화제의 사용을 들 수가 있지만 일 반적으로 사용되는 강화제는 섬유상(fi ber) 의 형태로 매트릭스에 첨가 되는데 매트릭스와 강화제의 구성관계는 표 8.3 에서 보는 바와 같다. 섬유의 종류는 출발원료에 따라 다음과 같이 나누어진다. i ) 위스커 (whis k er) : 금속 또는 비금속 무기 재료상에서 제조되고 구조내에 결함이 거의 없는 결정으로 우수한 특성을 나타내지 만 제조원가가 높다. ii) 세라믹스 섬유 : 탄소섬유, 붕소섬유 등과 같이 이미 상당 분야 에 실용화되고 있다. iii) 금속 또는 합금 섬유 : 텅스텐, 철강섬유 등의 높은 탄성을 지 니는 제품으로 세라믹스 섭유에 비하여 비중이 높다. iv) 유리섬유 : 용융상에서 비교적 쉽게 섬유상태로 뽑을 수 있다. 지름이 충분히 가늘고 표면상태가 양호하면 고강도를 나타낸 다. v) 고분자섬유 : 고리상의 고분자 재료 자체가 섬유상태로 된다. 나무에서의 셀룰로오스 (cellulose) 섬유가 한 예이다. 최근 국내에서도 복합재료의 연구 및 개발에 관한 산, 학, 연의 관 심이 매우 높아지고 있다. 현재 복합재료를 여러 가지 용도로 광범위 하게 사용하고 있으나 원료처리에서 제품생산에 이르기까지 기술축적 이 미 약하여 선진국의 기술도입 에 의존하는 경우가 많다. 운모(mi ca) 와 운모 복합재료, 에폭시 수지와 에폭시 복합재료, 규소 고무, 멜라 닌 수지 및 폴리에스터 수지 복합재료 등의 국산화가 시급하다. 특히 세라믹스 매트릭스를 이용한 복합재료의 연구개발과 제품의 국산화가 과학기술 및 산업발전에 절실히 요구된다. 섬유로 보강된 첨단 복합소재는 현재 인공위성, 기계산업, 자동차 산업, 스포츠용품 및 화학 플랜트 등에 활용되고 있다. 이는 첨단 복 합소재의 뛰어난 경도, 파괴인성, 탄성률, 내식성, 내마모성 등의 고
성능 기계적 기능과 고융점, 내화성, 열전도 등 고성능 열적 기능 때 문에 필요로 하는 설계 물성치 실현을 위한 선택의 폭이 큰 이유이 다. 경제성을 고려한 필요 물성치의 구현과 장기사용시 파괴현상을 조절하기 위하여 여러 가지 강화섬유를 혼용한 복합재료의 사용은 날 로 그 수요가 증가할 것이다. 이와 같은 복합재료의 연구개발의 관심도와 실용성의 증가는 국제 적인 추세라 하겠다. 그러한 사실은 미국에서 발간되는 학술지인 Cerami c Bulleti n 과 ]ourn a l of the Americ a n Cerami c Socie t y 에 1988~89 년의 최근 2 년간 발표된 논문의 30% 이상이 복합재료와 관 계된 연구논문인 것으로도 예측할 수 있다. 8-4— 2 TiB 2 - T iC 콤팩트의 제조 (1) HPCS 법 처리 TiB 2 콤팩 트와 TiB 2 매 트릭 스에 5, 10, 20 및 30 wt% T i C 를 포 함하는 TiB 2 -TiC 복합 세라믹스 (com p os it e ceram ic) 콤팩트를 제조 하기 위하여 T i ( < 40 µm의 입자 크기), 무정형 붕소 ( < 2 µm) 및 Ti C (< lµm) 의 출발물질 분말들을 적정 량 평 량한다. 각 평 량된 출발물질 을 에탄올 용매에 찰 혼합시킨 후 전공, 건조시켜 지름 6mm 와 길이 6mm 인 펠릿으로 가압, 성형시킨다. 이 펠릿 반응물을 B 형 HPCS 셀의 탄소 두관 히터 속에 넣고 고압장치인 입방모루 장치 66) 를 사용 하여 3GPa 까지 가압한 후 2, 3 초 동안 4 . 2kVA 로 점화시킴으로써 연 소반응 117) 이 시작되어 HPCS 법으로 잘 제조된다. 반응물과 생성물의 엔탈피 관계로부터 이상적인 단열계에서 TiB 2 연소합성시 얻을 수 있는 최고 반응온도는 그의 융점 3193K 와 일치 하는 것으로 계산 118) 되었다. TiB 2 생성의 발열반응열로부터 융해잠 열의 약 40% 를 보충할 수 있다. 광학온도계로 측정한 반응온도는 2900~3ooo·c 이고 합성된 T iB 2 의 SEM 사전을 살펴보면 입자간에
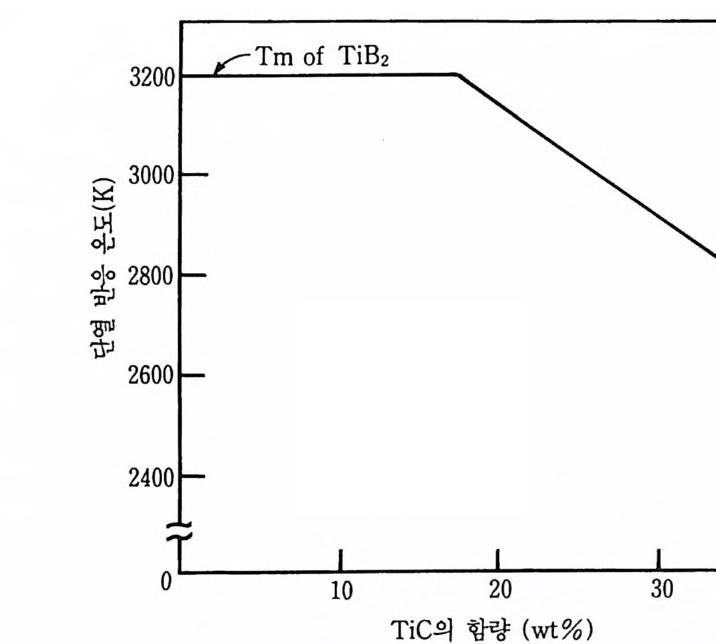 3200. -T m of TiB 2
3200. -T m of TiB 2
그림 8- 15 TiC 함량에 따른 단열 반응은도.
붙은 것으로 약간 용융되었음을 볼 수 있다. 이들 사실은 그 연소 반 옹이 거의 단열상태에서 전파됨을 나타낸다. 그러므로 그 반응 진행 앞면 근처의 Ti 금속분말은 발열반응열에 의해 녹고 붕소와 순간적 으로 반응하여 TiB 2 생성을 끝마친다고 생각된다. 반응물이 T i C 로 희석될 때 발열반응열은 감소되고 열역학적 계산 으로 산정된 단열 반응온도는 그림 8.15 에서 보는 바와같이 TiC 함 량이 17% 이상으로 증가함에 따라 감소한다. Ti C 입자들은 융점이 3210K 로 높기 때문에 완전히 녹지 않을 것이다. 그렇지만 그 연소반 웅 동안 나타나는 Ti, Ti- B 중간체 화합물 및 T iB 2 의 녹은 상들은 T iB 2-T i C 계 의 고밀도화를 도울 것이다. (2) TiB 2 -TiC 콤팩 트의 특성 x- 선 회절분석으로 육방정계인 T iB 2 와 단순 입방인 TiC 상들은 보존되며 단지 피크 강도가 1% 이하인 TiB 상이 미량 존재한다. 각
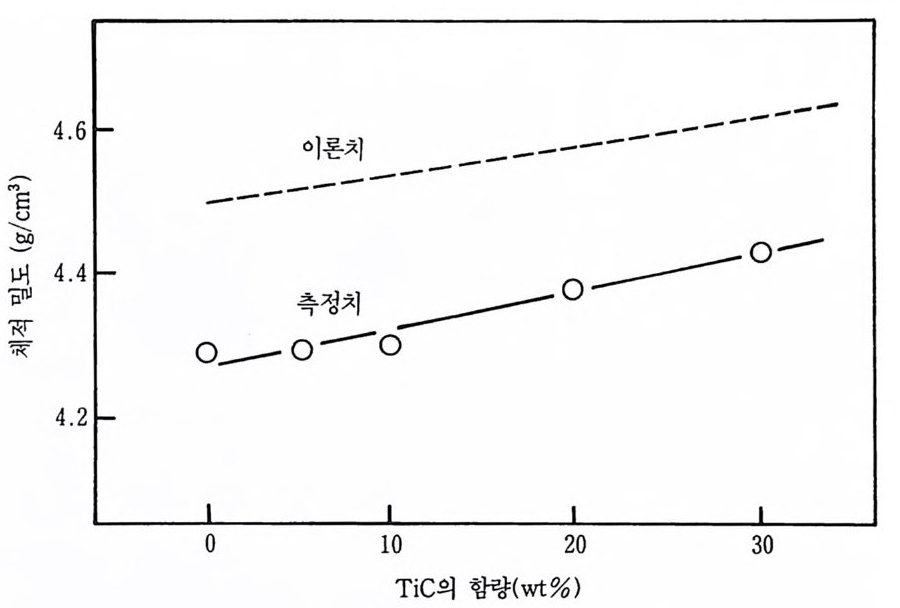 cEu t버]tlkFaB) 44. 641 」- o-----°-측이 --정론치--치-一- -o -- ---- ---- --0--- --- ----- -0- -- --
cEu t버]tlkFaB) 44. 641 」- o-----°-측이 --정론치--치-一- -o -- ---- ---- --0--- --- ----- -0- -- --
그림 a. 16 TiB 2 -T i C 복합체의 체적밀도.
복합 세라믹스에서 TiB 2 매트릭스의 격자상수들은 실험오차 범위내 에서 a=O.3031(1), c=0.3235(2) nm.로 거의 일정하다. 그림 8 .16 에서 보는 바와같이 TiC 함량이 증가함에 따라 체적밀도 (bulk dens ity)는 4.29 에서 4 . 43 g /cm3 으로 증가하였다. 그렇지만 상 대밀도는 95~96% 범위에서 거의 변하지 않았다. T i C 의 첨가는 반 응열을 감소시키는 것 의에 TiB 2-TiC 복합 세라믹스 낱알경계에 계 면에너지롤 증가시킬 것이다. 결과적으로 Ti B2 매트릭스에 TiC 입 자들이 증가하면 고밀도화가 어려울 것같이 보이지만 그 결과는 다르 게 나타났다. 생성물의 파열된 표면에서 마이크로 구조를 나타내는 SEM 마이크 로 그래프는 그림 8.17 에서 보는 바와 같다 . TiB 2 콤팩트의 평균 낱 알 크기는 약 lOµm 이고 TiB 2 -TiC 복합체에 있는 T i B2 의 낱알 크기 는 TiC 함량이 커지면 더 작아지려는 경향을 보인다. T iB 2 와 TiB 2 -TiC ( 5w t%) 콤팩트들에서는 낱알경계 파열 또는 낱알간 파열
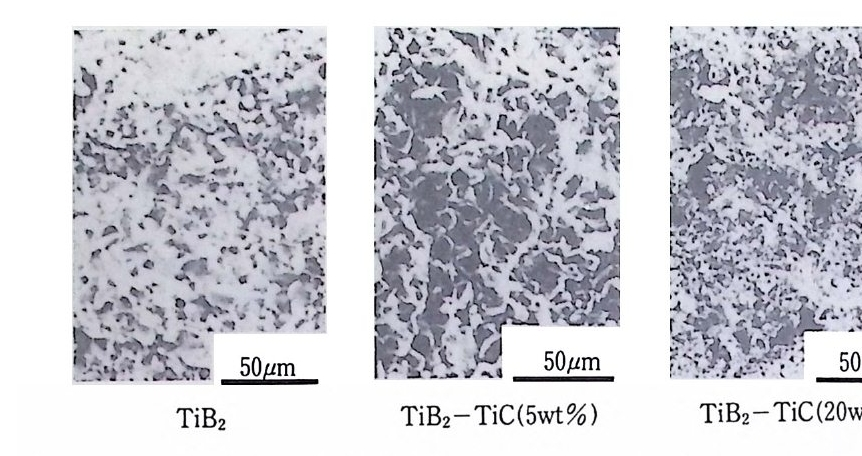 • ·. . ,1· '- ••r - 、
• ·. . ,1· '- ••r - 、
그림 8.17 소결된 콤팩트의 생성물들에서 파열된 표면의 SEM 마이크로 그래프.
(int e r gr an ular frac tu re ) 이 우세 하지 만 20w t% T i C 를 함유하는 Ti B2 -TiC 복합체에서는 낱알 통과 파열방식 (tra nsgr an ular frac tu r e mode) 이 증가되었다. Ti B2 -TiC ( 20w t%) 복합체를 10-4 t orr 와 l, 200°C 에서 열 식각한 표면 (the nnally etc h ed surf ac e) 의 SEM 사진은 그림 8 . 18 에 서 보는 바 와 같다. 미세한 TiC 입자들은 분산되어 Ti B2 매트릭스와 잘 결합 하고 있다. 반웅열의 감소와 TiC 입 자들의 분산은 T iB 2 의 낱알 성
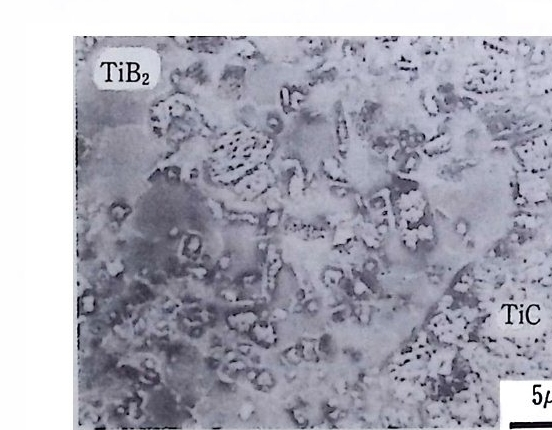 i. 5 ic -··,. ’. ·.., ••a . .
i. 5 ic -··,. ’. ·.., ••a . .
그림 8.18 TiB z -TiC ( 20w t%) 복합체를 열 식각한 표면의 SEM 마이크로 그래프.
장(gr a i n g ro wth)을 조절하는 것으로 생각된다. 미세한 낱알들의 생 성은 그 콤팩트의 고밀도화에 기여하는 것 같다. TiC 함량의 함수로서 Vic k ers 마이크로 경도를 표시 한 것은 그립 8.19 에서 보는 바와 같다. T i C 의 함량이 증가함에 따라 그 복합체들 의 그 경 도는 20wt % T i C 에 서 29GPa 로 최 대 값을 보이 며 증가하다 가 다시 감소한다. 파괴인성 KIC 를 TiC 함량의 함수로 도시한 것은 그림 8.20 에서 보는 바와 같다. KIc 역시 10~20w t% T i C 에서 최대 값 4 . 2MN/m3'2 를 보이며 TiC 함량에 따라 증가하다가 다시 감소한 다. TiB 2 매트릭스에 10 및 20wt % T i C 를 포함하는 복합체들은 마 이크로 경도, 파괴인성 및 더 미세한 낱알둘로 된 마이크로 구조 등 현저히 개선된 특칭들을 갖는다. T i C 의 첨가 때문에 생성물 희석은 T iB려 낱알성장을 조절하는 데 영향을 주지만 이 조성 범위에서 낱 알의 결합을 약화시키지 않는다는 것을 나타낸다. 그렇지만 30w t%
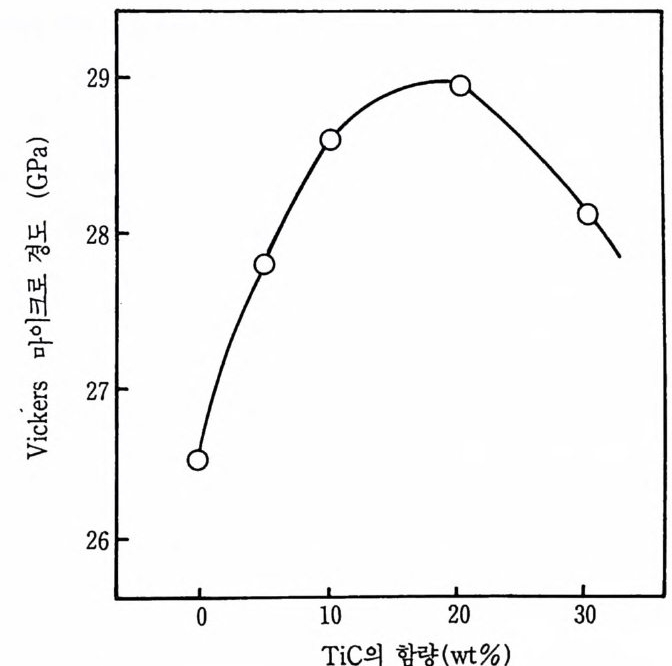 29
29
그림 8- 19 TiC 함량의 함수로서 TiB 2 -TiC 복합체의 Vic k ers 마이크로 경도.
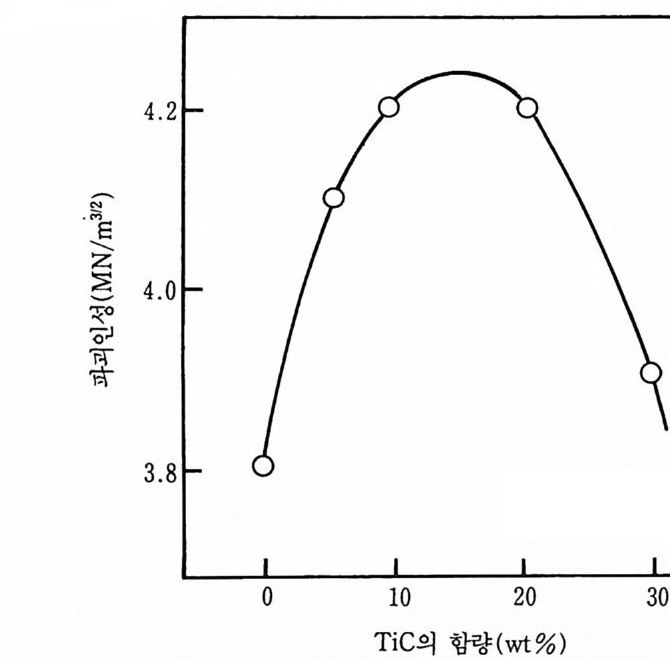 4.2
4.2
그림 8.20 T iC 함량의 함수로서 T iB2 - TiC 복합체의 파괴인성.
생성물 희석에서 마이크로 경도나 파괴인성이 감소하는 것은 단열온 도를 너무 감소시키는 데 그 원인이 있으며 아마도 연소반웅 중 액체 상의 결핍이 소결운동을 방해하는 것으로 설명할 수 있다. 8— 4— 3 T iB 2 -SiC 콤팩트의 제조 티탄과 붕소분말울 화학양론적 몰비인 1 : 2 로 평량하고 여기에 {3 -S i C(~0.3µm) 를 각각 5, 10, 20 및 30w t% 되게 가하여 에탄올 에 녹여 잘 혼합한 후 전공, 건조시킨다. TiB 2 -TiC 복합세라믹스 콤팩트 제조와 갇은 방법으로 B 형 압력 셀을 사용하여 4 .4 kVA 의 전력으로 2,3 초 점화시켜 HPCS 처리 22) 를 한다. 티탄과 붕소는 액체 상태로 TiB 2 매트릭스를 형성하는 균일반웅 모델에 해당한다. 한 상
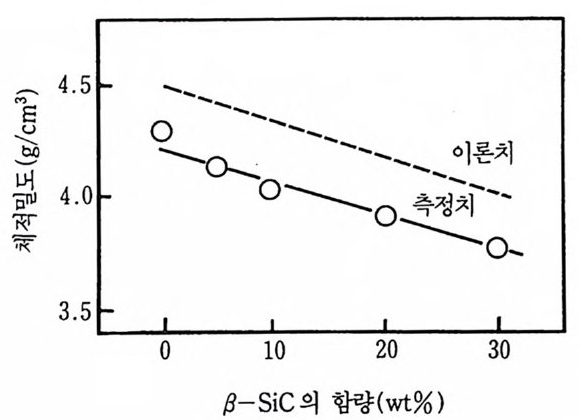 守머F]cuE(B) 45』卜400\` ` `- - .... ---... =..... _ ... : ..:.. :`1
守머F]cuE(B) 45』卜400\` ` `- - .... ---... =..... _ ... : ..:.. :`1
그립 8,21 SiC 함량의 함수로서 TiB 2 -Si C 복합체의 체적밀도.
의 계면 자유에너지가 다른 상의 그 자유에너지보다 작으면 낮은 자 유에너지를 갖는 상은 높은 에너지를 갖는 상으로 완전히 둘러싸이거 나 젖게 되며 이 과정 119) 을 통하여 계의 전체 자유에너지는 감소한 다. 낮은 자유에너지를 갖는 상은 주로 액체이고 공융점 이상으로 온 도가 증가하면 액체 양은 증가된다. 결과적으로 액상소결은 반응의 큰 추전력과 온도에 따라 지수함수로 증가하는 확산속도 때문에 자발 적으로 재빨리 일어난다. 단순 입방정계인 f]-S iC 분말 (a=4.360A) 과 육방정계인 Ti B2 매 트릭스 (a=3 . 031A, c=3.234A) 의 격자상수들은 Ti B2 -SiC 복합 세 라믹스 콤팩트 제조 후에도 실험오차 범위내에서 거의 변화가 없었고 그 상들도 보존되어 있었다. 그러나 X- 선 스펙트라에서 1% 미만의 피크 세기의 T iB가 존재함을 확인하였다. 그림 8.21 에서 보는 바와같이 그 복합 세라믹스의 체적밀도는 SiC 의 함량이 증가함에 따라 감소하였다. 이것은 S i C 의 밀도가 작기 때 문이고 계산한 이론체적밀도와 같은 경향으로 감소한 것을 알 수 있 으며 상대밀도는 이론밀도의 92~94% 범위에서 변하였다. 그림 8.22 에서 보는 바와같이 SiC 함량이 증가함에 따라 Vic k ers 경도값은 감
소함을 나타내었다. 그렇지만 그림 8 . 23 에서 보는 바와같이 파괴인성 (K 리값은 SiC 함량에 따라 3.8~4.1MN/ m 312 범위에서 변하였다.
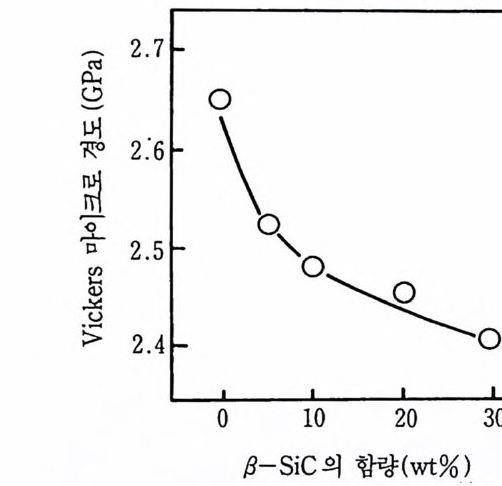 2.7 t-
2.7 t-
그림 B-22 SiC 함량의 함수로서 Ti B2 -S iC 복합체의 Vic k ers 마이크로 경도.
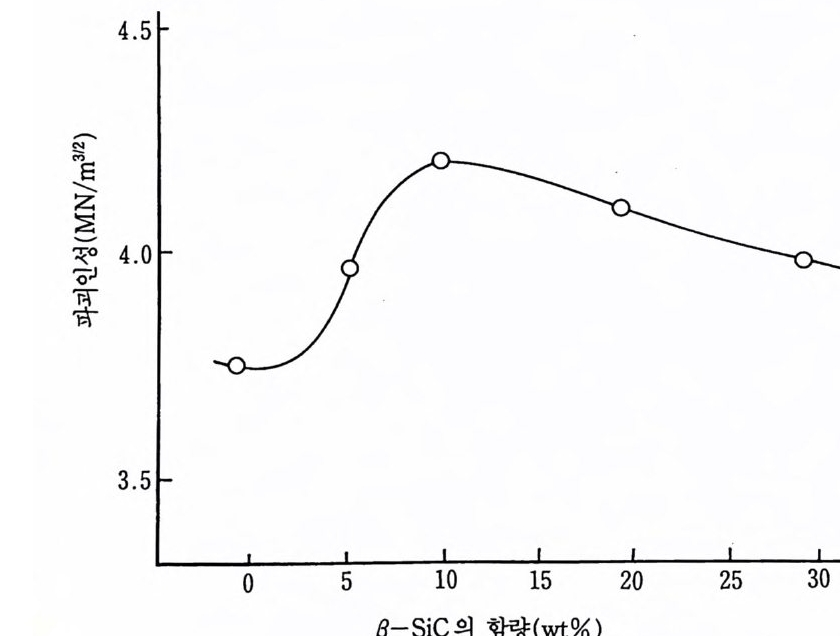 4.5
4.5
그림 8-23 SiC 함량의 함수로서 TiB 2 -SiC 복합체의 파괴인성.

그림 8.24 TiB2 -SiC (lOwt%) 복합체에 대한 파열 표면의 SEM 마이크로 그래프.
순수한 TiB 2 매트릭스의 경우보다 모두 큰 K,c 값을 보이며 SiC 함량 이 10w t% 근처에서 최대값을 나타내었다. 파괴인성 120) 이 크면 클수 록 부서 점 성 (b ritt leness) 은 더욱 더 낮으며 내 화성 세 라믹스로서 TiB 2 매트릭스의 주된 단점에 해당하는 부서짐성을 복합세라믹스를 제조함으로써 감소시킬 수가 있다. 그 복합 세라믹스의 갈라진 금 (ind enta t io n crack) 은 모두 측면 (lat e r al) 과 방사형 (Palmq vist) 크랙 119) 임을 보였다. 그림 8.24 에서는 SiC lO wt%를 첨가한 TiB 2 -Si C 복합 세라믹스 콤팩트에 대한 파열 표면의 SEM 마이크로 그래프를 나타내는데 낱 알경계 의 파괴가 많이 나타난다. TiB 2 낱알은 SiC 첨가에 따라 미세 해지는 경향이 있으나 TiC 첨가시만큼 현저하지는 않았다. 8-4— 4 T iB 2-Ab03 콤팩트의 제조 소결된 산화알루미늄 또는 알루미나는 상품이나 공업적으로 대단히 유용하고 풍부하며 비교적 간단한 내화성 산화물이다. 원자 또는 이 온의 이동도에 의한 알루미나의 확산성은 소결된 알루미나를 제조하 는 과정을 이해하는 데 가장 중요한 사항이다. 알루미나의 역학적 성 질에 관한 많은 연구 121)~124) 가 수행 된 바 있다. Ti, B 및 a-Al203
분말 적정량을 혼합하여 HPCS 공정으로 Ti B2 -Al203 복합 세라믹스 콤팩트를 제조하는 것은 상당한 가치가 있다. Ti B2 -TiC 복합 세라 믹스 제조와 같은 방법으로 TiB 2 매트릭스에 5, 10, 20 및 30 wt%의 Al203 를 포함하는 TiB 2 -Al203 복합 세라믹스 콤팩트 125) 를 각각 제조 하였다. x- 선 회 절분석 결과는 육방정 계 의 T i B2 와 삼방정 계 의 Al203 상들 이 TiB 2 -Al i03 복합 세라믹스에서 보존됨을 보였다. 각 복합체 콤팩 트에서 TiB 2 매트릭스의 격자상수도 실험오차 범위에서 일정하였고 1.0% 미만의 TiB 상을 확인하였다. 그림 8.25 에서 보는 바와같이 체 적밀도는 a-Al i03 함량이 증가함에 따라 4 . 29 에서 4 .10 g /cm3 으로 감소하였다. 그렇지만 그 콤팩트들의 상대밀도는 이론밀도의 약 95%
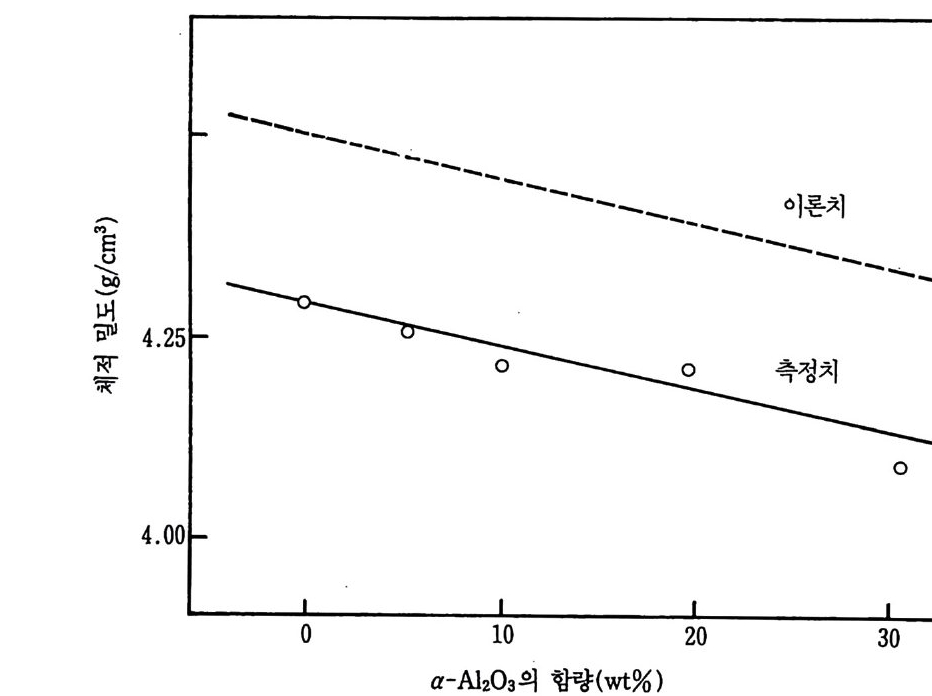 \p-버~T-ll 4.25 ------ - --- - -- -- - -- -- ----- - -이-론 -치- - ---
\p-버~T-ll 4.25 ------ - --- - -- -- - -- -- ----- - -이-론 -치- - ---
그립 8-25 a-Al203 함량의 함수로서 TiB 2 -Al203 복합 세라믹스 콤팩트의 체적 밀도.
였다. a-Al203 함량 증가에 따른 이론 및 측정밀도는 갇은 비율로 감소하는 것으로 보아 첨가한 a-Al203 의 낮은 밀도에 기인하고 TiB 2 매트릭스와 a-Al203 첨 가제 간에 어 떤 수축도 없음을 나타낸 다. 그 결과는 그 복합 세라믹스들에서 TiB 2 매트릭스의 격자 체적 이 일정한 것과도 일치된다. 그림 8 . 26 에서와 갇이 Vi ck ers 마이크로 경도 (Hv) 는 a-Al203 함
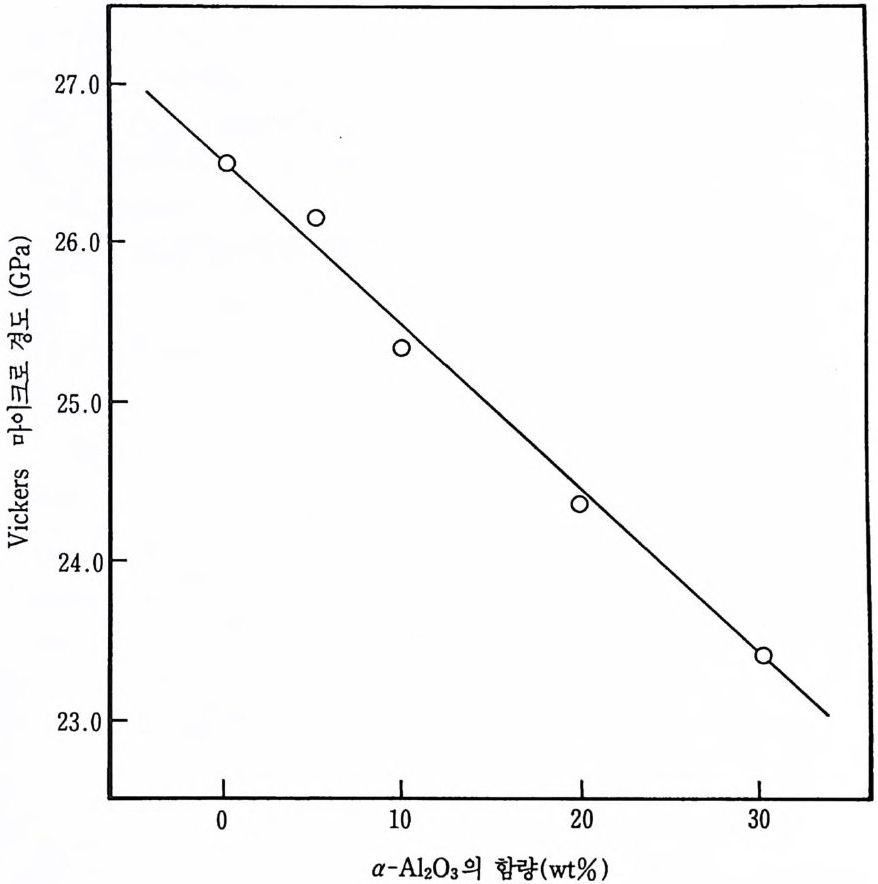 27. 0
27. 0
그립 8.26 a-Al203 함량의 함수로서 TiB 2 -Al203 복합 세라믹스 콤팩트의 Vic k ers 마이크로 경도.
량이 증가함에 따라 26.5 에서 24.0GPa 로 감소되었다. 그러나 그립 8 . 27 에 서 와 같이 파괴 인성 (K,c) 은 a-Al203 함량에 따라 증가하여 10~20w t%의 a-Al203 함량에서 최대값 4.2(3)MN/m312 을 보이고 다시 감소하였다. 이들 결과는 a-Al203 의 첨가 때문에 반응열의 희 석 또는 생성물 희석 (pr oduct dilu ti on) 이 T iB 2 의 낱알 생성을 조절하 는 데 영향을 주지만 낱알둘의 결합을 강화시킴을 나타낸다. 그러나 30w t% a-Al2°3 함량에서 파괴인성의 감소는 생성물 희석 때문에 단 열온도의 강하로 연소반응중 액상의 결핍이 빠른 소결 메커니즘을 방 해하는 것으로 볼 수 있다. 이러한 사실은 T iB 2-T i C 계 117) 와 유사하 게 TiB 2 -Al203 복합 세 라믹스의 SEM 마이크로 그래프의 조사로 확 인할 수 있었다. T iB 2 의 매트릭스보다 높은 파괴안성을 갖는 TiB 2
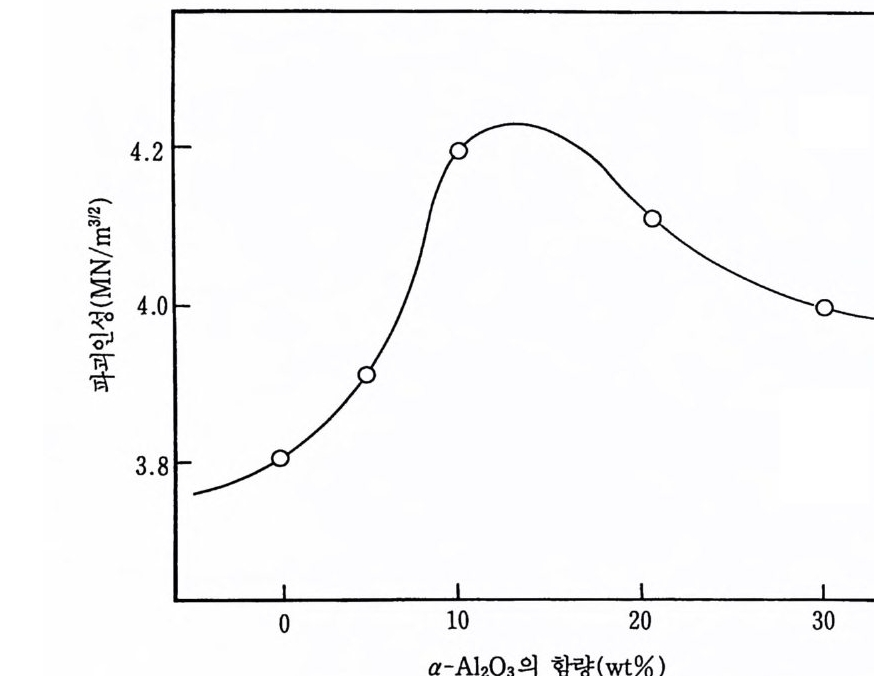 :룹 4 4..20 t - I ~Q
:룹 4 4..20 t - I ~Q
그립 8.2 7 a-Al203 함량의 함수로서 TiB z-A l203 복합 세라믹스 콤팩트의 파괴 인성.
-Al 요 복합 세라믹스 콤팩트의 제조는 Ti B2 콤팩트의 주결점인 부 서점성을 감소시킨 고성능 복합 세라믹스 재료를 얻을 수 있게 한다. 8— 5 HPCS 공정의 응용 8— 5— 1 응용 범위 이 새로 개발된 HPCS 공정의 응용은 소결된 정밀 세라믹스의 생 산뿐만 아니라 고압하에서 높은 발열반웅열을 사용함으로써 다음에 열거하는 광범위한 분야에도 기대될 수 있다• i ) 고압과 3000K 의 고온에서 새로운 재료(신소재)의 합성. ii) 새로운 고용체와 금속간 화합물의 합성. iiW 초 전도 재료의 생산. iv) 복합재료 및 서벳의 생산. v) 세라믹스코팅 및 세라믹스-금속과세라믹스-세라믹스계의용집. 이들 HPCS 의 광범위한 응용에서 세라믹스-금속 또는 세라믹스-세 라믹스 용접은 세라믹스 성분을 실제 장치에 조립하기 위하여 특별한 공학적 응용에 중요한 의미를 갖는다. 그러므로 가압 연소용접 (pre ssuriz e d combustio n weldi ng ) 이 라고 부르는 새로운 용접공정 만을 다음 소단원에서 설명하고자 한다. 8— 5— 2 가 압 연소용접 세라믹스를 금속에 용접하는 새로운 방법은 가압 연소반웅 30),103) 을 적용하여 개발되었다. Mo-T iB 2-Mo 와 Mo-T i C-Mo 의 두 가지 용집 된 쌍둘은 3GPa 압력하에서 Mo 원반(di sk) 사이에 T i와 B 또는 C 의
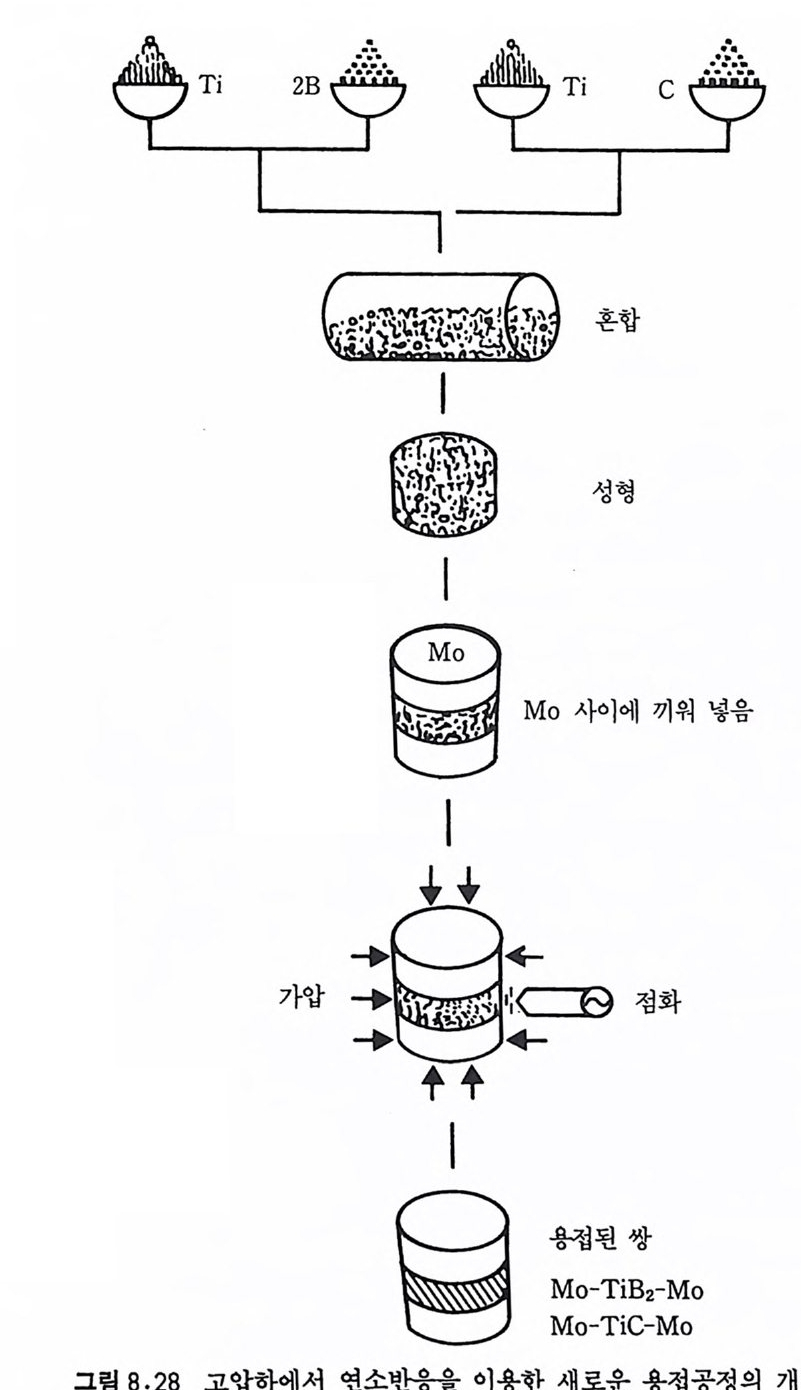 Ti 2B Ti C ...... ...... . . - ·
Ti 2B Ti C ...... ...... . . - ·
분말 혼합물들을 넣고 전기점화로 제조하였다. 그 연소반웅의 결과로 그 혼합반응물들은 각각 소결된 T iB 2 와 T i C 로 변하였고 그 연소의 높은 발열반웅열로 세라믹스와 금속간의 화학반응이 일어나고 그들을 용접시켰다. 그 새로운 용접공정은 그림 8.28 에서 보는 바와 같고 이 와 유사한 공정 은 테 르밋 용접 (the rmi te weldin g ) 으로 Al 과 Fe203 분 말 혼합물들의 발열반응을 이용한 것이다.
고압하에서 강한 발열반응으로 대단히 짧은 시간에 그들 조성원소 둘로부터 붕소화물 또는 탄화물 세라믹스들을 합성과 동시에 소결하 는 데 HPCS 가 사용된 것이다. 그 가압 연소반응은 소결을 위해서뿐 만 아니라 세라믹스의 용집에도 이용성이 기대된다. 내 화성 금속인 Mo 는 금속성분으로 사용되 었고 T iB 2 와 T i C 는 세 라믹스 성분으로 선택된 것이다. 이들 세라믹스들은 각각 -293 과 -232k J /mol 의 높은 표준생성 엔탈피 (~HJ) 때문에 연소반웅으로써 쉽게 생성된다. 계산된 단열온도 (Tad) 는 두 세라믹스 118) 에 대하여 약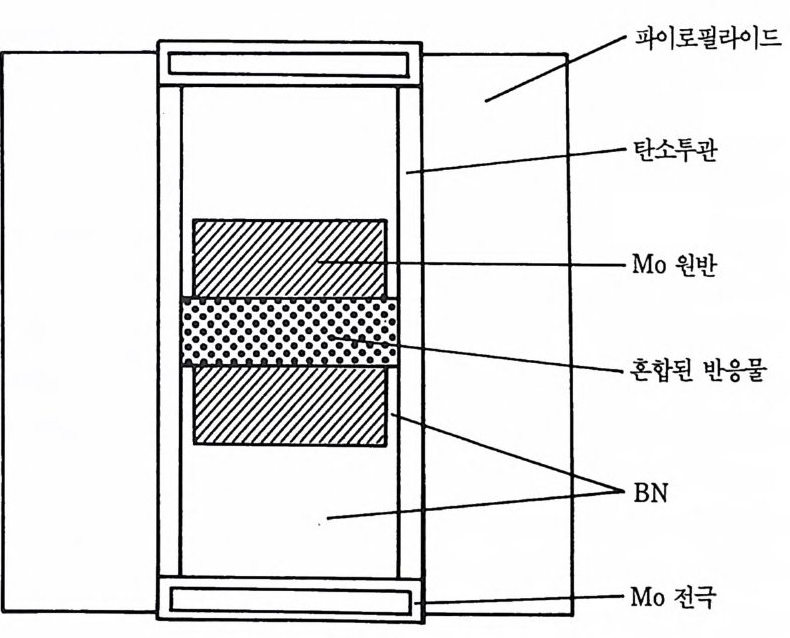 파이로필라이드
파이로필라이드
그림 8,29 가압연소용집에 사용된 고압 셀 장치.
2900°C 이며 이는 Mo 을 녹일 수 있는 온도이다. TiB 2 또는 T i C 와 Mo 사이의 열팽창계수 126) 는 상온에서 2ooo·c 까지 두 경우 모두 2X 10-GK-1 이 하였다. 40µm 이하의 입자 크기인 미세한 Ti 분말과 무정형 붕소 또는 무 정형 탄소를 각각 화학양론적인 몰비로 잘 혼합한다. 잘 혼합된 분말 들은 지름이 5.8mm 이고 두께가 2mm 인 얇은 원반으로 압축 성형하 여 크기가 5X2.5mm 인 두 Mo 원반 사이에 직접 끼워넣는다. Mo 과 이 끼워진 장치는 장력시험을 실시하여 용접강도를 평가하는 데 유용 하다. 용집을 위한 부분품들은 그립 8.29 에서 보는 바와같이 반응 셀 내에 넣어 고정시킨다. 전기절연체인 BN 투관은 Mo 원반과 점화를 위한 원통형 탄소 히터 사이에 배치하여 단지 혼합된 반응물만 탄소 히터와 접촉하도록 하였다. 시료는 입방모루 장치 (cub i c anvil devic e) 66) 에 의 하여 3GPa 까지 압력 을 가하고 1. 5 kVA 로 l 또는 2 초 동안 탄소 히터에 전류를 통하여 바깥둘레의 반응물이 점화되어 HPCS 법의 메커니즘에 따라 용접이 완료된다. 8— 5— 3 용 접 생성물의 특성 용집된 쌍인 Mo-TiB 2 -Mo 단면의 SEM 마이크로 그래프는 그림 8.30 에서 보는 바와같이 용접이 찰 일어난다. T i와 B 의 혼합물이 화학양론적 T iB 2 로 변환된 것은 X- 선 회절분 석을 통하여 알 수 있었다. 그 TiB 2 세라믹스는 기공과 균열(p ores andcrack) 이 거의 없이 5µm 의 평균 크기를 갖는 미세한 낱알로 이 루어진 고밀도체였다. T iB 2 와 두 Mo 원반간의 위와 아래 계면에서 반응영역이 형성되었는데, 이것은 각각 80 과 170µm 정도로 확장되 어 있었다. 그 주생성물은 X~ 선 회절분석으로 Mo2B 상으로 확인되 었다. 그 반웅영역과 그 영역에 원소 분포는 그림 8.31 에서 보는 바 와같다.
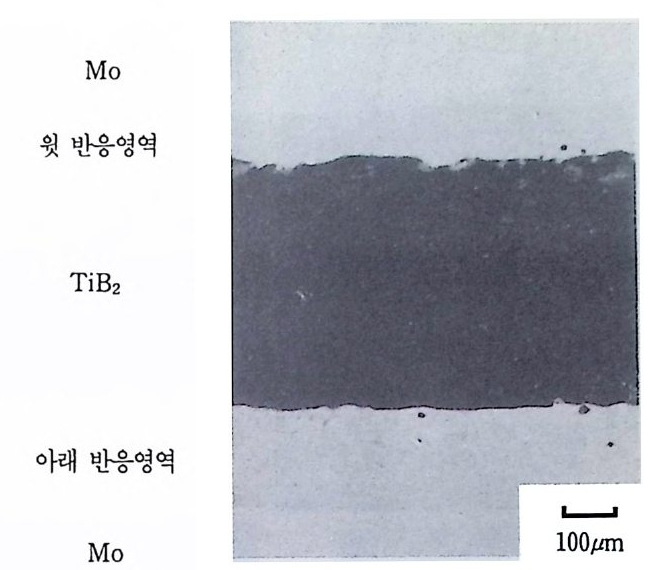 Mo
Mo
그림 8.30 Mo- Ti B 2 -M o 용집된 쌍 단면의 SEM 마이크로 그래프•
여 러 개 의 Mo- T iB 2 -Mo 쌍의 장력시 험으로 구한 용접 강도는 20~40MPa 범위였다. 그 상들은 Mo 과 반응영역 경계 또는 Mo 에 가 까운 반응영역에서 파열되었다. Mo-TiC -Mo 쌍의 경우에도 T i과 C 의 혼합물은 소결된 T i C 로 변 환되었고 Mo 와 용접되었다. 소결된 T i C 는 평균 15µm 인 큰 낱알을 갖는 다공체 (po rous body) 였으나 크랙은 관찰되 지 않았다. T i C 와 Mo 사이의 위아래 계면에는 각각 70~160µm 의 반응영역이 확장되 어 있었다. x- 선 회절과 전자탐침 마이크로 분석 (electr on pro be mic ro analys i s) 을 통하여 주된 반응상은 T i를 약간 녹인 Mo2C 인 것 을 나타내었다. 나뭇가지 모양의 마이크로 결정들의 침전과 판상직물 (lam ella tex tu re ) 이 그립 8 . 32 에 서 보는 바와같이 각각 아래 위 반응영 역에서 관찰된다. 그 나뭇가지 모양의 결정은 확인되지는 않았으나 전자람침 마이크로 분석 (EPMA) 으로부터 Mo 과 T i울 포함하는 탄화 물인 것으로 추리할 수 있다. 그 판상구조(l amella s tru c tur e) 의 조성 변이는 현재로서는 불명료하다. Mo-T iB 2-Mo 쌍과 유사하게 아래
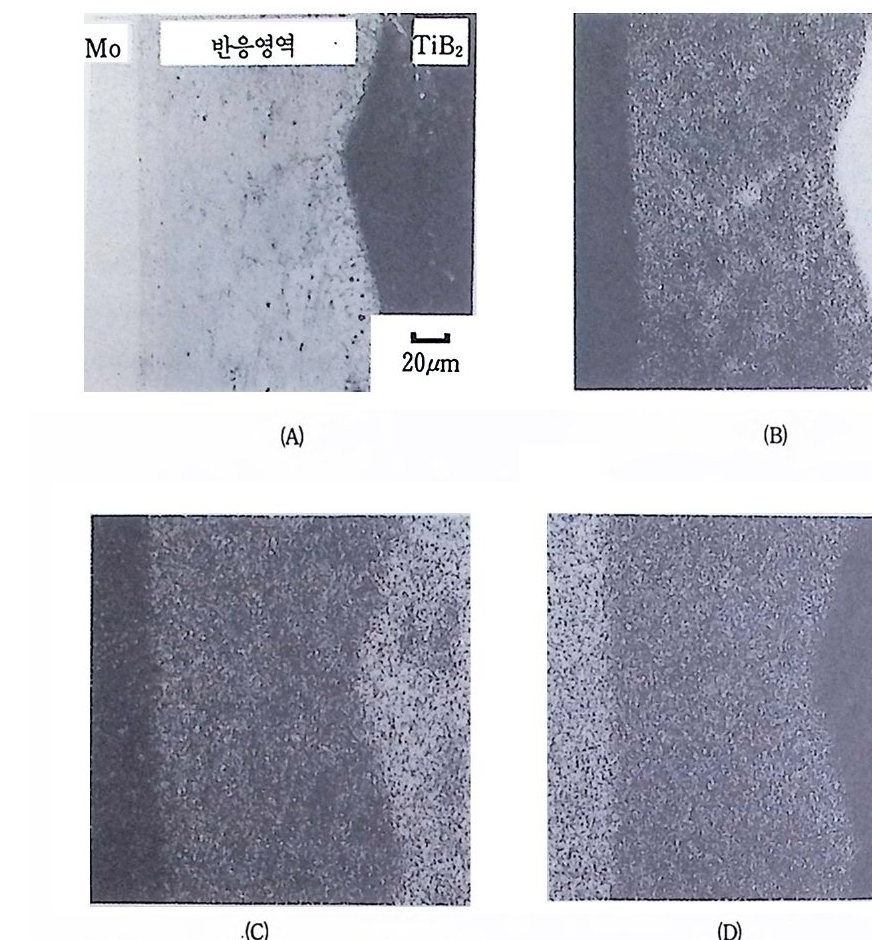 Mo
Mo
그림 8-31 TiB 2 ~ Mo 사이의 반웅영역 SEM 마이크로 그래프 (A) 와 붕소 (B), 티탄 (C) 및 Mo(D) 에 대한 원소분포의 X- 선상•
반웅영역의 더 두꺼운 폭과 결정의 침전은 현 시료장치에서는 용집부 의 바닥에 반응열이 축적되려는 경향이 있다는 것을 제시한다. Mo -TiC - Mo 쌍의 장력 (ten sile s tre n g th) 은 평 균 lOMPa 이 었고 파열은 다 공성 T i C 체에서 일어난다. 가압연소반응에 의한 용접은 점화를 위하여 단지 국부열을 사용하 므로 재빨리 수행된 것이 주목된다. 낮은 압력에서 용접하거나 강한
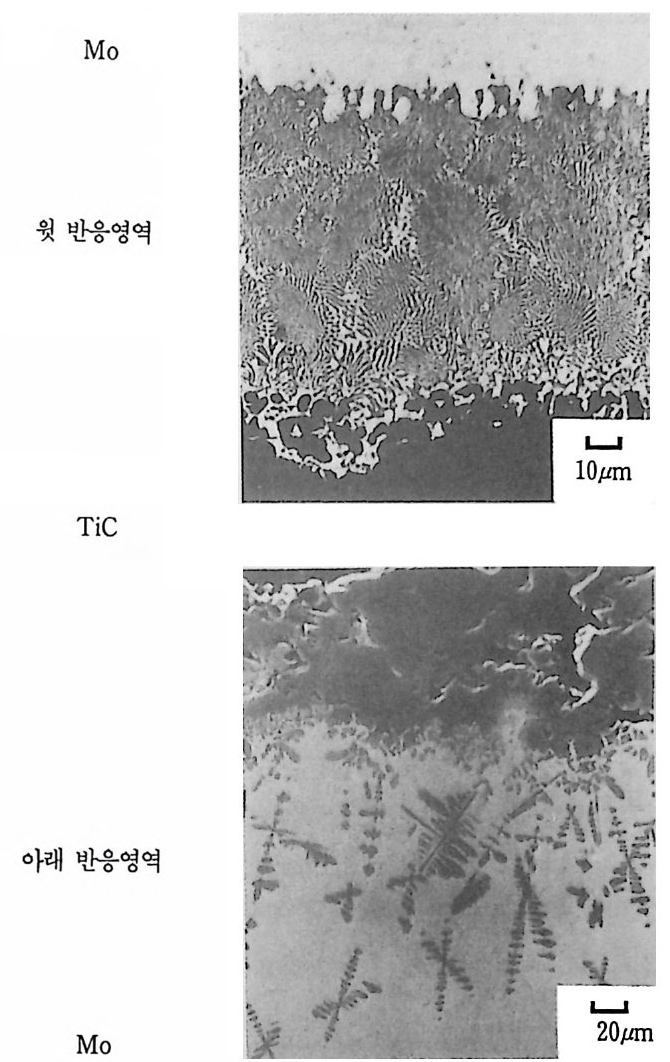 Mo
Mo
그립 8.32 Mo-TiC - Mo 쌍의 반응영역의 SEM 마이크로 그래프. 〈판상직조와 나뭇가지 모양 마이크로 결정의 다른 구조들이 각각 위 와 아래 반웅영역에서 나타난다.〉
결합제로 작용하는 효과적인 반응물들은 실제 사용에 폭넓은 응용을 위하여 더욱더 그 개발이 필요하다. 그러나 현재 이 방법은 세라믹스
-금속연결, 세라믹스-세라믹스 연결 및 세라믹스 도금을 위하여 새로 운 가능성을 갖는 것으로 믿어진다. Mo 에 T i C 와 T iB려 두터운 도 금은 핵융합로 (fusi o n reacto r ) 의 첫 번째 벽 의 건설에 유용하다. 8-6 새로운 가압 연소소결법 8— 6— 1 기체 압력 연소소결 연소소결을 개발하기 위하여 단순공정으로 고밀도 재료를 형성하는 효과적이고 경제적인 가압법이 고안되었다. 단축압, 등방압 및 충격 파압을 사용한 여러 가지 장치들이 많은 연구자들 127) 에 의하여 활용 되거나 시험되어 왔다. 그림 8 . 33 은 기 체 압력 연소소결 (ga s-pr e ssure combusti on sin t e r - i n g )12s) 법을 설명한 것이다. 이와같이 연소반응물을 포함하는 원료는 가압성형하여 HIP 의 유리 캡슐에 넣는 것과 똑같이 붕소규소화 유리 (borosili c a te gla ss) 용기 에 넣고 진공봉함 (vacuum sealin g ) 울 한다. 그 시료는 탄소도가니에 있는 연소제 속에 넣고 고압용기에 장치한다. 그 시료체와 유리용기는 그것을 보호하기 위하여 BN 분말로 덮는다. 연소제로는 많은 열을 방출할 수 있는 혼합분말이 사용된다. 많은 종류의 연소제가 쓰일 수 있고 그들은 세라믹스 분말로 변할 수 있 다. 이 경우는 약 3ooo·c 의 고온을 낼 수 있는 T i과 C 의 혼합분말이 사용되었다. 압력용기의 내부에는 유리용기가 유연하게 되도록 700°C 로 예열하고 Ar 기체압울 보통 lOOMPa 이하로 가한다. 점화 히터를 사용하여 3 초 동안 죽시 가열로 연소제가 타기 때문에 그 반응물이 점화되고 수분내에 고밀도 생성물로 변한다. 그 연소제는 높은 열을 공급하는 화학로 (che mi cal fu rnace) 로 작용하였고 반응물의 반응을 완 결시킬 수 있다.
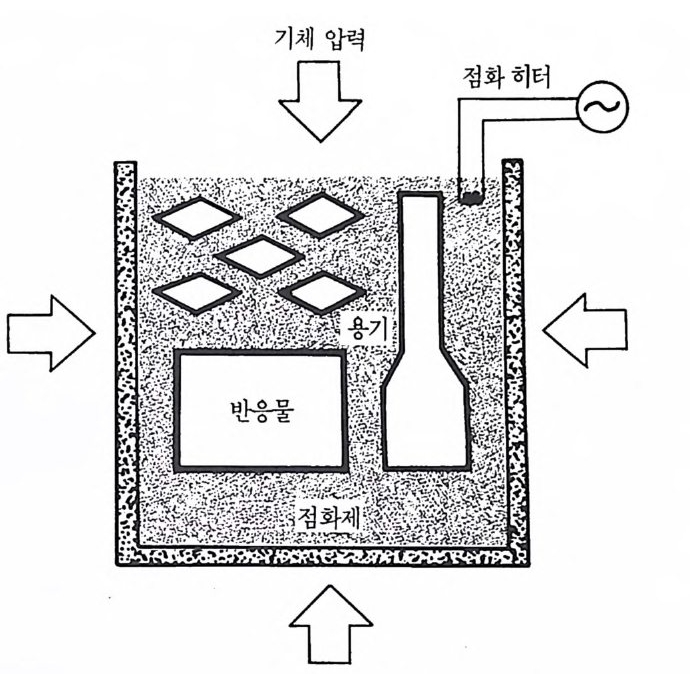 〔
〔
그림 8.33 기체압력 연소소결법의 개요도.
거의 완전한 고밀도 세라믹스인 TiB 2 및 T i C 와 TiC -Al203, TiB 2 -Ni 및 T i C-N i의 복합체 들이 이 기 체 압력 연소 소결로 lOOMPa 의 압력에서 얻어졌다. 실험실적 제품시료의 크기는 지름 또는 길이가 30mm 로 제한되어 있지만 등방기체압과 연소제의 사용은 유사그물형 (near-net shape ) 성분의 대 량생 산이 가능할 것 이 다. 종래 소결로 만 둘기 곤란한 유일한 재료가 이 새로운 소결공정으로 제조될 수가 있 다. 이 목적을 위하여 마이크로 구조와 빠르고 높은 온도반응을 조절 해야만 한다. 그 대상 재료들은 세라믹스-세라믹스 및 세라믹스-금속계들에서 세 라믹스 매트릭스의 복합체들이다. 일반적으로 복합 세라믹스는 균일 하게 혼합된 구조이다. 최근에는 기능적 기울기 재료 (Func ti onall y Gradie n t Mate r ia l s 또는 FGM) l29) 라고 부르는 불균일 구조를 갖는 새
로운 복합체들에 관십이 끌리고 있다. 세라믹스 매트릭스 내에 금속 상의 체적분율이 계속 증가하여 최종적으로 한쪽은 금속바탕을 이루 며 다른 한쪽에는 내화성 세라믹스 표면충으로 이루어전 마이크로 구 조를 가지고 있는 것이 FGM 이다. 그들은 낮은 내부열 스트레스와 좋은 파괴인성을 갖는 독특한 고온재료로 초음속 항공우주선에 사용 이 기대된다. 연소소결은 빠른 연소파 전파 때문에 원소확산이 제한되어 FGM 의 성분배열을 유지할 수 있다. Ti C -Ni 계의 경우에 T i +C 를 N i와 균 일하게 혼합한 반웅물은 T i C 와 Ni 상으로 된 생성물로 변환되며 그 들의 밀도는 여러 가지 Ni 함량에 대하여 이론밀도의 98% 를 넘는 다. 이들 복합체의 Vi ck ers 마이크로 경도는 그림 8.34 에서 보는 바 와 같다• 그 경도곡선의 기울기는 30~40wt% N i에서 변하여 그 조 성범위 안에서 매트릭스 상이 T i C 에서 N i로 변한 것을 나타내는 것 같다. 자국법 (ind enta t i on meth o d) 으로 구한 파괴 인 성 (frac tu r e tou g h-
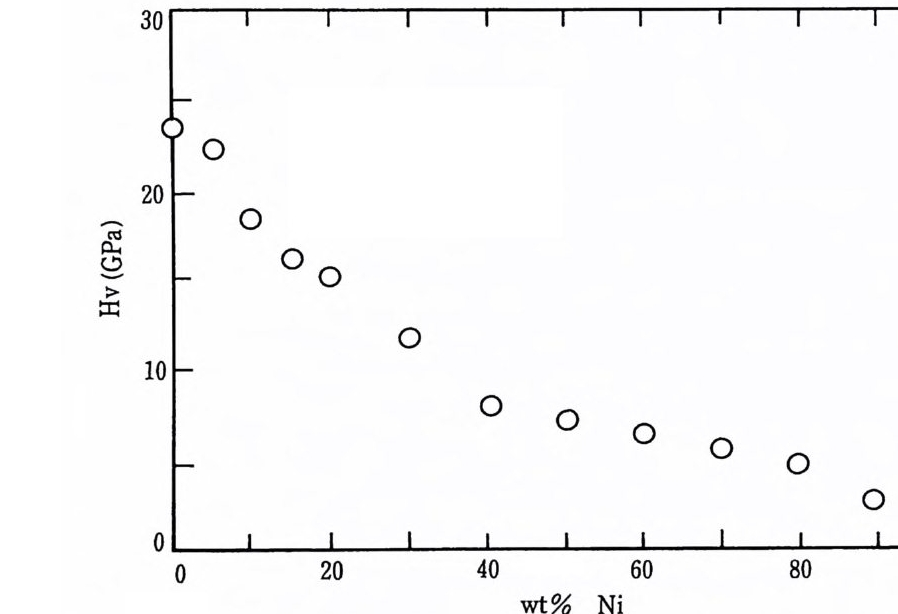 g2 0t 。
g2 0t 。
그림 8.34 Ni 함량의 함수로서 TiC - Ni 복합체의 Vic k ers 마이크로 경도.
 Ti + C Ti + C+5wt % Ni Ti+ C+10w t% Ni
Ti + C Ti + C+5wt % Ni Ti+ C+10w t% Ni
그립 8-35 Ni 조성의 변화에 따른 TiC +Ni 복합체의 마이크로 구조에 대한 SEM 뻔크로그래프
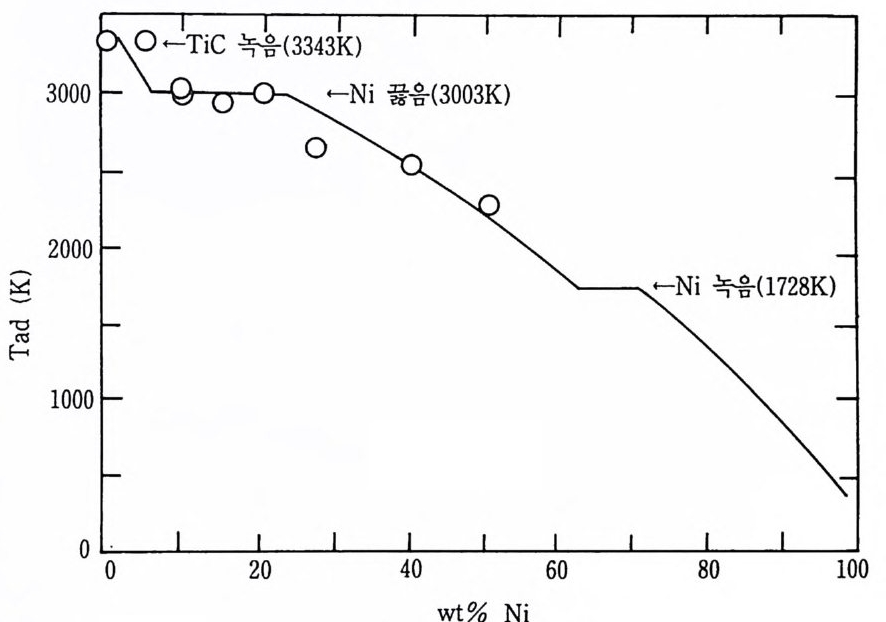 3000 +-Ni 끓음 (3003K)
3000 +-Ni 끓음 (3003K)
그림 8.36 N i를 첨가하여 T i C 생성시 연소온도의 변화. 〈실선과 원은 각각 열역학적으로 계산한 온도와 측정한 온도를 나타 낸다.〉
ness) 은 N i의 함량이 0 과 30w t% 사이에서 3.6 에서 17MPa • m112 로 현저 한 증가를 보였고 휨 강도 (flex ural str e ng th) 는 Ti C -10wt % Ni 복 합체에 대하여 580MPa 이었다. 그림 8.35 는 T i C 와 TiC - Ni 복합체 파열표면의 SEM 상을 보여준
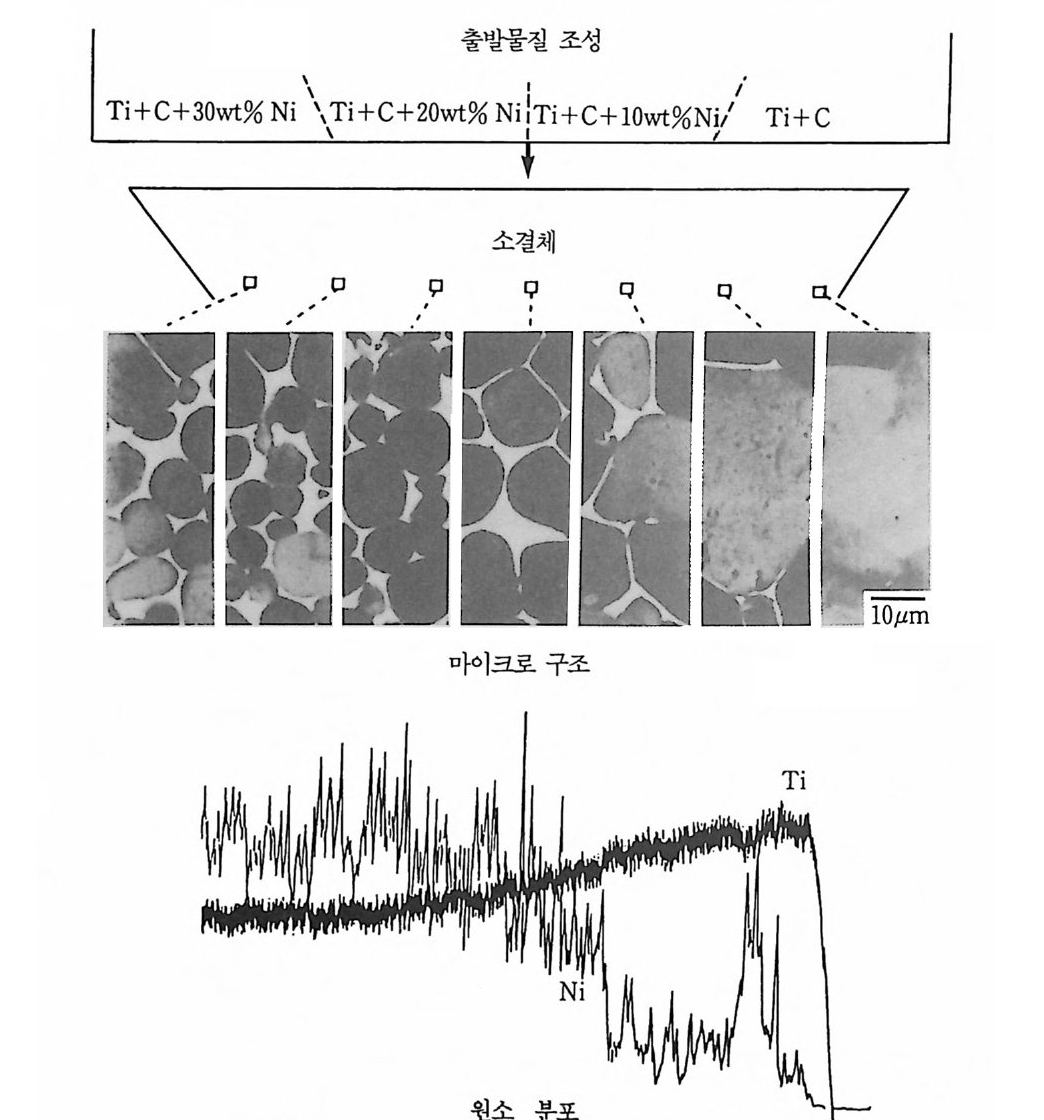 출발물질 조성
출발물질 조성
그림 8-37 TiC -Ni 계의 기능적 기울기 재료 (FGM) 의 구조와 원소분포.
다. Ni 함량이 증가함에 따라서 반응열이 감소하기 때문에 Ti C 낱 알이 미세해진다. Ar 기체압력하에서 TiC 연소합성 중 Ni 함량의 함수로서의 반응온도는 그림 8.36 에서 보는 바와 같다. 실선은 열역 학적으로 계산된 단열 연소온도 (Tad) 를 나타내고 열린 원은 광학고 온 온도계를 사용하여 측정한 온도이다. 그들의 좋은 일치는 연소반 응이 거의 단열상태에서 전파된다는 것을 의미한다. 결과적으로 예열 조건하에서 계산한 연소온도는 마이크로 구조를 조절하기 위한 상대 파라미터로 사용될 수 있다. T i C-N i계의 FGM 구조는 2그 림 8 . 37 에서 보는 바와 같다. T i와 C 에 0, 10, 20 및 30w t%의 Ni 함량을 갖는 네 가지 혼합분말층들이 소결전 본체로 단순히 적충되어 있다. 소결체는 약 15% 수축되며 낱 알경계와 삼중점들은 점차적으로 Ni 금속으로 채워지며 팽창된다. 이에 반해서 TiC 낱알둘은 작아지며 고립되다가 그 매트릭스는 TiC 에서 점차적으로 Ni 상으로 변한다. 그 시편을 통해 Ti C 낱알을 갇 은 크기로 조절하기 위하여 각 충에서 단열온도 (Tad) 를 일정하게 유 지하도록 TiC 분말을 첨가하는 것이 유용하다. 이들은 FGM 을 만들 기 위한 예비결과이다. Ti B2 -Ni 및 MoS i 2-T i Al 과 같은 다른 재료계들도 또한 연구되고 있다. 그들의 조성변화는 2000K 의 표면온도 및 열적응력(th ermal s tr ess) 과 열전도 129) 의 컴퓨터 모델화에 의한 lOOOK 의 FGM 을 통한 온도변화를 찰 견디는 데 활용되고 있다. 그 합성반응과 동시에 고밀 도화를 일으키기 때문에 유일한 마이크로 구조를 갖는 많은 다른 세 라믹스 복합체 (ceram ic com p os it es) 들도 제조될 것으로 기대된다. 8— 6— 2 질화 연소소결 표 8.9 에 수록된 바와같이 질화물 세라믹스 분말들은 가압된 질소 기체와 금속분말의 질화연소로 합성할 수 있다. 반응물들은 다공성
표 8.9 비기체 연소로 생산할 수 있는 고급 세라믹스, 합금 및 복합체. Ti C, Ta C, Hf C, Si C, B,C Ti B2, Zr B2 세라믹스 Si3 N , , A l N, SiA ION, BN, TiN , TaN, NbN M0Si2 , Ti Si2 M0S2, M0Se2, Cd S 합금 Ti Ni, T i Al, Ni Al, C oAI 3Ti0 z +4Al+3C -+ 3Ti C+ 2 Ab03 Ti 02 +Zr+C --+ Ti C+Zr 02 복합체 3Si0 z +4Al+3C -+ 3Si C+2A'2 0 a Si 0 2 +2M g + C -> Si C+2Mg 0 2Ti+ 2B+C --+ Ti C+Ti B2 탄소용기에 채우고 1~lOMPa 의 질소압력하에서 점화한다. 그 공정 중에는 오염은 거의 일어나지 않는다. 높은 품질의 질화물을 합성하 기 위하여 원료 금속분말에 적당량의 생성물상 분말을 첨가하는 것이 유용하다. 이것은 일반적으로 2300K 를 넘는 질화연소의 높은 반응열 울 희석하는 역할을 하고 불완전한 질화를 야기하는 녹은 금속입자들 의 엉김을 막는 주임물 역할도 한다. S i 3N4 분말은 증발된 규소와 질소의 반응 130) 에 의 하여 생 성 된다. 결 과적으로 그림 8 . 38 (A) 에서 보는 바와같이 입자 형 태 (morp h olog y) 는 질화 후에 완전히 변한다. S i와 C 의 혼합된 분말이 반응물로 사용될 때는 lOMPa 질소압력 하에서 49w t% S i C 까지 광범 위 한 조성 범 위를 갖는 S i 3N4 와 S i C 의 착물 (com p lex) 분말이 형성될 수 있다. 처음에 생긴 S i 3N4 는 그것의 반웅열에 의하여 . 증발되고 Si 증기는 탄소 131) 와 반응한다는 것을 반응분석으로 알 수 있다. 그들의 평균 입자 크기는 약 lµm 로 작은 편이다. 이들 분말들은 유리 캡슐에 넣고 HIP 으로 170MPa Ar 압력과 195o•c 에서 첨가제 없이 1 시간 동안 소결시켜 완 전히 고밀도화된다. HIP 소결된 Si3 N 4-SiC 복합체 의 파열표면에 대 한 SEM 상은 그립 8.39 에서 보는 바와 같다. 그들 복합체의 고온 내
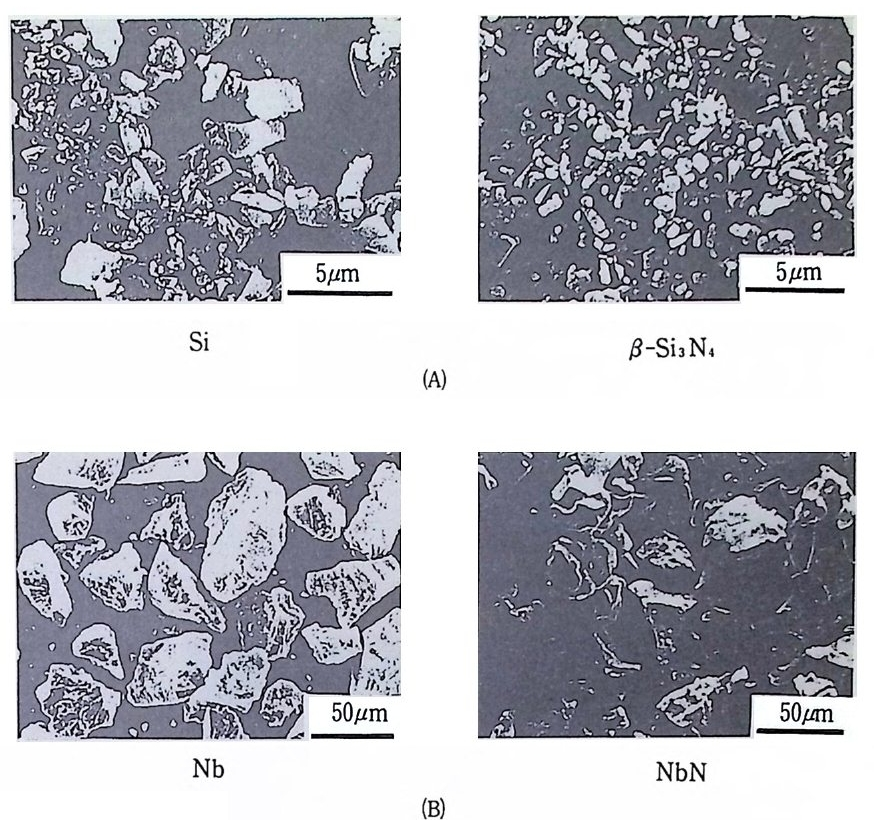 si /3- Si3 N ,
si /3- Si3 N ,
그림 8.38 출발금속 입자인 S i와 Nb 및 질화연소에 의하여 합성한 S i 3N4 와 NbN 의 SEM 마이크로 그래프.
구력은 SiC 함량의 증가에 따라 개선되었다 .132) 그림 8 . 40 은 Si3 N 4-3SiC 복합체의 TEM 마이크로 구조를 보여주 는데 그 구조는 [3- S~3N4, [3- SiC 및 작은 양의 Si2 N 20 상으로 되어 있다. 원료분말에 포함된 산소불순물은 Si2 N 20 상을 형성하는 것 같 다. 최초에는 S i C 로 도금되거나 S i C 를 포함하는 Si3 N 4 같은 유일한 입자들이 형성될 것으로 기대하였지만 각 상의 입자들은 그 소결체내 에 균일하게 분산되어 있었다. 그럼에도 불구하고 이 질화연소공정은 재료의 합성과 착물형성이 동시에 순간적으로 일어나기 때문에 그러
 3l 서 4
3l 서 4
 브 峯 S 述 +3S i C
브 峯 S 述 +3S i C
그림 8.39 Si3 N ,-SiC 복합체 들 의 파열표면에 대한 SEM 마이크로 그래프.
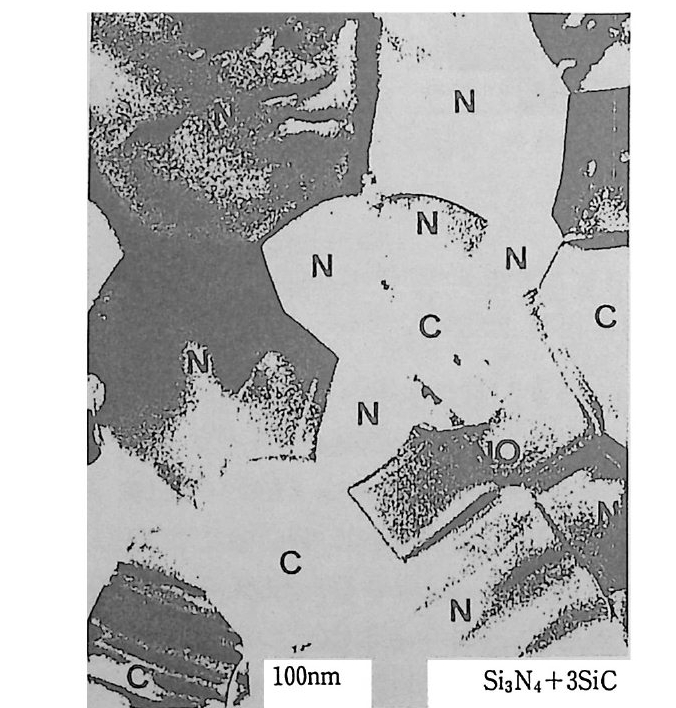 N
N
그림 8-40 SbN. -3 SiC 복합체의 TEM 마이크로 그래프.
한 유일한 세라믹스 분말들을 생산하는 가능성을 가지고 있다. NbN 과 TiN 갇은 전이금속 질화물들의 경우에 질화물 생성온 133) 그 금속으로 질소를 확산시킴으로써 얻어진다. 그러므로 그 입자 형 태는 그림 8 . 38(B) 에서 보는 바와같이 변하지 않는다. 이 결과는 연 소질화로 전이금속 성분울 질화 세라믹스 성분으로 변환시킬 수 있다 는 한 아이디어에 이르도록 한다. 예를 들면 Nb 금속판을 그림 8.4 1 에서 보인 바와 같이 Nb+NbN 금속분말의 연소제 속에 끼워 넣고
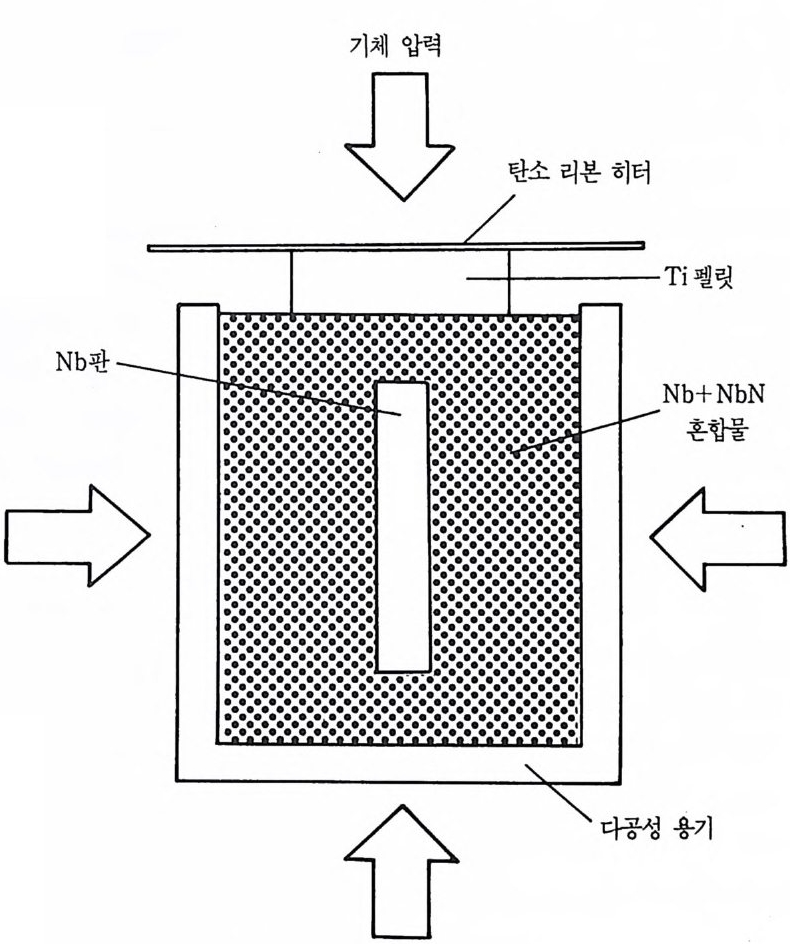 冒
冒
그림 8,41 금속 질화연소의 개요도.
 . ,
. ,
그림 8.42 Nb 금속의 질화연소로 만든 NbN-Nb 시료들의 모양.
3MPa 이상의 질소압력에서 그 연소제가 연소할 때는, 그 연소제의 반응열 때문에 주로 질화 (n itridi n g)가 일어나서 그 금속판은 NbN 세 라믹스판으로 변환된다. Nb 금속은 두께가 100µm 이하로 얇울 때 그것은 완전히 질화되고 Bl 형을 갖는 NbN 판은 1, 2 분 내에 합성된 다. 두꺼운 Nb 금속에 대하여는 NbN 과 Nb2N 충은 표면에서 형성 된다. 이같은 새로운 질화공정으로 그림 8.42 에서 보는 바와같이 임 의의 형을 갖는 NbN 성분을 쉽게 생성할 수 있다. 그 Bl 형 NbN 은 평형에서 1300°C 이상의 고온형이다. 그러므로 그 고온형은 연소의 매우 빠른 전파에 의하여 급냉되는 것으로 134) 생 각된다. 그 Bl 상 NbN 은 한 초전도 재료로 알려져 있다. 그 NbN 선 의 측정된 초전도도 임계상수들은 Tc=16.5K, Hc=I2T 및 4.2K 와 7.5T 에서 le( 임계전류) >8X104A/cm2 이었다. 그 결과는 초전도 장치 롤 위하여 요구되는 임계값들을 만족한다. Ti N 세라믹스 성분도 이 간단한 공정으로 또한 생성된다. 이들 질화 세라믹스 성분들은 마모, 부식 및 열 등의 내성을 갖는 공업용 재료로 사용될 수 있다.
제 9 장 비기체 연소합성법의 전망 이 장에서 논하고자 하는 비기체 연소합성법의 전망에서는 광범위 한 기본적 연구개발과 응용개발 단계로 기술이전을 하기 위하여 비기 체 연소합성법에 관한 계획적 지침을 제공하는 것이다. 이 분야에서 선진 소련과 미국에서만 성취된 것, 그들 프로그램의 현재상태 및 그 둘의 명확한 장점과 약점을 나타냄으로써 그 목적을 달성하기 위해 연역적 추리 (deducti ve reason i n g)가 사용되었다. 이들 반영의 결과는 후에 계속될 연구개발 활동과 미국 프로그램의 방향에 대한 제안의 형태를 갖추게 된다. 앞에서 이미 설명한 사항들이 중복되는 것도 있 겠지만 이러한 미래의 전망을 살펴보는 것은 대단히 중요한 일이라고 생각된다. 이것은 미국의 입장에서 본 전망이지만 비기체 연소합성법 전체에 대한 전망으로 간주할 수 있다. 9 一 1 역사적 배경 비기체 연소합성법에 대한 소련의 연구는 이미 SPCI35) 에서 발표한 광범위한 출판물에서 보여주듯이 1960 년대말 이후의 기간에 특별한 연구개발 프로그램으로서 인식되었다. 이 프로그램을 관리하기 위하
여 설립된 소련 국립회의 소장은 최근 이 프로그램에 대한 간략한 역 사적 고찰 136) 을 소개하였다. 그 소장인 Merzhanov 박사는 프로그램 을 두 가지 상(p hase) 으로 나누어 그 특성을 설명하였다. 그 첫번째 는 분말상으로 1977 년경을 통하여 확장되었다. 두번째는 고급의 상으 로 이 상에서는 고밀도 고체형 생성물이 강조되었다. 분말상은 생성 물의 응용면에서 매우 성공적이었다. 연마제, 표면처리 페이스트 (po lis h in g pa ste ) 및 공구로 사용되는 Ti C 분말 단 하나의 생 성물을 소개한 결과로 바기체 연소합성법에 관한 전체 프로그램 개발바를 충 당하고도 남아 국가경제에 이바지했다고 Merzhanov 는 주장하였다. 이 분말상이 성공한 주요 원인은 그의 실험실에서 파일럿 규모(pil o t scale) 의 분말 생산설바를 제작한 것이었다. 이 역할은 그가 소비자 들에게 기술보다는 분말을 공급할 수 있게 하였다. Merzhanov 는 비기체 연소공정 이 고밀도 고체를 제조하는 데 효과 적으로 사용될 수 있다고 결론을 내렸지만, 기술적인 문제는 더욱 다 양하고 또한 복잡하기 때문에 고급의 상을 위해서는 다른 행정적 해 결방법이 필요하다고 결정하였다. 고밀도 생성물 생성방식은 그 자체 에 특성이 있는 공업개발 프로그램으로 응용할 만하며 이에 반해 분 말생산에서는 다른 생산재료들간에 고도의 기술교환이 가능하다고 그 는 명백히 느꼈다. 그는 프로그램의 고급상에 필요한 장치가 분말생 산의 경우보다 형태가 다양하고 고가임을 실감하였고, 비기체 연소반 응과 가압(p ress i n g)의 결합 및 그 반응에 따른 생성물질의 직접적인 주물화 (cas ti n g) 생성을 강조하였다. 프레스 다이 (pr ess die) 에서 반응 한 세라믹스와 서멧 (cerme t)의 절삭기 (cutt ing too l), 질소기체 가압하 에 반웅 생성된 질화물 및 이중충 파이프를 포함하는 주물 생성물의 세 가지 생성물군을 또한 강조하였다. 그는 고등교육청의 협조를 얻어 기술전달을 촉진하는 데도 주력하 였다. 고등교육청은 기본적인 원리와 개념적인 면에서 기술의 주사용 자를교육시키고 있다. 소련의 R & D 프로그램과 그 산업적 파급효과가 큰 반면에 미국
의 R & D 프로그램은 1981 년경 이래 비교적 새로운 것으로 인식단 계였으며 산업적 파급효과는 찾아볼 수 없었다. 그러나 SPC 가 관여 한 DARPA/ LL NL 프로그램의 리뷰 (rev i ew) 에 명시되고 최근 미국 요업학회의 전국회의에서 137) 열린 이 주제에 관한 기술분과에서 표출 된 관심으로 보아 미국에서 비기체 연소합성법의 관심은 급진적으로 고조되었다. 국립 정부연구실, 방위 센터, 대학 및 산업체로부터 온 대표들에 의해 그 분과에서 다섯 편의 논문이 발표되었다. 미국과 소 련 프로그램 사이의 또 다른 명백한 차이는 미국 프로그램의 경우는 초기 참여자들 사이에서 목표가 크게 확산된 점이다. 이 목표의 확산 이 아마 지금까지도 유리한 점이었고 , 어떤 응용성과 생산면에 대한 증가된 목표의 초점도 곧 보장될 것이다. 비기체 연소합성이 오늘날 하나의 기술로서 무엇을 제공하며 또한 공업적으로 그것을 수행하기 위하여 무엇이 필요한지에 대한 반성은 미래의 진로를 설정하는 데 큰 도움이 될 것이다. 그 공정은 값싼 공 정열원, 극도로 높은 공정온도, 빠른 공정가열과 냉각의 가능성 및 고유의 화학적 정제효과 등을 제공한다. 이들 각각의 기여는 대부분 재료공정 응용을 위하여 바람직한 것으로 여겨진다. 그러한 기술의 빠르고 효과적인 공업적 수행에 있어서 기본적인 장애는 공정 조절에 관한 지식의 결핍이다. 산업적인 공정들은 확실히 조절될 수 있어야 하기 때문이다. 소련 프로그램에서 초기에 계획한 방법은 연소기술면을 연구하면서 동시에 간단한 생성물형인 분말을 생성하는- 것이었다. 그 배경으로 그 생성물 형태인 고밀도 고체를 생산하기 위하여 개발된 공정에 대 한 소련의 계획된 방법은 극적으로 수정되었다. 미국 프로그램의 다 음 단계의 계획은 소련의 배경과 초기 미국의 R & D 활동의 두 가 지 도움을 받을 수 있었다;
9— 2 미래의 전망 미국의 산업공정으로써 비기체 연소합성법의 가치와 유용성을 결정 할 기술적 및 경제적 문제들은 궁극적으로 산업계에 의해 해결되어야 할 것이다. 그 공정에 있어서 기본적인 연소개념은 이제 이해되었고 실험실에서도 실증되었기 때문에 산업계 브리핑만이 적절한 것으로 보인다. 더욱이 그 브리핑은 다음 두 목적에 알맞도록 체계화될 수 있다. i ) 바기체 연소합성법의 이론과 미국 및 소련의 업적들울 산업화 하기 위하여 기술적인 배경을 제공하도록 한다. ii ) 이전의 적절한 경험과 미래의 R & D 프로그램 방향에 관한 산업 계로의 귀 환(fe ed back) 을 격 려 하도록 한다. 내화성 분말시료의 생산에 있어서 비기체 연소의 가능한 사용에 관 한 산업계의 브리핑은 이미 시기적으로 적절한 주제의 한 예이다. 그 브리핑은 한편으로는 LLNL 의 실험실 연구와 압력을 가하지 않고 응 집되어 골격을 이룬 생성물을 생성하는 경향을 강조하였고, 다론 한 편으로는 이미 합성되었던 분말 생성물의 산업적 이용에 관하여 소련 의 주장을 강조하였다. 만약 탄화티탄의 생성물이 이 브리핑에서 강 조되었다면 그 브리핑의 산업계 참석자는 논리적으로 티탄 스폰지, 티탄 분말 및 탄화물 분말의 생산자를 포함할 것이다. 산업계 참석자 들의 요구되는 귀환(f eed back) 은 공정능력과 경제적인 부각에 대한 상업적인 이윤의 표시가 될 것이다. 다음 기회에 적당하다고 여겨지는 또 다른 브리핑은 고밀도 고체의 내화성 물질들을 만들기 위한 가압과 비기체 연소합성법을 결합시키 는 것이다. 그 브리핑은 LLNL 의 연구사업 세목, 소련의 경험을 논 의하는 것 및 호주에서 실행한 또 다른 실험을 81),82) 포함할 수 있다. 이들 응용은 아마 분말생산보다는 더욱 전문화된 것이다. 소련의 계 획된 방법과 같이 개별적인 양식의 R & D 프로그램이 각 생성물에
대하여 수행되어야 한다. 그러므로 산업계의 참여자들 중에는 접합된 탄화물 도구의 생산자둘(서멧의 합성자들), 엔진의 세라믹스 성분생산 에 관심있는 자들 및 알루미늄 정제시 사용되는 용융전극에 넣는 TiB 2 개 발업자들이 포함되 어야 한다. 비기체 연소합성의 응용 가능성에 대하여 몇 가지 특별한 제안들을 아래에 열거하였다. 이 제안들은 다음 기회에 산업계의 브리핑을 위 하기보다는 차기의 R & D 프로그램에서 고려한 주제가 되게 의도한 것 같다. 소련 비기체 연소합성 프로그램의 대부분이 보고되지 않아 서 소련 업적을 초월한 빠른 미국의 진척에 대한 기회가 주어졌다. 이 제안들은 또한 화합물을 합성하기 위하여 비기체 연소기술의 참재 적인 유일한 능력을 이용하고 다른 방법으로는 난해하며 고가인 공정 조작(p rocess i ng o p era ti on) 을 수행하도록 의도되어 4) 있다. (1) 복합 세라믹스 (ceram i c com p os it es) 의 합성 복합체의 합성 가능성은 거의 제한이 없이 광범위하다 . 초기 실험 에 대한 제언은 전이금속과 램프 그울음 분말을 상품으로 얻을 수 있 는 흑연섬유(잘게 나누어전 것이나 긴 상태인)와 함께 혼합하는 방법이 다. 주의 깊게 선택한 화학양론적 비로 된 가능한 생성물은 모든 경 우 생성물 조성 사이에 조화된 열팽창 성질을 갖는 섬유로 보강된 탄 화물, 탄화물 - 탄소 공융조합 및 탄소를 포함하는 탄화물들이다. 또 다른 제언은 분해경향과 증발을 방지하기 위하여 질소기체 압력하에 서 탄화규소섬유와 혼합된 규소분말을 반웅시키는 것이다. 기대되는 생성물은 섬유로 보강된 질화규소의 어떤 형태일 것이지만 상 구조 (ph ase str u ctu re) 변화는 조성 변화에 따라 다르다고 본다. (2) 착물 세 라믹스 화합물의 합성 비기체 연소합성법에서 미래의 R & D 를 설계할 때 3 성분 세라믹 스나 두 개 의 이중상을 갖는 중복 마이크로 구조 139> (dup le x micr os- tru c tu re) 로 이루어진 유일한 성질에 관한 소련의 주장을 주목해야 한 다. 이런 형태의 공정으로 열을 재빨리 올리고 내릴 수 있는 독특한 능력은 착물성분 (comp le x comp o sit ion ) 을 합성 하기 에 아주 적 합하다.
초기 합성실험에 대한 제언에는 전이금속 탄화물과 탄화질소화물 (carbonit ride ) 및 시 멘트로 된 탄화물 죽 Ni 접 합제 와 탄화크롬 또는 Mo 이나 Ti 접합제와 탄화티탄이 포함되어 있다. (3) 합성반응과 압력의 결합 비기체 연소합성법에서 대부분의 연구자들은 고밀도의 고체 형태를 82),135),139) 만들기 위해서 압력의 보조가 필요함에 동감하였지만 표준 분말 압력장치를 통해서 또는 원심분리기 안에서 그 압력을 제공하는 데 대부분의 노력을 경주해 왔다. 소련의 연구자들만이 변형된 테르 밋과정으로 7),8),63) 주물을 생산하는 열린 용기에서 기체압력을 사용하 였다. 압력의 보조와 비기체 연소합성법을 결합하기 위해 좀더 효과 적인 방법은 등방압축(i sos t a ti c p ress i n g)하는 것이다. 사실상 고열 등 방압 프레스 (HIP) 는 냉각 용기벽내에서 이루어전다. 제안된 실험방 법은 얇은 금속덮개 (meta llic sheath ) 내 에서 고밀도 콤팩트 물질을 캡 슐 형 태 로 만들고 냉 각 등방압 프레 스 (cold iso sta t ic pre ss 또는 CIP) 용기내의 압력하에서 그것을 반응시킨다. 닫혀진 덮개는 반응물질의 의부로부터 그것을 단열시켜 녹는 것을 방지하여야 한다. 이러한 단 열은 여러 가지 방법으로 수행될 수 있지만 직접적이고도 단순한 방 법은 덮개와 반응물간의 적당한 내부공간을 분말 생성물질로 채우는 것이다. (4) 원자로 연료의 합성 최근 우주선에 대한 핵력의 강조로 보다 높은 온도와 보다 높은 완 전연소 (h ig her bumup) 연료가 필요하게 되었다. 과거에는 원자로의 중앙반응로 연료는 우라늄과 플루토늄의 산화물들이었음에 반하여 더 욱 엄밀한 작동요건을 충족시키기 위해서는 탄화물, 질소화물 및 서 멧 조성들아 가장 좋을 것이다. 비기체 연소합성법은 원하는 조성의 분말 또는 최종 연료 형태를 제조하는 데 가능한 낮은 생산가 공정에 해당한다. Al 과 Mg 같은 환원제, 그 산화물들 및 탄소와 질소 등으 로 반응시켜 주물 생성물로 얻을 수 있다. (5) 적층 및 점충된 경량 군수품
군수품에 사용되는 가벼운 물질에 역점을 두어 세라믹스 화합물의 사용이 증가될 것이다. 또한 세라믹스충들 또는 세라믹스들과 금속둘 의 적층화가 사용될 것이다. 궁극적인 조성은 두 가지가 하나로 되는 부분 (monolith ic secti on ) 에 서로 다른 성 질을 갖는 적충된 충들의 장 점들을 나타내도록 점층화될 것이다. 비기체 연소합성법은 합성반응과 동시에 적층 결합을 가능하게 하 고 점층화된 조성을 합성하는 데 응용할 수 있을 것이다. 경량 군수 품 프로그램에서 이미 시험되었던 물질을 생산하고 이중 목적의 군수 품으로써 방사능 보호를 추가할 수 있게 하는 적당한 실험이 쉽게 계 획될 수 있다. (6) 금속 및 세라믹스 재료들의 강 표면화 표면 마모는 실험장비를 쓸모없게 하는 주원인이 된다. 세라믹스 표면 코팅은 그 확실한 해결책 중의 하나이다. 이러한 코팅의 효율적 인 사용에 있어서 만성적인 문제점은 코팅하는 것이 어렵고 코팅 후 약한 접착의 경향성을 보이는 것이다. 비기체 연소합성으로 얻을 수 있는 극초온 반응온도와 적충된 조성의 합성을 위한 그 응용은 금속 성 및 세라믹스 기질 위에 강한 내구적 표면의 접착을 제공하는 것이 확실하다. 개발계획에 대한 한 가지 제안은 비기체 연소합성 반응과 아크 용 접을 결합시키는 것이다. 예로서 티탄, 강철 및 램프 그을음 같은 분 말반응물들은 강철 같은 금속 용접선 또는 용접봉의 중심부에 놓을 수 있다. 비기체 연소합성 반응으로부터 방출된 발열은 강철 같은 기 질 표면에 티탄-철-탄화물 같은 세라믹스 화합물을 입힐 때의 아크 열에 부가될 것이다. 더욱이 반응물질의 조성을 혼합할 때에는 코팅 내부 기질 쪽에서는 집착을 중시하고 코팅 의부에서는 마모를 저항하 는 강도를 중시하는 조성의 조절이 가능하게 연속적으로 변화시킬 수 있다. (7) 무중력에서의 주물 복합체의 합성 산화물 반응물질과 환원제인 Al 과 M g를 사용하여 수정시킬 때 비
기체 연소합성 반응은 세라믹스 , 서멧 및 금속간 조성물의 주물을 만 들어내는 데 사용할 수 있다고 소련의 세 가지 특허를 7) , 8 ),9 ) 포함한 많 은 논문에 밝힌 바 있다. 이러한 공정수정 때문에 생기는 문제점은 산화물 슬래그의 생성인데 이 슬래그는 생성물질로부터 분리된다. 비 기체 합성반응에는 반응물질을 통해 얇은 연소파의 이동이 있기 때문 에 전체 질량을 거쳐 생성물과 슬래그를 분리하는 것은 산화물과 생 성물간의 밀도차이 때문에 중력의 도움이 있기는 하지만 조작상의 문 제점을 야기시키게 된다. 소련의 연구자들은 이 문제점을 원심압력 (centr ifuga l p ressure) 을 사용하여 해결하였다. 슬래그를 생성물에서 분리하기보다는 그것을 사용하여 강화된 복합 체 세라믹스 재료를 생성하는 한 제안이 고려된다. 그 한 예로서 분 산 또는 연속적인 산화알루미늄상을 갖는 탄화티탄은 어떤 극단적인 홍미로운 성질을 가지고 있음이 틀림없다. 이런 가능성을 조사하기 위한 한 가지 방법으로 우주선 실험실 같은 무중력상태에서 반응으로 실험해 보는 방법이다. 분산된 산화물상은 반응물의 혼합에서 알루미 늄 분말을 사용하여 얻을 수 있고 3 차원적 인 연속 산화물상은 반응 혼합물내에 미세한 알루미늄 선을 넣으므로 얻을 수 있다. 모든 예에서 실험실 R & D 는 분석적 공정 모델화와 결합되어야만 한다. 앞에서 이미 지적한 바와같이 한번 확증된 바 있는 단순 반응 모델들은 위에 제안한 공정응용 형태의 거동을 예측하기 위한 보다 정교한 형으로 확장될 수 있다. 9— 3 최근의 발전 현황 역사적인 배경과 미래 전망에서는 주로 소련의 선도적인 비기체 연 소합성법에서의 발전과 미국에서 R & D 프로그램의 주축이 될 수 있는 여러 가지 전망들을 제시하였다. 여기에서는 주로 일본의 발전
현황을 미래의 전망과 관련시켜 설명하고자 한다. 일본 과학기술 발전계획의 핵심적인 아이디어 상당 부분이 앞의 소 단원에서 밝힌 미래의 전망과 일치함을 알 수 있는데 이것은 그 전망 이 미래 R & D 프로그램으로 객관성을 포함하고 있음을 나타낸다. 미국의 SHS 에 관한 미래의 전망으로 후속될 R & D 프로그램을 위한 제언이 일본에서는 이미 이들 연구개발에 상당한 진전을 보고 있다는 면에서 그 업적을 높이 평가할 수 있다. 비기체 연소합성법과 압력의 결합은 제 8 장에서 고압 자체 전파 연 소 소결법 (HPCS) 으로 17),18) , 19) , 30) , 115) 자세히 설명한 바 있다. 한편 복합 세라믹스 제조의 경우는 HPCS 법으로 고성능 복합 세라믹스 콤팩트 16) , 2 2 ),125) , 13 2 ) 를 제조한 것에 대하여 논하였다. Odawara 교수는 원심 데르밋 공법 20) 으로 5m 길이 금속 파이프에 세라믹스 코팅을 하여 금 속-세라믹스 복합체 파이프롤 생산할 수 있게 하였다. 가압 연소반응 으로 세라믹스-금속의 용접 103) 방법도 성공시켰다. 그 밖에 기체압력 연소소결법과 1 2 8)~13 1) 질화연소에 의한 질화물 세라믹스 생성법도 개발 된 상태이다. 이상 논한 바와같이 일본의 비기체 연소합성법 연구개발은 고압을 결합시켜 HPCS 공법개발과 기체압력 연소소결법 개발로 획기적인 발전을 이루었고 산업적인 응용에도 박차를 가하고 있다 .
제 10 장 특성분석법 이 단원에서의 특성분석 (charac t e ri za ti on) 은 비기체 연소합성법 (SHS) 으로 얻은 분말 생성물과 고열 프레스 (ho t pre ss), 고열 등방암 프레스 (HIP) 및 고압 자체 연소소결 (HPCS) 법으로 얻은 고밀도화된 콤팩트 생성물의 특성을 분석하는 데 주안점을 두고 있다. 분말 생성 물의 경 우는 입 자 크기 분석 (pa rt icle siz e analys i s ) , 분말의 X- 선 구 조결정, 마이크로 구조결정, 물리적 성질 및 화학적 성질의 규명 등 필요에 따라 특성을 분석하게 된다. 한편, 고밀도화된 콤팩트 생성물 의 경우는 분말의 특성에 추가하여 보다 다양한 역학적 기능, 열적 기능, 그 밖에 특수기능에 수반하는 필요특성을 측정하여야 한다. 그 러나 여기서는 몇 가지 선별된 중요 특성분석만을 취급하고자 한다. 10-1 밀도측정 10-1-1 밀도 밀도는 단위 체적당 질량의 크기로 g/c m3 또는 lb/ i n3 의 단위를 갖 는다. 밀도라는 용어는 다음과 같이 여러 가지 방법 uo) 으로 설명될
수있다. i ) 결정학적 밀도 (c ry s ta llo gr a p h ic densit y) : 연속적인 결정격자를 갖는 조성으로부터 계산한 이상적인 밀도. ii ) 비중 (s p ec ifi c grav ity) : 결정학적 밀도와 같다. iii) 이론밀도(th eore ti cal density ) : 결정학적 밀도와 같지만 고용체 와 다중상 (mul tip le ph ases) 을 설 명 할 때 쓴다. iv) 체적밀도(b ulk densit y) : 모든 격자결함들, 상들 및 제조 다공 성 (fab ri ca ti on p oros ity)을 포함하는 세라믹스체의 측정된 밀도 룰 나타낸다. 밀도라는 용어는 첫 3 항목에 대하여 사용한다. 그들은 모두 제조 다공성아 없는 특성을 가지므로 단지 열린 공간은 그 구조에서 원자 들 사이뿐이다. 제조 다공성이 있는 모든 경우에 대하여는 체적밀도 와 이론밀도의 백분율을 나타내는 상대밀도 (rela ti ve dens ity)가 사용 표 10.1 세라믹스의 밀도. 물질 조성 밀도 물질 조성 밀도 a- 산화알루미늄 a-A l203 3.95 산화하프늄 Hf 02 9.6 8 7- 산화알루미늄 r-Al203 3 .•4 7 스포듀멘 LiAI Si, 06 3.20 질화알루미늄 AlN 3.2 6 코-디어리트 Mg 2 AI,Si, O ,. 2.65 뮬라이트 Al6Si, 0, 3 3.23 산화마그네슘 Mg O 3.7 5 탄화봉소 B,C 2.51 퍼-스데리트 Mg ,S iO , 3.20 질화붕소 BN 2.20 석영 Si0 2 2.65 산화베릴륨 BeO 3.06 트리디마이트 Si0 2 2.2 7 티탄산바륨 BaTiO . 5.8 0 크리스토발라이트 Si0 2 2.32 다이아몬드 C 3.5 2 탄화규소 SiC 3.17 흑연 C 2.1~ Z 질화규소 Si3 N 4 3.19 풀루오르화칼슘 CaF2 3.18 이산화티탄 Ti0 2 4.26 산화세륨 CeO2 7.30 탄화티탄 TiC 4.9 1 산화크름 Cr2°3 5.21 이붕소화티탄 TiB 2 4.5 0 스피넬 Mg A l20, 3.5 5 탄화텅스텐 WC 15.70 철알루미늄스피넬 FeAI2°4 4.20 산화지르코늄 zrO2 5.80 자철광 FeF~O, 5.20 지르콘 ZrSiO , 4.65
된다. 이온결합 세라믹스들은 비교적 열린 구조를 가지는 공유결합 세라믹스들보다 더 높은 밀도를 나타낸다. 여러 가지 세라믹스의 밀 도는 표 10 . 1 에서 보는 바와 갑다. 탄화텅스텐 (WC) 의 밀도가 탄화규소 (S i C) 의 밀도보다 약 5 배나 큰 것은 주목할 만하다. 산화지르코늄 (Zr02) 과 지르콘 (ZrS i 04) 의 경우에 는 단지 원자량만을 고려하면 지르콘이 보다 큰 밀도를 가질 것으로 기대할 수 있다. 그렇지만 지르콘 구조는 Si- 0 공유결합 때문에 아 주 열린 구조를 가지므로 Zr02 보다 작은 밀도를 나타낸다. 이론밀도는 결정구조 데이터와 포함된 원소들의 원자량으로부터 계 산할 수 있다. 세라믹스체 (ceram ic bod y)의 체적밀도는 여러 가지 방 법으로 구할 수 있다. 만일 그 세라믹스체의 기하학적 형태가 고체 원통형 또는 정방형 막대같이 간단하고 균일하다면 체적밀도 (B) 는 다음과 같이 시료의 건조무게(D)를 체적 (V) 으로 나누어 쉽게 구할 수 있다. 고체 원통 Bc= vD ;=D言 (10.1) 정방형 막대 또는 판 Br= -f=읊 (10.2) 여기서 r 과 h 는 원통형의 반지름과 높이를, a, b, l 은 정방형의 가 로 세로의 길이룰 각각 나타낸다. 그러나 복잡한 형태의 체적밀도는 Arch i medes 법을 사용하여 결정한다. 10-1— 2 A rc hi medes 법 Arc hi medes 법은 시료 부분의 대기 중의 무게와 물속에서의 무게 차이로부터 그 체적을 계산할 수 있으므로 체적밀도를 구하는 방법이
다. 표면-연결된 다공성 없는 시료 부분은 직접 물에 담글 수 있다. 그러나 표면-연결된 다공성을 포함하는 시료 부분은 밀도를 알고 있 는 왁스 혹은 물이 스며들지 않게 하는 다른 물질로 입히거나 또는 시험 및 재료명세서 ASTM C373w) 에 대한 미국학회에 의하여 정의 된 것과 같이 끓여야 한다. 그 기술은 체적밀도, 열린 다공성, 흡수 및 명확한 비중 직접측정과 닫힌 다공성의 간접평가를 할 수 있게 한 다. 첫째 과정은 그 시료 부분의 건조무게 (dry weig h t : D) 를 측정하는 것이다. 그 시료 부분을 물속에서 5 시간 끓이고 24 시간 동안 물속에 서 냉각시키도록 한다. 대기중에서 젖은 시료의 무게 W 와 수중에서 젖은 시료의 무게 S 를 측정한다. 그러면 다음과 같은 계산이 가능하 다. 의부면적 V=W 갑 (10.3) 최적밀도 B=D/V ( 10.4 ) 명확한 다공성 P=(W-D)/V (10.S) 스며들지 않는 물질의 체적 V'=D 접 (10.6) 명확한비중 T=D/(D-S)=D/V' (10.7) 물의 흡수 A=(W-D)/D (10.8 ) 명확한 비중 (s pecifi c gr av ity)은 편람이나 결정구조학적 계산으로부 터 얻을 수 있는 실제 비중과 비교할 수 있으며 닫힌 다공성 양도 계 산할 수 있다. 체적밀도의 측정은 요업재료 물성의 특성분석에 대단히 중요하다.
다공성 의 그 양과 분포는 강도 (str e ng th) , 탄성 율 (elastic modulus) , 산 화방지 (oxid a ti on resis t a n ce) , 마모방지 (wear resis t a n ce) 및 그 밖의 중요한 성질들에 강한 영향을 주기 때문이다. 이론밀도에 가까운 체적밀도를 갖는 고밀도화된 콤팩트들은 표면 연결된 다공성이 거의 없는 것으로 생각할 수 있어 직접 물에 담그는 체적밀도 측정법을 쓸 수 있다. 그 Arc hi medes 법을 단계적으로 설 명하면 다음과 같다. 1) 시료편의 무게를 정확히 측정하고 시료번호를 표시하며 표 10.2 의 시료 무게란에 기록한다. 2) 그림 10.1 에서 보는 바와같이 알루미늄판 위에 층류수를 넣은 비커 속에서 천칭 위 중앙에 연결된 니크롬선-나일론 줄 - 백금선
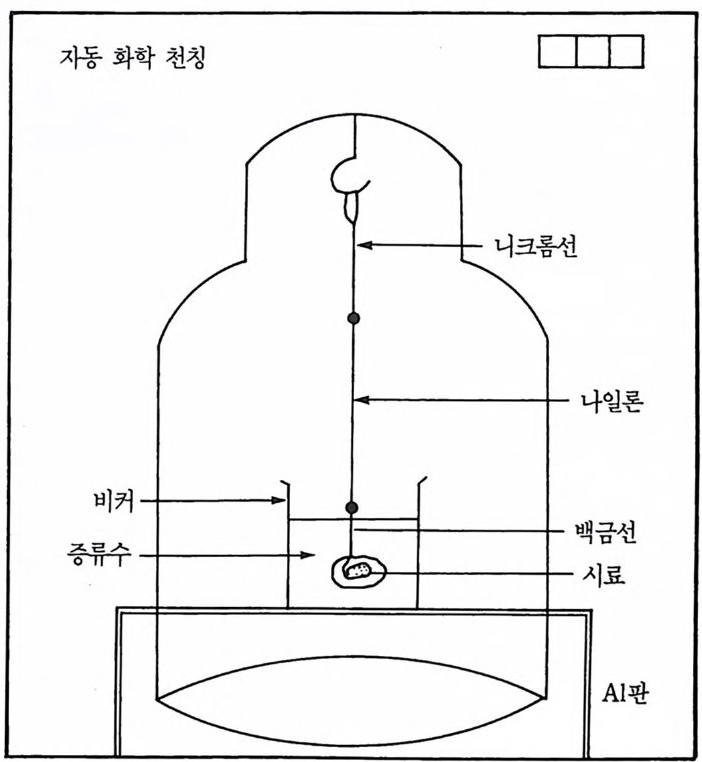 자동화학천칭 I I I I
자동화학천칭 I I I I
그림 I O• I Arch im edes 밀도측정 장치 개 략도.
표 IO.2 Arc hi medes 법에 의한 밀도측정 기록양식과 TiB - T iC ( 20w t%) 복합 세라믹스 콤팩트의 밀도측정 실례• 측정 년월일 : 1986. 9. 3. 이론밀도 : 4.5 7 7 No. 실험조건 시료중량 수중무게 부력 체적 밀도 Dob/Dt h (%) 1 상온상압 0.1 2 69 0.0980 0 . 0289 0 . 0289 4 . 391 95. 94 2 상온상압 0.1165 0.0 9 86 。 •0269 0.0 2 69 4.331 94. 63 3 상온상압 0.3040 0.2 3 52 0 . 0688 0 . 0688 4 . 419 96. 55 평균 4.3 8 0 95.70 No. A B C B_A 1 0.1143 0.2 1 25 0.1145 0.0 9 82 2 0.1 1 45 0.2123 0.1 1 44 0.0 9 78 3 0.1144 0.2124 0.1 1 43 0.0 9 80 4 0.1143 0.2 124 0.1 1 41 0.0981 5 평균 0.0 9 80 1 0.1 1 40 0.2 0 39 0.1 1 42 0.0899 2 0.1142 0.2038 0.1 1 44 0.0 8 96 3 0.1144 0.2 0 38 0.1 1 46 0.0 8 94 4 5 평균 0.0 8 96 1 0.1141 0.3494 0.1 1 45 0.2353 2 0.1 1 45 0.3 4 94 0.1 1 41 0.2 3 49 3 0 .1141 0.3 4 94 0.1 1 40 0.2 3 53 4 5 평균 0.2352 1 2 3 4 5 평균
으로 된 시료 바구니 (samp le basket) 를 물에 담그고 물속에 서 의 바구니 무게를 달아 표 10.2 의 A 란에 기록한다. 3) 시료를 우선 증류수에 적시어 기포가 없도록 한 다음 그 시료편 을 핀셋으로 백금시료 바구니 위에 놓고 물속에서 무게를 달아 표 10.2 의 B 란에 기록한다. 4) 다시 시료를 꺼낸 후 백금 바구니의 무게를 달아서 표 10.2 의 C 란에 기록한다. 이 방법을 두 차례 더 실시한다. A 란과 B 란 의 무게가 같아야 실험이 정확한 것이며 그 차이가 0.0005 이상 이 되어서는 안 된다. 5) B-A 가 나오면 3 또는 4 차례의 평균치를 구하여 B_A 의 평 균치란에 기록한다. 이것이 물속에서의 시료 무게이다. 6) 대기중에서 평량한 시료 무게_수중에서의 시료 무게는 물의 부 력에 의한 가벼워진 무게이다. 7) 시료의 체적 =부력/물의 밀도=부력 /1= 부력 체적밀도=시료 무게/시료 체적 (10.4 ) 10-1— 3 복합 세라믹스 콤팩트의 이론밀도 매트릭스와 첨가물의 무게비를 알고 각각의 이론밀도로부터 복합 세 라믹스의 이 론밀도를 계 산하는 방법을 TiB 2 -TiC , TiB 2 -SiC 및 T iB 2-Al203 를 실례로 둘어 설명 하고자 한다. (1) 이론밀도 계산법 T iB 2 에 첨가한 물질의 무게비를 x 라 하고 T iB 2 와 첨가한 물질의 이론밀도를 각각 g와 PA 라고 한다면 복합 세라믹스의 전체 체적 V (t o t al) 과 복합 세라믹스의 이론밀도 Px 는 다음과 갇이 표시할 수 있 다. V(to t a1 ) = VTIB, + vT t c= 꼬止P그T나 1f!PA. (10.9)
Px= W(1 급w) + 쁘 = PA(1P— Ax P) T+ p T X (10.10) PT PA (2) TiB 2 -TiC 복합 세라믹스의 이론밀도 pr =4.500(TiB 2 : hexag o nal sys t e m , 8-121 : ASTM) PA = 4 . 911 (TiC : cubic sys t e m , 32-1383 : ASTM) i ) TiB 2 (95w t% ) -TiC (5w t% ) px= pA 1~-x)+=p TX =~ 4.911=XO.945+4..5005X O .10 5 9 ii) Ti B2 (90w t% )-TiC ( lOw t%) : Px=4.538 iii) TiB 2 (80w t% )-TiC ( 20w t%) : Px=4.577 iv) Ti B2 (70w t% )-TiC ( 30w t%) : Px=4.616 (3) Ti B2 -SiC 복합 세라믹스의 이론밀도 PA = 3 . 2l5 (/3- SiC : cubic sys t e m , 29-1129 : ASTM) i ) Ti B2 (95w t% )-SiC (5wt %) PPxA(Pl=A-x )P+rP ~rX _-=3 .125~XO3..=2951+54X4.4SO. 5O0 .0X 4-07> 51 2 ii) Ti B2 (90w t% )-TiC ( 10w t%) : Px=4. 32 7 iii) Ti B2 (80w t% )-TiC (20wt %) : Px=4.167 iv) TiB 2 (70w t% )-TiC ( 30w t%) : Px=4.018 (4) Ti B2 -Al20a 복합 세라믹스의 이론밀도 PA=3.987(a-Al2 이 : tri g o nal sys t e m , 10-173 : ASTM) i ) Ti B2 (95w t% )-Al20a (5wt %)
Px= PA(~1-x)+=p TX =~ 3.9 8 7=X O .945+4..5 0 04X O .70 5 1 ii ) TiB 2 ( 90wt % )-Al203 (10wt %) : bx= 4 . 443 iii) T iB 2(80w t %)-Al2 아 (20 wt%) : Px=4.387 iv) TiB 2 ( 70w t% )-Al203 (30w t%) : Px= 4 . 333 10-2 X- 선 결정 구조 분석 만약 물질이 분자로 되어 있지 않고 결정이라면 그 확인은 보통 X 국 1 분말회절법으로 실시한다. 각 결정성 고체들의 확인을 위하여 지 문과 같이 사용될 수 있는 그들의 특성 X- 선 분말 패 턴 (pa tt er n) 을 가지고 있다. 대부분의 알려진 무기고체의 그 분말 패턴들은 분말회 절철 (Powder Diffrac ti on F il e) 의 최신판 142) 에 포함되어 있지만 알려지 지 않은 것들은 적당한 조사법으로 빠르고 명백하게 확인될 수 있다. 그 물질이 확인되면 다음 단계는, 그 구조가 알려지지 않았다면, 구조를 결정하는 것이다. 그 물질이 결정성이라면 X 국 1 결정구조학 이 사용될 수 있다. X- 선 회절의 문제는 고체화학에서 중심적 역할 울 하지만 여러 가지 X 강 1 기술 사용 중에는 X- 선 분말회절, 고온 x- 선 분말회절, 단결정 X- 선 회절 및 X 국 1 분광학 (X-ra y fluo res-
cence : XRF, absorp tion edge fine str uc tu re : AEFS 및 exte n ded X-ray absorp tion edge fine str uc tu re : EXAFS) 등이 있으나 여기서는 X- 선 분말회절 143) 에 관해서만 간단히 설명하고자 한다. 10— 2— 1 X - 선 분말회 절 x- 선 분말회절은 그림 10.2 에서 보는 바와같이 긴 도표지상 또는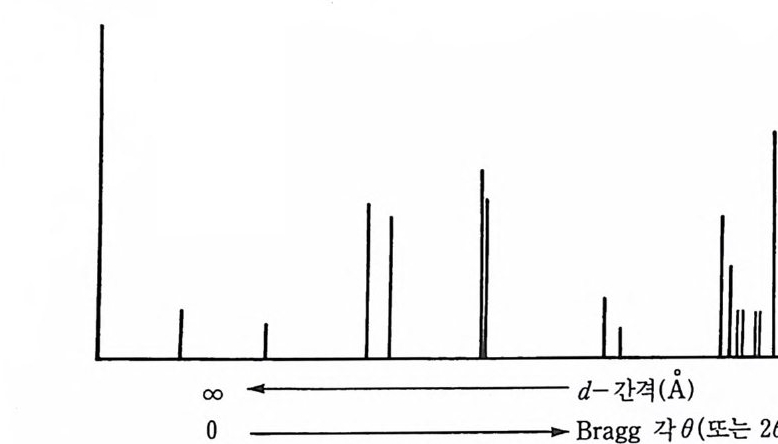 。
。
그립 10,2 개략적인 X- 선 분말희철 패턴.
한 조각의 사전 필름상에 각기 다른 세기와 위 치 (d- 간격 또는 Bragg 각, 8) 를 갖는 일련의 선 또는 피크들이다. 한 주어진 물질에 대하여 그 선 위치들은 본질적으로 고정되어 있고 그 물질의 특성에 해당한 다. 그 선의 세기는 시료의 제조방법과 기계적 조건에 따라서 시료마 다 약간 다를 수 있다. 확인 목적을 위하여 주된 기록은 세기의 반정 량적 고려와 같이 선 위 치 (line po sit ion s) 를 취 하는· 것 이다. x- 선 분 말회절의 몇 가지 응용 M3) 을 이제 설명하고자 한다. (1) 상 확인 (ph ase ide nti fica ti on ) 각 결정성 물질은 그것의 확인을 위하여 사용될 수 있는 특성분말 회절 패턴을 갖고 있다. 표준 패턴들은 J CPDS 철 또는 이전에는 ASTM 철로 알려 진 분말회 절 철 (po wder diffrac ti on file) 에 주어 진다. 분말 패턴에서 Hanawalt 지수는 8 개의 가장 센 선들을 사용하고 Fin k 지수는 가장 긴 d- 간격의 첫 8 선울 사용하는데 이 두 가지 방 법 중 한 가지로 물질들의 지수가 매겨진다. 물론 성분상들의 패턴들이 비교할 수 있게 얻어지므로 물질의 혼합 물들도 확인될 수 있다. 많은 응용을 위하여 특히 가능한 화합물의 수가 한정된 경우는 모든 새로운 시료에 따라 그 파일로 재분류하는
것보다는 한 필요한 세트의 표준 패턴들만 보관하는 것이 바람직하 다. 이것은 시료를 확인하기 위하여 Guin i e r 필름이 사용될 때 특별 히 그러하다. 분말 X- 선법은 만약 불순물들이 한 분리된 결정상으로 존재하면 순도의 대략적인 점검으로도 사용될 수 있다. 일상적 연구 에서 불순물상의 검출의 더 낮은 한계는 일반적으로 1~5% 범위이 다. 독특한 불순물을 찾을 때와 같이 좋은 조건하에서 그 검출한계는 회절 미터가 사용될 때는 감도를 증가시키거나 또는 필름법이 사용될 때는 노출시간을 증가시킴에 의하여 상당히 감소시킬 수 있다. (2) 정량적 상 분석 혼합물 내의 한 특별한 결정상의 양은 정량적 X- 선 분말회절로 결 정될 수 있다. 그 방법은 간단하지만 약간 지루하고 오차를 수반하기 쉽다. a-Al2 아와 같이 찰 결정화되는 상인 내부 표준을 꼭 맞게 조 절된 양(예를 들면 lO wt%)만큼 시료에 가하는 것이 필요하다. 관심 있는 상의 분말 패턴에 있는 한 선을 선택하고 그의 세기 (int e n sity ) 를 적당한 내부 표준선의 세기와 비교한다. 그 상의 양은 조성에 대 한 세기를 미리 만든 보정 그래프에 내삽시켜 결정할 수 있다. (3) 정확한 단위세포 파라미터의 결정 분말 패턴 내의 선의 위치 (d- 간격)는 단위세포 파라미터 (a, b, c, a, /3, r) 의 값에 의하여 조절된다. 단위세포 격자 파라미터(상수)는 보 통 단결정법으로 결정되지만 얻어진 그 값들은 단지 둘 또는 셋째 유 효숫자까지만 정 확하다. 더 욱 정 확한 세포 파라미터 (cell pa ramete r ) 는 만약 그 여러 선들이 Mi ller 지수 h, k, 1.£ 할당되고 그들 위치들 이 정확히 측정된다면 분말 패턴으로부터 얻을 수 있다. 오차를 최소 화하는 최소 자승법을 사용하여 넷 또는 다섯 유효숫자까지 정확한 단위세포 파라미터를 보통 얻을 수 있다. 정확한 단위세포 파라미터 둘은 특히 a) 복잡한 분말 패턴들을 지수 매기기가 가능하도록 하기 위하여, b) 세포 파라미터에 조성의 효과를 연구하기 위하여, 그리 고 c) 열팽창 계수를 측정하기 위하여 특별히 유용하다. (4) 고용체 격자 파라미터
고용체 계열의 격자 파라미터는 종종 조성에 따라 작지만 감지할 만한 변화를 보인다. 이는 고용체의 특성을 규명하는 데 유용한 방법 이 되고 원칙적으로 격자 파라미터는 조성의 한 지시계 (i nd i ca t or) 로 사용될 수 있다. 만일 그 조성 의존성이 선형이라면 소위 Ve g ard 의 법칙에 따른다. Ve g ard 법칙으로부터 벗어남은 금속 고용체에서 자 주 일어나지만 그 이유는 잘 해석되지 않는다. 비금속 고용체에서는 Veg a rd 법칙으로부터 벗어남은 그리 많지 않으며 만일 벗어남이 일 어날 때는 일반적으로 고용체에서 구조적 특칭에 기인하는 것으로 본 다. 예 로서 Veg a rd 법 칙 으로부터 양의 벗 어 남 (po sit ive devia t i on ) 의 한 원인은 명확히 균일한 고용체와 무작정한 고용체 계열들에서 초기 의 혼합되어 있지 않은 상태 때문이다. (5) 결정구조 결정 결정구조는 회절된 X- 선 빔의 세기를 분석함으로써 설명할 수 있 다. 일반적으로 단결정 시료가 사용되지만, 단결정을 얻울 수 없고, 그 구조가 상당히 간단하며 단지 한정된 수의 원자 배위자들만 그 구 조를 설명하기 위하여 정해져야 하는 경우는 분말이 사용될 수도 있 다. 후자의 한 예로서 스피넬 구조를 갖는 것으로 보이는 새로운 상 울 제조하였다고 가정하자. 분말회절법은 그 구조를 확인하기 위하 여, 그리고 그 구조가 정상인지 또는 역스피넬(i nverse s pi ne!) 인지 견 정하기 위하여 사용될 수 있다. (6) 입자 크기 측정 x- 선 분말회절법은 그 입자의 평균 지름이 약 2000A 보다 작으면 분말시료에서 평균결정 크기를 측정하는 데 사용될 수 있다. 분말회 절 패턴에서 그 선들은 한정된 폭을 나타내지만 만일 그 입자들이 대 단히 작다면 그 선들은 보통 때보다 더욱 넓어진다. 그 선 폭 넓어짐 온 입자 크기의 감소에 따라 증가한다. 그 한계는 약 20~lOOA 범위 로 입자 지름에 달한다. 그러면 그 선들은 대단히 넓어져서 그들은 효과적으로 자연방사선으로서 사라진다. 현저하게 구형이 아닌 입자 들에 대하여 분말 패턴에서 다른 선들이 정도가 다르게 폭이 넓어지
기 때문에 그 형태를 평가하는 것이 가능하다. (7) 비결정성 고체의 짧은 범위질서 (short rang e order) 결정성 고체는 그림 10 . 2 에서와 같이 많은 예리한 선들을 갖는 회 절패턴을 나타낸다. 유리 및 겔과 같은 비결정성 고체는 작은 수의 대단히 넓은 둥근 피크를 갖는 회절 패턴을 보인다. 이들 둥근 피크 로부터 공간구조에 관한 정보롤 얻을 수 있다. 그 결과는 일반적으로 방사방향 분포함수 (radia l dis t r i b u ti on fun cti on 또는 RDF) 로써 나타낸 다. 이것은 기준 원자로부터 거리의 함수로써 한 원자를 발견할 확률 을 나타낸다. 그로써 배위환경(첫째와 의각 구들)과 결합 길아에 관한 정보가 얻어진다. 그러한 정보는 비결정성 고체에 대한 구조적 모델 의 유효성을 시험하는 데에도 유용하다. 예를 들면 Si0 2 , B20s 등에 기초를 둔 간단한 유리와 무정형 탄소에 대하여 그 정보가 이용되어 왔다. 그 방법은 그같은 물질에 대한 구조적 정보를 제공하고 유리구 조의 이론을 시험하는 데 확실히 중요하지만 그 방법의 사용에 엄격 한 제한들이 있다. 데이터 분석은 간단하지 않고 복합 다성분 유리로 는 유용한 정보를 조금밖에 얻을 수 없다. 예로서 네오디뮴 레이저 유리, 무정형 반도체, 유리질 금속 및 이온적 전도성 유리와 같이 새 로운 유리질 재료들은 여러 가지 응용성이 발견되고 있기 때문에 유 용한 정보의 결핍은 유감스러운 일이다. 이들 재료에 대한 구조적 정 보는 대단히 필요하다. (8) 결정 결함과 무질서 결정성 고체에서 생기는 어떤 형태의 결함이나 무질서는 여러 가지 회절효과로 검출할 수 있다. X41 폭의 넓어짐으로부터 입자 크기의 측정은 이미 언급한 바 있다. 선 폭 넓어짐의 다른 가능한 원인은 결 정내에서의 변형 (s t ra i n) 이다. 이것은 소성적으로 변형된 금속에서 나 타난다. 절대영도 이상의 모든 물질에서 필연적으로 존재하는 원자의 열운동은 피크 세기의 감소와 자연방사선의 준위에서 증가를 일으킨 다. 이것은 특별히 시료의 융점에 접근할 때와 갇이 높은 온도에서 현저하다. 그러한 열운동의 고려가 소위 온도인자를 도입함으로써 구
조결정에서 취해진다. 작은 각 X- 선 산란 (SAXS) 기술은 10~lOOOA 척도의 불균일체들을 검출하는 데 사용된다. 회절된 방사선은 그림 10 . 2 의 왼쪽 끝에서 또 는 작은 각도수 20 와 같이 입사각으로부터 바로 벗어난 각에서 Kratt ky 카메라를 사용하여 측정한다. 이 회절된 방사선은 20 가 oo 에서 중심에 회절되지 않은 방사의 센 빔에 어깨 (shoulder) 로 나타난 다. 바람직한 경우로 고체 또는 액용체들에서 혼합할 수 없는 2 상구 조(t wo-p hase str u ctu r es) 같은 불균일체가 연구될 수 있다. 10— 2— 2 최 신 X- 선 분말기술과 그들의 응용 (1) 분말회 절계 (po wder_d iffrac to m ete r ) 가장 일반적으로 사용되는 X - 선 기기는 분말회절계 143) 이다. 이 기 기는 검출기로서 비례섬광 (s ci n till a ti on) 또는 가이거 계측기 (Geig e r coun t er) 를 가지고 있는데 그것은 도표기록계에 연결되거나 혹은 어 떤 때는 디지털 출력 (dig ital outp u t) 방법에 연결된다. 일반적인 사용 에서 그 계측기는 일정한 각속도로 20 값의 범위로 주사 (scan) 하도록 되었다. 일반적으로 10~80° 범위의 20 는 분말 패턴의 가장 유용한 부 분을 적용 (cover) 하는 데 충분하다. 그 눈금은 20 에서 선형이고 피크 들간 d - 간격은 Bra gg의 법 칙으로부터 계산되거나 20 대 d 의 표준표 로부터 얻어전다. 계측기의 주사속도는 일반적으로 20/m i n 값이 2 ° 이 므로 한 기록을 얻는 데 약 30 분이 필요하다. 대단히 정확한 연구가 진행되고 있지 않으면 세기는 피크 높이로부터 취하게 된다. 그 정확 한 연구의 경우는 피크의 면적이 측정되어야 하고 가장 센 피크를 100 으로 정하고 나머지는 그에 비례하여 척도를 매긴다. 만약 대 단히 정 확한 d- 간격 또는 세 기 가 필요하다면 (1/8) 0 의 20/ mi n 와 같은 보다 느린 주사속도가 사용된다. 정확한 d- 간격을 얻기 위하여는 d- 간격을 정확히 알고 있는 KCl 갇은 순수한 물질을 내부
표준으로 시료와 함께 혼합한다. 20 에 따라서 변하는 보정계수 (correcti on fa c t or) 는 관찰된 d- 간격과 내부 표준의 진가인 d- 간격의 차이로부터 얻어지고 측정되는 그 패턴에 응용된다. 정확한 세기는 면적계(p lan i me t er) 같은 장치로 피크의 면적을 측정하거나 회절계에 부착된 자동계측기를 사용함으로써 피크 면적으로부터 얻어진다. 회절법에 대한 시료는 여러 가지 형태를 갖는다. 죽 와셀린을 바론 유리 슬라이드에 미세한 가루를 살포한 얇은 충과 유리 슬라이드에 압축된 얇은 조각 동의 시료들이 사용된다. 사람마다 다른 방법의 시 료제조를 좋아하고 그 목적은 결정방향의 무작정 배열을 포함하는 시 료를 얻는 것이다. 그러므로 분말은 l~lOµm 의 크기로 잘 갈아야 하고 X - 선회절 전에 시료를 체 (s i eve) 로 치는 것도 좋다. 만일 결정 배열이 무작정이 아니라면 우선하는 배향이 있고 그러면 오차가 일어 날 수 있고 때로는 그 오차가 대단히 커서 그 측정된 세기로 나타난 다. 예를 들면 얇은 판으로 생기는 점토광물 또는 입방체로 결정화되 고 분쇄할 때 더 작은 입방체로 깨지는 어떤 입방물질과 갇이 구형이 아닌 모양의 특성으로 결정화되는 물질에 대하여 우선하는 배향은 심 각한 문제가 된다. 그러한 물질의 분말응집에 있어서 그 결정은 그들 의 표면에 위치하려는 경향이 있어 무작정 평균배향으로부터 멀어지 는 결과를 가져온다. 분말회절계를 사용하면 컴퓨터 프로그래밍까지 되어 있어 모든 선 의 d- 값과 그에 대응하는 지수 매기기 (i ndexa ti on) 까지 얻을 수 있어 편리하고 따라서 격자상수(l a tti ce p arame t er) 까지도 쉽게 얻을 수 있다. 과거 Deby e- Scherrer 카메 라의 큰 단접은 입 사 빔 과 회 절 빔 이 필 연적으로 약간 발산되어 낮은 세기를 갖는다는 것이다. 회철계와 최 신 초점 카메라에서는 수렴 X- 선 빔이 사용된다. 이것은 분해능에 있어서 국적인 개선을 가져왔고 더욱 더 센 빔이 사용되므로 노출시 간이 대단히 감소되었다. 최신 필름법 (Gu ini er 초점법)에서는 한 점에 수령하는 강한 입사 빔 이 사용되어 선들의 우수한 분해능이 얻어지고 노출시간도 1 시간에
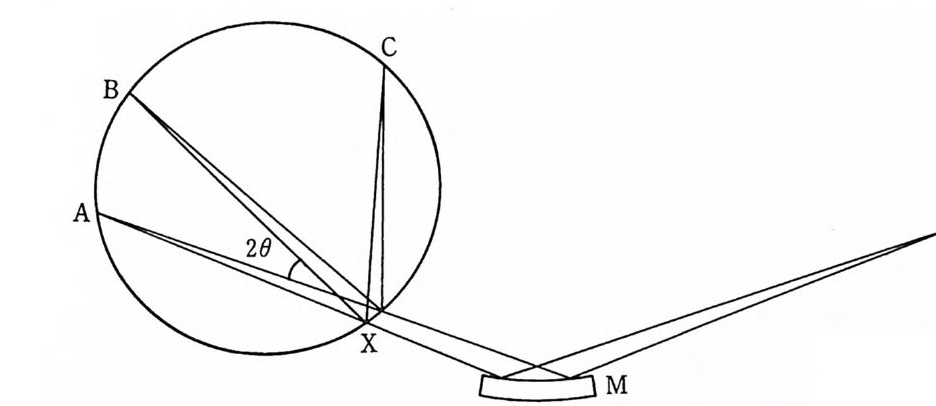 A s
A s
그림 10.3 카메라 초접을 맞추기 위한 결정단색화 장치 M, X- 선원 S 및 시료 X 의 배치도.
대하여 10 분을 감소시킬 수 있었다. x- 선원과 시료 사이에 구부러진 단결정 석영 또는 흑연을 위치시킴에 의해 수령된 X- 선 빔이 얻어진 다. 이 구부러진 결정의 배향은 입사 빔을 회절시켜 발산 빔을 수렵 빔으로 변화시킬 수 있도록 조절한다. 그 빔은 시료에 부딪히고 그 회절된 빔둘은 필름의 표면에 초점을 맞추도록 배열시킨다. 한 전형 적 인 Gu ini e r 필름 약도는 그립 10 . 2 에서 보는 바와 같다. (2) Guin i e r 카메 라 만일 평평한 결정 단색화 장치 (monochroma t or) 가 사용되면 X- 선 원으로부터 방출되는 X- 선 빔은 원래 발산하기 때문에 많은 Ka 방사 가 손실되어 단지 작은 양의 Ka 성분만 단색화 장치에 대해 정확한 Bra gg각에 놓이게 된다. 그 효과를 개선하기 위하여 결정 단색화 장 치를 굽히면 발산하는 X- 선 빔은 그 결정 단색화 장치에 회절되어 강도가 세고, 단색 파장이며, 그리고 수령된 빔을 준다. 결정 단색화 장치 M 을 사용하고 원의 이론을 사용한 Guin ier 카메 라 또는 초점맞추기의 배열은 그람 10.3 에서 보는 바와 같다. 단색 파장 방사선의 수령된 빔은 X 위치에 있는 시료를 통해 지나간다. 회절되지 않은 방사선은 A 에 있는 초점에 와서, 필름이 어둡게 되는
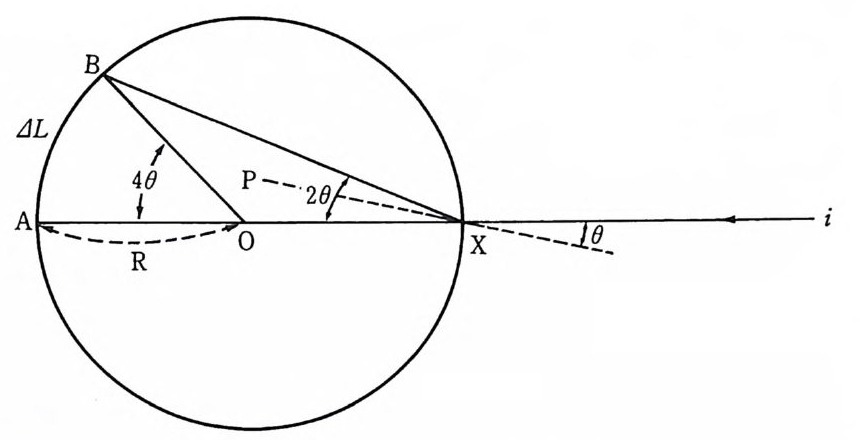 A OI
A OI
그림 1O.4 Guin i e r Lin e 필름의 d - 간격 측정도.
것울 방지하도록 그 필름 앞에 빔 정지 (beams t o p)가 놓여전다. 시 료에 의하여 회절된 여러 가지 빔둘은 B, C 등에서 초점이 맞게 된 다. 우리는 A, B, C 및 X 가 원주상에 놓여야만 하는 것을 그 원의 정 리로부터 안다. 필름은 짧은 실린더형이며 원 ABC 상에 놓인 한 카 세트에 위치시킨다 . 그 필름의 눈금은 회절계로부터 얻은 도표 출력 (chart ou tp u t)과 같이 20 에 대하여 선형이다. 도식적인 필름은 다른 높이의 피크들 대신 다른 세기의 선들 또는 다른 정도의 흑색도가 보 인다는 것만 제의하면 그림 10.2 에서 보는 바와 같다. (3) Guin ier Li ne 의 d 컨격 측정 필름의 크기는 1X15cm 로 취급하기가 대단히 편리하다. Guin ier Lin e 필름의 d - 간격을 측정하는 데 필요한 개 략도는 그립 10 . 4 에서 보는 바와 같다. 20 가 oo 또는 아간격이 00 에서 그 선은 그립 10.4 의 A 점 죽 회절되지 않은 빔에 대응한다. 이 점이 필름상에 기준 위 치가된다. 관측된 d 값을 계산하기 위하여 그립 10.4 에서 LOXP= 0 ; 맞꼭지각
LPXB=0 ; 반사각=입사각 L0XB=20 :. LAOB=40 ; 중십각 =2X 원주각 4 0 = l::.. L/R (radia n ) 40°R1r/180= l::..L 0° = l::.. L X 180/4 자? (10.11) 여기서 TCR=180mm 가 되도록 필름을 원형으로 고안하면 00=!::,. L/4 이 된다. A(cu) = 1. 54051 A 과 8° = t:,. L/4 을 Bra gg의 식 에 대 입 하 면 d= 2 sin ( AA L/4) = s0in. 7( 7A0 L25/54 ) (10.12) 가 된다. 이와갇이 기준점 A 로부터 필름상에 나타난 선들까지의 거 리 AL 을 부척이 달린 마이크로 자(mi cro-ruler) 또는 이동 현미경 (trav ellin g micr oscop e) 으로 재고 이 룰 (10 .12) 식 에 대 입 하여 관측된 d 값 (dobs) 을 얻는 방법을 Gu inier L i ne 이라 한다. 만일 4R = 200mm 와 Accu) = 1. 54051 A 을 Bragg 식 에 대 입 하면 d= 2sin ( !::,. L X,l 1 80/4 ;rR ) =- sin ( 0 .0 2.7867407295 5X 1::,. L) (10.13) 울 얻는데 이 식을 만족하도록 고안된 d- 간격 측정법을 Guin ier He igg라고 한다. Gu inier 법은 필요에 따라 정확한 d- 간격을 얻을 수 있는데 그 결 과는 대단히 느린 주사속도를 사용하여 회절계로 얻은 것과 비교할 수 있다. 필름상에 선들의 세기는 시각적으로 산정하거나 마이크로 농도계 법 (mi crodens it ome try)으로 정 량적으로 측정 할 수 있다. 시료 크기는 1mg 또는 그 미만으로 대단히 작으며 분말시료의 경우는 약

그림 10.5 SrLa2Fe201-y, Sr1.1 L a1.9 F e20 ,_y 및 Sr1,2 La l.8 F e201- y 고용체들의 Guin ie r Lin e 선들.
4X l 5mm 넓이의 스카치테이프에 두명하고 얇게 입힐 정도의 양이면 된다. 필요노출시간은 시료의 결정도 (c ry s t all inity)와 같은 인자와 X -선을 흡수하는 중원소 (hea vy elemen ts)의 유무에 따라서 5 분과 1 시 간 사이에서 변한다. 한 번에 2 개 이상의 다른 시료를 동시에 한 필 름상에 구분하여 프린트 현상할 수 있으므로 시료간에 상이 변해가는 모양을 상호 비교하는 데에도 유리하다. Sr 1+ xLa2-xFe201- y계 에 서 x = O, 0 .1, 0 . 2 에 대응하는 SrLa2Fe201-y, Sr1.1 L a1.9 F e201-y 및 Sr1.2 La1.S F e201-y 고용체 들의 Gu inier Lin e 필름 상에 프린트된 선들의 실례는 그림 10 . 5 에서 보는 바와 같다. 필름의 왼쪽 밖에 독립된 선이 회절되지 않는 X- 선의 감광된 기준선 A 점에 해당한다. 관찰된 d 값을 사용하여 대응하는 각 결정계 (단순 입방정계, 정방정 계, 사방정계, 육방정계 등)의 최소 자승법으로 지수 매기기(i ndexa tion ) 및 격 자상수 (lat t ice pas amete r ) 계 산을 실시 한다. 이 때 각 결정 계의 최소 자승법은 계산기 또는 컴퓨터의 프로그래밍을 사용하여 용 이하게 계산할수 있나.
10_3 주사 전자현미경 10 一 3 ― 1 주사 전자현미 경 주사 전자현미 경 (Scannin g Electr on Mi cro scop e 또는 SEM) l44) 이 란 전자선이 시료를 통과하지 않고 시료 표면 위를 주사할 때 시료에서 나오는 정보를 전기적으로 탐지하여 브라운관의 밝기 (br ig h t ness) 로 변조시켜 시료 표면의 형태를 영상으로 만들어 관찰하는 현미경이다. 이의 특칭은 광학현미경이나 두사 전자현미경과는 판이하여, 상을 맺는 데 렌즈가 채택되고 있지 않다는 점이다. 주사 전자현미경에서 의 렌즈는 단순히 전자선을 수령시켜 시료 표면에 미세한 전자선속을 만드는 데 사용된다. 따라서 전자선이 시료를 두과하는 것이 아니기 때문에 투과 전자현미경 (TEM) 과 같이 시료준비에 어려움도 없다. 주사 전자현미경의 가장 큰 특색은 심도 (de pth of fi eld) 가 깊다는 접이다. 그 심도 f는 주사 전자현미경에서 다음과 같은 수식으로 나 타낸다. I= 土 r/M2a- d (10.14) 여기서 r 은 눈으로 식별할 수 있는 최소 거리, M은 배율, d 는 전 자선의 지름, a 는 대물렌즈의 반각 (hal f an g le) 을 나타낸다. 주사 전자현미경의 분해능은 전자선의 지름이 작으면 작을수록 좋 으므로 전자선의 지름을 작게 하기 위하여 대물렌즈의 반각은 5.3X 10-3rad 정도로 작게 한다. 전자선의 지름이 lOOA 정도라면 (10.14) 식은 그림 10.6 과 갇이 나타낼 수 있다. 이 그립에서 알 수 있는 바와갇이 주사 전자현미경의 심도는 저배 율이나 고배율 모두 광학현미경에 비해 월등히 깊다. 더욱이 광학 현
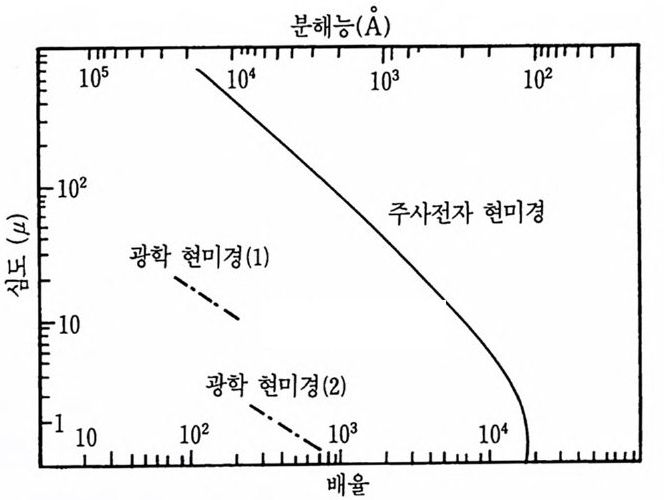 102
102
그림 10·6 주사 전자현미경과 광학현미경의 배율 (ma gnifi ca ti o !l)과 십도 (de pth o ffi eld) 의 관계 ; 주사 전자현미경은 저배율과 고배율 모두 심도가 깊어 입체적인 관찰이 가능하다.
미경으로는 관찰이 불가능한 고배율에서도 그 심도가 깊다는 것을 알 수 있다. 이는 주사 전자현미경을 이용하면 요철이 심한 시료라 할지 라도 입체적으로 관찰할 수 있다는 것을 의미한다. 이 절에서는 주사 전자현미경의 원리 및 기능은 생략하고 주사 전 자현미경에 분석장치를 붙여 미소부의 화학분석을 가능하게 하는 EPMA (Electr on Probe Mi cr o Analys i s ) 의 분석 한계 , 주사 전자현미 경 에 있어서의 시료 준비 및 그 응용에 대해서만 간단히 알아보고자 한다. 10 一 3-2 분석의 한계 입사된 전자선은 시료 내의 원자들과 작용하여 시료에서 특성 X -선과 연속 X- 선을 낸다. 특성 X- 선 중 특정원소의 X- 선만 분광결 정을 사용하여 분광시 켜 X- 선 검출소자로 그 강도(i n t ens ity) 를 측정
하여 정성이나 정량분석을 행할 수 있다. 이때 광학현미경이나 이차 전자상으로 시료를 직접 관찰하면서 미소부의 분석을 행할 수 있다. 정량분석이 가능한 것은 어떤 한 원소가 합금 속에 있을 때 특성 x- 선의 강도가 그 원소의 농도에 비례하여 발생하기 때문이다. 실제의 경우는 정량분석을 행할 때 X- 선의 발생점이 시료 내부에 있기 때문에 시료 내부에서 발생한 X- 선이 그 표면에 나오는 도중에 시료에 의하여 흡수되어 강도가 변하게 되므로 이를 보정하여야 한다 (홉수보정). 또한 타원소에 의하여 형광 X- 선도 발생하므로 이도 역 시 보정하여야 한다(형광보정). 이와 같은 보정을 행하면 실험이 정 확하다는 조건하에서 1% 의 상대오차로 미소부의 분석을 행할 수 있 다. x- 선에 의한 분석을 기능적으로 분류하면 다음과 같다. (1) 점 분석 (po in t analys i s ) 분석하고자 하는 시료의 한 점에 전자선을 고정시키고, x- 선 분광 기로 파장값을 연속적으로 변화시키면서 특성 X- 선의 세기를 기록기 에 기록한다. 검출된 특성 X- 선의 파장값의 해당 원소를 도표로 찾 아 그 파장이 어느 원소의 파장인지 확인하여 미소부의 정성분석을 행한다. (2) 선 분석 (line analys i s ) 시료 위의 임의의 직선에 따라 전자선을 이동 조사하여, 특정 원소 의 X- 선 강도를 기록기에 기록하여 임의의 직선에 따른 조성의 변화 룰 분석하는 방법이다. (3) 특성 X- 선 상(i ma g e) 시료 위의 일정영역을 전자선으로 조사하며 이것과 같이 일어나 움 직이고 있는 브라운관의 주사선의 밝기를 어떤 원소의 특성 X- 선의 검출 신호로 변조시키면 시료에서 어떤 원소의 2 차원적인 농도분포에 해당하는 영상을 얻을 수 있다. 이때 영상의 밝은 부위가 특성 X- 선 울 낸 원소가 많은 부분에 해당한다. 특성 X- 선에 의하여 분석이 가능한 원소는 원자번호 4 인 베릴륨에 서 92 인 우라늄까지이다. 검출이 가능한 한계는 중량 퍼센트로 약
0.001~0.1% 정도이며, 분석하고자 하는 부위의 크기는 수 µm 이 상의 크기이어야 한다. 10_3— 3 시료 준비 및 응용 (1) 시료 준비 시편은 반드시 전류가 호를 수 있도록 도전체 고정 (mounti ng ) 을 하 든지 도전 페인트(p a i n t)를 칠하여야 한다. 시료가 비전도성인 생물 이거나 세라믹스일 경우는 시료 표면에 전공증착 (vacuum dep o sit ion ) 법으로 급 (Au) 을 200~400 A 두께로 도금하여 관찰한다. 세 라믹스 시료의 경 우는 파열 표면 (frac tu re surf ac e) , 미세 하게 잘 연마한 표면 (po li sh ed surf ac e) 및 열 식 각 표면 (the rmally etc h ed su rfac e) 의 SEM 마이크로 그래프를 얻어 마이크로 구조를 분석한다. 시료의 파열 표면의 SEM 마이크로 그래프는 낱알경계 (grain bounda ry)를 따라 파열되는 난알간 파열(int er gr anular fr ac tur e) 과 난 알 자체까지 파열되는 낱알관통파열(tr ans gr anular fr ac tur e) 을 잘 구 별할 수 있어 Vi ck ers 경 도와 파괴 인성 (frac tu re tou g h ness) 을 마이 크 로 구조로부터 예측할 수 있다. 잘 연마된 시료 표면의 SEM 마이크로 그래프를 조사하면 난알 크 기 (grai n s i ze) 를 계산하는 대 편리하다. 한편, 잘 연마된 시료 표면 을 약 10-4mmH g의 진공과 1200°C 에서 열 석 각한 표면의 SEM 마이 크로 그래프는 난알간의 결합, 복합 세라믹스의 상호조성간의 분산 및 결정분정 (cry st a l seg reg a ti on ) 등을 잘 분석할 수 있다. (2) 확대 관찰 부분 주사 전자현미경의 분해능은 60A 정도로 두과 전자현미경보다 낮 으나 심도가 깊고 시료 준비상에 어려움이 없고 또한 저배율에서 고 배율까지 관찰이 가능하므로 표면 요철이 심한 시편의 관찰에 널리 사용된다.
투과 전자현미경의 복제물 (re p l i ca) 제작에 의한 표면 관찰법으로 연구되었던 표면의 연구는 주사 전자현미경으로 바뀌게 되었다. 대표 적 인 예는 파괴 해 석 (failu re analys i s ) 에 의 응용인데 저 배율에 서 고배 율 까지 시료 표면을 직접 관찰할 수 있을 뿐만 아니라 심한 요철도 높 은 심도로 인하여 모두 결상시킬 수 있기 때문이다. 그 밖에 특성 X -선을 이용한 미소부의 분석이 가능하므로 파괴를 일으킨 원인을 좀 더 쉽게 찾을 수 있다. 최근에는 특성 X- 선의 분석을 시간이 오래 걸리는 결정분광방식 (waveleng th dis p e rsiv e spe c tr o mete r ) 이 아니 라 정 확도는 약간 떨어 지 지 만 순간적으로 분석 이 가능한 에 너 지 분산 분광방식 (energy
할 수 있는 장점 때문에 생산 현장용 및 연구용 수단으로 널리 이용 되고 있다. 경도시험에는 i ) 주물과 같이 재료 자체의 불균일성이 커서 넓은 범 위 의 움푹 들어 간 자국(i nden t a ti on) 이 필요한 재료의 경 도를 조사 할 때 주로 사용되는 Brin e ll 경도 (Hs), ii) 회전 베어링 금속, 절삭 공구, 스프링판 등 가장 일반적으로 사용되는 다양한 척도로 넓은 범 위의 경도를 측정할 수 있는 Rockwell 경도 (HRc), iii) 시편에 압혼 을 남기지 않게 할 때나 시편이 클 때 비파괴적으로 측정할 수 있는 Shore 경도 (Hs), iv) 도금충이나 탈탄, 침탄 등과 갇이 측정하려는 부위가 좁은 경우에 사용되는 Knoop 경도 (HK) 및 v) 침탄, 질화, 탈탄, 도금충의 표면 변질층 및 정밀기기의 미소부품의 경도를 측정 할 때 사용되는 Vic k ers 경도 (Hv) 등이 있다. 이 소단원에서는 고성능 단순 및 복합 세라믹스 콤팩트의 작은 시 편의 경도측정 에 많이 사용되는 Vic k ers 경도만을 취급하고 그 밖의 경도측정법은 생략하였다. 10-4-2 Vic k ers 경도 (Hv) Vic k ers 경도는 Hv 로 표시하며 미소 부위의 경도를 측정하는 데 이용된다. 정각 a=136° 인 다이아몬드의 피라밋형 압입체로 시험편을 가압하였을 때 하중을 자국의 표면적으로 나눈 값으로 정의한다. Hv =히중/자국의 표면적 =PIA =2 P sin ( a/2) /d2 Hv =1854 .4P /(axb) (10.1 5 ) 여기서 P 는 하중 및 a 와 b 는 자국의 가로와 세로의 대각선 길이 (a
와 b 가 같을 때에는 d 또는 a 만으로 표시하기도 함)를 각각 나타낸 다. P 를 kg, a 와 b 를 µm 로 대 입하면 Hv 는 k g /mm 떡 단위로 표시 된다. (1) Vic k ers 경 도계 Vic k ers 경도계의 구조는 하중 가압장치와 자국을 측정 하기 위 한 현미경 부분으로 나누어진다. 압입체로는 정각 a=l36° 인 다이아몬드 의 피 라밋 (diam ond pyram id) 형 압입 체 를 사용하여 부하시 간 (loa din g ti me) 은 캠 (cam) 의 회전속도로 조철한다. 보통 Vic k ers 경도계에서 가하는 하중은 1 ~ 120k g이 다. (2) 마이 크로 Vic k ers 경 도계 Vic k ers 경도계와 원리는 같으나 특별히 작은 부위, 죽 박판, 가 는 선, 표면경화충, 도금충, 보석류, 금속조직의 특정 석출물 또는 상의 경도측정에 이용된다. 시험하중은 300g , 500g 및 1kg 정도까지 가할 수 있으며 하중 작용시간은 보통 15 초이고 200 배 또는 500 배 현 미경으로 자국을 측정한다. (3) Vic k ers 경 도 측정 방법 시 험 표면을 금강사지 (emery pa pe r ) 로 연마하여 자국 대 각선의 길 이를 0.002mm 까지 읽을 수 있게 하며, 시험편은 원칙적으로 평면으 로 하여 하중을 가하는 방향과 수직이 되도록 설치한다. 이때 시험편 의 두께는 자국 대각선의 길이의 1. 5 배 이상이어야 하며 경도를 측정 하고자 하는 중심위치는 인접한 자국과 4a 또는 4b( 자국의 대각선 길 이의 4 배) 이상, 시험편의 끝에서 2.5~3a 이상 떨어지도록 한다. 현 미경 시야의 20~70% 내에 자국의 대각선 길이가 들어가도록 시험하 중을 선택하며 특별히 제한이 없는 한 큰 하중을 사용하는 것이 좋 다. 하중의 작용시간은 15 초 또는 30 초를 기준으로 하나 철 및 강철 에서는 15~20 초면 충분하다. 시험기의 조작 요령은 먼저 모루 (an vi l) 위에 시험면이 압입체와 수직이 되도록 울려놓고 정해전 하중과 압입체를 설치한 후 예비시험 으로 자국의 중심과 현미경의 중심을 일치시킨다. 모루를 뒤로 밀어
시험편을 압입체의 바로 아래에 위치시키고 규정된 시간 동안 하중을 가했다가 제거시킨 다음 모루를 다시 앞으로 당겨 현미경으로 a 와 b 값을 측정하여 표 또는 환산기에서 경도값으로 환산한다. 10— 5 파괴인성 (frac tu re tho ug h ness 또는 K(c) 10— 5— 1 파괴인성에 관한 이론 Bha t 145) 는 자국 파열법 (ind enta tion frac tu re me thod) 은 c/a~3 의 값 에 대 한 Lawn 과 공동 연구자들 146) 및 Evans 와 Charles147) 의 분석으 로 파괴인성값인 KIc 의 확실한 데이터를 줄 수 있을 것이라고 지적하 였다• 그립 10.7 에서 보는 바와 같이 c 는 반구형 크랙 (m edi an crack) 148) 의 반지름이고 a 는 자국(i nden t) 또는 압혼의 반모서 리 길이 이다. 그렇지만 c/a::;::3 의 경우는 KIc 의 데이터는 불확실한 것으로 나타났
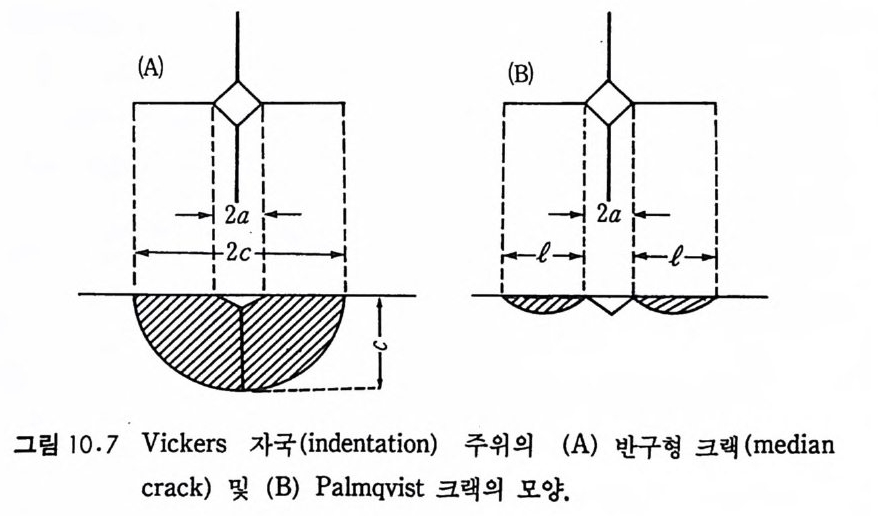 !ilI ( 重A ) 一 111I 2 2alc !:lI - 나!lI !~I!I 4n국 _i!I I2a l IF논I _-{ A 커l:!j
!ilI ( 重A ) 一 111I 2 2alc !:lI - 나!lI !~I!I 4n국 _i!I I2a l IF논I _-{ A 커l:!j
다. Marshall 과 Evans149) 는 자국내 기 과정 에 서 가능한 Po i sson 의 효 과 또는 마찰효과가 Bha t에 의해 알게 된 어긋남의 원인이 될 수 있 다고 그들의 답변에서 제시하였다. Lawn 과 공동 연구자들 1 4 6) 및 Evans 와 Charles”” 의 분석은 그림 10 . 7 의 (A) 에서 보는 바와같이 c/a 비의 수치에 무관하고 자국 주위에 형성되는 크랙은 반구형 크 랙의 형태를 취한다는 가정에 기초를 둔 것을 주목해야 한다. 유사한 어긋남을 또한 주목한 N ii hara 와 공동 연구자들 150) 은 c/a::s: : 3 인 경우, 자국낼 때 형성되는 크랙은 그림 10.7(B) 에서 보는 바와 같이 Palmq vist 크랙 151) 의 배 열을 갖는다고 제 안하였다. 그립 10 . 7 의 (A) 와 (B) 를 비교하면 2c/2a= (U+ 2a)/2a 이 고 c/a=f /a+1 이므로 f/a =c/a-1 {10.16) 인 것으로 나타난다. 만일 위 가정이 실제로 정당하다면 c/a < 3 에 대 한 자국파열 데 이터 의 분석은 c/ a..!i!.다는 I/a 비 에 근거를 두어 야 할 것으로 보인다. 많은 부서집성 물질들의 문헌 데이터 147),152),153) 에 대 하여 (K1c¢/Ha112) X (H/E¢) ”를 c/a 또는 £/a 의 함수로 도시 한 것 148) 이 위 가정에서 타당성을 확인시켜준다. 여기서 針큰 구속계수, H 는 Vic k ers 마이크로 경도 E 는 탄성계수를 나타낸다. c/a=2.5 에서 전 이가 일어나는 좋은 직선성을 보이는 두 개의 구별되는 집합의 데이 터로 나누어진다. c/a~2 . 5 인 반구형 크랙 (media n crack) 에 대하여는 그 데이터는 다 음 (10.17) 식으로 설명할 수 있다. (K1c/Ha1'2) (H/E¢) 0·4= 0 .12 9 (c/a) -3'2 ( 10.17) t/ a 효 .5 인 Palmq vist 크랙에 대하여 그 대응하는 식은 다음
(10.18) 식과 같다. f /a<2.5 는 c/a:,;;3.5 에 대응하지만 이것은 c/a~ 2.5 이상에서도 Palm qv i s t크랙이 존재할 수 있는 영역임을 나타낸다. (K1c¢/Ha112) (H/E¢)0·4=0.035( f/a)- 112 (10.18) 위 두 식의 왼쪽항을 c/a 또는 f /a 에 대하여 도시하면 직선에 데 이터들이 잘 맞는 것은 위 가정의 타당성을 나타내고 Bha t 1•s) 에 의해 제기된 문제의 만족스러운 답을 주는 것이 가능하다. 여기에 인용된 참고문헌에서 수집된 데이터들은 Palmq v is t 크랙에서 반구형 크랙 배열로의 전이가 잘 정의된 값 c/a=2 . 5 에서 일어난다. 그렇지만 이는 모두 부서점성의 물질들에 대해 보편적으로 옳지는 않다. c/a~2 정도로 낮은 값에서도 반구형 크랙을 형성한 것을 다 론 데 이 터 148) 에 나타낸 바 있다. Palmq vist 크랙 에서 반구형 크랙 기 하학으로 일어나는 전이는 더욱 연구할 가치가 있는 것 같다. 10-5— 2 파 괴 인성 측정 식 반구형 (half- pe nny) , 측면 (lat e r al) 및 방사상 (radi al ) 크랙 인 각각 me, le 및 re 의 상면과 단면도는 그립 10.8 에서 보는 바와 같다. 여
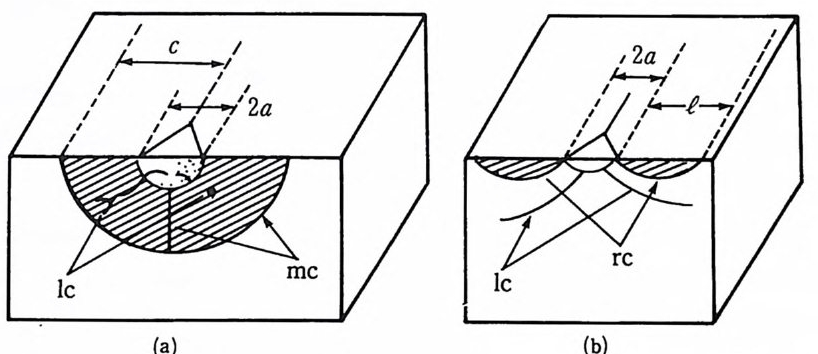 I C, , I► I/ I, I^ a , 2a /
I C, , I► I/ I, I^ a , 2a /
그림 10.a 반구형 크랙 (me), 측면 크랙 (le) 및 방사상 크랙 (re) 의 상면 및 단 면도.
기 서 le 와 re 는 Palmq vist 크랙 에 해 당한다. (1) c/a~2.5 인 반구형 크랙의 KlC (10.17) 식에 구속계수 : ¢~3 을 대입하면 (10.19) 식을 얻는다. (K1c /Ha 112)(H/E}°·4 = 0 . 06673 (c/a) -3'2 ( 10.19) 또 me 의 경우는 Lawn1s•) 등에 의해 제창된 중심에 응력이 집중된 반원판의 표면 크랙을 파괴역학 모델 155) 로서 다음 식을 유도했다. K1c /Ha 1'2 = 0 . 203 (c/a) -312 (10.2 0 ) (10.20) 식의 정수항은 고열압축 (Ho t Press) 한 B4C, SiC , Sia N 4, CVD 한 B.C, Sia N • 및 상암소결한 S i C 의 미소입자 압임파괴 (IM) 시 험 모델로부터 결정한다. 한편 경도, 탄성계수 (Youn g s modulus) 및 K(c 는 물질정수이므로 동일재료의 경우에는 정수로서 취급할 수 있 다. (2) f /a 회 .5( 또는 c/a~2.5) 인 Palmq vist 크랙의 KIC (10.18) 식에 구속계수 : ¢:::::: 3 을 대입하면 (K1c /Ha 112)(H/E)D · 4= Q. 018l(i /a) -li2 (10.21) 식을 얻는다. 자유표면의 보정등에 관련되는 (10.21) 식의 정수항은 ZnS, ZnSe, WC/Co, 고열압축 (Ho t Press) 한 S i 3N 凌 결정화유리의 IM 시험 모델로부터 결정된다. (10.20) 식과 (10.21) 식의 정확한 사용을 위해서는 Pc(pa lmq ui s t crack) 와 mc 의 식별이 필요하다. 두 식에 경도계산식 (H=0.464P/ 강)을 대입하면 하중 P 와 크랙 길이간에 mc 의 경우는 Pocc3/2 및 Pc 의 경우는 Poc .f의 관계가 각각 성립한다. 이 식별은 표면 관찰로부 터는 불가능하고 자국의 대각선에 연해서 시료를 판단한 크랙의 형상
울 직접 관찰하는 방법이 일반적이다. 이때 하중을 변화시키며 IM 시 험을 행하고 P 가 ¢또는 c 의 몇 승에 비례하는가로 me 와 Pc 를 식별 할 수 있다. 지금까지의 경험 155) 에 의하면 f /a< l. 5( 즉 c/a<2.5) 의 경우는 거의 모든 재료에서 Pc 가 지배적이다. (10 . 21) 식을 K,c 에 대하여 풀면 K1c=O .Ol8l x H0·6 x E0·4 x a/(f 112) (10.22) 식이 된다. 한편 (10.15) 식에서 a=b= &료 생각하면 Hv = 1854 . 4 X 균 ~k g/血균) (10.2 3 } = 1854 .4 X 갭겁 ~(k g /mm2) = 1854 . 4 X 10-9 x l06 X 醫붉 (kg /m 2) = 1. 8544 X 겔:책 (kg /m 2) = 1. 8544 X 醫챔 x 9 . 8 (m/sec2) (kg /m 2} =18.173X 醫봉 (N/m2) 또는 (Pa) = 18 .173 X l012 X 籍罰 (Pa)
Hv = l. 8173 X 107 X갑 隣罰 -(MPa) (10.2 4 } 식이 된다.
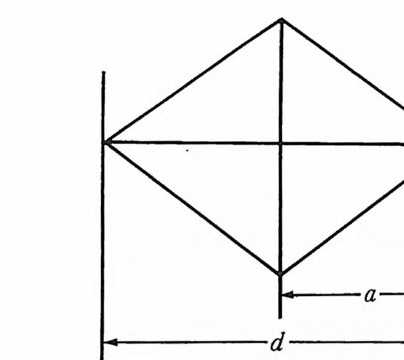 d
d
그림 10.9 자국의 모서리 길이 d 와 d/2=a 의 관계.
그림 10.9 에서 d2= (2a)2=4 강의 관계가 성립하므로 (10.24) 식은 Hv= l. 873 X l07 X갑 閑盟~ (MPa) Hv = 4 . 543 X l06 X~胃 ~ (MPa) (10.25) 식이 된다. (10.25) 식을 (10.22) 식에 대입하면 Kic = 0 . 0181 X [4 . 543 X l06 X 풀쁩깁 o.6 x Eo.4 x a/ (1112) =178.7X 터惡嗣 o . 6X 熹롱 2Yx 갑!;;;f 2
Ki c =0 .1787 x E0·4 [ 訂 晶 『 6 X 건::問 },2) (MN/m3/2) (10.2 6 } 식이 된다 . (10 . 26) 식에 압혼하중(i nden t a ti on load) P 는 kg , 자국의 반모서리 길이 a는 µm 및 Palmq vi s t 크랙의 길이 g은 µm 로 각각 대입하면 K[c 는 MN/(m312) 또는 MPa m112 단위로 얻어진다. 여기서 탄성계수 (Youn g s modulus) 의 단위도 MPa 이다. 10_5— 3 K Ic 측정 실례 (1) 몇 가지 계의 탄성계수 E 값 몇 가지 계의 탄성계수 E 는 표 10 . 3 에서 보는 바와 같다. 표 10,3 단순 세라믹스와 복합 세라믹스들의 탄성계수 E 값. Ex 1 0-s Ex 1 0-s 물질 (MPa) 물질 (MPa) TiB 2 5.3 ,0 TiB 2 -TiC (5wt° /o) 5.2 6 TiC 4.5 1 TiB 2 -TiC (lOw t° /o) 5.22 Al203 4.00 TiB 2 -T iC (20wt° /o) 5.14 SiC 3.8 6 TiB 2 -T iC (30wt% ) 5.0 6 TiB 2 -Al20 3 (5wt° /o) 5.2 4 TiB 2 -S iC (5w t<'/o) 5.2 3 TiB 2 -Al20 3 (10 퍼%) 5.17 TiB 2 -S iC (lOw t°/o) 5.16 TiB 2 -A b03 (20w t°/o) 5.0 4 TiB 2 -SiC (20wt %) 5.0 1 TiB r A l2°3 (30w t°lo) 4.9 1 TiB 2 -SiC (30wt° /o) 4.8 7 단순 세라믹스의 E 로부터 복합 세라믹스의 E를 구할 때는 백분비 의 합으로구하였다. (2) Ti B2 매트릭스와 복합 세라믹스 콤팩트의 KIc 계산식 i ) 순수 T iB 2 매트릭스 :
K1c = 0 .1787 X (5 . 30 X l0 이 o.4 x 昌麟 ]o.6 X 건::f 2) K1c=34.82[꼴 信汀 .6x 글巴罰 (MN/m312) (10.2 7 ) ii ) T iB 2 一 T i C(lO wt%) : K1c= 0 .1787 X (5 . 22 X l0 이 o.4 x [~껍麟 ]o.s X 간巳點 K1c=34.61[~껍 麟 ]O . 6x 궐巳告 (MPa m112) (10.2s) iii) TiB 2-Al203 (20wt %) : K1c=O .1787 X (5 . 04 X1 05) 0·4 X 昌麟 ]。 . 6 x 量冒鳥- K1c=34.13[~麟 (µ님 ]o . sX 홀릅 ~(MN/m312) (10.29) iv) TiB 2 -Si C (30w t%) : K1c=O .1787 X (4 . 868 X1 05) 0·4 X 〔息틀] O.6 X 글巴桐- K1c=33 . 66[ 플뵙y ]O.6x 궐巴罰 MPa m112) (10.3 0 ) 몇 가지 계의 KIc 계산식을 표시하였으나 갇은 방법으로 모든 계의 식을표시할수 있다. (2) Hv 와 KIc 의 측정 및 계산 자국법 (ind enta tion meth o d) 으로 실측한 P, a 및 b 값들로부터 Hv
를 얻고 P, a 및 { 값들을 앞에서 설명한 식들에 대입하여 KIC 를 구 한다. TiB 2 -TiC 복합 세라믹스 콤팩트의 Hv 와 KIc 계산 실례는 표 10 .4에서 보는 바와 같다. 표 10 . 4 에서 S-1 은 TiB 2 -TiC (5wt %), S-2 는 TiB 2 -TiC (lOw t%), S-3 는 TiB 2 -TiC (20wt %) 및 S-4 는 T iB 2-T i C(30 wt%)를 각각 나타 낸다. 표 10 .4에서 보는 바와같이 한 시료에 대하여 5 점을 전표면에 서 고루 분포되게 선택하여 IM 시험하고 Hv 와 KIc 를 구한 후 제일 작은 값과 제일 큰 값을 버리고 나머지 3 개 값을 평균하여 Hv 및 KIc 값을 얻는다. 표 1O.4 T i B2-T i C(5 wt%― 30 wt%)의 Hv 와 K1 총정 실례. (압혼 하중 : P=l .Ok g ) 시S료— N1o . 26a. 2 26b. 2 2H.7v0 Hv 26A.2 26B.2 13a. 1 25£. 2 4K.1,c3 KIC 28. 0 24.5 2.70 2.72 26.1 26.1 13. 05 25. 0 4.15 4.14 24.1 28.0 2.75 26. 1 26. 1 13. 05 25. 2 4.1 4 26. 4 26.4 2.66 26. 2 26. 2 13. 1 25.0 4.15 S— 2 3205..10 2251. .1 4 22..89 49 2265.. 62 2256..2 6 1132.1.8 2245..2 3 44..12 32 25.6 25.6 2.8 3 2.83 25. 6 25. 6 12. 8 24. 7 4.18 4.23 25.7 25.7 2.8 1 25.5 25.5 12.75 25. 8 4.1 0 25.7 26.4 2.73 25.6 25. 6 12.8 22.0 4.43 25.5 25.5 2.85 25.7 25. 7 12.85 23.5 4.29 S-3 26. 2 26. 2 2.70 25.3 25. 3 12. 65 27.3 3.9 6 25.1 25. 1 2.9 4 2.9 0 25.3 25. 3 12.65 24. 8 4.1 6 4.16 25. 8 24.6 2.9 2 25. 2 25.2 12.6 25. 0 4.1 5 25. 4 25.4 2.8 7 25.2 25.2 12. 6 24. 8 4.16 25. 2 25.2 2.92 25.2 25.2 12.6 24. 5 4.19 S-4 25. 8 26. 2 2.7 4 25.8 25.8 12.9 27.9 3.88 25.9 25. 9 2.76 2.7 8 25.8 25.8 12.9 27. 0 3.9 5 3.89 25. 6 25.4 2.8 5 25. 9 25.9 12.95 32.0 3.62 26. 5 26.5 2.6 4 25.8 25.8 12.9 22. 8 4.29 25.5 25. 5 2.85 25.5 26.1 12.9 28. 3 3.85
10— 6 꺾 임 강도 (modulus of rup tur e 또는 M.0.R) 꺾임강도는 세라믹스에 있어서 가장 널리 측정되고 있으며 그 측정 장치의 개략도는 그립 10.10 에서 보는 바와 같다. 하중 받침점의 수에 따라 3 점 꺾임강도 측정법과 4 점 꺾임강도 측 정법으로 대별할 수 있으며 JIS R 1601-1981( 파인 세라믹스 꺾임강도 시험법)에 표준화되어 있다. 꺾임강도 6 는 시료 파단시의 하중 P 와 그림에서 표시된 각 부분의 측정값으로부터 다음 식에 의해 계산된다. 3 점 꺾임강도 63= 23bPdL2 (10.31) 4 접 꺾임강도 64= 3P2(bLd2- £) (10.32)
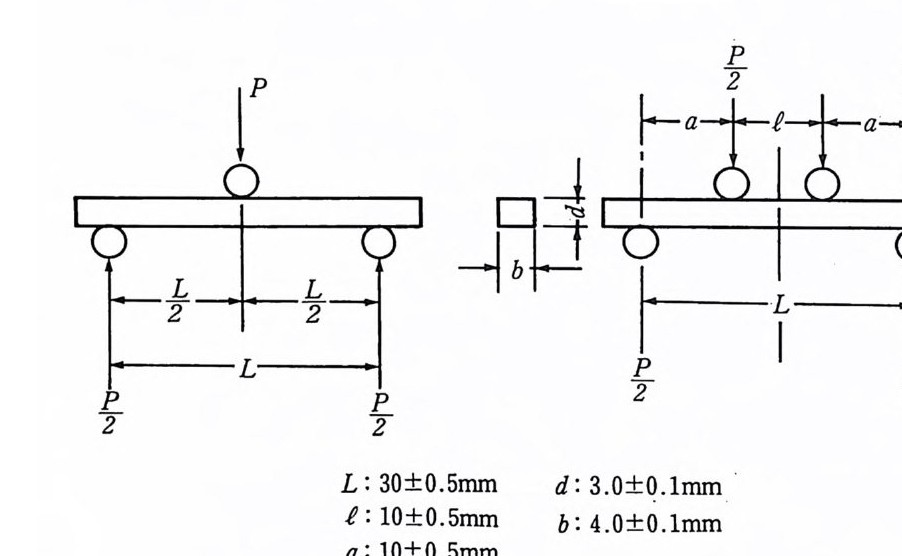 ·P r-a 2—P a TP _2
·P r-a 2—P a TP _2
그림 10.10 JIS 꺾임강도 시험법.
꺾임강도는 시험편에 생기는 최대 안장부가 파단될 때의 응력치를 측정 하여 강도를 산출한다. 따라서 그림 10 .10 의 시 험 편 아랫면만 최 대 인장응력이 작용하므로 야는 하중부 바로 아래만 최대 응력이 발 생하며, 64 는 안쪽 스팬 (s p an) 길이 E 의 범위에서만 최대 응력이 발 생한다. 따라서 3 점 꺾임강도는 똑같은 시편에 대해서 4 점 꺾임강도 보다 높은 값으로 측정된다. 실제 로 Si3 N 4 (Nort on Co. Nc-132 hot pre ssed Si3 N 4) 에 대 한 측정 결과를 32X64mm 의 단면을 가진 사각 기둥의 시편에 대하여 스팬 38mm 의 3 점 꺾임시험에 의한 파괴강도의 평균치는 930MPa 이었으며
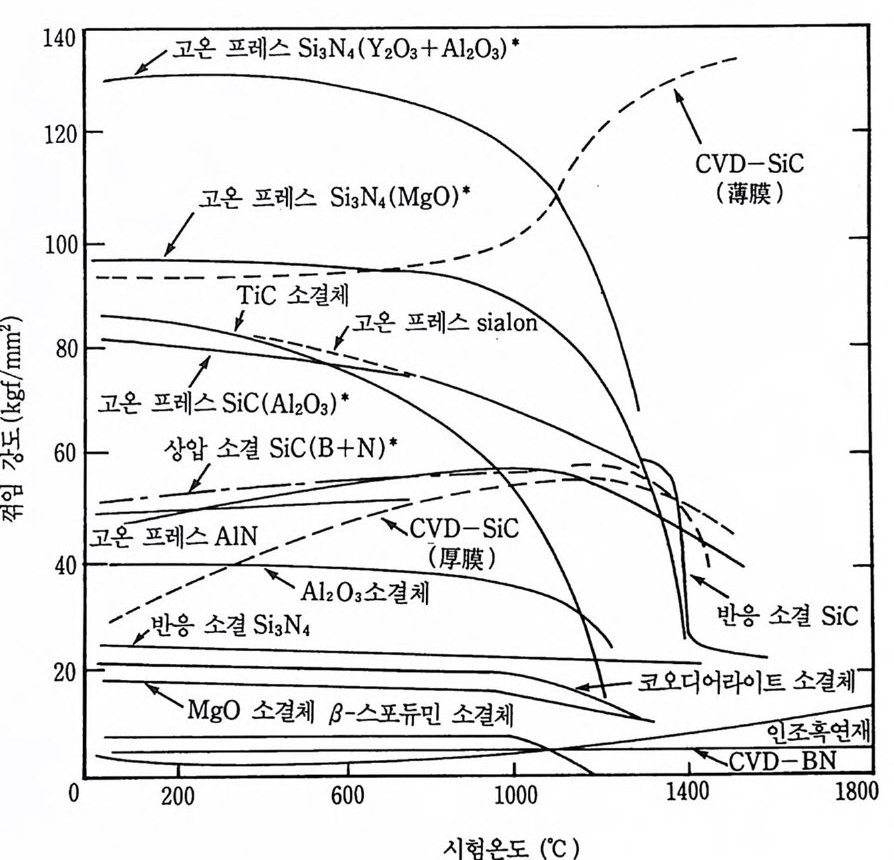 114200 乙고온 프레스 ShN4(Y2 아 +Al2 야)* / / / / / / --\-VDc sci )
114200 乙고온 프레스 ShN4(Y2 아 +Al2 야)* / / / / / / --\-VDc sci )
그림 10.11 각종 세라믹스의 꺾임강도(*괄호 속은 소결조제).
4 접 꺾임시험에 의한 파괴강도의 평균치는 724MPa 이었다. 세라믹스는 1000°C 이상의 고온에서 사용되는 일이 많으므로 이에 상당하는 온도 영역에 있어서 강도측정은 필수적인 것이다. 이와 같 은 고온측정을 할 때에는 시료의 지지, 로드 셀(l oad cell) 의 냉각 및 장치의 설계 등에서 상온측정과는 다른 준비가 필요하다. 아래의 그립 10.11 에서는 각종 세라믹스에 대한 꺾임강도의 온도 의존성 156) 을 나타내었다.
동 공공과 12yes n on ono on non on oys e ys e 기
도밀 ) cm(g/3 11 1.9 8. 8 .88 .90 9.8 9 .8 9 8.8. 9 2 .5 5.2 징 팅의)공 과정생물성의 특의성 특물생성석분학 화적 선분 -x상 석이%)론 ( 10 8 9 76 oMM ; 2Co7 5 2Co M 59 C2o M99 5. 2o MC Mo; 78 2CoM M o; 8 0M 2CoM o : 83 oMC26 9 5 . 2CoM 9 72C, C,VV V 43CVV2 C, , V 85 연( 소주조스캐체기압력심 원속 가)(g mt)(a 45 10 10 2001OlOg O OlOg001 300010g lO1OgO00 0g00115 0 1 001 A : 부록비 기체체기비 공주연조소정 물출조합 혼 발물성 388O 2Mao +g 2Cg11+ A0 g8l 525g 곱 0V2 C2g72+0lg A7 종성 생2 M2oC C V최 호 번l료k 112345678901on no noon e sy e sy no no no no no no no s ey s ey no I I| I .15 2.5 1.51.5 7.06.9 8.6 .96.86 .86 4.51 5.21135.8.4 8.28.1 C V,2C VV,C2 ,VVC,C,VC2V V 2CC V V,,C ir C3C ,rC, Cr C, r2CrCr ,C 3C. r 3C2CC r, C4r 3, C2rCC3CrC. , 2r CCCi, C CraC 4 rC, 2CW W, W2C WCC, 2CW Wo BB M oMoM,2 , oBoMM 2B ,BoM 49 50 878 85. 0 ·2 8 79.76 506 728 0 670 0 84 7 94.996 OOl Og OglO 5001g lOO Og 100g 1500 g 020010011001010200011000015100020011002000 C+00033 rg 42 C6l21A+g g 22Oa3 W+ g 45 1A+2lCg g O882oMg J+ 30l7A 210+62Bg g r3GCWCBMo
112 11 3 1415 16 71 18 19 20 21 22 32 245 2 26on n oo ns ey on on noes y es y no no no no I || |I I | I II
4.8 .18 81.8.2 8.2 5.8 .958.2 1.8 82. .28 .48 8.2 .713 oB,Mo M2M oB, oBMoM ,2B M oBo o,2MBMB,ooM 2BBM N ,V3VN, VV ,VN ,NV3 M,TC2o,T C ii , oM T MC 2,,oCi o MNi ,M C2T , NoCii C2T, Mo N,C ii Co2NT, M C,ii Co2T, M N,Cii C CC2Wo ,W , 06 87 78 829680909 579 9 9 9679 98 62 g OOlO OOg l g lOOO lOgO O lOgO lOOO g 11 000 101 1 000 100200 100 1 00051 0 10010 5 8g28곱Oo M 9gg1a20+2 70BMg 7sV2 5Ag025 +2g0l 7g 2 0o8M Tg0 l lg C+20+4i + +g50.0N1g36 i Al c 3+232gow g12 l5l+o+g C4g Al M oBVN tw %TC30i w% t6+0 oM20% t01+Nwi t% WCw,59 t% w+ oC5 2728293013233334533637383940on nono n on oo n noo nes y s ey no es y no I I I II I 7.1 3731. .14 1 3.81 7.134 01. 1.14 .1 41. 57 .75 .55 . 54 C,2C,W W Co,W CC,W2C o 2C Co W , CWW,,C , CW 2o,WC,,3 CWW CC o C, C2,WWACl, oA ,,lCCC ,W Wo2 C ,CW,2WC o ,CCT23Cr, C rTi ,i —-|| | |- I C, CrT 3C •r ,C2, i Ni —3C2, CT Cr, Ni iI II _ _2 CVV, CV, — _| ,evC2CV, o I 1I - 572806768067708265I789850I | 80 001 200 05 00 10 020 5100 020 0 1I 00 110002 001 I ct%w ogw232 30g921 +CW wt C8+g% 20l 0 Co 6g+toA0l w%t +CW20g2 23g3 1 W8C0 w6 9+0+%ogt Cg A64 l2+ oC0 tw%0g24 T 0540+ 2g20C Tii 03rCg75+N gw t%+65+04i i C2+l A0C g5C3r t%w+N10i I%tw 90 g0g+s44 OzCV64V I t%w CColA o gC+758+2g70+10 I I 1424 4 34 4 5446 748 49 450 15 52 35
no es y on o nes y o nn oes y no nos ey I I I I| |
5.4 6.8.85 5.8 5.65.54.5 57. 5.65.652. C o 2CC V VI ’2 BB oo,, M’oMM IooBM,MB 2N ,i BoM N, i VVCV, 2, C, CV,M n2 NVCi , , V,CzC NVMn i , , CV ,C2V V, CV 2 CV,VN, i C V, C2 N,Vn Mi, T,CT3C, rC2 i, i r C —一I I I 5 267 89 79- I 5757 98 2 597 96 67 0 2~0 I 0012 000 1 10002 001 0 0100 20 1 o 98M2180tgB20w07+o M %g 01+wN.9+02OtBN352g % ii + A57l1 g cv 085V5 2s52g%tw 25+7O9+CNg+N 0 1g%w tii +2A 8 6.l52 ++52gt% w ng M M n cv5805522V%gt s w 41+72++Ct%w6gN2 N g i i + Mnl%tw4+ nM g 54 CT %tw2081+T 0 gii 04+9/owtCr2CN+306O52r0 g g i,J:-i 01+20+NM t%g wCg7g+5 i M%tw5++ 8l 25 gAg 5455567585596061266364no on on se y se y n oon es y o n nos ey es y II I | T ,C2,CC3r Ti,1.5 i I Ni I iC,N5r,3 .CMC 1Tg ,ii iC ,Cr ,NM 3CTg i i,52. — 1-1| .126 W ,2BW W ,B2 W 126.W B ,2W .123 WB ,2W .124 2W ,CW W ,C.145,C2W ,n C MW341.,C2W, n C MW314. i,CCrCr C r3., C17. — LC o ,2MCr3 C,|C| r407.I 1 00 172000 96 6902 00— I|5Ol3O g 니 030 1 g60 0510 g106 0010501 27 g 16 2 001 87 002083 24 1 II 7 _ 00|51 I I peaals mmxaewt%ss e (C T54i 664)6 -+r4C41/w°:o,:/ i t %+1w0N i w %tlM+g 133Ww+& 2B79o+B02 3g I Al 72 g c w%t203o2329 Cw1W+ gg nM %tw 5+32nM+4Al g10+g %tw2CCaC C+20583r030 r4g g % wt M 518++2ooM g 2 6+1AIgI 56 6 667 68 9607 71 723 74 775 67
nonononononononononononono I I I || I I I| | | | I 7.0 . 06 75. 5.7 5.2 5 .15 3. .0 10.6 9 .6 9 6.0 8.1 7.8 I o
— —C 2C Mo3r,I III N7S2b6 b,N i bNbS Ni28 ,z N2NbS ,b i68 3V VS i, 78 3Sv v ,i80 3VlA, SVi ,3 8 Sh W0WS 2,1i77 S, WhW102S i 97 , W21W%0S i8 1 02M, MSoS3ii .588 — |2,CITMI - Mo C, i-仁 — —CC IM1 o -1 TI ,2 i 96OOlO g-I 001 g OOOlg OOlO g lOO g OOOl g OOOlg lOO g OOlO g OlOO g gsol 1oo g | 955010 g ~200 I010 001 10 10 010 1100 010 1 11 01I0 08g 곱N2b0 27200.7+ l2SA igg 1 03V6+26g 1A360l02S +3gg i w373S2600 o+g ig 73+ .8Alg o.2343M+0 g 3+A 63028lSgig 04g 급iO T IOgi O곱Mo 821A+5lC gg SNb2i 3SV i WS2 i M02 Si tw% C3T0i wt%07+ o2MC 77 7897 08 1882 834 8 586 87 8 88 89OU OU OU 음 C--• So. T0 -., 00 . gg. 8.VI !.L'Z!S zgwo g0zW -ozN z!s zb0!oO,0Jsw― L읊o 0 ,gI| •z I8-9z oowBm!J Ow 0, 「「― g도O '0ZgIBI! | SO O gI oggIH_bRL「 O' 3_-o03:0 A --Z0I 6Ag _I _ I—— i T-, C=> F-, OOI OOOg 오 zi%0홍9 zo0+2O!z6 S 4 £! !.. L4L~%+ + Z slOMot~ 0°IZl>W9+O0b !0OS 己0 0 09z !S없홍 9%0£gO0 o°WHwF+o~zi 죠琴공유++3 0 z O00!i[io.0oVL0zt 0 ~g없 +t oz경gCZ3 A哀홍03gggII+3+ c0A+ 凌홍OoN― 0cBB+09c090NW 6
부록 B : 비기체 연소반응에 관하여 선택한 소련 모델 의 요약 8-1 제목 : 비기체 연소이론 93) 저 자 : A. G. Merzhanov 초록 : 이 논문은 비기체 연소이론의 일반적인 리뷰 (re vi ew) 를 하고 표준 단열 열역학적 모델과 일차원적인 에너지 균형 모델을 나 타낸다. 이 일차원적인 모델은 정류상태로부터 비정류상태 반 응속도론의 경계치를 조사하는 데 사용된다. 이 논문은 또한 이차원적 정류상태 질량 및 에너지 균형 모델 94) 에 관한 결과를 나타내고 또 토의한다. 또한 그 논문은 압력, 반응속도 및 비 정류상태 반응속도론의 실험적 결과를 나타낸다. 모델 : 열역학적 모델(p .9) 이 논문에 간단히 설명한 열역학적인 모델은 Nov iko v 등이 1975 년에 발표한 하나의 소련 논문 95) 과 같다. 반웅 후에 계의 엔탈피는 반응 전의 엔탈피와 같다. 죽 계는 완전히 단열이라 고 가정하였다. 이 모델은 위에 인용한 논문에 설명되었기 때 문에 여기서는 다시 논하지 않을 것이다. 일차원적인 비정류상태 모델(p . 11) L 모델 이 모델은 단지 축적 (accumulati on ) , 확산 (diffusi o n ) 및 발생 항(g enera ti on t erm) 을 포함하는 일차원적인 에너지 균형이다. x- 축은 무한히 작은 반지름의 원동형 반응용기 아래로 세로 길이를 나타내도록 논의를 통해 가정되었다(그 인용된 논문의 95) p. 12, 그립 3 참조).
(accumulati on ) = (net dif fusi o n in) + (ge nerati on ) C_p d굶T_ = X_a2¥T+ Qp 사( T,n) 만약 속도가 일정(정류상태)하면 움직이는 관련 골격은 u= dx/dt 로 나타내서 응용될 수 있다. 2. 가정 1) 반웅체적은 일차원적이다. 죽무한소반지름의 원통형이다. 2) 비열 Cp 와 열확산 I는 관련범위를 통해 온도에 무관하 므로 유효 또는 평균값들이다. 이들 두 파라미터의 온도 의존성은 거의 조사되지 않았다고 그 논문에 설명되었다. 이것은 그 반응이 본래는 균일하다는 것을 암시한다. 3) 그 반웅생성물은 반웅 도중 또는 반웅 후에 확산되지 않 는다. 4) 그 반웅속도론은 Arrhe ni us 식 :
따라 명확히 정의된다. a=9 .l 군罰 _0.21- ft) a 키일 때 정류상태 연소가 되고, a< l 일 때는 진동상태 연 소가 된다. 이 식은 계산으로부터 얻어진 것으로 논문에 언급 되었다. 진동작용에 대한 조건들(임계치보다 더 큰 과잉 엔탈 피 죽 T> To 및 n :::::이을 그 모델에 대한 해에 삽입한다. B..:....2 제목 : 금속입자의 접화이론 Il . 생성물 필름과 고용체 96) 를 동시 생성 하는 금속입자들의 점화 저자 : A.B. Aruty unyan , S.L. Kharaty an 및 A.G. Merzhanov 초록 : 한 개의 구형입자에서 계면이동을 포함하는 2 차원적 반웅 모델 은 오래전 논문9 7) 에서 세워진 바 있다. 반응물들이 상호확산하 지 않는(여기서는 용해도가 중요함) 두 성분 상과 반응물이 상호 확산을 통해 고정된 띠 (r igi dband) 가 생성물을 형성하는 한 생 성물의 상 사이에 구별이 생긴다. 반응물의 용해도와 반응속도 가 변하는, 즉 계면이동에 대하여 경계조건이 변하는 반응계에 그 모델을 응용한 결과를 이 논문이 나타낸다. 이 모델은 비금 속을 고체금속 구형입자에 확산시키는 대 적용된다. 모델 : 일차원적인 · 비정류상태 (반지름, 시간) 1. 모델 질량과 에너지의 균형은 구형 금속입자에서 이루어진다. 의 부 생성물 상과 내부 금속반응물 상 간의 상 경계에 농도의 불 연속아 있기 때문에 분리된 균형이 각 상에 대하여 필요하다. 2. 가정 1) 완전한 구형 고체금속입자. 중심은 r=O.
2) 비금속 반응물은 생성물충을 통하여 그 상 경계(― r) 까지 확산된다. 그 상 경계에서 반응물은 생성물을 순간적으로 생성하도록 반웅하거나 또는 그 반웅 상 경계가 반응물에 이를 때까지 그 반응물은 금속반응물 상으로 확산된다. 3) 상 경계의 어느 한쪽에서 확산하는 비금속반응물의 농도는 시간에 무관하고 적당한 계의 상태도로부터 결정될 수 있 다. B— 3 제목 : 연소조건에서 고용체의 생성 98) 처자 : A.G. Merzhanov and E.N . Rumanov 초록 : 이 논문은 반응하지 않는 용질기체가 다공성 고체용매로 확산 하는 현상을 논의하고 모델화한다. 그러한 계의 예는 TiO , Ti N , ZrN, 및 몇 가지 다른 질화물들이다. 반응물의 띠구조 에서 실제적 변화가 일어날 때 (특히 여기서는 고체인 용매상)와 용매분자에 대한 용질의 화학량론적 비가 그 생성물 상에 적당 할 때 화학반응이 일어나는 것으로 간주한다. 용해도 원리로 설명할 수 있는 고용체는 한 반응용질이 주된 결합구조 변화없 이 용매반웅 상을 통해 확산될 때 생긴다. 그 고용체 범주는 이 논문에서 고려된다. 용질유체 (기체)의 확산은 다공성 가압 금속분말 용매상에서 일어나는 것으로 추측된다. 혼합의 열적 효과(지배적인 엔트로피)가 고려된다. 모델 : 용매내의 용질의 확산도 룹=발산 (D v a) D=ko exp (- E/RT)
E/R 은 일반적으로 105 의 차수를 갖는다. 8 一 4 제목 : 분말의 정류상태 연소 이론 99) 저 자 : A.G . Merzhanov and F.I. Dubov itsk ii 초록 : 간단한 일차원적 정류상태 에너지 균형 모델 T= T(x,u) 을 소 개하였다. 여기서 T 는 온도, x 는 위치 및 u 는 연소 진행앞면 의 속도이다. 반웅영역 (reacti on zone) 의 크기를 예측하는 데 이것이 사용된다. 이 모델에서 그 가정은 아주 제한되며 그 결 과를 사용하기 전에 주의깊게 재검토하여야 한다. 모델 : 일차원적인 에너지 균형 1. 모델 이 모델에 사용된 좌표계 (refe r ence fr ame) 는 연소 진행앞면 (La gr an gi an) 과 같이 움직이는 한 원점을 갖는다. u= 굶dx 인 것을 주목하고 연쇄규칙 (chain rule) 에 의 하여 dT dT U 孟=詞 이것은 한 누적항이다. 릅三당-+올 -k 。 exp( - E/RT) 누적 = 결합에의 순수에너지 + 반응에 의한 열발생
2. 가정 1) 반응 기하학적 구조는 일차원적 즉 무한소 반지름의 원통 형이다. 2) 반응은 발열반응이다. 3) 반응속도는 v=k 。 exp (-E/RT) 로 나타낸다. 4) 반응은 균일상으로 일어나고 확산 제한보다는 속도 제한 에 해당한다. 죽 반응의 존재는 충분한 양의 에너지 유효 성에 의해서만 결정되고 반응시간에 반응물의 유효성에 의 해서는 결정되지 않는다. B— 5 제목 : 분말의 연소 메커 니즘 100) 저자 : G.B . Manelis, A.G. Merzhanov, and F.I. Dubovit sk ii 초록 : 이 논문은 비기체 연소를 포함하지 않는다. 고체성 분말이 에 너지의 복사 방출하는 불꽃을 내며 기체상의 생성물이 되는 연 소반응에 관한 것이다. 설명되는 현상은 본체 고체상으로부터 떨어진 고체상 원자가 산화제와 어느 단계에서 반응하여 최종 적으로 기체상의 생성물이 되는 메커니즘이다• 그 분말은 본체 고체상으로부터 입자로 분산되고, 기체흐름으로 옮겨지며, 본 체 고체상 표면과 고열 불꽃영역 사이의 어느 곳에서 고체원자 로 분해 되거 나, 또는 불꽃영 역 (fram e zone) 에 입 자로 옮겨 져 그곳에서 반응한다고 저자들은 가정하였다. 본래 고체상의 표 면온도 함수로서 입자의 분산을 설명한 저자들의 지난 한 가지 연구 99) 중 개발된 식을 사용하면 입자의 수명 및 그 수명 동안 기체흐름으로 입자가 이동된 거리에 대한 식이 얻어진다. 모델 : 유동적인 기체흐름에서 고체입자의 열분해 1. 모델
값=占 a koe-E/RTs[~。 -〈 T;;E(1-nd)/c] (참고문헌 99 참조) 2. 관찰 저자들에 따르면 공간과 시간에 분산된 입자의 열분해 문제 의 완전한 해는 입자의 움직임을 통제하는 법칙 및 입자와 주 위 기체간의 열교환의 법칙의 지식으로부터 얻을 수 있다. 아 직 주어진 그 식은 고체입자들이 분해되는 입자 표면으로부터 기체상으로 확산하는 물질전달 양상(분산도, nd) 에 관련된 단 지 한 항만을 포함한다. 참고문헌 (99) 에서 이 〈완전〉해의 유 도를 알게 되는 것은 분명하게 될 것이다. 3. 결론 참고문헌 (99) 로부터 그 모델에서 구체화된 가정과 설명된 메커니즘하에서 그 입자들은 그 본체 고체상 표면 근처에서 원 자로 분해되고 기체흐름에 의해서 불꽃영역까지 옮겨지기 전에 300cal/ g 또는 그 이상의 열에너지를 방출하면서 그곳에서 그 둘은 산화제와 반응하여 생성물을 형성한다는 것을 저자들은 알았다. 8_6 제목 : 불균일 응축매질에서 연소과정의 이론을 위하여 101) 저 자 : B.I . Khaik i n 초록 : 이 논문은 2 차원적인 모델을 나타내고, SHS 실험적 연구를 이 론적 분석으로 뒷받침하는 저자들인 A.G. Merzhanov 와 네 사 람의 공동 연구자의 연구를 리뷰한 것이다. 이것은 비기체 연 소에 기초를 두고 있다. 이 논문에서 나타난 모델은 반웅물 A 층과 반응물 B 충간(가정을 보라) 상경계인 선형계면을 설명한
다. 연소 진행앞면(한 접)이 그 계면을 따라 전진할 때 그 생 성물이 형성된다. 이 계면의 한쪽에 생성물이 형성될 수 있기 전에 이제 생성물을 포함하는 반응물 A 는 이 생성물 충을 통 하여 새로운 반응물 B 에 달하도록 확산되어야 하며 역도 또한 같다. 모델 : 이차원적인 정류상태 및 에너지 균형 l. 모델 2 차원적인 모델은 순수한 균일상 반응물 B 로부터 순수한 균 일상 반응물 A 를 분리하는 1 차원적인 상 경계이다. 이 모델은 고체반응물 충들로 된 평평한 수평계의 수직적인 단면도를 나 타낸다. 그것은 하나의 A 와 하나의 B 로 된 고체반응물의 두 입자간의 경계를 묘사하는 데 사용된다. 질량균형은 시간의 함수로서 농도 분포를 결정하기 위하여 무한소 체적요소에 대하여 만들어진다. 그 모델은 기본적으로 다음의 형태를 갖는다. 누적 =순수확산 UC, 坐dx = 峰 _ 파뿡 움직이는 계면 y방향으로의 x 방향으로의 에서 물질흐름 순수분자확산 순수분자확산 그 모델은 원점이 연소 진행앞면과 같이 움직이는 Lagr an - gian 좌표계를 사용함으로써 정류상태가 만들어지게 한다. 그 속도 (u) 는 일정하다는 가정과 누적항 (accumula ti on t erm) 을 수 정함에 의하여 정류상태가 된다.
누적 =뭉=뿔씁 =u 꿈 A 가 생성물 상으로 들어가지만 -x- 방향으로 확산되기 때문 에 계면 y 1 에서 A의 흐름에 기여하지 않는 그 A 만큼 작게 y-방향에서 생성물상 AB 를 통해 A 가 분자확산하는 것으로 움직이는 계면의 질량흐름 (mass/L 2t)이 주어전다. -x- 방향으 로 확산하는 한 A 분자는 더 많은 A 분자를 만날 것이고 +x- 방향으로 움직이는 한 A 분자도 더 많은 A 분자들을 만나 는 반면에 그 한 분자는 그 계면과 B 를 마주치게 될 것이다. 한 유사한 균형이 에너지에 대해서도 수행된다. 한 균형은 일반적으로 엔탈피로 되어전다. 만약 고체상들이 상전이가 일 어나지 않는다고 생각하면 dH=Cp d T. 그 전체 균형식은 dH 보다도 dT 를 얻기 위해 Cp로 나누어질 수 있다. 누적 =4rt- =d4 t 4rx = u 4 rx- 晉확산 = 급룹) _ 딤풍) 2. 가정 그 반응은 일반적인 규칙으로 제한되는 확산이다. 그 반응속도는 빈응물늘의 접촉과 동시에 일어나는 것으로 가정된다. 그 열방출은 반웅과 동시에 일어난다. 반응에 의하여 방출되는 열의 분산에 관한 여러 가지 설명을 가하였다. 1) 반응열은 반응대를 따라서 균일하게보다는 생성물충 내에 서 국부적으로 분리된다. 2) 상호작용의 가정된 메커니즘은 상의 분리 표면상에 최대
로 편재된 열방출에 대응한다. 3. 경계조건 y=yi (x) 에서 즉 반응물 B 와 그 생성물충간의 x 에서 반응경계 (-f1
부록 C : AlN, TiB 2 및 T i C 의 합성에 관련된 열역학적 물성 표 C-1 열역학적 상전이 데이터. 법 례 : **LT mb,, T mL s,T, sL t및 및 T Lt( , K(k) J /gmo l) *t:.V m= V( 여제V () -페V( 각 번호 물질 데이터 1 알루미늄 Tm = 660.1 Tb = 2520 Lm = 10.47 Ls = 324.1 k = 291 .4 t:,.V m = 6.5% 2 Tu ..L ..,,.._ Tm = 2300 Tb = 2550 Ls = 577.8 3 탄소(혹연) Tm = 5000 Ts = 5000 Ls = 712 LI, (다이 아몬드一흑연) = 1.90 4 질소 Tm = —2 10.0 Tb = -195.8 L = .72 Lb = 5.581 t.Vm = 7.3% 5 티탄 Tm = 1667 Tb = 3285 Tt, (a ➔ 8)= 882 L = 18.8 L. = 469. 3
Lb = 425. 8 Lt, (a-+/3 ) = 3.4 3 6 | 이산화티탄 (T i 02) T1 , (a-+{3 ) = 991 Lt, (a--+/J ) = 3.4 3 • 표 C ― 2 상태함수에 관한 열역학적 데이터. 물질 _Ag2moH·oc ( lk에) J서 / 의g m성So (l질 J./ K ) 300K 50G0K—ib b6 .sG l자O(kO유JO /에Kg m 너o 1지l)5 0, 0K 2000K Al 。 28. 34 8.5 AIN 320.3 87.0 294.3 275. 9 Al203 1674.7 51. 1 1580.5 1517. 3 1359. 9 1143. 4 B( 결정) 。 5.9 1.8 B203 1281. 6 54. 0 1201 . 0 1148 . 9 C( 흑연) 。 5.69 1. 7 N2 。 191.63 57.5 02 。 205.24 61 .6 Ti 。 30. 31 9.1 Ti C 183.8 24. 3 180. 0 177.9 172.9 167.1 160.4 Ti O 518.7 34. 8 485. 3 467. 7 422.9 378.5 333.7 Ti 02 944.1 50. 2 862.1 827.3 739. 5 652. 7 564. 8 Ti 20 3 1519.4 78.7 1424.3 1373.3 1243.9 1115.4 986. 9 Ti sO s 2457. 2 129.4 2309.4 2224.4 2010.1 1797.0 1581 .8 표 C ― 3 열용량 상수에 관한 데이터. Cp =4.1868[a+10-3bT+l05cT 기 (J/m ol • K) 물질 상태 a b C 온도범위 (K) AAll 고액체체 74..90 4 2.9 6 T2m9—8 -1T2m7 3 AIN 5.47 7.8 0 298-900 Al20s 25.48 4.25 -6.82 298-Tm
BB 무결정정 형 34..08 31 53 22..31 96 5 --11..75 90 229988—- 1l2lO4O 0 B203 결정 13, 63 17. 45 -3.3 6 298-7 23 B 20 3 무정형 2.2 8 42. 10 2.9 8 -7 23 B203 액체 30. 45 900-1800 C 혹연 4.1 0 1.02 -2.10 298-2300 N2 기체 6.6 7 1.0 298-2000 TTTiii B 2 베알타파(f (3a)) 110651.... 9982 8323 270...148 00 1222199908880——-— 1 111128300050 0 0 0 TiC -3.5 8 TTiiOO 베알타파 ((a8)) 1101.. 5875 33..60 一1. 86 1229684-—1 218604 0 TTii22 00 3 3 베알타파(f (3a)) 374.. 36 18 531.. 352 一 10.2 247938— -184 07 03 TTii33 00 s 5 베알타파(/ (3a)) 3451.. 6470 289..500 425908 一— 14450 00 표 C-4 열전도도와 비열에 관한 데이터. 물질 온도, T('C) 비 열, Cp (J/gK ) 열전도도, k(w/mK) Al( 순도 99%) 100 209 Al( 순도 99. 5% ) 100 218 Al 20 900 238 100 938 238 200 984 238 300 1030 238 400 1076 238 660 1080 94.03 700 1080 95.37 800 1080 98. 71 900 1080 102. 05 1000 105.35 B 2077 2910
Ti 20 519 16 100 540 15 200 569 15 400 619 4 600 636 13 800 682 13 표 C-5 증기압 상수에 관한 데이터. log P= -( A/T)+B+C log T + 1 0- 3D T 물질 P(mm Hg ) A B C D T(K) ABl 1269490500 1123..8 386 --11..002 3 1210000-— T2 8m0 0 Bi2 0 3 23200 11. 74 _ 。 .66 Tm- T b TTii(( /a3 )) 1246490600 613.6. 41 8 -0.9 1 11310505 —一 ·1 T6 m 5 0 용어 풀이 Cp : 비열 gmo l : 그램몰 t::.G : Gib b s 자유에너지 H: 엔탈피 J:줄 k: 열전도도 ·c : 섭씨 온도 K: 켈빈 온도 Lm: 융해 참열 L.: 승화 참열 L t:전이 참열 Lv: 증발 참열 m: 미터 mm Hg : 밀리미터 수은 압력 Tb : 끓는점 s: 엔트로피 T: 절대온도 Tl: 전이온도 Tvm :: 녹체는적접 Tw.: : 승와화트접 t::.V m : V( 에세V )(- 피V ) ( 고세 )
j;:드부노 .%0~0叫lt: 옥포후r i’\r\tt 폭’。 모晶
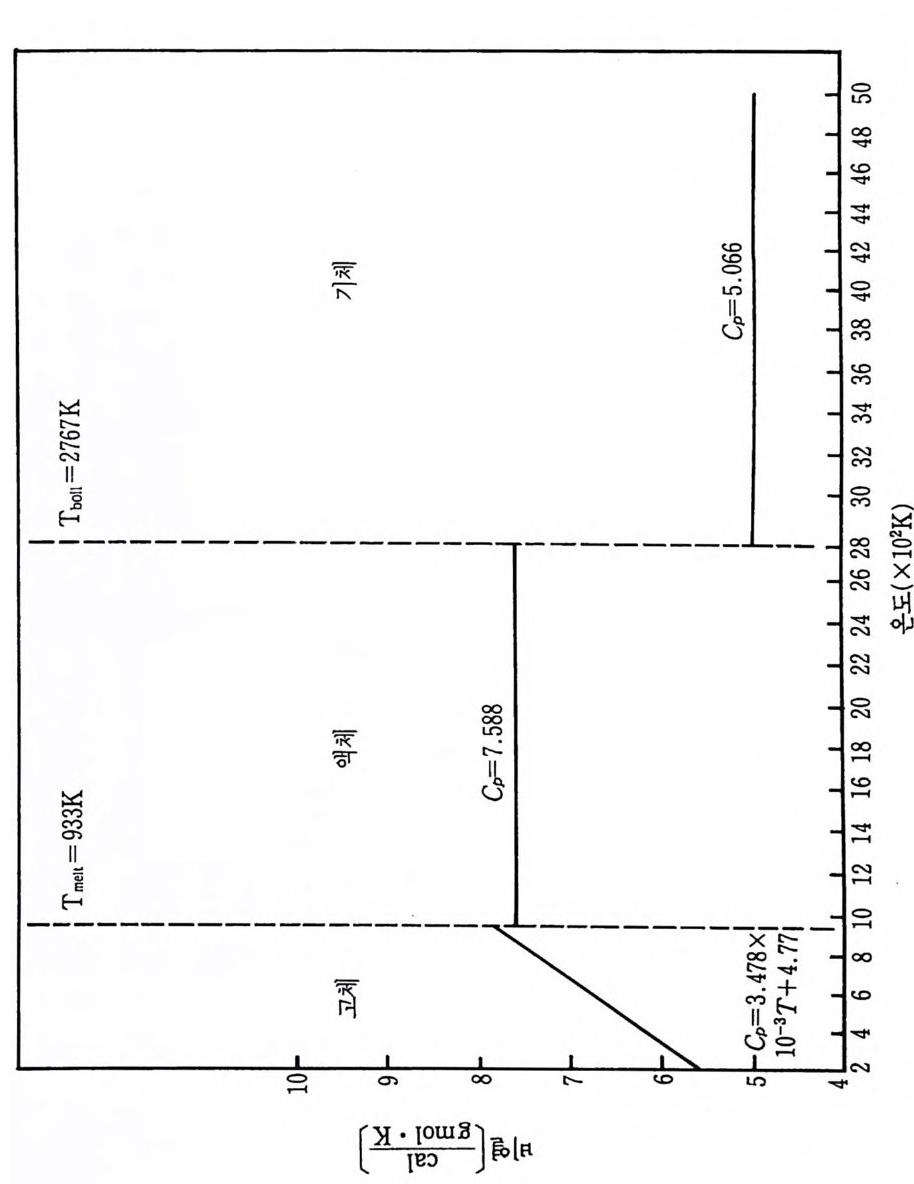 05
05
열, 비 른따 에 도 온 의 Al D-1 그립
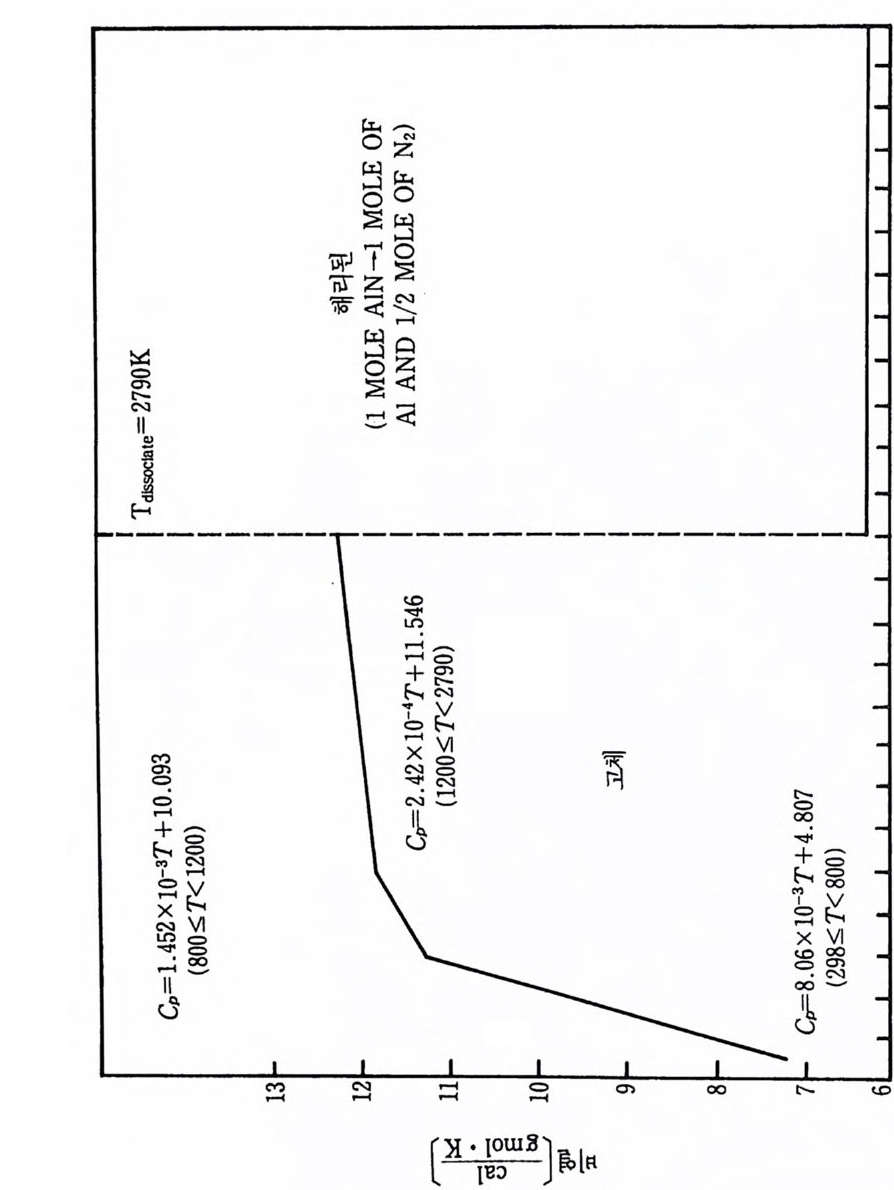 05
05
. 열 비 른따 에 도 온 의 N I A 2 -D 림 그
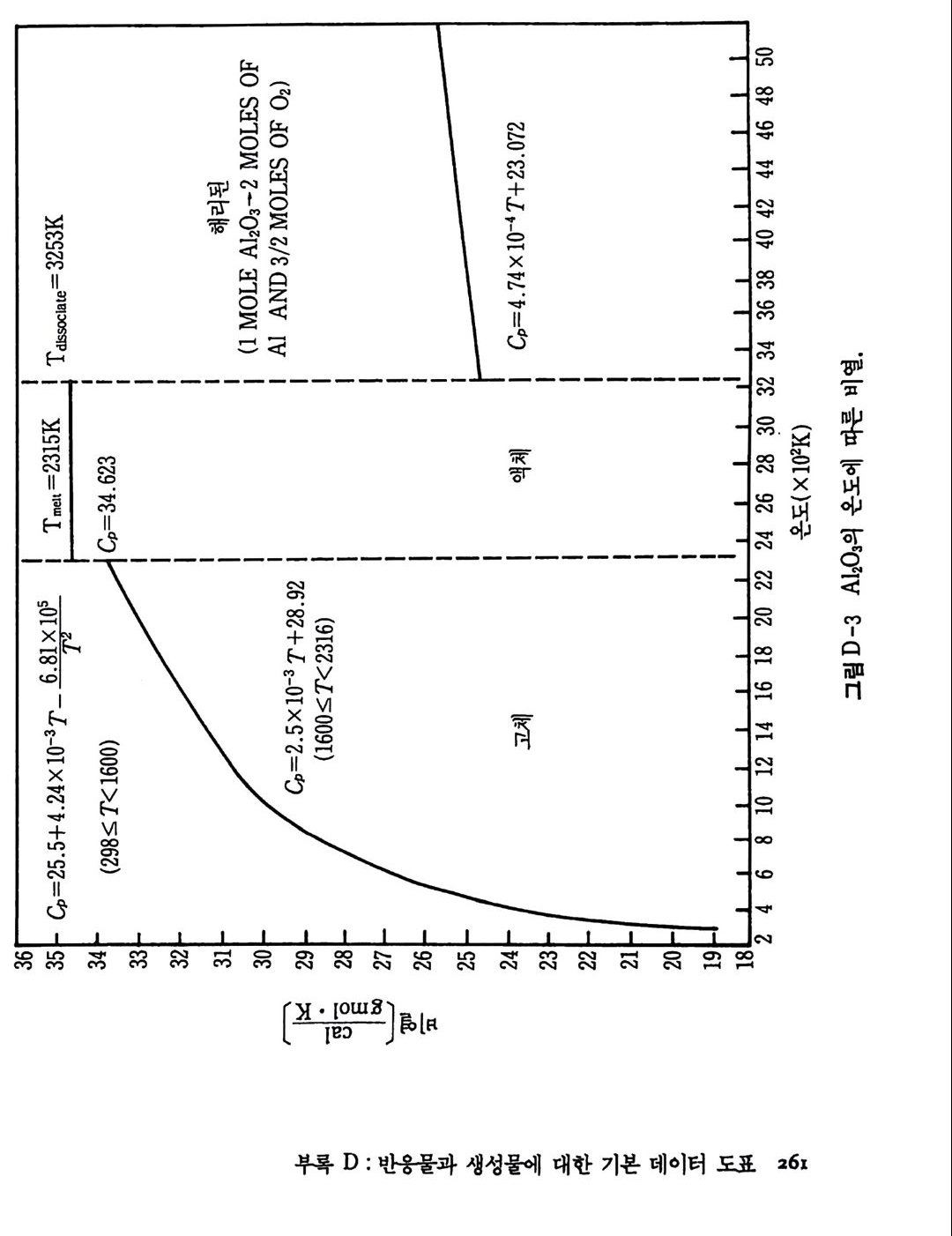 OS00>9pW2>OV
OS00>9pW2>OV
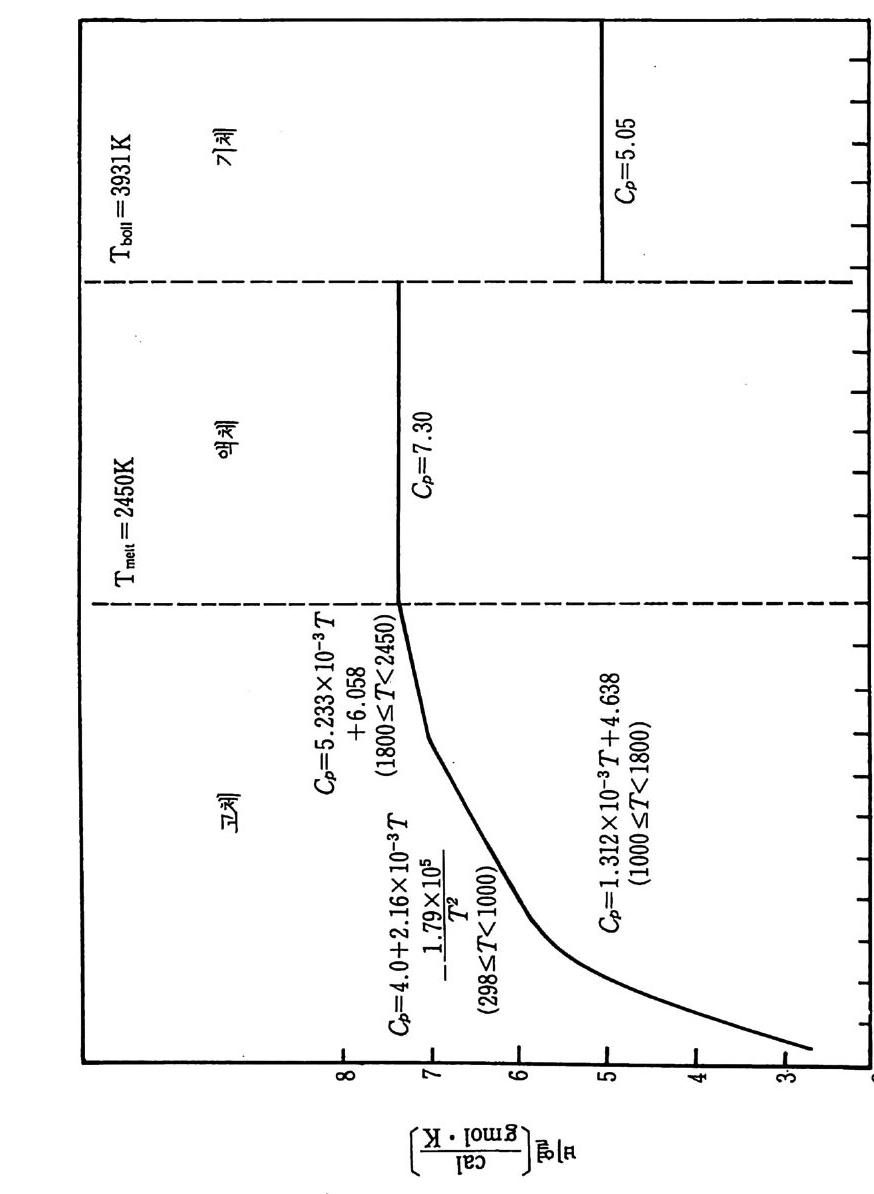 05
05
열. 비 른따 에 도 온 의 )B( 소 붕4D - 림그
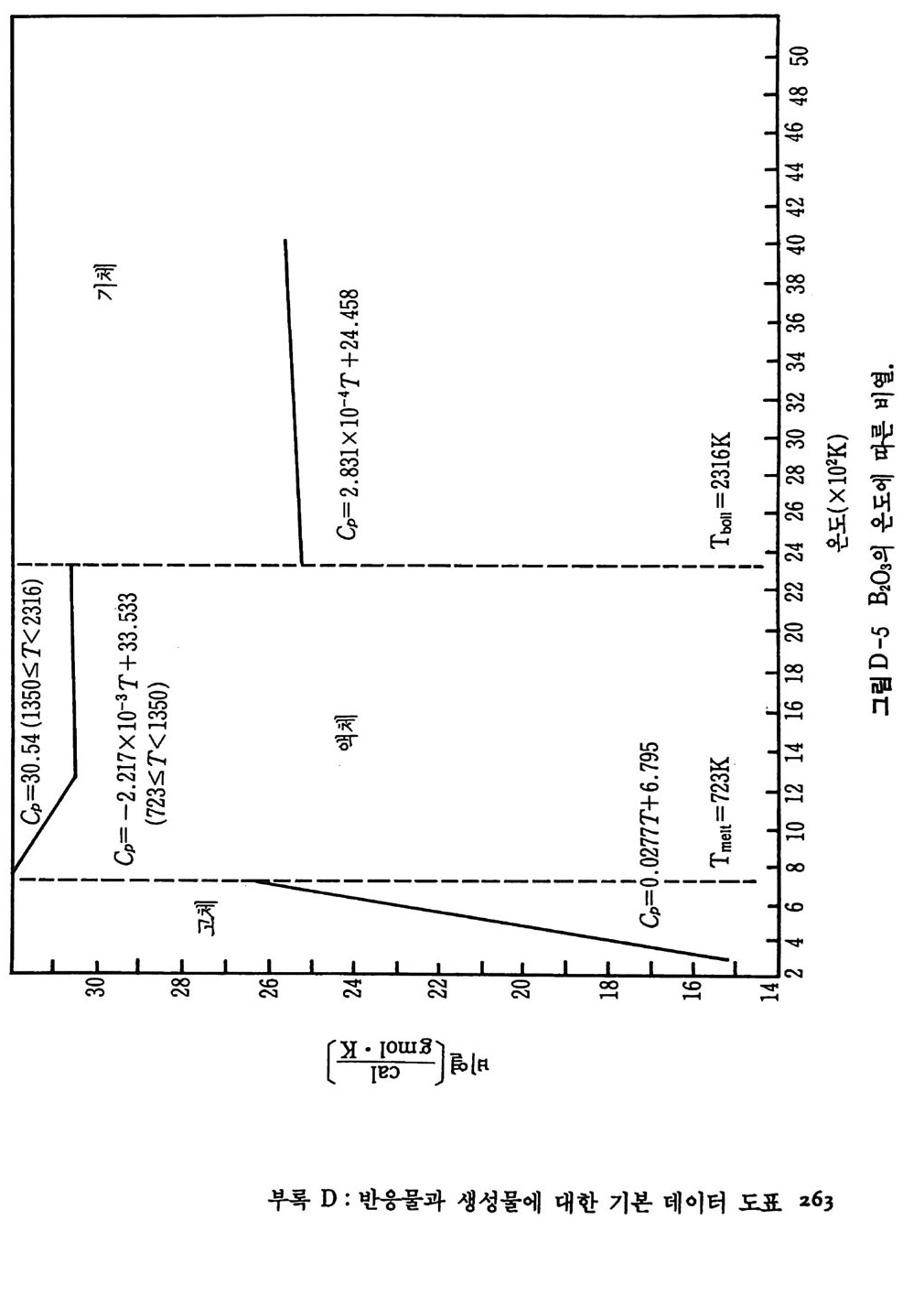 og00>9~
og00>9~
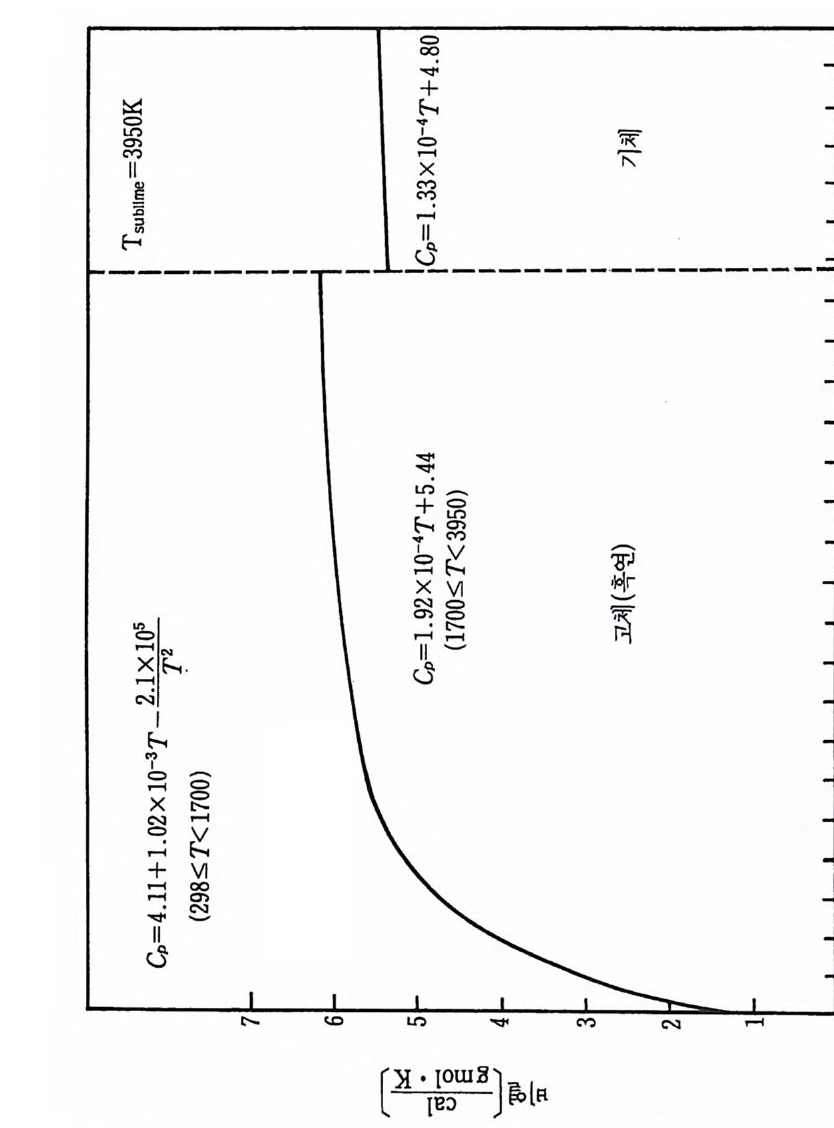
. 열비 른따 에 도 온의 소탄 6 -D 립 그
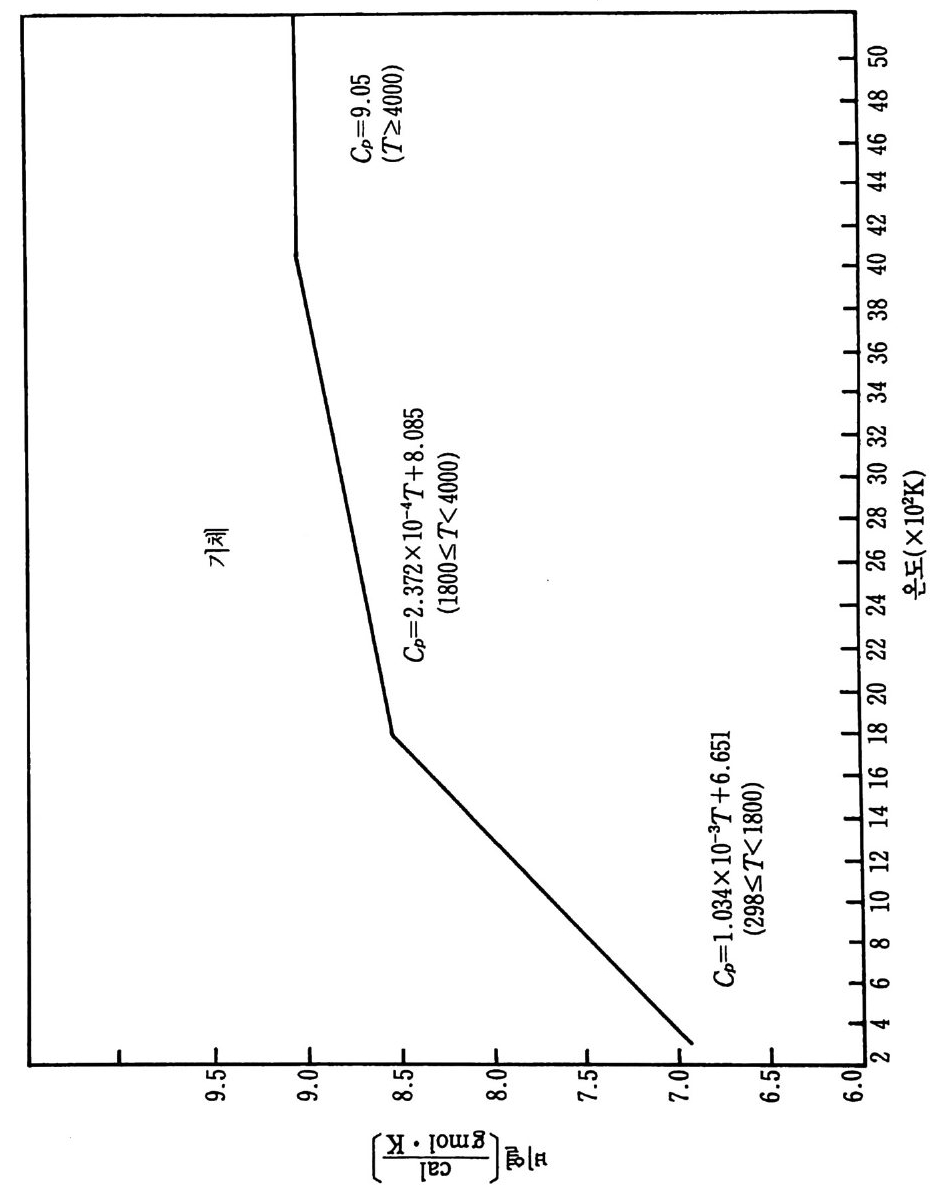 =C0 9.5p 0)040~(T6 4 5 804
=C0 9.5p 0)040~(T6 4 5 804
. 열비 른 따에 도 온 의 소질 7 -D 립 그
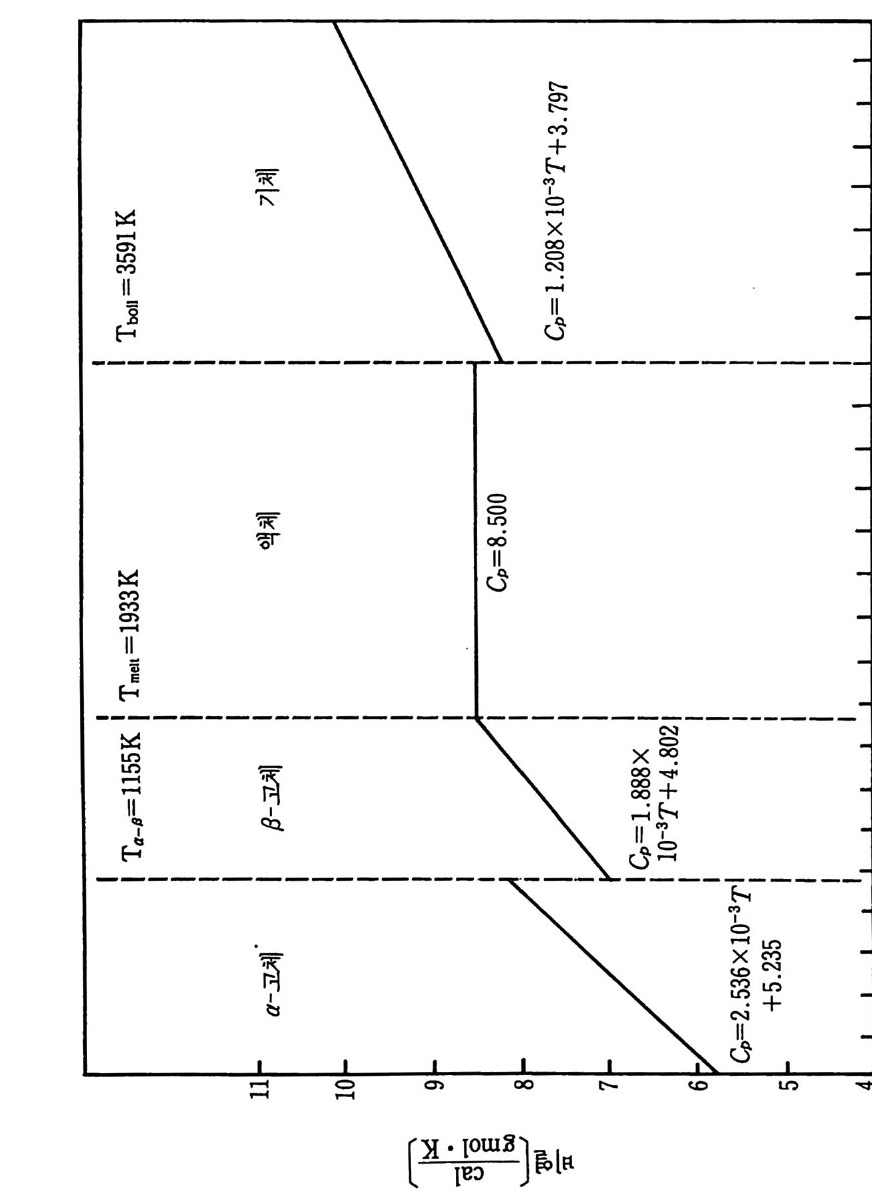 50
50
. 열비 른따 에 도 온 의 탄티 8 -D 립 그
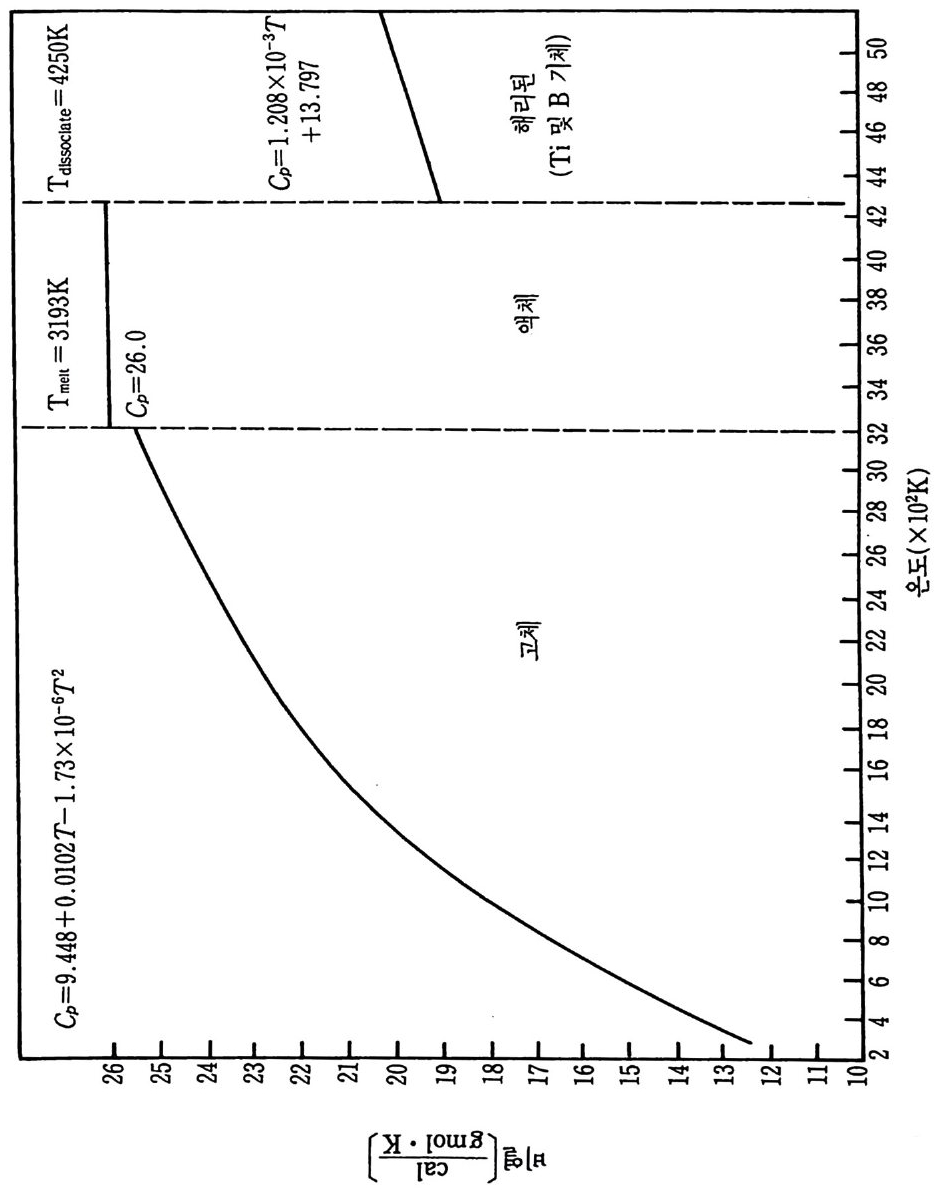 ale4 2KoSTesdl 0=5t c 8-X=01=T1302.p 973 .71+ 된리해 B (Ti 및기 )체44 44 0 58 6
ale4 2KoSTesdl 0=5t c 8-X=01=T1302.p 973 .71+ 된리해 B (Ti 및기 )체44 44 0 58 6
.열 비 른따 에 도 온 며 B i T 9 -D 립 그
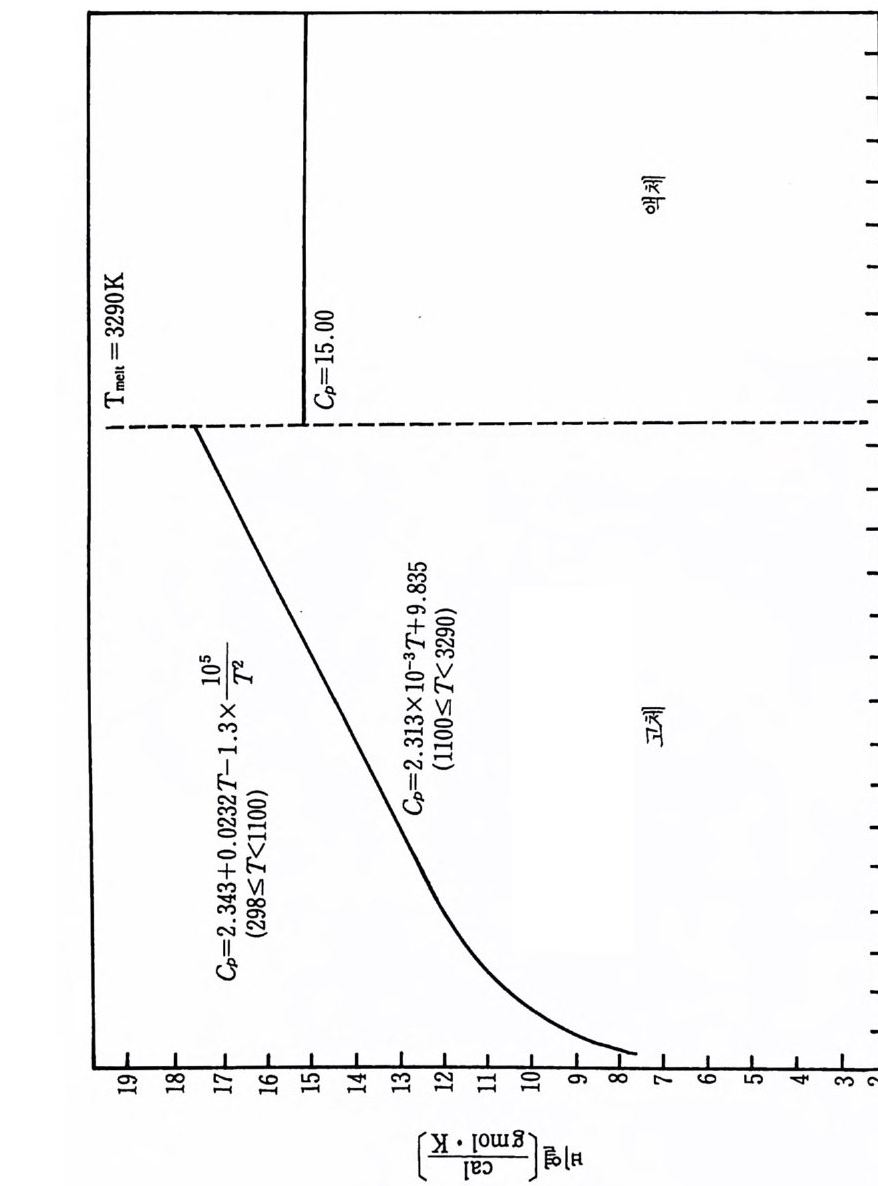 05
05
. 열비 른따 에 도 온 의 iC T 0 1 -D 그립
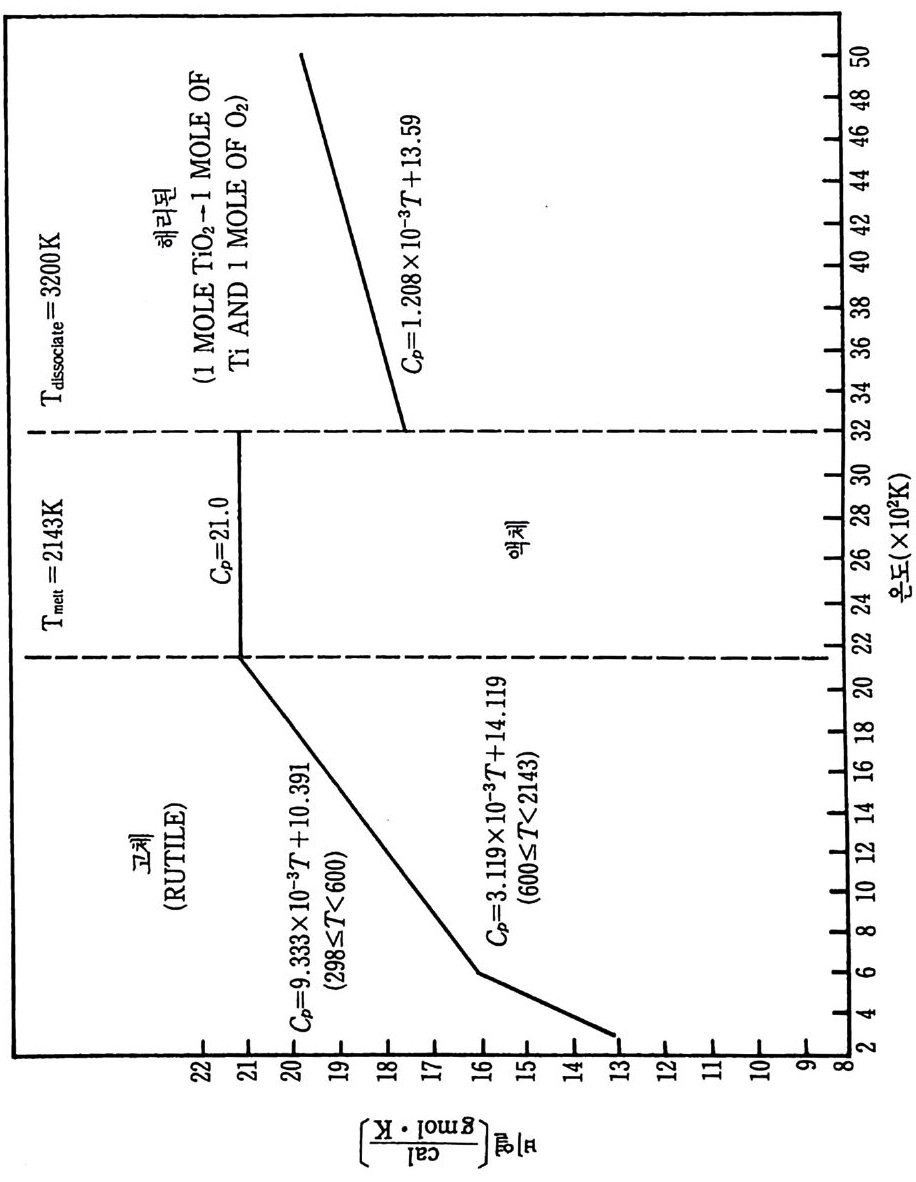 0O1 ed1Ssl=TK3a C02리 해된 E-O2lLOF0E OL MM Ti (1 0)OT M FO1 A LEND 2 i 624 448 04 4 4 05 83 634 3
0O1 ed1Ssl=TK3a C02리 해된 E-O2lLOF0E OL MM Ti (1 0)OT M FO1 A LEND 2 i 624 448 04 4 4 05 83 634 3
. 열비 른 따에 도 온 려Oi T 1 1 -D 립 그
다음의 표 D-1~D-11 에 보고된 데이터의 단위는 아래와 같다. 1) 온도 : K 2) 엔탈피 : cal • mo1- 1 3) 엔트로피 : cal • K- 1· mol-1 4) Gib b s 자유에너지 : cal • moI-1 표D- 1 알루미늄 (Al) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 Gib b s 자유에너지 300.00 10.51 6.81 -2033. 00 400. 00 609.20 8.53 -2803. 00 500. 00 1243. 00 9.94 -3729. 00 600.00 1911.00 11. 16 -4785.00 700.00 2614. 00 12. 24 -5956.00 890000..0000 43312525.. 0000 1134.. 2134 -—782539 09.. 0 000 1000.00 7397. 00 17.60 -10200.0 0 ll00.0 0 8156. 00 18. 32 -1 2000.00 1200.0 0 8915. 00 18. 98 -13860.0 0 1300. 00 9673. 00 19. 59 -15790.0 0 11540000..0000 1101413900.. 00 00 2200..6 175 —-117978 8200.. 00 00 1600.00 11950. 00 21. 16 -21910.00 1700.00 12710. 00 21. 62 -24050. 00 1800. 00 13470.00 22.06 -26230.00 1900.0 0 14230.00 22.47 -28460. 00 2000. 00 14980.00 22. 86 -3 0730. 00 22120000..0 000 1156754000..0 000 2233..5238 -—333503 3700..0 000 2300.00 17260.00 23.92 -37750.00 2400.00 18020. 00 24.24 -40150.0 0 2500.00 18780. 00 24.55 -42590.00 2600.00 19540. 00 24. 85 -45060.0 0 2700.00 20300.00 25.13 -47560.0 0 2800.00 90470.00 50.50 -50930.00 2900. 00 90980. 00 50.68 -55990.00 33100000..0000 9911949800..0000 5510.. 8052 -—661601 7600..0000
3200. 00 92500.00 51.13 -71270. 00 3300. 00 93000. 00 51 .33 -76400. 00 3400. 00 93510 . 00 51. 48 —-881656 4900.. 0000 3500. 00 94020.00 51 .63 3600. 00 94520.00 51 .77 -91860.00 3700. 00 95030. 00 51 .91 -97050. 00 3800. 00 95540. 00 52.05 -102200. 00 3900. 00 96040.00 52.18 -107500.00 표 D-2 질화알루미늄 (AIN) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자유에너지 430000.. 0000 -—775592 9300..0 000 74..80 65 --7787045500..0 000 500.00 -74380.00 8.9 3 -78850.00 600. 00 -73460.00 10.61 -79830. 00 700. 00 -72460.00 12.16 -80970.00 890000..0000 -—76 9190 4700..0 000 1154.. 1581 --8832942000.. 0000 111210000000...0 0 0000 -——666876764 923000...000000 111678...8 87328 ---888795205481000...0 0 0000 111435000000... 000000 —--666524280 645000...00 0000 122910.. .875133 -—-999315001 526000...0 0 0000 11760000.. 0000 -—66 1064 8700..0000 2232.. 3020 --9997365200..0 000 1800. 00 一 59280.00 23. 71 -102000.00 12900000.. 0000 —-558608 8800..0 000 2244..3 967 --110064480000.. 0000 2100. 00 -55670.00 25.56 -109400. 00 2200. 00 -54470. 00 26. 12 -111900.00 22430000..0000 -—553220 6500..0 000 2276..1686 --111147630000..0 000 2500.00 -50830.00 27.67 -120000.00 2600. 00 -49620.00 28.15 -122800.00
2700.00 -48400.0 0 28. 61 -125600.0 0 2800. 00 100600. 00 82.04 -129200. 00 2900.00 101200.00 82. 26 -137400.00 3000.00 101800. 00 82. 47 -145600. 00 3100.00 102400. 00 82.68 -1 53900. 00 3200.00 103100.00 82. 88 -162100. 00 3300.00 103700.00 83.07 -170400.00 3400.00 104300.00 83.26 -178800.00 3500.00 104900.00 83.44 -187100.0 0 3600. 00 105600.00 83.61 -195400.00 3700. 00 106200.00 83.79 -203800 .00 3800.00 106800'. 00 83.95 -212200. 00 3900.00 107500. 00 84.12 -220600.00 표 D-3 산화알루미늄 (Al203) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자뷰에너지 300.00 -400400.00 12.29 -404100.00 400.00 -398300 .00 18. 40 -405600.00 650000..0000 —-339953 930000..0000 2283..7 440 --440170730000..0 000 870000..0000 --339807960000..0000 3362..5 117 —-441136 480000.. 0000 900.00 -385100.00 39.49 -420600.00 1000. 00 -382200.00 42.52 -424700.00 1100.00 一 379300.00 45.31 -429100.0 0 11230000..0000 --337763320000..0000 5407.. 9314 —-443338 870000..0 000 1400.0 0 -370200.00 52.63 -443800.00 1500.00 -367000.00 54.79 -449200.00 1600.00 -363200.00 57.56 -455300.00 1700.00 -359900.0 0 59.56 -461200.0 0 1800.0 0 -356600.0 0 61. 47 -467200.00 1900.00 -353200.00 63.28 -473500. 00 2000.00 -349900.00 65.01 一 479900 . 00 2100.00 -346500.00 66.67 -486500.0 0
2200. 00 -343 000. 00 68. 27 -493 200.00 2300. 00 -339600.00 69.80 -500100.0 0 22540000..0 000 一— 330085 500000 .. 0000 8843.. 5165 --550186140000 ..0000 2600.00 -301600.00 85. 92 一 525000 . 00 2700.00 -298100.0 0 87. 23 -533600.00 2800.00 -294700.00 88.4 9 -542400. 00 2900. 00 -291200. 00 89.70 -551300.00 3000. 00 -287700.00 90. 87 -560400. 00 3100.00 -284300.00 92.01 -569500. 00 3200.00 -280800.00 93. 11 -578800.00 3300.00 225300.00 206.00 -454400.0 0 3400.00 227800.00 206.70 -475000.00 3500.00 230300. 00 207.40 -495700.00 3600.00 232700. 00 208.10 -516500.00 3700. 00 235200.00 208.80 -537400.00 3800.0 0 237700.00 209. 50 -558300.00 3900.00 240200.00 210.10 -579300.00 표 D-4 붕소 (B) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자유에너지 300. 00 4.87 2.67 -795.4 0 564000000...00 0000 1137933819...03 0000 354...635041 —-—121150010 874...00 0000 700.00 1696.00 6.11 -2580.00 800. 00 2226.00 6.82 -3227.0 0 900. 00 2785. 00 7.47 -3942.00 1000.00 3427.00 6.93 -3500. 00 1100.00 4029. 00 7.5 0 -4222.0 0 1200.00 4643.00 8.03 -4999. 00 1300. 00 5271. 00 8.54 -5828.00 1400.00 5912.00 9.0 1 -6706.00 1500. 00 6566.00 9.46 -7630.00 1600.00 7233.00 9.89 -8598.00
1700.0 0 7913. 00 10. 31 -9608. 00 1800. 00 8645.00 10. 73 -10670.00 1900. 00 9348. 00 11. 11 -11760.00 2000. 00 10060.00 11. 47 -12890.00 2100.00 10770. 00 11. 82 一 14060.00 2200. 00 11490. 00 12.15 一 15250 . 00 2300.00 12210. 00 12. 48 一 16490.00 22450000..0 000 1129904700..0 000 1125..2 799 —-117971 5500 .. 0000 2600.00 19800. 00 15.57 -20690.0 0 2700.00 20530. 00 15. 85 -22260.00 2800.00 21260.00 16.11 -23860. 00 2900.00 21990.00 16.37 -25480.00 3000.00 22720. 00 16.62 一 27130 . 00 3100.00 23450.00 16. 86 -28810.00 33320000.. 0000 2244191800..0000 1177..3091 —-330282 0200..0 000 3400.00 25640. 00 17. 53 -33960.00 3500.00 26370.00 17.74 -35730. 00 33670000..0000 2277183000..0000 1178..9155 -—337953 1200..0 000 3800.00 28560.00 18.34 -41140.00 3900.00 29290.00 18.53 -42990.0 0 표 D_5 산화봉소 (B203) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자 ~l 너지 300.00 —303 600.00 12.96 -307500. 00 400.00 -302000.00 17.69 -309000.00 500.00 -300000.0 0 21.97 -311000.00 600.00 -297800.0 0 25.98 -313400.00 700.00 -295300.00 29.80 -316200.00 980000..0 000 -287000.00 4414..9 296 -—33 2204 030000.. 0000 -283800.0 0 1ll00000..0000 一-2 27870670000..0000 4581.. 3280 -—332394 000000..0 000
1200. 00 -274500.00 53. 97 —339 200. 00 1300. 00 -271400.00 56. 43 -344700. 00 1400.00 -268300. 00 58. 70 -350500. 00 1500. 00 -265300. 00 60. 81 -356500. 00 1600.00 -262 200. 00 62. 78 -362700. 00 1700.00 -259200. 00 64. 63 -369000.00 1800. 00 -256100.00 66.37 -375600.00 1900. 00 -2 53100.00 68.02 -382300.00 2000.00 -250000.00 69. 59 -389200. 00 2100.00 -247000.00 71. 08 -396200. 00 2200.00 -243900. 00 72.50 -403400.00 2300. 00 -240900. 00 73.86 -410700. 00 2400.00 -150700.0 0 112.80 -421400. 00 22560000..0000 -—114485 270000.. 0000 111143.. 8800 --443424280000..0 000 22780000..0000 -—11443 0160000..0000 111165..8700 --446575470000..0000 2900.00 -138100.00 117.60 -479100. 00 3000. 00 -135600. 00 118. 40 -490900.00 3100.00 -133000 .00 119.30 -502800. 00 3200. 00 -130500.00 120.10 -514700. 00 3300.00 -127900.00 120. 90 -526800. 00 3400.00 -125400.00 121. 60 -538900. 00 3500. 00 -122900.00 122.40 -551100. 00 3600.00 -120300. 00 123. 10 一 563400.00 333987000000...00 0000 --—111111752 827000000...00 0000 111222435... 481000 —--655708508 761000000... 0 0 0000 표 D-6 탄소 (C) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs;(~ 에너지 300.00 3.90 1.32 -391 .60 400. 00 275.60 2.09 -561 .80 500. 00 627.5 0 2.8 7 -810.00 600.00 1025.00 3.60 -1134. 00
700.00 1452. 00 4.2 6 —15 27. 00 800. 00 1902. 00 4.86 -1984.00 900.00 2370.00 5.41 一 2497 . 00 1000. 00 2855.00 5.92 -3064. 00 1100.00 3354. 00 6.3 9 -3680.0 0 1200.00 3866. 00 6.84 一 4342.00 1300.00 4391.00 7.2 6 -5047.00 11540000..00 00 54497279..0 000 87..60 64 一— 655779 83 . .0000 11760000..0 000 66063968.. 0000 88..7406 -—784109 08..0 000 1800. 00 7274.00 9.0 9 -9090.00 122190000000...000000 987804531854...000000 999...497 009 -——1110010 99 267000...0 00000 2200.00 9604.00 10. 26 -12970.0 0 2300.00 10190.00 10.5 2 -14010.0 0 2400.00 10780. 00 10.77 -15070. 00 2500.00 11370.00 11. 01 -16160.00 2600.00 11960.00 11.25 -17270. 00 2700.00 12560.00 11.47 -18410.0 0 2800.00 13160.00 11.6 9 -19570.0 0 32090000.. 0000 1143735500.. 0000 1121..1900 —-22017 95500 ..00 00 33210000..0 000 1145596600..0000 1122..34 09 -—22341 47100..0 000 3300.00 16170. 00 12.68 -25660.00 3400.00 16780.00 12.86 -269 4 0. 00 3500.00 17390. 00 13. 04 -28240.00 3600.00 18000.00 13.2 1 -29550 . 00 33780000..0000 1189623100..0000 1133..53 48 -—33028 28200..00 00 3900. 00 19850.00 13. 70 -33590. 00
표 D— 7 질 소 (N) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자유에너지 300. 00 12. 83 45.81 -13730.00 400. 00 714. 10 47. 83 -18420. 00 500.00 1426. 00 49.42 -23280. 00 600. 00 2148. 00 50.73 -23290.00 700. 00 2880. 00 51. 86 -33420. 00 800. 00 3623.00 52.85 -38660.00 1900000..0 000 45313769..0000 5534..5 744 -—443994 9100..0 000 ll00.0 0 5913.00 55. 28 -54900.00 12Q O. O O 6697.00 55. 96 -60460. 00 1300.0 0 7491 .00 56. 60 -66090.00 1400. 00 8296.00 57. 20 -71780.00 1500.0 0 9111.00 57. 76 -77530.00 1600. 00 9936.00 58. 29 -83330.0 0 1700.0 0 10770. 00 58. 80 -89180.00 1800. 00 11710. 00 59.32 一 95070.00 122190000000... 000000 111243524 671 000...00 0000 566900...2 76243 —-—111001173 0 01000000...00 0 000 2200. 00 15130.00 61. 04 -119200.00 2300.00 15990. 00 61. 42 -125300.00 22222574860000000000.....00 00000000 1112109786345784626900000.....000 0000000 6666621223.....7114 898431 -————111113354517306 461490000000000 .....0 0 00000000 2900.00 21210.00 63. 44 -162300. 00 3000.00 220 9 0. 00 63. 74 -169100.00 3100. 00 22970.00 64.02 -175500.0 0 3200. 00 23860.00 64.30 -181900.0 0 3300. 00 24740. 00 64. 58 -188400.00 3400.00 25630. 00 64.84 -194800.00 3500.00 26520. 00 65. 10 -201300.00 3600. 00 27410. 00 65.35 -207900.0 0
3700. 00 28310.00 65. 60 -214400. 00 33890000..0 000 2309211100 .. 0000 6656..0 874 —一 2222 71060000.. 0000 표D- 8 티탄 (T i)에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 Gib b s 자유에너지 300. 00 10. 62 7.3 6 -2197.00 400.00 622.90 9.12 -3025. 00 500.00 1260. 00 10.54 -401 0. 00 600. 00 1923.00 11. 75 -5126.0 0 700. 00 2612.00 12.81 -6355.0 0 800. 00 3326.00 13.76 -7685.00 900.00 4065.00 14. 63 -9105.0 0 1000.00 4829.00 15. 44 -10610.0 0 1100.0 0 5619.00 16. 19 -12190.0 0 1200. 00 7379. 00 17. 74 -13910. 00 11430000.. 0000 88809350.. 0 000 1188..8 362 —-11577 51700..00 00 1500.00 9584.00 19.38 -19490.00 11670000.. 0000 1110135600..0 000 1290..8368 -—22134 45600..00 00 1800.00 11960. 00 20.82 ...:.25520 . 00 1900.00 12790. 00 21.27 -27630.00 2000.00 18040.00 23.97 一 29890 . 00 2100.00 18890.00 24. 38 -32310.00 2200.00 19740. 00 24.78 -34770.00 2300.00 20590. 00 25. 16 -37270. 00 2400. 00 21440.00 25. 52 -39800.00 22560000..0000 2232124900..0 000 2256..2 806 -—44243 97700..0000 2700. 00 23990. 00 26. 52 -47610.00 2800.00 24840.00 26. 83 -50280.00 2900.00 25690. 00 27. 13 -52970.00 3000.00 26540.00 27. 41 -5 5700.00 3100.00 27390.00 27. 69 -58460.00 3200.00 28240.00 27.96 -61240. 00
3300. 00 29090. 00 28.22 -64050. 00 3400. 00 29940. 00 28. 43 -66380. 00 3500.00 30790.00 28. 72 -69740. 00 3600. 00 133300. 00 57. 28 -72920.00 3700. 00 134100.00 57. 51 -73550.00 3800. 00 135000.00 57. 73 -84420.00 3900.00 135800.0 0 57. 95 -90200. 00 표 D 一 9 이봉소화티탄 (T iB 2) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자유에너지 300.00 -66860.00 6.6 3 一 68850 .00 400. 00 -65580. 00 10. 31 -69700. 00 500.00 -64210. 00 13.36 -70890.0 0 600.00 -62760.0 0 16. 01 -72360. 00 700.00 -61220. 00 18.37 -74080.00 800. 00 -59610.00 20.52 -76030.00 900. 00 -57920.00 22.51 -78180.00 1000. 00 -56170.00 24. 36 -80530.00 1100. 00 -54340.00 26.10 -83050.00 1111523400000000....0 0 000000 -—-—45584206544505 400000....00000000 22339072....72 374109 ---—88985941677 604500000 ....000 00000 111867000000...000000 -——4344923913 77000...00 0000 333346...81 5487 --11-900815050400000...0 0 0000 1900.00 -37730.00 37.35 -108700.00 2000. 00 -35460. 00 38.51 -112500,00 2100.00 -33150.00 39.64 -116400.00 2200. 00 -30810.0 0 40.73 -120400.0 0 2300. 00 -28450. 00 41. 78 -124500. 00 22540000.. 0000 --2263066500..0000 4423.. 7789 —-112383 810000..0000 2600. 00 -21230.00 44.73 -137500.00 2700.00 -18800.0 0 45.64 -142000.0 0
22890000..0000 ——116339 6100..0 000 4467..5 339 -一1 51416360000 .. 00 00 3000. 00 -11460.0 0 48.22 -156100. 00 33210000.. 0000 -197061100.. 0 000 4597..8 022 —一 11661 7040000..0000 3300.00 20210.0 0 58. 62 -173200. 00 3400. 00 22810. 00 59. 40 -179200. 00 3500.00 25410.00 60.15 -185100.00 3600.00 28010.00 60.89 -191200.00 3700.00 30610. 00 61.60 -197300.0 0 3800.00 33210. 00 62. 29 -203500.00 3900.00 35810. 00 62. 97 -209800.00 표 D ― 10 탄화티탄 (T i C) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자유에너지 300.00 -44000.0 0 5.84 -45750.00 400.00 -43110. 00 8.38 -46470.00 560000..00 00 -—442019 0800.. 00 00 1102..6647 --4487548200.. 0 000 780000..0 000 -—339875 9500..0 000 1146..1 560 --5419494800..0000 1900000..0 000 --337 6208200..0000 1178..6958 -—553510 7000..0 000 ll00.00 -34960.00 19.96 -56920.0 0 1200.00 -33710.00 21.05 -5897 0. 00 1300.00 -32440.00 22. 07 -61120. 00 11450000.. 00 00 --3219184200..0 000 2233..9 043 -—66353 78300..0 000 11760000..0 000 --2287418200..00 00 2245..6 830 —-67801 66900..0 000 1800.00 -25730.0 0 26. 42 -73290.00 1900.00 -24320.0 0 27.19 -75970.00 22100000..0 000 --2221843800..0000 2287..9 623 -—788175 3500..0 000 2200. 00 -19950.00 29.32 -84450. 00
2300.00 -18440.0 0 29.99 -87420.00 2400. 00 -16920.00 30. 64 -90450.00 2500. 00 -15370.00 31 .27 -93550.00 2600.00 -13790.0 0 31. 39 -96700.00 2700.00 一 12200.00 32.49 -99920.00 2800.00 -10580.00 33.08 -103200.00 2900.00 -8935.00 33.66 -106500.0 0 3000.00 -7269.00 34.22 -109900.00 3100.00 -5580.00 34.78 一 113400.00 3200. 00 -3869.00 35.32 -116900.0 0 3300.00 14410.00 40. 79 -120200.00 33540000..0 000 1157941100..0 000 4411.. 2637 —-112248 340000..0 000 33670000..0 000 2180491100..0000 4422..0509 -—113326 680000..0000 3800. 00 21910.00 42.90 -141100. 00 3900.00 23410. 00 43.29 -145400.00 표 D 一 ll 이산화티탄 (T i 02) 에 대한 상태함수 데이터. T(K) 엔탈피 엔트로피 G i bbs 자유에너지 340000..0000 -—22224 5480000..0000 1126..1013 -—222390 480000..0000 500. 00 -222900.00 19.29 一 232600.00 600.00 -221300.00 22.35 -234700.00 700.00 -219700.00 24.83 -237000. 00 800.00 -218000.00 27.03 -239600. 00 900.00 -216300.0 0 29. 01 -242400.00 1000.00 -214600. 00 30.81 -245400. 00 1100.00 -212900.00 32. 46 -248600. 00 1200.00 -211100.00 34.00 -251900.00 1300.0 0 -209300.00 35.45 -255400.00 1400.00 -207500.00 35.80 -259000.00 1500. 00 -205600.00 38.09 -262700.00 1600.00 -203700. 00 39.31 -266500.00 1700.00 -201800.00 40.48 -270600. 00
1800. 00 -199800.0 0 41. 60 —27 4700.00 1900.00 -197800.0 0 42. 68 一 278900 . 00 2000. 00 -195800.00 43.71 -283200. 00 2100. 00 -193800.0 0 44. 71 -287700. 00 2200. 00 -175500. 00 53.36 -292900.00 2300. 00 -173400.00 54. 29 -298300. 00 2400.00 -171300.0 0 55. 19 -303800.0 0 2500. 00 -169200.00 56.04 -309300.0 0 2600.00 -167100. 00 56. 87 -315000. 00 2700. 00 一 165000 . 00 57. 65 -320700. 00 2800.00 -162900. 00 58. 42 -326500. 00 2900.00 -160800.00 59.16 -332400. 00 3000.00 -158700. 00 59. 87 -338300.00 3100.0 0 -156600. 00 60. 56 -344300.00 3200. 00 -154500.00 61. 24 -350500. 00 3300.00 55350.00 125.50 -358700.00 3400. 00 57120.00 126.00 -371300.00 3500. 00 53890.00 126.50 -383900.00 3600. 00 60630.00 127.00 -396600. 00 3700.00 62430.00 127. 50 -409300. 00 3800.00 64290.00 128. 00 -422100.00 3900.00 66110. 00 128.50 -434900.0 0
부록 E : 압력단위 환산표 pas cal atm mrnHg bar dyn e /cm2 lb/in ' lb/ft2 (N/m') (기압) (tor r) (P.S .I ) 1 pas cal 1 9.8 6 9X 10-• 7.SOX10-3 10-5 10 l.45 0Xl0-' 2.09Xl0-2 1 atrn l.01 3X l05 1 760. 0 1.01 3 l.01 3Xl0' 14.70 2116. 8 1 mmHg 133.3 l.31 6X 10-3 1 1,3 33x10-3 1333 l.93 4X10-2 2.78 5 1 bar 105 0.9869 750.1 1 10• 14.50 2088 1dyn e /m 10-1 9.869X 10-7 7.50X10-• 10-• 1 1.45 0Xl0-5 2.088X10-3 1 Ib/in2 6895 6.8 0 5X 1 0-2 51. 71 6.8 9 5X 10-z 6.8 9 5X 10' 1 144 1 lb/ft ' 47. 88 4.7 2 6X10-• 3.5 9 X 10-1 4.7 9 x10-• 478.82 6.94X 10-3 1
참고문헌 1) K.A. Gabrie l , S.G. Wax, and J.W . McCauley, Mate r ia l s Process- ing by Self- P rop a g a ti ng High Temp e ratu r e Sy nthe sis ( SHS) , Proc. DARPA/ARMY SHS Sym p., Day ton a Beach, Florid a U.S. A., Oct. 21 -2 3 (1985) , 2) A.G. Merzhanov et al. , Combusti on of Porous Meta l Spe c i m ens in Gaseous Ni trog e n and Syn the sis of Ni trides ; on the Theme : Self- Prop a ga ti ng Hi gh -T e mp e ratu r e Sy nthe sis of Inorga n ic Com- po unds, Chernog o lovka, U.S.S . R . (1971) . 3) W.L. Frankhouser and S.T . Sulliv a n, Thermochem ica l Consid - erati on s in Self -S usta i n ing Sy nthe sis of Refr ac to r y Comp o unds, SPC Re po rt 814, Sy st e m Plan ning Corpo rati on , Aug us t( 1 982). 4) W. L. Frankhouser, K.W . Brendley, M. C. Ki es zek, and S.T. Sul- liva n, Gasless Combustio n Syn th e s is of Refr a cto r y Comp ou nds, pp. 4-145, Noy e s Public a ti on s, Park Ri dg e , New Jer sey, U.S.A. (1985) . 5) A.G . Merzhanov, Problems of Technolog ica l Combusti on , Com- busti on Processes in Chemi ca l Technology and Meta l lurgy , Cher- nog o lovka, U.S.S.R. (1975) . 6) W.L. Frankhouser, Sov iet Develop m ents in Reg a rd to Sup e rp la s- tici t y in Cerami c Mate r ia l s, SPC Re po rt 849, Sy st e m Plann ing Corp o rati on , Sep tem ber (1982) . 7) Unit ed Ki ng d om Pate n t Sp e cif ica ti on No. 1, 497 , 025, Meth o d of Produc ing Cast Refr a cto r y Inorga nic Mate rz ·ats , A. G. Merzhanov et
al., Jan uary 5 (1978) . 8) French Pate n t No. 76-19471 , Procedure for the Producti on of Refr a ct or y Mate r i als , A.G . Merzhanov et al., Ap r il 2 (1977) . 9) Y. Maksim ov et al., Gasless Combusti on as a Sim p le Model for the Combusti on of Non-Volati le Condensed Sy s te m s, Fiz i k a Goreniy a i Vzry v a, 1 (4) , 24-30 (1965) . 10) A.P. Hardt, Incendia r y Pote n ti al of Exoth e rmi c Inte r meta l lic Reacti on s, Lockheed Palo Al to Research Laborato r y , Technic a l Re po rt AFATL- T R- 7 1-87, Ai r Force Armament Laborato ry, Jul y ( 1971) . 11) Z.A . Mu nir, Sy nthe sis of Hi gh Temp e ratu r e Mate r ia l s by Self- Prop a g a ti ng Combusti on Meth ods, Ceram. Bull., 67 (2) 342-349 (1988) . 12) F. Booth , Theory of Self-P rop a g a ti ng Exoth e rmi c Reacti on s in Solid Sy st e m s, Trans. Farad, Soc., 49, 272- 28 1 (1953) . 13) J.D . Walto n , Jr. and N.E. Poulos, Cermets from Thermi te React ion s, J Am. Ceram. Soc., 42 (1) , 40- 49 (1959) . 14) J.F. Cri de r, Self -P rop a g a ti ng High Temp e ratu r e Sy nthe sis - A Sov iet Meth o d for Producin g Cerami c Mate ria l s, Ceram. En g. Sc i. P roc., 3 (9-10) 519-528 (1982) . 15) The jo urnal of Commerce, High -T emp . Exp e rim enta t i on Op e ns Doors, p. 3, December 8 (1986) . 16) M. Koiz u m i and Y. Mi ya moto , Recent Prog res s in Combusti on Sy st h es is of Hi gh Perf or mance Mate r ia l s in Jap a n , Intl . Sym p. Combustio n and Plasma Syn thesis of Hig h Temp er otu r e Mate r ia ls , J Am, Ceram. Soc., San Franci sc o, Octo b er (1988) . 17) Y. Mi yam oto , M. Koiz u mi , and 0. Yamada, Hi gh -Pressure Self-C ombustio n Sin t e r i ng for Cerami cs, Comm. Am. Ceram. Soc., 67, c-224 (1984) .
18) 0. Yamada, Y. Mi yam oto , and M. Koiz u mi , High -Pressure Combusti on Sin t e r in g of Ti tan iu m Carbid e s, Comm. Am. Ceram. Soc., 70(9), c-206-c-208 (1987) . 19) 0. Yamada, Y. Mi yam oto , and M. Koiz u mi , Hi gh Pressure Self -C o mbusti on Sin t e r in g of Sil ico n Carbid e , Am. Ceram. Soc. Bull., 64 (2) , 319-321 (1985) . 20) 0. Odawara and J. Ikeuchi , Cerami c Comp o sit e P ip e s Produced by a Centr i fu ga l-Exoth e rmi c Process, ]. Am. Ceram. Soc., 69 <:: 8 0-C-81 (1986) . 21) S. Ohta n i, T. Tanaka, and Y. Ishi za wa, Prepa rati on of Ti C Sin g le Cry st a l from Self -C ombusti on Rod by Floati ng Zone Me- tho d, ]. Cry st . Growt h, 83, 481-484 (1987) . 22) Y. Mi yam oto , C.H . Yo, Y. Takano, 0. Yamada, and M. Koiz u m i, Hi gh Pressure Combusti on Sin t e r in g of Ti B2 -TiC and TiB 2 -SiC Cerami c Comp o sit es , ]. Jap a n . Soc. of Powder and Powder Mata l lurgy , 35 (7) , 651-654 (1988) . 23) C.H . Yo, S.J . Lee, E.S. Lee, E.J. Oh, and M.S. Py on , Stu d y of Gasless Combusti on Sy nthe sis of TiS i x ( x =O . 6, O. 8, 1. 0, and 2 . O) Sy st e m s, ]. Kor. C hem. Soc., 33 (4) , 337-342 (1989) . 24) V. I. Matk ovic h , Boron and Refr a cto r y Borid e s, Sp r in g e r-Verlag, Berlin (1977) . 25) L.E_. T oth , Tran sition Meta l Carbid e s and Ni trides , Academ ic Press (1971) . 26) G. Schwi er , Industr ial Rare Meta l (in Jap a nese) , 73, 98(1980). 27) H. Tanaka, Re po rt of the Nati on al Insti tut e of Research for Inorga nic Mate r i als (in Jap a nese) (1967) . 28) A. Kato , ]ap. ]. Chem., 2, 188 (1980) . 29) J.W . McCauley, N.D. Corbin , T. Reseta r , and P. Wong, Sim ulta -
neous Prepa r ati on and Self-S in t e r in g of Mate r ia l s in the Sy st e m s Ti -B -C, Ceram. Eng. Sci . Proc., 3(9-10), 538-554(1 9 82). 30) 0. Yamada, Stu d ie s on Combusti on Sy nthe sis a nd High Pressure Sin t e r in g for Non-Oxid e Cerami cs , Doc tor al Thesis of Osaka Univ ., pp. 3-93 (1987) . 31) L. Fredin , G.P. Hansen, J.L. Margr av e, and R.G . Behrens, Laser Ign it ion Stu d ie s , Proc. DARPA/ARMY Sy m p os iu m on SHS, Day ton a Beach, Florid a U.S.A., pp. 123-29, Octo b er (1985) . 32) C.T .S . Chow, J.A . Mohler, and L.D . Abeny, Ign ition Stu d y of Thermi te Usin g Laser, ibi d , pp. 415-427, Octo b er (1985) . 33) A.G . Merzhanov and LP. Borovin s kaia , A New Class of Com- busti on Process, Combustio n Scie n ce and Technology (Briti sh ) , 10, 195-201 (1975) . 34) A.G . Merzhanov et al., New Phenomena in Combusti on of Condensed Sy st e m s, Doklady Akademi i Nauk SSSR, 208 (4) , 892-894 (1972) . 35) V.M. Shkir o et al., Str uctur e of Fluctu a ti on s Occurrin g in the Burn ing of Tanta l um-Carbon Mi xt u r es, Fiz i k a Goreniy a i Vzry - va, 14 (1) , 149-151 (1977) . 36) U.S. Pate n t No. 3 , 726 , 643, Meth o ds of Producin g Carbid e s, Bori des , Sil ic ide s,. a nd Ni tride s of Group s W, V, and VI of the Peri od ic Sys t e m , A.G . Merzhanov et al. (1973) . 37) U.S.S.R. Pate n t No. 431 , 253, Meth o d for Sy n th e sis of Re- fra ct or y Inorga n ic Comp ou nds, A.G . Merzhanov, March 2 (1971) . 38) U.S.S.R. Pate n t No. 58( 052, Meth o d for Obta i n i n g Refr a cto r y Comp ou nds, A.G. Merzhanov et al., May 4 (1975) . 39) A. Vy a tk in ( correspo ndent) , Tit an iu m alloy Cutt ing Tools Repl a ci ng Tung st e n Tools, Sots iali st ich eskaya Industr iya, 179 (3370) , 2 (1980) .
40) V. Adamy a nts ( tem p o rary correspo ndent) , On Transit ion Te-chnolog y, Kommunis t ( Yerevan) , 146, 3 (1980) . 41) Uniq u e Alloy s From Hi gh ~ T emp e ratu r e Self- P rop a g a ti ng Sy n- the sis , Moskovskaya Pravda, 300 (18520) , 2 (1980) . 42) A.D. Bratc h ik o v, Self -P rop a g a ti ng Sy nthe sis of Ti tan iu m Ni ck -eli de , Poroshkovaya Meta l lurgi ya, 1 (205) , 7-11 (1980) . 43) V. Meli k- Naborov, Ap pli c a ti on s of Self -P rop a g a ti ng Hi gh - Temp e ratu re Sy n th esis , Moskovskaya Pravda, 9 (18 529) , 3 (1981) . 44) Combusti on Surpr is e s, Sots i a l ist i ch eskaya Industr i y a, 50, 4 (1980) . 45) V.M. Maslov, Combusti on of the Sy s te m s Ni ob iu m -Alum inu m and Ni ob iu m -Germaniu m , Fiz i k a Goreniy a i Vzry va , 15 (1) . 49-57 (1979) . 46) U.S.S.R. Pate n t No. 644 , 728, Meth o d for Obta ini n g Tit an iu m Carbid e , A.G . Merzhanov et al., Jan uary 30 (19 79) . 47) U. S. Pate n t No. 4 , 161, 512, Process for Prep a ri ng Ti tan iu m Carbid e , A.G. Merzhanov et al., Jul y 17 (1979) . 48) U.S.S.R. Pate n t No. 460 , 115, A Meth o d for Obta i n i n g Pow- ders of Refr ac to r y Comp ou nds, A.G . Merzhanov et al., Sep tem -ber(1974) . 49) L.N . Kug ai et al., Some Chemi ca l Prop er t ies of Powdered Ti tan ium Carbid e s in Their Homog e neit y Rang e , Poroshkovaya Meta l lurgi ya, 9 (213) , 58-61 (1980) . 50) New Heat- R esis t a n t Powders for Powder Meta l lurgy , Sot- sia l is tich eskaya Industr iya, 165 (3356) , 2 (1980) . 51) M.P. Abruzov et al., Abrasiv e Powder of Ti tan ium Carbid e and Carbon itri d e , Poroshkovaya Meta ll urgiy a, 6 (222) , 78-81 (1981) . 52) A. G. Merzhanov et al., Tit an ium Carbid e Produced by Self-
Prop ag a ti ng High -Temp er atu r e Sy nthe sis ; Valuable Abrasiv e Mate r ia l , Poroshkovaya Meta ll urgiy a, 10 (226) , 50-55 (1981) . 53) 0. Kuli ge v, Powder-Meta l lurgy Plant' s Ti tan iu m and Ni trid e Product, Vys h ka, 22 (15584) , 2 (1982) . 54) U.S.S.R. Pate n t No. 552, 293, Meth o d for Obta i n i n g Hy d rid e s of Transit ion Meta ls , S.K. Dolukhania n et al. (1977) . 55) S. K. Dolukhania n , Ap pli c a ti on of Self- P rop ag a ti ng Hi gh - Temp er atu r e Sy nthe sis Processes in Hy d rid e Chemi st r y and Tech-nolog y, Izvestiy a Akademi i Nauk SSSR, Neorga nic h eskiy e Mate r - 56)i alEy .,V .1 A4 g( 9a) b , ab1y5 8a n1- e15t 8 a4l. ,( 19R78e)g u. la rit ies of Zir c oniu m Combusti on in Hy d rog e n at a Pressure Less Than At m osph eric , Fiz i k a Goreniy a i Vzry va , 16 (6) , 35-41 (1980) . 57) A.A . Andreasya n et al., Obta i n i n g Carbid e s, Borid e s, Ni trid e s and Sil icid e s of Transit ion Meta l s for Prepa rati on of Wear Resis - tan t Str e ng the ned Parts , Sb. Mosk. Inst. Sta l i Sp la vov, 99, 5-7(1977) . 58) A.G. Merzhanov et al. , Prop e rti es of WSe 2, Obta i n e d by Self- P rop ag a ti ng Hi gh -Temp e ratu re Sy n th e sis , Izvestiy a Akademi i Nauk SSSR, Neorga nic h eskie Mate r ia l y, 13 (5) , 811-814 (1977) . 59) V.K. Prokudin a et al., Sy nthe ti c Molyb denum and Tung s te n Disu lfid e s, Poroshkovaya Meta ll urgiy a, 6 (186) , 48-52 (1978) . 60) U.S. Pate n t No. 3 , 379 , 503, Macro Process for Di re ct Produc- tion of Tungs t e n Carbid e , E. N. Smi th. 61) A.S. Dubrov in, Combusti on Processes in Chemi ca l Technolog y and Meta l lurgy , Meta ll oth e rmi c Processes in Ferrous Meta ll urgy , Moscow, pp. 29-42 (1975) . 62) V.V. Barzyk i n et al., Result s o f the Second All-Un ion Con fer -
ence on Technolog ica l Combusti on (Octo b er 10-13 1978), Fiz i k a Goren i y a Vzry v a, 15 (5) , 148-151 (1979) . 63) U.S.S.R. Pate n t No. 617 , 485, Meth o d for Producin g Cast Re- frac to r y mate r ia ls , A.G . Merzhanov et al., Jul y 19 (1978) . 64) A.G. Merzhanov et al., Self -P r op ag a ti ng High -Temp er atu r e Syn the sis of Cast Inorga nic Refr ac to r y Comp o unds, Doklady Akademi i Nauk SSSR, 255 (1) , 120-124 (1980) . 65) V.I . Itin et al., Sy nthe sis of Cast Tit an i um Nic k elid e by Com- busti on Processes, lzvestiy a Akademi i Nauk SSSR, Neorga nic h es- kie Mate ri a ly , 16 (11) , 1957-1960 (1980) . 66) J. Osug i, K . Shim i zu , K. Inoue, and K. Yasunarn i, A Comp ac t Cubic Anv il H ig h Pressure Ap pa ratu s , Rev. Phys . Chem. Jap a n , 34 (1) , 1-6 (1964) . 67) A.R. Sarkis y a n et al., Laws of the Combusti on of Mi xt u res of Transiti on Meta l s wit h Sil ic o n and the Syn the sis of Sil icid e s, Fiz i k a Goreniy a i Vzry v a, 14 (3) , 49-55 (1978) . 68) V.M. Maslov et al., Combusti on of the Sys t e m s Ni ob iu m - Alumi nu m and Ni ob iu m -German ium , Fiz i k a Goreniy a i Vzry va, 15 (1) , 49-57 (1979) . 69) I.P. Borovi ns kaia et al., Gasless Combusti on of Mixt u r es of Powdered Transit ion Meta l s wit h Boron, Fiz ik a Goreniy a i Vzry v a, 10 (1) , 4-15 (19 74) . 70) V.M. Shkir o and I.P. Borov ins kaia , Investig a ti on of Combus- tion Regu la ri ties of Tit an i um -Carbon Mi xt u r es, Combusti on Processes in Chemi ca l E函 nee ri n g and Meta ll urgy , Chemog o lovka, pp. 253-258 (1975) . 71) V.M. Shkir o et al., Pri nc ip le s of Combusti on of Tanta l um- Carbon Mi xt u r es, Fiz i k a Goreniy a i Vzryv a, 14 (4) , 58-64 (1978) .
72) V.M . Shkir o et al., Reacti ve Prop er tie s Exh ibi t ed by Vario u s Ty pe s of Carbon Durin g the Prepa rati on of Ti tan iu m Carbid e by Self-P rop ag a ti ng Hi gh -Temp e ratu r e Sy nthe sis , Poroshkovaya Meta l lurgzy a , 10 (202) , 6-10 (1979) . 73) T.S. Azaty an et al., Some Pri nc ip le s of Combusti on of Tit an iu m -Sil ico n Mi xt u r es, Fiz ik a , Goreniy a i Vzry v a, 15 (1) , 43-49 (1979) . 74) V.M. Shkir o et al., Prepa rati on of Tanta l um Carbid e s by Self- Prop ag a ti ng Hig h -Temp e ratu r e Sy nthe sis (SHS) , Poroshkovaya Meta l lurgiy a, 4 (196) , 14-17 (1979) . 75) I.P. Borovin s kaia et al., Self -P rop ag a ti ng Hig h -Temp e ratu r e Sy nthe sis of Bori de s, In Refr ac otr y Bor ide s and Sil ic ide s, Nau-kova dumka, Ki ev (1977) . 76) U.S.S.R. Pate n t No. 465 , 544, Meth o d for Obta i n i n g Bor ides of Tran sition Meta ls , A.G . Merzhanov et al., Ap ri l 7 (1973) . 77) I.A. Knys h ev et al., The Prop er t ies Includin g Some Crys t a l lo-chem ica l Prop e rtie s of Mi xe d Borid e s of Group Na-V a Elements , jou rnal of Less-Common Meta ls , 67, 347-350 (1979) . 78) A.R. West, Solid Sta t e Chemi str y and its A p pli c a ti on s, Joh n Wi le y & Sons, New York, p. 37 (1984) . 79) U.S.S . R. Pate n t No. 556 , 110, A Meth o d ° for Obta i n i n g Re- frac to r y Comp ou nds of Bor ide s or Carbid e s, A.G. Merzhanov et al., Ap ri l 29 (1974) . 80) V. I. Itin et al., Use of Combusti on and Thermal Exp lo sio n for the Sy nthes is of Inte r meta l l ic Comp o unds and Their Alloy s, Poroshkovaya Meta l lurgiy a, 5 (209) , 24-28 (1980) . 81) U.S. Pate n t No. 3, 353, 954, Meth o d of Produci ng Comp on ents by Reacti ng Part icu late Ing re die n ts , L.S. Wi lliam s, November 21 (1967) .
82) R.K. Str i n g e r and L.S. Wi liam s, Reacti on Pressin g : A New Fabric a ti on Concep t for Inte r meta l l ic and Meta l -Meta l loid Com- po unds, Sp ec ia l Cerami cs 4, pp. 37-55, The Brit ish Cerami c Research Assoc iat i on (1968) . 83) J.B. Holt, Combusti on Sy nthe sis of Refr ac to r y Mate r ia l s, UCRL-53258, Lawrence Liv e rmore Nati on al Laborato r y , Febru- ary (1 982) . 84) S.S. Ordan'ya n et al., Densif ica ti on of Nonsto i c hiom etr ic Ti ta- nium Carbid e Durin g Sin t e r i ng , Poroshkovaya Meta ll urgiy a, 7, 43-47(1979). 85) F. Fit ze r et al., Reacti on Hot Pressin g of Refr ac tor y Meta l Germanid e s, Hi gh Temp era tu r es-Hig h Pressures, 3, 547-554 (1971) . 86) V. I. I tin et al., Volume Chang e s Exp e rie n ced by Porous Soli ds Duri ng Nonis o th e rmal Liq u id - Phase Sin t e r in g and Self - Prop a g a ti ng Hi gh -Temp e ratu r e Sy nthe sis , Poroshkovaya Meta l- lurgiy a, 2 (170) , 6-11 (1977) . 87) LP. Borovin s kaia , Self-P rop a g a ti ng Processes in the Formati on of Solid Soluti on in the Zir c oniu m -Ni tro g e n Sy st e m , Doklady Akademi i Nauk SSSR, 231 (4) , 911-914 (1976) . 88) V. I. V ershin niko v -et al., Pressure Dep e ndence of Rate of Gas- Free Combustio n , Fiz i k a Goreniy a i Vzry v a, 5, 42-47 (1978) . 89) R.A . Andrie v skii , Some Novel Ef fec t s D isc overed in Reserch on Refr ac to r y Comp o unds, Izvestiy a Akademi i Nauk SSSR, 15 (4) , 563-568 (1979) . 90) S.M. Kats et al., Comp re ssiv e Creep of Alloy s of the ZrC-ZrB2. and Ti C -TiB 2 Sy st e m s, Poroshkovaya Meta ll urgiy a, 12 (228) , 70-75 (1981) . 91) M.A . Jan ney, Mechan ica l Prop e rt ies and Oxid a ti on Behavi or of
a Hot- P ressed SiC -15-vol%-TiB 2 Comp os it e, Am. Ceram. Soc. Bull., 66 (2) , 322- 32 4 (19 87) . 92) J,L. Woolfr ey , D.M . Levi ns , R.S .C. Smart, and M. Ste p h e nson, Eff ec t of Hot- P r essin g Condit ion s on the Str u ctu r e and Lea-chabil ity of Sy n roc, Am. Ceram. Soc. Bull., 66 (12) , 1739-1746 (1987) . 93) A.G. Merzhanov, Theory of Gasless Combusti on , Arch. Procesow Spa l ania , Serie s 5, Issue 1, pp. 17-39 (1974) . 94) A.P. Aldushi n et al., Prop a g a ti on Condit ion s of Ste a dy -S t at e Combusti on Wave, Re po rt s of the U.S .S .R . Academy of Scie n ces, Vol. 243, No. 6 (1978) . 95) N.P. Nov iko v et al., Thermodyn a mi c Analys i s of Self- Prop ag a ti ng High -Temp er atu r e Sy nthe sis Reacti on s, Combusti on Processes in Chemi ca l Technology and Meta ll urgy , Chernog o lovka, pp. 174-187 (1975) . 96) A.B. Aruty unya n et al., Theory of the Ign ition of Meta l Parti- des-Il . Ign ition of Meta l Part icl es wi th the Sim ulta n eous For-mati on of Product Fil m and a Soli d Soluti on , Fiz ik a Goreniy a i Vzry v a, 16 (2) , 10-19 (1980) . 97) A.B . Aruty unya n et al., Theory of the Ign ition of Meta l Part i- des-I . Ign it ion of Meta l Parti cl es in the Formati on of Soli d Soluti on , Fiz ik a Goreniy a i Vzry v a, 15 (3) , 16-22 (1979) . 98) A.G . Merzhanov and E.N. Rumanov, Formati on of Soli d Solu- tion s Under Combusti on Cond ition s, pu blic a ti on unknown, Mos-cow, pp. 161-165 (19 75) . 99) A.G. Merzhanov and F.I. Dubovit sk ii , Towards a Theory of Ste a dy -S ta t e Combustio n in Powders, Doklady Phys i c a l Chemis try, SSSR, 129 (1) , 153-156 (1959) . 100) G.B . Maneli s et al., The Mechanis m of the Combusti on of
Powders, Doklady Phys ic a l Chemi st r y, SSSR, 133 (Z) , 399-400 (1960) . 101) B.I . Khaik i n , Towards a Theory of Combusti on Processes in Hete r og e neous Condensed Media , Combusti on Processes in Chemi - cal Technology and Meta l lurgy , Chap ter N, Moscow(1975). 102) V.M. Maslov et al., Problem of the Mechan ism of Gasless Combusti on , Fiz i k a Goreniy a i Vzry va , 12 (5) , 703-709 (1976) . 103) Y. Mi yam oto , T. Nakamoto , M. Koiz u mi , and 0. Yamada, Cerami c- to - Meta l Weldin g by a Pressuriz e d Combusti on Reac- tion , ]. Mate r. Res., 1, 7-9 (1986) . 104) N. P. Novik o v, I. P. Borov ins kay a, and A. G. Merzhanov, Thermody n am ic A nalys i s of Self- P rop ag a ti ng Hig h -Temp er atu re Sy nthe sis Reacti on , Combustio n Processes Chemi ca l Technology and Mata ll urgy , Edit ed by A.G . Merzhanov, Chemog o lovka (1975) . 105) R.B. Bir d et al., Trans po rt Phenomena, Joh n Wi el y & Sons, Inc., New York, p. 245(1960). 106) F.P. Incrop er a and D.P. Dewi tt, Fundamenta ls of Heat and Mass Tri( lS/e r, Second Ed., Joh n Wi ley & Sons, Inc., pp. 37-47 (1985) . 107) Handbook of Chemi stry and Phys ics, 53rd Edition , Chem ica l Rubber Comp a ny (CRC) Press, Cleveland, Oh io, P.F-284 (1972) . 108) C.J. Smi thel ls, ed., Meta ls Refe r ence Book, 5th Edition , Publi - shed by Butt er wort h and Co., Ltd., London, Eng la nd (1978) . 109) Nati on al Bureau of Sta n dards U.S. Depa r bnent of Commerce, JA NAF Thennochemi ca l Tables, 2nd Edit ion , NSRDS-NBS 37, Washi ng ton , D.C. (1971) . 110) T. Baumeis t e r et al., eds., Marks' Handbook of Mechanic a l Eng ine eri ng , 8th Edit ion , McGraw-Hi ll Book Co., New York (1978) .
111) A. Gulya ev, Phys i c a l Meta l lurgy , Vol. 2, MIR Publi sh ers, Moscow (1980) . 112) R.B. Kote l fii ko v, S.N . Bushli'k ov, Z.G. Gali ak barov, and A.I. Kashta n ov, Handbook of Hi gh ly Refr a ct or y Elements and Com- pou nds, Table 4, Meta l lurgi ya, Moscow (19 69) . 113) M. C.I . C. Re po rt, Eng ine eri ng Prop er t y Data on Selecte d Cer-ami cs , 2, 5 . 2 . 4-11, Batt le Columbus Laborato r ie s (l979) . 114) Re po rt of the Nati on al Insti tut e of Research for Inorga nic Mate ri a ls (in Jap a nese) , No.1 (1972) . 115) S. Adachi , T. Wada, T. Mi ha ra, Y. Mi yam oto , M. Koiz u mi , and 0. Yamada, Fabric a ti on of Ti tan ium Carbid e Cerami cs by Hi gh - Pressure Self- C ombusti on Sin t e r in g of Ti tan ium Powder and Car-bon Fib e r, J Am. Ceram. Soc., 72 (5) , 805-809 (1989) . 116) KOFST, Fabric a ti on and Ap pli c a ti on of Comp o site Mate r - ial s, Proc. Sp ring Workshop of 1988 Academi c Confe r ence of Domestic and Foreig n Korean Scie n ti st and Technic i a n , May 11-12, Korea Research Insti tute of Chemi ca l Technolog y, Dae- jeo n, pp. 3-74 (1988) . 117) C.H . Yo, Y. Mi yam oto , Y. Takano, 0. Yamada, and M. Ko- izu m i, Fabric a ti on of TiB 2 -TiC Cerami c Comp o sit es by High - Pressure Combusti on Sin t e r i ng , MRS Intl. Mt g. on Adv. Mats ., 5, 119-124 (1989) . 118) J.B . Holt and Z.A . Mu nir, Proc. 1st Intl . Sym p . on Cerami c Comp on ents for Eng ine , Toky o , Jap an , ed ited by S. Somi ya, E. Kanai, and F. Ando, KTK Scie n ti fic Publi sh ers, New York, p. 721 (1983). 119) K. Ni iha ra, R. Morena, and D.P.H. Hasselman, Furt he r Rep ly to Comment on Elasti c/ Plastic Indenta t i on Damage in Ceram ics : The Medi an /Rad ial Crack Sy st e m , Comm. Am. Ceram. Soc., 65,
c-116 (1982) . 120) R.K. Govil a, lndenta t i on -Precrackin g and Double-Torsio n Meth o ds for Measurin g Fractu r e Mechanic s Paramete r s in Hot -Pressed Si3 N 4, ]. Am. Ceram. Soc., 63 (5-6) , 319-326 (1980) . 121) F.F. Lang e and K.C. Rad for d, Heali ng of Su rfac e Cracks in Polyc rys t a l l ine A li아,” ]. Am. Ceram. Soc., 53 (7) , 420-421 (1970) . 122) J.D . Snow and A.H . Heuer, Slip Sy st e m s in Al i03 , J Am. Ceram. Soc., 56 (3) , 153-157 (1973) . 123) T.K. Gup ta, Crack Healin g and Str e ng then i ng of Thermally Shocked Alumi na , ]. Am. Ceram. Soc., 59 (5-6) , 259-262 (1976) . 124) R.M . Cannon, W.H. Rhodes, and A.H Heuer, Plasti c Defo rm a- tion of Fin e -Grain e d Alum ina (Al 요) : I, Inte r f ac e-Contr o lled Di- ffus io n al Creep, ]. Am. Ceram. Soc., 63 (1-2) , 46-53 (1980) . 125) C.H . Yo. Y. Mi yam oto , and M. Koiz u mi , Sy nthe sis o f Ti Si :r by SHS Meth o d and Fabric a ti on of Ti B2 -Al20a Ceram ic Comp o sit es by HPCS Meth o d, Proc. 5th Korea-Ja p a n New Cerami cs Semi na r, Cheju , Korea Nov. 3-5, p. 91 (1988) . 126) Y.S. Touloukia n , Thermop hy s i c a l Prope r t ies of Matt er, IFI/ Plenum, New York, Vol. 12, p. 208, for Mo (1975) , Vol. 13, p. 778 for TiB 2 , and p. 891 for TiC (1977) . 127) J.B. Holt, The Use of Exoth e rm ic Reacti on s in the Sy nthe sis and Densif ica ti on of Cerami c Mate r ia l s, MRS Bulleti n, Octo b er 1-Nob. 15, pp. 60-64 (1987) . 128) Y. Mi yam oto and M. Koiz u mi , Pote n ti al i ty of Hi gh Pressure Combusti on Sin t e r i ng to Produce Ceram ic Based Multi- P hase Comp o nents , Proc. Intl . Insti tut e for the Sc ien ce of Sin t e r i ng (11SS) Sym po siu m , Toky o , Jap a n, pp. 511-516 (1987) . 129) T. Hira no, T. Yamada, J. Teraki, M. Ni ino , and A. Kumakawa,
A Stu d y on a Functi on ally Gradie n t Mate r ia l Desig n Sy s te m for a Thrust Chamber, P roc. 16th Intl . Syp o siu m on Spa c e Te ch nology and Sci en ce, Sapp o ro, Jap a n, pp. 375-380 (1988) . 130) K. Hi ra o, Y. Mi yam oto , and M. Koiz u mi , Combusti on Reac- tion Characte r is t i cs in the Ni trid a ti on of Sil ico n, Advanced Cerami c Mate r i als , 2 , 780-783 (1987) . 131) 0. Yamada, K. Hira o, M.Koiz u m i, and Y. Mi yam oto , Combus- tion Sy nthe sis of Sil ico n Carbid e in Ni tro g e n At m osph e re, ]. Am. Ceram. Soc., 72 (9) , 1735- 17 38 (1989) . 132) J. Zeng, Y. Mi yam oto , 0. Yamada, and M. Koiz u mi , Hot Isosta t i c Pressin g of ShNi .- SiC Comp os it e Powders Prepa r ed by the Ni triding Combusti on Reacti on , Proc. 2nd Intl . Confe re nce on Hot Isosta tic Pressin g-T heori es and Ap pli ca ti on s, Gait he rsburg, Mary la nd (l990) . 133) K. Hira o, Y. Mi yam oto , and M. Koiz u mi , Reacti on Analys is of the Combusti on Sy nthe sis of Transit ion Meta l Ni rtride s, Proc. Intl . Insti tut e for the Scie n ce of Sin te r in g (IISS) Sy m p os iu m , Toky o, Jap a n, pp. 551-556 (1987) . 134) T. Sahara, K. Hi ra o, Y. Mi yam oto , and M. Koiz u mi , Combus- tion Sy nthe sis of NbN Powders and Their Sup e rconducti ng Transi- tion Temp e ratu r es, J. Soc. Mat. S ci . Jap a n , 37, 55-59 (1988) . 135) Bib l i og rap h y on Gasless Combusti on Sy nthe sis , Ap pe ndix D. Advanced Mate r ia l s Technolog y, SPC Repo r t 932, Sy st e m Plan ning Corp o rati on , Sep tem ber (1983) . 136) A.G. Merzhanov, From the Academ ic Idea to Industr ial Pro-ducti on , Orga niz a ti on and Eff ecti ve ness of Sc ien ti fic Stu d ie s , pp. 30-36, circ a (1980) . 137) Self-P r op ag a ti ng High Temp er atu re Sy nthe sis - SPHTS, Tuesday A 仕 emoon Sessio n , Jan uary 18 (1983) , 7th Annual Con-
Jer ence on Comp os it es and Advanced Cerami c Mate r ia ls , Ame- rica n Cerami c Soc iet y , Inc., Cocoa Beach Floli da , Jan uary 16-19 (1983) . 138) Assessement of Sovie t Refr ac to r y Mate r i al s Technolog y, Secti on C, Chap ter Il , Advanced Mate r ia l s Tec?J lol og y, SPC Re po rt 932, Sy st e m Plan ning Corp o rati on , Sep tem ber(1983). 139) J. B. Holt, Exoth e rmi c Process Yi el ds Refr ac t or y Ni tride Mate r ia l s, Industr ial Research and Develop m ent, pp. 88-91 , Ap r il (1983) . 140) D.W. Ric h erson, Modern Cerami c Eng ine erin g, Marcel Dekker, Inc. New York, pp. 32- 36 (1982) . 141) ASTM Sp ec if ica ti on c-3 7 3, ASTM St a ndards, Part 13, Americ a n Soc iet y for Testi ng and Mate r ia l s, Ph ila delph ia (1969) . 142) JCP DS, 1985 Powder Dif frac ti on Fil e , Inorga nic Phases, Al- ph abeti ca l Index, Inte r nati on al Centr e for Di ffrac ti on data , Swar- thm or, Penn. (1985) . 143) A.R . West, Solid Sts te Chemi stry and its Ap pli ca tio n s, Joh n Wi el y & Sons, New York, NY, pp. 47-186 (1984) . 144) 맹선재 • 신명철 • 정영훈 • 이규환 • 현도빈, 『재료시험』, 한국과 학기술연구소, 재료시험 연구실, PP. 39-48 및 pp. 167-180. (1980) . 145) D.G. Bhat, Comment on Elasti c/ Plastic Indenta t i on Damage in Cerami cs : The Me dian /Rad ial Crack Sy st e m , ]. Am. Ceram. Soc., 64 (11) , c-165- c- 166 (1981) . 146) B.R. Lawn, A.G. Evans, and D.B. Marshall, Elasti ca l/ Pla sti c Indenta t i on Damage in Ceram ics : The Med ian /Rad ial Crack Sy s- ter n, J Am. Ceram. Soc., 63 (9- 10 ) , 574-581(1980) . 147) A.G . Evans and E.A . Charles, Fractu r e Tou gh ness Dete r m ina - tion s by Indenta ti on , ]. Am. Ceram. Soc., 59 (7-8) ,
371-372 (1976) . 148) K. Ni iha ra, R. Morena, and D.P.H. Hasselman. Futh e r Rep ly to Comment on Elasti c/ Plasti c Indenta t i on Damag e in Cerami cs : The Media n /Radia l Crack Sy st e m , Comm. Am. Ceram. Soc., 65, c-116 (1982) . 149) B. Marshall and A.G . Evans, Repl y to Comment on Elasti c/ Plasti c Indenta t i on Damage in Cerami cs : The Med ian /Radia l Crack Sy st e m , ]. Am. Ceram. Soc., 64 (12) , c-182-c-183 (1981) . 150) K.N i iha ra, R. Morena, and D.P . H . Hasselman, Evaluati on of K1c of Brit tle Solid s by the Indenta ti on Meth od wi th Low Crack-to - Indent Rati os , ]. Mate r . Sci . Lett. , 1 (1) , 13-16 (1982) . 151) S. Palmq vi s t, Occurrence of Crack Formati on Durin g Vi ck ers Indenta t i on as a Measure of the Toug hn ess of Hard Meta l s, Arch. Eis en huect en wes, 33 (6) , 629-633 (1962) . 152) A.G . Evans and T.R. Wi lsh aw, Qu asi Sta t i c Soli d Partic l e Damage in Brit tle Solid s : I, Acta Meta l l., 24 (10) , 939 -956 (1976) . 153) W. Daw ihl and G. Altm e ye r , Meth o d for Dete r mi na ti on of the Resis t a n ce to Defo r mati on of Heat- R esis t a n t Mate r ia l s, Par- ticu larly Hard Meta l in a Crack Formati on , Z. Meta ll kd., 55 (5) , 231-237 (1964) . 154) B.R . Law and E.R. Fuller, ]. Mate r. Sci., 10, 2016 (1975) . 155) 新原皓一, 「 Ceram ic s 의 微少壓子 壓入 破壤」 , 『 特集 Cerami c 의 力學的 特性 評價 』 , 20(1), 12-18(1985). 156) 柳田博明, 『金屬 』 , 50 (10) I 55 (1980)
찾 o~ S!.J I
기 가압연소용접 171 가열대 26 가이거 계측기 212 강표면화 195 강합금 20 건조무게 201, 202 게르만화물 19 격자성수 213 결정 결합 211 결정 단색화 장치 (Monochromato r ) 214 결정 분정 (Cris ta l seg reg a ti on ) 221 결정도 (Cr yst a l li nity) 217 결정 분광방식 (Waveleng th
고속비디오 23 고압고열 프레스 (HPHP) 74, 75 고압 연소 소결법 (HPCS) 22, 23, 37, 52 고압 자체 연소 소결법 (HPCS) 137 고압셀 A 형 145 고압셀 B 형 145 고압 자체 연소 소결 공정의 응용 171 고열-압력 소결 51 고열 등방압 프레스 (HIP) 44, 52, 74, 75, 139 고열 프레스 (Ho t Press) 74, 139 고열-가압 (Ho t pre ssin g) 51, 52 고온 S i C 반도체 기질물질 23 고온측정 31 고온구조물 20 고체-고체계 반웅 24 고체-기체계 반응 24 고체-액체계 반응 24 고체 윤활제 21 곡선적합도 136 공정 단순화 78 공정 변수 53 공정별 연소온도 17 과잉 엔탈피 46 광학고온측정 29 광학다중 동로분석기 23 Gu inier Heig g 216 Gu inier Lin e 215, 216
Gu i n i er 초점법 213 Guin ier 카메라 214 구조 소재 (str uc tu ral mate r i al) 13 구조화대 26 규소화물 20, 45, 53 금속 또는 합금섬유 158 금속열반응 46 금속초전도체 21 금속간 화합물 17, 19, 20, 45 금속열 과정 44 금속열반웅공정 17 금속열 반응(산화-환원 반응) 19 금속영화물 25 금속반부견소 37 기능적 기울기 재료 (FGM) 179 기체불꽃점화법 26 기체입력 연소소결 178 기체압력 연소소결법 52 꺾임 강도 (M.0 . R) 234 꺾임강도 236 L 난류 96 난알 통과 파열 방식 162 낱알간 미끄러짐 72, 73 난알간파열 221 낱알간형 151 낱알관통파열 221 난알관통형 151
내화성 물질 20 내화성 생성물 19 내화성 세라믹스 22 내화성 화합물 17 냉각속도 59 냉등방암 프레스 (CIP) 74 냉압축된반응물 24 Nb 18 NbN 23 니켈화티탄 41 니켈화물 19 드 단열 반응 온도 81, 113, 119, 122 단열 반응한계 55 단열온도 84, 85 단위세포 파라미터 209 DARPA 13, 22 DARPA/ L LNL 프로 1 램 81, 191 대기압력 증가법 50 대류 96 대이터 곡선 적합도 129 Debye - Scherrer 카메라 213 띠녹음 (zone meltin g) 142 띠정제 (zone Nefin ing) 63 2 Reyn o ld 수 106
레이저 점화법 26, ·29 로드 셀 (load cell) 236 로렌스수 88 Rockwell 경도 223 루이스수 90, 99 Le Chate l ie r Braun 원리 120 □ 마디 온도 129, 132, 134 마스터 합금 40 마이크로경도 143 마이크로구조 17 마이크로 농도계법 (micro densi- tom etr y) 216 마이크로분석 151 맥동 59 맥동진동수 36 면적계 (pla nim ete r ) 213 모세 분산 48 모형화 73 몰리브덴 디스크 139 무정형 붕소 119 물리적 변수 58 물질흐름 96 미래의 전망 192 미분조절 부피 91 Mil ler 지수 209 밀도측정 199 밀도측정 실예 204
t:I 반구형 크랙 225, 226 반복연소 37 반복해석식 134 반응압축기 71 반웅 역학 99 반응완결도 130 반응 전대 (pre reacti on zone) 68, 69 반응제동 61 반웅파라미터 81 반응 현상학 96, 98, 102 반응물분말의 밀도 56 반응물분말의 입자크기 58 반응물 펠릿의 밀도 56, 58 반응물펠릿의 지름 55 반응전 콤팩트 (Green comp ac t) 27, 44,49, 68,71, 74 발열체 21 방사방향 분포함수 211 방사상크랙 227 Vega r d 법칙 210 변환 효율 146, 149 보호코팅 20 복사경계 조건 134 복합세라믹스 193 복함 세라믹스 제조 155 복합소재 21 본 성 체 적 변 화 (Int r ins ic Volume Cha nge) 151, 152
본체-고체상 111 본체-기체상 105 본체액체상 105 부생성물 19 분말생성물 41,42 분말야금 13 분말회절철 207 분말상 190 분산경화밀어내기 43 분석 모델 78, 127 불안정 연소 34, 35 불안정 연소방식 62 불안정 연소영역 47 붕소 18 붕소의 녹는접 119 붕소화몰리브덴 19 붕소화물 20,45 Bragg 각 208 Bri ne ll 경도 223 BN 두관 139 비결정성 고체 211 비기체 연소생성물 17 비기체 연소합성법 15 비기체 연소 합성법의 전망 189 비기체 연소활성법 16 비례성광 212 비산화물연소합성 24 비아레니우스 열발생 루틴 135 Vic k ers 경도 223, 224 Vic k ers ll~l 크로 경도 148
人 산화몰리브덴 19 산화황선제 19 산화 r 슬래그 196 상 C ' 밀도 200 시정물 희석 58, 60, 61 서멧 19, 17, 45 선분석 220 섬유상강화재료 157 세라믹스 17, 19 세라믹스분말 22 세라믹스섬유 158 세라믹스철단기 40 세라믹스제법 137 세라믹스 코팅 22, 23, 195 세라믹스콤팩트 24 세라믹스군닫f 복합충 23 셀 장치 139 셀렌화물 19,43 Shore 경도 223 소결 메커니즘 63, 151, 155 소성흐름 72 수소화물 19, 20, 40, 43 S t oke 법칙 106 스피넬구조 210 스핀 연소 36 슬래그 19,44 십도 (dep th of f ield ) 21s 써브루틴 128
THERM LIST 12s the rm 132 。 아레니우스 열 생성항 129 Arch im edes 법 106, 201 Acheson 법 25 AIN 23 알루미늄화물 19 압력 구배 69 압력 장치 72 압입 (IM) 파괴 시험 228 압혼하중 231 액화법 44 에너지분산 분광방식 222 SH 혜 13, 15-17, 21, 22, 24, 137 SPC 13, 78, 96, 189 SPC (sy st e m pla n ning corp o rati on ) 의 목표 127 Si3 N 4 23 S i 3N ◄ -S i C 계 184 SiC 22, 25, 153 S i C 연소소결 메커니즘 153 S i C 콤팩트 제조의 상 데이터 156 SiC 콤팩트의 제조 149 Si ~ HPCS 처리 149 S i O 기 단열온도 149 S i 0 긱 반웅열 149 X 선 결정구조 분석 207
x- 선 먀가크로 분석 143 M0Si2 4o MoSi2 -T iA I 계 183 EPMA 219, 222 역사적 배경 189 연마 43 연마제 21 연연삭소 강4도3 “ 연소 메커니즘 80, 97 연소반응현상학 77 연소방식 34 연소속도 56 연소엔탈피 35 연소온도 54 연소온도의 조절 57 연소제동 53 연소조절 53, 60 연소 진행 앞면 (combusti on fron t) 26, 33, 38, 85 연소활성화 53 연소대 17, 25, 26 연소파 15 열 덮개 66, 67 열분해 반응 25 열성크 32 열 입력 134 열 저항체 22, 88, 89 열 전도도 (k) 87 열 파러미터 134
열 흐름 95, 96 열식각표현 221 열유속방정식 93 열전도속도 32 열폭발 60 열확산 방정식 90, 93, 95 열확산도 (a) 87 영상사진촬영 31 예비 반응가열 40 예열 60 예형 펠릿 143 온도 의존성 물성 편차 135 운동량흐름 96 원십 가속법 49, 50 원심 압력 196 원십 데르밋 23, 197 원자로 연료의 합성 194 위스커 (Whisk er) 158 유동띠법 (floa tin g zone meth o d) 23 유리 섬유 158 윤활제 20 이론 밀도 201, 205 이중상결합 18 이차원적 전이모델 132 인장응력 235 일차원적 전이모델 129 일차원적 파동모형 35 입방 모루 (cub ic anvi l) 74, 139 입자상분산 157
x: 자국파열법 225 자동진동연소 62 자체 전파 14 자체 전파발열반응 21 자체 지속 14 자체 유지 단열반응 77 자체 전파 고온합성 (SHS). 77, s1 자체 점화 61 자체 지속연소 33 작은 각 X 선 산란 기술 (SAXS) 212 전기 방전법 26 전기 스파크 27 전기 화학퍼텐셜 117 전기적 두과 71 전이 열 확산식 129 전자 탐침 마이크로 분석 175 전지소재 21 정분석 220 점화공정 27 점화기 26 점화정점 67 집합 18, 22 정류상태 연소영역 47 정류상태 연소 34, 35 정상반복연소 37 정상소결 51 정지 조절부피 68
제조다공성 200 조절 체적 78 주물복합체 195 주물생성물 44, 9 7 주물 생성법의 발달 상태 44, 50 주사 전자 현미경 (SEM) 147, 21s 중원소 (Hea vy Element) 217 ZrBr2 59 ZrN 23 Zr02 지지대 27 지수 매기기 213 진공증착 221 전공창 30 진동연소 36 질량이동 35 질소연소소결 183 질소화연소반응 23 질소화물 20 질화금속 85 질화 알루미늄 23, 99 질화 알루미늄 반응의 상 데이터 103, 104 질화 알루미늄의 반응현상학 102 질화 알루미늄의 자유에너지 값 100 질화물 45 天: 착물세라믹스 193 착합성체 18
착화합물 45 창방출기 23 첨가제 48 체적밀도 201 초가소성 (Sup er p la stic ity) 18 초강연마제 20 초소성 거동 73 추가분쇄 60 측면 크랙 227 더 Carbon itride 18 칼코겐화물 20, l9 combust 129 Combus 떠 결점 135 Knoop 경도 223 크리핑 운동 106 E 탄성 계수 228, 231 탄소 리본 히터 27, 28 탄소연쇄 60 탄소두관 139 탄소 두관 히터 27, 28, 146, 149 탄소봉전극 27, 28 탄화물 19, 20, 4:5 탄화지르코늄 43 탄화텅스텐 (WC ) 44
탄화티탄 (T i C) 16, 1s, 21, 22, 25, 147, 153 탄화티탄 분말 42, 43 탄화티탄서멧 46 탄화티탄의 합성 107 테르밋 반응 23, 29 테르밋 점화 33 두과 전자 현미경 (TEM) 21s 특성 분석법 199 틈새형 화합물 54 TaN 23 TiB 2 22, 23, 25 TiB 2 콤팩트의 제조 142 TiB 2 합성의 상 대이터 120, 121, 123, 126 TiB 2 합성의 자유에너지 값 118, 124 TiB 2 -Al203 콤팩트 167 TiB 2 -Ni 계 180, 183 TiB 2 -SiC 콤팩트 164 T iB 2-T i C 콤팩트 159 T iB려 합성 118 TiC 콤팩트의 제조 145 TiC 합성의 상 데이터 115 TiC 합성의 자유에너지 값 113 TiC o .85 148 T i Cx 의 마이크로 경도 147 Ti ~ Gib b s A~ 에너지 107, 113 Ti0 HP g1 리 145 T i여 녹는접 107
T i O 긱 합성 상 데이터 109, 115 TiN 23 工 파괴 강도 18, 236 파괴 인성 151, 221, 225 파괴해석 (failur e analys i s ) 222 파동속도 37 파이로미터 23, 31 파이로 필라이트 셀 139 파이로필라이트 (pyrop hy l ite) 15 3 파일럿 규모 190 판상형 물질의 모델화 134 Palm pvi s t크랙 225, 226 평균파속 36 평형 변환 86 Pois io n 효과 226 포멧 (form at) 129 표면코팅 41 푸리에 법칙 87, 93 필름계수 134 필름 입자 134 -lo 하소 (Calcin ing) 60 하중받침점 234 핵에너지 20 핵형성 자리 99
형상기억 합금 41 화학 양론적 비 54, 55 화학활성제 60, 62 화학로 40, 65, 67, 178 확산 96 확산메커니즘 74
확산질량 134 황화물 19, 43 휨 강도 182 혹연화 60 흡착자리 104
여철현 공주사범대학 화학과 졸업(이학사) 연세대학교 대학원 석 ·박사과정(이학석 ·박사) 이스라엘 We i zmann 연구소 연구원 (Pos t -Doc t or) 프랑스 Bordeaux 제 1 대학 CNRS 고체화학연구소 연구원 일본 Osaka 대학, ISIR SANKEN 연구원(J SPS Fellow) 현재 연세대학교 이과대학 화학과 교수 및 자연과학연구소 초고온고압연구실 실장 비기체 연소합성 (SHS) 대우학술총서 자연과학 7I 1991 년 5 월 10 일 찍음 1991 년 5 월 20 일 펴냄 지은이·여철현 펴낸이•朴孟浩 펴낸곳•民音社 출판등록 1966. 5 .1 9 . 제 1-142 호 135-120 서울 강남구 신사동 506 번지 강남출판문화센타 5 층 우편대체번호 010041-31-0523282 은행지로번호 3007783 515-2003~5( 편집부) 515-20'0 0 ~2 (영업부) 515-2007, 515-2101 (팩시밀리) 값 9,500 원 @ 1991, 여철현 자연과학 KDC/434.1 Pri nt e d in Seoul Korea
대우학술총서 자연과학 1 소립자와 게이지 46 급변론 박대현 상호작용 김진의 서 생체에너지 주충노 2 동력학특론 이병호 48 리이만 기하학 박 을 용 3 질소고정 송승달 49 群표현론 박승안 4 相轉移와 임계현상 김두칠 50 비선형 편미분 방정식론 5 촉매작용 진종식 하기식 6 외스바우어 분광학 옥항남 미 생체막 김형만 7 국 미량원소의 영양 승정자 52 수리분류학 고철환 8 수소화 봉소와 53 찰스 다윈 정용재 유기 붕소화합물 윤능민 54 금속부식 박용수 9 항생물질의 전합성 55 양자광학 이상수 강석구 56 효소반응 속도론 서정헌 l0 국소적형태의 Aliya h- Si n g e r 57 화성암 성인론 이민성 지표이론 지동표 58 확률론 구자홍 11 Muc op ol y sacchar i des 의 59 분자 분광학 소현수 생화학 및 생물리학 박준우 60 벡터속 이론 양재현 12 천 체물리학 홍승수 61 곤충신경생리 학 부경생 13 프로스 E 달라딘 합성 김성각 62 에너지띠이론 모혜정 14 천연물화 학 연구법 63 수학기초 론 김상문 우원식 64 신경 과학 박찬웅 • 김승업 15 脂防營養 김숙회 65 BCH 부호와 Reed- 16 결정화 유리 김병호 Solomon 부호 이만영 17 고분자의 화학반응 66 양자전기역학 김영덕 조의환 • 67 군환론 박재걸 18 과학혁명 김영식 68 대수기하학 조영현 19 한국지질론 장기홍 69 양자장 이 론 아재형 20 정보이론 한영열 70 해 양오염과 생태계
