

심재형 서울출생 서울대학교 문리과대학 식물학과 졸 업 캐나다브리티쉬 컬럼 비아대학교 이학박사 ( 생물해양학 ) 현재 서울대학교 자연과학대학 해양학과 교수 한국해양학회 회장 주요논문 「한국동남 해역의 플랑크톤 연 구」 외 60 여 편
해양오염과생태계 
 해양오염과생태계
해양오염과생태계
책 머리에 오늘날 지구상의 거의 모든 대륙의 연안 주변은 산업과 상업, 여가선 용과 주거지롤 목적으로 인간에 의해 그 사용이 점점 증가하고 있다. 연 안 지역의 천해 수역은 산업과 도시의 배출로부터, 그리고 폐기물의 해 양 투기로부터 실로 광범위한 오염물질을 직접적으로 받아들이고 있다. 더구나 이러한 직접적인 투입 이의에도 보다 확산된 수많은 오탁물질이 유입되고 있다. 죽 농경수와 내륙 하천이나 강수에서의 폐수 방출에 따 른 유입, 도시로부터의 폐수 유입, 해안 지역의 주거지와 산업단지로부 터의 폐수 유입, 공장 굴뚝과 자동차 배기관을 근원으로 하는 대기로부 터의 유입 등이 그것이다. 이러한 폐기물은 대부분이 전세계 수산생물 생산의 90% 이상을 차지하는 대륙붕 해역에서 혼합되고, 결과적으로 해 양환경의 질적 악화가 불가피하게 촉진된다. 엄밀히 말해서 환경의 질적 악화는 인류가 최초로 취락을 이루고, 불 을 사용하였을 때부터 시작된 것이지만 기하급수적으로 팽창하는 인구와 급속도로 발전하는 산업화 사회로부터 계속 증가하는 영향 아래서 환경 의 문제가 심각하게 대두된 것은 근래의 일이다. 죽 공기, 물, 토양 등 의 자연환경과 식품 등의 인위적 환경의 오탁은 생태계를 구성하고 있는 동물 및 식물 군집의 지속적 유지에 대한 위협이 되어왔고, 궁극적으’로
는 인류의 생존 자체도 위협할 수 있는 정도에 이르고 있다. 그럼에도 불구하고 인류의 염원에 따라 진행되는 문명의 발달은 연료, 운송, 공업 화합물, 비료, 살충제 등, 무수한 인위적 산물의 양적 증가를 불가피하 게 만들고, 따라서 모든 종류의 폐기물 역시 지속적으로 배출, 증가하는 것은 당연한 귀결이다. 해양에서의 폐기물 두기는 현대 사회가 심각하게 안고 있는 폐기물 처 리 문제에 대한 어쩔 수 없는 대안이다. 그런데 바다에서의 투기는 육상 의 그것과는 본질적으로 성격을 달리 한다. 해양에서는 두기된 폐기물이 그 자리에 남아 있지 않고 해수의 유동에 따라 이동하기 때문에 상당한 범위의 해역에 영향을 미칠 수 있는 반면에, 해수의 방대한 희석능력에 의해서 무해한 농도로 희석될 수가 있다. 따라서 해양에서의 오영 영향 울 평가하기 위해서는 어떠한 종류의 오염물질이 얼마만한 양으로 바다 에 두입되며, 이들 물질이 해수중에서 어떻게 변화하는가, 또한 이들 물 질이 해양의 생물에게 어떠한 영향을 미치고 궁극적으로 이들 물질의 동 태가 인류의 건강과 복지에 대하여 직접, 간접으로 어떠한 위협을 주는 가를 알지 않으면 안 된다. 또한 해양오염과 관련된 많은 분쟁은 연안 해양환경의 다양한 이용으로부터 야기된다. 이러한 분쟁의 해결은 오염 물질의 유입 성질과 크기, 해양에서의 오염물질의 분산과 지속, 그리고 해양자원 생물에서의 축적과 영향 등에 대한 상세한 정보가 요구된다. 이들 정보는 해양환경에서 폐기물 두기의 결과를 예측하고 그 투기를 관 리하는 수단을 개발하는 데 필수적인 요건이다. 이와 같은 과정을 통해 서 얻어진 결론이라 해도 후에 새로운 정보나 경험에 비추어 수정되지 않으면 안 되는 경우가 해양오염에 관련된 문제에서는 언제나 가능하다 는 점을 염두에 두어야 한다. 세계적인 추세의 하나이지만 우리나라에서도 최근에 해양오염과 그 결 과에 대한 인식이 점차로 증대하고 있을 뿐만 아니라 그 대응책에 대한 요구도 비등하고 있다. 대부분의 경우에 규제하는 정부 당국은 이러한 사회적 압력에 과민하게 반응을 나타내고, 해양환경으로의 폐기물 투기
를 금지시키려는 것이 보통이다. 그러나 이러한 금지 조처로 나타나는 양상은 반드시 긍정적인 것은 아니다. 최근의 경험은 많은 경우에 있어 서 해양 투기를 대신하는 대안이 해양 투기 그 자체보다 환경에 더 해롭 다는 사실이 드러나고 있다. 따라서 규정이 완화되어 폐기물 두기에 대 한 해양환경의 동화능력을 이용하도록 허용하는 것이 현재 선진국에서 취하는 방향이다. 한편, 이러한 해양환경의 자정능력을 광범위하게 이용 하더 라도 환경 의 수용능력 Carr ying capa ci ty 의 범 위를 넘 어서 지 않도록 하는 것은 무엇보다 중요한 일일 것이다. 그러기 위해서는 해양과 해양 환경에 관한 전문가들이 해양의 안전한 동화능력을 측정하고 이 능력에 과도한 부담을 주지 않도록 하는 폐기물 투기의 합리적인 체계를 세워야 할 것이다. 폐기물 두기 장소로서의 해양 공간을 하나의 자원으로 간주 할 때, 이 자원의 개발은 질서와 균형의 토대 위에 이루어져야 한다. 해양은 아직도 미지의 분야라 할 수 있고, 대부분의 환경 기술자들이 해양환경에 대하여 익숙하지 않은 반면, 많은 해양 과학자들은 오염 문 제에 대하여 잘 모르고 있음도 사실이다. 이 책은 기본적으로 대학원 수 준의 학생들을 위해 집필된 것으로서 환경기술 분야와 해양과학 분야, 그리고 기타 분야로부터 오염에 관련된 정보를 종합하여 해양환경에서 오염의 영향을 이해하고 조절하는 데 대한 통일된 접근 방식을 제시하고 자 하였다. 따라서 문제가 되고 있는 각종 오염원에 대한 출처와 평가, 그 유입에 따르는 문제의 정도, 오염으로 인한 해양의 물리, 화학, 생물 학적 영향, 생태학적 • 환경학적 방법울 통한 악영향의 기작(機作) 등을 설명하여 학생들은 물론 해양오염과 관련된 연구자들에게 도움이 되고자 하였다. 이상과 같은 저자의 의도에서 이 책의 구성은 제 2 장에서 해양학의 기 초개념을 통해 해양환경의 특성을 이해하도록 하였고, 제 3 장 및 제 4 장에 서는 해양 생태학적 원리를 통해 오영 문제에 접근할 수 있도록 먹이연 쇄론과 일차 생산론을 서술하여 생태계의 생물학적 과정을 파악함으로써 해양오염으로 야기되는 환경의 악영향에 대한 기작을 이해토록 하였다.
제 5 장에서는 오영원에서 나오는 유독물질이 생물에게 미치는 영향에 대 하여 그 측정과 자료 해석에 관하여 다루었다. 제 6 장부터 제 11 장까지는 주요 오염원, 죽 유기물질, 금속, 산업폐수, 살충제, 유류, 방사성 물질 등의 특성과 출처, 해양생물과 해양 생태계의 영향 등을 비교적 상세히 서술하였다. 제 12 장에서는 우리나라 연근해역 오염 현황을 개략적으로 기술하여 우리나라 해양환경의 오염실태를 소개하였다. 끝으로 제 13 장에 서는 현대 환경오염 분야에서 새로운 경향으로 관심을 끌고 있는 해양오 염의 생물학적 예측에 관하여 현재 이해하고 있는 내용과 전망을 밝혀 오염 연구의 지향점을 제시하려고 하였다. 해양환경에서의 오염은 흔히 변화성이 매우 크기 때문에 저자의 편견 이 배제되도록 가능한, 논거의 양면을 나타내고자 하였으나 집필을 끝내 고 보니 처음에 기도하였던 바와는 달리 미흡한 점이 한두 가지가 아님 울 보게 된다. 이 점에 유의하고, 또 앞으로 독자 여러분의 아낌없는 질 정과 친절한 조언을 얻어 판을 바꾸어 가면서 고칠 것은 고치고 새로운 정보는 추가하여 보완할 것을 다짐하는 바이다. 이 책을 펴냄에 있어서 무엇보다도 주제에 관하여 저술할 기회를 마련 함으로써 저자로 하여금 해양환경과 오염의 문제를 정리할 수 있도록 도 움을 준 대우재단에 대하여 심심한 사의를 표한다. 아울러 공부하는 사 람의 만만치 않은 뒷바라지를 한결같이 따뜻한 마음으로 감내하며 지켜 주고 있는 아내에게 고마운 마음을 전한다. 1991 년 3 월 관악산록 연구실에서 저자
해양오염과생태계
차례책 머리에 5제 1 장 서론 • 131-1 해양오염의 현황 131-2 해양환경과 오염물질의 투기 151-3 해양오염의 정의 181-4 측정 단위 19제 2 장 해양학의 기초개념 • 212-1 서언 212-2 해양의 일반적 특징 212-3 해양의 지형 232-4 해양의 물리학적 특칭 252-5 해양의 지질학적 특칭 382-6 해 양의 화학적 특칭 432-7 해양의 생물학적 특칭 54제 3 장 먹이연쇄의 개념 • 63
3-1 먹이전달효과와 먹이연쇄 643-2 수계에서의 물질 순환 683-3 생태적 피라밋 693-4 먹이망의 구조와 물질의 농축 72제 4 장 해양 일차생산량 • 774-1 일차생산량의 의의 774-2 해양에서의 일차생산량의 제한요인 794-3 영양원소의 실험적 배경 85제 5 장 오염물질의 독성 • 895-1 급성 및 만성 독성 905-2 독성의 측정 935-3 독성자료의 해석 99제 6 장 유기성 폐기물 • 1076-1 생물분해성 유기물질 1076-2 유기물질의 측정 1086-3 해양환경에 대한 생물분해성 유기물질의 영향 113 6-4 병원균의 유임 1146-5 부영양화 1246-6 생활하수의 처리 131제 7 장 금속 • 1377-1 금속의 섭취와 생물축적 1377-2 수은 1407-3 카드뮴 1487-4 구리 152
7-5 납 1537-6 철 156제 8 장 산업폐수 • 1578-1 산소 감소 157 8-2 펄프 산업 160 8-3 제당 산업 166제 9 장 할로겐화탄화수소 • 1699-1 저분자량 화합물 1699-2 살충제와 PCB-1709-3 국 해양환경으로의 유입 1739-4 해수중에서의 동태 1749-5 할로겐화탄화수소의 생물학적 작용 175 9-6 해양환경에의 영향 180제 10 장 유류 • 18310-1 유류오염의 출처 18410-2 석유의 성질 18910-3 해양환경에 대한 유류 유출의 영향 19310-4 해수중에서 유류의 변화 202제 11 장 방사성 폐기물 • 22111-1 방사능의 본질 22211-2 방사선의 특성 22811-3 방사선의 생물학적 영향 22911-4 해양환경에 대한 방사선 핵종의 영향 23211-5 해양에서의 방사능 출처 234
11-6 핵폐기물의 관리 243제 12 장 우리나라 연안해역의 오염실태 • 25112-1 연안해역의 특성 25112-2 생활하수 및 공업단지 조성에 따른 연안오염 25312-3 간척 • 매립사업에 따른 연안오영 25512-4 천해양식과 자가오영 25912-5 방사성 물질과 온배수 열의 문제 26012-6 연안해 역의 일반 수질 현황 26112 구 중금속 26512-8 영양영 26612-9 적조 26812-10 유류오영 270제 13 장 해양오염에 대한 생물학적 예측 • 27313-1 배경 27313-2 생화학적 및 세포학적 반응 27413-3 생물 개체상의 반웅 27713-4 모의 군집 28113-5 개체군 동태에 있어서의 변화 28313-6 군집 동태와 구조 28413-7 맺음말 286참고문헌 289찾아보기 297제 1 장 서론 1-1 해양오염의 현황 해양의 오염이 일반의 관심을 크게 끌게 된 것은 근래의 일로서 1960 년대 후반에서 1970 년대 초반에 각종 매스컴에 의해 해양오염에 관한 보 도가 확대되었고 이에 따라 정치적인 압력이 증가하고 해양과학자들의 해양오염에 관한 연구가 활발하게 되었다. 그러는 동안 일반의 관심은 에너지와 경제위기의 문제로 돌려져 관심이 감소되었다. 그러나 1980 년 대에 들어서자 방대한 양의 쓰레기 두기에서 오는 문제, 서독 및 네덜란 드에 서 titan iu m dio x id e (Ti0 2 ) 제 품으로부터 의 폐 기 물 등이 일반의 상당 한 관심을 야기시켰다. 우리나라에서도 이 시기에 주로 항구에 한정된 것이기는 하나 연안 수역의 수질오염에 대한 관심이 주어지기 시작하였 다. 지구상에 남아 있는 유일한 낙원이라 할 수 있는 바다를 어떠한 대 가를 치르더라도 깨끗하게 유지해야 한다는 점에 전반적인 합의가 이루 어져 있음에도 불구하고 해양오영 문제에 보다 더 적극적인 조처가 이루 어지지 않는 데에는 몇 가지 이유가 있다. 첫째, 연안 해역에서, 또는 선박에 의한 바다의 오염을 감소 내지 방 지하기 위한 여러 가지 방법은 이미 강구되었다. 공업선진국에서는 관청 이나 관계기관에서 연안 해역 내에서의 새로운 공장건설을 엄격히 감시
하고 있으며, 폐기물처리 공장들이 건설중이거나 계획되고 있다. 뿐만 아니라 오염방지를 위한 법이 제정되고 규제기관으로부터 긍정적인 결과 를 얻기 시작하고 있으며 이러한 결과로 새로운 참사를 방지하고 모르는 사이에 전행되는 파괴과정을 중지시키거나 최소한 그것을 둔화시킬 수 있게 되었다. 둘째, 해양오영에 대하여 효과적으로 대처하기 위한 비용이 너무 크므 로 그 비용을 감당하기 어렵고 이에 따라 해양생물에 대한 위협을 체념 하려는 경향이 있다. 이 점은 유류와 염화탄화수소의 예를 들어 증명할 수가 있다. 유류에 의한 오영은 가장 결정적인 방법으로 대처하지 않으면 안 된다. 그러나 돌발적인 사고가 있을 수 있고 이러한 사고는 해상수송과 해저 송유관을 제거하여야만 방지할 수 있다는 사정을 누구나 알고 있다. 상당량의 DDT 를 포함해서 염화탄화수소가 해마다 약 8 만톤 가량 대 기를 통해 바다로 유입된다. 이 문제는 저개발국가들이 경제적, 기술적 이유로서 모기와 곤충을 박멸하기 위해서는 DDT 를 사용할 수밖에 없다 는 주장을 철회하지 않는 한 별 방법이 없다. 다시 말하면 과학이 중요 한 새로운 주장을 발전시키지 않는 한 달라지는 것은 아무것도 없을 것 이다. 이러한 것들은 해양 연구가 스스로, 한편으로는 생물과 생태계의 질적 문제, 다른 한편으로는 경제적 이해와 실제의 문제 양자 사이의 갈 등을 노출하는 두 예가 될 것이다. 셋째, 1971 년 ~1980 년 사이에 유류 사고 이의에는 해양 재해에 관한 놀라운 사건이 없었다. 이는 그 이전까지의 암담하거나 위협을 주는 여 러 가지 발견을 수정할 수 있게 되었다. 예컨대 수은 (H g)은 해수중에 자연상으로는 소량 존재하지만 분명한 독극물이며 생명 과정에 유해한 것이다. 이것이 지역적으로 축적되는 곳에서는 큰 재해를 초래한다. 그 러나 인간에 의해 방출되는 수은의 양이 전 세계적으로 해수중의 농도를 상당히 증가시키기에는 불충분하다는 것이 알려져 있다• 그럼에도 불구하고 여전히 잠재적으로 위험한 물질이 여러 가지 있다. 합성유기화합물이 환경 내에서 생태적으로 어떻게 행동하는가 하는 문제 에 대해서는 그 체계적인 연구가 겨우 시작된 단계이다. 무엇보다도 해
양 연구 자체가 아주 새로운 분야임을 유의할 필요가 있다. 해양오영에 관한 연구는 40 여 년 전 해양에 두기된 방사성 폐기물에 대한 연구로서 바롯되었고 그 결과를 검토하기 위해 제 1 차 국제해양오 영회의가 1959 년에 개최되었다. 그러나 실제로 문제가 얼마나 심각한지 롤 당시에는 알지 못하고 있었다. 해양 관련 국가들에 의해 해양오영 연 구의 수많은 결과들이 출판된 것은 1966 년 이후이며 우리나라의 학계가 해양오염에 관심을 둔 것은 1970 년대의 일이다. 시간의 경과와 결과로 나타나는 객관적 실재 없이 발전에 관해 보고하는 것은 피상적인 일이 다. 그러면서도 그렇게 하는 일은 연구에 의해 소비되는 비용을 설명하 고 여전히 해양오염의 문제에 매우 큰 관심을 갖고 있는 사람들에게 정 보를 주기 위해서 필요하다. 앞으로는 평론의 형태로 해양오영의 전 영역을 나타내기는 점점 더 어 려울 것이다. 1972 년까지는 대략 100 여 편의 논문을 읽고 해양오염의 문 제를 개관할 수가 있었으나 그 이후로는 훨씬 더 많은 논문의 출현으로 불가능하게 되었다. 1975 년에 발표된 해양오염의 관찰 논문의 총수는 868 편이나 되었는데 이를 크게 부류를 나누어 보면 다음과 같다 (Gerlach, 1981 ) . 일반조사 30 지역연구, 생활폐수, 부영양화 70 폐열 20 병원체 28 세척제 11 석유, 탄화수소 246 생물지표에 의한 유해물질 조절 23 미량원소 204 염화탄화수소 및 합성유기화합물 94 공장폐수, 두기 및 소각 53 유해물질분산 및 독성에 대한 모델 55 기타 34
따라서 연구상의 특수화는 해마다 증가하는 것이 분명하다. 죽, 바전 문가에게 관심을 일으키고 그가 평가할 수 있는 기초적인 문제로부터 전 문가만이 평가할 수 있는 지구물리학적, 생화학적, 독물학적, 지화학적, 생물학적 문제로 발전하고 있다. 해양오염 문제에 대한 연구와 바다에서 생명의 기초에 대한 연구는 공히 밀접하고 복잡하게 얽혀 있다. 해양오 영으로부터 오는 피해영향의 결정은 해양과 해양생물의 지식을 기초로 하지 않으면 안 된다. 한편, 해양오염 문제에 대한 계획된 연구는 해양 화학과 해양생물학에 커다란 활력을 불어넣었다. 30 여 년 전만 해도 해양에서 자연적으로 존재하는 용존유기물질이 알 려지지 않았다. 후에 해수중의 유해 유기물질을 분석하지 않으면 안 되 게 되었고 그렇게 하기 위한 수단과 방법이 발전하였다. 미량원소의 생 물축적을 이해하게 된 것은 더 후의 일이다. 오늘날 우리는 해수로부터 흡수되어 해로운 영향없이 축적되는 유해물질의 전 종류를 찰 알고 있 다. 이들 물질은 부분적으로 비타민합성과 효소유지에 필요하다. 따라서 새로운 연구영역, 죽 미량원소의 섭취, 저장, 제거에 관련된 기작을 연 구하는 분야가 발전하였다. 오늘날 〈해양대기화학〉 분야가 존재하는 것은 20 여 년 전 대기가 유해 물질에 대한 운반매체임이 발견된 것에 기인한다. 〈지구화학〉은 유해물 질의 운명을 추적하고 있어서 이룰 통해 해양에서의 퇴적조건에 대한 우 리의 기초지식이 확대되고 있다. 해수의 방사능 측정은 해수운동에 대한 연구에 새로운 길을 열었다. 환경에 관련성이 있는 CO 같은 독성가스도 해양식물에 의해 생산되고 있다. 해양오염 문제에 대하여 연구하는 동안 에 기대하지 않았던 결과가 발생하는 일이 자주 있다. 이러한 경우는 실 험을 계획할 당시 기대하였던 것보다 종종 더 홍미로운 결과를 보게 된 다. 해양생물에 대한, 그리고 해산생물을 먹고 바다에서 수영도 하는 인간 에게 미치는 건강문제에 대한 여러 가지 뚜렷한 위험이 확인되어왔음은 분명한 일이다. 이들 문제는 현존하는 기술과 감당할 수 있는 비용으로 해결될 수 있었다. 그러나 과학은 한걸음 더 나아가서 소규모의 오염 영
향을 확인하고 평가하지 않으면 안 된다. 자연적인 배경으로부터 인위적 인 영향을 분리하는 것은 어려운 일일 뿐만 아니라 매우 자주 겪는 일이 기 때문에 바다에서 여러 요인의 자연적 변이성에 대한, 그리고 대기 - 해양 경계면 및 해수 - 퇴적물 경계에서의 물리 • 화학적 상호작용에 대한 훨씬 더 발전된 지식은 과학의 전보에 있어서 필수적이다. 또한, 해양환 경에 대한 염화탄화수소의 계속적인 위협을 보다 잘 평가하기 위해서는 대기오염의 경향과 대기중에서의 오염물질의 운명에 대한 더 많은 지식 울 필요로 한다. 1-2 해양환경과 오염물질의 투기 해양은 방대하며, 이론상 모든 폐기물의 두기를 추적할 수 없을 만큼 희석시킬 능력을 갖고 있다. 그러나 이들 폐기물의 부하량은 전체 해양 으로 일정한 모양으로 분산하지 않는다. 오히려 거의 변함없이 취약성을 지닌 해안을 따라 농축된다. 현저한 손상은 해양의 희석능력이 이들 오 염물질에 작용하기 전에 나타날 수 있다. 전세계 어업의 대부분은 연안 해역에서 이루어지고 있으며 하구 수역은 많은 해양생물의 번식장소가 된다. 현재 세계 인구 중 20 억 이상이 소비하는 동물단백질의 50% 혹은 그 이상을 해양이 공급한다. 해양 투기장에서 발견되는 농축된 폐기물은 이러한 필수자원에게 심각한 영향을 미친다. 해양오염이 도처에서 나타 나고 있고, 틀림없이 세계의 해양에서 증가하고 있다고 할 때 우리는 모 든 해양으로 폐기물 두기를 중지하지 않으면 안 되는가? 이 질문은 다 음과 같은 설명을 통해서 부정적일 수밖에 없다. 바다는 거의 손상을 입지 않고서도 폐기물질을 동화하고 정화시킬 수 있는 커다란 능력을 갖고 있다. 생물분해성 유기화합물은 해양생물에 의 해 상당히 빨리 분해된다. 실제로 이들 유기물질과 통상 이들 물질과 함 께 나타나는 영양소는 해양생물의 먹이로 작용하고 따라서 생산성을 증 가시키기 때문에 유익한 경우가 많다. 금속은 흔히 해저로 침전하는데
대부분이 퇴적물에 동화되므로 많은 경우에 간섭을 받지 않는 한 미래의 생태적 영향으로부터 효과적으로 배제된다. 실제로 해양에서의 거대하고 적절한 폐기물의 두기는 엄청난 희석과 분산으로 나타난다. 따라서 폐기 물을 받아들이고 정화시키는 바다의 능력은 간과되어서는 안 될 방대한 자연의 자원으로 생각할 수 있다. 그러나 결코 찰못 이용되어서는 안 될 것이다. 다시 말하면 해양은 적절히 이루어진다면 많은 폐기물의 투기에 대해서 편리하고 유용하며 생태적으로 안전한 장소를 마련한다. 우리가 당면한 일은 해양의 자정능력 (自淨能力)의 범위를 잠 이해하고 그 한계성 을 지키는 것이다. 특정 장소에서 바다의 자정능력을 시험하고 이 능력에 과도하게 부담 이 가지 않도록 확실하게 하는 것이 바다에서 활동하는 환경과학자의 책 임이다. 이를 위해서는 철저한 해양학적 지식은 물론 당면하게 될 오염 물질의 형태, 해양환경에 대한 이들 물질의 영향, 그리고 이들 물질을 억제할 수 있는 방법 등에 대한 울바론 지식이 요구된다. 가장 중요한 것은 해수중에서 오영물질의 동태에 대한 지식이다. 해수의 운동은 극단 으로 복잡하고 한 장소에서 다론 장소에 이르는 동안 크게 변화한다. 이 처럼 유동하는 수역 내에서 오염물질은 끊임없이 물리적, 화학적, 생물 학적 변화를 받게 되고 이 모든 변화는 오염물질의 궁극적 동태에 영향 울 미치게 된다. 이러한 복잡한 영향을 적절하게 검정하는 유일한 방법은 수리모델을 만드는 것이므로 해양환경과학자는 모델링에 익숙해야 한다. 1-3 해양오염의 정의 UN 의 산하기 관인 정부간해 양위 원회 Inte r go vernmenta l Oceanog rap h ic Comm i ss i on 는 국제적으로 가장 권위 있는 해양 관계 기관이며 해양오염 울 다음과 같이 정확하게 정의하고 있다. 〈해양오염이란 인간에 의해 직 접, 간접으로 물질이나 에너지가 하구를 포함한 해양환경으로 유입되고 그 결과로서 생물자원에 대한 피해, 인류건강에 대한 위험, 어업을 포함
한 해양활동의 저해, 그리고 해수 이용에 대한 질적 손상과 위락성의 감 소 등을 일으키는 것 〉 을 말한다. 1-4 측정 단위 농도의 표시는 분명히 분석 중에 있는 한 물질의 총량에 대하여 유해 물질의 양을 관련시키는 것이다. 35%0 의 염분을 갖고 있는 해수 1l 는 대략 1. 028k g의 무게를 가지므로 농도를 l 나 k g으로 인용하더라도 대략 계산에서는 별반 차이가 없다. 한편 습중량, 건중량, 혹은 추출성 지질 (脂 質 )이나 탄소가 측정의 기본이 되면 그 차이가 크다. 어류, 패류 및 갑각류 등은 75~80% 의 물을 포함한다. 습중량에 의한 농도수치는 건습 량 농도를 유도하기 위해서 4 나 5 로 곱해 주어야 한다. 한 생물의 지질 함량이 10% 라면 습중량으로의 농도 수치는 10 을 곱해야 한다. 그러나 생물과 조칙의 물 및 지질함량이 크게 다르기 때문에 대략 측정의 적용 에는 매우 주의하지 않으면 안 된다. 흔히 사용하는 ppm , ppb , ppt 등의 단위도 혼동되는 경우가 있으므로 정리해 둘 필요가 있다. pp m (l O 기 : µg/g 혹은 mg /k g, 약 mg / l pp b(lO 기 : ng /g 혹은 µg/k g, 약 µg/ l 혹은 mg /m 3 ppt(1 0-12) : pg/g, ng/ k g 혹은 µg/t, 약 ng/ l 혹은 µg/m 3 식물 영양소가 관련되면 생물해양학자와 화학해양학자는 흔히 µg- at/ l 혹은 더 새로운 단위인 µmol/l 로 표시한다. 이 단위는 µg /l 을 원 자량이나 분자량으로 나눈 것이다.
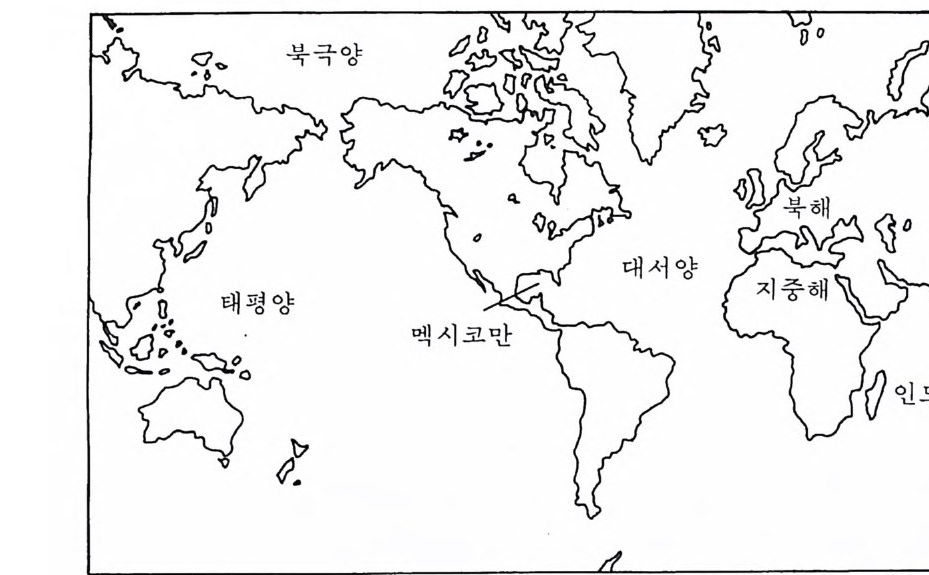
제 2 장 해양학의 기초개념 2— 1 서언 지구의 광대한 부분은 물로 덮여 있다. 세계의 여러 해양은 지구 표면 의 약 71% 를 차지하며 해양의 평균 수심은 약 3,700m 에 달한다. 이에 반해 해수면(海水面) 위로 솟아나온 육지의 평균 높이는 불과 830m 이어 서 해양은 육지의 높이에 비해 훨씬 더 깊다. 해양저(海洋底)의 구조는 수많은 해양 산맥과 해구(海溝)로 이루어져 있어서 육상의 지형보다 훨 씬 더 불규칙하다. 해양의 광대성, 그 거친 환경, 장소에 따른 변화성 때문에 해양은 아직도 미지의 세계로 남아 있는 지구상의 가장 큰 생태 계이다. 2-2 해양의 일반적 특징 해양 분지(盆地)와 대륙은 지구 표면상에 불균등하게 분포한다(그림 2-1). 지구상의 모든 주요 해양들은 서로 연결되어 있어서 하나의 커다 란 해양으로 볼 수도 있지만 · 보통은 5 개의 대양, 죽 태평양, 대서양, 인 도양, 북국양 및 남국양으로 나눈다.
 국터 구., o。lc 0 0
국터 구., o。lc 0 0
그림 2-1 세계의 주요 대양과 바다
태평양은 대양 중 가장 크고 깊으며 지구 표면의 33% 를 차지한다. 대 서양은 비교적 좁은 해양이며 지중해, 발틱해, 카리브해, 멕시코만 등을 포괄한다. 지구 표면의 대부분의 육상 부분은 북반구에 있는 (67%) 반면 에 남반구는 대부분 물로 (80%) 덮여 있다. 표 2-1 은 세계 해양의 면적, 체적 및 평균 수심에 관한 자료이다. 또한 표 2 강에서 보듯이 지구상의 표 2-1 세계 대양의 면적, 체적 및 수심 대양 면적 (l06 km2) 체적 (106cm2 ) 평균수심 (km) 태평양 181 714 3. 94 대서양 94 337 3. 58 인도양 74 285 3. 84 북극해 12 14 1.1 2 계, 평균수십 362 1,350 3.73 자료 : Menard and Sm ith, 1966
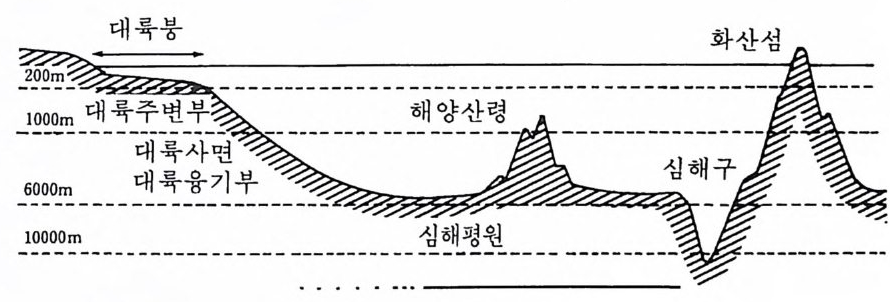
표 2-2 지구 수권의 질량과 분포 질량 (1015 ton ) 점유율(%) 해수 1, 410 86.5 호수, 강 0. 5 0.03 대륙붕 얼음 22 1. 3 대기중의 수증기 0. 013 0.001 퇴적물 및 퇴적암중의 물 200 12.2 계 1,632 100 자료 : Poldervaart, 1955 거의 모든 물은 퇴적암의 공국수(孔隊水)를 제의하고는 해양에 몰려 있 어 약 97% 를 차지하며 이에 비해 모든 호수와 강의 물은 전체 물의 0. 03% 에 불과하기 때문에 결국 지구상의 물 순환은 해양이 주요 역할을 담당한다. 2-3 해양의 지형 해양으로 이루어지는 분지의 지형은 크게 3 개의 주요 단위로 나눈다. 죽 대륙주변부(대륙붕과 대륙사면), 심해분지 및 대양산령(大洋山嶺)이 그 것이다. 깊이에 대한 이들의 관계는 그림 2-2 와 같다.
 대륙붕
대륙붕
그림 2-2 해저 포형과 유형
대륙 주변부는 물로 덮여 있으나 대륙괴(大陸魂)에 밀접히 연관된 특 칭을 갖는데 이에 포함되는 대륙붕과 대륙사면은 해수에 덮여 있기는 하 나 구조상 대륙의 일부이며 대륙사면의 기부가 대략 대륙의 끝단이 된다. 대륙붕은 대륙의 가장자리를 형성하고 대륙사면은 대양분지 쪽으로 더 나간다. 대륙봉은 비교적 평평하고 일반적으로 수심이 130m 이내이나 깊이의 폭은 35m 이내로부터 240m 에 이른다. 대륙붕의 의해측 끝을 정 의하는 기준은 사면에서의 경사도가 현저히 변화하는 것으로서 결정된 다. 즉 대륙붕은 약 1 : I, 000 의 구배를 갖는데 바해 대륙사면은 I : 2 내 지 1 : 40 의 구배를 갖는다. 대륙봉의 폭은 수 km 에서 수백 km 에 이르 며 특히 빙하작용을 받은 곳이 더 넓다. 넓은 곳의 예는 미국 북동부 연 안의 Grand Banks 이며 좁은 곳으로는 남 캘리포니아 연안이나 우리나 라의 동해역을 둘 수 있다. 대륙붕의 의해측은 대륙사면이다. 이곳은 수심이 I, 600~3, 600m 에 이르며 이 사면에는 수심이 1, 200m 에 달하는 많은 해저협곡(海底峽谷) 이 있다. 이 협곡은 사면을 흘러내려온 많은 퇴적물을 포함하는 저탁류 turb id ity current 에 의해 깎인 것으로 믿어지며, 이는 많은 협곡이 주로 강 하구 부근에 형성되어 있는 사실로서 확인된다. 대륙봉으로부터 흘러 내리는 퇴적물은 이들 협곡을 통해 심해로 운반되는 동안 대륙사면의 하 단에서 가라앉아 해양저 쪽으로 완만한 경사를 이루게 되는데 이 곳을 대륙융기부(大陸隆起部)라고 하며 그 구배는 1 : 50 내지 1 : 800 정도가 된다. 대륙융기부는 대서양과 인도양에서는 잘 발달되어 있으나 태평양 에서는 좁거나 존재하지 않는다. 대양분지저(大洋盆地底)는 대륙 주변부에서 의해 쪽으로 뻗어나가며 심 해 평 원 aby ss al pla in , 대 양저 산맥 oceanic ris e , 해 저 산 seamount, 해구 tren ch 등을 포함한다. 심해평원은 대륙융기부 끝에 위치하며 구배가 I : I,00 0 이하인 평평한 평원으로서 대륙융기부로부터 흘러오는 되적물의 퇴적에 의해 형성된다. 대양저 산맥은 심해저 위로 융기된 다소 독립된 지역을 뜻한다. 이곳은 낮은 언덕에서부터 I,525m 나 되는 산까지 포함되는데 가장 좋은 예는 버뮤다 Ris e 이다. 해저산은 해저 위로 수천 m 솟은 독
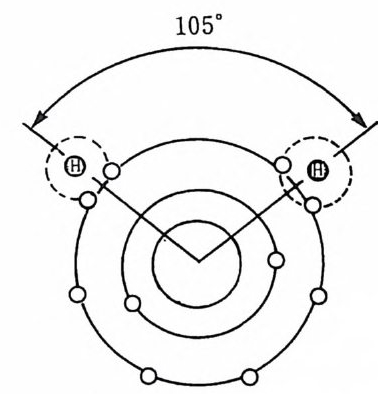
립 된 봉우리 인데 그 근원은 화산이고 주로 단충대 (斷 層 帶 fau lt zone) 부 근에서 발견된다. 해구는 깊이가 6,lOOm 를 넘는 해양저상의 깊고 좁은 함몰지 역 이 다. 가장 깊은 곳으로 알려 진 곳은 Maria n a Trench 로서 깊 이가 11, OOOm 에 달한다. 해구는 활화산과 관련이 있고 대륙지각 밀에 해양지각이 굽혀 들어감으로써 야기되는 것으로 알려져 있다. 2-4 해양의 물리학적 특징 2-4-1 물의 구조 순수한 물은 해수의 기본적인 물질이다. 순수한 물의 물리적 성질은 해양에서 물리적 • 화학적 과정을 지배하는 에너지의 상호작용에 크게 관 여한다. 그러므로 순수한 물의 화학적 특칭을 철저히 이해하는- 것이 해 수 화학을 아는 첩경이 된다. 하나의 물 분자는 2 개의 수소 원자에 결합된 산소 1 분자로 구성된다. 각 수소 원자는 산소 원자에 대하여 하나의 전자를 제공하고 그럼으로써 화학적인 균형을 유지한다. 산소원자가 갖는 전자구름의 배열 때문에 물 분자 속의 두 수소 원자는 분자의 한 쪽에 105° 의 각도로 자리잡는다(그 림 2-3).
 105°
105°
그립 2-3 물 분자의 구조
 ----
----
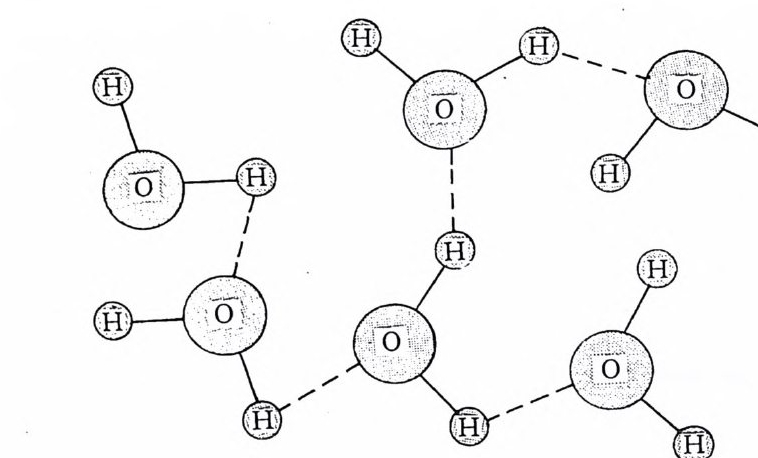
그림 2-4 물 분자 사이의 수소 결합
이 배치 때문에 분자는 한쪽 끝에 수소 원자들에 의한 2 개의 양전하 (陽 電 荷)를 띠고 다른 한쪽에는 산소 원자에 의한 음전하( 陰電 荷)를 띠는 이극성(二極性)이 된다. 결국 가까이 있는 물분자들은 반대 전하 간의 인력으로 결합하려는 성질을 갖는다. 한 분자의 양으로 하전된 수소 원 자와 음으로 하전된 산소 원자 사이의 결합을 수소결합 hy dro g enbond i n g 이라고 한다(그림 2-4 ). 만일 이 수소 결합이 없다면 물 분자는 모여 있 지 않게 되고 물은 지구 표면에서 정상적으로 발견되는 온도와 압력하에 서는 액체보다 기체로 되어 있을 것이다. 물에 염 salt 이 첨가되면 보통의 물의 성질은 변화한다. 해수중에 있는 Na+ 과 c1- 이온은 다른 이온과 함께 염에 대한 이온 전하( 電 荷)와 물 분자의 극성 때문에 물과 회합한다. 이온과 물 분자 사이의 이온결합은 영수가 끓거나 결빙할 때 파괴되어야만 하고 이 파괴에 소요되는 추가적 인 에너지가 담수에 비해 해수의 비등점을 증가시키고 빙점을 낮추는 원 인이 된다. 증기압 역시 영분의 증가에 따라 감소되어 증발이 더 적어지 며 염의 첨가로 물의 밀도 또한 증가된다. 물이 얼어서 얼음이 될 때는 수소결합 때문에 6 면체인 3 차원의 결정구 조가 된다. 물 분자의 이러한 구조는 비교적 견고하고 액체상의 물보다
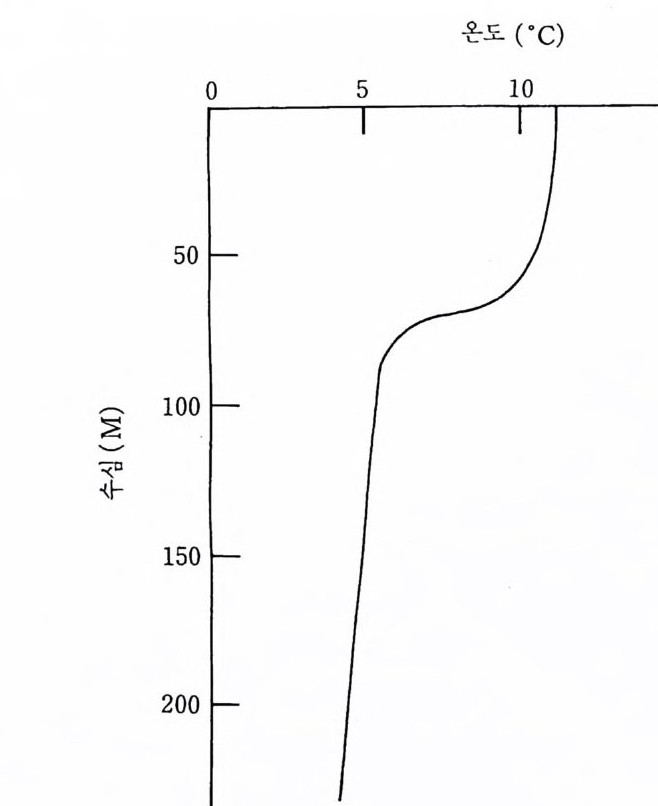
개방적이어서 밀도가 감소되며 따라서 얼음은 물에 뜨게 된다. 해수가 결빙할 때는 염이 물 분자간의 공간에 맞지 않기 때문에 배출된다. 그러 므로 바다의 얼음은 일반적으로 해수보다 적은 염을 포함하고 그 결과 얼지 않은 해수를 더 짜게 만든다. 2-4-2 물의 열성질 물은 주어전 온도 변화에 대해서 거의 어떤 물질보다도 더 많은 열량 을 흡수한다. 첨가된 열에너지의 양과 그 결과로 생기는 온도의 변화 사 이의 관계를 물질의 비열이라고 하는데 일정한 양의 물의 온도를 1°C 울 리기 위해서는 같은 양의 토양의 온도를 울리는 것보다 훨씬 많은 열이 요구된다. 이러한 이유로 태양으로부터 받은 열은 하루 동안이나 주야로 토양의 온도를 크게 변동시 킬 수 있는 반면 부근에 있는 물의 온도는 비 교적 일정하게 남아 있다. 이러한 현상은 연안의 대기 형태에 커다란 영 향을 미친다. 물속에 저장된 에너지는 숨은열 late n t hea t로 알려져 있다. 적절한 조 건하에서 이 열은 대기로 혹은 보다 찬 물로 방출되기 때문에 지구의 기 상계에서 중요한 역할을 한다. 바닷물 속에 저장된 열은 증발하는 동안 에 방출된다. 그 결과로 생기는 수증기는 잉여의 열을 갖고 있어서 이 증기가 바나 눈으로 농축될 때 대기로 방출된다. 이러한 현상이 겨울철 에 습기 많은 연안 지역에서 대기의 온도를 상승시키게 된다. 해수의 온 도는 광선이 대기로 들어오는 각도와 표면에 도달하는 에너지양에 의존 한다. 광선을 직접 받는 양이 많을수록 더 많은 에너지를 흡수하고 따라 서 수온이 더 높아질 것이다. 대부분의 광에너지는 해수 표면으로부터 100m 아내의 수심에서 흡수 된다. 해저와 표충 사이의 한정된 해수의 순환 때문에 광에너지를 받지 못하는 찬 해수와 그 위를 덮고 있는 따뜻한 해수 사이에 수온의 심한 구배가 생긴다(그립 2-5). 짐작할 수 있는 바와 같이 수온은 수심에 따라 감소한다. 그러나 해수 의 혼합과 대류 작용으로 바다의 상층부에서 약간 변화하게 된다. 어떤
 온도 c·c)
온도 c·c)
그림 2-5 수온 약충을 보여주는 수온의 수직 분포
깊이에서는 해수가 짧은 수직 깊이에 걸쳐 훨씬 더 차게 되는데 이처럼 깊이에 따라 수온이 갑자기 변화하는 것을 수온약충th ermocl i ne 이라 한 다. 수온약충의 아래에서는 혼합이나 대류가 거의 일어나지 않기 때문에 수온이 비교적 일정하다. 열대해역에서는 수온약충이 통상, 표면에 가깝 고 매우 날카로운 반면 온대해역에서는 수온약충의 깊이가 계절에 따라 변동한다. 바다의 수온은 一 2°C 로부터 3o·c 의 범위에 있으나 평균변화는 3. s·c 이다. 2 -4구 밀도 해수의 밀도는 세 요인, 죽 온도, 염분 및 압력에 의해 지배된다. 밀
 영분 (% o)
영분 (% o)
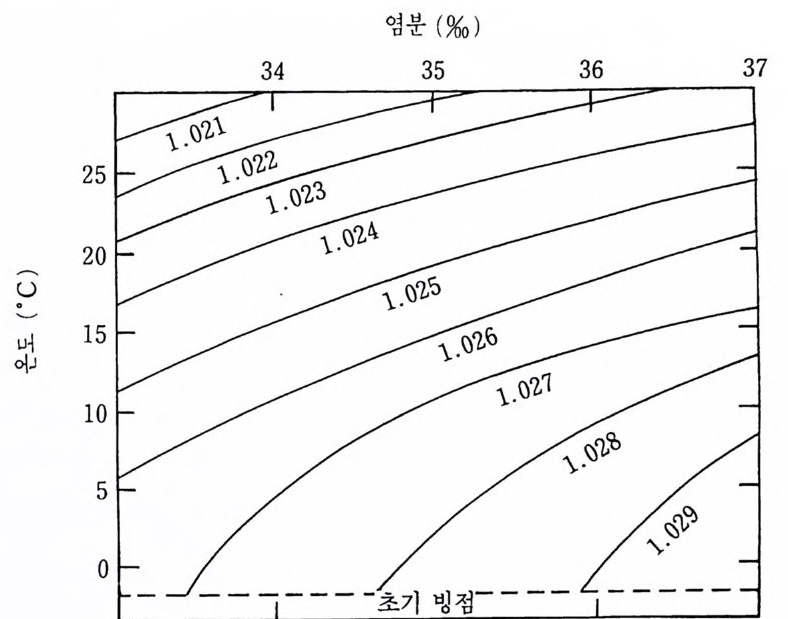
그림 2-6 수온 및 염분상의 변화로 야기되는 해수 밀도의 변화
도는 염분이나 압력의 증가에 따라 증가하지만 온도가 증가되면 감소한 다. 밀도의 변화는 해수의 순환에 있어서 아주 중요한 요인이고 미세한 변화라도 일부 생물의 분포에 상당한 영향을 미칠 수가 있다. 한편 대양 에서 발견되는 밀도의 범위는 매우 적기 때문에 그 측정에는 정밀성이 요구된다. 해수의 밀도는 일반적으로 1.0 24~1 .0 30g /c rn3 범위에 있다. 그림 2-6 은 염분아 35~37%0, 온도가 _3~3o•c 사이에 있는 해수의 밀 도 변화를 나타낸 것이다. 보다 깊고 보다 찬 해수는 밀도가 더 크고 해저에 머무는 경향이 있 다. 중력과 부력 때문에 밀도가 큰 물은 가라앉울 것이고 보다 가벼운 물은 표면으로 상승할 것이다. 이러한 성질이 해양에서 안정된 밀도성충 (密度成層 density s t ra tifi ca ti on) 을 형성하며 표충수와 심층수를 효과적으 로 분리해주는 것은 이 밀도의 차이 때문이다. 해수밀도의 변화는 해수면에서 증발에 의해 염분이 증가하는 과정, 혹
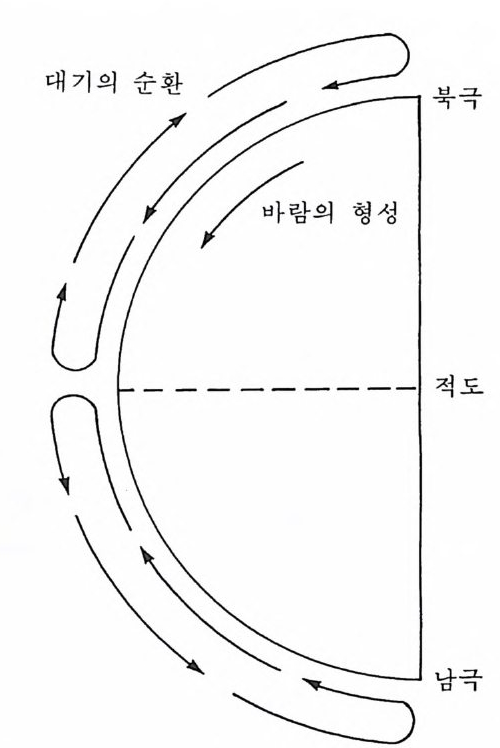
은 강, 하천 등의 담수 유입에 따른 해수의 희석으로 염분이 감소되는 과정 같은 현상에서 유래한다. 2- 4-4 빛 해수가 빛을 전달하는 능력은 매우 중요한 현상이다. 왜냐하면 빛이 없이는 광합성이 이루어질 수 없고 따라서 바다에서 생물이 존재할 수 없을 것이기 때문이다. 광선은 해수에 의해 급속히 흡수된다. 광도는 맑 은 해양 수역의 경우 약 lOOm 수심에서 표충값의 10% 정도로 감소하는 반면 더 혼탁한 연안 수역에서는 10~30m 수심에서 1% 정도까지 감소 하고 아주 탁한 해안에서는 3m 이하로 떨어진다. 따라서 광투과는 바다 에서 생존하는 생물의 형태와 분포에 대해서, 또한 수온에 대해서 매우 커다란 영향을 미친다. 2-4-5 해양의 순환 해양에서 해수의 순환은 중대하고도 복잡한 현상이다. 이것은 일차적 으로 바람과 대양의 가열로서 조절된다. 바람이 해수를 가로질러 이동할 때 커다란 수괴(水境)가 밀리게 된다. 열대해양의 저장열은 대류나 물의 이동에 의해서 보다 찬 수역으로 전달된다. 표충해류 저층 대기의 순환과 해양의 표면은 밀접하게 연결되어 있다. 적도상의 따뜻한 공기는 지구의 열 균형을 유지하기 위해 고위도 지방으로 이동하 려는 경향이 있다(그립 2-7). 적도상에서는 공기가 가열되고 따라서 팽창 하면 상승하게 된다. 팽창하는 공기는 저기압 지역을 형성하며 주변지역 의 보다 차고 무거운 공기는 적도상의 저기압 지역으로 움직인다. 양극 지방에서는 공기가 냉각, 응축되어 낮게 가라앉아 고기압 지역을 형성한 다. 극지방 공기는 저기압 지역인 적도를 향해 이동함으로써 일정한 바 람울 일으킨다 (Ross, 1977). 그러나 지구의 회전 때문에 실제적인 대기 순환은 꼭 이와 같이 일어나지는 않는다. 지구가 회전할 때 공기의 이동
 북국
북국
그림 2-7 지구가 회전하지 않을 때의 대기순환
 북
북
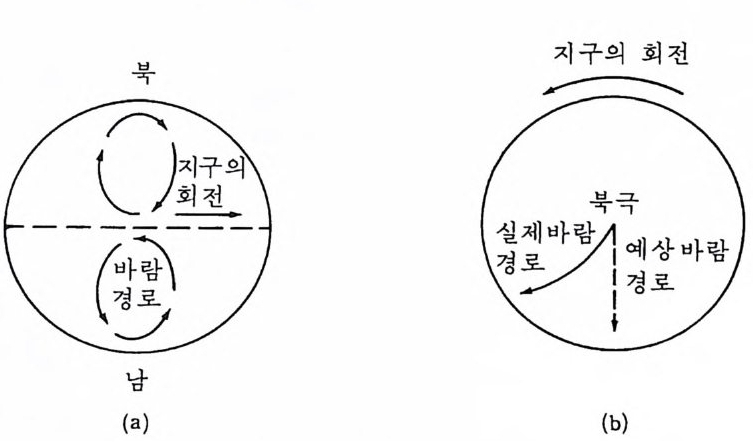
그림 2-8 코리올리 효과에 의한 이동성 물체의 편향
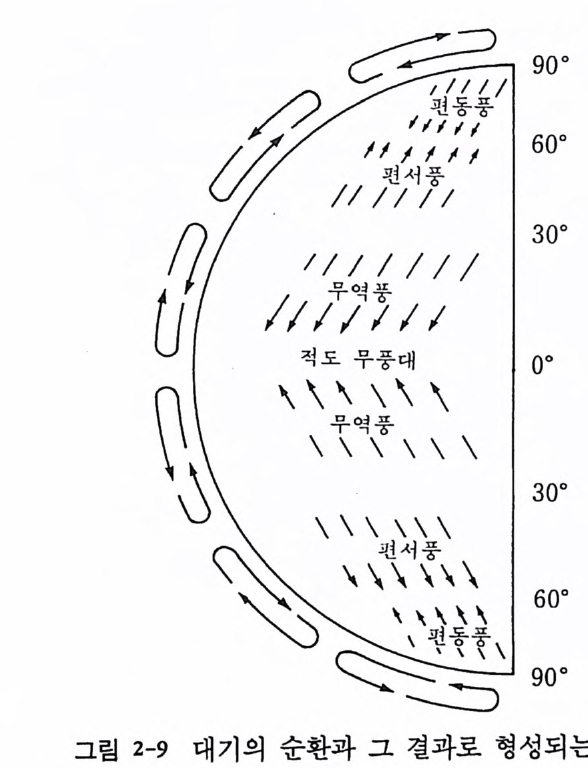
은 북반구에서는 우측으로, 남반구에서는 좌측으로 편향(f烏向)을 일으킬 것이다. 따라서 공기의 이동은 직선보다는 굴곡된 경로를 따르게 된다 (그립 2-8). 이러한 바람의 편향은 코리올리 효과 Cor i ol i s e ff ec t로 알려 져 있다. 북반구에서는 그림 2-7 에서 보는 것과는 달리 실제로는 공기 이동에 있어 세 요소가 있다. 적도상에서 발생된 따뜻한 공기는 북쪽으로 흐르 기 시작하지만 계속 진행하지 않고 북위 약 30° 에서 냉각되고 결과적으 로 침강한다. 이 공기의 일부는 다시 적도측을 향해 가는 한편 일부는 계속 북쪽으로 이동한다. 극지를 향해 이동하는 공기는 따뜻해짐에 따라 다시 상승하여 또 다른 요소를 형성한다. 극 지역에서는 지상으로 침강 하고 이것이 충분히 더워져서 북위 약 60° 에서 다시 상승할 때까지 남쪽 으로 진행한다. 이 결과로 나타나는 바람과 그 순환의 양상은 그림 2-9
 ////二iI乙I 6900°°
////二iI乙I 6900°°
 () 0
() 0
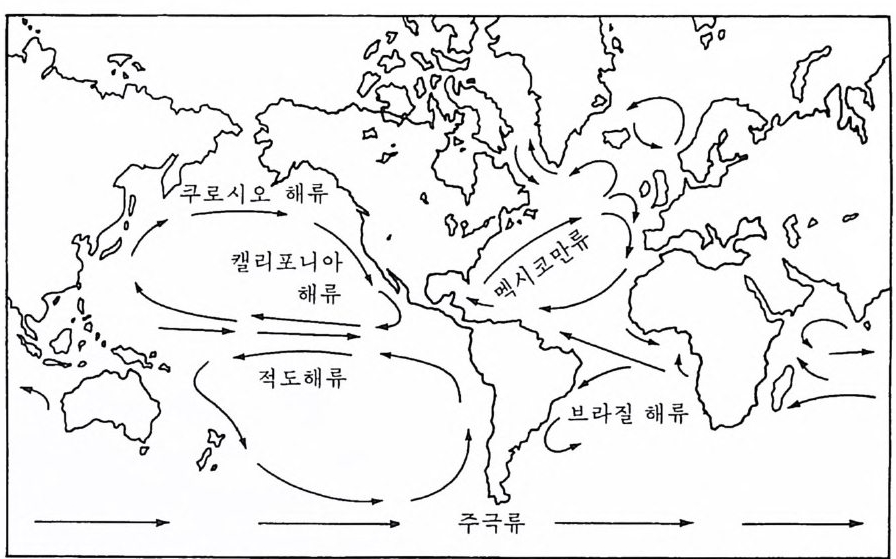
그림 2-10 해 양의 주요 표충류
에 서 보는 바와 같다. 이러한 풍계 (風 系)는 해양의 표충수를 몰아가는 경향을 갖 기 때문에 해양순환은 대체로 바람과 같은 양상을 따른다. 따 라서 해류는 북반구에서는 우측으로 편향하며 시계방향을 갖는다. 그립 2~ 10 은 중요한 해류의 일부를 도식화한 것이다. 표충해류는 저층 대기의 순환과 밀접히 관련된다. 물위로 이동하는 바 람은 마찰력으로 인해서 바람의 방향으로 물을 이동시킨다. 그러나 실제 로는 해류가 바람과 평행하지 않고 오히려 코리올리 효과로 편향하기 때 문에 탁월풍p reva il i n g wi nd 은 바람이 대양분지 부근에서 순환할 때 해 양의 중심을 향해 해수를 이동시키는 경향이 있다. 그 결과는 바람이 순 환하는 주변에서보다 중심에서 해수면 상승이 더 커지게 되며, 일반적으 로 이러한 현상은 대양의 서쪽 경계에서 나타난다. 바람, 코리올리 효 과, 중력성분의 조합으로 표충해류의 방향이 결정된다. 심해순환 심층수에서의 해류는 일차적으로 밀도 차이에 의해 생기며 이것은 다
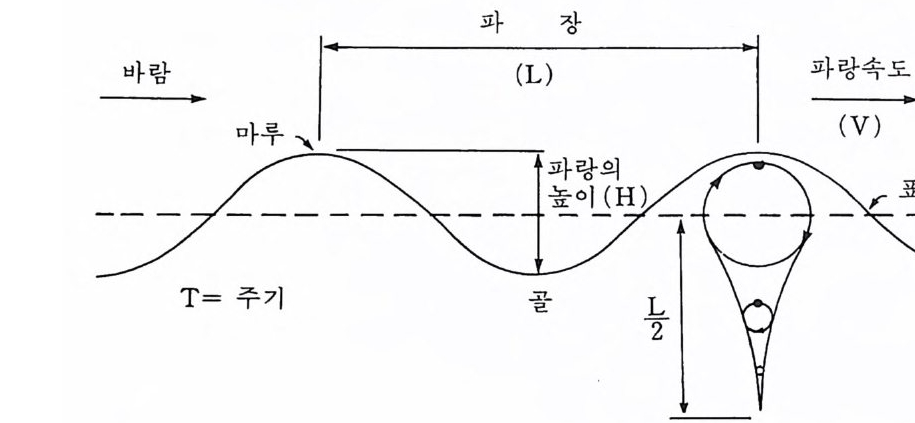
시 수온과 염분의 변화에 따라 지배된다. 이러한 순환형태를 열영분순환 the rmohalin e circ ulati on 이라 한다. 이것은 단순한 대류작용으로서 고위 도 지방에서 생긴 무겁고 찬 해수가 가라앉으면서 서서히 대양저를 따라 적도를 향해 흐른다. 이 심해 해류는 아주 천천히 움직여 표층으로 되돌 아오기까지 보통 500~2, 000 년이나 걸린다. 2-4-6 파랑 파랑은 일반적으로 해양의 표면을 가로질러 부는 바람의 작용으로 생 성된다. 죽 에너지가 바람으로부터 물로 전달되는 결과로서 생기게 된 다. 바람은 잔물결처럼 작은 것으로부터 파고가 30m 이상되는 파랑을 일으킬 수가 있다. 파랑은 극단으로 복잡한 현상이어서 그림 2-11 에서 보는 것 같은 이상적인 파형(波形)울 고찰하는 것이 쉽다. 파랑열(波浪 ~1], wave tr a i ns) 에는 마루 cres t와 골t rou g h 이 규칙적으로 연속된다. 연속적인 2 개의 마루 사이의 수평거리를 L, 마루로부터 골까 지의 수직 거리를 H, 2 개의 연속된 파랑의 마루가 고정된 점을 통과하 는데 소요되는 시간울 주기 T 라고 동상 표기하는데 이때 파랑의 속도 V 는
 파 장
파 장
그림 2-11 파랑의 성질과 물 입자의 운동
v = —LT 로 계산된다. 깊은 물에서 이동하는 파랑 속의 물 입자는 거의 원궤적 내에서 움직 인다. 파랑은 바람에 따라 움직이지만 개개의 물 입자는 이동하지 않는 다. 물 표면에 떠 있는 콜크는 각 파장마루를 향해 이동하고 또 골을 향 해 물러나지만 각기 완전한 파랑이 지난 뒤 콜크는 제자리에 남는다. 죽 오직 파형만 이동하고 파랑 자체는 이동하지 않는다. 표면에서의 물은 파고와 같은 직경을 갖는 원궤적으로 움직인다. 표면에서 멀어져 가면 궤적운동은 감소하고 궤적이 작아전다. 결국 파장의 절반 (L/2) 에 해당하 는 깊이에서 궤적운동은 소멸된다. 따라서 파랑을 일으키는 물 운동은 표면 가까이에서만 나타난다. 수심이 파장의 절반보다 얕은 곳에서는 해 저가 물의 운동을 방해하기 때문에 바닥 가까이 있는 물 입자는 수직적 으로 이동할 수가 없고 오직 수평적으로 이동할 수 있어서 타원형 궤적 을 만들게 된다. 파랑의 크기와 속도는 바람속도, 바람주기, 바람이 부는 거리 등에 의 존한다. 이론상 한 파랑의 높이는 그 파랑의 0.14 배를 초과할 수가 없 다. 이 것 이 초과되 면 백 파 whit e cap 와 분쇄 파 breakin g wave 가 된다. 파 랑이 해변에 접근하고 물이 얕아질 때 파랑주기는 변하지 않은 채 남아 있으나 파장은 짧아진다. 그 결과 파고가 증가하고 파랑마루는 불안정하 며 깨지게 된다. 파랑이 차단되면 파랑은 물의 난류를 통해서 그리고 해 변을 씻어내림으로써 에너지를 확대시킨다. 대형 파랑은 강한 폭풍이나 해저 사태 같은 이상 조건의 결과로 나타 난다. 이러한 파랑은 흔히 생명의 손상이나 손실을 유발시킨다. 지진해 파 seis m ic sea wave 나 해 일파 tsu nam i 는 종종 조석 파 tida l wave 로 잘못 불리는데 실제로 조석과는 아무런 관계가 없다. 지전해파는 해저 지진이 나 해저 화산폭발에 의한 운동으로 발생되며 수천 km 를 이동할 만큼 막대한 에너지를 갖고 있다. 이 파랑은 파장과 주기가 풍랑에 비해 엄청
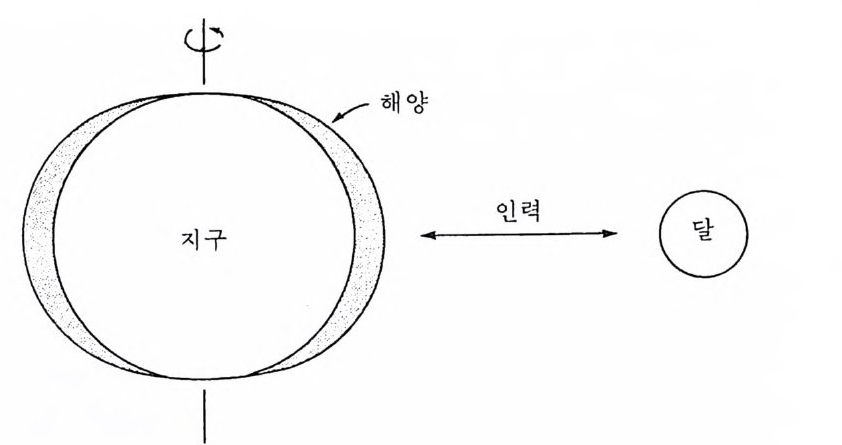
나게 길기 때문에 눈으로는 파랑을 식별하기 어렵다. 그러나 천해역에 이르게 되면 약 30m 까지 물기둥을 이루어 거대한 파괴력을 갖는다. 2-4-7 조석 해수가 주기적으로 상승하고 강하하는 조석현상은 최초로 연구된 해양 연구의 하나이다. 초기의 인류는 이미 해수면 변화를 기록하고 이룰 달 과 관련시켰는데 조석현상이 정확하게 설명될 수 있었던 것은 뉴턴이 중 력인력의 법칙을 발견한 뒤였다. 조석은 지구에 대한 태양과 달의 중력인력에 의해 야기되는데 하루-에 두 번 바다가 규칙적으로 상승하고 하강한다. 뉴턴의 법칙은 2 개의 물체가 서로 끌어당기는 힘을 설명하는데 이 힘 은 두 물체의 질량의 곱에 바례하고 두 물체 사이의 거리의 제곱에 반비 례한댜 죽 F= 중력, M1, M2= 두 물체 각각의 질량, d= 두 물체의 중 심 간 거리, g=중력상수라고 하면 F=g M1 따•M 2 로 표시된다. 결국 천체에 있는 모든 물체는 지구에 대하여 힘을 작용시 킨다. 그러나 태양과 달만이 상당한 영향을 미칠 만큼 매우 가깝고 충분 히 큰 질량을 갖고 있다. 지구와 달 사이의 인력은 지구가 달에 면하고 있는 쪽에서 가장 크다 (그립 2-12). 이 때문에 물이 달 쪽으로 끌려가 해양의 표면이 다소 찌그 러지게 만든다. 지구의 반대 편에서는 달의 인력이 최소가 되지만 지구 의 자전으로 생기는 원심력으로 물의 팽창이 일어나게 된다. 따라서 지 구의 양 반대 쪽에서 다같이 해수의 팽창이 일어난다. 지구가 완전히 1 회전 하는데 24 시간이 조금 넘기 때문에 지구상의 한 장소에서는 두 번 의 만조와 간조를 겪게 된다. 태양 또한 지구의 조석에 강한 영향을 미친다. 태양 조석의 평균 높이
 宁
宁
그림 2-12 해양에 대한 달의 인력으로 야기되는 조석
는 평균 태음 조석의 약 반 정도가 되며 이는 지구로부터 태양까지의 거 리가 훨씬 더 멀기 때문이다. 태양의 영향은 태양과 달이 지구와 일렬로 서게 될 때 더 중요해 진다. 두 천체의 중력인력은 더욱 커져서 매우 높 은 조석, 즉 대조(大潮 spr ing ti de) 를 이루게 된다. 대조는 대략 14 일 마다 초승과 만월에 나타난다. 매우 낮은 조석은 태양과 달이 지구를 중 심으로 직각으로 위치할 때, 즉 반달 때 나타난다. 이것을 소조(小潮, neap ti de) 라고 하며 약 12 시간 25 분의 주기와 지구 둘레의 반 (2 만 km) 이 되는 파장을 갖는 파랑과 같다. 해양이 불과 4km 이내의 수심을 갖고 있기 때문에 조석파는 천해파처럼 행동한다. 결국 해양저에 대한 마찰력 이 파랑 마루를 지연시켜서 마루의 위치가 달과 태양을 기초로 예측한 위치보다 다소 다르게 나타나게 된다. 다른 천해파와 갇이 조석은 조류(潮流)로 알려진 수평이동을 일으킨 다. 의해에서는 이 조류가 비교적 약하지만 해변 근처나 강, 또는 항구 에서는 해안이 이 조류를 차단하기 때문에 큰 속도를 갖는다. 해수가 연 안 쪽으로 밀려드는 것을 창조류fl oodcurren t라 하고 의해로 되돌아 흐 르는 것을 낙조류 ebb ti de 라고 한다. 흐름이 거의 없거나 정지하는 시간 에 낙조류와 창조류가 분리되는데 이 시기를 휴조(休潮, slack wa t er) 라
한다. 낙조시 및 창조시에 나타나는 큰 유속은 대량의 퇴적물을 이동시 킬 수 있기 때문에 매우 중요하다. 이것은 또한 하구 및 항구 부근에서 선박의 항해를 심하게 방해한다. 2-5 해양의 지질학적 특징 2-5-1 해양퇴적물 해양저의 많은 부분이 육지로부터 풍화된 대량의 퇴적물로 덮여 있다. 이들 물질의 대부분은 성질상 무기물이지만 일부는 유기질로 되어 있다. 퇴적물의 상당량은 바다 생물의 골격 유해나 혹은 해양에서 형성된 무기 침전물의 형태로 본래 바다에서 유래된 것이다. 이러한 데트리터스 de tritu s 물질은 수억년 동안 축적되어와서 평균 두께는 600m 정도이나 6, OOOm 까지 퇴적된 것도 있다. 이 퇴적물은 무게로 약 50% 까지는 물 울포함한다. 퇴적물은 입자 크기, 색, 구성, 혹은 조성 동의 물리적 성질을 토대로 분류된다. 일반적으로 입자의 크기가 62µm 이상인 것은 모래로, 62µm 이하인 것은 펄 mud 로 분류된다. 모래는 일반적으로 급속히 침전하여 연안을 따라 퇴적하기 때문에 대부분의 심해 퇴적물은 펄이 된다. 퇴적 물은 또한 기원과 퇴적 양식에 따라 크게 둘로 나뉜다. 즉, 해양에서 기 원하는 원양되적물p ela gi c sed i men t과 육성되적물(陸成淮 積 物, ter rig e nous sedim ent) 이 그것 이 다. 원양퇴적물 원양퇴적물은 일반적으로 의해에서 발견되는 것으로 동 • 식물 플랑크 돈의 골격물질과 미세립 검토로 이루어진다. 이들 입자는 아주 작고 해 저로 침전하는데 수년이나 걸리며 이 긴 기간 동안 퇴적물 입자와 해수 사이에 많은 화학 반응이 일어나도록 해준다. 이 원양되적물은 다시 3 계급, 죽 생물기원(生物起源) 퇴적물 b iog enous depo sit, 무기 (無機) 퇴적물
ino rga n ic dep o sits , 자생 (自生) 퇴적물 au thig en i c de pos it로 나뉜다. 유기물질이 30% 이상 포함된 퇴적물을 생물기원되적물 혹은 연니(軟 泥, ooze) 라 한다. 이들 퇴적물은 보통 엷은 색을 띠고 미립질(微粒質)이 다. 연니는 퇴적물 속에 가장 우세한 플랑크톤 생물의 이름을 따서 부르 게 된다. 예컨대 규조연니 dia t o m aceous ooze 를 들 수가 있다. 연니의 화학적 조성은 변화하지만 보통 플랑크돈의 골격이나 각에서 오는 CaCO 라 S i 02 를 포함한다. 북태평양의 경우를 제의하면 생물기원퇴적 물은 전세계에 걸쳐 원양되적물 중 가장 우세한 분포상을 나타낸다. 무기되적물은 유기물질이 30% 이하로 포함된 아주 미세한 입자이며 대부분 심해 분지에서 발견된다. 이것은 혼히 적점토(赤帖土, red cla y)로 불리지만 실제로는 산화되어온 까닭에 질은 갈색을 띠고 있다. 이 퇴적 물을 형성하는 입자들은 아주 미세하고 아주 늦은 속도로 침전한다. 오 랜 침전시간 때문에 유기물질이 생물분해를 겪어 제거된다. 자생퇴적물 은 해수 용액 중에 있는 이온으로부터 결정화된 소량의 무기물질이다. 가장 홍미 있는 자생퇴적물은 망간단괴 mang an ese nodule 이다. 이것은 망간, 철 등 10 여 종 이상의 광물이 복잡하게 혼합된 감자 크기만한 검 은 덩어리이다. 망간단괴는 대양의 넓은 지역에서 발견되고 있으며 가까 운 장래에 매우 유익하게 채광될 가능성을 갖고 있다. 육성퇴적물 육성퇴적물은 일차적으로 대륙암석물질의 파괴로부터 유래한다. 이들 물질은 강과 기타 육수(陸水)의 유입에 의해 해양에 도달하며, 따라서 이러한 퇴적물은 연안 가까운 곳에서만 우세하게 나타난다. 퇴적물의 입 자는 비교적 굵고 생물기원물질을 거의 갖고 있지 않은 점에서 원양되적 물과 다르다. 육성 펄은 색상에 있어서 변화하기 쉬운데 이 변화는 물질 의 근원이나 물질이 퇴적한 환경에 의해 야기된다. 예컨대 적색, 혹은 갈색 펄은 산화철이 존재하고 그 지역이 찰 산화된 것을 나타낸다. 흰색 펄은 CaC03 가 많고, 청색 펄은 유기질이 많으며 흑색 펄은 유기질과 황 화물이 많고 산소가 거의 없는 곳에 나타난다. 대부분의 육성퇴적물은
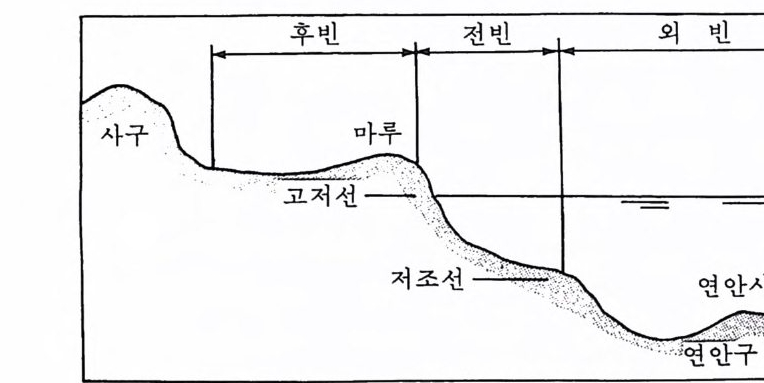
흔히 육상암석에서 유래하는 수정 및 장석 광물을 포괄하는 규산염으로 구성된다. 2-5-2 연안퇴적물 연안 지역은 광범위한 지질학적 형태를 감싸고 있다. 이 지역은 육상 과 해양에 의해 영향을 받으므로 양 조건의 중간 특성을 나타낸다. 대표 적인 형태는 해빈(海濱), 만(淸), 삼각주(三角洲)이다. 해 빈 (Beaches) 해빈은 각종 크기와 형태로 나타난다. 그 변화성은 바람, 파랑, 조류 등의 작용에 의해서 어느 해안에서나 끊임없이 계속적으로 변화가 일어 나기 때문에 더 커진다. 그러나 변화는 크더라도 모든 해빈은 공동의 특 칭을 나타낸다(그립 2-13). 해빈은 해변을 덮고 있는 모래와 왕자갈을 주로 하는 미고결퇴적물(未 固結淮積物 unconsoli da te d sedim ent) 로서 보통 파랑의 영 향을 직 접 받는 다. 밀물과 썰물의 중간 지 역 인 조간대 (潮間帶) 는 전빈 (前濱 for eshore) 이라는 것을 이루며 그 위쪽 후빈(後濱 backshore) 은 폭풍이 불 때 이의 에는 통상 해수의 영향 밖에 있다. 이 부위는 해수 쪽에 대해서 다소 융 기하여 마루를 형성한다. 해식철벽 (海鉉絶壁 sea cliff ) 이나 사구(砂丘,
 전빈 외 빈
전빈 외 빈
그림 2-13 해빈의 전형적 특징
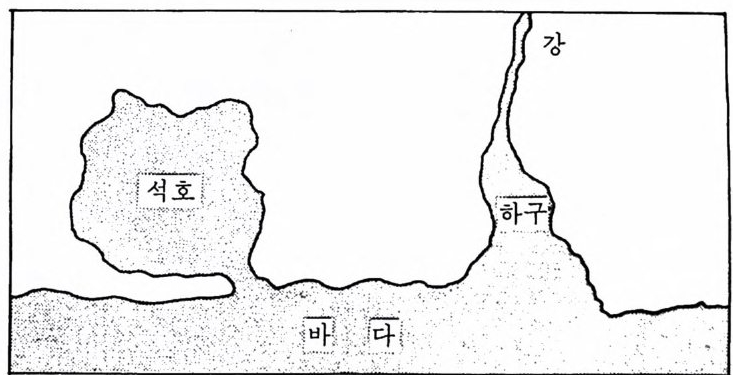
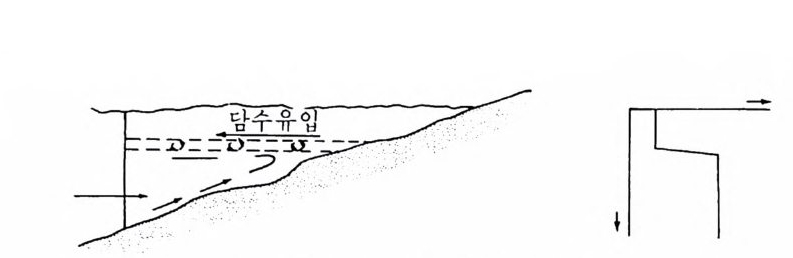
dune) 는 일반적으로 후빈의 뒤쪽에 위치한다. 의빈(外濱, o ff . shore) 은 해 저 경사가 비교적 완만하고 저부에 하나 혹은 수개의 연안사주(沿岸砂洲, long sh ore bar), 연안구(沿岸溝 long sh ore trou g h ) 등을 포함한다. 대부분 의 해빈은 암석 파편이나 근처 강으로부터 운반되어온 모래로 구성되며 이들 퇴적물을 일반적으로 분급(分용合)과 마모가 잘 되어 있다. 이 때문 에 흔히 건축용으로 채굴된다. 연 안만 (coasta l bay) 연안만은 의해 환경에 인접한 모든 폐쇄 혹은 반폐쇄 수역으로 가장 혼한 형태는 하구(河口)와 석호(潟湖 la g oon) 이다(그림 2-14). 이러한 지 역은 흔히 항구로 이용되고, 통상 생물 활동이 높은 곳이며, 많은 해양 생물의 생육장소가 된다. 하구는 육지에 의해 부분적으로 폐쇄된 연안수역으로서 강으로부터 담 수가 유입되는 곳이다. 하구에서 해수가 담수와 희석되고 혼합되므로 하 구의 염분은 담수의 유입량과 조수의 상태에 따라 변화한다. 대부분의 하구는 두 방향의 해수 운동을 갖는다. 강으로부터 오는 담수는 무겁고, 염분이 높은 해수 위로 바다를 향해 흐르며 해수는 조석에 따라 하구로 유입되고 유출된다(그립 2-15). 그러나 일부 하구에서는 바람이나 하구 형태 등의 요인으로 염수쐐기 salt w ed g e 가 파괴되어 두 흐름이 혼합된
 ·i .• ^바 , . .,. . t.,. ·,,'•.r . •,,.' . •· • ·. ·..j,E , .; . 스다 ,.. 一 , .. ;· '·'· ·,. ,
·i .• ^바 , . .,. . t.,. ·,,'•.r . •,,.' . •· • ·. ·..j,E , .; . 스다 ,.. 一 , .. ;· '·'· ·,. ,
그림 2-14 석호와 하구의 모형
 ,n
,n
그림 2-15 염수 쐐기를 갖는 하구
다. 하구는 퇴적물 축적률이 높은 경향이 있어서 때때로 대량의 퇴적물 울 운반하는 강수에서는 하구를 메우는 경우가 생긴다, 더구나 상당량의 퇴적물이 연안에서 하구로 운반되는 수도 있다. 그러므로 하구에서의 항 해를 원활하게 하기 위해서는 자주 준설을 할 필요가 생긴다. 연안 석호는 하구와 유사하지만 담수의 공급을 받지 않는다. 석호는 의해와의 한정된 순환, 또 담수 유입의 결핍 때문에 흔히 염분의 수준이 높 0} 전다. 삼각주 (del t a) 삼각주는 바다로 들어가는 강 어귀에 대량의 퇴적물 축적으로 형성된 다. 이와 같은 현상은 강이 되적물을 바다로 공급하는 속도가 파랑이나 해류가 최적물을 운반해내거나 분산시키는 속도보다 클 때에 일어난다. 이 결과로 삼각주로 알려진 3 각형의 퇴적이 생긴다. 강이 운반하는 퇴적 물의 양은 강에 따라 크게 다른데 예컨대 미시시피강은 매년 3 억 돈 이 상의 퇴적물을 멕시코만으로 운반하는 것으로 알려져 있다. 2-5-3 대륙붕 퇴적물 대륙붕 퇴적물은 그 구조와 조성이 매우 다양하다. 대륙붕은 일차적으 로 거대한 해수면 변화를 일으켰던 빙하에 의해 생겨난 것이며, 빙하가 발달함에 따라 방대한 양의 해수가 결빙하여 해수면이 낮아지고 광대한 면적이 육지로 노출되었다. 현재의 대륙붕은 대부분 이 당시에 해안 평 원이 되었고 북쪽에서는 빙하로 덮였다. 빙하가 녹기 시작하면서 해수면 이 상승하고 이 지역에 퇴적작용이 일어났으며, 이때 침전된 물질이 아
주 다양해서 퇴적물 조성에 대한 일반화된 법칙을 제시할 수가 없다. 2-6 해양의 화학적 특징 해양과 그 퇴적충은 육지로부터 유입하는 모든 물질의 궁극적인 종착 지라 할 수 있다. 또한 바다와 대기 사이에, 그리고 바다와 해저 사이에 는 끊임없는 물질교환이 이루어지고 있다. 결국 해수는 장소에 따라 변 화하는 아주 다양한 물질을 포함한다. 가스, 액체, 용존 및 비용존 형태 의 미립자들이 끊임없이 해양을 통해 순환하고 있다. 많은 유입으로 인 한 이러한 변화성에도 불구하고 실제로는 해수의 조성이 비교적 일정한 것은 놀라운 일이다. 2-6-1 해수의 화학적 조성 해수는 많은 종류의 원소와 용존 화합물을 포함한다. 바다 염의 c1- 표 2-3 해수중의 주요 원소 원소 평균농도 (m g /l) 체류기간(년) 염소 19,400 1Xl08 나트륨 10,800 2. 6Xl08 마그네슘 1,350 4. 5X l07 황 885 l.1X l07 칼슘 422 8. 0X l06 칼륨 416 1.1 x101 브롬 68 1Xl08 탄소 28 1x101 스트론튬 8 l. 9Xl07 TU ..L../ 4.5 1x101 자료 : Goldberg, 1963
표 2-4 해수중의 미량 원소 원소 평(m균g 농/l 도) 원소 평(m균g 농/l)도 규소 3 크립톤 0,0003 풀츠구오르- 1. 4 란탄 0.0003 질소 0. 5 스칸듐 0,0002 0} 르곤 0.45 이트륨 0.0002 리뮴 0.18 네온 0,0001 루비듐 0.12 T。 0.0001 인 0.07 카드뮴 0.0001 3q ? 亡 0.06 크세논 0.0001 바륨 0. 03 텅스텐 0.0001 몰리브덴 0.01 게르마늄 0.00006 알루1'.l]늄 0. 01 수은 0.00005 안티몬 0.005 토륨 0,00005 아연 0. 005 갈륨 0.00003 셀렌 0.004 지르코늄 0.00003 철 0.003 납 0.00002 구리 0.003 비스무트 0.00002 비소 0,003 니오브 。 •00001 우라늄 0.003 인듐 0.00001 니켈 0.002 주석 0.00001 망간 0.002 탈륨 0.00001 바나듐 0. 002 헬륨 7X10-6 티탄 0. 001 그'Cl 4X10-6 코발트 0.0008 베릴륨 6x10-1 크롬 0.0005 프로트악티늄 2X 10-9 세슘 0.0005 라듐 1X10-10 세륨 0.0003 라돈 6x10-16 자료 : Goldberg, 1963
형태인 염소, so42_ 형태인 유황, 이온 형태의 Mg 2+ , K+ , Ca2+ , Na+ 등이다. 분석결과에 따르면 해수에는 대부분의 자연산 원소가 존재하여 그 중 Na 와 Cl 이 전체의 85% 를 차지한다. 표 2-3 은 해수에서 발견되 는 가장 혼한 원소를 나타내는 반면 표 2-4 는 미량원소에 대한 대표적 농도를 보여준다. 미량원소 가운데 많은 종류가 여러 가지 해양 생물의 영양상 중요하며 이들의 상대적 유무는 존재할 생물의 형태를 나타내는 수가 혼하다. 염 분 (Salin i t y) 염분은 해수 염함량의 척도이며 해수 속에 녹아 있는 고형성분의 무게 총량이다. 이것은 천분율로 측정되는데 의해에서는 보통 33~38%., 범위 에 있고 평균은 35%0 이다. 이는 해수의 96.5% 가 순수한 물, 3.5% 가 용 존 무기염으로 구성됨을 의미한다. 염분변화는 일차적으로 증발과 강수 량에 의존하며 열대해역은 증발량이 크기 때문에 국지해역에서보다 더 높은 염분을 갖는다. 염분은 지역에 따라 아주 높거나 매우 낮은 경우가 있다. 육지에 인접 한 해역은 담수의 유입으로 해수가 희석되어 흔히 낮은 염분을 갖는 반 면 증발이 염울 농축시킬 만큼 순환이 한정된 해역은 매우 높은 염분을 갖는다 . 예컨대 홍해의 염분은 40%0 를 초과한다. 기수성(氣水性, brackis h ) 이 란 용어는 17%.. 이 하의 낮은 영분을 갖는 해수에 사용되 며 고영성 (高塩住 h yp ersa li ne) 이란 용어는 47%., 가 넘는 비정상적으로 영분이 높은 해수에 사용된다. 해수의 염분은 또한 해양의 위도와 깊 이에 따라 변한다. 증발로 인해 염분이 표충에서 증가하므로 해수는 밀 도가 더 높아지고 이에 따라 평형에 이르는 수심까지 침강하는 경향을 갖는다. 그러나 150~180m 수심에서는 일반적으로 염분이 아주 일정하 다. 해수의 염을 구성하는 용존물질의 조합이 매우 복잡하기 때문에 염분 울 직접 측정하기는 어렵다. 그대신 염분은 보통 해수의 염소 농도를 측 정하여 다음의 관계식으로부터 추산한다.
S= 1. 80655Cl S 는 염분 Cl 은 %로 표시된 염소 농도. 용존가스 (dis s olved gas ) 해수에서 발견되는 주요 가스는 질소, 산소, 이산화탄소이다(표 2-5). 소량으로 발견되는 다른 가스는 황화수소, 네온, 알곤, 크립톤, 세논 같 온 불활성 기체를 포함한다. 해수중에서 발견되는 거의 모든 기체는 대 기로부터 들어간다. 해수중에 있는 용존가스 총량의 약 64% 가 질소이다. 바다에 소량 서 식하는 남조류 blue- gr een alga e 이의에는 해양생물이 용존질소를 이용할 수 없기 때문에 바다의 생물학적 활동에는 거의 영향을 미치지 않는다. 해양생물의 질소요구는 질소화합물의 형태로서만 충족된다. 산소는 바다구대기 경계면에서 대기로부터 용해되거나 해양식물의 광합 성 부산물로서 해수중에 나타난다. 해수중의 산소 농도는 그러므로 크게 변화성을 갖는다. 해양의 표충에서는 그곳에서 혼합이 잘 되고 광합성 활동이 높기 때문에 일반적으로 산소가 풍부하다. 그러나 수심 약 lOOm 표 2-5 대 양 중의 가스 함량 가스 농도 (ml/l) 질소 8.4-14.5 산소 0-8.5 01 산화탄소 34-56* o t르곤 0.2-0.4 헬륨 미량 크립돈 미량 네온 미량 크세논 미량 * CO2 , H2C03, HC03-, Co/- 등 포함.
 。
。
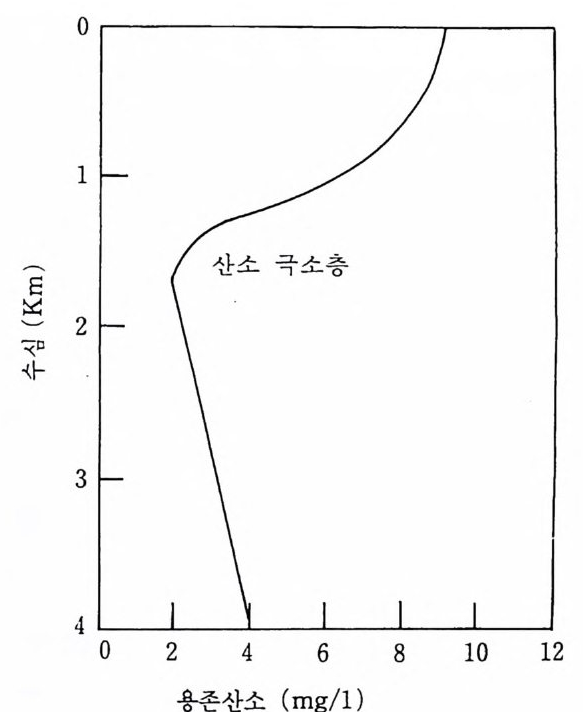
그림 2- 1 6 수심 에 따른 용존산소량의 수직 분포
이하로 내려가면 광합성이 절감되고 호흡이 유용한 산소를 소비하여 용 존산소의 농도가 감소한다. 경우에 따라서는 모든 용존산소가 고갈될 수 도 있으며, 극지방으로부터 산소가 풍부한 저충류가 흘러둘어오면 산소 가 다시 증가하여 산소극소총 oxy ge n minim um laye r 을 형 성한다(그립 2-1 6). 해수중에서 산소의 용해도는 염분이 증가할 때 감소하는 반면 수 온이 상승할 때 감소한다. 예컨대 l5°C 에서 포화상태일 때 해수는 불과 8.Om g /l 의 산소를 포함하지만 담수의 경우는 갇은 조건에서 10.2mg /l 룰 포함한다. 그림 2-17 은 온도, 염분 및 용존산소 포화농도의 상관관계 를 보여준다. 이산화탄소는 대기로부터, 그리고 호흡의 최종산물로부터 해수에 들어 간다. 이산화탄소는 쉽사리 물과 반응해서 탄산염과 중탄산염을 형성한다.
 15
15
그림 2-17 용존 산소 포화 농도에 대한 수온 및 염분의 영향
CO2+H20 ~ H2C03~ HC03-+H+ 노 C032-+2H+ 이것이 해수중에서 이산화탄소가 제거되었을 때 보충해주는 커다란 저 장소가 된다. 이산화탄소는 광합성의 필수물질로서 해양에 풍부한 식물 플랑크톤에 의해 대량으로 이용된다. 황화수소는 해수중에 보통 미량으로 존재한다. 그러나 산소가 결핍된 수역에서는 유기질의 생물분해 산물로서 비교적 대량 생산될 수 있다. 이러한 현상은 정체 수역이나 퇴적물 부근의 수충에서 흔히 나타난다. 황화물은 많은 종류의 해양생물에 대해서 매우 유독하므로 중요하다. 또 한 화학합성 박테리아에게는 중요한 에너지원으로 이용된다. 부유성 고형 물질 (pa rt icu late matt er ) 해수중의 부유성 고형물질은 유기 데트리터스, 유기 및 무기물질의 복 합체. 세립 광물질 등을 포함한다. 해양에서 이들의 농도는 크게 변화한다.
해수의 p H( 산성도 단위) 해수는 7.5~8.4 의 p H 를 갖는 다소 염기성인 완충액이며 평균 p H 는 7, 8 이댜 해수의 산성도나 염기도 상의 변화는 생물학적 성장과 활동에 대해서, 그리고 화학반응에 대해서 매우 중대한 영향을 미친다. 예컨대 해수가 만일 산성으로 된다면 많은 생물의 각을 형성하는 CaC03 가 용해 되고 말 것이다. 해수의 p H 는 또한 존재하는 용존 CO2 양과 관련해서 매우 중요하다. C02-2 용존가스로서 해수에 용해되지만 급속히 물과 반응하여 약산인 H 2 C0 3 ( 탄산)를 만든다. 이것이 다시 해수중에 존재하는 M g나 Ca 와 반응하여 탄산염이나 중탄산염을 만든다. CO2 + H20 ~ H2C 0 3 2H + +CO/ 간:. HCQ 3 -+H+ p H 의 감소(수소이온농도의 증가)는 더 많은 탄산염과 중탄산염으로 하 여금 탄산과 CO 2 형태로 되돌아가게 할 것이다. 이것이 낮은 p H 에서 각 shell 에 있는 CaC0 3 물 용해시키는 이유이다. 광합성이 일어나기 위해서는 CO2 가 존재하지 않으면 안 된다. p H 상 의 변화는 존재하는 CO 2 의 양에 변화를 일으키고 따라서 광합성 양의 변화를 초래한다. 한편 광합성은 물로부터 CO2 를 제거한다. C02 + H20+ 영 양물질 + 광에 너 지 一유기물질 +02 이 결과로 p H 가 상승한다. 따라서 표충수는 광합성이 일어나는 동안 C 아의 제거로 흔히 심층수보다 높은 p H 를 갖는다. 심층수처럼 광합성 이 일어나지 않는 곳에서는 유기물질을 분해하는 종속영양생물의 호흡이 co 려 농도를 증가시키고 p H 를 감소시킨다. 유기물질 +02-. C02+H20
그러므로 광합성 활동이 가장 큰 해수의 표충으로부터 해저에 이르기 까지 일반적으로 pH 의 점진적인 감소가 나타난다. 2-6-2 해수중의 체류시간 (Res i dence Tim e) 해양으로 들어가는 물질들은 그 상태를 변화시키거나 해수로부터 제거 되는 수많은 과정을 거치게 된다. 화합물은 다른 것과 반응하여 새로운 화합물을 만들기도 하고 생물은 이들을 동화시켜 생체조직을 만들며, 원 소는 용액으로부터 침전하기도 한다. 결과적으로 무기이온은 해양으로부 터 끊임없이 제거되고 있다. 이러한 손실은 강수로부터 바다로 유입되는 광물질에 의해 보충된다. 주어진 시간에 해양에서 발견되는 이온들을 완 전히 대치시키는 데 걸리는 시간을 이온의 〈체류시간〉이라고 한다. 대표 적인 체류시간은 앞에서 나온 표 2-3 에서 보는 바와 같다. 체류시간은 광범위하게 변화한다. 예컨대 Na 의 체류시간은 2 억 6 천만 년인데 반해
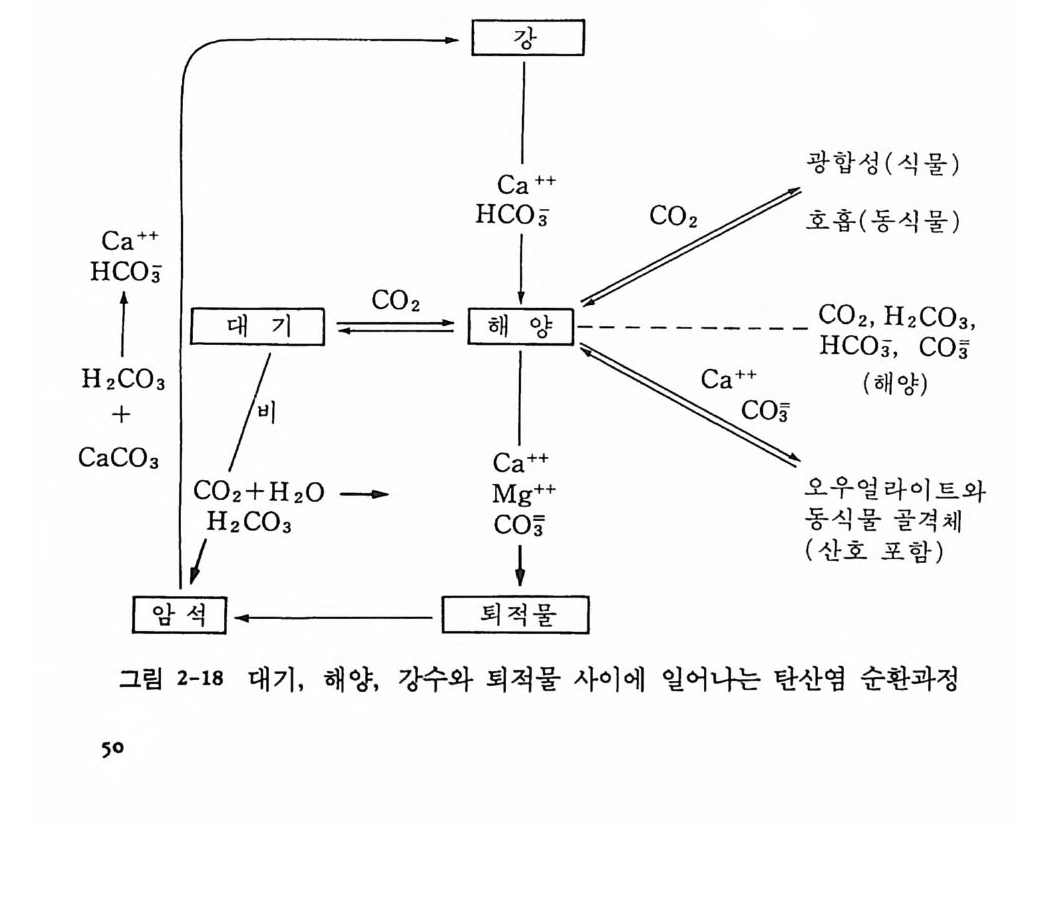 CHHac52CC+0!Ca그 OO 三+0림3 + a3 2-C1H80 22 C대+>0기H3,2 0해 —양/,_ -一g강 수와 퇴적――—―「럴iSHcHca— 二 물 사이 에 일어:나는 탄산동오\호 염C식우 oc 紀H물얼순 라 환 》 二g따골이과격 정트oeeo체銅 와 33= ’
CHHac52CC+0!Ca그 OO 三+0림3 + a3 2-C1H80 22 C대+>0기H3,2 0해 —양/,_ -一g강 수와 퇴적――—―「럴iSHcHca— 二 물 사이 에 일어:나는 탄산동오\호 염C식우 oc 紀H물얼순 라 환 》 二g따골이과격 정트oeeo체銅 와 33= ’
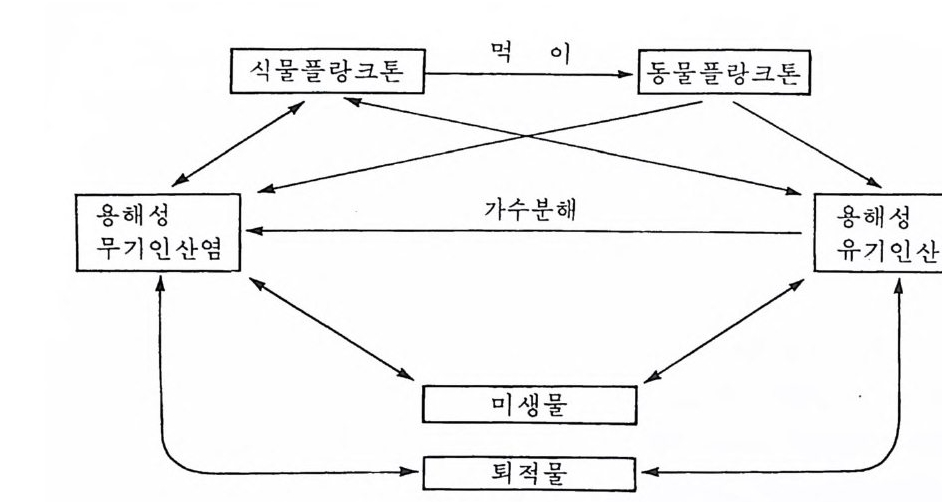
Al 의 체류시간은 불과 100 년이다. 이러한 차이는 이온의 상대적인 반응 성과 또 그것이 해양에서 발견되는 형태에 기인한다. 죽 Na 는 용해도 가 매우 낮은 화합물을 만들어서 오랜 기간 해수에 남아 있는데 반해 Al 은 통상 입자상으로 해수에 들어가서 급속히 가라앉는다. 건 체류시 간을 갖는 물질이 대량 해수로 들어가면 최소한 국지적인 해역에서 농도 의 점진적인 축적이 이루어질 수 있다. 탄산염과 중탄산염은 매우 짧은 체류시간을 갖고 있다. CO2, CO/-, HC03- 간의 상호작용은 이미 언급한 바 있다. 탄산염은 일차적으로 CaC03 의 형태로 오우얼라이트 ool it e 나 모래 같은 단괴를 이루면서 쉽사 리 침전한다. 그림 2-18 은 대기, 해양, 강수 및 퇴적물 사이에서 탄산염 의 순환을 나타낸 것이다. 2-6-3 영양소의 순환 생물의 성장에는 많은 원소가 필요하다. 이들 물질을 영양소 nu tri en ts 라고 한다. 영양소 가운데 가장 중요한 것은 질소 (N) 와 인 (P) 으로서 조 직 속에 동화되고 생화학적 반응에 사용된다. 규소 (S i)는 규조(珪碩)와 방산충(放散蟲) 의 골격 형 성 에 필요하다. 그 의 에 여 러 원소들이 필요한 데 이들은 미량만이 요구된다. 해양에서 영양소의 농도는 해양생물의 생 물학적 활동의 결과로 계절과 수심에 따라 변화한다. 영양소는 성장하고 있는 생물에 의해서 홉수되고 혼히 형태를 바꾸어 배출된다. 그러므로 농도상의 변화는 생물학적 활동이 가장 큰 곳에서 제일 심하다. 인의 순환 인은 해양에서 용존인산염 (H2PO.-, HP0.2 -), 가용성 유기화합물(단백 질, 지질, 당), 그리고 불용성 유기 및 무기화합물(인산칼슘, 인산철) 등 으로 발견된다. 해수중의 평균 인의 농도는 70µg / l 이며 이들의 대부분 이 무기형태이다. 인의 순환은 그립 2-19 에서 보는 바와 같다. 가용성 및 불용성 인산염은 풀랑크톤에 의해 홉수 이용되며 그 다음 유기 및 무기 인산염으로서 가용성 형태로 배출된다. 유기 인산염은 해
 /I一 식물플 랑크톤 I 가먹수 분이해 기동물플랑~크본|I \용해성
/I一 식물플 랑크톤 I 가먹수 분이해 기동물플랑~크본|I \용해성
그림 2-19 해양에서의 인 순환
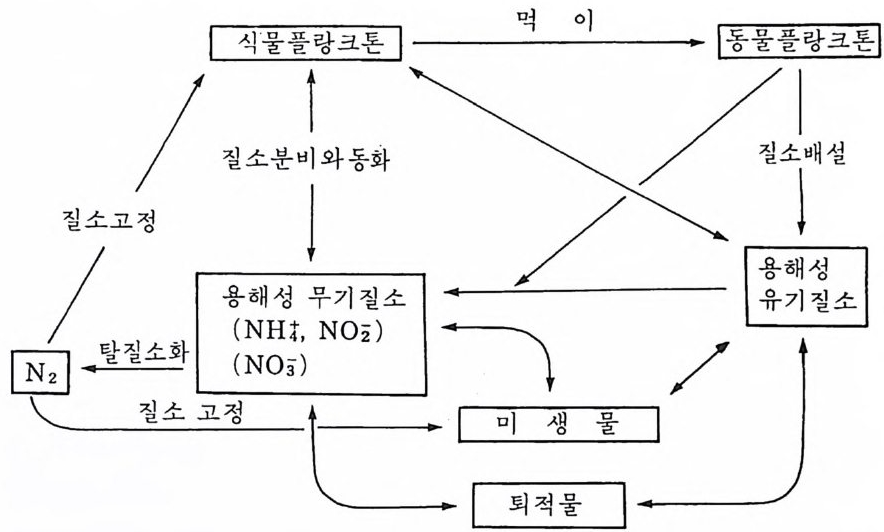
수중에서 무기 형태로 가수분해될 수도 있다. 이러한 상호변화는 퇴적물 에서는 물론 해수중에서 일어나며 이 두 상(相)간에 순환이 될 수도 있다. 일반적으로 인의 농도는 생물학적인 흡수가 가장 큰 표충 부근에서 가 장 낮다. 농도는 약 1,000m 수심에 이르기까지 일정하게 유지되지만 약 간 감소하는 경우도 있다. 질 소의 순환 (nitrog e n cyc l e) 질소는 바다에서 다양한 형태로 출현한다. 분자상의 질소 (N2) 가 가장 풍부하고 N02, N03 가 매우 혼한 결합형태이다. 플랑크톤이 무기 및 유 기질소를 섭취 하고 용해성 암모니 아나 유기질소를 배출한다(그립 2-20) . 해양생물 가운데 남조류와 일부 박태리아는 분자상의 질소를 고정하는 능력을 갖고 있다. 박테리아는 용존산소가 있을 경우에 유기질소를 산화 하여 암모니아로 변화시키고 이를 다시 N02- 와 N03- 로 변화시킬 수 있 다. 이 러 한 과정 을 질소화작용 nit rifica ti on 이 라 한다. Ni tro zomonas Ni trob acte r 유기질소一 NH3 ) N02_ l N03-
 질소고( 질석소물분플 Ul랑 와크동돈화] \\먹\ 이 Jl1배 동물플설랑크본 |
질소고( 질석소물분플 Ul랑 와크동돈화] \\먹\ 이 Jl1배 동물플설랑크본 |
그림 2-20 해양에서의 질소 순환
산소가 결핍된 수역에서는 퇴적물 속에서나 부근에서 흔히 볼 수 있듯 이 탈질소세균 denit rifying bacte r i a 이 N03- 와 N02- 률 분자상 질소로 환 원시킬 수 있다. N03-- . N02-- . N2 질소 순환에 있어서 모든 전환은 생물학적으로 조정되고 따라서 재생 은 인의 순환에서보다 더 느리다. 결국 질소는 해양미소생물에 대하여 재한영양소로 되는 일이 종종 일어난다. 질소의 수직분포는 인의 경우와 아주 유사하다. N03- 의 농도는 표충 에서 가장 낮고 약 1,O OOm 수심까지 증가하여 그 다음 일정하게 유지되 거나 길이에 따라 다소 감소한다. 규소순환 (sili co n cyc l e) 지각 암석의 풍화에서 유래하는 규소는 해수중에는 부유성 규산염
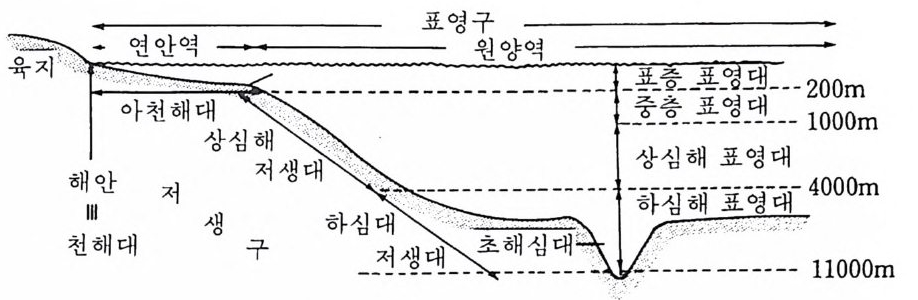
(S i 02) 형태로, 그리고 해저에서는 점토광물에서 발견된다. 규산염은 규 조류와 방산충류에 의해 이용되어 이들의 각을 형성한다. 순환과 분포는 인과 질소의 경우와 유사하다. 2-7 해양의 생물학적 특징 인류는 바다와 관련을 맺은 초기에서부터 해양생물에 관한 연구를 시 작하였다. Ar i s t o t le 은 최초의 생물학자 가운데 하나였으며, 지중해에서 해양생물을 연구한 기록을 남겼다. 그러나 실제로 과학적인 연구는 영국 의 식물학자인 E. Forbes(l815~1854) 가 19 세기 중엽 심해 수역에서 행한 생물연구로 비롯되며 이 업적으로 그는 해양생물학의 아버지로 불린다. 해양생물에 관한 가장 큰 초기의 업적은 18 72 년 챌린저호 탐사 Challeng e r Ex pediti on 로 이루어졌다. 전세계에 걸친 해양과 해양생물의 연구를 위해 영국 해군이 이 조사선을 마련하였다. 이 탐사는 3 년 6 개월 간에 걸쳐 수행되었고 항해 거리는 약 11 만 km 에 달하였다. 수집된 자 료는 매우 방대하여 분석하는 데 20 년 이상 걸렸고 50 권이나 되는 『 챌린 저보고서 』 에 수록 발간되었다. 이 획기적인 연구결과는 많은 과학자의 관심을 모았고 현대 해양학 발전에 기초가 되었다. 2-7..:..1 바다에서의 생물학적 분포 해양의 생물 영역은 크게 두 가지로 나눈다 . 즉 저생(底 生 ) 혹은 해저 환경 benth ic or sea-b o tt om env iro nment 과, 표영 (i 票 泳) 혹은 수충환경 pel agi c or wate r -column envir o nment 이 그것 이 다. 이 분류는 매 우 광범 위 해서 더 세분된다(그림 2-2 1 ). 표영환경은 바닥을 덮고 있는 해수이며 하조선(下朝線, low tide level) 으로부터 해양의 가장 깊은 곳까지 확대된다• 표영역은 대륙붕을 덮고 있는 연안역 ner iti c 과 대륙붕 너머로 덮여 있는 외양역 ocea ni c 으로 다시 나뉜다. 외양환경은 연안환경보다 화학적 조성이 더 일양(一樣)하고 일
 표영구원 양역
표영구원 양역
그람 2-21 해양 환경의 구분
반적으로 영양소의 함량이 더 적어서 이 점이 두 환경의 생물학적 차이 롤 야기시킨다. 저생환경은 썰물 때 노출되는 해변으로부터 해양의 깊은 퇴적층까지 광범위한 조건을 포괄한다. 이 환경은 보통 천해대 (i菱海帶 littor al zone) , 아천 해 대 sublitt or al zone, 심 해 계 deep -s ea sys t e m 로 나뉜 다. 천해대는 밀물과 썰물 사이에 나타나는 지역으로 흔히 조간대 inter - tida l zone 로 불린다. 이 지역의 폭은 조석범위와 바닥의 경사에 의존한 다. 이 지역은 바딧물이 들고 나갈 때 해수에 잠기거나 대기에 노출되고 해변에 부서지는 파랑으로부터 일정한 타격을 받게 된다. 조간대에 사는 생물은 이러한 조건에 견딜 수 있지 않으면 안 된다. 많은 생물은 썰물 때 바닥으로 구멍을 뚫고 들어가고 밀물 때 먹이를 구하기 위해 나옴으 로써 어려운 환경을 극복한다. 아천해대는 대륙붕의 해저이며 천해대로 부터 대륙사면까지 확대된다. 이 지역의 가장 얕은 부분은· 해양의, 저생 생물이 가장 밀집한 곳이다. 천해대로부터 수심이 더 깊은 곳으로 나가 면 빛 두과량이 감소하여 식물은 감소하지만 동물은 번성한다. 따라서 이 지역이 어업에 매우 중요한 해역을 이룬다. 심해계는 일반적으로 광 선의 결핍과 한정된 영양소 때문에 식물상이 존재하지 않는다. 동물량은 국단적인 압력, 추위, 어둠, 그리고 최소량의 먹이 등에 적응하지 않으 면 안 된다. 이 환경에 사는 대부분의 생물은 표충에서 떨어지는 테트리 터스를 먹고 산다. 깊은 수심 때문에 이들 생물에 대한 정보는 아직 미
미한 상태에 있다 . 2-7-2 주요 환경요인 주어전 해역에서 성장하는 해양생물의 형태를 결정하는 주요 요인의 하나는 그 환경의 상태이다. 이것은 그 해역의 화학적, 물리적 성질을 ' 포함한다. K비 해 양에서의 먹이망fo od web 은 녹색식물에 의해 광합성이 이루어지는 동안 흡수되고 후에 먹이의 형태로 다른 생물들에 의해 섭취되는 에너지 와 물질에 의존한다. 빛은 광합성의 에너지원일 뿐만 아니라 해양생물의 시력에 매우 중요하며 먹이와 숨을 곳을 찾고 열을 얻는 데 있어서도 역 시 중요하다. 순수한 물은 매우 투명해서 상당한 거리까지 빛이 투과하도록 해준다. 그러나 불순한 물은 이 투명도를 크게 감소시킨다. 해수는 순수하지 않 으나 연안에서 멀리 떨어전 의양역에서는 빛이 상당한 깊이까지 두과되 므로 광합성은 대략 lOOm 정도의 수심에서도 일어날 수가 있다. 물론 광도와 식물플랑크론의 밀도는 표충 가까이에서 가장 크다. 탁도는 빛 두과에 중요한 역 할을 한다. Beer-Lambert 의 법 칙은 광도 가, 빛이 물속을 통과할 때 깊이에 따라 비례적으로 감소함을 말해준다. 그 관계식은 다음과 같다• ld=I0e-kd 여기에서 Id= 수심 d 에서의 광도 Io= 표면에서의 광도 k= 소광계수 ex ti nc ti on coe ffici en t로 알려진 어느 특정파장에 대한 상수
계수가 작을수록 흡수가 적고 물의 두명도가 더 크다. k 의 대표적인 값은 순수한 물에서 0. 02, 해수에서 o.1 , 연안 해수에서 0. 4 이다. 이는 연안수역에서 50m 수심의 광도가 의해역에서의 광도보다 100 만분의 1 이하임을 의미한다. 온도 바다에서의 온도 변동은 이미 언급하였다. 수온약충 아래에서 온도는 전세계를 통해 거의 변화하지 않으며, 그곳에 사는 생물에게 약간의 영 향을 미칠 뿐이다. 수온약충 아래의 온도는 일정하게 낮고 따라서 내한 성생물( iffi t 寒 性 生物 )만이 생존한다. 수온약충 위의 온도는 계절에 따라서, 또한 위도에 따라서 변화한다. 이러한 현상이 현존하는 생물의 분포와 다양성에 주 영향을 미친다. 온도의 변화는 생물에 대하여 호흡과 대사 율에, 성장과 생식에, 그리고 수명에 영향을 미친다. 일부 이동성 생물 은 자신을 위한 적철한 온도를 유지하기 위해서 계절에 따라 해양의 한 부위에서 다른 곳으로 회유(回游)한다. 압력 수심 증가에 의해 야기되는 물의 무게는 현존하는 생물의 형태에 중요 한 영향을 미친다. 해양생물은 대부분 좁은 수심범위 내에서만 생활할 수 있는데 이는 이들의 중성부력 neutr a l buoy an cy 울 일으키는 대 이용되 는 부레에 대한 압력의 영향과 가스 용해도에 대한 압력의 영향 때문이 다. 잘 적응된 일부의 생물만이 아주 깊은 수심에서 큰 압력을 견디며 생존할 수가 있다. 염분 해양생물은 대부분 일정한 염분을 갖는 해수 생활에 적응되어 있어서 그 농도가 작은 범위로 변화할 때에만 견딜 수 있다. 예의는 염분의 변화 가 규칙적으로 변화하는 하구나 해안부근 수역에서 생활하는 동식물의 경우 이다. 이 때문에 하구에서의 생물학은 의해역의 그것과는 판이하게 다르다.
해수 01 동 해수이동은 일부 생물에게는 필수적인 반면 다른 생물에게는 매우 해 롭다 . 이동하는 물은 생물을 운반하고 영양소를 분포시키며, 폐기산물을 운반하고, 산소를 공급하는 등 역할이 다양하다. 그러나 또한 퇴적물을 부유시키고 그럼으로써 빛 투과를 감소시키며, 해저생물을 매몰시키고, 일부 생물의 여과장치를 막히게 한다. 파랑이나 조석 형태의 이동은 난 류(亂流), 생물교환, 또는 동식물의 주기적인 습윤( 濕 潤)과 건조 등을 일 으킨다. 이러한 상태는 일반적으로 현존하는 생물의 다양성을 제한하는 경향이 있다. 화학적 요인 영양소의 농도, 용존산소량, p H 및 CO2 농도 같은 화학적 요인도 주 어진 해역에 존재하는 해양생물의 형태와 수를 지배하는 요인이 된다. 포식 자 (pr edato r ) 바다에 사는 모든 생물은 다론 생물에 대하여 먹이로서 역할을 한다. 대부분의 해양생물의 먹이는 비교적 제한되기 때문에 포식자와 피식자 사이에 개체군의 균형이 확립되지 않으면 안 된다. 만약 피식자가 적절 히 존재하지 않으면 포식자는 피식자 선택을 바꾸거나 다른 곳으로 옮기 도록 강요될 것이다. 2-7-3 해양에서의 생물군 해양생물은 3 개의 넓은 계급으로 구분할 수가 있다. 즉 플랑크론, 유 영동물 및 저생생물이 그것이다. 아직도 초보적인 이해에 불과한 박테리 아는 또 다른 계급을 구성한다. 플랑크톤 풀랑크톤(부유생물)은 바다에서 피동적으로 부유하거나 미약하게 유영 하는 식물 죽 phy top l a nkto n 과 동물 죽 zoop la nkto n 을 말한다. 대부분의
플랑크톤은 현미경적인 크기를 갖지만 해파리처럼 대형인 것도 있다. 식 물플랑크돈이 지구상의 산소를 대량으로 긍급하고 많은 대형생물의 먹이 가 되기 때문에 이들의 중요성은 과소평가될 수가 없다. 식물플랑크돈은 광합성이 일어나기에 충분할 만큼 빛이 투과되는 수층인 수광대(受光帶) 에 한정적으로 분포한다. 대부분 단세포 생물로서 바다에서 자유로이 떠 다닌다. 식물플랑크톤 가운데 우세한 종류는 황갈색조류 (ch ry so p h yta ; yel low brown alga e ) 이 며 여 기 에 는 규조류 dia t o m 와 코콜리드류 coccoli tho - p hore 가 포함된다. 규조류는 단독, 또는 군집생활을 하는 단세포 생물이다. 이 종류는 많 은 상이한 모양과 크기를 가지며 각을 형성하는 규질(珪質)성분으로 구 별된다. 규조류는 생식주기가 빠르고 해양의 표층부근, 그리고 냉수역에 특히 풍부하다. 해저로 침전할 때는 대부분 보다 큰 생물에 의해 소비되 지만 상당히 많은 양이 퇴적해서 규조연니 (珪藏軟泥, dia t o m aceous ooze) 롤 형성한다. 코콜리드류는 크기가 규조류와 유사하나 탄산칼슘 골격을 갖는다. 죽어서 가라앉으면 칼슘연니를 형성하기도 한다. 식물플랑크톤 중 세번째 중요한 종류는 쌍편모조류 d i no fl a g ella t e 이다. 이들 또한 단세 포 생물이나 운동을 일으키는 편모(篠毛, fl a g ellum) 를 2 개 갖고 있는 점 이 유일한 특징이다. 적조(赤潮 red ti de) 를 일으키는 쌍편모조류는 해양 생물과 사람에게 해로운 독물질을 생산한다. 해양에는 다양성이 큰 동물플랑크론이 존재한다. 여기에는 원생동물, 강장동물, 환형동물, 연체동물, 절족동물, 극피동물, 척색동물 등이 포 함된다. 이들 중 가장 수가 많은 종류는 절족동물이며 갑각류가 대표적 인 종류이다. 동물플랑크톤은 대부분 그들의 먹이가 되는 식물플랑크론의 분포 때문에 해양의 표충 가까이에서 발견된다. 이돌 중 많은 종류가 수직적으로 이동하 는 능력이 있어서 밤에는 표충으로 울라오고 낮에는 깊은 곳으로 내려간다. 유영 동물 (nekto n ) 자유롭게 유영하는 어류와 수생 포유류는 유영동물 계급에 속한다. 유
영동물은 보다 좋은 환경으로 이동하고 활발히 먹이를 구하여 포식자를 피하는 능력을 갖고 있다. 이돌은 플랑크톤처럼 그 운동이 해류에 의존 하지 않는다. 유영동물에는 어류, 상어류, 거북류, 해양 포유류와 오징 어류 같은 일부 연체동물이 포함된다. 해양에서의 유영동물의 분포는 수 온, 영분, 산소, 먹이 등의 환경요인으로 결정된다. 저 생 생 물 (benth o s) 해저의 위나 속에서 생활하는 생물을 저생생물이라 하며 많은 종류의 동식물이 포함된다. 이들은 자유롭게 움직이거나 바닥에 부착하여 살고 있으나 먹이와 안정성에 있어서는 해저에 의존하고 있다. 따라서 해저의 조성이 존재하는- 생물의 촌재를 결정짓는다. 모든 저생식물은 부착성으로서 조류(慕類)에 속한다. 갈조류는 전정한 해양식물이다. 이들은 주로 냉수에 서식하는데 매우 크며 바다에서 발견 되는 대형조류의 대부분을 차지한다. 홍조류 또한 전세계의 해양에서 발 견되는데 바다 속으로 가장 깊이 두과되는 파장(청색과 보라색)의 빛을 이용할 수 있도록 적응되어 있으므로 200m 에 이르는 수심에서도 서석 한다. 남조류(藍溪類)는 흔히 다발(束) 또는 자리 모양으로 성장하는 사 상(絲狀)생물이다. 바다에서는 그다지 우세하지 않다. 녹조류는 해수에 서는 다수로 발견되는 일이 드물다. 해양환경에서 완전히 물에 잠겨 생활하는 현화식물은 한두 종에 불과 하다. 그러나 연안 늪지에는 부분적으로만 잠겨서 생활하는 것이 약간 있으며 대표적인 것이 초본식물(草本植物)인 Sp a rti na 와 ]uncus 이다. 저생동물은 다양성이 매우 크며 특히 대륙붕 지역에 많다. 이들 가운 데 일부는 해저의 표면에서 생활하는 반면 퇴적물 속에 구멍을 파고 생 활하는 종류도 있다. 해면, 산호, 연충류, 연체동물, 갑각류, 극피동물 등은 모두 생 활사 중의 한동안은 저생생 활을 한다. 여과섭식 filter feeding 하는 종류가 많고 일부는 초식성 (草食性) 이다. 저생생물은 해수 중 상충에서 떨어지는 테트리터스를 분해하고 영양소 를 수층으로 순환시키며 퇴적물의 과도한 축적을 막는다는 점에서 매우
중요하다. 해양 박테리아 (Mar i ne Bacte r ia ) 박테리아는 유기물질이 식물에 의해 재이용되도록 분해시키는 해양먹 이연쇄상의 아주 중요한 부분이다. 종속영양박테리아 (he t ero tr o p h ic bacte r ia : 탄소원으로서 유기물질을 이용하는 종류)와 독립영양박테리아 (auto t r op h ic bacte r ia : 탄소원으로서 무기물질과 이산화탄소를 이용하는 종 류)가 있다. 유기물질을 이용하는 것 이의에도 일부 해양 박테리아는 가 스상의 질소를 고정할 수 있고 질소화할 수 있으며 또 일부는 탈질소화 할 수 있다. 해양환경에서 발견되는 다양한 박테리아의 수는 매우 많다.
제 3 장 먹이연쇄의 개념 해양생태계는 흔히 생물 상호간, 그리고 생물과 물리 • 화학적 환경간 에 국단으로 복잡한 상호관계를 형성하는 다양한 생물의 집단으로 구성 된다. 그럼에도 불구하고 해양 자원의 현명한 관리와 이용을 위해서 한 시스템 내의 모든 상호작용에 대한 상세한 지식을 필요로 하는 것은 아 니다. 흔히 수 종의 중요한 상태계 구성종(構成 種 )에 대한 상세한 지식 울 토대로 약간의 일반적인 원리를 적용함으로써 해양생태계를 보존하고 합리적으로 관리하는 데 충분할 수 있다. 이제부터 고찰하려는 바와 같이 먹이연쇄 foo d cha i n 의 개념은 자연수 계(自 然 水系) 내에서 먹이 관계를 과도하게 단순화한 것이다. 그러나 먹 이연쇄 이론의 미비점을 잘 인식하고 유념한다면 이 개념을 해양오염을 포함한 많은 생태학적 문제에 대하여 유용하게 적용할 수 있다. 분명히 해양생태계에 대한 오염물질의 영향은 시스템을 통해서 오염물질을 포함 한 물질의 전달을 지배하는 섭식관계에 크게 좌우된다. 이 섭식관계는 흔히 아주 복잡한 경우가 많지만 그 상호관계의 결과로 나타나는 오염물 질의 효과는 최소한 정성적인 의미로 먹이연쇄 이론에서 유도된 비교적 간단한 원리를 적용함으로써 이해될 수 있다.
3-1 먹이전달 효과와 먹이연쇄 모든 생물은 한 형태, 또는 다른 형태로 먹이를 필요로 한다. 먹이는 연소되어 정상활동에 요구되는 에너지를 마련하거나 혹은 단백질, 지방, 탄수화물 및 기타 필수적인 구조나 대사 성분을 공급하는 화합물의 형태 로 생물체 속에 합성된다. 오탁된 먹이의 섭취는 오영물질이 생물권으로 들어가고 그 생물권 내에서 전이되는 분명한 하나의 기작(機作)이다. 예 컨대 어류가 수은으로 오염된 조류(溪類)를 먹는다면, 그리고 그 어류가 섭취한 수은을 계속 지니고 있다면 그 수은은 다시 어류를 먹이로 하는 새에게로, 더 나아가 아마도 인간이나 새를 먹이로 하는 다른 생물에게 로 전달될 수 있을 것이다. 이와 같이 먹이생물로부터 포식자에 이르기 까지 일련의 직접적인 오영물질의 전달은 오영물질이 공간적으로, 시간 적으로 멀리 이동하여 생태계의 각 부위로 전파되는 결과를 초래한다. 이상 설명한 오염물질의 직접 전달이 오염의 영향이 섭식관계의 결과 로서 널리 전파될 수 있는 유일한 기작을 나타내는 것은 아니다. 왜냐하 면 어느 특정 종 (種) 이나 먹 이 종류의 수도 (數度 Abundance) 를 증가시 키거나 감소시킴으로써 오영이 간접적으로 또한 극적으로 많은 생물의 수도에 영향을 미칠 수도 있기 때문이다. 예컨대 생활하수(生活下水)는 식물 성장에 필수적인 물질, 특히 N 과 P 를 고농도로 포함하고 있으나 비오영 수계에는 이들 물질이 흔히 식물성장을 제한할 만큼 적은 양을 갖는다. 만일 생활하수가 이러한 수계에 투기된다면 식물성장이 크게 촉 전되기 쉽다. 식물의 수도가 높아지면 초식동물 herb i vore 은 먹이가 많아 지는 것에 직접 반응하여 수가 증가할 것이다. 이러한 논리를 따르면 식 물에 대한 영양소를 초기에 공급함으로써 생태계 내의 얼마나 많은 동물 이 궁극적으로 영향을 받을 것인가를 쉽게 상상할 수가 있다. 식물생산 이나 동물생산에서 보는 이러한 자극은 결코 우리가 피해야 할 어떤 추 측적인 것이 아니다. 실제로 일부 수중 양식(樣式) 시스템은 정확하게 지금 설명한 기작으로써, 죽 식물성장을 자극시키기 위해 생활하수 배출
물을 사용함으로써, 그리고 이들 식물을 특정 생물의 먹이로 공급합으로 써 목적하는 생물의 생산을 촉진시킨다. 그러나 불행히도 인류가 크게 필요로 하는 생물을 포함하여 모든 생물이 다 이처럼 고생산성 시스템에 서 살기에 적절한 것은 아니다. 오히려 고생산성 시스템에서 풍부하게 성장하는 종류는 우리가 바람직하게 생각하는 생물이 아닌 경우가 적지 않게 나타난다. 이점에 대한 상세한 설명은 뒤에서 하게 될 것이다. 어떤 박테리아가 심해의 일부에서 일차생산자로서 중요한 역할을 담당 하고 있는 것(J a nni sch, 1977) 은 사실이지만 여전히 식물이 거의 모든 수 계(水系)에서 가장 중요한 일차생산자이다. 식물은 에너지원으로서 광선 울 이용하며 광합성으로 불리는 과정을 통해 CO2, 물 및 무기영양소로 부터 유기 화합물을 합성 한다. 예 컨대 glu cose 갇은 당(糖) 의 합성을 설 명하는 단순한 식은 다음과 갇이 쓸 수 있다. 광합성 에너지 +6C02+6H20 ----1 C6H1206( 당) +602 호흡 만일 반응이 좌측에서 우측으로 진행되면 에너지원은 광선이 된다. 이 에너지의 일부가 당분자 속에 화학적으로 저장된다. 다음 당분자가 산소 와 함께 연소함으로써 산화되면 반응이 우로부터 좌로 진행되며 이룰 호 홉이라고 한다• 이 경우에 당분자 속의 에너지가 방출되는데, 이것은 빛 에너지가 아니다. 이 에너지는 생물의 호흡과정과 여러 가지 대사과정에 필요한 에너지로 공급된다. 모든 생물은 에너지원을 주면 유기화합물을 한 형태로부터 다른 형태로 변형시킬 수 있고 그 결과 먹이룰 그들이 원 하는 화합물로 정확히 전이시키는 능력을 갖고 있다. 그러나 무기성 저 에너지 성분으로부터 유기성 고에너지 화합물을 만둘 수 있는 것은 식물 과 일부의 박테리아만이 가능하다. 그러므로 모든 생물은 먹이원으로서 석물과 일부 박테리아에 직 • 간접으로 의존하고 있다. 스스로 필요로 하 는 대부분 혹은 전부의 물질을 무기화합물로부터 생산할 수 있는 생물을
독립영양생물( 獨 立 營養生物 )이라 하는 반면 먹이의 대부분이나 전부를 유 기화합물의 형태로 취하는 생물을 종속영양생물(從 屬營養生物 )이라 한다. 균류(菌 類 )를 제의한 모든 식물은 독립영양생물이고 모든 동물은 종속영 양생물이다. 박테리아는 종속영양생물이지만 일부의 박테리아는 잘 발달 된 독립영양 능력을 갖고 있다. 식물에 의해 초기에 생산된 먹이(죽 식물 생체량)는 식물을 먹이로 하 는 종속영양생물, 죽 초식동물에 의해 소비된다. 식물 생체량의 대사에 의한 초식동물 생체량의 생산은 또 다른 종속영양생물, 죽 일차육식동물 (肉食動物, pri m ary carn i vore) 에 의해 먹히고 이 일차육식동물이 초식동 물 생체량의 일부를 일차육식동물의 생체량으로 전이시킨다. 초식동물의 생 산은 이 차생 산 secondary pro ducti on , 일차육식동물의 생 산은 삼차생 산 ter t iar y p roduc ti on 이 라 부른다. 일 차초식 동물은 이 차초석 동물 seconda ry carniv o re 에 의 해 먹 히 고 이 것은 다시 삼차육식 동물 ter t iar y carniv o re 에 의해 먹힐 수 있다. 생태학자들은 이러한 연속적인 먹이전달의 시스템을 먹이연쇄라 부르 고 먹이연쇄의 각 성분은 영양단계 ( 營養 段階, trop h ic level) 라 한다. 위의 경우에 식물은 제 1 영양단계, 초식동물은 제 2 영양단계, 일차육식동물은 제 3 영양단계 등을 이룬다. 이러한 먹이연쇄는 다음과 갇이 도식적으로 나타낼 수가 있다. I 이차육식동물 (제 4 영양단계) | 종속영양생물{ 일차육식동물 (제 3 영양단계) I 초식동물 (제 2 영양단계) I 독립영양생물 식물 (제 1 영양단계) | 무기영양소
해양생태계에서는 한 영양단계에서 그 다음 영양단계로의 먹이전달이 10~20% 의 비교적 낮은 효율로 나타난다고 알려져 있다. 즉 먹이가 한 영양단계에 의해 섭취되는 비율은 먹이가 다음 영양단계로 통과하는 비 율보다 5~10 배 크다. 이 효율은 생태효율(生態勃 車 ecolog ica l effi cien - c y)이라 하는데 한 영양단계에 의해 흡수된 먹이의 상당량이 호흡되어 에너지를 마련하거나 또는 상당량이 새로운 영양단계의 생체량으로 동화 될 수 없어서 배설되기 때문에 상태효율은 일반적으로 낮다. 호흡에 의 해 생산된 CO2 는 물론 석물에 유용하고 이런 의미에서 먹이연쇄 속으로 순환되어 되돌아가지만 종속영양생물에 대한 직접적인 먹이원이 되지는 않는다. 분비된 유기화합물은 그것이 용존상태이건 입자상태이건 박테리아의 먹이원이 된다. 이 미생물은 다론 종속영양생물에 의해 분비된 유기물질 의 대부분을 대사시킬 수 있으며, 실제로 박테리아 영양단계는 소위 데 트리터스 먹이연쇄 detr itus foo d chain 에서 첫단계를 형성하는 것으로 간 주된다. 데트리터스라는 용어는 생물의 사체나 유기입자의 분비에 생기 는 바 생 명 성 입 자상 유기 물질 non-liv i n g par t icu late orga n i c mate r i al s 울 말 한다. 그러므로 데트리터스 먹이연쇄는 식물 영양단계를 기초로 하는 생 식 (生食) 먹이연쇄 graz in g foo d cha i n 와 대조를 이룬다. 모든 영양단계에 서와 마찬가지로 박테리아 영양단계도 그것이 소비하는 데트리터스의 많 은 양을 호흡하고 분비한다. 분비된 화합물 가운데 일부 고도로 내화성 유기화합물(討火性有機化合物)은 거의 무한정 지속성을 갖고 궁극적으로 퇴적물에 매몰되지만 나머지는 다른 박테리아에 의해 이용된다. 입자에 부착한 박태리아는 다른 생물에게 섭취될 수 있고 이러한 양상으로 분비 된 유기물질은 간접적으로 생식먹이연쇄로 순환되어 들어갈 수 있다. 따 라서 대부분의 내화성 유기물질만이 생태계로부터 궁극적으로 소실되고 나머지 유기탄소생산은 결국 생식먹이연쇄를 구성하는 생물에 의하거나 박테리아에 의해 호흡된다.
3-2 수계에서의 물질 순환 호흡에 의한 합성유기화합문의 완전한 분해나 이화작용은 안정된 수계 를 유지하는 데 필수적이다. 평균하여 생산량이 호흡량을 초과하는 시스 템에서는 광합성 산물이 동 • 식물의 생체량이거나 데트리터스의 어느 형 태이든지 시스템 내에 축적된다. 결국 그 시스템은 유기퇴적물로 충만될 것이다. 실제로 담수역과 일부 해역에서는 극단으로 느리긴 하나 정확하 게 이러한 과정이 진행된다. 이 유기 찌꺼기의 축적은 제 1, 제 2, 또는 그 이상의 영양단계 생산의 일부 산물이 보다 내화성이고 박태리아나 영 양단계상의 다른 생물에 의해 효과적으로 분해되지 않는 데 기인한다. 만일 호흡이 생산을 초과한다면 이때는 생체량의 순소바가 그 시스템 내 에서 일어나게 되고 이러한 경우에는 의부 유입, 예컨대 강의 유출 등에 의해 보충되지 않으면 시스템이 존속할 수가 없게 된다. 호흡과 분비과정에서 기인하는 산물이 실제로 어떤 생물, 특히 석물과 박테리아에게 먹이원이 된다는 사실을 인식하는 것은 중요하다. 예컨대 호흡의 직접 산물인 CO2 는 광합성에 대한 탄소원이며 많은 해양생물이 분비하는 암모니아는 단백질과 아미노산 생산에 있어 질소원으로서 식물 에 의해 직접 동화된다. 박테리아는 이미 설명한 바와 같이 먹이원으로 서 용존형태 또는 입자형태의 분비산물을 이용한다. 노폐물은 그것을 생 산하는 생물에게는 흔히 유독하지만 위에서 지적한 바와 같이 균형이 잘 잡힌 생태계에서는 끊임없이 먹이원으로 이용되기 때문에 결코 높은 농 도에까지 이르지 않는다. 따라서 박데리아 및 기타 분해자(分解者, decomp o ser) 생물은 생식먹이연쇄에서 생산된 유기 노폐물을 소비함으로 써, 그리고 식물의 먹이인 무기 영양소를 생산하도록 이 노폐물을 대사 시킴으로써 해양생태계에서 결정적인 역할울 담당한다. 식물은 다시 이 무기 영양소를 이용하여 고에너지 유기 생체량을 생산한다. 유기 생체량 은 생식먹이연쇄의 경로를 따라 궁극적으로 데트리터스나 용존유기화합 물을 만들어 분해자 생물에게 이용된다.
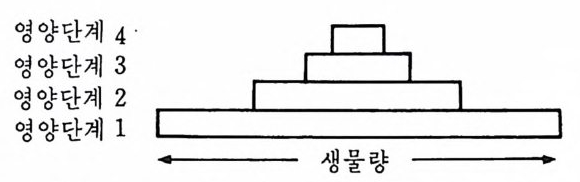
대부분의 수계에서는 물질의 재순환으로 인해서 도입된 영양소가 축적 되는 경향을 갖 는다. 유실이나 퇴적작용으로 영양소의 완전한 제거가 이 루어지지는 않는다. 이러한 영양소 및 유기물질의 축적과 퇴적에 의해 깊은 수심에서 증가하는 것은 모든 수생 생태계에서 실제적으로 일어나 는 자연적인 과정이며 이를 부영양화( 富營養 化, eu t ro p h ic a ti on) 라고 부른 다. 인간활동에 의해서, 죽 고농도의 영양소를 함유하는 생활하수의 투 기에 의해서 부영양화 과정이 가속되는 것은 문화적 부영양화 cultur al eutr op h ic a ti on 라 한다 (Laws, 1981) . 이 문화적 부영 양화의 사례 들은 해 양 오염 가운데에서 가장 일반적이고 광범위한 문제들을 제기한다. 3-3 생태적 피라밋 생태전이효율이 10~20% 에 불과하기 때문에 한 영양단계에서 그 다음 영양단계로의 먹이 유전은 먹이연쇄의 각 단계마다 일정하게 감소한다. 이러한 먹이의 손실은 궁극적으로 먹이연쇄 내의 영양단계의 수를 불가 피하게 제한시킨다. 왜냐하면 종국에 가서는 추가되는 영양단계를 유지 할 만큼 충분한 먹이가 남지 않게 되기 때문이다. R yth er (1 969) 는 의해 역의 해양먹이연쇄에는 대체로 5~6 개의 영양단계를, 그리고 연안해역과 용승( i勇 昇)해역에서는 각기 4 개 및 2~3 개의 영양단계를 유지하고 있음 울 계산한 바 있다. 먹이연쇄의 길이에 관계없이 더 높은 영양단계로 올 라감에 따라 먹이흐름의 일정한 감소는 연속적으로 더 높은 영양단계에 있는 생물의 총생체량의 감소를 초래한다. 따라서 각 영양단계의 총생산
 영영양양단단계계 42 三
영영양양단단계계 42 三
그림 3-1 가설상의 먹이연쇄에서 각 영양단계의 생체량
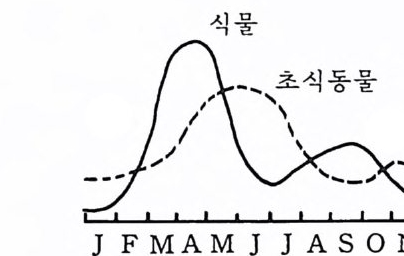
량을 그 양에 비례하는 막대로 표시하여 수평으로 놓는다면 그립 3-1 에 서 보는 바와 같이 피라밋 형태들 갖게 되는데 이것을 생태적 피라밋이 라한다. 생물량의 생태적 피라밋 개념을 이해하기 위해서는 두 가지 설명으로 정리할 수가 있다. 첫째 비정상상태 non-ste a dy sta t e 인 시스템에서는 2 개 혹은 그 이상의 영양단계상의 생물량 분포가 일시적으로 전도되는 일이 아주 보통이다. 다시 말하면 영양단계 생물량이 영양단계의 수가 증가함 에 따라 감소하기보다는 오히려 증가한다. 예컨대 온대 해양에서는 소위 식물 생물량의 대증식이 수온과 평균 일조량(日照 蓋 )의 증가가 나타나는 봄철에 일어날 수 있다. 이 식물 대증식은 일반적으로 초식동물 생물량 이 클 때에는 일어나지 않으며 초식동물의 생물량은 오히려 먹이생물의 증가에 칙접 반응하여 참시 뒤에 증가가 시작된다. 일반적으로 초식동물 의 섭식은 식물 생물량을 낮은 수준까지 감소시키는 반면, 초식동물의 생물량은 최고치에 달한 다음 떨어지게 된다. 초식동물 생물량의 감소는 초식동물의 먹이의 감소와 일차육식동물의 포식압력 등 두 가지 원인에 기인한다. 그립 3~2 는 식물과 동물의 생물량이 시간의 경과에 따라 변화 하는 것을보여준다. 그림 3-2 에서처럼 식물의 대번식에 뒤따라 짧은 기간 초식동물 생물량 이 식물의 생물량보다 더 커지는 시스템은 대규모로 계절적 순환을 겪는 많은 수계(水系)에서 나타나는 현상이다. 이 기간 동안 최초의 2 개 영양
 식물
식물
그립 3-2 온대 해양생태계에 나타나는 계절에 따른 식물과 초식동물의 생물량 변화
단계의 생물량은 전도된 피라밋을 형성한다. 왜냐하면 제 2 영양단계 생물 량이 제 1 영양단계의 그것보다 크기 때문이다 . 이러한 상황은 짧은 기간 지속되고 전체적으로는 그림 3 -1 에서처럼 정상적인 양상으로 되돌아간다. 생태적 피라밋에 관한 두번째 설명은 각 영양단계를 구성하는 생물의 크기와 관련된다. 일반적으로 포식생물은 먹이생물보다 클 것이고 따라 서 고영양단계의 생물이 저영양단계의 생물보다 더 커야 된다고 생각하 는데 이것은 일반적으로 실제 현상과 일치한다. 그 결과 연속적인 영양 단계 중 상위 단계에 있는 생물의 수는 총생물량보다 더 빨리 감소한다. 대체로 대형인 생물이 소형인 생물보다 더 많은 먹이를 소비하는 것이 사실이지만 단위 생물량당 먹이의 소비로 보면 대형생물이 소형생물보다 더 적게 소비하는 것도 일반적인 사실이다. 생물의 크기와 대사율 간의 관계를 보면, 두 생물이 크기(또는 무게)에 있어서 104 인수의 차이가 있 울 경우에, 대형생물이 소형생물에 비해 단위체중당 먹이를 10% 만울 소비한다고 기대할 수 있다. 바꾸어 말하면 대형생물은 소형생물보다 103 배 의 먹이를, 또는 단위 무게당 먹이를 103/104 0 / 10 ) 만큼 소비할 것이다. 두 연속적인 영양단계에 속하는 개체생물의 크기가 104 인수의 차이를 갖고, 영양단계간의 생태효율이 10% 인 경우를 생각해 본다면 두 영양단 계의 총생물량이 같아지는 안정상태의 상황이 존재할 수도 있을 것이다. 즉, 제 2 영양단계가 제 1 영양단계의 IO% 만을 받는다 해도 제 2 영양단계는 그것으로 주어전 생물량을 유지할 수 있을 것이다. 따라서 생물량의 생 태적 피라밋을 기대하는 논리적 주장은 연속적 영양단계상의 생물 크기 가 심하게 차이가 나는- 먹이연쇄에는 적용할 필요가 없다. 왜냐하면 그 러한 주장은 모든 생물의 단위 생물량당 먹이 요구가 동일한 것으로 가 정한 것이기 때문이다. 어느 정도 한정된 정보를 토대로 해서 보면 대부 분의 자연상의 먹이연쇄에서 생태적인 피라밋이 나타나는 것으로 보이는 데 이는 연속적인 영양단계에 있는 생물 크기의 차이가 낮은 생태효율을 상쇄시킬 만큼 크지 않음을 의미한다. 그럼에도 불구하고 연속적인 영양 단계 생체량에 있어서의 차이는 흔히 5~10 인수 이하이며 이것은 모든 생물이 단위 생물량당 동량의 먹이를 요구한다면 10~20% 의 생태효율을 .
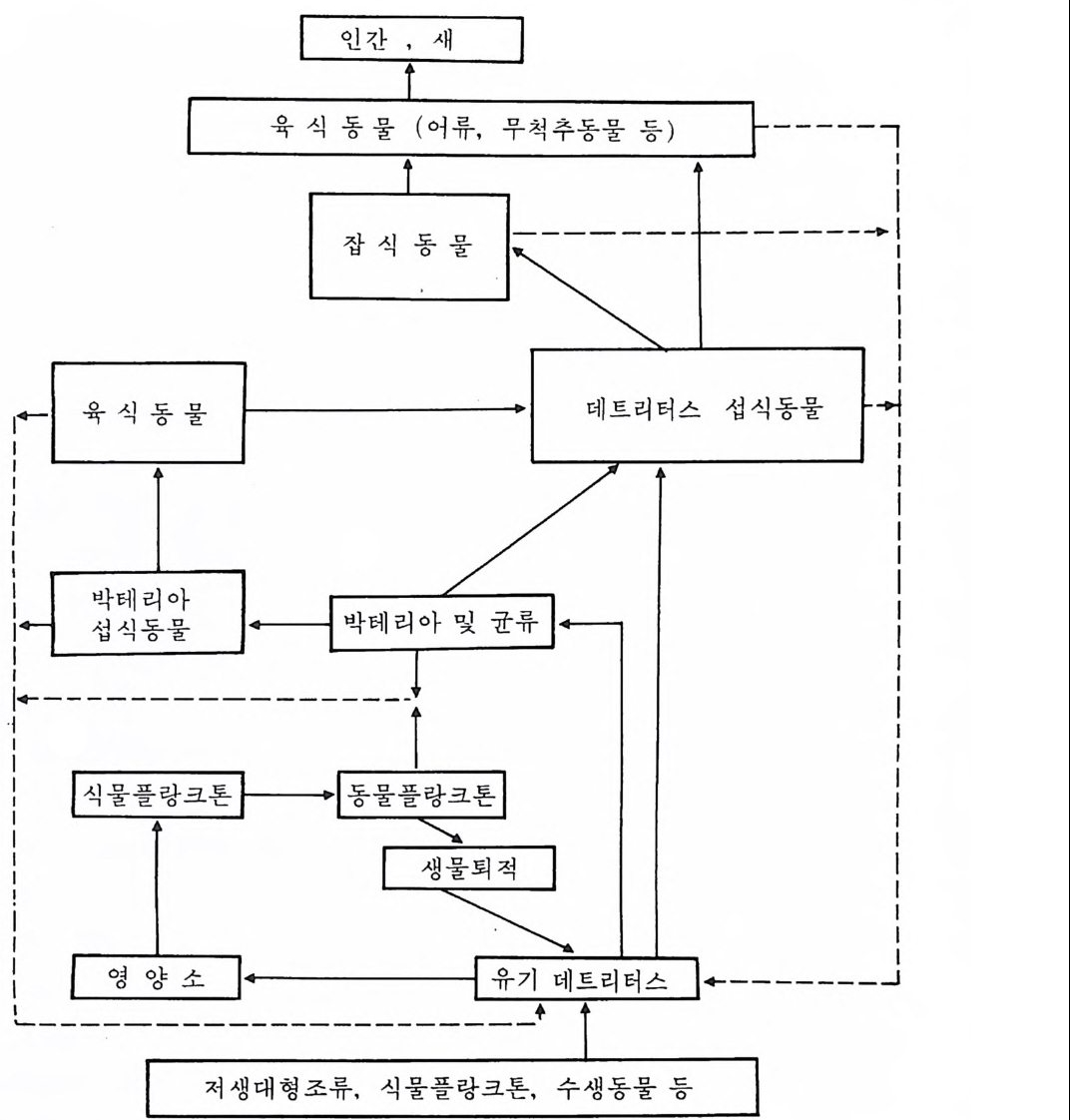
나타낼 것으로 기대할 수 있다. 따라서 생물 크기의 차이는 영양단계의 생물량구조에 대한 낮은 생태적 효율의 효과를 배제하는 것이 아니고 감 소시키는 경향이 있다. 3-4 먹이망의 구조와 물질의 농축 간단한 먹이연쇄 모델은 생태학적 문제를 검토하기 위한 개념적 기초 로서 발전한 것이므로 자연계가 실제로는 그렇게 단순하지 않다는 사실 울 상기할 필요가 있다. 대다수 동물의 섭식행동은 동물이 유일한 영양 단계에 매달리게 하지 않는다. 새우 같은 일부 동물은 식물, 데트리터스 및 기타 동물을 포괄해서 삼킬 수 있는 것은 거의 다 먹는다. 이처럼 일 상 먹이를 구별하지 않는 동물을 잡식동물(雜食動物, o mni vore) 이라고 한 다. 이들은 분명히 하나나 두세 개의 영양단계에 매이지 않는다. 또 다 른 생물은 어린 시기에는 제 1 영양단계에서, 후기 성장단계에서는 제 2 영 양단계에서, 그리고 성체는 제 3 영양단계에서 먹이를 취한다. 이러한 경 우에 그 종의 각 성장단계는 유일한 영양단계에 매이는 것처럼 상이한 생물로서 취급하지 않으면 안 될 것이다. 확실히 많은 생물의 섭식습관 은 이용할 수 있는 여러 가지 먹이의 종류와 양에 의해 영향받는다. 그 림 3-3 은 해양에서 발견되는 복잡한 섭식관계를 나타낸 것이다. 이와 같은 섭식관계를 표시하는 선의 양상이 일종의 망을 형성하기 때 문에 섭식양식은 먹이망으로 알려지게 된 것이다. 확실히 먹이망은 먹이 연쇄에 의한 것보다 훨씬 더 복잡한 시스템을 나타낸다. 그러므로 먹이 연쇄론으로부터 유도된 관계들이 훨씬 더 복잡한 것으로 생각되는 실제 상황에 적철한가 하는 의문이 제기될 수도 있다. 이점에 대해서는 다음 의 설명이 해답이 될 수 있을 것이다. 첫째로 많은 생물이 하나 이상의 여러 영양단계에서 먹이룰 취하는 것 이 사실이지만, 많은 생물이 한 종류 또는 다른 종류의 먹이에 대하여 선택성을 보이고, 따라서 일차적으로 하나 또는 두 개의 영양단계에 속
 인간 , 새
인간 , 새
그림 3-3 내만해역에서 나타나는 먹이망의 모식도
하고 있음을 합리적으로 정의할 수 있음도 또한 사실이다. 비록 이러한 원칙에 예의는 있지만 개념에 영향을 줄 만큼 많지는 않다. 둘째, 아마 더 중요한 것은 영양단계 이론의 일부 의미는 특정 생물이
특정 영양단계에 매이도록 유일한 단계를 요구하지 않는다는 사실이다. 먹이생물의 큰 비율이 포식자에 의해 호흡되거나 분비된다는 생각은 먹 이생물과 포식자의 일치와는 관계없이 유효하다. 따라서 이론상 먹이는 식물에 의해 생산되고 한 영양단계에서 다음 영양단계로 일련의 먹이전 달을 통과하며 이때 각 전달과정에서 대략 먹이의 80~90% 가 호흡되거 나 분비된다. 그러므로 평균적으로 이러한 전달과정 m 개를 통과한 먹 이의 생물량은 m-1 개의 전달과정을 통과한 먹이의 생체량보다 훨씬 적 을 것은 당연하다. 특정 생물이 특정 생물을 먹이로 한다는 의미로서가 아니고 일련의 먹이전달의 의미로 영양단계를 생각한다면 각 생물이 유 일한 영양단계에 매인다는 문제는 사라질 것이다. 이러한 두번째 설명에도 불구하고 특정 생물에 대한 오염물질의 영향 이 먹이연쇄상의 생물의 위치와 관련해서 종종 논의됨을 볼 수 있을 것 이다. 이러한 논의에 대한 먹이연쇄론의 적절성은 위의 설명 중 첫번째 에 근거를 두고 있다. 예컨대 펠리컨이라는 새는 동식물 플랑크톤이나 작은 새도 먹지 않고 고래, 돌고래 또는 강치도 먹지 않는다. 오히려 펠 리컨은 그 입으로 편하게 떠올릴 수 있는 수십 cm 크기의 어류를 먹는 다. 따라서 펠리컨은 대체로 제 5 영양단계에 매일 수 있다. 흠잡을 데가 없는 것은 아니지만 이와 같은 합리화는 크게 오류를 범하지 않는다. 하 지만 먹이연쇄 논쟁이 일어날 때마다 이 이론의 결점이 없지 않다는 것 과 일부 생물의 섭식관계가 극단으로 복잡할 수 있다는 것을 유념하여야 한다. 먹이연쇄론을 적용함에 있어서 가장 중요하고 논쟁의 여지가 있는 것 은 어떤 고영양단계 생물의 체내에 들어 있는 수은, 방사능물질, 살충제 갇은 오영물질의 농도를 설명하는 일이다. 단순한 먹이연쇄를 형성하고 있는 영양단계 중에서 오염물질 농도의 분포를 상세히 시험할 수 있는 경우에 그 결과는 종종 영양단계의 수가 증가함에 따라 농도가 일정하게 증가하는 것을 보여준다. 표 3~1 은 이와 같은 예로서 해수와 여러 생물 체 내에서의 살충제인 DDT 의 농도를 보여주는데 이는 미국 뉴욕주 롱 아일랜드의 해안 소택지에서 조사된 것이다. DDT 의 잔류량은 플랑크톤
표 3-1 해안 소태지 생물의 DDT 잔류량 생물 DDT 잔류량 (ppm ) 물 0.00005 플랑크톤 0.04 색줄멸잉어 0.23 양놀래기 잉어 0.94 강꽁치(포식어류) 1. 33 실고기(포식어류) 2.07 왜가리 3.57 제 비갈매기 3. 91 재갈매기 6.00 물수리알 13.8 비오리 22.8 가 nHL 지 26. 4 으로부터 소형 어류, 대형 어류, 그리고 어류를 먹는 새종류에 이르기까 지 일정하게 증가한다. 플랑크톤에서 어류를 먹는 새까지의 농도의 증가 는 약 600 배에 달한다. 이러한 관찰은 일부 먹이연쇄상의 고영양단계에 서 오염물질 농도가 증가하는 일반적인 기작이 있다는 근거가 되었다. 이러한 현상을 먹이연쇄 농축 또는 생물학적 확대 bio lo g ica l mag nifica - ti on 라 부른다 .. 생물학적 확대에 대한 논리적인 설명은 한 생물의 먹이와 함께 섭취된 어떤 오염물질이 먹이 생체량처럼 효과적으로 호흡되거나 분비되지 않는 다는 것을 가정할 경우 먹이연쇄론으로 쉽사리 가능해진다. DDT 는 그 러한 오염물질의 좋은 예이다. 왜냐하면 이 화합물은 생물학적 분해에 저항성을 갖고 있을 뿐만 아니라 생물이 대사에 사용할 수 없는 다른 노 폐물과 함께 직접 배출되기보다는 생물의 지방조직에 축적되는 경향이 있기 때문이다. 위의 DDT 를 예로 들면 영양단계간의 생리적 효율은 10 %이지만 DDT 는 호흡과 분비에 대한 저항성 때문에 그 효율이 50% 나
된다. 결국 포식자 속에서 정상상태의 DDT 농도는 먹이생물 속에서의 DDT 농도보다 5 배나 크게 될 것이다. 왜냐하면 포식자는 자신이 먹는 먹이 속의 잔류량보다 5 배 많은 양을 잔류시키기 때문이다. 이 과정이 3 개 영양단계 전달을 통해 되풀이된다면 제 4 영양단계 중의 DDT 농도는 제 1 영양단계의 DDT 농도보다 정 (625) 배로 늘어날 것이다. 이러한 종류의 합리화가 충분히 논리적이지만 위에 설명한 생물학적 확대가 실제로 일어난다고 보장하지는 못한다. 표 3-1 에 보인 오영물질 의 농축 경향은 생물학적 확대와는 매우 다른 기작으로 발생할 수도 있 울 것이다. 주의깊게 고안된 실험으로써만 이러한 농축 경향의 가능한 이유를 가려낼 수 있을 것이다• 중요한 점은 생물학적 확대 이론의 장단 점을 주장하는 것이 아니라 먹이연쇄의 특칭에 관한 지식이 얼마나 시험 할 가치가 있으며 오염물질 영향에 관한 논리적인 가설을 유도할 수 있 느냐를 보이는 데 있다. 건전한 생태학적 원리를 바탕으로 한 이러한 종 류의 논리적 사고와 가설검증은 해양오염에 관한 문제를 연구하고 해결 함에 있어 최선의 방법을 제시한다.
제 4 장 해양의 일차생산량 4-1 일차생산량의 의의 해양식물은 다른 모든 해양생물을 위한 먹이의 주생산자로서 해양의 먹이연쇄상 특유하게 중요한 위치를 차지한다. 그러므로 일차생산율을 지배하는 여러 가지 요인의 연구는 환경 내에서 변화들이 어떻게 해양생 태계에 영향을 미치는가를 검토하는 데에 첫단계를 이룬다. 해양식물은 대부분 육상식물과는 아주 다르다. 해양 생태계에는 목본 (木本)이나 초본(草本) 식물이 매우 적다. 해안에 따라서는 홍수림(紅탑 林, mang rov e), 삼목(杉木 cyp re ss) 등이 성장하여 수생식물을 이루고 있으나 빛이 효과적으로 해저까지 두과하는 천해 수역에는 저생조류(底 生藩甄 benth ic al g ae) 가 가장 중요한 일차생산자(一次生産者 prima ry p roducer) 이다. 그러나 식물이 광합성을 수행하기 위해서는 빛이 필수요 건이기 때문에, 그리고 물은 빛을 흡수하고 산란시키기 때문에 뿌리를 가진 수생식물이 생존할 수 있는 깊이의 범위는 분명히 한정된다. 물속 에 부유하는 입자물질이 고농도로 존재하는 곳에서는 빛이 더욱 분산되 고 흡수되므로 물의 투명도가 훨씬 더 감소한다. 대양의 가장 맑은 수역 에서도 입사광(入射光)의 1% 만이 약 lOOm 까지 두과하고 맑은 연안 수 역에서는 l% 의 광투과 수심이 20m 미만이다. 대부분의 수생식물이 입
사광의 1% 이하에서는 효과적으로 광합성을 수행할 수 없기 때문에 해 양의 광합성 수심, 죽 전광충( 眞 光 層 eup ho ti c z one) 은 맑은 연안 수역의 경우, 수십 m, 그리고 가장 맑은 의양역에서도 150~200m 에 한정된다. 이처럼 투광 수심의 한계가 입자상, 혹은 용존 유기물질을 상당한 농도 로 포함하고 있는 수역에서는 분명히 감소될 수밖에 없다. 이와 같은 이 유로 저생조류나 뿌리를 가진 식물이 진광충 이상의 수심을 가진 수계에 서는 발견되지 않는다. 전세계 해양 표면적의 93% 이상이 180m 이상의 수심을 갖고 있으므로 저생식물이 해양 전체의 일차생산량에 기여하는 부분은 극히 적다. 이상의 설명에서 이해할 수 있는 바와 같이 수심이 깊은 바다의 표충 에서 발견되는 해양식물은 전광충 내에서 부유하는 능력을 갖고 있지 않 으면 안 될 뿐만 아니라 광합성에 요구되는 모든 필수 영양소를 물에서 직접 끌어낼 수 있어야 한다. 이러한 능력을 갖는 식물은 예의적인 대형 갈조류인 Sarg a ssum 을 제의하고는 대부분 현미경적인 단세포식물 un i cel lular pla nts 이 다 . 이 들 마 세 한 식 물은 식 물플랑크돈 ph y top la nkto n 이 라 부르며 그 크기는 수 µm 로부터 육안으로 볼 수 있는 2mm 까지의 범위 를 갖는다. 식물플랑크톤의 여러 종류는 개체 세포는 보이지 않으나 군 체 colony , 혹은 건 사슬 long chain 울 형 성 하여 쉽 게 눈에 띄 기도 한다. 이처럼 미세한 생물이 해양의 방대한 일차생산울 담당하고 각종 어류 같 은 상위 영양단계에 있는 육식동물이 간접적이지만 전적으로 의존하고 있음을 이해하는 것이 중요하다. 그러나 이들이 궁극적으로 모든 해양 먹이연쇄의 일차생산자로서 필수적인 역할을 갖고 있음에도 불구하고 식 물플랑크톤이 해수역에서 어떤 농도의 한계를 넘을 경우에는 심각한 문 제를 야기한다. 예컨대 적조(赤潮, red ti de) 는 전세계의 많은 수역에서 자주 발생 하는 현상으로 주로 쌍편모조류 (겠靴毛 溪 類, din o fl ag el late s ) 에 속하는 식물플랑크톤이 폭발적으로 대증식을 일으키는 데 원인이 있다. 적조를 일으킬 때의 쌍편모조류는 그 농도가 매우 높아 수 km 에 이르 는 해역을 붉게, 혹은 갈색으로 변색시키게 된다. 적조를 일으키는 쌍편 모조류는 신경독소 neuro t ox i n 를 해수로 분비하여 대량의 작은 어류를
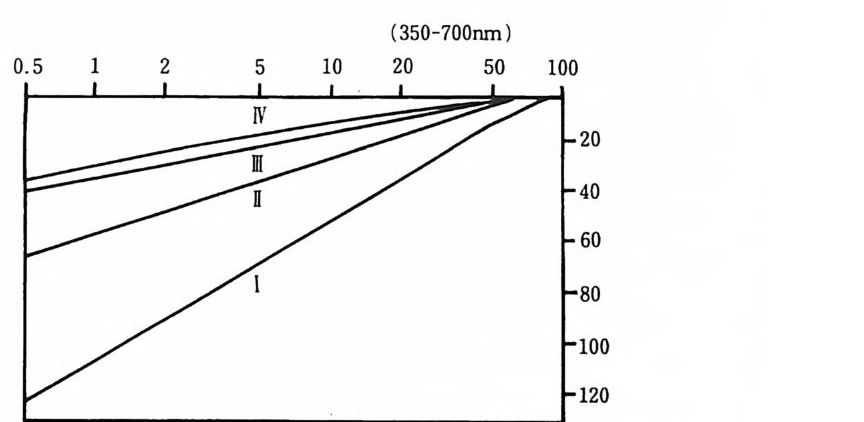
치사시키는 경우가 혼하며, 이 독소에 영향받지 않는 어패류에 농축될 수 있어서 결과적으로 어패류를 섭취하는 사람을 중독시키게 한다. 이 중독이 심한 경우에는 신경마비나 치사를 일으킨다. 식물플랑크톤 대증 식의 일부는 순전히 자연현상일 수 있으나 많은 경우 인간활동이 바람직 하지 않은 식물플랑크돈의 대증식을 유발하는 원인이 된다• 원하지 않은 석물플랑크톤의 과도한 성장을 자극하는 상태를 피하거나 바로잡기 위해 서는 식물플랑크톤의 성장률을 정상적으로 조절하는· 여러 가지 요인을 먼저 이해하는 것이 필수적이다. 4-2 해 %~l 서의 일차생산량의 제한 요인 빛이 해양환경에서 일차생산량을 제한하는 가장 중요한 요인임에는 의 심의 여지가 없다. 전 해양의 체적 중 95% 이상이 전광충 아래에 있고 따라서 석물의 생명을 유지시킬 수 없다. 그림 4-1 은 탁도가 다른 4 개의 해수역에서 수심에 따라 가시광선 (350~700nm) 의 감소를 나타낸 것이다. 가시광선만을 표시한 이유는 빛을 홉수하는 식물 색소가 가시광선 스펙
 (35 0-700run)
(35 0-700run)
그림 4-1 해주중에서 수심에 따른 가시광선의 감소 차례로 I. 가장 맑은 해수, IV. 연안해수(J erlov, 1976)
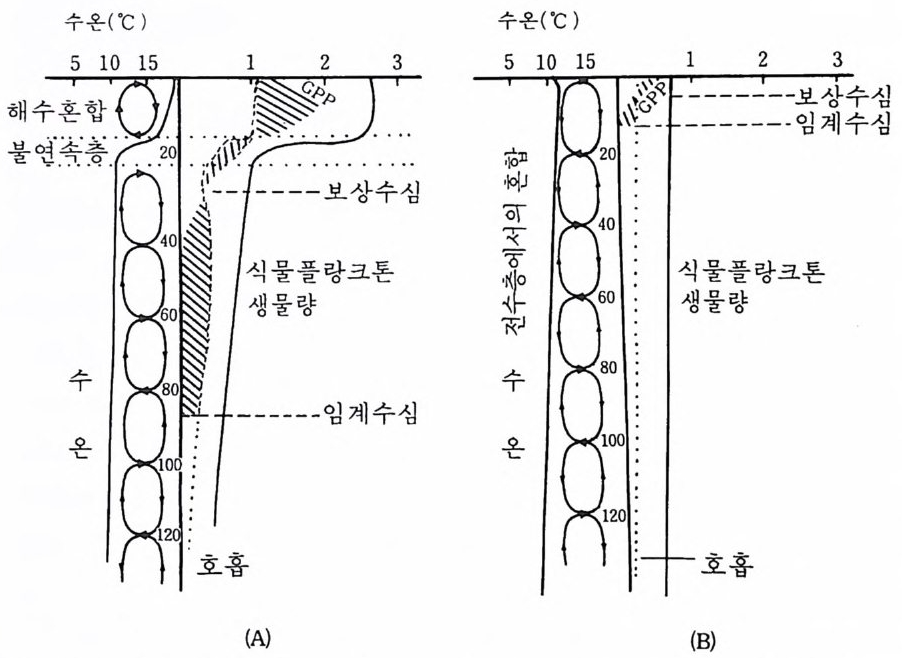
트럼의 어떤 부분을 홉수하는 데에만 효과적이기 때문이다. 예컨대 영록 소는 청색 및 적색광을 압도적으로 홉수한다. 실제로 가시광선의 모든 부분이 광합성에 동등하게 이용되는 것은 아니지만 가시광선의 총강도가 대략적으로 광합성에 이용될 광량의 편리한 척도가 된다. 위의 그림에서 알 수 있는 바와 같이 광도는 수충 내에서 수심에 따라 대체로 지수적으로 감소한다. 죽 처음에는 급속히, 그러나 길어짐에 따 라 보다 더 점진적으로 감소한다. 광합성률은 높은 광도에서, 특히 직사 광선에서는 저해받을 수 있으나 적절한 광도로부터 낮은 광도 사이에서 는 광합성이 거의 광도에 비례한다. 이러한 관계로 광이 일차생산울 제 한하는 범위 내에서는 식물플랑크톤의 성장률이 최적광도에 가까운 표면 근처에서 최대가 되지 않을 수 없다. 그러나 식물플랑크톤은 대부분이 운동능력을 갖고 있지 않으며 주로 난류(亂流)와 해류에 의해 수직 및 수평방향으로 움칙이기 때문에 수충 내에서 스스로 위치를 유지할 수가 없다. 해수 표면에서는 물위로 부는 바람이 파랑과 난류를 일으켜 수충 이 잘 혼합되고 이에 따라 식물플랑크톤의 농도가 균일하게 된다. 이 혼 합총mi xed-la y er 의 깊이가 전광총보다 얕으면 혼합총 내의 식물플랑크톤 에 의한 생체량의 총생산이 호홉과 분비에 의한 손실보다 커지게 되고 결과적으로 식물생체량의 순생산량 ne t p roduc ti on 은 초식동물을 위한 먹 이를 마련하거나 식물플랑크톤의 현존량을 증가시키게 될 것이다. 수충 내에서 총생산량이 식물플랑크톤의 호흡과 분비에 따른 손실과 정 확히 균형 을 이루는 깊이를 보상수심 (補償水深, comp en sati on dep th) 이 라고 하며 혼합충의 수심이 보상수심과 같아전다면 그 깊이에서는 순생 산량이 없을 것이다. 그러므로 전광충의 하한(下,長)은 논리적으로 보상 수십이라고 정의할 수 있다. 만일 혼합충이 보상수심보다 깊다면 혼합총 의 식물플랑크톤이 평균해서 호흡과 분비로 손실되는 생체량보다 더 적 은 양을 생산하게 될 것이며 그 결과 식물플랑크톤의 현존량이 일정하게 감소할 것이다. 이 감소하는 상태는 분명히 무한정 존재하지 못하고 식 물플랑크톤이 남지 않는 수충이 생길 것이다. 식물플랑크톤이 더 이상 생존할 수 없는 이 와 갇은 수십 울 임 계수심 (臨界水深, cri tica l dep th) 이 라
고 한다• 그러나 연안성 식물플랑크론 가운데 많은 종은 임계수심 이하 에서도 생존할 수 있는데 이는 이들 종이 모든 대사과정을 국소화시켜 부적절한 환경조건을 극복하는 휴면포자(休眠胞子, restin g s p ore) 를 형성 하는 능력을 갖고 있기 때문이다. 그림 4-2 는 혼합충이 보상수심 아래로 확대되었을 때 총생산량, 호흡 량, 생체량 등과 수심과의 관계를 나타낸 것이다 . 생산량은 수충을 통해 서 광도에 비례하는 것으로 가정한다. 이 그림에서 생산량은 보상수심 위에서는 양으로 나타나고 아래에서는 음으로 나타난다. 인간활동과 관 련 있는 오염의 어떤 종류는 해수의 탁도를 증가시킴으로써 전광충의 깊 이룰 감소시킨다, 예컨대 매립이나 건설현장에서 흘러나온 부유물질은 해수를 몹시 흐리게 하고 따라서 광합성에 필요한 광량을 크게 감소시킨
 수온 (· C ) 수온 (·C )
수온 (· C ) 수온 (·C )
그립 4-2 식물 플랑크톤의 수직 분포, 부상수심 및 임계수심에서의 변화를 나 타내는 그림. (A) : 늦여름, (B) : 늦가을, GPP : 총일차생산량 (Tait , 1981)
다. 이 경우에 식물플랑크톤의 개체군(個 體 群)은 남조류 (blue- gr een alga ) 로 우점될 수 있다. 이들 조류는 많은 종류가 부유성이 높은 특수한 기 포( 氣 胞)를 갖고 있어서 세포체를 해수의 표면 근처에 유지시킬 수가 있 다. 이 남조류는 특히 해안선을 따라 분포되었을 때 미관상 악영향을 미 친다. 식물의 필수 성장 영양소가 진광충으로 첨가되어 식물플랑크톤의 생산 을 과도히 자국하게 되면 해수 투명도의 변화보다도 조류에 의한 오영문 제가 빈번히 발생한다. 전광충에서의 식물플랑크톤 생체량이 빛에 이어 서 성장에 필수적인 어떤 영양소의 유용성에 흔히 크게 지배되기 때문에 영양소의 유입에 있어서의 변화가 식물플랑크톤의 생산량과 조성에 민감 하게 작용한다. 만일 영양소가 제한받는 식물플랑크톤 군집에 대해서 그 공급이 증가하면 영양소 공급량에 대체로 비례해서 생산량과 생체량이 증가할 것이다. 만일 빛이 부족하여 충분한 영양소가 있음에도 광합성을 할 수 없는 무광충에 이러한 영양소가 첨가된다면 분명히 식물플랑크돈 의 생산량이 즉각적으로 증가하지 않는다. 그러나 무광충의 해수가 후에 전광총으로 혼합되어 들어오면 결과적으로 표충에서 생산량이 증가하게 되며 이러한 과정은 모든 수생 생태계에서 때로 느리기는 하나 규칙적으 로 일어나는 현상이다. 통상 1 종류 혹은 2~3 종류의 영양소가 일정한 시간범위 내에서 식물풀 랑크돈 생체량 생산을 제한하는 것이 사실이지만 이들 영양소의 검증은 용이한 일이 아니다. 표 4-1 은 식물에게 필수적인 것으로 알려진 화학 영 양소를 추린 것 이 다. 다량영 양소 macro-n u tr ien t 는 미 량영 양소 micr o- nu tri en t에 비하여 상대적으로 더 많이 요구되는 영양소이다. 다량영양 소 가운데에서 C, H, O 는 탄수화물, 단백질, 지방 동의, 유기화합물을 구성하는 필수 성분이므로 가장 많은 양을 필요로 한다. N 과 P 는 다소 적게 요구된다. N 은 단백질, 핵산 및 일부 색소 chloro p h y ll 의 필수 성 분이며, P 는 포스포리피드p hos p ho lipi d 와 당인산염 sug a r p hos p ha t e 을 생 산하는 데 필요하다. 그 위 에 P 는 ATP adenosin e triph osph ate 와 같 은 분자상 고에너지 인산염결합을 형성하는 데 요구된다. 이 고에너지
표 4-1 식물체에 필수적인 다량영양소 및 미량영양소 필수다량영양원소 기호 필수미량영양원소 기호 산소 。 망간 Mn 탄소 C 동 Cu 질소 N 아연 Zn 기^- 4/- H TU T./ . L. B 유인황 sP 몰리규브소덴 MSio 칼륨 K 염소 CI 마그네슘 Mg 닙}나듐 V 칼슘 Ca 코발트 Co 철 Fe 나트륨 Na 자료 : Odum, 1971 결합은 일차적으로 유기분자의 단계적 분해로부터 유래하는 소량의 에너 지에 대한 편리하고 필수적인 단위이며 대사과정에 필요한 에너지원으로 서 생물이 언제든지 사용할 수 있는 것이다. 나머지 다량영양소는 식물 에 의해 보다 적은 양이 이용된다. M g은 chloro phy ll 구성의 필수 원소 로서 특별히 중요하다. 미량영양소는 많은 경우에 대사반응을 가~합]키 는 촉매로서 작용하는데 최소량이 요구된다. 이들 촉매는 스스로 조정하 는 반응에 의해 소비되거나 변화되지 않으므로 생물에 의해 소량만이 요 구되는 것이다. 표 4-1 에 열거한 필수영양원소에 대한 식물의 상대적인 요구량을 알면 이들 중 어느 원소가 식물플랑크톤 생체량을 가장 제한하기 쉬운가 하는 의문이 제기된다. C, H 및 O 는 최대량이 필요하지만 이들 원소는 물과 이산화탄소에서 쉽게 얻어진다. 해양에서 물의 결핍이란 있을 수 없고 이산화탄소는 대기중에서 발견되는 기체로 물속에 용해하여 대기중의 농 도와 비례적인 농도로 평형을 이루고 있다. 따라서 해수의 화학적인 작 용은 해양에서 광합성을 유지하기에 충분한 이산화탄소를 언제나 공급해
준다. 다시 말하면 대기는 해수계 혼 합총에 대한 C 아의 저장소의 역할 울 하고 대기로부터 해수로의 CO2 흐름은 비록 해수중의 CO2 농도가 낮더라도 식물플랑크톤이 광합성을 수행하는 데 필요한 CO 2 를 쉽사리 마련하기 때문에 자연적인 해양상태계에서 CO2 가 식물플랑크톤 생체량 을 제한하는 일은 거의 없다고 하겠다. 표 4-2 는 해수와 강수에서의 다량영양소 및 미량영양소의 평균 농도에 대한 자료이다. S(S0 4 2 - 의 형태로서), K, Mg , Ca, Cl 및 Na 는 해수중의 농도가 l03µM~5X l 05µM 범위에 있는 주요 염 salt 이 다. 바다에서 이둘 원소가 광합성을 제한한다는 증거는 없다. 미량영양원소는 대부분 다량 영양원소보다 훨씬 농도가 낮은데 역시 이 낮은 농도가 식물플랑크톤을 자주 제한한다는 증거는 거의 없다. 이는 필시 대부분의 미량영양원소가 국미량으로 요구되기 때문일 것이다. 예컨대 식물플랑크톤 중 규조류 표 4-2 주요 원소의 강수 및 해수에서의 평균 농도(농도단위 : µmol/l ) s 116 29,000 K 59 10,700 Mg 169 54, 6 00 Ca 38 10,550 Fe 12 0.05 Mn 0.10 0. 04 Cu 0. 08 0.05 Zn 0.15 0. 08 B 0.93 417 Si 143 36 Mo 0. 01 0.10 Cl 226 560,000 V 0.02 0.03 Co 0.003 0.001 Na 391 480,000 자료 : Ril ey and Cheste r , 1971
d i a t om 는 세포내용물을 감싸고 있는 규산염으로 된 정교한 각(穀)을 형 성한다. 때문에 규조의 Si0 2 요구량은 다른 식물플랑크톤 종류보다 훨씬 더 많다. 비록 규조류가 해양환경에서 분포함에 있어서 S i 02 의 이용성에 의해 영향받을 수는 있다하여도 해수의 Si0 2 농도가 해양규조류 생산울 한정한다는 증거는 없다. 2 개의 필수 영양소인 N 과 P 는 해수의 전광충 아래에서는 농도가 각 각 35µM 및 2~3µM 로 나타난다. 그러나 전광충 내에서, 특히 광합성 에 필요한 충분한 빛이 투과되는 여름철에는 N이 0.5~1 .O µM, P 가 0.lµM 정도이며 이는 다른 다량영양원소의 평균농도보다 낮은 값이다• 따라서 관측농도를 토대로 고찰하면 N 과 P 가 광합성을 가장 제한하는 영양소이기 쉽다. 그러나 많은 미량영양원소가 전광충 내에서 극단으로 낮은 농도로 존재하기 때문에 간단히 측정된 영양원소농도를 기초로 해 서 N, P 또는 미량영양원소의 하나가 일차생산을 제한한다고 결론짓기는 상당히 어렵다. 따라서 어떤 영양원소가 식물플랑크톤 생산을 제한하는 지롤 결정하기 위해서는 생물학적 정량검정 bio a ssay t es t에 의존하게 된 다. 이것을 영양원소 강화실험 nutr ien t enri cl unent exp e rim ent 이라고도 부른다. 4-3 영양원소의 실험적 배경 영양원소 강화실험에서 보통으로 취하는 방법은 정량적으로 측정될 해 수를 일련의 깨끗한 플라스크에 채우고 식물플랑크톤 생산에 어떤 영향 울 미치는지 알고자 하는 여러 영양원소로써 몇 개의 풀라스크를 보강하 는 것이다. 어떤 경우에는 해수를 여과하여 식물플랑크톤과 기타 생물을 제거한 뒤에 특정 식물플랑크돈 종의 단종배양(單種培養, monocul t ure) 을 한다. 또 다론 경우에는 해수를 여과하지 않고 자연 식물플랑크톤 군집 이 검정개체군(檢定個體群, tes t p o p ula ti on) 이 된다. 영양원소를 강화한 다음 플라스크를 적절한 빛 및 온도 조건하에서 배양하며 식물플랑크톤
생산은 영양소가 강화된 풀라스크와 강화되지 않은 대조 풀라스크를 통 해 일정기간 동안 다음의 방법으로 감시한다. 감시방법의 첫째는 식물플랑크톤의 생물량 측정인데 통상 세포수를 계 수하거나 클로로필 농도를 측정한다. 이때 영양원소의 영향은 강화된 것 과 대조구와의 생체량 차이로서 결정된다. 두번째는 각 풀라스크 속의 실제 광합성률이 영양원소 강화 후 일정기간(대략 1 일 ~1 주일)이 지난 뒤 에 측정된다. 이 양 방법에는 일장 일단이 있다. 만일 검정 개체군이 자연 식물플랑 크돈 군집으로 구성되어 있다면 풀라스크 속의 군집조성이 며칠 뒤에 변 화하였음을 흔히 보게 된다. 이러한 변화는 일부의 종이 인위적인 조건 하에서 분명히 찰 성장하지 못하고, 또 영양원소 강화가 모든 종을 동등 하게 자극하지 못하는- 수가 있기 때문에 일어난다. 생산량 실험이 자연 군집의 영양원소 제한 측정을 잘못 나타낼 수도 있다는 논의는 이 때문 에 가능하다. 즉, 영양원소 강화 플라스크 내의 상대적인 광합성률이 강 화 후에 크게 변화할 수도 있는데 이는 어떤 강화에 대한 식물플랑크톤 의 반응에 있어서 지연이 있을 수 있는 반면에 다른 강화는 생산량이 급 속히 증가하고 후에 감소하는 있기 때문이다. Menzel(1963) 등에 의하면 Sarga sso 해의 해수로써 행한 실험의 결과, N, P, Fe 로 강화된 플라스 크 내에서 수일 배양 후의 광합성률이 N 과 P 만 첨가한 것보다 충분히 높았기 때문에 처음에는 Fe 가 제한한 것으로 믿었으나 후에 Al 의 첨가 가 Fe 의 첨가와 거의 같은 효과를 일으킨다는 것과, 약 1 주일 배양 후 에는 N 과 P 만 첨가한 풀라스크가 N, P, Fe 를 첨가한 것과 같은 광합 성률을 나타냄울 발견하였다. 따라서 연구자들은 N 과 P 가 주요 제한 영양원소이고 Fe 나 Al 의 첨가는 N 및 P 의 첨가에 대한 식물플랑크톤 의 반응을 가속화시키는 것으로 결론지었다. 이 예는 영양원소 강화실험 의 결과가 조심스럽게 해석되어야 할 필요성, 그리고 확실하지 않은 결 론에 쉽게 이르는 것을 주의깊게 피해야 할 이유를 설명해준다. 영양원소 강화실험은 다음과 같은 요인들에 의해서 복잡하게 될 수 있 다.
® 강화된 풀라스크 내에서 배양할 때 시간에 따른 종조성상의 가능한 변화성. ® 상이한 영양원소 첨가에 대한 반응에 있어서 동일한 개체군의 시간에 따 른 변화성• ® 영양원소 첨가에 대응하는 세포조성 상의 변화성. 그러나 이러한 복잡화는 강화실험이 주의깊게 계획되고 강화된 풀라스 크를 자주 감시한다면 어려운 문제가 아닐 뿐만 아니라 실상 이러한 복 잡화는 연구자에게 유용한 통찰력을 제공하기도 한다.
제 5 장 오염물질의 독성 앞서 설명한 유기성 폐기물은 박태리아의 분해를 받게 되어 있으며 수 역이 과도한 폐기물이 쌓이면 용존산소 농도가 극히 낮아짐으로써 환경 이 손상된다. 또한 해저나 호수의 바닥은 유기물질로 덮히게 되어 환경 으로부터 저생동물을 제거시킨다. 그러므로 유기성 폐기물의 주 위험은 자연자원의 손상 가능성이다. 그러나 오염물질 가운데 독성을 갖고 있는 물질은 다른 문제를 제기한다. 이러한 물질은 박테리아의 공격이나 기타 분해의 대상이 되지 않으며 이들이 존재할 경우, 실제로는 해양환경에 대한 영구적인 증가를 나타낸다. 이러한 범주에 드는 물질들은 ® 수은, 카드뮴, 구리, 아연, 납 등과 감은 중금속. @ DDT 와 die l dri n 을 포함하는 할로겐화탄화수소물 및 pol yc h lori na te d bip h eny l( PCB) 군에 속하는 공업용 화학물질들을 말한다. 동물과 식물은 체내에 금속함량을 조철하는 능력에 있어서 광범위한 차이가 있으며 대부분의 생물이 한정된 범위 내에서만 조철할 수 있다. 금속과 할로겐화탄화수소물은 다같이 생물체 내에 흡수되면 변화하지 않 은 상태로 남아 있게 되며 생물이 생존하는 동안 계속 추가되어 생물축
적 b i oaccumula ti on 을 야기시킨다. 생물축적의 위험은 다음 예로써 설명 될 수 있다. DDT 는 사람에 대해서 아스피린과 대체로 동일한 독성을 갖고 있다. 아스피린의 치사량은 약 100 정 정도인데 DDT 도 같은 양이 면 치사를 일으킨다. 그러나 아스피린은 체의로 배출되기 때문에 하루에 0.5~l .O g 이라면 악영향을 받지 않고 무한정 섭취할 수가 있다. DDT 는 배출되지 않는다. 따라서 작은 양이라도 반복해서 섭취하면 치사량에 이르게 된다. 또한 생물축적을 일으키고 있는 생물을 먹이로 취하는 동 물은 이들 오염물질이 풍부한 먹이룰 취하는 결과가 되므로 체내에 유해 물질을 더 많이 축적하게 된다. 따라서 해양에서는 인간을 포함하여 상 위 포식자가 먹이에 들어 있는 매우 높은 농도의 오염물질에 노출된다는 점에 문제의 중요성이 있다. 오염물질이 유독하다면 먹이연쇄상의 어느 단계에서나 손상을 일으킬 수 있지만 위험도는 분명히 상위 포식자에 대 해서 가장 클 것이다. 그러므로 생물축적의 대상이 되는 오염물질은 자 연자원에 대한 위협일 뿐만 아니라 인류보건에 대한 참재적인 위험이며 실제로 인간의 사망에 대한 원인이 되어왔다. 이러한 이유로 독성 오염 물질은 심각하게 고려되어야 한다. 5-1 급성 및 만성 독성 담수어류인 잉어류는 수중의 납의 농도가 5~7m g /l 이면 치사가 일어 난다 (Pic k eri ng and Henderson, 1966) . 그러 나 잉 어 류의 생 존과 생 식 능력 에 대하여 식별할 만한 영향이 없다는 의미에서 안전한 납의 농도는 필 시 5~7m g /l 보다는 훨씬 낮울 것이다. 이러한 견해는 아치사 suble t hal, 혹은 만성 chronic 효과가 일반적으로 치사 le th el, 혹은 급성 acute 농도보 다 훨씬 낮은 오염물질 농도에 의해 야기된다는 사실에 근거를 두고 있 다. 그럼에도 불구하고 만성독성은 간 안목으로 볼 때 급성독성과 마찬 가지로 생물을 시스템에서 제거시킬 만큼 효과적이다. 비록 만성독성의 효과는 매우 다양하지만 일반적으로 생식, 발생이나 성장, 그리고 행동
에 대한 변화나 간섭으로 나누어 생각할 수 있다. 5-1-1 생식 어떤 특정 종의 생식을 간섭하거나 방해하는 오영물질은 분명히 개체 군의 성체 생물 수에 아무런 영향을 주지 않으면서 그 종을 시스템으로 부터 완전히 제거시킬 수가 있다. 예컨대 DDT( 혹은 DDE) 의 대사산물은 갈매기 같은 어류를 먹이로 하는 새의 생식정지와 관련된다. 새의 암컷 속에 DDE 가 고농도로 존재하면 껍질이 얇은 알을 낳게 되고 알을 품을 때 다 깨져버린다. 실제로 캘리포니아 해안에서는 펠리컨새가 1, 125 건의 둥우리 짓기를 하였으나 겨우 4 마리의 새끼를 출생시킨 사례가 있었다 (Anderson 의, 1975). 이처럼 낮은 생식률이 몇 년 계속된다면 이 새는 급속하게 절멸할 것이다. 그러나 DDE 는 보통 생식 이의에는 새의 활동 에 아무런 영향이 없는 것으로 알려져 있다. 5-1-2 성장 생물이 발생하고 성장하는 능력은 먹이룰 발견하고 섭취한 먹이를 적 절히 대사시키는 능력에 직결된다. 정상적으로 발생하고 성장하는 생물 의 능력을 간섭하는 어떠한 업압도 생물의 번식과 생존기회믈 심각하게 손상시킨다. 예컨대 미국 롱아이랜드의 오리 농장에서 배출된 영양소에 의해 대번식을 이룬 식물플랑크돈의 높은 농도는 주변 수역에 서식하는 굴의 여과 능력을 크게 간섭한다는 사실이 밝혀졌다 (R yth er and Dunsta n , 1971) . 굴은 아가미를 사용하여 물을 여과하는 여과섭식자로서 보통 정 도의 혼탁한 물도 효과적으로 여과한다. 그러나 고농도의 식물플랑크톤 은 아가미의 표면을 덮는 경향이 있어서 호흡과 섭식을 다 간섭한다. 결과 적으로 굴의 발생과 성장은 저지당하고 몇 년 이내에 굴생산은 소멸된다. 생물의 호흡률에 영향을 미치는 억압도 성장의 속도나 효율을 변경시 킬 수 있다. 예컨대 먹이의 제한이 없는 상태에서 연어 새끼는 용존산소 량이 lOmg / l 일 때의 성장률을 용존산소 3mg / l 일 때의 그것과 비교하 면 lOmg / l 일 때보다도 50% 나 더 빨리 성장함을 알 수 있다 (F i sher,
1963), 성장률에 있어서 이러한 차이는 먹이의 제한이 없울 때 산소량 3 m g / l 은 어린 연어의 호흡에 불충분하다는 사실과 직접 연관된다. 연어 가 3m g /l 의 산소량하에서 치사를 일으키지 않기 때문에 이러한 억압은 치사억압에 대응해서 만성억압이라고 부른다. 온도상의 변화도 호흡률을 변화시킴으로써 생물의 발생과 성장에 영향을 미친다. 모든 생물은 가장 효율적으로 성장할 수 있는 어떤 온도 범위를 갖고 있다. 이 최적 온도 범위 밖에 있는 온도는 성장률을 감소시킨다. 5-1-3 행동양식 행동양식에 대한 오염물질의 영향은 광범위한 효과를 나타낸다. 포식 자 회피, 이동행동, 먹이행동 및 기타 행동의 특칭이 쉽게 악화되거나 변동을 일으킨다. 예컨대 연어는 산란하기 위해서 대양을 회유하여 자신 이 출생한 담수 하천으로 되돌아오는 것으로 유명하다. 이러한 회유의 기작은 충분히 밝혀져 있지 않지만 하천으로 되돌아 가는 연어는 취각으 로 방향을 잡으며 연어가 냄새를 맡는 물질은 특정 하천의 독특한 물질 로서 확인되지 않은 휘발성 유기물질로 알려져 있다 (Hasler and Lassen, 197 1) . 해수오염에 대한 이러한 발견과의 관련성은 대량의 연어가 올라오는 것으로 특칭을 이루는 많은 하천이 공업폐수로 오염되었다는 사실에서 유래한다. 이들 하천 중 많은 곳에서 연어가 올라오는 것이 더 이상 관 찰되지 않거나 수가 급격히 줄었다. 연어가 하천으로 울라오지 못하게 하는 요인은 도시와 공장지대로부터 방출되는 폐수에서 기인하는 아주 다양한 유기오염물질이 하천수에 존재하는 데 있다. 이둘 유기성 폐기 물, 혹은 다른 형태의 오영물질의 존재가 하천수의 맛을 변화시켜서 연 어가 산란장소로 가는 올바른 경로를 찾아내지 못하게 한다는 사실을 추 리하기는 어려운 일이 아니다• 따라서 치사량에 훨씬 못 미치는 농도로 화학물질이 존재하여도 연어의 회유행동을 완전히 두절시킬 수 있을 것 이다. 수온의 계절변화는 해양생물의 행동에 있어서 다양한 반응을 일으킨
다. 발전소에서 나오는 가열된 냉각수의 방출은 국지적으로 정상적인 수 온의 계절변화 양상을 변화시키고 그 때문에 해양생물의 행동에 영향을 미치게 된다. 예컨대 미국의 뉴저지연안 수역에서 여름철에 발견되는 청 어가 보통 겨울철에는 노스 캐롤라이나 연안의 따뜻한 수역으로 이동한 다. 그러 나 뉴저 지 의 Bamege t 만에 설립 된 핵 발전소가 가동되 어 14°C 이상되는 냉각수를 방출함에 따라 이 따뜻한 물에 모여든 대량의 청어는 겨울철에도 남쪽으로 이동울 하지 않았다. 이 경우에 청어의 이동행위는 생리적인 악영향을 전혀 일으키지 않는 오염물질(溫排水)에 의해서 완전 하게 변화를 일으킨 것이다. 그러나 불행히도 발전소가 가동정지를 할 경우에는 수온이 급속히 떨어져 주변 해수와 같은 수준으로 돌아간다. 이와 같은 급속한 온도변화는 온도충격 the rmal shock 이 라 하는대 해 양 생물에게 심각한 영향을 미친다. 실제로 1972 년 1 월 28 일 핵발전소의 가 동정지로 인한 온도충격으로 약 10 만 ~20 만 마리의 청어가 치사된 사례 가 있다 (Clark and Brownell, 1973). 5-2 독성의 측정 독성이란 한 물질이 얼마나 유독한가, 또는 생물을 치사시키거나 손상 시키는 데 얼마나 많은 양이 필요한가 하는 기준을 말한다. 따라서 물질 의 독성이 클수록 치사량은 적어진다. 비록 독성의 개념은 직설적이지만 독성을 측정하는 일에는 많은 복잡한 요인이 개재된다. 5-2-1 측정방법 독물질이 생물체에 들어가는 경로는 매우 다양해서 입, 소화관 , 아가 미 표면, 외피 등을 통해 들어가며, 생물체에 손상을 일으키는 방법도 여러 가지이다. 수생생물에 대한 독성검사는 일반적으로 알고 있는 양을 두약하거나 동물이 얼마나 많은 독물질을 받아들이는가 하는 문제는 피 하고 생물이 살고 있는 물속에 녹아 있는 독물질의 농도를 측정하게 되
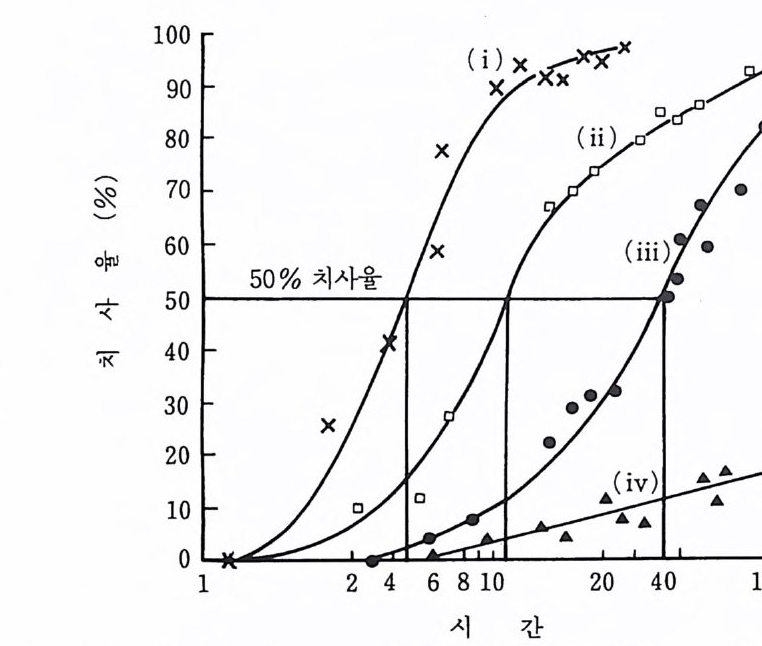
며 이러한 경우에 생물은 독물질의 단일 분량을 취하는 것이 아니라 그 양에 계속 노출되는 것이다. 독성실험을 수행함에 있어서 일단의 시험생물을 독물질의 측정 농도에 노출시키고 사망하는 데 얼마나 걸리는지를 측정하는 것이 관례로 되어 있다. 죽음의 순간을 정확하게 파악하는 일은 어려우며 보통은 방어 반 웅의 정지나 손실 같은 치명적인 손상의 인위적인 범주를 사용한다. 사 용되는 범주가 무엇이든간에 독물질에 대한 감도상의 변화 때문에 시험 생물은 동시에 모두가 사망하는 것은 아니다. 그 대신 치사율은 그립 5-1 에서 보는 바와 같이 노출시간에 대하여 S 자형의 관계를 나타낸다. 모든 시험생물이 사망할 때까지 실험을 연장하는 것은 실용적이 못 되고 필시 비현실적일 것이다. 그래서 사용되는 통계량은 시험동물의 50% 가 사망하는 데 요하는 시간이며 이를 평균치사시간(平均致死時間, media n
 100 。
100 。
그림 5-1 황화아연용액에 의한 홍합의 치사율 ( i ) 10-2mole, ( ii ) 10-3mo/e, (iii) 10-•mote , (iv) 10-smole (자료 : Clark, 1986)
leth a l tim e) 이 라고 부르고 다음과 같이 표기 한다. LTso 혹은 LTm 치사시간은 생물이 노출되는 독물질의 농도에 좌우되며 농도가 높을수 록 시간이 짧아진다. 그리고 그 이하에서는 독성을 갖지 않는 최저유효 농도 thre shold concentr a ti on 가 있다. 따라서 LTso 자체로서는 아주 유용 한 통계량이 못 되기 때문에 대신 특정한 시간 내에 시험생물의 50% 가 사망하는 독물질의 농도를 측정하는 것이 보통이다. 이 시간은 비록 무 척추동물의 유생 갇은 생물에 대한 시험은 2 시간에 불과하지만 보통 48
 1000 8 i
1000 8 i
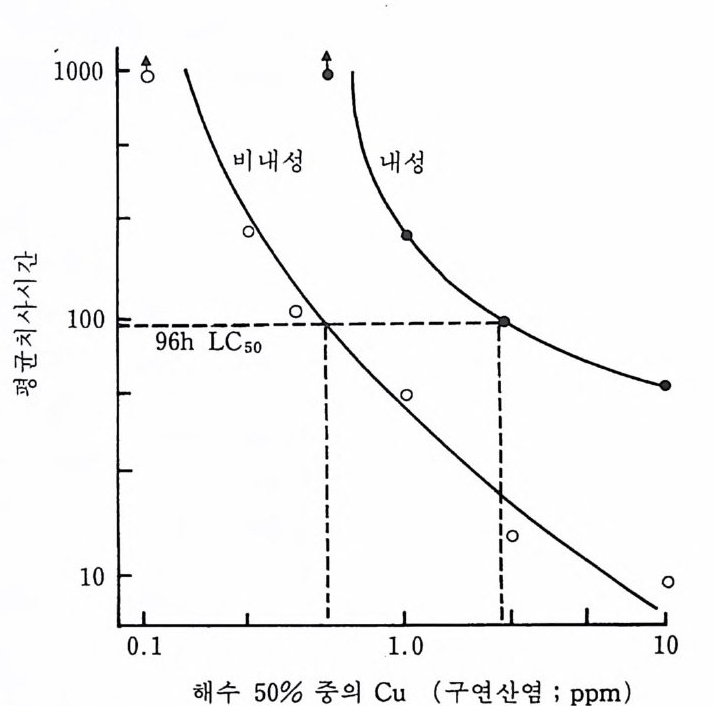
그립 5- 2 Cu ~ 내성 및 Cu - 비내성 해산 다모류 Nereis div e rs ico lor 에 대한 해 수 50% 중의 Cu 농도와 평균치사기간의 관계로 측정한 구리의 96h LCs 。 (자료 : Clark, 1986)
시간 혹은 96 시간으로 정하고 이때의 독성을 평균치사농도라고 부르며 다음과 같이 표기한다. 96h LCso 혹은 96h LCm 48 시간의 경우는 48h LCso 혹은 48h LCm. 평균치사농도는 여러 개의 상이한 농도에서 평균치사시간을 측정함으 로써 결정되는데 이때 농도는 로그 간격으로 주어지며 그 결과를 나타낸 그림 5-2 로부터 LCso 을 읽는다. 더욱 간단하게 하는 방법은 상이한 농도 에 96 시간 노출시킨 다음 치사율을 기록하고 50% 내의의 치사율을 일으 키는 농도에서 LC50 을 정하는 것이다. 시험동물이 주사나 경구투약에 의해 단일한 분량에 노출될 때에는 50% 의 치사율을 일으키는 분량의 크기로서 사용하며 LDso 혹은 LDm 으로 쓴다. 5-2-2 독성측정의 문제점 금속 독성은 금속이 동물에 대해서 나타나게 되는 형태에 좌우된다. 원자가는 해수중에서 변화될 수 있으며 금속과 유기물질 사이에 결합체 가 형성될 수도 있다. 표 5-1 은 해양에 존재하는 중금속의 형태를 나타 낸다. 그림 5 - 3 은 금속이 질산, 구연산 c it ra t e 또는 유기분자를 가전 결 합체로서 첨가될 때 혼합에 의한 납의 섭취를 보여준다. 금속 구연산염 들은 쉽게 용해되는 성질 때문에 보통 독성시험에 사용된다. 그러나 납 구연산영산은 흡수속도와 최종 조직 질산농도의 3~4 배를 갖는다. 유기 분자를 가전 결합체는 2 배의 흡수속도를 갖는다. 중금속의 유기결합체도 무기화합물보다 더 독성을 갖고 있어 유기수은제는 10~100 배 더 독성이 크다. 그러나 유기비소는 무기 비소화합물보다 독성이 낮다. 기타 독성물질은 실제 실험을 구상하는 데 상이한 문제를 제기한다. 예컨대 석유는 물과 혼합이 되지 않으며 독성은 보통 수용성 성분의 독 성이 측정된다. 자연환경에서 생물은 전체 석유가 유화(乳化)된 유적(油
표 5-1 해수중의 금속 평균농도, 총량 및 해수중에 존재하는 형태 금속 기호 평(균pp농b )도 용존형태 총톤)량 (백만 T。 Ag 0. 1 Ag C H- , Ag c g-, Ag C l2 137 알루미늄 Al 5 Al(OH)4 6,850 비소 As 2.3 HASO~- 3, 150 ?}드뮴 Cd 0.05 CdCl2, CdCI+, CdCl3 68 코발트 Co 0.02 CO2 +, COCJ + 27 크롬 Cr 0.6 (OH) ? 822 구리 Cu 3 CuC03, Cu2+ , CuCH+ 4, 110 久근J Fe 3 Fe(OH)3 ? 4, 110 수은 Hg 0.05 Hg C J~ - , Hg C bBr2-, Hg C li' 68 망간 Mn 2 Mn(0Hh4? 2,740 몰리브덴 Mo 10 Moo~- 13,700 니켈 Ni 2 Ni2 +, NiC J + 2,740 납 Pb 0.03 PbCl2, PbCJ +, PbOW 41 안티몬 Sb 0.2 Sb(OH)6 274 셀렌 Se 0.4 5 Seo~- 616 주석 Sn 0.001 (OH) ? 14 u t나듐 V 1. 5 v(Ho32-V?. 0 1 3) 4-, HVO i-, 2,060 아연 Zn 5 Zn2+ , ZnCl+ 6,850 자료 •. Clark, 1986 l商 )을 쉽사리 섭취한다. 더구나 휘발성 성분은 증발로 인해서 생물이 노 출되는 물질의 성질이 실험하는 동안에 변화를 일으킨다. 또 다른 예는 염화탄화수소인데 이 오염물질은 물에 대한 용해성이 매 우 낮으며 동물이 섭취하는 먹이입자에 이 물질들이 흡착되었을 때 동물 은 이 오염물질에 노출되는 것이다 . 실험실에서 모의실험이 불가능한 이 유는 입자가 실험탱크에서 바닥으로 침전하기도 하고 또 탱크 벽에 흡착
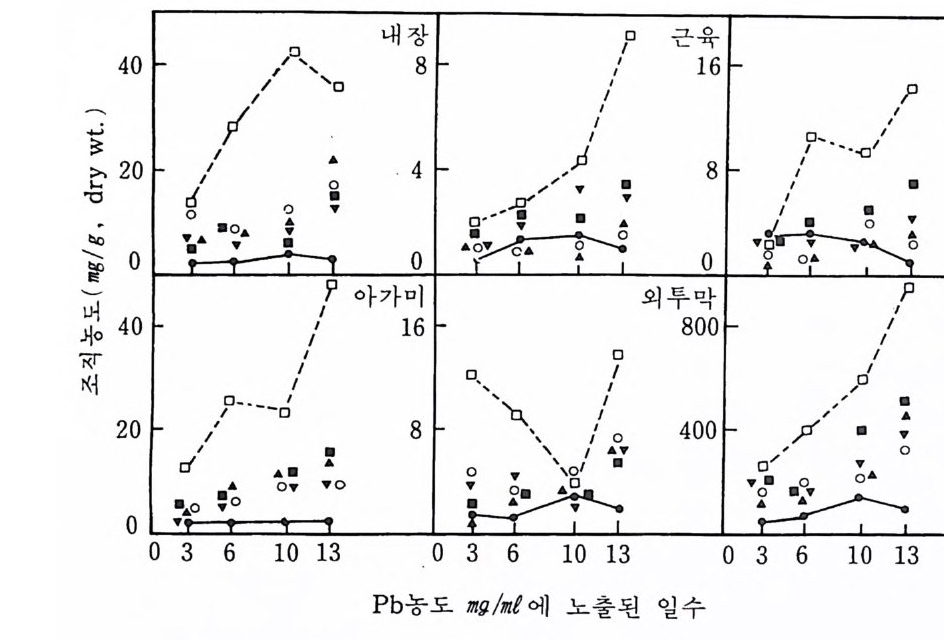 MIiF''서fi 本 /」며).pJ.(AA1 242000。0 L0 !.d.3걸!성.o . II 4II.II :0. .II0 :6。.- . ..급 I / '.1O/ ./ 0。~뺄. TC. ) ` `I I 1I ` ? w3鼻·o·0鼻 `· 。 아 가 내 1미。684장 8 。 蟲□E 3D `- ` -` - 드6:鼻、\曺f ,`, /(,i1 닝 0.•. I/I,' I .II1I ,Do3’••' c · /외' 두二l 4 8L- 0 0막1T。O006 8 。 w건蟲03 0· / I,’ •I ’鼻6oI°/ ` ` , ` , ` ,.1 .o-.0 0I . ./PI I I ’ I1I I P蟲`·o3P•. 신다장리
MIiF''서fi 本 /」며).pJ.(AA1 242000。0 L0 !.d.3걸!성.o . II 4II.II :0. .II0 :6。.- . ..급 I / '.1O/ ./ 0。~뺄. TC. ) ` `I I 1I ` ? w3鼻·o·0鼻 `· 。 아 가 내 1미。684장 8 。 蟲□E 3D `- ` -` - 드6:鼻、\曺f ,`, /(,i1 닝 0.•. I/I,' I .II1I ,Do3’••' c · /외' 두二l 4 8L- 0 0막1T。O006 8 。 w건蟲03 0· / I,’ •I ’鼻6oI°/ ` ` , ` , ` ,.1 .o-.0 0I . ./PI I I ’ I1I I P蟲`·o3P•. 신다장리
그림 5-3 홍합의 여러 조직에 의한 납의 흡수 (0 ) : 질산결합체, ( □) : 구연산영 결합체 , (~ ) : 홍산염 결합체. (T) : 할긴산영 결합체, ( ■ ) : 펙틴산염 결합체 자료 : dark, 1986
표 5-2 생물 검정시 변화를 일으키는 원인 변화원인 1:l l 교반웅 비율범위 실험 생물의 연령 성년:유년 0.01-1000 실험 생물의 성별 암:수 0. 5-5( 혹은 그 이상) 인자 형상의 차이 저항성이 큰인자형 : 1-100 (혹은 그 이 상) 저항성이 낮은 인자형 순화 (acclim a ti on ) 정도 순화형 : 바순화형 1-10 (혹은 그 이 상) 노출기간 단기검정:장기검정 1-100 자료 : Clark, 1986
되기도 하여 결국 실험생물에 대하여 점진적으로 그 농도가 감소하기 때 문이다. 독성물질에 대한 생물의 내성은 광범위하게 변화한다. 상이한 종이 내 성에 있어서 상이한 반응을 나타내는 것은 물론이려니와 동일한 종에 있 어서도 연령, 크기, 성별, 생식조건, 다른 억압에의 노출, 영양상태에 따라 내성이 좌우되며 실험생물의 유전구성도 영향을 받는다. 이돌 요인 에 의해 야기되는 광범위한 변화원인은 표 5-2 에 정리하였다. 이 결과를 보면 생물의 어린시기는 동종의 성체보다 100 배 이하로 내성이 적거나 1, 000 배 이상 더 예민함을 알 수가 있다. 5-3 독성자료의 해석 실험실에서 측정된 독성은 자연 상태에서 나타나는 경우와는 제한적으 로 관련되며 따라서 독성시험 결과는 반드시 주의해서 해석하여야 한다. 독성물질, 실험생물 및 독성실험방법에 관련되는 다양한 요인은 모두 결 과에 영향을 미칠 수 있다. 이들 요인이 적절히 조절된 경우라할지라도 종의 개체군 동태와 생태적 역할에 관련되는 상이한 범위의 요인들은 실 험실 검정결과가 자연환경에 적용될 수 있기 전에 참작되어야 한다. 표 5-3 은 용액중에 들어 있는 중금속의 독성에 영향을 마치는 요인들을 요 약한 것이다. 5-3-1 조절과 순화(目 I|{ t) 한 생물에게 주어진 억압의 효과는 여러 경우에 선행억압의 기간(시, 일, 주 등) 중 노출되어온 조건에 크게 좌우된다. 온도 억압은 이러한 종 류의 조건효과에 대한 가장 좋은 예를 보여준다. 그림 5-4 는 연어새끼에 대한 여러 가지 온도내성대(溫度討性帶)를 나타 낸 것이다. 상하 치사온도한계를 나타내는 것 의에 이 그림은 성장이 심 하게 감소되고 생식이 제한받을 온도 범위에 대한 경계를 보여준다. 조
표 5-3 용액중에 들어 있는 중금속 독성에 영향을 미치는 요인 晉의 룹 형태 { ::::; I \이久러온] 이트 이온 용존성 착 이온 입자성 [침전 흡착 꾹 룹이나 독룹의 존재 [ ;\승A ;~용 작용 길항(持抗)작용 \三::유:온도: : 생물의 생리 및 수중급속 pH 형태에 영향을 미치는 용존산소 생물의 상태 { 먹이결핍 활동성 추가적인 보호기능(피각) 금속에 대한 적응 행동반웅 변화된 행동 자료 : Clark, 1986 절의 관점에서 볼 때 이 그림의 가장 중요한 면은 내성 범위가 순화온도 의 상승에 따라 일정하게 높은 온도로 이동하는 사실이다. 예컨대 2o·c 온도에 순화된 어린 연어는 4°C 인 물에 들어가면 분명히 치사를 일으키
25 三/ 궁극초기치사 온 도 _II|_o『j버) 2100。 -0- ----- 5 5 % 1치///0 사한계 15 2J0I |I_l_25I II(15 3
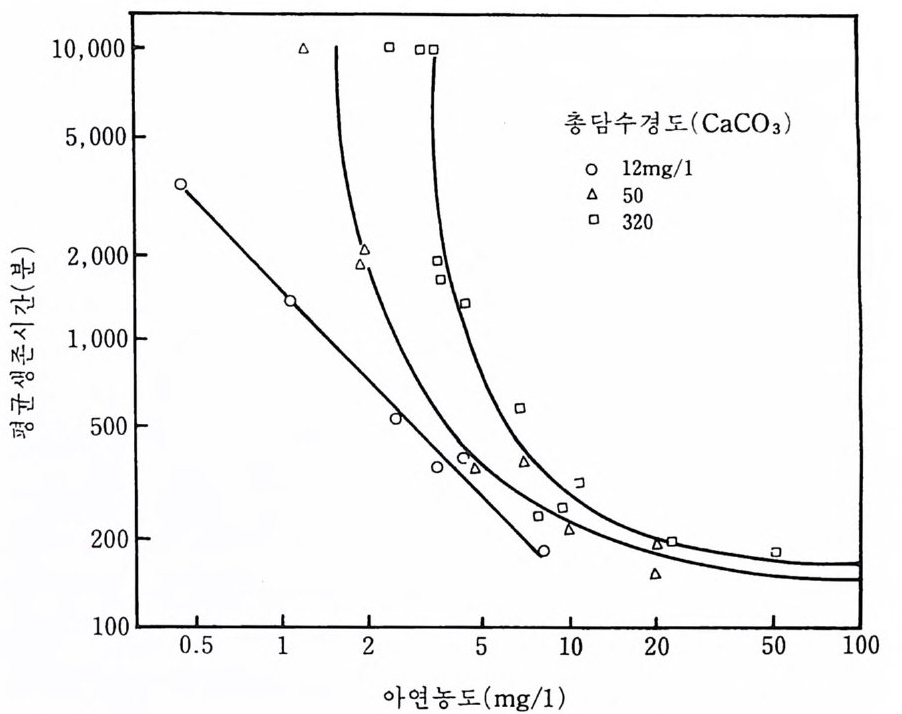
df° J/ 5 순 화온도 (° C ) 그림 5-4 순화온도의 함수로서 어린 연어에 대한 온도 내성 범위 자료 : Warren, (1971) 다는. 반면 10°C 온도에 순화된 어린 二연어는 4°C 에서 치사를 일으키지 않는 다. 생식과 성장에 대한 온도의 효과에 관해서도 같은 논거를 제시할 수 가 있다. 급성 및 만성 독성 효과에 대해서는 일정한 온도 범위 이상에 서는 생물이 순화될 수 없음이 그림에서 분명히 나타난다. 죽 어린 연어 는 순화온도에 관계없이 약 4~14°C 의 범위 밖에서는 산란이 불가능하 비록 경우에 따라 특정 억압에 대한 생물의 노출이 그 억압에 대한 생 물의 예민성을 증가시키는 수가 있으나 많은 경우에 이와 같은 비치사 억압에 대한 노출이 특정 억압에 대하여 생물을 둔감케 하거나 순화시킨다. 예컨대 어류는 고온 및 저온에 대한 것과 마찬가지로 저산소 농도에 도 순화될 수 있음이 알려졌다 (Warren, 1971). 급속히 번식하는 박테리 아 같은 생물에게는 순화가 실제로는 유전변화를 포함한다. 돌연변이 균 주(菌株)는 동일 종의 다른 개체보다 우연히 특정 억압에 대하여 더 저 항이 큰 종류로 이루어진다. 천천히 성장하는 생물 가운데에서 일어나는 단기 순화는 유전변화를 포함하지 않는다. 그렇지만 이러한 생물은 생화 학적, 생리학적, 행동적 조정을 통해 순화될 수 있다. 이러한 조정에 포 함된 과정이 대부분 아직 잘 알려져 있지 않지만 아마도 호르몬과 효소 의 기능에 있어사 그리고 생물 신경계의 반응 특성에 있어서 변화를 포 함할 것이다. 특정 업압에 대한 순화가 달성되는 일반적인 기작에 따르 면 생물은 크게 일치동물(一致動物, con fo rmer) 이거나 조절동물(調節動物, re gu la t or) 로 분류될 수 있다. 예컨대 냉혈동물은 체내 온도가 환경의 온 도를 밀접하게 따르기 때문에 온도에 관해서 일치동물이다. 한편 온혈동 물은 체내 온도가 의부 온도의 변동에도 불구하고 비교적 일정하게 유지 되기 때문에 온도에 관해서 조절동물이다. 물론 이 두 종류의 생물은 가 장 효과적으로 기능이 유지되는 최적내부상태가 있다. 일반적으로 조절 동물 가운데에서 순화는 조절동물이 그 내부 상태를 효과적으로 조절할 수 있는 의부 변수의 범위 내에서 변화를 일으키지만 생물의 최적내부상 태를 변화시키지는 않는다. 일치동물 가운데에서 순화는 생물의 최적내 부상태상의 변화를 포함할 수 있으며 보통 생물이 효과적으로 기능을 갖 을 수 있는 범위 내에서 내부 변화를 일으킨다 (Prosser, 1964). 5-3-2 비치사요인과의 상호작용 한 생물에 대한 특정 억압의 독성은 자체로서는 생물에게 아무런 억압 으로 작용하지 않는 상태나 물질에 의해서 크게 영향을 받을 수 있다• 그립 5 궁은 이러한 상호작용의 좋은 예이다. 무지개송어에 대한 아연의 독성은 분명히 물의 세기가 감소할 때 증가한다. 금속 독성에 대한 물의 세기의 효과는 아연에 대해서 특정적인 것은 아니다. 많은 중금속의 독 성은 물의 세기가 증가하면 감소하는 것으로 보인다 (EPA , 1972). 이러한
 10, 00 0
10, 00 0
그림 5-5 상 이한 경도 를 가전 3 개의 담수에서 아연농도의 함수로서 무지개송어의 평균 생존시간 (자료 : Warrenl971)
관계의 원인은 잘 알려져 있지 않지만 필시 물의 세기 변화와 결합된 금 속의 화학물질 생성과 관련이 있을 것이며 칼슘 및 마그네슘이 물속에 단순히 존재하는 자체로서는 중금속 독성에 영향을 미 치 지 않을 것이다. 구리의 경우에는 독성상의 변화가 물의 세기를 변화시키는 알칼리성에 의해 야기될 수도 있다. 구리의 독성은 또한 온도, 용존산소량, 탁도, 이산화탄소, 마그네슘영, 인산염 등에 의해 영향을 받을 수 있다. 따라 서 주어전 일련의 상태(예컨대 온도 , 물의 세기, 용존산소량 등)하에서 구 리에 대한 평균내성한계 값은 비록 환경상의 변화 자체가 생물에 대하여 거의 억압으로 작용하지 않더라도 다른 일련의 상태 하에서 얻은 평균내 성한계 값과 아주 상이할 수도 있을 것이다.
온도상의 변화는 왕왕 온도 증가에 따라 대사율이 지수적으로 증가하 는 경향의 결과 때문에 어떤 억압적 독성에 영향을 미친다. 온도일치 동 물에 있어서 대사율은 고온이 상위치사한계에 이르지 않는다면 온도가 1o·c 상승함에 따라 2~3 배 증가하는 것 이 보통이다. 따라서 수온이 15‘C 에서 25 ° C 로 상승한다면 어류의 호흡률은 2 배로 증가할 것이다. 분 명히 호흡률의 증가는 산소요구량의 증가로 나타난다. 이러한 사실은 수 온이 최고가 되는 여름철에 나타나는 부적당한 산소량에 의해 어류의 폐 사를 발생시키는 근거가 된다. 또한 호흡률의 증가는 아가미로 물을 끌 어들이는 속도를 증가시키게 되고 결국 수중의 독성물질에 어류의 노출 을 증가시키며 치사동도에 더 빨리 도달하는 결과를 초래하게 된다. 물 의 화학적 성질이 조금만 변해도 어떤 물질의 독성에 커다란 영향을 미 치는 경우가 종종 있다. 수계 내에서 NH3 가스와 NHt 간에는 평형이 이루어지고 있으며 그· 반응은 NH3+H+~ NH t로 표시된다. 암모니움 이온은 독성이 없으나 암모니움 가스는 어류에 대한 96- h LCso 이 0.8 m g/!로 독성이 높다. NH3~ NHt 간의 평형은 분명히 수소이온농도에 좌우되고 물의 pH 가 상승하면 (H + 의 감소) 총 암모니아 (NH3+NH t)의 비율이 더 높게 존재한다. 이러한 관계에서 만일 물의 p H 가 7 에서 8 로 상승하면 총암모니아의 비율은 10 배로 증가하게 된다. 따라서 p H 가 7 인 상태에서 어류에 아무런 치사효과를 갖지 않는 총암모니아 농도는 p H 가 8 로 상승하면 급성독성효과를 나타내게 될 것이다. 따라서 억압 에 관한 실험적인 연구가 수행된 수역의 물리 • 화학적 성질과 다른 수역 에 독성측정이 적용될 경우 그 결과가 크게 빗나갈 수 있다는 것을 유념 하지 않으면 안된다. 5-3-3 독성물질간의 상호작용 수중에 1 개 이상의 독성물질이 들어 있을 경우에 물의 독성은 어떻게 추정하는가를 예를 들어 설명해보자. 구리와 아연에 대한 특정 생물의 96 h LCm 을 각기 0.1 및 1.0 ppm 으로 가정하자. 양 독성물질에 의한 합동 영향을 연구하기 위하여 0.1
pp m 의 구리와 1.0 pp m 의 아연이 든 수용액을 준비하여 여기에 일부에 생물을 넣고 생존율을 결정하기 위해서 96 시간을 기다린다. 이 실험으로 몇 가지의 결과가 가능할 것이다. CD 96 시간 후 생물의 50% 가 사망하면 구리와 아연 사이에는 효과적인 상 호관계가 없었고, 따라서 우리는 아연이 없이도 0.1 ppm 의 구리가 96 시간 후에는 50% 의 생물을 치사시키라는 것, 마찬가지로 구리가 없 어도 1.0 pp m 의 아연이 96 시간 후에는 50% 의 생물을 치사시킬 수 있으리는 것을 기대할 수 있을 것이다. ® 만일 96 시간 후 50% 이하의 생물이 사망한다면 우리는 양 독성물질의 상호작용이 길항적(持抗的)이라고 말한다. 환언하면 두 물질의 혼합물 의 독성은 두 물결이 개별적으로 작용할 때의 한 물질의 독성보다 적 다. ® 만일 50% 이상의 생물이 사망한다면 다음의 해석이 가능하다.
 ETL /// / ---상-첨-가-효교` `` \...__
ETL /// / ---상-첨-가-효교` `` \...__
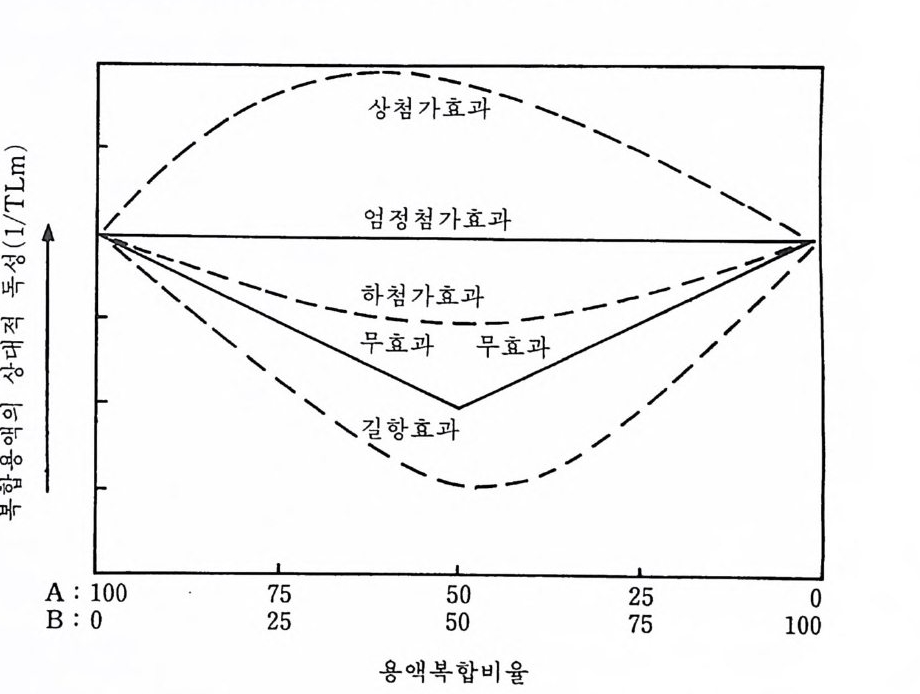
그림 5-6 이론적인 독성물질 A 와 B 사이의 가능한 상호작용
첫째, 정확하게 각 독성물질이 갖는 치사효과의 . 2 배로 나타날 경우에 는 엄정첨가효과(嚴正添加效果, str i c t l y addit ive i n t erac ti on) 라 하고, 둘째, 독성이 단독 물질의 효과보다 높지만 2 배 미만일 경우에는 하첨 가효과(下添加效果, infra -addit ive int e r acti on ) 라 하며, 셋째 독성의 효과가 2 배 이상으로 나타날 경우에는 상첨가효과(上添加 效果, sup ra -addit ive int e r acti on ) 라 한다. 그림 5-6 은 위에 설명한 상호작용의 종류를 설명해주는 것으로 상이한 독성물질 A 와 B 를 여러 가지 비율로 혼합한 실험결과인데 여기에서 100% A 용액의 독성은 100% B 용액의 독성과 동일한 것으로 가정한 것 o] 다. 일부 독성물질의 상호작용이 연구된 것은 사실이나 독성상호작용에 대 하여 아칙도 밝혀지지 않은 것이 많기 때문에 2~3 종 이상의 독성물질이 수중에 존재할 때에는 현재 지식으로 그 용액의 독성을 정량적으로 예측 하기는 불가능하다. 따라서 현재는 모든 독성물질의 상호작용은 엄정첨 가효과를 갖는다는 가정하에 검정하고 있다.
제 6 장 유기성 페기물 지금까지 수로(水路)나 하구, 연안수역에 투기된 폐기물의 가장 많은 양은 성질상 유기질이고 박테리아 분해성인 생활하수(生活下水)이며 많은 출처로부터 오는 아주 다양한 물질이 이 범주에 속한다. 6-1 생물분해성 유기물질 생물분해성 유기물질은 해양 배출구를 통한 도시와 공장의 폐기물 방 출, 준설물질의 해양두기, 도시 쓰레기와 산업 폐기물의 방출, 강의 유 입 등을 통해서 바다에 도달한다. 바다로 유입되는 대부분의 유기성 폐 기물은 생물 분해성이다. 즉 이들 물질은 종속영양(從屬營養) 박테리아에 의해 분해 가능하며 박테리아는 에너지를 얻기 위해 이 물질들을 이용할 뿐만 아니라 생합성 b i os ynth es i s 에 필요한 유기분자의 출처로서 이용한다. 박테리아는 생존하고 증식하기 위한 대사활동의 최종 전자수용체 electr o n accep tor 로서 용존산소를 필요로 하는 호기 성 세균 (好氣性細菌 aerobes) 과 유기물질을 산화하기 위해서 용존산소가 완전히 없어야 하는 협기성세균(鎌氣性細菌 anaerobes), 그리고 용존산소가 있을 때에는 전 자 수용체로 이용하지만 산소가 없이도 자랄 수 있는 조건적 형기성세균
fac ulta t i ve anaerobes 등으로 나누어 진다. 미생물에 의해 이용되는 전자수용체는 그 것 이 결과로 나타나는 반응의 완전성 정도를 결정하기 때문에 중요하다. 호기성 및 종속영양적 생물은 일반적으로 먹이를 완전히 산화하는 반면에, 형기성생물은 그렇지 못하 다. 유기물질+산소 ..... C0 2+ H 2 0 + 에너지 (호기성 대 사 ) 유기물질一환원 유기물질 + C0 2 +H20 + 에너지(형기성 대사 ) 형기성 조건하에서는 보통 유기산, 알콜, merca pt an(SH - 기 를 갖는 유 기화합물) 및 황화수소가 생산된다. 이들 물질은 악취가 있고 흔히 해양 생물에 대하여 매우 유해하며 완전 분해를 위해 산 소 를 필요로 한다. 해 양환경에서 유기물질의 호기성 분해는 분명히 바람직한 일이다. 유기물질의 호기성 분해에는 용존산소의 이용을 필요로 한다. 해수중 에는 한정된 양의 용존산소가 존재하므로 대기나 광합성으로부터 해수로 산소가 공급되지 않으면 농도가 감소될 것이다. 이러한 재폭기( 再賜氣 reaerati on ) 속도는 일반적으로 느리며, 생물분해성 유기물질의 많은 양 이 해수로 첨가되면 용존산소의 수준을 낮추고 필시 부패상태로 발전할 것이다. 이러한 현상은 주위에 있는 해양생물에게 매우 해로운 결과를 초래하게 된다. 6-2 유기물질의 측정 바다로 들어가는 폐기물의 유기성분은 보통 많은 상이한 탄소질 물질 의 혼합체이다. 결과적으로 특정한 성분보다는 일반적으로 유기성분울 측정하는 비특정 검정법이 발전하여왔다. 가장 보편적인 검정방법은 BOD, COD, TOC 의 3 개 검정법이다.
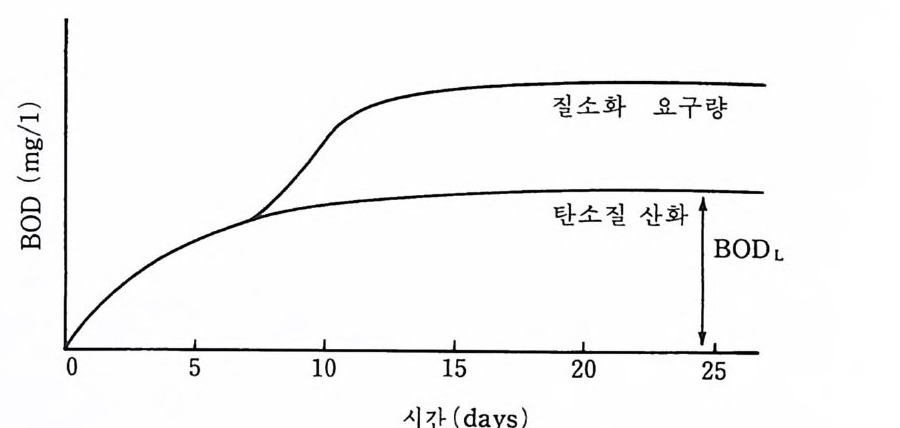
6-2-1 생화학적 산소요구량 (BOD : Bio c hemi ca l Oxy ge n Demand) BOD 검정은 유기오염 정도를 추정하는 데 가장 널리 사용되는 방법이 다. 이것은 시료 속에 포함된 유기물질의 산화를 위해 박테리아에 의해 이용되는 분자상 0 2 의 양을 측정하는 것으로 이는 존재하는 유기물질의 양을 간접 측정하는 것에 불과하지만 환경 내에서 생물분해가 일어나는 동안 이용될 02 의 양을 직접 측정한다. BOD 가 클수록 02 의 감소량이 더 커진다. 생화학적 산화는 서서히 일어나는 반응이고 이론상 완성에 이르기까지 는 무한정의 시간이 소요된다. 그러나 BODL( 총생화학적 산소요구량)의 95~99% 는 보통 20 일 이내에 완성되고, 거의 모든 폐기물에 대해서는 약 60~70% 가 5 일 이내에 완성된다. 이 5 일 주기가 통상 표준 BODs 로 사용된다. 시료 속에서 소비되는 0 2 를 시간에 대한 그래프로 그리면 그림 6-1 에 보는 바와 같이 변화한다. 커브는 실제로 2 개의 부분, 즉 탄소질 산소요 구량에 대한 것과 질소화에 대한 것으로 구성된다. 약 10 일간 배양 후 질소를 산화하는 생물이 우세하게 나타나기 시작한다. 존재하는 암모니 아를 질소화하는 데 대한 02 의 필요성은 새로운 산소 요구를 만들고 커
 ](IE 안 질소화 요구량
](IE 안 질소화 요구량
그림 6-1 BOD 커브
브상에 언덕을 형성한다. 유기물질의 산화속도는 어느 때나 남아 있는 유기물질 양에 직접 비례 하며 다음과 같이 표시할 수 있다. 건dL =K' Lt 여기에서 dL/d t :BOD 로 표시되는 유기물질의 산화속도 Lt : 유기물질의 농도 혹은 t 시간에 남아 있는 BOD K' : BOD 의 빈댕속도 상수 t =o 에서 L t =L( 총 BOD) 를 가정하고 위의 식을 적분하면 Lt = Le-k1 =L( lo- k'i) 여기에서 K= 2,K30' 3 어떤 주어진 시간에 대한 산소요구량 (BOD) 의 계산울 y로 표시하면 L=Lt+ y 여기에서 Lt : 남아 있는 유기물질의 산소 해당량 y : 시간 t 에 대해서 유기물질을 분해하는 데 이용된 산소량 혹은 BOD.
위의 식을 L t의 값을 바꾸어 정리하면 y =L ( l-1 0-kt) K 의 대표적인 값은 0. 05~0. 3/d a y 이며 20°C 에 서 오염수와 폐수는 평 균 0. 1 0/ da y 의 값은 갖는다. BOD 검정은 몇 가지 제한이 있다• 시료내 독성물질의 존재는 박태리 아를 제거하며 BOD 의 올바른 측정을 방해할 수 있으므로 시료의 사전 처리가 요구된다. 더구나 쉽사리 생물분해가 일어나는 유기물질만이 측 정된다. 바다에는 시간이 경과함에 따라 상당한 산소요구량이 필요한, 서서히 분해하는 유기물질이 대량 존재한다. 이러한 사실은 특히 이들 유기물질이 농축하는 경향을 갖는 해양퇴적물에서는 더욱 그렇다. 한충 더한 제한은 검정을 시작하는 데 필요한 순화종자세균(訓化種子細菌)이 대량 필요하다는 데 있다. 이러한 박테리아를 염분이 높은 시료로부터 얻기는 어려운 일이다. 해양 시료에 대하여 BOD 검정을 할 때 가장 큰 결점은 영분이 높은 물에 대해서는 기준과 믿을 만한 방법이 아직 확립 되지 않았다는 점이다. 문제는 종자세균의 확립에 대한, 그리고 측정을 가능케 하는 시료의 희석에 대한 기준이다. 일부의 연구자들은 회석하는 데 담수를 사용하는 반면 일부는 염수를 사용한다. 희석에 어떤 물을 사 용하느냐에 따라 시료의 염분과 결과적으로 나타나는 반응속도상수 K 에 현저한 영향을 미친다. 이러한 기준 결핍의 주원인은 해수가 일반적 으로 소량의 유기물질을 포함하는 한편 이 낮은 농도가 해양학자의 관심 밖에 있었기 때문이다. 그러나 해양의 유기오염(有機汚染)에 대한 최근의 관심은 기준의 확립을 기다리고 있으며 이 분야의 많은 연구가 요구되고 있다. 6-2-2 화학적 산소요구량 (COD : Chem ica l Oxyg e n Demand) COD 검정 역시 해수 속의 유기물질량의 간접지표로서 사용된다. 이 검정은 대부분의 유기화합물이 강산화제에 의해 산울 끓이는 조건하에서
CO2 와 물로 산화되는 원리에 기초를 두고 있다. 반응하는 동안 사용된 산화제의 양을 측정함으로써 유기물질의 산소 해당량을 결정할 수가 있 다. 황산이 있는 경우에는 중크롬산칼륨이 산화제로 사용된다. 촉매인 황산염은 일부의 유기화합물을 산화하는 데 쓰인다. 기본적인 반응은 다 음과갇다• 유기물질 (CaHbOc) +Cr20~-+H+ ~ Cr3++C02 + H20 동일 시료에서 측정된 COD 와 BOD 의 값 사이에는 흔히 차이가 생긴 다. COD 검정은 생물분해성이건 · 아니건 간에 근본적으로 모든 유기물질 을 측정한다. 더구나 황화물 sul fi des, 황산염 sulfa tes , 티오황산, 질산, 제 1 철화합물 등의 무기물질도 산화된다. 한편 COD 시약에 의해 완전히 산화되지 않으면서 BOD 검정으로 생물분해되는 유기화합물들이 있다. 이 가운데에는 벤젠, 톨루엔, 피리딘, 곧은 사슬형 산(酸), 알콜, 아미 노산 등이 포함된다. 해수 시료에 대한 COD 검정에 가장 큰 참재적 결점은 염화물 chlor i des 의 존재이다. 영화물은 황산은과 반응하여 염화은을 형성히는대 이것이 용액으로부터 침전한다. Ag S 04 + 2Cl-- + Ag C l2 + so~- 영화은으로서 한번 침전하면 은 s il ver 은 더 이상 촉매로 작용할 수 없 으며 이것이 찰못된 결과를 초래하게 된다. 염화물은 또한 크롬산염 chroma t es 과 반응하여 중크롬산염을 3 가 형태로 환원시킨다. 6CI-+ Cr20 궁- + 14H+-+3Cl2 + 2Cr3+ + 7H20 한편, 염화물에 황화수은을 첨가시키는 것과 갇은 수정안이 제시되었
으나 해수에서 나타나는 높은 염화물 농도에 만족할 만한 정도가 되지 못하였다. 따라서 해수시료에 대하여 보고된 COD 자료는 조심해서 사 용해야 한다. 6-2~3 총유기탄소 (TOC : Tota l Orga n ic Carbon) TOC 검정은 고온로(高溫 煥 )와 적의선분석기로 구성된 전자기기를 이 용한다• 소량의 시료가 고온로에 주입되면 이곳에서 유기물질이 촉매의 존재하에 산화되어 CO 2 로 산화된다. 생성된 CO2 는 적의선분석기에 의 해 정량적으로 측정된다. 이 값으로부터 시료 속의 유기탄소의 양이 아 주 정확하게 추정된다. 이 검정법은 매우 빨리 수행될 수 있어서 해양연 구에 보편화되어가고 있다. 6-3 해양환경에 대한 생물분해성 유기물질의 영향 해양에서 생물분해성 유기물질의 일차적 영향은 용존산소 결핍의 잠재 성과 산소결핍이 일으키는 결과이다. 이러한 영향의 대표적인 예의 하나는 뉴욕 만곡부( 灣 曲部)의 경우에서 볼 수가 있다. 이 수역은 생활하수 스럿지, 준설폐석 및 공장폐수 등이 정기적으로 두기되어온 곳이다. 이 수역의 표충수와 저충수간의 산소농 도의 차이는 2~3mg /l 로서 변화하며 7 월과 10 월 사이에 나타나는 저층 수의 산소결핍이 가장 심각하다. 폐기물 위에 덮인 저층수의 용존산소 농도도 역시 2~3mg / l 이다. 2mg /l 이하의 용존산소 농도는 여름철에 흔히 나타나는데 이 수준은 잘 균형을 이룬 해양생물들을 유지할 수 없 는 상태이다. 캘 리 포니 아의 Santa Cata l i na Island 근해 의 퇴 적 물은 폐 수처 리 장의 가동 전후로 메탄 생성 me th ano g enes i s 에 대해 감시가 이루어졌다. 미생 물에 의한 메탄 생산은 협기성 조건하에서 유기물질 안정화에 중요한 과 정이다. 처리장이 가동된 후 배출구 부근의 퇴적물은 훨씬 덜 환원되었
울 뿐만 아니라 훨씬 더 적은 유기물질을 포함하여 이로 인해 메탄 생산 속도가 30 분의 1 로 감소되었다. 또한 배출구 부근의 해수에서 용존산소 량의 증가가 뚜렷하였다. 캘리포니아의 San J ose 에 있는 처리장이 1979 년에 기능 저조현상이 생겨 부분처리된 생활하수를 샌프란시스코 만으로 매일 15 만 톤씩 수주 일간 배출하게 되었다. 그 결과 해수중의 산소가 만의 비교적 정체된 부 위에서 급속히 감소되었고, 어부와 해양생물학자들은 새우, 멸치류, 녑 치류, 농어류, 철갑상어 등이 단시일 내에 완전히 소멸되었음을 보고하 였다. 홍합과 조개 등을 포함하는 저생생물도 마찬가지로 사멸하였다. 연구결과 이 지역이 원상으로 회복되는 데에는 10 년 이상이 걸릴 것으로 추정하고 있다. 1970 년에는 런던에 있는 생활하수처리장의 종업원들이 파업하는 동안 미처리 폐수가 8 일간 템즈강 하구로 투기되었다. 이 사고 후 5 주일간이 나 물속의 산소농도는 포화농도의 10% 이하였다. 이러한 산소 수준이 하구에서 폐기물 분해로부터 오는 유독한 암모니아와 결합하여 대량의 어류치사와 함께 동물상의 다양성이 크게 감소하는- 결과를 초래하였다. 이상과 같은 부정적인 면에 반해서 해양환경에 대한 생활하수의 유익 한 결과에 대한 연구결과도 있다. 생활하수에서 유래하는 유기물질은 상 업상 유용한 해양생물의 성장을 촉진하는 먹이원이 될 수 있다. 그러나 이것은 충분한 생태학적 지식과 세심하게 첨가물질의 양을 조절할 수 있 지 않으면 안 된다. 그러나 항구나 하구 또는 해수순환이 제한울 받는 연안 수역으로 미처리된 생활하수를 투기하는 일은 금지시켜야 한다는 것이 환경학자와 환경기술자들의 일반적인 견해이다. 문제는 의해로 배 출하기 위해서는 고도의 처리가 요구된다는 점이다. 6-4 병원균의 유입 생활오수나 오수 스럿지가 해양에 미치는 영향의 가장 심각한 결과는
병원생물( 病源生 物)에 의한 병 전염의 가능성이다. 이 병원 미생물은 직 접 두기로 연안 수역에 유입한다. 주영향은 일반 대중의 보건에 대한 것 과 해산 식품의 질과 안전에 관한 것이다. 해수의 박테리아 오탁은 어업과 패류업울 폐쇄토록 하고 레크리에이션 울 위한 해변을 폐쇄케 함으로써 경제적인 영향을 미칠 수도 있다. 지중 해의 여러 곳이 연안 인구밀집지역으로부터 오는 미처리 폐기물 방출 때 문에 대체로 오영되어 있으며 북해연안도 마찬가지인데 이러한 곳들은 많은 종의 어패류가 박테리아로 오탁되어 사람이 소비할 수가 없을 정도 이다. 또한 미국의 경우도 향상되고는 있으나 미처리된 도시 생활하수가 표 6-1 해양오영 미생물에 의한 병 병원체 인체 발병 관련된 해양생물 인체 전달 방법 박테리아 : Clos tr idiu m 설사, 복통 어류, 패류 냉동처리가 잘 안된 어류와패류의섭취 Clostr id iu m 보틀리누스 발효 , 염장 및 가공 처리가 잘 안된 botu l in a 중독 훈제된 어류 어류및 패류의 섭취 Salmonella 장티프스 어류, 패류 어류 및 패류를 날 파라티프스 것으로 섭취, 또는 잘 조리되지 않은 것 울섭취 vib r io 설사, 복통 어류, 패류 바이러스: 전염병 간염 전염성 간염 패류 오염된 패류의 부적 바이러스 절한섭취 기생충: 장영 대구, 청어, 생선, 부분조리, 혹은 선충 고등어 훈제된 어류의 섭취 (Nemato d es) 자료 : Thath e r and Meit h-A vci n, 1978
여전히 방출되고 있어서 60 개 이상의 하구(河口)가 병원미생물의 오탁으 로 인해서 패류어업이 금지되었고 많은 곳에서 생산된 어패류가 시장으 로 반출되기 전에 정화시키도록 하고 있다. 분뇨방출에서 오는 병원성(病源性)이 가장 큰 균주( 菌 株)는 Salmonel- la, Shig e lla, Le ptos j )ira , 장병 원성 (腸病院性) 인 E. coli, Pastu r ella, Vib r i o, My c obacte r i um , 사람의 장 (n 房 ) 바이러스, 원생동물인 Endamoeba his - tol ica 및 십이지장충 유생 등이다. 이들 미생물에 의한 여러 가지 병을 수산생물에 의해서는 물론, 직접 접촉으로도 전달될 수 있다. 표 6-1 은 주요 병에 대한 내용을 요약한 것이다. 6-4-1 전염경로 사람이 바다에서 병원체에 노출되는 기본적인 경로는 오염 수역에서의 참수활동과 해산 식품의 소비이다. 위락수역에서의 감염 가망성은 병원체의 존재, 그 수, 생존능력, 감염 량 및 그 분산정도에 의존한다. 대부분의 연구결과를 보면 해수에서 수 영으로 감염되는 경우는 드물게 나타나는데 예의적인 것은 호기성 스피 로헤 타균인 Le ptos p ira 에 의 한 렙 토스피 라감염 증 Lep tos pi ro sis 이 다. 이 병원체는 숙주동물의 체의에서 증식능력이 있어서 그 수를 크게 늘리는 데 보통 피부의 상처 부위나 점막(*占膜)을 통해서 혈관으로 들어가고 콩 팥 간 및 중추신경계 등에 급성 감염을 일으킨다. 그러나 이 병원체가 해수중에서 생존하는 시간은 짧다. 수영을 통해 장(! 易 )바이러스가 전달 되는 경우는 극히 적다. 감염발생 수가 적은 것은 필시 병원체의 희석효 과, 수영하는 동안 체내에 흡수된 물의 양이 적은 점 등이 그 원인일 것 이다. 그러나 진단이나 보고된 것보다 더 많은 수인성병(水因性病)이 발 병했을 것으로 생각된다. 분뇨로 오염된 해수역에 노출된 어패류를 소비함으로써 장감염(腸感 染)이 발생한 예는 오래전부터 알려져 있다. 굴의 섭취와 관련된 장티푸 스의 전염은 1816 년 프랑스에서 처음 보고되었으나 그 관계가 잘 알려진 것은 1895 년 영국에서 생활하수로 오염된 굴과 홍합을 섭취한 주민이 장
티푸스에 대거 감염된 사건에서 비롯되었고, 그 후에 생활하수로 오염된 어패류의 소비와 관련되는 박태리아 및 바이러스 감염 발생이 전세계적 으로 많은 곳에서 보고되었다. 장병원생물( 腸 病 源生 物)의 운반체로서 어 패류의 인식을 통해 어패류에 대한 위생시설 규정을 제정하는 데에서, 또 해양 생활하수 투기에 있어서 향상을 가져왔다. 그 결과 실제로 영국 의 장티푸스 발생지역의 경우에 인구 1,000 명당 6.4 건에서 0.29 건으로 급속히 감소되었다. 감염에 일차적으로 관련되는 어패류는 굴, 조개, 홍합 같은 이매패(二 枚 貝 ) 연체동물류이다. 이 동물들은 모두가 여과식 섭석자여서 해수를 여과하여 그 속에 있는 플랑크돈을 먹이로 취한다. 박테리아와 바이러스 는 오탁수가 여과될 때 걸러지며 그 결과 연체동물의 몸속에 높은 농도 를 축적하게 된다. 게나 바닷가재 같은 각갑류도 박태리아와 바이러스를 축적하지만 이 동물들이 병원체를 위장에 축적하여 제거하는 까닭에 통 상 문제가 되지 않는다. 6-4-2 병원체의 지표생물(地標生物) 무수한 병원성 및 비병원성 미생물과 바아러스는 통상 소량으로 끊임 없이 해양환경으로 유입되고 있다. 특정적인 한 병원체의 검증은 시간과 경비가 극단으로 많이 들며 대량의 시료가 요구된다. 더구나 특정 병원 체의 부재(不在)가 다른 병원체의 부재를 의미하지는 않는다. 결국 분뇨 물질의 존재를 지표하고 그로 인해 장병원체의 존재가능성을 나타낼 지 표생물 몇 종이 요구된다. 문제는 어느 병원체가 해양환경에서 최상의 지표 생물이냐 하는 데 있다. 이상적인 지표미생물이 지녀야 할 성질은 다음과 같은 것들이다. ® 모든 형태의 물에 해당될 수 있어야 할 것. ® 병원체가 있는 곳에는 어디에나 존재해야 할 것. ® 생존시간이 적절히 길어야 할 것. ® 오염수역에서는 생식을 할 수 없어야 할 것.
® 인체에 해가 없어야 할 것. ® 오영수역에서의 지표생물의 밀도가 분뇨오염 정도와 직접 관계가 있어 야할것. ® 검정방법이 특이성과 예민성울 갖추고 있어야 하며 쉽사리 검정될 수 있어 야 할 것 (Scarp ino , 1975) . 박데 리 아는 대 장균군 coli -for m grou p , 분변계 연쇄 상구균 (冀便系連鎖狀 球菌 fec al stre p t oc occus) 및 Salmonella 등을 유용한 지표생물로 하여 분 뇨 오탁을 감시하는 데 전형적으로 사용되어왔다. 바이러스 검정은 최근 에 더 널리 이용되고 있다. 가장 최근에 개발된 검정은 장 미생물에 의 해 생산되는 스데로이드인 cop ro sta n ol 에 의한 것이다 . 그러나 이들 검 정법의 대부분이 현재 발전단계에 있어서 결과적으로 아직은 대장균검정 법이 해양 수역에서 병원체 오탁을 측정하는 데 기본이 되고 있다. 6-4 - 3 대장균군(大腸菌群, coli -form grou p ) 박테리아 가운데에서 대장균군은 병원체 존재의 지표생물로서 거의 보 편적으로 사용된다. 일찍이 미국 보건성에서는 물 100ml 당 대장균수 3 이하를 식수(食水)의 법정기준으로 확정하였고 그 후 세계적으로 각국의 보건 당국은 대장균을 기초로 유사한 기준을 정하였다. 대장균군의 주 장점은 이 미생물이 오탁수에서 많은 수가 발견되고 수가 적은 병원체보 다 계수(計數)가 쉽다는 것이다. 대장균군은 생화학적 및 혈청학적 톡칭에 있어서, 또한 자연상의 출처 와 서식지에 있어서 상이한 많은 세균으로 구성된다. 그러나 이들 미생 물은 모두다 호기성이거나 조건적 호기성이고, 비포자형성(非胞子形成)이 며 , 그람음성 gram -nega t i ve 이 다. 또한 35·c 에서 48 시 간 내 에 가스 형 성 으로 락토즈 la ct ose 를 발효시키는 간상(程狀)박테리아이다. 이러한 성질 은 검정을 쉽게 하여 주고 물속에 있는 대장균의 계수도 쉽게 해 준다. 불행히도 대장균군의 모든 종류가 인체의 장(腸)으로부터 기원하는 것 은 아니다. E. col i는 특칭적으로 사람과 온혈동물의 장에 기생하지만
Aerobacte r aerog en es 같은 다른 종류는 식물과 토양에서 흔히 발견된 다. 이 후자의 경 우는 분뇨오탁을 지표하지 않는다. Metc a lf 09 75) 는 어 패류에 있는 박태리아 및 바이러스 병원체의 지표로서 분뇨대장균의 적 용성을 연구하여 특히 분뇨오염이 보통에서 심한 정도의 범위일 때 매우 유용함은 발견하였다. 그러나 대장균 검정법을 이용하는 데에도 단점이 있다. 죽 락토오스를 발효시킬 수 있는 비대장균 박테리아가 일부 존재 하고, 따라서 잘못된 결과를 얻을 수가 있다. 또한 대장균보다 더 강하 고 모든 대장균이 죽은 후에도 여전히 존재하는 바이러스가 여러 종류 존재한다. 어떤 경우에는 대장균이 자연적으로 생식하여 높은 값을 나타 낼 수도 있다. 6-4-4 분변계연쇄상구균(冀便系連鎖狀球菌) 및 Salmonella 분변계연쇄상구균은 온혈동물의 장관(腸管) 속에 지속적으로 존재하며 물의 분뇨 오탁을 특징적으로 지표한다. 이 세균은 물속에서는 증식하지 않는다. 그러나 물속에서 오래 생존하지 않기 때문에 이 세균의 이용은 병원체의 지표로서보다는 오히려 분뇨 오탁의 지표로서 효용성이 크다. 일반적으로 새로 오염된 수역의 시료 중에는 분뇨대장균의 수보다 10 배 의 분변계연쇄상구균을 갖고 있다. Salmonella 도 다른 병 원체 의 존재와 마찬가지로 지표생물로서 흔히 감시되어왔는데 정량적인 방법이 다른 지표생물의 경우보다 덜 발전하였 고 방법의 정확성이 확립되어 있지 않은 상태이다. 6-4-5 바이러스 하수의 질에 대한 기본적인 지표생물로서 대장균검정의 가치는 오랫 동안 의문시되었는데 특히 하구와 해양수역에서 바이러스가 대장균보다 더 오래 생존할 수 있기 때문에 문제가 된다. 따라서 인체장바이러스 ente r ovir u se 나 대 장균을 공격 하는 바이 러스인 콜리파아지 coli- ph ag e 에 대한 감정법의 이용이 해양수역에서의 분뇨오염에 더 좋은 지표로서 제 안되었다. 바이러스는 살아 있는 숙주세포 내에서만 증식하기 때문에 해
수중에서는 시간이 지남에 따라 수가 감소될 것이다. 가장 미세한 병원체인 바이러스는 크기가 12~500mn(1 n m= 1 0-9m) 범 위에 있다. 각 바이러스의 입자는 한 총 혹은 두 충의 RNA 나 DNA 를 둘러싸고 있는 단백질 막으로 구성된다. RNA 나 DNA 만이 존재하기 때문에 기생적으로 행동하지 않으면 안 되고, 증식하기 위해서는 숙주세 포로부터 보조적인 핵산을 이용한다. 표 6- 2 인체 장 바이러스와 병명 바이러스 혈청형의 수 핵산의 형태 증 상 장 바이러스: Polio v i ru s 3 RNA 소 0~ 마l:I] Coxsackie viru s A 군 24 RNA 무균성뇌막염, 포진성구협염, 감기,소아설사 B 군 6 RNA 무균성뇌막염, 감 기, 신생아병, 급 성소아사망 징후군 Echov iru s 34 RNA 무균성뇌막염, 발열과 발진, 연성마비, 호흡기 감영 간염 바이러스: A 군 1 RNA? 전염성 간염 B 군 1 DNA? 혈청 간염 Adenovir u s 31 DNA 급성호흡기감염, 급성시각기감염 Reov iru s 6 RNA 발열, 호흡기감염, 설사 자료 : Vaug hn , 1974 ; Scarp ino , 1975
바이러스는 다양한 질병 가능성, 항생제에 대한 반응 결핍, 아직도 불 완전하게 이해되고 있는 성질 등으로 해서 공중보건에 대한 가장 큰 위 협의 하나로 간주된다. 생활하수와 오영수역에서 발견되는 장바이러스를 표 6-2 에 요약하였다. 6-4-6 Cop ro sta n ol (5/3 - cholesta n- 3/3 - ol) 수중의 분뇨 오탁에 대한 무생물적인 지표체를 개발하려는 노력의 결 과로 현재 가장 기대되는 검정법은 co p ros t anol 에 대한 것이다. 이 물 질은 고등동물 내에서 콜레스톨이 장박테리아에 의해 환원될 때 배타적 으로 만들어진다. 분뇨물질이 이 화합물의 유일한 자연적인 원천인 것으 로 알려져 있다. 지표체로서 cop ros t anol 을 사용하는 연구 결과를 보면 이 물질이 해양되적물 속에 비교적 대량 존재할 수 있고, 또 해양수역에 서 분뇨박테리아의 수와 밀접하게 부합됨을 보여준다. 6-4-7 해양환경 내 병원체 출현 앞에서 설명한 바와 같이 많은 하구 및 해양 수역은 분뇨물질로 오염 되어 있다. 병원체는 수충과 퇴적물에서 다같이 발견된다. 특히 심한 곳 은 제한된 반폐쇄성 수역이다. 해양 수역에서는 일반적으로 박테리아의 개체군의 수가 낮다. 그러나 전반적인 오탁은 박테리아의 수준을 높이는 결과를 초래하는 경우가 많 다. 스페인의 연안 수역에서는 분뇨 박테리아의 수가 30,000~50,000/ lOOml 인 반면 지중해에서는 100ml 당 100 만 이상으로 나타난다. 우리 나라의 마산 수역에서는 2.1x 1 07 MPN /l OOml(MPN= 最確數), 부산 수 역 24x l0 4MPN/lOOml, 군산 수역 5,200MPN/lOOml 로서 지역에 따라 큰 차이를 보인다. 대장균수는 보통 해양배출구 부근에서 가장 높고 멀어지면서 점차 감 소한다. 영국 해안에서는 배출구 부근에서 균수가 50,000/lOOml 인 반면 에, 폐기물을 처리한 다음 해안으로부터 5 마일 의해 쪽으로 두기하는 로 스앤젤레스 해변에서는 3/lOOml 이하로 크게 감소되었다.
표 6-3 뉴행프셔 하구에서 발견된 어패류 중의 병원성 박테리아 분뇨대장균 조사정접 시료수 굴 100 당 개체수 해수 100ml 당 개체수 1 15 120 19 2 13 330 33 3 10 25,000 790 4 6 6,750 131 자료 : Meta c alf, 1975 어패류 또한 병원성 박테리아에 의해 오탁되어 먹을 수 없게 된다. 이 는 어패류가 해수중의 박데리아를 섭취하여 체내에 축적하는 경향이 있 기 때문이다. 표 6-3 은 미국 뉴행프셔 하구의 4 개 조사 정점에서 취한 시료를 분석한 결과인데 해수중의 대장균 수와 굴 속의 대장균 수의 관 계를 명백히 알 수가 있다. 이와 비슷한 관계는 분변계연쇄상구균에 의 해서도 나타난다. 박테리아의 개체군은 일반적으로 바다에서 비교적 빨리 감소한다. 박 데리아의 사멸을 일으키는 요인은 여러 가지가 있는데 그중 가장 중요한 것은 영양소 결핍, 퇴적작용 등으로 이들에 의해 일차적으로 사멸이 지 배된다. 박테리아는 입자상 물질에 흡착되고 결과적으로 첨전되어 물로 부터 대량 제거된다. 햇빛은 박테리아에 대하여 치명적인 효과를 갖고 있으며 특히 스펙트럼의 자의선 부위가 그렇다. 해수는 통상 영양소 (C , N, P 등)에 있어서 생활하수에서 방출된 대량의 박테리아군을 유지할 수 가 없다. 그 의에도 보다 큰 생물에 의한 포식 ( t包 食), 박테리오파아지에 의한 공격, 조류와 박테리아에 의해 생성된 독물질, 그리고 물리화학적 요인(p H, 삼두압, 중금속 등) 등은 모두 병원성 박테리아 개체군을 감소 시키는 역할을 한다. 장바이러스 또한 생활하수로 오염된 해수와 퇴적물에 널리 퍼져 있다. 이것은 정상적인 처리방법으로는 바이러스를 효과적으로 파괴하지 못하
기 때문에 처리된 물은 물론이고 미처리된 물에서도 많이 나타난다. 미 국 마이아미 해변에 있는 해양배출구 부근에서 장바이러를 42PFU/400 ml(PFU=p la qu e forming unit , i容菌斑形成單位)까지 분리 하였다 (Edmond 의, 1978). 아스라엘의 텔아비브의 의해역에서 채집한 시료의 3 분의 1 이상이 장바이러스를 포함하고 있었는데 배출구에서 1.5 km 떨어진 해수 욕장의 해수는 12, OOOPFU/400ml 까지 분리되었다. 미국 텍사스의 레크 리에이션용 해변 수역은 분뇨 대장균이 발견되지 않아 청정수역으로 알 려졌으나 실제로는 장바이러스가 245PFU/400ml 까지 검출되었다. 이는 전통적인 세균지표 생물이 바이러스의 발병위험을 지표할 수 없음을 나 타내준다. 연안 수역으로 유입하는 바이러스는 쉽사리 입자성 물질에 흡착되어, 입자와 함께 침전하며 해저에 축적된다. 보통 해양수역에 있는 바이러스 의 99% 이상이 해양퇴적물에 흡착된다. 한편 퇴적물에서는 바이러스가 어패류에게 섭취되어 그 조직 속에 축적된다. 장바이러스는 해수중에서 비교적 오랫동안, 흔히 수주간 생존할 수 있 음이 알려졌다. 온도는 생존에 큰 영향을 미치는데 온도가 높을수록 바 이러스 전염성은 빨리 소실된다. 한 연구에서는 수개의 장바이러스가 4°C 의 해수중에서 46 주 동안 안정성을 유지할 수 있음을 보여준다 (Lo 등, 1926). 염분은 일반적으로 바이러스의 생존시간에 아무런 역할을 하 지 않는다. 생존시간을 지배하는 중요 요인의 하나는 부유물질의 양이 다. 바이러스는 보통 전염성을 잃지 않고 쉽사리 입자에 흡착한다. 연안 수역에는 살아 있는 세포, 세포 잔해물, 데트리터스, 미사(微砂) 및 점 토(*占土) 등을 포함해서 자연상으로 대량의 입자성 물질이 존재한다. 입 자들은 물리적 및 화학적 작용을 통해 바이러스를 보호한다. 그 방법이 무엇이든 간에 교질 collo i d 에로의 흡착은 바이러스의 생존시간을 크게 증가시킨다. 물론 해수중에는 바이러스의 기능을 무력화시키는 물질도 존재한다. 그러나 이 무력화 과정은 느리고 또 바이러스 자체가 이 작용 에 저항성을 갖고 있다. 그러므로 바이러스는 어패류를 감염시키기에 충 분할 만큼, 그리고 바이러스병을 발생시키기에 충분할 만큼 오래 생존한다.
6-5 부영양화 이미 언급된 바와 같이 생활하수는 다량의 유기 및 무기영양소를 포함 하고 있다. 이러한 하수가 해양으로 배출되면 해양생태계의 영양영 농도 를 과다하게 증가시켜 국지적인 부영양화로 전행하게 되고 결과적으로 지역 생태계의 생물학적 평형에 불균형을 초래한다. 6-5-1 영양원소 물질의 두입 영양소 물질이 해양으로 두입되는 대표적인 경로는 해양 파이프 배출 구에 의 한 유입 과 강수를 통한 유입 이 다. Pik e 와 Gameson 0970) 에 의 하면 해양 배출구가 의해역의 일차생산량에 미치는 영향은 매우 작으며 대부분의 경우 배출구 부근에서 유기물질이 퇴적되어 저생생물 군집에 커다란 영향을 미친다. 이러한 영향은 실제로 생활하수가 두기되는 해안 에서 저생생물의 종다양성(種多樣性)이 감소되는 사실과 일치한다. 따라 서 해수에 대한 영향이라기보다는 하수에 들어 있는 입자성 유기물질이 퇴적하거나 스릿지의 축적으로 인한 영향이 대부분이다. Ep ple y 등(1 972) 은 미국 남가주 연안의 배출구 부근에서 플랑크톤의 생산량이 정상적인 연안수역에 비해 2~3 배 높음을 규명하였다. 일반적 으로 배출구 부근에서 영양소와 용존유기물질의 수준이 정상적인 수역에 비해 다소 높은 경향을 보이는데 이는 매우 빠른 흡수와 해류에 의한 효 과적인 분산의 결과이다. 그러나 이와는 반대되는 경우도 있다. 예컨대 뉴욕 만과 리버풀 만에서는 영양소의 농도가 높은데도 불구하고 일차생 산량은 매우 낮거나 정상적인 수역과 유사한 값을 보이는데, 그 이유는 스럿지에 포함된 성장저해요소 때문인 것으로 알려져 있다. 또한 해양으 로 직접 두입되는 배출구나 스럿지 두기와 간접적으로 강수에 의해 투입 되는 것 사이에는 화학적, 생물학적 차이가 크다는 것을 둘 수 있다. 표 6-4 는 이 차이점을 요약한 것이다. 일반적으로 강수에 의한 생활하수의 배출물은 강을 경유하는 동안 처
표 6-4 생활하수가 해양으로 유입하는 경로와 특징 특징 관 배출구 투입 강수두입 초기 농도 매우높음 낮음 처리 미처리 처리 혹은 자정화 영양소 상태 미산화혹은 부분 산화 식물체로부터 질소물질 분비, 완전 분해, 영양소로 무기화 경로 배출구로부터 직접 유입 강수를 통하여 간접 유입 pH 다소산성 중성화 독성 유독 거의 무독 리과정을 거치거나 강수의 자정작용(自淨作用, sel f-p u rifi ca ti on) 에 의해 유용한 영양물질로 바뀌는데 이것의 일부는 강의 담수플랑크돈이나 부착 식물에 의해 소바되고 나머지는 해양으로 유입된다. 대도시에 인접한 강 은 결과적으로 생활하수, 농경수 및 공장폐수 등이 혼합되므로 유입하는 인접 해역과 하구수역에 막대한 영향을 미치게 된다. 예컨대 뉴욕 만에 서는 투기장소에 의한 유입량보다 강에 의한 영양영의 유입량이 훨씬 더 커 서 부근 해 역 에 서 식물플랑크톤인 Di dy m oc yst i s 의 대 번식 이 발생한다. 이 러 한 문제는 스코틀랜드의 Irv ine 만의 경우에 잘 나타난다. 이 지 역 해변은 약 14km 에 달하는 모래사장으로 되어 있고 모래사장의 가운데 로 Irv i ne 강이 유입되어 2 개 지역으로 나누어진다. 이 강의 상류 몇 지 점에서 생활하수와 공장폐수가 배출되고 있으며 이 배출수는 주로 N03_ 롤 풍부하게 포함하고 있다. 해안에서는 이 폐수가 처리되지 않는 채로 파이프 배출구를 통해 유출되어 다른 해안에서보다 영양원소의 농도가 훨씬 높게 나타났다. 클로로필의 양은 매우 높았고 저생생물도 대형동물 상(大型動物祖 macrofa u na,1mm 이상의 크기)은 대표적으로 풍부한데 반 해 소형동물상(小形動物相, meio f a u na, 1mm 이하의 크기)은 종다양성이 현 저히 낮았다. 소형동물상이 대부분의 지역에서 대표적인 성분인 접을 고 려하면 이 동물상의 종다양성 감소가 폐수 오염으로 인한 악영향의 최초
의 칭후라 할 것이다. 저충수는 상충수보다 비교적 덜 영향을 받으며 일 반적으로 크고 내성이 강한 대형 저생동물일수록 변화에 대한 대응력이 크며, 미세한 형태를 갖는 동물일수록 내성이 작다. 어류는 오염물질이 나 자연적인 환경의 변화에 민감하여 이룰 도피함으로써 피해가 적다. 6-5-2 생활하수 두기장소의 수질 두기장소 부근 수역에 대한 생활오수 스릿지의 영향은 폐수의 영향이 미치는 최대거리인 약 40km 밖에 있는 비오영해수의 N 과 P 의 값을 상 회하는 증가량(6. N, 6. P) 으로 판단할 수 있다. 투기장소의 현황이 잘 알 려진 수역들은 표 6-5 에서 보는 바와 같다. 여기서 스릿지에서 오는 영 양원소에 의해 영향받은 해수의 분산속도 R 은 다음과 같이 구할 수 있 다(여기서 P 는 인의 경우). R (p) (m2/day) = 수심연 (간m) 유x P입 의량 x증P가 의량 유(t:,,입.P 량 X( 0t. 0 /3d1a g y/)m 3) (N 의 경우 : t:,,.N X0. 014 g/m 3) 표 6-5 에서 R 의 값은 실제의 속도라기보다 화학적 의미로 〈축적〉 〈바 축적〉을 구별하는 지수의 의미를 갖는다(J ohns t one, 1976). 표 6-5 생활하수 두기 장소에서의 영양영 강화와 축적 강l 소 수(m십) 연(1간 00유 만입 t)량 AP AN (RP) (NR) 템즈강의해 18 5.0 o. 90 4.0 17 28 뉴욕만 37 4.5 0.47 2.5 14 20 리버풀만 18 0.55 。 •38 2.7 4.5 4.6 Garroch 하구 80 1.1 0.49 2.2 1. 0 2. 6 6.P : µg-a t P04-P/dm3 , c:,,. N:µg -a t N03-N/dm3 , R( 분산속도) : km2/day 자료 : Joh nsto n , 1976
이 지수로 분석하면 Garroch 하구는 〈 축적 〉 상태이고 템즈강 의해는 〈 비 축적 〉 상태인 반면 뉴욕 만은 리버풀 만보다 덜 〈 축적 〉 된 상태를 보여준 다. 템즈 강 의해는 유속이 크고 매우 혼탁하며 난류를 아루고 있어서 영양영류가 상당량 유입되어도 거의 커다란 반응을 나타내지 않는다. 이 에 비하여 영양영의 유입량이 거의 비슷한 뉴욕만의 경우에는 만의 깊은 수심, 넓은 수역, 의해로의 분산 등으로 해서 해수의 운동이 템즈강 의 해에서보다 비교적 느리기 때문에 때때로 식물플랑크톤의 성장이 높은 수준(약 15µg / l chloro p h y ll) 에 이른다. 그러나 실제로 식물플랑크톤의 성 장은 매우 높은 편이라기보다는 일정한 편이라 할 수 있는데 그 이유는 지역적으로 높은 탁도, 부영양화, 폐기물에서 나온 독물질, 그리고 입자 상 물질들과 함께 침전하는 등, 상당량의 영양영류가 이용되지 못하기 때문이다. 결과적으로 뉴욕만은 환경조건의 변화가 매우 커서 생활하수 에 의한 단기간의 영향을 평가하기는 어렵다. 리버풀만의 경우에는 강수 유입에 따른 염분의 국지적인 변화가 매우 크며 영양영류의 유입은 생활 하수 스럿지에 의한 증가보다는 강수에 기인하는 영양영류의 증가가 더 크다. 또한 NH4+ 에 의한 질소강화가 No2-, N03- 에 의한 것만큼 중요 하게 나타나 분산속도가 여전히 높은 수준을 유지한다. 이 수역에서는 영록소의 불균등한 분포(p a t ch) 가 수질 변화에 따라 단기적으로 나타나 며 연간 변화도 뚜렷이 보인다. 예컨대 1970 년에는 식물플랑크톤의 성장 저해가 일어나(클로로필의 양 0.4~0.9µg /l) 규조류가 희귀해지고 Phaeo cy s tis 종만이 출현하였는데 1971 년 여름에는 식물플랑크톤의 성장 이 정상을 회복하였으나 수역에 악영향을 미치는 쌍편모조류의 대번식이 일어났다. 두기장소 부근에서 영양영류의 불균등 분포는 상당기간 해수 이동이 제한되었음을 보여 주어 특정 종류가 대증식을 일으킨 원인을 설 명해준다. Garroch 하구 수역에서 저충수의 이동속도는 0. 01~0. 03 m/sec 로 매 우 느리기 때문에 분산이 극히 제한된다. 영양영류의 수준은 겨울에 어 느 정도 축적되나 여름과 가울에 걸쳐 식물플랑크톤의 성장(클로로필의 양, 5µ g /l) 으로 거의 다 소비된다. 이 수역에서는 비정상적인 식물플랑
돈의 대증식은 일어나지 않는다. 위의 4 개 수역의 경우를 비교해보면 난류와 해수 교환이 하수 스럿지 의 영향을 얼마나 변화시킬 수 있는가를 명백하게 보여준다. 템즈강 의 해에서는 영양영류가 급속히 해수로 분산하여 상당한 지역이 영양원소로 강화되어 지역적 영향을 받게 된다. 뉴욕만에서는 의해수로의 분산이 더 욱 촉진되어 영양영류의 축적이 덜 이루어진다. 리버풀만에서는 분산이 보통 정도로 이루어져 수질의 변화성이 커진다. 그리고 독성물질과 바람 직하지 않은 상태의 발전으로 식물플랑크톤의 성장이 둔화된다. 그러나 의해수가 들어오게 되면 정상으로 회복된다. Garroch 하구에서는 분산이 매우 느리지만 수심이 깊어 영양영류의 축적이 훨씬 적다. 또한 저충수 의 난류가 거의 없어 영양영류가 서서히 빠져나가기 때문에 적당히 식물 플랑크톤의 성장이 유지되고 이에 따라 풍부한 동물플랑크톤상이 이루어 진다. 6-5-3 부영양화의 일반적 영향 부영양화는 사실상 모든 수역에서 나타나는 자연적안 과정이다. 영양 소와 유기물질의 점진적인 축적은 생산량의 수준을 증가시킬 뿐만 아니 라 퇴적물 축적에 기인하는 평균수심의 감소가 일어나는데 이는 자연적 인 부영양화 과정이다. 이에 비해서 비자연적인 작용으로 부영영양화가 촉진되는 것을 단순히 문화적 부영 양화 cultu r al eutr o p h ic a ti on 라 한다. 이러한 비자연적인 촉진은 흔히 영양물질이나 유기폐기물이 수역으로 투 기됨으로써 이루어진다. 따라서 환경의 오염과 관련된 부영양화는 곧 문 화적 부영양화를 의미한다. 실제로 부영양화는 많은 수역에서 유익하게 작용할 수도 있다. 사실상 연못이나 유사한 폐쇄수역에 대하여 신중하게 비옥화(肥沃化)하는 일은 어류나 패류를 대량 생산하려는 양식(養殖) 활동의 기본적인 기술이다. 분명히 생산울 자극하는 것 자체에 근본적인 잘못은 없다. 그러나 부영 양화는 우리가 관심을 갖고 있는 수역이 적절하게 관리되지 않는 경우, 특히 증가된 생산량 수준과 이에 관련된 영향이 그 수역에서 더 중요하
다고 생각되는 다론 이용성과 조화를 이루지 못할 경우에는 다음과 갈은 여러 가지 문제가 야기된다. 첫째로 부영양화된 수역과 관련있는 생물이 왕왕 빈영양(貧 營 養)수역 에 특징적인 생물보다 인간의 관점에서 바람직하지 못하다는 것이다. 예 컨대 유기물질의 강화와 관련되는 남조류는 악취와 심미적 관점에서 좋 지 않은 식물이며, 오영 수역에서 우점하게 되는 어류들은 통상 오영되 기 전에 동일 수역에서 서식하였던 어류보다 가치가 적다. 하와이의 Kanehoe 만이 부영 양화된 후에 가치 없는 조류가 무성 하여 건강한 산호 군집을 완전히 파괴하였다. 오영된 수역에서 이와 같은 생물상의 변화는 결국 환경의 악변(惡 變 )을 초래한다. 죽 부영양화는 거의 예의없이 수역 의 생산성울 증가시키지만 생산된 생물의 가치는 경제적, 심미적, 과학 적인 관점에서 볼 때 혼히 감소한다. 둘째로 고도로 부영양화된 수역 내의 산소농도는 일반적으로 빈영양화 혹은 중영양화된 수역의 그것보다 훨씬 넓은 범위로 변동한다. 일부 생 물이 해수중의 산소농도가 포화상태에 가깝지 않으면 효과적으로 기능을 나타내는 것이 불가능하기 때문에 이러한 생물은 흔히 부영양화된 환경 에서는 존재하지 않는다. 낮은 산소농도는 부영양화된 호수의 심층수에 서 볼 수 있는 바와 같이 계절적인 현상이거나 높은 생산수역의 수충 속 에서 야간에 나타나는 현상일 수도 있다. 수백만 개체의 어류가 떼죽음 을 당하는 일은 경우에 따라 비교적 제한되고 고도로 부영양화된 수역에 서 밤새 나타나는 산소농도의 급속한 강하에 주로 기인한다. 일부 수역 에서 나타나는 심각한 부영양화 문제는 산소농도의 급강하에 따른 어류 의 대규모 때죽음과 바람직한 종류가 사라지는 일이다. 셋째로 수역 내에서 식물플랑크톤이나 대형식물이 과다하게 발생하는 것은 심미적인 문제를 야기하고 레크리에이션 자원으로서의 수역의 가치 를 감소시킨다. 순전히 심미적인 관점에서라면 고도로 빈영양화된 수역 에서 볼 수 있는 수정처럼 맑은 물의 특칭이 가장 바람직하다. 식물플랑 크돈의 높은 농도는 물을 혼탁하게 만들고 심미적 관심을 끌지 못한다. 또한 대형식물의 번성은 수영활동에 전적으로 부적당하다. 고도로 부영
양화된 수역에서 생산되는 대량의 식물 생체량은 초식동물에 의해 전부 소비되지 않기 때문에 대량의 잉여 식물생체량이 부패해서 악취와 함께 국도로 불결한 의관을 나타내게 된다. 넷째로 부영양화 수역에서 발생하는 특정 생물의 고농도는 종간(種間) 의 자원에 대한 경쟁과 포식압력을 크게 증가시킨다. 이러한 고도의 경 쟁과 포식은 물리화학적인 억압과 결합하여 때때로 생태계 내의 생존경 쟁을 특히 날카롭게 만든다. 그 결과 혼히 종의 다양성은 빈영양수역에 비해 훨씬 낮아지게 된다. 물론 어떤 특정 목적을 위해서는 수역 내에서 몇 종만으로 우점되는 것이 필요할 경우도 있다. 예컨대 양식업자들은 한 두 종류의 어패류를 생산하는 수역으로 만들고자 하는 목적으로 수역 울 관리한다. 이러한 수역은 생산성이 매우 높지만 균형을 이룬 환경을 유지할 수가 없다. 6-5-4 적조(赤潮 Red Tid e ) 부영양화된 수역에서 물리 • 화학적인 환경요인이 적절한 수준으로 변 화되면 식물플랑크톤이 돌연히 이상대증식(異狀大增植)을 일으켜 해수의 색을 변화시킨다. 이러한 현상을 적조라고 하며 연안역과 내만역에서 혼 히 나타난다. 우리나라에는 특히 전해만 수역이 적조다발지역으로 거의 연중 발생하여 피해가 매우 심각하다. 해수의 색은 적조 원인종(原因種) 의 체내 색소의 양과 생리상태에 따라 적갈색, 갈색, 녹색, 황색 등을 나타낸다. 해수는 점조성(*占桐性)과 특유의 냄새를 지닌다. 적조의 원인생물은 식물플랑크돈을 구성하는 수십 종류의 조류가 포함 되지만 특히 쌍편모조류와 규조류가 대표적인 종을 이룬다. 적조발생으 로 인한 상태계의 악영향은 여러 가지이지만 다음 4 종류로 정리할 수 있다. 첫째 대량의 플랑크돈이 발생하여 일정 기간이 지나면 역시 대량으로 폐사하게 되며 이에 따라 해수중에 유기물질이 크게 증가하고 세균의 활 동이 왕성하여 복잡한 분해작용이 진행된다. 이때 산소의 부족, H2S 의 발생, 유해물질의 생성 등으로 패류와 같은 저생생물의 대피해를 입게 된다.
둘째 쌍편모조류는 특히 다량의 점액질을 세포 의로 분비하는 종류가 많은데 이 점액질이 풀랑크톤의 폐사 후 대량 분비된다. 패류와 어류가 호흡하는 동안 이 점액질이 호흡기관에 부착하게 됨으로써 어패류의 질 식사룰 초래하게 되는 것으로 알려져 있다. 셋째, 적조생물의 폐사 후 많은 세균이 번성하면 세균 자체와 세균에 의해 분비되는 독물질이 어패류의 치사를 일으킨의 적조 중에 나타나는 세균의 일종인 간상균(棒狀菌)을 분리하여 9 종류의 어류에게 주사하면 5~47 시간 이내에 치사하게 되며 아 세균은 어체의 혈액 속에서 발견된 다. 그러나 감염 경로와 세균이 생성하는 독소는 아직 불확실하다• 넷째, 적조생물을 구성하는 대부분의 쌍편모조류는 다양한 유독물질을 생산할 수 있고 이 독소를 세포 내에 보유하기보다는 대부분 방출한다. 이 유독물질은 다모류를 제의한 광범위한 동물에게 신경과 근육장애, 호 홉장애 등을 일으키고 종류에 따라서는 불과 수시간 내에 어패류를 치사 케 한다. 또 어떤 유독물질은 용혈성(溶血性)을 갖고 있어서 어패류를 치사시킨다. 6-6 생활하수의 처리 생활하수의 처리는 일견 쉬운 일로 보인다. 즉 그 처리는 오랫동안 발 전되어왔고 그 결과 폐기물 속에 들어 있는 부유물질과 병원체를 제거하 는 일은 아주 성공적으로 이루어지고 있다. 그러나 질소와 인화합물을 모두 추출하기는 극단으로 어렵다. 미처리 생활하수는 고농도의 부유물 질, 영양물질, 병원체 등을 함유하고 있는데 현재 처리과정에서는 주로 부유고형물질 (SS), BOD, 영양소 등에 대한 처리가 이루어지고 있다. 하 수처리는 배출수의 질에 따라 여러 가지 단계가 요구된다(그립 6-2). 1 차 처리시설은 먼저 침사지(沈砂地)에서 대형 고체물질을 거르는 것 인데 침전탱크에 하수가 도착하면 밑으로 가라앉은 물질과 위에 뜨는 물 질이 있어서 이를 제거하게 된다 . 이러한 과정을 거쳐 남는 고형물질을
 I| _三___ 一 _ _ _ __ —一 _ _____I
I| _三___ 一 _ _ _ __ —一 _ _____I
그림 6-2 생활하수에 대한 1 차처리(단속선 내)와 2 차처리(정선 내)의 모형도
일차스럿지라고 한다. 2 차처리시설은 1 차처리에서 나오는 배출수가 두번 째 탱크를 지날 때 생물학적 과정에 의하여 BOD 를 제거하는 시설이다. 이 방법 에는 여 러 가지 가 있으나 활성스릿지 법 acti va te d sludg e sys t e m 과 삼수 여 과법 trick lin g filter sys t e m 이 대 표적 이 다.
표 6-6 각종 처리 방법에 의한 B0:1) 및 Ss' 의 제거효율 과정 BOD 재거율(%) SS 재거율(%) 정화조 25~65 40~75 1 차 처리 30~40 40~75 1 차처리 + 삼수여과 80~90 이상 80~90 이상 1 차처리+활성스럿지 85~95 이상 85~95 이상 자료 : Klein , 1 966' 삼수여과법은 2~3m 깊이의 원통에 2~10cm 지름인 자갈을 채운 원 형용기 속에 박테리아나 곰팡이를 넣고 다시 일부의 더 윗단계의 생물을 첨가한 뒤 스릿지를 통과하여 분해시킨다. 이 방법으로 통과한 BOD 의 70% 정도가 제거된다. 이때 배출수 속에 들어 있는 유기물질의 대부분 이 소비될 정도로 생물의 급속한 성장이 유지되고 또 생체량 성장 효율 이 낮게 유지되어야 한다. 활성스럿지법은 4 각형의 긴 탱크, 혹은 3~5 m 길이의 작은 탱크에 압축공기를 넣어 통기시킴으로써 배출수를 혼합 유동시킨다. 여기에 서식하는 생물은 박테리아가 주 분해자이고 곰팡이 는 두번째 중요성을 갖는다. 약 50% 정도의 유가물질이 탱크 속에서 산 화되며 스럿지의 양은 삼수여과법에 의해서 생기는 양의 2 배가 된다. 이 2 차 스럿지의 일부는 무산소 분해과정으로 전환되고 일부는 활성스릿지 탱크로 재순환된다, 표 6-6 은 여러 가지 생활오수처리 방법의 효율을 비 교한 것이다. 표에서 알 수 있듯이 활성스럿지 처리가 BOD 및 SS 제거 에 높은 효율을 나타낸다. 3 차처리는 대체로 영양소의 제거를 의미한다. 일반적으로 미처리 하수 의 영양소 농도는 원하지 않는 조류의 성장을 자극시킬 만큼 높다. 영양 소 문제를 이해하기 위해서는 미처리 하수 속에 있는 질소를 이용하여 생산될 수 있는 조류 생물량을 산화시키는 데 필요한 산소의 양과 미처 리생활오수에서 발견되는 대표적인 BOD 값인 200m g /l 을 비교해보는 것 이 좋다(표 6-7), 이때 생활하수는 통상 많은 식물플랑크톤의 요구량에
표 6-7 도시유수, 미처리 생활하수러 강우에 포함된 수 종 오염물질의 농도 도시유수 미처리 생활오수 강우 ss 227 200 13 BOD 17 200 <1 6 N 총량 3.1 40 1. 27 PO. 총량 (P 로서) 0.36 10 0,08 자료 : 미국 학술원, 1969 비해 낮은 N/P 율을 갖는다는 점을 상기할 필요가 있다. 미처리 하수의 질소 함량을 40m g /I 으로 하고 대표적안 식물플랑크톤의 산화가 다음과 같이 진행된다고 가정한다. (CH2 0)1 os(NHJ ) l6HJ P 0,+ 1 38 02- + 106 C02+ 1 22 H20 + 16 HN03+ H 3PO, 따라서 미처리하수 중의 질소로부터 생산된 식물플랑크톤 생물량을 산 화시키기 위해서는 (~길t N) (13186 갑~) (:킹鬪 )=789m g /l02 가 필요할 것이다. 이 결과 수역에서 심한 산소결핍현상이 발생한다. 이때 만일 스럿지처 리 쪽에 비중을 더 크게 두면 영양원소의 감소를 가져오고 02 처리 쪽에 비중을 더 두면 영양원소의 증가를 가져온다. 영양소 중 N 과 P 의 제거 방법은 다음과 같다. 6-6-1 p의 제거
P 의 제거는 주로 화학적 침전법을 이용한다. 배출수에 들어 있는 P 는 새로이 첨가된 CaO, AlSO., NaAl02 등과 결합하여 침전된다. 2 차표 6-8 생활하수 중의 인을 제거하기 위한 여러 가지 3 차 처리법의 제거효율과 비용 방법 P 의 제거효율(%) 바용 (S / 100 만 갤런) 화학적 침전법 58~95 10~70 흡착법 90~98 40~70 여과식 화학 침전법 95~98 70~90 이온교환법 86~98 170~300 역 삼두법 65~95 250~400 증류법 90~98 400~1000 자료 : Elia s sen and Tchobanog lo us, 1969 정화조에서 나오는 배출수에 이들을 넣으면 P 와 결합된 침전물을 비료 로 이용할 수가 있다. P 의 침전은 p H 의 영향을 받음으로 p H 의 조정 이 필요하다. Ca2 + 의 경우 pH 가 10 일 때 90~95% 가 제거되며 다른 원 소는 88~95% 가 제거된다. 표 6-8 은 생활하수에서 P 를 제거하기 위한 여러 가지 3 차처리의 제거효율과 비용을 나타낸 것이다. 표에서 보는 바와 같이 화학적 침전법이 많이 쓰이는 이유는 제거효율 이 높고 비용이 적게 들며 비교분석이 용이하기 때문이다. 6-6-2 N 의 제거 N 의 제 거 에는 암모니 아 스트리 핑 법 ammon ia stri pping 과 무산소 탈질 소법 anaerobic denit rifica ti on 이 많이 쓰인다. 전자는 2 차처리에서 나오는 무기질소의 대부분인 NH4+ 를 가스상태인 NH3 로 전화시켜 날려보내는 방법이다. NH4+ 와 NH3 의 평형상태는 pH 와 밀접히 관련되어 있어서 중성일 때에는 99% 가 NH4+ 쪽으로 이동하고 p H 가 11 이상에서는 98 % 이상이 NH3 쪽으로 이동하기 때문에 p H 를 11 이상으로 조정하여야 한다. 이 방법의 단점은 NH3 가스가 물에 대한 용해도가 크기 때문에 대량의 공기를 필요로 하는 접인데 lm3 의 배출수 중에 있는 NH3 를 95
표 e9 생활하수 중의 N 을 재거하기 위한 여 러 가지 3 차처 리법의 제거효율과 비용 방법 N 의 재거효율(%) 비 용 ($/100 만 갤론) 암모니아 스트리핑법 80~98 9~25 무산소 탈질소법 60~95 25~30 이온교환법 80~92 170~300 역 삼부법 65~95 250~400 증류법 90~98 400~1000 자료 : Eli as sen and Tchobanog lo us, 1969 % 제거하는 데 3000m3 의 공기가 소요된다‘ 탈질소법은 질소를 질소가스 (N2) 로 전환시키는 것이다 . 죽 N 을 N03- 로 산화한 뒤 N2 로 전환시키는 것이다 . 이 과정은 무산소 상태에 서 전행되며 N03- 로부터 유기질을 산화하기 위해서는 산소를 이용할 수 있는 특수한 미생물의 활동이 요구된다. 표 6-9 는 생활하수로부터 질소 를 제거하는 데 사용되는 여러 가지 3 차처리법의 제거효율과 비용을 나 타낸 것이다 . 적은 바용과 제거효율로 인해서 암모니아 스트리핑법이 많 이 쓰인다.
제 7 장 금속 7-1 금속의 섭취와 생물축적 금속은 해수의 자연 성분이며 토양과 암석의 풍화, 채광활동이나 화산 폭발 등으로부터 유래한다. 금속 가운데 많은 것이 생물에 대해서 필수 적이다. 예컨대 척추동물과 많은 무척추동물에서 발견되는 호흡색소인 헤모글로빈 haemo g lob i n 은 철을 함유하고 있으며, 많은 연체동물과 고등 갑각류의 호흡색소인 헤모시아닌 haemoc y an i n 은 구리를 포함한다. 피낭 류(被墓類)의 호흡색소에는 바나듐이 들어 있고 많은 효소가 아연을 포 함하며 비타민 B12 효소는 코발트를 함유한다. 이처럼 생물학적 연관을 갖는 금속은 다음과 같이 나뉜다. ® 수용액 중에서 보통 이동성 있는 양이온으로서 운반되는 경금속류(나트 륨, 칼륨, 칼슘등). ® 저농도에서는 필수적이나 고농도에서는 유독한 전이금속류(轉移金屬類) (철, 구리, 코발트, 망간 등). ® 일반적으로 대사활동에 요구되지 않으며 매우 낮은 농도에서 세포에 유독한 중금속 또는 준금속(淮金屬)류(수은. 납, 주석, 셀렌, 비소 등). 수용액으로부터 중금속 흡수는 일부 미생물과 성게 유생의 경우에 능
동수송계 (能動 翰 送系 acti ve tra nspo rt s y s t em) 에 좌우되지만 동식물에서는 일반적으로 표면에서의 흡착에 의해서, 그리고 표면세포 , 체액 등의 성 분으로 결합함으로써 이루어지는 수동확산( 受 動摘散,p ass i ve d iff us i on) 을 통해서 이루어진다. 동물에 대한 또 다른 중요한 경로는 금속이 음식에 흡착하거나 속에 존재할 경우와 이매패(二枚貝)의 아가미 같은 먹이집합 기작에 의해 입자성 또는 교질상의 금속을 흡수하는 경우이다. 동식물이 체내의 금속농도를 조절할 수 있는 정도에는 상당한 변화가 있다. 식물 과 이매패 연체류는 중금속 농도를 조철하는· 데 미숙하다. 십각류(十脚 類)와 어류는 일반적으로 아연과 구리 갇은 필수 금속을 조절할 능력을 갖고 있으나 수은과 카드뮴 같은 필수적이 아닌 금속의 조절은 능력이 훨씬 떨어전다. 해양생물의 금속농도가 동일 금속의 수중농도보다 수배나 더 높다는 사실은 금속이 해양의 먹이연쇄상에서 생물학적 확대에 의해 고영양단계 에서 점진적으로 농축된 것이라는 추측을 야기시켜왔다. 다랑어, 황새 치. 최상위영양단계 육식동물 등에서 발견되는 높은 수은 농도는 생물학 적 확대설과 일치한다. 표 7-1 캘리포니아-하와이 간에 채집한동식물플랑크톤중의 평균금속농도 (단위 : µg/g- orga nic dry weig h t) 금속 식물플랑크톤 동물플랑크톤 Cu 3.2 13.9 Zn 19 260 Pb 1. 0 8. 5 Fe 224 580 Mn 6. 1 4.4 Ag 0.2 0.25 Cd 1. 5 2. 3 Hg 0.19 0.14 자료 : Mart in and Knauer, 1973
표 7 - 1 은 캘리포니아와 하와이 사이에서 채집된 동식물 플랑크론 시료 에서 얻은 여러 금속 원소의 농도를 나타낸 것이다. 식물플랑크톤에서의 금속농도를 해수의 금속농도와 비교하면 약 3 배 이상 높으며 4 개의 금속 원소의 농도는 식물플랑크돈에서보다 동물플랑크돈에서 훨씬 더 높다. 비록 이 4 개의 금속농도가 동물플랑크론 중에서 증가한 것이 생물학적 확대를 암시하지만 이러한 효과는 전혀 상이한 기작, 죽 해수로부터 오 염물질의 직접 흡수와 해수와 생물간의 오영물질에 대한 교환평형상의 차이 등에 의해서 형성될 수도 있다. 따라서 표에서 나타난 이 4 개의 금 속에 대하여서는 동물 및 식물플랑크톤 사이에 농도상의 증가가 일반적 의미의 생물학적 확대와 생물 _ 해수간의 금속교환평형상의 차이를 어느 정도로 반영하는지를 말하기는 쉽지 않다 . 표 7 - 2 는 식물플랑크론, 동물플랑크돈 및 멸치들로 이루어지는 단일한 먹이연쇄상의 수은 농도를 조사한 것으로 최소한 이 금속에 관해서는 먹 이연쇄를 따라 확대되는 증거가 거의 없다. 실제로 떨치류의 각 부위별 수은 농도의 차이는 식물플랑크돈과 멸치류 사이의 농도상의 차이보다 더 크다. 멸치류의 상이한 부분에서의 수은 농도가 광범위하게 변화하는 오염물질은 농축시키는 상이한 조직에 대하여 영향을 미치는 생화학적 표 7-2 단일 먹이연쇄상에서의 수은 농도 영양단계 평 균수은농도 (ppb wet weig h t) 식물플랑크톤 28 동물풀랑크돈 12 멸치류 피부 10 생식소 15 아가미 30 근육 40 간 90 자료 : Martin and Knauer, 1973
요인의 중요성을 반영하는 것이다. 이러한 생화학적 혹은 생리학적 차이 는 또한 수중의 먹이연쇄상에서 생물의 상대적인 위치에 관계없이 어떤 생물이 다른 생물보다 훨씬 더 높은 수준의 오염물질을 농축시키는 데 중요한 역할을 하게 된다. 7 크수은 7-2-1 해양환경으로의 유입 경로 세계의 연간 수은 생산량은 1971 년 10,600 톤t을 최대로, 1977 년에는 6,000 톤으로 감소하였다. 공업국가에서의 대표적인 수은 사용 양상은 표 7-3 에서 보는 바와 같다. 수은의 연간 생산량 가운데 상당한 부분이 결 표 7-3 미국에서의 수은 소비량(단위 : 톤) 1968 1974~75 노o 겨o 118.3 91 . 4 아말감 9. 8 8.6 촉매 59.0 81. 8 치과용재료 120.1 131 .1 전가 기구 593.4 783. 2 염소 및 가성소다의 전해질용 601 .1 788.8 일반실험용 71.6 71. 6 공업 및 제어기기 307, 1 319.1 페인트 364.5 370.0 종이 및 펄프 12.9 8.6 제약 20.7 22.4 기타 269.6 2'05 . 6 겨 I 2,548.7 2,882.2 자료 : Clark, 1986
국 자연환경으로 돌아간다. 수년간 누적된 자료에 의하면 (Clark, 1986) 핀란드와 스웨덴에서 손실된 수은 총량의 약 절반은 영소-알칼리 공업에 서 나타난다. 염소와 가성소다는 수은전극을 이용해서 전해질방법으로 생산되며 이러한 과정을 통해서 이들을 1 톤 생산하는 데 150~200 g의 수은이 대기나 폐수로 손실되는 것은 보통이다. 손실된 수은 총량의 나 머지 반의 대부분은 수은 화합물을 불가피하게 환경으로 분산시키는 여 러 용도, 예컨대 제재 (製材) 및 제지 (製紙) 공업에서 곰팡이 제거용으로 쓰는 화학물질, 선박의 선체를 도장하는 방오페인트, 농경에서 사용하는 살충제와 각종 제약 등에서 유래한다. 이러한 환경으로의 유입은 전세계적으로 연간 약 5,000 톤으로 추정되 는데 여 기 에 화석 연료의 연소로부터 다시 연간 약 3, 000 톤이 추가된다 (Clark, 1989) . 원유와 석 탄은 수은의 흔적 만을 함유하고 있지 만 대 량이 연소되기 때문에 이처럼 많은 양이 대기 중으로 유입된다. 1960 년대초 인류보건에 대한 해수중의 수은의 위험이 발견됨에 따라 일부 지역에서 는 주요 출처로부터 수은 유입이 현저히 감소되었다. 오래된 공장에서는 폐수중의 수은함량을 8µg /g 이하로 감소시키는 데 어려움을 안고 있으 나 새로운 공장의 폐수로부터의 수은 유입은 현재 낮은 상태에 있다. 이 러한 출처로부터 대기로의 수은 손실은 배기가스를 냉각시킴으로써 감소 시킬 수가 있다. 수은의 자연적 안 유입은 2 개의 출처로부터 온다. 연간 약 3, 500 돈은 수은아 들어 있는 암석의 풍화에서 유래하고 연간 25,000~150,000 톤이 화산지역, 지열화도(地熱火道, vent) 등에서 대기로 들어간다. 확실하게 추정할 수는 없지만 수은농도가 0.001~0.05pp b 로 변화하는 대양역에서 는 이 대기로의 수은 유입이 중요하다. 연안 수역에서 수은의 주요 출처 는 강, 해양배출구 및 바다로 직접 두기하는 폐기물이다. 이러한 국지화 된 유입은 지역 플랑크론과 홍합류의 수은 함량을 증가시키는 것으로 나 타난다. 해수중의 용존수은은 염화물이 우세한 H g (OH)2 나 H g Cl2 의 형태로 있 지만 수은은 또한 상당한 정도로 입자성 물질에 흡착되어 있어서 수용액
중에 나타나지 않는다. 수은은 해수중에 나타나는 유기화합물, 특히 유 황함유 단백 질 및 부식 질 ( 腐 植 腐 hu mic substa n ce) 과 더 불어 안정 한 복 합물질을 형성한다. 무산소성 기질에서는 수은이 Hg , Hg S 및 Hg S 2 등 으로 존재한다. 바다에서 미생물계는 모든 무기 형태의 수은을 메틸수은 meth yl mercu ry으로 전화시킬 수가 있다. 이 물질은 퇴적입자에서 쉽사 리 물로 방출되고 생물에 의해 축적된다. 7-2-2 조류(漢類)와 무척추동물 속의 수은 유기 형태의 수은은 무기영보다 독성이 더욱 크다. 표 7-4 는 홍조류에 대한 여러 수은화합물의 18 hLCs 。울 보여준다. 이들 화합물의 독성은 따개비와 새우에 대하여도 유사한 양상을 나타내는 것으로 알려져 있다. 다른 금속과 마찬가지로 이매패 연체동물은 주변 해수로부터 수은을 매 우 빨리 흡수한다. 그림 7 - 1 은 상업 용 굴인 Crassostr e a vir g i ni c a 가 수은 아세테이트에 노출되었을 때 수은의 흡수를 보여준다. 그리고 그림 7 김 표 7-4 홍조류 (Plumari a eleg a n s) 에 대 한 여 러 가지 수은 화합물의 독성 화합물 l8h LCs 。 (ppb Hg ) Meth yl mercuric chlorid e 44 Eth yl mercuric chlori de 26 n-Prop yl mercuric chlori de 13 n- B uty l mercuri c chlori de 13 n-A my l mercuric chlori de 13 Isop ro p yl mercuric chlorid e 28 Isoamy l mercuric chlorid e 19 Pheny l mercuric chlori de 54 Pheny l mercuri c iod id e 104 Mercu ric iod ide 156 Mercu ric chlori de 3,120 자료 : Clark, 1986
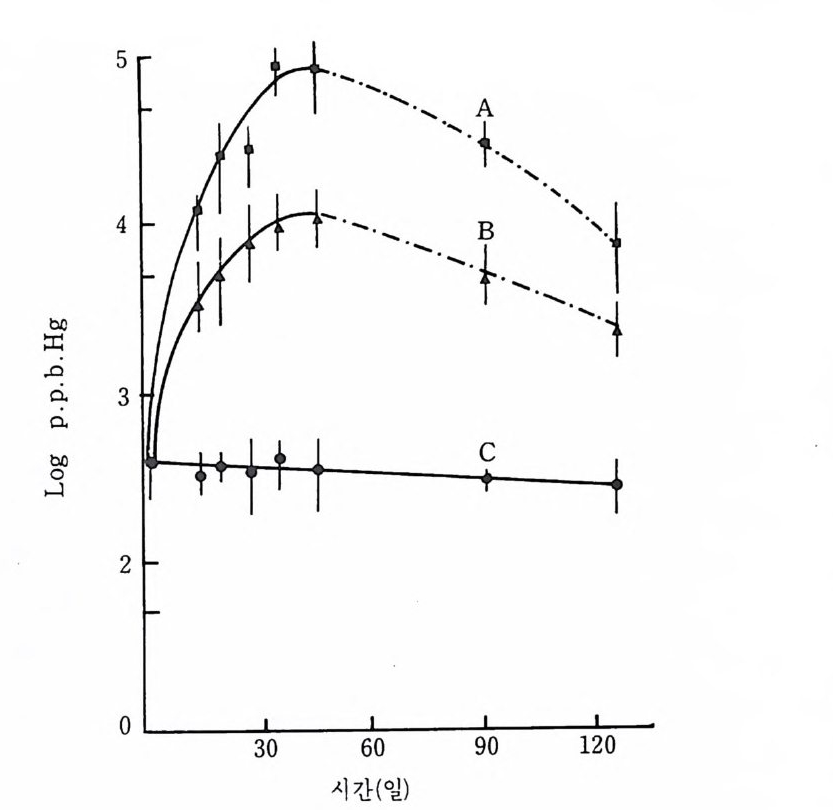 5
5
그림 7-1 대 형 굴 Crassostr e a virg i nic a 을 45 일 간 아세 트산 수은에 노출시킨 뒤 깨끗한 해수에 넣었을 때 수은의 섭취와 손실 A : mercuri c aceta t e 농 도 lOOp pb , B : mercuric nuta t e 농도 lOp pb , —C : co:n t오r o영l 된 해수 — · 一 : 깨끗한 해수 (자료 : Clark, 1986)
는 흡수된 수은이 조직 속에서 분포하는 양상을 나타내고 있는데 이매패 류의 경우에 내장에서 가장 높은 농도를 보이는 반면 근육에서는 농도가 가장 낮다. 일단 연체동물이 비오탁수역으로 되돌아가면 수은은 체내로 부터 손실되는데 그 손실률은 어떻게 섭취하였느냐에 좌우된다.
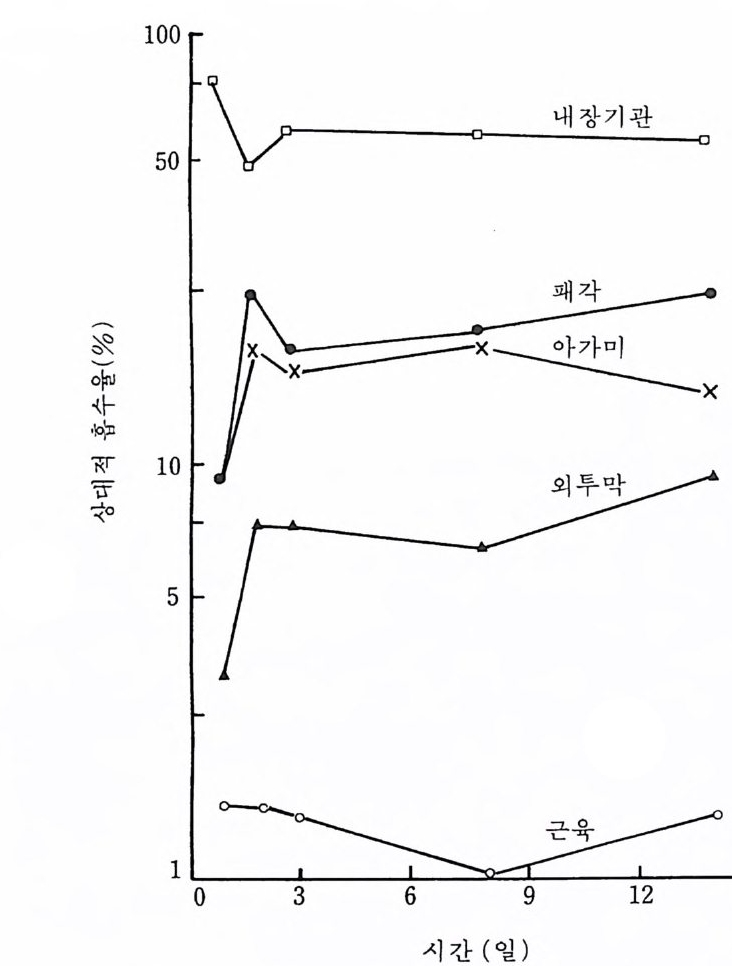 15000 \
15000 \
그림 7-2 새조개의 상이한 조직 내 수은 (H g Cl2) 흡수 (자료 : Clark, 1986)
7-2-3 어류 속의 수은 해양에 서식하는 어류는 오염수역에서는 훨씬 더 높은 값이 발견되지 만 대부분의 종류가 근육 속에 150µ g /k g (0.15 pp m) 의 수은을 함유하고 있다. 수은으로 심하게 오탁되어 있는 스웨덴과 덴마크 사이의 해협에 사는 대구는 1. 29 pp m 까지 수은을 포함하는 데 반하여 북해산 대구는 0.15~1 . 20 ppm , 그린랜드산 대구는 0. 01~O. 04 ppm 의 수은을 함유한
다. 한편 다랑어 , 황새치, 녹새치 등과 갇은 일부 대형 어류는 통상적으 로 높은 수은 농도를 갖고 있다. 근육 속의 수은 농도가 1. 0 pp m 은 보 통이며 4.9 pp m 까지 나타난다. 이러한 현상에는 몇 가지 이유가 있다. 이들 어류는 먹이연쇄의 끝에 있는 육석동물이며 따라서 이들의 먹이는 생물축적과 생물확대의 결과로 높은 수준의 수은을 함유하게 된다. 먹이 만이 수은의 원천이 아니다. 이들 어류는 매우 활동적이어서 대사율이 상당히 높다. 입을 벌린 채 계속 유영을 하기 때문에 아가미를 통해 강 한 해수의 흐름이 생기고 결과적으로 대량의 산소를 흡수하게 된다. 그 러나 이때 물속에 용존된 금속(수은 포함)도 아울러 흡수한다. 흡수되는 수은의 많은 양이 메칠수은의 형태이고 이러한 형태의 수은이 어류에 섭 취된 후에는 배출이 되지 않기 때문에 조직 속의 농도가 어류의 연령과 더불어 증가한다. 수은 함량이 높은 것은 대형이면서 연령이 오래된 어 류이므로 이들을 먹는 것은 위험한 일이다. 가자미류는 또 다른 오래 사는 종류로서 대량의 수은 농도를 축적한 다. 300k g되는 대형 가자미는 50 년이나 되었을 것이며 115kg 이상 나 가는 모든 큰 가자미와 60 kg 이상 나가는 것 가운데 반 이상이 근육 속 에 l ppm 이상의 수은 농도를 갖고 있다. 대부분의 다론 어류와 마찬가 지로 이 수은의 90% 이상이 meth y l mercu ry 이어서 이들 어류는 인간 이 소비하기에 부적당하다. 7-2-4 새 속의 수은 새는 간과 것 속에 수은을 축적하는 경향이 있고 그 농도가 어류보다 훨씬 높게 나타난다. 대형 바닷새는 20 년 혹은 그 이상 오래 사는데 상 위 영양단계에서 먹이를 취하는 새들이 수은을 축적하기 쉽다 . 특히 해 안이나 해안 가까운 곳에서 생활하는 종류가 가장 위험이 높다. 예컨대 해안에서 생활하는 검은바다오리는 의양에서 먹이를 취하는 종류보다 더 많은 수은을 함유한다• 발틱해의 오염은 물고기를 먹이로 하는 새의 수은 수준을 반영한다. 발틱해의 물수리 날개에서 나타나는 수은의 양은 같은 종이 겨울철 아프
리카에서 생활할 때보다 더 많다. 또한 발택해의 바다오리는 그린랜드의 바다오리에 비하여 5 배나 많은 수은을 함유한다. 심한 금속 오염에 노출된 새들은 주기적으로 깃갈이를 함으로써 것의 수은 축적에 대한 안전판 구실을 한다. 핀란드에서 물수리 새끼에 대한 연구는 먹이 속의 수은 농도와 깃털 속의 수은 농도 사이에 확실히 관계 가 있음을 보여준다. 시험에 사용된 물수리 새끼 중 2.5% 는 것의 수은 함량이 300 pp m 을 넘었다. 한편 비오염지역과 오염지역에서 채집한 물 수리 새끼의 비교는 간의 수은 함량이 오영지역 새끼의 경우 2 배나 더 높았다 (Clark, 1986) . 7-2-5 포유류 속의 수은 해양 포유류는 먹이로부터 대량의 수은을 축적한다. 그러나 셀렌이 수 은의 독성을 중화시키는 것으로 알려져 있으며 물개, 강치 돌고래 등의 조직 속에는 셀렌 함량이 수은 함량과 비슷하게 나타나고 있다. 특히 돌 고래 간의 결합조직에서 발견되는 mercury selen i de 는 분명히 먹이로부 터 섭취한 meth yl merceur y에 대한 해독작용의 산물이다. 7-2-6 미나마따병 (Mina mata dise ase) 수은이 인간에게 유독하다는 것은 수세기 전부터 알려져왔다. 금세기 에 들어와서는 인간에 의해 바다로 유입되어 인류의 사망을 초래한 유일 한 금속 오염물질이 되었다. 바다의 오염으로부터 유래한 수은 중독은 일본의 작은 어촌인 미나마 따에서 발생하였다. 이곳에는 주민의 일부가 어업에 종사하고 1952 년에 vin y l chlorid e 와 aceta l dehy d e 를 생 산하기 시 작한 공장이 하나 있 었다. 1953 년 처음 발생한 이 병은 어부와 그 가족에게서만 발병하였으나 1956 년까지는 그 원인이 미나마따만에서 잡은 어류와 해산물에서 연유하는 금속 중독임 을 알지 못하였다. 총 2, 000 건이 발생 하여 그중 43 명 이 사망 하였으며 생존자 중 700 명 이상이 영구적 인 무능력자로 남았다. 1957 년 초부터 이 만에서의 어업이 부분적으로 금지됨에 따라 발병은 중지되었
으나 수은이 이 병의 유독성분이라는 것이 알려진 것은 1959 년이었고 1960 년에 가서 야 수은의 출처 가 만으로 방출된 vin y l chlorid e 공장의 폐 수라는 사실이 규명되었다. 일본에서 수은 중독이 두번째로 발생한 것은 1965 년 아마고강 하구 부 근에 사는 어부들에 의해서였다. 미나마따 참사와 마찬가지로 공장폐수 에서 나오는 수은에 오영된 어류가 그 원인인데 이 경우 공장은 60km 나 떨어전 상류에 위치하고 있다. 미나마따 참사는 상세히 조사되 었으며 meth yl mercury 중독의 표본이 되었다. meth y l mercur y는 분비될 수 없기 때문에 무기수은보다 더욱 사람에게 위험하다. 따라서 이 물질은 축적성 독극물로 작용하고 뇌의 혈관으로부터 신경조직으로 침투하기 때문에 점진적이고 회복할 수 없는 뇌손상을 일으킨다. 무기수은에서 오는 주요 위험은 그것에 대한 만성 노출에 좌우된다• 메 틸화박테 리 아에 의 해 무기 수은으로부터 생 산되 는 meth yl mercu ry 의에 미나마따 공장폐수는 무기수은도 포함한다. 1950 년대에 이 공장은 mercuric sulph ate 를 촉매 로 사용하는 공정 에 의 해 aecta l dehy d e 를 생 산하였다. 이 방법으로 생산되는 aceta l dehyd e 1 톤당 보통 300~1 . OOOg 의 수은이 소실 되 고 이 가운데 5% 가 meth yl mercury 이 다. mercuric chlorid e 는 vin y l chlorid e 생 산에 서 촉매 로 사용되 며 생 산물질의 론당 약 lg 의 meth y l mercury 가 세 척 과정 에 서 소실된다. 1959 년 미 나마따 만에서 수행된 조사는 공장 배출구 부근의 오염된 퇴적물은 수은 함량이 200 pp m 이나 되었으며 좀 떨어진 곳에서는 12 pp m 으로 감소함을 보여 준다. 플랑크톤은 5p pm , 조간대지역의 이매패류는 10~39p pm , 어류는 10~55 pp m 의 수은을 포함하는데 어류 속의 수은은 대부분 메틸화된 것 이었다. 7-2-7 공중위생 기준 미나마따 참사에 이어서 오탁된 해산식품을 섭취하는 데에서 오는 수 은 중독이 널리 인식되었고 여러 나라에서는 상품화원 식품 중에 수은
허용기준을 도입하게 되었다. 세계보건기구 (WHO) 는 식품 중에 들어 있 는 meth y l mercur y의 최대 허용량을 0. 2 mg 또는 주당 최대 섭취 허용 량을 0.3m g으로 정한 바 있다. 어느 기준이나 어류 속에 들어 있는 수 은의 농도는 물론, 얼마나 어류를 섭취하는가를 참작하여야 한다. 해산식품 중에 들어 있는 수은의 최대 허용량 기준은 미국과 캐나다에 서 0.5p pm , 이탈리아 0.7p pm , 일본, 독일, 스웨덴, 스위스에서는 1.0 ppm . 그리고 노르웨이에서는 1. 5 pp m 이다. 7-3 카드뮴 7-3-1 해양환경으로의 유입 경로 카드뮴은 지각에 널리 분포하나 특히 아연과 결합되어 있으며 아연제 련의 부산물로서만 상업적으로 생산된다. 카드뮴은 대략 1950 년 이래 대 량 사용되어왔고 세계 · 총생산량은 연간 약 15, 000~18, 000 톤이다. 카드 뮴의 주 용도는 풀라스틱과 전기도금에서 안정제와 색소로 쓰이는 것이 지만 상당량이 땜납과 기타 합금, 그리고 밧데리에서 사용된다. 이들 일차 생산물에 사용된 카드뮴의 10% 이하가 재순환되고 나머지 는 환경으로 방출되는 것으로 가정하여야 한다. 수량화될 수는 없다 해 도 환경으로의 다른 유입은 다음과 같은 다양한 원천으로부터 온다. ® 카드뮴 생산은 물론 납 및 아연의 채광과 정련에 기인하는 연기, 먼지 및 폐수. ® l00~SOO pp m 의 카드뮴이 포함된 전기도금의 세척수. ® 강철, 제철, 비철금속 공업에서 나오는 먼지와 연기 및 폐수, 카드뮴 이 들어 있는 스럿지. ® 금속의 아연도금 피막에 사용되는 아연에 약 0 . 2% 의 카드뮴이 불순물 로 포함되고 이 카드뮴은 모두 4~12 년 이내에 부식으로 소실됨. ® 아연산화물 속에 불순물로서 20~90 pp m 의 카드뮴을 포함하고 있는 자동차 타이어의 마모.
® 인산염 암석이 100 pp m 의 카드뮴을 포함할 수 있고 인산영 비료가 환 경 내의 카드뮴 원천이다. @ 석탄은 0.25~5.0p pm , 난방용 기름은 0.3 pp m 의 카드뮴울 포함한다. 그러나 대기로의 방출량은 알려져 있지 않다. ® 생활오수 스럿지에는 3 Qpp m 까지 카드뮴이 포함된다. 세계 해양으로의 카드뮴 유입량은 연간 거의 8, 000 톤에 이르는데 이 양의 약 반은 인위적인 활동의 결과이고 나머지는 자연산이다. 강과 대 기 에 의 한 유입은 동등하게 중요하다. 연간 약 2, 900 톤의 카드뮴이 해 저 퇴적물(대부분이 대륙봉역)에 침전하지만 그 나머지의 동태를 설명하기란 어려운 일이다. 바다에서 알려진 카드뮴의 동태는 해양의 수급량과 균형 울 이루지 못하며 바다의 카드뮴 함량은 서서히 증가하고 있다. 7-3-2 해양 생물 속의 카드뮴 마지의 원인으로 카드뮴이 100 ppm 까지의 농도에서 식물플랑크톤의 광합성과 성장을 촉진하지만 생물체의 필수성분은 아니다. 인산염과의 결합 때문에 카드뮴이 식물플랑크톤이 흡수하는 것으로 생각되지만 두 경우를 제의하고는 카드뮴이 먹이연쇄상에서 축적되는 것 같지 않다. 예 컨대 카드뮴 2.1 pp m 을 함유하고 있는 식물플랑크톤을 먹이로 한 유우 파우시 아류 Mega n yc tip h anes norveg ica 는 9. 6 ppm 의 카드뮴울 포함한 배설물 입자를 내지만 전 체내의 농도는 0.7 pp m 에 불과하다 (Clark, 1986). 먹이망의 더 높은 단계에 있는 어류와 해양포유류는 대부분 수 ppm 정도의 낮은 카드뮴 농도를 지니고 주로 신장에 저장하는데 금속치 오닌을 생산함으로써 무독화시킬 수가 있다. 바다가마우지와 바다소금장이는 다같이 오염원과 거리가 먼 표충 동물 풀랑크톤을 먹이로 취하는데 높은 카드뮴 농도를 갖는 경향으로 보아 표 층에서 생활하는 동물플랑크톤은 높은 카드뮴 수준을 갖고 있음이 분명 하다. 바다가마우지는 간에서 49p pm , 신장에서 240 pp m 의 카드뮴을 각각 포함하며 바다소금장이는 보통 33 pp m 을 갖고 있지만 330 pp m 까
지도 포함한다. 연체동물은 대량의 카드뮴 농도를 축적한다. 이매패류에서는 특히 심 하여 2,000 pp m 까지 간에 축적하고, 해양 오징어류에서는 1,900 pp m 까 지 축적한다. 그 종류는 분명한 카드뮴 축적의 증거가 있어서 38 pp m 까 지 축적하는 반면 고동을 먹이로 하는 따개비는 불과 0.15 pp m 을 축적 한다. 7-3_3 카드뮴 독성 카드뮴의 독성은 수은과 유사점과 차이점을 갖는다. 수은의 그것에 마 찬가지로 카드뮴은 생명을 유지하기 위해서 소량이나마 요구되지 않는 다. 다른 점은 카드뮴 이온 (Cd”) 만으로도 독성효과를 나타내는 것으로 알려져 있다 . meth yl mercury 와 유사한 더 유독한 화합물로 카드뮴이 전화하는 것은 알려진 바 없다. 장(腸)에 의한 카드뮴의 홉수효율은 약 5~6% 이지만 칼슘이나 단백질의 부족시에는 창자의 흡수효율이 증가된 다. 여러 가지 식품, 공기, 물 등에 들어 있는 카드뮴 농도의 분석을 보 면 사람이 하루에 식품으로부터 45~80µg , 공기로부터 0.02~1.0mg , 물로부터 1. 0~2.5µ g의 카드뮴을 섭취하는 것으로 나타난다 (Fr i ber g et al., 1974) . 카드뮴은 한번 섭취되면 혈액에 의해 체내의 모든 부위로 운반된다. 거의 대부분의 기관이 Cd 울 흡수하지만 언제나 간과 신장에서 가장 높 은 농도가 발견된다. 체내 축적량의 대략 3 분의 1 이 간에서 발견된다. 수은과는 달리 Cd 중독의 가장 큰 관심은 섭취된 Cd 의 사람 몸 속의 잔류기간이 극단으로 길어서 16~33 년이나 된다는 사실이다. 결국 카드 뮴은 소량이 오랜 기간에 걸쳐 축적되어 급성 혹은 만성 수준까지 이르 는 잠행성 독물질이다. 사람의 경우 신생아에게는 카드뮴이 없지만 45~50 세에 이르기까지 꾸준히 체내에 축적된다. 체내에서 카드뮴은 치오닌thi one i n 이라는 저분자 단백질에 의해 간과 신장에 농축되는 경향이 있으며 이 단백질은 카드뮴은 물론, 수은, 아 연, 구리 등과 같은 중금속과 친화력이 있어서 금속치오닌 me t allo th-
i one i n 이라는 금속 단백질 복합체를 형성한다. 금속치오닌 내에서 중금 속을 결합시키는 일은 금속들이 중요한 효소계와 상호작용하는 것을 방 지하는 세포간의 방어기작을 이룬다• 카드뮴의 독성효과는 필시 유황, 질소 또는 기타 음성전기 작용기 elect ro neg at i ve fun cti on al grou p s 를 갖는 유기 배 위 자 (有機配位子) 에 대 한 금속의 친화력과 관련된다 (Ra y and Coff in, 1977). 금속은 아연을 포함하 고 있는 효소에 특히 친화력을 나타내므로 동물에 대한 카드뮴의 독성효 과는 아연을 투여함으로써 부분적으로 방지할 수가 있다. 가장 십한 독 성효과는 신장, 특히 세뇨관에 대한 손상으로 나타난다. 증세는 소변에 서 단백질과 카드뮴 양이 증가하는 것이다. 해양 어류와 패류에 대한 카드뮴의 초기 치사수준은 0.5~50 pp b 의 범위에 있다. 카드뮴은 해양생물에 의해서 해수의 농도보다 수십배 농축 될 수 있다. 예컨대 카드뮴 농도가 0.05 pp b 에 불과한 해수에서 채집한 식물플랑크톤의 평균 카드뮴 농도는 2.3~4.4 pp m 을 나타낸다 (Ma rti n and Broenkow, 1975) . 한편 새우와 굴에 대 한 카드뮴의 치 사농도는 각각 2 ppm , 40~ 100 ppm 인 것으로 보고되 어 있다. 7-3-4 이따이-이따이병 {itai-itai dise ase) 일본의 서부 전쭈강변에 있는 작은 마울에서 1955 년 이따이-이따이병 이 처음으로 발생하였는데 이 병은 특히 뼈와 관절에 영향을 주는 고통 스러운 병으로서 100 명의 사상자를 내었다. 이것은 아연의 제련과정에서 나오는 폐수에 들어 있는 카드뮴이 쌀에 오염된 데 기인한 것이다. 그렇 지만 현재는 이따이-이따이병이 카드뮴과 관련된 것인지 혹은 영양실조 및 비타민 결핍에 관련된 것인지에 대한 의문이 제기되고 있다. 굴 속에 들어 있는 고농도의 카드뮴과 아연을 섭취하여 많은 사람이 구토증을 일 으켰지만 카드뮴으로 오탁된 어패류를 먹음으로써 영구적으로 영향을 받 는다는 증거는 없다. 오염된 수역에서 생산된 굴, 전복 및 일부 이매패 류를 제의하고 해산 식품이 다른 식품보다 더 많은 카드뮴을 함유하지 않으며 특별한 위험을 나타내지도 않는다.
그러나 카드뮴은 수은 및 기타 위험 금속과 더불어 바다로 방출하거나 투기하지 않도록 국제적으로 합의된 물질의 하나이다. 7-4 구리 7-4-1 해양으로의 유입 경로 광석의 부식으로부터 바다로 들어가는 구리의 유입량은 연간 325,000 톤 정도로 추정된다. 인간활동으로 유발되는 유입량은 국지적이며 크게 변한다. 전기기구, 화학촉매, 선박의 방오페인트 및 목재방부제 동을 위 해 생산되는 구리의 양은 연간 75 만 돈에 이른다. 이러한 사용으로 구리 는 불가피하게 환경으로 들어가게 된다. 도시 생활하수는 상당량의 구리 룰 포함하며 이것이 두기장소에서 증가된 농도로 나타난다. 로스앤젤레 스의 도시폐기물로부터 연간 510 톤의 구리가 바다로 들어간다. 스페인의 콘월강과 리오 틴토강으로 유입하는 구리와 주석의 채광 찌꺼기는 강의 구리 및 아연의 농도를 크게 높이는 결과가 된다. 선박의 방오페인트는 그 속에 함유된 모든 구리 성분을 해수로 방출한다 . 이 양은 무시할 수 없는 정도로서 이 페인트는 l 당 500 g의 구리를 함유하고 있다. 따라서 산타바바라와 샌디에고 사이의 캘리포니아 연안 수역은 이 방오페인트에 의해서만 연간 180 톤의 구리가 해수로 방출된다 (Clark, 1986). 해수중의 용존구리는 CuC03, Cu2+ 및 CuOH + 의 형태로 존재하지만 구리는 쉽사리 용액에서 제거되어 입자에 흡착한다. 7-4-2 해양생물 중의 구리 구리는 동물의 필수성분의 하나로서 십각류(十脚類), 복족류(腹足類), 및 두족류(頭足類) 등에서 가장 높은 농도가 발견되는데 이들 생물의 호 홉색소인 헤모시아닌 haemoc ya ni n 이 구리를 함유한다. 잉여 구리는 통 상 간에 저 장하고 있 어서 문어 Octo p u s vulg a ris 의 간에 서 는 4,800 ppm 의 구리 가, 그리 고 바닷가재 Homarus ga mmarus 의 간이 자 hep a to p a ncreas 에
서는 2,000 pp m 의 구리가 측정되었다. 헤모시아닌울 갖고 있지 않은 굴 은 구리의 농도가 매우 높게 축적되는데 대부분 백혈구에 저장되며 구리 20, 000 ppm , 아연 60, 000 ppm 에 달한다. 비록 오염수역의 플랑크톤 , 어류, 패류 등이 바오영수역의 생물들보다 더 높은 구리농도를 갖지만 구리는 일반적으로 먹이연쇄상에서 축적되지 않는다. 먹이연쇄의 최상위단계에 있는 포식성 어류인 새치 Makair a i nd i ca 는 수은을 축적하지만 구리의 농도는 낮아서 간에 o.5~22.0p pm , 근육에 0. 3~ 1. 2 ppm 을 포함한다. 구리는 수은과 은 다음으로 광범위한 해양생물에 대하여 매우 유독하 다. 이 때문에 선박의 방오페인트에 사용된다. 잘 알려진 구리의 손상효 과는 1965 년 네덜란드 연안에서 불법으로 두기된 대량의 황산구리에 의 해 유발된 것으로, 이로 인해 0. 3 ppm 이상의 구리를 포함한 해수가 해 안으로 서서히 올라 옴에 따라 플랑크돈, 어류 및 패류가 사망하였다. 오염수에서 성장하는 이매패류는 구리를 축적하는 능력을 갖고 있어서 해수농도의 7, 500 배 까지 농축시 킨다. 다량의 구리가 축적 되 면 근육이 녹 색으로 변하는데 이는 굴에서 흔히 보게 된다. 이와 같이 변색된 굴을 상품화하려면 버오염수역에 1 년은 놓아 두어야 회복된다. 구리 섭취에 의한 인간의 치사량은 100mg 정도이므로 해산식품으로부터 구리 중독 의 위험은 없으나 구리가 식품에 5.0~7,5p pm 정도로 함유되어도 맛에 있어서 형오감을 느끼게 된다. 7-5 납 7-5-1 해양환경으로의 유입 경로 세계의 납 생산량은 연간 4,300 만 돈에 달한다. 금속형태, 밧데리, 종 아 파이프 등에 들어 있는 많은 납은 회수되어 재순환되지만 화합물 형 태로 사용된 대부분의 납은 환경으로 소실된다. 세계 납 생산의 약 10% 는 휘발유 첨가제로 사용되고 그 대부분이 공기로 소실된다. 인간활동의
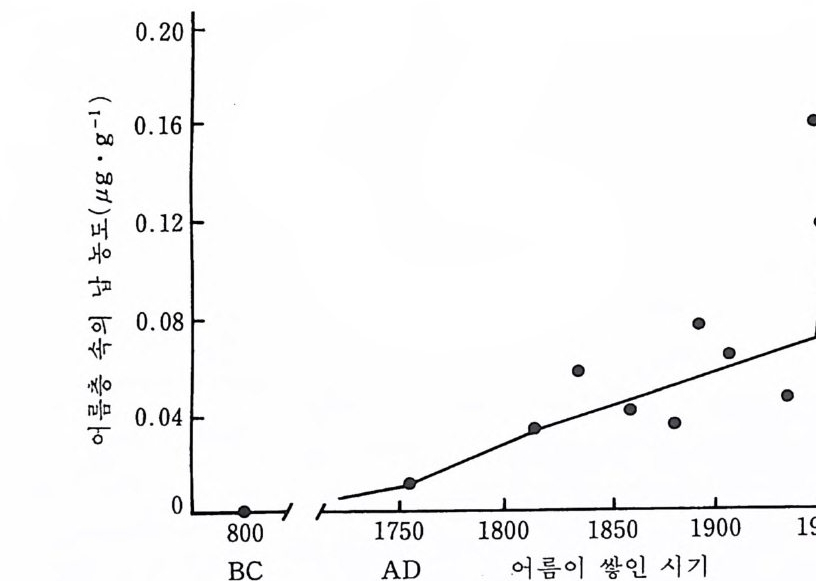 0.2 0
0.2 0
그림 7-3 그린랜드의 연간 쌓인 어름 충에 함유된 납의 농도 (자료 : Clark, 1986)
결과로 대기에 방출되는 납의 양은 연간 45 만 톤임에 반해 자연상으로 대 기 에 방출되는 양은 연간 25, 000 돈에 불과하다. 납 연무(煙霧)는 비와 눈에 섞여 지상에 도달하고 광범위하게 분산된 다. 해수중의 납농도에 대한 분석은 표충수가 심해수보다 더 높음을 보 여준다. 더욱 홍미로운 것은 그린랜드의 어롬 속의 납농도를 분석한 결 괴는 납의 농도가 기원전 800 년 이래 수배로 증가하였음을 밝혀준다. 이 증가는 1800 년경 분명히 증가가 시작되 었고 1940 년 이후에 매 우 크게 증 가하였다. 이 두 번의 큰 증가는 산업혁명의 영향과 자동차 수의 증가를 반영하고 있다(그림 7-3). 납의 농도가 국지적으로 높은 것은 특수한 여건과 관련이 된다. 로스 앤젤레스 부근의 캘리포니아 연안에서 잡힌 농어는 간 속에 납 22p pm 을 함유하고 있는 데 반해 의해역에서 잡은 농어는 9 pp m 을 함유하고 있음이 측정되었는데 이는 분명히 세계 최고의 자동차 밀도를 가전 로스
앤젤레스의 공기와 관련이 있는 것이다. 하수슬럿지 두기장소는 높은 납 농도를 갖는다. 영국의 글라스고에서 나오는 하수슬럿지는 납 771 ppm 울 포함하고 두기지역의 퇴적물에서는 납의 농도가 200~320pp m 을 나 타낸다. 7-5-2 해양 생물에 대한 영향 다론 금속과 비교해서 해수중의 납은 특별히 유독하지 않으며 질산납 Pb (N03) 2 은 농도 0. 8 ppm 까지 규조류인 Phaeodact ylu m 의 성 장을 증 가시킨다(그림 7-4). 저농도의 아치사효과는 섬모충류인 원생동물 Cri sti g er a 를 0.15 ppm 에서 8. 5%, 그리고 0. 3 ppm 에서 11. 8% 까지 성 장을 억압한다. 갑각류인 A rt emia의 성장은 5~10 pp m 에서 심하게 감소 되었고 홍합의 경우에 lO pp m 에서 노출을 연장시키면 사망률이 증가한다. 그렇지만 일부 생물은 분명한 손상을 입지 않고 고농도의 납을 축적할 수가 있다. 예컨대 공중낙진으로부터 오염된 샌프란시스코 부근 해역의
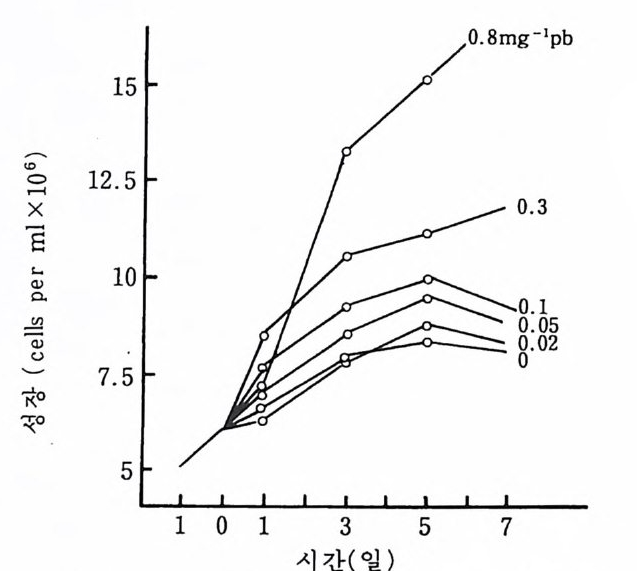 15 / 0.8 m g -1 p b
15 / 0.8 m g -1 p b
그림 7-4 여러 농도의 질산납이 첨가된 배양액에서의 규조류 Phacodacty lu m 의 성장 (자료 : Clark, 1986)
삿갓조개 Acmaea dig itali s 는 약 lOOp pm 의 납을 함유하며 , 납의 농도가 2, 175 ppm 이나 되는 영국 남서부의 간빌강 하구에 서식하는 이매패류인 Scrobic u lari a pla na 는 납을 991 ppm 까지 포함한다. 가장 저 항성 이 큰 홍합은 납의 함량이 3,000 pp m 까지 올라감이 알려져 있다. 홍합은 납에 대한 제독기능을 갖고 있어서 소화선 내에 과립상으로 대 량을 저장한다. 금속의 축적경향 때문에 홍합은 일정한 기간마다 감시되 어야 한다. 의국에서는 시장 상품화를 위해서는 납의 농도가 lO pp m 을 넘지 않도록 규제하고 있다. 납은 육상에서는 보건상 심각한 손상을 일으킴에도 불구하고 해수와 해산물 오염은 문제시되지 않는 것으로 생각된다. 7-6 철 철은 통상 바다의 중요 오염물질은 아니지만 보오크사이트로부터 산화 알루미늄을 추출하는 과정, 그리고 titan iu m d i ox i de 의 생산과정으로부 터 폐기물을 무기하는 곳에는 두드러지게 나타난다. 왜냐하면 이 두 종 류의 폐기물은 철을 대량으로 함유하고 있으며 폐기물의 생산량이 매우 크다. 죽 유럽에서는 연간 산성철을 약 750 만 돈을 생산하며 그 가운데에서 560 만 톤이 직접두기를 통해서, 또한 강을 통해서 바다로 방출된다. 두기물 속의 산은 대부분 극히 국지적인 영향을 미치지만 철분은 수화 산화물로서 침전하여 동물의 패각과 배갑(背甲)에 영향을 미친다. 또한 입자들은 어란과 유생에 부착한다. 수화산화제이철은 홍합에 있어서 체 중감소를 일으키고 사망률을 증가시킨다. 해수중의 철산화물의 행동을 실험실에서 재현하는 일은 불가능하며 두 기장소에서의 연구는 폐기물 중의 철의 영향에 대하여 확실한 증거를 보 여주지 못한다. 그러나 철폐기물과 관련된 영향 때문에 미국 환경청은 titan iu m diox id e 의 해 양두기를 해 안에서 90 마일 이 상 의 해 측에서 하도 록 권장하고 있다.
제 8 장 산업페수 산업활동으로부터 방출되는 일부의 폐수는 수질오염원 가운데 최악에 속한다. 산업폐수의 두기 결과로 나타나는 수질에 대한 역효과는 보통 아래의 두 경우 중의 양자나 하나가 원인이 된다. 첫째, 일부 산업폐수 중의 BOD 와 SS 는 미처리 생활하수 중의 BOD 와 SS 보다 10 배 이상 높을 수가 있으며 산소부족, 탁도, 퇴적 등의 문 제가 이러한 폐수의 방출로 야기될 수 있다. 둘째, 일부 산업폐수는 고농도로 독성물질을 포함한다. 흔히 상이한 여러 가지 독물질이 동일한 폐수 속에 치사량 또는 치사량에 가까운 농 도로 존재한다. 이러한 폐수가 처리되지 않고 방출된다면 결국 배출구 부근의 모든 생물이 죽게 될 것이다. 어떤 경우에는 이들 독물질이 어류 나 패류에 흡수되어 이들 생물아 안간에게 적합하지 않을 정도로 농축된 다. 특정 산업폐수에서 발견되는 독물질의 특성은 물론 관련된 산업에 전적으로 좌우된다. 8-1 산소 감소 펄프공장, 제당공장, 식품가공공장 갇은 산업체에서 나오는 폐수는 수
천 ppm 이상의 높은 BOD 를 갖는 경우가 보통이다. 이와 대조적으로 미처리 생활하수는 통상 약 200 pp m 의 BOD 를 갖는다. 만일 산업체가 폐수를 소량만 방출한다면 수역에 대한 영향은 많은 경우에 미미하게 나 타날 것이다. 왜냐하면 수역 내에서 배출수가 크게 희석될 것이기 때문 이다. 그러나 불행히도 그 반대의 경우가 보통이다. 예컨대 하루 500 돈 의 생산능력을 갖는 아황산법 펄프공장은 1, 650 pp m 의 BOD 를 갖는 폐 수를 하루에 약 30 만갤런이나 만든다. 이 공장 하나만으로도 폐수방출 량은 인구 24 만의 도시에서 나오는 생활하수의 양과 같으며 BOD 부하 량은 약 200 만 인구로부터 나오는 양과 맞먹는다. 만약에 이러한 대량의 BOD 가 철저하게 혼합되지 않는 수역으로 배출 된다면 산소 농도가 필연적으로 수생군집을 유지하기 어려운 수준으로 떨어지게 될 것이다. 이러한 경우는 BOD 가 높은 산업폐수가 강이나 하 구로 배출될 때 흔히 일어난다. 그림 8-1 은 BOD 가 높은 폐수를 배출하
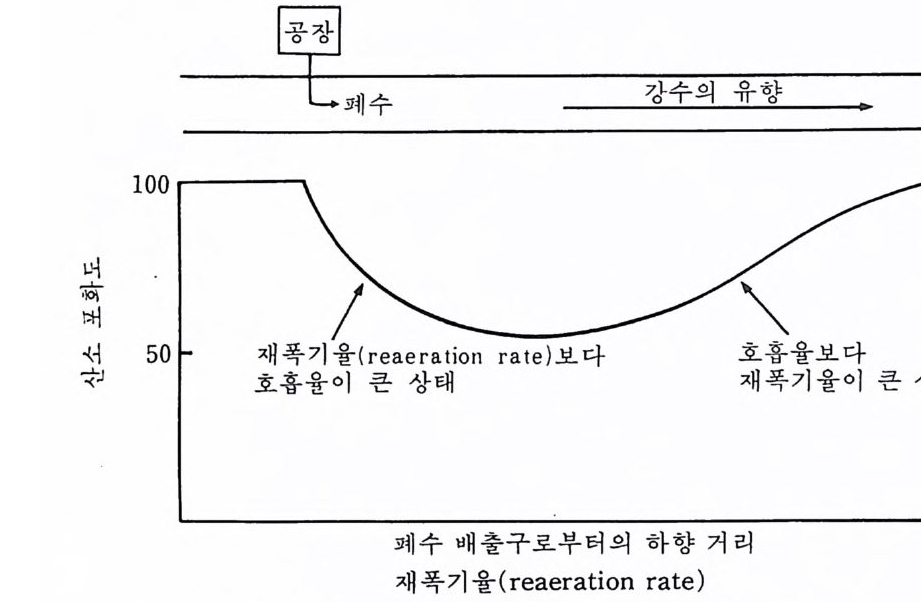 三폐수 강수의 유향
三폐수 강수의 유향
그림 8-1 높은 BOD 를 갖는 폐기물을 강수로 두기했을 때 용존산소량의 변화로 생기는 특칭적인 산소 감소 곡선
는 공장으로부터 하류에 내려가는 거리에 따라 용존산소의 농도가 어떻 게 변화하는가를 설명해준다. 폐수에 있는 미생물에 의한 호흡(산화)은 대기와 수계 사이에서의 산 소교환으로 산소를 공급할 수 있는 것보다 더 빨리 산소를 소비한다. 그 결과 폐수 배출구의 하류에서는 물속의 산소농도가 급속히 떨어진다. 미 생물에 의한 소비로 인하여 산화성 유기폐기물의 농도는 배출구로부터의 거리가 증가함에 따라 일정하게 감소한다. 대기로부터 수계로의 순 산소 유입량은 산소농도의 100% 포화와 물속의 실제 산소 농도와의 차이에 비례한다. 배출구로부터 멀어질수록 이 순 산소유입량률은 미생물의 호 홉률을 초과함으로써 물속의 산소량이 증가하게 된다. BOD 가 높은 폐 수의 배출구로부터 하류에 나타나는 산소농도의 특칭적인 강하와 상승을 보통 산소감소 oxy ge n sag 이 라고 한다. 그리고 도표에 나타난 곡선은 산 소감소곡선 oxyg e n sag curve 이 라 한다. 산소감소곡선에 나타난 두 개의 변화는 특히 중요하다. 만일 배출구의 BOD 부하량이 충분히 크다면 하천에서의 산소농도는 결국 영 zero 으로 떨어지고 상당한 거리에 이르기까지 그 수준이 남아 있을 것이다. 극단 의 경우에는 무산소 수역이 수 km 에 달할 수도 있다. 이러한 무산소 수 역에서는 동물상이 완전히 제거되는 결과를 초래한다. 두번째 변화는 2 개 혹은 그 이상의 산업체가 동일 하천의 아주 가까운 거리에서 폐기물 을 배출하는 경우에 나타난다. 결국 2 개 혹은 그 이상의 산소감소가 결 합된 영향은 수질에 대해 훨씬 더 해로울 것이다. 많은 공장폐수가 갖는 산소 소비의 참재력은 국도로 높기 때문에 각 산업체는 그 폐수의 특성을 면밀히 감시할 수 있도록 주의를 기울여야 한다. 혼히 산업체에서는 그들의 배출수 중에 들어있는 산화성 물질의 양의 지표로서 BOD 를 사용하지 않는 경향이 있는데 이는 일차로 표준 BOD 검정법이 5 일간이란 시간이 소요되기 때문이다. 배출수의 산소소비 잠재력이 얼마나 급속히 증가하는가를 찾아내는 데 5 일이란 시간을 동물 상에 대하여 쉽사리 재앙을 불러울 수도 있다. 이 문제를 극복하기 위해 서 산업체에서는 흔히 COD 검정법을 사용한다. COD 는 시료내 유기물
표 8-1 미처리 생활하수 및 도시유수 중의 COD 와 BOD 비교 COD(pp m ) BOD(pp m ) COD/ BO D 미처리 생활하수 350 200 1. 8 도시유수 111 17 6.5 자료 : Weib e l, 1969 질이 강산화제에 의해 산화될 때 소비되는 산소량과 동일한 값이다. 보 통 COD 는 시료를 크롬산과 황산의 혼합물 속에 2 시간 동안 환류시킴으 로써 측정하는데 이 산화방법은 거의 변함없이 표준 BOD 검정법보다 더 큰 산소소바를 일으킨다. 왜냐하면 내화력 때문에 직각적으로 미생물의 먹이로 이용되지 않는 많은 유기물질이 시약에 의해 쉽사리 산화되기 때 문이다. 반면에 수중 미생물에 의해 이용되는 aceti c acid 같은 일부 화 합물은 표준 COD 검정법으로 쉽사리 산화되지 않는다. 서로 다른 폐수 의 유기물 조성에 있어서 변화성 때문에 COD/ B OD 율은 한 형태의 폐 수로부터 다른 폐수에 이르기까지 크게 변화할 수 있다. 표 8 - 1 은 COD / BOD 율이 얼마나 변화할 수 있는가를 보여준다. COD 측정은 짧은 시간에 결과를 얻을 수 있으므로 유용성이 크다. 그러 나 방출된 폐수 중에서 기대되는 단기 산소소비량을 이 방법으로 더 정확 히 추정할 수 있으리라고 믿을 수는 없다. 오히려 그 반대일 수도 있다. 그 러나 특정 산업폐수와 관련된 주어진 COD 부하량으로부터 기대되는 산 소억압의 크기를 추정하는 것은 가능하다. 따라서 COD 농도를 감시함으 로써 산업공장의 관리자는 그의 공장으로부터 나오는 배출수가 언제 배출수 역에서 심각한 산소 결핍문제를 야기시킬 것인가를 추정할 수가 있다. 8-2 펄프 산업 펄프제조과정에서 사용되는 물의 양은 펄프를 만드는 방법과 펄프의
특성에 따라 크게 좌우된다. 신문용지를 만드는 데 쓰이는 쇄목펄프 gro undwood pul p 생 산량 1 톤당 약 21 m3 에 불과하지 만 고급용지 (사무용) 의 경 우는 1 톤당 250 ~ 350 m3 의 용수가 필요하다. Wi lbe r (19 69) 에 의 하 면 펄프산업에서는 펄프 1 톤당 평균 약 200m3 의 용수가 필요한 것으로 알려져 있다. 연간 약 500 만 돈의 펄프를 생산하는 공장에서는 연간 폐수를 약 1 km3 를 방출할 것이다. 펄프공장 폐수의 특성이 펄프롤 만드는 방법에 크게 좌우되므로 어떻게 펄프와 종이가 만들어지는가를 고찰해볼 필요가 있다. 8- 2 -1 종이의 생산단계 1) 통나무는 먼저 제재실에서 껍질이 벗겨지고 펄핑 p ulpi n g에 적절한 작은 조각으로 자른다. 2) 다음 단계는 펄프 자체의 생산이다. 이 과정에서는 목질조직의 세 포벽을 구성하는 셀루로스와 리그닌을 부분적으로 분해시켜 부드럽고 물 렁물령한 펄프를 만든다. 펄핑과정은 기계적이거나 화학적 방법, 혹은 양자의 조합으로 완성된다. 3) 펄프가 생산되면 생산하려는 종이의 질에 따라 다양한 처리를 하게 되는데 처리에서는 다음의 과정을 포함한다. 첫째 펄프의 암색성분을 제 거하기 위한 표백과정에서 염소화를 거치게 되며, 이때 형성된 염소화리 그닌을 제거하기 위해서 수산화나트륨에 용해시킨다. 둘째 펄프에 필요 한 바탕을 주기 위해 재생 종이를 첨가한다. 또한 종이의 광택을 위해서 점토를 첨가하며 종이의 바탕을 조절하기 위하여 펄프를 크기별로 분류 한다. 4) 마지막으로 일련의 단계를 거쳐 펄프를 종이로 전화시키는데 압착 롤러로 펄프롤 압착하여 종이를 만들고 재단할 수 있도록 건조시키는 데 에서 공정이 끝난다. 이 일반적인 공정은 모든 펄프공장에서 거치는 과정이며 공장폐수의
역겨운 성질을 결정하는 주요 요인은 나무칩으로부터 펄프를 만드는 데 사용되는 방법이다. 기계적인 펄핑은 주로 신문용지를 위한 펄프롤 생산하는 데 사용된다. 소위 쇄목펄프는 물의 존재하에서 돌바퀴로 나무칩을 갈아서 만든다. 이 과정에서 나오는 폐수는 비교적 적은 양의 용존유기물질과 대량의 목재 섬유로 구성된다. 화학적 방법으로 펄프롤 생산하는 데에는 보통 두 가지 방법이 있다. 두 가지 방법이 다 셀루로즈와 리그닌의 분해롤 촉진하기 위해 여러 가 지 화학 약품을 첨가한 고압솥에서 나무칩을 처리하는 일로 이루어전다. 소위 아황산법은 칼슘, 마그네슘, 혹은 기타 나무를 처리하기 위한 염 기와 함께 아황산 (H2SO 어울 첨가한다. 처리 용액은 산성이다. 이 아황 산법은 처리용액 내에 있는 화학물질의 회수가 거의 이루어지지 않는다. 이 공정에서 오는 폐수는 미처리 하수의 경우보다 약 10 배의 BOD 를 갖 고 있다. Wald ic huk (1 962) 에 의하면 아황산법을 사용하는 공장에서는 소비된 원목의 55 내지 63% 가 폐기물로 나오는데 이때 나무칩과 섬유 또는 용존유기물질의 형태를 취한다• BOD 의 많은 부분이 목재당(木材 糖)으로 생성되는데 이 물질은 미생물의 좋은 먹이원이 된다. 용존유기 물질은 또한 지방산, 지질, 리그닌 및 셀루로즈를 포함한다. 용존유기물 질의 일부는 폐수와 함께 방출된 미사용 아황산이 유독한 것처럼 수중 생물에게 분명히 유독하다. 소위 크래프트 펄프법에는 목재가 NaOH 와 Na2S 가 포함된 염기성 재료 속에서 처리된다. 처리화학물질의 횟수는 이 크래프트법의 불가결 의 부분이다. 처리화학물질의 약 95% 가 재순환되고 배출액의 BOD 는 아황산법에비교하여 약 10% 에 불과하다. 그러나 폐수의 독성은 일반적 으로 더 큰데 이는 일차적으로 크래프트법에서 사용되는 화학물질의 존 재 때문이다. 유화수소와 여 러 가지 유기유화물 (CH3SH 등) 이 특히 유독 성분이다. 크래프트법을 쓰는 공장의 폐수는 또한 수중생물에게 유독한 수지(레전)와 지방산 비누를 포함하는데 이들은 산화조건하에서는 유기 유화물과 H2S 보다 더 안정하다.
8- 2 -2 펄프공장 페수의 특성 부유물질 (suspe n ded solid : SS) 펄평방법에 관계없이 펄프공장 폐수는 높은 부유물질 농도를 지니며 부유물질은 일차적으로 작은 나무칩과 섭유로 구성된다. 전형적인 아황 산법 공장은 배출수 중에 약 6, 000 ppm 의 고체농도를 포함한다. 이 가 운데 용존고체가 주를 이루지만 부유입자 물질도 상당량 포함된다. 이 입자성 물질은 배출 수역의 바닥으로 침전하여 자연저생군집을 완전히 파괴할 정도로 축적될 수 있다. 자연저생군집이 상위 영양단계 생물에 대하여 먹이와 피신처를 제공하기 때문에 저생생물의 파괴는 예의없이 전 수충의 생물에게 영향을 미친다. 어류 또한 저생생물군을 산란지역과 육종지역으로 이용한다. 자연저생생물군이 펄프공장 스럿지로 덮이면 수 생태계에서의 그 일상적인 역활이 정지된다. 그 좋은 예로 캐나다의 부 리티시 컬럼비아 연안에서 펄프공장 스릿지에 의해 저생생물군이 파괴된 것 (Waldic h uk, 1962) 을 들 수가 있다 . 이 폐수는 아황산 및 크래프트 펄 프, 신문용지, 그리고 특수용지의 생산에서 오는 폐수의 혼합물로 구성 된다. 입자성 물질은 바닥으로 침전하고 이 스럿지의 분해는 퇴적물과 해저를 무산소 상태로 만들었다. 부근에서는 살아 있는 동물을 볼 수 없 었으며 퇴적물이 표충으로 울라울 때에는 유화수의 냄새가 심하게 났다. 펄프공장폐수 중의 SS 는 어떤 생물에게는 직접 독성효과를 나타낸다. 예컨대 펄프공장 폐수의 SS 는 어류의 아가미를 막아서 질식사를· 일으킨 다. 또한 저농도에서도 같은 기작을 통해 만성적인 억압을 줄 수 있을 것이다. 그러나 펄프공장 폐수의 주된 악영향은 다음과 같이 요약할 수 있다. 죽 해저에 축적됨으로써 저생생물의 기질을 완전히 변화시키고 자 연저생군집을 이동시키는 결과를 초래한다. 그리고 해저상에서의 분해는 많은 경우에 퇴적물과 저충수를 무산소 상태로 진행시킨다. 용존 유기물질 펄프공장폐수 중의 유기물질은 처리과정 중에 분해되고 용해된 나무
성분이 거의 대부분이다. 기계적인 펄핑과정은 화학적인 과정보다 용존 유 기물질을 적게 생산한다. 이 유기물질은 다양한 수질오염 문제를 야기한다. 목재의 당 같은 많은 용존유기물질은 박테리아와 기타 미생물에 의해 쉽사리 이용되는데 이와 같은 먹이로서의 산화과정은 배출액의 BOD 를 매우 높게 만드는 요인이다. 만약 폐수가 담수로 방출되면 그 하류에 협 오성 점액 균류 sl i me fun g i 가 발생하게 된다. 이 점액은 어류의 알과 주 변수 사이의 가스의 교환을 방해하기 때문에 어란의 성장을 크게 감소시 키게 된다. 펄프공장폐수 중에 용해된 일부의 유기물질은 배출수액에 거품을 만드 는 성질을 갖고 있다. 일반적으로 거품은 염수에 의해서 억제되는 경향 이 있지만 크래프트나 아황산폐수가 고농도일 때에는 해수에서도 상당량 의 거 품을 생 성 시 킨다. 비 록 독물학적 tox ic o log ica l 관점 에 서 는 거 품이 비교적 덜 중요하지만 거품으로 덮인 물이 심미적으로 매력이 없음은 의 심의 여지가 없다. 이와 같은 표면활성제는 해수와 대기간의 산소교환 역시 지체시킴으로써 높은 폐수 함량에 의해 야기되는 산소결핍 문제를 더욱 악화시킨다. 아황산 및 크래프트 공장폐수는 뚜렷한 색상을 갖고 있다. 아황산 폐 수는 특칭적인 호박색인 데 반하여 크래프트 폐수는 암갈색이다. 이러한 색은 용존유기물질, 특히 리그닌의 형태에 기인한다. 거품과 마찬가지로 색 자체나 색을 만드는 화합물에 대한 특정한 독성이 있지는 않으나 이 러한 색깔 있는 물의 출현이 반가울 까닭은 없다. 그럼에도 불구하고 이 색상은 폐수의 예민한 지표물질이 된다. 독성물질 새로 배출된 크래프트 폐수는 아황산 폐수보다 더 유독하다. 이보다 큰 독성은 크래프트 공정에서 사용된 화학물질 중 일부 화합물에서 유래 한다. 황화수소와 여러 가지 황화유기물질이 그중에서도 가장 유독하다. 아황산법의 특칭적인 폐기산물인 아황산 역시 수중생물에 대하여 유독하 다. 크래프트 및 아황산 폐수에는 다같이 수중생물에게 유독한 수지, 지
방산 비누 같은 용존유기화합물을 포함하며 경우에 따라 이들 용존유기 물질이 배출구 바로 부근에 떨어전 곳에서는 크래프트 독성의 주범이 된 다. 왜냐하면 황화유기물질과 유화수소는 더 유독하지만 또한 보다 불안정 하기 때문이다. 펜타클로로페놀과 펜타클로로산나트륨은종이와 나무펄프 를 보존하기 위해서 펄프산업에서 사용되는 방부제이다. 이들 방부제는 폐 수와 함께 불가피하게 방출된다. 불행히도 이 두 방부제는 수중생물에게 유독하며 어류에 대한 치사수준은 0.2~0.6 p pm 이다 (W il ber , 1969). 펄프 폐수의 독성연구는 흔히 담수나 해수의 미처리 폐수와의 희석정 도, 그리고 여러 가지 생물에 대한 희석폐수의 영향을 검증하는 일 등이 내포된댜 펄프공장폐수에 의한 독성 연구는 굴과 어류에 대하여 많이 이루어 졌 는데 이들 생물에 대한 아황산 폐수의 초기 치사수준은 대략 폐 수 : 해수의 비율이 1 : 1, 000 에서 치사가 일어나는 것으로 알려져 있다 (Wi lb er, 1969) . 그러 나 H2 S 와 유기 황화물질은 불안정 하기 때 문에 크래 프트 폐수에서의 치사 수준은 10~15 %정도로 높다. 불행히도 굴에 대한 만성효과는 급성독성 농도보다 훨씬 낮아서 3~16 pp m 의 아황산 농도에서 굴이 성장과 생식의 영향을 받는다. 다시 말하 면 굴에 대한 만성효과를 방지하기 위해서는 폐수를 약 100 만 배로 희석하 여야 한다. 따라서 희석은 이 문제를 해결하는 데 실제적인 방법이 못된다. Spr a gn e 와 Mcleese (1 968) 는 펄프공장 폐수를 제독시킬 수 있는 가능 한 방법을 제시하기 위한 실험에서 좋은 결과를 얻었다. 즉 새로 배출된 탈색 크래프트 폐수를 정지 상태로 2 주까지 저장한 디옴- 이 폐수가 연어 새끼와 바닷가재의 유생에 미치는 독성을 실험하였다. 저장기간 동안 폐 수중의 산소농도는 미생물에 의한 유기질의 분해 때문에 l~2m g//까지 감소하였다. 폐수에 통기를 시켜주지 않았지만 2 주 후에는 연어 새끼에 대한 폐수의 독성이 없어졌다. 죽 2 주간 저장하였던 100% 의 폐수에 7 일 간 노출시켰음에도 단 한 마리의 연어도 죽지 않았다. 그렇지만 바닷가 재 유생에 대한 독성에는 변화가 없었다. 이 결과는 바닷가재 유생과 연 어 새끼에 대한 급성 독성효과가 폐수 중에 들어 있는 상이한 물질에 의 해서 야기되는 것이며 2 주 경과 후 미생물 활동이 연어 새끼에 독성을
갖는 성분을 분해시킨 반면에 바닷가재 유생에 독성인 성분에는 영향을 미치지 못했음을 의미한다. 크래프트 폐수의 미생물 분해롤 가속·화시키 는 방법으로는 생물학적 산화시스템을 도입하여 미생물(박테리아와 원생 동물)의 성장을 촉진시키게 되는데 이러한 생물산화의 첫 1 주간에는 산 소농도가 lm g /l 로 강하하지만 제 2 주 동안에는 8m g /l 로 회복된다. 이 러한 처리를 한 2 주 후에 바닷가재 유생에 대한 폐수의 독성시험 결과는 유생의 생존시간이 36 시간으로 증가되었고 이 폐수를 56% 로 희석시킨 환경에서는 유생의 생존시간이 7 일까지 연장되었다. 위의 사실은 일부의 미생물이 펄프공장 폐수의 급성 독성성분을 부분 적으로 분해할 수 있음을 보여준다. 활성스럿지 처리과정에 생물산화 시 스템을 설치하거나 산화촉진연못 oxid a ti on po nd 울 마련함으로써 폐수의 독성을 크게 감소시킬 수가 있다. 크래프트 공장폐수의 경우에는 H2S 와 유기황화물의 제거가 주관심사인데 이는 메틸메르캄탄 me thy l mer- ca pt an 이 약 l pp m 의 농도에서 어류의 치사가 일어나고 H2S 는 약 1 ppb 에서 위험하기 때문이다. 그러나 다행히도 이 두 물질은 산소의 존 재하에서는 급속히 분해된다. 생물산화 시스템의 도입은 분명히 독성감 소에 있어서 매우 훌륭한 방법이다. 다만 폐수의 배출량에 따라서 상당 히 넓은 면적이 요구되는 것이 어려운 점이다. 8-3 제당 산업 제당공장으로부터 나오는 폐수가 해양으로 방출되면 여러 가지 오영문 제를 일으키게 된다. 폐수에 의한 갈색의 물줄기가 연안을 따라 배출구 로부터 3 km 이상 퍼지는 것이 보통이다. 해수의 투명도는 배출구 부근 에서 5~10cm 에 불과하다. 총대장균수는 배출구로부터 3~5km 에 이 르기까지 1,000/lOOml 을 초과한다. 사탕수수 찌꺼기를 루기하는 공장은 또 다른 수질오영 문제를 일으킨다. 사탕수수 찌꺼기는 폭 50m, 길이 1. 5km 나 되는 크기로 엉켜서 떠다니는 경향이 있다. 이러한 엉컴은 보
기 흉하고 항해에 위험을 주며 어업을 방해한다. 그리고 해안으로 부는 바람은 해변으로 밀어붙여 해변을 황폐시킨다. 이 찌꺼기가 해변으로 밀 리지 않으면 결국 해저에 가라앉는다. 제당공장 폐수에서 나오는 찌꺼기가 해저로 퇴적되면 저생생물군집에 심각한 영향을 미친다. 하와이에 있는 호노카 제당공장의 폐수 배출구 부근에서는 그 찌꺼기가 3m 두께로 퇴적되었으며 배출구로부터 1.5 km 범위에 이르기까지 자연산호군집을 폐사시켰다 (EPA, 1971). 배출구 부근 에서 어류의 개체군은 그 수나 다양성에 있어서 감소한다. 이러한 변화 는 어류가 먹이를 탐색하는 데 영향을 주는 탁도의 감소, 그리고 어류의 보호지역 손실 등으로 일어난다. 제당공장 폐수는 일반적으로 BOD 와 COD 가 높기 때문에 해수의 순 환이 활발하지 못한 수역으로 폐수가 방출될 경우에는 심각한 산소결핍 울 초래한다. 뿐만 아니라 엄청난 양의 부유물질을 포함하고 있어서(표 8-2), 일차적으로 배출구 부근의 어류 개체군이 감소하게 된다. 이러한 변화는 대부분의 국지적인 어류군이 호흡의 장애를 일으키고 또 대부분 이 시각을 이용하여 먹이를 찾기 때문이며, 부분적으로는 어류에 대하여 먹이와 숨을 곳을 마련해 주는 자연저생군집의 사멸에 기인한다. 4 종의 어류를 대상으로 행한 독성실험의 결과 (EPA, 1971) 는 제당공장 폐수에 표 8-2 제당공장 폐수 및 미처리 생활하수에 포함된 주요 성분의 평균 농도 서0 건닌 제당공장 폐수 미처리 생활하수 분뇨대장균 53, 000/lOOml ~106/lOOml 부유성 고형 성분 6, 900 ppm 200p pm 침전성 고형 성분 6, 600 ppm BOD 755p pm 200 ppm COD 2,033p pm 350 ppm 총질소 39p pm 40p pm 초0 이'- 15p pm lO ppm 자료 : 미국환경보호청, 1971
적절한 통기를 시켜주었을 때 3 종은 96 시간 생존하였으나 정어리는 6~10% 의 공장폐수를 포함한 물속에서도 46 시간밖에 생존하지 못했음을 보여준다. 제당공장 폐수가 상당히 높은 BOD 와 COD 를 포함하고 있지만 배출 구가 의해 쪽으로 향했을 경우 크게 문제가 되지 않는다. 하와이의 제당 공장의 폐수 배출구 부근에서는 산소 농도가 대조구의 그것과 유사하다. 즉, 두 지역에서 저층의 산소 농도는 포화도의 80~90% 임에 반해 그 의 의 수충에서는 보통 90% 이상으로 나타난다• 이것은 배출폐수를 분산시 킴에 있어서 해양의 효력을 의미한다. 따라서 반폐쇄성 수역에 투기된 공장폐수는 심각한 산소결핍 문제를 일으키기 쉽지만 순환이 활발한 외 해역에서는 쉽게 이를 극복할 수가 있다. 미국환경보호청(1 971) 의 연구 결과는 사탕수수를 원료로 하는 제당공장에서 폐수를 해양으로 방출할 때 다음과 감은 문제들이 발생함을 밝힌 바 있다. ® 불유쾌한 쓰레기(오물, 찌꺼기) 혹은 해저침전(퇴적물, 사탕수수 쓰레기, 버개스 (ba g asse) 등). ® 물위로 떠돌아 다니는 물질(사탕수수 찌꺼기, 버개스 등). ® 불유쾌한 해수의 색상 또는 탁도. ® 병원성 생물. ® 총 영양원소 농도(배출수에 들어 있는 총 N 및 P 의 양). 이에 따라 제당공장 조업과 관련된 수질 문제를 감소하거나 제거하기 위하여 다음 세 가지 방법을 권장하고 있다. ® 사탕수수 쓰레기나 버개스가 공장폐수로 두기되지 않도록 한다. ® 모든 공장 폐수는 해양으로 배출하기 전에 부유성 고형물질을 최소화 시키도록 처리하여야 한다. ® 세척수의 재이용을 위하여 배출 폐수를 연못이나 제방시설을 통해 저 수시킴으로써 불유쾌한 물질의 방출을 최소화한다.
제 9 장 할로겐화탄화수소 할로겐화탄화수소는 불소, 염소, 브롬 또는 옥소(할로겐족)를 포함한 탄화수소인데 이것은 화학적 산화나 박테리아 작용에 의해 쉽사리 분해 되지 않기 때문에 석유탄화수소와는 다르다. 금속과 마찬가지로 이들 물 질은 본질상 환경으로 영구 첨가되는 것이지만 금속과 다른 점은 이들 화합물의 대부분이 인위적으로 합성된 것이며 천연적으로 출현하지 않는 다는 것이다. 이들 물질의 대다수는 염소를 포함하고 있어서 집합적으로 염소화 탄화수소 또는 유기염소제 화합물로도 알려져 있다. 9-1 저분자량화합물 할로겐화탄화수소는 매우 광범위한 화합물을 포괄하고 있다. 저분자량 탄화수소, 특히 메탄은 해조류와 필시 몇몇 무척추동물에 의해 합성되며 영소, 브롬, 혹은 때때로 옥소를 포함한다. 따라서 해수중에서 이들 물질 의 농도가 증가되는 것은 자연적이며 인간활동의 결과가 아닐 수도 있다. 그러나 휘발성인 저분자량인 살충제가 대량으로 제조되고 이 생산량의 거의 대부분은 궁극적으로 환경으로 들어간다. 최대량으로 생산되는 물 질은 공업 용매인 디클로로에탄 (CH3CHCI2) 과 비닐염화물 (H2C=CHCI2)
로서 총량이 약 3, 000 만 톤에 이른다. 세계 총생산량이 연간 100 만 톤에 달하는 다른 용매는 사영화탄소 (CCl4), 과염화에틸렌 (Cl2C=CCI2), 삼영 화에탄 (CH2Cl3) 및 삼염화에틸렌 (CIHC=CCh) 등이다. 프레온화합물 (CCbF 와 CCI2F2) 은 냉각제, 에어로졸 추전제, 거품수지 등에 사용되는 데 프레온의 세계 생산량은 1986 년에 100 만 톤을 넘기에 이르렀다 (Clark, 1989) . 이들 화합물의 일부는 대기중에 아주 광범위하게 분포하고 있어서 남 극의 공기에서도 추적할 수가 있다. 이들 물질은 산업 중심부에 가까운 해수에서는 추적할 수 있을 만한 양으로 나타난다. 대기권 상부 오존층 에 대한 프레온 영향의 가능성에 대한 관심이 야기되고 생산량을 감소시 키기 위한 약간의 노력이 있으나 해수중에서 저분자량 탄화수소는 심각 한 위협으로 생각되지는 않으며 해양생물 속에 축적되지 않는 것으로 알 려져 있다. 9-2 살충제와 PCB 동물의 지방 조직 속에 축적되는 고분자량 염소화탄화수소에 대하여서
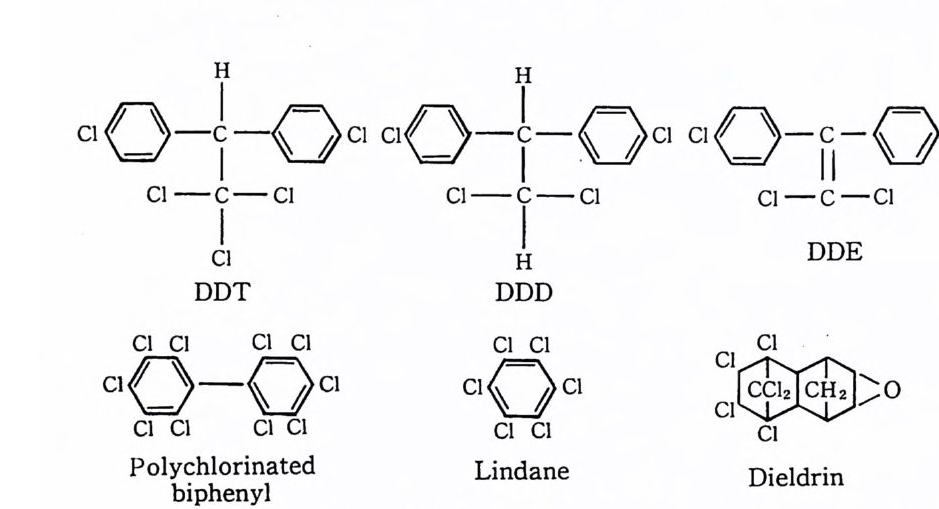 CIO— !1 _O Cl Cl0\HO Cl CIO— fI_ oCl
CIO— !1 _O Cl Cl0\HO Cl CIO— fI_ oCl
그립 9-1 일부 염소화탄화수소의 구조
는 특별한 관심을 기울여 왔다. 이들 속에는 살충제와 PCB 가 포함 된다(그림 9-1 ) . 9- 2 -1 DDT 와 연관 화합물 DDT (dic h loro-d i p h eny l- tr i c h loroeth a ne) 가 알려 진 것 은 18 세 기 였 으나 이것이 살충제로서 소개된 것은 1939 년이었다. 이 화합물은 여러 가지 면에서 이상적인 살충제라 할 수 있다. 죽 (D DDT 는 곤충에 대해서는 국단으로 유독하나 다른 동물에게는 훨씬 덜 유독하다• @ DDT 는 지속성이 커서 토양 속에서 약 10 년의 반감기를 갖는다. @ DDT 는 매우 오랜 시간 동안 살충 성질을 유지한다. @ DDT 는 비교적 값이 싸다. 이 의에 몇 개 다른 살충제도 표적생물에 대해 특수하게 영향을 미치 는 성질을 갖고 오랫동안 효과적이기 때문에 단 한 번의 적용으로 충분 하고 그것에 노출되는 인간의 안전에도 유효하다. DDT 의 사용은 2 차대전 중과 직후에 금지되었으나 아프리카와 국동지 역에서 말라리아 및 기타 곤충 매개병을 억제하기 위한 세계보건기구 계 획의 기초를 마련한 바 있다. 그러나 개발도상국에서의 DDT 의 일차적 인 사용은 삼림과 농경지역에서의 역병 방제에 있었다. DDE (dic h loro-dip h eny l- eth a ne) 는 DDT 의 유도체 로서 DDT 분자 중 에서 -CC13 기로부터 c1- 한 원자를 잃은 형태이다. 이것은 곤충에 대한 독성이 낮아서 살충제로서 사용되지는 않는다. 해수중의 염소화탄화수소 중 대부분과 해양생물 중에 있는 양의 80% 는 DDE 의 형태이고 필시 이 둘의 거의 전부는 DDT 의 파괴에서 유래하였을 것이다. DDD (dic h ~oro- di p h eny l- dic h loroeth a ne) 는 DDT 의 또 다른 유도체 로서 DDT 의 - CC13 기 중에서 Cl 하나가 H 와 치환된 것이다. 이것은 곤충에 대하여는 독성이 있으며 어류에 대해서는 DDT 보다 덜 유독하다. 이러
한 이유로 어류에 대한 낮은 독성이 필요한 곳에 살충제로 이용된다. 상업용 DDT 는 DDT 가 가장 많으면서 DDE 및 DDD 와 혼합되어 있다. 9-2-2 앨드린나루사펜류 (Ald i rn- t oxap hene gro up ) 상호관련이 있는 이들 살충제류는 앨드린, 헵타클로르 he pt achlor, 엔 드린 endri n, 디 엘드린 die l drin 등을 포함한다. 이 들 화합물은 모두가 극 단으로 지속성이 크고 분해산물 역시 유독하다. 앨드린은 분해하여 디엘 드린으로 되고 헵타클로르 에폭시드 he pt ahlor e p ox i de 로 된다. 이들 분 해산물은 더욱 유독하다. 이들 살충제는 종자처리제로 쓰이고 높은 독성과 지속성이 요구될 때 에는 벌레 유충의 방제제로 쓰인다. 이들 살충제의 주요 단점은 포유류 에 유독하다는 것이어서 1970 년대 이래 사용이 중지되었다. 섬유질 방충 에 대한 디엘드린의 사용은 최근까지 계속되었으나 현재는 단계적으로 폐쇄되고 있다. 9-2-3 감마 HCH, 린덴 BHC 감마핵소클로로사이클로핵산 r-hexochlorocyc l ohexane 또는 린덴 lin- dane 은 전에는 벤젠핵사쿨로라이드 benzene hexa~hlor i de(BHC) 로 알려진 것이다. 이것은 DDT 와 거의 같은 시기에 출현하여 곤충에 대한 접촉독 (接觸毒)으로서 작용한다. 이것은 휘발성으로 고온에 안정하기 때문에 연기로서 훈중소독(煙蒸消毒)에 쓰이고 종자처리제로도 사용된다. 그러나 먹이연쇄상에 축적되는 경향 때문에 여러 나라에서 폐지되거나 사용이 제한되고 있다. 9-2-4 목사펜 (Toxa p hene) 독사펜은 1940 년대 중반에 도입된 것인데 분자당 6~10 개의 염소원자 를 갖고 있는 캄펜 cam p hene 화합물의 혼합체이며 총 염소량은 무게의 68% 나 된다. 이것은 목화, 채소, 가축에 대한 살충제로 쓰이는데 어류 에 대한 급성 독성이 있어서 때때로 호소에서 어류 근절을 위해서 사용
되기도 한다. 미국에서 가장 많이 사용되고 있으나 현재 규제를 받기 시 작하고 있다. 9-2-5 PCB . PCB 는 1930 년대 초기로부터 사용되어왔다. 이들 화합물은 살충제가 아니고 전기기구, 페인트, 풀라스틱, 접착제, 도포제, 복사지 등의 제조 에 사용된다. 이들은 화학적으로 매우 안정하기 때문에 화학적 침식에 저항이 크고 발화지연제로 작용한다. 염소화탄화수소 살충제가 환경에 축적되는 사실에 대한 관심이 증대됨 에 따라 PCB 의 사용을 감소시키려는 여러 가지 단계가 취해졌다. 미국 의 PCB 제조업체의 하나인 몬산토회사가 1970 년 자전해서 생산량을 33, 000 톤에서 18, 000 돈으로 감축한 이 래 PCB 의 사용을 제 한하기 위 한 다양한 방법이 채용되었다. 1985 년에 네덜란드에서는 PCB 의 생산이 전 면 금지된 바 있다. 그러나 현재 전세계의 생산량은 연간 100 만 돈을 상 회하며 그 대부분이 자연환경 속에 분산된다. 9-3 해양환경으로의 유입 DDT, 앨드린 및 톡사펜은 물에 불용성이며 이들 물질이 바다로 들어 가고 해수에 존재하는 양상은 입자에 흡착하여 이루어전다. 살충제와 PCB 는 자연환경에 광범위하게 분포되지만 살충제가 축적되는 주요 근 원은 농경지이다. 캘리포니아의 과수원과 채소 경작지에서는 대량의 살충제를 주로 공중 살포 방식으로 투여하는데 투여량의 약 50% 는 지상에 도달하지 않고 공 기에 의해 먼 거리까지 이동된다. 식물과 토양에 떨어전 살충제는 빗물 에 씻겨 강우를 통해 바다로 들어가게 된다. 홍수기에는 특히 대량의 미 세한 토사가 운반되는데 농경지를 흐르는 물을 통해 토사에 흡착된 살충 제가 엄청난 양으로 바다에 유입된다. 건조한 지역이 관개로 대량의 경
작이 이루어지는 곳에서는 살충제가 먼지에 싸여 운반된다. 공기에 의한 운반은 유기염소제 살충제를 전세계로 분포시키는 결과를 낳는다. 예컨대 DDT 는 자연상에는 존재하지 않는 합성물질이며 1940 년 에 출현하였는데 불과 20 년 이내에 전세계에 고루 퍼졌다. DDT 가 사용 되는 곳에서 수천 km 나 떨어진 남극의 펭귄새에서까지 검출되었다. 염 소화탄화수소의 제조과정에서는 통상 다양한 유사 화합물이 생산되는데 그중 하나만이 필요한 것이다. 정제하는 동안 이들 불필요한 탄화수소는 상당량이 추출되어 바다로 폐기된다. 국지적으로는 염소화탄화수소가 공장폐수 속에 섞여서 바다로 향한 배 출구에 나타난다. 로스앤젤레스에 있는 몬트로즈 화학회사는 세계에서 가장 큰 DDT 생산업체인데 이 공장폐수가 유입되는 로스앤젤레스의 생 활하수계에는 연간 2 1. 6 돈의 DDT 잔재가 유입되고 이것이 해양배출구 롤 통해 바다로 들어간다. 그러나 1971 년 이래 DDT 의 제한 조치로 이 양은 연간 0. 73 톤으로 크게 감소하였다 (Clark, 1986). 생활하수 스릿지 또한 다량의 할로젠화탄화수소를 포함하고 있어서 바다로 투기할 경우 추가적인 오염을 일으킨다. 9-4 해수중에서의 동태 살충제는 포화농도가 1 pp b 에 불과할 만큼 극단으로 물에 불용성이지 만 지방에 용해되고 입자에 강력하게 흡착한다. 따라서 해양에서의 분포 는 결코 일정하지 않다. 이들 물질의 대부분은 무기입자 또는 규조류 같은 미생물에 흡착하며 이러한 현상은 분석상의 문제를 야기한다. 왜냐하면 여러 가지 살충제 사이의 구별의 어려움은 차치하고서도 어느 것이 생물 속에 동화된 것이 고, 어느 것이 생물의 의부에 흡착된 것인가를 결정하기 어렵기 때문이 다. 전자는 그 생물에게 영향을 미칠 것이고 후자는 영향을 미치지 않으 나 오탁된 생물을 섭취하는 동물에게 영향을 미칠 수 있다.
무기입자에 흡착된 살충제는 궁극적으로 해저에 퇴적한다. 그러나 부 유하는 입자나 재부유하는 입자는 그 크기가 적당하다면 보통 여과식 섭 식동물에 의해 섭취되어 살충제가 이러한 경로를 통해 먹이사슬로 들어 가게 된다. 해수의 표충은 두께가 수 µm 내지 1mm 정도 되는 막인데 많은 지방 산을 포함하고 있다. 따라서 살충제는 지질(脂質) 용해성이기 때문에 표 충 막에 축적되고 그 양이 크지는 않지만 표충에서 생활하는 생물이나 새에 대해서는 아주 중요하다. 대기와의 교환 장소인 바다의 표충은 여 러 가지 이유로 매우 중요하지만 연구하기는 극단으로 어려워서 여전히 이해하기 어려운 상태에 있다. 살충제, 특히 대부분의 DDT 와 그 유도체들은 각종 환경에서 모든 생 물에서 발견되는데 바다에서는 상당량이 생물체에 축적되어 먹이망 속에 서 순환된다. 9-5 할로겐화탄화수소의 생물학적 작용 9_5_ 1 분석의 문제점 석유 탄화수소와 같이 할로겐화탄화수소는 관련된 화합물이 무수히 많 다. 하나의 견본에서 100~150 개의 상이한 유기영소의 구별이 가능한데, 이처럼 많은 관련 화합물 때문에 이들 물질 중 어느 것이 관찰된 생물학 적 영향을 일으킨 것인가를 밝혀내는 것은 매우 어려운 일이다. 그 가운 데서도 PCB 는 상업용 생산품이면서 혼합체이므로 문제가 가장 심각하 다. PCB 의 정확한 조성은 염소처리의 정도, 제조업체에 따라 다르다. 하나의 견본에서 70 개의 PCB 화합물이 존재할 수 있고 분석자는 혼합 물의 총 PCB 양을 추정하거나 개개의 성분을 구별하여 측정할 수도 있 다. 후자의 경우에는 시간과 경비나 너무 많이 드는 단점이 있다. 두번째 문제는 보다 더 근본적인 것이다. 1965 년까지 DDT 를 그 대사 산물인 DDE, DDD 와 그리고 디 엘드린과 구별할 수가 없었으나 2~3 년
뒤에는 거의 모든 분석실험실에서 분리가 가능해졌다. PCB 는 30 여 년 간 사용되어 환경으로 방출되었으며 거의 모든 시료에서 나타난다• PCB 는 다른 유기영소의 검출과 측정을 방해할 수 있기 때문에 필시 DDT 오염의 초기 기록은 대부분이 정확하지 않을 것이다. 광범위한 오 염물질의 하나인 목사펜은 1980 년에 이르기까지도 염소화탄화수소의 분 석에서 잘 검출되지 않았다. 현재 정교하고 예민한 새로운 분석방법에도 불구하고 많은 유기염소가 간과되고 있고 그 일부는 생물학적으로 활발 하다. 그러므로 할로겐화탄화수소의 생물학적 영향을 관찰하여 그 결과 를 해석하는 데에는 반드시 조심하여야 한다. 9-5-2 저장과 생물축적 살충제는 분비가 어렵고 따라서 생물체내에 축적하는 경향을 갖는다는 증거가 있다. 이들 물질이 지질용해성이기 때문에 다른 조직보다는 지방 조직에 훨씬 더 높은 농도로 나타난다. 이러한 현상은 두 가지 위험을 수반하게 된다. ® 섭식이 불충분한 시기에 동물은 지방저장분을 동원하여 이용하는데 이 때 염소화탄화수소를 체내에 순환시켜 위험 수준에 이르게 될 수도 있다. ® 다른 생물축적 오염물질과 마찬가지로 먹이망을 통한 전달과 이에 따 라 생물확대의 가능성이 크며 실제로 수많은 동물에서 이러한 현상이 발견된다. 할로젠화탄화수소가 지방조직에 결합되는 경향 때문에 상이한 생물에 서의 오영수준을 비교하는 데 있어서 주의가 요구된다. 상이한 양과 농 도가 지방조직, 근육, 생식소 등에서 나타나기 쉽고 총량이 알려져 있다 하더라도 살찐 동물과 야윈 동물에 대한 그 의미가 아주 다르다• 유기영소의 축적률은 종간에 변화가 크다. 그림 9-2 는 독일의 북해 연 안에 있는 베젤하구의 오염수역에 사는 5 개 저생종의 PCB 및 6 개의 유 기영소 살충제의 평균 농도를 나타낸 것이다. 실제 농도는 동물의 지질
 26 0 0000000000000
26 0 0000000000000
그림 9-2 하구에 사는 천해성 동물에서 검출된 PCB 및 살충제의 평균 농도 a : PCB , b : DDD, c : die l drin , d :a-H CH, e : r-HCH, f : DDE, g : Endosulph a n (자 료 : Clark, 198 6)
함량과 먹이연쇄상의 위치와 관련해서 얻어전 것인데 무척추동물보다 두 배 이상의 지질을 갖 고 있는 서대(어류)는 그만큼 더 많이 오염되어 있 음을 알 수가 있다. 서대, 자주새우 및 갯지렁이는 살충제보다 PCB 를 더 많이 함 유하고 있는 반면 새조개는 PCB 를 거의 흡수하지 않고 린덴 을 더 많이 함유한다. 자주새우는 다른 종에 비해 현저히 적은 양의 DDT 와 DDD 믈 축적한다. 실제로 각 종은 각기 나름대로의 유기염소제 의 축적양상을 나타낸다. 한 종내에서까지도 유기염소제의 총량에는 상당한 변화가 있다. 담치 는 함유하고 있는 DDT 잔재와 PCB 양에 있어서 크게 변화한다(표 9-1). 이러한 변화에도 수많은 요인이 작용하는데 모두가 알려져 있지는 않으나 생물의 연령 , 살고 있는 조석 수준 , 성 , 연간 번식주기에서의 단 계 등은 물론 동물이 노출되는 유기염소제의 농도가 포함된다. 종과 개체에 따라 변화가 크기 때문에 일반화하기는 어려우나 최고의 농축률은 70, 000 으로서 굴, 조개 같은 연체동물에서 발견된다. 갑각류와 어류에서의 농축률은 100 과 10,000 사이에 있고 새에 대해서는 10 이하
표 9-1 해수와 담치에서 발견되는 PCB 및 DDT( 혹은 DDE) 의 농도 해역 및 연도 해(n수g 농/l)도 담치 (m중g의/l )농 도 농축률 PCB : 立 랑 스 : 까상말발로마라르,리해세 ,변유1 ,,971 49 171499 7744 001o.... 69698045 0000.... 0 22465538 264379070000,,,,000000000000 캘리포니아 : 로샌스프앤란젤시레스스코,, 11997752 01.. 2908 00..20368 16990,,000000 DDT 또는 DDE: 立 랑 스 : 말발상까로마라르,리해세 ,유변1 ,,917 49 7119497 744 o001.... 25335045 0000.... 000091550321 2694190000,,,,000000000000 캘리포니아 : 로샌스프앤란젤시레스스코,, 11997752 50..1110 01.. 060050 34150,,000000 자료 : Clark, 1986 이다. 9-5-3 생물학적 영향 식물과 동물에 대한 할로겐화탄화수소의 영향을 정확히 안다는 것은 어려운 일이다. 이들 물질은 수용성(水溶性)이 낮기 때문에 유기염소제 가 입으로 두여되지 않는 한 실험실에서 수생생물에 의해 실제로 섭취되 는 양에는 상당히 불확실 점이 있다. 유기염소제가 체내의 지방조직에 저장되기 때문에 지방조직이 이용될 때에만 생물학적으로 영향을 미친 다. 그러므로 동물은 살충제의 체내 부하량이 많아지지만 지방 저장분이 이용되는 먹이결핍상태를 제의하고는 병적 영향을 나타내지 않게 되고 이러한 사실이 실험실 검사를 어렵게 만든다. 식물플랑크론의 실험실 배양에서는 DDT 와 PCB 가 일차생산량을 감
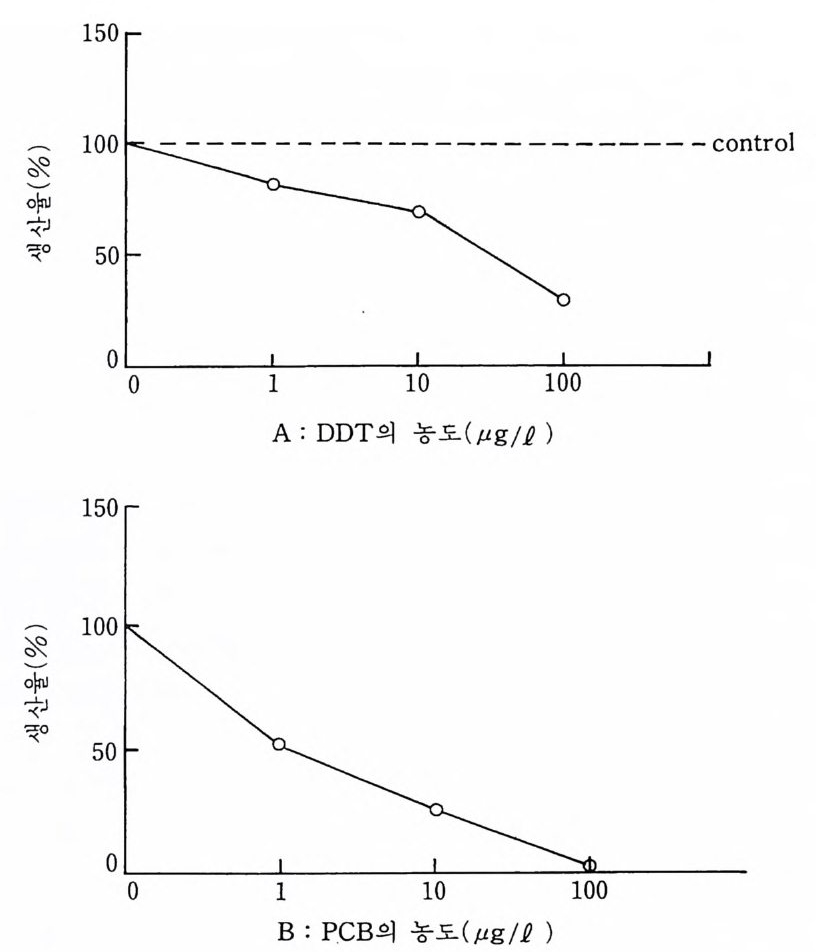 150
150
그림 9-3 A : DDT 에 노출된 실물플랑크톤의 생산율 B : PCB 에 노출된 식물플랑크론의 생산율 자료 : Clark, 1986
소시킨다(그립 9-3). 이 실험에서 PCB 의 경우에는 1 pp b 에 불과한 농 도에서 일차생산량이 50% 까지 감소한다. 해양 갑각류와 어류 역시 유기 염소제에 매우 민감한 것으로 나타난다. DDT 의 96hLCso 은 0.4~89 ppb 범위에 있으며 복어, 숭어, 뱀장어 등의 경골어류는 0.9~34 pp b 의
범위를 갖는다. 자주새우와 집게는 DDT 와 디엘드린에 대해서 각각 0. 6~6.0 및 7~50 pp b 의 범위를 갖는다. 한편 해를 입지 않고 유기영소 살충제를 축적할 수 있는 이매패류는 96h LCs o 이 10,000p pb 이상이다. 할로겐화탄화수소가 생물축적 및 생물확대를 하는 것으로 알려져 있기 때문에 대부분의 관심은 먹아연쇄상의 상위동물에 대한 영향에 집중된 다. 한 번의 경구두여로 포유류나 새를 치사시키려면 체중 k g당 수 g 이나 되는 다량의 PCB 와 DDT 가 요구된다. 물론 이러한 양은 자연환 경에서는 분명히 발견되지 않고 훨씬 낮은 수준으로 오염된 먹이에 노출 되지만 동물은 이 낮은 양의 오염에 계속적으로 또는 만성적으로 노출되 는데 문제가 있다. 새와 포유류에 있어서 살충제의 두 가지 아치사효과는 생태학적 중요 성을 갖는다. DDT 와 그 잔재는 칼슘대사를 방해하며 새의 알껍질을 얇 게 만든다. PCB 는 새와 포유류에 공히 생식에 대한 직접적인 영향을 미친다. PCB 에 오염된 새의 알은 부화능력이 감소된다. 실험실 쥐의 먹이 속에 포함된 PCB 는 새끼생산을 감소시키고 출생된 새끼의 생존율 을 감소시킨다. 9-6 환경에의 영향 1960 년대 동안 대부분 DDT 인 지속성 살충제의 광범위하고 집중적인 사용이 자연환경에 대하여 바람직하지 않은 결과를 초래한다는 징후가 증가하였다. 1964 년 어류가 살충제인 파라치온을 제조하는 공장의 해양 배출구 부근에서 죽어가고 있음이 발견되었다. 바닷가재는 훨씬 더 넓은 지역에서 영향을 받았는데 공장배출수가 50 , 000 배로 희석된 물에서도 치 사를 일으킨다는 것이 알려졌다. 라구나 마드르 석호는 미국 텍사스주 해안에 있는 생산성이 높은 대규모 석호(潟湖)인데 주변에 있는 농경지 로부터 유입된 살충제로 심하게 오영되었다. 1964 년에 1 헥타르 당 74 톤 이었던 이 해역의 어획고논 해마다 급격히 감소하여 1969 년에는 0.4 톤으
로 감소하였는데 이 원인은 어류의 살충제 중독에 기인한 것이었다 (Clark, 1986) . 야생동물에 대한 유기염소제 살충제의 악영향은 송골매의 경우에서 가 장 뚜렷한 증거를 볼 수가 있다 (Ra t cl iff e, 1970). 영국에서는 1945 년 이 후 송골매를 보호하기 시작하여 1950 년대 중반까지는 송골매의 개체군이 극적으로 증가하였다가 급격한 감소가 나타났다. 이러한 현상은 번식의 실패에 기인한 것이었다. 즉 송골매가 비정상적으로 껍질이 얇은 알을 낳고 이 알들의 대다수가 포란하는 동안 깨져버렸다. 오리와 닭의 모이 에 DDT 가 섞여 있을 경우에 껍질이 얇은 알을 생산한다는 것이 실험적 으로 알려져 있고, 1960 년대 중반의 송골매에서는 고농도의 DDT 잔재 가 검출되었다• 따라서 송골매 개체군의 감소는 DDT 가 주원인이었음은 의심의 여지가 없었고 영국에서 농경을 목적으로하는 DDT 의 사용을 중 지시킴에 따라 송골매의 수가 예전의 수준으로 증가하였던 것이다. 작은 어류를 섭취하는 새들은 유기염소제 살충제에 의해 그렇게 심하 게 영향받는 것으로는 보이지 않는다. 이러한 예는 제비갈매기와 솜털오 리에서 볼 수가 있다. 네덜란드의 로테르담 근처에 있는 화학공장에서 나오는 배출폐수에는 디엘드린, 앨드린 및 텔로드린 등이 포함되어 있는 데 이것이 1965 년에 제비갇매기 집단이 20,000 마리에서 650 마리로 격감 한 원인이었다. 배출수의 방출이 금지된 후 1974 년까지 제비갈매기의 수 는 5,000 마리로 증가하였다• 새의 죽음을 해석하는 데 있어 어려움은 1969 년 가울에 아일랜드해에 서 일어난 해조의 대량치사로써 설명된다. 이때 50,000 또는 10,000 마리 가 죽은 것으로 추정되는데 모두가 수척한 상태였으며 부검을 한 새들에 서는 PCB 에 의해서 발생하는 간병변(肝病變)과 신장병변이 발견되었다. 이러한 사실은 이들 수척한 새들의 지방손실의 결과로 생기는 염소화탄 화수소의 재분배가 체내에서 이루어짐을 의미하며 PCB 의 농도가 간에 서 8~880 pp m 으로 크게 변화성을 갖는 것으로 증명된 새들을 근거로 한다. 비록 PCB 가 일부 새에게는 치사를 일으킬 수 있지만 염소화탄화 수소의 중독이 대량 치사를 유발한 것이라고 결론을 내릴 수는 없다. 더
구나 해조의 대량 치사는 이들 화합물이 출현하기 오래 전인 19 세기에서 도 때로 기록이 보인다. PCB 는 포유류의 배란과 발생에 간섭하는 것으로 알려져 있다. 캘리 포니아 연안 물개의 경우 PCB 의 농도가 145 ppm 에 이르면 유산의 원 인이 된다고 설명한다. PCB 의 오염은 발틱해산 물개가 폐색 (r! I塞)을 일으키지 않고 수태율이 50% 에 불과한 이유를 설명할 수는 있으나 물개 의 40% 가 불임을 일으키는 자궁폐색에 대해서 PCB 가 관련된다는 증거 는 없다. PCB 와 살충제에 대한 주요관심의 하나는 환경 내에서 이들 물질의 지속성이 높다는 점이다. 이 지속성 때문에 심각한 환경오염을 단시간 내에 환원시킬 수가 없다. 죽 이들 물질이 생태계 내에서 계속 순환하므 로 수년 이상 지속된다. 이 지속성의 칭후로 북대서양에서 분명한 증거 가 나타났다. DDT 및 PCB 의 생산과 환경으로의 손실률을 근거로 Harvey 등 (1973) 은 육상환경에서의 PCB : DDT 잔재의 비율이 0.1 임에 반해 해양 대기, 표충해수, 식물플랑크톤 등에서의 이 비율이 30 임을 발 견하였다. 이 발견을 토대로하면 PCB 의 지속성은 DDT 잔재에 비해 약 300 배가 됨을 알 수 있다. 최근에 PCB 를 대사시키는 박테리아 균주가 생산되었다 (Ma rti n, 1977) . 이 박테 리 아는 생 활하수에 들어 있는 있는 PCB 를 1 주일내 에 300, 000 pp b 로부터 19 ppb 까지 감소시킬 수 있다. 비록 1 주일은 확실히 도시하수처리장에서 하수를 처리할 수 있는 것보다 길지만 이 분야가 더 개발되면 필시 PCB 의 생물산화방법이 가능할 것으로 보인다.
제 10 장 유류 모든 해양오염 가운데 기름과 석유탄화수소는 국제적, 정치적, 과학적 으로 가장 큰 관심의 대상이었다. 초기에 이러한 광범위한 관심이 야기 된 것은 일차적으로 해변을 더럽히는 유류오염과 기름막, 표면 수역의 타르, 그리고 해양 생물에 대한 기름과 석유탄화수소의 치명적인 영향 등에서 오는 커다란 가시적인 영향 때문이었다. 따라서 이에 대처하려는 노력은 일반의 지지를 얻기가 쉬웠다. 최근에 보다 잠행성인 유류오염의 장기적 영향이 명백해 지고 이 때문에 세계의 각 해양으로 기름을 방출 하는 일이 최소화되도록 조치가 강화되고 있다. 해양환경에서 기름의 존재는 자연 및 인위적으로 생산된 자원에 대해 서 다같이 악영향을 줄 수가 있다. 자연계에 대한 영향에는 다음의 것들 울둘수가있다. ® 오염된 식품을 섭취하는 데에서 오는 인간에의 위험. ®어류, 해조(海ii)' 새, 해양포유류및 기타야생생물에의 손상. ® 해변 및 기타 위락지역의 손상. @ 일부 종의 개체군을 제거시키거나 감소시킵으로써 해양생태계를 손상시키는 일. ® 생물의 재이식 (再移植)을 지연시키거나 방해함으로써 서식지를 변화시키는 일. 해양으로 유입하는 유류물질의 출처가 무수하고, 기름이 수천의 상이
한 화합물로 구성될 뿐만 아니라 이들 물질의 동태가 많은 독립적인 물 리적, 화학적, 생물학적 요인에 의해 지배받기 때문에 해양의 유류오염 에 대한 연구는 극단으로 복잡하다. 10-1 유류오염의 출처 인류가 유류산물을 사용하기 훨씬 전부터 해양에서는 유류오염이 있었 다. 죽 해양저의 도처에서 해수로 계속 스며드는 자연적인 해저유출이 있어 왔으며 이러한 기름은 수백 만 년 동안 바다로 들어가고 있는 것이 다. 또한 해양 동식물의 분해로부터, 그리고 공기에 의해 운반된 탄화수 소의 침강으로부터 기름 물질이 해수에 도달한다. 자연상으로 나타나는 이 기름의 대부분은 해양 박테리아에 의해 생물분해되므로 환경에 대한 영향은 최소화된다. 이 모든 현상은 약 100 년전 소위 〈석유시대〉의 도래와 함께 변화하였 다. 그 이후로 세계의 석유생산량은 극적으로 증가하였고(표 10-1) , 해 양환경의 유류오영은 격증하여 커다란 문제를 야기시키고 있다. 유류는 수 많은 출처를 통해 해양환경으로 유입한다. 물론 유류오염의 가장 두드러진 출처는 유조선 조업의 결과이지만 유조선의 사고에서 오 는 석유유출, 혹은 벌지 b i l g e 와 연료유, 기타 채유과정에서 오는 유출이 표 10-1 1938-1978 년 동안 세계 석유 생산량 연도 총생산량 (100 만톤) 연도 총생 산량 (100 만톤) 1938 272 1965 1,054 1946 375 1970 2,335 1950 525 1975 2,709 1955 770 1978 3,055 1960 978 자료 : Bert ran d, 1979
약 300 만 돈을 상회하는 것으로 알려져 있다. 출처별 유입량은 표 10-2 에 나타낸 바와 같다. 10-1-1 연해 석유람사와 생산 우발적 사고를 제의하고는 연해석유 및 가스의 시추와 생산 과정에서 바다로 유입하는 석유의 양은 비교적 적다. 일일 조업을 통해 전세계 해 양으로 유입되는 석유의 양은 연간 약 5 만 톤 정도로서 해양의 체적에 비교한다면 극미량에 불과하다. 이러한 손실은 일차적으로 플랫폼에서 석유를 분리할 때 영수를 방출하는· 데서 기인한다. 해저에서 퍼 울린 석 유는 물을 포함하고 있으며 이 물은 석유를 육지로 운반하기 전에 분리 하여야만 하기 때문이다. 연해 플랫폼의 실제적인 영향은 정상조업에서 오는 손실이 아니라 우 발적 사고로부터 오는 손실이다. 유정 (油井)의 폭발, 플랫폼의 구조적 결함, 장비고장 및 충돌 등이 유류유출의 원인을 이룬다. 10-1-2 해운(海運) 해양으로의 유류유입 형태 중에 가장 시각적으로 분명한 것은 Amoco Cad iz 호와 Argo Merchant 호의 경 우와 같은 유조선 사고이 다. 비 록 양 적으로는 크지만 이러한 유출의 범위는 다른 유류오염원으로부터 방출되 는 유류의 양과 비교할 때 극히 적다. 유조선 사고가 대형 문제를 야기 하는 이유는 한 장소에 비교적 대량의 유류를 거의 일시에 방출하기 때 문이다. 이것은 국지적으로 높은 유류농도와 결과적으로 심각한 환경손 상을 초래한다. 따라서 유조선 사고는 비교적 작은 해역에서 i 급성 영향 울 야기하는 반면에 다른 유류방출은 매우 넓은 해역에 걸쳐 만성 혹은 장기 영향을 미치게 된다. 긴 안목으로 보면 후자가 해양의 건강에 더 심한 영향을 미친다. 해운으로부터의 유류손실은 다음 출처에서 연유한다. 유조선사고 전세계 거의 모든 원유 생산은 국제적으로 의양항해 유조선으로 운반
다. 또한 도시 폐기물이나 산업폐기물, 대기낙진 등, 육상에서 유입하는 양도 상당한 수준에 이른다. 해양으로 유입되는 석유탄화수소의 총량을 계산하기는 매우 어려우나 최근의 추정량은 연간 1 백 70 만 톤에서 8 백 8 십만 톤에 이르며 평균 연간 표 10-2 연간 전해양으로 유입하는 석유탄화수소의 추정량 출처 유입량 (100 만톤) 총량 해운 유조 선 조업 0. 70 유조선 사고 0.40 빌지와 연료유 0.30 드라이 독 0.03 유조선의 선박사고 무 1. 45 고정시설 연안 정유공장 0. 10 의해 석 유생산 0. 05 해운터미날 麟 。• 17 기타출처 도시 폐기물 0. 70 산업 폐기물 0. 2 0 도시 유수 0.12 강유수 0. 04 대기 낙진 0. 30 해양두기 무 1. 38 자연 유입 뚜 총계 3.25 자료 : Clark, 1989
한다. 이 석유를 운반하기 위한 대형 선박과 많은 선복량은 대형 유조선 을 처리할 수 있는 소수의 항구 문제와 함께 유조선 사고를 점점 증가시 키고 있다. 지금까지 가장 큰 유조선 사고는 1978 년에 Amoco Cad i z 호 에 의한 것으로 23 만 3 천 톤의 석유를 유출하였다. 현재 100 만 배럴의 석유를 선적할 때마다 160 배럴이 바다로 유출하고 있는데 비율로는 매우 적은 양이지만 전세계에서 선적되는 석유의 총량 울 감안하면 석유 유출량이 매우 커서 연간 약 40 만 돈이 유출된다. 유조선조업 바다로 유입하는 유류의 최대량은 유조선 사고로부터 오는 것이 아니 고 정상적인 유조선 조업으로부터 온다. 이러한 유출은 국제적 현상이고 피할 수가 있다. 이 가운데에서도 가장 큰 유출은 바닥짐 (ballas t)을 제거하는 데에서 온다. 유조선은 각 탱크가 다 찼을 때 항해하기 좋도록 고안되어 있다. 따라서 항구에 짐을 다 푼 뒤에는 너무 가벼워서 새로운 짐을 싣기 위해 되돌아갈 때에는 바람과 파도에 밀려 조정하기가 어렵게 된다. 결국 이 러한 경우에 통상 선적량의 25~30% 의 해수를 바닥짐으로 채우는 것이 상례로 되어 있다. 이 바닥짐 물은 새로운 석유를 선적하기 전에 다 방 출해야 된다. 그렇지만 기름을 부릴 때에 탱크 용량의 0.1~1 .5 % 정도 의 석유는 탱크의 바닥과 벽에 남게 되고 이것이 바닥침 물과 섞여서 나 중에 방출된다. 이 결과 석유오염이 발생하게 된다. 약 20 년 전까지는 모든 바닥짐 물과 이에 섞인 석유가 다 직접 바다로 방출되었으나 현재는 유조선의 80% 가 LOT( loa d on t o p)기법으로 알려 진 방법을 사용함으로써 기름의 유출을 최소화하고 있다. LOT 기법이란 요컨대 바닥짐 물이 기름과 섞인 채 탱크 속에서 몇 일 지나게 되면 대 부분의 기름이 충을 이루며 서서히 표면으로 올라오고 밑에는 거의 완전 한 해수만 남게 되는 원리를 이용하여 유조선에 석유를 선적하기 전에 해수를 빼낸 다음 각 탱크에 남아 있는 기름을 페기물 탱크로 모으는 방
법이다. 이 방법은 90% 의 효율을 갖고 있어서 나머지 10% 는 여전히 바 다로 방출된다. 10-1-3 육상으로부터의 유입 해양환경으로 들어가는 방대한 양의 기름은 육상에 기원을 둔 것으로 서 연안 정유공장, 도시 및 공장의 폐수방출, 강수의 유입 등이 포함된 다. 또한 일차적으로 교통수단에서 뿜어나오는 대기 중의 탄화수소의 낙 진도 추가적인 근원이 된다. 이들 중 가장 큰 유입의 하나는 일반적으로 자동차 내연기관의 크랭크 케이스 폐유인 것으로 생각된다. 대부분의 크랭크 케이스 폐유는 엔진 오일을 교환할 때 모아지는데 이 폐유가 여러 가지로 재이용이 가능하지 만 경제성이 없기 때문에 하수로 폐기되거나 땅에 묻게 된다. 땅에 묻은 것이나 하수구로 들어간 폐유는 궁극적으로는 바다로 유입한다. 1972 년 에 해양으로 유입된 윤활유 폐유의 양은 70 만 톤을 넘는 것으로 알려져 있다 (Grosslin g , 1976) . 유출수를 통해서 해양으로 들어가는 석유탄화수소의 양도 상당해서 연 간 강우를 통해서 들어가는 양이 30 만 돈에 이른다. 또한 빗물 속에도 평균 3.7mg / l 의 탄화수소가 포함되어 있고 이 가운데 86% 는 입자들과 결합되어 있다 (Hun t er 등, 1979). 연안 폐수처리장에서 방출되는 석유탄화수소의 총량은 연간 20 만 돈 이상으로 추정되며 이들 기름의 거의 전부는 연안 해수 중에 남아 있기 때문에 이 양을 감소시킬 필요성이 크다. 연안 수역의 회복을 달성하려 면 도시 및 산업폐수로부터 탄화수소를 제거시키는 더 좋은 방법을 개발 하지 않으면 안된다. 이 점은 아마 연해에서의 석유 유정에 대한 안전장 치의 개발보다 더 중요할 것이다. 10-1-4 자연적인 유출 현재 전세계 해양에 잔류하는 탄화수소의 상당히 많은 부분은 자연적 인 유출의 결과이다. 바다 밀에 있는 지각 표면에서 자연적으로 기름이
새어나오는 곳은 현재 190 여 곳으로 알려져 있고 이들은 일차적으로 심 해저와 구조지질학적으로 활동하는 지역에 위치한다. 유출되는 양은 장 소에 따라 크게 다르지만 대략 연간 25 만 돈 정도이고 이 중에서 10% 정도만이 대륙봉해역에서 유출되는 것으로 알려져 있다. 10-2 석유의 성질 많은 형태의 석유탄화수소가 해수로 들어가지만 표 10-3 에서 볼 수 있 는 바와 같이 원유가 압도적으로 많은 양을 차지한다. 원유는 분자량이 16~100,000 에 이르는 극단으로 복잡한 혼합물이다. 탄소와 수소 의에도 이들 탄화수소는 소량의 산소, 유황, 질소와 극미량 의 금속을 포함한다. 소위 석유를 형성하는 개별 화합물의 수는 무수히 많아 수 10 만에 이른다. 이들 물질은 광범위한 비동점을 갖고 있어서 휘 발성 찌꺼기로부터 납 찌꺼기까지 다양하다. 더구나 성분 또한 크게 다 양하다. 원유로부터 선택된 부분만을 취하는 가솔린이나 연료유 같은 정 표 10-3 방출되는 석유탄화수소의 형태 형태 유출량(t) 비율(%) 원유 46,335 61. 5 아스팔트 혹은 찬류 연료유 830 1.1 기타연료유 5,357 7.1 디젤유 5,764 7. 6 가솔린 3, 768 5. 0 액체 화합물 5,409 7. 2 폐유 1, 960 2. 6 기타 5,956 7. 9 겨 l 75,379 100 자료 : 미국 정부 간행물, 1978
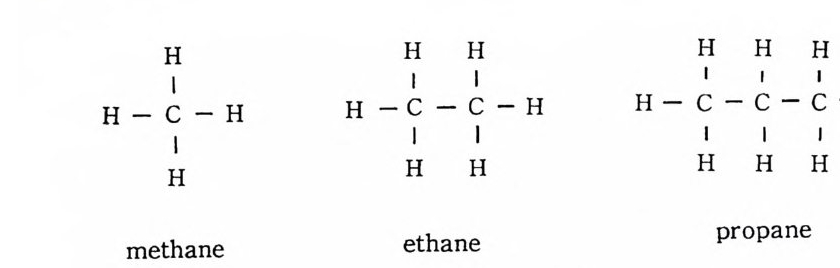 H H H H H H
H H H H H H
그림 10-1 간단한 알칸류의 구조
유산물까지도 완전히 정의하지 못하는 복잡한 혼합물인 것이다. 원유에서 발견되는 탄화수소의 기본은 알칸(파라핀), 시클로알칸(나프 텐) 및 방향족화합물 등 3 종류이다. 불포화 연쇄화합물인 울레핀이 미량 포함되어 있다. 알칸류 alkane 나 지방족 화합물은 직선상 또는 분지상 연쇄화합물로서 그 속의 각 탄소원자나 다론 4 개의 원자와 직접 결합하고 있다(그림 10-1) . 전형적인 기름에서는 알칸류의 약 절반이 곧은 사슬 화합물이고 나머 지가 가지난 사슬 화합물이다. 알칸류는 보통 원유의 약 20% 를 형성하 며 가솔린과 연료유에서는 아주 보통으로 나타난다. 알칸류는 포화화합 물로 불리는데 이들 화합물 속에서 보는 포화결합 satu rat e d bond 은 알칸 류와의 반응을 매우 어렵게 만든다. 저분자량 알칸류(탄소원자수 6 개 이
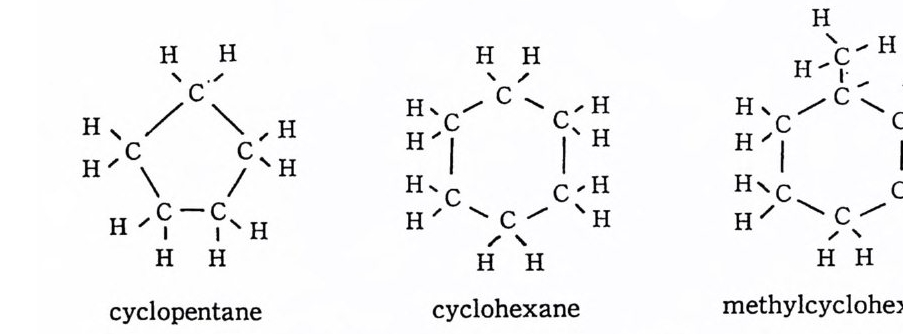 H
H
그림 10-2 간단한 시클로알칸류의 구조
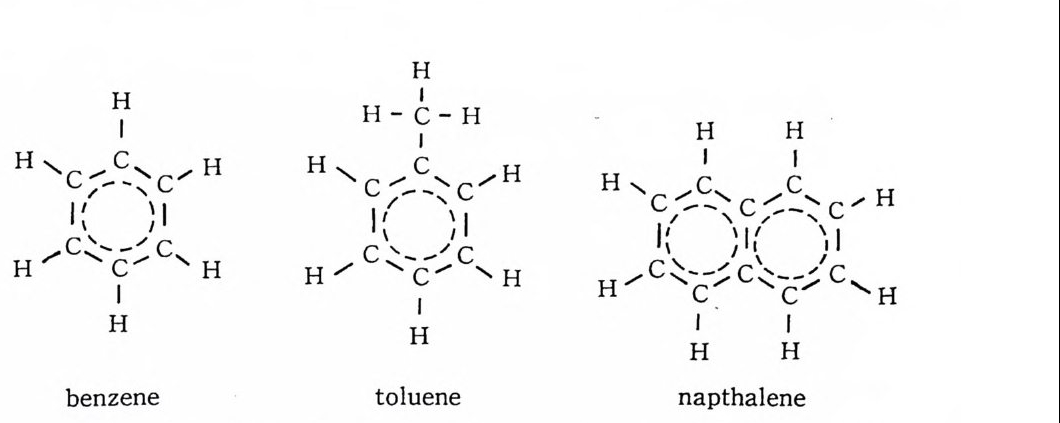 HICIC-cIH
HICIC-cIH
그립 10- 3 원유에서 발견되는 간단한 방향족 화합물. (6 각형 탄소고리 속에 있 는 원형은 추가적 인 전자결합을 표시한다)
하)는 일반적으로 기체인 반면 고분자량 지방족은 고체이다. 시크로알칸 c y cloalkane 류 역시 포화화합물이지만 다수의 원자가 결합 울 이루어 포화고리를 형성한다(그림 10-2). 이들 화합물은 원유의 약 50 % 를 차지하며 그 중 가장 많은 것이 시클로펜탄과 시클로핵산이다. 방향족은 벤젠고리를 갖고 있는 화합물이다. 원유에서 통상 발견되거 나 정유과정에서 생산되는 방향족은 벤젠, 톨루엔 및 나프탈렌(그림 10-3) 을 포함한다. 이들 화합물은 모두 6 탄소 벤젠고리를 하나 또는 그 이상을 갖고 있다. 방향족 화합물은 통상 원유 속에 20% 미만이 포함되 어 있으나 동물과 식물에 공히 아주 유독하기 때문에 심각한 문제를 야 기시킨다. 또한 많은 것이 발암성 물질인 것으로 알려져 있다. 아스팔트는 기름 속에 교질현탁으로 들어있는 고분자량 물질(평균 10, 000) 이다. 이들 물질은 원유의 약 20% 를 차지하며 구조는 알려져 있지 않다. 원유에서 나타나는 대부분의 유황, 질소, 산소 및 유기적으로 착 화된 니켈과 바나듐은 아스팔트 부분에서 발견된다. 여러 가지 탄화수소 부분은 상이한 온도에서 비등하고 증류라고 알려 전 과정을 통해 정유하는 동안 분리할 수가 있다. 표 10-4 는 원유의 전 형적인 부분분리의 결과를 보여준다. 여러 가지 부분의 범위는 유정에
표 10-4 원유의 전형적 부분분리 부분 빙점범위(%) 분자크기 체적(%) 정유가스 <2 5 c3 ~C4 2 가솔린 40~150 c4 ~C10 25 나프타 150~200 C10~C12 6 케로신 200~250 C12~C16 10 가스오일 250~300 c16~C20 15 윤활유 300~400 C20~C2 6 17 잔류오일 >4 00 c26 25 자료 : Ry an , 1977 따라서 그리고 생산일에 따라서 크게 다르지만, 이 표는 그 대표적인 값 을나타낸다. 원유 및 석유산물의 전형적인 특칭은 표 10-5 에 표시하였는데 이들 물 질은 일반적으로 밀도가 낮고 유출된 기름은 해수 표면에 부유한다. 웅 고점의 값은 물질이 응결하는 온도를 나타낸다. 표 10-5 원유 및 석유산물의 전형적 특징 유황 왁스무게 아스팔트 종류 비중 동적 유동점 무게비율 비율 무게비율 접성도 ('C ) (%) (%) (%) 원유 0. 8~o. 99 4-25 (-35) ~ (+7. 0) 2. 0 5-1 2 0, 05-3. 0 가솔린 0.70
전형적인 기름은 대략 파라핀 10%, 나프틴 45%, 지방족 25% 와 질 소, 유황, 산소 등을 포함하는 화합물 20% 로 구성된다. 제 6 연료유 또는 벙커 C 유는 대부분이 C3o 이상의 범위를 갖는 화합물로서 석유의 가장 무거운 증류부분으로 되어있다. 전형적인 제 6 연료유는 파라핀 15%, 나 프틴 45%, 지방족 25%, 질소, 유황, 산소 화합물 15% 로 구성된다. 디 겔유 혹은 제 2 연료유는 중간의 증류부분을 대표하는데 파라핀 30%, 나 프틴 45%, 지방족 25% 로 구성된다. 케로신은 파라핀 35%, 나프틴 50 %, 지방족 15% 로 구성되는 반면 가솔린은 파라핀 50%, 나프틴 40%, 지방족 10% 로 구성된다. 일반적으로 원유의 독성은 탄화수소 계열에 따라 증가한다. 죽 알칸류 는 시클로알칸류 및 알킨류보다 독성이 적고 이들 후자는 지방족보다 독 성이 적다. 탄화수소의 계열 내에서는 저분자량 화합물이 고분자량 화합 물보다 더 큰 독성 을 지 닌다 (Ry an , 1977) . 10-3 해양환경에 대한 유류 유출의 영향 기름과 석유탄화수소는 모든 해양오염 가운데에서 국제적, 정치적 및 과학적으로 가장 큰 관심의 대상이 되어왔다. 그리고 바다에서 석유 유 출이 미치는 영향의 몇 가지는 아주 명백하며 그 중 대표적인 것은 바닷 새의 죽음이다. 또한 어패류는 안전한 경우라도 죽거나 오탁이 되면 먹 울 수가 없으며 해변은 매우 지저분해 진다. 그러나 눈에는 보이지 않고 오랜 시간이 경과한 뒤에만 밝혀질 수 있는 해로운 영향이 많이 나타난 다. 이와 같은 아치사효과는 결과적으로 더 넓은 해역으로 전파될 수 있 기 때문에 해양환경에서는 몇몇 특정 생물의 죽음보다 훨씬 더 커다란 위험을 지니고 있다. 아치사효과는 해양생물의 개체군의 특칭이나 해양 생물군집의 생태적 구조에 있어서 변화를 야기할 수 있다. 그 영향은 세 포 및 생리기능의 간섭을 초래하고 정상적인 먹이활동과 생식양상을 파 괴하는 쪽으로 유도된다.
석유 유출은 바다에 사는 모든 동물에 대해서 해로운 영향을 미칠 수 있다. 죽 수충 내에 있는 생물은 기름의 독성 때문이건 기름이 생물을 덮음으로써 오는 질식 때문이건 물속에 있는 기름에 의해 영향을 받는 다. 유출된 석유는 많은 양이 얇은 막으로서 해수표면에 부유하는데 이 매끈매끈한 면에 내려 않는 새종류에 대해서 엄청난 영향을 줄 수가 있 다. 또한 기름은 결과적으로 많은 양이 해저에 침전하며 이곳에서 저생 생물군집의 황폐를 초래할 수도 있다. 해변에 밀려오는 기름은 매우 불 결한 환경을 만들지만 더 중요한 것은 이 석유가 아천해대 생물들을 중 독시키고 해변 식물상과 소택지 식물을 파손시키는 일이다. 더구나 어류 와 패류는 그 조직 속에 탄화수소를 축적할 수 있기 때문에 사람이 먹었 울 경우 위생문제가 제기된다. 10-3-1 해양생물에 대한 유류 독성 원유와 충분한 농도를 지닌 많은 정유산물은 모두 해양생물에게 유독 하다. 성체인 해양동물에 대해서 광범위하게 시행된 생물검정시험 결과 를 보면 석유 및 석유산물의 용해성 부분에 의한 치사효과가 l~lOmg / l 범위에 있음을 보여준다 (H y land and Schneid e r, 1976). 불용성인 석유 부분은 생물을 덮음으로써 질식을 유발하거나 식용생물 울 먹을 수 없게 하므로써 손상을 일으킨다. 그러나 독성에 관계되는 것 은 용해성 부분이다. 비등점이 낮은 방향족 탄화수소 계열이 가장 유독 하여 생물치사에 일차적인 원인을 이루는 것으로 알려져 있으며 벤젠, 톨루멘 크실렌, 나프타렌, 펜안트렌p henan th rene 등이 여기에 속한다. 분자량이 낮은 지방족은 해수에 쉽사리 용해되며 낮은 농도에서 생물의 마취와 마비를 일으킨다. 농도가 높을 때에는 특히 해양생물의 유생시기 에 세포 손상과 치 사를 야기 한다. 일부 헤 테로고리 화합물 hete r ocy cl ic com p ound 도 유독하지만 석유 유출시의 농도보다 더 높은 농도일 때 독 성을 나타낸다. 비동점이 더 높은 원유부분은 3.4-benzo pyrene 과 기타 다환성 po lyc y c l ic 인 지방족화합물 등을 이루는데 암을 유발하는 것으로 알려져 있다.
표 10-6 은 여러 가지 해양생물에 대한 원유 및 제 2 원료유의 치사효과 롤 요약한 것이다 . 표시된 농도는 생물의 치사를 일으키는데 필요한 평 균 96 시간의 치사농도이다. 용해성 방향족화합물을 대량 포함하는 제 2 연 료유가 원유나 잔류산물보다 현저하게 독성이 큰 것은 주목할 일이다. 일반적으로 석유에 대한 감수성은 하등무척추동물로부터 고동무척추동 물에 이르면서, 또한 고등무척추동물로부터 어류에 이르면서 증가하는 경향을 갖는다. 그러나 어류는 유영능력을 갖고 오염수역을 피할 수 있 기 때문에 저항성이 큰 다론 하등동물보다 피해가 적을 수 있다. 보통 표 10-6 해양생물에 대한 원유 및 제 2 연료유의 치사 효과 96-h LC, mg tot a l hy d rocarbons/l 종류 서식지 원유 제 2 연료유 어류 : 연어 표영성 1. 50 o. 54 곤들메기 표영성 2.2 7 0. 72 횟대 표영성 3.82 2.41 강도다리 저생성 >4. 69 >1. 72 베도라치 조간대 >5. 89 >1. 72 갑각류: 단각류 TuoT 서o >7. 40 >O. 48 미새시우드 조닙' 하0” 대서 ° >93..19 24 >00..4559 집게 조하대 >6.94 >8.19 왕게 저생성 4.70 0. 81 환형동물: 갯지렁이 조간대 >6.94 >8.19 극피동물: 불 7~ 사리 조간대 6.94 >8.19 자료 : Ric e 등, 1979
유생시기에 있는 동물이 가장 예민한 반응을 나타낸다. 석유 독성에 대한 감수성은 생물의 서식지와 제일 관련이 깊다. Ri ce 등(1 979) 은 표영성인 어류와 새류가 [당 총탄화수소의 96 시간 평균치사 농도가 1~3mg / l 수준으로서 원유나 제 2 연료유에 가장 민감하고, 저생 성인 어류, 게, 국자가리비 등은 3~8m g / l 으로서 중간 정도, 그리고 조 간대 생물인 어류, 게, 불가사리 및 많은 연체동물은 8~12m g / l 으로 가 장 저항이 크다는 것을 발견하였다. 아치사효과는 낮은 ppb 범위의 석유농도에서 관찰되는데 그 독성으로 나타나는 증상은 식물플랑크톤의 세포분열 지연, 어류의 비정상적인 산 란, 게 등에서 보는 섭식활동의 감소, 짝짓기 저해, 생활사 기간의 감소 등을포함한다. 10-3-2 해양생물군집에 대한 영향 석유 오탁에 의한 손상은 단일한 유류유출에서 기인하는 수도 있고 낮 은 농도이나 계속적인 방출로부터 올 수도 있다. 단일한 유류유출일 경 우에는 저항성이 적은 생물의 치사를 일으키는 심각한 초기 영향을 일으 키는 수가 많다. 그렇지만 종국적으로는 그 해역이 정화되고 해양생물군 표 10-7 해양 개체군 및 군집에 대한 석유의 영향 군집 혹은 개체군 형태 예상되는 초기 영향 정도 예상회복률 풀랑크톤 경미 -➔ 보통 급속->보통 암석조간대 군집 경미 급속 모래나 펄조간대 군집 보통 보통 조하대 군집 심함 완만 어류 경미-+보통 급속一보통 AI 심함 완만 해양포유류 경미 심한 영향의 경우 완만 자료 : Hy la nd and Schneid e r, 1976
집이 회복될 것이다. 이러한 회복은 지역이 급속히 정화될 수 있는 암반 해안에서는 불과 수 주일이면 이루어 지는데 반해 석유의 잔류가 장시간 지속되는 갯벌이나 습지에서는 수년 이상이 소요될 수도 있다(표 10~7). 항구, 정유공장, 폐기물처리장 등으로부터 오는 낮은 농도의 계속적인 오탁은 군집구조상에 갑작스러운 변화를 일으키지는 않으나 석유의 만성 아치사효과로 인한 점진적이고도 영구적인 개체군 변동을 유도할 수 있다. 해양미생물에 대한영향 유류 성분은 일반적으로 해양 박테리아의 성장을 저해한다. 석유의 많 은 성분이 미생물 개체군에 대하여 독성을 갖울 뿐만 아니라 미생물에 의한 탄화수소의 분해로 형성되는 산물들 역시 원래의 탄화수소보다 더 유독한 경우가 많다 (B artha and At la s, 1977). 일반적으로 석유탄화소에 노출된 해양환경에서는 미생물의 수와 다양성에 있어서 감소가 일어난 다. 그러나 경우에 따라서는 탄화수소의 첨가가 일차적으로는 탄화수소를 이용하는 미생물에 대해서, 그리고 2 차적으로는 탄화수소 이용 미생물에 의해 생성된 대사산물을 유용하게 활용하는 미생물에 대하여 풍족한 환 경을 형성하게 될 것이다. 특히 만성적으로 석유탄화수소가 유입하는 해 역에서는 결과적으로 이들 미생물이 증가될 것이다. 이 경우에 필시 종 의 다양성은 감소할지라도 박테리아 개체군은 전반적으로 증가하게 된다. 해양 플랑크톤에 대한 영향 국지적인 해역에서 석유 유출은 수면에 뜬 기름 속에 들어 있는 유독 성분과의 접촉 때문에 식물 플랑크톤이나 원생동물 개체군의 감소를 일 으킬 수 있으나 플랑크톤 군집 전반에 대한 영향은 통상 미세한 것으로 알려져 있다. 이들 생물은 매우 빨리 번식하고 어떤 개체군의 감소가 일 어나면 급속히 회복된다. 그러나 플랑크톤군집의 일부 생물군인 어류, 갑각류 및 연체동물의 유생 등은 심하게 영향을 받을 수 있고 이 경우에 회복은 수년 이상 걸리게 된다.
저생생물에 대한 영향 해저의 기부가 석유를 축적하고 저생생물이 본질적으로 이동성이 없어 서 유류오영으로부터 도피할 수 없기 때문에 저생생물군집이 유류오염의 영향을 가장 심하게 받는다. 수층은 석유 유출 직후에 바교적 기름이 없 고 따라서 표영성 생물의 피해를 면케 해주는 반면에 , 해저에서는 생물 이 기름에 쌓인 환경 에 수년 간 직 면하지 않을 수 없다. 1978 년에 발생 한 유조선 Amoco Cadiz 호의 사고는 223, 000 톤의 원유를 바다에 유출시 켜 부근에 있는 브르타뉴해안의 생물군집에 엄청난 피해를 입혔으며 10 년이 지난 후에도 회복이 되지 않고 있다 (B i sho p , 1983). 조간대지역은 파랑작용에 의해 보다 빨리 정화될 수 있기 때문에 통상 보다 빨리 회복 된다. 같은 이유로 암반해안은 사질해안보다 더 빨리 회복될 것이다. 어류에 대한 영향 어류에 대한 석유의 악영향은 어류의 상업적 가치로 인해 중요성이 커 진다. 유류오염에 의한 어류의 치사가 보고되어 있지만 심한 정도는 아 니다. 이것은 유류오탁지역으로부터 도피하는 어류의 능력에 기인할 것 이다. 석유생산기지 주변수역에서는 어류수의 감소가 거의 나타나지 않 는다. 어류군집 가운데 가장 큰 위협은 고농도의 석유에 접하게 되는 저 생성 어류, 그리고 어류의 어린 시기가 석유 중독에 가장 예민하기 때문 에 산란장 해역에서 나타난다. 어류 치사의 증거가 충분하지 않더라도 어류의 조직 속에 암유발성 방향 족 화합물의 축적은 심각한 문제가 된다. 석유탄화수소의 농도가 Img /l 의 낮은 수준에 노출되어도 일부의 어류는 해독을 일으킨다. 사람의 경우 는 5~20p pm 범위의 농도로 동물 조직 속에 들어 있는 석유탄화수소의 맛 울 느낄 수가 있다. 더구나 어류와 패류는 그 조직 속에 발암성 방향족 화 합물을 생 물축적 한다는 사실 이 알려 져 있다 (Bernhard and Zett er a, 1975) . 바닷새에 대한영향 바다에서 생활하는 많은 새들은 해수표면에 떠 다니고 또 먹이룰 취하
기 위해 물속으로 날아둘 때 기름에 접촉하게 되므로 석유오영에 특히 취약하다. 새들이 기름에 접촉하게 되면 기름이 깃털을 젖게 하고 깃털 이 갖고 있는 방수 및 단열기능을 파괴하므으로써 새들이 추위에 떨고 물에 노출되어 죽게 된다. 또한 새들은 흔히 것에 묻은 기름을 닦아내기 위하여 주둥이를 사용하게 되고 그러므로써 기름을 섭취하게 되어 체내 손상을 야기한다. 석유를 정화하므로써 바닷새를 구하려는 노력은 불행 히도 성공하지 못하였다. 새들은 비교적 수명이 길고 생식률이 낮기 때 문에 개체군 손실에 대한 회복은 아주 완만하게 이루어 진다. 이로 인해 서 석유오염은 해양생물 가운데 어떠한 종류보다도 바닷새에 대해서 더 욱 손상을 일으키는 것으로 생각된다. 해양포유류에 대한 영향 해양 포유류동물은 비교적 수가 적고 고도로 운동성이 있으며 따라서 석유유출에 접하는 경우가 적다. 그러나 접하게 될 경우에 눈이 멀거나 털의 기능이 약화된다는 일부의 결과가 알려져 있다. 10-3-3 해양생태계에 대한 석유의 영향 해양의 주요 생태계에 있어서 석유오염에 의한 영향의 심각성과 예상 되는 회복률은 생태계의 특성에 따라 크게 변화한다. 예컨대 의양에서의 유류 유출은 악영향을 거의 일으키지 않으며 회복이 빠르다. 한편 하구 역, 항구수역, 혹은 습지의 석유류 오탁은 심한 손상을 일으키고 회복은 보통 매우 느리게 진행된다. 따라서 이러한 지역에 유류가 도달하는 것 울 막고 도달하였을 경우에는 즉각 제거하도록 노력이 경주되어야 한다. 유류 유출의 정화에 대한 필요와 정도는 영향받은 생태계의 형태에 의해 서 결정되어야 한다. 해번에 대한 유류오염의 영향 해양 유류오염의 가장 뚜렷한 영향은 암반, 사질 및 동식물을 검은 기 름막으로 덮고 해변과 해안선에 남게 되는 찌꺼기이다. 기름의 풍화로
형성된 타르 덩어리는 해안에 표류하고 또한 걸리게 된다. 이들 물질의 모양과 냄새는 해안지역의 심미적 매력을 손상시킨다. 불행하게도 해변 에서는 이러한 물질의 출현이 급속히 증가하고 있다. 기름에 의해 어느 정도 오탁이 되지 않은 해변을 찾아 보기가 점점 어려워 지고 있다. 유류가 유출된 해변을 정화하려는 기도가 과거 수년 동안 아루어져 왔 으며 이 과정에서 통상 오탁된 물질의 물리적 제거나 혹은 잠재적으로 유독한 화합물인 기름 분산제의 첨가가 수반된다. 그러나 최근에 이러한 정화방법이 흔히 유류의 오염물질 자체보다도 더 큰 생물학적 손상을 야 기한다는 사실을 연구자둘은 인식하게 되었다. 따라서 심미적으로 가치 가 있는 해안을 유지하려는 욕구와 다른 한편으로 해안 생태계를 보호하 려는 필요성간에 상충이 생기게 된다. 생산수 (pro ducti on wate r ) 일상적인 석유생산에 의한 환경의 영향에 대하여서는 알고 있는 바가 아주 적다. 앞서 언급한 바와 갇아 연해석유 생산기지의 일상적인 조업 으로부터는 두 가지 형태의 석유방출이 발생한다. 첫째는 기름 속에 있 으면서 기름이 해안으로 수송되기 전에 분리되는 생산수이고 둘째는 석 유저 장 시스템으로부터 오는 변위수 dis p l a cement wate r 이 다. 이 러 한 소 금물은 불가피하게 어떤 탄화수소를 포함한다. 그러므로 이러한 물이 방 출되기 전에 기름과 가스가 최소화 되도록 처리하지 않으면 안 된다. 생산수는 석유탄화수소와 페놀 같은 유기물질 및 중금속울 포함한다. 생산수의 조성과 여러 가지 성분의 농도는 그 원천, 석유의 질, 유정의 연령 등에 따라 크게 변화한다. 그러나 이들 물질의 그 어느 것이라도 해양환경에 대하여 해로운 영향을 미친다. 그러나 다행히도 대부분의 연 구 결과를 보면 미국 환경청에 의해 정해전 방출량에 따른 생산수의 영 향은 최소임이 알려져 있다. 왜냐하면 방출량을 지킬 경우 급속한 회 석과 분산으로 환경의 안정을 유지할 수 있고 이러한 사실은 실제로 석유생산기지 주변해역에서 나타나는 커다란 어군의 존재가 그 증거가 된다.
탄화수소의 분산은 일반적으로 상당히 빠르게 진행된다. 희석이 크게 일어나는 의에 농도를 감소시키는 경향을 지닌 증발, 에멀션화작용 및 생물분해 등을 포함한 풍화를 거치게 된다. 예컨대 해저 상부 50m 수충 에서 40m g / l 의 탄화수소를 함유하고 있는 생산수를 1, OOOm3/h 로 방출 할 경우에, 저충 해류를 90m/ h, 수직확산계수를 20m2/h, 수평확산계수 를 2, OOOm2 / h 로 가정하면 2, 800m 에 홀러간 곳의 최대 해저농도는 4 m g / !에 불과할 것이다 (Read and Blackman, 1980). 또한 석유생산기지에 서 나오는 방출수 중에 있는 2~60mg / l 범위의 농도는 그 지기로부터 1.6 Km 이내의 수역에서 1mg / l 이하로 감소된다. 따라서 생산수의 방 출에 의한 어떠한 해로운 영향도 방출량의 한계를 지킨다면 극히 국지적 인 문제만을 유발할 것이다. 시추니(試維泥)와 커팅 (cutt ing ) 연해 유정에서 오는 또 다른 오염원은 유정을 시추하는 동안에 방출되 는 시추니 drill ing mud 와 커 팅 의 파편들이 다. 하나의 유정 을 뚫을 때 구 멍을 메우고 있던 진흙, 모래, 암석 등이 제거되기 마련이다. 이들 물질 이 표면에 울라오면 혈암분리기(頁岩分離機)로 옮겨지고 여기서 시추 자 스러기가 제거되며 진흙과 함께 바다에 버려져 다시 바닥에 쌓인다. 이들 물질은 많은 성분을 포함하고 있으며 전체량으로서의 이들 물질 자체가 해양생물에게 유독하다. 이들 물질은 또한 즉각적으로 높은 산소 요구량을 나타내고 고농도의 유기탄소, 질소 및 인을 함유한다. 미국 환 경청은 시추액이 때때로 고도로 유독하고 발암성이며 해양생물에 의해 섭 취 됨을 발표한 바 있는데 이 러한 독성은 일차적으로 유해한 pen ta c hlo- ro p henol 의 존재에 기인한다. 이 물질은 그 상태가 해양되적물 속에서 수년 간 지속된다. 해저에서 다양한 군집을 형성하는 생물들이 이러한 물질로 오탁된 되적물에 노출될 경우에는 성장이 불가능하다. 이처럼 높 은 유독성 때문에 pen ta c hlorop he nol 을 시추액 에 첨가하는 것 이 금지 되 었고 그 결과 독성은 크게 감소되었다. 커팅 그 자체는 암석 파편으로서 무독하다. 그러나 이것이 해저에 쌓
이면 저생생물군집을 덮어서 질식시킨다. 따라서 이 영향은 국지적으로 나타난다. 10-4 해수중에서 유류의 변화 수백만 년 동안 해양으로 석유가 둘어갔으나 해수표면에 기름막이 존 재하지 않았고 많은 양의 석유가 해수중에서 발견되지 않았다. 근래의 대형 석유 유출이 나타났지만 영구적인 변화를 일으키지 않고 있으므로 분명히 자연은 석유가 유입된 해양을 정화시키는 방법을 갖고 있다고 할 것이다. 이러한 과정들은 최근에 알려지게 되었다. 유류는 해양환경으로 들어가자마다 많은 물리 • 화학적 변화를 겪는데 그 변화들은 다음과 같은 것들이다. 슬릭 형성 분해작용 증발 중합반웅 에멀션화 기름속 물 에멀션 (wa t er in oil emulsio n ) 물속 기름 에멀션 (o i l in wate r emulsio n ) 무기화작용 미생물분해 퇴적작용 플랑크톤섭취 타르 덩어리 형성 이들 과정을 총합적으로 〈석유의 풍화〉라 부른다. 대부분의 유출은 죽각적으로 표면 술릭을 형성하고 이것은 바람, 파 랑, 해류작용 등으로 이동된다. 이 슬릭은 해수 표면의 넓은 면적에 걸
쳐 아주 얇은 기름막을 형성하면서 급속하게 퍼진다. 기름 속에 포함된 많은 탄화수소는 휘발성이서 죽시 증발한다. 석유가 퍼지고 슬릭이 더 얇아지면 증발속도가 증가한다. 가벼운 휘발성 물질의 손실은 기름의 밀 도를 높여주고 따라서 표면에 뜨기 보다는 가라앉게 해 준다. 일부 극성 탄화수소의 성분은 해수 속으로 용해되어 슬릭의 밀도와 점성을 더욱 크 게 만든다. 해수의 난류는 기름속 물 에멀션이나 물속 기름 에멀션을 형 성시킨다. 이 모든 작용이 일어나는 동안 광화학반응으로 기름의 특징이 바뀔 수 있고 미생물 분해작용으로 존재하는 기름의 양이 감소되기도 한 다. 얇은 유막의 형성과정, 휘발성 성분의 증발, 탄화수소의 용해 등은 유 출이 된 후 수일 내에 약 50% 까지 유출량을 감소시킬 수 있다. 개솔린 같은 정유산물은 거의 완전히 소실되는 반면에 점액성이 있는 원유는 25 % 미만으로 감소된다. 표 10-8 은 전형적으로 원유가 바다에서 변화를 일으키는 경로를 요약한 것이며, 그림 10-4 는 이러한 경로를 도식한 것 이다. 이제부터 이러한 물리적, 화학적, 생물학적 경로를 보다 상세히 검토 해 보기로 한다. 표 10-8 원유의 환경 변화 경로 시간(일) 비율 증발 1~10 25 용해 l~10 5 광화학반웅 10~100 5 생물분해 50~500 30 붕괴와침전 100~1,000 15 잔류 >100 20 겨] 100 자료 : Butl e r 등, 1976
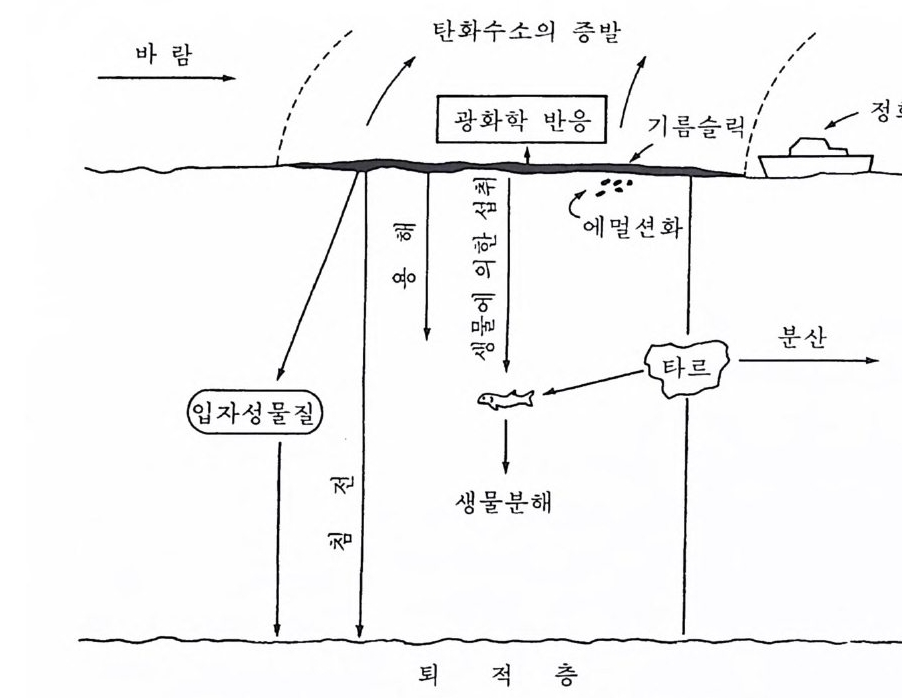 바타C ,/, I / / / 앞曰- 화三수[. 소三의. 曰(증-:발-:- •1 소 기 름_슬 릭: , /I I / / // 정화작업
바타C ,/, I / / / 앞曰- 화三수[. 소三의. 曰(증-:발-:- •1 소 기 름_슬 릭: , /I I / / // 정화작업
그림 10-4 기름 슬릭 ( oil s l i ck) 의 변화 경로
10-4-1 확산 조용한 수역으로 유출된 대부분의 기름은 중력과 표면장력의 결과로 얇고 연속적인 충으로 확산되어 나간다. 석유충의 두께를 통해 하향으로 작용하는 중력은 석유의 점성이 확산력과 균형을 이룰 때까지 옆으로 퍼 지는 경향을 갖는다. 보다 더 중요한 것은 표면장력 효과가 막을 더욱 확산시키는 요인이 되는 점이다. 예컨대 lOOm 떡 원유는 유출된 지 불 과 17 분 후에 평균 0. 55 mm, 3 시간 후에는 0.12 mm, 그리고 28 시간 후 에는 0.33mm 로 얇게 확산된다. Fa y(l 971) 는 유막의 확산과 두께의 정도를 결정하는 수식을 다음과 같 이 제안하였다. 깁간 max= A = 105 V0·2 5
여기에서 Rm o.x = 원형으로 가정한 석유 확산면적의 최대 반경 (m) A= 유막의 면적 (m2) V= 유출된 석유량 (m3) 유막의 두께 hoil 은 다음과 같이 계산한다. hoi l=A~V lOOm 떡 석유가 유출되었다고 가정하고 위의 식을 이용해 계산하면 유막의 확산면적 3. 16 X l06m2 , 직 경 1, 000 m, 그리고 유막의 평균 두께 가 0.03mm 가 되는데 이는 유출 해역에서의 실제 관측치와 잘 일치한 다. 확산이 일어날 때 동시에 바람과 파랑운동이 기름막을 이동시키면 유 막 면적이 더욱 길어지고 찌그러든다. 바람과 바람으로 일어나는 파랑에 의한 석유막의 유동속도는 바람속도의 대략 3.4% 임이 알려져 있다. 유 막 중심의 실제속도를 계산하기 위해서는 이 속도에 표충류의 속도를 추 가하여야 한다. 바람과 파랑작용은 기름막을 분쇄하여 작은 유막과 유막의 줄을 형성 하는 경향이 있고 이 가운데에서 두꺼운 층은 훨씬 얇은 막으로 둘러 싸 인다. 바람의 방향으로 놓인 길고 좁은 리본형의 기름막은 유출량의 약 90% 를 차지한다. 기름 줄은 1~20mm 의 두께믈 갖는 반면에 얇은 충 은 0. 01~0. 001 mm 의 두께를 갖는다. 10-4-2 풍화 슬릭의 특징과 슬릭 속의 석유 조성을 변화시키는 자연적인 과정은 많 이 있다. 이들 과정 가운데 증발, 용해, 에멀션화, 수층으로의 하향 확 산 및 생물분해 등이 속하며 이 과정들을 총칭해서 풍화라고 한다.
증발 석유가 해수중에 유출되면 이내 증발이 일어나게 되는데 확산이 진행 되고 유막이 더 얇아짐에 따라 증발속도는 증가한다. 이때 증발하는 양 과 속도는 석유중에 들어 있는 가볍거나 휘발성인 성분의 비율에 의존한 다. 대략 C15( 탄소 수 15) 이하(비등접이 250°C 이하)인 모든 탄화수소는 10 일 이내에 해수 표면으로부터 증발된다. C15~C25 범위에 있는 (비등접 250°C ~400°C) 탄화수소는 휘발성이 한정되어 대부분이 슬릭 속에 남게 된다. c25 이상(비등점 4oo·c 이상)인 탄화수소는 거의 손실이 없다. 그 림 10-5 는 이 러 한 증발속도를 도표로 나타낸 것 이 다. 따라서 바다에 유출된 석유의 상당한 부분이 증발에 의해 급속하게 대 기로 소실된다. 전형적인 원유는 며칠 동안에 증발로 체적의 약 50% 가 소실될 것이다. 그러나 벙커 C 유 감은 무거운 기름은 휘발성분의 결핍 때문에 체적의 10% 미만이 소실된다. 제 2 연료유(디젤유) 같은 고도로
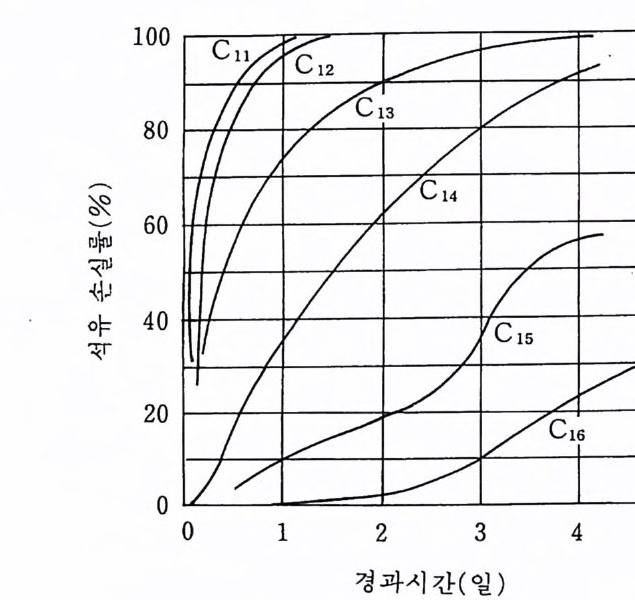 100
100
그림 10-5 석유의 증발률 자료 : Bis h op , 1983
정제된 석유는 체적의 75% 이상을 증발로 소실될 것이다. 가솔린이나 케로신은 증발이 진행된 2~3 일 만에 흔적만이 남게 된다. 슬릭 속의 기름이 증발함에 따라 보다 가벼운 성분이 제거되고 보다 무겁고 밀도가 높으며 점성이 큰 잔해가 남게 된다. 그러므로 풍화된 원 유의 조성과 성질은 유출된 원래의 원유의 그것과는 전적으로 다르다. 석유의 가벼운 성분은 독성의 관점에서는 방향족과 지방족이 가장 위험 하다. 따라서 이들 성분이 휘발작용으로 슬릭으로부터 급속히 제거되는 것은 생물계에 대한 위험성을 감소시키는 경향을 갖는다. 석유 유출이 의해에서 일어날 경우에 많은 예에서 보듯이 취약한 해안지역에 그 물질 이 도달하기 전에 증발이 끝난다. 물론 해수 표면으로부터 증발된 탄화수소가 파괴되는 것은 아니다. 오 직 상태만이 변형되어 해양 상공의 대기 속에 들어 간다. 이들 물질의 일부는 강우를 통해서 다시 바다로 돌아 울 수도 있지만 대기중에서 일 어나는 광화학적 산화 때문에 그 양은 적다. 특정 석유 유출로부터 예상되는 증발량을 추정하기 위해서 수식을 사 용할 수 있으며 증발률 자체는 존재하는 석유의 형태, 그 온도, 슬릭 떤 적 등에 의해 영향을 받기 때문에 이러한 요소가 수식에 포함된다. 석유 는 몇 개의 성분으로 나누어지고 각 성분의 증발속도는 다음 식에 의해 결정된다• Ef= KReCTiP i 여기에서 Ef = 증발량 (mo l/ cm2 • sec) Ke= 증발전달계수 (cm/sec) Ci= 석유 중의 i 번째 성분 농도 (mole frac ti on ) R.= 석유온도에서 순수한 성분의 증기압 R= 보편 가스 상수
T= 석유 술릭 상의 대기 온도 u=P i풍는속 기 (cm준/ 치s 가ec ) 이나 다와. 있고 K e 는 Ke=O.005U0·1 8 로서 구하는데 이때 어느 시간 t에서 총증발은 2 시간 동안 각 성분의 증발속도의 합으로 써 결정될 수 있다. 즉 E = jEJ ( MW) dt 여기에서 E= 전체 증발속도(g / cm 2 ) MW= i번째 성분의 분자량이다. 광화학적 산화 해수 표면에 부유하는 원유나 정유산물의 많은 성분은 대기중의 산소 와 빛의 작용을 통해 광화학적 산화를 겪게 된다. 이 반응이 일어나는 크기와 속도는 일차적으로 석유의 화학적 조성과 홉광도에 의존하는데 홉광도는 광복사의 흡수량을 결정한다. 이러한 반웅이 일어날 때 슬릭 속에 있는 산소가 첨가된 화합물의 부분이 증가하여 석유의 조성이 바뀌 게 된다. 일부 탄화수소는 다른 것에 비해서 광화학적 산화를 더 쉽게 받는다. 예컨대 방향족 화합물과 알킬이 치환된 시클로알칸 등은 정상적이거나 곧은 사슬 지방족 화합물보다 더 빨리 산화되는 경향이 있다. 이러한 반 웅의 일부 산물은 원래의 성분보다 더 낮은 분자량을 갖는 수도 있으나 대부분 더 무겁다. 이들 고분자량 물질은 오래 동안 지속하는 불용성인 끈적끈적한 찌꺼기와 타르를 형성하기 쉽다. 주요한 산화 산물은 지방족
및 방향족의 산 종류, 알콜, 에텔, 디알킬 과산화물, 카보닐 화합물 등 이다. 이둘 물질은 통상 물에 녹고 자연적으로 희석된다. 매우 느린 과정인 광산화의 효과는 석유 조성에 의존된다. 예컨대 바 나듐 성분은 촉매로서 작용하여 산화를 증진시키는데 반해 높은 유황 함 량은 산화를 감소시킨다. 용해작용 일부 석유성분은 용해에 의해 슬릭으로부터 소실된다. 그러나 저분자 량 탄화수소와 유황, 질소, 산소 같은 극성 원자단기를 포함하는 탄화수 소만이 물에 상당한 용해력을 갖는다. 만일 원유나 연료유와 물을 1 : 10 의 비율로 섞는다면 극히 작은 부분인 약 0.02% 만이 액상으로 추출될 것이다. 그러나 이 추출과정은 추출물 속에 가장 유독한 성분이 포함되 어 있기 때문에 중요하다. 여러 가지 탄화수소의 용해도는 해수에 대해 서 C10 이상에서는 무시할만 하지만 방향족 탄화수소는 용해성이 더 크 다. 결국 저분자량 탄화수소만이 해수에 상당량 용해한다. 이들 물질은 쉽게 휘발하는 탄화수소이기도 하다. 석유 슬릭 밀에서 채취한 해수 시 료 중에서 용해된 탄화수소의 농도를 조사한 결과는 이들 저분자량 물질 울 거의 발견할 수 없었고 따라서 이들 물질에 대한 주요 경로가 증발과 정임을 나타내 준다. 에멀션화작용 석유 슬릭 밀에 용해된 기름이 극히 적다고는 하지만 이것이 수층에 기름이 존재하지 않는다는 의미는 아니다. 슬릭 밀의 해수를 검사해 보 면 슬릭의 에멀션화 작용의 결과로 세분된 많은 유적 (油ijij)을 볼 수가 있다. 물속 기름 에멀션 oil -i n - wate r emuls i ons 의 형성은 기름의 중요한 분산 방식이다. 난류와 파랑작용은 석유의 표충을 바다의 상충으로 혼합시켜 수 많은 극히 작은 유적의 형성을 촉진시킨다. 이 유적은 상당한 깊이까 지 급속히 분산하고 현탁상태로 오랜 시간 남아 있어서 해류에 의해 유
출장소로부터 먼 거리까지 운반될 수도 있다. 유적의 크기는 5µm 로부 터 수 mm 까지이며 수충 내에서는 30m 수심에서 발견되고 약 250km 까지 분산된다. 물속 기름 에멀션은 궁극적으로 수충에 용해되기도 하고 고형입자물질에 부착해서 생물분해나 퇴적 속에 들어가기도 한다. 기름속 물 에멀션 wa t er- i n-o il - emuls i on 은 특히 무거운 원유와 잔류기 름에서 형성된다 . 이 에멀션은 80% 의 물을 함유하고 있으나 반 고형의 구조를 갖는다. 쉽사리 분산하지 않고 파열되지 않으며 해수 표면에서 상당한 시간 지속한다. 이들은 왕왕 함께 엉켜서 상당히 두꺼워지기도 한다. 오랜 시간이 지나간 뒤 이것은 부숴져 타르 덩어리가 되지만 그러 는 동안 해변으로 씻겨간다. 타르 덩어리 형성 대부분의 모든 해변과 대양의 거의 모든 부위에서 타르 덩어리를 보게 된다. He y erdahl(1971) 은 그의 갈대로 만든 배안 Ra II 를 타고 대서양 울 횡단한 기록 속에서 대양의 중앙 해역에 떠돌아 다니는 부드러운 아 스팔트 같은 덩어리가 많이 목격되고 있음을 적고 있다. 타르 덩어리의 농도가 가장 높은 곳은 지중해와 Sar g asso 해인데 이곳에는 평균 약 10 m g/!이 나타난다. 이 타르 덩어리는 주로 유조선의 탱크에 있는 기름 슬럿지롤 세척하는 과정에서 생기며 또 사고로 인한 석유 유출이 풍화를 거치는 동안 형성 되는 것도 중요한 과정이다. 물론 해저로부터의 자연 유출도 타르 덩어 리를 형성한다• 타르 덩어리의 형성은 환경에 노출되는 석유 표면적을 제한하고 분해를 지연시키기 때문에 덩어리로 된 기름은 지속성이 크다. 따라서 심각한 환경문제를 야기시킨다. 퇴적작용 유출된 석유의 일부는 궁극적으로 침강한다. 앞서 설명한 여러 가지 과정들이 기름의 밀도를 높이고 결국 침전시킨다. 증발과 용해작용은 가 볍고 밀도가 낮은 부분을 제거시키고 광화학적 반응과 아울러 반 고형인
타르 덩어리의 형성을 유도한다. 이들은 작고 농밀한 입자로서 침강한 다. 수충에 분산된 석유 입자들이 집적된 다음에는 부유하는 우기 퇴적 물 상에 흡수되는데 이러한 현상은 많은 부유 퇴적물이 존재하는 연안 수역과 하구역에서 종종 나타난다. 세립점토 물질도 다량의 용해된 탄화 수소를 물로부터 흡수한다. 미생물에 의한생물분해 광화학적 산화 이외에는 분산이나 풍화작용의 어느 것도 실제적으로 환경으로부터 탄화수소를 제거하지 못한다. 실질적인 분해는 생화학적 산화과정을 통해서만 일어난다. 결국 생물분해 작용은 석유가 바다로부 터 사라지는 기본적이며 장기적 수단이 된다. 지방족 및 방향족 탄화수소는 전 환경을 통해 도처에 분포되어 있다. 모든 살아 있는 생물이 오랜 역사를 통해 이들 화합물과 접촉해 왔기 때 문에 많은 생물들이 이들 화합물을 산화시킬 수 있는 효소계를 진화시켜 왔음도 놀라운 일은 아니다. 자연수 중에 존재하는 다양한 범위의 미생 물에 의해 탄화수소 분해가 아루어 지고 있음이 알려져 있다. 석유 속에 존재하는 많은 탄화수소는 해양생물에 대하여 매우 유독하 다. 그러나 어떤 경우에는 생태계로의 기름의 첨가는 탄화수소를 이용할 수 있는 미생물에 대하여, 그리고 탄화수소 이용 미생물에 의해 생산된 대사산물을 이용할 수 있는 다른 생물에 대하여는 생태계를 풍요롭게 해 줄 것이댜 따라서 이러한 현상은 계선장과 항구, 연안역과 하구역, 도 시 및 공장폐수 배출구 같은 석유산물의 만성적 유입이 있는 곳에서 종 종 발생한다. 탄화수소를 산화시키는 미생물은 석유로 오염된 해역에서 는 전 미생물 개체군의 5~50% 를 이룬다. 따라서 존재하는 석유 분해자 의 수는 주로 장소의 오염 기간으로서 결정되고 석유로 오영된 기간이 긴 해역일수록 더 많은 석유분해 미생물을 포함하고 있다. 물속에서 탄화수소를 분해하는 박테리아는 현재 수백 균주가 동정되어 있는데 특히 다음의 속, 죽 Pseudomonas, Achromobacte r , Ar thr obact er, Mi cr ococcus, Nocardia , Ente r obact er, Vibn ·o, Klebs iell a, Flavobact er i um
등에 속하는 박테 리 아와 수종의 균류가 주류를 이 룬다 (Aus ti n et al. , 197 7) . 어떠한 미생물 종류도 원유의 모든 성분이나 혹은 한 탄화수소군의 모 든 화합물을 공격할 수가 없다. 그러므로 완전한 분해는 많은 미생물 사 이에 복잡한 상호 역할에 의존된다. 생물분해의 기작 앞서 본 바와 갇이 해수중으로 유출된 유류가 용존 상태로 존재하는 양은 극히 적다. 그러므로 탄화수소 이용 미생물은 불용성 석유를 공격 하는 방법을 갖고 있다. 석유에서 미생물 성장은 전형적으로 석유와 물 의 경계에서 일어난다. 많은 석유 분해 생물이 탄화수소에서 성장하는 동안 물속 기름 에멀션을 형성하는 능력을 갖고 있다. 이것은 미생물에 의한 펩티드와 지방산의 분비에 기인하는 것인데 이 두 물질은 원래의 탄화수소의 부분적 생물분해에서 유래하고 계면활성제로 작용하여 계면 장력을 감소시켜서 기름을 에멀션화 시킨다. 에멀션화 착용은 유용 표면 적을 증가시키고 따라서 공격할 수 있는 탄화수소의 기부를 더 많이 만 들게 된다. 증가된 표면적은 또한 액상으로 용해하기 위한 탄화수소의 양을 증가시키고 이곳은 미생물에 의해 쉽사리 섭취된다. 이 섭취는 미 생물의 세포막 중의 리피드 속으로 탄화수소가 흡수됨으로써 이루어 전 다. 석유를 분해하는 미생물의 능력은 존재하는 탄화수소의 성분에 크게 좌우된다. 미생물 분해는 일반적으로 저분자량 화합물에 우선적으로 시 작되고 다음에 고분자량 화합물로 진행된다. 즉 저분자량 알칸류와 방향 족이 먼저 분해되고 고분자량 알칸류가 다음에 분해된다. 다핵 방향족은 매우 서서히 분해된다. Ba rth a 와 A t las (l 977) 는 다음과 같은 일반 개념 울 제시한 바 있다. 1. n-alkane 류, 특히 C10 과 C2s 사이에 있는 것들은 가장 광범위하게, 그 리고 쉽사리 이용되는 탄화수소이다.
2 . iso -a l kane 류는 성 장 물질로서는 일반적으로 n-alkane 류보다 하위 이 다. 3 . olefi n 류는 상응하는 알칸류보다 유독성 이 크고 쉽사리 이용되는 정도 가낮다. 4. 저분자량 방향족 탄화수소는 미생물에 대하여 아주 유독하지만 저농도 로 존재할 때에는 쉽게 대사된다. 농축된 다핵성 탄화수소는 덜 유독하 지만 대사 속도는 매우 느리다. 5. 시클로알칸류는 독성이 크며 예의적인 경우에만 미생물의 성장물질로 작용한다. 그러나 어떤 것은 혼성 미생물 군집의 공동 대사공격에 의해 쉽게 분해된다. 탄화수소의 분해는 분자상 산소의 첨가로 이루어 진다. n- p ar affin류 의 산화는 말단산화t erm i nal ox i da ti on 를 경유하여 진행되고 결과적으로 베 타산화 /3- oxid a ti on 에 의 해 C2 단위 와 카르보닐산이 나온다 (그립 10-6) . 방향족 탄화수소의 박테리아 분해의 경우에는 고리분활이 디히드록시
 R- C H2 — CH 2- C H3 알칸
R- C H2 — CH 2- C H3 알칸
그림 10-6 알칸의 붕괴에 대한 대사경로
H OH OH 0+으 :(유: o ,,, OH 벤젠 카테 콜 (Ca t echol ) +0/ \+02 H o_e0H=0OHC 雲 HH _l((_Hoou 。~二CI) ++OH HO雲2200H 산oe 화C아H세3C트OO산H + CCHH숙I 22 신--CC산OO OOHH 그립 10-7 방향o족 화합물 붕괴에 대한 대사경로 H
화cis -d 반io응 l ,의 형산성소 분등자이의 필양요하 원게O 자된가다 (고그리림 1속0-으7)로. 들어가는 것, 그리고 만일 방향족 탄화수소가 알H킬 화 되면 초기 공격은 흔히 고리 분열에 앞서서 결사슬에서 일어난다(그림 10-8). 다핵성 탄화수소의 생물 분해는 아주 유사한 방법으로 일어난다. 그림 10-9 에서 보는 바와 같이 나프탈렌의 분해는 다핵성 탄화수소가 생물 분 해를 일으키는 하나의 예이다. 탄화수소 생물 분해의 궁극적인 산물은 이산화탄소와 물이지만 고분자 량 탄화수소의 생물 분해는 많은 중간 산물을 생성하며 이들의 일부는 억제 수준까지 축적한다. 예컨대 방향족 탄화수소의 생물 분해는 석탄산 과 안식향산의 중간 생성물을 낸다. 생성물 억제는 중간 생성물의 혼합 OH 二H :H2 二 OcH H2Il :CO。0H0HH1leoo1:2cO/c H0
OH 二H :H2 二 OcH H2Il :CO。0H0HH1leoo1:2cO/c H0
그림 10-8 곁사슬 방향족 화합물 붕괴에 대한 대사경로
 HOH OH
HOH OH
그림 10-9 나프탈렌 붕괴에 대한 대사경로
때문에, 그리고 존재하는 미생물의 혼합 개체군 때문에 석유 슬릭의 생 물 분해에 있어서는 일반적으로 제한요인이 아니며 타르 입자 속과 기름 속 물 에멀션 속에 잡힌 분해 중간 생성물이 미생물 공격에 대해서 저항 성을 줄 수 있다. 환경의 제요인 해양환경 내에서 생물 분해 속도는 기름의 조성에 크게 좌우되지만 다 른 환경요인이 이에 관여한다. 풍화의 정도는 흔히 생물 분해 속도에 영 향을 미친다. 풍화가 일어나는 동안 고도로 독성인 성분의 많은 것이 증 발이나 용해에 의해 슬릭으로부터 소실되어 훨씬 덜 독한 잔재물이 남게 된다. 이러한 현상은 따뜻한 해수에서는 통상 수 시간 내에 발생하지만 냉수에서는 증발과 용해 속도가 크게 감소하기 때문에 수 주일 걸리기도 한다. 모든 생화학적 과정에서와 마찬가지로 온도는 석유의 생물 분해 속도 에 중대한 영향을 미친다. 온도는 일반적으로 성장속도를 증가시키고 그 러므으로써 생물 분해를 증가시킨다. 온도의 상승은 또한 독성이 큰 많 은 성분의 휘발성을 증가시키고 석유의 점성을 감소시킨다. 따라서 유화 (乳化)의 기회를 증가시키고 미생물 활동과 용해도를 확대시킬 표면적을 증가시키게 된다. 산화 속도는 20°C 에서 보다 l0°C 에서 최소한 10 배 정 도 느리며, 해수가 결빙온도 가까이 되면 훨씬 더 느리게 된다. 그러나 극단으로 찬 해수에서도 석유유출의 주요 부분은 수 개월이 소요되기는 하지만 생물 분해를 겪게 된다. 생화학적 산화에 필요한 적절한 양의 산소가 있느냐 하는 것이 무엇보 다도 가장 중요하다. 탄화수소는 그 성질 때문에 산화방식으로만 변화될 수 있는 유기기질로 완전히 환원된다. 전자 수용체로서 역할을 하는 질 산 및 황산염과 함께 탄화수소의 무산소 산화가 일어난다는 주장이 있지 만 이러한 경로의 역할은 바다에서 석유 화합물의 분해에 있어서는 극히 적은 것으로 믿어전다. 의양에서는 수충의 상층부에 석유 생물 분해에 필요한 용존산소가 보
통 충분하고 특히 난류가 있는 곳에서 그러하다. 그러나 심해 수역이나 퇴적충에는 용존산소의 공급이 거의 없고 타르 덩어리나 기름속 물 에멀 션이 가라앉아 산소가 한정될 수 있다. 석유의 높은 산소 요구량 (3~4 Oi/ gH C) 과 해수중에서 낮은 산소용해도는 기름이 많이 존재하고, 재폭 기 reaerati on 속도가 낮으면 무산소 상태로 진행된다. 이러한 조건에서 는 생물분해 속도가 현저히 감소되고 석유탄화수소는 아주 오랜 기간 지 속하게 되는데 해양 퇴적물에서 흔히 나타나는 현상이다. 미생물은 산소 의에도 탄소, 질소, 인, 유황, 칼슘 등 많은 영양소를 필요로 한다. 많은 탄화수소는 비록 소량의 유황, 질소, 중금속을 갖고 있으나 탄소만을 공급한다. 따라서 박테리아는 기타 영양소를 환경으로 부터 섭취하지 않으면 안 된다. 불행히도 이들 물질은 대양에서는 종종 공급이 충분치 못하게 되고, 결국 질소나 인의 공급이 때로는 한정된다 (Davis 등, 1977). 만과 같이 둘러싸인 해역에서는 질소와 인을 첨가하여 인공적으로 탄화수소의 생물분해 속도를 증가시키는 일이 가능하다. 그 러나 의해역에서는 희석과 분산이 영양원소를 급속히 운반해 가버려 그 러한 일이 불가능하게 된다. 끝으로 하수오물에서 볼 수 있는 것같이 쉽사리 분해되는 유기물아 대 량 존재할 때에는 석유의 생물분해가 방해를 받는다. 따라서 폐수에 존 재하는 기름은 급속하게 분해되지 않는다. 생물분해 속도 기름의 형태, 해수중의 유류오염 내력, 존재하는 미생물의 수, 수온, 적절한 영양소 양의 존재 및 기타 많은 요인에 따라 기름이 분해되는 속 도와 정도는 크게 변화한다. 그 범위는 25~2,500g /(ma)(Year) 이다. 생물상에 의한 섭취 바다로 방출되는 석유탄화수소의 종극적 운명은 해양생물에 의한 섭취 이다. 대양에서나 해저상에 존재하는 석유 중 많은 것은 비록 소량이 용 해된 상태로 있기는 하지만 분산된 입자 석유, 혹은 떠돌아 다니는 타르
덩어리의 형태로 존재한다. 형태야 어떻든 이들 탄화수소 물질은 해양 먹이연쇄에 이르게 된다. 생물은 아가미를 통해서, 또는 물을 마실 때 입자를 섭취하거나 용해, 분산된 석유를 흡수한다. 섭취는 보통 아주 빠 르다. 생물 체내에 들어가면 석유는 퍼지게 되는데 이들 화합물의 일부 는 생물에게 암울 유발시킨다. 생물을 통과해 나온 것들은 변 속에 들어 가고 이것이 다른 생물에 의해 먹히고 대사되어 체내에서 흔히 간과 지 질 물질 속에 저장된다. 해산 식품의 오탁을 야기하는 것은 이 저장 물 질이다. 해양 생물이 영소화탄화수소와 중금속을 생물축적 시킬 수 있다는 것 은 앞서 논의한 바 있다. 죽 조직의 단위 무게 당 물질량은 연속적으로 더 높은 영양단계에서 증가한다. 그렇지만 이러한 생물확대가 석유 탄화 수소에서도 증명된 바는 없다. 해수나 퇴적으로부터 기름의 직접 섭취는 아마 먹이연쇄로부터의 섭취보다 더 중요할 것이다. 일부의 해양 생물, 특히 조개, 굴, 홍합 등은 정화 능력을 갖고 있다. 죽 이들 생물은 3 주 내지 8 주 동안 비오염 수역에 옮겨 놓으면 전부는 아니지만 대부분의 석유를 배출해 낸다. 어떤 어류와 갑각류는 채내에 저장된 석유 탄화수소를 2 주 내에 대사시킴으로써 자신을 정화시킬 수가 있다. 그러나 플랑크톤과 저생생물 속에서의 대사는 매우 느리다. 따라 서 대형 생물은 유출된 석유 탄화수소를 궁극적으로 파괴하는데 기여를 하고 그러므로써 미생물에 의한 생물분해를 보충하게 된다• 10-4-3 유류 유출의 동태 위에서 본 바와 같이 특정한 유류 유출의 동태를 결정하는 과정은 매 우 복잡하다. 유출되자 이내 기름은 분산하고 바람, 파랑, 해류 등의 작 용으로 이동할 수 있는 표면 슬릭을 형성한다. 일부 가벼운 탄화수소와 일부 극성 성분은 수충 속으로 용해되어 들어가기 시작하지만, 이들의 대부분은 증발을 통해 대기 중으로 소실된다. 거친 바다에서는 파도에 부대껴서 기름의 일부가 유화(乳化)되어 미세한 분산 유적(油流)으로서 수층으로 들어간다. 이들 유적은 조수와 해류의 작용 때문에 널리 분산
되거나 혹은 부유성 입자 물질에 흡착되어 천천히 해저에 가라앉는다. 파랑작용 또한 기름속 물 에멀션을 형성케 한다. 이 두껍고 무거운 에멀 션은 초콜릿 색상을 갖는다. 이것들은 더 풍화하여 타르 뭉치를 이루게 된다. 보다 가볍고 독성이 큰 부분은 슬릭으로부터 빨리 소실되어 독성을 감 소시킨다. 잔재물의 분해는 광화학적 반응이나 미생물학적 생물분해롤 통해 일어난다. 충분한 시간이 경과하면 풍화와 생물분해가 결합된 작용 이 유출된 기름의 대부분을 제거하고 수년 간 지속할 수 있는 아주 질은 아스팔트 상의 타르 뭉치를 남기게 된다. 불행히도 자연은 언제나 시간을 충분히 갖고 있는 것이 아니다. 그 결 과 기름은 해변을 망치거나 생물학적으로 예민한 조간대 혹은 하구로 밀 려와 심각한 손상을 입힌다. 이러한 경우에 기름의 이동을 중지시키거나 영향받은 지역울 깨끗이 하는 것이 무엇보다 급선무라 하겠다.
제 11 장 방사성 페기물 1942 년 이전까지는 인류가 이온화 방사선에 노출되는 것이 자연 방사 능과 X- 레이에 한하였다. 그 이후 무기, 전력 및 의학용으로 원자 에너 표 11-1 원자 에너지원과 이용 에너지원 출력 이용 원자로 증기, 전기 전력, 탈영, 선박 추전력 열, 전기, 중성자 우주선 및 인공위성 동력, 우주선 추전력, 연구용 물질 생산 핵폭발 운동에너지 군 및 민간 이용, 굴착 캡슐형 방사선 전기 향해기기, 무인 기상관측소, 인공 동위원소 장기 감마및 베타 식품보존, 중합반웅, 의료기기소독 방 A t선 두께 측정기 방사선 핵종 베타 및 감마 의료 이용, 과학연구의 추적자 방사선 자료 : 미국 학술원, 1971
지를 이용함에 따라 인공 방사선에 노출되는 일이 크게 증가하였다(표 11-1). 이것은 참재적으로 인류 모두에게 심각한 위험을 노정시킨다. 방 사능 물질 가운데 많은 것이 백만년이 넘는 반감기를 갖고 있기 때문에 이 들 물질이 환경으로 들어가는 것을 최소화시키는 일은 필수적이라 하겠다. 방사능과 방사선 동위원소는 다음과 같은 방법으로 해양환경에 들어 간다. 죽, 자연 방사능, 핵무기 실험의 낙진, 원자로 조업, 폐기물 처 리, 폐기물 재생공장, 원자력 선박 등이다. 지금까지 해양에서 나타나는 방사선 핵종의 최대의 근원은 핵무기의 공중 실험이었다. 검문토제하에기 로접 한근다하.기 ‘ 앞서 우선 이온화 방사선과 그 특칭에 관한 이론을 11-1 방서능의 본질 방사능은 기본적으로 원자 현상이기 때문에 원자의 구조를 개략적으로 고찰하는 것이 무엇보다 도움이 된다. 하나의 원자는 많은 ·상이한 종류의 입자로 구성되어 있지만 여기서는 원자의 중앙에 양으로 하전된 핵을 갖고 있고, 핵 주위에 핵과 균형을 유지하기 위해 음으로 하전된 충분한 수의 전자들이 돌고 있다는 사실을 고찰하는 것이 중요하다. 원자의 거의 모든 질량은 핵에서 유래한다. 그 렇지만 핵의 칙경은 원자의 그것에 비해 아주 작다. 이러한 현상은 핵이 국단으로 높은 밀도를 갖는 결과가 되어 그 값아 2Xl014 g /cm3 에 달한다. 11-1-1 핵 핵은 고체 단위가 아니라 양자와 중성자의 혼합체로 구성된다. 양자는 그 질량이 원자량 스케일로 1. 0 에 아주 가깝고, 그것의 양전하가 전자의 음전하와 같은 입자이다. 중성자는 양자와 거의 같은 질량을 갖고 있지 만 전하룰 갖지 않는다. 그러므로 하나의 핵은 질량수로 특징을 이루며
이것은 핵이 갖고 있는 중성자 및 양자의 수와 같다. 그리고 원자번호는 핵속에 있는 양자의 수와 같다 • 원자번호는 특정 원소의 특징이며, 따라 서 주기율표 상의 특정 위치를 나타낸다. 자연상으로 출현하는 대부분의 원소는 여러 가지 형태를 가진 원소의 혼합체이다 . 예컨대 자연상의 수소는 푸로뮴, 중수소 및 삼중수소로 구 성된다. 푸로듐 또는 보통 수소는 단 하나의 양자로 구성된 핵을 지니며 단연 가장 큰 부분을 이룬다. 그러나 6,000 개의 수소 원자 가운데 하나 는 핵이 양자 하나와 중성자 하나를 지니는 것이 있는데 이것을 중소수 라고 한다. 삼중수소는 불안정하고 그 원자는 질량이 같은 헬륨(양자 2 개)으로 변하는 경향을 갖는다. 이렇게 변하기 위해서는 방사선 형태로 에너지가 방출되지 않으면 안 된다. 그러므로 삼중수소는 방사능이 있는 것으로 간주된다. 이들 원소는 각기 !H, fH 및 f H 으로 표시한다. 왼쪽 어깨 숫자는 질 량수이며 중성자 수와 질량 변화에 따라 변화한다. 아래 숫자는 원자번 호이고 주어진 원소에 대해서는 일정한다. 이러한 표기법은 모든 원소에 대하여 사용된다. 개별 원자의 종은 핵종 (nucl i de) 이라고 한다. 그러므로 푸로튬과 중수소 그리고 삼중수소는 모두 수소의 핵종이다. 다수의 양자와 중성자를 핵속의 아주 작은 공간으로 모으려면 매우 강 력한 결합력이 있거나 양자 사이의 정전기 반발력이 밀어내지 않으면 안 된다. 핵이 깨어지는 분열과정에서 방출되는 것은 이 에너지이다. 11-1-2 전자 전자는 양자의 전하와 동등한 음전하를 갖고 있는 입자로서 질량은 양 자의 1, 840 분의 l 이다. 정상 원소는 전기적으로 중성이기 때문에 전자의 수는 원소번호와 동일하여야 한다. 이들 전자는 핵으로 부터 상이한 거 리에 정전기 힘에 의해 궤도를 형성한다. 11-1-3 방사선 붕괴 대부분의 원자핵은 완전한 안정성을 유지하고 모든 화학 과정이 바깥
쪽 전자에만 관여하기 때문에 이들 과정을 통해서 변화되지 않는다. 그 렇지만 일부 불안정하고 에너지의 손실과 함께 붕괴하는 핵들이 있다. 이러한 손실을 방사선이라 부른다. 방사선에는 몇 가지 형태가 있고 이 가운데 가장 중요한 것은 알파 방 사선 «-radia t i on , 베 타 방사선 /J- ra dia t i on , 감마 방사선 y- radia t i on 및 X -선 방사선 등이다(그림 11-1) . 알파 방사선은 핵으로부터 알파 입자가 방출됨으로써 발생한다. C(거j 자의 하나는 헬륨핵 (~H) 이다. 이 입자는 비교적 커다란 질량을 갖 고 있
 : a- pa rtIc le
: a- pa rtIc le
그림 11-1 방사선 방출의 기작
고 때로 l09cm / sec 에 달하는 매우 빠른 속도로 움직인다. 베타 방사선은 중성자의 파괴와 고속의 전자 방출로 생긴다. 이때 새 로운 양자를 남기게 된다. /3-입자는 극히 작은 질량을 갖지만 운동 에 너지를 갖고 있어서 그 이동 속도가 광속의 99% 에 달한다. 감마 방사선은 파장이 극히 짧은 (l0-8~10-11cm) 전자파 방사선으로 핵 으로부터 방출된다. 이것은 입자가 아니기 띠문에 질량을 갖고 있지 않 다. x- 선은 또 다론 형태의 전자파 방사선이지만 핵으로부터가 아니고 궤 도를 도는 전자의 영역으로부터 나온다. 이 방사선은 y-방사선보다 더 긴 파장 uo-6~10-9cm) 을 갖고 있다. 주어전 핵이 붕괴하면 a- 입자나 /3-입자를 소실한다. 이때 잉여 에너 지가 y-방사선의 형태로 방출이 되는 경우도 있고 그렇지 않을 수도 있 다 . 붕괴하는 동안 핵이 입자를 잃기 때문에 원자번호가 바뀌고 새로운 원소가 형성된다. 예컨대 라듐 핵이 붕괴하는 동안 a - 입자들이 방출된 다. 따라서 라듐 핵의 질량은 4 만큼 감소한다. 뀜 Ra 一합 l Rn+me /3 붕괴가 일어나는 동안 f3-입자의 질량은 무시할 정도이므로 핵의 질 량은 본질적으로 변화하지 않지만 그것의 원자번호는 하나 증가한다. 왜 냐하면 하나의 중성자가 양자와 /3-입자로 분열하기 때문이다. 예컨대 청t Th— ➔ ~t Pa+{J - 가된다. 11-1-4 반감기 어느 순간에도 방사선 핵종의 일정한 핵 부분은 붕괴하고 있다. 이 부
분은 핵종의 특칭을 나타내고 압력, 온도, 혹은 화학적 상태 같은 어떠 한 의부 힘에 대해서 완전하게 관계가 없다. 붕괴속도는 주어전 원소 질 량의 절반이 사라지는 시간을 편의상 숫자로 표시하고 이롤 동위원소의 반감기라고 부른다. 그러므로 붕괴는 기하급수적이다. 죽 두번의 반감기 가 지나면 원래의 방사능의 25% 가 남고 세번의 반감기가 지나면 12.5% 가남는다. 만일 주어진 핵종의 원자수롤 N로 표시하면 붕괴속도는 후dt =AN 로 주어지고 이때 t는 시간, i 는 이 종의 붕괴상수이다. 이 식은 홉=,1 dt 로 고쳐 쓸 수 있고 다음과 같이 적분할 수가 있다. N=Nae-•t 여기에서 No 는 존재하는 핵의 원래의 수, N 은 t시간 후에 남은 수이다. 만일 우리가 반감기 (t 112) 를 방사능 종의 원자 수를 반감시키는 시간으 로서 정의한다면 그것은 N= 강N 0 이며 t=t1 12 일 때 나타나고 따라서 ln= (麟)= _A tI /2
또는 l1,2 = lTn 2= _ —0 . T69 _3 이 된다. 따라서 핵종의 반감기와 붕괴상수는 직접 관련이 되고 그 종의 특성을 이룬다. 반감기는 수초로부터 수백만 년까지 변화한다. 보통 핵종들의 경우 그것들의 반감기는 표 11-2 에 수록한다. 핵폐기물에 의해 야기되는 가장 큰 문제는 장기간 계속적으로 방사선 울 방출하는 일이다. 예컨대 우라늄 -238 의 한 단위로부터 나오는 방사선 이 반으로 주는 데에는 10 억 년 이상이 소요되고 그 방사능이 현재의 값 의 10 분의 1 로 감소하는 데에는 150 억 년이 걸린다. 따라서 이러한 장구 한 방사능 물질은 영구적이라고 생각하는 편이 안전하다. 표 11-2 보통 핵종의 반감기와 주요 방사 물질 핵종 반감기 주물요질방 사 핵종 반감기 주요물방질 사 fH 1 2 .3 년 f3 23J T h 7. 6xl04 년 a,y 1tC 5 , 570 년 f3 떻 Th 1. 4Xl010 년 a,'Y 셉 P 14 . 3 일 /3 옆 U 2 . 5 X 105 년 a,y tKS 87 일 /3 뀜 U 7.1Xl0 년 a,'Y 셉 K 1. 25X10 년 /3, Y 떻 U 4 . 5 X l09 년 a! 챔 Co 5.27 년 /3, Y 떻 N p 2.1 X 1Q4년 a’ 짧 Sr 28 년 /3 영 Pu 2. 4Xl04 년 a’ k29I 1. 6 X 10 년 /3 깝 Pu 13 년 a’ 섭 II 8.1 일 /3, 'Y 껍i Am 460 년 a ~Ce 17 시간 /3 쌍 Am 150 년 8 밝 Ce 30 년 /J, Y 껍 ~Am 7. 4Xl03 년 a’ 럽R a 1,622 년 a,'Y 떻 C f 18 년 a’ 자료 : 미국 공중 위생국, 1970
11-2 방사선의 특성 a- 임자를 구성하는 헬륨 핵은 비교적 무겁고 이중 양하전을 하나 갖 고 있다. 입자들은 비교적 서서히 움직이지만 그 질량 때문에 높은 운동 량을 갖는다. 입자들은 아주 쉽사리 정지하지만 주변 매질을 통과하는 동안 강력한 국부적 이온화를 일으킬 수가 있다. 〈이온화〉는 그림 11-2 에서 보는 바와 같이 양이온을 발생하면서 하나의 원자로부터 1 개 또는 그 이상의 바깥쪽 전자를 제거하는 것이다. 대표적인 a- 입자는 그 에너 지를 소비하기 전에 공기 중에서 약 20 만 개의 양이온을 생성할 수가 있 다. 이러한 이온화 능력은 만일 a- 입자가 예민한 생물 조직에 접촉할 경우 심각한 생물학적 손상을 야기한다. 다행히도 a - 입자는 멀리 이동 하지 않는다. 즉 공기 중에서는 약 60mm, 수중에서는 0.07mm 정도를 이동할 뿐이다. /3집자는 핵으로부터 매우 높은 속도로 방출된다. /3 - 입지는· a- 임자 보다 훨씬 더 멀리 두과하지만 질량이 적고 속도가 빠르기 때문에 이온 화의 강도가 훨씬 낮다. /3-입자의 범위는 공기 중에서는 수 m, 수중에 서는 수 mm 에 이른다. a- 입자가 물질과 상호 작용하면 이차적인 X- 방 사선이 발생된다.
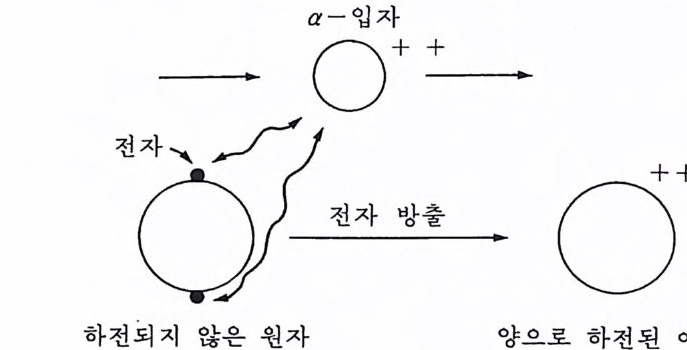 a 一입자
a 一입자
그립 11-2 a- 방사선의 이온화 효과
T 방사선은 붕괴반응 서열에서 중간 단계의 하나가 안정을 유지하기 에 너무 많은 에너지를 갖고 있을 경우 방사능 붕괴 과정에서 때때로 방 출된다. 즉 잉여 에너지가 y-방사선으로 방출된다. 이것은 질량이 없는 진정한 방사선이며 광속으로 이동한다. y선은 파장이 짧기 때문에 극단 으로 강력하고 먼 거리를 이동하는데 심각한 생물학적 손상을 일으킨다. 방사능을 측정하는데 사용하는 기준은 큐리 (C i)이다. 큐리는 원래 라 듐 l g 의 붕괴속도로서 정의하였지만 현재는 3. 7X 1 010dp s( dis in t e g r at io n s pe r second, 매초 붕괴변수)로서 정의한다. 큐리가 엄청난 양의 방사선을 나타내므로 밀리큐리 (mC i =10-3C i)와 마이크로큐리 (µC;=l0 -6 C i)가 흔히 사용된다. 11-3 방사선의 생물학적 영향 이온화된 방사선이 물질을 통과할 때 에너지는 물질에 의해 흡수된다. 살아 있는 세포 속에서 이러한 에너지의 홉수는 분자상 흥분이나 이온 화, 또는 자유 라디 칼 free rad ica l 을 생성하는 결과를 초래한다. 자유 라 디칼이 세포 내에서 산화와 환원 반응을 감소시키는 경향을 갖기 때문에 가장 위험하다. 더구나 분자 분활에 의해 생성되는 토막은 H202( 과산화 수소)갇은 매우 반응성이 큰 새로운 화학물질을 형성할 수 있다. 〈 뢴트겐, (roen tg en) 〉이란 용어는 방사선 조사량을 정하는 데 흔히 사 용된다. 그것은 공기 중에서 X - 방사선에 의해 생성된 이온화량으로부터 유래되고 공기 1cm3 당 약 87er g의 에너지를 흡수하는 것과 같은 방사 선량을 나타낸다. 〈뢴트겐〉이란 용어는 흔히 보건물리학에서 사용하지만 공기와 X- 방사선의 상호작용만 간주하기 때문에 그 사용이 제한적일 수 밖에 없다. 다른 용어는 다른 종류의 물질 속에서 다른 형태의 방사선으 로부터 나오는 방사선량을 정의하는 데 사용된다. 물질에 의 해 흡수된 방사선 량은 rad (radi at i on absorbed dose) 로서 표시 하는데 1 rad 는 흡수물질 g 당 100 erg 를 홉수하는 것에 해당한다. 주어
진 방사선량에 대해서 rad 의 수는 각 형태의 물질이 상이한 양을 홉수 할 것이기 때문에 흡수물질에 따라 변화한다. 사람이나 기타 생물에 대한 방사선의 영향은 방사선을 쪼인 개체에 영 향을 미치는 신체적인 경우가 있고 또는 개체에 영향을 미치지 않고 후 손에 영향을 미치는 유전적일 경우도 있다. 신체적 영향은 조사 후 1~2 주 이내에 나타나는 급성적인 경우일 수도 있고 조사 후 수년 동안 그 영향이 뚜렷하지 않은 장기적인 경우일 수도 있다. 방사선의 급성 영향 으로는 혈액변화, 구토, 사망 등을 들 수 있고 반면 장기 영향으로는 백 혈병의 생성, 백혈구의 무절제한 과다 생산, 백내장, 또는 암유발 등을 열거할 수 있다. 생식기관이 조사되었을 경우 유전적 영향도 나타날 수 있으며, 개체에 게는 눈에 띄는 영향이 없으면서 생식세포 내 염색체의 유전인지는· 손상 울 입을 수 있다. 이러한 변화나 돌연변이는 개체의 후손의 유전적 특칭 에 영향을 미칠 수 있다. a, /3 및 Y- 방사선의 생물학적 영 향은 이들 방사선이 모두 조직 속에 서 에너지 흡수를 유발하기 때문에 기본적으로 같다. 그러나 정량적으로 는 이들의 질량과 에너지 수준에서의 차이 때문에 아주 다르다. 결국 어 떤 방사선의 상대 생 체 유효율 (relati ve bio l og ica l eff ec ti ve ness : RBE) 을 측 정하기 위한 방법이 요구된다. 이것은 특정 방사선에 의해 생긴 손상을 표준 방사선과 비교함으로써 가능하며 RBE 는 다음과 같이 정의한다. RBE= 주어진 영향을 일으키는 데 필요한표준 방사선 원의 양 동일한 영향을 일으키는 주어진 방사선의 양 RBE 는 X- 방사선, /3-방사선 및 y-방사선에 대해서는 1, 그리고 a- 방 사선에 대해서는 10 과 동일한 것으로 간주되는데, a- 방사선은 그것의 이온화 능력이 크기 때문에 더 높다. RBE 는 유효한 생물학적 선량을 결정하기 위하여 흡수된 방사선과 결
합될 수가 있다. 이 결과 를 rem(roentg e n equ iv a lent man : 인체 뢴트겐 당 량)이라고 한다. 1 rem=l radx R BE 이 식은 상이한 형태의 방사선에 의해 생간 상대적 손상을 비교하게 해 준다. 예 컨대 a - 방사선에 의한 1 rad 의 조사량은 , /3 혹은 y-방사선 에 의한 10 rad 의 조사량과 같으며 이들은 모두 lO rem 과 같다. 그러나 세포나 조직에 의해 흡수된 방사선의 총량은 방사선의 형태에 크게 좌우됨을 기억하지 않으면 안 된다. a- 방사선은 훨씬 국부적인 생 체 손상을 일으키지만 아주 멀리 두과하지는 않는다. 사람의 피부 표면 에 놓인 이미터 (em itter : 입자방출체)로부터 나온 a- 입자는 처음 한두 충 의 세포충에 의해 정지될 것이고 손상은 거의 일어나지 않는다. 그러나 만일 a 이미터가 홉수되고 간요한 기관에 직접 a_ 입자가 접촉한다면 심 각한 손상이 일어날 수가 있다. 따라서 a 와 /3 - 방사선은 그 방출체가 섭취되었을 경우에 커다란 위험이 되고 의부에서 오는 방사선은 거의 해 표 11-3 국제방사선보호위원회가 제의한 방사선 제한량 신체부위 제한량(연간) 직업상노 출 : 전신 5 rems 피부 15 rems 손 75 rems 팔 30 rems 기타 기관 및 조직 15 rems 임신부(잉태기간) 0.5 rem 일반인: 개인 0. 5 rem 학생 0.1 rem
를 일으키지 않을 것이다. 그렇지만 T 방사선은 강력한 투과력 때문에 방출체가 신체에 대해서 내부에 있든지 의부에 있든지간에 참재적인 위 험이 된다. 국제방사선보호위원회는 인류에 대한 방사선 허용량의 제한을 제의한 바 있으며 이는 표 11-3 에서 보는 바와 같다. 11-4 해양환경에 대한 방사선 핵종의 영향 해양환경으로 유입하는 방사선 핵종은 세 가지 국면, 죽 해수, 무기 및 유기입자, 그리고 해양생물 가운데로 분활된다. 궁극적으로 해저는 이들 모두가 모이는 장소이다. 방사선 핵종의 침전, 떨어지는 입자성 물 질 위의 흡착, 방사선 핵종을 포함하고 있는 생물의 치사 등은 모두가 퇴적물 속에 방사능 물질을 축적하는 결과가 된다. 특히 관심을 끄는 것은 해양생물이 방사선 핵종을 축적하고 농축시키 는 경향성이다. 연구 결과는 일부 해산종의 체내에 주변 해수중에 존재 하는 방사능 원소의 양보다 수십 만배까지 농축 시킬 수 있다는 것을 보 여 준다. 이것은 생물에 대해서나 해산석품을 소비하는 인류에 대해서 신체적 또는 유전적 손상을 초래할 수 있다. 해양생물에 의한 방사선 핵종이나 기타 화학물질의 섭취를 표현하는 한 가지 방법은 주변해수 중의 온도에 대한 생물의 조직 중 〈농축률〉을 결정하는 일이다. 대표적인 농축률은 표 11-4 에서 보인 바와 같다. 식물 풀랑크톤은 일반적으로 화학물질을 가장 많이 농축하는데 루테늄 (Ru) 에 대해서는 20 만배까지 농축한다. 해양생물에 의해 상당히 농축되는 원소 들은 생물에 의해 구조나 촉매의 목적으로 이용되는 것들 (C, N, P, Fe, Cu, Co 등), 무거운 2 가 원소 (Ba, Ra), 무거운 할로겐 (Br, I), 그리고 해 수의 pH 에서 쉽 사리 가수분해 하는 원소 (Al, Ce, Pu 등) 들을 포함한다. 이들 원소가 바다에서 발견되는 보다 중요한 방사선 핵종들이다. 해양으로 둘어가는 방사능 물질의 많은 양이 침전하는 입자성 물질과
표 11-4 해양 생물에 대한 평균 농축률 원소 저생조류 식물 플랑크돈 동물 플랑크돈 연체 동물 근육 갑각류 근~ 어류 근육 C 4,000 3,600 2,8 0 0 4,700 3,600 5,400 N 36,000 24. 00 0 47,500 44,000 65,000 Al 15,000 100,000 100, 000 9, 0 00 12, 00 0 10,000 P 10,000 34, 00 0 13.000 6,000 24,000 33,000 Fe 4,800 45,000 25, 00 0 9,600 2,4 0 0 1. 600 Co 800 1, 500 700 600 500 10 Ru 390 200,000 34,000 3 100 0. 5 Cu 100 30,000 6,000 5,000 1, 000 Ba 17, 000 900 8 Sr 96 1 3 0.1 Ra 1. 400 12,000 190 1,300 140 130 Y 480 1. 000 105 12 250 Ce 670 90,000 1, 000 360 2 0. 3 Pu 1. 300 2,600 2,600 260 3 3 Po 1. 000 자료 : 미국 학술원, 1971 결합되기 때문에 퇴적물은 통상 해수보다 훨씬 더 많은 방사능을 갖는 다. 따라서 해저에 사는 생물은 해수중의 플랑크돈보다 더 많은 방사선 울 흡수하며 퇴적물에서 사는 생물은 더더욱 많은 방사선을 흡수한다. 해양생물에 대한 낮은 방사선량의 장기 영향에 관해서는 알려진 바가 거의 없지만, 어란 치사량의 증가, 부화율의 감소, 기형 어란의 증가 등 울 일으키는 것으로 믿어전다. 가장 큰 위험은 필시 방사선에 대한 만성 노출로 야기되는 유전적인 변화일 것이다. 이것은 변화된 특성의 전달이 나 한 개체군의 전멸을 유도할 것이다. 그렇지만 가장 큰 위험은 방사능으로 오탁된 해산 식품을 소비함으로 써 인류에게 오는 것이다. 결국 해양에서의 폐기물 두기는 식용 해양생 물 속에 방사선 핵종의 축적을 억제하도록 조절되어 왔다• 해산식품을 먹는 습성과 안전할 것으로 생각되는 방사능 물질의 최대허용 농도를 기 초로 제한이 설정된다. 이들 제한도 나라에 따라 변화한다. 예컨대 영국
은 미국보다 더 많은 방사능 물질의 방출을 허용한다. 미국에서의 허용 한계는 소련에서 보다 3~10 배 가량 더 높다. 미국에서는 해수중에 최대 허 용 농도가 “No 에 대 한 0. 16 mCi / l 로부터 go sr 에 대 한 8 x 10 - ◄ mC i / l 및 32 p에 대한 5 X 10-smC i /l 에 이르기까지 범위가 변화한다. 11-5 해양에서의 방서능 출처 해양에서는 방사능 물질의 주요 출처가 3 종류 있다. 즉, 자연 방사능, 핵무기 실험으로부터 오는 대기 낙진 및 원자로 폐기물이 그것이다. 11-5-1 자연 방사능 자연 방사선은 우주선 cosm ic ray 활동과 토양, 물, 공기 에서 자연적으 로 출현하는 방사능 물질로부터 유래한다. 자연 선량은 100~125 m rem/yr 로 변화한다. 자연적으로 나타나는 60 여 개 이상의 방사성 핵종 둘은 지각 속에 존재하는 것으로 알려져 있다. 이것들이 정상적인 풍화 와 침식 과정이 일어나는 동안 해양으로 운반된다. 자연적으로 출현하는 것 가운데 해양에서 가장 일반적인 방사선 핵종은 칼륨 -40, 루비듐 -87, 우라늄 -235, 토륨 -232 및 우라늄 -238 이다. 의계에서 기원하는 우주나선은 계속 지구를 충격하여 질소, 산소, 알곤 및 기타 원소의 방사선 핵종을 만들어 낸다. 이들 역시 바다에 이르게 된다. 해수중에 있는 자연 방사 능 물질의 농도는 매우 낮다. 평균해서 해수 ll 중에는 자연적으로 출현 하는 방사선 핵 종이 불과 약 0. 34 pC i (pico curie s : 10- 12 Ci) 를 함유하고 이들의 대부분은 떤(과 “Rb 에서 유래한다. 여러 해양을 통해서 이들 방사성 핵종의 농도는 출처와 반감기, 그리고 생물권, 부유성 및 입자성 물질과의 상호작용에 좌우되 면서 크게 변화한다. 11-5-2 방서능 낙진 모든 핵폭발 실험은 지하폭발의 경우를 제의하고는 일차적으로 대기
낙진울 통해서 대량의 방사능 물질을 해양으로 유입시킨다. 낙진으로부 터 해양으로 도입된 방사성 핵종의 많은 것들이 인공적인 것이어서 환경 내에서는 자연적으로 발견되지 않는다. 다행히 미국, 소련, 영국 등이 1963 년 핵실험금지조약을 수락하고 당 시의 모든 공중 및 수중 핵실험을 중지하였다. 그 당시까지 연간 대략 20.000C i의 플루토늄이 대기로 방출되고 있었다. 그 후 해양 표면에서 의 방사선 수준은 1966 년을 최고로 현저히 감소하였다. 불행히도 프랑스 와 중공은 그 조약에 서명하지 않고 실험을 계속하였다. 이어서 다른 국 가들도 공중 핵실험을 시작하였으며, 아마 5,000C i의 플루토늄이 매년 대기로 첨가될 것이다. 해양에 대한 이들 실험의 영향은 알려져 있지 않 으나 필시 좋지 않을 것이다. 11-5-3 원자로 가까운 장래에 핵분열 발전소에서 나오는 핵폐기물과 방출이 해양에서 다른 모든 방사능 원을 초과할 것이라는 것이 예견된다. 현재 핵폐기물 은 미국의 경우 워싱톤주의 핸포드, 사우드캐롤라이나주의 사반나 • 리 버, 아이다호주의 아이다호 • 폴즈에 있는 특정 장소에 저장되고 있다. 액체 폐기물은 알칼리성으로 만들어 탱크 속에 저장된다. 액체 폐기물은 점 차로 증발하여 결정 황산나트륨 Na2S04 • lOH20 죽 망초 salt cake 가 되 고 이것이 탱크 속에 저장된다. 현재 300X106Ci 이상의 고농도 방사능 울 갖는 물질이 저장되어 있고 아 양은 원자로 생산의 성장 결과로 급속 히 증가하고 있다. 곧 이들 물질에 대한 보다 더 영구적인 저장소가 발 견되어야 하며 해저는 가능한 매립장소의 하나로서 제시되어 왔다. 미국은 1970 년 이래 방사능 폐기물의 해양 두기를 하고 있지 않지만 그 이전에 낮은 수준의 방사능 폐기물을 해양에 퇴적시켰다. 아직도 4 개 의 주요 장소가 존재하는데 2 개 장소는 태평양 측에 샌프란시스코 연해 의 40 마일과 50 마일 지점에 있으며 다른 2 개 장소는 대서양 측에 메릴랜 드와 델러웨어 연해의 120 마일과 200 마일 지점에 위치한다. 보다 작은 장소들은 태평양과 대서양 연안을 따라 설정되었다. 최근에 상당한 관심
을 끄는 곳은 보스턴 항에 있는 것으로 해안으로부터 불과 수 마일 떨어 진 아주 생산성 높은 어장 부근에 있다. 거의 모든 방사능 폐기물은 55 갤론 짜리 기름통에 들어 있고 이 폐기물 속에는 트리튬, 토륨, 우라늄, 플루토늄은 물론 다양한 다른 방사성 핵종이 섞여 있다. 총 방사능은 100, 000 Ci 정도이며 그 대부분이 대서양 측 장소에 있다. 일부 유럽 국가들, 특히 영국, 벨기에, 네덜란드, 스위스 등은 정기적 으로 방사능 폐기물을 해양으로 계속 두기하고 있으며 일본도 앞으로 그 럴 계획이다. 총 약 65,000 톤의 포장된 방사능 폐기물이 유럽 국가들에 의해 동북 대서양에 있는 수십 약 4,000m 되는 지점에 투기되어 왔다. 이것의 대부분은 과거 짧은 시간 속에 이루어졌다(표 11- 5) . 핵발전소 폐기물에 대한 가능한 두기방법을 논의하기 전에 이들의 출처롤 검토하는 일이 필요하다. 여기에는 우라늄 채광, 연료생산, 원 자로 가동, 연료 재처리 연료봉 (s p en t - fu el - rod) 무기 등이 포함된다(그 표 11- 5 저 준위 방사능 폐기물의 해양 두기 (1967~1979) 방사능 Ci 연도 두기량(t) a’ /J 및 y 1967 10,840 250 7,600 1969 9, 180 500 22, 0 00 1971 3,970 630 11, 200 1972 4,1 3 0 680 21, 600 1973 4,350 740 12,600 1974 2, 270 420 100,000 1975 4,460 780 60,500 1976 6,7 7 0 880 53,500 1977 5,605 958 76, 45 0 1978 8,000 1, 100 79,500 1979 5,400 1,400 83,000 자료 : Dy er , 1980
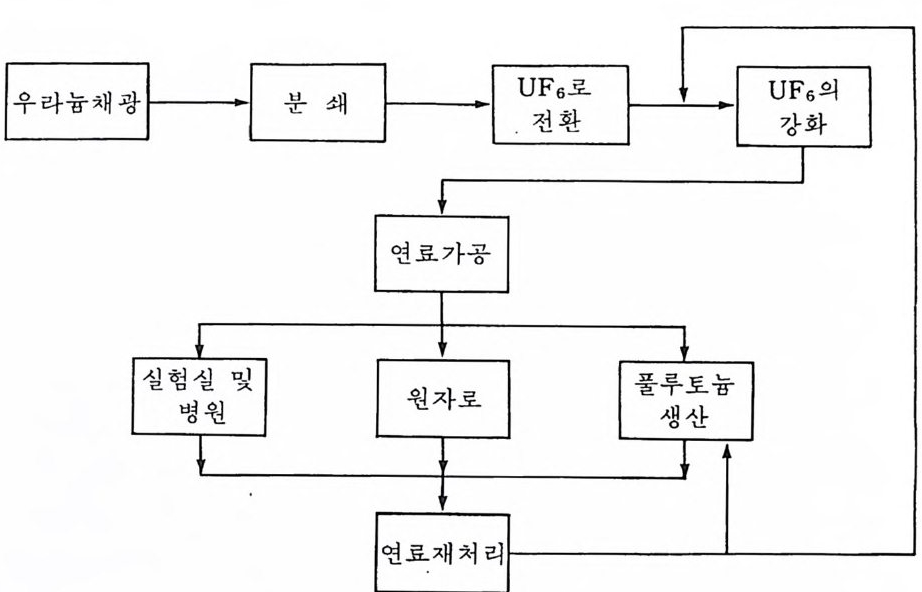 두曰广
두曰广
그림 11-3 원자력 산업으로부터 나오는 폐기물 출처
립 11- 3) . 우라늄채광과농축 우라늄의 채광은 노천 및 지하의 방법이 다 사용되며 일반적으로 방사 능 폐기물은 거의 생산하지 않는다. 채광된 광석은 황산이나 탄산나트륨 으로 처리하여 우라늄을 농축한다. 이 결과로 생기는 농축물은 약 85% 의 산화 우라늄 (U3 아)을 함유한다. 분쇄기 폐기물과 기록되지 않은 우라 늄 및 토륨을 포함하는 대량의 폐수가 찌꺼기 연못으로 방출된다. 농축물 은 가스안 6 플루오르화우라늄 (UF6) 으로 전화되고 이것은 기체확산으로 235U 를 농축하고(약 3. 3 %) 238U 울 남긴다. 농축된 UFs 는 알맹이로 된 이산화우라늄 (U02) 으로 전화되어 연료 성분을 이룬다. 이 농축단계에서 는 소량의 고형 및 액체 방사능 폐기물만이 유래된다. 원자로가동
원자로 가동의 기초는 핵분열 또는 원자 분활이다. 우라늄 -235 의 핵이중성• 자 틀 o:六 자 홍一 분 된O 핵- 불 8 분〔-분 열 된열 00묘!广一\/: IY•중0tt성Oai:뻔iBO 자I •一/]\•-/ • • •O-\\BB -D •그림 11-4 235U 의 분열 중성자에 충돌하면 두 부분으로 분열하고 각己 부분은 원래 원자량의 약 반을 갖게 되며, 또한 2 개 혹은 더 많은 중성자가 방출될 것이다. 이들 중성자는 주변에 있는 우라늄 핵과 충돌하여 분열을 일으키게 할 것이다 (그립 11-4) . 우라늄 -235 를 분할함으로써 생성되는 대부분의 토막들은 불 안정(방사성)하고 Y- 방사선울 방출하면서 방사선 붕괴를 더 진행시킨다. 우라늄 -235 의 핵속에는 질량 태로서 각 토막둘의 에너지의 총합보다 더 많은 에너지가 저장되어 있기 때문에 열로써 발산되는 유용한 잉여 에너 지가 있다. 증기나 전기를 생산하기 위해서 원자로에서 사용되는 것은 이 열이다. 농축 연료는 쉽사리 분활될 수 있는 우라늄 -235 를 약 3.3% 만을 포함 한다. 죽 그 나머지 96.7% 는 통상 분활하지 않는 동위원소인 우라늄 -238 이다. 우라늄 -238 은 우라늄 -235 의 분할에서 나오는 중성자를 잡아서 풀루토늄 -239 를 생성하는데 플루토늄은 핵무기의 기초로서 이용되는 또
다른 고도의 방사성 물질이다. 연료봉의 전형적인 수명은 3 년인데 그동안 모든 가용 핵분열 물질이 다 이용되는 것은 아니다. 초기 연료의 매 1, 000k g(대략 33k g의 우라늄 -235 와 967 kg 의 우라늄 - 238 로 됨 ) 에 대 해 서 우라늄 -235 25 kg 과 우라늄 -238 24k g이 소비되어 3.3% 의 우라늄 농축비를 0.8% 로 감소시킨다. 소바되는 우라늄은 800 X l06kwh 의 전기 에너지와 여러 가지 분열산물 로 전화되는데 이 가운데에는 8.9k g의 여러 가지 플루토늄 동위원소, 4. 6 kg 의 우라늄 -236, 0. 5 kg 의 넵투늄 -237, 0.12 kg 의 아메 리슘 -243, 0. 04 kg 의 퀴륨 및 35 kg 의 기타 핵분열 생성물이 포함된다. 핵분열 과정으로 생성된 열은 냉각수에 홉수되고 보일러로 전달되며 보일러에서 증기로 바뀌어 발전기가 전기를 일으키는 데 사용된다• 우리 나라와 미국에서는 물이 냉각 액체로 사용되는 반면 영국에서는 이산화 가스가 사용된다. 액체 나트륨이 미래의 냉각제로 제시되고 있는데 이는 액체 나트륨이 원자로에서 나오는 대량의 열을 재빨리 제거시킬 수 있기 때문이다. 연쇄반응을 통제하지 않고 그냥 진행하도록 내버려 두면 생성되는 중 성자의 수와 핵분열의 수가 시간이 지남에 따라 기하급수로 증가할 것이 고 이것은 엄청난 양의 열을 생산하여 대참사를 일으킬 것이다. 그래서 연쇄반응은 보론 (B) 이 들어 있는 철봉을 원자로 속으로 집어 넣어서 조 절하게 된다. 보론은 중성자를 홉수하고 따라서 연쇄반응을 둔화시킨다. 철봉이 많이 들어갈수록 반응은 더 지연될 것이다. 우라늄의 핵분열로 생성된 산물들은 연료체의 피복 cladd i ng 속에 남게 된다. 그러나 일부 중성자는 피복을 통과하여 냉각제 중의 불순물(특히 부식산물) 과 접촉하며 또 원자로 격 납 용기 conta i n m ent vessel 와 접촉해 서 이들 물질 속에서 방사성 물질을 생성할 수가 있다. 연료체 내에서 생성된 핵분열 산물은 사용하지 않은 연료를 찾아내는 화학 재처리 시설 에서 제거될 수가 있다. 생성된 방사성 폐기물의 잔재는 발전소 내에서 처리되거나 다른 장소로 보내야만 한다. 이 방사능의 대부분은 원자로 냉각제에서 기원한다 . 방사성 기체는 냉
각 증기로부터 진공 배출기를 이용해서 제거하고 대기로나 기체 저장탱 크로 직접 내보낸다. 탱크에서는 짧은 수명의 동위원소가 방출되기 전에 붕괴할 수 있다. 기체상 폐기물 중의 핵종은 일차적으로 13N 과 “Ar 로 구성된다.
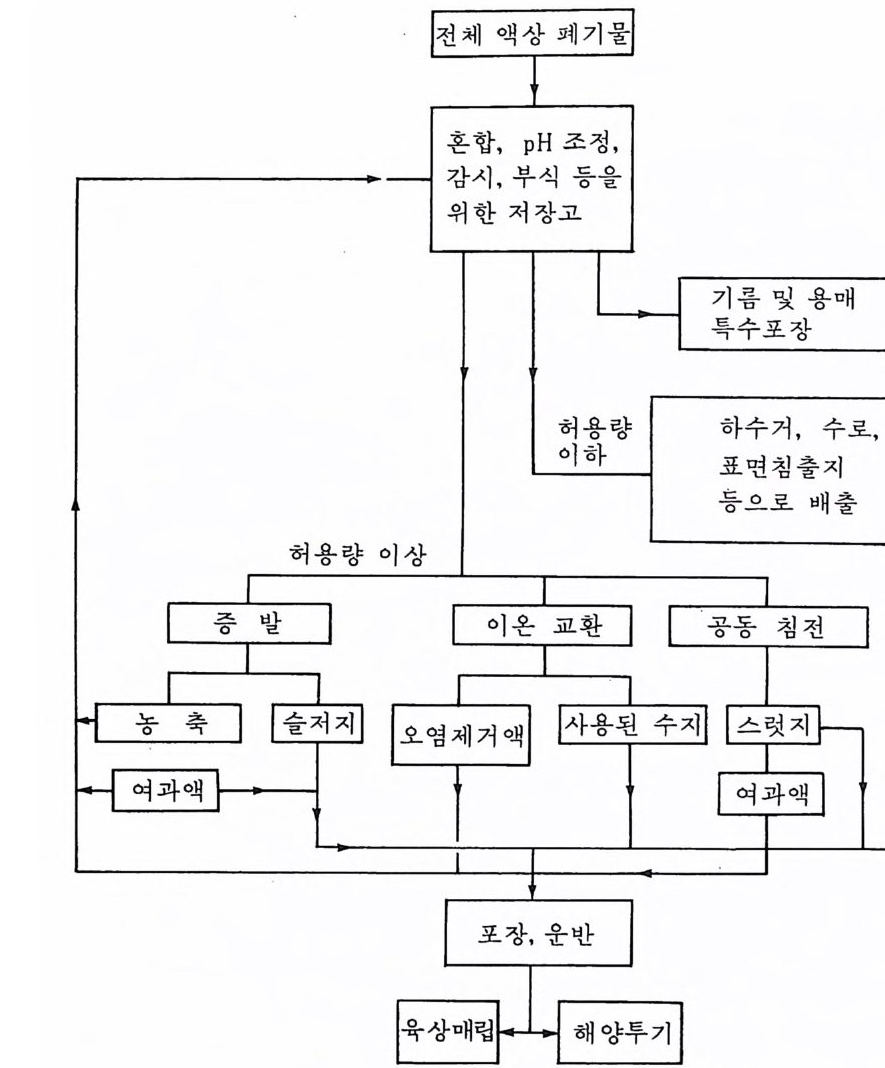 전체 액상 폐기물
전체 액상 폐기물
그림 11-5 액상 방사성 폐기물의 처리과정
냉각수는 원자로 계통 내에서 부식률을 감소시키고 배관계통에서 방사 선을 억제시키기 위해서 계속 광물을 제거하지 않으면 안된다. 이것은 보통 여과기에 선행하는 혼합 이온교환기의 사용으로 이루어진다. 냉각 수에서 발견되는 방사성 핵종은 원자로에서 나오는 대부분의 핵분열 산 물은 물론, 3H, 32P, s1cr, 59Fe, soco, 1311, 137Cs, 13BCs, 140Ba 같은 활성 화 된 부석 산물도 포함한다. 활성도가 낮을 경우 액체 폐기물은 일반적으 로 10-1 mCi /ml 이하로 희석시켜 발전소로부터 방출한다. 광물이온제거 기 회수에서 나오는 다른 액체 폐기물은 저장 탱크로 수거되어 농축되고 시멘트와 혼합시켜 드럼 속에 넣어 매립장소로 보낸다. 전형적인 처리과 정은 그림 11-5 에서 보는 바와 같다. 연안지역에서는 해수가 풍부한 냉각수 원이 된다. 해수가 원자로플 통 과할 때 연료체 중에서의 누출이나 해수중에 있는 물질의 중성자 방사화 neutr o n acti va ti on 에 기인한 방사능으로 오탁될 수 있다. 이러한 방사 능은 가열선 냉각수와 함께 계속해서 해양으로 방출된다. 원자력 발전소에서 만들어지는 다른 방사성 폐기물은 세탁소, 분석실 험실, 오염제거 작업 등에서 온다. 이 폐기물 또한 포장하여 육상 매립 장소로 보낸다. 그 의의 방사능 폐기물은 원자로의 폐기와 해체에서 오 며, 전체 원자로와 격납용기 건물은 낮은 수준의 폐기물로서 처리하지 않으면 안 된다. 발전소에 의해서 얼마나 많은 핵 폐기물이 만들어 지는가를 추정하기 는 어렵지만 평균 1, 000 메가와트 원자로가 연간 200 과 500m3 사이에서 방사능 폐기물을 생산하는 것으로 추정된다 (B i sho p, 1983). 연료재처리 훨씬 더 어려운 문제는 사용된 연료봉에서 온다. 사용기간이 지난 후 연료는 서서히 그 성질을 변화시키기 시작하여 방사능 물질의 핵분열에 서 오는 토막들과 초우라늄 원소(우라늄보다 무거운 원소)들이 점점 더 많 이 구성된다. 가장 중요한 핵분열 산물은 “Sr 과 137Cs 이다. 사용된 연 료봉에서 발견되는 가장 일반적인 초우라늄 원소들은 표 1l_6 에서 보는
표 11-6 사용된 연료봉에 나타나는 초우라늄 원소 반감기 일정기간 후 연료 t당 발생하는 g량 핵종 (년) 10 년후 100 년후 1,000 년후 231Np 2.1 X 106 760 770* 810 238Pu 89 6 3 0,007 239Pu 2. 4X i o ◄ 27 28* 34* 2,op u 6. 8X lQ3 20 40* 37 2,1p u 13 3 0.025 。 242Pu 3. 8X 105 1. 8 1. 8 1. 8 2“Am 458 54 50 1. 8 243Am 7. 6X l03 90 90 13 244Cm 18 21 。 •7 83 총계 983 983 979 방사능 약 10, 000 Ci 약 2, 200 Ci 약 600 Ci *핵종이 존재하는 다른 방사능 핵종의 파생적 산물이므로 증가함 자료 : Bowen, 1979 바와 같다. 여기서 보면 1, 000 년이 지난 뒤에까지 많은 양의 방사능이 여전히 남으리라는 것을 알 수가 있다. 그러나 연료봉의 열생산 효과는 핵분열 토막들이 새로운 핵분열 반응을 방해하기 때문에 감소한다. 이 시점에서 연료봉은 새로운 것으로 대체된다. 사용한 연료봉을 어떻게 처리할 것이냐는 아주 복잡한 문제이다. 이것 들은 재처리되어 미사용된 우라늄과 플루토늄이 원자력 발전소에서 재 사용을 위해 추출될 수도 있다. 상당히 가치 있는 우라늄이 잔류하기 때 문에 이것은 가장 효과적인 해결책이다. 더욱이 고방사능의 폐기물이 작 은 용적으로―― 1,000 메가와트 원자로로부터 연간 폐기물을 2m3 정도 로――농축이 가능하다. 그러나 추출되는 플루토늄이 크게 농축되고 이것 이 참재적으로 테러리스트 등에 의해 핵무기 제조에 사용될 수가 있다.
재처리가 이루어지면 우라늄과 플루토늄은 2 개 혹은 그 이상의 단계로 추출된다. 첫단계는 99% 이상의 핵분열 산물의 방사능을 포함한다. 고 방사능 폐기물로 알려진 이 물질은 지하 저장탱크에 저장된다. 그 다음 의 재처리 단계는 미분열 우라늄을 더욱 정제하기 위하여 이루어 진다. 그 결과 상당히 적은 양의 방사능을 갖는 폐기물이 대량 나오게 된다. 영국과 프랑스에서는 이 폐기물을 연안 해역으로 방출한다. 영국의 윈 드 • 스케일 화학 재처리 공장에서 방출하는 양은 약 60,000C i/yr이다. 전망 원자력 발전소 건설에 대한 저항과 최근 체르노빌 원자력 발전소에서 증명된 참사의 가능성에도 불구하고 예견할 수 있는 미래에 핵에너지가 필수적임은 어쩔 수 없는 명백한 일이다. 석유와 가스 매장량이 고갈되 어 가고 석탄 사용이 환경과 건강상의 위험을 심각히 야기시키기 때문 에, 그리고 태양에너지의 발전이 아직 초기 단계에 있기 때문에 핵에너 지는 다른 덜 위험한 형태의 에너지가 나울 때까지는 이용하지 않을 수 없다. 따라서 핵폐기물 두기로 일어나는 문제는 가까운 장래에 불가피하 게 증가할 것이며 이 폐기물의 두기장소로서 해양의 이용은 더욱 큰 압력 을 받게 될 것이다. 그 제안의 가능성과 그에 따른 결과를 보기로 한다. 11-6 핵페기물의 관리 핵폐기물 관리의 목적은 가능한 최소량의 폐기물을 생성시키고, 그것 을 취급과 저장에 편리한 형태로 전화하며 사회의 건강에 최대로 안전하 게 처리, 저장 및 폐기의 조합을 선택하는 일이다. 폐기란 환경으로의 분산이나 앞으로의 재생 의도가 없이 두기하는 것을 의미한다. 핵폐기물 폐기에는 기본적으로 3 개의 대안이 가능하다. 죽, 환경으로 의 분산, 극단으로 장기에 걸치는 저장, 또는 폐기물이 다시는 인류나 그 주변에 접촉될 수 없는 장소로 배치하는 것 등이다.
11-6- 1 분산 낮은 농도의 방사능 폐기물을 강과 바다로 계획적으로 방출하는 일은 전 세계에서 행해지고 있다. 1960 년대에는 강물을 사용하는 단일 패스 냉각계를 갖는 원자로가 보통이었으며, 그 결과 연료체의 누출로부터 , 또 원자로 속에서의 중성자 활동으로부터 많은 상이한 방사성 동위원소 가 강과 바다로 방출되었다. 그 후, 규정이 강화되어 현재는 연안 수역 으로의 핵폐기물 방출이 상당한 정도로 감소되었다. 그러나 일부의 국가에서는 중간 정도 수준인 핵폐기물의 분산 매체로 서 해양을 계속 사용하고 있다. 가장 크고 가장 오래된 방사능 폐기물 방출시 설은 영국의 윈드 • 스케 일 공장으로서 1957 년 이 래 이 공장은 연 료 재처리에서 나오는 낮은 수준의 액체 폐기물을 아이리쉬 해로 방출하 였다. 월간 8, 000 Ci 까지 핵분열 생성물이 연안에서 2 마일 되는 곳에 방출된다. 이들 핵분열 생성물은 주로 /3-이미터이지만 a 및 Y- 이미터도 상당량 존재한다. 기타 국가에서는 프랑스의 갚드라아그 연료 재처리 공 장에서 복해로, 그리고 이탈리아 타란토 만에 있는 공장과 인도 봄베이 부근에 있는 공장에서 각각 방출된다. 그 의의 국가에서도 편리성 때문 에, 그리고 적절한 저장 시설이 없기 때문에 해양 두기를 하고 있거나 고려하고 있다. 윈드 .-스케일에서의 조업은 면밀하게 감시되어 왔다. 그곳에서의 방출 은 소량이지만 해수, 어류, 플랑크톤, 해조류 및 해안 퇴적물에서의 방 사능 물질의 양이 측정할 수 있을 만큼 증가되었다. 그렇지만 폐기물로 오탁된 해산 식품의 소비로 인해 인체에 추가로 증가된 방사선량은 자연 방사선량의 0. 2% 에 불과하였다. 한편 여전히 남는 문제는 해양 분산이 핵폐기물 두기의 안전한 방법이 냐는 것이다. 많은 과학자들은 그렇게 생각하지 않는다. 만약 폐기물이 전 해양을 통틀어 철저히 희석될 수 있다면 자연 방사선량에 첨가하여 증가되는 양은 무시할 수 있을 것이다. 그러나 완전한 희석이란 불가능 하다. 해양 혼합은 두기 장소 부근에서 맴도는 물질의 많은 양을 충분히 희석시키지 못하며 또한 대부분의 핵종이 보존성 있는 양상으로 행동하
지 않는다. 이들 물질은 해양 생물 속에서 또는 이온교환 반응 때문에 부유 물질이나 퇴적물에 급속히 농축된다. 결국 방사선의 많은 양이 널 리 분산되기 보다는 지역적으로 농축되는 경향을 갖는다. 필시 낮은 수준의 폐기물에 대한 한정된 해양 분산은 계속되겠지만 두 기 장소에 대한 상세한 연구가 있은 뒤에만 이루어져야 한다. 이러한 연 구는 그 장소에 대한 해양 순환과 생물학에 대한 조심스러운 연구를 포 함하지 않으면 안 된다. 11-6-2 저장 현재 고농도 및 중간 농도의 모든 핵폐기물은 적절한 투기 기술이 개 발될 때까지 저장되고 있다. 이 저장법에는 통상 증발에 의한 폐기물 농 축이 포함된다. 그 결과로 찌꺼기를 시멘트로 고형화 하는 것, 55 갤런 들이 드럼으로 컨테이너를 만드는 것, 육상 매립 등으로 처리된다. 연료 재처리와 소모 연료봉에서 나오는 고농도의 폐기물은 보통 지하 저장 탱 크에 물을 채우고 그 속에 저장한다. 이때 발생되는 열의 양이 방대하므 로(온도가 480'C 까지 상승한다) 보통은 폐기물에 대한 공기 냉각이나 냉각 수가 필요하다. 영국에서는 연료 재처리에서 나오는 고농도 농축 폐기물을 수냉식 스 텐레스 탱크 속에 저장한다. 이 탱크는 스텐레스로 된 이중 용기로서 콘 크리트 지하 저장고에 들어 있다. 그러나 정교하고 고가인 이 저장 탱크 는 불과 30 년간을 지탱하도록 고안된 것이어서 수명이 짧은 핵종에 대하 여는 적절하지만 수명이 긴 핵종에는 적절하지 않다. 수명이 긴 핵종은 수백 년 또는 수천 년간 저장하고 냉각시켜야 할 것이며, 전기간을 통해 주의 깊게 감시해야 한다. 그러므로 저장 탱크는 일시적 해결책으로 생 각하여야 할 것이다. 일반적으로 폐기물을 장기간 저장하려면 누수가 생 기지 않도록 먼저 고체화하지 않으면 안 된다. 11-6-3 영구적 두기 방사능 폐기물 두기에 대한 나머지 대안은 사람의 관심을 끌지 않도록
접근할 수 없는 장소에 안전하고 영구적으로 방사능 폐기물을 분리시키 는 것이다. 이것은 미래에 잠재적 가치를 가질 수 있는 방사능 물질의 전면적 손실을 뜻하지만 인류에 대하여 가능한 어떤 위험도 방지할 것이 다. 그렇다면 문제는 고도로 활성을 지닌 이들 폐기물을 두기할 수 있는 가장 안전한 장소가 어디냐는 것이다. 한때는 해양이 너무 방대하여 이들 폐기물을 해양으로 간단히 투기하 는 것으로 충분하다고 생각하였다. 1946 년과 1970 년 사이에 약 10 만 드 럼의 방사능 폐기물이 미국 주변 해양으로 투기되었고 영국에서는 약 5 만 드럼을 두기하였다. 이들 폐기물은 손실되지 않고 해저에 운반될 수 있도록 고안된 드럼 속에 포장되었다. 하지만 해저상에서 높은 압력과 부식이 결국 드럼을 분해시켜 방사능 내용물을 해양으로 누출시킨다. 실 제로 아주 위험한 드럼들이 해변으로 휩쓸려 온 사례들이 있다. 이처럼 영구적 두기를 위한 여러 가지 제안 가운데에는 로켓을 사용하 여 태양으로 두기하는 것도 포함되어 있으나 경비문제로 실현성이 희박 하며, 가장 가능성 있는 대안은 육지나 심해저에 지질학적 저장소를 마 련하는 것이다. 지질학적 저장소 지질학적 두기의 목적은 지진이나 화산작용에 의한 파열로부터 안전하 고, 물과의 접촉에서 안전한 장소에 고농도의 폐기물을 매립하는 것이 다. 이러한 두기 지역은 지질학적으로 보아 전적으로 비활성 지역이지 않으면 안 된다. 물은 핵종을 용해하여 대수충(帶水層)으로 운반하기 때 문에 접근할 수 없어야 한다. 더구나 물이 존재하면 폐기물에 의해 발생 하는 대량의 열이 증기 폭발을 일으킬 수가 있을 것이다. 괴상인 암염 돔, 화강암 및 혈암 등이 지질학적 저장소로서 가장 적합한 것으로 보인 다. 가능한 장소들이 미국 전역에 산재해 있고, 서독에도 많은 대형 암 영충이 있어서 현재 암염 속에 고농도의 폐기물을 두기하는 기술이 개발 되고있다. 폐기물은 그것들이 붕괴하는 데 필요한 시간인 수천 년 동안 누수가
생기지 않도록 고체화할 필요가 있다. 유리, 도자기 및 복합체 등 여러 가지 이용될 수 있는 기질에 대하여 많은 연구가 진행 중에 있으며 그 중 유리 가 현재 로서 는 가장 유망하다. 유리 화 vit rifica ti on 로 알려 진 과정 은 액 상 방사능 폐 기물을 융해 무수규산 sil ica 과 봉사 borax 와 혼합시 키 고 이 혼합체를 고형화하는 것이다. 따라서 폐기물은 유리의 구성물이 된다. 이 유리는 화학적으로 불활성이고 실제로 불용성이어서 핵종을 영 구히 페쇄시키는 결과가 된다. 그러나 불행히도 완전히 불용성인 유리는 아칙 개발되지 않고 있다. 누수율은 매우 낮지만 수천 년의 기간에 걸쳐서는 상당량이 누수될 수도 있다. 또한 유리는 높은 온도에 의한 손상에 저항성을 갖지 않으면 안된 다. 유리-폐기물 기질이 만들어전 후 처음 50 년 동안 유리는 약 3X107 rad 의 방사선량을 갖게 될 것이다. 이 복합체의 초기 온도는 대략 2 00 ° C 이며 50 년이 지난 뒤라야 약 80°C 까지 냉각될 것이다. a- 선에 의 해 생기는 헬륨 가스 누적이 또한 손상을 일으키는데 이 분야에 있어서 는 많은 연구가 계속되고 있다. 유리 - 폐기물 기질은 가능한 누출을 방지하기 위해서 스테인레스 상자 에 넣고 지하 저장실에 영구 저장하게 될 것이다. 성공적인 장벽 때문에 생물권으로부터 유리화된 폐기물의 격리는 완전 한 것으로 예상된다. 방사능 물질은 화학적으로 유리에 결합하고 다시 스 데인레스 철로 둘러싸인다. 더구나 저장실의 지질학적 성질은 물의 틈 입을 최소화 시킬 것이다. 물이 폐기물에 다다르면 먼저 스테인레스 상 자를 두과하고 이어서 유리 - 폐기물 기질을 용해시킬 것이다. 이 물은 다 음에 표면으로 울라울 때까지 상당히 먼 거리를 이동하게 될 것이고 이 과정은 아마 수천 년이 소요될 것이다. 방사능 물질은 이온 교환 작용에 의해 암석이나 점토 광물 속에 잔류될 것이기 때문에 물보다 훨씬 느린 이동속도를 갖는다. 이러한 폐기물질의 정체는 물의 이동과 비교하여 그 이동을 약 100 배 가량 느리게 해 준다. 이러한 지질학적 퇴적을 통한 대 표적 유속은 30cm/day 이내이고 그 거리는 수십 내지 수백 km 에 이른 다. 이 속도로는 100km 를 이동하는 데 약 1, 000 년이 걸리고 누출된 방
사능 물질이 표면에 도달하기까지 10 만 년이 걸릴 것이다. 물론 방사능 붕괴는 이 기간을 통해서 계속될 것이므로 시간이 지남에 따라 보다 적 은 핵종이 잔류하게 될 것이다. 해저투기 해양저의 여러 부위는 지질학적으로 안정하고 혼합현상이 없기 때문에 물리학적으로 격리되어 있다. 많은 사람들은 이러한 부위에 놓아 둔 방 사능 폐기물이 해양과 인류와의 가능한 모든 접촉이 효과적으로 차단될 것으로 믿고 있다. 다른 하나의 제안은 이들 폐기물을 심해 해구에 투기 한다는 것이다. 이것은 지각구조판t ec t on i c p la t es 의 가장 자리에 있는 해구에 두기된 방 사능 물질이 지구의 중심부로 운반될 것이라는 점을 가정한 것이다. 한 연구는 지각구조판의 변두리에 구멍을 뚫고 여기에 폐기물을 넣어서 하 강하는 판이 폐기물울 지구의 내부로 운반케 하는 방법을 제시하고 있 다. 이 연구는 그 비용이 1, 000 메가와트 발전용량을 가진 원자로 하나 당 불과 373 만 불일 것으로 추정한다 (Kru t ena t, 1978). 이것은 킬로와트 시 당 5 원 정도에 해당한다. 그러나 필요한 시추기술은 아직 개발되지 않고 있다. 더구나 이 변두리 지역에 대해서는 알려진 바도 거의 없다. 또 다른 해저 두기의 대안은 해저상에 직접 폐기물을 버리는 일이다. 이렇게 하기 위한 최상의 위치는 대형 지각구조판의 중심 부위에 있으며 이곳은 지진활동이 거의 없는 곳이나, 영국 국립 방사능 보호위원회의 상세한 연구 결과에 의하면 폐기물을 먼저 유리화(琉璃化)한다면 폐기 장소로 해저를 이용하지 못할 이유가 없다는 것이다. 유리화된 폐기물의 용해는 약 3,500 년이 걸릴 것이고 그동안 방사능의 대부분은 파괴되고 나머지는 잘 분산되어 있을 것이다. 적절한 장소를 택하기 위한 지침은 아래 와 같다 (Anon, 1977) . ® 트롤(tr awl) 의 활동에 의해 발견될 가능성이 없어야 하며 약 1,ooom 내 지 5,000m 의 수심이어야 한다.
® 그 지역은 대륙붕보다 의해이어야 하며 어장으로부터 멀리 떨어져야 한 다. ® 그 지역은 심해 해류가 폐기장소로부터 대륙봉으로 직접 흐르거나 용승지 역이어서는 안 된다. ® 해저 케이불이 없는 곳이어야 한다. ® 알려진 광물자원으로부터 멀리 떨어져야 한다. ® 그 장소는 화산 활동, 또는 지질구조판의 수령이나 분지가 일어나지 않는 지역이어야 한다 . @ 그 장소는 실제적인 두기 작업이 편리하게 이루어지도록 선택되어야 한 다. 이러한 지역을 투기 장소로서 이용함에 있어서 참재적으로 중요한 장 점은 해저가 부드럽고 점성이 있는 두꺼운 점토로 덮여 있다는 점이다. 이 점토 충이 갖고 있는 이온보존 특성과 투과성이 낮은 특성은 유출할 지도 모를 여하한 폐기물을 화학적으로나 물리적으로 수용하는데 적절할 것이다 (Ho lli s t er, 1977). 이것이 사실로 입증된다면 이들 장소는 기술적 및 정치적 관점에서 실재적인 최상의 장소가 될 것이다.
제 12 장 우리나라 연안해역의 오영실태 12-1 연안해역의 특성 우리나라는 남북으로 뻗은 대표적인 반도 지형을 이루고 있어서 연근 해 해역을 통상 동해, 남해, 서해로 구분한다. 동해안은 융기해안으로서 매우 좁은 대륙붕을 형성하고 직벽의 급경사로 이어지며 해안선이 단조 롭다. 대부분의 남해와 서해는 침강해안으로서 넓은 대륙봉을 이루고 해 안선의 형태가 매우 복잡한 특유의 리아스식 지형을 형성한다. 연안지역 의 사회적 특성을 보면 행정구역과 인구, 그리고 총생산량을 비교할 때 해안선을 중심으로 8km 에 포함되는 육역과 3 해리에 해당하는 해역을 묶어 연안지역으로 구분할 수 있으며 전국토에 대한 연안지역의 비율은 시가 3.4%, 군이 37.4%, 인구 33%, 그리고 국민 총생산량의 약 33% 를 이 연안지역이 점유하고 있다. 우리나라는 5 차에 걸친 5 개년 경제개발계획의 강력한 추진으로 급속한 경제성장을 이룩하면서 산업화가 크게 촉진되었다. 특히 대규모의 공업 화가 이루어지면서 연안지역에 공업단지가 조성되고 인구의 도시 집중으 로 대량의 산업폐수와 생활하수가 수계(水系)로 유입되어 해양의 오영이 가속화되고 있다. 또한 산업 발달에 따른 에너지원과 교역 상품의 폭발
적인 증가는 해상 운송량을 크게 증가시키고 이에 따라 대소의 선박 사 고 등이 연안해역에 대한 오영 증대와 피해를 일으켜 문제가 대형화되는 추세에 있다. 표 12-1 해역수질 환경기준 조정 (환경처) 기준치 드o- ,u_ 구분 pH (mCOg /DI ) (D%O) (msg s/ I ) 대 (장1M 0 0균P m군 lN) /수 유(m g /분 I) 총(m 질 g/I소) 총(m g /인 I) 현행 7.8~ l 이하 포화율 10 이하 200 이하 멈출되어 8. 3 95 이상 서는안됨 I 조정 II 이1. 하5 포90 화이율상 II II ” 0이.0하5 0이.0하07 현행 6.5~ 2 이하 포화율 25 이하 100 이하 II 8,5 85 이상 n 조정 II 3 이하 포80 화이율상 II II ” 이0. •하 l 0이.0하15 현행 6.5~ 4 이하 포화율 8. 5 80 이상 血 조정 II 5 이하 포화율 0.2 이하 0.03 50 이상 이하 6 가크롬 (Cr+6) : O. 05 mg / l 이하 시안 (CN), 유기인, 수은 (H g). 비소 (As) : 0. 05 mg // 이하 포리크로리네이티드비페닐 (PCB) 특 현행 카드뮴 (Cd) : O. 01 mg // 이하 : 검출되어서는 안됨. 유刀j 납 (Pb) : 0.1 mg / l 이하 해 크롬 (Cr) : 0. 05 mg / l 이하 시안 (CN), 유기인, 수은 (H g). 멸r 비소 (As) : O. 05 mg // 이 하 포리크로리네이티드비페닐 (PCB) 질 조정 카드뮴 (Cd) : 0. 01 mg // 이하 :검출되어서는 안됨 등 납 (Pb) : o: 1 mg // 이하 구리 (Cu) : 0. 02 mg // 이하 아연 (Zn) : O.1 mg / l 이하
우리나라 연안해역의 오염을 원인 별로 분류해 보면 선박의 폐유, 정 유공장 폐수, 유조선 사고에 의한 석유 유출 등을 원인으로 하는 유류 오염, 중화학 공장과 각종 공장에서 나오는 무기성 폐기물에 의한 오염, 식품가공 공장 , 전분 공장 , 주정 공장 등에서 나오는 유기성 폐수에 의 한 오염, 도시하수 및 분뇨폐기에서 오는 오염, 그리고 매립 • 건설공사 에 따른 토사와 부유물질에 의한 오영 등으로 구분할 수가 있다. 그 의 에도 농약을 다량으로 포함하고 있는 관개수의 유입에 의한 오염, 온배 수 배출에 따르는 열오염이 문제가 되고 있으며, 방사성 동위원소에 의 한 오염도 참재적 위험이 되고 있다. 이에 따라 우리나라의 환경처에서는 의국의 경우와 같이 해수의 수질 을 양호한 정도에 따라 3 개의 등급으로 나누고 각각의 수질 기준을 정한 바 있으며 최근에 이를 다시 조정하여 발표한 바 있다(표 12-1). 12-2 생활하수 및 공업단지 조성에 따르는 연안오염 우리나라 연안역은 오래전부터 수산활동과 해운을 중심으로 한 주요 생활공간으로 이용되어 왔다. 특히 지난 20 여 년 동안 국가경제의 급격 한 성장에 따른 산업단지 조성, 여가선용 활동의 확대 등으로 연안역의 개발이 크게 촉진되어왔고 전인구의 약 30% 이상이 직 • 간접으로 연안 역에 연계되어 있으며, 현저히 팽창된 이들의 문화생활의 결과로 대량의 생활하수와 산업폐수가 그대로 바다로 방출되어 연안오염의 주 원인이 되고 있다. 1984 년에 바다로 유입된 생활하수의 총량은 202 만 6 천m 떠나 되고 이 것을 BOD 부하량으로 환산하면 45 만 돈에 달한다. 생활하수에 의한 연 안해수의 오염은 강수가 · 유입하는 하구역에서 훨씬 심한데 전체 생활하 수의 75% 가 강수로부터 유입된 것이고 나머지 25% 가 연안지역에서 유 입된 것이다. 이와 같은 추세로 생활하수가 정화되지 않은 채 유입된다 면 2001 년에는 BOD 부하량은 1984 년의 2. 3 배가 증가된 101 만 4 천 돈에
표 12-2 수질기준 적용시 연안해역별 수질등급 수질등급 연안해역 수질등급 설정구역 해역이용 현황 현행 조정 인천연안 인천내항 선박정박, 인천공단앞 m 매 해역 반월내만 선박정박, 반월공단앞 Ill III 해역 군산연안 군산내만 선박정박 III 때 군산의만 Il Il 목포연안 목포내항 선박정박 때 III 목포연안 Il Il 광양만 삼일항과 여천공단주변 선박정박, 여천공단앞 m 패 광양제철소 부근해역 해역 Il III 사천연안 삼천포내항 선박정박 n 패 삼천포의항 한려해상국립공원 I I 충무연안 충무내항 선박정박 III 血 충무의해 수산양식장 I I 진해연안 행암만 선박정박 DI III 마산만 선박정박, 공단앞해역 Il, 冊 m 부산연안 부산내항 선박정박 Ill III 낙동강하구 Il Il 수영만 요트정박및요트경기장 Il Il 울산연안 울산내항 선박정박 매 매 장생포항 선박정박 Il lII 온산항(의황강하구) 선박정박 Il 매 포항연안 형산강하구 선박정박 III 매 포항내만 일부 선박정박 n 패 동해연안 삼척오십천 하구 선박정박 Il 血 묵호 및 북평연안 선박정박 ll, m JI I III 속초연안 선박정박 Il , lII n,m 자료 : 환경처, 1987 •
달할 전망이다(환경처, 1987). 연안오염은 생활하수뿐만 아니라 공업단지의 산업폐수에 의해서도 심 각한 문제를 야기하고 있다. 마산, 전해, 포항 등의 해역은 해수 유동이 느리고 정체가 심한 곳이며, 인천, 부산, 울산, 군산 , 안산, 목포 등의 해역은 하구역과 인접하고 임해공단과 연안도시가 집결해 있어서 산업폐 수와 생활하수가 집중적으로 방출되는 오염 취약지역을 이루고 있다. 이 러한 지역의 오염방지는 폐수, 분뇨, 하수 등의 종말처리장 시설에 의존 하는 것인데 시설의 태부족 상태이므로 연안오염이 심각한 상태에 이르 고 있다(표 12-2). 12-3 간척 • 매립사업에 따른 연안오염 연안 환경 중에서 기수역과 조간대는 생산성이 대단히 높아서 의양해 역에 비해 14~20 배, 대륙봉해역에 비해서는 5~16 배나 생산성이 높으 며, 수산생물 생산의 약 60~70% 가 연안역과 직 • 간집으로 연계되어 있 다 (Clark, 1977) . 우리 나라 서 해 안과 남해 안은 조간대 가 광범 위 하게 발달 된 지형으로 높은 생산력을 갖고 있는 생명력이 풍부한 지역이다. 그러 나 근래 간척 매립 등 대대적인 연안 개발사업의 추전으로 해양 생산력 의 기본이 되는 연안 생태계의 생물학적 생산성과 참재력을 상실하게 되 어 연근해의 황폐화가 우려되는 실정이다. 그림 12-1 에서 보는 바와 같 이 대소 주요 간척 • 매립사업이 서해안과 남해안에 집결되어 있고 앞으 로도 계속 추전될 전망인데 이대로 간다면 전연안역의 생산성이 크게 떨 어지게 되고 따라서 수산자원에 대한 의존도가 높은 우리나라로서는 국 민 전체에 대한 식량공급에 미치는 영향이 클 것으로 보인다. 연안역별 로 간척과 매립사업의 추진으로 야기되는 수산자원의 피해는 표 12-3 에 서 보는 바와 같다(한국농촌경제연구원, 1987).
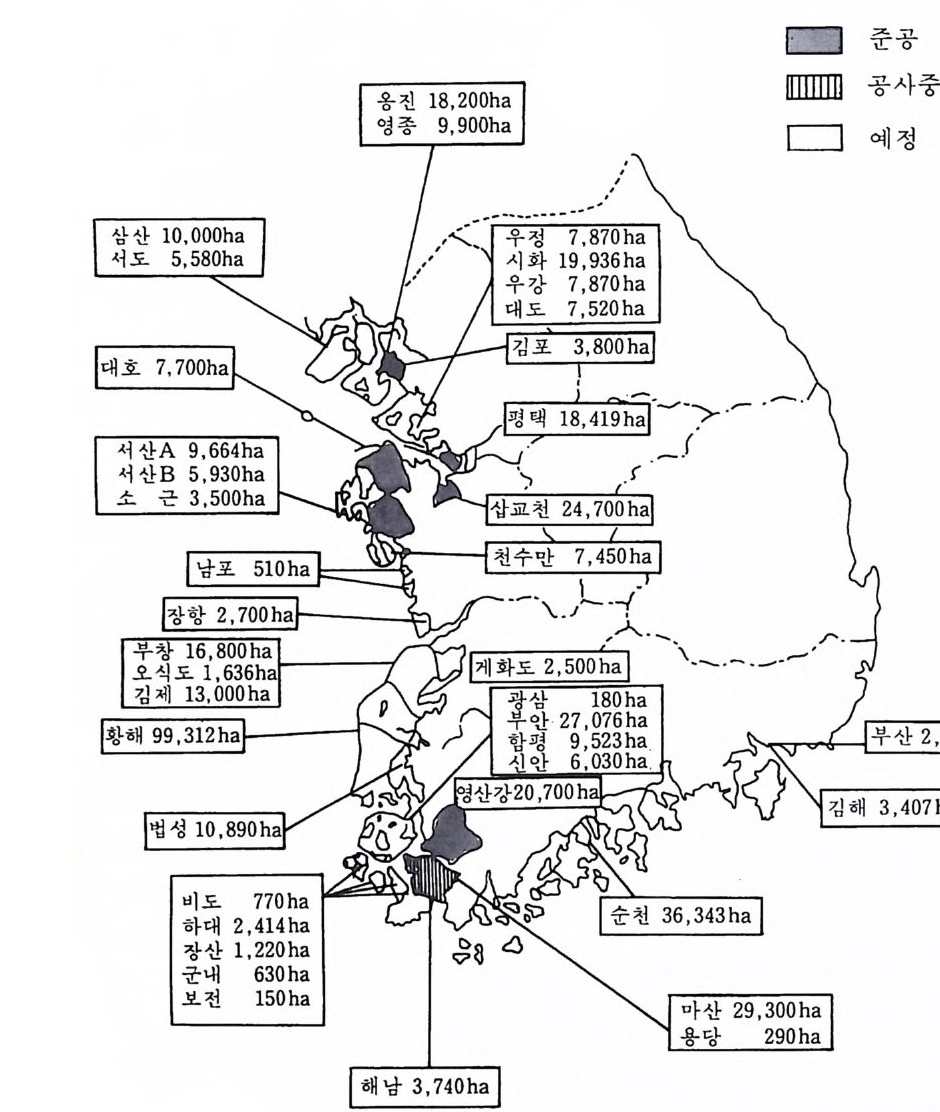 亡 건Z 츠 고o
亡 건Z 츠 고o
그림 12-1 우리나라의 간척 • 매 립 현황
표 12-3 간척 • 매립에 의한 수산자원 피해 현황 도별 간척지 배립면적 터장상실 수산자원 보호 생태계 변동으로 생산 및 수급에 (천 ha) 면적 상의 지역 특성 인한 지역 특산 미치는 영향 (천 ha) 품종에미치는 영향 경기 시화 3 월하순 ~5 월 대사한란장 상 가무락 등 패류 중순 우이도~ 실로 자원감소 생산량(년간 약 대부도간대하 및 어획부진 예 1~4 천돈)감소 산란장 AJ - 로 가무락 등 우이도는 가무 가무락, 바지 종패단가 상승, 락치패 발생장 락, 동죽, 백합 양식업 경제성 등생산감소 저하 ’ 6 3.9 우정 25.바지락 양식의 바지락 등 패류 년간 4,600 톤의 주생산단지 양식장 상실로 바지락 등 생산 간석지 양식 불 감소로 인한 양 가능 식어업 위축 및 공급 부족 현상 예상 충남 서산 9.6 o. 9 귤, 바지락등 바지락, 김, 갯 년간 6, 560 여톤 각종 양식장 및 지렁이 등의 생 의, 굴, 바지락, 꽃게, 대하등 산량 감소와 연 김, 실치 등의 회유성 어족 서 안 회유어족의 생산 감소 예상 식지 서식 지역 상실 로 어획 감소 예상 전북 김제 동죽, 백합, 개 각종 패류의 산 연간 3,52 아론의 량조개의 산란 란 및 양식장 생산감소 예상 및 치패 발생장 상실로 생산량 실뱀장어 종축 만경강, 동진강 감소 부족현상초래 은 실뱀장어 회 실뱀장어 회유 유로 로 차단으로 종
묘 수급 차질 초래 부창 21. 7 3.0 바지락 등 각종 바지락, 김등의 연 간 13,500 여 패류 및 김의 양식 불가능 돈의 패류, 해 생산단지 조류의 생산감 소가 예상되고, 연안어장의, 어 획부진초래 전님 함평 첫새우의 산란 전국 생산량의 첫새우 및 연안 장). 30~40% 점 하 회유성 어류, 숭어, 농어, 뱀 는 첫새우는 산 김 등의 생산량 장어 등의 연안 란 및 서식에 감소 회유성 어족 서 크게 영향 초래 식지 숭어, 뱀장어 등의 회유로 차 단 및 김 양식 장상실 I 무안 89. 3 14.1 숭어산란장 및 숭어, 농어, 복 해역의, 생태계 ll} 산 농어, 복어, 해 어 등연안성 어 변동으로 연안 파리, 새우, 낙 족의 산란장 상 어족 생산량 감 지 등 산란 서 실 및 뱀장어 소 식지 회유로 차단. 김, 미역 등 해 조류 생산차질 우려 득량 피조개 등의 각 피조개, 새꼬막, 연간 약 3,400 종 패류양식 주 키조개 등 패류 론의 생산 감소 생산단지 및 각 양식장 상실 및 예상 종 어류성육장 지반 변동으로 생산량 감소와
어류 회유로 차 단으로 어황 부 진 우려 순천 피조개, 새꼬막 지반변동 및 조 연간 약 43,600 등의 패류 양식 류소통 불량으 돈의 생산감소 주생산단지 로 양식장 황폐 예상 숭어, 전어 등 화, 생산감소 의 산란서식지 회유성 어족의 회유로 차단으 로 연안어업 생 산성 저하 자료 : 한국농촌경제 연구원, 1987 12-4 천해%택과 자가오염 우리나라 연안해역은 동해안을 제의하고는 파도와 조류가 비교적 약하 고 관리가 용이한 내만 해역이 많아서 일찍부터 천해양식이 발달하였으 며, 특히 1960 년대 이후 천해양식장이 급격히 신장하여 굴, 홍합, 피조 개, 바지락 등의 패류와, 김, 미역, 다시마 등의 해조류 양식에 의한 생 산고가 연근해 어업의 그것과 비교할 수 있을 만큼 성장하였다. 우리나라 천해양식의 가용면적은 약 19 만 ha 인데 (농수산부, 1986), 이 가운데 51. 5% 가 개발되어 이용하고 있다. 이처럼 증가일로에 있는 천해 양식업은 어민의 소득증대와 국만경제에 기여하는 긍정적인 면을 무시할 수 없으나 양식어장의 개발, 이용에 따라 필연적으로 수반되는 환경오염 문제는 지금껏 도의시하여 온 실정이다. 원래 해수교환이 양호하지 않은 곳에 발달하는 내만의 수산양식은 과 도한 밀집양식이 계속될 경우 양식장 자체의 자가오영으로 환경이 열악 해지고 그 정도가 심화되면 어패류의 대량 패사가 일어난다. 따라서 일
정한 기간이 경과하면 양식장의 위치는 다른 해역으로 이동시켜 주는 것 아 상례이다. 그러나 우리나라 천해 양식장의 경우 이와 같은 환경의 재 생에 대한 고려가 없아 장기간 양식업을 계속해 온 까닭에 자가오염에 따른 환경의 악화가 심화되고 있는 실정에 있다. 12-5 방사성 물질과 온배수 열의 문제 우리나라는 급증하는 전력수요를 충족시키기 위해 지난 1978 년 4 월에 준공된 고리 원자력 발전소 1 호기를 시발로 1989 년 9 월까지 도합 9 기의 원자력 발전소가 가동되고 있으며 이들은 우리나라 총 발전량의 50.1% 룰 담당하고 있다. 표 12-4 에서 보는 바와 같이 이미 착공된 2 개의 원전 이 1996 년까지 완공될 예정이고 다시 2001 년까지 5 개의 원전이 추가로 건설될 계획이다. 표 12-4 우리나라 원자력 발전소 현황 호기 용 량 (1, 00 0 kw ) 원자로 착공 준공 고리 1 587 Westi ng House (미 ) 1970.9 1978.4 고리 2 650 I/ 1977. 5 1983.7 고리 3 950 II 1978.1 1985.9 고리 4 950 II 1978.1 1986.4 월성 1 678.7 AECL( 캐) 1976. 1 1983.4 영광 1 950 Westin g House (미 ) 1979,3 1986.8 영광 2 950 II 1979.3 1987.6 영광 3 1,0 0 0 GE(미) 1989.6 1995.3 영광 4 1,000 II 1989.6 1996.3 울전 1 950 프라마톰(프) 1981 .1 1988.9 울전 2 950 II 1981 . 1 1989.9 1-5( 추가분) 2001 까지
우리나라 연안해역에서 방사성 물질의 방출에 대한 증거는 나타나지 않고 있지만 방사성 오염의 피해가 다른 오염원에 의한 것보다 엄청나게 크다는 사실과 오영의 참재적 위험 때문에 엄격한 감시와 철저한 관리가 무엇보다 중요한 일이다. 또한 원자력 발전소에서 배출되는 온배수 양이 방대하고 원전이 밀집해 있는 우리나라의 경우에 온배수 열의 방출이 연 안 생태계에 미치는 영향을 지속적으로 연구 • 감시할 필요가 있다. 12-6 연안해역의 일반 수질 현황 해양의 오영문제가 중요한 사회문제로 점점 크게 부각되는데 비해서 오염의 현황 자료는 최근에 수년을 제의하고는 매우 빈약한 상태에 있고 오염에 대한 연구 역시 부진한 형편이다. 표 12-5 한국 연안해역의 수질 현황(1 987 년 평균) 굼o L 모., 평균 인천 군산 목포 여수 충무 pH 8.07 8.00 7. 92 8.13 8.14 8. 10 D O(mg /l) 8.6 9.4 10.2 9.1 8.4 9.2 S S(mg /I) 17.63 27.62 28.96 28.39 12.46 12.22 Transpa r ency (m) 3.1 1. 7 2.7 1. 0 1. 7 3.9 T-N(µg / l 288. 05 305. 18 360. 64 264.33 197.68 242.53 POcP (µgp/1 ) 70.25 64.41 47.59 79.30 74.75 43.40 Si0 2 -P (µgS i/ l) 261 . 20 387. 85 235. 25 367.08 416.39 113.69 Cu (µg/l) 4.87 13.24 3.25 2.74 4.80 3.94 Zn(µg /l) 20.3 32.35 23.36 16.20 17.28 23.31 Fe(µg /l) 72. 36 89.74 73.98 106. 99 61. 90 57.15 ·Cr (+6) (µg/1) 0. 31 0.40 0.30 0.25 0.28 0. 26 Cd(µg /!) 0.36 0.24 0.38 0.22 0. 54 0.15 Pb(µg /l) 3. 72 2.57 7.09 3.39 2. 37 3.00
표 12-5 계속) 홍냐 부산 울산 포항 동해 속초 제주 pH 8.00 8. 09 8.23 8.1 2 7.97 8.11 D.O ( m g/ l) 7.1 7.1 9.5 8. 6 7. 9 8.7 S.S(mg / I) 23.31 20.02 7. 98 8.80 14.42 9. 70 Transpa rency (m) 2.9 3.9 4. 4 5.1 2.9 4.1 T-N(µg / l) 354. 00 350. 05 151 . 72 218.10 352. 16 372.12 PO,-P (µgp/l) 54. 79 68, 70 46.5 9 58. 59 113.98 120.70 Si0 2 -P (µgS i/ l) 230.19 155.62 227.20 180.96 279.18 279.80 Cu(µg /I) 6.22 4.04 2.49 • 2.11 5.50 5. 27 Zn(µg /l) 28.75 14.44 13.57 7.12 26.14 17.82 Fe(µg /!) 79.24 51. 88 42.11 43.83 107. 63 81. 56 Cr(+6) (µg/l) 0.33 0.34 0. 31 0.34 0.32 0.29 Cd(µg /I) 0.26 0.65 0.53 0.38 0. 38 0.25 Pb(µg /!) 3.97 3.10 3.42 2.65 6. 93 5.24 자료 : 해양경찰대, 1988 표 12-5 는 우리나라 연안의 주요 11 개 지역 부근해역에서 측정된 수질 지표 항목에 대한 자료이며(해경, 1988), 각 항목별 현황은 아래와 같다. 12-6-1 수소이온 농도(p H) 우리나라 연안해역의 평균 수소이온 농도는 8.07 이며 해역별로는 동해 의 포항 연안이 8.23 으로 가장 높은 반면, 서해의 군산 연안이 7.92 로 가장 낮다. 해역간의 변화폭은 서해와 남해 사이에서 크게 나타나는데 군산과 충무의 부근 해역에서 수소이온 농도가 각각 7.4~8.1 및 7. 6~8. 3 의 범위로 0. 7 정도의 차이를 보인다. 환경청이 고시한 수질 기준에 따라 지역별 수소이온 농도의 평균값을 비교하면 우리나라 연안의 전해역은 항만이나 일부 내만해역을 제의하고 는 아직 수질이 크게 악화되지는 않은 것으로 보인다.
12-6-2 용존산소 (D i ssolved Oxyg e n) 연안해역 전체의 평균 용존산소량은 8.6m g /l 이며 남해의 부산 부근 과 동해의 울산 부근에서 평균 7.1m g /l 의 값울 보여 가장 낮게 나타난 다. 가장 심하게 용존산소의 결핍울 보이는 곳은 시기에 따라 차이가 있 으며, 남해의 부산 부근에서 10 월에 3. 8 mg / l, 마산 부근에서 8 월에 4. 9mg / l, 동해의 울산 내항에서 10 월에 3.8mg / l 등 매우 낮은 값을 기록 하고 있으며 최근 3 년간의 경향은 부산과 울산 부근 해역에서 계속 감소 하는 추세를 보인다. 12-6-3 두명도 (Trans p arenc y) 투명도의 해역별 값은 차이가 매우 크다. 동해의 경우에 평균값이 5.1 표 12-6 연안 해역별 COD 현황 (단위 : mg //) 연안해역 1981 1982 1983 1984 1985 인천연안 3. 4 4.1 4.2 3. 6 2.3 서산연안 군산연안 4.1 3.4 3. 2 2. 3 1. 9 목포연안 2. 9 1. 9 1. 7 2.2 2.5 순천만 1. 3 0. 9 광양만 2.6 2.4 제주연안 1. 8 1. 8 서귀포연안 1. 3 1. 2 사천연안 1. 3 1. 9 충무연안 1. 9 1. 7 진해연안 6.5 4.9 4.3 3. 9 3.8 부산연안 3.3 3. 6 2.9 2. 7 2.3 울산연안 4.0 3.0 2. 5 2. 4 2.4 포항연안 2. 0 2.6 2.2 1. 8 1. 8 동해연안 1. 5 1. 9 2.1 1. 4 1. 2 자료 : 환경처, 1987
m 로서 상당히 맑은 상태인 반면, 남해의 목포 부근해역에서는 1. 0m 로 가장 탁한 수역임을 보여준다. 같은 해역이라도 의해역과 내해역에 따라 차이가 크게 나타나는데 동해의 의해역은 10.5m 로서 가장 맑은 해역임 표 12-7 연안 해역별 수질 (COD) 개선 효과 (단위 : mg /!) 1991 1996 2001 연안해역 대책전 대책후 대책전 대책후 대책전 대책후 인천연안 3.7 3. 0 3. 9 2.5 4.3 2.1 군목산포연연안안 31.. 01 31..01 13.. 76 01.. 79 42..21 o1.. 53 광양만 8.8 7.6 12.6 10. 8 13.6 11. 7 사천연안 1. 6 1. 6 1. 7 1. 5 1.8 1. 0 충무연안 충무항 2.6 2.0 2.9 1. 6 3.2 1. 5 해역 1. 6 1. 3 1. 7 1.1 1. 8 。 •9 진해연안 마산내만 8. 3 5. 3 9.5 3.5 11. 5 3. 0 진해만 2.5 2. 2 2.8 2. 0 3. 2 1. 0 부산연안 낙동강하구 3. 0 1. 8 3. 3 1. 7 3.7 1. 6 부산항 4.5 3. 5 5.3 2.5 6. 0 1. 8 수영만 9. 0 1. 7 13. 5 1. 5 18. 0 1. 3 울산연안 태화강하구 7. 5 4.5 9.0 4.3 11. 0 4.0 의황강하구 4. 5 2.7 5.0 2.5 5. 5 2.4 의만 1. 0 1. 0 1. 0 1. 0 1. 0 1. 0 포항연안 형산강하구 3. 4 3. 4 4.1 3.0 4. 9 2.7 내만 2. 7 2.1 3.3 2.4 4.0 2.1 의만 1.4 1. 4 1. 5 1. 3 1.7 1. 2 동해연안 동해시어항 3.0 3. 0 3. 5 2.5 4.5 1.5 전천하구 2. 0 2. 0 2.5 1. 8 3.0 1.5 오십천하구 1. 8 1. 8 2.0 2.0 2. 3 2.3 해역 1. 7 1. 7 2. 0 1.4 2,3 o. 9 자료 : 환경처, 1987
을 입증하고 있는 반면 속초항은 4.1 m 에 불과하다. 12-6-4 화학적 산소 요구량 (Chem i cal Oxyg e n Demand) 해수의 수질상태를 가장 잘 지표해 주는 것은 화학적 산소요구량 (COD) 이다. 우리나라 연안해역의 COD 현항을 보면(표 12-6), 동해와 남 해의 일부 해역을 제의하고는 모두 Il 급 및 IlI 급의 수준이며 특히 진해, 군산, 인천 부근 해역에서 4.0mg / l 이상의 값을 보여 오염 정도가 가 장 심함을 알 수가 있다. 최근의 변화 추세는 광양만, 마산 내만, 부산 수 영만, 태화강 하구역 등에서 COD 의 중가가 현저하여 2001 년에는 COD 10 mg / l 이상으로 수질이 극히 악화될 것으로 보인다(환경처, 1987). 이러한 점을 감안하여 환경처에서는 서해안의 인천, 군산, 서산, 목포 동 4 개역, 남해안의 순천만, 광양만, 사천, 충무, 진해, 부산, 제주, 서 귀포 등 3 개역으로 전 해안을 15 개 관리권역으로 구분하여 해역수질을 관리하기로 하였으며 해양 수질오염 측정망을 28 개 연안 199 개 지점으로 설치하여 해안 해역별 COD 농도의 개선을 위해 노력하고 있다(표 12-7). 12-7 중금속 해안 가까이 공업시설이 발달하고 인구가 증가하면 부근 해역에 중금 속의 농도가 증가하게 마련인데 우리나라 연안 해역의 중금속 농도는 아 직 위험 수준에는 이르고 있지 않다. 12-7-1 구리 전해역의 평균 구리 농도는 4.87µ g /l 이며 최고 농도를 나타내는 해역 은 인천 부근으로 13.24µg /l , 최저 농도를 나타내는 해역은 동해 부근 해역으로 2.11µ g /l 이다. 표충과 저층의 차이도 매우 커서 인천 부근 해 역의 경우 표충의 구리 농도는 6.25µ g /l 인데 반해 저층에서는 20.24 µg/t ol 다.
해수의 수질기준 (20µ g / l 이하)과비교해 보면 전해역이 기준치 이하를 유 지하고 있으며 다만 인천 부근 해역의 저충에서만 기준치를 초과하고 있다. 12-7-2 납 전해역의 평균 농도는 3.72µg /l 이며 가장 높은 농도를 보이는 곳은 군산해 역으로 7. 09 µg /l 이고 가장 낮은 농도를 보이는 곳은 여수 해 역으 로 2.37µ g을 나타낸다. 해수 수질기준 (100µ g /l) 과 비교해 보면 전해역 이 기준치 이하를 유지하고 있다. 12-7-3 아연 전해역의 평균 농도는 2.03µ g /l 이며 가장 높은 농도는 32.35µ g /l 로 서 인천 부근에서 나타나고 가장 낮은 농도는 7. 12 µg /l 로서 동해 부근 에서 나타난다. 아연의 경우 역시 해수 기준치 이하를 유지하고 있다. 12-7-4 카드뮴 카드뮴 농도의 전연안 해역의 평균 값은 0.31µ g/ l 이며 해역별로는 인 천 부근에서 0. 40 µg /l 로 가장 높은데 반해 목포 부근에서는 0. 25 µg/ l 로 가장 낮다. 해수 기준치가 lOµ g /l 이므로 전 해역이 기준치에 못 미 치고 있다. 12-7-5 철 전국 해안역에 있어서 철의 평균 농도는 72. 36 µg /l 이며 최고 및 최저 평균 농도는 속초 해역과 포항 해역에서 보이는데 그 값은 각각 107.63 µg/l , 42. 11 µg /l 이다. 12-8 영양염 우리나라는 1970 년대에 여러 곳의 임해 공업단지의 조성과 인구의 집
중으로 각종 폐수의 해양 두기가 기하급수적으로 증가하여 왔으며 이에 따라 연안 해역의 부영양화가 가속되었다. 1981 년 7 월에는 미중유의 대 규모 적조가 발생하였으며 적조의 발생빈도가 더욱 높아 가는 추세에 있다. 12-8-1 총 질소 (To tal Nit rog e n ) 총 질소의 분포는 해역에 따라 차이가 크다. 일반적으로 높게 나타나 는 해역은 부산 (354µ g//), 울산 (350µ g/l), 속초 (352µ g//), 제주 (372µ g/ l), 군산 (361µ g/l) 등이며 가장 높은 값을 보이는 곳은 반월 부근으로서 5.7µ g /l 을 기록하였다. 비교적 낮은 값을 보이는 해역은 충무 (243µ g/ l), 여수(1 98µ g/I), 포항(1 52µ g//), 동해 (218µg /l) 등이다. 표 • 저충의 차이는 별로 현저하지 않으나 계절에 따라서는 차이가 크다. 해수 수질기준에 따르면 1 등급수 50µg / l 이하, Il 등급수 100µg / l 이하, 빼등급수 200µg / l 이하로 정하고 있는데 아와 비교해 볼 때 포항 부근 해역은 m 등급에 해당하며, 그 의의 해역들은 ill등급을 초과하고 있어서 부영양화의 진행을 볼 수가 있다. 최근 수년간의 측정치를 보면 목포, 부산, 울산 등의 해역에서는 매년 급격히 증가하는 경향을 보이고 있고, 특히 부산과 울산의 부근에서 암모니아태 질소의 농도가 현저히 증가하고 있다. 12-8-2 인산염 전 연안 해역에 있어서 인산염의 평균 농도는 70µ g /l 이며 가장 높은 해역은 제주 부근으로서 121µg //, 가장 낮은 해역은 충무 해역으로 43 µg /l 로 나타난다. 표 • 저층의 차이도 커서 속초 부근에서 표충의 농도 가 147µ g /l 인데 비해 저층의 농도는 81µ g /l 이다. 해수의 수질기준은 1 등급수 7µ g /l 이하, II 등급수 15µ g /l 이하, 凰등 급수 30µ g /l 로 이하로 정하고 있는데 이와 비교해 보면 전해역이 매등 급을 초과함을 알 수가 있다. 최근 수년간의 경향은 제주 부근 해역에서 급격히 증가하는데 반해 충무와 여수 해역에서는 점차 감소하는 추세에 있다.
12-8-4 규산염 (Si0 2 ) 전 연안 해역의 평균 규산염 농도는 261 µg / I 이며 최고 농도는 여수 해역에서 416µ g /I 를 나타내고 최저 농도는 114µ g / I 로서 충무 해역에서 나타난다. 최근의 변화 양상은 인천, 군산, 제주, 충무, 부산 등의 해역 에서는 매년 감소 추세를 보이고 있으나, 목포, 포항, 속초 부근에서는 증가하고 있다. 12-9 적조 우리나라에서는 1962 년 남해의 진동만에서 처음으로 적조가 발생하였 는데 1977 년까지는 그 규모가 작았다. 그러나 이미 언급한 바와 같이 1981 년에는 진해만 해역에서 엄청나게 큰 규모의 적조가 발생하여 주변 양식장의 패류 600 여론을 폐사시킴으로써 18 억원의 피해롤 입혔다. 이 후 적조의 발생은 매년 빈발하고 대형화되고 있는데 그 이유는 연안 해 역의 부영양화가 급속히 진행되어 온 데에 있다. 우리나라의 적조 발생 을 살펴보면 (박, 1987) , 1962~ 1970 년 중반까지 에 는 진해만을 중심으로 주로 내만 해역에서 규조를 원인종(原因種)으로 하여 발생하였으나, 1980 년대에 들어와서는 종전의 내만국지성 단기적조 (內灣局地性 短期赤潮)로 부터 유독종(有毒種)을 포함하는 편모종류에 의 해 발생되어 1 주일 이상 수 개월까지 지속하는 의만확대성 장기적조(外 灣大性 長期赤潮)로 변화되었다. 적조의 발생시기와 그 밀도는 대체로 7 월, 6 월, 5 월, 9 월 및 4 월의 순 으로 나타나는데 5 월 ~7 월까지는 유사하게 나타난다. 전체적으로 볼 때 마산만과 행암만 해역에서는 전 기간에 걸쳐 발생하였고 기타 해역에서 는 6 월 ~9 월에 발생하고 있다. 적조의 원인종은 표 12-8 에서 보는 바와 같이 각 해역에 따라 그 종류 와 밀도가 다르다. 울산만에서는 Proto c entr u n mi ca ns 를 비롯해서 다른 해역에서는 보이지 않는 Peri. di n i u m tro choid e um 이 10. 540 cell/ml 나
표 12-8 한국 주요 연안의 적조 발생상황과 원인종 (점 유율, 밀도 해역 발생일시 적조원인종 %) (cells/ml ) 위 산만 '82. 5. 25 Prorocentr u m mi ca ns (95) 10,260 '83. 3. 29 Peri din i u m tro clwi de um (95) 10,540 온산만 '83. 7. 27 Skeleto n ema costa .tum (49) 4,700 Thala ssios i ra sp. (46) '84. 6. 18 Prorocentr u m mi ca ns (63) 4,000 Skeleto n ema costa .tum (32) '84. 8. 29 Skeleto n ema costa .tum (95) 12,000 '85. 6. 9 Hete ro s igm a akashiw o (95) 70.000 인천만 '84. 7. 24 Nocti luc a sci nt i lla ns (98) 400 '86. 7. 6 Nocti luc a sci nt i lla ns (95) 380 여 자만 '84. 9. 20 Chaeto c eros (40) 8,200 Skeleto n ema costa .tum (42) '85. 7. 25 Nocti' luc a sci nt i lla ns. (90) 300 가막만 '85. 7. 25 Nocti luc a scin t i lla ns (85) 240 '85. 9. 6 Prorocentr u m. (90) 10,000 광양만 '85. 7. 4 Skeleto n ema costa .tum (80) 2. 400 '86. 9. 6 Skeleto n ema costa .tum (92) 72,100 진주만 '85. 9. 10 Cochlodin i u m sp. (80) 2,000 '86. 7. 2 Skeleto n ema costa .tum (90) 15,300 영 일만 '86. 6. 24 Prorocentr u m. (68) 8,200 Hete ro si gm a akashiw o (10 ) Gym n odin i u m sp. (5) 전해만 '82. 6 Prorocentu rm sp. (83) 55,970 (마산) '84. 6 Hete ro si ng m a akashiw o (99) 186,552 '86. 6 Prorocentr u m sp. (89) 42,500 자료 : 박, 1987 나타나고 있으며, 온산만에서는 연별로 그 원인종이 다르게 나타나서 1983~1985 년에는 Skeleto n ema costa tum 이 교대로 출현하였고, 유기물 오염의 대표적 지표종의 하나인 Hete r osig m a akashiw o 가 우점하여 이 해역이 심각한 오염이 발생하고 있음을 나타낸다. 인천만에서는
Nocti luc a scin t i lla ns 가 우점하는 적조로서 특징을 이룬다. 여자만, 광양 만, 진주만, 영일만에서는 주로 규조류에 의한 적조가 발생하는데 반해 여자만에 인접한 가막만에서는 편모조류에 의한 적조 발생이 대조적이 다. 특히 진주만에 서 의 Cochlodin i u m 적조는 다른 해 역 에 서 는 볼 수 없 는 현상이다. 진해만 역시 수 종의 편모조류가 주요 종을 이루는 혼합형 적조이며 밀도는 전국 적조 발생 해역 가운데 가장 높게 나타난다. 이와 같은 유독성 편모조류로 인한 적조의 근본적인 방지는 그 해역의 오염방 지 대책에 달려 있다. 죽, 과도한 부영영화를 방지하고 특정 편모조의 대발생에 필요 영양소인 미량 금속 원소의 유입을 제한하는 등 특별한 대책이 요구된다. 12-10 유류오염 우리나라 연안 해역에서 발생하는 오염 가운데 사회적으로 가장 문제 가 되는 것은 유류오염으로 이것은 울산 정유공장이 가동된 이래 해수의 수질오염을 발생시킨 최초의 오염원이다. 이어서 호남 정유공장이 가동 된 뒤 폐수의 배출량이 증가되고, 유조선의 사고, 각종 선박 사고, 유저 장 탱크와 송유관으로 부터의 기름 유출, 유조선 물밸러스트의 항내 폐 기, 선박 폐유, 각종 공장 폐수에 포함된 유류 배출 등으로 인한 오염이 날로 증가하고 있다. 특히 정유공장의 가동 초기에는 유조선의 물밸러스 트 폐기와 각종 기름의 유출 때문에 울산 정유공장 부근에서는 최고 360 pp m 까지, 그리고 호남 정유공장 부근에서는 광양만 일대에 6,915p pm 까지 기름이 검출된 사례가 있다. 또한 유조선의 좌초나 침몰은 주변 해 역의 상당히 넓은 범위에 이르기까지 막심한 피해를 준다. 유조선과 각종 선박의 운항 등, 해상활동에 의한 유류오염은 경제발전 에 비례해서 늘어나는 선복량으로 더욱 심화되고 있다. 표 12 - 9 는 1979 년 ~1987 년 사이에 우리나라 연안 해역에서 발생한 유류오염 사고를 나 타낸 것이다. 이 기간 동안 오염 사고의 발생 건수는 총 1, 577 건으로 기
표 12- 9 연안 해역 유류오염 발생 현황 (1979~1987.6) 발생 건수 유출량(t) 피해액 (1 00 만원) 연도 겨 I 유류 폐기물 계 유류 폐기물 요구액 방제비용 보상액 1979 128 109 19 486 324 162 100 30 28 1980 140 130 10 401 400 1 2,651 133 38 1981 185 166 19 983 976 7 6, 1 72 903 1, 894 1982 221 202 19 141 139 2 287 102 197 1983 248 217 31 362 342 20 6, 7 08 1. 235 2,490 1984 226 200 26 201 119 82 412 962 418 1985 166 154 12 2,204 2,146 58 5,407 448 587 1986 158 135 23 2,618 2, 6 11 7 3,294 796 916 1987 85 82 3 225 226. 9 0.1 21,024 497 5,924 겨l 1, 557 1, 395 162 7,6 2 3 7, 283. 9 339. 1 45, 772 5, 1 06 12,497 자료 : 해경, 1987 롬과 기타 폐기물을 합쳐 약 7,600 돈이 연안 해역으로 배출되었다. 이로 인한 피해액은 450 억원에 달하며, 실제 보상액은 125 억원이었다. 그러나 해양 생태계에 미천 영향은 조사된 바가 없으며 매우 클 것임에 틀림없다. 유류오염 사고의 발생 추세를 보면, 1979~1983 년 사이에는 증가하고 있으나 1984 년 부터 점차 감소하는 경향을 보이고 있다. 그러나 선박의 고속화, 대형화에 따라 기름의 유출 사고도 대형화하고 있으며 1985 년 이래 석유의 유출량과 피해액이 크게 증가하고 있음을 주목할 필요가 있다. 석유 오영 사고의 해역별 현황을 보면(해경, 1987), 남해에서는 794 건 (51% )으로 4,700 톤 (6 1. 7%), 서해에서는 468 건 (30%) 으로 652 톤 (8.6%), 그리고 동해에서는 259 건 (19%) 으로 2,270 톤 (29.7% )으로 나타나 남해에 서의 석유 오염 발생률이 압도적으로 높다. 남해는 청정해역으로 지정되 어 있고 또한 각종 양식장이 밀집되어 있는 해역임을 감안할 때 유류오 영 방지를 위한 특별한 관심과 대책이 요구된다.
제 13 장 해양오염에 대한 생물학적 예측 13-1 배경 해양환경에서 오염원 방출의 전반적 영향을 예측하기 위해서는 개체생 물과 개체군의 반응은 물론, 이러한 반응에 대한 적응 성질을 이해하는 것이 요구된다. 생물에 대한 오영물질의 영향은 전통적으로 표준실험실 검 정 기 법 (sta n dard laborato r y bio a ssay tec hniq u e) 을 이 용해 서 평 가하여 왔 다. 이 검정기법에서 독성 스트레스에 대한 생물의 반응을 결정하기 위 해 사용하는 주요 기준은 LC5o 값, 죽 실험 대상생물이 주어진 노출시간 동안 50% 의 치사율을 일으키는 오염물질의 농도를 측정하는 것이다. 이 와 같은 생물검정실험의 결과는 배출액 중의 오염물질의 최대 허용농도 롤 정하려는 목적으로 환경처감은 규제기관에서 이용하게 된다. 또한 치 사 노출에 관한 이들 자료는 측정 오염물질에 대한 생물의 내성을 검정 하는 일, 여러 가지 오염물질의 상대적 독성을 비교하는 일, 그리고 참 재적 폐수 지침울 확립하는 일 등에 있어서 유용하게 사용된다. 그러나 만성 노출에 의해 야기될 수 있는 중요한 생리적, 행동적, 생태적 변화 는 이 표준생물검정법으로는 측정되지 않는다.
표 13-1 해양생태계 내에서 오영물질에 대한 반응단계 단계 생물체제 연구에 요하는 시간 IIl 생화학적 및 세포 수 분~수 시간 생물개체 수 시간~수 개월 매 모의 제어 군집 수 일~수년 VW개체군동태 수 개월~수십 년 군집의 동태와 구조 수 년~수십 년 자료 : U.S . Nati on al Academy of Sci en ces, 1971 그렇다면 생물검정기법 의에 오염물질에 대한 반응은 어떻게 측정될 수 있는가? 해양환경에 있어서 오염물질에 대한 반응은 생물 체제상의 5 개 단계에서 측정될 수가 있다. 죽 1) 생화학적 및 세포상의 반응, 2) 생리적 , 행동적 변화를 포함하는 생물 개체로서의 반웅, 3) 모의 제어 조건 sim ulate d contr ol led condit ion 하에서의 군집반응 , 4) 자연조건하에서 의 개체군 동태의 변화, 5) 자연조건하에서의 군집동태 및 군집구조상의 변화 등이 그것이다(표 13-1). 해양생태계에 있어서 오염물질의 환경관 리는 이들 5 개 단계에서의 영향들을 평가하지 않으면 안 된다. 13-2 생화학적 및 세포학적 반응 오염 스트레스를 감시하기 위하여 생화학적 기법을 사용하는 것은 해 양 환경오염으로부터 초래하는 스트레스 상태의 신속한 지표를 마련할 수 있는데 보통 두 가지 형태의 반응이 평가에 고려될 수 있다. 즉 어떤 일단의 화학물질에 의해 유도되는 특정적인 반웅, 그리고 영양 스트레스 를 포함하는 광범위한 환경조건에 의해 유발되는 일반적인 반웅이 그것 이다. 해양동물에서 관찰되는 두 개의 특정 반응은 석유탄화수소와 PCB 갇 은 유기성 오염물질에 대한 노출결과로 혼합기능 산소화효소(mi xed
fun cti on oxyg e nase : MFO) 를 유 도 하 는 것 과, 금 속 치 오 닌 단 백 질 meta l loth ion ein pro te i n 에 일부 중금속을 결합시키는 것으로 나타난다. cy toc hrome p -450 에 의해 매개되는 MFO 반응들은 많은 자연산 유기화 합물대사는 물론, 여러 가지 오염화합물 대사 및 그 영향과 관련이 있다 (St ag e man, 1978). MFO 활동의 유발은 여러 어류와 무척추동물을 유기 성 오염물질에 노출시킴으로써 증명되었지만, 또 다른 환경 및 생물학적 조건, 즉 온도, 성별, 번식기, 먹이 등에 의해서도 영향을 받는다. 따라 서 MFO 활동을 통해 자연개 체 군 fiel d po p u lati on 을 감시하는 일은 급성 및 만성 석유오염 환경을 검사하는 데 있어서 유용하다. 그러나 예측값 이 충분히 이용되려면 MFO 반웅의 한계와 그 변형 요인에 대한 이해가 선행되어야 한다• 일부 중금속이 금속치오닌 단백질과 결합함으로써 그 독성이 제거되는 사실은 많은 해양 어류, 연체동물 및 갑각류에서 연구된 바 있다. 이들 의 제독과정은 금속치오닌의 결합능력과 관련되며 결합능력을 넘어서게 되면 독성효과가 분명해진다. 예컨대, 연어를 수은 농도가 5 pp m 인 해 수에 노출시키면 효소 • 단백질 풀p ool 과 결합한 수은의 농도가 상당히 증가하면서 동시에 성장이 감소된다. 반면, l pp m 인 해수에 노출시켜서 는 아무런 영향도 관찰되지 않는데, 이는 필시 금속치오닌의 결합력 때 문일 것이다 (Pa yn e, 1976). 오염된 생태계의 동물 속에서 금속치오닌울 검출하는 것은 감시방법으로 제한이 따르지만, 그 유용성은 연구할 가치 가 충분하다 (McIn tyr e and Pearce, 1980) 고 하겠다. 오염물질 스트레스에 대한 일반적인 생화학적 반웅의 하나는 에너지 대 사와 막기 능 membrane func ti on 과 관련된 반웅이 다. 이 반응은 리소좀 l y sosome 막의 불안정화이다. 온도 스트레스, 저산소증 hyp ox i a, 오염물 질에의 노출 등, 다양한 스트레스 상태에서는 일반적으로 많은 기질에 대하여 불투과성인 리소좀막이 그 두과성을 증가시키며 결과적으로 분해 성 리소좀 효소가 활성화되고 세포계가 파괴된다(그립 13-1) . 불안정화 정도는 스트레스의 정도 및 기타 생리적 지표와 상관되며, 따라서 오염 된 생태계의 동물의 상태를 평가하는데 유용한 것으로 나타난다.
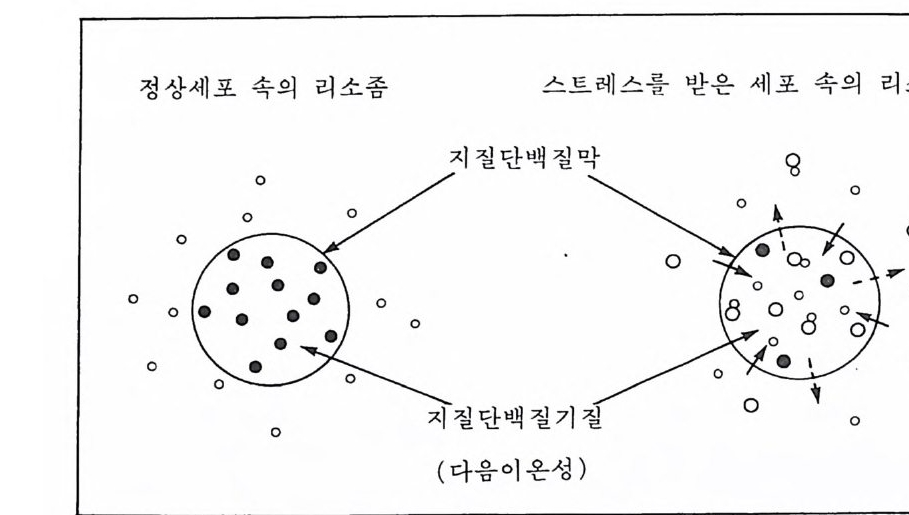 정상세포 속의 리소좀 스트레스 를 받은 세포 속의 리소좀
정상세포 속의 리소좀 스트레스 를 받은 세포 속의 리소좀
그림 13-1 정상세포에서 리소좀은 기질에 대하여 불두과성이며 리소좀 효소도 불활성이다. 스트레스를 받으면 리소좀막이 불안정해져서 두과성 을 증가시키고 효소를 활성화 시켜 결국 세포계가 파괴된다. 작은원 : 기질, 검은 원 : 불활성 리소좀 효소, 큰원 : 활성 리소좀 효소 (자료 : Moor, 1980)
생화학적 반응의 또 다른 예는 아데 닐 에너 지 충전 (adenulate energy charge : AEC) 을 측정 하는 것 이며 , 이는 아데 닌누클레오티드풀 (ATP, ADP, AMP) 로부터 생물에게 유효한 대사 에너지의 지표를 마련한다. 죽 AEC=ATP+l/2 운꼽 +ADP+AMP AEC 값은 광범위한 동물의 생리상태와 관련되어 있고 스트레스 상태 의 지표로서 유용한 것으로 보인다 (Sa li sb ury and Ross, 1985). 건강하게 성장하는 생물에 있어서 활성세포의 AEC 값은 0.8~0.95, 제한 환경에 처한 세포의 그것을 o.5~0.75, 그리고 때로 심하게 불가역적으로 억압 된 세포의 그것은 o.5 이하의 값을 갖는다. 염소화탄화수소나 PCB 는
전자전달계의 저해를 일으킬 수 있는데, 이둘 오영물질에 대하여 AEC 는 특히 유용한 지표가 될 것이다. 13-3 생물 개체상의 반응 오염물질 스트레스에 대한 생물의 반응은 생리적, 행동적 변화로 증명 될 수 있다. 죽, 질병과 갇이 환경 스트레스에 대한 취약성의 증가, 그 리고 생식과 발생단계에서의 변화 등이 그것이다. 고찰해야 할 가장 중요한 생리적 변화는 한 생물의 성장과 생존에 악 영향을 미치는 것들이고, 따라서 개체군의 유전자 풀에 기여할 참재능력 이다. 한 동물의 에너지 수지 energy bud g e t에서 먹이로서 소비된 에너지
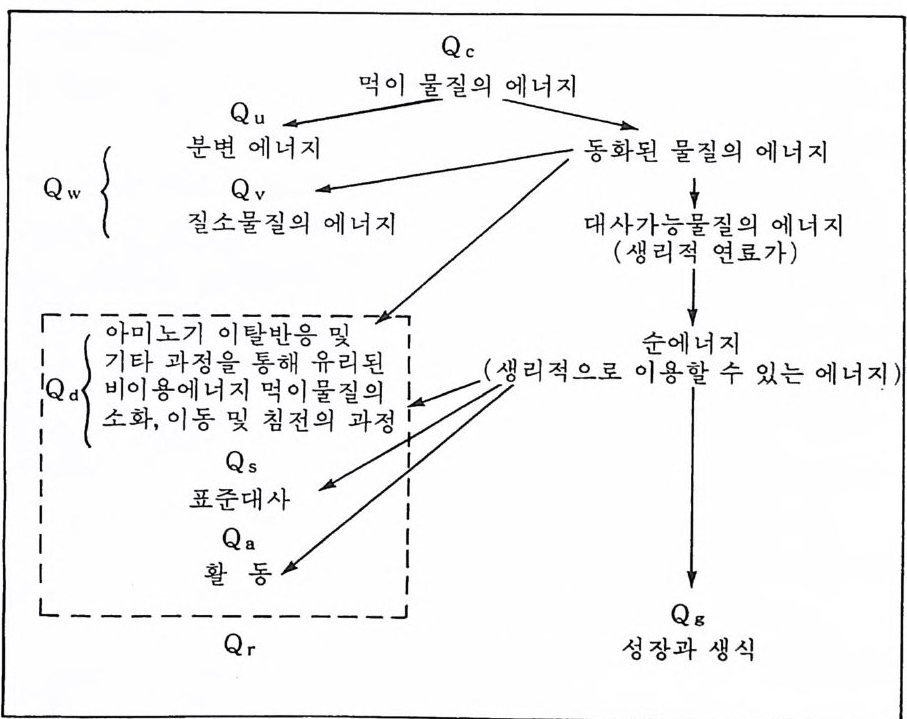 Qw l 분질변소QQ물 : ul질 너-의지 -에--너먹--지이-- 물--질-의/- -에/--너-/-지동- 대-화사-된가 능\ 물질질의의 에에너너지지
Qw l 분질변소QQ물 : ul질 너-의지 -에--너먹--지이-- 물--질-의/- -에/--너-/-지동- 대-화사-된가 능\ 물질질의의 에에너너지지
그림 13-2 한 생물의 에너지 수지 (Warren and Davi d, 1967)
Q c 는 소비에너지 Q w 와 대사, 성장 및 생식에너지 Qg와 Q r 로 나눈다(그 립 13-2). 에너지 수지상의 변동은 오염 스트레스로 인한 먹이행동, 호 홉대사, 또는 소화효율 등에서 변화된 결과로 일어난다. 다른 에너지 요 구가 만족된 후 성장에 유효한 에너지의 지표로서 성장한계는 비록 이것 이 계절적으로, 또 한 종의 발생단계에 따라 변화할지라도 실험실과 현 장 연구에서 공히 유용한 오염 스트레스의 자료가 된다는 사실이 밝혀졌 다 (Warren and Davi d, 1967). 그러나 에너지 수지에 대한 비오영생태계에 서의 에너지 수지에 대한 적절한 배경 정보가 요구된다. 또한 0 : N rati o ( 단백질의 이화작용으로부터 분비된 암모니 아성 질소에 대 한 호흡과정을 통해 소비된 산소의 원자 비율)는 단백질, 지질 및 탄수화물 사이에 이화작용의 균형을 나타내는 지표이다. 죽 낮은 0 : N ra ti o( 약 7) 는 에너지 이용에 있어서 완전한 단백질 의존도를 반영하는 반면에, 더 높은 0:N ra ti o 는 지질이나 탄수화물에의 더 높은 의존도를 의미한 다. 스트레스를 받고 있는 생물에 있어서 0 : N rati o 가 변동을 일으키 는 것은 실험실과 현장에서 증명되었으며 에너지 변화에 대한 가능한 생 화학적 설명을 제시해 준다. 오염 스트레스에 대하여 나타나는 생물의 행동상의 반응은 해로운 오 염물질의 농도를 검출하는 데 이용할 수 있는대 이 경우에 섭식행동을 변화시키거나 도피반응을 일으키는 등 적응기작의 촉발이 따른다. 스트 레스의 극단적인 수준에서 적응행동이 압도당하면 환경자국에 대응하는 생물의 능력은 그 스트레스가 제거될 때까지는 일시적으로, 또는 화학감 지기작이 불가역적으로 손상될 경우에는 영구적으로 약화된다. 오염 스 트레스에 의해 나타나는 행동상의 반응은 여러 가지가 있으나 이것들을 감시 도구로서 이용하는 데에는 한계가 있고, 앞에서 논의한 생리적 및 생화학적 기법들과의 상호관계 속에서 보다 광범위하게 고려되어야 한 다. 오염물질의 스트레스에 대한 해양동물의 병리학적 반응은 조직의 염증 과 퇴화, 손상조직의 회복과 재생, 신생물(新生物, neo p lasm) 의 형성 등 을 둘 수 있으며, 형태적 변형을 일으키는 유전자 손상을 포함하는 유전
자교란이 있을 수 있다. 비록 이러한 변화들이 다른 환경조건에 의해 유 발될 수도 있지만 오영과 관련된 병과 변형의 발생은 근년에 분명히 증 가하고 있다. 어류에서 보는 지느러미의 부식, 갑각류에서 나타나는 껍 질병 등은 오염물질의 영향과 병원생물에 의한 손상조직의 침범이 결합 해서 유발되는 것으로 알려져 있으며 가장 중요한 상태에 속한다. 보통 잠복상태로 나타나는 어류와 패류의 병리적 증상은 환경 스~트레스가 주 어지면 활성화될 수도 있다 . 환경 스트레스의 결과로 나타나는 형태상의 변형은 어류의 골격손상, 일부 어패류의 종양, 어란과 유생단계에서의 염색체 변이 등이 포함된 다. 가자미 생활사의 여러 단계에 대한 오염물질의 잠재적 영향은 그림 13-3 에서 보는 바와 같다. 이와 같은 정보를 토대로 얻은 결론은 심하게 오염된 해역에서의 실험적 감시계획은 오염 스트레스와 병리적 상태의 상관관계에 관한 광범위한 기준을 마련할 수 있다는 것이다.
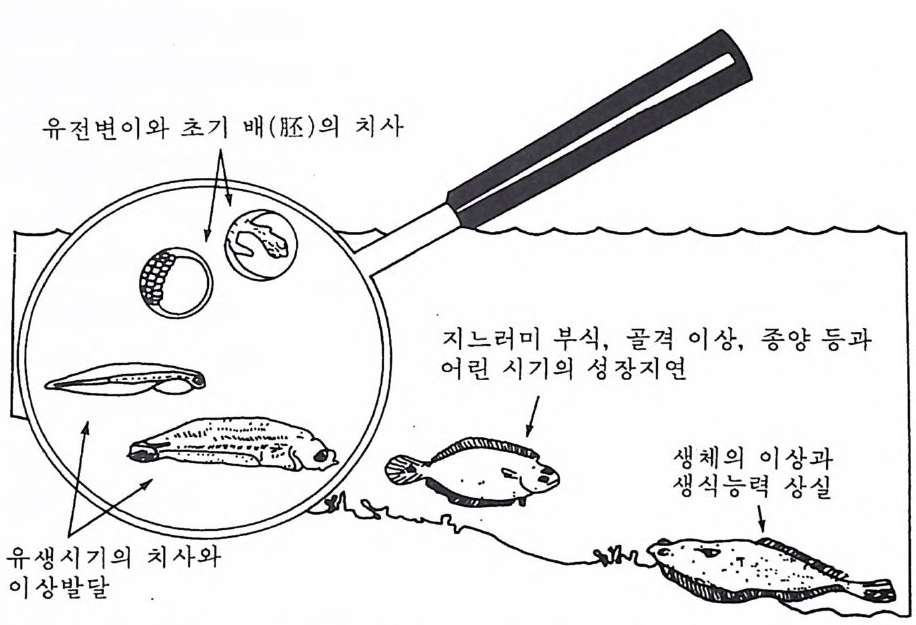 지느러미 부식, 골격 이상, 종양 등과
지느러미 부식, 골격 이상, 종양 등과
그림 13-3 가자미의 생활사에 대한 오염물질의 가능한 영향 (자료 : Sin d ermann, 1980)
이와 관련된 대표적 해양생물로서 홍합같은 정착생물은 해수로부터 여 러 가지 오염물질을 섭취, 농축함으로써 살아있는 감시자의 역할을 할 수가 있다. 1976 년에 미국 연안 해역에서 홍합감시계획 Mussel Watc h Pro gr am 이 시작되었는데 이 계획은 캘리포니아대학 스크립스 해양연구 소에 의해 수행되었고 연구비는 정부에 의해 지원되었다. 여러 가지 오 염물질의 분석은 우즈 • 홀 해양연구소를 포함하는 미국의 우수한 5 개 연 구기관에서 이루어졌다. 이 연구에서는 대서양과 태평양 해안에 선정된 조사정점에서 미량원소, 석유탄화수소 및 방사능 핵종 등의 축적농도를 측정함으로써 오염상태의 총체로서 홍합과 다른 이매패류를 사용하였으 며, 오염된 정점과 비오염 정접으로부터 취한 이매패류에서 여러 가지 오염물질의 농도를 비교함으로써 중요한 환경관심지역을 지정할 수가 있 었다. 3 년에 걸친 연구 결과로서 배경농도의 기본자료와 이매패류의 조 직 속에 증가된 농도로부터 다 같이 다양한 오염문제를 제기하는 자료를 확인하였다. 홍합감시계획은 더욱 확대되어 미국환경처가 주관하는 연안환경평가조 사정 점 계 획 (Coasta l Envir o runenta l Assessment Sta t io n s Prog ram : CEAS) 으 로 발전하였다. 이 계획의 목적은 생리적 반응과 오염물질의 축적을 상 호 연관시키는 것으로서 실험실과 현장연구를 결합시키는데 주안점을 두 고 있다. 실험 내용은 비오염 지역으로부터 채집된 홍합을 오영구배에 따라 선정된 조사정점에 설치한 우리 case 속에 넣고 각 조사정점에서 오 염물질의 섭취와 성장 정도를 측정하도록 구성되어 있다. 로드아일랜드 의 Narra g anse tt만의 경우에는 Pro vi dence 강의 심하게 오염된 환경으 로부터 하류부근의 만이 비교적 오염이 덜 된 지역까지 오영구배에 따라 조사정점들이 선정되었는데, 성장지수의 범위 내에서의 감소는 금속과 석유탄화수소의 높은 체내 축적농도와의 상관관계를 나타내었다 (NAS, 1980). 또 하나의 진행중인 감시계획은 미국 해양기상국 (NOAA) 의 수산연구 팀이 주관하는 해양동향계획 Ocean Pulse Pro gr am 이다. 이것은 서북 대 서양에서 대륙붕의 환경조건을 평가하기 위한 기초자료를 확립하고자 고
안된 것이다. 이 계획은 조사 해역내 주요 생물종의 생리적, 생화학적, 병리학적, 유전적, 행동적 차이들 의에 종의 수도 abundance 및 분포양 상을 분석하고, 이들 요인에 대한 오염물질의 영향에 관하여 현재 진행 중인 실험실 연구와 비교하는 연구를 포함하고 있다. 13-4 모의 군집 오염 스트레스에 대한 생물반응의 총체는 공존하는 종의 경쟁 행동에 서 반영될 수 있고, 생태계 내의 에너지 흐름에서 변화를 일으킨다. 이 들 변화를 모의조건하에서 평가하기 위하여 여러 가지 계획이 고안되어 왔다. 유명 한 제 어 생 태 계 오영 실 험 (Contr ol led Ecosys t e m Polluti on Exp er i me nt: CEPEX) 계획은 국제해양탐사 10 개년 계획의 일부로서 미국 과학재단에 의해 연구비가 지원되었으며 이것은 플랑크톤 군집들에 대한 오염의 영 향을 평가하기 위한 것이다 (Brown and Parsons, 1978). 제어생태계로서 여러 가지 크기 (68~1 , 700m3) 의 풀라스틱 주머니를 사용해서 (그림 13-4) 대량의 해수와 자생종을 넣어 캐나다 서부해안의 Saan ich Inle t에 설치 하였다. 수온, 염분, 영양영류 농도 등의 물리화학적 변수와 동 • 식물 플랑크톤의 개체군 측정 등이 주기적으로 이루어졌다. 중금속과 석유탄 화수소같은 오염물질을 첨가하여 인위적인 오영생태계를 만들고 그 속의 미생물, 식물플랑크론, 동물플랑크톤의 개체군 변화를 비오염 제어생태 계의 그것들과 비교하였다. 세대기간이 짧은 박테리아와 식물플랑크톤은 동물플랑크돈보다 오염물질의 첨가로부터 더 빨리 회복되었고, 더구나 중금속 첨가에 대한 동물플랑크톤의 반응은 크기가 작은 종류가 큰 종류 보다 더 민감하여 오염에 대한 반웅이 생물의 크기와 관련됨이 알려졌 다. 스코틀랜드의 서해안인 Loch Ewe 에서 수행된 유사한 일련의 실험에 서는 표영생태계에 대한 북해 석유의 영향이 평가 되었다 (Da vi es and
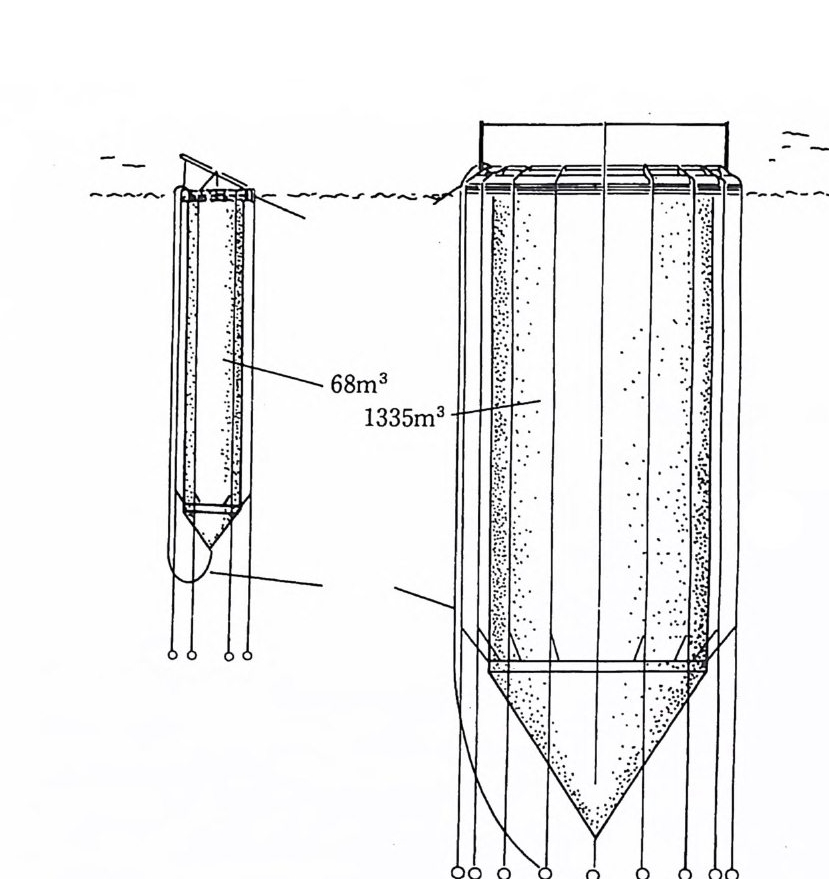 --~-`?^· f 8 m313 3 m 3 1-\:..:.l4、 1‘` ,정f.\`r:, · 5 一 _ . .건'. .....z.:..? ...E3·.:...” .• ...,... . . .· ' · 경 장 ' 선1홍g.v..., `F`42성첼5.1;· $ , • l--}~
--~-`?^· f 8 m313 3 m 3 1-\:..:.l4、 1‘` ,정f.\`r:, · 5 一 _ . .건'. .....z.:..? ...E3·.:...” .• ...,... . . .· ' · 경 장 ' 선1홍g.v..., `F`42성첼5.1;· $ , • l--}~
그림 13-4
Gamble, 1979). 선정된 탄화수소의 미생물 분해, 종속영양생물의 활동, 일차생산량, 동 • 식물플랑크톤의 개체군 측정 등이 감시되었다. 역시 모 의 생태계의 성분 중 가장 심하게 영향받은 것은 동물플랑크톤이었으며, 특히 석유 첨가의 결과로 가장 큰 영향을 받은 것은 동물플랑크톤의 난 (卵)과 발생단계였다. 미국 로드아일랜드대학의 해양생태계연구 실험실은 폐쇄생태계 enclos- · edecos y s t em 에서 표영성분과 저생성분의 양자를 고찰하도록 고안되었다 (Gi bs on and Gri ce , 1980) . 실험 에 서 는 플랑크론 군집 과 에 너 지 동태 , 그 리고 저생군집과 다양성에 대한 만성 석유오염의 영향이 측정되고 제어 생태계와 비교되었다. 이 계획의 추가적인 면은 표영서식지와 저생서식
지 사이에서 탄화수소 및 그 대사산물들의 생지화학적 순환을 감시하는 것이다. 비록 폐쇄생태계들이 오영 스트레스에 대한 개체군 및 군집의 반응을 예측함에 있어서 그 인공성 때문에 어느 정도 제한이 있지만, 다음 사항 들을 입증하는데 유용하다는 사실이 알려지고 있다. ® 제어된 오영 스트레스에 대한 여러 영양단계에서의 상대적 감수성. ® 생물군과 오영물질의 화학적 상호작용 및 생태계 내의 오염물질의 지 속성과 생지화학적 순환에서의 기대되는 경향. ® 오염 스트레스의 결과로서 에너지 흐름에서의 참재적 파괴. ® 오염 스트레스의 제거 후 생태계의 회복 참재력. 따라서 모의군집의 이용은 스트레스에 대한 개체생물의 반응을 이해하 는 이상의 차원을 마련해 주며, 기능적 생태계의 상황내에서 생물체 반 응을 확인 할 수 있게 해 준다. 13-5 개체군 동태에 있어서의 변화 오염물질 첨가와 개체군 동태에서의 변화 사이에 원인 관계를 정의하 는 것은 국단으로 어려울 뿐만 아니라 때로는 달성할 수 없는 것처럼 보 인다. 오염 스트레스에 대한 개체군의 반응은 일반적으로 비특정적이어 서 혼히 자연스럽게 나타나는 변이성이나 자연적인 환경 동요로 초래되 는 변화와 구별이 잘 되지 않는다. 생활폐수나 석유유출같은 특정 오염 물질에 의해 유발되는 급성영향은 나타나는 변화가 짧은 시간내에 현저 하기 때문에 쉽게 추적할 수가 있다. 그러나 많은 오염물질의 장기적인 유입과 환경파괴가 증가하는 데에서 기인하는 만성영향은 쉽사리 추적되 지 않는다 (Sanders et al., 1 980) . 오영영향에 대한 개체군의 변화를 연구함에 있어서는 다음의 사항들이 관심의 대상이 된다.
® 출현범위뿐만 아니라 효과적인 생식범위까지 고찰하는 개체 종의 수도 (abundance) 와 분포. ® 여러 세대와 세대를 확인하는 개체군 구조. ® 여러 세대 내에서의 개체 성장률 ® 다산성, 생식계철 및 개체군에 대한 새로운 개체의 가입량 등의 분석 울 포함하는 번식성공도 (re p roduc ti ve success). ® 병의 발생률. 개체군에 대한 이상과 같은 변수의 자연 변이성과 오염에 의한 변화성 의 비교를 위해서는 현존하는 비오염 서식지로부터 또는 오염상태가 진 행되는 과정으로부터 개체에 관한 적절한 기초자료를 필요로 한다. 상업 적으로 중요한 종은 분포, 생식 및 가입량 등에 관한 배후자료가 많이 있어서 당대의 연구와 함께 아주 유용하게 쓰인다. 그러나 많은 다른 종 에 대하여서는 이러한 자료가 존재하지 않고, 따라서 우리는 유사한 서 식지들(오영서식지 대 비오영서식지)은 개체군과 비교하지 않으면 안되며, 또는 오염구배에 따라 오염의 정도와 개체군의 차이룰 상호 연관시켜야 한다. 어느 경우에나 samp ling 전략은 개체군의 시간적 • 공간적 변화, 〈유사한〉 서식지로 정의되는 것들 중에서의 가능한 차이, 오염물질의 운 명과 영향, 그리고 측정된 영향의 의미 등이 고려되지 않으면 안 된다. 개체군 동태상에 있어서 개체 종들의 오염 유발성 변화의 평가는 개체 군에 대한 변수의 자연 변이성, 이 변이정에 대한 자연환경의 동요에서 오는 영향, 그리고 변이성에 대한 인위적, 자연발생적 동요 사이의 가능 한 상승작용 등에 대한 몇 개체 수준에서의 다른 감시기술과 아울러 개 체군 스트레스의 초기 경고 징후를 추적할 수 있고, 개체군과 군집내에 영구적 변화가 일어나기 전에 오염 저감방안이 마련될 수 있다. 13-6 군집 동태와 구조 군집이란 개체군들의 생물학적 상호작용, 그리고 개체군과 물리적 환
경과의 상호작용을 통해 구성되는 개체군들의 집단으로 정의된다. 군집 을 지배하는 물리적, 생물적 상태가 안정되고 예측 가능할 때, 군집은 수와 종조성에 있어서 매우 다양하며 비교적 안정하다. 오염물질아 환경 으로 첨가되는 것 같은 환경 동요로 군집은 스트레스를 받고 민감한 종 은 제거되며 다양성은 감소하고 기회적 종의 개체군이 증가한다. 개체군에서와 마찬가지로 오영 스트레스에 대한 군집 반응은 비특정적 이며, 급성 및 만성 오염에 다같이 나타날 수 있다. 급성 영향으로는 훼 손된 군집의 회복이 일련의 천이단계를 거쳐 기회종의 우점과 군집의 종 다양성을 시작으로 결국 다양하고 안정된 군집으로 재구성됨을 특칭으로 하며 만성영향은 한 군집의 회복 잠재력이 충분히 실현되지 않을 수도 있다. 또한 군집은 구조와 기능 단계에서 다같이 평가될 수도 있다. 구조적 특칭은 종조성, 수도 abundance, 영양상태, 생물량 및 다양성의 평가와 이들 평가의 시간적, 공간적 변화성이 포함된다. 종별 개체의 수도와 관 련되는 다양성 지수는 예컨대, Shannon-Wi en er Index 같은 것이며, 전 통적으로 군집의 비교에 이용되어 왔고 군집 구조의 장기변화를 지표하 는 데 유용하다. 그러나 〈건강한〉 군집을 예측함에 있어서 이들의 유용 성은 군집의 다른 특칭 때문에 자주 차단된다. 예컨대 1969 년 미국 매사 츄세츄주의 서 Falmouth 연안에서 발생한 제 2 연료유 유출사고에서 알 려진 바로는 개체군의 회복에 있어서 여러 개의 천이단계가 밀도 및 종 조성이 안정된 수준으로 회복되기에 앞서 높은 다양성 시기를 갖는 특칭 울 나타낸다. 따라서 단기 스트레스에 더 민감한 지표들과 함께 종 변화 성과 종 수도에서의 자연 동요와 관련되는 여타의 지표들도 다양성 지수 와 공동으로 사용되지 않으면 안 된다. 일단 오염 스트레스로부터 초래되는 변화들이 군집 수준에서 나타나고 확인 되었으면 개체 생물과 개체군의 적응 반응을 능가하는 것이지만, 군집 변화를 감시하는 일은 생태계의 적응 능력, 군집회복의 기간과 정 도의 지표를 마련해준다.
13-7 맺음말 환경에서 오염물질의 영향을 평가하는 것은 쉬운 일이 아니다. 그것은 생물 체제상의 각 수준에서의 적응적 및 파괴적 반웅들과 그 반응둘이 다음 수준에서 어떻게 영향을 미치는가에 대한 이해롤 필요로 한다. 표 표 13- 2 오염물질에 대한 해양생물의 반응단계 생물수준 반응상태 다음 단계에서의 영양 I 생화학적 및 세포 대사경로의 손상 에너지 동태상의 파괴 학적 단계 에너지 저장상의 감소 제독작용 개체의적웅 I 개체생물단계 대사변화 개체군 기능의 감소 행동변이 질병발생율의 증가 성장 및 생식울의 감소 질병방어 개체군의 조절과 적응 속도기능의 조정 매 개체군 단계 개체군 동태상의 변화 공존하는개체와 군집에 대한 영향 스트레스에 대한 군집단계에서의 무변화 개체군의 적응 IV 군집단계 종조성과종다양성에서 군집의 파괴 의 변화 이차생산량 감소 에너지 흐름에서의 군집의 다양성광 감소 안정성에서의 무변화 생태계 적응 자료 : Cap uz zo et al. , 1985
13-2 에서 볼 수 있는 바와 같이 모든 반응들이 자연상에서 파괴적인 것 은 아니며 체제상의 다음 수준에서 쇠퇴로 나타나는 것도 아니다 . 다시 말하면 현수준에서의 보상 또는 적응기작이 실패하기 시작할 때만 다음 수준에서 해로운 영향이 분명해지기 시작한다. 예측 목적을 위해서 우리 는 보상기작이 압도 당하기 전에 각 수준에서 스트레스의 초기 경고 칭 후를 알지 않으면 안 된다. 생화학적 수준으로부터 군집수준에 이르기까 지 체제가 갖는 복잡성의 정도, 유효한 보상기작의 수, 반응을 측정하기 위한 경과 시간 등이 기하급수로 증가하게 된다. 따라서 각 수준에서의 예측상의 난점 이 그만큼 증가한다. 현재 이용되고 있는 표준생물검정실험은 해양 생태계 내에서의 생물학 적 체제상 어떤 수준에서의 오염물질의 영향을 예측하기에 부적절하며, 해양환경에 대한 오염물질의 영향을 상세하고 체계적으로 평가하기 위해 서는 생물체제의 각 수준에서의 반응에 대한 지속적인 연구가 요망된다.
참고문헌 농수산부 ; 「농림 수산 통계 연보」, 1986. 박주석 ; 「적조 발생 상황의 변천과 대책」, 국립수산진홍원, 「적조현상과 어장 보전」, p. 7-17, 1987. 한국농촌경제연구원 ; 「연안 어장 목장화 계획 연구」, 1987. 환경처 ; 「해양 오염 방제」, 388 PP, 1987. 해양경찰대 ; 「시험 연구보」, 제 3 권, 298 PP, 1988. Anderson, A & W. Bis s ell ; Inte r natio n al Coo pe ratio n for the Preventio n of Mari ne Oil Polluti on , Univ . of Mi am i Sea Grant. Tech. Bull., No. 33, 1977. Anon ; Sea-bed dis p o sal. Safe aft er all? , Natu re , 266(5600) : p. 294-295, 1977. Austi n, B., J. Calomi ri s, J. Walker & R. Colwell ; Numeri ca l tax onomy and ecolog y of pet r ol eum- de g rad i ng bacte r i a, Ap pl. Envir o nm. Mi cr ob iol. , 22 : p. 225-266, 1977. Basth a , R. & R. At la s, The micr obio g y of aqu ati c oil spi lls, Adv. Ap pl. Mi cr obio l. , 22 : p. 225-266, 1977. Bert ran d, A. ; Les Pri nc i pa ux Acci de nts de Deversements Petr o lt e s en Mer et la Banqu e de Donnees de L 'ins tit u Francais du Petr ole sur !es Acci rlen ts de Navir e s (19 55-1979), Rev. d e L'ins tit ut Francaiz de Petr ol e, 34(3) : p. 483 -541, 1979. Bernhard, M. & A. Zatt er a ; Majo r po lluta n ts in the mari ne env iror unent, in
Pearson and Frang ipa ne (eds.), Mari ne Polluti on and Waste Dis po sal, Perga m on Press, Oxfo rd , p. 195-300, 1975. Bis h op, P. L. ; Mari ne Polluti on and Its contr o l, M cGraw- H il l, New York, p. 356, 1983. Bowen, V. ; Transusrani c e lements and nuclear waste s , Oceanus, 1 8 (1) : p. 4 2 -54 , 1979. Brown, D . A & T. R. Parsons ; Relati on ship betw een cyt op l a sm ic dis t r ibu ti on of mercury and tox ic effe c ts or zoop la nkto n and chum salmon exp os ed to mercury in a contr ol led ecosys t e m , J Fis h . Res. Bd. Can. , 3 5 : p. 880 -88 4, 1978. Butl e r, J., B. Morr is & T. Sleete r ; The fate of pe tr o leum in the ope n ocean. Sources, eff ec ts and Sin k s of h yd rocarbons in the Aq ua ti c eny ir o runent, Tlze Am. Inst. B io l . S ci ., p. 2 87-297, 1976. Capu z zo, J. M. , W. V: Bu rt, I . W. Duedall, P . K . Park & D. R. Keste r ; The im p a ct of waste dis p o sal in nearshore envir o runents , Vol. 6, Ne ars hore Waste D ispo sal, In : B. H. Ketc h um et a l. (eds). Waste s in the Oce an , Wi ley -Inte r scie n ce Pub!., New York, p. 5 34, 1985. Clark, JR. ; Coasta l Ecosy s tem Mana gem e nt . A Tec h nic a l Manual for the Conservatio n of Coasta l Zone Resources, Wi ley & Sons, New York, 1977. Clark, R. B. ; Mari ne Polluti on , Claredon Press, O xfo rd , p. 220, 1989. Clark, J. & W. Brownell ; Elec t ric P ower Plant in the Coasta l Zone : En vir o n- menta l Issues, Americ a n Littor al Soc iet y Spe ci al Publi ca ti on No. 7, High lands, N. J., 1973. Davi es , J. M . & J. C . Gamble ; Exp er i m ents wit h large enclosed ecosys t e m s, Phil. T rans. Roy. Soc. London, Serie s B, 256 : p. 523-544, 1979. Davi s, S. C. Gib b s & K. Pug h ; Qu anti tat iv e stu d ie s on marin e bio d g rad ati on of oil, Envir o n. Poll., 1 3 (3) : p. 203-215, 1977. Dunste r , H. ; Polluti on resultin g from the release of r adio a cti ve waste mate r - ial s to the sea, Mar. P oll. Bull., 9 (5) : p. 118-122, 1978. Dy er , R. ; Sea disp o sal of nuclear waste : a bri ef his t o r y , pre pa red for The Fonn on Nuclear Waste Mana gem ent : The Ocean Al tern ativ e, George
Washin g t on Univ ., Law Cente r , W ash., 1980. Edmond, T., G. Schaib e rge r & G. Gerba ; Dete c ti on of e nte r ovir u ses near deep marin e sewag e outf all s, Mar. Poll. Bull., p. 9(9) : 145-147, 1978. Elia s sen, R. & G. Tchobanogl o us ; Removal of n itro g en and ph osph orus from waste wate r , Envir on . Sci. Technol., 3 : p. 536-541, 1969. EPA ; Hawaii Sug a r Industry Waste Stu d y. San Franci sc o, Calif ., 106 pp, 1971. —— ; Wate r Quali ty Cri teri a . EPA-R 3-73-033, Washi ng ton , D. C., p. 594, 1972. Ep ple y, R. W., A. F. Carlucci , 0 . Holm-Hansen, D. Kiefe r, J.J. McCart hy & P. M. Wi lliam s ; Evid e nce for entr op h ica ti on in the sea near South e rn Califo rn ia coasta l sewage outf all s. Calif. Co-op . Oceanic . Fis h . Invest. Re p. 16, p. 74, 1972. Fay, J. ; Phys i c al pro cesses in the spr e ad of oil o n a wate r sur fac e. Proceed- ings of the Joi n t Confe re nce on Preventi on and Contr o l of Oil Spi lls. Amer. P etr o l. Inst., Wadh ing t on , p. 463-467, 1971 . Fis h er, R. J. ; Infl uen ce of Oxy ge n Concentr a ti on and of Its Diur nal Fluctu a- tion s on the Growt h of j uv enil e Coho Salmon, M. S. T hesis, Orego n Sta t e Univ ., Corvalli s, p . 48, 1963. Frib e rg, L. M., M . Pis c ato r , G. F. Nordberg & T. Kijell str om ; Cadmi um in the Envir JJ n ment, 2nd ed. Chem ica l Rubber Co., Cleveland, Oh io, p. 248, 1974. Gerlach, S. A. ; Mari ne Polluti on , Spr i n g e r -Verlag, New York, p. 218, 1981 . Gib s on, V & G. D. Gric e ; A comp ro m ise betw e en a beaker and a bay : the big bag . Oceanus, 1 3 : p. 21-25, 1980. Goldberg, E. ; The Oceans as a Chem ica l Sys t e m , in M. Hil l(ed .) , The Sea., Inte r sci en ce Publi sh ers, a div isi o n of J oh n Wi le y & Sons. Inc., New York, 1963. Goldberg, E. D. ; A Guid e to Mari ne Polluti on , Gorden & Breach Sci en ce Publi sh ers, New York, p. 168, 1972. Grosslin g , B. ; An estim ate of the amount of oil e nte r i ng the oceans, Sources, Eff ects and Sin k s or Hy dr ocarbons in the Aq ua ti c Env iro nment, the Americ an Instit ute of Bio l og ica l Scie n ces, p. 5-36, 1976. Guth rie, F. E. & J. J. Perr y (ed) ; Intr od ucatio n to Env iro nmenta l Tox ico logy ,
Elsevi er , New York, p. 484, 1980. Harvey, G. R., W. G., S te in h auer & J. M. Teal ; Polyc h lorin a te d bip h eny ls in Nort h Atl a ntic ocean wate r s, Sci en ce, 180 : p. 643-644, 1973. Hasler, A. D. & J. A. Larsen ; The hom ing salmo11, In : J.R. More (ed.), Oceanog ra ph y . Readin gs from Sci en ti fic Ameri can , Freeman, San Fran-cisc o, p. 252-256, 197 1. Heye r dahl, Tho! ; The Ra Exped it ion s, Doubleday and Co. Inc., G ardon Cit y, N. Y., 1971. Holl iste r , C . ; The seabed opt ion , Oceanus, 20(1) : p. 18-25, 1977. Hunte r , J ., T. Sabati no , R. Gomp er ts & M. , MacKenzie ; Contr ib u ti on of urban runoff to hyd rocarbon po lluti on , J Wat. P oll. Contr . Feder., 51(8) : p. 2129-2138, 1979. Hy la nd, J. & E. Schneid e r ; Petr ol eum hyd r ocarbons and the ir eff ec ts on mari ne orga n i sm s, po pu lati on s, communit ies , and ecosys t e m s, Sources, Eff ects and Sin k of Hy d rocarbons in the Aq ua ti c Envir o nment., The Ameri ca n Inti tute of Bio lo g ica l Sci en ces, p. 463-506, 1976. Hy ne s, H. B. N. ; The Bio lo g y of Pollute d Wate rs , Univ . of Toronto Press, p. 202, 1974. Jan nasch, H. W. & C. 0. Wi rse n ; Mi cro bia l life in the deep sea, Sci en ti fic Ameri ca, 236(6) : p. 42-52, 1977. Jer lov, N.G . ; Mari ne Optics, Elsevi er . Amste r dom, p. 231, 1976 Joh nsto n , R. ; Mari ne Polluti on , Academ ic Press, London, p. 729, 1976. Klein , I. ; Riv e r Polluti on . 3. Contr o l, Butt er wort h, Washi ng t on , D. C., p . 484, 1966. Krute n at, R. ; A pro p o sal for the per manent disp o sal of nuclear and oth e r tox ic waste s uti lizin g off sh ore tec hnolog y, Proc. Tenth Offs h ore Tech. Conf, Ameri can Instit ute of Mi ni n g , Meta ll urgc a l and pet ro leum En- ginee rs, rv, p. 2523-2528, 1978. Laws, E. A. ; Aq ua tic Polluti on , Wi ley - l nte r scie n ce, New York, p. 482, 1981 . Lo, S., J . Gil be rt & F. Hetr ick ; Sta b il it y of human ente r ovir u ses in estu a rin e and ma rine wate r s, Ap pl. Envir o n. Mi cro bio l. , 32(2) : p. 245-249, 1976.
Mart in, J.H. and G. A. Knauer ; The elementa l comp o sit ion of pla nkto n , Ge oc him . Comochim . Acta , 37 : p. 1639- 16 53, 1973. Mart in, R. G. ; PCBs-po lyc h lor ina te d bip h enyl s , S p o rt Fis h in g Insti tute Bulleti n No. 288, Sept ., P . 1-3, 1977. Mart in, ]. H. & W. W. Broenkow ; Cadm ium in pla nkto n : elevate d concentr a- tion s off Baja , Cali forn ia , Sc ien ce, 1 90 : p. 884-885, 1975. McInty re, A. D. & J. B. Pearce, (eds) . ; Bio l og ical Eff ec ts of Marin e Polluti on and the Problems of Mon itor i ng , Proceedin g s fro m ICES Works 神 held in Beaufo r t Nort h Carolina , 26 Febry uary- M arch 1979. Ra pp. p.-V . Reun. cons. int . Explo r. Mer, 179 : p. 1-346, 1980. Menard, H. & S. Sm ith ; Hy ps ometr y of ocean basin pro v inc es, Jou rn. Geop hy s i,ca l Research, 71 : p. 4305-4325, 1966. Menzel, D. W., E. M. Hulbu rt & J. H. Ry the r ; The eff ec ts of enr ich i ng Sar- ga sso Sea wate r on the pro dudti on and spe cie s comp o sit ion of ph y to- pla nkto n , Deep - Sea Res., 10 : p. 209-219, 1963. Metc a lf , T . ; Evaluati on of shellfis h san itar y qu ality by ind ica to r of sewage pol luti on , In A. Gameson (ed.) , D isch arge of Sewa g_e from Sea Outf alls , Perga m on Press, Oxfo rd , p. 75-84, 1975. Moor, M. N. ; Cy toc hem ica l dete r m ina ti on of cellular respo nses to evi ro n- menta l str e ssors in marin e orga n ism s, Rapp P.-V. Reun cons. int . Explo r. Mer., 179 : p. 7-15, 1980. Nati on al Academy of Sc ien ce ; Petr o leum in the Man·n e Envir o nment. W ash in- gton , D. C., 107 pp, 1975. Odum, E. P. ; Fundermenta ls of Ecology (3rd ed), Saunders, Ph ila dellph ia, p. 574, 1971 . ParsonPsr,o cTe.s sRe.s, (M3r.d Teadk.),a hPaesrhg ia, maon nd PBr.e sHs, aOrgxr fao vr de , ; pB. i3 o 3lo0 g, i1c9a8l 4.O ceana/gra ph ic Payn e , J. F. ; Fie l d evaluati on of benzo pyren e hy d roxy la se ind ucti on as a mon itor for mari ne po lluti on , Sc ien ce, 191 : p. 945-946, 1976. Pic k eri ng , Q. H. & C. Henderson ; The acute tox ic ity of some heavy ni~at a l s to differ ent spe cies of warm wate r fish es, Int. ]. Ai r-w ate r Pollut., I O : p.
453-463, 1966. Pik e , E. B. & A. L. H. Gameson ; Wate r Polluti on Contr o l, 6 9 : p. 355, 1970. Poldervaart , A. ; Chemi stry of the Eart h ' s Crust, Geolog ical Socie t y of Amer- ica . Spe c i al Pape r 62. Crust of the Eart h, A Sym po siu m , p. 121, 1955. Prosser, L. ; Perspe c ti ve s of a dap tation : the oretic a l aspe c ts . In : D. B. Dil l, E. F. Adolph , and C. G. Wi lb er (eds.), Ad apto.tion to the Envir o nment (Ha nd- book _of Phys iolo g y, Sectio n 4), Amer. P hys o l. Soc. Washin g t on , D. C., P. 11-25, 1964. Ratc l if fe, D. A. ; Chang es att ribu ta b le to pes tic ide s in egg breakage freq u ency and egg sh ell thick ness in some Briti sh bird s, J Ap pl. Ecol., 7 : p. 67-107, 1970. Ray, S. & J. Coff in ; Ecolog ical eff ec ts of cadm ium po lluti on in the aqu atic envi ro nment : a revi ew , Fis h eri es and Mari ne Servic e Technic a l Re p. No. 743, Canadia n Dep t. of Fis h eri es and the Env iro nrn. Halif ax , Nova Scoti a, p. 18, 1977. Read, A. & A. Blackman ; Oi ly wate r dis c harge s from off sh ore Nort h Sea Insta l lati on . ape r spe c ti ve , Mar. Poll. B ull., 11(2) : p. 44-47, 1980. Rice , S., A . Moles, T. Ty lo r, & J. Kari ne n ; Sensiti vity of 39 Alaskan marin e spe c ie s to Cook Inlet crude oil and No. 2 fue l oil, Proc. of the 1979 Oil Spi ll Confe re nce, Los Ange l es, Amer. Petr ol . Inst., p. 549- 55 4, 1979. Riley , J. P. and R. Cheste r , Intr o ductio n to Mari ne Chemis try, Academ ic Press, New York, p. 465. Ross, D . ; Intr o ducti on to Oceanog ra p h y, Prenci ce -Hall, Inc., E ng le wood Cli ffs, N. J, 1977. Ry an , P. R. ; The comp o siti on of o il- a guide for readers, Oceanus, 20(4) : p. 4, 1977. Ry the r, J. H. ; Photo s yn the sis a nd fish pro ducti on in the sea, Sci en ce, 166 : p. 72-76, 1969. Ry the r, J. H, & W. M. Dunsta n ; Ni trog e n , ph osph orus, and eutr op h ica ti on in the coasta l mari ne env iro runent, Sci en ce, 171 : p. 1008-1013, 1971 . Salis b u ry, F. B. & C. W . Ross ; Plant phy s iolo gy (3rd ed) ., Wadsworh Pub!.
Co., Belmort , p. 540, 1985. Sanders, H . L., J . F. qra ssle, G . R. Hamp so n, L. S. Morse, S. Garner-Pric e & C. C. Jon es ; Anato m y of an oil s pi ll : long -ter m eff ec ts from the grou nd- ing of the barge Florid a off West Falmouth , Massachusett s, J Mar. Res., 38 : p. 265-380, 1980. Scarp ino , P. ; Hwnan ente r ic vir u ses and bacte r io p h a g es as ind ic a to r s of sewag e pol luti on , In A. Gameson (ed.) , D isc harge of Sewa ge fro m Sea Outf alls , Perga m on Press, O xfo r d. p. 49-6 1 , 1975. Sin d ennann, C. J. ; The use of pat h o log ica l eff ec ts of pol luta n ts in mari ne envir o runenta l monit or in g po rgr am s, Ra pp. p.- V . Reun cons, int . Exp/o r. Me r., 179 : p. 129-134, 1980. Sp ra gu e, J. B. & D. W. Mi lee se ; Differ ent tox ic mechan ism s in kraft pul p mill eff lue nt for two aq u ati c an im als, Wete r Res., 2 : p. 761- 76 5, 1968. Ste g e man., J. J. ; Infl ue nce of env iro runenta l conta m ina ti on of cyt oc hrom p -450 mixe d-fu n cti on oxyg e nases in fish : im p lica ti on s of recovery in the Wi ld Harbor marsh, J Fis h. Res. Bd. Can., 35 : p. 668-674, 1978. Tait , R . V. ; Elements of Mari ne Ecology (3rd ed.) , Butt er wort h, London, p. 356, 1981 . Thacher, P. & M. Meit h-A vci n ; The Oceans, Health and Prog no sis , in Eli sa beth Borge se and Nort on Gin s burg (eds.), Ocean Yearbook I, Un iv. of Chic a g o Press, P. 293-339, 1978. U. S. Government Prin t i ng Of fice ; Coast Guard's Resource Needs for Re spo nd- ing to Oil s pills , Hearin g befo r e the Subcom mittee of the Com mittee on Ap pro p ri a t i on s of the Un ited Sta t e Senta t e , 1978. U.S . Nati on al Academy of Scie n ces ; Mari ne Env iro nmenta l Quali ty , Su gges te d ressarch pro g ra ms for understa n din g man 's effe cts on the oceans, 107 pp. Washin g ton , D. C., 197 1. U.S. Nati on al Academy of Sc ien ces ; The Inte r natio n al Mussel Watc h . Re po rt of the Workshop Spo n sored by the Envir o nmenta l Research Coundl, p. 77, Washin g ton , D. C., 1 980. Vaug h n, J. ; Hwnan vir u ses as mari ne po lluta n ts , Oceanus, 18(1) : p. 24-28,
1974. Vemberg, F. J ., A . Calabrese, F. P. Thurberg & W. B. Vemberg (eds.) ; Plzy s io lo ,흉. cal Res po nses of Mari ne Bio ta to Polluta n ts , Academi c Press, New York, p. 462, 1977. Waldic h uk, M. ; Some wate r po lluti on pro blems connecte d with the dis p o sal of pul p mill waste s , Can. Fis h . Cultu rist., 31 : p. 3-34, 1962. Warren, C. E. ; Bio lo g y and Wate r Polluti on Contr o l, W. B. Sanunders, Ph ilad elph ia, p . 434, 1971 . Warren, C. E. & G. E. Davi s ; Laborato r y stu d ie s in the fee din g , bio e nerge t i cs , and grow th of f ish , In the Bio lo gi ,ca l Bas is of Frsehwate r Fih Productio n , S. D. Gerkin g , ed., p . 175-214, Oxfo rd , Blackwell Publi ca ti on s, 1967. Weib e l, S.R. ; Urban drain a g e as a fac to r in eutr op h ic a tio n , in Eutr op hi c a - tion , Causes, Consequ e nces, Correcti ves , Nati on al Academy of Sci en ces, Wash ington , D.C. , p. 383-4 03 , 1969. Wi lbe r, C. G. ; The Bio lo gi ,ca l Asp e cts of Wate r Polluti on , C. C. Thoman, S p ing - field , I II., p. 296, 1969. Wolfe , D.A . (ed.) ; Fate and Eff ects of Petr o leum Hy d rocarbons in Mari ne Ecosy st em and Orga n is ms, Perga m on Press, Oxfo rd , p. 478, 1977. Woodwell, G. M., C. F. Wurste r & P. A . Isaacson ; DDT resid u es in an east coast estu a ry : a case of b10!og ica l concentr a ti on of per sis t e n t in- sectic ide , Sci enc e, 156 : p. 821-824, 1967.
찾아보기 금속농도 138 기 금속 치 오닌 meta l loth ion ein 150 Garroch 하구 127-128 금속 치 오닌 단백 질 meta l loth ion ein 가자미 145, 279 pro te i n 275 감마 방사선 y-ra dia t i on 224, 229, 기름속 물 에멀션 wate r -in - oil -e muls- 230 ion 210 감마 핵소클로로사이클로핵산 r-he x-기름 슬릭 oil slic k 204 ochlorocyc l ohexane 172 기름의 조성 193 검정 개체군 tes t po p u lati on 85 기수성 brackis h 45 격납용기 conta i n m ent vessel 239 길항적 105 계면활성제 212 고리 원자력발전소 260 L 고영성 hyp e rsali ne 45 나프탈렌 nap h ta l ena 191 골 tro ug h 34 나프탈렌 붕괴 215 과염화에틸렌 170 낙조류 ebb tide 37 광양만 270 남조류 blue-gr ee n alga 60, 82 광화학적 산화 208 납 Pb 89, 153, 266 구리 Cu 89, 152, 265 내만 국지성 단기적조 268 구연산염 96 내한성 생물 57 국제방사선보호위원회 232 냉각수 241 국제해양오영회의 15 뉴욕만 113, 127 굴 165 뉴턴의 법칙 36 규소순환 53 능동 수송계 acti ve tran spo rt sys t e m 규산염 268 138 규조류 dia t o m 59, 85 규조연니 diat o m aceous ooze 39, 59 c: 그람음성 118 다량 영 양소 macro-nutr ien t 82 급성독성 90 di a t om( 규조류) 59
다환성 지방족 화합물 194 단종배 양 monocultu re 85 단층대 fau lt zone 25 당 인산염 sug a r pho sph ate 82 대구(어류) 144 대륙붕 24 대륙봉 되적물 42 대륙사면 24 대륙융기부 24 대륙주변부 24 대양분지저 24 대양산령 23 대양의 가스 함량 46 대양의 면적 22 대양의 수심 22 대양의 체적 22 대 양저 산맥 ocean ic rise 24 대 장균군 coli -form grou p 118 대조(大潮) sp ring tide 37 대형동물상 macrofa u na 125 데트리터스 detr itus 67 데트리터스 먹이연쇄 detr itus foo d chain 67 독립 영 양 박테 리 아 auto t r op h ic bac- ter i a 61 독립 영 양생물 auto t r op h 66 독성물질 164-166 독성측정 93-99
두족류 152 DDE 91, 171 DDT 14, 89-91, 171-182 DDT 잔류량 75 디 엘드린 deie l drin 89, 170 디클로에탄 169 dps ; disin t e g r at i on s per second 229 E: rad ; radi at io n absorbed dose 229 rem ; roentg en equ i v a lent man 2 31 Le ptos p ira 116 렙토스피라 감염증 lept os pi ro sis 116 Loch Ewe 281 LOT 기법 187 뢴트겐 roentg e n 229 루테늄 Ru 232 리버풀만 127 리소좀 lys o some 275, 276 린덴 lind ane 170, 172 口 마그네슘 Mg 83 마루 crest 34 마리아나해구 Mari an a Trench 25 My ca bacte r iu m (장병 원균) 116 Makair a i nd i ca( 어류) 153 만성독성 90
만성억압 91 망간단괴 mang an ese nodule 39 망초 salt c ake 235 매립피해현황 257-259 mercuric sulph a te 147 mercu ry selen ide 146 mercuric chlorid e 147 먹이망 72-74 먹 아 연쇄 foo d chain 63 먹이연쇄상의 수은 농도 139 Mega n yc t ip h anes norve gica (유 우 파 우 시아류) 149 메르캅탄 mercap tan 10s 메탄 meth a ne 190 메 탄생 성 meth a nog e nesis 113 메 틸수은 meth yl mercu ry 142, 146 -147 meth yl mercu ry 147 메 틸 메르캅탄 meth yi mercap tan 166 메틸스크로핵산 190 메틸화 박테리아 147 모의 제 어조건 sim ulate d contr ol led co-ndit ion 274 무기 퇴 적 물 ino rga n ic dep o sits 39 무산소탈질소법 anaerobic den itri- fica ti on 135 문화적 부영 양화 cultu ral eutr op h ic a-
tion 69, 12s 물속 기름 에멀션 oil -in- wate r emu!-sio n 209 물수리 146 물의 구조 25 물의 열성질 27 물입자운동 34 미 고결 되 적 물 Unsolid a te d sedim ent 40 미 나마따병 Mi na mata dise ase 146 -147 미 량영 양소 micr o-nutr ien t 82 밀도 28 밀도성충 densit y str at i fica ti on 29 1::1 Barnege t 만 93 바다오리 146 바닷가재 유생 165-166 viny l chlori de 147 바이러스 viru s 119 반감기 225-227 발라스트 ballast 187 발틱해 145 방사능 낙진 234 방사능 폐기물의 분산 244 방사능 폐기물의 영구두기 245 방사능 폐기물의 저장 245
방사능 폐기물의 지질학적 저장 246 방사능 폐기물의 해저두기 248 방사선 붕괴 223 방사선량 229 방사선 핵종 232 방사성 폐기물 15 방오페인트 152 방향족 화합물의 붕괴 214- 21 5 백파 whit e cap 35 버개쓰 bag a sse 168 버뮤다 라이스 Bermuda Ris e 24 베타 방사선 fl-ra di at i on 224, 230 8- 입자 225, 228 벤젠 benzene 191 벤젠 핵사클로로라이드 benzen hexa- chlorori de 172 벤조피렌 3, 4-benzop yren e 194 변위수 dis p l a cement wate r 200 병원생물 115 병원체 지표생물 117 보론 B 239 보상수십 comp en sati on dep th so 복족류 152 부영 양화 eutr op hica ti on 69 부유물질 suspe nd id soli d: SS 163 부유성 고형물질 48 분변계 연쇄상구균 119, 122 분쇄 파 brea.k in g wave 35
분해 자 decomp o ser 68 바닐 염화물 169 Vib r i o ( 비브리오균) 116 BHC 172 Beer-Lambert 법 칙 56 비열 27 비 정 상상태 non-s t e a dy sta t e 70 비타민 B12 137 빛 30, 56 人 사구 dune 4o 사염화탄소 170 산소감소 oxy ge n sag 159 산소감소곡선 oxy ge n sag curve 159 산소국소층 oxy ge n minim um lay e r 47 산소결핍 134 Santa Cata l i na Island 113 San Jos e 114 산화촉진연못 oxid a ti on po nd 166 Salmonella 115, 119 살충제 . 171, 181 삼각주 delta 42 삼수여 과법 trick lin g filter sts tem 132 삼영화에탄 170 삼염화에틸렌 170
삼차육식 동물 ter t iar y carn ivo re 66 3 차 처리 133, 136 상 대 생 체 유 효 율 relati ve bio l og ica l eff ec ti ve ness: RBE 2 30 상첨 가효과 sup ra -add itive int e r ac- tion 106 Sarga s sum (갈조류) 78 쌍편모조류 dino fl ag e llate 59, 78 새 180-182 생물기원 퇴적물 bio g e nous sed im ent 38 생물분해 211-216 생 물축적 bio a ccumulati on 89 생물학적 정량검정 bio a ssay tes t 85 생 물학적 확대 bio l og ica l mag nifica - tion 75 생 산수 pro duc tion wate r 200 생식먹이연쇄 graz in g foo d chain 67 생 태 효 율 ecolog ica l eff icien cy 67, 71 생화학적 산소요구량 Bio c hem ica l oxy ge n demand: BOD 109-111, 157-160, 253 석유산물의 특칭 192 석유의 광화학적 산화 209 석유의 미 생물 분해 211 석유의 분해기작 212 석유의 영향 196-199
석유의 용해작용 209 석유의 증발 206 석유의 치사효과 195 석유의 타르형성 210 석유의 되적작용 210 석유의 특칭 192 석유의 풍화 205 석유탄화수소의 추정량 185 석호(潟湖) lag o on 41 세계보건기구 WHO 148 소광계수 exti nc ti on coeff icie n t 56 소조 (小潮) neap tide 37 소형동물상 meio f a u na 125 수권의 질량 23 수도 abundance 64 수소결합 26 수소이온 농도 pH 262 수온약충 the rmoclin e ·28 Hg 수은 14, 89 수은농도 139 수은 소비량 140 수은의 최대 허용량 148 수은 화합물 142 수용확산 pas siv e diffus io n 138 순생 산량 net pro ducti on so 순화 99 숨은 열 late n t heat 27 Shig el la (병 원균) 116
스럿지 slud ge 132 Scrobic u lari a pla na 156 Spa r tz ·n a (해 양초본류) 60 시추니 201 시토크롬 P-450 Cy toc hrom P-450 275 시크로알칸 cyc l oalkane 191 식 물 플 랑 크 톤 ph y top la nkto n 78, 178-179 신경독소 neuroto x in 78 십 해 계 deep -s ea sys t e m 5 5 심해분지 23 심해순환 33 심 해 평 원 aby ss al pla in 24 십각류 152 。 아데 닐 에 너 지 충전 adenulate energy charge : AEC 276 아르고 머 천트호 the Argo Merchant 186 아모코 가디 즈호 the Amoco Cadiz 186-187,198 aceta ld ehy de 147 아연 Zn 89, 266 아천해 대 subli ttor al zone 55 아치 사 subleth a l 90 Acmaea d igita l is(삿갓조개) 156
아황산펌프법 162 알칸 alkane 190 알칸의 붕괴 213 알파 방사선 a-radia t i on 224, 230 a- 입자 224, 228 암모니 아 스트리 핑 법 ammon ia str ip -ping 135 압력 57 앨 드 린-목 사 펜 류 aldri n- to xap h ene grou p 172 어류 198 Irvin e 만 125 엄 정 첨 가효과 str ict l y addit ive int e r- acti on 106 에너지 수지 energy budg et 277 에멀션화작용 209 에탄 eth a ne 190 x- 방사선 229 endosulph an 177 Endoamoeba h ist oli ca( 원생동물) 116 연니 ooze 39 연료봉 239, 242 연료 재처리 241 연 안구 long sh ore trou g h 40 연안만 coasta l bay 41 연안수질 261-262 연안수질등급 254 연 안사주 long sh ore bar 40
연안퇴적물 40 연안환경 평가 조사정점 계 획 Coasta l Envir o nmenta l Assessment Sta t i on Prog ram : CEAS 2so 연어 165 연해석유탐사 186 염 salt 84 영분 45, 57 영수쐐기 salt wedg e 41 영 양단계 trop hic level 66 영 양소 nutr ien t 51, 266-268 영양원소 강화실험 nutr ien t enric h- ment exp er im ent 85 O:N rati o 278 오우얼라이트 ooli te 51 Octo p u s vulg a ri s (문어 ) 15 2 온도 57 의빈 off -s hore 41 온도내성대 99 온도충격 the rmal shock 93 온배수 260 온산만 269 의만 확대성 장기적조 268 용존가스 dis s olved ga s 46 용존산소 Diss olved oxyg e n 263 용존유기물질 163 용존인산염 51 용해작용 209
우라늄 237-239 우주선 cosm ic ray 234 울산만 268 원양퇴적물 pe lag ic sedim ent 38 원유의 부분분리 192 원자로 235 원자에너지 이용 221 원자 핵 222 윈드 • 스케일 공장 244 유류오영 270 유리 화 vitrifica ti on 247 유영 동물 nekto n 59 유조선 사고 186 유조선 조업 187 육성 퇴 적 물 ter r ige nous sed im ent 39 이극성(二極性) 26 이 따 이-이 따 이 병 itai - i t ai dis e ase 151-152 이미터 em itter 231 이 차생 산 secondary pro ducti on 66 이 차 육식 동물 secondary carn ivo re 66 이차처리 132 E. coli (대 장균) 116 인 pho sph o rus 82, 85 인산염 267 인의 순환 51 인의 제거 134
인체 렌트겐 당량 231 인체 장 바이러스 ente r ov iru s 119 일차생산자 prima ry pro ducer 77 일차 스릿지 132 일 차 육 식 동 물 prim ary carn ivo re 66 일차 처리시설 131 일치동물 con for mer _102 임 계 수십 cri tica l dep th so 입사광 77 x: 자가오염 259 자생되적물 auth ige n ic sed im ent 39 자연방사능 234 자유 라디 칼 free radic a l .22 9 자정능력 (작용) self -pu rif ica ti on 18, 125 잡식동물 om nivo re 72 장바이러병 120, 123 장변원생물 117 재폭기 reaerati on 108 저생생물 benth o s 60, 198 저 생 조류 benth ic alga e 77 저 생 환경 benth ic env iro runent 55 저 탁류 turbi d ity current 24 적조 red tide 78, 130-131, 268-270 적조 원인종 269
전빈 for e shore 40 전자 electr on 223 전자 수용체 electr on accep tor 107 정 부간 해 양위 원회 Inte r go vernmenta l Oceang rap hic Com miss io n 18 제어생태계 오영실험 Contr ol led Eco-sy st e m Polluti on Exp e rim ent: CEPEX 2a1 조 건 적 형 기 성 세 균 fac ulta t i ve anaerobes 107 조류 37 조석 36 조석 파 tida l wave 35 조절동물 regu la to r 102 종 다양성 124 종 속 영 양 박 테 리 아 hete r otr op h ic bacte r ia 61, 107 종속 영 양생 물 hete r otr op h 66 zoop l ankto n (동물플랑크톤) 58 중성부력 neutr al buoy a ncy 57 중 성 자 방 사 화 neutr on acti va ti on 241 Jun cus (해 양초본류) 60 중크롬산염 112 지 열화도 vent 141 지진해파 seis mic sea wave 35 지표생물 117 전광충 eup h oti c zone 78
진동만 268 진주만 270 진해만 268 질소 Nit rog e n 82, 85 질소의 순환 52, 267 질소의 재거 135 질소화작용 nitrifica ti on 52 창조* 류 floo d current 37 챌 린 저 호 탐사 Challeng e r Exp ed i- tion 54 천해대 littor al zone 55 철 156, 266 체류시간 resid e nce time 50 초우라늄 원소 241, 242 총 암모니아 농도 104 총 유 기 탄 소 tot a l orga n i c carbon 113 최 저 유 효 농 도 thres hold concentr a- tion 95 치사억압 91 치오닌 thion ein 150 구 Kanehoe 만 129 카드뮴 89, 148, 266 카드뮴 독성 1:;o
코리을리 효과 Cori oli s e ff ec t 32 coccolith o ph o re (코콜리 드류) 59 구 立 쿠 人타놀 cop ro sta n oi 121 콜리파아지 coli ~p h age 119 큐리 Ci 229 Crassostr ea virg in i c a (굴) 142 크래프트 펄프법 162, 164- 1 65 크롬산염 112 클로로필 chlorop h yl l 82-83 Clostr idi u ,n (병 원균) 115 Clostr idi u m botu li na (병 원균) 115 드 타르 덩어리 형성 210 탁월풍 pre vaili n g wind 33 탄산염 순환과정 50 목사펜 tox aph ene 172 톨루엔 tol uene 191 두명 도 Transpa rency 263 템즈강 127 퇴적작용 210 titan i um diox id e (Ti0 2 ) 13, 156 고 파랑 34 파랑열 wave trai n s 34 Pas tu re/la( 장병원균) 116 Phaeodacty lu m (규조류) 1, ,
Phaeo cys tis(규조류) 127 Ph yt o p lank t on( 식 물플랑크론) 58, 78 Falmouth 연안 285 펄핑 pul pi ng 161 펜안트렌 phe nanth ren e 194 펜타클로로산나트륨 165 펜타클로로페놀 165, 201 평균치사농도 96 평 균치 사시 간 med ian leth a l tim e 94 포스포리피드 pho sph o li pid s2 포식 자 pre dato r 58 표영환경 pel ag ic env iro nment 54 표준실험실 검정기법 sta n dard labo- rato r y bio a ssay tec h niqu e 273 표충해류 30 푸로판 pro p a ne 190 프레온 화합물 170 플랑크돈 59 플랑크톤의 평균금속농도 138 플루토늄 235 피복 cladd ing 239 PCB 89, 170- 17 4, 175- 18 2 궁 하구 estu a ry 41 하첨 가효과 infra- add itive int e r acti on 106
할로겐화 탄화수소 89, 169-182 해구 tre nch 24 해 빈 beaches 40 해수이동 58 해수의 조성 43 해수의 pH 49 해수의 환경기준 252 해수 중의 미량원소 44 해수중의 주요 원소 43 해식절벽 sea clif f 40 해 양동향계 획 Ocean Pulse Prog ram 280 해 양박테 리 아 mari ne bacte r ia 61 해양오영(정의) 18 해양의 순환 30 해양되적물 38 해양포유류 199 해운 186 해일파 tsu nam i 35 해저산 seamount 24 해저 협곡 24 핵 붕괴속도 226 핵실험금지조약 235 HCH 172 헤모글로빈 haemog lo bin 137 헤모시아닌 haemocya n in 137 해 태로고리 화합물 hete r ocy cl ic com- po und 194
헵타클로르 172 형기성 세균 anaerobes 107 형오성 점액균류 164 호기성 세균 aerobes 107 혼합기 능 산소화효소 mixe d func ti on oxyg e nase: MFO 274-275 혼합충 mixe d-laye r so Hormarus ga mmarus( 바닷가제) 152 홍합 155 홍합감시 계 획 Mussel Watc h Pro- gram 280
화학적 산소요구량 Chem ica l Oxy ge n Demand: C OD 111-113, 159-160, 265 화학적 요인 58 활성 스릿 지 법 acti va te d sludge sys t e m 132 황갈색 조류 chry so p h yt a 59 후빈 backshore 40 휴면포자 restin g spr o e 81 휴조 (休潮) slack wate r 37
심재형 서울출생 서울대학교 문리과대학 식물학과 졸업 캐나다 브리티쉬 컬럼비아대학교 이학박사(생물해양학) 현재 서울대학교 자연과학대학 해양학과 교수 한국해양학회 회장 주요논문 「한국 동남해 역의 플랑크돈 연구」 의 60 여 편 해양오염과 생태계 대우학술총서 • 자연과학 70 찍은날 • 1991 년 4 월 10 일 펴낸날 • 1991 년 4 월 20 일 지은이•십재형 펴낸이·朴孟浩 펴낸곳•民音社 출판등록 1966. 5. 19 제 1-142 호 은행 지로번호 3007783 우편대체번호 010041-31-0523282 135-120 서울 강남구 신사동 506, 강남출판문화센터 5 층 515-2000~2 (영 업부) 515-2003~5 (편집부) 515-2007( 팩시밀리) © 심재형, 1991 자연과학 • 해양생물학 KE:/477.3 Pri nt e d in Seoul, Korea 값 9,500 원
대우학술총서 자연과학 l 소립자와 게이지 상호작용 김진의 • 2 동력학특론 이병호 3 질소고정 송승달 4 相轉移와 임계현상 김두칠 5 촉매작용 진종식 6 외스바우어 분광학 옥항남 7 극미량원소의 영양 승정자 8 수소화붕소와 유기붕소화합물 윤능인 9 항생물질의 전합성 강석구 10 국소적형태의 Aliy a h- S in g er 지표이론 자동표 11 Muco po l y sacchar i des 의 생화학 및 생물리학 박준우 12 천체물리학 홍승수 13 프로스타굴라딘 합성 김성각 14 천연물화학 연구법 우원식 15 脂防營養 김숙회 16 결정화유리 김병호 17 고분자의 화학반응 조의잔 18 과학혁명 김영식 19 한국지질론 장기홍 20 정보이론 한영열 21 원자핵반응론 정운혁 22 파괴역학 김상철 23 분자궤도이론 이익춘 24 반응속도론 정경훈 25 미분위상수학 이현구 26 磁器共鳴방법 조성호 27 풀라스마을리학과 핵융합 최덕인 28 천문관측과 문석 이시우 29 석탄에너지 변환 기술 김상돈 30 해양微古生物學 백광호 31 편미분 방정식론 김종식 32 대통일이론 소광섭 33 금속전자계의 다체이론 김덕주 34 액정중합체 진정일 35 복합재료 권숙인 36 단백질 생합성 박인원 37 한국의 광물종 김수진 38 일반상대론 이철훈 39 레이저 광산란 분 광학 김종진 40 복소다양체론 김상문 41 疾學的 연구방법 김일순 42 핵구조물리학 민동필 43 후리에 해석과 의미분 작용소 김도한 44 한국의 고생을 이하영 45 질량분석학 김명수 46 급변론 박대현 47 생체에너지 주충노 48 리이만 기하학 박을용 49 群표현론 박승안 50 비선형 편미분 방정식론 하기식 51 생체막 김형만 52 수리분류학고철환 53 찰스 다윈 정용재 54 금속부식 박용수 55 양자광학 아상수 56 효소반응 속도론 서정헌 57 화성암 성인론 이민성 58 확률론 구자홍 59 분자 분광학 소현수 60 벡터속이론 양재현 61 곤충신경생리학 부경생 62 에너지띠이론 모혜정 63 수학기초른 김상문 64 신경과학 박찬웅 • 김승업 65 BCH 부호와 Reed · Solomon 부호 이만영 66 양자전기역학 김영덕