 김형만
김형만  김형만
김형만
저자는 서울대학교 문리과대학 화학과를 졸업하고 예일대학을 거쳐 크라크대학에서 물리화학분야로 이학박사학위를취득한후 위스컨신대학에서 연구원과 교수직을 역임하였다. 귀국후국방과학연구소 책임연구원으로 근무하였고 현재는 한국과학기술원 생물공학과 교수로 재직중이다 . 용액 내에서의 확산과, 초원심분리법과생체막에 대한다수의 논문을발표하였다.
 生體膜
生體膜
 生體膜
生體膜
책 머리에 세포를 둘러싸고 있는 원형질막의 존재는 세포설이 제창된 19 세기 중 엽에 이미 가정이 되었었지만 이것이 확인된 것은 약 100 년 후 주로 전 자현미경의 발전에 의한 것이었다. 전자현미경을 통한 연구로 세포에는 원형질막뿐만 아니라 그 내부에 광범위한 막 조직이 존재하는 것을 알게 되었고 무수한 세포기능이 이들 생체막에서 이루어지는 것이 발견되었 다. 그러나 이러한 광범위한 기능들이 생체막의 어떠한 분자구조에 의해서 이루어지느냐 하는 문제는 대부분의 경우 아칙도 해결이 되지 않았으며 현재 대단히 활발한 연구가 진행되고 있다. 생체막의 구조로서 가장 많 이 인용되고 있는 것은 S i n g er 와 N ic holson 이 제 안한 유체 mosa i c model 로 지방질 이분자층이 생체막 구조의 기본적인 바탕을 이루고 이 이분자 층 내부에 그 일부가 파묻혀 있거나 이분자층 표면에 부착되어 있는 단 백질이 막기능을 부여하는 것이다. 그러나 수용성 단백질과는 달라 막에 묻혀 있는 단백질은 그의 분리정 제가 힘들고 그의 기능에 막이라는 특이한 환경이 필요한 것이어서 구조 와 기능과의 관계에 대한 연구가 대단히 어려웠었다. 근래에 와서 세탁 제에 의한 생체막 단백질의 용해정제 방법이 개선되고 또 model 막에 이 둘을 재구성시키는 기술의 발전과 2 차원적결정의 전자현미경에 의한 정 확한 구조결정방법이 개선되고 여러가지 분광학적 방법을 이용함으로써 생체막의 연구는 급진적인 발전을 가져오고 있다. 그래서 생체막에 대한 우리의 개념은 아직도 유동적이어서 새로운 사실의 발견과 함께 그 개념 도 급속히 변화하고 있다. 이 책은 지난 6 년간에 걸쳐 한국과학기술원에서 대학원 학생들을 대상 으로 한 강의 내용을 정리한 것이다. 이 강의는 생체막의 생화학적인 측
연보다는 그 구조적인 면을 강조하였다. 이 분야가 유동적이기 때문에 강의 내용을 매년 수정했어야 했고 이 때문에 이 책의 작성이 힘들었으 며 앞으로도 자주 수정이 필요하다고 생각된다. 끝으로 이 책의 작성에 많은 도움을 준 한국과학기술원 생체막연구실 학 생들에게 감사의 뜻을 표한다. 1987 년 12 월 김 형 만
生體膜――차례
책 머리에 ―― 5 제 1 장 생체막의 분포와 화학적인 성분 • 11 1.1 생체막의 분포 ―― 14 1.1.1 원형질막(Plasma membrane) ―― 14 1.1.2 핵막(Nuclear envelope) ―― 22 1.1.3 소포체(Endoplasmic reticulum) ―― 25 1.1.4 Golgi체 ―― 26 1.1.5 Mitochondria ―― 28 1.1.6 엽록체(Chloroplast) ―― 29 1.1.7 기타생체막 ―― 29 1.2 생체막의 화학적인 성분 ――33 1.2.1 생체막의 분리 ―― 33 1.2.2 지방질 ―― 34 1.2.3 단백질 ―― 45 1.2.4 당분 ―― 50 제 2 장 Liposome • 52 2.1 소수성도(Hydrophbicity) ―― 52 2.2 Micelle ―― 562.3 Liposome의 형성 ―― 63 2.4 Liposome의 물리적 성질 ―― 70 2.4.1 두께(Thickness) 70 2.4.2 상 전이 (phase transition) ―― 72 2.4.3 상 분리 (phase separation) ―― 79 2.4.4 Cholesterol의 영향 ―― 81 2.4.5 지방질 내부에서의 운동 ―― 84 2.4.6 지방질 분자의 운동 ―― 86제 3 장 단백질과 지방질의 상호작용 • 90
3.1 Liposome과 주변단백질, 수용성단백질의 상호작용 ―― 90 3.2 Liposome과 내재단백질의 상호작용 ―― 103 3.2.1 내재단백질의 재구성 방법 ―― 103 3.2.2 지방질 이분자층의 두께 ―― 106 3.2.3 둘레지방질 (Annular lipid) ―― 108 3.2.4 상 전이와 상 분리 ―― 112 3.2.5 내재단백질의 이동속도 ―― 114 3.2.6 지방질 이분자층에서의 내재단백질의 구조 ―― 114 3.2.7 Amino산의 배열과 막 내에서의 위치 ―― 119 제 4 장 생체막의 구조 • 126 4.1 지방질 이분자층 ―― 126 4.2 생체막 성분의 비대칭적 분포 ―― 129 4.2.1 지방질 ―― 129 4.2.2 단백질 ―― 132 4.2.3 탄수화물 ―― 147 4.3 생체막 성분의 이동성 ―― 148 4.3.1 생체막에서의 상 전이 ―― 148 4.3.2 지방질의 이동도 ―― 149 4.3.3 단백질의 이동도 ―― 151 4.4 생체막 구조의 Model ―― 157 4.5.1 Danielli-Darson model(1935) ―― 158 4.5.2 Robertson의 단위막 model ―― 158 4.5.3 Singer-Nicholson의 fluid-mosaic model ―― 160 제 5 장 생체막을 통한 물질의 확산 • 162 5.1 용해-확산의 과정 ―― 163 5.2 촉진확산 (Facilitated diffusion) ―― 169 5.2.1 포도당의 이동 ―― 169 5.2.2 음 ion 교환 ―― 1765.2.3 ATP/ADP 교환 —— 177
5.3 구멍을 통한 확산 —— 177 5.3.1 Porin —— 178 5.3.2 Connexon——179 5.3.3 구멍을 형성하는 수용성 단백질 —— 181 5.4 Ion 운반물질 —— 181 5.4.1 운반매체 (Carrier) —— 183 5.4.2 구멍 (Pore) —— 185 5.4.3 전압에 의해 형성되는 구멍 —— 190 제 6 장 능동운반 • 191 6.1 일차능동운반 —— 192 6.1.1 Na⁺,K⁺-ATPase —— 192 6.1.2 Ca²⁺-ATPase —— 207 6.1.3 Bacteriorhodopsin —— 209 6.1.4 결합단백질 (Binding protein)에 의한 이동 system —— 211 6.2 이차능동운반 —— 213 6.3 분자단 운반 (Group translocation) —— 217 제 7 장 생체전기현상 • 220 7.1. 전압에 의해 열리는 통로 —— 220 7.1.1 활동전위 (Action potential) —— 222 7.1.2 전압에 따르는 膜門(gate) —— 232 7.2 화합물에 의해 열리는 통로 —— 233 7.2.1 Synapse -- 238 7.2.2 종판전압(End-plate potential) —— 242 7.2.3 Acetylcholine 수용체(receptor) 단백질 —— 246 7.2.4 Ach-chcycle —— 253 7.3 기타방법으로 열리는 통로 —— 262 제 8 장 생체막에서의 신호전이 • 269 8.1 Hormone의 수용체 —— 2708.1.1 Adenylate cyclase ―― 275
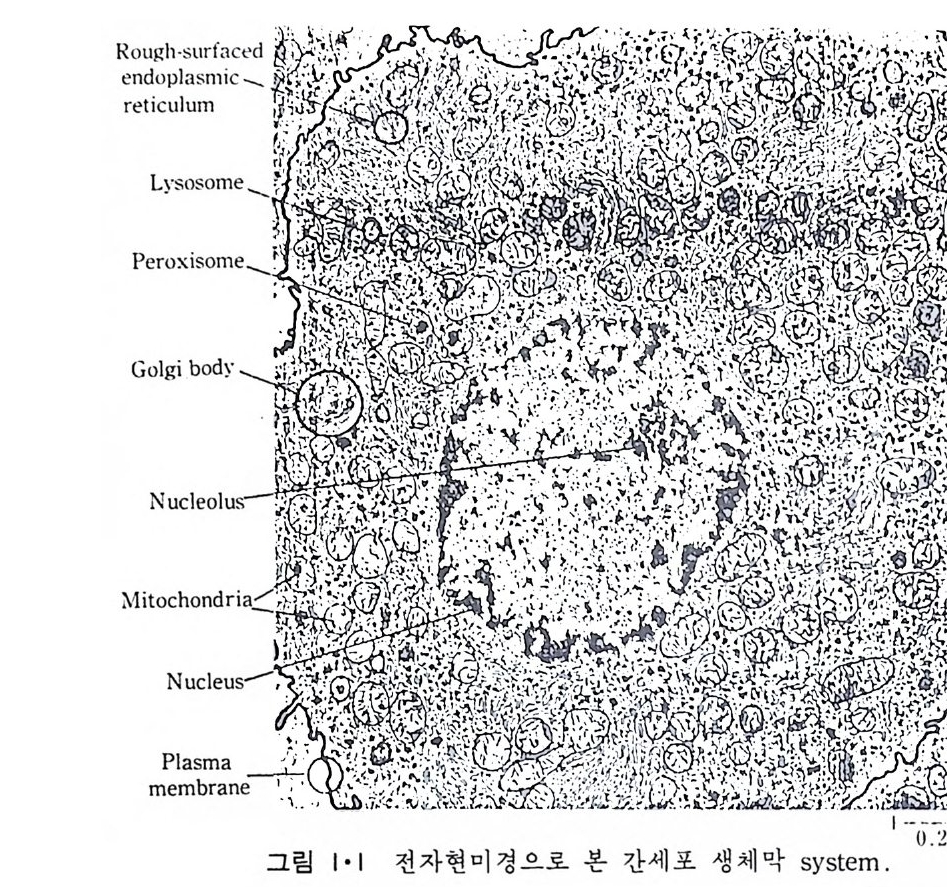
8.1.2 Insulin 수용체 ―― 285 8.1.3 신경 hormone ―― 288 8.2 물질 주성(Chemotaxis) ―― 291 8.3 면역(Immune) 수용체 —— 296 제 9 장 생체막에서의 energy 전이 • 304 9.1 Mitochondria —— 305 9.1.1 전자 전달 (Electron transport) ―― 306 9.1.2 산화적 인산화 ―― 319 9.2 엽록체 ―― 324 9.2.1 광채취 복합체 LHCⅡ ―― 327 9.2.2 광 SystemⅡ(PhotosystemⅡ) 복합체 ―― 328 9.2.3 Cytochrome b₆-f 복합체 ―― 331 9.2.4 광 system Ⅰ (PSI) ―― 332 9.2.5 ATP synthetase ―― 334 9.2.6 Thylakoid 막에서의 단백질 분포 ―― 336 9.3 호흡 세균막에서의 energy 전이 ―― 340 제 10 장 생체막의 융합 • 343 10.1 세포의 융합 ―― 344 10.2 세포 내에서의 융합 ―― 353 10.3 인산지방질 막소포의 융합 ―― 365 10.3.1 금속 양 ion에 의한 융합 ―― 366 10.3.2 단백질에 의한 막융합 ―― 376제|장 생체막의 분포와 화학적인 성분 생명체의 기본단위가 되는 세포는 얇은 原形質膜(p lasma membrane) 으 로 둘러싸여 있어 외부와의 경계연을 이룬다는 것은 세포설이 제창된 1830 년대에 이미 제의가 되었다. 그러나 이 원형질막의 존재가 보편적으 로 받아들여지게 된 것은 비교적 근래에 와서인데 이는 전자현미경의 발 명과 이 룰 이용한 광범위한 연구의 결과라고 볼 수 있다. 전자현미경에 의한 중요한 연구 결과의 하나는 세포 표면에 이를 감싸 고 있는 원형질막이 존재할 뿐만 아니라 세포 내부에도 대단히 많은 膜 조직이 있어 여러가지 중요한 기능을 담당하고 있다는 것이다. 그림 l·l 은 진핵 세포 (euka ry o t e) 의 대표적인 생체막 조직을 보여준다. 원형질막이 細胞質 (c yt o p lasm) 과 외부를 격리시키는 것과 마찬가지로 세 포내의 膜 조직들은 여러가지 小器官 (or g anelle) 내부를 세포질로부터 격리 시켜 이들이 특수한 역할을 할 수 있도록 한다. 이들 중에서 중요한 것 은 核 膜 (nuclear envelop e) 과 mi toc hondria , 小胞 體 (endop la smi c reti - culum), Gol gi체와 l y sosome 동을 둘러싼 막들이다. 광합성을 하는 식물 에는 막으로 구성된 葉綠體 ( chloro p las t)가 있다. 동물 세포 내에서의 생 체막의 분포는 표 l·l 에 보여준다. 이렇게 생체막의 다양성이 근래에 와서 인식되어 가고 있는 것과 같이 생체막의 기능도 생각했던 것보다는 훨씬 광범위한 것을 알게 되었고 생 체막과 관련된 생체 현상은 아직도 계속해서 발견되고 있다. 생체막의
 1-- O- .-2 5 - - µ· - m- · - I
1-- O- .-2 5 - - µ· - m- · - I
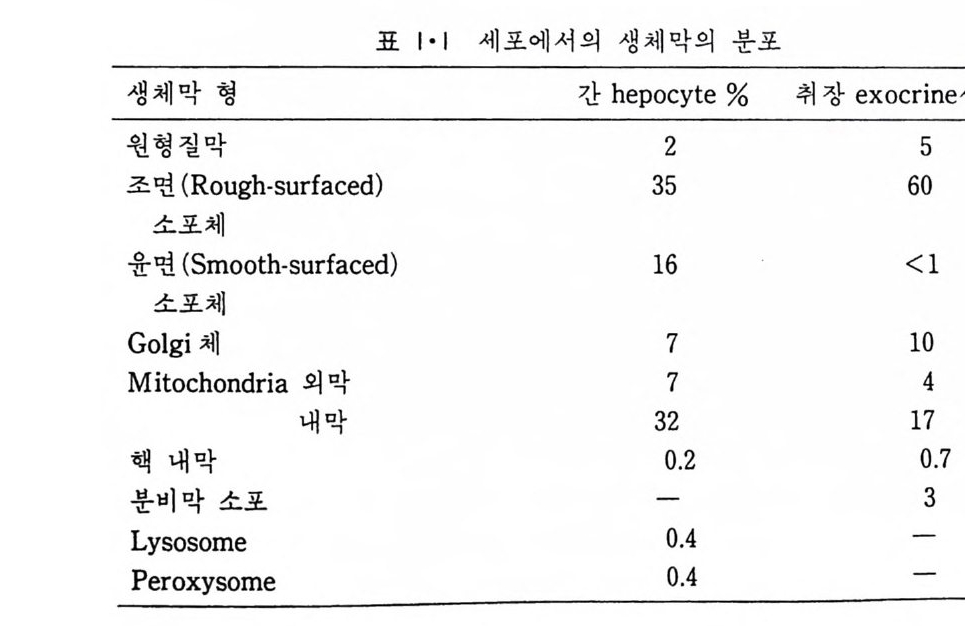 표 |나 세포에서의 생체막의 분포
표 |나 세포에서의 생체막의 분포
기능을 크게 나누면 다음과 같다. ( i ) 세 포 기 능의 격 리 (co mp a rt m enta t i on ) 세포 를 극히 얇은 소수성 ( h y drop hob i c ) 막으로 둘러쌍으로써 세포가 한 단위로서의 특성 (i den tity ) 을 갖게 하며 세포밖에 분포되어 있는 극성 분 자들이 세포질 내의 물질과 자유로 섞이는 것을 방지한다. 세포 내에서 도 여러 가지 기능들을 격리시켜 그 능률을 높이기 위해 소기관들이 막 을 가지게 된다. ( ii ) 물질 수송 ( t rans p or t ) 의 조절 (regu la ti on ) 세포와 세포 내의 여러가지 기능을 격리시키기 위하여 막이 존재하지 만 이들 기능에는 물질과 energy 대사가 필요하다. 그래서 생체막에는 물질들을 능률적으로 수송할 수 있는 기능이 존재한다. 특히 생체막이 ion 둘의 이동 속도를 조정함으로써 전위차 (elec t r ical po te n ti al gr ad i en t)를 형 성 하며 신 경 세 포 (ne uron) 와 근육 세 포에 서 는 이 것 이 통신 (communic a- ti on ) 의 수단으로 이용되고 있다. (ii i) 능률적인 생화학 반응 생체막은 수용액 내에서의 생화학적인 만응을 격리하여 그의 능률을 향상시킬 뿐만 아니라 막 자체에서 여러가지 반응을 단계적으로 그리고 능률적으로 진행시킨다. 이의 대표적인 예가 여러가지 ener gy전이 (tr a nsducti on ) 현 상이 다. 많은 수용성 효소들도 생 체 막과의 경 계 면에 서 좀 더 능률적 인 반응을 가져 오게 한다. (iv) 외부와의 통신 단세포 생체도 주위 환경에 적응해야 되고 특히 다세포 생체에서는 세 포간의 통신뿐만 아니라 외부 자국의 식별 등이 그의 생존에 중요한데 이들이 모두 생체막에서 이루어진다. 원형질막에서는 다른 세포를 식별 하고 비슷한 세포와 뭉쳐서 조직 (ti ssue) 을 형성하며 인접해 있는 세포간 에 통신을 할 수 있는 능력이 발전되었고 또 hormone 受容體 (rece pt or) 에 의해 얼리 떨어져 있는 세포끼리의 통신이 가능한데 이들이 모두 원형질 막에서 이루어진다.
 . .·.·. . .. . ..
. .·.·. . .. . ..
l·l 생체막의 분포1) -3) 1·1·1 原形 質膜 (Plasma membrane) 4>-s> 그림 1·2 는 적혈구 원형질막의 전자현미경 사진이다. 여기서 봉 수 있 는 3 겹 구조(t r il amellar s t ruc t ure) 는 세포질 내부에 있는 생체막들에서도 볼 수 있어 모든 생체막이 근본적으로 동일한 구조를 갖는 것을 알려 주 고 있다. 원형질막의 제일 중요한 기능은 세포질을 외부로부터 격리시키는 것이 라 볼 수 있다. 세포질 무게의 80% 정도가 물이기 때문에 원형질막 없 이는 외부와 그대로 섞여 버릴 것이다. 세포가 모든 생물체의 기본단위 가 될 수 있게 하는 것이 곧 원형질막이다. 그러나 세포질이 외부와 격 리만 되어서는 세포의 기능을 할 수 없으므로 원형질막에는 세포 기능에 필요한 여러 가지 화합물을 수송(t rans p o rt)시키는 특수한 mechan i sm 이 존재하고 외 부와 연 락하는 기 능, 또 다른 세포를 식 별 (recog nize ) 하고 유
 TJ. uig nch tti . o ns
TJ. uig nch tti . o ns
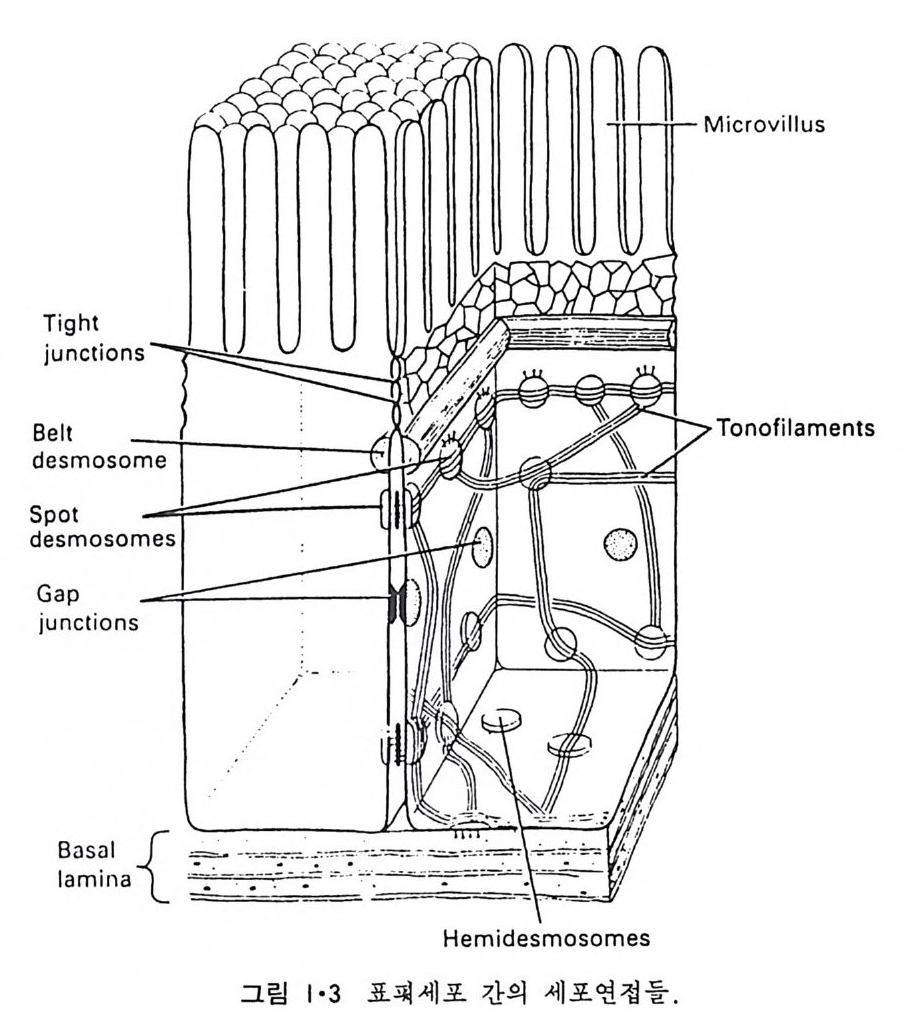
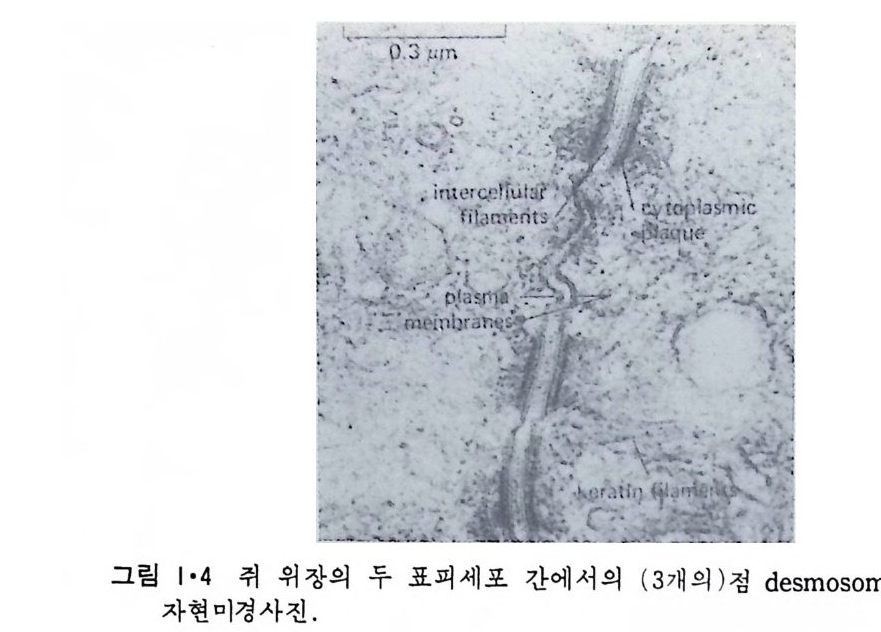
사한 세포끼리 부착하여 조직(ti ssue) 을 형성하며 이들 사이에 접촉하는 기능을 보유한다. 그림 1·3 은 세포끼리의 접촉을 보여준다. 세포간의 접 촉은 여 러 가지 종류의 세 포 연 접 (cell ju.,ct i on ) 으로 이 루어 진 다. 세포 연접은 크게 나누어 세 가지로 구분이 된다. 첫째는 부착 연정 (adher ing jun cti on ) 으로 여 러 가지 desrnosorne 들이 여 기 에 속한다. 그림 1·4 는 점 (sp o t) desrnosorne 을 보여준다. 이는 세포를 서로 부착시켜 조 직을 이루게 하는 것으로 desmosorne 에서 세포 사이의 간격에는 섬유성 물질(fil amen t ous ma t er i al) 로 차 있으나 그것이 무엇인지는 아직 모른다. 이들 desrnosorne 근처 세포 내부에는 act in filam ent 등이 원형질막과 접촉되어 있으면서 평행하게 배열되어 있는 것을 볼 수 있다. 두번째 집
 ` `一 -.~. 3^ iII r. I• :. .
` `一 -.~. 3^ iII r. I• :. .
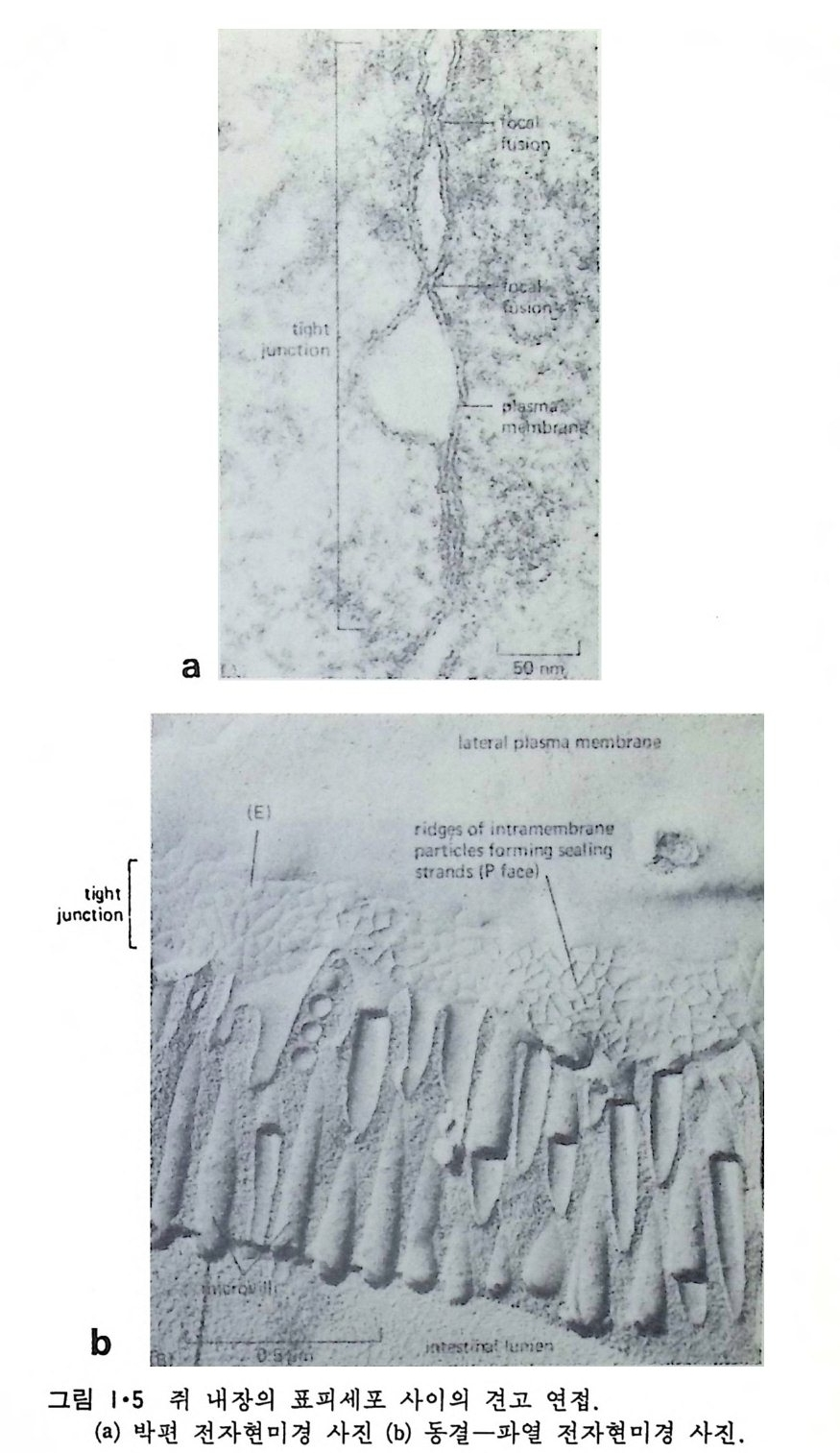
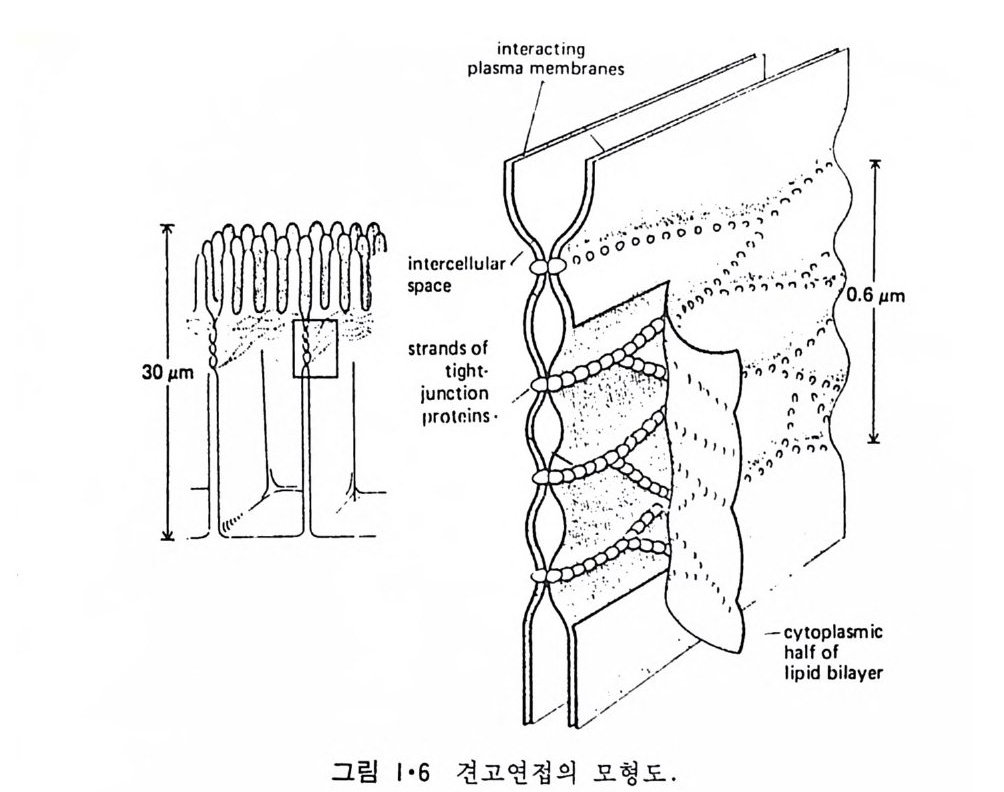
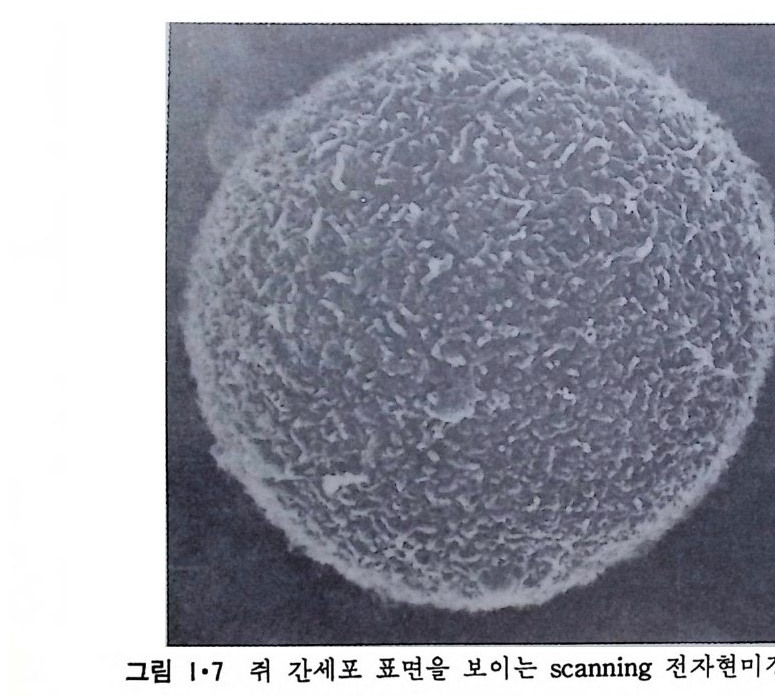
촉은 불투과 연접 (im p e rmeable j unc ti on ) 으로서 견고 연접 (tig h t jun cti on ) 이 그 대표적인 예이다. 그림 1·5 는 견고 연접의 전자현미경 사진이다. 이들 중 동결-파열(fr eeze - fr ac t ure ) 사진에는 원형질막 내부에 파묻힌 입자 (int r a membrane pa rt icle , IMP) 들이 선을 이루고 있는데 접 촉 하고 있는 두 원형질막에 있는 이들 단백질 선들이 회합하여 연접을 이룬다고 해 석 이 되고 그 model 을 그림 1·6 에서 볼 수 있다. 이들 견고 연접은 세포 사이 의 공간에서 물질이 통과되는 것을 막기 때문에 방광에 있는 屈 를 다 른 데로 가지 못하게 하는 등의 역할을 한다. 세번째 접촉은 연락 연접 (communic a ti ng j unc ti on) 으로 간격 연접 (ga p jun cti on ) 과 화학적 인 s yn a p se 가 그의 대 표적 인 예 이 다. 간격 연 접 은 두 세포막이 통로 (channel) 로서 연결되어 두 세포 사이에서 작은 물질들이 자유로 이동할 수 있도록 하는 것이며 이는 제 5 장에 자세히 설명할 예 정이다. 화학적인 s yn a p se 는 신경세포 사이의 연락이 이루어질 수 있도 록 하는 것으로 제 7 장에서 더 설명이 된다. 세포 연정들의 위치를 결정하는 것은 세포질에 있는 세포 골격 (cy tos keleto n ) 으로서 이 성 분인 미 세 단성 유 (mi cro fi lam ent) 와 미 세 소관 (micro t ubule) 은 세포의 모양도 세포의 기 능에 따라 조정 하게 된다. 그림 1·7 은 간세포의 표면을 주사 (scann i n g) 전자현미경으로 본 것인데 적혈구
 .1 .-.• ;; . (! !江亨 . 4 r ’
.1 .-.• ;; . (! !江亨 . 4 r ’
 rnt e ractr n g
rnt e ractr n g
 그립 1•7 취 간세포 표면흥 ―오 이는 scannin g 전자현미경 사진.
그립 1•7 취 간세포 표면흥 ―오 이는 scannin g 전자현미경 사진.
 몬Y
몬Y
 -··-· . ..,. .. .. .
-··-· . ..,. .. .. .
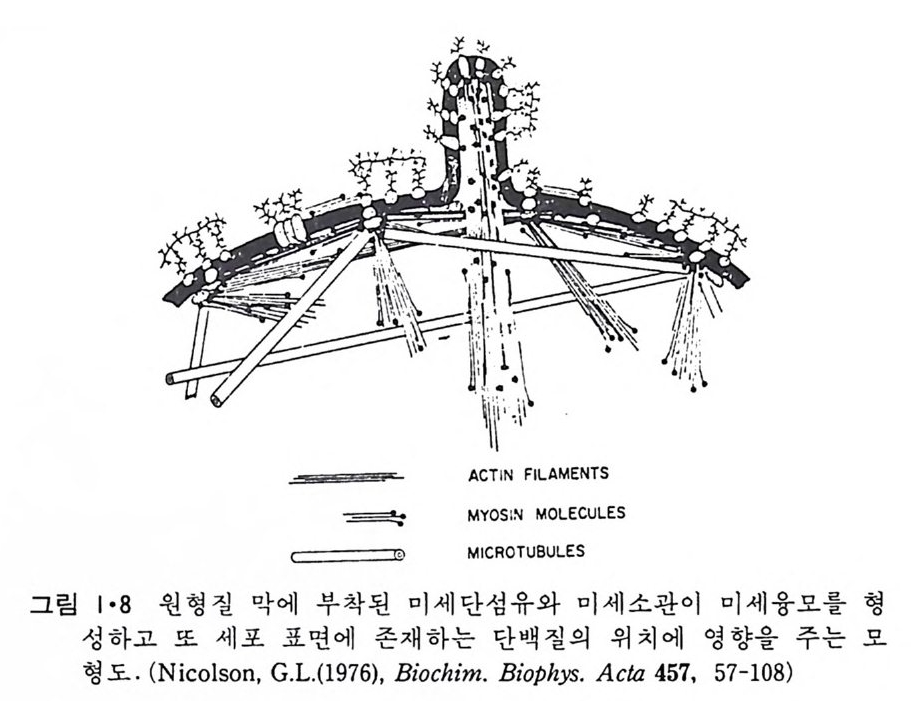
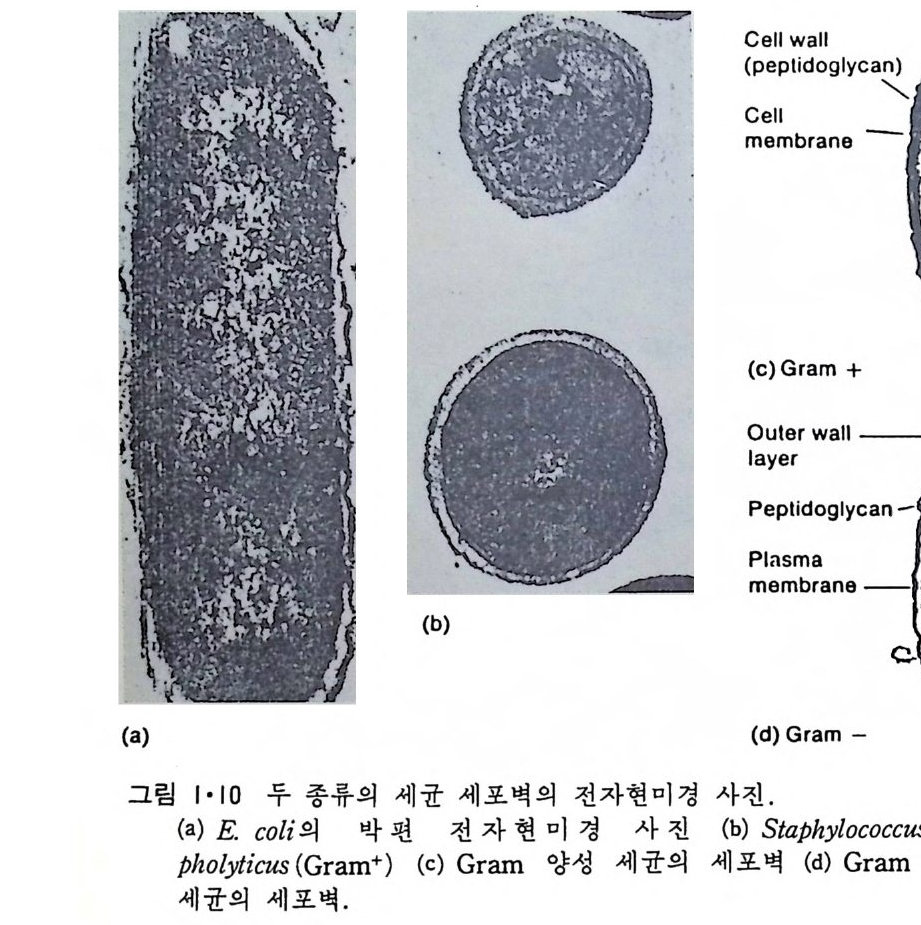
원형질 표면(그럼 1·2 ) 과는 달리 그 표떤에 미세융모 ( m i crov i ll i ) 가 있어 표면적이 대단히 크다 . 이렇게 미세응모의 형성은 그링 l·8 에서와 같이 세포골격계에 의한 것인데 이는 그림 l·9 에서 보인 전자현미경 사진으로 알 수 있다. 원형질막 밖에는 동물세포인 경우 점다당류 ( muco p ol y sacchar i de) 와 colla g en 으로 구성된 기처막 (basemen t membrane ) 이 있고 식물세포인 경 우 cellulose 로 구성된 세포벽 (cell wall) 이 있다. 원핵세포(p roka ry o t e) 들은 내부 소기관들이 없기 때문에 그 막이 진핵 세포에 비해서 훨씬 간단하다. 여기서는 원형질막만이 존재하지만 Gram 양성 세포일 때에는 원형 질막이 두꺼운 p e pti do g l y can 층으로 둘러 싸여 있고 Gram 음성인 세포는 두 개의 원형질막 사이에 얇은 pe p tido g ly c an 층이 존재한다(그럼 l·10).
 Cellwall
Cellwall
 ,f? ·-;' ; .,;¢ • ,1
,f? ·-;' ; .,;¢ • ,1
 pcr in u clcar spa ce
pcr in u clcar spa ce
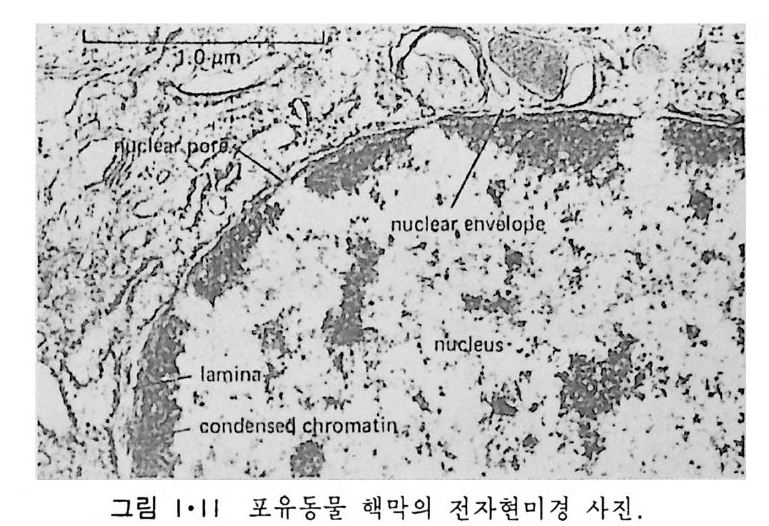
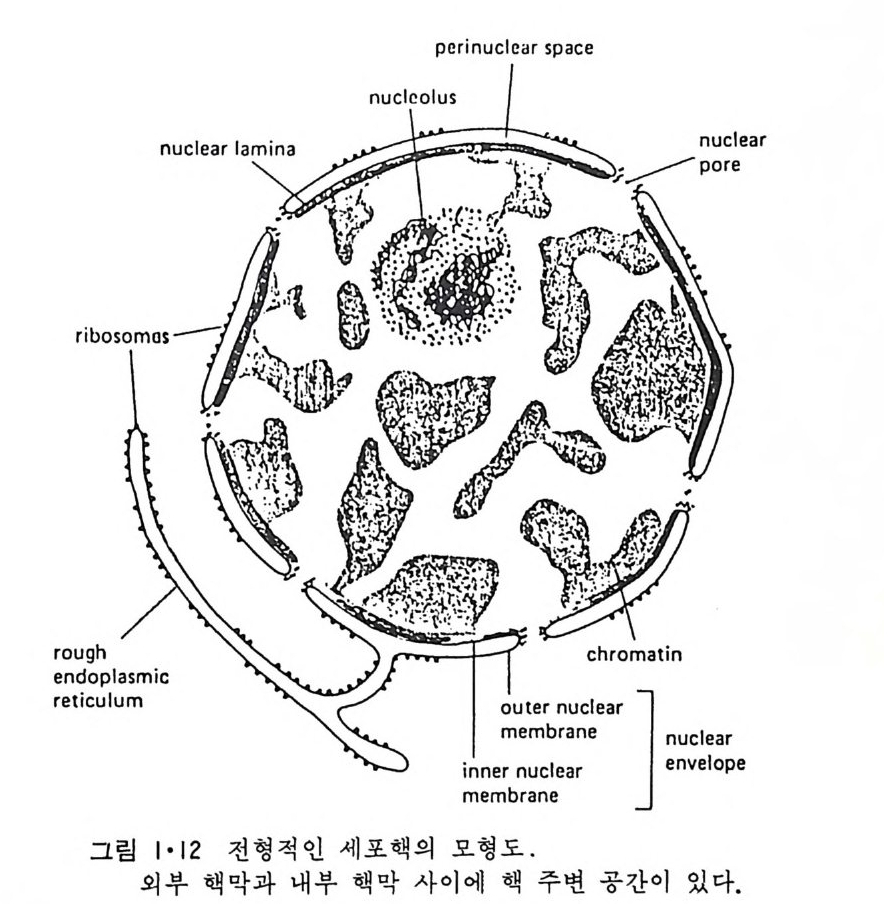
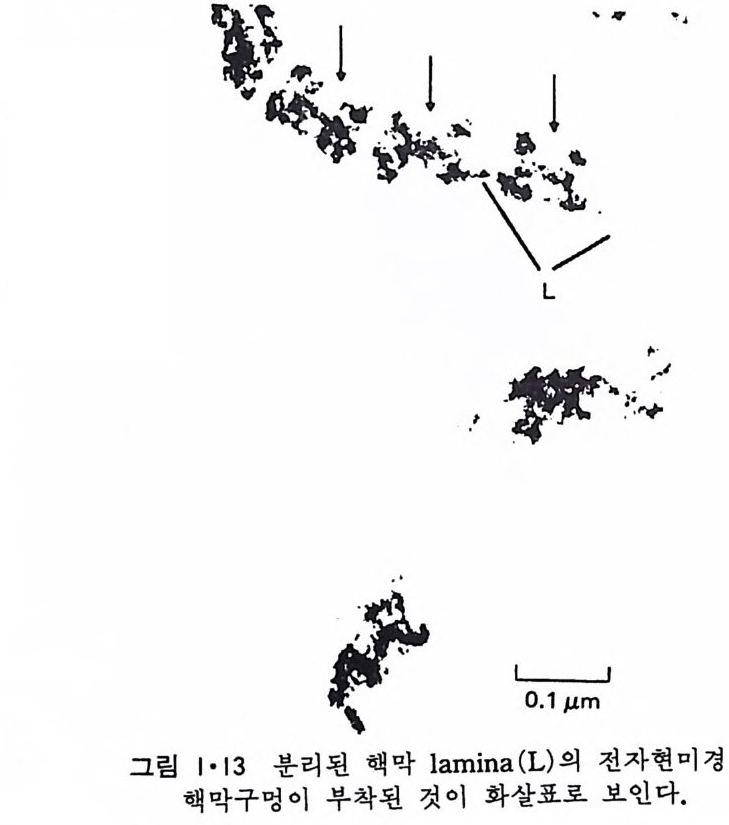
1 • 1 • 2 核膜 (Nuclear envelop e) 9> 그림 l·l 에서 핵이 막으로 둘러싸여 있는 것을 볼 수 있고 이 핵막의 존재 유무가 진핵세포 (euka ry o t e) 와 원핵세포(p rokar y o t e) 의 차이를 보여 주는 가장 중요한 점이다. 그림 l·11 에서 보는 바와 같이 핵막은 이중막 으로서 막 사이의 간격은 20~50nm 정도이다. 이 이중막의 군데군데에 는 이들이 융합되어 형성된 핵구멍 (nuclear p ore) 이 존재한다. 내부 핵막 (inn er nuclear membrane) 안쪽에는 lam i na 라고 불리는 섬유성 단백질충 이 부착되어 있고 의부 핵막 (ou t er nuclear membrane) 은 소포체와 연결이 되어 있다(그림 1·12). 그래서 두 개의 핵막 사이의 공간과 외부 핵막은 소포체의 연장이라고 생각할 수가 있다. Lam i na 는 세 가지의 단백질이 회합하여 이루어진 것으로 이것을 내부 핵막에서 분리해내면 핵구멍을 형성하는 단백질까지 연결되어 나오게 된 다(그링 l·13). Lam i na 는 내부 핵막에 있는 단백질과 회합하며 또 핵내
 L
L
 = i l r l l/ j— I E==
= i l r l l/ j— I E==
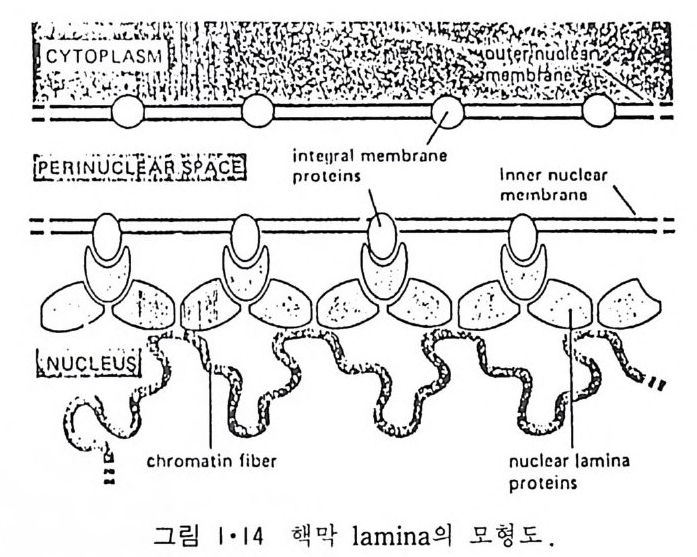
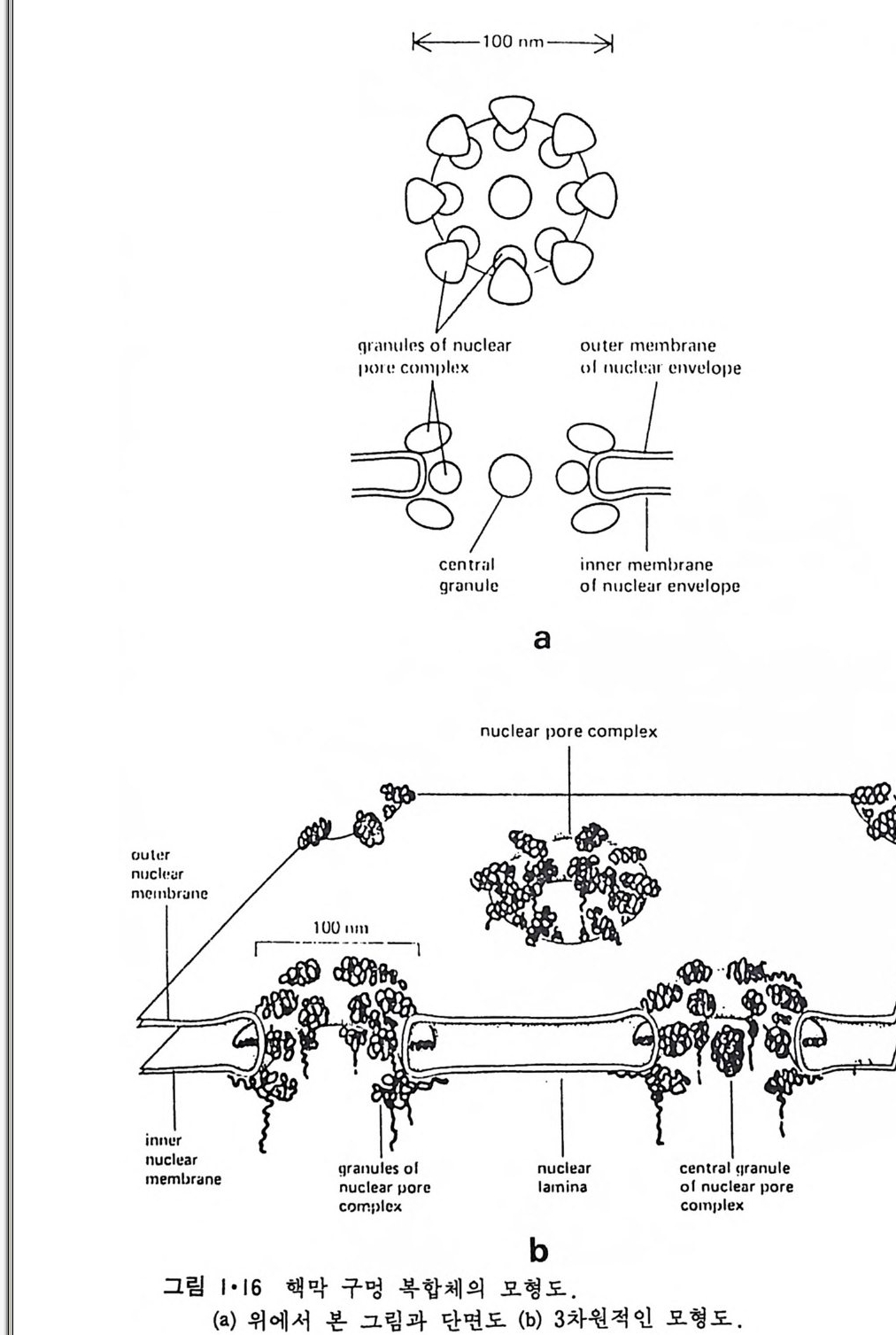
chroma ti n 과 결합이 되어 있다 ( 그링 1·14). 그래서 유사분열 (m it os i s) 때 에 핵막이 없어졌다가 다시 생기는데 lam i na 가 역할을 한다고 생각되고 있다. 핵막의 구멍은 내경이 약 80nm 가 되는 단백질 복합체로 형성되어 있 고 (그림 l·15) 그림 1·16 에서와 같이 외부와 내부 핵막 쪽에 각각 8 개
 그림 I•15 Xenop us ooc yt e 의 핵막구멍의 전자현미경 사진.
그림 I•15 Xenop us ooc yt e 의 핵막구멍의 전자현미경 사진.
 1< 100 nm >
1< 100 nm >
의 단백질 소단위가 있으며 때 로는 이 구멍 한가운데 입자가 보이나 이 는 이 구멍을 통과하고 있는 고분자 물질로 생각되고 있다• 핵막 구멍을 통하여 큰 분자들이 이동된다고 생각되는데 분자량이 약 50kDa 정도까 지의 입자가 핵 내부로 들어가는 것을 관찰할 수 있어 직경이 약 9nm 의 통로 (channel) 가 존재하는 것을 알 수 있다. 그러나 핵막 구멍은 rib o some 소단위 ( subun it )와 nuclease 와 같은 보다 큰 분자를 통과시 킬 것이므로 이때에는 이들 거대분자가 핵막 구멍과 작용하여 그 모양이 변 화를 가지면서 통과한다고 생각된다. 1 • 1 •3 小胞 體 (Endop la smi c reti cu lum) 그림 l·l 에서 세포핵과 원형질막 사이에 가장 널리 분포되어 있는 막 s y s t em 이 소포체 이 다. 이 막 s y s t em 은 .:::z. 크기 와 형 태 가 다양하여 핵 막 과 연결이 되어 있는 부분으로부터 시작하여 (그림 1·17) 수송 막소포 (tra nspo rt ves i cle) 를 거쳐 Gol gi체와 연결이 되어 있고 이 후자는 분비 막소포 (secre t ary ves i cle ) 를 통하여 원형질막에 연결이 된다. 그림 1·18 에 서와 같이 소포체의 구조는 대단히 복잡하지만 한 세포에는 한 개만의 소포체막이 lumen 을 둘러싸고 있다고 생각된다.
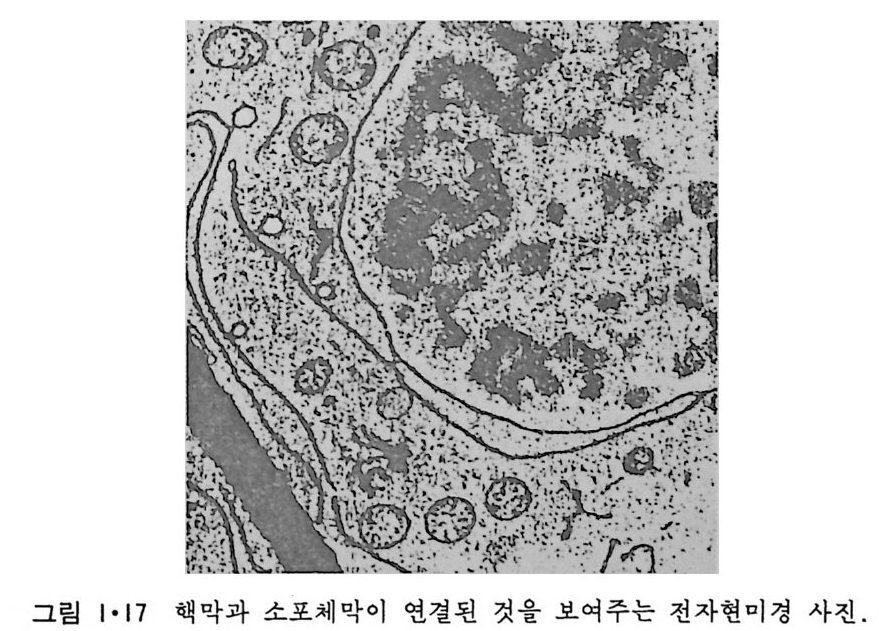 그림 I•17 핵막과 소포체막아 연결된 것을 보여주는 전자현미경 사진.
그림 I•17 핵막과 소포체막아 연결된 것을 보여주는 전자현미경 사진.
 b,.n
b,.n
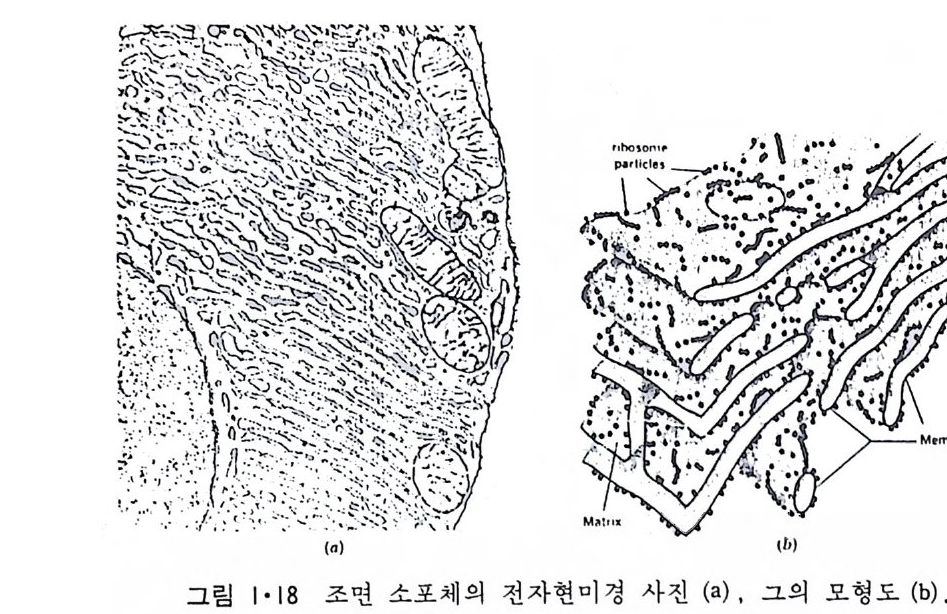
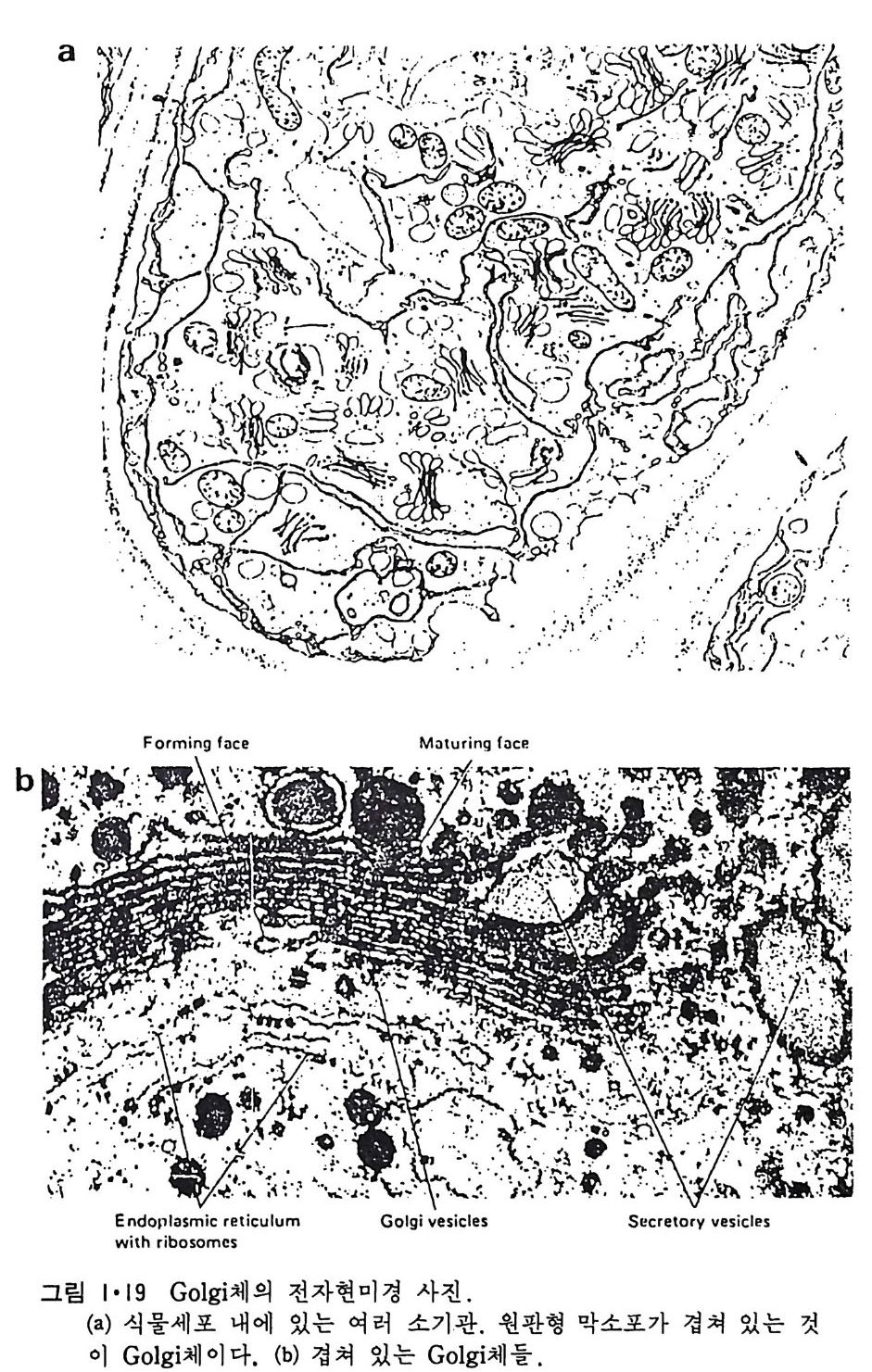
소포 체 에 는 rib o some 이 부 착 되 어 있 는 租面 소 포 체 (roug h -surfa c ed endop la smi c reti cu lum) 와 r i bosome 이 없는 滑面소포체 (smooth surfa c ed endop la smi c re tic ulum) 가 있다. 租面소포체 (그림 1·18) 의 중요한 기능은 세포에서 외부로 분비되는 단백질과 생체막에 묻혀 있는 내재단백질 (int e g ra l pro te i n ) 을 합성 하여 Gol gi체 물 통하여 분비 하거 나 다른 생 체 막 으로 전달하는 것이다. 소포체의 lumen 쪽에서 내재단백질에 당류가 가해 진다. 생체막의 지방질도 소포체에서 합성되어 소포체막으로 투입되기 때문에 거의 모든 생체막 성분이 이 소기관에서 형성되는 것이다. l • l • 4 Golg i 체 이 막 s y s t em 도 세포의 종류에 따라서 그 모양이 조금씩 다르지만 그 특징은 여러 개의 원반 (d i sk) 같이 생긴 막소포가 겹쳐 있고 근처에 작은 구형의 막소포가 존재하는 것이다(그림 1·19). Gol gi체와 소포체와의 관 계는 아직도 분명치는 않으나 滑面소포체가 떨어져 나와서 막소포가 형 성되어 기존의 Gol gi체와 합친다는 것이 알려져 있다. 이렇게 하여 Gol gi체의 주 역할은 소포체에서 합성된 단백질 분비의 중간 매개체 역 할을 한다. 여러가지 실험 결과로 Gol gi체는 그 성질이 균일하지 않고 화학적인 성분이나 막의 두께가 소포체 쪽에서 원형질막 쪽으로 가면서
 a
a
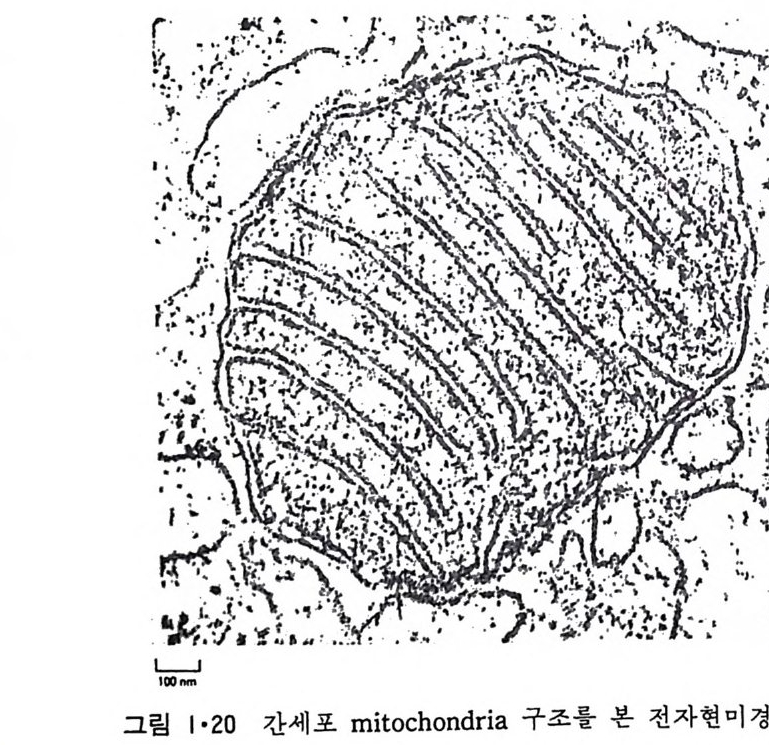
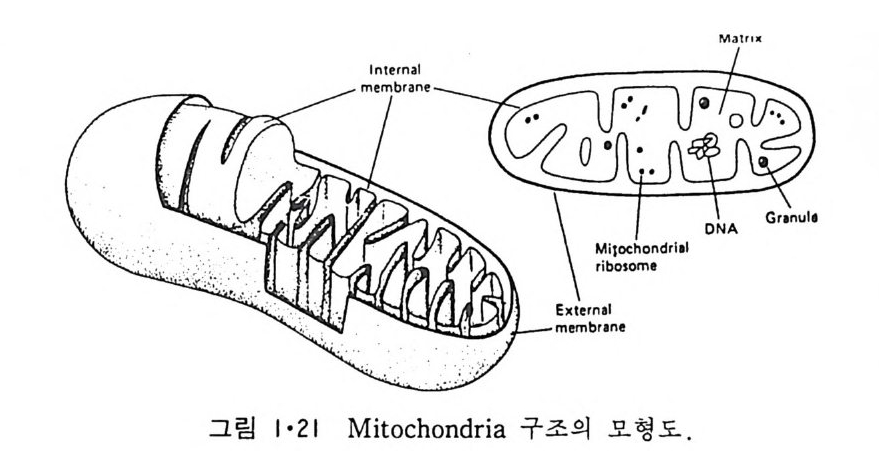
점접 달라지는 것을 볼 수 있다. 이것은 생체막이 정적인 것 이 아니고 동적이어서 한 막 s y s t em 에서 다른 s y s t em 으로 유동되는 순환적 이동 (cyc lic movemen t)을 한다는 것을 시사한다. l • l • 5 Mi toc hondria 好氣性 ( aerob i c) 세포에 제일 많이 존재하는 소기관은 m it ochondr i a 로 이 것의 막 구조는 그림 1·20 에 보여주며 그림 1·21 은 그의 model 을 보여 준 다. M it ochondr i a 는 外膜 (oute r membrane 혹은 exte r nal membrane) 과 이보다 구조가 더 복잡한 內膜(i nner membrane 혹은 int e r nal membrane) 으로 구성되어 있다. 이 內膜으로 둘러싸인 부분을 ma t r i x 라 하며 여기 에서 citri c ac id c y cle 의 대사회로가 일어나고 內膜에서 산화적 인산화 (oxid a ti ve ph osph ory la ti on ) 가 일 어 나 ATP 를 합성 한다. 이 ma t r i x 에 DNA 와 r i bosome 이 존재하여 내막에 존재하는 내재단밸질의 일부가 합 성되지만 대부분의 내재단백질과 ma t r i x 에 있는 단백질은 세포질에서 합 성 되 어 ma t r i x 로 수송 (tra nslocate ) 된 다.
 11 00'_ I
11 00'_ I
 MaI 『'
MaI 『'
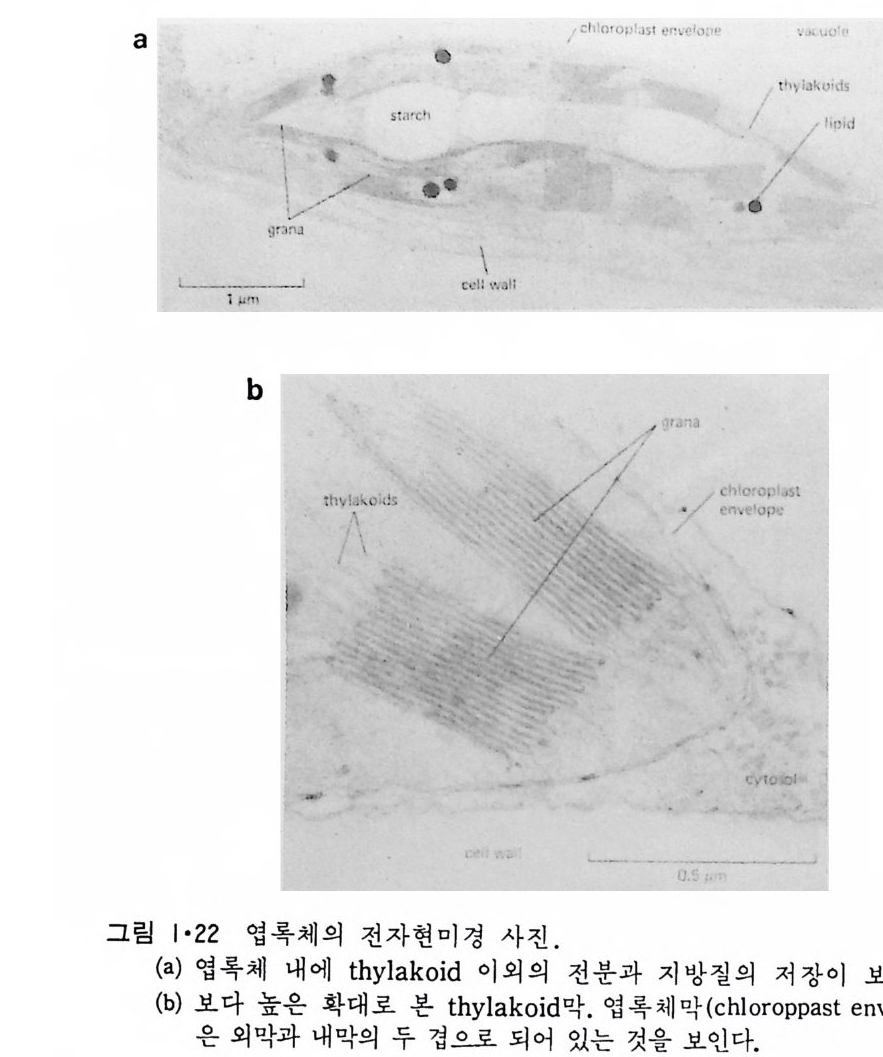
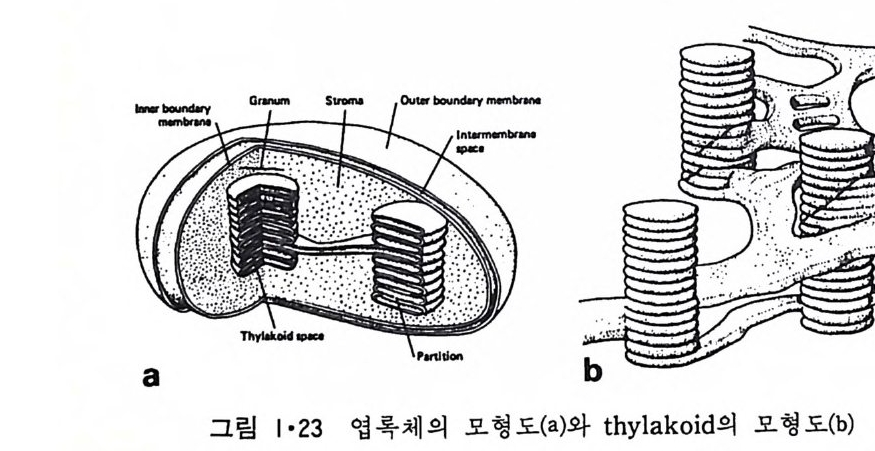
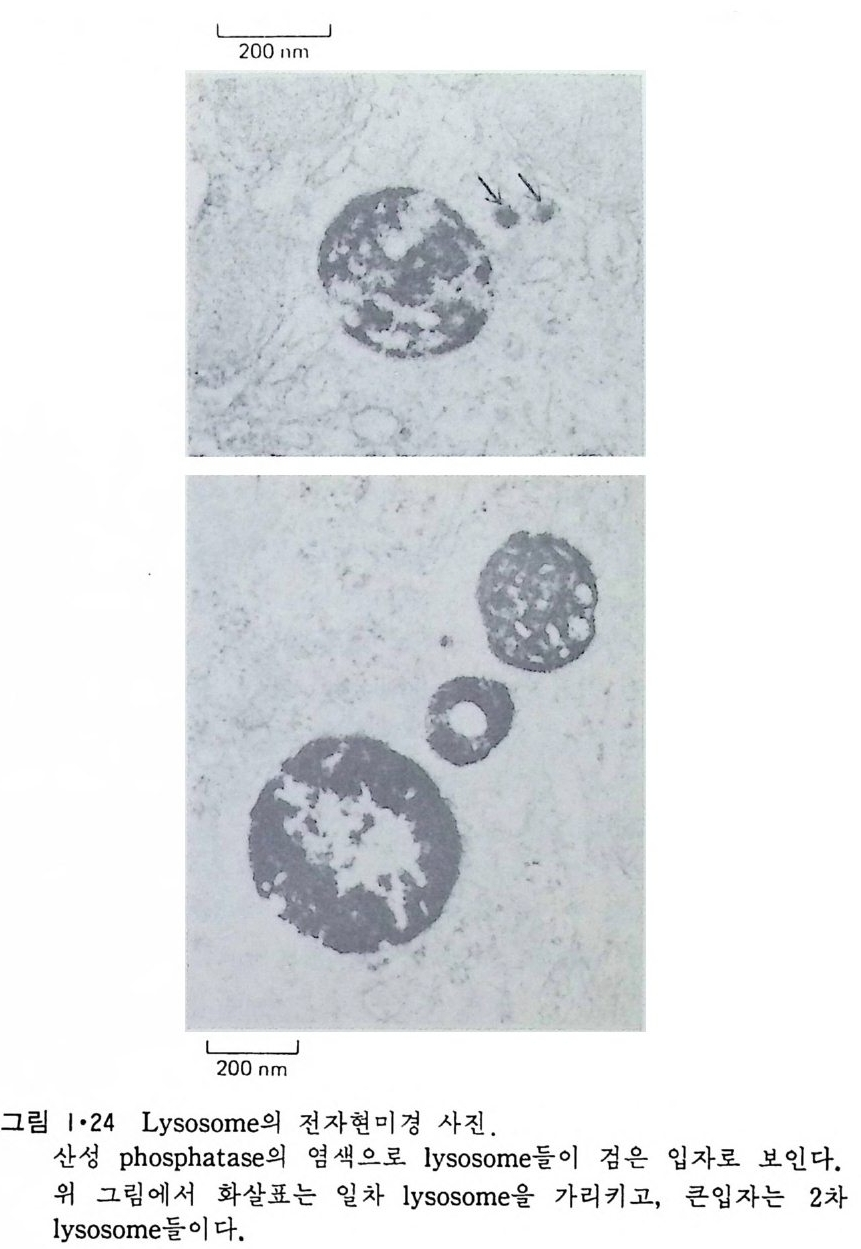
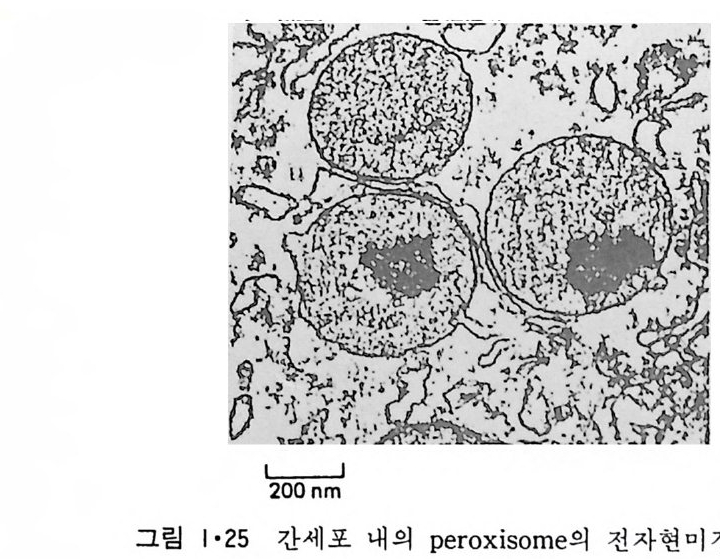
이렇게 m it ochondr i a 가 자체 내에 유전자(g ene) 을 가지고 있는 것과 그 크기가 원핵세포 ( p roka ry o t e ) 와 비슷한 것으로 미루어 보아 아 소기관 은 진화 과정중에 원핵세포가 진핵세포에 침입해 공생 (s y mb i os i s) 을 하여 시작된 것으로 생각되고 있다. 원핵세포에서 산화성 인산화는 원형질막 에서 이루어진다. 1 •1 •6 엽 록 체 (Chlorop la st) 光合成을 하는 엽록체는 葉綠素 (chloro phy ll) 를 함유하고 있는 막을 가 지고 있는데 아것도 m it ochondr i a 와 유사하게 外膜과 內膜으로 구성되어 있다(그림 l·22). 내막으로 둘러싸인 공간은 mit ochondr i a 의 matr i x 에 해당되는데 이부분은 s t roma 라 부른다. 이 s t roma 에는 t h y lako i d 의 복잡 한 막 s y s t em이 존재하며 ( 그림 1·23) 아 막에 chlorop h y ll 둥 색소와 광 합성의 光反應에 필요한 성분들이 있다. 탄수화물의 합성 자체는 str o ma 의 용액내에서 이루어진다. 1·1·7 기타 생체막 이상 열거한 생체막 sys t e m 이외에도 막으로 둘러싸인 소기관에는 가 수분해 효소를 함유하는 l y sosome( 그림 l·24), 산화성 효소를 가지고 있 는 p erox i some( 그림 l·25) 그리고 기타 여러가지 exocy tos is 막소포와 endocy tos is 막소포 가 있 다.
 a 。 ’ ch'()1( ) r!.' t.' P 묘 '1\; :· p ,.\.u ,,
a 。 ’ ch'()1( ) r!.' t.' P 묘 '1\; :· p ,.\.u ,,
 a
a
 I I
I I
L y sosome 은 약 40 종류의 산성 가수분해 효소를 포함하고 있는 막소 포로서 그 크기 가 다양하다. 이는 Gol gi체에서 떨어져 나온 일차 (pr im ary ) l y sosome 과 이것이 여러가지 다른 막으로 둘러싸인 액포와 융 합하여 생성된 2 차 (secondar y) l y sosome 으로 구분이 된다. L y sosome 의
 I l
I l
막에 는 ATP 를 가수분해 하여 그 내 부로 양성 자 를 p um pi n g하는 ATPase 가 있다고 생각되는데 이것을 통해 lys o some 내부의 p H 가 5 로 유지되어 산성 가수분해 효소의 활성도가 최적화가 된다. 이 효소들은 en- doc yt os i s 에 의해 세포로 들어온 물체를 가수분해하여 세포의 영양분으로 이용되도록 하는 역할을 한다. Perox i some 은 그 직 경 이 0.5µm 정 도 되 는 막소포로서 D-ami no ac id oxid a se, urate oxid a se 와 cata l ase 등 산 화 성 효 소 를 가 지 고 있 어 m it ochondr i a 와 함께 산소를 소모하는 소포체이다. 이 소포체 내부에서 는
RH2 + 02 一 R + H202 와 같은 반응이 일어나 여러가지 물질이 산화되며 여기서 생성된 H202 는 ca t alase 에 의해 다음과 같이 물과 산소로 변형된다. 2H202 一 2H20 + 02 Perox i som 呼 활면 소포체에서 떨어져 나와 형성된 소기관이다. 이상 예거한 생체막들은 두 면을 가지고 있는 것을 볼 수 있다. 즉 세 포질을 향한 면과 그 반대편을 향하고 있는 면인데 그림 1·26 에서 굵은 선으로 표시된 면이 외부를 향하는 면이고 가는 선으로 표시된 면이 세 포질을 향하고 있는 면이다. 앞에서 이야기한 바와 갇이 생체막둘은 유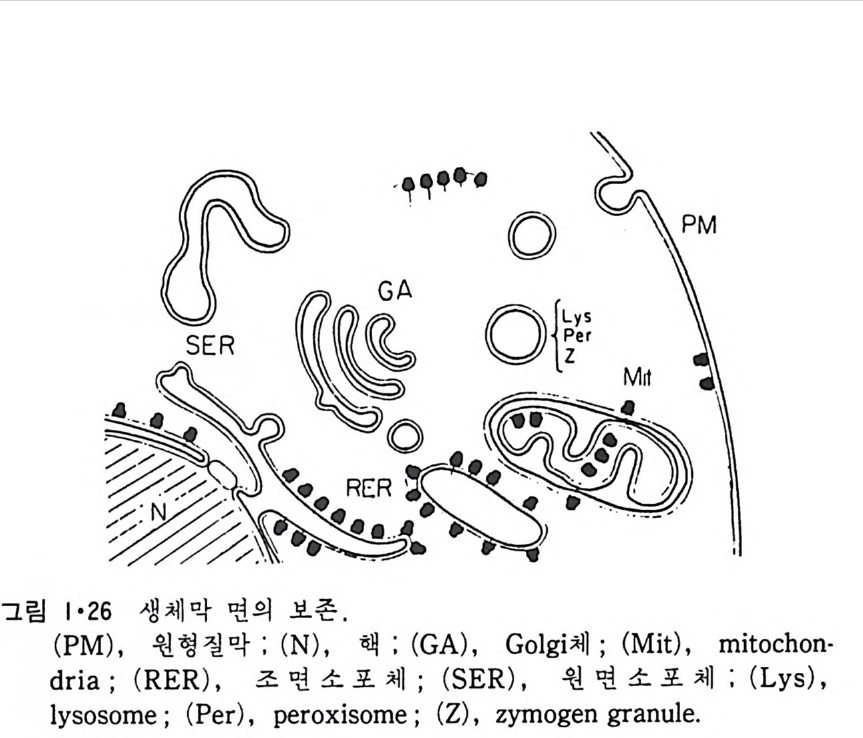 `
`
동적이어서 융합(fu s i on) 에 의해 원형질막이 세포 내부의 소기관 막과 합 칠 수도 있고 효소, hormone 등의 분비시 소포체막이 종국에는 원형질 막과 융합하기도 하는데 그림 1·26 에서 볼 수 있는 것과 같이 세포질을 향하는 면은 어디로 가나 항상 같은 쪽을 향하게 되어 방향성을 유지하 게 된다. 1·2 생체막의 화학적 인 성분 10) 1·2·1 생체막의 분리 생체막의 구조를 연구하는 데 필요한 첫째 과정은 각각 다른 종류의 생체막을 분리하는 것이다. 세포나 조칙을 균등기 (homo g en i zer) 등 기계 적인 방법으로 파괴한 후 얻는 소기관과 소포체가 쪼개져서 생성된 m i crosome 들은 밀도, 크기와 전기적인 성질의 차이를 이용하여 분리할 수가 있다. 이중에서도 초원 십분리기 (ul t racen trifug e) 를 이용하는 것이 제 일 보편화된 방법이다. 낮은 회전 속도에서 핵과 세포 폐물을 우선 침전
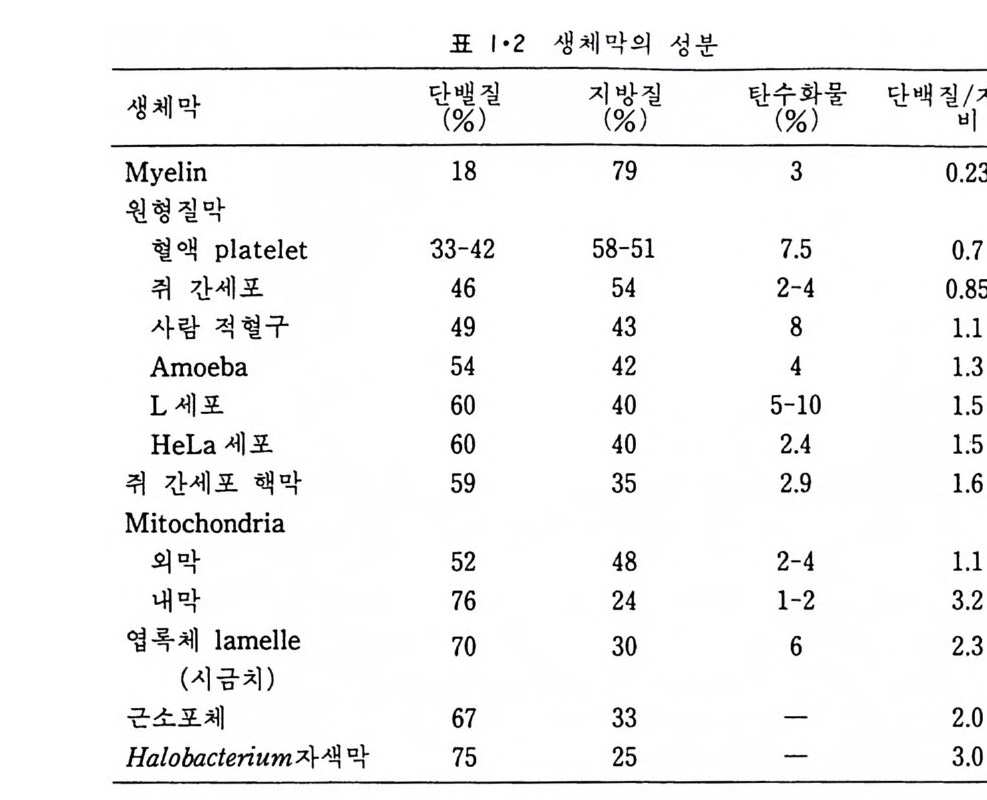 표 I·2 생체막의 성분
표 I·2 생체막의 성분
시키고 남은 용액을 고속도로 회전시켜 m it ochondr i a 와 l y sosome 을 침 전시킨다. 이 침전물은 설탕농도기울기 (sucrose concentr a ti on gr ad i en t)원 심분리 방법으로 각각의 성분으로 분리시키며 용액 (su p erna t an t)내의 m i crosome 과 고분자 물질은 더 높은 회전 속도로 분리시킬 수 있다. 생체막의 주성분은 지:J-질, 단백질 그리고 탄수화물인데 여러가지 생 체막의 성분들은 표 1·2 에 보여준다• 이 표에서 m y e li n 이 단백질 함량은 10% 로 제일 적으며 이것은 m y e li n 이 신경세포의 axon 을 감싸 전기 절 연막의 역할만을 하기 때문이다. 한편 생화학적인 기능을 많이 갖는 생 체막일수록 단백질 함량이 많은데 m it ochondr i a 의 내막과 자색막 둥이 약 75% 가 단백질이 되는 것으로 이 사실이 반영된다. 1·2·2 脂訪質 생체막으로부터 지방질을 추출하는 데는 chlorofo r m, e t her 와 benzene
동 비국 성 유 기 용매 가 쓰이는데 이중에서 가장 능률적인 것은 chlorofo r m-meth a nol 혼합 용매 이 다. 추출된 지 방질은 얇은막 ( t h i n laye r) chroma t o gr a ph y로서 각각의 성분으로 분리해낼 수 있다. 생 체 막에 존재 하는 지 방 질 은 크 게 나누면 gly c eroli pid, sph in g o li pid 와 s t erol 로 구분이 된 다. Gl y cero lipi d 는 제일 널리 분포되어 있는 지방질로서 다음 구조를 갖는 g l y cerol 을 바탕으로 하고 있 다 . H— cH- cH— CH— H I I I OI HOI HOIH 이중 가장 중요한 것이 p hos p ho g l y cer i de 로서 그 구조는 다음과 같다. 1CoH2 - 2CoH ― 3CH2-0 一 ?&P - 0 — X C=O C=O R1 R2 이 구조식 에 서 두 개 의 지 방산 R1COOH 와 R2COOH 는 두 개 의 gly c erol OH 와 este r 결 합을 하고 있고 국성 인 X기 는 p hos p ha t e 와 연 결되어 있다. 생체막에 흔히 존재하는 지방산(fatty a ci d) 은 표 1·3 에 표 시하였고 인산(p hos p ha t e) 기에 연결된 X- 기는 표 1·4 에서 보는 것과 같 다.
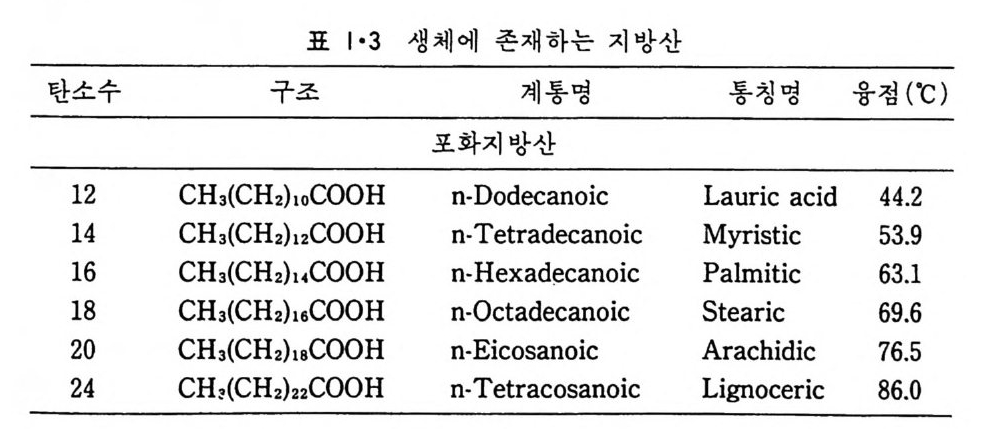 표 I•3 생체에 존재하는 지방산
표 I•3 생체에 존재하는 지방산
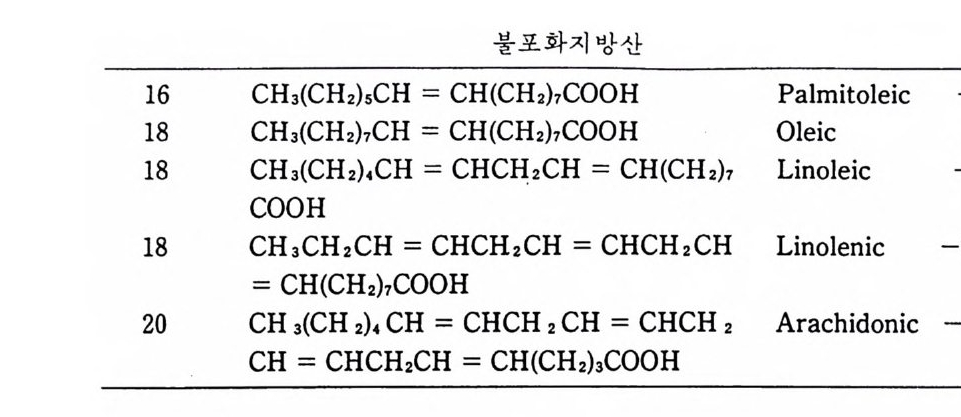 불포 화 지 방 산
불포 화 지 방 산
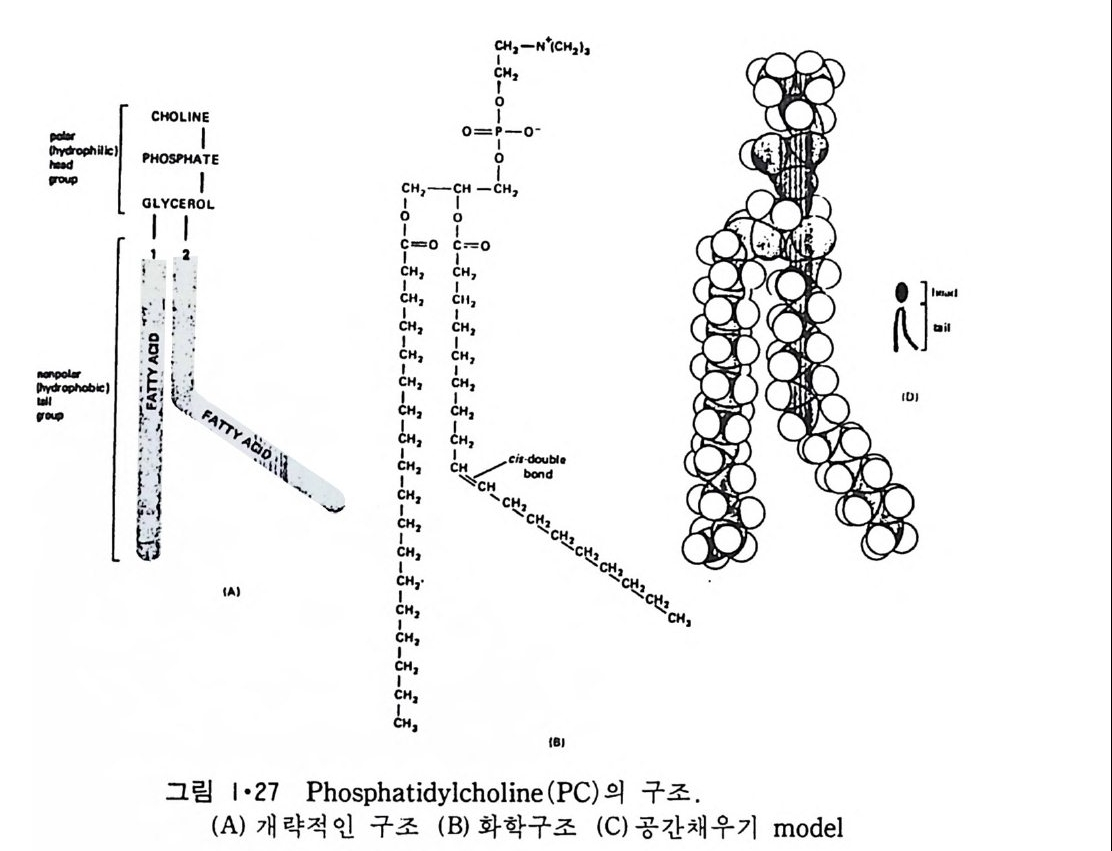
그림 1 •2 7 은 대 표적 인 p hosp ho g l y cer i de 인 ph osph ati dy lc holi ne (PC ) 의 구조식과 분자 model 을 보여준다. 이 그림은 1-ste a ry l, 2-oleil -ph os- p ha ti d y lcho li ne 으로 2 번 위치는 인산기 바로 옆에 있는 ac y l 기를 가리키 며 1 번 위치는 더 떨어져 있는 ac y l 기를 가르킨다. Phos p ho g l y cer i de 의
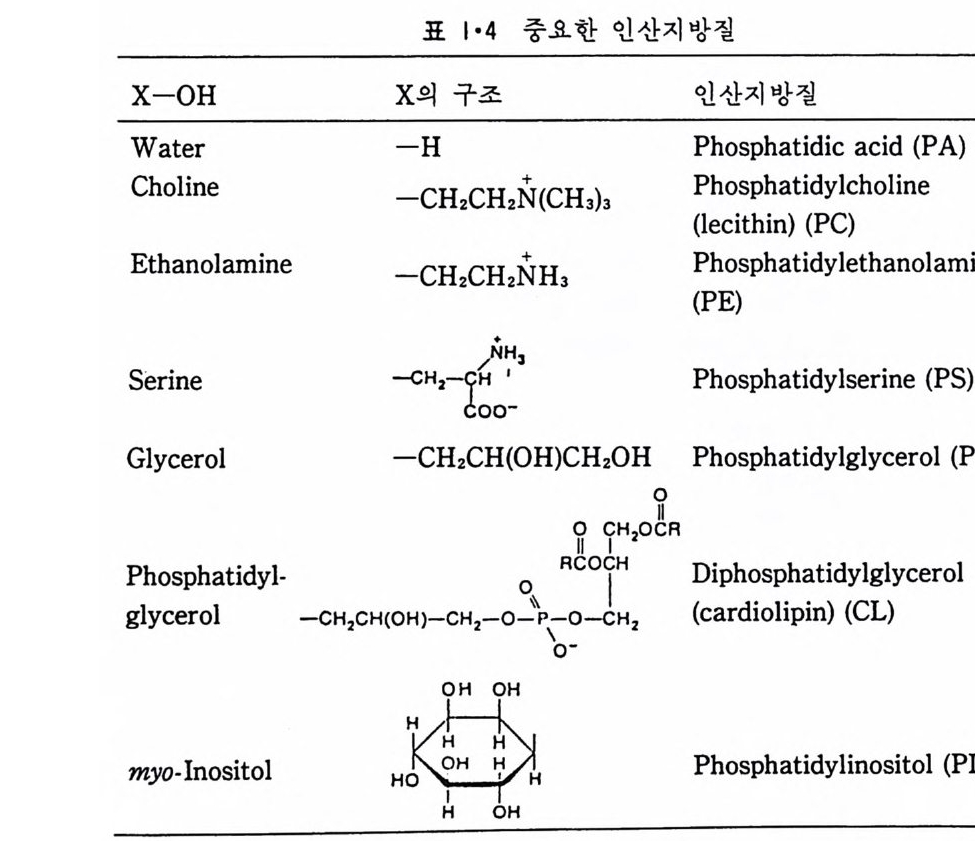 표 I•4 중요한 인산지방질
표 I•4 중요한 인산지방질
 C’H,.I_I5fC.,cH'ur05l''_. o5IC}cHHc5/H ` 7I I ,
C’H,.I_I5fC.,cH'ur05l''_. o5IC}cHHc5/H ` 7I I ,
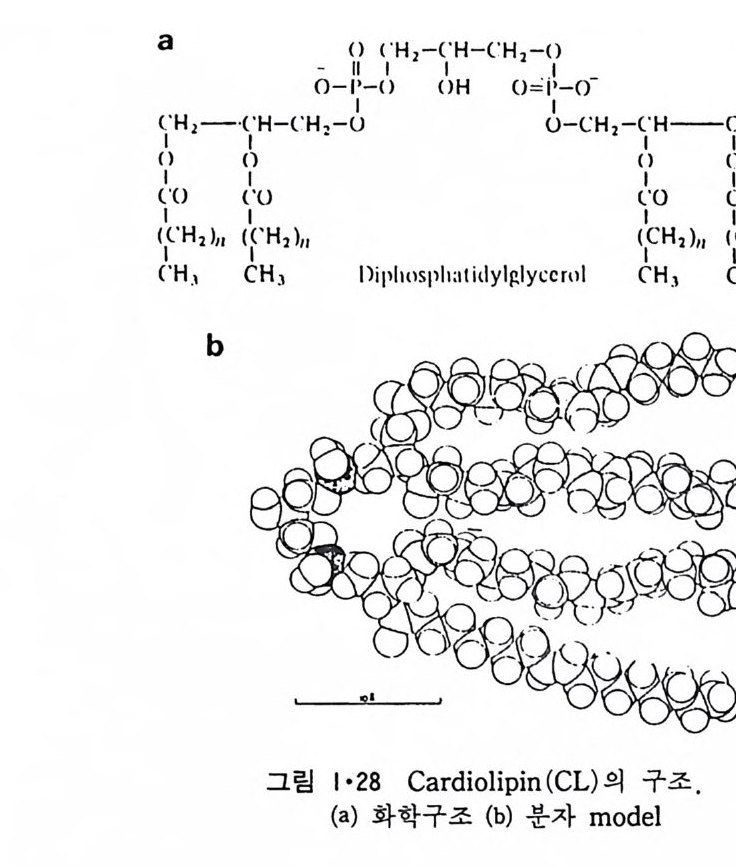
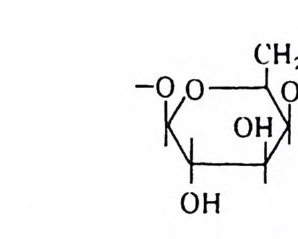
두 acy l 기 가 같을 때 에 는 예 를 들 어 1, 2-dis t e a ry l p hos p ha ti dy lcho li ne 으 로 명명한다. M it ochondr i a 의 內膜에 많이 존재 하는 card i o lipi n 은 다른 pho sp h og - l y cer i de 와는 달 리 2 重 ph osph o g ly c e rid e 이 다 (그 림 1 • 28) . Gl y co lipi d 는 두번째의 g l y cero lipi d 로서 그 기본적 인 구조는 다음과 같 다. CH2 — CH2 ― CH2 ― O 一 X 0I 0I CI =O CI =O RI , RI2 여기서 R 과 R2 는 ph osph o g ly c e ri de 때와 같고 X 는 ga lacto s yl d i ac y l- g l y cerol 의 경 우
 a~(l)· Hi — ·((l). H -CH-z- U(II) (I 'H -2-CI H-('H2-- (uI) - L'H2-((I)H — C(l)H 2
a~(l)· Hi — ·((l). H -CH-z- U(II) (I 'H -2-CI H-('H2-- (uI) - L'H2-((I)H — C(l)H 2
 _::H
_::H
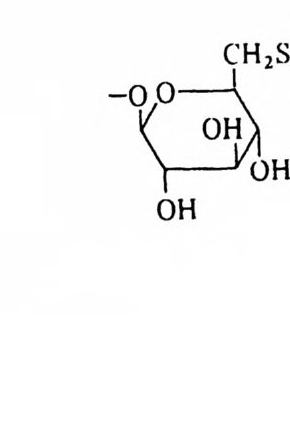
이고 6-sul fo -a-D- q u in ovosl y의 경 우는
 o三) 3 H
o三) 3 H
38
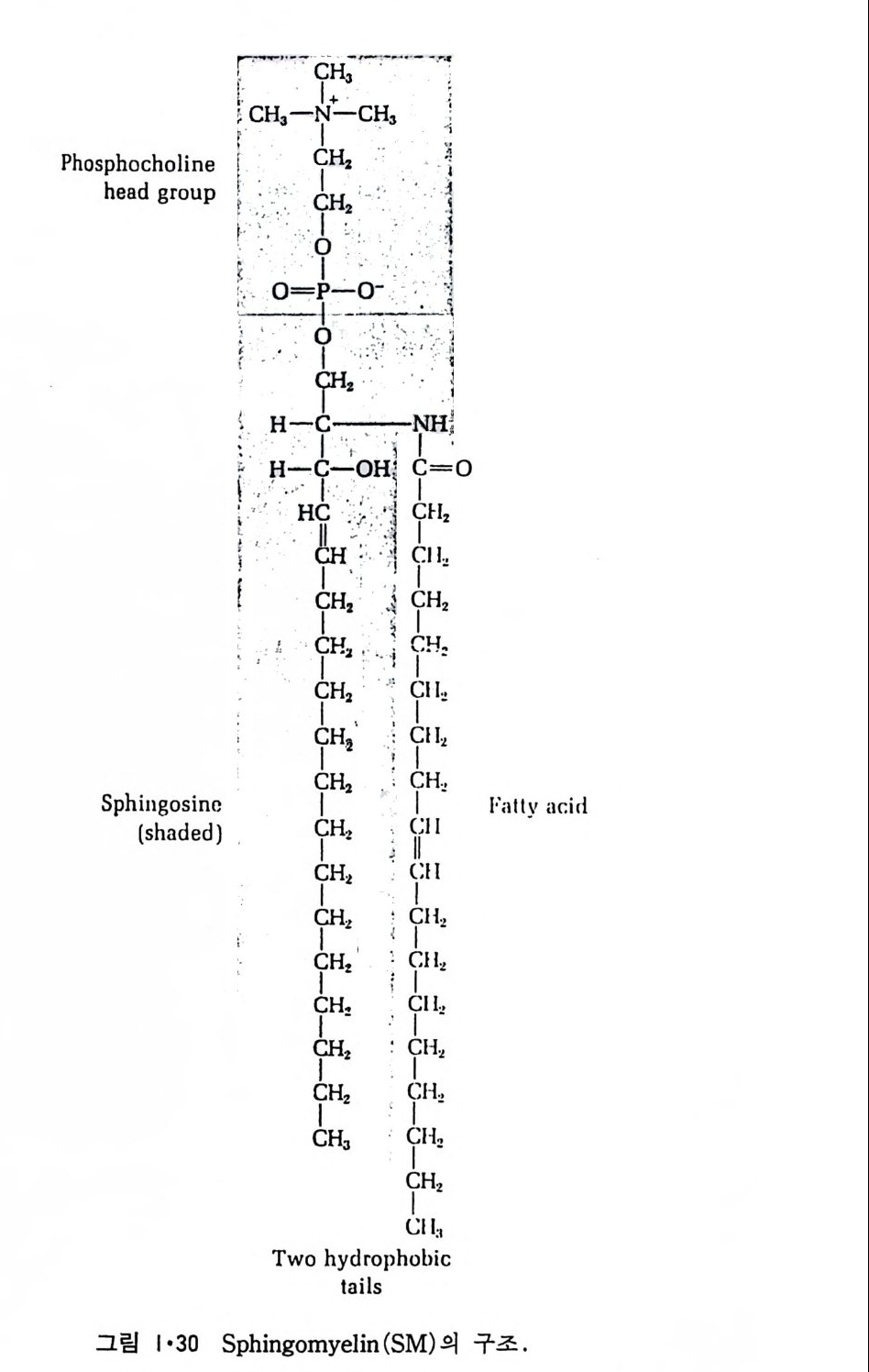
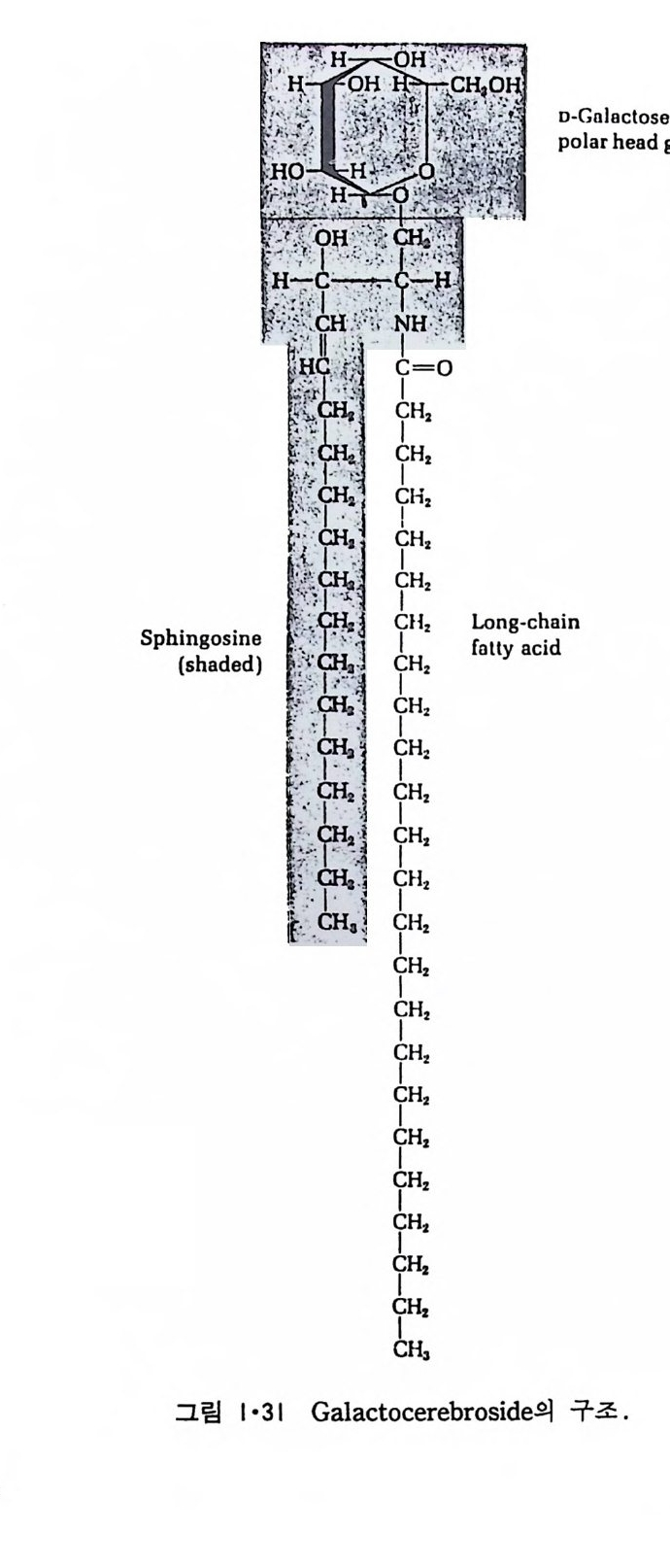
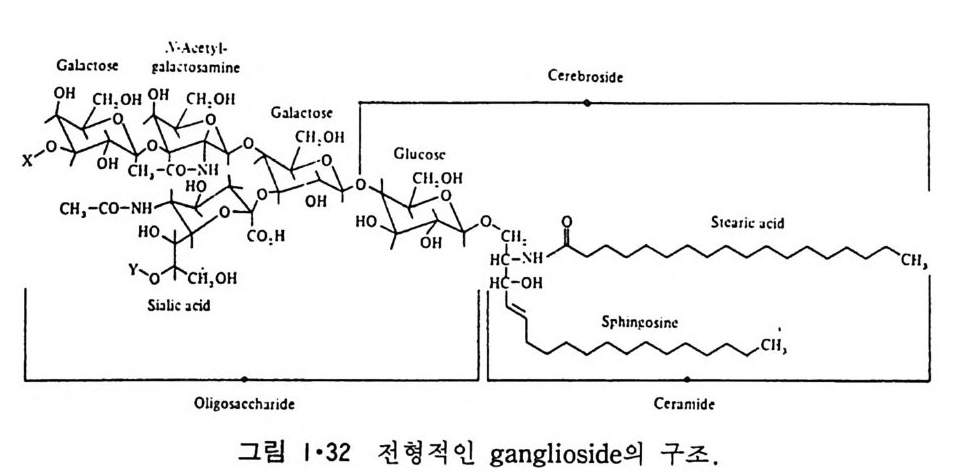
이다. 세 번째 g l y cero lipi d 는 p lasmalo g en 으로 1-0-alky l'-e ny l- 2- ac y l ph os- p ho g l y cerol 이 다. 여 기 서 1 번 위 치 는 este r bond 가 아니 라 eth e r bond 를 가지고 있다. ?- CH2 - CH ― CH2 一 O _ P ― 0 一 X || 0 0 0 CH C=O CIHI R2 십 1 X기 는 cho li ne 과 e t hanolam i ne 인 데 이 들은 choli ne p lasmalo gen 과 eth a nolami ne p lasmalo g en 이 다. S ph i n g o lipi d 들도 역 시 한 개 의 국성 인 머 리 부분과 두 개의 비 국성 인 꼬리 부분을 가지고 있으나 g l y cerol 을 골격으로 하지 않고 그림 1·29 에 서 보여주는 s ph i n g os i ne 이 기본적 인 구조가 된다. 이 것과 이중결합에 두 개의 수소 원자가 첨가되어 생성된 d i h y dros p h i n g os i ne 을 토대로 한 긴 사슬둘을 갖는 ami no alcohol 이 포유동물에 널리 분포되어 있다. S ph i n g o lipi d 는 다시 sph in g o my el i n, cerebros i de 와 g an gli os i de 로 구분 이 된다. 이들은 전부 s ph i n g os i ne 의 am i no 기에 지방산이 결합되어 ami de 결합을 형성해 생성된 ceram i de 의 유도체들이다. S ph i n g om y e li n 은 그림 1·30 에서와 같이 ph osph ocholi ne gr ou p울 가졌 거 나 이 대 신에 p hos p hoe t hanolam i ne 을 가지 고 있고 그 성 질 이 ph osph ati dy lc holi ne (PC) 이 나 ph osph ati dy le th a nolami ne (PE) 과 유사하 다. Phos p ho g l y cer i de 와 sph in g o my e li n (SM) 은 ph osph oli pid 라 고 통 칭 된다. Cerebros i de 는 그 국성 gr ou p이 하전되지 않은 하나 또는 여러 개의 당분으로 구성되어 있으며 그 대표적안 g alac t ocerebros i de 를 그링 1·31 에 나타내었다. Gan gli os i de 는 가장 복잡한 s ph i n g o lipi d 로서 여 러 개 의 당분으로 구성 된 큰 머 리 부분을 가지고 있고 그 대표적 인 ga ng lios id e GM 을 그림 l· 32 에 나타내었다. 이 그림은 cerami de , cerebros i de 와 g a ngli os i de 의 관계
 H。 —H IHI_HC』 E_c_HzHO』 H
H。 —H IHI_HC』 E_c_HzHO』 H
 Phosph ocholi ne
Phosph ocholi ne
 o-Golecto s e, th e
o-Golecto s e, th e
42
 .\ •• . -\ cC I )· I ·
.\ •• . -\ cC I )· I ·
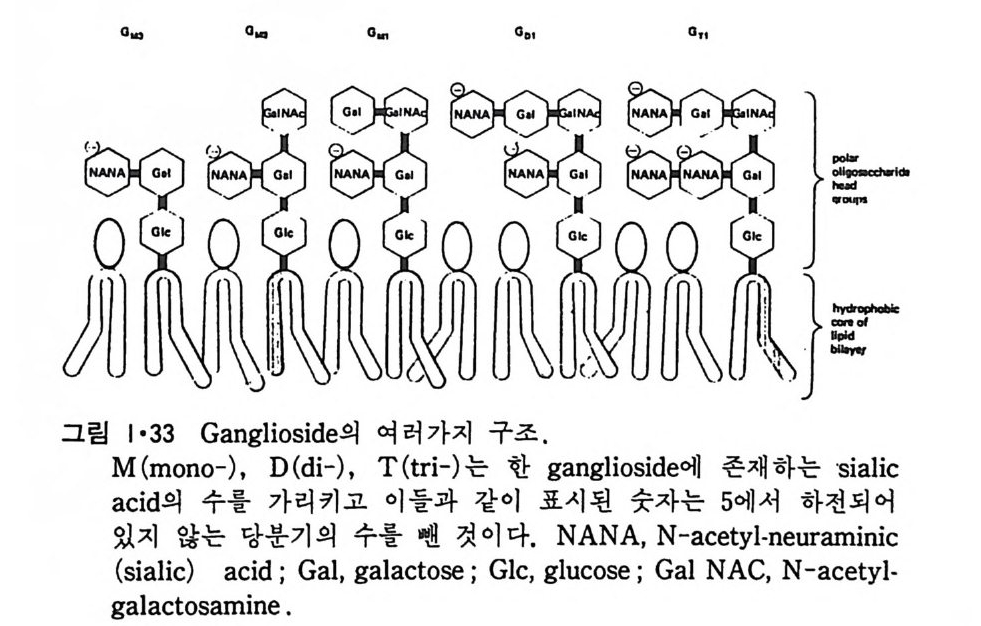
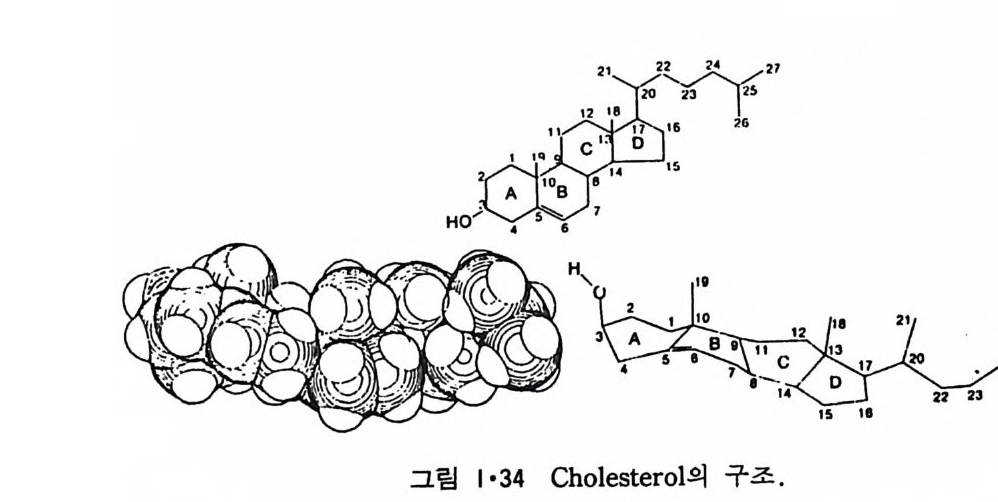
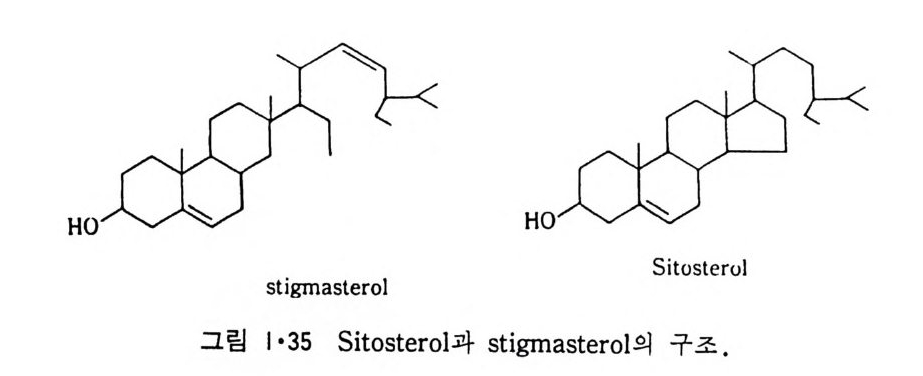
그림 1·33 은 대표적인 g an gli os i de 들을 보여준다. 표 1·5 는 여러 종류의 막의 지방질 분포를 비교한 것이다. Ste r ol 중에서 생체막에 가장 많이 존재하는 choles t erol 은 그림 1·34 에 보여준다. 이것이외에도 1·35 에 보여주는 두 개의 s t erol 도 생체막에 존재한다. 이들 지방질의 성질에서 가장 중요한 것은 한 분자내에 극성인 머리 (head) 부분과 두개의 비극성인 꼬리(t a il)부분으로 나뉘어져 있는 것이다.
 0 .. o. .. 0m o., 0,,
0 .. o. .. 0m o., 0,,
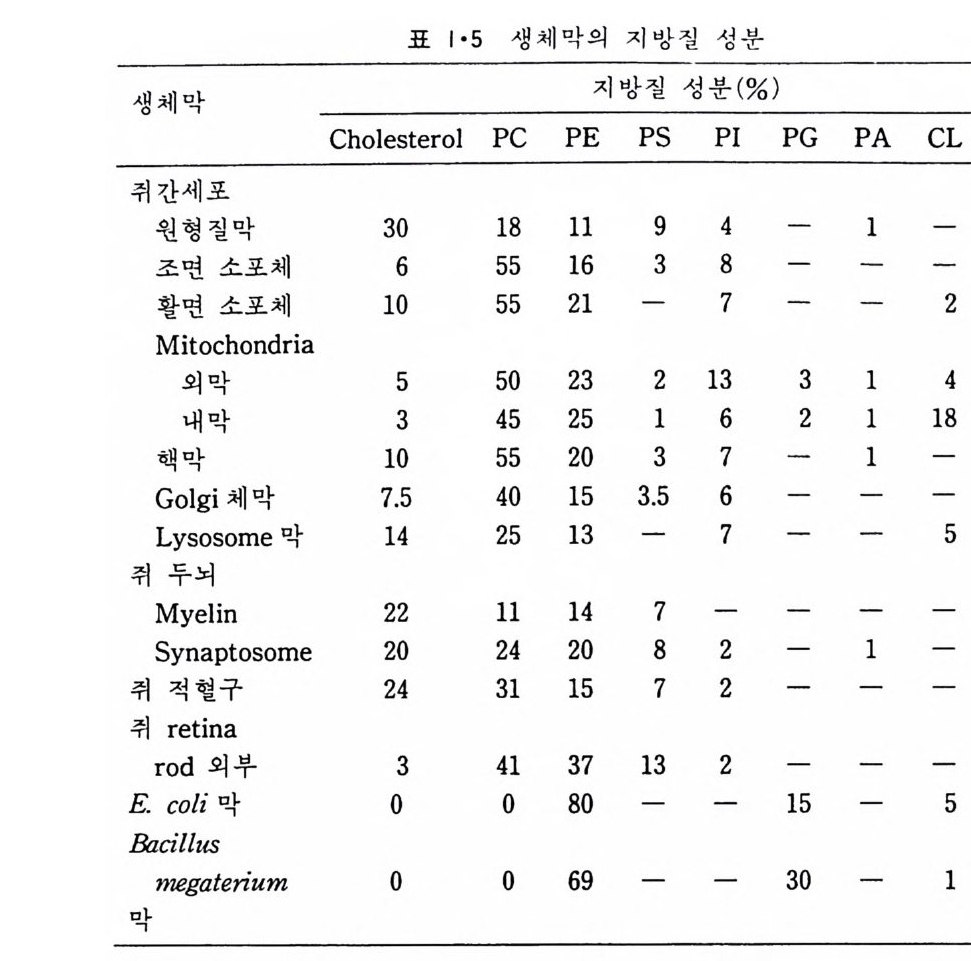 표 I•5 생체막의 지방질 성분
표 I•5 생체막의 지방질 성분
 /2 S 27
/2 S 27
 HO HO
HO HO
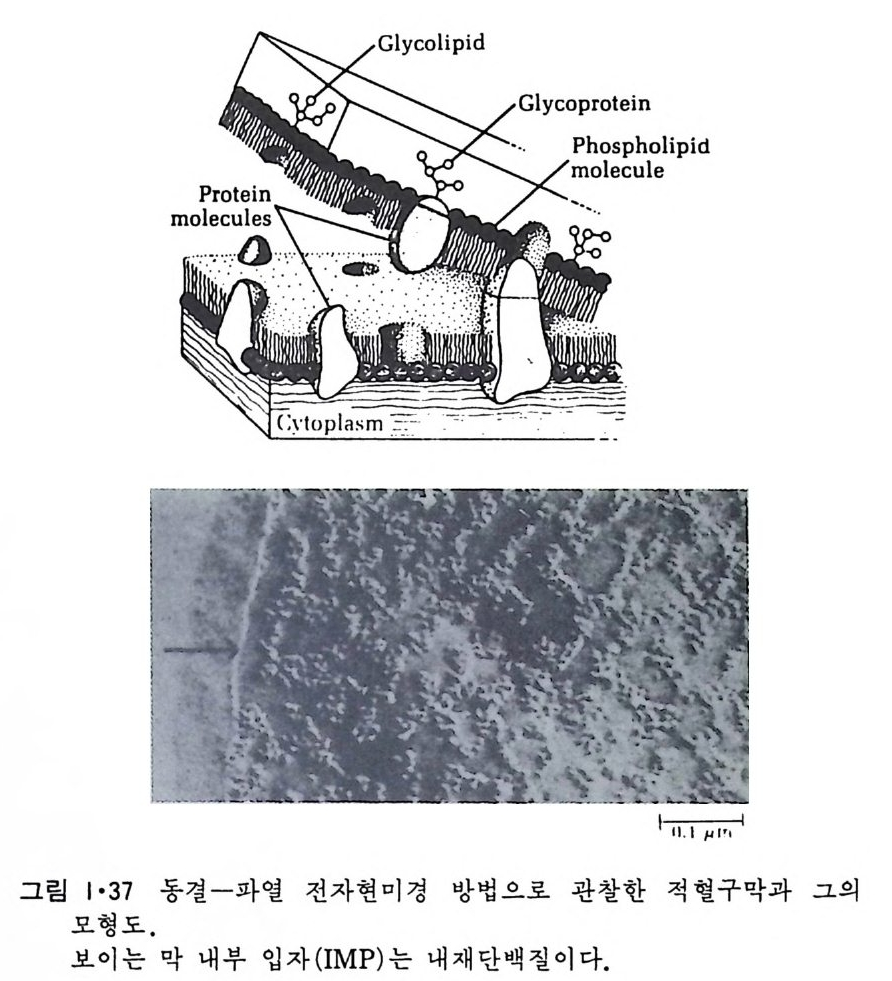
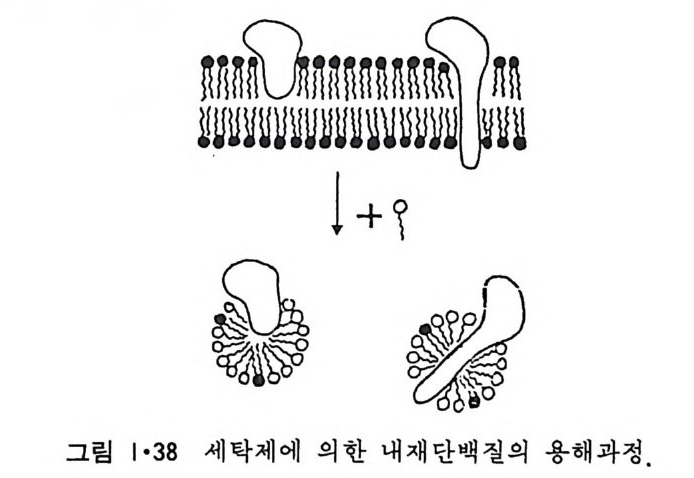
그래 서 이 것 을 양천 성 분자 (am p h ip h ili c molecule 혹은 am p h ip h il e) 이 라고 부른다. 이 양천성 물질의 근본적인 성질은 그 분자의 일부는 찬수성 (h y dro p h ili c) 이 고 나머 지 부분은 소수성 (h ydro p hob ic)인 것 이 다. 인산 지방질(p hosp ho lipi d) 의 국성인 머리 부분은 인산기에 의해 음성 하전을 띠거나 갇이 존재하는 4 차(q ua t erna ry) ammon i um 기 때문에 zwi tter i on 을 형성한다. 그래서 생체막은 보통 음성하전을 띠고 있다. 비극성 꼬리부분을 형성하는 acy l 사슬은 e t h y lene 기의 수가 항상 짝수 이 며 그 중 C16, C1s 과 C20 지 방산이 80% 이 상을 차지 하고 불포화 acy l 사슬에서는 하나에서 여섯 개까지의 이중결합이 있고 18 :1, 18 :2, 18 :3 과 20:4 종류가 90% 이상을 차지한다. 인산 지방질은 일반적으로 한 개의 포화 acyl 사슬을 g l y cerol 골격의 1 번 위치에, 불포화 acy l 사슬을 2 번 위치에 갖는다. 1·2·3 단백질 11)12) 단백질은 세포 내외에 널리 분포되어 있고 또 일부 수용성 단백질이 생체막에 가역적으로 결합되어 있는 것도 있고 하여 생체막 단백질과 다 론 수용성 단백질을 구별하기가 힘들 때가 있다. 그래서 생체막 단백질 은 생리적인 용액으로 계속 씻어서 제거할 수 없는 단백질로 실험적으로 정의하는 것이 통례이다. 생 체 막 단백 질은 주변 단백 질 (extr i n s ic pro te i n 혹은 periph eral pro te i n ) 과 내 재 단백 질 (int r i n s ic pro te i n 혹은 int e g ral pro te i n ) 의 두 가지 로 구분이 된다(그림 1·36). 주변 단백질은 생리적으로 필요한 생체막 단백질이지 만 비교적 약한 정전기적인 (elec t ros t a tic) 힘으로 생체막에 결합되어 있어
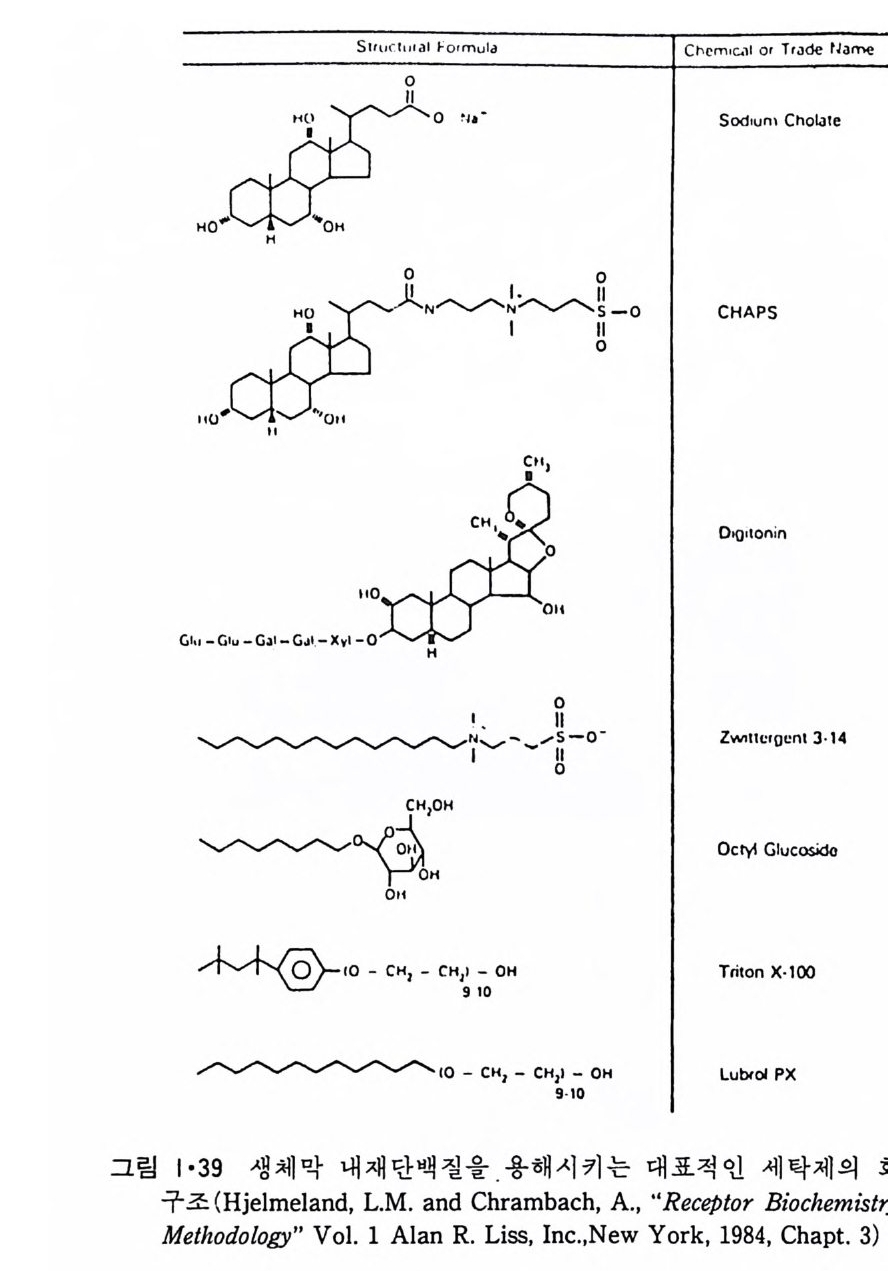
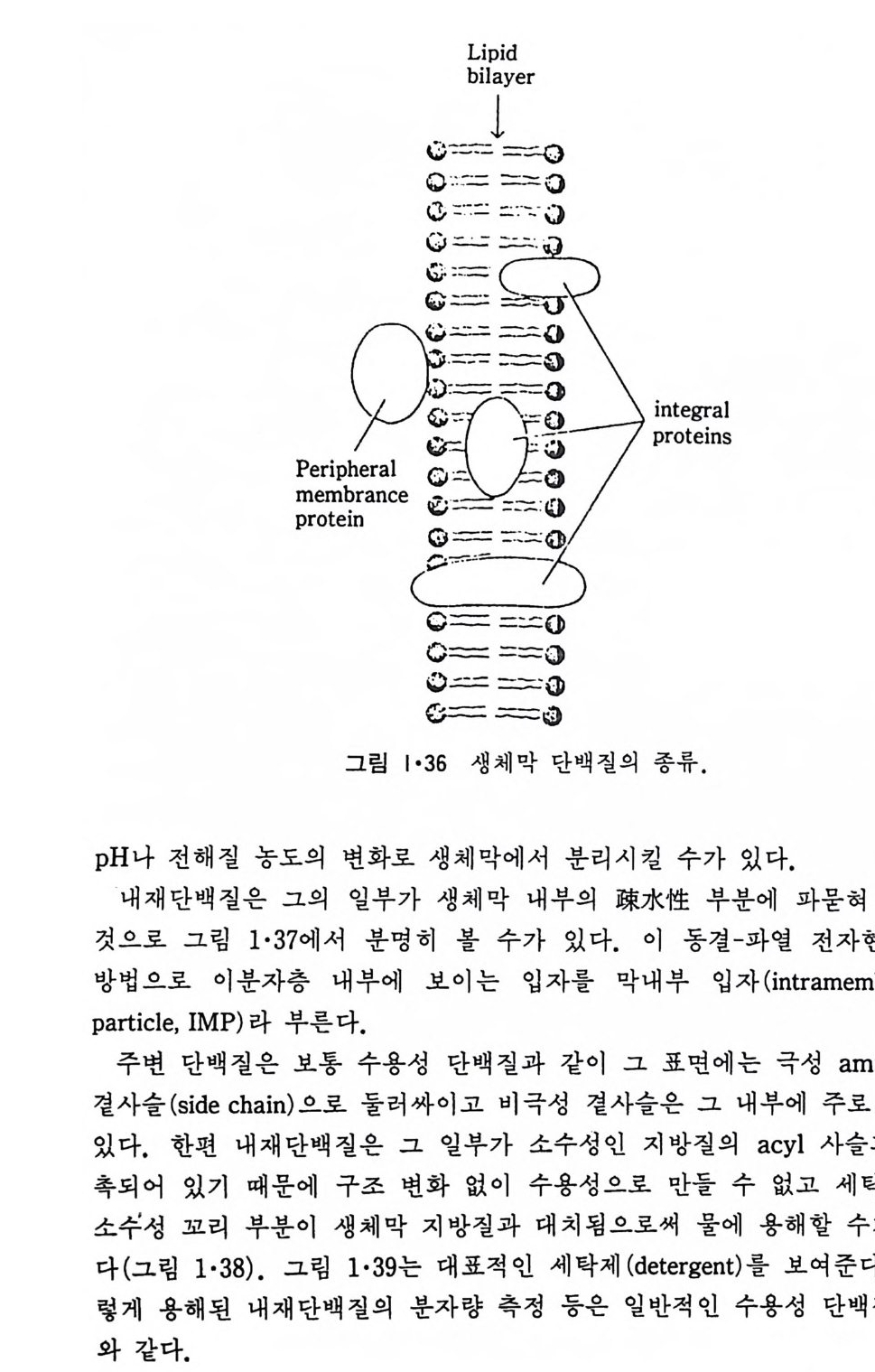 있방p것 H다주법으 .나변로으 로전한단그 해편림백이질 질내 분1은농재·자3도 7층보 에의 통서 내 변 부수분화에용명로 성히 보 생 L0gb 단이체3볼=-』-一 _`_一l―u二i]=도i백l 는o 0Lp퍄i막l_― 0질수l - 에dl『i_『三:나3 -『0 ery과가 입서&0 자 G같(있분를L이다3리 .e 시막 그0 킬내이 0pi n 표부rto/ 수 e동 t면 g e 가i r결 n에a입 sl - 자 는있(파다 i열국. n t 성 r전a m자aemm현b i rn미ao경n 산e
있방p것 H다주법으 .나변로으 로전한단그 해편림백이질 질내 분1은농재·자3도 7층보 에의 통서 내 변 부수분화에용명로 성히 보 생 L0gb 단이체3볼=-』-一 _`_一l―u二i]=도i백l 는o 0Lp퍄i막l_― 0질수l - 에dl『i_『三:나3 -『0 ery과가 입서&0 자 G같(있분를L이다3리 .e 시막 그0 킬내이 0pi n 표부rto/ 수 e동 t면 g e 가i r결 n에a입 sl - 자 는있(파다 i열국. n t 성 r전a m자aemm현b i rn미ao경n 산e
 I II.I µm l
I II.I µm l
 !;;:Unlfnu:! ?i! i:!\
!;;:Unlfnu:! ?i! i:!\
 SI' '' aI k.O ' m ula Chcm , c. 기 1 O, T, a 어 ”am
SI' '' aI k.O ' m ula Chcm , c. 기 1 O, T, a 어 ”am
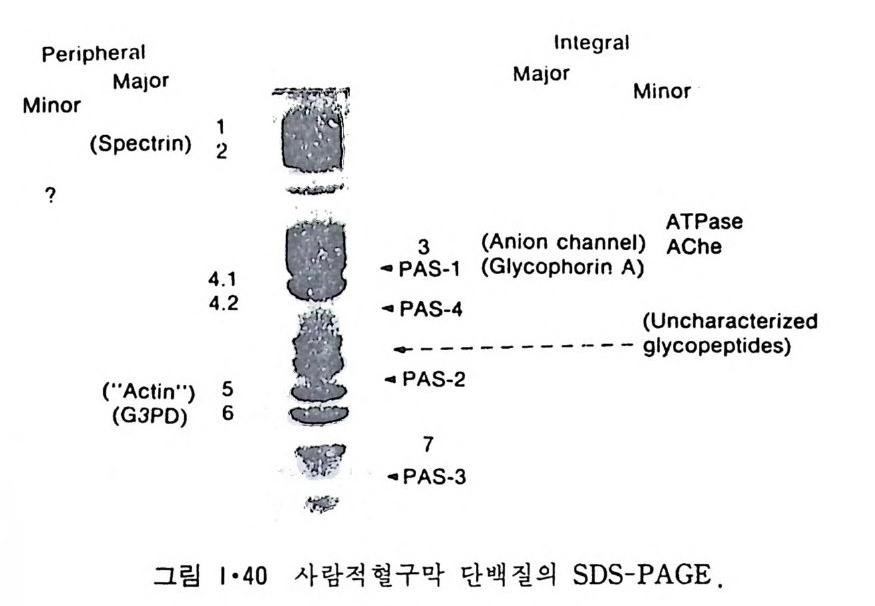
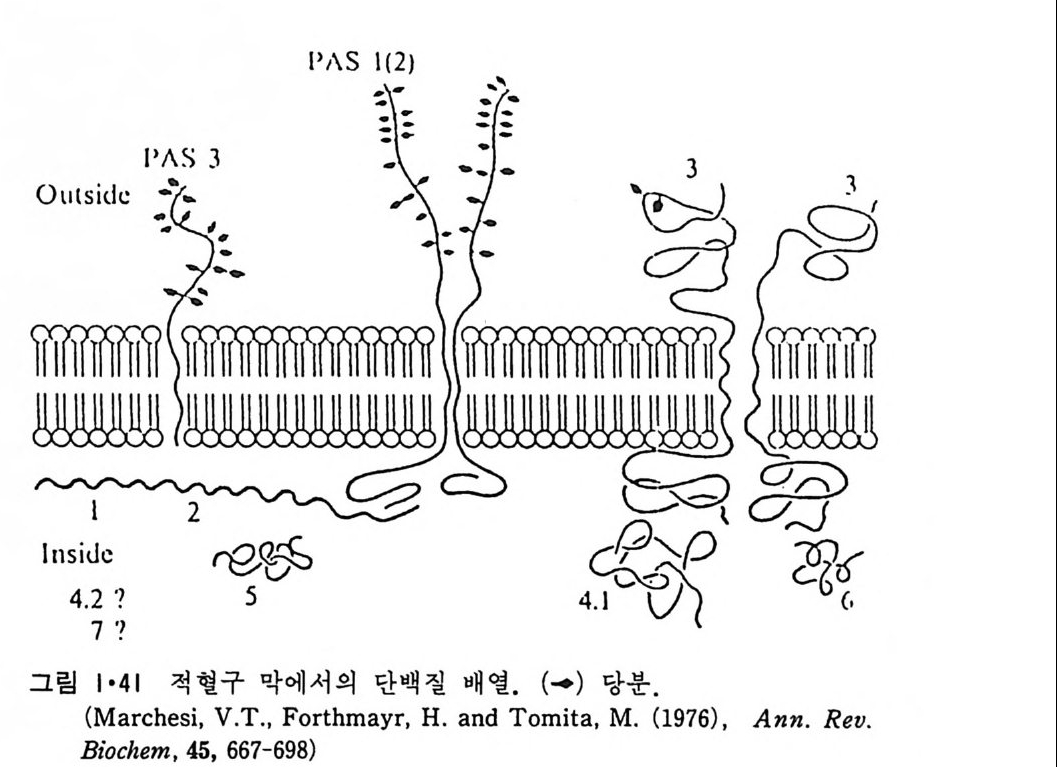
지금까지 생체막 단백질의 성분에 대한 연구가 제일 광범위하게 된 것 은 적혈구막이다. 그림 1·40 은 이 막의 모든 단백질이 SDS-po lya cry- lami de ge l 전기 영동 (SOS-PAGE) 으로 분리된 것을 보여주며 그림 1·4 1 은 이들 단백질들의 적혈구막에서의 위치를 보여준다.
 Perip h eral Inte g ra l
Perip h eral Inte g ra l
 ) ^s 1` `s A s 問캇 .尸p1
) ^s 1` `s A s 問캇 .尸p1
 H( 二 H H 戶 HHO巴 》 H
H( 二 H H 戶 HHO巴 》 H
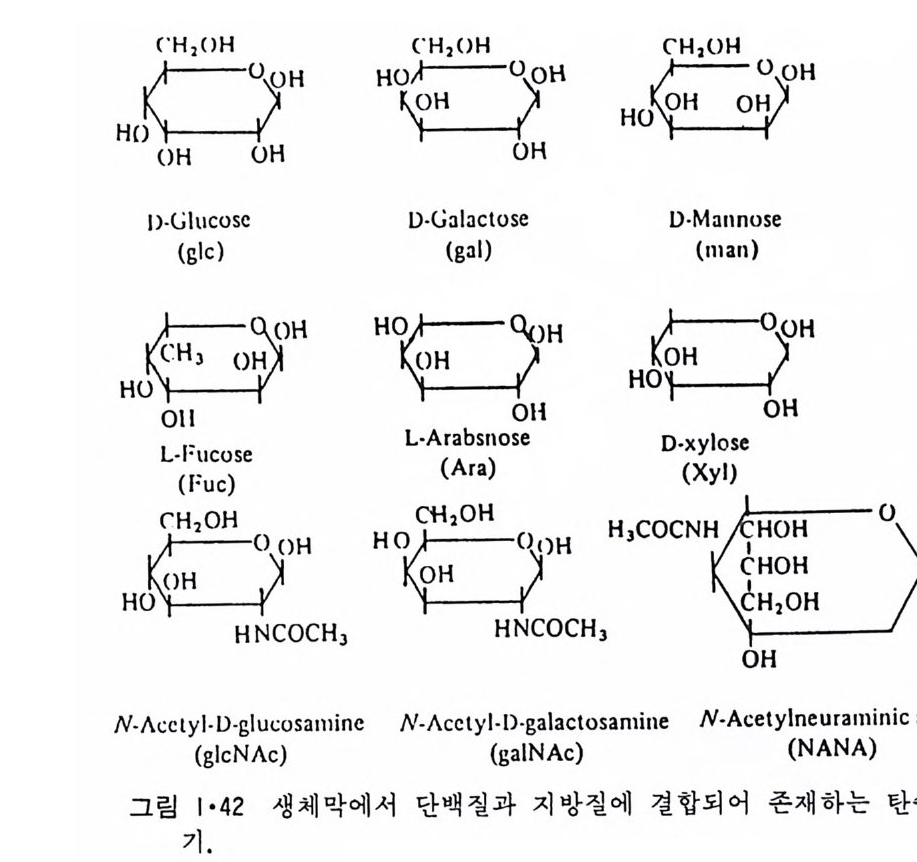
1·2·4 당분 생체막의 약 2~10% 가 당분으로 구성되며 이들은 단백질이나 지방질 과 공유 (covalen t)결합으로 연결되며 거의 전부가 원형질막의 외부에 위 치한다. 원형질막 근처에는 접다당류(또는 g l y cocal y x) 충이 존재하나 이 는 원형질막의 분리 과정 중에 제거되어 생체막 당분과는 분리가 된다. 당분들은 일 단 g l y co lipi d 와 g l y co p ro t e i n 으로서 분리 한 후 화학적 으로 처리하여 탄수화물을 분리해낸다. 이들 당분은 8 개의 당분기까지 갖는 o lig osacchar i de 로 존재하며 이는 그림 1·42 에 보여준다. * I 장 참고문헌 (1) De Robert is, E. D. P. and De Robert is, E. M. F. Cell and Molecular Bi ol ogy ,
Saunders, Phil a delph ia , 1980. (2) Albert s, B., Bray, D., L ewi s, J., Raff , M ., Robert s, K. and Wats o n, J. D. Molecular Bi ol ogy of the Cell, G arland, N. Y. 1983. (3) Darnell, J., Lodis h , H. and Baltim ore, D. Molecular Cell Bi olo g y, Scie n ti fic Americ a n, N. Y. 1986. (4) Malhotr a , S. K. The Plasma Membrane, W iley , N. Y. 1983. (5) Inouy e, M. (ed), Bacte ri al Oute r Membrane W ile y, N. Y. 1979. (6) DiRi e n zo, J. M., Nakamura, K., and Inouy e, M. (1978) Ann. Rev. Bio c hem. 47, 481-532. (7) Ni ka id o , H. and Nakae, T. (1979) Adv. Mi cr obio l . Phys i o l . 14, 163-250. (8) St ae heli n, L. A. and Hull, B. E. (1978) Sc i. Am. 238(5) , 140- 15 2. (9) Franke, W . W ., S cheer, V. , Krohne, G. and Jar asch, E. D., (1981) ]. Cell Bi ol . 91, 3ls-50s (10 ) Jai n , M. K. and Wagn e r, R. C. Intr o dvcti on to Bi ol og ica l Membranes, W iley -Inte r scie n ce, N. Y. 1980. Chap t, 3. (11) Heleniu s , A. and Sim ons, K. (1975) Bi oc hem. Bi op h y s . Acta . 415, 29-79. (I~ Tanfo rd , C. and Rey n olds, J. A . (1976) Bi oc him . Bi op h y s . Acta . 457, 133-170.
제 2 장 Lip o some 생체막은 단백질, 지방질 그리고 탄수화물이 물리적 및 화학적인 회합 으로 형성된 것으로 그 기능은 주로 단백질에 의한 것이지만 구조의 바 탕은 지방질에 의해서 결정된다. 지방질이 생체막 구조를 형성하는 것은 양친성 (am ph ip h ili c) 물질인 이 분자의 국성인 머리부분과 비극성인 꼬리 부분이 물과 작용하는 방식이 매우 다른 점에 기인한다. 따라서 본장에 서는 생체막 지방질의 소수성 꼬리부분과 물과의 작용 및 생체막 지방질 을 물에 넣었을 때 자발적으로 형성되는 lip osome 의 여러가지 성질을 이 야기하고자 한다. 2 • 1 소수성 도 (Hy d rop h obic ity) 1> 물분자는 그 쌍국자 (d ip ole) momen t가 커서 고체상태나 액체상태에서 서로 수소결합을 하고 있다. 물속에 천수성 물질이 들어가면 물과 국성 상호 반옹으로 수화 (h y dra ti on) 되어 안정하게 된다. 따라서 친수성 물질 의 물에 대한 용해도가 크다. 이들 화합물이 물에 용해될 때에 entr o p y 로 보아서는 불리하지만 en t hal py가 크게 감소하기 때문에 자유(fr ee) ener gy도 따라서 크게 감소한다.
 a b
a b
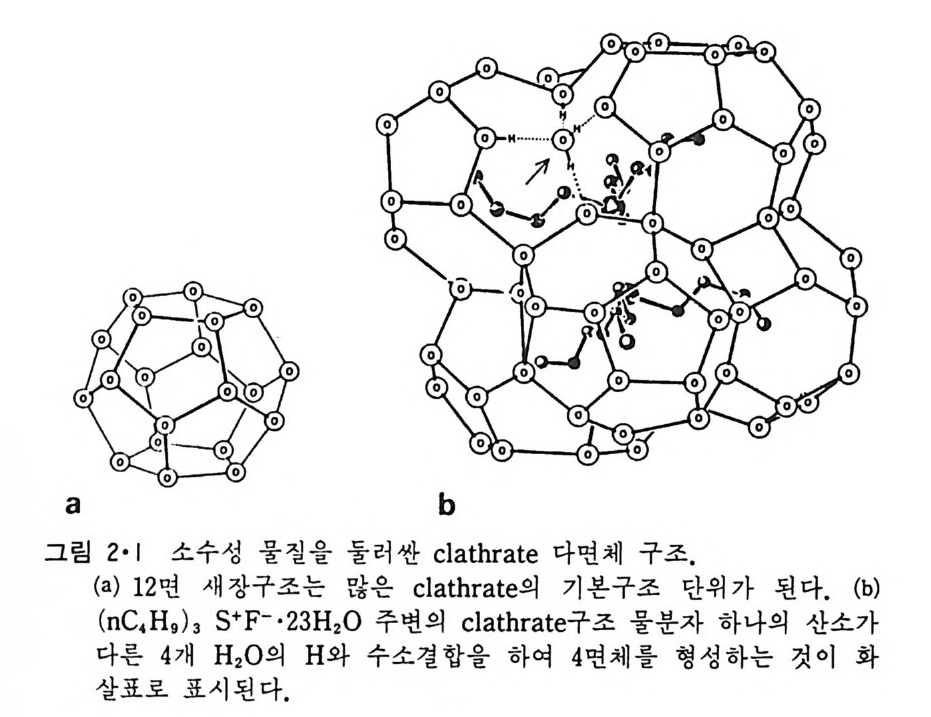
한편 지방질 꼬리부분의 탄화수소 (h y drocarbon) 같은 비국성 분자가 물과 접촉할 때는 물분자가 이 소수성 분자 주위에 새장과 같은 (ca g e- li ke) 구조를 갖는 다면체 (p ol y hedron) 를 형성하여 안정한 수화물 결정을 이룬다(그림 2·l). 이러한 물분자 사이의 수소결합으로 형성된 다면체구조를cla t hra t e 라고 부른다. 이때의 enth a lpy 변화를 표 2·1 에 나타냈는데 이 표에서 서로 다른 비국성 분자들의 en t hal py변화는 거의 비슷해서 15kcal/ mo l 칭도가 된다. 이는 enth a lpy 번화(t::. H) 가 용질과 물과의 상호
 표 2•I 비국성 물질이 수화될 때 발생하는 enth a lpy
표 2•I 비국성 물질이 수화될 때 발생하는 enth a lpy
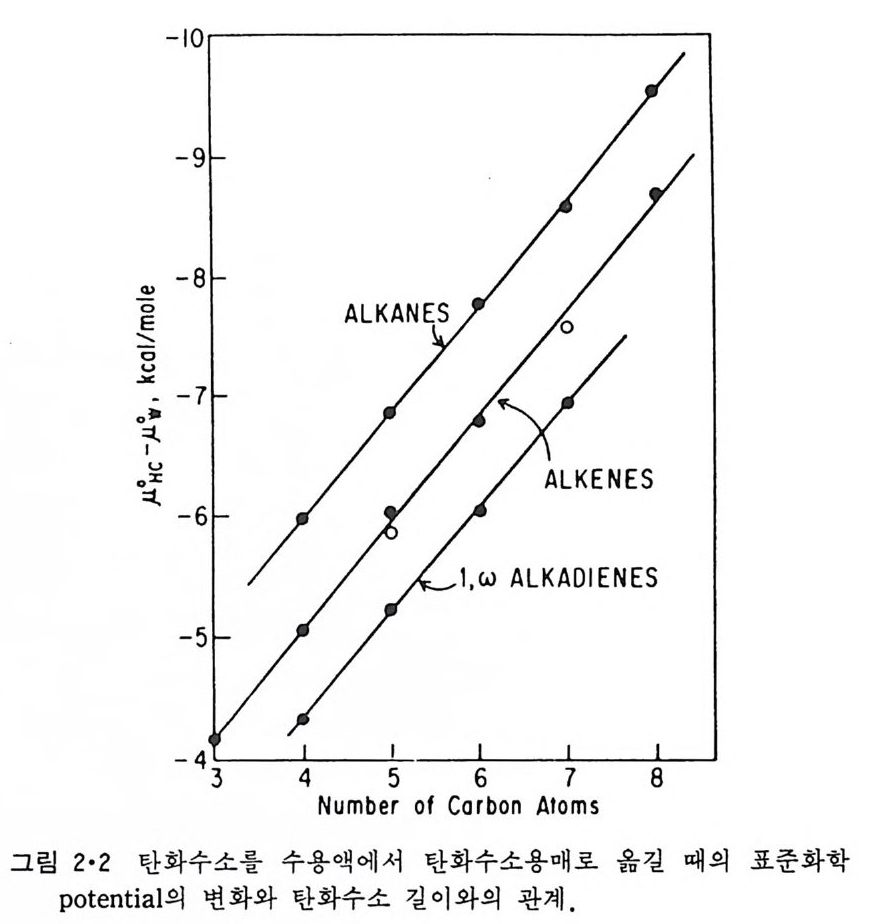
반옹에 의한 것이 아니고, 물분자가 서로 수소결합을 이루어 용질 주변 에 다면체 구조를 형성할 때에 방출되는 열이기 때문이다. 이때 AH 는 감소하지만 entr o p y 변화 (AS) 의 감소에 의한 자유 energy 변화 (AG) 의 중가가 너무 커서 비극성 물질이 물에 찰 용해되지 않는다(식 2·1). AG=AH-TAS 이 식에서 T 는 절대온도 (absolu t e t em pe ra t ure) 를 나타낸다. 이렇게 비국성 물질 주변에 물분자 cla t hra t e 가 형성되는 것과 이에 따 르는 en t ro py의 감소로 인해 비국성 물질이 물에 찰 안 녹는 성질을 소 수 성 효 과 (hy d rop h obic eff ec t) 라 고 한 다. 이 소 수 성 의 정 도 (hy d ro· p hob icity)는 탄화수소를 수용액에서 탄화수소 용매로 옮길 때 필요한 자 유 ener gy로 정의할 수 있다. 탄화수소가 물에 용해되었을 때의 화학 p o t en ti al 은 다음과 같이 나타 낸다. µw = µ~ + RT lnXw + RT lnf w (2·2) 이 식에서 µID 는 탄화수소가 물에 녹았을 때의 화학 p o t en ti al 이고, µ~ 는 표준상태 에 서 의 무한대 로 희 석 (inf i ni t e dil ut i on ) 된 탄화수소의 화학 p o t en ti al 로 탄화수소와 물과의 상호작용을 전부 포함하고 있다. R 은 기 체상수 XID 는 수용액에서의 용질의 몰분율 (mole frac ti on ) 그리고 /w 는 그 활성 도 계 수 (acti vi t y coeff icien t) 이 다. RTlnXw 는 화학 po t en ti a] 중 혼합 en t ro py에 의한 순전히 통계적인 부분만을 표시하며, RTlnfw 는 용질간 의 상호작용에 의한 화학 p o t en ti al 을 표시한다. 탄화수소가 유사한 구조를 가진 용매에 녹았을 때의 화학 p o t en ti al 은 다음과 같이 표시된다. µhe = µ,.c + RTlnXhc + RTlnfh c (2·3) 여기서 Xhc = /he = 1 이므로 µhe = µ,,려고 또 탄화수소가 물에 포화상 태로 용해될 경우 순수한 탄화수소 상과 탄화수소로 포화된 수용액상이 접촉되어 있어 µw = µhe 이므로 식 (2·2) 와 식 (2·3) 으로부터 따 c -µ~ = RTlnXw (2·4) 이때에 품은 용액만을 고려했기 때문에 fw = 1 조건이 성립된다. 식 2·4 에서 µ,.c 는 용질인 탄화수소가 이들 두 용매내에서 나타내는 본질적인
 -10
-10
성질의 차이이다. 따라서 물에 대한 탄화수소의 용해도로부터 µ,,c _ µ; 의 값을 계산할 수 있으며 이 값이 탄화수소의 소수성의 척도가 된다. 그림 2·2 는 탄화수소의 길이와 소수성도와의 관계를 나타낸 것이다. µ,,c _ µ묘값이 탄화수소 분자의 길이예 바례함을 알 수 있다· 그림 2·2 에 서의 직선은 포화 탄화수소의 경우 다음 실험식으로 표시할 수 있다. µ,.c - µ;'.,, = -2 436 - 884 nc (cal/ mo l) (2·5) 또는 µ,.c - µ;,, = -2102ncH3 - 884ncH2 (2·6) 이들 식에서 nc 는 탄화수소 분자의 탄소수, ncH3 는 _CH3 기의 수 그리고 ncH2 는 e t hy lene 기 의 수를 표시 한다.
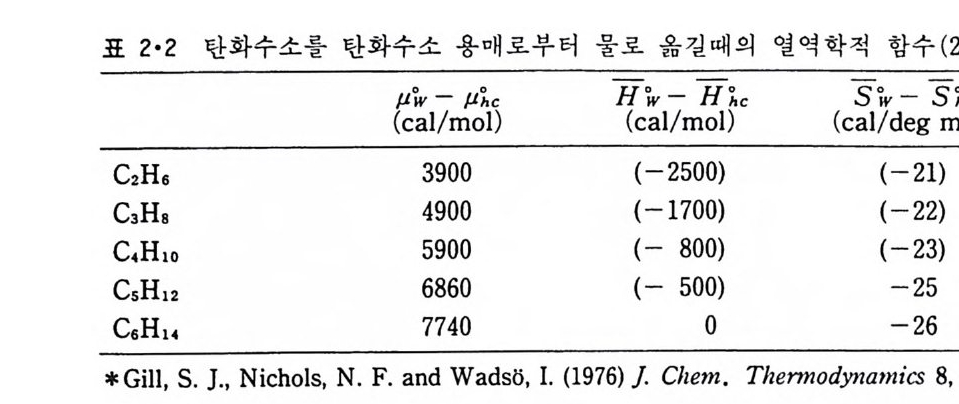 표 2·2 탄화수소를 탄화수소 용매로부터 물로 옮길때의 열역학적 함수 (25•c)
표 2·2 탄화수소를 탄화수소 용매로부터 물로 옮길때의 열역학적 함수 (25•c)
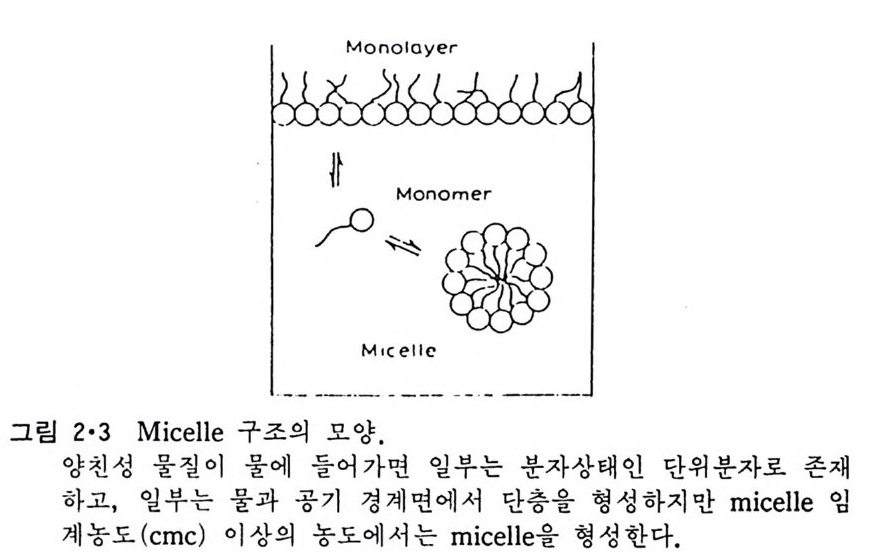
화학 p o t en ti al 과 분몰 enth alpy (H) 및 분몰 en t ro py (S0) 와의 관계는 식 2·7 로 표시된다. µ,,c- µ;',, = llh~ -l !; - 穴 sh~ -s 읽 @刀 표 2·2 는 비교적 간단한 탄화수소의 용해도를 여러 온도에서 측정하여 얻은 열 역 학적 함수를 나타낸 것 이 다. 이 표에 서 en t hal py변화만 가지 고 는 탄화수소가 물에 녹는 것이 열역학적으로 유리하지만, en t ro py변화가 불리한 방향으로 변화하기 때문에 자유 ener gy의 중가로 결국 탄화수소 가 물에 찰 녹지 않게 된다는 것을 알 수 있다. 2·2 Mi cel le1> 미량의 양천성 물질이 물에 들어가면 이들은 용해되어 분자 단위로 독 립적으로 존재하지만 소수성 꼬리 부분 때문에 그 용해도는 적다. 따라 서 농도가 어느정도 이상으로 되면 더 가해진 양천성 물질은 협동적 (coo pe ra ti ve) 으로 회합하여 큰 입자를 형성하므로 분자 상태로 존재하는양천성 물질의 농도는 더이상 중가하지 않는다. 이렇게 형성된 큰 입자 를 m ic elle 이라 하며 (그림 2·3) 이와 공존하는 분자 상태 양천성 화합물의 농도를 mi cel le 임 계 농도 (criti ca l niice lle concentr a ti on , cmc) 라 한다 (그림 2·4). M ic elle 의 형성은 천수성인 머리 부분과 소수성인 꼬리 부분의 물 과의 작용 방식이 매우 다른 데 기인하는 것으로 相(p hase) 의 분리가 국
 Monolay e r
Monolay e r
한된 범위내에서 이루어지는 것이라 볼 수 있다. 그림 2·3 은 m ic elle 의 구조를 보여주는데 국성인 머리는 수용액을 향하고 비극성인 꼬리 부분 은 m ic elle 의 내부를 향한다. 그림 2·4 는 mi ce lle 형성시 분자 상태의 양 천성 물질, 즉 단위분자 (monomer) 의 농도와 전체 농도와 관계를 나타낸 것이다. 또 이 그림은 m ic elle 형성이 상분리와 유사한 것을 보여준다. 그
 E 1.5 •-
E 1.5 •-
링 2·3 에 보이는 구조는 탄화수소 사슬 (cha i n) 이 하나만 있는 양천성 분 자가 형성하는 m ic elle 이고 사슬이 두 개인 양친성 물질은 보통 이분자층 (b i la y er) 을 형성하는데 흔히 m ic elle 은 넓은 의미로 이 양자를 다 포함하 나 여기서는 전자만을 의미하는 것으로 한다. M ic elle 의 내부를 향하고 있는 탄화수소 꼬리 부분은 순수한 탄화수소 와 그 성질이 유사한데 이는 열역학적으로 다음과 같이 증명된다. Mi ce lle 내 부에 용해 된 탄화수소의 화학 p o t en ti al 은 다음 식 으로 나타 낼 수 있다. µm ic = µ~ic + RT!nXmi c + RT!nf mi c (2 ·8) 여 기 서 m ic은 m ic elle 내 에 서 탄화수소의 여 러 가지 열 역 학적 인 함수를 의미한다. 탄화수소를 수용액에서 m ic elle 내부로 옮길 때의 화학 p o t en ti al 의 변화는 식 2·2 와 식 2·8 에서 얻을 수 있는데 그 결과는 식 2·9 와 같다. µ';,,;c - µ'w = RT[n (Xw/Xm;c) (2 ·9) 몸은 용액만을 고려하면 이때 활성계수 (ac ti v ity coe ffici en t)는 1 이 된다. Mi ce lle 용액에서 수용액과 m ic elle 내부에서의 탄화수소의 용해도를 각 각 측정하여 얻은 결과를 식 2·9 에 대입하여 얻은 실험식은 µ;'.,,ic - µ'w = —193 4 - 77lnc (2 • 10) 인데 이들 상수는 식 2·5 의 값보다 약간씩 작다. 여기서 얻은 열역학적 함수를 표 2·3 에 나타냈는데 이 표안의 숫자는 탄화수소를 수용액에서 탄화수소 용매로 옮길 때의 함수와 유사하다. 이것은 m ic elle 의 내부에
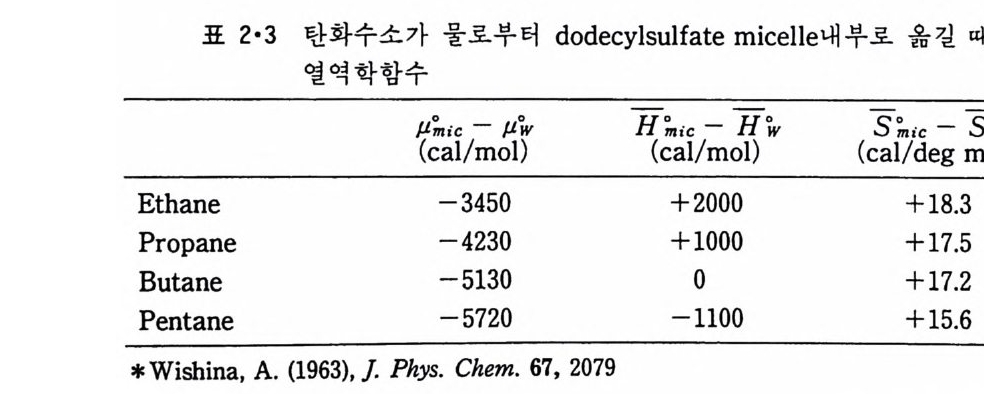 표 2•3 탄화수소가 물로부터 dodecy ls ulfa te m ic elle 내부로 옮길 때의
표 2•3 탄화수소가 물로부터 dodecy ls ulfa te m ic elle 내부로 옮길 때의
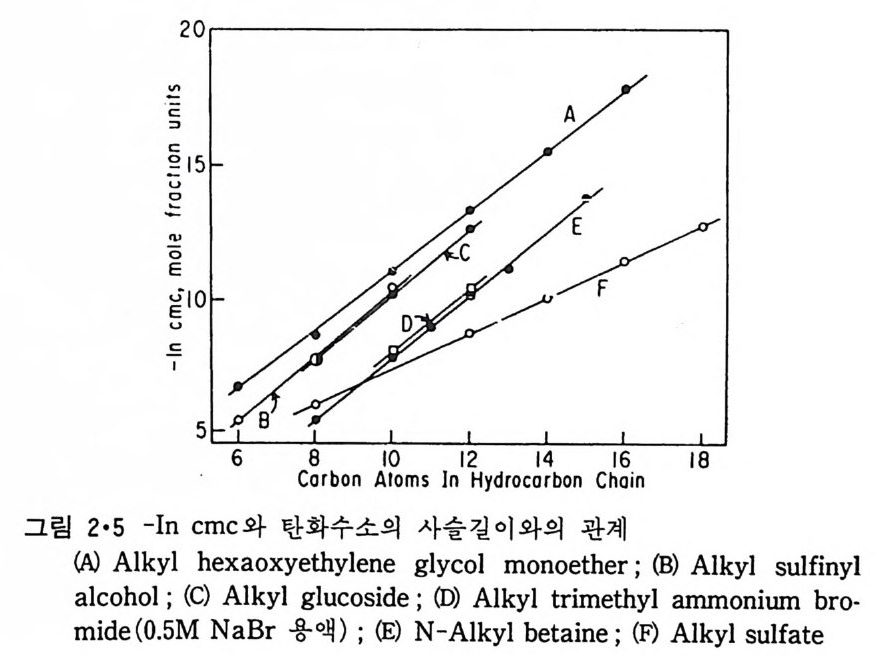
액체 탄화수소와 비슷하다는 것을 의미한다. 이 표에서 en t ro py와 en t hal py의 값이 탄화수소 용매 때보다 약간 작은 것은 mi ce lle 표면에서 탄화수소 사슬이 운동의 제한을 어느 정도 받는 것으로 설명이 된다. 수용액 내에서 m ic elle 과 이의 성분인 양천성 분자 사이의 평형은 상 분리로 간주하며 다음 식으로 표시할 수 있다. µa,;.;c - µ' =:,, RTlnX'w (2 • 11) 이 식에서 (')는 식 2·7 의 경우처럼 탄화수소 화합물이 아니라 양천성 물 질 자체의 열역학적인 함수를 의미한다. Mole 분율인 X'규 큰 cmc 이므로 µ<>,;.;c - µ';~ ~ RTlncmc (2 • 12) 그림 2·5 는 몇 가지 양천성 물질의 cmc 값을 식 2·12 에 대입하여 얻은 값과 양천성 물질의 탄화수소 사술들의 길이와의 관계를 나타낸 것이고 그중 n-alk y lbe t a i ne 인 경 우 다음과 같은 실 험 식 을 얻 었 다. µ;,;ic - µ,; = 2514 - 709nc (2 • 13) 다른 양천성 물질에 대해서도 유사한 실험식을 얻었는데 여기서 철편 (i n t erce pt)은 식 2·10 과는 달리 +이고 nc 기울기도 전보다 작다. 이것은
 20
20
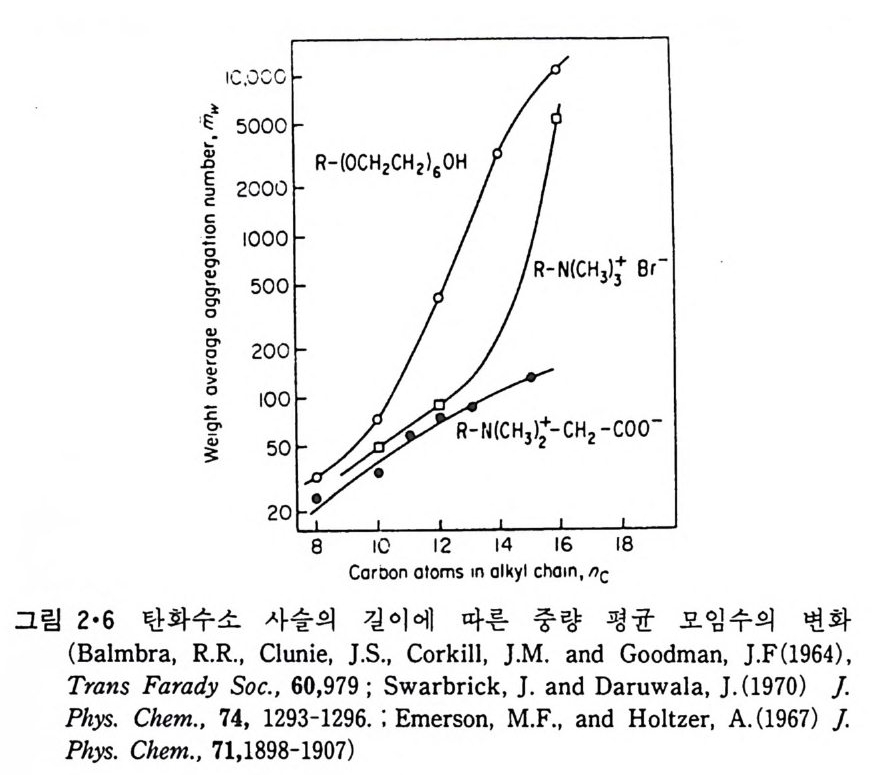
양천성 물질에서 국성인 머리 부분에 기인하는 것으로 생각할 수 있다. M ic elle 의 형성은 다음 두 가지의 서로 상반되는 힘에 의해서 지배된다. (a) 탄화수소 꼬리끼리 서로 응집하려는 소수성 힘, 죽 상분리를 일으키려는 경향. (b) 국성의 머리 부분 상호간의 반발력, 즉 서로 멀리 떨어지려는 경 향. 탄화수소 부분이 상분리를 하여 뭉치면 소수성상의 주변에서 수용액과접촉하고 있는 극성 머리 부분끼리 거리가 가까워져서 상호 반발력(rep u lsiv e for ce) 이 작용하므로 m ic elle 의 크기 가 어 느 이 상이 되 면 더 커지지 못한다. 식 2·5 와 식 2·13 에서 1Ic 의 값이 같을 때 µ젊 1C' - µ?; 값이 µ,,c _ µt 값보다 큰 이유는 국성 머 리 부분끼 리의 반말력 ( re p따히 ve fo rce) 과 또 이 머리 부분에 인접해 있는 -CH2 一기는 용매로서의 효력이 없기 때문이다. 이렇게 m ic elle 의 탄화수소 꼬리 부분은 회합하여 상분리를 하려 하기 때문에 큰 입자를 형성하려는 경향이 있고 국성인 머 리 부분은 이에 반하여 m ic elle 의 크기에 제한울 주게 되는데 표 2·4 는극성인 머리 부분이 m ic elle 의 크기예 많은 영향을 주는 것을 보여준다. C10H21NH!Br- 의 4 차 ammon i um 기의 수소를 me t h y l 기로 계속 치환하면 그 모임수는 계속 감소한다. 그림 2·6 은 탄화수소 꼬리 부분의 길이 가 늘어감에 따라 모임수가 증가하는 것을 보여준다. 여러가지 실험 결과에 의하면 작은 m ic elle 들의 모양은 구형에 가까우나 큰 m ic elle 들은 구형에서 현저히 벗어난다. 이 이유는 양천성 분자의걸이보다 더 큰 반경을 갖는 구형의 m ic elle 은 형성될 수가 없으므로
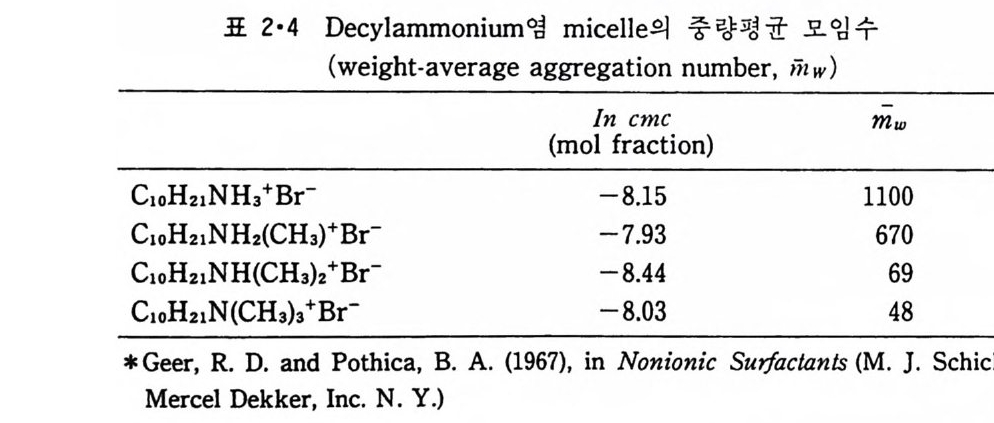 표 2•4 Dec y lammon i um 영 m i celle 의 중량평균 모임수
표 2•4 Dec y lammon i um 영 m i celle 의 중량평균 모임수
 」c 3Q c oo
」c 3Q c oo
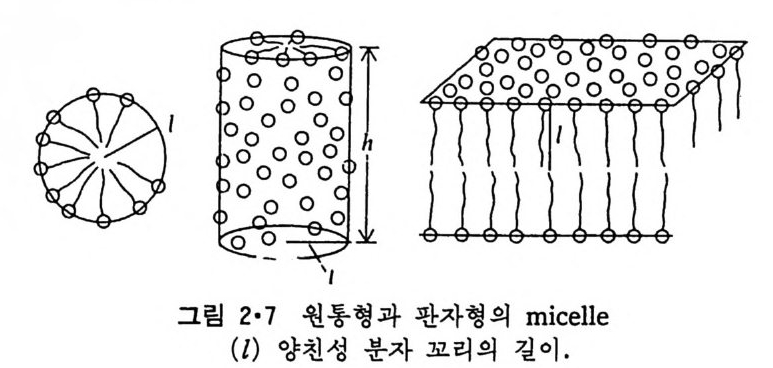
m ic elle 이 커질 수 있는 방법은 타원체형을 이룰 수밖에 없기 때문이다. 따라서 안정한 m ic elle 들은 대부분 타원체형을 가지고 있고 양천성 물질 의 농도를 국단으로 증가시키면 타원체에서 원통형 (rod sha pe)으로 또는 판자형 (sheet fo rm) 으로도 변한다(그림 2·7). 그러나 물이 충분히 존재하 는 상태에서 꼬리 부분이 하나인 양천성 물질의 m ic elle 의 안칭한 모양은 구형이나 타원체인데 그 이유는 원통형이나 판자형에서는 머리 부분끼리 의 거리가 너무 가깝기때문이다.
 l^h
l^h
타원체에 가까운 100 개의 양천성 물질 분자로 이루어진 m ic elle 에서 10000 개 분자의 m ic elle 로 커 질 경 우 머 리 하나가 차지 하는 넓 이 가 20% 이상 감소한다. 이때에 생기는 큰 반발력 때문에 회합하는 정도가 작게 되고 따라서 원통형에 그치고 만다. 한편 꼬리 부분이 두 개인 양천성 물질에서는 구형이나 타원체를 형성하면 머리 부분끼리의 거리가 너무 멀어진다. 그 경우 용매인 물이 소수성 꼬리 부분까지 접촉하게 되어 머 리 부분끼리의 거리를 줄이는 방법은 이분자층을 형성하는 것이다. 그립 2·8 에서 꼬리 부분이 하나인 양천성 물질은 머리 부분이 꼬리 부분보다
 a LIPID PHASE MOLECULAR
a LIPID PHASE MOLECULAR
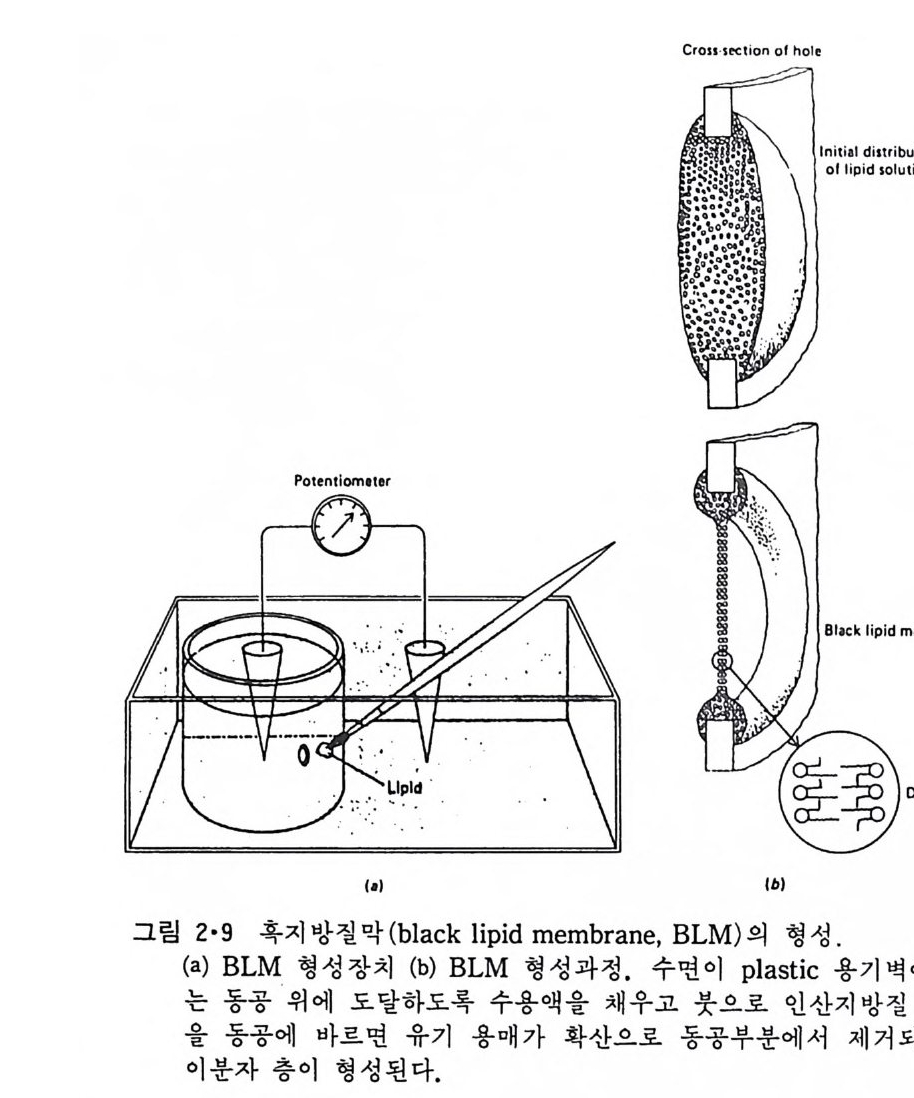
커서 원 통 을 이루어 그럼 2·8a 와 같 이 회합하면 자 연적으 로 구형을 형 성 하고 그림 2·8b 에서와 같 이 꼬리가 둘인 양천성 분자 는 원통이기 때문에 회합하면 평면을 이루어 이분자층이 된다. 한편 소수성 꼬리 부분이 물 에 전혀 노 출 되지 않는 구조는 막소포를 형성하는 것이다. 이상은 생체 막에 존재하는 지방질 분자가 머리 부분 하나에 꼬리 부분 둘이 연결되 어 있는 이유도 된다. 한 조건에서 이분자층을 형성하는 인산지방질도 다른 조건하에서 꼬리 부분의 단백질이 머리부분 단면적보다 커질 때에는 그림 2·8c 에서 보이 는 것과 같이 6 각 형상 혹은 Hn 상을 형성하게 된다. 2 • 3 L ip osome 의 형 성 2)- 5 ) 두 개의 꼬리 부분윷 가진 인산지방질이 물 속에서 자발적으로 이분자 층을 형성한다는 사실을 발견할 것은 Mueller 등 6) 이다. 이들은 소의 두 뇌에서 추출한 인산지방질을 유기 용매에 용해시켜 그림 2·9 에 나타낸 것과 같 은 p las tic용기의 기벽에 뚫린 種孔에 바르면 용매가 제거됨에 따 라 인산지방질의 이분자층이 형성되는 것을 관찰하였다• 이때에 생긴 막 의 두께가 바춘 광선의 파장보다 작기 때문에 검은 접으로 보여 혹 지방 질 막 (black lipid membrane, BLM) 이 라고 불 리 어 진 다. 수용액에서 원형질막이나 세포 내의 여러 소기관의 막과 유사한 이분 자층 막소포가 자발적으로 형성되는 것은 Ban g ham 과 Horne” 이 처음 발견하였다. 인산지방질 용액에서 유기 용매를 증발시킨 후 울을 넣어 휘저으면 그림 2·10 처럼 여러 겹의 이분자층 막이 同心圓的으로 형성된다. 이 것은 lipo some 또는 多 層 膜小胞 (mul ti lamellar vesic l e, MLV) 라고 불리며 여러모로 보아 획기적인 발견이었다. 첫째로는 인산지방질 스스로가 자발 적으로 생체막과 유사한 막을 형성할 수 있다는 것을 알게 되었고 둘째로 이 인공적인 막을 이용하여 생체막뿐만 아니라 세포나 세포소기관에 대 한 연구가 모형계 (model s y s t em) 를 동하여 이루어질 수 있게 된 것이다. 따라서 현재는 인공세포의 형성에까지도 접근하려는 추세가 보인다. Lip osome 은 이렇게 생체막 연구의 모형계로 중요해졌을 뿐만 아니라 藥 物의 體內共給 (dru g deli ve ry ) s y s t em 으로서도 많은 관심을 모으게 되었
 Cro1M tcl io n of hol e
Cro1M tcl io n of hol e
다. 이들 목적을 위해서는 다층막소포보다는 한 겹의 이분자층으로 구성 된 單層막소포 (monolamellar ves i cle) 가 유용하기 때문에 여 러가지 방법 이 개발되었는데 그 대표적인 것은 다음과 같다. ( i ) 機械的인 힘에 의한 방법 여기서는 MLV 를 일단 형성시킨 후 음파세기 (son ic a ti on) 로 처리하거 나, 고압력의 French p ress 를 동과하게 하여 단충 막소포를 형성하는 것 이다. 음파세기 방법은 제일 오래된 방법으로 MLV 를 p robe 형이나 bath 형 음파세 기 로 처 리 한 후 gel chroma t ogra p h y에 의 해 큰 입 자를 제 거 하
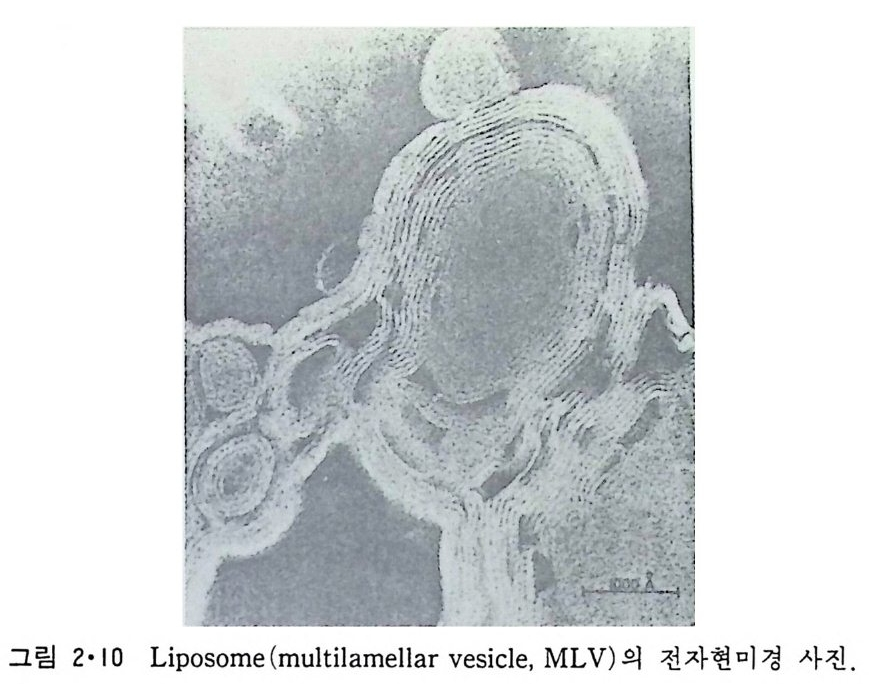 그림 2·IO Lipo some( m ulti la mellar vesic l e, MLV) 의 전자현미경 사진 .
그림 2·IO Lipo some( m ulti la mellar vesic l e, MLV) 의 전자현미경 사진 .
면 칙 경 250 A 의 작은 단층 막소포 (sm all unil am ellar vesic l e, SUV) 를 얻 게 된다(그림 2·11). 이 그림에서 나타낸 것과 같이 크기가 균일하고 또한 광학적으로 투명한 막소포를 얻을 수 있다. SUV 는 그 曲率 (curva t ure) 의 반경이 크기 때문에 인산지방질의 60 내지 70% 가 외부 단층면에 존재하 며 혼성 지질로 구성된 SUV 에도 지방질의 분포가 비대칭으로 존재한다.
 그림 2· 11 단충 PC 박소포 (SUV) 의 전자현미경 사진.
그림 2· 11 단충 PC 박소포 (SUV) 의 전자현미경 사진.
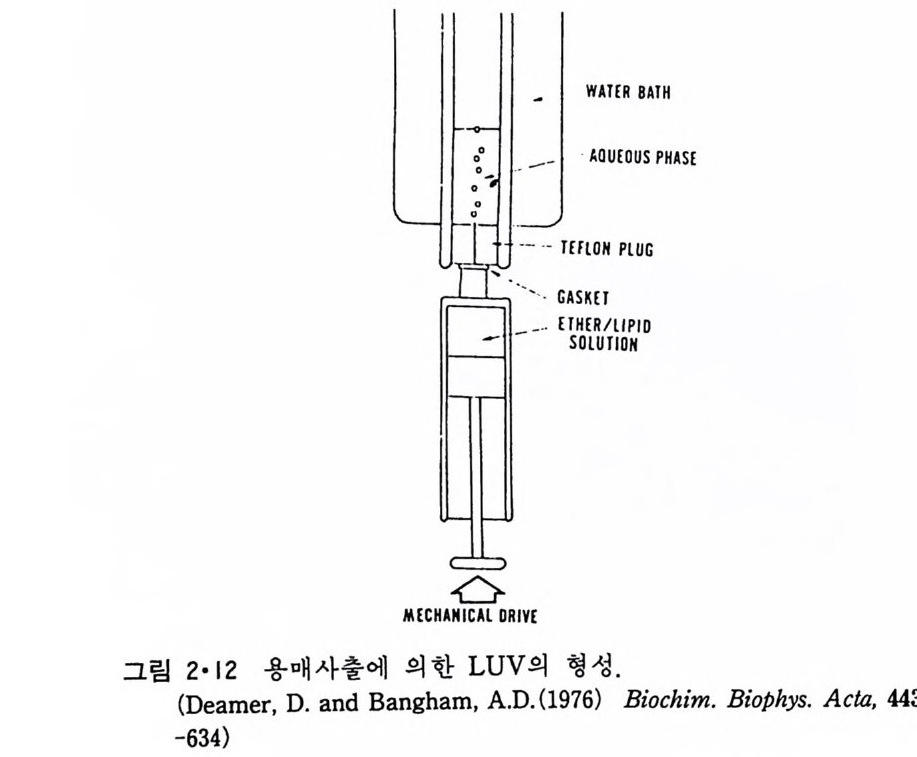
MLV l ip osome 을 French p ress 로 20,000 p .s .i의 힘으로 몇 번 동과시 키면 직경 260~630 A.의 SUV 가 형성되며 이룰 son ic a ti on 방법에 바해서 대량으로 SUV 형성할 수 있다는 장점이 있다. ( ii ) 洗潘劑 (De te r ge nt) 제 거 방법 이 방법은 원래 내재단백질을 지방질 이분자층에 재구성시키는데 이용된 것으로 인산지 방질을 세탁제로 용해시 킨 후 이 세탁제를 透折 (d i al y s i s) 으 로 제거하면 직경이 lOOOA 이상이 되는 큰 단충 막소포(l ar g e unil a mel- lar vesic l e, LUV) 가 생성된다. 세탁제의 제거에는 g el 여과(filt ra ti on) 또는 침강 (sed i men t a ti on) 등도 이용된다. 이 방법의 단점은 세탁제 를 완전히 제거하기가 힘들어 생화학적인 실험에 지장을 줄 수가 있다. ( iii ) 용 매 사출 (Solvent inj e c ti on ) 방 법 이 방법에서는 인산지방질을 e t her 나 e t hanol 같은 유기 용매에 녹여 주 사기로부터 그림 2·12 에 보이는 것과 같이 bu ff er 용액에 사출한다. 인산
 WTEA8ARuAOHnLHTOuH SMT EPuRILTCUl 0
WTEA8ARuAOHnLHTOuH SMT EPuRILTCUl 0
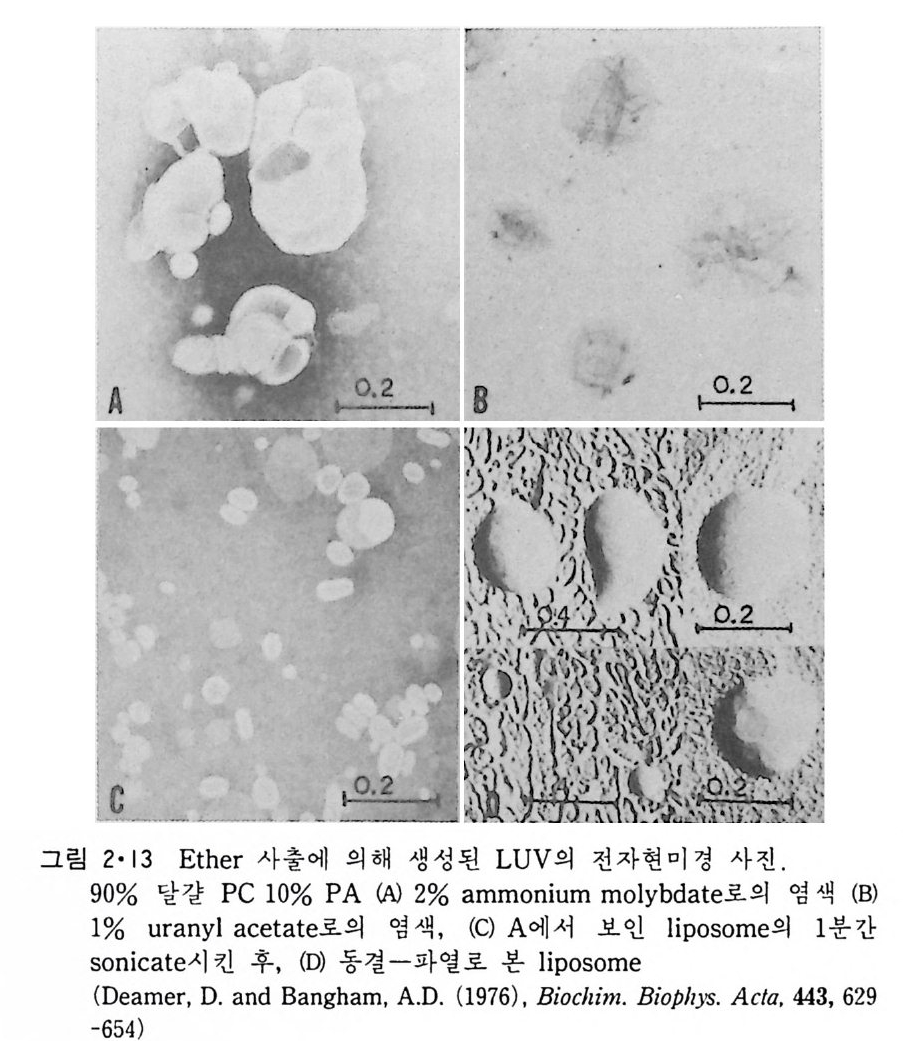 그림 2·13 Et he r 사 출 에 의해 생성된 LUV 의 전자현미경 사진 .
그림 2·13 Et he r 사 출 에 의해 생성된 LUV 의 전자현미경 사진 .
지방질을 d i e t hy le t her 나 이 용매와 me t hanol 의 혼합 용매에 녹인 다음 55~60°C 로 유지된 buff er 용액에 사출시키면 1500~2500A 칙경의 큰 LUV 가 생성된다(그림 2·13). E t hanol 을 용매로 쓸 경우에는 SUV 이 생 성된다. (iv) 逆相 증발 (Reverse ph ase evap o rati on ) 방법 이상 설명한 방법에 의해 형성된 막소포들은 수용액 내에서 생성되기 때문예 수용액에 용해된 물질은 막소포내에 포착 (en t ra p)시키는 효율이 대단히 낮다. 이 약점을 보강하기 위한 방법으로 인산지방질을 유기 용
 [{\]广 二 >::
[{\]广 二 >::
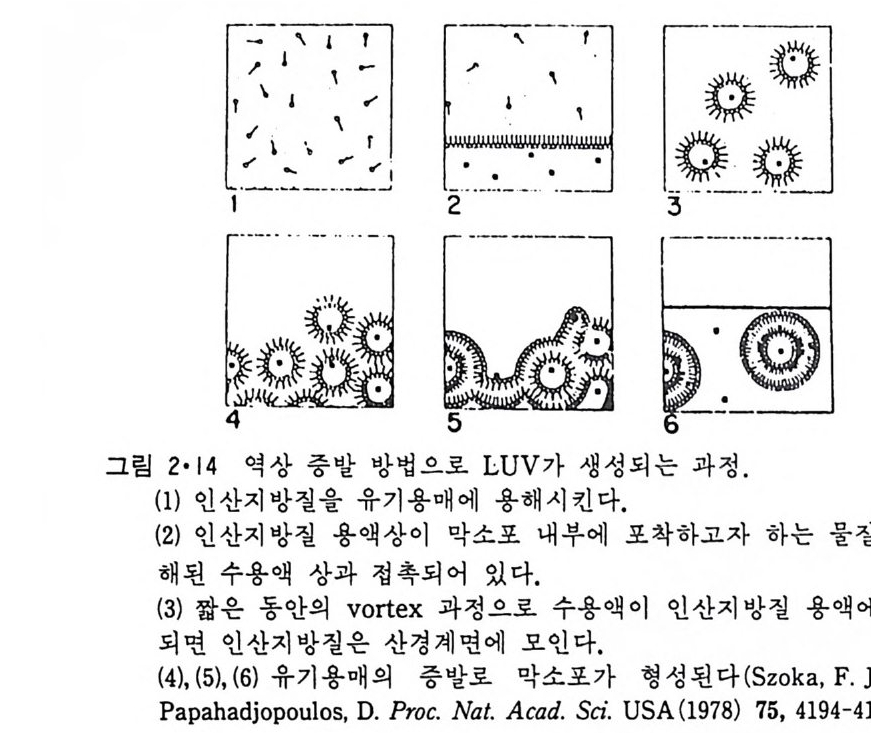
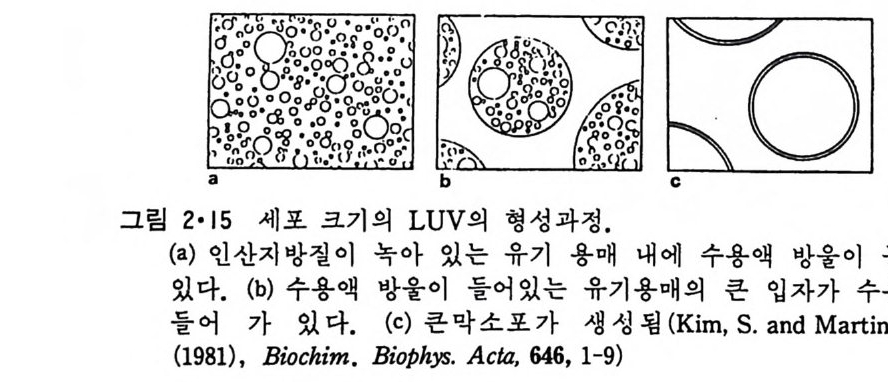
매에 용해시킨 후 여기에 포착 시키려는 물질이 녹아 있는 buff er 용액을 가하고 짧은 시간 동안 초음파를 통하면 수용액이 유기 용매에 분산이 된다. 다음 유기 용매를 감압 조건 하에서 증발시키고 일정량의 bu ff er 용 액을 첨가하고 vor t ex 하면 그림 2·14 에 보이는 과정을 거쳐 LUV 가 생 성된다. 이렇게 하면 수용액에 녹아 있던 용질의 20~70% 를 막소포내에 포착시킬 수 있다. 이룰 개선한 방법으로는 그림 2·15 에서 보이는 것과 같이 언저 수용액
 a b C
a b C
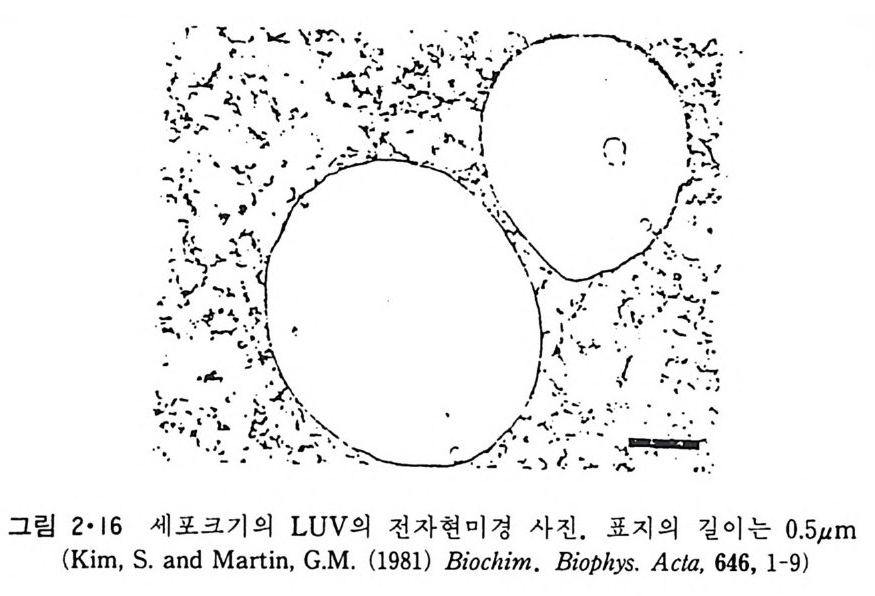 그림 2•16 세포크기의 LUV 의 전자현미경 사진. 표지의 길이는 0.5 µ m
그림 2•16 세포크기의 LUV 의 전자현미경 사진. 표지의 길이는 0.5 µ m
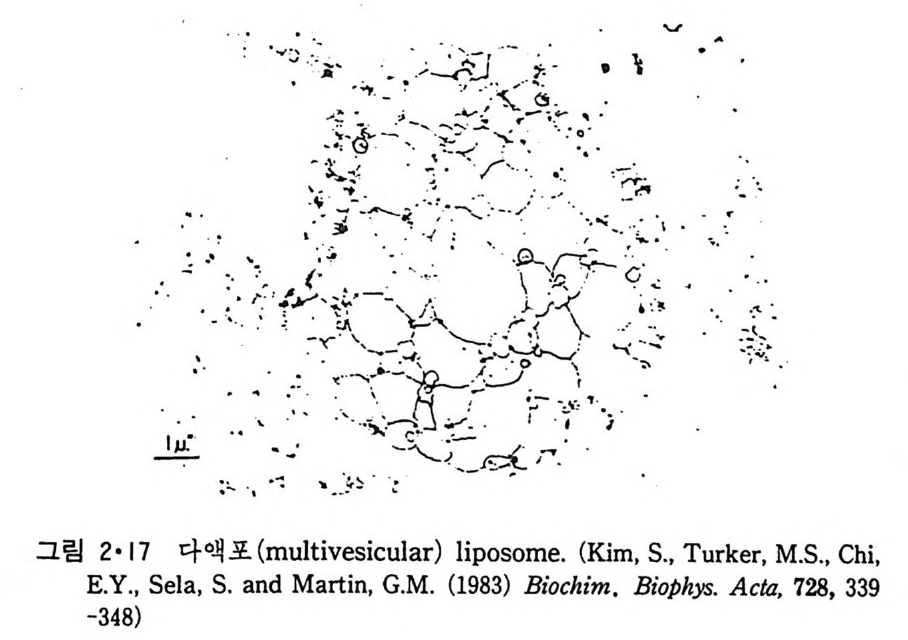
을 인산지방질이 녹아 있는 유기 용매에 분산시키고 이 전체를 다시 수 용액에 분산시킨 후 유기 용매를 증발시켜 세포 크기의 LUV 를 얻고(그 링 2·16) 또 때로는 다액포 (mul ti ves ic ular) lip osome 도 얻을 수 있다(그 림 2·17)
 .• .., . `• •· - ` •• ` _. .- · _ `-. A .
.• .., . `• •· - ` •• ` _. .- · _ `-. A .
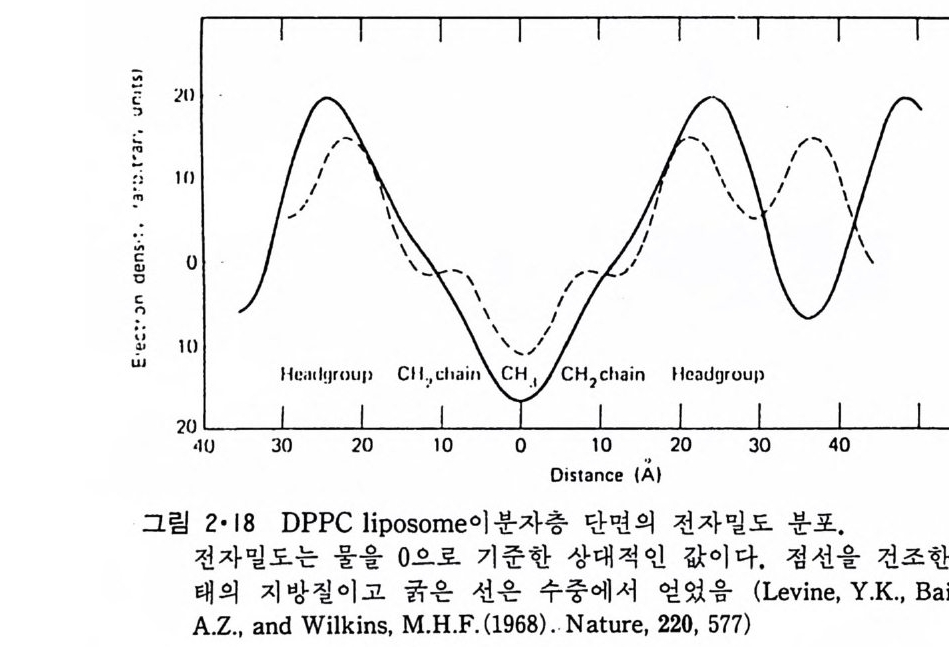
2·4 Lip osome 의 물리적 성질 8) - 9) 생체막으로부터 추출 정제한 인산지방질만을 물에 넣어도 자발적으로 아분자층을 형성하는 사실은 지방질이 생체막 구조의 기본이 된다는 것 을 시사한다. 이러한 지방질로 구성된 막소포가 세포와 그 안에 존재하 는 여러 소기관들의 내부를 외부로부터 격리시킨다는 생체막의 중요한 역할을 할 수 있지만 그 이외의 생체막의 기능에 인산지방질의 이분자층 의 울리적인 성질이 중요하다. 2·4·1 두께 (Thic k ness) 생체막을 전자현미경으로 관찰하면 그 두께가 40~50A 가 되는 것을 볼 수 있는데 lip osome 의 이분자층의 두께도 이 칭도로 나타난다. 인산 지방질의 분자 model 로부터 얻을 수 있는 값을 약 60A 정도이다. 이들보 다 좀더 정확한 방법은 X- 선 회절로서 전자 밀도를 보는 것이다. 그림 2·18 은 한 방향으로 배열된 DPPC 의 전자 밀도 분포를 보여준다. 여기서
 -slER
-slER
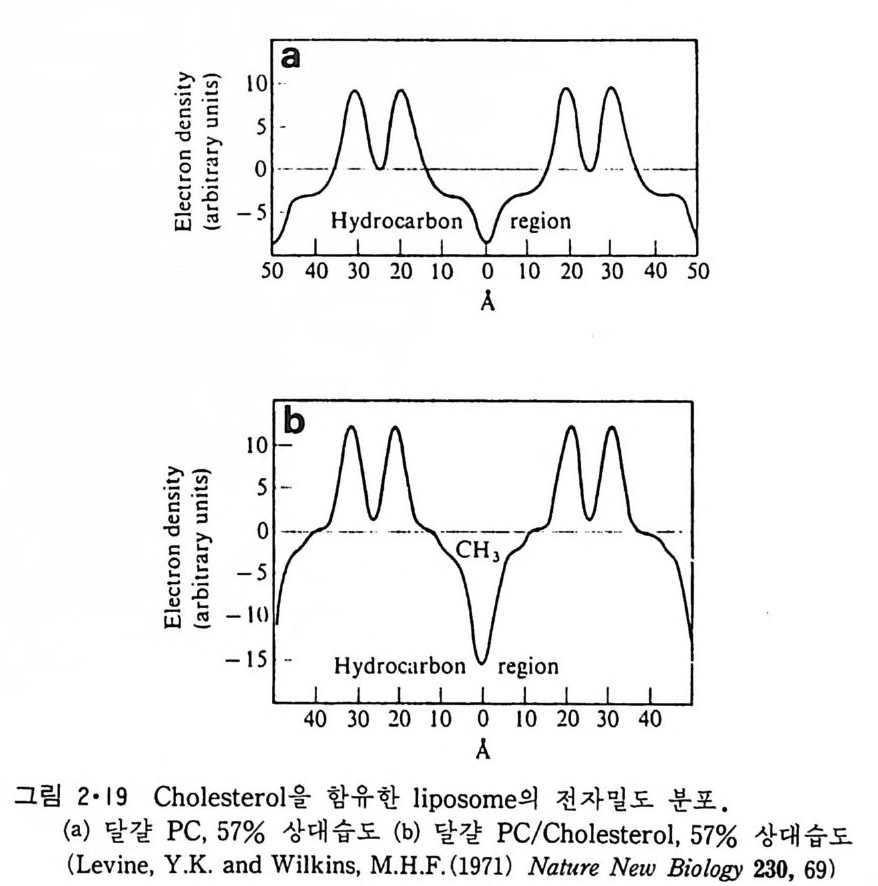
굵은선은 지방질이 울로 포화되어 있을 때이고 접선은 울이 약간만 존재 할 때이다. 물의 전자 일도를 0 으로 기준을 정한 것으로 전자 밀도가 제 일 큰 지접이 극성인 머리 부분이고 최처 지점이 me t h y l 기를 나타낸다고 해석이 된다. 이 그림에서 물의 존재하에서 지방질 이분자층의 두께가 중가하며 또 울이 없는 상태에서 전자 밀도 분포도의 중간에 위치하던 CH 기에 의한 낮은 지접이 없어진 것은 물의 존재하에 꼬리 부분의 alk y l 기의 유동성이 증가한 때문이다. 이때 이분자층의 두께는 약 52A 이 된다. 생체막의 choles t erol 의 함량은 7% 에서 50% 에까지 이르는데 이 화합 뭉 자체로는 m ic elle 이나 이분자층을 형성하지 못하지만 인산지방질 내부 에 들어가연 이분자층의 구조에 영향을 준다. 그링 2·19 는 choles t erol 이 지방질의 alky l 꼬리 부분의 운동을 저해하는 것을 보여준다. 이것은 (b) 에서 ― CH3 에 의한 전자밀도가 (a) 보다 더 낮아진 것으로 알 수 있다.
 hl!SU(s;1>1p un 。 .a
hl!SU(s;1>1p un 。 .a
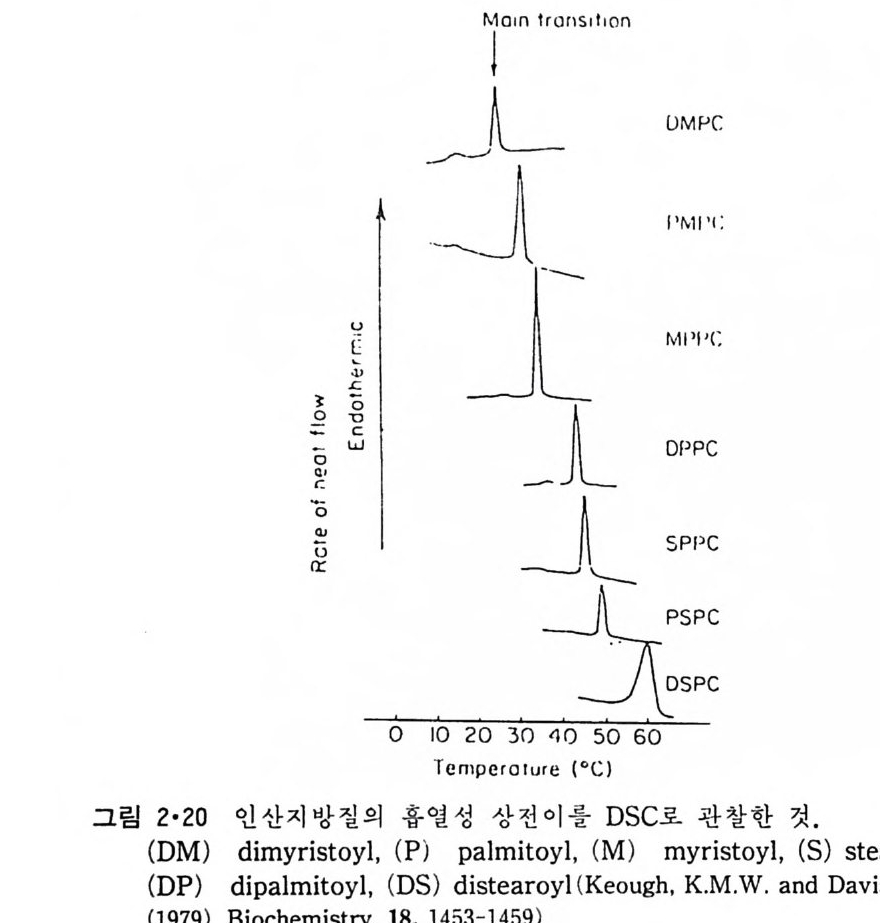
2·4·2 상 전이 (Phase tra nsit ion )101- 13 1 탄화수소가 특정한 융점 (m e lt in g p o i n t )을 가지고 있는 것과 마찬가지로 지방질도 물에서 그 화합물에 특유한 융점이 있는데 이것을 상 전이 온 도(p hase tra nsit ion tem p e ratu r e) 라고 부른다 . 그림 2 · 20 은 여 러 종류의 인산지방질의 상전 이 현상을 미분주사 열량계 ( d iff eren ti a l scannin g calo- rim ete r , DSC ) 로 관찰한 것이다. 이 상전이 온도보다 낮은 온도에서 인산 지방질의 꼬리 부분은 고체의 성질을 나타내며 이것 을 g el(L /J)이라고 부 르고 상 전 이 온도 이 상에 서 는 액 체 결 정 (liqu id crys t a l lin e , L 김 이 라고 부른 다. 이들 상 전이는 항상 홉열적이고 각각의 인산지방질은 고유한 상 전
 Mla in tro nsit ,o n
Mla in tro nsit ,o n
 CH3
CH3
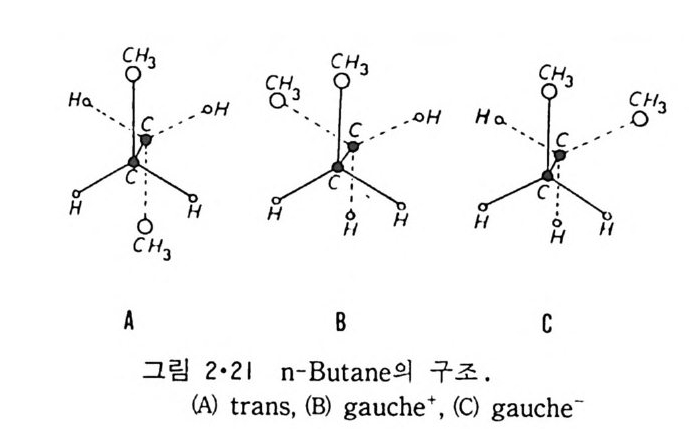
이온도 (T 니값을 가지며 이는 acy l 사슬의 길이, 불포화 정도와 이중결합 의 위치 그리고 극성 머리 부분에 따라 좌우된다. 순수한 인산지방질의 상 전이는 o.2·c 의 좁 은 온도 범위 내에서 일어나며 gel 상에서 액체결정 상으로의 변화 과정에서 한 분자가 차지하는 연적 이 0 .4 8run2 에서 0.71un2 로 증가하며 반면 이분자층의 두께는 7A 정도 감소한다. 수중에서의 지방질 상전이는 순수한 탄화수소와 마찬가지로 ac y l 사슬의 구조가 t rans 에서 g auche 구조로 변하기 때문이 다. n-Alkane 사술어]서 c-c 절 합의 회전은 비교적 쉽게는 일어나도 완전히 자유롭지는 못하다. 예 를 들 어 간단한 n-alkane 인 n-bu t ane 은 그랑 2·21 에서와 같이 3 개의 안정한 구조 를 가질 수 있다. 이중에서도 가장 안정한 구조가 t rans 형인 데 이 것 과 ga uche 형 과의 energy 차이 는 불과 400~800ca l/ mol 이 어 서 쉽게 구조 변경이 있을 것 같으나 이 변화에 필요한 활성화 ener gy가 3. 6kca l/ mol 이 되어 어느 정도 제한울 둔다. Trans 형에서 한 개의 결합만
 R..
R..
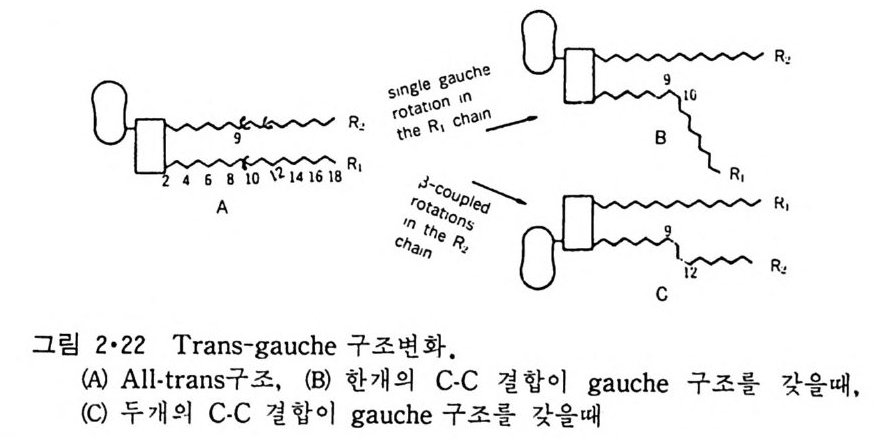
이 g auche 형으로 바뀔 때에는 그림 2·22 에서 보이 는 것과 같이 더 많은 공간을 차지하게 되므로 g auche 형이 또 하나 생겨 t rans 형과 평행으로 된다. 지방질이 g el 상에서 액체결정형으로 변화하는 것은 바로 모든 acy l 기의 c-c 결합이 t rans 형으로 존재하던 상태에서 그의 일부가 g auche 형 으로 바뀌는 현상으로 이때에 acy l 사슬의 길이가 줄고 한 acy l 사슬이 차지하는 면적이 넓어지는 것은 이 때문이다. 한편 C = C 이중결합 자체는 회전하지 않지만 근접하여 있는 c-c 결합 아 회전할 때에 필요한 활성화 ener gy가 2kca l/ m 이밖에 되지 않아서 tra ns-ga uche 변형 이 쉽 게 일어 난다. 이 중결 합을 많이 가지 고 있는 지 방 질일수록 그 상변화 온도가 낫은 이유가 여기에 있다. 표 2·5 은 여러가지 인산지방질의 상 전이온도 를 보여준다 . 이 표에서
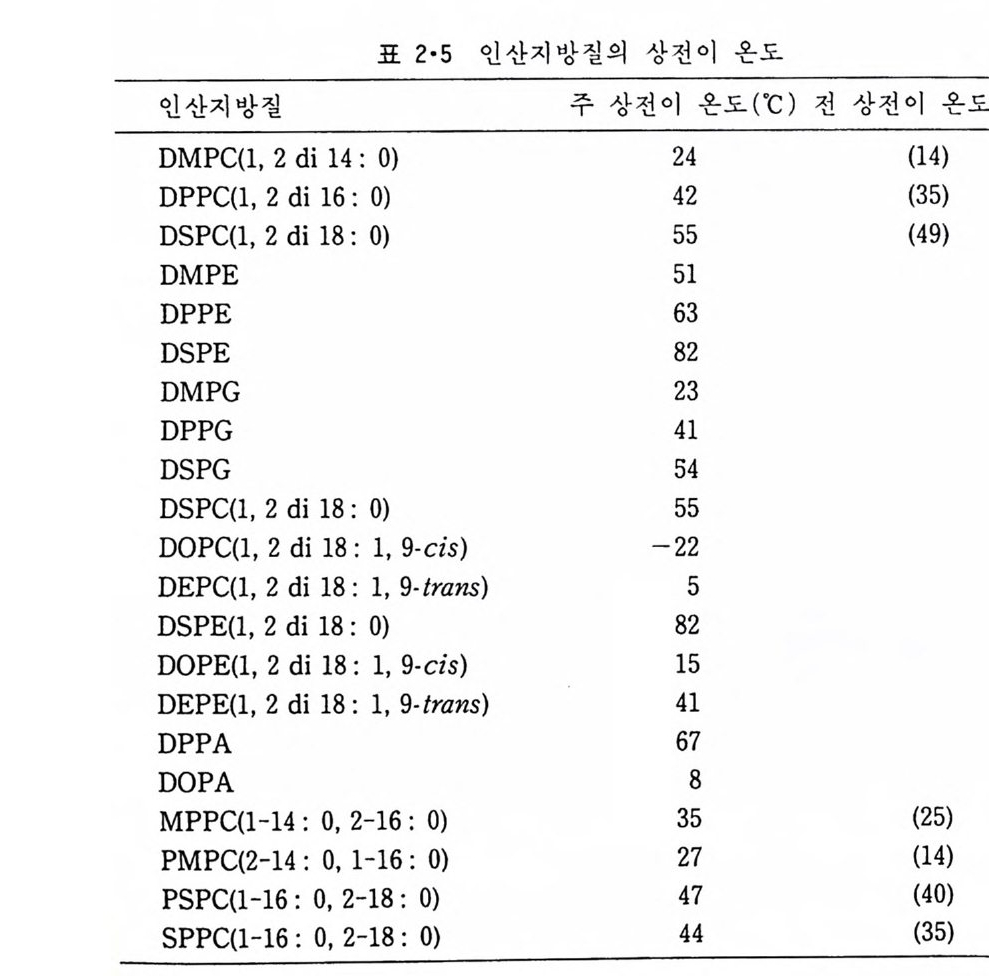 표 2·5 인산지방질의 상전이 온도
표 2·5 인산지방질의 상전이 온도
하나의 인산지방질에 존재하는 두 개의 사슬이 같을 때 아들의 길이가 길수록 상 전이온도가 높아지고 불포화 이중결합이 많을수록 Tm 이 낮아 진다. 자연에는 불포화 ac y l 사슬 하나와 포화 acy l 사슬 하나를 가진 인 산지방질이 많이 존재한다. a 와 b 의 두 개의 다론 acy l 사슬을 가진 인 산지방질의 Tm 은 a 만으로 구성된 지방질의 상 전이온도와 b 만으로 구성 된 지방질의 상 전이온도와의 중간온도에 위치한다. 두 개의 다른 acy l 사슬이 공존할 때 이 사술들의 gly c e rol backbone 에서의 위치에 따라서 Tm 이 달라진다. 상 전이온도는 그 소수성 acy l 사슬뿐만 아니라 극성의 머리 부분이 무엇이냐에 따라서도 달라진다. 일반적으로 하전되어 있는 인산지방질은 전기적인 배척 때문에 불안정하여 상 전이온도가 낮다. 또 하전되어 있 지 않은 지방질들도 머리 부분의 구조에 따라서 상 전이온도가 달라진 다. 예를 들어 수화가 잘된 PC 인 경우 g el 상에서는 그 acy l 사슬이 완전 히 뻗쳐 있어도 막표면에 수직된 방향이 아니고 이 방향으로부터 일정한 각도로 경사를 이룬다. 이때에 acy l 사슬의 말단끼리의 안정화 효과가 작아 상 전이온도는 비교적 낮다. 이에 반해서 PE 의 경우 acy l 사슬은 막표면에서 수직된 방향으로 배열된 꼬리 부분의 말단끼리의 상호작용으
 .., Ma in tr\ a ns,hon
.., Ma in tr\ a ns,hon
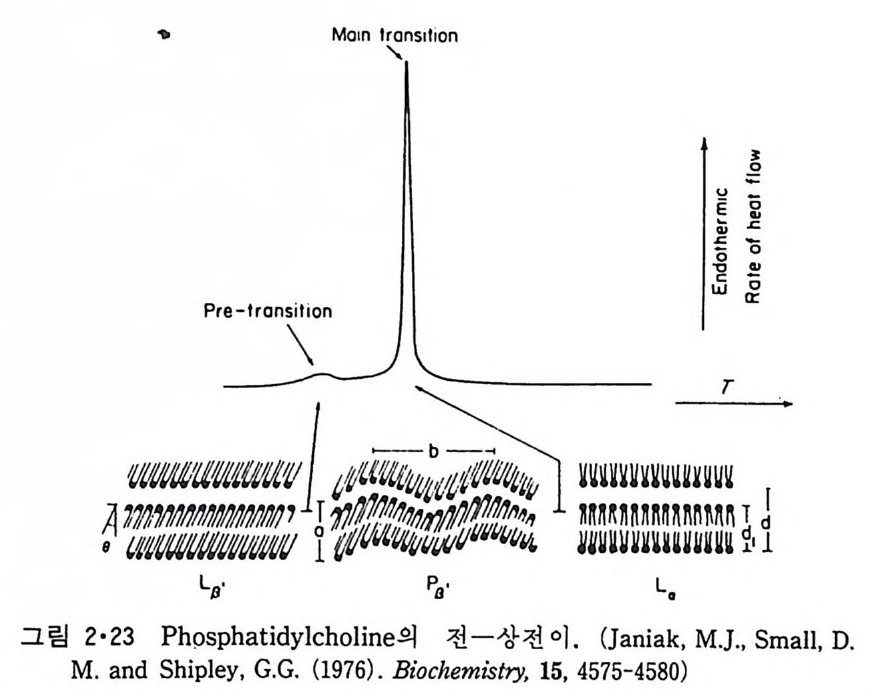
댜로해D상P P전C이 의온 상도 가전 이보온다도 높는다 .4 1·이c 는밖 에D PP되E지 의 않상는 전것이으온로도 가보 아63 °C알 인 데수 반 있 그림 2·20 과 2·23 에서 주 상 전이온도보다 낮은 온도에서 홉열량이 훨 씬 적 은 전 상 전 이 (pre -tr a nsit ion ) 를 볼 수 있는데 이 것 은 PC 와 PG 에 만 존재한다. x- 광선 회절, NMR 과 Raman 광산란 결과에 의하면 이 두 인산지방질들은 전 상 전이온도 이하에서는 탄화수소 사슬이 완전히 뻗 친 t rans 형으로 존재하지만 막의 표면과 수직되는 방향과 일정한 각도로 경사를 이루고 있으며 이것을 L /I'상이라고 부른다. 이러한 경사 를 갖는 이유는 PC 의 머리 부분 단면적이 꼬리 부분 단면적보다 커서 acy l 사슬 이 경사를 가짐으로써 그 면적이 머리 부분과 비슷해지기 때문이다. 이
 .,'그-,
.,'그-,
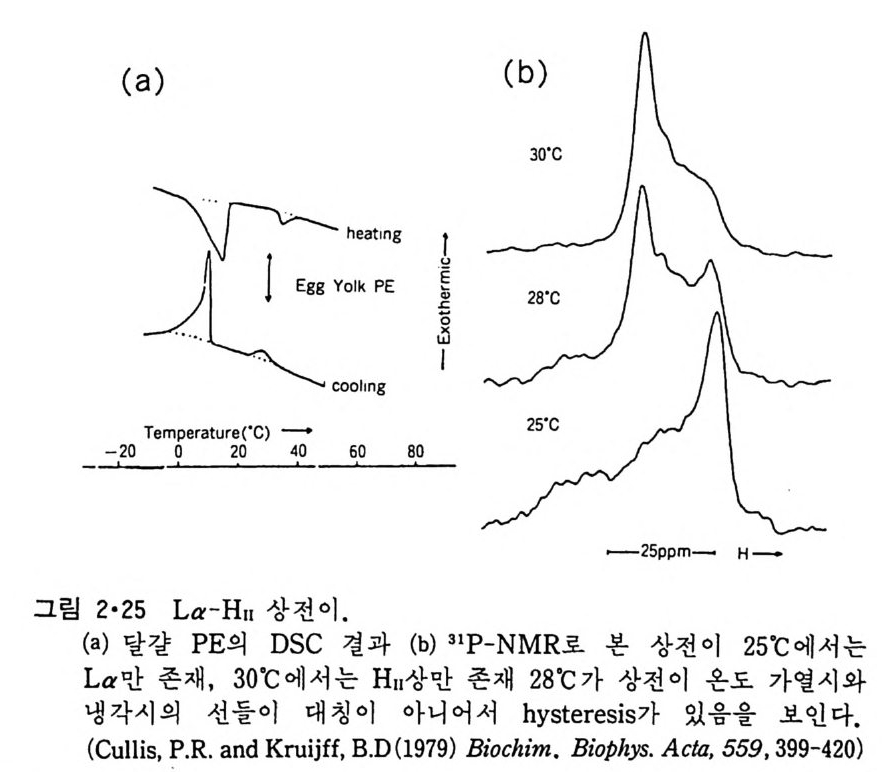
각도는 온도에 따라 변하며 온도가 높을수록 감소된다. 이들 인산지방질 은 전 상 전이온도와 주 상 천이온도 사이에서는 이차원적인 monoclinic lattice 상 (P/) 으로 천환되는데 이때에 막의 표면은 그렁 2-23 에 보이는 것과 같이 울결모양 (ripple) 을 갖는다. 그럼 2-24 는 이 P p ’상을 전자현미 경무로 관찰한 것이다. 이 그럼에서 a 는 L/ 상을 보여주는데 동결파열 과정에 따라 때때로 나선형 결함 (spiral defect) 을 보이지만 그 표연은 비 교적 명탄하고 이 상에서 P/ 상£로 변천이 되면 b 에서와 같이 물결모양 이 표면에 나타난다_ c 는 La 상으로 그 표면이 완천히 평탄해 진다. PE 는 gel 과 액체 결정상 사이의 상 전이 이외에도 이보다 약 10'C 더 높은 온도에서 이분자충-육각형 (Hn) 상 전이가 일어난다(그럼 2-8c)_ 상 변화의 L1 H 값은 주 상 전이 때에 비하여 훨씬 작 A 며 hysteresis 도 보여준다(그럼 2-25)_ 이러한 La-Hn 상전이는 31P-NMR 와 동결파열 전 자현미경법으로 관찰이 되었다 Hn 상을 가질 수 있는 인산지방질은 PE 와 낮은 pH 에서의 PS 와 PA 그리고 Ca+ 2 존재하에서의 PA 와 CL 들이다. 이들이 Hn 로 전이되는 조건은 전부 그림 2-8c 에서와 같이 머리부분에 비
 (a)
(a)
 a
a
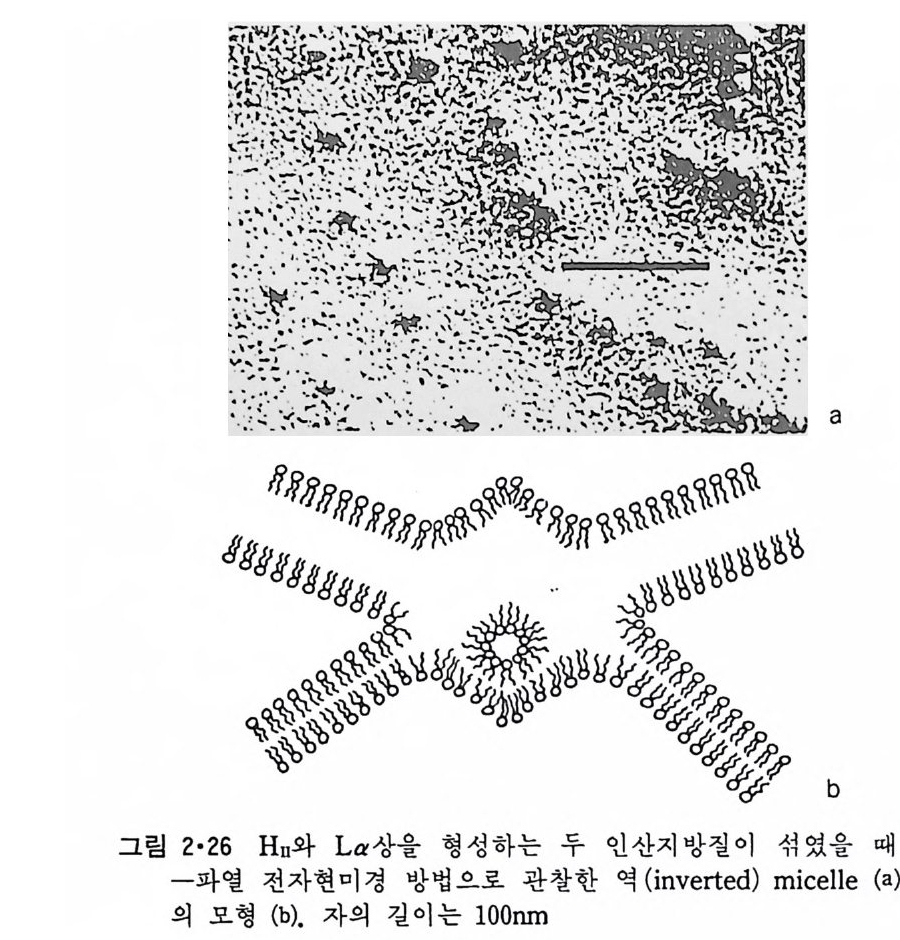
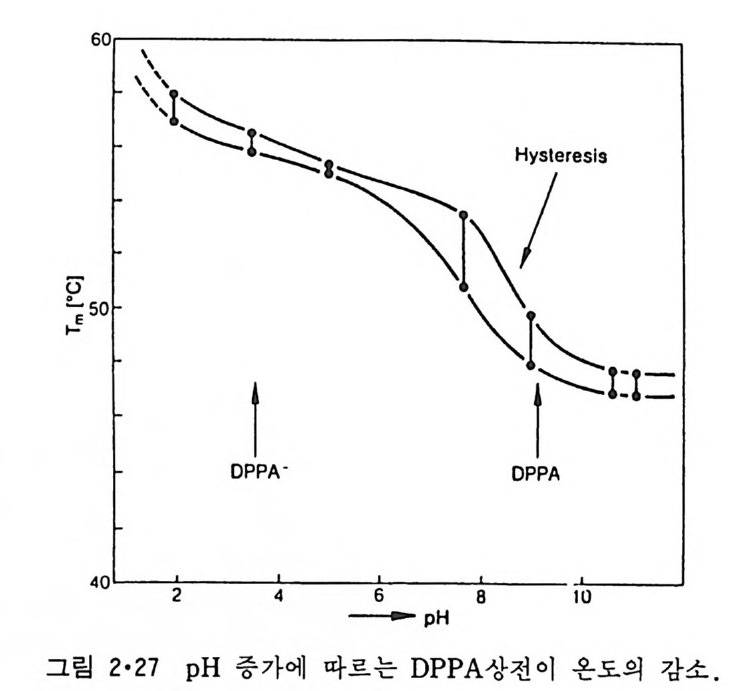
해서 꼬리의 단백질이 커지는 경우이다. PE 등 Hn 를 형성할 수 있는 인산지방질과 안정한 La 을 유지하는 인산 지방질이 섞였을 때에 그림 2·26a 와 같은 입자를 동결과열시킨 후 현미 경으로 볼 수 있는데 이는 그림 2·26b 에서와 같이 역 (i nve rt ed)m ic elle 을 형성하는 것으로 해석되고 있다. 이상 열거한 온도 변화에 따르는 상 전이뿐만 아니라 머리 부분에 하전을 가진 안산지방질의 겨우에는 p H 와 ion 강도 (st ren gth)에 따라서도 상 전이가 일어날 수 있다. 머리 부분이 음전하를 가지고 있을 때 이돌 사이의 배척력 때문에 머리 부분간의 간 격을 크게 하려는 경향이 있을 때 이는 ac y l 기가 gel 형태로 됨으로써 이 루어진다. p H 가 높아질수록 i on 화에 의해서 음전하의 밀도가 커져 상 전이온도는 낮아진다. 그림 2·27 은 DPPA 의 상 변화온도가 p H에 따라
 60
60
변하는 것을 보여준다. 이 변화는 특히 음성 하전이 하나에서 둘로 변하 는 p H 에서 심해져 약 1o·c 칭도의 차이를 보인다. 한편 하전된 머리 부분끼리의 배척을 ion 강도의 증가에 따라 감소하 고 특히 ca +2 와 M g요는 음성으로 하전된 머리 부분과 결합하므로 머리 부분끼리의 배척을 감소시킨다. 이들 효과의 결과는 상 전이 온도의 증 가를 초래하는 것이다. 2 •4 • 3 상분리 (Phase sep a rati on ) 지금까지의 상 전이에 대한 이야기는 한 가지 종류의 인산지방질만이 존재할 때에 한한 것이었지만 생체막에는 많은 지방질이 섞여 있어 상 전이의 성격이 대단히 복잡하게 된다. 높은 온도에서는 모든 성분이 액 체결정으로 존재하여 대부분의 경우에는 균일한 상을 이루지만 온도를 내리면 어떤 성분은 액체결정 상태로 존재하고 다른 성분은 g el 상태로 되어 그 두 상이 분리될 뿐만 아니라 각각 다른 성분들의 ge l 상까지도 분리된다. 이것은 액체결정 상에서는 여러 성분이 완전히 섞이지만 ge l 상태에서는 잘 섞이지 않기 대문이다. DMPC(C 14: 0) 와 DPPC(C 16:
 ’ Tr
’ Tr
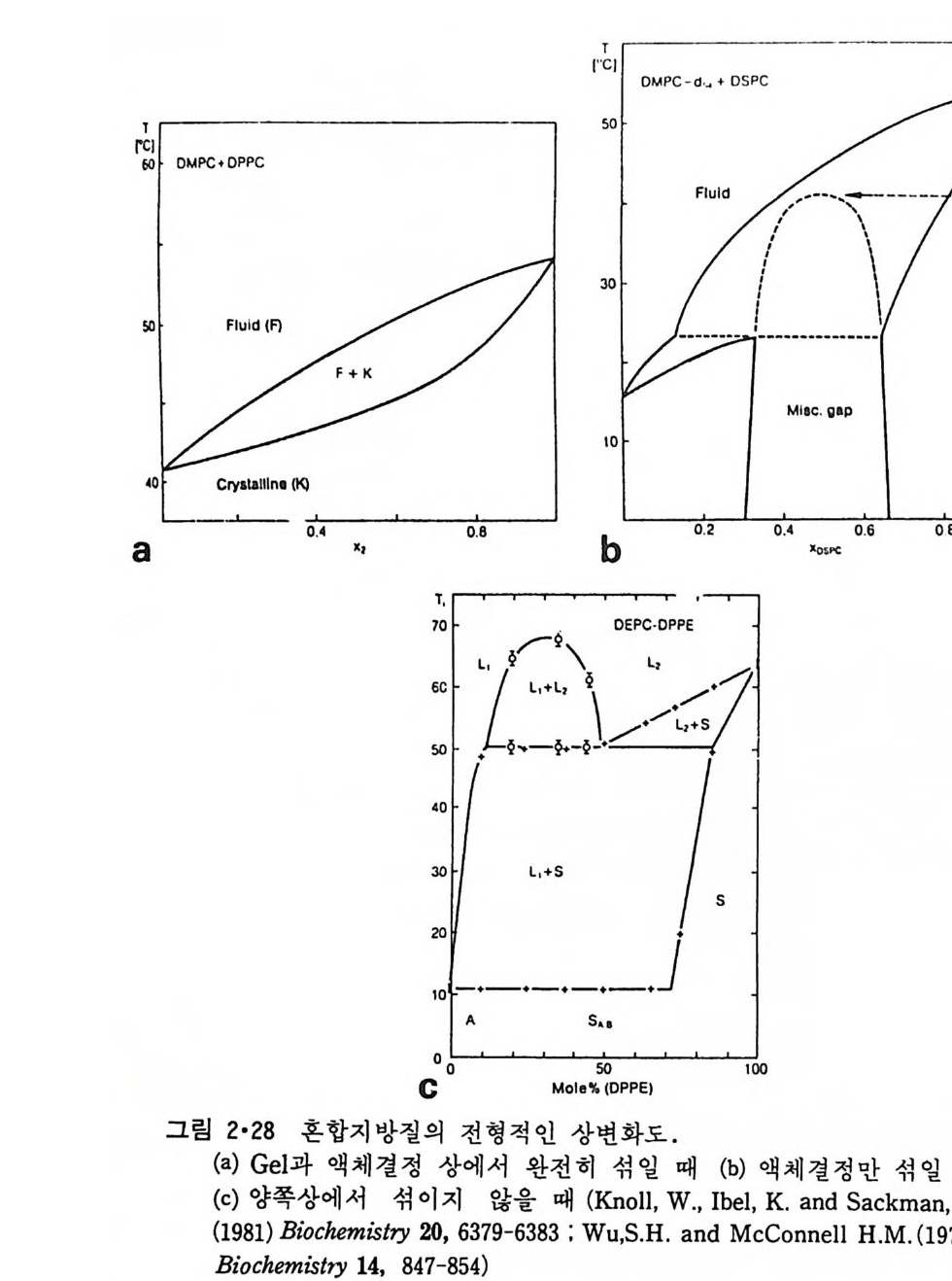
o) 와 같이 머리 부분이 동일하고 ac y l 기가 거의 비슷할 때에는 액 체 결정 때나 g el 때나 완전히 섞여 균일한 상을 가지나 그 이외의 경우는 상분리 가 생긴다. 이러한 현상은 그림 2·28 의 상圖形(p hase d i agr am) 에서 볼 수
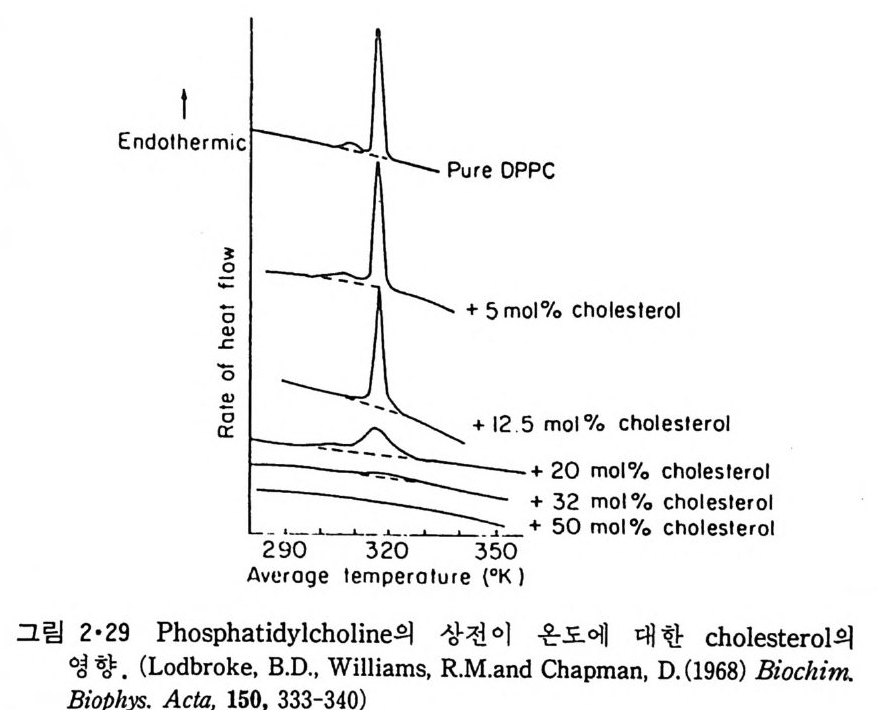
있다. 여기서 a 그림은 두 성분이 g el 상태나 액체결정에서 완전히 섞이는 경우이고 b 그림은 액체결정에서는 섞이나 gel 상태에서는 섞이지 않는 경우이다. C 그림은 양쪽상에서 모두 섞이지 않는 경우이다. Ca 요동 양 i on 이 산성 인산지방질의 상 전이 온도를 높이는 것은 이미 언급이 되었는데 산성 인산지방질을 함유하고 있으면서 액체결정 상으로 존재하는 lip osome 에 Ca” 을 가하면 산성 인산지방질만이 g el 상으로 변 하면서 상분리가 일어난다. 2·4·4 Choles t erol 의 영 향 그림 2·29 는 PC lip osome 에서 choles t erol 의 함량을 중가시 켰을 때 상 전이 4H 가 감소되는 것을 보여준다. Choles t erol 의 mole% 가 50 이상이 되면 상 전이가 일어나지 않는다. 이는 choles t erol 아 g el 상에서 ac y l 사슬 이 t rans 구조를 갖는 것을 저해시키고 반면에 액체 결정에서는 ac y l 사슬 이 g auche 구조를 갖지 못하도록 하여 결국 PC 의 양 상에서의 구조적인 차이룰 감소시키며, choles t erol 의 함량이 높아지면 이 두 상 사이의 성
 I
I
 ”。’ ’ `\ resIn c Ied 一 -u naf fec te d -
”。’ ’ `\ resIn c Ied 一 -u naf fec te d -
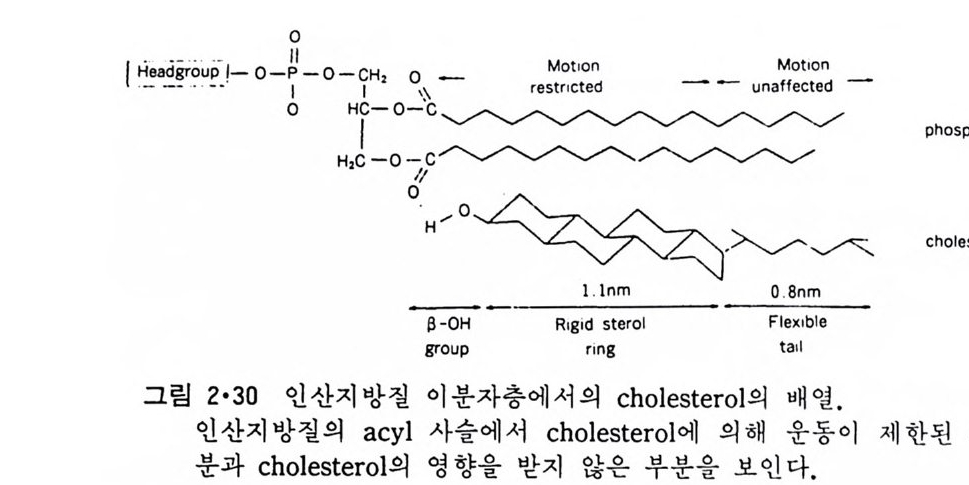
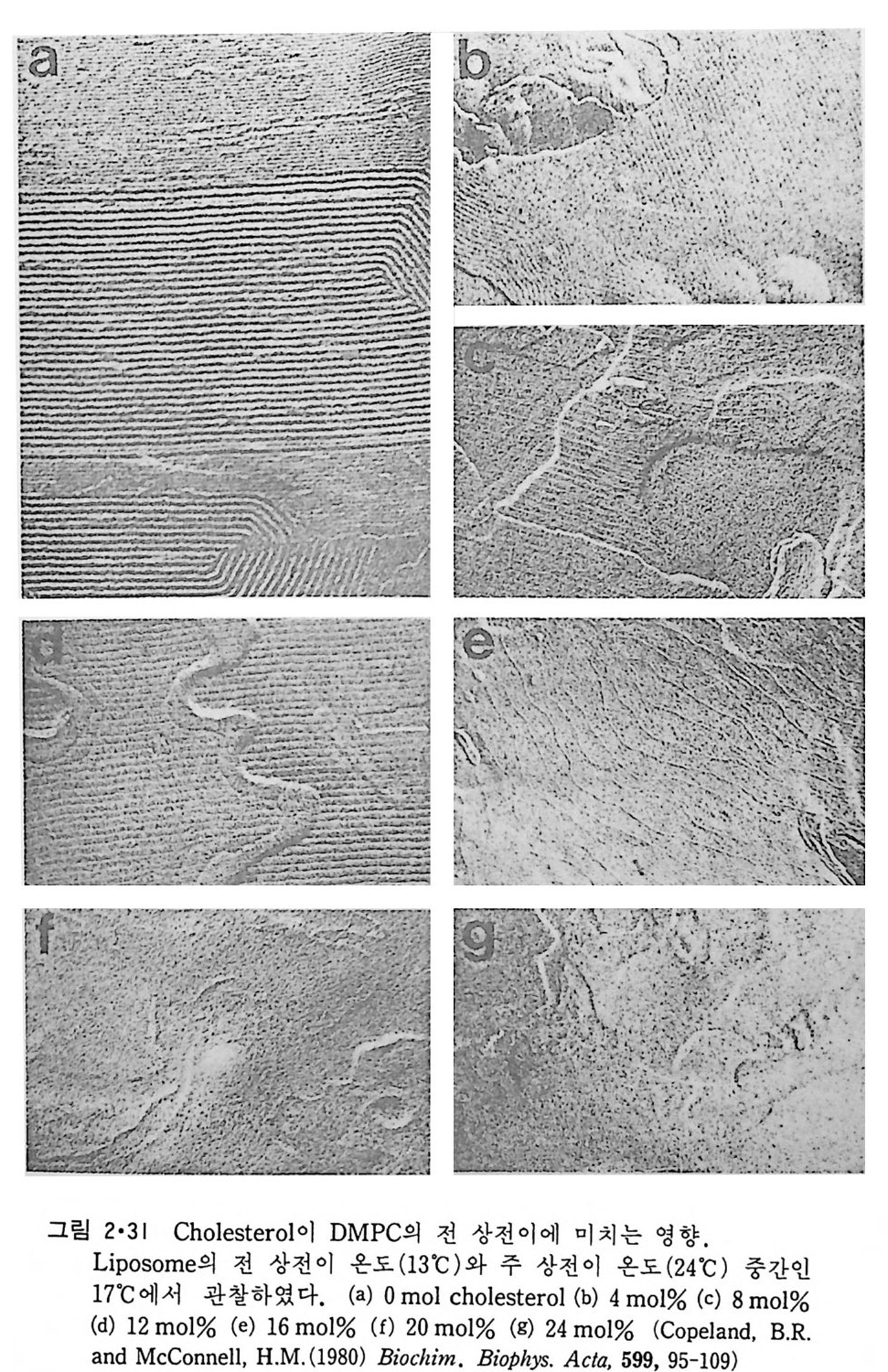
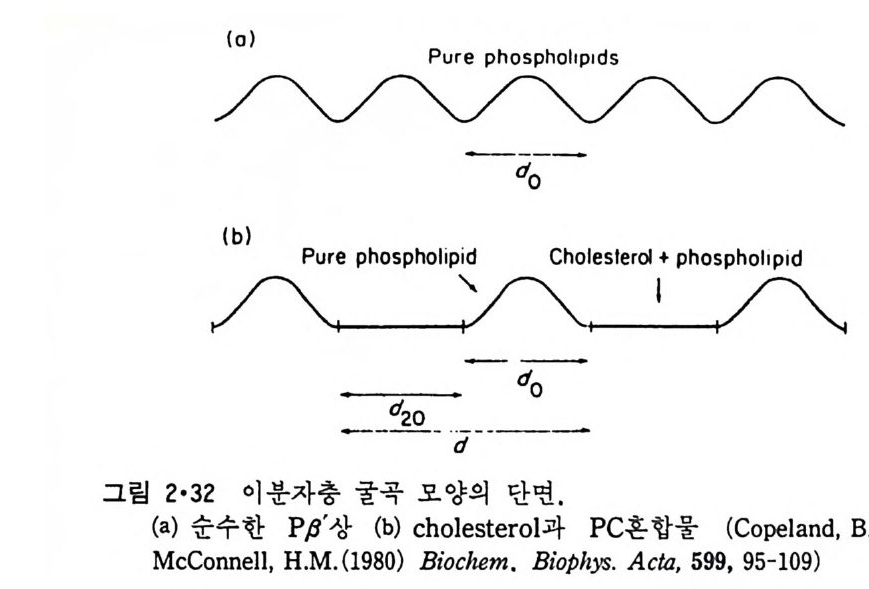
질의 차이가 없어쳐 상전이가 일어나지 않기 때문이다. Choles t erol 의 lip osome 의 이분자층내에서의 위치는 그럼 2·30 에서 보여준다. Choles- t erol 의 3 /J -h ydrox y기 는 인산지 방질 머 리 부분의 este r 결 합의 carbony l 기 와 수소결 합을 하고 있고 choleste r ol 분자는 인 산지 방질 분자와 평 행 되는 방향으로 배열되고 있다. 인산지방질 상 전이 온도 이상에서는 편 편한 ste r ol rin g 때문에 acy l 사슬이 g auche 형을 이루기 힘들어 그 유동 성 이 감소되 며 , 상 전 이 온도 이 하에 서 는 ac y l 사슬과 choles t erol 구조의 차이로 인해 acy l 사슬의 전부가 tra ns 형을 가질 수가 없어서 이분자층 의 유동성을 증가시칸다. 결국 전에 언급한 것과 같이 choles t erol 은 두 상에서의 성질의 차를 감소시킨다. 그링 2·29 에서 choles t erol 이 DPPC 의 전 상 전이도 없애는 것을 봅 수 있는데 이는 ge l 상태에서 DPPC 의 acyl 사슬이 막 표면과 수칙이 아 닌 방향으로 향한 L /I'구조를 갖던 것 이 choles t erol 의 존재 하에 서 막 표 면과 수직이 되는 방향인 L/I 구조로 변화되어 전 상 온도와 주 상 온도 사이의 P /I'구조를 감소시키기 때문이다. 그림 2·31 은 P /I'구조를 갖는 온 도에서 choleste r ol 함량의 변화에 따른 동결파열 전자현마경 사진이다. Choles t erol 의 함량이 증가함에 따라 물결 모양 부분 사이의 간격이 커지 며 이의 설명은 그림 2·32 에서 주어진다. 액체결정 상에서 choleste r ol 함량을 접 점 중가시 키 면 결국 choleste r ol 상의 분리 가 이 루어 지 는데 이 것은 인산지방질의 머리 부분의 구조에 따라 좌우된다. 약 50% 몰 농도 에서 시작해 choles t erol 의 함량이 67% 까지 이르러도 상 분리가 안될 수
 1_·- -二.,: ., ___ 一- ) - • ~. ~
1_·- -二.,: ., ___ 一- ) - • ~. ~
 (o) Pure ph osp ho hp 1d s
(o) Pure ph osp ho hp 1d s
도 있는데 상 분리가 찰 안되는 정도는 다음 순서와 같다. s p h i n g om y e li n 가 PS, PG>PC 익 PE 2·4·5 지방질 내부에서의 운동 용액내에서의 분자 운동은 방향성이 없지만 지방질 이분자충내에서의 분자 운동은 방향에 따라 그 성질이 다르다. 이분자층에서의 운동은 분 자내의 운동과 분자 전체로서의 운동의 두 가지로 나눌 수가 있다. 분자 내의 중요한 운동은 이미 설명한 바 있는 c-c 결합의 회전, 탄화수소 사슬의 혼들림 운동, 극성 머리 부분의 구조 변경 등이 있다. 지방질 이분자층은 상 전이온도 이상에서 그 acy l 사슬이 액체에 가깝 지만 gly c e rol backbone 이 막의 ma t r i x 를 형성하기 때문에 이것에 가까 운 부분일수록 유동성이 감소될 것으로 기대된다. 이것은 13C-NMR 분 광범으로부터 얻은 sp in- latt ice 이완시간 (relaxa ti on tim e) 으로부터 알 수 있는데 그 결과는 그림 2·33 에서 보여준다. 여기서 한 acy l 사슬에서 me t hy l 기 에 가까운 탄소일수록 이 동이 찰되 는 것을 볼 수 있는데 이 결 과는 acy l 사슬이 그네와 갇은 (sw i n gi n g) 운동을 한다고 볼 수 있다. 이 러 한 운동의 정 도를 때로는 order pa ramete r S 로 표시 가 되 는데 이 함수
 3C.H3 31C.H8 2 C1.H1 2 (C0.H6 2 ) 100C.H2 2 0C.H1 2 g2. O3 y0 .H1 2
3C.H3 31C.H8 2 C1.H1 2 (C0.H6 2 ) 100C.H2 2 0C.H1 2 g2. O3 y0 .H1 2
의 정의는 다음 식으로 나타낸다. S = ½<3 cos28-1> 여기서 < 〉는 모든 열역학적으로 안정한 구조의 평균을 의미하고 O 는 acy l 사슬의 평 균 방향과 acy l 사슬의 한 부분이 갖는 방향의 각도이 다. 그림 2·34 는 DPPC acy l 사슬의 S 값을 준다.
 0.5 ·A
0.5 ·A
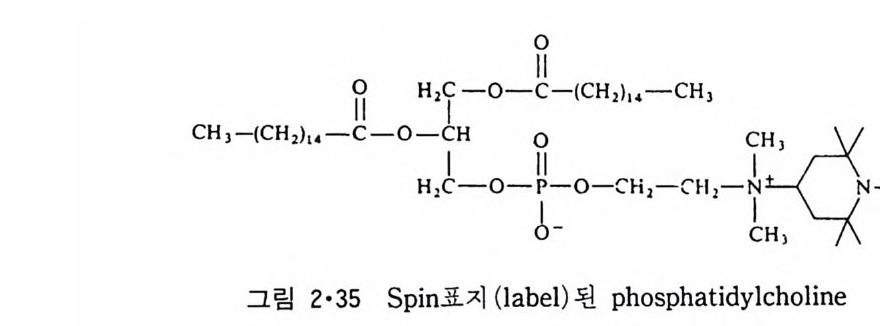
그 링 2·33 에 서는 국성의 어리 부분도 그 이 동성 이 비 교적 큰것을 보 여 주 고 특히 choli ne 부 분 이 잘 움 직 이는 것 을 알 수 있다. 2·4·6 지방질 분자의 운동 이분자층에서의 지방질 분자 운동은 회전 확산 ( ro t a ti onal dif fus io n ), 평 면 확산 ( la t eral dif fus io n ) 그리고 막 의 횡 단 운동 세 가 지 로 나 눌 수 있다. 지방질 이분자층에서의 회 전 운동은 spi n 표지가 된 지방 질 에서 나오 는 ESR s p ec t ra 의 선 넓이 (line w i d t h ) 로부터 추 정 할 수 가 있다. 회 전 확 산 계수는 대개 l010sec - 1 의 값을 갖 는데 이것은 acy l 사 슬 에서의 c - c 결 합의 회전의 약 10 분의 1 이 되며 hemo g lob i n 의 수용 액 에 서 의 값 6 X 106 se c- 1 에 바해 훨 씬 큰 것으로 보아 빠 론 회 전을 하고 있는 것을 알 수 있다. 이분자층 평면에서의 확 산도 그림 2·35 에 보이 는 spi n 표 지나 형광표 지로 측정이 되어 왔다 확산계수 를 처 음 얻은 것 은 그림 2·36 에서와 갇
 c H ) c H2 . I I ‘ 。 出H―. _H—_O -——IIC—— 2O I 4II -PH~LH卜) 2 广➔ 。
c H ) c H2 . I I ‘ 。 出H―. _H—_O -——IIC—— 2O I 4II -PH~LH卜) 2 广➔ 。
 (al tb) tc)
(al tb) tc)
 Hours o·
Hours o·
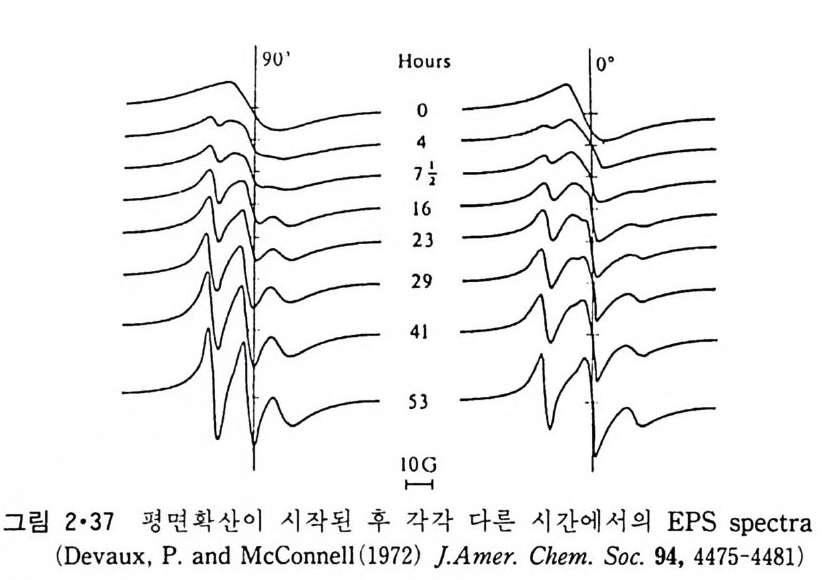
이 sp in 표지된 PC 를 표지가 안된 PC 와 접촉시키면 처음에는 표지된 부 분에 서 의 sp in- sp in 상호 작용으로 넓 은 li ne 이 모 이 다가 sp in 표지 된 PC가 차차 주위로 확산됨에 따라 li ne 이 좁아진다(그림 2·37). 이 좁아지는 속도로부터 확산 계수를 구할 수 있다. 두번째 많이 쓰이는 방법은 광표백 후 형광성 회복(fl uorescence recovery aft er ph oto b leachin g , FRAP) 방법 으로, 여 기 서 는 형 광성 물질로 표지 된 이 분자층의 국히 작은 평 면을 pu lsed laser beam 으로 쬐 어 표백 을 시킨 후 주변에 있는 형광성 지방질아 표백된 부분으로 확산에 의해 서 이동되어 일어나는 형광의 증가 속도를 측정하여 확산계수를 계산하 는 것이다. 표 2·6 은 이들 방법에 의해 얻어진 평면 확산계수 (D) 를 보여준
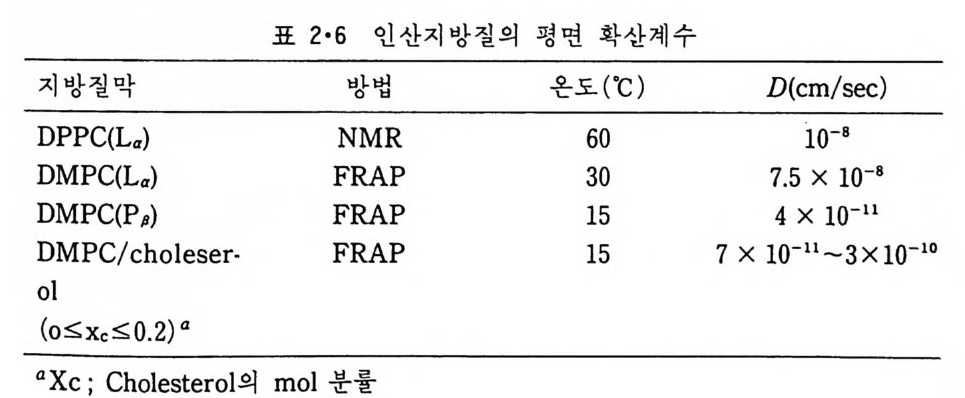 표 2•6 인산지방질의 평면 확산계수
표 2•6 인산지방질의 평면 확산계수
 (A) Ls1ppi no8- s 言할 l잊oa mbee성 t亮 Rlloefd oh epohd\ ~xg hro詞詞鬪 ou0lp i p i d 8s (88) Lis o bree`dlif u+ua?col七Rgj s ecxot 口r·v08e b' r ‘on at\'- e l. _ ~5i.u r &fRo 、그,' e、c. me o veg osc(oCr)b lEgno C}I \Je b )oF5 le?鬪짜 01 3c3g0R iw'&1e Cl 2hc h 、邊검,'、 oo sllecnogr b e o re
(A) Ls1ppi no8- s 言할 l잊oa mbee성 t亮 Rlloefd oh epohd\ ~xg hro詞詞鬪 ou0lp i p i d 8s (88) Lis o bree`dlif u+ua?col七Rgj s ecxot 口r·v08e b' r ‘on at\'- e l. _ ~5i.u r &fRo 、그,' e、c. me o veg osc(oCr)b lEgno C}I \Je b )oF5 le?鬪짜 01 3c3g0R iw'&1e Cl 2hc h 、邊검,'、 oo sllecnogr b e o re
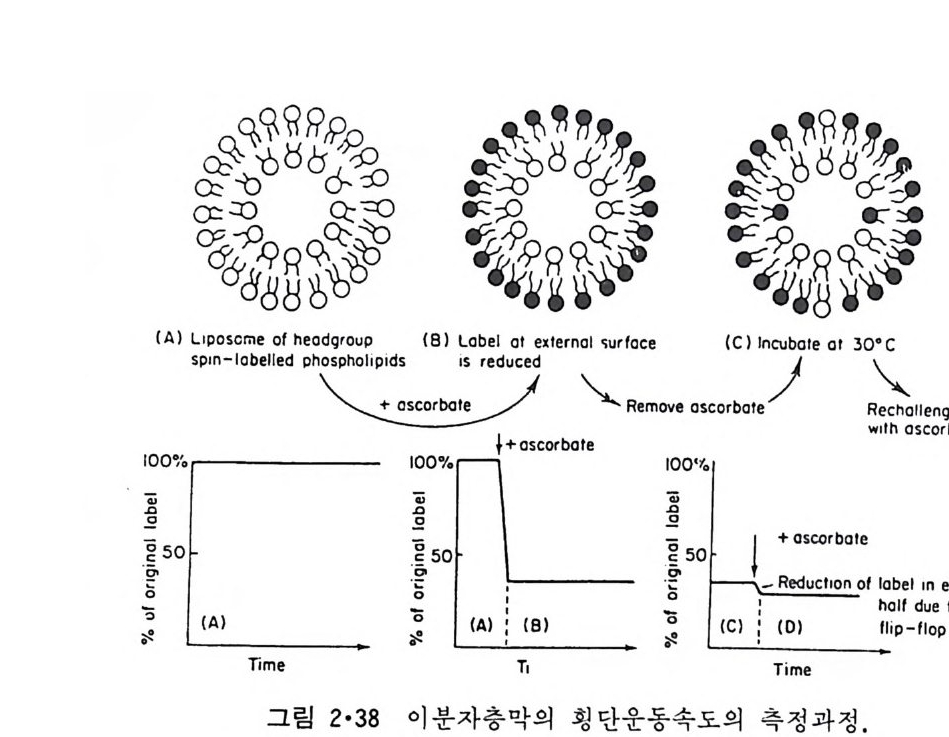
다. 이 표에서 지방질의 확산계수는 수용액에서의 여러 물질의 확산계수 보다는 작지만 지방질 이분자층에서는 상당히 빠른 속도로 횡 적인 운동 을 하는 것을 알 수 있다. 지방질 이분자층의 한 충에서 반대충으로 횡단 이동하는 것은 flip-flop 이 라고도 부르는데 이 의 속도는 sp in 표지 된 PC 가 섞 인 막소포 를 형성하여 이것을 낮은 온도에서 ascorbic a ci d 로 처리해 외부에 있는 pa ramagn e ti c p robe 를 제 거 한 다음 내 부에 남은 sp in p robe 가 밖으로 나 오는 속도를 측정하여 얻는다(그림 2·38). 표 2·7 은 이러한 flip-flop 운 동의 속도로 보여주는데 이 운동이 대단히 느린 것을 알 수 있다. 이 상 lip osome 의 여 러 성 질로부터 의 결론은, (a) 생리 온도에서 지방질의 액체의 物性을 띠고 있고
 표 2•7 인산지방질의 막횡단(flip-fl o p)속도
표 2•7 인산지방질의 막횡단(flip-fl o p)속도
(b) 온도가 일정해도 ca + 2 이나 p H 의 번화에 의해 국부적안 상전이와 상분리가 가능하며 (c) choles t erol 은 지방질 이분자층막의 물리적인 성질에 큰 영향을 주 며 (d) 지방질은 이분자층막에서는 평면이동이 크며 (e) 이분자층막을 횡단하는 운동속도는 대단히 느리다는 것이다. *2 장 참고 문헌 (1) Tanfo r d, C. The Hy d rop h obic Eff ect : Formati on of M ice lle and Bi ol og ica l Membranes, 2nd Ed. W iley , 1980. (2) Greg o ria d is , G.(ed) Lip o some Technology , Vol. I , II and III, CRC Press, 1983. (3) Ostr o , M. J.(e d) Lip o somes, Dekker, 1983. (4) Bang h am, A. D., Hi ll, M. W. and Mi ller , N. G. A. (19 74) Meth o ds in Membrane Bio l ogy , 1, 1-68 (5) Szoka, F., Jr. and Pap a hadjo p o ulos(l980) Ann. Rev. Bi op h y s . Bi oe ng . 9, 467 -508. (6) Mueller, P., Rudin , D. 0., T i en , H. T. and Wescott , W. C.(1962) Natu r e 194, 979. (7) Bang h am, A. D. and Home, R. W.(1962) Natu r e, 196, 952. (8) Houslay , M. D. and Sta n ley, K. K. Dyna mi cs of Bio lo g ica l Membranes, W ile y, 1982, Chap t, 2. (9) Hop pe , W., Lohmann, W., Markle, H. and Zie g le r, H.(eds) Bio p h ys i c s , Sp r in - ge r-V erlag , 1983, Chap t. 12. (IO) Lee, A. G.(1977) Bi oc him . Bi op h ys . Acta . 472, 237-281 . (II) Gruner, S. M. et al( l98 5) Ann. Rev. Bi op hy s . Bi op hy s . Chem. 14, 211-238. (12 ) Cull is, P. R. and Kruij ff, B. D. (19 79) Bi oc him . Bi op h ys . Acta . 559. 399-420. (13) Thomp s on, T. E. and Huang , C. (1980) in Andreoli , et al( ed s) Membrane Phys i o l ogy , Plenum, 1980, Chap t. 2.
제 3 장 단백질과 지방질의 상호작용 Lip osome 의 여러가지 물리적 성질이 생체막 구조의 바탕이 되고 반면 에 생체막의 기능은 주로 단백질에 의해서 이루어지지만 이들 두 성분은 서로의 성질에 영향을 미친다. 따라서 lip osome 과 단백질의 상호작용에 대한 연구는 생체막의 구조와 기능의 관계를 규명하는데 중요한 역할을 하게 된다. 이에는 생체막 외부에 존재하는 주변단백질(p er ip heral p ro t e i n) 과 생체막 내부에 그 일부가 파묻혀 있는 내재단백질(i n t r i ns ic pro te i n ) 뿐만 아니 라 수용성 단백 질과 lip osome 과의 상호작용의 연구도 중요하다. 수용성 단백질은 그 구조가 주변단백질과 유사해서 이들과 lip osome 의 상호작용의 연구는 주변 단백질과 지방질 이분자층 (lipid b il a y er) 과의 상호관계를 이해하는 데 도움이 될 뿐 아니라 생리적인 조 건하에서 많은 수용성 단백질이 생체막에 부착하므로 그 자체의 mechan i sm 의 해명도 중요하다. 3·1 Lip osome 과 주변단백질, 수용성 단백질의 상호작용1) -3) 수용성 단백질과 lip osome 의 상호작용은 주로 정전기력에 의해 이루어 지며 단백질과 lip osome 의 구조에 큰 변화를 주지 않는 경우와 결합에
 N'-p0lE E ua a시53 7,o oa00 o'I,― uo \1o 1oo1o1IJo 1' / /多 4( ' i ? -—/ 1 0EN.1p, 225 。0 。, b
N'-p0lE E ua a시53 7,o oa00 o'I,― uo \1o 1oo1o1IJo 1' / /多 4( ' i ? -—/ 1 0EN.1p, 225 。0 。, b
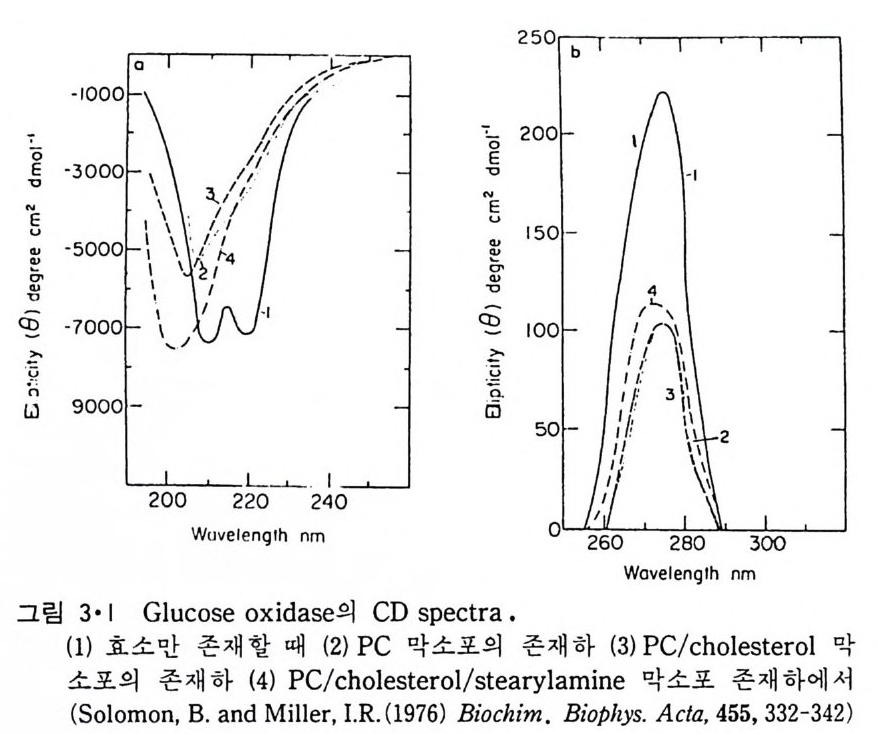
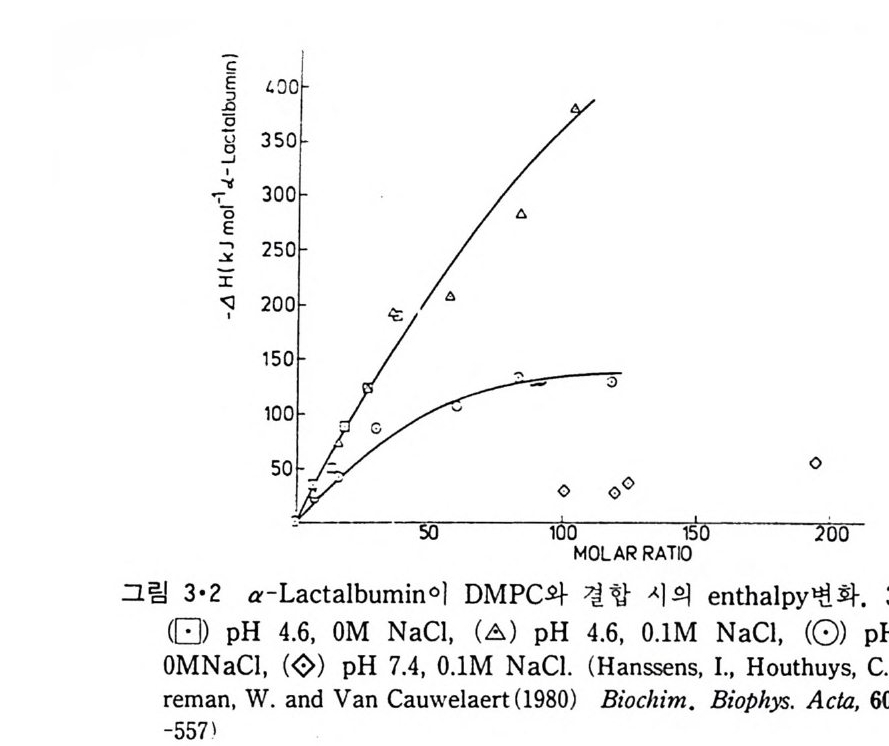
의해 많은 구조 변화를 가져 오는 경우가 있다. 그러나 전자의 경우에도 약간의 구조 변화가 병행하는 것은 효소 활성도 등의 변화로 알 수 있 다. Py r uvate ox i dase 의 경우 PE 의 존재하에는 Km 값이 8 .4 X 10 - 2M 에 서 0.7 X 10-2M 로 감소되 고 Vmax 값은 0.39 X 105 에 서 4.75 X 105 로 중가한 다. 한편 glu cose ox i dase 에 서 는 PC/choleste r ol/ ste a ry la mi ne 이 분자층 에 의해서 효소 활성도가 중가될 뿐만 아니라 그림 3·1 에서와 같이 구조 변화까지도 관찰이 되었다. 그림 3 • 1 에서 이 효소만 존재할 때 단백질 의 20~25% 가 a- 나사선룰 이루는데 지방질 막소포 (ves i cle) 와 접촉하면 대부분의 a- 나사선 구조는 없어지는 것을 볼 수 있다. 지방질 이분자층에 결합하여 그 일부가 이분자층 내부에까지 들어가는 단백 질 중에 서 제 일 많이 연구가 된 것 이 a-lac t album i n 이 다. 이 단백 질 온 내 재 단백 질 인 ga lacto sy l t rans fe rase 와 결 합하여 lac t ose 합성 에 촉매 역할을 하는 주변단백질이다. 그림 3·2 는 a-lac t album i n 이 PC 막소포와 작용할 때의 en t hal py의 변화를 열량계로 측정한 것을 보여준다. 이 단 백질의 동전점(i soele ct r i c p o i n t)인 p H5 보다 높은 p H 에서는 그 상호작용 이 약하고 i on 강도에 민감한 데 반해서 낮은 p H 에서는 결합이 강하고
 응 ,~o
응 ,~o
ion 강도에 좌우되지 않는 것을 볼 수 있다. 이 단백질의 농도가 클 때에 는 이분자층이 파괴되어 긴 모양의 복합체를 형성한다(그림 3 • 3). 그림 3 • 4 는 지 방질 이분자층이 유지되는 조건하에서 a-lac t album i n 이 막소포 에 부착되는 양이 p H에 따라 어떻게 변하느냐를 보인 것이다. pH 7 에서 는 결합이 안 일어나고 pH 5 이하에서는 산성의 중가에 따라 결합되는
 그림 3•3 DMPC 와 a-lacta l bwnin 복합체의 전자현미경 사진.
그림 3•3 DMPC 와 a-lacta l bwnin 복합체의 전자현미경 사진.
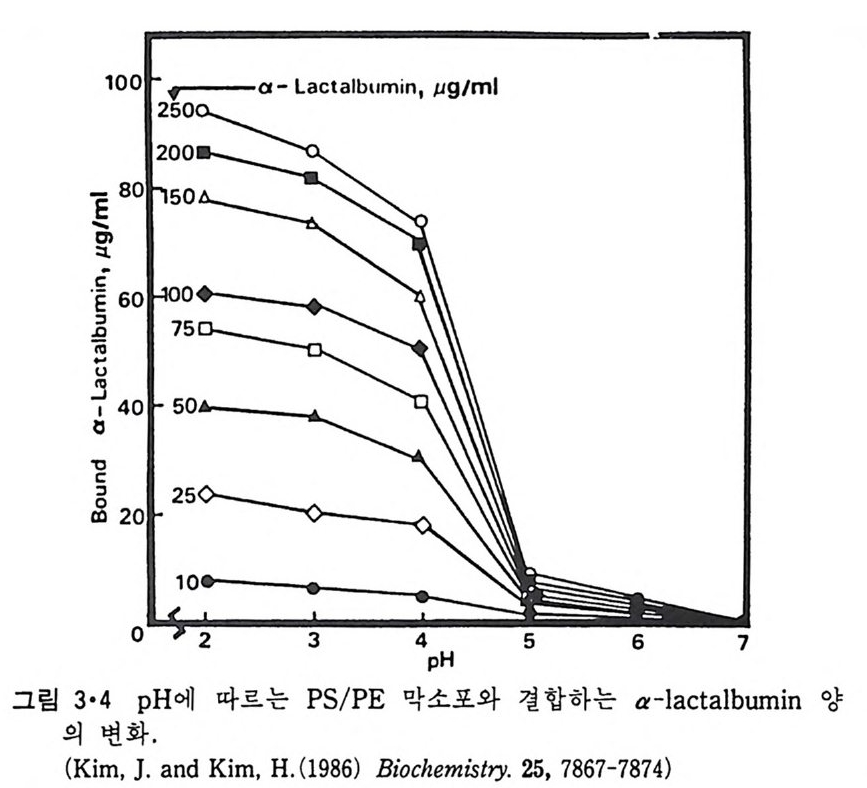 100 『 ,r---a- La cta lbumi n, µg/ ml
100 『 ,r---a- La cta lbumi n, µg/ ml
 pH
pH
정도가 급속히 증가된다. 일단 낮은 p H 에서 결합이 일어나면 p H 를 7 로 변화시켜도 그 일부는 그대로 남아 있어 부분적인 바가역성을 보여주고 이 비가역성은 p H 가 낮아침에 따라 감해진다. 이러한 비가역성은 소수 성 힘이 이 결합에 가담한다는 것을 시사한다. a-Lac t album i n 은 낮은 p H 에서 소수성인 am i no 산 결사슬이 노출되어 이것이 지방질의 이분자 층과 결합하면 그 일부가 이분자층 내부에 들어가는 것으로 보인다. 이 단백질의 일부분이 산성 p H 에서 지방질 이분자층 내부로 파고 들 어가는 것은 단백질 가수분해효소로의 처리와 소수성 표지로 입중이 되 었다. a-Lac t album i n 을 산성에서 PS/PE 막소포와 결합시킨 후 p H 를
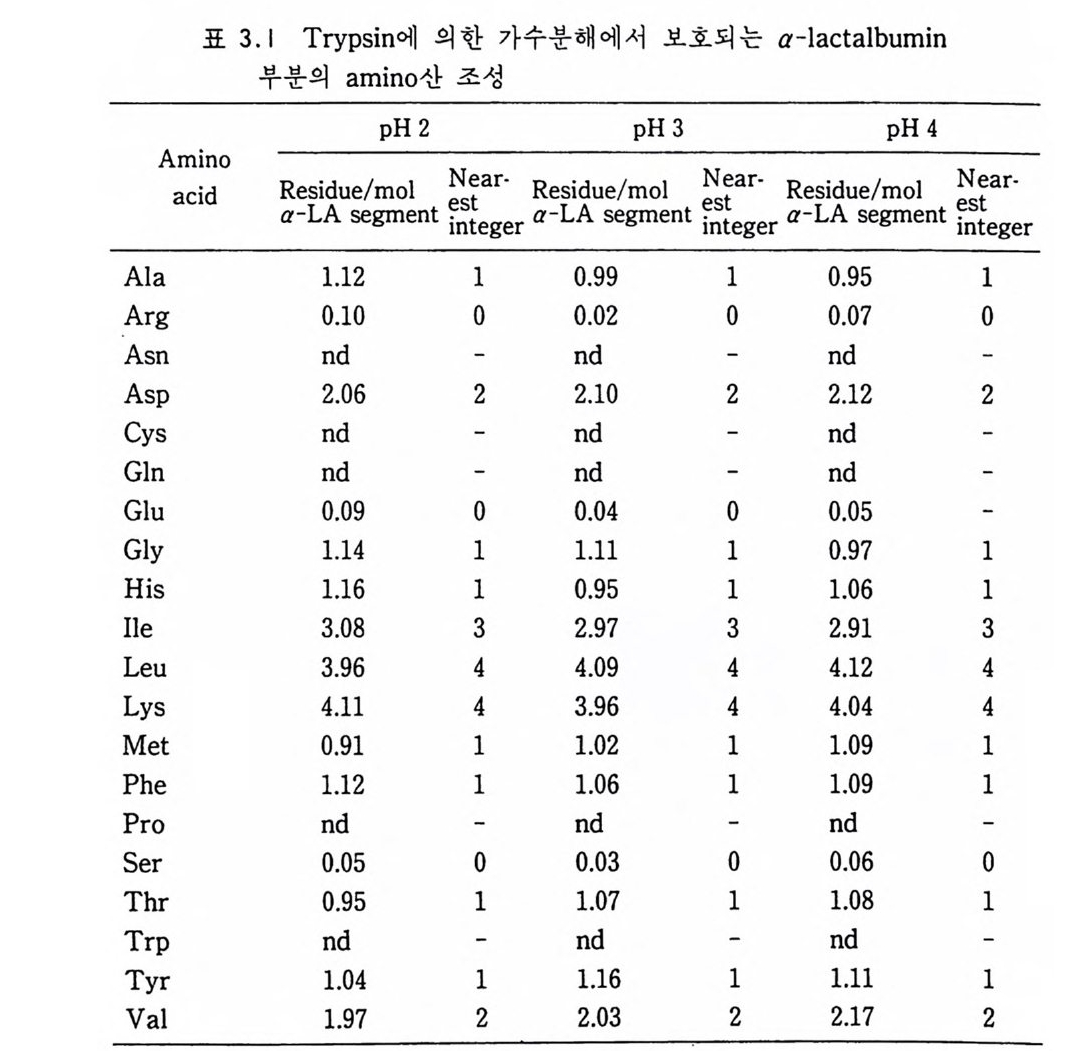 표 3 . 1 T ryp s i n 에 의 한 가수분해 에 서 보호되 는 a-lacta l bumi n
표 3 . 1 T ryp s i n 에 의 한 가수분해 에 서 보호되 는 a-lacta l bumi n
 112.1 1- C lu-Cl n-l
112.1 1- C lu-Cl n-l
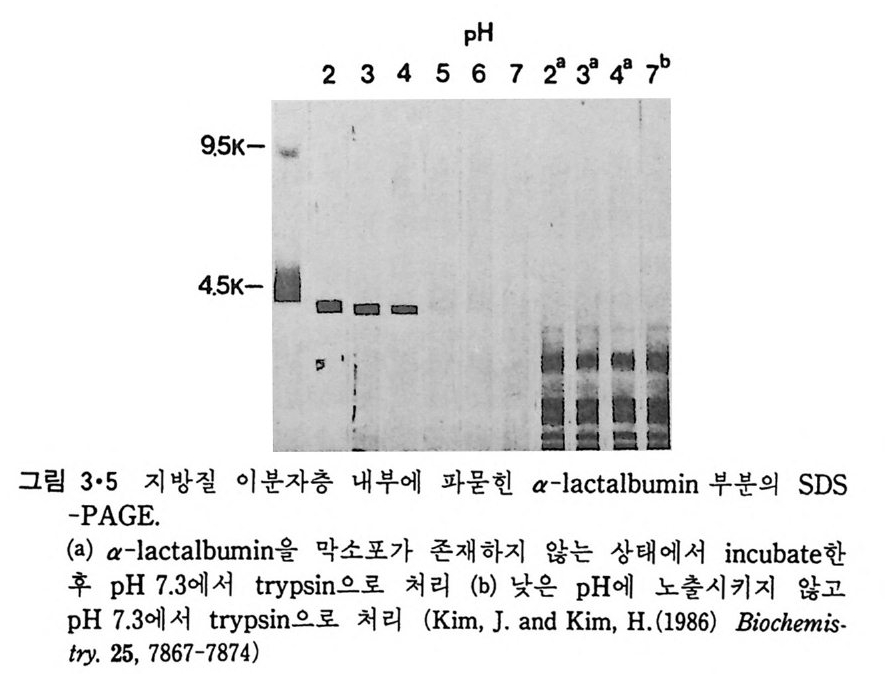
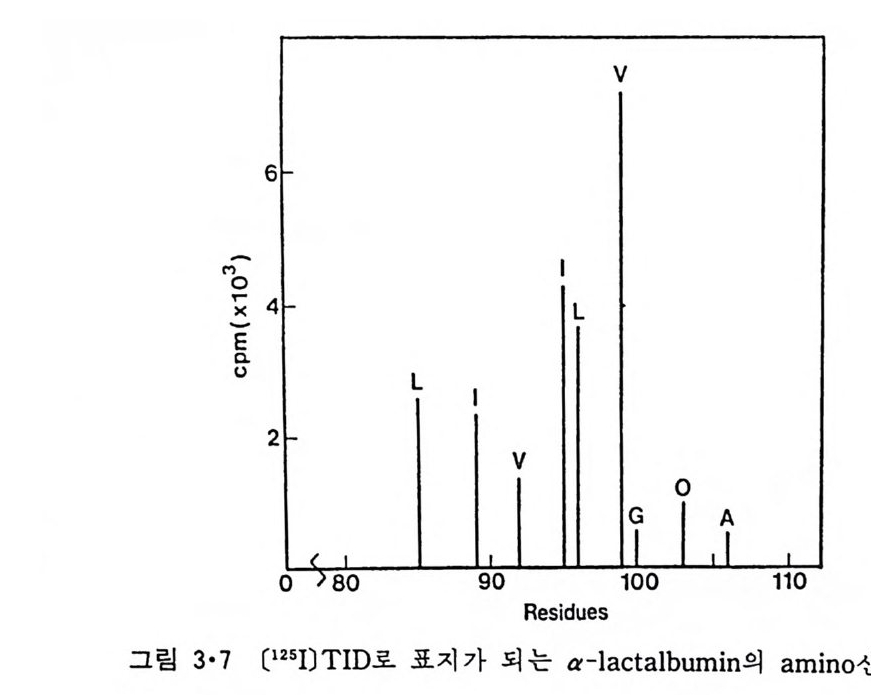
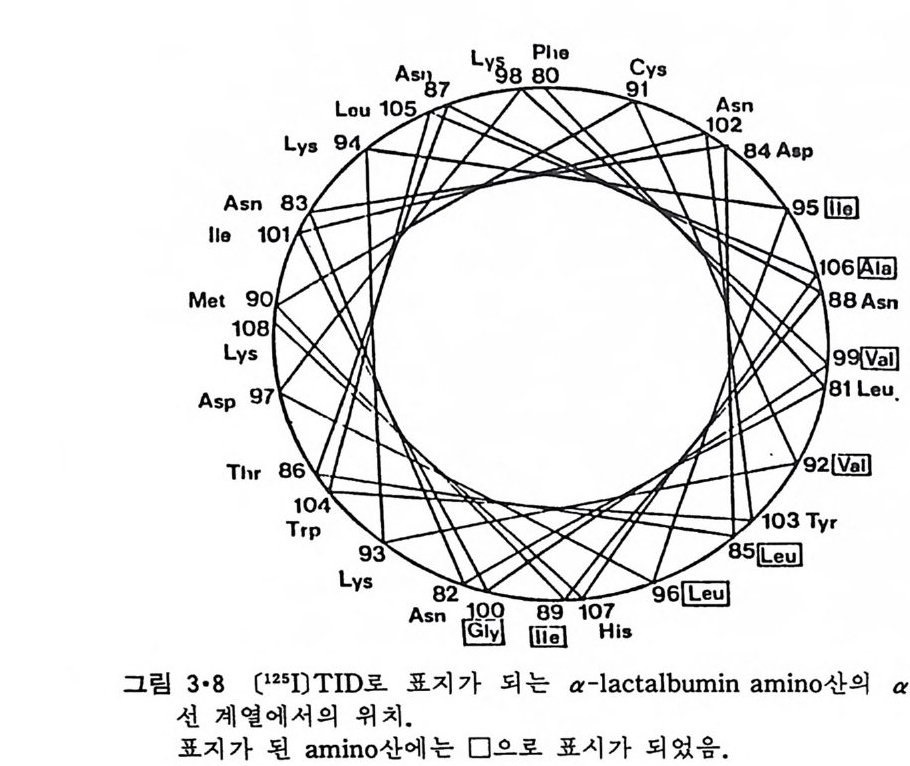
중성으로 조정하고 tryp s i n 으로 처리한 후 막소포만을 분리하여 단백질을 추출하여 SDS-PAGE 륭 한 결과 그림 3 • 5 를 얻었다. 모든 p H 에서 분 자량이 약 4,000 이 되는 조각이 단백질 가수분해효소로 처리한 후 막소포 에 남아 있고 이 po lyp e p tide 사슬은 p H 가 낮을수록 더 많이 막소포에 들어가는 것을 알 수 있다. Ch y mo t r yp s i n 으로 처리해도 같은 결과가 얻 어 지 는데 이 때 얻 어 지 는 p ol ypepti de 의 분자 량은 약 5,000 이 다. Tr yps in 처리에 의해 생성된 p ol yp e pti de 의 am i no 산 조성은 표 3·1 와 같다. a-Lac t album i n 에 는 me t h i on i ne 이 하나 존재 하는데 이 들 효소로 처 리 해 생 성 된 p ol yp e pti de 에 도 하나가 남아 있 어 이 것 이 a-lac t album i n 의 am i no 산 서열의 어디쯤 있는지를 알 수 있다. 그링 3·6 은 a-lacta l - bum i n 의 서열 중에 어느 부분이 단백질 가수분해효소에 의해 쪼개지지 않는가를 추정한 것을 보여준다. 이 부분의 양쪽이 모두 tryp s i n 에 의해 가수분해된 것으로 이 부분이 이분자층으로 들어갈 때에는 고리형을 이우는 것을 알 수 있다. a-Lac t album i n 의 일부가 인산지방질 이분자층으로 파고들어간다는 더 확실한 증거는 소수성 표지에 의해 이루어진다. T ryp s i n 으로부 터 보호되 는 부분을 [12 5l]TID (3-tr i f luo rometh y l- 3-(m -[1 2 5 I]io d oph eny l) dia z ir i n e ) 로 소수성 -광 표지 (hy d rop h obic ph oto l abeli ng ) 를 시 킨 후 am i no 산의 서열을 결정하면 어느 am i no 산이 표지되었는가를 알 수 있는데 그림 3·7 은 소수성 am i no 산 기가 표지되는 정도를 보여준다. 그립 3·8 은 이 부분이 a- 나사선을 형성할 때 그 나선형의 한쪽 끝에서
 v
v
 L PIIO
L PIIO
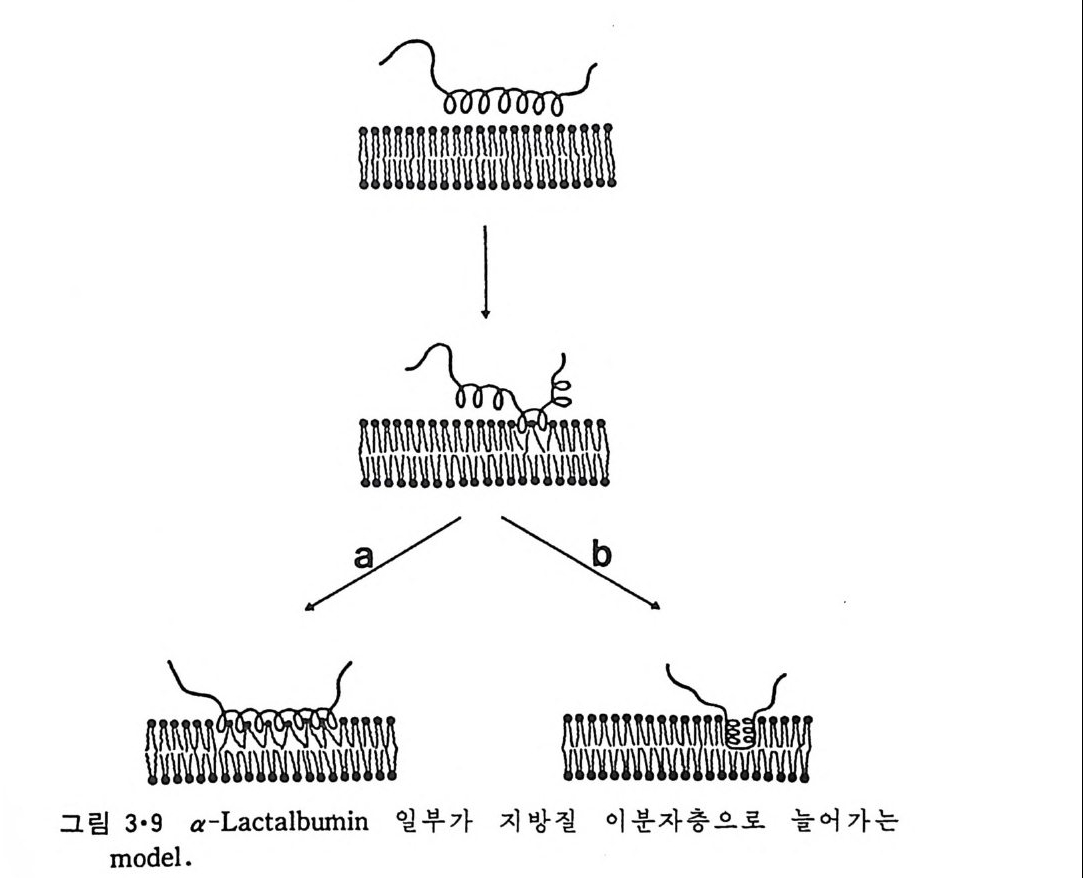
본 am i no 산의 배열을 나타낸다. 표지가 한쪽 편에만 되었는데 그 반대편에는 [125I]TID 가 접근 할 수 없 는 것을 알 수 있다. 여기서 결론은 막에 들어가는 부분은 a- 나사선을 이루고 있고 그림 3·8 에서 같은 표지가 되려면 그림 3·9b 에서 보이는 것 과 같은 밀착된 고리형을 이루며 이분자층 내부로 들어가거나 그림 3·9a 에서와 같이 이 a- 나사선의 친수성면이 이분자층 밖을 향해야 한다. L y soz y me 과 cy toc hrome c 도 유사한 실험을 통하여 그 일부가 이분자 충 내 부로 들어 가는 것 을 알 수 있 었 다. Cy toc hrome c 는 mi toc hondria 내막의 외부표면에 존재하는 주변단백질인데 이의 ap o cy toc hrome c 가 세포질에서 합성된 후 외막을 통하여 이동되면서 heme 이 결합된다. 이 단백 질 이 m it ochondr i a 의 외 막을 통과할 때 내 재 단백 질 구멍 을 통과하는 지 또는 지방질 이분자층을 통과하는지는 알지 못했으나 다음 실험으로 지방질을 횡단하는 가능성이 높아졌다.
 \
\
 tI nryh pi bs ii t no r +
tI nryh pi bs ii t no r +
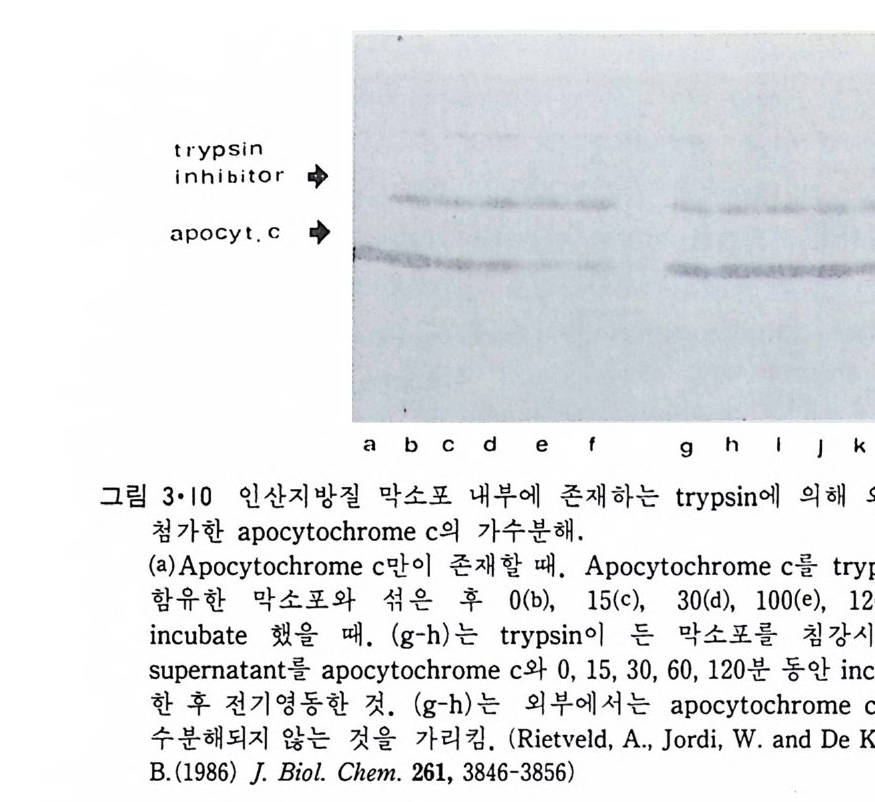
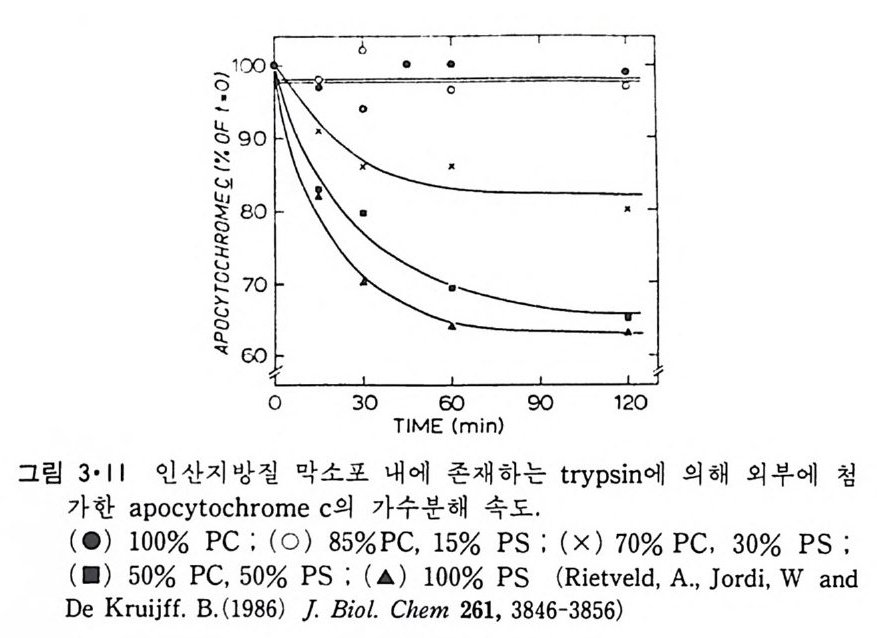
PC/PS 막소포 내 에 typ s i n 을 포착시 킨 후 ap o cy toc hrome c 를 첨 가하 여 일정한 시간간격으로 단백질을 추출하여 SDS- P AGE 실험을 하면 그 링 3·10 과 같은 결과를 얻었다. 여기서 h- f는 시간이 감에 따라 이 단백 질이 전기영동으로 탐지되지 않을 칭도로 작은 단위로 가수분해가 되는 것을 알 수 있다. 이는 ap o cy toc hrome c 가 인산지방질 이분자층 을 동과 하는 것이라고 해석된다. 그림 3·11 은 시간에 따르는 이 통과속도를 보 여준다. PS 의 함량이 클수록 빨리 막을 횡단하는 것을 알 수 있다. 이상의 결과는 수용성단백질이 조건에 따라서 구조변경을 일으켜 지방 질 이분자층에 깊이 들어갈 뿐만 아니라 막을 횡단할 수도 있다는 것을 보여준다. a - Lac t album i n 의 농도가 클 때에는 그림 3·3b 에서와 같은 PC 와의 복 합체를 형성하는데 이의 구조는 아직도 밝혀지지 않았다. 이와 유사한 현상은 혈액의 고밀도 지방단백질의 ap o li po p r ote i n A-1(ap o A-1) 과 DMPC 와의 상호작용에서도 일어난다. 죽 ap o A-1 농도가 작을 때에는
 1 00 b
1 00 b
DMPC 막소포 표면에 이 단백질이 부착된다. 반면에 단백질 농도가 클 때에는 원판형 (d i sco i dal) 의 복합체가 형성되는 것을 전자현미경으로 관 찰할 수가 있다(그림 3·12). 이 원판의 두께는 55A 정도이고 Tm 도 DMPC lip osome 의 값과 같아서 이 복합체의 DMPC 는 이분자층을 이루 고 있고 단백질이 그림 3·13 에서 보이는 것과 같이 원판 둘레를 감싸고 있는 것으로 생각되고 있다. 이때 지방질의 acy l 사슬을 향한 단백질면은 소수성이라야 되고 외부면은 친수성이라야 되는데 그림 3·14 는 이 단백 질이 9 개의 a- 나사선을 형성할 수 있으며 이 a- 나사선 둘은 소수성과 천수성 표면을 가질 수가 있는 것울 보여준다. A-1 a p o 단백질의 농도가 작을 때 이 것 이 어 떻 게 DMPC 의 막소포에 부착되 는지 또 A-1 의 농도가 커짐에 따라 어떠한 과정을 거쳐 원판형으로 되는지는 아칙 모르고 있 다. A-1 단백질 이외에도 다른 혈액 지방 단백질의 a p o 단백질, am y lo i d 와 g luca g on 등 단백질들이 PC 와 유사한 복합체를 이룬다. 여러 단백질들은 지방질 이분자층에 결합되어 구멍을 형성하는데 이때 흡착된 단백질이 이분자층을 횡단하여 내재단백질과 유사한 구조를 형성 할 것으로 생각된다. 이들 구멍을 형성하는 수용성 단백질들은 대부분 독소(t ox i n) 로서 그중 제일 간단한 것이 벌의 me litti n 이다. 이의 ami no
 산 그서림 열 은3· 12H 2AN p- oG-Ally -과 I leD—P PG Cly 와- A의 la복-V합一&i서a체l - 의 L 蓬沼쏘― 겁e음u성-L 영y s 색 - V전al 자—현 L e미u -경T hr
산 그서림 열 은3· 12H 2AN p- oG-Ally -과 I leD—P PG Cly 와- A의 la복-V합一&i서a체l - 의 L 蓬沼쏘― 겁e음u성-L 영y s 색 - V전al 자—현 L e미u -경T hr
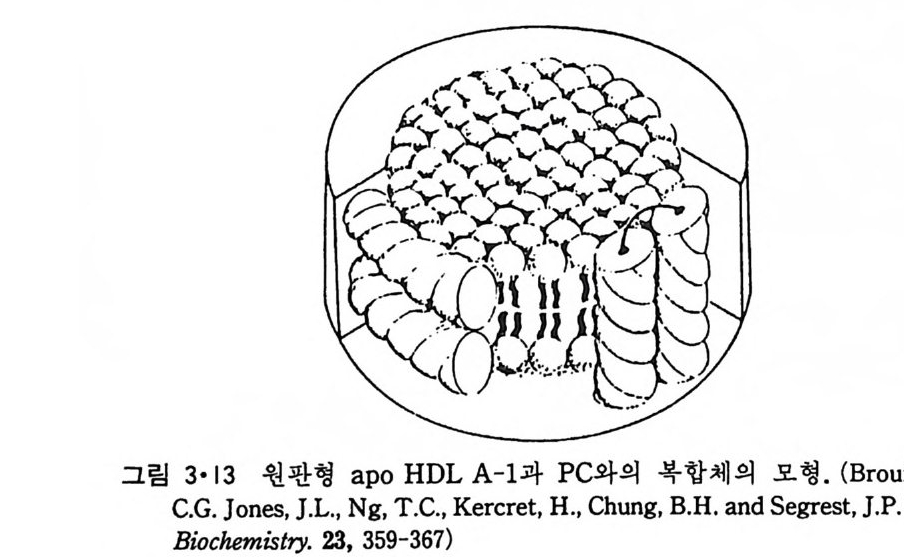 그림 3· 13 원판형 ap o HDL A-1 과 PC 와의 복합체의 모형. (Brouil let t e,
그림 3· 13 원판형 ap o HDL A-1 과 PC 와의 복합체의 모형. (Brouil let t e,
 二\( m〔〔씁 〔 )
二\( m〔〔씁 〔 )
 `、 8 `훈` : 8 2 ! \:`\ `느/三二 \'I
`、 8 `훈` : 8 2 ! \:`\ `느/三二 \'I
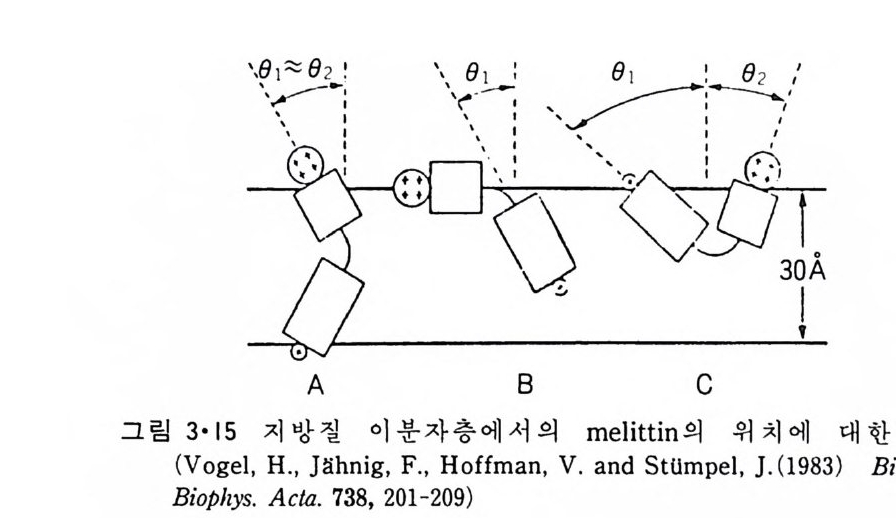
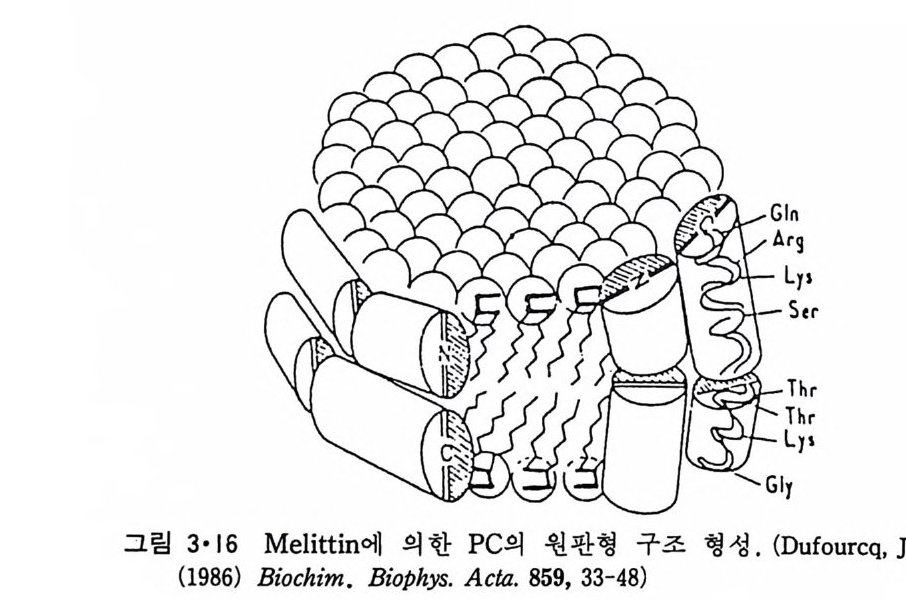
p rol i ne 이 있는 부근에서 구부러져 두 나사선 사이에 120° 의 각을 형성한 다. 이 단백질은 지방질 이분자층과 작용하여 전압 (vol t a g e) 에 의한 ion 의 두과율을 증가시키는 것으로 구멍을 형성하는 것을 알 수 있다. Me litti n 의 막내에서의 구조는 그림 3·15 에서 보이는 것과 같이 몇가지 가능성 이 있으나 線型赤外線二色性(li near inf r ar ed dic h rois m ) 등 실험으로 처음 구조의 가능성이 제일 크다. Me litti n 도 농도가 높을 때에는 그림 3·16 에 보이는 dis c oid a l 복합체를 형성하는 것이 X- 선 회철 실험으로 알게 되었다.
 Ser
Ser
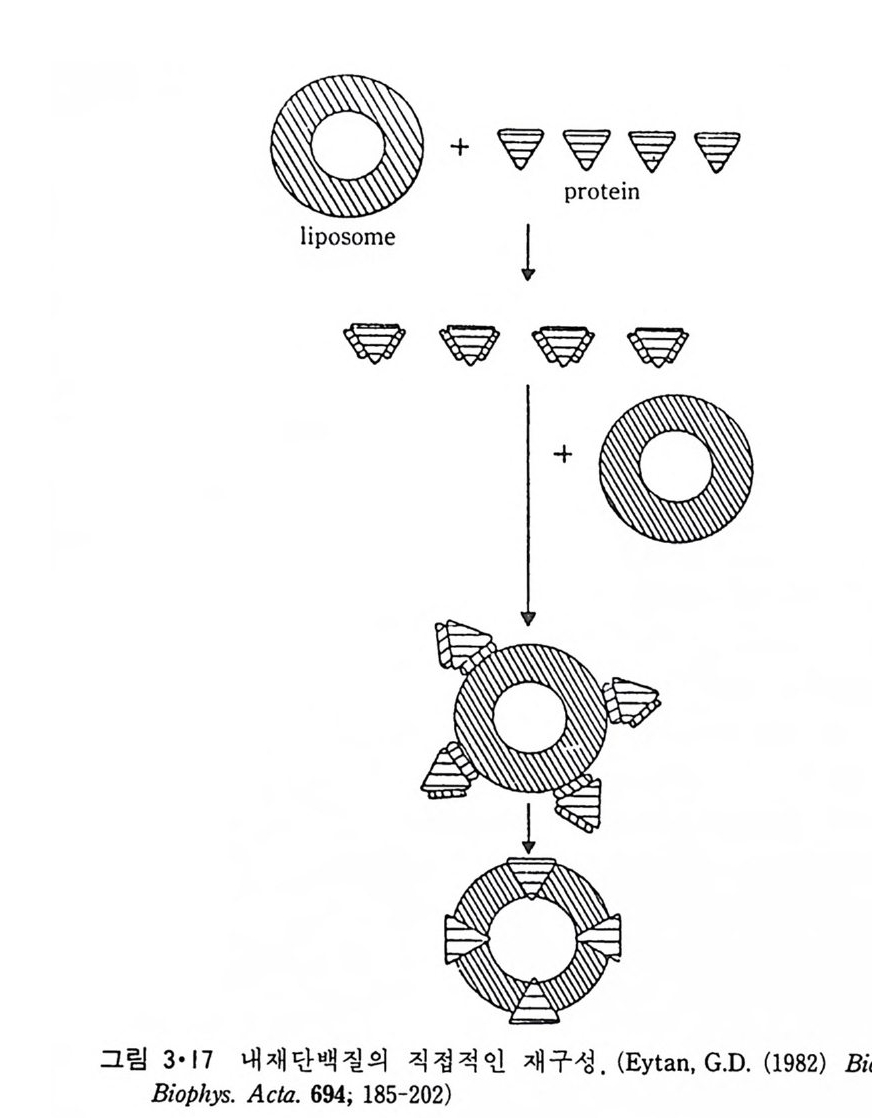
이상 예로 수용성 단백질이 지방질 이분자층 막과 작용하는 것을 구체 적으로 본 예는 별로 없지만 수용성 단백질과 지방질이 작용할 때 크고 작은 구조 변화가 흔히 일어나는 것을 볼 수 있다. 국단적일 때에는 수 용성 단백질의 일부가 이분자층 내부에까지 들어가거나 구멍을 형성할 수 있기 때문에 이 경우에는 내재단백질과 주변단백질의 구분이 사실상 힘들게 된다. 3·2 Lip osome 과 내재단백질의 상호작용I) 4) 내재단백질과 lip osome 의 상호작용을 연구하는 데는 순수한 단백질이 지방질 이분자층에 존재하는 것이 중요하다. 이것을 위해서 세 가지 방 법 이 이 용되 고 있 다. 첫 째 는 Halobacte r i um halobiu m 의 자 색 막 (pu rpl e membrane) 에 서 의 bac t er i orhodo p s i n 과 같이 생 체 막에 한가지 만의 단백 질 이 존재할 때 이 생체막을 정제하여 그대로 쑬 수가 있다. 두번째는 생 체막에 하나의 내재단백질이 농축되어 있을 때 다른 단백질들을 선택적 으로 제거하여 그 단백질만을 남게 하는 것이다. 세번째 방법은 생체막 에서 단백질을 세탁제로 추출하여 다른 단백질로부터 분리한 후 lip osome 에 넣 는 방법 인데 이 것을 재구성 (reconsti tut i on ) 이 라고 한다. 위에 예 를 든 세 방법 중에서 처음 두 경우는 비교적 드물고 세번째 방 법이 제일 보편적으로 이용되어 생체막 단백질들의 기능의 mechan i sm 을 해명하는 데 불가결한 방법이 되었다. 3·2·1 내재단백질의 재구성 방법 5) 여기에는 여러가지 방법이 이용되었는데 이중 중요한 것은 다음과 같 다. ( i ) 직접적인 재구성 그림 3·17 에서와 같이 lip osome 과 내재단백질을 섞으면 lip osom~ 일부 는 파괴가 되며 내재단백질 표면에 부착이 되고 다음 단계로는 단백질 -지방질 복합체가 지방질 이분자층으로 들어가게 된다. 초음파를 쪼이면
 0+ 뺨뺨pro 옆te i n 틈 ’
0+ 뺨뺨pro 옆te i n 틈 ’
이 과정을 촉진시킬 수도 있다. (ii) 세탁제 제거법 이것은 가장 많이 쓰이는 방법으로 인산지방질과 내재단백질을 모두 세탁제로 용해시킨 후 두석에 의해서나 g el 여과로 세탁제를 제거하면 인 산지방질은 막소포로 되면서 내재단백질이 그 내부에 들어가게 된다(그 림 3·18). 이외에도 이들 방법을 수칭한 과정에 의해 많은 내재단백질이 재구성
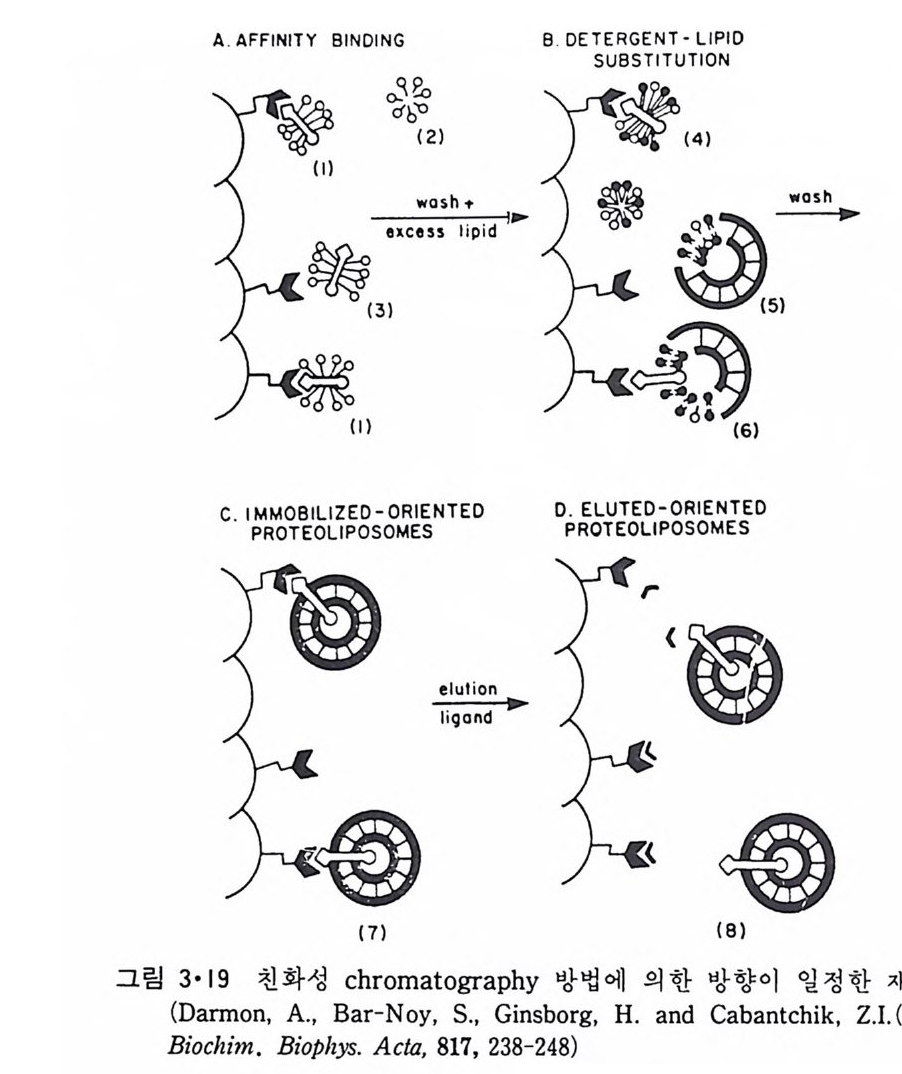
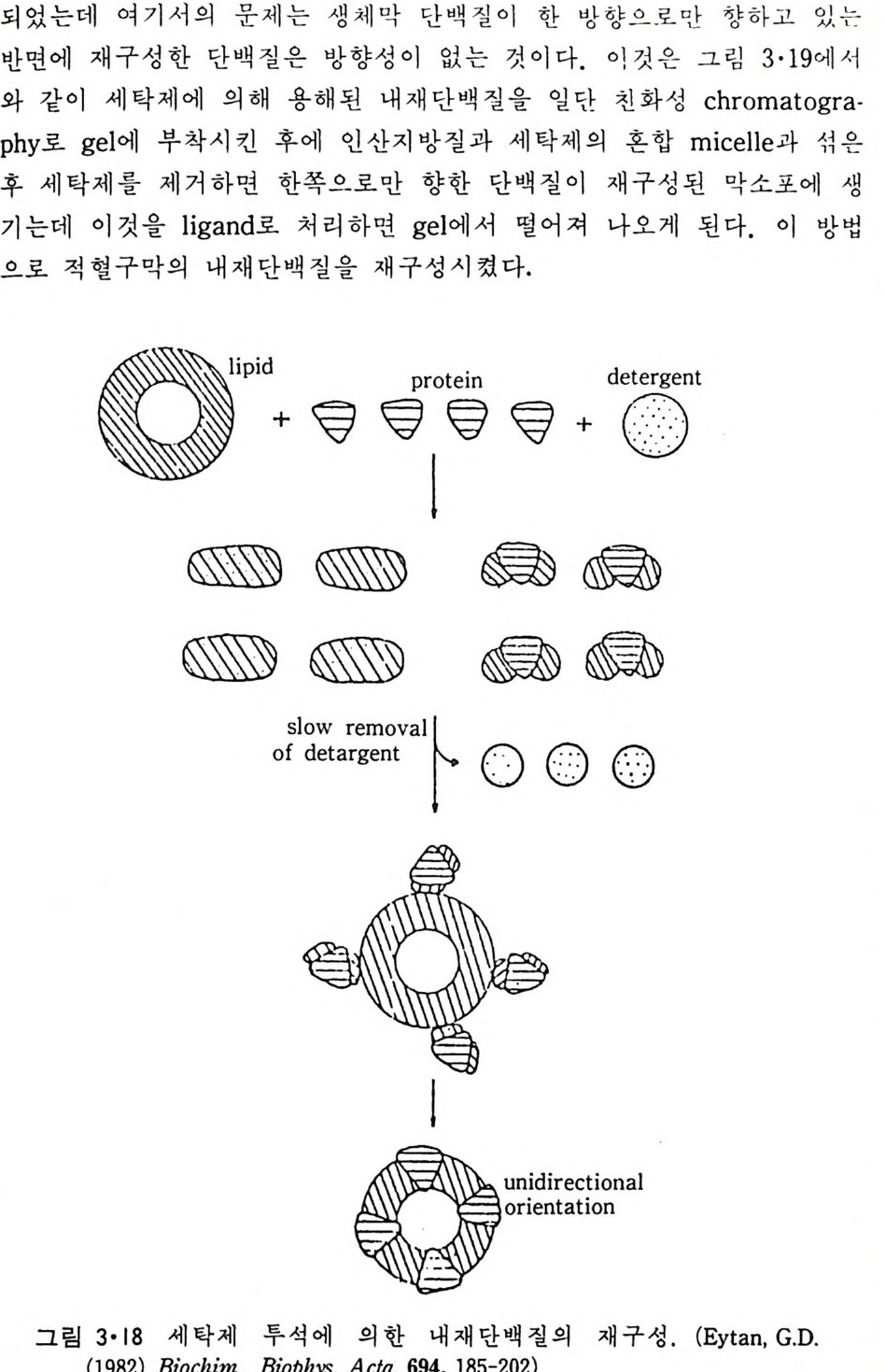 되었는데 여기서의 문제는 생체막 단백 질 이 한 방향 으로만 향 하 고 있 는
되었는데 여기서의 문제는 생체막 단백 질 이 한 방향 으로만 향 하 고 있 는
 A. AFFINITY BINDING B. DETERGENT· LIPID
A. AFFINITY BINDING B. DETERGENT· LIPID
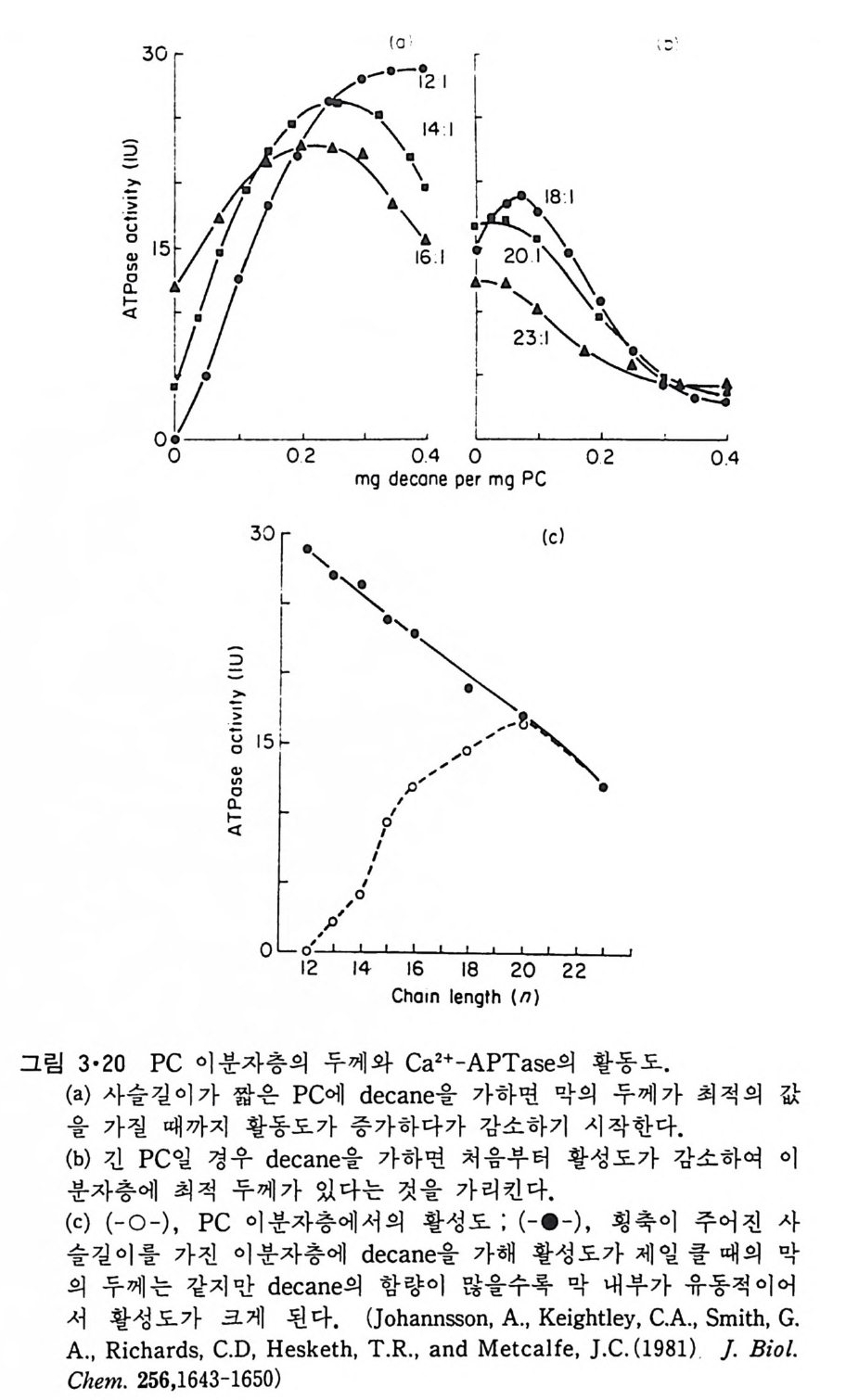
3·2·2 지방질 이분자충의 두께 내재단백질을 지방질 이분자 층에 재구성시킬 때 지방질의 ac y l 사슬의 길이가 중요하다는 것은 Ca2+-ATPase 의 재구성실험에서 입증이 되었 는데 이 결과는 그림 3·20 에 보여준다. 이 그림에서 이중결합이 하나있 는 acy l 사슬에서 최적의 길이는 탄소수가 20 일 때이고 그것보다 작거나 크거나 하면 Ca2+-ATPase 의 활성도가 감소된다. 이 효소를 재구성시 킬 때 decane 을 첨가하면 짧은 ac y l 사술인 경우에는 활성도가 늘고 긴
 ', () ` ~
', () ` ~
 a
a
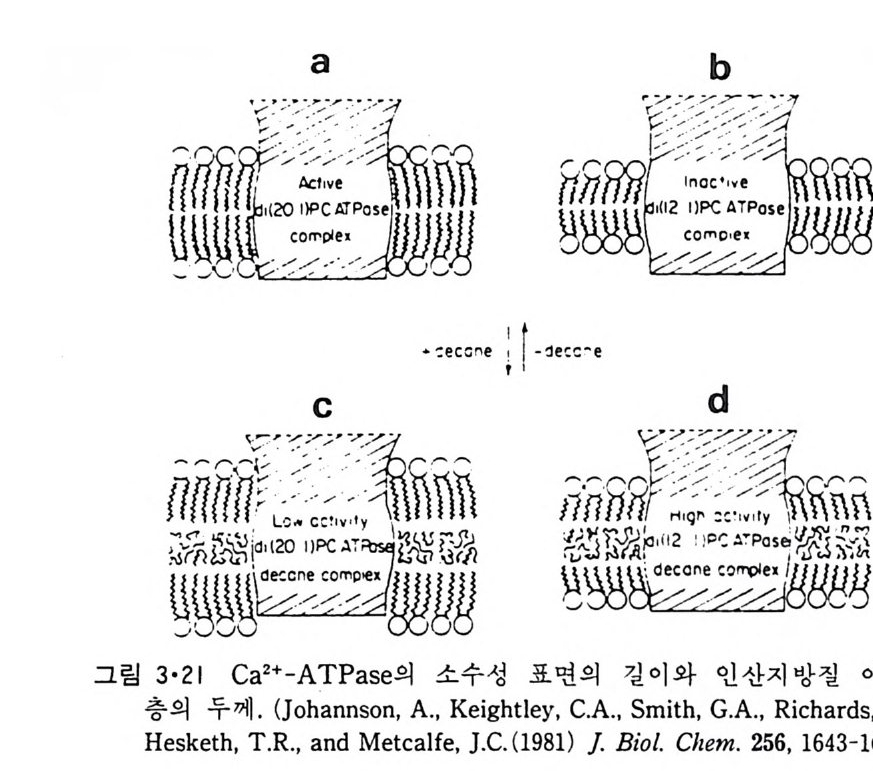
acy l 사슬인 경우에는 활성도가 감소된다. 이것은 Ca2+-ATPase 와 같아 이분자층을 횡단하는 내재단백질인 경우 이 단백질에 국성인 표면과 비 극성인 표면이 있어 이것에 맞는 지방질 이분자층이 필요한 것을 보여준 다. 그림 3·21 에서 a 는 단백질의 국성 부분과 지방질의 국성 부분이 인 접하여 있고 단백질의 소수성 표면의 길이와 acy l 사슬의 길이가 갇아 이 효소활성 에 최 적 의 상호작용을 하는데 이 이 분자층이 decane 에 의 해 더 두꺼워지면 c 같이 되어 활성이 떨어진다. 반면 b 에서는 acy l 사슬이 너무 짧은데 decane 을 가해 주면 d 가 되어 활성이 커진다. a 와 d 경우에 는 국성 -국성 작용과 비 국성 -비 국성 작용은 같으나 decane 존재 하에 이 분 자층의 소수성 부분이 더 유동적이어 효소활성도가 더 커지게 된다. 3·2·3 둘레지방질 (Annular lipid) 내재단백질이 그 주변의 지방질과 결합되어 있다는 것은 여러가지 실 험으로부터 알게 되었다. 이렇게 내재단백질을 둘러싸서 다른 지방질같
 aSD6d0ltf '
aSD6d0ltf '
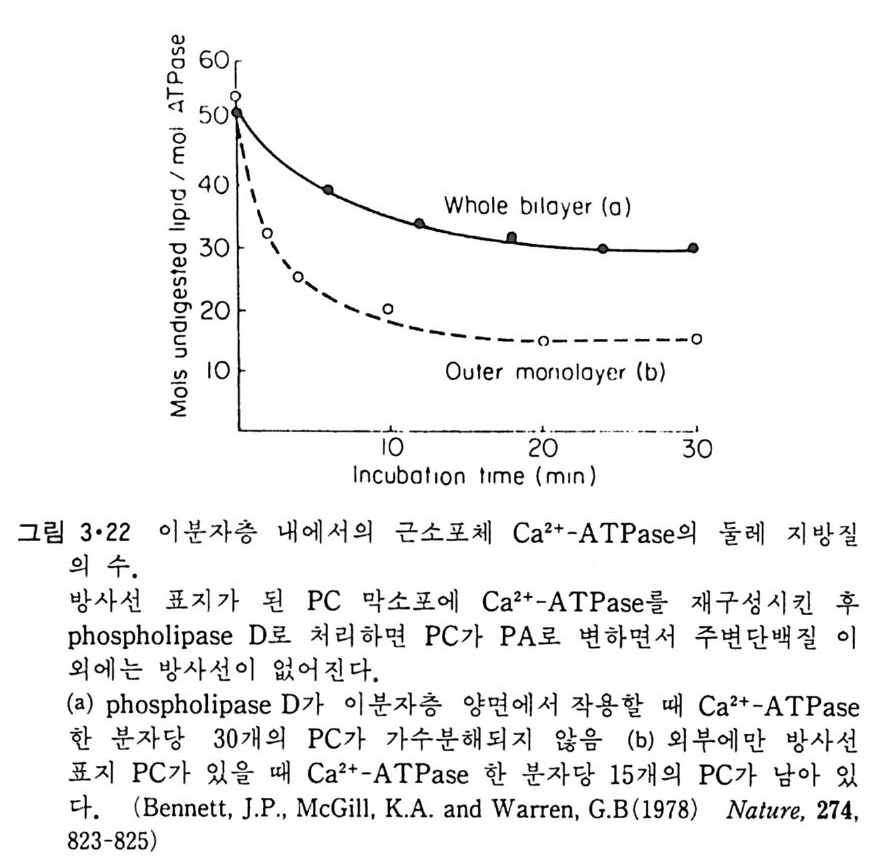
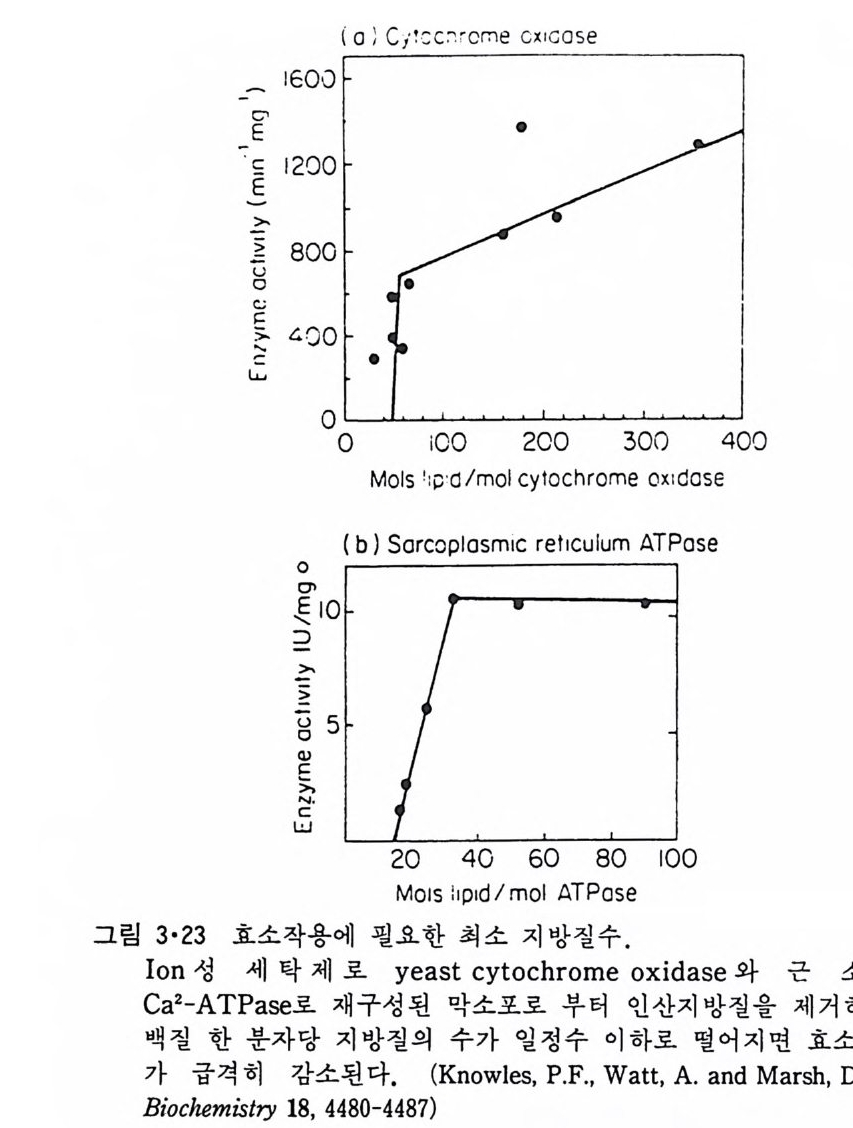
이 자유로운 운동을 할 수 없는 지방질을 둘레지방질이라고 부른다. 이 둘레지방질의 수는 내재단백질에 따라 다른데 PC 막소포 이분자층에 들 어가 있는 Ca2+-ATPase 를 p hos p ho lip aseD 로 처리하면 둘레지방질 이 외의 지방질은 전부 PA 로 가수분해되기 때문에 남은 둘레지방질의 수를 알 수 있다. 그림 3·22 에서 Ca 2+ -ATPase 의 경우 둘레지방질의 수가 30 이며 이것들이 지방질 이분자층의 양면에 똑같이 분포되어 있는 것을 알 수 있다. 한편 내재단백질로 재구성된 lip osome 에서 지방질을 세탁제로 차차 제 거하면 단백질 하나에 대한 지방질의 수가 어느 수 이하가 될때에 갑자 기 효소활성도가 감소되어 (그림 3·23) 이로부터 둘레지방질의 수를 측정 할 수 있다. 이 방법으로서도 Ca2+-ATPase 의 경우 30 개의 둘레지방질 이 있는 것을 알 수 있고 cy toc hrome ox i dase 의 경우 55 개의 둘레지 방 질이 존재한다. 이 실험은 둘레지방질이 내재단백질의 구조와 기능을 유
 IoE0\ O }1 Coj ? ::2 c ;,rco4me c ~1 c ose
IoE0\ O }1 Coj ? ::2 c ;,rco4me c ~1 c ose
지하는데 대단히 중요하다는 것을 시사한다. 이 사실은 혼합지방질 이분 자층에서도 볼 수 있다. 그림 3·24 는 PC 와 PA 로 구성된 막소포 이분자 층에 들어간 Ca2+-ATPase 의 활성도와 이 두 지방질의 분자비와의 관계 륭 보인 것으로 지방질의 전체량이 둘레지방질 수와 같은 때에는 PC 가 PA 로 치환이 되면 활성도가 칙선적으로 감소된다. 반면에 지방질의 양 이 쿨 때에는 PC 가 Ca2+~ATPase 에 선택적으로 흡수되어 활성도에 별로 영 향을 미 치 지 않는다. Choles t erol 만은 둘레 지 방질 역 할을 하지 못한다.
 120
120
 `0 98755L3,‘
`0 98755L3,‘
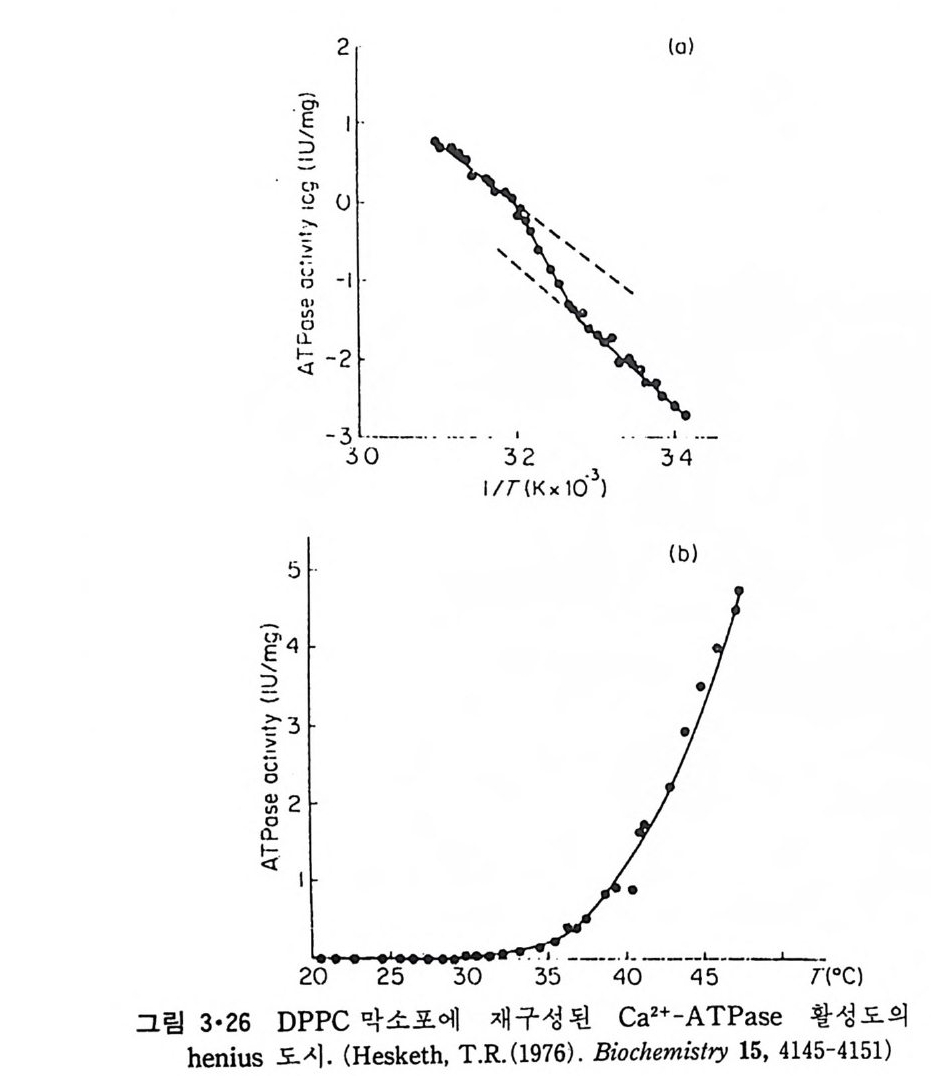
둘레 지방질은 내재 단백질에 의해서 그 이 동능력 이 감소되어 있는데 이 는 EPR 에 의해서 연구되었으며 그럼 3·25 는 그 절과룹 보여준다. 여o 햐o 을 받는 것은 둘레지방질이나 그 다음 지방질도 작은 영향을 받는 거入으己 알 수 있다. 3·2·4 상이전과 상분리 이상의 결과는 전부 지방질의 상 전이 온도 이상에서 일어나는 것이고 그 이하에서의 현상은 좀더 복잡하다. 그럼 3·26 은 PC 이분자층 막에 둘
 2 (a)
2 (a)
 그립 3·27 CaH-ATPase 로 재구성된 DMPC 막소포의 동결―파열 전
그립 3·27 CaH-ATPase 로 재구성된 DMPC 막소포의 동결―파열 전
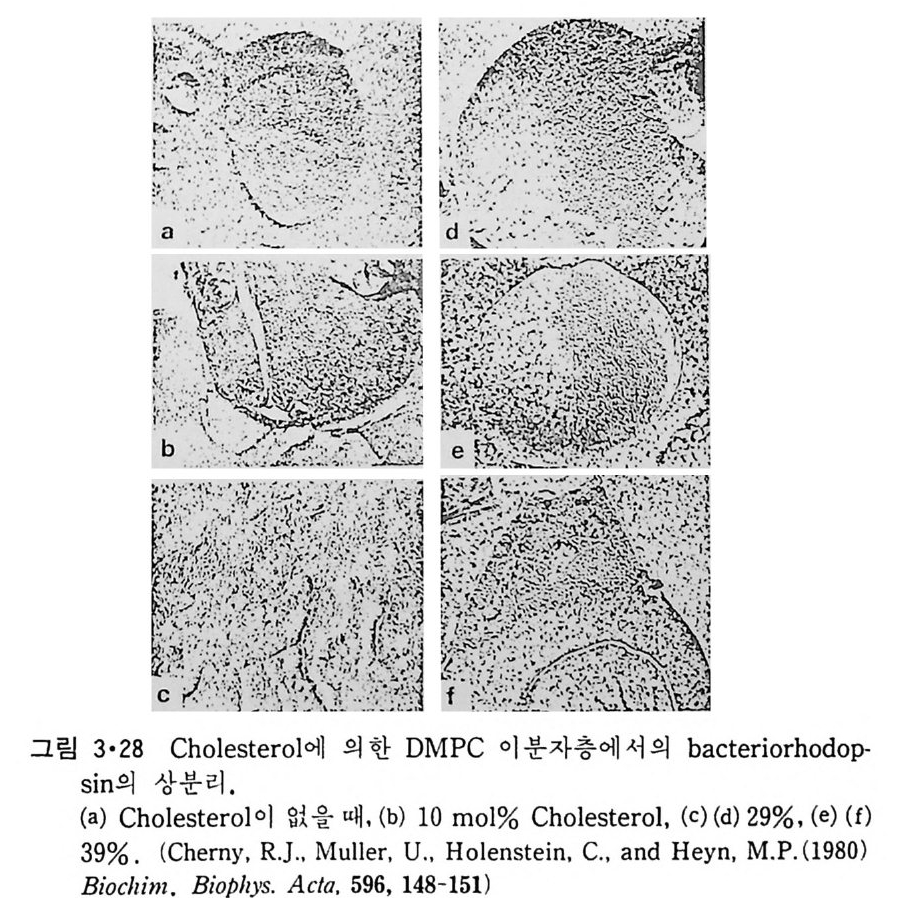 그림 3•28 Choles t erol 에 의한 DMPC 이분자층에서의 bacte r io r hodop -
그림 3•28 Choles t erol 에 의한 DMPC 이분자층에서의 bacte r io r hodop -
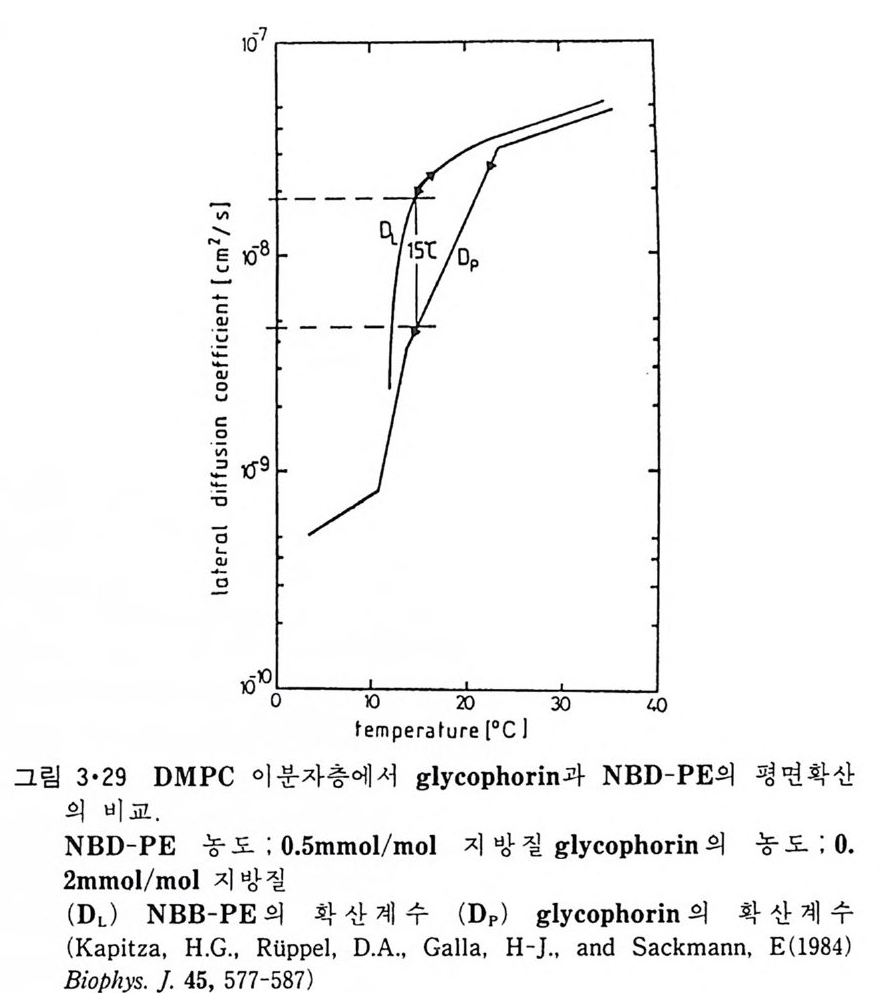
어 간 Ca2+-ATPase 의 황성도가 온도에 따라 변하는 것을 Arrhen i us 식으 로 표시한 것이다. 이 그링에서 두 개의 굴곡점이 있는데 42°C 에서 일어 나는 변화는 DPPC 의 상 전이 온도이고 30°C 에서 일어나는 변화는 둘레 지방질의 구조변화에 의한 것이다. 지방질의 상 전이시 ac y l 사슬의 유동성의 변화뿐만 아니라 이와 동시 에 일어나는 상 분리도 내재단백질의 구조와 기능에 영향을 마친다. 그림 3·27 은 DMPC 막에 재구성된 Ca2+-ATPase 가 이 지 방질 상 전이 온도 이하에서 상 분리로 따로 몰려 있는 것을 보여준다. 상 분리는 choles t er 이 존 재 하 에 서 도 일 어 나는 데 이 는 그 림 3 • 28 에 보 여 준 다. Choles t erol 의 농도가 높을수록 bac t er i orhodo p s i n 아 한쪽으로 모이는 것 을 볼 수 있다. 3·2·5 내재단백질의 이동속도 6) 전장에서 lip osome 내의 지방질은 상 전이 온도 이상에서 회전운동과 평면이동이 비교적 자유로운 것을 알았는데 여러가지 물리적인 방법으로 내재단백질의 운동도 현저하다는 것을 알게 되었다. Lip osome 에 재구성 된 단백질의 회전확산계수는 별로 측정되지 않았는데 bacte rio r hodop si n 의 경우에 얻어진 값은 ~8x1o•sec-1(~3o·c) 로서 인산지방질의 값 ~1 Xl010sec-1 보다 훨씬 작은 것을 알 수 있다. 단백질의 평면확산계수는 지방질의 값과 유사한데 Tm 보다 높은 온도에서 내재단백질의 평면확산계 수는 l0- 8 ~5x10-8cm2/sec 범위에 있어 비교적 균일하고 Tm 이하의 온도 에서는 거의 이동이 없는 것을 그림 3·29 에서 볼 수 있다. 생리온도에서 내재단백질의 확산이 대단히 빠른 것은 생체막 단백질들의 기능에 대단 히 중요하다. 3·2·6 지방질 이분자충에서의 내재단백질의 구조 수용성 단백질이나 주변단백질들은 물과 am i no 산 기와의 상호작용에 의해서 그 구조가 지배되어 국성 am i no 산은 주로 표면에 노출되고 비국 성 am i no 산은 내부에 위치하게 된다. 그러나 내재단백질은 그의 일부가 소수성인 지방질 이분자층 내부에 위치하고 있어 이 부분의 구조는 소수 성의 환경에 의해 지배될 것이다. 내재단백질의 구조에 대한 연구가 제
 1 군
1 군
 그림 3•30 자색막 ( pur p le membrane) 에서의 ba ct er i orhodo p s i n 의 전자
그림 3•30 자색막 ( pur p le membrane) 에서의 ba ct er i orhodo p s i n 의 전자
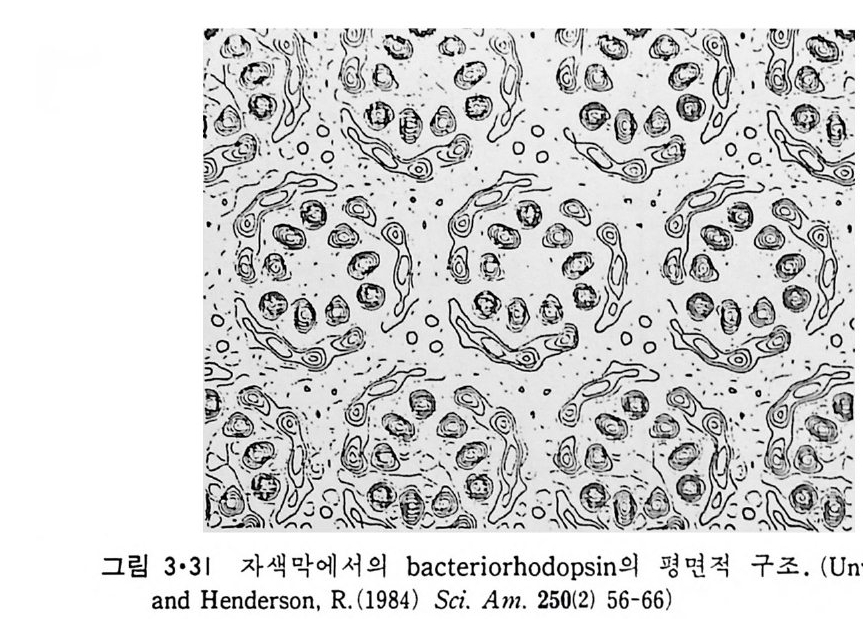 그림 3•31 자색막에서의 bac t er i orhodo p s i n 의 평면적 구조. (Un wi n, N .
그림 3•31 자색막에서의 bac t er i orhodo p s i n 의 평면적 구조. (Un wi n, N .
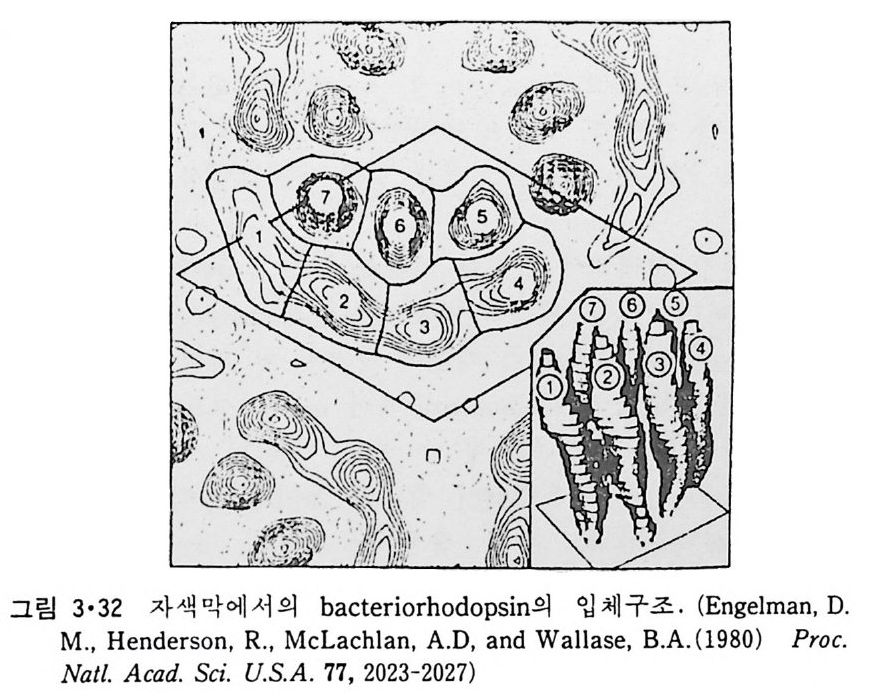
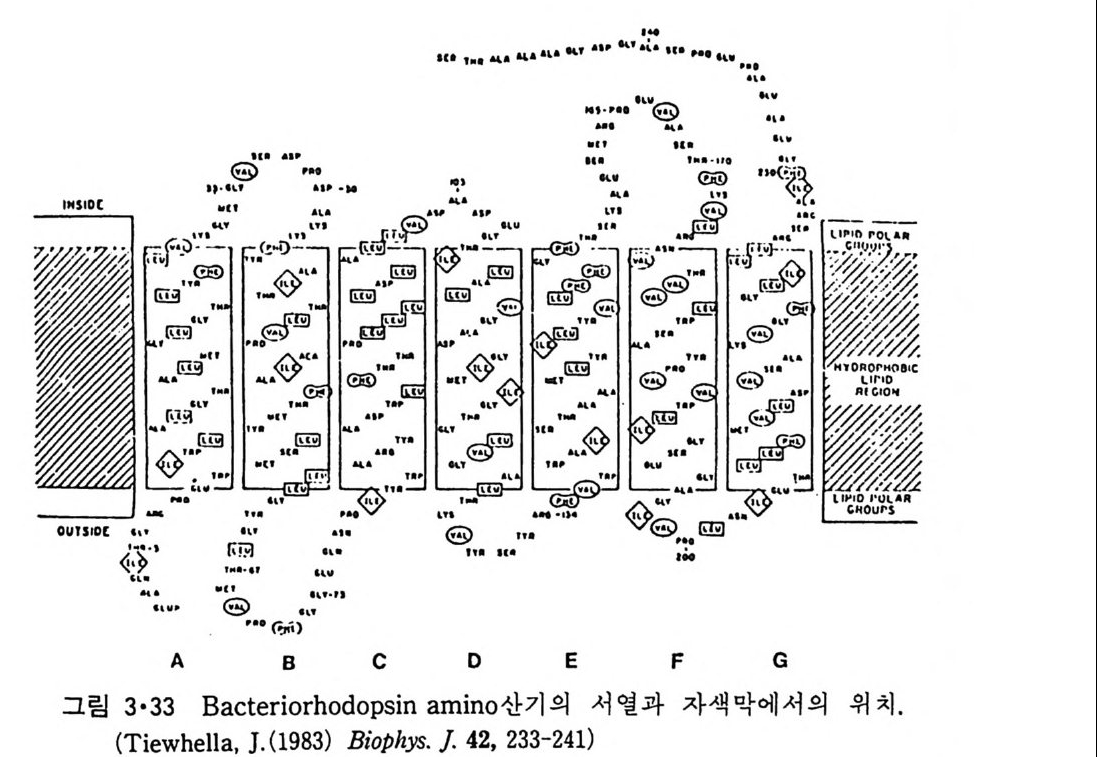
일 자세히 이루어진 것은 Halobacte n ·um Jia lob iu m 의 자색막에 있는 bac t er i orhodo p s i n 으로 이 것 이 내 재 단백 질 구조를 결 정 하는 원 리 의 바탕 울 이루게 되었다. 자색막은 bac t er i orhodo p s i n 만이 농축되어 일정하게 배열되어 있어 2 차원적 결정을 형성하는 것으로(그림 3·30) 전자회절로 그 구조를 결정할 수 있었다. 그림 3·31 은 그 이차원적 구조를 보여주는 데 이것은 막 평면에서 수직되는 방향으로 전자일도분포를 보이는 것이 다. 전자굴철 실험을 여러 각도로 하면 그링 3·32 에서 보이는 3 차원적인 구조도 얻을 수가 있다. 이들 결과에 의하면 ba ct er i orhodo p s i n 은 7 개의 a- 나사선이 자색막을 횡단하고 이들 a- 나사선은 짧은 p ol yp e pti de 로 연 결이 되어 있다. 그림 3·31 에서 3 개의 bac t er i orhodo p s i n 분자가 회합되어 하나의 원형의 단위를 형성하고 이 회합체 하나 주위에 6 개의 회합체가 둘러싸고 있는 것을 알 수 있다. 이 단백질의 am i no 산 서열도 결정이 되어 그림 3·33 과 갇이 자색막 내에서의 이 단백질의 위치가 제안되었으 나 아직도 잠정적이라고 생각되어야 한다. 자색막 내에서는 이 단백질이 비교적 구형에 가까운 모양을 갖는 것은 a- 나사선 부분의 양성 하전을 가진 am i no 기 와 음성 하전을 갖는 am i no 기 사이 에 i on 쌍이 형 성 되 어 안 정화되는 것으로 생각된다. 중성자 산란실험으로부터 국성인 am i no 산은 내부를 향하고 비극성인 am i no 기는 밖을 향하고 있는 것이 관찰되어 내 재 단백 질은 수용성 단백 질과 그 구조가 정 반대 여 서 ins id e -out 단백 질이
 。
。
 。IM SIDICO r•A•` -“.” ~Ot g.g“t 2· .$fmg” ”· ·I im5 I~~'.~5 @”i' I 戶已懿:“~ . 허기의f國i 函 ~ T,I I詞:: 잴:'\ f.鬪:口g
。IM SIDICO r•A•` -“.” ~Ot g.g“t 2· .$fmg” ”· ·I im5 I~~'.~5 @”i' I 戶已懿:“~ . 허기의f國i 函 ~ T,I I詞:: 잴:'\ f.鬪:口g
라고도 불리어진다. 이러 한 구 조는 다 론 내재 단 백 질 들 에게 노 보편적인 것 이라는 것이 차차 드러나고 있다. 즉 막 내 부 에 위치 하는 p ol yp e pti de 의 부분은 a- 나사선룰 이루고 이들 a- 나사선 들 이 i on 쌍으 로 결합 되 어 비교 적 구형에 가까운 밀집된 모양을 이루는 것 이 내재단백 질 구조 의 바탕이 된다. a- 나사선 구조가 막내에서 안정한 이유는 그림 3·34 에서 po lya lanin e 울 예로서 설명된다. 막을 횡단하는 a- 나사선의 p ol yp e pti de 의 길이는 약 20 개의 am i no 산기를 포함하기 때문에 여기서 이 길이만 을 고려한다. 수용액 내에서 불규칙 구조 (random co il ) 에서 a- 나사선으로 쉽 게 변하여 자유 ener gy차이는 0 에 가깝다고 볼 수 있다. 그러나 소수 성 a- a lanin e p ol yp e pti old 의 나사선이 수용액에서 막내로 들 어 갈 때의 ener gy변화는 약 _30kcal/mol 이 된다. 한편 불규칙구조형 이 수용액에서 는 그 p e p e ti de 결합의 극성기가 용매와 수소 결 합을 하여 안정하지만 막내에서 는 용매와 수소결합을 가질 수 없어 불안정하다. 그래서 막내에서 a- 나 구사조선적으 로인의 e nt수r o소 p y결 2합4k으c로a l / m안ol칭 을화 되가는해 주것어은 도약 —_7906 kkccaal/ lm/ mo oll 인정 데도 로여 기안서정 화가 된다. 이들 값에서 불규칙구조가 수용액에서 막내로 들어가기 위해 서는 40kca l/ mol 의 자유 ener gy가 필요한 것을 알 수 있다. 이상의 설명 으로서 a- 나사선 구조가 막내에서 안정할 뿐만 아니라 불규칙구조가 막 내로 들어가서 나사선이 되는 것보다 일단 a - 나사선이 형성되어 막으로 들어가는 것이 더 쉬운 것이 분명하다. 이렇게 a- 나사선구조가 막내에서
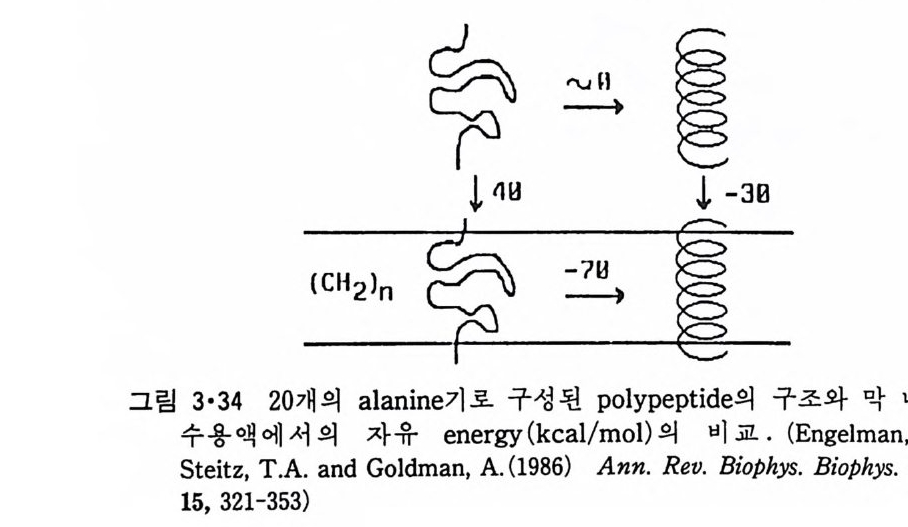 그림 3•34 20 개의 al二an i ne 기 로孛멸i卒 구성된~ IpI o )) l yp e pti 丈등들de 의 구조와 막 내부와
그림 3•34 20 개의 al二an i ne 기 로孛멸i卒 구성된~ IpI o )) l yp e pti 丈등들de 의 구조와 막 내부와
 Ho2r0 를틀G, __.〔 \G2 .广
Ho2r0 를틀G, __.〔 \G2 .广
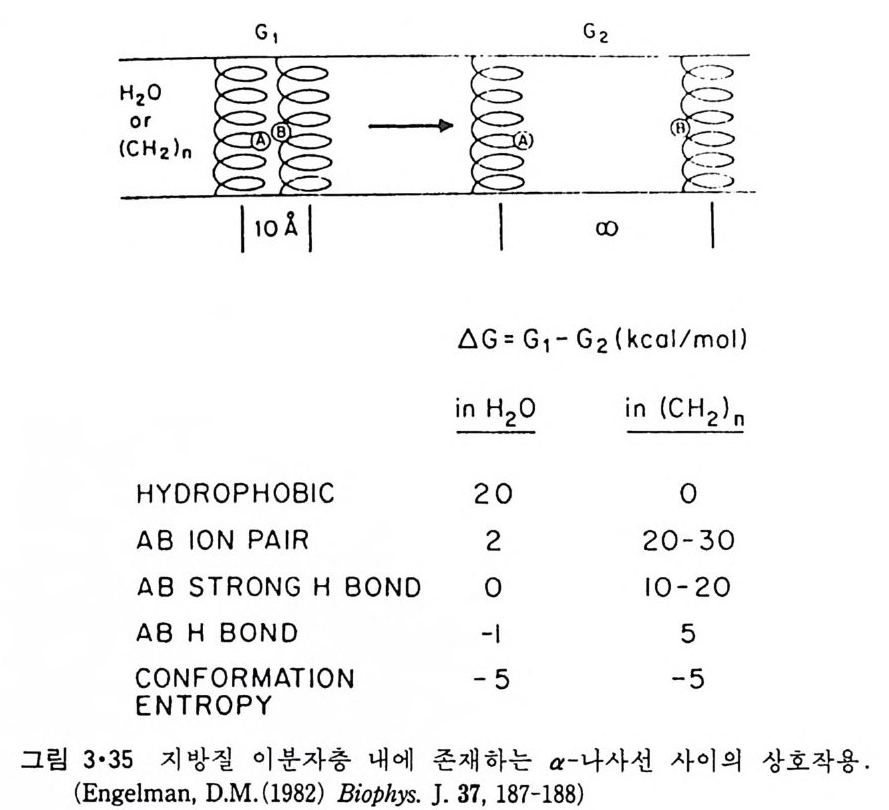
안칭한 근본적인 이유는 p e pti de 결합 자체의 수소결합이 가능해서인데 g-판상 (shee t)구조로 그 수소결합의 일부를 만족시킬 수는 있으나 전부를 만족시킬 수 없기 때문에 막내에 8- 판상 구조룽 갖는 가능성은 희박하 다. Bac t er i orhodo p s i n 과 같이 a- 나사선 p ol yp e pti de 가 여 러 번 막을 횡 단 하는 단백질이 비교적 구형인 구조를 형성하는 이유는 그림 3·35 에서 알 수가 있다. 비국성 환경에서 a- 나사선 사이의 i on 쌍이나 수소결합이 강 해서 i ns i de-ou t구조가 안정한 것을 이 그림이 보여준다. 3·2·7 Am i no 산의 배열과 막내에서의 위치 8) 많은 내 재 단백 질의 am i no 산 배 열 이 bac t er i orhodo p s in을 위 시 하여 차 차 결정됨에 따라 이로부터 p ol ypepti de 의 어느 부분이 막 내부에 들어 가 느냐를 예측하려는 노력이 계속되어 왔다. 이중 K yt e 와 Doo litt le 의 방법
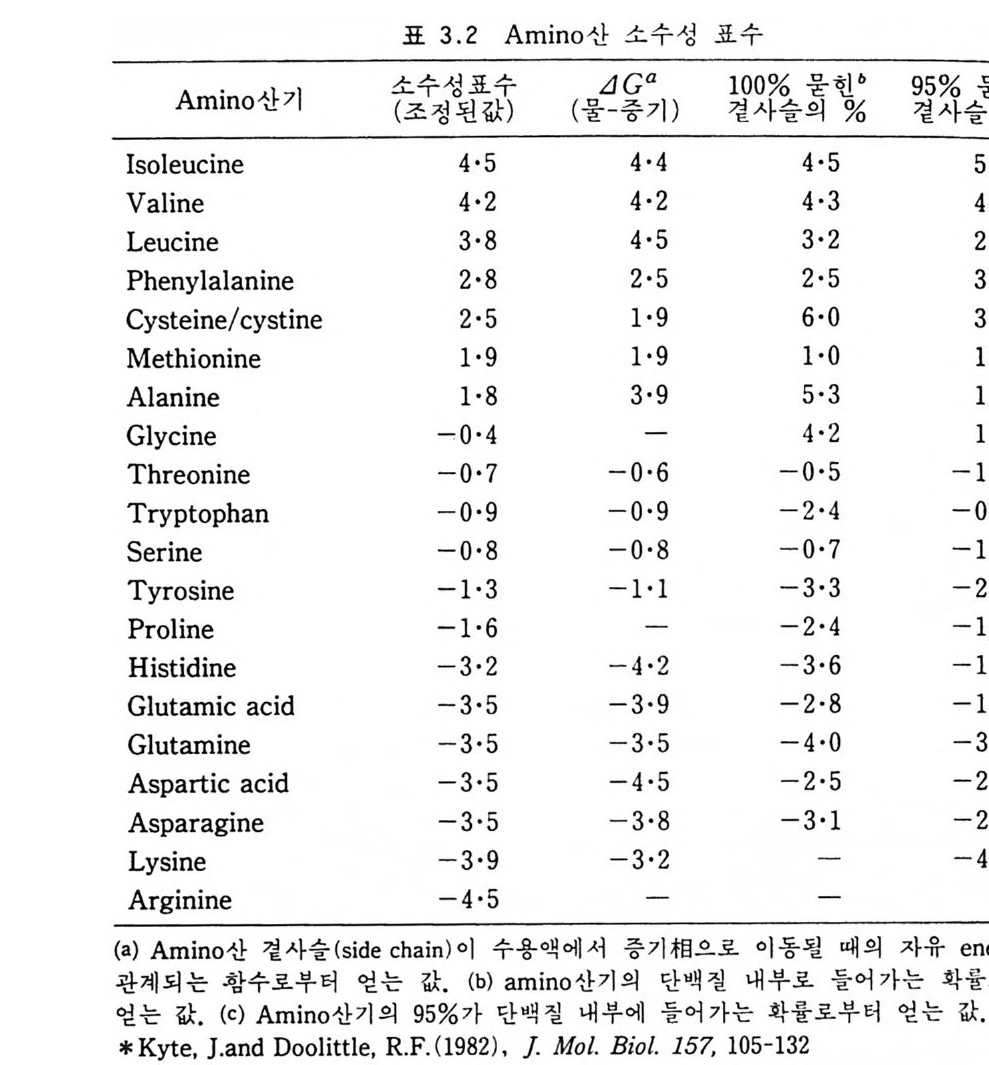 표 3.2 Am i no 산 소수성 표수
표 3.2 Am i no 산 소수성 표수
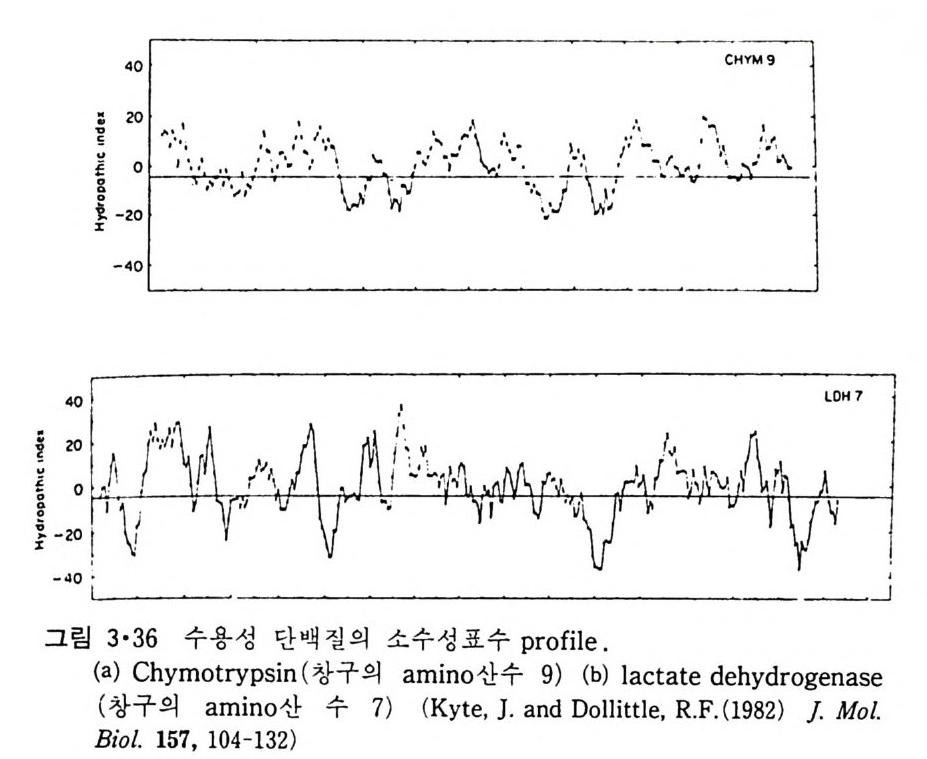
이 제일 많이 쓰이며 이들은 표 3·2 에서와 같이 각 am i no 산에서 소수성표수 (hy d rop h obic ind ex) 를 할당한 후 p ol yp e pti de 사슬의 한 말단에 서 시작하여 일 정 한 숫자에 인 접 한 am i no 산 창구 (wi nd ow) 의 소수성 표수를 평균해서 이 값을 중앙에 위치하고 있는 am i no 산으로 할당하는 것이다.소수성표수는 몇 가지 실험치를 참고로 하여 어느 정도 임의로 결정된 수이 다. 그림 3·36 을 chy mo tryp s i n 과 lacta te h ydro g enase 의 소수성표수p ro fil e 을 그린 것이다. 이 그림에서 0 의 윗부분은 단백질 내부에 존재하고 아랫부분은 표면에 위치한 것인데 이들은 독정한 경향을 보이지 않는
 40
40
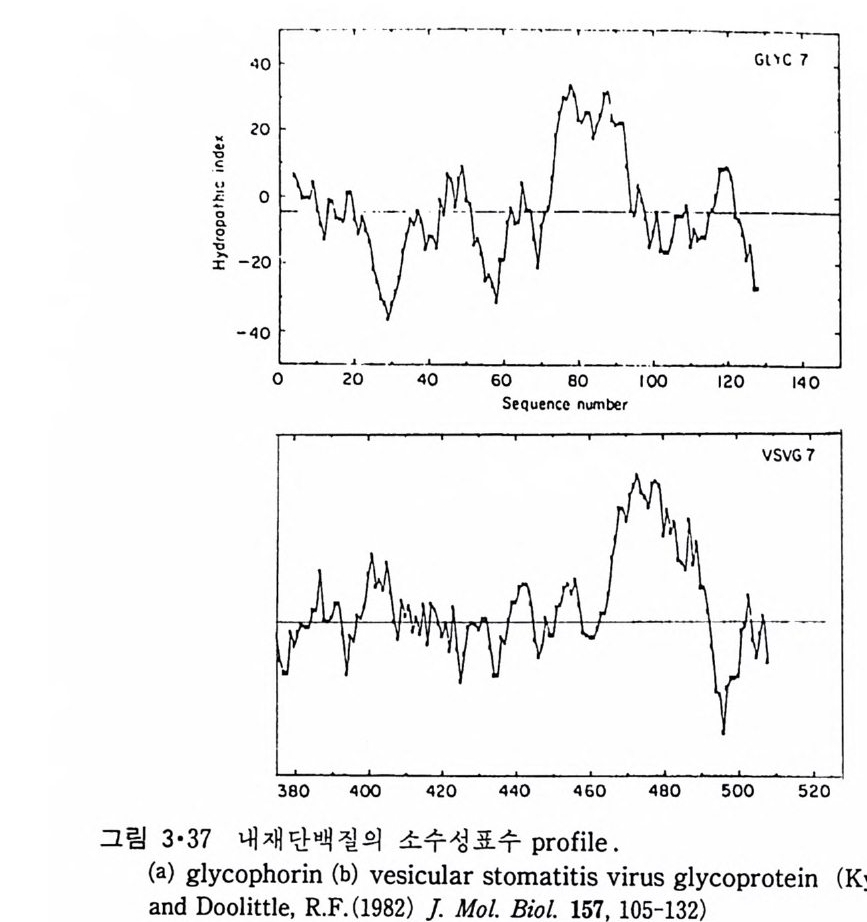
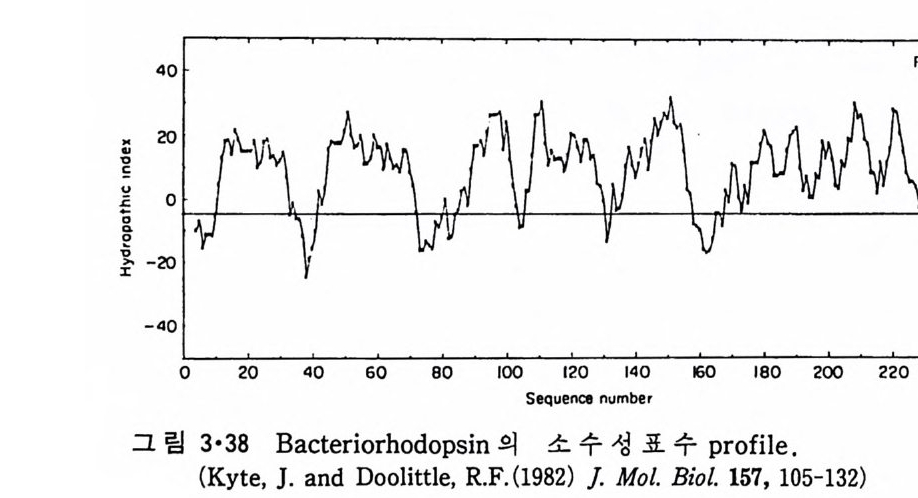
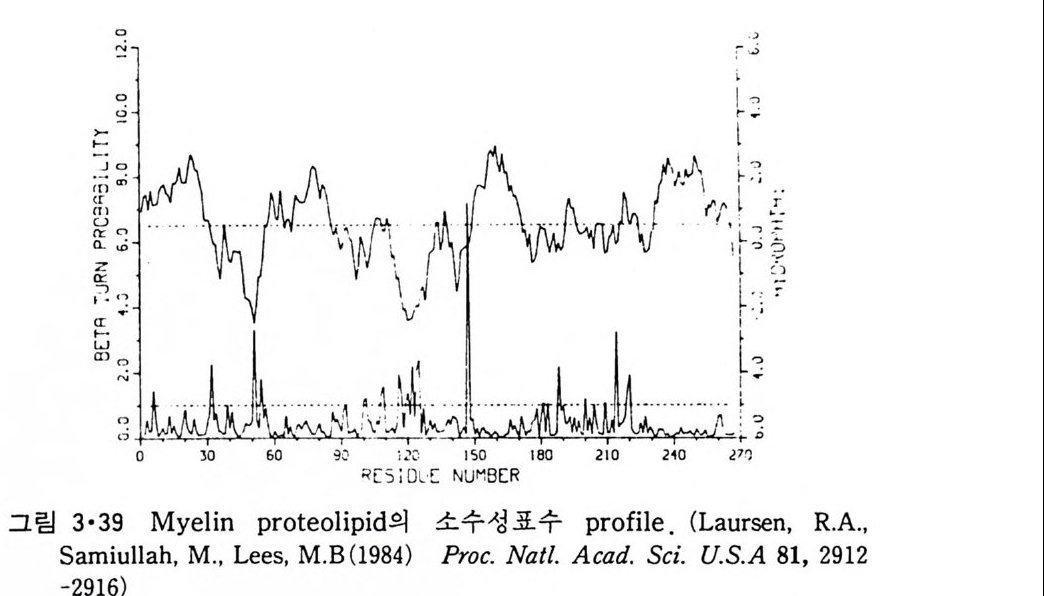
다. 한편 적혈구막 내재단백질인 g l y co p hor i n 인 경우 그림 3·37 에서와 같이 C- 말단 근처에 약 20 개의 연속된 부분의 소수성표수값이 큰데 이것 은 a- 나사선이 막을 횡단하는 길이이다. 그래서 g l y co p hor i n 은 막을 한 번만 통과하는 내재단백질이고 N- 말단의 큰 부분이 막 외부의 노출되어 있고 C- 말단의 작은 부분도 막 외부에 노출되어 있다. Vesic u lar sto mati tis v i rus 막의 단백질도 같은 식으로 많이 들어가는 것을 볼 수 있 다. Bac t er i orhodo p s i n 경우는 그림 3·38 에서 7 개의 p ol ypepti de 부분이 막 내부에 들어간 것을 볼 수 있다. 이는 다시 말해서 막을 7 번 횡단하는 것을 의미한다. 그림 3·39 는 소 두뇌의 my e li n p ro t eo lipi d 의 소수성표수 p ro fil e 로서 이로부터 그림 3·40 과 같은 막에서의 p ol yp e pti de 의 위 치를 얻었다. Pro t eo lipi d 는 생체막내에 많이 분포되어 있는 내재단백질로서 이의 특유 한 성질은 수용액의 형태로도 얻을 수 있는 것이다. 표 3·2 에 주어 진 소수성표수 이외에도 다른 표수들이 쓰였으나 근본적 으로 같은 결과를 얻었다.
 -·- - , • - - ·-一 , ,· - - 、-- ,-·- · -·- - `— — . , . --
-·- - , • - - ·-一 , ,· - - 、-- ,-·- · -·- - `— — . , . --
 40 RHOO 7
40 RHOO 7
 O.~
O.~
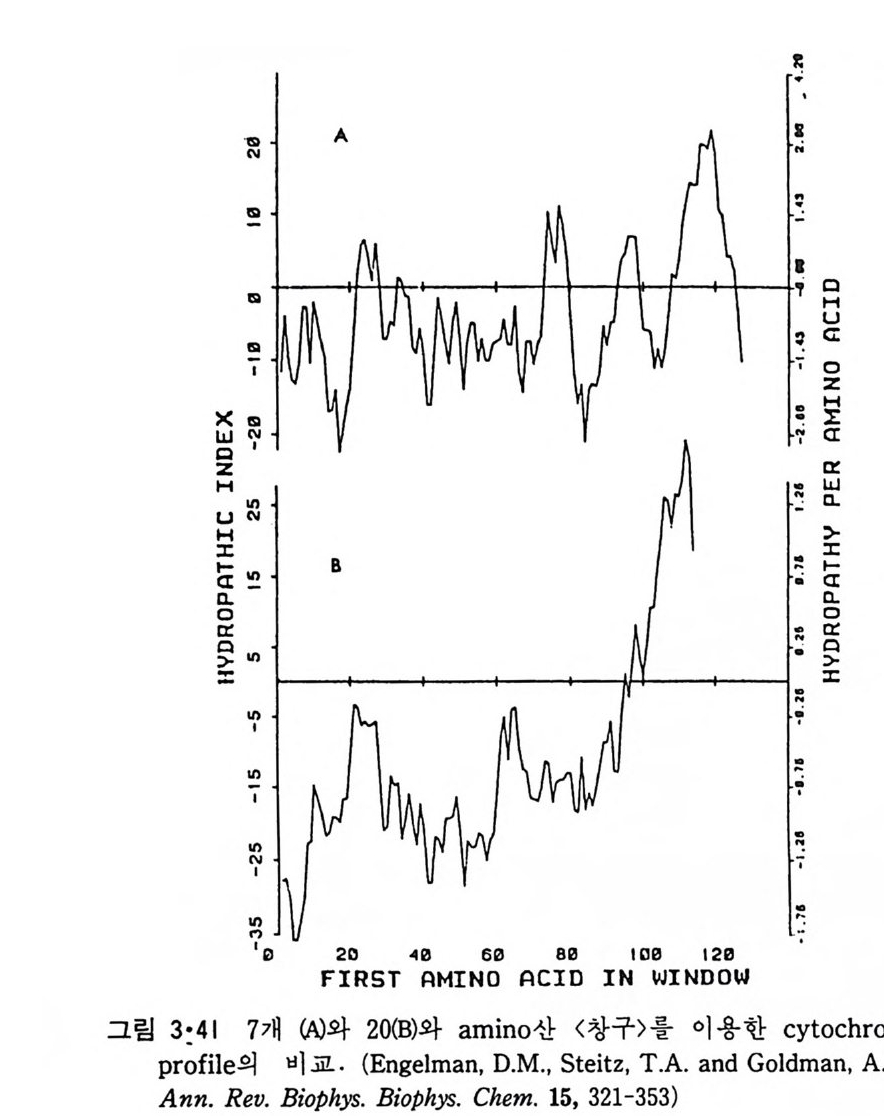
하나의 am i no 산기에 할당되는 평균소수성표수를 얻는데 있어 그 창구 내의 am i no 산 수는 5 에서 10 에 이르기까지 사용되었는데 이 창구에 소 수성 am i no 산만이 존재할 때에는 am i no 산이 몇개인가에 상관없지만 극 성 am i no 산이 많이 존재할 때에는 20 개 am i no 산을 이용하는 것이 적당
 MEXETMRBARCAENLEL ULAR SPACE —|F
MEXETMRBARCAENLEL ULAR SPACE —|F
 鬱,. `
鬱,. `
하다는 결론을 그림 3·41 을 통해 내 릴 수 있다. 창구에 7 개의 am i no 산 을 썼을 때에는 몇개의 pe ak 가 존재하지만 20 개를 쓸 때는 C- 말단에 하 나만 보이 는데 cy toc hrome bs 는 C- 말단뿐만이 막에 파묻혀 있는 것으로 보아 후자가 더 정확한 것을 알 수 있다. 막을 차단하는 am i no 산의 수 는 약 20 개이므로 창구에 20 개 이상을 고려하는 것도 무의미하다• 이 그 림에 보여준 cy toc hrome bs 의 p ro fil e 에서 약 20 개의 C- 말단 am i no 산의 소수성표수가 큰 것으로 보아 내재단백질은 C- 말단 부분이 막 내에 박혀 있고 나머지 부분이 막 외에 노출된 것을 알 수 있다.
* 3 장 참고문헌 (1) Gennis , R.B . and Jon as, A( 19 77) An. Rev. Bio p hy s . Bio e ng . 6, 195-238. (2) Ki m , J. and Ki m , H. (19 86) Bio c hemi stry 25, 7867-7874. (3) Ki m , J. a nd Ki m , H. (19 88) Bio c hemi stry 27, (4) Houslay, M.D. and Sta n ley, K.K. Dynam i cs of Bi ol og ica l Membranes, W iley , 1982. Chap t. 33. (5) Ey tan , G.D. (19 82) Bio c him . Bio p h y s . Acta . 694. 185-202. (6) Cherr y, R.J. (19 79) Bi oc him . Bi op h y s. Acta . 559, 289-327. (7) Unwi n, N. and Hendersen, R. (19 84) Sc i. A m. 250(2) 56-66. (8) Eng e lman, D.M., Ste i t z, T. A. and Goldman, A. (1986) Ann. Rev. Bio ph ys , Bio ph ys . Chem. 15, 321-353.
제 4 장 생체막의 구조 인산지방질을 물에 넣으면 이분자층 막이 자발적으로 형성되고 또 내 재단백질을 추출 정제하여 이분자층 막에 재구성시키면 그의 원래의 기 능을 계속 유지하는 것으로 보아 이들이 생체막의 model s y s t em 으로 이 용할 수가 있는 것을 알게 되었다. 그러나 생체막에서는 보통 100 종류 이상의 단백질들이 있으며 이와 비슷한 종류의 지방질이 존재하여 이들 간의 복잡한 상호작용이 생체막의 구조와 성질에 영향을 미칠 것아다. 또, 생체막은 세포 내의 여러 효소 득히 막의 성분을 합성하는 효소의 작용과 세포골격 (c yt oskele t on) 등 다른 성분과의 상호작용과 세포 외부의 여 러 성 분들의 영 향에 의 해 상당히 동적 (dy n ami c) 인 구조를 갖는다. 4·1 지방질 이분자층 생체막의 무게의 평균 50% 가 단백질이기 때문에 이들이 지방질 이분 자층에 과연 어떠한 영향을 주느냐가 문제인데 생체막도 이분자층으로 구성되어 있다는 것은 전자현미경으로 볼 수 있는 3 경 (t r il amellar) 구조로 추측이 된다. 이보다 앞서 Gor t or 와 Grendel') 은 물과 공기 경계면에서의 단충 (monola y er) 실험결과로부터 생체막이 지방질의 이분자층으로 구성된
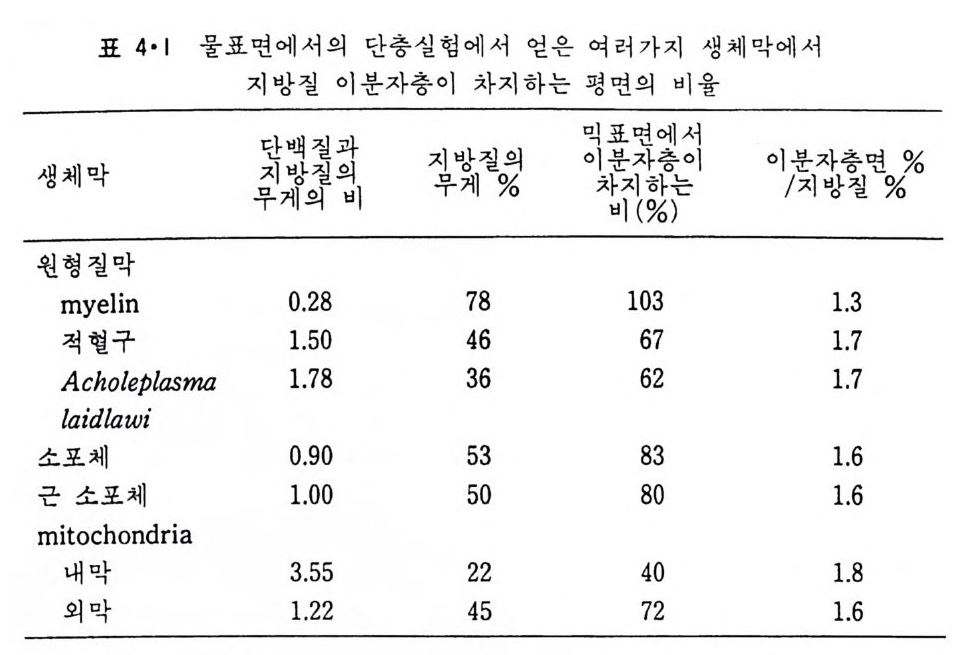 표 4•I 뭉표면에서의 단충실험에서 얻은 여러가지 생체막에서
표 4•I 뭉표면에서의 단충실험에서 얻은 여러가지 생체막에서
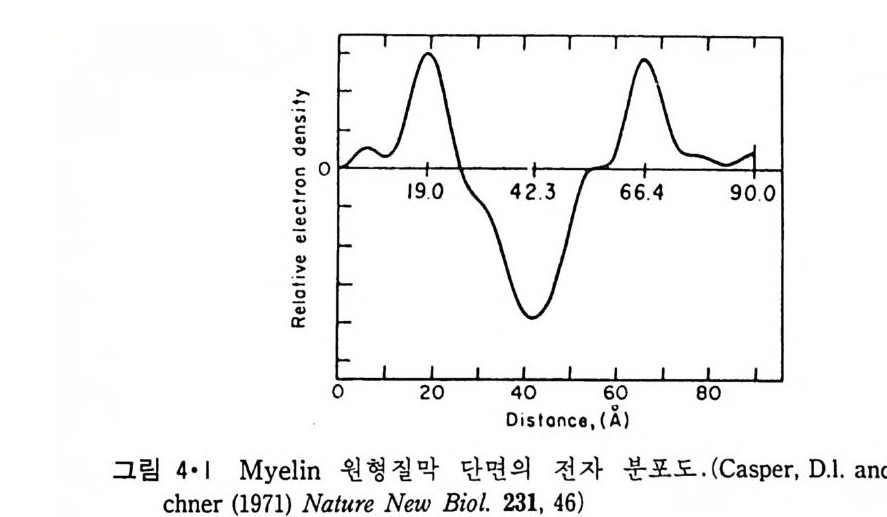
다는 것을 제안하였다. 이들은 적혈구의 지방질을 ace t one 으로 추출하여물 표면에 지방질 단층을 형성하여 그 표면적이 적혈구 표면적의 2 배가되는 것을 관찰하였다. 이 실험이 오늘날의 지방질 이분자층설(lipi d bil a y e r th eor y)을 시작한 공헌은 있으나, 그 실험 자체는 정확하지 못했다. 그후에 다시 정일하게 측정한 결과에 의하면 적혈구 표면의 약 70%만이 이분자층으로서 존재할 수 있다는 것을 알게 되었다. 표 4·1 은 여 러가지 생체막의 지방질 함량과 단층면적에서 얻은 이분자층이 차지할수 있는 면적의 바율을 준다. 이들 두 양이 대체로 비례하는 것을 알 수있다. 만일 단백질이 차지하는 생체막의 표면이 그 무게에 비례한다고가정하면(이분자층면 %/지방질 %)가 일정한 값을 가져야 될 것이다. 생체막이 이분자층을 갖느냐 하는 문제는 인산지방질만이 존재할 때와같이 X- 선 회절방법으로도 결정할 수 있으나 생체막이 일정한 방향으로배열된 것이 별로 없기 때문에 rn y e li n 과 망막원주 (re ti nal rod) 에서만 이 것이 얻어졌다. 그림 4·1 은 rn y e li n 의 X- 선 회철실험에 의해 얻어진 그원형질막 단면의 전자분포를 본 것이다. 그림 2•19 에서의 choles t erol 을함유하고 있는 인산지방질 이분자층의 전자분포와 유사한데 이것은rny e li n 원형질막 지방질의 약 29% 가 choles t erol 이기 때문이다. 그러나, 이 그림에서 이분자층의 탄화수소의 전자밀도 분포가 상당히 비대칭성을
 i1 1suap
i1 1suap
보여주는데 그 원인은 my el i n 내에서 choles t erol 의 분포가 비대칭으로 되어 있는 데 있다. 이 생체막에는 내재단백질이 상당히 작게 존재하기 때문에 전형적인 생체막이라고는 할 수 없다. 보다 전형적인 생체막인 망막원주 (re ti nal rod) 의 X- 선 회절결과는 그림 4·2 에서 보여준다. 이 생 체막에서는 단백질의 함량이 50% 정도가 되는데 이 그림은 choleste r ol 이 없는 순수한 지방질 이분자층의 전자밀도 분포와 유사하다. 이상의 예로서 생체막에서도 지방질의 이분자층이 구조의 바탕이 된다는 것을
 -0---0 Unl.J l eached
-0---0 Unl.J l eached
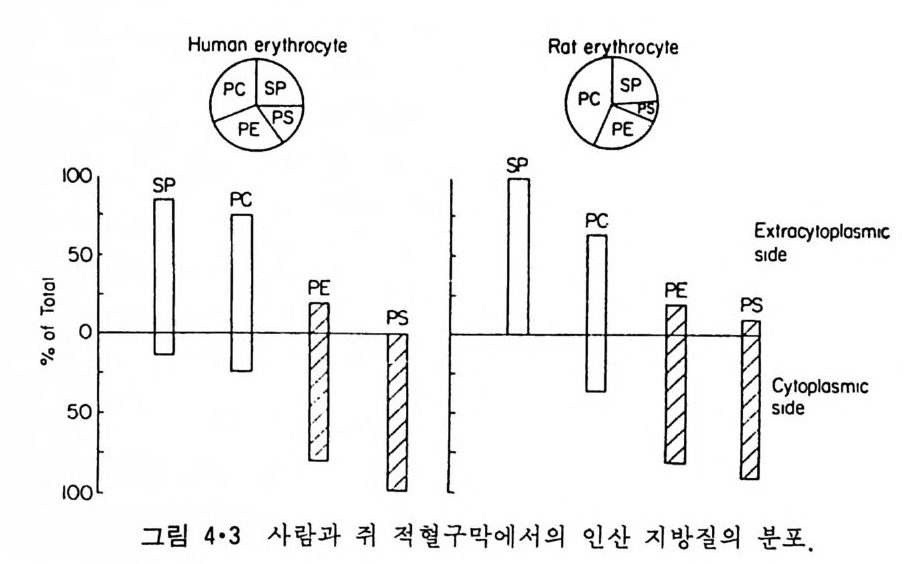
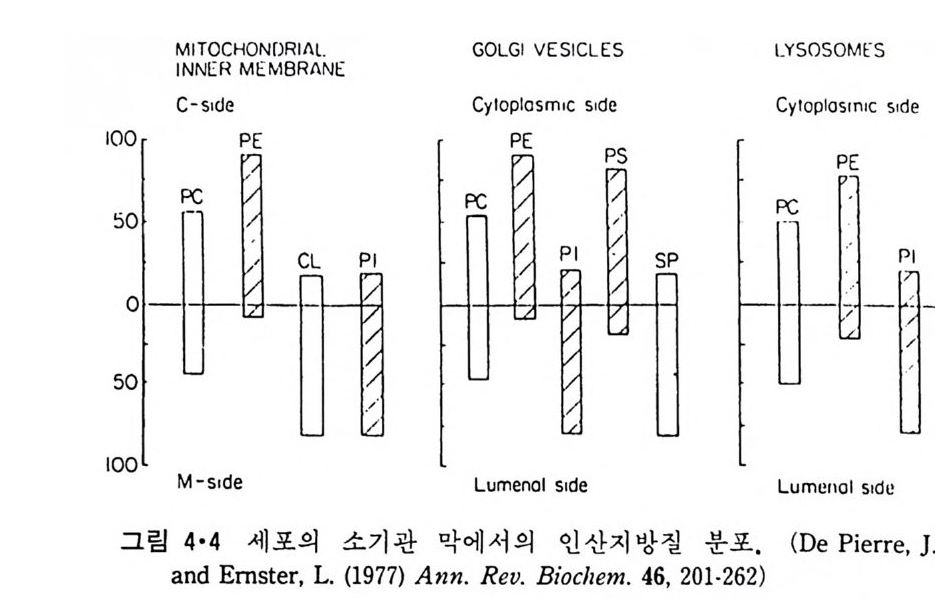
알 수 있다. 4·2 생체막 성분의 비대칭적 분포 2)-5) 생체막에서 이분자층을 구성하는 두개의 단층의 지방질 구성온 서로 다르다. 즉 모든 지방질이 양쪽 단층에 존재하나 그 상대적인 농도가 다 르다. 이와 반대로 단백질과 당분의 비대칭적인 분포는 절대적이다. 당 분은 한쪽 표면에만 존재하고 단백질은 크기 때문에 많은 경우에 양쪽 단충에 걷쳐 있으나, 한쪽 방향으로만 배열되어 있다. 4·2·1 지방질 그림 4·3 은 적혈구 막에서의 비대칭적인 지방질의 분포를 보여주고, 그림 4·4 는 세포내부 소기관막의 지방질 분포가 비대칭적이라는 것을 보 여준다. 이들 분포에 어느 특별한 경향을 보이지는 않으나, 세포질 쪽에 PE 와 PS 가 집중되어 있는 것을 볼 수 있다. 지방질의 분포를 결정하는 실험방법 중에서 제일 많이 쓰이는 것은 TNBS( tr i n i t ro benzenesulfo n ic aci d) 같은 막을 투과하지 않는 표지 화합물 (lab el) 을 이 용하는데 TNBS 는
 H흡uman eryt hr oc y te R출ot er:rl !lro cyt e
H흡uman eryt hr oc y te R출ot er:rl !lro cyt e
 MITOCHO N DRl/ll . GOLGI VESICLES LYSOSOMf S
MITOCHO N DRl/ll . GOLGI VESICLES LYSOSOMf S
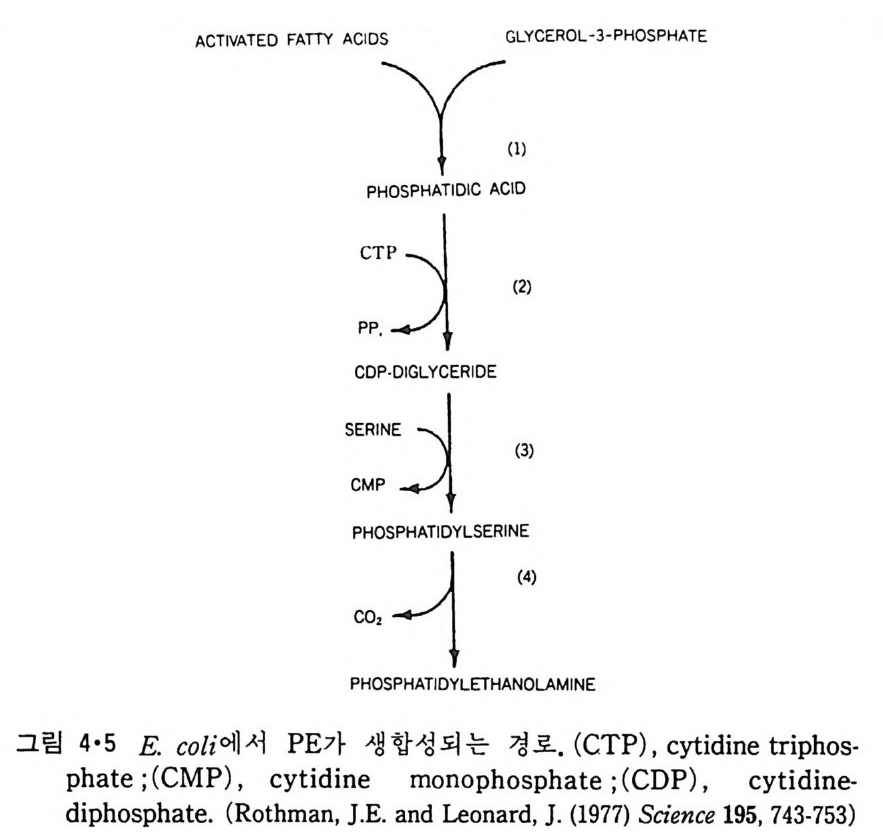
일차 am i ne 기와 결합하기 때문에 외부에 노출된 PE 와 PS 를 표지할 수가 있다. 그래서, 세포나 소기관을 TNBS 로 처리한 후 인산지방질을 유기 용매로 추출하면 생체막에서 외부를 향한 단층에 존재하는 PS 는 TNBS 와 결합되기 때문에 내부에서 영향을 받지 않는 PS 와 박충(t h i n-la y er) chroma t o gr a ph y (TLC) 에서 구분이 되어 이분자층 양면에서의 PS 의 상대 적인 양을 알 수가 있다. 또다른 방법들은 외부에 존재하는 인산지방질 은 phos pho lip ase 로 처리하면 가수분해가 되기 때문에 내부것과 구별이 되며 한편, 인산지방질 교환 단백질을 이용해 외부지방질만을 방사선 지 방질로 교체해서 내부와 외부성분들을 식별할 수도 있다. 지방질이 바대칭적으로 분포되는 원인은 두 가지로 볼 수 있다. 첫째 는 이들 성분의 생합성이 세포질에서만 이루어져서 기존의 소포체막에 삽입이 되고, 둘째로는 막을 횡단하는 이동속도가 대단히 느리기 때문이 다. 인산지방질의 합성이 세포액 쪽에서 이루어진다는 것은 Escheri ch ia col i에서 확립이 되었다. 그림 4·5 는 이 세균에서의 PE 의 생합성 반응을 보이는데 이 과정의 중간생성물이나 효소들이 모두 세포액에 존재하는 것을 관찰하였다. 이 반응에서 PS 합성과정까지는 수용성효소에 의해서 이루어지고 단계 (4) 는 원형질막의 내부표면에서 이루어진다. PE 의 생합 성과 그분포에 대해서 상세히 연구가 된 것은 Baci llu s meg a t e ri um 으로 서 이 세균의 원형질막의 조성은 단순하여 지방질 전체의 70% 가 PE 이
 ACTIVA TED FATTY ACI DS GLYCEROL·3-PHOSPHATE
ACTIVA TED FATTY ACI DS GLYCEROL·3-PHOSPHATE
고 나머지는 PG 로 구성된다. TNBS 표지 방법으로 PE 의 33% 는 원형질 막 외부표면에 존재하고 나머지는 원형질막 내부표면에 존재하는 것을 알았다. 다음 이 세 균을 “P- p hos p ha t e 로 1 분간 단속표지 (pu lse-label) 한 후 위의 방법으로 그 분포를 결정하면 밖에 있는 PE 가 32 p로 표지되지 않는 것으로 이 인산지방질의 합성이 세포액 쪽에서 이루어지는 것을 알 수 있다. 이렇게 단속표지한 후 NH20H 로 PE 의 합성을 중지시키고 세 균을 방사선이 없는 배지 (med i a) 에서 배양(i ncuba t e) 을 하니 새로 합성된 PE 는 반생기 (ha lf-tim e) 가 5 분이 되는 속도로 막을 횡단한것을 관찰하였 다. Lip osome 이나 생체막에서 지방질이 막을 횡당하는 속도는 극히 느 리기 때문에 이렇게 새로 합성된 인산지방질이 빨리 횡단하는 mechan i sm 은 아칙도 찰 이해가 안되나, 이는 번식하는 세균 등에서는 지방질이 막을 빨리 횡단시킬 수 있는 성분이 존재하고 있다고 생각되고 있다. 또, 생체막이 일정한 인산지방질의 분포를 갖는 것은 이러한 초기 횡단속도와 합성속도의 비에서 결정된다고 생각되고 있다.
4·2·2 단백질 6)- 7 ) 생체막 단백질의 분포는 적혈구에서 제일 자세하게 연구가 되어왔다. 그 이유는 포유동물 적혈구에는 원형질막만이 존재하여 다른 종류의 막 을 제거해야 될 과정이 필요없기 때문이다. 또, 용액의 삼두 몰농도 (osmolar ity)를 서서히 감소시킴으로써 적혈구를 부풀게 하여 hemog lo - b i n 이 새 어 나온 후 .::z. 막을 통하여 큰 분자들이 자유롭게 통과되 는 상태 로 유지되거나, 다시 새지않는 상태로 원상복귀시킬 수가 있다. 적혈구 막을 작은 막소포로 쪼갤 수도 있고 이때에 막의 세포액 쪽 표면이 원래 대 로 안으로 향하게 할 수도 있고 또 밖을 향하여 뒤 집 혀 진 (ins id e out) 막소포로 만들 수도 있다. 그래서 적혈구 막의 양면을 별도로 표지 등으 로 처리하거나, 동시에 처리할 수도 있다. 단백질의 막에서의 방향성을 결칭하는 방법은 표지하는 것과 단백질 가수분해 효소로서 pe p tide 결합을 끊는 것이다. 표지하는 데는 TNBS 와 같이 일차 am i ne 기와 결합하는 것이 있고, lacto p e roxid a se 존재하에 서 막단백질의 tyr os i ne 기를 요드화(i od i na ti on) 하는 것이 있다. 생체막의 막세 포를 단백 질 가수분해 효소 (pro te a se 혹은 pro te o lyt ic enzym e) 로 처 리 한 후 단백질의 peptide 결합이 끊어졌는가의 여부는 SDS-PAGE 로 알 수 있고 또, 효소인 경우에는 효소기능의 상실여부로 알 수 있다. 단백 질 가수분해 효소들은 그 기질 (subs t ra t e) 의 특이성이 각각 다르기 때문에 막 외부로 노출된 p e pti de 결합을 끊기 위해서는 여러가지 효소가 이용되 어야 한다. 적혈구 막의 단백질들은 SDS-PAGE 전기영동에서 이동되는 순서로 식 별이 되었다(그림 1·41). 이 방법으로는 PAS 에 의해 염색되는 4 개의 band 가 보이고, 10 여개의 Coomassie blue 에 의해 염색되는 band 가 존재 한다. 이들 이외에 약 20 개의 희미한 band 도 보인다. 이들 모든 band 들 은 적혈구막 내외로 가해진 작용제에 의해 표지되거나, 변형되므로 막내 에 완전히 파묻혀 있는 내재단백질은 존재하지 않는 것 갇다. 1, 2, 4.1 , 4.2, 5 와 6 band 둘은 주변 단백질로서 적혈구 막단백질의 약 40% 를 차지 하며 전부 세포질 쪽에 위치하고 있다. 다른세포에서도 주변 단백질은 대부분 세포질 쪽 막 표면에 부착되고 있는 것이 관찰되었다. Band 3 와 PAS-1 들이 적혈구막 단백질 중에서 제일 많이 존재하는 내
 Corbohy dr ole` ..
Corbohy dr ole` ..
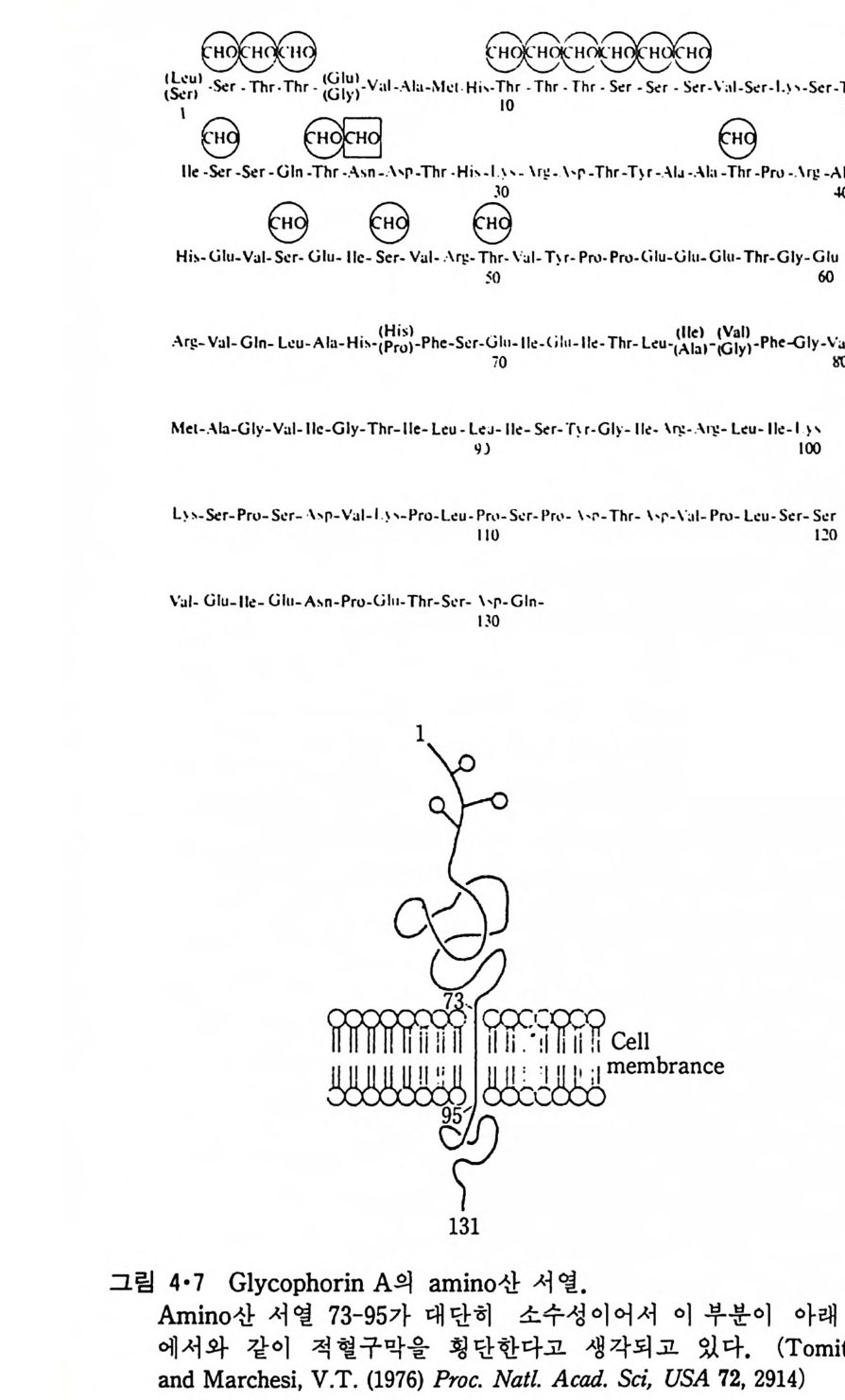
재 단백 질 이 다. Band 3 은 당단백 질 (gl y c o p ro te i n ) 로 탄수화물의 함량이 5 ~8% 가 된다. 이 단백질은 분자량이 93kDa 이 되고 방사선동위원소로 표지되는 것과 단백질가수분해효소에 의해 쪼개지는 것이 적혈구막 양쪽 에서 이루어진다. 그러니 band 3 은 막을 횡단하는 내재단백질이어서 그 p ol yp e pti de 사슬이 막 양표면에 노출된 것을 알 수 있다. 단백질 가수분 해에 의해 찰라지는 지점이 적혈구막 어느 쪽에 효소가 있느냐에 따라 다르기 때문에 이 내재단백질이 비대칭적으로 막을 횡단한다는 것을 알 수 있다. 동결파열 전자현미경 방법에 의하면 IMP 가 세포액쪽에 보이는 것으로 부터 이 내재단백질의 대부분이 세포질면에 가까이 있다는 것을 알 수 있다(그림 4.6). 적혈구를 p ronase 로 처리하면 탄수화물 전부가 떨어져 나오는데 이것은 탄수화물이 외부에 노출된 po lyp eptide 부분에만 결합되고 있다는 것을 의미한다. 이 실험결과로부터 이 내재단백질이 예 외없이 한쪽방향으로 배열된 것도 알 수 있다. 적혈구를 탄수화물만 표 지시키는 작용제로 처리하면 모든 band 3 단백질이 변형되는 것으로도 이 내재단백질의 분포가 절대적아라는 것을 보여준다. PAS-1 은 gly c op h orin A 라고도 불리우며 이 내재단백질 무게의 60% 가 o lig osacchar i de 이다. 이 단백질의 am i no 산 서열을 그림 4 . 7 에 보이는데 am i no 산 73 번부터 95 번까지는 현저한 소수성을 띠우고 있어 이 부분이
 臨H`IIi~c , -8 S(·.CSjlc u『r - -. VST ea hrl e- •rSG·TcIhrn-re .
臨H`IIi~c , -8 S(·.CSjlc u『r - -. VST ea hrl e- •rSG·TcIhrn-re .
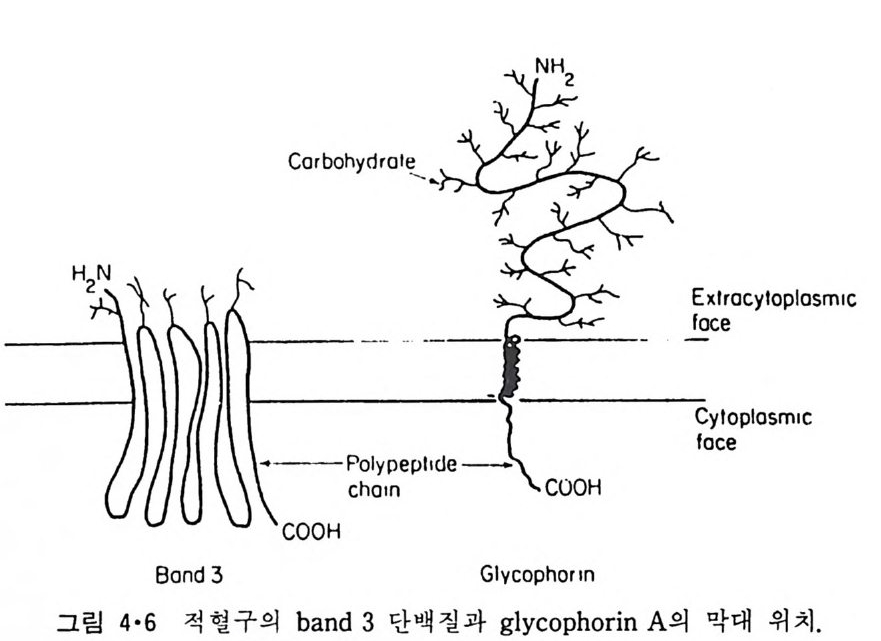
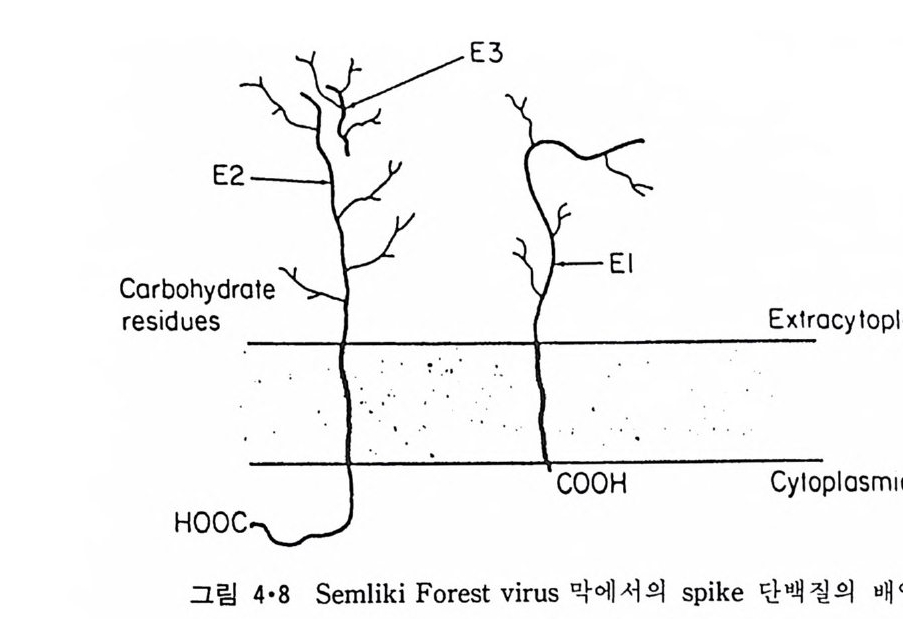
막을 통과한다고 생각되고 있다(그림 4.6). 그럼 3.37 의 소수성표수 pro fil e 도 이 단백질이 막을 한번만 통과하는 것을 보여 주었다. PAS-1은 PAS-2 의 이 합체 라고 생 각된 다. Band 3 때와 마찬가지로 gly c o p h orin A 도 결합된 탄수화물이 예외없 이 세포밖울 향하고 있다. 이 단백질 p ol yp e pti de 사슬의 55% 가 외부를향하고 있고 15% 는 막을 횡단하는 나사선부분, 그리고 세포질 쪽에는30% 의 단백 질 이 존재 한다. PAS-3 단백질도 당단백질(g l yco p ro t e i n) 이고 분자량이 약 25kDa 이 된 다. 이 단백질은 PAS-1 보다 쉽게 막으로부터 추출할 수 있어 소수성인C- 말단 부분만이 원형질 막에 박혀 있는 것으로 생각된다. 적혈구 이외의 원형질막은 순수한 형태로 얻기가 힘들어 막단백질의 위치가 그리 많이 알려져 있지는 않으나, 방향이 결정된 것들은 모두 예 외없이 절대 비대칭분포를 가지고 있다. 이러한 비대칭적인 분포는 다른생체막에서도 볼수 있는데 표 4·2 는소포체막의 단백질의 위치 그리고, 그림 4·8 은 Seml iki Forest v i rus 막의 단백질들의 막 내 위치를 보여준다. 이 모든 막내 단백질의 막 내에서의 배열에서 N- 말단과 C- 말단의 위치는아무런 균일성을 찾아볼 수 없다. 죽, N- 과 C- 말단이 같은 쪽에 있을수도 있고 서로 반대편에 있을 수도 있으며 N- 말단과 C- 말단이 세포액 쪽에 있을 수도 있고, 반대쪽에 있을 수도 있다. 주변단백질은 주로 세포질면에 존재한다고 했는데 이들의 일부는 세포골격의 성분이라는 것을 알게 되었다. 그림 4·9 는 적혈구의 내재단백질과 주변단백질과의 관계를 보여주는데 이러한 단백질의 조직으로 적혈구의 모양이 결정된다.
 표 4•2 소포체의 존재하는 효소의 acti ve s it e 의 방향
표 4•2 소포체의 존재하는 효소의 acti ve s it e 의 방향
 E3
E3
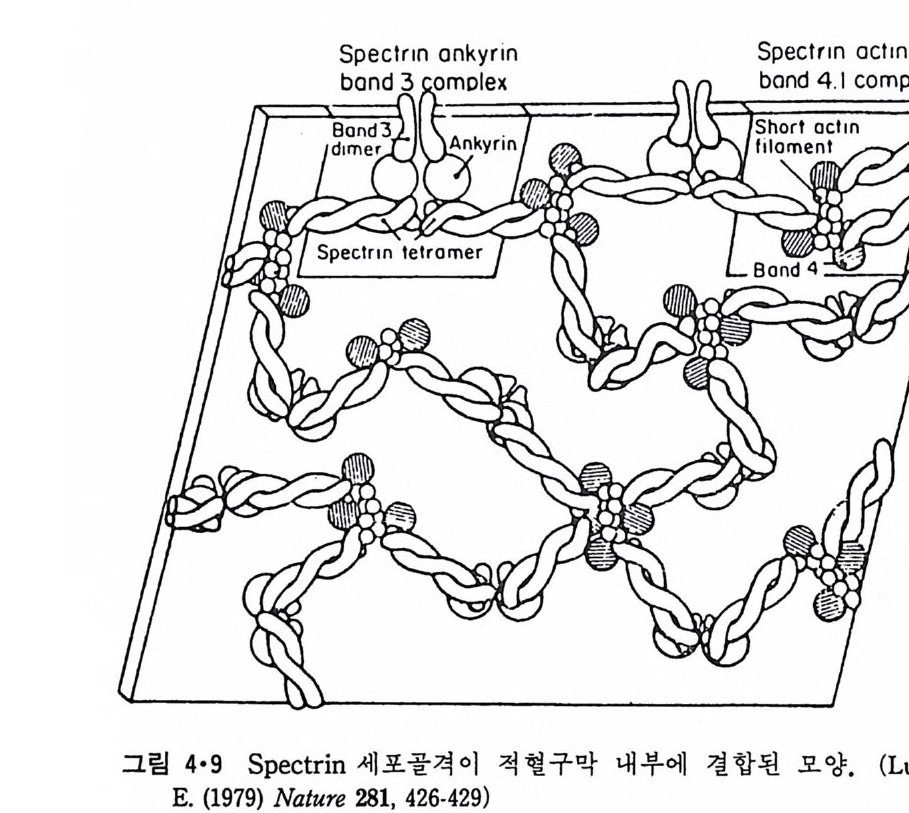 그림 4•9 Sp e ctr i n 세포골격 이 적 혈구막 내부에 결합된 모양. (Lux, S.
그림 4•9 Sp e ctr i n 세포골격 이 적 혈구막 내부에 결합된 모양. (Lux, S.
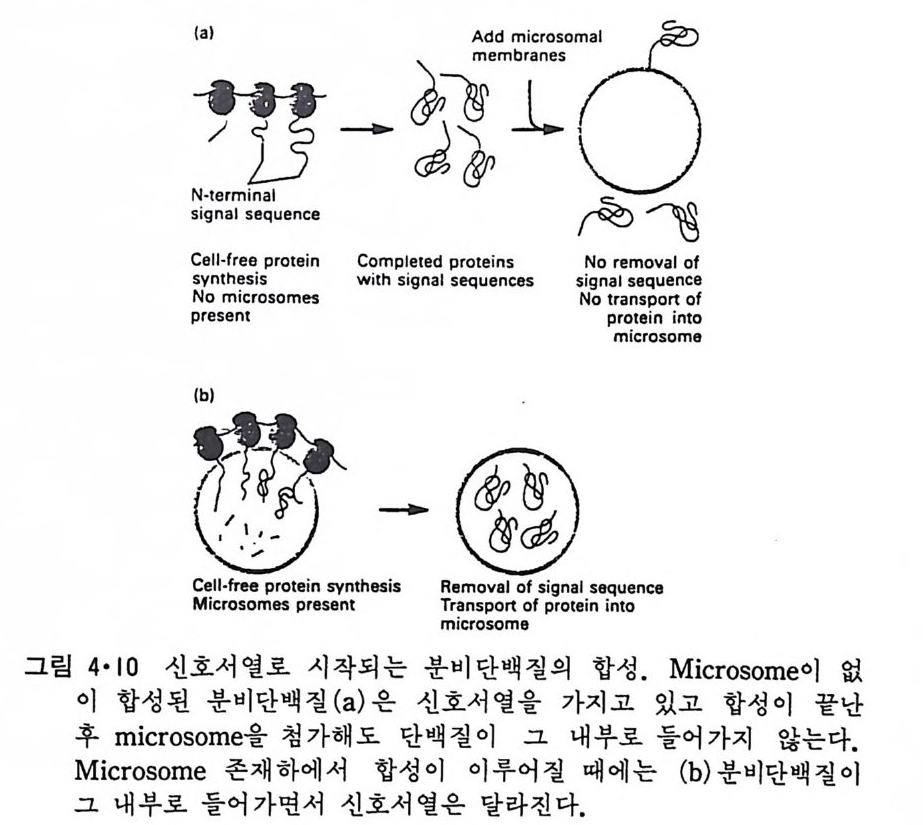
생체막 단백질이 철대 비대칭적인 분포를 갖는데 있어서 세포질의 r i bosome 에 의해 합성된 주변단백질과 내재단백질이 세포질쪽에 부착되 는 것은 쉽게 이해가 되지만 막을 횡단하는 주변단백질이나 세포질 반대 쪽에 위치하고 있는 내재단백질이 어떻게 소수성 막내부를 통과하느냐는 문제는 아직도 완전히 해결되지 않았다. 이것은 세포질에서 합성된 hormone, 혈청단백질 등 세포외부로 분비되는 단백질이 막을 통과하는 문제와 같으므로 이들을 위한 가설을 내재단백질에 대해서도 적용을 시 키려했다. 분비되는 단백질이 소포체의 막을 통과하는 mechan i sm 은 M il s t e i n 동 에 의해서 처음으로 밝혀졌는데 이들은 쥐의 my el oma 암세포에서 항체 (i mmuno g lobul i n) 의 가벼운 사슬이 형성될 때에 조면소포체 존재하에서 합성된 것과 소포체가 없는 상태에서 합성된 것에 크기에 차이가 있는 것을 관찰하였다• 조연소포체 (또는 mi cr osome) 없이 p ol yri bosome 에서 합 성된 p ol yp e ti de 사술은(그림 4·10a) 소포체 (또는 mi cro some) 존재하에서
 엷 :;?;:;\ence 촙 잡
엷 :;?;:;\ence 촙 잡
합성된 것 (그링 4·10b ) 보다 1500 da lt on 만 큼 분자량이 더 컸 다. Blobel 과 Dobbers t e i n9) 은 이 실험 결과 로부터 신호 가설 (s ign al h yp o t hes i s ) 을 제안하였는데 이 가설에 의하면 수출(혹은, 분비)하려는 단백질을 위한mRNA 의 ini t iat i on codon 바로 뒤에 신호 codon 이 있어 세포질의 r i bosome 에 의해서 신호서열 (s ign al se q uence ) 이 합성이 되면 신호서열과함께 r i bosome 이 소포체에 붙는다. 다음 신호서열이 소포체막에 있는 단 백질구멍을 통해 통과되고 이에 연결된 나머지 p ol yp e pti de 가 계속해서 합성되면서 소포체의 lumen 안쪽으로 끌려들어가게된다. 이 과정중에 소포체막의 lumen 쪽에 있는 효소에 의해서 신호서열이 잘리고 분비될 단백 질이 lumen 안으로 완전히 들어간다. 그 후에 이 들 단백 질은 소포체의 막에서 떨어져나온 막소포에 담겨 Gol gi체에 들어가고 여기서 나온 분비 막소포에 담겨 원형질막에 가서 이 막소포의 막과 원형질막 사이에 융합이 일어나 세포 밖으로 분비하게 된다. 신호가설은 거의 모든 분비되는 단백질에 적용이 되는 것이 그후에 증명시되었고 이들의 신호서열에는 소수성 am i no 산기가 나열되어 있는 것 이 발견되었다(표 4·3). 단백질이 합성되는 과정중 신호서열이 소포체막
 표 4• 3 분비 단백 질 (secreto r y pro te i n ) 의 신호서 열 (sig na l seq u ence)
표 4• 3 분비 단백 질 (secreto r y pro te i n ) 의 신호서 열 (sig na l seq u ence)
과 결합하는데는 신호 감 지입자 ( s ign al recog nition pa rt icle , SRP ) 와 이 입자 의 수용체 단백 질 (S RP recep tor pro te i n 또는 dockin g pro te i n ) 이 필요하 다. 조면소포체에서 얻어진 m i crosome 에서 r i bosome 을 제거한 후 0.5M NaCl 로 처리하면 그 내부로는 새로 합성되는 분비단백질이 들어가지 못 한다. 그런데 0.5 M NaCl 로 추출해낸 고분자 물질은 m ic rosome 용액에 다시 첨가하면 합성되는 단백질이 m ic rosome 내부로 들어간다. 이 분자 는 6 개 의 p ol yp e pti de 와 300-n u cleoti de RNA 로 구성 되 어 있 다. 한편
 (al No SRP. no SRP recep tor , no m icr osomes
(al No SRP. no SRP recep tor , no m icr osomes
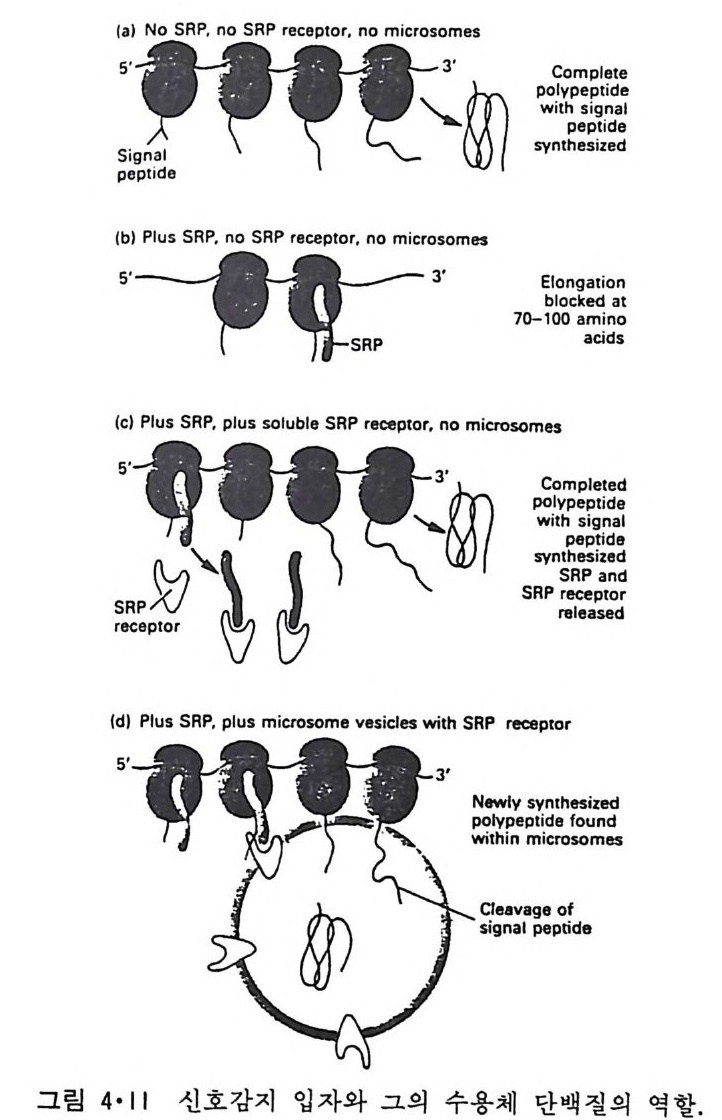
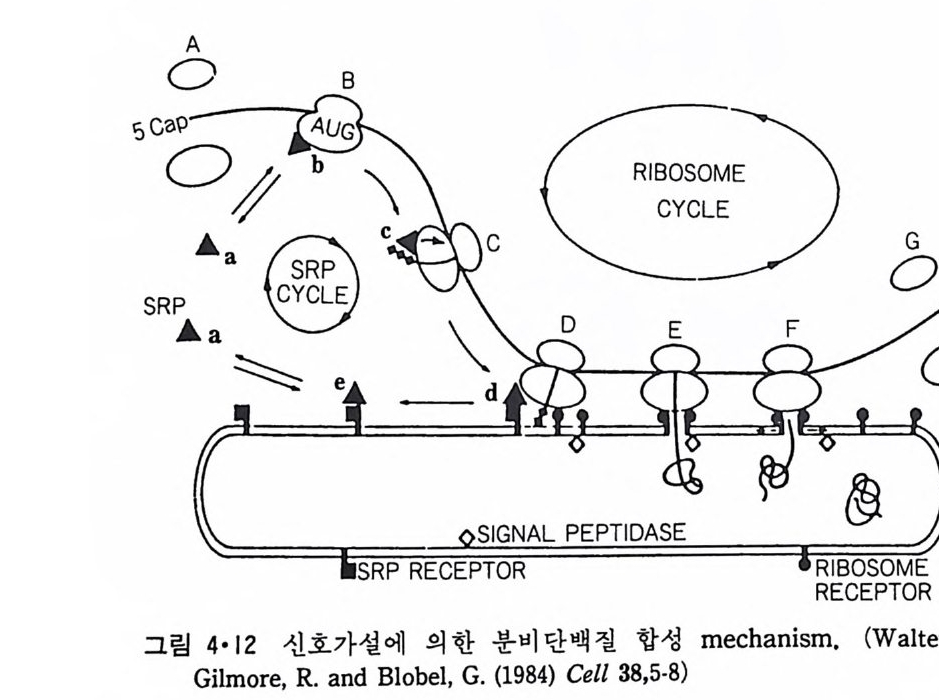
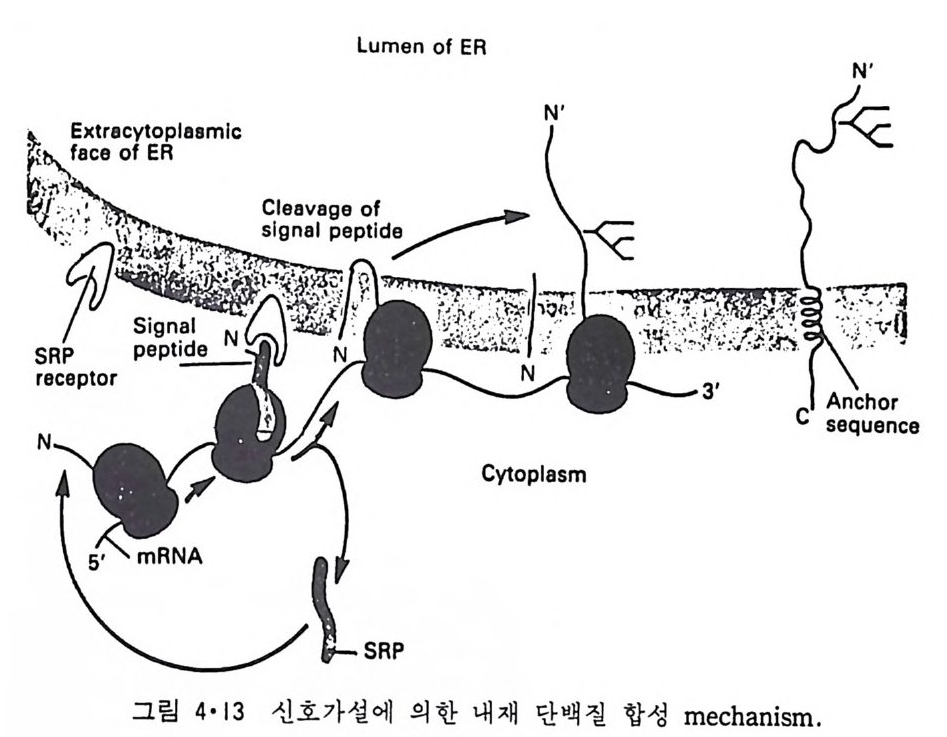
m ic rosome 막을 세탁제로 용해시킨 후 SRP 를 고정시킨 colwnn 을 통해 친화성 chroma t ogr a phy 를 한 결과 650 개의 am i no 산 기를 가진 내재단백 질이 분리되었다. SRP 만이 존재할 때에는 r i bosome 에 의해 분비단백질 의 70-100 am i no 산기만이 연결되고는 정지되는데 SRP 수용체와 같 이 있 을 때에는 단백질합성이 완성된다(그림 4·11). SRP, SRP 수용체와 m ic rosome 이 다함께 존재할 때에는 분비단백질이 합성되면서 mi - crosome 내부로 이동되며 이와 동시에 신호서열이 끊어진다. 이상 단계 적인 실험의 결과로부터 그림 4·12 에 보이는 것과 같은 mechan i sm 이 제 안되었다. 먼저 세포질에 존재하는 r i bosome 에 의해서 단백질합성이 시 작되면 SRP 와 결합이 되어 70-100 am i no 산기 가 연결된 후 합성 이 더 진 행되지 않는다. R i bosome 과 결합된 SRP 는 소포체막 표면에 있는 수용체 단백질과 결합이 되면 p ol yp e pti de 의 연결이 계속되며 동시 에 신호서열을 선두로 하여 분비 단백 질 이 소포체 lwnen 으로 들 어 가면서 신호서 열 이 잘 라진다. SRP 와 수용체 단백질은 다시 떨어져나와 이 c y cle 이 계속된다. 많은 내재단백질도 조면소포체 표면에서 합성되고 또 신호서열을 가지 고 있다가 막에 들어가면서 신호서열이 제거되는 것을 알게 되어 분비단 백질과 내재단백질은 같은 방법에 의해서 합성된다고 생각된다 . 분비단
 AB/@
AB/@
 ::宁Lumen of ER: 1N' \ _° 냐$ Juh' :;ce
::宁Lumen of ER: 1N' \ _° 냐$ Juh' :;ce
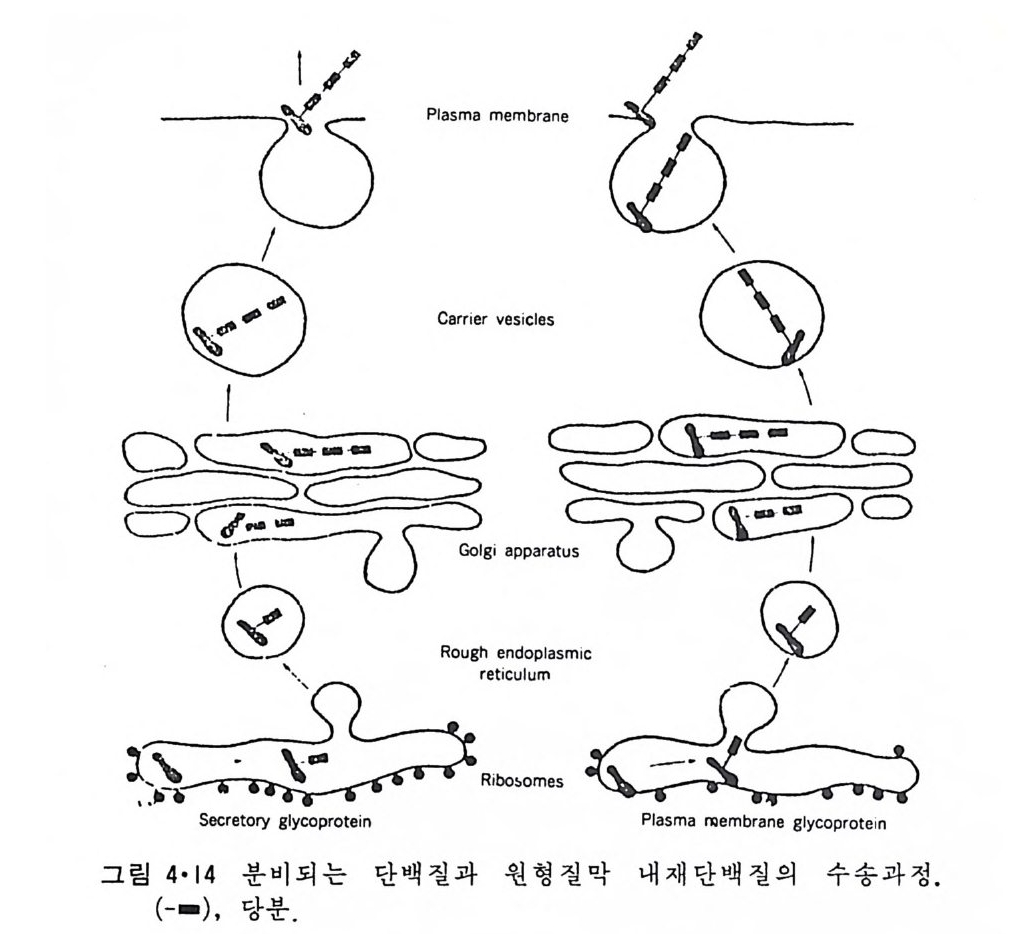
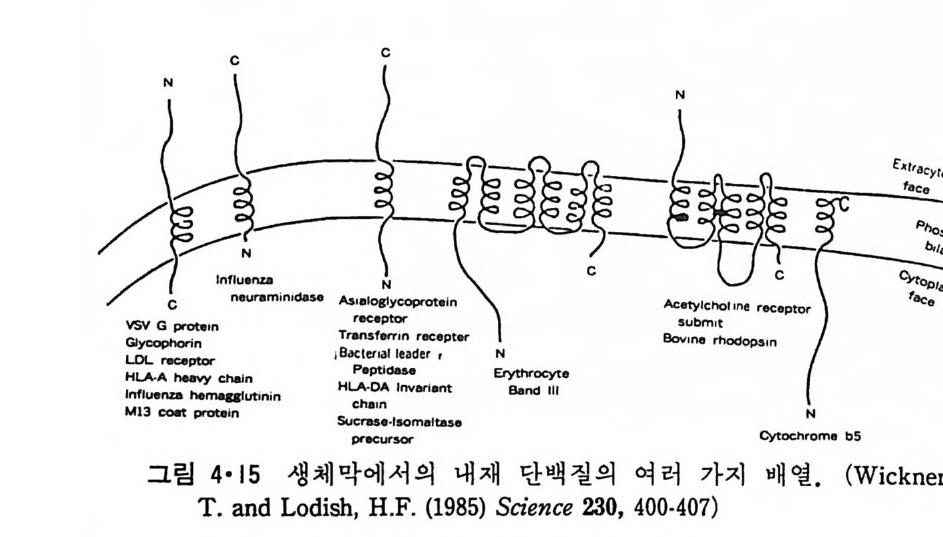
백질은 조면소포체막을 완전히 통과하는 데 반해서 내재단백질은 막을 통과하다가 소수성 서열이 막 내부로 들어가면 거기서 멈춘다고 생각되 고 있다. 그래서 신호가설은 내재단백질의 합성과 막 내부로 들어가는 mechan i sm 에도 그대로 적용이 되었다(그림 4·13). 소포체막에 들어간 내재단백질은 분비되는 단백질과 유사하여 소포체에서 떨어쳐 나와 Gol gi체를 거쳐서 최종목표의 생체막으로 가서 융합에 의해서 그 막으로 옮기게 된다. 분비단백질의 배설과칭과 내재단백질이 원형질막으로 들어 가는 것은 그림 4·14 에 비교되었다. 이 내재단백질에 적용된 신호가설은 그후 여러 경우에 적용되는 것이 판명되었는데 그것은 신호서열의 존재가 확인된 때문이다. 그러나, 이 신호가설의 문제점은 N- 말단이 반드시 세포질의 반대쪽에 위치하여야 한다는 것과 또 p ol yp e pti de 사슬이 막을 한 번만 횡단해야 된다는 것이 다. 많은 경우에 C- 말단이 세포질의 반대쪽에 있고 또, bac ter i or hodop - s i n 등의 경우에는 한 개의 p ol ypepti de 사슬이 막을 여러 번 횡단한다(그 림 4·15). 더우기 많은 내재단백질의 경우 신호서열이 존재하지 않는다. 이들 문제점을 해결하기 위해서 제안된 것이 막시발 (membrane trigge r)
 I/
I/
 [
[
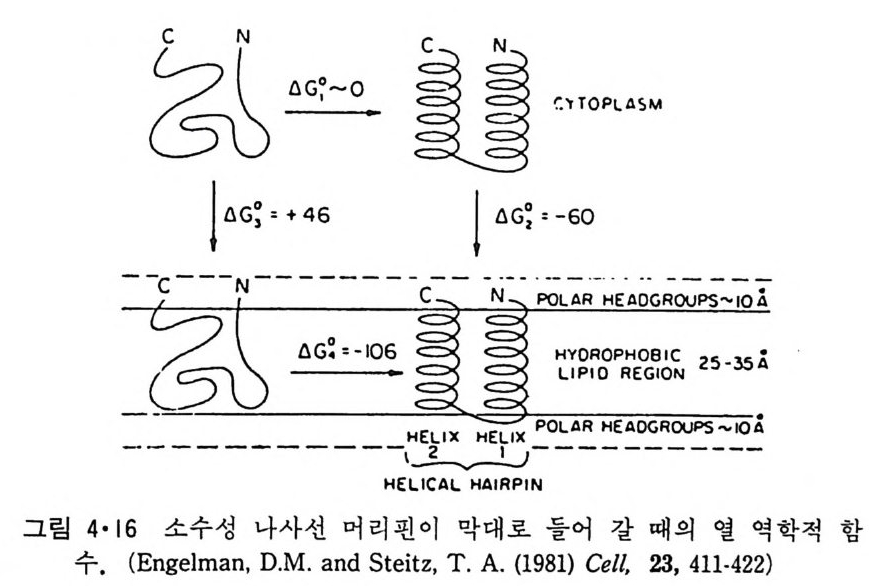
가설 10 ) 이다 . 아가성에 의하연 어미 산 ·공유의 내재단백실온 두 가기 구 조 륭 가질수 있다 . 즉, 천수성 표면을 가진 구조와 소수성 표면옹 가 진 구 조이다. 이 단백질이 합성되면 처음에는 물에 용해될 수 있는 형태로 존 재하고 이것이 소포체막과 접촉이 되면 소수성 막내부에 들어갈 수 있는 구조로 변한다• 막시발가설을 지지할 만한 실험적 증거는 아직 없다. 단, my e li n p ro t eo lipi d 같은 내재단백질들이 유기용매에 녹는 성질과 물 에 녹는 형태가 각각 있 다는 것은 매우 홍미있는 것이다. 막시발가설의 문제접은 합성된 단백질이 어떻게 막으로 들어찰 수 있느냐는 구체적인 제안이 안된 것이다 . 이 문제접을 보완하고 또, 이상의 두 가정을 종합하여 제안된 것이 En g elman 과 S t e it z 의 나사선 머리핀가설 II) 이다. 이 가설에 의하면 단백 질의 생합성시 막의 소수성 내부를 나사선으로써 침두할 수 있는 길이의 소수성 서열이 생기면 이것 은 그림 4·16 에서와 같이 막 내부로 들어가는 것이 열역학적으로 안정하기 때문에 인접해 있는 부분을 끌고 머리핀 모 양으로 막 내부로 들어간다. 이 나사선 머리핀가설은 분비되는 단백질과 여러가지 다론 구조를 가진 내재단백질이 막으로 들어가는 과정을 설명 할 수 있는 장접이 있다. 그림 4·17 은 분비되는 단백질이 생체막을 동과 하는 과정을 보여주는데 소수성인 신호서열이 계속 합성된 부분과 나사 선 머리핀을 형성하여 막에 들어간다 . 이 신호서열 이외의 po lyp e p tide
 二 二 鬪 r 、 TOPLASM
二 二 鬪 r 、 TOPLASM
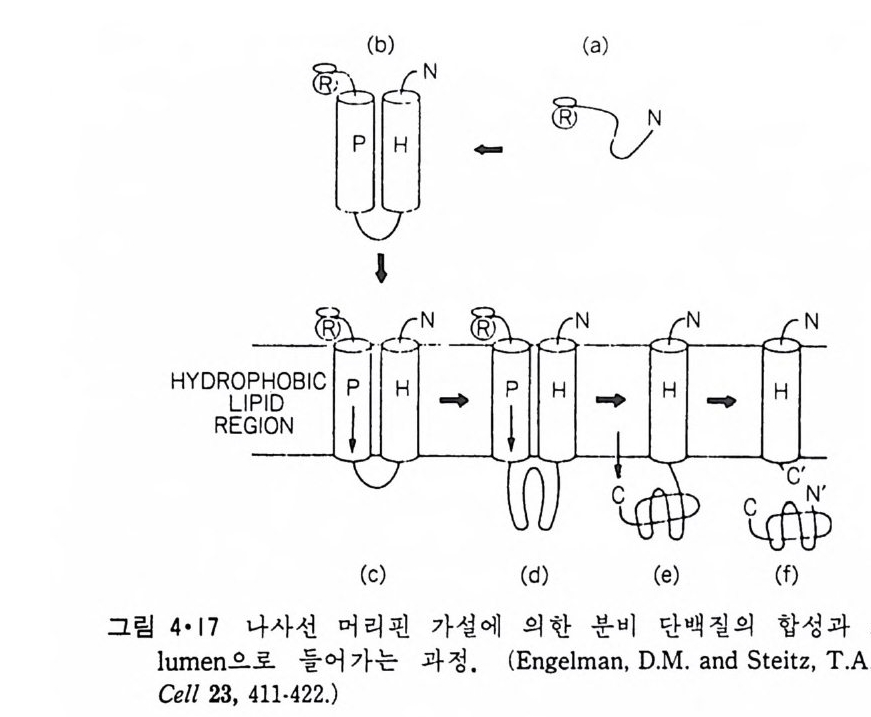 (b) -(a) P
(b) -(a) P
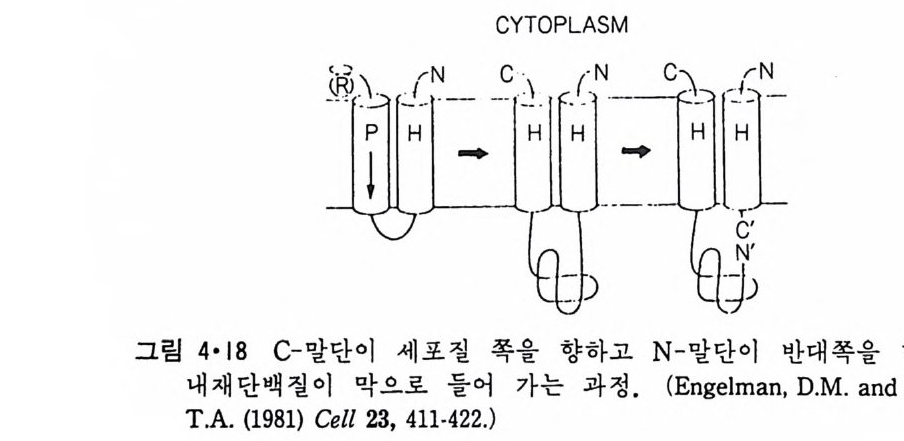
부분은 소수성 이 아니 므로 연 장 (elong a ti on ) 이 되 는 대 로 막을 동해 소포 체의 lumen 쪽으로 이동되어 C- 말단이 lumen 에 들어오면 단백질 가수분 해효소에 의해서 신호서열이 떨어진다. 그림 4·18 은 C- 말단이 세포질을 향하고 막을 한 번만 횡단하는 내재단백질의 합성과정이다. 이때에는 신 호서열이 필요하며 이후에 계속해서 합성되는 부분은 lumen 으로 들어오 다가 소수성 서열이 막을 횡단하면 그이상 더 움직이지 않는다. 이 다음
 CYTOPLASM
CYTOPLASM
 二
二
에 신호서열이 잘리면 N- 말단이 lumen 을 향하게 된다. 여기서 처음 나 사선은 신호서열의 역할을 한다. C- 말단이 lumen 쪽을 향하는 경우는 이 처음 소수성 나사선 부분을 따르는 부분에 막을 횡단할 수 있는 길이의 소수성 부분이 없으면 C- 말단까지 lumen 내부로 들어 가기 때문에 이 내 재단백질이 어디로 가든지 세포질의 반대쪽에 C- 말단이 위치하게 된다.
 굽®二:@[
굽®二:@[
 Ba nrnluc.c,clvlles,oa or qnldnniclUo ()ll cvo cln Noo— '—-—`olr a.ng s -m 5'D eospsd oannnuas:c na.l nhaolgr, nnporpt gnneasuM-itilit sn amd nor esnoIlti >\ .F981 .)( 5 odn h ,asl.Hic지LWW(.Tici ,rnek .msnhace
Ba nrnluc.c,clvlles,oa or qnldnniclUo ()ll cvo cln Noo— '—-—`olr a.ng s -m 5'D eospsd oannnuas:c na.l nhaolgr, nnporpt gnneasuM-itilit sn amd nor esnoIlti >\ .F981 .)( 5 odn h ,asl.Hic지LWW(.Tici ,rnek .msnhace
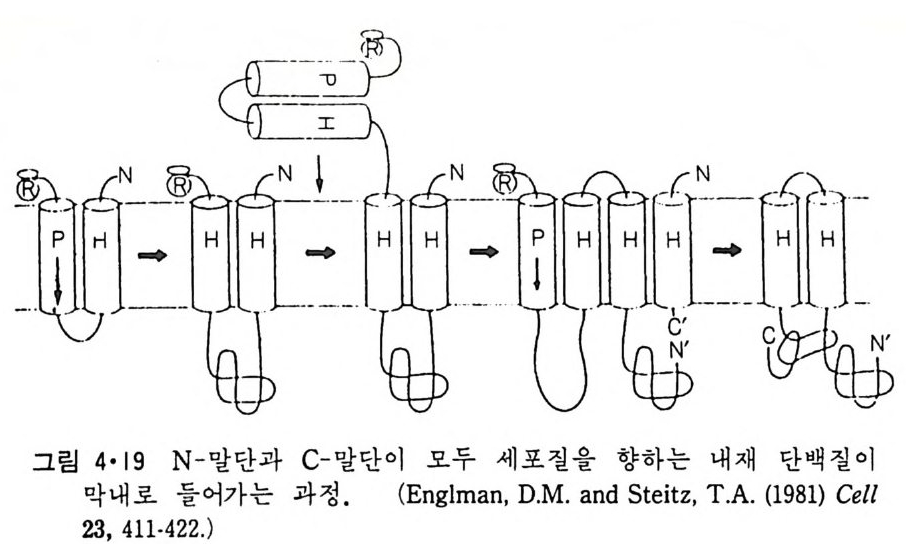
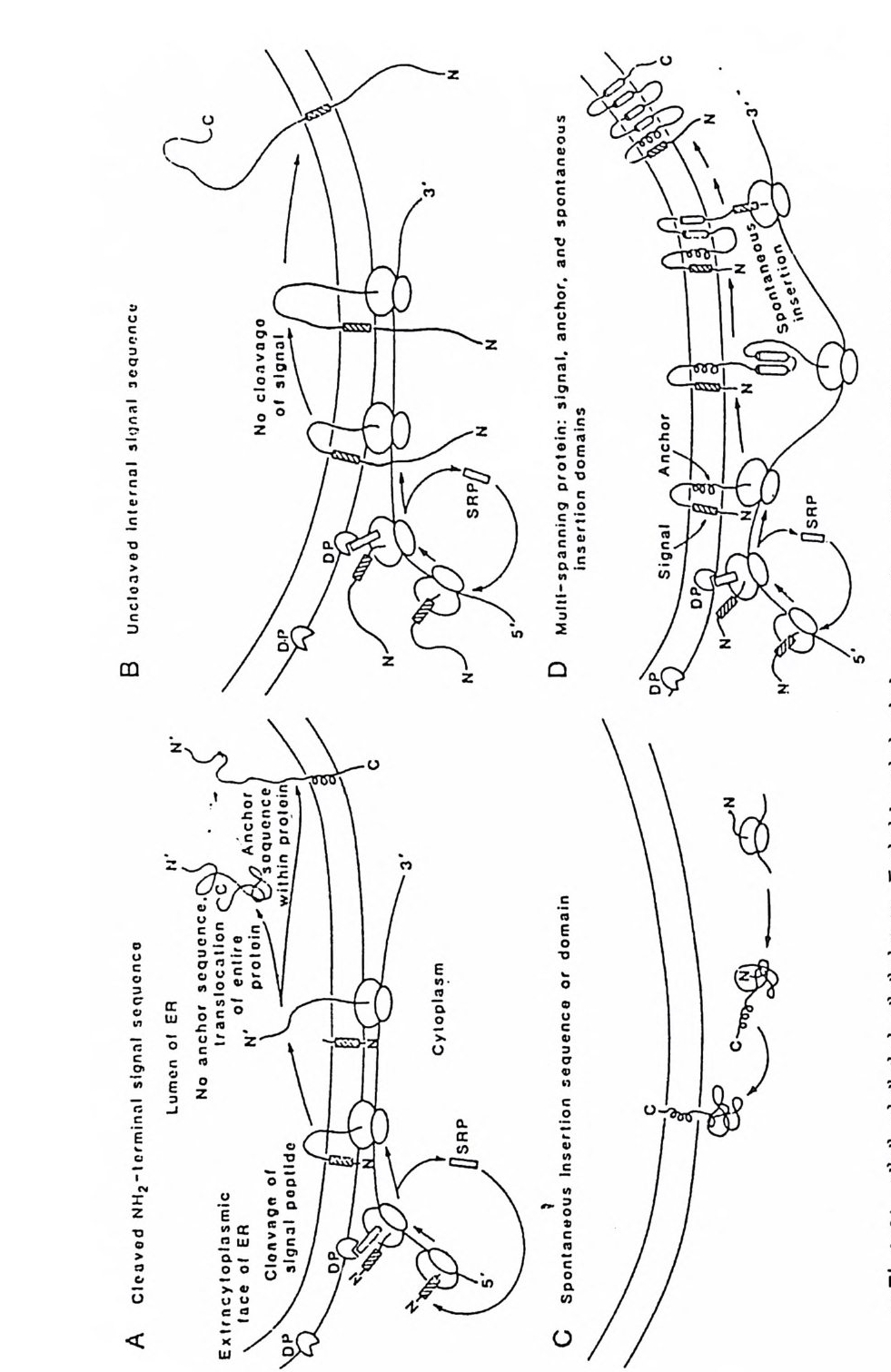
다음 N- 말단과 C- 말단 이 동시 에 세포질을 향 하는 경우는 이 나사 선 머 리핀의 양쪽 나사선이 모두 소수성인 경우 그대로 막에 들어가면 되고, 방향이 반대인 경우는 그림 4·19 에서 보이는 것과 같이 3 개의 소수성 나 사선이 막에 들어간 후 C- 말단이 lumen 으로 들어가게 되어 처음과 두번 째 소수성 나사선이 끊어지면 된다. 마지막으로 막을 여러 번 횡단하는 막단백질의 합성은 그림 4·20 에서 보여준다. 막을 횡단할 만한 길이의 소수성 나사선이 계속 연결되는한 이 부분들이 막으로 들어가면 bac t er i orhodo p s i n 과 같은 막 내 배열을 갖게 된다. 이 model 도 아직은 실험적으로 중명이 된 것은 아니고 특히, 소수성의 긴 부분이 세포액내 에서 어떻게 잠칭적이나마 존재할 수 있느냐가 문제가 된다. 그림 4·21 은 위 가 설 을 종 합 하여 몇가 지 가능한 mechan i sm 을 본 것이다. 내재단백질이 합성된 후 무슨 mechan i sm 에 의해서든지 소포체막에 둘 어가면 소포체의 막이 떨어져 나와 Gol gi체 막과 융합이 되고 여기서 다 시 떨어져 나와 원형질막이나 다른 막과 융합이 된다. 아 전반적인 과정 은 분비되는 단백질이 밟는 과정과 비슷하다(그림 4·14). 이렇게 내재단 백질이 소포체막에서 다른 막으로 옮겨지는 과정에서 막 표면의 방향은 항상 보존이 되어 합성시 세포 질 을 향하던 부분은 다른 막으로 옮겨져도 같은 방향으로 향하게 된다. 4·2·3 탄수화물 탄수화물이 생체막의 한쪽에만 존재해 절대적인 바대칭성을 아룬다는 실험적 관찰은 처음에 적혈구에서 이루어졌다. 적혈구에 있는 모든 sia l i c a ci d 는 막을 동과하지 않는 neuram i n i dase 에 의 해 서 제 거 되 기 때 문에 이들은 전부 외부에 위치함을 알 수 있다. 또 하나의 중요한 실험 결과는 특정한 탄수화물과 결합하는 lec ti n 의 f err iti n 유도체로 oli go sac- char i de 의 분포를 보았더니 원형질막의 외부나 세포의 소기관의 내부 표 면에만 분포되어 있는 것을 발견하였다. 즉, 세포질과 반대되는 표면에 만 분포되어 있다. 탄수화물의 이러한 절대적인 비대칭적 분포는 이들이 소포체와 Golgi 체의 lwnen 쪽에서 지방질과 단백질에 공유결합을 하게 되고, 이때 세포 질의 반대 표면에만 이것들이 결합되기 때문에 계속해서 이 표면에만 존 재하게 된다(그림 4·14).
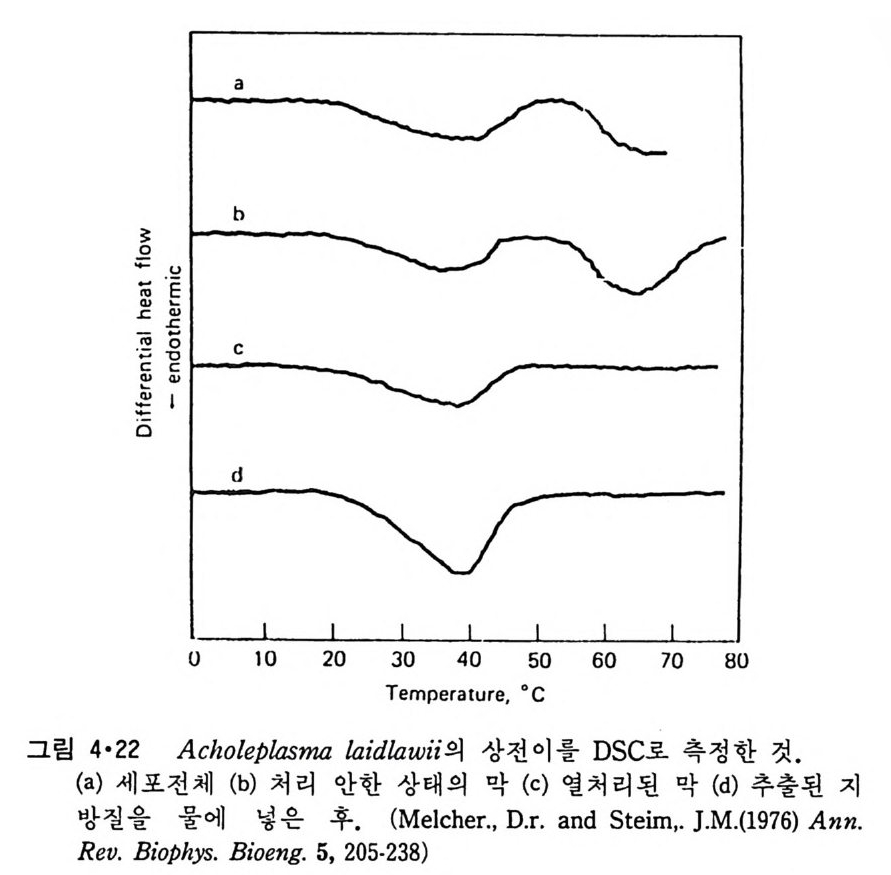
4·3 생체막 성분의 이동성 앞서 상전이온도 이상에서는 lip osome 내에서의 지방질의 이동성이 상 당히 크며 lip osome 에 재구성된 내재단백질도 그의 회전화산계수와 평면 확산계수가 커서 이동이 자유로운 것을 알았다. 성분 구성이 대단히 복 잡한 생체막에서 그 지방질과 단백질의 유동성도 역시 커서 한 막 s y s t em 에서는 이들 성분이 균일하게 분포되려는 경향이 있다. 그러나, 생체내에서의 특이한 여러가지 조건에 의해서 보통 때에는 자유로운 운 동이 제약이 되고 때로는 한 가지 단백질이 생체막의 작은 표면에 모여 서 필요한 기능을 하기도 한다. 4·3·1 생체막에서의 상 전이 막의 이 분자층을 구성 하는 지 방질 이 액 체 결 정 (liqu id cry st a l l ine ) 형 태 로 있느냐 또는 g el 형태로 있느냐에 따라 지방질 자체뿐만 아니라 거기에 들어가 있는 내재단백질까지의 유동성이 결정된다. 그러나 생체막에서의 지방질의 상 전이에 대한 da t a 는 별로 없는 형편이다. 그림 4·22 은 Achole pla sma la i dlaw ii의 상전 이 룰 DSC 로 측 정 한 것 이 다. 여 기 서 a 선은 세포 자체의 상전이를 본 것이고 두 상전이 온도를 보이며, b 는 분리해 낸 원형질막의 상 전이로 세포전체 때와 유사하다. c 는 가열에 의해 단 백질을 변성시칸 후 얻은 것으로 이는 추출해낸 지방질의 상 전이 d 와 유 사하다. 그래서 a 와 b 에서 60°C 근처에서 일어나는 변화는 단백질의 변 성에 의한 것이고 생리적 온도 근처에서 일어나는 변화는 지방질의 상전 이에 의한 것이다. 지방질의 상전이 온도는 생체막에서 단백질의 존재 하에서 변하지 않는 것을 알 수 있다. 위의 경우에는 지방질의 상전이 온도가 37°C 정도이지만 진핵세포에서는 생리온도보다 훨신 낮은 온도에 서 상 전이가 있기 때문에 생리적인 온도에서는 지방질이 액체 결정상으 로 존재한다. 지방질의 70~95% 정도가 상전이에 가담하는데 나머지는 내재단백질을 둘러싼 지방질이라고 생각된다.
 a
a
4·3·2 지방질의 이동도 12) 표 4·4 는 생체막 내에서 인산지방질의 평면확산계수를 보여준다. 여기 서 확산계수는 model 막 지방질 이분자층에서의 숫자와(표 2·8) 비슷한 것을 볼 수 있다. 그림 4·23 은 사람 fi broblas t의 원형질막과 이 세포에 서 추출한 지방질로 구성된 이분자층에서의 확산계수를 비교한 것이다. o·c 에서 4o·c 까지에 걸쳐서는 원형질막 내에서의 확산계수가 가장 적고 세포 전체에서 추출한 지방질의 이분자층에서의 확산계수가 제일 큰데 여기서 원형질막에서 단백질의 존재가 확산계수를 감소시키며 세포전체 지방질 이분자층 내에서의 확산계수가 원형질막에서만 추출해낸 지방질 의 이 분자층 내 에 서 의 확산계 수보다 큰 이 유는 후자에 choles t erol 이 많 이 포함되어 탄화수소의 꼬리 부분이 좀더 고체에 가까운 성질을 띠기
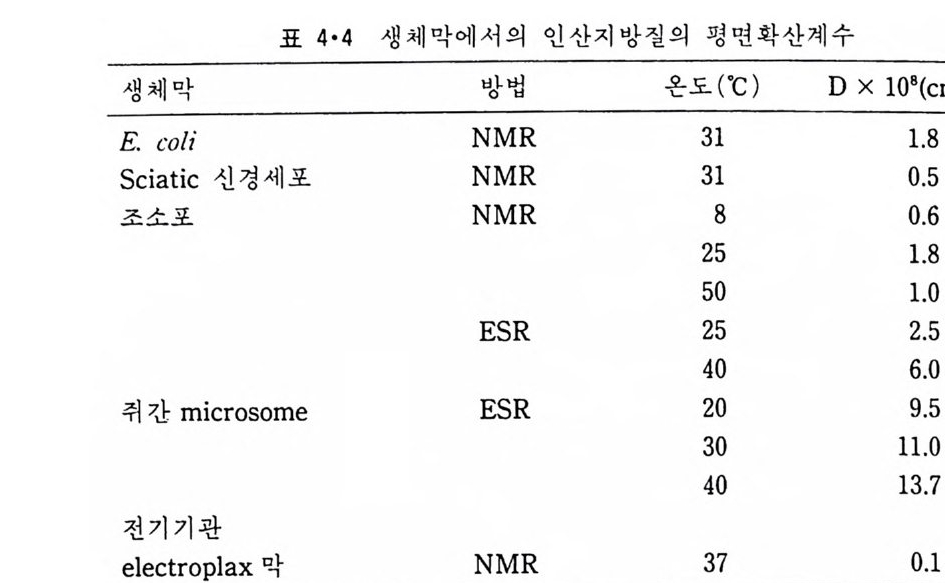 표 4•4 생체막에서의 인산지방질의 평면화산계수
표 4•4 생체막에서의 인산지방질의 평면화산계수
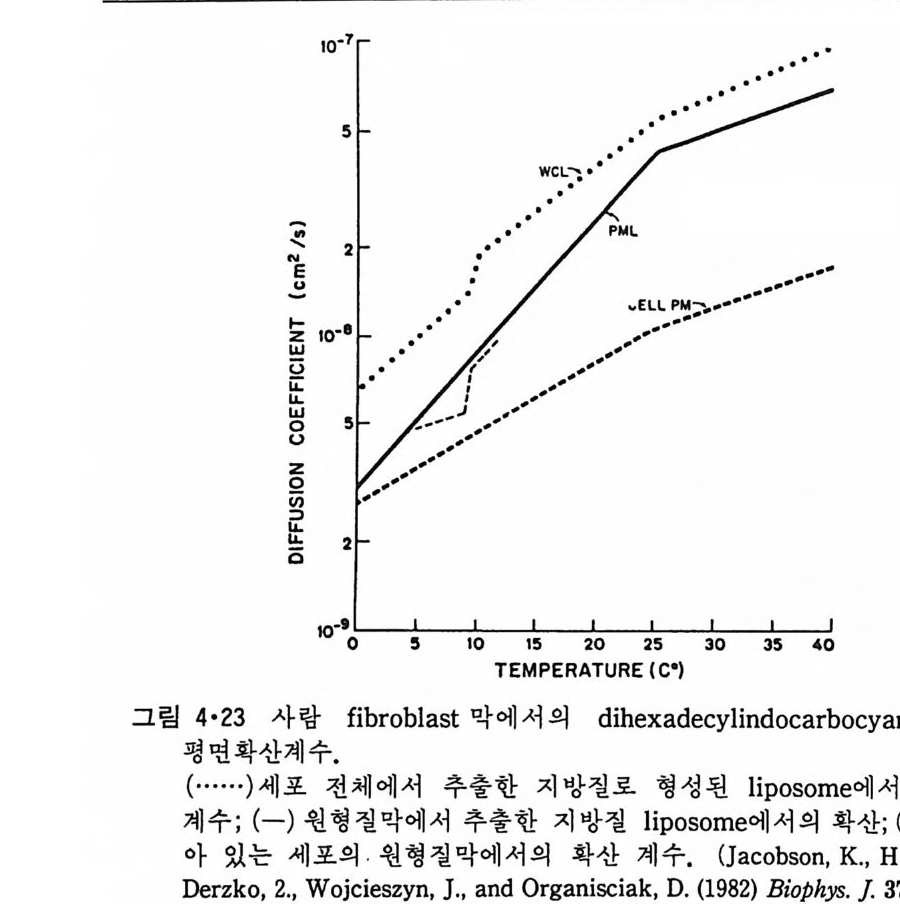 10·7 .. .. .. . .
10·7 .. .. .. . .
때문이라고 해석이 된다. 한편, 생체막의 한 단층에서 반대쪽으로의 지방질의 이동은 지방질 이 분자층에서의 값과 별 차이가 없다. 이러한 이동이 극히 느린 과정이라 는 것은 생체막 내에서 지방질의 분포가 원형질막 양면에 비대칭적으로 유지되는 것으로부터 알 수 있다. 4·3·3 단백질의 이동도 13) 생체막내에서 지방질이 여러가지 분자운동을 하므로 그 안에 존재하는 단백질도 이동이 되리라고 추측이 되는데 이것은 여러가지 실험으로 증 명 아 되 었 다. Fr y e 와 Ed i d i n14) 은 사람 적 혈구와 쥐 적 혈구를 Sendai v i rus 로 융합하여 형 광항체 (fluo rescent anti bo dy ) 방법 으로서 이 두 가지 적혈구의 항원 (an tig en) 이 섞이는 과정을 관찰하였다. 융합이 끝난 후 5 분내에는 이 융합된 두 적혈구의 항원이 분리되어 있었으나, 40 분 후에 는 완전히 섞이는 것으로 보아 사람 적혈구 막에 있던 내재단백질과 쥐 적혈구 막에 있는 내재단백질이 횡적 확산을 하여 완전히 섞인 것을 알 수 있다. 한편, Fowler 와 Bran t on 은 사람 적 혈구의 내 재 단백 질을 fluo rescein i so t h i oc y ana t e(FITC) 로 표지시킨 다음 표지가 안된 적혈구와 융합시켜 표지 된 내재단백질이 확산되는 것을 관찰하였다. 두 적혈구가 융합된 직후에 형 광사진을 찍은 것은 한쪽 적혈구만 보이지만 상대조(p hase contr a st) 사진 으로 융합된 것이 보인다(그림 4·24). 융합 후 일정한 시간 후에는 확산
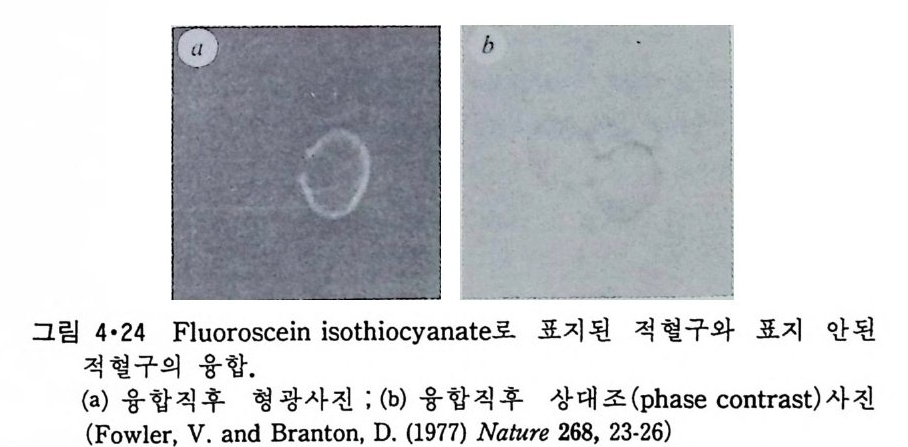 그림 4•24 Fluoroscein i so t h i oc y ana t e 로 표지된 적혈구와 표지 안된
그림 4•24 Fluoroscein i so t h i oc y ana t e 로 표지된 적혈구와 표지 안된
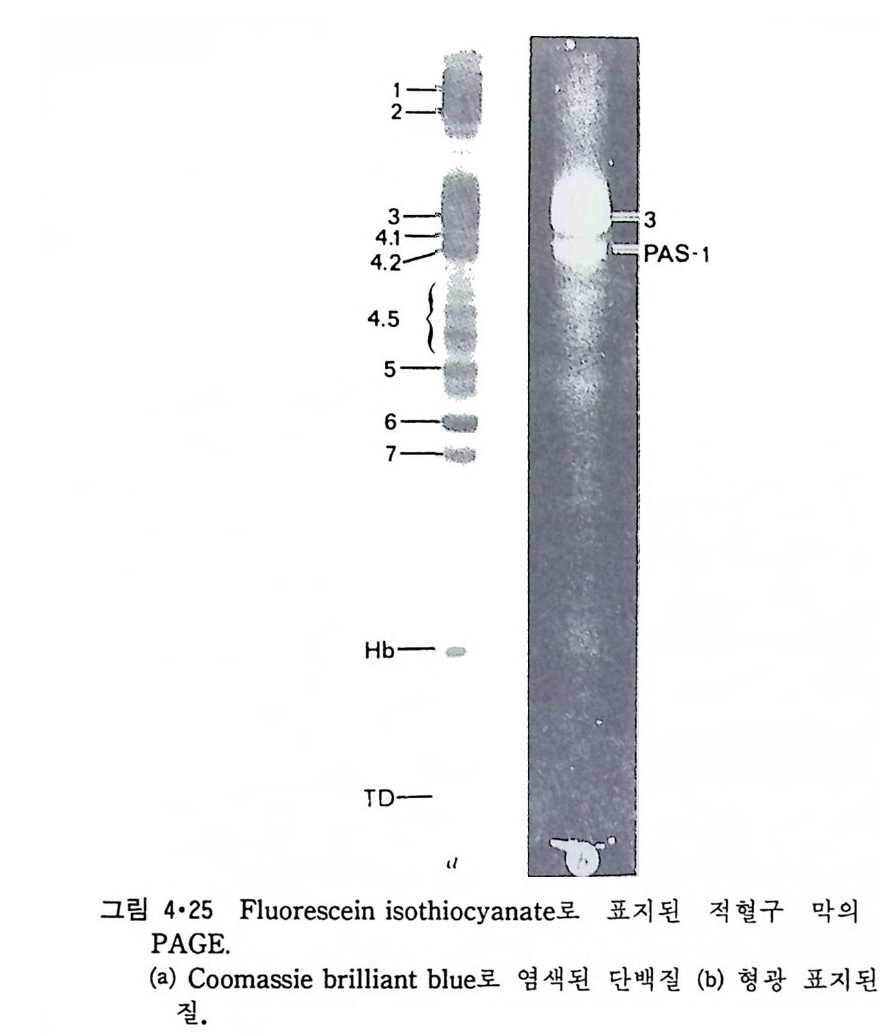 21 一一
21 一一
의 결과 두 세포가 모다 형광성을 보인다. 그림 4 • 25 는 이 표지된 단백 질을 석 별 하기 위 해 SDS-po lya cry la mi de 전 기 영 동을 한 것 이 다. Band 3 와 PAS-1 의 내재단백질들이 형광표지가 된 것으로 이들이 횡적 이동을 한 것을 알 수 있다. 그림 4 • 26 는 이돌 평면확산과정의 속도를 본 것이 고 표 4·5 는 이로부터 얻은 확산계수이다. 이들 값은 lip osome 에 재구성 시킨 단백질의 확산계수보다 훨씬 작은데 이는 전에 언급된 것과 같이 적혈구막에서는 주변단백질의 조칙에 의해 단백질의 운동이 저해되기 때 문이다. 그후에 세포융합 없이 하나의 생체막 내에서의 확산계수를 측정 하는 여러 방법이 도입되었는데 이중 가장 많이 쓰이는 방법이 형광표백
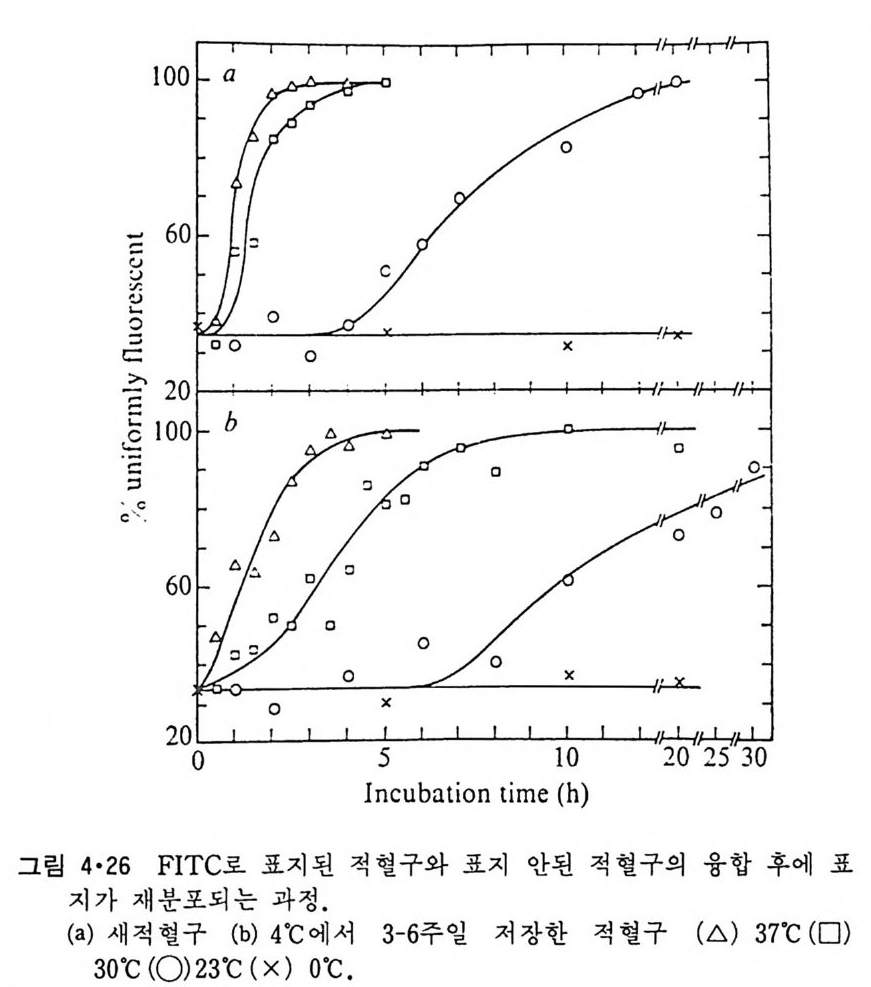 100 a
100 a
회 수방법 (fluo rscene recovery aft er ph oto b leachin g , FRAP) 이 다. 이 방법에 서는 lµm 직경정도의 막 면적에 단속(p ulsed)laser 광선을 쬐어 혀0 과0 서0 염색체를 비가역적으로 표백시킨 후 주위에 있는 형광표지가 그 안으로
 표 4•5 적혈구 단백질 확산계수
표 4•5 적혈구 단백질 확산계수
 표 4·6 생체막 내에서의 내재단백질 확산계수
표 4·6 생체막 내에서의 내재단백질 확산계수
확산되어 형광강도가 증가하는 속도를 측정해 확산계수를 계산하는 것이 다. 이때 내재단백질을 형광물질로 표지시켜 이의 확산계수물 측정한다. 표 4·6 은 이 방법과 기타 방법으로 얻어진 내재단백질의 확산계수를 보 여준다. 이 표에서 많은 경우 형광의 회복률이 100% 가 안되는데 이는 내재단백질의 일부가 전혀 확산이 안되는 것을 의미한다. 또, 확산계수 는 10-8cm2sec-1 에서 10 - 12cm2sec-1 에까지 이루어 그 분포가 넓다. 이로써 모든 생체막 단백질은 비교적 자유로이 회전 및 횡적인 이동을 하는 것을 알 수 있으나 이들 운동은 몇 가지 외적 조건으로 제한울 받 울 때가 있다. 그링 4·27 은 생체막의 내재단백질의 운동을 제한하는 4 가 지의 요소를 보여준다. 여기서 (a) 는 단백질의 농도가 많을 때 회합하는것이고 이것의 예로는 자색막에서의 bac t er i orhodo p s i n 이 2 차 결정을 형 성하는 것이다. (b)는 지방질의 상분리때에 일어나는 단백질의 농도증가에 따르는 회합의 경우이다. (c) 는 주변단백질이나 주변에 있는p ol y sachar i de 와 내재단백질이 결합하는 것이다. 이의 좋은 예는 적혈구에서의 주변단백질인 s p ec t r i n 과 ank y r i n 이 band 3 단백질과 결합되는것으로 이미 그림 4·9 에서 보여주었다. 이 주변단백질들에 의한 이동의 제한은 이들 주변단백질을 제거하면 없어진다. S p ec t r i n 은 적혈구 이외의 생체막에서는 발견되지 않았지만 ank y r i n 은 많이 분포되어 있어 이러한주변단백질에 의한 내재단백질의 운동의 제한은 보편적인 것으로 보인다. (d) 는 세포골격 등에 의한 내재단백질의 운동제한이다. 이 현상온항원 ca p형성에서 불 수 있는데 이렇게 원형질막 표면항원이 한곳에 모이 는 것 이 세 포골격 의 회 합을 방해 하는 cy toc halasin B 와 colob ici ne 에 의해서 저해되는 것으로 보아 세포골격이 내재단백질 위치를 조절할 수있는 것 같으나 이 현상은 아직도 자세히 알 수 없다.
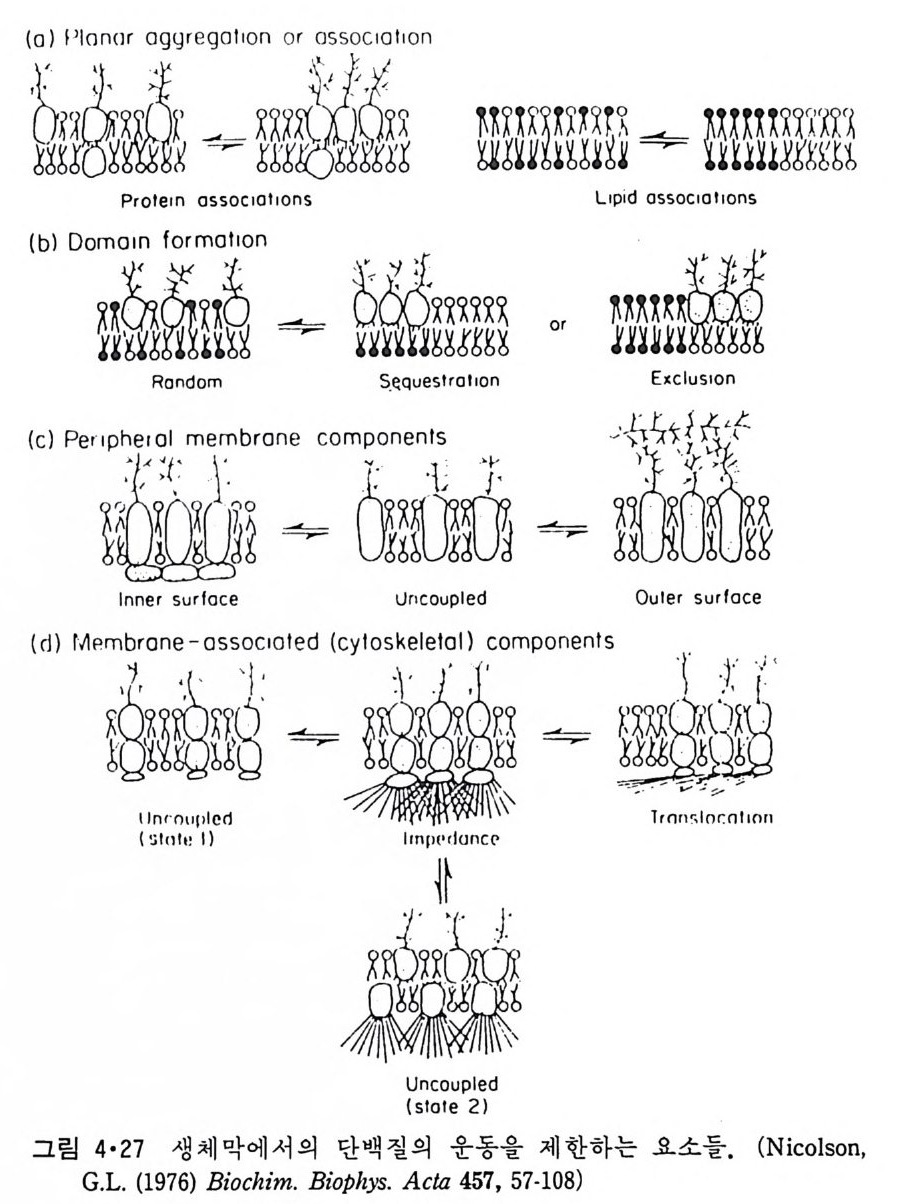 (昌a ) l言'lo`n o\r a:g yre \g a t 1\o n o\r os:soc1:atio n 鬪鬪!}수血鬪區
(昌a ) l言'lo`n o\r a:g yre \g a t 1\o n o\r os:soc1:atio n 鬪鬪!}수血鬪區
4·4 생체막의 순환 생체막은 생리적인 온도에서 유동성이 있을 뿐만 아니라 세포 내에서
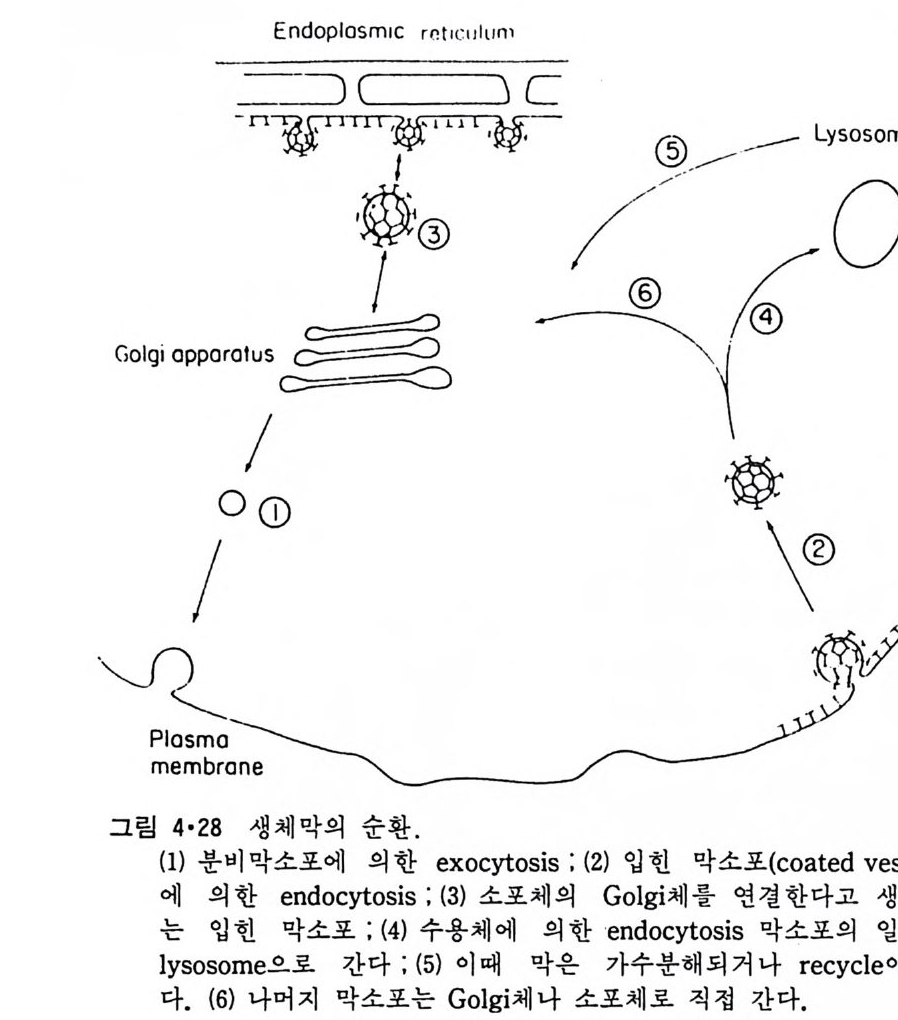 Endop lo sm1c rr.t ,c ,J ! u m
Endop lo sm1c rr.t ,c ,J ! u m
계속해서 순환을 한다. 그럼 4·28 에서 보이는 것과 같이 exoc yt os i s 과정 에서 조면소포체막이 여러 단계를 거쳐 원형질막으로 가고, endocy tos is 과정에서 원형질막이 세포내 소기관막으로 이동이 된다. 이러한 생체막 의 순환과정은 au t orad i ogra p h y로서 알 수 있는데 방사성 동위원소로 표 지된 am i no 산을 세포에 가하면 방사선이 먼저 소포체에 나타나고 다음 Gol gi체를 거쳐 원형질막으로 간다. 그림 4·29 온 소포체, Gol gi체와 원형질막의 성분을 비교한 것이다. Gol gi체 막 성 분은 소포체 막과 원형 질막 성 분의 중간에 위 치 하며 막순 환설을 지지한다.
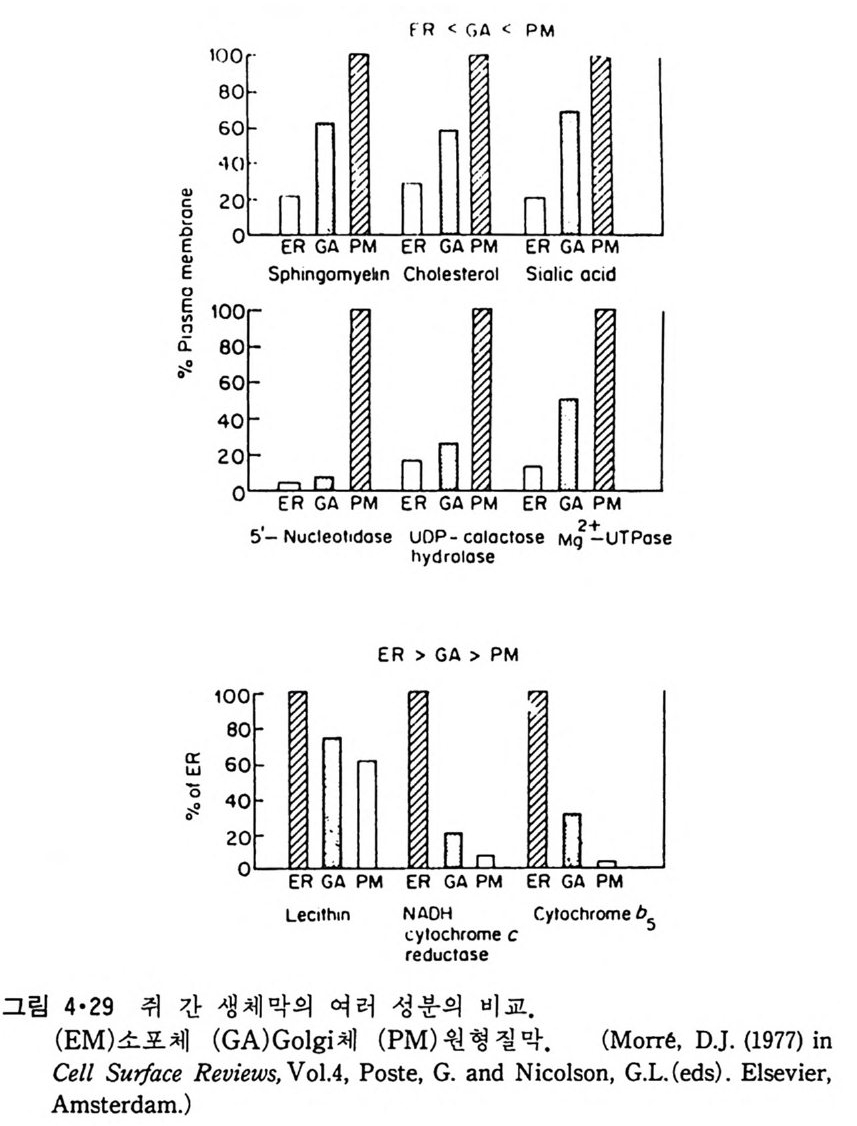 fR < (,A < PM
fR < (,A < PM
4·5 생체막 구조의 Model 생체막은 대 단히 복잡한 s y s t em 이 기 때문에 수많은 model 들이 제 안되 었다. 그중 중요한 3 개만을 고려해 보기로 한다.
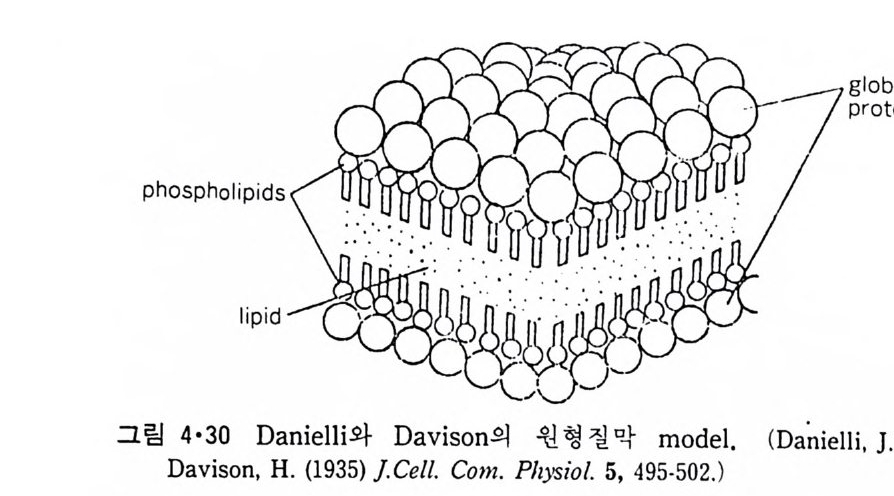 ph osph olip i ds
ph osph olip i ds
4 • 5 • 1 Danie l l i-D avson model(1935) 15> 이는 그림 4·30 에서 보여주는 것과 갇이 지방질 이분자 층 이 원형질을 둘러싸고 있고 구형의 단백질이 이분자층 양쪽 표 면에 부착되어 있다• 이 model 은 Go rt on 과 Grendel 의 지방질단층 실험 결 과 를 토대로 한 것으 로 ac y l 사슬이 고정되었다고 가정하였다. 그 후에 이 model 을 수정하여 단백질로 둘러싸인 구멍의 존재도 제안되었다. 4·5·2 Rober t son 의 단위막 (un it membrane) modeJ1 6 > M y e li n 등 생체막을 전자현마경과 X- 선 회절 방법으로 광범위하게 연
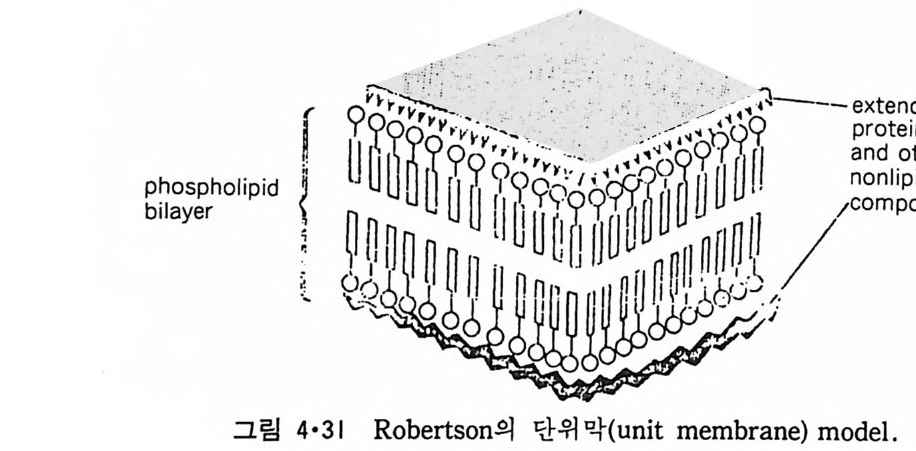 t,Lt! ·L.-• .· : . .•. .阜 . · .. ·., . ... epxrot et ne di ne sd
t,Lt! ·L.-• .· : . .•. .阜 . · .. ·., . ... epxrot et ne di ne sd
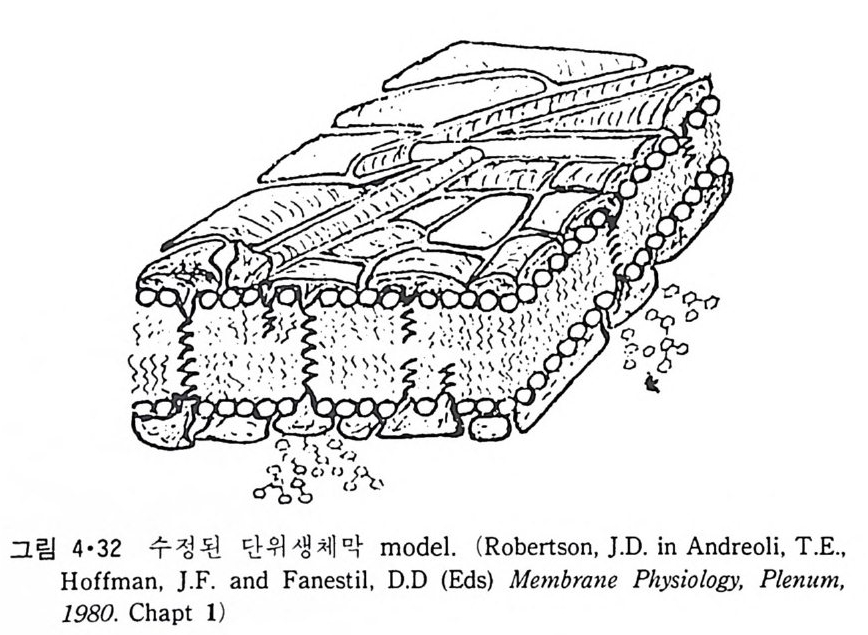 l 뎅\`
l 뎅\`
구한 후 Rober t son 은 Danie l li- D avson model 을 토대로 하여 새 model 을 제한하였는데 여기서 지방질의 이분자층 주변에 구형단백질 대신 펼쳐진 단백질의 구조를 가정하였고 또 원형질뿐만 아니라 세포 내부의 많은 막 sys t e m 같은 구조를 갖는다고 제안하였다(그림 4·31). 그 후에 단백질의 p ol yp e ti de 사슬이 막 내부에까지 침투하는 것으로 수정하였다(그림 4· 32) .
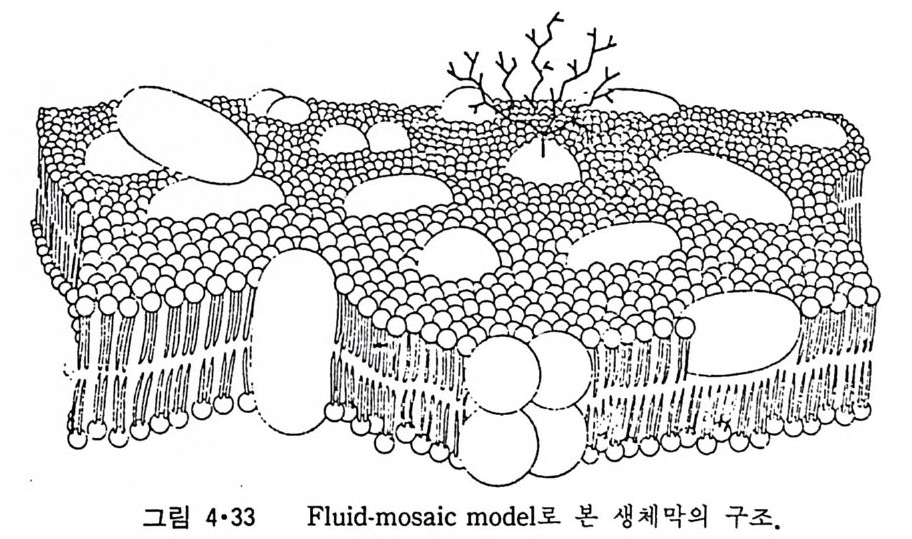 그림 4·33 Fluid - mosaic model 로 본 생체막의 구조.
그림 4·33 Fluid - mosaic model 로 본 생체막의 구조.
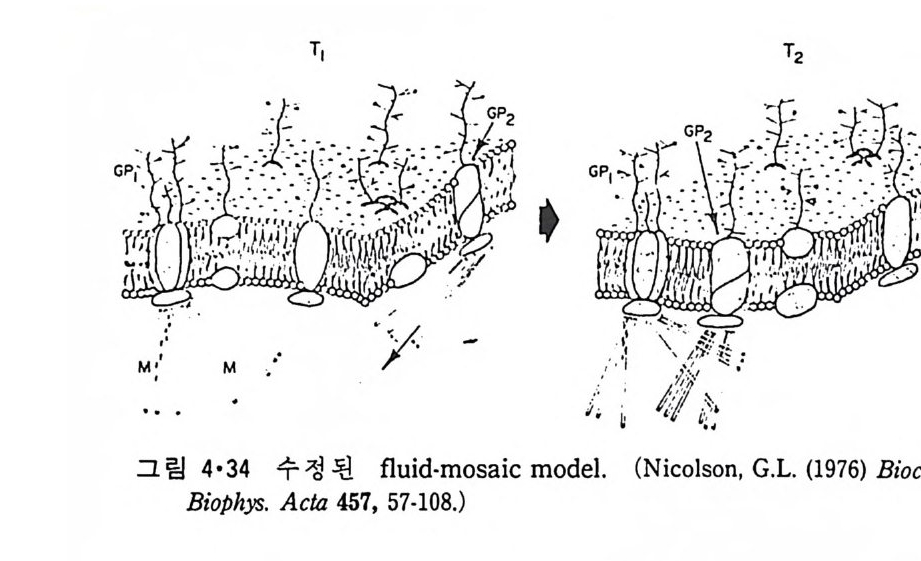 墓답 라,'M...¥., . 3.... . 냐 . .. .. .MT l.E,7 , L /l广1\ i \ 군之T 2
墓답 라,'M...¥., . 3.... . 냐 . .. .. .MT l.E,7 , L /l广1\ i \ 군之T 2
4·5·3 S i n g er-N ic holson 의 fluid- mosaic model' 7> 이것은 현재 가장 많이 인용되는 model 로서 생체막의 성분의 이동성을 고려한 것으로 단백질을 주변단백질과 내재단백질로 구분하였다(그림 4· 33). 이 model 에서는 막의 유동성을 강조할 뿐아니라 이 성분이 비대칭 적으로 분포되어 있다고 가정하였다. 그러나, 앞서 이야기한 바와 같이 내재단백질은 세포골격에 의해 조처0 이 많이 되기 때문에 그림 4·34 와 같이 flui d - mosaic model 이 수정이 T리 었다. * 4 장 참고문헌 (1) Gort er , E. and Grendel, F. (1925) J Exp. Med. 41, 439-443. (2) Roth m an, J. E. and Lenard, J. (19 77) Sc ien ce 195, 743-753. (3) De Pie r re, J. W. and Ernste r , L. (1977) Ann. Rev. Bio c hem. 46, 201-262 (4) Lodis h , H. F. and Roth m an, J. E. (1979) Sci. Am. 240(1), 48-63. (5) Op den Kamp , J. A. F. (1979) Ann. Rev. Bio c hem. 48, 47-71. (6) Walte r , P., Gi lmo re, R. and Blobel, G. (1984) Cell 38, 5-8. (7) Wi ck ner, W. T. and Lod ish , H. F. (1985) Scie n ce 230, 400-407. (8) Mi lste i n , C., Brownlee, G., Harris o n, T. and Math e ws, M. B. (1972) Natu re New Bio l . 239, 117-120.
(9) Blobel, G. and Dobberts t e i n , B. (1975) ]. Ce ll Bio l . 6 7, 852- 86 2. (10) W ick ner,W . (1980) Sc ien ce 210, 861- 86 8. (II) Eng e lman, D. M. and Ste i t z, T. A. (1981) Cell 23, 411-422 (12) Edid i n , M. (1974) Ann. Rev. Bio p h y s . Bio e ng. 3, 179-201 (13 ) Cherry , R. J. (19 79) Bio c him , Bi op h y s . Acta 559, 289-327. (14) Frye , L. D. and Edid i n , M. (1970) ]. Cell Sci. 7 , 319-335. M Danie l l i, J. F. and Davson, H. (1935) ]. Cell Comp . Phys i o l . 5, 495-502. (16 ) Robert so n, J. D. The Ult ra str u ctu r e of Cell Membranes and Their Deri va- tive s, Bio c hem Soc. Sy m p o sia No. 16, Cambrid g e U. Press, London, 1959, 3-43. (11) Sin g e r, S. J. a nd Ni co lson, G. L. (1972) Scie n ce, 175, 720-731 .
제 5 장 생체막을 통한 물질의 확산 생체막의 가장 중요한 기능의 하나는 세포내에서의 여러 종류의 반응 들을 서로 독립적으로 진행하도록 하는 것인데, 이것을 위해서 세포 내 부와 외부가 격리되어야 할 것은 물론이고 세포 내에서도 mi toc hondria 나 lys o some 등의 소기관 내부를 세포질에서 격리시켜야 한다. 그러나 세포의 생존을 위해서는 외부에서 물질과 ener gy가 계속해서 공급되어야 하고 세포내에서 생성된 물질은 계속 밖으로 배출되어야 한다. 이 두 가 지 상반된 목적을 위하여 우선 생체막이 소수성 장막을 형성하여 물질의 이동을 저해하고 다음 생체막에 특수한 물질을 이동시키는 mechan i sm 이 이루어진다. 친수성인 물질들은 이들 특수한 mecha qi sm 을 통해 막을 통 과하지만 비교적 비국성인 물질들은 생체막을 직접 통과할 수도 있다. 생체막을 동한 물질의 이동은 다음 다섯 가지로 크게 구분된다. (a) 용해一확산 (b) 촉 진 화산 (facilitat e d dif fus io n ) (c) 구멍을 통한 이동 (d) 능동운반 (acti ve tra nspo rt ) (e) 대 량 이 동 (bulk movement) 이중에 (a), (b), (c) 은 본장에서 다루고 (d) 는 제 6 장에 설명되며, (e) 는 세포막 융합에 의한 것이어서 제 10 장에 포함된다.
5·1 용해-확산의 과정 용액내에서는 분자들이 열 ener gy에 의해서 계속 운동을 하고 있는 데, 용질이 농도계수 (concen t ra ti on gr ad i en t)의 존재 하에서 이 농도계수 룹 없애려는 방향으로 이동하는 현상을 확산 (d iff us i on) 이라고 한다. 이 확산의 칭량적인 표현은 F ic k 의 1 차 법칙에 의해서 ]=— D— aaxc (5-1) 이 식에서 J는 단위 시간동안 단위 면적을 통과하는 용질의 질량, C 는 농도, x 는 확산이 일어나는 방향의 거리, D 는 확산계수이다. 용매에 대 해서도 같은 식이 적용되며 2 성분 용액에서는 용매와 용질의 확산계수는 같다. 비 가역 열 역 학 (irr eversib l e the rmody na mi cs) 에 의 하면 확산계 수와 마찰 계수(fricti onal coe ffi cen t)사이에는 다음과 같은 관계가 성 립된다. D =綴 [l + C~ 전 ] (5-2) 여기서 N 은 Avo g adro 수, f는 마찰계수, y는 활성도계수 (ac ti v ity coe ffici en t)이다. 이 식은 붉은 용액에서는 (C->O) D= 隔 (5-3) 이 식에서 확산계수는 용질의 마찰계수(J)의 함수이고, 용질이 구형을 이루고 용매보다 훨씬 더 쿨 때에는 다음 S t oke 의 석에 의해서 f는 반경 r 에 비례한다. f= 67[7 Jr (5-4) 이 식에서 n 는 용매의 접도 (v i scos ity)를 표시한다. 식 5-3, 5-4 와 이 구 형의 부피의 입방근 (cub ic roo t)은 r 에 비례하고 부피는 분자량에 비례하 는 관계로부터
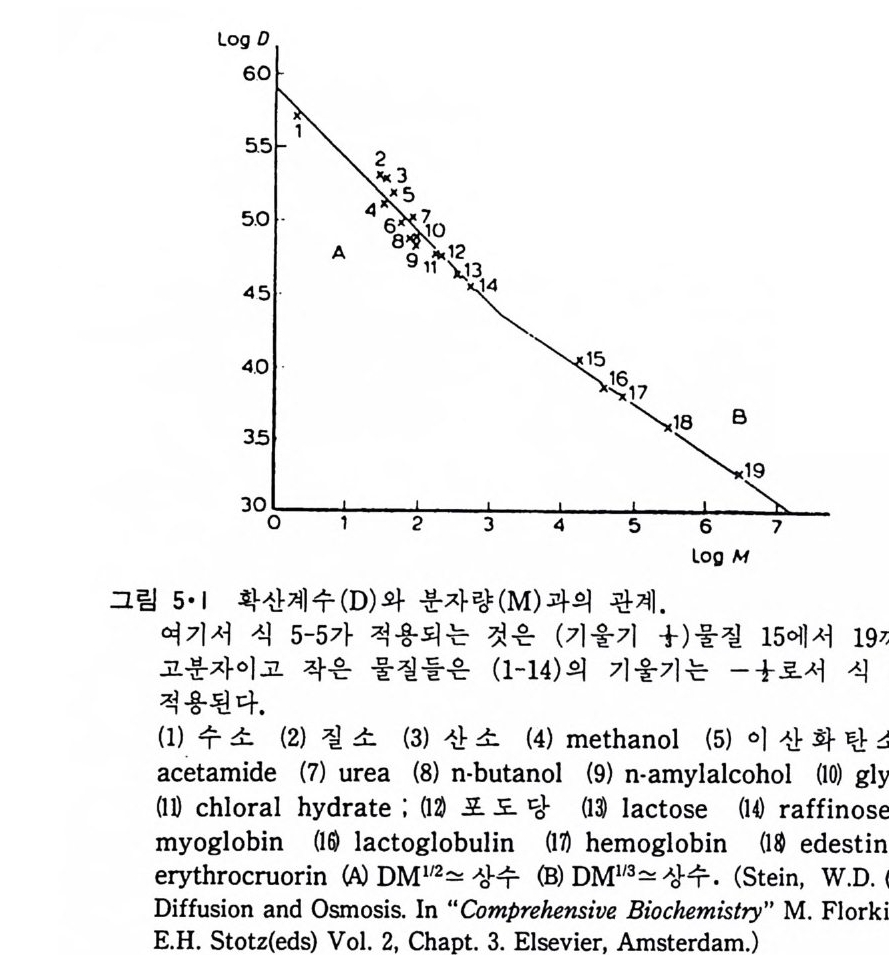 Log D
Log D
DMl/3 :::,e상수 (5-5) 그림 5·1 은 수용액에서 여 러 용질의 lo g D 와 lo g M 의 관계를 보인 것이 다. 이 그림에서 식 5-5 의 관계가 적용되는 경우는 용매 분자보다 훨씬 큰 단백질에 국한되는데 그 이유는 이들에게만 S t oke 의 법칙이 엄밀히 적용되기 때문이다. 작은 용질들에는 다음 실험식이 적용된다. DMl/2 :::::::상수 (5-6) 전해질 용액인 경우에는 양 i on(l) 과 음 i on(2) 의 이동도 (mob ility)차이 로 확산전위계수 (d iffu s i on po te n ti al gr ad i en t)가 생기는데 이들간의 관계는 다음 식으로 표시된다.
發ax =E:J 工 Ww2 너_- WW2I 4 dx (5- 7) 여 기 에 서 p는 전 위 (ele ctr i c a l po te n ti al ) , w 는 이 동도, 3 는 Farada y상수 이다. 용액 전체는 전기적인 중성을 유지해야 되기 때문에 양 i on 과 음 i on 은 갇은 속도로 이동하게 되며 그 확산계수는 다음 식으로 표시된다. D= 후N Ww1I+WW2 2 (5-8) 이 식에 w j =NA?/232 을 대입하면, D=재 ~+A g 효32 (5-9) 이 식 에 서 A 는 i on 당량 전도율 (conducti vi t y) 이 다. 생체막을 통한 물질의 이동일 경우 막의 두께가 불확실하므로 그 관계 식은 J= _P4C (5-10) 이 때 P 는 투과계 수 (pe rmeabil ity coeff ice nt) 로 P=D_l (5-11) 이 식에서 l 은 막의 두께이다. 용질이 수용액과 막상 (membrane p hase) 사이에 분배계수(p a rtiti on coef- ficc i en t) KP 를 갖는다면 그림 5·2 와 갇은 분배를 보여준다. 이때의 관계 식은 ]=— DK4PCz (5-12) 여기서, P=DKp/ l (5-13) 그림 5·3 은 이 식을 이용하여 Chara ceratip h y ll a 원형질막을 통한 여러가 지 비전해질의 두과계수를 o li ve 유와 뭍 사이의 분배계수에 대하여 도시 (plo t)한 것이다. 이 그림온 생체막 연구에 있어서 매우 중요한 실험결과 를 보여주는 것으로, 이로부터 생체막이 비국성 지방질로 구성되었다는
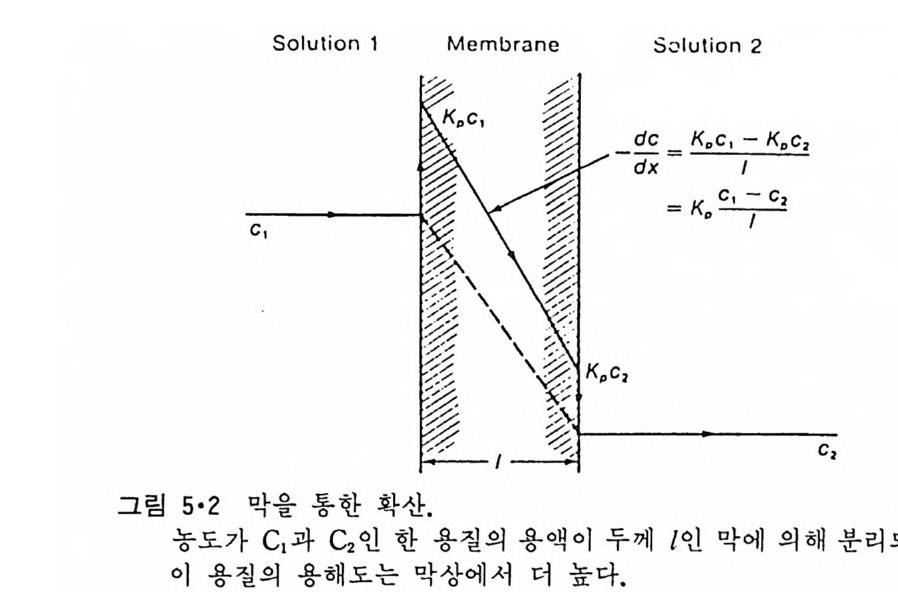 Soluti o n 1 Membrane S::l lu ti on 2
Soluti o n 1 Membrane S::l lu ti on 2
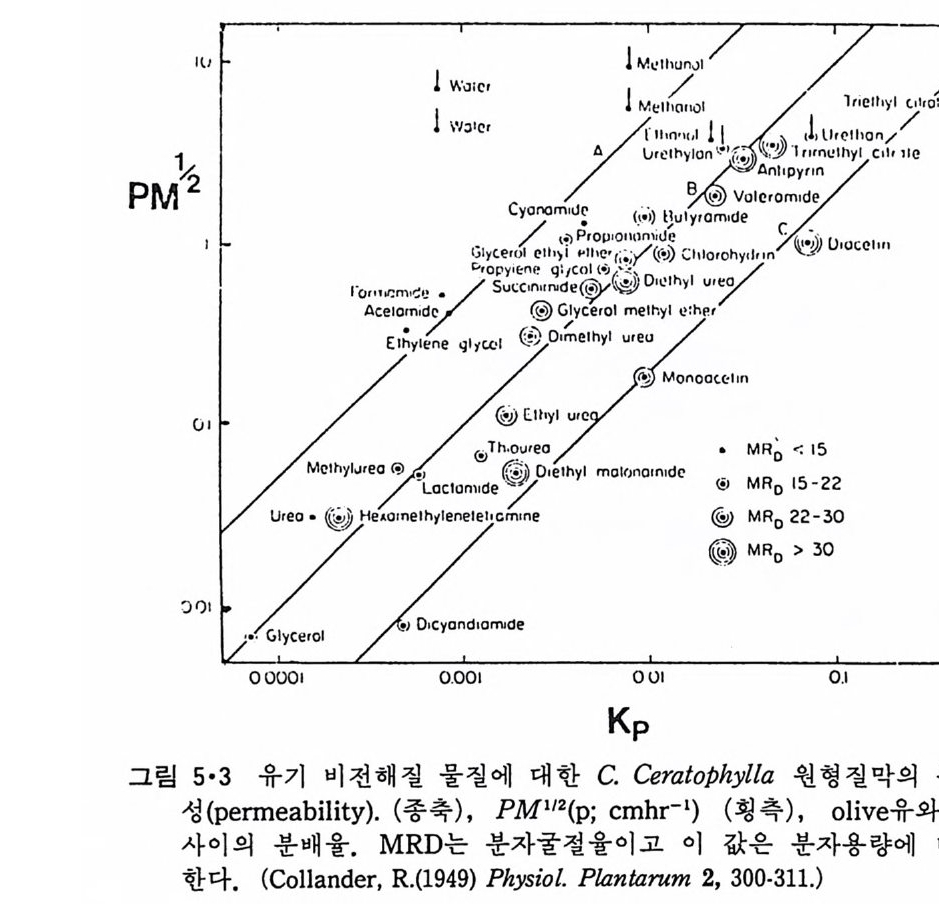 l I /근/l아 6 걸 `,
l I /근/l아 6 걸 `,
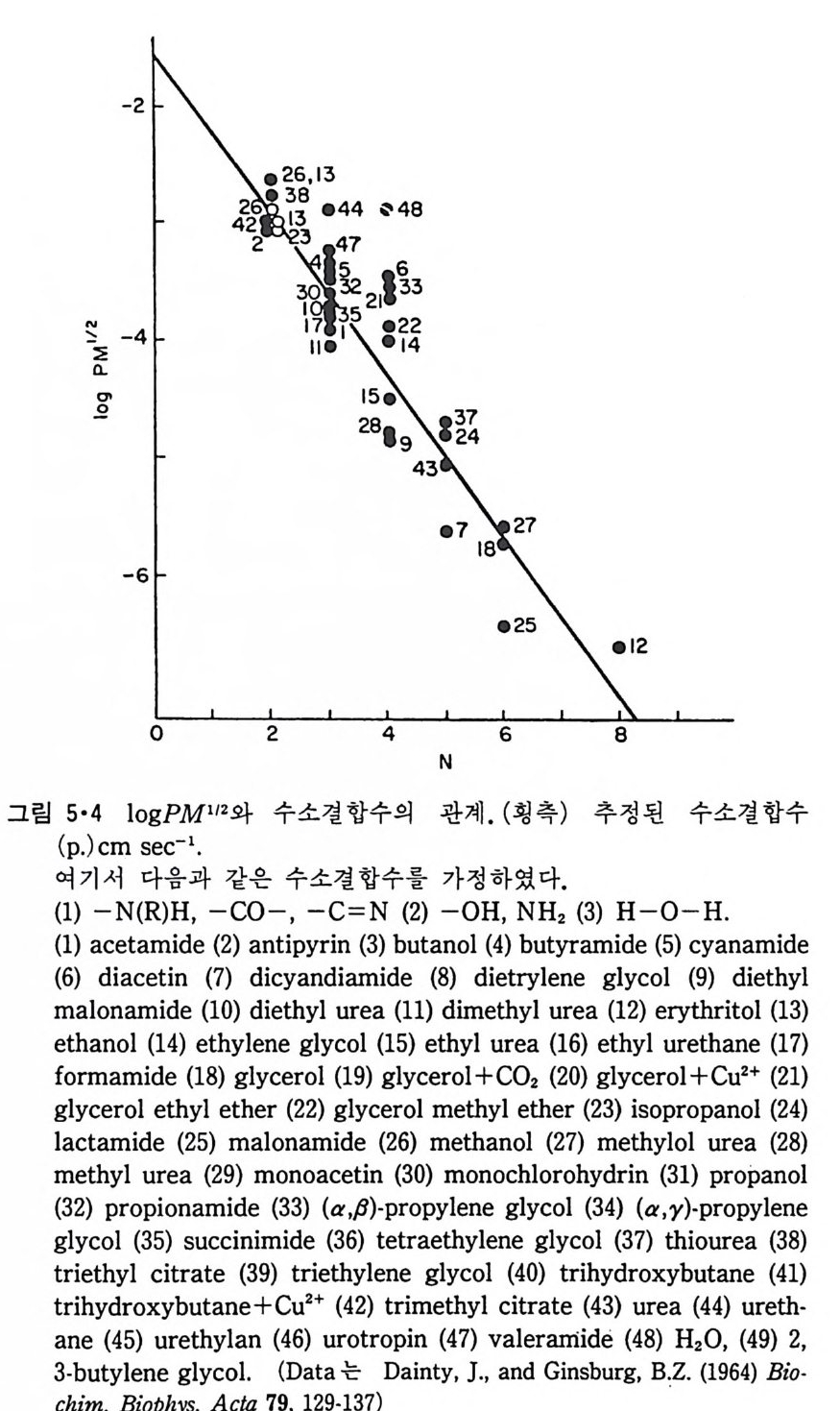 -2
-2
것을 알 수 있다. 식 5-6 과 식 5-13 에서 PM1 1 2ocKp 관계를 얻을 수 있어 이 그림에서 모든 점이 직선 근처에 분포되어 있는 것이 설명된다. 이돌 물질들의 투과속도는 광범위한 농도에서 농도차이에 비례하고 또 단백질 울 변화시키는 화합물에 영향을 받지 않는 것으로 인산지방질 이분자층 을 동한 확산이라고 간주된다. 물과 같이 칙선에서 많이 벗어나는 물질 은 구멍을 동해 확산이 이루어진다고 해석되고 있다. 위 물질들은 모두 물분자와 수소결합을 하고 있어 생체막의 소수성 내 부에 들어가기 전에 이 물분자를 떨어뜨려야 한다. 따라서, 물질의 투과 속도는 그 물질이 가지고 있는 수소결합의 수에 반비례할 것이 예상된 다. 그림 5·4 는 그림 5·3 에서 투과계수가 결정된 물질들의 lo g PM1'2 를, 그들이 수용액에서 물과 수소결합을 하는 수를 도시한 것으로 대부분의 화합물이 일직선 근처에 있는 것으로서 수소결합을 이루고 있는 물분자 룰 떨어뜨리는 것이 투과속도에 중요하다 것을 알 수 있다. 한편, 유사한 유기화합물인 경우 이들의 두과속도는 소수성 내부에 찰
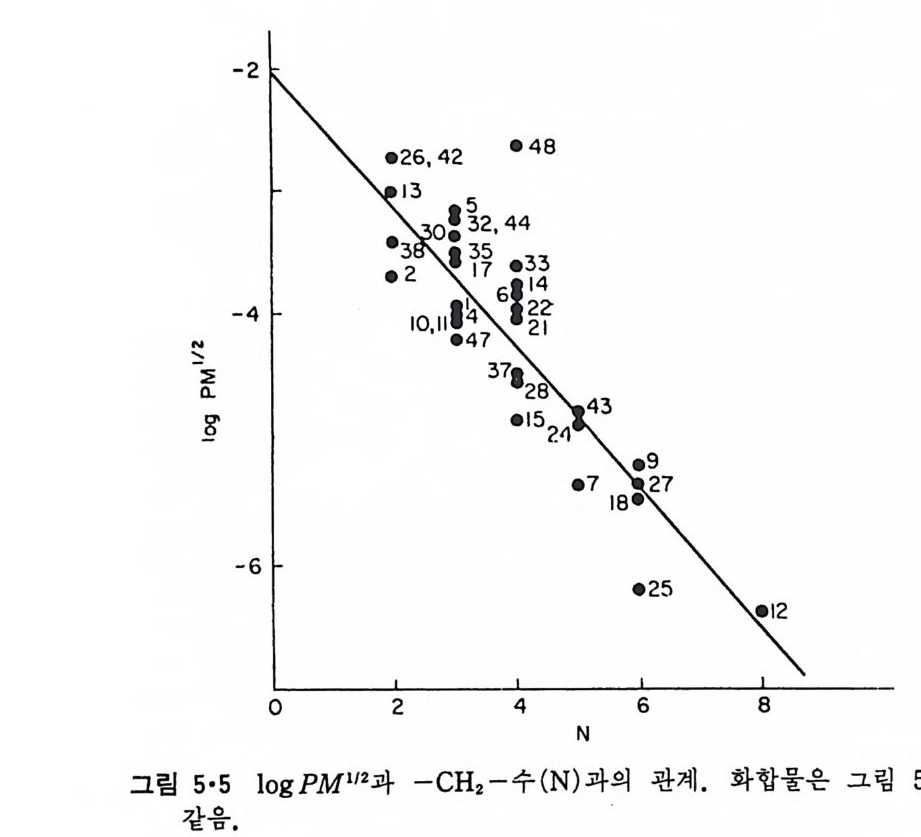 -2
-2
용해될수록, 즉 KP 가 쿨수록 크므로 화합물 분자 내의 e t h y lene 기의 수 에 따라 변할 것이 기대되는데 이는 그림 5·5 에서 잘 보여준다 . 이상의 결과는 비교적 비국성인 물질이 생체막을 통과할 때, 막 표면 에서 일단 수소결합을 하고 있는 물을 제거한 후 생체막의 소수성 내부 에 용해되고 확산에 의해 막을 동과하여 반대쪽 표면에서 다시 물과 결 합함으로써 막에서 떨어져 나가는 것을 보여준다. 이러한 mechan i sm 에 의 한 물질의 이 동은 비 교적 드물지 만 ste r oid hormone 등 몇가지 중요한 화합물들을 그 대표적인 예로 들 수 있다. 5·2 촉진 확산 (Facil itat e d dif fus io n ) 생리적으로 중요한 여러 물질들은 지금까지 고려한 바와 같은 용해적 ;L 산에 의한 과정으로는 설명할 수 없을 정도로 빠른 속도로 이동이 된다. 이의 가장 좋은 예는 포도당으로서 이 화합물은 5 개의 수소결합을 하는 OH 기를 가지고 있음에도 불구하고 계산한 PMl/2 값보다 약 l04 배나 되 는 투과속도를 갖고 있다. 이러한 과정을 촉진확산이라 하며 중성물질이 농도계수를 따라 이동되는 것과 하전된 i on 의 교환에 의한 이동 두 가지 가 있다. 5·2·1 포도당 (Glucose) 의 이동 2) 포도당의 촉진화산의 특정은, (a) 촉진확산의 원동력은 화학적전위기울기 (chemi ca l po te n ti al grad i- ent) 로서 농도차이 만이 필요하며 ener gy공급은 필요하지 않다. 그러 나 두과속도는 그림 5·6 에서와 같이 포화 k i ne tic s 에 따른다. (b) 화학적인 선택성이 엄격하여 이 수송과정은 이동되는 물질의 구조 에 민감하다. 예를 들어, D- 포도당 중에서 pyr anose 의 의자형 (chair fo rm) 에서도 Cl 형이 적혈구막을 동과하는 이동속도가 lC 형에서 보다 빠 르다(그림 5·7). (c) D-mannose, D-ga lacto s e, D-xy lo se 들도 적 혈구막을 동하여 어 느 정도 이동되며 D- 포도당의 이동은 이들 당분의 존재하에서 감소된다. 죽
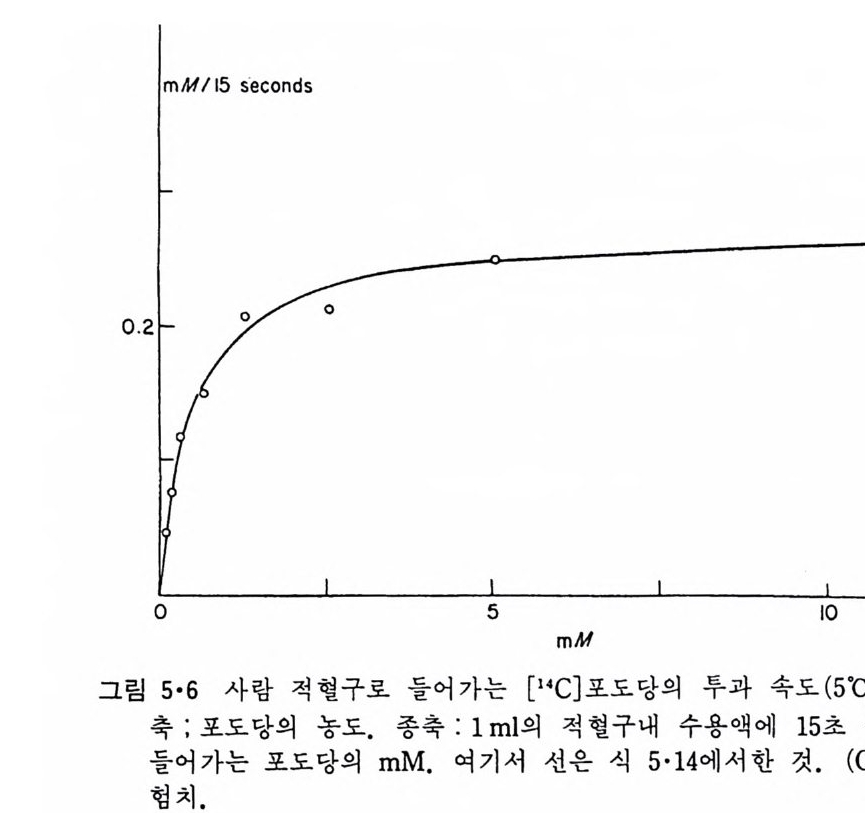 mM/ 15 s·e c onds
mM/ 15 s·e c onds
경 쟁 저 해 (comp etitive inh ib i t ion ) 의 성 질 을 나 타 낸 다. 예 를 들 면 , D -mannose 가 적 혈구의 안팎에 같은 농도로 존재 할 때 이 것 이 D- 포도당의 이동을 처해한다. 그러나, L- 포도당은 D- 포도당의 이동을 저해시키지 않는다.
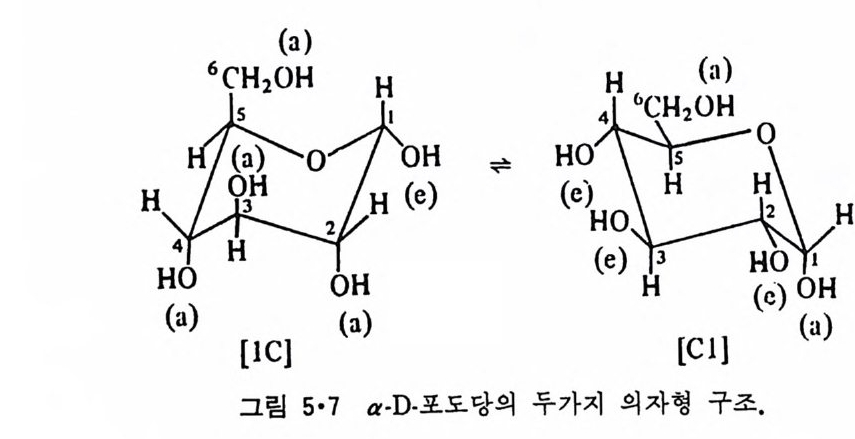 (a)
(a)
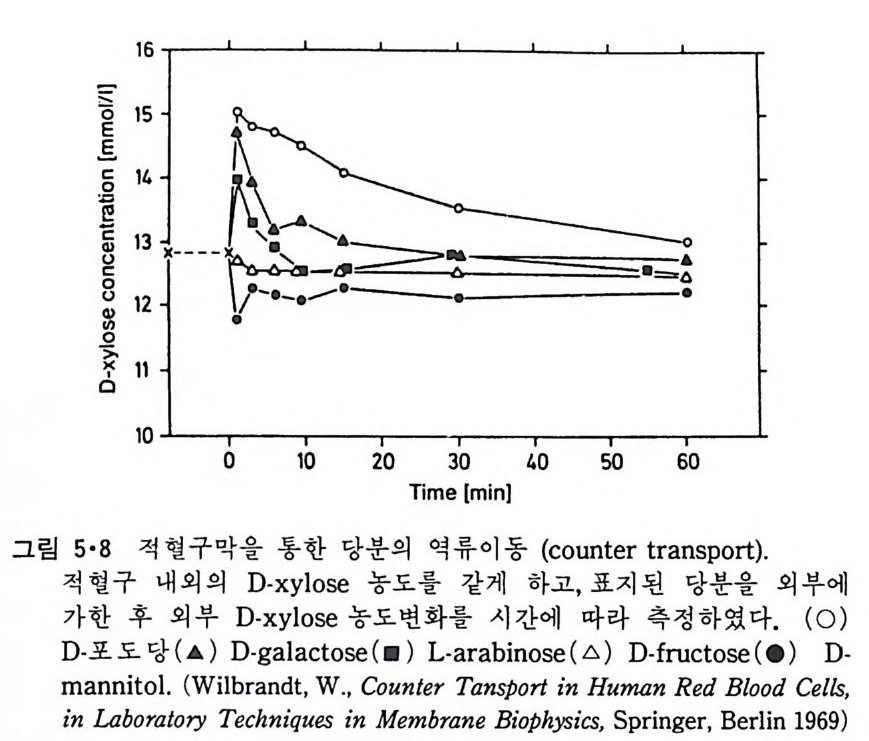 16
16
(d) 당류의 이동은 p hlore ti n 과 같은 구조가 전혀 다른 화합물에 의해 서 비 경 쟁 적 저 해 (noncomp e ti tive inh ib i t ion ) 를 받는다. (e) 당분의 이동은, 함께 존재하는 두번째 당분의 농도기울기 (concentr a ti on g rad i en t)에 의해서도 야기될 수 있다. 죽 적혈구막 안팎의 D-x y lose 의 농도가 같아도 밖에 D- 포도당을 첨가하면 D-x y lose 가 밖으 로 잠정 적 으로 이 동된 다. 이 러 한 이 동은 역 류수송 (counte r tran spo rt ) 이 라 고 불리며, 그림 5·8 은 적혈구막에서 몇가지 당분에 의한 D-x y lose 의 역 류수송을 보여준다. 외부에서 첨가해 주는 물질의 이동속도가 빠를수록 역류수송은 중가한다. 이상의 여러 현상을 설명하기 위하여 처음 제안된 것이 운반매체 (carr i er) 가설인데, 그림 5·9 는 이의 model 을 보여준다. 여기서 운반매 체 (E) 는 이동되는 물질 (S) 과 가역적으로 결합 (ES) 하여 막을 횡단한 후 반대표면에서 방출시킨다. 이러한 조건 하에서 일어나는 초기 이동속도 는 다음 식으로 표현된다. J= SV+mKSm (5-14)
 tJ- jH
tJ- jH
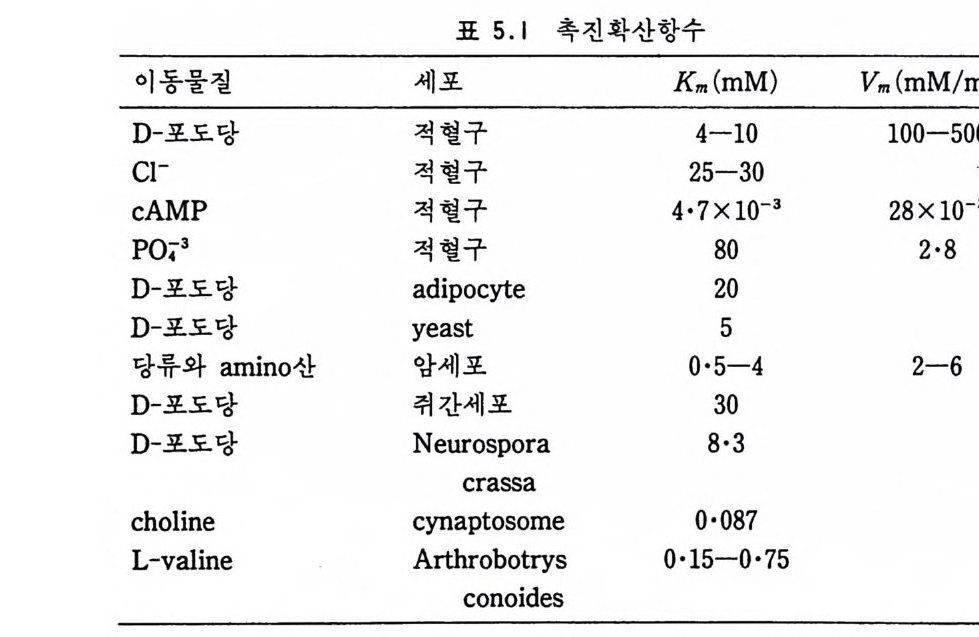 표 5.1 촉진확산항수
표 5.1 촉진확산항수
이상의 결과는 운반매체가설을 지지하지만 아직까지 생체막 내에서 이 동물질과 결합하여 확산하는 운반매체는 발견하지 못하였고 그 대신 내 재단백질이 촉진이동을 야기시킨다는 여러가치 중거가 늘어나고 있다. 즉 내재단백질과 이동되는 물질이 결합하여 단백질의 구조변형에 의해 막을 동과하는 것으로 생각된다. 촉진화산에 단백질이 관계된다는 것은 이 과정이 효소반응과 유사하다는 또 하나의 증거가 된다. 단백질이 포 도당 이동에 중요한 것을 여러가지 -SH 작용제에 의해서 이 기능이 저 해되는 것으로부터 알게 되었다. 특히 p-c hloro-mercurib e nzenesul- fon ate ( pC MBS) 같은 화합물은 적 혈구막을 두과하지 않는 ― SH 작용제 이 기 때문에, 이 작용제에 의해 포도당의 이동이 저해되는 것으로부터 적 혈구 외부에 존재하는 ― SH 기가 중요한 것을 알게 되었다. 적혈구막 단 백질 중에서 어느 것이 포도당을 이동시키는지를 결정하기 위하여 여러 방법들이 쓰여왔는데 그 중 중요한 것은 다음과 같다. 첫째는 포도당을 이동시키는 단백질을 기질 (subs t ra t e) 유사화합물이나 저 해 작용제 로 공유결 합 (covalent) 표지 시 키 는 것 둘째는 추출된 이 단백질과 D- 포도당이나 가역적인 저해제 cy to- chalasin B 둥을 반옹시 키 는 것 세번째는 적혈구막 단백질을 용해 분리한 후 지방질막소포에 재구성 시켜 D- 포도당을 이동시키는 단백질 성분이 무엇인가를 알아내는 것이 다. 아직도 적혈구의 어느 내재단백질이 포도당을 이동시키는지 확실히 결 정 된 것 은 아니 지 만 band 3 (M.W. 100 kDa) 와 band 4 • 5B (M.W. 55 kDa) 가 가장 가능성 이 높은 것으로 생각되고 있다. 그림 5·10 은 이들 단백질로 재구성된 막소포의 D- 포도당 이동성질을 보여준다. Band 4·5B 는 band 3 가 단백질가수분해효소 작용에 의한 분해 생성물인지의 여부가 결정되 어야 하고, 이들 단백질의 막 내부구조가 밝혀져야 D- 포도당의 이동 메 카니즘이 밝혀지게 될 것이다. 적혈구 포도당 수송단백질과 유사한 사람 Hep G2 hep a to m a 세포 수 송단백질의 am i no 산 서열은 결칭되었으며 그림 5·ll 은 이로부터 얻어진 소수성표수 p ro fil e 과 p ol yp e pti de 사슬의 막내배열의 model 을 보여준다. 492 개의 am i no 산기로 구성된 이 단백질의 12 개의 소수성 부분이 막을 동과하고 이중 몇 개의 양천성 나사선구조가 막 통로를 형성하여 포도당 을 통과시킨다고 생각되고 있다.
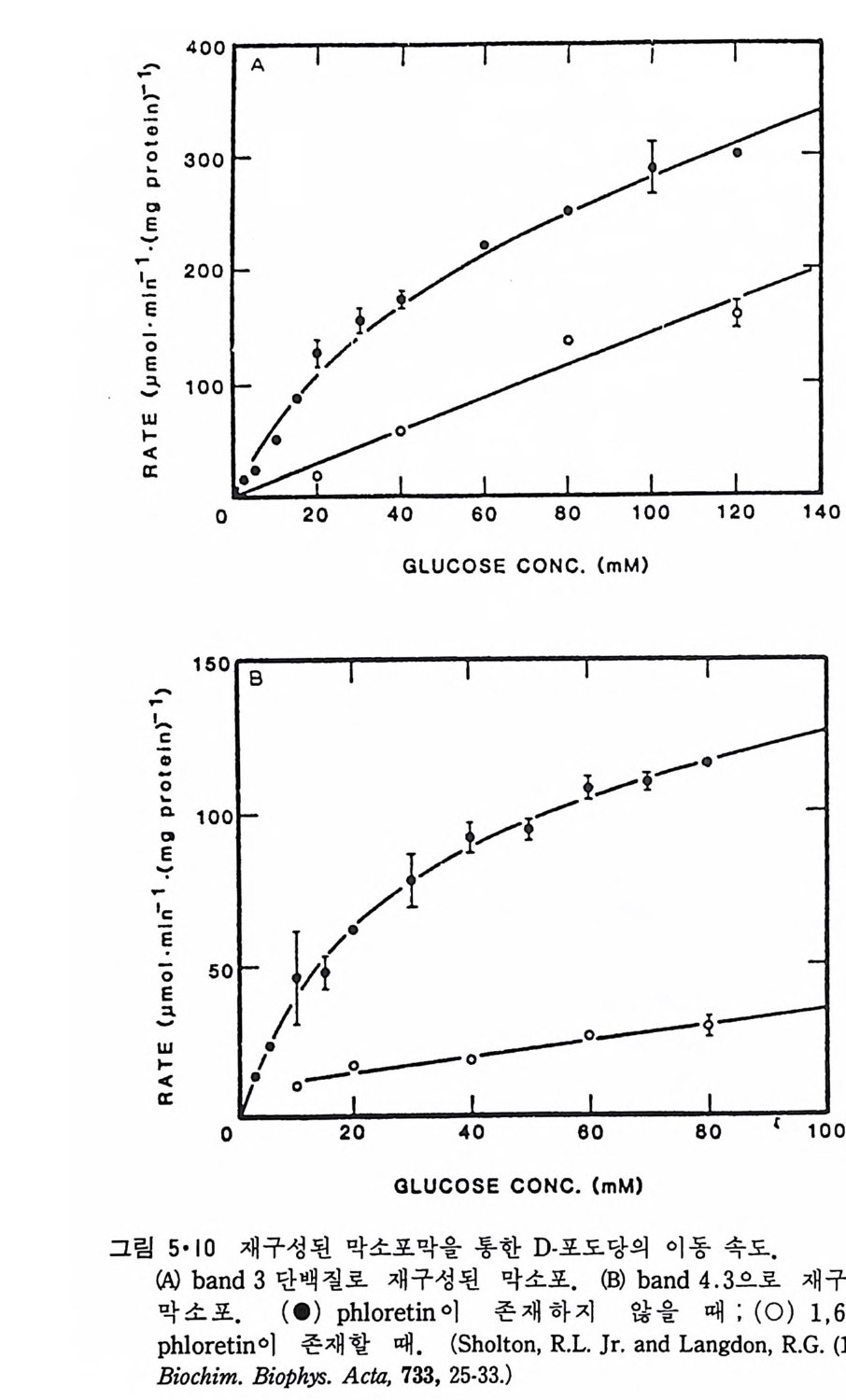 .^. 400 I A
.^. 400 I A
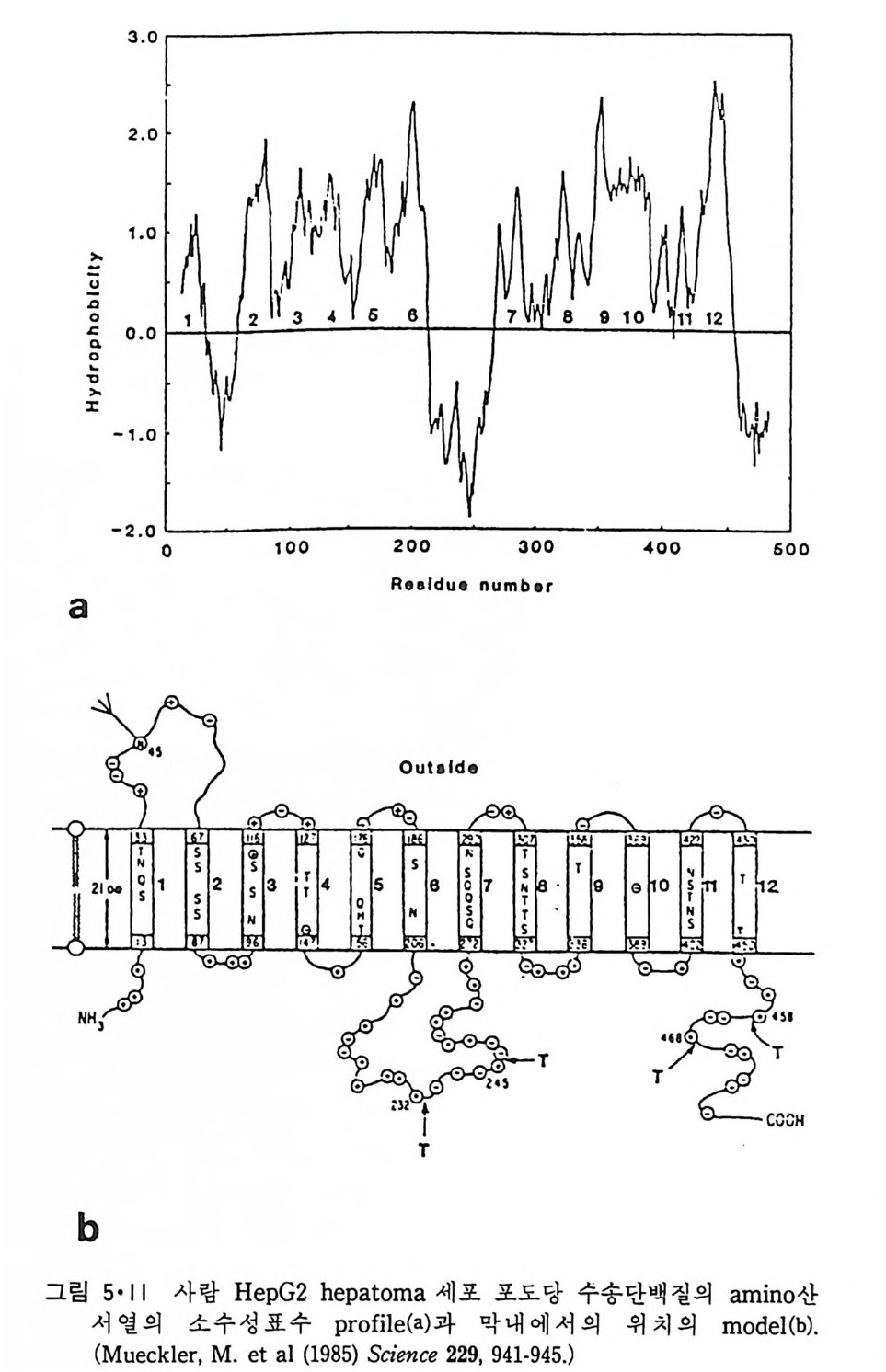 3.0
3.0
5 • 2 • 2 음 i on 교환 3 )4) 포도당의 촉진확산은 전기적으로 하전되지 않는 물질의 이동이지만, 하전된 음 ion 촉진확산 과정으로 운반될 수 있다. 이의 대표적 인 예가 적 혈구막을 통한 c1-동 음 i on 의 이 동으로서 이 i on 은 탄산 i on 과 1 대 1 의 교환촉진확산을 하며 이 과정은 생리적으로 중요하다. 적혈구가 조직 모세혈관을 통과할 때 HC03- 가 조직에서 적혈구 내로 들어가면 같은 mole 수의 Cl- 가 반대방향으로 이동되고, 이 적혈구가 허파 모세혈관에 도달되면 먼처와는 반대방향으로 이동되어 CO2 는 신체 밖으로 배출되게 된다. 적혈구막에서의 c1- i on 의 교환투과속도는 10-3cm/sec 로, 이 값은 지방 질막소포의 막을 동한 c1- 의 이동속도인 ~10-12cm/sec 에 비해 훨씬 높 으며 음 i on 둘의 루과속도의 순서는 Cl->F->Br->SCN->HCOi > 1-> sm- 이 다. 또 음i on 교환속도는 그림 5·12 에서 보여주는 것과 같이 포화 성 k i ne tic s 를 갖는다. 음i on 교환 역시 적혈구막에 존재하는 내재단백질에 의한 것임이 판명되었으며 공유결합 p robe 에 의한 표지로 band3 단백질 이 이에 가담하는 것이 밝혀졌다.
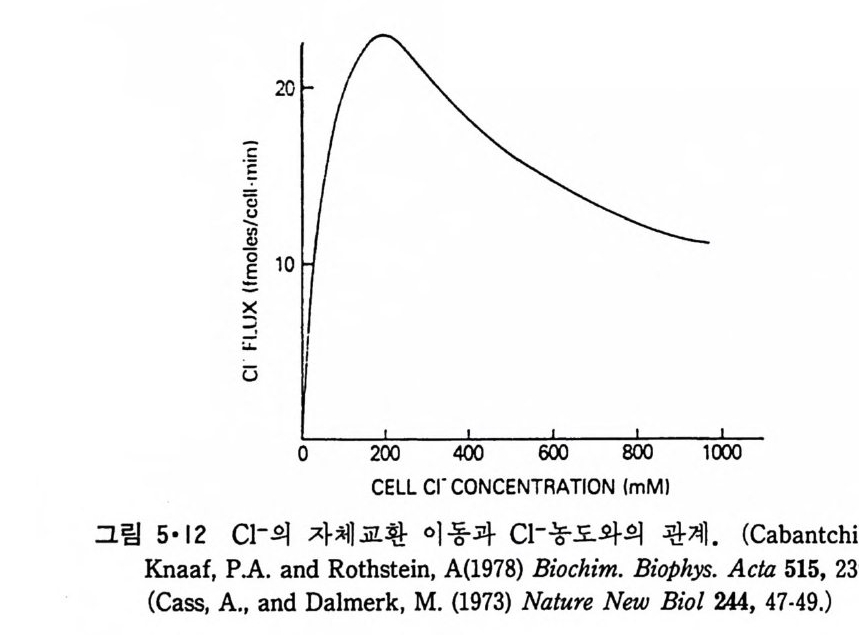 20
20
이 내재단백질을 지방질막소포에 재구성시키려는 시도는 많이 이루어 져 왔으나 아직까지는 부분적인 성공에 그치고 있다. 5·2·3 ATP/ADP 교환 5) 구) ATP 와 ADP 의 교환은 먼저 이야기한 음i on 교환때와는 달리 교환되는 음i on 의 전하값이 다르다. M it ochondr i a 의 ma t r i x 에서 ATP 가 합성되어 세포질로 이동되는 것은 세포질에 있는 ADP 와 교환됨으로써 이루어진 다. 세포질에서의 [ATP]/ 〔 ADP 〕값은 항상 ma t r i x 보다 높지만 ATP 가 밖으로 교환되어 나오게 되는 이유는 m it ochondr i a 내부막에서 일어나는 전자이동에 의해 ma tri x 의 p H 가 높아져 외부에 비해 더 많은 음성하전 올 갖게 되기 때문이다. 그래서 이 교환이동은 능동운반 (ac ti ve t rans p o rt) 으로도 보이나 이 이동 s y s t em 을 통해서 ATP/ADP 와 ADP/ADP 교환 도내 재신 속단히 백 질일 어의 나므분로 리 촉는진 확(35산 s으 〕 C로AT (간c주ar되bo고x y있햐 다m. 야 짜이 a 떠A와T P/A(35D sP] A교 T환R (a t rac ty la t e) 를 이용하여 이루어졌으며 SDS- g el 전기영동으로 얻은 분자 량은 약 29 kDa 이 었고 Seph a rose 6B chroma t ogra p h y로는 약 65 kDa 정 도를 얻었다. 그래서 m it ochondr i a 의 내부막의 ATP/ADP 교환단백질은 2 합체 (d i mer) 로 존재하는 것을 알 수 있다. 5·3 구멍을 통한 확산 내재단백질이 촉진확산을 추진시킨다는 것은 여러가지 실험적 증거에 의해 확실하다고 볼 수 있는데 그 mechan i sm 은 아칙 해명이 되지 않았 다. 이들 단백질 자체가 이동하여 물질을 수송시키는 운반매체 mechan i sm 은 일어나기 힘든 것이므로 두 개 이상의 소단위 사이에 존재 하는 구멍을 동한 이동의 가능성이 더 크다고 생각된다. 물질이동에 가 담하는 단백질들이 항상 여러 개의 소단위 (subun it)로 구성되어 있는 것 도 이것을 지지하는 것이다. 이 소단위들로 구성된 구멍은 작으므로 물 분자로 차 있을 가능성은 작으나 명개의 s y s t em 에서는 큰 구멍이 존재하 여 비교적 큰 분자까지 통과시킬 수가 있다. 이의 대표적인 예가 Gram
음성 세균의 외부막에 존재하는 p or i n 과 간격 연접 (ga p j unc ti on) 에 있는 connexon 이다. 그리고 d ip h t her i a 독소, comp le ment 둥의 수용성 단백질 들은 숙주세포 (hos t ce ll) 생체막에 부착되어 잠정적인 구멍을 형성한다. 5 • 3 • 1 Porin8 > 9> Gram 음성세균의 외부막에는 분자량이 600 인 물질까지 자유로이 통과 시키는 구멍이 존재한다. 이 외부막에서 그림 5·13 과 같은 lrun 직경의 구멍을 직접 볼 수 있다. 이 구멍들은 내재단백질인 p or i n 으로 구성되어 있으며 아는 3 합체(t r i mer) 의 6 각형 격자(l a ttic e) 를 구성한다. 그림 5·13 에서 3 개의 neg a ti ve s t a i n 으로 채여진 구멍이 함께 모여 있다. Gram 음 성세균의 외곽평면과 수직이 되는 각도로 전자회절을 하면 막 내에서의 p or i n 의 입체구조를 관찰할 수 있으며 그 결과는 그림 5·14 에서 보여준 다. 외부에 가까운 충에서 (A) 따로 존재하는 3 개의 구멍이 막간공간 (pe rip la smi c s p ace) 으로 가면서 (D) 하나로 융합되어 p or i n 구멍의 복잡성을 보여준다. Por i n 을 세 탁제 로 생 체 막에 서 용해 정 제 하여 침 강평 형 (sedim enta t i on e q u ili br i wn) 방법으로 측정한 분자량은 약 lOOkDa 이고 이것을 열처리하여 얻는 p ol yp e pti de 의 분자량은 32~36kDa 이기 때문에 막 내에서 3 합체로 존재한다고 생각되고 있다. 이 단백질을 지방질막소포에 재구성하여 뭉 질이동의 성질을 연구한 결과에 의하면 구멍이 형성되는 것은 막 전위차 (membrane p o t en ti al) 와 p H 에 좌우된다.
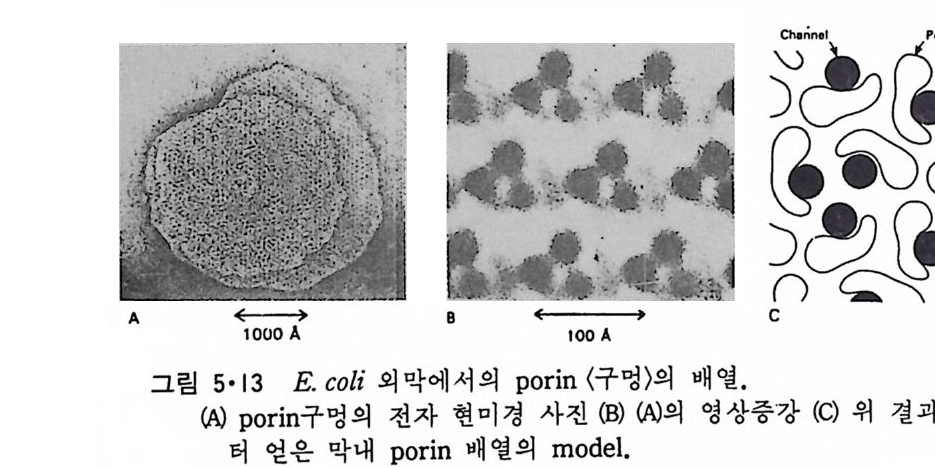 Channel Po rin t
Channel Po rin t
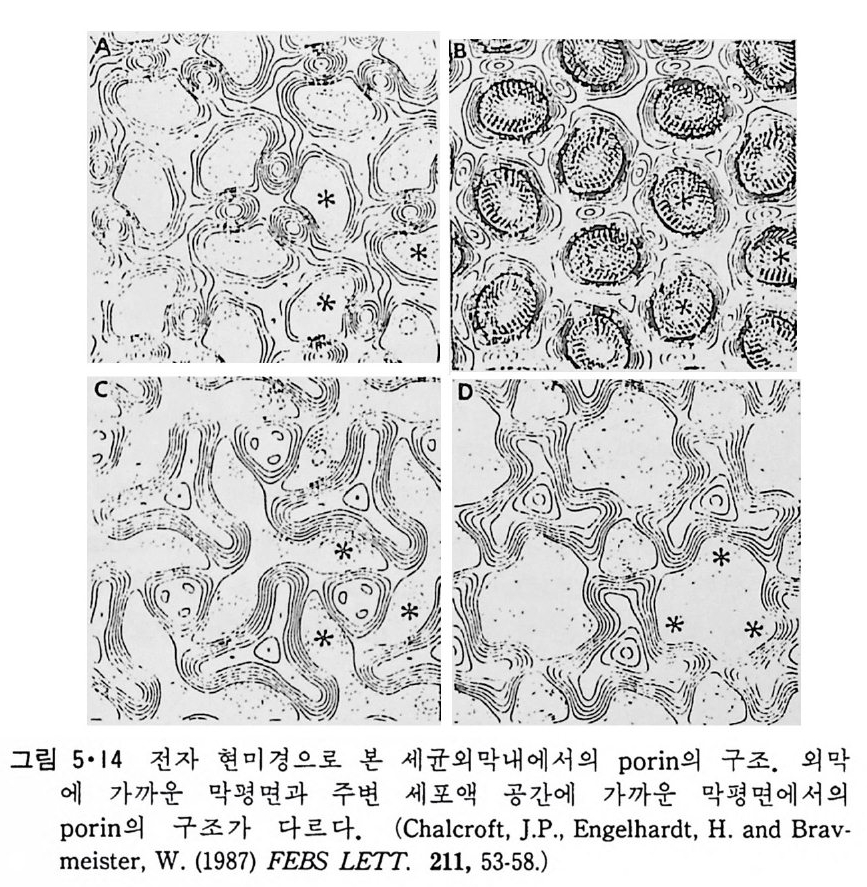 그림 5•14 전자 현미경으로 본 세균의막내에서의 p or i n 의 구조. 외막
그림 5•14 전자 현미경으로 본 세균의막내에서의 p or i n 의 구조. 외막
5·3·2 Connexon10>11> 진핵세포에서 가장 찰 알려져 있는 막구멍은 간, 내장, 신장, 두뇌 그 리고 근육세포 사이를 연결하는 간격연접(g a pj unc ti on) 이다. 그림 5·15 는 간격연점막에 존재하는 connexon 의 배열과 이들이 형성하는 구멍들을 보여준다. 간격연접에는 connexon 이 농축되어 있어 세탁제로 처리해 다 른 단백질들을 제거한 후 X- 선 회절과 전자회절로 그 구조연구가 광범위 하게 이루어졌다. 그림 5·16 은 간격연정에서 두 인접된 원형질 사이의 간격은 약 30A 정도가 되며 한 원형질막을 횡단하는 connexon 이 인접 해 있는 원형 질막의 connexon 과 서로 연결된 것을 보여준다. 이 렇게 형 성된 동로 (channel) 는 한 세포에서 인접하여 있는 세포로, 분자량이 1000 까지의 천수성 분자를 몽과시킨다. 각 connexon 은 6 개의 소단위
 {a) (b)
{a) (b)
(subunit ) 인 connex i n 이 회 합하여 중간에 구멍 을 형 성 한다. Connexon 의 분자량은 취 간인 경 우 약 26kDa 이 다. Connexon 으로 형 성 된 구멍 의 직 경은 약 10A 이 되지만 이는 막 전위차, pH 그리고 Ca2+ 농도에 따라 변
 그림 5•16 X- 선 회전실험으로 얻은 간격연정의 구조(취간세포).
그림 5•16 X- 선 회전실험으로 얻은 간격연정의 구조(취간세포).
 a b
a b
한다. 그림 5·17 은 Ca2+ 이 존재할 때와 없을 때의 구멍의 모양을 보여준 다. 5·3·3 구멍을 형성하는 수용성 단백질 여러 수용성 단백질독소(t ox i n) 가 생체막에 구멍을 형성하는데, 전장에 서 이미 me litti n 의 예를 들었다. 또 하나 바교적 연구가 많이 된 것은 d ip h t her i a 독소로 이 단백 질 이 지 방질 이 분자층과 접 촉하면 전 압차의 존 재하에서 음i on 을 전달시킨다. 이 음i on 의 이동은 p H4 와 4·9 사이에서 가장 많이 일어난다. 이 단백질의 소수성 부분만으로 구성된 po lyp eptide 는 지 방질 이 분자층에 큰 구멍 을 형 성 하여 octa s acchari de , r-cyc l odex- t r i n 과 po lye t h y le ne gly c o l, PEG 1500 까지 도 투과시 킨다. 5·4 Ion 운반물질 12),13) 자연에 존재하는 많은 화합물과 합성된 화합물은 생체막과 지방질 이 분자층에서 i on 을 신속히 이동시킨다. 이들 화합물에 의한 이동 mechan i sm 의 해 명 은 생 체 막에 서 여 러 가지 분자와 i on 이 이 동되 는 과정
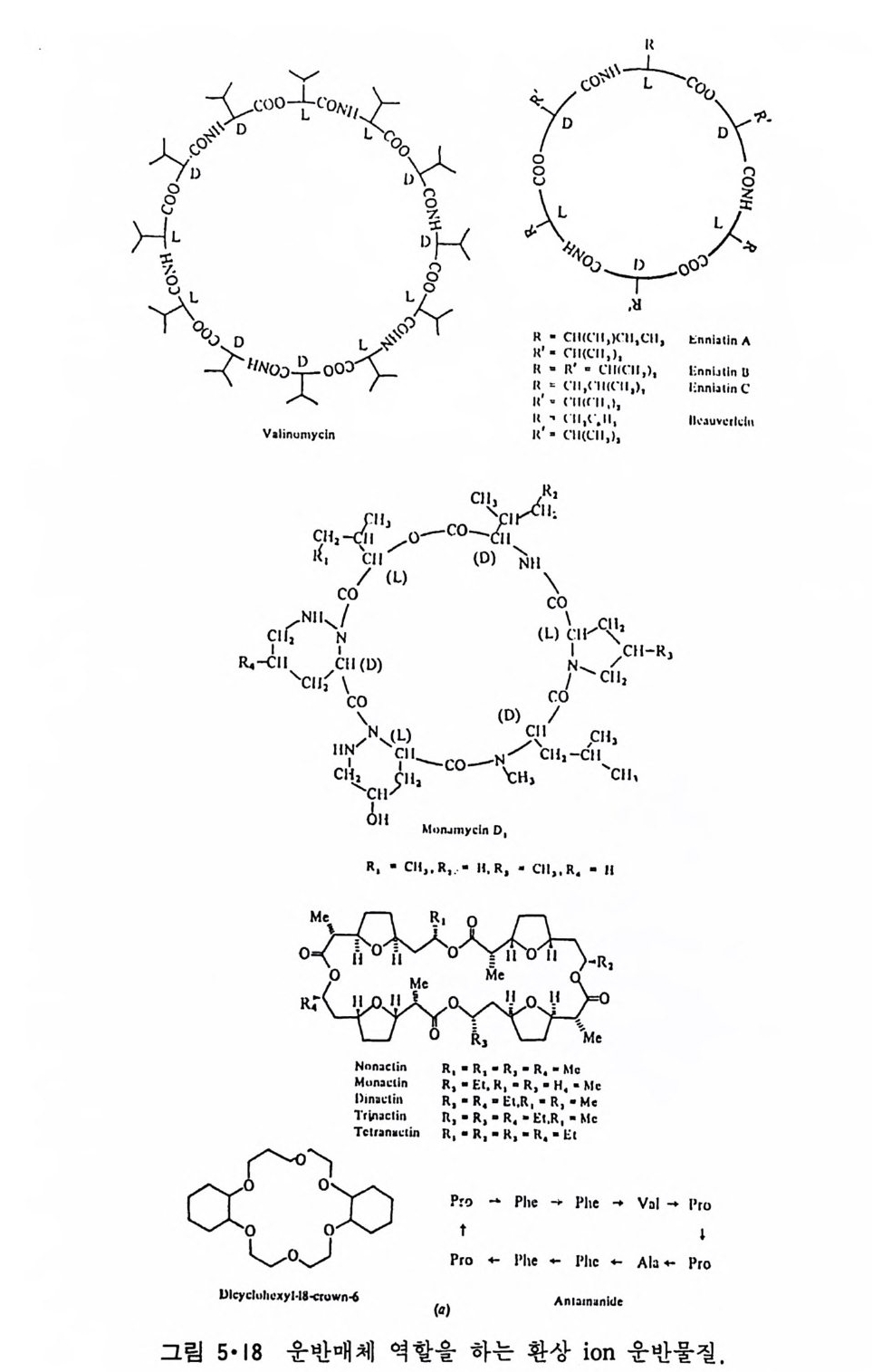 강우今°〈 0u01 . oD: 수多尸 D LCo%+> cO0O A 3W. L L\l8ll:JLDN난°z宁g ~oco; 0 X +>IIk>
강우今°〈 0u01 . oD: 수多尸 D LCo%+> cO0O A 3W. L L\l8ll:JLDN난°z宁g ~oco; 0 X +>IIk>
의 해명에 도움이 될 것이다 . 이 렇게 i on 들을 이동시키는 화합물을 i on 운 반물질(i ono phore ) 라고 부르는데 이들을 크게 나누어 두 종류로 볼 수 있 다. 그 중 하나는 운반매체의 역할을 하는 것이고 다른 하나는 지방질 이분자층에 구멍을 형성하는 화합물 이다. 5·4·1 운반매체 (Carrie r ) 운반매체 역할을 하는 i on 운반물 질 은 그림 5·18 에 서 보이는 것과 같이 환상 (c y cl ic)구조를 갖는 것과 그림 5·19 에서와 같이 열린 구조를 갖는
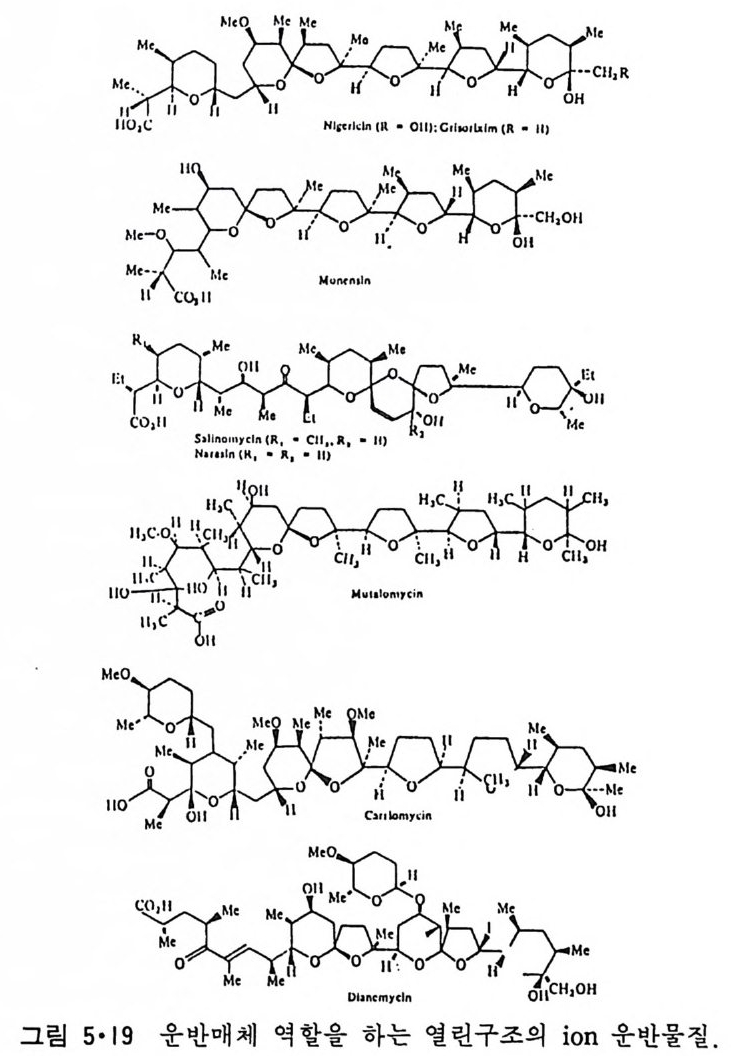 le
le
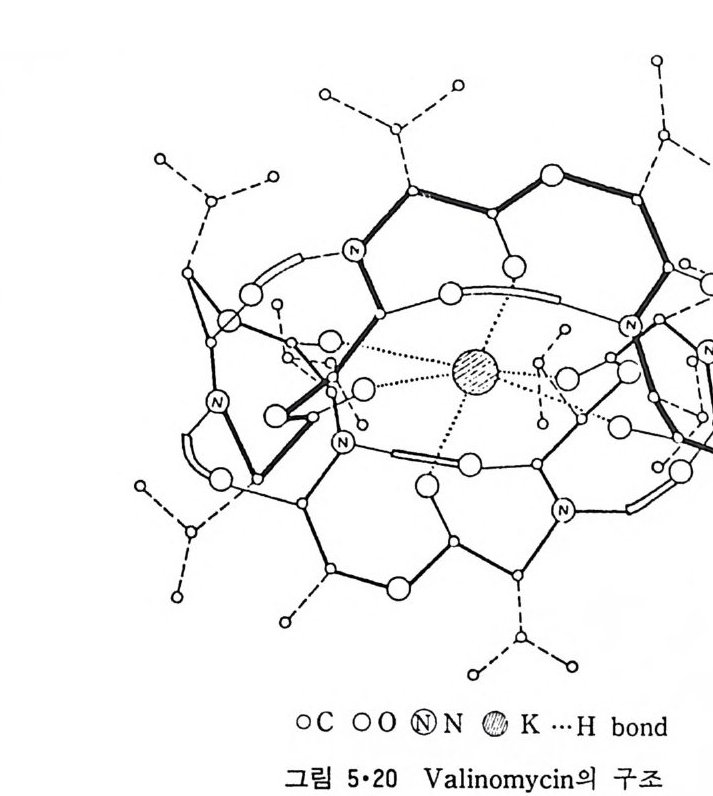 o'
o'
것이 있다. 이 두 종류의 i on 운반물질들은 i on 과 결합하여 확산과정에 의해 신속히 지방질 이분자층을 두과하여 반대표면에 도달하면 i on 을 해 리하여 방출한다. 이들 중에서 제일 연구가 많이 된 va li nom yci n 의 구조 는 X- 선 굴철 결과에 의하면 그림 5·20 과 같다. 이 화합물은 3 개의 L -valin e ➔ D-a-hy d roxy va li c acid ➔ D-vali ne ➔ L-lacti c grou p 이 반 복 된 환상 구조를 갖는데 , 6 개 의 pe p tide bond 와 6 개 의 este r bond 로 구성 되 어 있다. 이 분자는 높이가 4A 이고 직경이 8A 인데 peptide 결합의 분자 내 수소결 합에 의 해 그 구조가 안정 화되 며 6 개 의 este r bond 의 산소가 중심부를 향하여 반경이 1·4A 인 구형을 형성한다. 그래서 이 구형의 공 간에 K+(l·33A .) 또는 Rb+(l·45A) 이 쉽게 들어갈 수 있고 cs+(1·69A .) 도 어느칭도 들어갈 수 있으나 Na+ (0 •95A) 과 Li +(0·6A) 은 너무 작다. 그래서 선택성의 순서는 Rb+>K+>cs+>Na+> Li+가 된다. 이들 양 ion 들이 이동될 때에는 수화 (h y dra ti on) 된 뭉분자들을 벗은 후 vali no my cin 내부 공간에 들어갈 수 있고, 한편 이 분자의 소수성기는 전부 외부를 향하고 있어 i on 들을 가진 채로 지방질에 잘 녹아 들어간다.
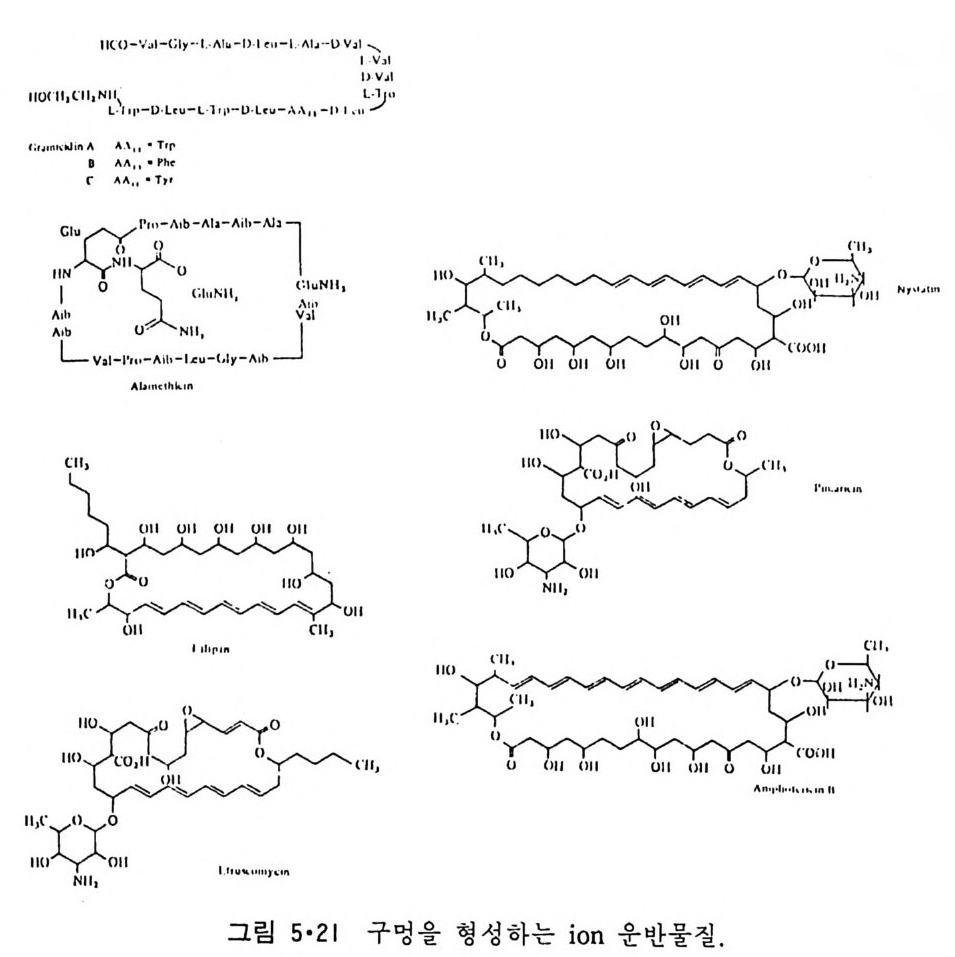 IK( )-,Ja I -'··l . . ^' -Il· l e ,, - I .. AI 』 - O WII , V,1
IK( )-,Ja I -'··l . . ^' -Il· l e ,, - I .. AI 』 - O WII , V,1
5·4·2 구멍 (Pore) 구멍을 형성하는 i on 운반물질의 구조는 그림 5·21 에 보여주고 이 중에 서 amp h ote r ic in B 의 분자모형은 그림 5·22 에 보여준다. 이 화합물은 소수성 사슬과 양천성 (amp h ip h il ic) 인 사슬이 융합된 환상의 ior i 운반물질 로서 그림 5·22 에서 보이는 것과 같이 양천성 사슬의 한쪽 면온 소수성 이고 그 반대쪽에 친수성 면을 갖는다. 그리고 이 분자의 한쪽 끝에는 am i no 당분과 ― COOH 기가 있고 이와 반대되는 끝에는 -OH 기가 하나 존재한다. 이 분자가 생체막에 들어가면 그림 5·23 에 보여주는 것과 같 은 복합체를 형성한다고 생각된다. 아 분자들이 회합하여 환형을 이룰
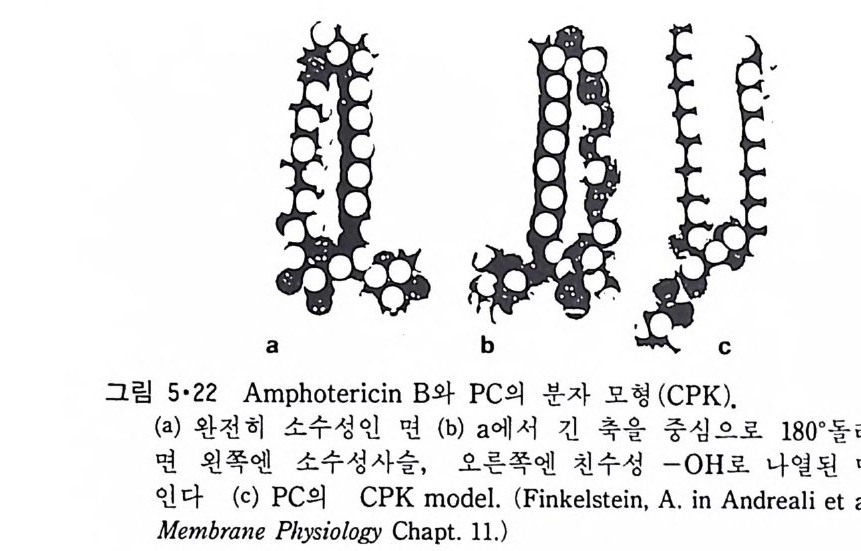 a b
a b
때 각 분자의 소수성 사슬이 다음 분자의 양천성 사슬의 소수성 표면과 접촉하고 친수성 표면이 내부 를 향하여 구멍을 형성하게 되는데 소수성 기들이 구멍 밖으로 향하여 지방질 이분자층 내부엔 들어갈 수 있다. 그 링 5·22 에 보이는 PC 의 길이가 amp h ote r ic in B 의 길이와 유사하며 그림 5·23 의 구멍은 지방질 이분자층의 반, 즉 단층을 차지할 것이고 이분자 층의 반대쪽에서 .시작된 같은 구멍의 반이 -OH 기의 수소결합에 의해 연
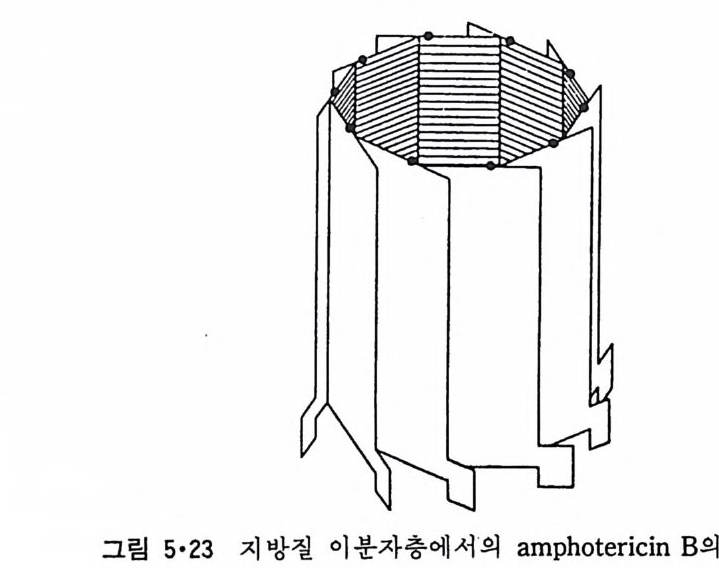 그림 5 • 23 지 방질 이 분자층에 서 의 amp h ote r ic in B 의 구조.
그림 5 • 23 지 방질 이 분자층에 서 의 amp h ote r ic in B 의 구조.
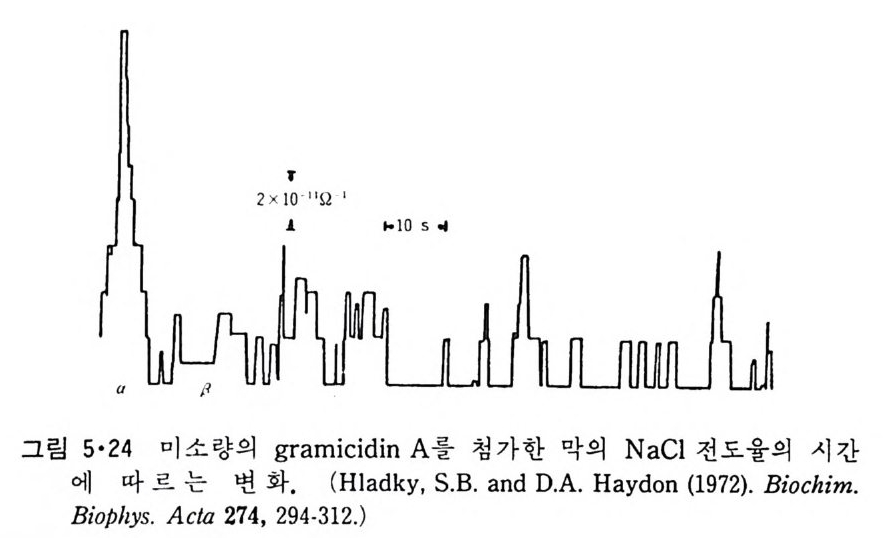 1'
1'
결되면 이분자층을 횡단하는 구멍이 된다. 이렇게 생긴 구멍은 그 칙경 이 4A 정도여서 포도당보다 큰 분자는 통과시키지 않는다. 또 i on 의 두 과속도가 amp h ote r i cin B 의 농도의 4~12 승에 따르는 것으로 이 분자가 막 내부에서 4~12 개의 분자가 회합되어 구멍을 형성한다는 것을 알 수 있다. Grami cidi n A 가 지방질 이분자층에 구멍을 형성하는 것은 시간에 따 르는 i on 의 전달성의 변화로부터 추측할 수가 있다. 그림 5·24 에서 보는 것과 같이 이 i on 운반물질이 미량이 존재할 때 낮은 전압에 의한 전달성 의 변화는 최소 단위의 몇 배가 된다. 이때에도 주어진 전압에 의해 통 과되는 i on 의 수가 운반물질에 의해서 이루어지기에는 너무 커서 구멍이 생 성 된 다고 해 석 된 다. 또 투과계 수는 gram i cidi n A 의 농도의 자승에 비 례하는 것으로 보아 두 개의 분자가 회합하여 구멍을 형성한다고 생각되 었다. Grami cidi n A 로 구성된 구멍은 .:Z. ion 선택순서가 H+>NH t >C$ 之 Rb+~K+>Na+> Li+으로 구멍의 크기와 이 분자의 길이로부터 직경이 냐인 군 (L,D) 나사선을 형성한다고 제안되었다. 두 개의 나사선이 회합 하여 구멍을 형성할 때에는 그림 5·25 에 보이는 4 가지 가능성이 있는데 여러가지 실험 결과에 의해 C- 말단이 외부에 노출된 첫번 째 모형이 맞 는 것으로 판단되었다. 그림 5·21 에서 보이는 것과 같이 gram i cidi n A 는 D-am i no 산과 L-am i no 산이 교대로 연결된 po lyp e p tide 사슬로서, 소수 성 환경에서 길이가 2·5~3m 가 되고 나사선를 형성한다. Grami cidi n A
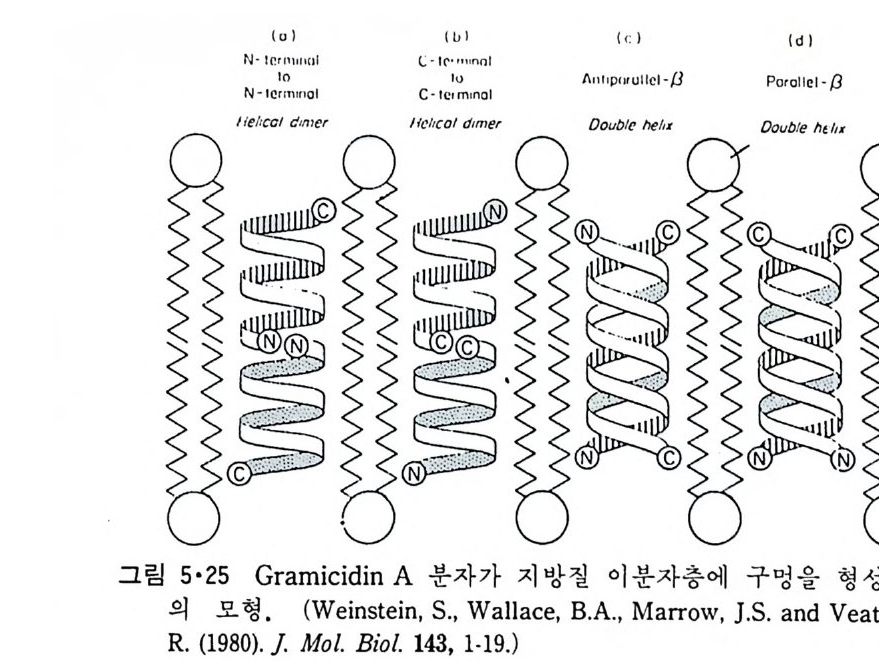 (u I Ibl I( ) (d I
(u I Ibl I( ) (d I
와 Cs+ i on 과의 복합체를 유기용매로 부터 결정을 얻어 x- 선 회절 실험 을 통해 얻어진 구조가 그링 5·26 에 보여준다. 여기서 이 i on 운반물질은 내경이 4A 정도되는 구멍을 가진 나사선구조를 갖 고 있으며 천수성 am i no 산기는 구멍쪽으로 배열되어 있고 소수성 am i no 산기들은 외부로 향해 막 내에 있는 지방질의 ac y l 사술과 접촉할 수가 있다.
 a
a
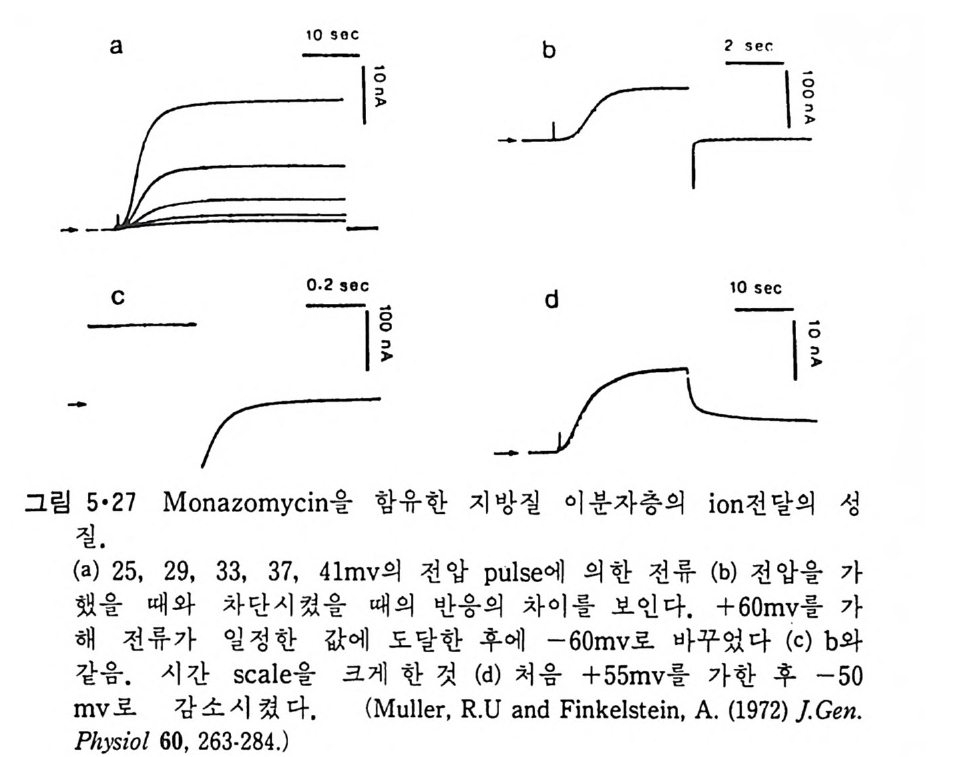 a .' O 广― -b /广 2 se r. |:
a .' O 广― -b /广 2 se r. |:
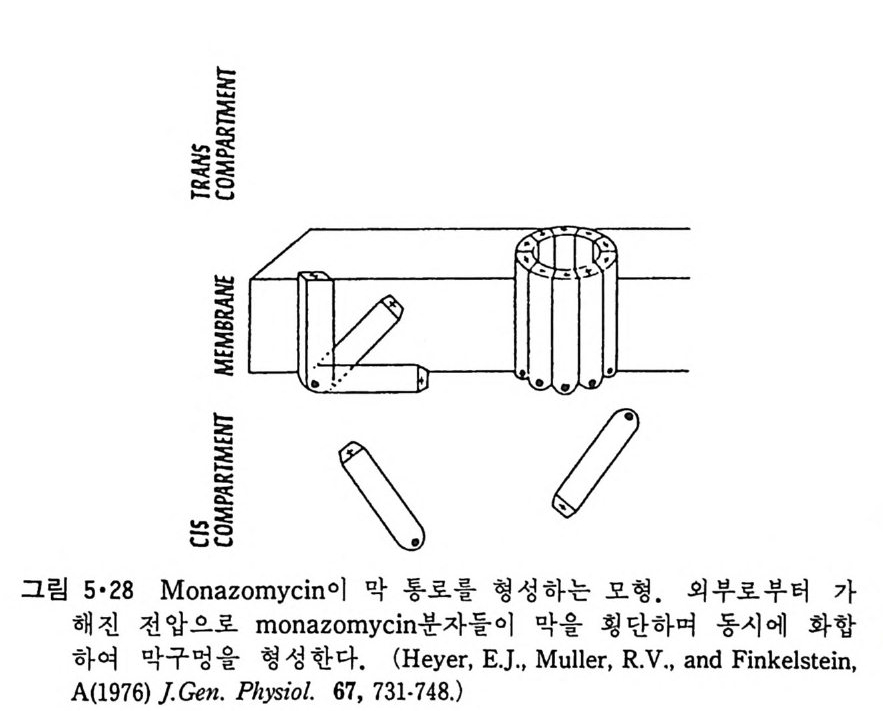 D
D
5·4·3 전압에 의해 형성되는 구멍 생리적으로 대단히 중요한 것은 i on 운반물질이 전압을 가해 주었을 때 지 방 질 이 분자층 내 에 구 멍 을 형 성 하는 것 이 다. 이 러 한 현 상운 monazomy cin 둥 몇가지 화합물에 의해서 이루어지는데 그림 5·27 은 전 압에 따르는 전달정도의 변화를 보여준다. 이때에 전압과 전달도의 변화 가 S- 형 을 이 루어 coo p era ti ve 현 상을 보 이 고 monazom yci n 분자 한쪽 끝 에 있는 1 가 양전하가 이분자층을 횡단하여 구멍을 형성하는 것으로 해 석 이 된다(그림 5·28). * 5 장 참고문헌 (1) Ste i n , W.D. (1967) The Movement of Molecules Across Cell Membranes, Academi c, N.Y. 1967. (2) Jo nes, M.N. and Ni ck son, J.K . (1981) Bio c him Bio p h y s . Acta , 650, 1-20. (3) Cabantc h ik , Z.I ., Knauf, P.A. and Roth s te i n , A. (1978) , Bio c him . Bi op h y s . Acta , 515, 239-302. (4) Jen nin g s , M. L. (1984) J. Memb, Bio l . 80, 105-117. (5) Klin g e nberg, M., in The Enzym e s of Bi ol og ica l Membranes, Mart on osi, A. (ed) Plenum. N.Y. 1976. pp3 83-438. (6) Kl ing e nberg, M. (1979) Trends Bio c hem. Sc i. 4 , 249-252. (7) Lanoue, K.F. and Schoolwert h, A.C. (1979) Ann. Rev. Bi oc hem. 48, 871-922. (8) Ni ka id o , H. and Nakae, R. (1979) Adv. Mi cr obio l . Phys i o l . 20, 163-250. (9) Benz, R., Hancock, R.E .W. and Nakae, T. in Anto l in i , e ta l (eds) Tran- spo rt in Bio m embranes : Model Sy st e m and Reconsti tut i on . Raven, NY. 1982. pp2 13-134. (IO) Hert zb erg, E.L., Lawrence, T.S. and Gi lula , N.B. (1981) Ann. Rev. Phys iol. 43, 479-491 . (II) Bennett , M. and Sp r ay, D. (eds) Gap ]unctic n s. Cold Sp ri n g Harbor Labo- rato r y , 1985. (12) Pressman, B.C. (1976) Ann. Rev. Bi oc hem. 45, 501-536. (13 ) Fin k elste i n , A in Andreoli , T.E., Hoff m an, J.F . and Fanesti l, D.D. (eds) Memhrane Phys iolo gy . Plenum, N.Y. 1980. Chap t. 11.
제 6 장 능동운반 능동운반 ( ac ti ve tra nspo rt ) 은 어느 물질이 자기자체의 전기화학 전위 기 웅기 (eletr o chemi ca l po te n ti al grad ie n t) 에 역 해 서 생 체 막을 통하여 이 동 되는 현상으로 이룰 위하여 ener gy의 공급이 필요하다. 능동운반은 그림 6·1 에 보여주는 것과 같이 3 개의 수송과정으로 세분이 된다. 여기서 1 차 능동운반(p r i mar y acti ve t rans p o rt)은 energy 공급이 이루어지는 지점에서
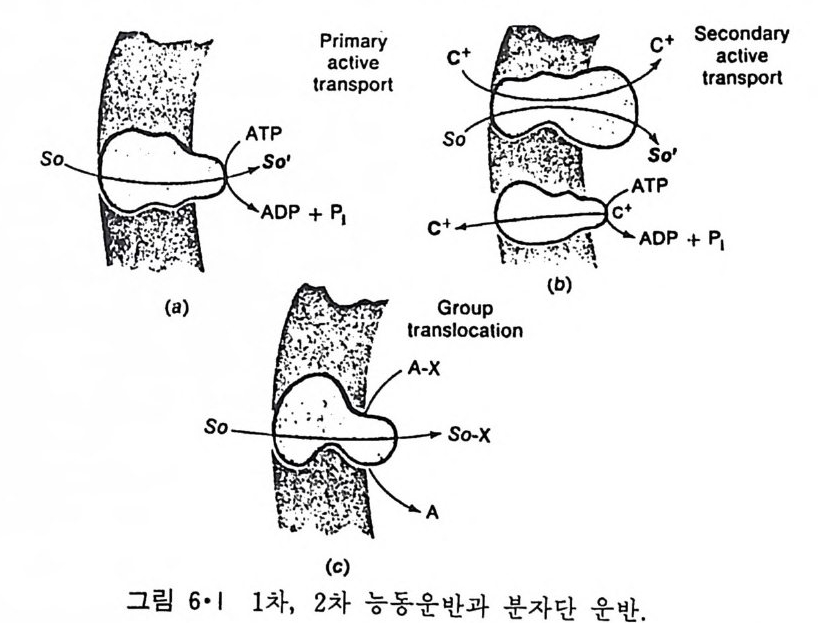 trPaar nc i mstia pv e o아 r t c+ Steraac ncostni pvd eoa rrty
trPaar nc i mstia pv e o아 r t c+ Steraac ncostni pvd eoa rrty
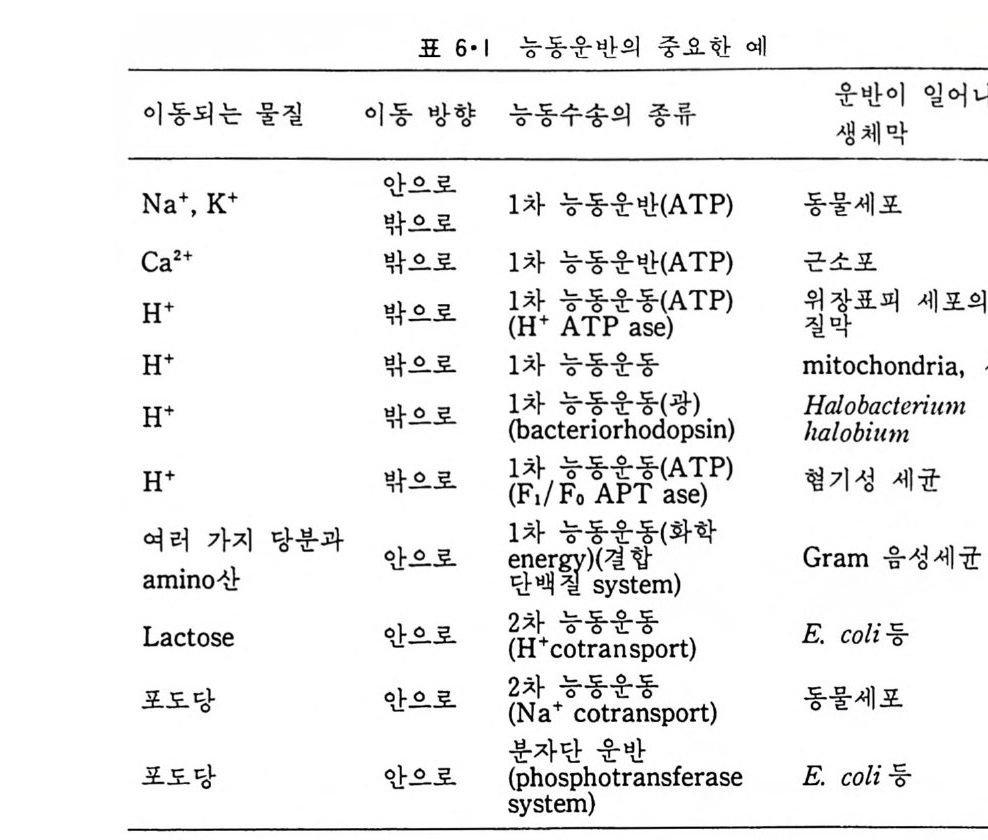 표 6·I 능동운반의 중요 한 예
표 6·I 능동운반의 중요 한 예
물질수송이 직 접 되 는 것 이고, 2 차 능동운반 (seconda ry acti ve tra nspo rt ) 은 1 차 능동운반으로 생성된 한 물질의 화학 전위기울기를 이용하여 두 번째 물질이 자기자신의 전기화학 전위기울기에 반해서 수송되는 과정을 말한다. 분자단 운반은 물질이 능동적으로 수송될 때에 이 물질에 화학 적인 변화가 수반되는 경우이다. 표 6·1 은 능동운반의 대표적인 예를 든 것이다. 능동운반으로 수송되는 물질의 종류는 적어도 이러한 양식으로 수송시키는 생체막의 종류는 다양하다. 6·1 1 차 능동운반 6·1·1 Na+, K+-APTase1>-s> 1 차 능동운반 중에서 가장 많이 알려져 있는 것은 Na+ 와 K+ 를 수송시
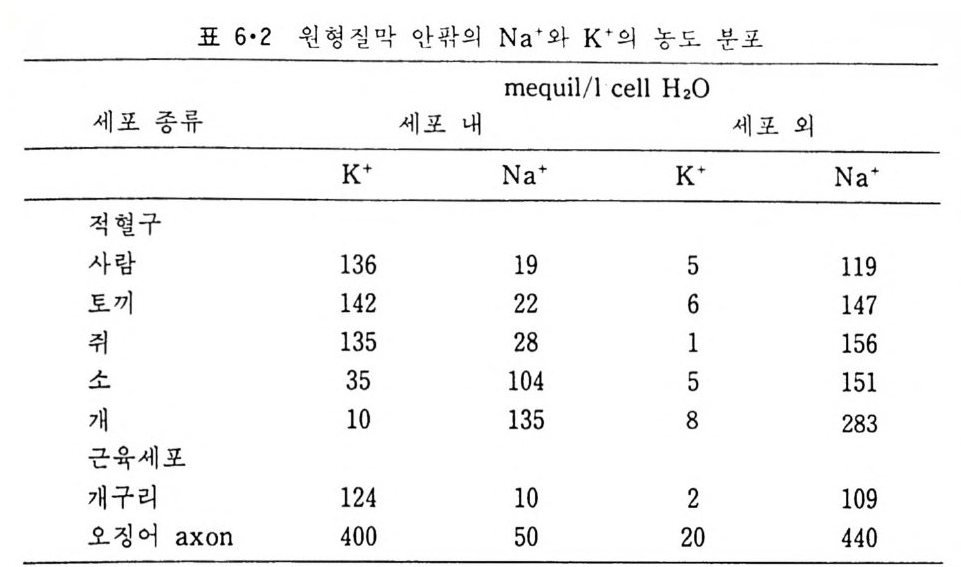 표 6·2 원형질막 안팎의 Na: t K 떠 농 도 분포
표 6·2 원형질막 안팎의 Na: t K 떠 농 도 분포
키는 ATPase 이다. 표 6·2 에서 보는 것과 같이 많은 세포는 그 내부와 외부의 Na+ 와 K 적 농도분포가 다르다. 죽 K + 의 농도는 세포내부에서 항상 높고 Na+ 농도는 그 반대의 분포를 보인다. 처음에는 이러한 i on 분 포는 세포가 생성될 때 이루어지고 원형질막은 i on 을 통과시키지 않기 때문에 이 농도차가 계속 유지된다고 생각되었다. 그러나 1930 년대 이후 여러가지 실험결과를 통하여 i on 들이 비교적 빨리 원형질막을 통과하는 것을 알게 되었다. 예 를 들면 개의 혈관에 22Na + 를 주사하였을 때 적혈 구 내부에 22Na+ 가 들어 가는 것을 발견하였고 또 낮은 온도에서는 적 혈 구와 혈청 사이의 Na + 와 K+ 의 농도 차이가 없어지지만 온도를 다시 3TC 로 올리면 원래의 농도 차이가 신속히 복구되는 것을 관찰하였다. 그러므로 생체막에는 Na+ 와 K+ i on 들의 이동에도 불구하고 이들 i on 의 농도 차이를 유지하는 mechan i sm 이 존재하는 것이 분명해졌다. 이러한 세포 내외의 i on 이 비대칭적인 분포를 유지하는데는 Gib b s- Donnan 평형에 의한 수동적인 성분과 실제로 i on 둘을 운반하는 능동적인 성분이 있다. 세포내외에서의 G i bbs-Donnan 막평형에 의한 i on 들의 분포 는 세포내에 음성하전을 띈 고분자들이 존재하기 때문이다. 그림 6·2 는 반투과막 (sem ip ermeabe membrane) 을 사이에 두고 전해질 K+A- 가 분 포되고 있는 것을 보여주는데 여기서 0 쪽의 농도가 i쪽보다 낮고 음 ion K 는 막을 통과하지 못하는데 반해서 양 ion K+ 는 자유롭게 동과한다고 가정한다. 이때에 전기화학 전위 i는 다음 식들로 표시가 된다.
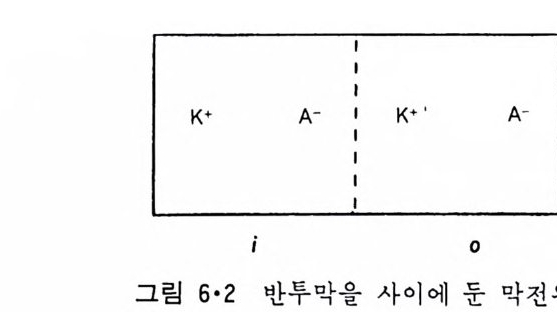 K• A- K+ ’ A-
K• A- K+ ’ A-
µK, = µt + :J'Pi = µt + RTlnaK, + :Jcp, (6·1) µKo = µ°Ko+RTlnaK0+ :Jcp。 (6·2) 이들 식에서 a 는 활동도 (ac ti v ity), :J는 Farada y상수, ¢는 전 위 를 나 타낸다. 이 두 식으로부터 얻는 막 전위차 A¢ 는 다음과 같다. A ¢ = ¢i - ¢。 = 쨩 ln 는 ::::: 뿡 ln 운 (6·3) 이 식 이 Nerns t방칭 식 이 다. 만일 0 쪽에서의 K+A- 의 농도가 0 이면 식 6·3 은 다음과 같이 표시된다. A 少 = ―뿡 lnCK, (6·4) 다음에 그림 6·3 에서와 같이 K+A- 는 i쪽에만 있고 양쪽에 KCI 이 있 을때 전위차는 다음과 갇다. A# = -효3 ln 요CcI, (6·5) 식 6·3 과 식 6·5 를 합하면
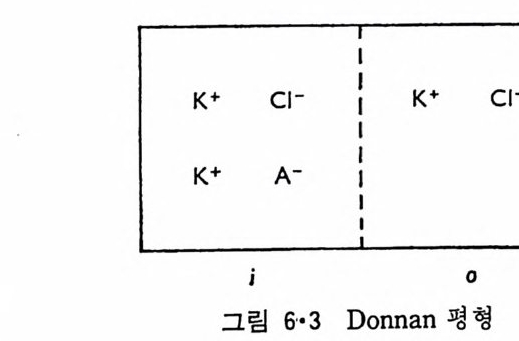 K+ c1- K+ CI-
K+ c1- K+ CI-
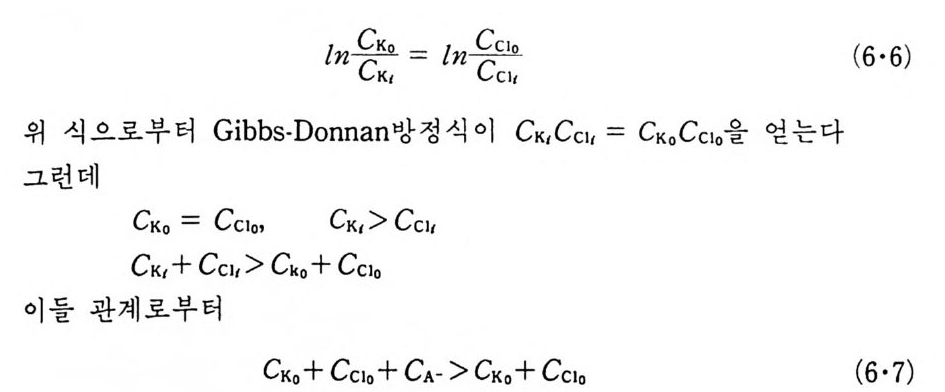 ln 요CK으t = ln 요CCIt (6· 6)
ln 요CK으t = ln 요CCIt (6· 6)
아직까지는 삼두압 (osmo tic p ressure) 을 고려하지 않았는데 식 6·7 에 의세하면 물의 활성도가 0 쪽이 더 커서 i쪽으로 수송이 될 것이다. 실제 포에서 A- 는 단백질이나 다른 큰 유기 i on 으로 구성이 된다. 그러므로 식 6·7 이 정성적으로 적용이 되어 물이 세포 안으로 수송되어 결국에는 세포가 파괴될 것이다. 이것을 방지하기 위하여 만일 생체막이 Na+i on 을 동과시키지 않으면 그림 6·4 에서와 같이 밖에 존재하는 Na+ i on 에 의 해 Dor1I1an 평형이 이루어지며 또 삼두 평형도 만족시키게 된다. 그러나 Na+ i on 도 생 체 막을 통과하기 때 문에 이 의 해 결 책 으로 p um pi n g에 의 해서 계속 Na+ i on 을 의부로 배출시키면 같은 효과를 얻게 된다. 실제로 는 이 이 중 Donnan 평 형 을 유지 하기 에 필요한 것보다 더 빠른 Na+ i on 의 수송이 이 루어 지 고 K+ i on 도 반대 방향으로 수송이 된다. 이러한 능동수송에 대사 ener gy가 필요한 것은 여러가지 실험에 의해 서 증명이 되었다. Hod g k i n 과 Ke yn es 는 오징어 신경 axon 을 방사선 Na+ i on 으로 채운 후 이것이 외부로 수송되는 속도를 측정하였다(그림 6·5). 이때에 호기적 대사( aerobic me t abol i sm) 의 저해작용제인 2, 4 -d i n it ro p henol(DNP) 를 첨 가하면 Na+ i on 의 능동운반이 급격 히 감소되 고
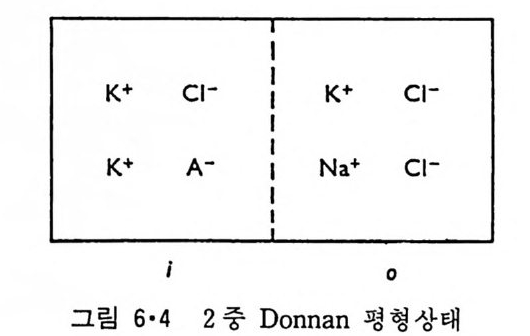 K+ CI- K+ c1-
K+ CI- K+ c1-
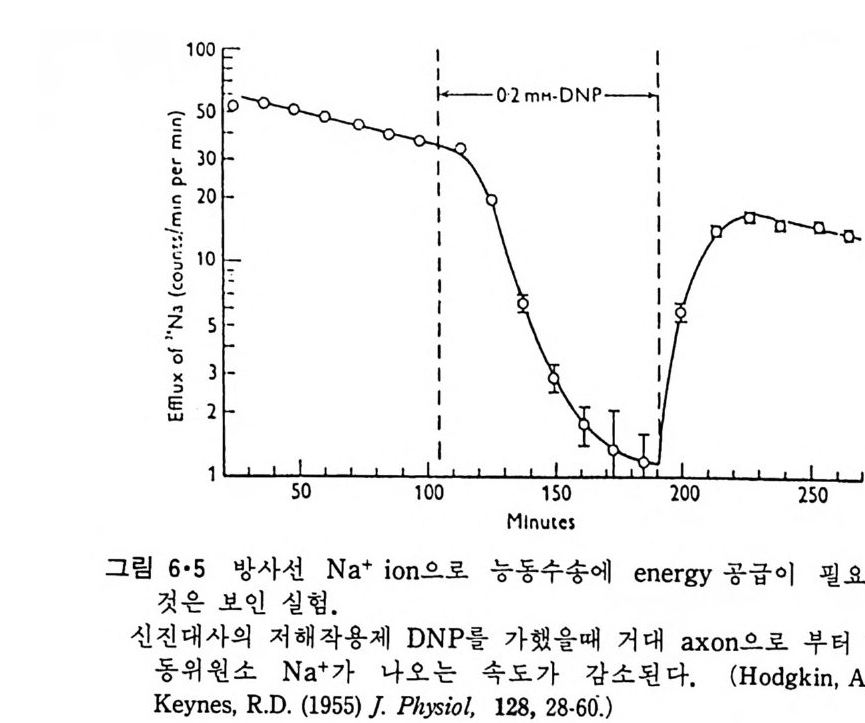 (U1I0E0s, ~do.o 3020-10s II 』 。 2 m” D NP 「_ ._II'II _
(U1I0E0s, ~do.o 3020-10s II 』 。 2 m” D NP 「_ ._II'II _
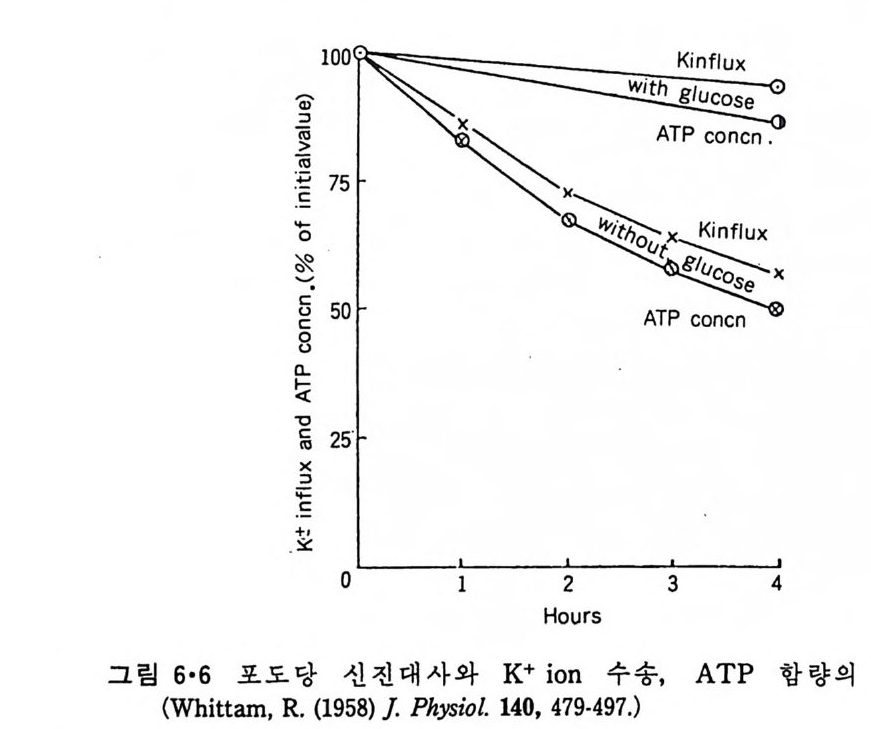 100•·
100•·
이 처해작용제를 제거하면 다시 원 상태로 Na+ i on 의 수송이 계속된다. 산화과정을 통한 대사 기능이 없는 포유동물 적혈구에서는 포도당을 제 거 하거 나 해 당작용 (gly c o lys i s ) 의 저 해 작용 제 인 fl uor i da t e 나 iod oaceti c a ci d 를 첨가하면 양 i on 의 수송이 없어진다. 그림 6·6 은 포도당을 제거했 을 때 K+ i on 이 안쪽으로 수송되는 것이 포도당이 존재할 때에 비해 감 소되고 또 이것이 ATP 의 함량의 감소와 평행되는 것을 보여준다. 포도 당이 없으면 해당작용에 의한 대사가 정지되는데 K+ i on 의 수송이 서서 히 감소되는 것은 해당작용 자체보다도 이 반응의 생성물인 ATP 와 관계 가 있는 것을 보여준다. ATP 가 관계한다는 직접적인 증거는 c yan i de 로 저해시킨 오징어 axon 에 ATP 를 가했을 때 양 i on 의 능동운반이 다시 회복되는 것으로 볼 수 있다(그림 6·7). Na+ i on 과 K+ i on 의 수송에 ATP 가 직접 가담하는 것으로 보아 ATP 가 가수분해되어 얻어지는 ener gy가 이들 i on 의 능동수송에 이용되는 것 으로 추측이 되었다. Skou6 는 이러한 기능을 위하여 생체막에 ATPase 가 존재 하며 이 효소의 작용에 는 Na+ i on 과 K+ i on 이 활성 작용제 (ac ti va t or) 로 필요하다고 생각해서 이 효소의 분리를 시도한 결과로 게의 신 경 으로부 터 M g2+ i on 으로 활성 화되 는 ATPase 를 발견 하 였 다. 이
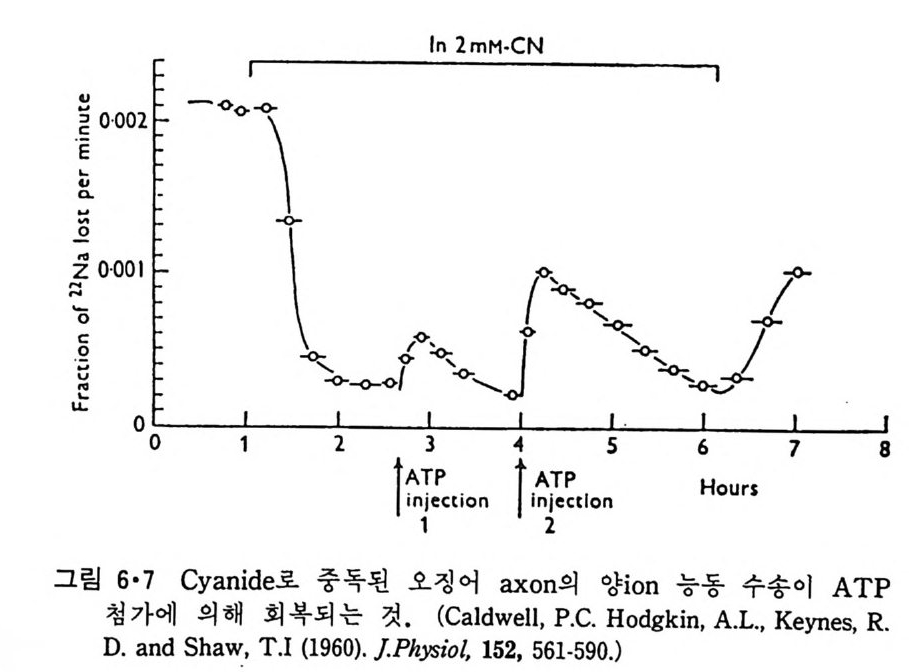 ngu!ow 0 02o0-0。 I。 q \ 4 In 2mM- C N
ngu!ow 0 02o0-0。 I。 q \ 4 In 2mM- C N
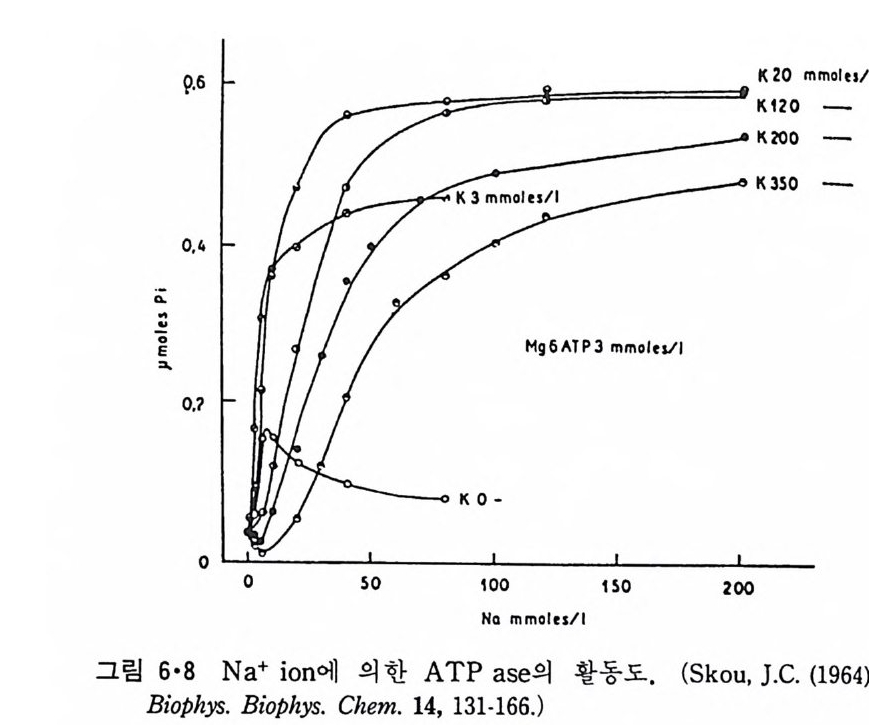 Q.6 K 20 mmolu/1
Q.6 K 20 mmolu/1
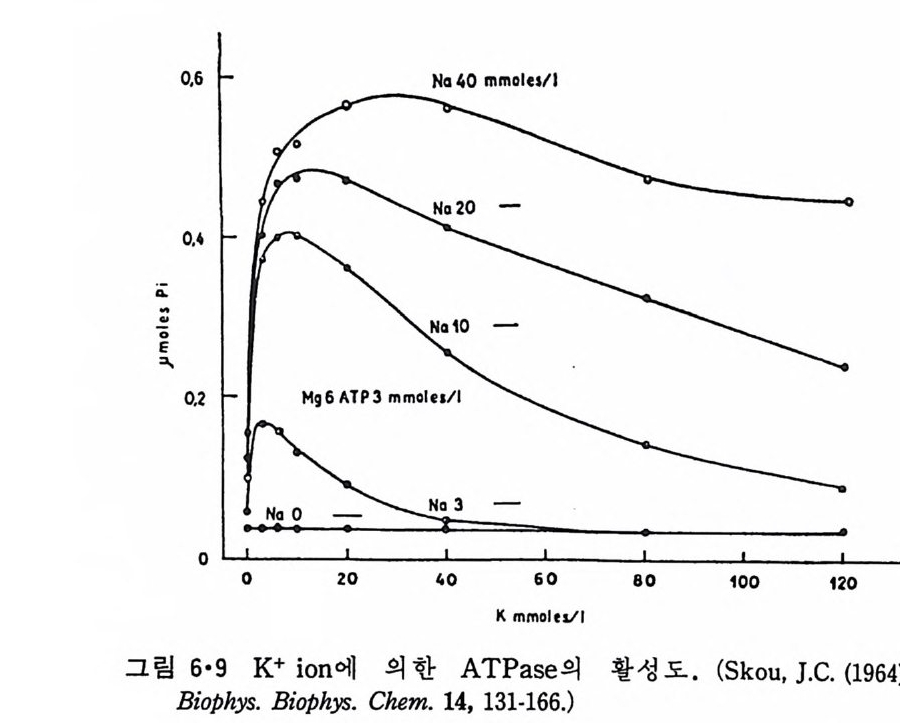 0,6 Na 40 mmolu/1
0,6 Na 40 mmolu/1
ATPase 는 Na+ i on 과 K+ i on 의 존재 하에 서 그 활동도 (ac ti vi t y) 가 훨 씬 중가되며 이 증가된 만큼의 활성도는 ouaba i n 과 같은 g l y cos i de 에 의해 완전히 저해된다. 그 후에 Na+ i on 과 K+ i on 을 수송하는 모든 생체막에 는 이 효소가 존재하는 것을 발견하였다. 포유동물에서 ATP 의 약 30% 가 Na+ K+-ATPase 에 의해서 가수분해가 된다. 그림 6·8 과 그림 6·9 는 각각 Na+ i on 과 K+ i on 에 의 한 ATPase 의 활 성도를 보여준다. 그림 6·8 에서 s igm o i dal 곡선을 볼 수 있으며 K+ i on 의 농도가 0 일 때는 Na+ i on 의 농도 증가에 따르는 최대활성접을 보여주나 다론 K+ i on 의 농도 중가에 따라 ATPase 의 활성 도가 중가하다가 다시 감 소하는데 이는 그림 6·9 에서 더 명백히 보여준다. 이런 현상은 ATPase 에 서로 영향을 주는 두 개의 활성위치 (ac ti ves it e) 가 따로 있어 Na+l -f - K+ i on 의 농도가 커지면 활성도가 커지지만 농도가 너무 높아지면 상대 방 i on 의 결 합자리 에 결 합하여 경 쟁 적 저 해 (comp et i tive inh ib i t ion ) 를 일으 키기 때문이 다. 또 s igm o i dal 곡선은 두 개 이상의 i on 들의 협동 (coo pe ra ti ve) 효과를 보인다. 그림 6·10 은 ATPase 의 i on 선택성을 보여준다. 여기
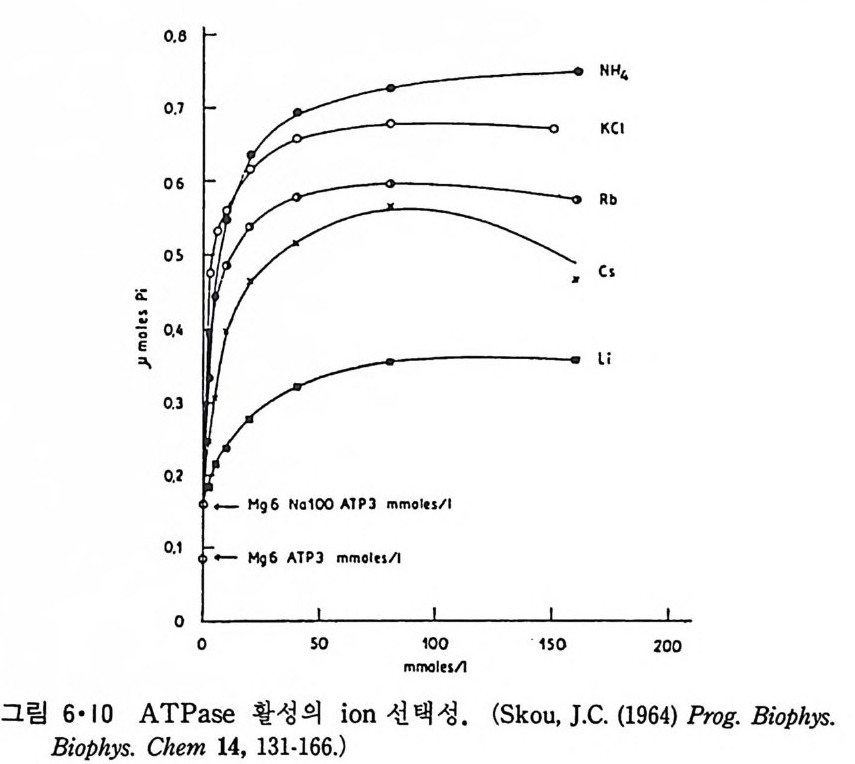 0.8
0.8
서 NH.+ i on 으로 K+ i on 울 대치시킬 수 있는 것을 알 수 있다. 생 체 막에 존재 하는 Na+ , K+-ATPase 가 Na+ i on 과 K+ i on 의 능동운반 을 한다는 중거를 종합해 보면, (a) ATPase s y s t em 과 Na+ i on 과 K+ i on 의 수송 s y s t em 이 모두 생체 막에 존재한다. (b) 이 두 s y s t em 이 모두 ATP 를 사용하는데 이와 유사한 ITP 와 같 은 화합물은 효력이 없다. (c) 양쪽 기능이 모두 Na+ 와 K+ i on 이 동시에 존재하여야 하며 K+ i on 대신 NH.+ 로 대치시킬 수가 있다. (d) Na+ 와 K+ i on 둘의 반최 상활성 (half -m axim al acti va t ion ) 농도는 이 두 s y s t em 에서 동일한 값을 갖는다. (e) 여 러 가지 cardia c g l y cos i de 에 의 해 이 양쪽 기 능이 처 해 를 받으며 또 갇 은 반저 해 (half inh ib i t ion ) 농도를 갖는다. (f) K+ i on 이 이 두 s y s t em 에 서 ouaba i n 의 작용을 감소시 킨 다. 이 들은 Na+, K+-ATPase 가 Na+ i on 과 K+ i on 을 능동적 으로 수송한다 는 좋은 간접적인 증거라 볼 수 있는데 직접적인 증명은 다음에 나오는 재 구성 (reconsti tut i on ) 에 서 이 루어 졌 다. 또 하나 중요한 점은 이들 두 i on 의 수송과 같이 ATPase 의 작용도 방
 S01>
S01>
향성이 있다는 사실아다. 이것은 주로 적혈구에서 hemo g lob i n 을 없앤 빈 껍질을 이용하여 얻은 결과인데 이를 종합해 보면 다음과 같다. (a) Na+ i on 은 적 혈구 내부에서 적 혈구 막에 존재하는 ATPase 를 활 성 화시 키 면서 밖으로 이 동되 며 K+ i on 은 밖에 서 ATPase 를 활성 화시 켜 안으로 수송된다. (b) ATP 는 내 부에 서 가수분해 된 다. (c) p,는 내부에서 생성되어 서서히 밖으로 새어 나온다. 그림 6·ll 은 ATP 한 분자가 가수분해되면 2 개의 K+ i on 이 수송되고 3 개의 Na+ i on 이 반대 방향으로 수송되는 것을 보여준다. 이 Na+, K+ - ATPase 의 작용에 대한 연구는 생체막 조각이나 세포 자 체를 통한 kin e ti cs 실험을 통하여 대단히 광범위하게 진행되어 왔다. 이 들의 결과를 종합해 보면 다음과 같다. 그림 6·12 에서 보통 조건하에서 는 시계 방향으로 반응이 진행되지만 경우에 따라서는 반대 방향으로 진 행되기도 한다. 이 과정을 세분하면,
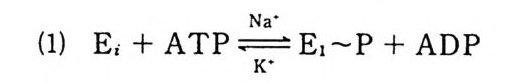 (1) E; + ATP =NKa=· · E,~P + ADP
(1) E; + ATP =NKa=· · E,~P + ADP
인산화(p hos p ho ry la ti on) 된 중간생성물은 r-P32 로 표지된 ATP 와의 반 응으로 확인되었다. 이 반응에는 Na+ i on 과 M 답+i on 이 필요하고 K+ i on 을 첨가하면 Pi가 가수분해로 떨어져 나온다. ATP 도 M g 2+ 가 없을 때는 결합된다.
 (2) E,~P == E2P
(2) E,~P == E2P
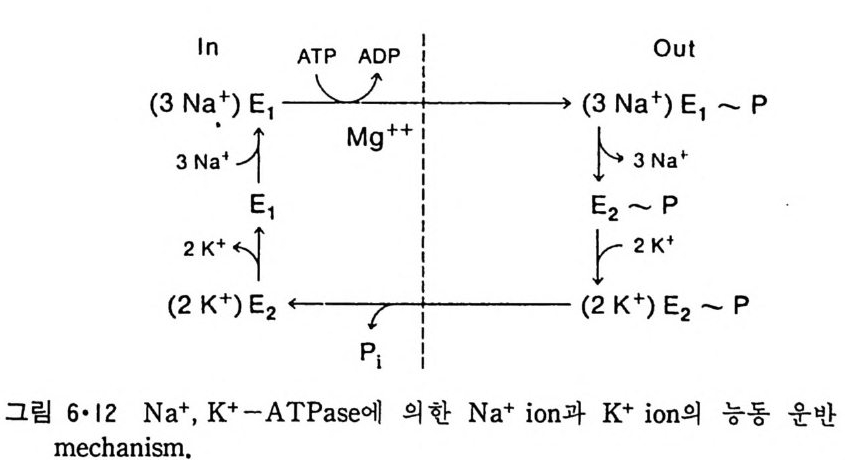 In ATP ADP Out
In ATP ADP Out
E1 은 내부를 향하고 있는 陽i on 결합자리를 가지고 있으며 이 자리는 Na+ i on 과의 친 화력 (af fini t y) 은 크고 K+ i on 과의 친 화력 은 작은 반면 E2 는 陽 ion 결합자리가 밖을 향하며 이 자리는 Na + i on 과의 친화력은 작고 K+ i on 과의 천화력은 크다. 그래서, Na+ i on 은 안으로부터 밖으로 수송되어 떨어져 나오고 陽 ion 결 합자리 는 K+ i on 과 회 합한다.
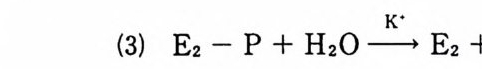 (3) E2 -P + H20 一K· E2 + Pi
(3) E2 -P + H20 一K· E2 + Pi
이 반응은 K+ i on 에 의해서 촉진이 되고 ouaba i n 에 의해서 저해된다. 그러나 E 는 내부로 방출된다. (4) E2~E1 이 단계에서 결합된 K+ i on 이 내부로 수송되고 거기서 방출된다. 이상 결 과로서 Na+, K+-ATPase 가 생 체 막을 횡 단하여 존재 하는 내 재 단백 질 이 라 는 것이 침작된다. Na+, K+-ATPase 의 mechan i sm 은 아주 자세히 모르지만 그림 6·13 은 Na+ 와 K+ 수송의 model 을 보인다. 이 그림에서 양 ion 결합자리가 내 부를 향하여 Na+ i on 과 천화력 이 더 큰 E1 구조와 양 ion 결 합자리 가 외 부로 향해 K+ 과의 친화력이 더 큰 E2 형을 보여준다. 이렇게 Na+, K+-ATPase 에 대한 k i ne tic s 의 연구는 적혈구를 이용하여 대부분 이루어졌지만 이 효소에 대한 구조연구는 N 학의 수송을 전문적 으로 하며 Na+, K+-ATPase 가 농축되 어 있는 신 장의 외 부 renal
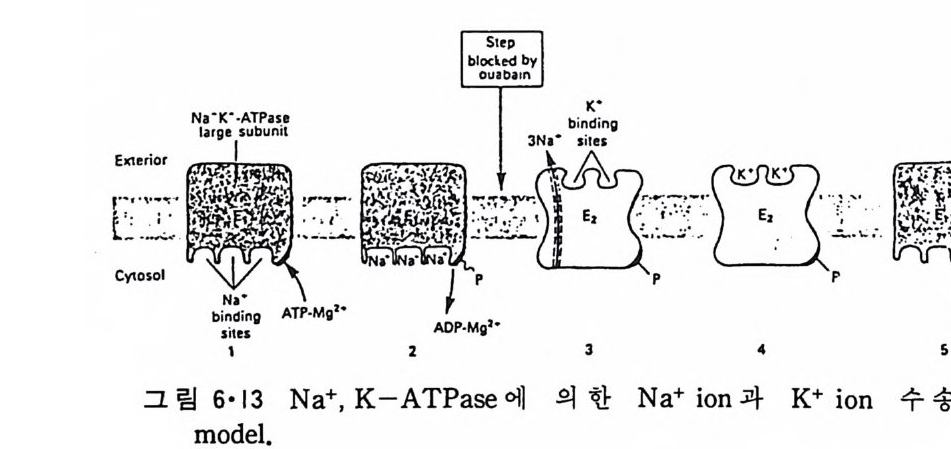 lECm.r;i讓o or : 서:;b;isNn `i.麟dt .\.i .n. t 9 t u .t ,At TP丁.M9,. 〕2 AOiP 〉Mpg ·I 3N_·· 난3 ,n9- ·- \ 4 : 노 2K• p,
lECm.r;i讓o or : 서:;b;isNn `i.麟dt .\.i .n. t 9 t u .t ,At TP丁.M9,. 〕2 AOiP 〉Mpg ·I 3N_·· 난3 ,n9- ·- \ 4 : 노 2K• p,
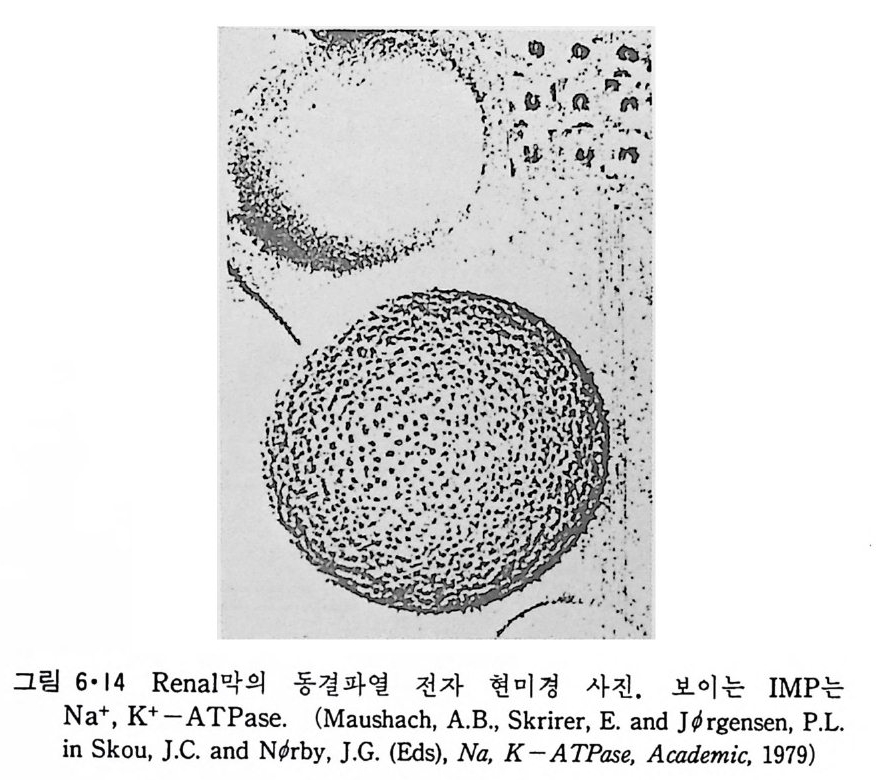 :'•...i·- .', •? : -t영 : . . · .·澤 ' .. 鬱.. 궁 동g• ,t;(\.·i . ' ,·., .\ r¥• ••\. '• ' •.. .. , \1 ,~bp드~ .·냐··: ,. .•.• .•\ -•~, ? . ..'• ,, .. .0 ,• ,•만; , · .' 수 • :갑.· ’ • .(, %•,, ! ,.` _ •’'.n~. .;, ,. .; .. . :., '. .` ,' : '. .: i'.:
:'•...i·- .', •? : -t영 : . . · .·澤 ' .. 鬱.. 궁 동g• ,t;(\.·i . ' ,·., .\ r¥• ••\. '• ' •.. .. , \1 ,~bp드~ .·냐··: ,. .•.• .•\ -•~, ? . ..'• ,, .. .0 ,• ,•만; , · .' 수 • :갑.· ’ • .(, %•,, ! ,.` _ •’'.n~. .;, ,. .; .. . :., '. .` ,' : '. .: i'.:
 medulla, do gfi sh 의 recta l gla nd, 전 기 뱀 장어 (elect ri c eel) 의 elec t ro p lax 와
medulla, do gfi sh 의 recta l gla nd, 전 기 뱀 장어 (elect ri c eel) 의 elec t ro p lax 와
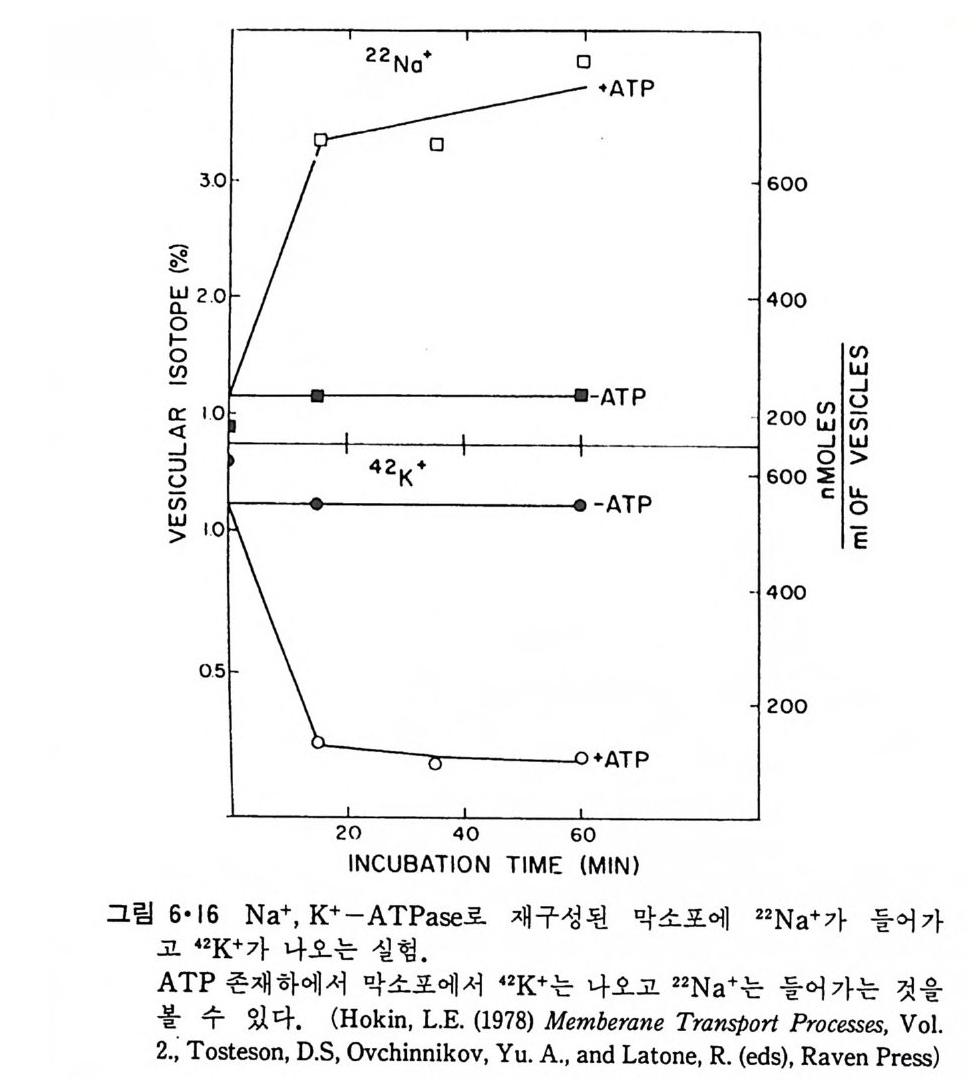 22No ♦ 0
22No ♦ 0
141~170kDa 정도로 추정 이 됐으며 그 s t o ic h i ome t r y는 af )이고 교차결 합 (cross- i nka g e) 실험으로 일부는 (af ) )2 와 (af)) 3 단위로 회합하는 것을 알게 되었다. 이들 생체막에서 존재하는 Na+, K+-ATPase 가 Na+ i on 과 K+ i on 을 능 동적으로 수송한다는 칙집적인 중명은 재구성 실험에 의한 것인데 이 결 과는 그림 6·16 에 보여준다. Na+, K+-ATPase 의 두 pol yp etide 사슬 중에 서 ouabain , ATP 와 R 는 a- 사슬에 결합이 되며 이것을 촉매사슬이라고 부르며 f)사슬에는 탄수화
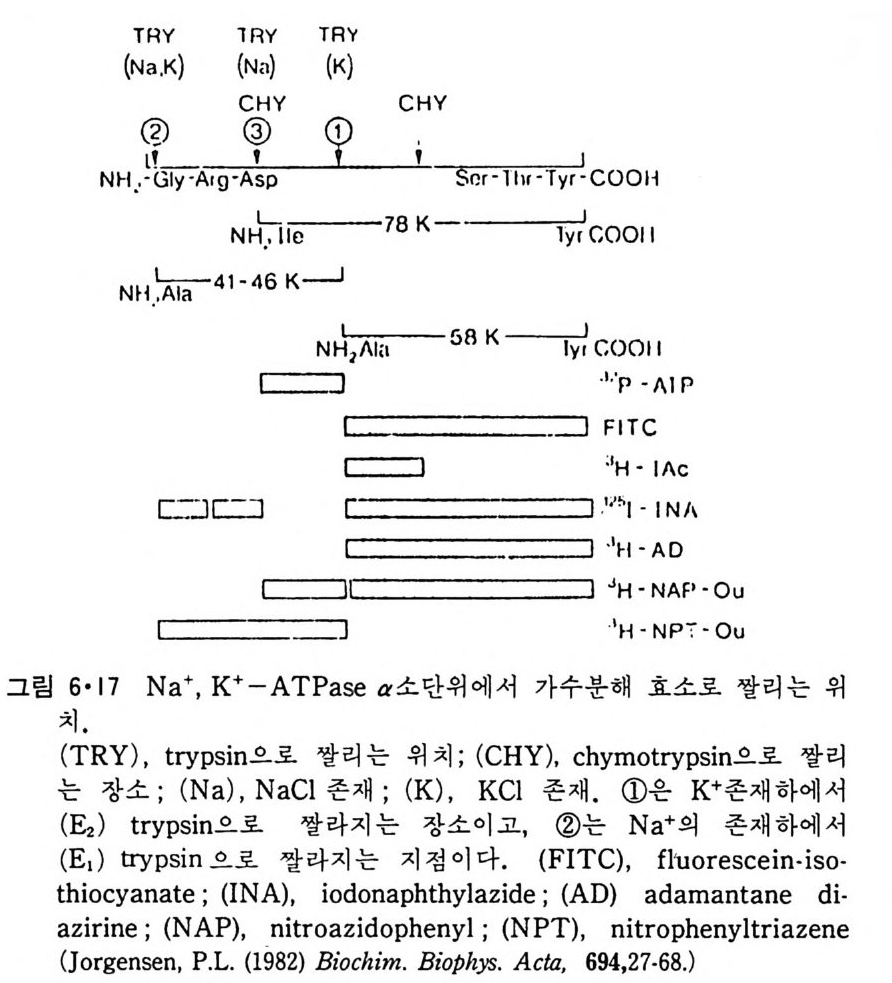 TRY lRY TRY
TRY lRY TRY
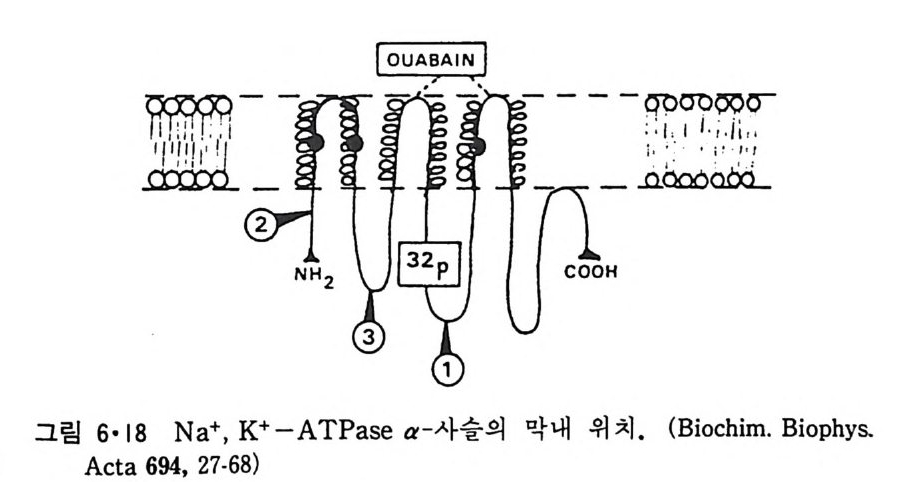 루.
루.
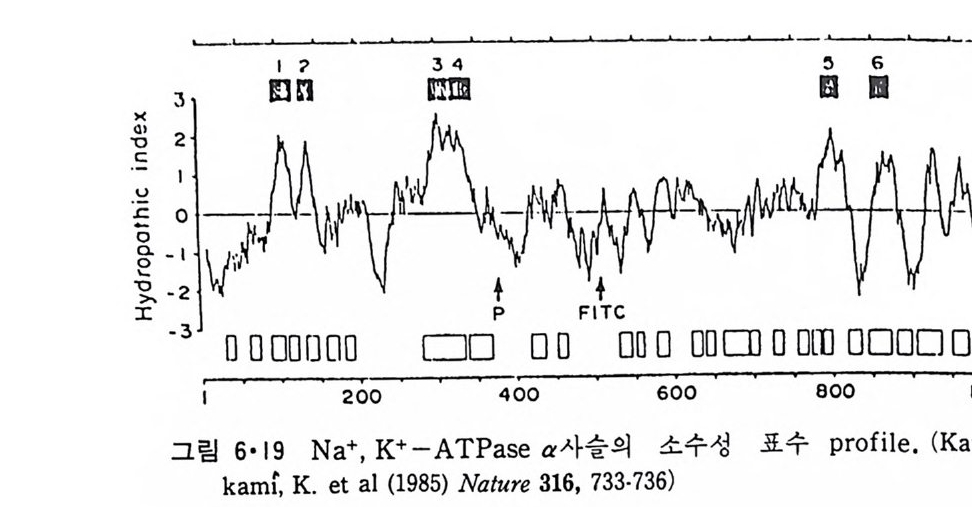 'IOnM g , , ,_,3 m-, 6 , , . ,-
'IOnM g , , ,_,3 m-, 6 , , . ,-
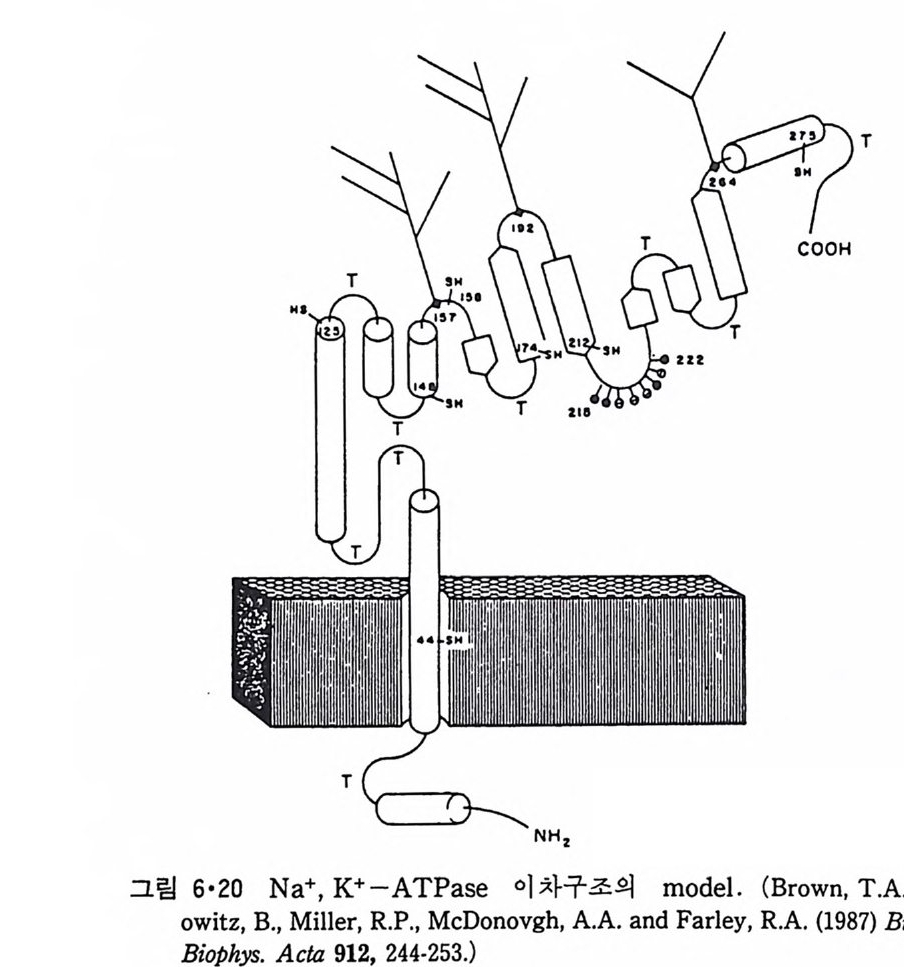 T
T
물이 공유 결합 ( covalen t ) 으로 결합되어 있고 이 p ol yp e ti de 의 기능은 아직 분명치가 않다. a 사슬은 생체막에 존재하는 상태에서 단백질 가수분해 효소들에 의해서 작은 단위로 쪼개지는데 이것과 여러가지 종류의 작용 제와의 반응을 그링 6·17 에 종합하여 나타내었다. 특히 주목해야 될 것 은 Na+ i on 의 존재 하에 서 E1 형 과 K+ i on 의 존재 하에 서 의 E2 형 (그림 6· 12) 의 a 사슬이 쪼개지는 장소가 다른 점이다. 이것은 이 두 가지 구조가 뚜렷이 다르다는 것을 의미하는데 형광실험과 구조실험으로도 증명이 되 었다. 그림 6·18 은 그림 6·17 의 결과로부터 생체막에서의 Na+, K+-ATPase 의 a- 사슬의 위 상 (top o leg y) 을 얻 은 것 이 다. 최근에 와서 여러 생체막에서 얻는 Na+, K+-ATPase 의 am i no 산 서열 이 결정되었는데 그림 6·19 는 전기가오리 Na+, K+-ATPase a- 사슬의 am i no 산 서열의 소수성 표수 p ro fi le 을 보여준다. 최소한 6 개의 막을 횡 단하는 a - 나사선 부분을 생각할 수 있다. 그림 6·20 은 /3-사슬의 am i no 산 서열의 소수성 표수 p ro fi le 로부터 얻은 위상(t o p olo gy)이다. a- 사슬이 막 을 여러번 횡단하는 것에 반해서 /3-사슬은 한 번만 통과하고 그 사슬의 대부분은 외부에 노출되어 있다. 6 • 1 • 2 Ca2+ -ATPase1> 5> Calciu m adenosin e tr i p h osph ata s e (Caz+ - ATPase) 는 근육세포의 근 소포체 (sarcop la smi c reti cu lum) 막에 존재 하며 근육수축 후 이 완시 Ca2+ i on 을 능동적으로 수송한다. 이 효소의 k i ne tic s 연구는 근소포체로부터 얻은 막소포를 주로 이용하였는데 그 전반적인 반응은 2Ca2+(out) + ATP(out) _M 균 ➔ 2Ca2+ (fn) + ADP(out) + P;(out) 이고, 이 mechan i sm 은 그림 6·21 에서와 갇다. 이 그림과 그림 6·12 를 미 교하면 Na2+ 를 Ca2+ 로 치 환되 는 것 이 외 에 는 이 두 ATPase 의 mechan i sm 은 본질 적 으로 동일 하다. Ca 2+ -ATPase 를 막에서 세탁제로 추출하여 SDS-po lya cryl a mi de ge l 전기영동법으로 분자량을 측정한 결과 무게가 119kDa 인 p ol yp e ti de 사슬 하나의 band 가 나타났다. 이 사슬의 am i no 산 서열은 결정되어 그의 소 수성표수 p ro fil e 로부터 10 개의 막을 통과하는 a- 나사선사슬이 존재한다
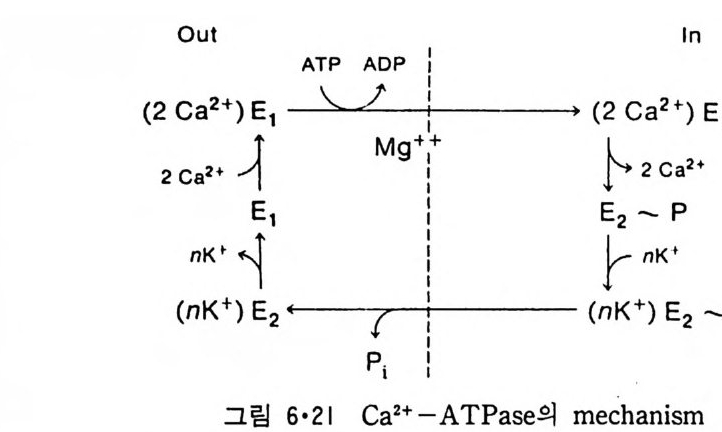 Out IIIIII+ In
Out IIIIII+ In
고~ 생각되고 있다(그림 6·22). 전자현미경으로 이 효소를 잘 관찰하면 원형질에 노출된 큰 입자와 막 사이에 줄기 (s t alk) 가 보이는데 이 줄기에 carbox y l 옆사슬이 많이 모여 Ca2+ i on 이 결합한다고 생각되고 있다. 이 상의 두 ATPase 와 유사한 또 하나의 i on 수송에 관여 하는 ATPase 는 위장상피 (e pit he li cal) 세포의 원형질막에 존재하는 H+-ATPase 이 다. 이 효소는 위장액을 산성으로 만드는 역할을 하는 것으로 그 구조가 Na+, K+-ATPase 나 Ca2+-ATPase 와 유사하다. H+-ATPase 도 약 lOOk Da 의 p ol ypepti de 사슬로 구성 되 어 있고 H+ 의 이 동시 잠정 적 으로 인산화 가 된다. 구조가 비슷한 H+-ATPase 가 곰팡이나 y eas t세포에서도 존재 한다.
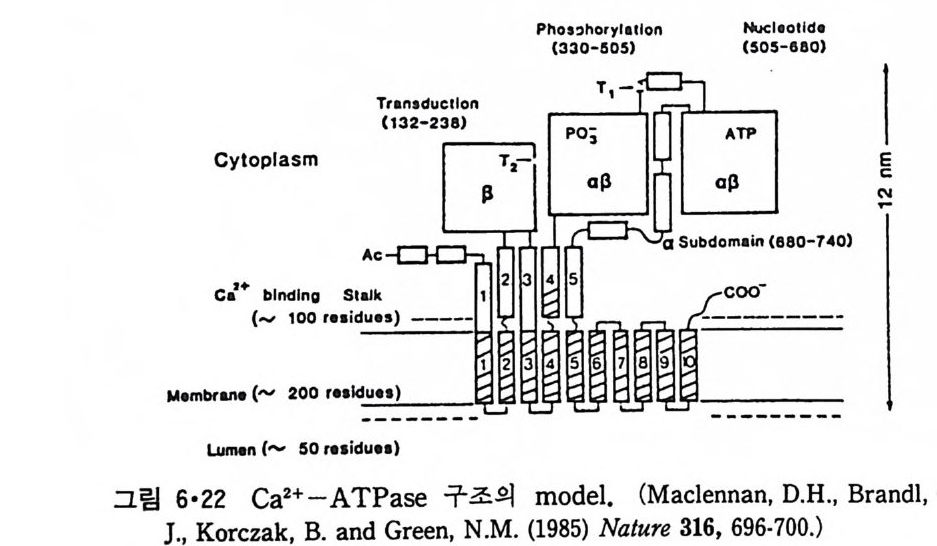 Phos~hory la t lon Nucl•otI d •
Phos~hory la t lon Nucl•otI d •
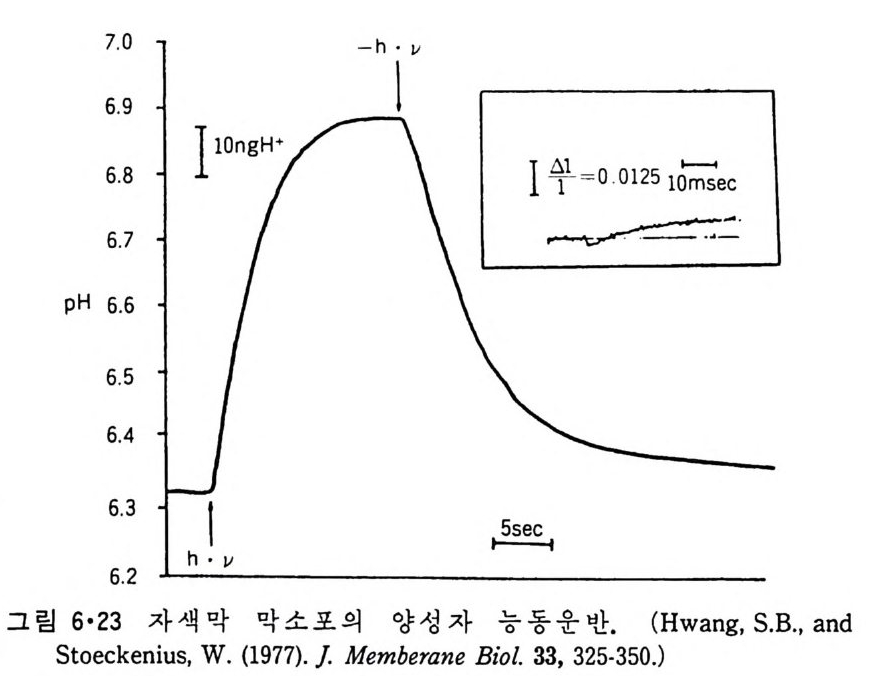 7.0 h • v
7.0 h • v
6·1·3 Bacte r io r hodop si n 9> -11> W 의 능동운반은 ATP 의 가수분해 뿐만 아니라 전자이동이나 광 ener gy에 의해서도 이루어진다. M it ochondr i a 의 내부막에서는 전자이동 이 H+ 농도차를 야기 시 키 고 엽 록체 의 t h y lako i d 막에 서 는 광을 흡수하여 생성된 전자가 이동하면서 H+ 농도차를 생성시키며 Halobacte r i um holobiu m 의 자색 막 (pu rpl e membrane) 에 서 는 광 ener gy가 직 접 H+ 를 능 동적 으로 수송시 킨 다. 이 들 s y s t em 에 서 형 성 된 양성 자 moti ve fo rce 는 ATP 합성에 이용된다. M it ochondr i a 와 엽록체에서의 H+ 수송은 energy 전이에서 다루기로 하고 여기서는 자색막에 대해서만 간단히 설명한다. 자색막의 bac t er i orhodo p s i n 에 빛을 쪼이면 양성자가 세포내부에서 외 부로 능동적으로 수송된다. 그림 6·23 은 PC 막소포에 재구성시킨 bac t er i orhodo p s i n 에 의해 양성자가 수송되는 것을 보여준다. 이 막소포 에 서 는 bac t er i orhodo p s i n 의 막내 에 서 의 배 열 이 자색 막때 와는 반대 로 향 해 있어 양성자가 밖에서 안으로 수송된다. 이 막이 자색 Umax = 570nm) 울 띠는 것은 vit am i n A 유도체인 re ti nal 이 그림 6·24 에 보는 바와 같이 bac t er i orhodo p s i n 의 l y s i ne 기 와 Schif f base 결 합을 동해 서 연 결되 었 기 때
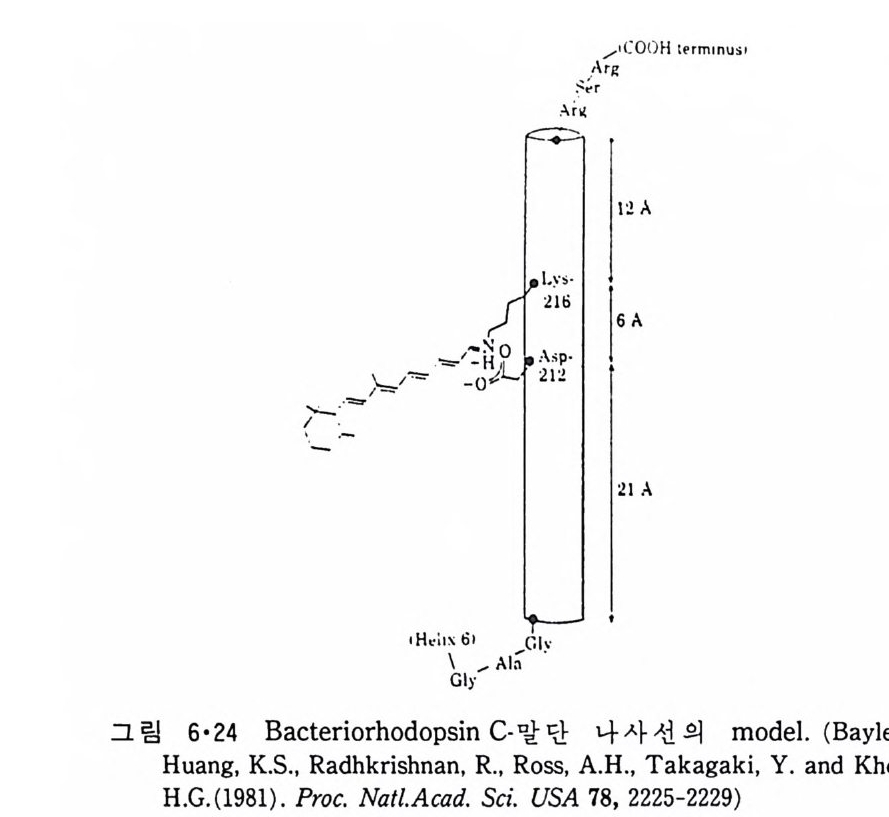 ,,,.,COO H ter m in us ,
,,,.,COO H ter m in us ,
문이 다. Bac t er i orhodo p s i n 의 광화학반응은 대 단히 복잡한데 광이 re ti nal 에 홍수되면 Schif f base 에서 양성자가 떨어져 나와(그림 6·25) 412run 에 서 최 대 흉 수 (maxim um absorp tion ) 를 갖 는 구 조 로 변 한 다. Re ti nal 에 양성 자가 다시 결 합하면 bac t er i orhodo p s i n 은 c y cle 을 거 쳐 570run 형 으로 돌아간다. 그러 나 bac t er i orhodo p s i n 의 광흡수가 어 떠 한 분 자적 인 machan i sm 을 통해 서 양성 자를 이 동시 키 는지 아직 모르고 있다.
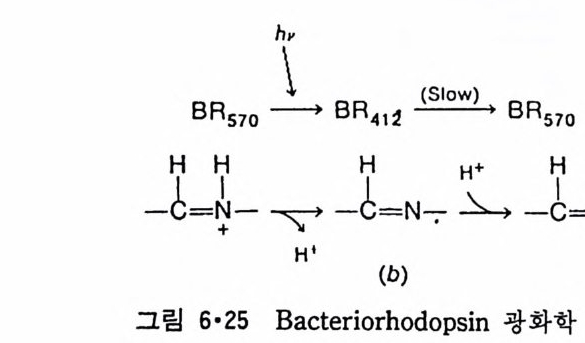 h\
h\
6·1·4 결합단백질(Bi n di n g p ro t e i n) 에 의한 이동 sy s t em 12>-15> Gram 음성 세균의 주변세포액 공간(p er ip lasm ic s p ace) 에 존재하는 여 러 단백질은 당분, am i no 산, 무기 i on 과 결합하여 이들을 원형질막을 통 해 능동운반 시킨다. 이들 세균을 lys ozy me , EDTA 또는 삼투충격 (osmot ic shock) 으로 처리하면 결합단백질이 제거되어 원형질막이 작은 분자들을 수송시키는 능력아 없어진다. 이들의 수송은 포화성 k i ne tic s 의 성격을 띠며 단백질을 변성시키는 화합물에 영향을 받는다. 표 6·3 은 결 합단백질들의 성질을 보여준다. 결합단백질의 특성은 수용성이고 분자량
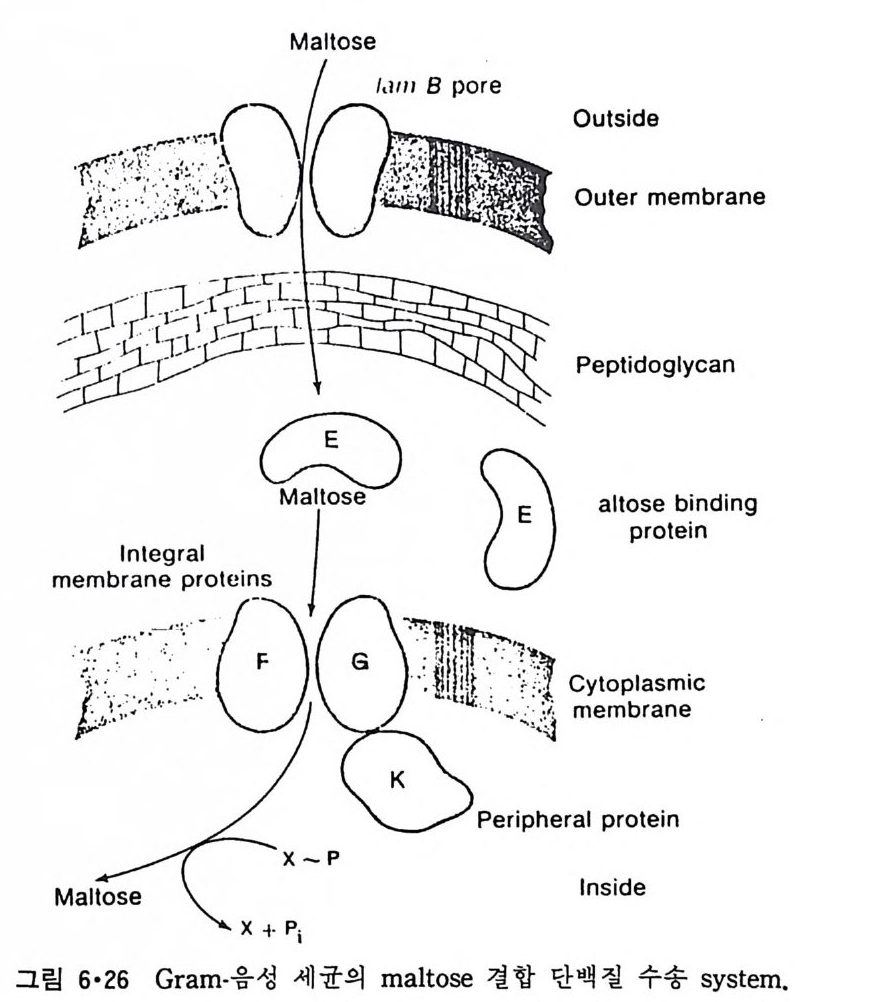 Malto s e
Malto s e
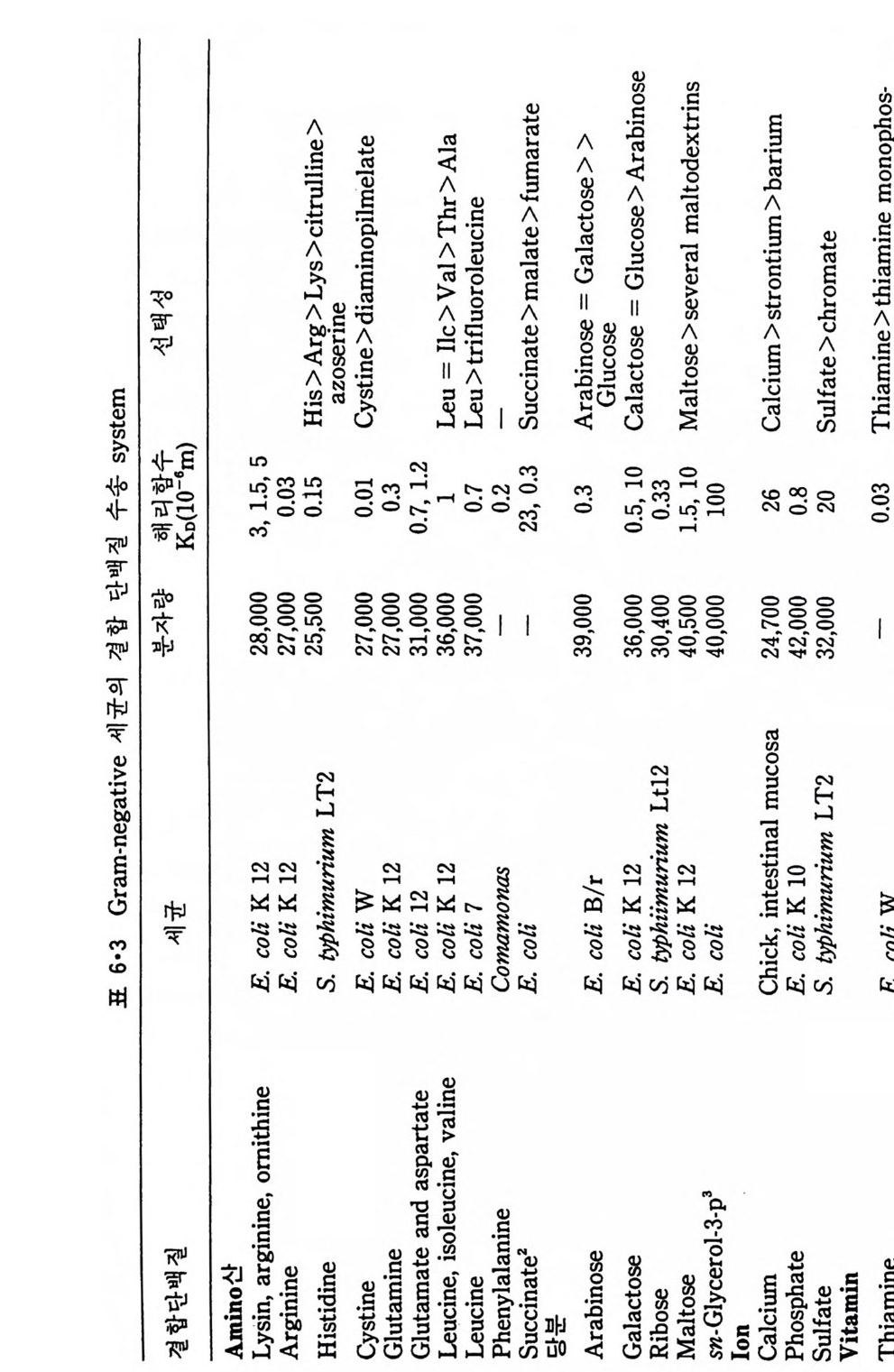 yse mst송 질 수 성택선D해6)0 함m (1리-수 K 35, 5 , 1. . 300 1.0 5y HeArLs senu>>>rr >en slilitigiczao mne0y.0 e a1ollspe tCdai mn>itii 03 .0.,7 21.= 1>lluehI ale> LATarV>7. 0e>no eu ulreroLutifcil 0. 23,. 302 malrae e au> uSea ncftatm> tic = 3.0 aces>aloensb Gar> oA it esoculG =, 1050. s eoeossaAuoc >caGlal re Cnbti.3 03 ,15 0sr nx esaollolmeva daMere>s ittt.1 001 62 > m ummu blcanor >arus tiiCti .80 02 e a e >tlSuomrchatf ma30.0 e >nnmah eiiiThitSO·mon盆s e en hdo t>eahami pttipih 00.06
yse mst송 질 수 성택선D해6)0 함m (1리-수 K 35, 5 , 1. . 300 1.0 5y HeArLs senu>>>rr >en slilitigiczao mne0y.0 e a1ollspe tCdai mn>itii 03 .0.,7 21.= 1>lluehI ale> LATarV>7. 0e>no eu ulreroLutifcil 0. 23,. 302 malrae e au> uSea ncftatm> tic = 3.0 aces>aloensb Gar> oA it esoculG =, 1050. s eoeossaAuoc >caGlal re Cnbti.3 03 ,15 0sr nx esaollolmeva daMere>s ittt.1 001 62 > m ummu blcanor >arus tiiCti .80 02 e a e >tlSuomrchatf ma30.0 e >nnmah eiiiThitSO·mon盆s e en hdo t>eahami pttipih 00.06
은 20 에서 40kDa 정도이며 작은 물질과 선택적으로 결합하고 KD 값은 10 내 ~10-14M 이 된다. 이들 결합단백질은 주변세포액 공간에 존재하며 아무 런 생화학적인 촉매역할을 하지 않는다. 결합단백질이 용질수송에 관여 하는 것은 분명하지만 이들이 내재단백질아 아니기 때문에 간접적으로 작용하는 것으로 생각된다. 모든 결합단백질 수송 s y s t em 은 작은 물질들 의 수송에 대사 ener gy를 이용한다. 결합단백질 중에서 ma lt ose 의 수송이 가장 많이 연구가 되었는데 이는 그림 6·26 에 보여준다. 여기서 mal t ose 는 세균의 외부막이 구멍을 통과 한 후 주변세포액 공간에 존재하는 결합단백질 E 와 결합한다. Malto s e 와 결합한 E 단백질은 원형질막의 내재단백질인 per mease F 와 G 와 반 응하여 높은 energy p hos p ha t e 에 의 해 서 원 형 질 막을 동과한다. K 단백 질 은 원형질막 안쪽에 있는 주변단백질로서 mal t ose 수송에 필요한데 그 정 확한 역할은 아직 모른다. 6·2 2 차 능동운반 16 )1 7) 표 6·4 는 1 차 능동운반에 의해서 생성된 Na+ 와 H+ 의 농도기울기 (concentr a ti on gr ad i en t)에 의해서 2 차 능동운반이 되는 물질들을 보여준 다. 그림 6·27 은 Na+, K+-ATPase 에 의해서 생긴 Na+ 기울기를 따라 포 도당이 수송되는 것을 보여준다. 이렇게 Na+ i on 이 수송되는 방향으로 2
 표 6.4 2 차 능동운반 sys t e m
표 6.4 2 차 능동운반 sys t e m
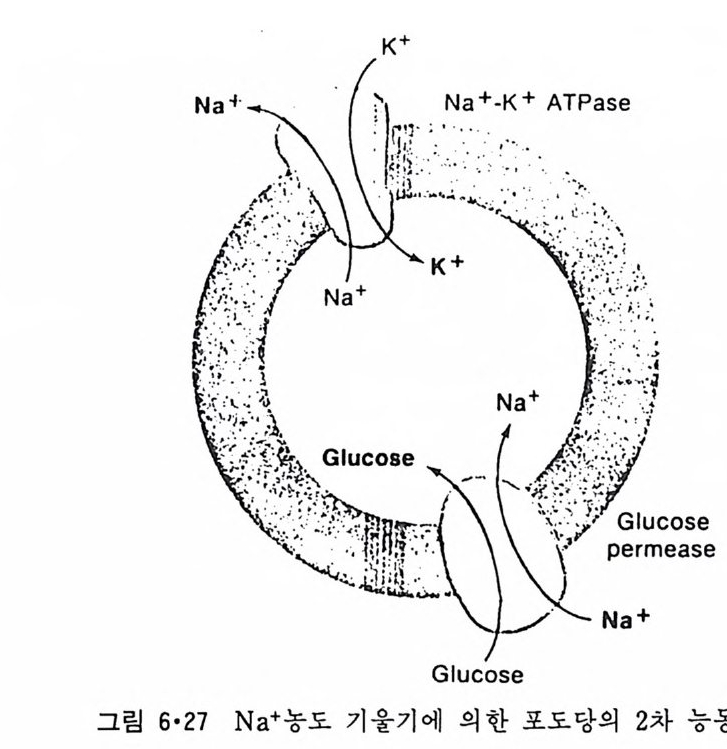 K+
K+
차 능동운반이 일어나는 것을 공동운반 (co t rans p o rt 또는 s ymp o rt)이라고 부른다. 그림 6·28 에서 보는 것과 같이 공동수송은 가역적이어서 lacto s e 같은 이차 능동수송이 되는 물질의 gr ad i en t하에서 일차 능동수송되는 물질이 이동되기도 한다. 양성자(p ro t on) 가 야기시키는 2 차 능동운반의 mechan i sm 은 1963 년 M it chell 이 그의 화학삼두 (chem i osmo tic) 가설의 일환으로서 제안한 것 으로 여기에 따르면 그림 6·29 에서와 갇이 ATP의 가수분해나 호홉 (respi ra ti on ) 에 의 해 생 성 된 양성 자 전 기 화학 기 울 기 (pro to n electr o - chem ica l grad ie n t) 가 여 러 가지 분자나 i on 을 수송하는 ener gy의 근원 이 된다. 양성자 전기화학 기울기는 다음 식으로 표시가 된다., !!,. µH+I:; = !!,.
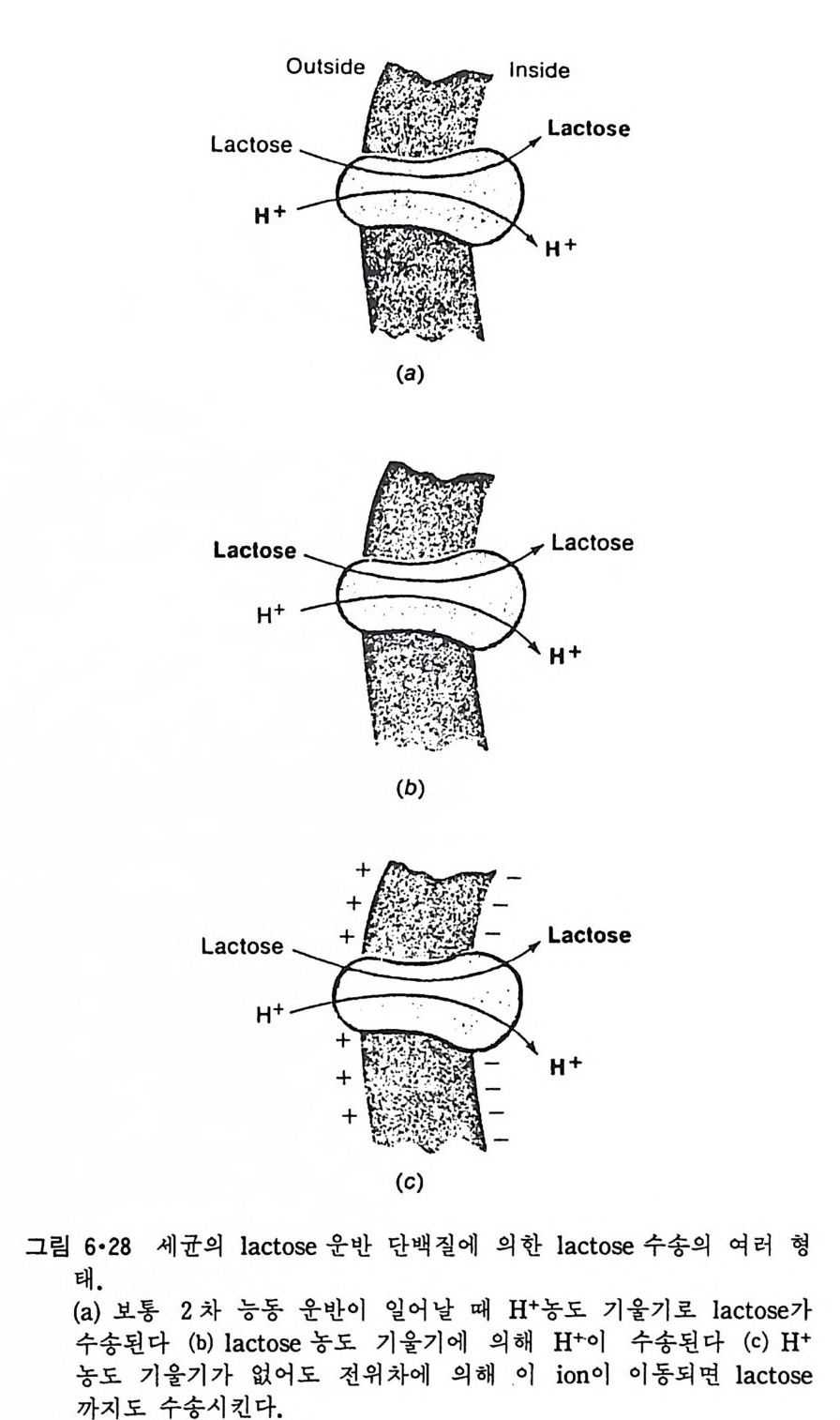 Lacto s e Lacto s e
Lacto s e Lacto s e
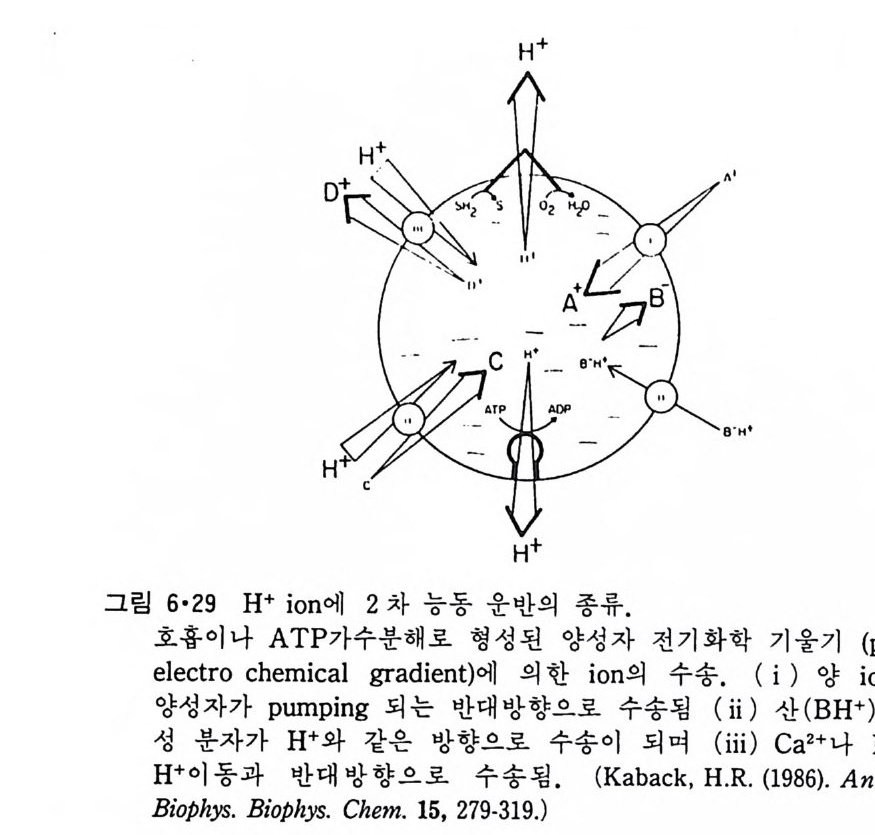 H+
H+
lac t ose 등은 H+ 와 같은 방향으로 이동되며 Na+ 와 Ca2+ 같은 i on 둘은 반 대 방향으로 이동된다. 2 차 능동운반 sy st e m 중에서 lac t ose 의 수송이 가장 찰 알려져 있다. Lac t ose 의 수송이 화학삼두 mechan i sm 에 의 한 것 이 라는 것은 M itch ell 이 1963 년에 제창하였고 E. coli 에서 lac t ose 가 수송됨과 동시에 외부용 액의 p H 가 높아지는 것이 관찰되었다. Lac t ose 수송은 2, 4-din i t r- o p henol 같이 막의 양성자 기울기를 없애는 화합물에 의해 저해가 되고 E. col i의 전자이동을 촉진시키는 화합물에 의해서 가속이 되는 것으로 보야 양성자의 수송과 lac t ose 의 수송이 직접 관계되는 것을 알 수 있다. Lac t ose 를 수송하는 lacto s e pe nnease 는 내재단백질로서 비 i on 성 세 타제로 분리할 수가 있다. 이 단백질은 lac t ose 를 이동시키지 않는 E. col i의 돌연변이체 (muta n t) 에 첨가하면 이 물질을 이동시키는 능력이 생기며, 정제된 lacto s e pe nnease 를 인산지방질 막소포에 재구성시키면 인공적으로 생성된 H+ 농
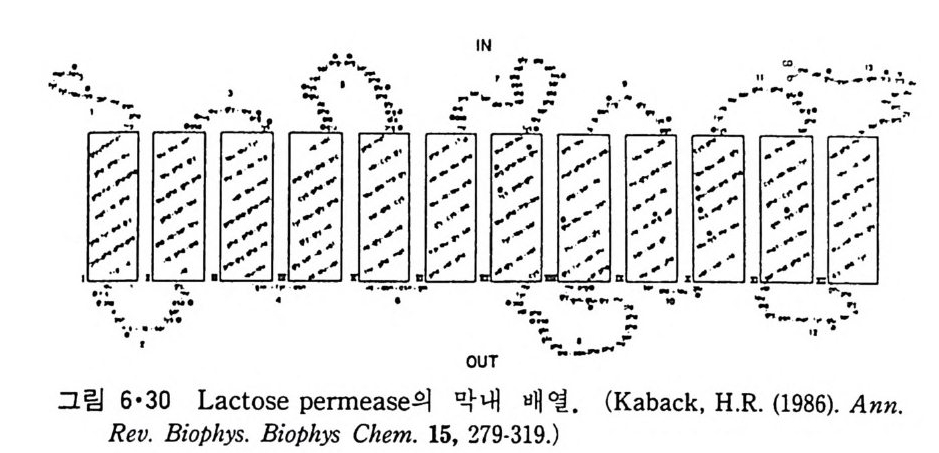 1-.~..., : 낫,IN --.. ~o ...를- • ._. •. . - ~· --,' ••
1-.~..., : 낫,IN --.. ~o ...를- • ._. •. . - ~· --,' ••
도 기 울기 존재 하에 서 lac t ose 를 수송시 킨 다. Lacto se p ennease 의 분자 량은 SDS-PAGE 방법에 의하면 약 33kDa 이 된다. CD 실험결과로는 막 내에서 이 단백질의 85% 가 나사선 2 차 구조를 갖 고 있으며 그 am i no 산 배열로부터 그럼 6·30 에서 보는 바와 같이 a- 나사선이 막을 12 회 횡단하 는 것으로 생각되고 있다. 6·3 분자단 운반 (Group tra nslocati on ) 12'•13 > 이것은 물질이 막을 동해 이동시 화학적인 변화를 동반하는 것으로 제
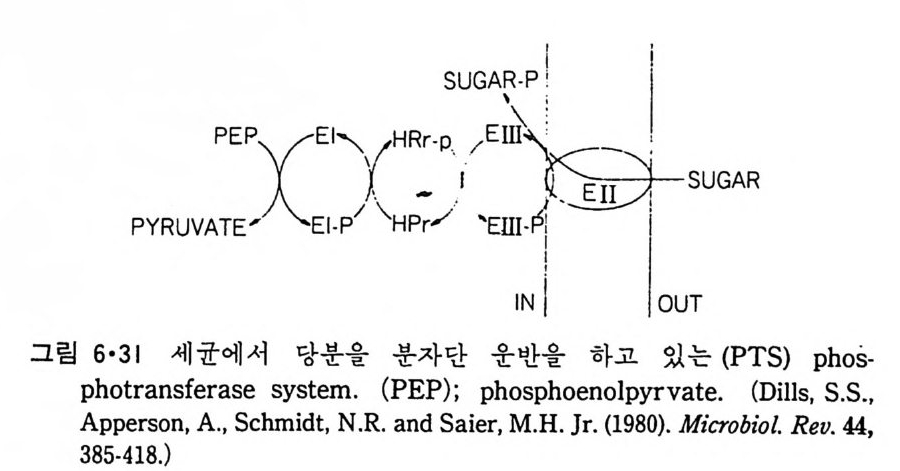 그림 6•31 세균에서 당분을 분자단 운반을 하고 있는 (PTS) ph os-
그림 6•31 세균에서 당분을 분자단 운반을 하고 있는 (PTS) ph os-
일 연구가 많이 된 것 이 세균의 당분 ph osph otr a nsfe r ase s y s t em(PTS) 이 다. PTS 는 당분을 원형질막을 통해 수송할때 동시에 인산화시킨다. 이 때 에 ph osph oenolpy ruv ate ( PEP) 가 P 의 주개 (donor) 역 할을 한다. 이 s y s t em 에 의해서 세균의 원형질막을 통해 수송되는 당분은 포도당, mannose, fruc to s e, N-acety lg l u cosami ne , manit ol, g lu cit ol 과 ga lacto t a l 이다. PTS 에 의한 당분 수송의 개요는 그림 6·31 에 보여준다. 이 s y s t em 은 몇 개의 수용성 단백질과 몇 개의 내재단백질로 구성되어 다음 순서로 당E분nPz이Ey mP수 e + 송 IE된 ~n다zPy. m+ e HIP r= === E HnPr~P + Enzy me I zy me I ~ P + pyru vate HPr~P + 당분 (ou t) ~(EEnnzzyy mm ee DII I) HPr + 당분(i n)-P PTS s y s t em 에서 Enzy me I 과 HPr 은 세포액 내에 있는 수용성 단백 질로서 모든 당분 수송에 공통되는 단백질들이다. Enzy m e II 는 내재단 백질로서 한가지 당분만을 p hosp ho ry la ti on 시 ~l 는 동시에 수송시킨다. Enzy me II 는 항상 필요한 것은 아니고 포도당 등 몇 가지 수송을 하 는 PTS s y s t em 에만 존재한다. 이것도 역시 당분에 대한 선택성을 갖고 있고 생체막 단백질인지는 확실치 않다. 원형 질막을 통한 지 방산 p ur i ne 과 pyri m i d i ne 동도 분자단 운반 mechan i sm 에 의해서 수송된다고 제안은 됐지만 이들에 대한 중거는 아 직 미흡하다. * 6 장 참고문헌 (1) Dahl, J. L. and Hokin , L. E. (1974). Ann. Rev. Bi oc hem. 43, 327-356. (2) Glyn n, I. M. and Korlish , S. J. D. (1975) Ann. Rev. Phys i o l . 37, 13-55. (3) Skou. J. C. (19 75). Quart. R ev. Bi op h y s . 7, 401-434. (4) Jo rge nsen, P. L. (1982). Bio c him , Bio ph ys . Acta . 694, 27-68. (5) Skou, J. C. and Norby, J. G. (eds) Na, K-ATPase, Str u ctu re and Ki ne ti cs. Academi c. N. Y. 1979. (6) Skou, J. C. (1957) Bio c him . Bi op h y s . Acta . 23, 394-401 . (7) Ikemoto , N. (1982) Ann. Rev. Phys i o l. 44, 297-317. (8) Hasselbach, W. and Oetl ike r, H. (1983) Ann. Rev. Phys i o l . 4 5, 325-339. (9) Sto c keniu s , W., Lozie v , R. and Bog o molni, R. (1979) Bio c him . Bi op h ys . Acta .
505, 215-278. (10 ) Sto c keniu s , W. (1980) Acc. Chem. Res. 13, 337- 34 4. (11) Sto c keniu s , W. and Bog o molni, R. A. (1982) Ann Rev. Bio c hem. 52, 587-616. (12) Rosen, B. P. (ed.) Bact e r i al Trans po rt . Dekker, N. Y. 1978. (13 ) Dil ls, S. S., Ap pe rson, A., Schmi dt , M. R. and Saie r , M. H. Jr. (19 80) Mi cr obia l . Rev. 44, 385- (14 ) Kaback, H. R. (19 86) Ann. Rev. Bio p h y s . Bio p h y s . Chem. 15, 279-319. (15) Saie r , M. H. Mechansim and Regu lati on of Carbohyd rate Trans po rt in Bacte r i a, Academi c. N. Y. 1985. (16 ) Ullri ch , K. J. ( 1979) Ann. Rev. Phys i o l . 41. 181-195. (11) West. I. C. (1980) Bio c him , Bio p hy s . Acta . 604, 91-126.
제 7 장 생체전기현상 원형질막을 동한 Na+ i on 과 K+ i on 의 능동운반은 막전위차를 형성하여 세포 내부가 의부보다 약 60mV 만큼 낮은 전위를 갖게 한다. 생물체는 이 막전위차를 신경전달 등 세포 내에서나 세포 사이의 동신 (commun ic a ti on) 에 주로 이용하고 있지만 전기닌심장어 등은 실제로 전기를 발산하여 공격과 방어의 수단으로 이용한다. 이러한 생체전기현상 (b i oelec t r ic p henomena) 은 원형질막을 통한 i on 의 두과속도가 잠정적으로 그리고 선 택적으로 변할 때 일어나는 것이다. 잠정적인 i on 투과속도의 변화는 원 형질막 내의 내재단백질로 구성된 막문(g a t e) 이 가해진 자극예 의해서 열 리기 때문인데 이 자국에는 전위차, 화합물, 광선, 압력들이 있다. 신경 과 근육의 생체전기현상은 전위차와 화합물에 의한 것이고 시각은 광선 에 의한 것이며 청각은 압력에 의한 것이다. 7 •1 전 압에 의 해 열 리 는 통로 (Volt ag e -ga t ed channel) 전압에 의해 열리는 통로는 신경세포내에서의 신경신호의 전달 (nerve im p u lse 또는 sig na l conducti on ) 의 기 본이 된 다. 그 림 7 • 1 은 전 형 적 인 신 경세포를 보여준다. 신경세포도 다른 세포와 마찬가지로 생존에 필요한
오든 기능을 갖추고 있지만 다른 세포와의 형태학적인 차이접은 신경신 호를 받아들는 돌출부인 den t r it e 가 많고 신호를 다른 신경세포나 근육세 포로 전달하는 건 axon 이 있다는 접이다. 신경세포나 근육세포와 같은 감각세포들과 다른 세포와의 차이는 원형질막에 여러가지 자국을 감지하 여 i on 의 통과속도를 가해진 자극에 따라 증가시키는 내재단백질이 있는 것이다.
 NODE OF RANVIER
NODE OF RANVIER
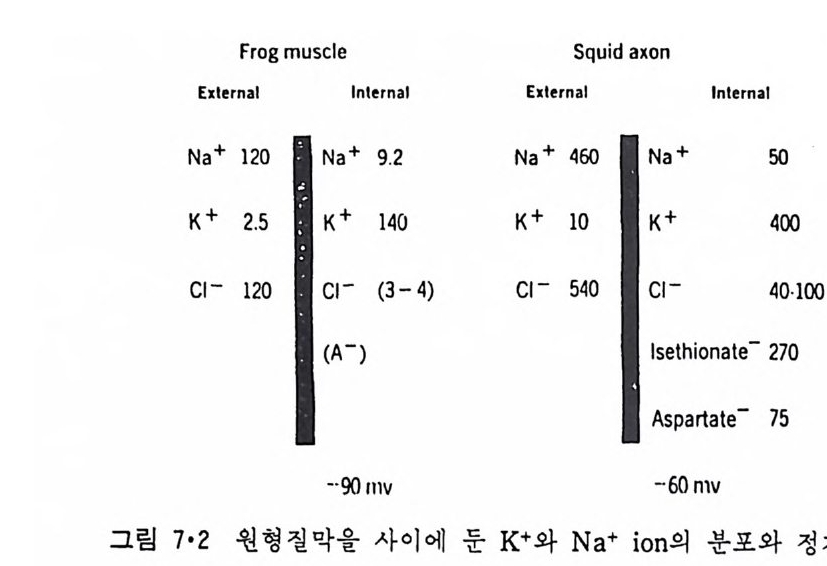 Frog muscle Sq ui d axon
Frog muscle Sq ui d axon
7 • 1 • 1 활동전 위 (Act ion po t en t ial) Na+ , K+ - ATPase 에 의한 i on 들의 능동운반은 세포내의 전위를 외부에 비해 낮게 만드는데 그림 7·2 는 개구리 근육과 오징이 axon 의 원형질막 양쪽에서의 양i on 들의 분포와 전위차를 보여준다. 이 전위차를 정지전위 (resti ng po te n t ial ) 라고 하는데 이 는 Donnan 막 전 위 차와 i on 들의 능동운 반에 의한 것이다. 신경기능이 전기와 관련이 있다는 것은 이미 19 세기 초에 Galvan i에 의해서 밝혀졌는데 생체전기현상의 mechan i sm 의 해명에 크게 공헌한 것 온 1930 년대부터 오징어의 거대한 axon 을 전기생리학적으로 연구한 Hod g k i n 과 Huxle y이 다. 이 axon 의 칙 경 이 0 • 1 ~ 1mm 나 되 어 직 경 0 • 5 µm 정도의 작은 전국으로 전기적인 성질을 측정할 수가 있었다. 그림 7· 3 은 전형적인 실험방법을 보여준다. 이 장치에서 자국전국 (s ti mula ti n g elec t rode) 으로 전류 p ulse 를 통하고 그 반응을 기록전국 (record i n g elec t rode) 으로 측정하는 것인데 이 두 전국의 거 리는 약 50µm 정도로 유 지한다. 양쪽 전국이 모다 외부에 위치하고 있을 때에는 전류 p ulse 를 동해도 아무 반응이 없고 기록전국이 axon 내부로 들어갔을 때에도 기록 전위만 기록될 뿐 전류 p ulse 에 대한 반응은 없다. 자극전국까지도 axon 내부에 들어간 후에는 전류 p ulse 를 통하면 반응이 나타나기 시작한다.
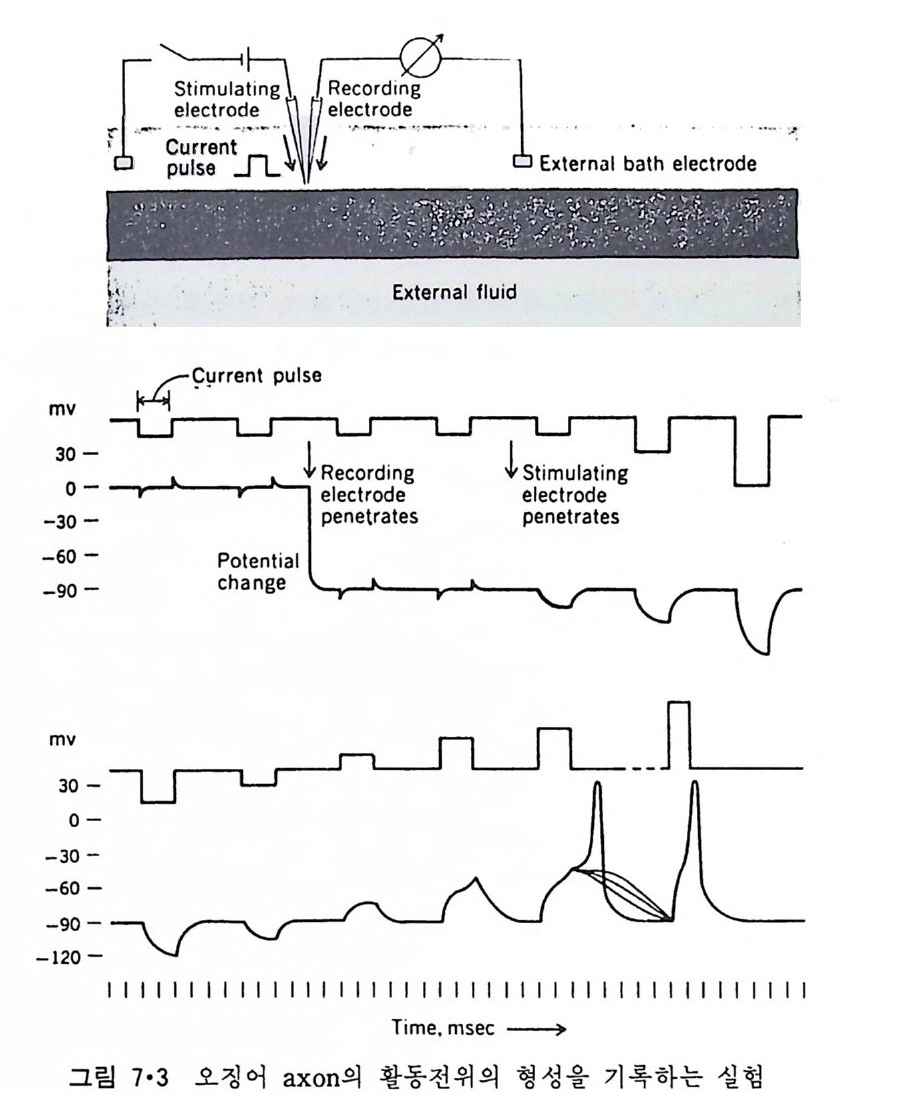 3o0--I_`p:' t5 4 u ~ 广 2 2’ i5 三 빠nt『 끄\ t>Re: leeFcco t.r r:odl ::dm eE广二> g<만t er广 nal? fl.ui d 5 .D ?Ex t: e.r n? a > b. a§ th ,; ;e ':e c .t ' r, 。· 홍d e •I /.
3o0--I_`p:' t5 4 u ~ 广 2 2’ i5 三 빠nt『 끄\ t>Re: leeFcco t.r r:odl ::dm eE广二> g<만t er广 nal? fl.ui d 5 .D ?Ex t: e.r n? a > b. a§ th ,; ;e ':e c .t ' r, 。· 홍d e •I /.
가해진 전류가 axon 내부를 더 음성으로 만들면 기록전국에도 보다더 음 성인 신호가 기록되나 이것은 신호 p ulse 와 모양이 달라 전위차가 서서 히 중가하다가 전류가 끊어 지 면 서 서 히 감소한다. Pulse 의 증폭을 증가 하면 이에 대한 반응도 비례해서 증가한다. Axon 의 내부가 정지전위보 다 더 양성이 되도록 전류를 통하면 먼저의 경우와 대칭이 되는 반응을 보여준다. 그러나 가해준 전압의 세기가 어느 값 이상이 되면 일정한 크 기의 전위차가 생성된 것이 기록되며 이 전위차는 일정한 속도로 axon 을 따라 이동된다. 이 활동전위 (acti on p o t en ti al) 는 신경신호 전달의 기본이
되는데 이것을 일으키는 최저의 전위차를 시발점(t hreshold) 이라 하며 그 이 하의 전 위 차를 亞시 발전 압 (subth r eshold po te n ti al ) 이 라고 한다. Axon 은 여 러 가지 의 미 에 서 海底電線 (marin e cable) 과 비 슷하다. Axon 내의 세포질 (axo p lasm) 이 전기를 통하는 銅線 역할을 하고 그 막이 절연 체(i nsula t or) 역할을 한다고 볼 수 있다. 그러나 수용액인 axo p lasm 은 그 전기전달도 (conduc ti v ity)가 구리에 비해서 수백만분의 1 밖에 안되고 막도 상당히 약한 절연체 역할밖에 못해 axon 에 짧은 전류 를 통했을 때 이것 이 전달되는 거리는 상당히 짧다. 이러한 약점을 보강하기 위한 것이 활 동전위에 의한 증폭현상이다. 그림 7·4 는 활동전위의 여러가지 단계를 보여준다. Axon 이 전기적으 로 자국되면 정지전위인 ― 60mV 에서 전압이 급속히 중가해 내부가 +40mV 정도 까지 올라갔다가 서서히 내려와 정지전위로 되돌아오나 일 단 전보다 낮은 전위차를 가진다. 이 현상을 설명하기 위하여 Hod gk i n 과 Huxle y는 Na- i on 가설을 제안 하였다. 이 가설에 의하면 axon 내부의 전위가 중가하여 시발점 (thr eshold po in t ) 에 도달하면 Na+ i on 의 막투과속도가 중가되 어 Na+ i on 이 급속히 axon 안으로 들어 가게 되고 이렇게 되면 내부의 전위가 더 증가되며 이 러한 연쇄반응이 계속된다. 곧 이어서 K+ i on 의 막두과속도도 중가되는 데 이 것도 내부의 전위 가 높을수록 커 진다. 막두과속도의 중가로 K+ ion
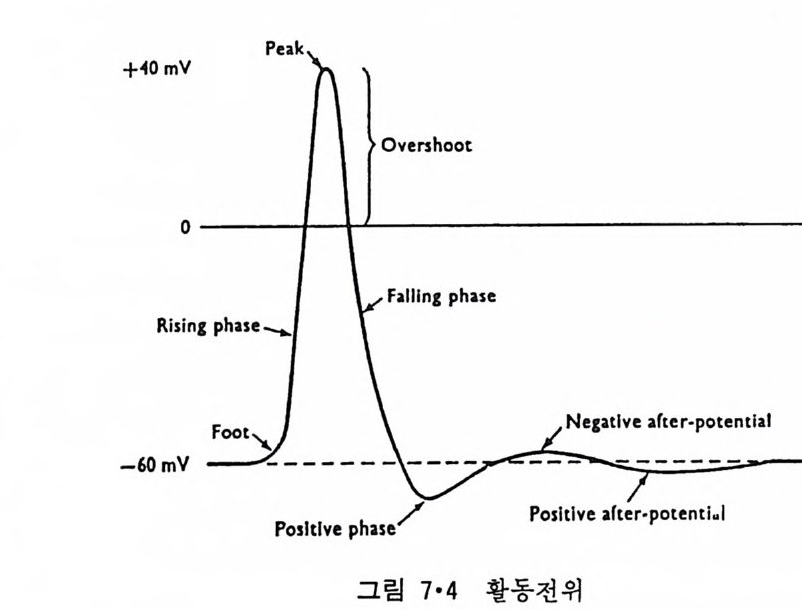 + ◄ OmV
+ ◄ OmV
이 밖으로 많이 나오면 내부가 더 음성이 되며 이것은 K 가 on 의 막투과 속도를 감소시키고 이 결과는 Na + 이동의 효과와 정반대가 된다 . 한편 Na+ i on 의 막투과속도 증가는 잠정적인 현상이며 K + i o n 이 이동될수록 활 동전위를 감소시키고 이렇게 되면 K+ i on 의 이동이 더 감소된다 . 이러한 두 효과는 막전위차를 서서히 정지전위로 회복시키는 결과를 가져온 다. 그러나 정지전위로 접근하기 전에 Na+ ion 막 이동속도의 급격한 감소가 K+ ion 이 동속도에 의 한 axo n 내 부의 음성 화를 감당하지 못해 a x on 내 부
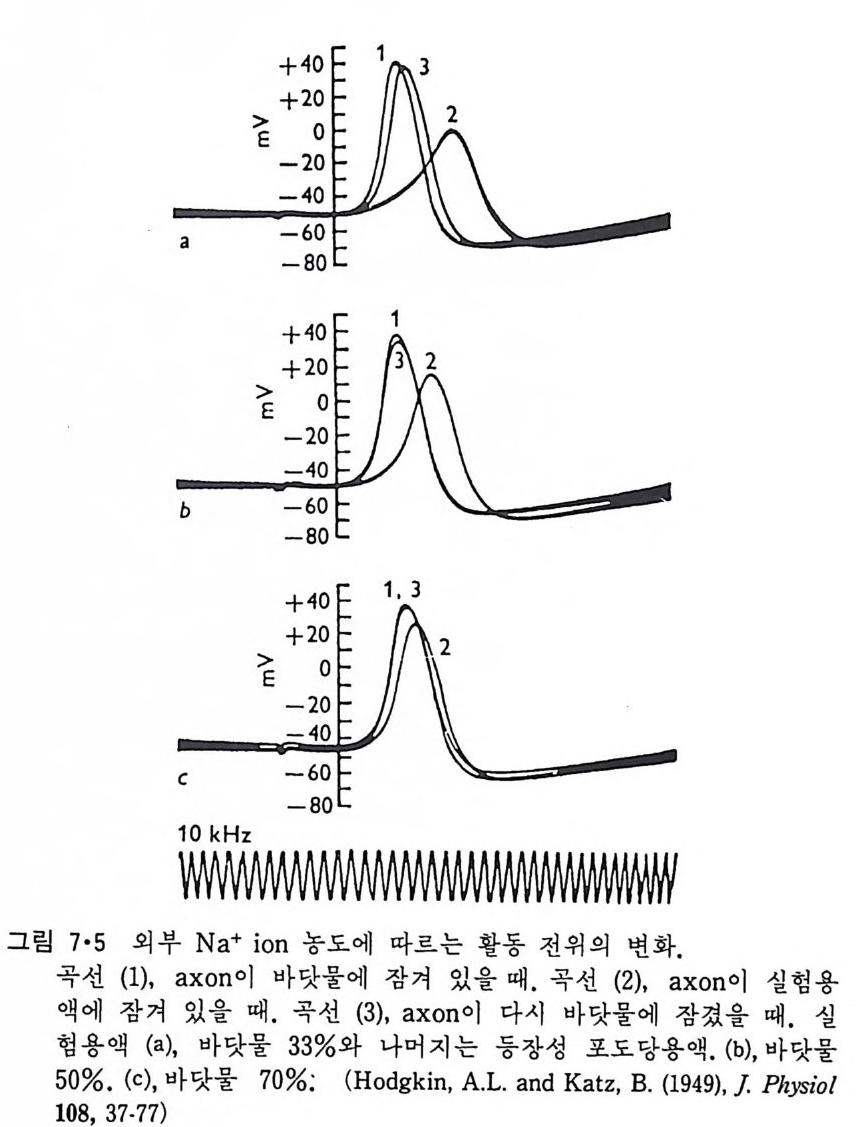 +40
+40
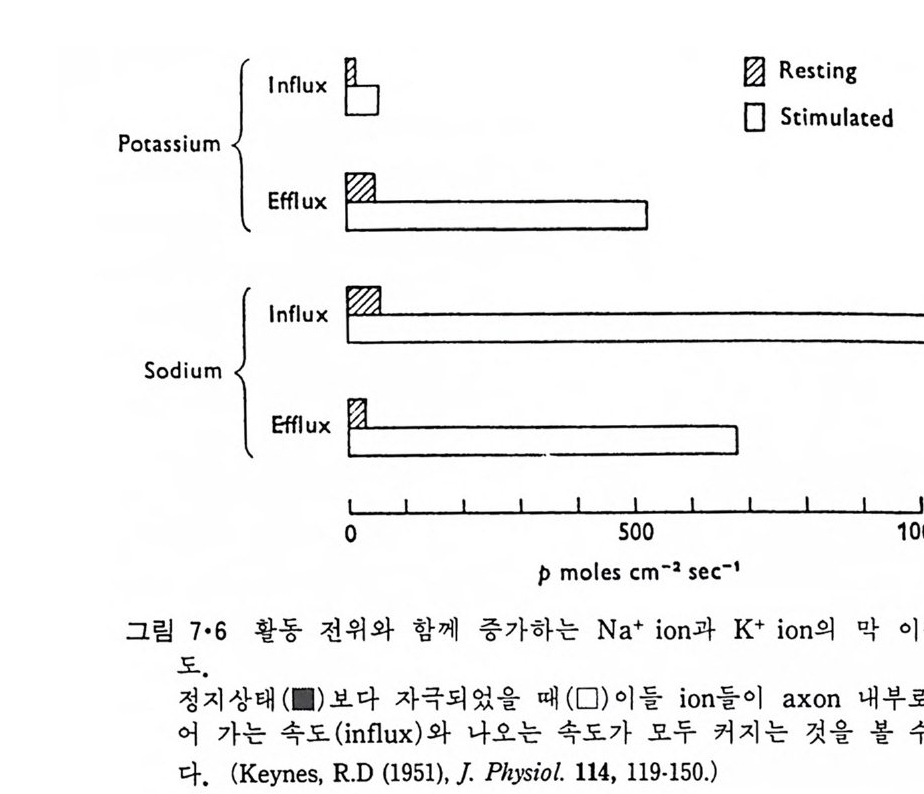 Infl ux ~ ~D RSteis mti u nlga t e d
Infl ux ~ ~D RSteis mti u nlga t e d
가 잠정적으로 정지전위보다도 더 음성이 된다. 이상의 Na- i on 가설의 실험적인 증명은 우선 밖의 Na+ 농도가 감소되면 활동전위가 감소되는 것으로 알 수 있고(그림 7·5), 다음 활동전위가 진 행될 때 실제로 이 두 i on 이 정지전위 때보다 훨씬 더 많이 이동되는 것 울 방사선동위원소 측칭으로 알게 되었다(그림 7·6). Na+ 와 K 며 막두과속도가 전위차에 좌우되는 것은 전압고정 (volt ag e clam p)실험에 의해서도 증명이 되었는데 이 방법의 원리는 그림 7·7 에 보여준다. 여기서 막 전위차를 f eedback 회로(ci rcu it)에 의해 일정한 값 으로 고정시킨 후 전류가 시간에 따라 변하는 것을 측정한다. 그림 7·8 에서 보이는 것과 같이 처음에 전류는 안쪽으로 흐르고 다음 방향이 변 하여 외부로 흘러 일정한 값으로 접근한다. 이 전류-시간 곡선에는 Na+ 에 의한 전류와 K+ 에 의한 전류 두 성분이 있다. 그림 7·9 는 전압을 0 으 로 고칭시켜 놓고 두 외부 Na+ 농도에서 전류를 각각 측정한 것을 보인 다. a 는 오징어 axon 을 바닷물에 담그고 실험을 한 것이고 b 는 바닷물 은 10% 함유하고 나머 지 는 cho li ne 을 첨 가해 서 등장성 (iso nic ) 은 같지 만
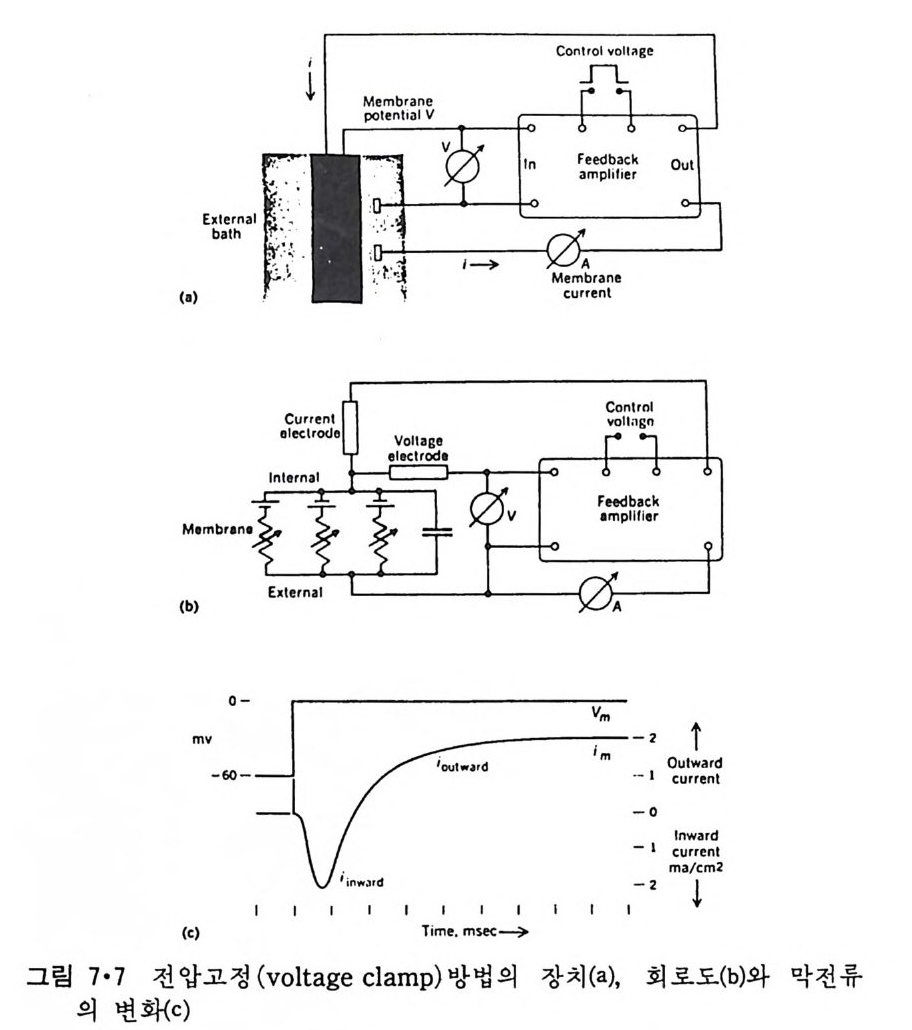 Ltt
Ltt
Na+ i on 의 전기화학적인 전위차는 0 이 되는 조건하에서 전류를 측정한 것이다. b 의 경우에 전류는 K+ i on 의 이동에서만 생기는 것이라고 볼 수 있다. a 곡선에서 b 곡선을 빼면 c 선이 되는데 이것이 N 갑에 의한 전류라 고 볼 수 있다. 이들로부터 고정된 전위차 하에서 Na+ 는 내부로 급속히 이 동되 고 약 500µsec 후에 는 이 속도가 감소되 기 시 작해 서 5msec 후에 는 N 갑이동이 정지된다. 한편 K+ i on 은 Na+ i on 전류가 시작된 잠시후에 밖으로 이동이 시작되어 계속 중가하며 6~7msec 후엔 일정 속도에 도달 하여 이 값을 유지하게 된다. 그림 7·10 은 전위차에 따라 i on 들의 이동 도가 달라지는 양상을 보여준다. 죽 N 찰의 아동도나 K+ 의 이동도나 모
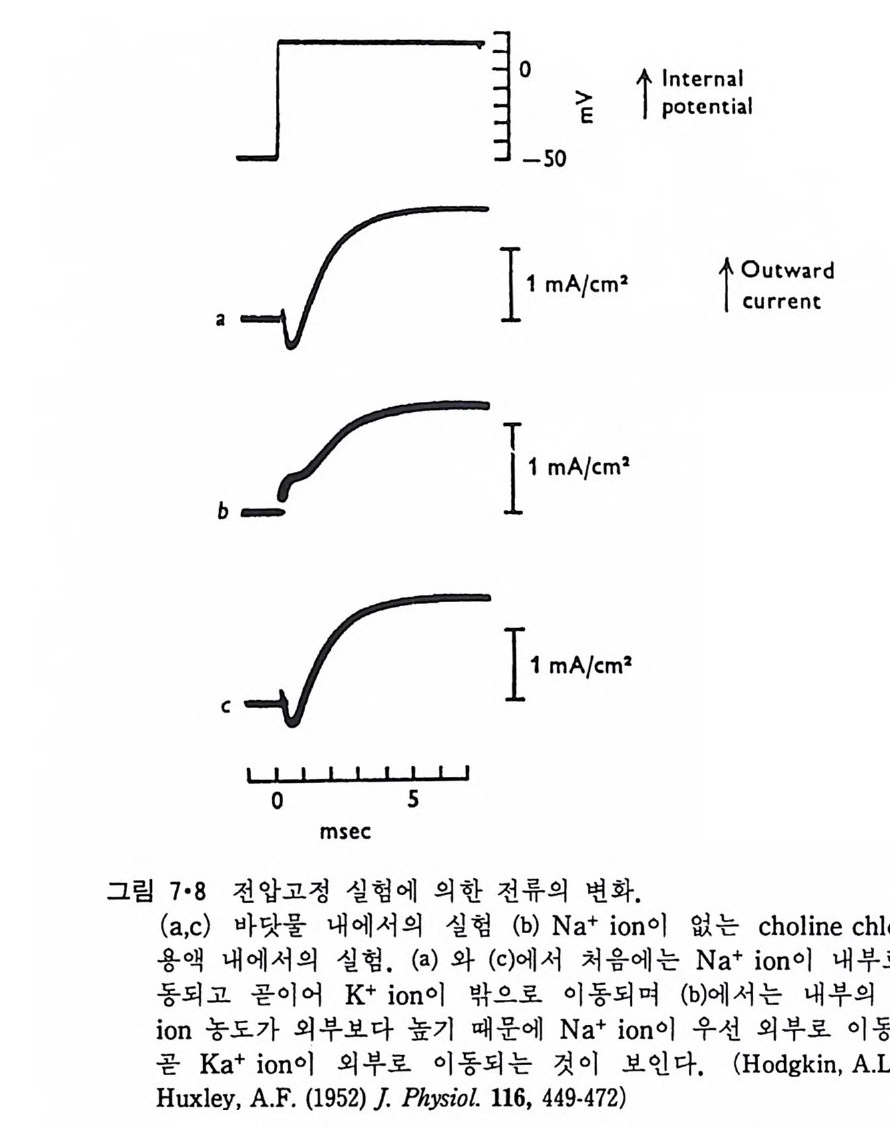 」 『- 50 즘 1pIn ott ee r nntai la l
」 『- 50 즘 1pIn ott ee r nntai la l
두 전위차가 클수록 그 값이 커지고 또 이들은 각각 독특한 시간적인 변 화를 갖게 된다. Hod gk i n 과 Huxle y는 이들 Na+ 와 K+ 의 이동도가 전위 차와 시간에 따라 변하는 함수로 실험식을 얻어 이것으로부터 활동전위 를 계산하여 이 결과가 실험치와 일치하는 것을 보였다(그림 7·11). 이 것으로부터 그들은 감국화 (de p olar i za ti on) 에 의해서 전압변화에 민감한 막문이 열리어 i on 들의 이동도가 중가되는 것이며 또 두 i on 에 의한 전류 의 변화가 시간적으론 다른 것으로 보아 Na+ 와 K+ 가 각각 다른 막문을
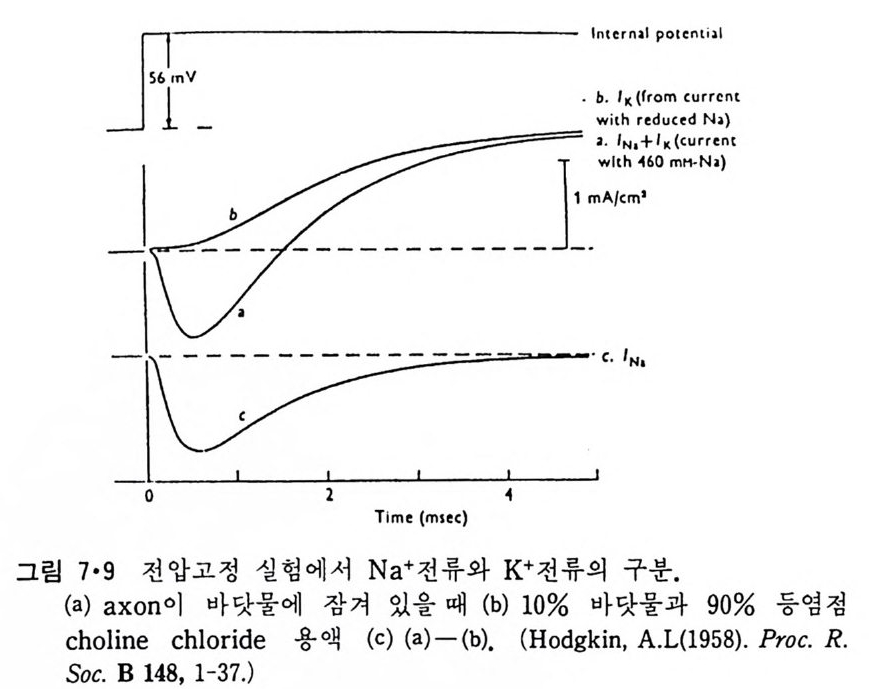 戶J1m I n:t e:[ rn;• l! op:o1 t tcnu t r;, :1' ;:
戶J1m I n:t e:[ rn;• l! op:o1 t tcnu t r;, :1' ;:
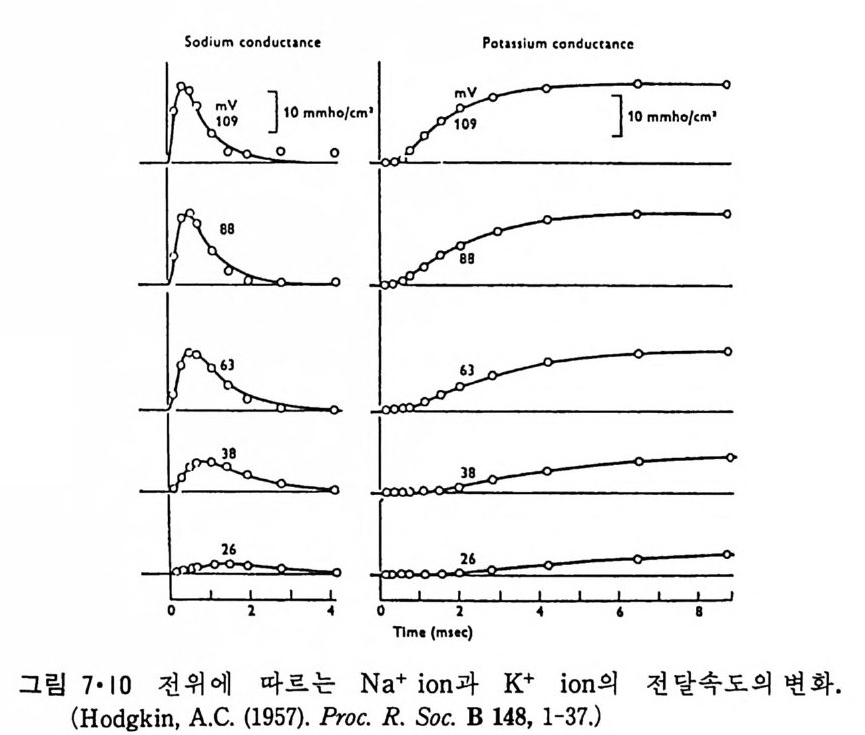 Sodiu m condumnc t Pot 1 11l um to ndumnce
Sodiu m condumnc t Pot 1 11l um to ndumnce
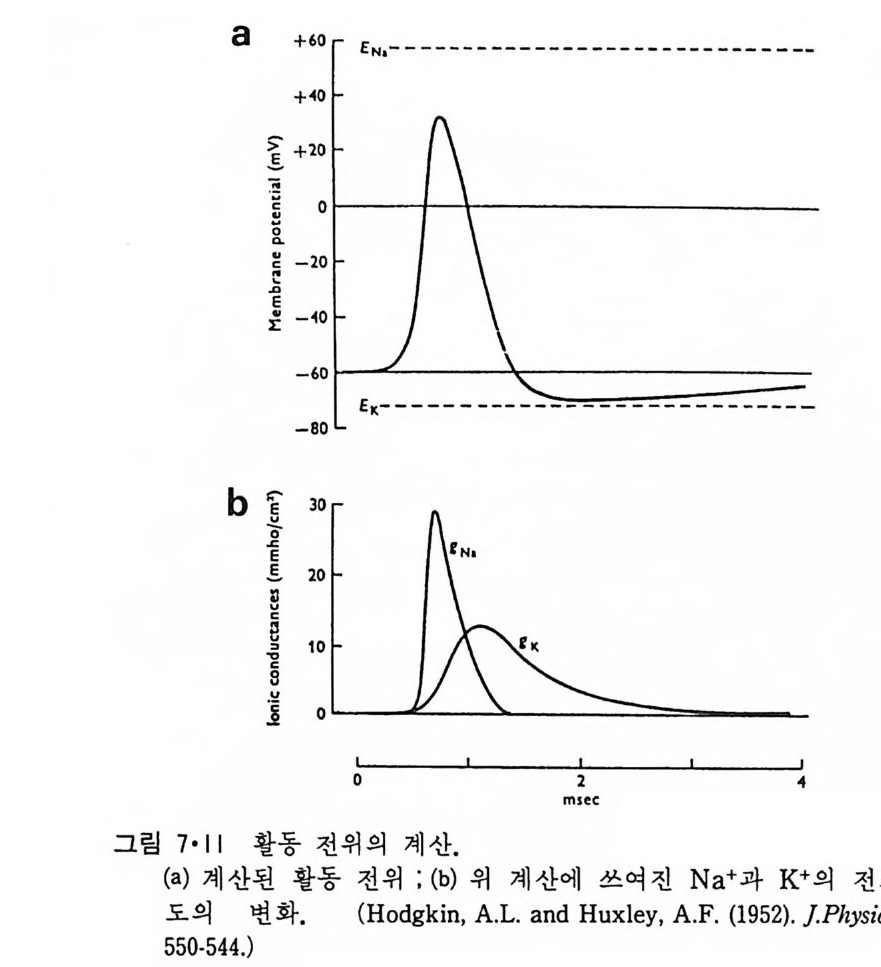 a +60 EN,-- - --- -- ---- ---- --- -- ---- --- - -
a +60 EN,-- - --- -- ---- ---- --- -- ---- --- - -
통과한다고 결론을 내렸다. 이상의 결과로서 신경신호의 전달은 전기적인 자국에 의해서 Na+i on 의 이동도가 중가하다가 감소하여 원래상태로 돌아오며 이와 동시에 K+ 이 이동속도가 증가하여서 이루어지는 것이다. 어느 한 위치에서 활동전 위가 일어나면 이와 인접하여 있는 부분의 전위차가 시발(t hreshold) 전위 보다 높아져 활동전위가 생기며 이 과정이 계속되어서 결국 신경말초에 까지 활동전위가 도달하게 된다. 모든 척추동물의 axon 은 오징어 ax 야 과는 달리 m y el in으로 감싸여 있다. 척추동물에서는 신경의 전달사항이 대단히 복잡해 많은 종류의 정보가 신속히 전달되어야 한다. 이를 위하 여 axon 의 신호전달 능률이 오징어에 비해 크게 향상되어야 하는데 이는
axon 의 많은 부분을 절연(i nsula t e ) 시킵으로써 이루어졌다. 그림 7·12 는 m y e li n 으로 감싸여진 axon 을 보여준다. Axon 표면의 거의 전부가 m y e li n 으로 감싸여 있지만 일정한 간격을 두고 노출된 부분이 있는데 이 것 을 Ranv i er 의 마 디 (node) 라고 부른 다. 이 m y el i n 에 의 한 절 연 때 문에 전 위 의 감소 (att en uati on ) 가 훨 씬 적 게 된 다. 한 Ranv i er 의 마 디 에 서 활
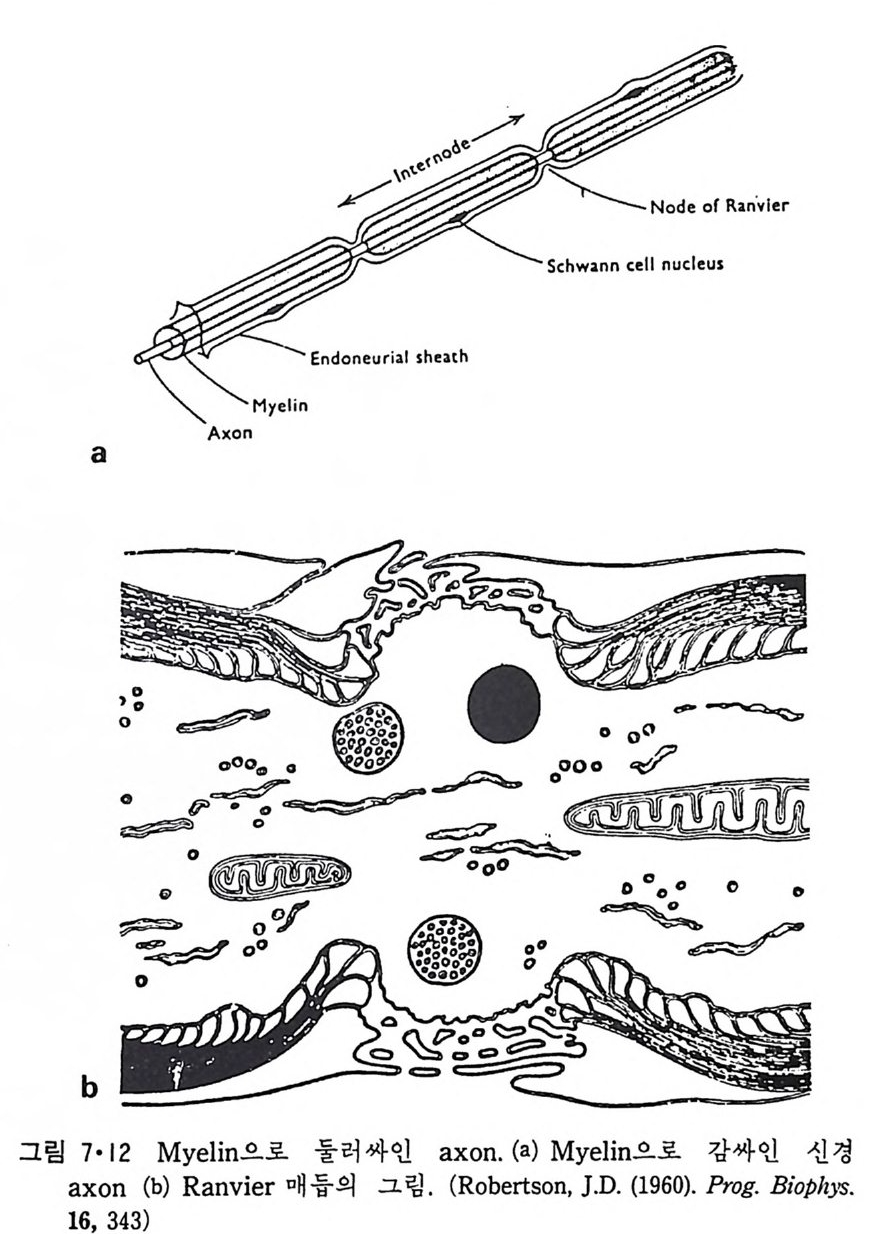 Schwann cell nucleus
Schwann cell nucleus
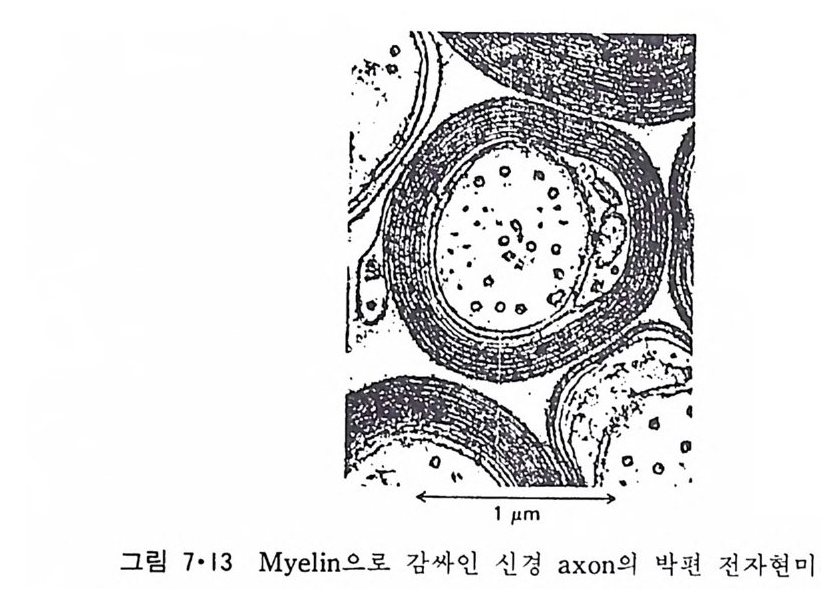 그림 7· 13 M y e li n 으로 감싸인 신경 axon 의 박편 전자현미경사진
그림 7· 13 M y e li n 으로 감싸인 신경 axon 의 박편 전자현미경사진
동전위가 일어나면 절연된 부분은 전위의 감소가 적어 장거리를 빨리 웅 직여 다음 Ranv i er 의 마디까지 신호가 빨리 가고 거기서 다시 활동전위 의 증폭이 일어난다. 이렇게 m y e li n 으로 감싸인 axon 은 직경이 작으면 서도 신호를 신속히 전달할 수 있게 한다. M y e li n 이 axon 을 절연시킬 수 있는 것은 그림 7·13 에서 볼 수 있는 것과 같이 주로 지방질로 구성된 m y e li n 막이 여러 겹으로 axon 을 감싸 고 있기 때문이다. M y e li n 막은 20~30% 의 단백질과 나머지는 지방질로 구성되어 있다. 7·1·2 전압에 따르는 膜門(g a t e)5 >-B> Hod g k i n 과 Huxle y의 전압고정실험 결과는 Na+ 와 K+ 의 이동이 각각 독립적으로 이루어지는 것을 의미하기 때문에 이들이 통과하는 두 가지 막문이 있다는 결론이 된다. 여러가지 단백질의 작용제에 대한 반응으로 부터 이들이 단백질이라는 것이 판명되었다. 표 7·1 은 이 두 막문을통한i on 들의 상대적인 투과속도를수록하였다. Na+ 막문에 서 hydrox y lam i ne 과 u+ i on 은 거 의 Na+ i on 과 같이 찰 통과되 나 K+ i on 은 Na+ 의 약 1/12 의 속도로 밖에 통과시 키 지 않는다. K+ 막문은 Rb 니끝 잘 통과시키지면 Na+ i on 은 통과시키지 않는다. 그래서 이 실험
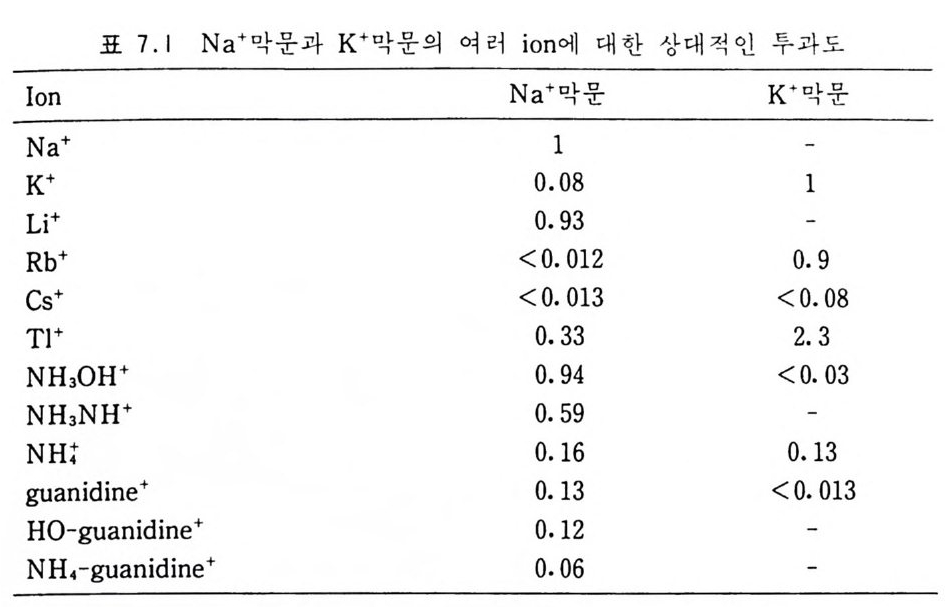 표 7.1 Na + 口-,l-문과 K 딱문의 여러 i on 에 대한 상대적인 투과도
표 7.1 Na + 口-,l-문과 K 딱문의 여러 i on 에 대한 상대적인 투과도
결과는 막문과 이룰 통과하는 i on 이 크기와 모양이 서로 맞아야 된다는 것을 시사한다. 그러나 위 조건만 가지고도 충분치 못하다는 것을 Na+ 막문이 hy d roxy la mi n e(0H-NHt ) 이 나 hy d razin e (NH2-NH! )를 찰 통과시켜도 이와 크기가 거의 같은 me t hy larn i ne(CH3 一 NH!) 을 통과시 키지 않는 것으로 볼 수 있다. 이것의 설명은 Na+ 구멍은 음성하전을 떤 산소가 그 내부 표면에 존재하여 OH 기나 NH2 기를 갖는 양 i on 을 수소 결합을 통해 쉽게 동과할 수 있지만 소수성기인 CH3- 기를 갖는 양i on 은 수소결합을 할 수 없기 때문에 이 것은 통과하지 못한다. Na+ 막구멍에 -c?- o 기가 있다는 것은 p H 가 낮을 때 양 i on 의 두과속도가 감소되며
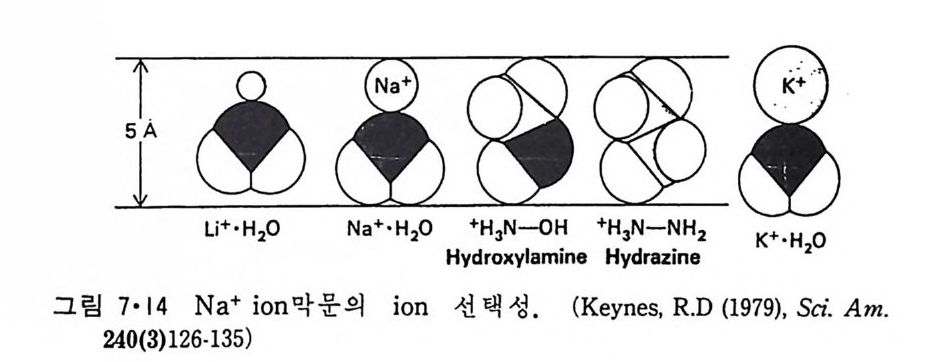 u+•H20 Na+·H20 .. +~3N- 0H +H3N-NH2 K+.H2°
u+•H20 Na+·H20 .. +~3N- 0H +H3N-NH2 K+.H2°
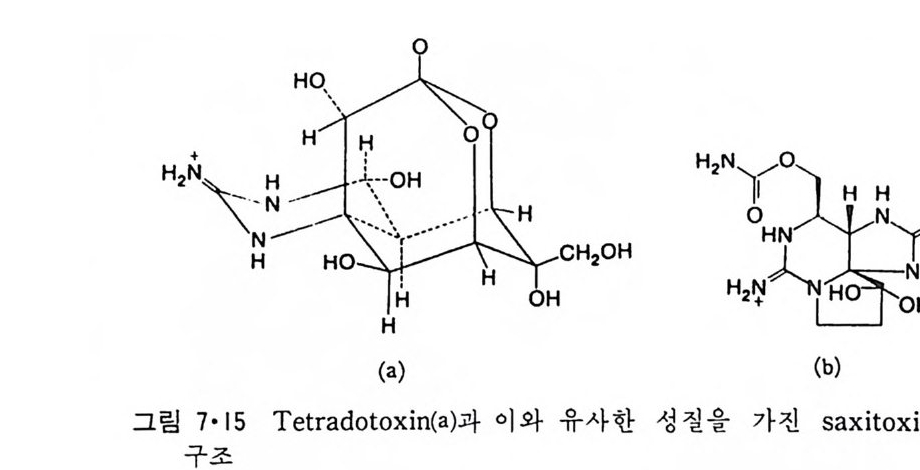 \섭H 一 H CH20H H2 N\/_-NOHo人H 2N 노+ IN
\섭H 一 H CH20H H2 N\/_-NOHo人H 2N 노+ IN
p H 에 따르는 투과속도는 p Ka 값이 5.2 인 carbox y l 기 의 적 정 curve 와 갇 은 것으로 알 수 있다. 그림 7 • 14 는 Na+ i on 이 수화물분자 (h y dra t ed wa t er) 하나물 대동해서 Na+ 막문을 통과하는 model 을 보여주는데 K+ i on 인 경우에는 물분자 하나와 수화되어 있으면 너무 커서 막구멍을 통 과하지 못하게 된다. K+ i on 막문에 대해서는 아칙 잘 알려져 있지 않다. 1952 년에 Hod gk i n 과 Huxle y는 i on 의 두과속도가 전 압에 영 향을 받는 것으로 보아서 이 구멍들에 하전되어 있는 막문이 있어 이들이 웅칙일 때 구멍이 열리고 닫히고 한다고 제안하였다. 만일 그렇다면 하전되어 있는 입자가 움직일 때 생성되는 전류를 측정할 수 있어야 되는데 이 g a ti n g전류는 Na+ i on 에 의한 전류가 너무 커서 측정할 수 없었다. 이 문제는 Na+ 구멍을 선택적으로 막는 독성물질인 t e t rado t ox i n 과 sax it ox i n( 그림 7·15) 이 발견됨으로써 해결이 되었다. 이들 화합물의 gu an i d i um 기 가 Na+ i on 과 유사하여 Na+ 구멍 에 서 제 일 좁은 쪽에 부착 하여 구멍을 완전히 막는데 axop la sm 안쪽에 있을 때에는 전혀 영향이 없는 것을 보아 Na+ 를 선택적으로 통과시키는 부분이 이 구멍의 외부쪽 에 있는 것 같다. 그림 7 • 16 은 Ranv i er 의 매듭에의 Na+~ 구멍을 t e t rado t ox i n 으로 막은 후 전압고정 실험을 한 결과를 보여준다. 잠정적안 ca p a city전류를 상쇄 하기 위해 전압고정실험을 정지전위의 양쪽으로 대칭적으로 실험을 하여 그 차이 를 얻은 것 이 곧 g a ti n g전류이 다.
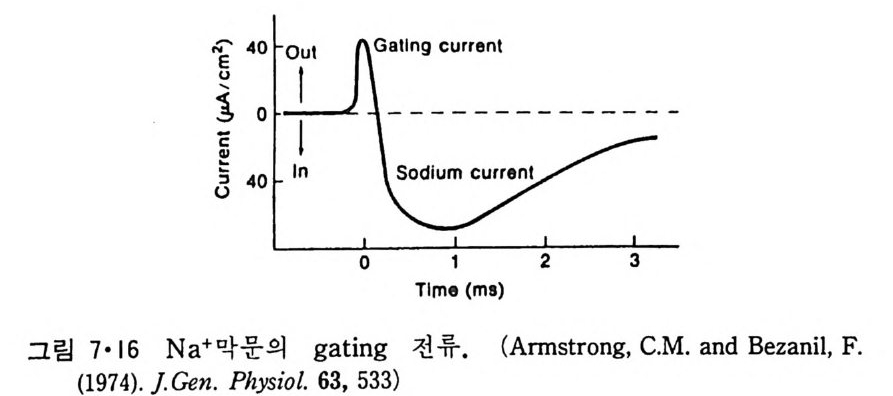 - 침`uaun。3
- 침`uaun。3
아칙까지의 실험결과로부터 얻어진 Na+ 구멍의 선택성과 ga ti ng mechan i sm 을 그림 7·17 의 model 에서 종합해 본다. 여기서 막을 횡단하 는 내재단백질이 구멍을 형성하고 있으며 axon 막의 외부표면 근처에 ion 을 선택하는 부분이 있고 내부에 막문이 있어 이것이 전위의 sensor 와 연결이 되어 있다. 전위차에 변화가 오면 sensor 의 구조변화로 막문이 열리게 된다.
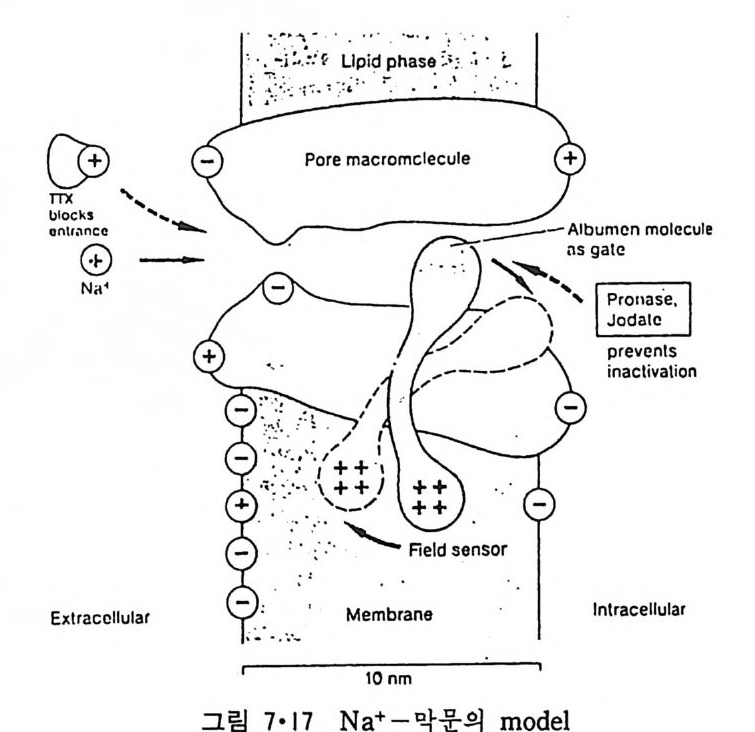 '•: `:. • •1』 '·. .::입 .·•: :.. . • ;. ,~ 、 . . ;. :: :- . . f , •..;. U ..·· .•p . ·. i .d•. ~ p.. h· -a. · s .e.. .~ ., ; ., _ :. , • :..
'•: `:. • •1』 '·. .::입 .·•: :.. . • ;. ,~ 、 . . ;. :: :- . . f , •..;. U ..·· .•p . ·. i .d•. ~ p.. h· -a. · s .e.. .~ ., ; ., _ :. , • :..
 1 2 3 4 5 6
1 2 3 4 5 6
이상의 반응속도 (k i ne tic s) 방법들에 의한 연구들은 Na+ 통로가 열리고 닫히는 mechan i sm 의 윤곽을 보여주지만 이것을 분자적인 단계에서 자세 히 이해하려면 내재단백질을 분리 정제해서 구조의 연구가 이루어져야 한다. 전기뱀장어의 전기기관에서 추출한 t e t rodo t ox i n 과 결합하는 내재 단백질은 한개의 p ol ypepti de 사슬로 구성되어 있고 그의 분자량은 260k Da 이다. 한편 쥐 두뇌에서 얻어진 Na 나통로단백질은 그림 7·18 에서 보이 는 것과 같이 a,Pl,[]2 의 세 가지 p ol yp e pti de 로 구성 되 어 있다. P-Merca pt oe t hanol 이 없을 때는 분자량이 300kDa 정도 되는 단백질과 37kDa(Pl) 이 되는 po lyp e p tide 두 band 가 보이는데 이황화물결합 환원 작용제의 존재하에서는 300kDa 단위의 것이 260kDa p ol yp e pti de(a) 와 39kDa (P2) 로 갈라진 다. Tr iton X-100 으로 용해 된 Na 다공로의 내 재 단백 질의 분자량은 약 316kDa 이 된다. 그래서 이 통로의 s t o ic h i ome try는 aPlP2 임을 알 수 있다. 이 Na 다공로의 내재단백질을 막소포에 제구성시키면 그림 7·19 에 보이 는 것과 같이 Na+ 통로의 성질을 그대로 나타낸다. 활동전위가 신경말단에 도달하면 전위차 변화에 의해 열려진 Ca2+ 통로
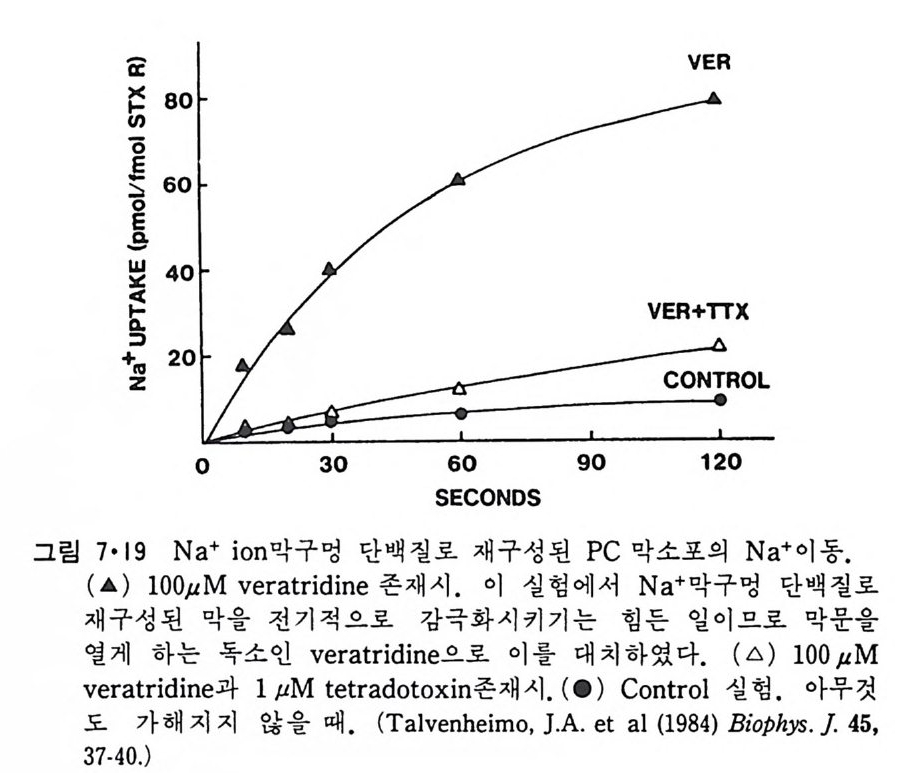 Ie •o I VER
Ie •o I VER
에 의해 Ca2+ i on 이 세포액으로 들어가 신경세포 사이나 신경세포와 근육 세포간에 신호가 전달되는 복잡한 과정이 시작된다. 한편 근육세포 내의 원형 질막의 활동전위 가 근소포체 (sarcop la smi c re tic ulum) 의 Ca2+ 통로를 열면 Ca2+ i on 이 세포액으로 들어가 근육을 수축시킨다. 이들 Ca2+ 동로 의 구조에 대해서는 자세히 밝혀지지 않고 있다. 7 •2 화합물에 의 해 열 리 는 통로 10)-12) Na+ 막동로와 K+ 막통로가 전위차의 변화에 따라 開閉되는 과정으로 활 동전위가 생성되고 이 활동 전위가 axon 을 따라 신경 끝까지 도달되면 다음 신경이나 근육세포로 신경신호가 전달되어야 한다. 세포 사이는 대 부분의 경우 원형질막으로 연결되어 있지 않기 때문에 전혀 다른 방법으
로 신경신호가 전달된다. 죽 신경말단에서 화학적인 전달물질 (chem ic al t ransm itt er) 이 분비돼 확산에 의해 인접해 있는 세포에 도달하면 그 원형 질막에서 막문을 형성하는 내재단백질과 선택적으로 결합되어 이 원형질 막에 활동전위를 야기시킨다. 이때 화합물이 막문을 형성하는 단백질과 결합되어 그 구조변경으로 i on 의 두과속도 변화를 일으키는 것이므로 화 합물에 의 해 열 리 는 막통로 (chemi ca lly ga t ed channel) 라고 부른다. 7·2·1 Sy n ap se 그림 7·20 은 두 신경세포 사이의 접촉을 보여준다. 이 전자현미경 사 진에서 원형질막으로 둘러싸인 axon 의 말단이 보이고 이것과 다음 신경 세포와의 사이에 간격이 있는 것을 보여준다. 이러한 신경세포 사이의 부분을 s yn a p se 라 하고 이 200~500A 이 되는 간격을 s y na p se 간격이라고 부른다. S y na p se 간격 바로 윗부분에 작은 구형 의 s y na p se 막소포 (sy na p tic ves ic le) 들이 많이 보인다. Sy na p s e 막소포 바로 아래 원형 질막 부분을 sy na p se 전 막 (pre sy na p tic membrane) 이 라 하고 sy n ap s e 간격 아
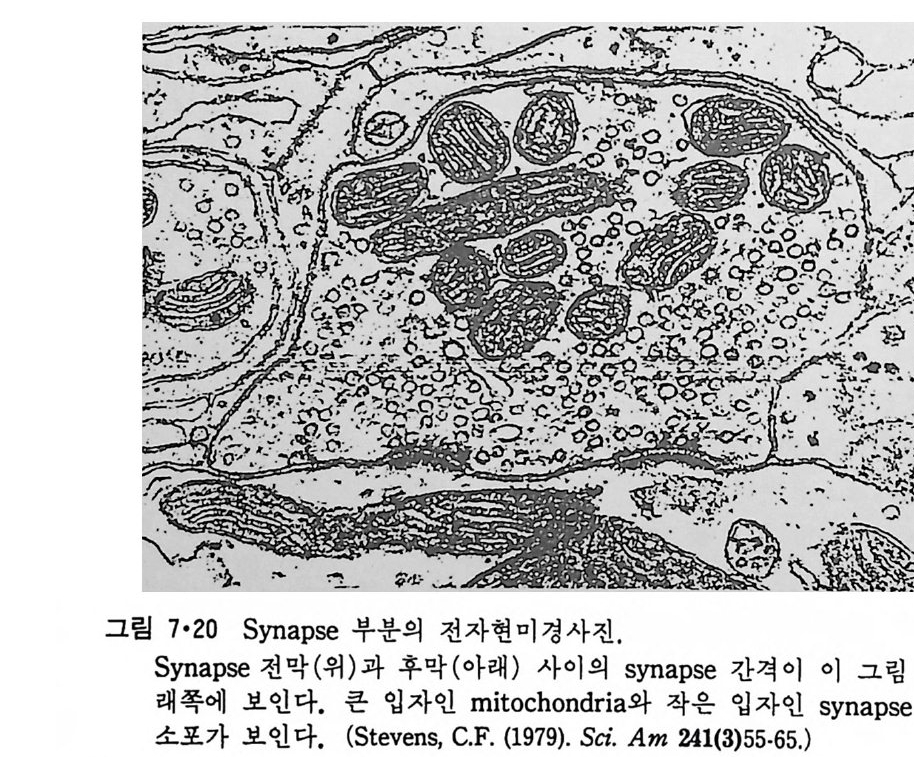 그림 7•20 Sy na p s e 부분의 전자현미경사진.
그림 7•20 Sy na p s e 부분의 전자현미경사진.
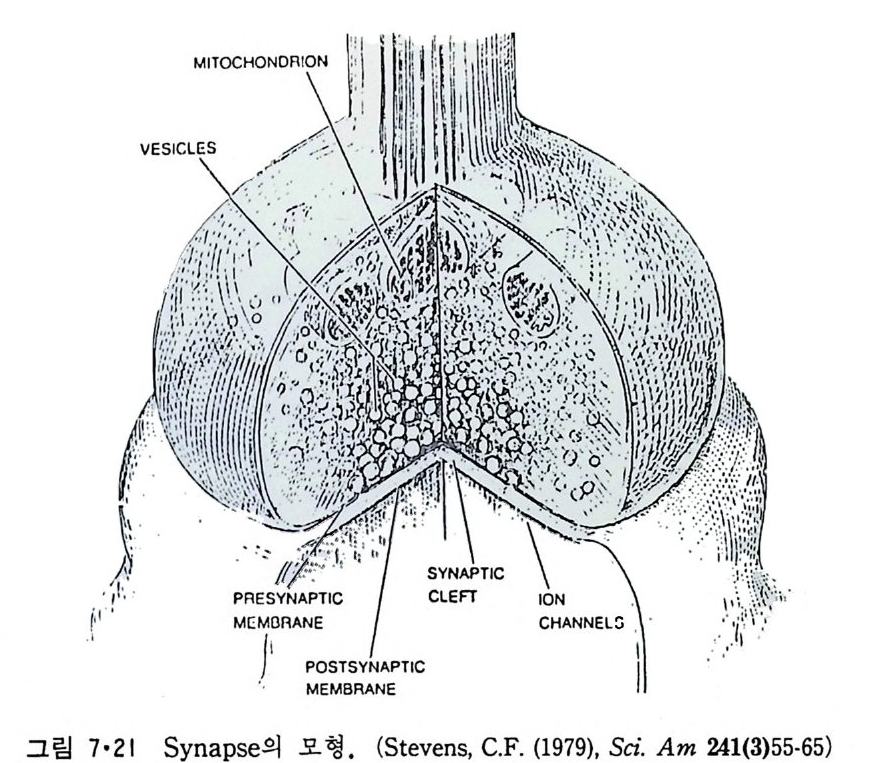 『 . - - - . . . - .. . .... . . ”
『 . - - - . . . - .. . .... . . ”
래쪽만을 s y na p se 후막(p os t s yn a pti c membrane) 이 라 한다. 그림 7·21 은 s yn a p se 의 모형 을 보여 주는데 신경 말단은 axon 보다 커 져 단추모양을 갖 는다. 그림 7·22 는 신경세포와 근육세포 사이의 신경근접합부 (neuromus cular j unc ti on) 의 전자현미경 사진을 보여준다. 여기서도 신경 axon 말단 부근에 많은 s yn a p se 막소포가 보이며 s yn a ps e 후막에는 신경세포 사이와 는 달리 원형질막이 접혀져 있다. 신경근접합부는 s yn a p se 보다 넓어 500 ~1000A 이 된다. 이러한 s y na p se 간격이나 신경근접합부의 간격을 통해서 전기적으로 신 경신호가 전달되는 것은 불가능하다고 생각되여 19 세기에 화학적인 전달 이 론 (chemi ca l tra nsmi ss io n the or y) 이 제 안되 었 다. 이 가설 에 의 하면 신 경 신호가 신경 말단에 도달하면 s yn a p se 전 막에 서 화학적 인 전 달물질 이 방출 되 며 s yn a p se 간격 내 에 서 확산에 의 해 서 sy na p se 후막으로 이 동이 되 어 수용체 (rece pt or) 에 결합함으로써 신경황동전위를 일으킨다는 것이다. 표 7·2 는 오늘날까지 알려져 있거나 추측이 되고 있는 화학적인 전달물질을 나타내며 그림 7·23 은 몇 개의 중요한 전달물질의 구조식을 보여준다.
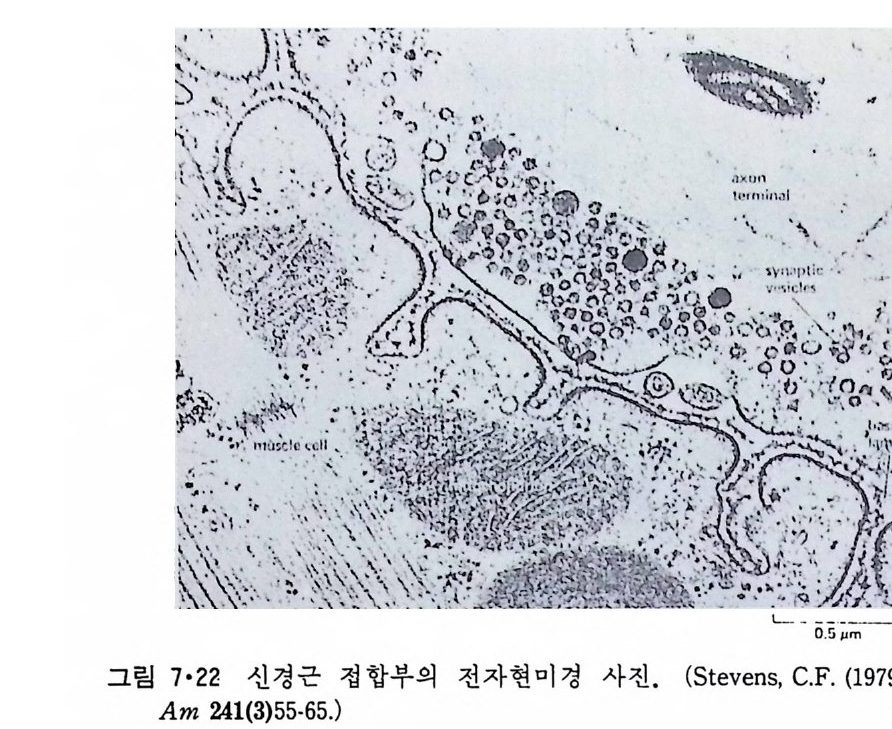 느 _ _o._5 . µ -m I
느 _ _o._5 . µ -m I
 표 7.2 화학적 인 신경 산호 전달물질
표 7.2 화학적 인 신경 산호 전달물질
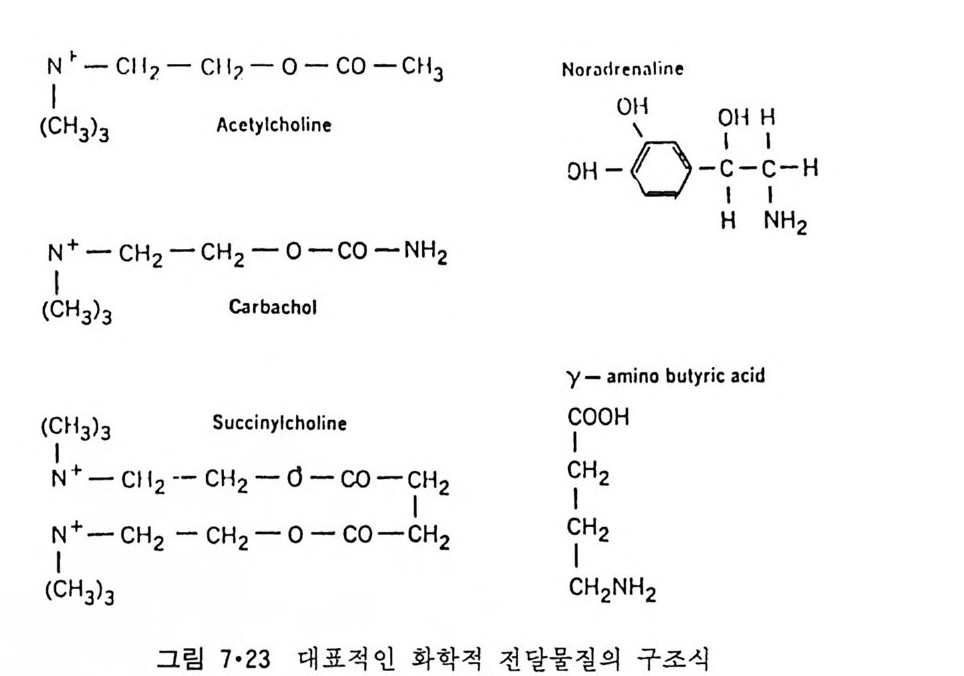 N ~-Cl !? —ClI ;,-0 -CO -CH3 Norarlren~l,ne
N ~-Cl !? —ClI ;,-0 -CO -CH3 Norarlren~l,ne
운동신 경 세 포 (moto r neuron) 를 자국시 켰을 때 acety lc holi ne (ACh) 이 방출되는 것을 처음 관찰한 사람은 Dale(1936)13) 이었는데 이 운동산경과 근육 사이의 신경근접합부에서 ACh 이 신경전달제 역할을 하는 것은 다 음 사실로부터 알 수 있었다. (a) 신경말단에 ACh 뿐만 아니라 이를 합 성 하 는 choli ne acety lt r a nsfe r ase 도 존 재 하 며 , (b) 신 경 근 접 합 부 에 ace ty lcho li nes t erase 가 있고, (c) 이 효소를 저 해 시 키 면 ACh 이 syn a p se 간격 용액에 축적된다. 그러나 ACh 이 정말 전달체로서 역할을 하려면 이것이 s yn a p se 전막에 서 방출되어야 하며 s yn a p se 후막과 작용하여 활동전위를 일으켜 근육수 축을 초래하여 야 한다. ACh 이 syn a p se 전막에서 방출되는 중거는 (a) 신경을 제거한 근육을 자국시켰을 때 ACh 이 방출되지 않으며, (b) curare 갇은 화합물로 근육의 수축을 저 지 시 켜 도 ACh 은 방출되 며, (c) syn a ps e 막소포는 신경말단에만 존재하고 또 이들 s yn a p se 막소포 근처에 choli ne ace ty l t rans f erase 가 있어 여기서 ACh 이 합성된다는 것을 알 수 있다. 한편 ACh 이 syn a p se 후막과 작용하는 직접적인 중거는 신경을 자 국시키지 않고 i ono p hores i s 에 의해 ACh 을 가했을 때 근육이 수축되는 것을 관찰한 것이다.
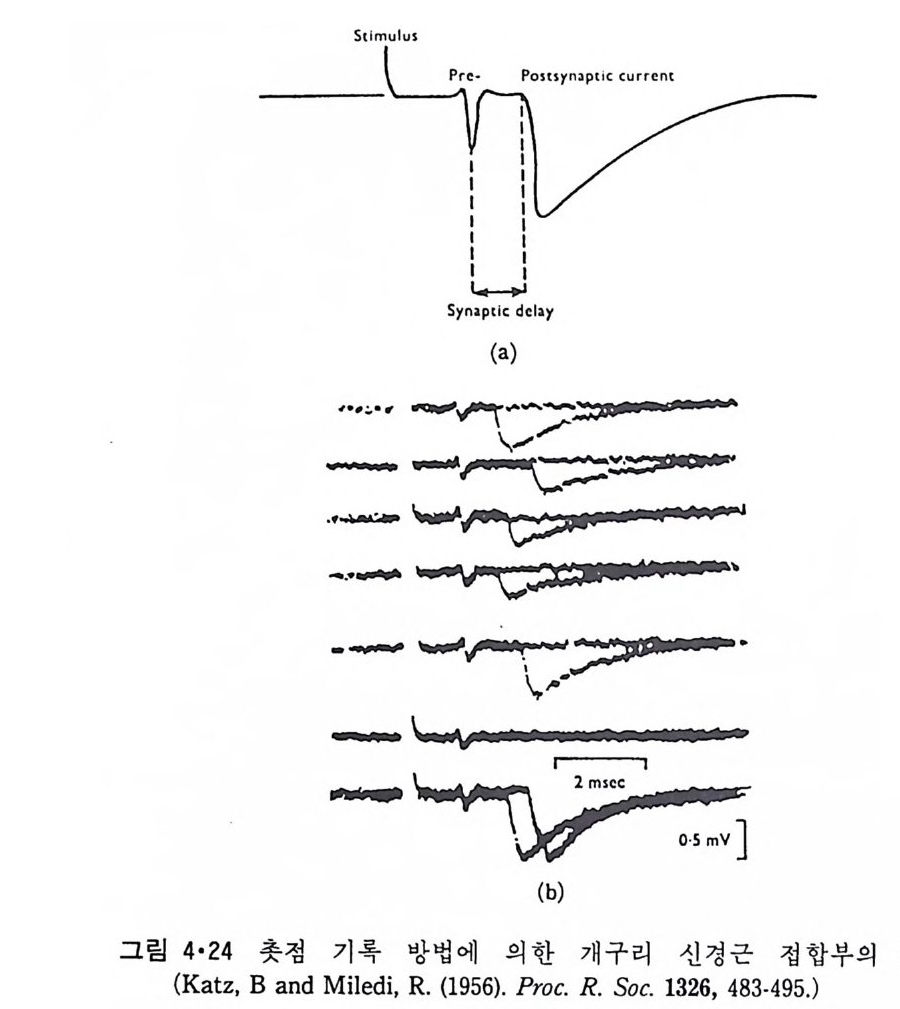 St im ulus
St im ulus
7·2·2 종판전 압 (End-pl a te po te n ti al) 신경근정합부에서의 신경전달과칭이 전기적인 현상이 아니라는 사실은 그림 7·24 에서 알 수가 있다. 여기서 기록전극을 신경근접합부 근처에 꽂고 근육의 활동전위가 일어나지 못하도록 Ca2+ 농도를 감소시키고 동시 에 M g2+i on 농도를 중가시킨 후 신경세포를 자국시키면 처음에 산경말단 에 i m p ulse 가 도착하는 것이 기록되고 약 0.5msec 후에 근육의 종판 (end pla te ) 에 서 야기 되 는 종판전 압 (end-pl a te po te n ti al ; EPP) 이 기 록된 다. 이 신경신호의 전달이 전기적으로 이루어진다면 0.5msec 만큼 지체될 이유가
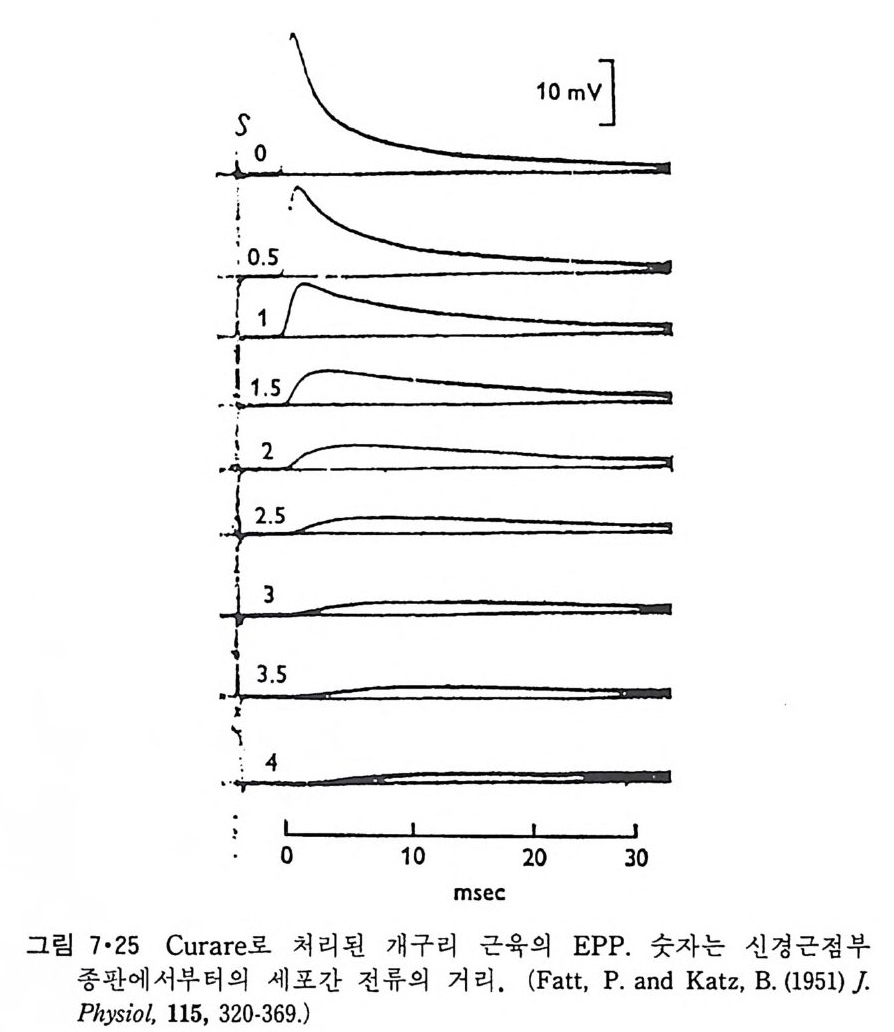 10 mV]
10 mV]
없기 때문에 화학적인 전달과정이라는 것을 알게 되었다. 이렇게 종판전 압의 형성이 지체되는 이 유는 ACh 이 방출되 는데 그 만큼 시간이 필요한 데 있다. 그림 7·25 는 기록전극을 근육세포 안에 넣어 얻은 EPP 이다. 이때에는 curare 로서 EPP 의 진폭을 작게 해서 근육세포에서 활동전위가 일어나지 못하게 하였다. 종판에서 얼어질수록 그 진폭이 감소되는 것을 볼 수 있 다. 다시 말하면 신경근접합부에서만 ACh 방출에 의해 활동전위를 시작 할 수 있는 것이다. 그림 7·26 은 전압고정실험 결과로서 EPP 가 i on 전도 도 (conduc t ance) 의 중가에 의한 것을 보여준다. 그림 7·27 은 ion op h or-
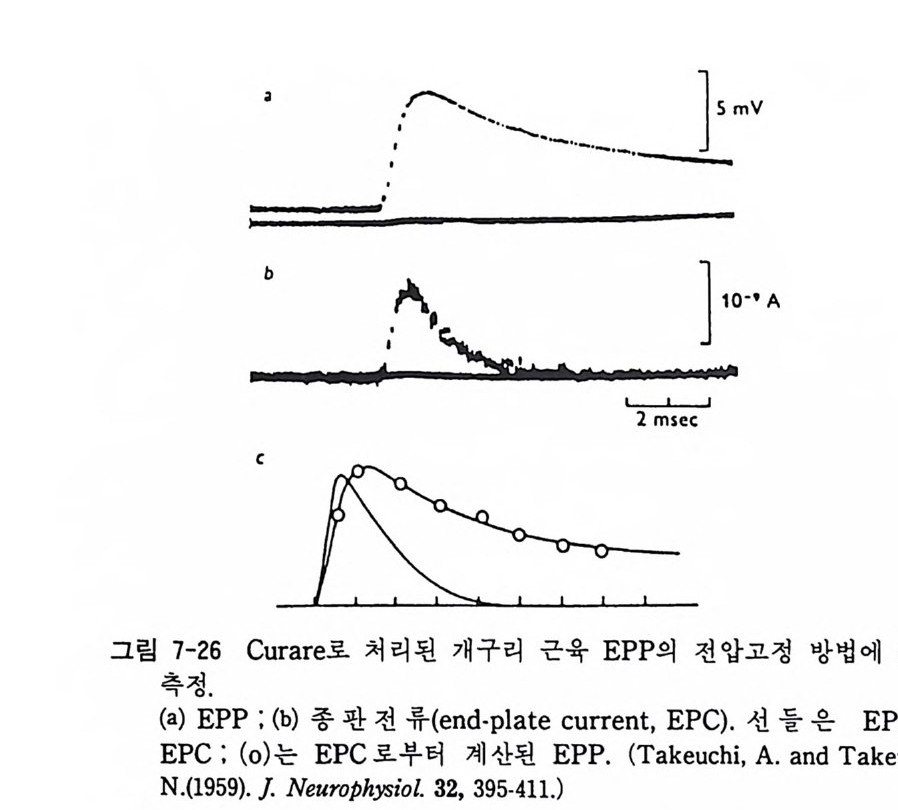 -.: ~~- ·-·-·二m V
-.: ~~- ·-·-·二m V
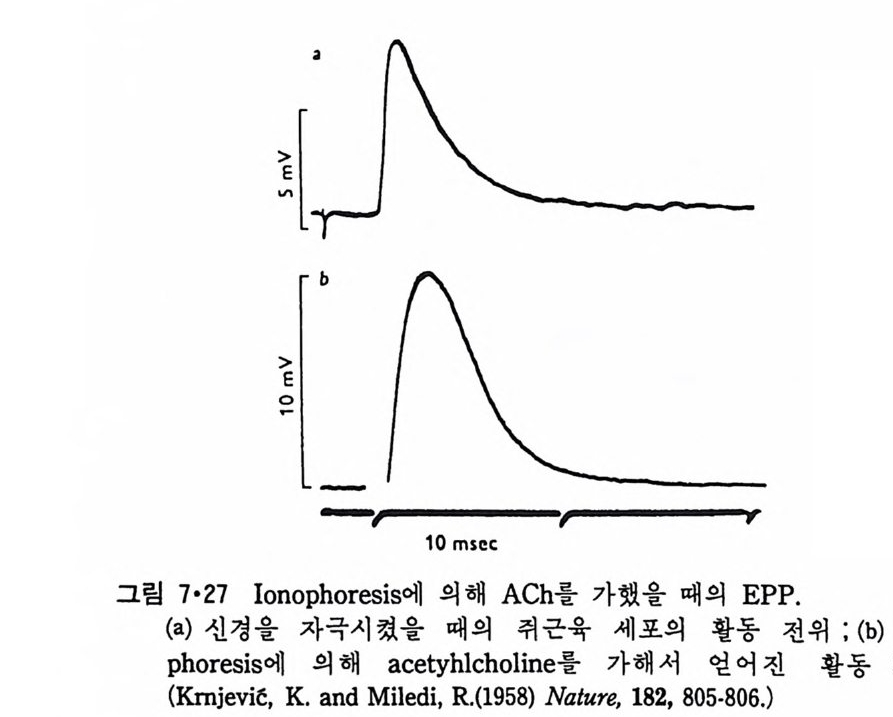 --
--
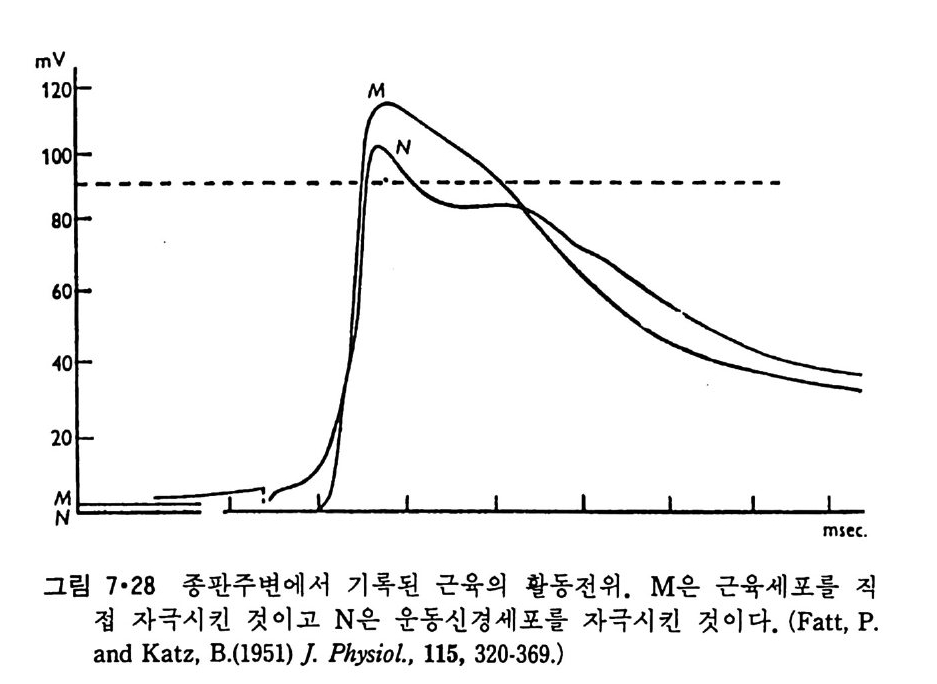 mV
mV
es i s 로 ACh 를 종판에 직접 가해도 신경세포를 자국했을 때와 유사한 전 압이 생성되는 것을 보여주는데 이는 s yn a pse전막에서 방출된 ACh 에 의 해서 발생되는 것을 증명한다. 그림 7·28 은 근육의 활동전위를 두 가지 방법으로 얻은 것을 보여준 다. 여기서 N 선은 신경세포를 자국시켜 ACh 에 의한 신경전달로 얻어진 근육의 활동전위이고 M은 근육세포를 직접 자국하여 얻은 것이다. M은 axon 에서의 활동전위와 유사한데 다만 그 시간이 길다. N 선의 上昇相 (risi n g p hase) 에 있는 굴곡점 (inflec ti on p o i n t)은 EPP 에서 활동전위로 가 는 단계라고 본다. 그림 7·29 는 신경세포를 자극해서 얻은 근육세포의 활동전위를 종판에서의 거리의 함수로 측정한 것이다. 종판에서 거리가 멀수록 근육을 직접 자극한 활동전위 모양에 가까운 것을 볼 수 있다. 이상의 여러 실험으로부터 얻은 결론은 신경신호가 신경말초에 도달하면 거기서 ACh 이 방출되고 이 화합물이 신경근정합부를 건너 근육세포의 종판의 수용체 (rece pt or) 와 작용하여 EPP 가 생성된다. 이것은 인정해 있 는 근육세포막을 시발점 (thres hold) 이상으로 감국 (de p olar iz e) 시키기 때문 에 근육세포에서 활동전압이 시작되어 신경세포의 axon 때와 마찬가지로 근육세포막 끝까지 전달이 된다.
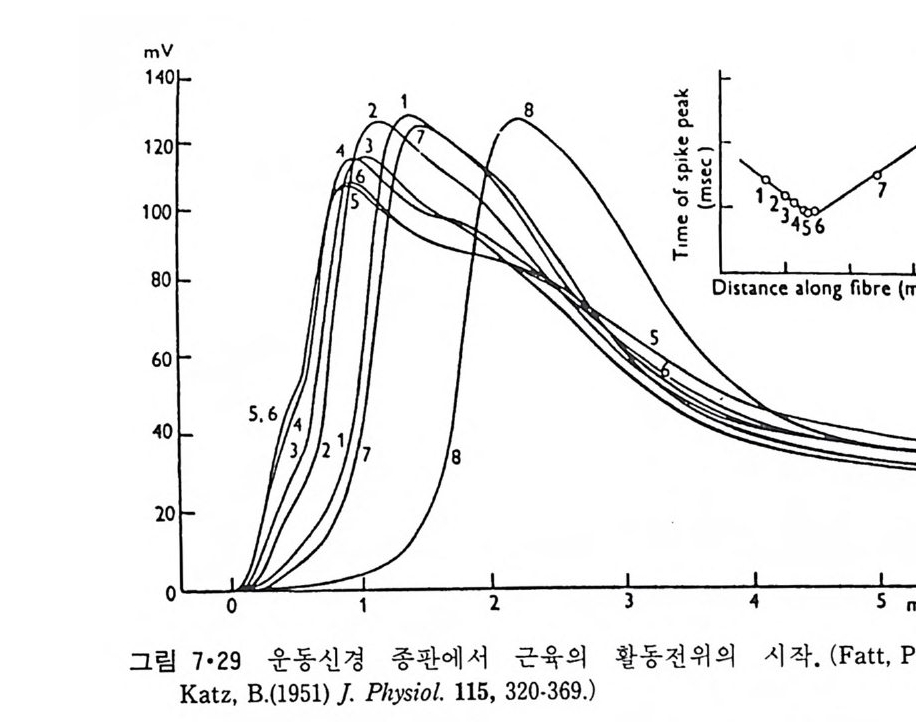 mV
mV
7·2:3 Ace ty lcho lin e 수용체 (recep tor ) 단백질 II) 이미 1955 년에 s yn a p se 후막에 존재하는 ACh 수용체는 단백질이며 ACh 와 결합하면 이 단백질에 구조변화가 일어나 막의 ion 이동속도가 증가 하여 EPP 가 생긴다고 제안이 되었다. 이것은 전압의 변화를 감지해서 열리는 막통로와는 달리 화합물의 결합에 의해 열리는 막동로이기 때문 에 화합물막동로라고 불린다. 그림 7·30 은 ACh 수용체가 집중되어 있는 s y na p se 후막을 전자현미경 으로 관찰한 것이다. 이 s yn a p se 후막표면에 보이는 입자들이 ACh 수용체 단백질이라는 것아 판명되었으며 이 단백질이 명개의 소단위 (subun it)로 구성되어 있고 이 소단위들이 중앙에 존재하는 구멍을 둘러싸고 있는 것 을 볼 수 있다. 이 사진을 전자계산기로 영상보강(im a g e enhancemen t)을 하여 얻은 것이 그림 7·31 에 주어진다. 여기서 수용체 단백질의 소단위 들이 비대칭적으로 배열되어 있으며 이 막을 측면에서 보았을 때 내재단 백질이 막 양면에 돌출된 것을 볼 수 있다(그림 7·32). 이 내재단백질은
 그 립 7·30 Sy n ap s e 후 막 의 전 자 현 미 경 사 진. (Zi ng s heim , H. P. ,
그 립 7·30 Sy n ap s e 후 막 의 전 자 현 미 경 사 진. (Zi ng s heim , H. P. ,
 그림 7•31 ACh R 내재단백질의 전자현미경 사진(A)과 전자 계산기로의
그림 7•31 ACh R 내재단백질의 전자현미경 사진(A)과 전자 계산기로의
 무., `. ? ` `A; · E-. 오 ` ·七 ` 、 .• • : \ . 는. `.\ t. ? . `언 • :'.' . .: {… ..... L ·서E
무., `. ? ` `A; · E-. 오 ` ·七 ` 、 .• • : \ . 는. `.\ t. ? . `언 • :'.' . .: {… ..... L ·서E
s y na p se 간격 쪽에는 약 55A 정도가 노출되어 있고 세포질 쪽으로는 약 15A 정도가 노출되어 있다. 그림 7·33 은 이들 전자현미경으로의 관찰을 종합하여 얻은 이 수용체 단백질의 모형을 보여준다. ACh 수용체에 단백질을 약한 세탁제로 용해하여 친화 chromato g rap h y 로 분리 정제한 후 전자현미경으로 찍은 사진도 sy n ap s e 후막에서의 이
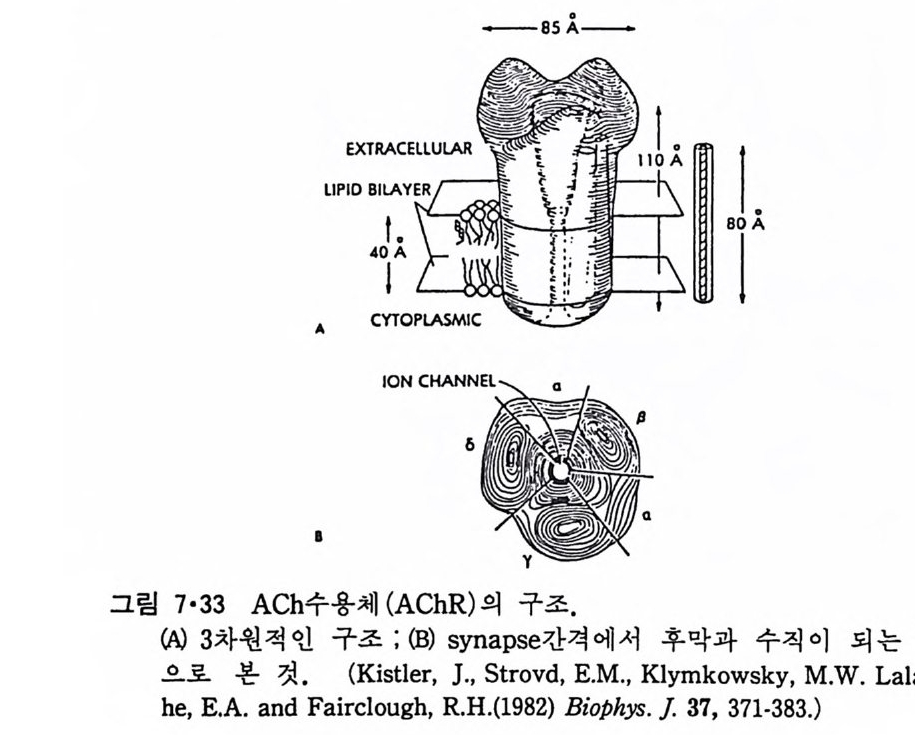 -esA-
-esA-
단백질의 모양과 유사하다. 이 정제된 단백질의 분자량은 약 500kDa 이 고 SH 작용제로 환원시키면 250kDa 단위로 처리된다. 이 내재단백질은 SDS-PAGE 로 4 개 의 소단위 로 분리 가 되 며 이 들의 분자량은 각각 40 (a), 50(/J ), 60(r) 와 65kDa(8) 이 된다. 분리된 각 소단위의 상대적인 양으로부터 이 내재단백질의 s t o ic h i ome try는 a2BY8 임을 알았다. 막 내 에서는 두 개의 250kDa 단위의 단백질이 -s-s- 결합으로 연결되어 있다. 이 단백질은 인산지방질 막소포막에 재구성시켜 Na+ i on 의 두과성을 측정한 것이 그림 7·34 에 보여준다. 그림 7·34A 에는 ACh 수용체를 포함 하고 있는 막소포의 Na+ 두과성질을 보이고 그림 7·34B 는 이것이 없는 막소포의 경우이 다. ACh 의 유사화합물인 carbamy lc holi ne 존재 하에서
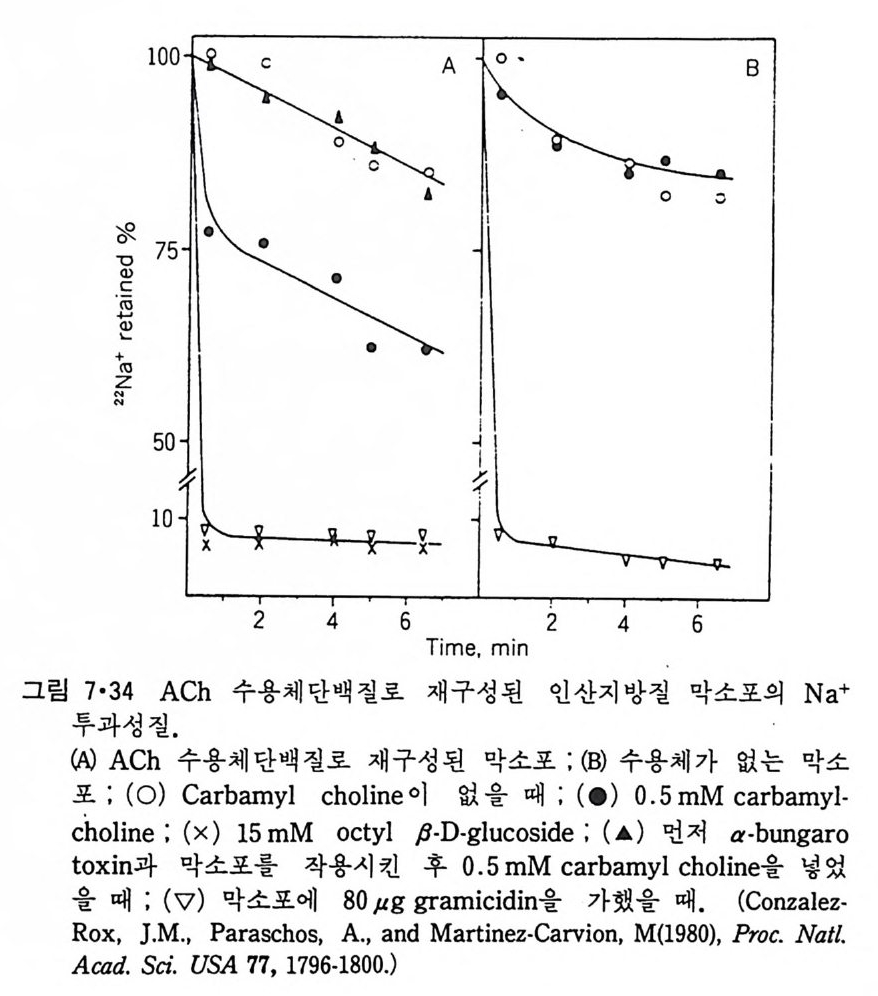 100 A ° ` B
100 A ° ` B
Na+ i on 의 두과는 대단히 빠르나, 이것이 없을 때나 있을 때에도 s yn ap se 에 서 EPP 를 생 기 지 않게 하는 a-bun g aro t ox i n 존재 하에 서 는 수 용체 단백질이 없는 막소포에서의 Na+ 투과성질과 유사하다. 이 수용체 단백질은 a- 나사선의 함량이 34% 가 되고 이들 이차구조를 형성하는 부분이 막을 통과한다고 생각되고 있다. 이 단백질의 am i no 산 서열은 결정이 되었는데(그림 7·35) 이 4 종류 (a, {3 ,r,8) 소단위의 ami no 산 서열이 유사하다는 특징이 있다. 이들 소단위들의 am i no 산 서열 중 에는 약 20 개의 소수성 am i no 산이 연결된 부분이 있어 아들이 막을 통하 는 a- 나사선부분이라고 생각되고 있다 (M1,Mz,M J ,M ◄). 그러나 이 부분 의 소수성은 bac t er i orhodo p s i n 의 막을 통하는 부분 보다 더 크다. Bac t er i orhodo p s i n 의 경 우와는 달리 ACh 수용체 단백 질 은 구멍 을 형 성 하 며 이 통로의 표면은 천수성이기 때문에 평균적으로 소수성은 오히려
 ;.‘‘、. 홑 1· fF. L 1 CHs言•Yf VR . •lH ·.H찮 짧 I훑T L VV LV 짧옮룰IFIIsS AtA 홀LC1AE 2LYLLG. .G•sVVG ..Li S C6GV SRA E·SSS·V:노앙 EGNv 鉛JllVN_R3 특 시 SAE 셉 球블EN'ET 蓬 듦롭cDvH 앓접 릅g 홍E틀HOHTTKVuT6KLs言HDD 쩝累H HH ITE l言v T홍唱 IA占i ;言-•'. 一書雲홀s 삽 .EEt • .K 홀/V. 읽 챔I-T톡HL,TI”一5 [옮 싶少F홀Vw.. R L RLOIH노vIO'khN나바〕 pJEljLA A 셜Ii 홍〕 D 급짧짧 찮 露텁A해 5·A ss
;.‘‘、. 홑 1· fF. L 1 CHs言•Yf VR . •lH ·.H찮 짧 I훑T L VV LV 짧옮룰IFIIsS AtA 홀LC1AE 2LYLLG. .G•sVVG ..Li S C6GV SRA E·SSS·V:노앙 EGNv 鉛JllVN_R3 특 시 SAE 셉 球블EN'ET 蓬 듦롭cDvH 앓접 릅g 홍E틀HOHTTKVuT6KLs言HDD 쩝累H HH ITE l言v T홍唱 IA占i ;言-•'. 一書雲홀s 삽 .EEt • .K 홀/V. 읽 챔I-T톡HL,TI”一5 [옮 싶少F홀Vw.. R L RLOIH노vIO'khN나바〕 pJEljLA A 셜Ii 홍〕 D 급짧짧 찮 露텁A해 5·A ss
 N-Termlnl
N-Termlnl
bac t er i orhodo p s i n 이 더 높아야 될 것이다. 그래서 앞서 이야기한 4 개의 소수성 부분 이 외 에 막을 통과할 만한 부분을 찾게 되 어 C- 말단에 가까 운 두 소수성 a- 나사선중간에 (그림 7·36) 양천성 a- 나사선가 존재함을 알게되었다. 그림 7·37 은 이 부분은 a- 나사선구조로 나열한 결과 나사선 의 한쪽면 이 극성 am in o 산으로 배 열 되 어 있고 나머 지 는 소수성 am i no 산 으로 배열되어 있는 것을 보여 준다. 그래서 이들 5 개의 po lyp eptide
 a R. P
a R. P
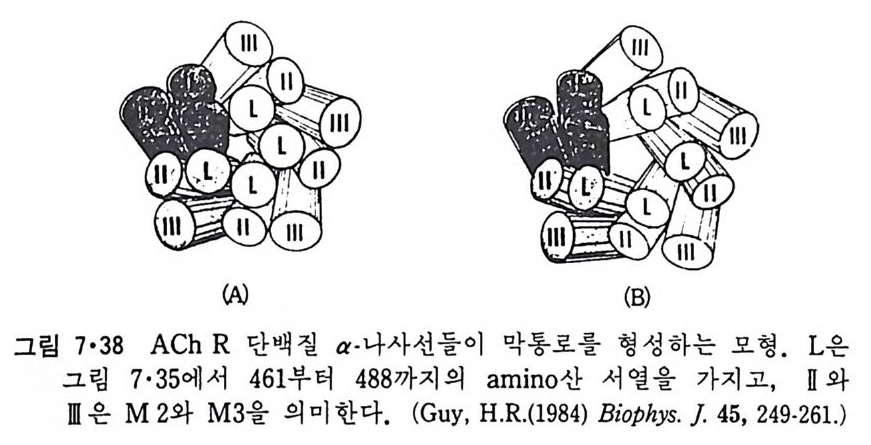 (A) (B)
(A) (B)
(a2 /3 r8) 의 양찬성 a- 나사선들의 국성표면이 구멍을 이루고 그 이외의 a- 나사선부분들이 막의 인산지 방질의 ac y l 사슬과 접 촉이 된다. 그림 7· 38 은 통로를 둘러싼 두층의 a- 나사선룹 보이는데 이들의 외각에 10 개의 a- 나사선가 존재해 인산지방질과 접촉하고 있다. 통로가 열리고 닫히는 것은 이들 a- 나사선가 막평면과 이루는 각의 변경으로 이루어진다고 가 정되고 있다. 여러가지 표지실험에 의하면 ACh 와 결합하는 것은 a 소단위라는 것이 판명되었다. 이 단백질의 구조에 대해서 좀더 자세히 알아야 통로가 열리는 메카니 즘이 규명될 것이다. 7·2·4 ACh-Ch cyc le1'·2' ACh 아 ACh 수용체 단백질의 a 사슬에 결합되면 s yn a p se 후막의 통로가 열리게 되는데 다음 신경신호가 전달되려면 빨리 통로가 닫혀져야 한다. 이 것 은 s yn a p se 간격 에 있 는 acety lc holi ne ste r ase (AChase) 에 의 해 서 ACh 가 신속히 가수분해되어 제거됨으로써 이루어진다. 이 효소는 주변단백 질로서 전기 기관 등으로부터 높은 NaCl 용액으로 추출해낼 수가 있다. 그림 7·39 는 AChase 의 전자현미경 사진으로 구형의 단백질 2 단위 들이 500 A.길이의 섬유성 단백질 소단위와 결합되어 있는 것을 볼 수 있다. 이 복합체의 분자량은 약 l,OOOkDa 으로 여러가지 조건하에서의 g el 전기 영동의 결과로 그림 7·40 과 갇은 model 이 제안되었다. 여기서 분자량이
 . .i ’舊 圖 틀醫읽:
. .i ’舊 圖 틀醫읽:
80kDa 이 되 는 촉매 소단위 가 -s-s- 결 합으로 2 합체 를 형 성 하며 이 것 이 또하나의 2 합체와 회합하여 한 개의 머리를 형성한다. 한편 3 개의 머리 가 각각 -s-s- 결 합으로 colla g en 과 화학적 인 조성 이 유사한 po lyp e p tide 사슬과 연결되며 이 3 개의 사슬이 3 중 나사선룬 형성한다. 이 효소는 낮 은 io n 세 기 (ion ic str e ng th) 에 서 는 chondroit in sulfa te 와 같 은 g l y cosam i no g l ycan 의 존재하에서 큰 입자로 응집된다. 이들로부터 이 효 소의 colla g en 과 유사한 꼬리부분이 chondroit in sulfat e 를 통해 sy n ap se 간격 에 있는 basemen t막의 type IV colla g en 과 결 합하여 이 효소가 거 기 에 고정된다고 생각된다.
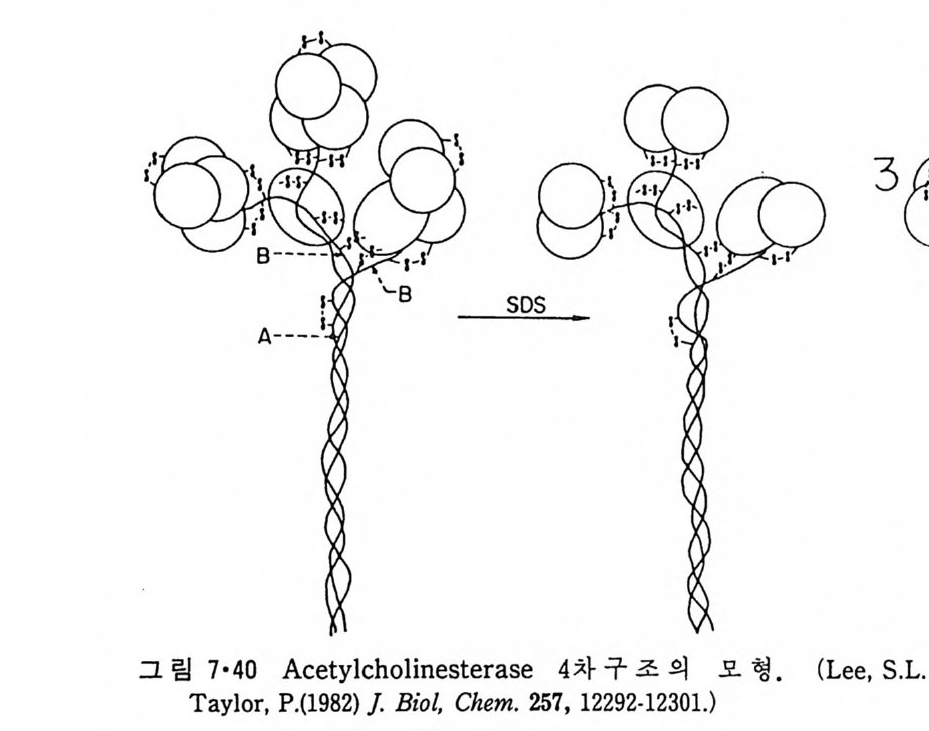 g 3>
g 3>
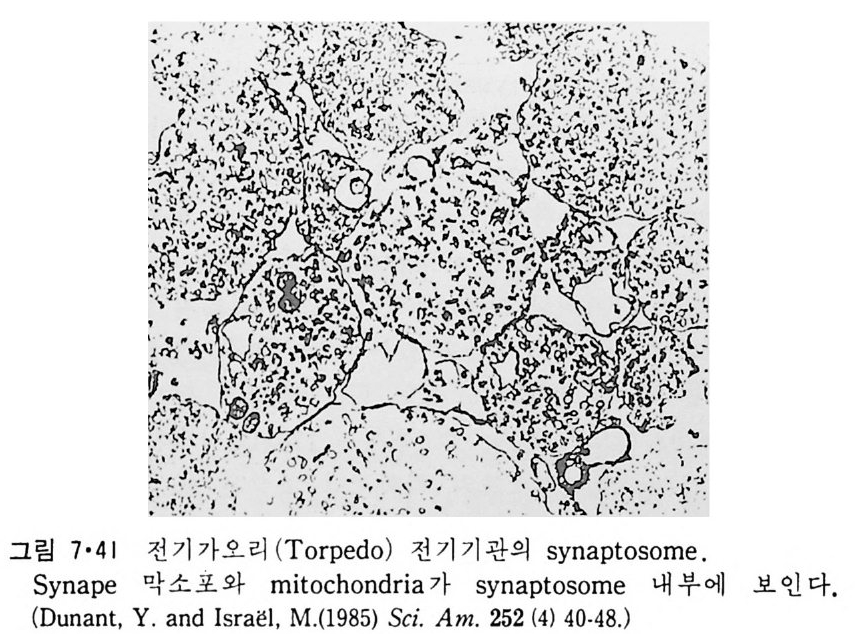 그림 7•41 전기가오리 (T orpe do) 전 기기 관의 syn ap tos ome.
그림 7•41 전기가오리 (T orpe do) 전 기기 관의 syn ap tos ome.
AChase 에 의해서 ACh 가 가수분해되면 chol i ne(Ch) 과 초산이 생성 되 는 데 choli ne 은 syn ap s e 전 막 에 존 재 하 는 고 친 화 성 (hig h aff ini t y) cho li ne 섭취 계열에 의해 재흡수가 된다. 이것은 기계적인 처리로 신경말 단이 떨어져나와 막소포를 형성한 s yn a pt osome( 그림 7·41) 을 이용해 얻 은 결과인데, Ch 의 수송에는 Na+ i on 의 농도차이가 있어야 하며 Na+ i on 이 막외부에서 내부로 이동되면서 Ch 까지도 같은 방향으로 운반하는 2 차 능동수송이 다. 이 s y na p se 전 막에 는 많은 내 재 단백 질 이 존재 하는데 그중 >200, 54 와 34kDa 의 분자량을 가진 단백질이 Ch 의 흡수에 필요하 다는 것이 재구성실험에서 판명되었다. 신경말단에는 cho li ne 을 합성하는 기능이 없기 때문에 s y na p se 간격에서 생성된 cho li ne 을 효율적으로 흉수 하는 것이 중요하다. 이 렇 게 신경 말단으로 흡수되 어 들어 간 cho li ne 은 ace ty l-CoA 의 acety l 기를 받아서 ace ty lcho li ne 으로 전환되는데 이 반응을 촉매하는 효소가 choli ne ace ty l t rans fe rase 이 다. 이 효소는 분자량이 비 교적 작은 단백 질 로서 약 15% 정도는 내재단백질로서 존재하고 나머지는 수용성 단백질로 서 존재한다. 이 수용성 상태의 효소는 몇 개의 동질효소(i soz ym e) 로 존 재하며 수용성 상태와 내재단백질 상태의 효소는 그 촉매특성과 저해성 질이 다르나 이렇게 두 가지의 전혀 다른 형태로 존재하는 이유는 아직
도 분명하지 않다. 새로 합성된 ACh 의 일부는 s y na p se 막소포 내부로 들어가고 나머지는 세포질에 존재하는데, 이것도 s y na pt osome 을 이용하여 결정이 되었다. 그림 7·41 에서 s yn a pt osome 은 s y na p se 막소포와 m it ochondr i a 를 함유하는 것 울 볼 수 있고 s yn a pt osome 과 s y na p se 막소포를 동시에 파괴하여 전체의 ACh 농도를 결 정 할 수 있 다. 한편 s y na pt osome 을 얼 린 다음 서 서 히 온 도들 높이면 그 막은 파괴되나 s y na p se 막소포는 파괴되지 않아 이들 막 소포를 분리하여 (그림 7·42) 함유하고 있는 ACh 농도를 결정할 수 있다. S y na p se 막소포를 전자현미경으로 보면 이는 한겸의 막으로 둘러싸여 있고 그 반경은 420A 정도가 된다. 그 무게는 l76kDa 이 되 며 이 무게의 70% 가 물이다. 이 s y na p se 막소포의 화학적인 조성은 표 7 · 3 에 보여준 다. 단백질보다 지방질을 훨씬 많이 함유하고 있고 萬개 단위의 ACh 와 ATP 가 그 내부에 존재한다. 세포액의 ACh 농도는 0·03M 인데 비해 s y na p se 막소포 내의 ACh 농도는 0·15M~0·6M 로 ACh 이 s y na p se 막소포 내로 들어갈 때에는 낮은 농도에서 높은 농도로 운반되는 것이기 때문에 능동수송이 될 것 이 다. 이 는 s yn a p se 막소포 밖으로 활성 중심 부 (acti ve
 그 림 7 • 42 Sy n aps e 막 소 포. (Dunant, Y. and Israel, M.(1985) Sc i. Am.
그 림 7 • 42 Sy n aps e 막 소 포. (Dunant, Y. and Israel, M.(1985) Sc i. Am.
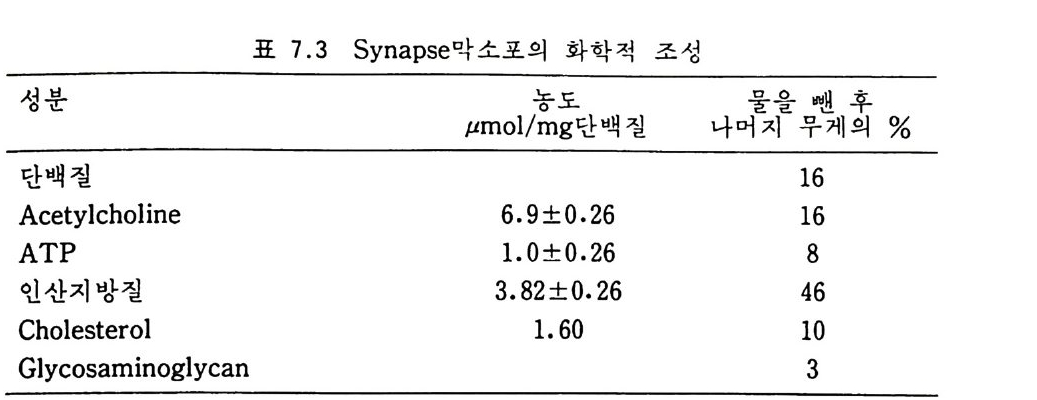 표 7.3 S y na p se 막소포의 화학적 조성
표 7.3 S y na p se 막소포의 화학적 조성
cen t er) 가 노출되어 있는 ATPase 에 의해서 ATP 가 가수분해되면서 양성 자(p ro t on) 가 내부로 운반되어 2 차 능동수송에 의해서 ACh 도 syn a p s e 막 소포내부로 들어간다. 신경 i m p ulse 가 신경 말단에 도달하면 복잡한 과칭을 거쳐 ACh 이 방출 되는데 이 과정도 s yn a pt osome 을 이용하여 연구가 되었다. 그림 7·43 은
 110 Km+2 d Miecp 0° +,a'a + r · z a t · 。n
110 Km+2 d Miecp 0° +,a'a + r · z a t · 。n
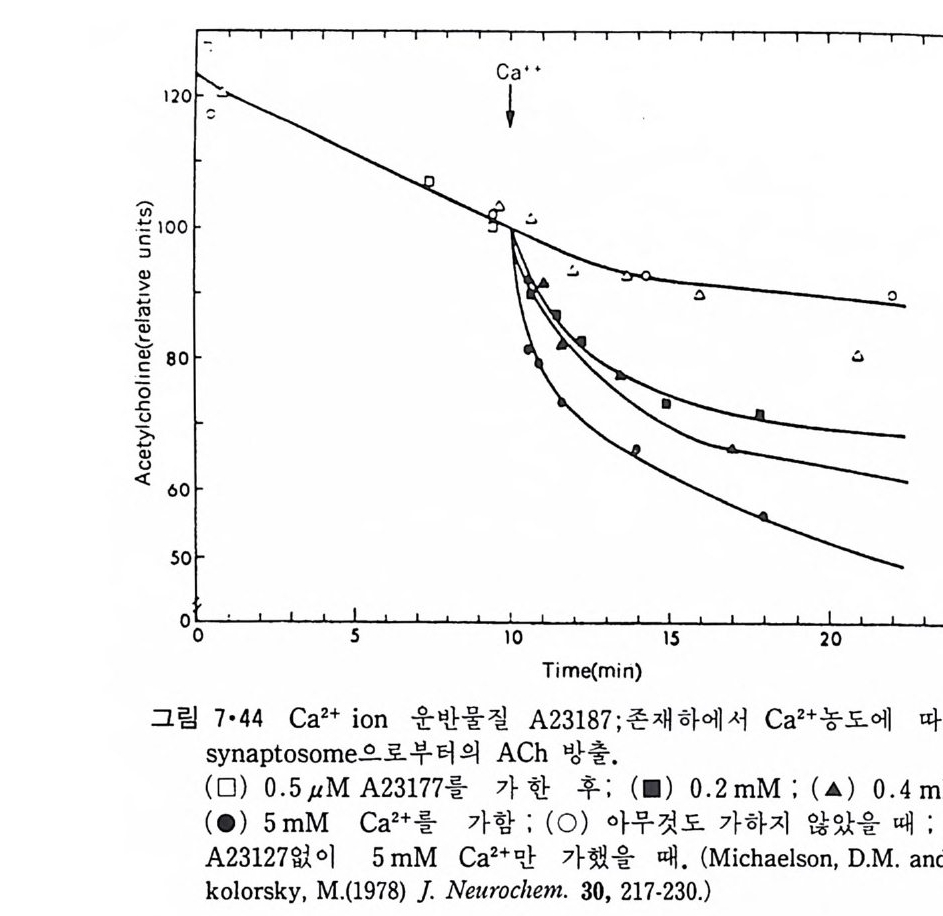 ca .. *
ca .. *
K+ i on 의 농도가 클수록 ACh 방출속도가 큰 것울 보여준다. 그림 7·44 는 Ca2 + i on 을 동과시키는 i on 운반물질인 A23187 이 존재할 때 Ca2 + i on 의 농 도가 클수록 ACh 방출속도가 빠른 것을 보여준다. 이들 실험결과로부터 신경 imp ulse 가 신경말단에 도달하면 전압차의 변화에서 오는 K+ 통로가 열려 K+ i on 이 밖으로 나오고 Ca2 + i on 의 구멍도 역시 전압차의 변화로 열리게 되어 Ca2+ i on 이 내부로 들어가 이것이 ACh 을 방출시킨다. 처 음에 는 Ca2+ i on 이 s yn a p se 막소포와 s yn a p se 전 막을 융합시 켜 ACh 을 s y na p se 로 방출한다고 생각하였는데(그림 7·45) 신경을 자국시켰을 때 s y na p se 막소포 밖에 있는 ACh이 먼저 방출되는 것으로 보아 이 mechan i sm 이 를린 것을 알게 되었다. 이것은 s yn a pt osome 실험으로도 확인된 것 인데 i on 운반물질에 의 해 Ca2+ i on 이 s y na pt osome 에 들어 가면 s y na p se 막소포 내부의 ACh 농도에는 변화가 없는 상태에서 외부 ACh 은
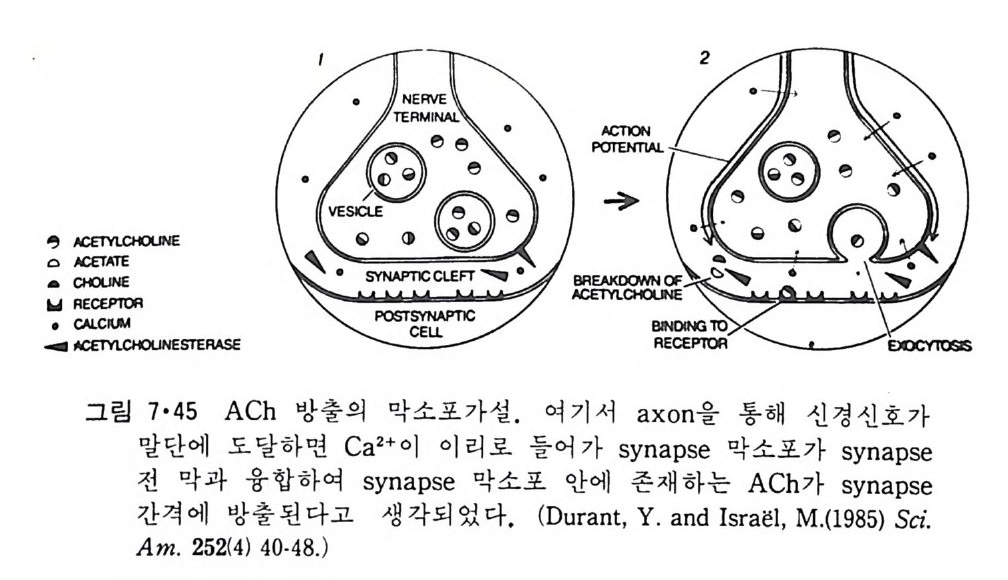 '0NK
'0NK
모두 s y na pt osome 에서 없어지는 것을 관찰하였다. 막 융합에 의해 ACh 이 s y na p se 간격으로 방출되는 것이 아니라면 s y na p se 전막에 Ca2 + 에 의해 열리는 통로가 있어야 될 것인데 이는 동결 -파열 전자현미경 방법으로 해명이 되었다. 그링 7·46 은 정지상태와 자 국상태에서의 s y na p se 전막 내부의 단백질입자(I MP) 를 본 것이다. 정지 상태에서는 입자크기가 5nm 에서 20nm 에 이르는 단백질이 보이는데 자 국이 되면 작은 입자수는 감소하고 큰 입자수는 증가한다. 그래서 신경 말단에 Ca2+ i on 의 농도가 증가하면 내 재 단백 질의 회 합에 의 해 ACh 의 통
 a b
a b
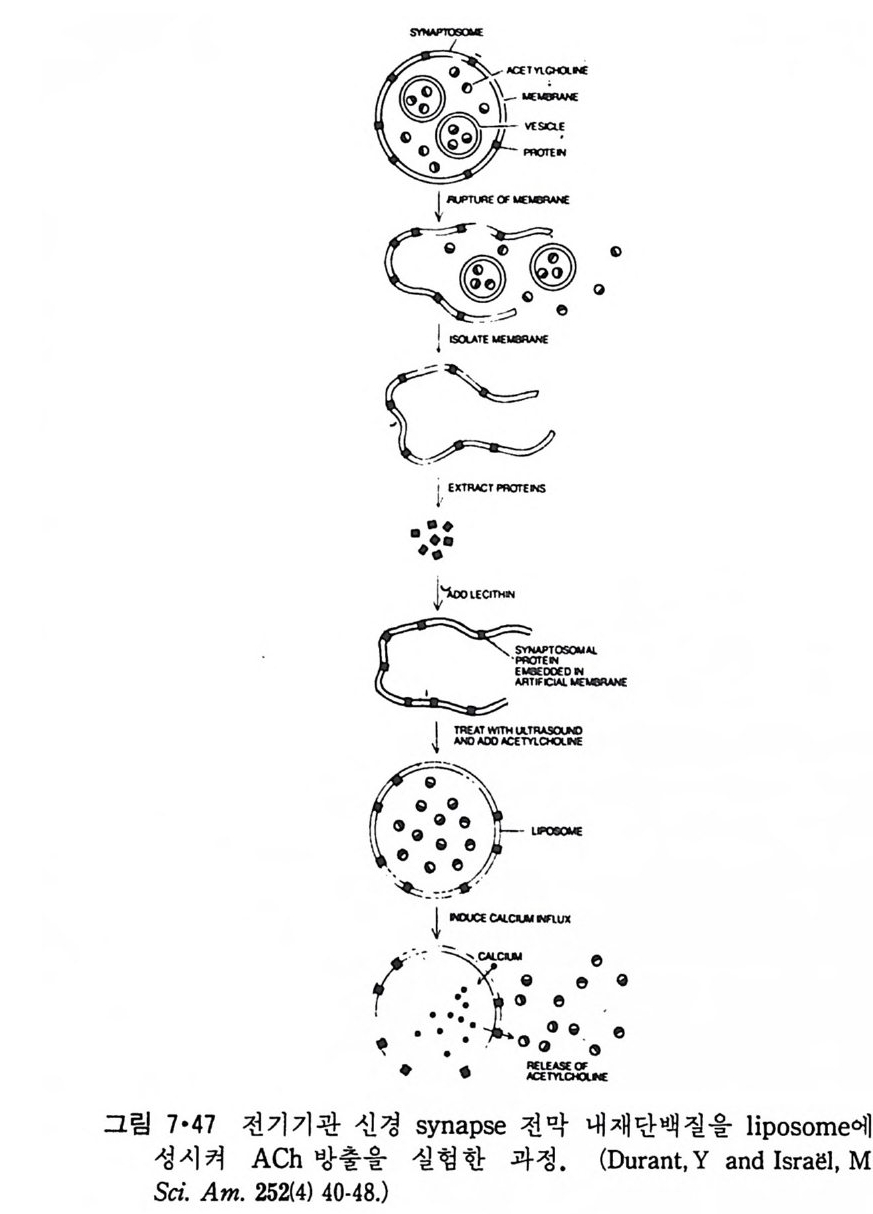 o-n’'H ..
o-n’'H ..
로가 생긴다고 해석이 되었는데 아는 재구성실험에서 확인이 되었다(그 링 7·47). S yn a pt osome 에 서 내 부에 존재 하는 s yn ap se 막소포와 m it ochondr i a 를 제 거 한 후 s yn a pt osome 막을 동결 건조하여 이 를 인산지 방질에 재구성시 킬 때 막소포에 ACh 을 넣고 i on 운반물질로 Ca2+ i on 을 막소내에 두입하면 ACh 이 새어 나오는 것을 관찰하였다.
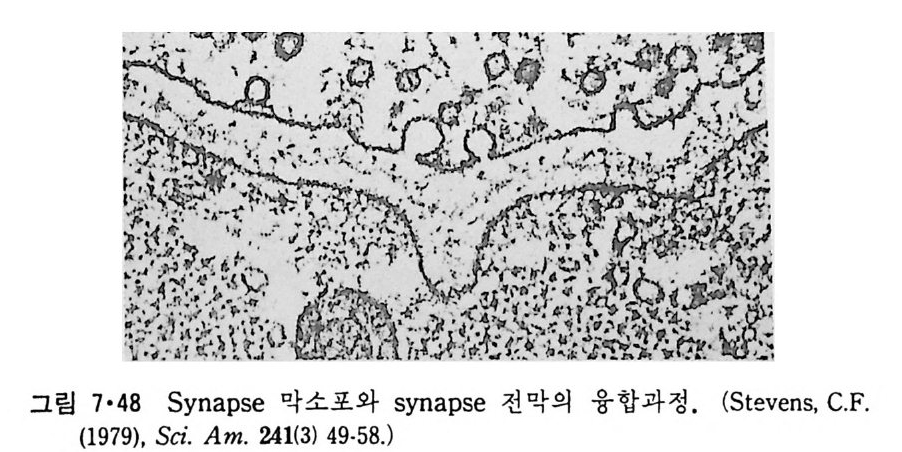 그림 7·48 Sy n aps e 막소포와 syn a p se 전막의 융합과정. (St ev ens, C .F .
그림 7·48 Sy n aps e 막소포와 syn a p se 전막의 융합과정. (St ev ens, C .F .
그러면 sy n ap s e 막소포 역할이 무엇인가가 문제인데 그림 7·48 에서와 갇이 이들 sy n ap se 전막과 실제로 융합되는 것이 관찰되었으나 이 융합 은 ACh 이 sy na p s e 간격 에 방 출 된 후에 야 일어 난다. 신경 말단을 장시 간 계속 자국시키면 s y na p se 막소포에서 ACh 은 없어지고 Ca2+ i on 이 대신 그 안으로 들어 가는 것 으로 보아 이 s yn a p se 막소포의 역 할은 여 분의 ACh 을 저 장하고 Ca2+ i on 을 흉수함으로써 신경 말단에 들어 온 Ca2 + 을 세 포액으로부터 제거하여 다음 신호가 올 수 있도록 하는 것으로 생각된 다. 이렇게 흡수된 Ca2 + 이 결국은 융합을 통해 외부로 방출되는 것으로 추측되고 있다. 그림 7·49 는 이 전 과정을 보여준다. 이 렇게 ACh 이 s y na p se 로 방출되 면 근육세 포에 EPP 를 야기 시 키 고 곧 가수분해 되 어 서 cho li ne 으로 변형 이 되 면 신경 말단에 다시 흉수되 어 ACh 로 다시 변형 되 는 c y cle 을 이루는데 이 과정에 생성된 근육세포의 활동전위는 axon 때와 마찬가지로 근육세포 원형질막을 통해 퍼진다. 이 활동전위는 근소포체 (sarcop la smi c reti cu lum) 막에 존재 하는 전 압차변화로 열 리 는 Ca2+ 동로 를 열게하며 Ca 2+i on 이 lumen 에서 세포액으로 들어가면 근육을 수축시키 고 그후 Ca2+ i on 이 Ca2+-ATPase 에 의 해 다시 lumen 안으로 능동적 으로 수송이 되면 근육이 이완이 된다. 지 금까지 아 야기 한 것 은 신 경 근접 합부에 서 의 choli ne rgi c s yn a p se 의 mechan i sm 이었는데 신경세포 사이의 s yn a p se 에서 신경신호가 전달되는 과정은 더 복잡하다. 신경세포 간에도 신경 신호의 전달이 대부분 화학 적인 전달물질에 의해서 s yn a p se 간격을 통하여 이루어지고 또 전달물질 은 s y na p se 막소포에 저 장되 어 있 다가 s y na p se 전 막과 융합합으로써 방출
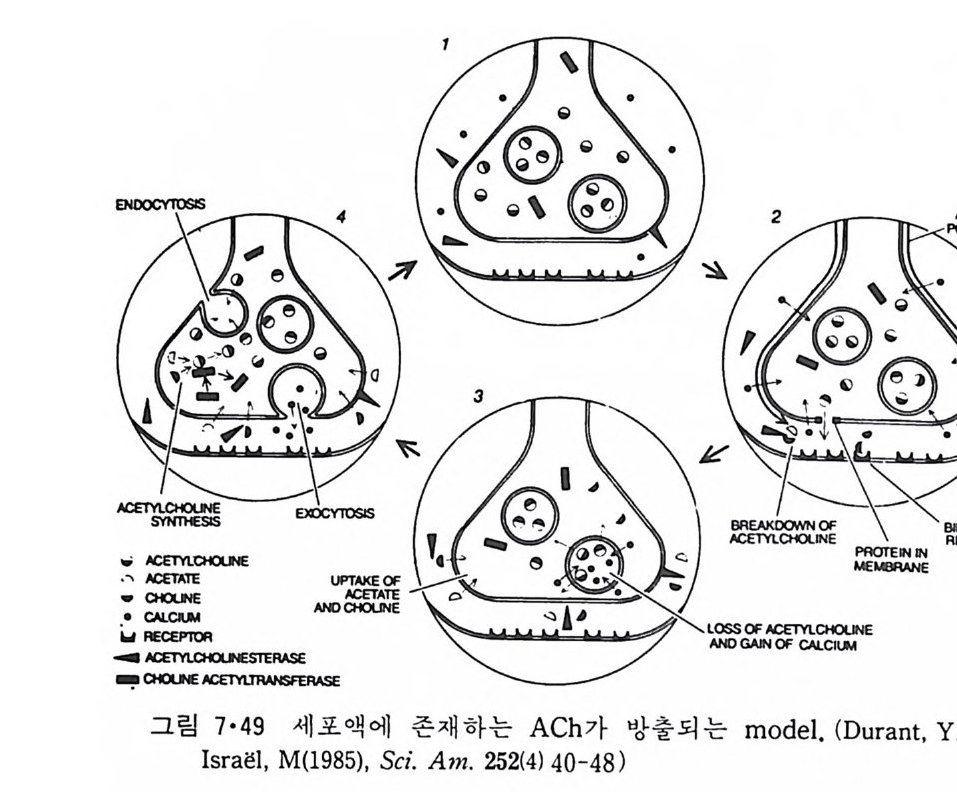 그림 7·49 세포액에 존재하 는 ACh 가 방출되는 model. (D urant, Y. and
그림 7·49 세포액에 존재하 는 ACh 가 방출되는 model. (D urant, Y. and
되는 것은 신경근접합부와 같다. 그러나 신경세포간의 s y na p se 에서 전달 물질이 방출되면 s yn ap se 후막을 감국 (de p olar i ze) 시킬 때도 있지만 과극 화 (h yp er p olar i ze) 시켜 도리어 작용전위가 시작되는 것을 저해시키기도 한 다. 이 는 s yn a p se 후막의 수용체 구멍 에 전 달물질 이 결 합되 면 K+ i on 만이 s y nap se 로 나오거나 c1- i on 이 안으로 들어가 내부를 더 음성을 띠게 하 기 때문이다. 여기서 개개의 신경신호전달은 시발접에 못 미쳐서 여러 신호가 합쳐진 다음에야 신호를 받아들이는 신경세포에서 작용전위가 시 작된다. 7·3 기타 방법으로 열리는 통로 14)15) 이상은 전위차의 변화와 화합물과의 결합으로 구멍을 형성하는 내재단 백질의 구조변화가 일어나 i on 의 막이동속도가 중가되어 막의 전위차를
가져오는 경우인데, 이 들 전 기적인 그리 고 화 학적 인 외부자 극 이외에 기 계적인 자극, 광선에 의한 자국 들 에 의해서도 생체전기현 상 이 일어나고 이들이 생물체의 외부에 대한 감각의 바탕이 된다. 이렇게 외부자국이 전기적인 ener gy로 변해 결국 신경세포를 통해 두뇌에까지 도달되는데 그 처음과정을 감각전이 ( sensor yt ransduc ti on ) 라고 부른다. 이들 감각전 이는 전부 생체막에 존재하는 수용체인 내재단백질에 의해서 이루어지는 데 듣고 접 촉을 느끼 는 기 계 적 수용체 (m echanorecep tor ) 는 이 것 이 전 기 적 인 ener gy로 직접 변형되어 외부자극이 막단백질에 오면 이 단백질의 구 조변경이 일어나 구멍이 열리게 되어 i on 이 이동된다. 이와 반대로 척추 동물의 시각인 경우 광수용체 ( p ho t orece pt or ) 에 광선이 도달하면 이것아
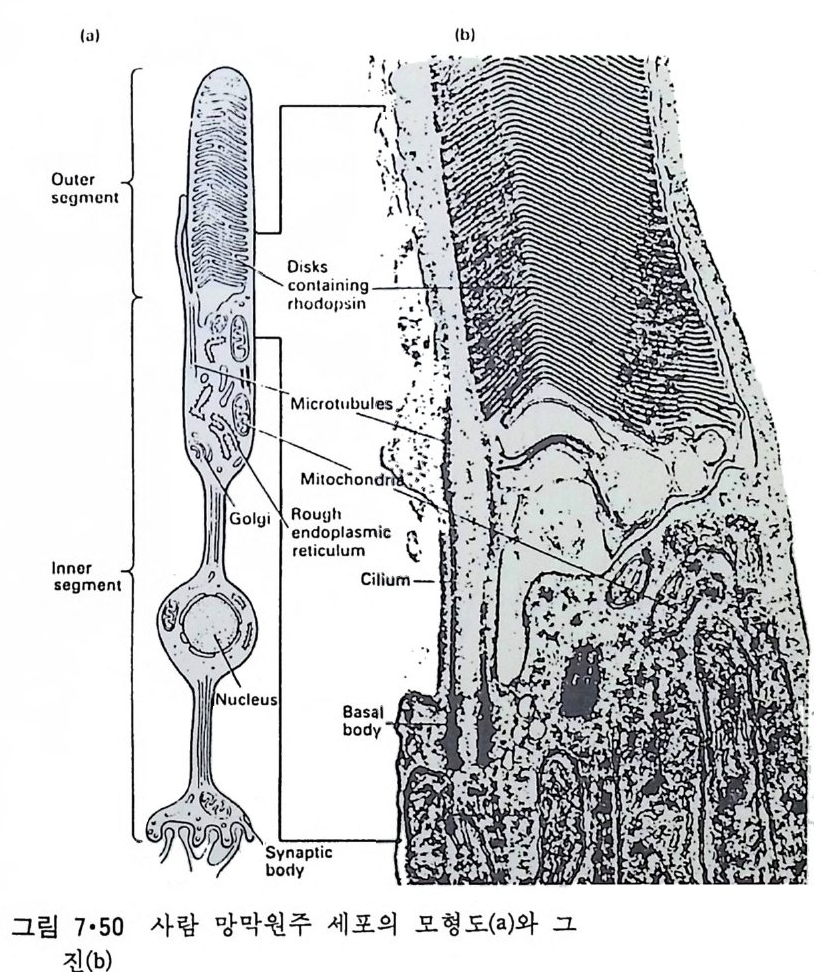 la) lb)
la) lb)
간접적으로 원형질막의 i on 이동속 도를 변경시켜 막의 전위차에 변화 를 가져온다. 시각은 눈 뒤쪽에 위치하고 있는 망막에 빛이 도달하면 이루어지는데 망막에는 색깔을 식별할 수 있는 원추세포와 어두울 때에 빛을 감지하는 원주세포가 있다. 그림 7·50 은 사람눈의 망막원주 ( re ti na rod) 세포의 모형 과 그 일부의 전자현미경사진을 보여준다. 이 세포의 외부 를 향한 쪽에 는 많은 원판 (d i sk) 이 겹쳐 있고 반대쪽에는 s yn a p se 가 존재해 신경세포 와 접촉이 되어 있다. 원주세포의 원판막에는 내재단백질인 rhodo p s i n 이 있는데 p ol yp e pti de 사슬 o p s i n 의 l y s i ne 기 에 re ti nal 이 Schif f base 로 연겅 이 되어 있다. O p s i n 의 am i no 산 서열은 결칭아 되었고 이로부터 그림 7·51 과 같은 소수성표수 p ro fil e 을 얻을 수 있어 그링 7·52 에 보이는 막 내 배열이 제안되었다. Bac t er i orhodo p s i n 경우와 마찬가지로 7 개의 p ol yp e pti de 부분이 막을 통과한다. Rhodo p s i n 의 re ti nal 이 빛을 흡수하면 그림 7·53 에 보이는것과같이 op s in 에 결 합 된 11-ci s- reti na l 에 iso meriz a ti on 이 일 어 나 all-tr a ns -re ti nal 로 변형되면 이것이 o p s i n 에서 해리됨과 동시에 o p s i n 이 활성화 된다. 한편 원주세포내에는 cy cl ic gua nin e mono phasp ha t e(cGMP) 의 농도가 큰데 cGMP 는 원형질막의 Na+ 막통로에 결합하여 Na+ i on 의 이동도를 (그림 7·54) 증가시켜 세포의 칭지전위를 -30mV 정도로 유지시킨다. 원
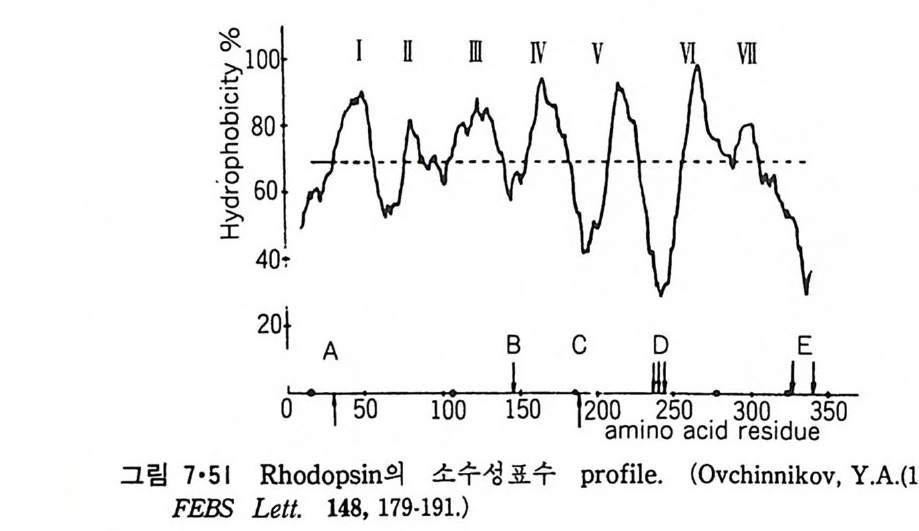 ·~ 춘(.) 100~ Il Ill IV V VI_ VII
·~ 춘(.) 100~ Il Ill IV V VI_ VII
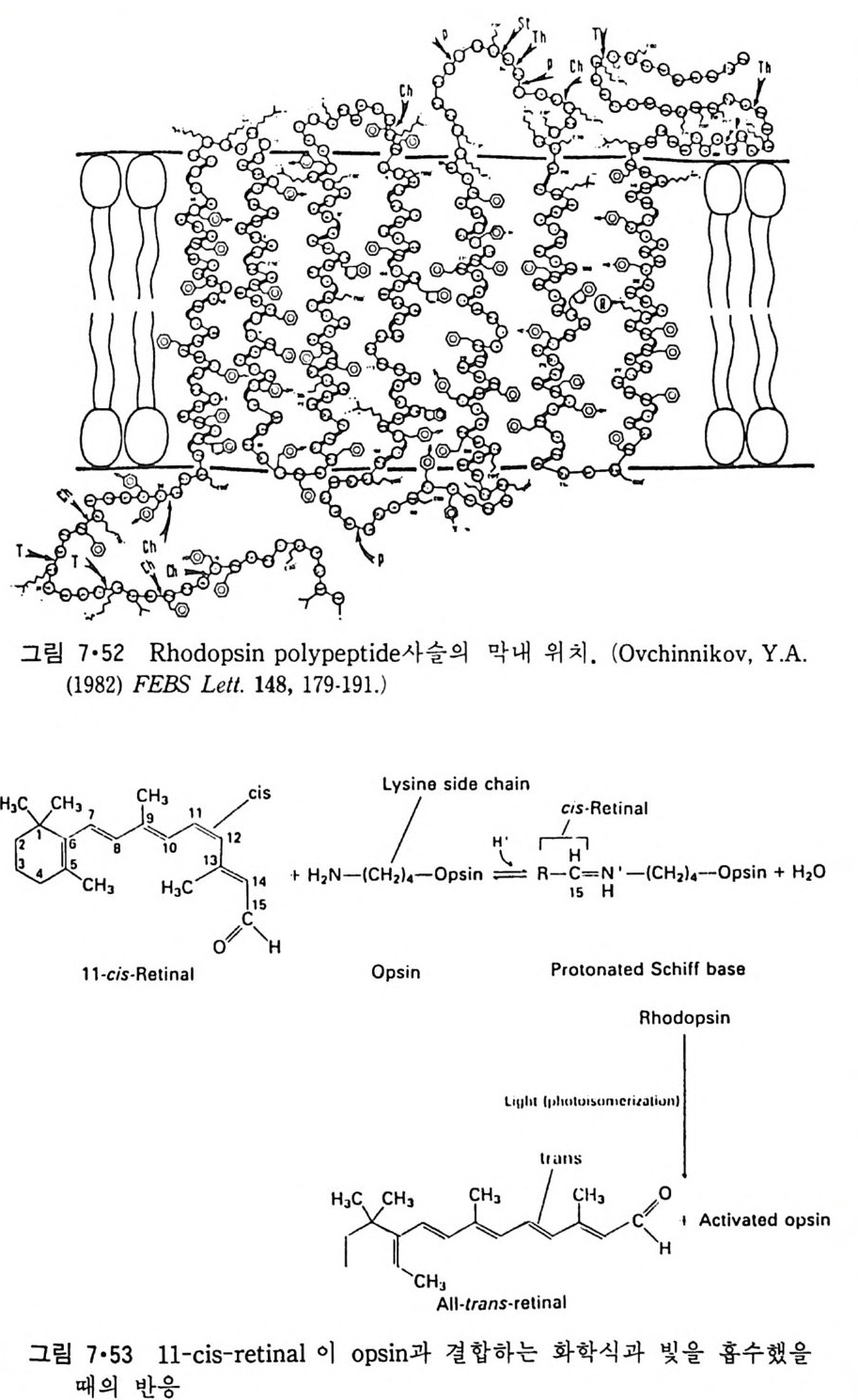 그림言 7 • 52> Rh odo\p si n p o~l Hy2pN e 一 pt (iC dLHe>2 사)4n술-e0S의 pI sd ei n c 막H:;:\:h:.: ::내 :I:n:: R•「위 -; CI치HS 7= · R. N e(I lO' n-a( vC| cHh2in) 4n -i k 0o pv s, inY +.A H. 20
그림言 7 • 52> Rh odo\p si n p o~l Hy2pN e 一 pt (iC dLHe>2 사)4n술-e0S의 pI sd ei n c 막H:;:\:h:.: ::내 :I:n:: R•「위 -; CI치HS 7= · R. N e(I lO' n-a( vC| cHh2in) 4n -i k 0o pv s, inY +.A H. 20
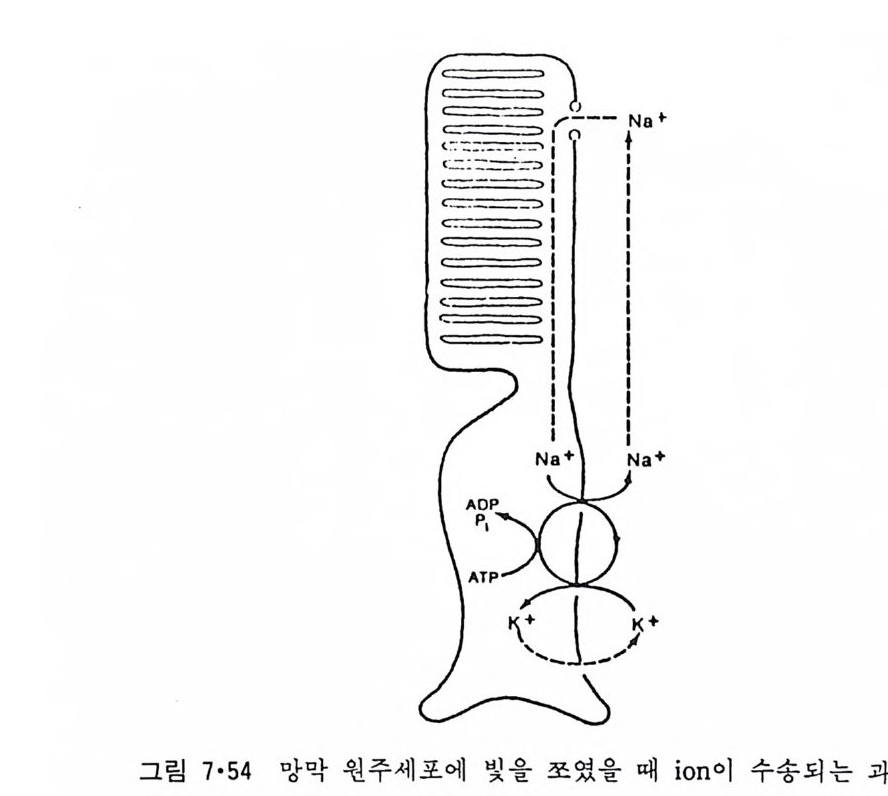 ’二《==드 令―= : = .=== == _、'’ I1i/ (nI 스-- +iN a ~
’二《==드 令―= : = .=== == _、'’ I1i/ (nI 스-- +iN a ~
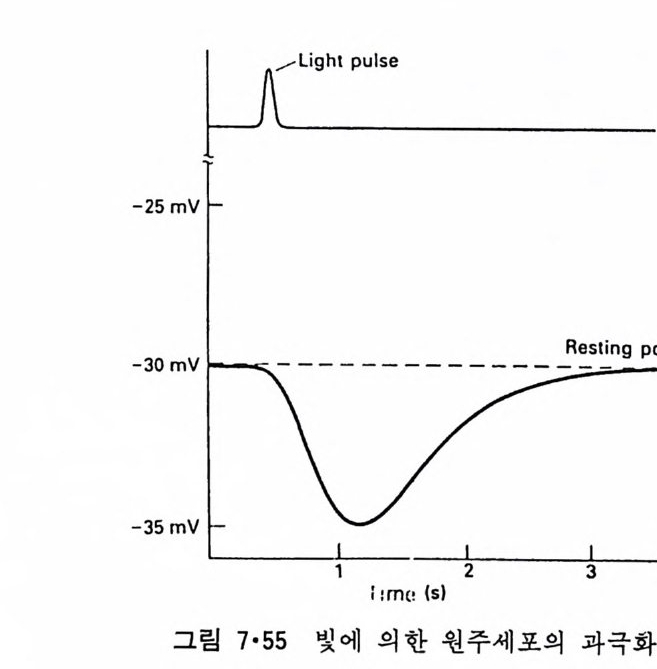 二/ LI g hI pu lse
二/ LI g hI pu lse
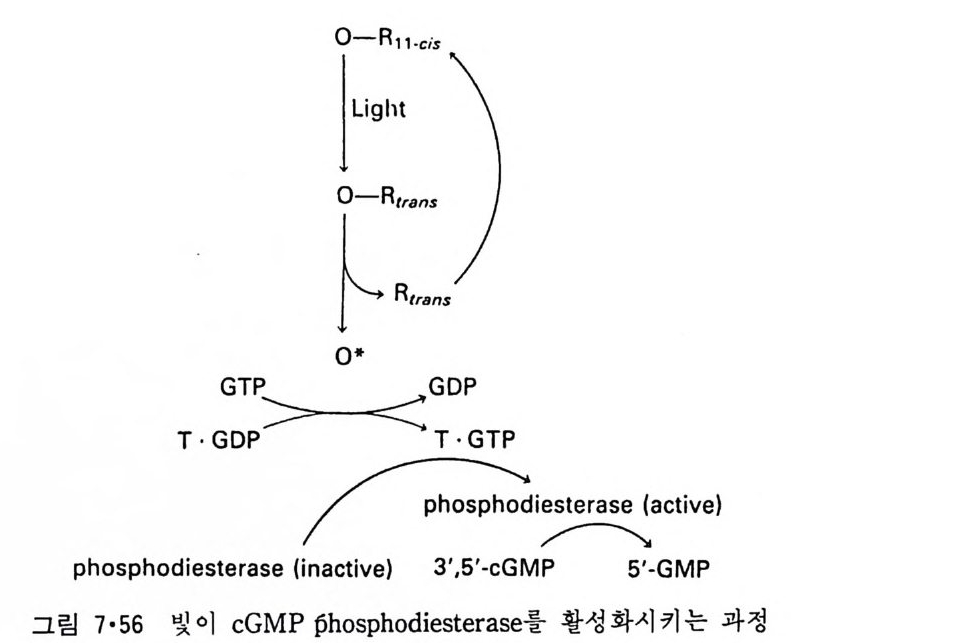 ?uR`'1 .tc·I ItSRrnrs an
?uR`'1 .tc·I ItSRrnrs an
주세포에 빛을 쪼이면 막전위를 과국화 (h yp e rp olar i za tri on) 시킨다(그림 7·55). 이렇게 막전위차가 -30mV 에서 -35mV 로 떨어지면 원주세포의 s yn a p se 에서 신경전달체가 방출되어 인접해 있는 신경세포에 신호가 전 달되며 궁극적으로는 두뇌로 가게 된다. 빛에 의해서 막전위가 과국화되는 mechan i sm 은 그림 7·56 에서와 같이 re ti nal 이 떨어져나가 활성화된 o p s i n 이 주변단백질인 t ransdu ci n 에 부착 된 GDP 가 GTP 로 치환되면서 활성화되며 활성화된 t ransdu ci n 은 또 cGMP p hos p hod i es t erase 를 활성 시 켜 cGMP 를 5'-GMP 로 전 환시 키 면 막동로가 닫히는 때문이라고 생각된다. * 7 장 참고문헌 (1) Katz , B. Nerve, Muscle and Syn ap s e , McGraw-Hi ll, 1966, (2) Ai dl ey, DJ . The Phys iolo gy of &citab le Cells, Cambrid g e , 1975. (3) Sie g e l, G.J . et al (eds) . Basic Neurochem istry, 3rd ed. Lit tle, Brown, Co. (4) Ste v ens, C.F . (1979) , Sc i. Am 241(3), 49-58. (5) Hi lle, B. (1976) Ann. Rev. Phys i o l. 38, 139-152. (6) French, R.J. and Horn, R. (1983) Ann. Rev. Bio p h y s . Bio e ng. 12, 319-356.
(7) Keyn e s, R.O . (19 79) Sci '. Am. 240(3), 126-135. (8) Hi lle, B. Ionic CJ ian ne ls of Exdta b le Membranes. 2nd ed. Sunderland, Mass. 1984. (9) Hodg k in , A.L. and Huxley, A. E. (1952) ]. Phys i o l . 1 17, 500-544. 00) Hess, G.P., Cash, D.J . and Aoshim a , H. (1983) Ann. Rev. Bio ph ys . Bio e ng . 12, 443-473. 01) Canti -T ranconi, B.M . and Raft er y, M.A. (1982) Ann. Rev. Bi oc hem. 51, 491-530. 떄 Durant, Y. and Israel, M . (1985) Sci '. Am. 252(4), 40-48. 떄 Dale, H.H., Feldherg, W. and Vog t, M. (1936) ]. Phys iol. 86, 353-380. 0-0 Chabre, M. (1985) Ann. Rev. Bio p h y s . Bi op h y s . Chem. 14, 331-360. 05) Altm a n, J. (1985) Natu re 313, 264-265.
제 8 장 생체막에서의 신호전이 외적 자국에 의해 일어나는 원형질막에서의 ion 이동속도의 변화는 생 체 전기현상을 일으키며 이는 생체에서 여러가지 정보전달의 수단으로 쓰인다. 이것과는 달리 순수한 화학적인 과정으로 외부에 대한 정보가 세포 내에 전달케 되는 경우가 있는데 그중 중요한 것이 hormone 의 작 용, 세 균 둘 의 物 質 走 性 (chemota x is ) 과 면 역 (im mune) 현 상 둥 이 다. Hormone 의 작용은 多細胞 生物體에서 세포 사이의 협조를 위한 통신수 단으로 쓰이는 것이고 물질주성은 세균이 외부 화합물에 접근, 또는 피 하는 수단이며 면역 현상은 유해한 외부 물체가 존재할 때 그 정보가 세 포 내로 전달되어 이에 대한 방어책을 강구할 수 있도록 하는 것이다. 이들 정보전달의 공통적인 점은 원형질막의 내재단백질인 수용체에 외 부 물질이 결합되면 이 단백질에 구조변화가 일어나고 이것이 세포질과 접촉하고 있는 내재단백질과 주변단백질 구조에 영향을 주어 세포액 내 부에 여러가지 생화학적인 반응을 일으켜 외부자국에 대옹하도록 하는 것이다. 이렇게 외부 정보가 생체막을 통해 세포내로 드러가는 과정을 신호전 이 (sig na l tra nsducti on ) 라고 부른다.
8·1 Hormone 의 수용체 1)2) 다세포 생물체는 그 생존을 위하여 세포간의 공동협조 (coord i na ti on) 가 필요한 데 이를 위한 세포간의 동신 (commun ic a ti on ) 은 대부분은 화합물 에 의해서 이루어진다. 화합물 이외의 수단은 간격연접에서 인접해 있는 세포들이 connexon 에 의해 직접 연결되어 전기 신호뿐만 아니라 작은 분자들까지 도 왕래 할 수 있는 것 이 다. 화합물에 의 한 정 보 (inf o r mati on ) 의 전달 방법은 크게 나누어 두 가지로 볼 수가 있다. 그 하나는 이미 제 7 장에서 기술한 바와 같이 신경계열 (nervouss y s t em) 의 s y na p se 에서의 신경신호의 전달로서 한 세포에서 인접해 있는 세포로 칭보가 전달되는 것이고 또 하나는 내분비 계열 (endocr i ne s y s t em) 에서 이 한 세포에서 분 비되어 혈액순환을 통해 멀리 떨어져 있는 세포에 정보를 전달하는 것이 다. 경우에 따라서는 신경 전달 물질로 알려져 있는 화합물이 혈액순환 에 의해 다른 組織에 있는 세포에 정보를 전달하는 경우가 있는데 이들
 표 8•I Hormone 의 종류와 그의 대표적인 예
표 8•I Hormone 의 종류와 그의 대표적인 예
울 신경 honnone(neurohormone) 이 라고 불린다. Hormone 들은 목표된 바의 세포에 도착하면 많은 생화학적인 또는 생 리적인 반응을 일으키는데 이중에서 중요한 것은 단백질 합성, 신진대사 에 관여하는 효소의 작용이나 원형질막을 동한 물질이동 등에 영향을 주 는 것이다. 이들 hormone 은 화학적인 구조에 따라서 세 가지로 크게 나 뉘어지는데 표 8·1 은 이들 hormone 의 대표적 인 예를 보인다. Pep tide hormone 은 am i no 기가 3 개로 된 t rip e pti de 로부터 am i no 기를 수백개 가 지 고 있 는 p ol ypepti de 에 까지 이 른 다. Ami ne hormone 들은 am i ne 기 를 가지 고 있는 ty ros i ne 유도체 이 고 ste r oid hormone 은 choleste r ol 유도체
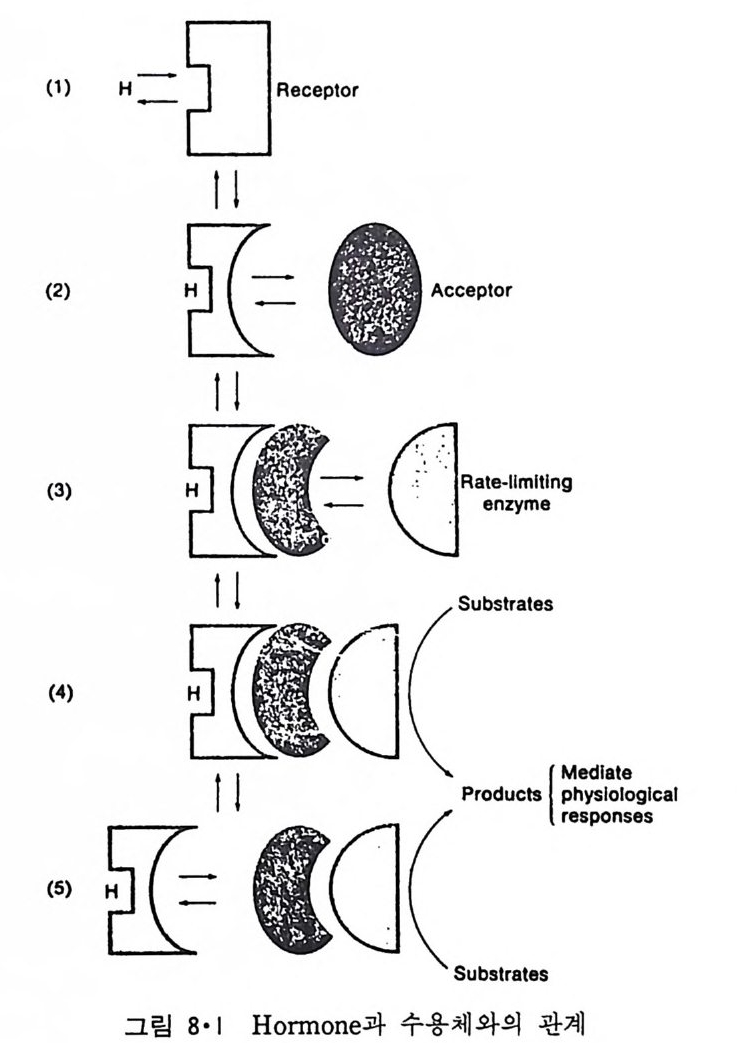 (1) H 二 曰 R•cept or
(1) H 二 曰 R•cept or
둘이 다. Pep tide hormone 과 ami ne hormone 이 극성물질인 것에 반하여 ste r oid hormone 은 비 극성 용매 에 녹는다. Hormone 둘은 단백 질 인 수용체 에 결 합함으로써 그 기 능을 발휘 하는데 이들 수용체는 높은 선택성 (s p e cificity)과 천화력 ( a ffi n ity)을 가지고 hormone 과 결 합하여 이 들 작용을 중재 (media t e ) 시 킨 다. 많은 경 우에 는 수용체 이외에 acce pt or 까지 hormone 의 작용에 가담한다(그림 8·l). 이 때에 hormone 과 결합이 되면 수용체와 acce pt or 에 구조 변화가 일어난 다고 생각되고 있다. S t ero i d 와 t h y rox i ne 은 원형질막을 동과할 수 있기 때문에 수용체가 세포질 내에 존재하지만 나머지 hormone 은 원형질막을 통과할 수 없기 때문에 그들의 수용체는 세포 표면에 내재단백질로서 존 재한다. Hormone 의 분비는 체계적인 여러 단계를 거쳐서 일어나는데 ( 그림 8· 2) 그 전체적인 동제를 두뇌의 일부인 hyp o t halamus 에서 이루어진다.
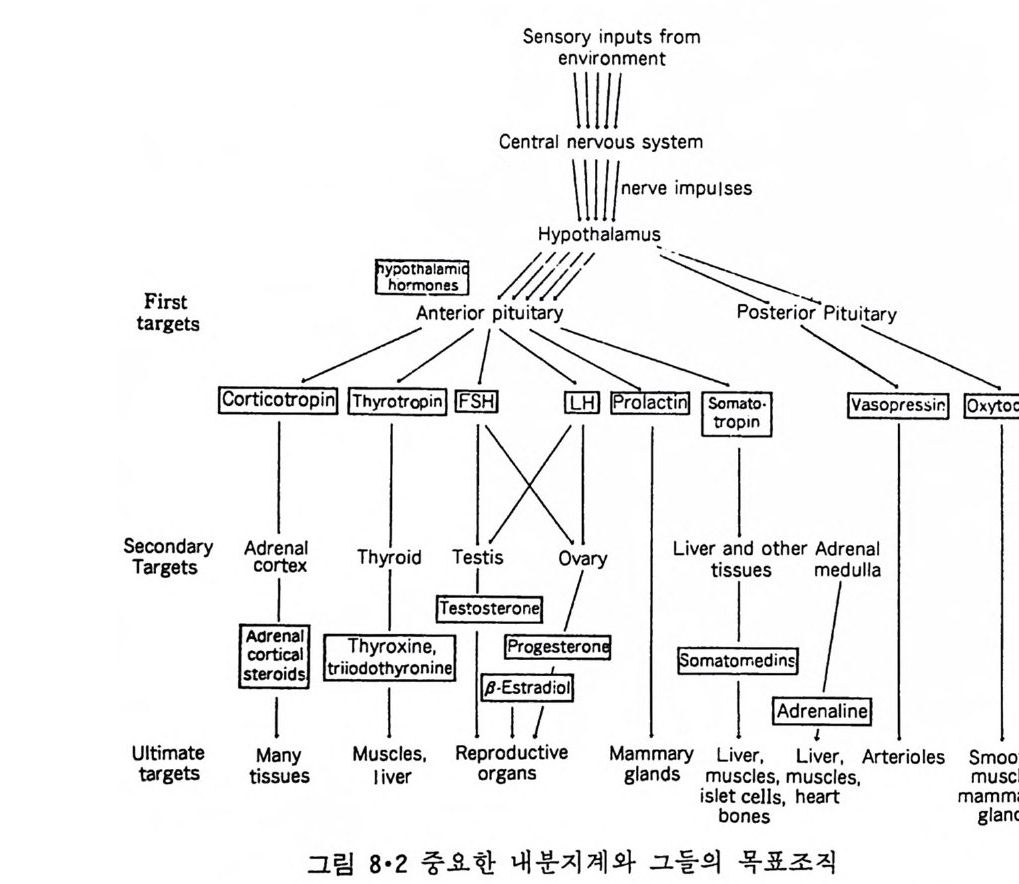 Sensory inp ut s from
Sensory inp ut s from
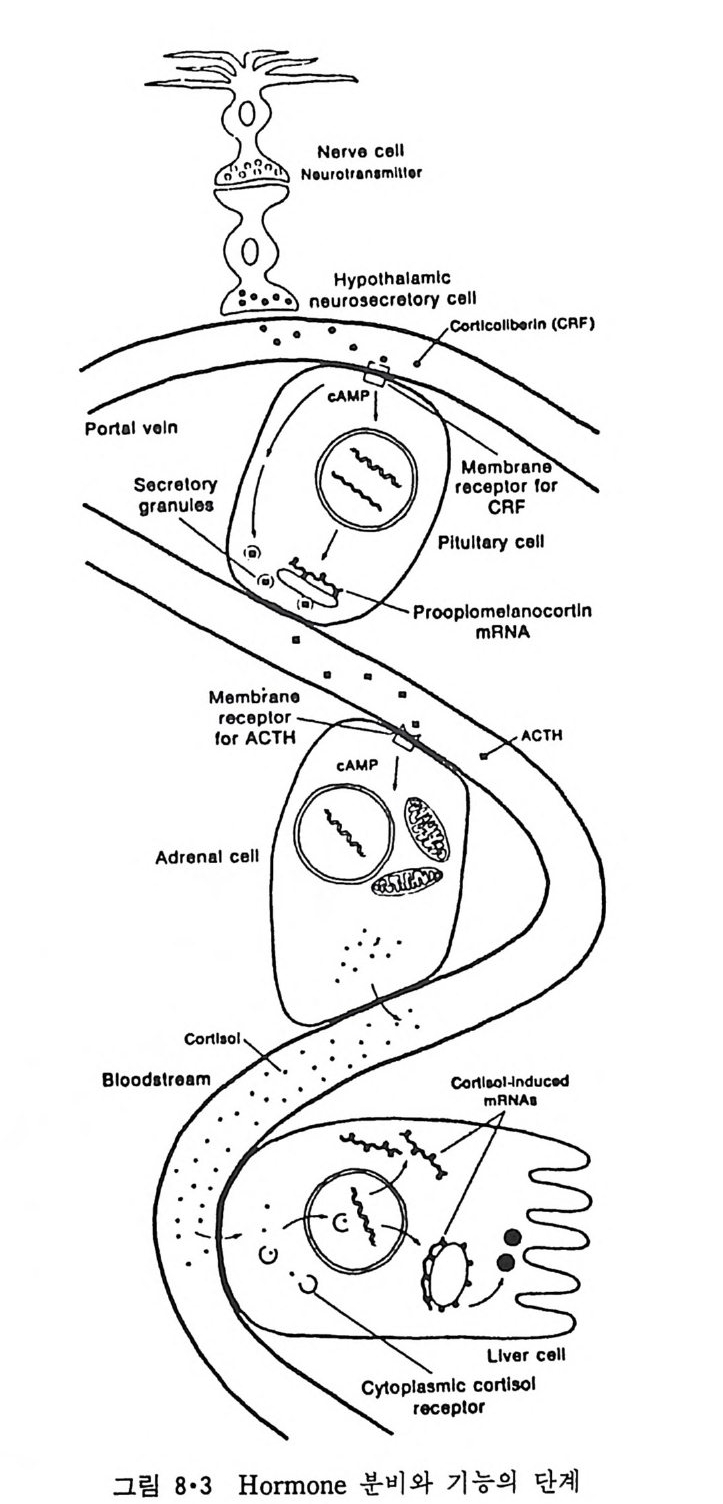 Nerve cell
Nerve cell
여기서 분비되는 hormone 이 1 차 목표 세포에 도달하면 이 돌 세포에서 다른 hormone 이 합성 분바되어 2 차 목표 세포에 가고 거기서 또 합성 분비된 homone 들이 최종 목표인 세포로 운반되어 여러가지 필요한 생화 학적인 기능을 발휘한다. 이러한 단계적인 hormone 의 분비 과정은 그림 8·3 에 보여준다. 이 그림에서는 ste r oid hormone 의 분바 과정을 예로 보 여 주지 만 다른 hormone 도 같은 방법 으로 분비 가 된 다. S t ero i d 같은 소 수성 용매에 녹을 수 있는 물질은 세포내에서 합성이 되면 용해-확산 과 정으로 원형질막을 통과하여 순환되는 혈액으로 들어가서 같은 과정으로 최정 목표 세포 내부로 들어간다. Pep tide hormone 이 합성될 때에는 신 호 서열 (s ign al se q uence) 로서 소포체의 lumen 으로 들어가 exoc yt os i s 과정
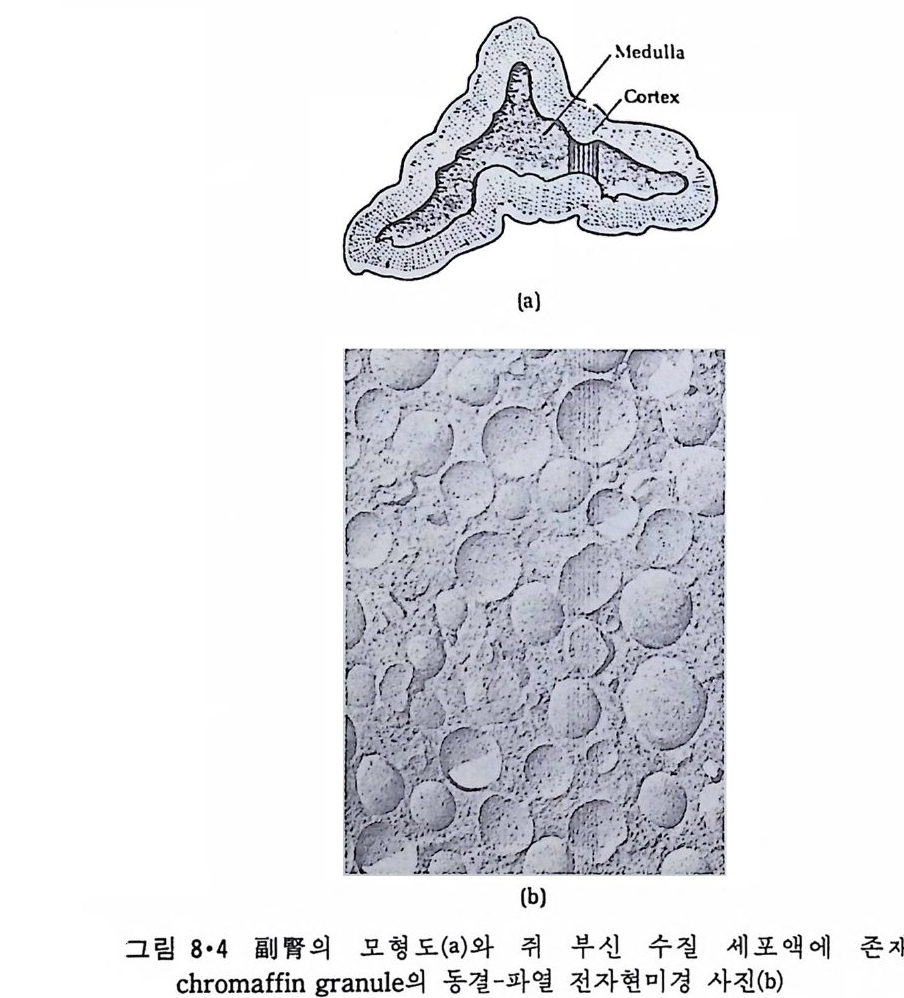 [a)
[a)
으로 세포막을 통과하여 혈액 으로 들 어 가고 ami ne horm one 들 은 합성되 는 대로 막소포 과립 ( gr anule ) 에 저장되었다가 (그링 8·4) 역시 exocy tos is 과정을 거쳐 혈액으로 들 어간다. 8 • l • l Adeny la te c y clase3> ◄ > 대 부분의 pe p tide hormone 과 ami ne hormone 의 경 우 그 수용체 들은 알려져 있지만, 세포 표면에서 일어나는 수용체와 hormone 의 결합이 어 떠한 과정을 거쳐 세포 내부에서 일어나는 생 화학적인 반응에 영향을 주 느냐 하는 것은 아직도 찰 모르는 형편이다 . 그러나 많은 hormone 의 작 용에는 공통점 이 있는데 이 는 세포내에서 cy c lic 3', 5'- A M P(c-A MP) ( 그 링 8·5 ) 가 생성된다는 것이다. 만일 hormone 을 세포간 통신의 1 차
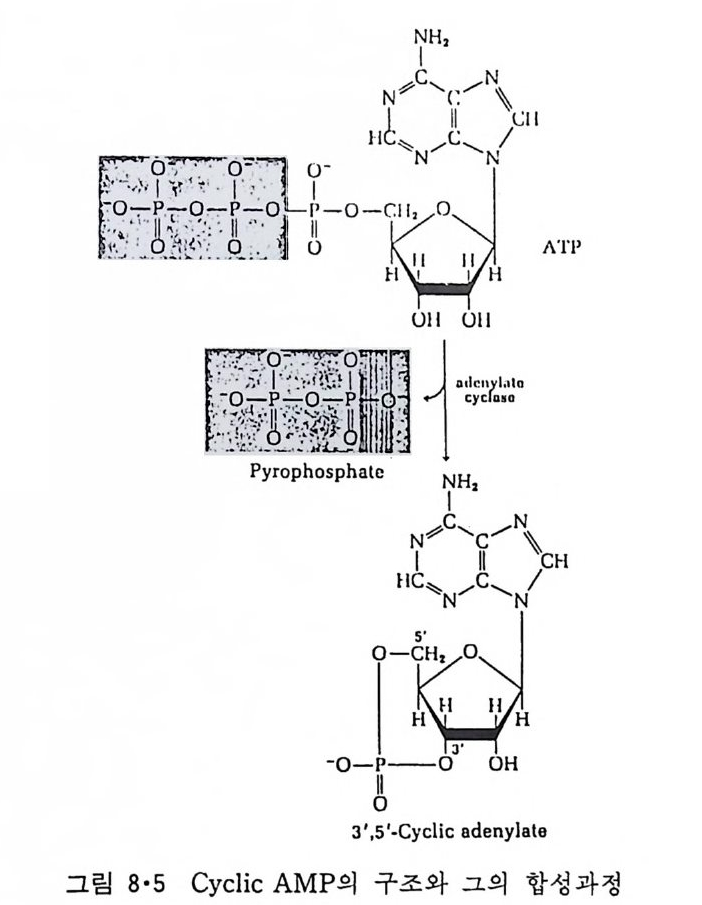 f 言〉L. .... _ p曰y디 니 『간, 7OO」妹-먼』psO IP _o。I _I一 H 0凰atcP N /_`U따` / NlNcNi0_l lt / 出/O\ h ¢|c_Icc 幽UI. 》 CC I 11c2I >N 。 &H\r N %/ \ cN ^ HI I) H
f 言〉L. .... _ p曰y디 니 『간, 7OO」妹-먼』psO IP _o。I _I一 H 0凰atcP N /_`U따` / NlNcNi0_l lt / 出/O\ h ¢|c_Icc 幽UI. 》 CC I 11c2I >N 。 &H\r N %/ \ cN ^ HI I) H
messeng er 라고 하면 c-AMP 는 2 차 messen g er 라 부를 수 있을 것 이 다. 즉 1 차 messeng er 는 원형질막을 동과할 수 없기 때문에 원형질막에서 수 용체를 동해 정보를 세포내에 있는 2 차 messen g er 에게 전달하는 것이다. 그래서 c-AMP 가 세포 내에서의 생화학적인 반응에 영향을 미치는 것이 다. c-AMP 의 합성은 원형질막에 존재하는 내재단백질인 adeny la te c y clase 와 hormone 과 결 합된 수용체 의 상호작용에 의 해 서 이 루어 진 다. Adeny la te c y clase 는 모든 동물세포에 존재하며 표 8·2 에 주어진 hormone 들에 의해 자국된다. 이들 hormone 이외에 gu an i ne 이나 이와 관계되는 p ur i ne 이 adeny la te c y clase 작용에 필요하다. 근육세포에서 e pi ne p hr i ne 이 나 간 세포에서 g luca g on 아 adeny la te c y clase 를 자국시 켜 ATP 를 c-AMP 로 전 환시 키 면 이 c-AMP 는 cascade mechan i sm 에 의 한 g l y co g enol y s i s 를 일으킨다. 즉 생성된 c-AMP 가 한 단백질 k i nase 의 촉 매 소단위를 조절 (re gu la t o ry) 소단위로부터 분리시키면 활성화된 촉매
 표 8·2 Adeny la te c y clase 를 활성화 하거나 처해시키는 hormone 둘
표 8·2 Adeny la te c y clase 를 활성화 하거나 처해시키는 hormone 둘
소단위 는 ph osph ory la se k i nase 를 인 산화시 키 고 이 는 gly c o g e n ph os- p hor y lase 를 활성화시킨다. 이 전 과정은 파괴된 세포에서도 일어나는데 이 cascade 의 첫째 단계인 ATP 가 c-AMP 로 전환되는 과정은 원형질막 에서 일어나는 것이 발견되었다. 죽 adeny la te c y clase 는 막에 존재하는 단백질이다. 이 단계에서 hormone 수용체의 존재는 알지 못하였기 때문 에 hormone 이 이 효소를 직접 활성화시키는 것으로 생각되었지만 곧 여 러 종류의 hormone 이 같은 adeny la te c y clase 를 활성 화시 키 는 것 으로 보 아 수용체의 존재가 고려되기 시작되었다. 이 렇 게 많은 종류의 hormone 이 adeny la te c y clase 를 활성 화시 키 는 데 있어서 이 효소가 각 hormone 의 수용체와 각각 결합되어 있는 것이 아 니고 각 hormone 에 대한 수용체와 ade~y la te c y clase 가 독립적으로 원형 질막 내에서 존재하다가 hormone 이 수용체와 결합하면 이 복합체가 효 소와 회합하여 c-AMP 를 생산시킨다는 것이 여러가지 실험으로 판명이 되었다. 이들 실험 결과의 하나는 몇 가지 다른 hormone 의 수용체를 갖 고 있는 원형질막을 한 hormone 으로 포화시킨 후 두번째 hormone 을 첨
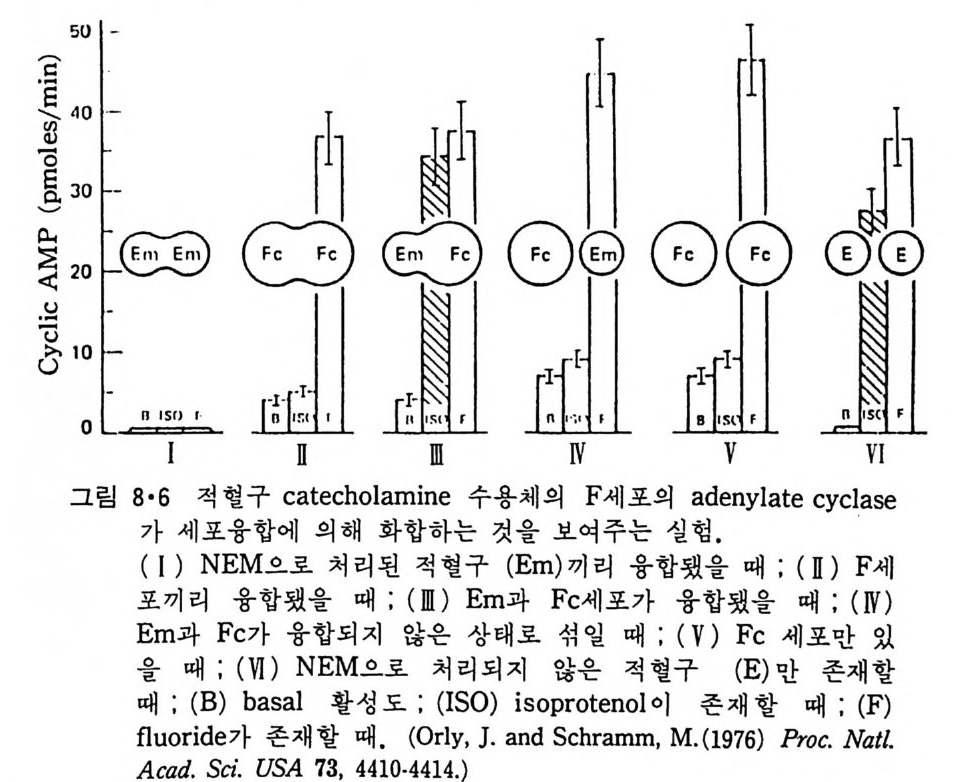 dW50>3'lH4304 i尸3 30 2010 i沿l
dW50>3'lH4304 i尸3 30 2010 i沿l
가했을 때 이 효소의 활성도가 증 가되지 않 는 것은 adeny la te c y clase 가 공통적인 p ool 로 존재하며 이미 수용체로 포화된 것을 의미한다. 좀더 결 정 적 인 증거 는 N-e t hy lmale i m i de 나 열 처 리 로 adeny la te c y clase 를 파 괴시킨 칠면조 적혈구와 {3- adrenergi c 수용체가 없는 F 세포 를 Sendai v i rus 로 융합시 킨 후 {3 -adrenal 을 첨 가했을 때 adeny la te c y clase 의 활성 도가 나타는 것을 볼 수 있었던 것이다(그림 8·6). 여기 서 수 용 체 없 이 adeny la te c y clase 만 있는 F 세포는 붕소화합물 ( fl uor i de ) 에 의해서 효소 반응을 나타낸다. 이 실험은 전혀 다른 세포 내의 수 용 체 와 adeny la te c y clase 가 회합하여 hormone 에 의한 효소 활 성 을 보여주 기 때문에 aden y la t ec y clase 가 막 내에 공통적인 p ool 로 존재 한 다 는 것을 증 명한 다. Hormone 에 의 해 활성 화되 는 adeny la te c y clase 의 작 용에 는 gu anin e nucleo ti de 가 필요하기 때문에 이 효소는 촉 매단백 질 과 조철 단백질의 두 단위로 구성되어 있다고 추측되었는데 이는 다음 두 가지 실험으로 증명 이 되었다. 첫째 비둘기 적혈구막을 비 i on 성 세탁제인 Lubrol PX 로 추 충하여 GTP 를 고정 시 킨 ag a rose column 에 통과시 키 면 얻어 진 용액 의 adeny la te cy cl ase 활동도는 현 저 히 감소된 다. 이 column 을 GTP 나 가수 분해 가 되 지 않는 유사 화합물인 Gpp ( NH) p(gua ny !- 5 ' -y l im i do dip h os• ph ate ) 로 용 출 (elute ) 시 켰 을 때 이 용 출 액 (eluent) 자 체 는 adeny la te c y clase 의 활동도가 없지만 이것을 먼처 colwnn 에 흡 수되지 않은 용액과 합치면 이 효소의 활성도가 나타난다. 여기서 GTP column 에 흡착 되는 단백질은 gua nin e nucleo ti de 와 결합되는 조절단백질이고 이 colwnn 에 흡착되지 않는 부분이 촉매단백질이라고 생각되었다. 두번째 실험은 원 형질막을 세탁제로 추출한 용액을 가열하면 그 adeny la te c y clase 의 활성 도가 없어지는데 이 가열된 용액을 adeny la te c y clase 의 활동도가 없는 S49 lym ph oma 세 포 (e y e 기 에 가하면 hormone 에 의 해 자국을 받는 이 효 소의 활성도가 생긴다. 이 결과의 해석은 eye - 세포에는 hormone 수용 체와 촉매단백질만 존재하고 세탁제로 추출한 용액에서 adeny la te e y clase 의 두 단백질 중 촉매단백질은 가열로 쉽게 파괴되는 데 비해서 조절단백질은 온도에 대해 안정하다는 것이다. 죽 adeny la te e y clase 는 두 개의 물리적 성질이 다른 단백질로 구성되어 있다. 이들 실험으로부 터 hormone 에 의해 자국되는 adeny la te e y clase 의 활 성도에는 원형질막 에 hormone 수용체 단백질, 조절 단백질, 그리고 촉 매 단백질 등 세 가
지 단백질이 필요하다는 것을 알 수 있다. 이들 네 가지 내재단백질은 거의 모든 원형질막에 존재하는데 명가지 막에서만 이들의 분리 정제가 가능하였다. Hormone 수용체 단백질은 약 8 만의 분자량을 가진 큰 p ol yp e pti de 이 다. 조절 단백 질 (G-pr o te i n 또는 N -p ro t e i n) 은 a 사슬(분자량 42kDa) 과, /3사슬(분자량 37kDa) 로 구성되어 있는데 r 사슬(분자량 lOkDa) 도 같이 존재한다고 생각되고 있다. Aden y la t ec y clase 인 촉매단백질 (C- p ro t e i n) 은 세탁제 용액에서 불안정하 여 정확한 분자량은 모르나 10 만이 넘는 것으로 추정된다. 이렇게 c-AMP 의 합성을 촉진시키는 hormone 이외에도 이것을 저해 시키는 hormone 도 존재한다(그림 8·2). 여기서는 저해수용체(i nh i b it o ry recep tor ) 가 저 해 조절 단백 질 (inh ib i t or y G pro te i n ) 과 작용하여 adeny la te c y clase 의 작용을 방해 한다고 생 각된 다. 저 해 수용체 의 분자량은 자국수 용체 (sti m ulato r y recep tor ) 와 유사하고 저 해 조절 단백 질도 a 사슬 (41k Da), /3사슬 (35kDa) 과 7 사슬(l OkDa) 로 구성되었다고 생각된다. 조철단 백질의 /3사슬인 경우 am i no 산의 조성과 다른 성질들이 동일한것으로 보 아 자국 조철단백질과 저해 조절단백질은 동일한 p ol yp e pti de 라고 생각된 다. 그림 8·7 은 원형질막에서 이들 내재단백질이 배열되어 있는 model 을 보여준다. 수용체단백질들은 hormone 과 결합이 되는 부분이 세포외부로 향하고 조절단백질의 GTP 와 결합하는 부분과 촉매단백질의 활성부위
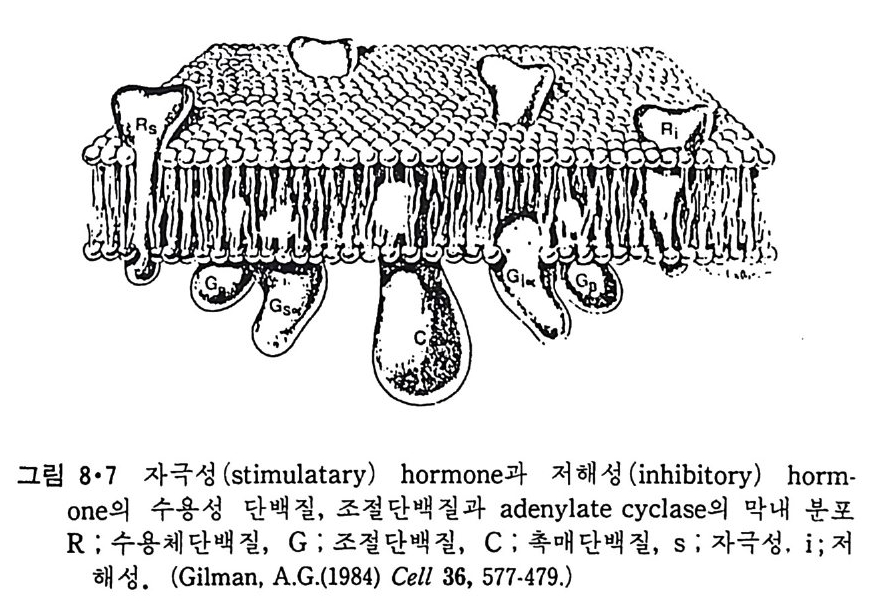 그림 8•7 자국성 (sti m ulata r y) hormone 과 처해성 (inh ib i t or y ) honn-
그림 8•7 자국성 (sti m ulata r y) hormone 과 처해성 (inh ib i t or y ) honn-
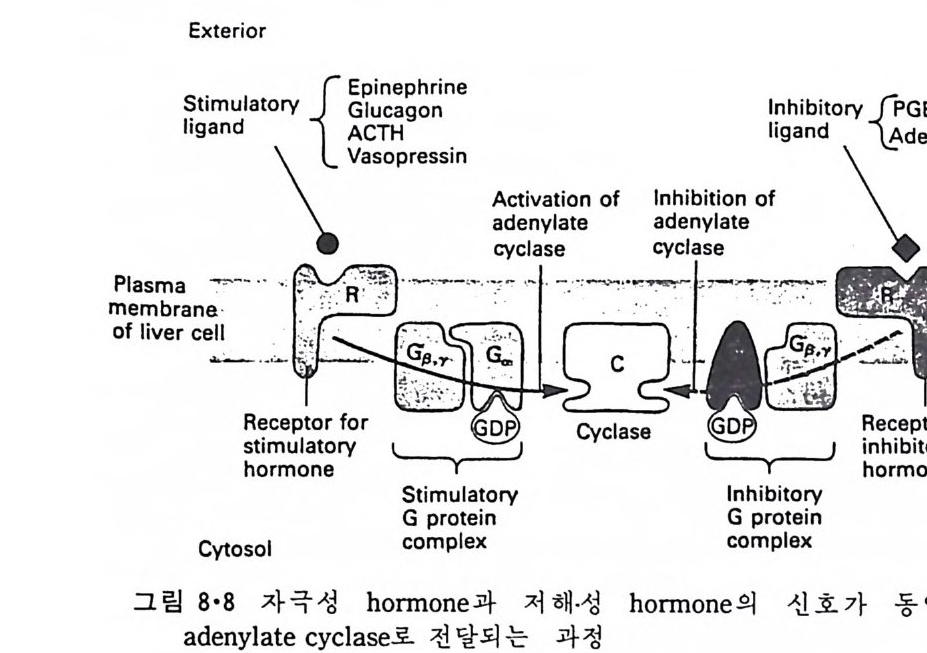 Exte rio r
Exte rio r
(acti ve cen t er) 는 세포질쪽을 향한다. 그림 8·8 은 자국성 hormone 과 저 해 성 hormone 이 같은 adeny la te c y clase 에 영 향을 주는 것 을 나타낸 다. 조절단백질이 신호전이의 중간역할을 하는 것은 이 내재단백질이 hormone 수용체 단백질이나 adeny la te c y clase 과 결합할 수 있으나 수용 체와 촉매단백질은 직접 결합하지 않는 것으로 알 수 있다. 조절단백질 과 촉매단백질이 보통 같이 존재하는 것은 이미 설명하였다. Hormone 이나 a g on i s t존재하에서 세탁제로 용해된 수용체 단백질이 조철단백질의 a 사슬과 결합하는 것은 ge l filtra ti on chroma t o gr a p h y로 관찰이 되 었다. Hormone 신호의 전이에 필요한 세 개의 내재단백질간의 관계에 대해 서는 많은 연구가 되어 왔는데 그 중요한 결과는 다음과 갇다. (a) GTP 의 존재 하에 서 수용체 에 대 한 hormone 의 친 화력 은 감소한 다. 이는 hormone 수용체가 조절단백질과 회합하는 결과라고 해석된다. (b) Hormone 이 수용체와 결합하면 조철단백질에 결합되어 있던 GDP 가 GTP 로 치환이 되는 반응을 야기시킨다. (c) Hormone 은 조절단백질의 GTPase 활성도를 촉진시킨다. 이는 조 철단백질의 a 소단위가 B 와 r 에서 떨어져 나오는 결과이다. 죽 B 와 결합 되어 있으면 8 소단위의 GTPase 활성도가 저해되고 있다가 8 가 떨어져
나가면 이의 효소황성도가 나타나기 때문이다. (d) 조철단백질에 GTP 가 결합되면 c-AMP 합성이 촉진된다. 이는 GTP 와 결합된 조절단백질의 a 소단위가 adeny la te c y clase 와 결합하여 이 효소를 활성화시킨다고 생각된다. 그러나 GTP 가 분해되어 GDP 로 전 환되 면 adeny la te c y clase 의 효소기 능 이 없 어 진 다. G pp (NH) p나 GTP-r -s (gua nosin e -5 ' -0 - (3-th i o t r i p h osph ate ) ) 와 같이 가수분해 되 지 않는 GTP 유사화합물은 GTP 보다 더 유효하여 adeny la te c y clase 를 활성 화된 상태 로 지속시킨다. Cholera 독소의 A 소단위는 조절단백질을 ADP-rib o syl a - ti on 시켜 (그림 8·9) GTPase 를 저해시켜 c-AMP 가 계속 생성하도록 한
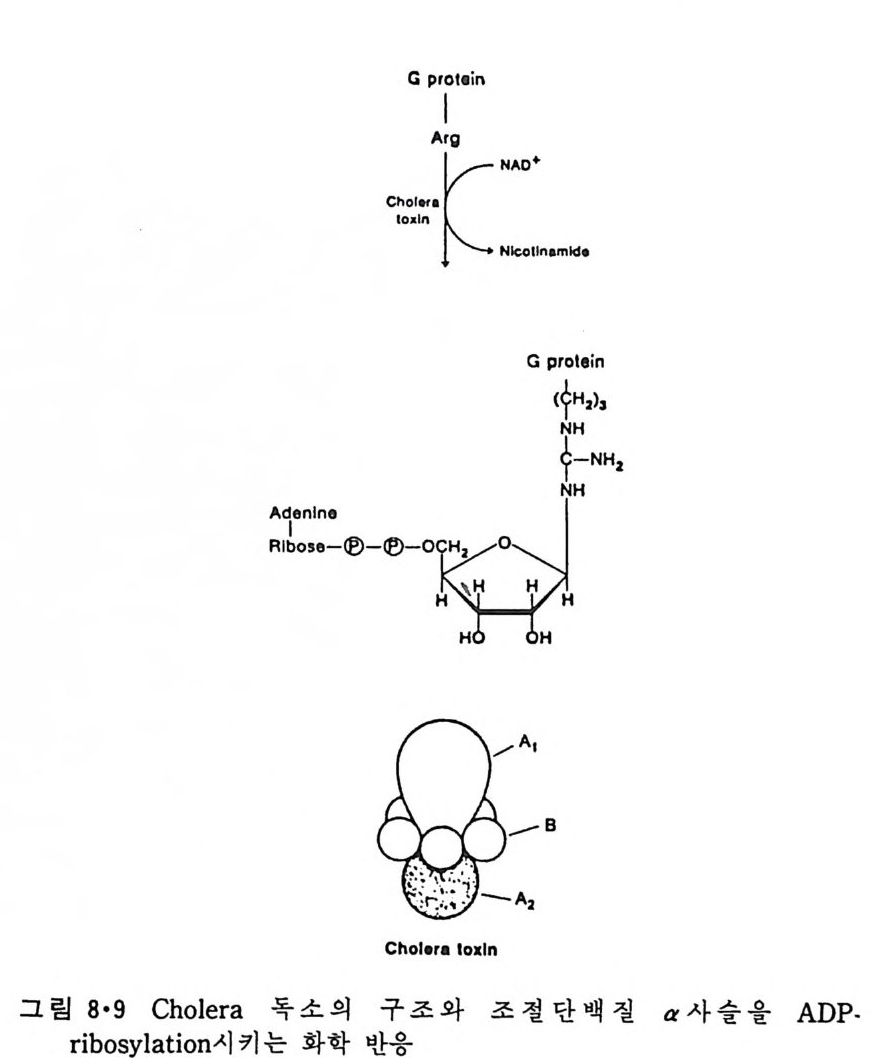 GTkN A♦D Nleo
GTkN A♦D Nleo
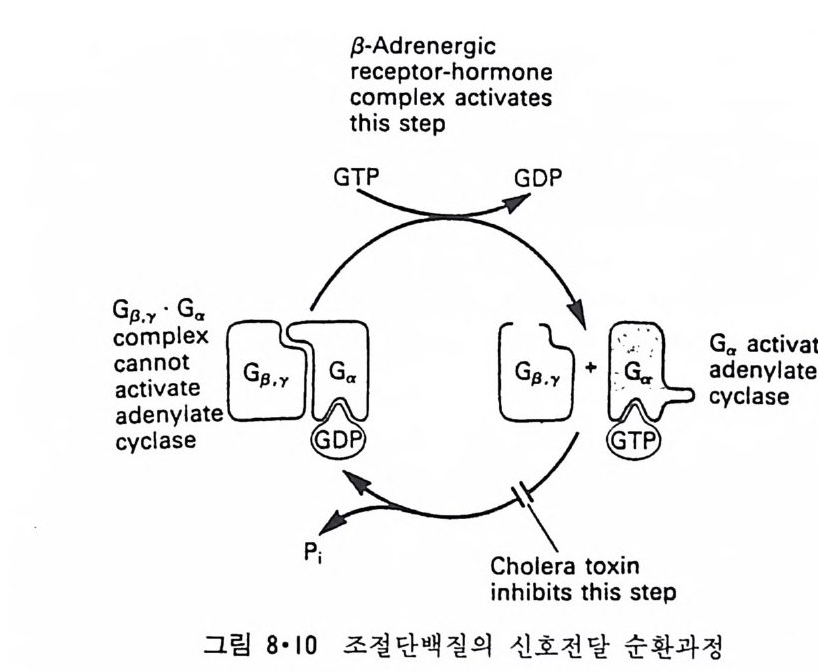 /tcr3heo-c iAms e d pps rt tleeeo n x pr e - hragcoitr cim v a otne es
/tcr3heo-c iAms e d pps rt tleeeo n x pr e - hragcoitr cim v a otne es
다. 그래서 조절단백질의 GTPase 작용은 adeny la te c y clase 를 잠정적으 로만 활성화하는 역할을 한다. 위의 실험결과들은 조절단백질이 그림 8·10 에서와 같이 순환 반응을 동해 신호전이의 중추적 역할을 하는 것을 보여준다. 그림 8·11 은 homrone 에 의 한 adeny la te cyc l ase 활성 화 mechan i sm 의 개 요올 보여 준 다. Hormone 이 없는 상태에서 3 개의 내재단백질들은 독립적으로 존재 하며 조절단백질의 a 소단위에는 GDP 가 부착되어 있다. Hormone 이 외 부에서 결합하면 수용체 단백질에 구조변화가 일어나 조철단백질과 화합 한다. 이때에 조절단백질이 활성화되어 GDP 가 GTP 로 세포 내부에서 치환된다. 이와 동시에 a 소단위가 나머지 단위로부터 해리되며 adeny la te c y clase 와 결합되어 이 효소를 활성화시켜 c-AMP 가 세포내부 에 생성된다. 이 단계에서 a 소단위의 구조변화가 일어나 GTPase 가 활 성화되어 GTP 가 GDP 로 전환되면 a 소단위와 나머지 소단위가 다시 회 합한다. 이는 hormone 이 계속 존재하는 한 다시 수용체 단백질과 결합 하여 위 과정을 반복할 수 있다. 이러한 복잡한 과정을 거쳐서 hormone- 수용체 복합체는 여러 개의 조 절단백질을 활성화시키며 활성화된 한 개의 조철단백질은 또 여러 개의
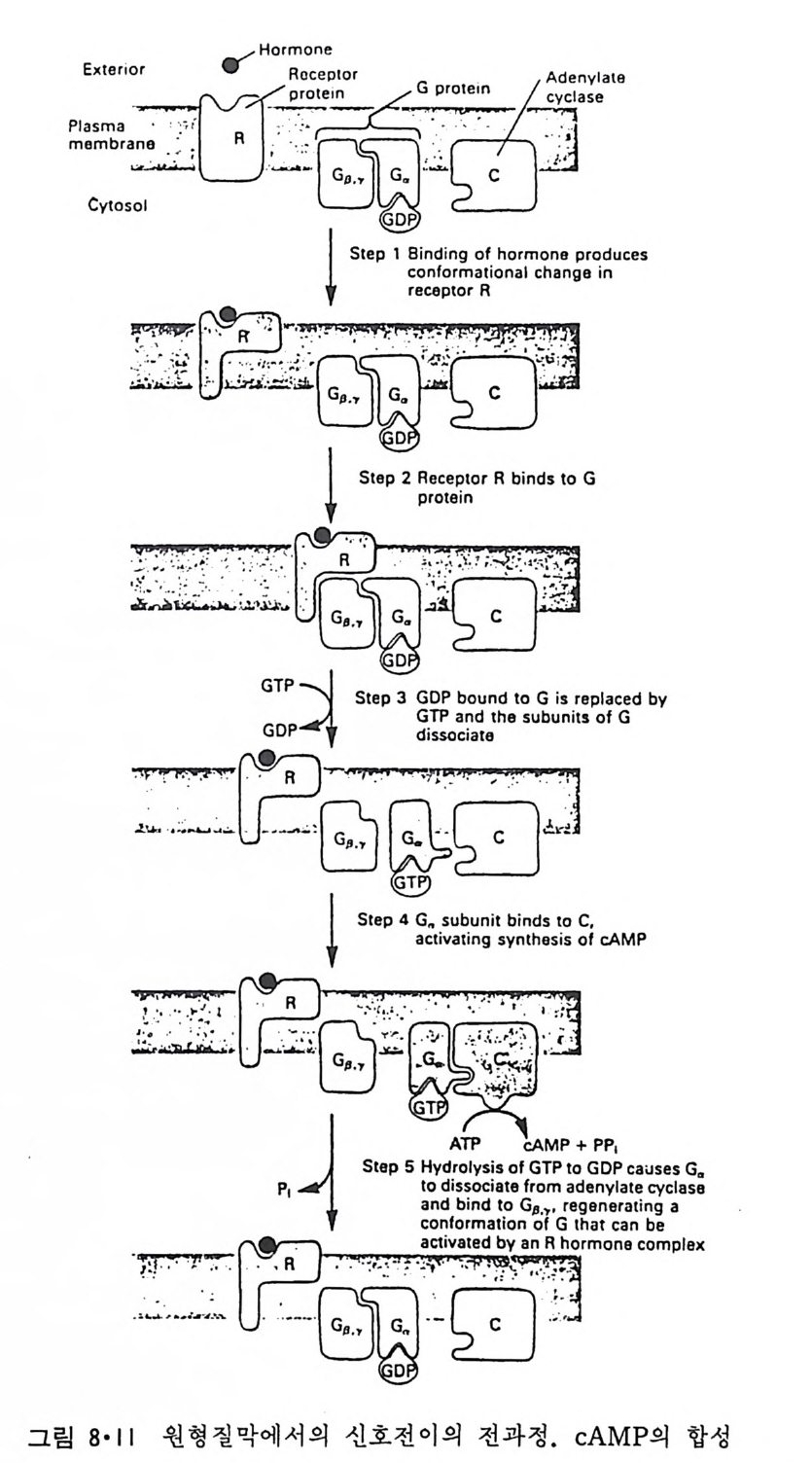 t ::;,:~~t•~ion al chang e in e s
t ::;,:~~t•~ion al chang e in e s
adeny la te c y clase 를 활성화시킨다. 결국 한 개의 hormone 에 의해서 수 백 개의 c-AMP 가 합성이 된다. 두번째 이유는 hormone 의 농도가 감소 되면 c-AMP 의 합성은 신속히 종결시킬 수 있다. 조절단백질에 부착된 GTP 가 신속히 가수분해되어 hormone 이 계속해서 존재하지 않는 한 c -AMP 의 합성은 중단되고 만다. GTP 가 가수분해되면 hormone 에 대한 수용체의 친화성이 중가되어 hormone 농도 중가에 즉시 대응할 수 있다. 세번째 이유는 한 종류의 조절단백질과 adeny la te c y clase 가 여러가지 hormone 으로부터 신호를 전 이 할 수 있는 것 이 다• 한 개 의 adeny la te c y clase 가 여러 가지의 hormone 수용체와 상호작용하는 것은 이미 설명 되었다. 이들 칭제된 3 가지 단백질은 인산지방질 막소포에 재구성은 아직 못했 으나 수용체 단백질과 조절단백질을 함께 재구성시키는 것은 최근에 성 공하였다. 이 두 성분의 공존하에 a g on i s t의 결합 천화력은 증가했고 그 림 8·12 에 보이는 것과 같이 G pp (NM) p존재하에 i so p ro t erenol 의 결합이 감소된다. 또 그림 8·13 은 a g on i s t의 존재 하에 GTPase 의 활성도가 중 가하는 것을 볼 수 있다. 이는 생체막에서 관찰할 수 있는 실험결과와 같다.
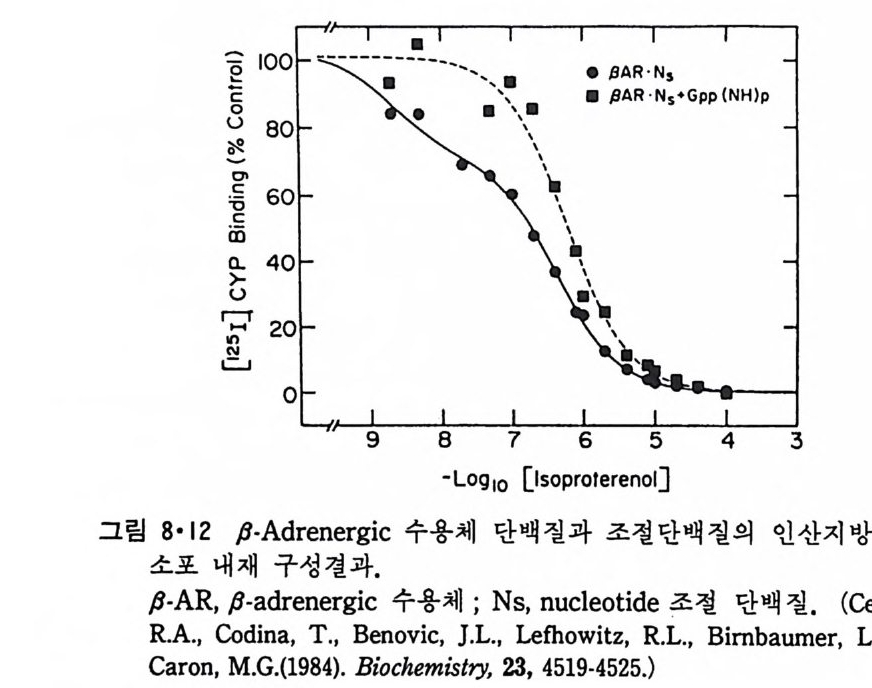 l1 广2 00\■• BfJAA RR · ·NN s s •Gp p (NH)p
l1 广2 00\■• BfJAA RR · ·NN s s •Gp p (NH)p
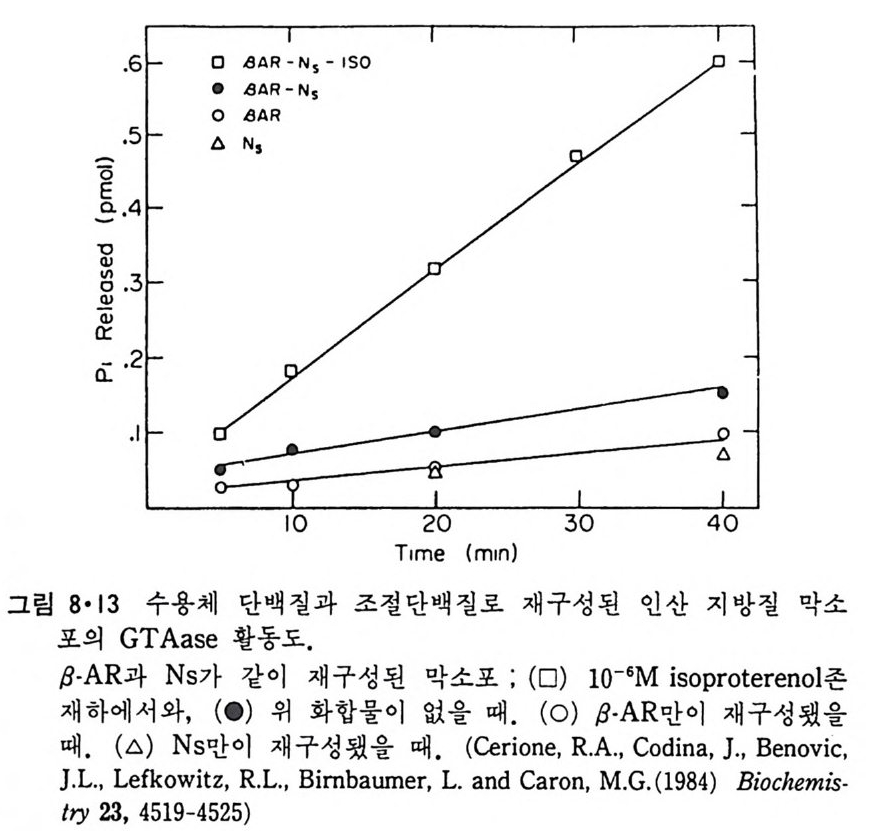 6 □ .BA R -N 5-I SO
6 □ .BA R -N 5-I SO
이 렇 게 adeny la te c y clase 를 활성 화시 켜 c-AMP 를 생 성 케 하는 hormone 과 이 효소를 처 해 시 키 는 hormone 들 (표 8 • 2) 이 외 에 epi ne - ph rin e , vasop r essin , t h yr o t ro pi n 등은 Ca2+ 를 세 포 내 에 방출시 키 나 그 자세한 mecham i sm 은 아직 모른다. 8·1·2 Ins ulin수용체 5)6) Insu li n 은 포도당, am i no 산, nucleo ti de 등 영 양분들 이 원 형 질 막을 통해 세포내로 들어가는 것, 단백질, gly c o g e n, DNA 로 고분자의 합성 및 lip o g enol y s i s 를 촉진시키는 동 다양한 역할을 한다. Insu li n 이 포도당의 두과도를 중가시키는 mechan i sm 은 그림 8·14 에서 보이는 바와 같이 원 형 질막 근처 에 있는 포도당 pe nnease 를 갖는 막소포가 융합에 의 해 원 형질막으로 이동되기 때문이라고 관찰되었다. Insu li n 은 이 hormone 의 목표세포인 근육, ad ip ose 조칙, 간, l ymp hoc yt e 동의 원형질막에 분포되
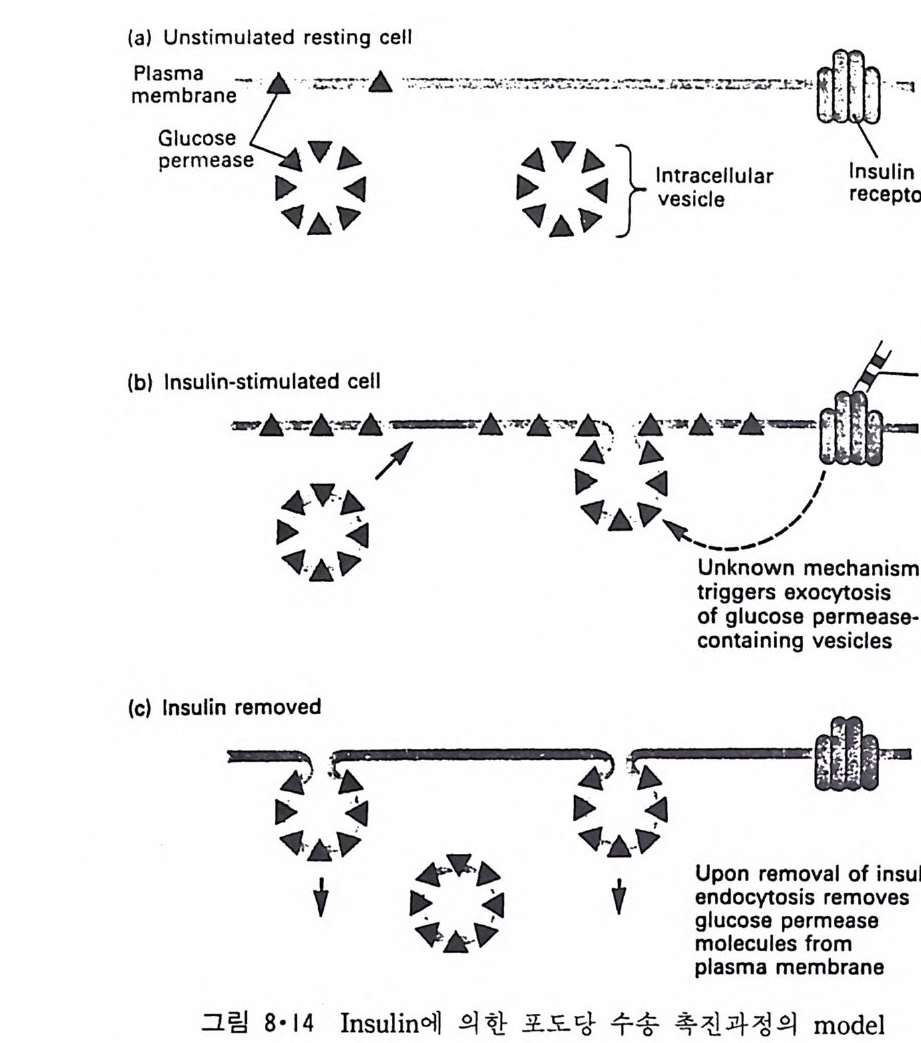 l Pm히a pUe n saE mgg『〔b l IGu-e:elr ► 뺄 w eis t『鼻 w ◄mg ~ 소 - C ell ― 一 i~ 죠 ►i一뺄 ‘ RWi. `{.i鼻◄ ~ 一{} } .I-ngevt srl. ati ee le[lule l a5r 4 i. i肅g.l in。p r t
l Pm히a pUe n saE mgg『〔b l IGu-e:elr ► 뺄 w eis t『鼻 w ◄mg ~ 소 - C ell ― 一 i~ 죠 ►i一뺄 ‘ RWi. `{.i鼻◄ ~ 一{} } .I-ngevt srl. ati ee le[lule l a5r 4 i. i肅g.l in。p r t
어 있는 수용체단백질에 견고하게 결합된다. 이것은 1 2s1 로 표지된 i nsu li n 으로 측칭할 수 있으며 i nsul i n - 수용체 복합체의 해리상수는 10-10 M 이다. Insu li n 수용체의 선택성은 커서 i nsu li n 이나 그의 유도체하고만 결합이 된다. 이 수용체의 농도는 대단히 적어서 지방질 세포에 한 µm2 당 한 개의 수용체만 있어서 106 인 지방질 분자에 한 개의 수용체가 있 는 셈이다. Insuli n 수용체 는 Trito n X-100 같은 세 탁제 로 용해 시 킨 후 i nsu li n 을 부착시킨 ag a rose 친화성 column 에 통과시켜서 정제되었다. Gel filt ra ti on 과 SDS-p o lya cry la mi de 전 기 영 동 법 에 의 해 그 st oi c h io m et ry
술를 두구 한개 가결 과- s분-s자-량결이 합 으13로5k D연a 결인 되a어 사 슬( a/ 두3 ) 2 의개 와구 조분를자 량형이성 하95는kD a것 인을 ( 3알사 았다. Insu li n 이 세포 표면에 있는 수용체와 결합이 된 후에 어떻게 세포 내의 여러가지 기능에 영향을 주는가는 아직 모르고 여기에도 2 차 messeng er 가 있는지 여부도 알지 못하고 있다. 그런데 i nsu li n 이 세포 내의 몇가지 단백질의 인산화를 조철하는 성질이 있기 때문예 이 hor in one 이 단백 질 k i nase 를 자국시 키 거 나 단백 질 phos p ha t ase 를 저 해 시 키지 않나 생각되었다. 그후 i nsu li n 수용체 자체가 여러가지 조건 하에서 인산화되고 또 이것의 정도가 i nsu li n 에 의해서 조절되는 것이 발견되었 다. Insulin 수용체가 단백질 kin a se 역할을 한다는 것은 r-32P-ATP 표 지로 발견하였다. 그림 8·15 에서 이 nucleo ti de 로 표지된 것이 (3사슬 이 라는 것을 알 수 있다. a- 사슬이 i nsu li n 과 결합한다는 것은 1251-in s uli n 과의 cross-li nk in g 실험으로 확인되었다. 그래서 ins uli n 수용체는 기능 이 따른 두 개의 소단위로 구성되어 있는데 a 소단위는 i nsu li n 과 결합하 고 8 소단위는 kin a se 활성도를 가지고 있다. 그러나 i nsu li n 과의 결합은 세포 외부에서 이루어지고 k i nase 의 활성도는 세포 내부에 존재한다. 이
 A OrBig in -> o b c d o
A OrBig in -> o b c d o
단백질 kin a se 역할이 수용체 자체의 인산화에서 그치는지 또는 세포 내 의 다른 단백질을 인산화시키는지 아직 모르고 있으며 특히 홍미있는 것 은 이것이 cascade mechan i sm 의 시발점이 되어 세포 내의 신진대사를 조철하느냐의 여부이다. 8·1·3 신경 hormone7)8) 1967 년 이전에는 세포간의 통신은 두 가지 방법으로만 이루어진다고 생각되었다. 죽 신경 s y s t em 에서 전달물질이 한 세포에서 방 출 되어 인접 해 있는 세포로 확산이 되면 이의 수용체에 결합되어 i on 의 두과 속도가 변하고, 내분비 (endocr i ne) s y s t em 에서는 hormone 이 분비되어 혈액 순환 울 통해 목적 세포에 도달하여 그의 수용체와 결합하면 세포 내에 2 차 messen g er 가 생성되어 이것이 신진대사 반응을 조정한다는 것이다. 그러 나 신경 s y s t em 에도 hormone 수용체가 존재해서 c-AMP 를 세포내에 생 성하게 하고 이 결과로 원형질막의 물질이동 속도를 변화시키거나 신진 대사를 조칭한다. Cy cl ic AMP 가 두뇌의 기능에 관계한다는 것은 1967 년 이후에 많은 중거가 나타났다. 첫째 syn a p se 후막이 부착되어 있는 두뇌
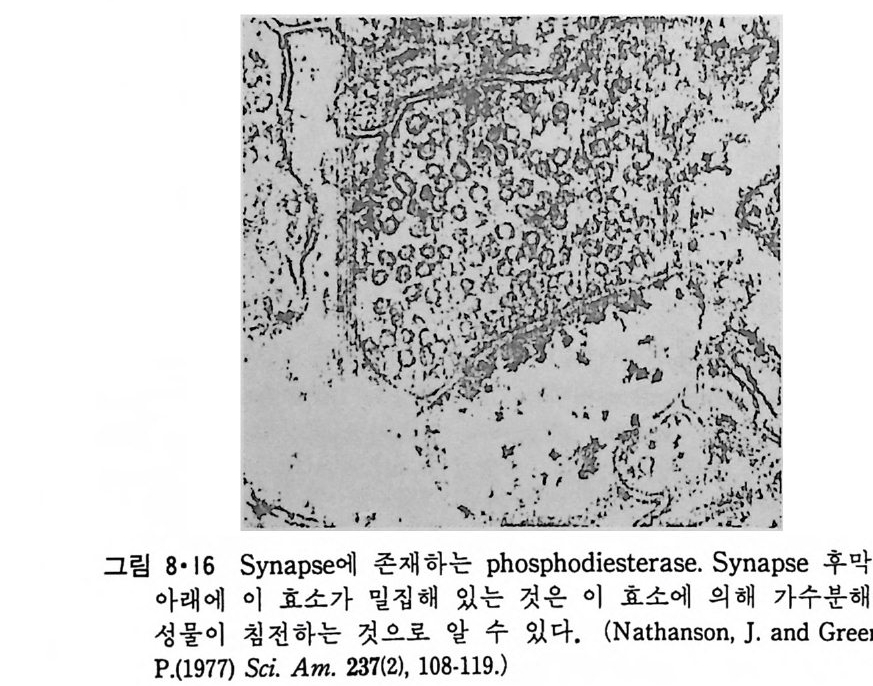 그림 8• 16 S yn a p se 에 존재하는 ph osph odie s te r ase. Sy n aps e 후막 바로
그림 8• 16 S yn a p se 에 존재하는 ph osph odie s te r ase. Sy n aps e 후막 바로
s yn a pt osome 에 adeny la te c y clase 가 많이 존재하고 둘째로는 c-AMP 를 가수분해시키는 p hos p hod i es t erase 가 많이 sy n ap se 후막에 있는 것을 전 자현미경으로 알게 되었고(그림 8·16), 신경 조직을 전기적으로 자국하 거나 또는 do p am i ne 같은 신경전달 물질을 가하면 c-AMP 의 농도가 높 아지는 것을 발견하였다. 이들은 간접적이기는 하지만 신경전달물질이 c
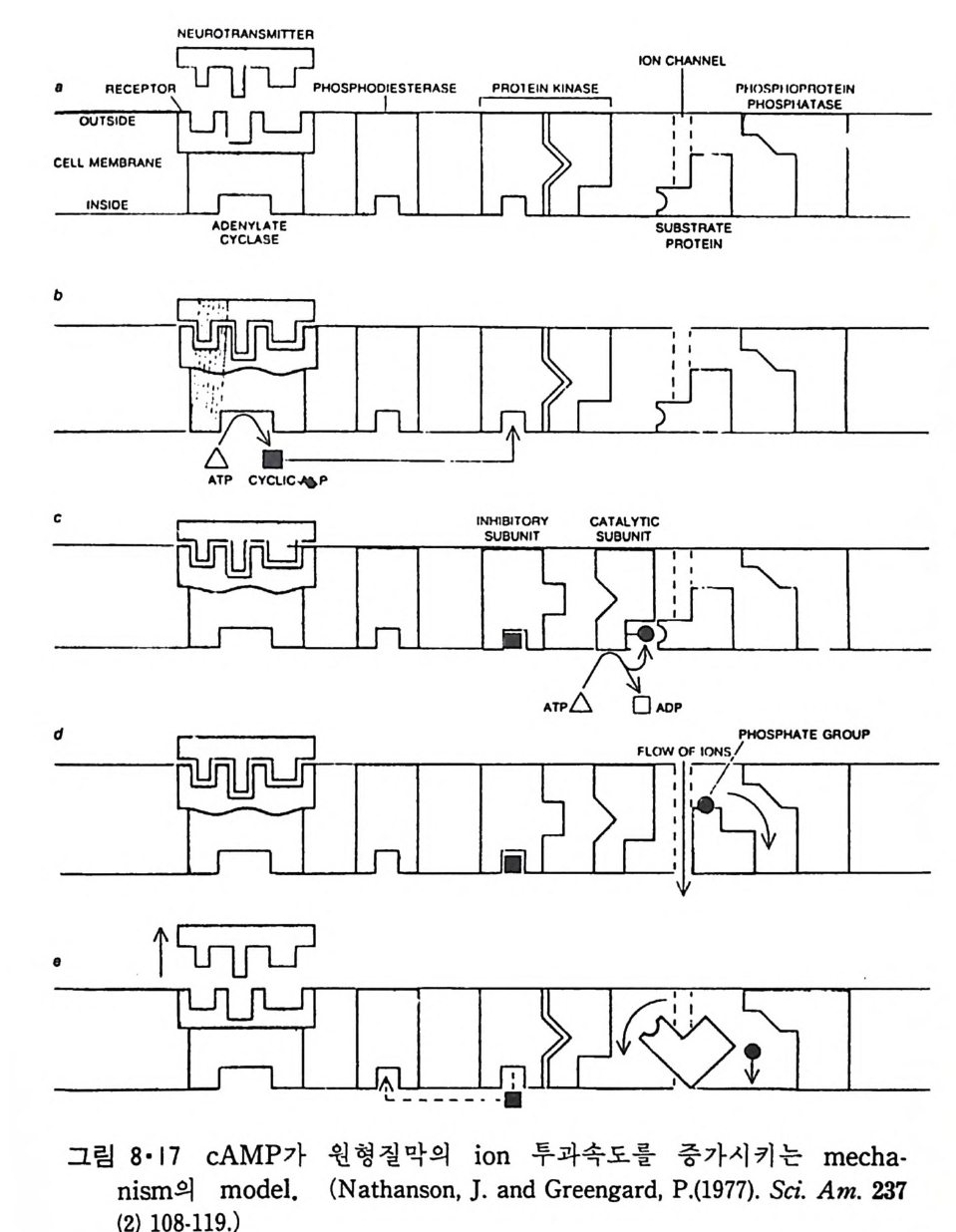 NEUROTRANS .. ITTER
NEUROTRANS .. ITTER
-AMP 생 성 을 야 기 시 킨 다 는 것 을 시 사 한 다. Dop a mi ne 이 외 에 norep ine p h rin e , sereto n in , h i s t am i ne 과 oc t o p am i ne 도 c-AMP 를 생 성 하 는 신경전달물질이다. S y na p se 에서도 hormone 수용체와 유사한 신경전 달 물질의 수용체 가 존재 하여 이 것 이 adeny la te c y clase 를 자국시 키 는 것 으로 생각되고 있다. 그러면 이렇게 생성된 c-AMP 가 어떻게 원형질막의 양i on 이동속도를 증가시키는 것이 문제인데 이는 s yn a p se 에 존재하는 단백질 k i nase 와 이
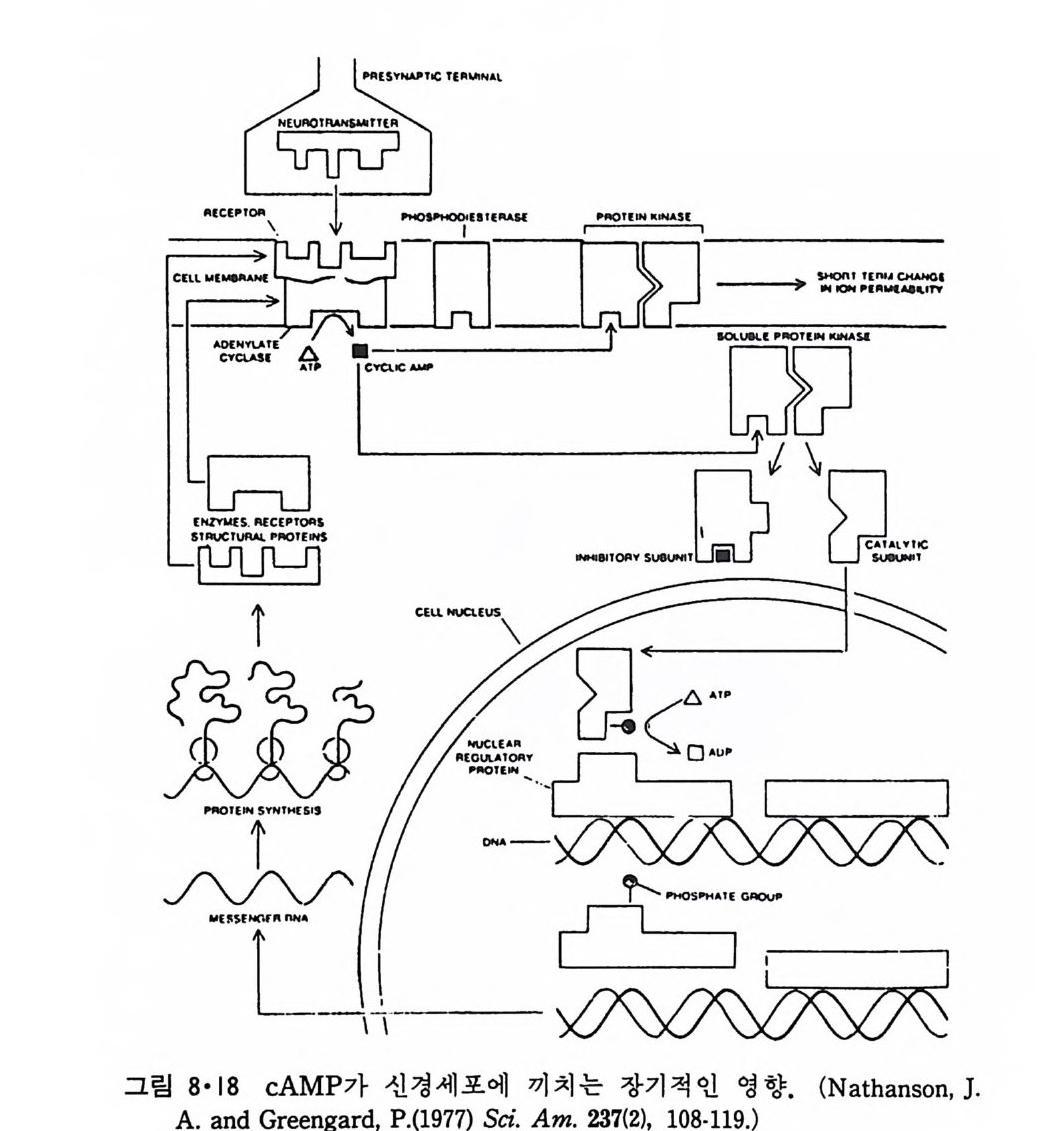 -, (r r ...'.· ~C'T'‘I'
-, (r r ...'.· ~C'T'‘I'
효소에 의해서 인산화되는 단백질에 의한 것이라고 생각된다. 그링 8·17 은 c-AMP 가 원형질막의 ion 이동속도를 증가시키는 mechan i sm 의 model 을 보여준다. 여기서 신경전달 물질이 syn a p s e 후막에 있는 수용 체와 결합하면 이 수용체와 adeny la te c y clase 가 서로 작용하여 효소가 활성 화되 어 c-AMP 를 형 성 한다. 다음 이 c-AMP 가 단백 질 k i nase 의 저 해 소단위와 결합하면 이 효소의 촉매 소단위가 활성화되어 이 활성화된 단백질 k i nase 에 의해서 막 구성의 문을 형성하는 단백질을 활성화시켜 막이 열림으로써 ion 이동속도가 중가된다. 다음에 저해 소단위와 결합 된 c-AMP 가 p hos p hod i es t erase 에 의해서 파괴되고 인단백질 pho s- p ha t ase 에 의해서 문을 형성하는 단백질이 탈인산화되면 원상 복귀된다. 아직도 이들 내재단백질의 성질은 잘 모르고 있다. 신경계에서의 c-AMP 의 역할은 원형질막을 통한 i on 의 이동속도를 변 화시키는 단기적인 효과 이외에 이 물질이 핵내부로 들어가 핵조절 단백 질 (nuclear regu la to r y p ro t e i n) 을 인산화하여 세포내의 단백질 합성의 양상 을 변화시켜 장기적인 효과를 주기도 한다. 이것이 기억의 근본이 된다 고 제안이 되어 있다. 그림 8·18 은 c-AMP 의 이러한 단기적인 효력과 장기적인 효력을 보여준다. 8·2 물질 주성 (Chemota x is )9 >-11> 물질 주성은 세포가 영양분 등 자기가 필요로 하는 용질의 농도가 증 가하는 방향으로 이동하고 해로운 용질을 피해서 움직이는 현상을 말하 는 것인데 이러한 성질은 원핵세포와 단세포동물뿐만 아니라 백혈구 (leu kocy te) 같은 진핵세포도 생체 내에서 보여준다. 뭉질 주성이 가장 많이 연구된 것은 E. co li인데 이 세균이 움직이는 것은 그림 8·19 에서 보이는 것과 같이 편모(fl a g ella) 가 내막에 부착되어 있는 회전자 (ro t or) 에 의해서 회전되기 때문이다. 편모가 시계 반대 방향 으로 돌면 그림 8·20A 에서 보여 주는 것과 같이 한 방향으로 움칙 이고 편모가 시계 바늘 방향으로 돌면 세균 전체가 딩굴며(t umble) 움직이기 때문에 일정한 방향으로 이동하지 않고 방황하게 된다. 외부에서 자극이 없을 때에는 그림 8·21A 에서와 같이 이 두 가지 회전이 교대로 일어나
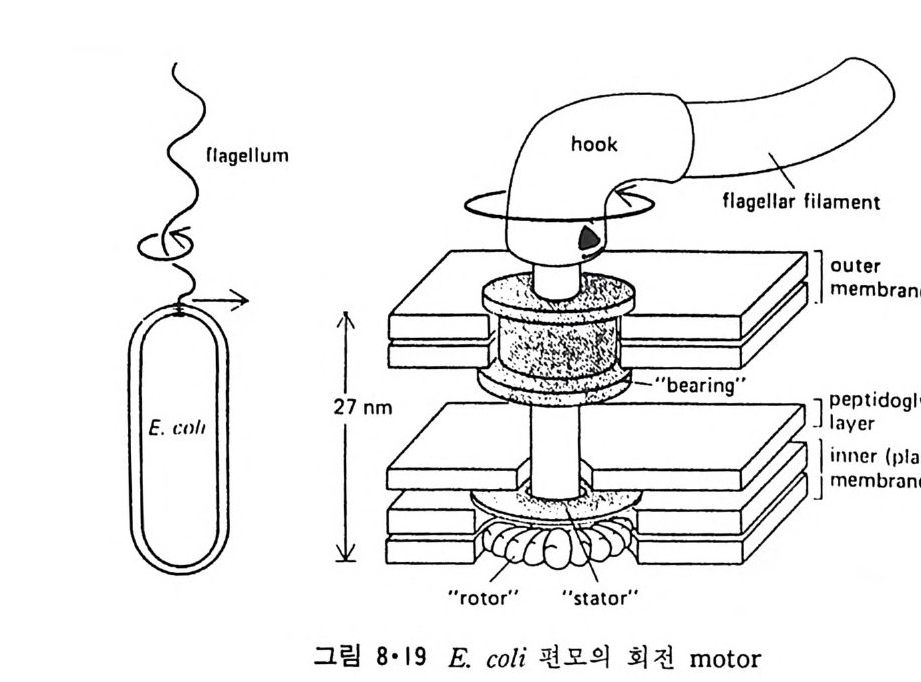 llag el lum
llag el lum
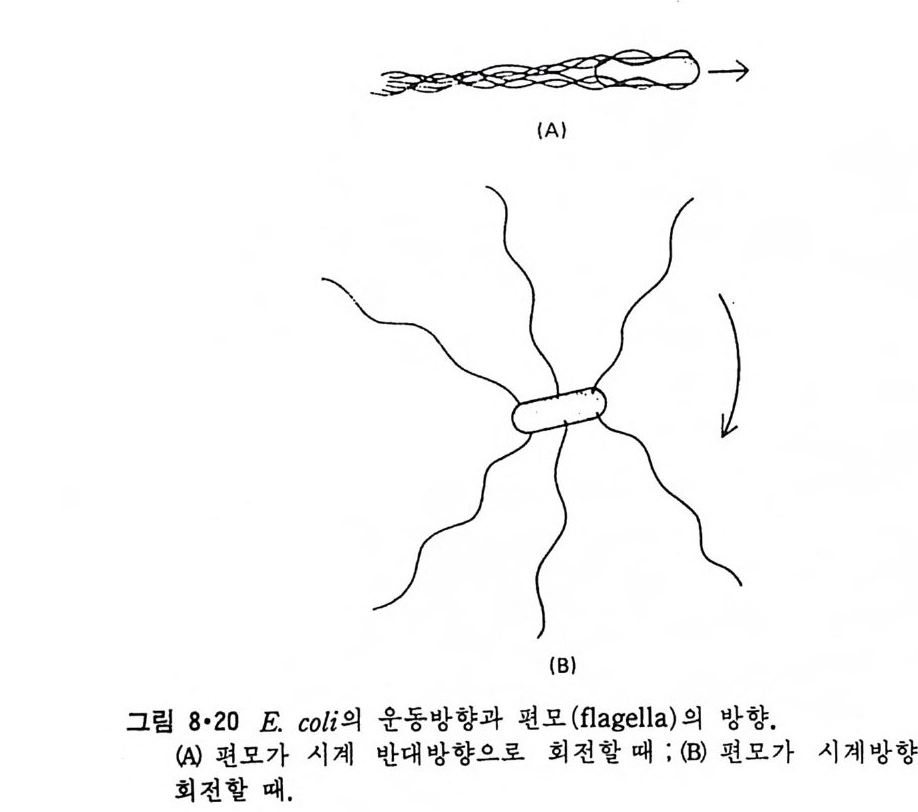 -호一
-호一
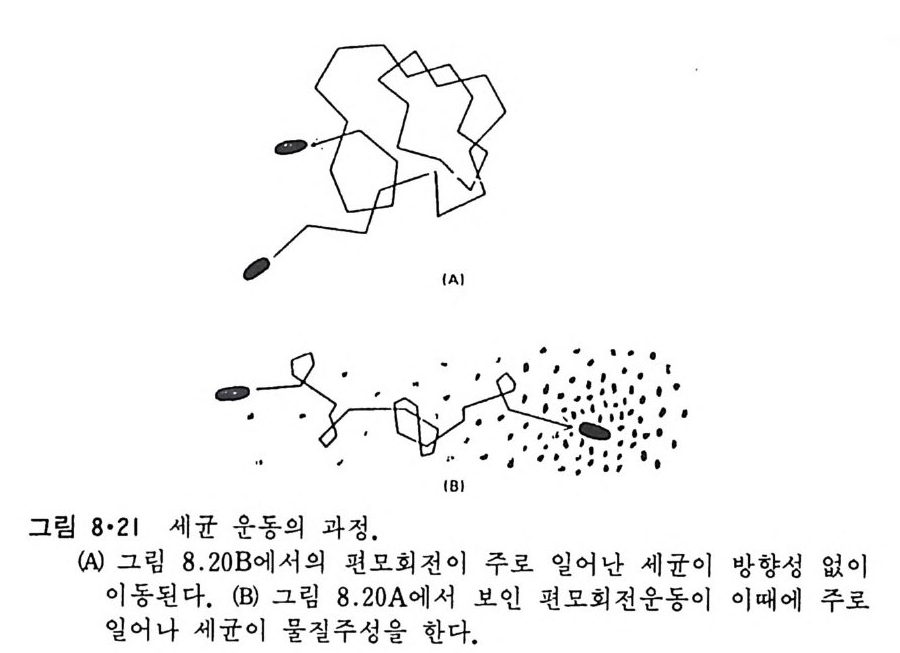 ,
,
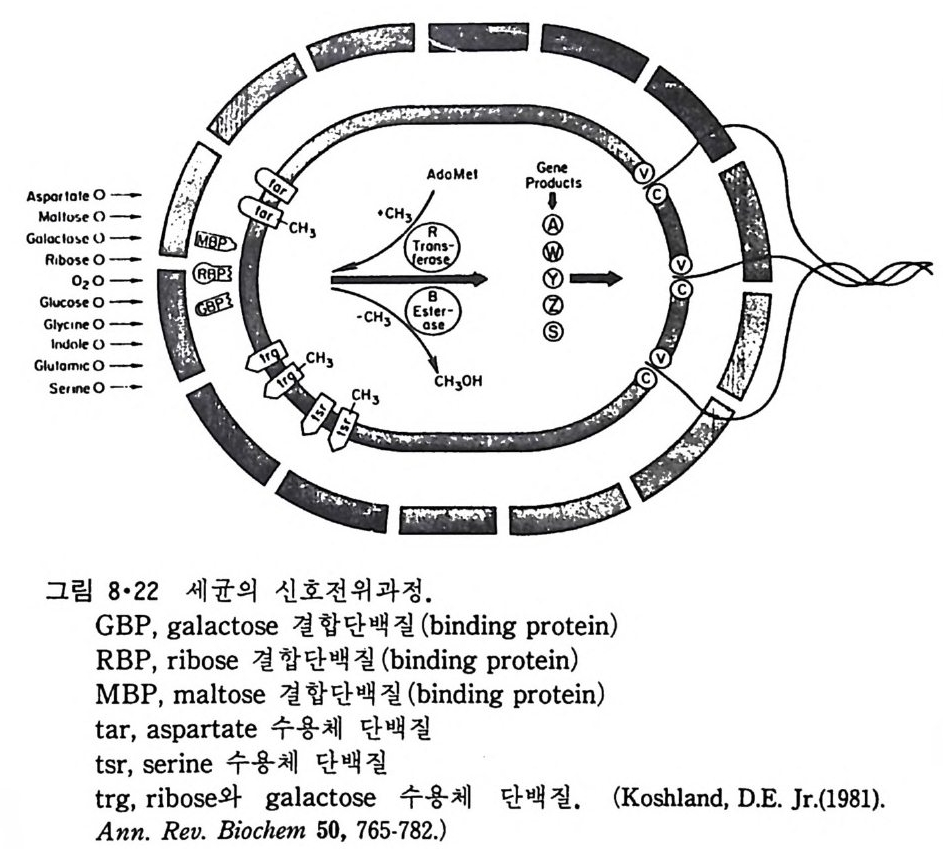 Asp o,la le O -
Asp o,la le O -
일정한 방향이 없이 방황을 하고 한쪽 방향에서 자국이 있으면 편모가 시계의 반대 방향으로 주로 회전하여 자극이 있는 방향으로 움직이게 된 다. E. coli 운동의 특이한 점은 이 세균이 영양분의 농도 증가를 감지하 여 농도가 증가하는 방향으로 이동되고 농도가 균일할 경우에는 곧 적응 (ada pt a ti on) 이 일어나 자국이 없을 때와 마찬가지의 방황 운동을 하는 것 이다. 물질 주성에서 신호가 전이되는 과정은 그링 8·22 에 보여준다. 여러 가지 돌연변이체 (mu t an t)를 이용한 유전학적 인 연구 결과로는 당분과 am i no 산등 영양분이 주변 세포질 공간(p er ip lasm ic s p ace) 에 있는 결합단 백질과 결합되면 이 복합체가 원형질막에 존재하는 내재단백질과 결합하 여 신호 전이가 세포 내부로 전달되어 편모의 회전 방향을 조정하게 된 다. 여기서 E. co li에서의 물질 주성의 수용체에는 두가지 종류가 있는 것을 알 수 있다. 그중 하나는 분자량이 약 30kDa 가 되는 결합 단백질 로서 이들 단백질이 am i no 산과 당분을 능동 수송하는 것은 이미 제 6 장 에서 설명하였다. 두번째 것은 내재단백질로서 분자량이 약 60kDa 정도 가 된다. 그림 8·23 에서와 같이 rib o se, ga lacto se, mal t ose 의 경우에는
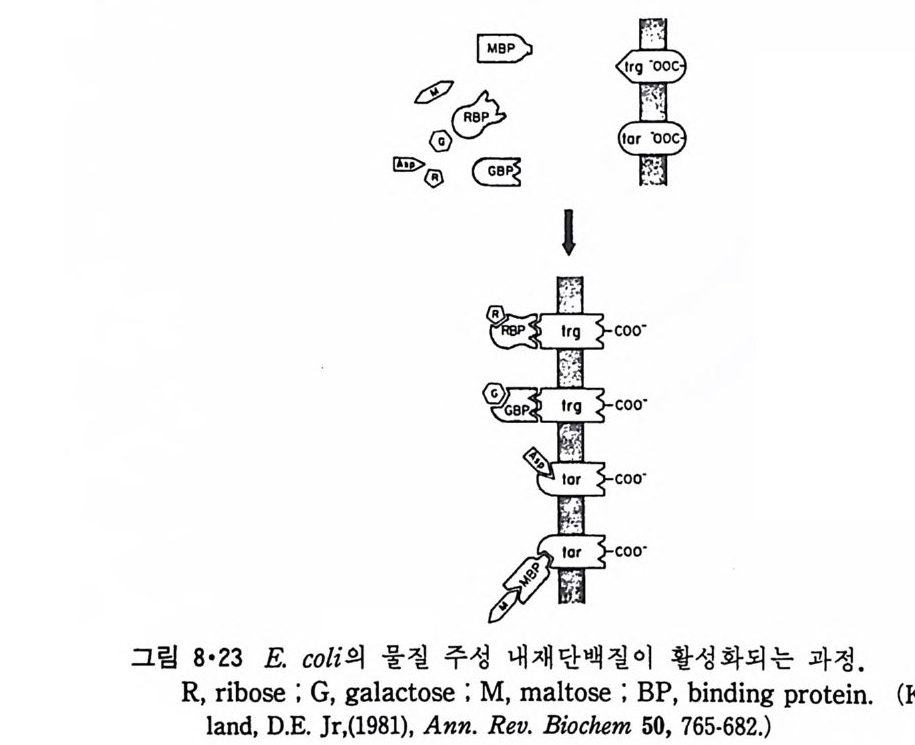 E
E
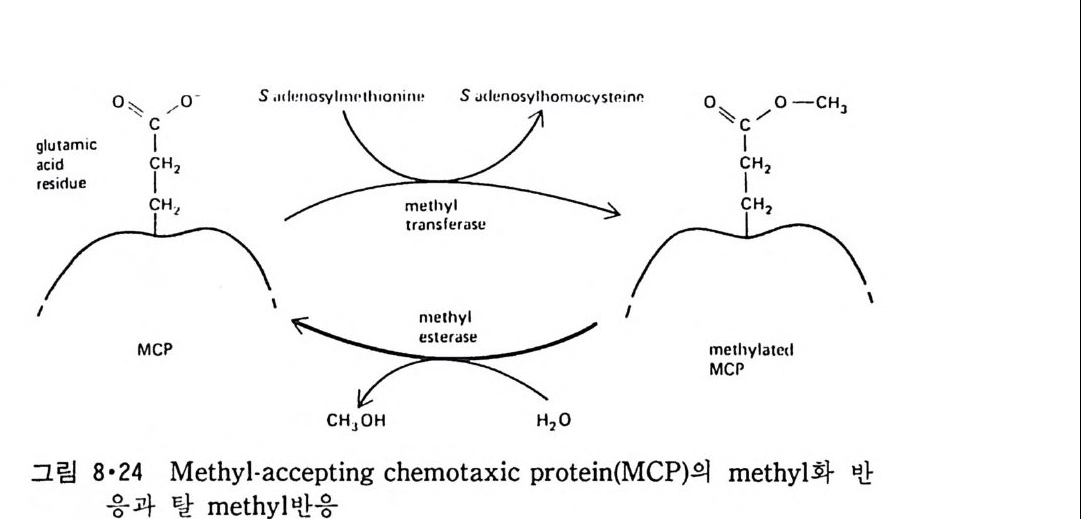 麟res,~a ume 1 C °` \: /: o - s .II1 t I IO sv 1mI ·Ih IO1 ', s J( lcn osv lho mocvsIm nn 。 \ c/lc 。 I c H3
麟res,~a ume 1 C °` \: /: o - s .II1 t I IO sv 1mI ·Ih IO1 ', s J( lcn osv lho mocvsIm nn 。 \ c/lc 。 I c H3
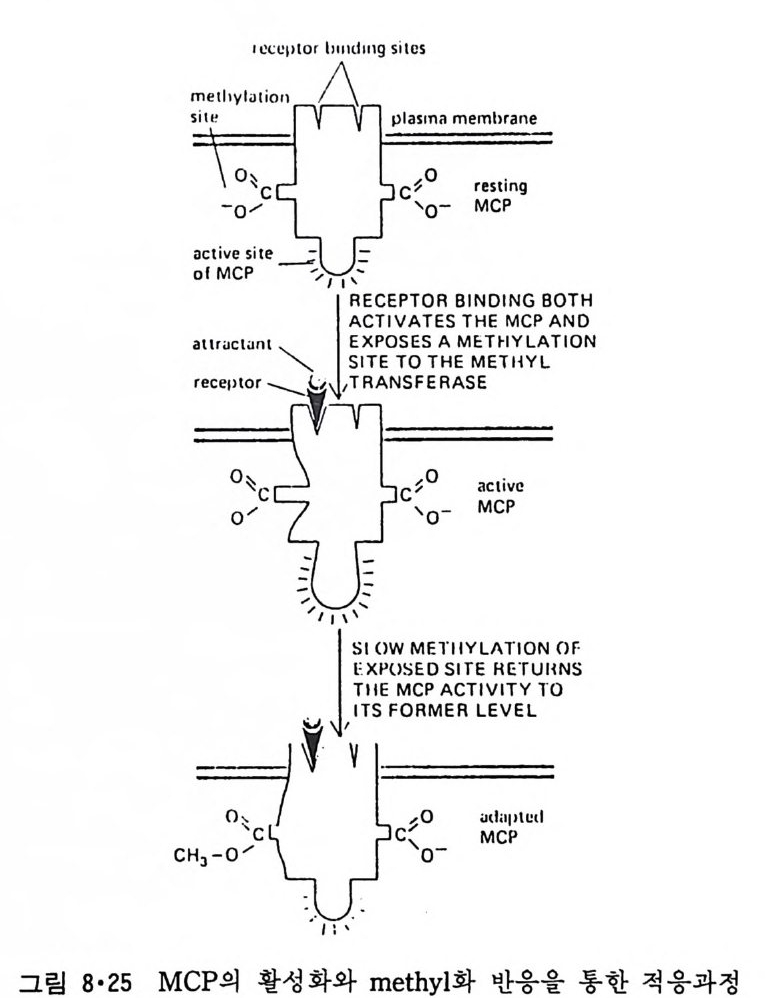 m eth y la t ,o n
m eth y la t ,o n
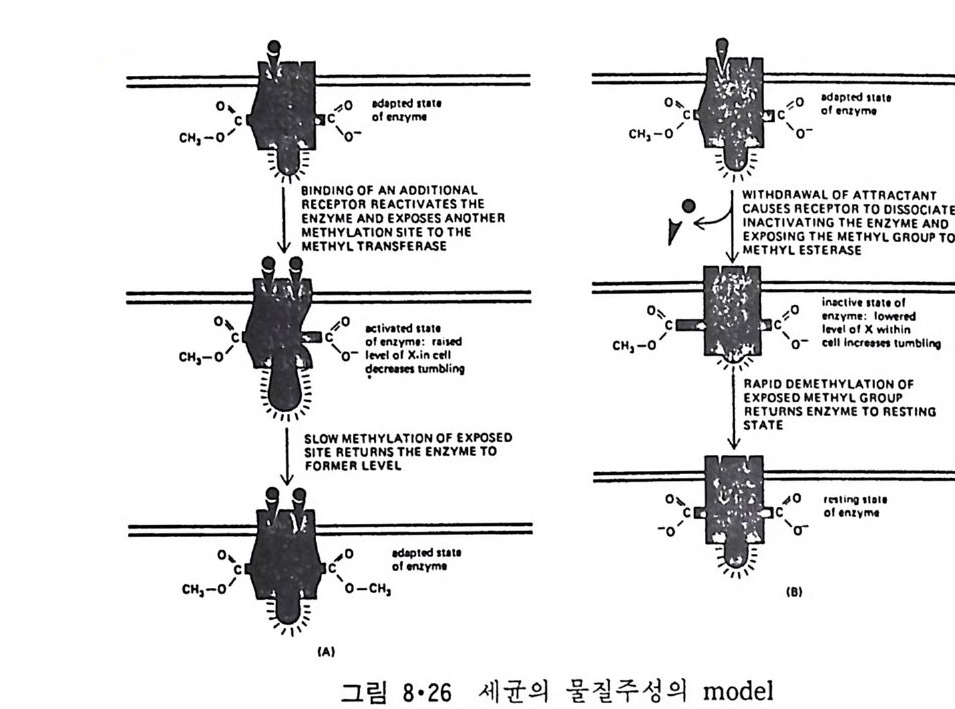 c4 'o°- o” .hpmtvm'· c\ 짜o _ .h''러m'·
c4 'o°- o” .hpmtvm'· c\ 짜o _ .h''러m'·
결합단백질이 1 차 수용체가 되며 as p ar t a t e 와 ser i ne 은 내재단백질 수용 체와 직접 결합한다. 이들 내재단백질의 구조와 이 단백질이 신호전이룰 하는 machan i sm 은 아직 모른다. 신호전이에 이어서 곧 이 내재단백질의 세포액쪽에 glu ta m i c a ci d 기가 노출되어 me t h y la ti on 이 일어나며 (그림 8·24) 이는 적응을 시키 기 때문 에 신호전이의 효과를 없앤다(그림 8·25). 세균이 이동하는 방향으로 영 양분의 농도가 증가하면 적응이 되었어도 더 신호전이가 일어나기 때문 에 계속 같은 방향으로 웅칙이게 된다(그림 8·26). 8 •3 면 역 (Immune) 수용체 12) 고등동물에는 외부에서 침입해 오는 세균이나 독소(t ox i n) 에 대해 방어 를 할 수 있는 면역 s y s t em 을 가지고 있다. 이 것은 백혈구인 lym ph ocy te 표면에 있는 내재단백질에 의해서 항원 (an tig en) 이 감지되고 이 신호가 원형질막을 동해서 세포 내부로 전이가 되어 방어작업이 시작
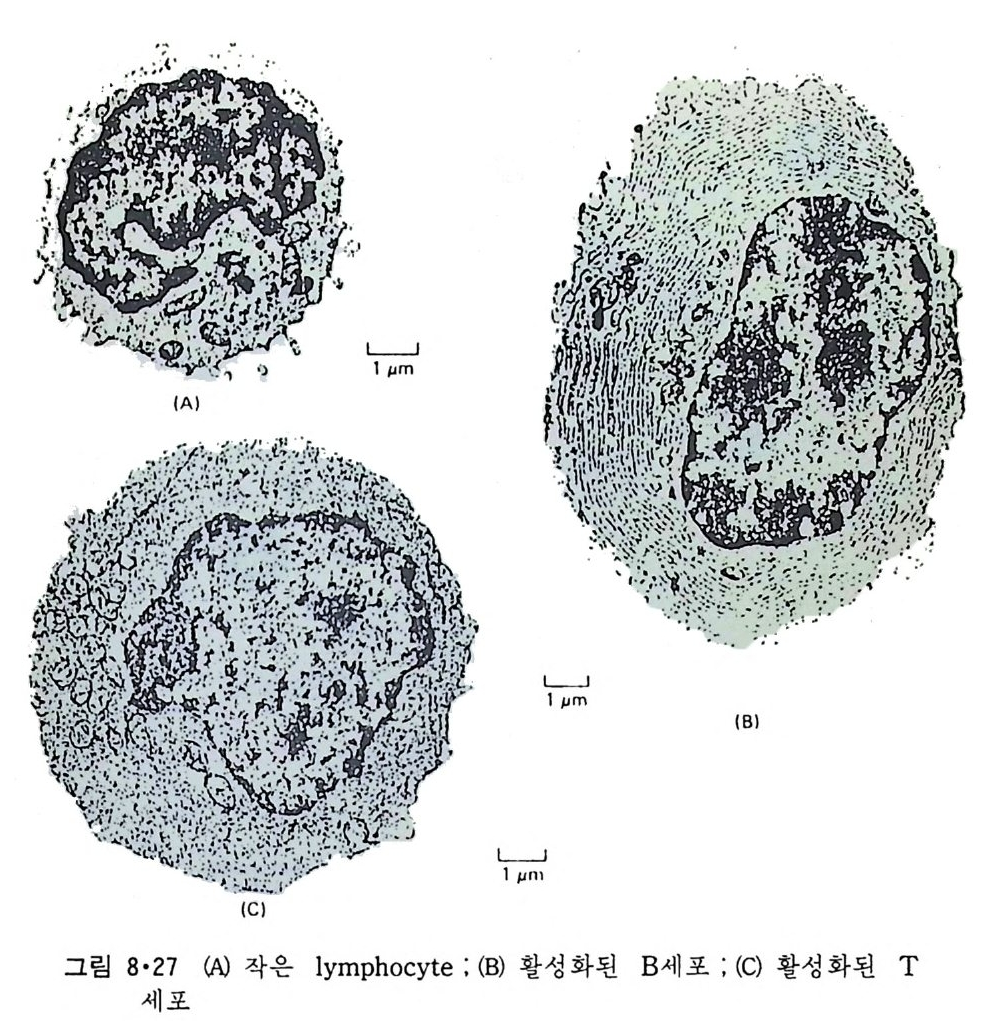 ‘
‘
되어 이루어진다. L y m p hoc yt e 에는 두 가지가 있는데 이것을 B 세포와 T 세포라 부른다. 보통때에는 이 두 가지 세포를 구분할 수 없으나 어느 특정한 항원의 존 재 하에서는 그림 8·27 과 같이 활성화된 세포로 변형된다. 활성화된 B 세 포는 조연소포체가 밀집해 있어 분비될 단백절합성이 왕성한 것을 알 수 있다. 즉 항원의 자국으로 B 세포는 항체 (an ti bod y)를 합성 분비하는 역할 울 한다. 그림 8·28 는 이 과정을 보여 주는데 B 세포 표면에 있는 수용체 단백질과 항원이 결합하고 동시에 활성화된 T 세포와 접촉하면 그의 번석 이 촉진되어 활성화된 B 세포가 많이 생겨 항체가 대량 생산되어 분비되 게 된다.
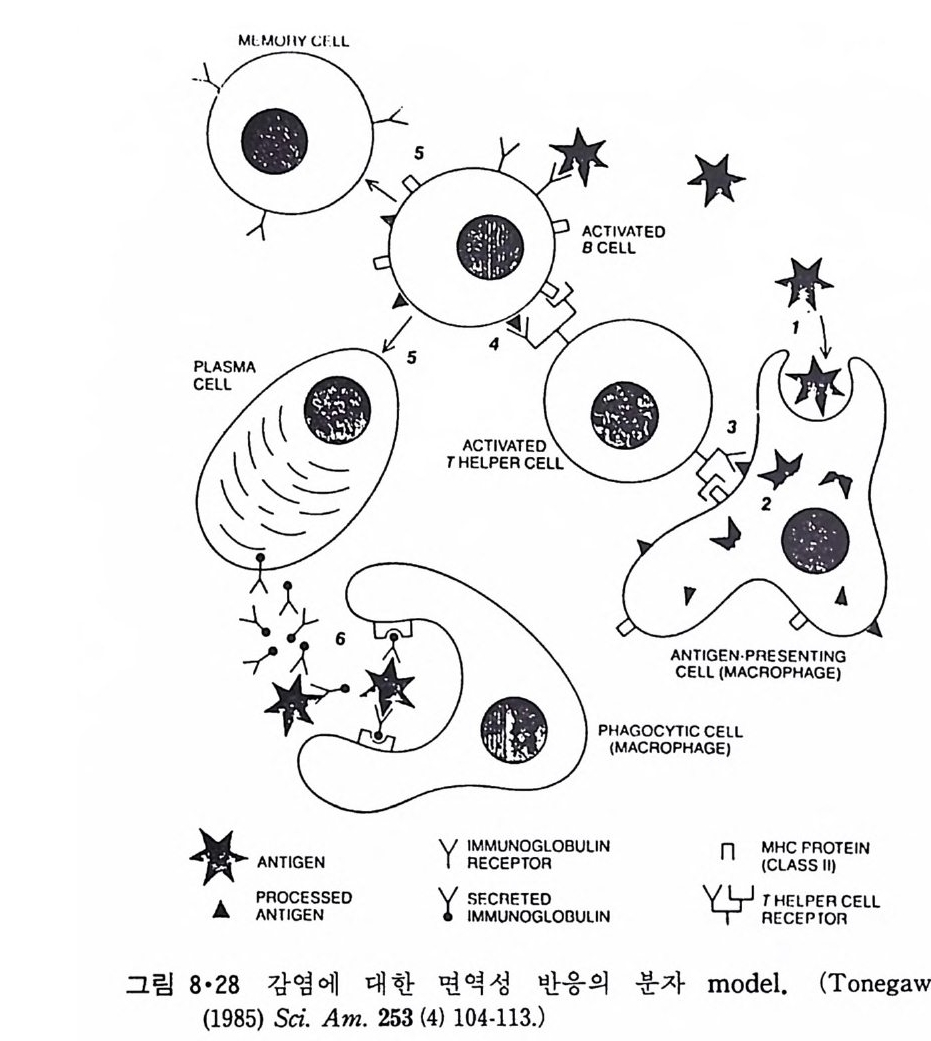 MUAUIIYCF .L L
MUAUIIYCF .L L
과 항두체개는씩 의그 림가 벼8·운29 에사 슬보 (이L 는사슬 것)간과에 같-이s -s두-개결씩 합의으 로무 거구운성 되사어슬 (있H 고사슬 )이 들의 N- 말단 쪽에 항원이 결합된다. 분비되는 항체와 수용체 항체 (recep tor an ti body)의 구조는 근본적으로 같으나 H 사슬의 C- 말단 근처 에 am in o 산 서열이 다르다. 죽 수용체항체 H 사슬의 C- 말단 근처에는 생체막에 들어갈 수 있는 길이의 소수성 am i no 산 서열이 존재한다. 이 두 종류의 항체는 같은 유전자로부터 시작되지만 B 세포에서 그럼 8·30 에 보이는 것 같은 과정으로 둘 중 하나를 택해 합성할 수 있다. 분비된 항체는 항원과 결합 후 그림 8·28 에 보이는 것과 같이 대식세
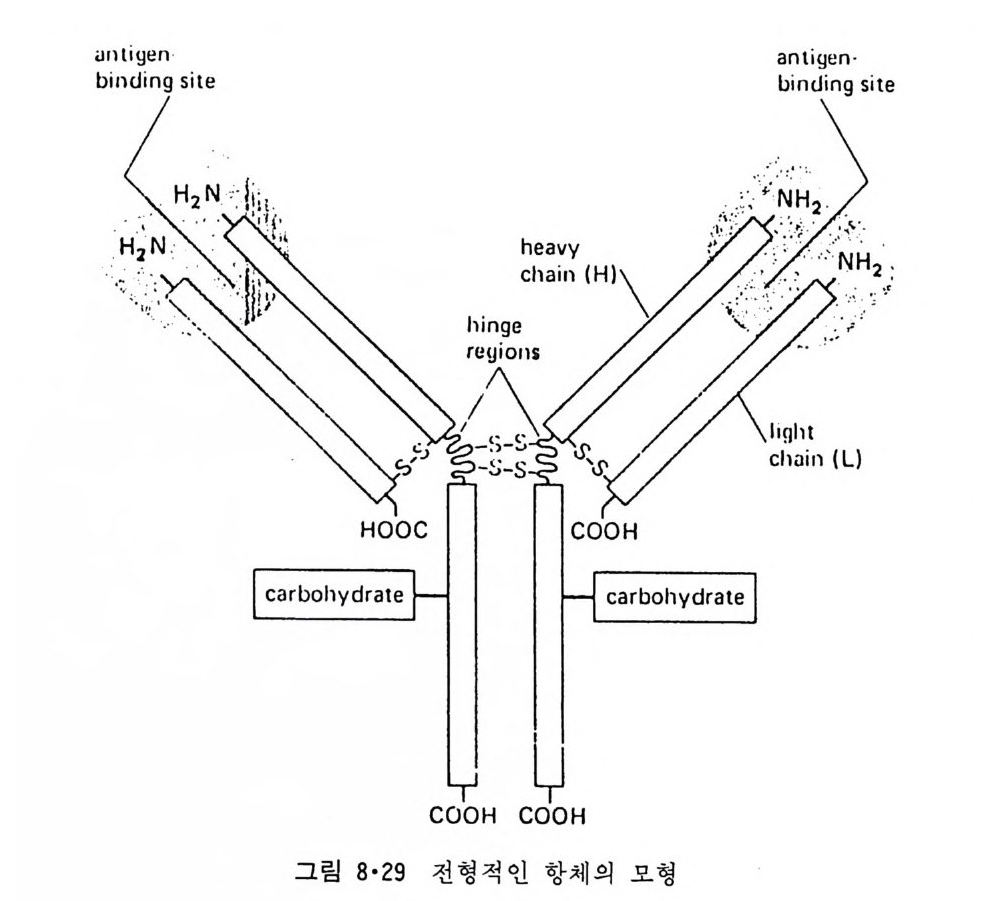 unuy en anliy e n·
unuy en anliy e n·
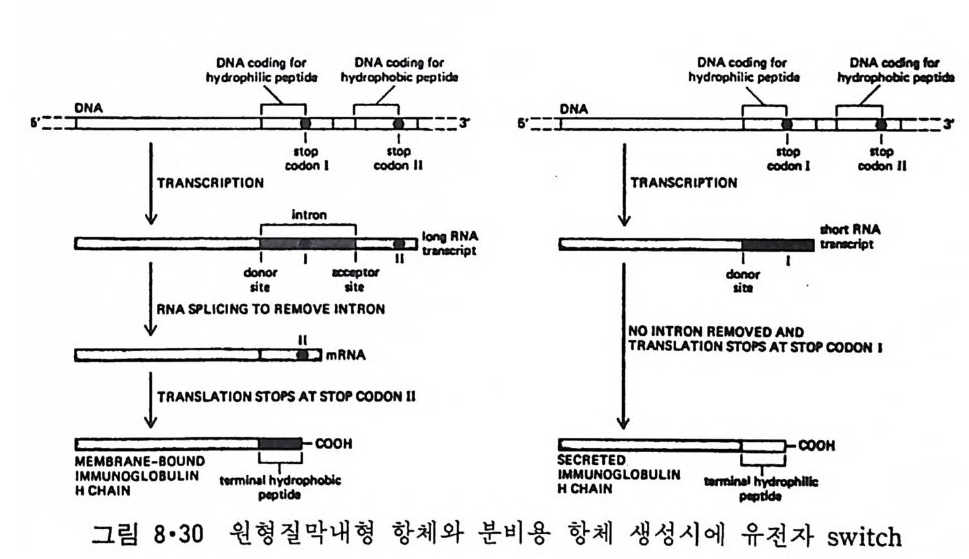 •·:: DNA lTR ..N SChRyD .IN,.To AIpO chNIo>I dl ei 때m느 ' dd o , hr广DlN 다A느 c,o心 o, 에 o'I: 걸: : r S.::]D NA lmNSCmhyD IdN Om^N~i尸 I& k 때 .'•.스.& , * ll겁 h1 니스(다~ ,11t브 a-,r
•·:: DNA lTR ..N SChRyD .IN,.To AIpO chNIo>I dl ei 때m느 ' dd o , hr广DlN 다A느 c,o心 o, 에 o'I: 걸: : r S.::]D NA lmNSCmhyD IdN Om^N~i尸 I& k 때 .'•.스.& , * ll겁 h1 니스(다~ ,11t브 a-,r
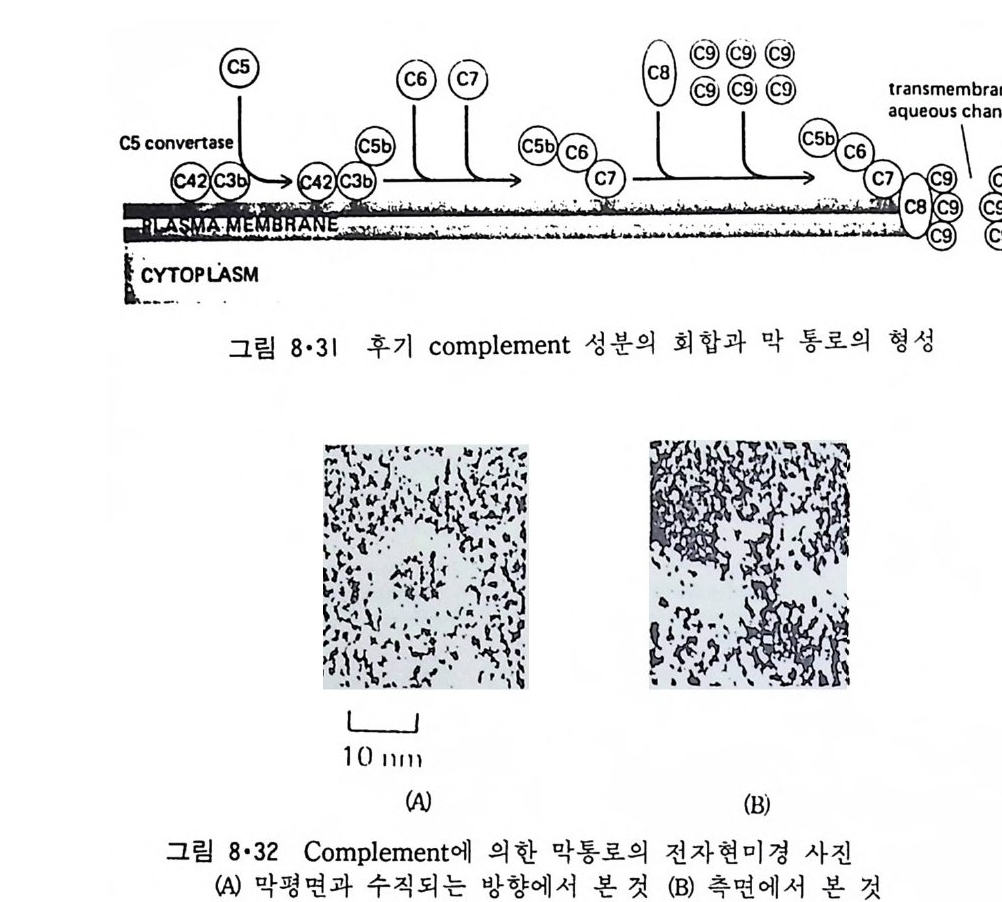 @ @ @ 三81 麟 I tra nsmemc \bh戶 rane
@ @ @ 三81 麟 I tra nsmemc \bh戶 rane
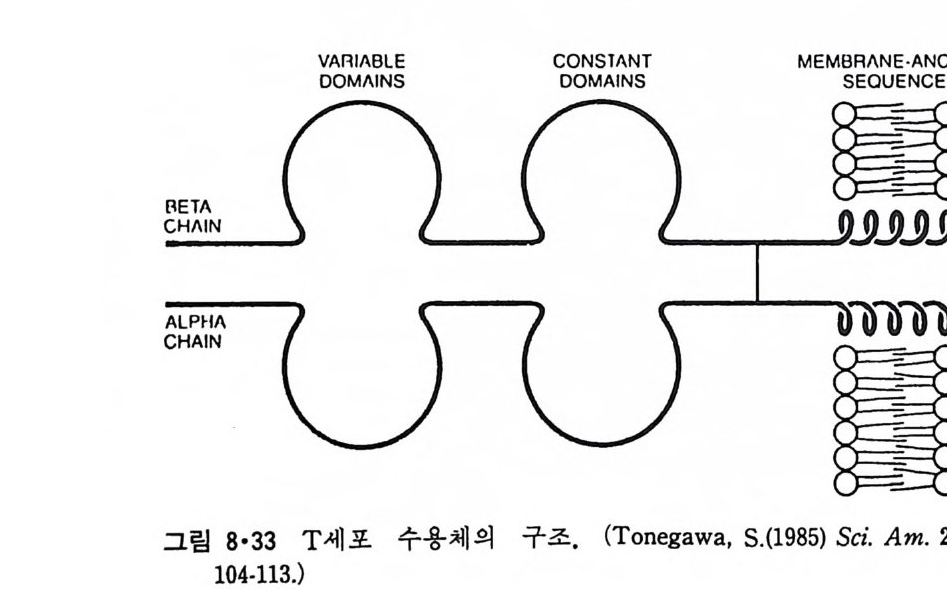 VDAORMI/ /II BINL ES CDOONMSATIANNST MEMBSRE/Q \NU EE-N AC NEC HOR
VDAORMI/ /II BINL ES CDOONMSATIANNST MEMBSRE/Q \NU EE-N AC NEC HOR
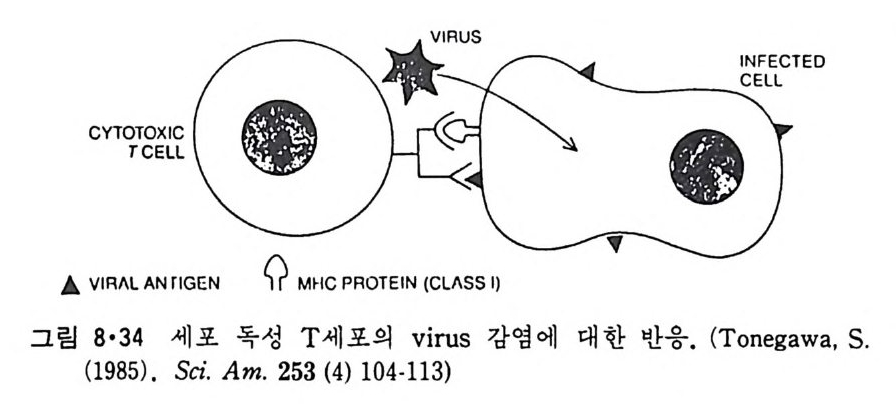 CYT 연g ;Lf /-`二
CYT 연g ;Lf /-`二
포 (macro p ha g e) 에 p hag oc yt o ci s 시켜 파괴하거나 그림 8·31 에 보이는 것 과 같이 comp le ment s y s t em 을 활성 화시 켜 침 입 한 세 균막에 큰 구멍 을 형성하여 파괴하기도 한다. 그림 8·32 는 com p lemen t에 의해 생긴 막구 멍을 보인다. T 세포의 수용체 단백질은 내재단백질로서 (그림 8·33) a 와 /3 두 사슬
 class I/ MH C po lyp e p tide
class I/ MH C po lyp e p tide
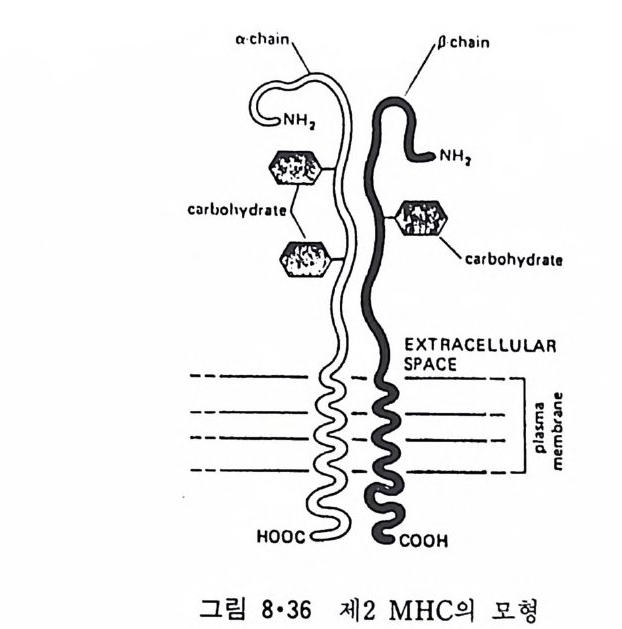 c chaIn
c chaIn
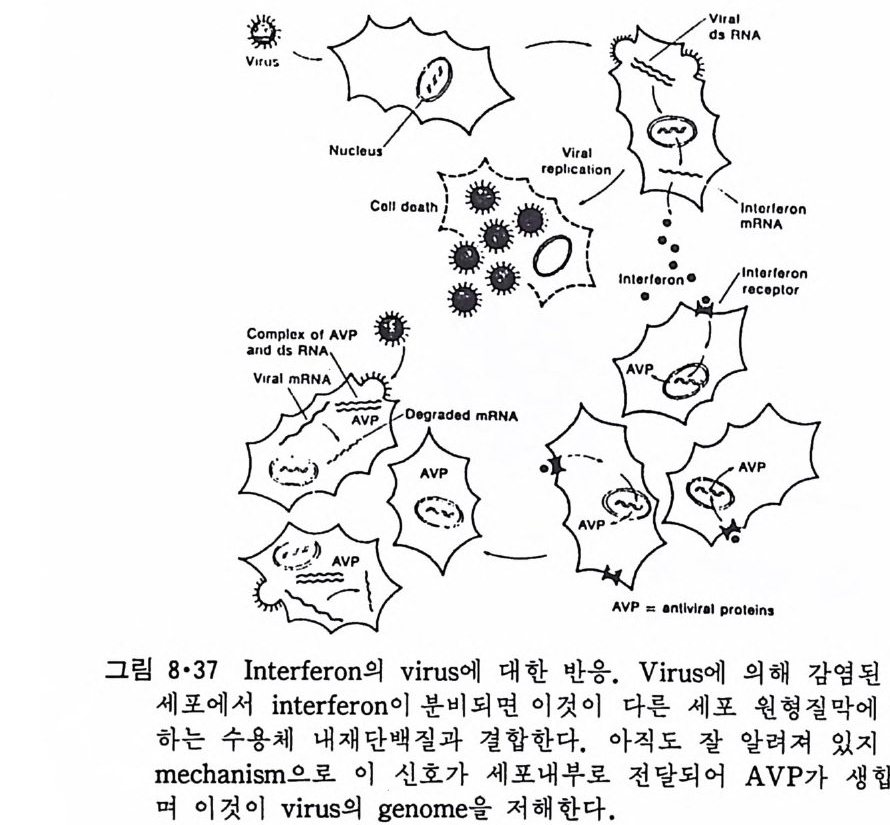 그림 8•37 In t e rf eron 의 v i rus 에 대한 반응. V i rus 에 의해 감영된 숙주
그림 8•37 In t e rf eron 의 v i rus 에 대한 반응. V i rus 에 의해 감영된 숙주
로 구성되어 있고 항체와 유사한 점이 많다. 그래서 이 수용체 단백질이 항원과 결합하는 것으 로 생각된다. 그러나 T 세포 수용체의 경우는 항체 와는 달리 항원을 가진 세포의 원형 질막에 MHC 라는 g l y co p ro t e i n 이 존 재할 때만이 세포와 결합되어 파괴시킬 수 있다(그림 8·34) . MHC 는 두 가지의 내재단백질이다(그링 8·35, 8·36). 최근에 관심을 많이 끌고 있는 i n t er f eron 은 v i rus 에 의해 감영된 백혈 구, fi broblas t나 면역세포에서 분비되는 분자량이 약 20kDa 인 단백질로 서 이들은 근처의 다른 세포의 수용체와 결합하여 그 세포로 하여금 반 vir u s 단백 질 (anti vi r v s pro te i n , AVP) 을 생 성 하여 v i rus 에 의 한 감영 이 퍼지는 것을 저해한다 ( 그림 8·37). 이들 i n t er fe ron 에 대한 수용체의 연 구는 최근 활발히 진행되고 있으며 사람세포인 경우 1251 로 표지된 int e r f er on 과 수 용 체 와 의 화 학 적 인 cross-li nk in g 실 험 과 SDS- pol ya cryI a mi de 전기영동 실험에 의해 분자량이 140~150kDa 이 되는 내 재단백질이라는 것이 판명되었다. * 8 장 참고문헌 (1) W ilso n, J. D. and Foste r , D. W . Wi lli a m 's Textb o ok of Endoc rino logy , 7th , ed. Saunders, 1985. (2) Zubay, G. Bi oc hemi stry, Addis o n-Wesley 1983, Chap t. 29. (3) Ross, E. M. and Gi lma nn, A. G. (1980) Ann. Rev. Bio c hem. 49, 533-564. (4) Gi lm ann, A. G. (1984) Cell 36, 577-579. (5) Kahn, C. R. (1981) Recent Prog. in Hormone Res. 3 7, 477-583. (6) Lien hard, G. E. (1983) Trends Bio c hem, Sc i. 8 , 125-127. (7) Nath a nson, J. A. (1977) Phys i o l . R ev. 57, 158-256. (8) Nath a nson, J. A. and Greeng a rd, P. (1977) Sci . Am. 237(2), 108-119. (9) Berg, H. (1975) Sci . Am. 233(2), 36-44. (JO ) Adler, J. (1976) Sci. Am. 234(4), 40-47. OU Koshland, D. E. Jr. ( 1981) Ann. Rev. Bi oc hem. 50, 765-782. (12 ) Toneg a wa, S. (1985) Sc i. Am. 253(4), 104-113.
제 9 장 생체막에서의 Ener gy전이 생명현상이란 조직이 형성되고 이것이 유지되어야 하기 때문에 계속해 서 외부로부터 ener gy가 공급되어야 한다. 지구에서의 궁극적인 energy 근원은 태 양광선으로 녹색 식 물과 남조 (blue-gr ee n alga e) 에 서 는 태 양 광선 의 ener gy가 생체내에서의 ener gy이 근원인 ATP 합성에 직접 이용되고 동물에서는 식물체에서 시작된 유기물질의 산화과정을 통하여 ATP 가 합 성된다. 이렇게 한 가지의 ener gy형태가 다른 형태로 변화되는 과정을 ener gy전이(tr ansduc ti on) 라고 부르며 이러한 현상은 생체막에서 많이 일 어나고 있다. ATP 는 2 차적인 ener gy의 근원이 되며 이들은 생체 내에 서 여러가지 전기적, 화학적 그리고 기계적인 일을 한다. 녹색식물에서 는 엽 록체 내 에 있는 t hy lako i d 막에 서 ATP 가 합성 되 고 남조류에 서 는 색 소를 가지고 있는 내부막에서 이 합성이 일어난다. 한편, 동물세포에서 는 m it ochondr i a 의 내부막에서 ATP 가 생산되고 남조류 이외의 원핵세 포에서는 원형질막에서 ATP 가 많이 합성된다. 남조류와 엽록체는 여러 모로 비슷하고 또 원핵세포와 m it ochond ri a 도 유사한 점이 많다. 따라서 엽록체는 진화과정에서 남조류가 진핵세포에 침입한 후 공생 (s y mb i os i s) 현상으로 존재하는 것으로 생각되었고 m it ochondr i a 도 세균에서 시작된 것이라고 생각되고 있다. 이들 생체막에서의 ener gy전이는 크게 두 단계 로 구분이 된다. 첫째는 높은 음성 산화환원 전압 (ne g a ti ve redox po te n ti al) s y s t em 의 전자가 여 러 전자 운반 (electr o n tra nspo rt ) 의 성 분을
동해서 산화환원 전압이 감소되는 방향으로 이동되며 이때 / 방출된 ener gy가 양성 자 (pro to n ) p um pi n g에 쓰 이 며 둘째 로는 이 렇 게 생 성 된 굿 샹성 자 농도 차이 가 ATP s y n t he t ase 에 의 해 이 용되 여 ATP 를 합성 하는데 이 것 이 M it chell 의 화학삼두 (chemi os moti c) 가설 로서 오늘 날 많은 지 지 를 받고 있다. 9 • 1 Mi toc hondria 1 >-5> 녹색 식물체는 光 ener gy를 ATP 합성에 직접 이용하지만 동물체와 원 핵세포에서는 이들 식물체에서 형성된 탄수화물, am i no 산 그리고 지방
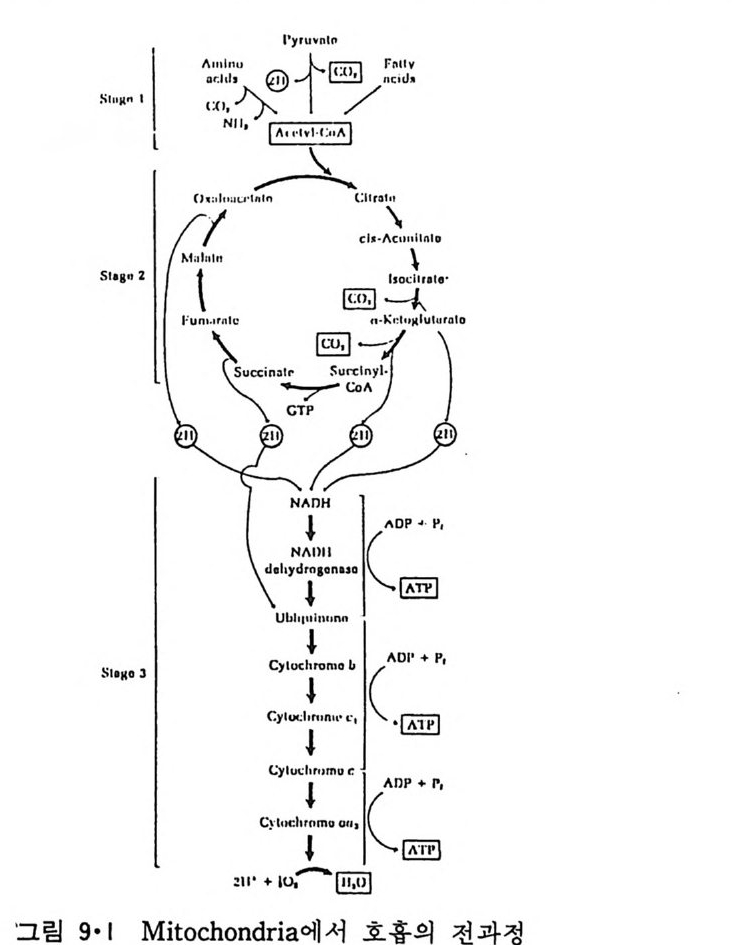 s’’’” ” I l ^:::':N저'; 'I J, / 尸El'y_, u_\,o -l〕o - - nr\ :: ;:
s’’’” ” I l ^:::':N저'; 'I J, / 尸El'y_, u_\,o -l〕o - - nr\ :: ;:
질이 산소에 의해서 산화되는 과정에서 방출된 ener gy가 ATP 합성에 이 용된다. 동물체에서는 이것이 m it ochondr i a 의 내막(그림 1·21) 에서 이루 어지는데 이 산화과정은 전자전달 (elec t ron t rans p o rt)을 동해 이우어지며, 이렇게 ATP 가 합성되는 전과정을 산화적 인산화 (ox i da ti ve p hos p ho ry la ti on) 라고 한다. 그링 9·1 은 m it ochondr i a 에서의 호흡을 보여주는 것으로 동물체 가 흉수한 영 양분은 제 1 단계 (sta g e 1) 에 서 ca t abo li sm 과정 으로 ace ty l-coA 로 변형되고 이 화합물이 m it ochondr i a 의 ma t r i x 에서 citri c aci d( tr i c a rboxy lic a ci d)c y cle( 제 2 단계, s t a g e2) 을 거 칠 때 발생되 는 수소 가 NADH 로 가면 전자가 내막에 존재하는 전자전달계를 거쳐 최종적으 로 산소로 가고(제 3 단계, sta g e 3) 이때 생성되는 양자 농도 기울기에 의 해 서 ATP s yn t he t ase 가 활성 화되 어 ATP 가 합성 된 다. 9·1·1 전 자 전 달 (Electr o n tra nspo rt) 3> •> 그림 9·2 는 m it ochond ri a 의 내막에사 전자를 NADH 에서 산소까지 이 동시키는 과정을 보여준다. 전자 전달에 가담하는 성분들은 단백질안 flav oenzym e , cy toc hrome, 금 속 단 백 질 (meta l lop r ote i n ) 들 과 NAD + 와 coenzym e Q (ub iq u i none) 과 같은 작은 분자들이다. 산화적 인산화에는 5
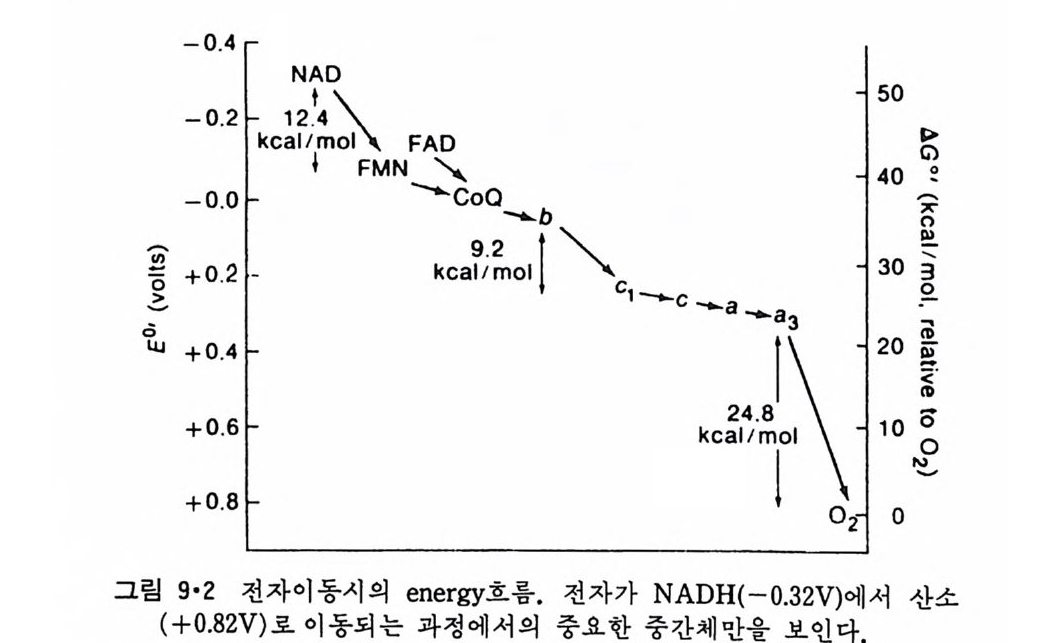 -0.4
-0.4
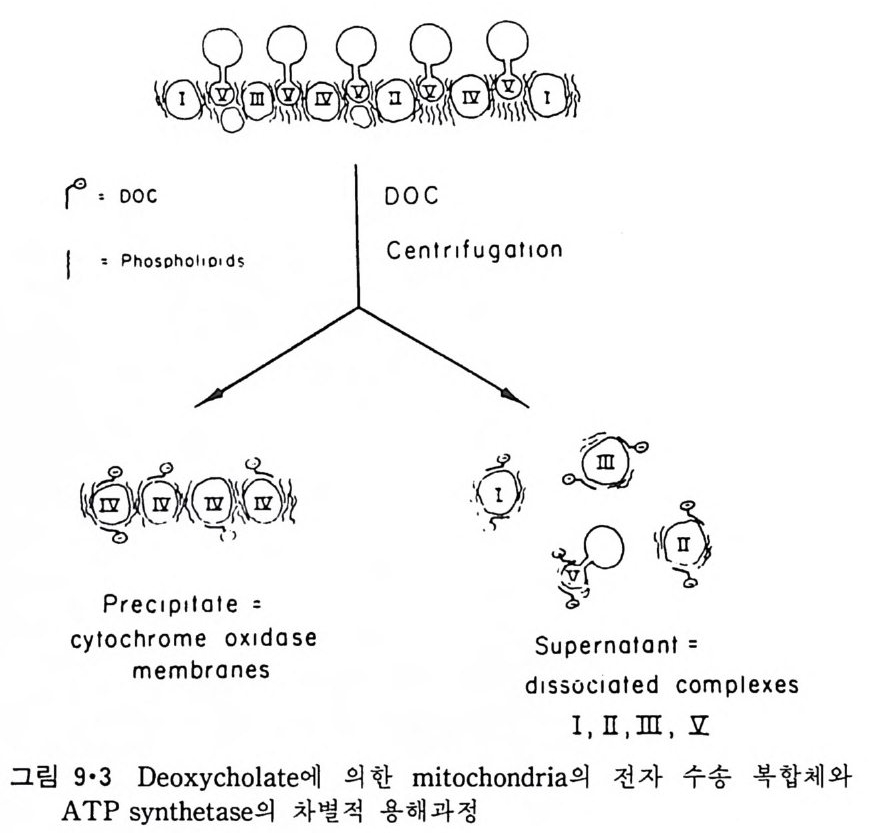 \o\®二 ::巳}
\o\®二 ::巳}
개의 효소 복합체가 가담하고 있는데 이중 4 개의 복합체는 전자 전달의 역할을 하고 있고 1 개는 인산화 과정에 가담한다. 이들이 mi toc hondria 내막 단백질의 대부분을 이루고 있고 이들 복합체는 그림 9·3 의 과정을 거 쳐 deox y chola t e 로 m it ochondr i a 의 내 막을 용해 분리 하여 얻을 수 있 다. 이때에 복합체 W 만 막에 남고 나머지는 용해되며 용해된 복합체를 여러가지 방법에 의해 분리해낼 수 있다. 복합체 성분 단백질은 대부분 세포질의 r i bo~orne 에 의 해 합성 된 후 m it ochond ri a 내 막에 수송되 지 만 일부는 m it ochondr i a 내의 r i bosome 에 의해 합성된다. 그림 9·4 는 효소 복합체의 주성분들간의 관계를 보여준다. 이들 복합체는 내막에서 내재 단백질로 존재하고 전자의 이동성 전달체로 coenzym e Q와 cy toc hrome C 가 있다. NADH : Ubiq u in o ne oxid o reducta s e(cornp le x I ) -이 효소 복합체는 다음과 같은 반응을 촉매한다.
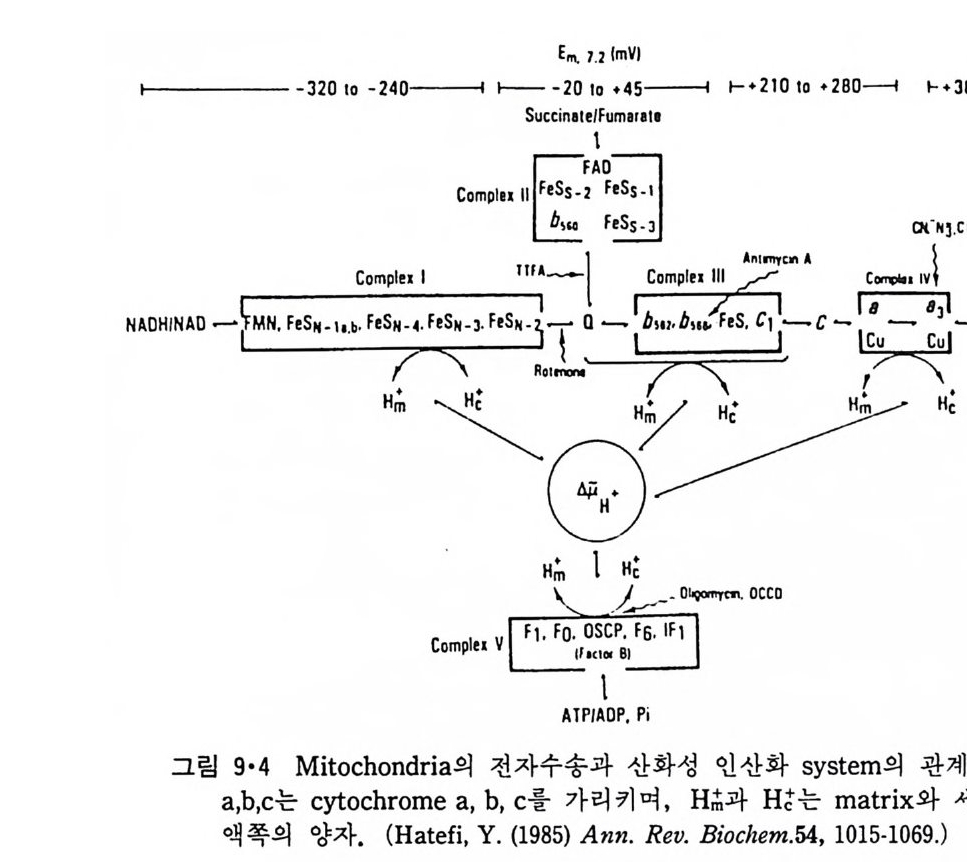 --320 10 -2 40- -----l ~— -E2. 0.. ,lo.2 lm+ V J4 5~ t-•2 10 lo +280- i I- ♦ 385-
--320 10 -2 40- -----l ~— -E2. 0.. ,lo.2 lm+ V J4 5~ t-•2 10 lo +280- i I- ♦ 385-
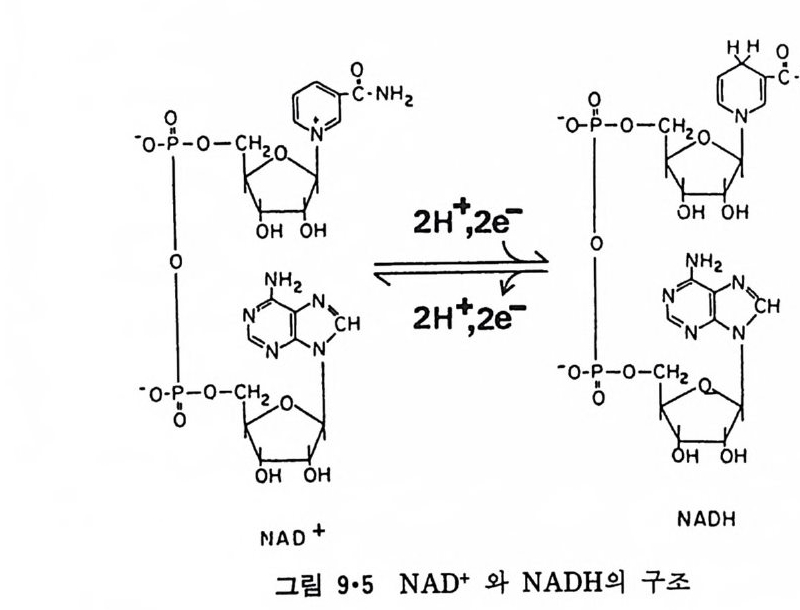 NAD+ NADH
NAD+ NADH
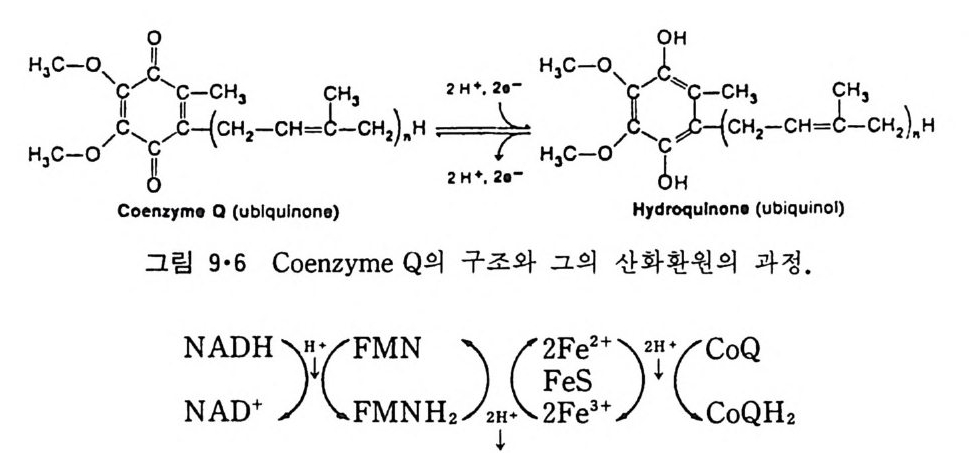 0 OH
0 OH
NADH 와 coenzy me Q의 구조와 이들의 산화환원 과정을 그림 9·5 과 그림 9·6 에 보여준다. 이러한 NADH 가 산화되고 Co Q가 환원되는 과정 에 서 양성 자는 ma t r i x 에 서 흡수되 고 m it ochondr i a 의 막간공간 (int e r mem- brane s p ace) 으로 방출된다. 죽 복합체 1 이 NADH 로부터 Co Q로 전자가 이동되는 것을 촉매하는 과칭에서 양성자를 ma t r i x 내부에서 외부로 p um pi n g한다. 복합체 1 은 그 무게가 약 850kDa 이 되며 이의 약 20% 가 지 방질이고 나머지는 약 25 개의 소단위 내재단백질로 구성되어 있다. 이 복합체를 chaot ro p ic 작용제로 처리하면 수용성 flav op ro te i n ( FP), 수용성 철―유 황 단백질(i ron-su lf ur pro t ei n , IP) 과 인산지방질울 함유하고 있는 비수용
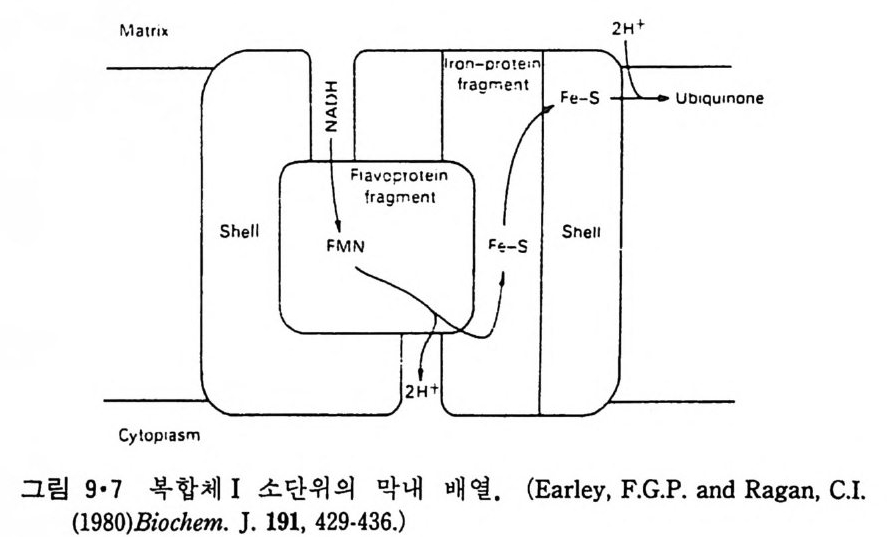 M a1 『 Ik 2H+
M a1 『 Ik 2H+
성 단백질 (HP) 의 세 부분으로 분리된다. 이 복합체 성분 중에서 HP 만 이 인산지방질과 접촉하는 것을 소수성 표지에 의해서 알게 되었고 또 천수성 표지로는 HP 와 IP 는 수용액과 접촉이 되어 있어도 FP 는 표지가 되지 않아 이 부분은 복합체 I 의 내부에 파묻혀 있는 것으로 생각되고 있다. FP 는 NADH deh y dro g enase 로서 3 개의 소단위로 구성되어 있으 며 이 효소는 복합체 내부에 깊이 묻혀 있음에도 불구하고 그 reacti on cen t er 는 matr i x 쪽과 통해 있다. HP 와 IP 는 각각 약 16 개와 6 개의 소 단위를 갖고 있으며 효소기능은 없다. 이상의 실험결과로부터 복합체 I 의 성분들은 그림 9·7 과 같이 막내에 배열되어 있다고 제안되었다. Succi na te : Ubiq u in o ne ox i doreduc t ase(com p lexII) 一전자전달 사슬에 서 coenzym e Q는 전자를 NADH 로부터 뿐만 아니 라 citri c ac id c y cle 의 suc ci na t e 로부터도 받을 수 있다. 이 전체 반응su은cc m다at음e 과 ) <같F 다A D ><2 Fe2+ > T
복합체 Il 는 suc ci na t e 가 f umara t e 로 산화되 고 동시 에 Co Q가 Co Q H2 로환원되는 과정을 촉매하는데 이때에 양성자가 ma t r i x 에서 반대 방향으로p um pi n g된다. 이 복합체는 수용성 인 succi na te deh y dro g enase(SDH) 와비 수용성 인 cy toc hrome bsss, non-heme p ro t e i n 으로 구성 되 어 있 다. SDH 는 분자량이 70kDa 과 27kDa 인 두 개의 소단위를 갖고 있으며 한개의 FAD 를 갖고 있다. Ubiq u in a l : Cy toc hrome c ox i droreduc t ase(com p lex ill)-이 복합체는다음과 같이 coenz ym e Q H2 로써 cy toc hrome c 를 환원시킨다.
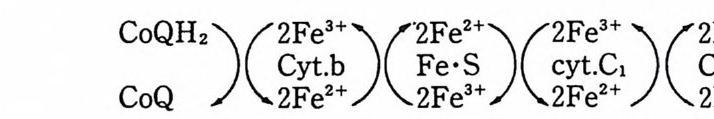 二 H2)(:: :i)(〔;:;++)(ir: :+1)(::;;
二 H2)(:: :i)(〔;:;++)(ir: :+1)(::;;
여기서는 Co Q H2 가 산화되는 동시에 cy toc hrome c 의 heme 기에 있는Fe3+ 가 환원되며 양성자가 ma t r i x 에의 외부로 p um pi n g이 된다 Cy toc hrome c 는 m it ochondr i a 에서 i on 세기 중가나 p H 변화로써 쉽게 떨 어 져 나오는 주변단백 질 이 다. 포유동물의 cy toc hrome c 는 104 개 의 am ino 산으로 구성되고 분자량은 12kDa 이고 am i no 산의 서열이 알려져
있다. 그 3 차 구조는 출처 에 상관없이 거의 비슷하다. Heme g rou p은 14 와 17 번째의 c y s t e i ne 기들과 t h i ae t her 결합을 이루고 있고 대부분이 소수 성 구멍에 파묻혀 있다. 복합체 111 전체의 무게는 약 250kDa 이고 c yyt ochromeb 와 cy toc hrome C1 를 함유하고 있으며, 비i on 성 세탁제의 존재 하에서 높은 i on 세기에 의 해 3 개의 작은 단위로 분해가 된다. 그링 9 • 8 은 복합체 III 와 여기에서 해리된 이들 작은 단위들의 SDS - PAGE 결과로 그들의 구성소단위를 보 여 준 다. Cy toc home b 는 m it ochondr i a 내 부의 r i bosome 에 의 해 합성 된 다. 복합체 III 전체로 구성된 1 차 경정과 cy toc hrome b 와 c 만을 함유한
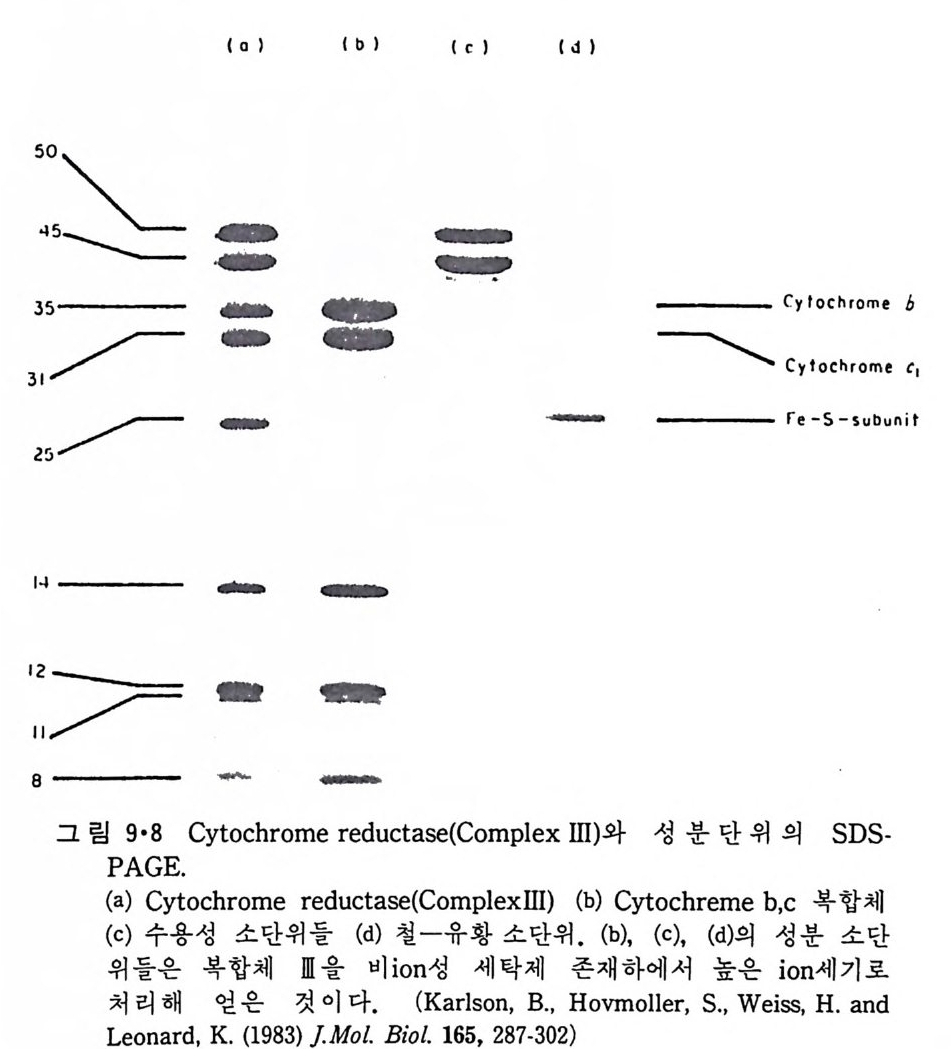 ( o ) I b ) ( C ) ( d I
( o ) I b ) ( C ) ( d I
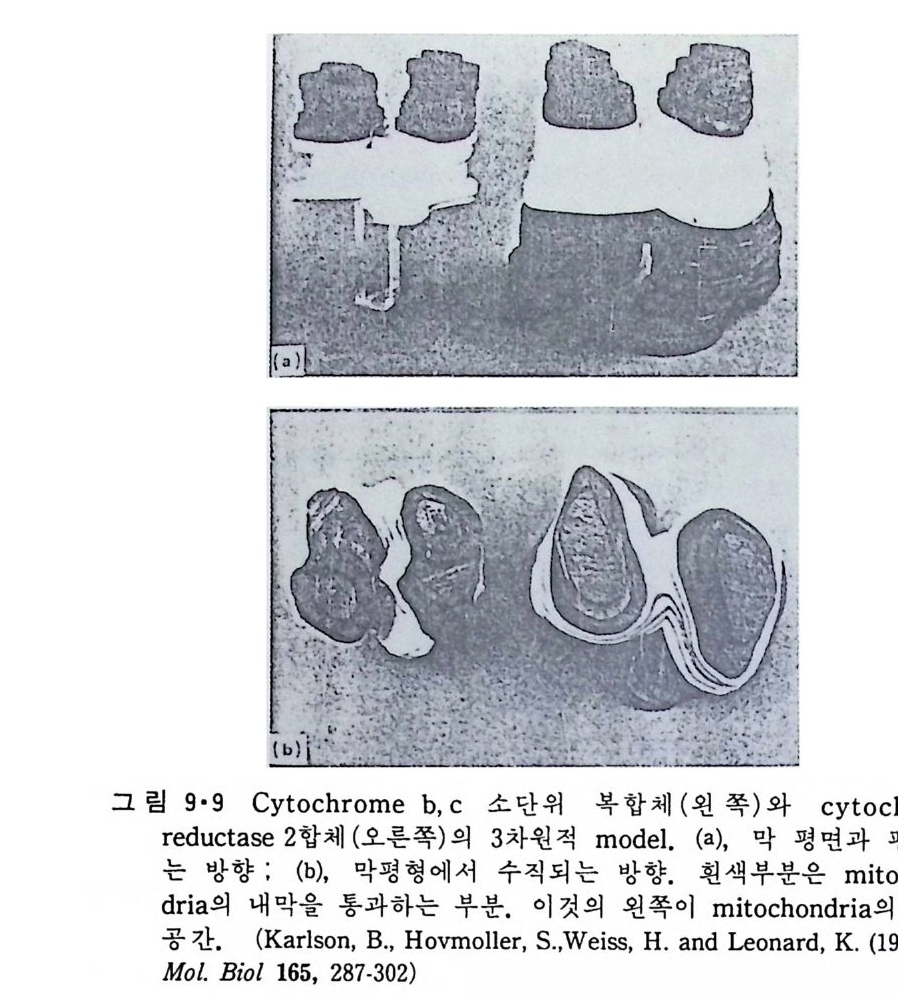 그 림 9·9 Cy toc hrome b, c 소단위 복합체 (왼 쪽) 와 cy toc home
그 림 9·9 Cy toc hrome b, c 소단위 복합체 (왼 쪽) 와 cy toc home
단위로 구성된 2 차 결정들울 각각 전자현미경에 의해 관찰한 결과로부터 그림 9·9 에 보여주는 model 들을 얻었는데 이 그림에서 복합체 III 는 막 내 부에서 2 합체를 형성하고 있으며 c yt ochromeb 와 C1 부분은 막간공간 쪽 에만 위치하고 있는 것을 알 수 있다. 화학적인 표지, 교체결합 (cross -li nk i n g)과 항체에 의한 연구 결과로 복합체 III 의 구조는 그림 9·10 과 같 다는 것을 알게 되었다. 복합체 III 의 여 러 단백 질 중에 서 cy toc hrome c1 과 FeS 단백 질은 수용성 이다. Cy toc hrome c1 은 분자량이 27,924 와 9,175 가 되는 두 개의 소단위 로 구성 되 어 있고 이 들의 am i no 산 서 열도 결 정 되 었 다. Cy toc hrome b 의 am in o 산 서열도 결정되었는데 분자량이 42kDa 인 이 내재단백질에는 막
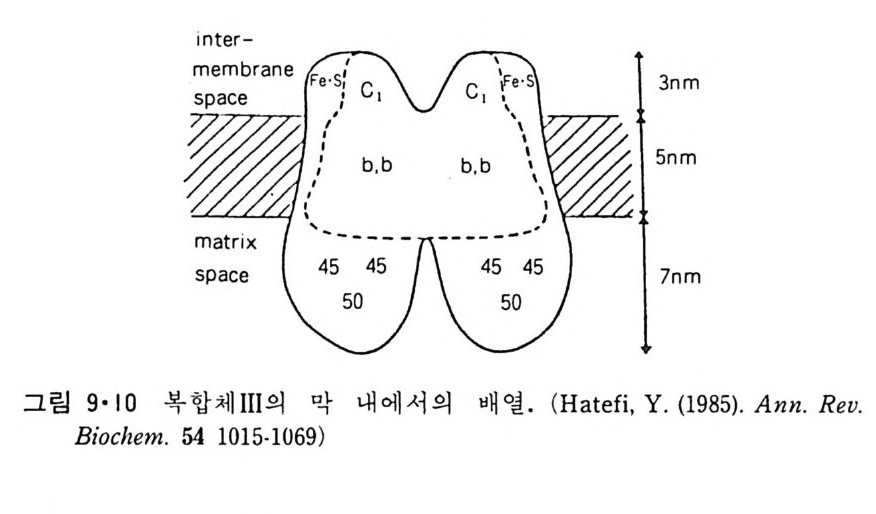 函cl2 ’ 'b’` `` ` 3nm
函cl2 ’ 'b’` `` ` 3nm
을 F동er과ro할cy t 수oc h있ro을m e만 c 한: O소xy수 g성e n o부x분id 이o r ed8u~c9t a개 s e가 ( co존 m재p 한l e다x. I V ) —이 효 소 복합체는 다음과 같은 반응을 촉매한다.
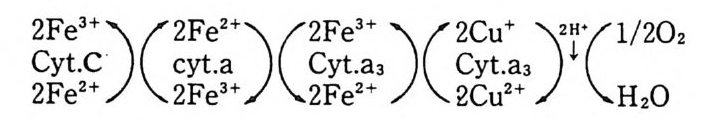 霜2F)e“ (;2『Fee2 ?++ ) (:2걷F단e한3+3 )( 2gC;u+2 ~〉2H ·( Hl2/2 00 2
霜2F)e“ (;2『Fee2 ?++ ) (:2걷F단e한3+3 )( 2gC;u+2 ~〉2H ·( Hl2/2 00 2
여기서 cy toc hrome c 는 산화되고 전자는 복합체 W 에 의해서 이동되며 결국 산소로 가서 이것을 물로 전환시킨다. 여 러 다른 종류의 세포에서 얻는 cy toc hrome c ox i dase( 복합체 W) 는 유사한 촉매 성 질과 울리 적 성 질을 가지 고 있으며 그 분자량은 200~250 kDa 이 된다. 소단위 (subun it)의 수는 아직도 확실치 않지만 8~9 개로 추 산되고 있다(그림 9·11) Cy toc hrome c ox i dase 의 생합성에는 세포액에 존재하는 r i bosome 과 m it ochondr i a 의 ma t r i x 에 있는 rib o some 양쪽이 모두 관여 한다. 소단위 l , n와 1Il (그림 9·11) 는 m it ochondr i a 의 r i bosome 에서 합성되며 이들 의 am i no 산 서 열은 m t DNA 의 유전자의 서 열로부터 결 정 되 었고 am i no 산 서열과 유전자 서열을 비교하면 보면 이들 소단위들은 합성된 후 더 잘 리지 않고 그대로 m it ochondr i a 의 내막으로 들어간다. 나머지 소단위들 온 세포액에서 합성되어 여기서 내막으로 들어간다. 이들 소단위들의 am i no 산 서열도 결정되어 정확한 분자량이 알려져 있으며 표 9·1 에 나 타내었다.
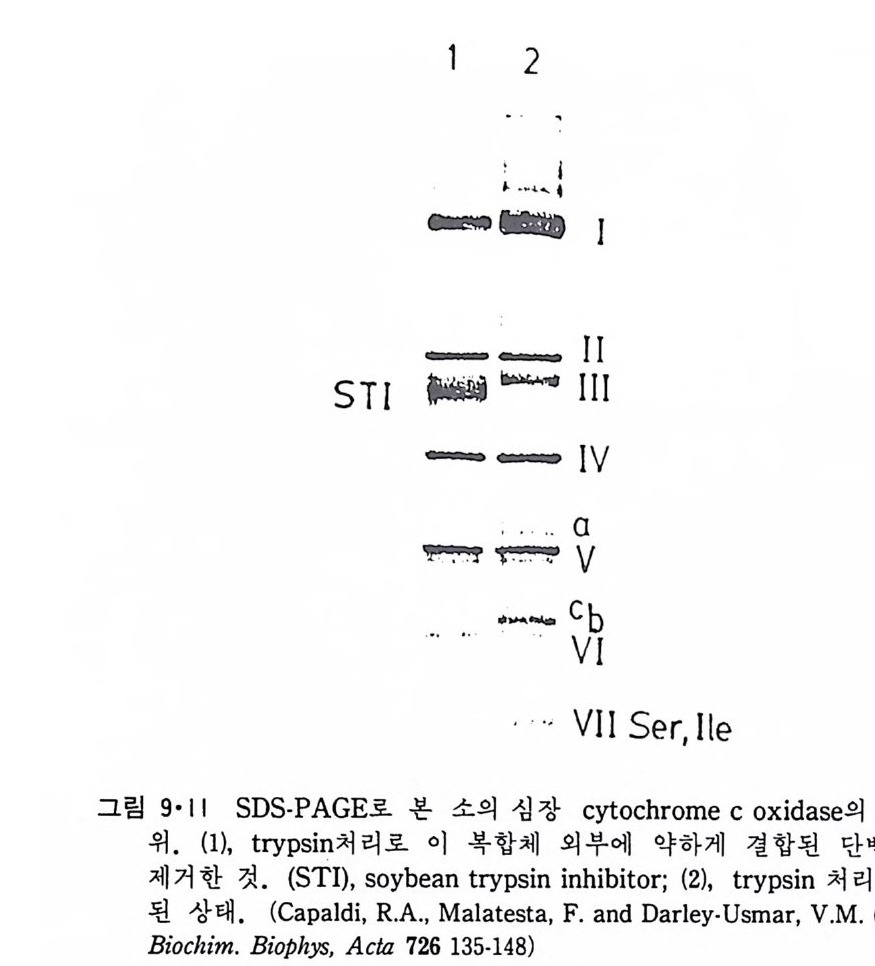 2
2
 표 9 . 1 소의 십 장 cy toc hrome oxid a se p ol yp e pti de 의 분자량
표 9 . 1 소의 십 장 cy toc hrome oxid a se p ol yp e pti de 의 분자량
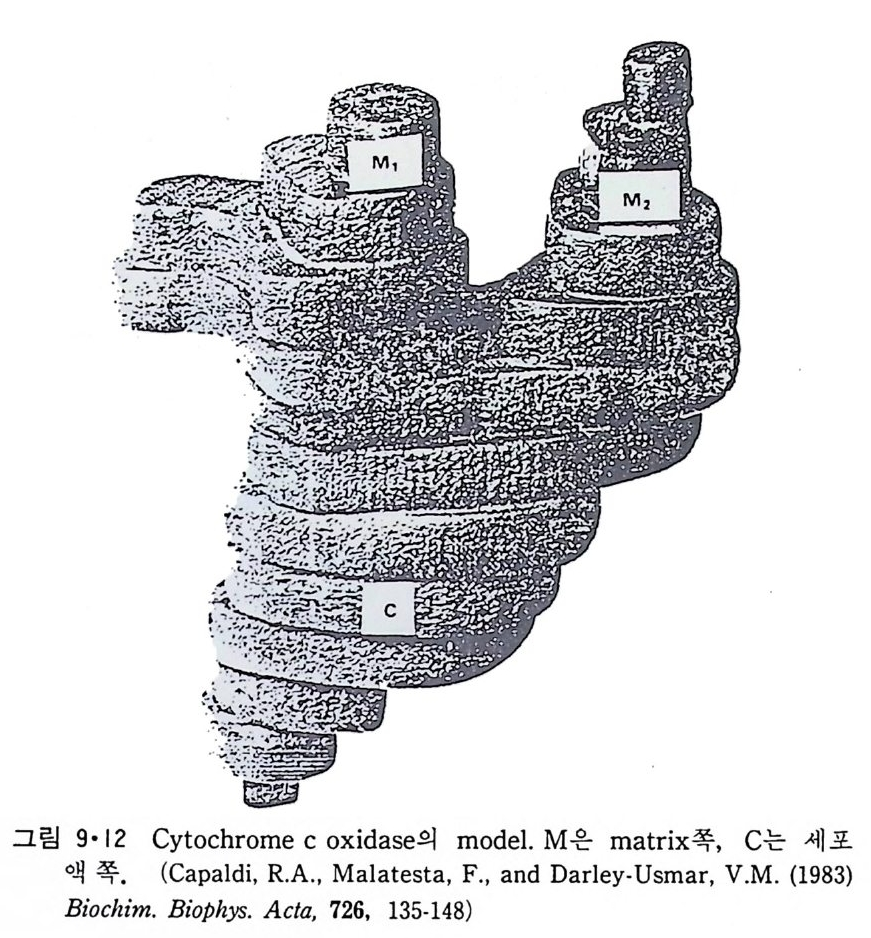 그림 9· 12 Cy toc hrome c ox i dase 의 model. M은 ma t r i x 쪽, C 는 세포
그림 9· 12 Cy toc hrome c ox i dase 의 model. M은 ma t r i x 쪽, C 는 세포
Cy toc hrome c ox i dase 는 세탁제 용액에서 이합체로 존재하고 높은 p H 에서는 소단위로 해리가 된다. 이 복합체의 2 차원적인 결정을 전자현 미경으로 관찰하여 얻어진 3 차구조는 그림 9·12 에 보여진다. 이 복합체 는 Y 자형을 이루고 있고 c 는 세포액 쪽으로 향하고 55A 정도 막간공간 으로 뻗어 있다. 이 복합체는 matr i x 경계면 근처에서 두갇래로 나뉘어 져서 약 20A 정도가 ma t r i x 로 노출되어 있으며, 막내에서는 아합체를 형 성한다. Cy toc hrome c oxid a se 소단위내에서의 p ol yp e pti de 서열은 교차결합 방 법으로 연구가 되었는데 그 결과는 그림 9·13 에서 보여준다. 소단위 I ' II, III, IV 와 V11 은 막을 동과하는 p ol yp e pti de 이고 이들 소단위들의 ami no 산 서열로 부터 이를 침작할 수 있다. 이때에도 bac t er i orhodo p s i n 때와
 그림 9· 13 화학적 인 표지 의 cross-lin k in g 실 험 에 의 해 얻은 cy to-
그림 9· 13 화학적 인 표지 의 cross-lin k in g 실 험 에 의 해 얻은 cy to-
 oc`, 'co。 , B
oc`, 'co。 , B
마찬가지로 막을 통과하는 내재단백 질 의 부분 은 a- 나사 선 구조 를 가 질 것으로 기대된다. 그럼 9·14 는 소단위 II 의 자유 energy p ro fil e 을 보여준 다. 이 소단위에서는 am i no 산 서열 25-48 과 63-82 부분이 막을 통과할 것이 예측되며, 같은 분석에 의하면 소단위 I 에는 10 개의 막을 통과하는 부분, 소단위 III 에 는 6 개 그리 고 IV, Vllser 과 Vi l~Ile 에 는 각각 1 개 씩 의 막 울 동과하는 부분이 있어서 전부 21 개의 부분이 막을 통과하게 된다. Cy toc hrome c ox i dase 에는 4 개의 보결분자단(p ros t he tic grou p ) 이 있다 (그럽 9·15). 즉, a 형 heme, a3 형 heme 그리고 두 종류의 Cu” 를 포함 하고 있는 복합체가 소단위 II 와 결합되어 있고 양성자 구멍은 소단위 III 에 존재한다. 이상의 전자전달 사슬에 의한 전자의 이동과 양성자 p wn pi n g의 총괄
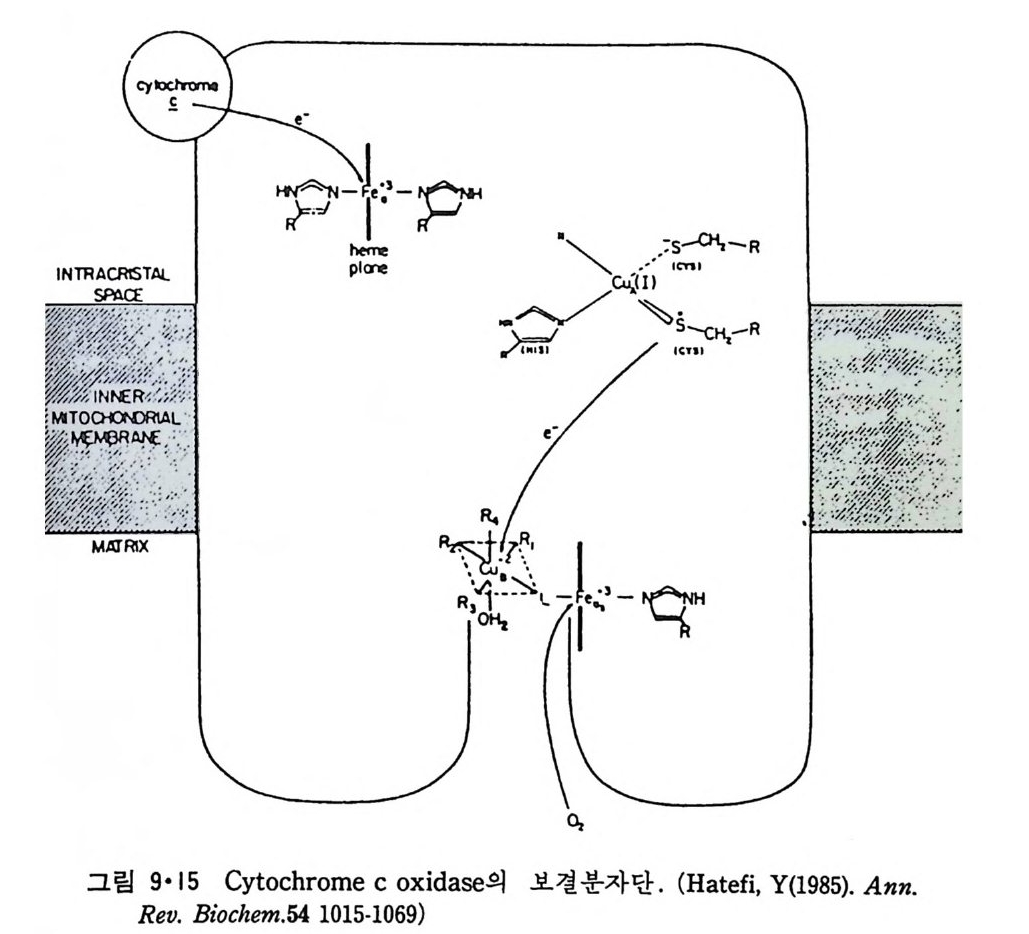 터e .:-: .
터e .:-: .
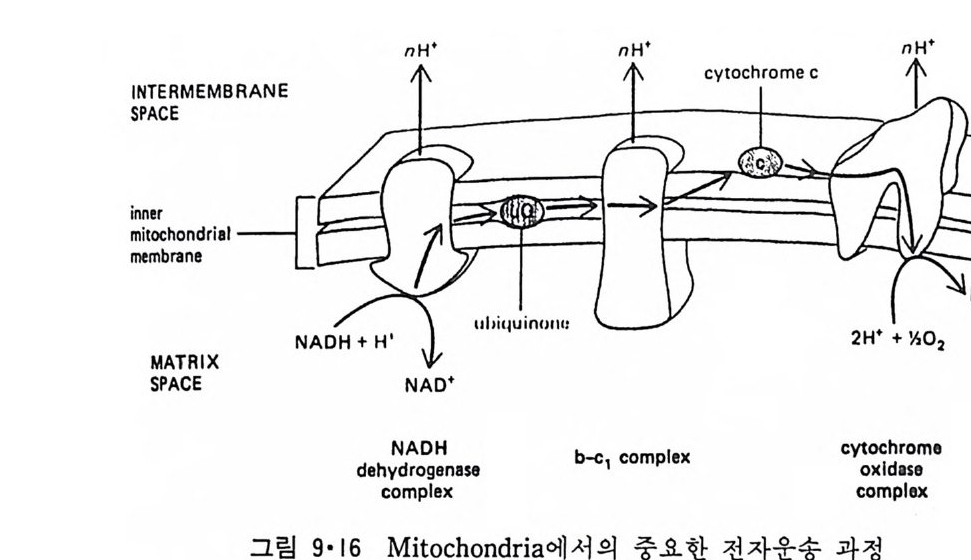 nH' nH`
nH' nH`
적인 반응은 그림 9·16 에 보여준다. 여기서 전자전달의 최종 결과는 이들 복합체들에 의해서 양성자가 m it ochondr i a 의 ma t r i x 에서 막간공간으로 이동되는 것이다. 이렇게 형성된 양성자 농도 기울기에 의한 자유ener gy가 ATP 합성에 이용된다. 전자가 NADH--+comp le x I --+CoQ --+comp le x III--+cy toc hromec--+comp le x IV--+02 의 경로로 이동되려면 이들성분간에 접촉이 있어 야 하는데 독히 단백질의 함량이 75% 나 되는m it ochondr i a 의 내막에서 이들이 일정한 순서로 배열되어 있는지 혹은자유롭게 웅칙이고 있는지가 홍미로운 일이다. 그래서 mi toc hondria 내
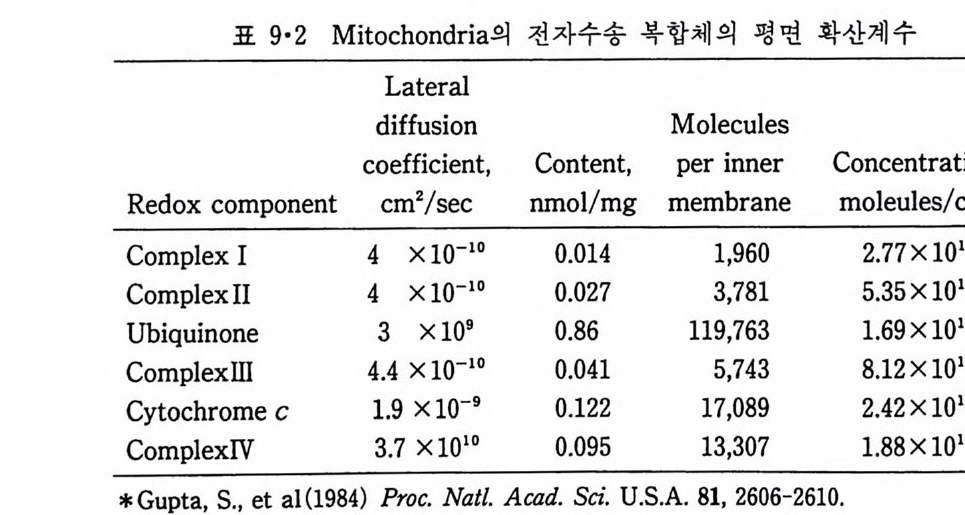 표 9·2 M it ochondr i a 의 전자수송 복합체의 평면 확산계수
표 9·2 M it ochondr i a 의 전자수송 복합체의 평면 확산계수
막에서 몇 개 성분의 평면 확산계수를 추정하였는데 (표 9·2) 이들의 확 산계수는 보통 내재단백질의 값과 별 차이가 없다. 이로부터 전자전달 사슬의 성분들은 막내에서 자유로이 이동하고 있으면서 충돌에 의해서 전자이동이 이루어진다는 것을 알 수 있다. 9·1·2 산화적 인산화 M it ochondr i a 에서 전자가 NADH 에서 산소로 이동되는 호흡과정이 ATP 가 합성되는 것과 관계가 있다는 것은 1940 년대부터 찰 알려져 있던 사실이다. 이 개념의 첫 중거는 m it ochondr i a 의 호흡은 ADP 의 존재하 에서만 일어나고 산소 한 분자가 호흡과정에서 소모되었을 때 얻어진 ATP 의 분자수는 3 이라는 일정한 값을 갖는 사실이 발견되었다. 이 전자 전달 과정과 ADP 의 인산화 과정을 연결시키는 중간체는 오랜 논란이 계 속되어 왔는데 오늘날에 와서는 1961 년에 M it chell 이 제안한 화학삼두 (chem i osmo tic)가설이 많은 지지를 받고 있다. 이 가설에 의하면 산화성 인산화는 m it ochond ri a 의 내막에서 일어나는데 (a)m it ochondr i a 의 내막 은 양성 자와 다른 i on 을 찰 통과 시 키 지 않고, (b) m it ochondr i a 의 내 막 에는 전자전달 성분들이 전자와 양성자를 비대칭적으로 이동시키도록 배 열되어 있어 결과적으로는 내막을 사이에 놓고 양성자 농도차가 생겨 양 성자 moti ve fo rce 가 형성되며 (그림 9·16), (c) m it ochondr i a 의 내막에 는 가역 적 으로 양성 자를 동과시 키 는 ATPase 가 있고 이 ATPase 는 ATP 를 가수분해해서 양성자 원동력을 형성하거나 반대로 이 힘을 이용 해서 ATP 를 형성한다. 이상 M it chell 의 화학삼두가설에서 가상된 세 가지 점은 오늘날 사실 상 중명되었다. 내막을 사이에 놓고 호흡이 일어날 때 pH 차이가 1 .4가 되는 것이 측정되었는데 이를 pro to n moti ve fo rce( p m f)로 계산하면, 4p =4¢-2.3RT4p H /3 식으로부터 0.14V 가 된다. 이 식에서 ¢는 전위 (electr i c a l po te n ti al ) , :J 는 Farada y이다. 내막이 양성자를 잘 통과시키지 않는 것도 관찰되었 다. 이렇게 전자전달계가 양성자를 능동적으로 수송하기 위해서는 이들 이 막횡단 단백질이어야 하는데 실제로 복합체 I,m 와 IV 에는 양성자를 이동시키는 내재단백질들이 있다. 마지막으로 내막에 있는 ATPase 는 비
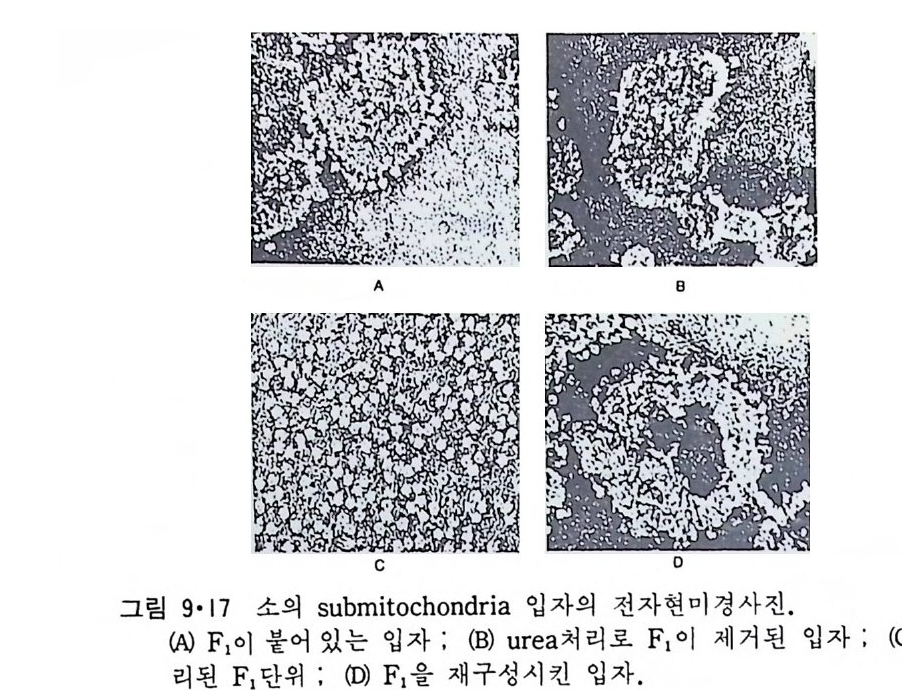 AC B
AC B
대칭적으로 배열되어 있고 p H 차이가 존재하며 ADP 를 인산화시킨다는 것이 증명이 되었다. 그림 9·17A 에는 m it ochondr i a 의 내막에서 얻어진 막소포의 외부 표면 에 존재하는 85A 직경의 입자들이 보인다. 이 입자들은 길이 50A, 직 경 30A 인 줄기 모양의 부분에 의해서 내막과 연결이 되어 있고 이들은 기계적인 방법이나 chaotr o p ic 작용제로 막에서 떨어뜨리면(그림 9·17B) 나머지 내막으로 구성된 막소포는 전자이동을 시키나 ATP 의 합성이나 가수분해는 시키지 않는다. 한편 막소포에서 떨어져 나온 입자들은 ATPase 의 ac ti v ity를 갖는다. 다시 mi toc hondri a 막소포에 부착시 키 면 그림 9·17C 전자전달도 이루고 ATP 도 합성시킨다. 전자전달 과정을 거 치지 않고 인공적으로 p H 차이룰 형성했을 때 ATP 가 형성되는 것은 처 음에 t hy lako i d 에서 관찰되었고 근래에 와서는 양성자를 빛에 의해서 p wn ping시 키 는 bac t e ri orhodo p s i n 과 m it ochondr i a 의 ATPs ynt he t ase 를 동시에 막소포에 재구성시켰을 때도 관찰되었다. 그래서 M it chell 의 화 학상투가설은 여러 실험 결과로 보아 옳은 것이 판명되었다. 나머지 문 제 는 ATP s ynth e t ase 가 양성 자 농도 차이 룰 어 떻 게 이 용하여 ATP 를 합성하느냐의 분자적인 mechan i sm 을 규명하는 것이다.
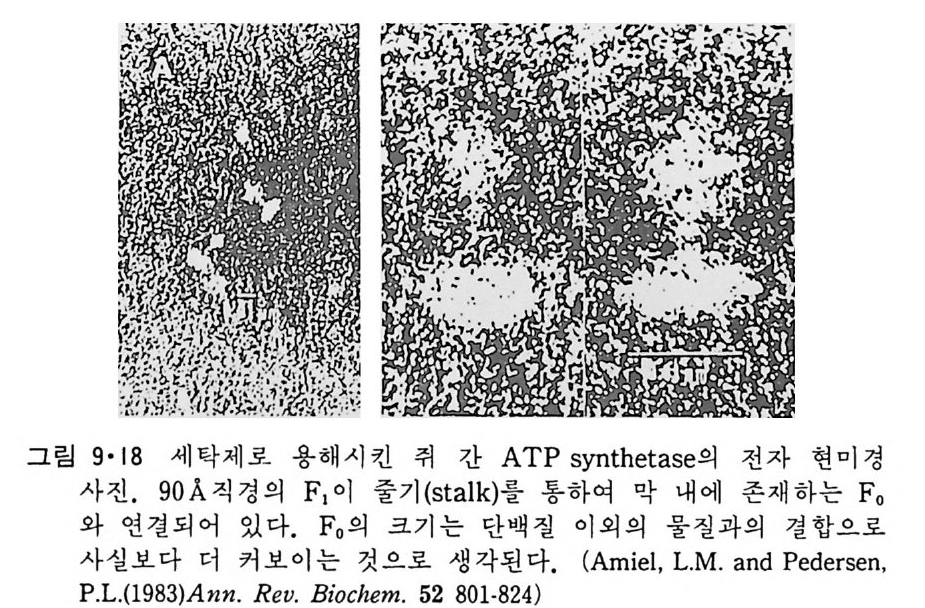 그림 9•18 세탁제로 용해시킨 쥐 간 ATP s ynt he t ase 의 전자 현미경
그림 9•18 세탁제로 용해시킨 쥐 간 ATP s ynt he t ase 의 전자 현미경
그림 9·17A 와 9·17C 에 밖으로 돌출되어 나온 입자는 R 이라고 불리며 ATP 의 합성에는 내재단백질인 Fo 와 F 려 결합한 복합체가 필요하다. 그림 9·18 은 세탁제로 용해시킨 F 。 R 복합체를 보여준다. 이 전자현미경 사진에서 90A 직경의 구형 입자가 F1 이고 이는 줄기 모양 부분으로서 막내에 존재하는 Fo 과 연결되어 있다. 그림 9·19 는 F1 과 F1F 。 복합체의 SDS-po ly a cryl a mi de 전기영동법으로부터 얻은 소단위의 분포를 보여준 다. E 에 다섯 개의 소단위는 그의 출처가 어떤것이든지 관계없이 모두
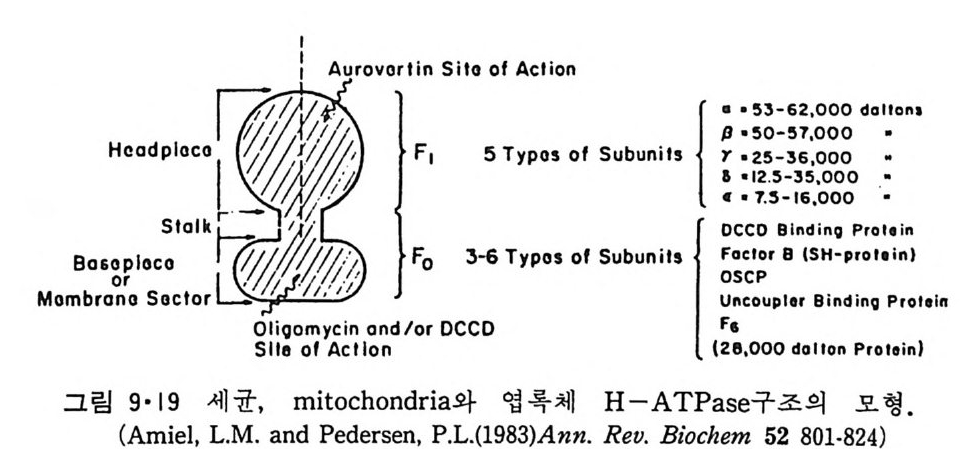 Hoodp lo co. (/// /! {/ /A ;ur(a vo、 rt匡i n Sit o 5 o fT Ay pcot iso no f subumt s Ig ;:::틀。 d01;on1
Hoodp lo co. (/// /! {/ /A ;ur(a vo、 rt匡i n Sit o 5 o fT Ay pcot iso no f subumt s Ig ;:::틀。 d01;on1
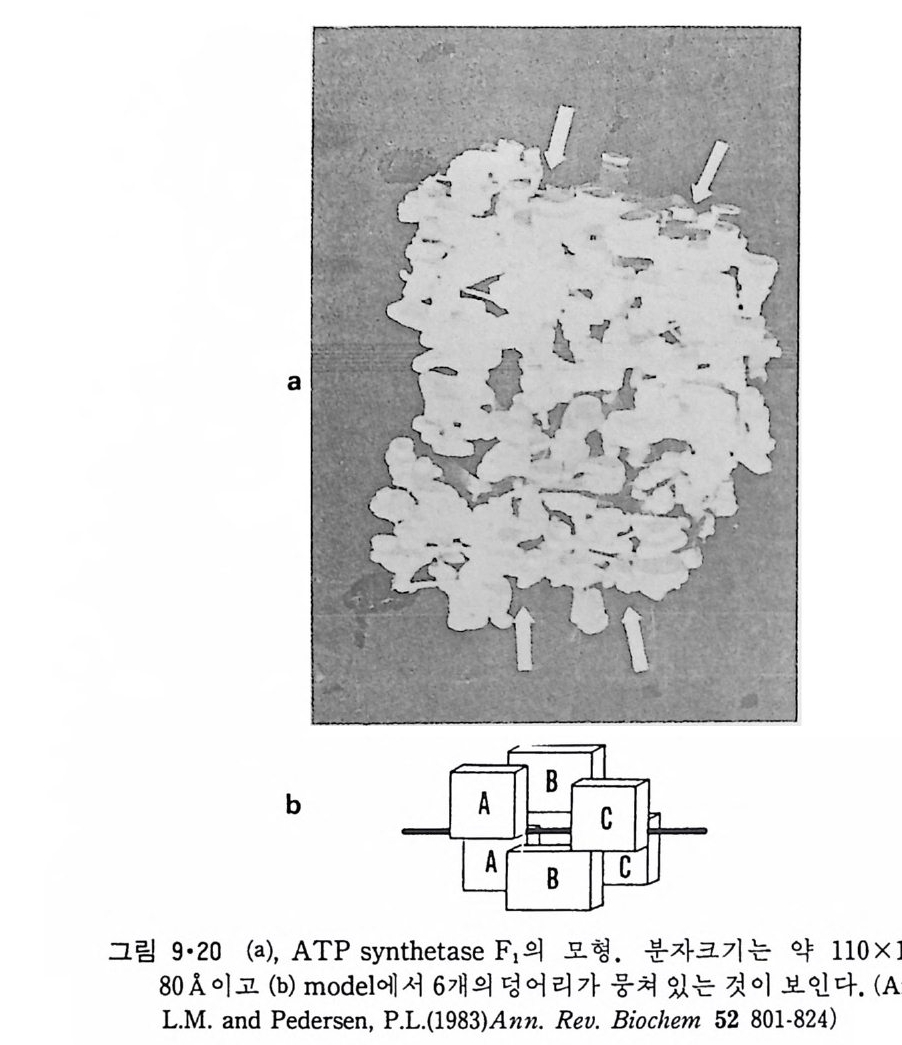 a
a
같지만 Fo 의 소단위들은 원핵세포에서는 3 개이고 진핵세포에서는 6 개까 지도 존재한다. 4 차구조는 아직 결정되지 않았다. R 의 s t o ic h i ome try는 a3 f3 3r8c 로 추정되고 있다. F1 의 결정은 근래에 와서 얻어졌고 이 결정의 X- 선 회절로 얻어진 9A resolu ti on 의 구조는 그림 9·20 에 보여준다. 이 결과와 a3f3 3 r8c s t o i c hi ome try를 만족시키기 위해서 그림 9·21 에 보여준 model 이 제안되 었다. Fo 에는 유기용매에 녹는 소단위가 존재하는데 이렇게 특이한 용해성을 가진 p ol yp e pti de 는 분자량이 약 8kDa 인 작은 내재단백질이고 그 무게의
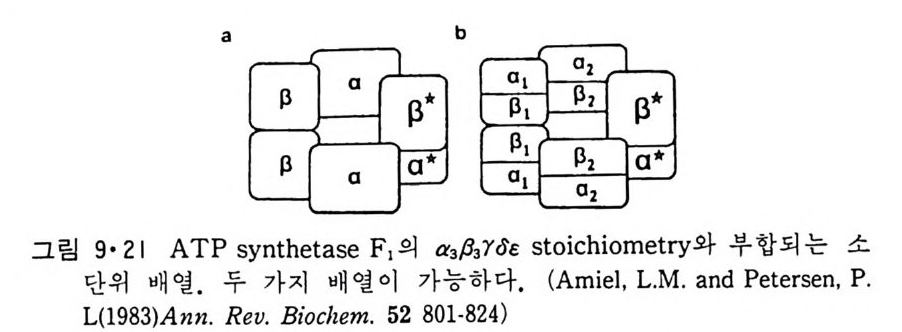 a b
a b
75% 가 소수성 am i no 산으로 되 어 있고 F 。 한 분자에는 6 개의 p ro t eo lipi d 가 존재 한다. Fo 을 가진 막에 DCCD 를 가하면 양성 자의 이 동 이 처해되는데 DCCD 가 이 p ro t eo lipi d 에 결합되는 것으로 보아 이 단백 질로 구성된 o lig omer 가 양성자의 막구멍 역할을 하는 것으로 생각된다. 이 단백질을 막소포에 재구성하여 얻은 CD 결과에 의하면 그 po lyp e p tide
 ,. .
,. .
사슬의 83% 가 a- 나사선, 13% 가 /3 sheet, 4 % 가 /3 t urn 로 이 루어져 있으 며 random co i l 은 함유하지 않는다. 이 p ol yp e pti de 의 am i no 산 서 열을 보면 두 부분이 소수성을 띠고 있어 이로부터 그림 9·22 와 같은 model 이 얻어졌다. 여기서 N- 말단과 C- 말단들은 모두 막간공간에 노출되고 F1 은 반대 방향에서 ma t r i x 쪽에 노출된 부분에 부착된다. 이렇게 F1 과 Fo 의 막에서의 구조의 윤곽은 드러나기 시작하지만 양성 자 이동과 ATP 합성이 어떻게 이루어지느냐 하는 mechan i sm 은 이들 구 조가 좀더 명확해진 후에 밝혀질 것이다. 9·2 엽록체 7)-11) 태양은 지구상의 모든 ener gy의 중요한 근원이 되며 이 태양 ener gy는 광합성을 하는 생물체가 공기 중의 CO2 를 다음 반응식에 있는 과정으로 탄수화물로 전환시키는 데 쓰인다. 6C02 + 6H20 + 빛 --+ C6H 1202 + 602 식물체에서의 광합성은 엽록체에서 일어나고 이는 그림 9·23 에 보이는
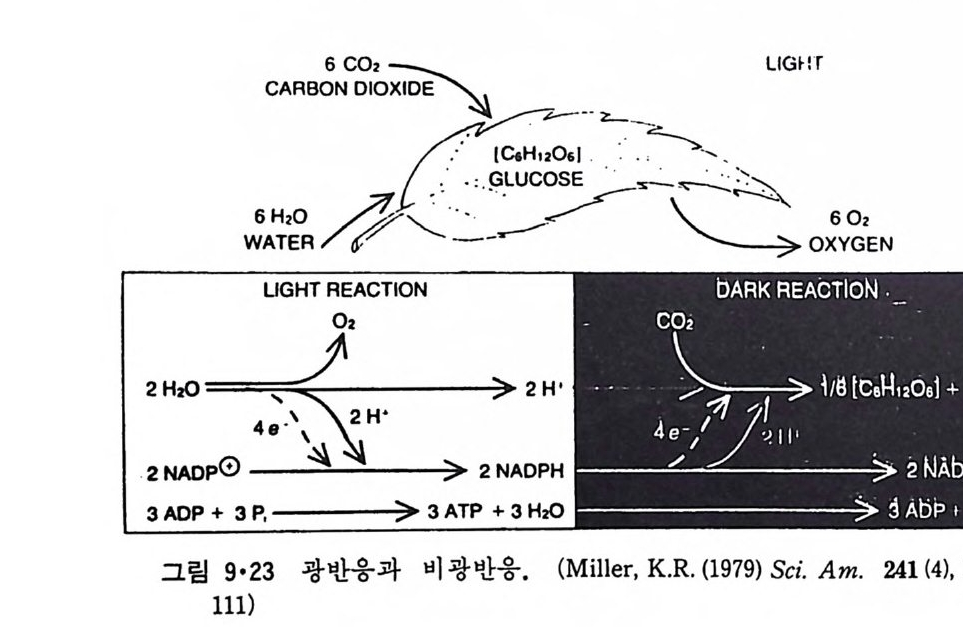 CARBO6N C DOI2O 교 r LIGHT
CARBO6N C DOI2O 교 r LIGHT
것 같이 크게 두 단계로 나누어진다. 이 중에서 광반응(lig h t reac ti on ) 에 서는 물의 수소가 광 ener gy에 의해서 NADP 를 환원시키며 동시에 ATP 가 합성되고 산소가 방출된다. 이것은 엽록체 내의 t h y lako i d 막에서 일어나며 광 ener gy가 화학적인 ener gy로 이전되는 과정이다. 비광반응 (dark reac ti on) 은 탄수화물이 합성되는 과정으로 수용액내에서 일어난다. 광산학적 인산화(p ho t oox i da ti on- p hos p ho ry la ti on) 의 과정은 분광학적 인 방 법으로 연구가 많이 이루어져 그 윤곽은 알려졌으며 그림 9·24 는 광산화 (p ho t oox i da ti on) 과정에서의 전자전달 상황을 보여준다. 이 과정을 동해 서 양성자가 엽록체 안의 s t roma 쪽에서 thy la koid 내부로 이동되어 생긴 양성자 원동력에 의해 th y la koid 외부에 있는 ATP-s ynt he t ase 가 ATP 룰 합성하며 이와 동시에 얻어진 NADPH 와 함께 비광반응으로 탄수화 울이 생성된다.
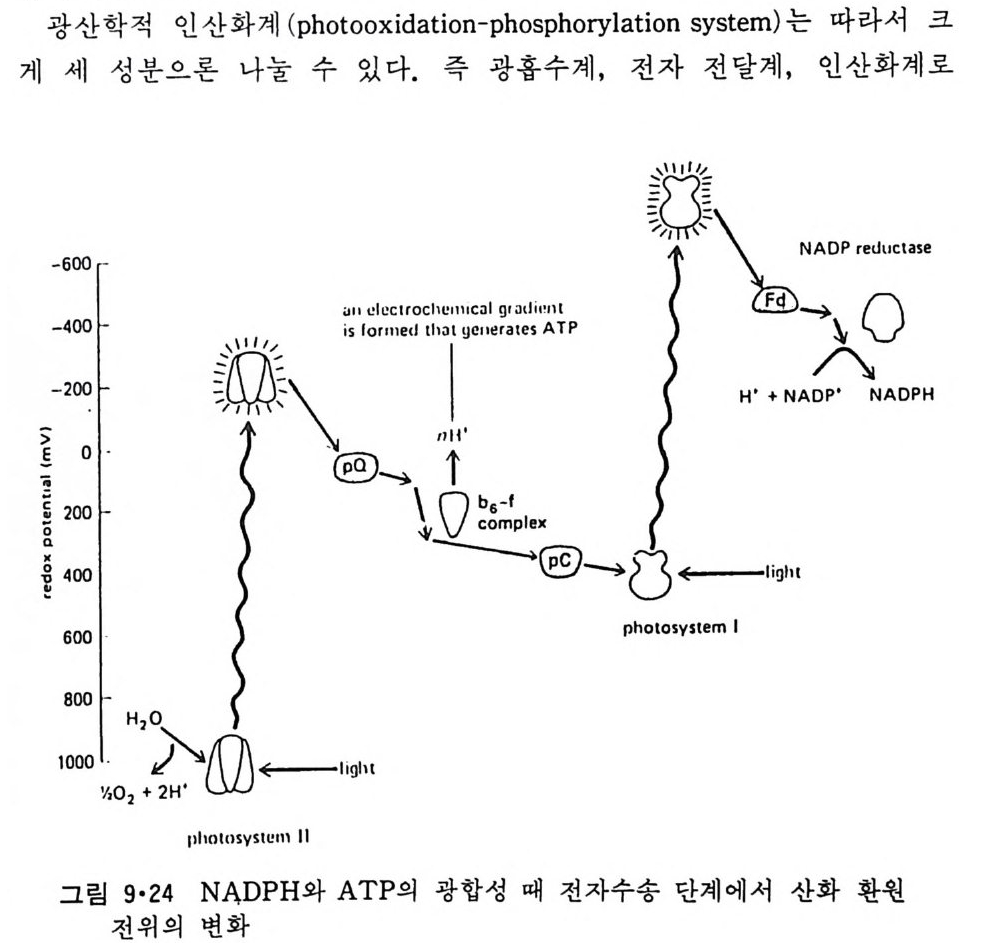 광산학적 인산화계 (ph oto o xid a ti on -ph osph ory la ti on s y s t em) 는 따라서 크
광산학적 인산화계 (ph oto o xid a ti on -ph osph ory la ti on s y s t em) 는 따라서 크
이들은 전부 th y la koid 막에 존재하는 내재단백질과 주변단백질 그리고 작은 유기물질로 구성되어 있다. 광 s y s t emII 의 reacti on cente r (P 6 80) 가 680run 파장의 광을 흡수하면 P680 엽 록소가 산화되 어 전자가 같은 s y s t em 에 있는 acce pt er 로 이동된다. 이때 산화된 엽록소는 전자를 물에 서 받아 산소와 양성자가 생성된다. Acce pt er 가 받은 전자는 전자전달 사슬을 따라 내려가 광흡수로 전자를 잃고 산화된 광 sys t e m I 의 P700
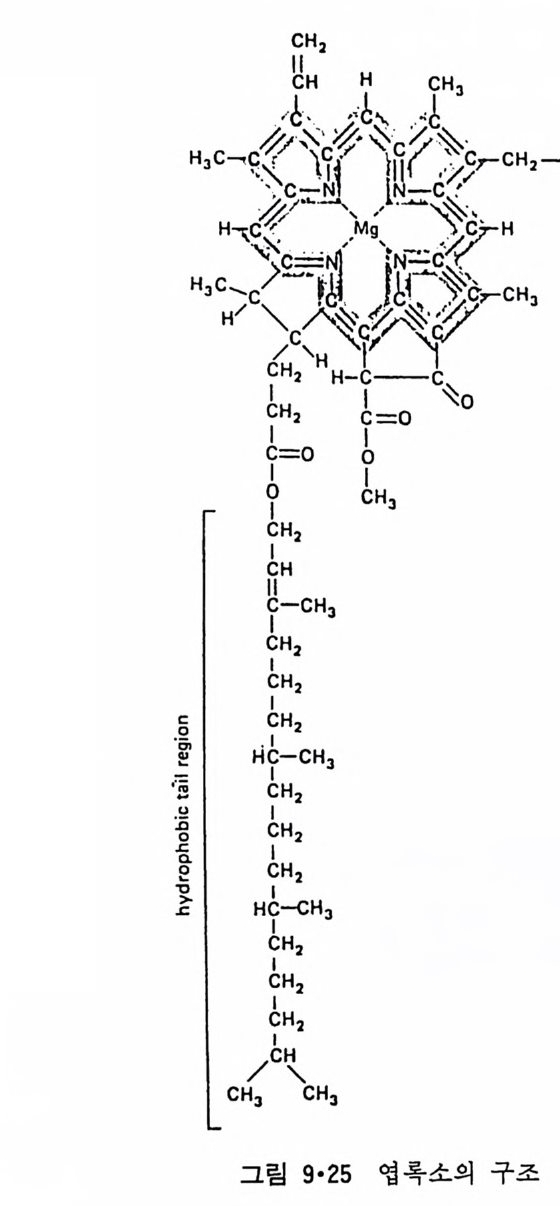 5CH
5CH
엽 록소에 이 르 러 이 룰 다시 환원 시 킨 다. 광 sys te m I 의 reacti on cente r (P700) 는 700run 의 광선을 홉수하는데 이때 acce pt er 로 간 전자는 전자 전달계를 거쳐 NADP 나춘 환원시킨다. 이러한 전자이동 과정에서 양성자 가 thy la koid 내부로 들어간다. 대부분의 thy la koid 막 단백질은 다섯 개 의 복합체로 존재하며 아들은 광채취 복합체 (ligh t harvesti ng comp le xII, LHCI I), 광 sys te m II (ph oto s ys t e m II, PSII) 복합체, 광 sys te m I (ph oto s ys t e m I , PS I ) 복 합 체 • cy toc hrome b s-f 복 합 체 와 ATP s yn t he t ase 복합체이다. 나머지 전자전달 성분은 막 내에 존재하는 유기 물질이거 나 주변단백질이다. Th y lako i d 에서 광의 흡수는 PS I , PSII 와 LHC 에 존재하는 엽록소 ( 그림 9·25) 와 caro t endo i d 들에 의해 이루어진 다. 엽록소는 소수성 꼬리 부분을 가지고 있어 t h y lako i d 막 내에 독립적 으로 존재할 수도 있 겠 으나 그의 전부가 PS I , PSII 와 LHC 의 내재단 백질과 회합되어 있다. 이것은 t hy lako i d 막을 세탁제로 용해하여 g el 전기 영동법에 의해 엽록소의 위치가 단백질의 위치와 일치하는 것으로 알수 있다. 광 s y s t em 에 있는 엽록소는 두 가지로 나눌 수가 있다. 이들의 대 부분은 광채취 복합체에 있고 소수만이 reacti on cen t er 에 있다. 광채취 복합체 의 ante n na 색 소가 광을 흡수하면 이 ener gy는 공명 ener gy전 달의 mechan i sm 을 통하여 신속하게 reacti on cen t er 에 전 달된다. Reacti on cen t er 에 있는 엽록소가 이들 ener gy를 받으면 여기서 전자가 떨어져 나 와 acce pt er 로 가서 이 를 환원시 킨 다. 9·2·1 광채취 복합체 II (LHCII) LHCII 는 엽록소 a 와 b 를 포함하고 있으며 고등식물인 경우 thy la koid 엽록소 단백질 복합체의 반 이상을 차지한다. LHCII 는 비 i on 성 세탁제 로 용해시켜 비중 기울기 원심분리법으로 쉽게 분리할 수 있으며 분자량 이 21~29kDa 의 p ol yp e pti de 로 구성되어 있고 한 p ol yp e pti de 에 3 개의 엽록소가 부착되어 있다. 저농도의 세탁제와 적당한 i on 강도의 조건 하 에서 LHCII 는 결정을 형성하기 때문에 x- 광선 회절로 그 구조가 연구 되었다. 이 결과에 의하면 LHCII 는 6 개의 p ol yp e pti de 가 한 단위를 형 성하여 8mn 입자를 구성한다. 정제된 LHCII 를 인산 지방질 막소포에 재 구성시키켜 동결파열 전자현미경 방법으로 관찰하면 이 8mn 입자가 보인 다. 몇 종류의 LHCII 유전자의 nucleoti de 배열이 결정되었는데 이것과
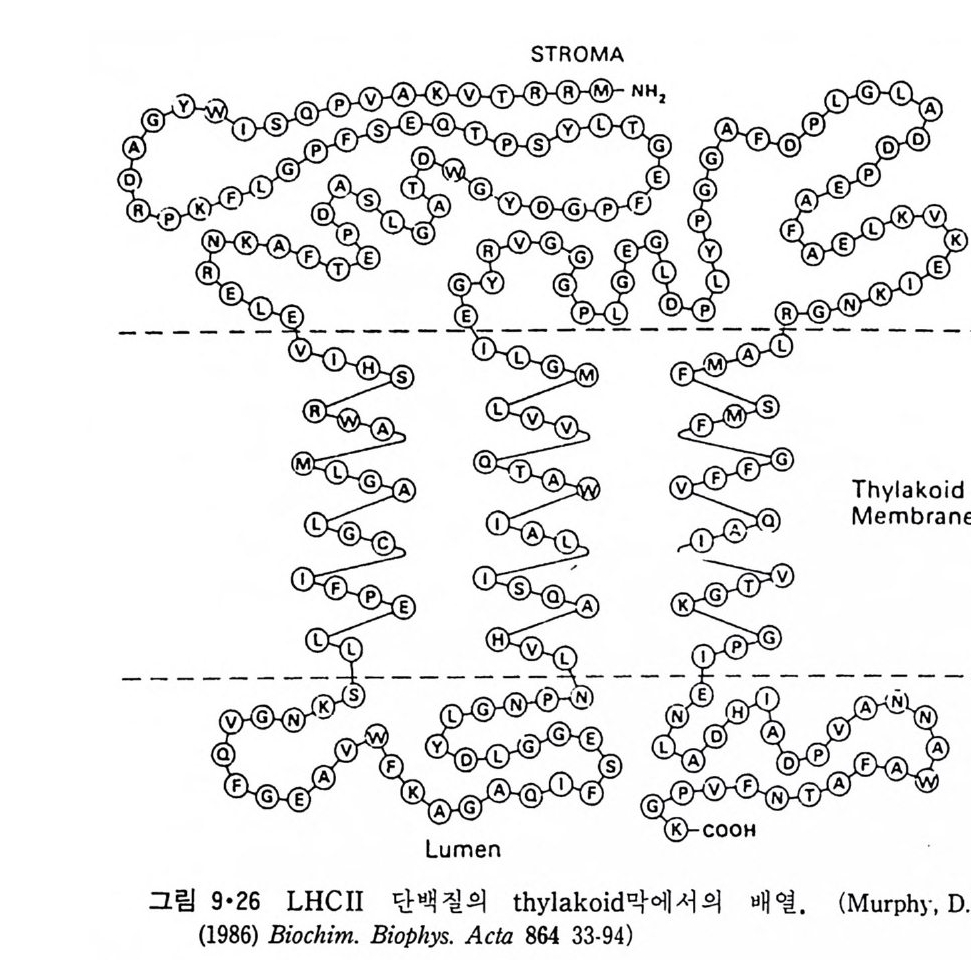 STROMA
STROMA
LHCII p ol ypepti de 의 배 열을 바 교하면 이 단백 질들은 보다 큰 p ol ypepti de 로 합성되어서 엽록체 내부로 수송된 후 그 신호서열 부분이 찰라지는 것을 알 수 있었다. 이 단백질의 막 내에서의 구조는 아직 모 르나, 그 am i no 산 서열로부터 그림 9·26 과 갇은 막내구조가 제안되었 다. 9 • 2 •2 광 S y s t em ll (Photo s ys t e m ll ) 복 합체 LHCII 에서 받아들인 광 ener gy는 공명 ener gy전달 과정을 거쳐 광 s y s t emll 로 간다. 이 복합체는 엽록소 a 만을 함유하고 있으며 thy la koid 엽록소의 약 15% 를 차지한다. PSII 복합체는 다음과 같이 적어도 다섯
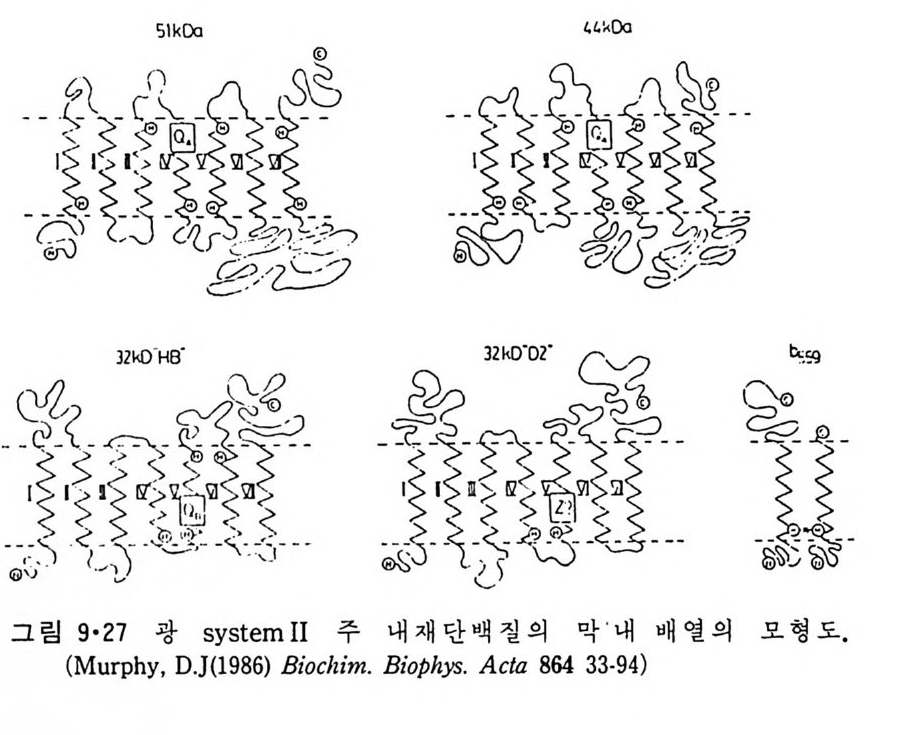 51k() a LLk() o
51k() a LLk() o
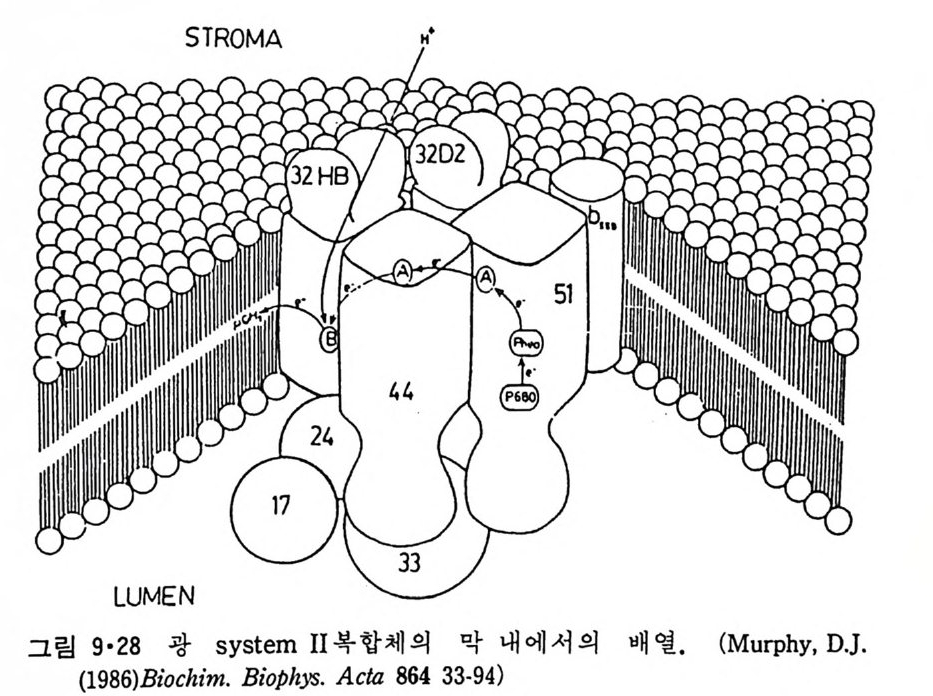 STROMA H.
STROMA H.
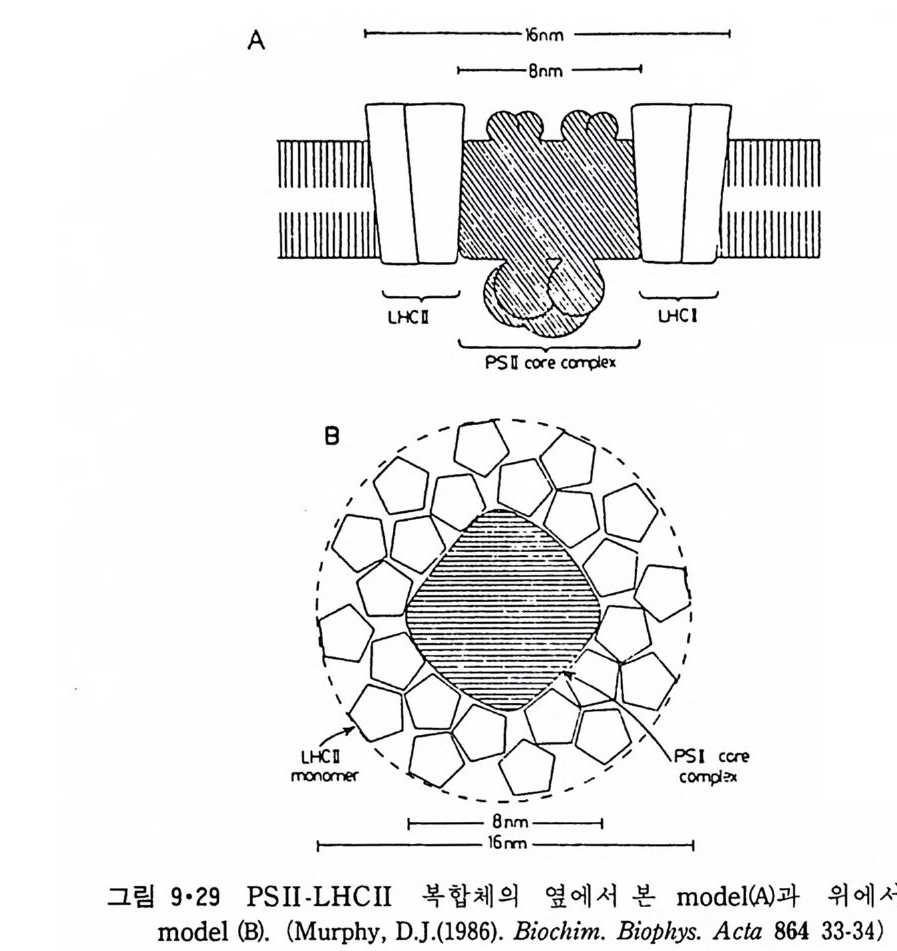 A -16nm-
A -16nm-
개의 내재단백질로 구성되어 있다. (a) 4~5 개의 엽록소 a 와 1 분자의 f] -caro t eno i d 로 결합되며 있는 51k Da po lyp e p tide . 여 기 에 P680 reacti on cen t er 가 존재 한다고 생 각된 다. (b) 4~5 개의 엽록소 a 와 1 개의 f] -caro t eno i d 를 함유하고 있는 44kDa po lyp eptide . 이것은 보조적인 광 수집 기능을 가진다고 생각된다. (c) p last o q u i none 과 결 합하는 32kDa 의 po lyp e ti de . (d) 기능이 아칙도 확실치 않은 32kDa po lyp e p tide . (e) lOkDa 의 cy toc hrome b-559. 이들 내재단백질들의 am i no 산 서열이 결정되었고 이것으로부터 그림 9·27 에 보이는 것과 같이 막 내에서의 구 조를 갖는다고 추측되고 있다. 이들 내재단백질 이외에 PSII 는 3 개의 분자량이 각각 33kDa, 24kDa,
그리고 18kDa 인 주변단백질을 가지고 있는데 이들은 산소 발생에 가담 하는 것으로 생각되고 있다. 그링 9·28 은 t h y lako i d 막에서 PSII 단백질 둘의 서열을 보여준다. 여러가지 화학반응 속도, 전자현미경 그리고 면역학적 연구를 통해서 LHCII 와 PSII 는 복합체를 형성하는 것으로 추측되는데 그의 model 은 그림 9·29 에 보여준다. 9·2·3 Cy toc hrome b6-f 복합체 PSII 에서 시작된 전자이동은 p las t o q u i none 과 cy toc hrome b6-f 복합 체를 거쳐서 p las t oc y an i ne 을 동해 광 sys t e m I (PS I )로 가게 된다. 그래서 cy toc hrome b6-f 복합체는 pla sto q u in al-pl asto c y a nin e oxid o r- educ t ase 역할을 한다. 이 과정에서 양성자가 t h y lako i d 내부로 pu mp ing 이 된다. 이 복합체는 34kDa 의 cy toc hrome f, 23kDa 의 cy toc hrome bs63, 20kDa 의 Fe2S2 단백질, 15~17kDa 의 구조 p ol yp e pti de 와 기능이 확실치 않는 5kDa p ol yp e pti de 등 다섯 개의 내재단백질로 구성되어 있다. 이중 cyt ochrom 들과 17kDa p ol yp e pti de 의 am i no 산 서 열 은 결 정 이 되 어 있고 이로부터 막내구조가 추정되어 그림 9·30 에 보여준다.
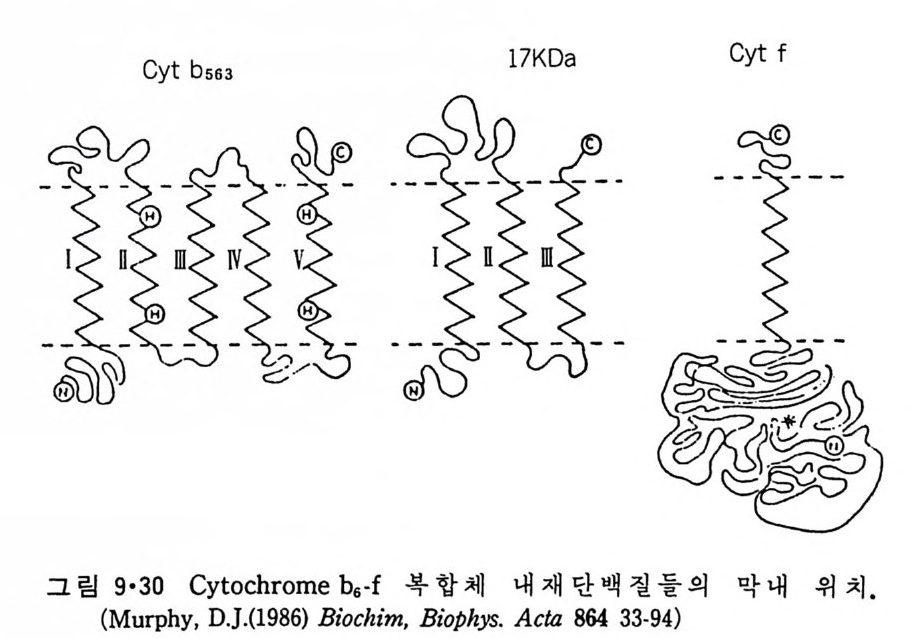 Cy t bss3 17KDa Cy t f
Cy t bss3 17KDa Cy t f
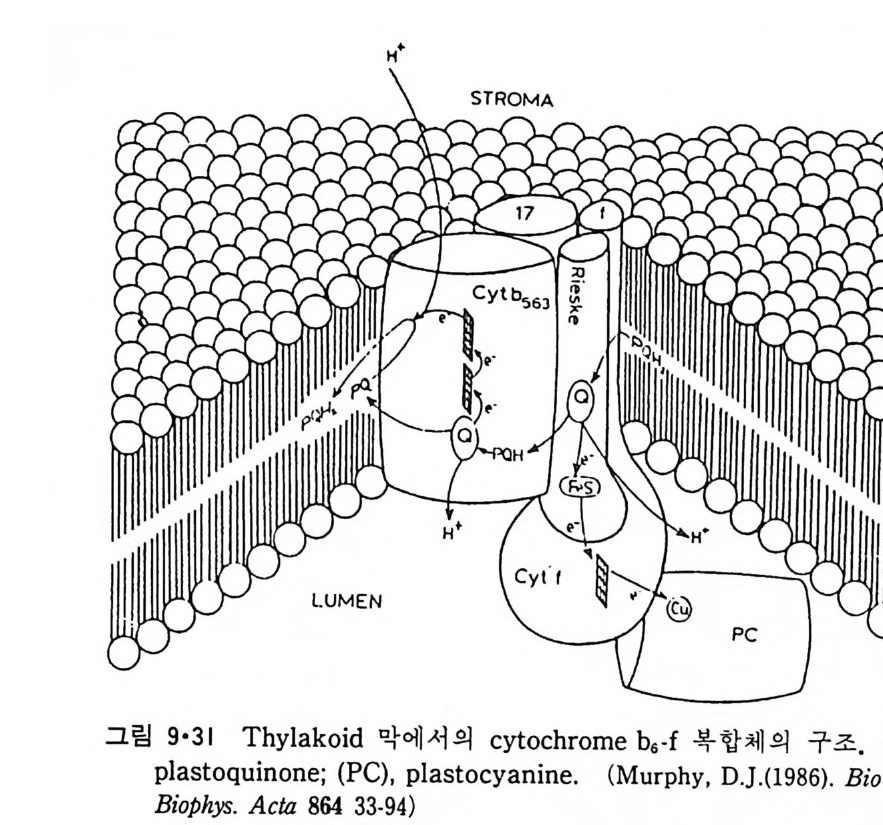 ♦
♦
그림 9·31 는 t hy lako i d 막내에서의 cy toc hrome b 다복합체의 배열을 보 여준다. Cy toc hrome f의 무게의 대부분은 lumen 에 노출되 어 pla s- t oc y an i ne 과의 상호작용을 촉진시킨다. 9·2·4 광 S y s t em I (PS I ) PS I 온 thy lako i d 엽록소의 약 3 분 1 을 차지하고 있으며 중심부 복합체 (core comp le x) 와 광채 취 복합체 (ligh t harvest comp le x I , LHCI) 가 결 합 되어 있는 거대복합체아다. PS I 중심부 복합체는 하전분리 (charge se p ara ti on) 와 전자이동에 필요 한 모든 성 분을 함유하고 있으며 2 개 의 70kDa, 1 개 의 18kDa 과 1 개 의 15 kDa 의 p ol ypepti de 로 구성 되 어 있 다. P100 reacti on cen t er 엽 록소는 2 개 의 70kDa 소단위 와 결 합되 어 있고 이 들 p ol yp e pti de 는 각각 20 개 의 엽 록 소 a 를 함유하고 있 다. 18kDa 과 15kDa 의 p ol yp e pti de 는 전 자를
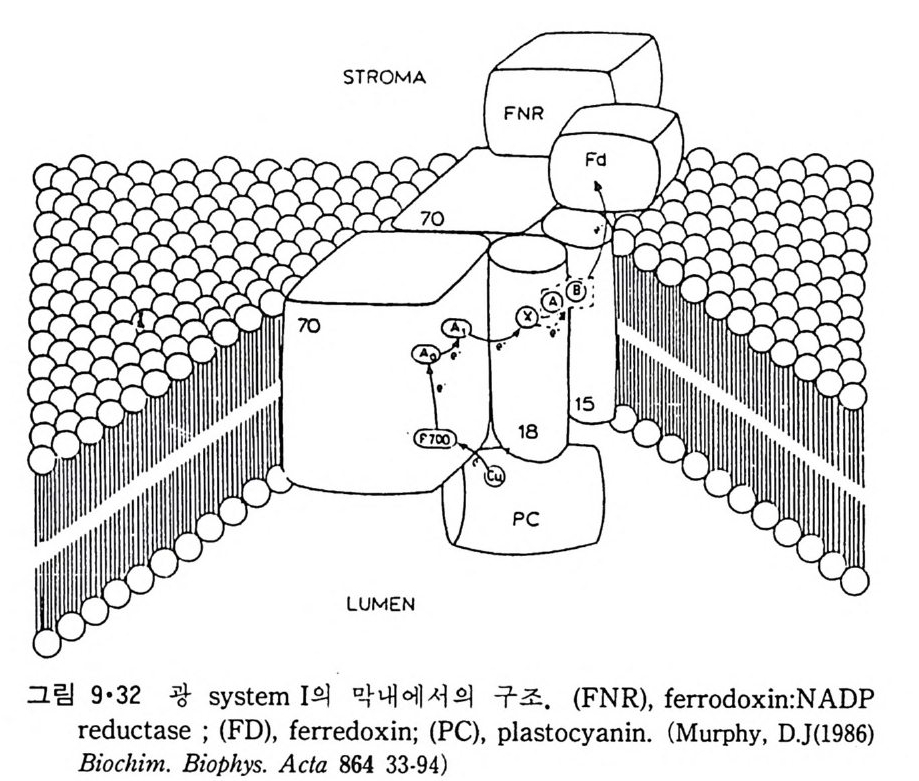 그림 9·32 광 sys t e m I 의 막내에서의 구조. (FNR), fer rodoxin : NADP
그림 9·32 광 sys t e m I 의 막내에서의 구조. (FNR), fer rodoxin : NADP
f erredox i n 으로 운반하는 역할을 한다. Ferredox i n 으로 간 전자는 fer redoxin ; NADP reduc t ase 를 거 쳐 NADP 를 환원시 키 게 되 는데 이 들 은 주변단백질이다. Ferredox i n 은 Fe2S2 를 가지고 있는 분자량이 llkDa 인 단백 질 이 고 fer redoxin ; NADP reduc t ase 는 분자량이 34kDa 인 fl avo p ro t e i n 이 다. 그림 9·32 는 t h y lako i d 막에서의 PS I 중심부분 단백질 들의 배열을 보여준다. PS I 에서 전자
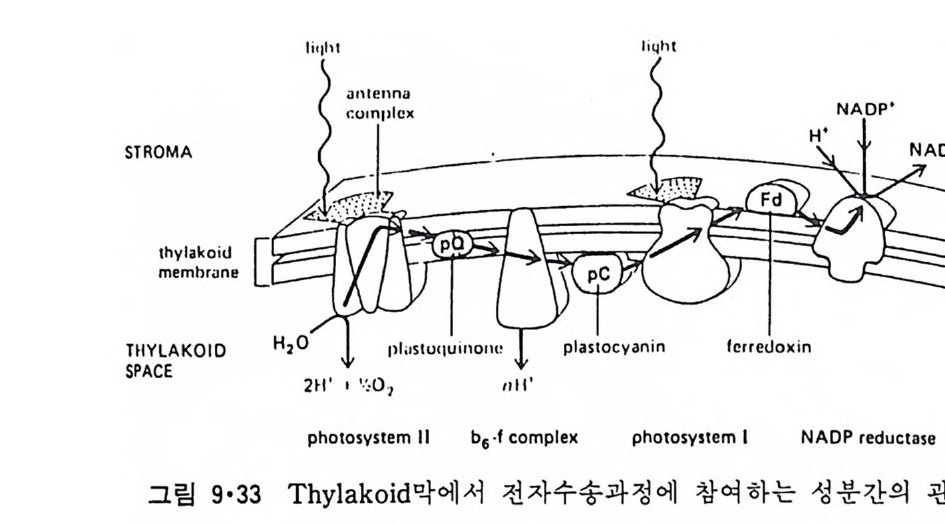 li,1 h t li4 h t
li,1 h t li4 h t
cy toc hrome b6-f 복합체 이 다. 9 • 2 • 5 ATP sy n t he ta s e 그 림 9 • 34 는 thy la koid 막 표 면 에 존 재 하 는 coup ling fac to r CF, (ATPase) 를 보여준다. M it ochondr i a 의 CF1 과 그 구조가 유사하지만 t hy lako i d 에 서 는 밖을 향하고 있 다. Th y lako i d 의 CF1 도 EDTA 등 화합 물이 존재할 때 쉽게 수용성형으로 얻을 수 있고 CF1 CF 。복합체는 세탁 제에 의해서 용해되며 이들을 인산지방질 이분자층에 재생시키면 p H 농 도 차이의 존재하에서 ATP 를 합성시킨다. CF 1 은 SDS-po lya cryl a mi de ge l 전 기 영 동 법 에 의 해 다 섯 종 류 의
 그림 9•34 엽록체 thy lako i d 막에 보이는 ATP s ynt he t ase 의 전자현미
그림 9•34 엽록체 thy lako i d 막에 보이는 ATP s ynt he t ase 의 전자현미
p ol yp e pti de 로 구 성 된 것을 알 수 있으며 그 s t o i ch i ome t r y 는 a3 /3 3 YOc2 로 생각되고 있다. CF1 의 분자량 은 325kDa 이고 그 성 분 p ol yp e pti de 의 우 게 는 a = 59kDa, /3 = 56kDa, r = 37kDa, o = 17kDa, e = 13kDa 이 다. 촉 매 와 nucleo ti de 와 결 합하는 기 능은 a 와 /3사슬에 있고 a2 /3 2 복합체 가 ATPase 활성을 갖는다. Y 소단위는 양성자의 투과 속도를 조절하며 8 소 단위는 CF, 을 CFo 에 연결하는 역할을 한다. 이들 소단위들의 상대적인 위치는 cross-lin k in g 작용제에 의해서 그림 9·35 에 보여주고 있다. 세타제에 의해서 용해된 CFl CF 。복합체는 그 분자량이 405kDa 이 되며 CF, 에 있는 p ol yp e pti de 사슬 이 외 에 분자량이 각각 17.5, 15.5, 13.5 과 8k Da 이 되는 소단위들이 있다. 이 중 9kDa 소단위는 p ro t eo lipi d 로서 아것 만이 지방질 막소포에 재구성되면 양성자를 통과시키는 것을 관찰할 수
 STRCMA -\ ’·' / p
STRCMA -\ ’·' / p
있다. 아칙까지 알려져 있는 광인산화의 과칭은 종합해 보면 an t enna( 또는 광채취)복합체에 의해 광이 흡수되면 공명 energy mechan i sm 에 의해서 광 s y s t em 의 reacti on cen t er 에 전 달되 며 거 기 의 acce pt er 를 환원시 켜 전 자가 전기음성도 (elec t rone g a ti v ity)가 감소되는 방향으로 이동되면서 동시 에 양성 자는 thy lako i d 내 부에 이 동된 다. 이 기 울기 는 th y la koid 막을 사 이에 두고 이루어지며 양자가 ATP s yn t he t ase 를 동해 이동되면서 ATP 가 합성된다. 9·2·6 Thy la koid 막에서의 단백질의 분포 Thy la koid 막 내에서의 단백질들의 분포는 동결-파열 전자현미경 방법 으로 관찰되어 왔다. 그림 9·36 은 t hy lako i d 막에 크기가 다른 IMP 들이 불균형하게 분포되어 있는 것을 보여준다. 이는 그림 9·37 에서와 갇이 t h y lako i d 가 gr ana 를 형성할 때 두 개의 막이 겹쳐지는데 동결-파열 전
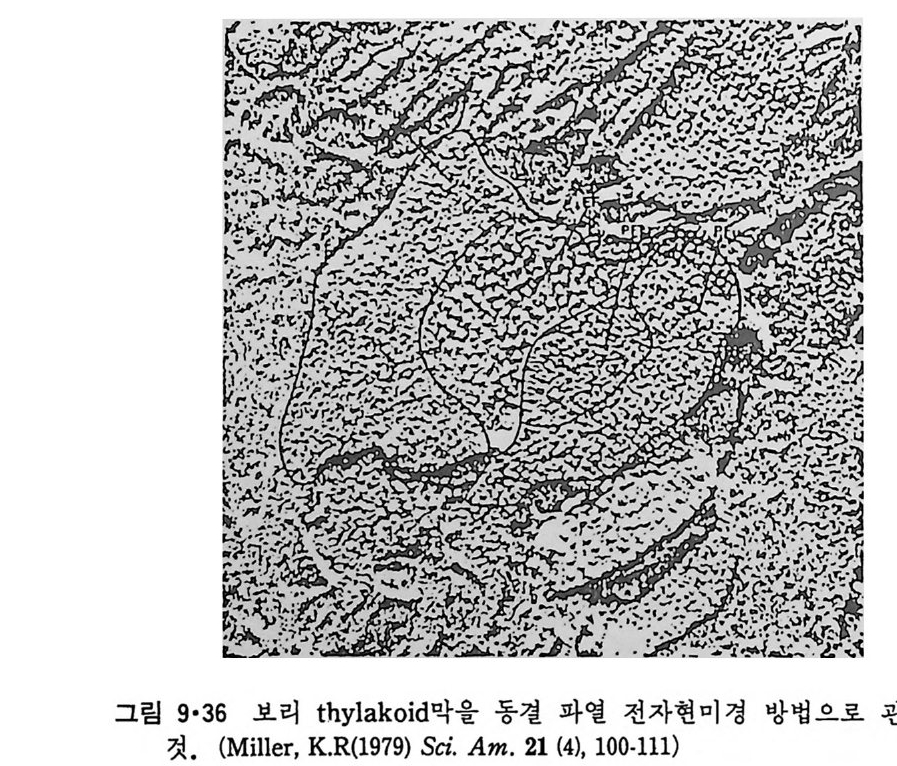 그림 9•36 보리 t h y lako i d 막을 동결 파열 전자현미경 방법으로 관찰한
그림 9•36 보리 t h y lako i d 막을 동결 파열 전자현미경 방법으로 관찰한
 그림 9•37 Th y lako i d 막에서 비대칭적인 단백질의 분포를 동결과열 전
그림 9•37 Th y lako i d 막에서 비대칭적인 단백질의 분포를 동결과열 전
자현미경 방법이 이 두 개의 겹친 막을 동시에 보여주기 때문이다. Th y lako i d 에 기 계 적 인 힘 을 가하면 무거 운 막 부분과 가벼 운 막 부분으 로 나뉘어진다. 이 무거운 부분은 gr ana 를 형성하는 두경막에서 유래한 것으로 여기에는 PSII 기능과 광채취 기능이 농축되어 있고 가벼운 부분 은 기타 부분에서 떨어져 나온 것으로 PS I 의 기능이 집중되어 있다. 그 링 9·36 에서 보이는 큰 입자는 PSII 와 광채취 복합체이고 작은 입자는 PS I 이라고 추측된다• 이것은 PSII 의 기능이나 PS I 의 기능이 없는 thy lako i d 들의 동결_파열, 전자현미 경 사진에서 큰 IMP 나 작은 IMP 가 보이지 않는 것으로도 알 수 있다. ATPase 의 활성도도 가벼운 부분에만 있다. 그림 9·38 은 이러한 무거운 부분과 가벼운 부분이 떨어져 나오는 과정과 위에 설명한 실험에 의해서 얻어진 t h y lako i d 막에서의 광 sys t e m 들의 분포를 보여준다. PS I 과 PSII 는 thy la koid 막의 각각 다론 위치
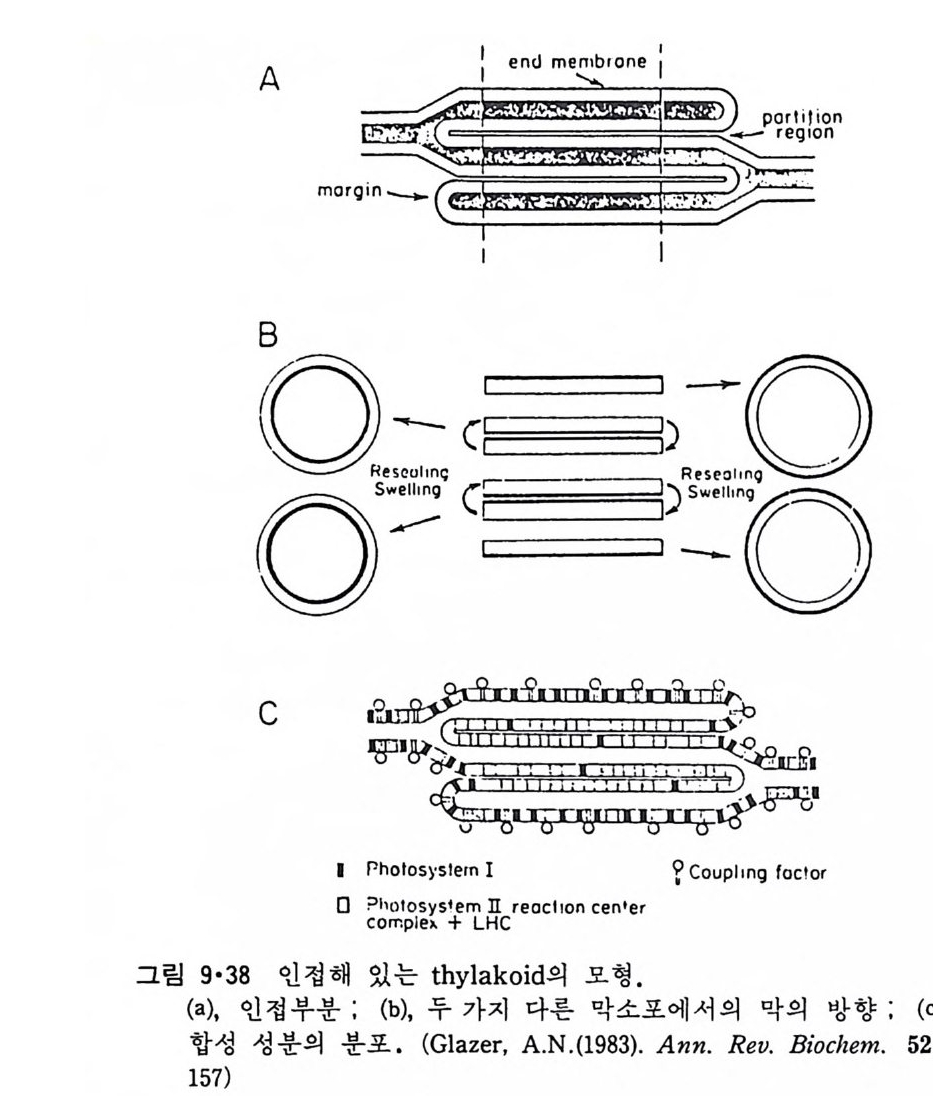 A encl membrane I’
A encl membrane I’
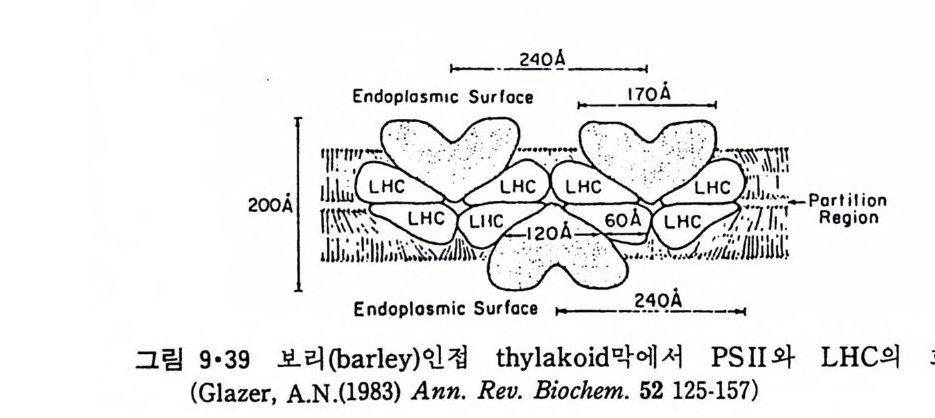 , - 240A- I
, - 240A- I
 `\\ \\_l//\\\\l\|| ,
`\\ \\_l//\\\\l\|| ,
에 격리되어 있다. 여러가지 실험을 동해서 광채취 복합체가 gr ana 를 형 성하는 데 필요한 것이 판명되었고 이들이 어떻게 회합하여 gr ana 에서 두 개의 막을 접촉하느냐 하는 model 을 그림 9·39 에 보여준다. LHCII 가 t h y lako i d 를 겹쳐 gr ana 를 형성하며 단백질들의 불균일한 분포를 갖 는 것은 LHCII 로 재구성된 막소포가 유사한 성질을 갖는 것으로 확인이 되었다. 9 · 3 호홉 세 균막에 서 의 ener gy전 이 12) 13) 호홉 세균의 원형질막에서도 m it ochondr i a 막 내에서와 유사한 산화적 인산화로 ATP 가 합성되는데 전자전달시 일어나는 양성자 p um pi n g에 의 해 생성된 양성자 농도 기울기는 ATP 합성과 2 차 능동수송에 아용될 뿐 만 아니라 靴毛(fl a g ella) 를 회전시켜 세균이 움칙이게 하는 데도 쓰인다 (그림 9·40). E. col i와 같은 세균의 편모는 filam ent, hook .:z.리고 기 처 (basal) 가 연 결된 것인데 기저구조가 세포표면에 부착된 이 부분을 세탁제로 용해하 여 전자현미경으로 보면 그림 9·41 에서 보이는 것과 같은 4 개의 고리가
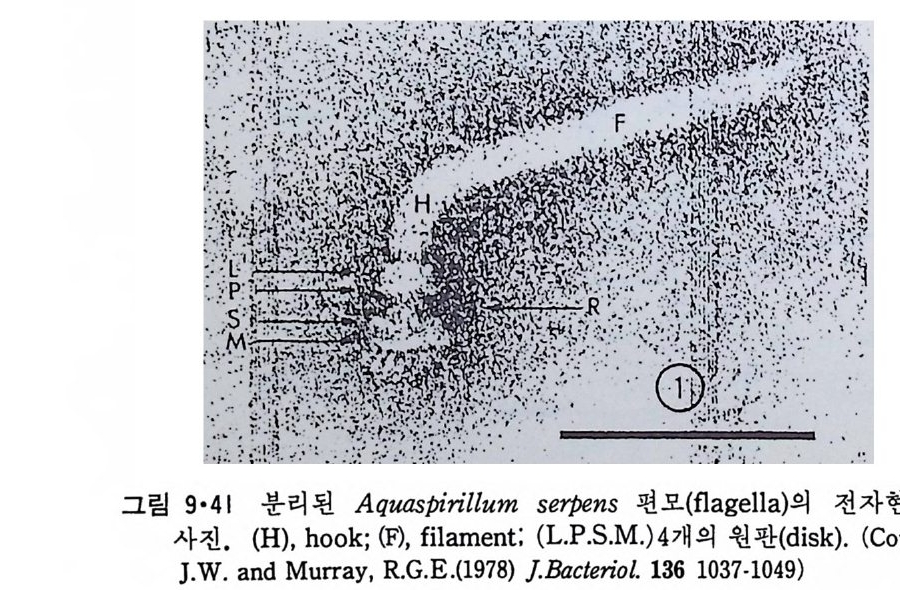 ' 그 4 ; 다 .l.,. _ · ·누 .•• : ~ , •• , 노 · · · ·, , • ..:..- - • ,·.~ . • ···, . _. ·- ·
' 그 4 ; 다 .l.,. _ · ·누 .•• : ~ , •• , 노 · · · ·, , • ..:..- - • ,·.~ . • ···, . _. ·- ·
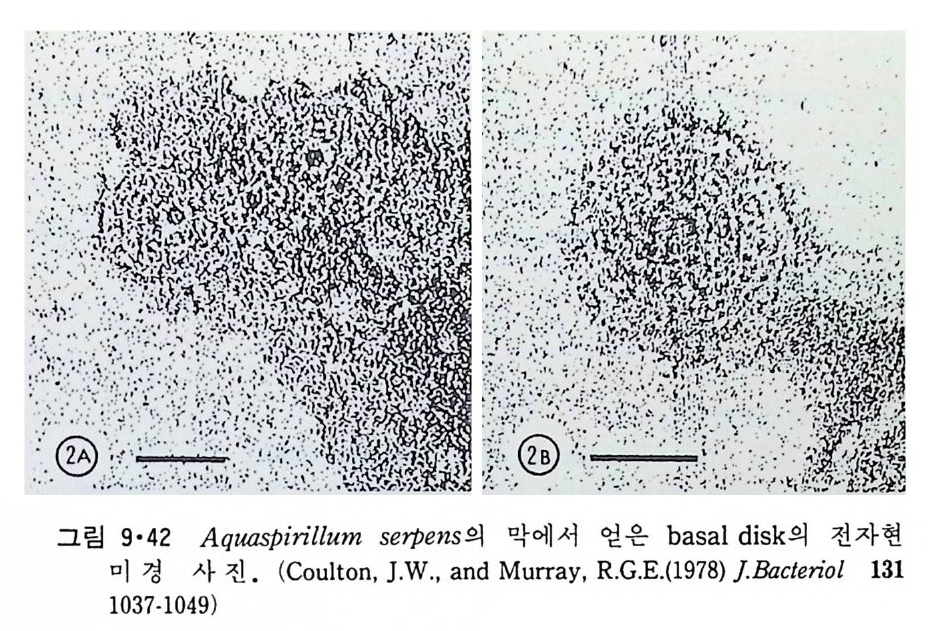 그림 9·42 Aq u asp irillu m se rp ens 의 막에서 얻은 basal d i sk 의 전자현
그림 9·42 Aq u asp irillu m se rp ens 의 막에서 얻은 basal d i sk 의 전자현
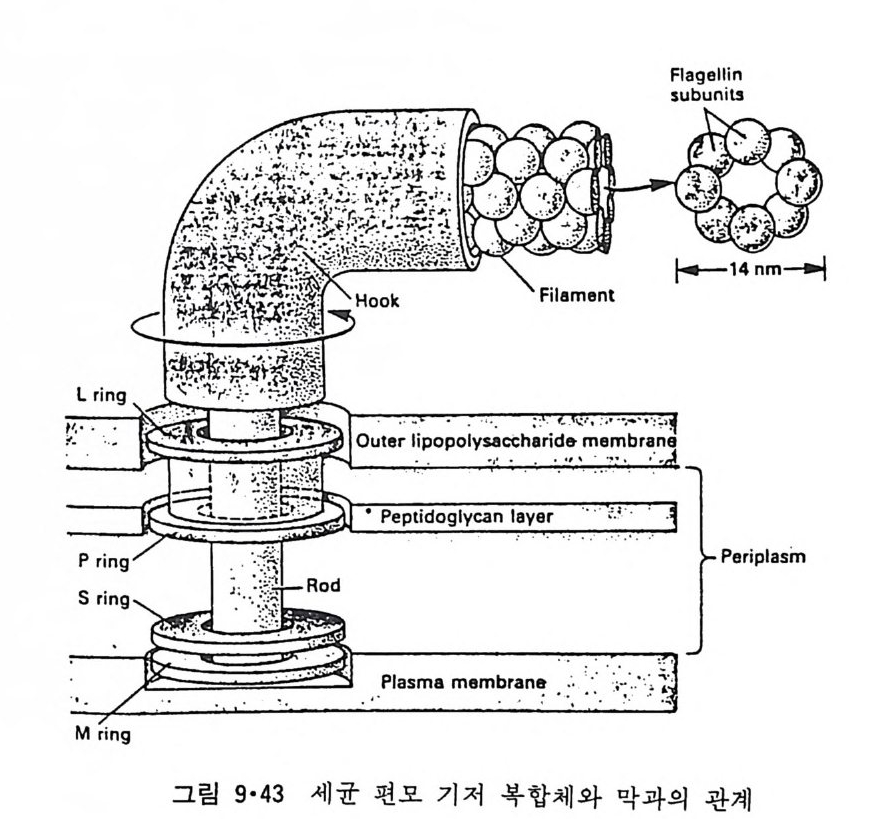 Flag e llin
Flag e llin
연결되어 있고 이 고리는 여러 개의 단백질 소단위로 이루어졌다(그림 9·42). 이러한 전자현미경의 사용에 의해 얻은 model 은 그림 9·43 에 보 여진다. 아직도 이들의 세부적인 구조와 세균막과의 관계는 찰 모르며 더우기 p H 기울기가 어떠한 mechan i sm 을 통하여 편모를 회전시키는 방식은 밝 혀지지 않았다. *9 장 참고문헌 (1) Hink le, P.C . AND McCart y, E. (1978) Sc i. Am. 238(3), 104-123. (2) Whit tak er, P.A. and Danks, S.M . Mi toc hondna Str u cft, r e, Functi on and Assembly, Long ma n, N.Y. 1979. (3) Fil ling a me, R.H. (1980) Ann. Rev. Bio c hem. 49 1079-1113. (4) Tzago loff , A. Mi toc hondri a, Plenum N. Y. 1982. (5) Hate f i , H., Rag a n, C.Z. and Galante , Y.M . in Marto noi, A. (ed) The Enzym e s of Bio l og ica l Membranes, Vol. 4. 2nd ed. Plenum, N.Y. 1985. (6) Hate f i , Y. (19 85) Ann. Rev. Bio c hem. 54, 1015-1068. (7) Mi ller , K.R. (19 79) Sc i. A m. 241(4), 100-111 . (8) Malkin , R. (1982) Ann. Rev. Pla ,n t Phys i o l. 33, 455-479. (9) Cog d ell, R.J. (1983) Ann. Rev. Pla ,n t Phys iol. 34, 21-43. (IO) Glazer, A,N. (1983) Ann. Rev. Bi oc hem. 52, 125-157. (10 Murph y , D.J. (1986) Bio c him . Bio p h y s . Acta . 864,33-94. (12) Berg. H. (19 75) Sci, Am. 233(2), 36-44. (13 ) Macnab, R.M . and Ai za wa, S.I . (19 84) Ann. Rev. Bi op h y s . Bio e ng. 13, 51 -73.
제 10 장 생체막의 융합 생체막은 지방질과 단백질로 구성된 막이 밀폐된 액포를 형성한 것으 로 생체막 내에서 성분들이 유동성을 가지고 있을 뿐만 아니라 막소포 자체도 신축성을 가지고 있어 한 액포가 두 개로 나누어지기도 하고 두 개 이상의 액포가 합쳐 한 막소포를 형성하기도 한다(그림 10·1). 이렇 게 갈라지거나 합칠 때 막 사이의 접촉부분에는 막 구조에 근본적안 변 화가 일어나는데 이러한 현상을 막 융합 (membrane fu s i on) 이라고 하고 이 는 생체 내에서 많은 중요한 기능의 기본이 되고 있다. 생체내에서 자발적으로 일어나는 막 융합은 크게 나누어 세포의 융합 과 세포 내에서의 융합으로 구분할 수가 있다. 원형질막 사이의 융합은
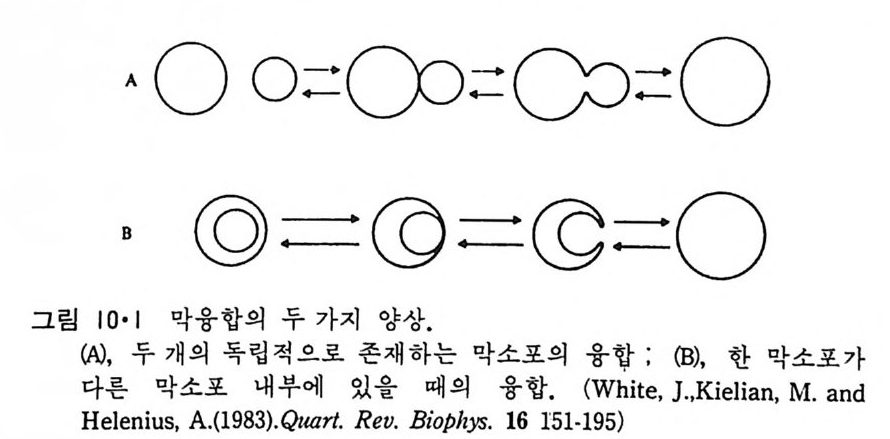 A O o 二〈〉 3 二〈〉 3::O
A O o 二〈〉 3 二〈〉 3::O
비교 적 드문 데 이의 예 로서는 세 포분열 , 정 자와 난자 사 이에의 수 정, 근 원세포 (m y oblas t)가 다 핵 세포로 되는 과정, 미 소 식세포 (m ic ro p ha g e) 융합 과 피 막성 (envelo p ed) v i rus 가 세포 를 감 염시키 는 과정을 들 수 있다. 세 포 내에서의 융합에는 endocy tos is , exocy tos is 그리고 내재단백 질 의 수 송의 전과정 동이 존재하며 이 과정 은 생체 내에서 대단히 활발히 진행 되고 있다. 10·l 세포의 융합 1) - 5) 세포의 유사분열이나 감수분열은 대단히 복잡한 과정인데 한 세포가 분열이 되어 두 세포로 되려면 그 원형질막도 갈라져야 되기 때문에 원 형질막의 융합과정을 거쳐야 한다. 그림 10·2 는 세포분열의 마지막 단계 인 세포질분열 과정을 보여준다. 이 그림에서 세포의 중앙부가 좁아지고 있는데 이 부분의 원형질막 바로 아래에 미세단섬유 (m ic ro fil amen t)가 일 집되어 있는 것으로 이 원형질막을 졸라매는 과정예 세포골격이 가담하 고 있는 것으로 추측이 되고 있다. 한편 핵막은 세포분열의 그림 10·3 에 서 보여주는 것과 같이 일단 막소포로 분해되었다가 세포분열 후 다시
 그림 10·2 분열되고 있는 쥐알의 전자현미경 사진. 화살표는 세포분열
그림 10·2 분열되고 있는 쥐알의 전자현미경 사진. 화살표는 세포분열
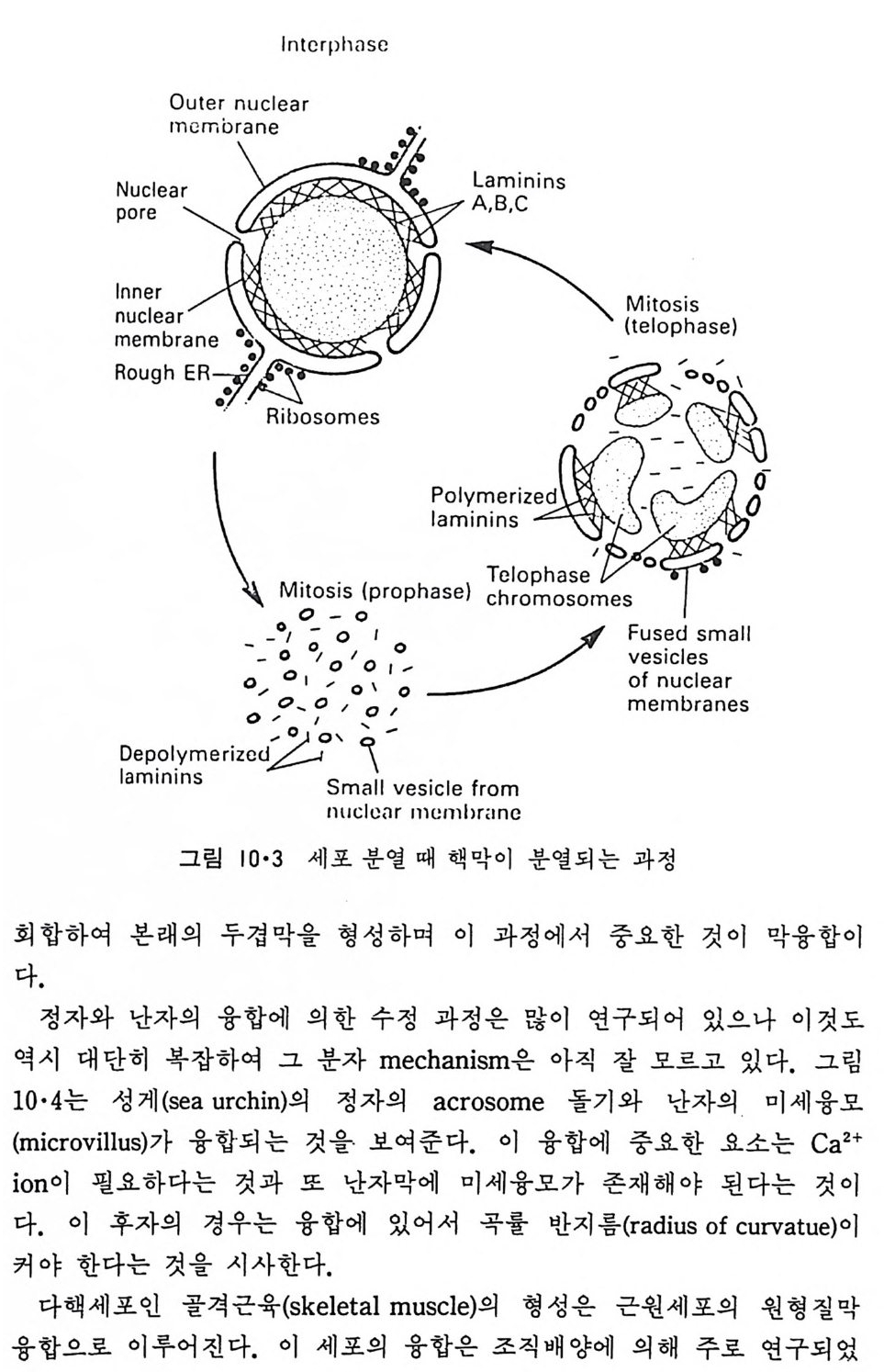 lnt cr p h o sc
lnt cr p h o sc
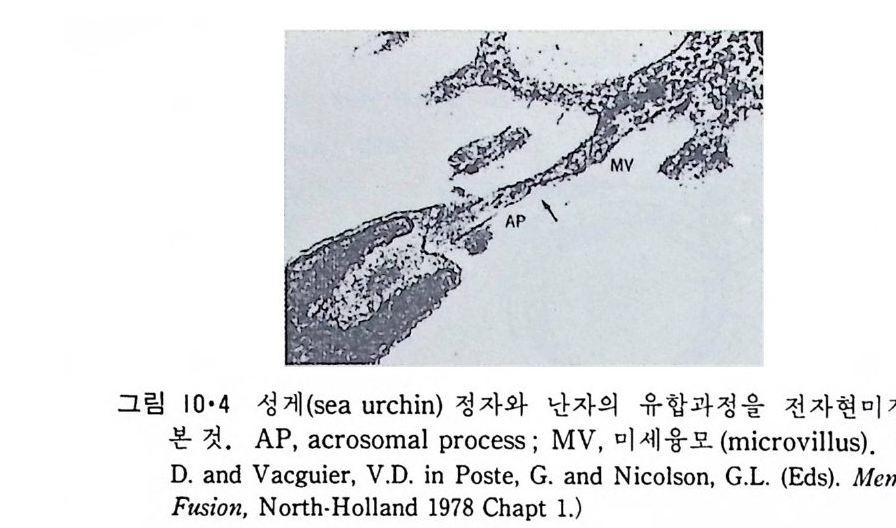 , -.zr
, -.zr
는데 이들은 처음에 자승속도 (ex p onen ti al ra t e) 로 번식하고 그 동안에는 융합이 일어나지 않는다. 번식이 어느 정도에 도달되면 융합이 시작되는 데 유사한 근원세포끼리에만 일어나며 일정 수의 세포가 융합되어 m y o t ubule 을 형성한다. 이때에도 Ca2 + 이 필요하며 융합을 위해 접촉되 는 원형질막들 근처에서 IMP(in t r a membraneus p a rti cle) 가 회합과 동시에 제거되어, 즉 접촉면에는 지방질 이분자층만이 남게 된다. 피막성 (envelo p ed) v i rus 가 숙주세포 (hos t cell) 에 침입하는 것도 원형질 막 사이의 융합에 포함시킬 수 있다. 피막성 v i rus 는 Sendai vir u s, inf l ue nza v i rus 와 같이 생체막으로서 둘러싸인 v i rus 로서 이들이 숙주세 포에 들어가는 과정은 그림 10·5 에서 보이는 것과 같이 두 가지가 있다. 처음 것은 (A) 원형질막과 v i rus 의 피막이 직접 융합되는 것이고 둘째 것 온 (B) endoc yt os i s 에 의한 것이다. 직접 융합하는 것은 p H 에 의존되지 않지 만 endoc yt os i s 에 의 한 과정 에 는 endosome 이 나 lys o some 내 부의 p H 가 낮아져서 일어난다. 막 융합에 의 해 v i rus 가 숙주세 포에 침 입 하는 경 우 v i rus 막과 숙주세 포 의 원형질막이 융합될 뿐만 아니라 숙주세포끼리의 융합도 일으킨다. V i rus 에 의한 세포융합의 연구가 가장 많이 된 것이 Sendai v i rus( 또는 HVJ , hemog glu ti na ti ng vir u s of J a p an) 로서 이 v i rus 가 세포융합을 일으키 는 과정은 그림 10·6 에 보여준다. 그림 10·7 은 Sendai v i rus 가 적혈구막 과 융합하는 초기단계를 보여준다. 그림 10·8 에 보이는 것과 같이 HVJ
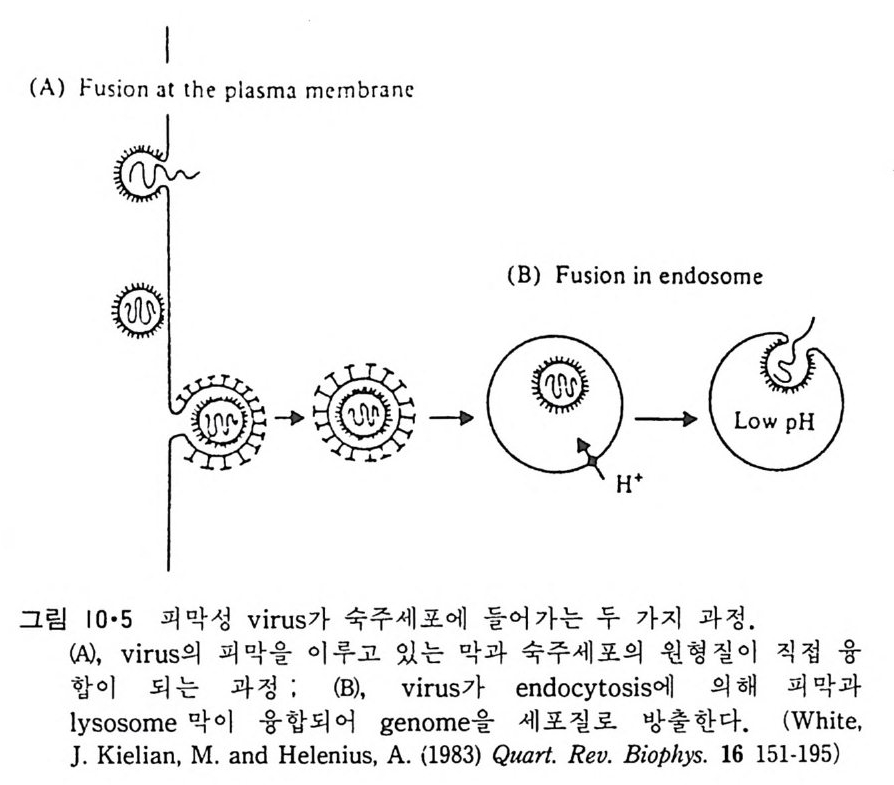 (A) fu sio n at th e pla sma membrane
(A) fu sio n at th e pla sma membrane
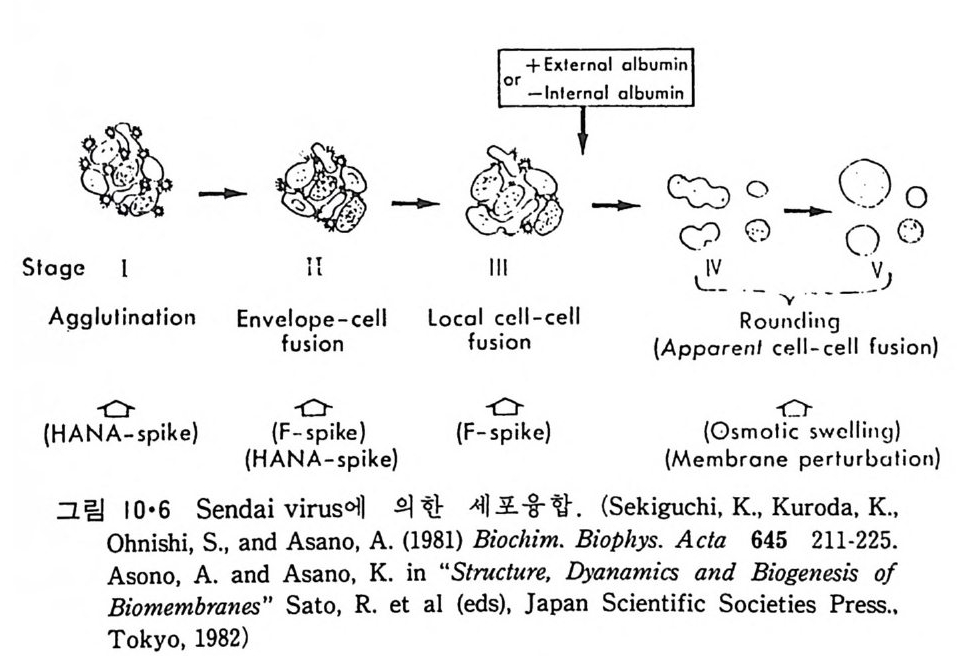 ar +-I Enxtte e r r nnaal l aalblbuummi i nn
ar +-I Enxtte e r r nnaal l aalblbuummi i nn
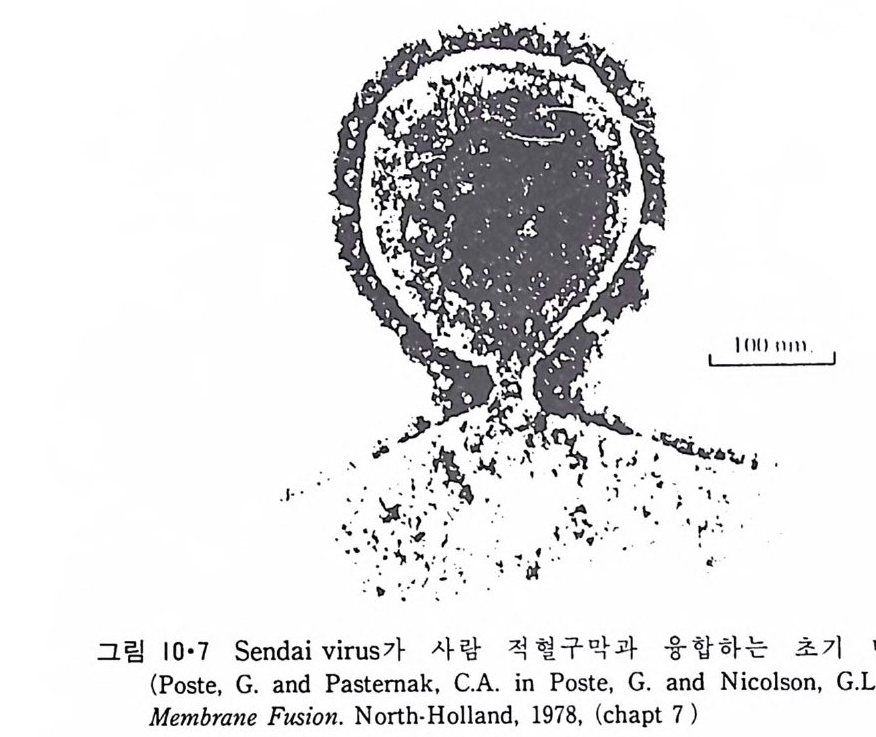 I l '· I
I l '· I
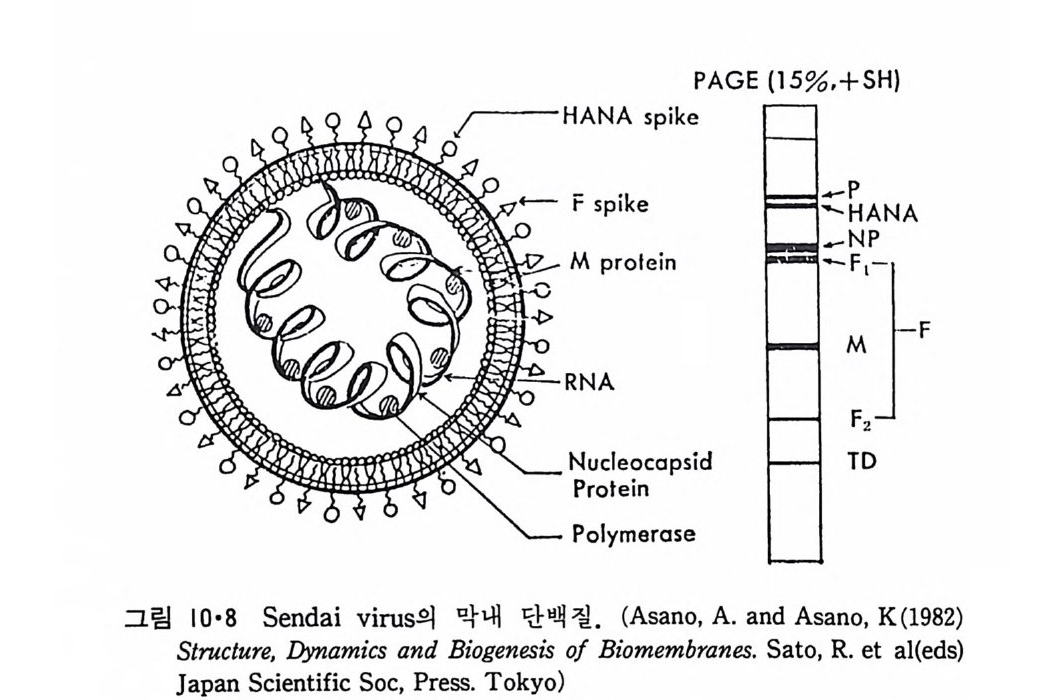 PA GE 雪그-+SPHA HlNPNAF l MF
PA GE 雪그-+SPHA HlNPNAF l MF
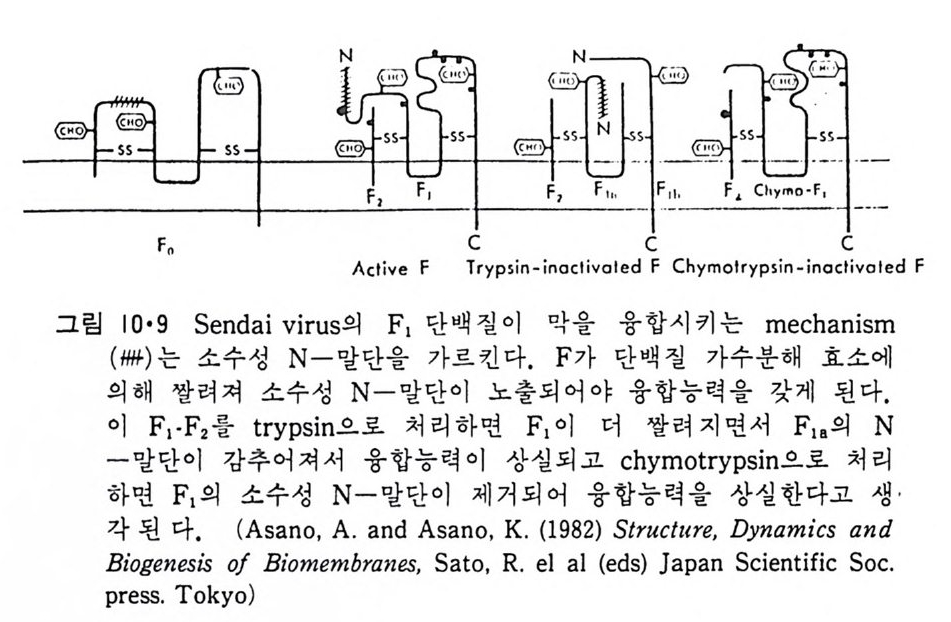 F 。 C C C
F 。 C C C
피 막에는 적 혈구 옹집 반응성 (he mag glu ti na ti ng ac ti v ity ) 과 neurami ni d a se 의 기능을 가진 HANA 단백질과 융합에 가담하는 F 단백질이 존재한다. F 단백질을 /3- mercap toe th anol 존재 하에서 전기영동을 하면 F1 과 F2 의 두 개의 band 로 나타나지만 이 두 가지 단백질이 동시에 있을 때 융합을 야기시킨다. F 단백질은 분자량이 53kDa 이며 생합성때 Fo 인 하나의 p ol yp e ti de 가 생성되었다가 이것이 단백질 가수분해 효소에 의해서 R 과 F 루 끊어지지만 이들은 -s-s-결 합으로 연결된 상태로 막에 존재한다. 이 중 E 의 N - 말단은 약 15 개 의 소수성 am i no 산으로 구성 되 어 있고 이 부분이 제거되면 융합의 기능을 상실하는 것으로 보아 이 am i no 산 서열 이 융합에 중요한 것임을 알 수 있다(그림 10·9). 이 렇 게 v i rus 피 막이 원형 질막과 직 접 융합하는 것은 p aram y xov i rus 에 국한되 고 나머 지 동물 피 막성 v i rus 는 endoc yt os i s 에 의 해 서 endosome 으 로 둘러싸인 채로 세포 내에 들어간다(그림 10·5). Endosome 내부의 p H 는 세 포 액 의 pH 보 다 낮은 데 이 러 한 낮은 pH 에 서 만 피 막과 endosome 막이 융합되어 v i rus 의 g enome 이 세포액으로 들어가게 된다. 그림 10·10 는 몇가지 피막성 v i rus 막과 융합이 일어나는 정도와 p H 와의 관계를 보여준다. 여기서 Sendai v i rus 는 p H에 영향을 받지 않고, 나머 지는 pH 6 이하에서 융합이 일어나는 것을 볼 수 있다.
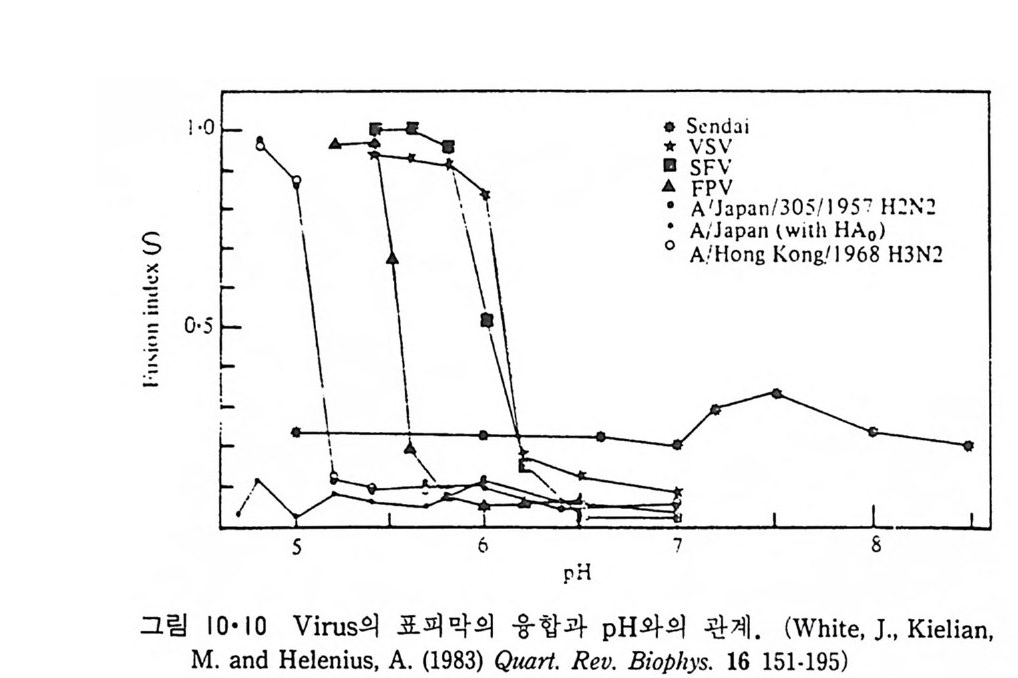 1·0 \ i ?\ •* Svrsndva 1
1·0 \ i ?\ •* Svrsndva 1
Endoc yt os i s 에 의해서 숙주세포에 침 입하는 vir u s 중에서는 inf lue nza v되 i r고us 가p H 제가일 낮 을많 이때 에연는구 되융었합다에.` 의이해 v i칙 ru접s 는 세중포성에 p들 H어 에가서며는 또en dliopcoy s tooms ies 과도 융합을 한다. 이 v i rus 의 막에는 두가지 sp ike 당단백질(g l y co p ro t e i n) 이 있는데 (그림 10·11) 이중 NA 는 neuram i n i dase 이고 HA 는 적
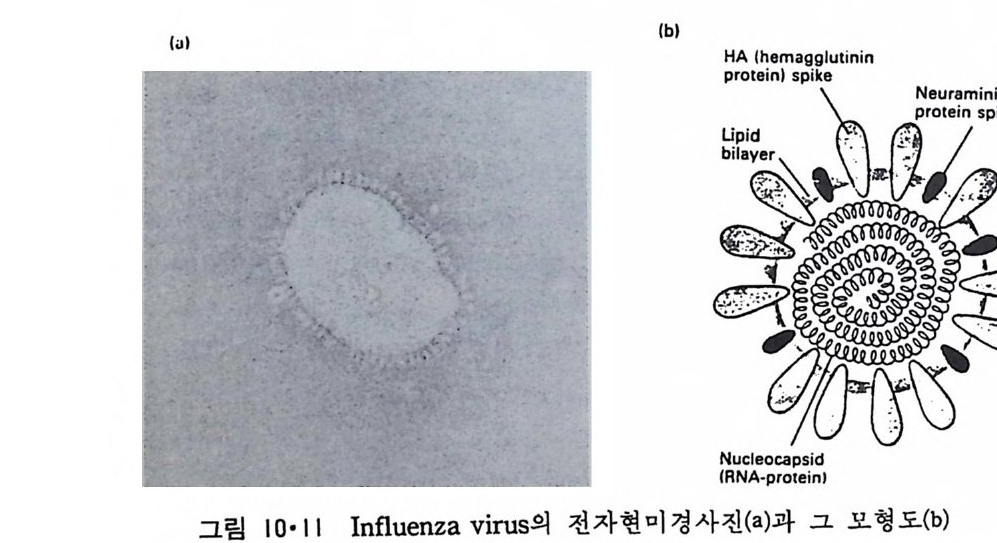 (al (b,
(al (b,
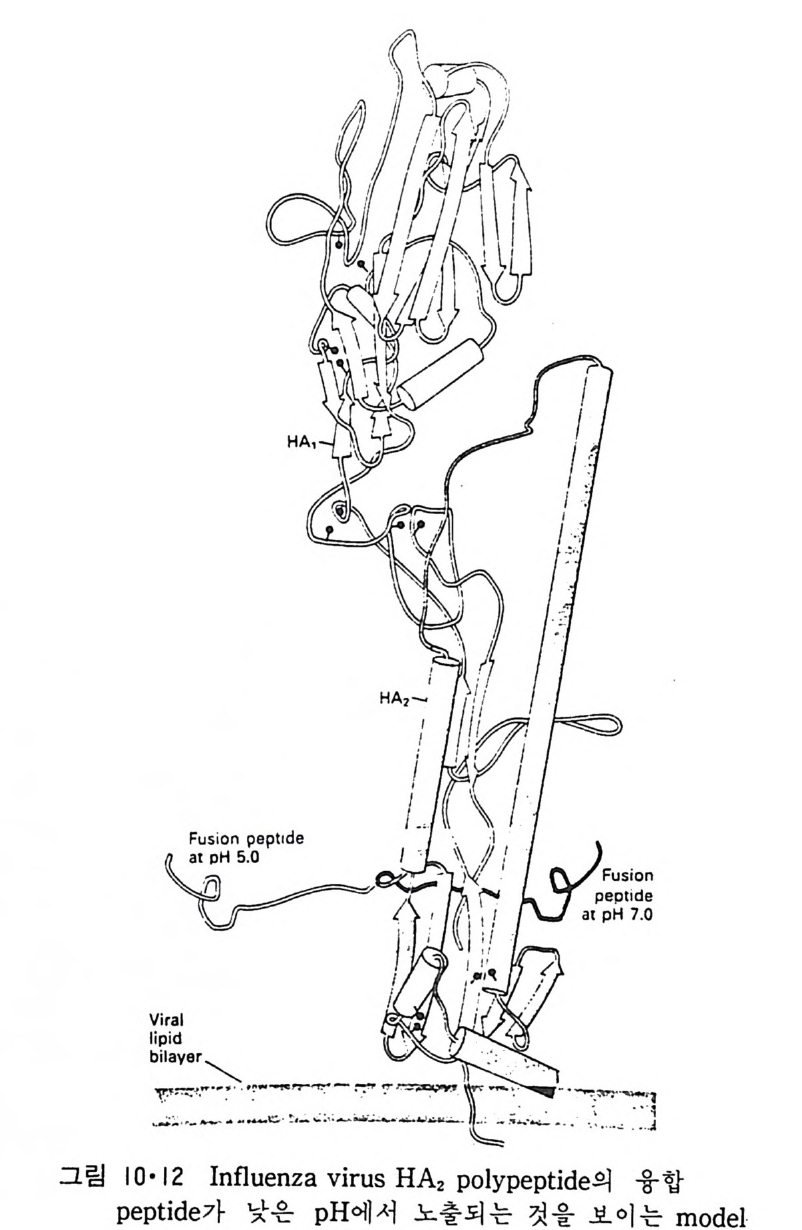 HA
HA
혈구 응집반응성과 세포를 융합시키는 기능을 함게 가지고 있다. HA 는 gp ol y lycop pe et ipdtei d e사 인슬 (HHAA1o 과 가 H A2단)백 로 질찰 려가졌수으분나해 이들효이소 에- s-s의- 해결 서 합 으두로 개연 결의 된 것 이 다. 3 개 의 HA1-HA2 단위 가 회 합하여 막에 서 삼합체 (tri mer) 를 이룬다. 이 삼합체는 피막 밖으로 약 130A 정도 돌출되어 s pi ke 를 형성
한다. 이 v i rus 를 bromela i n 으로 처리하면 HA2 가 지방질 이분자 층 에 들 어가는 지점 근처에서 끊어져 BHA 단위를 형성하는데 이는 HA 무게의 약 95% 를 차지하는 p ol yp e pti de 로서 물에 녹기 때문에 결정을 얻을 수가 있어 3A 해상도 (resolu ti on) 까지의 X 광선 회절분석이 되어 있다. 이 BHA 의 성질 등에서 중요한 것은 p H 가 낮을 때 구조가 변경되어 소수성인 표면을 노출시키는 것이다(그림 10·12). 이것은 낮은 p H 에서 Trito n X -100 같은 세탁제가 결합되고 또 lip osome 에도 결합되는 것으로 알 수 있 다. 그림 10·13 은 BHA 가 lip osome 에 결합되는 정도가 이 v i rus 에 의한 세포융합이 p H에 따라 변하는 것을 비교한 것이다. 아러한 현상과 융합 과의 관계는 아직 자세히 모르는 형편이다. Seml iki Forest v i rus(SFV) 도 inf l ue nza v i rus 와 유사한 융합성 질을 가 겼는데 중성 p H 에서는 endoc yt os i s 에 의해 숙주세포에 들어가고 낮은 p H 에서는 융합에 의해 세포로 들어가며 lip osome 과도 융합한다. 이때도 spi ke 당단백질에 의해서 융합이 이루어진다. 이렇게 소수성 말단 서열이 단백질 가수분해 효소에 의해 생성되거나
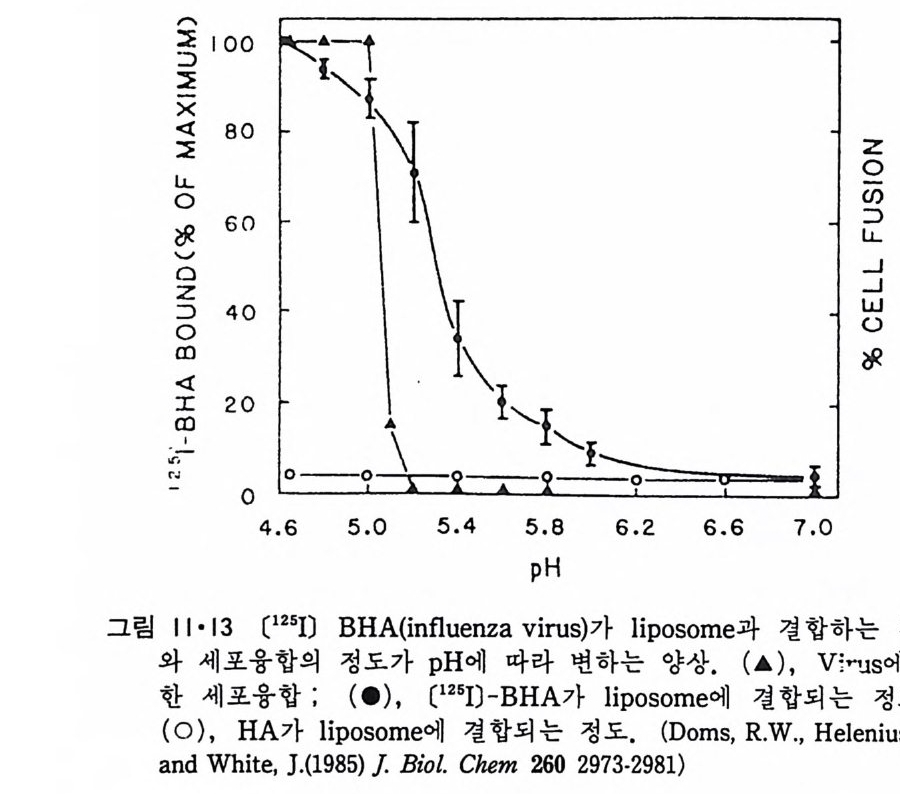 (ri
(ri
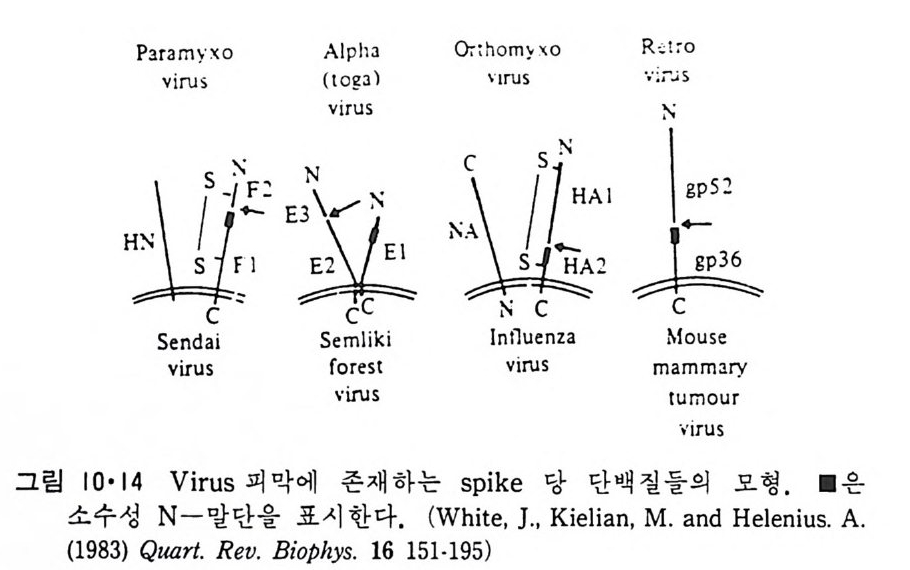 Parvarmuys x o (Atlop2 hJ 3 ) Cr.:h `.oIrmu s i , XO R···;,:;r t j ~ S o
Parvarmuys x o (Atlop2 hJ 3 ) Cr.:h `.oIrmu s i , XO R···;,:;r t j ~ S o
이미 존재하거나 하는 것은 여러 vir u s 피막단백질의 공통된 현상이다. 이것은 그림 10·14 에 보여주며 그림 10·15 는 이들의 am i no 산 서열을 보 여준다. 특히 이들 중 과반수가 낮은 p H 에서 그 소수성인 부분을 노출 시키는 것이 주목할 만한 것이다., V i rus 가 원형질막과 융합하여 그 g enome 을 세포액에 침입시킬 때에는 숙주세포 사이의 융합도 야기시켜 커다란 다핵세포 (mul ti nuclea t edcell) 를 형성시킨다. 그래서 이것을 이용해서 자외선 조사(i rrad i a ti on) 등으로 g enome 이 파괴된 v i rus 를 이용하여 세포끼리 융합시키는 연구가 많이 진행되고 있다. 이 이외에도 많은 융합작용제(fu so g en i c a g en t)가 보통 상 태에서는 융합이 안되는 세포융합에 이용되고 있다. 이들 융합작용제에 는 NaN03, Ca2+ 동 무기 물과 po lye th y le ne gly c ol( PE G), lys o lec ithi n , 세 탁제 등이 있다. 또 작은 인지방질 막소포도 좋은 융합작용제이다. 물리적인 세포융합 방법으로는 짧고 강한 전기 p ulse 에 의해 텃 가지 세포융합이 이루어졌으나 그 mechan i sm 은 아직 밝혀지지 않고 있다. 10·2 세포내에서의 융합 6)-8) 원형질막을 동한 물질의 이동은 주로 용해확산, 촉진확산, 또는 능동
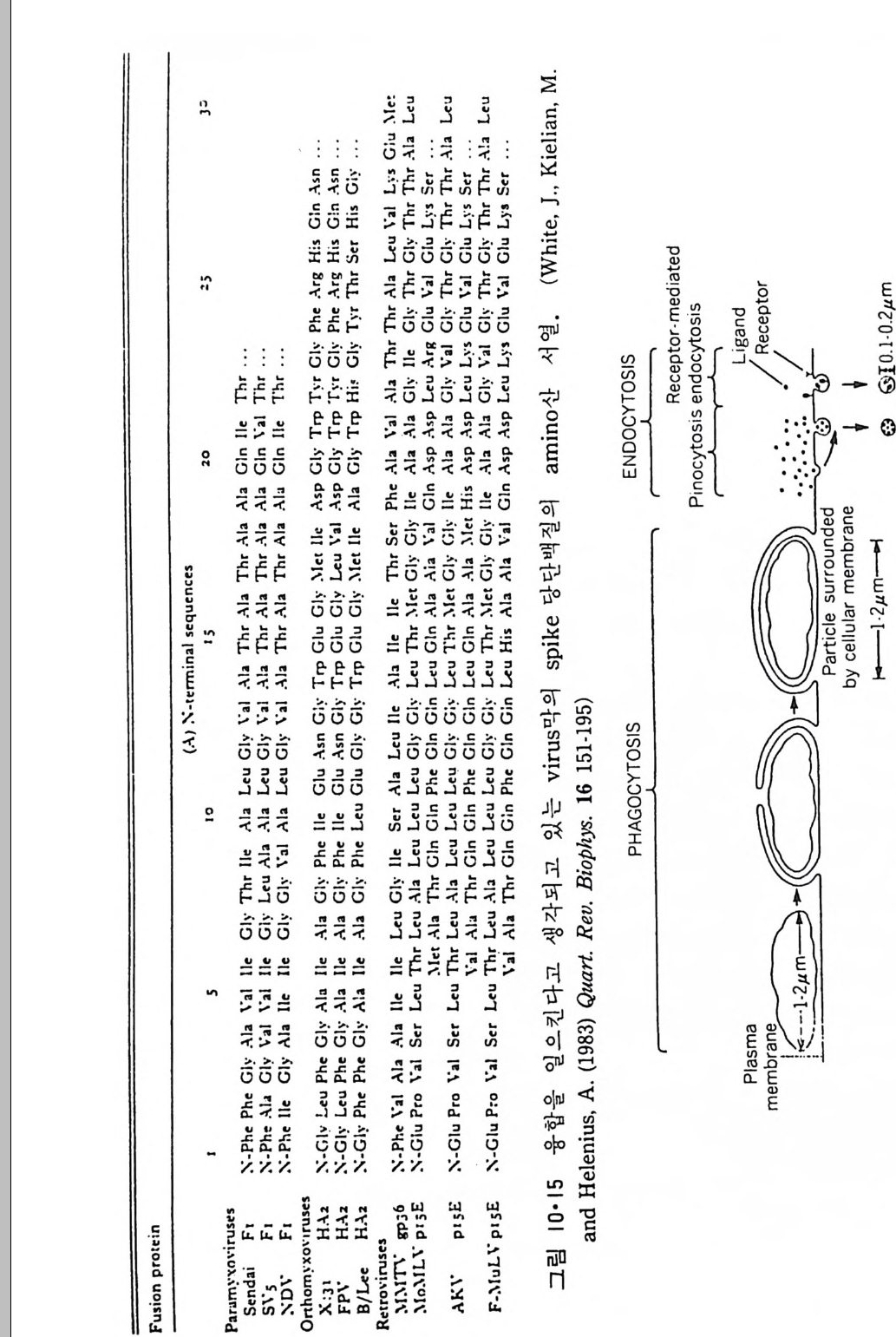
수송에 의해서 이루어지지만 큰 입자나 또는 세포 외부의 용액까지도 대 량수송에 의해서 세포내부로 이동될 수 있다. 이 과정에서 원형질막이 세포 안쪽으로 주머니를 형성한 후 이것이 막융합에 의해 원형질막에서 떨어져 나와 세포내부에 들어오게 된다. 이러한 대량수송에는 그림 10· 16 에 보 이 는 것 과 같 이 ph ag o cy tos is , pi noc yt os i s 와 수용 체 에 의 한 (recep tor -media t e d ) endocy tos is 세 종류가 있는데 pi noc yt os i s 와 수용체에 의 한 endoc yt os i s 를 endoc yt os i s 라고 통칭 한다. Pha g oc yt os i s 는 ameba 나 macro p ha g e 등 세포가 세균이나 쪼개진 세포 등 큰 입자를 흡수하는 과정으로 그 mechan i sm 은 아직 찰 알려저 있지 않다. 큰 입자가 원형질막과 접촉되면 이 부분의 원형질막이 넓어지면서 입자 를 완전히 둘러 싼 후 융합에 의해 세포질에 끌려 들어와 다시 융합 으로 li sosome 내부로 들어 가 가수분해되 어 영 양분으로 이용된다. Pha g oc yt os i s 에 는 원 형 질 막 바로 아래 에 존재 하는 미 세 성 유 (m i cro fil a men t)가 가담한다. 이때에 ATP 형의 ener gy가 필요하고 cy toc halasin B 와 같은 물질로 저해되는 것으로 보아 세포골격 (c yt oskele t on) 이 이 과정
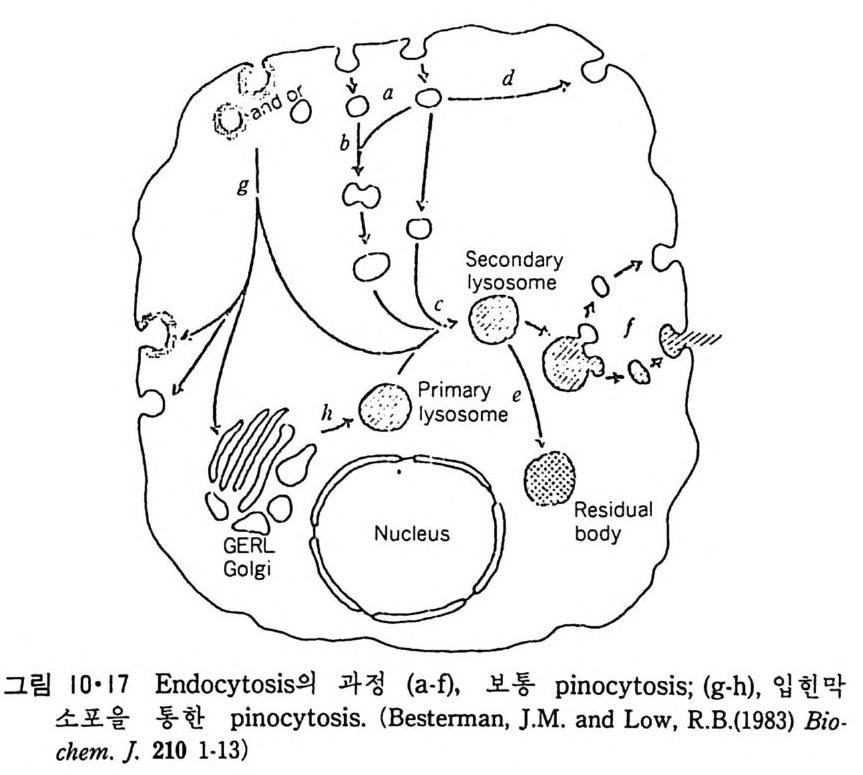 Ollll\/I_\\l/P
Ollll\/I_\\l/P
에 중요하다는 것을 알 수 있다. 그림 10·17 은 pi noc yt os i s 의 과정을 보여주는데 이때에도 내부화 (i n t ernal i ze) 되 는 과 정 에 서 원 형 질 막으로 감싸 생 성 된 endocy tos is 막소포 는 l y sosome 과 융합되어 그 내부로 들어가 가수분해된다. 이렇게 pi noc yt os i s 는 선택성이 없는 데 비해 입힌 막소포 (coa t ed vesic le ) endoc yt os i s 는 그 선택성 이 크다. 원형 질막 표면에 있는 입 힌구 멍 (coa t ed pit)의 세포질을 향한 표면에는 격자 (la tti ce) 구조가 있고 반대쪽 에는 수용체가 존재하여 (그림 10·18) 특정한 단백질이나 입자와 결합하 여 endoc yt os i s 를 시킨다. 이 과정예 의해 세포 안으로 들어오는 물질들 은 처장단백질, 항체, 단백질 hormone, tra nsfe rrin 둥이다. 그림 10·18 은 입힌 구멍 (coa t ed pit)에서 주머니가 형성되고 이것이 융합과정을 거쳐 입힌 막소포로서 세포 내로 떨어져 나오는 과정을 본 것이다. 입헌 구멍 (coate d pit)의 세포질 쪽의 원형 질막 표면과 입 힌 막소포 바깥표면에는 분자량이 180kDa 이 되는 단백질인 cla t hr i n 이 중합으로 격자구조를 형성
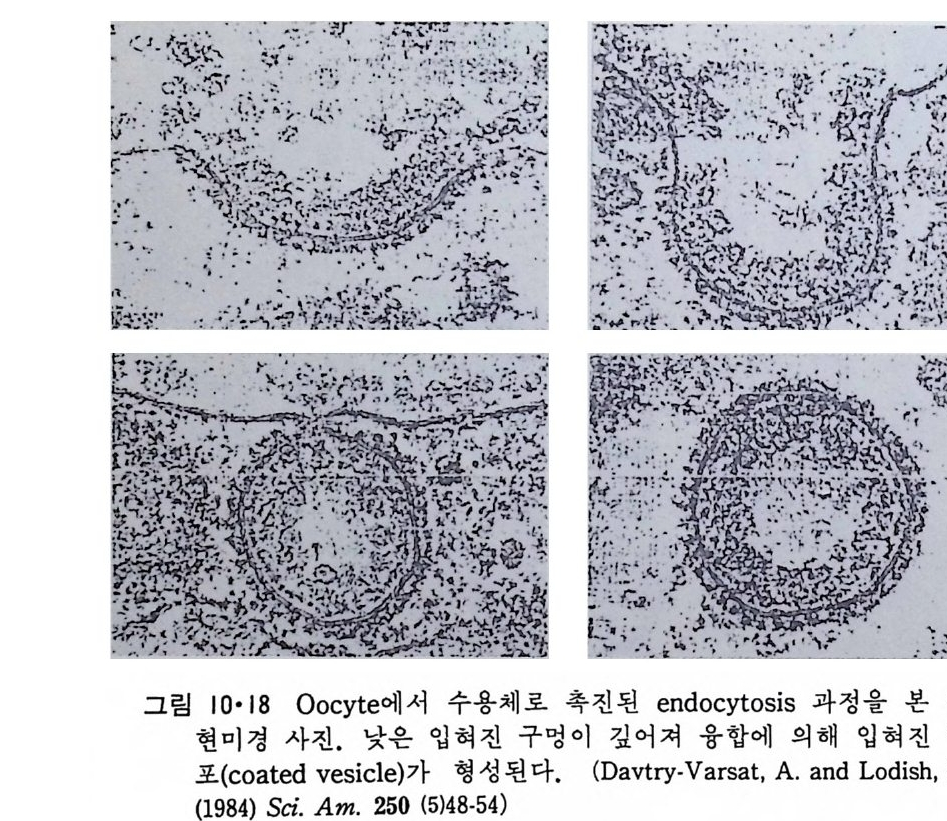 L:• 、 ... ; t •.? r· ; '?.:?s~\.;.. 、 • . :~
L:• 、 ... ; t •.? r· ; '?.:?s~\.;.. 、 • . :~
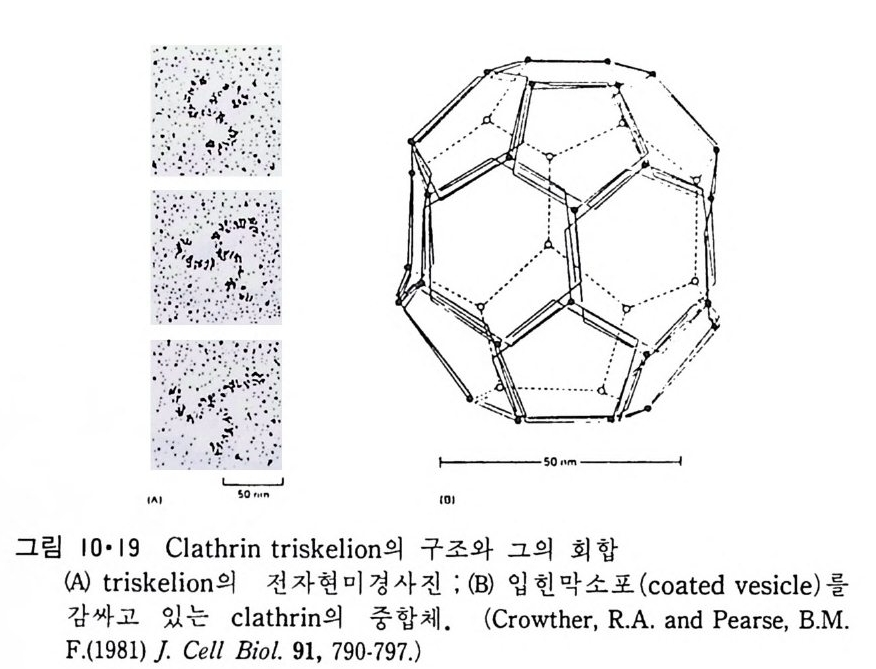 ..•,-'• ? :•; ·· ’:. •... , '.·.• • .• •\: ,· •우 느f ..,’s '.·,... , .• ,., .A , * , ’. <. _‘. . . .5 &·. .· .'.-· .. . ' ··~ :,'. ·g .: .'• : . • :·... .. ••. . ... .
..•,-'• ? :•; ·· ’:. •... , '.·.• • .• •\: ,· •우 느f ..,’s '.·,... , .• ,., .A , * , ’. <. _‘. . . .5 &·. .· .'.-· .. . ' ··~ :,'. ·g .: .'• : . • :·... .. ••. . ... .
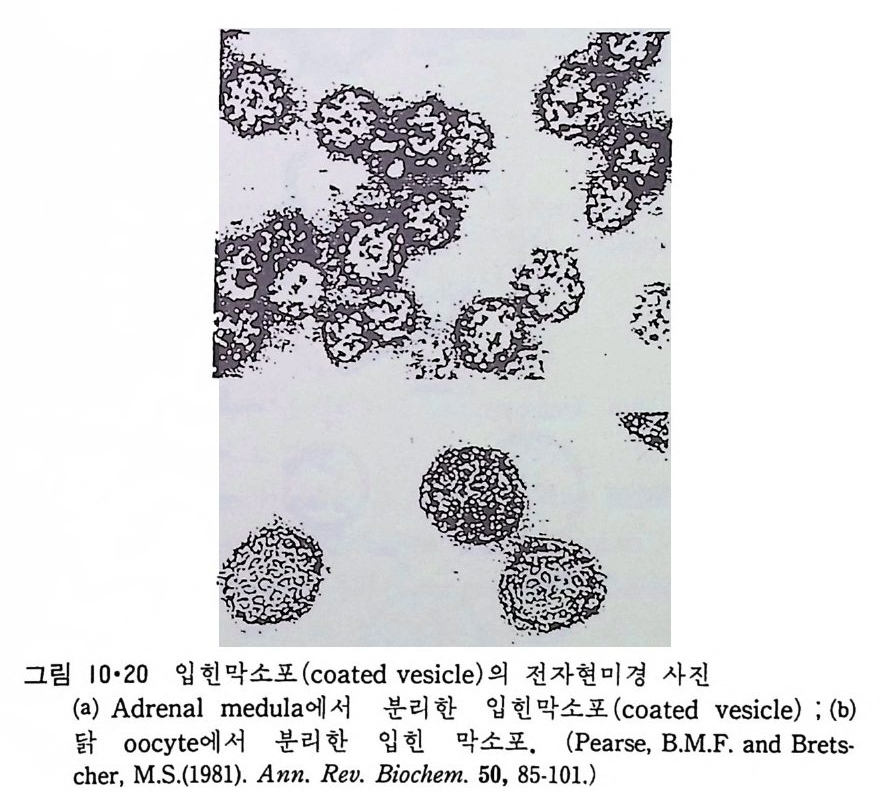 F‘’`、 t*r中t.
F‘’`、 t*r中t.
하고 있다. 3 개의 이 단백질은 3 개의 가지가 펼쳐진 구조물 가진 t r i ske li on 을 형성하여 이 소단위가 중합이 되면 그링 10·19 에서 보여주 는 5 각형과 6 각형이 모인 격자구조가 이루어진다. 그림 10·20 은 떳 가지 의 입힌 막소포를 보여준다. 입힌 구멍이 입힌 막소포로 떨어져 나오는 과정은 이미 구멍에 존재하는 cla t hr i n 의 격자에 cla t hr i n 이 더 첨가되어 이루어진다. 입한 막소포가 형성된 후에는 곧 cla t hr i n 은 다 떨어져 나가 고 서로 융합되어 endosome 을 형성한다(그림 10·21). 여기서 떨어져 나
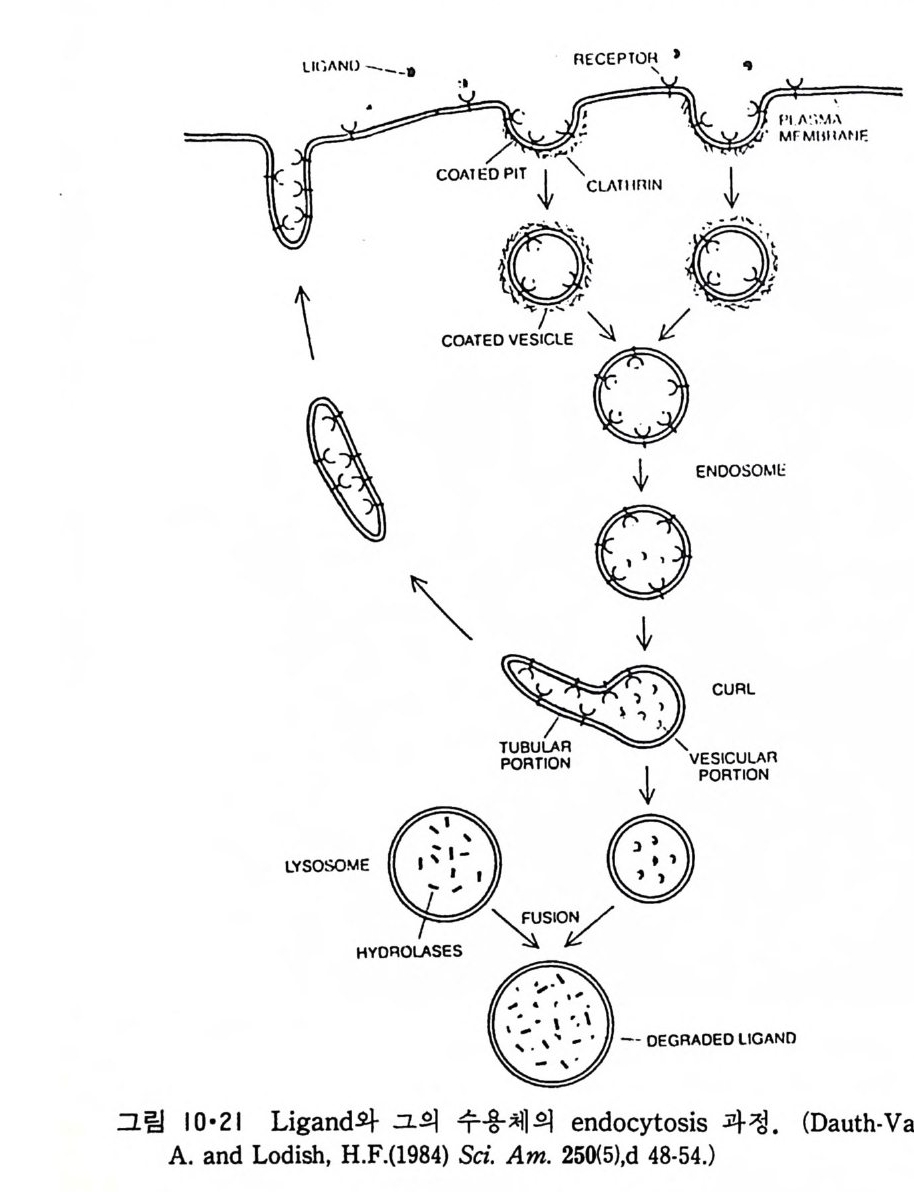 Lll,A NI J- ~- • RECEPTOH` > `
Lll,A NI J- ~- • RECEPTOH` > `
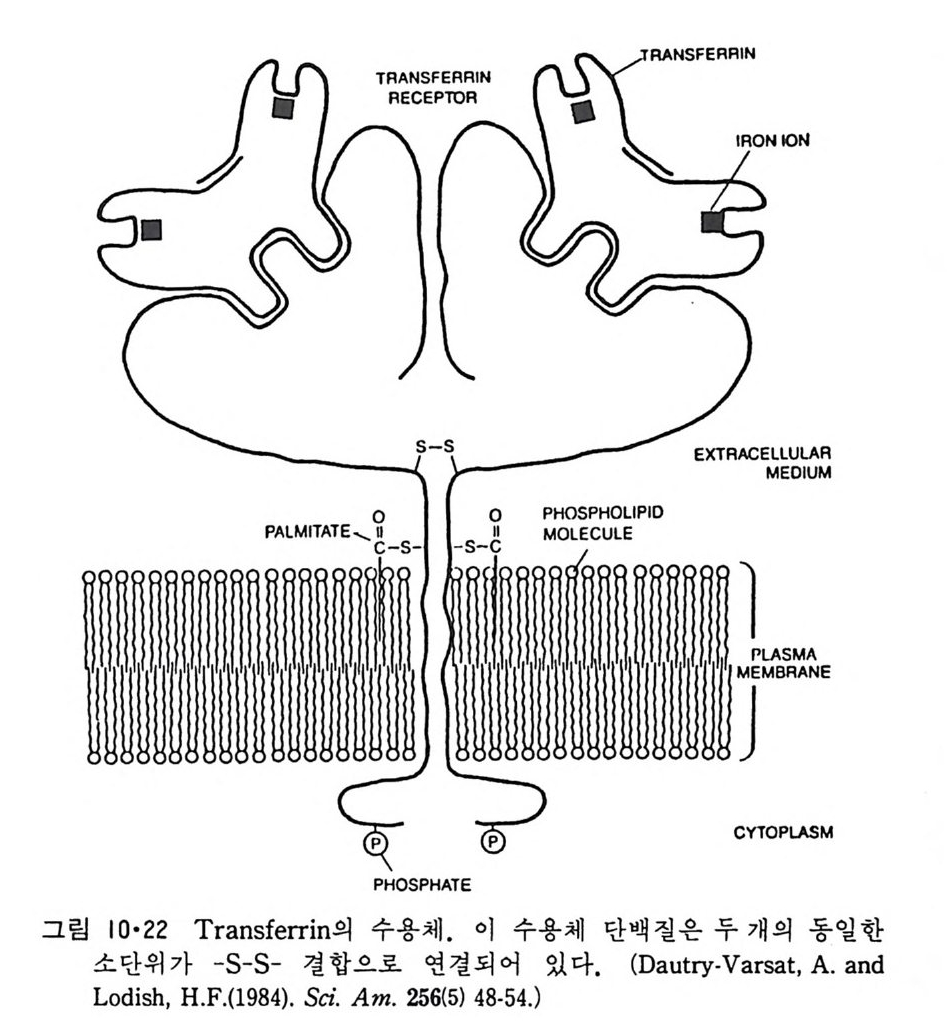 PALMITATE-.`... ~c - I I O PHOSPHOLIPID
PALMITATE-.`... ~c - I I O PHOSPHOLIPID
시온E질l에막한0n 에수·마쪽d2돌c이o 용2다 l sa아는부동끝 체t o h간 되착만m그r 에e 철i다 어된이에n 이 은분 고 의 을것이원 형해한세 생을 형성당 부포e각e 질된되nn분보액d되d막 는o인이o에고후c에c다 yy t• t결내 존수 o있o 박ss국재다 용재i i 혀 s이s. 단 시체는하 e 백n수키 다있d그질단용는o가으 s인백체 나선ot me질의 r 택xea수은자 o에 n성cs용대 세 서 y f이e체te부한 nro dis분( 떨 n커 roi s의구e은어s 에서co e조져 mp수t외e 는의 eonr 용부나)해d 한가o체에와밝 c쪽 단y 혀 원t이존노이 백o져형재 s 출 질i질 한돌s막 되있가이다막출소어지 .으된되포 원 로 가는않있형그부 다고 림질물.분원,다
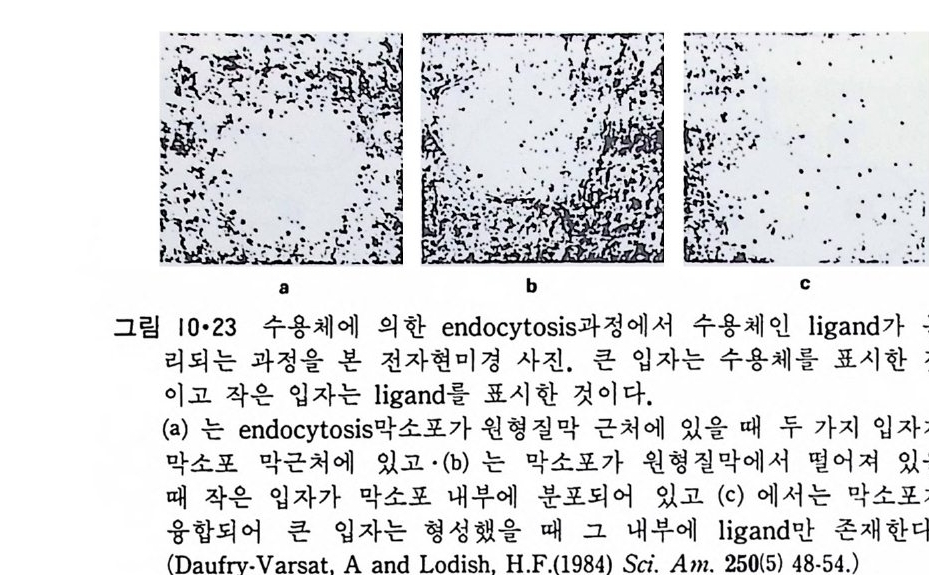 ;묘•_ _~ :•••- ? · 모· ·\ ~ .• ._ + •g.:」 . ’ 첼`〕 -·I 綱麟一― ―,l · · -7- :· . '훑:-隣 rrg 了q 만 tr흡.E :: 군 . •s .· \\ . · 드 _• •\.•, • . .. _`. •• •二•
;묘•_ _~ :•••- ? · 모· ·\ ~ .• ._ + •g.:」 . ’ 첼`〕 -·I 綱麟一― ―,l · · -7- :· . '훑:-隣 rrg 了q 만 tr흡.E :: 군 . •s .· \\ . · 드 _• •\.•, • . .. _`. •• •二•
형질막과 융합된다(그림 10·19). 나머지 endosome 은 l y sosome 으로 가게 된다. 이렇게 수용체 단백질이 있는 막소포가 떨어쳐나가 원형질막으로 돌아가는 과정은 그림 10·23 에서와 같이 이중표지 (double-label) 현미경 방 법으로 증명 이 되었다. 처음 그림에는 endosome 이 형성된 직후에 수용 체에 결합된 항체에 있는 큰 금입자와 endoc yte 되는 lig and 와 결합된 항 체에 있는 작은 금입자가 모두 표면 근처에 보인다. 다음 endosome 이 세포 내부에 들어 왔을때 큰 입자는 t ube 모양의 막소포에 보이고 작은 입자는 endosome 내부에 있다. 마지막 그림에서는 endosome 내부에 있 는 lig and 만 보인다. 이렇게 수용체와 cla t hr i n 이 rec y cle 되는 전과정에서 몇 단계의 막 융합이 일어나지만 cla t h ri n 이 이 융합을 야기시키는 mechan i sm 은 현재까지 밝혀지지 않고 있다. Endoc yt os i s 와는 정반대로 세포 내에서 합성된 여러 물질이 세포 밖으 로 분비 되 는 현 상을 exoc yt os i s 라 하며 효소, hormone, im munog lo buli n, 신경전달물질 둥이 이 과정으로 분비가 된다. 그림 10·24 는 췌장 exoc ri ne 세포에서 합성된 단백질이 분비되는 과정을 보여준다. 분비되는 단백질이 합성되어 소포체 lumen 으로 들어가는 과정은 이미 제 5 장에서 설명되었다. 합성된 단백질은 소포체의 평탄한 표면의 끝에 축적이 되고 이 부분은 융합에 의해서 잠정(t rans iti on) 막소포들이 떨어져 나온다. 이 잠정 막소포들 사이에 융합이 이루어지고 또 Gol gi체에서 나온 Golgi 막
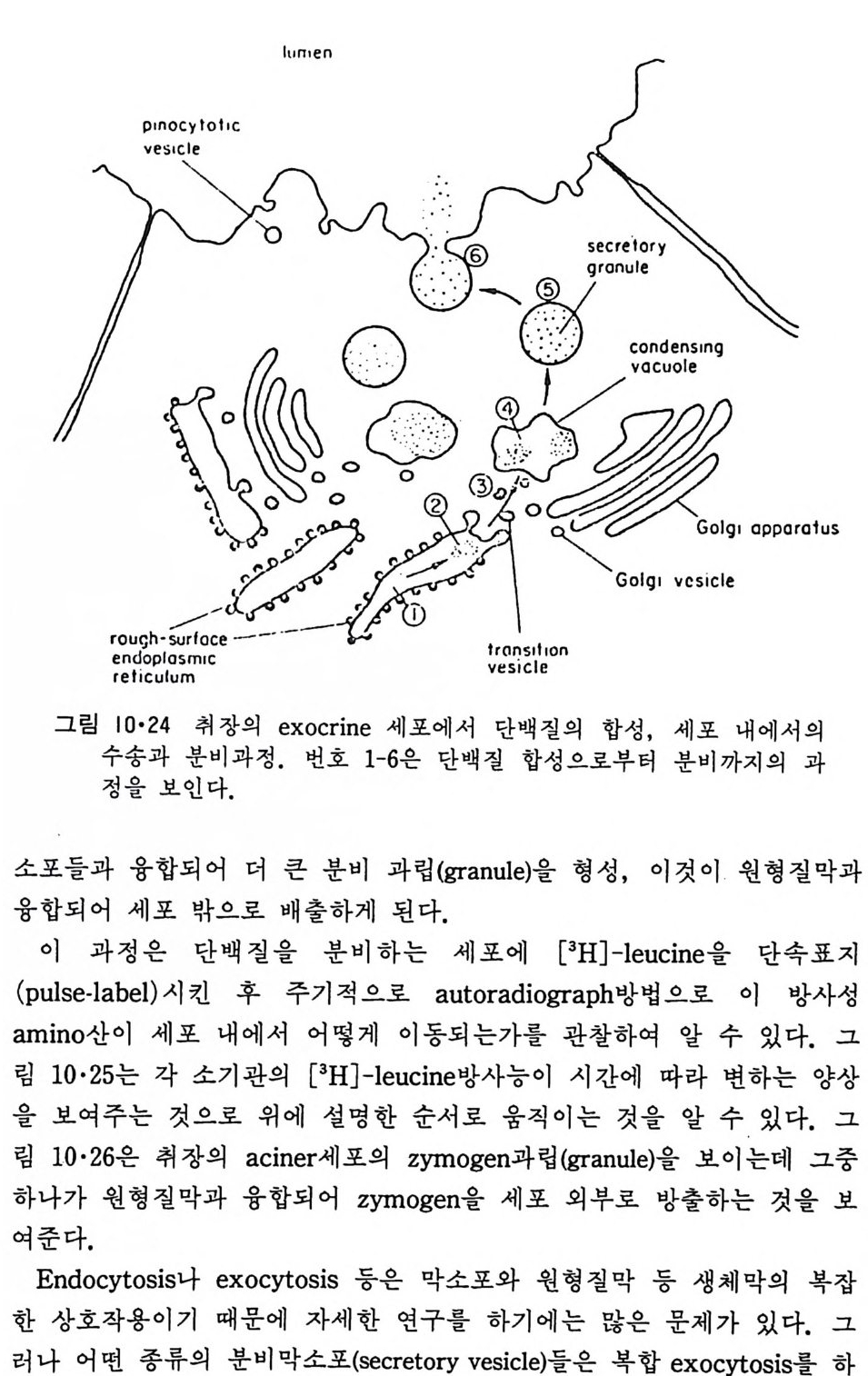 lum en
lum en
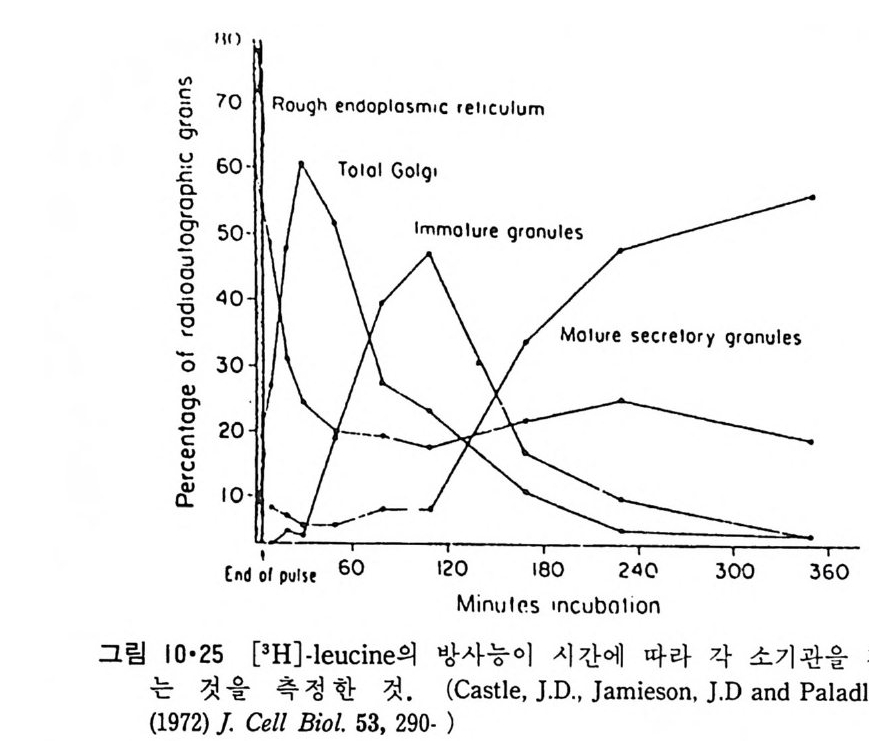 111)
111)
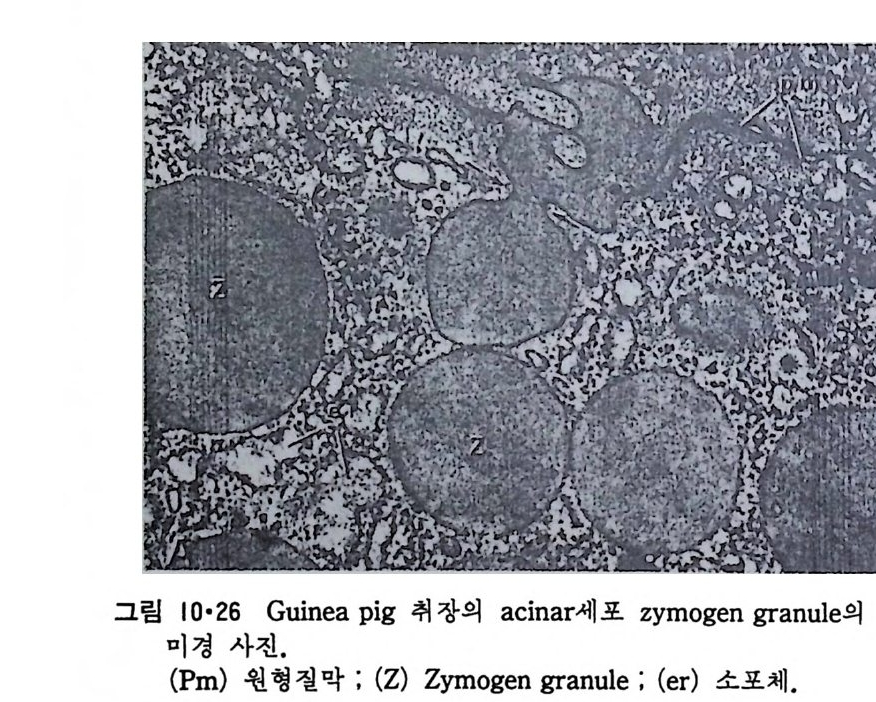 그립 10•26 Gu ine a pig 취장의 a ci nar 세포 zy m og en gr anule 의 전자현
그립 10•26 Gu ine a pig 취장의 a ci nar 세포 zy m og en gr anule 의 전자현
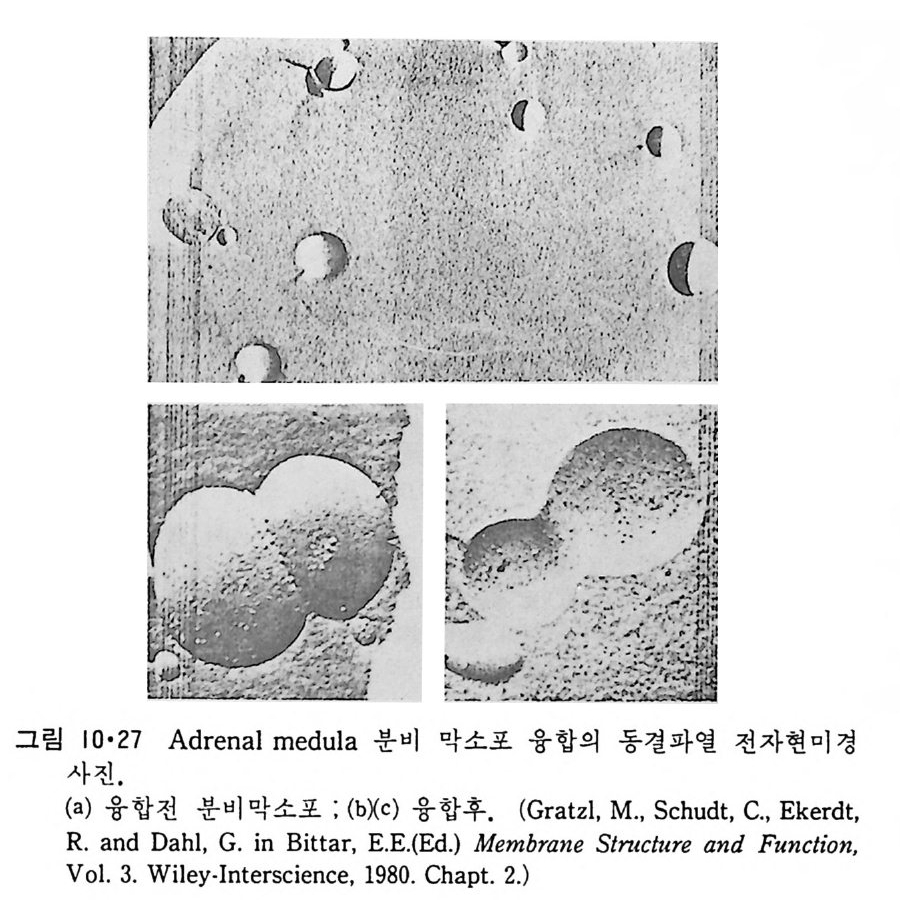 >나广i' 제 ':; 노:십날;A :'' \3<, \ ' ; ,\'?.\ :' ' .··. 표,‘' ;나:1 :\ ?.: ;J: i ? ' §\'\ ''\ ;\\ 』:나 , 1. 』 ',::、 ;,j . :?〈 ?틀',\\ \ \. .` 雲?‘ l,.3》 1'.. :量':; :깊.? ; ;\ .i \t'' :;I ;호! `: )? ' :. ': .召: '' • \.` !•t亨\ ; ,.1; ''. }', % ,. 令'{ · ?\성'; .\:. : . ,: ., ' ':i .\• :''. \< ' ( , /. ! ;1)•]t\
>나广i' 제 ':; 노:십날;A :'' \3<, \ ' ; ,\'?.\ :' ' .··. 표,‘' ;나:1 :\ ?.: ;J: i ? ' §\'\ ''\ ;\\ 』:나 , 1. 』 ',::、 ;,j . :?〈 ?틀',\\ \ \. .` 雲?‘ l,.3》 1'.. :量':; :깊.? ; ;\ .i \t'' :;I ;호! `: )? ' :. ': .召: '' • \.` !•t亨\ ; ,.1; ''. }', % ,. 令'{ · ?\성'; .\:. : . ,: ., ' ':i .\• :''. \< ' ( , /. ! ;1)•]t\
여 막소포들 사이에도 융합이 일어나기 때문에 막소포들을 분리하여 이 들 사이의 융합과정을 연구할 수가 있다. 이중 가장 많이 연구가 된 것 이 adrenal medula 막소포들로서 그림 10·27 은 이들 사이의 융합을 보여 준다. 그림 10·28 은 몇 가지 분비막소포 간의 융합에 필요한 Ca2+ 농도를 보여준다. 약 10-smol/ l 정 도이면 융합을 일으키는 것을 알 수 있다. 다음 adrenal medula 막소포의 융합에 단백질의 가담여부를 알기 위해 이들 막소포를 neuram i n i dase 나 p ro t ease 로 처리하면 융합이 일어나지 않는다는 것을 알았다. 그림 10·29 는 이 분비 막소포에서 추출한 지 방질 로써 구성된 lip osome 의 융합과 이 분비막소포의 융합을 비교한 것을 보 여준다. Neuram i n i dase 로 처리한 분비막소포의 융합과 lip osome 의 융합 에 필요한 Ca2+ 농도가 같은 것으로 보아 당단백질이 융합에 필요한 Ca2+ 농도를 상당히 감소시키는 것을 알 수 있다. 한편 이 분비막소포의 회합
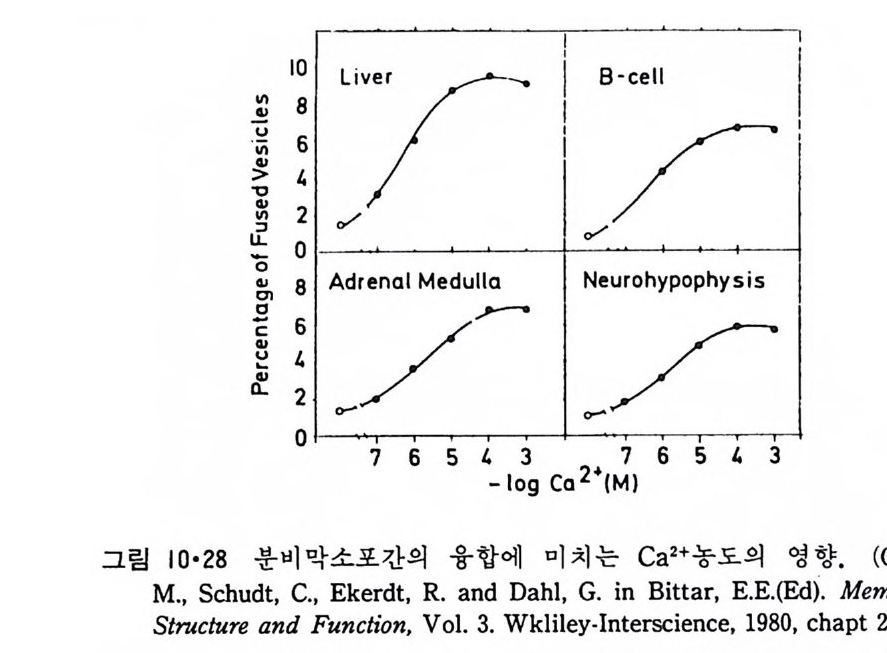 si,a\l uI 。8 二 /8-cel/l !i
si,a\l uI 。8 二 /8-cel/l !i
(a ggr e g a ti on) 을 촉진시키는 분자량이 47kDa 인 수용성 단백질이 근래에 분리되었고 이 단백질 (s ynex i n) 이 인산지방질 막소포를 융합시키는 것이 발견되었다.
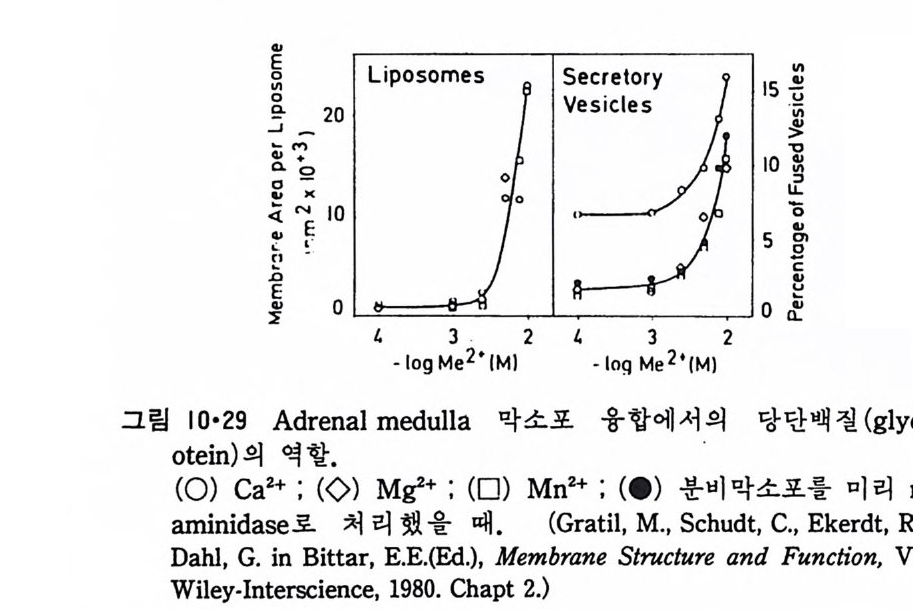 Eo으 Lip o somes ISsa-uI1Sil 0s0
Eo으 Lip o somes ISsa-uI1Sil 0s0
10·3 인산지 방질 막소포의 융합 9 )1 0) 생체막의 융합은 흔히 일어나고 또 중요한 기능을 가지고 있어 많은 연구가 이 루어 졌지 만 아직 도 그 mechan i sm 은 규명 되 지 못하였는데 이 어려움의 한 이유는 생체막의 성분이 너무 복잡하기 때문이다. 그래서 순수한 인산지방질로 형성된 막소포의 융합에 의한 연구가 과거 약 10 년 간에 많이 진행되어 왔다. 이들 model 막은 그 성분지방질의 조성을 임의 로 조철할 수 있으며 또 외부에서 여러가지 융합에 영향을 주는 화합물 을 첨가해 이들이 융합을 유도하는 과정을 관찰할 수 있는 장점이 있다. 자연에서 일어나는 막융합은 주로 Ca2+ 갇은 2 가 i on 과 단백질에 의해서 이루어지기 때문에 금속 i on 과 단백질과 단백질 유사화합물에 의한 인산 지방질 막소포의 융합이 제일 많이 연구가 되어 왔다. 지방질 막소포의 융합을 관찰하는 실험 방법은 4 가지로 볼 수 있다. 그 첫째는 입자의 크기의 증가를 측칭하는 것이다. 융합이 일어나면 입 자의 크기가 중가하는데 입자가 커진다고 반드시 융합이 일어나는 것은 물론 아니다. 단순한 회합도 입자를 크게 하기 때문에 이 점을 조심하여 야 한다. 입자 크기를 관찰하는 방법에는 흉광 분광기로 홉광도 (o pti cal density , 0.D. )를 측정 하거 나 빛 산란 분석 기 (ligh t scatt er in g i ns t rumen t)로 측정 할 수 있고 또 하나는 ge l filtra ti on chroma t o gr aph y로 용출 용적 (eluti on volume) 으로부터 입자의 크기를 결정할 수 있다. 두번째 방법은 두 가지 각각 다른 지방질로 구성된 막소포들이 융합이 될 때에 지방질이 섞이는 것을 측정하는 것이다. 여기에는 DSC 로 상변화 온도를 측정하는 것과 형광의 q uench i n g의 감소나 공명 energy 전달의 정도를 보는 것이 있다. DSC 의 경우 상변화 온도가 다른 지방질로 구성 된 막소포를 같이 섞었을 때, 융합이 일어나면 혼합지방질이 생기므로 그 상변화 온도는 각각 성분의 상변화 온도의 평균이 될 것이다. 또 형 광성 물질로 표지된 막소포와 표지되지 않은 막소포를 섞었을 때 융합이 일어나면 형광성 물질이 희석되어 q uench i n g이 줄어든다. 또 공명 ener gy가 전 달될 수 있는 두 형 광성 물질을 따로따로 막소포에 넣 었을 때 이들 사이에 융합이 일어나면 energy 전이가 일어난다. 여기서 조심
할 것은 인산지방질 교환 단백질이 용액에 없는 것을 확인해야 한다. 만 일 이 단백질이 있으면 융합 없이 두 가지의 지방질이 섞일 수 있기 때문 이다. 세번째 방법은 막소포 내부용액이 융합에 의해 섞이는 것을 관찰하는 것이다. 만일 두 화합물이 섞였을 때 형광이 나면 막소포를 만들 때 그 중의 한 화합물을 막소포 일부의 내부에 넣고 다른 화합물은 나머지 막 소포 속에 넣어 이들 막소포가 섞였을 때 융합이 일어나면 그 내용물도 섞여 형광이 나타나는 것이다. 네번째는 전자현미경으로 직접 융합 여부를 관찰하는 것이다. 10·3·1 금속 양 i on 에 의한 융합 자연에서 일어 나는 많은 막융합이 Ca2+ i on 의 존재 하에서 일어 나기 때 문에 이 2 가 양i on 이 막 융합에 주는 영향은 상당히 광범위하게 연구되 어 왔다. 그럼 10·30 은 PS 막소포의 융합을 전자현미경으로 관찰한 것이
 그림 10•30 PS 막소포의 융합과정의 전자현미경 사진. (Pap ah adjo p o ulos,
그림 10•30 PS 막소포의 융합과정의 전자현미경 사진. (Pap ah adjo p o ulos,
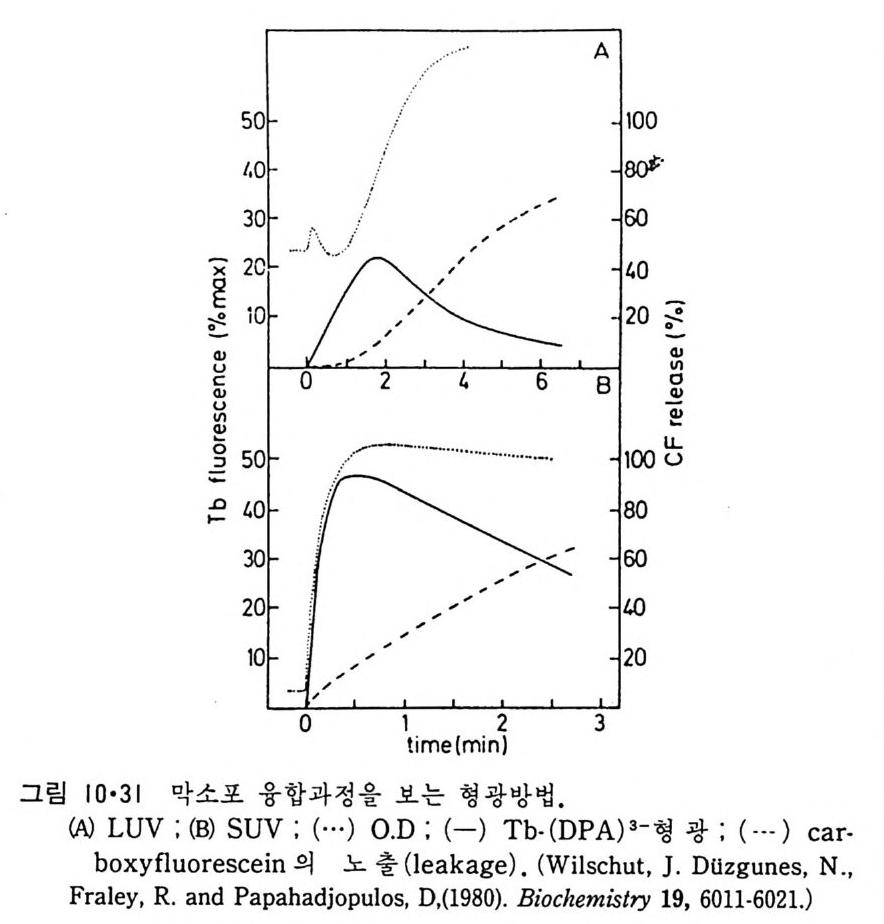 A
A
다. A 에서 보이는 작은 막소포가 Ca2+ i on 의 첨가로 융합되어 그 크기가 훨씬 중가되나 B 에서와 같이 둘둘 말아진 cochla t e 형을 이룬다. 이때 EDTA 를 충분히 가하면 C 에서 보여주는 것같이 거대한 막소포가 형성된 다. 그림 10·31 은 PS 막소포에 Ca2 + 을 첨가한 후 융합이 되는 과정을 기 록한 것 이 다. 여 기 서 ter biu m i on(Tb”) 이 들어 있는 막소포와 dip ico lin ic a ci d(DPA) 가 들어 있는 막소포를 융합시 켰을 때 이 두가지 막소포의 내 용물이 혼합되어 생긴 Tb(DPA)3- 에서 발산되는 형광을 측칭하여 융합되 는 정도를 측정한 것이다. 이와 동시에 막소포가 커지는 것을 광산란 방 법으로 측정했고 이 막소포의 물질 두과성은 별도의 실험에서 막소포에 농축되어 q uench i n g을 하고 있던 carboxy fl uoresce i n 이 밖으로 새어나 와 희석함으로써 중가되는 형광의 세기를 기록한 것이다. 이들로부터 융
합은 1 분 정도면 끝나고 융합 후 서서히 막소포 내용물이 새어나오는 것 울 볼 수 있다. 한가지 종류의 지방질로 구성된 막소포의 융합에 대한 연구결과를 종 합하면 우선 막소포가 음성의 전하를 띠어야 한다. 죽 PS, PA 와 PG 의 막소포만을 융합시킬 수 있다. 둘째는 인산지방질의 상변화 이상의 온도 에서 만 융합이 일어 난다. 그림 10·32 는 DMPG 막소포와 DPPG 막소포의 융합이 온도에 어떠한 영향을 끼치는 것을 보여준다. DMPG 의 Tm 은 24. 5•c 이고 DPPG 의 Tm 은 42.C 인데 45•c 와 60°C 에서 융합이 되나 DPPG 의 Tm 보다 낮은 36 C에서는 융합이 일어나지 않는다. Ca2+ i on 은 산성 인산
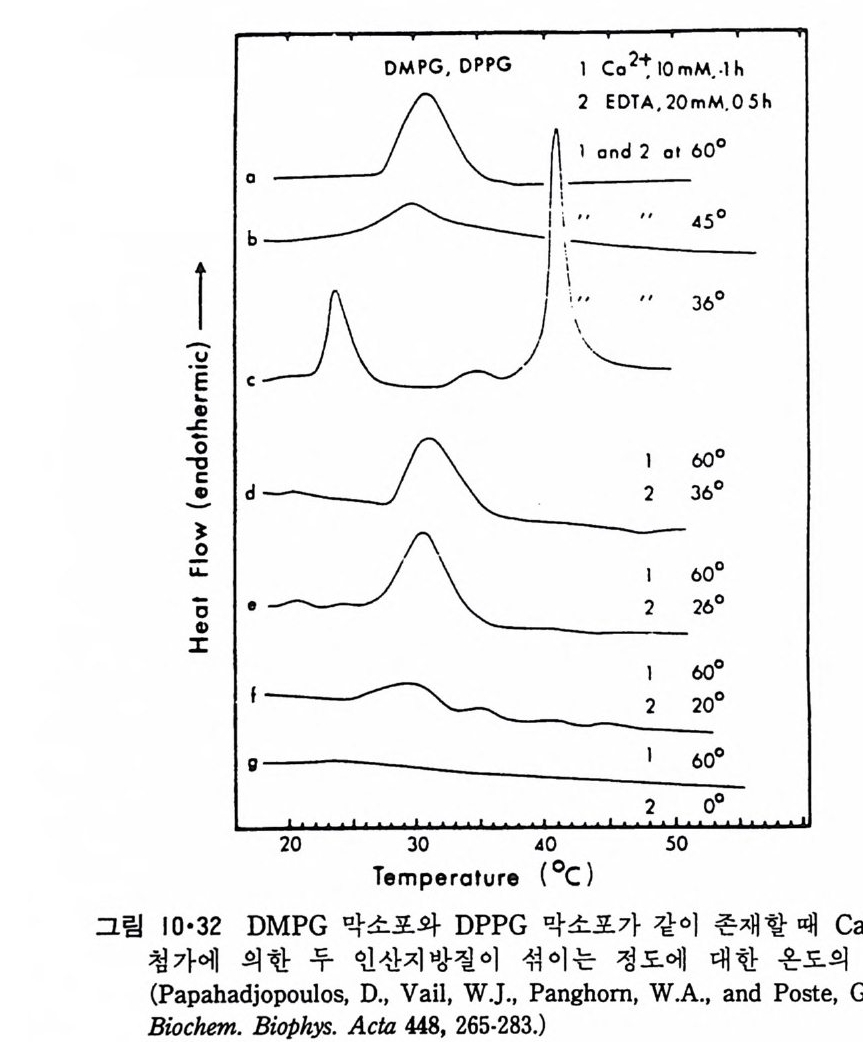 。: _~/OM\PG\, O_PPG \ 二1 Ca2으:1 :0m:M:0. -0l h 5 h
。: _~/OM\PG\, O_PPG \ 二1 Ca2으:1 :0m:M:0. -0l h 5 h
지방질과 결합되는데 (1mol 의 Ca2+ 당 2mol 의 인산지방질 ) 이때에 Ca2+ i on 이 산성인산지방질의 Tm 을 높이는 것은 이미 언급하 였 다. 위 실험에 서 EDTA 를 첨가하는 이유는 Ca2+ 를 제거해야만 Tm 결정에 의해 융합 여부를 알 수 있기 때문이다. Ca” 이나 다른 2 가 금속 i on 에 의한 융합에는 이들 i on 의 농도가 일정 한 값 이 상이 되 어 야 하는데 이 농도를 시 초농도(t hreshold concentr a ti on ) 라 한다. 그림 10·33 은 Ca2+ i on 농도 중가에 따르는 DMPG 막소포의 웅 합 정도를 보여준다. Ca2+ 농도가 5mM 일 때까지도 융합이 일어나지 않
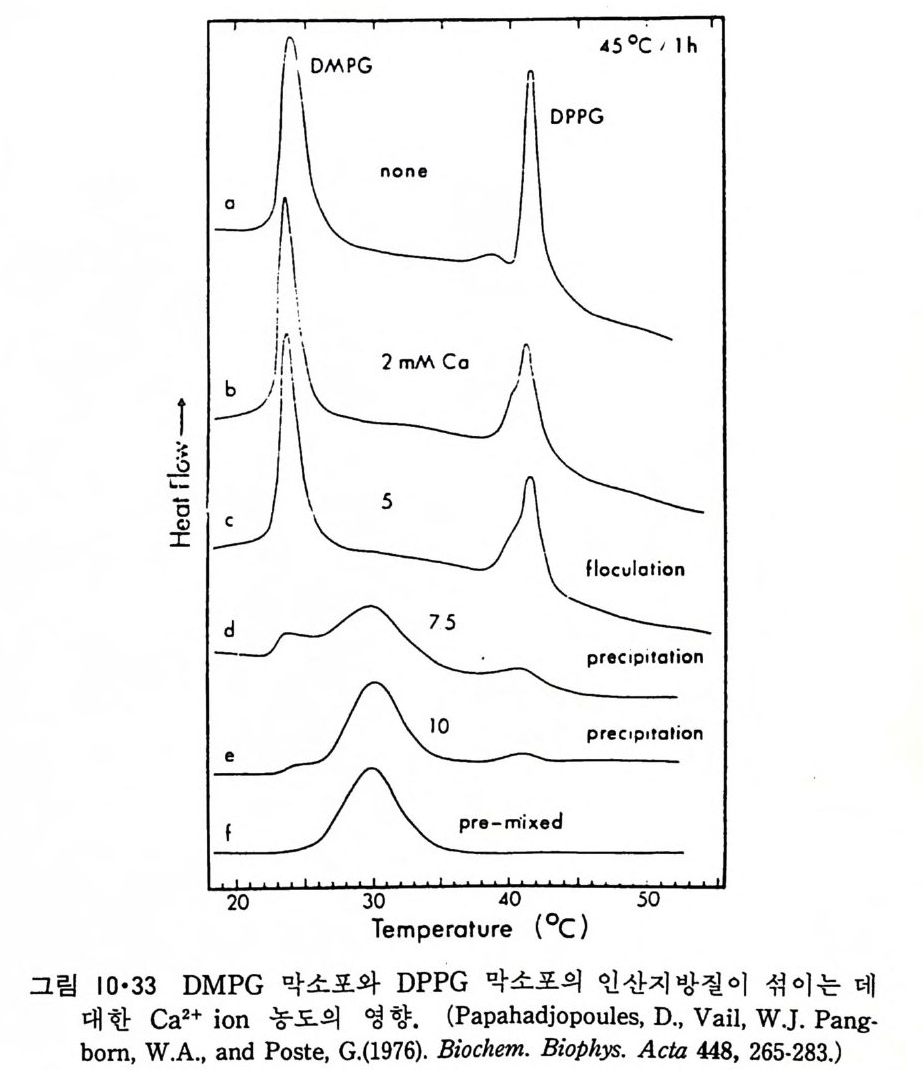 A5°C I lh
A5°C I lh
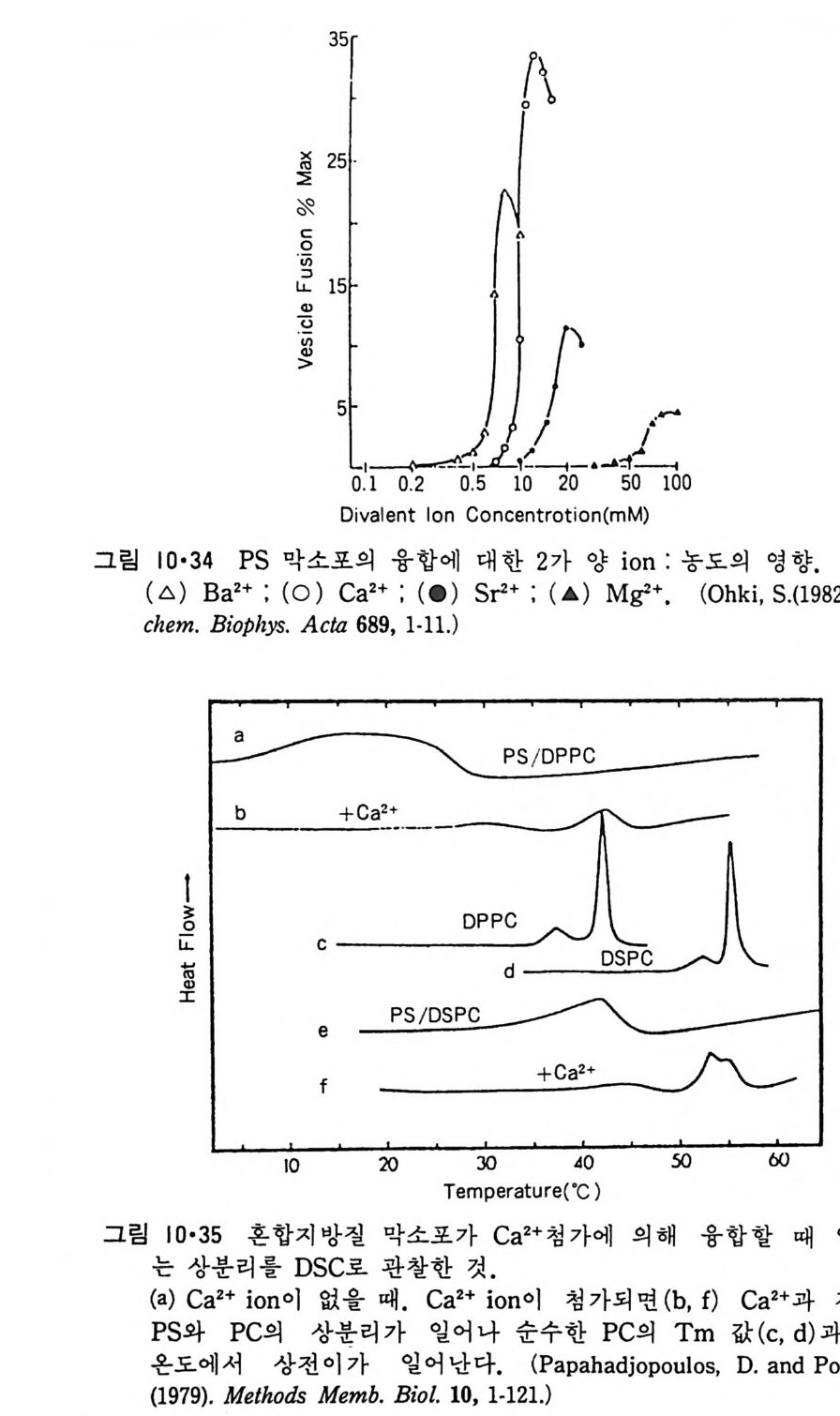 35-
35-
고 시초농도는 약 lOmM 정도가 된다. PS 막소 포 의 시초농도는 O.lmM Ca2 + 아고. PA 막소포의 시초농도는 0.2mM Ca2 + 이다. Ca ” 에 의해서는 PS 막소포가 제 일 잘 융합되 는데 그림 10·34 은 몇가지 2 가 양 i on 의 시 초농도를 보여준다. Ba 2 + 의 시초농도는 Ca2 + 의 시초농도보다 오히려 작 지만 Ba 2+ 는 생체에서 중요하지 않기 때문에 Ca ” 에 대한 관심이 더 크 다. 아직까지는 한 종류의 인산지방질만이 존재할 때의 경우였는데 생체막 에는 여러가지 지방질이 섞여 있기 때문에 두 가지 종류 이상의 인산지 방질로 구성된 막소포의 융합의 성질이 중요하다. 그림 10·35 는 PS 와 DPPC 의 혼합 막소포가 Ca” 에 의해서 융합될 때에 DPPC 의 상이 분리 해 나오는 것을 보여준다. Ca2+ i on 이 없을 때 이들 막소포는 2o·c 근처에 서 넓은 Tm 을 보이지 만 Ca2 + 의 존재 하에서 DPPC 의 Tm 이 나타난다. 이는 Ca” 와 결합된 PS 상으로 DPPC 상이 분리되어 이중성 인산지방질 의 독특한 Tm 값을 보여준다. 그림 10·36 은 이 상분리를 칙접 동결-파열
 그림 10•36 PS/DPPC 혼합성분 막소포의 Ca2 + 첨가에 의한 상분리의
그림 10•36 PS/DPPC 혼합성분 막소포의 Ca2 + 첨가에 의한 상분리의
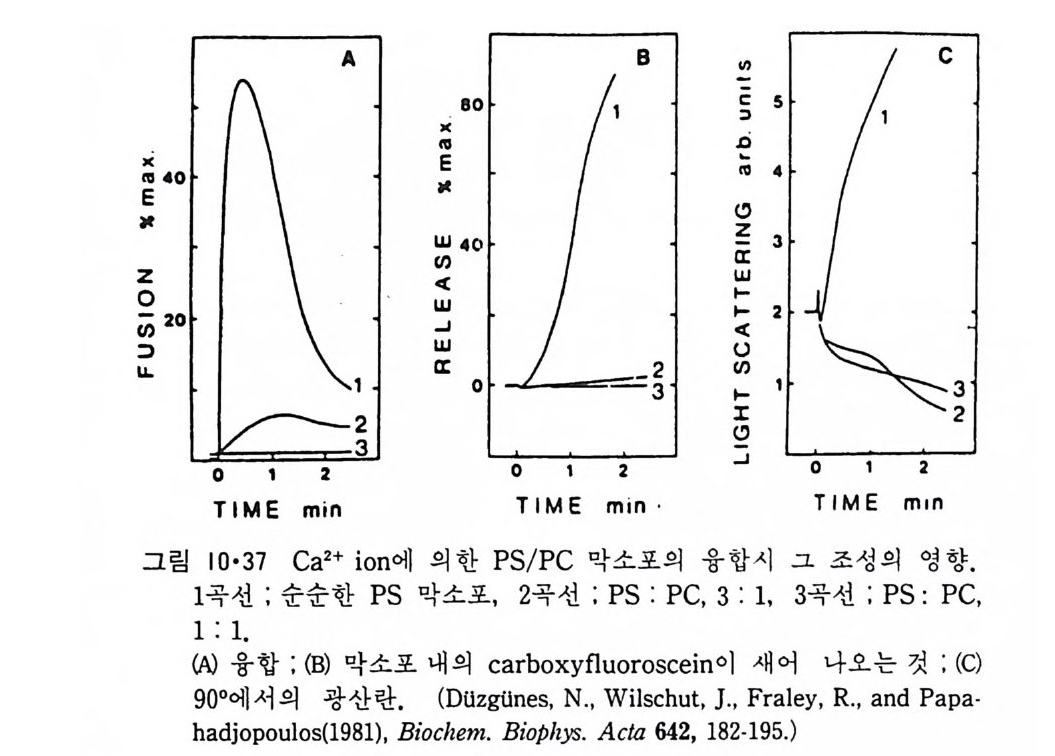 !=Uzu。>. •2 o0 t 。I \\ 2 A깁 1I .WUwwcc翼«.xJ:(,) 4110。0 。 2 B I x.I(u。~<。kza。.。mc`크./-J- ··:』) ' ‘s23 I 。\ I ;2 C
!=Uzu。>. •2 o0 t 。I \\ 2 A깁 1I .WUwwcc翼«.xJ:(,) 4110。0 。 2 B I x.I(u。~<。kza。.。mc`크./-J- ··:』) ' ‘s23 I 。\ I ;2 C
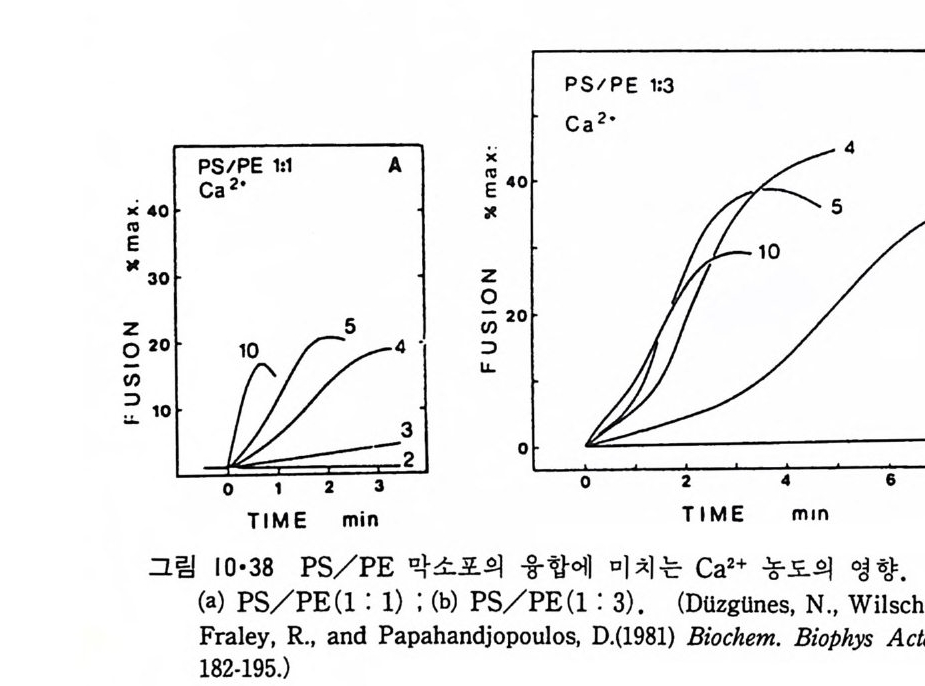 PS/PE 1:3
PS/PE 1:3
전자현미경 방법으로 관찰한 것이다. Ca2+ 을 가하기 전에 얻어진 동결 -파열 전자현미경 사진은 평탄한 데 비해서 Ca” 을 넣은 후에는 상분리 에서 생긴 조각들이 보인다. 이러한 혼합 인산지방질로 구성된 막소포의 융합정도는 PC 의농도가 중가할수록 감소하는데 이는 그림 10·37 에 찰 보여준다. PS/PC 의 비가 1 이하에서는 융합이 일어나지 않는다. 이와는 반대로 PE 도 중성머리 부 분을 가짐에도 불구하고 PS/PE 막소포의 융합을 도리어 증가시킨다(그 링 10·38). 이 상 순수한 인산지 방질로 구성 된 막소포가 Ca” 을 비 록한 2 가 양 ion 에 의해서 융합되는 성질을 설명하였는데 이들이 어떠한 mechan i sm 을 통해 융합되는지는 아칙 모른다. 여태까지 제안된 mechan i sm 은 Ca2+ i on 이 음성 인산지방질과 결합한 후 상변화와 상분리에 이어 상경계면이 불안정해진다는 것(그림 10·39) 과 이들 2 가 양i on 에 의해서 이분자층막
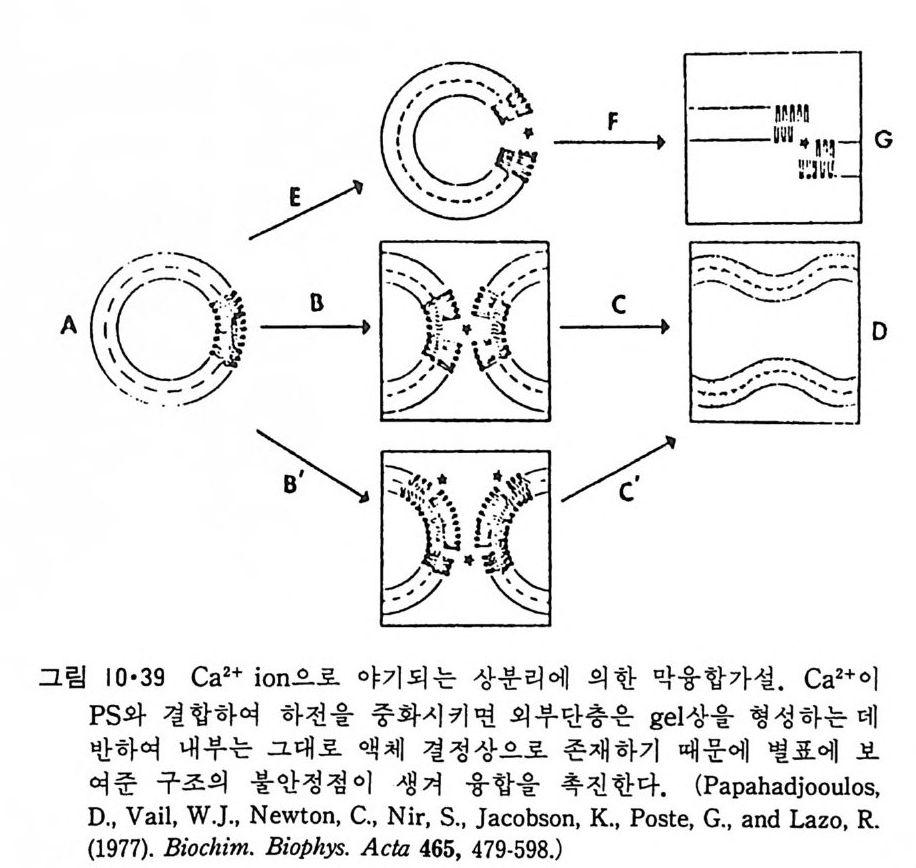 > \\\ A 전? F ’ .__ ___ u,U i':l'; li서!. 니 G
> \\\ A 전? F ’ .__ ___ u,U i':l'; li서!. 니 G
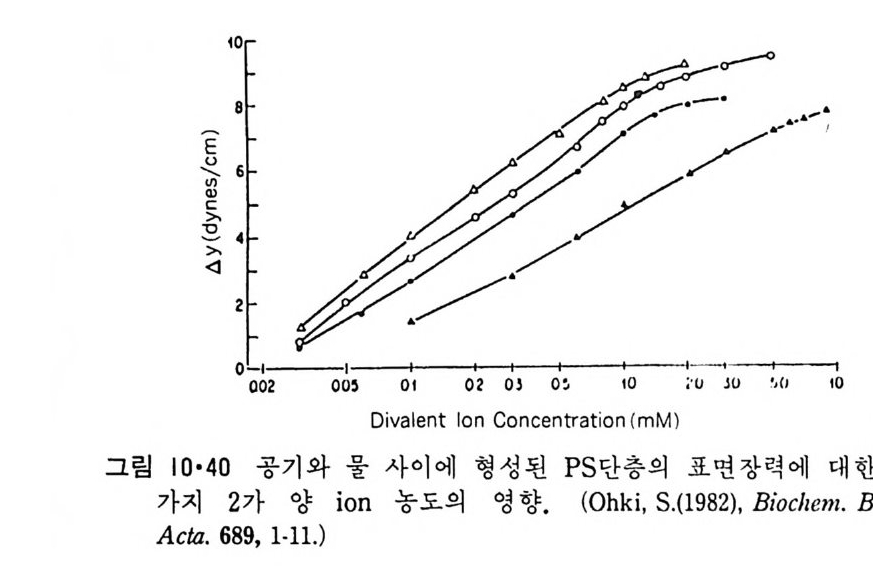 10
10
과 뭍 사이의 표면장력이 증가된다는 것(그림 10·40) 등이다. 한편 CL 이나 PE 가 함유된 막소포의 융합인 경우 Hl1 형성’이 융합의 중간단계라고 제의되었다(그림 10·41). 그런데 이러한 Ca2+ i on 에 의한 model 막의 융합과 생체 내에서 일어나 는 막융합 사이에는 두 가지 차이점이 있다. 첫째 exocy tos is 동에 필요
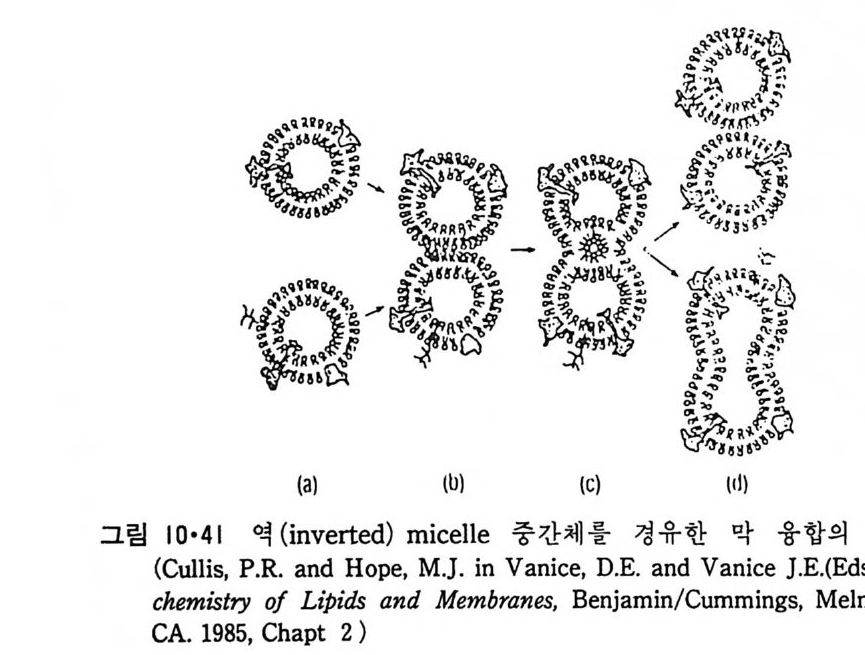 효邸
효邸
한 Ca2+ 의 초기 농도가 이들 model 막 융합 때보다 100 내지 1000 분의 1 밖에 안되고 둘째로는 생체막에는 산성 인산지방질의 함량이 융합시킬 수 있는 model 막보다 훨씬 적다. 그래서 세포 내에 Ca2+ 에 의한 융합을 촉진시키는 다론 화합뭄이 존재한다고 생각되었다. Adrenal medulla 에서 chromaff in gr anule 들을 회합시키는 분자량이 47kDa 인 s y nex i n 이 분리 되었고 이 단백질이 PS/PE 막소포에 필요한 Ca2+ 의 시초농도를 많이 감 소시키는 것을 발견하였다. 그러나 PS/PC 막소포는 회합을 시켜도 융합 을시 키 지 는 않았다. S y nex i n 이 막융합에 가담하는 mechan i sm 은 아직 모르나 Ca2+ ion 존재 하에 이것이 큰 입자로 회합이 되며 이것이 두 개 의 막을 접촉시킨다고 제시되었으나 더 많은 연구가 필요하다. 이외에 spe rmi ne 같은 p ol y am i ne 이 PA/ PS/ PE/ Cho 막소포의 Ca2+ 에 의 한 융 합을 촉신시키는 것이 관찰되었다(그림 10·42). 그러나 생체 내에서 왜
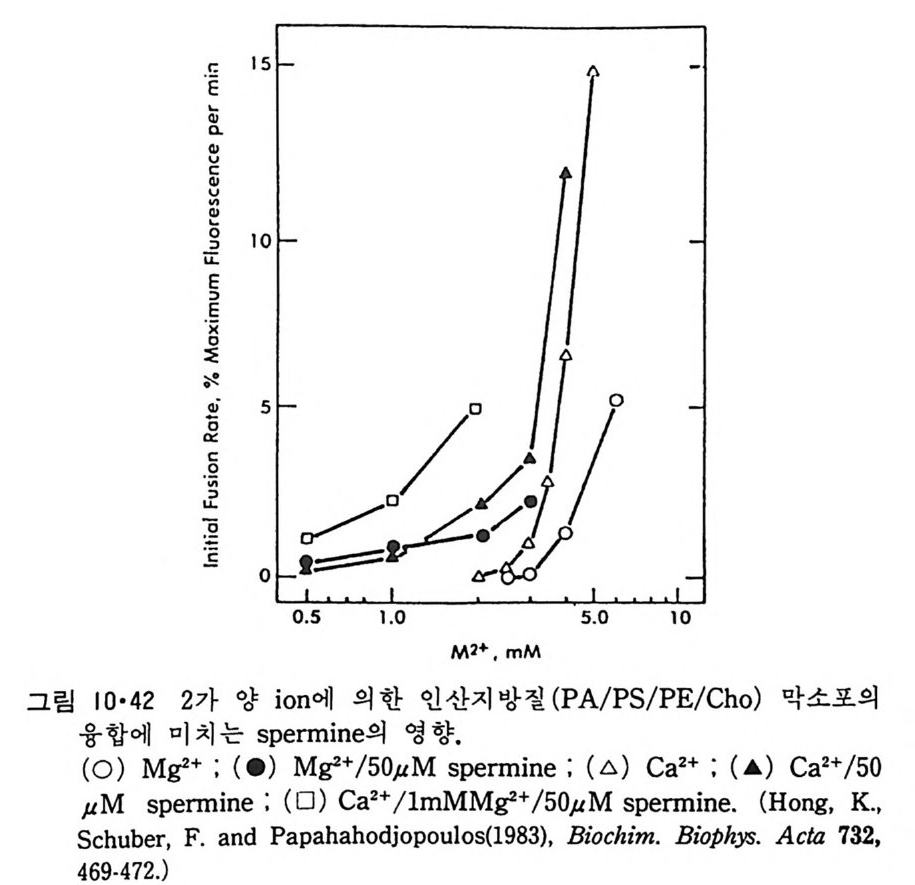 드 15 ^
드 15 ^
작은 농도의 Ca2+ 이 융합을 일으킬 수 있느냐 하는 문제는 아 직 해 결 되 지 않고 있다. 10·3·2 단백질에 의한 막융합 생 체 막 융합에 서 그 mechan i sm 이 제 일 잘 알려 져 있는 것 이 v i rus 피 막단백질에 의한 융합인데 여러 단백질과 단백질 유사화합물에 의한 model 막의 융합도 많이 연구가 되어서 그 결과는 표 10·1 에 보여준다. 이들 고분자들의 융합 성질에는 아직도 통일된 경향을 찾기가 힘 들 지만 많은 경우 이 소수성 단백질 표면의 노출이 융합의 전제조건으로 보인 다. 아 러 한 현 상온 bovin e serum albumi n, dip h th eria 독소와 cla t hr i n 의 경우에 뚜렷이 보이는데 실제로 융합과 소수성 단백질 부분의 이분자충 내부로의 침 입과의 관계를 보인것은 a-lac t album i n 의 경우이 다. 그림 10·43 은 몇 가지 단백질이 pH 3 에서 PS/PE 막소포의 융합을 일 으키는 것을 Tb/DPA 형광으로 mon it or 한 것이다. 이 모든 단백질이 약
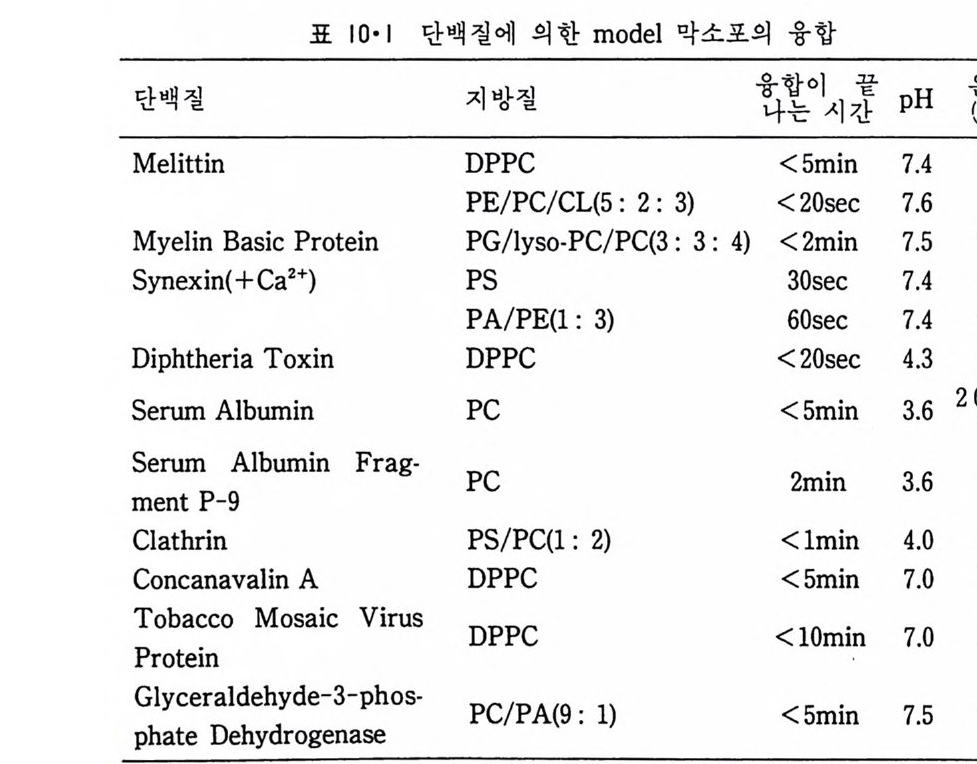 단백질 표 10·I 단백지질방에질 의 한 model 막소포의t t융o합] 시 간 끝 pH 은(°C도 )
단백질 표 10·I 단백지질방에질 의 한 model 막소포의t t융o합] 시 간 끝 pH 은(°C도 )
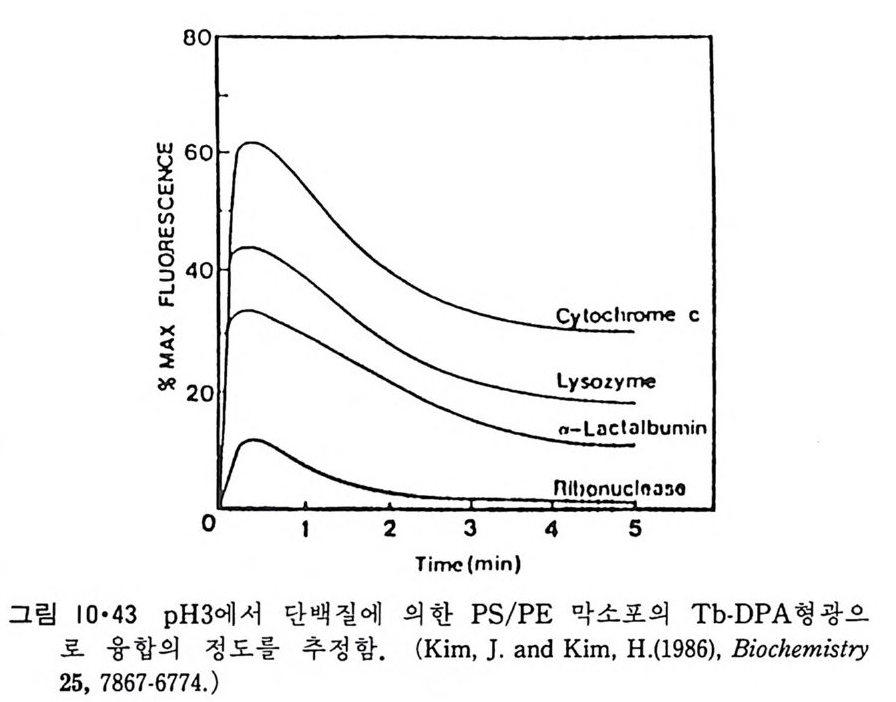 OO
OO
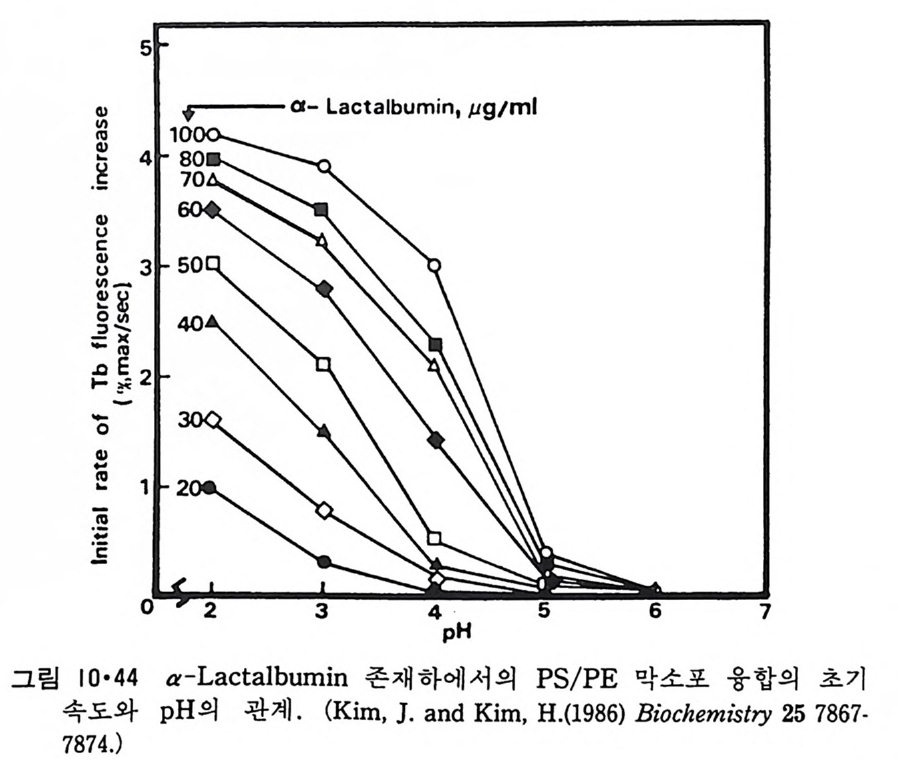 5
5
1 분 내에 막융합을 종결시키는 것을 볼 수 있는데 이 융합속도는 Ca” 에 서 한 속도와 유사하다(그림 10·28). 그림 10·44 는 여 러 a- la cta l bumi n 농도에 서 의 p H 에 따르는 PS/PE 막소포의 융합속도를 보여 주고 이 는 각 p H 에서의 이 단백질이 PS/PE 막소포에 결합하는 성질과 유사하다(그림 3·4). a-Lac t album i n 의 일부가 낮은 p H 에서 이분자층 내부를 들어가는 것은 이미 제 3 장에서 설명하였다. a-Lac t album i n 의 한 부분이 이분자층 내부로 들어가는 과정은 빛에 의 해 소수성 표지 로서 [12 5l ]-T ID(3-(tr i f luo rometh y l) -3-(m-[ 12 51] -iod o- ph eny l) d i az i r i ne) 를 막소포에 넣 은 다음 a-lac t album i n 을 가해 일 정 한 시간간격으로 잠시 동안 빛을 쬐어 얻었다. 그림 10·45 는 i ncuba ti on 시간 과 [125 1]-r- coun ti n g으로 얻은 소수성 표지가 되는 칭도를 본 것인데 표 지되는 시간은 융합이 되는 시간과 유사하다. 이미 그림 3·8 에서 시간을 충분히 주었을 때에 a- 나사선의 한쪽 표면에만 표지되는 것이 설명되었 다. 이외에도 l y soz ym e 과 cy toc hrome c 도 lip osome 을 융합시키는 조건 하 에서 그 일부가 이분자층으로 파고들어 가는 것을 관찰할 수 있어 이것
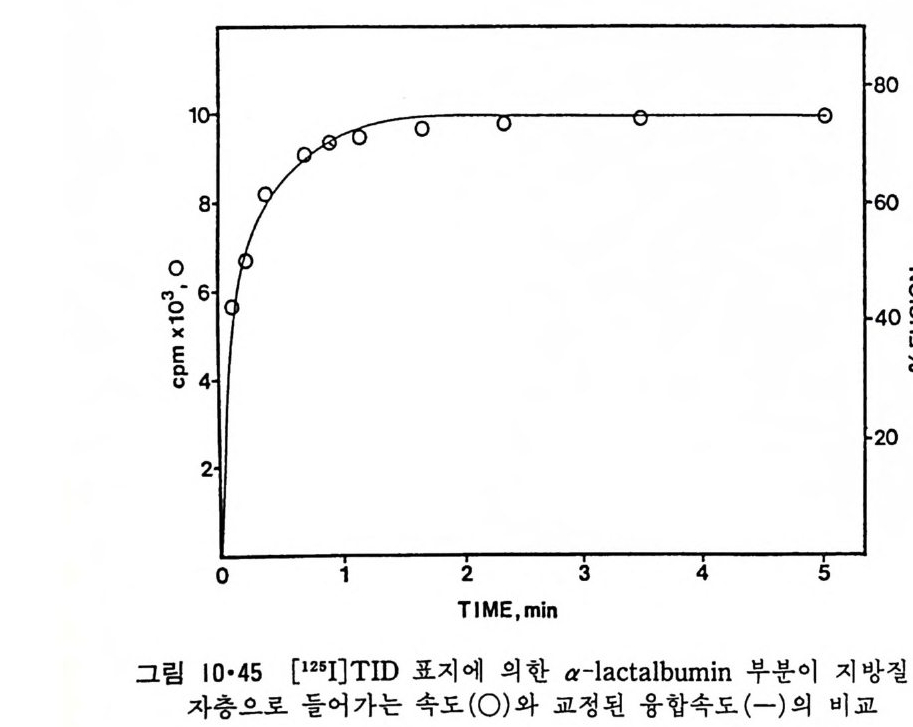 80
80
이 융합의 원인이 될 가능성이 상당히 크다. 앞으로 이들이 이분자층으 로 들어간 후의 t o p olo gy와 구조가 더 자세히 알려지고 또 이러한 단백 질의 침투가 이분자층의 인산지방질의 성질에 어떠한 영향을 주다가 밝 혀지면 단백질에 의한 lipo some 융합의 mechan i sm 을 알 수 있게 될 것 이다. * 10 장 참고문헌 (1) Poste , G. and Ni ch olson, G. L. (eds.) Membrane Fusio n , Elsevie r /Nort h- Holland, Amste r dam, 1978. (2) Cib a Foundati on , Cell Fusio n , Pit ma n, London, 1984. (3) Poste , G. and Al liso n, A. C. (19 73) Bio c him . Bio p h y s . Acta . 300, 401-465. (4) Beers, R. F. Jr. and Bassett , E. G. (eds) Cell F.露io n, Gene Transfe r and Transfo r mati on , Raven, 1984. (5) Whit e, J., Ki el ia n , M. and Heleniu s , A. (1983) Quart. R ev. Bio p h y s . 16, 151 -195. (6) Dantr y-V arsat, A. and Lodis h , H.F. (1984) Sci. A m. 250(5), 48-54. (7) Pasta n , I. and Wi lling h am, M. C. (19 83) Trends Bio c hem. Sci . 8, 250-254. (8) Pearse, B. M. F. and Brets c her, M. S. (19 81) Ann. Rev. Bio c hem 50, 85-101. (9) Pap a hadjo p o ulos, D . and Poste , G . (1979) Meth o ds Membrane Bio l . 1 0, 1-121 . (10 ) Wi lsc hut, J. and Hoekstr a , D. (1983) Trends Bio c hem. Sc i. 9, 474-483.
기 간격 연 정 16,178,279 감국화 228 감각전이 263 견고연접 16 경 쟁 저 해 170,199 공동운반 214 공생 29,304 광반응 325 과국화 267 광산화적 인산화 325 광합성 29 광체계 ll 331 광 채취 복합체 327 광 홉수계 325 균등기 33 근원세포 344 근소포체 207,237,261 기저막 20 기록전위 222 L 나사형 머리핀 가설 143 남조류 3o4 내 재 단백 질 46,45,90,160 C 능동운반 I62,I 다충막소포 63 당단백질 I33 단충막소포 64 대량이동 162 대식세포 298 동질효소 255 둘레지방질 Io8 E, 마찰계수 163 막 내부 입자 46
막시발 가설 141 막융합 343 면역세포 296 면역수용체 296 물질주성 269 미분주사 열량계 72 미세단 섭유 16,344,355 미세소관 16 미세융모 20 미소식세포 344 l::f 백혈구 291,296 반두과막 193 보결 분자단 317 부착연정 15 분배계수 165 분비 막소포 25,361 I 불두과 연정 16 분자단 운반 217 비가역 열역학 163 비경쟁적 저해 171 비광반옹 325 人 산란 분석기 365 산화성 인산화 28,306,319 삼겹구조 14,126 삼두몰농도 132 삼두충격 211 상도형 80 상분리 79,112 상전이 72,112,148 생체전기현상 220 세포벽 20 세포골격 16,355 세포연정 15 세포질 14 세포질 공간 294 소수성 120
소수성-광 표지 95 소포체 I 1,22,25,274 수송막소포 2, 수용성 단백질 90 수정 3 신경근 접합부 239 신경계열 270 신호가설 138 신호감지입자 139 신호서 열 138,274 신호전이 269 쌍극자 。 아 시발전압 224 액체결정 72 양천성분자 45, 역류수송 171 연락연접 16, 역상증발 67 엽록소 29,326 엽록체 11,29,324 용매사출 66 용해-확산 162 원핵세포 20 운반매체 171 운동신경세포 241 원주세포 264 원추세포 264 원형질막 11,l4 유사분열 다 이분자충설 127 z: 자국전위 222 자색 막 34,103,1:5 4, 209 적혈구 I32 적혈구막 48 전기화학전위 I 전압고정 226
전 상전이 76 접다당류 50 점도 163 정지전위 222 조면소포체 26,139,156,297 주변단백 질 45,90,160 종판전압 242 주변세포°석공간 2ll 지방질막 63 진핵세포 ll 철-유*황 단백질 3o9 초 원심분리기 33 촉진화산 162,169 침강평형 I78 E 루과계수 165 포 편모 291,340 평면확산 86 평면확산계수 I14,149 굴 해당작용 I97 핵막 II,22 핵 II 핵구멍 22 형광광표백회수방법 I53 형광성회복 87 형광항체 I5I 화학적 전위 기울기 I69 화학삼두 2I4,305,3I9 확산계수 87,I52 확산전위계수 I64 활동전위 222 활면소포체 26 회전 화산 86,II4 호르몬 수용체 I3
A acety lc holin e (Ach) 241 acrosome 345 acti n filam ent 15 acti on po te n ti al 222 acti ve tra nsp o rt 162,191 adeny la te cyc l ase 275 adherin g jun cti on 15 adrenal medular 375 ag o nis t 280 amp h ip h il e 45,52 amp ho te r ic in B 185 annular lip id 108 anti vi r u s pr ote i n ( AVP) 303 ap o lip o p ro te i n A-1 98 ap oc y toc hrome c 97 Arrheniu s eq u ati on 114 'Na .. , K~ATPase .19 2 Ca2~ ATPase 108,207 ATP sy n th e ta s e 334 atr a cty la te 177 axon 221 B bacte r io r hodop si n IO3,I I4,I 54,209,3 Band 3 I32,I52,I54,I97 basement membrane 20 bio e lectr i c ph enomena 220 black lipid membrane(BLM) 63 blue-g ree n alga e 304 bulk movement 函 C carboxy fluo rescein 367 cardio l i pin 37 cascade mechanis m 288 cata l ase 32 carote n oid 330
cell jun cti on 15 cell wall 20 cerebrosid e 39 chemi ca l po te n ti al gra die n t 169 chemi os moti c the ory 214,319 chemota x is 269,291 chlorop la st 11,29 chlorop yll 29 choleste r ol 43,71,87 chondroit in sulfa te 254 chromaff in gra nule 375 citri c ac id cy cl e 28,306 clath rate 53 Coenzy m e Q 306 collag en 254 communic a ti ng jun cti on 16 comp e ti tive inh ib i t ion 170,199 comp le ment 301 connexon 178,270 cotr a nsp o rt 214 counte r -tr a nsp o rt 171 criti cal mi ce lle concentr a ti on (cmc) 56 Curare 241,243 cyc l ic gu anid i n e monop ho sph ate (cGMP) 264 cy toc halasin B 173,355 cyt oc hrome b5 3 11 cy toc hrome c 97,3 u cy toc hrome oxid a se 109,313 cy top la sm 11 cy tos keleto n 16,355 D dark reacti on 325 dendrite 221 desmosome 15 decane 106 dif fus io n 163 dif fer enti al scannin g calorim ete r
72,148,365 din i t ro p h enol 195 dip h th e ria tox in 181 dip ico lin i c acid (DPA) 367 dip o le moment 52 dis c oid a l comp le x 99 dockin g pro te i n 139 dop am i ne 290 drug deli ve ry sys t e m (DDS) 63 E end-pl a te po te n ti al 꾸 endocy tos is 346,349 endop la smi c reti cu lum 11,25 endosome 349 ep ine p h rin e 285 eukary o te 11 exocy tos is 274,360 extr i n s ic pro te i n 45 F facilitat e d dif fus io n 162,169 ferr edoxin 33 3 fibr oblast 303 flag e lla 291,340 flav in pro te i n (FP) 306,309 flip-flop 88 fluo rescein iso th i o c y a nate 151 fluo rescence recovery aft er ph oto b leachin g (FRAP) 87, 153 G ga lacto s yl tra nsfe r ase 91 ga ng lios id e 39 ga p jun cti on 16,178 Gib b s-Donnan equ il ibr iu m 193 gly c e rol 35 gly c eroli pid 35,37 gly c o calyx 50 gly c o g en ph osph o ry la se 277
gly c o lys is 197 gly c o p h orin A 133 gly c o p ro te i n 121, 1 33 gly c osami no g ly c an 254 gram i cidi n A 函 gran a 336 grou p tra nspo rt 217 H Halobacte r i um lzalobiu m 209 his t a m i ne 290 homog e niz e r 33 hy d razin e 233 hy d rop h obic ity 52,120 hy d rop h obic - p h o to - labelin g 95 hy d roxy la mi ne 233 hyp e rpo lariz a ti on 262,267 hy st e r esis 77 I im mune 269 im munog lo buli n 360 im p e rmeable jun cti on 16 inf l ue nza vir u s 350 ins uli n 285 int e g r al pro te i n 26,45 int e r fe r on 303 int r a membrane pa rtic l e (IMP) 16,46,133,259,346 int r i n s ic pro te i n 45,90 inv ert ed mi ce lle 78 ion op h oresis 241 iro n-sulfu r pro te i n (IP) 309 irr eversib l e the rmody n ami cs 163 iso zym e 255 L a-lacta l bumi n 91,376 lacto p er oxid a se 132 lacto s e 91
lacto s e pe rmease 216 lami na 22 large unil a mellar vesic l e 66 late r al dif fus io n 86 lecti n 147 leukocy te 291 lig h t harvesti ng comp le x 327 ligh t reacti on 탸 lipid bil a y e r the ory 127 lipo some 63 liq u id crys t a l l ine 72 lys o lec ithi n 353 lym p h ocy te 296 lys o some 11,29,31 lys o zy m e 97,211 M macrop h ag e 3ox mellit in 99 membrane tri g ge r hy po th e sis x4x mi ce lle 56 MHC 303 mi cro fi la ment 16,344,355 mi cr op h ag e 344,355 m1crosome 33 mi cro tu b ule x6 mi cro vil li 20,345 mi toc hondria xx ,28,304 mi tos is 23 monazomy cin x89 monolamellar vesic l e 64 moto r neuron 24x my el in 34,x27,23x my o blast 344 my o tu b ule 346 N NADH dehy d rog e nase 310 neurami ni d a se 147 neuromuscular jun cti on 239
non-comp e ti tive inh ib i t ion 171 norep ine p h rin e 290 nuclear envelop e 11,22 。 op si n 264 octo p a mi ne 290 orga nelle 11 osmoti c shock 211 osmolarity 132 ouabain 199 oxid a ti ve ph osph oryl a ti on 28,306 P pa ramy x ovir u s 349 pa rti tion coeff icien t 165 PAS-1 132,I52 pe rip h eral pro te i n 45,90 pe rip la smi c spa ce 211,294 pe p tido g ly c an 20 pe rmeabil ity coeff ici e n t 165 per oxis o me 29,32 ph ago cy tos is 301,355 ph ase dia g r a m 80 ph ase sep a rati on 79 ph ase tra nsit ion 72 ph loreti n 171 ph osph ati dy lc holin e 36 pho sph o die s te r ase 289 ph osph og ly c erid e 35 ph osph oryl a se kin a se 277 ph osph otr a nsfe r ase sys t e m . 218 ph oto s ys t e m 329 ph oto o xid a ti on 325 pino cy tos is 35 5 pla smalog e n 39 pla sma membrane 11,14 pla sto q u in o ne 330 po lye th y le ne gly c ol (PEG) 353 po rin 178
pre -tr a nsit ion 76 pro kar) ·o t e 20 pro sth e ti c grou p 四 pro to n moti ve for ce 319 pu rpl e membrane 103,209 pyran ose 169 pyru vate oxid a se 91 R Ranvie r 's n ode 231 reacti on cente r 326 resti ng po te n ti al 222 reti na l 209,264 roug h -surfa c ed endop la smi c reti cu lum 26 reverse ph ase evap o rati on 67 rhodop si n 264 rota t i on al dif fus io n 86 s sarcop la smi c reti cu lum 207,237,261 saxit ox in 234 Schif f's base 209 secreta r y vesic l e 25,361 sedim enta t i on eq u il ib r iu m 178 Semlik e Forest Vi ru s 135,352 Sendai vir u s 151,278,346 sereto n in 290 8-sheet I I9 sia l i c aci d 147 sig na l hy po th e sis 138 sig na l recog nition pa rt icle (SRP) 139 sig na l seq u ence 138,274 small unil am ellar vesic le 65 smooth - surfa c ed endop la smi c reti cu lum 26 solvent inj e c ti on 66 spe r mi ne 375
sph in g o li pid 39 sph in g o my el in 39 sti m ulati ng electr o de 222 Sto k e's eq u ati on 函 str o ma 29,325 subth r eshold po te n ti al 224 succin a te dehy d rog en ase 3 x o sym bio s is 29,304 sym p o rt 214 syn ap se 16,238,270 syn ap tos ome 256,289 syn exin 沿 T Tb 367 tet r a doto x in 234 thy la koid 29,304,325 TID 95,378 tigh t jun cti on 16 TN BS 129, 132 tra nsfe r in 359 tra nspo r t vesic l e 25 tri t on X-100 286 u ultr a centr i fu ga ti on 33 V valin o my c in 184 vis c osit y 163 z zwi• t ter •io n 45 zy m og e n 361 -I .:1.l OIU 一 8 .4 4 69 -8.0 3 48 Nonio n ic Sur fact a n ts (M. J. Sch
김형만 서웅대학교 문리과대 학 화학과 졸업 예일대학을 거쳐 크라크대학 이학박사학위취득(물리화학) 위스컨신대학 연구원과 교수 국방과학연구소 책임연구원 등 역임 현재 한국 과학기술원 생물공학과 교수 〈용액 내에서의 확산과 초원심분리법과 생체막〉에 대한 논문 다수 生 體 膜 대• 우학술총서 • 자연과학 찍은날 I987 년 12 월 I5 일 펴 낸날 1987 년 12 월 30 일 • 지은이 김형만 펴낸이 朴孟浩 펴낸곳 民音社 ■ 충판등록 1966. 5. 19 제 I·I42 호 우편대 체 계 좌번호 OIOO4·3I·523282 IIO 서웅 종로구 관철동 ”•I 734-4234 • 6IId (편 집 부) 734·2000 • 2IOI, 735·8, 나(영업부) ■ 값 8,000 원 파본은 바꾸어 드립니다. ©김형만, 1988 자연과학, 생물학 • KDC/ 5u • 3
대우학술총서 • 자연과학 I 소립자와 게이지상호작용 金祖흉 著 / 값 4, 800 원 2 動力學特論 李丙昊 / 값 5, 400 원 3 질소고정 宋承達 동 / 값 2, 800 원 4 相轉移와 臨界現象 김두철 著 / 값 2, 800 원 5 觸媒作用 陳宗植 著 / 값 2, 800 원 6 뫼스바우어分光學 王恒南著 / 값 2,800 원 7 극미량원소의 영양 昇正子著 / 값 6,500 원 8 水素化해素와 有機視素化合物 尹能民 著 / 값 5, 000 원 9 抗生物質의 全合成 姜錫久 著 / 값 9, 000 원 lO 국소적 형태의 A t iy ah - S i ng er 지표이론 지동표품 / 값 2, 800 원 11 Muco p ol y sacchar i des 의 生化學및生物珪學 박똔著 값 3,800 원 12 ASTROPHYSICS ( 天體物理學 ) 洪承樹著 / 값 4,700 원 13 프로스타글란딘 합성 金賢旺著 / 값 3,600 원 l4 천연물화학연구법 禹源植著 / 값 7 , 000 원 15 脂防營養 金淑喜著 / 값 6, J OO 원 16 結晶化유리 金炳蕙 著 ( 값 4, 500 원 17 高分子의 化學反應 趙義煥 著 / 값 4, 000 원 18 과학혁 명 金永植 著 / 값 4, 200 원 19 韓國地質論 童基弘 著 / 값 4, 000 원 20 정보이론 한영열 著 / 값 4, 500 원 21 原子核反應論 歸雲赫著 / 값 8,500 원 22 破壤力學 金相哲 著 / 값 4, 700 원 23 분자궤도이론 이익춘著 / 값 3, J OO 원 24 ~속도론 정경훈 홉파, 000 원 25 미분위상수학 李鉉求 示값 2 , 500 원 26 자기공명방법 좌}호툴 값 4, 8 00 원 27 플라스마물리학과 핵융합 최덕인 훌값 4 , 8 00 원 28 천문관측과 분석 李時雨 풀 값 4, 800 원 29 석탄에너지 변환 기술 金相敦 꼴 값 6 , 5 00 원 30 海洋續古生物學 白光浩 훌 값 6, 400 원 31 편미분방정식론 김종식暑 값 4, 00 0 원 32 大統-理論 소광십 舊값 5 , 000 원 33 金 屬電 子系의 多體理 論 金德洲 풀 값 6, 6 00 원 34 액정중합체 陳政 - 著 값 6,200 원 35 복합재료 檔肅仁 著 값,5, 200 원 36 단백질 생합성 朴仁星 풀 값 9 , 000 원 37 한국의鑛物種 金洙鎭졸 값 7 ,000 원 38 일반상대론 李哲勳著 값 5,000 원 39 레이저광산란분광학 金鍾鎭著 값 5,000 원 40 복소다양체론 金相文 蒼 값 7, 0 00 원 산 역학적 연구방법 金駐舜훌 값 4,200 원 42 핵구조물리학인 동설뭏 값 5, J OO 원 43 후리에해석과의마분작용소 김도한률 값 5 , 8 00 원 44 한국의 古生物 李河榮 著 값 9,0 00 원 45 질량분석학 김명수뭏 값 6 , 8 00 원 46 급변론 백현 뭏 값 5, 00 0 원 47 생체에너지 朱忠魯붉 값 8 ,500 원 48 리이만기하학 박윤룡 잡 값 6 ,00 0 원 49 群表現 論 朴勝安 법 / 값 6, 2 0 0 원 50 비선형 편미분 방정 식 론 하기식 著 / 값 6, 0 00 원 51 生 體膜 김형만 著 / 값 8, 000 원