
저자는 서울대학교 문리과대학 화학과 및 同대학원을 졸업하고, 벨륨, 겐트대학교에서 이학박사학위를 취득했다. 캐나다국립연구소 객원연구원, 미국위스콘신대학교 분자생물학교실 방문교수, 프랑스 국립보건의학연구소 연구원을 역임했으며 현재는 서울대학교 자연과학대학 화학과 교수로 재직중이다.
단백질 생합성 
 단백질 생합성
단백질 생합성
머리말 이 책은 지난 수년간 서울대학교 대학원 화학과 학생들에게 강의한 내용들을 바탕으로 하여 저술되었다. 단백질 생합성 반응둘은 백 수십 가지의 성분들이 관여함으로써 이루어진다. 나는 이 책에서 단백질 합 성을 관계되는 성분들의 구조와 기능에 중접을 두고 다루었다. tR ~A 의 아미 노아실화 과정 을 tR NA 의 구조와 아미 노아실-t RNA 합성 효소의 구조들 사이의 상호작용의 국면에서 다루었으며, 리보송 상에서의 펩 티드 결합 형성의 개시, 연장 및 종결 과정들도 t RNA 둘, rRNA 들, mRNA, 리보송, 리보솜의 성분 단백질들, 그리고 관계되는 인자들의 구조적 국면에 기초하여 다루었다. 단백질 생합성에 관한 책을 저술한다는 것은 너무나 방대한 일이어서 이러한 일을 계획해 본 적이 없었는데, 대우재단의 논저지원사업이 이 저술을 가능하게 하였다. 나는 이 저술을 통해서 단편적이었던 강의내 용들을 체계화하고자 시도하였으며, 가능한 한 최근의 연구결과들을 소 개하고자 노력하였다. 나는 이 책을 쓰는 동안 국내에서 구하기 어려운 단행본들과 연구 논문 등 귀 중한 자료들을 구해 서 보내 준 미 국의 Bowlin g Green 대 학교 생 물학 과 김영희 박사, 이 책을 쓸 수 있도록 늘 격려해 주고용기를 북돋워 주 었고생물학용어문제들에 있어서 귀중한 도움을준 서울대학교동물학과 강만식 박사, 그리고 연구비를 지원해 준 대우재단과 이 책을 훌륭하게 편집해 준 민음사 편집부 여러분둘에게 심심한 사의를 표하는 바이다. 이 책 이 학생들의 공부에 조금이라도 도움이 된다면 처자는 그 이상 바랄 것이 없겠다. 독자 여러분들의 비평과 조언은 불완전한 이 저서를 완성시키는 데 크 게 도움이 될 것으로 믿는 바이다. I986 년 4 월 朴仁源
단백질 생합성·차례
머리말 3서문 11제1장 tRNA 및 아미노아실-tRNA 합성효소들 141.1 tRNA의 발견 151.2 아미노아실화반웅 161.2.1 화학양적 관계와 에너지 역학적 관계 161.2.2 아미노아실-tRNA의 구조 171.2.3 아미노아실화 반응의 교정 201.2.4 분석범 271.2.5 양이온들에 대한 요구 271.3 아미노아실-tRNA 합성 효소들의 구조와 특이성 281.3.1 한 아미노산에 대한 효소들의 복수성 281.3.2 효소의 구조 281.3.3 기질 특이성 331.3.4 세포들에 있어서의 합성효소들의 조직 341.4 tRNA의 구조 351.4.1 개요 351.4.2 단백질 생합성에 있어서의 tRNA의 역할 361.4.3 한 아미노산에 대한 tRNA종들의 복수성 371.4.4 tRNA의 일차구조와 이차구조 391.4.5 tRNA의 일반적 특징 및 기능 421.4.6 tRNA의 변형된 누클레오시드들 461.4.7 tRNA의 변형된 누쿨레오시드들의 기능 511.4.8 tRNA의 결정구조 541.4.9 용액에 있어서의 tRNA의 형태 671.5 아미노아실-tRNA 합성효소-tRNA 인식작용 731.5.1 합성효소-tRNA 상호작용의 물리적 국면들 741.5.2 인식 작용의 분자적 근거 78
1.6 미토콘드리아에서의 암호 해독 911.6.1 미토콘드리아의 tRNA들 911.6.2 미토콘드리아의 유전암호 94* 참고문헌 95제2장 리보솜의 구조와 기능 1012.1 리보솜의 구조와 기능에 대한 개요 1032.1.1 리보솜의 기능 1032.2 리보솜 단백질들의 비교법 1062.3 리보솜의 단백질들 1072.3.1 리보솜 단백질들의 일차구조 1102.3.2 리보솜 단백질들의 이차구조 1152.3.3 리보솜 단백질들의 삼차구조 1192.3.4 리보솜 단백질들의 모양 1232.4 원핵세포의 리보솜의 RNA들 1242.4.1 5S rRNA 1242.4.2 16S rRNA 1362.4.3 23S rRNA 1492.4.4 리보솜 RNA들의 기능 1552.5 원핵세포의 리보솜의 구조 1632.5.1 개요 1632.5.2 리보솜 입자들의 모양과 크기 1652.5.3 리보솜 단백질들의 공간 배열 1682.5.4 리보솜 내에서의 RNA들의 공간 배열 1822.6 원핵세포의 리보솜의 기능영역에 대한 Stoffler 모형 1872.6.1 30S 하위단위체 상에서의 개시 및 암호해독이 일어나는 부분의 위치 1872.6.2 50S 하위 단위체의 기능영역 1912.6.3 70S 리보솜 상에서의 기능영역 1952.7 원핵세포의 리보솜의 기능영역에 대한 Lake의 모형 1952.7.1 작은 하위단위체들의 기능영역들 1952.7.2 큰 하위 단위 체의 기능영역 198
2.7.3 70S 리보솜의 기능영역의 모형 2002.7.4 인식자리 2012.8 진핵세포의 리보솜의 구조와 기능 2052.8.1 개요 2052.8.2 진핵세포의 리보솜의 일반적 특성 2062.8.3 진핵세포의 리보솜과 폴리솜의 형태 2092.9 진핵세포의 리보솜의 성분들 2122.9.1 진핵세포의 리보솜의 단백질들 2122.9.2 인산화된 리보솜 단백질들 2192.9.3 진핵세포의 리보솜 RNA들 2222.9.4 진핵제포의 리보솜 입자들의 단백질 가수분해 및 핵산 가수분해 작용들 2332.9.5 그 밖의 성분들 2342.10 리보솜 성분들의 상호작용, 공간 배열 및 기능 2342.10.1 단백질들과 RNA들의 상호작용 2352.10.2 진핵세포의 리보솜 내에서의 단백질들 및 RNA들의 공간 배열 2382.10.3 리보솜 단백질들의 기능 2462.10.4 리보솜 RNA들의 기능 2492.11 리보솜과 막 사이의 상호작용 2532.11.1 자유 폴리솜 및 막에 결합한 폴리솜의 활동성 2532.11.2 자유 폴리솜 막에 결합된 폴리솜 사이에서의 리보솜 하위단위체들의 동적 관계 2542.11.3 자유 리보솜 또는 막에 결합한 리보솜의 화학적 성질들 2552.11.4 리보솜을 막에 결합시키는 성분들과 결합 메카니즘 2552.11.5 막에 결합한 폴리솜들로부터 폴리펩티드 사슬들의 방향성 방출 259* 참고문헌 264제3장 전령 RNA (mRNA)의 구조와 기능 2793.1 원핵세포에 있어서의 mRNA의 구조와 기능 2793.1.1 다시스트론성 mRNA 2793.1.2 개시 코돈은 보통 AUG이다 2833.1.3 개시 코돈 주위의 연속부분 2863.2 진핵세포에 있어서의 mRNA의 구조와 기능 291
3.2.1 진핵세포의 mRNA 들은 단일시스트론성이다 2913.2.2 AUG가 유일한 개시 코돈이다 2943.2.3 전사후 변형 2953.2.4 5' 끝에 있는 번역되지 않는 연속부분 3003.2.5 3' 끝에 있는 번역되지 않는 연속부분 3073.3 세포소기관의 mRNA 3083.4 mRNA의 구조의 변형으로 생기는 결과 310* 참고문헌 311제4장 단백질 합성의 개시과정 3174.1 원핵세포에 있어서의 단백질 합성의 개시과정 3184.2 E.coli의 개시 인자들의 성질 3194.3 70S 개시 복합체를 형성시키는 개개의 부분 반응들 3204.3.1 70S 리보솜의 해리 3204.3.2 30·IF-1·IF-2·IF-3 복합체의 형성 3214.3.3 30S 개시 복합체의 형성 3214.3.4 30S 개시 복합체의 형성과 IF-2의 재이용 3314.4 원핵 세포에 있어서의 개시 과정에 관한 결론 3344.5 진핵세포의 개시 복합체 형성과 관련된 성분들 3354.5.1 개시 인자들 3374.5.2 개시 인자들의 기능을 보조하는 인자들 3404.6 개시 인자들의 물리적 성질들 3424.7 80S 개시 복합체의 조립에 관여하는 부분 반응들 3424.7.1 진핵세포의 리보솜 하위단위체 풀의 생성 3424.7.2 삼성분 복합체 형성 3434.7.3 삼성분 복합체와 40S 하위단위체와의 결합 3444.7.4 mRNA의 결합 3454.7.5 단백질 합성의 개시 과정에 있어서의 5' 갓의 역할 3464.7.6 갓 결합 단백질 3474.7.7 40S 리보솜 하위단위체에 의한 진핵세포의 mRNA의 AUG 코돈의 인식 3484.7.8 mRNA 결합에 있어서의 ATP의 역할 3514.7.9 80S 개시 복합체의 형성 352
* 참고문헌 353제5장 단백질 합성의 연장과정 3595.1 원핵세포의 연장인자들 3615.1.1 물리적 성질 3625.1.2 EF-Tu의 기능 3625.1.3 EF-Ts의 기능 3645.1.4 EF-G의 기능 3655.2 원핵세포의 리보솜 상에서의 연장 3675.2.1 아미노아실-tRNA의 리보솜에의 결합 3675.2.2 펩티드 결합 형성 3685.2.3 원핵세포에 있어서의 자리옮김 3735.2.4 GTPase의 작용 및 연장에 있어서의 GTP의 역할 3765.3 진핵세포에 있어서의 연장인자들 3765.3.1 물리적 성질 3775.3.2 EF-1의 기능 3785.3.3 EF-2의 기능 3815.4 진핵세포의 리보솜 상에서의 연장 3865.4.1 펩티드 결합의 형성 3865.4.2 자리옮김 386* 참고문헌 387제6장 단백질 합성의 종결과정 3916.1 종결 코돈 3916.2 무의미 돌연변이의 억압 3946.3 방출인자들 3996.4 종결 코돈 인식 4006.5 RF-3 및 GTP 가수분해의 요구 4036.6 펩티딜-tRNA의 가수분해 4046.7 RF가 결합하는 리보솜의 자리 4066.8 펩티드 사슬 종결 단계에서의 조절 407
* 참고문헌 408제7장 단백질 합성의 방해물질들 411개요 4117.1 원핵세포에 대한 항생물질들의 작용방식 4227.1.1 단백질 합성의 개시 및 종결에 미치는 영향 4227.1.2 생체 내에서의 푸로마이신 반응에 미치는 항생물질들의 영향 4227.1.3 리보솜의 GTPase 반응들의 방해 4247.1.4 유전정보의 오독 4257.2 원핵세포의 리보솜에서의 항생물질의 결합자리 4267.2.1 자연상태의 항생물질의 리보솜에의 결합 4267.2.2 항생물질의 친화표지 유사체의 리보솜에의 결합 4277.2.3 리보솜의 부분적 재조립법에 의한 항생물질 결합자리의 조사 4297.3 항생물질에 대한 원핵세포의 리보솜의 저항성 4307.3.1 리보솜 단백질들에 의해서 결정되는 저항성 4307.3.2 리보솜 RNA에 의해서 결정되는 저항성 4317.3.3 티오스트렙톤에 대한 저항성 4327.4 진핵세포에서의 개시반응의 방해물질들 4347.4.1 개시 tRNA의 인식을 방해하는 물질들 4347.4.2 mRNA 인식 (단계 b)의 방해물질들 4377.4.3 하위단위체의 결합(단계 C1)의 방해물질들 4387.4.4 개시 tRNA가 주개 자리에 자리잡는 것을 방해하는 물질들 4387.5 연장반응의 방해물질들 4387.5.1 아미노아실-tRNA 인식 (단계 d) 방해하는 물질들 4397.5.2 펩티드 결합 형성의 방해물질들 4417.5.3 자리옮김 (단계 f)의 방해 물질들 4427.6 진핵세포에서의 종결의 방해물질들 443* 참고문헌 443색인 447서문 D NA 의 이중 나사선 구조가 알려진 이후로 유전적인 복제, 즉, 세포 내 에서 의 염 색체의 복제 를 화학적으로 설명할 수 있게 되었다. 이중 나사 선 형 구 조 는 구아닌 (G) tt시 토신 (C) 그리 고 아데 닌 (A) tt티 민 (T) (RN A 에 있 어서는 우라 실 (U)) 등과 같은 수소결합에 의한 염기 짝지움 에 기 인됨 이 알려졌다. 이 염기 짝지움은 모든 유형의 유전정보의 전 달에 있어 서의 추진력이 되고 있다는 것이 분명해졌다. 세 가지 전사 과 정들 , 즉 세포분열이 일어날 때의 DNA 의 복제, 레트로비루스들의 증식 이 일어날 때의 RNA 의 DNA 로의 전사 및 전령 RNA 를 합성하 기 위 한 D N A 의 RNA 로의 전사들은 모두 염기 짝지움의 바탕에서 일 어나고 있다. 그뿐 아니라, 전령 RNA 의 암호를 단백질로 번역할 때도 전령 R N A 와 아미노아실-t RNA 사이의 At tU 및 Gt tC 등의 염기 짝 지움 메카니즘에 의해서 일어나고 있다. 폴리누클레오티드합성의 모든 경우에 있어서, 합성되고 있는 사슬에 재로 첨가 될 부분의 배열은 주형에 있는 염기와의 상보적인 수소결합 으로 이루어지며, 누클레오티드 삼인산에서 얻는 에너지를 이용하여 바 로 앞에 있는 누클레오티드와 결합한다. 풀리누클레오티드로부터 폴리펩티드의 아미노산 결합순서로의 번역에 있어서도 유사한 메카니즘이 적용될 것이라는 Cr ic k 의 제안은선견지명 이 있는 예언이었다. 찰 알려져 있는 바와 갈이, 이 목적을 만족시키려
면 아미노산울 특이하게 결합할 〈아답터〉가 있어야 하며, 이 아답터는 아미노산에 독이한 삼중체를 가지는 작은 폴리누클레오티드 운반체이고 산중체가 폴리누클레오티드 주형 상의 자기 자리에 놓이게 될 것이라고 재안하였다 . 실제로 이러한 아답터의 역할을 하는 t RNA 가 발견됨으로 써 아담터 가설이 옳다는 것이 증명되었다. 아미노산 암호전달은 생물학에 있어서 가장 홍 미있는 현상들 중의 하나이다. mRNA 상의 코돈과 t RNA 상의 역코돈의 상호작용이 있음으 로 하여 DNA 에 저장된 정보가 생명의 가시적 형질 의 형태로 표 현 될 수 있는 것이다 . 누클레오티드 삼중체들로 이루어지는 아미노산 코돈 들 에는 64 가지의 조합이 가능하다 . 단백 질을 만드는 아미 노산들의 종 류는 20 여 가지 가 있다. 그러므로, 한 아미노산에 대한 코돈은 여러 개가 있게 된다. 둘째 문자 u c A G 麟} Phe uucccu l Ser \ UU.A.\C;} Ty r I UUGG C鬪 Cy s I uC u UUUUAGJ}L e u UUCCAG UUAAAG AOMCHBRERE UUGGGA TAMrpB ER AG 자 문째첫AC AcCCAACAUUUuUUUUCAGGACuU llM LIleeeuut AAACCCACCCCCCCCCGAUCAGUC PTrhor I 麟AACCCCAAAAAA A G 깁깁 } } GHALsyii s u ps N N AAACCCCAGGGGGGGGUCAUGCAG} J} SA Aerrrg g AGuACGuC I 세까문자 G GGUUUC Val GGCCCU l Ala GGAAUC} Asp GGGGCU Gly uC GGUUGA GGCCGA GGAAAGJ}G !u GGGGAG AG . 유전암호 유전암호
사실, 64 가지의 코돈들 중 종결 코돈의 역할을 하는 제 개몰 제외한 나머 지 61 가지 의 코돈둘은 20 가지 아미 노산의 암호문이 되 고 있다. 코돈둘의 중복성 (또는 축퇴 성 ) 은 Cric k 로 하여 금 코돈-역 코돈 인 식 작용예 대 한 〈동요〉가설 을 제 안하게 하였다. 이 가설 은 후에 많은 t RNA 들의 역코돈의 결합순서가 알려침으로써 실제로 옳다는 것이 확 인되었다. 진핵세포의 미토콘드리아에서 불 수 있는 의견상 예의적인 코돈의 경우를 제의하면, 코돈둘은 모든 생체에서 보편적인 암호로 읽히 고 있다 ( 표 1-10 과 비교하라). 동요 가설에 의한 코돈의 세번째 염기와 역코돈의 첫번째 염기와의 짝짓기 역코돈 의 첫째 염기 코돈의 세째 영기 ucAG 십 G
uuCl J止g5 단백 질 합성장치는 약 200 가지의 고분자 물질들(핵산들 및 단백질 둘 ) 아 관여하고 있는 것으로 믿고 있으며, 펩티드 결합 형성에 있어서 의 그들의 상호작용에 관해서는 많은 것이 알려져 있지만 그들의 상호 작용의 자세한 메카니즘은 확실히 알려져 있지 않다. 여러 성분들(또는 인자들) 중에서도 리보솜의 구성성분들의 경우가 목히 그러하다. 단백질 합성은 전령 RNA 의 지시에 따라서 티보솜 상 에서 단계적으로 일어난다. 단백질 합성 과정을 이해하려면 여러 의문 들이 해결되어야 한다. 전체 과정에 있어서의 개개의 단계들의 본질은 무엇인가? 각 단계에서의 분자적 반응 메카니즘은 무엇인가? 이 단계 들을 촉매하는 것은 무엇인가? 고도의 충실도와 정확도로 일어나는 단 백질 합성에 있어서 오차의 교정은 어느 단계에서 일어나는가? 단백질 합성의 여러 단계에서 일어나는 단백질 • RNA 및 단백질 • 단 백질 복합체들의 구조와 그들의 기능적 형태변화가 밝혀져야 단백질 합 성의 본질을 이해할 수 있게 될 것이다.제 1 장 tR NA 및 아미 노아실-t RNA 합성 효소들 1.1 t RNA 의 발견 유전정보의 흐름에 있어서 매우 중요한 고리들 중의 하나는 주어전 아미노산이 전령 RNA 상의 염기 삼중체와 회합하는 단계이다. 유전적 표현의 정확성은 단백질 합성에 있어서의 정확성에 의해서 결정된다. 특 히, 전령 RNA 코돈에 의한 아미노산 선택의 정확성으로 결정된다. 이 선택과정은 아미노아실화된 t RNA 가 전령 RNA 의 코돈과 서로 목 아하게 작용하는 리보솜 상에서 일어난다. 그러나, 단백질 합성의 정확 성은 리보솜 상에서 일어나는 사건들에 의해서만 결정되는 것아 아니라 그 이전에 일어나는 사건들, 즉, 아미노아실-t RNA 합성효소에 의해서 아미노산들이 개개의 t RNA 에 결합하는 반응에 의해서도 결정된다. 생 물에는 특정한 tR NA 분자들에 특정한 아미노산을 결합시키는 이러한 합성 효소들아 20 여 가지 가 있다. 아 직 t RNA 가 발견되지 않았던 1955 년에 Cr i ck 가 사신으로 회람시 킨 그의 아담터 가선 (후에 간단한 논문형식으로 발표하였음 (Cr i ck, 19 57) )에서 그는, 풀리누클레오티드 상의 한 벌의 염기둘은 물리화학적 작용으로 특정한 아미노산을 직접 인식하여 선택해낼 수는 없다고 지 적하였다. 그 당시, 이미, 단백질에 있어서의 아미노산들의 결합순서는 단백질마다 독특하며, 주형 RNA 의 누클레오티드 결합순서에 의해서
결정될 것이라고 생각되고 있었다. 이러한 사실을 논리적으로 설명굽1- 기 위해서 Cr i ck 는 아답터 가선을 제창하였던 것이다. 그는 아담터가 3 개 내지 6 개의 누클레오터드들로 이루어져 있을것이라고생각 했었 다 . 그는 또한 아미노산을 활 성화시 켜 서 아답터에 결합시키는 효소가 있 을 것이라고 예언하였다. t RNA 가 발견되기 이전에 이미, Hoa g land 는 아미노 산활성화효소들 이 있다는 것을 알았으며 (Hoag la nd, 1955), 이 효소들은 아미노 산에 목 이하며, 효소와 결합한 아미노아 실 아데닐산 을 발생 시 킨 다는 것이 밝혀 쳤다 (Ber g, 1956; Hoag la nd 둥 , 1956; DeMc ss 와 No Yelli, 195 6; Da vie 등, 1956). 그러나 이 효소가 아미노산 을 t RNA 로 전달하는 반응도 축 매한다는 것을 알게 된 것은 아미노산 을 받아 들 이는 t R);A 가 실제 로 발 견됨으로써 가능하였다 (Ber g와 Of en g a nd , 1958 ; Schweet 둥, 195 8). 개개의 t RNA 는 그 역코돈 고리에 유전 정보에 상보적인 깅 보 를 지 니고 있기 때문에, 유전 정 보 를 정확하게 단백질로 번역하기 위해서는, 아미 노산이 상응하는 tR N A 로 결 합되 는 반응들이 고도의 독 이 성 들 로 써 일 어 나야 한다 . 이 반응둘은 아미 노아 실 -tRN A 합성 효소들에 의 해 서 일 어 난다 . 아미 노아실 -tRK A 합성 효소들에 관한 훌륭한 평 론서 가 있 다 (Soll 과 Schim mel, 1974 ; Kalusek 와 Konig s berg, 1975 ; Of en g a nd . 1977 ; Sch im mel 과 Soll, 1979) . 1. 2 아미 노아실화 반응 1. 2. l 화학양적 관계와 에너지역학적 관계 아미노아실-t R N A 합성효소들은 단백질 합성에서 관건이 되는 역할 을 하는 한 부류의 효소들이다. t RNA의 아미노아실 화 반응은 보통 (1)-(3) * 식들로 나타낸다• AN + ATP + E' ~ £i•A N-AMP + PP (1) E1· A A-AMP + tR NN ~ AN-tR NN + AMP + E' (2) AN + ATP + tR NA ~ AN-tR NN + AMP + PP (3) • 깨AA글=자 아 i미는노 목산 정또한는 아아미미노노산신울기 ;표 시E한= 다환; 성 화.효 는 소 :비 공AA유- 결A합M 성P =상 아호마작노용아 을실 표아시데한닝다 산. , 어
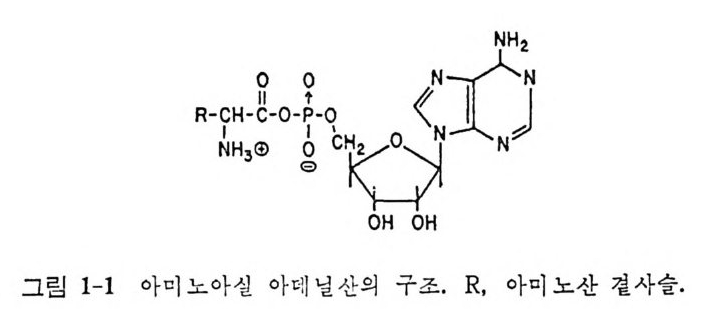
첫째 단계에서는 효소에 결합된 아미노아실 아데닐산(그림 1-1) 을 합 성하면서 피로인산을 방출함으르 써 아미노산들이 활성화된다. 둘째 단
 R-i HH :-o-l-oc::
R-i HH :-o-l-oc::
계 에서는 AMP 불 방출하 고자유 효 소 를재생 시키면서 아미노산이 tR ~A 로 전달된 다. 전체 반응 ( 3 ) 의 화학양적 관계는 정확하며, 반응은 가역 적 으로 일어난다 (Ber g 등 , 1961) . 위의 식으르 나타낸 전체 반응의 평 형 상수는 밭릴 -tR~ A 의 경 우 0. 32 이 고 (Berg 등, 1961) , 트레 오닐 -t R N A 의 경 우 0. 37 이 고 (Le a h y 등, 1960) , 아르기 닐-t RNA 의 경 우 0.2 5 등인 것으로 미 루어 보아 서 대개의 경우 1 보다 작을 것으로 생각 한 다. 그러므로 형성된 AA- t RNA 는 ATP 와 거의 같은 정도로 높은 예 너지 수준에 있다. 또한 아미노아 실 아데닐산은 기-전달 퍼텐셜이 크 며 , 중합 반응 들에 있어서 아미노 산의 아미노 기와 같은 친핵체에 아미 노아 실 기 를 전달하게 된다. 아미노산-t RNA 결합의 상대적 불안정도는 아미 노산의 종류에 따라서 달라지 지 만, 이 결 합은 약한 알카리 성 용액 에 서 매 우 불 안정 하다 (Chouste r man 등, 1966) . 안정 도는 아미 노산의 아미노 기 에 대한 이온 화 상수 (Hen t zen 등, 1972) 와 리보오스에 있는 안 접 한 히 드록시 기 의 존재 여 부 (St ri c k land 와 Jac obson, 1972) 와 관계 가 있 다. 리보오스의 C-2’ 과 C-3' 사이의 결합이 끊어져서 인접한 히드록시 기가 더 이상 인접해서 존재하지 않을 때와 (O f en g and 와 Chen, 1972), 또는 이 히드록시 기둘 중의 하나가 수소로 치환되었을 때는 (S p rin zl 과 Cramer, 1973) 가수분해 속도가 감소한다. 1.2.2 아마노아실-tR NA 의 구조 전체 반응의 생성물, AA- t RNA 는 t RNA 의 말단에 있는 아데노신의
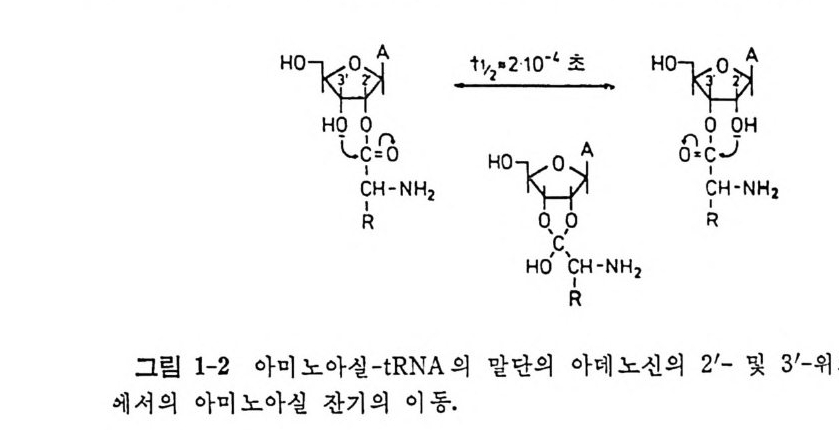
리보오스 부분의 2'- 또 는 3' -히드록시 기와 아미노산 사이의 에스테르 이다. 평 형 혼합물의 조성은 보통 3' -히드록시가 70% 이고 2' -히드록시 가 30% 이다. 두 이성실체둘의 반감기는 약 2x10 기초이다.
 HOHQ냐 QC~R요H - N H2 -t11H 2O• 2 집·1H 00O -` ' C, ’`0초C H -NH2 H0I O\雪 oCCRIII . H .)g~- NHH 2
HOHQ냐 QC~R요H - N H2 -t11H 2O• 2 집·1H 00O -` ' C, ’`0초C H -NH2 H0I O\雪 oCCRIII . H .)g~- NHH 2
에스페르 결합이 리보스오의 2' -위치에서 일어나는지 또는 3' -위치에서
 x 玉」 x~ x才 o{
x 玉」 x~ x才 o{
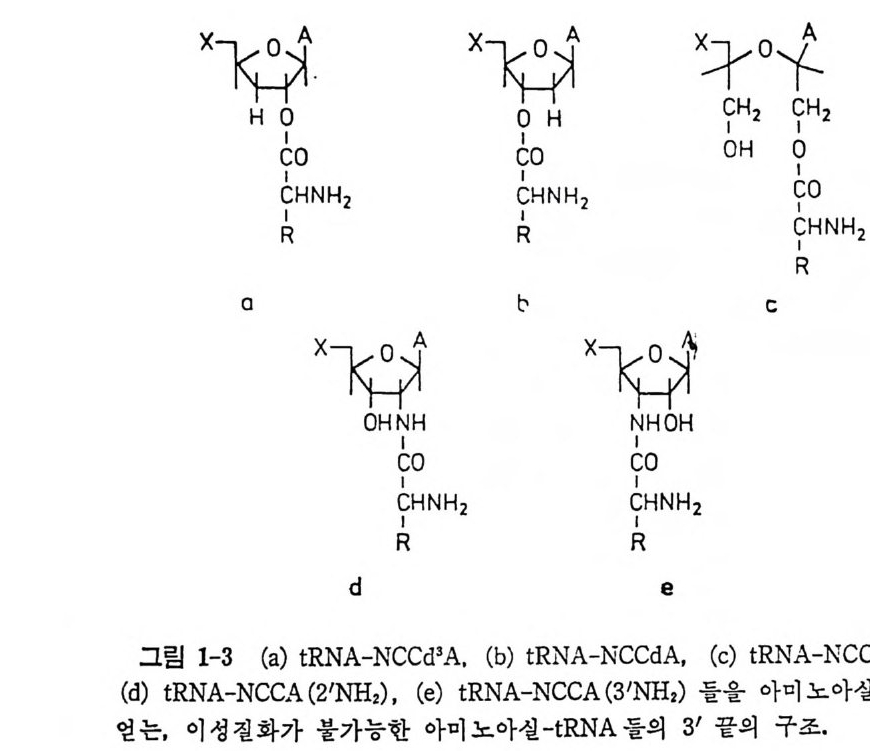
인어나는지는 오랫동안 해결되지 않고 있던 문제였다. 3'- 또는 2'- 위 치듄이 3 ' -데옥시아데노신 또는 2 ' -데옥시아데노신으로 변형됨으로써 이 성 질 화가 일어날 수 없는 tR NA 유사체들을 얻게 됨으로써 이 문제가 새로운 접근법으로 다시 연구되기 시작하였다(그립 1-3). 이 유사체들 은 효소로 아실화될 수 있다. 3 ' -데옥시아데노신 치환법으로 (S p r i nzl 과 Cramer, 1973), 또는 과요오드산 산화로 말단의 리보오스고리를 열고, 다음 에 환 원으로 히드록시 기를 재생시킴으로써 (Of en g a nd 등, 1974a) 두 경우 모 두 동족의 아미노아실-t RNA 합성효소들을 사용하여 완전히 아 미 노아 설 화 시킬 수 있었으며, 아미노아실화 반응은 2 ' -히드록시 기에 서 만 일어났 다. 효 모 이외의 다른 생둘종에서 얻은 한과 t RNAPhe 들 울 시험해 보 았웅 때 도 동 일한 결 과 를 얻을 수 있었다 (O fe n g and 등, 1974a ). 모든 경우 에 2 ' -히드록 실 의 아미노화가 90% 이상인 것으로 미 루어 보아, EPh c 에 의한 변 형 되지 않은 t RNAP h e 의 아미노아실화의 정상 적인 위치가 2 ' - 히 드 록 시 기일 가 능성이 크다. 그러나, 모 든 합성효 소 들에 대 해 서 사정이 같은 것은 아니다. 효모의 Es 과 E. (oh 의 EL) ’, EH1 ' , 그리 고 EGly 둘을 사용한 아실화 반응은 3'- 히 드록시 기 에 특 이 하 며 , E. coli 와 효모의 ET 과 E. coli 의 ECy ' 들과 같은 그 밖의 합 성 효소 들 의 경우 에 는 아실화되는 히드록시 기에 대한 독 이 성 의 차 이 를 찾 아 볼 수 없 었 다 (Cramer 등, 1975 ; Sp ri n z l 과 Cramer, 1975 ; Fraz e r 와 Ric h , 1975) . t RNA 둘 의 삼 차 구조 들 이 서로 유사할 것이라는 것과 아미노아실화반 응이 모든 t R N A 들 에 대해서 같은 부분에서 일어난다는 사실을 고려하 면, 2'- 또는 3 ' - 위치들 중 어디에서 아미노산의 결합이 일어날 것인가 는 t RNA 의 특성으로 결정되는 것이 아니라 독정한 합성효소들에 의해 서 결 정될 것이 확 실하다(표 1-1 을 보라). 이것은 직접적인 실험들로 확 인되었다 (S p r i nzl 과 Cramer, 1979). 효모로부터의 페닐알라닐-t RNA 합성 효소는 tR NAPh•-NCCd3A 만을 아미 노실 화시 키 므로 2' -에 스테 르화 효소이다. 이 효소는 E. col i로부터의 t RNALr’ 을 찰못 아미노아실화시켜 서 Phe- t RNA!.” 을 형성시킨다. 3' -에스테르화효소인 리실-t RNA 합성 효소는 t RNAL y s-NCCdA 만을 아미노아실화시키지만, 효모의 페닐알라 닐一t RNA 합성 효소는 E. coli 의 tR NALy s_ N CCd3A 를 페 닐알라닐화시 킬 수 있지 만 tR NALY•-NCCdA 를 페 닐 알라닐 화시 키 지 못한다. 아직은 여러 합성효소들 사이에서 보는 아미노아실화의 특이성들의
표 1-1 연옥시〉 t RNA 들을 효소로 아미노아실화시켜서 결정한 에스테르 화 반옹이 일 어 나는 초기 의 자리 (Sp r in z l 과 Cramer, 1979) 아미노산의 결합 아미노아실-t RNA 합성효소 특이성 E위. c치o li I 효위지모: I 소위의치 간 알라닌 3' 3/ 3' 아르기닌 2' 2' 2' 아스과라긴 2' 2', 3' 2', 3' 아스과르트산 미정 21, 31 3' 시스테인 2', 31 21, 3' 3' 글루타민 미정 3' 미정 글루탐산 2/ 미정 미정 글리신 3' 3' 3' 히스티먼 3' 3' 3' 이소루신 2' 2' 2' 루신 2' 2' 2' 리신 3' 3' 3t 메티오닌 2' 2' 미정 페닐알라닌 2' 2' 2' 프롤린 3' 3' 미정 세린 3' 3' 3' 트레오닌 3' 3' 3' 트립토판 2' 3' 3' | 발티린로 신 2안' ,3' 22'', 3' 22'', 3' I
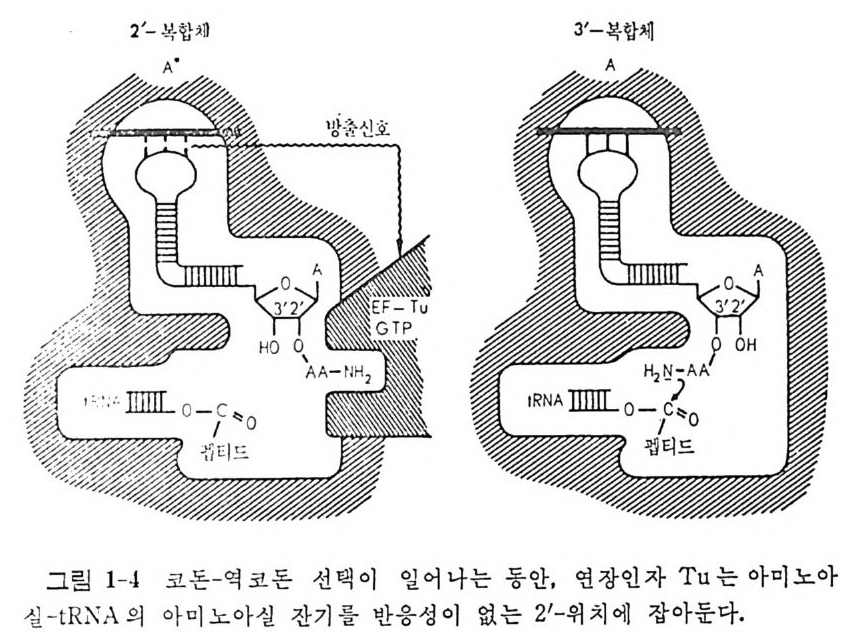
차이가 무슨 의미를 가지는지는 잘 모르고 있다. 단백질 합성의 연장 단 계에서의 EF-Tu • GTP 복합체와 AA- t RNA 의 인식작용에서 아마도 2' -이성체에 대한 특이성을 가지고 있기 때문에, 화학적 이동의 신속한 속도가, 본래 어느 히드록시 기가 아실화되었는지에 관계 없이 AA- t RNA 가 EF-Tu • GTP 복합체와 작용할 수 있게 할 것으로 생각된다 (그림 1-4). 1.2.3 아미노아실화 반응의 교정 E. co li에 있어서의 DNA 복제의 오차율은 중합되는 누클레오티드
 2 '- 복합체 3'- 복합 세
2 '- 복합체 3'- 복합 세
109 내 지 1010 개 당 하나이고, DNA 를 전사하여 그 RNA 를 단백질로 번역할 때의 전체 오차 을 은 결합 되는 아미노산 잔기 104 개 당 하나 정 도이다. 이 오차율은 간단한 효소들에 대한 열역학적 한계치 이하의 작 은 값 이 다. 그러 므로, 〈 교정 하는〉 메 카니 즘은 효소가 진화하는 과정 에 서 생겼을 것 이 틀림 없다. 중합 반응에 관여하는 효소들은 합성 반응을 촉매하는 활성 자리 이 외 에 도 잘못된 중간물질들이 생기자마자 분해시키는 가수분해 자리를 진화시켰 다. 그러므로, 합성 과정은 착오둘이 영구히 결합되기 전에 그 것들 을 제거시키기 위해서 각 단계에서 이중으로 검열을 받게 된다. 아미노산의 활성화 반응은 반응식 (1) 과 (2) 로 나타내는 이단계 반응 이다. 원칙적 으로는, 두 가지 선택과정이 있다. 먼저, 효소에 의한 올 바른 아미노산의 식별 이고, 그 다음에는 올바른 t RNA 의 인식이다. t RNA 들은 큰 분자이기 때문에 식별에 필요한 독특한 구조적 차이의 원안이 될 수 있는 요인들이 많아서 t RNA 의 인식에는 별문제가 없다. 그러나, 아미노산들은 작은 분자이고 일반적으로 구조가 매우 유사하기 때문에 그 들을 식별하는 데에는 엄격한 독이성이 있어야 한다. 한 아미
노산과 그의 동족체를 구별함에 있어서의 어려움은 알라닌과 글리신의 예에서 볼 수 있다. 알라닐-t R~A 합성효소의 활성 자리에 있는 등공 은 알라닌을 받아들이기에 충분히 크기 때문에, 이 동공은 더 작은 글 리신을 쉽게 받아들일 수 있다. 두 아미노산 들 사이의 식별은 효소와의 결합 에너지들의 차이에서 생길 것 이다. 이러한 둔 제 는 이소 루실- t RNA 합성효소와 발린, 그리고 트레오닐_t RNA 합성효소와 세린의 경우도 마 찬가지이다• 다른 한편, 옳은 기질보다 큰 아미노 산들은 , 활성 자리가 너무 작기 때문에 생기는 입 체적 인 장애로 인하여 효과적으로 재거된다 . 아미 노아실-t RNA 합성 효소들은 더 작은 아미 노산들을 활성 화시 키 는 단계 (반응식 1) 에 서 착오들을 범 할 우려 가 있지 만 아미 노산동을 tR XA 로 전달하는 단계에서는 상당히 정확하다는 것 이 이미 실첩직으로 안려 쳐 있다. 부분 반응(반응식 1) 의 정확도가 작은 데 비해 전체 반응의 정확 도는 크다는 모순은 Norris 와 Berg (l965) 의 실 험 으로 그 이 유를 설 명 할 수 있는 실마리를 얻게 되었다. 〈옳은 반응〉에서 생기는 E11 • ·lle-A:\1IP 복 합체와 〈옳지 않은〉 반응에서 생기는 E11••Val-AMP 복합체에 tR NAC 을 첨가하면 아래의 식들로 나타낸 바와 같이, 옳지 않은 복합체는 각 성분으로 가수분해되었으며, 옳은 복합체는 Ile- t RNA11• 을 형성시켰다. E11•-AMP 브~ Ile-tR NN1• + E11• + AMP (4) E11• •V al-AMP 으~ Val + tRN A11• + E11• + AMP (5) 이러한 발견이 있은 뒤에, 아미노아실-t RNA 합성효소들이 아미노아 실-t RNA 에 대해서 약한 에스데르 가수분해효소라는 것을 알게 되었 다. 이 에 스데 르 가수분해효소로서 의 활동성 은 잘못 아실 화된 tR NA 에 대 해 서 더 크다는 것 을 알게 되 었 다 (Eldred 와 Schim mel, 1972 ; Yarus, 1972). 발릴-t RNA 합성효소에 의한 아미노산 활성화의 교정 반응이 어 떻게 일어나는지에 대해서는 Fersh t의 연구진에 의해서 많이 연구되었 다 (Fersht 와 Kaeth n er, 1976 ; Fersht 와 Din gw all, 1979a) . 옳지 않은 아미노산(예, 발린과 입체구조가 거의 비슷한 트레오닌, 또는 메틸렌기 하나가 적 은 a- 아미 노부티 르산) 은 정 상적 으로 활성 화되 어 tR NAVa1 으로 전달된다. 그러나, 찰못 아실화된 t RNA 는 효소에 부착된 상태에서 신 속하게 또 특이하게 탈아실화된다.
EV•1, Thr-AMP .3.t.6.R: = sN..e:A..c:V..':a >l AMP-EV•1 •Thr-tR NA매v 4우0 •s다1e르c게~' Ev•1 + Thr + tRN Av•I (6) 합성 반응의 활성 자리 에 결 합하는, 아미 노아실화 반응의 정 상적 기 질 들 이 잘못 아실화된 t RNA 에 대한 가수분해 반응의 방해물질이 되지 않 는 것으로 미루어 보아서 활성 자리와는 다른 별개의 가수분해 자리가 있 다는 것을 안 수 있다. 발릴 -t R N A ' 1 의 발릴-t R~A 합성효소에 의한가 수분해 속도는 불과 0. 015 sec-1 이 라는 것을 참고로 알아 두자. 옳계 형 성된 아미노 아 실 -t R NA 도 상응하 는 합성효소에 의해 서 가수분해되지 않 는 컷은 아니지만 그 반응 속도가 매우 느린 것이다 . 위 에 서 말한 실 험 적 관찰들에 근거 하여 Fersht 등은 아미 노산들의 식 벌 작용은 그 크기와 화학적 특성에 따라서 두 자리 (활성화 자리와 가 수분해 자리)에서 일어난다고 제안 하였다 (Fersh t, A., 1977; Fersh t와 Din g w all, 1979b) . 먼 저 이 소루실 -tR N A 합성 효소의 경 우를 살펴 보기 로 하자. 이 효소 는 이소 루신(옳은 기질)과 발린 (옳지 않은 기 질 , 그러나 입 체구조가 이소루신과 비숫하지 않음)을 활성화시킬 수 있다. 이 효소의 활성 자리는 이소루신을 받아 들일 수 있 을 만큼 충분히 크기 대문에 발 린도 물론 받 아 들인다 . 그러나 그 가수분해 자리는 이소루신을 받아들이 기 에 는 너두 작은 편 이고 발린을 받아들이기에는 적당한크기를갖고있 는 된이다 . 또 한 , 이소루신보다 더 큰 아미노산은 활성 자리에서 거절당한다. 이 와 갈 이, 원하는 것을 선별하기 위해서 입체적 배척의 원리가 두 번 사 용된다. 위의 경우는 크기에 의해서만 선별되기 때문에 아주 단순하다. 트레오닌과 발린과 같이, 입 체 구조가 아주 닮은 아미노산들이 경쟁을 하는 경우는 그들의 화학적 특성들이 선별 요인으로 추가된다. CCHH33 / c-cNI H—3+ c0 - o- CHHOs/ c-cNIH -3c+0 - o- \H H I| \H H II L- 발린 L- 트레오닌 발릴-t RNA 합성 효소의 가수분해 자리 는 수소 결 합을 주고받는 자리 가 있어서 트레오닌의 히드록시 기는 결합되지만, 발린의 상옹하는 소수성
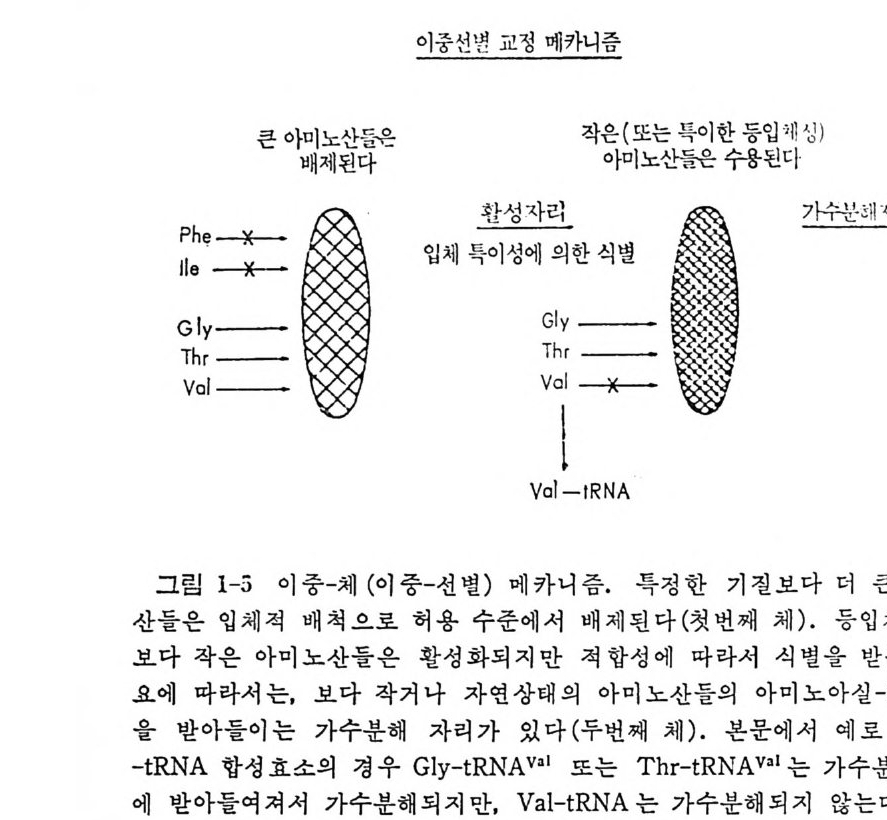 산그들립은PT h he1r 입v-a5체l一 」=二 적이 중배-척체’으 (로 이 중허이_중용선선별 수)변 준교메정에三카V 서메a니vThro 카l즘-배니t•R 즘제N A별一二 된 특다 정(한첫’ 번기째 질 체보)다.가 수 등더분 입해큰자체 리적아 이미고노
산그들립은PT h he1r 입v-a5체l一 」=二 적이 중배-척체’으 (로 이 중허이_중용선선별 수)변 준교메정에三카V 서메a니vThro 카l즘-배니t•R 즘제N A별一二 된 특다 정(한첫’ 번기째 질 체보)다.가 수 등더분 입해큰자체 리적아 이미고노
메틸 기는 배척될 것이다. Fersh t는 이 메카니즘에 대해서 〈이중선별 교 정 >( double- si e v e edit ing ) 가설 을 제 안하 였 다 (Fersht, 1977 ; 1979c) (그 립 2-5 를 참조하라). 이 자선은 많은 실험적 사실들을 찰 설명할 뿐만 아니라, 다음과 같은 예견도 가능하도록 한다. 교정을 받게 될 아미노산 둘은 옳은 기질보다 작은 것이거나, 옳은 기질과 비슷한 입체구조로 된 것들이다. 합성효소의 가수분해효소로서의 작용이, 상응하는 t RNA 의 CCA 말 단에 있는 2'- 또는 3'- 위치의 히드록시 기들이 직접 관여하는 반응이라 는 견해도 있다. 죽, 2' -위치에 아미노아실화되어 있으면 3' -위치의 히 드록시 기가 촉매작용에 직접 관여된다는 것이다 (I g lo i와 Cramer, 1978; Sp rinz l 과 Cramer, 1979 ; Cramer 등, 1979) . 앞에서 말한 반응식 5 의 경우, 만일 E11•.Val-AMP 복합체에 tR NAe
-N C CA 대신에 t RNA11•-NCCd3A 를 첨가하면 발린의 전달 반응이 제대 로 일어난다. 즉, E11• • Val-AMP + tR NA11•-NCCd3A -
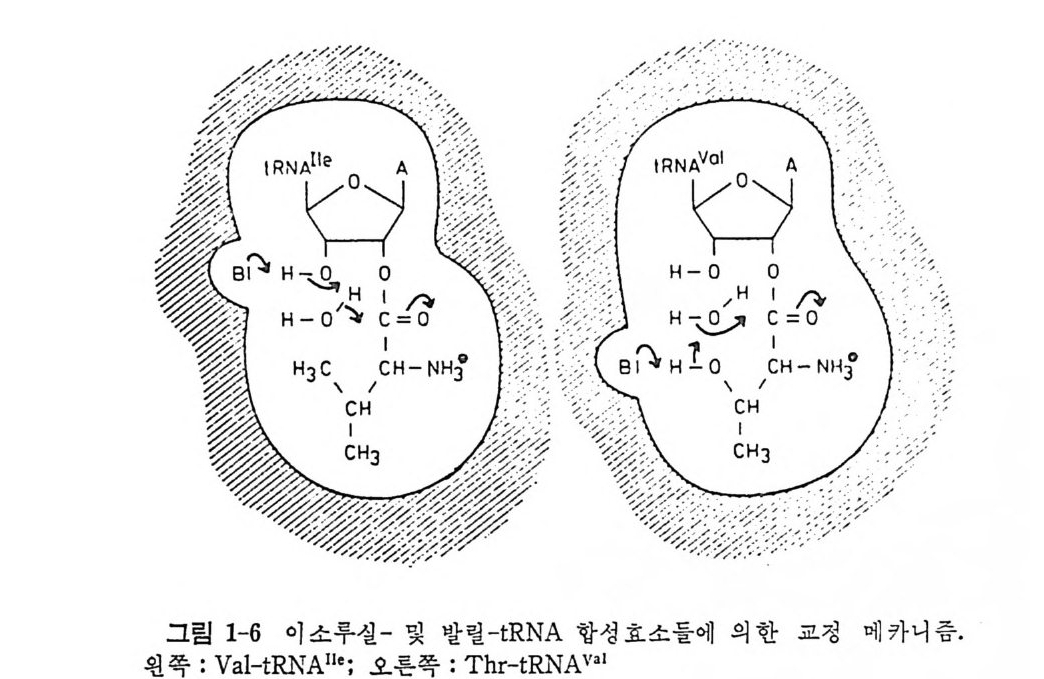
Val-tR N A11•-NCCd3A + AMP + E11• tR NAe 은 2' _히 드록시 기 에 아미 노아실화되 는 tR NA 이 기 때 문에 , 그 위치에 발린이 잘못 아실화될 수도 있는데, t RNA110-NCCA 를 첨가함 으로씨 E11•Val-AMP 복합체가 각 성분들로 해리된다는 것은 3' _위치 의 자유 히드록시 기의 존재로 가수분해가 촉진된다는 것을 암시한다 (표 1-2 와 표 1-1 을 참고하라) . 표 1-2 여러 가지로 변형된 효모로부터의 t RNAe 을 이소루실-t RNA 합 성 효소로 이 소우신화 또는 발릴화시 킬 때의 전환수 (S p r i nzl 과 Cramer, 1979). 효소의 목 이성 | 아미노산 t RNA 의 종류 I 전아환 미노수(아m 실 in 화 -1 의) I Ile Ile tRN A110-ACCA 62 tRN A1Ie-ACCd3A 45 tRN A11•-ACCdA 。 Ile Val tRN A110-ACCA 。 tRN A11'-ACCd3A 2. 9 tRN AII•-ACCdA 。 아미노아실-t RNA 합성효소의 기질-결합 주머니에 있는 표적에 상응 하는 인식 자리가 tR NA 상의 어디인지를 알아보고자 하는 연구들은지 금까지 성공적인 결론을 얻지 못하고있었다. 그렇지만, 위에서 말한바 와 같이 t RNA 의 말단의 아데노신의 2'- 또는 3' -위처의 히드록시 기들 이 합성효소의 기질 특이성을 결정짓는 데 관계가 있음을 알았다. von der Haar 및 Cramer 와 그들의 공등연구진들은 tR NNb•-CCA 의 유도 체 들인 tRN APhe-CC, tR NAp h e-CCF (F 는 아데 노신의 유사체 인 포르마 이 신이 다) , tR NNh•-CCd3A, 또는 tR NAPhe-CCdA 의 페 닐 알라닐-t RNA 합성효소에 의한 아미노아실화반응의 반응속도들을 측정하여 아미노아 실화는 아미노아실-t RNA 합성효소의 형태 의 전이를 두 단계에 걸쳐서 유발한다는 것을 알았다 (Von der Haar, 1978a). 세릴-, 트레오닐-, 이 소루실-, 및 발릴-t RNA 합성효소들을 사용한 실험들에서도 동일한 결 론을 얻 었 다 (Von der Haar 와 Cramer, 1978b) . 이 결 론을 다음과 같은식으로 나타낼 수 있다. EPh• + tR NA fh• ~ (EPb• • tR NNh•J1 ~ [EPh• · tR NN· '] 2 -----+ 단1 겨 l I 단2 계 II E+ 생성물 tR NAPh•-CCA 및 변형된 t RNAPhe 둘 은 신속히 결합하여 촉매로서 의 작 용 능력이 없는 복합체 I 를 형성한다. 이 복합체는 말단의 A 에 의해 서 촉매 능력이 있는 복합체 II 로 전이된다. 이 형 태 전이는 3 ' - 말 단의 A 에 있는 3'-0H 가 있어야 일어날 수 있다. 이러한 연구 결과들에 기초하여 van der Haar 등 (1979) 은 잘못 갑성화 된 아미노산의 교정에 관해서 3 ' -0H 와 물 분자가 관여하는 교 정 메카 니 즘을 제 안하였다 (그림 1-6) . 찰못 활성 화된 아미 노산은 합성 효소와 동
 /, ·.군/f ,/ • , '? ::.”· ' , ,r
/, ·.군/f ,/ • , '? ::.”· ' , ,r
종인 tR NA 의 3' -말단의 A 의 2'-0H 또는 3'- 0 H 에 참정 적 으로 전 달 된다. 그다음에 효소로 촉매되는 에스테르 결합의 가수분해가 일어나는 데, 그 반응 메카니즘은 관련된 아미노산의 구조에 따라서 달라진다. 이
소두십-t RNA 합성효소에 의한 발린의 찰못된 활성화의 경우에 있어서 는, 뭉 분자가, 없어진 메틸 기가 차지했을 자리를 차지하게 된다(그림 1-6 의 왼쪽)물 분자는 3 ' -0H 에 의해서 활성화되는데. 이와는 달리 발 릴 -tRN A 합성 호소의 경 우, 복합 체 안에 있는 아미 산 (찰못 활성 화된 아 마 노산 ) 에 있는 작용기를 사용하여 물 분자를 활성화시킨다. 이 경우에 있어서는 t RNAVll 의 2'- 0H 위치에 잠정적으로 결합된 트레오닌의 {3- OH 를 통하여 결합자리에 있는 물을 활 성화시킨다(그림 1-6 의 오른쪽 을 참조할 것) . 1.2.4 분석법 반 응 1 은 정방향 으로 일어나는 E·AA-AMP 의 형성을겔 거르기에 의 해서 측 정할 수 있고, 또한 아미노산 의존적으로 역방향으로 일어나는 ATP 로의 32p p 의 교환 반응을 측정 함 으로써 분석 할 수도 있다 (Santi 등, 1974). 반응 1 에서 3 까지 에서 찬 산으로 침전될 수 있는 것은 아미노산울 함유한 아미노아 실 -t RNA 뿐 이므로, 산-침전물에 결합된 방사성 아미노 산의 양을 측정함 으로써 아미노아실-t RNA 의 형성을 축정하는 것이 된 다. 이 분석법은 전체 반응, 즉, 반응 3 을 측정하는 것이다. 1.2.5 양이온들에 대한 요구 교환 반응으로 반응 1 을 분석할 때에는 M g 2+ 이 필요하다는 것이 오 래 전부터 알려져 있었다. 그러나, 매우 느린 속도로 일어나기는 하지 만 Mg 2 + 이 없는 조건에 서 도 AA-AMP 복합체들의 형 성 이 가능하다는 주장도 있 다. 그러나 후자의 경우에도, 그 효과는 한 효소 분자에 단단 하게 결합되어 있는 한 개의 Mg 2+ 이온의 존재에 기인한다는 것이 밝혀 졌 다 (Chouste r man 과 Chap ev il le , 1973) . 또한 M g 2+ 이 Mn2+ 으로 대치될 수 있는 경우들도 있다 (Yarus 와 Rash- baum, 1972) . :vl g 2+ 은 소량만이 필요하지만 활성화 반응에는 필수적인 반면에, t RNA 의 아미노아실화 반응에는 양이온돌이 전혀 필요하지 않다. 반응 2 에 요구되 는 Mg 2+ 또는 폴리 아민들의 기 능은 tR NA 의 구조를 안정
시키는 것으로 생각된다. 1. 3 아미 노아실-t RNA 합성 효소들의 구조와 득이 성 1.3.1 한 아미노산에 대한 호소들의 복수성 한 아미노산에 대해서 여러 가지 t RXA 들 이 있을 수 있지만 , 지금까 지 알려진 바로는 각 아미노산 에 대해서 한 가지 합성효소만이 촌재한 다. 정제된 단일 합성효소가 세포에 있 는 상 응하는 등수용상 t R:\A 동 (iso accep tor tR NAs) 을 모두 아실 화시 킬 수 있 다. 원 핵 세 프 에 있 어 서 , 여러 가지 방법으르 같은 합성효소에 독립적으로 유발한 돌연변이 등 이 같은 유전 자타에 위치한다는 것 이 알 려 져 있다. 또한, 순수한 효소 에 대한 항체는 조잡한 제포 추출액에 들어 있는 등수용 성 합성호소둘의 작 용을 방해한다. 위의 두 연구결과는 합성효소는 한 유전자 에서 오는 효 소임 을 암시 한다 (Loft fiel d, 1971) . 진핵 세포들에 있어서는, 한 가지 t RNA 들에 대해서 여러 합성효소 둘이 검출되지만, 그들의 존재는 세포소기관들과 관계가 있다. 미트 콘 드리아, 엽록체, 및 핵 등에는 많은 아미노산들에 대해서 별 도 의 합성 효소들이 존재한다. 전부가 그러한 것 은 아니지만, 세포소기 관에 들어 있는 몇 가지 합성효소들은 그들의 세포소기관 t RNA 들에 대해서 목 이하게 작용하고, 세포질의 합성효소들은 세포질 t RNA 들에 대해서 독 이성을 가지고 있다. 조사해 본 몇 가지 경우들에 있어서, 세포소기관 합성효소들의 유전자는 핵에 위치하고 있음이 밝혀졌다 (Bo g us lm Y sk i 등 1974 ; Hecker 등, 1974) . 1.3.2 효소의 구조 아미노아실-t RNA 합성효소들의 분자량, 하위단위체 구조들, 기질에 대한 결합 자리들의 수들을 표 1-3 에 요약하여 실었다. 합성효소들은 한 부류의 효소들이므로 분자량이 거의 같을 것으로 기대되지만 놀랍게 도 광범위한 분자량 값들을 가지고 있다. 예를 들면, E. col i의 경우만 을 보더라도 Glu-tR NA 합성효소의 분자량이 59kdal 달돈이고, Gly -
표 1-3 AA-tR NA 합성효소들의 분자량 및 하위단위체 구조 효소 I 분자량 (kdal) I 결합자리 수 아미노산 ( 충처) 1 유형 I a I /3 1 그갑:나아미 노산 I ATP J !겁p I tR NA It LHGLLHSMP:\eyerl liiyeeutours ss s/ tt 11( ( ( ({ ( ((e£ E ESE E효EH효r 1. ... . 1. .. 모 1 令occccsc\poo o o):to l /lcllll1l1 ilii aii)l) ) )) ) l/r1 m o1 s1- )1 r i 11111) aaaaaaaaaa22222222,8 I 44856646547826960036 46 11111199033782804505820452 22222 22242 22 212 II| .SQe crr 냐( 효닭 모간 ) ) aa2: 6600 112200 2 2 Trp l E. coli ) a2 37 74 2 2 Tr p ( 효 모 ) a2 50 110 TTrr pp \( 사소 람예 :ti隨 ) aa22 5548 111088 2 2 2 2 TTTArryyIt g)rnh: cc '<( . HEBrBr , ; 1...; . 1 .· 0osscc J/ 5!l1oo cc/h! ul1aai i/ 1rl))ru oo 1 ss-- aaaa2 :2 443485 ' 97975570 11--22 11-2 1~2 1 Ar1ryI c( 1r3; .1 1도 os p t) l c 1 a1 /r 1o 1-s a 78 1 1 LLGAlIeee lsuun p( £( (( ( EE8 효. . . . c ocsc/to1ocl) /ai1 )r) o - aaaa! 11100615920 1 11 11 111 I TVVVGPPahh laayltty ee llrhl z ,( \ (c((c( 효£ E / Er효후3rm..n.. 모 도習osccc pot)o o) e l/l 1laI it 1 ii)r) /) l o t ut-ss aaaaaaaa22 2 ;; 897044 363339 11121221114226760052070 1122 11 1222 1122 | PThrep (( 쥐L. l간u)te u s 씨 ) aa2, 74 69 229000 TTr y pr ((효물 모소) 뇌) aa43 115156 Schim mel 과 S611(19i 9) ; Ofe n g an d(l\J 77)
tR NA 합성 효소의 것 이 227 kdal 달튼이 댜 다른 생 물종에 서 얻 는 효소 는 더 큰 분자량을 가지는 경우도 있다. 다음으로 두드러진 특징은, 효소들이 여섯 가지 유형의 하위단위체구 조들, 즉, ab 야, a3, a4, a /3, 및 a2/3 2 형 들을 이 루고 있 다는 것 이 다. 하위단위체 구조들과 분자량들이 왜 이렇게 다양한지는 아직 그 이유 가 불분명하다. 아미노아실-t RNA 합성효소들의 구조들을 연구함에 있어서 으뜸가 는 관심들 중의 하나는 효소와 효소의 기질들, 즉, ATP. 아미노산 및 tR NA 돌 사이의 상호작용의 본질과 특이성에 관한 것이다. 매우 비슷 한 기능들을 가진 이 합성효소들이 그 분자량들은 다양 하 지만 단백 질 들 의 아미노산 결합순서들에 있어서 상동 부분들을 찾아볼 수 있을 것으 로 기대할 수 있다. 적어도 효소의 기질-결합 자리들을 구성하는 아미 노산 연속 부분들이 진화 과정을 통하여 보존되어 있을 것으로 기대할
 :-말단으로 ` ` 5
:-말단으로 ` ` 5
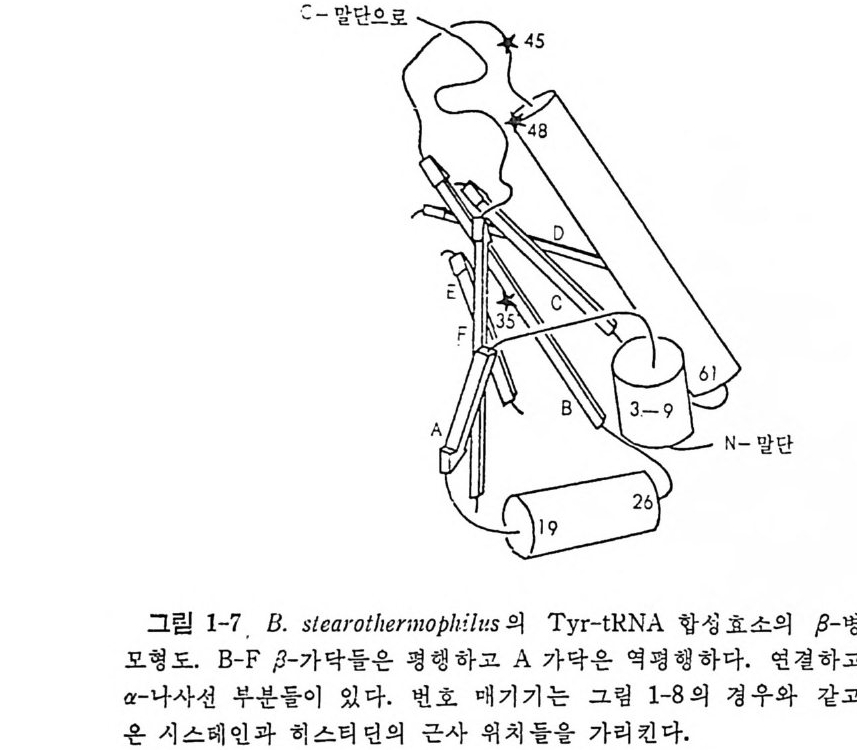
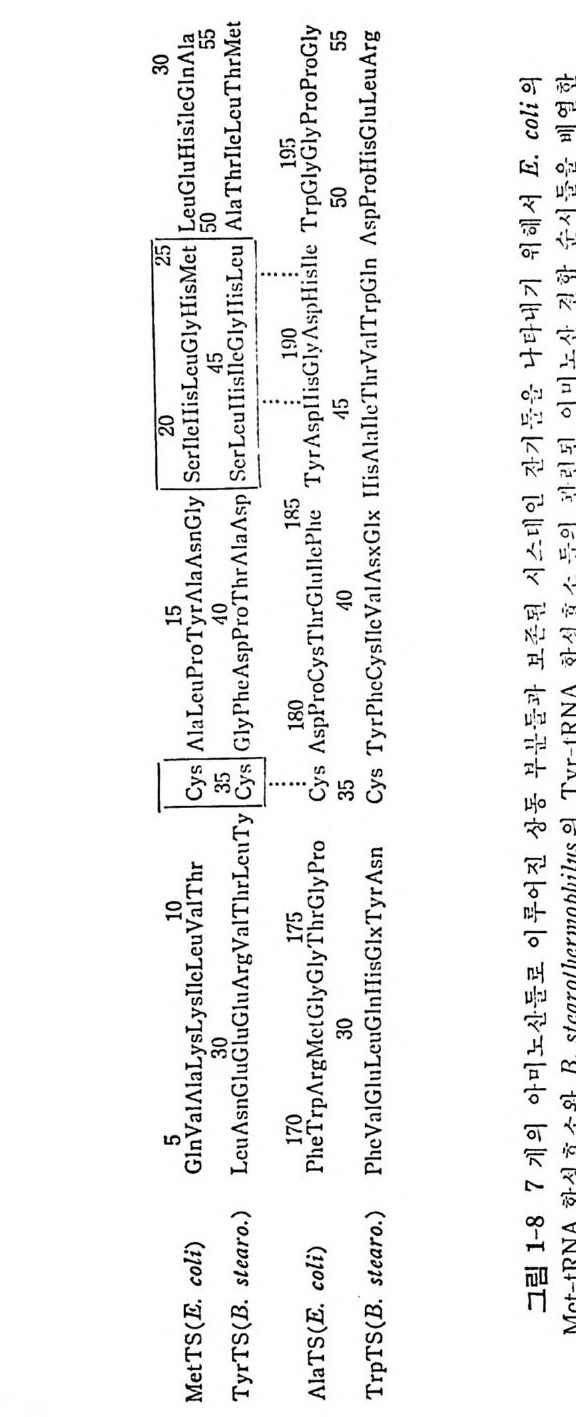
수 있다. 이러한 문제들을 풀기 위해서 합성효소들의 일차구조를 분석하는 연 구들이 진 행 되 고 있 다. B. ste a rotl z ermop hi l u s 의 Trp- tRN A 합성 효소와 Ty r- tR NA 합성효소들 사이의 일차구조의 상동성과(Wi n t er 등, 1979) E. coli 의 Ala-tR NA 합성 효소와 Ty r- tR NA 합성 효소들 사이 의 일 차 구 조 의 상동성 (Putn e y 등, 1981) 을 분석하였다. 그렇지만 아무런 상동 성을 찾 아 볼 수 없었다. 단편적인 아미노산 연속 부분들만이 보존되어 있음을 알았다. 그러 나, 현재, B. ste a roth e rmop lzi lu s 의 Ty r- tR NA 합 성 효소 (Bhat 동, 1982) 와 E. coli 의 Met- tRN A 합성 효소 (Zelwer 등, 198 2 ; Barker 등 , 1 98 2) 들의 X- 선 결정학적 구조들 및 완전한 일차구 조 들 이 알려져 있다. 이 두 효소들은 위상기하학적 유사성들울 가지는 데 , 특 히 , 번갈아 일어나는 욥병풍 구조를 한 a/{3 N- 말단 영역들을 둘 다 가지고 있다(그립 1-7 을 보라). 티로실-t RNA 합성효소의 구조예 있 어 서 활 성 화된 티 로신 (Ty r- AMP) 은 /3-병 풍구조의 C- 말단의 특이 한 자 리에 결합한 다. 그러니까 이 부분은 효소의 활성 자리의 일부분임을 확 인 할 수 있 다. 최 근에 Barker 와 Wi nt e r (1982) 는 B. ste a rotl z ermop hi lu s 의 Met- tRN A 합성 효소와 Ty r- tR NA 합성 효소의 일 차구조들을 이 효소 둘의 유전자들의 결합순서를 바탕으로 하여 결정하였다• 두 효소들에 있어서 시스테인과 히스티딘 잔기들의 자리들을 함유하고 있는 두 연속 부분들 사이에 단편적인 상동성이 있음을 알았다(그림 1-8). 이 잔기들 은 삼차원 구조들에서 상응하는 위치들을 차지하고 있으며, 활성 자리 에 가까운 자리들에 있다(그림 1 ― 7 과 비교하라). 따라서 이 잔기들은 아미노산 활성화와 그의 동족 t RNA 에로의 전달을 촉매하는 메카니즘 에 직접 관여할 것으로 추측되고 있다. 이 문제와 관련하여, 최근에 여러 아미노아실_t RNA 합성효소들에 대 한 돌연변이체들이 얻어진 것은 여러 면에서 중요한 일이다. 득히, 온 도 민감성 돌연 변이체 들 의 분리는 합성효소들에 관한 일반 정보를 제공 하는 데 크게 기 여 하고 있 다 (La Rossa 와 Soll, 1978) . 또한, 적 절 한 둘 연변이체들을 얻을 수 있게 됨으로써 플라스미드들 또는 파지 따위의 운 반체들에 독정한 야생형 합성효소의 유전자를 도입 복제하여 선택할 수 있게되었다. 짝바꿈한폴라스미드상에 합성효소유전자를가지고있는 세포들은 여러 갑결로 증폭한 효소 수준을 가지고 있다. 그러므로, 합 성효소 유전자를 도입 복제함으로써 효소의 일차구조 분석과 결정학적
 00152 53 _ 2 051 』r01王AGThrhAac孟h PTIh안三」TueLa:IlrpsAy:무LP\I vylsV~Tcc ~cSc~GlrT~AciAlcaarnllLllsaiGoLhclL;IuG~~A,APMluis!uLnLrslHGAal u VcClsslsuG ySi)yyycliM.Ety oe( iH TtII I I ruoT?:c T.GhAlnLr)auTlcGaVsuLuTsu(SIerlrABy\ y .g :08: 1 9 57 755019; 1:18 011 y;iiGrsoss;l-Tcs~A 1AhllTlPlAsPcl1GlGlMG~'rPllrT1os1r ole-rrHGolGlPcGh GC ACrP rIr;s !ppyiyyyif'yi ipyyg pyitoaiclT (ES ) Al. 5453 03 040 5 5 5 VrACrpcPhlhsPrTares GlsllaAs cnsaArAnlsTlx GsGllxnLlGxulGrL 1Als1lVlGaleTVcCouPThcluTygiy iiHpHyyp(a. ) roes.B STrTt 18 -·서용 부문동c해 기의립진어위 이 로 인문데i산노스기마아시 의내루개l된진 촌다상 그보나 과분 o등 .E 7 pyi시이 의 순배던 노란한 합의 문긴 와소소윤 효 성합겐 효성 영산문 합 미 Rr-TsIlhmrchloracsl.o B ANeMNttR-t \Jt t pi i효성의성s 합 1/A갑R1/Iaj,결o1 의들l:rc1N .E11 시o/R해/r I위a 기o소보s1· 해A 교. 미3 -rl효N립 그1T와 소의 J\ ./c N더꾸로으단 는자.다있심 께함. 을-나부분 일 이숫의니서말순거합 의
00152 53 _ 2 051 』r01王AGThrhAac孟h PTIh안三」TueLa:IlrpsAy:무LP\I vylsV~Tcc ~cSc~GlrT~AciAlcaarnllLllsaiGoLhclL;IuG~~A,APMluis!uLnLrslHGAal u VcClsslsuG ySi)yyycliM.Ety oe( iH TtII I I ruoT?:c T.GhAlnLr)auTlcGaVsuLuTsu(SIerlrABy\ y .g :08: 1 9 57 755019; 1:18 011 y;iiGrsoss;l-Tcs~A 1AhllTlPlAsPcl1GlGlMG~'rPllrT1os1r ole-rrHGolGlPcGh GC ACrP rIr;s !ppyiyyyif'yi ipyyg pyitoaiclT (ES ) Al. 5453 03 040 5 5 5 VrACrpcPhlhsPrTares GlsllaAs cnsaArAnlsTlx GsGllxnLlGxulGrL 1Als1lVlGaleTVcCouPThcluTygiy iiHpHyyp(a. ) roes.B STrTt 18 -·서용 부문동c해 기의립진어위 이 로 인문데i산노스기마아시 의내루개l된진 촌다상 그보나 과분 o등 .E 7 pyi시이 의 순배던 노란한 합의 문긴 와소소윤 효 성합겐 효성 영산문 합 미 Rr-TsIlhmrchloracsl.o B ANeMNttR-t \Jt t pi i효성의성s 합 1/A갑R1/Iaj,결o1 의들l:rc1N .E11 시o/R해/r I위a 기o소보s1· 해A 교. 미3 -rl효N립 그1T와 소의 J\ ./c N더꾸로으단 는자.다있심 께함. 을-나부분 일 이숫의니서말순거합 의
구조 분석 목적들에 필요한 다량의 효소를 얻을 수 있게 되었다. 1.3.3 기질 특이성 가 ) 아마노산 단백전 합성에서 요구되는 충실도로부터 한 종류의 합 성효소듄은 그들의 동족 아미노산에 대해서만 높은 특이성을 가진다는 것을 알 수 있다. 그러나 특이성은 절대적인 것이 아니다. 자연계에 있 는 미 동족성 아미노산들은 인식되지 않는 다. 자연계에 있는 아미노산들 의 합성 효 소들에 대 한 Km 값은 5 내 지 150 µ\'I 이 다 (Ki ss elev 와 Favor- ova, 197 °1 ) . 앞에 서 기 술한 바와 같이 , 아미 노산들은 비 동족성 합성 효 소 에 의해서 합성화될 수 있지만 , 절대로 t R NA 에 안정하게 결합될 수 없 다. 예 를 둔연 , E. co li의 Val-tR NA 합성효소는 트레오닌에 의한 교 환 반응 을 촉 진하지만(반응 1), 트 레 오닌에 대한 Km 값 은 발린에 대한 값 보다 100 배 나 더 크며 , Ile- tR N A 합성 효소의 발린에 대 한 Km 값은 이소루 신에 대한 것보다 50 배나 더 크다. 마찬가지로, 자연계에 존재하 는 아미노산 유도체들은 반응성이 없다. 어떤 특별한 유사체는 이 유사 체롤 생합성시칸 세포로부터의 ( 등종성) 합성효소와는 작용하지 않지만, 다른 종의 세 포로부터 의 (이 종성 ) 합성 효소들과는 상당히 활발하게 작용 할 수 있다 는 것은 매우 홍 미 있는 일이다. 어떤 아미노산 유도체들은, 그들아 자연계에 존재하는 것이든 합성한 것이 든, 특정한 합성효소들을 목이하계 방해하는 독소들로서 작용한다. 이러한 경우돌에 있어서도 이 독 소 를 합성한 생체로부터의 합성효소들은 이 독소의 영향을 받지 않는 다 (Lo ft f iel d , 1972) . E. coli 와 B. ste a rotl ze r111op hi l1 1 s 둘 로부터 의 ETy ’ 을 제 의 한 모든 경 우에 있어 서 , 합성 효소들은 L- 아미 노산들에 만 특이 하다. D- 티 로신이 ET) ’ ’ 에 의해서 t RNAT y ’에 아마노아실화될 수 있지만, L- 이성질체에 바 해서 느린 속도로 일어난다. 두 이성 질체들에 대한 ET y’의 Km 값은 거 의 같지만, Vmu 값은 L- 티로신에 대한 값에 비해서 D- 이성질체에 대한 값이 훨 씬 작다. 이것은 반응 속도의 차이를 결정하는 요인은 결합양식 에 있는 것이 아니고 촉매작용의 양식에 있음을 의미한다. 아미노아실 화 반응에 있어서 차이가 있을 뿐 아니라, E. coli. 또는 다른 생체들에 서 얻는 ETy ’ 가 존재할 때, D- 티로실-t RNA” 은 L- 티로실-t RNA 브 다 훨 씬 더 빨리 가수분해 된 다 (Jo seph 와 Muench, 1971) . 이 러 한 작용
에 의해서 D- 이성질체가 단백질로 결합되어 들어가는 것을 확실하게 방 지할 수 있다. 나) ATP ATP 만이 작용하며 (Km 값은 40 내 지 2300 µM) , dATP 는 훨씬 높은 Km 값과 낮은 Vmax 값으로 작용한다. 그밖의 누클레오시드 삼인산들은 작용하지 않는다. 일반적으로, AMPP(CH2)P 를 재 외한 ATP 유사체들은 합성효소들을 방해하거나 작용을 하지 않는다. AMP P (CH2) P 는 약간의 합성 효소들과 작용한다 (Chap ev il le , 1972) . 아 노데신도 역시 반응 1 과 반응 3 을 ATP 와 다소 경쟁 적 으로 방해 한다. 다) tRN A 한 아미노아실-t RNA 합성효소는 하나의 tR NA 또는 하나 이 상의 tR NA 들 (등수용성 tR NA 들) 에 대 해 서 독이 하게 아미 노산울 전 달한다. 합성효소들의 t RNA 들에 대한 선택성에 관해서는 t RNA 의 구조 를 먼 저 기술한 다음에 논의하기로 하겠다(1. 5 절을 참조). 1.3.4 세포들에 있어서의 합성효소들의 조직 원핵세포들의 조잡한 세포 파쇄액을 살펴보면 합성효소들의 분자량들 은 자유 합성효소 또는 E·tR NoA 복합체라고 생각했울 메 기대 할 수 있 는 값들을 가진다 (Nass 와 St f fier , 1967). 그러나, 진핵세포들의 경우 에 있어서는 합성효소들의 분자량이 1. 5X106 이 넘는 고분자량의 복합 체 들로 존재 한다는 많은 관찰이 있 다 (Of en g a nd, 1977 ; Dang 둥, 1982) 이러한 복합체들은 거의 모든 진핵세포들에 존재함이 알려져 있으며 탄 수화물류, 지 방류, 리 보핵 산류 (tR NA 와 4S RNA 등) , 및 고분자 상태 의 RNA 들을 복합체에 함유하고 있다. 이 복합체들은 매우 쉽게 망가 지기 때문에 추출하는 데 실패하기 쉽다. 이 합성효소들의 복합체가 생 체내에 있다는 사실온 의심할 바 없다. 고분자량 상태의 아미노아실 -tRN A 합성효소 복합체들의 기능이 무엇인지는 거의 모르고 있는 형편 이 다. 그러 나, 아미 노아실-t RNA 합성 효소들이 단백 질 생 합성 장치 의 성분들 및 그밖의 다른 효소들과 상호작용할 수 있다는 사실은 진핵 세 포의 단백질 생합성이 보통 생각되고 있는 것보다 더 높은 수준의 조칙
화된 장치에서 일어날 것이라는 가능성을 암시하는 것으로 생각된다. 예를 들면, tR NA 변형효소들 및 연장 인자들은 아미노아실-t RNA 합 성효소들을 함유하고 있고, 큰 복합체들과 회합하고 있다. 1.4 t RNA 의 구조 1.4.1 개요 Cric k (19 57) 의 아담터 가설 은 토끼 간의 추출액 에 서 아미 노산들을 특 이 하게 결합할 수 있 는 작 은 RNA 분자들이 발견됨으로써 확인되었다 (H oag la n d 1960) . 이 RNA 는 약 80 개 의 누클레 오티 드로 구성 된 폴리 누 클레 오 티 드이며, 한쏙 끝 에서는 5 ' -인산으로 시작하고 다른쪽 끝에서는 공 통 되는 연 속 부분 CC A 로 끝 난다. 단백질 생합성에 있어서의 tR NA 의 키능은 펩터 드 결합 형 성이 을 바른 순서로 일어나게끔, t R ~ A 에 에 스테르 화 된 아마노산을 리보솜으로 운반하는 것이다. 이 중요한 기능을 발휘하는 과 정에서 t RNA 는 mRNA 가 지니고 있는 유전 정보를 해독 합 으로 써 아 담터 로서의 역 할 을 하는 것 이다. 말하자면, t RNA 는 단백 질 과 핵산 사이의 경계면이라고 봉 수 있다. 박 테리 아의 세포에 있어서 전체 t RNA 의 양은 마른 무게로 약 1% 이 므로, 이 러 한세포에는 55 가지 정도의 t RNA 분자들이 약 4x10 타서 있을 것 이다. t RNA 둘은 세포에 있어서 적 어도 80% 정 도 아미노아실화되어 있다고 보며, 충분한 아미노산아 있을 경우에는 거의 전부가 아미노아 싣화되 어 있을 것으로 보고 있다 (Clark, 1979). 1982 년 까지 의 보고에 의 하면 효모의 tR NAp b c (Ki m 등, 1974 ; Ladner 등, 1975) , 효모의 tR NAGly ( vVrig h t 등, 1979) , 흐모의 tR NAA•P (Maraf 둥, 1980a) , 그리 고 E. coli 의 tR ~AO!ct 등 네 가지 tR NA 들의 삼차원 구조와 113 가지 이 상의 tR NA 들의 일 차구조가 알려 져 있 다 (Gauss 등, 1979) . 이들은 모두 예상되는 클로버 잎 모양의 이차구조를 가진다 (Holley 등, 1966) . 현재까지 알려진 t RNA 둘의 결정체들의 구조들이 매우 비슷한 것은 사실아지만, 세포액에서 또는 단백질 합성에 관여하는 여러 인자들 또 는 단백질들과의 복합체 상태에서의 구조가 결정체의 구조와 같을 것안
지는 아칙 확실히 모르고 있다. 단백질 생합성 과정에 있어서의 t RNA 의 형태의 변화를 연구하기 위해서 많은 연구자듄은 X- 선 결정구조학적 방 법, 화학적 변형법, 효소 반응속도론적 측정들, 핵자기공명, 전자스핀 공명, 레이저 광 산란, 형광법 등과 같은 물리화학적 방법들을 사용하 고있다. 1.4.2 단백질 생합성에 있어서의 t RNA 의 역할 단백전 생합성에 있어서의 t RNA 의 생물학적 기능, 또는 더 정확하 게 말해서 생물학적 작용들에 관한 오늘날의 지식을 표 1-4 에 요약하 였다. 표1 4 76 2935814딘 mAE<다나조백아포FlIF 자철呼질르에미料RN r억되A 리억u노일 A PC“의아기에에의제러압접 한자임자) 의「실인에 성 〈江〔錢託대에祠있 해인효뭉한잡 어tR일옹식4신독 :닌N7A 에11 , 호 분A의 `|li| J의i의 t연 한인장R 의N 인 A식Kl' 식 의리 入. 성잡 뭄7 ` _1 힉t'j 7 ! 적A 빼 작 용 둘가 「
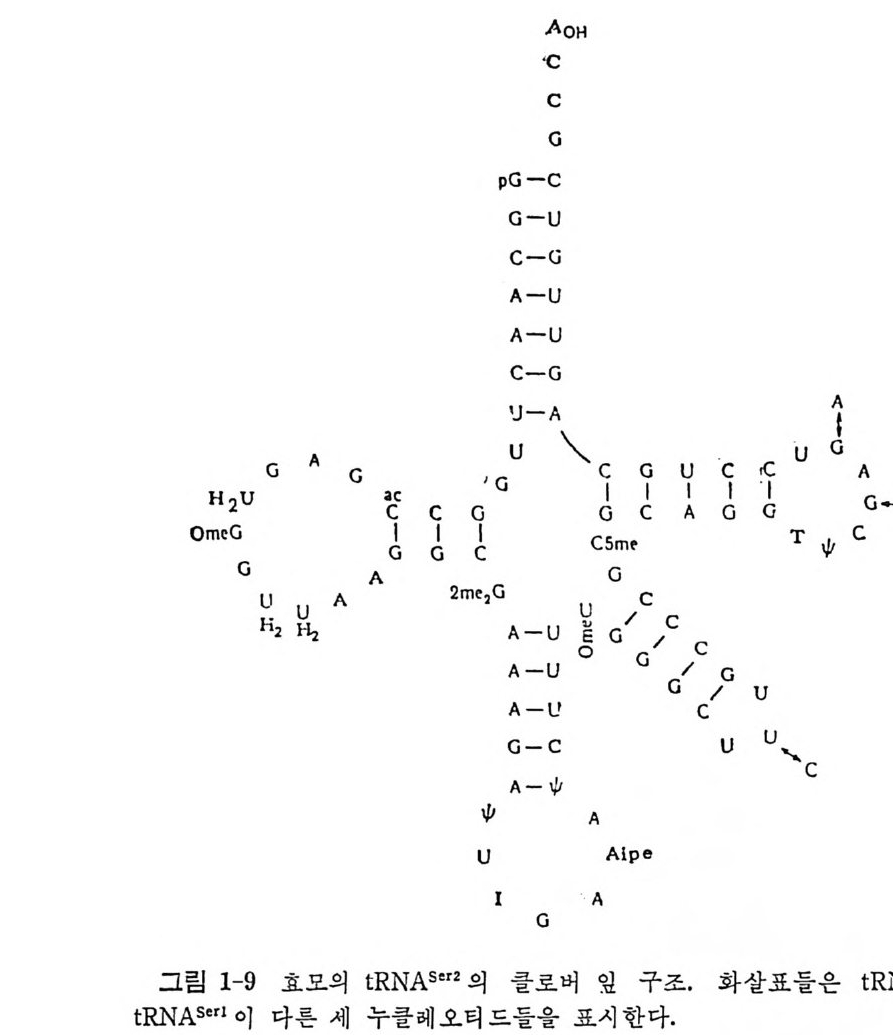
요자세t R히N A논 둘의의될 단것백이질다 .합 성여자에기 서있는어 간서단의히 작요용점들만은을 제열 4거,5하 및고 자6 장한에다서. 더 t RNA 는 아미노아실-t RNA 합성효소의 작용으로 아미노아실화된다• 아마노아실-t RNA 들은 여용러 가지 인자들과 작용하여 리보솜으로 옮겨 진다. 단백질 합성의 개시 단계 는 독특한 t RNA 들에 의해서 이루어진다. 원핵 세포들에 있어서는, 포르밀메티오닐-t RNNM••( f Me t-t RNNM•• )가 개 시 인자들과 작용하여 리보솜의 30S 하위단위체와 결합한다. 진핵 세포들에 있어서는, 메티오닐-t RNA}kI( 또는 Me t-t RNN1) 가 개시 인자들과 작용하여 40S 하위단위체와 결합한다. 연장 단계에 있어서는, 아미노아실화된 t RNA 둘이 연장 인자들과 GTP 와 함께 리 보솜 상으로 옮겨 져 서 각 아미 노산에 상응하는 mRNA 상의 코돈을 인식하게 된다. 원핵 세 포의 Met- tR NA 'M• t 는 포르밀 기 를 전 달하는 효소의 작용으로 fM et- tRN A 'Met 로 된 다. 1. 4. 3 한 아미노산에 대한 tR NA 종들의 복수성 감은 생체 내에서도 , 주어진 아미노산에 대해서 득이한 t RNA 가 하 나 이상 있다. 동수용성 t RNA 들이 존재하는 이유는 유전 암호를 살펴 브면 명백해진다 . 한 아 마 노산에 대한 암호문이 여러 가지가 있다. t RNA 의 아담터로서의 작응을 고려하면, 각 암호문은 동수용성 t RNA 들 중의 어느 하나에 상응하여야 할 것이다. 이렇게 따지면, 세포 소기관 들에 독이하게 존재하는 t RNA 둘을 제의하더라도, 세포에는 61 가지의 t RNA 가 있게 될 것이다 . 그렇지만, 동요 헌상으로 인해서 코돈-역코 돈 짝짓기예 있어서의 정상적인 A·U 및 G·C 짝들 이의에도 다른 짝짓 기가 가능하므로, 한 역코든은 둘 또는 세 개의 코돈을 읽을 수 있다. 또한, 모든 생체들에 있어서, 모든 코돈이 사용되는 것이 아니다. 그러 므로, 실제로 필요한 개개의 t RNA 의 수는 61 개보다 적다 . 한 생체 내 에 있는 t RNA 종들의 수를 정확히 알 수는 없 으나 40 내지 60 종 정도 로 추정되고 있다 . 그 밖에도 가짜 등수용성 t RNA 들이라고 생각할 수 있는 것들이 알 려져 있다 . 이것들은 정 상적인 물리적 상태에 있는 완전한 분자들이지 만, 몇 가지 이유로 해서 진짜 등수용체들이라고 불 수 없다 . 그들은 서르 몇 개의 염기듣에 있어서만 차이가 있을 뿐 이며, 유전자 중복으로 하나 의 유전자에서 생겼으며, 뒤에 양쪽 . 유전자들에, 또는 둘 중 어느 하나 에 돌연변이가 일어난 것일 것이다 . 예를 들면, E. col i의 t RNAT y r! 과 tR NAT)''2 , tRN AV•I2A 와 tR NAml2B, 그리 고 효모의 tR NA5•rl 과 tR NA5•r2 등이 이러한 부류의 t RNA 들이다. 구체적 예로서, 효모의 t RNa5” 에 있 어서의 두 가지 등수용체를 그림 1-9 에 나타내었다. 그 밖의 것들에 관 해서는 이 책의 부록을 참조하면 된다.
 AoH
AoH
몇 가지 아미 노아실-t RNA 들은 단백 질 합성 에 는 사용되 지 않고, 세 포벽의 생합성과 같은 다른 기능들에 적응되어 있다. 이러한 t RNA 들 온 그들의 합성효소들에 의해서 정상적으로 아미노아실화되지만 단백 질 합성에는 작용하지 않는다. 진핵 세포들에서 단백질 합성의 개시 단계에 특이하게 작용하는 t RNA tf e t의 경우는 특별하다. t RNA갑와 tR NAt lct 둘 다 같은 코돈을 읽 지 만, tR NAt ' 만이 개 시 작용에 서 기 능 을 가지고, t RNA 뿐는펩티드사슬의 연장에서만 활동한다. 둘 다 같은
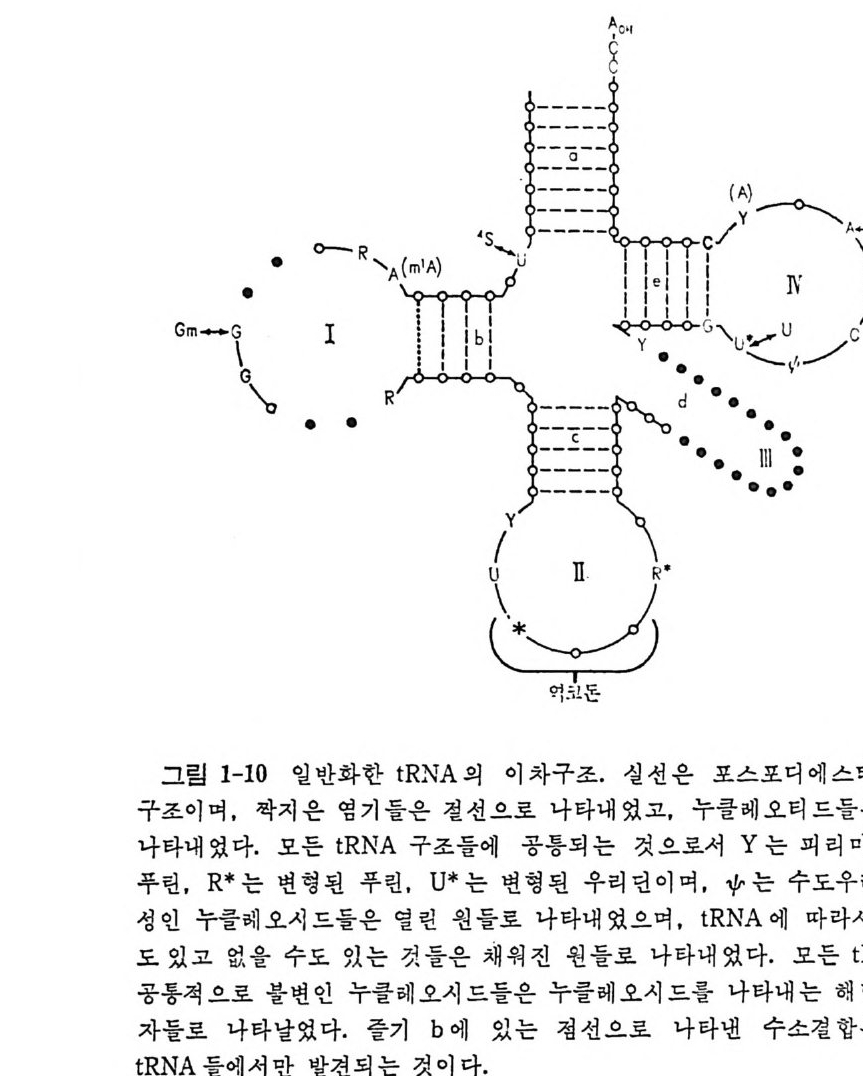
합성효소에 의해서 아미노아실화되지만, 그들의 일차구조는 상당히 다 르다 (Schim mel 등, 1979) . 위에서 말한 메티오닌 t RNA 둘의 경우를 제의하고는, 같은 생체에서 얻는 진짜 동수용성 t RNA 들이면서 누클레오티드 결합 순서가 다른 t R NA 둘 은 같은 역코돈을 가지는 것이 하나도 없다. 이것은 등수용성 tR NA 종들의 일차적인 기능이 유전 암호의 축퇴성을 활용하는 것이라 는 개념과 맞는 것이다. 1. 4. 4 tRN A 의 일차구조와 이차구조 1965 년 에 Holle y와 그의 동료들이 효모의 알라닌 t RNA 의 일차구조 룰 결 정 한 이 래 로 (H olley 등, 1965) 177 가지 이 상의 tR NA 들의 일 차구 조가 결 정 되 었 다 (Gauss 와 Sp ri n z l, 1981) . Holley 가 효모의 알라닌 t RNA 의 일차구조 를 분석하 는 데는 정제 된 tR NA 시료가 1 그람 정도 까지 다량으로 소요 되었으 며, 결합 순서의 분석을 완성하는 데 여러 해 가 결렀다. 그러나 오 늘날에 는 t RNA 의 결합 순서 를 분석하는 간편한 방 법들이 고안되어 있어서 결합 순서의 분 석 은 몇 주 이내로 완성할 수 있 게 되 었다 (Pe att ie, 1979; Sta n ley 와 Vassile nko, 1978; Donis - Keller 등 1977 ; Krup p 와 Gross, 1979 ; Gup ta 와 Randerath , 1979 ; Tanaka 등, 198 0) . 알려 진 모든 tR N A 둘 의 일차구조들은 Holley 와 그의 동료들이 Wat- son-Cric k 형 염기 짝짓기가 최대가 되도록 배열한 것에 기초하여 처음으 로 제안한 바와 같은 〈클 로버 잎 〉 모양으로 배열 될 수 있다. 일반화한 클로버 잎 구조를 그림 1-10 으로 나타내 었다. Wats o n~Cric k 짝들은 a, b, C, 및 e 둘로 표시 한 4 개 의 이 중나사선 형 줄기 부분들을 이 룬다. 그 중 셋은 영기 짝을 이 루지 않은 고리 부분들 I , II, lil, 및 N 둘로 닫혀 있 다. 이 들 네 줄기들은 이 차 구조 를 클 로버 잎 모양으로 배열시키게 된다. 줄기와 고리 를 합쳐서 〈팔〉 이라고 부르기도 한다. 팔 d 는 t RNA 의 종 류에 따라서 작은 것도 있고 큰 것도 있다. 1978 년 Cold Sp ri n g Harbor tR NA 모임 에 서 tR NA 에 대 한 동일 된 번호매기기 방식 문제를 논의하였지만 좋은 안을 얻지 못하였다. 거의 모든 tR NA 들이 클로버 잎 모양으로 배 열 될 수 있고, 그 삼차원 구조 들도 거의 비슷할 것으로 생각되며, 단백질 합성에 관여하는 여러 단백
 선A0
선A0
질 또는 RNA 들과의 복합체 형성에 있어서도 공통되는 유사점들이 알 려지고 있기 때문에 t RNA 의 누클레오티드들의 번호매기기를 체계화하 는 것은 매우 유익할 것으로 생각한다. 이러한 취지에서 회의 참석자들 은 t RNAPb• 의 번호매기기에 기초하여 그밖의 t RNA 들의 번호매기기 방 식을 제안하였다. 이 방식을 그립 1-11 로 설명하였다.
 00_00_00—00 ———®
00_00_00—00 ———®
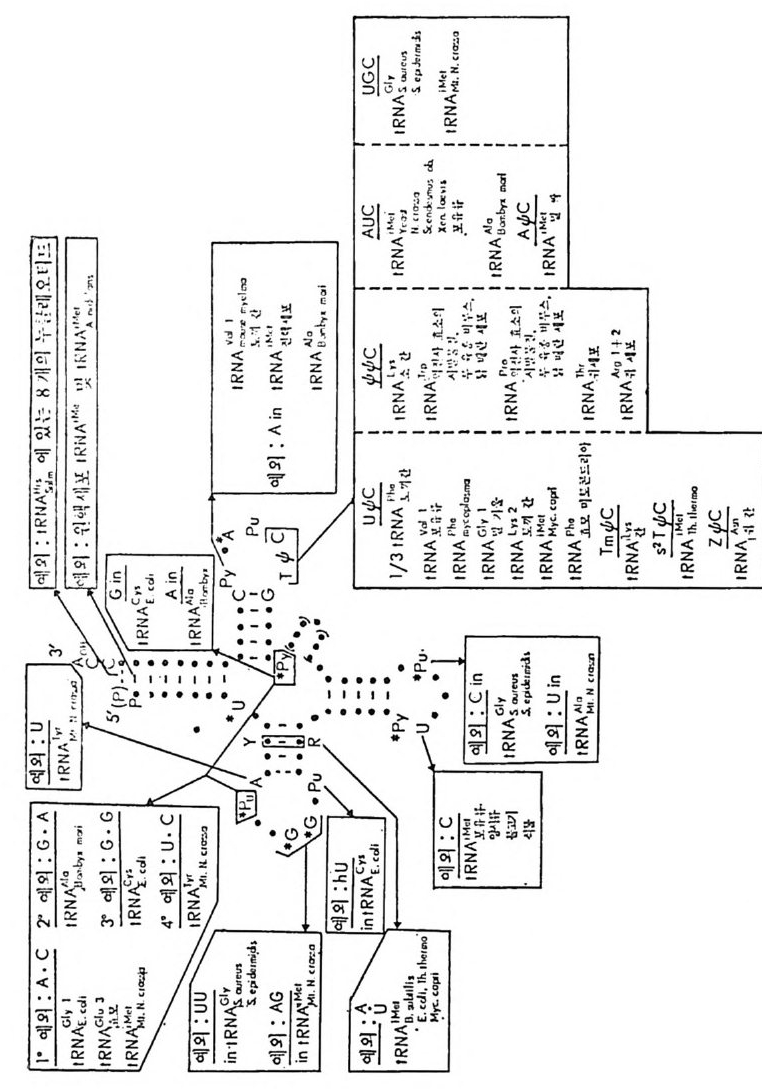
1.4 .5 t RNA 의 일반적 특징 및 기능 결합 순서들이 결정된 tR NA 종들의 누클레오티드들을 비교해 보면, 어떤 잔기들은 언제나 강은 위치에 있다는 것을 알 수 있다. 공통되는 누클레오타드들에는 14 가지가 있다. 그밖에도 약간의 위치들은 일반적 으로 푸린 염기류 또는 피리미딘 염기류로 점유되어 있다. 이러한 잔기 둘로서는 9 개가 있다(그림 1-12). 그림 1-12 에서 불변성인 위치들은 누쿨레오티드를 나타내는 문자들로 표시하였다(그립 1-10 과 비교하라 ) . 한편, 반불변성인 위치들은 R( 푸린 누콜레오티드) 또는 Y( 피리미딘 누 클레오티드)들로 표시되었다. 어떤 사람들은 21 번 위치의 잔기가 불변 성 인 A 라고 인정 하고 있다 (Clark, 1979) . 그러 나 E. coli 의 두 tR NAL•u 은 이 위치에 G 를 가지고 있다• 이 책에서는 Dir h eim er 등 (1979) 의 제 안에 따라서 21 번 위치의 찬기를 반불변성인 것으로 인정하였다(그러 나, 원저자가 사용한 그림을 그대로 소개한 경우에 있어서는 21 번 위 치가 불변성인 잔기로 간주된 그 림 이 가끔 인용되고 있다). 불변성 및 반불변성 누클레오티드들에는 예의들이 있다(그립 1-12). 5' 끝에서 8 번 위치에는 언제나 U 또는 s4U 가 있다. 많은 t RNA 들 의 경우 피리미딘 11 • 푸린 24 쌍이 있다. 원핵세포의 개시 t RNA 들에 는 이 득칭이 없고, 이 자리에 푸린 11 • 피리미딘 24( 예, All • U24) 쌍 을 가지고 있다. N. crassa 를 제의하고는 14 번과 15 번 위치에는 A-Pu 연속 부분이 있다. Lev itt (1969) 의 조사에 의 하면 , 15 번 위 치 에 G 를 가지 는 tR NA 둘은 1/l'C 줄기 앞의 위치에 (즉, 48 번 위치) C 가 있고, 한편 15 번 위치 에 A 를 가지는 t RNA 들에 있어서는 'IJl'C 줄기 앞에 U 가 있다. 15 번 위치와 48 번 위치 들은 t RNAPhe 의 삼차원 구조에서 삼차 수소결합들 (G15 • C48 및 Al5 • U48) 을 이 루는 자리 들이 라는 것 이 tRN APhe 의 삼차 원 입체구조가 밝혀침으로써 확인되었다 (K i m, 1979) (69 면의 그립 1- 26B 를 참고하라). 이 일반성에서 벗어나는 몇 가지 예의들이 E. col i와 Salmonella typh ym uriu m 에 서 얻 는 GGG 코돈에 특이 한 tRN AGly! , 효모 에 서 얻는 tRN AGiu s, 그리 고 N. crassa 의 미 토코드리 아에 서 얻는 개 시 t RNAr•1 들에서 관찰되었다. 이 세 가지 t RNA 둘은 이 위치에 A·C 쌍
 GCU l, CN~ ',AIR' 'm',i 뇨소 k.0 C소2ANR .•I
GCU l, CN~ ',AIR' 'm',i 뇨소 k.0 C소2ANR .•I
은두
잦모 이은* ,빈형듄tANR 의.예들포의세 의핵서진어있 ,는 에들우에경오드티레않을았 쿨 누지 되성적변지불 반 히 별및특성변 의 .불 예 둘의 서의NAR t 에 어있 정 결된 urbumucr/l 서순 가o쌉rbol:c 112- 결합 t◊R ,NA; ; .것이 들다의 립 들질그기포찬세울 가지고 있다. 그러므로 이 위치들 사이에서의 염기 짝짓기는 지금까 지 보고된 거의 모든 t RNA 둘의 염기 결합순서들에서 일어날 가능성은 있지만, tR NA 구조의 보편적인 톡칭은 아니다. A·C 짝짓기는 분자를 비 듦으로써 가능하게 된 다. 최 근에 Bomby x mori 의 tR NAAla 에 는 G • A 쌍이 (Sp ra q u e 등, 1977) , 그리 고 E. coli 의 tRN ACY’ 에 는 G •G 쌍 이 Mazzara 와 rvic C lain , 1977) 존재 한다는 것 이 알 려 졌 다. 단백질 합성에 관여하는 거의 모든 t RNA 들은 D 고티에 G18G19 또 는 Gm18Gl9 연속 부분을 가지고 있다. 단백질 합성에는 관여하지 왕 고 세 포벽 의 펩 티 도글리 칸 합성 에 관여 하는 Sta p l zy la coccus aurea s 와 Sta p h yl o coccus epi de rmi di s 들에 서 발견되 는 예 외 적 인 tR NAGly 종들에 서는 이 GG 연속 부분이 발견되지 않았다 ( Rober t s, 1972; 197,1 ). 이 두 G 찬기들은 D 고리와 1JtC 고리 를 결합시키고 있으므로 (그립 1-17 또 는 그림 1-26A 및 26B 를 브라), 이러한 t R~A 둘은 단백질 합성에 관 여 하는 tR NA 들과는 구조가 많이 다를 것으르 생 각된다. N. crassa 의 개시 t RNA 는 이 자리에 AG 연속 부분을 가지고 있다 (Heckman 둥, 1978) . 'IJfC 고리 의 안 와 A 와의 짝짓 기 는 전 형 적 인 Wats o n-Cric k 수소 결합들로 이루어질 수 없다. 왜냐 하면, 이 t R 2\ A 는 이 고티에 망대신 에 G 를 가지고 있다. 역코돈 고러의 첫번째 자리에는 언제나 피티미딘이 있고, 역코돈 뒤 에는 푸린이 있지만, 단백질 합성에 관여하지 않는 t RNAGl y등에는 이 푸린이 발견되지 않는다. 역 코돈 뒤 에 있는 푸린은 아마도 울바론 코든 • 역코돈 짝짓기에 필수적인 것으로 생각된다. 이 짝짓기는 펩티도클리칸 합성 에 관여 하는 tR NA1Y 의 기 능에 는 요구되 지 않는다. 펩 티 도글리 칸 합성에는 티브송과 mR~A 들이 필요치 않다. 또 하나의 예의는 최근에 결 합순서 가 분석 된 N. crassa 의 미 토콘드리 아의 tR NAA1• 의 경 우인데 , 이 t R~AAl• 은 이 위치에 푸린 대신에 U 를 가지고 있다(그 립 1-12 를 보라). 이 t RNA 의 암호 해독의 메카니즘은 매우 홍미 있을 것으로 생 각 된다. 역코돈 앞에 있는 U 는, 포유류, 양서류, 및 어류 둥에서의 단백질합 성의 개시 단계에 :i 기능이 제한되어 있는 t RNA 판'들을 제외한, 모든 t RNA 들에서 발견된다. 그러나 효모, 청조류 및 원핵세포들의 tR NAIMe t 에는 U 가 늘 존재한다. 현재로서는 여러 가지 역코돈 고리들의 분자적 구조에 관해서는 거의 알려진 것이 없기 때문에, 이 염기의 치환이 가
지는 의미는 분명하지 않다. 얼 마 전까지 만 하여 도 도든 tR NA 둘은 ,trC 고리 에 T,t rC 연속 부분이 있다고 생각되어 왔지만, 최근에 이 고리 에는 몇 가지 다른 연속 부분 둘이 들어 있는 예들이 확인되었다. 첫째로, 약간의 t RNA 둘은 T,f rC 연속 부분에 있어서의 U 의 T 로의 변형이 불완전하거나 전혀 일어나지 않는다• 최근에 세 가지 간 tR NALfO 둘이 2'-0- 리 보오스 메 틸화된 T 를 가지 고 있으며 (Di rh eim er 등, 1979) , Tlzcrmus tlz ermop h il u s 로부터 의 개 시 tR NA 가 s2T 를 가지 고 있음이 발 견 되 었 다 (W ata n abe 동, 1975) . 둘째 르, Dir h eim er 의 연 구진 은 소 간으로부터 의 tR NAT” 에 서 T,t rC 대 신 에 ,fr,trC 연 속 부분을 발견 하였 다 (Fournie r , 1978) . 이 연 속 부분 은 루 육종 비 루스 (Ro us Sarcoma Vir u s) 로 감염 된 닭 세 포들로부터 의 t RNAT” 에서도 발견되었다. 이 t RNAT” 은 역전사효소를 위한 시발물 질이다 ( Harada 둥, 1975) . 그밖에, 쥐 백혈병 비루스로 감염된 세포들 에 서 는 tR NAP” 가 역 전 사효소를 위 한 시 발물질 이 며 , 이 tR NA 도 ,fr,trC 연 속 부분을 가지 고 있 음이 밝혀 졌 다 (Di r h eim er, 1979) . 세째로, 오늘까지 결 합순서가 분석된, 진핵세포의 세포질에 있는모든 개시 t RNA 둘은 이 고리에 T,f rC 연속 부분 대신에 AUC 연속 부분을 가 진다 (G i lum 등, 1976). 이 특칭이 확 고하게 보존되어 있다는 사실은 이 연속 부분이 매우중요한기능적인 역할을 가지고있다는것을암시한다. 이 연속 부분이 이 tR NA 로 하여 금 리 보솜의 A 자리 에 결합하지 못하도록 하는 역할을 하는 것인지는 앞으로 밝혀져야할문제이다• 한가지 강조 해 두고 싶 은 것 은, E. coli, B. subti lis, Str e p toc occus fae calis, My co - pla sma, (청 조류 Cy an op lz y ce ae) , 및 T. tlzer mop lz i lu s 들과 같은 원핵 세 포의 tR NAf \! 들은 T,t rC 또는 s2T,f rC 연 속 부분을 가지 고 있 다. B. mor i에서 얻는 t RNAAI• 가 AUC 연속 부분을 가진다는 것은 놀 라운 일이다. 이 t RNA 가 단백질 합성의 개시 t RNA 로 작용하는지는 아직 모른다. 펜티도글리칸 합성에 관여하는 t RNAGIY 은 AUC 연속 부분을 가지고 있다• 이 종류의 tR NA 들은 리 보송과 상호작용을 하지 않기 때 문에 놀 라운 일이 아니다. 더 놀라운 일은 Neuros p ora 의 미토콘드리아로부터 의 개시 t RNA 가 이 연속 부분을 가진다는 사실이다• 마지막으로, T,t rC 고리의 마지막 염기는, 이 자리에 A 를 가지고 있
는 진핵세포의 개시 t RNA 를 제외하고는 언제나 피리미딘이다. 그렇지 만, 이 마지 막 A 는 포유류의 tR NN'11 (Pip e r 와 Clark, 1974 ; Jan k 둥 1977) 과 B. mori 로 부터 의 tR NAAl• 들 에 도 있 는 것 으로 보아서 진 핵 세 포의 개시 t RNA 들의 목칭이라고 말할 수는 없는 것으로 보인다. 일반화한 tR NA 구조에는 세 가지 예외가 있다는 것이 지직되어야 한 다. 첫째로, E. coli, S. t lz yp h i mur i um 둘의 t RN AH i ■ ! 에는 아미노산 줄 기에 8 개의 염기쌍들을 가지고 있다(그밖의 모든 t RNA 들 은 아 줄 기에 7 개의 염기쌍들이 있다) (S i n g er 와 Smi th, 1972; Sin g e r 등, 1972). 이 줄기는 5' 끝이 누 클레 오티드 하나만큼 더 길며, 아 미노산 줄기의 3' 끝은 -CCA 삼중체만이 단일 가닥 부분으로 있다. 물론, 아미노아실 화된 이 t RNA 는 단백질 합성에 관여하지만 히스티딘 생합성의 조절에 도 관여한다. 두번째 예외는 청조류 Anacys t i s 11 i dula11s 를 포함한 모든 원핵세포들 의 포르밀화된 개시 t RNA 들에 있어서, 5' 말단의 염기와 3' 끝으로부 터 다섯번째의 염기 사이에 Wats o n-Cric k 염기 쌍이 없지만, 원핵세포 인 Halobacte r cu ti rubr tt m 으로부터의 포르밀화되지 않은 개시 t RNA 는 아미노산 수용 줄기에 정상적인 Wats o n-Cric k 염기 쌍을 가지고 있다 (Rich 와 RajB handary, 1976) . Schulman 과 Her (l973) 그리 고 Schulm an 과 Pelka (1975) 는 E. coli 의 tR NAIMet 가 E. coli 의 EF-Tu 에 결 합 하지 못하는 것과 E. col i의 포르밀메티오닐-t RNA/Me t가 펩티딜 기 전 달효소의 작용에 대해서 저항성을 가지는 것은 이러한 염기 쌍을 이루 지 못하는 데 원인이 있을 것이라고 생각하고 있다. 마지 막 예 외 는 효모의 tR NAv•1 (Takemura 등 1968) 와 효모의 tR NAGly (Yoshid a , 1973) 들의 경우인데, 이 t RNA 들은 가변성 고리에 , 누클레오 티드가 세 개뿐이어서 t RNA p be 과 같은 삼차원 구조를 취할 수 없다. 1. 4. 6 tR NA 의 변형된 누클레오시드들 모든 t RNA 둘은 여러 가지 비정상적인 변형된 누클레오시드들을 함 유한다 (Dirhe im er, 1979 ; Nis h im ura, 1979a, 1979b) . 오늘날까지 50 가 지 이상의 변형된 누클레오시드들이 알려져 있다. tR NA 에 있는 변형 된 누클레오시드들의 함량 비율은 매우 크다. 예를 들면, t RNASer1 의 87 개의 누클레오티드들 중 17 개가 변형되어 있다. 또한 변형된 누클레
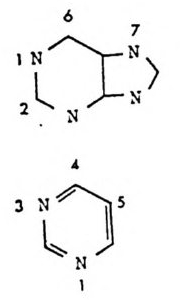
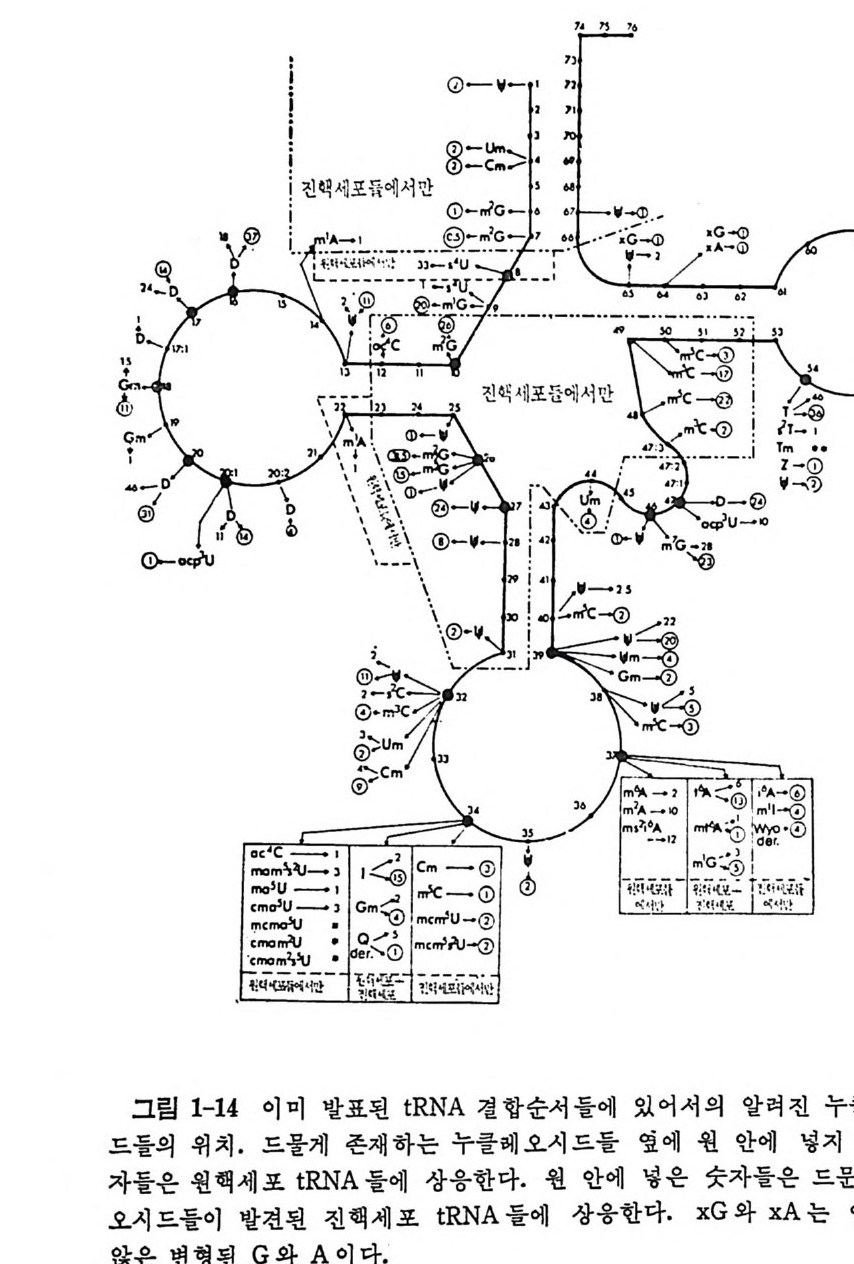
오시 드들의 구조가 매 우 다양하다. 약간의 것들은 영 기 또는 리 보오스의 2' 히드록시 기가 메틸화되어 있고, 다른 것들은 과변형되어 있다. tR NA 들에서 발견된 변형된 누클레오시드들을 그림 2-13 에 실었다. t RNA 들에 있는 변형된 누클레오시드들의 위치는 매우 특이하다(그 림 1-14). 예를 들면, 아미노산 줄기에는 변형된 누클레오시드들이 비 교적 드물게 존재한다. 1 번 위치에는 中만이, 4 번 위치에는 Um 또는
1) N- 메 틸 화된 누쿵케 오시 드들 m1A, m'G, m1G, m1I mm~2 GG == NN22,- MN2e-tD h y i m lg eu tah ny o lsg iun ae n osin e m 었 = N°-M eth y la denosin e m3 C
 亡:〉
亡:〉
2) C 一메틸화된 누클레오시드들 m 냉 ; msc ; T = ms u 3) 0-2' 메틸화된 누쿨레오시드들 Gm ; Cm : Um ; ym ; Tm 4) IP5n,s oe6su-iDdn oei u hry i ddr i on eu rid i n e === D,It r 또는 hU
5) mm5 oc위m5U치5 U에 있==는 55 --UMM 의eett hh oo그 xx밖 yyu c의a rr i bd 유oi nn e도 y :l체m —e들tOh Cy H l u sr id i n e : -CH2- CO OCHs cmmaom55UU == V5-=M e5t-h Cy a lar mboi xnyo r moee tthh oy x lu y ruidr ii dn ie n e: ―: _ CH。2― 一 C NHH2 ―一 CCHOsO Hs cmam5U = —5-CCaHrb 2o-xNy'H r n -eC thH y 2 la— m Ci nOo Om He th y lu rid i n e : 6) 3 위치에 있는 U 의 유도체들 acp 5U = 3-(3 -Ami no -3-carboxyp ro p yl) uri di n e COOH = X = -CH2-CH2-CH\N( H2
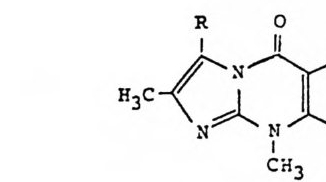
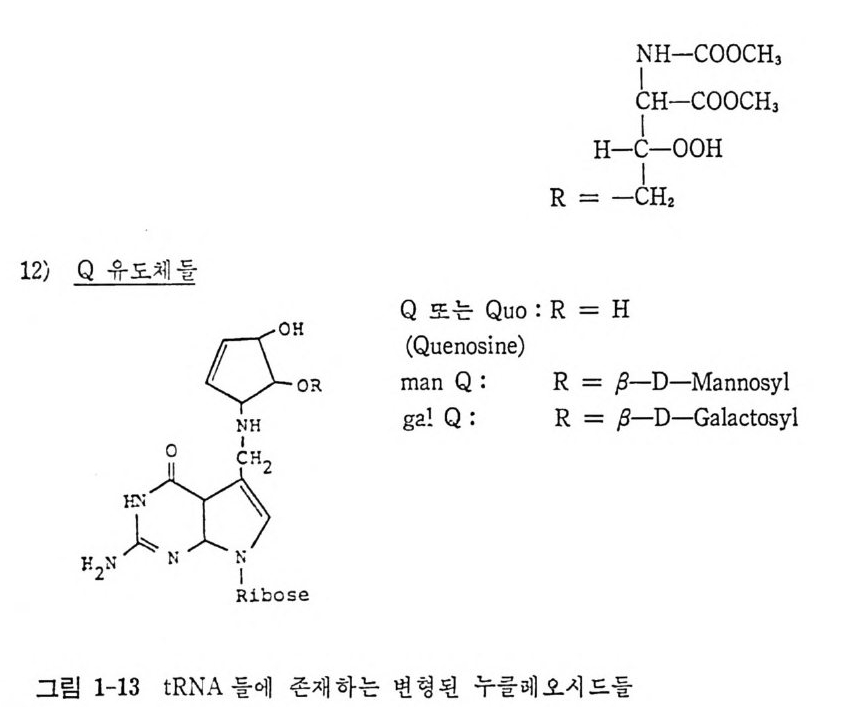
7) 4 위치에 있는 C 의 유도체 ac1C = N'-Acety lq 1 :idi n e : -NH ― co 一 CH, 8) U 와 C 의 티오유도체등 s'U = 4-Thio u rid i n e m 냥 U = 5-11leth y l- 2-th io u rid i n e=s2T mcm5U2 = 5-(:' ll e th o xy c ar b ony lr neth y l )-2-th io u rid i n e mam 냥 U = 5-Meth y l (arnin o rneth y l)- 2-th i o u rid i n e cmam5s2U = 5-Carboxy rn eth y la rnin o meth y l -2-th io u rid i n e s2C = 2-Thio c y tidi n e 9) A의 이소펜데닐 유도체들 im6As 2 i6 A == N2-6M-lesothp y e nl t the i n o y- lia6 d A e nosin e H\ K/C H2_CH=C/C\C HH3, 1 10) A 의 N6-Threonin o carbony ] 유도체 들 t6A = J\'LT hreonin o carbony la denosin e (R1=H) mt 'A = N6-Meth y l- t6 A (R1 = CH,) CH3 0 H CI HOH II I I R1\ /C-N-C-COOH N/ I I H 11) Wy e 유도체들(이전에는 Y 유도체라 하였음) -Wy o = Wy o sin e (이 전 에 는 Yt R=H
-(M e02) Fn Bto Wy o = Wy b uto s in e (이 전 에 N는H — YCO) O CHs R = -CCtIIH HH22- C O OCHa -02 (MeO) 2Fn Bt o W yo =Perox ywyb uto s in e (이 전 에 는 Yr, Yw 또는 per oxy Y)
 H3C 仁RI 〕cIOia 3 〉RHI i b os e
H3C 仁RI 〕cIOia 3 〉RHI i b os e
 NH— COO CH3
NH— COO CH3
C 가, 6 번 및 7 번 위치들에는 m2G 가, 그리고 67 번 위치에는 中가 있 올 수 있다. 진핵세포들만이 이 위치들에 변형된 누클레오시드들을 가 진다. 9 번 및 13 번 위치들과 감은 약간의 위치들에 있는 염기들은 진 핵세포들과 원핵세포들 두 경우 모두 자주 변형된다. 10 번 위치의 m2G 또는 26 번 위치의 m 덩 G 들과 같은 약간의 변형된 누클레오시드들은 진 핵세 포들에서만 발견된다. ac J C 는 진핵세포들에서는 12 번 위치에만 있 지만, 원핵세포들에서는 역코돈 고리의 34 번 위치에만 존재한다. 그러 므로 ac J C 를 형성시키는 변형 효소는 진핵세포들과 원핵세포들에 모두 존재하지만 그 특이성들이 다르다는 것을 알 수 있다. t R N A의 어떤 위 치들 (예, 8 번 및 12 번)에서는 한 유 형 의 변형된 누클레오시드가 발 견되는 반면에, 다른 위치들 (4 번, 9 번, 그리고 26 번)에서는 여러 가지 유형의 변형된 누클레오시드들이 발견된다. 진핵세포와 원핵세포 t RNA 들의 D 고리는 주로 D 와 Gm 들을 함유 하고 있지 만, 최 근에 쥐 의 tR NAA” 의 20: 1 번 위 치 에 서 acp3 U 가 발견 되었다 (Chen 과 Roe, 1978). 14 번 위치의 m1A 는 진핵세포들에서만 발 견되었다.
 :l: 진색 세 포듄에서만 :0-:11:1-],, \n,, ; '. ;:
:l: 진색 세 포듄에서만 :0-:11:1-],, \n,, ; '. ;:
역코돈 줄기는 그 칭 끝쪽으로 자주 ,fr를 가지지만, 진핵세포들에서 만 그러함이 알려져 있다. 역코돈 고리에는 변형이 자주 일어나는 자리 둘이 다섯 군데가 있다. 동요 위치에는 I 이외에도 t RNA 의 다른 위 치에서는 볼 수 없는 U 의 몇 가지 유도체들과 mam 냥 U( 원핵세포에서 ) 와 mcm5U( 진핵세포에서)와 같은 과변형된 누클레오시드들이 있다. 역 코돈에 인접한 인 위치에는 때때로 변형된, 및 과변형된 푸린둘이 존재 하는데 그 들 중 약간은 원핵세포들에서만 볼 수 있고, 다른 것들은 진 핵세포들에서만 볼 수 있다. 가변성 팔은 46 번 위치에 m 7G 를 가진다. 47 번 위치에는 진핵세포 들 에서는 D 만이 있고, 원핵세포들에서는 m5C 만이 있다. 앞에서 이미 말한 바와 갇이 , T,f r 연 속 부분은 공통성 이 매 우 크지 만, T 가 s2T, Tm 또는 미지의 누클레오시드 Z 둘로 치환되어 있는 경우들도 있다• 미토콘드리아에는 그들 목유의 변형 효소들이 있으며, 그 변형의 정 도, 양식, 목이성 들은 세포질에 있어서의 누클레오시드들의 변형에 대 한 것들과 다르다. 그러나 이 효소들에 대한 유전자들은, 적어도 효모 에 있어서는 , 핵에 있는 것 으로 생각되고 있다. 미토콘드리아의 누클레 오시 드들의 변 형 에 관해 서 는 Dir h eim er (1979) 를 보라. 1. 4. 7 tR NA 의 변형된 누클레오시드들의 기능 변 형 된 여 러 누클레 오시 드들의 구조의 복잡성 , 그들이 tR NA 분자 상에서 존재하 는 특이한 자리들, 그리고 그들이 여러 가지 많은 생체들 에서 언제나 볼 수 있다는 사실 등은, 그들이 t RNA 둘의 기능에 있어 서 중요한 역할을 할 것이라는 것을 암시해주고 있다. 그러나, 이것을 증명할 만한 직접적안 증거들은 극히 드물다. t RNA 들과 개시 인자들, 연장 인자들, 리보솜 단백질들, 리보솜 RNA 둘, 그리고 단백질 합성에 관련된 그밖의 단백질들 사이의 상호작용에 있어서의 변형된 누클레오 시 들의 역할에 관해서는 뒤에서 관련된 주제들과 연관시켜 다룰 것이며 t RNA 들과 아미노아실-t RNA 합성효소들 사이의 상호작용에 있어서의 변형된 누클레오시드들의 역할에 관해서는 1.5 절에서 논의한다. 여기서 는 주로 코돈과 t RNA 의 역코돈 부분과의 인식작용에 있어서의 변형된 누클레오시드들의 역할둘만을 논의하겠다. 지금까지의 연구결과들은 변 형된 누쿨레오시드들이 특이한 기능들을 가질 것입을 강력히 암시하고
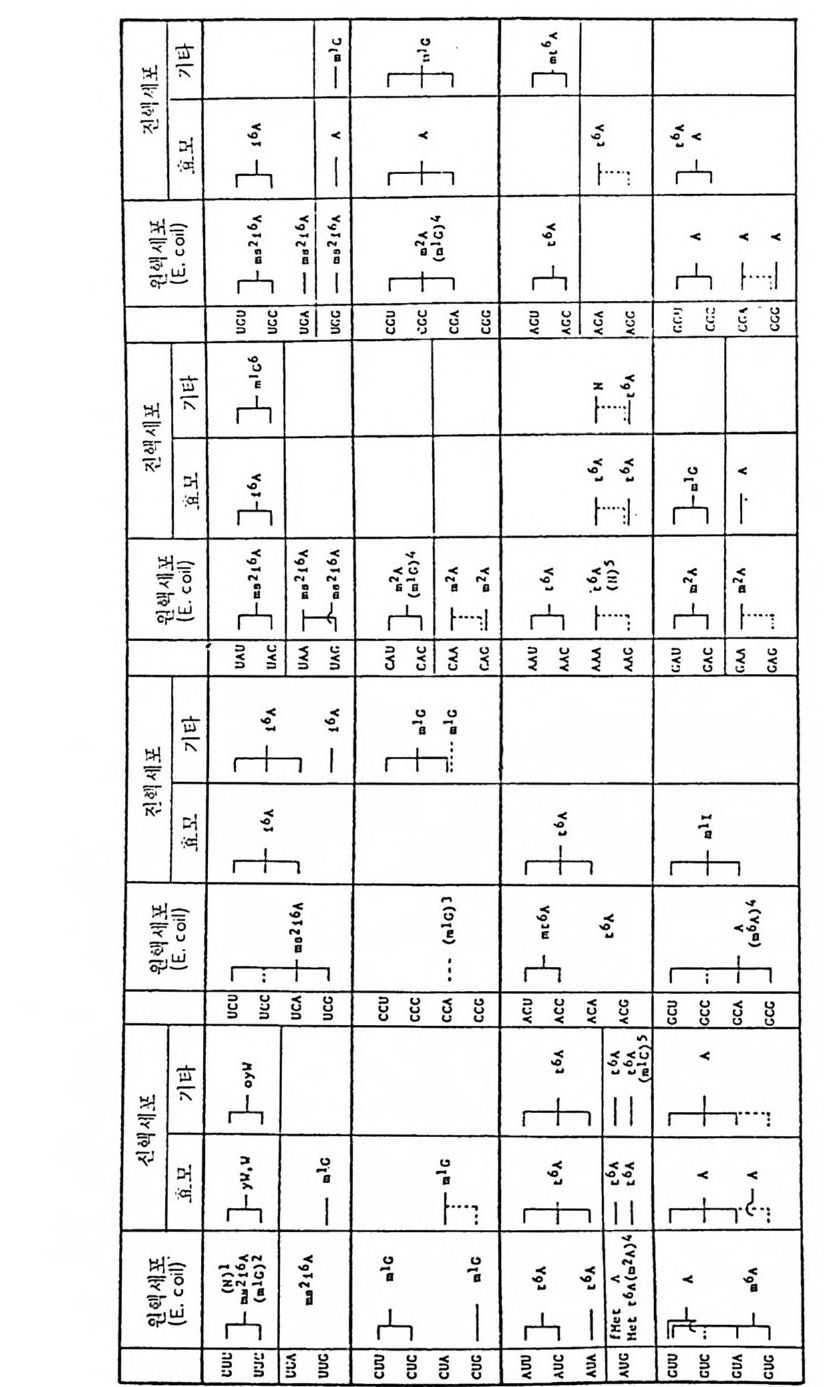
있지만, 약간의 경우 들 에 있어서는 확실한 실험결과들을 얻지 못하고 있다 . tR NA 의 역 코 돈이 mRNA 의 상응하는 코돈을 인식 할 때 역 코돈의 3' 말단에 인접한 특별하게 변형된 누클레오시드 들 은 독특한 규칙을 이 룸 울 볼 수 있다(그립 1-15 를 보라). 예를 들면, i6A 또는 그의 유도체 들과 같은 소수성 누 쿨 레 오시 드들은 U 로 시 작하는 코돈둘을 인식 하는 t RNA 들 에서 거의 언제나 불 수 있다. 또한, A 로 시작하는 코돈을 안 식하는 거의 모든 t RNA 들 은 t6A 또는 그 유도체 들 과 같은 천수성 변 형 누 쿨 레오시드 들을 함유한다. A·U 쌍은 G·C 쌍보다 에너지적으로 약 하다. 과 변 형 은 A•U 쌍을 안정화시키는 역할을 하는 것으로 생각된 다. 역코돈의 3' 쪽 으로 있는 이러한 과변형된 누클레오시드들이 tR NA 의 아미노산 전달에 필수적이라는 증거둘이 많이 보고되어 있다. 예를 들면, 역코돈에 인접한 자리에 A 를 가진 E. col i의 억압 t RNAT y r 는 아미 노아실 화 되 기 는 하지 만, 아미 노산을 전 달하지 는 못한다 (Geft er 와 Russel, 1969) . 또한 i6A 를 거 의 함유하지 않는 Saccharomy ce s cerevis i a e 의 한 돌연변이체의 코돈 UAA 를 인식하는 억압 t RNAT y r 은 티로신을 거의 삽입하지 못하는 것이 알려져 있다 (La t en 등, 1978). 역코돈의 첫번째 자리는 소위 〈등요〉 위치로서 과변형된 누클레오시 드들이 자주 나타난다. Cric k 가 말한 아 노신 (I) 이 그 좋은 보기 이 다. 역코돈의 첫째 위치에서 동요 현 상을 일으키는 · 염기로서는 그 이외에도 05U 와 mo5U 들이 있다 . 그들은 역코돈의 세번째 자리에 있는 u, c, 및 A 들과 염기 쌍들을 이루는 반면에, o5U 와 mo5U 는 U, A , 및 G 들과 염 기 쌍들을 이 물 수 있 다 (Ni sh im ura, 1979) . 등요 짝짓 기 와는 반대 로 역 코돈의 첫 번째 위 치 에 있는 s2U 또는 그 유도체 들인 mcmm5U, mcm 냥 u, 및 mnm 냥 U 들은 코돈의 세번째 자리의 A 또는 G 들 중에서 A 를 선 택적으로 인식한다• U 가 s2U 로 변형되면 U·U 짝짓기가 일어나지 못 하게 되는 것으로 생각된다. 역코돈 고리 이의의 다른 부분들에 있는 변형된 누클레오시드들에 대 해서는 다음과 같은 기능들이 있을 것으로 암시되고 있으나, 이들에 대 한 증거는 더 연구되어야 할 것이다 . (1) t RNA 둘의 GT,f rC 연속 부분 은 리보솜의 5S RNA 를 안식한다 . (2) 변형된 누클레오시드들은 tR NA 의 형태를 안정화시킨다. (3) 핵산 가수분해효소들에 대한 저항성을 증 가시 킨다. (4) 아미 노아실-t RNA 합성 효소들에 의 한 인식 특이 성 을 종
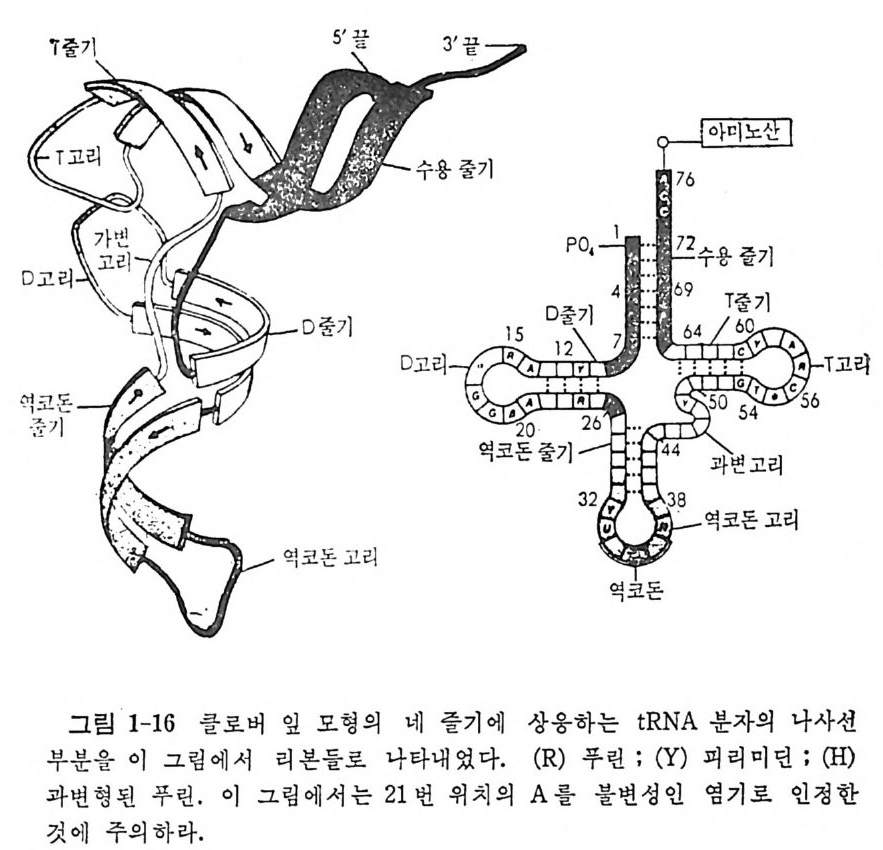
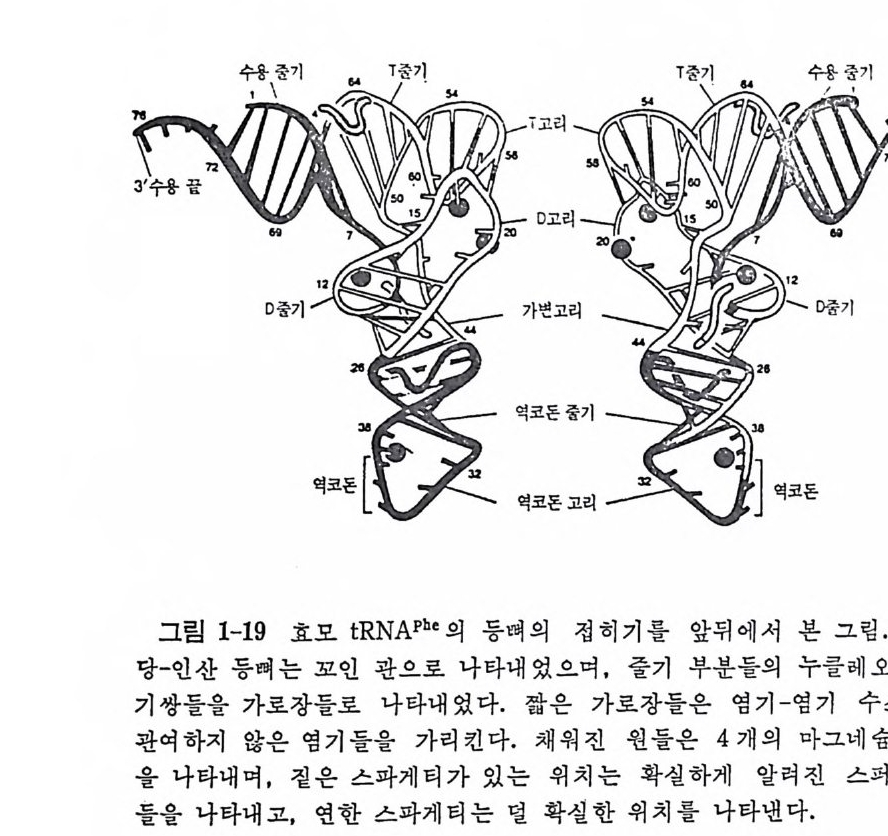
진시킨다. 1. 4. 8 tR NA 의 결정구조 IGm 등 (1974) 이 처 음으로 효모의 tR NAPhe 의 삼차원 구조를 밝힌 이 후로 E. coli 의 tR N A111••, 효모의 tR NACly 들의 결 정 구조가 밝혀 졌 다. 이 세 tR NA 들은 tR NAPhe 과 마찬가지 로 L 자 모양의 삼차구조 물 가진 다. 그러 나, 최 근에 밝혀 진 효모의 tR NA&p (Moras 등, 1980b) 은 L 자 모양이 아니라 부메랑 모양을 하고 있으며, 꺾여진 부분의 각도가 90° 가 아니 라 110° 를 이 루고 있음아 알려 졌다. 효모의 tRN APhe 과 tRN AA•P 삼차구조들 사이에는 중대한 차이점들이 있음이 발견되었다 . 먼처 tR NNh• 의 삼차구조를 논의 한 다음에 tR NAA” 의 삼차구조 급 살펴 보자. 효모 t RNAPb• 의 결정구조의 독징들을 다음과 같이 요약할 수 있다 (IGm , 1979) (그림 1-16 올 보라). (1) 분자의 전체 모양은 L 자형이다. (2) 클로버 잎 모양의 이차구조에 있을 것으르 생각되는 이중나사 선 줄기들이 삼차원 구조에서 실제로 보지되며, 모두 우회전성이고 역평행 한 이중나사선 구조를 이루고 있다. (3) 아미노산 수용 줄기와 T 줄기들은 연속된 이중나사선 부분을 이 루는데, 몸재가 한 군데 있다. D 줄기와 역코돈 줄기들은 두 군데에 틈새를 가진 근사적으로 연속된 또 다른 이중나사선 부분을 이룬다. 이 연속된 두 이중나사선 부분들아 L 자를 형성한다. (4) 펩터드 연장이 일어나는 3' 끝은 L 자의 한쪽 끝에 있고 mRNA 상의 코돈을 인식하는 역코돈은 L 자의 다른 끝에 있다. D 고리와 T 고리들이 L 자의 모퉁이를 이룬다. 5S 및 5.8S rRNA 를 인식하는 자 리라고 생각되는 T 고리는 바로 이 모퉁아에 있다. 이와 같이, 기능적으로 중요한 세 자리들이 최대한으로 분리되어 있 다. 이것은 세 자리들 상호간의 간섭을 최소한으로줄이는 데 도움이 될 것이다. (5) L 자의 두 팔은 직경이 약 20A 이고 길이는 약 6oA 이며, 두 팔 의 끝들 사이의 길이는 약 80A 이다. 가) 염기-염기 상호작용 이 부류의 상호작용에는 2 가지가 있다. 그
 76
76
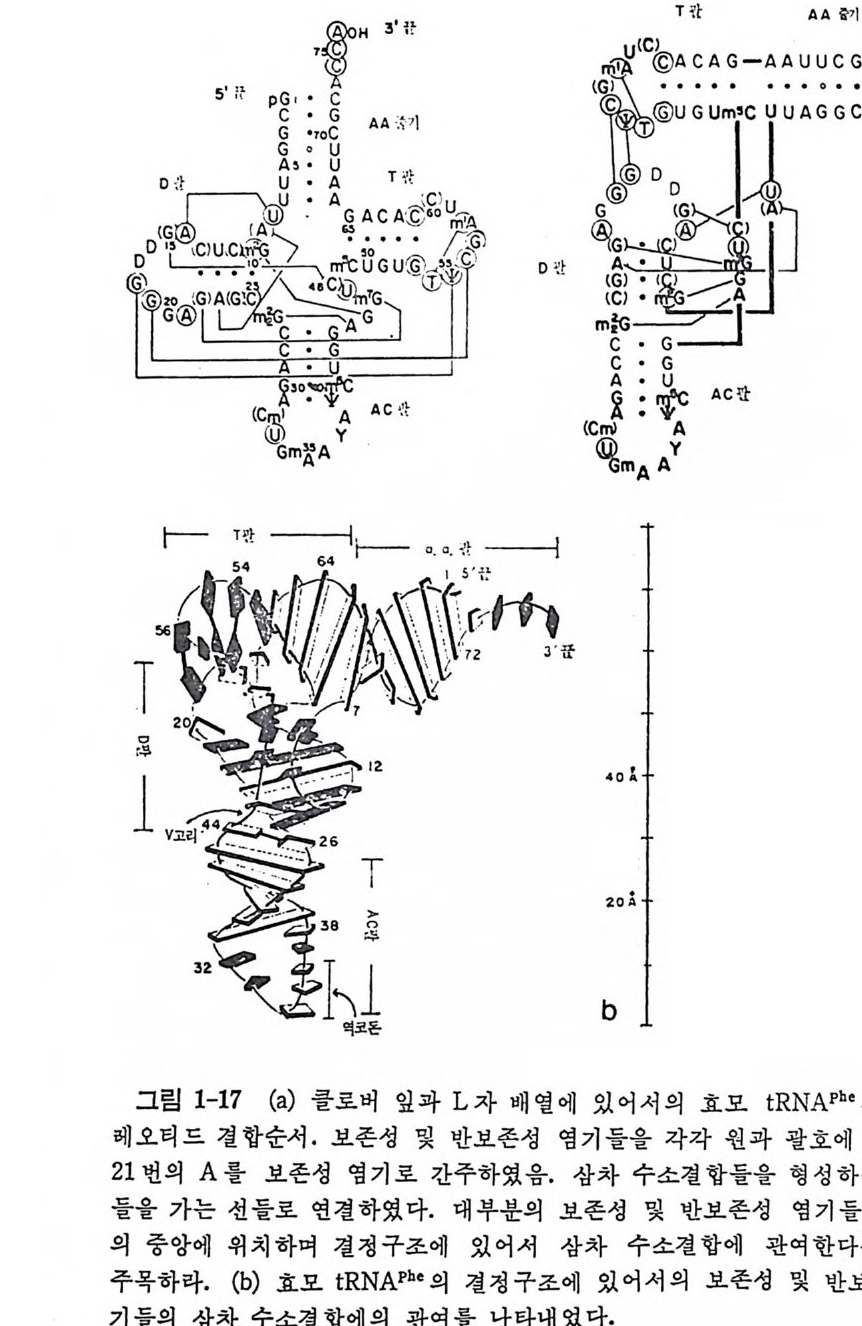
하나는 염기 치쌓기이고 다른 하나는 수소결합들에 의한 염기 짝짓기아 다. tR NA 분자에서 줄기 부분들에 있는 염기들은 55% 뿐이지만, 삼차 원 구조에 서 는 다섯 개 의 염 기 들 (D16, D17, G20, U47, 및 A76) 을 제 외한 모든 염기들 (93% 에 해당함)이 치쌓기에 관여하고 있다(그림 1-17 b). 염기 치쌓기가 이렇게 광범위한 것은 자유 상태의 핵산들의 보편적 인 성질이라고 생각한다. 삼차 수소결합이라는 것은 이차 수소결둘 이의의 수소결합들을 말한 다. t RNAPhe 의 결정구조에는 불변성 (보존성) 및 반불변성 (반보존성)염 기들 사이에 아홉 군데에서 삼차 염기쌍을 이룬다(그림 1-17a 를 보라). 그들 중 Gl9·C56 쌍을 제 외 한 다른 삼차 염 기 쌍둘이 Wats o n-C r ic k 형 이 아니다. 이러한 관찰에 기초하여 모든 종의 tR NA 분자들이 일반적
 GG ••r oCU AA ·안· 1 〉: ::AAc G군 기: : p笑多
GG ••r oCU AA ·안· 1 〉: ::AAc G군 기: : p笑多
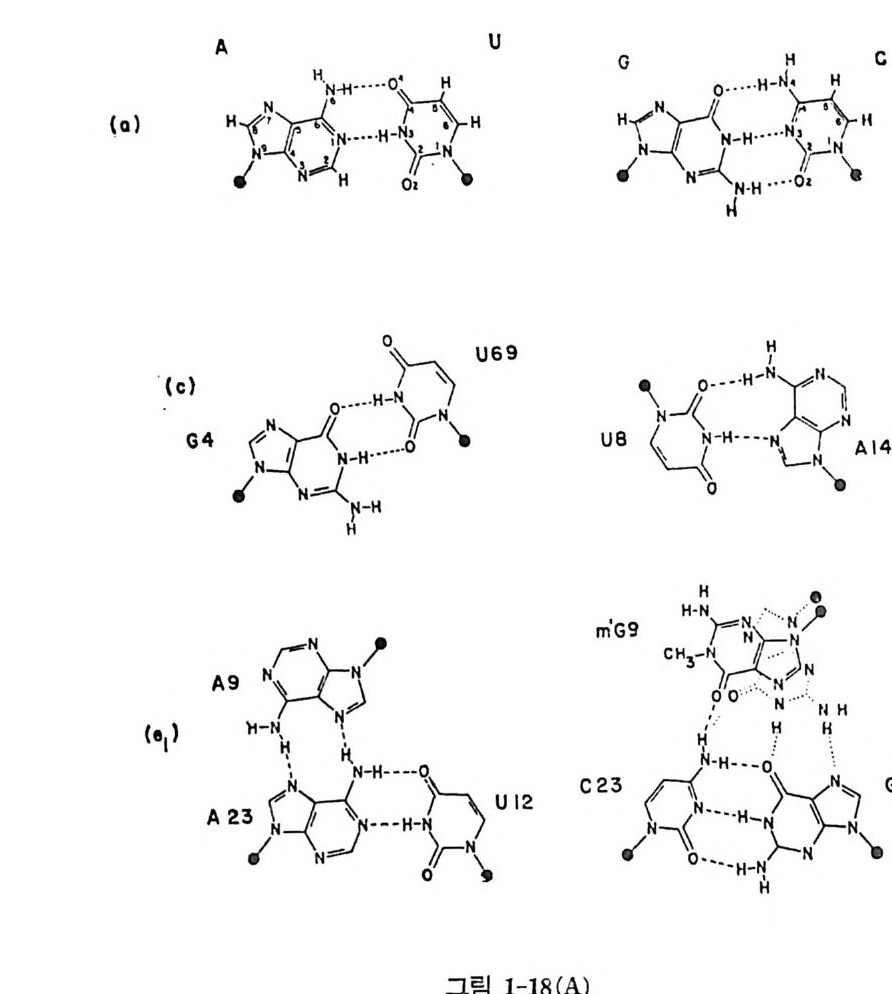
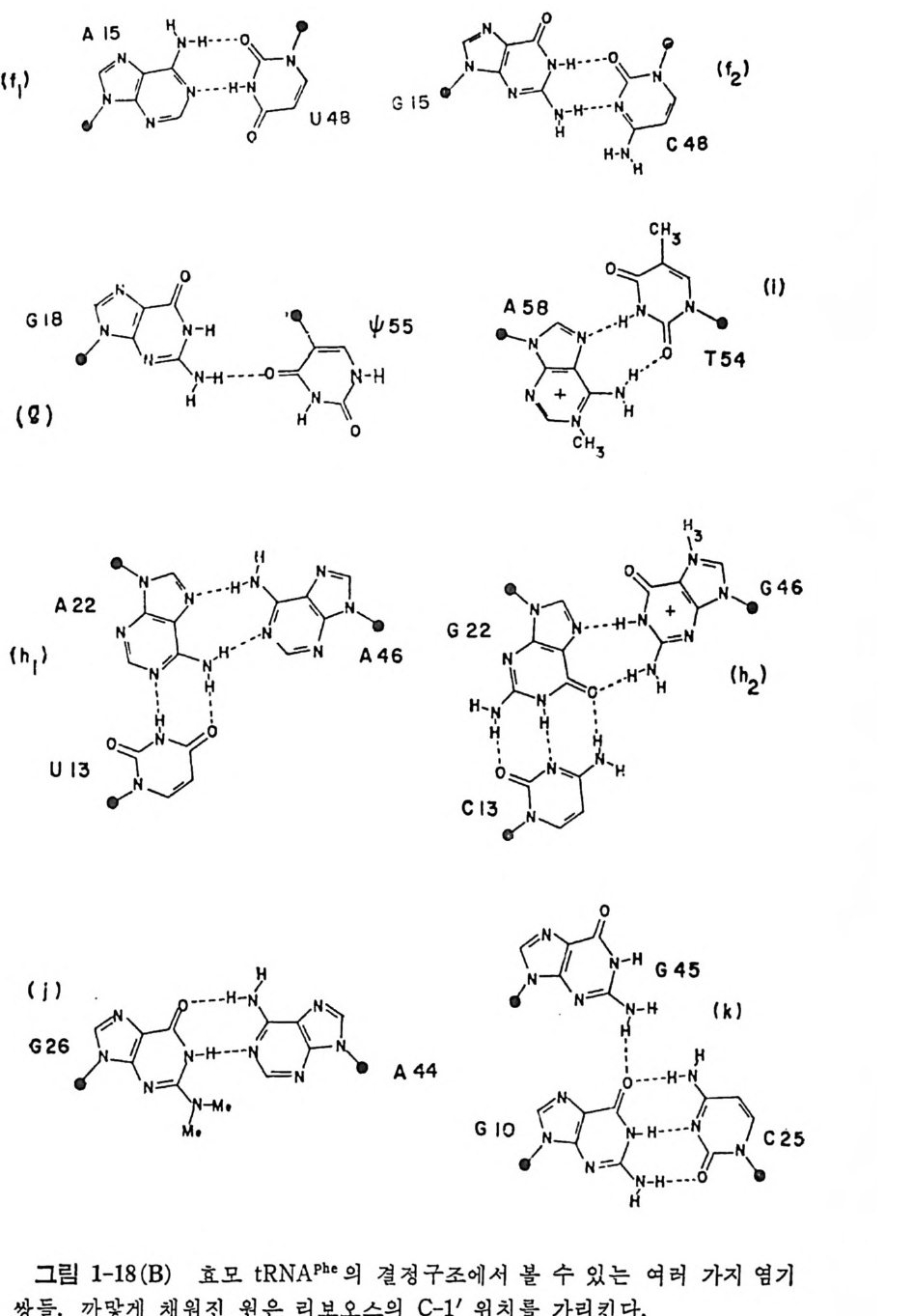
으로 유사한 구조를 취할 것으로 생각할 수도 있다. 더우기, 이들 삼차 수소결합들이 L 자의 두 팔둘이 만나는 곳에 위치하고 있어서 L 자 모 양의 구조를 유지하는 데 필 수적이다. 그밖에도 삼차 수소결합으로 짝지어진 염기들이 더 있다(그림 2-18). 나 ) 염기 - 등뼈 상호작웅 아직은 등뼈가 관여되는 삼차 수소결합들의 위 치를 정확하게 알지 못하고 있다. 이 문제에 관해서는 연구 자들 의 의 견이 아직 일 치하지 않고 있다. 이 종류의 수소결합으로서는 5 개 정도 가 있다고 생각되는데, 그 중 5 개의 2'- 0 H 7] 들이 관련되고 있다. 다 ) 등뼈 - 등뼈 상호작용 이 부류의 수소결 합들을 정 확하게 결 정 하기 는 매우 어 렵 다. 이 경우에도 리보오스의 2 '- 0H 기들이 여러 군데에서 관여 하는 것으로 생각된다. 2'- 0 H 기들이 광범위하게 삼차 수소결합들의 형성에 관여 할 수 있는 속성이 아마도 t RNA 들과 rRNA 들과 갇은 RNA 들이 DNA 대신에 구 조적 핵산들로서 사용되는 이유일지도 모른다. 라 ) 역코돈 고리 역코돈 고리는 삼차수소결합들이 비교적 적은 부분 이다. 역코돈 삼중체를 포함한 5 개의 염기들이 고리의 한쪽에서 치쌓 여 있고, 다른 쪽에 는 두 개의 염기들만이 있다(그림 1-17b 를 보라)• 이 고리는 마그네슘 수화 이온에 의해서 더 안정하게 된다. M g 2+ 은 찬 기 37 번의 인산의 산소와 직접 배위결합을 형성하며, M g 2+ 에 배위된 물 분자들은 이 고리에 있어서 가까운 염기들과 몇 개의 수소결합들을 형 성 한다 (Holbrook 동, 1977 ; Quigle y 등, 1978) . 그러 나, 만일 리 보 솜의 성분들에 의해서 수화된 마그네숨 이온야 제거되면, 역코돈 고리가 유연성을 가지게 되어서 아미노아실 자리에서 펩티딜 자리로 자리옮김 이 일어나는 동안에 요구되는 형태의 변화가 가능하게 될 것으로 생각 된다. 마) 금속 이온-t RNA 상호작용 득이한 위치에 결합한 M g 2+ 이온돌은 t RNA 들의 기능적 형태를 안정화시키는 역할을 한다는 것이 알려져 있 다 (Fresco 등, 1966 ; Ste i n 과 Croth e rs, 1976) . 수화된 마그네 슘 이 온 들의 결합 자리들은 D 고리예 2 개, 역코돈 고리에 하나, 8 번에서 12
 (al A d>`Nf 三같 H. ·· ··. . 01릅\. H u GVhH >/0- Nd서 · H H . 군값\. I I c ( b)
(al A d>`Nf 三같 H. ·· ··. . 01릅\. H u GVhH >/0- Nd서 · H H . 군값\. I I c ( b)
 A立 15 〉HN-H- ··H--·广0 ? u 48 G 15 / 다N」 N< j。 : --HH··-·\·\O)}C-z4 8( f2)
A立 15 〉HN-H- ··H--·广0 ? u 48 G 15 / 다N」 N< j。 : --HH··-·\·\O)}C-z4 8( f2)
번까지의 잔기들로 이루어지는 급회전 부분에 하나 있다(그립 2-19). M g 2+ 이 위치한 자리들로 미루어 보아서 이 이온들의 기능적 역할은 t RNA 의 기능적 형태를 유지하기 위해서 t RNA 분자에 있는 고리들과 급회전 부분들을 안정시키는 것임을 뚜렷이 알 수 있다. 바) 스퍼민-tR NA 상호작웅 스퍼먼 같은 풀리아민들은 tR ) rA 구조의 기능적 형태를 안정시키는 것 으 로 알려져 있다. 스퍼민의 가능한 세 위
 수'용 \중 기 T `혼 기Z ”Z 、 T 고리 수용 중기
수'용 \중 기 T `혼 기Z ”Z 、 T 고리 수용 중기
치들이 암시되어 있는데, 그 중 둘은 D 줄기와 역코돈 줄기들로 형성 되는 이중나사선의 깊은 고랑에 위치하고 있으며, 다른 하나는 아미노 산 줄기와 T 줄기들로 형성되는 이중나사선의 깊은 고랑에 위치하고
있다 (Holbrook 둥, 1978). 스퍼민의 역할은 tR NA 분자의 깊은 고랑에 결합하여 t RNA 의 이중나사선 부분을 안정시키는 것이다• 사 ) tRN APhe 이외의 tR NA 둘의 결정구조 tR NA 들은 다양한 기 능을 가 진 분자들이며, 단백질 합성 장치의 여러 성분들과 상호작용한다. 리 보솜들과의 상호작용에서 볼 수 있는 바와 같이, 이 분자들의 약간의 기 능들은 도든 tR NA 들에 공통적 이 다. 그러 나, 아미 노아실-t RNA 합 성효소 들과의 결합은 개개의 t RNA 들에 있어서 목이하다. 그러므로, 모든 tR NA 분자둘은 삼차원 수준에 서 의 구조적 인 유사접 들을 가지 고 있지만, 그 들 의 기능을 위한 특이한 차이접둘을 가질 것으로 생각한 다. 따라서, t RNA 의 다기능적인 성격을 더 잘 이해하기 위해서는 여 러 종류의 t RNA 들의 구조들에 관한 지식이 필요하 다. 더우기, 최근 에 밝혀 진 몇 가지 tR NA 둘의 결 정 구조들은 효모의 tR NAp h e 의 것과 공통접과 유사 점들 이 있기는 하지만 동일하지는 않으며, 매우 중요한 차이점들이 있음을 예시해 주고 있다. 효모의 tR NAPhe 이외에 알려진 그 밖의 t RNA 들의 삼차구조에 있어서의 중요한 점들을 알아 보기로 하자. Wrig h t 등 (1979) 은 효모의 tR NAGly 의 결 정 구조를 3. 5A. 의 분해 능에 서 결정하였다 . 효모의 t RNAPhe 의 경우에서와 같이, 그 삼차구조를 세 밀하게 분석할 수 있는 단계는 아니지만, 전체 삼차구조에 있어서의 t RNAGl y의 클로버 잎의 팔둘의 상대적인 배치는 아미노산 수용 줄기를 제외하고는 상당히 비슷하다. 아미노산 수용 줄기의 3' 부분은 그 말단 부분이 역코돈 줄기의 5' 축에 접근하면서 활모양을 만든다(그림 1-20 을 보라). 이와 같이, t RNAGl y의 형태는 그의 아미노산 수용 줄기가 풀려 있다는 것이 독칭이다 . 개시 t RNA 둘은 사슬 연장 t RNA 들과 여러 점에서 구별된다. 제일 중요한 점은 아미노아실 화된 개시 t RNA 들은 직접 리보솜의 P 자리로 들어가는 데 반해서, 그밖의 모든 아미노아실화된 t RNA 둘은 처음에는 A 자리로 들어가고 사슬의 연장 과정이 일어나면서 비로소 P 자리로 들어가는 것이다 (5.2.2 절을 보라). 개시 t RNA 들의 구조와 그 독특 한 기능들 사이의 관계를 알기 위해서는 개시 t RNA 들과 다른 tR NA
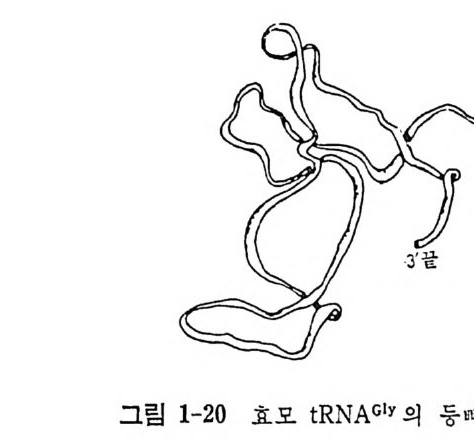 그림 1-20 효모 t RNAGly 의 등뻐 의 형 태
그림 1-20 효모 t RNAGly 의 등뻐 의 형 태
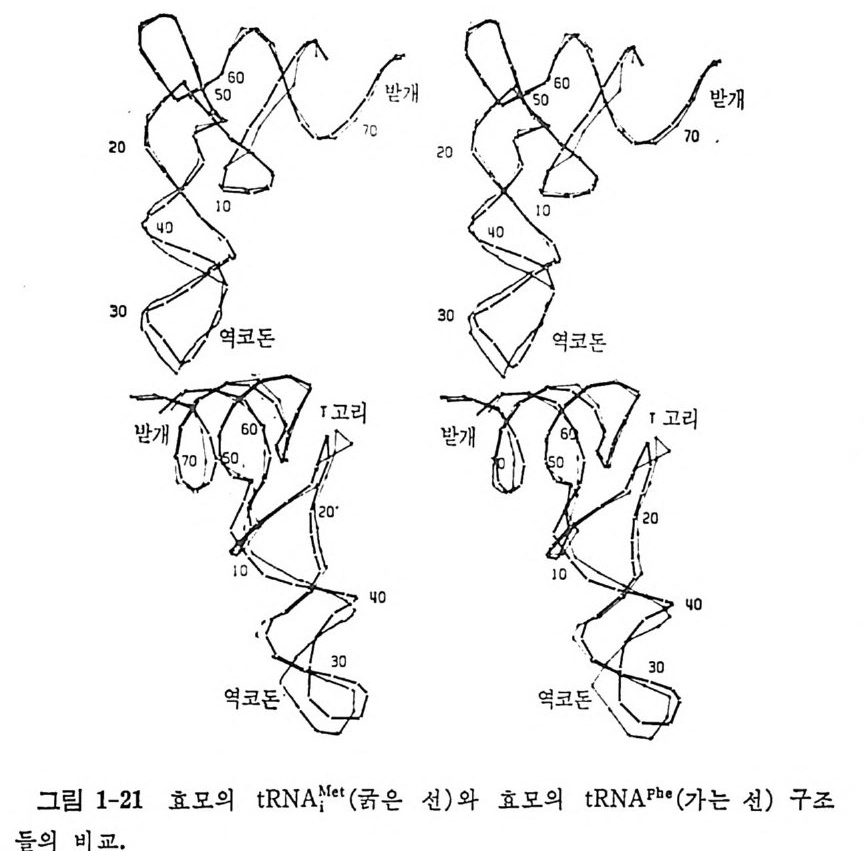
들의 구조들에 있어서의 차이점을 알아내야 할 것이다. 삼차원 구조가 밝혀진 개시 t RNA 들에는 원핵세포인 E, col i의 개시 tR NA'M••(Woo 등, 1980) 와 진핵세포인 효모의 개시 t RNA 판 '(Sc hev it z 등, 1979) 들이 있 다. 이 두 개 시 tR NA~1 들은 효모의 tR NNh’ 와 같은 L 자 모양의 상차구조를 한다(그림 1-21 및 그림 1-22 를 보라). 그러나 그들은 서로 몇 가지 큰 차이점들을 가지고 있다. 효므의 개 시 t RNA 판' 와 효모의 tRN APhe 둘의 삼차구조에 있 어 서 의 큰 차이는 역코돈 팔 부분에 있다(그림 1-21). 역코돈 팔의 배향은 굳 게 고정되어 있는 것이 아니라 D 줄기와 역코돈 줄기 들은 t RNAPbe 의 구조에 대해서 암시된 것처럼, 구조의 기능적 변화가 일어날 때 돌쩌귀 의 역할을 할 것으로 생각한다• 여기서 말한 효모 개시 t RNN'” 는 4 .5A 의 분해능에서 분 석된 것이 므로, E. coli 의 개 시 tR NAIMet 또는 효모의 tR NAPhe 의 구조들과 더 세 밀히 비교하기 위해서는 더 높은 분해능에서의 분석 결과가 얻어져야 한다. E. coli 의 개 시 tR NArM” 의 삼차구조는 2. 8 A의 분해 능으로 분석 되 었 기 때문에 많은 정보를 얻을 수 있다. 그림 1-22 에 E. coli 개시 tR NA '~le t 와 효모 tRN APh• 들의 이 차구조를 제 시 하였다. E. coli 의 개 시 tRN AIMet 의 이차구조의 특징은 Cl 이 A72 와 염기쌍을 이루지 않으며, D 고리 에 Cl6Cl7Ul7:1 연속 부분이 있는 것이 특징이다. E. coli 의 개 시 tR NA™•t 의 구조는 다음과 같은 세 가지 특칭 들에 의
 /1 〈 개
/1 〈 개
해서 효모의 t RNAPhe 의 구조와 구별된다. 첫째로, 3' 말단 부분에 있는 5 개의 누클레오티드 연속 부분이 수용 말단 쪽으로 꼬여 있다(그림 1-23). 개 시 tR NA 에 서 보는 이 형태는, tR NA 의 이 끝 부분의 유연 성을 암시하는 것으로서 이 t RNA 의 생물학적 역할을 고려할 때 · 합목 적적이라고 생각할 수 있다. 다시 말하면, 3' 말단 부분의 유연성은 갓 생긴 폴리펩티드를 다음 t RNA 로 옮겨 주는 기능에 알맞는다. 두번째의 차이점은 개시 t RNA 의 D 고리의 a 부분이 t RN Af h• 의 것 보다 더 큰 것이다. 개시 t RNA 는 그의 기다란 a 부분을 바깥쪽으로 내밀고 있지 않고 오히려 tR NA 본체 쪽으로 받아둘이고 있다. 그래서 이 부분이 t RNAPhe 보다 더 조밀한 구조를 이루게 된다(그림 1-23). 세번째 차이점은 역코돈의 팔의 형태와 관련된다. 주요 차이점은 개 시 t RNA f 1e1 의 역코돈 고리의 33 번 위치의 U 가 바깥쪽으로 돌출된 배

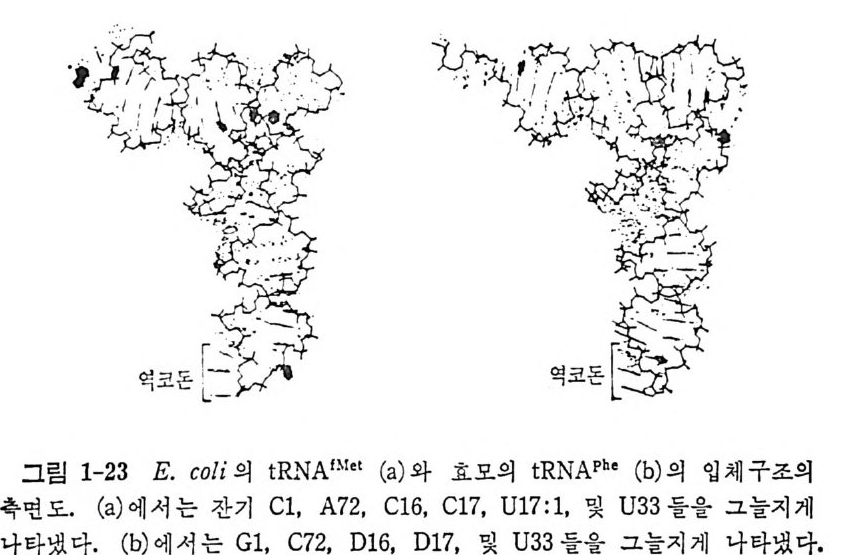 그림 1-23 E. coli 의 tR..NA 1Met (a) 와 효모의 tRN APhe (b) 의 입 체 구조의
그림 1-23 E. coli 의 tR..NA 1Met (a) 와 효모의 tRN APhe (b) 의 입 체 구조의
위를 가지고 있다는 것이다. 이와는 대조적으로 효모의 t RNA p be 의 U33 은 역 코돈 고리 의 안쪽으로 향하고 있다. E. coli 의 tR NNM 와 효모 의 t RNA pbe 의 역코돈 고리들에 있어서의 형태의 차이는 리보솜 상에서 t RNA 가 자리를 옮길 때 일어나는 형태의 전이일 수도 있을 것이다. 최근에 연장 t RNA 의 하나인 효모의 t RNAA” 의 삼차구조가 세밀하
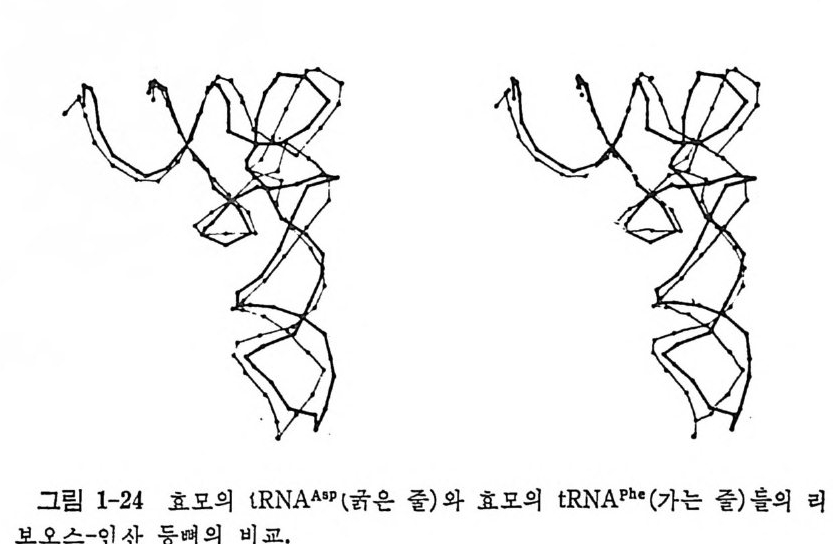 그립 1-24 효모의 tRN AA•P t굵은 줄) 와 효모의 tRN APh• (가는 줄) 을의 리
그립 1-24 효모의 tRN AA•P t굵은 줄) 와 효모의 tRN APh• (가는 줄) 을의 리
게 밝혀 졌 다 (Moras 등, 1980b) . 이 tR NA 는 효모의 tR NAp h e 와 일 반 적인 구조는 비슷하지만 대단한 차이접둘을 가지고 있다. 그립 1_24 는 아미 노산 줄기 와 D 줄기 들이 가능한 한 많이 중 첩 되 게 끔 효모의 tR NAA•p 와 t RNNh• 의 둥뼈들을 배치한 그림이다. 첫째로 T,f rC 고리, D 고리 및 역코돈 고리 부분들에서 구조적 차아가 두드러지게 크다는 것을 알 수 있다. 더우기, 효모의 t RNAA” 는 20° 이상과 20° 이하의 두 온도들 에서 그 결정구조가 다르다는 놀라운 발견이다. 두 결 정상태에 있어서 의 D 고리와 T,J rC 고리들의 내부 영역의 상호작용의 양식이 뒤엎여진 다. 그뿐 아니라, D 고리와 역코돈 고리의 형태가 한 형 태 에 서 다론 형
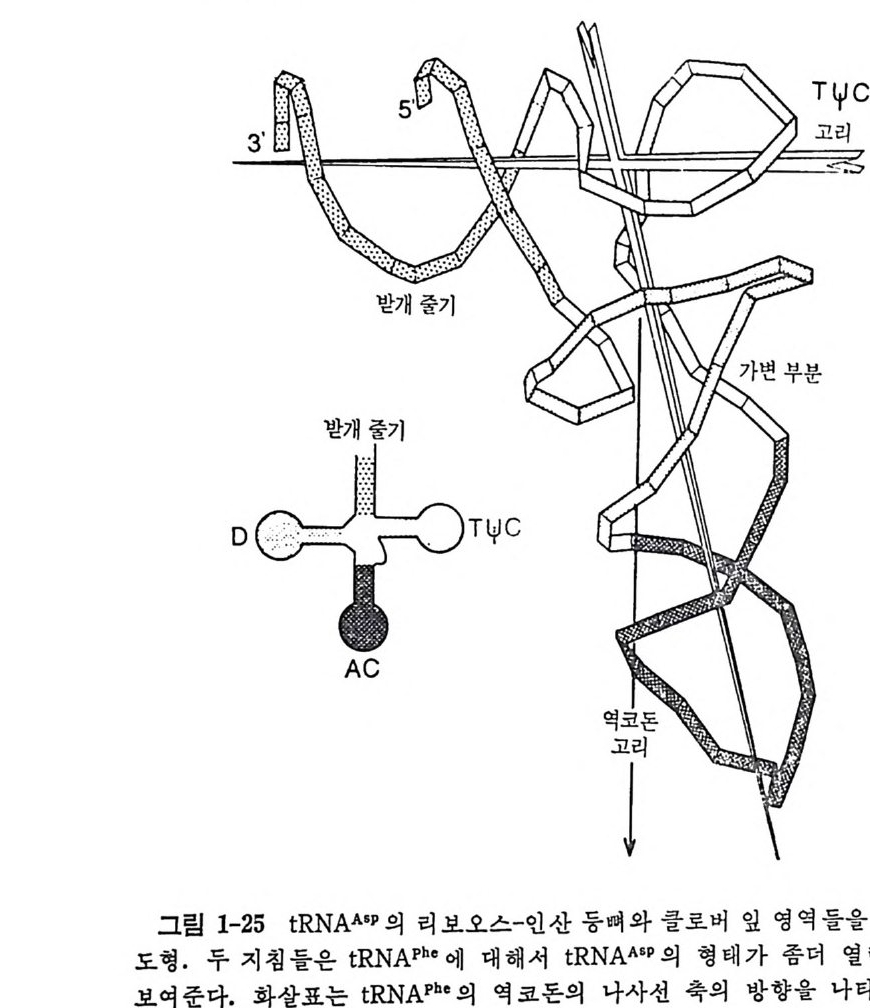 받개줄기
받개줄기
태로 변할 수 있다. 이러한 관찰은 한 가지 누클례오티드 연속 부분이 조건의 변화에 따라서 여러 가지 형태를 취할 가능성이 있디는 것을 증 명해 주고 있다. 이러한 성질은 지금까지의 효모의 t RNAP h e 의 삼차구 조의 분석결과로는 예기치 못하였던 것이다. 둘째로, 효모 t RNAA” 의 L 자 형 구조에 있어서의 두 팔둘이 많이 열 려 있음을 알 수 있다. 효모 t RNAA” 의 L 자의 두 팔들은, 말하자면, 부메 랑 구조를 이 루고 있다(그림 1-25). 세 째 로, t RNA A ” 의 역코돈 (GUC) 들은 상호간의 상보성으로 인하여 서 르 인식 함 으로써 t RNAA” 의 이합체 를 이를 수 있다. 이 현 상은 tR XA 의 역 코돈이 mRNA 의 코돈을 인식 할 때 의 상호작용과 유사하기 때 문 에 매우 홍마 있는 일이다. 우리는 위에서 결 정 구조가 밝혀진 몇 개의 t R NA 둘의 구조들을 비교 해 보았다. t RNA 둘 의 전체적인 삼차구조들이 공통성을 가지고 있는 반 면에, 개개의 t RNA 들 마다 독특한 구조적 특칭을 가지고 있다는 것을 침작할 수 있다. 또한, 개개의 t RNA 들은 리보솜 상에서의 단백질 합성 의 주어진 단계에 참여하는 동안, 단백질 합성 장치의 관련된 인자들에 의해서, 각기 특유한 형태 변화의 유발효과를 받을 것으로 생각된다. 1.4.9 용액에 있어서의 tR NA 의 형태 X- 선 결정구조학적 방법으로 결정한 구조가 생물학적 활동성을 가지 는 수옹액에서의 구조와 같을 것인지를 확인하는 것은 매우 중요한 일 이다. 결정상태의 효소들의 경우에는 결정상태에서 효소 황동성을 측정 함으로써 생물학적 활동성의 문제를 해결할 수 있다. 그러나, t RNA 의 생물학적 기능들은 더 복잡하기 때문에, 결정체에서의 형태와 용액에서 의 형태에 관한 문제들을 해결하기 위해서는 간접적인 방법들을 사용해 야 한다. 다행히도, 이러한 간접적인 방법들을 이용하여 많은 문제들을 해결할 수 있었다. 흔히 이용되는 방법들로 얻은 몇 가지 실험 결과들을 요약해서 살펴 보자. 가) 염기-특이적 화학 변형 t RNA 의 결정구조가 알려지기 전에도 화학 적 변형법은 염기들의 노출 정도에 관한 많은 정보를 제공했다 (Koche t kov 와 Budowsky, 1969; Brown, 1975). 온화한 조건에서 염기들과 특
및 아미노아실-t RNA 합성효소들 67
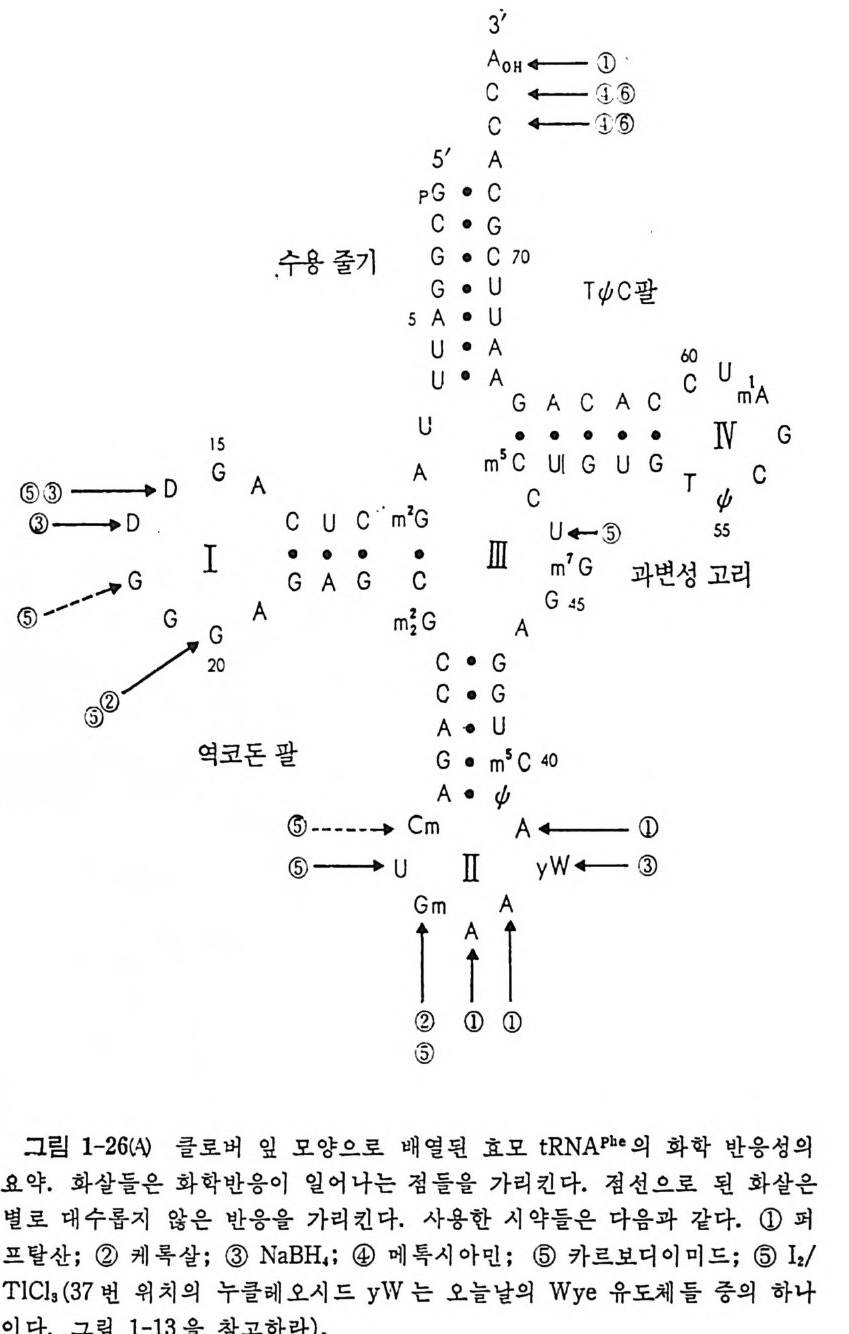
이하게 반응하는 시약들이 몇 가지 있다. 이러한 시약들과 그들과 목이 하게 반응하는 염기들을 표 1-5 에 실었다. 카르보디이미드를 바롯한 몇 가지 시 약둘이 효모 tR NAp b e 의 영 기 들과 작용하는 위 치 들을 그 림 2-26 에 함께 나타내었다 (Clark, 1979). 화학반응성이 있는 염기들은 tR NA
표 1-시5 약영 기에 I독반 이 $하L게I 작 용공하격는받 는시 약염들기 1 반옹 생성물* HMye dthr oo xx yya amm ii nnee , I 7 Cy tos in e 。 NH人 /_〈따 。 H
 3i
3i
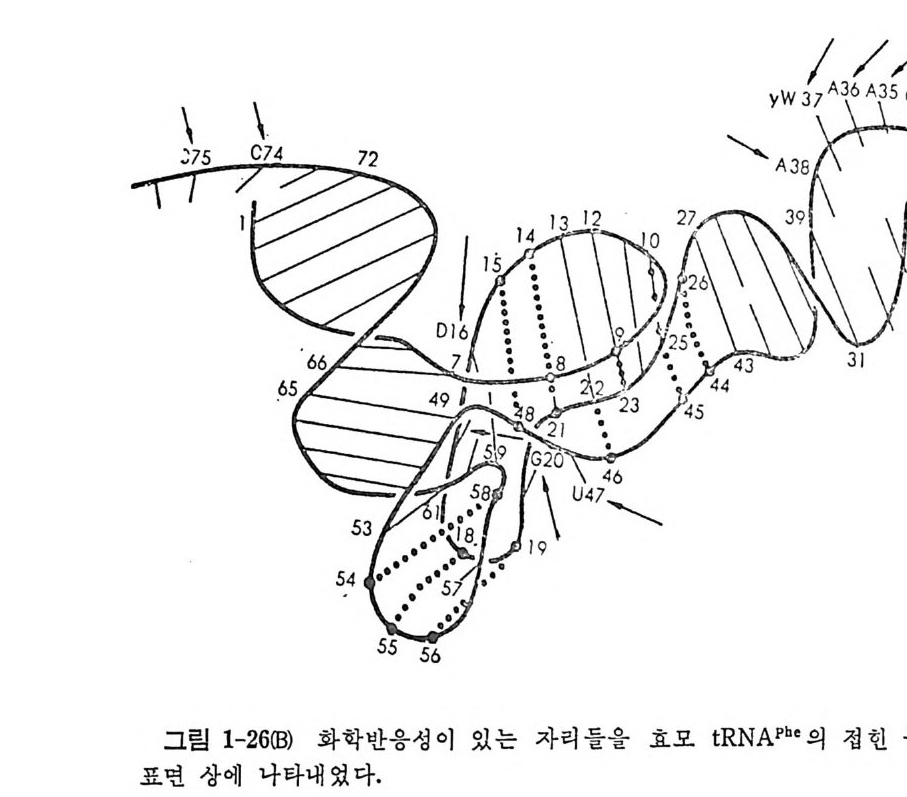 그립 1-26(B ) 화학반응성 이 있는 자리 들을 효모 tR NAPh• 의 접 힌 구조의
그립 1-26(B ) 화학반응성 이 있는 자리 들을 효모 tR NAPh• 의 접 힌 구조의
의 삼차원 구조에 있어서 노출된 위치들이라는 것을 알 수 있다. 반응 하지 않는 염기들은 이중나사선 부분들에 있는 것들이든가, 삼차구조 를 유지하는 데 관여된 것들이든가, 또는 분자 안에 묻혀 있는 염기 들 이다. 화학반응성 들로부터 추정 한 tR NAPhe 의 삼차구조가 tR NAp h e 의 결 정 구 조와 매우 찰 일치함을 알게 됨으로써, 이러한 접근법을 그밖의 tR NA 들에도 적용시킬 자신을 가지게 하였다. 더우기, 화학적 연구 들 은 용액 에 있는 t RNA 에 대해서 시행한 것이므로, 효모의 t RNAPI 모은 결정화 되어도 그 형태가 크게 변하지 않을 것으로 생각된다. 나) 상보성을 가진 울리고누클레오티드의 결합하기 특정한 결합순서의 트 리누클레오티드 또는 더 긴 울리고누쿨레오티드들은 중간정도의 이온 세기를 가진 수용액에서 그 자신과 상보적인 결합순서를 가진 t RNA의 노출된 부분과 특이하게 그리고 강하게 결합할 수 있다. 이러한 결합하가
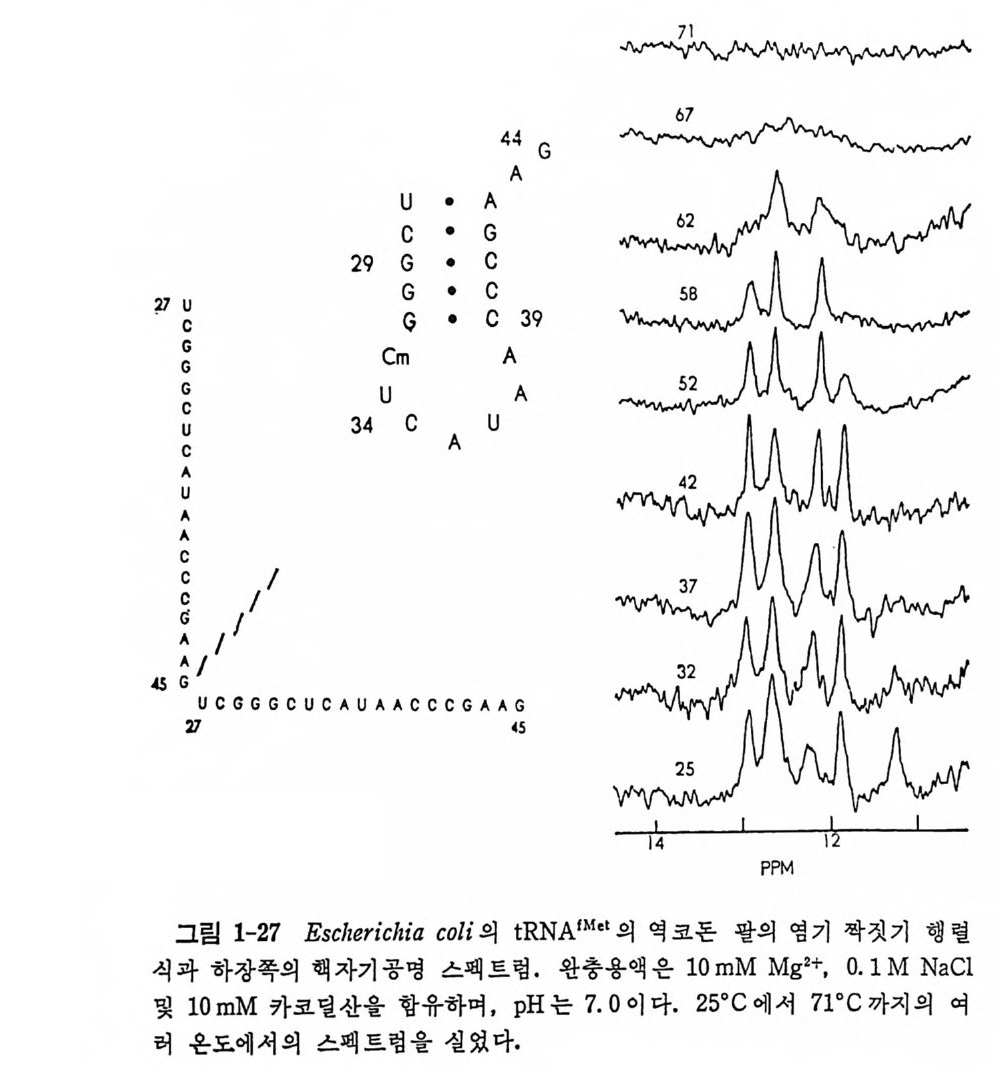
성 질 을 이 용하여 효모의 tR NAPbe 을 포함한 몇 가지 tR NA 들에 관한 연 구에서 얻은 결과들로부터 어느 정도의 일반성을 찾아 분 수 있다 . 거의 모든 t RNA 둘이 분자의 3/ 끝 부분에 있는 세 개 또는 네 개의 염기들에 상보적인 울리고누클레오티드들을 결합할 수 있다. 또한, t RNA 의 역 코돈 부분에 상보적인 을리 고누클레오티드 들을 결합할 수 있다. 클로버 잎의 줄기 부분들의 경우에는 전혀 결합이 일어나지 않는다. T,f rC 고티 둥에 도 실 질 적으로 결 합 이 일어나지 않는다. D 고리의 경우에는 약간의 결 합이 일 어 나지 만 약하게 일 어 나는 것 이 브몽아 다 (Freie r 와 Tin o co, 1975) . 구 체 적인 실험예를 하나 소개함으로써 이 〈울리 고누쿨레오티 드 결합법 〉 은 , t RNA 둘이 리보솜 상에서 복합체들을 형성할 때 받는 형태의 변 화들 을 조사하는 데 이용 할 수 있다는 것을 보자. 효모의 tR N Ap h e 의 역 코돈 부분의 5'···Cm32U33Gm34A35A36Y37··· 인 연속 부 분은 U'C C A 또는 UUCAG 들과는 강하게 결 합하지 만, 코돈 UUC 와 는 약하게 결 합한 다 (Po ng s 등, 1973) . 이 결 과는 역 코돈이 코돈과 상호 작용할 때 역코돈 고리의 형태가 달라진다는 것을 암시한다. 이 문제는 뒤에서 단백질 합성의 개시 및 연장 반응들을 기술할 때 자세히 말하기 로 하겠다. 다) NMR 분광학적 분석 용액 상태 의 tR NA 분자에 있는 수소결 합들에 관여하는 수소 원자들을 알아내기 위한 탐침으로서 최근에 와서 NMR 분 광법을 사용하고 있다 (Kearns, 1976). 이것을 가능하게 한 발견은, 수 소 결합에 참 여하고 있는 고리 상의 N_H 의 수소 원자들은 물과 교환반 응을 일으킬 수 있지만, 〈나사선 수명〉이 충분히 걷기 때문에, 이 양성자 둘로부터의 공땅은 하장쪽으로 충분히 멀리 이동되어 있어서 물의 양성 자들이 나타내는 큰 봉우리로부터 분리될 수 있다는 것이었다. 염기들의 치쌓기에서 유발되는 NMR 스펙트럼의 상장쪽으로의 화학 이등은 대부분의 경우 인접한 아데노신과 구아노신들의 이른바 〈고리 전 류 효과〉로 유발된다. t RNA 에서 유도한 울리고누클레오티드들은 그 결합순서와 성질들이 이미 자세히 관찰되어 있기 때문에 NMR 분광법의 좋은 연구 모형이 된 다. E. coli tR NNM•t 의 역 코돈 팔 부분을 사용한 실험 예 를 보면, NMR 분광범아 t RNA 의 수소결합들의 위치를 분석하는 훌륭한 탐침이 될 수 있다는 것을 알 수 있다.
E. coli tR NA '~1•1 의 27 번 부터 45 번 까지 의 누클레 오티 드들을 포함하는 역코돈 팔 부분으로 행렬식을 만든 다음, 상보성을 가진 목정한 행과 열에 있는 염기들을 사선으로 표시한다. Wats o n-Cric k 염기쌍이 셋보 다 적은 줄기가 형성되는 예가 없으므로 그러한 것들은 맨 다. 마찬가지 로, 세 개보다 적은 염기들로 된 고리도 형성되지 않으므로(적어도 역 코돈 부분에서는) 이러한 것들도 맨다. 그러면, 그림 1-27 에 보인 행 렬식을 얻게 될 것이다. 이것은 5 개의 영기쌍을 가진 나사선 부분이 형 성될 가능성이 제일 크다는 것을 의미한다. 손상되지 않은 원래의 E.
 71
71
coli tR NAt M et 분자는 실제로 그림에 나타낸 바와 같은 5 개의 염기쌍을 가진 나사선을 가지고 있다. 낮은 온도에서 스펙트럼은 다섯 개의 봉우 리를 가지고 있 다. 전체 세기는 다섯 개의 영기쌍이 아니라 여섯 개의 염 기쌍에 상응한다. 12. 8 pp m 에서의 봉우리는 그밖의 봉우리들의 세기의 두 배이다. 〈 과외 〉 의 공명예 해당하는 스펙트럼이 상장에 위치하고 높 은 온도에서는 쉽게 사라지며, 다른 t RNA 에서도 관찰되는 것으로 미 루어보아서 ~11. 3p pm 에서의 〈과의〉의 공명은 보호된 U33 에 기 인되 는 것으로 생각한다. NMR 분광법은 t RNA 분자에 있는 개개의 영기쌍둘의 형태와 동적 운 동을 분석할 수 있는 근거를 제공한다. NMR 분광법으로 얻은 tR NA 의 용액에 있어서의 구조에 대한 정보는 결정체 구조와 찰 일치하고 있다. 위에서 소개한 방법들 이의에도 수용액에 있어서의 t RNA 의 삼차구 조를 분석하는 방법들이 있다. 특정한 위치의 염기를 형광 물질로 변형 하고, 형광 에너지의 전달에서 인접한 영기와의 거리를 계산할 수 있다. 단일 가닥으로 된 부분에만 작용하는 특수한 핵산 가수분해효소에 대한 민감도로부터 tR NA 의 어 느 부분이 단일 가닥을 이 루고 있는지 를 알 수 있 다 (이 문제 의 일 반적 평 론은 Rich 와 RajB handary, 1976 을 보라) . 1. 5 아미 노아실-t RNA 합성 효소-t RNA 인식 작용 특정한 t RNA 에의 아미노산의 부착은 핵산에 있는 정보가 처음으로 아미노산과 교신하는 사건이 된다• 각 아미노산에 대해서 각기 특유한 합성효소와 하나 또는 하나 이상의 t RNA 둘이 있으므로, 합성효소 -tRN A 계들은 단백질-핵산 상호작용을 연구할 수 있는 많은 국면들을 제시하였다. 단백질들과 핵산들의 종류는 광범위하기 때문에, 동족의 복합체들뿐 아니라, 비동족 합성효소-t RNA 복합체들도 조사할 수 있 다. 많은 훌륭한 방법들을 동원하여 교묘한 조사들을 하였음에도 불구하 고 아직 특정 한 합성 효소-t RNA 상호작용의 메 카니 즘을 밝힐 수 있는 결 과를 얻지 못하고 있는 형편이다• 문제의 난접은, 거의 모든 t RNA 들이
비슷한 삼차구조를 가지면서도 각기 미묘한 기능 적 차 이 판 가지고 있다 는 데서 생긴다. t RNA 둘의 구조들이 서로 비슷 하기는 하지만 동인하 지는 않다. 합성효소들은 tR NA 구조들에 있어서의 세부적인 차이점들 또는 특성들을 구별할 것이 돌림없 다. 1. 3.2 절에서 기술한 바와 같 아 몇 가지 합성효소들의 결정구조가 밝혀졌 으므로 멀지 않 아 합성효 소 tR NA 복합체의 결정구조도 밝혀질 것으로 기대된다. 먼저 물리 학적 관접 에 서 합성 효 소-t R NA 복합체 의 독성 을 알아보 고 몇 가지 간접 적 인 방법 들로 얻 은 결 과둘로부터 합성 효소 - t R :\'A 인 식 작 용의 분자적 근거 를 살펴 보자. 이 문제 에 관한 평 론 은 lg lo i 와 Cr:im er (1978) 와 Sch im mel 과 Soll (1979) 을 참 고하라. 1.5.1 합성효소-t RNA 상호작용의 물리적 국면둘 가) 평형상태에서 측정한 안정도 상수는 등족성 복합체들이 바동족동 복합체둘 보다 더 크다는것을보여 준다 합성효소-t RNA 복합체들은 니트로 셀룰 로 스 거르게에의 결합, 관 크로마토그래피, 침강, 형광 소광효과 및 평형 분배 등의 방법들로 연구되었다. 복합체 형성은 좀 낮은 p H 에 서 잘 일 어난다. M g 2+ 도 복합체의 안정도에 영향을 미치는데 최상의 안 정 도는
 표 1-6 동족 및 바동족 합성효소-t RNA 복합체들에 대한 회합 상수들 ( Lam 과
표 1-6 동족 및 바동족 합성효소-t RNA 복합체들에 대한 회합 상수들 ( Lam 과
M g 2+ 의 농도가 1 내지 5mM 일 때이다. 몇 가지 회합 상수들을 표 1-6 에 실었다. 이 실험치들은 동족성 및 동종성 복합체들이 제일 강하다는 것 을 보여 주고 있다. 예를 들면 , pH 5. 5 에 서 E. coli 의 Ile-tR NA 합성 효 소는 E. coli 의 tR N A1 1· 에 대 한 회 합 상수가 10° M-1 이 다. E. coli 의 다른 tR NA 들에 대 한 이 합성 효소 의 회합 상수는 상당히 작다 . 한편, 시험해 본 효모의 t RNA 들과의 비 동족성 회 합들은 상당히 크다. 그러 나, 결 합 목이 성 은 이 종성 (hete r o- log u s) 인 경 우 들 보다 동종성 (homolog o us) 인 계 들에 있 어 서 더 큰 것 으 로보인다. 나 ) 열역학적 변수들 . 복합체 형성은엔트로피를증가시킨다 동종성 동족 복 합체 및 이 종성 비동족 복합체 경우에 대한 회합 상수들을 온도의 함 수로서 분석한 결과들을 표 1-7 에 실었다. 이 표에 주어진 실험치들
표 효1소-7 합성효t소R N •tA R NA 복합체들의조 형건성 에 있어서|의 갭 갑열역t학 ea적 l. I변일 수읽들 l•de g• E-합t. R성cN 효oAli소 I le tER. N cAolie 520 m rMnM M Ng aC I,p, hpo Hsp h6 .a 5te 1, 7° I o. o I 34 합-E-합효tt.RR성모 성 NNc 효효oAAlPi소소 h eI l e tt효효RRNN모모 AA PVh•eI 0M532.00 mg 0 mm2M5+ MMM, M pKNKHg Ca8 7 l.i>p ,2h O,p1oS pHO s 2p h m 4 h6 a° .taM 5te,e ,1 7° I -38..50 2504 합-효tR성모N 효 AP소 he tER.cN oAliT y r 30M0. g0 mz5+MM, KpKH 훈 7. 2 s,l oO pm2 4ha°Mt e 15 75
로부터, 동종성 동족 복합체들의 형성에 있어서 엔트로피의 큰 증가가 합성효소-t RNA 복합체의 열역학적 안정도에 크게 기여한다는 것을 알 수 있다. 사실, 같은 조건에서 E. col i의 Ile-tR NA 합성효소·t RNAII• 복합체 형성에 대한 4H° 값은 영아다. 표에 주어진 두 이종성 비동족 복합체들의 엔탈피 변화들이 큰 것으로 보아서 복합체 형성이 안될 것 으로 생각되지만, 엔트로피 증가는 오히려 동종성 동족 복합체들의 경 우의 값들보다 더 크다. 이것은 복합체를 안정시키는 데에는 정전기적
상호작용들 (주로 tR NA 들의 인 산기 들과 효소의 염 기 성 아미 노산들 사 이의)이 더 중요한 역할을 한다는 것을 암시하는 것이다. 4S0 의 큰 값 둘은 복합체를 형성하면서 하전된 잔기들로부터 용매화에 관여되었던 물 분자들이 배척되는 데에 기인될 것이다. 그러므로, 하전된 자리들을 서 로 접근시킬 때 일어나는 용매화의 변화들아, 일반적으로, 단백질-핵 산 상호작용에 있어서의 열역학적 특성을 지배하는 것으로 생각할 수 있다. 다 ) 합성효소-t RNA 상호작웅의 속도. 동족 복합체 형성에 있어서의 이단계메 카니즘 효모의 Ser-tR NA 합성 효소-효모 tR NAser 및 효모의 Phe-tR NA 합성효소-효모 tR NASer 계들에 대해 복합체 형성에 관한 집중적인 연구 들로부터 복합체의 형성에는 두 이완 단계가 관여된다는 증거둘을 얻었 다. 이것을 아래와 같은 간단한 이단계 메카니즘으로 설명할 수 있다. E + tR NA ~k1 E·tR NA ~k: E'· t R NA ' k-1 k-2 f f 선별, 확인, 확인 형태의 변화 여기서 E 는 효소를 나타낸다. 식으르 · 나타낸 바와 같이, 복합 체 형성 이 일어난 다음에 일분자적 형태 변화가 뒤따라 일어나게 된다 (R ig ler 등, 1976). 표 1-8 합성 효소-t RNA 복합체 들의 형 성 의 속도 상수들 효소 l tRN A I 조건 I(MEis -I )I 검- II) I 검: 1) I 갑-i) 효합Se모성r- t효R 소N A t효R모N A 5•' O0M. .g0l 3CM l M2, K pKCH! ,.p 2h .5 o2m , spM 2h a4t° e , J 2. 7 X 10 기 2201 7201 33( P합효h성모e- 효tR 소 NA t효RN모 A Phe l0KO. C0m!3, MMp H MK7 g .p C2 h l, 2o2 ,s4p0° . ha2 t 옮 I 2x10 기 2501 4201 75( P효합h모성e- 효tR 소N A EtR, N cAoTli r r 0KlO. C0mI3, MMp HM K 7 g. pC 2h,l 2 o,2sp04 h°. t0 e 5, M | 8 x 10 기 1, 600
이분자적으로 일어나는 단계의 반응속도 상수 k12108 M-1s-1 인데, 이 값은 확산지배의 한계치에 가깝다. 해리 속도 상수 k-1 과 일분자적 형 태 변화와 관련된 속도 상수들은 102 내지 103 s-1 의 범위에 있다. 이 실험치들은, 초기의 복합체 형성은 신속하고 독이성이 무던 것에 바 해서, 형태 변화는 정 확한식별 단계를 나타내고있음을 의마하는것으로 해 석 되 고 있 다. 이 견 해 는 효모 Phe-tR NA 합성 효소 -E. coli t R NATy r 와 7같 은 이종성 비동족 쌍에서 얻은 실험치들에 의해서 뒷받침되고 있다. 이 경우, 하나의 이완 과정만이 검출 되는데 이것은 이분자적으로 일어나는 복합 체 형성에 해당한다 ( 표 1-8 을 보라). 이분자적 속도 상수 k1 은 확 산지배의 한 계치 와 가까운 값을 가지는데, 이것은 복합체 형성이 아무런 어려움 없이 일어난다는 것을 보여준다. 이 메카니즘에 있어서 두번째 단계가 없 다는것은 이것이 바로식별에 중요한단계라는것을 암시한다. 이 와 관 련 하여 , 효모의 Phe-tR NA 합성 효소는 E. coli 의 tR NATy r 에 페닐알라닌을 결합시키지 못한다는 것을 주목하여야 한다. 라 ) 최대 속도 ( Vm3X ) 가 인식작용에 있어서 주요한 역할을 한다 표 1-6 에 서와 같이, 동종성 계에 있어서는 합성효소는 그의 동족 t RNA 에 제 일 강하게 결합한다. 그러나, 약간의 경우들에 있어서, 식별작용은 결합 독이성에만 의존하는 것이 아니라 최대 속도 (Vmu) 가 더 중요한 역할을 한다는 것 이 알려졌다 (Ebel 등, 1973) . 표 l-9A 에서 볼 수 있는 바와 같이, 잘못된 아미노아실화 반응둘의 경우 Km 값들은 옳은 아미노아실 화 반응들의 것들보다 대강 102 배 정도로 크지만, 잘못된 아미노아실화 표 1-9A 울바른 아미노아실화 반응둘 및 찰못된 동종성 아미노아실화 반응에 대한 반응속도 변수들 효소 tRN A Km(µM) I( 임vm의ax의 단위) 효모 Val-tR NA 합성 효소 | 효모 tRN AV•I 0.04 1 효모 tRN APbe 14 0.0001 효모 tRN AAla 2.5 0.0002 효모 Arg- tRN A 합성 효소 효모 tRN AArg 0. 1 1 효모 tRN AASp 10 0.0004 이 실험둘은 55mM Tris- HCl(pH 7.5) 30 ° ~37•c 에서 실시한 것이다 (Ebel 등. 1973).
반응들에 대한 Vmax 값들은 103 내지 104 배나 작 다. 이러 한 결과들 로 미 루어 보아서 서로 구별되는 두 가지 인식 수준 들 이 있을 것 으로 생각힐 수 있다. 그 하나는 기 질을 결합하는 .수준에서 일어나고, 다른 하나는 촉매작용의 수준에서 일어난다. 표 1-9B 효모 Phe-tR NA 합성 효소의 옳 은 아미 노아실 화 반옹 및 윤 지 않은 이종성 아미노아실화 반웅들에 대한 반응속도 변수 들 tR NA Km (µM) (v임m의ax 의 단위) 효모 tR NAPhc 0.83 1. 0 밀 tRN APb• 0.56 1. 2 E. coli tR NAPhe 5.8 0.2 E. co[i tR NAvau 3.7 0.1 E. coli tR NAA1• 1 4.2 0.0 5 E. coli tRN ALY• 5.2 0.0 2 E. coli tR NAA1•2 3.4 0. 02 E. coli tRN Av•12A,28 1. 5 0.01 E. coli tRN A11• 1. 3 0.0 0 7 E. coli tR NAM et 1. 0 0.007 아미 노아실 화 반옹은 30° C, 50 mM Tris, 40 mM Mg C I,, pH 8. 2 에 서 실 시 한 것 임 (Ro, 등. 1973). 이러한 이단계 식별작용은 Roe 등 (1973) 이 관찰한 실험결과로도 분명 해진다. 표 1-6 의 결과들을 가지고 앞에서 논의한 바와 같이, 이종성 효 소들과 t RNA 들 사이에서의 비동족 결합은 동종성 계들에 있어서의 비 동족 tR NA 들과의 상호작용들보다 일 반적 으로 훨 씬 더 강하다• 실 제 로 효모의 Phe -tRN A 합성 효소는 E. coli 의 tR NA 들과 여 러 가지 잘못된 아미노아실화 반응을 일으킨다. 표 l-9B 에서 보는 바와 같이, 잘못된 이종성 아미노아실화 반응들에 대한 Km 값들이 동종성 동족 아미노이 실화 반응들의 값들과 거의 같다. 그러나, 이 찰못된 아미노아실화 빈 옹둘은 훨씬더 작은 최대 속도들로 일어난다. 이 실험 결과에서 우리는 실질적인 식별작용이 최대 속도의 변화와 상관성이 있다는 것을 확인힐 수 있다. 표 l-9A 및 B 들에 실린 실험치둘을 검토함으로써 이원적 식 별작용의 개념을 확립시킬 수 있다.
1.5.2 인식작옹의 분자적 근거 앞에서 본 바와 같이, 비동족 t RNA 가 효소와 결합할 수 있다는 것 은 효소와 상호작용하는 tR NA 의 독이 한 부분들을 확인하는 일 이 특히 어려울 것이라 는 것을 암시한다. 많은 방법들을 사용하여 이 문제를 연 구하였음에도 불구하고 인식작용의 본질을 해결할 만큼의 만족한 답을 얻지 못하고 있다. 그렇지만, 오늘날까지 얻은 결과들로부터 문제의 주 요한 특징들을 개관할 수 있다 (Sch i mmel, 1979; Sch i mmel 과 Soll, 1979 ; Ig lo i 와 Cramer, 1978 등의 평 론서 뭍 참고하라) .
 HO
HO
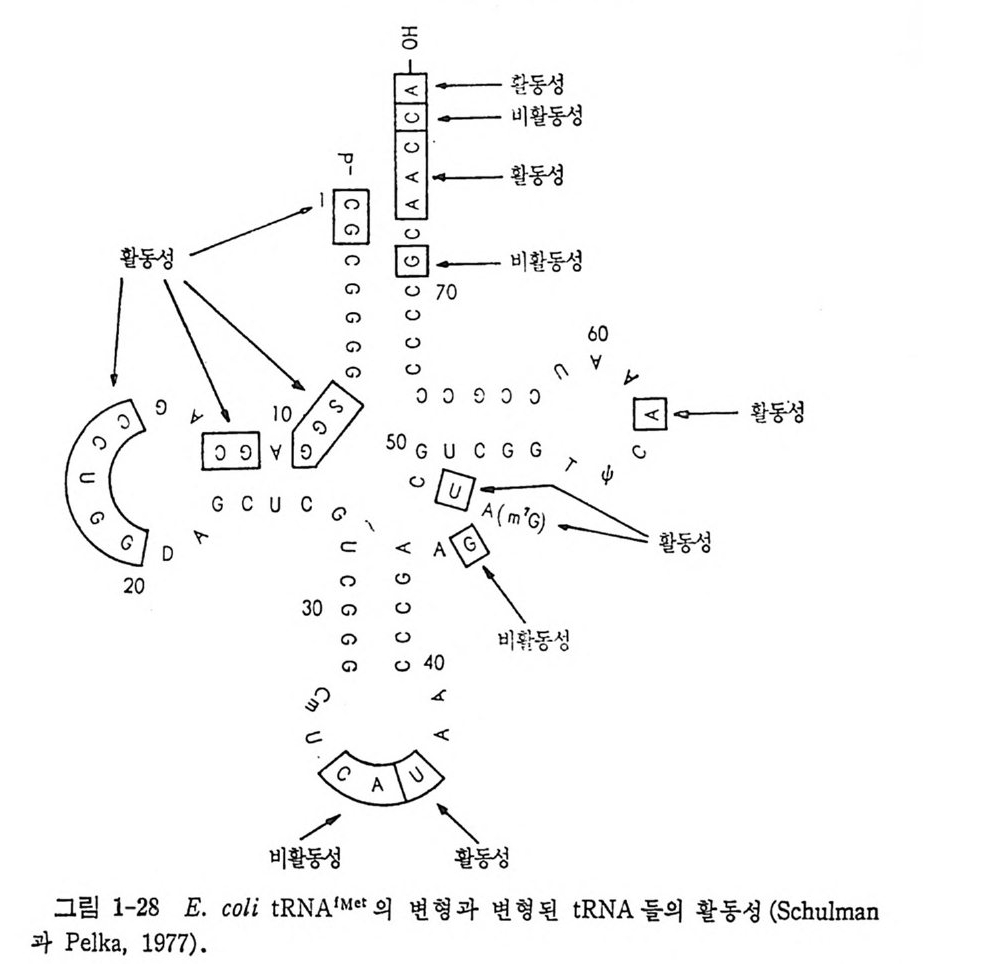
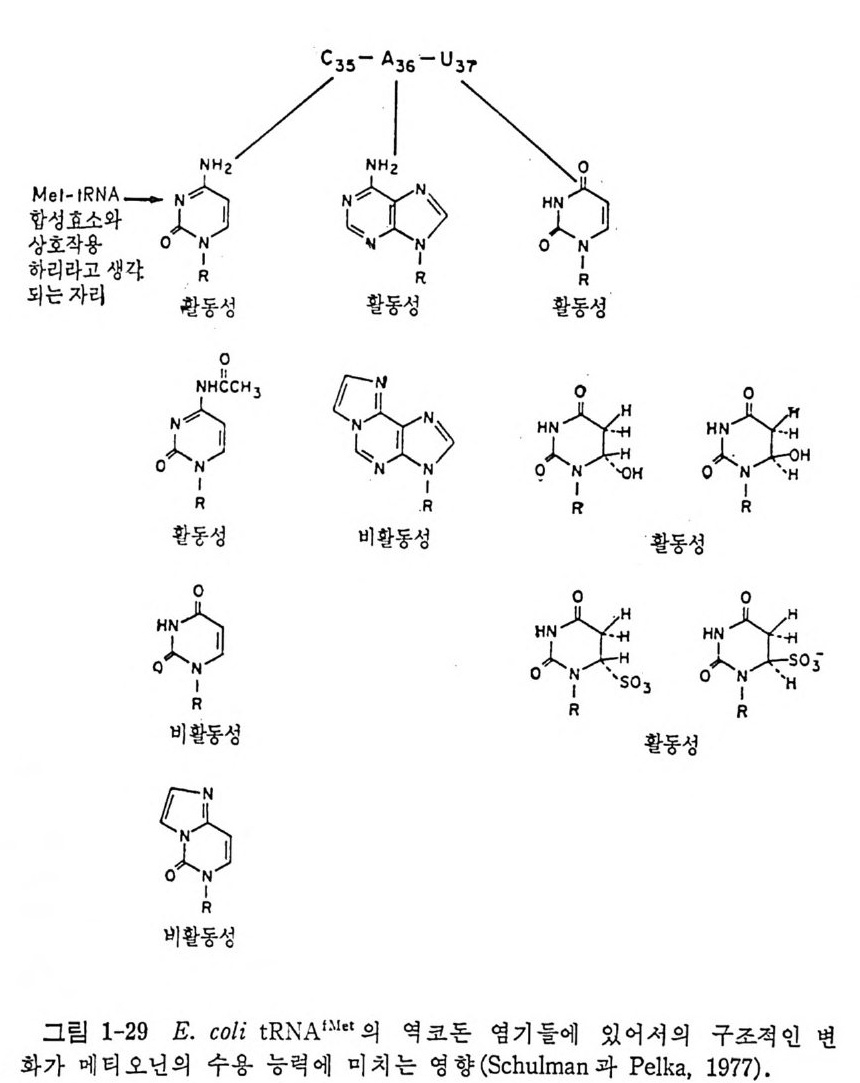
가) t RNA 들의 화학적 변형 많은 화학적 변형법들이 t RNA 에 적용되 었다. 아황산수소 (HSO 더에 의한 시터던의 우리던으로의 전환, 시아노 에 틸화, 커口루살화, 클로로아세 트알데 히 드 처 리 , N- 산화, 염 료 또는 스 핀 표지물들울 특이한 위치에 결합시키는 방법, 및 광산화 등이 많이 이 용되고 있다. 화학 변형법으로 가장 많이 연구된 것은 E. col i의 tR NAf M ct 이다 (Schulman 과 Petk a , 1977) . 많은 자리 들이 변 형 되 었 으며 , 변 형 된 tR NA 들을 Met- tRN A 합성효소와의 상호작용을 시험해 보았다. 얻은 결과들 을 그립 1-28 로 나타내었다. 이 그림에 나타낸 결과에서, 합성효소 -tRN A 상호작용에 중요한 자리 들은 tR NA 구조의 역 코돈 고리 , 아미 노산 수용 줄기, 및 가변성인 과의의 고리들에 위치하고 있다는 것을 알 수 있댜 예를 들면, 역코돈 또는 3' 끝에서의 변형은 비 활 동성인 tR NA 를 만들 수 있다. tR NA 의 삼차원 구조에 서 이 두 부분들은 약 80A 떨어져 있다. 이 사실은 합성효소가 tR NA 구조의 대부분을 음미 할 수 있으며, 여러 부분들에 광범위하게 분리되어 있는 결정적 잔기들 을 선택적으로 인식할 수 있음을 암시한다. 역코돈 부분의 변형에서 얻 은 Schulman 과 Pelka (1977) 의 결 과로 C35 가 메 티 오닐 -tRN A 합성 효소 의 중요한 리간드라는 것을 알 수 있다. 화학 변형이 아미노산 수용 능 력에 미치는영향을그림 1-29 에 나타내었다• C35 의 N3 위치와 A36 의 Nl 위치들이 합성효소와 결합하는 가능한 자리들일 것이다. 나) 돌연변이적으로 변형된 tR NA 둘을 이응한 연구 인식 작용의 문 제 해 결 의 또하나의 훌륭한점근법은 유전적인 수단으로단하나의 염기 의 변 화 를 가진 돌연변이 t RNA 를 얻어서 이용하는 것이다 (Sch i mmel, 1979; Schim mel 과 Soll, 1979) . 이 러 한 tR NA 들은 자연 그대 로의 tR N A 종 들이므로, t RNA 의 화학적 변형시에 생길 것으로 우려되는 대폭적인 형 태의 변화는 없을 것이다. 야생형과 비교하여 합성효소 인식작용이 서로 다른 여러 돌연변이 tR NA 들이 E. coli 에 서 분리 되 었 다 (표 1-9) . E. coli 의 암버 억 압 (su+ l) t RNA Tyr을 유전학적으로 조작하여 많은 돌연변이 t RNA 들을 얻었다. 이 tR NA 들의 누클레 오터 드 결합순서 를 분석 하여 이 t RNAT y『 종들은 모두 아미노산 수용줄기의 끝부분에서 단 · 하나의 영기가서로 다르다는 것을 알았으며, 생체 내 및 시험관 내에서 글루탐산으로 아미노아실화될 수
 霜臼想leM :隔 표핫AN 와생 간-O白 RNO1~RI 占 。 c/`/ >田〔〉二 IRRI QHi °1활 >NRI /
霜臼想leM :隔 표핫AN 와생 간-O白 RNO1~RI 占 。 c/`/ >田〔〉二 IRRI QHi °1활 >NRI /
있 음이 밝혀 졌다. 그뿐 아니 라, 이 tR NA 들은 Ty r- tR NA 합성 효소에 의해서 여전히 인식되었으며 시험관 내에서 티로신으로 아미노아실화될 수 있었다. 비슷한 유전학적인 방법으로 암버 억압 (su +2) t RNAG i n 에서 출발하여, 돌연변이 t RNA 둘을 분리하였는데, 여기서는 역코돈 부분의 단일 염기둘의 변화가 있었고 아직 알려지지 않은 아미노산으로 아미노 아실화되었다 • 이러한 유전학적안 연구들이 인식작용의 분자적 근거를 확정하지는
표 1-10 합성효소 상호작용에 영향을 미치는 E. coli t RNA 들의 돌연변 이 둔 (SchtRim N mAe l 과 Sol돌l, 연19변7이9) . | 갑입어\ 1 있어서 1 돌연변이에 대한 효과 Glyl | 역코돈 I Gly- tRN A 합성 효소에 의 한 아 마 노아실화의 속도가 크게 감소됨 Gly2 I C36 ➔ U36 I 역 코돈의 천 번 Gly -tR NA 합성 효 소에 의 한 아디 째 염기 노아실화의 속도가 크게 감소됨 Gly3 I C35 ➔ U35 | 역 코든의 두번 Gly -tRN A 합성효소에 의한 아디 째 염기 노아실화의 속도가 크게 감 소됨 SIt+ 3Ty r I A82 ➔ G82 1 수용 줄기 글루타만으로 잘못 아미 노 아실화 됨 s11+3Ty r I C81 ➔ A81 \ 수용 즐기 1 글루타민으로 잘못 아마노아실화 됨 SIt+ 3Ty r I G2 ➔ A2 I 수용 즐기 1 글루타민으로 찰못 아미노아실화 됨 S1t + 3TyT I Gl ➔ Al I 수용 즐기 | 글루타민으로 잘못 아미 노아실화 됨 su+1Trp I C35 ➔ U35 I 역 코든의 두번 글루타민으로 찰못 아미노아 실 화 째 염기 됨 s11+2Gln2 I 1fr3 7-A37 j 역 코돈 고리 미지의 아미노산으로 아마노아실 화됨 su+2Gln2 | ,r 37 ➔ C37 I 역 코돈 고리 |미지의 아미노산으로 아미노어실 화됨 s11+2Gln2 I 1Jr3 8-C38 | 역 코돈 고리 | 미지의 아미노산으로 아마노아실 화됨 s11+2Gln2 I y37 -A37/I l 트됨립토판으로 찰못 아미노하실화 G29 ➔ A29 못하였지 만, 적 어 도 합성 효소-t RNA 의 인식 작용이 극히 정 확하며 단하 나의 염기의 변화에 의해서 영향을 받을 수 있다는 것을 밝혀 주었다. 다) 합성 효소-t RNA 복합체들의 광화학적 교차결합법에 의한 연구 t RNA 와 단백질 어느 쪽에도 중대한 구조적 교란을 일으킴 없이 위상기하학적 득칭들과 점촉점들을 밝힐 수 있는 약간의 연구 점근법들이 있다. 효 소와 t RNA 와의 교차결합과 t RNA 의 동위원소 표지는 이러한 목적에
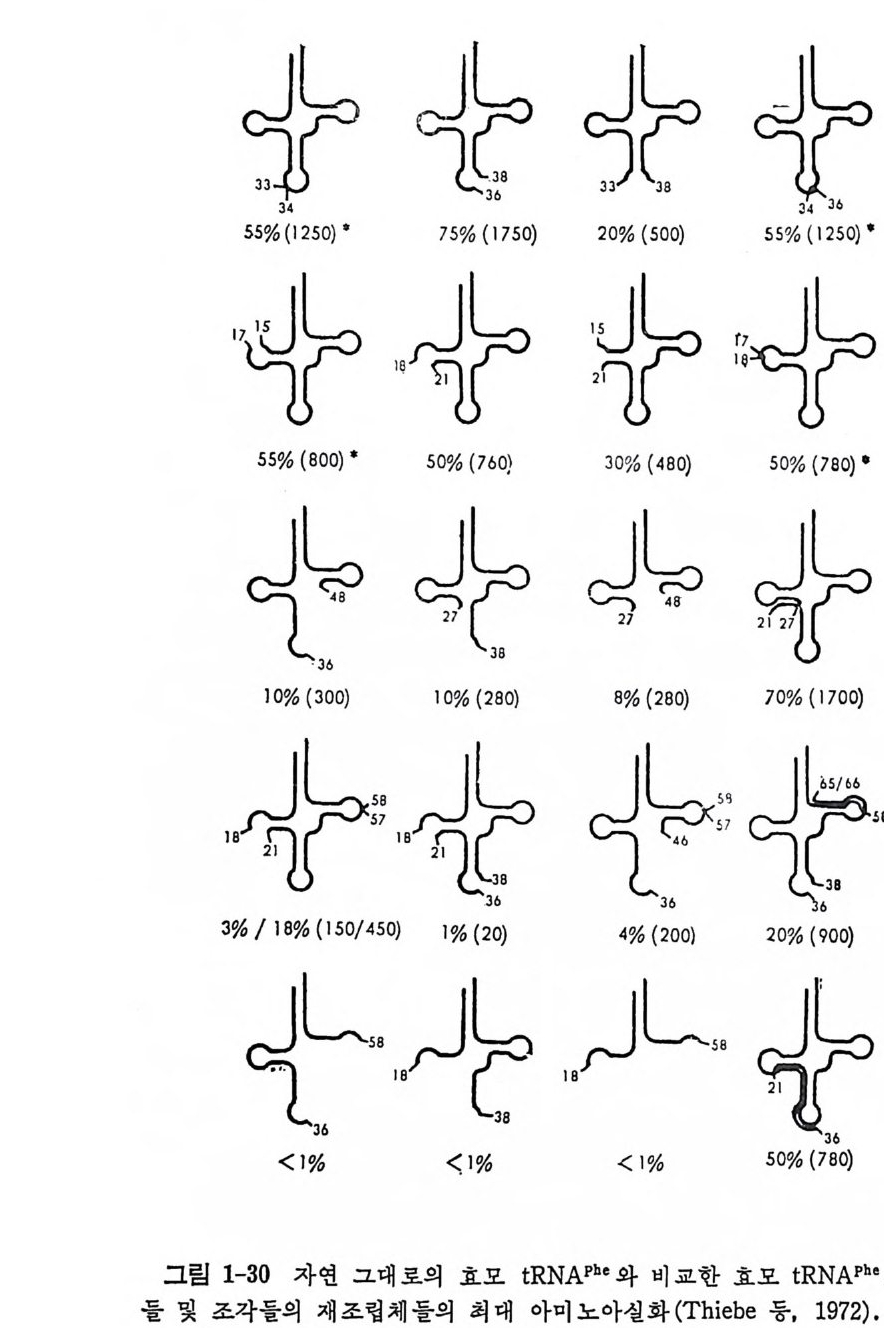
유용하다. 254nm 에서의 직접 조사로 광화학적 교차결합을 형성시킬 수 있다. 자의선의 조사로 여러 가지 누클레오시드들과 아미노산 결사순 둘이 공유결합으로 연결될 수 있으므로 자외선은 교차결 합을 도입 하 는 이상 적인 수단이다. 여 섯 가지의 합성효소-t RNA 복합체들에 있어서의 tR NA 분자들 상에서 교차결합에 관여된 부분들을 분석하여 얻은 결과 들에 의 하면 , 합성 효소-t RNA 복합체 들의 구조적 조직 에 는 및 가지 공 통접둘이 있 다는 것을 알 수 있다. 즉, 합성효소와 t RNA 가 접촉하는 곳은 tR NA 분자 상의 D 줄기 의 5' 쪽, tR NA 의 3' 말단 부분, 그리 고 역코돈 부분들이다. 이 결 과를 그림 1-31 에 나타낸 결과와 비교하라. 라 ) 〈 절개 〉 접근법 이 방법 은 tR NA 구조에 서 합성 효소-t RNA 인식 작 용에 필요치 않은 부분을 제거하 고 필수적 인 부분들을 남겨 두고, 이 나머 지 부분 분자가 합성효소와 어느 정도로 인식하는지를 조사하는 것이다. 합성효소와의 인식 작용은 절개된 tR NA 조각들, 또는 이 조각들을 그림 1-30 에 나타낸 바와 같은 구조들로 재조립하여 그들의 아미노아실화의 청도를 측 정 하여 분석한다. 이러한 방법으로 여러 가지 종류의 t RNA 둘 의 합성효소들과의 인식작용을 분석하였다 (Chambers, 1971; Thie b e 등 1972). 그림 1-30 에 효모의 t RNA p he 에 대한 철저한 연구 결과를 소개 하였다. 손상되지 않은 t RNAPhe 의 페닐알라닌 수용도와 바교한 절개된 부분 분자들의 수용도와 부분 분자들의 합성효소에 대한 결합도(회합상 수 )를 표시하였다. 이 결과에서, 역코돈 고리와 D 고리들의 큰 연속 부분이 제거되 어도 아미노산의 수용 능력을 손상시키지 않음을 알수 있 다. 이 것 은 앞에 서 말한 E. coli 의 tR NA(\!ct 에 대 한 화학 변 형 들에 서 얻 은 결과와 여러가지 t RNA 들에 대한 유전학적 조작들에서 얻은 결과와 상반되는 결과일뿐 아니라 전개 분자 접근법으로 효모의 t RNAV•l 에 대 한 연구에서 얻는결과와도모순되는결과이다. 이러한 상반되는 결과는 조각들로부터 그림 1-30 에 나타낸 바와 같은 부분 분자의 재조립이 제 대로 일어나지 않은데에 기인되거나, 약간의 효소들은 합성효소-t RNA 인식작용에 있어서 역코돈 고리와 D 고리들을 필요로 하지만 그밖의 효소들에는 이 고리들이 필요치 않기 때문이라고 생각할 수 있다. 마) 자유 tR NA 및 합성효소-t RNA 복합체 내의 tR NA 에 대한 핵산 가수분해 효소에 의한 가수분해 접근법 코브라 (Na j a ox i ana) 의 독액에서 추출한
 55%43 二了《(<800) • 50|%2 7 宁二寬( 760|) 3 38|석0% 了《亨(48|0 R) 48 50% 二〉 {<宁47 80) •
55%43 二了《(<800) • 50|%2 7 宁二寬( 760|) 3 38|석0% 了《亨(48|0 R) 48 50% 二〉 {<宁47 80) •
RNase(RNase Vl) 는 염기에 관계 없이 이중나사선을 이룬 부분들을 가 수분해 하는 효소이 다 (Favorova 등, 1981 ; Lockard 와 Kumar, 1981) . 아미 노아실-t RNA 합성 효소와 복합체 를 형 성 함으로써 보호된 tR NA 분 자 상에 서 의 가수분해 자리 를 조사함으로써 tR NA 가 합성 효소와 복합 체 물 형성할 때의 접촉 부분들을 알 수 있다. Ebel 과 그의 공동연구자 들 (19 79) 은 이 방법 을 사용하여 효모의 tR NAV•I 와 효모의 tRN APbe 들 에 대해서 조사하였다 . 그들의 연구 결과를 그림 1-31 로 나타내었다. 이 그립에서 볼 수 있는 바와 같이, 상호작용을 하는 부분들은 발린과 페닐알라닌 두 계들에서 모두 t RNA 의 L 자형을 이루는 두 팔의 안쪽 으로 있다. R i ch 와 Sch i mmel(1979) 도 이것과 거의 비슷한 모형을 제 안한 바 있다.
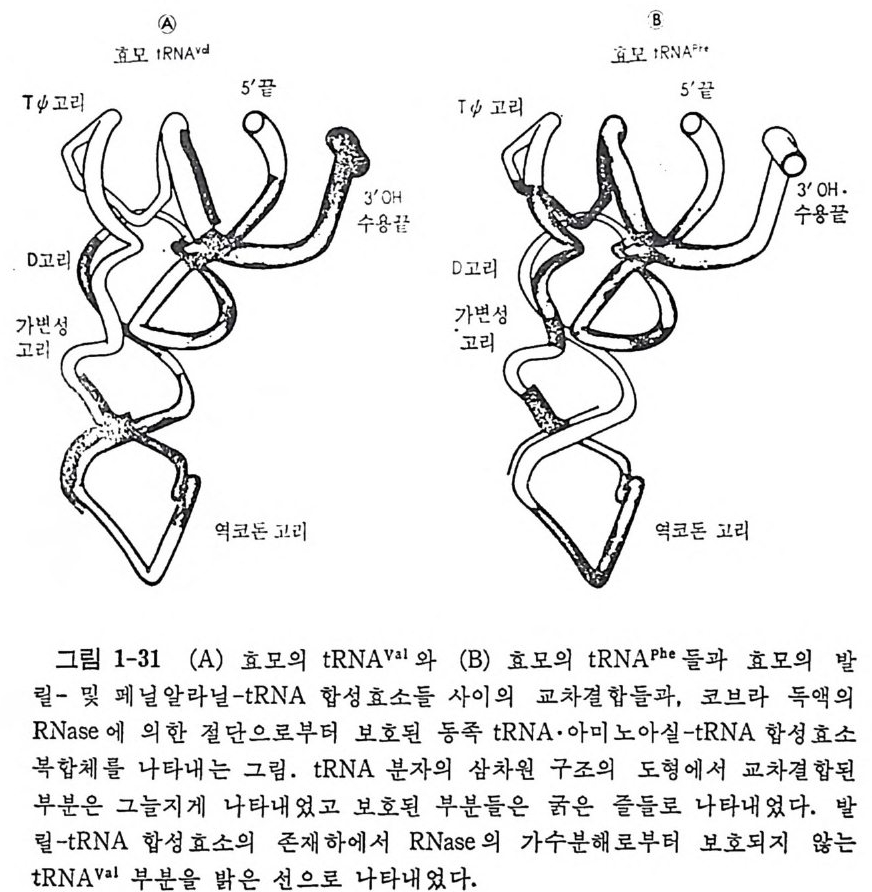 ® ®
® ®
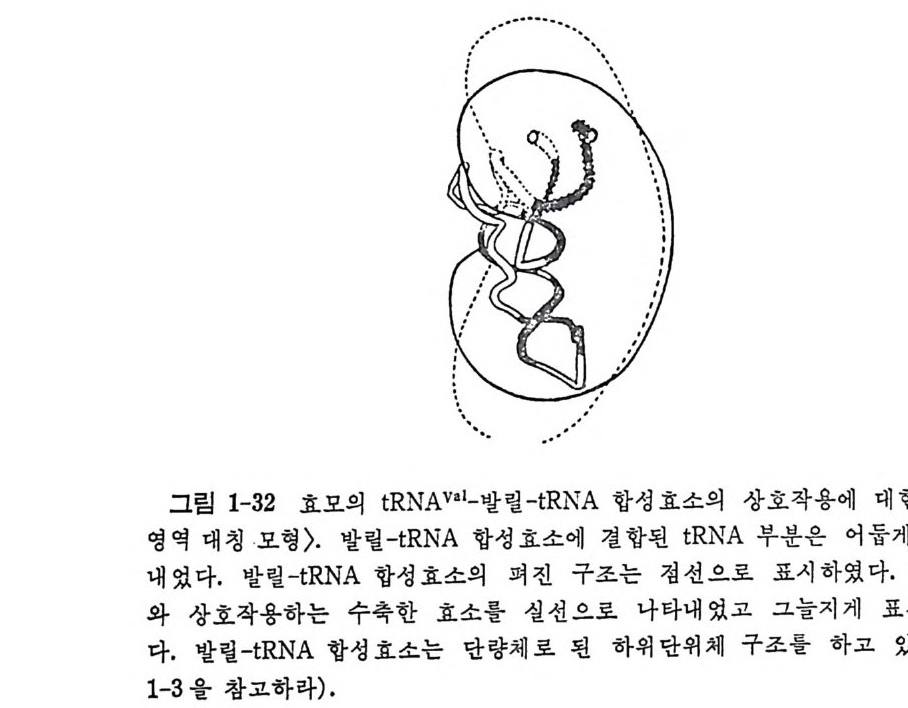
뭉리학적 방법들르 분석한 결과들이 합성효소와 tR NA 사이의 접촉접 들에 대한 부분적안 정보를 제공하였다. Ebel 의 연구진은 발릴-t RNA 합성효소가 t RNA 들(동족성인 것들과 비동족성인 것들)과 복합체를 형 성할 때의 형태 변화를 중성자 산란법으로 연구하였다 (Zacca 등, 1979) 이 연구에서 그들은 t RNA\'al 아 복합체의 중심 부근에 결합하며, 합성 효소의 구조를 수축시키는 것을 관찰하였다. 이러한 형 태의 변화는 이 은의 세기에 따라서 달라지며, 효소의 수축은 t RNA 가 강하게 겅합된 때, 죽 동족 t RNA 가 결합할 때만 일어나는 것을 알았다. t RNA p he 의 구조가 사이비 이중 대칭성을 가지 는 사신과 가상적 합성 효소가 짝수 개의 〈단위 영역〉들로 구성되며 이 등은 서로 사이비 아중 대칭성을 가진다는 가정에서 제안한 K i m(l976 ) 의 가성과, 발릴 -t RNA 합성효소의 일차구조에서 반복되는 연속 부분이 대칭 적 으로 존재한다는 발견 (Bruto n , 1975) 과 발릴 tR NA 합성 효소가 수축성 을 가진 다는 사실 들에 기 초하여 Ebel 등 (1979) 은 발릴 _tR NA 합성 효소 • tR NA'1 복합체 형성에 있어서의 인식작용에 대해서 그림 1-32 로 나타낸 〈 이영역 대칭 모형 〉을 제안하였다. 이 모형에 따르면, t RNA V•I 은 아마노아 설 tR :\'A
 ;' ...• • • ••• ---•• •. `. \
;' ...• • • ••• ---•• •. `. \
합성효소의 두 영역들 사이에 결합하여 이 두 영역들을 더 가깝게 접근 시킬 것이다. t RNAV>l 와 합성효소들은 그 분자량들아 상당히 차이가 있음에도 불구하고, 그들의 상대적 크기가 비숫한 것으로 보아서 tR NA 는 아미 노아실-t RNA 합성 효소의 광범 위 한 부분과 상호작용할 것으로 생각된다. 안 말단의 A 는 밭릴-t RNA 합성효소의 한 영역에 위치한 촉 매 자리와 상호 작 용 할 것이며, 이 영역과 대칭적인 둘째 영역에 위치한 또 다론 자리에서 역코돈 부분이 상호작용할 것이다. 지금까지 위에서 기술한 관 찰 들에 기초하여 t RNA 와 아미노아실 -tRi \ A 합성효소와의 인식작용의 특징들을 다음과 같이 요약할 수 있다. (1) t R~A 와 아미노아실 합성효소 사이의 상호작용에 관련되는 에너 지의 대부분은 정전기적 힘들에 키인한다. 그러나 이온성 자리들(예; 인 산 기들 ) 의 수는 한 정 되어 있다. (2) tR NA 에 있는 대 부분의 변형 된 누클레 오티 드들은 tR NA 를 아미 노아실화시키는 작용 에 직접 관여하지 않는다. (3) L 자형 tR NA 분자의 두 팔들의 안쪽에 위치하고 있는 광범위한 부분이 아미노아실-t RNA 합성효소에 밀접하게 근접되어 있다. (4) 효모의 t RNA” 은 단량체형 (a 형)인 발릴-t RNA 합성효소의 중 심에 대칭적으로 자리잡고 있으며, 효소는 형태 변화를 받는다. 효모의 t RNNh’ 는 사합체형 (a2 f3 2 형) 페닐알라닐-t RNA 합성효소의 8 하위단 위체들에 자리잡고 있다. 이 경우의 상호작용도 역시 형태 변화를 유발 할 것이며, 이 변화는 3' 말단의 A 잔기에 의해서 유발될 것이다. (5) t RNA 들은 아미노아실-t RNA 합성효소와 작용할 수 있는 몇 개 의 독립적인 영역들을 가지고 있을 것이다. 삼차원 구조가 하는 역할은 이 영역들의 입체구조를 일정하게 유지시킴으로써 3' 말단의 A 잔기가 가장 효과적인 자리를 참도록 하여 결국은 아미노아실화 반응이 제일 찰 일어날 수 있게 하는 데 있다. 그러나 t RNA 의 조각들도 아미노아실화 될 수 있기 때문에, 아미노아실화가 일어나기 위해서 이 영역들이 모 두 다 필요한 것으로 생각할 수 있다. 여기서 우리는 왜 t RNA 와 합성 효소와의 상호작용의 세기가 아미노아실화의 활동성과 관계가 없는지의 이유를 알수 있다. 또한, 이것은 아미노아실화의 특이성이 결합의 세기 보다는 오히려 최대속도에 따라서 달라지는 일반성을 이해할 수 있다 (1. 5.1 철의 표 1-2B 를 참고하라). 합성 효소가 tR NA 의 L 자형 구조의 안쪽 부분의 자리 들과 인식 작용
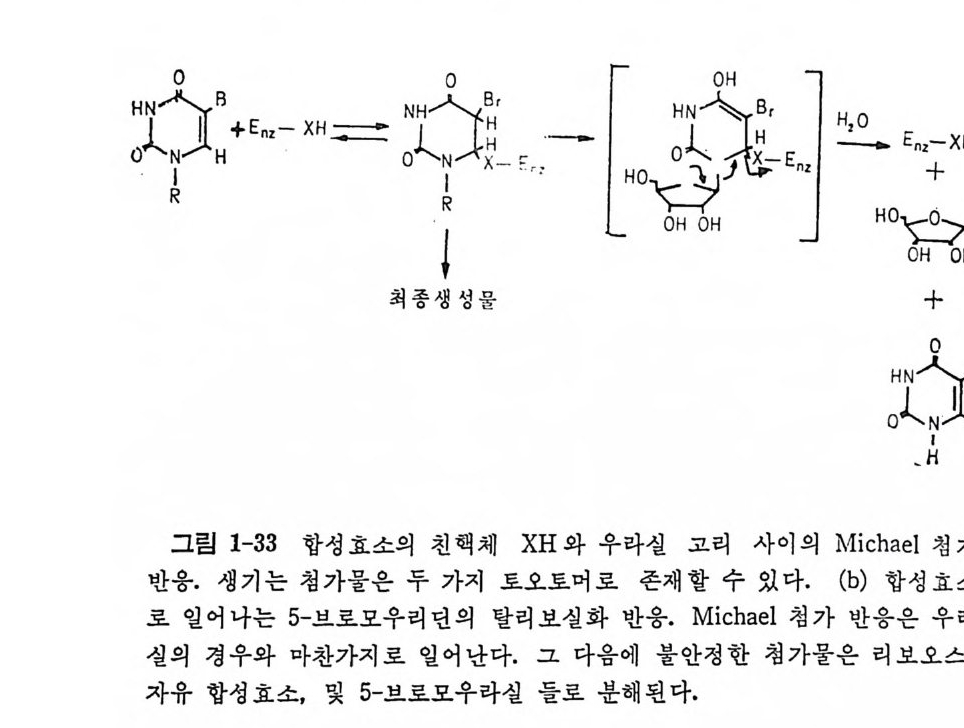
을 할 것이라는 최 근에 밝혀진 증 거를 보도록 하자. 1.4 .5 절 에서 기술 한 바와 같이, t RNA 둘의 8 번 위치에는 언제나 우리딘이 있다. 이 우리 딘 찬기는 tR NA 구조의 L 자의 두 팔이 만나는 부분의 안 쪽 으로 위치 하고 있 다. 최 근에 Koontz 와 Schim mel (1979) 은 이 우리 단 이 Ala-tR NA 합성효소와 목이하게 상호작용하는 자리 라는 것을 밝 혔 다. 그 들 은 이 문 제를 더 연구하여 t RNAAI • 의 U8 의 피리미딘 고리의 5 번 위 치 의 H 가 합성효소로 촉매되는 물과의 교환 반응을 받게 되며, 이 결과로 U 의 C-6 위치가 천핵성 공격을 받기 쉽게 되어서 C_6 과 합성 효 소 사이에 공유결합이 형성된다는 것을 증명하였다 (S t arz y k 둥, 1982) (그립 1-33).
 HN_°R4< B_+>HE n z xH ―一 NH04ZH BXrHL Fr ·` L -IRLl 。_ HH N\'~O|OHH l E: 伊5-H || ~>O H +g
HN_°R4< B_+>HE n z xH ―一 NH04ZH BXrHL Fr ·` L -IRLl 。_ HH N\'~O|OHH l E: 伊5-H || ~>O H +g
만일 합성효소가 그의 우리던 인식 자리에서 우리던 또는 할로우리던과 안정한 공유결합성 첨가물을 어떻게 해서든 만들면 이 효소는 t RNA 를 아미노아실화시키지 못할 것이다. 다시 말하면 t RNA 의 U8 과 합성효 소와의 공유결합성 상호작용은 합성효소의 기능에 꼭 필요하다. 우리던 인식 자리의 역할어 무엇인지는 아칙 모르고 있다. 그러나 U8 과의 공유결합성 상호작용은 tR NA 의 3' 끝과 효소에 결 합한 아미 노이
싣-아데닐산과의 반응이 쉽게 일어날 수 있게 하는 역할을 가지고 있을 것으로 생각한다. 이 문 제 와 관련하여 Schim mel 과 그의 공동연구자들은 Ala-tR NA 합 성효소는 기능이 각각 다른 두 영역들로 이루어져 있다는 것을 밝혔다 (Putn e y 등, 1981) . Ala-tR NA 합성 효소 를 단백 질 가수분해 효소로 가볍 게 치리하면 분자의 중앙 부분에서 철단되어서 440 개의 아미노산 잔기 둘 을 가진 N- 말단의 조각과 아미 노산 잔기 가 435 개 로 된 C_ 말단의 조 각 들 이 언어진다. N_ 말단의 조각은 아미노아실-아데닐산울 형성시키 는 기 능을 가지는 영역이고, C- 말단의 조각은 t RNA- 의존성 단계를 위 한 영 역 이다. U8 과의 상호작용은 이 C- 말단의 조각에서 일어난다. 그 러므로, 합성효소 분자 상에서 아미노아실_아데닐산 형성이 일어나는 영 역과 t RNA 와 결합하는 두 부분 사이에 일종의 조정이 일어남으로써 t RNA 의 아미노아실화가 일어나게 될 것이 룰림없다. 합성효소와 U8 사이의 결합이 이러한 조정을 유발할 것으로 생각된다. 최근에 Ebel 과 그의 공동연구자들은 Phe-tR NA 합성효소는 3' 끝의 A% 제 거 한 불완전 한 tR NAPh• 가 Phe-tR NA 합성 효소와 결 합하면 아데 노신 모노누클레오시드 를 아미노아실화시킬 수 있다는 것을 관찰하였다. 이 연 구결 과는 합성 효소와 불완전한 tR NNh• 의 U8 사이 의 상호작용만 제 대 로 일 어 나면 이 t RNA- 합성 효소 복합체 가 아데 노신 모노누클레 오시 드를 아미노아실화시킬 수 있는 형태를 취할 수 있다는 것을 알려 주는 것으로 생각한다. t RNA 에는 U8 이외에도 t RNA 의 인식을 결정하는 그밖의 누클레오 티드 연속 부분들이 있을 것이다. 이 연속 부분들은 합성효소가 각각 동 족성 또는 바 동족성 tR NA 와 접 촉하는가에 따라서 효소가 U8 찬기 에 접근할 수 있게 하든가 또는 접근하지 못하게 할 것으로 생각된다. 비 동족 t RNA 가 합성효소와 결합하더라도 아미노아실화되지 않는 이유는 U8 과의 공유결합성 첨가 반응이 일어나지 않기 때문이다. 비동족성 합 성효소-t RNA 혼합물에서 H-5 의 교환 반응이 일어나지 않는다는 사실 은 이러한 견해와 찰 일치한다.
 포르밍 메티오닌 E1로AAJ 1 GAGcCAAGUGCcGuVcuUcAAAAUGu
포르밍 메티오닌 E1로AAJ 1 GAGcCAAGUGCcGuVcuUcAAAAUGu
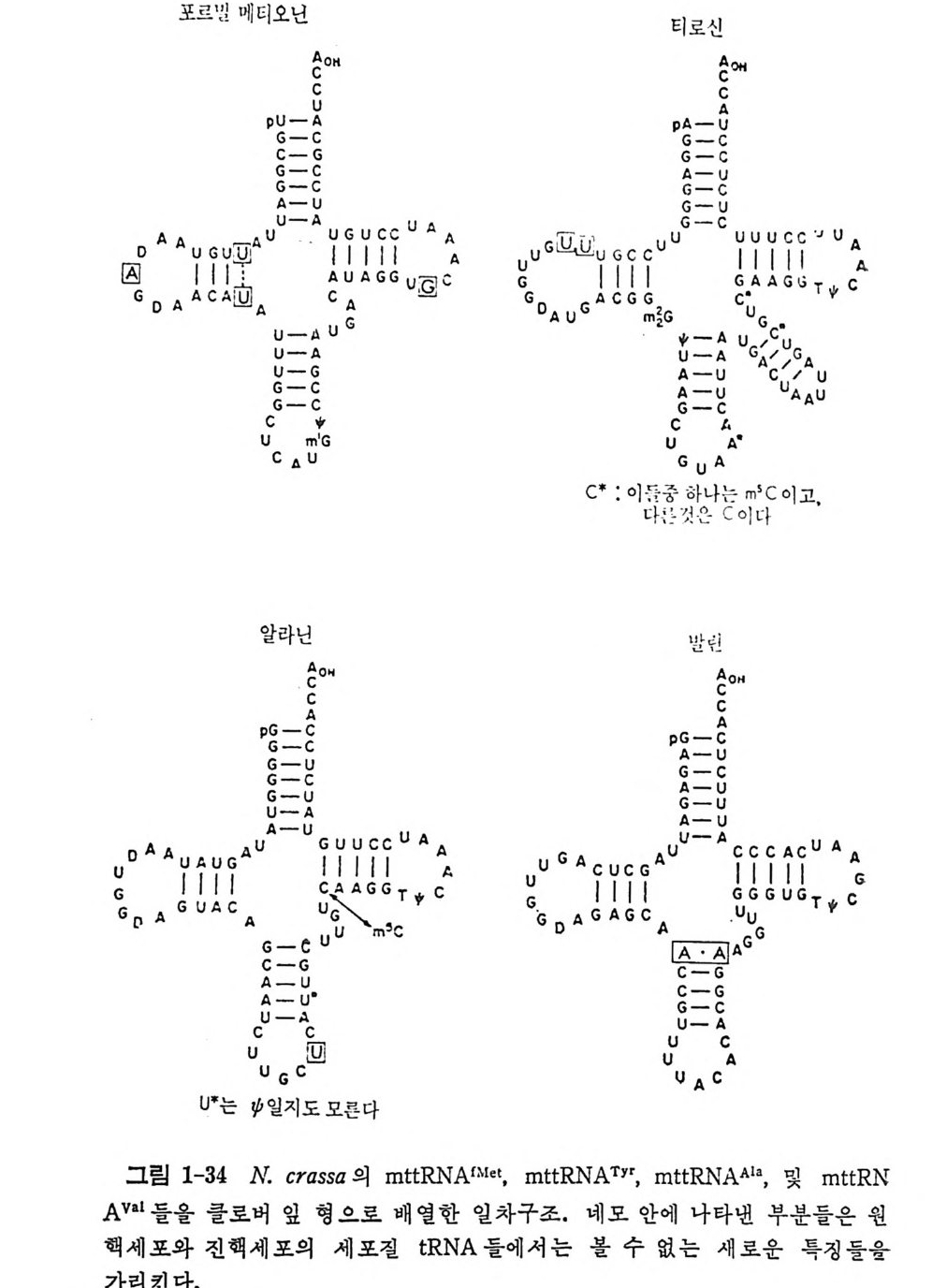
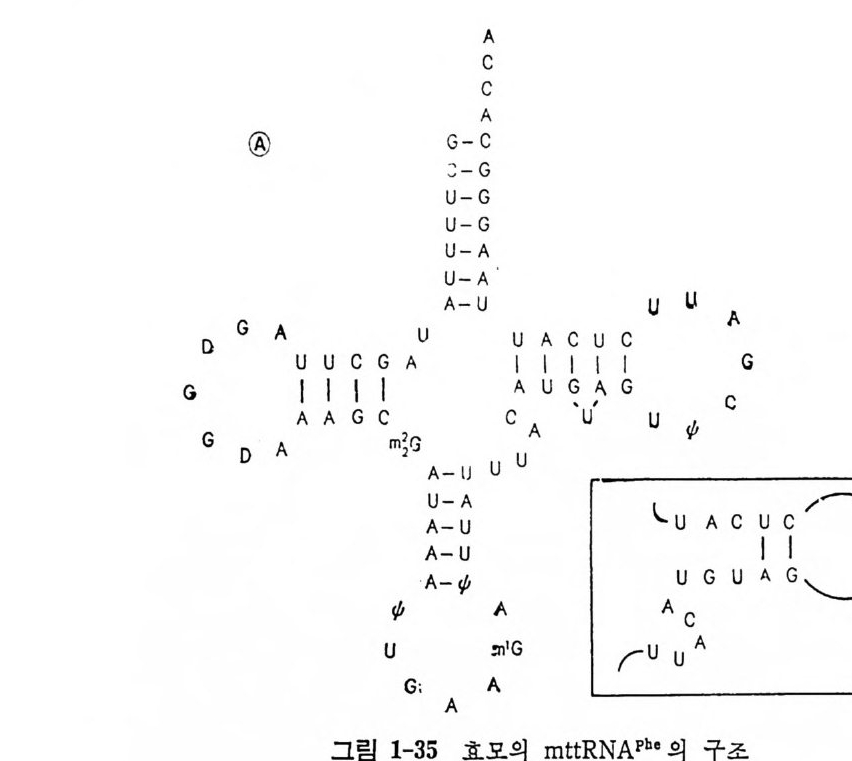
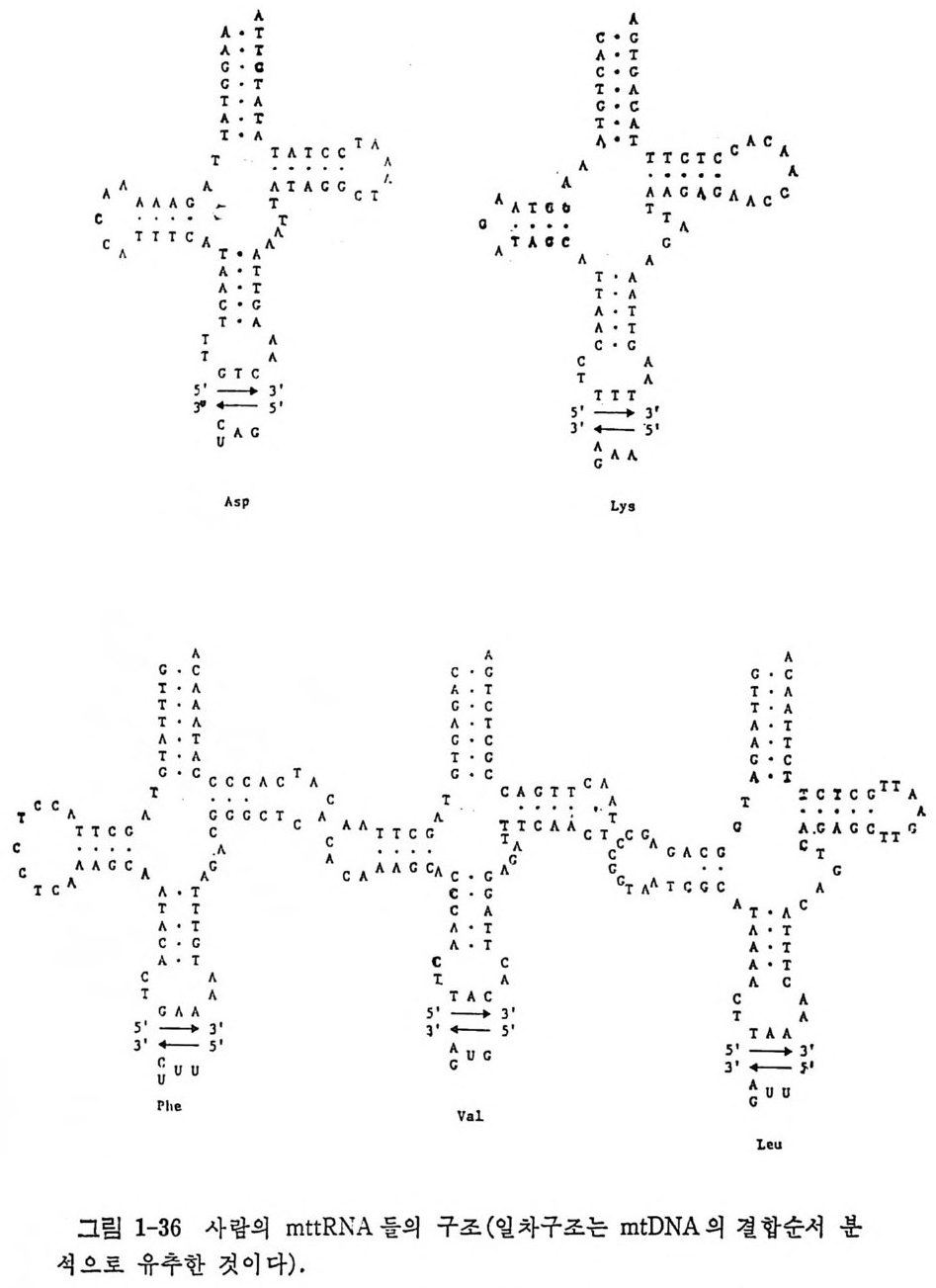
1.6 미토콘드리아에서의 암호 해독 1. 6. 1 미토콘드리아의 tR NA 둘 일반적으로 미트콘드리아의 t RNA(m tt RNA) 는 그 일차구조가 짧으며, 세포질의 t RNA 둘의 일반화된 구조와 비교하면 다른 점들이 많이 있다 (그립 1-10 과 비교하라). 22 가지의 미토콘드리아의 t RNA 들의 일차구 조가 결정되어 있다 (Barrel 등, 1980) . m tt RNA 들에는 여러 가지 변형된 염기들이 있다. 그들 중에는 ,Jr, m5C, m1G, m2G, m1A, 및 t6A 등이 있 다(더 자세한 것에 관해서는 1. 4.5 질의 그림 1-12 를 참조하라). 몇 가지 생물종들의 m tt RNA 의 구조적인 독칭을 실례를 들어서 알아 보자. 먼저 Neurosp or a crassa 의 mt tRN A 들을 클로버 잎 모양으로 배 열 한 것 을 그 림 1-34 에 나타내 었 다. N. crassa 의 mt tRN Ar. .le t 는 몇 가 지 홍미있는 특징을 가지고 있다. D 즐기의 첫 염기쌍은 U·U 이다. 그뿐 아니라, D 고리와 T,J rC 고리에는 모든 t RNA 들에서 볼 수 있는 연속 부분 GG 와 ,JrC 또는 UC 가 존재하지 않는다. 그 대신에, D 고리에는 연속부분 AG 가 있고 T,J rC 고리에는 연속부분 GC 가 있다. 효모의 tR NNb• 에 서 는 D 고리 의 GG 와 T,J rC 고리 의 ,JrC 가 삼차적 상호작용 울 하고 있다는 것울 상기하자(1. 4.8 절의 그림 1-19 를 참조하라). mt t RNAA1a 에 있어서는 역코돈 바로 옆으로 (3' 쪽으로) 피리미단 염기를 가 지고 있다. 세포질의 t RNA 들은 이 위치에 푸린 염기 (보통은 과변형된 푸린 염기)를 가지고 있다. 효모의 m tt RNNh• 의 구조(그림 1-35) 도 특이하다. 먼저 G+C 함량 은 75 개의 누클레오티드 중 25 개로 매우 적다(효모의 세포질 tR NAp he 의 경우에는 76 개 중 40 개이다. 그림 1-22 를 참고하라). 그리고 역코 돈 줄기는 A·U( 또는 A 사) 염기쌍들만으로 이루어진다. ,JrC 줄기를 연 역해내기가 어려웠다. 왜냐하면, 관례적 방법으로 배열하면 그림 1-35 의 (b) 와 같은 이차구조를 가지게 되기 때문이다. 사람의 m tt RNA 들(그립 1-36) 도 특이한 구조를 가지고 있다. 세포질 의 t RNA 들에 적용되는 원칙들이 m tt RNA 둘의 줄기 (또는 팔) a 과 e 들에서는 적용되지 않는다. 줄기 b 는 2 개의 염기쌍을 가지는 매우 짧
 A
A
은 것이 있다(예, mt tRN AL”). 고리 I 은 3 개의 찬기 를 가지는 것도 있 다 (예 ; mt tRN N11) . 어 느 tR NA 에 나 존재 하는 G18Gl9 쌍이 mt tR N A L•11 몰 제외하고는 존재하지 않는다• 줄기 e 는 작은 것은 3 개의 염기 쌍 , 큰 것은 6 개의 영기서J-울가지고있다(보통은 5 개, 그림 1-10 과비교하라) . 가장 중요한 것은 고리 N 에 공통적으로 존재하는 연속부분 GTTCA 또 는 GTTCG 가 mt tRN AL” 를 제 외 하고는 존재하지 않는다 . 제일 많이 달라지는 팔들 (D 줄기와 ,frC 줄기)은 t R N A 의 삼 차 구조에 서 상호작용하는 부분이며 (그림 1-19 를 보라), 또 이 부분이 리보솜과 결합하는 자리라고 생각되고 있기 때문에 (2.6.1 절의 〈나〉 항울 보라) 매우 홍미 있는 것이라고 생각된다. 아미노산을 받는 줄기 a 와 역코돈 줄기 (줄기 c) 는 정상적인 크기를 가진다는 것도 매우 홍미있는 일이다. 미토콘드리아의 t RNA 둘의 특이한 구조들로 보아서 이들의 리보솜과의 상호작용도 매우 특이할 것으로 생각된다. 실제로, 미토콘드리아의 터 보솜들은 세포질의 리보솜과 현저하게 다르다는 것이 알려쳐 있다.
 A A
A A
1.6.2 마토콘드리아의 유전암호 최근 (1983 년)까지의 연구결과에 의하면 유전암호의 보편성에 관한 일 반적인 결론은 대수롭지 않은 예의를 제의하고는 원핵세포와 진핵세포의 경우에는 맞는 말이지만, 미토콘드리아에서는 놀라운 차이접들이 있다 는 것을 알게 되었댜 원핵세포에서는 종결 코돈인 UGA 가 진핵세포에 서 는 트립 토판의 코돈이 다. 또한, AUA 는 사람의 미 토콘 드리 아 에 서 는 이소루신의 코돈이 아니라 메티오닌의 코돈이 된다 (Barell 등, 19 79 ). 미 토콘드리 아는 마 토콘드리 아에 만 전 문화된 효소들, 그 들의 rRNA, 및 그들의 t RNA 둘을 위한 유전자들을 함유하고 있는 미토 콘 드리아 자 신의 DNA 를 가지고 있다. 물론, 이 D NA 는 미토콘드리아의 출처 에 따라서 다르다. 예컨대, 효모의 미토콘드리아에 있어서는 UGA 가 트립 토관의 코돈이고 CUA 는 트레오닌의 코돈이다. C UA 가 트레오닌의 코 돈이라는 것은 매우 충격적인 발견이었다. 왜냐하면, 이 C UA 는 정상 표 1-11 유전 암호의 여 러 가지 변 형 들. Ee 는 E. coli, NM 은 Neuros p or a 의 미토콘드리아. YM 은 효모의 미토콘드리아, 그리고 HM 은 사람의 미트 콘드리아이다. 단일문자 표기법으로 아미노산들을 나타내 었 다 ; i는 개시, CT 는 사슬 종결을 나타낸다. 아미노산 약자들 : A, ala; C, cy s; D, asp ; E, gin; F, ph e; G, gly : H, hi s; I, ile ; K, ly s; L, leu; NI, met ; N. asn ; P, pro ; Q, glu ; R, arg; S, Ser; T, thr ; V, val; W, trp.
염기짜 칫鬱 曺 u ..LFE.I.cl . . ..YLF.둥.IMl .따. u염. .NLF.기.|Ml . . ..HLF.M.Il . . ESe2 YSMI ,..` NSMI SI CTETle TCYTlM AI cT NlMr CTlT .…EWC l.RI • .• ..WYC- -MII • •G II!II· ·NWC MII • ...HW C : 나II · ·!li' 'CJAG ’ 염기 세지 HM HM Ee C L2 Tl LI LI P2 PI Pl Pl ..H..I. . ..H..I .. ..H..I .. ..H..I .. R2 RI RI RIAu~ A M”i 2 M” i2 MJIi 2 ••M Il..,:iii 2• • T2 Tl Tl Tl ENKlIl ENKIll ENKllI ENKlIl SRII RSII RsI, I CsT, G~GA G .V.V. 2 ,.i. . VI VI VI A2 Al Al Al . ..Q0.1.I .. ..D.0.1I . . ••00•11• 를 • ..D.Q.II. . G2 GI GI GI I'J!
적으로는 루신예 대한 코돈이기 때문이다. 그뿐 아니라, CUA 는 사람 의 HeLa 세포 또는 소의 간의 미토콘드리아에서는 정상이지만, UGA 는 트립몬의 ' 코돈이고, AUG 이의에도 AUA 와 AUU 는 개시와 관계되 는 메티오닌의 코돈이고, 종결 코돈으로서는 정상적인 UAA 와 UAG 뿐 아니라, AGA 와 AGG( 정상적으로는 아르기닌에 대한 코돈)이 있다(표 1-11 을 보라). 이러한 불규칙성은 해당하는 t RNA 들의 암호 해독의 성질들에 의해 서 일어나는 것으로 선명되고 있다. 사람과 소의 미토콘드리아의 유전 구조 를 이루는 전체 DNA 의 일차구조가 Sang er 의 연구진에 의해서 결 정 되 었 다 (Barrell 등, 1980) . 놀라운 사실 은, 미 토콘드리 아에 는, 22 개 의 tR NA 들 에 대 한 유전 자들만 있 다는 것 이 다. 동요현 상 (wobbli ng ) 이 일어난다고 할 때 세포질에는 적어도 31 개의 t RNA 가 있어야한다. 그 러므로, 몇 가지 tR NA 종들은 박테리아, 효모 세포, 및 동물 세포의 세포질에 있어서보다 더 많은 코돈둘을 해독하는 것이 분명하다. 죽 미 토콘드리아의 t RNA 들에 의한 코돈 인식의 양식이 목이하다. 만일 정 상적인 유전암호 해독에서 코돈의 세번째 염기만이 다르고 그 코돈이 한 아미노산울 지령하는 코돈족들(이러한 코돈족들은 8 가지가 있다. 서문 부분에 있는 유전 암호의 표를 참조하라) 을 각각 한 tR NA 가 해 독을 할 수 있다면 최소한으로 필요한 t RNA 의 종류의 수는 23 가지가 된다(위 에 서 말한 8 가지 의 코돈족들은 CUN, GUN, UCN, CCN, ACN, GCN, CGN, 및 GGN 둘이 다 (서 문의 유전 암호표를 보라) ) . 그러 므로 아직 도 한 개의 t RNA 가 모자라는 결과가 되는데 이것은 t RNAM• t가 하나밖에 없으므로 필요한 t RNA 는 모두 22 가지로 되어서 필요한 t RNA 는모두 다 있게 되는 셈이다. 미토콘드리아의 t RNA 의 암호 해독의 성질이 확 대된 것은 동요가설을 확장함으로써 설명할 수 있다. 즉, t RNA 들의 역 코돈의 첫째 위치에 있는 U 는 코돈의 세째 위치에 있는 네 가지 염기 들을 모두 해독할 수 있으며, 역코돈의 첫째 위치에 있는 변형된 U(U* ) 는 푸린 염기 (A 또는 G) 를 해독할 수 있다. 지금까지 미토콘드리아에 있어서의 암호 해독에 대한 실험적인 증거로 보아서, 만일 이러한 동요 현상의 확장이 옳게 적용된다면, 유전암호의 보편성은 모든 단백질 합 성계에서 성립된다고 말할 수 있다.
* 참고문현 Barker, D. G. , Ebel, J. -P. , Jak es, R. , Bruto n , C. J. (19 82) , Eur. ]. Bi oc lzem. 127, 449. Barrell, B.G., Anderson, S., Bankie r , A. T., de Bruij n, M.H . L. , Chen, E., Coulson, A.R., Drouin , J., Ep c ron, I.C ., Ni er lic h , D.P., Roe, B.A., San g er . F., Schreie r , P.H., Smi th, A.J, H . , Sta d en, R., Young , I.G . (19 80) , Proc. Natl . Acad. Sci. 77, 316-1 . Barrell, B.G. , Bankie r , A. T ., Drouin , J. (1979) , Xatu r e 282, 189. Berg, P. (1956) , ]. Bi ol . Chem. 222, 1025. Berg, P., Bergm an, F.H., Ofe n g an d, E.J. , Die c kmann, l\I. (1961), ]. Bio l Chem. 236, 1726. Berg, P. , Of en g an d, . E. J. ( 19 58) , Proc. Natl . Acad. Sci. 44, 78. Bhat, T.N. , Blow, D. M. , Bric k , P. , Ny bo rg, J. (1982) , J. Mal. Bi ol . 158, 699 Brown, D.M. (1975), Basic P;·i:z c ip lc s in Nucleic Acid Clzc m i st r y ( Ed ., P.0.F Ts'o) , vol. 2, p. 2 , Academi c Press, New York. Bruto n , C.J. (1975) , Bi oc hc m . ]. 147, 191 . Vhambers, R. W. (1971) , Prag. N11cl. Acid s Res. Mo!. Bi ol . 11, 489. Chape vil le , F. (1972) , The Mcc/ 1a ;zis a 1 of Prote i n Sy nt h e sis and its Reg 11 lat i1 (Ed. , L. Bosch) , p. 5, North - H olland Pub!. , Amste r dam. Chouste r man, S., Chap ev il !e, F. (1973) , Eur. f. Bi oc hem. 35, 46. Chouste r man, S. , Hervt'! , G. , Chape v il le, F. (1966) , B11!1 . Soc. Clzi m . Bi ol . 4: 1295. Chen, E.Y., Roe, B.A. (1978) , Bi oc hem. Bi op h y s . Res. Com1111111. 82, 235. Clark, B. F. C. (1975) , Nonsense Muta t i on s and tR NA Sup pr essors (Ed. , J. E. Ce! J. D. Smi th) , Academi c Press, New York. Cramer, F., Faulhammer, H., von der Haar, F., Sp ri n z l, M., Ste r nbach, (1975) , FEBS Lett . 56, 212. Cramer, F., von der Haar, F., lgl o i, G.L . (1979) , Transfe r RNA: St r11 c t11 Prope rti es, and Recog en it ion (Ed.; D. Soll, J.N . Abelson, P.R. Schim mel) , 267, Cold Sp ri n g Harbor Laborato r y , Cold Sp ri n g Harbor. Cric k , F. H. C. (1957) , Bi oc /z e m. Sy m p . 14, 25. Dang , Chi V., Joh nson, D.L., Yang , D.C.H. (1982), FEES Lett ., 142, 1. Davie , E.W ., Konnin g sb erge r , V.V., Lip m ann, F. (1956) , Arch. Bi oc h Bi op / zys. 65, 21. DeMoss, J.A., Novell i, G.D. (1956) , Bi oc lzim . Bi op l z y s. Acta 22, 49. Di rhe im er, G. , Keit h, G. , Sib l er, A. -P. , Mart in, R. P. (1979) , Transfe r Rl
Str u ctu r e, Prop er ti es, and Recog n it ion (Ed. , P. R . Schim mel, D. Soll, J.N , Abelson) , p. 19, Cold Sp ring Harbor Laborato r y , New York. Donis - Keller, H. , Maxam, A. M. , Gi lbert, W. (19 77) , Nucleic Acid Re s 4, 2528. Ebel, J.-P . , Gie g e , R. , Bonnet, J. , Kern, D. , Befo r t, N. , Bollack, C. , Fasio l c.. F. , Gang lo ff , J. , Di rh eim er, G. (1973) , Bi oc lzim i e 55, 547. Ebel, J.-P ., Renaud, M., Die t r i c h , A., Fasio l o, F., Keit h, G., Favorova, 0. 0., Vassile nko, S., Baltz i n g e r, M., Ehrlic h , R., Remmy , P., Bonnet, J., Gie g e , R. (1979) , Transfe r RNA: Str u ctu r e, Prop er ti es, and Recong n it io;z (Ed . , P. R. Schim mel, D. Soll, J.N . Abelson) , p. 325, Cold Sp ri n g Harbor Laborato r y , New York. Eldred, E. W. , Schim mel, P. R. (1972) , ]. Bi ol . Che m . 247, 2961. Favorova, 0.0., Fa sio l o , F., Keit h, G., Vi si le nko, S.K ., Ebel, J.P . (1981), Bio c hemi st r y 20, 1006. Fersht, A. (19 77) , E11zy m e Str u ctu re and Mechanis m , ch. 11, W.H. Freeman & Co., Read in g and San Francis c o. Fersht, A. R. , Kae th ner, .1vl . M. (19 76) , Bi oc hemi st r y 15, 3342. Forunie r , l\1. , Labouess e, J. , Dir h eim er, G. , Fix , C. , Keit h, G. (1978) , Bi oc lzim Bi op l zy s. Acta 521, 198. Fraser. T. H. , Ric h , A. (1975) , Proc. Natl . Acad. Sci. 72, 3044. Freie r , S. H , Ti no co, I. Jr. (1975) , Bi oc hemi st r y 14, 3310. Fresco, J. R. , Adamx, R. , Accio n e, R. , Henley, D. , Lin d ahal, T. (1966) , Cold Sp rin g Harbor Sy m p . Qz mat. Bio l . 31, 527. Gauss, D. , Sp ri n z 1 (19 81) , Nucleic Acid Res. 9 : rl. Gauss, D. H. , Gri.it er , F. , Sp ri n z l, M. (1979a) , Transfe r RNA: Str ttct u r e, Pro- pcr ti es, Re cog ll it io;z (Ed., P.R. Schim mel, D. Soll, J.N . Ab elson), p. 255, Cold Spr i n g Harbor Laborato r y, New York. Geft er , M. L. , Russel, R. L. (1969) , ]. Mo!. Bi ol . 39, 145. Gil u m, A.M., Urqu hart, N., Smi th, M., RajB h anda ry, U.L . (1975), Cell6, 395. Gup ta, R. , Randerath , K. (1979) , Nucleic Acid s Res. 6, 3443. von der Haar, F. , Cramer, F. (1978a) , Bi oc hemi st r y 17, 4509. von der Haar, F. , Cramer, F. (1978b) , Bi oc lzeil listr y 17, 3139. Harada, F. , Sawy er , R. C. , Dahlberg, J. (1975) , ]. Bi ol . Chem. 250, 3487. Hecker, L.I., Eg a n, J., Rey no lds, R.J., Ni x, C.E., Schif f, J.A., Barnett , W.E. (1974) , Proc. Natl . Acad. Sci. 71, 1910. Heckman, J.E ., Hecker, L.I., Schwart zb ach, S.D . , Barnett , W.E., Baumsta r k, B. , RajB h andary , U. L. (1978) , Cell 13, 83. HHeonatgz lea nn,d ,D M., . BM. a(n1d9e5l5, ) ,P .,B iG oca lrzei!m , . J.BPi . o (p 1/ z9y7s2. ),A cBta i o c1 lz6i, m .2 8B8.i op l zy s. Acta 281, 228 .
Hoag la n d , M. B. (1960), Nucleic Acid s (Ed., E. Cha rg a ff, J.N . Dav id s on ), vol. 3, p. 349, Academi c Press, New York. Hoag l a nd, M. B. , Keller, E. B. , Zamecknic k , P. C . (19 56) , ]. Bi ol . Ch em . 218, 345. Holbro o k, S., Sussman, }., W arr ant, R., Church, G. , Ki m , S.-H. (19 77) , Nuc lei c Acid s . Re s. 4, 2811 . Holley, R.W ., Ap ga r, J., Everett , G.A., Madis o n, J.T . , I \Ia rqu is e e, M., ~lerrill , S.H ., Penswi ck , J.R . , Zami r, A. (1965), Scic i lc e 1<17 , 1-16 2. lgl o i, G.L ., Cramer, F. (1978), Trn11sf a r RN A( Ed ., S. Altm an) , p. 29-l, MIT Press, Cambrid g e, Massa chuset t s. Kalrusek, F., Konig s berg, W. H. (19 74) , Bi oc lwm i st r y 13, 999. Keams, D.R . (1976), Pr ag, Nt! c l. Acid Re s. Mo/. Bio l . 18, 91. Ki es selve v , L.L., Favorova , 0.0 . (19 74 ), Ad v. Eil zy a 1 0I. 40, 1-11. Ki m , S.-H. (1976), Prag. Nucl. Acid Ras Mo!. Bi ol . 17, 18 1. Ki m , S.-H. (1979) , Trails / er RN A: Stn tcl urc, Pr op er t i e s , aad Racog :z i ti o;z (Ed . P.R. Schim mel, D. Soll, }.N . Abelson), p. 83, Cold Sp ri n g Harbor Laborat ory , New York. Ki m , S.-H., Sussman, J.L . , Suddath . F.L . , Qu ig l e y , G.}., McPh er son, A. Wang , A. H. J., Seeman, N.C., Ric h , A. (1974) , Scie n ce 185, -13 5. Kochetk o v, N. K. , Budowsky, E. I . (1969) , Prag. Nucl . Acid s Re s. aild Mo, Bi ol . 9, 403. Koontz , S. W. , Schim mel, P. R. (1979) , J Bi ol . Clze m. 254, 122 7. Krup p, G., Gross, H.J. (1979), Nucleic Acid s Res. 6, 3481 . Ladner, J. E . , Jac k, A. , Robertu s , J D. , Brown, R. S. , Phodes, D. , Clar k, B.I C., Klug , A. (1975) , Proc. Nae! . Acad. Sci. 72, 4414. Lam, S. S. M. , Schim mel, P. R . (1975) , Bi oc lzemi st r y 14, 2775. LaRossa, R., Soll, D. (1978), Transfe r RNA(Ed., S. Altm an), p.1 36 , I\II Press, Cambrid g e, Massachusett s. Late n , H. , Gorman, }., Bock, R.M . (1978), Nuclei c Acid s Re s. 5, 4329. Leahy, J. , Glassman, E. , Schweet, R. S. (1960) , J Bi ol . Chem. 235, 3209. Levit t, M. (1969) , Natu re 244, 759. Lockard, R.E ., Kumar, A. (1981), Nucleic Acid s Res. 9, 5125. Loft field , R. B. (1971) , Prote i n Sy nt l ze sis ( Ed. , E.H . McConkey) , vol. 1, p. Dekker, New York. Mats u zaki, K., Taketa , Y. (1973) , Bi oc lzim . Bi op l zy s. Acta 308, 399. M 터 ara, G. P. , McClain , W. H. (1977) , ]. Mal. Bi ol . 117, 1061 . Moras, D., Comarmond, M.B. , Fis h er, J., Weis s , J., Thie r ry , J.-C ., Ebel, J .- Gie g e, R. (1980a) , Natu r e, 288, 669.
Moras, M. , Coma rm o nd, M. B. , Fis h er, J. , Weis s , R. , Thie r ry , J. C . (19 8 0b) . NaN ssa, tu Gr .e, 2 S8t8e , f fl6e 6r ,9 . G . (19 6 7) , Mal. Ge n. ge1 1et . 100, 378. Nis h im ura, S. (19 7 9) , Tra,z sfe r RN A: St ru ctu r e, Pr op er ti es, a;z d Re cog n it ion (Ed ., P.R . Sc him mel, D. So ll , J.N . Abelson), p. 59, Cold Sp ri n g Ha rbor La bo rat o r y , New York . Norris , A. , Berg, P. (19 6 5 ) , Pr oc. Natl . Acad. Sc i. 52, 330. Ofc n g a nd, J. ( 19 7 7) , :Ho le c ular Me cl za,z i sm s of Prot e i n Bi os y; z tl z es is ( Ed ., H. \Ve is s b ach , S. Pest k a ) , p. 7, Academi c Press, New York. Of cn g an d , J. , Chen, C. -!\L (19 7 2) , ]. Bi ol . Che m . 247, 204 9. Of en g an d, J., Chlad ek, S., Robil a rd, G., Bie r baum, J. (19 7 4) , Bi oc hem i st r y 13, 5425. Peat t ie, D.A . (19 7 9) , Pr oc. Natl . Acad. Sci. 76, 1760. Pong s, 0., Bald, R. , Re in w a ld , E. (19 73) , Eur. ]. Bi oc lze m. 86, 153. Putn e y , S.D . , Roy al , ~.J. , De Veg v ar, H.N ., Herlih y , W.C. , Bie m ann, K., Schim me l, P. R . (19 8 1 ) , Scie n c e 213, 149 7 . Putn e y , S.D . , Saue r, R. T ., Sc h im me l, P.R . (19 81), .J Bi ol . Che m . 256, 198. Qu ig le y , G. J . , Teet e r , H M. , Ri ch , A. (19 78) , Pr oc . Na tl . A cad. Sci. 75, 64. Renaud, M. , Bacha, H. , Remy , P. , Ebe l, J. P. (1981) , Proc. Natl . Acad. Sci. 78, 1606. Ric h , A. , Ra jB h a ndary , U. L. (1976) , Ann. Re v. Bi oc lze m. 46, 805, Academi c Press, N~w York. Rig le r, R. , Pachmann, U. , Hi rs ch, R. , Zachau, H. G. (1976) , Eur. J. Bi oc lzem. 65, 307. Roberts , R. J. ( 1972) , Natu r e New Bi ol . 237, 44. Roberts , R. J. (1974) , ]. Bi ol . Che m . 24 9, 478 7. Roe, B. , Sir o ver, M. , Dudock, B. (1973) , Bi oc he mi st r y 12, 4146. Santi , D.V., Webste r , R.W ., Cleland, W.W. (1974), Meth o ds in En zy m olog y, 29, 620. Schevit z, A. D ., Podja r ny , A. D ., Kris h namachari, N., Hug h es, J.H . , Sin g le r, P . B. (1979) , Natu r e 278, 188. Schim mel, P.R. (1979) , Trans/er RNA: Str u ctu r e, Pr op er t i es, and Re co g n it ion (Ed., P.R. Schim mel, D. Soll, J.N . Abelson), p. 297, Cold Sp r in g Harbor Laborato r y , New York. Schim mel, P. R ., Soll, D. (1979), Ann. Re v. Bi oc lzem. 48, 601 . Schim mel, P.R ., Soll, D. , Abelson, J.N . (1979), Tr an s f e r RNA: Str 1 1cl11re, Pro- per ti es and Recog n it i on (Ed ., P .R. Schim mel, D. Soll, J.N . Abelson), p. 518, Cold Sp ri n g Harbor Laborato r y , New York.
Schulman, L.A ., Her, l\I.O . (19 73) , Bi oc l1e111. Bi op l zy s. Re s. Co1111111111. 51, 275. Schulman, L. A. , Pelka, H. (19 75) , J Bio l. Chem. 240, 542. Schulman, L. H. , Pil k a, H. (19 77) , Bi oc hemi st r y 16, 4256. Schweet, R. S. , Bovard, F. C . , Allen, E. , Glassman, E. (1958) , Proc. Natl . Acad. Sci. 44, 173. Sin g e r, C. E. , Smi th, G. R. (1972) , J. Bi ol . Chem. 247, 2989. Sin g e r, C.E ., Smi th, G. R . , Corte s e, R., Ames, B.N . (1972), Natu r e New Bio l. 238, 72. Soll, D. , Schim mel, P. R. (1974) , The E:z zy m es (Ed. , P. D. , Boy er ) , 3rd ed. , vol. 10, p. 489, Academi c Press, New York. Sp ra gu e , K.U ., Hag e nbuchle, 0. , Zunig a , M.C. (19 77), Ce ll , 11, 561 . Sp ri n z l, M., Cramer, F. (1973) , Natu r e New Bi ol . 245, 3. Sp ri n z l, M. , Cramer, F. (1975) , Proc. Natl . Acad. Sc i. 72, 3049. Sp ri n z l, M., Cramer, F. (1979), Proc. Nucl. Acid Res. Mal. Bio l. 22, 1. Sp ri n z l, l\I. , Geute r , F. , Sp el zhaus, A. , Gauss, D. H. (1980) , N11cleic Acid s Res. 8, 1. Sta n ley, J. , Vassile nko, S. (1978) , Natu r e 274, 87. Sta r zyk , R.M ., Koontz , S.W., Schim mel, P. (1982), Natu r e 298, 136. Ste i n , A., Croth e rs, D. (1976) , Bi oc hem i st r y 15, 157. Str i c k land, J.E ., Jac obson, K.B . (19 72) , Bi oc hemi st r y 11, 2321 . Takemura, S. , Mi zu ta n i, T. , Mi yaz aki, M. (1968) , Jpn . J Bi oc hem. 64, 827. Taketa , Y. , Ohnis h i, T. (1975) , J. Bi ol . Chem. 250, 3878. Tanaka, Y., Ky er , T. A., Brownlee, G.G. (1980), Nucleic Acid s Res. 7, 1259. Thie b e, R., Barbers, K., Zachau, H. G. (1972), E11r. J. Bi oc l1em. 26, 144. Wata na be, K. , Oshim a, T. , Ni sh im ura, S. 9 (1976) , Nucleic Acid s Re s. 3, 1703 Wi nt e r , G. P. , Koch, G.L.E . , Dell, A., Hartle y B.S . (1979), Transfe r R:V .1- . Str z1 ct1 tr e , Prop er ti es, and Recog n it ion (Ed. , P. R. Schim mel, D. So ll , J. 卜 Abelson) , p. 255, Cold Sp ri n g Barbar Laborato r y, New York. Woo, N. , Roe, B. , Ri ch , A. (1980) , Natu r e 286, 346. Wr igh t, H.T., Manor, P.C . , Beurlin g , K., Karpe l , R.L . , Fresco, J.R . (19 79 Transfe r RNA: Str u ctu r e, Prop er ti es, aud Recog ;zitio1 1 (E d., P.R Schim me D. Soll, J.N . Abelson.), p.1 45, Cold Sp ri n g Harbor Laborato r y , New York Yarus, M. (1972) , Proc. Natl . Acad. Sc i. 69, 1915. YZaacrcuasi,, MG.. ,, MRaosrhibn ,a umM,o rSin. ,( 1P97. 2J) a, r cBoit o, c hBem., i sMt r oyr a1s1, , D2.0 ,4 3T. hie r ry , J.C ., Gi eg e , (1979) , J. Mal. Bi ol . 129, 483. Zelwer, C., Risle r, J.L ., Brunie , S. (1982), J. Mo. Bi ol . 155, 63.
제 2 장 리보솜의 구조와 기능 리보솜은 모든 세포에 보편적으로 존재하며, 단백질 합성의 자리아기 때문에 세포의 성장과 세포의 생활을 유지함에 있어서 가장 중요한 역할 을 맡고 있는 세포 소기관이다. 리보솜은 세포의 종류에 따라서 그 자체 의 크기뿐 아니라 구성성분들의 수와 크기들이 상당히 다르지만(표 2-1 및 그림 2-1 을 보라), 단백질 합성에 있어서의 기능은 근본적으로 같 다. 리보송의 중요한 특칭은 긴 진화과정을 거치면서도 그 구조와 기능 이 그대로 보즌되어 왔다는 사실과 매우 중요한 〈 살림살이 효소 〉 의 하 나로서의 기능을 가지고 있다는 사실이다. 리보솜 상에서의 mRNA 의 단백질로의 번역은 모든 세포에서 일어나 는 보편적인 과정으로서 지난 이십 년 동안 집중적인 연구 대상이었다. 많은 복잡한 분자들이 참여하는 이 번역 과정은 많은 단계들을 거치면 서 리보솜에서 일어난다. 이러한 복잡한 기능을 수행하기 위해서 리보 송 자신은 여러 가지 단백질과 RNA 들로 구성된 복잡한 구조를 가질 것 이 틀림없다. 지난 수년 등안에, 단백질 합성에 있어서의 개개의 기능 적 단계들은 단일한 리보솜 성분들에 기인되는 것이 아니라 몇 개의 성 분들의 부분들로 이루어지는 영역둘이 관여한다는 것이 밝혀졌다. 그러 므로, 단백질 합성에 있어서의 문제들을 알기 위해서는 리보솜 그 자체 의 구조 를 알아야 한다. 그동안 가장 집중적으로 연구된 리보솜 종은 원핵세포인 E. col i의 것
이다. 그밖의 박테리아의 리보송도 상당히 연구되고 있다. Bacil lu s sub til£ s 의 리보송의 성질들이 많이 조사되고 있다 . E. col i의 리보솜이 집중적인 연구 대상이 된 데에는 몇 가지 이점이 있기 때문이다. 첫째 진핵세포의 리보솜에 바하여 구조가 더 간단하다. 둘째, E. co li의 세 포는 쉽게 다량으로 배양 할 수 있을뿐 아니라, 여러 가지 돌연변 이 종들 을 이용하여 유전학 적인 연구를 할 수 있다. 세째로, E. col i에 있어서 의 단백질 합성의 여러 반응들이 바교적 철저하게 조사되어 있기 때문 에 여기서 얻은 정보들을 리보솜의 특정한 성분(또는 성분 들) 의 성질과 상관시켜 봉으로써 이 성분들의 기능을 추정할 수 있다. 그러나, 원래 리보솜은 Palade(1955) 가 진핵세포에서 처음으로 발견 하였다는 것을 알아야 한다. 진핵세포의 리보솜의 구조와 기능이 원핵 세포의 리보솜의 구조와 기능처럼 많이 밝혀지지 않았지만, 최근 진핵 세포의 리보솜에 관한 연구가 활발하게 이루어지고 있으며, 매우 중요 한 것들이 밝혀져 가고 있다. 표 2-1 원핵세포와 진핵세포의 리보솜둘의 몇 가지 성질들의 비교 E. coli 쥐 간 효모 리보솜(모노송 형) S 값 70S 80S 80S 큰 하위단위체 50S 60S 60S 작은 하위단위체 30S 40S 40S RNA 둘 : 큰 하위단위체 23S 28S 25S 5S 5.8S 5.8S 5S 5S 작은 하위단위체 16S 18S 18S 성분 단백질들의 종류 큰 하위단위체 32 ~49 ~45 작은 하위단위체 21 ~33 ~35 단백질 함량 /RNA 합량 37/63 50/50 60/40 몇 가지 리보솜둘의 성질들을 표 2-1 에서 비교하였다. 모든 리보솜들 은 두 개의 하위단위체들로 구성된다. 그 하나는 작고 다른 하나는 좀 크다. 리보솜 내의 단백질과 RNA 의 함량의 비는 세포에 따라서 다르 지만 대개 50 : 50 이다. 이 표에 실은 것은 대표적인 예에 지나지 않는
다. 단량 체 로서의 리보 솜( 모노송), 큰 하위단위체, 작은 하위단위체, RNA 의 종류와 수 및 크기, 그리고 성 분 단 백질들 의 종류와 수 및 크 기 들은 세 포의 종류에 따라서 다르다. 리보 솜의 구조는 매우 복잡하기 때문에 그 구조를- 경정한다는 것은 쉬 운 일이 아니다. 최근에 E. col i의 리보 솜의 결정체를 얻는 데 성공함 으로 써 머지 않아서 그 구조를 X- 선 결정학적인 방법으로 분 석할 수 있 게 될 것 으로 생 각한다 (W ittm ann, 1982) . 현재 로서 는 친화표지 법 , 교 차결합법, 전자현미경사진법 , 면역화학 , 및 중성자 산란법 등과 같은 바 교직 조 잡 한 기 법 들을 사용하여 리 보솜의 구조를 분석 할 수밖에 없는 실정이다. 뒤에서 곧 이 문제들을 다루겠지만 이러한 기법들로 얻은 결 과 들 은 리보 솜의 기능들에 관해서 많은 유용한 정보들을 제공해 주고 있다. 2.1 리보 솜 의 구조와 기능에 대한 개요 2. 1.1 리보솜의 기능 단백질 합성의 반응들은 리보솜 상에서 일어나고 있으므르, 우리가 리 보솜에 관해서 알아야 할 문제는 리보솜은 과연 무엇이며, 무엇을 하며 또 어떠한 방법으로 그 기능을 나타내는가?라는 것들이다. 몇 가지 tR NA 들의 구조가 밝혀 짐 으로 써 리 보솜의 구조와 기 능의 분 석에 중요한 결과를 가져 왔다. 첫째로, 단백질 합성이 일어나는 동안 에 아미노아실-t RNA 와 리보솜 상에서의 그의 결합 자리 사이에서의 상 호작용을 분석하는 데 필 요한 정보를 제 공하였으며, 둘째로, 리보솜의 구조와 기 능을 분석 하려 면 tR NA 들의 경 우와 마찬가지 로 결정 구조학적 인 방법을 사용하여야 할 것이라는 것을 암시해 주었다. 그러나, 앞에 서 말한 바와 같이, 리보솜의 구조와 기능에 관한 연구는 비교적 조잡 하고 간접적인 방법을 쓰고 있으므로, 리보솜의 기능을 정확하게 이해 한다는 것은 현재로서는 요원한 일이라고 생각된다. 그러나, 간접적이 고 조잡하기는 하여도 이 방법들로 얻은 견과들은 리보솜의 구조와 기 능에 관해 서 많은 것을 알려 주었다. 리보솜으로 결합해 들어오는 아미노아실-t RNA 를 처리하기 위해서
리보솜 상에는 적어도 두 개의 중요한 자리가 있어야 합 것이다. 각 자 리는 아미노아실-t RNA 에 대해서 각각 입체적으로 목이하게 상호작용 할 것이다. 한 자리는 아미노아실-t RNA 분자의 선택에 관여할 것이 확 실하며, 따라서 이 자리는 아답터로서의 t RNA 의 목성을 인식해야 할 것이다. 이와는 달리, 또 하나의 자리는 아미노아실-t RNA 들에 있어서 의 공동된 구조물 인식하는 것이어야 할 것이다. 이 두번째 자리는 무 엇보다도 아미노산과 tR NA 사이의 에스데르 결합의 구조 를 인식할 수 있어야 할 것이다. 그래야만 모든 아미노산은 리보솜 상에서 성장하고 있는 폴리펩터드 사슬에 옳게 삽입될 수 있다. 참으로 다행스러운 것은 이 두 개의 중심 자리는 리보솜의 두 하위단 위체에 각각 찰 분리되어 위치하고 있기 때문에 따로 학인할 수 있다. mRNA 의 결합을 예로 들어 보면, 그 결합 자리는 30S 하위단위체에 국한된다. 따라서 tR NA 분자의 선덱은 적어도 이 하위단위체가 관여한 다는 것을 의미한다. 이것을 뒷 받침하는 실험적 증거로서 tR NA 선택 의 오차 빈도를 달라지게 하는 돌연변이들은 모두 30S 하위단위체의 성 분들에서 일어난다 (Gor i n i, 1971) 는 것을 들 수 있다. 마찬가지로, 번역 의 오차 반도를 달라지게 하는 항생물질들은 예의 없이 30S 하위단위체 와 상호작용한다 (Pestk a , 1971) . 다론 한편, 50S 하위 단위 체 는 목이 한 tR NA 분자들의 선 택 과는 관계 가 없는 것으로 보인다. 지금까지 알려진 모든 증거둘은 이 하위단위체 의 t RNA 와의 상호작용은 t RNA 들의 안 끝에 있는 CCA 연속부분 또 는 보편적 으로 존재 하는 T,t rCG 고리 와 같은 공통되 는 구조부분에 서 일어날 것으로 생각된다 (R i ch t er 등, 1973). 또한, 펩티드 결합의 형성 을 촉매하는 펩티딜기 전달효소도 50S 하위단위체 상에 위치하고 있다 (Monro, 1967). 그러므로, 큰 하위단위체의 기능은 펩티드 결합의 형 성과 펩티드의 연장을 반복적으로 일어나게 하는 일뿐이다. 리보솜이 두 개의 다른 물리적 하위단위체들로 나뉘게 된 이유는 아 미노아실-t RNA 들을 인식하기 위한 두 가지의 상호작용 자리들이 필요 하기 때문만은 아닐 것이다 . 단백질 합성이 일어나는 동안게 리보솜의 두 하위단위체들이 상대적으로 움직여야 한다는 것을 고려하면, 리보솜 의 구조적 특징들을 더 쉽게 이해할 수 있을 것으로 생각한다. 죽, 두 개의 하위단위체들의 기계적인 움직임에 의해서 촉진되는 번역 메카니 즘의 몇 가지 국면들을 고려하여야 한다.
먼저 고려해야 할 가장 근본적인 국면은 mRNA 의 번역이 순차적으 로 일어나야 한다는 것이다. 다시 말하면, 완성된 단백질의 N- 말단에 서 c- 말단까 지의 아마노산들에 대한 코돈둘이 한 번에 하나씩 읽혀져야 한다. 이것은, 리보 송 이 하나 또는 그 이상의 공유결합의 가수분 해 로 발 생되는 자유에너지를 리보솜과 mRNA 의 상대적 운동과 같은 방향성을 가진 기 계적 과정, 즉, 바가역적인 기계적 과정으로 전환시킬 수 있어 야 한다는 것을 의미한다. 두번 째의 움직임은 펩 터드 결합이 매번 형성된 후에 일어나는 tR NA 의 움직 임 이 다. 이 것 을 자리 옮김 (tra nslocati on ) 이 라고 부른다. 그러 나, 자리 옮김은 mRNA 의 움직임과는 달라서 티보솜 상에서의 t RNA 의 세 부적인 형태 변화에 지나지 않는 추상적인 움직임일 수도 있다 (Woese 1973). 그 런데 많은 실험결과들에 의하면 성장하고 있는 풀리펩티드 사 술은 tR NA 분자에 부착되 어 있으며 , 이 펩 티 딜-t RNA 가 리 보솜 상에 서 두 개의 독아한 자리들에 결합할 수 있다는 것을 보여 주고 있다 . 펩티딜-t RNA 를 리보솜 상에 결합하는, 물리적으로 구별되는 두 개의 자리가 있다는 것은 두 자리들 중의 하나가 푸르마이신의 작용에 대해 서 민감하고 다른 것은 저항성이 있다는 사실에서 알게 되었다. 푸로마 이신에 민감한 자리를 P 자리라고 부르며, 저항성이 있는 자리를 A 자 리라고 부른다. mRNA 에 의해서 정보를 받은 아미노아실 t RNA 는 리보솜의 푸로마 이신예 대해서 저항성을 가진 A 자리로 들어온다 . 푸로마이신에 대해서 민감한 P 자리에 있는 다른 t RNA 에 결합된 갓 생긴 풀리펩티드는 펩 티드 결합 형성이 일어난 다음에 A 자리에 새로 들어온 t RNA 로 전달 된다. 그 다음에 펩티딜-t RNA 는 P 자리로자리옮김한다. 이렇게 되면 이 계는 또 한 차례의 연장 회로를 작동할 수 있는 상태가 된다. 이 〈두 자리〉 가설은 일찌기 Wa t son(1964) 에 의해서 제안되었는데 많 온 실험적인 발견들을 찰 설명해 주고 있다. 그렇지만, 이 물리적 두자 리들 사이에서의 〈자리옮김〉을 증명해 즐 수 있는 칙접적인 연구결과는 아직 없다. 리보솜의 구조와 기능에 관한 연구들이 나날이 발전하여 중 요한 결과들이 얻어지고 있으므로 이 문제도 머지 않아 밝혀질 것으로기 대된다. 마지막으로, 리보솜의 하위단위체의 동적인 움직임은 번역 메카니즘 의 또 하나의 국면을 위해서 기여할 것으로 생각한다. 단백질 합성의 연
장 과정을 지금까지 너무 단순하게 설명하려고 하였는대 사실은 그 렇 지 않을지도 모른다. Cric k 동 (1961) 이 오 래 전에 말한 바와 같이, 전령의 전달은 어떤 의미에서는 구 듯점 으로 중단된 것으로 불 수 있다. 리보송 상에서 일어나는 개시, 연장, 및 종결 방식의 특유한 성질들이 그것을 암시해 주고 있다• 리보솜 상에서 일어나 는 번역의 여러 단계들 사이의 전이는 하위단위체들의 재배열에 수반되어야 할 것 으로 생각한다 . 바로 이 재배열이 번역의 구듯점 역 할을 할 것이라는 견해도 있다. 2.2 리보솜 단백질들의 비교법 여러 가지 생물체들로부터의 리보솜 단백 질들을 바교하기 위하여 주 로 사용하는 방법들은 이차원 풀리 아크 릴 아마드 겔 전기이등법, 면역화
 .t' .`
.t' .`
학적 방법들 그리고 단백질 화학적 방법들이다. 가) 이차원 겔 전기이동 리보솜 단백질들의 분리의 목적으로 목별히 개 발한 이 방법을 사용함으로써 E. col i의 리보 솜 단백질들의 수 를 정확 하게 결정 할 수 있다 (Kal t schm i d t 와 W ittm ann, 1970). (그림 2-1 에 보 기 를 주었다). 이 방법은 오늘날에도 많 이 활용되고 있다. 나 ) 면역학적 방법들 리보솜둘, 하위단위체들, 그리고 박테리아, 식뭉 및 동물들과 같은 여러 생체들로부터 얻은 고도로 정제된 개개의 리보 솜 단백진들 에 대한 항체들을 토끼 또는 양에서 만든다. 여러 가지 생 뭉중 등 의 리보송 업자들에 대한 항혈청들을 면역 확산 , 면역전기이동, 면 역침전 또는 헴 -웅집 등의 방법들로 성질들을 서로 바교한다. 다 ) 단백질 화학적 방법둘 상이 한 생 물들로부터 분리 한 리 보솜 단백 질 들의 아미노산 결합순서둘을 비교 함 으로써 단백질들 사이의 상동성에 관 해서 더 직접적이고, 정확하 고, 정량적인 정보를 얻을 수 있다. 이 목 적을 위해서, 펩티드들의 분리와 그들의 미량 결합순서 결정 등을 위한 고도로 개량된 단백질 화학적 방법들이 고안되었다 (W itt mann-L i ebold, 1977). 그러나, 이 방법은 아직도 장시간을 요하고 상당이 많은 량(분 자량 20 kdal 의 단백질의 경우 약 0.5-3 미크로몰)의 정제된 단백질이 필요하기 때문에 그렇게 손쉬운 방법은 아니다. 그러나 최근에 와서 30 -100 나노물의 단백질을 가지고 신속히 분석할 수 있는 새 방법이 고 안되었다 (W itt man-L i ebold, 1980). 가까운 장래에, 피코몰 정도의 극미 량의 단백질 시료를 가지고 결합순서를 결정할 수 있는 장치가 고안되 어 사용될 것으로 기대되고 있다. 2.3 리보솜의 단백질들 가) 원핵세포에 있어서의 리보솜 단백질들의 수 박테 리 아의 리 보솜에 는 50-60 개의 리보솜 단백질들이 있고, 진핵세포의 세포질에 있는리보솜에 는 70-80 개의 리보솜 단백질들이 있는 것으로 생각되고 있다. E. col i의 리보솜으로부터 추출한 단백질 부분을 이차원 풀리아크릴아미드 겔 전기 이동으로 분리하면 작은 하위단체에서는 21 개의 반점들 (S1 에서 S21 까지
을 봉 수 있고, 큰 하위단위 체 에서는 34 개의 반점둥 ( Ll 에서 L34 까지) 을 볼 수 있다. 작은 하위단위체의 경우에는 반점들의 수가 개개의 단 백질들의 수에 상응하지만, 큰 하위단위체의 경우에는 반검 L8 은 세 가 지 단백 질 , 즉, L7/L12 와 LlO 들의 복합체 임 이 밝혀 졌 다 (W ittm ann 과 Wi ttm ann-Lie b old, 1974; Pete r son 등, 1976) . 그 뿐 아니 라, 큰 하 위 단위 체의 L26 은 S20 과 동일하다는 것이 단백질 화학직 분 석 과 단백질 면 역 학적 분석 결 과들에 의 해 서 밝혀 졌 다 (Wi ttm ann 과 W ittm ann-Lie b old 1974; Sto f fe r , 1974). 단백질 S20 과 단백진 L26 의 화 아 양적 관게 (0.8: 0.2) 가 한 개의 70S 리보솜 당 한 복사물에 해당하는 층 량에 상웅하므 로, 이 단백 질은 70S 리 보솜이 두 개 의 하위 단위 체 들 로 해 리 한 매 두 하 위단위체들로 부분적으로 분포되는 것으로 생각된다. 그러므로, E. coli 의 리보솜의 큰 하위단위체에는 32 가지의 단백 전 이 있다. 이 들 중의 한 단백질 L7 은 그 N- 말단의 아미노기가 아세 틸 기로 변 형 된 침 만이 Ll2 와 다르지만 L7 과 L12 는 각각 다른 단백질로 인정되고 있다(됴 2-2 를 참조하라). 나) 단백질의 단리 E. col i의 모든 리보솜 단백질들이 단리되었으며, 그들의 화학적, 물리적 및 면역학적 성질들이 조사되었다. 첫번째 분 리 절차는 67% 아세트산으로 티보솜에서 단백질들을 추출한 다음에 셀 를로오스 아온교환 수지를 사용한 대통 크로마토그래피로 분 획 으로 나 누고, 6M 우레아의 존재에서의 겔 거르기로 더 분리하는 것이었다 (Wi ttma nn, 1974). 이러한 방법으로 분리된 단백질들은 주로 분자 량 결 정, 단백질 화학적 분석 및 면역학적 분석 목적에 사용되었다. 그러나, 우레아의 농도가 높을 때는 우레아의 분해로 생기는 시안산 에 의해서 단백질이 부분적으로 변성되므로 CD 또는 NMR 들 과 같은 뭉 리학적인 연구, 도양의 결정 및 결정체의 제조 등과 같이 천연의 구조 가 보존되어야 하는 목적에는 사용할수가 없다. 그래서, 아세트산과우 레아를 전혀 사용하지 않으며, 동결전조 절차도 거치지 않는 새로운 단 리 법 이 고안되 었다 (Di jk 와 Lit tle chil d , 1979) . 아 방법 에 서 는 LiC [ 또 는 NaCl 의 농도를 점진적으로 증가시키면서 리보솜의 하위단체들을 씻 어서 일부분의 단백질들을 제거한 다음에 CM- 세파덱스 크로마토그래피 와 세파덱스 G-75 상에서 더 분획한다. E. col i의 리보솜의 30S 와 50S 하위단체들의 리보솜 단백질들, 그들
표 2-2 E. co li로부터 얻은 리보송 단백질둔 ( 및 관련된 단백 질들)의 아 미노산 찬기둔의 수와 분자량. 단백질 | 잔기의 수 | 분자향 1 군백 질 1 찬기의 수 | 분자량 S1 557 61, 159 L10 165 17, 73 7 S2 240 26.613 L11 141 14,874 S3 232 25, 852 L12 120 12,178 S4 203 23. 137 L13 142 16,019 S5 166 17, 515 L14 123 13, 541 S6 135 15,704 L15 144 14,981 S7K 177 19.7 32 Ll6 136 15,296 S7B 153 17, 131 L17 127 14. 364 S8 129 13,99 6 L18 117 12,770 S9 128 14, 5fl9 Ll9 114 13,002 S10 103 11, 73 6 L20 117 13,366 S171 128 13, 728 L21 103 11,565 S12 123 13, 606 L22 110 12,227 S13 117 12,968 L23 99 11, 013 S14 97 11, 06 3 L24 103 11, 185 S15 87 10,001 L25 94 10,694 S16 82 9,191 L26=S20 86 9,553 S17 83 9,573 L27 84 8,993 S18 74 8, 806 L28 77 8,875 S19 91 10,299 L29 63 7,274 S20 86 9,553 L30 58 6,411 S2 1 70 8,369 L31 I 62 6,971 L1 233 24 , 599 L32 56 6,315 L2 269 29,4 16 L33 54 6,255 L3 209 22,258 L34 46 5,381 L4 201 22,087 IF-1 71 8,119 L5 178 20, 171 IF-3 181 20,695 L6 176 18,832 EF-Tu 393 43,225 L7 120 12,220 NSl 90 9,226 L9 147 15, 531 NS2 90 9.535 의 아미노산 찬기의 수, 및 그들의 분자량을 표 2-2 에 주었다. S7K 와 S7B 는 각각 E. coli K12 와 E. co/£ B 에서 얻은 S7 단백질이다.
2. 3. 1 리보솜 단백질들의 일차구조 53 가지 의 단백 질 들의 완전 한 아미 노산 결 합순서 둘이 W ittm ann- L i ebold 와 그녀의 공동연구자 들 에 의해서 분석 되 었 다 (결합순 서들은 Brim acombe 등 (1978) , W ittm ann 등 (19 80) , W ittm a n n-Lie b o ld ( 19 80) 의 평론서 에 수 록 되어 있다). 결합순서 분석치에 의하면, E. coli K12 로부 터의 30 S 하위단위체 의 21 개의 단백질 들 에 들 어 있 는 아미노산 들 의 총 수 는 3,10 8 개 이 며 , 그분 자 량 은 3 5 0 k dal 이다. 이에 비 해 서 50S 하위 단위체 는 3 2 개의 단백질들 을 가 지 며, L7 / L12 가 50S 하위단위 체 하나에 네 개의 복사 등 이 있 다고 간주 하 면, 아미노산들의 총 수는 4 ,228 개이고 그 분 자 량은 46 0k d al 이 된다. 30S 단백 질들의 총 분자량과 16S rRN A 의 분자량을 합치 면 30S 하위단위 체 의 화학 적 분자 량 은 850kdal 이 된다. 50S 하위단위체에 대 해서도 단백질들, 23S rRNA . 및 5S rR NA 의 분 자량들 을 합치 면 화 학 적 분자량이 1, 450 kdal 이 된다. 두 하위 단위 체 들 의 분자 량들 의 합 에 서 E. coli 의 70S 리 보솜의 분자량은 2, 300 kdal 이 된 다. 결 합순 서 분석 으 로 결정한 30S, 50S, 및 70S 입자들에 대한 분자량들은 물리적 인 방법 으로 결 정 한 값들, 즉, 30S, 50S, . 및 70S 입 자 들 에 대 한 90 0-1, 000, 1, 600-1, 800, 및 2, 600 一 2, 900 kdal 의 값들보다 상당히 작 다 . 그 러 나, 티보솜에 존재할 금속 이온들 (M g 2+ 및 K+ )과 스퍼미던 둘 의 질량융 합 치면 실험오차 범위에서 찰 일치 할 것으로 생각한다. E. col i의 리보솜 단백질들 중 9 가지는 변형된 아미노 산들을 함 유하 고 있음이 확인되었다. S5, S18, 및 L17 둘의 N- 말단들이 아 세틸화 되 어 있으며 , S11, L3, L7/L12, L11, L16, 및 L33 둘이 메 틸 화되 어 있 다. 가장 많이 메틸화된 단백질은 L11 인데, 이 단백질은 그 사 슬 의 세 자리들에서 9 개의 메틸기를 함유하고 있다. 리보솜 단백 질들 의 변 형 은 번역 후에 일어난다. 리보솜 단백질들 중 결합순서가 분석된 것들로서는 E. col i 의 모든 단 백질들과 그밖의 9 가지의 다른 생체들로부터의 15 개의 리보솜 단백질 들과 관련된 2 개의 단백질들의 완전한 아미노산 결합순서가 결정되어 있다(표 2-3). 또한, 그밖의 많은 리보솜 단백질들의 부분적인 결합순 서 둘이 알려 져 있다 (Amons 와 Moller, 1980; Yag uc hi 와 Math e son,
표 2-3 E. coli 이의의 다른 생체들로부터의 리보솜 단백 질 들 ( 그리고 리 보송과 관턴된 생단백물 질 들 ) 중 완전한 결합단순 백서질가 밝혀진아잔 기 미것 망 . I EAoL. c오oo- 7 1l -단는 백질 Bacil lu s stc a roth e rmop lz i lu s BLlO 177 EL6 B. s/ca roth e r m op h i/1 1 s BL17 147 EL9 B. ste a rot/ 1er 111op lz i lu s BL29 104 EL24 B. ste a rotl ze rmop lz i lu s BL34 62 EL30 B. slearot/ 1e rmop h i/u s IF-3 183 IF-3 B. s/ca ro//1 e r11 1op lz i lus BSb 90 NS2 B. sublil is BL9 122 L7/L12 Mi cr ococrns lys o deik t i cu s MAl 118 L7/L12 1\J, lys o deik t i cu s MA3 128 Str e pt om y ce s gr is e u s A 126 L7/ L12 NRCC 11227 A 122 L7/Ll2 Halobacte r iw n cut irub nmz HL20 112 L7/L12 Saccharomy ce s cerevis i a e YP-Al 110 L7/L12 S. cerevis ia e YP44 103 S. cerevis ia e YP55 88 Arte m i a sali na eL12 111 L7/L12 쥐 (간) P3 104 L7/Ll2 1980; Ito h 동, 1980; Math e son 등, 1980; Hi go 등, 1980; ·wi ttm ann, 1982). 리보솜 단백질들의 아미노산 결합순서 분석 결과들을 다음과 같 이 요약할 수 있다• (1) B. ste a roth e rmop lzi lu s 와 B. subti lis 들로부터 의 염 기 성 및 산성 단백질들의 완전한 또는 부분적인 일차구조들이 알려쳐 있으므로, E. col i의 일차구조와 비교해 볼 수 있다. 대부분의 경우에 있어서 구조적 으로 높은 상동성 이 존재 한다. 상등성 은 B. subti lis 와 B. ste a rotl z ermo- p lz ifo s 둘의 리보솜 단백전들 사이에만 있는 것이 아니라, 그람-음성인 E. col i로부터의 단백질들과 두 가지의 그람-양성인 Bac i llus 둘의 단백 질들을 비교하였을 때도 검출할 수 있다. 부분적인 결합순서 분석 결과 와 완전 한 결 합순서 의 분석 결 과에 기 초하여 E. co/£ 와 Bacil l us 의 리 보솜 단백 질들의 상동성 을 찾아내 어 상호연관시 킬 수 있다. 그림 2-2 는 B. subti lis 로부터 의 단백 질 B-L9 과 E. coli 로 부터 의 단백 질 E-L12 의 완전한 일차구조를 비교해 본 것을 나타낸다. 두 단백질에 있어서 50%
이상의 아미노산 잔기들이 동일하다 . (2) E. coli 의 리 보솜의 L7/L12 단백 질 에 상응하는 산성 리 보솜 단 백질들인 〈 A- 단백질들〉이 비교칙 쉽게 탄리되 였 다. 현재 13 가지의
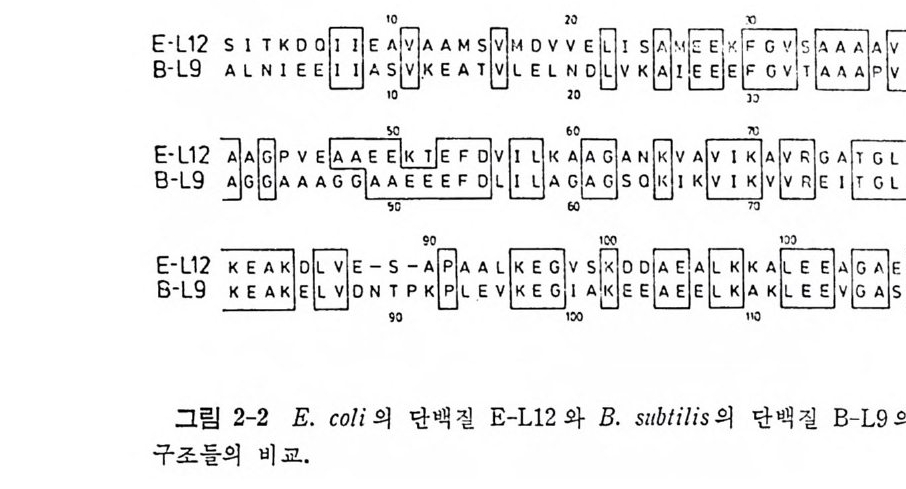 :접 ::;때:탑 :'1『:00 雲 t: ::2i2 0 달-:--『 醫,.,-言 --걷 ~: ~:
:접 ::;때:탑 :'1『:00 雲 t: ::2i2 0 달-:--『 醫,.,-言 --걷 ~: ~:
A- 단백질들이 박테티아, 식물 효모, 및 동물들로부터 단리되어 그 결합 순서가 완전히 또는 부분적으로 결정되었 다 (Ya g uch i 둥 (1980) 의 평론 서를 보라). 진성 박테티아들 사이에서뿐 아니라 E. col i의 L7 / L12 와 시금치로부터의 산성 리보솜 단 백질 사이에서도 강한 상동성이 존재한 다. 다른 한편, 진성 박테리아와 진핵세포들로부터의 A- 단백질들 사이 에 는 매우 약한 상동성이 있을 뿐이며, 반면에, 효모, 바다 새우, 밀 및 쥐 들과 같은 진핵세포돌에서 분리한 세포질에 있는 리보송의 단백질들 사 이 에 는 강한 상동성 이 검 출되 고 있 다 (W ittm ann-Lie b old, 198 0) . (3) 여러 생체들로부터의 리보솜 RNA 들에 관한 비교연구 들에 기초 하여 Woese 와 Fox(1977) 는 생물계를 세 가지로 분류 할 것을 가정하였 다. 즉, 진성 박테리아, 원시 박테리아, 그리고 진핵생체 둥이 그 제 가 지 아 다. 국도의 호염 세 균인 Halobacte r iu m cuti rub rum, 메 탄 세 군인 Meth a nobacte r iu m the rmoauto tro p hi u m , 그리 고 Sulfo l obus 와 Thermo- p lasma 들과 같은 그밖의 박테리아들이 원시 박테리아에 속한다. Halo- bacte r iu m 과 Meth a nobacte r iu m 으로부터 의 A- 단백 질 들을 단리 하여 결 합순서 를 부분적 으로 분석 해 보면, 그들 사이 에 는 강한 상동성 (56%) 아
있음이 발견되었다 (Ma t heson 등, 1980). 그들의 일차구조는 진성 박태 리아의 A- 단백질들, 특히 , 그람-양성 박테리아의 A- 단백질들과는 확연 히 다르며, 오히려 그들은 진핵세포의 A- 단백질에 더 가깝다. 예를 들 면 , Meta n obacte r iu m 의 A- 단백 질 과 효모의 A_ 단백 질 사이 의 상동성 (약 46% )은 두 진핵생체 Ar t em i a 와 효모 사이의 상동성과 거의 같다 . 이러한 결과들은, 적어도 몇 가지 진핵생체들의 리보솜 단백질들은 원 시 박테리아로부터 진화하였음을 암시해 준다(자세한 것은 Yag uc hi 등 (1980 ) 의 평론 서 를 보라) . 아마도 원시 세포가 초기에 진성 박테리아와, 원시 박테리아와 진핵 세포의 공통선조로 분기한 다음에, 이 공통선조는 두 가지 세포계로 분리되 었을 것으로 생각된다. 리보솜 단백질들의 N- 말단 의 아미노기들이 변형되어 있는 것들이 많 이 있다. S5, S18, 및 L7 등은 N- 말단이 아 세 틸화 되 어 있고, S11, L11 L16, L33 및 IF-3 들 과 같은 단백 질 들의 말단 아미 노기 들은 메 틸 화되 어 있다(표 2-4). 최근에 와서는 E. col i의 몇 가지 리보솜 단백질들에 대한 유전자들 의 DNA 결합순서가 결정되었기 때문에 누클레오티드 결합순서를 이미 발표된 아미노산 결합순서와 비교할 수 있게 되었다. L1, L7/L12,L11, 표 2-4 E. col i의 리보송 단백질들에 있는 변형된 아미노산들 단백질 위치 변형된 아미노산 단백질 위치 변형된 아미노산 S5 1 N- 아세틸 알라닌 Lll 1 N- 트리메틸 알라닌 S11 1 N- 모노메틸 알라닌 Lll 3 N,- 트리메틸 리신 S12 88 아스파르트산의 유도체 Lll 39 N, -트리메틸 리신 S18 1 N- 아세틸 알라닌 Ll6 1 N- 모노메틸 메티오닌 L3 150 N5- 모노메 틸 굳루타민 L16 81 아르기닌의 유도체 L7 1 N- 아세틸 세린 L33 1 N- 모노메틸 알라닌 L7/L12 81 N,- 모노메 틸 리 신 IF-3 1 N- 모노메틸 데터오닌 L14, S11, 그리고 S12 들과 같은 단백질들의 경우에는 완전한 일치를 보 여 주고 있지만, 단백질 S17 과 LlO 들의 경우에는 아칙 해결되어야 할 일치하지 않는 점들이 있다. 예를 들면, S17 의 63-65 위치들에 있어서 의 결 합순서 Arg- P ro-Cy s 이 DNA 결 합순서 에 서 유추한 Cy s- Arg- P ro 과 맞지 않는다 (Pos t 등, 1978; Post 등, 1979).
(4) E. col i의 돌연변이체의 리보솜 단백질들의 결합순서 분석. 이차 원 겔 전기이동법으로 E. col i의 많은 돌연변이종들에서 아미노산 치환 이 일어난 단백질들이 검출되었다. E. col i의 거의 모든 리보솜 단백질 들에 대한 돌연변이종들이 알려져 있다. 이 돌연변이종들은 대부분 그 들의 온도민감성 또는 항생물질들에 대한 그들의 반응성의 변화 등에 의거하여 분리되었다. 이러한 돌연변이종들로부터의 단백질들이 화학적으로 광범위하게 분 석되었다. 특히, 돌연변이로 변경된 단백질 S5 와 S12 가 집중적으로 분 석되었는데 그 결과들을 그림 2-3(A) 와 그립 2-3(B) 에 나타내었다. 그
림 2-3(A) 는 단백질 S5 에서 밝혀진 아미노산 치환들을 요약하였다. 스 패티노마이신 저항성 돌연변이체들에 있어서의 아미노산 치환은 이 단 백질의 19-21 위치에 몰려 있다. 아미노산 치환둘이 군집되는 현상은 네 아민 저항성 돌연변이체의 S5 와 에리트라마이신 저항성 돌연변이체의 L4 들에 서 도 발견 되 었 다 (W ittm ann 등 (1980) 의 평 론서 를 보라) • 그립 2-3(B) 는 단백질 S12 에 있어서의 아미노산 치환을 보여 준다. 이 결과에서 두 가지 결론을 얻을 수 있다. 첫째, 모든 치환둘은 단백 질 S12 의 두 개의 짧은 부분에 군집되어 있다. 즉, 42 번 위치와 85 一 91 번 위 치 에 서 치 환이 일 어 난다• 지 금까지 이 두 부분 이 외 의 다른 부분 에서 치환이 일어나는 것을 검출한 예가 없다. 둘째, 단백질 S12 의 단 한 개의 아미노산 치환으로 리보솜에게 스트랩토마이신 저항성을 줄 수 있다. 리보솜의 재구성 시험에서, 단백질 S12 만이 스트랩토마이신 처 항성을 변경시키는 데 관여한다는 것이 밝혀져 있으므로, 단백질 화학 적 분석결과로부터 E. col i의 리보송에 있는 7,336 개의 아미노산 잔기 둘의 단 하나만을 치환하여도 항생물질에 대한 리보솜의 반응을 변화시 킬 수 있다는 것을 알 수 있다. 2.3.2 리보솜 단백질들의 이차구조 리보송 단백질들의 이차구조에 관한 정보는 두 가지 점근법으로 얻을 수 있다. 그 하나는 아미노산 결합순서에 기초하여 예상하는 방법이고, 다른 하나는 원편광 이색분광법 (CD) 이다• 가) 이차구조의 예상 일차구조들이 알려진 리보솜 단백질들에 대한 이 차구조들을 예 상할 수 있 다 (W ittm ann-Lie b old, 1977) . a- 나사선 , 仕-병 풍구조, 마구잡이 코일, 및 회전 또는 굽음 등과 같은 형태적 상태들을 계산하기 위해서 네 가지의 다른 예상법들이 사용된다. 이러한 방법으 로 얻은 결과를 표 2-5 에 소개하였다. 예상법으로 결정된 네 가지 형 태적 상태들을 그림 2-4 로 예시하였다. 이 예에서는 두 개의 상동성 단 백질들 E-L7/E-L12 와 B-L9 를 비교하였는데 그들의 이차구조에는 상 당한 유사성이 있음을 볼 수 있다. 아미노산 잔기들의 형태적 상태에 있 어서, 네 가지 예상 중 적어도 세 가지가 일치할 때, 단백질의 특정한 부분에서의 특정한 구조가 생길 가능성이 가장 큰 것으로 간주한다.
표 2-5 아미노산 결합순서에 기초한 이차구조의 예상 . 단백질 |나사선% | 펴 \5구 조 1 회전% | 단백질 |나사선 %1 펴 \6구 조 1 회전% S3 25 12 17 Ll3 27 4 22 S4 28 4 18 Ll4 15 15 25 S5 34 8 18 L15 26 6 28 S6 36 4 10 L16 27 9 24 S7 38 5 13 L18 44 9 15 S8 36 5 14 Ll9 25 9 11 S9 18 6 20 L20 49 2 19 S10 19 5 12 L21 20 n.c. 23 S11 16 9 26 L22 28 6 11 S12 7 13 16 L23 35 8 14 S13 21 n.c. 19 L2 4 9 8 21 S14 34 n.c . 18 L25 42 10 10 S15 30 n.c. 14 L26 64 n.c. 5 S16 22 5 15 L27 10 6 30 S17 13 8 16 L28 22 14 16 S18 15 5 15 L29 67 n.c. 5 S19 15 6 25 L30 n.c . 9 2 S20 64 n.c. 5 L31 n.c. 5 24 S21 57 n.c . 4 L32 16 2 34 Ll 29 4 13 L33 33 6 15 L3 18 12 22 L34 17 n.c . 24 L5 26 6 15 IF-1 11 7 17 L6 24 10 17 IF-1 11 7 17 L6 24 10 17 IF-3 34-37 6-8 15-17 L7/L12 64 n.c. 3 NSl 43 n.c . 14 L1O 47 3 9 NS2 43 1 16 Lll 33 6 17 n.c. : 이차구조의 예상에서 얻은 결과들에 의하면 리보솜 단백질들은 각기 특다유는한 것 을이 차알구 조수를 있 다가.지 며많,은 그단밖백의질 들모의든 단경백우질 들a-의 나 사이선차 구함조량들은 과2 0다— 르40 %이다 . 예상한 펴진 구조의 함량은 20% 이하로 작지만, 예상된 회전 의 함량은 대부분의 단백질의 경우 10 一 30% 이다. 이 예상법들로 얻은 결과에 기초하여 리보솜 단백질의 삼차원 모형을
조립할 수 있다. 이 것은 전자계산기에 의한 산법으로 더 쉽게 할 수 있 다. 그러나, 삼차원 모형을 조립하려면 양성자 자기공 명법과 분자 내 교 차 결합에 관한 연구 들 로부터 단백 질 사슬의 접힘에 관한 정보들 이 더 보 충되어야 한다.
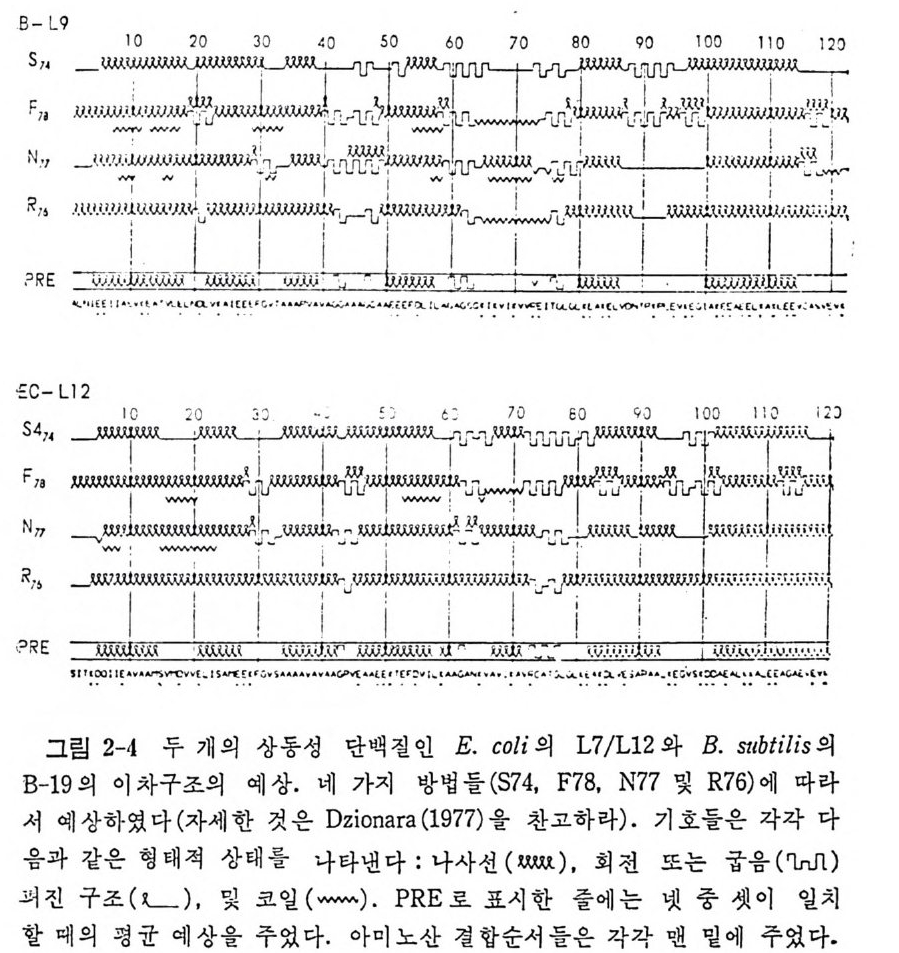 B- L 9
B- L 9
나) 원편광 이색분광법 리보솜 단백질들의 광회전분산 (ORD) 또는 원 편광 아색성에 관한 연구들이 많이 이루어져 있다. 단백질의 이차구조 에 관한 보다 정밀한 정보는 주로 원편광 이색분광법에 의한 연구들에 서 얻을 수 있다. CD 스펙트럼 분석에 사용한 리보솜 단백질들이 어떠
한 조건에서 추출되고 정제되었느냐에 따라서 결과가 크게 달라질 수 있 다. 아세트산으로 추출하고 우레아가 든 용액으로 용리한 S4 단백질과 염 용액으로 추출한 S4 단백질은 그 CD 스펙트림 들 이 다르다(그림 2-5 룬 보라). 아세트산과 우레아를 사용하는 경우에는 단백질들이 변성되 어서 a- 나사선 구조의 함량아 적어진다. 우례아와 아세트산이 존재하지 않는 온화한 조건에서 분리한 단백질의 경우에 있어서 실험적으로 측정 한 a- 나사선 구조의 함량과 예상하는 값이 매우 잘 일치한다. 그러나 몇 가지 단백질들의 경우에는 일차구조에서 예상한 a- 나사선 함량과 실 험치가 많이 어긋나는 경우도 있다. 그 이유는 아 직 장 모르고 있다. 현
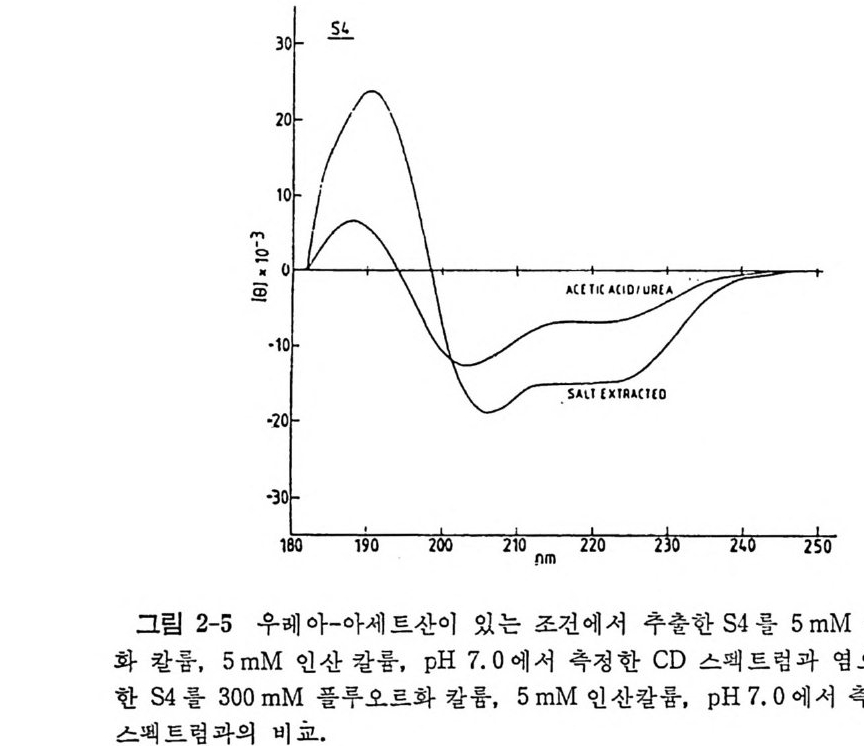 3200' 」 10노I
3200' 」 10노I
재까지 E. col i의 리보솜의 30S 하위단위체의 17 개의 단백질과 50S 하 위단위체의 18 개의 단백질의 CD 스펙트럼이 조사되었다. 이 연구들에 의하면 30S 단백질들은 a- 나사선 구조의 함량이 크고 f3-병풍 구조의 함 량은 작다. 다론 한편, 50S 단백질들은 f3-병풍 구조를 매우 많이 함유 하고있다.
2. 3. 3 리보솜 단백질들의 삼차구조 리보솜 단백질들의 삼차구조에 관한 정보를 얻기 위해서 아래와 같은 몇 가지 물리적 및 화학적 방법들이 이용되고 있다. 이를테면, 단백질 의 제한 가수분해, 양성자 자기공명, 단백질들의 결정화와 X- 선 분석, 형광분광범, 그리고 미량열계량법 등이다. 뒤의 두 방법들로는 별로 좋 은 결과룹 얻지 못하고 있으므로 처음의 세 방법들에 대해서만 기술하 고자한다. 가 ) 단백질 제한 가수분해 온화한 조건에 서 추출한 단백 질들을 단백 질 가수분해효소 들 로 0°C 에서 단시간 처리한 후에 가수분해되지 않은 저 항성 옹어리 입자들이 있는지를 알아보는 일을 하였다. 그 결과 많은 리 보솜 단백질들이 저항성 조각들을 낸다는것이 발견되었다. 그림 2-6 에 서 몇 가지 예를 보여 주었다. 가수분해에 대한 단백질들의 저항성에 따 라서 네 가지의 무리들로 나눌 수 있다. (1) 단백 질 S15, S16, S17, 및 L30 등은 여 러 가지 단백 질 가수분해 효소들에 대해서 완전한 처항성을 나타낸다. 양성자 자기공명법에 의하 면, 이들 바 가지 단백질들은 모두 뚜렷한 집힘 구조를 가지고 있다는 것을 보여 준다. (2) 단백 질 S1, S3, S4, S14, S20, S21, Ll, Lll, L16, Ll9, L25, 및 L28 동은 단백질 가수분해효소의 처리에 의해서 큰 조각들로 분해된 다(그림 2-6 의 몇 가지 실례를 참조하라). 조각들의 크기는 손상되지 않은 〈자연상태〉의 단백질의 69 ― 90% 에 상응하며, 일반적으로, 사용한 단백질 가수분해효소들에 무관하다. 이것은 가수분해 양식을 지배하는 것은 효소가 아니라 단백질의 구조라는 것을 암시한다. (3) 단백 질 S5, S7, S8, L3, L6, L23, L24 및 L32 들은 단백 질 가 수분해효소로 처리되면 비교적 작은 조각들(단백질 컬이의 25-60%) 을 낸다. (4) 단백 질 S2, S6, S9, L2, L27, L29 및 L33 들은 단백 질 가수분 해효소로 완전히 분해된다• 그러므로 이 단백질들은 집혀지지 않은 열 린 구조를 가지고 있음을 알 수 있다. 그런데, 이들 중의 하나인 L29 의 결정체를 분석한 바에 의하면 이 단백질은 a- 나사선 구조 또는 8- 병풍
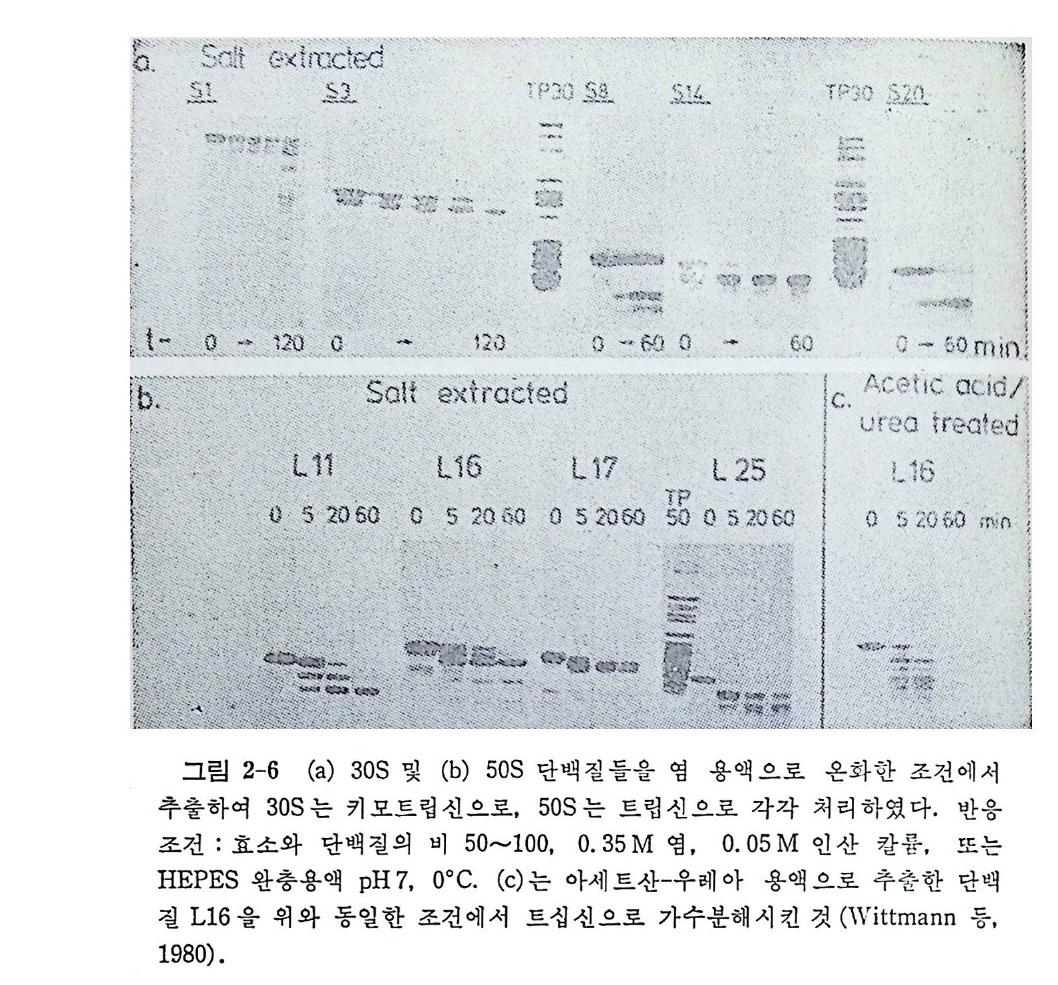 '.,.5S.r,’'·..웅' LtC .i ` `효 S론w’. l 라 、` `.f ~ }훈、 會 5e4 ‘ ` ..x •.Yi• 2t 7; ` \b i후.. GCi ;요 iEt .` `~. .•급.\~ ` `,、3t` : ~.•\’. . ;:..` : ..、 ` : r•.. , ; 0... · ....X. `. ... .t `t m 2_:1 .' ) ..댜 1합td., ek’. ..f~ .3 ,’:?• 、컵~` d2 一{ `, • 3 .,. 요..: $;,;.i\. ; ~.·노요_.. ,.~.~. ....,. 、, ,, .,.,, ~ ,, - 요 현E,t, -: 착,}J,,. ‘’ ;`0·;~' -尸` 뇨 .모. I ' ^• '.:,, ~ . i?.. .. 0g8 ' 't·'안E'.r`\'、, `•-' ;`같c!.;.下 ..t . •`.^•~·、, ,•`、'. •'•.E. ~ 一이 & ’: • !, 3수``• : .`' , 0 니 j ·. A 1( ·,C ‘ . , 후 S C小J,d ‘c 》 04 >t.占성.1lFfi· 1’ '쇼,t}I5 t tr·,3S 3·Res 0 & Q3i C mt 0fl. i.b”. 1 ,’0 i dv)/. 겨 '44;'·','~;';'; i,''i7',ai'/I';'i,'' 2'1,';i : .
'.,.5S.r,’'·..웅' LtC .i ` `효 S론w’. l 라 、` `.f ~ }훈、 會 5e4 ‘ ` ..x •.Yi• 2t 7; ` \b i후.. GCi ;요 iEt .` `~. .•급.\~ ` `,、3t` : ~.•\’. . ;:..` : ..、 ` : r•.. , ; 0... · ....X. `. ... .t `t m 2_:1 .' ) ..댜 1합td., ek’. ..f~ .3 ,’:?• 、컵~` d2 一{ `, • 3 .,. 요..: $;,;.i\. ; ~.·노요_.. ,.~.~. ....,. 、, ,, .,.,, ~ ,, - 요 현E,t, -: 착,}J,,. ‘’ ;`0·;~' -尸` 뇨 .모. I ' ^• '.:,, ~ . i?.. .. 0g8 ' 't·'안E'.r`\'、, `•-' ;`같c!.;.下 ..t . •`.^•~·、, ,•`、'. •'•.E. ~ 一이 & ’: • !, 3수``• : .`' , 0 니 j ·. A 1( ·,C ‘ . , 후 S C小J,d ‘c 》 04 >t.占성.1lFfi· 1’ '쇼,t}I5 t tr·,3S 3·Res 0 & Q3i C mt 0fl. i.b”. 1 ,’0 i dv)/. 겨 '44;'·','~;';'; i,''i7',ai'/I';'i,'' 2'1,';i : .
구조륭 많이 가지고 있다는 것을 보여 주고 있으므로, 이 단백질은 이 차구조를 분명히 가지고 있음을 가리킨다. 이러한 모순된 문제는 앞으 로 더 연구되어야 할 것이다. 두번째와 세번째 무리에 속하는 단백질들을 가수분해하여 얻는 조각 들을 분리하여 구조적 및 기능적 연구들에 사용할 수 있다. 메티오닌 다 음의 펩티드 결함울 특이하게 결단하는 CNBr 와 같은 시약들을 사용하 여 단백질들을 화학적으로 처리함으로써 추가적인 조각들을 얻을 수 있 다. 이러한 방법으로 단백질 S1 으로부터 몇 개의 조각들을 분리하였으 며, 이 조각들과 효소 처리로 얻은 조각들의 생물학적 기능을 분석하는 데 사용하였다 (Subramania n , 1981 ; Gi er gi ni s , 1980) . 557 개 의 아미 노
산 찬기들을 가진 단백질 Sl 의 N- 말단 부분 (1 번一 193 번)은 리보송 결 합 영역에 상응하며, Sl 의 중 앙 부분 ( 224 번— 309 번)은핵산을결합하는 영역이라는 것이 밝 혀 졌 다. 약 150 개의 아미노산 찬기들로 이루어지는 c- 말단 부분은 별로 중 요 한 기능을 하지 않는 것으로 생각된다. 그 이 유는, 이 부분이 결 여된 Sl 분자 를 가진 돌연변이체들이 거의 정상적으 로 자 랄 수 있기 때 문이 다 (Subramania n 과 Mi zu shim a, 1979) . 위 에 서 말 한 S1 상의 기능 영역들은 X- 선 산란 실험둘로 발견된 결과들과 잘 일치한다. Bacil lu s ste a rotl zer m op hi l u s 에 서 추출한 단백 질 들을 단백 질 가수분해 효소로 치리하여 저 항 성 조각들을 내는 능력을 시험해 보았다 (A pp el t 동, 1979). 대 개 의 경 우, 이 단백질들은 E. col i에 있어서의 상응하는 단백질 들 보다 저항성 이 훨 씬 더 컸 다. 시험해 본 모든 고온성 단백질들 은 완전히 가수분 해되 는 것이 하나도 없었다. 아마도 이 단백질들은 〈보 다 단단한〉 구조 를 가지고 있는 것으로 보인다. 결정화된 단백질 B-L17 은 위에 말한 시 험조 건에서 완 전한 저항성을 가지고 있다 (A pp el t 동, 1979). 나) 양성자 자기공명 ( PMR) 고분해능의 기기를 사용한 PMR 분광법은 단백질 분자들의 삼차구조를 분석할 수 있는 강력한 방법이 되고 있다. 아미노산 곁사슬둘은 어느 정도의 가등성을 가지고 있으므로 변성된 단 백질들의 경우와는 달라서 명확한 삼차구조를 가지고 있는 단백질들의 스펙트럼둘의 공명은 일반적으로 널리 퍼진 상태를 나타낸다. 소수성 아 미노산 결사술들의 무극성 메틸기들과 방향족 아미노산들(특히 트립토 판) 사이의 상호작용은 PMR 스펙트럼의 상장 부분 (0~l pp m) 에 있어 서의 고리-전류 효과로 일어나는 공명 발생위치의 이동과 6~9p pm 부 분에 있어서의 방향족 고리의 수소 원자들의 섭동된 공명에 의해서 알 아낼 수 있다. 그뿐 아니라 단백질 분자의 삼차구조에 있어서의 히스티 딘의 환경에 관한 정보를 얻을 수 있다. E. col i의 리보송의 여러 단백질들에 대한 PMR 분광범에 의한 분석 과 단백질 가수분해에 의한 처항성 응어티의 형성을 서로 비교해 본 결 과 찰 일치한다는 것이 알려져 있다. 예를 둘면, P.M R 분광범으로 S15, S16, S17 및 L30 들은 명확한 삼차구조가 있다는 것을 알 수 있는대, 실제로 이 단백질들은 단백질 가수분해효소들에 대해서 완전한 저항성
올 가지고 있었다. 이와 반대되는 경우에도 양성자자기 공명법이 매우 정확하다는 것을 발견하였다. 죽, PMR 스펙트럼의 분석에 의하면 S6, 12, L27 및 L29 등의 단백질에는 촘촘한 구조가 있다는 중거를 찾아 볼 수 없는데, 실제로 이 단백질들은 단백질 가수분해효소들에 의해서 완전히 가수분해된다. 단백질을 효소적으로 또는 화학적으로 분해하여서 얻는 조각 둥에 대 한 PMR 분석을 함으로써 단백질의 어느 부분이 찰 형성된 삼차구조를 가졌는지 를 확인할 수 있다. 예 를 들면 단백 질 S4 의 C- 말단의 조각 (Newberry 등, 1977) 과 Lll 의 N- 말단 부분 (Tumanova, 1981) 이 〈자 연상태의〉 분자에서 관찰되는 구조의 대부분을 함유하고 있음이 알려졌 다(그림 2-7 을 보라).
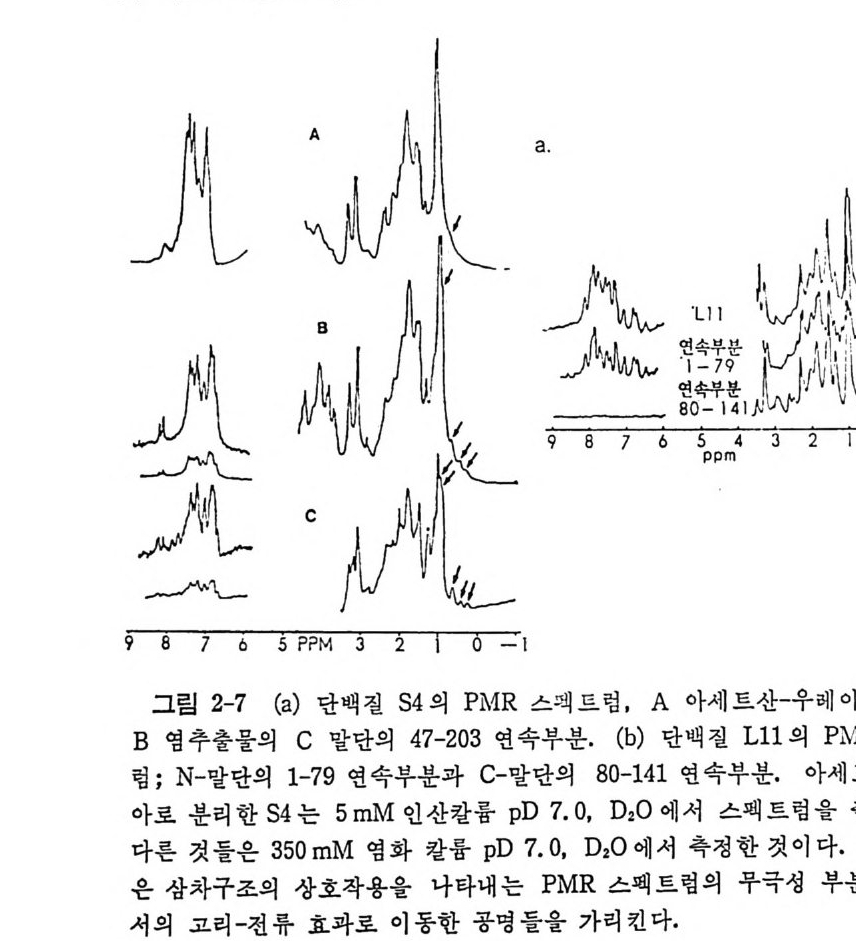 j!L IIhII a b
j!L IIhII a b
다) 결정체화 단백질들의 삼차구조 를 알 기 위한 가장 직 접 적인 방법은 대단히 어렵기는 하여도 결 정 체 를 얻어 서 X- 선 회절법으로 구조분 석 을 하는 것 이 다. 지 금 까지 는 L7/ L 12 복 합체 의 N - 말 단 및 C- 말단의 조각 둘의 구조가 이 러 한 방법으로 각 각 4A 과 2.6 A 의 분 해능 으로 분 석 되 어 있다. L7/Ll2 조 각들 이의에도 E. col i의 L29 가 결정체로 얻어졌다. 그리 고 Bacil lu s ste a r oth e r n zop hi l u s 의 B-L17, B-LlO, 및 B-L34 단백 질 들 이 견정체 화 되어 그 구조 들 이 분 석 되 었 다 (App el t 등, 1979; Ap pe lt 등, 1981). 2.3.4 리보솜 단백질들의 모양 리보송의 큰 하위단위체와 작은 하위단위체의 단백질들의 용액에 있 어서의 입체 모양아 X- 선 산란과 중성자 산란 등의 방법과 침강, 확산, 및 점성도 측정 등과 같은 유체역학적 방법들을 병용하여 결정되었다 (Brim acombe (1978) , G i r i등 (1979) , W ittm ann-Lie b old 등 (1980) , Ser-dy uk 등 (19 8 1 ) 의 평 론서 를 보라) . 일반적으로, 아세트산과 우레아 를 사용하지 않는 온화한 조건에서 단 리한 단백 질들 을 가지고 모양 분석을 한다. 지금까지 조사된 바에 의하 면, L17, L25, L28, L29 및 L30 둘은 촘 촘 하고 대칭성을 가지고 있으 며 , L2, L3, L9, L11, L15, L23, L27, L28 및 L30 들은 뻗 친 구조를 가지며, L24 는 위의 두 구조의 중간 정도의 구조를 가지고 있음이 알 려져 있다. 최근에 와서 중성자 산란법을 사용하여 리보솜 내에서 자리잡고 있는 원래의 상태에서의 단백질들의 모양을 결정할 수 있는 칙접적이고 재로 운 대 조변 차범 (contr a st varia t i on tec hniq u e) 이 라는 방법 이 개 발되 어 50S 하위 단위 체 의 단백 질 들에 응용되 었 다 (Moore, 1980) . 이 방법 의 원 리는 E. col i를 각각 76% 와 84% D20 에서 기른 다음에 76% D20 에서 기른 세세포에서 추 출 한 리보솜 RNA 와 86% D20 에서 기른 세포에서 추출한 리보솜 단백질들로써 50S 입자를 재구성한다• 각각 76% 와 84% D20 에서 자란 세포들에서 얻는 50S 하위단위체와는 달라서, 중성자 선 속에 대해서 균일한 성질을 가진 50S 하위단위체를 이러한 방법으로 얻 을 수 있다. 만일 이렇게 재구성된 50S 입자에 있는 단백질들 중 하나
가 진적으로 가벼운 수소 를 가진 것 으로 대치되 어 있다고 하면 , 중성자 산란법으로 그 단백질의 회전 반 지음을 결정할 수 있을 것 이다. 이 러 한 방법으로 50S 에 자리참고 있는 상태에서의 L 4 의 회전 반지 름 이 20 土 2A 으로 결정 되 었다. 이 값은 축 비 율 3 : 1 에 상응한다. 이 방법을 옹 용함으로써 리브솜 입자 내에 있는 찮 은 단백 질들의 모 양을 결정할 수 있을 것이며, 그 밖의 방법으르 용액에서 의 리보 습 단백 철문 의 도양 을 결정할 때 경험하게 되는 어려 움을 피 할 수 있 을 깃 으로 생각핀다 . 2.4 원핵세포의 리보솜의 RNA 들 박테 리 아의 리 보솜의 질 량의 약 2/3 정 도가 리 보 습 R:\' .. \ (rR :\ .. \) 들 로 이루어져 있다. rRNA 들에 관한 연구는 최근에 와서야 알발하게 연구 를 하기 시작하였다• 지금은 rR:,;'A 둘의 구조와 기능 의 중요한 것둘 이 많이 밝혀 져 있다. 16S 및 23S rR;,;A 들의 일 차구조 를 밝히 기 위 해 서 그 동안 상당한 노력을 하였음에도 불 구하고 중요한 결과를 얻지 못하 고 있었지만, 최근에 RNA 및 D~A 의 염기 결합순서 를 신속하게 결정 할 수 있는 여러 가지 훌륭한 방법들이 개발됨으로 씨 rRNA 들의 신속 한 구조 결정의 돌파구가 열리었다. 리보솜 단백질들의 경우에 그 러했 던 것과 같이, rRNA 들의 이차구조, 삼차구조, 리보 솜 입자 내에서의 그들의 공간 배열, 그리고 그들의 기능을 알기 위해서는 우선 rR NA 둘 의 일차구조의 결정이 선결문제이다. 몇 년 전까지만 하여도 rR I\ A 들 은 리보솜 조립을 위한 발관 이의의 다른 구실을 하지 않는 것 으로 인 정 되 고 있었지 만, 오늘날 rRNA 들은 mRNA 및 tR N A 들과의 결 합 , 리 보솜 하위단위체들의 희합, 그리고 항생물질들에 대한 저항성의 부 여 등 리보솜 상에서 일어나는 단백질 생합성의 많은 과정에 직접 참여하 고 있 다는 것이 밝혀져 있다. 뒤의 소절들에서 5S, 16S, 23S rRNA 둘의 구 조, 이 rRNA 들 상호간의 작용, 또는 이 rRNA 들과 리 보솜의 다른 성 분들 사이의 상호작용을 알아 보자. 2. 4. 1 5S rRNA 가) E. co li로부터의 5S RNA 5S rRNA 는 작은 RNA 로서 원핵세포와
진핵세포의 리보 송 의 큰 하위단 위체 에 결합 되어 있다. t RNA 들과 거의 같은 크기 의 R N A 이지 만 , 원핵 세 포의 5S rR N A 는 t RNA 들에 서 볼 수 있는 바와 같은 변형 된 누 클레 오 지 드 들을 가지고 있지 않다. 16S 와 23S rRN A 들에 비 해 서 5S rRN A 는 120 개 의 누 쿨 레 오티 드를 가 진 작 은 분 자 이 며 세 가 지 리 보 솜 단 백 질 들 과만 상호작용한다. 그러 므로, 이 차구조와 삼차구조 그 리 고 결 합하 는 세 가지 단 백 질 들 과의 상 호 작용 등운 16S 와 23S rR N A 들의 경우 보다 더 쉽게 연구 할 수 있다. RXA 의 일 차구조를 분석 하 는 좋은 방법 들 이 많 이 개 발 되 어 있으므로 (l\fox a m 과 Gi lb e rt , 197 7; Sta n ley , 1978 ; Gup ta 와 Randerath , 1979; Peatt ie , 197 9 ) 5S rRKA 의 일 차구조 는 여 러 생 물종둘의 것 들이 많이 분 석 되 어 있 다. 지금까지 일차구 조 가 분석 된 5S rRNA 의 수는 원핵세 포 의 것만도 약 100 가 지 정 도나 된다 (1983 년까지의 분석치들은 Erdm- ann 등 (19 8 3) 의 수 록 웅 참 고하라 ) . 화학적 및 물리적 방 법들에 의 한 여러 가지 분석들과 진화론적 비교 들 에 기초하여 이 차 구조 에 대한 몇 가지 모 형 들이 제안되었다. 몇 가지 도 형들을 그 림 2-8 에 나 타내었다 . 효모의 알라닌 t RNA 에 대한 클로버 잎 모양 의 이 차 구조 모 형 이 발 표된 이 후 로 이 모형이 많은 t RNA 들에 대 해 서도 옳 다는 것 이 증 명 되 었 다. 5S rRN A 들에 대해서도 염기 짝지 움이 최대한 이 되도록 배열함으로써 그들의 이차구조의 모형을 만들어 보고자 시도하였다. 제안된 모 형 들이 타당한 것인지 아닌지는 핵산 가 수분해효소에 의한 반응성 또는 핵산 염기들에 득이하게 작용하는 시약 들에 의한 반응성 ( 예, 이차구조의 고리부분에 있는 구아닌 영기에 독이 하게 반응하는 케독살 또는 글리옥살) 등을 조사함으로써 확인하였다. Fox 와 Woese(l975) 의 E. col i의 5S rRNA 에 대한 모형과 그 밖의 모 형 들을 그립 2-9 에 나타내었다. 나사선을 이문 부분이 네 군데 있는 것 이 이 모 형 의 특칭 이 다. 그러 나 Luhrsen 과 Fox (l981) 는 사람의 • 5S rRNA 에 대해서는 나사선 부분이 다섯인 모형을 제안하였다. 최근에 De Wachte r 등 (1982) 은 원핵 세 포와 진핵 세 포의 5S rRNA 들에 대 해 서 다 적용이 될 수 있는 이차구조를 제안하였다(그림 2-8 의 C 와 f를 보 라) . De Wachte r 동아 제 안한 E. coli 의 5S rRNA 와 Drosop hi l a me!- anog as te r 의 5S rRNA 에 대 한 모형 들을 그 림 2-10 에 나타내 었 다. 핵 산 가수분해효소에 의한 처리는 이돌이 제안한 모형의 고리 부분에서만 일어 난다는 사실 , 수소 (삼중수소) 교환은 제 안한 나사선 부분에 서 제 일
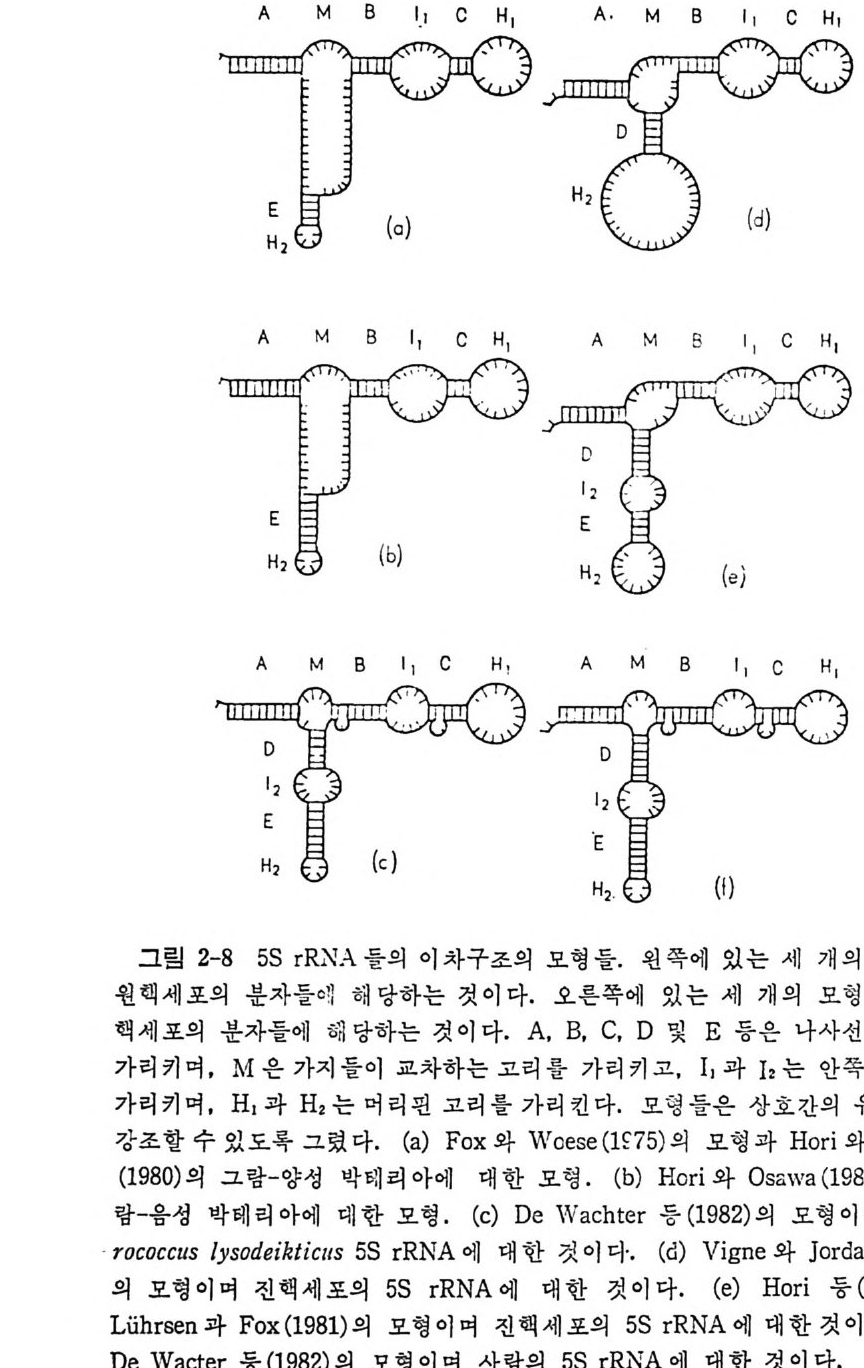 A M B 1_1 C H1 A, M 8 I 1 C H1
A M B 1_1 C H1 A, M 8 I 1 C H1
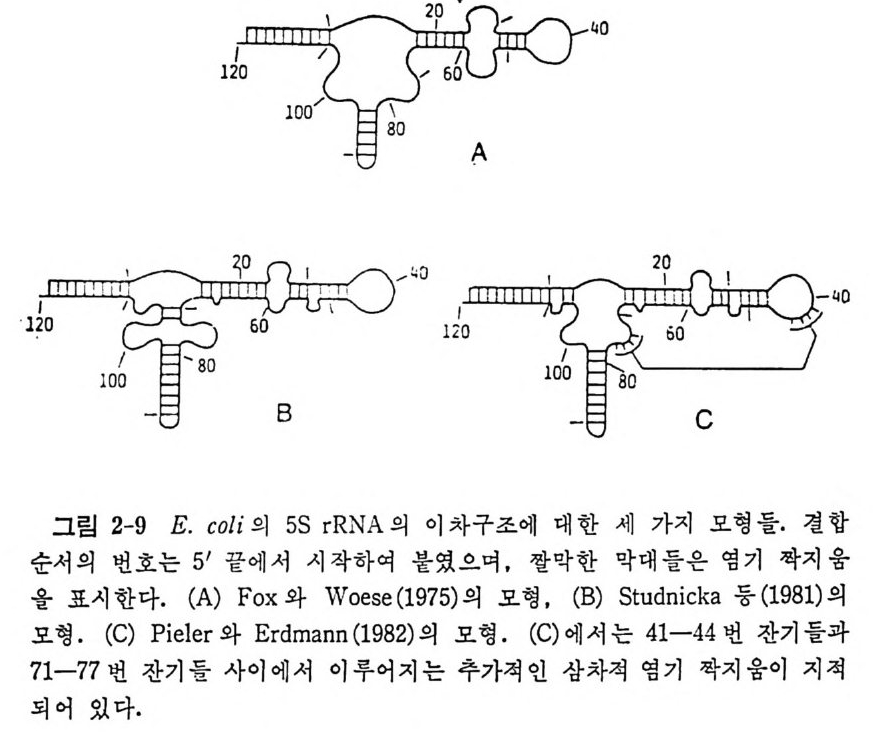 40
40
느리게 일어나는 사실, 케독살에 의해서 변형되는 구아닌 영기들은 제 안한 고리 부분에 서 만 일 어 나는 사실 , 또한 프소랄렌 (ps oralen) 에 의 한 U 와 U 사이 의 교차구결 합의 분석 결 과가 Thomp so n 동 (1981) 의 실 험결과와 완전히 일치하는 점들로 미루어 보아 이 모형들은 매우 홍미있 는 것이라고 생각된다. 여러 연구진에서 제안한 5S rRNA 의 모형들을 비교해 보면 중요한 구조적 특징들에 관해서는 대부분 의견이 일치하고 있지만, 5S rRNA 의 이차구조와 단백질들을 결합하는 자리들에 관해서는 몇 가지 차이점 이 있다. 이러한 차이가 생기는 이유는 아마도 시험재료로 사용한 5S rRNA 와 리보솜 단백질들의 성질의 차이, 사용한 완충용액의 조건 (M g 2+ 의 농도, pH 및 온도)의 차이, 연구진에 따라서 얻은 실험결과 들을 어디에다 중점을 두고 해석하는가 등에 따라서 생길 것으로 생각 된다. 최 근에 Piel er 와 Erdmann (1982) 은 E. coli 의 5S rRNA 에 대 한 재 로
운 이차구조의 모형과 삼차구조의 모형을 제안하였다. 그들은 단일 가 닥으로 된 고리 부분에 목이 하게 작용하는 핵 산 가수분해 효소 Sl 과 나사 선 부분에 만 목이 하게 작용하는 코브라 독액 의 핵 산 가수분해 효소 (Naja naja oxia n a) 로 5S rRNA 또는 5S rRNA • 단백 질 (E-L5, E-Ll8 및 E- L25) 복합체들을 처리한 결과에 기초하여 새 모형들을 제안하였다. 그 둘의 분자 모형의 크기 80x140A( 그립 2-llB 를 보라)은 낮은 각 중 성 자 산란법 (Lorenz 등, 1980) 과 전 자현 미 경 법 (Tesche 동, 1980) 으로 측정한 값과 일치할뿐 아니라, 5S rRNA· 단백질 복합체에 있어서의 E- Ll8 과 E-L25 의 질량 중심돌 사이의 거리가 75-85A 로 측정되었는데 (Lorenz 동, 1980) 아것도 그둘의 모형 상에서의 거리와 칸족스럽게 일치 한다. 이들이 제 안한 이 차구조의 모형을 그립 2-10 과 그립 2-12 로 냐 타내었으며 삼차구조와 기능 영역들을 그림 2-11 로 나타내었다. 보존되어 있는 누클레오티드들은 대부분 영기 짝지움을 하지 않은 부 분에 있으며, 몇 개의 보존된 〈내밀린〉 아데닌들 (E. col i에서는 아데닌 -52, -53, -57, -58, 및 -66) 이 있는데, 이돌은 단백질들의 인식 또 단 백질과의 상호작용과 관련이 있을 것으로 생각된다. 여러 가지 접근법으로 연구를 하였지만 5S rRNA 의 기능에 관해서는 별로 알려진 것이 없다. 현재로서는 다소 간집적인 실험중거에 근거한 · 것이기는 하지안 5S rRNA 는 t RNA 를 리보송의 A 자리에 결합시키는 기능을 가지고 있다고 생각되고 있다. E. col i의 5S rRNA 의 42-47 번 위m e치g a의 t e r iCu mC G 둘A의A C5 S 연r 속RN부A분, 의 B40a—c il4 l5u s번 st위e a 치ro 의th e rCmCoGp hAi Al u Cs 와연 속B부ac분il lu 들s 은 원핵 세포의 tR NA 의 GT,f rC -R 연속부분과 상호작용할 수 있을 것으 로 생각된다 (Erdmann, 1976). 그러나 t RNA 의 T, frC G 부분과 5S rRNA 의 CCGAAC 연속부분 사이의 상호작용을 확증할 수 있는 UV- 교차결 합과 같은 증거는 없다. 최 근에 와서 Erdmann (1976) 의 가설 은, GAAC 연 속부분이 제 거 된 5S· rRNA 를 가지고 있는 리브송을 이용하여 시험관 내에서의 합성한 풀리 (U)의 번역 실험을 실시해 본 결과, 이에 의하여 도전을 받기 시작숭) 였 다 (Pace 등, 1982) . 이 연구진은 아 연구를 더 자제히 시행하여 GAAC 연속부분이 단백질 합성에 있어서 필수적인 것이 아니라는 것을 증명하였다 (Za g orska 둥, 1984) .이들은 5S rRNA 의 GAAC 연속부분이 여러 가지 방법으로 절단
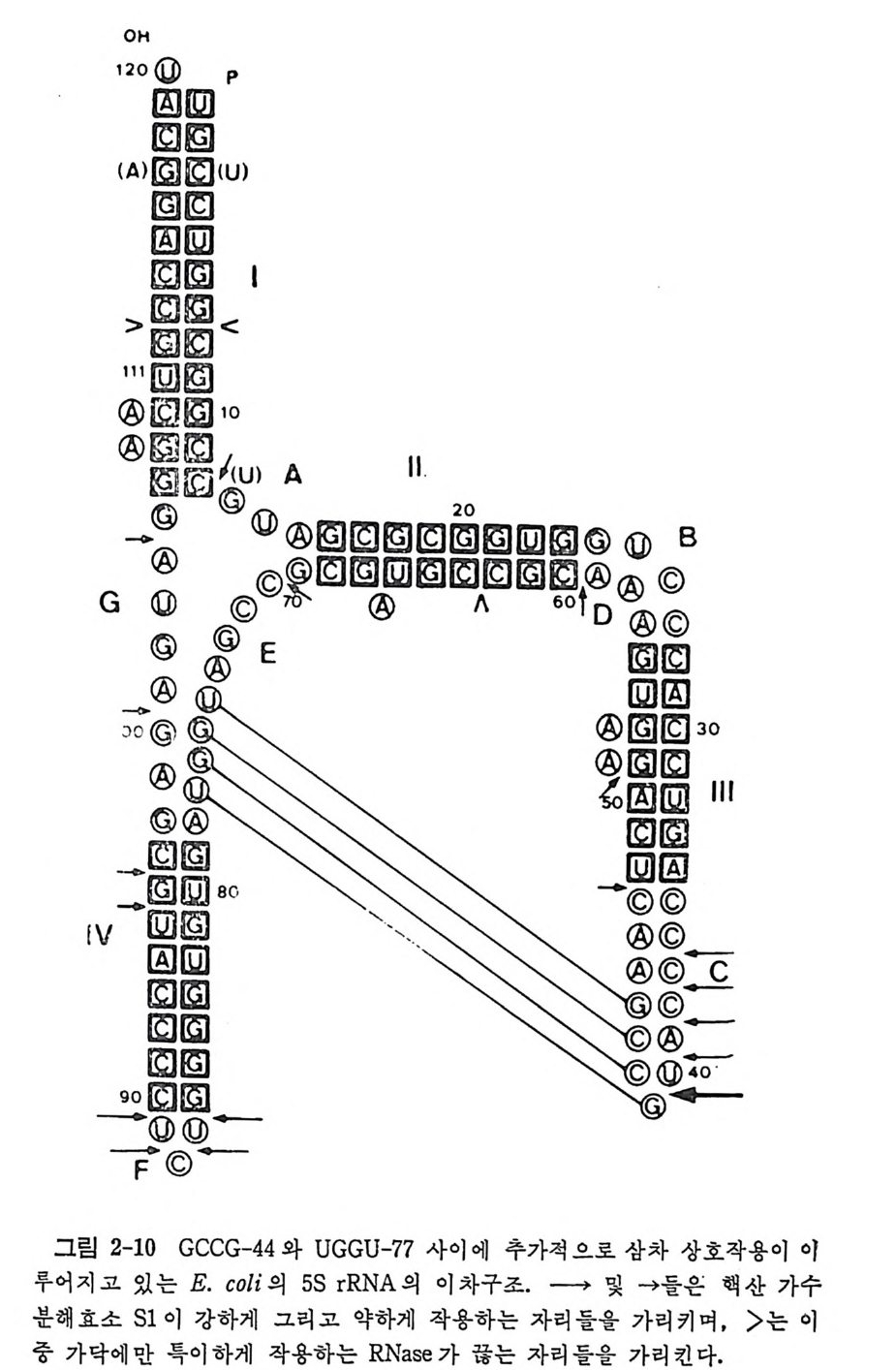 OH @mlEEEEEEEE3E2=
OH @mlEEEEEEEE3E2=
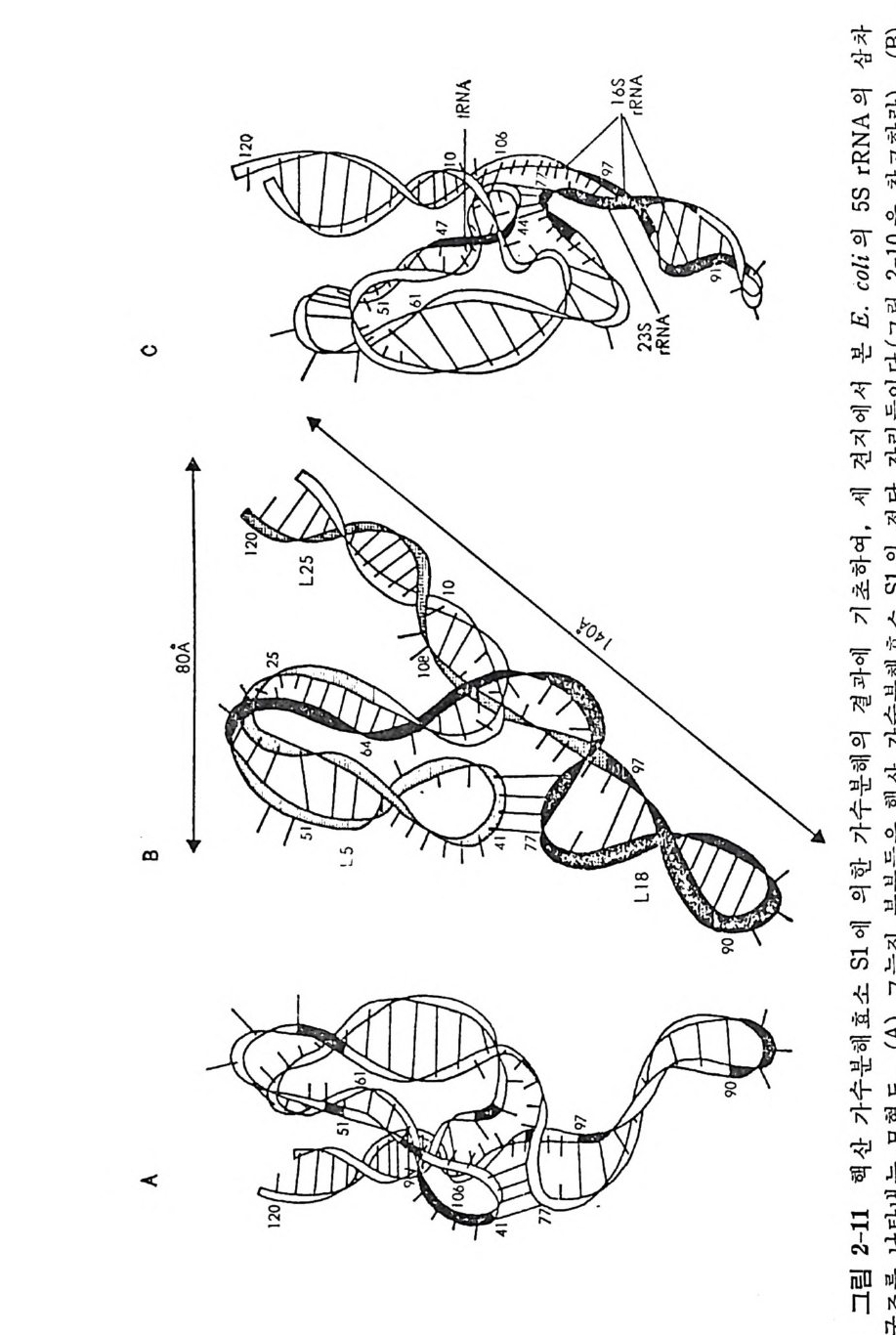 c A B0k 8S해삼서oc분 가 .r 산 5 ,수세 기핵S한EN그1R하본 1과초분의 1l차에의에-A의견에 의 해지i소가2림결여수효 )A) (B( 는그.조)를효분타 다산1- 들 나리해0진자 부(수참 내라핵단분가모을도 립의 2소은.1구 형 그늘고절 하들 S이 (. C1 - E-EL,,L85E )합산결추 이 둘를5서L다E에수 형 체였치 자하한전 모립 조 의시과분자들분2 .한-하는 분부표 및 23n )9 79),.m1a5,dSc6ad9r7 (A ,Arero(ElloS61N9l ANAR r1 5NrRReHN (ASnN,1Rr zr)7 it 와 와 이의 고리들 그사 정추 로으것 있 용.작호다상킨 서에리가 이윤들분을부 는있 고되
c A B0k 8S해삼서oc분 가 .r 산 5 ,수세 기핵S한EN그1R하본 1과초분의 1l차에의에-A의견에 의 해지i소가2림결여수효 )A) (B( 는그.조)를효분타 다산1- 들 나리해0진자 부(수참 내라핵단분가모을도 립의 2소은.1구 형 그늘고절 하들 S이 (. C1 - E-EL,,L85E )합산결추 이 둘를5서L다E에수 형 체였치 자하한전 모립 조 의시과분자들분2 .한-하는 분부표 및 23n )9 79),.m1a5,dSc6ad9r7 (A ,Arero(ElloS61N9l ANAR r1 5NrRReHN (ASnN,1Rr zr)7 it 와 와 이의 고리들 그사 정추 로으것 있 용.작호다상킨 서에리가 이윤들분을부 는있 고되
0
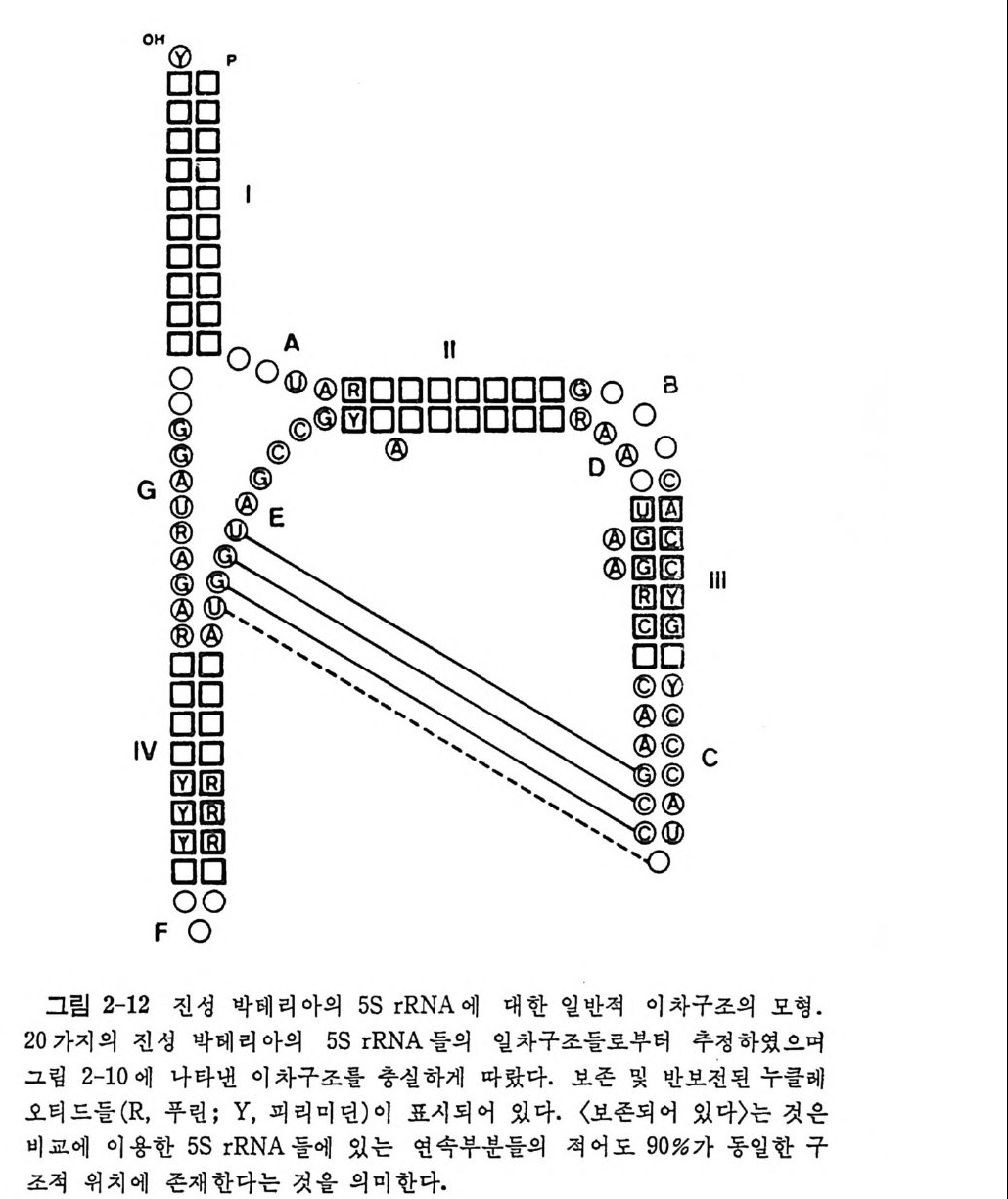 0®OOp OOOGOOOOD00@@®@V®®@®®0D00 (8(818Do
0®OOp OOOGOOOOD00@@®@V®®@®®0D00 (8(818Do
되거나 제거된 것을 가지고 있는 50S 하위단위체를 재구성하게 되며, 이 재구성된 50S 하위단위체를 가지는 리보솜 입자 상에서의 MS2 RNA
의 번역을 시험관에서 시 험하 였다. 그 분석 결과를 표 2-6 에 싣기는 하였으나 이 연구진은 동시에, 같 은 실험조건에서 Ap U p G 또는 MS2 RNA 의 지시에 의한 flVI et -tRN A 의 결합과 pp G pp의 합성이 상딩히 감소된다는 사실을 관찰을 동해 알 표 2-6 5S rRNA 변조물 을 함유한 리 보솜에 의 한 MS2 RNA 의 번역 . 실험 I 재구성된 5S rRNA I 제거된 연속부분 〔先\ 젊 e 활 동성 I cp m % 1 손상되 지 않은 5S rRNA 7860 100 2 1-41/42-120 i 5700 72 3 1-41/47-120 CCGAA-46 5007 64 4 1-41/53-120 CCGAACUCAGA-52 5314 67 5 5S rRNA 를 첨 가하지 않음 987 13 6 50S 삭제 220 3 7 MS2 RNA 를 첨 가하지 않음 199 3 8 자연의 50S 7875 100 게 되 었 다. 그 러 므로, Zag o rsk 등 (1984) 의 발견 은 tR NA 의 GT,[ rC 연 속부분과 리보솜의 어떤 자리와의 상호작용이 있는 것은 확실 하지만, t RNA 와 5S rRNA 의 GAAC 연속부분 사이에 존재할 것으로 생각되던 상호작용은 일어나지 않는다는 것을 결정적으로 증명해 주는 것이라고 생각된다. 5S rRNA 가 결여된 전적으로 재구성된 리보솜 입자의 기능분석을 하 였다. 이 리보솜 입자는 EF-G 의존성 GTPase 의 활동성을 완전히 가 지고 있었지만, 펩티딜 기 전달효소의 활동성과 리보솜의 P 자리에 tR NA 를 결합시키는 활동성은 철저하게 감소되어 있었으며, t RNA 를 A 자 리에 결합시키는 활동성이 전혀 없었다. 따라서 5S rRNA 는 EF-G 의 존성 GTPase 의 활동성에 있어서는 아무런 역할을 하지 않지만 펩티딜 기 전달효소의 활동성과 t RNA의 P 자리에의 결합에는 중요한 역할을 하고 있으며, 또 t RNA 의 A 자리에의 결합에 직접 관여할 가능성이 있다는 것 을 보여 주는 것 이 다 (Dohme 와 Ni er haus, 1976) . 이 실 험 의 뒷 부분의 결과는 t RNA 의 고리 N 에 있는 GT,[ rC 연속부분과 5S rRNA
에 있는 CCGAAC 연속부분이 리보송의 A 자리에서 상호작용한다는 것 을 암시해 준다 . 앞에서 이미 기술한 바와 같이 , 단백질 L5, L18, 및 L25 둘이 5S rRNA 와 결 합한다는 것 이 밝혀 져 있 다 (Er dmann, 1976) . 최 근에 는 네 번 째 의 단백 질 로서 L31a 가 결합한다는 것 이 밝혀 졌 다 ( Fann i n g 과 Traut, 1981) . 이 단백 질들 은 적 당한 조건 에서 는 5S rRNA 와 협동적으로 또 화 학양론적으로 결합 하며, 5S rRNA 는 단백 질 과 결합함으로씨 형태가 반 한다는 것 이 알려져 있다. 티보솜 단백전등의 결합 으로 유발되는 5S rRNA 분자의 형태의 변화 는 mR NA 와 리보 솜 사이의 상대적 움직임의 원인이 되는 것으로 가정 되고 있다 (Erdmann 등, 1980). 이 가설 은 홍 미있고 또 이것을 뒷받침하 는 약간의 실험결과들도 있지만, 이것을 확신 하기 위해서는 더 많은 실 험적 증거둘이 요구되고 있다. 5S rRNA- 단백 질 복합체 가 형 성 됨 으르 써 5S rRNA 의 형 태 가 변하는 문제와 관련하여 P i e l er 와 Erdmann(1982 ) 의 실험결과는 매우 홍미있는 앙시를 제공해 준다. 핵산 가수분해효소 Sl 이 주로 작용하는자리는우 리 딘 -40 부근이 기 때 문 에 , E-LS, E-Ll8 및 E-L25 들이 존재 할 때 5S rRNA 의 가수분해가 어떻게 달라지는지를 분석해 보았다. E-L5 와 E- L18 을 첨 가하면 핵산 가수분해효소 Sl 에 의한 5S rRNA 의 결단이 방해 되 지 만, E-L25 를 첨 가하여 도 아무런 효과가 없다 (표 2-7) . E-LS 의 결 합에 전혀 영 향을 미치지 않는 E-L25 는 놀라운 영 향을 미친다. 죽 E- L5 만이 있을 때의 핵산 가수분해효소 S1 의 작용의 방해를 없애버린다• (표 2-7). 표 2-7 에서 보는 바와 같이 세 가지 단백질이 다 함께 있을 때 우리딘 -40 에서의 가수분해의 방해효과가 제 일 크다는 것을 알 수 있다. 이 결과는 5S rRNA 의 중앙 부분이 특히 E-L5 와 E-Ll8 에 의해서 중 요하게 형태 변화를 받는 부분이라는 것을 말해 준다. 그림 2-11 의 B 와 C 로부터, 5S rRNA 분자의 중앙 부분은 단백질 합성아 일어나는 동 안 5S rRNA- 결합 단백질들에 의해서 조절되면서 tR NA , 16S rRNA 및 23S rRNA 들과 상호작용하기가 수월해질 것이라고 상상해 볼 수 있다. 큰 하위단위체에 있는 5S rRNA 와 작은 하위단위체에 있는 16S rRNA 사이의 염기 짝짓기가 리보솜의 두 하위단위체들의 가역적 회합에 관여 할 것이라는 가설이 제안되고 있지만 이것도 앞으로 더 연구되어야 할 문제 이 다 (Azad, 1979 ; 그림 2-llC 도 참고하라) .
표 2-7 E-L5, E-L18, 및 E-L25 둘의 E. coli 5S rRNA 에 의 결 합이 핵 산 가수분해효소 S1 의 우리던 -40 에서의 가수분해에 미치는 영향 단백질 % 방해 E-L5 27 E-Ll8 20 E-L25 。 E-L5/L18 41 E-L5/L25 。 E-L18/L25 18 E-L5/18/25 58 나) 그 밖의 박테리아로부터의 5S rRNA 들 여러 가지 생체들로부터의 많 온 5S rRNA 둘의 일차구조에 기초하여 그들의 이차구조의 모형이 제안 되었으며, 그둘의 계통수가 만들어졌다. Hor i와 Osawa(1980) 는 5S rRNA 둘을 네 유형으로 구분하였다. (1) 진성 박테 리 아에 서 볼 수 있는 116-N- 형 : 이 5S rRNA 는 116 개 (또는 때때로 117 개)의 누클레오티드를 가지고 있으며, 그람-양성 박테리아에 존재한다. (2) 진성 박테 리 아의 120-N- 형 : 이 유형의 5S rRNA 는 120 개의 누클레오티드를 가지고 있으며 그람-음성인 박테리아에 존재한다. 이돌 두 유형의 5S rRNA 둘의 이차구조들은 특성적인 차이점을 가지고 있다. (3) 메 타박테 리 아형 : Halobacte r iu m , Sul/olobus, 및 Thermop la- sma 들의 5S rRNA 가 이 유형 에 속한다. 121 개 의 누클레 오티 드 를 가 진 이 유형은 진성 박테리아의 유형보다는 진핵세포의 유형에 더 유사 하다. (4) 진핵세포의 유형 : 이 유형의 5S rRNA 는 식물에서는 116~ 118 개의 누클레오티드를 가지며 그밖의 진핵세포에서는 120 개의 누클 레오티드를 가지고 있다 (2.8.3 절을 보라). 이 유형의 5S rRNA 둘은 앞에서 말한 진성 박테리아의 두 유형의 것들과 그 이차구조들이 특성 적 으로 다르다 (그림 2-13 를 참고하라) . 그림 2-13 의 모형 들을 비 교해 보면 진핵세포와 메타박테리아의 5SrRNA 둘이 더 유사성이 큰 것을 볼 수 있다 (A 고리 부분과 B 고리 부분을 비교하라). 그러나 C 고리 부 분에 있어서는 누콜레오티드의 수 (13 개)와 결합순서에 있어서 대타박 테리아는 진성 박테리아에 더 유사한 것을 볼 수 있다. 따라서 메타박 테리아와 7같 은 고대 박테리아는 진성 박테리아가 출현한 다음에 출현한
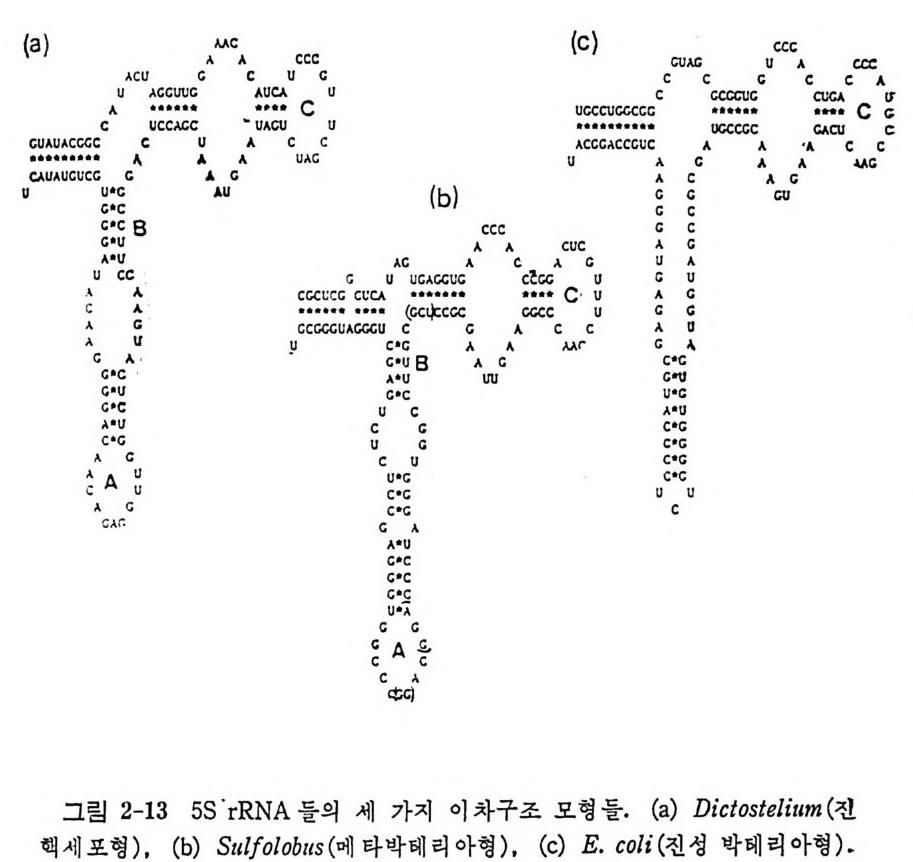 (a} cA U A CU A.uCc.Cc.U,.iU .;Cc. C A MCA • C A.U U.ACC. UA. U C CCC C Uu (u•c•c) c• c••u•c•c c• c••c C C C UAC CCu. Cc.Cc.Cc.Uc.Cc.C U C CC AC Co. .\lOC.A.J C C CO :A CtC r
(a} cA U A CU A.uCc.Cc.U,.iU .;Cc. C A MCA • C A.U U.ACC. UA. U C CCC C Uu (u•c•c) c• c••u•c•c c• c••c C C C UAC CCu. Cc.Cc.Cc.Uc.Cc.C U C CC AC Co. .\lOC.A.J C C CO :A CtC r
것 으로 생 각된 다 (Hori 동, 1982) . 다른 종류의 박태리아의 SS rRNA 둘은 재구성법으로 B. ste a roth e r- mo p h i lus 의 50S 하위단위체에 결합시킬 수 있지만, 진핵세포의 SSrRNA 들은 결합시킬 수 없다. 이 결과는 원핵세포와 진핵세포의 SS rRNA 분 자들이 중요한 점에 있어서 차이접을 가지고 있다는 것을 암시해 준다 (Erdmann, 1976) . 5' 말단 부분과 3' 말단 부분들이 염 기 짝지 움을 하 여 이루는 나사선형 줄기를 화학적으로 변형시킨 SS rRNA 둘을 가지고 재구성 실험을 해 본 결과들에 의하면 SS rRNA 의 이 줄기 부분은 생 물학적 활동성에 있어서 중요한 역할을 하지 않는다는 것이 알려쳐 있다.
2. 4. 2 16S rRNA 가) 일차구조 및 이 차구조 16S rRNA 와 같은 큰 RNA 의 일 차구조의 연구는 신속한 RN A 결합 순서 분 석 법이 개 발될 때 까지 는 부진하였다. 최 근에, 도입복 제 된 DN A ( cl oned D NA) 를 사 용 하는 R NA 의 결 합순서 결정 법 (Brosiu s 등, 1978) 과 Str a sbourg 의 연 구진 이 개 발 한 신속한 RNA 결 합순서 분 석 법 (Carbon 둥, .19 78) 이 개 발 됨 으로써 E. col i 의 16S rRNA 의 일차구조 분 석 에 있어서 중요한 결과 들을 쉽게 얻 을 수 있게 되었다. 그 결과로 이 분자의 구조 및 리보솜 단 백질들 이 결합 하는 RNA 상의 자리들을 정 확 하게 분석 할 수 있게 되 었 다. 그 뿐 아니라 일 차구조의 결정은 이차구조를 결정할 수 있는 새로운 화학 적 및 물리적 방법들울 한충 더 발전시켰다. 지금까지 20 가지 이상의 작은 하위단위 체의 rRNA 와 10 여 가지의 큰 하위단위체의 rRNA 의 일차구조가 분 석되어 있다(표 2-8). 표 2-8 올 보면 16S 및 23S 와 같 은 rRNA 들의 크기들이 2 배 내지 3 애의 범위에서 다르다는 것을 알 수 있다. 크기가 국단적으로 다르다고 해서 구조적인 제약이 없다는 의미는 아니다. 뒤에서 곧 논의하겠지만, 모든 출처로부터의 rRNA 둘의 이차구조 또는 삼차구조들 사이에는 분 명한 상동성이 존재한다. 그뿐 아니라, rRNA 의 어떤 부분 들 에서는 일 차구조가 매우 찰 보존되어 있다. rRNA 에 있어서 전사 후에 변형된 누클레오티드의 함량은 t RNA 의 것보다 훨씬 적으며, 원핵세포의 경우를 보면 1% 이하이다. 진성 박테 리아에 있어서는 대부분의 변형은 염기 상에서의 메틸화이다 . E. co lt'의 16S rRNA 에 있어서, 변형이 일어나는 부분을 여섯 군데로 구분할 수 있다. m7 G 527; m5G966 과 m5C967; m2Gl207; m~Cl402 와 m5 Cl 407; mU1498 ; m2Gl516 ; m~A1518 과 m~A1519 (Brosiu s 둥, 1978 ; Carbon 등, 1979). E. col i의 23S rRNA 에 있어서는, 염기와 리보오스들의 변형 이 외에도 수도우리던과 리보티미단이 있다. X. la e v i s 의 18S rRNA 에 있 어서는, 일반적으로 진핵세포의 세포질의 rRNA 들의 경우에서 그러한 것처럼, 염기의 변형 이외에 리보오스에서의 메틸화도 많이 일어나고 있 다. 대부분의 경우에 있어서, E. co li의 16S rRNA 의 전사 후 변형은 완전한 30S 하위단위체에 있어서 화학적 변형을 받을 수 있는 부분, 죽,
표 2-8 일차구조가 결정된 16S 및 23S 와 갇은 rRNA 둘 생물종 1 찬기의수 II 생뭉종 1 찬기의수 <16 S와 갇은〉 rRNA Asp er gi lls 1437 (작은 하위 단위 체 의 rRNA) Parameciu m (16 07) 진성 박테리아 口J 1957 E. coli 1542 옥수수 (1962) B. brevis (1540) • P. vulga ris 1544 <23 S 와 갇은〉 rRNA A. 11i d1 1la11s (1487) (큰 하위 단위 체 의 rRNA) 엽록체 진성 박테리아 옥수수 엽록체 1490 E. coli 2904 담배 엽록체 1485 B. ste a roth ennop hi l tt s 2931 E11g le 11a 엽록체 1491 영록체 Clzlamy do1 11011as 엽 록체 1475 옥수수 영록체 2903 고대 박테리아 담배 엽록체 2904 H. volcanii 1469 진핵체 진핵체 S. cerevis i a e (2GS) 3392 S. cerevis i a e (세 포 질 ) (18 S) 1799 S. carlsberge nsis ( 26S) 3393 Phys ar 111n (26S) 3788 X. /aevis ( 18S) 1825 X. laevis ( 28S) (4110) 쥐의 간 (18S) 1874 쥐 (28S) 4718 Dic tos ta l iu m (17S) 1873 미토콘드리아 옥수수 (18S) Tryp a1 10s0111e 1152 미토콘드리아 사람 1559 Tryp a nosome (9S) 597 소 1571 사람 954 생쥐 1582 소 958 쥐 1584 생쥐 956 Parameciu m (2380+) 쥐 953 효모 3273 효모 1686 Aspe r gi /111 s 2768 a: 성숙한 tR NA 사슬의 실재 길이가 불확실한 것에 대해서는 최선의 추정치를 괄호 안에 주었다. 단일 가닥으로 되어 있고 찰 보존되어 있는 부분에서 일어나고 있다. 먼저 Noller, Woese, 및 그들의 공동연구자들 (Noller, 1979; Woese 등, 1980 ; Noller 와 Woese, 1981 ; Gup ta 둥, 1983) 이 E. coli , Haloba-cte r iu m volcanii 둘로부터 의 16S rRNA 들의 이 차구조의 모형 을 보기 로
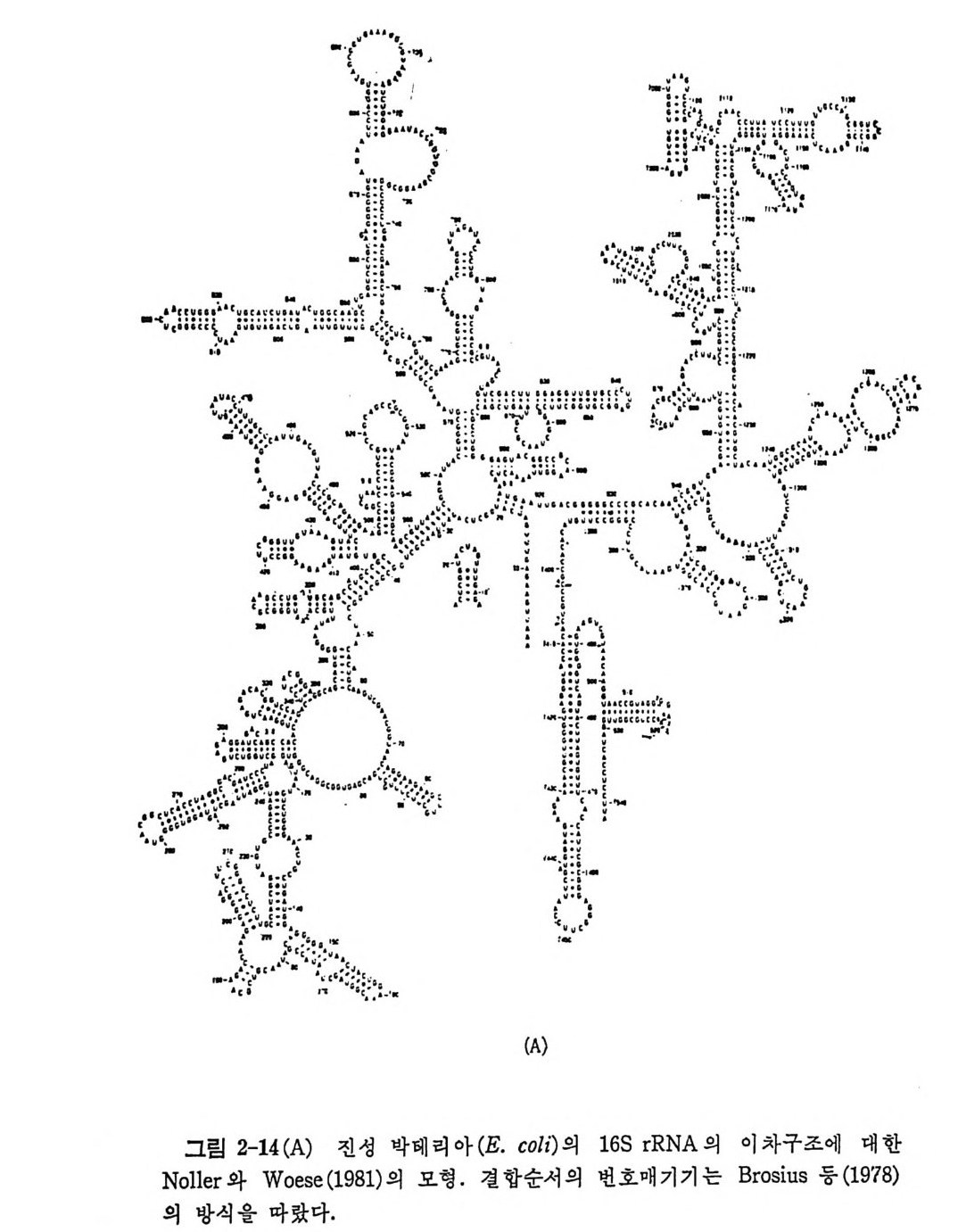 ..-.Y. •• ~나상`& •r'.,., ..., . '• •.‘. ,·- t, “1菜”.?`.-.”“i당_‘&。.i .• .L'“ • ‘r성r .:••.·u. •‘t. •. mE·,.'Eii . ..,•:‘g.•;•、s·. ,•·3 .•,.:?. ·• • ‘.. •t‘‘•, ,,‘나, .'..•T. ,‘•. • C‘ .•..•. . ·''•C55• ,-.., ••, ‘ ‘ ' •• ..,. e달·‘i t•.•P :' ‘,c.일'·.• .,.u• -.,' '•-5-.•g• , ..;. ;:•.t.. .,.,`• •. .`•‘n‘.J‘i,‘”••••‘,c ‘ t‘•.•• •‘c-Y•‘ d. .•.•,넬,,‘ ”..'C'‘‘, ‘-~ c .•'i•..,t.c•t5i.·‘ .‘.•i..’S...-‘.•,• .5.•.•' ‘• .‘• •••,•‘.••..,•;'•.,c … :. k , ‘L;.t •'..•‘ •••....- •.‘.‘.5‘,'.· ‘••‘.. .、 `.•.• ‘’-t... ss ..F.• s\•: r, •• - ...니..5t&c', •.i .. ..-. .,,: .• • ’ C..., '’말.: ‘c- 1•.c•. .CF‘,.,.‘~일 e9 .,-C`` ‘....‘”; . .,. . :,. / .·i. •.‘•‘ .아-..‘1i.. : _일iF,'., 』td:.?M,‘`` :‘일..t : ..;+. •’,,. .'』. ‘C'..•5.P.,;:•‘•..••,•, ‘ ‘ ‘ •‘‘.•7 I ..,..,.. .‘..'- . •.•.f •’‘'...,. ..'...i;'‘,. .,iie c '•일.C;.h c.” ,... ..‘.• •. ‘. . . .’-. ..:. . .‘l.-,..5 ...,....'...`•.,. ” ,. ,.'J..•일-,'..' • •3 . ,...' ,?.tF...'•-s‘ .c '. F•,..‘ .(‘.••? 3 t'‘••‘일‘·.. 5 A‘’ ‘L‘•.•.•.c‘ia,· '‘•, .8 •.V’~)` ., g5’• .•c •‘‘ ‘,‘.•Y .,,‘d•'• ’ ••... ..;‘v .‘.‘ ••,•.. 'c ·•J• ;.F•..c:·..•. ,•:, .•‘; : ...,.,'..•.•,‘.: 열 • ( c‘•. . .> ~..,.,,- ,•., ..: .•` •,-,.. '. • •’ . , .F‘i-.,’.•.이• -..• : ·. .. e.••., ••: ‘ ••t‘, C•. ••‘ 'g , ‘.,. •‘. ,i•• •;,••U. .• '.• . , •. .••• •c 7 . ' •. .,,• ’,,a. ‘ • ....넬’, 5.,. ' .,.c •‘.· ,U.r.•..열. ;.. '.‘‘.‘ C -...c .:• .‘.r.'•.‘‘‘.·. ‘c‘.·,,• F’.--‘..5. :_•• ‘5-·'. .‘. -’.... ‘ R .. .F-..,,.‘. . . i,:c.s•• •‘`· ,..,‘ •.널c',,•,• .E.' ... . : .f•. •. g•..;..E5.:.. ~사.t-.E-,^ .8 · . ,c ‘ . ’:.” c• ‘i- .,닐-.날‘:', c‘ 일 ,.』,!..‘' ‘‘', -',‘‘ ..-. ;f, . .-.'.·‘,•..·;;'.. ....., ... ..,c.•.-.. ...c, ”..,‘.•c•’,.,,''‘’..,.,.. ..鼻,.' .•.,.C,.•-.,.•c,,•'’t, ;c 이' .. .• . 5 .C .c .; t. .g.,.g-m ?- . ”..5`...‘' 3. ,i · .'‘. ` :.’, g;' ‘. . .. . 5 ?..J..2c‘,5.M Fr\、.•“. .'. ,,‘‘ •,...d • `' mp‘l .,.,';1.C4·C,r,‘ u..'·널.,,..‘ .q `5 ‘ 넬·. ?.; .,',7l 8. ·ig.. , •'..瓚.. ..r . .,':,‘-..·'J . 2 g.‘. ' . : C .-· ,,. c .g~,널 'u.•.,·‘,• ,''';,,,.C• .' •< - g.•:•,' ` • :•'‘scc · ' ’.• c,.. .C . ..,'..'.: ,. `·.‘.· ‘Cc ‘• 5· . ` . ,·b,’55 ' ·•..,
..-.Y. •• ~나상`& •r'.,., ..., . '• •.‘. ,·- t, “1菜”.?`.-.”“i당_‘&。.i .• .L'“ • ‘r성r .:••.·u. •‘t. •. mE·,.'Eii . ..,•:‘g.•;•、s·. ,•·3 .•,.:?. ·• • ‘.. •t‘‘•, ,,‘나, .'..•T. ,‘•. • C‘ .•..•. . ·''•C55• ,-.., ••, ‘ ‘ ' •• ..,. e달·‘i t•.•P :' ‘,c.일'·.• .,.u• -.,' '•-5-.•g• , ..;. ;:•.t.. .,.,`• •. .`•‘n‘.J‘i,‘”••••‘,c ‘ t‘•.•• •‘c-Y•‘ d. .•.•,넬,,‘ ”..'C'‘‘, ‘-~ c .•'i•..,t.c•t5i.·‘ .‘.•i..’S...-‘.•,• .5.•.•' ‘• .‘• •••,•‘.••..,•;'•.,c … :. k , ‘L;.t •'..•‘ •••....- •.‘.‘.5‘,'.· ‘••‘.. .、 `.•.• ‘’-t... ss ..F.• s\•: r, •• - ...니..5t&c', •.i .. ..-. .,,: .• • ’ C..., '’말.: ‘c- 1•.c•. .CF‘,.,.‘~일 e9 .,-C`` ‘....‘”; . .,. . :,. / .·i. •.‘•‘ .아-..‘1i.. : _일iF,'., 』td:.?M,‘`` :‘일..t : ..;+. •’,,. .'』. ‘C'..•5.P.,;:•‘•..••,•, ‘ ‘ ‘ •‘‘.•7 I ..,..,.. .‘..'- . •.•.f •’‘'...,. ..'...i;'‘,. .,iie c '•일.C;.h c.” ,... ..‘.• •. ‘. . . .’-. ..:. . .‘l.-,..5 ...,....'...`•.,. ” ,. ,.'J..•일-,'..' • •3 . ,...' ,?.tF...'•-s‘ .c '. F•,..‘ .(‘.••? 3 t'‘••‘일‘·.. 5 A‘’ ‘L‘•.•.•.c‘ia,· '‘•, .8 •.V’~)` ., g5’• .•c •‘‘ ‘,‘.•Y .,,‘d•'• ’ ••... ..;‘v .‘.‘ ••,•.. 'c ·•J• ;.F•..c:·..•. ,•:, .•‘; : ...,.,'..•.•,‘.: 열 • ( c‘•. . .> ~..,.,,- ,•., ..: .•` •,-,.. '. • •’ . , .F‘i-.,’.•.이• -..• : ·. .. e.••., ••: ‘ ••t‘, C•. ••‘ 'g , ‘.,. •‘. ,i•• •;,••U. .• '.• . , •. .••• •c 7 . ' •. .,,• ’,,a. ‘ • ....넬’, 5.,. ' .,.c •‘.· ,U.r.•..열. ;.. '.‘‘.‘ C -...c .:• .‘.r.'•.‘‘‘.·. ‘c‘.·,,• F’.--‘..5. :_•• ‘5-·'. .‘. -’.... ‘ R .. .F-..,,.‘. . . i,:c.s•• •‘`· ,..,‘ •.널c',,•,• .E.' ... . : .f•. •. g•..;..E5.:.. ~사.t-.E-,^ .8 · . ,c ‘ . ’:.” c• ‘i- .,닐-.날‘:', c‘ 일 ,.』,!..‘' ‘‘', -',‘‘ ..-. ;f, . .-.'.·‘,•..·;;'.. ....., ... ..,c.•.-.. ...c, ”..,‘.•c•’,.,,''‘’..,.,.. ..鼻,.' .•.,.C,.•-.,.•c,,•'’t, ;c 이' .. .• . 5 .C .c .; t. .g.,.g-m ?- . ”..5`...‘' 3. ,i · .'‘. ` :.’, g;' ‘. . .. . 5 ?..J..2c‘,5.M Fr\、.•“. .'. ,,‘‘ •,...d • `' mp‘l .,.,';1.C4·C,r,‘ u..'·널.,,..‘ .q `5 ‘ 넬·. ?.; .,',7l 8. ·ig.. , •'..瓚.. ..r . .,':,‘-..·'J . 2 g.‘. ' . : C .-· ,,. c .g~,널 'u.•.,·‘,• ,''';,,,.C• .' •< - g.•:•,' ` • :•'‘scc · ' ’.• c,.. .C . ..,'..'.: ,. `·.‘.· ‘Cc ‘• 5· . ` . ,·b,’55 ' ·•..,
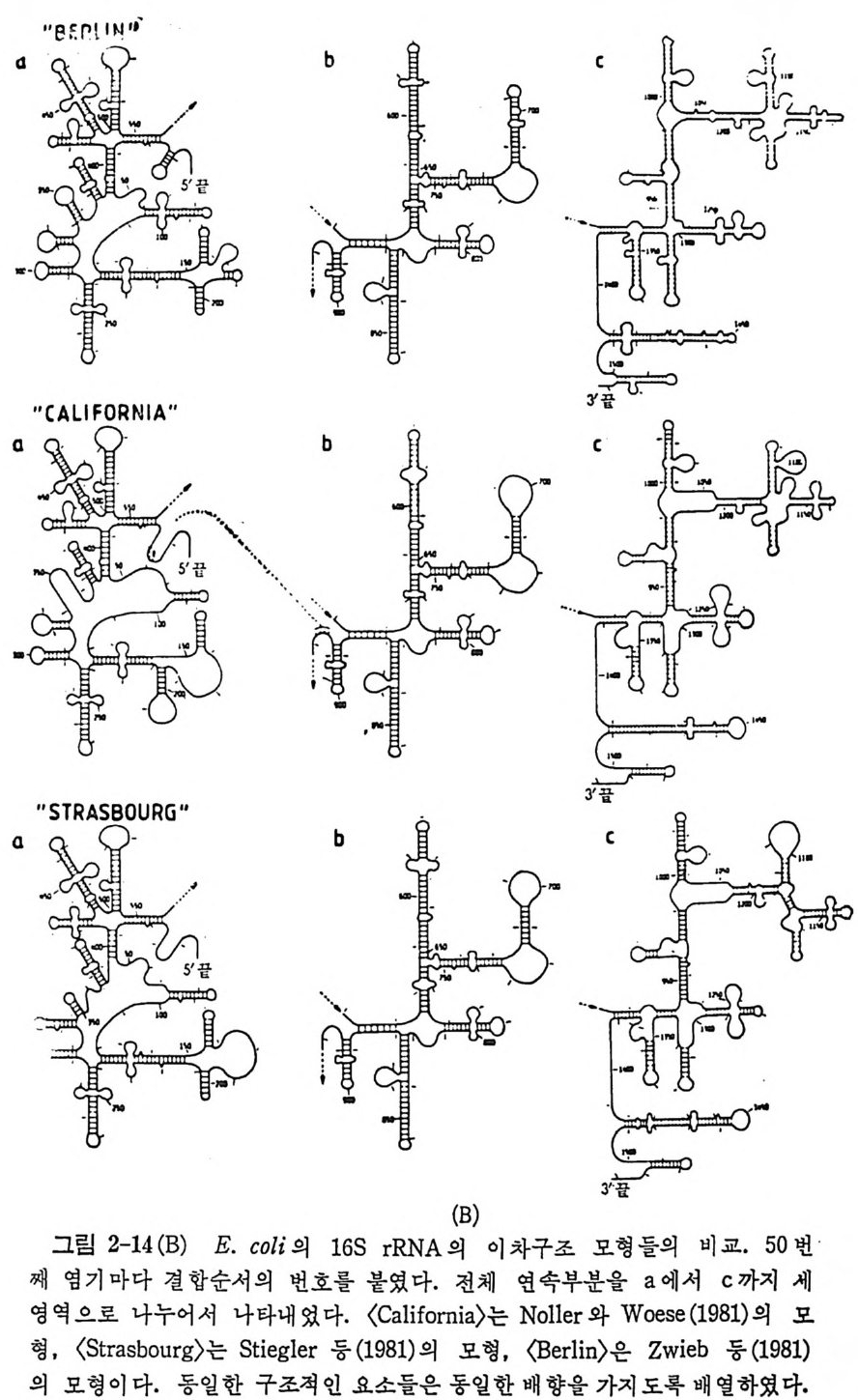 d ”Ef P l ’ N’, 、 b
d ”Ef P l ’ N’, 、 b
하자. Noller 와 Woese (19 81) 는 16S rRNA 의 이 차구조를 제 안하였 는 데, 그것을 그림 2-14(A) 에 나타내 었다. 그밖에 연구진 들이 재 안한 모형 들을 그림 2-14(B) 에 나타내었다. 이 모형은 여러 가지 화학적 변형법 또 는 리보핵산 가수분해효소에 의한 처리에서 생기는 조각들의 분석에 의 해서 거의 증명되었다. 단일가닥 부분에만 작용하는 핵산 가수분해효 소 S1 을 가지 고 한 Ross 와 Brim acombe (1979) 의 분석 결 과를 보면 핵 산 가수분해 효소 S1 이 작용하는 자리 는 모두 Noller 와 Woese (1981) 가 제안한 모형의 고리 부분에서 일어난다는 것이 알려져 있다. 그렇지만 이 모형과 맞지 않는 실험결과를 얻은 사람들도 있다. Wollenzie n 등 (1980) 은 16S rRNA 를 히 드록시 메 틸트리 메 틸프소랄렌 (핵 산의 염 기 쌍들 의 치쌓임 사이에 끼어 들어가는 작용물)의 존재에서 광활성으로 교차결 합시켰는데, 교차결합된 염기들은 나사선 부분에 있는 것들이 아니라 고리 부분에 있는 염기들이라는 결과를 얻었다. 이 사실은 Noller 와 Woese(l981) 의 모형은 앞으로 더 세밀히 분석해 불 필요가 있다는 것 을 말해 준다. 최 근에 Gup ta 등 (1983) 은 원 시 진 핵 체 (urkaryo t e ) (고대 박테 리 아) 인 Halobacte r iu m volcani£ 의 16S rRNA (1472 개 의 누쿨레 오티 드) 의 일 차구 조를 결정하여 그 이차구조를 제안하였다(그림 2-15). 이 박테리아의 16S rRNA 의 이차구조는 진핵세포의 18S rRNA 보다는 진성 박테리아 의 16S rRNA 에 유사한 점이 더 많다• 그렇지만 세부적인 면에서는 진 핵세포안 것처럼 보인다. 그리고 이 두 박테티아의 16S rRNA 들의 이차 구조의 두드러 진 특징 은 두 16S rRNA 둘의 일 차구조가 같지 않음 계 도 불구하고 이차구조가 의외로 찰 보존되어 있다는 것이다. 이러한 경향 은 단일 가닥으로 된 고리 부분에서 더 크고 나사선 부분(머리 핀 구조 부분) 에 서 약하다는 것을 알 수 있다. 16S rRNA 둘의 일 차구조가 제 일 찰 보존되어 있는 부분은 짝짓지 않은 부분이다(약 62%). 최근에 Leff er s 와 Garett (1984) 는 고대 박테 리 아의 하나인 Halococcus morrlzua 의 16S rRNA( 누클레오티드의 수, 1,475 개)의 일차구조를 분석하고 그 이차구조를 구성하였는데 H. volcan ii의 이차구조와 거의 동일함을 알 았다. Br ima combe 와 그의 공동연 구자들 (Zwi eb 등, 1981 ; Glatz 와 Brim -acombe, 1980) 은 16S rRNA 의 일 차구조와 분자 내 에 서 의 교차 결 합 실 험들에서 얻은 결과와 단일 가닥에 목이하게 작용하는 핵산 가수분해효
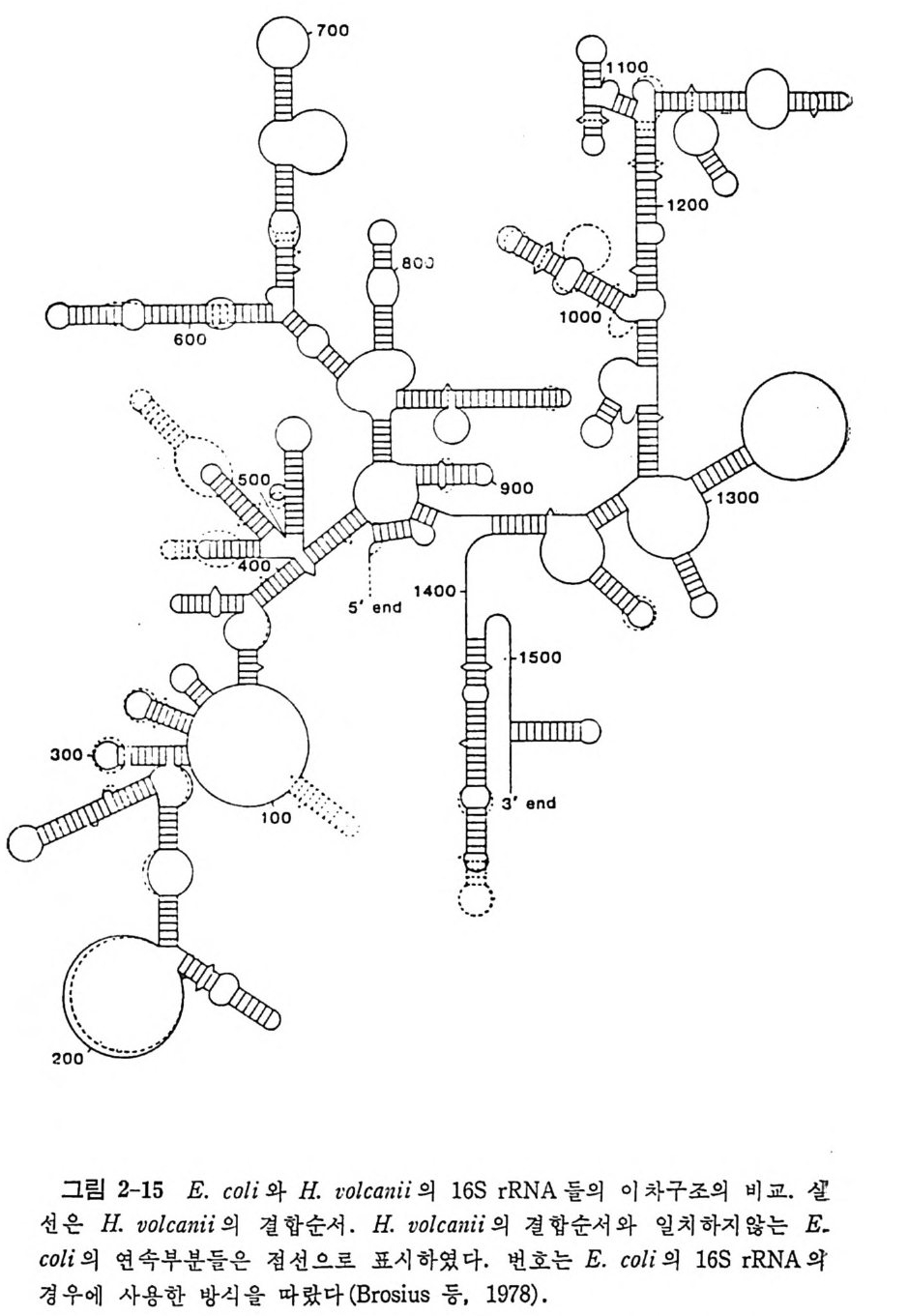 5' , end 1-4 0 0
5' , end 1-4 0 0
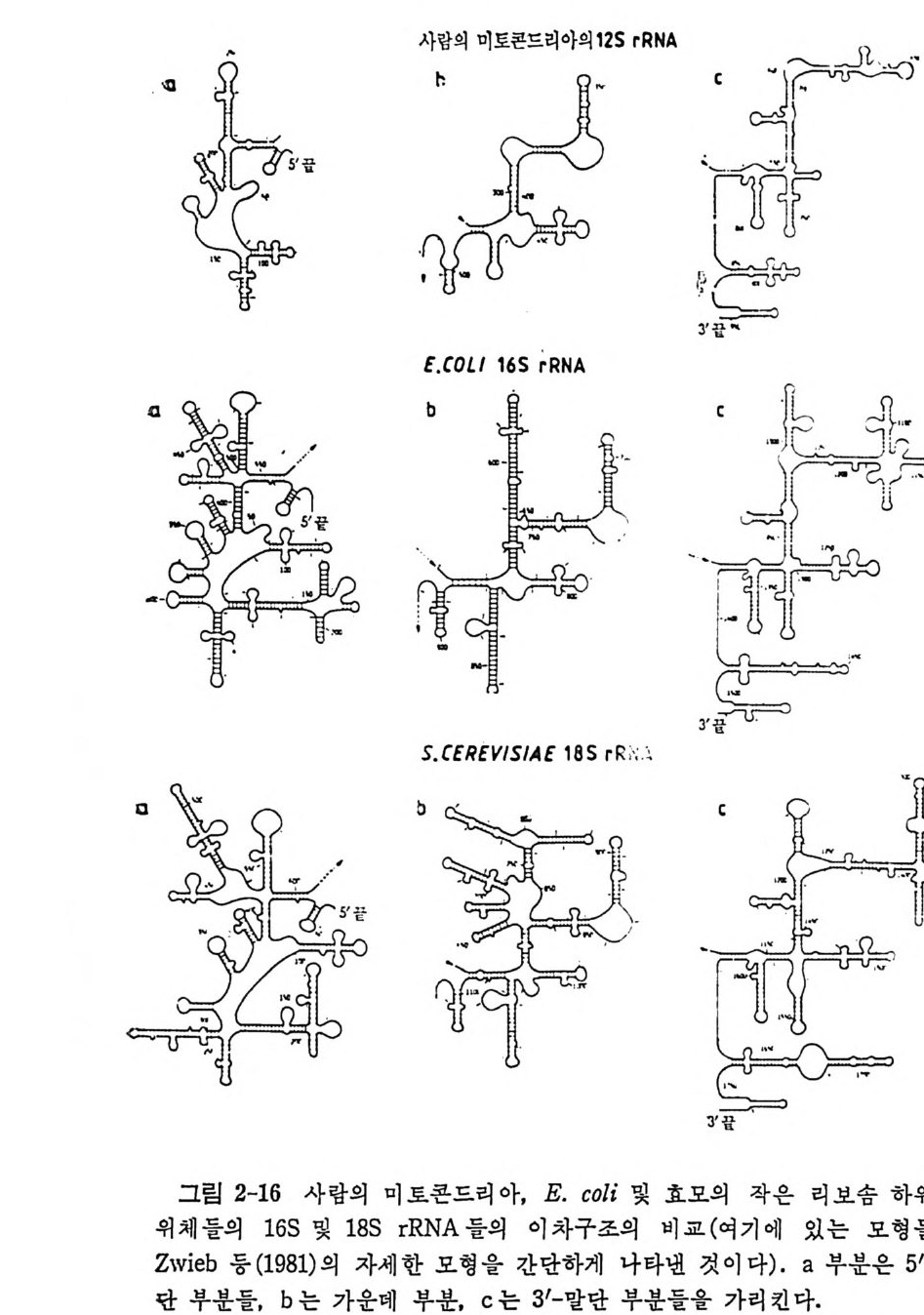 사람의 미토콘드리아의 12S rRNA
사람의 미토콘드리아의 12S rRNA
소 S1 또는 Tl 로 처리하여 얻은 염기쌍 부분 을 분석한 결과들에 기초 하여 모형 을 제 안하였 다 (그 림 2-15) . 특히 Zw i eb 둥 (19 8 1) 은 세 쌍의 작은 하위단위체의 리보솜 RNA 분자들에 대한 이 차 구조 모형들을 제 안하고, 그들의 이 차구조들을 서 로 비 교하였 다 (그 립 2-1 6) . E. coli 의 세포질과 Z. ma y s( 옥수수)의 엽록체의 16S rRNA 둘, 사람과 생쥐의 미 토콘드리아의 12S rRNA, 그리고 S. cerev i s i ae 와 X. la e i-i s 의 세포질의 18S rRNA 둘을 연 구대 상으로 하였 다. E. coli 의 16S rRNA 의 이 차구 조를 근거로 하여, 12S, 16S 및 18S rRNA 둘 사이에서 일차구조의 상 동성 을 살펴 보고, 각 쌍의 결 합순서 둘의 추정 상의 나사선 부분에 있어 서의 보상적 염기 변화(예, A·U ➔ G·C) 를 살펴봉으로써 이차구조를 유 도하였다. 이 모형 들은 리 보솜 RNA 의 이 차구조는 진화하는 과정 에 서 찰 보존되어 있을 것이라는 견해를 뒷받침해 주고 있다• 또 이 모형들 에서 세 종류의 rRNA 돌 사이의 길이상의 차이는 rRNA 분자들의 독 특한 부분들에 있어서의 구조적인 차이에 의해 조절되고 있다는 것을 볼수 있다. Sti eg le r 동 (1981) 도 E. coli 의 16S rRNA 에 대 한 이 차구조의 모형 을 발표하였는데 이 이차구조는 Woese 의 연구진이 발표한 이차구조 (Woese 등, (1980) ; Noller 와 Woese (1981) ; Gup ta 등 (1983) ; 그 림 2-14 또는 2-15 를 참고하라) 와 Glotz 와 Brim acombe (1980) 가 발표한 이 차구조와 도 일 치 하는 점 이 많다. 또한 이 Str a sbourg 의 연 구진은 P. vulg ar is의 16S rRNA 의 완전한 일차구조를 분석하였는데, E. col i의 16S rRNA 와의 상동성은 93% 이 었다 • 이 연구진은 E. col i와 P. vul g ar i s 의 16S rRNA 둘은 공통의 이차구조를 이룰 수 있다는 것을 알았다 (Carbon 과 Ehresmann, 1981) (그림 2-17). 계동적으로 매우 밀접한 관계에 있는 두 생 물종의 rRNA 들의 결 합순서 를 바 교 분석 해 봉으로써 보상적 변화들 을 쉽게 검출할 수 있을 것이며, 이차구조의 모형이 옳은지를 시험해 보는 데 필요한 유용한 정 보를 제 공한다는 것을 알았다. 이 미 5S rRNA 들의 이차구조의 구성에 있어서도 일차구조의 비교분석이 중요하다는 것을 보았지만 (2.4.1 절을 보라), 16S rRNA 들과 같은 큰 RNA 들의 연구에 있어서도 일차구조의 분석치들의 계통학적 비교가 매우 중요한 기준이 된다는 것을 알 수 있다. 16S rRNA 분자는 세 벌의 〈장거리에 걸친 염기 짝짓기 상호작용〉에 의해서 제 개의 주요한 구조적 영역들과 하나의 작은 영역으로 나눌 수
 ‘`I’—.. ‘ `, i.,':-군` .,• \· @ ·, t ~' 왕 . ‘ _.....? .:,. `·:• '’ ': _.•‘':.’ •'; •:' t` • &‘ . ·: · .',상: . •:\ .·;..心 .: ··, •....; .·’· , , :·' '. : ·,: •.· • 4:• :, :;. - . 』 ? ’ . ’`‘“, : 8 ' . , •' ·.• ;• • q ••!.' '; ? .j , . ,. •• . ..• ,, . ”
‘`I’—.. ‘ `, i.,':-군` .,• \· @ ·, t ~' 왕 . ‘ _.....? .:,. `·:• '’ ': _.•‘':.’ •'; •:' t` • &‘ . ·: · .',상: . •:\ .·;..心 .: ··, •....; .·’· , , :·' '. : ·,: •.· • 4:• :, :;. - . 』 ? ’ . ’`‘“, : 8 ' . , •' ·.• ;• • q ••!.' '; ? .j , . ,. •• . ..• ,, . ”
있 다. 5' 영 역 (1-556 까지 의 잔기 들) 은 27 一 37/547-556 과 39-44/3 9 8 -403 의 두 나사선들로 결정되며, 중앙 영역 (56 4 一 912 까지의 잔기들) 은 564 一 570 / 880-886 과 576-580/761-765 의 두 나사선 들로 결 정 되 며 3' 말단의 주요 영 역 (926-1391 까지 의 찬기 들) 은 926 一 933/1384-1391 의 나사선으로 결정되며, 3' 말단의 작은 영역은 1392-1542 까지의 찬 기들로 전정된다. 이 영역들의 범위는 리보솜에 있어서의 16S rRNA 의 실질적인 구조와 모순아 없는 것으로 생각되고 있다 (2.4.3 절을 보라). 세 개의 주요 영역들에 대해서 밀집하게 상응하는 16S rRNA 의 조각들 이 실제로 분리되었다 . 리보솜 단백질들의 어떤 것들이 16S rRNA 조 각들에 붙어서 남아 있거나 제거 후에 재결합할 수 있다는 것은, 이 영 역들이 진정한 구조로서 존재하고 있음을 뒷받침해 준다. 영역들 사아 에 서 도 광범 한 상호작용이 존재 하고 있 다 (Ehresmann 등, 1980) . A 와 G 가 대개의 경우 나사선의 끝 또는 가끔 안쪽 위치에 가지런히 놓이는 경우가 많은데, 이것은 rRNA 에서 anti -an ti A-G 짝짓기가 일 어 남을 암시 한다 (Noller 등, 1980) . A-G 염 기 쌍은 m~G 가 관여 되 기 는 하지 만 tRN APbe 의 구조에 서 도 볼 수 있 다 (Ri ch 와 RajB h andary, 1976) . 16S rRNA 의 이 차구조에 서 볼 수 있는 놀라운 특칭 은, 16S rRNA 에 는 완전한 이중 가닥으로 된 기다란 줄기가 하나도 없으며, 길어야 10 쌍 정도의 영기 짝지움을 하고 있다는 것이다. 그렇지만 염기 짝지움을 하지 않는 고리 부분을 가운데 두고 짤막한 줄기들이 주위에 배열되어 있는 구조적 요소들이 많이 있다. 이 작은 고리 부분들은 16SrRNA 에 유연성을 중으로써 리보솜의 조립이 일어나는 동안에 RNA 가 조밀하게 접힐 수 있게 할 것으로 생각된다. 또, 작은 나사선 부분들이 많이 있 음으로써 16S rRNA 는 구형 단백질에 있어서와 같은 삼차원 구조를 만 들 수 있을 것이다. 중요한 사실은 rRNA 둘의 이차구조에는 매듭이 한 군데를 제의하고는 하나도 없다는 것이다. 매듭이란 나사선 부분에 둘 어 있는 고리가 그 나사선 이의의 다른 부분에 있는 연속부분과 짝지움 함으로써 생 긴 다. 16S rRNA 에 있 어 서 는 9 一 13/21 一 25 나사선 이 형 성 되면 17 ― 20/915 一 918 나사선과 함께 매듭을 만들 수 있다. 매듭을 만 들지 않는 것은 리보솜의 조립 과정에서 생길지도 모를 막다른 저항을 피하기 위한 책략의 일부라고 생각할 수 있다. 나) 삼차구조 및 사차구조 rRNA 의 생물학적 역할을 이해하는 데 가장
중요한 것은 단백질들과 회합한 16S rRNA 의 삼차구조를 설명하는 것이 될 것이다. 제일 확실하고 직접적인 방법은 X- 선 결정구조학적인 방법 이지만 아직 좋은 결과를 얻지 못하고 있다. 지금 사용되고 있는 접근법 은 리보솜 및 그의 하위단위체들의 구조에 대한 전자현미경 모형을 출발 점으로 하는 것과 rRNA 들에 대한 이차구조의 모형을 출발 점으로 하여 이것을 삼차원으로 접도록 시도하는 점근법이다. 2.5.3 절에서 기술할 것이지만 리보솜의 개개의 단백질들의 위치는 면역전자현미경법 (Lake, 1980 ; Sto f fie r 등, 1980) 과 중성 자 굴절 법 (Moore, 1980) 등에 의 해 서 결 정되었다. 이들 중의 어떤 것들은 rRNA 상에서의 결합 자리가 알려져 있으므로, rRNA 의 위치를 합리적으로 추측할 수 있다. 최근에는 16S rRNA 사슬에 있는 특유한 위치에 있는 메틸화된 누클레오티드와 5' 또 는 3' 말단에 결합시킨 합텐에 대한 항체들을 만듦으로써 이러한 자리 들을 직접 면역전자현미경법으로 결정할 수 있는 방법이 개 발 되었다 는(2 .5G.3l3 7절9)을 , S보8라 ()~.59 0이— 러65한0 까집지근 의법 에잔기 의들)해 ,서 ,S l5S (7~(6U5l02 一40 7 과50 까C지13 7의8 또잔 기 들) , 및 S20 (~250 一 280 까지 의 찬기 들) 들융 사용하여 확인 한 16S rRNA 의 자리들을 상응하는 단백질둘의 위치들을 분석함으로써 결정 할 수 있다. 마찬가지 로, m7G527, m~Al518 및 m~A1519, 그리 고 16S rRNA 의 5' 및 3' 말단들의 위치를 직접 결정할 수 있었다. 이 결과를 그림 2-19 에 나타내 었다. 두번째 접근법은 RNA 의 이차구조 모형 상에서 멀리 떨어져 있는 부 분들 사이의 근정성을 알려 주는 분석결과들에 기초하여 RNA 분자를 삼차원으로 집는 것이다. 이러한 근집성을 알려 주는 실험들로서는 교 차 결합과 단일상-단일상 에너지 전달 등의 방법이 있다. 프소란렌을 사용한 교차 결 합법 에 의 하여 16S rRNA 의 360/1330, 620/1420, 960/ 1510 등의 부분들이 가깝게 있음을 알았으며, 전자현미경법에 의해서 1/680, 10/1180, 490/980, 610/1320, 930/1540 등의 부분들이 가깝게 있음을 알았다. 이러한 결과들로 영역들 사이에는 상호작용이 있으며 5' 과 인의 주요 영역들 사이에도 상호작용이 있음을 알았다. 30S 리 보솜 단백 질 들 (예 , S4, S7, SB, Sl5, S17 및 S20) 이 16S rRNA 에 단독으로 그리고 또 특이하게 결합하는 자리들이 많이 알려져 있다. 단백질들의 16S rRNA 에의 결합을 분석하기 위해서 여러 가지 물리적 및 화학적 방법이 사용되고 있다. (1) 어떤 리보솜 단백질을 rRNA 에
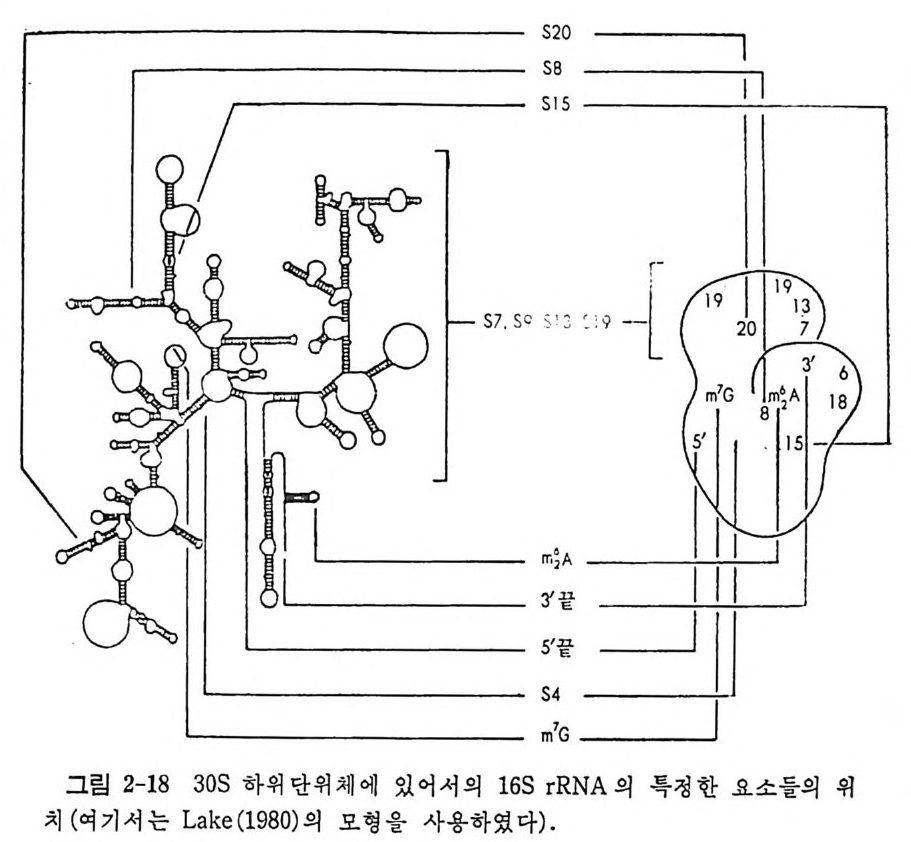 S20~
S20~
결 합시 킨 다음에 핵 산 가수분해 효소들로 보호되 지 않은 rRNA 부분들 을 가수분해해 버린 다음에 보호된 부분을 분석한다(결합-씹기 접근법). (2) rRNA 가닥을 몇 개 의 커 다란 조각들로 쪼깬 다음에 이 조각들이 어 떤 단백 질들과 결 합할 수 있는지 를 알아본다. (3) 마찬가지 로, 단백 질을 몇 개의 조각들로 쪼깬 다음에 이것들이 rRNA 가닥에 결합할 수 있는지를 시험한다. (4) 부분적으로 펼쳐진 하위단위체들을 핵산 가 수분해 효소로 처 리 하여 생 기 는 RNA- 단백질 복합체 들을 분리 하여 그들 이 함유하는 RNA 부분과 단백질들을 분석한다. (5) UV- 조사 또는 화 학약품들에 의한 처리로 생기는 교차 결합들을 분석함으로써 서로 가깝 게 접촉하고 있는 RNA 와 단백질의 결합 부분들을 확인할수있다. (6) 단백질이 RNA 에 결합하기 전과 결합한 후에 단일 가닥에 특이하게 작 용하는 케독살과 같은 시약들에 의해서 변형되는 누클레오티드들의 위
치들을 찾 아낸다. (7) 개개의 아미노산들을 화학적으로 변형한 다음에 이 변 형 이 독정한 단백질의 RNA 에의 결합에 어떤 영향을 미치는지를 조사한다. (8) 돌연변이로 달라진 단백질과 야생형 단백질의 결합능을 비교해 본다. (9) RNA 상에서의 단백질의 결합 자리를 전자현미경으 로 분석 한다. (10) 막거 르기 또는 그밖의 분석 법 들을 사용하여 단백질 둘의 결합상수를 결정한다. (11 ) 작은 각 X- 선 회전법 및 중성자 산란 법, 유체역학적 방법, CD 측정 동과 같은 물리적인 방법들 은 단백질이 RNA 에 결 합함으로써 유발되 는 가능한 형 태 변화들을 검 출할 수 있다. (12) 리보솜 단백질에 있는 방향 족 아미노산들이 자 발적 으로 내는 형광 울 분석함으로써 단백질이 RNA 에 결합한 후 이 아미노산 둘러 1 의 환경 변화에 관한 정보를 얻을 수 있다. 위에서 말한 연구법들에 의해서 S4, S17, S20 들이 16S rRNA 의 5' 말단 쪽의 삼분의 일 부분에서 결합하며, S8, S15 둘 이 중앙 부분에서 결 합하며 , S7, S9, S13 및 S19 들은 3' 말단 쪽의 삼분의 일 부분에 서 결 합한다는 것 이 밝혀 졌 다 (St ieg le r 등 (1981) , 및 Zim mermann (1979) 의 평론서를 보라) (그림 2-19 에 나타낸 결과와 비교하라) . 최 근에 Serdy uk 등 (1983) 은 X- 선 산란 , 중성 자 산란 , 및 속도 침 강 등 과 같은물리적인 방법들을 사용하여, 단리된 상태 및 리보솜 단백질들과 복합체를 이룬 상태에 있는 16S rRNA 의 모양을 결정하여 다음과 같은 결 론을 얻 었다. (1) 충분한 Mg 2+ 농도에 서 의 16S rRNA 의 모양은 30S 입자에 있는 16S rRNA 의 것과 같다. (2) 단백질 S4 와 복합체를 이문 16S rRNA 는 단리 된 상태 의 16S rRNA 의 모양과 조밀 성 이 비 슷하다. (3) 네 가지 핵심 단백질들, 즉, S4, S7, S8 및 S15 들 과 복합 체를 이 룬 16S rRNA 는 단리 된 16S rRNA 의 모양과 조밀성 이 비 슷하다. (4) 6 개 의 리 보솜 단백 질 들, 죽, S4, S7, S7, S15, S16 및 S17 들은 16S rRNA 가 30S 입자 내에서 가지고 있는 조밀성을 가질 수 있게 하는 필 요하고도 충분한 성 분들이 다. 이 러 한 결과들로부터 이 연 구자들은, 16S rRNA 의 전반적인 특이한 집힘은 그 자신의 분자내 상호작용에 의해서 지배되고 유지되며, 몇 가지 리보솜 단백질들이 추가적인 접험과 최종 의 조밀성을 안정시키는 데 추가로 요구될 것이라고 제안하였다.
2. 4. 3 23S rRNA 가) 일차구조 및 이 차구조 Brosiu s 등 (1980) 이 E. coli 의 23S rRNA 의 완전한 일차구조를 rrnB 오페론에 있는 DNA 를 이용하여 결정한 이후 로 또 하나의 원핵체의 23S rRNA 의 일차구조가 결정되었다. 그밖에도 진핵세포의 세포소기관 및 세포질의 23S 와 같은 rRNA 둘의 일차구조 16 가지가 더 알려져 있다(표 2-8 을 보라, Noller(1984) 의 평론서를 보 라) . E. coli 의 23S rRNA 의 이 차구조에 대 한 Noller 등 (1981) 의 모형 을 그립 2-19 에 나타내었다. 16SrRNA 에 있어서와 갇이, 23SrRNA 에도 A·G 염기쌍이 두개가 나란히 (즉, 1039/1116 및 1040/1115) 있다. 이 A •G 영 기 서강들은 B. ste a roth e rmop hi lu s 와 Zea mays 에 있 어 서 는 G·C 와 A•U 염기쌍으로 치환되어 있다. Glotz 등 (1981) 은 E. col 떠 Z. mays 의 23S rRNA, 그리 고 사람과 생 쥐 의 16S rRNA (큰 하위 단위 체의 것 , 표 2_8 을 살펴보라)들의 이차구조들을 계통학적으로 비교해 본 결과에서 진화적으로 먼 이 네 가지 생체의 리보솜의 <2 3S와 같은〉 rRNA 둘의 이차구조들이 상당히 유사한 접이 많으며 6 개의 명확한 영 역들로 구분된다는 것을 알았으며, 16S rRNA 들에서 관찰한 이차구조 의 〈절제〉 또는 〈축소〉 현상이 23S rRNA 들에서도 일어난다고 주장하 고 있다. 세 연구진에서 제안한 E. col i의 23S rRNA 의 이차구조의 모 형들을 그립 2-20 에 나타내 었다. E. col i의 23S rRNA 의 5' 부분(약 160 개의 누클레오티들)은 여러가 치 진핵체들의 5.8S 에 상응하며 (Ja cq , 1981), 3' 부분은 영록체의 리보 송의 큰 하위 단위 체 에 있는 4. 5S rRNA 에 상응한다 (Machatt , 1981) 는 것이 밝혀졌다 • 여러 가지 박테리아의 23S rRNA 둘 사이에는 60% 내 지 90% 정도의 상동성이 있을 것으로 생각되고 있다. 또한, 16S rRNA 에 대 해 서 Noller 와 Woese (l981) 가 제 안한 〈스위 치〉가 23S rRNA 들에도 있다고 생각되고 있다 (Glo t z 등, 1981). 이 〈스 위치〉는 rRNA 의 배열의 변이와 리보솜 입자(또는 그 하위단위체들)의 동적 형태변화를 조종하는 〈부분〉이라고 생각되고 있다(자세한 것은 2.4.4 절을 보라). 23S rRNA 의 스위치는 큰 하위단위체 내에서의 23S rRNA 와 5S rRNA 의 상호작용을 가능케 할 것으로 생각되고 있다 (Glotz 등, 1981) .
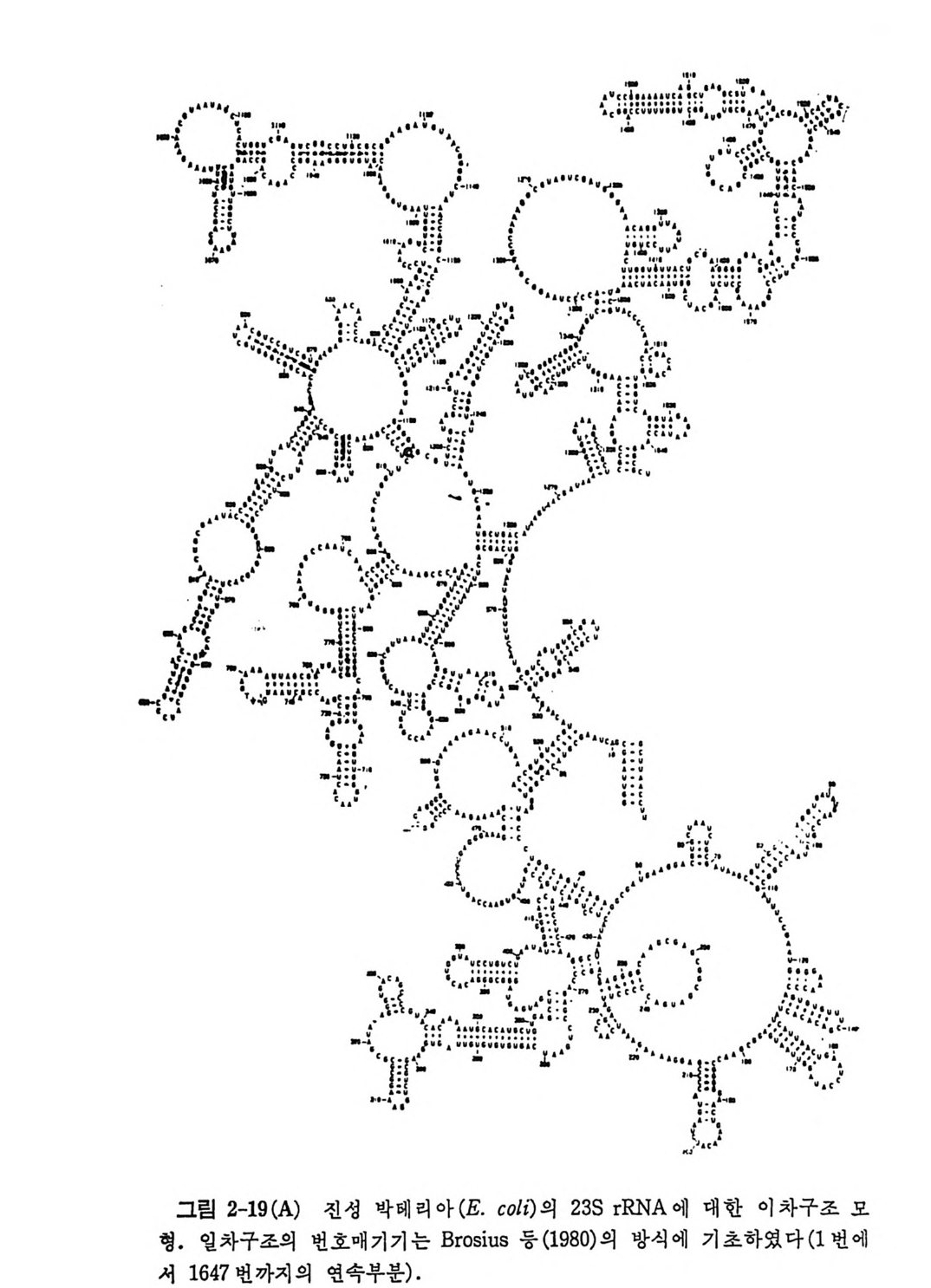 - -.7‘••.& .•• .”』••L/.. . ~. r*f.{·i i삼f.. .:....' .. ..-f.. .t.......:. ‘ . .i.f.'-멍i-.2 '.f&향 전g.ia:i.』 ,. t2 g ‘f요~.Y뇽” -법 5 ..•,• ... iJ’...‘·.-.A...c-. ` ?론:~.~t~ -압i ,‘겔,軍,Fii.,g껍.. ..EF,-데 8.,윙 '「.-”,먼.i..7’` .‘•.:. . •. .-.•f.. · .‘•‘rg.? 심甘iB따.. •iC·.. .•. .f장사 •‘. • •‘1i,-•.5• ...따 ~.L. . .g.•. J` ’ ._ •~gi', /'”뗀페풍홍.T.‘\.정·宁.판'i .o짜• -.g L `? •,. .. • `.Jg.J,.’‘. 나5c.E7앗청-,옮.f,-헛‘I. .l ; .,. ..'..... .. e r....4' t .:.ii\.~哥f.- .팝'4-. ..5 .,\.·성J '. • .”. ..: •.r ... . ,5l •‘•.'.t •e .A& .r i.,-..田?'\.: ‘:..r:,. 훑.• .,. ,.Jg,:..접.‘‘\. *. .'”'..‘ ••5..;,'.,... .. ,.'1...,..ktk..’.--’정,.g5&‘..‘ .' ’ ,” L5 -,..1·:”행 .• g、J,',..J, .'’. ;.',.` .i•. ..” .1,.1,자 ‘빠~g. •1...\c ,.;홍,. i‘리.i장&.5잎Ci, '.. ••. ',.. • . ...,, .'., .,... •,’.‘001.• •,.•, •.` A .J••:'. 5. . •Ll 5 •• :• •-•.• '· ••• ’` • , .. .? ·성 ,'‘.'• . ,•..,.g,’겨??m.;'•이꿉가가•거::::‘ .• ..’.s .,•\' ' ... t ,.‘•'•`.•,•.L,5, ,••:‘ .5 .•'.'• •••.. .",만”p’J.-.t‘,.... , ‘•'. • • . , . : •‘ ' . •' '. •,.‘t ‘‘,’•.• . .., ” '.• ,-• •a.,‘:•T S.‘.,•.,’나t.•‘ .t'' h, ••. ... -~‘.. :•..:. •, .‘. ., .•‘.•'•, .-.3•. ..•· .'‘• ,,.''.• , ”’.”.' .”.•t.-., . . ,, . . :.' , .‘ i •‘ ','?`;直... -. ' .'••'.e‘p,.'•,•' ,‘.·• ,,.p • . •:•. • ;•r:` i.'이\.,' 1•, •;'‘:,.... ' .';.,납• g`.,f ,다呂〔따요〉.:: •.I .. .• `. ' . .i.. ‘I. - ,g'F f’9.. ..t, ...‘ . ,I..l - . · t , a,.. '. ” ' . .. ,, .‘....”.;'; ,.,’? E
- -.7‘••.& .•• .”』••L/.. . ~. r*f.{·i i삼f.. .:....' .. ..-f.. .t.......:. ‘ . .i.f.'-멍i-.2 '.f&향 전g.ia:i.』 ,. t2 g ‘f요~.Y뇽” -법 5 ..•,• ... iJ’...‘·.-.A...c-. ` ?론:~.~t~ -압i ,‘겔,軍,Fii.,g껍.. ..EF,-데 8.,윙 '「.-”,먼.i..7’` .‘•.:. . •. .-.•f.. · .‘•‘rg.? 심甘iB따.. •iC·.. .•. .f장사 •‘. • •‘1i,-•.5• ...따 ~.L. . .g.•. J` ’ ._ •~gi', /'”뗀페풍홍.T.‘\.정·宁.판'i .o짜• -.g L `? •,. .. • `.Jg.J,.’‘. 나5c.E7앗청-,옮.f,-헛‘I. .l ; .,. ..'..... .. e r....4' t .:.ii\.~哥f.- .팝'4-. ..5 .,\.·성J '. • .”. ..: •.r ... . ,5l •‘•.'.t •e .A& .r i.,-..田?'\.: ‘:..r:,. 훑.• .,. ,.Jg,:..접.‘‘\. *. .'”'..‘ ••5..;,'.,... .. ,.'1...,..ktk..’.--’정,.g5&‘..‘ .' ’ ,” L5 -,..1·:”행 .• g、J,',..J, .'’. ;.',.` .i•. ..” .1,.1,자 ‘빠~g. •1...\c ,.;홍,. i‘리.i장&.5잎Ci, '.. ••. ',.. • . ...,, .'., .,... •,’.‘001.• •,.•, •.` A .J••:'. 5. . •Ll 5 •• :• •-•.• '· ••• ’` • , .. .? ·성 ,'‘.'• . ,•..,.g,’겨??m.;'•이꿉가가•거::::‘ .• ..’.s .,•\' ' ... t ,.‘•'•`.•,•.L,5, ,••:‘ .5 .•'.'• •••.. .",만”p’J.-.t‘,.... , ‘•'. • • . , . : •‘ ' . •' '. •,.‘t ‘‘,’•.• . .., ” '.• ,-• •a.,‘:•T S.‘.,•.,’나t.•‘ .t'' h, ••. ... -~‘.. :•..:. •, .‘. ., .•‘.•'•, .-.3•. ..•· .'‘• ,,.''.• , ”’.”.' .”.•t.-., . . ,, . . :.' , .‘ i •‘ ','?`;直... -. ' .'••'.e‘p,.'•,•' ,‘.·• ,,.p • . •:•. • ;•r:` i.'이\.,' 1•, •;'‘:,.... ' .';.,납• g`.,f ,다呂〔따요〉.:: •.I .. .• `. ' . .i.. ‘I. - ,g'F f’9.. ..t, ...‘ . ,I..l - . · t , a,.. '. ” ' . .. ,, .‘....”.;'; ,.,’? E
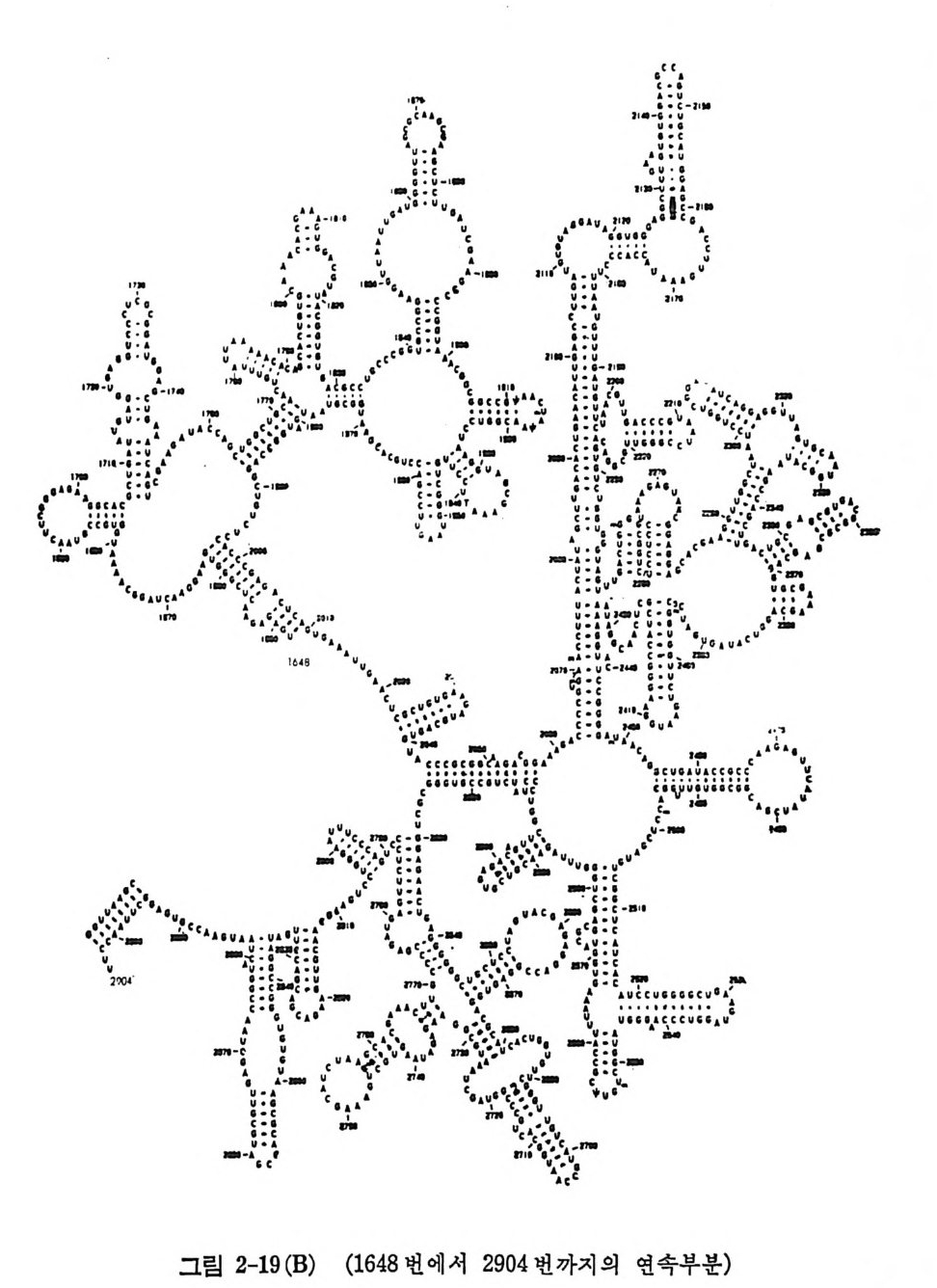 ,•.길 ••·•떤•.나',. ;',.•:;C'나.u ,,:,i•u ' :v,:2• . 나:,'• ;•안 ;·•. C••,~;,-C• C•:::• .· ' •. .:· .••:, ,:•: • • -,.,,':u ;•c: . C• •..,• ·'•.: '. , ·, !•k , ..•,1· .. •· . ·.. u· • . · \.',.·~UR,..·-:''-., -:·.; --, •,,i ,.•·.' ...U &F ··&•.昌•,w'A;-i: , 、~ .; u- •‘,,, ,C:-..C; •U . .. e· •” '.::. ..•• C•. •m;. • ·h.‘; •. u ., ,•,., ` .• ; ·f c, •, u.;t, -••e :- ’ • . .; ,m• . •' : •_ .•- •선?:` ·‘; 다`•-'.• ·-• ·, ,, ,' ;,_,:••, .·Cu :Dc · • 군·· .' •.•기••.:,..· • •• ; , ,-- ,. ,' . •U,- ,u ,•,-i-•' • . . • u ‘. ' '?Uo..•-:; .u , ,.' ., •~·, .' . u !.•.-..u· •-, , ' •, ..: •.· · : ,·. •.u. ,,. '' • 군•., u ‘ ·? • ‘ - o•\ •`· ' ., •:. ..•, %u ?•,u : '.. ; ,U u‘나.{. , •.u (’,• ‘'. •·'UC心• -:U‘' C -···'_.'.i'. ,.‘ ,•d. •. 、’,,1. .: ‘ ,.. c :‘.~c‘U'u',•·:.,C,’‘u,•·, ‘' •‘ ,., ,._. .:u·' .• -'.. 내나 \U .' ••·. : : ..• ‘u•-.... •;' . .c! ,‘,.. •이 cc·•· · ,i.• •, •. - • -‘ ' '; • .. .‘ •. ,•,•- 1 ; ., : , •.;. . ?,u-1‘• ,. ., ., U- - ’,c.• u, '‘. :••소,. •'c• C ' .•••: •••C-’ •• ••서 • •:•',_:••: ,• _ •••,:Cu•`u ·,? m_• ,t:••` ; •' • ,`. .•_u:• •, . : , • -, _' .!'•C•u•‘鼻성C '·• 노· ' .c U, ‘ C,u•·,?사' ,~ . ,· &C : ,*.. C, '• •‘:,.'i ' : 'C.:,::••, (•.‘; ' ...••-~'i'•·'uu •’-.• • ‘.- . -(.: -• • • -•• ‘.;, . 다 u• c .. ,· .• ·. • \-.~ . c - -.C• :`..•?:· ·.:• m:r,.••:U ' ,:;i; t :t~, : ·C』.,,·.• :: - : •: .: •••. ·•\eA鼻:.:•.:::=.:•: •.•• · :•;.U.s•• :•. - '::u U; ,• e•C•:•U:•:•: ,. 자:,:,:• :,나 · 만 • ” U·. :~ .·:• A·••:••: .•,.-:r`·': ' . . :u . '_1. -,. •.-•,?,•••··; .,u,,_ ' .나,·:,. , . ..r;• .. ,, : • . (.. ,;.• . . . : .“:- g·..노-.' •·r :.;•· .t 躍, .f,'. .., ,•; .:,.:• .. ;”· .:. E:,,: ‘_,•..;•: '''v일 .'. • ,U . •t'·:.-:;. •.••M .• Uu::’':.. ”' -.,•'• !;.•', :.,.:• ·-:? ·. •buI e •: ‘ .. .`.I .:t; -,• ·•,., ' ,.•i '. •: •u u.·,•,,, .eI; ‘. : u 。• .• . .•.U ; '.•',,,, .• . . -;, u묘노.y‘.. •.'..,• •,. 3 . .‘' • • . . ·u·,• U• • •.` u,•.,e • '. :g•- .••. ; u • ,,.’' .. ' :•:.u'•''·c: ' · ·. :. .·'',•. - ‘나'- ,·.\u•‘‘ -~.; ··나.m f-U ,仁•.; : ''·.;' u· , •' ‘ ', . Cu.• :c. · i ,• : '• ' u산‘ •’•, ` -
,•.길 ••·•떤•.나',. ;',.•:;C'나.u ,,:,i•u ' :v,:2• . 나:,'• ;•안 ;·•. C••,~;,-C• C•:::• .· ' •. .:· .••:, ,:•: • • -,.,,':u ;•c: . C• •..,• ·'•.: '. , ·, !•k , ..•,1· .. •· . ·.. u· • . · \.',.·~UR,..·-:''-., -:·.; --, •,,i ,.•·.' ...U &F ··&•.昌•,w'A;-i: , 、~ .; u- •‘,,, ,C:-..C; •U . .. e· •” '.::. ..•• C•. •m;. • ·h.‘; •. u ., ,•,., ` .• ; ·f c, •, u.;t, -••e :- ’ • . .; ,m• . •' : •_ .•- •선?:` ·‘; 다`•-'.• ·-• ·, ,, ,' ;,_,:••, .·Cu :Dc · • 군·· .' •.•기••.:,..· • •• ; , ,-- ,. ,' . •U,- ,u ,•,-i-•' • . . • u ‘. ' '?Uo..•-:; .u , ,.' ., •~·, .' . u !.•.-..u· •-, , ' •, ..: •.· · : ,·. •.u. ,,. '' • 군•., u ‘ ·? • ‘ - o•\ •`· ' ., •:. ..•, %u ?•,u : '.. ; ,U u‘나.{. , •.u (’,• ‘'. •·'UC心• -:U‘' C -···'_.'.i'. ,.‘ ,•d. •. 、’,,1. .: ‘ ,.. c :‘.~c‘U'u',•·:.,C,’‘u,•·, ‘' •‘ ,., ,._. .:u·' .• -'.. 내나 \U .' ••·. : : ..• ‘u•-.... •;' . .c! ,‘,.. •이 cc·•· · ,i.• •, •. - • -‘ ' '; • .. .‘ •. ,•,•- 1 ; ., : , •.;. . ?,u-1‘• ,. ., ., U- - ’,c.• u, '‘. :••소,. •'c• C ' .•••: •••C-’ •• ••서 • •:•',_:••: ,• _ •••,:Cu•`u ·,? m_• ,t:••` ; •' • ,`. .•_u:• •, . : , • -, _' .!'•C•u•‘鼻성C '·• 노· ' .c U, ‘ C,u•·,?사' ,~ . ,· &C : ,*.. C, '• •‘:,.'i ' : 'C.:,::••, (•.‘; ' ...••-~'i'•·'uu •’-.• • ‘.- . -(.: -• • • -•• ‘.;, . 다 u• c .. ,· .• ·. • \-.~ . c - -.C• :`..•?:· ·.:• m:r,.••:U ' ,:;i; t :t~, : ·C』.,,·.• :: - : •: .: •••. ·•\eA鼻:.:•.:::=.:•: •.•• · :•;.U.s•• :•. - '::u U; ,• e•C•:•U:•:•: ,. 자:,:,:• :,나 · 만 • ” U·. :~ .·:• A·••:••: .•,.-:r`·': ' . . :u . '_1. -,. •.-•,?,•••··; .,u,,_ ' .나,·:,. , . ..r;• .. ,, : • . (.. ,;.• . . . : .“:- g·..노-.' •·r :.;•· .t 躍, .f,'. .., ,•; .:,.:• .. ;”· .:. E:,,: ‘_,•..;•: '''v일 .'. • ,U . •t'·:.-:;. •.••M .• Uu::’':.. ”' -.,•'• !;.•', :.,.:• ·-:? ·. •buI e •: ‘ .. .`.I .:t; -,• ·•,., ' ,.•i '. •: •u u.·,•,,, .eI; ‘. : u 。• .• . .•.U ; '.•',,,, .• . . -;, u묘노.y‘.. •.'..,• •,. 3 . .‘' • • . . ·u·,• U• • •.` u,•.,e • '. :g•- .••. ; u • ,,.’' .. ' :•:.u'•''·c: ' · ·. :. .·'',•. - ‘나'- ,·.\u•‘‘ -~.; ··나.m f-U ,仁•.; : ''·.;' u· , •' ‘ ', . Cu.• :c. · i ,• : '• ' u산‘ •’•, ` -
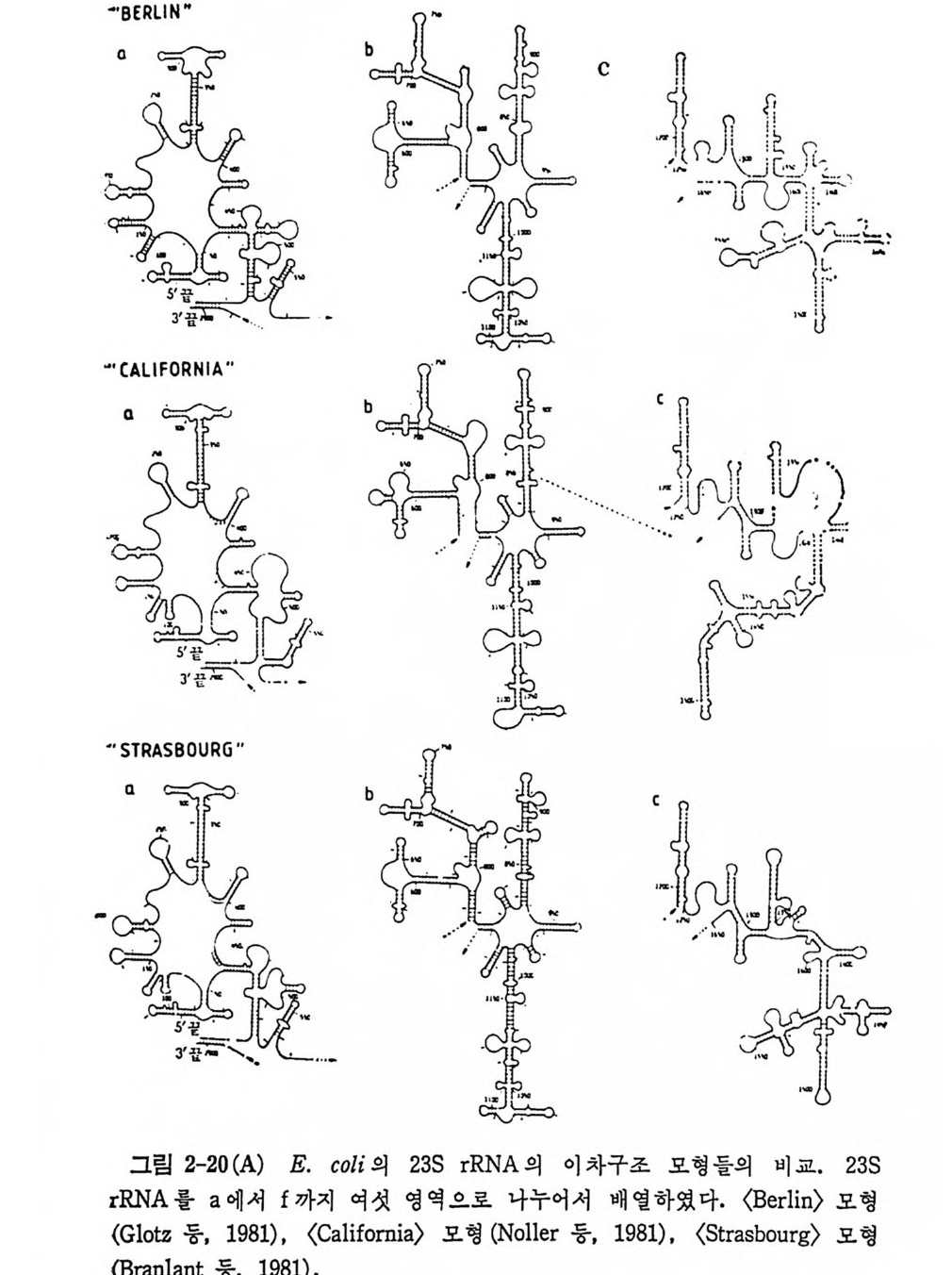 빼 ' BERLIN
빼 ' BERLIN
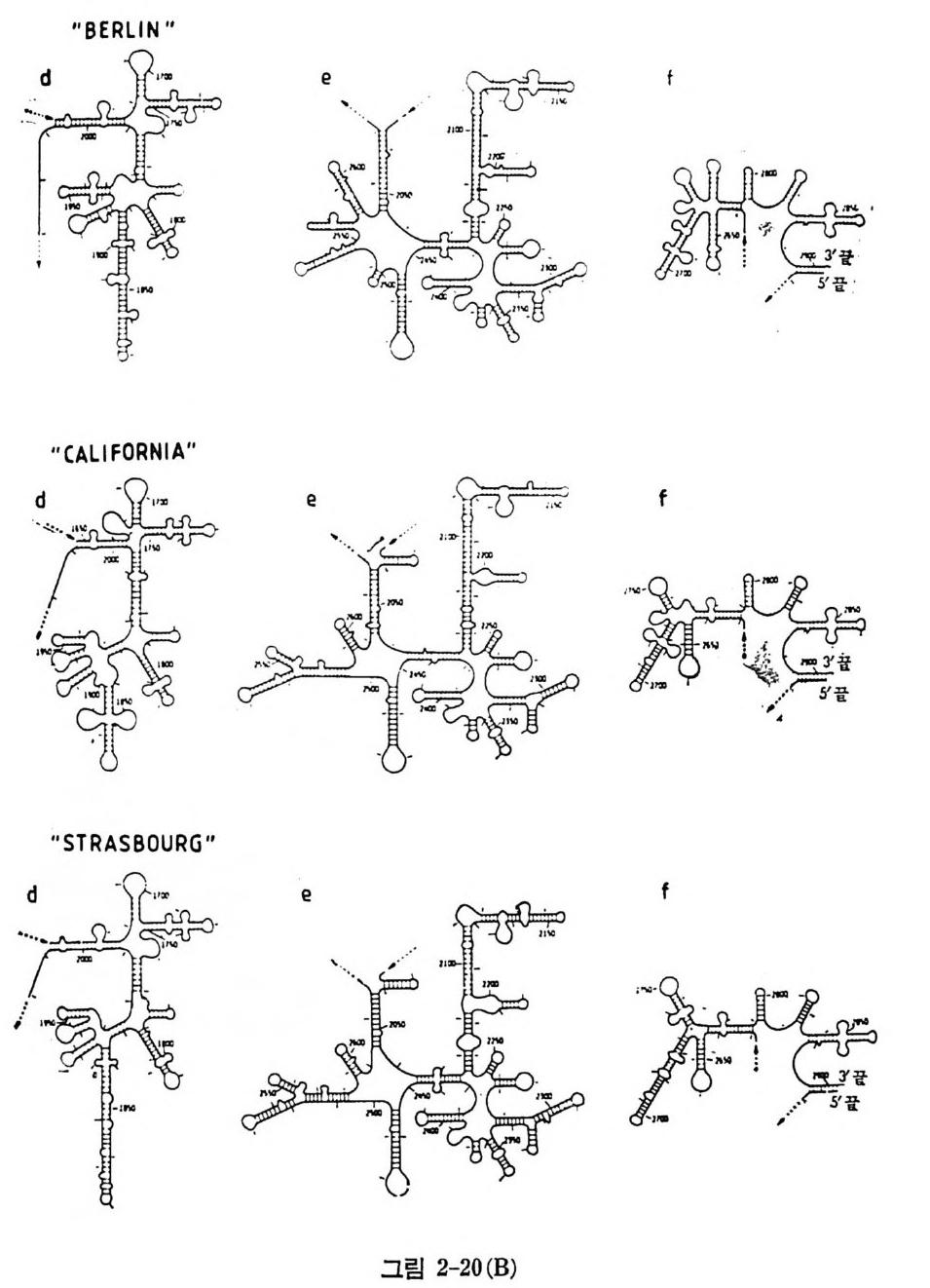 BERLIN
BERLIN
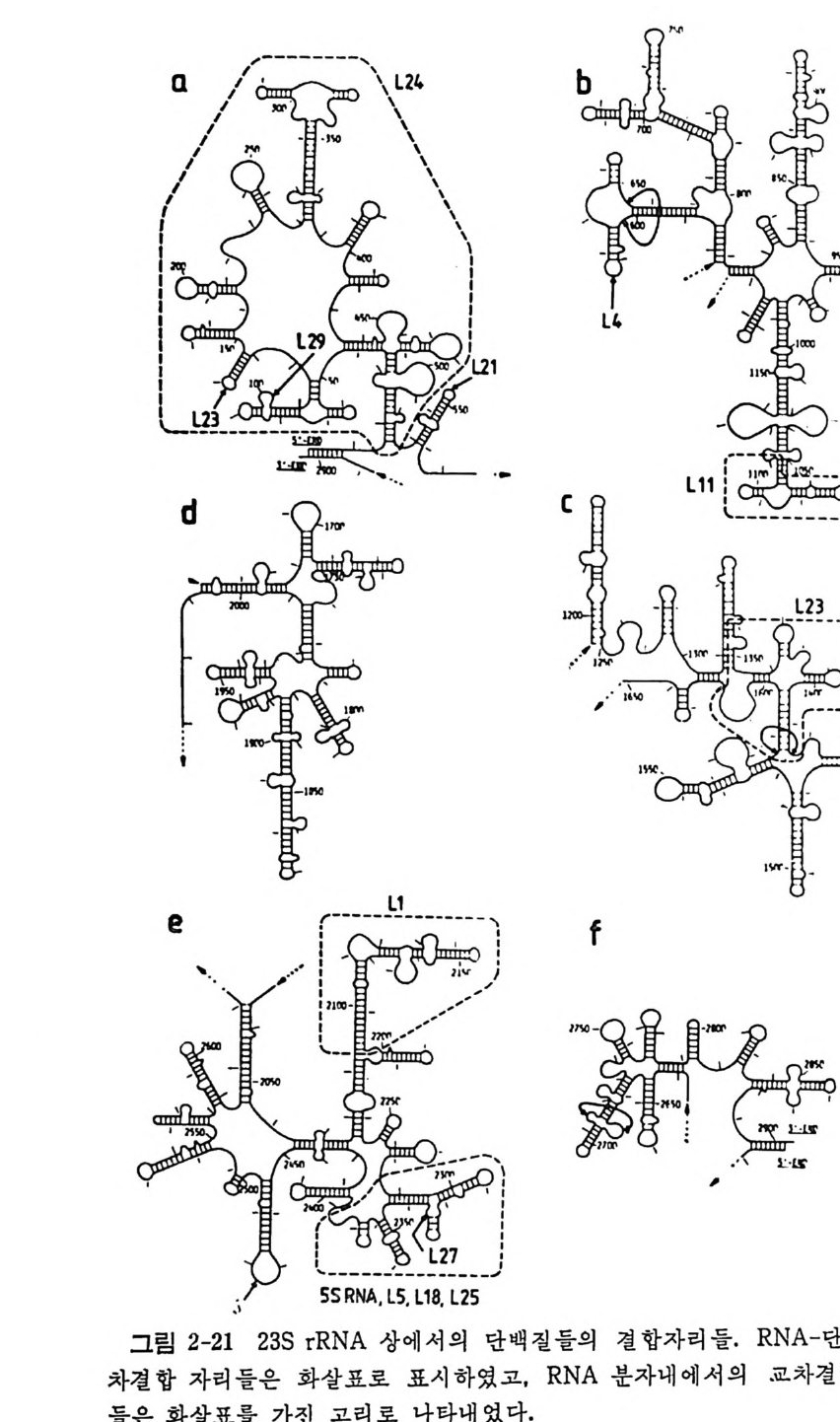 [Q '],L,24 I
[Q '],L,24 I
나 ) 23S RNA 의 삼차구조 및 사차구조 23S rRNA 와 리 보솜 단백 질 들의 결합에 관한 연구는 주로 E. col i에 대해서 조사하였다. 그 결과를 그립 2-21 에 나타내었다. 그림 2-16 에서 지적한 단백질들 이의에도 Ll, Lll, L20, L23, L24 및 S8 둥이 23S rRNA 에 결합한다는 것이 알려져 있 다. 특히, L1 과 S8 은 G·U 염기쌍이 많이 있는 나사선 부 분에 결합된 다는 것이 분석되어 있다. 50S 하위단위체에 있어서의 단백질들과 23S rRNA 사이의 정확한 집 촉 점들이 UV- 조사 또는 특이한 이 작 용기성 시약들에 의한 처리 둥으로 교차결합시킵으로써 결정되었다. 예 를 들면, L6 은 2473-24 81 번 위치 에 상응하는 울리 고누클레 오티 드에 서 , L21 은 540-548 번 위 치 에 서 , L23 은 137-141 번 위 치 에 서 , L27 은 2332-2337 번 위 치 에 서 그리 고 L29 는 99-107 번 위치에서 교차결합한다. 이러한 교차결합들은 특정한 단백질 과 RNA 사이의 인점성을 알려 준다. E. col i의 리보솜 단백질들의 몇 개 는 Bacil lu s 의 rRNA 와 결 합할 수도 있다 (Gausse 등, 1981) . 2.4.4 리보솜 RNA 들의 기능 초기의 연구들은 리보솜의 기능에 직접 관여하는 성분들은 리보솜 단 백질일 가능성이 크다고 강조하는 경향이 있었다. 효소가 생체에서 일 어 나는 모든 반응들의 촉 매 로 작용한다고 하는 관념 이 너 무나 확고하였 기 때문이다. 효소들은 단백질로 되어 있기 때문에 리보솜의 단백질들도 번역과정에 있어서 여러 가지 기능을 일으키는 것으로 기대하는 것은 있 을 법한 일이다. 리보솜의 돌연변이체들 중에서 특히 항생 제 에 대한 저 항성을 가진 것들은, 최초에는, 변이된 단백질에 기인되는 것으로 알았 다 (Dav ie s 와 Nomura, 1972) . 이 러 한 결 과를 얻 게 된 것 은 아마도 이 러 한 종류의 유전 학적 연 구들이 유전구조예 다수의 rRNA 유전자들이 들어 있어서 rRNA 와 유관한 현상형들이 일어났다 하더라도 그것을 가리워 버릴 수 있는 E. co li나 그밖의 진성 박태리아들로 이루어졌기 때문일 것이다. 2.5.3 절에서 논의한 리보솜의 시험관 내에서의 재조립 의 실험결과에 의해서도 리보솜 단백질들이 기능적으로 중요하다는 것 을 알 수 있다. 마지막으로, 단백질은 본성적으로 rRNA 보다 화학반응 성이 더 크기 때문에 친화표지법과 화학변형법 동에 의한 많은 분석들 이 주로 단백질과 관계되는 것으로 이루어졌다.
그러나, 현재까지의 견해와는 반대되는 견해, 즉 리보솜의 기능의 본 질은 rRNA 들에 들어 있으며 리보솜 단백질은 rRNA 의 기능을 더 증진 시키는 역할을 한다는 견해를 뒷받침해 주는 많은 중거둘이 있다 . 먼저 고 려해 봐야 할 것은 닭이 먼저냐 알이 먼저냐 하는 식의 리보솜의 진화에 관한 문제가 되지만, 원래의 리보솜은 단백질을 이용할 수 없었을 것이다 . 왜냐 하면, 최초의 리보솜이 단백질을 만들어야 했었기 때문이다. 단백 질이 먼저 생긴 다음에 rRNA 를 만들었다고 보는 것보다는 리보솜은 본 래 RNA 로부터 구성되었고 진화과정을 거치면서 단백질 들 이 첨가 되었 다고 생각하는 것이 더 합리적이다. 그뿐 아니라, 시험관 내 또는 세포 내에서의 연구결과들에 의하면 개개의 단백질들이 결여된 리보솜둘이 기 능적으로 활발하다는 것이 증명되어 있다 (Gare tt, 1983). 매우 중요한 것은 최 근에 RNA 의 이 어 맞추기 (sp lic i n g ) 가 RNA 자체 에 의 해 서 촉매 된다는 것이 발견된 이후로 (Kru g er 동, 1982), 핵산이 직접 공유결합 을 합성시킬 수도 있고 또 분해시킬 수도 있다는 개념은 이제 더이상 공상이 아니라는 것이 밝혀지기 시작하였다. 그동안 RNA 의 화학적 본 질이 너무 과소평가되어 왔다고 할 수 있다. 최근에 와서 리보솜의 RNA 의 기능적 성질에 관한 연구들이 여러 가지 실험방법으로 이루어져서, rRNA 의 특정한 자리들이 특정한 기능 들과 관계가 있다는 것이 밝혀졌다. 가) rRNA 의 유전학적 분석둘로부터 얻는 결파 rRNA 의 기능적 역할에 관한 실험적인 증거들이 유전학적 연구들에 의해서 얻어지고 있다. rRNA 의 메틸화 또는 메틸화의 결핍은 카수가마이신, 에리트로마이신, 비오마이신, 및 티오스트랩론들과 같은 항생제들에 대한 저항성예 영 향을 미친다(단백질 생합성의 방해물질로 작용하는 항생제들에 관해서 는 제 7 장에서 기술하겠다). 미토콘드리아의 리보솜들에 있어서의 항생 제에 대한 저항성은 거의 언제나 rRNA 유전자들에 있어서의 점 돌연 변이에 기인된다(대부분의 진성 박테리아와는 달라서 미토콘드리아는 보통 한 벌의 rRNA 유전자들을 가지고 있다.). 예컨대, 클로람페니콜 (Dujo n , 1980 ; Kearsey 와 Craig 1981 ; Blanc 등, 1981a 및 1981b) , 에 리 트로마이 신 (Sor 와 Fukuhara, 1982) 및 파로모마이 신 (Li 등, 1982) 등에 대 한 저 항성 은 효모와 포유동물의 미 토콘드리 아의 rRNA 유전 자들 에 있어서의 점돌연변이에 인한 것임이 알려졌다. 저온_민감성 돌연변
이도 미토콘드리아의 rRNA 유전자들 상에서의 돌연변이로 일어나는 것 이 밝혀 졌 다 (Boloti n- Fukuhara, 1979) . 최 근에 , E. coli 에 있어 서 의 에 리 트로마이 신 저 항성 이 플라스미 드에 도입 된 rRNA 유전자에 있어 서 의 돌연변이에 기인됨이 밝혀졌다. 매우 홍미 있는 최근의 발견은 효모 미 토콘드리아에서 오크르 (ochre) 억제 돌연변이가 일어난다는 것인데, 아 돌연변이의 자리가 효모의 15SrRNA 유전 안에 있거나 아니면 가까운 곳에 있 다는 것 이 다 (Fox 와 Sta e mp fli, 1982) . rRNA 의 공유결 합 구조 에 조그마한 변형을 일으켜도 큰 효과를 나타낼 수 있다는 좋은 보기들 · 이 콜리신 E3 와 a- 사르신에 의해서 제공되었다. 이 독성 단백질들은 rRNA 에 있어서의 단 하나의 포스포디에스테르 결합을 끊음으로써 단 백질 생합성 을 완전히 일어나지 못하게 한다. 죽, 콜리신 E3 은 16S rRNA 의 A14 83 -G1494 결 합을 끊으며 , a- 사르신은 <23 S와 같은〉 rRNA 둘의 G2661-A2662 결 합을 끊는다. 이 두 절 단은 모두 보편적 으 로 보존되 어 있는 연 속부분들에 서 일 어 난다 CWoese 등 1983) . 나) mRNA 와의 상호작용 Shin e 과 Dalga rno (1975) 가 제 안한 mRNA 의 개시 자리들과 16S rRNA 의 3' 말단 부분 사이의 상호작용과 단백질 합성의 개시에 관해서는 제 3 장과 제 4 장에서 자세히 기술하기로 하고. 여기에서는 간략하게 설명한다. 아 문제에 관한 최근의 평론서로서는 Ste i tz ( 1979), Gold 등 (1981), 그리고 Kozak(1983) 등이 있다. 많은 종 류의 원핵세포들의 mRNA 의 일차구조를 비교분석해 보면 mRNA 의게 시 코돈의 5' 쪽에서 위쪽으로 약 10 개의 누클레오티드 떨어져 있는 위치 와 16S rRNA 의 1535-1539 위 치 의 보존된 연 속부분 CCUCC 사이 에 정 도의 차이는 있지만 상보성이 있다는 것을 볼 수 있다(그림 3-1 또는· 표 3-1 을 참고하라). 이러한 상호작용이 실제로 일어나고 있다는 것은 생화학적 및 유전학적 연구들에 의해서 광범하게 관찰되고 있다. 그러 나, 이 메카니즘은 진성 박테리아와 원시 박테리아에서는 작동하고 있 지만 친핵체의 세포질의 리보솜과 대부분의 미토콘드리아 리보솜에서는 작동하지 않는 것으로 생각되고 있다. 번역의 개시가 일어날 때 바어 있는 70S 리보솜을 해리시키고. mRNA 의 30S 하위단위체에의 결합을 촉진시키는 역할을 하고 있는 개시인자 IF-3( 제 4 장을 보라)은 오래전부터 16S rRNA 에 결합되는 것으로 생각 되 어 왔다. IF-3 의 16S rRNA 에 의 교차결 합은 UV 조사에 의 한 광화
학반응으로 이루어졌다. 교차결합이 일어나는 자리들 중의 적어도 하 나는 3' 말단 부분에서 일어난다. 3' 말단의 콜리신 조각을 제거하면 IF-3 의 30S 하위단위체에의 결합이 감소한다. 최근에 49 개의 누클레오 티 드로 된 콜리 신 조각과 IF-3 와의 상호작용에 관한 연 구에 서 16S rRNA 의 3' -말단 부분의 독정 한 잔기 들이 보호된 다는 것 이 증명 되 었 다 (W ic- kstr o m, 1983) . 더 구체 적 으로 말하면 , IF-3 는 콜리 신 조각의 5' 끝 부 근에 있는 약간의 찬기 들을 핵 산 가수분해 효소 S1 의 작용으로부터 보 호하지만 그밖의 다를 잔기들 옆에서의 S1 의 작용을 더 강하게 만든다. 이 결 과에 기 초하여 W ick str o m (1983) 은 16S rRNA 의 3' 말단의 49 개 의 누클레 오티 드로 된 부분의 이 차구조를 그림 2-22 와 같이 제 안하였는
 G'm~A
G'm~A
데, 이것은 그 립 2-14 에 나타낸 Nolle r 와 Wo ese( l9 8 1 ) 가 제안한 3' 말 단 부분의 모 형 과 다르다. 오 히 려 van Charldorp 등 (19 8 2) 이 제 안한 16S rRNA 의 이차구 조 와 잔 일치한다. 이 결과는 IF-3 는 나사선 부분 과 강력히 결합하 며 나사선 구조룹 탈안정화시키는 역합운 하는 것으로 생각 된 다. 이러한 탈안정화는 16S rR NA 의 3' - 말단이 mRNA 의 Shin e - Dalga rno 연 속부분 (p. 286 을 보라) 과의 상호작용을 용이 하게 할 것 이 며 더 나아가서 mRNA:rRNA 사이 의 영기 짝짓기가 쉽게 일어날수있 게끔 30S 하위단 위체의 형태를 변화시킬 것으로 생각되고 있다 (Pon 등 1982). 카수가 마이산 은 개시 t RNA 가 리보솜에 결합하는 것을 방해하 며, 이러한 성진로 보아서 번역의 개시반응의 목 이한 방해물로 생각되 고 있다. 이 항생제에 대한 저항성은 16S rRNA 의 1518 과 1519 번 위 치에 있는 두 아데노신 잔기들이 메틸화되지 않음으로써 (정상적으로는 N6,NG- 디메틸화되어 있다) 생긴다는 것 이 밝혀졌다 (Helser 등, 1972). 이와 같이, 여러 각도에서의 실험결과로부터 16S rRNA 의 3' 말단 부 분이 번역의 개시반응에 직접 관여된다는 것은 거의 확실하다. 다) 리보솜의 하위단위체둘의 회합 30S 하위단위체와 50S 하위단위체가 회합하여 70S 리보솜울 만들 때, 단일 가닥 또는 이중 가닥에 득이하게 작용하는 탐침들(화학적인 것 및 효소적인 것)의 작용을 받을 수 있는 자리 들이 가리 워 진 다 (Chap m an 과 Noller, 1977 ; Vassil e nko 등, 1981) . 16S rRNA 의 보호되는 부분들은 주로 3' 에 있는 작은 영역과 중앙 영 역이다. 50S 하위단위체와 결합함으로써 30S 하위단위체의 형태가 더 조밀하게 되어서 16S rRNA 가 탐침들과의 친화도가 감소되는 것으로 생각되고 있다. Herr 등 (1979) 은 30S 하위 단위 체 를 케 톡살로 처 리 하면 50S 하위 단위 체와의 회합이 이루어지지 않음을 관찰하였는데, 케톡살화의 정도를 바 꾸어 가면서 부분적으로 변형한 30S 하위단위체로 조사해 보면 50S 하 위단위체와의 회합에 결정적인 역 할을 하는 것은 16S rRNA 의 3' 말단 부분이라는 것과 이 부분이 70S 리보솜에서 두 하위단위체들 사이의 경 계면에 있다는 것을 확인하였다 (2.6.1 절을 참조하라). 이 발견은 번역 과정에서 rRNA 가 직접적인 기능적 역할을 하고 있다는것을 말해 준다. 라) t RNA 리보솜 상호작용 어 떤 tR NA 들은 그들의 역 코돈둘의 동요
위치에 변형된 염기들을 함유하고 있는데 이 자티에서 UV- 광화학반옹 을 일으킬 수 있다. 이 변형된 염기들은 리보솜의 P 자리에 있을 때 16S rRNA 의 C1400 과 고리 화 첨 가반응을 효과적 으로 일 으킨 다. 이 발견 이 뜻하는 것은 코돈-역 코돈 상호작용의 자리 가 16S rRNA 의 잘 보존되 어 있는 연속부분인 1390-1410 과 아주 가깝게 (~4A) 있다는 것이다. 바 르 앞에서 언급한 바와 같이, 16S rRNA 의 이 부분은 두 하위단위체둔 의 경계면에 위치하고 있다. 파로모마이신-저항성 돌연변이체들은 16S rR~A 의 이 부분에 접한 나사선 줄기의 밀 부분에서 염기 변화들을 가진다는 것 이 알려져 있다. 예를 들면, 효모의 미토콘드리아에서는 C1409 가 G 로 치 산 되어 있으며 (Li 등, 1982) , Tetr a hy m ena 의 18S rRNA 에 서 는 G1491 이 A 로 치 환되 어 있다. 두 경우에 있어서 1409/1491 의 염기 쌍 이 파열되어 있다(그림 2-14 를 보라) . 몇 가지 tR NA 들의 역 코돈과 교차결 합하는 16S rRNA 의 부분 가까운 자리에서 염기 변화가 일어남으로 써 , 〈잘 못 읽기〉의 착 오를 일으키는 것으로 알려진 파로모마이신에 대한 저항성을 얻게 된다 는 것은 놀라운 일이다. 빈 70S 리보솜에서는 16S rRNA 의 몇 개의 자리돌이 여전히 케톡살화 반응을 받는다. 그러나, 풀리송이 형성되고 여기에 결합한 t RNA 의 양 이 증가함에 따라서 530, 966, 1338 및 1517 동 네 자리 에 서 의 케 독살화가 실질적으로 방해된다 (Brow 와 Noller, 1983). 이 자리들은 케독살화의 결과로 t RNA 의 결합이 불활성화되는 자리들과 일치한다. 특히 주목해 야 할 점은 이 자리들이 16S rRNA 의 잘 보존되어 있는 고리 부분에 있으며 〈 16S 와 같은〉 rRl'. J A 들의 공통되는 이차구조의 특징을 이루는 부분들이라는 것이다. tR NA 와 5S rRNA 와의 가능한 상호작용에 관해 서 는 2. 4. 1 절 에 기 술하였다. 마) 펩티딜 기 전달효소 펩티드 결합의 형성을 일으키는 리보솜의 활동 성을 펩티딜 기 전달효소라고 부른다. 다음과 같은 두 가지 접근법에 의 한 분석으로 이 효소의 활동은 23S rRNA 의 영역 V 에 있는 부분 또는 가까운 부분에 있음을 알 수 있다. 한 가지 접 근법 은 클로람페 니 콜一저 항성 (Vazqu e z, 1979) 및 에 리 트로 마이신-저항성 (Sor 와 Fukuhara, 1982) 인 돌연변이체들을 이용하여 이
항생제들에 대한 저항성과 관련이 있는 23S rRNA 상의 위치를 찾아내 는 것이다. 클로람페니콜-저항성을 가진 여러 가지 미토콘드리아의 23S rRNA 들의 돌연 변 이 자리 들이 2447, 2451, 2452, 2503 및 2504 에 위 치 함 이 밝혀 졌 다 (Dujo n , 1980 ; Kearsey 와 Craig , 1981 ; Blanc 등, 1981a 및 1981b). 미토콘드리아에 있어서의 에리트로마이신-저항성 돌연변이는 23S rRNA 의 2058 번 위치에 상응하는 위치에서의 염기 치환으로 일어 나는 것이 밝혀졌다 (Sor 와 Fukuhara, 1982). 이 자리도 역시 영역 V 에 있는 중앙 고리 상에 있다 (그림 2-20 을 보라) . Sta p h y l o coccus 에 있 어서의 에리트로마이신-저항성은 23S rRNA 의 어디엔가 있는 GAAC 연속부분에 있 는 아데닌의 디메틸화에 기인한다는 것이 알려져 있다. 23S rRNA 의 2057-2061 번 위 치 에 있는 GAAC 가 아마도 박테 리 아에 있어서의 에리트로마이신에 대한 민감성에 결정적인 역할을 하는 연속 부분일 것으로 생각된다. 또 하나의 접근법은 t RNA 의 아미노아실 끝 또는 펩티딜 기 전달효소 의 활동성과 관련이 있을 것으로 생각되는 항생제에 반응성 원자단들을 부착시킨 것들을 사용하여, 펩티딜기 전달효소의 친화표지의 탐침둘을 만들었다(자세한 것은 Coo p erman(1980) 의 평론서를 보라). 이 탐침 돌은 23S rRNA 와 반응하는 것이 밝혀졌다. 특히, 최근에, Bar t a 와 Kuechler(1983) 는 친화 탐침으로써 Phe- t RNA 의 벤조페논 유도체 3- [4- 벤질패닐〕-프로피오닐 -Phe- t RL' .J A 를 사용하여 t RNA 가 푼리 (U) 로 프르그람된 리보솜의 23S rRNA 에만 교차결합된다는 것을 관찰하였다. 탐침으로 표지되는 정확한 위치는 23S rRNA 의 U2584 임이 밝혀졌는데, 이 결과도 역시 펩티딜 기 전달효소의 위치가 영역 e 의 중앙 고리 가까 운 곳에 있음을 가리키는 것이다(그림 2-20 참조). 바) 연장 -GTPase 활동성 항생물질 티오스트랩본은, 리보솜의 GTPase 활동성 이 EF-G, EF-T 또는 IF-2 에 의 존성 인 것 이 든 아니 든, GTPase 의 활동성 을 직 접 방해 하는 것 으로 보인 다 (Cuntl if f e ( 1980) 의 평 론서 를 보라) . Str e pt om y ce s azttr e us 의 티 오스트랩 본-저 항성 은 23S rRNA 의 Al067 의 리보오스 부분의 메틸화에 기인된다는것이 밝혀져 있다. 이 위 치는 GTPase 와 관련된 기능에 강력하게 관여하고 있는 단백질 Lll 이 결합하는 자리이기도 하며 23S 와 유사한 rRNA 들의 영역 b 에 상응한 다. 최 근에 Sk6ld (l983) 는 디 에 폭시 부탄을 교차결 합 작용물로 사용하
여 EF-G 와 E. col i의 23S rRNA 와를 교차-결 합시 켜 그 자리 가 1055- 1081 까지의 연속부분이 라는 것을 알았다. 이 결과 또한 A1067 이 GTPase 의 활동성과 관련될 것이라는 가설을 뒷받침하는 것이다 . 사) 스위치 번역이 일어나는 동안 리보 송은 mRNA 를 따라서 움직인 다. 그밖의 분자간 또는 분자내의 운동이 번역이 일어나는 동안 일어날 수도 있을 것이며, 리보솜에는 〈움직이는 부분들〉이 있어야 하지 않을 까하는 문제가 제기된다• 만일 이러한 〈움직 이는 부분 들〉 이 실제로 있 는 것이 밝혀진다면 그들의 움직임은 번역에 있어서 매우 중요한 것 일 것이며, 그들은 적어도 부분적으로라도 rRNA 로 부터 구성뭘 가능성 이 매우 크다. 그러나 현재로서는 스위치의 존재를 증명합 결정적인 실험 격 증거들을 얻지 못하고 있다. 이전에는 rRNA 구조의 움직임은 나사선 구조들을 〈만들 고 해체하 는 것 〉에 서 생 길 것 이 라고 제 안되 었 으나 (Noller, 1980 ; Brim acombe 등 19 83; Fox 와 Woese, 1975) 차차 더 많은 rRNA 들의 일 차구조들이 분석 되고 이것들을 비교분석해 봄으로써 그러한 제안들이 옳지 않음이 확인 되었다. 상호간에 배타적인 나사선 구조들을 이 룰 수 있는 것으로서 유 일하게 알려져 있는 것은 앞에서 말한 16S rRNA 에 있어서의 〈매듭〉 이 다 (2.4.2 철의 때 항을 보고 그림 2-14 를 보라). 그러나 생화학적 탐 침 실험들에 의하면 이 매듭은 단일 가닥에 독이한 작용물들에 가끔 민 감하기 때문에, 이 매듭의 두 나사선들이 세포 내에서 공존할 수 있을지 는 현재로서는 의문이다. 스위치 메카니즘에 관한 또 하나의 매력적인 가설은 나사선 구조들이 공축 상에서 치쌓임과 치쌓임의 해체가 교호적으로 일어난다는 것 이다 (Sta h l 등, 1981 ; Woese 등, 1983 ; Noller 등, 1981) . 이 러 한 매 카니 즘 은 염기쌍이나 그밖의 수소결합들을 파열시켜야 하는 일에 관여됨이 없 이 정확하고 대규모적인 형태의 변화를 야기시키게 될 것이다. 그러나 이 가설을 증명할 수 있는 근거도 아직은 없다• 그러나 삼차구조와 관련되는 스위치는 우리가 생각할 수 있는 또 하 나의 홍미있는 가능성이다. 단리한 5S rRNA 의 경우이기는 하지만 삼차 구조의 변화에 대 한 직 접 적 증거 가 최 근에 관찰되 었 다 (Kao 와 Croth e rs, 1980). 이 연구자들은 10°c 에서 40°c 까지의 온도 범위에서 E. co li의 5S rRNA 의 녹음 전 이 (meltin g tra nsit ion ) 를 조사하였 다. 염 류가 핵 산
의 안정성에 미치는 흔히 볼 수 있는 효과와는 반대로 일가 및 이가의 양이온돌을 첨가함으로써 전이점 (t,,,)을 감소지키는 것을 알았다. 또한, 의의로, t., 이 생리적 pH ( 7~ 8) 범 위에서 pH 에 크 게 좌우된다는 것을 알았다. 확산 상수의 측정 결 과들은 저 온형 이 고온 형 보다 마창계 수가 약 10% 만큼 더 크다는 것을 보여 주었다. 이 결과는 저온형 삼차구조는 수소이온을 결합할 수 있음을 의미이다. 생리적 조건에 가까운 범위에서 pH , 온도, 또는 양이 온의 농도들을 종가시 키 면 양이 온돌을 더 많이 결 합하고 수소이온은 덜 결 합하는 더 조밀한 형태로 바뀐다. 위예시 언급한 실형질과들은 바람 직한 도든 성질들을 가지고 있다. 즉, 형태의 전이는 생리적 이온 조건에서 일어나며, 수천 분의 일 초의 지간 최도에서 일어나기 때문에 단백질 합성에 있어서의 순환식 과정 예 알맞을 정도로 신속하게 일어나고 있다. 확산 상수에 있어서의 10% 의 변화로 나타나는 조밀성의 변화는 5S RNA 분자의 치수로 보면 약 15A 의 치수의 변화에 해당하는데 이것은 t RNA 와 mRNA 들이 리보솜 예 대한 상대적인 움직임을 일으키기 에 충분한 치수라고 생각한다. 그 러므로, 5S rRNA 가 저온형과 고온형 사이에서 주기적으로 형태변화를 일으킨다는 것은 단백질 합성의 본질적 부분이라고 생각된다. 사실이 그러하다면 5S rRNA 가 단백질들과 복합체를 이루었을 때도 형태의 변 화가 있을 것이며, 궁극적으로는 리보승 자체에서도 일어날 것이다. 리 보솜 단백질들은 rRNA 주변의 pH 환경을 근소한 범위에서 바꾸는 역 할을 할지도 모른다. 2.5 원핵세포의 리보솜의 구조 2.5.1 개요 단백질 생합성은 리보솜 상에서 일어나고 있으며 여러 단계들로 구분 되어 순차적으르 진행한다. 지금까지 이 문제가 광범위하게 연구되어서 단백질 생합성의 과정과 단계들에 관해서 어느 정도 서술적인 설명이 가능하게 되었지만, 리보솜의 구조와 기능의 상호관계에 관해서는 아직 초보적인 단계에 머무르고 있다. 그러나 리보솜에 관한 최근의 활발한 연구에 의해서 단백질 합성의 개시, 연장, 및 종결 단계들에서 일어나
는 반응 메카니즘이 조금씩 밝혀지기 시작하고 있다. 리보 솜의 구조와 성분들에 관한 명확한 통찰력없이는 단백질 생합성 과정예 관한 우리들의 지식은 서술적인 수준웅 벗어날 수 없을 것 이며, 펩티틸-t RNA 의 자리 옮김 또는 펩티달 기 전달효소의 작용 , 그리고 여 러 가지 인자들, mRNA , tR NA 및 항생물질들과 리보솜 사이의 상호 작용들의 분자적 메카니즘에 관한 문제의 본질이 밝혀질 수 없을 것 이다. 1960 년대 에 와서 리 보솜이 많은 단백 질 들과 RN A 분자들로 구성 되 는 복합 체 형태의 입자라는 것이 알려진 이후로 화학적 , 물리적 및 면역학 적 방법들을 사용하여 티보솜의 성분들융 단리하여 그 성질을 규명하 고 자하는 연구들이 이 루어져 왔다 . 2 . 3 절과 2.4 절 들에서 기술한 바와 같 어, 이러한 연구들은 주로 E. col i의 리보솜에 대해서 실시되어 중요 한 정보 를 얻게 되었다. 지난 10 년 동안 리 보솜 입자들의 구조, 죽 리보솜 입자들의 모양과 그들의 RNA 및 단백 질 성분들의 리보솜 입자 내에서의 공간 배열을 밝 히기 위한 많은 방법들이 개발되었다 .. 가장 널리 사 용 되는 방법들에는, 첫째로, 면역 전자현미경 사진법이 있다. 이 방법은 리보솜의 하 위단위 체용들된의 다 (모Ste양 f f과le r 그등,들 의1 98표0 ;면 L에a ke있, 어1서98의0) . 단백둘째질 들르,의 리위 보치송를 하밝위히 단는위 데 체 사에 있어서의 단백질들의 질점들 사이의 거리를 측정하는 중성자 산란법이 있다 (Moore, 1980, 방법 에 관해 서 는 Koch 와 Pil t z (l979) 를 참고하라) . 세째로, 여러 가지 이작용기성 시약들을 사용하여 단백질-단 백질 의 교 차결합을 분석하여 리보솜 입자 내에서의 단백질들의 근접성과 70S 리 보솜에 있어서의 두 하위단위체들의 경계면에 있는 단백질들이 어떤 것 둘인지를 밝힐 수 있다. 네째로, 비슷한 방법으로 RNA- 단백질 교차 결합을 분석함으로써 단백질과 RNA 의 근접성을 알 수 있다 (Z i mmer mann, 1980). 다섯째로, 리보솜의 특이한 자리들에 부착시킨 두 가지 형광성 색소들 사이에서 일어나는 단일상태-단일상태 에너지 전달을 분 석함으로써 두 자리들 사이의 거리를 측정할수 있다 (Can t or 등, 1974). 끝으로, 리보솜의 재조립 과정을 조사하여 조립도를 구성해 봉으로써 리 보솜 단백질들의 입체배열에 관한 간접적인 정보 를 얻을 수 있다. 위에서 말한 방법들 중에서 E. col i의 리보솜의 구조를 밝히는 데 중 요하게 기여한 것들은 주로 면역 전자현미경 사진법, 중성자 산란법, 교차결합법 등이다.
2, 5. 2 리보솜 입자들의 모양파 크기 가 ) 작은 각 분산법으로 얻은 결과 작은 각 X- 선 회절법 과 유 체역학 적 측정 들 로 얻은 결과에 의하면 리보솜의 하 위단 위체들의 대강 한 구조는 타원 체로 나타나 고 있다(자세한 수치들에 관해서는 van Hol de 와 Hi ll (1974) 의 평론서를 보라) . 30S 입자의 치수는 대강 5.5x22x22nm 로 계산되고 있다. 50S 히위단위체는 1 1. 5x23x23nm 의 타원체의 치수를 가지고 있다. 50S 하위단위체의 치수는 전자현마경 사진법에 의한 결 과 와 잘 일치하고 있지만 , 30S 하위단위체의 경우에는 사용한 방법들에 따 타 서 그 치 수들이 상당히 다 르다. 증성자 산란법에 의한 연구르 리보솜과 그 하위단위체들 내에 있어서 의 단백질과 RNA 의 분포를- 조금은 알 수 있게 되 었 다. 30S 입자에 있 어서는 R NA 의 회전반경은 약 6nm 이다. R NA 와 단백질은 거의 공중심 을 가지게끔 분포되어 있지만 균일하게 분포되어 있는 것은 아니다. 다 시 말하면, RNA 는 주로 입자의 중심 쪽으로 자리잡고 있지만 단백질 은 입자의 외곽 쪽 으로 있다. RNA 및 단백질 부분들에 대한 질량중심 들은 거의 일치한다. 또한 30S 입자 내에 있는 16S rRNA 를 산란법으 로 분석 하여 얻 은 16S rRNA 의 구조 (Se rdy uk 등, 1979 ; 1983) 는 단리 한 16S rRNA 분자 또는 30S 하위단위 체에 서 단백질을 거의 다 제거한 16S rRNA 입자를 전자현미경 사진법으로 결정한 V- 자형 구조와 찰 일 치 한다 (Vasili ev 등, 1977; 1978) (그림 2-23) .
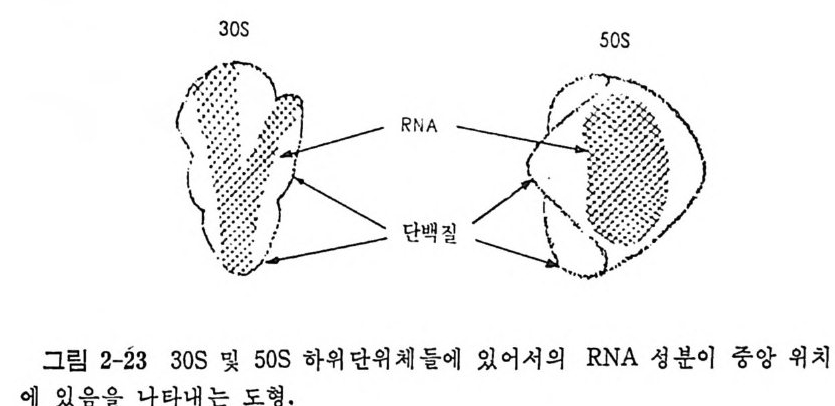 30S 50S
30S 50S
50S 입자 내에서의 RNA 와 단백 질의 분포에 관해서 여러 연구진은 오랫동안 상치된 견해를 가지고 있었다. 그러나, RNA 와 단백질 부분 들이 크게 떨어져 있지 않다는 사 실과 RNA 와 단백질의 희전반경들(각 각 5-6nm 와 9-10nm) 이 크게 차이가 있는 사실로 보 아 서 R NA 는 주 로 내부에 자리잡고 있고, 한편 단백 질 은 50S 하위단위 체의 외곽 부분 에 공중심적으로 분포되어 있다고 생각된다 (Scrd y uk 등 , 1979) ( 그 립 2-23 을 보라). 70S 입 자에 있어 서 의 RNA 와 단 백 질 부분 둘 의 회 전 반 경 은 각각 7nm 와 10nm 이다. 개개의 하위단위 체들과 70S 리 보 솜 에 대 한 산란법에 의 한 실험치들을 비교해 봄으로 써 , 하위단위 체들 이 회합 할 때 그 들 의 헝 태가 심하게 달라지지 않는다는 것을 암시해 준 다. 나) 전자현미경 사진법으로 얻은 결과 원리적으로 말하면, 전자현미경 사 진법은 리보송과 그 하위단위 체들의 전체적인 모양과 대강한 구 조를 연 구할 수 있는 가장 직접적인 방법이다. 따라서, 이 방법이 티보솜 연구 에 가장 많이 사용되고 있다. 티보솜은 그 크기가 비교적 작고 짢 이 수 화 되어 있기 때 문 에 전자 선 으로 조사하면 손상되기 쉽고, 또 탈수하면 그 형태가 이그러 지기 쉽 다. 따라서, 전자현미경 사진법으로 리보 솜의 구조 를 연구하는 사람들은 티 보솜의 구조에 대해서 주관적인 견해을 가지게 되므로 여 러 가지 모 형 들이 제안되고 있는 것은 놀라운 일이 아니다(그림 2-2 4 를 보 라). 여러 가지 모형들 사이에는 차이점들이 있지만, 30S 하위단위 체 가 대 개 23x14nm 의 치수를 가진 비대칭적인 길쭉한 구 모양의 입자라는 점 에서는 일반적으로 일치한 견해를 가지고 있다. 30S 하위단 위체는 입자 의 삼분의 일쯤 되는 〈머리〉 부분, 삼분의 이쯤되는 〈몸통〉 부분, 그 티고 이 두 부분을 분할하는 〈목〉 부분과 하나 또는 두 개의 돌출 부 (〈귓불〉 또는 〈플랫폼〉)들로 구성되어 있다. 그림 2-24 에 나타낸 도형 들로부터 알 수 있는 바와 같이, 모 형들 사이의 차이는 하위단위체의 비대칭성의 정도, 돌출부의 수, 크기 및 모양, 그리고 또 〈머리 〉 와 〈몸 동〉 사이의 분할 부분의 깊이 등에 있다. 큰 하위단위체에 대한 여러 가지 모형들은 작은 하위단위체의 경우에 서보다는 비교적 찰일치한다. 두 가지의 주요한 모형이 제안되어 있다. 그 하나는 준대칭성을 가진 〈왕관〉형이고(그림 2-24 a) 의 또 하나는 바
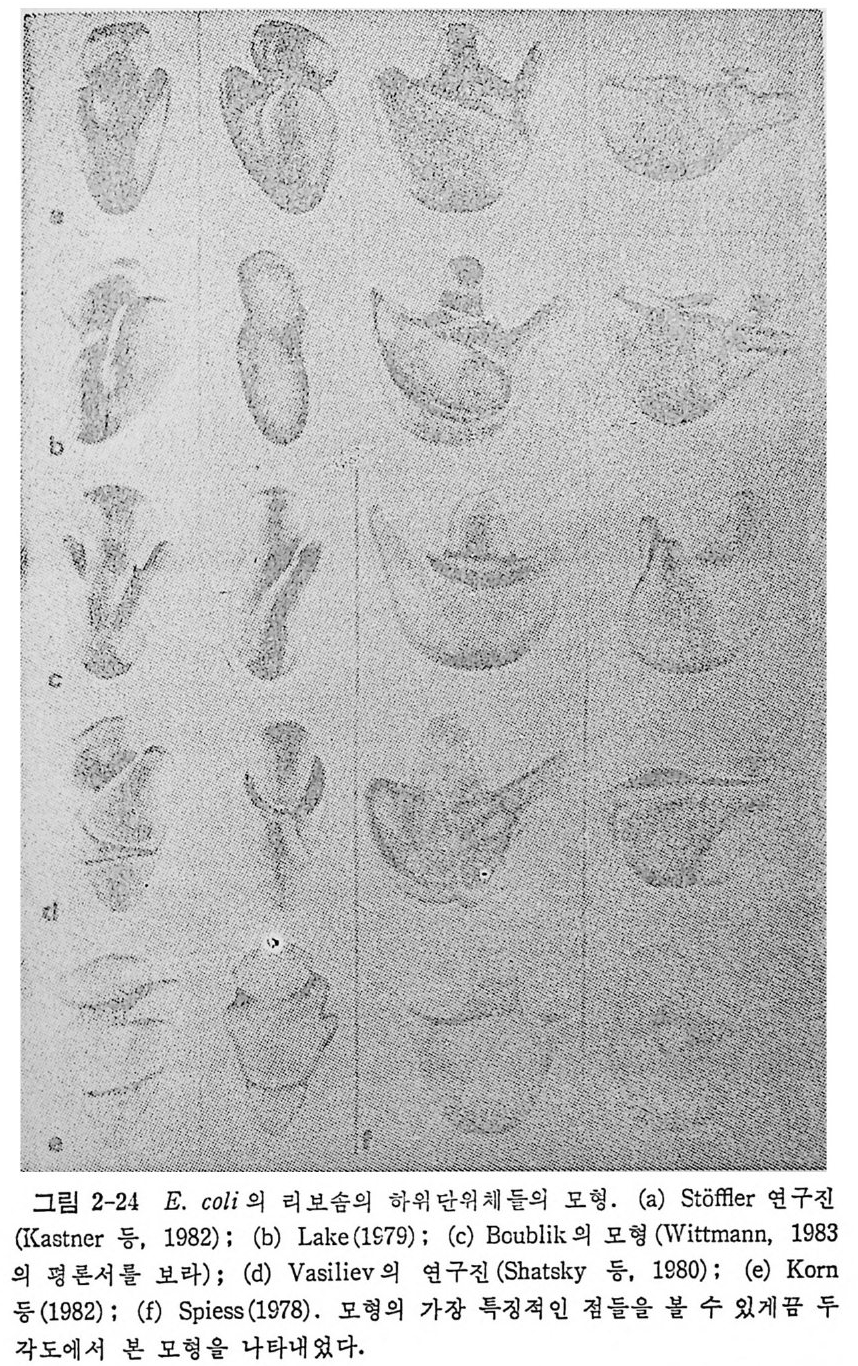 ,'.,‘.'..A&'·'·f,yt,':;.t“:t'.tf'·f4't&‘ . . . . t . , . ’ `8u..J,f s 2.` \..i :f.,죠E감.걸유 .g었f .,玉-집~二〉까`. 것".'cI,'4`?': ., J\ .`~. . s ,. . r> A.3 ‘.•,•,?g '. C . .' . ‘,. 7 &:.k (
,'.,‘.'..A&'·'·f,yt,':;.t“:t'.tf'·f4't&‘ . . . . t . , . ’ `8u..J,f s 2.` \..i :f.,죠E감.걸유 .g었f .,玉-집~二〉까`. 것".'cI,'4`?': ., J\ .`~. . s ,. . r> A.3 ‘.•,•,?g '. C . .' . ‘,. 7 &:.k (
대칭성을 가진 〈콩팥〉형 (또는 〈초승달〉형)이다(그림 2-24 의 b). 그립 2-24 에서는 큰 하위단위체의 전면과 측면을 볼 수 있게 나타내었다. 이 입자는 칙경이 약 23nm 되는 반구 형 이고, 크기와 모양아 다른 세 개의 돌출부를 가지고 있다. 중앙에 있는 둥그스름한 돌출부(〈코〉) 의 양쪽 옆으로 두 개의 돌 출부가 있는데, 그 하나는 막대 모양을 하고 있고 (〈줄기〉), 단백질 L7 / L12 를 네 벌 가지 고 있으며, 입자의 한쪽 옆으로 8-12nm 의 길이로 뻗쳐 있다. 그 반대편으로 있는 돌출 부 (〈 등마루 〉 또 는 〈 L1- 어깨〉)는 약간 둥그스름하며 단백질 L1 이 여기에 위치하 는 것 이 특징이다. 전자현미경 사진법에 의한 연구에 의하면, 70S 리보송 입자는 목별한 구조적인 특칭을 가지지 않으며, 직경 이 약 23nm 의 둥 그스 름한 구의 모양을 가지고 있음을 알 수 있다. 여 러 가지 모형 들을 그 림 2-25 에 나 타내었다. 이 모형들을 보면, 70S 입자의 구조는 그 안에서 작은 하위 단위체와 큰 하위단위체가 서로 어떠한 방향으로 배치되는가에 다라서 다르다는 것을 알 수 있다. 이들 중 세 모형(그림 2-25 의 a,b,d) 에 있 어서는 작은 하위단위체의 머리가 큰 하위단위체의 L1- 어깨와 중앙의 돌출부 사이 에 비 스듬하게 대 각선 상으로 놓여 있다. 또 하나의 모형 (그 림 2-25 의 c) 에 있어서는 70S 리보솜 내에서의 작은 하위단위체의 배향 은 그 머리를 큰 하위단위체의 줄기에 가깝게 두고 큰 하위단위체의 두 돌출부둘 사이에서 왕관 부분을 길다랗게 가로지르고 있다. 위에서 본 여러 모형들은 두 하위단위체들 사이의 경계면이 또한 다르다. 모형들 이 서로 일치하지 않는 이유는 제안된 하위단위체들의 모형들이 다르기 때문이다. 한 가지 공동점은 모든 70S 모형들에 있어서 작은 하위단위 체의 돌출부들이 큰 하위단위체의 골짜기 면을 향하고 있다는 것이다. 2. 5. 3 리보솜 단백질들의 공간 배열 가) 면역 전자현미경 사진법에 의한 분석 온전한 리보솜 내에서의 53 가 지의 리보솜 단백질들의 공간 배열에 관한 지식은 리보솜의 구조적 조 직과 구조와 기능 사이의 관계를 이해하는 데 꼭 필요하다. 전자현미경 사진법은 리보솜 표면에 있어서의 단백질들의 공간 배열 을 밝힐 수 있는 중요한 정보를 제공하였다. 전자현미경 사진법을 이용 하자면 각 리보송 단백질에 대해서 특이하게 작용하며 교차반응을 하지
않는 항체 를 얻 는 것 이 선 결 문제 이 다 (Sto f fll e r 와 Wi ttm ann, 1971a 및 b). 그뿐 아니라, 단리한 단백질들에 대해서 만든 특이한 항체들이 온 전한 리보솜 입자에서도 동족 단백질들과 반응할 수 있어야 한다. 면역 전자현미경 사진법이 리보솜 연구에 처음으로 이용된 이래로 리 보솜의 두 하위단위체들의 단백질들의 위치들이 많이 결정되었다. 이 연 구결과에는 오차가 생기는 수가 흔히 있었는데, 그것은 제조한 항체가 불순하였기 때문이었다. 최근에 친화 크로마토그래피를 이용하여 순수 한 항체들을 얻을 수 있게 되었다. 따라서 단백질들의 위치를 더 정확 하게 결정 할 수 있게 되 었다. 최 근까지 얻은 결과를 그림 2-26 과 2-27
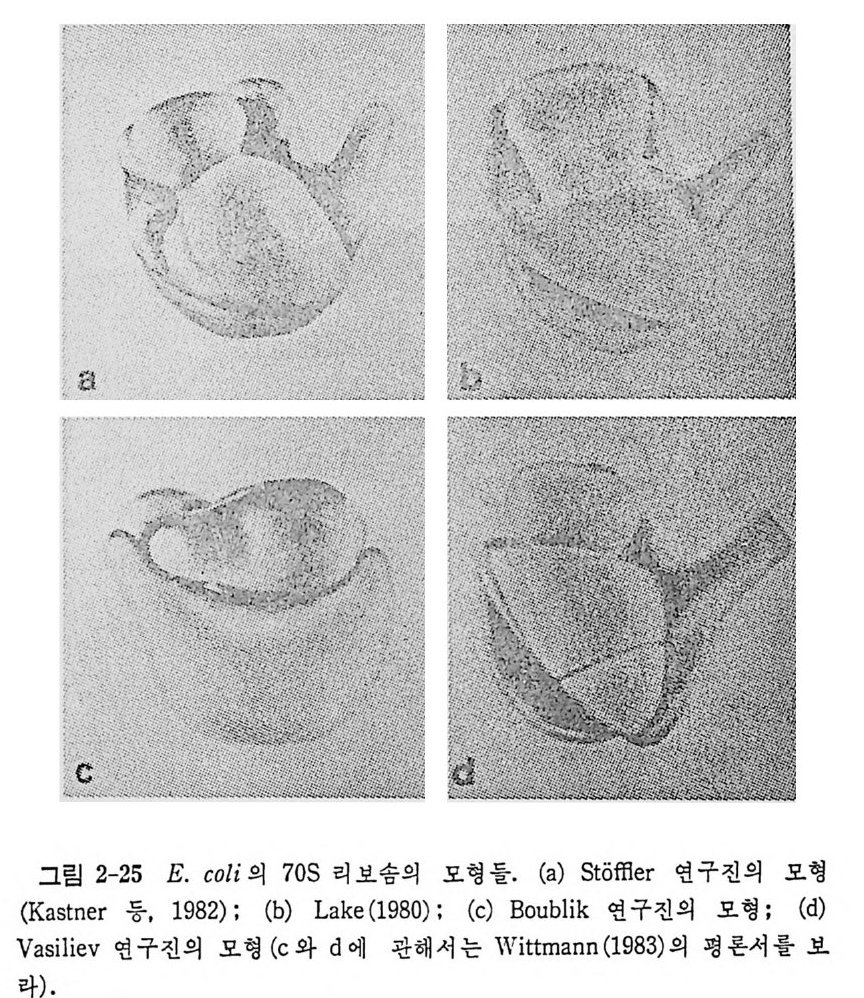 그립 2-25 E. coli 의 70S 리 보솜의 모형 들. (a) Sti iffler 연 구진 의 모형
그립 2-25 E. coli 의 70S 리 보솜의 모형 들. (a) Sti iffler 연 구진 의 모형
 ,.· .••
,.· .••
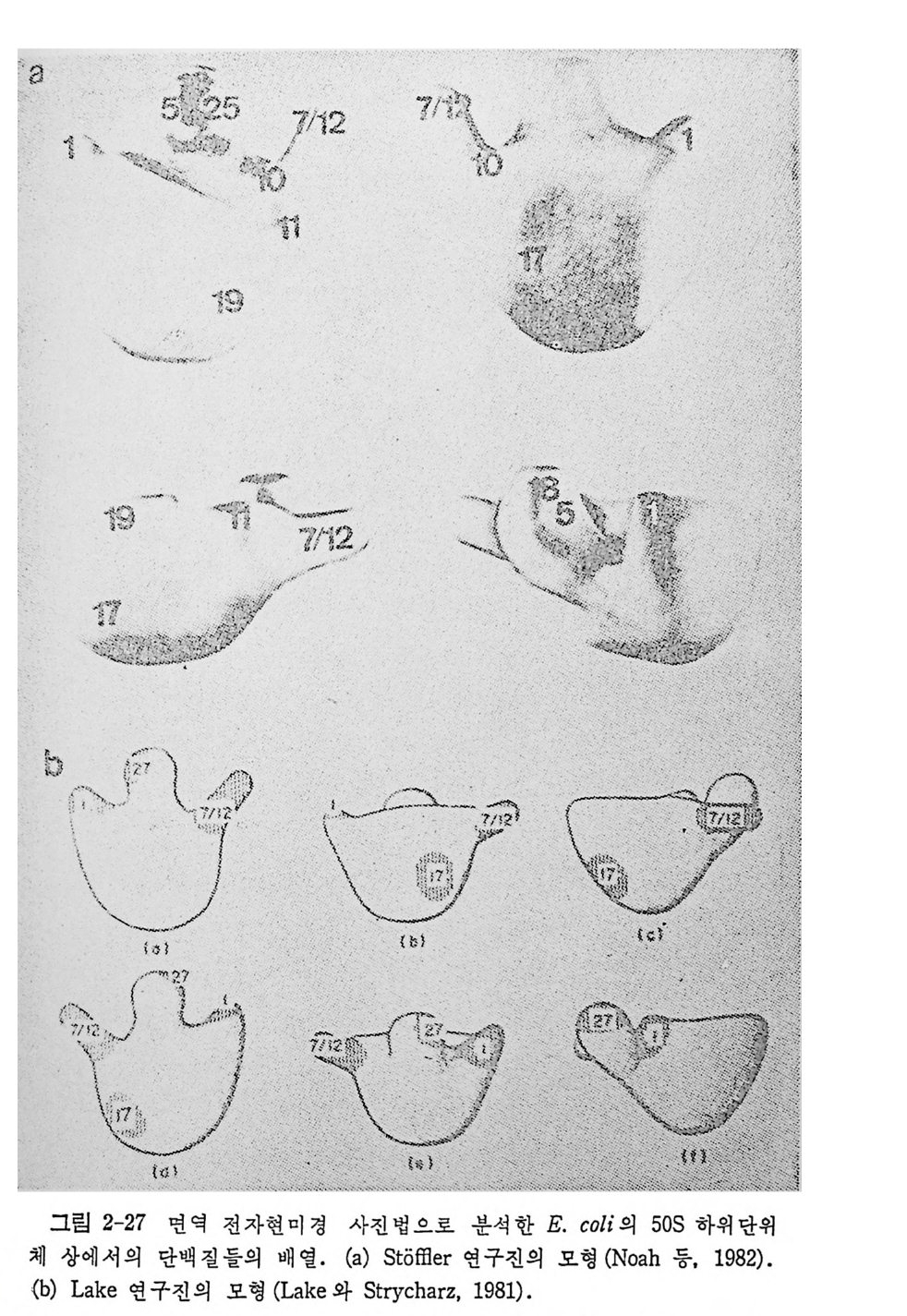 2 숫‘ ``'· `와 < . `\`:,<~ .',S. 1냐다 ;` :r;쌍건,~. 혹 ;-뚜· ;~,' r> ’깡출 1 3rS . ` f/미' ?떠 ' 1 2 w.. t 2`서 , ?iA沼ff f b` 언 2 A4 r여3 <· &'.5.. , .} ,. . .'&.,, ..` . 5 ·홍 ’소꾼핥 ', .. # %t ’,, '~.F, ' `... .:Jt.~, 친•.,,'..'t, .r4쓰,.:..3‘5/ :. ...껑•f I.羽故/g%J•Eg ki값갱건g3'` 경장'3'성'.•多$.서겁 .십겅간r. , . ' . , .. (.~
2 숫‘ ``'· `와 < . `\`:,<~ .',S. 1냐다 ;` :r;쌍건,~. 혹 ;-뚜· ;~,' r> ’깡출 1 3rS . ` f/미' ?떠 ' 1 2 w.. t 2`서 , ?iA沼ff f b` 언 2 A4 r여3 <· &'.5.. , .} ,. . .'&.,, ..` . 5 ·홍 ’소꾼핥 ', .. # %t ’,, '~.F, ' `... .:Jt.~, 친•.,,'..'t, .r4쓰,.:..3‘5/ :. ...껑•f I.羽故/g%J•Eg ki값갱건g3'` 경장'3'성'.•多$.서겁 .십겅간r. , . ' . , .. (.~
에 나타내었다. 전자현미경 사진법으로 E. col i의 리 보송의 구조문 연 구하고 있는 두 주요 연구진 들의 결과는 비교적 장 일치하는 모형들올 주고있다. 나) 중성자 산란법에 의한 분석 이 방법은 가벼운 수소와 무거운 수소 는 각각 중성자를 상이한 정도로 회절시키는 사실을 이용한다. 중수소 로 표지된 리보솜 단백질들의 질량 중심들을 결정하여 단백질들 사이의 거리를 측정할 수 있을뿐 아니라 리보솜 하위단위체 들 또는 리보송 입 자 내에서의 단백질들의 모양을 결정할 수 있다. 먼저, D20 에서 키운 E. coli 세포에서 중수소로 표지된 개개의 리보솜 성분 들을 단리한다 . 그 다음에, 조사하고자 하는 두 가지 단백질은 중수소로 표지된 것을 쓰고 다른 19 가지 단백질은 가벼운 수소로 표지된 것을 써서 30S 하위 단위체를 재조립한다. 중수소로 표지된 단백질 쌍을 여러 가지로 바꿔 가면서 재조립한 30S 하위단위체들에 있어서의 두 단백질 쌍들의 질량 중심둘 사이의 거리를 측정할 수 있다. 지금까지 약 14 가지의 단백질 들에 대한 질량 중심둘이 결정되었다. 두 질점들 사이의 거리를 삼각
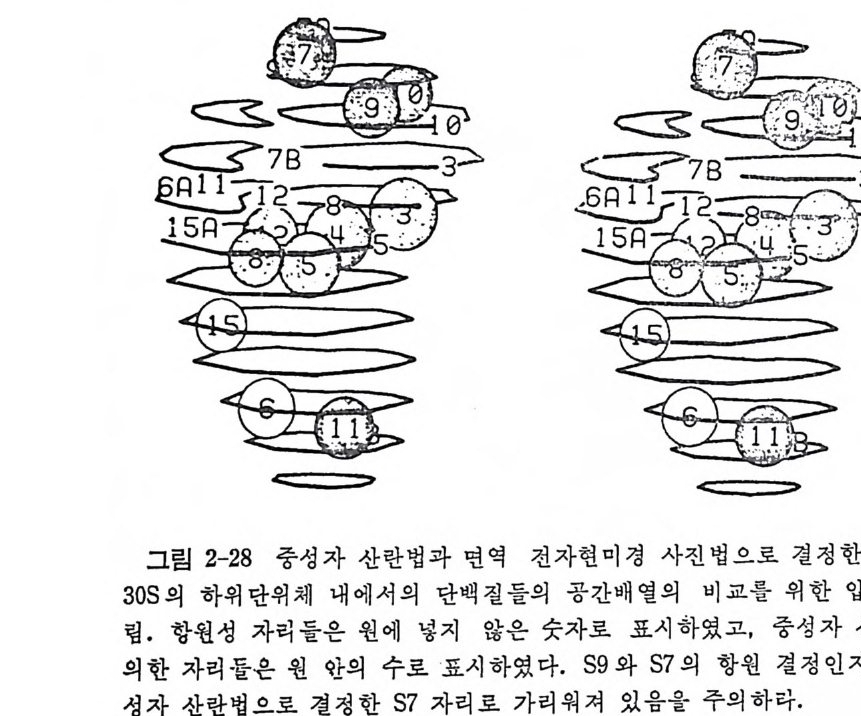 二
二
측정법으로 계산함으로써 이 단백질들의 공간 배열을 결정할 수 있다. 중 성자 산탄법과 면역 전자현미경 사진법으로 결정한 30S 하위단위체 내에 서의 공간 배열은 매우 잘 일치한다(그림 2-28 을 보라) (Moore, 1980). 다) 형광표시법에 의한 분석 두 가지의 리보송 성분들(단백질 또는 RNA) 중 하나는 주개로 작용할 형광 색소로 표지하고 다른 하나는 받 개로 작용 할 형광 색소로 표지한 다음에 하위단위체를 재조립한다. 단 일상태-단일상태 에너지 전달을 측정하여 형광성 표지물들 사이의 거리 를 계산 할 수 있다. 이 방법을 사용한 초기의 연구들은 주로 30S 입자 내에서의 단백질 들 사이의 거리 측 정에 관심을 두고 있었지만 (Glor i a 와 Kanto r , 1979 ; Ep e, 1982) , 지 금은 이 방법 이 50S 입 자뿐 아니 라 5S, 16S 및 23S rRNA 들에 도 응용 할 수 있다 (Odon 동, 1980; Lee 동, 1981 Zante m a 등, 1982; S t e i nh 걸 user 등, 1982) . 또한 형 광표지 법 은 리 보솜 상에서의 t RNA 들, 개시인자들, 스트랩트마이신과 에리트로마이신과 같은 항생물질들의 위치들을 결정하는 데에도 이용된다 (Pes t ka, 1977; Weil 과 Hershey, 1981) . 형광법으로 조사한 결과들을 중성자 산란법, 전자현미경 사진법 및 교 차결합법 등으로 조사한 결과들과 비교해 보면 대개의 경우 서로 찰 일 치하고 있지만 약간의 경우에는 일치하지 않는 경우도 있다. 이러한 차 질이 생기는 이유는 에너지 전달의 정도는 형광성 색소들 사이의 거리에 따라서만 결정되는 것이 아니라 색소들의 상대적인 배향과 같은 그밖의 요인들에 의해서도 달라지기 때문인 것으로 생각된다. 이러한 약간의 제한이 있음에도 불구하고 형광표지법은 리보솜 성분들의 공간 배열에 관해서 유용한 정보를 제공해 주고 있다. 특히 특수한 잔기들에만 색소 가 결합하는 경우에는 리보솜 입자 내의 독수한 단백질들 사이의 거리 를측정할수있다. 라) 단백질-단백질의 교차결합에 의한 분석 이 작용기 성 시 약들을 사용하 여 리보솜 내에 있어서의 인접한 단백질들을 확인하고자 하는 점근법은 꽤 일찍부터 응용되었다. 최근, 제일 흔히 사용되는 시약은 2- 이미노티 올란인 데 (Traut, 1980) (그림 2-29 및 2-30) , 이 시 약은 RNA- 단백 질 교 차결 합에 도 사용된 다 (Wower, 1981) . 여러 연구진들이 두 하위단위체들과 70S 리보솜을 가지고 교차결합
연 구를 광범 위 하게 하였 다 (Peretz , 1976 ; Kurland, 1977 ; Exp er t-B eza. neon 등, 1977). 이 분야에 있어서의 Traut 연구진의 기여는 매우 크
 H/24c _ _3· \야 @ e
H/24c _ _3· \야 @ e
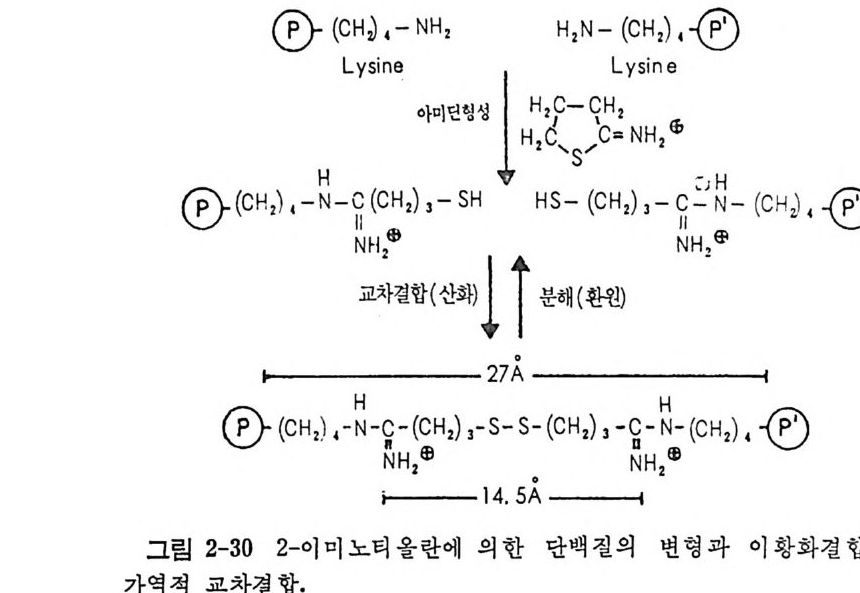 ®-(CH ~ , -N H2 H2N - (CH2) , 순)
®-(CH ~ , -N H2 H2N - (CH2) , 순)
다 (Traut (1980) 의 평 론서 , Cover 동, . 1981 ; Boil e au 등, 1981) . 교차 결합에 의한 몇 가지 분석결과를 그림 2-31 에 나타내었다. 교차 결합 법, 중성자 산란법 및 면역 전자현미경 사진법 들에 의한 결과들은 서 로 찰 일치한다. 일반적으로, 교차결합될 수 있는 단백질들은 다른 두 방법으로도 서로 인접해 있음이 알려져 있다. 두 단백질들이 서로 인접 하고 있으면서도 교차결합되지 않는 경우가 있는데, 이것은 아마도 교 차결합용 시약이 접근할 수 있는 위치에 리신이나 시스테인들과 같은 적 절한 아미노산 잔기들이 없어서 그러할 것이다.
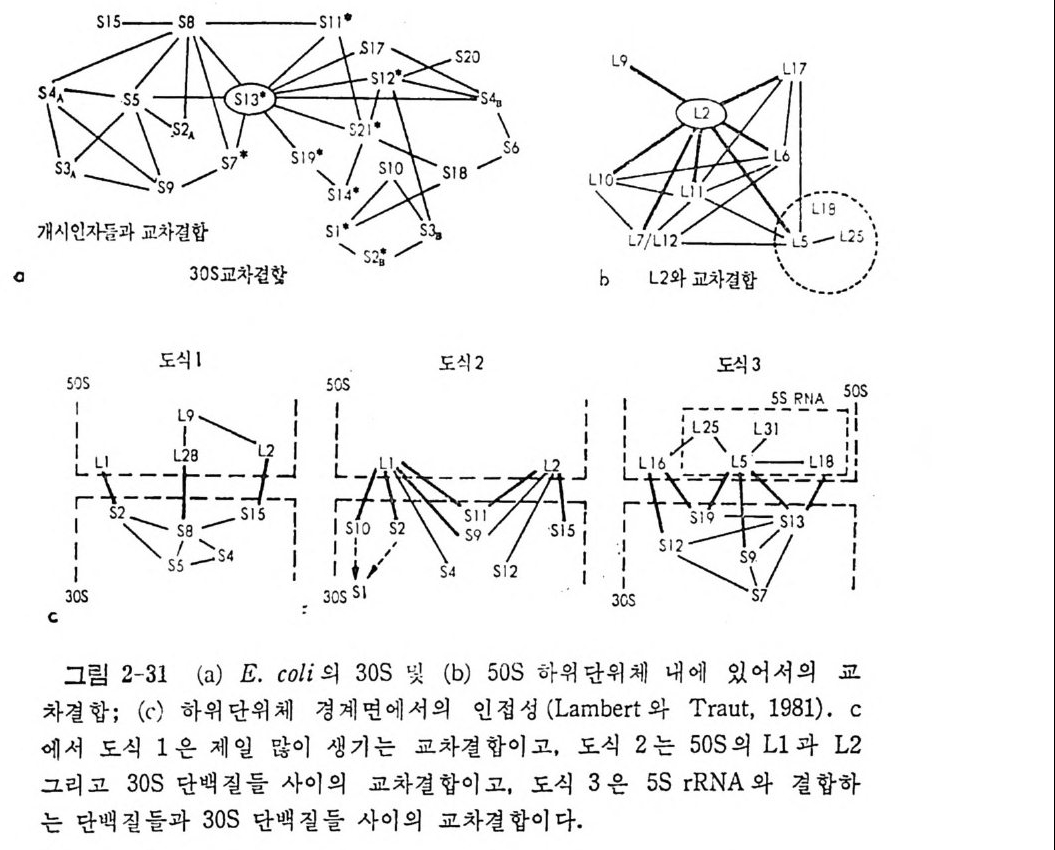 ~S15/-S8h - _kS모11• 's \녹 ? I`
~S15/-S8h - _kS모11• 's \녹 ? I`
교차결합에 의한 분석치들은 30S 와 50S 하위단위체들에 관한 정보 뿐 아니라 두 하위단위체들 사이에 생기는 경계면에 관한 공간 배열에 관한 정보도 제공한다. 그림 2-31 에서 작은 하위단위체와 큰 하위단위 체의 단백질들 사이 그리고 5S rRNA 와 단백질들 사이의 교차결합을 알 수 있다. 이 그림에서 5S rRNA 와 회합하는 단백질 L5 와 Ll8 들은 30S 하위 단위 체 의 S9, S13; 및 S19 들과 교차결 합함을 알 수 있고 이 결과에서 5S rRNA 복합체가 경계면에 위치한다는 것도 알 수 있다. 이 복합체의 세 가지 단백질들 (S9,S13 및 S19) 이 작은 하위단위체의 머리 에 자리잡고 있으며 (그림 2-26 을 보라), 5S rRL\ J A 와 결합하는 큰 하 위단위체들의 단백질들이 큰 하위단위체의 중앙 돌출부(코)에 자리잡고 있다는 결과(그림 2-27 을 보라)와 찰 일치한다(그림 2-25 에 나타낸 70S 입자의 모형과 비교해 보라).
E. col i의 리보솜 단백질들의 일차구조들이 알려져 있으므로, 아작용 기성 시약으로 교차결합된 단백질 사술들 내에서의 아미노산 잔기들의 정확한 위치 듈을 쉽게 결정할 수 있다. 이러한 방법으로 단백컬 S8 의 13 번 위치가 S5 의 166 번과 교차 결합한다는 것 이 분석되었다 . 이 결 과에서 30S 하위단위체 내에서 이 두 아미노산들은 사용한 이작용기성 시약의 결침 거리인 0.8nm 이상 딸어져 있지 않음을 암시히 준다. 이 러한 분석이 정확하다는 것은 166 번 잔기물 가지지 많는 돌연변이체의 단백질 S5 를 가지고 실시한 대조 분석에서는 예기한 바와 같이, 교차결 합이 전혀 일어나지 않는다는 사실로 확 인되 었다 (Allen 등, 1979) . 마) 단백질 복합체들의 형성 리보솜의 단백 질들을 개별적으로 단리하려 고 할 때 둘 또는 둘 이상의 단백질들 사이에서 여러 가지 목이한 복합 체들이 따로 분리되는 것을 흔히 불 수 있다. 제일 집중적으로 연구된 복합체 들은 L7/ L 12 를 함유하는 것 들인 데 , 이 들은 사합체 ( (L7/ L 12) 4) 또는 이 사합체 가 LlO 과 결 합하여 만드는 오합체 ( (L7/L12) cLlO) 등으 로 분리된다. 면역 전자현미경 사진법으로 알려진 바와 같이, L7/ L 12 의 네 분자들은 50S 하위 단위 체 의 〈줄기 〉를 만들며 , 그들의 N- 말단들 이 단백질 LlO 에 결합한다(그림 2-27 을 보라). (L7/L12) cLlO 복합체 이 의 에 도 여 러 가지 단백 질 복합체 들이 단리 되었다. 그중에서도 S13-S19 복합체는 매우 홍미있다. 이 복합단백질은 같은 리보솜에서 얻은 16S rRNA 에 결합하는데 개개의 단백질들이 단 독으로는 결 합하지 않는다. 이 것 은 단백 질 S13 과 Sl9 가 30S 하위 단위 체 내에서 서로 인접해 있음을 암시한다 (D ij k 동, 1977). 단백질-단백질 상호작용을 연구하는 또 다른 방법은 개개의 단백질들 울 섞 었을 때 생 기 는 복합체 를 조사하는 것 이 다 (Tin d all 과 Aune, 1981) . 득이한 몇 가지 단백질들 사이에서 몇 가지 복합체들이 형성된다. 이 복 합체 들의 회 합상수는 104-106 이 어 서 비 교적 단단하게 회 합하고 있다. S3-S4, S3-S5, S3-S5-S10, S4-S5, S4-S20, S5-S8 및 S5-S10 등의 복 합체들이 확인되었다• 이 복합체들의 대부분은 중성자 산란법, 단백질 교차결합법, 면역 전자현미경 사진법 등으로 얻는 단백질들의 공간 배 열과도 찰 일치한다. 그러므로, 이 복합체들은 30S 하위단위체 내에서 의 상옹하는 단백질들 사이의 목이한 상호작용들을 반영하는 진짜 복합 체들이라고 볼 수 있다.
바) 조립 지도 (1) 작은 하위단위체 리보솜 단백질들의 공간 배열에 관한 최초기의 정보는 사실은 조립 지도분석에서 얻을 수 있었다. 적당한 재조립 조건하에서 E. col i에서 추출한 16S rRNA 와 단백질들을 항온처리하면 30S 입자가 형성되는데, 이 입자는 물리적으로나 기능적으로나 자연의 30S 하위단위체와 차이 가 없다. 초거의 연구결과는 Traub 와 Nomura (1 968) 에 의해서 발포 되 었으며, 최근의 연구결과들은 W itt mann ( 1983 ) 의 평론서에 요약되어 있 다. 낮은 온도에서 30S 단백질들의 약 삼분의 아가 16S rRNA 에 결합 하여 21S 에서 침 강하는 중간 입자 를 형성한다 . 37°C 로 가열하면 입자 는 단백 질의 수가 전혀 증가됨이 없이 형태 변화를 받아서 26S 에서 침 강하는 조밀한 형태가 된다. 형태 변화의 결과로 새로운 결합 자리들이 생겨서 나머지 삼분의 일의 단백질들이 낮은 온도에서도 결합할 수 있 게 된다. 이렇게 해서 형성된 30S 입자는 기능적으로 완전한 활등성운 가지고 있다. 중간 입자들이 조립될 때의 단백질들의 결합 서열과 개개의 단백질들 사이의 상호작용을 분석해 봄으로싸 조립 지도를 구성할 수 있다 (Traub 와 Nomura, 1968; Mi zu shim a 와 Nomura, 1970) . 그림 2-32a 는 30S 단백 질 들과 16S rRNA 와의 상호작용 및 30S 단백 질 들 상호간의 작용을 나타낸 것이다. 이 그림에서 볼 수 있는 바와 같이, 일곱 가지의 단백 질들이 독립적으로 그리고 또 칙집적으로 16S rRNA 와 결합한다. 일차 적으로 결합하는 단백질들(일차 결합성 단백질들)이 RNA 와 결합한 다 음에 야 비 로소 다른 단백 질 들이 결 합할 수 . 있다. S3, S6, S10, S14, S18 및 S21 들과 몇 가지 단백질들은 이차 결합성 단백질들까지 결합된 다 음에야 결합한다. 조립 지도에서 볼 수 있는 상호의존성은 단백질들 사이의 칙접적인 접촉 이의의 다른 요인둘에 기인할 수도 있으므로, 조립 지도에서 화살 표로 연결된 두 단백질들은 리보솜 입자들 내에서 반드시 인접해 있다 고 볼 수는 없다. 그러나 조립 지도로부터의 분석치들을 면역 전자현미 경 사진법, 교차결합법 및 중성자 산란법 등으로 얻은 공간 배열과 비교 해 보면 일반적으로 잘 일치한다• 즉, 조립 지도 상으로 상호작용하는 단백질들은 다론 방법들로 조사하였을 때도 거의 언제나 30S 하위단위체 내에서 인접하고 있음을 알 수 있다. 따라서, 조립 지도는 다소 간접적
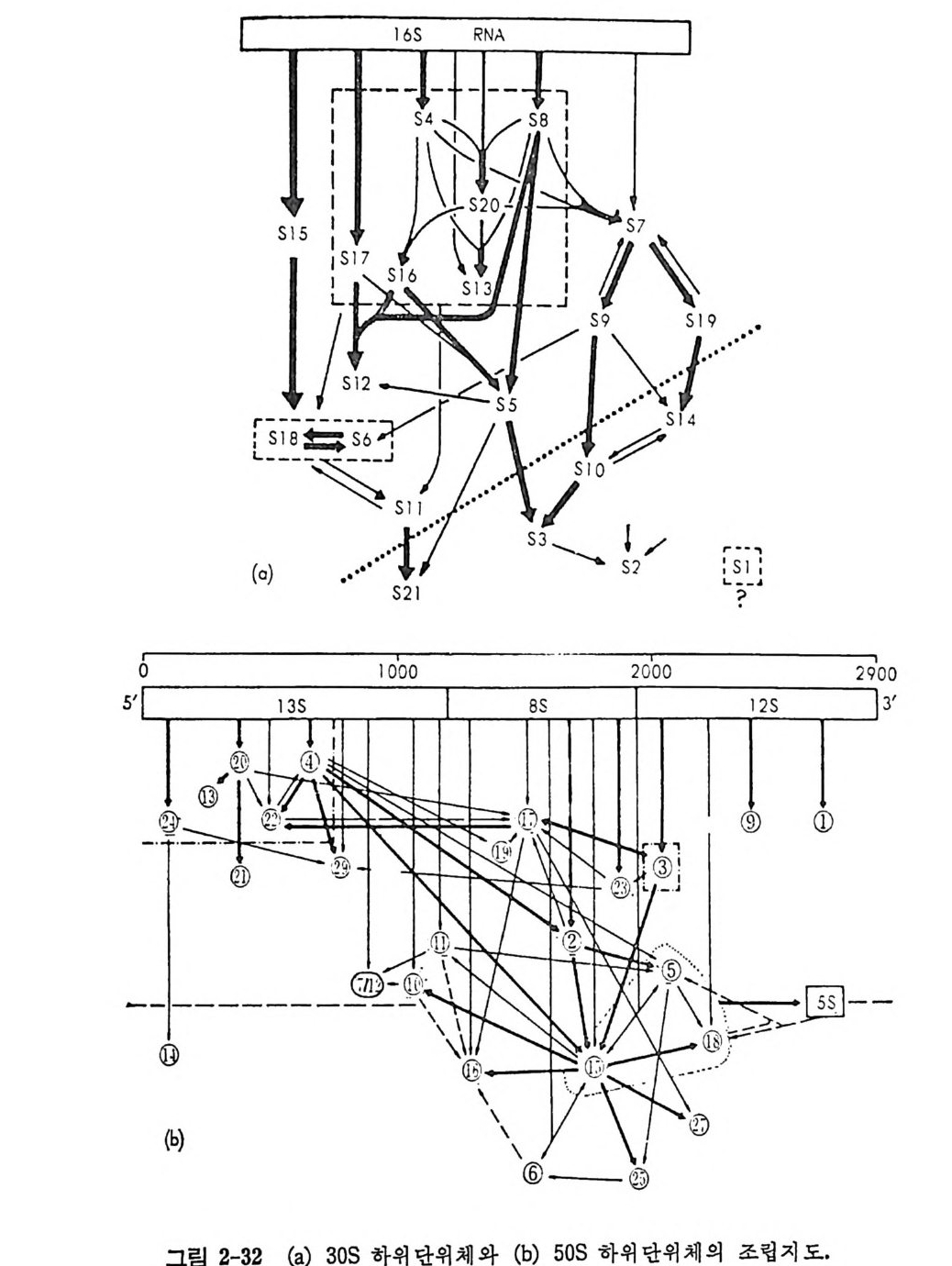 16S RNA
16S RNA
이기는 하지만 단백질들의 공간 배열에 관한 유용한 정보를 제공한다. (2) 큰 하위단위 체 E. col i의 30S 하위 단위체의 조립 조건과 비 슷한 조건에서 E. col i의 50S 하위단위체 를 조립하려는 시도는 오랫동안 실패를 거듭해 왔다. 아 마도 그 가능한 이유는 조립 과정의 속도지배단 계 에서 높은 활성화 에 너지를 요구하기 메문에 50°C 의 고온으로 가열하여야 했기 때문일 것 이다. 그러나, 50°C 이상의 온도에서는 큰 하위단위체의 단백질이 변 성하기 시작하므로 더 이상 활동성인 입자 를 재조립할 수 없다. 그래 서 Nomma 연 구진 에 서 는 고온성 박테 리 아 B. ste a roth e nnop hi l u s 를 가지고 큰 하위단위체의 시 험 관 내 조립을 시도하여 성공할 수 있었다 (Nomura 와 Erdmann, 1970) . Ni er haus 와 Dohme (1974) 은 고온처 리 과 정을 거치는 E. col i의 50S 입자의 재조립 조건을 알아내는 데 성공하 였다(최근의 평 론 에 관해서는 N i erhaus(1980) 을 참고하라). 시험관 내 에 서의 E. col i의 50S 하위단위체의 조립은 E. col i의 30S 하위단위체의 경우와는 달리 두 단계 항온처리를 해야 한다. 첫 단계는 44°c 와 4mMM g 2+ 에서, 그티고둘째 단계에서는 50°C 와 20mMM g 2+ 에서 항온처리한다. 조립 과정은 적어도 네 단계로 진행하며 침강상수 가 33S,41S, 및 48S 인 세 가지 중간입자들이 형성된다. 50S 하위단위체 의 조립 단계들을 표 2-9 에 요약하였다. 표 2-9 E. col i의 리보송 단백질들르부터의 50S 하위단위체의 조립• 23S + SS rRNA 11 L2 I Q范 | LS 0°C, 4 m:M Mg 2+ Riso (1) (33S) + 18 가지 단백 질 L9 LlO Lll |旦경 I L17 Ll9 匡Q I L21 匡흥 1 L23 |~I L29 L33 Riso (1) 44°C, 4 rnM Mg :+ RI*so (1) (41S) RI*so (1) + 8 L6 Ll5 Ll6 L25 44°C, 4 mM Mg 2+ Rlso (2) (48S) 가지 단백질들 L27 L28 L30 L32 또는 50°C, 20 mM Mg 2+ Rlso (2) 50° C, 20 mM Mg 2+ 50S 하위 단위 체 L7/L12, L18, L26, L31 및 L34 들은 지 칭 되 지 않음 0°C, 4mM Mg 2+ 또는 44'C, 4mM M g”라는 조건은재조립의 첫 단계의 이온 조건 운 정의하고. 50'C, 20mM M g’+라는 조건은 둘째 단계문 정의한다. RI*,o(l) 의 형성에 중요한 단백질들은 네모 안에 넣었다. 재조립된 중간체들의 S 값을 괄호 안에 주었다.
첫 단계에서 23S rRNA 와 결합하는 단백질들의 수(약 20 가지)가 많 음에도 불구하고 두 가지 〈개시 단백질둔〉 (L24 와 L13) 만이 조립과정을 개시할 수 있으며, 33S 입자 내에 있는 20 가지 단백질들 중 5 가지만이 44°c 에서의 41S 입자의 형성에 필요하고 충분한 것들이다. 이 5 가지 단백질들 중 L20 과 L24 두 가지가 이 단계에서 철대적으로 필요한 것임 이 밝혀졌다. 그러나, 41S 입자가 형성된 다음에는 이 두 단백질들을 제 거하여도 그 후의 조립과정에 아무런 영향을 미치지 않으며 조립으로 생기는 50S 하위단위체의 온전한 활동성에도 아무런 손상이 없다. 그러 므로, 이 단백질들은 성숙한 50S 입자에서 아무런 기능을 가지지 않는 단순한 조립 단백질들이라고 말할 수 있다 (N i erhaus, 1980). 홍마있는 사실은, 조립의 초기단계에 필수적인 단백질들이 23SrRNA 의 5' 끝에 결합하는 데 반하여 조립의 후기단계에서 결합하는 단백질들 은 이 RNA 사슬의 3' 쪽의 반에 결합한다는 것이다. 이 발견은 조립기 울기라는 것이 있음을 암시하는 것이다. 죽, 조립과정은 RNA 사슬의 생합성이 완성되지 않은 시점에서 시작되며, 생체 내에서의 조립과정은 성장하고 있는 RNA 사슬이 있어야 함을 암시한다 (N i erhaus, 1980). 조립과정에 있어서 단백질들의 상호의존성을 살펴보면, 30S 입자의 조립에 있어서와 마찬가지로 50S 입자의 조립에 있어서도 비슷한 체계가 있음을 알 수 있 다 (Roth 와 Ni er haus, 1980 ; Rohl 과 Ni er haus, 1982) . 죽, 일차 결합성 단백질들이 23S rRNA 에 결합한 다음에야 이차 결합성 단백질들이 결합되며, 그 다음에 삼차 결합성 단백질들이 결합할 수 있 다. 그림 2-32b 와 표 2-9 에 실온 결과들을 살펴 보면, 각각 L20 과 L15 단백질들을 중십으로하여 적어도 두 군데의 조립 영역이 있다는 것을 알 수 있다• L20 영역에 있는 대부분의 단백질들은 조립과정의 초기단계에 중요한반면에, L15 영역의 대부분은조립과정의 후기단계와관련되는단 백질들이다. 한때 이 영역의 단백질들은 펩티딜 기 전달효소의 활동성 또는 연장인자들의 결합자리 등의 기능을 가전 것으로 생각되었다 (Coo per man, 1gs o ) (2. 4. 4 절의 (마) 항을 참조하라) . 50S 의 조립 지 도, 교 차결합 및 영 농도를 증가시키면서 50S 입자로부터 축차적으로 단백질들 을 제거하는 연구들에 기초한 단백질들의 공간 배열의 결과들은 일반적 으로 찰 일치한다. 그뿐 아니라, 조립 지도와 어떤 리보솜 단백질들의 유전자둘의 오페론 내에서의 유전자들의 조칙 사이에는 어떤 상관성이 있다는 것이 밝혀졌다 (Rohl 와 Ni er haus, 1982; 염색체 상에서의 리보솜
 __,Po , CP_PsP。 , sa 0 7SILIS3 8 S1 1S1 S4, S91S2 31IL5 L3l120 BI L5 G1L2L ,96I42L 44LL5 1 L'S l2 LL53l L4, LL1273lhI olo I ! 56 4 3’ ’ ’---------_----------------一-一广一一-一一一------------'~-~- -~-i p—TSR _ _o cPsP,s -P-7 G1 ST u2S P。 EA slu3~ I IH 5 9門「I ;I; . ·- .875 24 101 6 9. ) 2 .2 01.E 33-2s3u f!i염자였유웅하치 림 그시 의표들자 전 유로 의.들서 에상물위 체색성염다신사 생.전체색 2은D분린로열부 한시표분 의,N며밖아부리리가 테 키을 분박부 자 전의유은으그 A분울의지 파부aa 살직화 .p며다킨키구리가 전은리 들 는되유자자단절숫를 로으리 RI의가o조!밀Ec수i 선은들표p 듄각의 조들IRocE유 위한 대 전단 단솜 사보리 전.다백네 이개의윤분백개 전의기네자 크의는 에의 위 의)로모P( 은자전으유위된단촉 쪽사전사왼 의개 네 전서.진다에였둥쪽하분들른구 오로다두치 981oP rauomN( .s 0) ,t 와
__,Po , CP_PsP。 , sa 0 7SILIS3 8 S1 1S1 S4, S91S2 31IL5 L3l120 BI L5 G1L2L ,96I42L 44LL5 1 L'S l2 LL53l L4, LL1273lhI olo I ! 56 4 3’ ’ ’---------_----------------一-一广一一-一一一------------'~-~- -~-i p—TSR _ _o cPsP,s -P-7 G1 ST u2S P。 EA slu3~ I IH 5 9門「I ;I; . ·- .875 24 101 6 9. ) 2 .2 01.E 33-2s3u f!i염자였유웅하치 림 그시 의표들자 전 유로 의.들서 에상물위 체색성염다신사 생.전체색 2은D분린로열부 한시표분 의,N며밖아부리리가 테 키을 분박부 자 전의유은으그 A분울의지 파부aa 살직화 .p며다킨키구리가 전은리 들 는되유자자단절숫를 로으리 RI의가o조!밀Ec수i 선은들표p 듄각의 조들IRocE유 위한 대 전단 단솜 사보리 전.다백네 이개의윤분백개 전의기네자 크의는 에의 위 의)로모P( 은자전으유위된단촉 쪽사전사왼 의개 네 전서.진다에였둥쪽하분들른구 오로다두치 981oP rauomN( .s 0) ,t 와
I 8
단백 질 들의 유전 자들의 조직 에 관해 서 는 Nomura 와 Post ( 1980) 의 평 론 서를 보라) (그림 2-33 에 나타낸 형질전달성 박태리오파지 ;!fu s3 의 염색 체 상에서의 리보솜 단백질들의 유전자의 조칙과 그림 2-32b 의 조립지 도 상에서의 해당하는 단백질의 상호의존관계를 비교해 보라). 조립 의 존성과 상응하는 개개의 단백질들의 유전자 군집체들과의 놀라운 일치 는 큰 하위단위체의 단백질들의 유전자들의 배열이 중요하고도 결정적 인 의미를 가질 것임을 암시한다. 5S rRNA 와 23S rRNA 가 복합체룹 형성할 때 관련되는 단백질들 (L5, Ll5 및 L18) 이 같은 유전자 군집체에 들어 있다는 것도 이러한 관점에서 홍미있는 일이다(그립 2-32b 와 그립 2-33 을 비교하라). 리보송 단백질들의 유전자 들 이 군집 체를 이루고 있 다는 놀라운 사실을 어떻게 설명할 것인가? 아마도 같은 전사 단위 내 예 있는 유전자들의 청보로 합성되는 단백질들로 이루어지는 복합체가 먼저 형성되 는 것이 아닐까? 개개의 단백질들이 리보솜의 중간체 입자 르 회합하는 것보다는 미티 형성된 단백질 복합 체 들이 회 합 하는 것이 조 립과정을 단축시키고 조립과정의 협동성을 증가시키는 데 더 효과적일 지 모른다. 2.5.4 리보솜 내에서의 RNA 둘의 공간 배열 리보솜 RNA 들의 리보솜 내에서의 삼차구조 또는 사차구조에 관해서 는 이 미 2. 4. 1, 2. 4. 2 및 2. 4. 3 절 에 서 언급되 었고, rRNA 들의 기 능에 관해서도 2.4.4 절에서 언급되었으므로 여기서는 지금까지 언급되지 않 은 것을 중심으로 간단히 선명하고자 한다. 리보솜 내에서의 rRNA 둘 의 공간 배열에 관해서는 아직 그 연구가 초창기에 있는 형편이다 . 그 러나 최근에 와서 16S rRNA 또는 23S rRNA 그리고 진핵세포의 여러 가지 rRNA 둘의 일차구조의 분석이 신속하고 간단하게 이루어지게 됨으 로써 리보솜 내에서의 rRNA 의 공간배열에 관한 연구가 활발히 이루어 지고 있다. 그러나 아직은 교차결합, 교차결합과 전자현미경 사진법의 병용, 그리고 면역 전자현미경 사진법 등과 같은 간접적인 방법들을 쓰 고 있다. 몇 가지 방법으로 얻은 최근의 연구결과들을 소개하고 rRNA 돌의 리보솜의 하위단위체들 또는 리보솜 입자 내에서 공간배열을 알아 보기로 하자.
가) RNA 분자 내에서의 교차결합 RNA 분자 내 에 서 의 교차결 합에 관해 서는 앞에서 이미 몇 가지 소개하였다. 많이 사용되는 시약들로서는 황 무스타드, 질 소 무스타드, 디 에 폭시 부탄, 1, 4- 페 닐 디 글리 옥살과 같은 이 착용기성 시약, 광활성을 받는 프소탈렌 유도체들 및 단 순한 자의선 조 사 등이다. 최근에 프소랄렌 유도 체들을 이용하여 유용한 결과들을 얻 고 있다(이 문제는 뒤에서 곧 언급될 것이다). 프소랄 렌 은 핵 산의 이중 나사선 부분에 끼어들 어 가는 성질을 가지고 있다. 최 근에 Ha n cock 와 Wag n er (1982) 는 1, 4- 페 닐 디 글리 옥살을 사용하여 G41 과 G72 잔기들 사 이 에서 교차결합이 형성 됨을 확인하였다. Rabin 과 Croth e rs (19 79) 는 프소 랄랜 반웅의 광가역 성 을 이 용하여 5S rRNA 의 줄기 부분에서 교 차결합 이 일어나는 것을 관찰하였다. 그밖에도 많 은 보기들이 있지만, 몇 가지 예만 보더라도 교차결합은 이차구조 〈내〉 에서 일어나 거나 아차구조 〈바깥〉에 있는 가까운 영기들 사이, 또는 삼 차구조 상호작용을 이루는 곳에서 일어난다는 것을 암시해 준다. RNA 분자 내에서의 교차결합 싣험을 위한 이러한 분석법은 5SrRNA 에 대해서는 많이 응용되었는데 16S rRNA 와 23S rRNA 에 대해서는 그리 많은 분석결과가 없다 . 왜냐하면 큰 rRNA 둘의 핵산 가수분해효 소에 의 한 가수분해 물들은 너 무 복잡하다. 그러나 최근에 Can t or 의 연구진에서는 프소랄렌으로 16S rRNA 또는 30S 하위단위체에서 교차결합을 생기게 한 다음에 겔 전기이동으로 교 차결 합된 RNA 분자둘을 분리 하는 방법 을 개 발하였 다 (Wollenzie n 등, 1982). 풀리아크릴아미드 겔은 포름아미드와 저농도의 염 농도를 가지 고 있어서 전기이동이 진행하는 동안 RNA 분자들이 변성될 수 있게 하 였다. RNA 분자들의 이동도는 분자 내에서의 교차결합의 위치에 좌우 된다. 고리가 큰 분자는 느리게 이동하고 고리가 작은 분자는 빨리 이 등한다. 겐 상에서 분리된 rRNA 분자들을 추출하여 전자현미경으로 고 리의 크기 를 측정하여 교차결합이 일어난 위치를 결칭할 수 있었다. 교 차결합이 일어나는 위치의 국성 (5' 말단 쪽으로인지 또는 3' 말단 쪽으 로 인지)을 결정하기 위한 방법도 같은 연구진에서 개발하였다 (Tham mana 등, 1979; Wollenzie n 등, 1979). 프소랄렌 교차결합의 위치들을 그립 2-18 에 요약하였다. 이러한 방법으로 얻은 결과들은 16S rRNA 의 이차구조를 삼차원으로 〈집는 데〉 도움이 된다. 16S 또는 18S rRNA 둘의 3' 말단 1393 -1 401 번 위 치 (16S rRNA 의 경
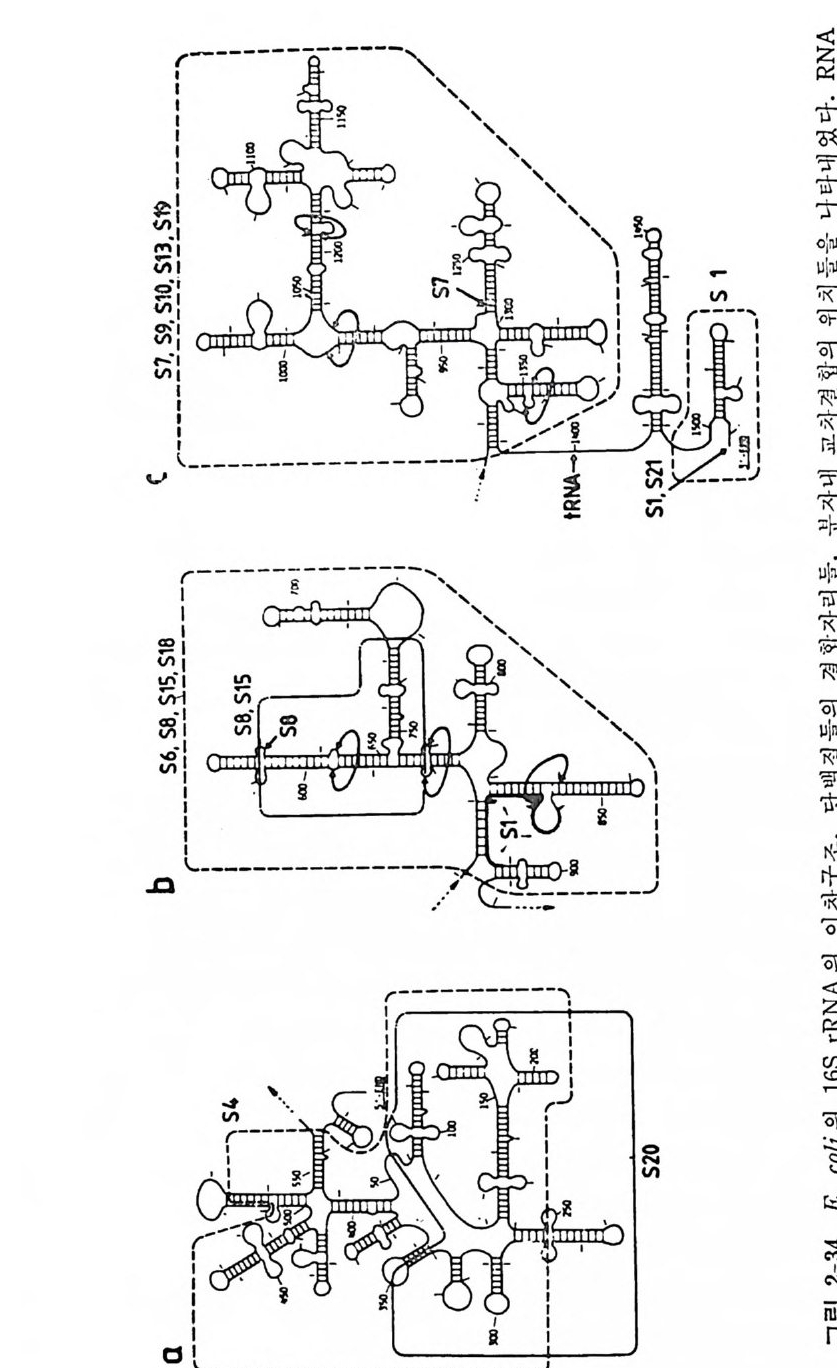 ` bu--ss--a8-8 1 1U YC ,.~ . S0 13S1SS7 .S96-5(‘- '- r_II IIIIIIIIIIIIII(I-、 --- ----------------·---,---(I IIIII' l i----. -TII、III'IIIII I' / I' // / /' ../ d/ . ... / // // / // / / / / / J / A tNR / HD ••/I ,_ /III' g-/ / / /J 2 0S / .S17-- -유、-합-\’ : s 1! -'-- ----- ANR 다. 을었들내타치나위의결합차 교내S 6 1 4-3합,2.자 분자리 듄E 결의들진단백 .구조차 이의ARr의 ilNco 림그 로으 .랄다였소 렌ANR프 로표살화시하표 형리 고은합결차교 의서에내 자분. 다었내타나 로표살전차교 화 은합질백-단 0415 10 450 541 04 510,이사 과 과,사이450, 이사 510 ,이시과 과309 은들위치 한깅대 는둘입니어언 이견치 교된유빌 078 055 0014 095• 다.이 등이사이사 과 과
` bu--ss--a8-8 1 1U YC ,.~ . S0 13S1SS7 .S96-5(‘- '- r_II IIIIIIIIIIIIII(I-、 --- ----------------·---,---(I IIIII' l i----. -TII、III'IIIII I' / I' // / /' ../ d/ . ... / // // / // / / / / / J / A tNR / HD ••/I ,_ /III' g-/ / / /J 2 0S / .S17-- -유、-합-\’ : s 1! -'-- ----- ANR 다. 을었들내타치나위의결합차 교내S 6 1 4-3합,2.자 분자리 듄E 결의들진단백 .구조차 이의ARr의 ilNco 림그 로으 .랄다였소 렌ANR프 로표살화시하표 형리 고은합결차교 의서에내 자분. 다었내타나 로표살전차교 화 은합질백-단 0415 10 450 541 04 510,이사 과 과,사이450, 이사 510 ,이시과 과309 은들위치 한깅대 는둘입니어언 이견치 교된유빌 078 055 0014 095• 다.이 등이사이사 과 과
우) 와 1400 번 위 치 의 C 잔기 가 tR NA 의 역 코돈의 결 합자리 가 된다는 실험적인 증거에 관해서는 2.6.1 절의 (나)항에서 이미 자세히 기술하 였다(그립 2-34 와 그립 2-35 를 참조하라). 나) 리보솜 하위단위체들 내의 rRNA 의 전자현미경사진 면역 전자현미경 사진법에 의한 분석으로 E. col i의 리보솜의 하위단위체들에 대한 몇 가 지 모형이 제안되어 있으며, 개개의 리보솜 단백질들의 분포가 분석되 어 있다 (2.5 절을 보라). 그런데, 리보솜 하위단위체에서 대부분의 리 보솜 단백질들을 재거하여도 전자현미경으로 본 하위단위체들의 형태는 거 의 그대 로 유지 된 다 (Vasil ie v 와 Kote l ia n sky, 1977) (2. 5. 2 절 을 보라) . 이것은 하위단위체의 전체적 모양을 결정짓는 것은 rRNA 라는 것을 암 시한다. 단리 한 rRNA 의 3' 끝둘을 과산화요오드산으로 산화하여 적 절한 합 텐과 반응시킬 수 있다. 이 렇 게 변형한 RNA 를 가지고 리보솜 하위단 위체를 재조립한 다음에 합텐에 목이한 항체로 처리한다. 이 접근법을 사용하여 5S, 16S 및 23S rRNA 돌의 3' 끝들의 하위 단위 체 상에 서 의 위 치를 결정할 수 있었다. 30S 및 50S 하위단위체들에 있어서의 3' 끝들 의 위치들을 그림 2-35 에 나타내었다. 합텐 부착에 의한 rRNA 말단 위 치들의 분석은 5' 말단에 대해서도 이용하였다. 16S rRNA 의 5' 끝의 위 치가 이러한 방법으로 결정되었다. 그러나 23S rRNA 의 5' 끝은 이러 한 방법으로 결정할 수 없었다. 그렇지만 오늘날 제안된 23S rRNA 의 이차구조 모형이 옳은 것이라면 23S rRNA 의 5' 과 3' 끝둘은 실질적으 로 같은 위치에 존재할 것이다(그림 2-20 을 보라). N6, N6 - 디메틸아데노신의 위치 결정에 관해서는 2.6.2 절을 참조하라 (Thammana 와 Canto r , 1978) . 16S rRNA 의 3' 끝으로부터 23 번 째 위 치 에 서 로 인 접 하여 두 개 의 mg A 찬기 들 (즉, m~A1518 와 m~A1519) 이 있 다. 30S 하위단위체에 있어서의 그들의 위치를 그림 2-35 에 표시하였다. 리보솜의 P 자리에 교차결합하여 합텐화한 t RNA 에 대한 항체들도 주로 30S 리보솜의 같은 부분에 결합한다는 것은 주목할 만한 사실이다. 전 령 RNA 의 인식에 있어서 16S r Ri~ A 의 3' 말단이 관여한다는 것은 찰 알려진 사실이므로(제 3 장을 보라), 30S 하위단위체의 이 부분이 전령 을 해독하는 자리라는 것은 확실하다고 생각할 수 있다. 16S 및 23S rRNA 둘의 몇 가지 부분들의 위 치 는 RNA- 단백 질 상호
작용으로부터 추축할 수 있다. 단백 질 L1 의 결 합자리 를 구성 하는 23S rRNA 의 2090-2200 번 위치의 누클레오티드들은 단백질 L1 에 대한 항 체 결 합자리 근방이 될 것 이 다 (그림 2-35 를 보라) . 마찬가지 로, 16S rRNA 의 925 -1395 번의 누쿨레 오티 드들은 30S 하위 단위 체 의 〈머 리 >부 분을 구성 할 것 으로 생 각된 다 (Brim acombe 등, 1978) . 이 누클레 오티 드 연 속부분과 희 합하 는 단백 질 S7, S9, SlO, S14 및 S19 들은 모두 〈머 리 > 부분에 위 치 한다는 것 이 밝혀 져 있다 (St ar ner 등 , 198 0 ; La ke. 1980) (그림 2-26 및 그림 2-27 을 보라) . 두 하위단위체들이 이루는 경계면에 위치하는 rRNA 들의 부분(죽 경계면 쪽으로 노출된 rRNA 부분들)에 관한 정보도 많 이 얻어져 있다. 두 하위단위체들이 분리되어 있는 상태와 회합한 상대에서의 케독살에 의한 변형 청도의 차이 또는 핵산 가수분해효소에 의한 가수분해 정도 의 차이로 유추할 수 있다. 그러나 아칙은 이러한 정보들로부터 리보송 하위단위체들에 있어서의 rRNA 의 삼차원적안 접힘을 정확하게 해석할 수 있을 정도는 아니다.
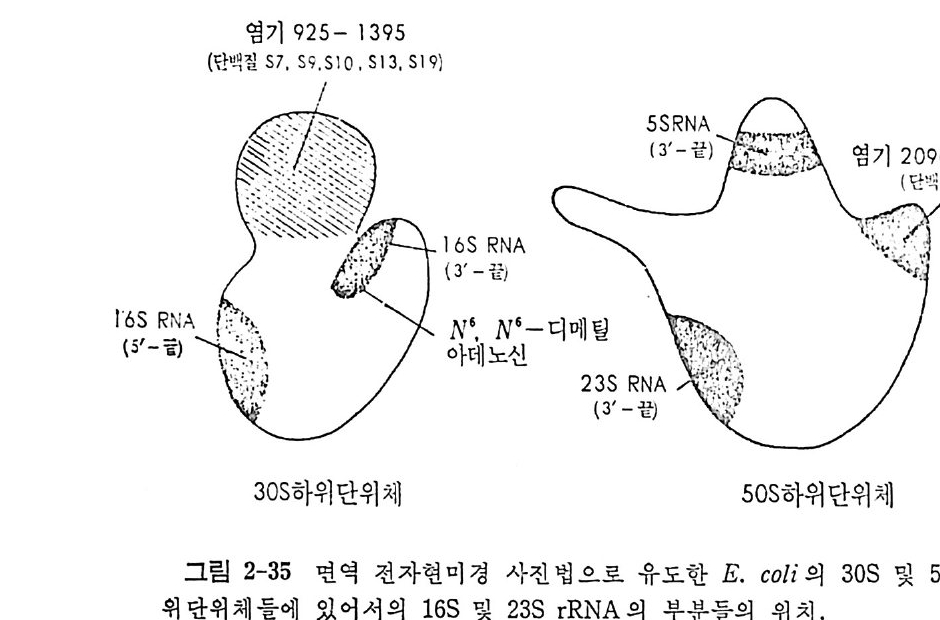 「 6S R广N 염기 925-1 3 95 NI. NI- 디\메틸 \ \깁·
「 6S R广N 염기 925-1 3 95 NI. NI- 디\메틸 \ \깁·
2.6 원핵세포의 리보송의 기능영역에 대한 Ste f fle r 모형 리보솜을 연구하는 이유는 리보솜 성분들의 구조와 기능과의 관계를 앎으로써 단백질 생합성의 각 단계들에서 일어나는 반응들을 분자 수준 에서 이해하자는 데 있다. 앞에서 여러 차례 언급한 바와 같이 , 리보솜 및 리보 송의 하위단위체 들의 구초 에 관한 연구가 많은 연구진들에 의해서 광범하게 연구되고 있어서 몇 가지 모 형들 이 제안되었다. 이 모형들은 서로 약간의 차이는 있지만 중요한 많은 점들에 있어서 잘 일치하고 있다. 여러 모형들이 일 치하지 않는 이유는 개개의 연구진들이 얻은 실험결과들의 해석에 있어 서 기준들이 다르기 때문 이다. 물론 사용한 실험방법 자체에 따라서 동 일한 문제에 대해서 상이한 분석치를 얻을 수 있는 데도 기 인될 것이다. 독일의 S ti:iffi er 의 연구진과 미국의 Lake 의 연구진 사이의 중요한 견 해차는 30S 하위단위체의 구조에 관해서이다. 먼저 S ti:iffi er 의 모형을 알아 보고 다음에 Lake 의 모형을 알아 보자. 2.6. I 30S 하위단위체 상에서의 개시 및 암호해독이 일어나는 부분의 위치 30S 개시 복합체의 형성과정에서 mRNA, 개시 tR NA, 그리고 세 가 지 개 시 인 자들 (IF-1, IF-2 및 IF-3) 이 30S 하위 단위 체 에 결 합한다. 개 시과정에서 16S rRNA 의 3' 말단은 mRNA 가 정확하게 배열되게끔 한 다(제 3 장을 참고하라). 가) 16S rRNA 의 3' 말단의 위 치 결정 16S rRNA 의 3' 말단의 아데 노 신을 N-(r-DNP) 아미노부티르산 히드라지드로 변형시키고, DNP-16S rRNA 와 30S 리 보솜의 모든 단백 질 들로써 기 능을 가진 30S 하위 단위 체 를 재조립하고 이 30S 입자를 DNP 에 특이한 항체들과 항온처리한다. 전자현미경 사진에서 큰 귓불의 안쪽에 부착 자리가 하나 있음을 불 수 있다(그림 2-37Aa) (Ste f fle r 와 Sto f fie r -Meil ick e, 1981; Shats k y 등, 19 79 ; Mckusk ie-O lson 과 Gli tz, •1 979) . 16S rRNA 의 3' 말단 부분은 mRNA 의 개시자리를 인식하는 역할
제 2 장 리보송의 구조와 기능 I87
을 하고 있으므로 30S 개시 복합체 헝성에 있어서 중요한 역 할 을 한다 (제 3 장 참조) (2. 4. 4 절도 참고하라) . 나) tR N A 의 결합자리 16S rRN A 의 3' 끝 으로 부터 24 번과 25 번 위 치 들(즉, 16S rR NA 의 1518 번과 1 5 19 번 위치 들)에 위 치 하고 있는 N6. N 6 - 디메 틸 아 데노 신 ( D MA) 은 진 화 과정을 거치는 동안 잘 보 존 되어 있는 염 기 들 이며 개시 반응에서 t R NA 를 결합 시 키는 역 할운 하는 것 으로 알려 쳐 있고 항 생물질 성 방해물 인 카 수가 마이 신에 대한 저항성을 준 다는 점 이 알려 져 있다 ( 2. 4 . 4 절의 ( 나)항을 참 조 하라 ). DMA 에 대한 항체를 써서 이 변 형 된 아데 노 신 들 의 위치가 30S 하위단위 체 의 머리와 몸등사 이에 형 성된 고 랑 의 밀부분 이 라는 것 이 밝혀졌다( 그 립 2-37~.\ b ). 이 자 리는 16S rRNA 의 3' 말 단 의 옆에 있 다. 그 러 나 이 두 자리들은 서로 구분되 는 별 개 의 자리 들이 다. Politz 와 Glit z (197 7) 도 동 일 한 결 과 를 얻 었다. Ofe n g a nd 등 (1979) 은 역 코돈의 5' 위 치 에 각 각 cmo5U 또 는 mo5U 를 가진 E. coli 의 AcVal-tR l'.JA 와 B. sub t i l is 의 AcVal-tR N A 들을 P 자 리에 결합시킨 다음에 UV 로 조사하여 16S rRNA 와 교 차결합 되는 자 리 를 분석 하였다. 그 자리 는 16S rRNA 의 UACACACCG1 4 01 의 연 속부 분에 있다. 그런데 이 연속부분은 30S( 원핵체)와 4 0S( 진핵체 ) 리보솜하 위 단위 체 의 16S 또는 18S rRNA 에 두루 있는 GUACA C ACCGm4 Cm C CGUm5CA 의 일부분이며, 두 경우의 부분적인 차이 를 제외 하 면 원 핵 체, 세포소기관, 효모, 곤충, 양서류 등 26 가지의 조 사한 생 물종 의 작 은 하위단위체의 RNA 들에 찰 보존되어 있냐 따라서 16S rR NA 의 3' 말단의 이 연속부분은 t RNA 의 역코돈 고리가 직접 결합 하는 자리일 것으로 생각된다. 실 세 로 최 근에 Ofe n g a nd 등 (1982) 은 AcVal-tR N A1v •1 이 효모의 40S 하위단위체에만 교차결합하며 P 자리에서만 일어난다는 것을 밝혔다. 그리 고 AcVal-tR N A1'1 의 역 코돈 (cmo5UAC) 의 5' 위 치 의 변 형 된 염 기 (cmo5U ) 가 18S rRNA 의 1400 번 위 치 의 C 에 교차결 합된 다. 18S rRNA 에 결합하는 AcVal- t RNA1v•• 의 양은 90% 이었다. 이 교차결합은 강 한 코돈 특이성을 나타낸다. p GUU 가 존재할 때는 20 분의 UV 조사후 85% 가 교차결합되는데 GUA 가 존재할 때는 불과 3% 만이 교차결합 한다. 따라서 원핵세포와 진핵세포의 단백질 합성에 있어서 해독과정의
국면에 있어서 절대적으로 필요한 부분이라는 것을 알 수 있다(그림 2- 35 를 참조하라). A 자리와 P 자리에 결합한 t RNA 들의 역코돈둘 또는 아미노아실 꾼 들보다는 t RNA 의 중앙 부분, 죽, L 자형 모형에서 꺾어지는 부분이 티보솜과 결 합하는 자리를 알아 보는 것이 실험적으로 더 용이하기 때 문에 47 번 위 치 에 acp 3U 를 가지 고 8 번 위 치 에 4S 롤 가진 효모의 tRN APn’ 을 이 용 하 여 실 험 하였 다 (Of en g a nd 동, 1980; Ofe n g a nd 등, 1981) . 4- 티 오우리 던 (4S ) 은 브 롬 화 S- 〔p-아지 도페 나실 J (APA-Br) 과 브 롬화 S- 〔p-아지도 페 나실아세틸〕( APAA-Br) 을 SH- 기와 작용시켰고 3- (3- 아미 노 -3_ 카르복 시 프로 필 ) 우리 단 (acp 3U ) 의 아미 노기 는 히 드록시 숙신 이 마 드로 활 성 화한 6- ( 2- 니 트로 -4- 아지 도페 닐 아미 노)-카프로산 (NAK) 과 N-(2- 니 트로 -4- 아 지 도페 닐 ) 글리 신 (NAG) 으로 반응시 켰 다. 연장인자 Tu ( EF-Tu ) 의 존재 하에서 APA 로 변형된 Phe-tR NA(Phe- t RNAAPA) 를 리보솜의 A 자리에 결합시킨 다음에 310-325nm 에서 조 사하여 교 차결 합되는 단백질을 찾아내었다. APA 원자단의 길이가 9A 밖에 안되므로 매우 가까운 데 위치한 단백질과 교차결합한다. 비슷한 방법 으로, NAK 로 변 형 된 Phe-tR NA (Phe-tR NNAK) 를 P 자리 에 결 합 시킨 다음에 450nm 에서 조사하여 리보솜의 단백질들과 교차 결합시켰 다. A 자리에 결합한 APA 탐침과 P 자리에 결합한 NAK 탐침이 모두 단백질 S19 에 결합한다는 것은 중요한 의미를 내포하는 것으로 생각한 다. 즉, A 자리와 P 자리가 리보솜 상의 별개의 부분으로 구성되어 있 는 것이 아니라 단백질 합성의 개시 및 연장에 있어서의 여러 단계들에 상응하는 리보솜의 특수한 형태에 지나지 않을 것이라고 생각되고 있다. U47 위치와 U8 위치가 각각 NAG 와 APA 로 표지된 효모의 tR NAp b• 의 입체구조를 그립 2-36 에 나타내었다. 다) IF-3 결합자리 이 자리의 결정도 IF-3 에 대한 항체들로 결정되었 다. 우선 수베리미드산을 써서 IF-3 을 작은 하위단위체와 교차결합시 킨 다음에 , 30S·IF-3 복합체 를 IF-3 에 대 한 항체 와 반옹시 켰 다. IF-3 결합자리의 위치는 머리의 밀부분에서 귓불까지의 범위에 국한된다(그 림 2-37 Ac). 라) mRNA 의 결합자리 합텐 (예 , DNP) 을 부착한 mRNA 의 유사체 풀 제 2 장 리보송의 구조와 기능 I89
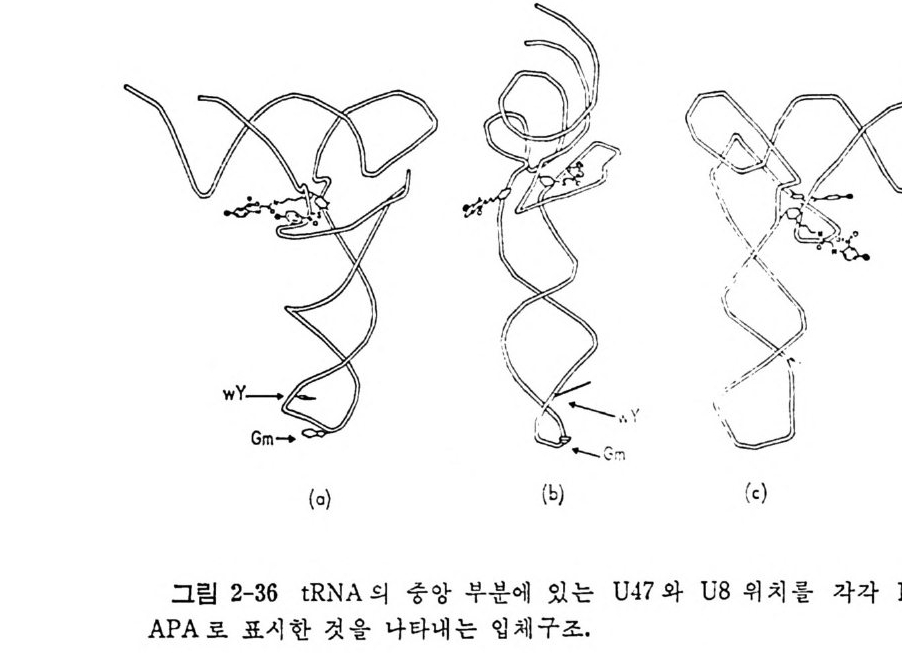 (a} (b) (c)
(a} (b) (c)
리 -4- 티오우리 털산의 결합자리를 DNP 에 특이한 항체로 분석하였다. 그 자리의 위치도 목 부분에 있음이 밝혀졌다(그림 2-37 Ad). 친화 탐침 으로 표지된 mRl지 A 유사체들을 사용한 분석결과를 아래의 표에 주 었다.
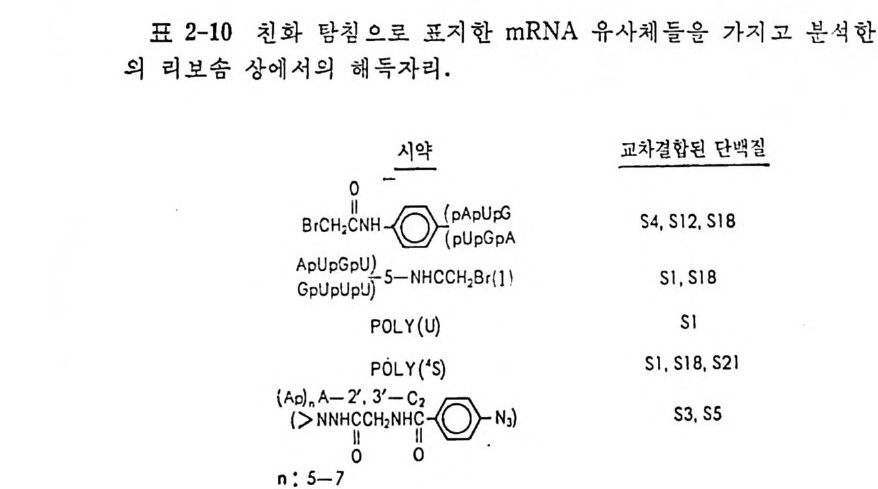 표 2-10 친화 탐침 으로 표지 한 mRNA 유사체 들운 가지 고 분석 한 E. coli
표 2-10 친화 탐침 으로 표지 한 mRNA 유사체 들운 가지 고 분석 한 E. coli
위에서 기술한 연구결과 들을 종합해 보면 개시와 관련된 기능 영역들 과 합성 및 자연의 mRNA 의 결합과 관련된 기능 영역 들 이 30S 하위단 위 체 를 삼분의 일 부분과 삼분의 이 부분으로 분 할하는 분계 부분에 자 리 장고 있음을 알 수 있다. 이 러 한 결론은 Keren-Zur 등 (19 79) 이 DNP 로 아미노아실화한 Val- t RNA 를 가지고 한 싣험에서 얻은 결과와도 잘 일치 한다 (그림 2-37) . Val-tR NA 의 DNP 유도체 를 UV 조사로 30S 하 위단위체와 결합시킨 다음에 항 -DNP 항체로 그 위치를 결정하였다 • 2.6.2 50S 하위단위체의 기능영역 앞에서 기술한 연구들은 코돈 인식이 일어나는 자리들을 확인하기 위 한 것들이었다 . 두 분자의 t RNA 가 70S 리보솜에서 배열되는 상태를 알기 위해서는 펩티딜 기 전달효소의 위치가 결정되어야 한다. 펩티달 기 전 달효소의 작용을 방해 하는 푸로마이 신 또는 클로람페 니 콜의 50S 하위 단위체 상에서의 결합 자리들을 면역 전자현미경 사진법으로 분석하여 P 자리와 A 자리에 관한 훌륭한 정보를 얻을 수 있다. N - 브로모아세틸푸로마이신을 친화표지의 탐침으로 사용하여 푸로마이 신의 결합 자리가 결정되었다. 이 탐침을 50S 하위단위체에 공유결합으 로 결합시킨 다음에 푸로마이신에 특이한 항체로 그 위치를 분석할 수 있었다(그림 2-37e). 비슷한 방법을 사용하여 30S 하위단위체 상에서의 푸로마이신 결합 자리도 결정할 수 있었다 (Mckus ki e-Olson 둥, 1980) (그림 2-37). 요오도암페니콜을 친화표지의 유사체로사용하고항체는클로람페니콜 에 목이한 것을 사용하여 클로람페니콜의 결합 자리를 분석하였다. 푸 로마이신 자리가 있는 위치, 죽, 중앙의 돌출부(코)와 L1- 어깨가 만드 는 골짜기에 항체 결합자리가 단일하게 관찰되었다(그림 2-37). 클로람 페니콜은 펩티딜-푸로마이신의 형성을 방해하므로, 클로람페니콜의 결 합자리는 펩티딜 기 전달효소에 상응할 것이다. 이와 같이, 펩티딜 기 전달효소 중심은 두 가지 독립적인 방법으로 .5O S 입자 상의 동일한 한 자리에 위치한다는 것이 관찰되었다. 한편, t RNA 의 아미노아실 말단부분을 변형한 것들을 친화표지와광 친화표지의 탐침들로서 사용한 분석결과에 의하면 P 자리와 A 자리에 있는 성분들로서 표지되는 것들은 단백질 L2, Lll, L15, 116, 118,

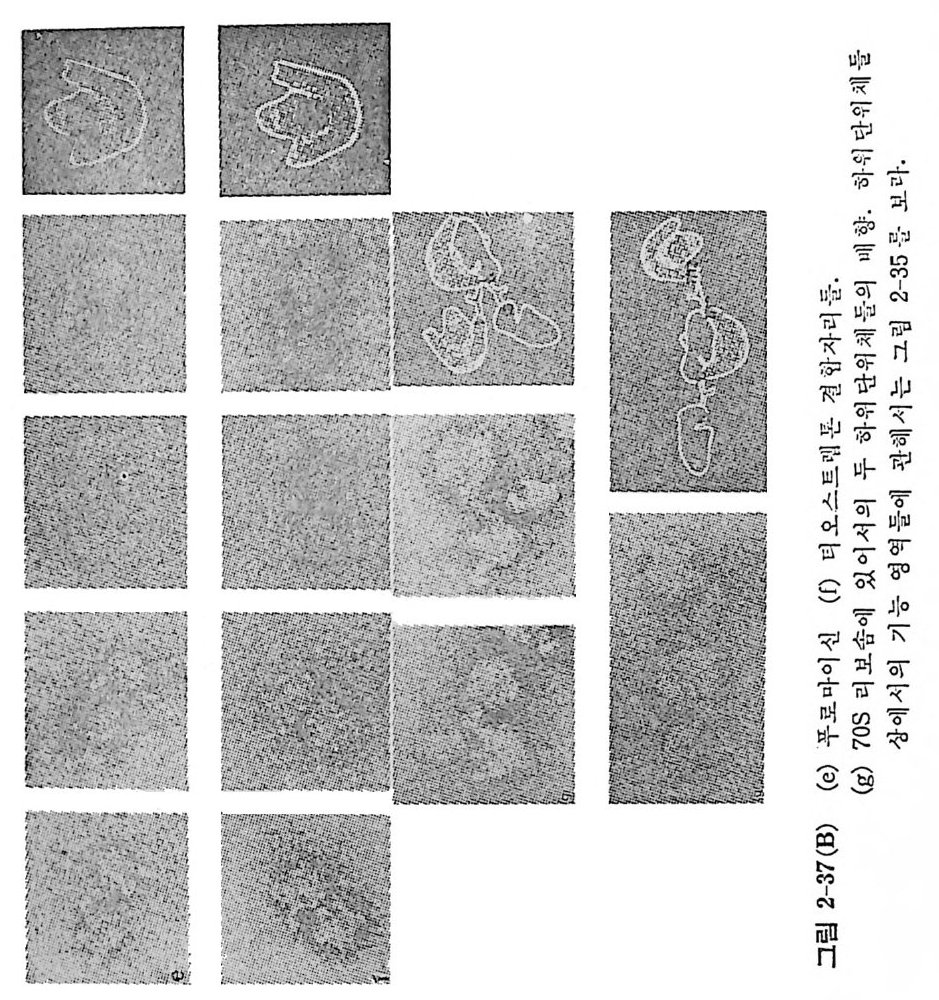
L27 및 23S rRNA 의 3' 끝의 삼분의 이 부분들이 다 (Of en g a nd, 1980) . 이 여섯 개의 단백질들 중 5 개가 50S 하위단위체의 좌대 및 중앙 돌출부와 오른쪽 돌출부 사이의 골짜기에 위치한다(그립 2-38 과 그립 2-37 과 비 교하라). 최근에 Ma i me t s 둥 (1984) 은 단백질 L16 의 기능과 관련한 연구 에서 L16 은 디펩티드의 형성에 관여하는 것이 아니라 t RNA 의 3' 끝을 리보솜의 A 자리에 결합시키는 역할을 한다는 결과를 얻었다. 이 연구진 은 단백질 Ll6 을 메고 재조립한 50S 입자에서 푸로마이신은 여전히 디 펩티드를 형성할 수 있음을 밝혔다 (Ma i me t s 둥, 1983). 이 결과에서 단 백질 L16 은 펩티딜 기 전달효소의 작용을 하지 않을 것임을 유추할 수 있다. 이 결과는 23SrRNA 의 U2584 가 P 자리에 결합한 Phe- t RNA 의 3' 끝 부분을 결 합시 키 는 자리 라는 것 을 밝힌 Barta 와 Kuechler (1983) 의 연구와 비교하면 매우 홍미있는 일이다 (2.4 . 4 절의 (마)항을 보라).
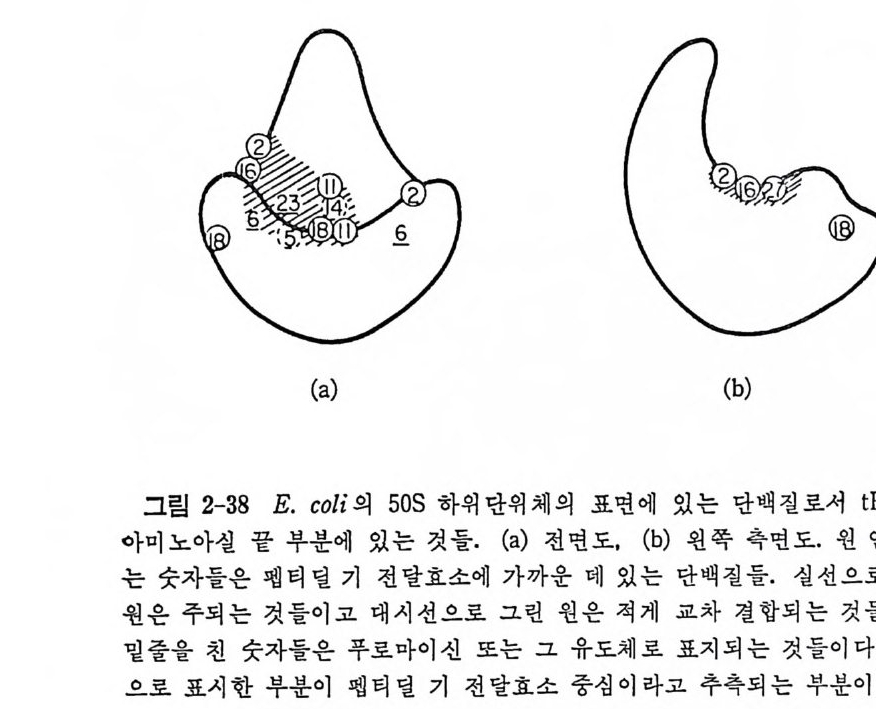 (a) (b)
(a) (b)
티오스트랩톤은 단백질 합성에 있어서 개시 , AA- t RNA 의 결합, 자 리옮김, 종결 등에 대해서 강력한 방해물로 작용한다 • 티오스트랩몬의 50S 하위단위체에 대한 결합상수는 매우 크기 때문에 거의 비가역적으
로 결합한다. 따라서 천화표지법을 사용하지 않고서도 티오스트랩톤의 결합자리를 면역학적으로 분석 할 수 있다. 티오스트 랩톤의 항체 를- 사용 하여 티오스트랩톤의 결합자리를 분석한 바에 의하면, 50S 하 위단위체 의 좌대의 중앙에 단일 자리가 있으며 그 단백질은 Lll 임 이 밝혀졌다. 단백질 Lll 은 A 자리를 형성하는 단백질들 중의 하나이다. 단백질 Lll 은 티오스트랩톤이 리보솜에 결합하는 데 필수적인 것아 며, Lll 이 결여된 리보솜둘은 이 약품에 대해서 저항성을 가지고 있다. 티오스트랩돈이 결합하는 자리는 GTPas . e 의 작용중심 (EF-G) 일 것이라 는 실 험 적 중거 가 있 다 (Sto f fie r 와 Sto f fle r -Meil ic k e, 1981) . 2. 6. 3 70S 리보솜 상에서의 기능영역 앞의 질들에서 기술한 바와 같이, 펩티딜 기 전달효소 중심은 50S 하 위단위체의 중앙의 돌출부분과 왼쪽 측면의 돌출부분이 이루는 모서리 에 자리 잡고 있다. 또, 16S rRNA 의 3' 끝, mRNA, 개 시 인자 IF-3 위 치들은 30S 하위단위체의 머리와 몸통 사이의 고랑에 자리잡고 있다. 이 결경 계합 자면 들리에들 은해 당70하S 는리 것보 이솜 에다. 있이 어러 서한는 사 실두 에 하 기위 초단하위여체 들St의o f fle안 r 와쪽 S면t,o f fl죽e ,r - Ivleil ick e (1981) 는 그림 2-39 에 나타낸 모형 을 시 험 적 으로 제 안하였 다. 이 모형은 mRNA 가 70S 리보솜의 두 하위단위체들 사이에 형성되는 홈울 동하여 궤뚫고 지나갈 것이라고 제안한 R i ch(l974) 의 견해와 찰 일치한다. 이 모형은 단백질 생합성에 있어서의 리보송의 구조와 기능 을 연구하는 길잡이가 될 수 있는 유용하고 홍미있는 가정이라고 생각 된다. 2.7 원핵세포의 리보솜의 기능영역에 대한 Lake 의 모형 2. 7. 1 작은 하위단위체들의 기능영역들 리보솜의 하위단위체들에 있어서의 각 성분들의 공간배열을 분석하는 방법들은 앞에서 이미 여러 차례 기술한 것들과 동일하다. Lake 모형 에 있어서의 성분 단백질들의 공간배열을 그립 2-39 로 나타내었다 . .:z.
중 9 가지의 단백질들만을 선정하여 그들의 기능을 알아 보자. Ste f fle r 의 연구진과 Lake 의 연구진의 모형들에 있어서의N 차이\에 대해/서는 그 립 2-25(30S 하위단위체)와 그림 2-26(50S 하위단위 체 )을 보라.
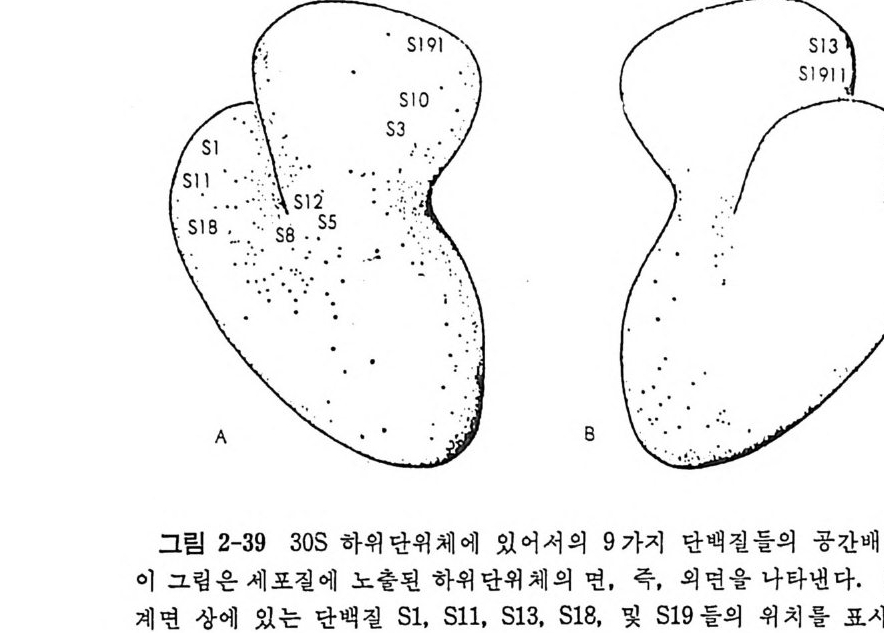 s0
s0
30S 하위단위체의 플랫폼(귓불)은 독특한 모양과 위치를 가지고 있는 데 아마도 이 부분이 특이한 역할과 관계되는 부분이라고 생각된다. 진 화과정에 있어서 광범하게 보존되어 있는 이 톡칭은 여러 원핵세포에서 는 뭉른이고 포유동물에서도 불 수 있다. 예를 들면, 쥐의 간, 토끼의 적 혈 구 (Emannil o v 등, 1978) , 그리 고 E. coli ( Lake 와 Kahan, 1975) 등 의 30S 하위단위체들에서 특징적인 플랫폼의 구조가 보존되어 있다. 70S 리보솜에 있어서, 플랫폼의 한 면은 세포질을 면하고 있고, 다른 면은 큰 하위단위체를 면하고 있다. 이 플랫폼의 두께는 매우 얇기 때문에 (~30A), 어떤 단백질들은 플랫폼의 바깥면과 경계면 양쪽으로 노출될 수도 있다. Sl, S11 및 S18 들이 플랫 폼에 위 치 한다. S1 과 S18 은 mRNA 와의 결 합과 관계가 있다고 생각되고 있다. 이것은 . S1 과 S18 들이 mRNA 와 교차 결 합하는 것 으로 침 착할 수 있다 (Coop er mann, 1980) . 단일 성 분
생략법에 의한 실험결과에 의하면 스트랩토마이신으로 유 발되는 단백질 합성에 있어서의 오독은 Sll 과 S12 이의의 단백질들의 경우에는 민감 하지 만, Sll 이 결 여 된 경 우에 는 오독 (폴 리 -U 로 지 시 되 는 계 에 서 의 이 소루신, 티로신 및 세린 동이 페닐알라닌 대신에 삽입되는 일)은 6.5 배 로 증가한다. Sll 을 빼었을 메 이외에는 착오 반도가 증가되는 일이 알 려져 있지 않다. 그러므로, Sll 은 울바른 t RNA 의 선택, 죽, 올바른 코돈-역 코돈 상호작용 에 직 접 작용하는 단백 질 이 라고 말할 수 있다. 16S rRNA 의 m~ A1 518 과 m~A1519 둘이 플랫 폼에 위 치 한다. 따라서 플랫 폼 이 유전암호 해독이 일어나는 영역이다고 생각할 수 있다 (2 . 4.4 철의 (나)항을 보라). 단백 질 Sl, Sll 및 S18 들은 코돈-역 코돈 상호작용에 관여 할 것 이 라는 증거둘이 많이 있다. 따라서 코돈-역코돈 결합자리는 플랫폼이라고 생 각한다. 이것이 Lake 의 모 형의 특징이다 • 개 시 인 자 IF-1, IF-2 및 IF-3 둘이 결 합하는 부분은 1/3- 부분 (죽, 머 리)에 있는 S13, S19II, 그티고 S12 들과 플랫폼 상에 있는 S11 사이에 이루어지는 고랑 전체에 걸쳐서 자리잡고 있다. 이것을 그림 2-40 으로
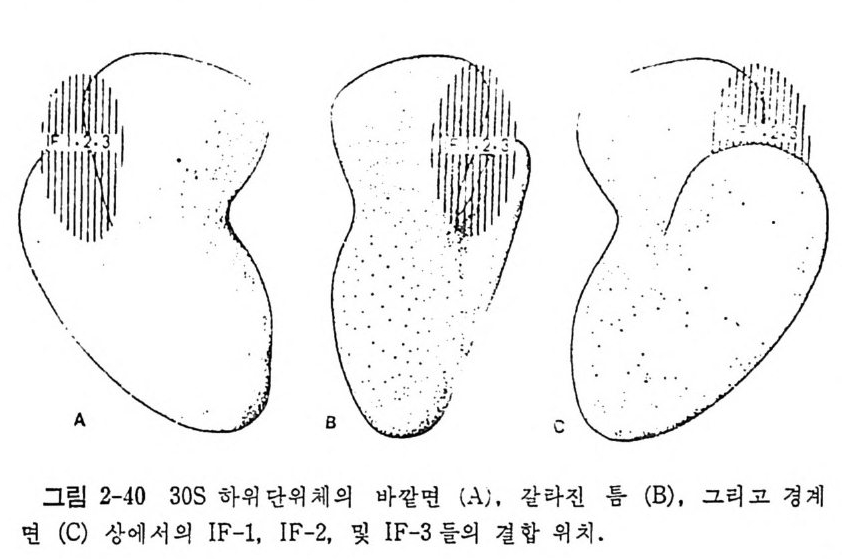 L>
L>
나타내 었 다. IF-2 는 포르밀 메 티 오닐 -tRN A1Met 가 30S 하위 단위 체 에 결 합하는 것을 촉진하며, 70S 리보솜 상에서의 GTP 의 가수분해를 촉진 한다 (Lucas-Lenard 와 Lipm ann (1971) 의 평 론서 와 Hasekorn 과 Roth m
an-Denes(1973) 을 보라). IF-2 는 IF-1 과 IF-3 과 함께 있을 때, 단백 질 Sl, S2, Sll, Sl3, S14 및 S19 들과 효과적 으로 교차결 합한다 . mRNA 가 30S 하위단위체에 결합하는 데 있어야 하는 IF-3 은 단백질 S7,Sll, S12 및 Sl9 들과 교 차결 합한다 (Van Duin 등, 1975; Heim ark 등 , 19 76). 2.7.2 큰 하위단위체의 기능영역 가) 단백질 L7/Ll2 리 보송 단백 질 L7/L12 는 특유한 몇 가지 성 질 들 을 가지고 있다. L7 의 아미노 말단은 아세 틸화 되어 있고 L12 의 아미 노 말단은 아세틸화되어 있지 않다는 것을 재외하고 단백질 L7 과 L12 는 동일한 아미노산 결합순서를 가지고 있다. L7 과 L12 는 리보솜 단 백질들 중 여러 복사물로 존재하는 단백질들이다 (2.3 절을 보라). 두 단 백질은 연장인자 Tu(EF-Tu), 연장인자 G(EF-G) 및 개시 인자 -2(IF-2) 들의 존재에 의존하는 GTP 의 가수분해에 깊이 관련되어 있다. 따라서 L7/L 12 줄기 의 위 치 의 결 정 은 EF-Tu, EF-G 및 IF-2 들의 리 보솜에 서 의 결합자리에 관한 정보를 제공해 줄 것이다. L7 과 L12 의 70S 리보솜에 대한 위치를 그림 2-41 에 나타내었다. 참 고로 작은 하위단위체의 단백질들의 위치도 표시하였다. 큰 하위단위체 는 해리한 상태에서 주로 볼 수 있는 형태 (그림 2-41A) 와 70S 리보송 에서 주로 볼 수 있는 형태(그립 2-41B) 로나타내었다. 그렇지만, 어느 경우에서든 L7 과 L12 는 하위단위체의 갈라진 톰(그림에서 왼쪽)으로부 터 멀 리 떨 어 쳐 있다. Marsh 와 Parmeg gian i (1973) 는 S1, S2 및 S9 아 의에 S3, S5 및 S14 둘이 빠진 하위단위체는 EF-G 와 50S 하위단위체 의 존재에 의존해서 일어나는 GTP 의 가수분해를 촉진할 수 없다는 것 을 알았다. 이 가수분해 작용은 S5 와 S9 를 첨가하면 회복된다. 이 사 실은 L7/L12 의 위치가 작은 하위단위체의 S5 가 있는 부분에 가까운 곳 이라는 것을 의미한다. 그런데, IF-2, EF-Tu 및 EF-G 둘의 분자의 크 기가 비교적 크기 때문에, 이 인자들의 결합자리들(그림 2-34 를 참고하 라)은 70S 의 상당히 많은 부분과 접촉하고 있을 것으로 생각된다. 실 제 로 L7/L12 줄기 는 EF-G (Acharya 등, 1973) , 또는 EF-Tu (San Jos e 등, 1977) 과 교차결합된다는 것이 알려져 있다.
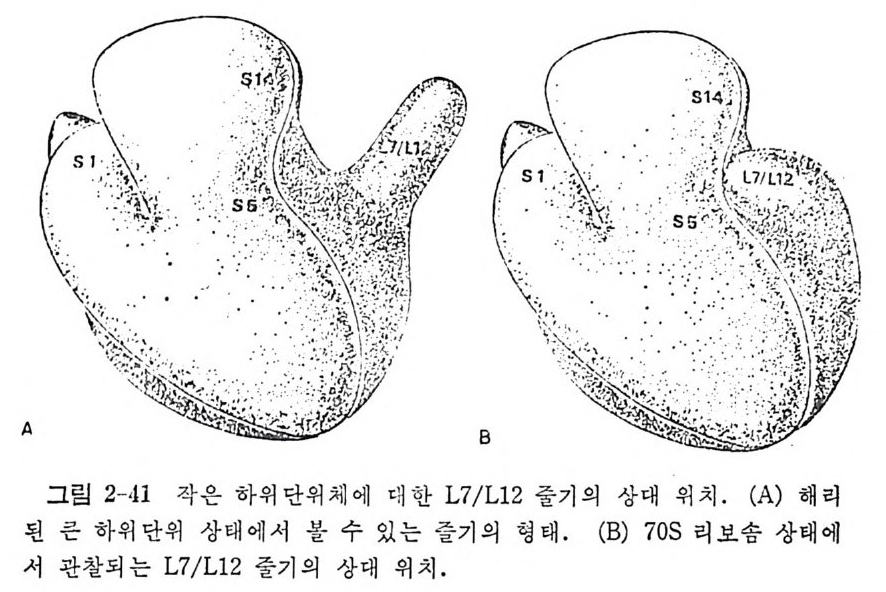 A -..,~ 8
A -..,~ 8
을그비 림교나)주 해 의2그 -하4보 라2밖라 )에의.. 5표단0S시백 하단질였백 다질L1들(7 그과립큰 L 2하21-위 2의7단 의위위 치S체 t들 6의 f이f i e네 r 두 의가 모지모 형형단에에백서서질 의들다 의르위 다치위는들치 것과를
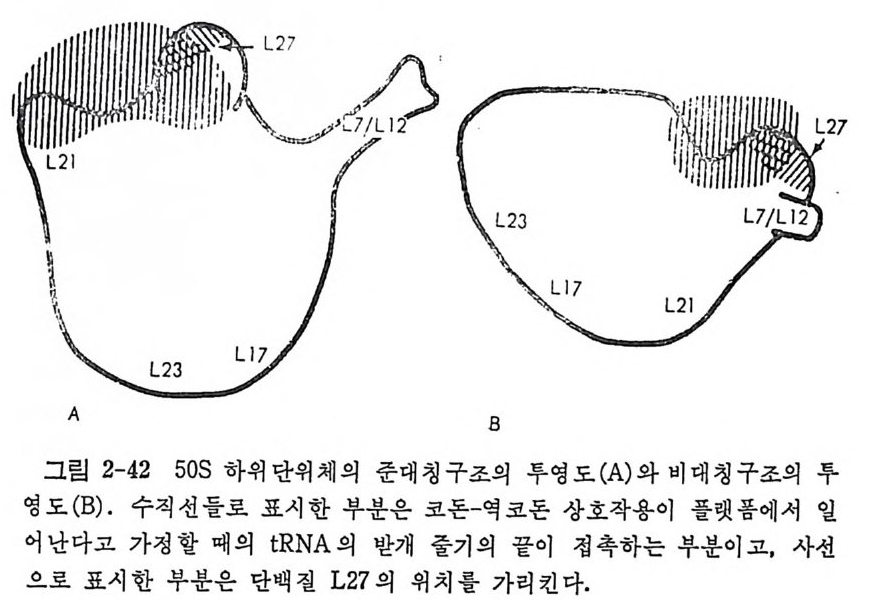 :>
:>
단백질 L27 은 펩티딜 기 전달효소 가까이에 있는 것으르 생각되고 있 다. 단백질 L27 은 P 자리와 A 자리에 결합한 친화표지물르 변형된 아 미노아실-t RNA 에 의해서 표지되는 단백질이다. L27 이 펩티딜 기 전달 효소 중심이 있는 자리에 있을 것이라는 암시는 아실-메티오닝-t RNA'\ i e t 에 의한 리브솜의 표지에서 주로 표지되는 단백질이 L2 와 L27 이라는 데서 얻을 수 있다. 따라서, L27 은 개시 tR NA 및 P 자리와 A 자리에 있는 t RNA 들의 친화 표지의 유사체들에 의해서 일치하게 펩티틸 기 전 답효소에 가까운 곳에서 표지되는 것으로 보인다. 2.7.3 70S 리보솜의 기능영역의 모형 바로 앞의 두 절에서 기술한 바와 같이, Sl, Sll 및 S18 들의 위치들, 그들의 mRNA 와의 결합, IF-3 의 결합자리, m~A 의 위치, t RNA 의 아 미 노아실 끝의 위 치 의 분석 결 과에 기 초하여 코돈-역 코돈 상호작용은 30S 하위단위체의 플랫폼 상에서 일어날 것으로 생각된다. L7/Ll2 를 제거하여도 펜티딜 기 전달효소의 활동성이 그대로 보존된 다는 것 은 L7/Ll2 와 펩 티 딜 기 전 달효소 중심 이 상당히 떨 어 져 있음을
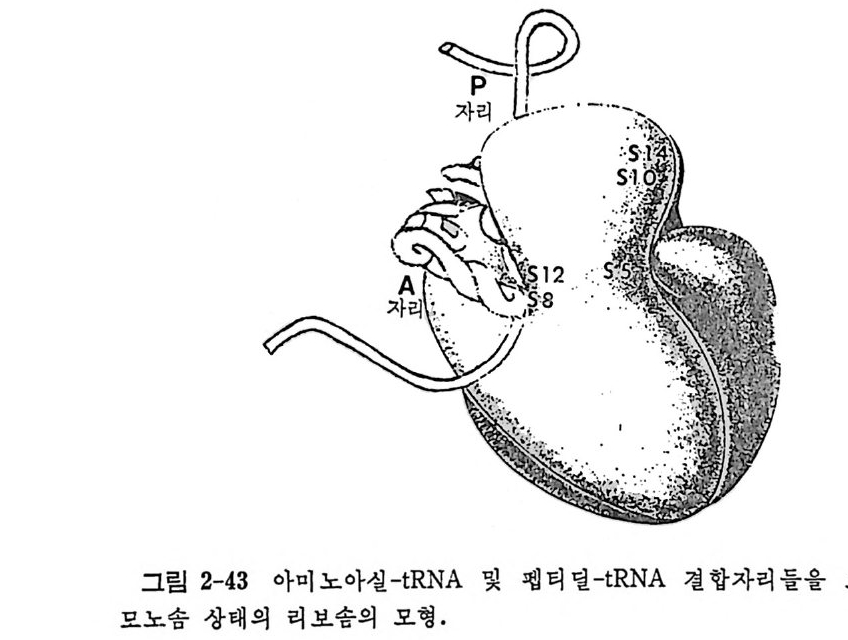 :广_-``
:广_-``
암시 한다 (Hamel 등, 1972) . 펩 티 딜 기 전 달효소의 근방에 결 합하는 에 리트로마아신과 L7/L12 사이의 거리를 단일상태-단일상태 에너지 전달 법으로 측정한 결과에 의하면 약 70A 떨어져 있다 (Lan g lo i s 등, 1976). tR NA 가 코돈, IF-2 결 합부분, 펩 티 딜 기 전 달효소들과 동시 에 접 촉하 려면, 이 tR NA 분자는 A 또는 P 자리를 그립 2-43 에 근사적으로 나 타낸 바와 같이 자리잡아야 할 것이다. 이 그림에서, 쉽게 알아 볼 수 있게끔 작은 하위단위체의 바깥면의 몇 가지 단백질들의 위치들을 표시 하였다. 30S 하위단위체의 바깥면에 있는 단백질들이 제일 중요한 단백질 군 집체인 것으로 보인다. 바깥면에 있는 단백질들은 S8 을 제의하고는 7 가지 (S3, S4, S5, S10, S12, S14 등) 가 모두 tR NA 의 결 합과 인식 작용 에 있어서 중요한 역할울 한다는 것이 알려져 있다. t RNA 의 결합에 관여하고 있는 단백질들 중에 30S 하위단위체의 바 깥면에 위치하는 단백질 군집체가 포함된다는 사실은 A 와 P 지리들 이 외에 또 다른 tR NA 결합자리가 있음을 암시해 준다. 이러한 사실에 기초 하여, Lake(1977) 는 단백질 합성의 개시 단계에 있어서 코돈 인식작용 은 A 또는 P 자리가 아닌 구조적으로 독특한 인식자리에 결합한 tRL '.J 'A 에 의해서 일어난다는 가설을 주장하게 되었다. 2.7.4 인식자리 단백질 합성의 연장 회로의 전반적인 윤곽은 찰 알려져 있다(제 4 장 참조). 단백질 합성과정에서 일어나는 주요사건들을 요약하면, 코돈 인 식, 펩티드 결합 형성, 자리옮김 등 제 단계로 구분된다. 그립 2-44 의 A 에서는 한 연장 회로가 끝난 다음에 n+l 번의 코돈이 올바른 tR NA 에 의해서 읽혀질 수 있는 자리에 있다• 다음번 연장 희로의 첫 단계에 서 코돈이 인식되고(초기의 코돈 인식작용, 그림 2-44 의 B), 울바른 아 미노아실-t RNA·EF-Tu·GTP 복합체가 리보솜과 결합한다. 두번째 단 계 (펩티드 결합 형성 단계, 그림 2-44 의 C) 에서 GTP 가 GDP 와 R 로 분해되며, EF-Tu·GDP 복합체와 R 가 리보솜에서 떨어져 나오며, 펩 티드 결합이 완성된다. 이 단계에서 n+l 번째의 tRi~ A 는 아마노아실 자리를 차지하고 있다. 세번째로 일어나는 일, 즉, 자리옮김은 펩티딜 -tRN A 가 아미 노아실 자리 (그 림 2-44 의 C) 에 서 펩 티 딜 자리 (그림 2-44
의 D) 로 옮겨가는 것을 말한다. 이 단계에서 EF-G 와 GTP 의 분해가 이용되며, EF-G, GDP, Pi, 및 빈 t RNA 들이 떨어져 나오게 된다. 그립 2-44 에 나타낸 세 상태들은 각각 연장 회로에 있어서 기능적으
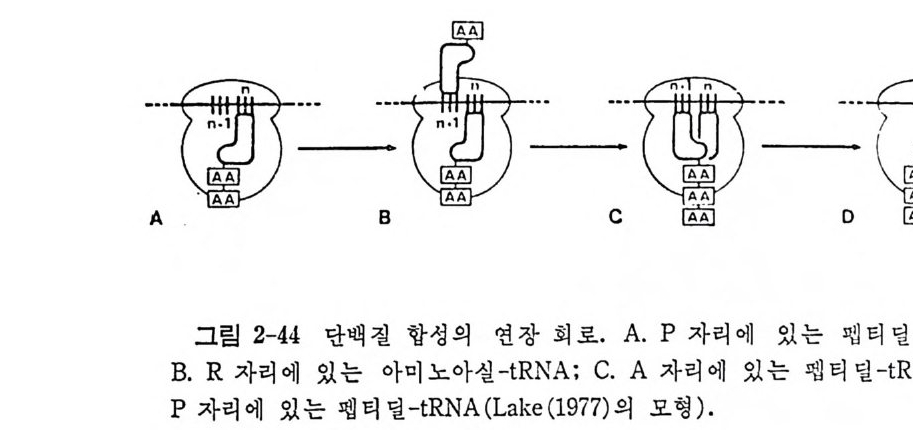 A . B C ~ 0
A . B C ~ 0
로 구분되는 상태들(따라서, 물리적으로 구별되는 상태들)이다. 세 가지 상태가 기능적으로 구분될 수 있다는 것은 다음과 같은 기준에 의거해 서 말할 수 있다. 만일 펩티딜-t RNA 가 푸로마이신과 반응하면 그것은 팬터털 자리에 있다는 것을 의미하며, 펩티틸-t RNA 가 푸로마이신과 반 응하지 않으면 그것은 아미노아실 자리에 있다는 것을 의미한다. 마찬 가지 로, 만일 아미 노아실-t RNA 가 인식 자리 에 있으면 (EF-Tu 와 GTP 의 비가수분해성 유사체인 GMPP(CH2)P 의 존재 하에서) 펩티딜기의 전달은 일어나지 않지만 펩티딜 기 전달효소의 아미노아실 자리는 비어 있을 것이다. 왜냐하면, 이 상태에서 펩티딜-t RNA 는 두로마이신과 반 응하기 때문이다. 아미노아실-t RNA 및 펩티딜-t RNA 결합자리들이란 어떤 물리적 상태에 있는 리보솜과 결합한 t RNA 둘이라고 정의하는 것 과 똑같이, 인식 자리라는 용어는 초기의 코돈 인식과정에서 리보솜과 결 합한 아미 노아실-t RNA 의 독특한 물리 적 상태 를 말한다. 앞에서도 말한 바와 같이, 30S 하위단위체의 바깥면에 t RNA 를 결합 하는 7 가지 단백질들이 군집해 있다는 것은 이 부분이 인식 자리의 유 력한 후보라는 것을 암시해 준다. 인식 자리 (R 자리)의 가능한 위치를 그림 2-45 에 나타내 었다. 만일 인식 자리 가 그림 2-45 에 나타낸 것과 같다면 인식 자리 에 결 합한 아미 노아실-t RNA 는 바깥면 에 있는 단백 질
S3, S5, S8, S10, S12, S14 및 S19-I 들과 접 촉할 수 있 으면 서 , 동시 에 그 역코돈은 코돈과 영기 짝지움을 한다. 이것은 앞에서 언급한 tR NA 결합에 대한 이 단백질들의 작용과도 잘 일치하며, 코돈이 플랫폼에 있 다는 가정과도 찰< 일치한다. 인식자리에 결합한 t RNA 의 D 줄기가 단백질 S5 와 S12 에 가까운 곳에 있을 것으로 생각한다 . 그 이유는
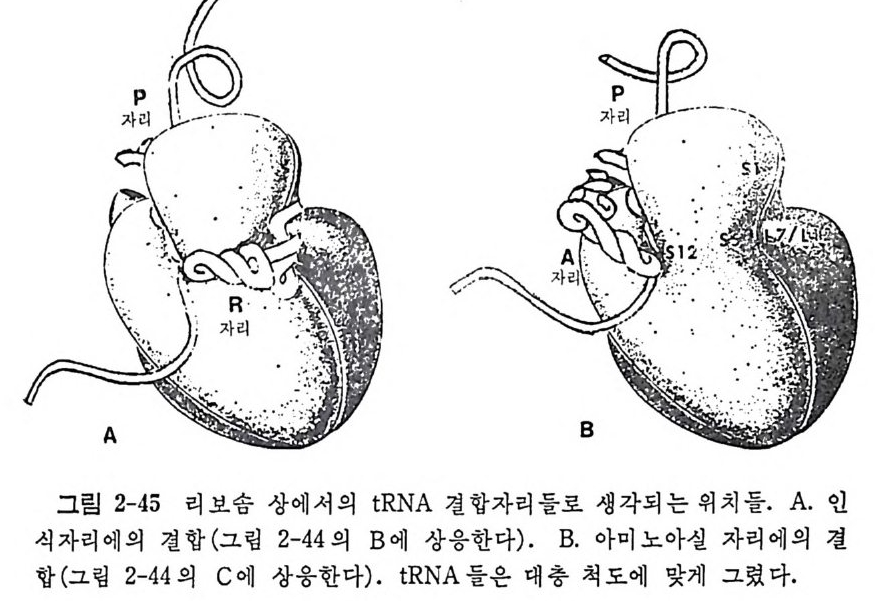 자 p 리 ` 三. -. \ ,
자 p 리 ` 三. -. \ ,
t RNAi값가 무의 미 돌연 변 이 의 억 압 tR NA 로 작용하는 사실 은 t RNA 꿉& 의 D 줄기의 어떤 부분에 돌연변이가 있을 것으로 생각되는데 실제로 그러 하기 때 문 이 다 (Hirs h, 1970 ; Kurland, 1979) . E. coli 의 su+ ( UGA) 에 있어서 D 줄기의 G24 가 A24 로 치환되어 있으며, 그 역코돈은 트립 토판에 대한 정상적인 역코돈의 영기 결합순서 (CCA) 를 가지고 있음에 도 불구하고 종결 코돈 UGA 를 인식할 수 있다. Kurland(1979) 는 이러 한 현상을 형태의 선택이라는 개념으로 설명하고자 하였다• 죽, tR NA 가 코돈과 리보솜에 동시에 작용할 수 있게끔 자리잡는 것은 코돈-역코 돈 상호작용의 특성에 따라서 결정된다는 것이다• Lake 가 주장하는 인 식자라는 인식작용이 일어나는 동안 t RNA 의 D 줄기와 단백질 S5 및 S12 가 가깝게 있을 것으로 생각되고 있다.
만일 tR NA 인식 자리가 30S 하위단위체의 바깥면에 있다면, 인식자 리로부터 아미노아실 자리에로의 자리바뀜 메카니즘이 필요할 것이다 . 이 자리바뀜 메카니즘은 인식자리에서 아미노아실 자리로 자리바뀜이 일어날 때 리보솜에 대한 mRNA 의 상대적인 움직임이 없어야 한다는 관찰과도 일치하여야 할 것이다. Gup ta 등 (1971) 은 리보솜에 의해서 보호된 mRNA 부분을 조사한 연구에서 개시 복합체의 형성 , 아미노 아실-t RNA 가 EF-Tu 와 결합하는 과정, 펩티드 결합의 형성 과정 둥 에서 mR NA 가 움칙이지 않는다는 것을 발견하였다 . 이 것은 tR NA 그 자체가 자리바뀜 메카니즘의 필수 요소임을 간접적으로 암시하는 중거 이다. R 자리에서 A 자리에로의 자리바뀜이 일어나 기 전후의 모형을 그림 2-46 에 나타내었다 (Lake, 1980). 자리바뀜이 일어날 때 역코돈 고리는 5' -치쌓임 형태와 3 ' -치쌓임 형태라고 하는 두 형태를 취할 것으로 생각 한다 .5 ' -치쌓 임 형태에서는 역코돈 고리의 5' 끝 쪽에 있는 5 개의 염 기들이 치쌓 여 있고, 3' -치쌓임 형태에서는 역코돈 고리의 3' 꾼 쪽에
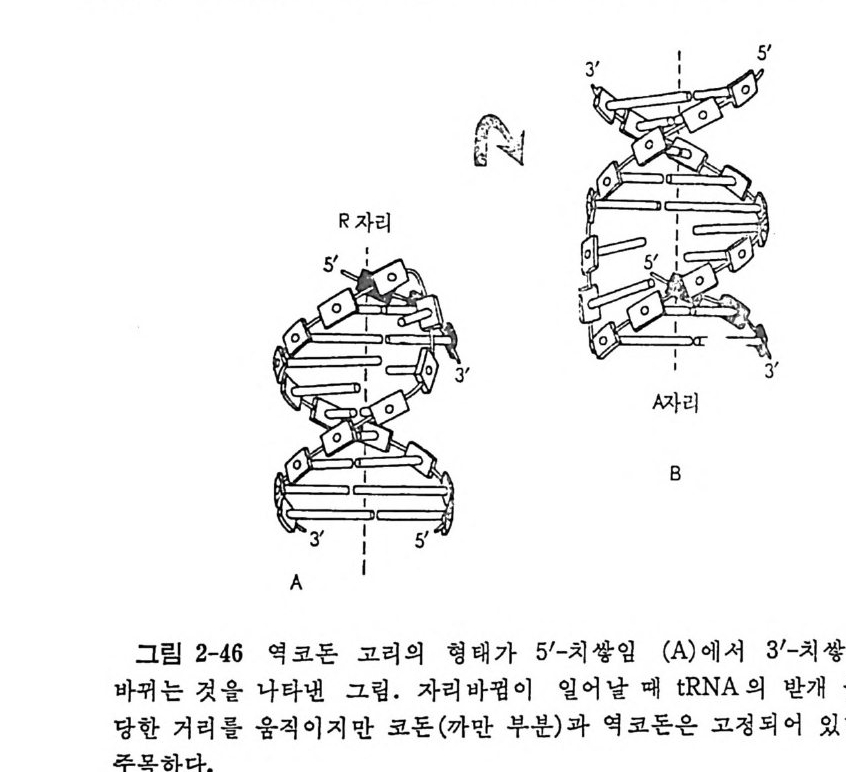 5'
5'
있는 5 개의 염기들이 치쌓여 있다. 3' -치쌓임은 효모의 t RNAPhe 에서 실제로 존재한다는 것이 알려져 있다 (K i m 등, 1974). 5' -치쌓입 형태 도 가능한 것으로 생각되고 있지만 아직 확실한 중거는 없다. R 자리에 서 A 자리에로의 자리바뀜이 일어날 때 5' -치쌓임 형태가 3' -치쌓임 형 태로 바뀔 것으로 생각되고 있다. 이 모형에서 주목해야 할 것은 tR NA 분자의 아미노산 받개 부분의 이동거리는 상당히 크지만 mRNA 와 역 코든의 움직임은 없다는 것이다. 2.8 진핵세포의 리보솜의 구조와 기능 2.8.1 개요 앞에서 이미 고 찰한 바와 같이, 원핵세포의 리보솜에 관해서는 많은 것이 알려 져 있지만, 진핵세포의 리보솜에 관해서는 훨씬 적게 알려져 있다. 티브송은 원래 Palade(1955) 에 의해서 진핵 세포에서 처음으로 발 견되었다. 그럼에도 불구하고 오늘날 원핵세포에 관한 연구가 더 많이 이루어져 있는 이유는 다음과 같은 사실에 기인된다. 첫째, 구성성분들 의 관점에서 불 메 원핵세포의 리보솜은 진핵세포의 것보다 덜 복잡하 다. 둘째, 박테리아에 있어서는 리보솜과 관련되는 여러 가지 돌연변이 체들이 알려져 있기 때문에 리보솜 성분들의 기능을 이해하기가 쉽다. 진핵세포의 리보솜의 구조적 및 기능적 구성이 E. col i의 것과 거의 비숫하거나 심지어는 같은 것으로 생각되고 있지만, 리보솜의 성분들 (단백질 및 RNA) 의 수와 성질들, 그리고 리보솜 입자들의 물리적 및 화학적 성질들이 세부적인 점에서는 많이 다르다. 진핵세포의 리보솜둘 은 원핵세포의 것들보다 약간 더 크다. 죽, 진핵세포의 리보솜은 80 개 정도의 많은 단백질들을 가지고 있으며 (원핵세포인 E. col i는 53 개의 단백질을 가진다), 또 원핵세포의 리보솜에는 없는 RNA 분자들을 추 가로 가지고 있다. 그뿐 아니라, 단백질과 핵산의 크기는 평균적으로 원 핵세포의 것들보다 더 크다. 진핵세포의 리보솜이 단백질 합성을 촉매 한다는 보편적인 기능에 있어서는 원핵세포나 다름이 없다는 것을 고려 하면, 리보솜의 크기에 차이가 있다는 것은 모순된 일로 보인다. 더우 기, 원핵세포와 진핵세포의 리보솜둘은 단백질 합성 과정에 있어서 동
일한 부분 반응을 일으키고 있다. 과의의 단백질 성분들의 수의 증가와 크기의 증대를 생기게 한 진화 압력은 과연 무엇이었을까? 아마도 진 핵세포의 리보솜은 원핵세포의 리보솜 이상의 어떤 기능들을 하고 있을 지도 모른다. 아마도 진핵세포에 있어서는 유전적인 프로그램을 실현하 는 데 에는 전사 수준에 있어서의 조종 이의 에도 번역 수준에 있어서의 조절이 더 중요한 역할을 하는지도 모른다. 그러자면 진핵세포의 리보 솜은 더 고도로 조직화된 장치가 되어야 할 것이다. 약간의 과의의 단백질들은 소포체에 있는 〈도킹〉 단백질 또는 리보포 린 I 과 II 라고 하는 목수한 수용체와 상호작용하는 목별한 역할을 합 지 도 모른다 (Sabati ni 와 Kreib i c h , 1976 ; Wate r 와 Blobel, 1981) . 진 핵 세포의 리보솜에는 펩티드 형성에는 무관하지만, 리보솜의 구조 롱 만들 거나 그것을 유지하는 데에만 필요한 단백질, 즉, 세멘트 단백질들이 있 을지도 모른다. 이러한 단백질들에 대한 필요성은 리보솜 생성 과정의 독수성에서 울 수 있다. 죽, 리보솜 단백질들은 세포질에서 합성되고핵 안으로 수송되어서 거기에서 전사되고 있는 rRNA 의 선구체에 부착함 으로써 하위단위체들로 조립된다• 선구체들은 가공되어야 하며 핵의 또 다른 자리에서 합성된 rRNA 가 큰 하위단위체와 결합되어야 한다. 두 하위단위체들은 핵으로부터 세포질로 수송되어야 한다. 과의의 단백질 들에는 하위단위체들의 조립 또는 조립된 하위단위체둘의 수송에서 어 떤 일을 할지도 모른다. 2. 8. 2 진핵세포의 리보솜의 일반적 특성 원핵세포의 리보솜과 마찬가지로 진핵세포의 리보솜은 크기, 입자의 질량, 모양, 화학적 조성 및 기능 들이 서로 다른 두 개의 하위단위체 둘로 구성되어 있다. 가) 물리적 특성 진핵세포의 리보솜의 큰 하위단위체의 침강계수 S20,w 는 60S 이고, 작은 하위단위체의 침강계수는 40S 이다. 완전한 리보솜의 침강계수는 약 80S 이다. 하위단위체들과 완전한 리보솜 입자의 침강계 수들은 리보솜의 출처에 따라서 다르다. 몇 가지 예를 표 2-11 에 실 었다• 표 2-11 에 주어진 바와 같이, 진핵세포의 리보솜의 작은 하위단위
표 2-11 80S 형 진 핵 세 포의 리 보송둘의 몇 가지 성 질 둔 리 보솜 입 자의 출 처 鬪 :\V? \!\〔)량 1 1;:\ 』 :법: R합( N량幻 A 단함( 백% 질량) 쥐의 모간노 송 79.4 4. 55I 1. 61 I o. 6351 5 0. 9I 48. 6 4. 351 1. 57 49.1 4. 091 1. 57 50.3 큰 하위단위체 59.1 3. O I 1. 62 57. 2\ 45 2. 971 1. 61 59.0 2. 7 11 1. 60 57.0 1. 575 작은 하위단위체 40.9 1. 5 I 1. 49 50. 81 55 1. 4 I 1. 55 44.3 1. 381 1. 578 47.0 1. 515 1. 635 생쥐의 간 모노송 4.56 큰 하위단위체 3. 0 11 1. 610 56.8 작은 하위단위체 1. 531 1. 556 46.6 HeLa 세포 모노송 1. 56 큰 하위단위체 1. 60 작은 하위단위체 1. 52 L 새포 모노송 1. 55 큰 하위단위체 1. 57 작은 하위단위체 1. 49 랑의 간 모노송 4. 251 1. 583 51. 8 큰 하위단위체 2. 781 1. 610 56.8 작은 하위단위체 1. 531 1. 551 4g. 6 닭의 근육 모노송 78.1* 5. 21 1. 61* 81. 1 ** 1. 60** 바다 성계 모노송 74 4. 091 1. 575 54.1
큰 하위단위체 56. 2 2·59 150 1. 5.1 19561 55 0 45.4 작 은 하위단위체 35.8 · . 45.4 Artc m i a salin a 모노송 81 3. s I 1. 5701 o. 63 49. 51 50. 5 Para;/IC CI. Ii; ;: 3.4 5 57 Ncurospo r a crassa 도노송 77-78 4. 051 1. 575 50 큰 하위단위체 56 2. 501 1. 590 53 작은 하위단위체 36 1. 551 1. 550 45 효모 모노송 80.4 3.9 5 。~ 6763636523 5057 큰작 은하 위하단위위단체위 체 683270 ..78 123... 605107 ~on~O~ 50 · 5 완두 싹 모노송 78 3. 931 1. 581 51 3.8 4 3.97 큰 하위단위체 56 2. 481 1. 591 53 2. 441 1. 59 53.3 2.45 작은 하위단위체 36 1. 531 1. 552 46 1. 521 1. 575 45. 8 1. 39 50 주 : 모노송과 두 하위단위체들에 대해서 여 러 수치들이 주어진 것은 여 러 연구진에서 독 립적으로 얻은 값둥 아다 (B i elk(1982) 의 평론시룹 참조하라) . * 자유 리보 송 ** 풀리승에서 체의 질량은 일관하게 약 1.5 x103 kdal 정도인데 반하여, 큰 하위단위 체의 질량은 식물에 있어서의 2.4 x1 03 kdal, 바다 섬계에서 있어서의 2. 8 x 103 kda], 포유동물에 있 어 서 의 3. 0 x 103 kdal 등의 값들에 서 알 수 있는 바와 같이 , 서로 많이 다르다. 따라서, 진핵세포의 리보솜들 입자들의 질량 증가는 주로 큰 하위단위체의 질량에 있어서의 차이로 생 기는 것이다. 또한, 큰 하위단위체의 질량의 증가는 주로 큰 rRNA 의 분자량의 증가에 기 인한다.
나) 화학적 특성 리보솜은 주로 RNA 와 단백질로 구성된다. 작은 하 위단위체의 RNA 함량은 45% 정도이고, 큰 하위단위체의 RNA 함량은 50-55% 정도이다(표 2-11 을 보라). 작은 하위단위체는 한 가지의 고 분자량의 RNA, 즉, 18S 형 rRNA 를 함유하며, 큰 하위단위체도 한 가 지의 고분자량의 RNA . 즉, 28S 형 rRNA 와 두 가지의 저분자량의 RNA 를 추가로 함유한다. 그 하나는 5S rRNA 이 고 다른 하나는 5. 8S rRNA 이다. 주로 쥐 간의 리보송에 대해서 알려진 것에 의하면 진핵세포의 80S 리보송은 적어도 70 가지의 다른 단백질들로 구성되어 있다 . 그 중 40 가지는 큰 하위단위체에 있고, 30 가지는 작은 하위단위체에 있다. 2. 8. 3 진핵세포의 리보솜과 폴리솜의 형태 진핵세포로부터의 리보송 입자의 대강한 형태에 관한 연구에는 전자현 미경사진법 (Luts c h 등, 1979; Emanuil o v 등, 1978; Kis e lev 등, 1978) 과 작은 각 X 맹 산란법 또는 중성 자 산란법 (Muller 등, 1978) 들을 사 용하고 있다. 티보솜 입자의 표면에 있어서의 조직에 관해서는 면역 전 자현미경 사진법으로 더 자세한 정보를 얻는다. 가 ) 전자현미경 사진법으로 얻은 형태 진핵세포들의 리보솜의 초미세구 조예 관한 몇 개의 보고가 있다 (Lake 등, 1974; Cox, 1977; Bie l ka, 19 82) . 집중적으로 연구된 진핵세포는 쥐 간, 생쥐 간, 토끼 망상 적혈구 종양세 포들, Locusta , Arte m i a, Plasmodia , 효모 세 포들, Geotr i c l wm, Tetr a hy m ena, Nett ro sJ;m ·a 및 여 러 가지 식 물들이 다 (vVool (1979) 와 Bie lk a (1982) 의 평 론서 를 참고하라) . 진핵세포의 리보솜의 톡칭은 대칭성이 없다는 것이다 • 진핵세포의 리 보솜들은 그들의 모양, 단백질과 RNA 부분들의 분포, 큰 하위단위체 와 작은 하위단위체의 상호간의 위치 등에 있어서 비대칭성을 가지고있 다. 원핵세포의 리보솜에 있어서처럼, 진핵세포의 리보솜의 입체구조 에 있어서 성분들이 반복적으로 배열되어 있는 경우는 없다. 다만, 원 핵세포의 단백질 L7/L12 가 네 복사물이 있는 바와 같이 진핵세포의 단 백질 eL12 p는 약 두 개의 복사물이 있음이 알려져 있다 (2.8.2 절을 보 라).
취 간의 리보솜에 관한 연구가 비교적 광범하게 이 루어겨 있으므로, 아래에서는 주로 이 리보솜울 예로 들어서 기술하고자 한다. 전자현미경 사진법에 의한 분석결과에 기초하여 구성한 모노송(단량 체 상태의 리보솜), 작은 하위단위체, 큰 하위단위체 들의 모형들을 ::::z.. 립 2-47 에 주었다• 전자현미경 사진에서 작은 하위단위체들은 두 가지 상으로 브이는 것을 알 수 있다. 작은 하위단위체는 길쭉한 모양을 한 235x130A 의 상에서 머리와 몽동 두 부분으로 구분되고 있다(그립 2-47 의 a 및 b). 또한 이 그림에서 약간 구부러진 250x175A 크기의 상은 앞에서 말한 상의 장축 주위로 g oo 의 각으로 회전시켜서 얻는 상이다. 이 상에서는 작은 하위단위체를 세 부분으로 나누는 두 경계선이 있다. 머리와 몸통 사이에 조그마한 돌출부분이 있는 것을 볼 수 있다. 이 돌 출부분은 40S 입 자와 60S 입 자의 접 촉 에 관여 한다. 최근에 Lake 의 연구진에서는 효모의 리보솜의 두 하위단위체의 전자 현 미 경 사진 을 얻 었 다 (Lake 등, 1982; Henderson 등, 1984) . 이 것 을 그림 2-48 에 나타내었다. 진핵체의 작은 하위단위체의 몸통 아래 부분 으로 두 개의 귓불이 있는 데 반하여 원시박테리아와 진성 박테리아의
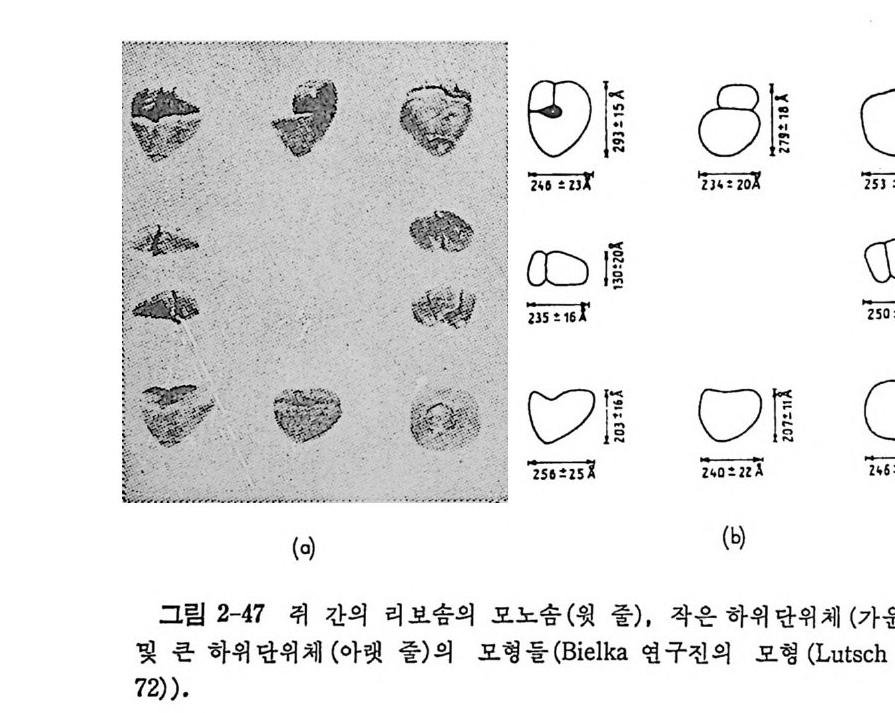 {.. .’. :군·一 홀~4 델티’2 'n:l' 1己2n:20l ll 0m:i~il'
{.. .’. :군·一 홀~4 델티’2 'n:l' 1己2n:20l ll 0m:i~il'
하위단위체는 이 귓불이 없는 것이 특이다. 한편, 원시 박테리아와 진 핵체의 작은 하위단위체는 머리 부분에 부리가 있는 것이 특징이다. 큰 하위단위체들은 진성 박테리아, 원시 박테리아 및 진핵체들에 있어서 유사하지만 다소 차이가 있다(그림 2-48 을 보라). Lake 등 (1982) 은 이러한 관찰에 기초하여 원시 박테리아, 진성박테
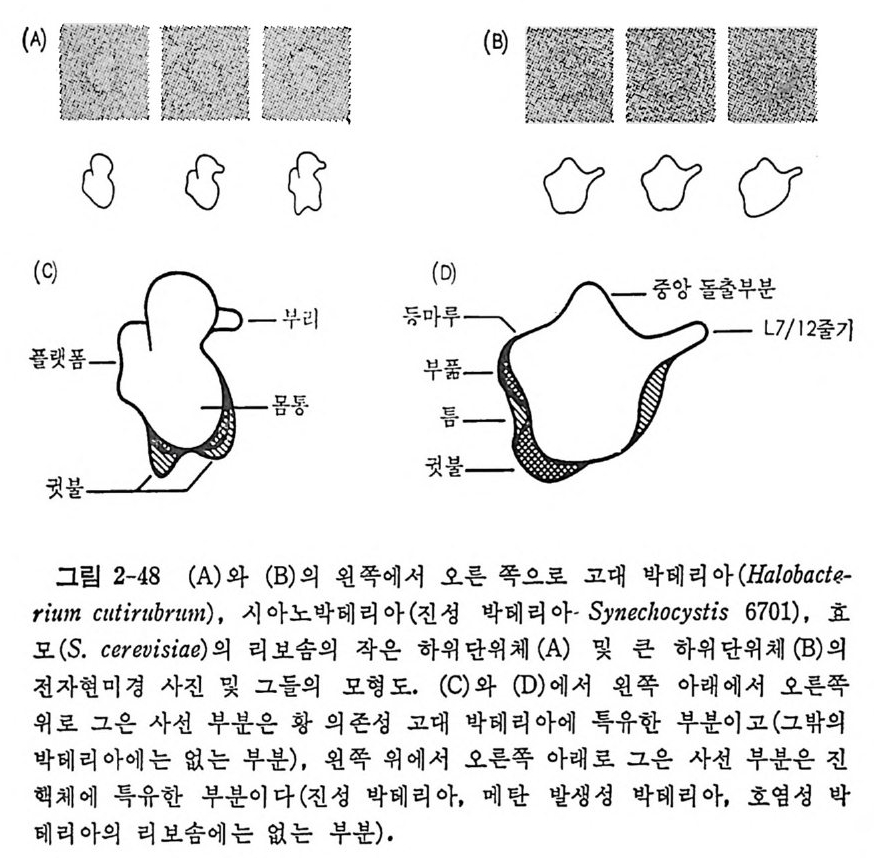 (B)
(B)
리아 및 진핵체의 리보솜둘의 진화의 계통수를 다음과 같은 그림으로나 타내었다. 이 문제는 rRNA 들, 단백질 합성의 자세한 메카니즘에 있어 서의 차이 둥에 관한 연구결과가 얻어져야 확인될 것으로 생각된다. 그 뿐 아니라 무엇보다 중요한 것은 그들의 계통수 구성에서 가정한 고생 대박테리아(p aleoc yt e) 의 존재가 확인되어야 할 것이다.
나) 작은 각 X- 선 산란법으로 얻은 모형 용액에서 산란법으로 얻은 리보 송의 치수는 단리상태의 리보솜에 바해서 rn-20% 만큼 더 크다. 이 차이는 리보솜의 용매화로 생긴다. 60S 하위단위체의 최대적경이 280A 인 데 비 하여 리 보솜의 최 대 칙 경 은 370 A 이 다. 80S 입 자의 최 대 직 경 의 증가는 25% 이고 60S 하위단위체의 직경의 증가는 10 % 분 이다. 작은 하위단위 체 가 평원형 (0 형)과 편장형 (P 형)들과 감은 두 가지 알로스테리 형태를 취할 수 있다고 가정하면, 0 형태에서 P 형태로 변 이될 대 치수가 25 %(9 0A) 만큼 증가할 것으로 생각된다. 주기적인 전 이 P-0-P-O-P··· 는 〈래 크와 희 전〉 (rack-and-roll) 이 라고 하는 리 보슴에 관한 동적 모형의 기초가 된다. 이 모형은 연창과정에 있어서의 리보솜 의 자리옮김을 설명하 고자 제안된 것이다. X- 선 산란법으르 얻은 전과 에서 리보솜은 응어리-껍질 모 형 으로 조직되어 있다는 결론을 얻었다. 즉, 응어리 부분은 단백질 함량이 크고, 껍질 부분에는 rRNA 함량이 크다. 용액에 있어서의 쥐 간의 풀리솜은 퍼진 구조가 이니라 조밀한 구조 를 가지고 있다. 풀리솜에서의 리보솜돌사이의 공간은 약 7oA 이다. 8 개 의 리 보솜 입 자를 가진 풀리 솜의 최 대 직 경 은 1, 300 A 이 다. mRNA 에 결합한 리보솜둘의 나사선형 배열은 용액에 있어서의 폴리솜이 취할 수 있는 가장가능한구조라고생각된다. 이러한 나사선 구조의 핏취(pit ch) 는 330 A 이 다. 풀리 송의 나사선 구조가 가능하려 면 mRNA 분자가 각 리 보솜에서 약 110° 굽어야 하는데 이것은 작은 하위단위체가 편장형일 것이라는 의견과 찰 일치한다. 2.9 진핵세포의 리보솜의 성분들 2. 9. I 진핵세포의 리보솜의 단백질들 여러 가지 진핵세포들에서 리보솜 단백질들이 이차원 전기이등으로 분리되었다. 대부분의 연구들이 포유동물의 리보솜, 특히 쥐의 간파 토 끼의 망상 적혈구의 리보솜의 단백질들을 써서 이루어졌다. 표 2-12 에 여러 가지 생물종들과 미토콘드리아 및 엽록체의 리보솜 및 그들의 하 위단위체들의 단백질 수를 주었다. 분리한 40S 및 60S 하위단위체들에
서 단리한 단백질 혼합물들은 각각 30 가지 및 40 가지의 성분들로 분리 된다. 단백질들은 이차원 전기이동 분리 양식에서 왼쪽에서 오른쪽으 로 한 충씩 내려가면서 번호를 붙여서 명명한다. 진핵세포의 리보솜 단 백질들의 명명은 연구자들 사이에서 아직 의견의 일치를 보지 못하 고 있다. 일 반적 으로 McConkey 등 (1979) 이 제 안한 명 명 법 통일 안을 사용하고 있는데, Werner(l982) 는 효모의 리보솜 단백질들에 대해서 Kruis w i jk 와 Planta (1974) 가 재 안한 안을 사용하는 것 이 좋다고 주장 하고 있다. 앞으로 진핵세포의 리보솜 단백질에 관한 연구가 성숙되면 원핵세포에서와 같은 명명법 통일안이 제정될 것으로 믿는다. 이 책에 서 는 McConkey 등 (1979) 의 명 명 법 을 사용하였다.
표 2-12 리보송 입자들에 있어서의 단백질의 수 (B i elka, 1982) 리보솜의 출 처 80S 모노송 하위6단0S위 체 하위40단S위 체 쥐 간 76 34 27 39 31 40 30 69-72 39 30 28 40 33 36 26 46 42 77 43 34 취 근육 69 38 31 생쥐 간 70 39 31 토끼 간 75 37 33 토끼 망상 적혈구 62-63 36-37 26 40 33 46 30 39 32 70 40 30 75 42 33 사람 태반 64-66 36 28 사람편도선 35 34 BeLa 세포 37-38 29
40 47 35 Krebs II 복수 세 포 35-3 7 28-2~ L 세포 45 34 중국산 합스터 세포 72 41 31 Xe11op 11s 난자 37 26-28 Artc m i a sali11 a 32 완두 28 24 83 44 -5 5 32 -4 0 47 32 밀싹 30 Di ct y o ste / i11 m dis c oid e1 1111 38 32 Podospo r a anserin a 41 28 Saccharomy ce s carlsberge n sis 39 30 41 30 Sacclzaromy ce s cerevis i a e 67 37 30 42 34 40-41 28-30 74 45 28 Chlamy d omonas 39 26 44 31 56 Polyt om a mi ru ,n 53 Eug le na 73-83 37-42 33-36 Ne11rosp or a 31 21 미토콘드리아 Neurospo r a 39 30 Kenop us 77-84 40 44 취 간 36 30 40 30 효모 38 33 영록체 Chlamy d omonas 26 22 30 20 34 25 Eug le na 56-60 30-34 22-24
리보솜 단백질의 수 또는 종류에 관한 분석결과가 연구실마다 다른 이유는 사용한 실험조건들이 서로 다르기 때문이다. 첫째로, 리보솜울 제조하는 방법에 따라서 일부분의 리보송 단백질을 잃을 수 있고 비리 보솜성 단백질이 리보솜에 함유될 수 있다. 예컨대, 리보송을 단리하고 정제할 때 씻지 않은 리보솜둘은 산성 단 백질들 이 더 많 이 함유되어 있 다. 또 다론 한편으로는, 허슨하게 결합된 리보솜의 구조적 단백질들이 제거될 수 있으며 이 결과로 전기이동의 분리 모양이 달라질 수 있다. 둘째로, 리보솜 단백질은 단백질 가수분해효소들에 의한 분해작용, 시 안산 암모늄에 의한 카르바모일화, 또는 SH 기의 산화 등으로 변형된 물질들을 생기게 할 수 있다. 세째로, 리보솜의 두 하위단위체들을 분 리시키는 조건에 따라서 작은 하위단위체에 속하는 단백질이 큰 하위단 위체의 성분으로 혼입될 수도 있다. 진핵세포의 리보솜에는 다량의 염기성 단백질들뿐 아니라 약간의 산 성 단백질들이 있다. 특히, 큰 하위단위체에 있는 인산화된 단백질들에 관해서는 최근에 많은 연구가 진행 중이다 (2.9.2 절). 가) 아미노산 조성 및 아미노산 결합순서 리보솜 단백질의 전체 혼합물 의 아미노산 조성은 하전된 아미노산 함량이 크다는 것이 특징이다 (Welfle 둥, 1969 ; Brug ge r 와 Boschett i. 1975 ; Fay e 둥, 1979) . 쥐 간 의 리보솜 단백질 총량의 21. 5 -22.4 몰 백분율이 Ly s, Arg 및 H i s 둘 이고, 산성 아미 노산인 Asp 와 Glu 들의 몰 백 분율은 17. 2 이다. 아미노산 조성은 리보솜의 출처에 따라서 다소 차이가 있다. 지금까 지 발표된 리보솜의 개개의 단백질들에 대한 아미노산 조성의 분석치들 온 찰 일치하지 않고 있다. 정확한 결과를 얻기 위해서는 앞으로 더 많 은 연구가 이루어져야 할 것이다. Arte m i a sali na 로부터 의 리 보솜의 산성 단백 질 eL7/L12 의 부분적 인 결합순서 분석 이 이루어져 있고 (Amons 등, 1980), 최근에는 eL12/eL 12-P 의 완전 한 일 차구조가 분석 되 었으며 (Amons 등, 1979) , 밀 의 리 보 송의 산성 단백질의 아미노말단의 결합순서와 효모의 리보솜의 큰 하위단위체의 44 번 단백질의 완전한 결합순서가 분석되었다(It oh 와 Wi ttm ann-Lie b old, 1978) . 나) 번역후 변형 다른 많은 단백질들과 마찬가지로 리보솜의 단백질들
도 여러 가지 번역 후 변형을 받는다. 매우 홍미 있는 것으로서는 인산 화가 있다. 이 문제는 2.9.2 절에 서 따로 다룰 것이다. 그밖의 변형들 로서는 메틸화와 아세 틸화가 있다. (1) 메틸화 메털화된 아미노산 잔기를 함유하는 리보솜 단백질 들이 여러 생물종 의 리보솜에서 검출되었다. 메틸화된 단백질들은 두 하위단위체들에 서 다 검 출된 다. E-N- 모노 메 틸 리 신 이 Blasto c ladie l la emerso11ii 의 리 보솜 단 백질들에 서 발견되는 주되는 메 틸 화된 아미노산이다 ( Comb 등 , 1966). 그밖에도 N6,N6- 디메틸아르기닌과 e- N - 트리메리메 틸 리신이 HeLa 세 포의 리보송 단백질들에서 발견되었다 ( Chan g 둥, 1976) . 효모의 리 보송의 단백 질 S31 과 S32, 그리 고 L15 와 L41 동이 메 틸화 되어 있음이 발견되었다. 하위단위체의 단백질 들 의 메 틸화는 세포 주기 의 단계에 따라서 변하며 Gl 단계에서 최고 수 준 에 도달한다. 다른 한 편으로, 60S 하위단위체 단백질들의 메틸화는 세포 주기의 단계에 따르 는 변화가 크지 않고, Sl 단계에서 최고 수준을 보인다. (2) 아세틸화 쥐 간의 리보솜 단백질에서 검출되는 아세틸화된 아미노산들에는 N- a_ 아세틸리신과 N-E- 아세틸리신 들이 있다 (L i ew 와 Gornall, 1973). 토 끼의 망상 적혈구를 uc- 아세틸 -CoA 와 항온반응시키면 60S 리보솜하위 단위체의 단백질들 중에서 분자량 29kdal 의 단백질이 아세 틸화 되는 것 이 밝혀졌다. 다) 변형된 단백질들을 가진 리보솜 돌연변이체들 변형된 단백 질들은 대 부분의 경우 에리트로마이신 및 스트랩토마이신에 대해서 저항성을 가 진 Chlamy do monas re i nlzard ii의 돌연변이종들의 엽록체의 리보솜들에서 검 출되 었 다 (Brug ge r 와 Boschett i, 1975 ; Mets 와 Bog o rad, 1972 ; Dav- ids on, 1974; Ohtt a 둥, 1975). 돌연변이로 달라진 리보송 단백질들은 Eu g lena 의 스트랩토마이신 저항성 돌연변이체에서도 발견되었다. 진핵 세포의 세포질의 리보솜 단백질로서는 곰팡이 Podospo r a anser i na 의 시 클로헥시미드 저항성 돌연변이체에서 변이된 리보솜 단백질이 검출되었 다 (Bequ e ret 등, 1977) . 라) 종 특이성 및 진화 상이한 포유동물들로부터의 리보솜 단백질들은
전기이동으로 분석한 결과만을 가지고 보면 매우 비슷하거나 심지어는 동일 하다 (McCco nke y 등, 197 9) . 그뿐 아니 라, 포유동물 , 조류 , 파충 류 및 어류 등과 같은 여러 가진 문의 동물로부터의 리보솜 단백질들 사 이 에도 마미한 차 이 가 있을뿐이다. 이러한 연구들로부터 척추동물들 의 진화과정에서 리보 솜 단백진들은 서서히 진화하였다 고 결론을 내릴 수 있 었 다 (D elaunay 등 , 197 3) . 최근에 쥐 , 토끼, 닭 및 송어둘로부터의 리보 솜 단백질들을 몇 가지 전기이동법으로 세밀하게 비교하는 연구가 이 루어졌다 . 대부분의 리보 송 단백질들은 이차원적 분리양식에 있어서 동일한 위치를 가지지만, 및 가지 단백질들의 경우에는 명확한 차 이가 있음을 알았다. 상이한 단 백전 등 의 수는 비교한 생물종들 사이의 진화 상의 거리가 멀어질 수록 층가한다 . 하동동물종들과 식물들로부터의 리보솜은 그들의 단백 질들의 수와 분 자량에 있어서는척추동물들로부터 리보솜과 유사한 성질들을 가지고있 다 . 그러나 개개의 단백질들의 이 차원적 전기이동을 바교해 보면 현저 하게 다르다는 것을 알 수 있다. 이것은 이차원적 전기아동 분리양식에 있어서의 단백질 반점들은 일치하지 않음을 의미한다. 그러므로, 척추 동물과 무척추동물들의 상관된 티보솜 단백질들을 확실하게 관계를 짓는 것 은 아직 불가능하다 (D elaunay 등, 1973) . 한 가지 예 외 는 쥐 간과 .rlrt c m i a sali; za 에 있 는 산성 인 산단백 질 eL7/L12 이 다. 이 단백 질 은 효 모 리보솜의 인산단백질 L44 에 상응하는 것으로 생각된다(lt oh 와 Wi tt mann-L i e b old, 197 8) . Dro so p lz i la 의 여러 가지 변종들에서 얻은 리보솜 단백질들을 전기이 동법 으르 비 교해 보면 D. melanog as te r 와 D. sim ula ns 는 완전 히 동일 하며 진화 상에서 먼 관계에 있는 D. melano g as t er 와 D. v i r ili s 는 두 개의 단백질 반점만이 다르다. 리보솜 단백질들이 진화과정에서 고도로 보존되어 있다는 것은 외떡 잎 형 옥수수와 쌍떡잎형 콩의 싹들에서는 리보솜 단백질들의 이차원적 전기이동 분리 모양이 매우 유사하다는 데서 알게 되었다 (Gualerz i 등. 1974) . 마) 미토콘드리아 및 엽록체의 리보솜 단백질들 효모와 Neuros p ora 의 미 토콘드리아의 리보솜은 60 내지 70 개의 단백질들을 가지고 있으며 그
둘의 분자량은 크다. 그리고 미토콘드리아의 티보솜 단백질들은 세포질 또는 E. col i의 리보솜 단백질들보다 산성이 더 크다. 동물세포의 리보 솜들에는 70 내지 100 가지의 단백질들이 있음이 발견되었다 (Le i s t er 와 Dawi d, 1974). 물론 이 70 내지 100 가지 단백질들에는 우발적으로 회 합해서 들어간 비리보솜성 단백질들이 포함되어 있 을 가능성을 배제할 수 없다. 실제로, O'Brie n 등 (1976) 은 리보솜의 하위단위체들을 원심분 리하는 동안에 소의 미토콘드리아의 리보솜의 단백질 조성을 KVMg ” 비 를 변화시 키 면서 조사해 보았더 니 단백 질의 수가 K+/Mg +2 비 를 증가 시킴에 따라시 감소한다는 것을 알았다. 그렇지만 펩티딜 기 전달효소가 상실되지 않을 정도로 조건을 유지하면서 리보솜울 씻는 조건을 가혹 하게 할지라도 소의 미토콘드리아의 리보솜은 약 90 가지의 단백질들을 가지고 있다. 지금까지 연구한 모든 생물체들에 있어서의 미토콘드리아의 대부분의 리보솜 단백질들은 전기이동과 항원성 자리들로 볼 때 세포길에 있는 리 보솜 단백 질들과는 다른 독특한 단백 질 인 것으로 생 각된 다 (Hallermey e r 와 Neup er t, 1974) . 그러 나, Neurospo r a 와 E. coli 의 리 보솜 단백 질 들 올 면역화학적으로 비교해 보면 몇 가지 단백질들은 공통되는 항원성 결 정인자들을 가지는 경우도 있다. 아칙 엽록체의 리보송 단백질들을 충분한 양으로 얻지 못하고 있어서 아미노산 결합순서의 분석이나 항원성이 연구되지 못하고 있다. Cap el 과 Bour q ue(1977) 는 이차원 겔 전기이동법을 사용하여 담배잎의 리보 송 단백질은 그 작은 하위단위체에 20 내지 24 개가 있고 큰 하위단위 체 에 는 34 내 지 38 개 가 있 다고 보고하였 다. Brug ge r 와 Boschett i (19 ' 75) 는 Chlamy d omonas 의 엽 록체 의 리 보솜의 작은 하위 단위 체 는 25 개 의 단백질을 함유하며 큰 하위단위체는 34 개의 단백질을 함유한다고 보고 하였다. 많은 연구진들이 영록체의 리보솜 또는하위단위체들과 원핵세포의 리 보솜 또는 하위단위체들의 면역학적 교차반응들을 알아보기 위해서 연 구하였다. 시금치와 콩의 엽록체의 리보솜 또는 하위단위체들은 E. coli, Bacil lus subti lis 및 Bacil lu s ste a roth e rmop hi l u s 들에 서 얻 은 리 보솜 또 는 하위단위체들에 대한 항체와 전혀 교차반응하지 않음을 관찰하였다. 그뿐 아니라, 콩 또는 시금치의 엽록체의 리보솜에 대한 항체들은 청조 류 Anacyt is 로부터 의 리 보솜 단백 질과 교차반응을 하지 않는다 (Gualerzi
동, 1974). 앞으로 이러한 문제들은 더 정제된 리보솜 단백질들이 얻어 진 다음에 더 세밀하게 연구되어야 할 문제라고 생각된다. 2.9.2 인산화된 리보솜 단백질들 진핵체들에 있어서의 리보솜 단백질의 인산화는 Kaba t (l970) 에 의해 서 처음으로 보고되었다. 리보솜 단백질의 인산화는 원핵세포에서는 일 어나지 않는다. E. col i가 박테리오파지에 의해서 감염되었을 때는파지 에 의해서 유발된 단백질 키나제에 의해서 E. col i의 단백질들이 인산 화될 수는 있 다 (Rahmsdorf 동, 1974) . 최근에 와서 리브송의 인산화는 많은 관심을 끄는 문제가 되고 있다. 그 이유는 생체 내에서의 인산화가 여러 가지 자국들에 의해서 영향을 받는 것으로 보아서 리보솜 단백질의 인산화는 아마도 번역 수준에서의 단백질 합성의 조절에 관여할 것으로 인정되고 있기 때문이다. 현재로 서는 명확한 중거를 얻지 못하고 있지만, 리보솜 단백질의 인산화와 단 백질 합성의 번역 수준에 있어서의 조종 사이에는 어떤 관계가 있을 것 이라는 실험적 중거들이 상당히 있다. 이 문제에 관해서는 제 4 장에서 단백질 합성의 개시 단계의 조종에 관한 문제를 다룰 때 다시 말하기로 하겠다. 가) 생체외 및 생체내 인산화 단리된 많은 단백질들은 시험관내에서 여 러 가지 단백질 키나제들에 의해서 인산화된다. 생체의 인산화는 주로 -cA MP 의 존성 단백 질 키 나제 를 써 서 연 구하였 다 (Wool, 1979 ; Bie lk a, 1982) . 리보솜 단백질의 인산화는 세린 잔기 상에서 일어나는 것이 보동이고 트레오닌 상에서 일어나는 예는 아주 드물다 (B i elka, 1982). 정상적인 세포에서의 생체내 인산화는 작은 하위단위체의 단백질 S6 과 두 산성 단백질들(쥐 간에서 얻은 Pl 과 P2, 그리고 Arte m i a salin a 에서 얻은 eL12 와 eL12' )만이 주로 인산화된다. 그밖에도, S2, S3/S3a, S16, 16 및 L14 둥이 어느 정도 인산화된다는 것이 알려져 있다. (1) S6 의 인산화 S6 의 인산화의 정도는, 특히, 조칙들의 생리 조건에 따라서 다르다. S6 의 인산화에 영향을 미치는 자국들에는 cAMP, 비루스의 감염, 세포
배양에 있어서의 성장 조건의 변화 등 여러 가지가 있다(표 2-13). 표 2-13 의 예들을 보면, 단백질 S6 의 인산화는 단백질 합성 이 왕성 할 때, 단백질 합성의 방해물이 존재 할 때, 단백질 합성에 큰 변화가 없을 때 표 2-13 리브송 단백 질 S6 의 인 산화 운 변 화시키는 조건 들 S6 인 산화 의 증가 S6 안 산화 의 강 소 호르돈 글루카곤 당뇨병에 걸 린 등 몽 에 티독신 인슐린 을 주었을 때 당뇨병 에티오닌 에피네프린 고리형 AMP 비루스의 감영 박시나 비루스 수포성 구내염 비루스 제포 성장 조건의 변화 간 재생 세포 주기 간상해 단백질 합성의 방해물질 (푸로마이신과 시클로핵시미드) (가령, 굴루카곤이 존재할 때) 일어난다 (Gressner 와 Wool, 1976). 그 러므로, 단백질 S6 의 인산화가 생물학적으로 무슨 역할을 하는지를 알 기 가 매 우 어 렵 다• 그러 나, Terao 와 Og a ta (1979a ; 1979b) 는 40S 하위 단위체와 풀리 -U 가 자의선 조사로 교차결합되는 것을 알았으며, 특히 단백질 S6 아 인산화되었을 때 더 잘 교차결합됨을 발견하였다. 이 결과 에 기초하여 단백질 S6 은 리보솜 상에서 mRNA 를 결합하는 역할을 할 것이라고 제안하고 있다. (2) 산성 리보솜 단백질들 몇 가지 리보솜 단백질들이 진핵세포들에서도 발견되었다. 이 단백질 둘은 전기이동적 분리에서의 이동 양식, 큰 산성, 폴리아크릴아미드 겔 에서의 착색의 어려움, 비슷한 분자량 (12.5-16kdal) 을 가지는 점 등으 로 보아 E. coli 의 산성 단백 질 L7/L12 와 성 질 이 비 슷하다. E. coli 의
50S 하위단위체를 토끼의 골격근육에서 얻은 단백질 키나제와 r-[32 p ]_ GTP 와 항온처리하면 L7/L12 가 선택적으로 인산화되는 것이 관찰되었 다 (Traug h 와 Traut, 1972) . 쥐 간의 리보솜들에서는 이리한 단백질이 두 가지, 즉, Pl 과 P2 가 발견 되 었 다. 그리 고 Pl 과 P2 에 는 각각 Pla 와 Plb, 그리 고 P2a, P2b 및 P2c 들과 같은 인산화된 유도체들이 있다. Pl 과 P2 자체들이 원래 부터 인산화되어 있었는지 아닌지는 아직 밝혀져 있지 않았다. Pl 과 P2 단백질의 특징은 다량의 알라닌을 함유하고 있는 점이다. Pl 과 P2 의 트립신 펩 티드들의 지문들이 비슷하기는 하지만 이 두 단백질들이 공통 의 선조가 되는 유전자의 분기진화로 생긴 것인지에 관해서는 아직 아 는바 없다. 앞에서 말한 바와 같이 , E. col i의 L7/L12 와 쥐 간의 Pl 과 P2 사이 에는 몇 가지 유사점들이 있기 때문에 이들 단백질의 구조와 기능에도 유사점이 있을 것으로 생각할 수 있겠지만 , 그들의 아미노산 조성은 상 당히 다르며, 면역학적으로도 상동성이 발견되지 않는다. 오히려, 쥐 간 리보솜의 큰 하위단위체에 있는 또 다른 상동성 단백질 쌍인 L40 과 L41 이 L7/L12 에 면역학적으로 더 유사할 것 으르 생각되고 있지만 L40 과 L41 들이 단리된 상태로 얻어지지 못하고 있기 때문에 그것을 확인하지 못하고 있 다 (Sherto n 과 ·wo ol, 1974) . Arte 11 1i a salin a 의 리 보솜에 서 P2 와 유사한 eL12 와 eL12' 두 단백 질 을 얻 었 다 (Amons 등, 1977 ; van Ag tho ven 등, 1978) . 부분적 인 연 속 부분들의 분석 에 의하면 eL12 와 eL12’ 은 밀접한 관계를 가전 독특한 유전자들로부터 유래된 것임을 암시해 주고 있다. 또 두 단백질들은 인 산화된 형 태 들, 즉, eL12-P 와 eL12'-P 로서 도 존재 한다. Arte m i a salin a 의 티 보솜의 eL12-P 와 eL12'-P 는 각각 1. 8 개 및 0. 9 개 의 복사물을 가지고 있다 . 쥐 간의 P2, Arte m i a salin a 의 eL12, E. coli 의 L7/L12, 효모의 산 성 단백질의 알라닌을 많이 함유한 연속부분의 아미노말단 부분의 아미 노산 결합순서를 비교해 보면 이 단백질들 사이에는 상당한 유사성이 있 음을 알 수 있다 (Amons 등, 1977; Amons 등, 1978). 이와 같이, 적 어도 이 산성 단백질 한 가지는 곰광이 (효모)에서 무척추동물(바다 새 우)로 그 다음에 포유동물(쥐)로 진화하는 과정에서 변함 없이 보존되어 왔을 것 으로 생 각된 다. Arte m i a 의 eL12 는 EF-1 의 존성 아미 노아실
-tRN A 의 결 합 및 EF-2 로 촉매 되 는 GTP 가수분해 동의 반응들에 필 수적으로 요구되고 있는데, 이것은 E. col i의 L7/Ll2 가 같은 반응들에 서 요구되 는 것 과 꼭 같다 (van Ag tho ven 등, 1977) . 또 E. coli 의 L7/ Ll2 단백질들과 마찬가지로 진핵세포의 산성 리보솜 단백질들은 리보송 의 두 하위단위체들의 경계면에 위치하고 있을 것으로 생각되고 있다 (Horak 와 Schif fm ann, 1977) . 2.9.3 진핵세포의 리보솜 RNA 들 2.4 절에서 원핵세포의 rRNA 들에 관해서 기술할 메 진핵세포의 rRNA 들에 관해서도 일차구조, 이차구조, 삼차구조, 그리고 기능에 관해서 중 요한 것은 언급되었다. 따라서 이 절에서는 진핵세포의 rRNA 에 관해 서는 간단히 기술하고자 한다. 진핵세포의 리보솜 단백질들과 달라서 rRNA 들은 단리하기가 쉽기 때 문에 단리한 상태의 rRNA 들에 관한 연구는 상당히 많이 이루어져 있 다. 특히, 최근에 RNA 일차구조 분석의 신속하고 좋은 방법들이 개발 되어서 일차구조 및 이차구조에 관한 연구결과들이 급숙히 증가하고 있 다 (2.4 철을 참고 하라). 가) 고분자량의 리보솜 RNA 들 진핵세포의 리보솜의 큰 하위단위체와 직은 하위단위체들은 모두 고분자량의 RNA 를 하나씩 가지고 있다. 생 물종에 따라서 큰 하위 단위 체 에는 25-28 S rRNA (28S 와 같은 rRNA) 가 있고 작은 하위 단위 체 에 는 15 -18S rRNA (18S 와 같은 rRNA) 가 있다. (1) 분자량 작은 하위단위체에 있는 18S 형의 rRNA 의 분자량은 여러 동물종들 에서 거의 일정하지만, 큰 하위단위체에 있는 28S 형 rRNA 의 것은 더 진화된 종일 수록 분자량이 더 크다 (표 2-14 와 표 2-15 를 보라) . (2) 변형된 염기들 rRNA 둘은 메틸화된 염기들 메틸화된 리보오스 (2'-0- 메틸리보오스) 그리고 그밖의 변형된 염기들을 함유하고 있다. rRNA 의 메틸화는 조 사한 모든 진핵세포들에 존재하며, 엽록체와 미토콘드리아에도 존재한 다. 그러나 미토콘드리아의 경우에는 메틸화가 적게 일어나며, 그것도
표 2-14 세포질에 있는 28S 형 및 18S 형 rRNA 들의 분자량 (x10-s kdal) . 종 I 큰 하저단위체피 r 핥iA | 작은 하위단위체의 rRNA 곰팡이 1. 36 -1. 39 0. 65-0. 70 고사리 1. 34 0.72 조류 1. 3 0.69 식뭉 1.2 -1. 3 0. 65-0. 71 원생동뭉 아메바 1. 57 0.83 Tetr a hy m ena 1. 35 0.7 효모 1. 21 0.72 동물 AL11r1t1e1m bri iac 1 1s 11.. 3431 o0.. 6666 Galleria 1.4 0.7 Drosop lzi /a 1. 4 0. 65-0. 73 Teneb r io 1. 5 0.7 바다 섭계 1. 37 0.65 어류 1.4 -1. 5 0.65 개구리 1.4 -1. 5 0.6-0.7 파충류 1. 5 0.62 닭 1. 6 -1. 65 0.65 생쥐 1. 65 -1. 7 0.65 주 1 1. 44 0. 66 원숭이 1. 66 0. 65 HeLa 세포 1. 66 0.65 큰 하위단위체의 rRNA 만 메틸화되고 작은 하위단위체의 rRNA 에서는 메 틸 화가 일 어 나지 않는 것 으로 알려 져 있 다 (Klein 과 Klootw ij k, 1976) . 메틸화는 전사 후에 RNA 의 선구체 (45S RNA) 상에서 일어난다 (Maden 등, 1974). 대부분의 메틸화반옹은 rRNA 선구체에 있어서 18S 5.8S 및 28S rRNA 부분 상에서 일어나며, 개입부분에서는 일어나지 않 는다 (Gl ibe rt 등, 1975) . 메틸화된 연속부분들은 진화과정에서 찰 보존되어 있다. 예를 들면, 작은 하위단위체의 rRNA 의 메틸화된 연속부분 m 홍 Am~ACUG 는 박테 리아, 효모 및 Novik o ff 간암 세포 들에 다 존재하는 것이 확인되었다.
표 2-15 미 토콘드리 아 및 엽 록체 의 rRNA 들의 분자 량 ( x 10-s kdal) 종 | 큰 하위단위체의 rRNA | 작은 하위단위체의 rRNA 미토콘드리아의 리보송 1 효모 1. 29 0.72 옥수수 1. 25 0.76 밀 1. 3 0.75 Tetr a hy, ne 11a 0.90 0.47 Neurospo r a 1. 28 0.72 Smi ttia 0.6 6 0.31 쥐간 0.95 0.50 HeLa 0.7 0.4 엽록체의 리보솜 Chlamy do mo11as 1. 07 0.54 Plzaseo lu s 1.1 0.56 시금치 1. 28 0.54 (Fe llner, 1969 ; De Jon g e 등, 1977 ; Choi 와 Busch, 1978) . 메 틸 화된 염 기 들로서 는 m1G, m7G, m 당 G; m1A, m2A, m6A, mi A; m3C, m5C, m4C, m3U, T 둥이 있다. 염기들의 메틸화 이의에도 드물게 변형되는 누클레오티드들이 rRNA 들에서 발견된다. 예를 들면, 수도우리딜산, 2 ' -0- 메틸수도우리던, 2'- o- 메틸이노신, 1- 메틸 -3-r-(a- 아미노 -a- 카르복시프로필)-수도우리 던, 2'-0- 메틸수도우리던, N4- 아세틸시티딘 동이 있다. rRNA 에 존재하는 변형된 염기 또는 누클레오티드 들은 rRNA 선구 체의 정확한 가공과 리보솜 생성에 있어서의 선구 rRNP 의 형성에 꼭 필요한 것 으로 생 각되 고 있 다 (Caboche 와 Bachellerie , 1977) . (3) 염기 결합순서 최근에 큰 RNA 의 염기 결합순서 분석법이 개량되면서부터 상당히 많 은 rRNA 들의 일차구조가 결정되었다 (2.4.2 절의 표 2-8 을 참고하라)• 그밖에도 여러 가지 생물종들의 18S rRNA 의 3' 및 5' 끝의 짧은 절 편들의 결합순서둘이 분석되었다. 18S rRNA 의 3' 말단에 GAUCAUU- AoH 의 연속부분이 검출된 생물종들은 HeLa 세포, 토끼 망상 적혈구, 초파리 , 15 158Y 생 쥐 세 포, Xenop us levis , Bombyx mori, 효모, Tetr a hy m ena pyri f orm i s, 행스터 근육아세포 등이다. 절족동물들에서는-
AUUAoH 의 3' 말단에 AUUAo H 연 속부분이 있다 (Ish ik a wa, 1976) . 식 물에서는 3' 말단의 누클레오시드가 아데노신 대신에 구아노신으로 대 치 되 어 있 다 (Oakden 과 Lane, 1976 ; Hag en bii ch le 둥 1978) . 홍미 있 는 사실은 진핵세포의 18S rRNA 의 3' 말단에는 E. col i의 16S rRNA 의 3' 말단 근처에 있음으로써 mRNA 와의 결합에 관여하고 있는 CCUCC 연 속부분이 검 출되 지 않는다는 것 이 다 (Shin e 과 Dalga rno, 1974) . 생 쥐 , 닭 및 Di ct y o ste l iu m 동의 작은 리 보솜 하위 단위 체 의 rRNA 의 5' 말단부분에는 UACCUG 연속부분이 있다. 5' 끝에 있는 우라실 대신 에 아데 닌 을 가진 바 슷한 연 속부분 AACCUG 가 Tetr ah y m ena 에 서 발 견 되 었 다 (Ni le s, 1977) . 그런 데 Bombyx ino ri 에 서 는 UCCUCG 가 발견 되었다 (S p ra gu e 둥, 1975). 따라서, 진핵세포의 리보솜의 18SrRNA 의 탄 말단의 누쿨레오티드 결합순서는 어느 정도의 상동성을 가지고 있지 만 동일하지는 않는 것으로 보인다. Novik o ff 간암 세포의 18S rRNA, 효모의 17S rRNA, 그 리 고 E. coli 의 16S rRNA 둘의 안쪽에서 변형된 염기를 함유하고 있는 상동성 연속 부분들이 발견되었다 (De Jon g e 등, 1977 ). 간암 세포의 18S rRNA 의 (m;Am; AC U) Gp 는 E. coli 의 16S rRNA 의 m;Am~ACCUGp 및 효모 의 17S rRNA 에 따 Am;ACUCG p 와 유사하고, 18S rRNA 의 AAC (m1 acp3 , yC AC) ACGp 는 효모의 17S rRNA 의 AACm1acp 3, yC ACACGp 에 유사하다 (Maden 동, 1975) (그림 2-17 및 2-18 을 참조하라) . 이 러 한 구 조적인 상동성에서 우리는 원핵세포의 16S rRNA 르부터 포유동물의 18S rRNA 에로의 진화는 원핵세포와 진핵세포의 약간의 연속부분들아 보존되면서 진행하였다는 것을 알 수 있다 (2.4.2 절을 보라). (4) 이차구조 18S 형 및 28S 형 rRNA 둘의 이 차구조들에 관해 서 는 2. 4. 2 절 과 2. 4. 3 절을 보라. 나) 저분자량의 리보솜 RNA 뜰 세포질의 리보솜둘의 큰 하위단위체는· 28S rRNA 이의에도 두 가지 저분자량의 rRNA 들, 죽, 5S 및 5.8S rRNA 둘을 1 : 1 의 몰 바율로 함유하고 있다. 죽, 60S 하위단위체에는 28S, 5. 8S 및 5S rRNA 둘이 각각 한 분자 씩 들어 있 다. 5S rR ~iA 는 영록체와 미토콘드리아의 리보솜들에도 들어 있지만, 5.8S rRNA 는 이 세포소기관들에 존재하지 않는다. 몇 가지 성질들과 기능면에서 불 때
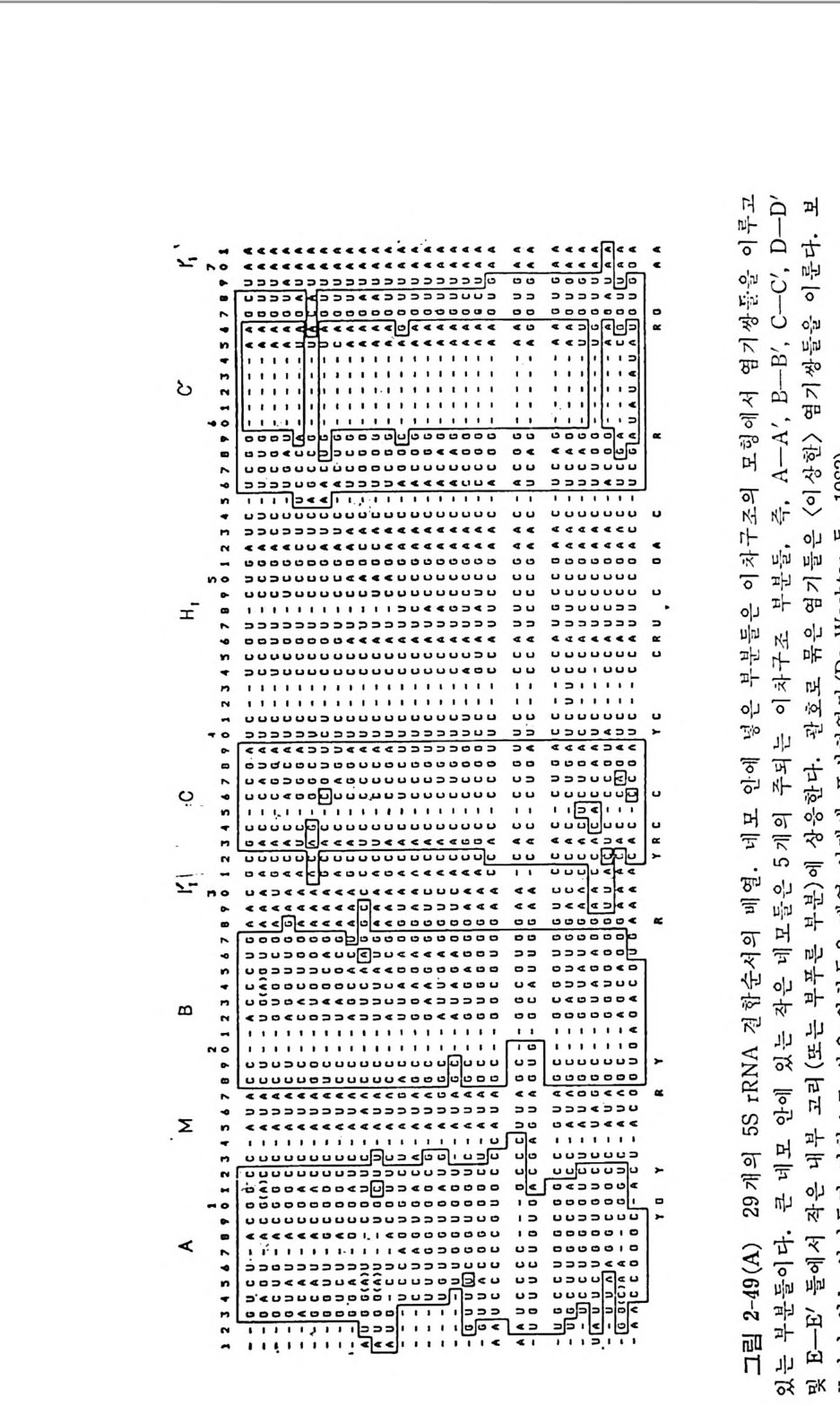 . ••
. ••
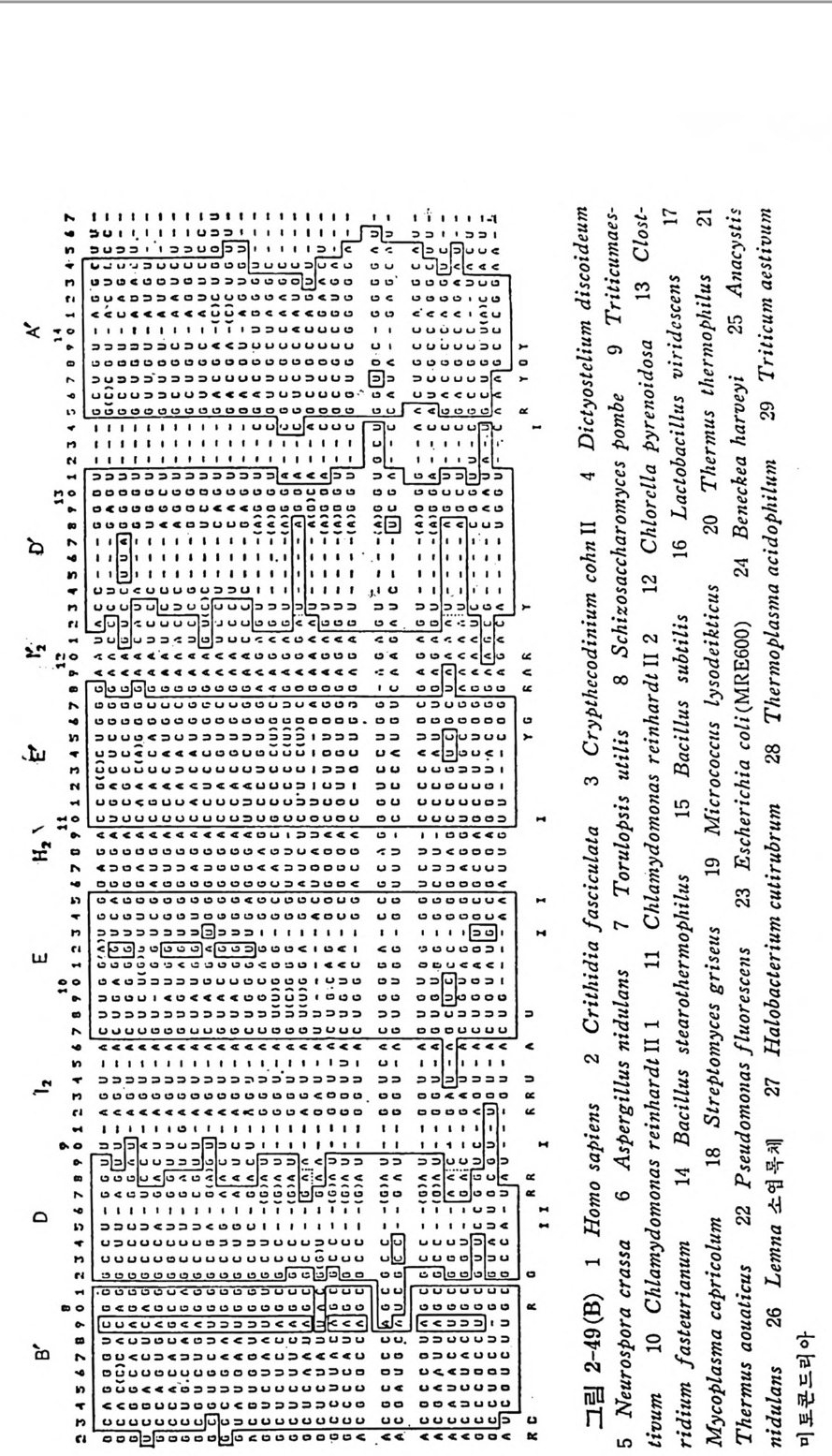 ccG C GAY GC u `
ccG C GAY GC u `
원핵세포의 5S rRNA 와 관계가 있는 것은 진핵세포의 5S rRNA 가 아 니고 5.BS rRNA 이다. 여기에 관해서는 뒤에서 곧 기술될 것이다. (1) 5S rRNA 약 50 여종의 진핵세포들의 세포질의 5S rRNA 들의 일차구조 또는 이차구조가 분석되어 있다 (Erdmann 동, 1983). 진핵세포의 대부분의 5S rRNA 는 121 개의 누클레오티드를 가지고 있는데, 식물의 5SrRNA 들은 116 내 지 118 개 의 누클레 오티 드를 가지 고 있 다. 효모 S. cerevis i e a 의 SS rRNA 가 한 개의 수도우리던을 가지고 있는 경우를 제의하고 (S. carlsberge n sis 는 中 이 없 음) , 5S rRNA 는 변 형 된 염 기 들을 가지 고 있 지 않다. 지금까지 분석된 5S RNA 의 일차구조들을 비교해 보면 포유 동물의 5S rRNA 둘은 오랜 진화과정 을 거 치 면서 도 일 차구조가 찰 보존
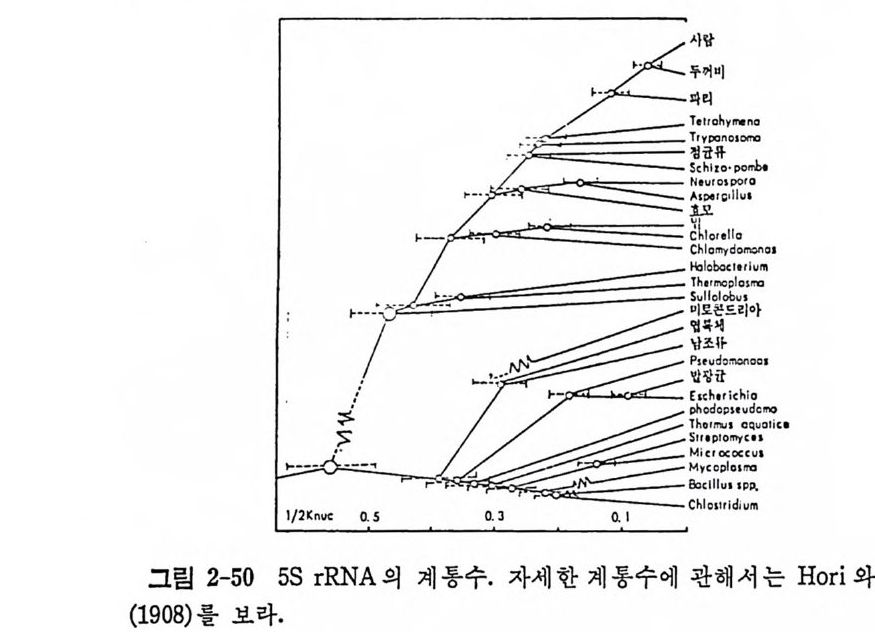 사암
사암
되어 있음을 알 수 있다 (5S rRNA 들의 일차구조의 배열과 계통수를 ::L. 립 2-49 와 그림 2-50 에 나타내었다. 5S rRNA 돌의 계통수에 관해서는 Hori 와 Osawa (l980) 가 많은 연 구를 하였다. ) . 그뿐 아니 라, 진화 상 으로 거리가 상당히 떨어져 있는 생물종들의 5S rRNA 들도 매우 유사 하다. 예 를 들면, 닭의 5S rRNA 는 포유동물의 5S rRNA 와 7 개 의 위 치들에서만 다르고, Xeno p us 의 5S rRNA 와는 8 개의 위치들에서만 다
르다. (2) 5S rRNA 의 이차, 삼차 및 사차 구조들에 관해서는 2.4 전을 참 고하기 바란다. 지 금까지 밝혀 진 모든 진핵 세 포의 5S rRNA 둘은 Py G AUC 라는 연속 부분운 가지고 있는데, 이것은 진핵세포의 개시 t RNA 인 t RNA}'e t에만 있는 GCUG 에 상보적이다. 따라서 5S rRNA 는 단백질 합성의 초기 단 계에 참여하여 큰 하위단위체의 P 자리 부근에서 Me t-t RNN1• t와 상호 작용할 것 으로 인 정 되 고 있 다 (Bi e! ka, 1980) . (3) 5. 8S rRNA 5. 8S rRNA 는 154 내 지 171 개 의 누클레 오티 드를 가지 고 있으며 , 5S rRNA 와는 달라서, 몇 개의 변형된 누클레오티드를 함유하고 있다 (Erdmann 둥, 1983) . 일 차구조가 결 정 된 5. 8S rRNA 는 약 30 종 된 다 (Erdmann, 1983) . 사 람, 쥐, 및 생쥐의 5.8SrRNA 들은실직적으로 동일한누클레오티드결 합순서를 가지고 있다(그림 2-51). 포유동물의 5.8S rRNA 와 효모의 5.8S rRNA 분자들 사이에는 75% 의 상동성을 가지고 있다. 그러나 Novik o ff 간암 세포와 약간의 꽃식 물의 5. 8S rRNA 돌 사이 에는 상동성 이 조금밖에 없다. 한편, 여러 가지 식물들의 5.8S rRNA 들의 누클레오 티 드 결 합순서 들은 매 우 유사하다 (W o!edg e 등, 1974) . 지 금까지 알려 진 결합순서둘을 종합적으로 비교해 보면 5.8S rRNA 의 구조는 진화해 오면서 광범하게 보존되어 있음을 알 수 있으며, 따라서 5.8S rRNA 는 진핵세포에 있어서의 단백질 합성에서 매우 중요한 역할을 하고 있는것 으로 생각된다. 5.8S 는 리보솜의 A 자리의 일부분을 형성하며, 연장 tR NA 들이 A 자리 에 결 합하는 데 작용할 것 으로 생 각된다 (B i elka, 1980). 일차구조가 알려진 몇 가지 5.8S 와 〈 28S 형〉 rRNA 들로부터 이 두 가지 rRNA 둘의 상호작용에 대한 모형이 제안되었다 (Urs i 둥, 1982; Mi ch ot 동, 1982; Veldman 둥, 1981). 그 모형을 그림 2-50 에 나타내 었다. 원핵세포의 5S rRNA 와 진핵세포의 5.8S rRNA 의 유전자들은 각각 의 유전구조에 있어서 유사한 위치들에 자리참고 있다. 그러나, 진핵세 포의 5S rRNA 의 유전자는 따로 분리된 특수한 위치에 자리잡고 있다. 이러한 사실에서 진핵세포의 5.8S rRNA 와 원핵세포의 5S rRNA 는 갇 온 조상에서 유래된 것으로 생각할 수 있겠지만, 이 두 rRNA 둘은 우
 uc AvvAu
uc AvvAu
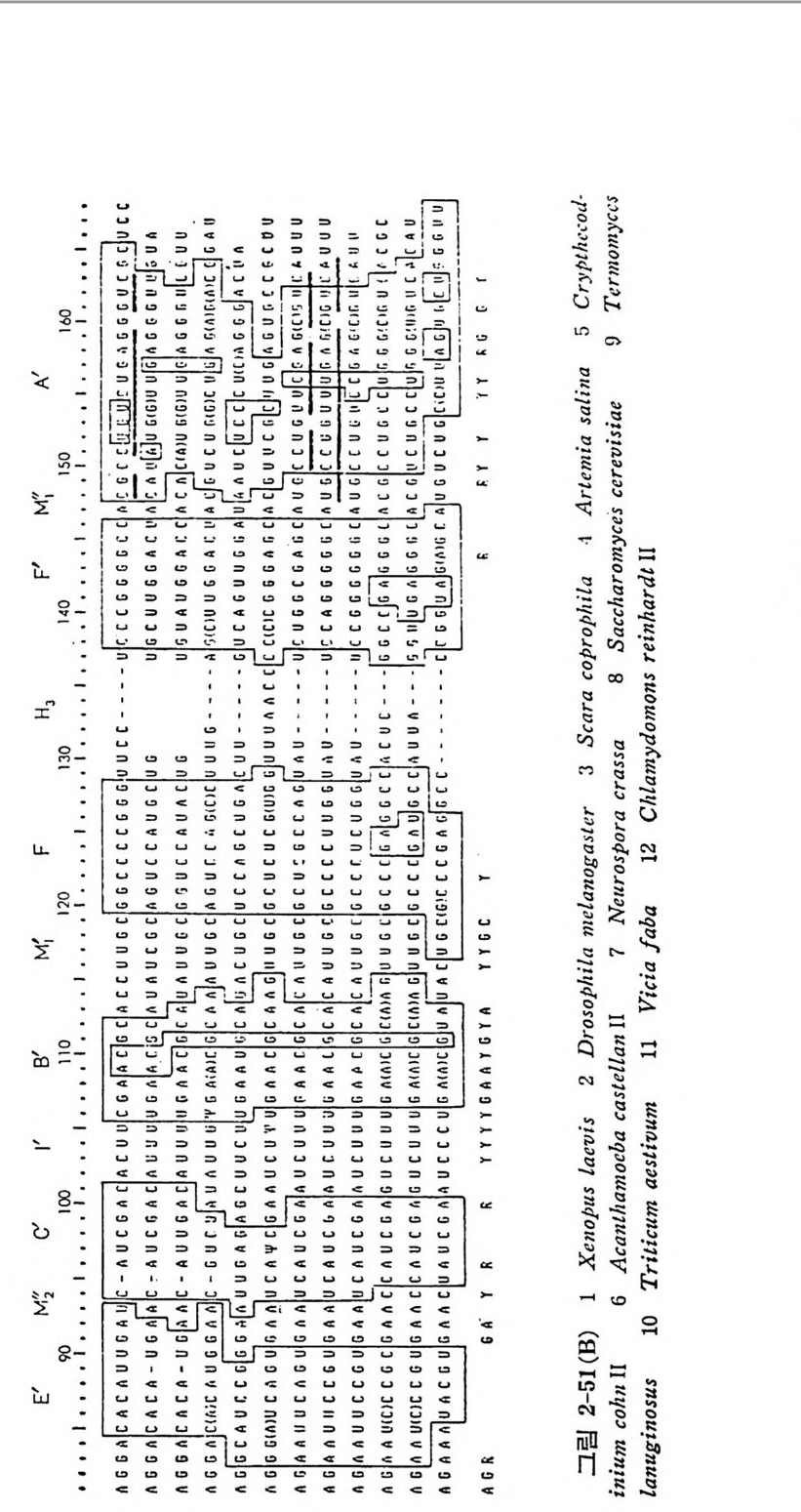 G
G
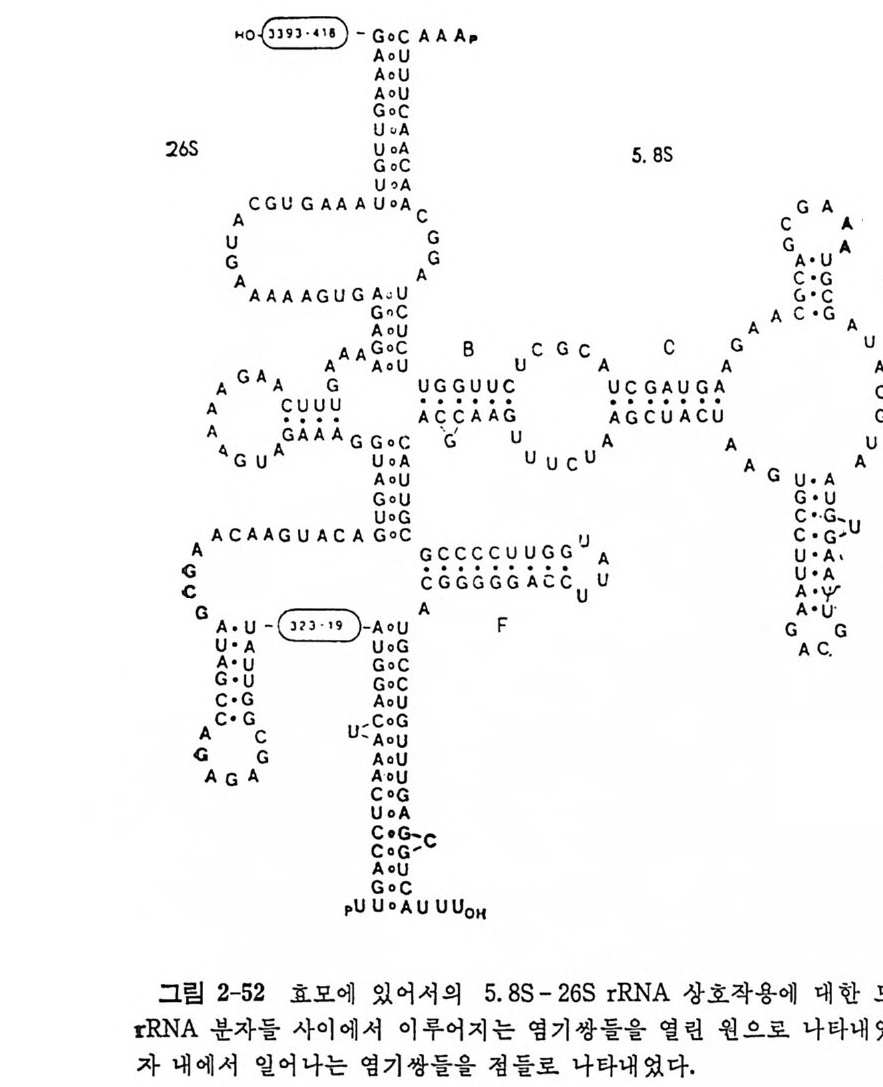 HO 특 ~ GoC A A A~
HO 특 ~ GoC A A A~
연히 마구잡이로 일치하는 부분들을 제외하면 거의 상관관계가 없음이 알려졌다 (Ceder gr en 과 Sankoff , 1976). 그런데 두 rRNA 둘은 리보솜 단백질들을 결합하는 성질에 있어서 상당한 유사성을 보이는 것으로 보 아서 일차구조보다는 이차구조의 유사성이 이러한 결과를 가져오는 것 으로 생각된다 .
5.8S rRNA 에 대한 여러 가지 이차구조 모형이 제안되어 있다. Nazar 등 (1975) 의 모형은 최대 영기짝지움과 부분 핵산가수분해에 기 초한 것 이 고, De Wachte r 의 모형 (Ursi 동, 1982) 은 일 차구조들의 비 교 로 만든 모 형 이다(그립 2-53).
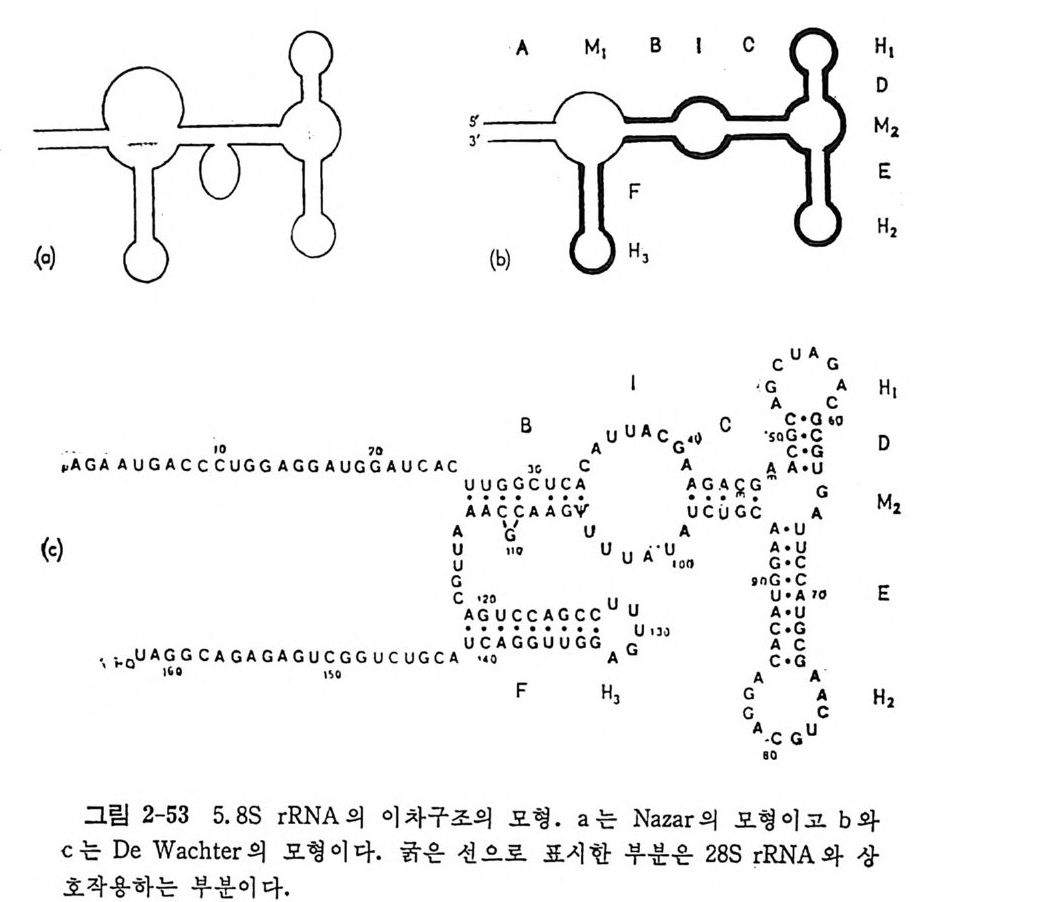 H1D2M E
H1D2M E
2.9.4 진핵세포의 리보솜 입자들의 단백질 가수분해 및 핵산 가수분해 작용둘 쥐 간과 HeLa 세포의 리보솜에는 펩티드 가수분해효소들이 있는 것으 로 알려져 있다. 이 효소작용을 가진 단백질은 리보솜 입자에 단단하게 결합되어 있어서 0.5 M 의 NH4Cl 또는 KCI 로도 씻어낼 수 없다.
또한, 여러 가지 진핵세포들의 리보솜에서 리보핵산 가수분해효소의 활동성도 검출되었다• 아 효소작용도 표준법으로 제조한 리보송에 단단 히 결합되어 있다. 지금까지로서는 리보솜의 단백질 가수분해효소 및 리 보핵산 가수분해효소의 활동성이 어느 리보솜 단백질들에 기인하는 것 인지에 대해서 밝혀진 것이 없다. 또 이 효소작용들이 생물학적으로 우 슨 중요성을 가지고 있는지 전혀 모르고 있다. 2.9.5 그 밖의 성분들 K+ 이온과 Mg 2• 이온 및 디아민들이 진핵세포의 리보송의 구성성분 으로서 존재 한다. Mg 2• 이 온이 리 보솜의 기 능과 구조에 매 우 중요하다 는 것은 리보솜 연구의 초기부터 찰 알려져 있었다. 간의 리보솜에서는 스퍼미딘과 카다베린, 그리고 다소 낮은 농도로 1,3- 디아미노프로판이 발견되었다. 효모의 리보솜에서는 스퍼미던, 푸 트레신, 및 혼적량의 스퍼민들이 발견되었다. 리보솜의 제조물에 풀리아민을 첨가하면 리보솜 입자의 안정도를 증 가시키며 낮은 Mg 2• 이온의 농도에서 일어나는 하위단위체들의 해리를 막으며, 무세포 계에서의 단백질 합성을 증진시킨다 (S p r i n, 1969). 스 퍼민은 굴로빈 mRNA 의 40S 하위단위체에의 결합을 증진시킨다. 스퍼 미딘을 함유하는 펩티드 항생제인 에데인을 써서 행한 실험결과는 40S 하위단위체 상에 있는 풀리아민 결합자리가 삼성분 복합체 GTP·elF-2· Me t-t RNAM? 의 GTP 를 GDP 로 가수분해시키는 반응에 관계된다는 것 을 암시 해 주고 있다 (Odon 등, 1978) . 그뿐 아니 라, 풀리 (U) 를 mRNA 로 사용하여 밀 싹으로부터 제 조한 무세포 계에서의 단백질 합성을 분석해 보면, 페닐알라닌 대신에 찰못 결합되어 들어가는 루신의 양으로 추정한 단백질 합성의 충실도는 풀리 아민을 첨가함으로써 증진된다는 것이 알려져 있다 (Abraham 등, 1979). 2.10 리보솜 성분들의 상호작용, 공간 배열 및 기능 리보솜 구조의 분석, 특히 입자들 내에서의 개개의 성분들 사이의 상 호작용과 그들의 공간 배열에 관한 연구는 번역과정에서의 완전한 리보
송의 기능을 이해하는 데 매우 중요한 선결조건이다. 원핵세포의 리보 송의 구조의 연구에 있어서와 같 이 단백질들의 철단, 화학적 변형, 효. 소에 의한 분해, 친화표지, 화학적 교차결합, 및 면역 전자현미경 사진 법 둥이 진핵세포의 리보송의 연구에 사용되고 있다. 그뿐 아니라, 리 보솜 또는 그 하위단위체들과 mRNA , tR NA , 연장인자들 및 개시인자 돌 사이에서 이 루어지는 복합체들에 관한 연구 들 로 번역과정에 있어서 의 개개의 단 백질들과 RNA 분자들의 기능을 알게 될 것이다. 2. 10. 1 단백 질들과 RNA 둘의 상호작용 일가의 양이온의 농도의 증가, 우레아 또는 포름아미드 등으로 리보 솜 입자에서 단백질들을 때어내는 실험을 해 봉으로써, 완전한 구조의 리보솜은 주로 이온결합과 수소결합으로 유지되어 있다는 것을 알았다. 개개의 단백질 들의 축자적인 분리는 LiC ! 또는 KC! 의 농도를 단계적 으로 중가시킴으로써 이룩 할 수 있다. 3 M L i C! 의 추출에서도 떨어져 나오지 않는 응어리 단백질들은 rRNA 에 단단히 결합되어 있는 것들 이다. 표 2-16 데어내기 조건에 기초한 리보송 단백질들의 분류. LiCI 농도 40S 하위단위체 단백질들 60S 하위단위체 단백질들 0.4 M S7,S10,S17,S20,S21 L5,L9,L22,L23/23a,L38,L39 0.6 M S3,S3a,S3b,S4,S30 Lll, L30, L31, L36, L36a 0.8M S2, S9, S14, S15, S23, S24, 17, 18, 112, 113/13a, 114, 115, S26,S29 117, 119, 121, 124, 126, 128, L29,L32,L33,L35,L37 1.0 M L16,L18 옹어리입자 S5,S6,S8,S11,S13/16, L3, L4, L6, L7a, L18a, S15a,S18,S19,S25,S27,S28 L27/27a,L34 쥐 간, Xenop us laevis , 토끼 의 망상 적 혈 구 등의 60S 하위 단위 체 를 EDTA 로 처리하면 5S rRNA 와 L5 단백질로 이루어지는 7S 복합체를 방출한다. 이 이성분 복합체는 5.8S rRNA 와도 상호작용한다(M e t s p alu 등, 1980) (표 2-17 참조). 이 복합체는 큰 하위단위체의 기능에 철대적
OH120no @
@p pp 回回回回回回*10F0一一v 回回回回囚回@®ElgE回EE@@回-EE®回53E*回回囚回回 回@回回回回回回®回回回回回回回®回@@ 170©®回回A:*®*® ©醫©f@X 回回 E*NIOI 回뿜 P @_US 回回LA 읊E囚 l V8!S_ /탭 l0 짧겅f®D/ 40 - @탭룹@@回©_ ®回®回일© @E]@回©回00回@@回B回回®0c3 -刊 E一90 EE®@ 그립 2-54 Xenop us la e v i s 의 5S rRNA 의 일차구조에서 디에틸피로탄산 을으 로받 게변 형되되는는 위아치데를닌 가영리기킨들다의. 위치. 화살표는 단백질과 결합함으로써 변형으로 필요하다. 이 7S 복합체 는 ATP 와 GTP 를 가수분해 하는 활동상 을 가지고 있다 (Grumm t 등, 1974). 따라서 이 복합체는 큰 하위단위 체의 P 자리 또는 P 자리에 가까운 위치에 자리잡고 있는 것으로 생각 되고 있다. 최근에 P i eler 와 Erdmann(1983) 은 디에틸피로탄산염에 의한 화학적 변 형 법 으로 7S 복합체 의 5S rRNA 가 A74, A77, A90, AlOO 및 Al03: 동의 위치들에서 보호됨을 관찰하였다. 이 아데닌둘의 대부분은 이차~ 조 상에서 단일 가닥으로 된 부분들에 자리잡고 있다(그림 2-54). 단시간의 열처리 또는 포름아미드 처리를 하면 5.8S rRNA 가 5S· rRNA 와 함께 효모의 60S 하위 단위 체 에 서 떨 어 져 나온다 (Nazar, 1978) . 26S rRNA (효모) 와 상호작용하는 이 5. 8S rRNA 는 0. 4 M K+ 이 온과 6mM Mg 2+ 이온 을 함유하는 완충용액에서 큰 하위단위체와 재회합 한다. RNA 를 세파로오스 6B 에 고정시키고, 이 친화크로마토그래피 대롱 에다 리보솜의 하위단위체 단백질들을 통과시킬 때 고정된 RNA 에 결 합하는 단백질들을 표 2-15 에 주었다. 최근에 Reboud 등 (1983) 은 작은· 하위단위체 • 풀리 (U) • Phe- 〔 32 円-t RNA 복합체를 직접 자의선으로 조 사하여 t RNA 가 주로 결합하는 단백질이 S10 임을 발견하였다. 그들은· 친화표지법을 사용한 것이 아니고 자연의 복합체에다 UV 를 조사하였 기 때문에 매우 의미있는 결과라고 생각된다. 표 2-17 고정된 rRNA 및 t RNA 에 결합한 쥐 간의 리보송 단백질들. RNA의 유형 | RNA 와 결합한 단백질들 5S rRNA I Ll8/18a (LS, L35) 5. 8S rRNA I LL56,, LL6l,9 (LL77,, LL1283,' , LL1297, /2S79',, LL83,5 ')S L1339 ) , L5 tRN A I S6, S14, S23/24 (S3b, S8, S9, S11, S18) L6, Ll3, L19, L21, L26, L32, L35, L36 (L5, L7, LS, L14, L18, L25, L27, L29, L31) L35a, S15, S10, S6-6a, S30, S2, S13-15 진핵세포의 리보솜 입자 또는 하위단위체들에 관한 재조립의 연구 7 l 다소 이루어져 있기는 하지만 E. col i의 리보솜의 경우와 같은의미있는·
결과는 아칙 얻지 못하고 있다 (2.5.3 절의 (바)항을 참조하라). 밀 싹 (Oakden 등, 1977 ; Ni ch olas 와 Wi jes in g h e, 1978) , 보리 의 배 (Azad. 1977 ; Azad, 197 8) , Crota l us (뱅 의 일 종) (Gi or gi ni 와 Delucca, '19 76) , 그리 고 생 쥐 의 육 종 (Azad, 1977 ; Azad, 1978) 둥 에 서 5. 8S 와 28S rRNA 돌 사이 뿐 아니 라 5S 와 18S rRNA 들 사이 에서 도 rRNA 둘 이 상호작용하는 것으로 밝혀졌다. 진핵세포의 rRNA 둘의 이 리 한 상호 작용이 생물학적으로 어떤 의의를 가지는지는 아직 모르고 있다. 2. 10. 2 진핵세포의 리보솜 내에서의 단백질들 및 RNA 둘의 공간배열 가) 리보솜 입자들에 있는 단백질들의 화학적 변형법에서 얻는 결과 리 보솜 대에서의 아미노산들의 화학적 변형은 리보솜 단백질들의 삼차구조 및 사차구조에 의해서 많이 좌우되기 때문에, 변형된 아미노산들을 분석함 으로써 리보솜 입자의 표면에서의 단백질들의 위치 또 는 두 하위단위체 들의 접촉 부위에 관한 정보를 얻을수 있다. 뿐만 아니라, 화학적 변형 의 결과로 생기는 생화학적 기능의 방해가 어느 단백질에 기인되는지를 알수 있다. 화학적 변형에 사용되는 시약에는 프로시온 청, p-히드록시머큐리벤 조산, 요오도아세 트아미 드, 염 화 단실, 2- 메 목시 -5- 니 트로트로폰, 글루 타르알데히드, 메틸아세티미드산, p-니트로페닐아세트산 둘이 있다. 화학적 변 형 법 으로 S2, S3, S3b, S7, S10, LS, Lll, Ll9, L26, L28, L29, L30, L31, L36, L36a 및 L38 등이 리 보솜 입 1자 의 표면으로 노출되어 있는 단백질들이고, S6, S11, S18, S19, S23, S24, S28, L3, L13, L13a, L15, L18a, L27, L27a 및 L32 등은 다소 묻힌 단백 질 임 을 알게 되었다. 나) 리보솜 단백질들과 RNA 둘의 효소적 분해로 얻는 결과 트립 신과 키 모 트립신을 써서 리보솜 단백질들을 분해할 때 그 단백질들이 하위단위체 의 구성성분으로 들어 있을 경우에는 가수분해 반응을 덜 받는다. 또한 하위단위체 내에 있는 단백질들이 효소로부터 보호되는 정도는 하위단 위체의 구조, 리보솜에 있어서의 단백질들의 위치, rRNA 둘 또는 다른 단백질들과의 상호작용 동에 따라서 달라진다. 리보송 하위단위체의 구
조는 EDTA, 피로인산 등으로 처리하면 허슨 하게 되어서 디 많 은 단백 질둘이 노출된 상태를 가지게 되므로 단백질 가수분해효소 들 에 의한 가 수분해 가 더 쉬 워 진다 (Hultin 과 dstn e r, 1968; Hultin , 1972) . 췌장의 리보핵산 가수분해효소와 Tl 리보핵산 가수분 해 효소 둘을 사 용한 실험에서, 리보솜 입자를 단단하게 유지시킨 조건에서도 rRNA 둘 이 이들 효소에 의해서 가수분해된다는 것이 관찰되었다 (L i nd 등 1975; Mario n 등, 1976) . 다 ) 리보솜 입자에 있는 단백질들의 시험관내 인산화에서 얻는 결과 리 보솜 단백질들은 생체 내에서도 인산화되고 시험관 내에서도 인산화된다. 리 보솜에서 단리한 단백질 들을 ATP 의존성 단백질 키나제에 대한 기질로 사용하면, 완전한 하위단위체를 기질로 사용할 때보다 더 많은 단백질 들이 인 산화된 다 (Dani 등, 1976 ; Fie l der 등, 1978) . 작은 하위 단위 체 의 경 우 제 일 강하게 인 산화되 는 단백 질 은 S6 이 다 (St ah l 등, 1972 ; Sta h l 동, 1974; Cenati em p o 등, 1977) . 그밖에 단백 질 S3a, S4, S7, S9, S10, Sll, S13, S14 및 S15 둘이 인산화되기는 하지만, 그 양은 매우 적다. 큰하위단위체의 경우에는 인산화되는 단백질들의 종류가 좀 많다. L3, L6, L18, L24, L28, L29, L34, 산성 단백질 등이 인산화된다. L27, L35, L36 둘은 미 미 하게 인 산화된 다. 그러 나 80S 모노솜 또는 폴리 송을 인 산화하면 단백 질 S6, L6, L18 또 는 L18a, 그리고 큰 하위단위체의 산성 단백질들만이 반응을 받는다 (lssin g e r, 1977 ; Cenati em p o, 1977 ; Genot 등, 1979) . 이러한 연구결과로 단백질들의 인산화는 두 하위단위체들의 경계면에 있어서의 단백질들의 위치, mRNA 또는 펩티 딜-t Rl~A 와의 상호작용, 두 하위단위체들의 회합 또는 해리에 수반하는 형태변화 등에 따라서 달라진다는 것을 암시해 주고 있다. 라) 리보솜 하위단위체 내에서의 단백질둘의 교차결합 시험에서 얻는 결과 3, 8- 디 아자 -4, 7- 디 옥소 -5, 6- 디 히 드록시 데 칸비 스이 미 드산, 디 메 틸 수베 리 미 드산, 및 디 메 틸 5, 6- 디 히 드록시 -4, 7- 디 옥사 -3, 8- 디 아자데 칸비 스이 미 드산 동과 같은 교차결합 시약들에 의해서 교차결합되는 40S 하위단위 체의 단백질 이합체들에는 다음과 같은 것들이 있다 (B i elka(1982) 의 평 론서를 보라).
S2-S3 S4-S15a Sll-S15 S2-S4 S4-S23/24 Sll-S25 S2-S7 S4-S28 S13/16-S17 S2-S15a S5-S7 S13/16-S 2 5 S3-S3a S5-S13/ 16 S13/16-S27 S3-S2b S5-S20 Sl4- S 15 S3/3a-S11 S5-S25 S14-S17 S3-S8 S5-S29 S14-S20 S3-S17 S6-S8 S15-S15a S3-S20 S6-S23/24 S15a-S17 S3a-S13 S7-S10 S15a-S20 S3a-S3b S7-S14 S16-S19 S3b-S4 S7-S18 S19-S27 S3b-Sll S7-S20 S20-S23/24 S4-S6 S10-S17 S23-S24 S4-S10 S10-S20 S27-S28 S4-S14 산화적 이황화결합의 형성, 또는 디메틸수배리미드와 디메틸티오비스 프로피온이미드산 등에 의한 교차결합으로 형성되는 이합체들은 다음과 같은 것들이 있다. L3-L5 L7/7a-L36 L3-L7/7a L8-L35 L3-L8 L8-L36 L4-L6 L13/13a-L35 L4-L26 L14-L15 L4-L30 L15-L19 L6-L29 L18a-L27/27a L7/7a-L15 127/27a-L30 L7/7a-L21/23/23a E. co li의 리보솜둘의 공간 배열에 관한 연구가 가역적인 교차결합제 인 2- 이미노티울란울 사용하여 많이 연구되어 있다 (Tra tit 등, 1980) (2. 5. 3 절 의 (라) 항을 참조하라) . Tolan 과 Traut (l981) 는 같은 교차
결합 시약을 사용하여 토끼 의 망상 적혈구의 40S 하위단위체의 단백질 둘의 공간 배열을 분석하였다(표 2-18). 이 분석결과에 기초하여 그들은 표 2-18 40S 리보송 단백 질 들 사이의 교차결합 빈도. 높은 빈도 중간 빈도 낮은 빈도 S3a-S14 S2-S3 S3- S1 0 S8- S ll S3a-S 3 S3a-S5 S12-S27a S3a-S4 S3a-S26 S15-S18 S4-S6 S5-S6 S23-S30 S4-S24 S5- S ll S5-S14 S5- S l3 S5-S25 S5-S19 S6-S26 S6-S30 S7-S11 S10- S2 9 s10-s 1 2 S11-S12 S10- S2 7a Sll-S27a S13-S 1 9 S11-S29 S14- S2 5 S19-S29 S14-S27a S25-S30 S16-S27 S26-S29 S27a-S 2 9 Sll-S12-S27a
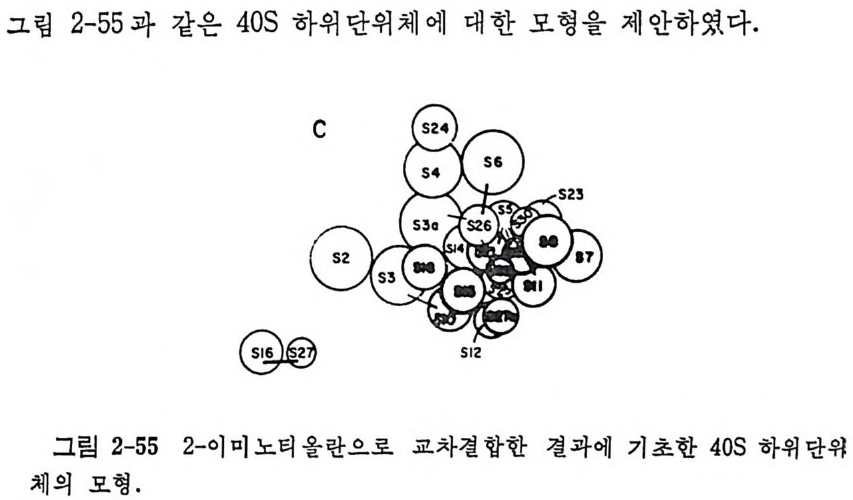 그립 2-55 과 같은 40S 하위단위체에 대한 모형을 제안하였다.
그립 2-55 과 같은 40S 하위단위체에 대한 모형을 제안하였다.
Weste r mann 과 Bie l ka 의 연 구진 (Weste r mann 등, 1981 ; Ny ga rd 동 1981) 은 사성 분 개 시 복합체 (eIF-2 •G TP • Met- tRN A~\e1 •4 0S 리 보송 하위 단위 체 ) 의 Met- tRN AM? 가 eIF-2(3 에 교차결 합하며 eIF-2a 와 eIF-2r 들 은 S3, S3a, S6, S13/16, S15 및 18S rRNA 에 교차결합된다는 것을 알 았다. 이러한 관찰에 기초하여 40S 하위단위체 상에서의 eIF-2 결합자리 에 대한 모형을 제안하였다(그림 2-56). eIF-2 의 a 하위단위체는 GTP 결합 자리를 가지고 있다. a 및 r 하위단위체들은 40S 입자 상에서 eIF-2 를 결 합하는 여 러 성 분들 (S3, S3a, S6, S13/16, S15, S15a 및 18S rRNA) 과 가장 가깝게 접 촉하고 있고, elF-2 의 하위 단위 체 와 40S 하위 단위 체 (S3a 와 S6 이 위치한 부분) 사이에는 Me t-t RNA\11e1 가 차지할 공간이 있다. 한편, 단백질 S3a 는 18S rRNA 의 3' 말단에 결합하는 것이 알 려 져 있다 (Svoboda 와 McConkey. 1978) .
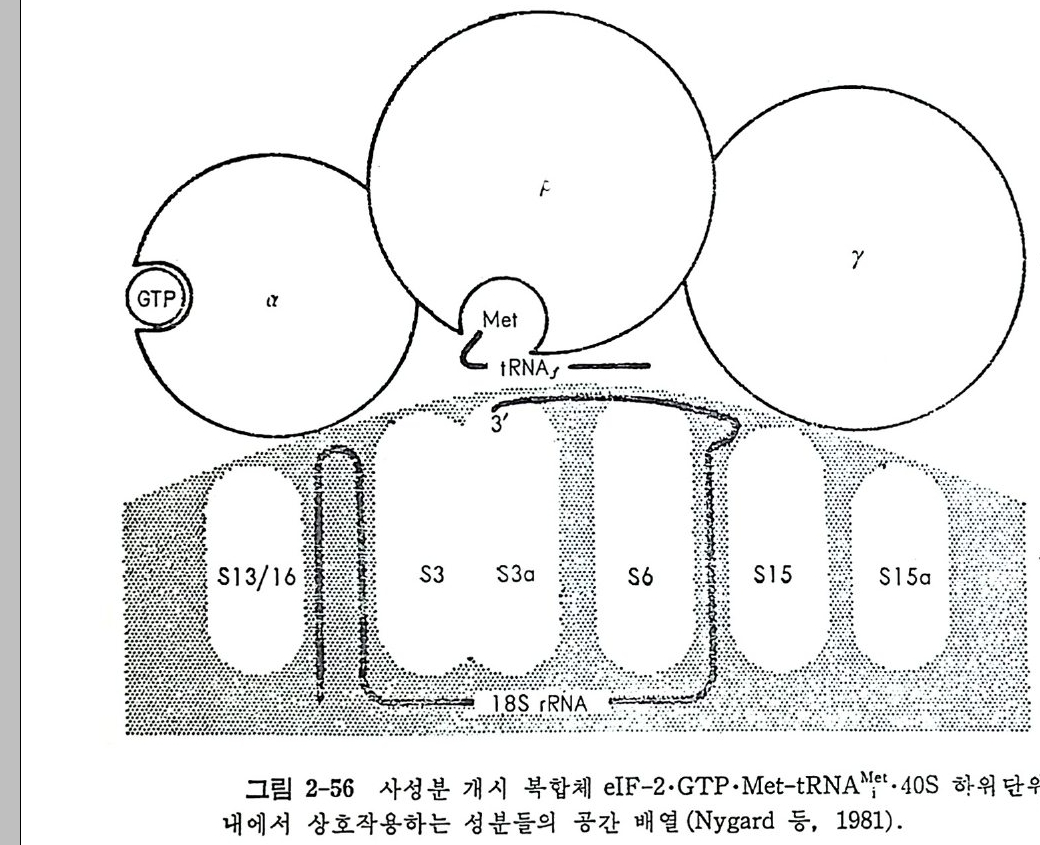 olF-2
olF-2
마) 면역 전자현미경 사진법에 의한 리보솜 단백질들의 공간 배열 결정 2.8.3 절 (가 )항 에서 말한 바와 같이, 취 간의 리보솜의 구조가 비대칭 적이기 때문에 개개의 구성 단백질들에 대한 항체 들의 결합자리들융 결 정함에 있어서 이 비대칭성을 배향 결정의 표지로 삼을 수 있다. 조사한 바에 의하면 쥐 간의 작은 하위단위체의 모든 단백질들은 상 응하는 항체들에 의해서 접근이 가능하다는 것이 알려져 있다. 지금까 지 작은 하위단위체의 약 10 가지 단백질들의 위 처가 면역 전자현미경 사진법으로 분 석 되어 있다 (B i elka(1982) 의 제 10 장 을 보라). 그 중 항 -S3 항체 및 항 -S17 항체와 작은 하위단위체들 사이에서 형성되는항원
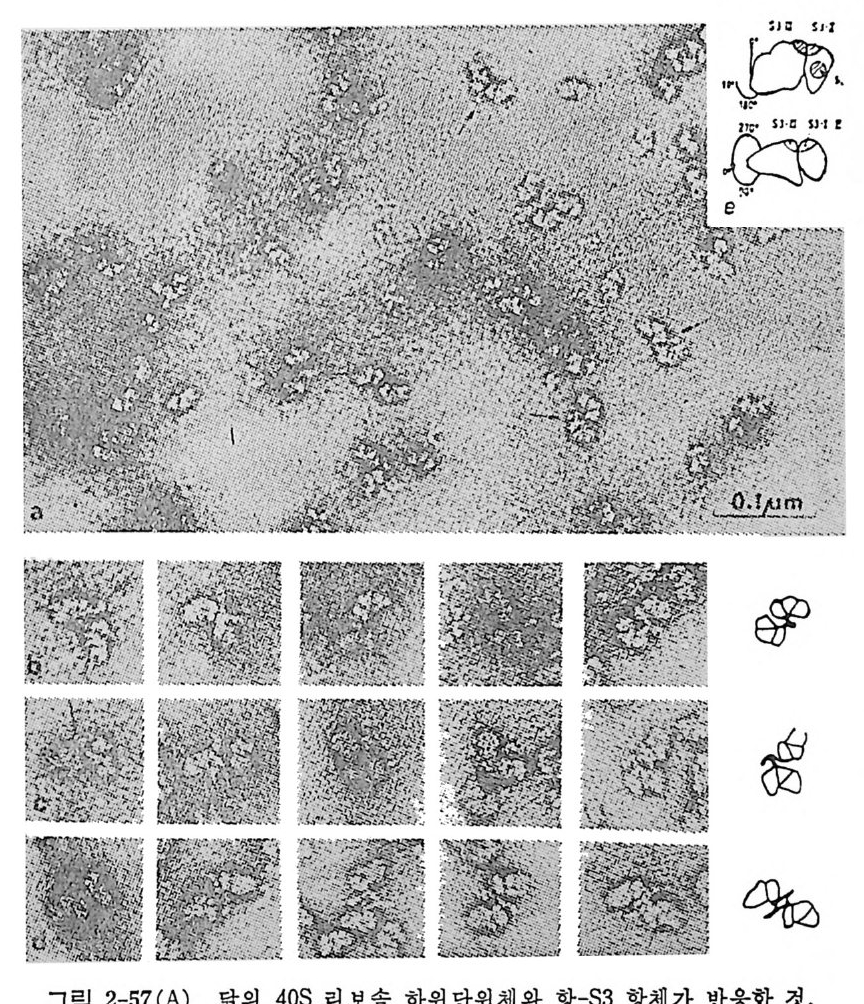 ’
’
-항체 복합체의 전자현미경 사진을 그림 2-57 에 나타내 었 다. 이 러 한 방 법으로 분석한 결과에 기초하여 단백질들의 공간 배열 의 모 형을 그림 2-58 로 나타내 었다 (Bi el ka (1982) 의 p. 172) . 지 금까지 조사한 모든 단백 질 들은 둘 (S5, S6, S17 및 S21 들의 경 우) 또는 세 개 (S2, S3, S3a 및 S7 둘의 경우)의 항체-결합자리를 가지고 있다(그림 2-58 을 보라). 작은 하위단위체에 있는 단백질들은 각각 한
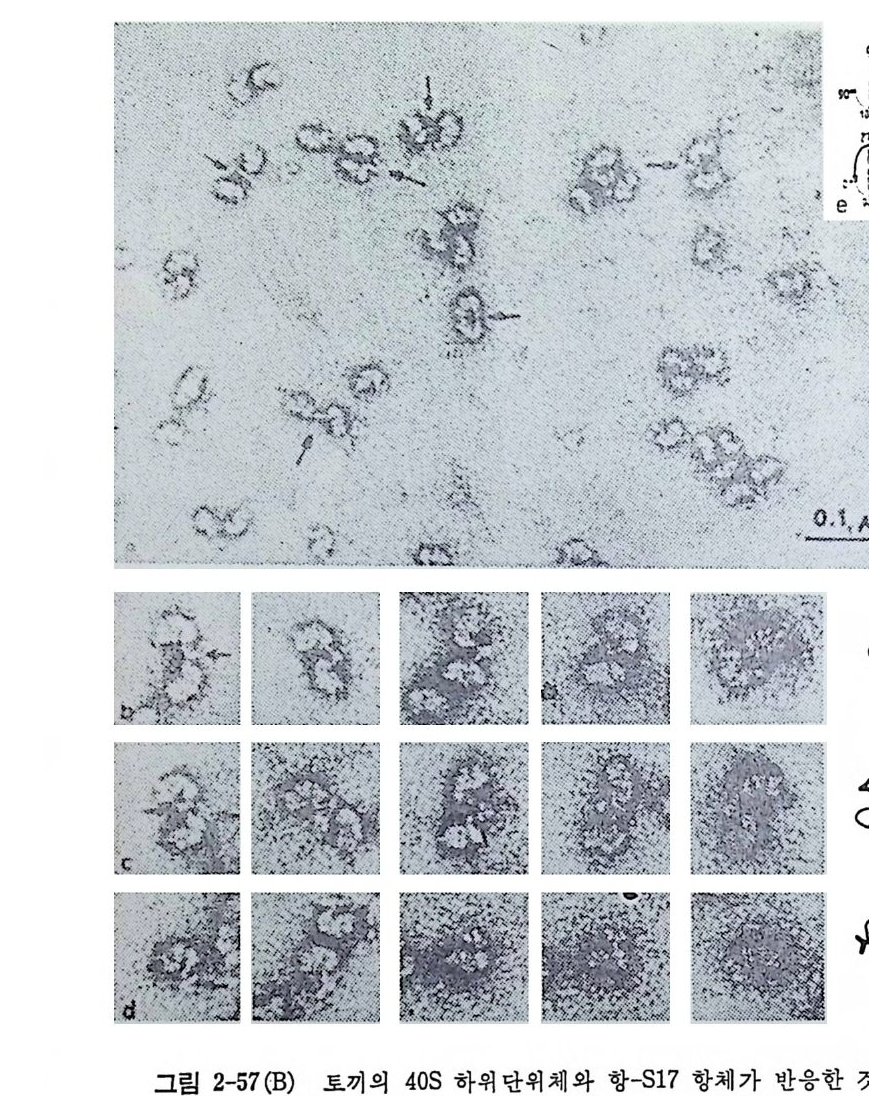 ;··
;··
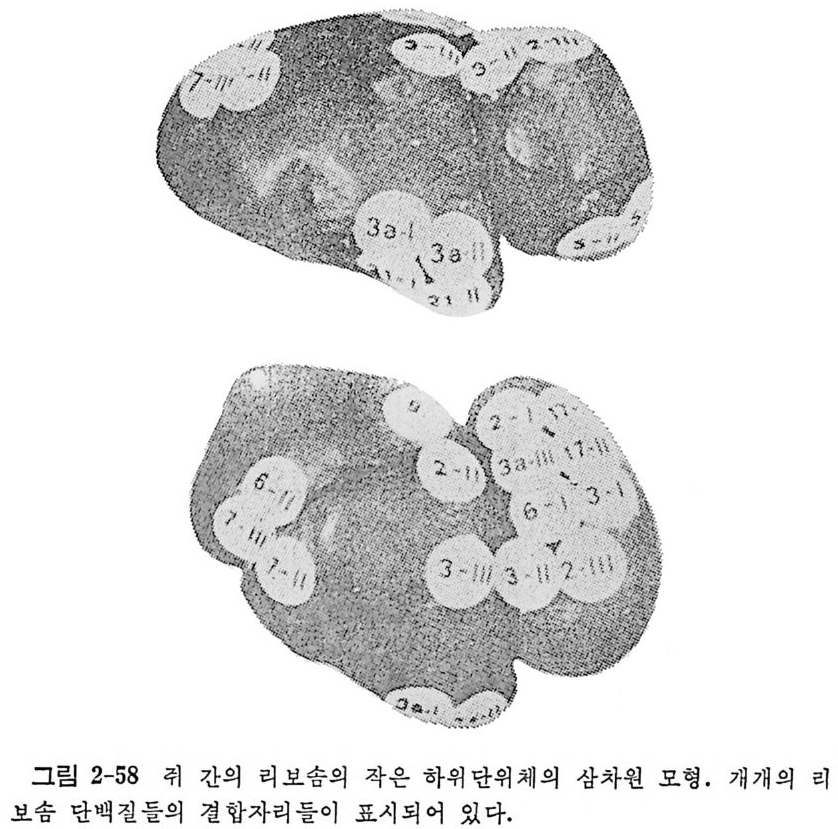 나·어 f4.,.f\ 、 '、 、.
나·어 f4.,.f\ 、 '、 、.
분자만이 있다는 사실과 교차반응성이 없는 항체들을 사용하였다는 사 실에서 개개의 리보솜 단백질들은 각각 수 개의 항원성 결정안자들을 가지고 있음을 알 수 있다. 면역 전자현미경 사진법으로 리보솜 입자 내에서의 개개의 단백질들의 모양을 결정할 수 있다. S2, S3a, S6 및 S7 둘의 항원성 결정인자들은 멀리 떨어져 있는 데 반하여 S5, S17 및 S21 등은 아주 가깝게 자리잡고 있다(표 2-19). 그러므로, 리보솜 입자 내에서 어떤 단백질들은 좀 길 쭉한 모양을 하고 있고 다른 것들은 구형에 가까운 모양을 가지고 있다 는 것을 알 수 있다• 유체역학적인 방법으로 측정한 결과에 의하면 단백 질 S2, S3, S6 및 S9 들은 다소 펴 진 분자들인 데 반하여 단백 질 S17, Sl9 및 S21 둘은 타원체형 또는 구형에 가까운 모양을 가지고 있다. 이 러한 관찰은 리보솜 단백질들이 단리한 상태로 용액에 있을 때와 리보
표 2-19 쥐 간의 리보송의 작은 하위단위체의 단백질들의 크기와 항원성 결장 인자의 수. 단백질 I 접갑口 앙검 | 최대거리 (A) 1 m 忠 k1?A )'tt백질 SS32 33 ~~110800 I 113946 S3a 3 ~200 미정 S5 2 근정 마정 S6 2 ~180 154 S7 3 ~200 117 S9 1 128 S17 2 근정 77 S21 2 근접 80 솜 입자 내에 있을 때 그 모양이 크게 달라지지 않는다는 것을 암시해 준다. 2. 10. 3 리보솜 단백질들의 기능 가) 록정한 단백질을 제거한 후의 리보솜의 기능 조사에서 얻은 결과 쥐 간 의 리보솜울 1.0 M NH4Cl 과 50% 에탄올로 처리하면 AcPhe- t RNA 의 결합과 EF-T 의존성 Phe-tR NA 결합이 일어나지 않는다. 이 계에다 121, 124, 127, 128, 및 L29 둘을 첨가하면 〈부분 반응〉이 부분적으로 회복된다 (Mal ki n 과 Rich , 1967 ). 효모의 리보솜에서 산성 단백질을 재 거한 다음에 박테리아의 단백질 L7/L12 를 대신 첨가하면 본래의 기능이 회복된다. 이것은 효모의 산성 단백질이 박테리아의 L7/L12 와 비슷한 기 능을 가지 고 있다는 것 을 의 미 한다. Arte n ia sali na (Blobel 과 Doff er - ste i n , 1975a) 와 효모 (Sabata n i 와 Blobel. 1970) 로부터 산성 단백 질 을 제 거하면 EF-G 의존성 GTP 가수분해, 폴리페닐알라닌의 합성, 또는 EF-T 의존성 아미노아실-t RNA 결합 동이 방해되는데, 이것은 산성 단 백질이 두 연장인자들의 결합에 관여하고 있음을 암시한다. 한편, 쥐 간의 리보솜으로부터 산성 단백질을 제거하여도 나머지 응어리 입자가 가지는 펜티딜 기 전달효소 활동성에는 아무런 영향을 미치지 않는다. 이 관찰은, 연장인자들의 리보솜과의 결합이 E. col i의 L7/L 12 단백질
에 대한 항체에 의해서 방해되는 데도 불구하고 펩티덜 기 전달효소 활 동성 은 손상되 지 않는다는 관찰과도 잘 일 치 한다 (Howard, 1976) . 나) 화학적 변형에 의한 리보솜 단백질의 기능으 1 분석 P- 히드록시머큐리벤 조산, N- 에틸말레이미드 (NEM), 쇼도마이신 또는 중금속 이온(이상온 주로 단백질의 -SH 기와 반응한다) 동으로 진핵세포의 40S 하위단위체 를 처리하면 폴리 (U) 의존성 Phe- t RNA 의 결합이 방해된다 . 이 경우 S4 와 SlO 이 변 형 되 는데 , 그중 SlO 은 A 자리 단백 질 임 이 확인 되 었다 (Bie l ka (19 82) 의 제 10 장을 보라) . NEM 은 EF-1 또는 rRNA 와 반응 하지 않으며 풀 리 (U) 를 손상시 키 지 도 않는다. 따라서 아미 노아실-t RNA 의 결합의 방해는 A 자리의 한 단백질이 변형됨으로써 생기는 것이 분 명하다. NEM 과 반응할 수 있는 술프히드릴 기들의 수는 리보솜 입자의 구조 적 및 기능 적 상태에 따라서 다르다. 가령, A 자리에 펩티딜-t RNA 를 표 2-20 쥐 간의 리보송의 기능자리들의 구성에 관여하는 단백질 및 RNA 의 역할 기능 | 작은 하위단위체의 단백질 1 집;:위단위체의 I RNA 폴리 (U ) 의 결합 I S9, S15, S18, j L6, L29 18S rRNA S24,S3/3 a ,S26 연장인자 EF-1 S5,S9,S10 j Ll8, L24, L38 의 결합 연장인자 EF-2 S10,S14 | L3, L32 의 결합 A 자리의 구성 S10, S23, S24 L4, L28, L29, L30 5.8S rRNA P 자리의 구성 S15, S15a, S19 L5,L8 5S rRNA 팹티딜 기 전달 110, L31, L26, 28S rRNA 효소 L24, L28, L36, L31, L29, L23, L32/33 개시인자 eIF-2 S3, S3a, S6, 의 결합 S13/16,S15 개시인자 elF-3 S2, S3, S3a, S4, 의 결합 S5, S7, S13, S14
가진 리보솜은
마) 항생제에 대한 저항파 렉틴 결합과 관련된 리보솜 단백질들 EF-2 의 존 성 자리옮김의 강력한 방해물질인 에메틴에 대해서 저항성을 가진 중 국 행스터 세포는 그 작은 하위단위체에 비정상적인 전기이동도를 가진 한 단백질을 가지고 있다. 그 러므로, 이 단백질은 에메틴을 결합하는 단 백질, 즉 자리옮김과 관계가 있는 단백질이라고 인정되고 있다 (Boersma 둥, 1979 ; Reic h e nberge r 와 Caskey, 1979) . 쥐 간의 80S 또는 큰 하위단위체의 어떤 한 자리에 리신 (r i c i n) 이 결 합하면 리보솜과 연장인자 사이의 상호작용이 방해되는데, 이것은 리보 솜의 A 자리 부근에 당단백질 이 있다는 것을 암시한다 (Hedblom 등, 19 76; Cowley 동 , 1979 ). 진핵세포의 리보솜의 큰 하위단위체에 당단백 질이 있다는 것은 콘카나발 린 A 가 리보솜 단백질에 결합하는 것으로 확 인 할 수 있다고 주장하는 사람들도 있지만 (Howard 와 Schwebli , 1977) 이와 반대되는 결과 를 얻은 사람들도 있어서 이 문제는 아직 해결되지 않고 있다. 2.10.4 리보솜 RNA 둘의 기능 박테리아 리보솜의 RNA 들의 기능에 관해서는 바교적 많이 알려져 있으나 진핵세포의 rRNA 들의 기능에 관해서는 알려진 것이 별로 많지 않다. 그러나 최근에 와서 진핵세포의 rR NA 들의 구조들이 원핵세포의 것들과 이차구조 및 삼차구조 들어 있어서 유사한 점이 많을 것임이 밝 혀짐으로써 진핵세포의 rRNA 둘의 기능들이 쉽게 밝혀질 것으로 기대 된다. 진핵 세 포의 5S rRNA 는 잘 보존된 Py G AU 연 속부분을 가지 고 있 다. 이 부분은 진핵세포의 개시 t RNA 의 N 번 고리에만 있는 AUCG 연속 부분과는 상보적 이다 (Erdmann, 1976). 따라서 진핵세포의 5S rRNA 는 개 시 tR NA (Met- tRN AM?) 와 상호작용함으로써 단백 질 합성 의 개시 단계에 관여할 것으로 생각된다. 5S rRNA 는 큰 하위단위체의 P 자리 또는 P 자리에 가까운 곳에 자리잡고 있을 것이다. 실제로 5S rRNA 는 단백질 L5 와 회합하여 복합체를 이루며 이 복합체는 ATP 를 가수분해시키는 활동성을 가지고 있다 (Grumm t 등, 1974) (진핵세포에 있어서의 단백질 합성의 개시반응이 일어날 때 ATP 가 가수분해되어야 한다) (Trachsel 등, 1977 ; Benne 와 Hershey, 1978) (4. 5. 1 철 을 보라) •
진핵세포의 5S rRNA 가 위에서 말한 목이한 역할을 한다는 의견은 이 rRNA 가 그밖의 rRNA 들 (즉, 5. 8 S, 18S, 및 28S rRNA 둘) 에 대 한 유 전자와 다른 특별한 유전자의 전사물이고, 이 유전자가 원핵세포에는 존 재하지 않는 사실로 뒷받침된다. 그뿐 아니라, 5S rRNA 가 18S rRNA 와 상호작용하는 것으로 보아서, 5S rRNA 는 개시과정 에서 두 하위단 위체들이 회합하는 데 관여할 것으로 생각할 수 있다. 2. 9. 3 절 의 (나) 항의 (3) 에 서 기 술한 바와 같 이 5. 8S rRN A 는 28S rRNA 과 복합체를 형성하는 것으로 생각되고 있다. 이 러한 복합 체 가 리보솜의 기능과 어떠한 관계가 있는지는 아직 알려진 것이 없다. 쥐 간의 40S 리보솜 단백질들인 S13 과 S9 가 5.BS rRNA 와 전압 한 다는 것은(표 2-15 몰 보라), 5. BS rRNA 가 리 보솜 의 두 하위 단위 체 둡 이 회합하여 80S 리보솜 입자 를 형성하는 데 관여할 것 이라는 것을 암 시 한다. 5S 및 5. 8S rRNA 에 결합하는 단백 질 L6 는( 고 2-15 를 보라) 이 두 rRNA 들에 대한 분리된 두 자리 물 가지고 있음이 밝혀졌 다 (Woo!, 1982) . 5S 및 5. 8 S rRNA, 그리 고 그들과 회 합하는 단백 질 L6, L8 및 L19 둘은 60S 하위단위체에서 서로 근접해 있다는 것을 추칭 할 수 있 다. A 및 P 자리들의 일부분이 이 영역에 들어 있을 것으로 생각된 다. 바로 앞에서 기술한 바와 같이, 원핵세포의 5S rR NA 와 진핵세포 의 5.8S rRNA 는 리보솜 입자에 있어서 비슷한 기능을 가질 것으로 추측 되고 있다. 이오: - 반면에, 원핵세포의 5S rRNA 와 진 핵세포의 5S rRNA 는 기능이 다룬 것으로 생각된다. 원핵세포와 진핵세포의 5S rRNA 는 그 일차구조에 있어서 차이가 있다. 매우 중요한 것은 진핵 세포의 5S rRNA 는 모든 원핵세포의 5S rRNA 둘이 가지고 있는 CGA AC 연속부 분이 없다 . 이 연속부분은 모든 연장 t RNA 들과 원핵세포의 개시 tR NA 의 고리 N 에 있는 T ,fr CG 와 상보적이다(그러나, 원핵세포의 5S rRNA 의 CGAAC 연속부분이 t RNA 와의 상호작용과는 아무 런 관계가 없 다 는 것이 확증되었음을 상기하자) (2.4.1 절의 (가)항을 보라). t RNA 의 T, frCG 연속부분은 원핵세포 및 진핵세포의 5S 및 5.8S rRNA 둘의 상 보적인 연속부분과 회합할 것이라는 Erdmann(1976) 의 가 설은 최근에 이루어진 Zag o rska 등 (1984) 의 연구결과로 사실이 아님 이 밝혀지기는 하였지 만 (2. 4. 1 절을 보라) , T, frCG 조각은 EF-1 의 존성 으로 일 어 나는 아미노아실-t RNA 의 원핵세포 및 진핵세포의 리보솜에의 결합을 방해 하는 것으로 보아서 5.8S rRNA 는 리보솜의 A 자리 볼 형성하여 연장
t RNA 들의 결합에 관여할 것으로 생각된다. 왜냐하면 진 핵세포 의 개 시 t RNA 의 P 자리에의 결합은 T'tf rC G 조각에 의해서 아무런 영향을 받지 않는다. 앞에서도 말한 바와 같이, 5S rRNA 는 P 자리 룹 형성하 여 개시 t RNA 의 결합에 관여한다. 진핵세포의 18S rRNA 의 기능에 관해서는 확실하게 알려 진 것이 없 다. 그러나 포유동물, 개구리, 누에, 효모, 밀 싹 등과 같은 진핵세포에 서 얻은 18S 형 rRNA 들의 3' 말단에 푸린이 많이 있는 -CCUGCGGA AGGAUCAUUAoH 연속부분이 찰 보존되어 있는 것으로 브아서 이 연 속부분이 진핵세포의 mRNA 의 피리미딘이 많은 3' 말단의 연속부분과 염 기 짝지 움을 함으로써 , 원핵 세 포 계 에 서 와 같은 Shin e -Dalga r no 매 카 니즘으로 진핵세포에서의 단백질 합성의 개시반응을 일으킬 것으로 생 각되고 있다 (Ha g enbuchle 등, 1978). 그러나 이것은 실험으로 증명되 지는 않았다. 진핵세포의 18S rRNA 의 3' 말단에는 박테리아의 16S rRNA 의 3' 말 단에서 발견되는 CCUCC 연속부분이 없기 때문에 Shin e -Dalga rno 상호 작용은 진핵세포에 있어서의 mRNA•rRNA 의 경우에는 없을 것으로 생 각되 고 있 다. 최 근 에 Sarga n 등 (1982) 은 18S rRNA 의 3' 말단의 머 리핀 형 이차구조의 밀부분에 있는 염기들이 많은 진핵세포의 mRNA 의 개시 코돈 앞에 오는 찰 보존된 CCACC 연속부분과 상호작용할 것 이라는 가설을 내었는데, 이것도 실험으로 증명되어 있지는 않다(그림 2-59). 여하튼간에 진핵세포의 18S 형 rRNA 가 mRNA 의 개시 코돈을 인식하는 데 관계가 있다고 하더라도 Shin e -Dalga rno 상호작용은 강하 지는 않을 것으로 생각된다. 진핵세포의 작은 리보솜 하위단위체에 있는 rRNA 의 mRNA 와의 상 호작용에 대해서는 제 3 장에서 다시 논의할 것이다(최근의 평론에 대해 서 는 Kozak (1983) 를 보라) . 28S rRNA 의 기능에 관해서 알려진 것은 거의 없다. 그러나 앞으로 더 많은 28S 형 rRNA 의 일차구조가 분석되면 그 기능에 관해서도 많 은 것이 알려질 것으로 기대된다. 2.9.3 절의 (나)항에서 말한 바와 같 이 28S rRNA 의 5' 말단 부분이 5. 8S rRL~A 의 3' 말단 부분과 머 리 핀 모양의 이차구조를 이루는 것으로 생각되고 있기 때문에 28S rRNA 의 3' 말단은 5.8S rRNA 와 함께 진핵세포의 리보솜에서 A 자리를 형성 할 것으로 추측된다.
(') m2‘A C m!`A U C-G c-G U-A G •U ISS ,RNA 의 3'-맙 단 C-G G-C G-C A-U A-U -31 .H.O_ A U U A C UA AU CG GC AU GU CG (lAC) A,7A U -G5 ' 무 지개 · 숭어 프로타 민 (b) AUCCACCAUG 업소 a- 급로빈 A C C C A C CA 、U G 사합 a- 급로빈 . P AGACACCAUG 염소와 사합의 a- 글로빈 P A A C CAA C C (X) 3 A U G P, mi/ ior l, Hi1 l on• H2A AACCAUC i\.U G. A U c0c A C C A U G P. mi liari , Hil la n• H2B AUCAACCAUG P. mil iar i, Hil le n• Hf C U. C C A U A A U G A U CGC A C U(Xb 소L 으 P. mi/ iar i, Hi, tan t H4 GUUCACCAUG 닭오발무만 A C C C A G C(,. X• •) 13 소. 모•• 요 : . 닭론알부민 C C C C A A C A U G CC UU UC CC AA CG CC( (XX)h ISA A U U G G 생쥐 께 · 합로티오네인 1 UUCCAACAUG 취프대프로인슐보 U U C C A A C (X)1 소브으 B. nior i 명주 피브로인 ACUCACCAUG 사합 I.v. A U C A A C C(X) 27 A U G 사합인터에든 L111 AUCCACC 계일 갑맞는연속부분 그립 2-59 18S rRNA 의 3' 말단 부분과 진핵세포의 mRNA 들의 5' 말단 쪽의 선도 연속부분 사이에 이루어지는 가능한 이차구조.
2.11 리보솜과 막 사이의 상호작용 2. 11. 1 자유 폴리솜 및 막에 결합한 폴리솜의 활동성 생화학적 방법과 전자현미경 사진법에 의한 조사에 의하면 단백질 합 성에 관여하고 있는 리보솜둘은 세포진에 자유롭게 있거나(자유 리보솜) 주로 소포체의 막에 부착된 상태로 있다(결합된 리보솜)는 것을 알 수‘ 있다. 자유 리보솜 및 결합된 리보송의 상대적인 비율은 조직들의 유형 과 생리상태에 따라서 달라진다. 단백질들의 기능의 관점에서 볼 때, 자유 리보솜과 막에 결합된 리보 송에서는 다른 종류의 단백질들이 합성된다고 일반적으로 믿어지고 있 다. 소포체의 막에 부착된 풀리솜 상에서는 두 종류의 단백질들이 선텍 ` 적으로 형성된다 • 즉, 첫째로, 외부로 분비될 단백질들 또는 세포 내의 다른 간막이들로 수송될 단백질들, 그리고 둘째로 , 소량이기는 하지만· 막 단백질들이 합성된다. 그러므로 새로 합성된 단백질들은 풀리솜둘이 막과 결합함으로써 격리되거나 간막이들로 들어가게 된다. 그러나 자유 풀리솜 상에서는 주로 가용성 단백질들이 합성된다. 자유 리보솜 및 결합된 리보송의 단백질 생합성에 있어서의 기능적 성 질들이 다른지 또는 같은지는 아칙 확실하지 않다. 어떤 연구자둘은 쥐 간의 자유 리보솜 및 결합된 리보솜 들에 있어서의 Me t-t RNAMt 1의 결 합과 펩티딜 기 전달효소의 기능이 조금도 차이가 없다고 보고하고 있~ (lnnanen 과 Nic h ols, 1974) . 한편, 쥐 간의 자유 폴리 솜 상에서 의 아미 노산돌의 결합이 더 효융적이라고 생각하는 사람들도 있고 (MacDonald 와 Korner, 1971) , 다른 사람들은 자유 리 보솜은 결 합된 리 보솜보다 덜 활동적 이 라고 주장하고 있 다 (Kraft -C reech 와 Lochmann, 1978) . 이 러 한 모순되는 결과들을 확실히 설명할 만한 정확한 연구결과들이 없다. 소포체 막의 성분들이 부착된 풀러솜둘의 활동에 영향을 미칠 것아 라는 것은, 자유 풀리솜 상에서의 풀리펩티드 합성의 활성화에너지가 25. 5 kcal/ mo le 인 데 비 하여 결 합된 폴리 솜둘의 경 우에는 그 값이 16 kcal/ mo le 이 라는 관찰에서 유추된다 (Towers 등, 1972) . 자유 리보솜과 막에 결합된 풀리솜에 있어서의 활동성의 차이를 암시 해 주는 또 하나의 사실온 두 종류의 풀리솜 상에서의 단백질 합성들에
대해서 분리되고 상호교환이 안 되는 아미노아 실 -t RNA 풀(p ool) 을 발견 한 데에서도 얻을 수 있다 (Ilan 과 Sin g er , 1975). 2. 11. 2 자유 폴리솜과 막에 결합된 폴리솜 사이에서의 리보솜 하위단위체들의 동적 관계 가) RNA 표지 실험 자유 폴리솜 및 결합된 풀리솜의 리보솜 입자들이 같은 풀로부터 유래된 것인지 또는 다른 풀로부터 유래된 것인지를 알 기 위해서, 생체에서의 RNA 선구체들이 rRNA 부분으로 결합되 어 둘 어가는 것을 두 종류의 폴리솜들에 대해서 조사하였다. 이러한 조사분 석 에 의하면 두 종류의 풀리솜들의 RNA 입자들에 있어서의 RNA 의 표 지 율은 매 우 유사하다는 것 으로 나타났다 (Hay as hi 와 Kazmi er oski, 19 75; Mechler 와 Vassail li , 1975) . 그러 므로, 자유 폴리 솜 및 결 합된 풀리 솜의 리보솜둘은 동적인 평형상태에 있으며, 그들은 자연상태의 리보솜 하위단위체들로 이루어진 동일한 선구체들의 풀로부터 유 래된다 고 생각 할수있다. 그뿐 아니라, 자유 리보솜 및 결합된 리보송의 생물학적 반감기는 같 음이 밝혀 졌 다 (Mi sh ra 동, 1972 ; Izawa 와 Ichii , 1973) . 쥐 간의 리 보 송의 RNA 의 반감기는 5 일 내지 6 일이다. 나) 재회합 실험 시험관 내에서, 두 종류의 폴리솜 또는 리보솜, 또는 리보솜의 하위단위체들이 소포체 막에 결합하는 것을 조사한 결과 아무 런 차이도 없음을 알았다(R olles t on, 1972; Mechler 와 Vassail li , 1975). 그리고 하위단위체들을 가지고 조사한 바에 의하면, 리보솜 윤 제거한소 포체에는 주로 60S 하위단위체가 결합하며, 40S 하위단위 체는 60S 하위 단위체가 먼저 소포체에 결합되어 있을 때에만 효과적으로 결합된다는 것이 밝혀졌다 (Ekren 등, 1973; Borge s e 등, 1973). 시험관 내의 실험 에서, 갓 생긴 폴리펩티가 리보솜으로부터 방출되면 막에 결합된 분획 의 작은 하위단위체는 자유 폴리송에서 유래된 작은 하위단위체들과 교 환될 수 있는데 큰 하위단위체들은 별로 교환반응이 일어나지 않는 것 이 밝혀졌다 (2.11.4 절의 (가)항에 기술한 것과 비교하라).
2. 11. 3 자유 리보솜 또는 막에 결합한 리보솜의 화학적 성질들 자유 리보송과 막에 결합된 리보솜 사이에는 구조적인 차이가 있는 것 일까? 막에 결합되는 리보솜들은 어떤 구조적인 차이가 있어서 특별히 막에 의해서 선택되는 것안지 ? 이 문제를 살펴 보기 위해서 RNA 부분 과 단백질 부분에 대해서 여러 측면으로 조사하였다. 가) 리보솜의 RNA 쥐 간 및 쥐 비 장의 28S rRNA 와 18S rRNA, 그리 고 망상 적혈구의 5S rRNA 둘은 자유 리보솜의 것이든 결합된 리보송의 것이든 염기 조성에는 차이가 없다. 그리고 HeLa 세포의 rRNA 를 췌장 의 리보핵산 가수분해효소 또는 Tl 리보핵산 가수분해효소로 처리하여 얻는 조각들의 지문을 보면 자유 리보솜과 결합된 리보솜 사이에는 큰 차아 가 없 다 (Khan 과 Maden, 1976) . 나) 리보솜의 단백질들 리보솜의 단백질들에 관한 조사에서는 상치되는 실험결과 들 이 얻어지고 있다. 아크릴아미드 겔 상에서의 이차원 전기이 동을 보았을 때 자유 리보솜 및 결합된 리보솜의 단백질들에는 아무런 정성적이 차이가 없다는 연구진도 있고, 몇 가지 특수한 성분 단백질들 이 과외로 존재한다고 주장하는 연구진도 있다. Mcconkey 와 Harber (1975) 는 막 에 결 합한 큰 하위 단위 체 에 특수하 게 더 존재하는 단백질들은 60S 하위단위체가 막에 결합하는 데 관여하 는 단백질들일 것이라고 말하고 있다. 2. 1 1. 4 리보솜울 막에 결합시키는 성분들과 결합 메카니즘 가) 리보솜 하위단위체의 역할 전자현미경 사진법 에 의한 연구 (Florendo, 1969; Unwi nn , 1977) 와 앞에서 기술한 생화학적인 접근법 (2.1 1. 2 절)에 의하면 리보솜은 큰 하위단위체에 의해서 막에 결합한다는 것이 밝혀졌 다(그림 2-60). 이러한 발견들과 일치하는 결과들을 벗기기 실험에서도 얻는다. 거친 소포체 분획을 저농도의 EDTA 로 처리하면 리보솜의 작 은 하위단위체만이 떨어져 나온다. EDTA 의 농도가 커지면 막에서 떨 어져 나오는 큰 하위단위체의 양이 중가한다.
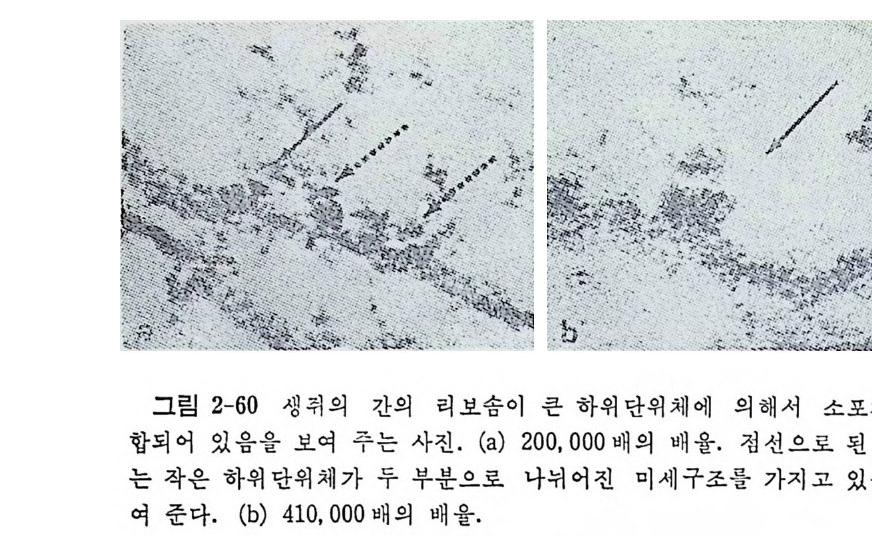 '-,` ` ._촛 .'·_ ,. _업.-c-
'-,` ` ._촛 .'·_ ,. _업.-c-
자유 리보솜 및 결합된 리보솜의 하위단위체의 성분 단백질들의 조성 이 다르다는 사실과 자유 리보솜에 비하여 결합된 리보솜이 덜 인산화 되 거 나 (Cenanti em p o 등, 1977) 덜 요오드화된 다 (Lewi s 와 Sabati ni , 19· 77) 는 사실로부터 큰 하위단위체의 몇 가지 독이한 단백질들은 막과의 상호작용에 관여할 것이라는 것을 알 수 있다. 나) 막 성분들의 역할 주로 쥐의 간 계들을 사용하여 실시한 재구성 연구에서 소포체의 매끈한 막은 거친 막과 동일한 친 화 력으로 리보솜 을 결합한다. 그러나 〈 벗겨진 〉 거친 소포체 막은 매끈한 소포체보다 더 찰 리보솜울 결합한다는 것이 관찰되었다 (Khawaza 와 Rain a , 1970; Rollesto n 과 Mak, 1973 ; Shir e s 등, 1973 ; Rollesto n 과 Lam, 1974) . 또 는 쥐 간의 소포체의 매끈한 막에의 폴리솜의 시험관 내에서의 결합은 〈벗겨진〉 거친 막에의 결합보다 이온의 세기에 더 민감하다는 것이 밝 혀졌다. 적혈구의 허깨비는 리보솜울 특이하게 결합할 수 없는데 반하 · 여 망상 적혈구의 세포막은 폴리솜둘을 결합한다. 후자의 경우 망상 적혈구의 성숙이 진행함에 따라서 결합능이 감소하는데, 이것은 세포의 분화와 더불어 막성분, 특히, 리보솜을 결합하는 데 관여하는 단백질 둘이 달라질 것이라는 것을 암시하는 매우 홍 미있는 관찰이다 (Burk 와
Schic k lin g , 1970; Borge se 등, 1974) . 소포체 막의 리보솜 결합능은 트립신, 키모트립신, 파파인 및 누라민 산 가수분해효소 동의 처리로 상실된다 (Sh i res 등, 1971; Shir e s 등, 1973 ; Scott -B urden 과 Hawt ry , 1973 ; Borge se 둥, 1974 ; Jothy 등, 1975) . 거 친 소포체 를 단백 질 분해 효소들로 처 리 하면 소포체 막으로부 터 리보솜이 떨어져 나오는 사실 및 단백질 가수분해효소로 처리한 막 들이 리보솜을 다시 결합하는 능력을 상실한다는 사실은 어떤 단백질들 이 막의 〈리 보 솜 수용체들〉을 형성하고 있을 것임을 암시한다. 누라민 산 가수분해효소로 처리한 소포체 막이 리보솜을 결합하지 못하게 된다 는 사실은 어 떤 당단백질들이 리보솜 결합자리를 구성하는 성분일 것임 을 암시한다. 실제로, 거친 소포체 막에서는 매끈한 소포체 막에는 존재하지 않 는 분자량 36kdal 의 복 이한 단백질이 발견되었다 (Bor g ese 등, 1974~ Rollesto n 과 Lam, 1974 ; Bail e y 등, 1974) . Kreib i c h 등 (19 78 a, 1978b) 은 쥐 간의 거 친 소포체 의 표면 에 리 보포 린 I 과 리보포린 II 라고 하는 두 가지 구성 단백질들이 있다는 것을 보고하였다. 이 두 단백질들의 분자량은 각각 65kdal 및 63kdal 이다. 그티고 이 단백질들은 리보솜에 교차결합시킬 수 있다. 독아한 막 단백질들이 리보솜의 결합에 관여한다는 것은 다음과 같은 연구에 의해서도 확인되었다. 즉, 막에 결합한 효소의 하나인 단백질이 황화물-이성질화효소(단백질에 있는 -S-S- 결합을 재배열하는 효소)의 활동성은 폴리솜의 결합으로 가리어지지만 폴리솜을 제거하면 다시 활 성화된다 (Dan i 등, 1976; Fie l der 동, 1978). 또한, 부착된 리보송에 의 해서 막혀진, 거친 소포체 막 상에 있는 약간의 항원성 결정인자들은 리보솜융 제거하면 항체와 다시 결합할 수 있게 된다. 이것은 소포체막 의 독이한 단백질들이 리보송의 결합에 관여한다는 것을 암시한다. 최근에 Prehn 동 (1980) 은 개 췌장의 거친 소포체 막의 세포질로 면 한 쪽으로 단백질 선구체들에 대한 특이한 수용체가 있다는 것을 발견 하였다. 이 수용체는 단백질 가수분해효소에 민감하다. 이 실험에서 사 용한 선구 단백질인 프레프로인슐린의 신호 연속부분은 매끈한 소포체 막과 적혈구의 원형질 막에는 결합할 수 없었다• 다) 이온의 세기 및 갓 생긴 펩티드 사슬의 역할 여러 가지 방법과 시약
둘을 사용하여, 막 또는 리보솜 입자 들 의 구조를 손상시킴이 없이 폴리 송과 리보솜을 소포체의 막으로부터 메어낼 수 있다. EDTA 가 가장효 과적인 물질로서 사용되고 있다 (Khawa j a, 1972; Faif er man 동, 1973; Dobberste i n 동, 1974; Krup pa 와 Sabati ni , 1977) . 그런 데 EDTA 로 처 리하여도 막에 결합한 폴리솜들의 일정한 양이 떨어지지 않고 남아 있 다는 것은 리보솜이 막에 결합할 메 관여하는 것은 이가의 양이온에 의 한 다리결합 이의에도 다른 결합력과 성분들이 관여한다는 것웅 암시 한다. 높은 농도의 I 단 이온으로 처리하거나 번역의 방해물인 푸로마이신으 로 소포체를 처리하면 막에 부착된 리보솜 들을 데어낼 수 있다. K+ 이 온 처리와 푸로마이신 처리를 따로 하면 리보송의 제거가 부분적으로 일 어난다. 그러나 높은 농도의 KCl 과 푸로마이신을 함께 사용하면 막에 결합된 리보솜이 전부 떨어져 나온다 (Blobel 과 Pott er , 1967; Adelman 등, 1973 ; Eng e lman 와 Baraja s , 1975 ; Krup pa 와 Sabati ni , 1977) . 이 러한 관찰은 리보솜이 막에 결합하는 것을 매개하는 것은 이온결합뿐 아니라 갓 생긴 팹티드 사슬이라는 것을 말해 준다. 토끼의 망상 적혈구의 자유 리보솜 또는 풀리솜을 500mM 의 KCl 로 처리하여 얻은 추출뭉과, 리보솜을 제거한 세포액 분획에서 막으로부터 리보솜을 때는 역할을 하는 분리인자를 발견하였다. 라) mRNA 의 역할 mRNA 가 소포체의 막에 직접 결합한 다음에 리 보솜이 선택될 것이라 생각된 적이 있었다. 그러나 Oj ak ia n 둥 (1977) 은 미크로송을 RNase 로 처리하면 리보솜둘이 떨어져 나오지몰 않고, 막 상에서 리보솜둘이 측면 이동을 하여 응집되는 것을 관찰하였다. 그러나 EDTA 처리 또는 KCl 과 푸로마이신 처리로 리보솜 들을 소포 체에서 완전히 제거한 다음에도 일부분의 mRNA 가 막에 부착된 상태 로 있다는 것은 mRNA 가 리보솜의 막에의 결합에 어느 정도 관여하고 있음을 암시해 준다 (Lande 등, 1975). mRNA 의 3' 말단에 있는 풀리 (A) 꼬리가 리보솜과 막과의 결합에 관여할 것이라는 의견도 있지만 아 칙 확인되 지 않고 있다 (Krup pa 와 Sabati ni , 1977) . 지금까지의 연구결과에 의하면, 분바성 단백질들 및 그밖의 약간의 단백질들에 대한 mRNA 둘은 풀리솜둘을 막에 결합시킹에 있어서 간 접적이기는 하지만 매우 중요한 역할을 하고 있는 것은 확실하다. 죽,
mRNA 의 5' 말단의 연속부분은 단백질의 이른바 〈신 호 연 속 부분〉에 해 당하는 정보를 가지고 있다. 이 〈신호 연속부분 〉은 디 보 송 이 소포체의 수용체 에 결 합하게 한다 (Blobel 과 Dobberste in , 197Sa, 1975b) (2. 11. 5 결을 보라). 마) 리보솜-막 상호작용에 미치는 단백질 합성의 방해물둘의 작응 앞에서 기술한 바와 갇이, 소포체의 막에 본래 결합 되 어 있던 리보솜 입자들은 푸로마이신으로 처리함으로써 떨어져 나온다. 푸로마이신 치 리는 갓 생 긴 펩 티 드 사술들을 리 보솜으로부터 방출시 킨 다 (Vazq ue z, 1974 ) . 리 보 솜의 하위단위체들과 함께 mRNA 의 일부분도 막에서 방 출된 다. 주로 단백질 생합성의 연장 단계의 자리옮김 반응 을 방해하는 시클로 핵시미드는 풀리솜에 있는 mRNA 의 막에의 결합을 약 50% 방해한다. 그렇지만, 작은 자유 풀리솜둘의 형성을 증가시킨다 (Rosbash, 1972). 또한, 개시 복합 체 의 형성을 방해하는 NaF 는 리보솜이 막에서 많이 이탈되게 하며, 개시 복합체의 형성을 방해하는 아우린 트리카르복시산· 도 리보솜이 미크로솜 막에 결합하는 것울 방해한다 (Ble i ber g 동 1972). 다른 한편, RNA 합성의 방해물인 악티노마이신 D 는 결합 상태의 리 보송과 자유 상태의 리보솜의 바율을 변화시킴이 없이 큰 풀리솜둘을 작 은 풀리솜들로 전환시킨다 (Blobel 과 Pott er , 1967). 이러한 결과들로부터 리보솜과 막과의 결합은 세포질에서 먼저 리보 송이 폴리송으로 된 다음에 일어나는 일임을 알 수 있으며, 이것은 〈신 호 가설〉과도 찰 일치한다. 2. 11. 5 막에 결합한 폴리솜둘로부터의 폴리펩티드 사슬둘의 방향성 방출 앞에서 기술한 바와 같이, 소포체의 막에 부착한 리보솜둘은 갓 생긴 풀리펩티드 사슬들에 의해서 막에 고정된다. 결합된 폴리솜둘 상에서 합 성이 자연적으로 종결된 분비성 풀리펩티드 사술들 또는 푸로마이신에 의해서 막에 결합된 리보솜으로부터 방출된 갓 생긴 폴리펩티드 사슬둘 은 막과 결합되어 있다 (S hi res 와 Pit ot, 1973). 그러나 뇌와 근육에서 막 에 결합된 풀리솜 상에서 합성된 비분비성 단백질들은 세포액으로 칙집 방출된다. 이러한 사실로 미루어 보아서 분비성 조직과 비분비성 조작
의 소포체 막에의 리보솜의 부착 방식에는 큰 차이가 있을 것이며, 이 러한 차이로 인해서 갓 생긴 단백질들의 배향된 방출이 일어날 것으로 생각된다. 리보솜 입자들과 막들에 의해서, 갓 생긴 폴리펩티드들이 단백질 가 수분해효소들의 작용으로부터 부분적으로 보호되는 사실은 막에 결합된 리보솜 상에서 합성된 단백질들이 소포체의 막 구조 안으로 또는 소포 체 의 강 (lumen) 안으로 방출된다는 것을 암시해 준다 (Blobel 과 Sabati ni 1970; Sabati ni 와 Blobel, 1970) . 리 보솜의 큰 하위 단위 체 에 묻힌 폴리 펩티드의 C- 말단의 절편은 약 30 내지 40 개의 아미노 산 잔기들로 된 길 이인 데 반하여, 막에 결합된 리보솜에 있어서는 단백질 가수분해효소 의 작용으로부터 보호되는 폴리펩티드 절편 (N- 말단의 절편)은 훨씬 더 길다.
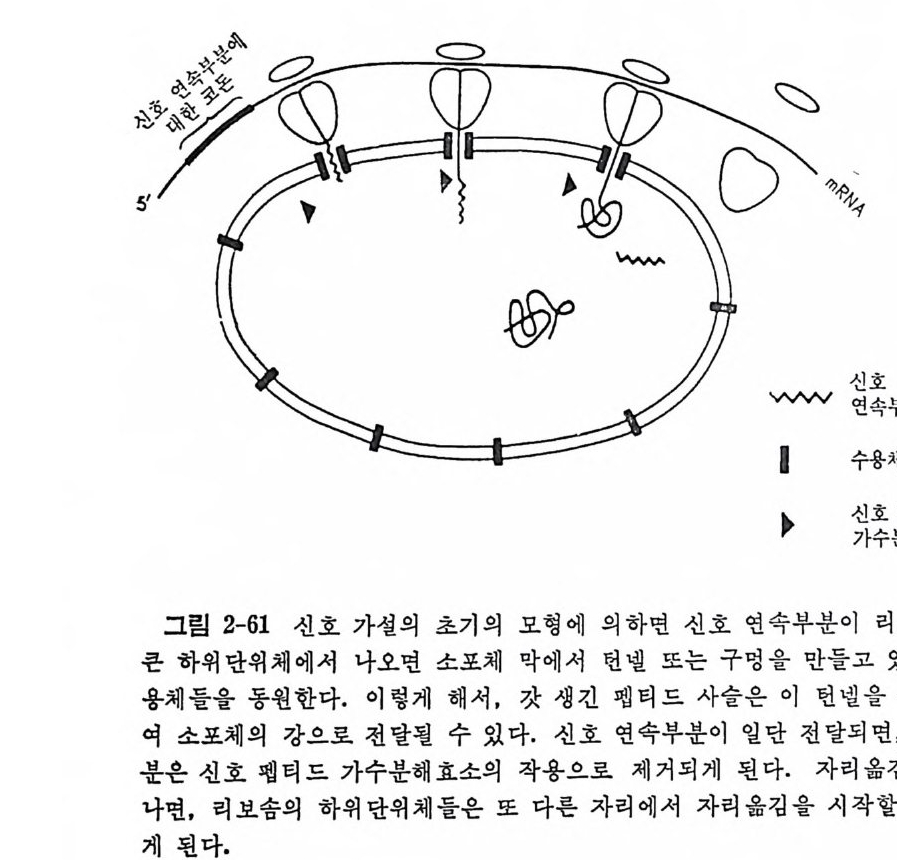 왕 :多c %`
왕 :多c %`
주로 이러한 싣험결과들에 기초하여, 번역과 등시에 소포체 막융 가 로질러 단백질이 전달 될 때 일어나는 일련의 분자적 사건들을 설명하는 신 호 가설 이 제 안되 었 다 (B lo b el 과 Sabati ni , 1971 ; Blobel 과 Dobberste i n 1975a; Blobel 과 Dobberste i n , 1975b) (그림 2-61). 분비성 단백 질 및 막 단백질 들의 선구체들의 특징은 N- 말단에 약 15 내지 30 개의 소수성 아 미노산 찬기들이 있는 것이다. 이 부분을 신호 연속부분이라고 부른다. 신호 연속부분들을 가진 폴리펜티드들만이 번역과 동시에 소포체의 막 을 가로질러 전달되거나 막에 삽입될 수 있다. 신호 연속부분은 보통 전 달과 동시에 제거된다. 신호 가설의 가장 중요한 가정은 미크로솜 막에 있는 특이한 수용체가 신호 연속부분을 가지고 있는 갓 생긴 폴리펩티 드 사슬둘을 선 택 적 으로 인 식 한다는 것 이 다 (Blobel 과 Dobberste i n , 19 75a ; Blobel 과 Dobberste i n , 1975b) . 이 러 한 수용체 의 존재 를 확인 하는 몇 가지 실험적 중거들이 있다. 첫째로, 화학적으로 합성한 신호 연속부 분이 자리옮김에 있어서 분비성 단백질 또는 막 단백질과 경쟁적이라는 것 이 밝혀 졌 다 (Lin g a p pa 등, 1978 ; Majz o ub 등, 1980 ; Prehn 둥, 19 81). 둘째로, 단백질 가수분해효소들 또는 알킬화 작용물들에 의해서 미 크로송 단백 질 들이 비 활 성 화된 다 (Ja ckson 등, 1980 ; Prehn 등, 1980) . 또한, 염 용액 추출 또는 단백질의 분해 등으로 미크로솜 단백질들을 제 거 하면 자리 옮김 이 방해 된 다 (Warren 과 Dobberste i n , 1978 ; Walte r 등, 1979; Mey e r 와 Dobberste i n , 1980) . 따라서 , 갓 생 긴 풀리 펩 티 드 사슬 둘이 있기만 하면 막을 통과할 수 있다는 견해는 옳지 않다 (W i ckner, 1979; Eng e lman 과 Ste i t y, 1981) . 초기의 연구에서 여러 연구자들은, 미크로솜이 전달될 단백질들을 인 식하는 것은 번역 개시 후 수 분 이내에 일어난다고 생각하였다 (Blobel 과 Dobberste i n , 1975a ; Blobel 과 Dobberste i n , 1975b ; Roth m an 과 Lodis h , 1977) . 시 험 관 내 에서 실 행 한 실험 결과로 추정 한 이 시 간 간격 은 신호 연속부분이 리보솜에서 나와서 그의 수용체에 리간드로서 결합 할 때가지의 시간에 해당한다. 단백질 합성이 더 신속하게 일어나고 있 는 생체 내에 있어서는 이 시간이 불과 몇 초밖에 되지 않는다. 막 단 백질 또는 분비성 단백질의 합성은 세포질에서 시작되므로 신호 연속부 분이 가깝게 있는 동안에 인식이 이루어지도록 보장하기 위해서는 갓 생긴 폴리펩티드 사술과 리보솜 사이의 복합체가 우선 막에 상당히 가 까와야 할 것이고 그 다음에는 올바른 방향으로 이동해야 할 것이다.
모든 풀리펩터드 사슬둘이 전달되려면 이 시간 요소가 제거되어야 할 것이다. 신호 연속부분이 노출되자마자 번역이 중단될 수만 있다면 모 든 단백질들은 그둘의 전달을 매개하는 분자 를 찾아내는 데 필요한 시 간을 얻게 될 것이다. 실제로, 자리옮김이 일어나기 전에 단백 질 합성 이 참정적으로 중단된다는 것이 밝혀졌다. 거찬 미크로송을 고농도의 염 용액으로 씻 으 면 갓 생 긴 단 백질들 의 자리 옮김 능력 이 없 어 진 다 (Warren 과 Dobberste i n , 1978) . 염 추출르 얻 은 인자는 분자량이 250 kdal 인 단백 질 복합 체 이 다 (Walte r 와 Blobel, 1980 ; Walt er 와 Blobel, 1981) . 리 보솜 자 체 에 대 한 이 인 자의 친 화 도 는 작지만, 분비성 및 막 단백질을 합성하고 있는 리보솜에 대 한 친화 도는 매우 크다. 이 높은 친화도는 신호 연속부 분 이 갓 생긴 풀리펩티 드 사술의 일부분으로 있을 때 나타난다. 이 복합체 를 밀 싹의 무세 포 단 백질 합성계에 넣었을 때, 갓 생긴 폴 리펩티드 사 슬 이 분비성 및 막 단 백질로서 인식될 정도로 길어지자마자, 즉, 신호 연속부분이 노 출되 자 마자 번역은 중단된다. 이 방해 작용은 염 용 액 으로 씻은 거친 미크르 솜울 첨가할 때까지 계속되다가 이 시점에서 번역이 다시 계 속되 면서 자리 옮김 이 시 작된 다. Walte r 와 Blobel (1981) 은 분자 량 250 kdal 인 이 러 한 인자를 신호 인식 단백 질 (sig na l recog n it ion pro te i n ) (SRP) 이 라고 불렀다. 이 인자는 처음에는 거친 미크로솜의 염 추출액에서 정제되었 지만, 최근에 이 인자는 세포질에도 있으며 따라서 리보솜에 이미 결합 되어 있을지도 모를 것으로 생각되고 있다 (Me y er 등, 1982). 신호 인식 단백질이 세포질에도 있으므로, 실질적으로 갓 생긴 펩티 드는 막과 접촉하는 데 필요한 무한정의 시간을 가지게 된다. 갓 생긴 분비성 또는 막 단백질이 그들의 신호 연속부분을 노출시키개 되면 세 포질에 있는 신호 인식 단백질이 그들을 인식하여 결합함으로써 번역이 더 이상 계속되지 않게끔 닫혀진다. 이 방해작용은 삼성분 복합체, 즉, 갓 생긴 펩티드 사슬 • 신호 인식 단백질 • 리보솜이 거친 소포체에 도달 하여 그것과 결합할 때까지 지속된다. 신호 인식 단백질이라는 득이한 분자가 번역을 참정적으로 방해한 것 과 마찬가지로, 전달 과정이 진행되기 위해서는 다음으로 이 방해가 제 거되어야 한다• 이 계는 다음과 같은 특징을 가져야 할 것이다. 죽, 이 계는 방해를 극복해야 하며, 이 극복작용은 다른 데가 아니고 소포체 상 에서 특이하게 일어나는 것이어야 한다. 최근에 이러한 기능을 가진 성
분이 실제로 거친 소 포체 막에서 얻어졌다 (Me y er 와 Dobberste i n , 19 80 ; Mey er 둥, 1982a ; 1982b) . 이 단백 질 은 거 찬 미 크로송을 엘 라스타 제와 고농도의 영 용 액으로 처리하여 얻을 수 있 었 다 . 이 단백질의 분소 자량은 60kd a l 이다, 그러나 이 단백질에 대한 항체로 조사한 결과 이 단백질은 분자량 72kdal 인 악 단백질 복합체의 한 영역에 해당하는 것 임이 밝혀졌 다. 이 영역은 세포질 쪽으로 면하고 있는 것도 밝혀졌다. 매우 중요한 사실은 이 단백질을 무새포 단백 질 합성 계 에다 첨가하면 r 신호 인식 단백질로 유 발 된 분비성 단백질 합성의 방해작용이 해소된다 는 것이다. 따라서 이 단백질은 신호 인식 단백 질을 받아들이는 막에 있 는 수용 체 이며, 신호 인식 단백질에 의해서 방해 된 리보솜울 거친 소포 체에 결합시키는 역 할 을 하 는 단백 질 이다. 그래 서, 이 단백질을 〈도킹 단백 질〉 (d ock i n g p ro t e i n ) 이 라고 부른다( 그림 2-62 를 보라).
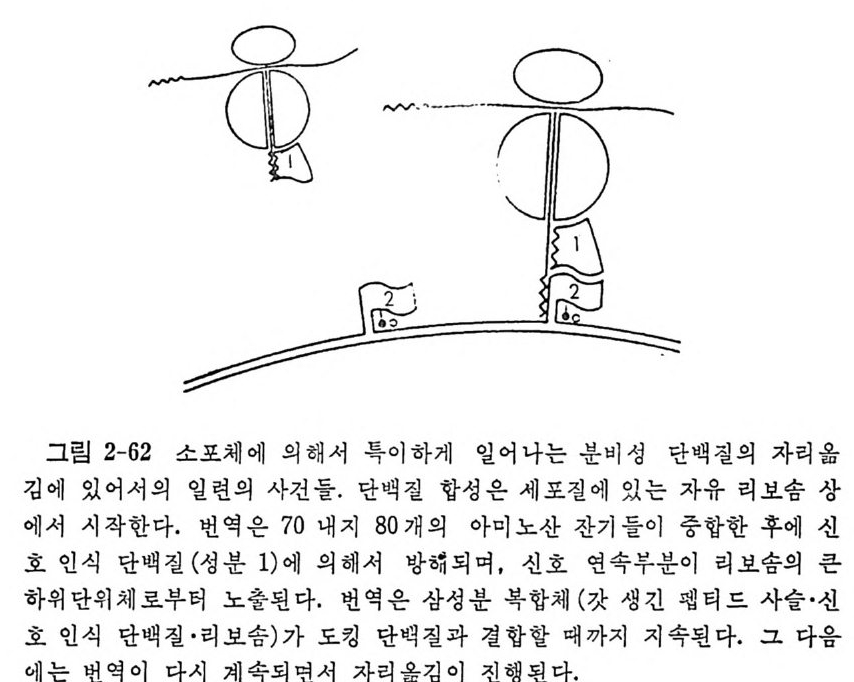 〈一 , 二
〈一 , 二
리보솜이 막에 있는 신호 인식 단백질이나 도킹 단백질에 의해서 간 집적으로 소포체 막에 결합할 수 있다는 것은 분명하지만, 아칙 리보솜 의 어느 특정 성분이 막과의 결합에 직접 관여하는지에 관해서는 찰 알 려져 있지 않다.
* 참고문현 Abraham, A. K. , Olsnes, S. , Pih l , A. (1979) , FEES Lett . 101, 93 . .Ac harya , A. S. , lVI oore, P. B. , Ric h ards, F. M . (1973) , Bio c lzemi st r y 12, 3108. Adelman, M.R., Saba ti ni , D.D. , Blobel, G. (1973) , ]. Cell Bio l . 56, 206. Allen, G. , Cap as so , R. , Gualerzi, C. (1979) , ]. Bio l . Che m . 254, 980 0 . .Am ons, R., Moller, W. (1980). Ge ne t i cs and Ev ol uti o ; z of RN A Polym erase, tR NA and Ri bo some s( Ed., S. Os aw a, H. Ozeki, H. Uchid a , T. Yura), p. 601 Elsevie r Biom ed, Amste r dam . .Am ons, R., Pluij m s , \V., Moller, W. (19 79), FEBS Let t . 104, 85. Amons, R. , van Ag tho ven, A. , Pluij m s, W. , Moller, W. (19 77) , FEES Lett , 86, 282. Ap pe lt, K. , Di jk, J. , Ep p, 0. (1979) , FEES Lett . 103, 66. Ap pe lt, K., Dij k, J., Rein h ardt, R., Sanhuesa, S., Whit e, S.W ., Wi ls on, K.S ., Yonath , A. (19 81) , ]. Bio l . Chem. 256, 11787 . .Az ad, A.A._ ( 1 977) , Proc. Austr a l. Bi oc he m . Soc. 10, 58 . .Az ad, A. A. (1978) , Bio c hem. Bi op l zy s. Res. Co1111111m. 83, 259 . .Az ad, A. A. (1979), Nucleic Acid s Res. 7, 1913 . .Az ad, A.A., Deacon, N.J . (1979) , Bi oc he m . Bi op l zy s. Re s. Commu;z. 86, 568 . .Ba il e y, D. J . , Murray, R. K. , Rollesto n , F. S. (1974) , Can . ]. Bi oc he m . 52, 1003 . .Ba rt a, A. , Kuechler, E. (1983) , FEES Lett . 163, 319 . .Bequ eret, J.. Perrot, M. , Crouzet, M. (1977) , Molec. Gen. Geneti cs 156, 141 . .Be nne, R., Hershey, J.W .B. (1978), ]. Bio l . Che m . 253, 3078 . .Biel ka, H. (1980) , Trends Bi oc hem. Sci. 3, 156. Bi el ka, H. (1982) , E11karyo t i c Ri bo some (Ed. H. Bie l ka) , p. 1~338. Sp ri n g e r , Heid e lberg. Blanc, H., Adams, C.W ., Wallace, D.C. (1981a) , Nucleic Acid s Ra s. 9, 5785. :Bl anc, H., Wrig h t, C.T., Bib b , M. J. , Wallace, D.C., Clay ton , D.A. (1981b), Proc. Natl . Acad. Sci. 78, 3789 . .Bl eib e rg, I. , Zauderer, M. , Bag li o n i, C. (1972) , Bi ch em. Bio p h y s . Acta 269, 453 . .Bl abel, G. , Dobberste i n , B. (1975a) , ]. Cell Bi ol . 67, 835. :Bl obel, G. , Dobberste i n , B. (1975b) , ]. Cell Bi ol . 67, 852. Blobel, G., Sabati ni , D.D. (1970), ]. Cell Bi ol . 45, 130 . .Bl obel, G. , Sabati ni, D. D. (1971) , Bio m embranes 2, 193. Blobel, G. , Pott er , V. R. (1967) , ]. Mo/. Bi ol . 26, 293. Boersma, D., McGil l, S.M., Mollendamp , J.W ., Roufa , D.J. (1979), Proc. Natl .
Acad. Sci. 76, 413. Boil ea u, G. , Sommer, A. , Traut, R. R. (1981) , ]. Bio l . Che m . 256, 8222. Botg e se , D., Blobel, G. , Sabati ni , D.D. (1973), ]. Mal. Bio l . 74, 415. Boublik , M., Robakis , N. , Hellmann, W. , Wall, J.S . (1982), Eur. ]. Cell Bio l . 27, 177. Brug ge r, M. , Boschett i, A. (1975) , Eur. ]. Bio c he m . 58, 603. Brim acombe, R. , Sto f f ier , G. , Wi ttm ann, H. G. (1978) , Amz. Re v. Bio c lzem. 47, 217. Brosiu s , J.. Dull, T.J. , Noller, H.F. (1980) , Proc. Na tl . A cad. Sci. 77, 201 . Brosiu m s, J., P almer, M. L. , Kennedy , P.J ., Noller, H. F. (1978), Proc. Natl . Acad. Sc i. 75, 4801 . Brow, D.A. , Noller, H.F. (1983) , ]. Mal. Bi ol . 163, 27. Burka, E. R. , Schic k lin g , L. F. (1970) , Bio c hemi st r y 9, 459. Caboche, M. , Bachellerie , J. P. (3977) , E11r. ]. Bi oc lzem. 74, 19. Canto r , C.R., Huang , K.H ., Fair c loug h , R. (1974), Ri bo some s( Ed., M. Nomura, A. Ti ss ie r es, P. Leng ye l) , p. 587, Cold Sp ri n g Harbor Laborato r y , Cold Spr i n g Harbor. Carbon, P., Ebel, J.P . , Ehres mann , C. (1981), Nucleic Acid s Re s. 9, 2325. Carbon, P., Ehresmann, C. Ehresmann, B., Ebel, J.P . (1979), Eur. ]. Bi oc lzem. 100, 399. Cap el , M.S., Bourqu e, D. P. (1977), Plant Phy si o l . 59, s-1 1 0. Cedergr e n, R.J., Sankoff , D. (1976), Natu r e 259, 74. Cenati em p o, Y., Cozzone, A.J., Genot, A., Reboud, J.P . (1977), FEES Lett . 79 115. Chang , F.N ., Navic k as, I.J., Chang , C.N., Dancis , B.M . (1976), Arc/z. Bio c lzem Bio p h y s . 172, 627. Chap m an, N.M., Noller, H. F. (1979), ]. Mal. Bi ol . 109, 131 . Choi, Y. C. , Busch, H. (1978) , Bio ch emi st r y 17, 2551 . Chu Gloria , Y., Canto r , C.G. (1979), Nucleic Acid s Res. 6, 2363. Clark, B. (1980) , Trends in Bio c lze m . Sci. 5, 207. Comb, D.G., Sarkar, N., Pin z in o , C.J. (1966), ]. Bio l . Chem. 241, 1857. Coop er man, B. S. (1980) , Ri bo somes: Str u ctu r e, F11ncti o11 and Geneti cs (Ed. , G. Chambliss , G. R. Craven, J. Davis , K. Davis , L. Kahan, M. Nomura) , p. 531, Univ e rsit y Park Press, Baltim ore. Cover, J.A . , Lambert , J.M . , Normann, C.M ., Traut, R.R. (1981), Bi oc hemi st r y 20, 2843. Cowley, D. B. , Hedbrom, M.L., Huusto n , L.L . (1979), Bi oc hem i st r y 18, 2648. Cox, R. A. (1977) , Proi Bi op h y s . Mo/. Bi ol . 32, 103.
Cric k , F.H.C., Barnett , L., Brenner, S., Watt s- Tobin , R.J . (19 61) , Natu r e 192, 1227. Cundli ff, E. (1980) , Ri bo some s: St ru ctu r e, F1111ct io11 and Ge 11 ct ics (Ed, . G. Cha m - bli ss, G.R ., Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura), p. 555, Univ e rsit y Park Press, Baltim ore. Czernil o fs k y, A.P., Collatz , E., Gressner, A.M ., Wool, I.G ., Kuchler, E. (19 77) Molec. Ge11. Geneti cs 153, 231 . Dani, H. M. , Fie l der, J. A. , Ra b in , B. R . (1976) , FEES Lett . (19 76) , 65. 377 . David s on, J.N ., Hanson, M. R. , Bog o rad, L. (19 74) . Molec . Gc a. Ge uc t i c s 132, 119. De Jon g e, P., Klootw i jk, J., Plan ta , R.J . (19 77) , N.1c l ei c Acid s Re s. 4, 3655. Delaunay, J. ; Creusot, F. , Schap iro , G. (19 73) , Eur . ]. Bi oc / 1c 11 1 . 39, 305. De Wachte r , R., Mi n- Wei Che n, Vandenbergh e, A. (1981) , Bi oc him i c 6,1, 311 . De Wachte r , R., Chen, M.W., Vandenbergh e, A. (19 82) , Bi oc / 1i m i e 6,1, 311 . Dijk, J., Lit tle chil d , J., Garett , R. A. (1977) , FEES Lett . 77, 295 . Dohme, J., Ni er haus, K.H . (1976), Proc. Natl . Acad. Sci. 73, 2221 . Dujo n , B. (1980) . Cell 20, 185. Dzio n ara, M. , Robin s on, S. M. L. , Wi ttm ann-Lie b old, B. (1977) . Hop pe -Sey l e r's Z. Plzys i o l . Che m . 358, 1003. Ehresmann, C., Sti eg l e r, P., Carbon, P., Ung ew i ck ell, E., Garett , R.A. (1980), Eur. ]. Bi oc lzem. 103, 439. Emanuil o v, I. , Sabati ni , D. D. , Lake, J. A. , Freie n ste i n , C. (1978) , Proc. Na tl Acad. Sci. 75, 1389. Eng e lmann, D.M., Ste i t z, T.A. (1981), Cell 23, 411 . Eng el mann, G. , Baraja s , L. ) 1975) , E.tp. Cell Res. 92, 102. Ep e, B., Woolley, P., Ste i n h auser, K., Lit tle chil d , J. ( 1982), Eur. ]. Bi oc hc m . 129, 211 . Erdmann, V.A. (1976) , Prog . Nucl. Acid . Res. Mo!. Bi ol . 18, 45. Erdmann, V.A ., Fahnesto c k, S., Hi go , K., Nomura, M. (1971), Proc. Natl . Acad. Sci. 68, 2932. Erdmann, V.A . , Huy sm ans, E. , Vandenbergh e , A. , De Wachte r (1983) , Nucleic Acid Res. 11, r105. Erken, T. , Shir e s, T. , Pit ot, H. C. (1973) , Bi oc / ze m. Bi op l zy s. Res. Co111111m1. 54, 283. Faie r man, I., Pog o , A. 0., Schwart z, J., Kaig h n, M.E. (1973), Bi oc lzim . Bi op h y s . Acta 312, 492. Fannin g , T.G., Traut, R.R. (1981), Nucleic Acid s Res. 9, 993. Faye , G., Sor, F., Glati gn y, A., Lederer, F., Lesqu a y, E. (1979), Molec. Gen. Geneti cs 191, 223.
Fellner, P. (1969) , Eur. J. Bi oc lzem. 11, 12. Fil de r, J.A ., Dani, H.M ., Ri dg e , D., Rabin , B.R . (1978), Bi oc hem. ]. 172, 109 Florendo, N. T. (1969) , ]. Cell. Bi ol . 41, 335. Fox, G. E . , Woese, C. R. (1975) , Natu r e 256, 505. Fox, T.D., Sta e mp fli, S. (1982), Proc. Natl . Acad. Sci. 79, 1583. Garett , R.A . (1983) , Trends Bi oc hem. Sci. 8, 75. Gi lb ert, F., Ti ol lais , P., Eladari, M.E. (1975), Eur. ]. Bi oc /z e m. 55, 239. Gio r gi ni , J. F. , De lu cca, F. L. (1976) , Nucleic Acid s Res. 3, 165. Gio r gi ni s , S. , Subramania n , A R. (1979) , ]. 1vlo l. Bi ol . 127, 41. Gir i, L. , Franz, A. , Di jk, J. (1979) , Bi oc hemi st r y 18, 2520. Glotz , C. , Brim acombe, R. (1980) , N11cleic Acid s Re s. 8, 2377. Glotz , C. , Zwi eb , C. , Brim aco:n b e, R. , Edwards, K. , Kosse!, H. (19 81) , N11c !ei c Acid s Res. 9, 3287. Gold, L., Prib n ow, D., Schneid e r, J., Shin e dlin g , S., Sin g e r, B.S ., Sto r mo, G. (1981) , Ami . Re v. Mi cr obia l . 35, 365. Gorin i , L. (1971) , Natu r e, Ne w Bi ol . 234, 261 . Gourse, R.L., Thurlow, D. L. , Gerbi, S.A ., Zim mermann, R.A . (1981), Rroc. Natl . Acad. Sci. 78, 2722. Gressner, A. M. , Wool, I. G. (1976) , ]. Bi ol . Che m. 251, 1500. Grummt , F. , Grummt , I. , Erdmann, V. (19 74) , Eur. ]. Bi oc l1em. 43, 343. Gualerzi, C. , Jan da, H. G. , Passow, H. (1974) , ]. Bi ol Chem . 249, 3347. Gup ta, R. , Lante r , J. M. , Woese, C. R. (1983) , Scie n ce 221, 656. Gup ta, R. C. , Randerath , K. (1979) , Nucleic Acid s Res. 6, 3443. Gup ta, S.L . , Wate r son, J.. Sop o ri, M.L. , Wein m an, S.M., Leng yel , P. (1970), Bi oc hemi st r y IO, 4410. Hag e nbii ch le, 0., Sante r , M., Ste i t z, J.A ., !\fan s, R.J. (1978), Cell 13, 551 . Hancock, J. , Wag ne r, R. A. (1982) , N11cleic Acid Re s. IO, 1257. Hallermey er , G. , Neup er t, W. (1974) , FEBS Lett . 41, 264. Hamel, E. , Koda, M., Nakamoto , J. (1972), ]. Bi ol . Chem. 247, 805. Hami lt o n , M.G., O'Brie n , T.W. (1974), Bio c hemi st r y 13, 5400. Haselkorn, R., Roth m an-Denes, L.B . (1973), Ann. Rev. Bi oc lzem. 42, 379. Haword, G.A. (1975) , ]. Mal. Bi ol . 606, 623. Hay as hi, T.T., Kazmi er owske, D. (1972), Bi oc hemi st r y 11, 2371 . Hedbrom, M.L., Cowley, D.B ., Husto n , L.L. (1976), Fed. Proc. 35, 1356. Heim ark, R.L ., Kahan, L., Joh nsto n , Kl, Hershey, J.W .B., Traut, R.R . (1976), ]. Mo/. Bi ol . 105, 219. Helser, T.L. , Davie s , J.E ., Dahlber, J.E . (1972), Nat1 1 re New Bi ol . 235, 6. Henderson, E., Oakes, M., Clark, M.W., Lake, J.A ., Math e son, AT., Zil lig,
W. (1984) , Scie n ce 225, 510 . Herr, W. , Chap m an, N. M. , Noller, H. F. (1979) , J. Mo!. Bio l. 130, 433. Herr, W. , Noller, H. F. (19 75) , FEBS Lett . 53, 248. Hi go , K., I., Itoh , T., Kamazaki, T., Os awa, S. (19 80) , Ge1 1et ic s and Evol11t io11 of RNA Polym erase, tR NA, a;1d Ri bo somes (Ed . , S. Os awa, H. Ozeki, H. Uhid a , T. Yura) , p. 655, Elsevie r Bio m ed, Amste r dam. Hirsh , D. (1970) , Natu r e 228, 57. Horak, I. , Schif fm ann, D. (1977) , FEBS Lett . 82, 82. Hori, H. , Osawa, S. (1980), Geuti c s a;1d Ev ol uti on of RNA Polym erase, tR NA and Ri bo somes (Ed. , S. Osawa, H. Ozeki, H. Uchid a , T. Yura) , p. 539, Else-vie r Bio m ed, Amste r dam. Hori, H. , Itoh , T. , 0 책 wa, S. (1982) , Arclzaebacte r ia ( Ed. , 0. Kandie r ) , p. 18, Gusta v Fis c her Verlag , Stu t t gar t. Howard, G. A. , Schwebli, H. P. (1977) , Proc. Natl . Acad. Sci. 74, 818. Hultin , T. (1972) , Ei oc lzim . Bi op lzy s. Acta 269, 118. Hultin , T. , bstn e r, U. (1968) , Bi oc him . Bi op h y s . Acta 160, 229. Ilan, J. , Sin g er , M. (1975) , J Mal. Bi ol . 91, 39. Innanen, V.T., Ni ch ols, D.M. (1974), Bi oc lzim . Bi op l zy s. Acta . 361, 221 . Ishik a wa, H. (1976) , Bi oc lzim . Bi op l zy s. Acta . 435, 258. Issin g e r, 0.G. (1977) , Bi oc lzim . Bi op lzy s. Acta . 477, 185. Itoh , T., W ittm ann-Li eb old, B. (1978) , FEES Lett . 96, 399. Itoh , T. , Hi go , K. I. , Ota k a, E. , 03awa, S. (1980) , Geneti cs an d Evol11t io11 of RNA Polym erase, tR NA, and Ri bo somes(Ed., S. Osawa, H. Ozeki, H. Uchi- da, T. Yura) , p. 609, Elsevie r Bio m ed. , Amste r dam. Izawa, M., Ichi, S. (1973) , ]. Bi oc lzem. 74, 623. Jac kson, R.C ., Walte r , P., Blobel, G. (1980), Natu r e 286, 174. Jac q, B. (1981) , Nucleic Acid s Res. 9, 2913. Jot h y , S. , Bi lo deau, J. L. , Sim p k in s , H. (1975) , Can. ]. Bi oc hem. 53, 1039. Kabat, D. (1970) , Bi oc hemi st r y 9, 4160. Kalts c hmi dt , E., W ittm ann, H.G. (1970). Anal. Bi oc lzem. 36, 406. Kao, T.H., Croth e rs, D.M. (1980), Proc. Natl . Acad. Sci. 77, 3360. Kastn e r, B., Sto f f ier -Meil ic k e, M., Sto f f ier , G. (1982) , Electr o n M icr oscop y, Int. Cong r. E/ectr . Mi cr oscop y, Hamburg, 3, 105. Kawaza, J. A. , Rain a , A. (1970) , Bi oc lzem. Bi op l zy s. Res. Commun. 41, 512. Kearsey, S.E., Craig , I.W . (1981), Natu r e 290, 607. Keren-Zur, M., Boubli k, M., Ofe n g a nd, J. (1979), Proc. Natl . Acad. Sci. 76, 1054. Khan, M.S.N., Maden, B.E.H. (1976), Bi oc /z e m. ]. 155, 197.
Khawaja , J. A. (1972) , FEBS Lett . 21, 49. Ki m , S.H., Suddath , F.L ., Qu ig le y, G.J. , M cPherson, A. , S ussm an, J.L., Wang . A.H.J. , Seeman, N.C., Ric h , A. (1974), Scie n ce 185, 435. Kis e lev, N. A. , Ste l ' m ashchuk, V. Ya. , Luts c h, G. , Noll, F. (1978) , ]. Mal. Bio l . 126, 109. Klein , J. , Klootw i jk, J. ( 19 76) , Anal. Bi oc lzem. 74, 263. Koch, M. H. J. , Stu h rmann, H. B. (1979) , Meth o ds in Enzy; izo lozy, vol. 59, p. 670, Academi c Press , New York. Kozak, M. (1983) , Mi cr obio l og ica l Revie w s 47, 1. Kraft -C reech, J. , Loc hm ann, E. R . (1978) , Bio c lzim . Bi op h ys . Acta 521, 426. Kreib l ic h , G., Freie n ste i n , C.M., Perey ra , B.N., Ulric h , B.L ., Sabati ni , D.D . (1978b) , J. Cel l. Bio l . 77, 488. Kreib l i ch , G., Ulric h , B.L ., Sabati ni , D.D. (1978a), J. Cell Bio l . 77, 464. Kruis w i jk, T. , Planta , R. J. (1974) , Mo/. Bio l . Rep. 1, 409. Krup pa , J. , Sabati ni , D.D. (1977) , ]. Ce ll Bio l . 74, 414. Kurland, C.G. (1977) , Ann. Rev. Bio c lzem. 46, 173. Kurland, C. G. (1979) , No11sense Muta t i on s and tR NA S11p pr es s ors (Ed., J. E. Celi s, J. D Smi th) , p. 97, Academi c Press, New York. Lai, C.J. , Dahlberg, J.E ., Weis b lum, B. (1973), Bi oc he m i st r y 12, 457. Lake, J.A . (1977) , Proc. Natl . Acad. Sci. 74, 1903. Lake, J.A . , Henderson, E., Clark, M.W. , Math e son, A.T . (19 82) , Proc. Natl . Acad. Sci. 79, 5948. Lake, J.A ., Kahan, L. (1975) , ]. Mo/. Bi ol . 99, 631 . Lake, J. A. (1980) , Ri bo s om e s: Str u ctu r e, Fw1cti on , a11d Ge;zcti cs (Ed. , G. Cham- bli ss, G.R . Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura), p. 207, Univ e rsit y Park Press, Baltim ore. Lake, J.A ., Sabati ni , D.D. , Nomura, Y. (1974), Ri bo somes(E d ., l\'l. Nomura, A-Ti ss i~ r es, P. Leng ye l) , p. 543, Cold Sp ri n g Harbor Laborato r y , New York. Lake, J. A. , Str yc harz, W. A. (1981) , J. Mo/. Bi ol . 153, 679. Lee, C.C. , Canto r , C.R ., Wi ttm ann-Lie b old, B. (1981), ]. Bio l . Chem. 256, 41 - Lewi s, J.A ., Sabati ni , D.D. (1977), ]. Bio l . Chem. 252, 5547. Lie w , C.C. , Gomall, A.G. (1973), J. Bi ol . Chem. 248, 977. Lie w , C.C., Yip , C.C. (1974), Proc. Natl . Acad. Sci. 71, 2988. Li, M., Tzago loff , A. , Underbri nk -Ly o n, K., Mart in, N. C. (1982), J. Bi ol . Clzenz. . 257, 5921 . Lin d , A. , Vi llem s, R. , Saarma, M. (1975) , ]. Bi ol . Chem. 51, 529. Lin g a pp a, V.R ., Katz , F.N., Lodis h , H.F., Blobel, G. (1978), ]. Bi ol . Chem :.. 253, 8667.
Loeb, J. E. , Blat, C. (1970) , FEES Le tt . 10, 105. Lucaso Lenard, J. , Lip m ann, F. (1971) , Ann. Re v. Bio c / 1e 11 1 . 40, 409 . Luts c h, G., Noll, F., Theis e , H., Enzmank G. , Bie l ka, H. (19 79) , Malec. Gen. Ge :zet . 176, 281 . Liihr sen, K.R., Fox, G.E. (19 81), Proc. Natl . Acad. Sci. 78, 2150. MacDonald, R. , Korner, A. (1971) , FEES Lett . 13, 62. Machatt , M.A., Ebel, J.P ., Branlant, C. (1981) , Nu clei c Acid s Re s. 9, 1533. Maden, B.E.H ., Salim , M., Roberts o n, J.S . (1974) , Rib o so m e s( E d ., M. Nomura, A. Ti ss i e r es, P. Leng y el ) , p. 829, Cold Sp ri n g Ha rb or Laborato r y, New York. Maden, B. E. H. , Salim , M. , Summers, D. (1972) , Natu r e, Ne w Bio l og y 237, 5. Maim ets , T., Remme, J., Vi llem s, R. (1984), FEES Le tt . 166, 53. Maim ets , T., Usta v , M., Vi llem s, R. (1983), FEES Le tt . 135, 127. Majz o ub, J.A ., Rosenblatt , M. , Fennic k , B., Maunus, R., Kronenberg, H.M ., Pott s, J.T ., Habener, J.F . (1980) , ]. Bi ol . Che m . 255, 11478. Malkin , I.I. , Ric h , A. (1967) , ]. Mo!. Bi ol . 26, 329. Mario n , M.J. , Mario n , C., Arpi n, M., Reboud, A.M . , Re bo ud, J. P. (1976) , Nucleic Acid s Re s. 3, 2563. Math e son, A.T., Nazar, R.N ., W ill ic k , G.E., Yag u chim M. (1980) , Ge neti c s and Evoluti on of RNA Polym e ra se, tR N A, a11d Ri bo so m e s (Ed . , S. Osawa, H. Ozeki, H. Uchid a , T. Yura) , p. 625, Elsevie r Bic 7 1ed , Am ste r dam . Math e son, A.T ., Yag uc hi, M., Balch, \V. E., Wolf e, R.S . (1980) , Bi oc him . Bio p l zy s. Acta , 626, 162. McConkey, E.H ., Bie l ka, H. , Gordon, J., Lati ck , S.M. , Lin , A., Og at a , Kl, Reboud, J.P ., Traug h , J.A ., Traut, R.R ., Warner, J.R . , Welf le , H. , Wool, I. G. (1979) , Mo/ec. Ge n. Genet. 169, 1. McConkey, E.H ., Hauber, E.J. ( 1975) , j. Bi ol . Chem . 250, 1311. McKuskie - Olson, H. , Gl itz, D.G. (1979) , Proc. . N atl . Acad. Sci. 76, 3769. Mckuskie - Olson, H. , Grant, P. G. , Gli tz, D. G. , Coop e rman, B. S. (19 8 0 ) , Proc. Natl . Acad. Sci. 77, 890. Mechler, B., Vas 마, P. (1975) , ]. Ce ll. Bi ol . 67, 16. Mets , L.J., Bog or ad, L. (1972), Proc. Natl . Acad. Sci. 69, 3779. Mets p a lu, A. , Toots , J. , Saarma, M. , Vi llem s, R. (1980) , FEES Le tt . 119, 81. Meye r , DJ . , Dobberste i n , B. (1980) , ]. Cell Bi ol . 87, 498. Meye r , DJ . , Krause, E. , Dobberste i n , B. (1982a) , Natu r e 297, 647. Meye r , D.I., Louvard, D., Dobberste i n , B. (1982b), ]. Ce ll Bi ol . 92, 579. M ish ra, R.K., '\\7beldrake, J.F ., Feeth a m, L.A .W . (1972), Bio c /z inz . Bi op l zy s Acta 281, 393.
Mi zu shim a, S., No mura, M. (19 70), Natu r e 226, 121 - 1. Mochalova, L. V. , Shats k y , I. N. , Bog da n o v , A. A. , Vasi l iev , V. D. (19 82) , ]. Mo /. Bio l . 159, 637. Monro, R. E. (19 6 7 ) , f. Mo/ Bio l . 26, 147 . Moore, P. M . (19 8 0) , Ri bo s om e s: Str u ctu r e, Fun cti on and Ge ;ze ti cs (Ed . , G. Cham bliss , G.R . Craven, J. Da vie s , K. Dav is , L. Kahan, M. No mura) , p.1 1 1, Univ e rs i t y Park Press, Balti m ore. Morris o n, C.A ., Lit tle ch il d , J., Di jk, J., Bradbury , E.M . (19 7 7), FEBS Lett . 65, 281 . 1'Iiille r, J.J., Da m a sch un, G., Bie l ka, H. (1978), Eur. J. Bio c lzem. 90, 547. Nakashim a , K.E ., Darzy n kie w i cz , E., Shatk in , A.J. (19 80) , :Va tu r e 286, 5770. Nazar , R. N. (1978) , f. Bio l . Che m . 253, 4505. Na zar, R. N. , Sit z, T. O. , Busc h, H. (1975) , ]. Bi ol . Clze m. 250, 8591 . Newberry , V., Yag uc hi, M., Garrett , R.A . (1977), Eur. ]. Bi oc he m. 76, 51. Ni ch olas, J,L., Wi jes in g h e, W. (1978), Can J Bio c / zem . 56, 760. Ni er haus, K. H. , Dahme, F. (19 74 ) , Proc. Natl . Acad. Sci. 71, 4713 . .Nier haus, K. H. (1980) , Ri bo some s: Str u ctu r e, Functi on and Ge ne ti es (Ed. , G. Chambli ss, G.R . Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura), p. 267, Univ e rsit y Park Press , Baltim ore. Ni le ss, E. G. (1977) , Bi oc hem i st r y 16, 2380. Noah, M. , Sto f fle r -Meil ic h e, M. , Sto f fle r , G. (1982) , Electr o n Mi cr oscopy , Int. Cong r. Electr l . Mi cr oscopy , Hamburg 3, 101 . Noller, H.F., Kop , J., Wheato n , V., Brosiu ;: ;, J., Gute l l, RR . (1981), Nucleic Acid s Re s. 9, 6167. Noller, H. F. , Weese, C. R. (1981) , Scie n c e 212, 403. Nomura, M. , Erdmann, V. A. (197) , Natt lre 228, 744. Ny ga rd, 0., Weste r mann, P., Hultin , T. (1981), Acta Che m . Scand. B35, 57. Oakden, K.M ., Azad, A.A ., Lane, B.G . (1977), Can. J Bi oc / 1e1 11. 55, 99. Oakden, K. M. , Lane, B. G . (1976) , Can. ]. Bi oc lzem. 54, 261 . O'Brie n , T.W. , Math e ws, D.E . , Denslaw, N.D. (1976). Genet i cs and Bi og e nesis of Chlorop la sts and Mi toh ondria , p. 741, Elsevie r /Nort h- Holland Biom ed., Amste r dam. •Od om, 0. W ., Kramer, G., Henderson, A.B ., Pin p h anic h akarn, P., Hardesty , B. (1978) , ]. Bio l . Che m. 253, 1807. Odom, O. W. , Robbin s , D. J. , Ly nc h, J. , Dott av io - Mart in, D. , Kramer, G. , Har-desty , B. (1980) , Bi oc hemi st r y 19, 5947. Ohta , N. , Sag er , R. , Inouy e, M. (1975) , J Bio l . Chem. 250, 3655. ,Of e n ga nd, J., Gornic k i, P., Chakraburtty , K., Nurse, K. (1982), Proc. Natl .
Acad. Sci. 79, 2817. Ofe n g an d, J. , Lin , F. L. , Hsu, L. , Boubli k, M. (19 81) , Molecular Ap pro ach to Gene Exp re s s io n and Prote i n Str u ctu r e ( Ed. , M. A. Q. Sid d iq u i, M. Krauskop f, H. Weis s bach) , p. 1, Academi c Press, New Yo rk. Ofe n ga nd, J. , Lin, F. L. , Hsu, L. , Keren-Z u r, M. , Boubli k, M. (1980) , Annals N. Y. Acad. Sci. 346, 324. Of en g an d, J. , Lio u , R. (1981) , Bi oc he m is t r y 20, 552 . Of en g a nd, J. , Lio u , R. , Koh11t, J. , Schwarz, I. , Zim merman, R. A. (1979) , Bio - chemi st r y 18, 4322. Pace, B. , Matt ew s, E. A. , Joh nson, K. D. , Canto r , C. R. , Pace, N. R. (19 82) , Proc. Natl . Acad. Sci. 79, 36. Palade, G. E . (1955) , ]. Bio p h y s . Bio c lze m . Cy tol . 1, 59. Peatt ie, D. A. (1979) , Proc. Natl . Acad. Sci. 76, 1760. Peretz , H., Towbin , H., Elson, D. (1976), Eur. ]. Bio c lzem. 63, 83. Pestk a , S. (1971) , Alm . Rev. Mi cr obia l . 25, 487. Pestk a , S. (1977) , Molecular lv!e c lza11is m s of Prote i n Bio s y n th e s i s ( Ed . , H. Weis - sbach, S. Pestk a ) , P.4 6 7, Academi c Press, Ne w York. Pett er sson, I. , Hardy, S. J . S. , Li ljas , A. (1976) , FEBS Lett . 64, 135. Pie l er, T., Erdmann, V.A . (1982), Proc. Natl . Ac ad. Sci. 79, 4599. Poli tz, S.M ., Glit z, D.G. (1977), Proc. Natl . Acad. Sci. 74, 1468. Pon, C.L ., Pawlik , R.T ., Gualie r zi, C. (1982) , FEBS Let t . 137, 163. Post, L.E ., Arfs ten , A.E., Reusser, F., Nomura, M. (1978) , Ce ll 15, 215. Post, L.E ., Str yc harz, G.D . , No mura, M., Lewi s, H., Dennis , P.P. (1979), Proc. Natl . Acad. Sci. 76, 1967. Prehn, S., Nurnberg, P., Rap po rt , T. A. (1981), FEBS Le tt . 123, 79. Prehn, S. , Tsamaloukas, A. , Rap op o rt , T. (1980) , Eur. ]. Bi oc he m . 107, 185. Rabin , D. , Croth e rs, D. M. (1979) , Nucleic Acid s Res . 7, 689. Rahmsdorf , H.J. , Pai, S.H . , Ponta , H., Herrlic h , P., Roskoski, R., Schweig e r, jr., M., Stu d ie r , W. (1974), Proc. Natl . Acad. Sci. 71, 586. Reboud, AM., Dubost, S., Reboud, J.P . (1983) , FEBS Lett . 158, 285. Reic h enberge r , V.E. jr., Caskey, C.T . (1979), ]. Bio l . Che m . 254, 6207. Rich , A., RajB handary , U.L. (1976), Ann. Re v. Bio c lzem . 45, 805. Ric h te r , D., Erdmann, V.A. , Sp ri n z l, M. (1973), Natu r e Ne w Bio l og y 242, 230. Rollesto n , F., S., Lam, T. Y . (1974), Bio c hem. Bio p h y s Res. Commun. 59, 467. Rollesto n , F.S., Mak, D. (1973), Bi oc hem. ]. 131, 851 . Rosbash, M. (1972) , ]. Mo/. Bio l . 65, 413. Ross, A. , Bri m acombe, R. (1979) , Natu r e 281, 271 .
Roth , H. E. , Ni er haus, K. H. (1980) , Eur. ]. Bi oc he m . 103, 95. Roth man, J. E. , Lodis h , H. F. (1977) . Natu r e 269, 775. Rohl, R. , Nie r haus, K. H. (19 82) , Proc. Natl . Acad. Sci. 79, 729. Sabati ni , D. D. , Blobe 'l, G. (1970) , ]. Cell Bi ol . 45, 146. Sabati ni , D. D ., Kreib i c h , G. (1976), The Enzy m es of Bio l og ica l Membranes(Ed A. Mart ino si) , 2, 531, Plenum, New York. San Jos e, C., Kurland, C.G., Sto f f ier , G. (1977) , FEES Lett . 71, 133. Sarga n, D.R ., Greg o ry , S.P., Butt er wort h, H. W . (1982), FEBS Lett . 147, 133. Scott -D urden, T. , Hawt ry , A. O. (1973) , Bi oc hem. Bi op l zy s. Res. Commun. 54, 1288. Serdy u k, LR ., Ag a larov, S. Ch., Sedelnik o va, S.E. , Sp iri n , A. S. , May , R.P . (1983) , ]. Mo/. Bi ol . 169, 409. Serdy uk , I.N ., Grenader, A.K., Zaccai, G. (1979), ]. Mol. Bi ol . 135, 691. Serdy uk , I.N ., Sarkis i a n , M.A ., Gog ia, Z.V. (1981), FEES Lett . 129, 55. Shats k y , I.N ., Esta fiev a, A.G., By st r o va, T.F., Bog d anov, A.A., Vasil iev , V. D. (1980) , J Mo/. Bi ol . 159, 637. Shats k y, I.N ., Mochalova, L.V ., Kojo u harova, M.S., Bog d anov, A.A., Vasil :ev , V.D. (1979) , ]. Mol. Bi ol . 133, 501 . Sherto n , C.C., Wool, I.G . (1974), J Bi ol . Chem . 249, 2258. Shin e , J. , Dalga rno, L. (1974) , Proc. Natl . Acad. Sc i. 71, 1342. Shir e s, T.K. , Narurkar, L., Pit ot, H.C. (1971), Bi oc lzem. J 125, 67. Shir e s, T.K., Pit ot, H.C. (1973), Bi oc lzem. Bi op l zy s. Res. Commun. 50, 344. Skold, S.-E. (1983) , Nucleic Acid s Res. 11, 4923. Sor, F. , Fukuhara, H. (1982) , Nucleic Acid s Res. IO, 6571 . Sp ra g u e, K.U.R., Kramer, R.A ., Jac kson, M. B. (1975), Nucleic Acid s Res. 2, 2111. Sta h l, D.A., Luehrsen, K.R., Woese, C., R., Pace, N.R. (1981), Nucleic Acid s Res. 9, 6129. Sta h l, J., Bohm, H., Pozdnja k ov, V.A., Gi rs hovic h , A.S. (1979), FEES Lett . 102, 273. Sta h l, J., Dressler, K., Bie l ka, H. (1974), FEES Lett . 47, 167. Sta h l, J., Welf le, H., Bie l ka, H. (1972), FEES Lett . 26, 233. Sta n ley, J. (1978) , Natu re 274, 87. Ste i n e rt , P.M., Balig a , B.S., Munro, H.N. (1974), ]. Mo/. Bi ol . 88, 895. Ste i n h auser, K. G. , Woolley, P. , Ep e, B. , Dijk, J. (1982) , Eur. ]. Bi oc lzem. 127 587. Ste i t z, J. A. (1980) , Ri bo somes: Str u ctu r e, F1111ct io11 and Geneti cs (Ed. , G. Cham- bliss , G. R. Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura) , p. 479,
Univ e rsit y Park Press, Balt im ore . .Stieg l e r, P., Carbon, P., Zuker, M. Ebel, J.-P ., Ehresmann, C. (1981), Nucleic Acid s Re s. 9, 2153. Sti iffier , G., Bald, R., Kastn e r, B., Lii hr mann, R., Sti iffler -Meil ic k e, M., Ti se - hendorf, G. (1980) , Ri bo somes: Str 11 cfl lre , F1111ct io11 and Geneti cs (Ed. , Chamb- liss , G. R. Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura) , p. 171, Univ e rsit y Park Press, Baltim ore. Sti iffier , G. (1974), Ri bo somes(ed., M. Nomura, A., Ti ss ie r es, P. Leng ye l), p. 615, Cold Sp ri n g Harbor Laborato r y, New York. Sti iffier , G., Sti iffler -Meli ck e, M. (1981) , Inte r nati on al Cell Bi ol og y (Ed. , H.G. Scweig er ) , p. 93, Sp ri n g e r , Heid e lberg. Sti iffier , G., Wi ttm ann, H.G. (1971a), Proc. Natl . Acad. Sci. 68, 2283. Sti iffier , G., Wi ttm ann, H.G. (1971b), J Mol. Bi ol . 62, 407. Sti iffler -Meil ic k e, M. , St6 f f ier (1982) , Electr o n M icr oscop y, Int. Co11g r . E/ectr . Mi cr oscop y, Hamburg, 3, 99. Subramania n , A.R., Mi zu shim a, S. (1979), ]. Bi ol . Chem. 254, 4309. Subramania n , A.R., Rein h ardt, P., Ki m ura, M., Sury an ary an a, T. (1981), Eur. ]. Bi oc lzem. 119, 245. Svoboda, A.J., McConkey, E.H. (1978), Bi oc hem. Bi op h y s . Res. Co111m1111. 81, 1145. Terao, K., Og at a , K. (1979a) , ]. Bi ol . Chem. 86, 597. Terao, K. , Og ata, K. (1979b) , ]. Bi ol . Chem. 86, 605. Thammana, P. , Canto r , C. R. (1978) , Nucleic Acid s Res. 5, 805. Thammana, P., Canto r , C.R ., Wollenzie n , P., Hearst, J.E . (1979), ]. Mo/. Bi ol 135, 271 . Thomp so n, J.F ., Wegn e z, M.R ., Hearst, J.E . (1981), ]. Mol. Bi ol . 147, 417. Tin d al, S.H., Aune, K.C. (1981), Bi oc hemi st r y 20, 4861 . Tolan, D.R., Traut, R.R. (1981), ]. Bi ol . Chem. 256, 10129. Towers, N.R ., Rais o n, J.K., Kellerman, G.M., Lin n ane, A.W. (1972), Bio c him . Bi op l tys. Acta 287, 301 . Trachsel, H., Emi , B., Schreie r , M.H., Sta e helin , T. (1977), ]. Mo/. Bi ol . 116, 755. Traub~ P., Nomura, M. (1968), Proc. Natl . Acad. Sci. 59, 777. Traug h , J. A. , Traut, R. R. (1972) , Bi oc hemi st r y 11, 2503. Traut, R.R., Lambert , J.M ., Bail e au, G., Kenny , J.W .)1980), Ri bo somes: Str - uctu r e, Functi on and Geneti cs (Ed., G. Chambli ss, G.R. Craven, J. Davie s , K Davis , p. 89, Univ e rsit y Press, Balti m ore. Tremp e, M.R., Ohg i, K., Glitz , D.G. (1982) , ]. Bi om . Chem. 257, 9822.
Tumanova, L.G., Gudkov, A.T ., Bushuev, V.N., Okon, M. S. (1981), FEES Lett . 127, 241. Unwi n, P. N. T. (1977) , Natu re 269, 118. Ursi, D., Vandenbergh e, A., De Wachte r , R. (1982), Nt,c/ eic Acid s Res. 10, 3517. Ursi, D., Vandenbergh e, A., De Wachte r , R. (1983), Nucleic Acid s Res. 11, 8111. Van Ag tho ven, A.J. , Maaseen, J.A . , Moller, W. (1977), Bi oc hem. Bi op h y s . Res. Comm1111. 77, 989. Van Ag tho ven, A. , Krie k , J,, Amons, R., Moller, W. (1978), Eur. ]. Bi oc lzem. 91, 553. Van Duin , J., Kurland, C.G., Dandon, J., Grunberg- M anag o, M. (1975), FEES Lett . 59, 287. Van Holde, K. E. , Hi ll, W. E. (1974) , Ri bo somes (Ed. , M. Nomura, A. Ti ss ie r es, P. Leng ye l) , p. 53, Cold Sp ri n g Harbor Laborato r y , New York. Vasil iev , V.D., Kote l ia n sky , V.E. (1977), FEES Lett . 76, 125. Vasil iev , V.D., Kote l i an sky, V.E. , Shats k y , I.N ., Rezap k in , G.V. (1977), FEES Lett . 84, 43. Vasil iev , V. D. , Seli va nova, 0. M. , Kote l i an sky , V. E. (1978) , FEES Lett . 95, 273. Vasil iev , V.D., Zalite , 0.M. (1980), FEES Lett . 121, 101 . Vassil en ko, S.K., Carbon, P., Ebel, J.-P ., Ehresmann, C. (1981), ]. Mo/. Bi ol . 152, 699. Vazq ue z, D. (1974) , FEES Lett . 40, S.6 3 . Vazq ue z, D. (1979) , Inhib i t ors of Prote i n Bi os yn th e sis , Sp ring e r-Verlag, Berlin - Heid e lberg • New York. Vig ne, R. , Jor dan, B. R. (197 7) , J. Mo/. Evol, 10, 77. Walte r , P. , Blobel, G. (1980) , Proc. Natl . Acad. Sci. 77, 7112. Walte r , P., Blobel, G. (1981), J. Cell Bi ol . 91, 545. Walte r , P. , Tackson, R. C. , Marcus, M. M. , Lin g a ppa , V. R. , Blobel, G. (1979) , Natl . Acad. Sci. 76, 1795. Warner, J. R. (1982) , The Molecular Bio l og y of The Yeast Saccharomy ce s (Ed. , J. N. Str a th e rn, E. W. Jon es, J. R. Broach) , p. 529, Cold Sp ri n g Harbor Labo- artor y , New York. Warren, G., Dobberste i n , B. (1978), Nat1 1 re 273, 569. Wats o n, J.D . (1964) , B11/1 . Soc. Chim . Bi ol . 46, 1399. Weie l , J., Hershey, J.W .B. (1981), Bio c hemi str y 20, 5859. Welf le, H., Bie l ka, H. , Bott ge r, M. (1969), Molec. Gen. Geneti cs 104, 165.
Welf le, H., Goer! , M., Bie l ka, H. (1978); Molec. Gen. Geneti cs 163, 101 . Weste r mann, P. , Ny ga rd, 0, Bie l ka, H. (1981) , Nucleic Acid s Res. 9, 2387. W ick ner, W. (1979) . A1111. Rev. Bi oc lzem. 48, 23. Wi ck str o m, E. (1983) , Nucleic Acid s Res. 11, 2035. Nin k elmann, D.A., Kahan, L., Lake, J.A . (1982), Proc. Natl . Acad. Sci. 79, 3111 . Wi ttma nn, H.G. (1982) , Ann. Rev. Bi oc lzem. 51, 155. W ittm ann, H.G. (1983) , A1111. Rev. Bi oc lzem. 52, 35. Wi ttm ann-Lie b old, B. (1980) , Geneti cs and Evolllti on of RNA Polym erase, tR NA and Ri bo somes (Ed. , S. Osawa, H. Ozeki, H. Uchid a , T. Yura) , p. 639, Elsevie r -Bio m ed. , Amste r dam. Wi ttm ann-Lie b old, B. (1980) , Solid Phase Meth o ds ill Prote i n Scq1 1 e11ce Atza lys i s (Ed. , B. Bir r ) , p. 49, Elsevie r -Bi om ed. , Amste r dam. Wi ttma nn-Lie b old, B., Robin s on, S.M. L. Dzio n ara, M. (1977), FEBS Lett . 77, 301. Wi ttm an, H. G. , Lit tlec hil d , J. A. , Wi ttm ann-Lie b old, B. (1980) , Ri bo somes: Str u ctu r e, Functi on and Ge11et ics (Ed., G. Chambli ss, G.R . Craven, J. Davie s , K. Davis , L. Kahan., M. Nomura), p. 51, Univ e rsit y Park Press, Baltim ore. Wi ttm ann, G.G. (1974), Ri bo somes(Ed., M. Nomura, A. Ti ss ie r es, P. Leng yel ) p. 93, Cold Sp ring Harbor Laborato r y , New York. W ittma nn, -Lie b old, B. (1975) , Ri bo some (Ed. , M. Nomura, A. Ti ss ie r es, P. Leng yel ) , p. 115, Cold Sp ri n g Harbor Laborato r y , New York. Woese, C. R. (1973) , J. Theor. Bi ol .. 3 8, 203. Woese, C.R . , Fox, G.E. (1977), Proc. Natl . Acad. Sci. , 74, 5088. Woese, C.R., Gute l l, R.R., Gup ta, R., Noller, H.F. (1983), Mi cr obio l . Rev., Woese, C.R., Mag rum, L.J. , Gup ta, R., Sie g e l , R.B ., Sta h l, D.A., Kop , J., Crawf ord , N., Brosiu s , J., Gutt el , R., Gog an , J.J., Noller, H.F. (1980), Nucleic Acid s Res. 8, 2275. Woledg e, J., Corr y, M.J. , Pay n e, D. I. (1974), Bi oc lzim . Bi op h y s . Acta 349, 339 Wool, LG. (1979) , Ann. Rev. Bi oc hem. 48, 719. Wool, I. G. (1982) , Prote i n Bi os yn th e sis in E11karyo t e s (Ed. , R. Perez-Bercoff ) , p. 69, Plenum, New York. Wower, J., Mein e ke, M., Br ima combe, R. (1981), Nucleic Acid s Res. 9, 4285. Yagu c hi, M., Math e son, A.T ., Vi se nti n, L.P., Zucker, M. (1980), Geneti cs and Evolt ttion of RNA Polym erase, tR NA and Ri bo somes (Ed. , S. Osawa, H. Ozeki H. Uchid a , T. Yura) , p. 585, Elsevie r -Bi om ed, Amste r kam. Zaga rs ka, L., Van Du in, J., Noller, H. F. , Pace, B., Joh nson, K.D., Pace, N.R. (1984) , ]. Bi ol . Chem. 259, 2798.
Zante m a, A. , Maassen, J.A., Kr iek , J., Moller, W. (1982b), Bi oc hemi st r y 21, 3077. Zante m a, A., Massen, J.A ., Moller, W. (1982a), Bi oc hemi st r y 21, 3069. Zim mermann, R.A . (1980), Ri bo somes: St ru ctu re , F11ncti on and Geneti cs (Ed., G. Chambli ss, G. R. Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura) , p. 111, Univ e rsit y Park Press, Baltim ore. Zwi eb , C., Glotz , C., Brim acombe, R. (1981), Nucleic Acid s Res. 9, 3621 .
제 3 장 전령 RNA(mRNA) 의 구조와 기능 3.1 원핵세포에 있어서의 mRNA 의 구조와 기능 3. 1. 1 다시스트론성 mRNA 박테리아와 박테리오파지의 유전자들은 거의 언제나 무리로 전사되며 1 이렇게 해서 생기는 다시스트론성 일차 전사물은 mRNA 로서의 기능을 가질 수 있다. 원핵세포의 mRNA 는 유전정보를 내리는 첫 연속부분 앞 : 으로 길이가 20 내지 200 개 누쿨레오티드가 넘는 번역되지 않는 5' 연 : 속부분을 가지고 있는 것이 보통이다(표 3-2 를 참조하라). 개시 코돈 이 전 끝에서 바로 시작하거나, 5' 끝으로부터 몇 개의 누클레오티드 안 쪽으로 위치하는 예는 지금까지 두 가지밖에 알려져 있지 않다 (P t ashn e- 등, 1976; Pit ro tt a, 1979), 울리고 (A) 또는 폴리 (A) 로 끝나는 약간의 ; 원핵세포의 mRNA 둘이 있지만, 진핵세포의 경우에 비하면 거의 예의 ’ 적 으로 밖에 볼 수 없 다 (Nakazato 동, 1975; Gop a lakris h na 등, 1981 ;: Gop al akris h na 와 Sarkar, 1982) . 대 부분의 박테 리 아의 mRNA 들에 있 어서, 1 내지 400 개의 누클레오티드로 되는 길이의 연속부분이 두 사 스트론들을 서로 갈라놓고 있다. 그러나, 유전정보를 내리는 두 연속부 분 끝둘이 서로 인점하고 있거나 심지어는 중첩되어 있는 예들도 많이 볼 수 있다. 원핵세포의 한 유전자의 옆구리로 붙어 있는, 번역되지 않
는 절편의 길이는 광범위하게 다르지만, 전체적인 경향을 보면 이러한 연속부분들의 길이는 짧은 것이 보통이다. 예를 들면, 박테리오파지 懿 174 의 게놈을 이루는 5,386 개의 누클레오티드 중 5,169 개가 아미 노산들에 대 한 유전 암호를 지 령 하며 (Sang e r 동, 1978) , 박테 리 오파지 T7 DNA 의 왼쪽 끝 으로 있는 삼분의 일에 해당하는 11,200 개의 누 클레오티드 중 번역 되 는 누쿨레오티드의 수는 10,500 개이다 (Dunn 과 St ud ie r , 1981). 三의 보기와 같이, 한 시스트론의 종결 코돈 과 다음 시스트론의 개시 코돈 사이에 중첩이 일어나는 일도 드문 일이 아 니다. 이러한 연속부분 은 너무나도 교모한 구조이므로, 이 부분이 단백 질 합성을 조절하는 중요한 역할을 할 것이라고 생각하는 사람도 있었 다 (Chris t i e 와 Platt . 1980) (그림 3-1) . 한 시 스트론의 종결 코돈이 다 음 시스트론의 개시 코돈과 중첩하는 경우에 있어서, 상류 쪽에 있는 시스트론의 번역이 그 다음에 뒤따르는 시스트론의 번역을 간섭하는 원 인이 된다는 것을 보여 준 예는 없다 (Dunn 등, 1981; Schump er Ii 등, trpE -tr p D GCA CAG GAG ACT TTC TI 迅끄! GCT GAC ATT CTG trpD - tr p C GCG GCA CGA GGG TAAATG싣뜨~ CAA ACC GTT TTA trp C - tr p B GCA TAT TAAGGAAAGGAACA 쓰!:Q ACA ACA TTACTT trp B - tr p A GCA CGA GGG GAA ATC TGATG GAA CGC TAC GAA 그림 3-1 E. coli 의 trp 오페 론의 시 스트론 사이 의 부분들의 비 교. 1982). 하류 쪽으로 있는 시스트론의 번역이 앞에 있는 시스트론의 번 역보다 먼저 일어나야만 하는 예들도 있기는 하지만, 이것은 언제나 시 스트론들이 중첩되는 경우에서만 불 수 있는 것은 아니고 중첩하지 않 는 경우(그렇지만 가까게 이웃하고 있는 경우)에서도 볼 수 있는 일이다 (Pauza 등, 1982) . 현재 로서 는, 종결 코돈과 개 시 코돈의 중첩 된 배 열 을 합리적으로 설명할 만한 실험결과가 없다. 만일 이러한 중첩 배열이 조절 역할을 한다면 이 중첩 양식이 많은 유전구조들에서 고도로 보존 되어 있어야 할 것이다. 그러나 이러한 가정을 증명할 만한 중거는 아 칙 발견되지 않았다. 현재까지 알려져 있는 보기들은 서로 상반되는 경 향을 보여 주고 있다. 예 를 들면, E. colt ' 와 Salmonella 의 trp 오페 론
들에 있는 시스트론들 사이의 부분이 잘 보존되어 있지만 ( Chr i s ti e 와 Platt , 1980) 그밖의 경우에서는 그러한 보존성을 볼 수 없다. E. coli 의 trp C 뒤에 오는 14 개의 누클레오티드로 된 번역되지 않는 부분과 s. typh in m rim uriu m 의 trp C -trp B 접 속부분의 12 개 의 누클레 오티 드로 된 상응하는 부분의 연속부분을 보기로 나타내었다. E. coli GCA TAT TAAGGAAAGGAACAATG ACA ACA TTA CTT S. typh im uriu m GCA TAT TAAGGAAA A AAC ATG ACA ACA CTT CTC Muller 와 Wells(l980) 는 ¢X174 의 J 및 F 유전자들 사이의 부분을 실험적으로 늘 리거나 줄여 보았는데 파지의 생장에 미치는 영향이 아주 적다는 것을 알았다. 이와 같이, 유전자들 사이의 번역되지 않는 연속 부분의 길이의 장단에는 관계없이 번역은 아무런 지장을 받지 않는 것 으로 생각된다. 아마도 시스트론들 사이에 있는 번역되지 않는 간격부 분의 수축경향은 진화가 게놈의 경제성을 이룩하려는 방향으로 진행한다 는 것을 반영하는 것일지도 모른다. 원핵세포의 유전자들이 직접 인접하거나 또는 중첩하는 경향이 조절 메카니즘과 명확한 관계를 가지고 있지 않더라도, 원핵세포의 mRNA 의 다시스트론성 구조는 전사와 번역 두 과정에 있어서 심대한 조절효 과를 가지고 있다. 한 유전자의 번역이 막힘으로써 그 유전자의 하류에 있는 유전자의 전사가 일어나지 않는 현상은 감쇠작용과 갇은 조절 메 카니 즘 에 서 널 리 알 려 져 있 다 (Adhy a 와 Gott es man (1978) , Yanofs k y (1981) 동의 평론서를 참고하라). 그리 흔히 일어나는 현상온 아니지만 한 시스트론을 번역할 수 있는 능력이 앞에 있는 시스트론의 우선적 인 번역에 좌우되는 일을 가끔 볼 수 있다. 예를 들면, 콜리파지 MS2 RNA 의 경우, 3' 끝에 가까운 중합효소 유전자의 표현이 일어나려면 앞 서 있는 외피 단백질 시스트론의 우선적인 번역이 일어나야 한다. 이것 온 중합효소 시스트론의 리보솜 결합자리가 외피 단백질 시스트~ 안에 있는 21 개의 누클레오티드 절편과 상보적인 염기 결합순서를 가지고 있다는 것으로 설명 할 수 있다(그림 3-2 를 보라, Mi n Jou 등, 1972). 리보솜이 외피 시스트론을 통과해 감에 따라서 염기 짝지움을 이룬 부 분이 파열되면서 중합효소 시스트론의 개시자리를 노출시킨다. 이 이의
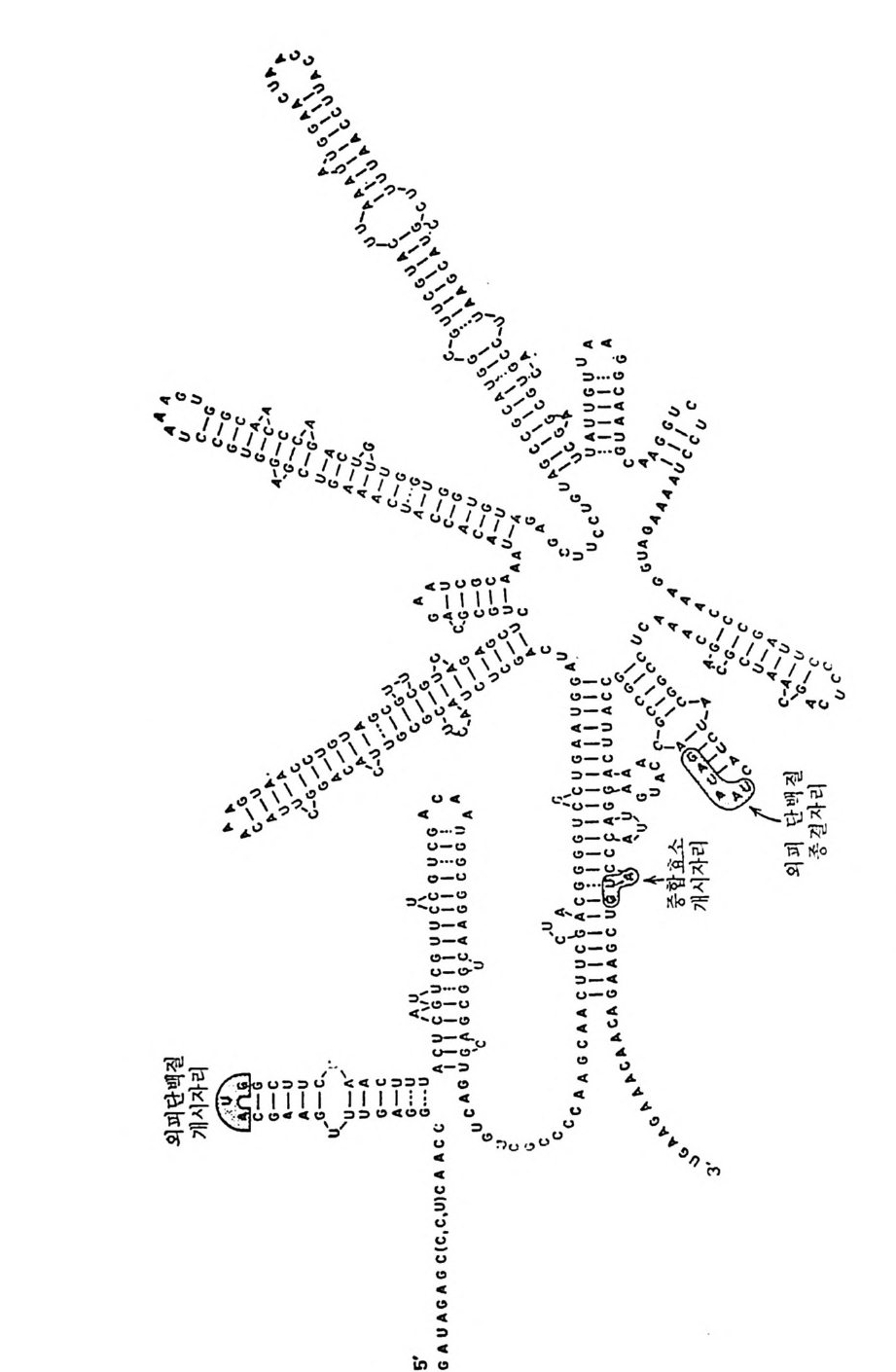
에도 번 역 의 짝 지움 현 상이 몇 가지 알려 져 있지만 아직 그 메카니즘은 찰 이 해되 어 있 지 않 다. 이 러 한 현 상의 실 례는 E. col i의 trp 및 ga l 오 페 론들 과 E. coli 리보 솜 단백 질 들에 대한 정 보를 내리는 각 오페론에서 봅 수 있다 (N i chols 둥, 1981; Schump er li 둥, 1982). Schump er li 둥 은 E. co l i의 g a!T 와 ga lK 시스트 론 사이에 무의미 돌 연변이 또는 구 조이 등 돌연 변이 을 도입하여 상 류 쪽 에 있는 시스트론(g alT) 의 번역 이 하류 쪽에 있는 시스트론(g a!K) 의 번역의 효율에 미 치 는 영향을 조 사 하 였다. 이 실험에서 그들은 상류 쪽 번역이 g u!K 의 개시부분(리보 솜 인식자 리) 에서 종 결 될 때 g a!K 의 번역이 상당히 증진되지만, 반대 로 상 류 의 번역이 ga lK 개시부분보다 위에 있거나 아래에 있을 때는 g a!K 의 번역이 심하게 감소되는 것을 관찰하였다. 이것은 한 시스트론 의 리보솜 인식자리의 구조 를 변형시킴으로써 그 시스트론의 번역 효율 에 직 접 영 향 을 미친다는 것을 말해 주는 것이다 . 이러한 연구결과들은 리보솜이 하 류 쪽 의 시스트론에 처음부터 개시반응을 일으킬 수 없으며 리 보솜이 상 류 의 시 스트 론 을 다 동과한 다음에 같은 리 보솜이 다음에 오 는 시스트 론 으로 진행하 여 그 시스트론을 읽게 된다는 것을 암시한다. 이 문 제에 대 해서 는 앞으로 더 많 은 연구가 이루어져야 하겠지만, 어떻 든 간에 원핵세 포의 mR N A 들 의 다시스트론성은 그들의 번역에 있어서 밀접한 연계성이 있을 것만은 분명하다. 3.l.2 개시 코돈은 보통 AUG 이다 트리누쿨레오티드들을 주형으로 사용하여 리보솜의 결합에 관한 실험 울 한 1960 년대 에 AUG, GUG 및 UUG 둘이 fM et- tR.t\rA 의 E. coli 리 보솜에의 결합을 안정시킨다는 것을 알았다 (Clark 와 Marker, 1966). 결합순서가 알려진 풀리누클레오티드를 주형으로 사용하여 실시한 실험 에서 AUG 보다 효율은 낮지만 UUG 와 ACG 들도 개시 코돈이 될 수 있다는 것이 확인되었다 (Thach 둥, 1966). 그 후에 박테리아 및 비루스 의 mRNA 둘의 결합순서가 분석됨으로써 원핵세포의 리보솜은 AUG 만 을 개시 코돈으로 인식하는 것이 아니라는 것이 확인되었다. 현재까지 알려진 원핵세포의 리보솜 결합자리들 중에서 12 개의 유전자는 GUG 를, 세 개는 UUG 를, 한 개는 AUU 를 개시 코돈으로 사용하고 있다 (표 3-1 을 보라). 그밖에도 무의미 코든들에 뒤이어서 〈재출발〉 자리
자개 스개
앞나부 서난일이 분에 개된 자리시 la(.o cc El i 제 억 의인 에부는자있내 전유 )32 리자시 r BII지의 리4시콜(파 T 서 론어트의에부있내)l NI l 및리자시AG U개시 A서의이코서에 의 돈있의 외들에N 어R 거이겼연점변생 가 새돌로리·개자 시활돌화이로변의미 연무성 G CUGUCUGCUGCGS2M ) 단지A질 콜백( -리파 I I 3)IMl지( 리자전콜 파 유UCGGAAUAGAUU AGUC8.2 7 )T 백지 파리질콜단(GUGAC/AAU AUGGUGGAAG)31( SE. i질 의솜단백c lo보 리 _ '.A/3E(NR 소i의효oc합중 .l 체위하단위 ) pt(. Ea 유i ,o오자론 c의 l페전 )4 .(E알 i의ol c성리카 인탈산 수소효해분가 ). (E 효i의원환ol c 산)르마푸소 . (E락 제i 억ol c 스 의자오) 토인 ).uT (E 연 i의olc 자인장 .E(자저인의i달olc 전 성 항 pl Are 전유 )자 A NR .(Et-히 i의olc 딜합티 스 )소효성 1-3의아m및테박 리 루 스비표 시개 연자의코돈 GAUGUUCA CGGCUGGUAGU GGGGUAUGAUUCG UACAAGGACUGA UUUGAGGACGUCAGGUGGAA AGGUGCCGACGGGAAG AUAUGGUGGUAG UGUUACCAGA GAAGAAGGAGAUAAUAGCG AUGCGUGGGUAGUGGGU AGGAUGAGUUUCGGAGC AUAAGGGAUGUGGAG AUGAGUACGGAGA GUAUGUAG GUAS)UG02GGC UGUC (.GG E GrAIGAGAAUCGGBIU U질 솜o단의 리 백보ilc 트4 지 T(스의시파 개부론 의내 서에있 어GGAGUCUAUUCGAG AGG.E ( 아환의 틴l코 oi원니 미형bc 넨 )리시자 티드레쿨닌누데탈디 오아 드효수 )소소AUUUG GUGAUAUUGGGCUAGAUCC.lGcA GaGU GCEA(G S .( 효 해소)s3 1-팀11farea분의락1 자lo의 i제 c억 인 내 부유의있 서에어 전자F) I3AGAA EAAGG GUAUA.UAU (UGAUG2) 6인개 시o 의li c자 리개자시 AU A AUAUUAUUAAGAAGAB IrI변 연 돌의지T4 파(62 DH)<3 체 이 AAlA.UUUUAGUGAz (Sir1i선1 의1z11ilpy1t 1111s 체 ,드변연리이팹도돌 d658)9 AAUCAUUGUAUAGAGGCUQf 3단 의피지 리 (콜파백• C)4C/3 변 연질돌체 ,이 noalDra-en ag타나 로자 큰 윤분부내숙인Sh.환 다있 추 되칭과돈코 시개는i G이U U해시G 암G운입들리자시개 U진가4 T 운능 기 윤및 인지 는 에BIJr 는있거증 시 b돈 코유진인지하 `t로,만 ·충 성지하재합주 는기 . 다했못 지시되 확 로집 과깅 한분직운인전백단는 된 다않 지지가 운능기 는 c는. 비 시개 서에리자합긴 송보서에c1•3 의.다이는작유효° 는있에632DH 는 서C5리2에 역 의형아 .다하 민 이유효생 d만다보인자인개 가GUA 은익반 의5689 체시이빈연 듄 / 3서C 에4C 가GGA 의U서에지마체 형생A야이A. 다르다변AU 가연둘합전서에대군 두 헝생야는 -1C/3가C 재이빈연돌 서순진가 운능기 e . 었없 수할합결 다융솜보 체이변연돌른다 또 진가 윤리 서에관 험시 는ANR분부속연 GAUA .다였하번 로
로 작용하는 GUG 및 UUG 삼중체들이 오는 에 둘 이 많 이 있다 . 돌연변 이가 일어난 약간의 리보솜 결합자리들에 있어서는, 개시 코돈이 AUA 로 달라졌음에도 불 구하고 리보 솜 이 조금은 결합할 메도 있다 . 표 3-1 에 준 실험결과에서 개시 코돈둘의 조성은 놀랄 만한 유연성을 가지고 있다는 것을 알 수 있다. 그러나, AUG 대 신에 재일 흔 히 나타나는 ,GU G 코돈이라 하여도 아무 제약없이 AUG 를 대신 할 수 있는 것은 아 니 다. 예 를 들면 , TJ r II B 유전 자 (N 24* ) 의 101 번 위 치 에 서 103 번 위 치에 있는 AUG 삼중체는 기능을 가진 개시 코돈이지만, 같 은 위치에 있는 GUG 삼중체 는 개 시 코돈으로 작용하지 못한다 (N 24 의 경 우) (Nap ol i 등, 1981). 또한 이 두 돌연변이체들은 가능한 개시 코돈 앞에 있는 두 위치에서 서로 다르다. 즉, 돌연변이체 N24 * 에서는 C AA 뜨 ~A 이고, 돌연변이체 N24 에서는 UG 으 !&A 이다. 개시 코돈 옆 에 있는 누 클레오티드들에 있어서의 차이가 GUG 에서 개시가 일어나 지 못하게 하 는 원인일지도 모른다. 자연의 mRNA 에 있어서는 GUG, UUG 및 AUU 들이 좀처럼 개시 코돈으로 사용되지 않는다는 사 실은 이 대용 개시 코 돈들이 개시과정의 어떤 단계에서 AUG 보다 덜 효율적으로 작 용한다는 것을 암시한다• 아마도 이러한 약점을 보완하기 위해서 AUG 이외의 개 시 코돈을 사용하는 mRNA 둘은 기다란 Shin e -Dalga rno 연속부분을 가 지는지도 모른다. 그러나 이것은 표 3-1 에 열거한 돌연변이체들의 자 리와 재출발 자리들에 대해서는 해당되지 않는다. 3. 1. 3 개시 코돈 주위의 연속부분 박테리오파지와 박테리아의 mRNA 둘의 개시 코돈의 측 면에 붙어 있 논 부분들은 리보솜에 의해서 인식될 특칭을 가지고 있다. 개시 코돈 자 체 이외에 보편적으로 존재하는 특칭은 개시 코돈으로부터 약 10 개의 누클레오티드 상류 쪽으로 푸린 염기들이 많이 있는 연속부분이 있다 (표 3-2) . 이 러 한 사실 은 Shin e 과 Dalga mo (1974) 가 처 음으로 주목한 것인데, 이 푸린 연속부분은 16S rRNA 의 3' 말단과 상보적안 결합순 서를 가지고 있다• 이 이른바 Shin e -Dalga mo 연속부분의 핵심적인 역 할에 관해서는 제 4 장에 더 자세히 논의하겠다. 원핵세포의 리보솜이 결 합하는 그 밖의 자리들에서 볼 수 있는 준보존된 구조적 특징이 기능적 으로 어떠한 중요성을 가지고 있는지에 대해서는 아직 확실히 모르지만
G G AGA GU CAC U UU CAU G UG GC C u · UC G U A CA C UAGUAGUUUUUUCAACGCAGG GUUCUUUCU U A AA A AGG CA UU GTAT TCA
UU UUU U CAA CAAA ACUA U UUACA A AAGA ACU AU CA A UC A U AU CG U TTC CCT ACG C UGCUU CUU AGAAA AAA AA G AA AACC U GC A AC A CG CG U A U U GTG C CAA CGACAGGUCCGUGCUCCUAGCU UCGAUGUCA AA AC A A AG C CA A GATTGAG A GUGUAG AGU UGAAG UGU AGAU U G AC UC UGAA UG A U GG U A U GA G UAG TAGAT AmNR 23-분부연속듄드래 오 클누티리시등의에자시개 등의 핵세원포의 표 분연 부 속개의자시리 CGUCAAG GU UUG UCGAU GCASUM 2 백질A단- CUCG UUA UGGA GA UGC AUU GC17R질A백 단一 cc C GA UUGAGG ACGU ACA CU2SM 피외 ccGGAC AGUU U GGCG C AA C71RU외 피CCC UAA UGGAG AAU 7C1A,SR 2AM 소효합중CAUG A UAAGGAUG GU AA CACU/3Q 백전 꾹단A CU·UU UG A CUGGAA AUGU UCAA/3Q 피외 U GCA A GAG G UAUCA A A U AGAQ 3f 효중합소C UUAA CA UAA UGGUUlf 피 외 AGACG GUA(UU)GCCG AA C CCU 2피 외f A AU C A GC A AG CA A AU GA C, NARmr 」으[브pt 연도 속 신>I it .TE T A CAAGA A A U A U UAAG A AG A A C NARm pE rtI A G C UU GA G AGG GCA CG A A AGm ANR Ar\ J tpI I GU C ,CrA A AG C A CA U U AA C UNHc Z nImJ\ \ JJ\ I G A U U A GC U GAGA A UC C GA A UAA NH mEla g A4 7lXT TTTTTG CGGG TTC TAA AC>I< *자진유\ J B 4 7lXAATA G C./\ GGA TGAA CT GGAA s·- J ' 방향
s·- J ' 방향
다음과 같은 일들이 주목을 끈다. 리 보솜이 결 합하는 자리 들 중 Shin e -Dalga rno 연 속부분 이 의 의 부분 에 는 G 잔기 들이 적 다 (Scherer 동, 1980 ; Sto r mo 등, 1982) . Shin e - Dalga rno 연속부분과 개시 코돈 사이 에서뿐 아니 라 Shin e -Dalga rno 자 리의 바로 상류 부분에는 A 또는 U 둘이 존재하는 경향이 크다. 콤퓨터 를 이 용하여 조사한 바에 의 하면 (Scherer 동 (1980) 은 68 가지 의 mRNA, Sto r mo 동 (1982) 은 124 가지 의 mRNA 를 조사대 상으로 삼았 다), _3 번 위치와 +4 번 위치에서 +7 번 위치까지의 누클레오티드들의 선택이 마구잡이로 이루어지지 않음을 알 수있다. 죽, -3 번 위치에서 는 A 찬기가 더 선택되며, +4 번에서 +7 번까지의 위치의 누클레오티 드들(즉, 개시 코돈 바로 뒤의 코돈을 아루는 연속부분)은 GCUA 또는 AAAA 연속부분이 존재하는 확률이 크다(개시 코돈을 +1 에서 +3 까 지로 번호를 붙이고 이어서 유전정보를 내리는 연속부분의 위치들을 +4, +5 동등으로 번호를 붙인다. 개시 코돈 바로 앞의 위치를 -1 번 이 라고 한다) • Sto r mo 동 (1982) 이 주목한 바와 같이 , 코돈 GCU (알라 닌)와 AAA( 리신)를 읽는 t RNA 들이 E. coli 세포에 제일 많이 있다는 것은 매우 홍미있는 일이다. GCUA 또는 AAAA 연속부분들이 정보를 내리는 연속부분의 머리 부분에서 많이 나타나는 원인이 자명해진다. Scherer 등 (1980) 은 68 가지 의 mRNA 들의 5' 끝 쪽의 46 내 지 48 개 의 누클레오티드로 이루어진 연속부분을 비교 분석하여 E. coli 리보 솜(1의97 8)결 의합 을연 구촉도진 시참 고키 하는라 )역 .할 을이 들하은는 이자 리연 를속 부제분 안과하 였16다S r(SRcNhAer e의r 등3'
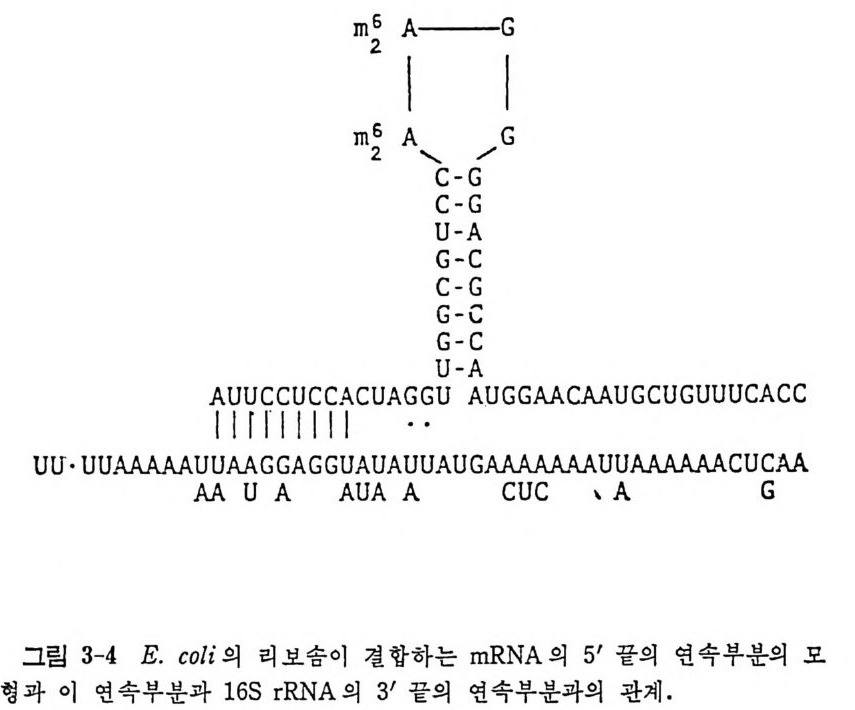 m6 A-G
m6 A-G
끝과의 인식에 대하여 그립 3-4 로 나타낸 모형을 제안하였다. 이들의 연구결과에 의하면 리보솜이 결합하는 자리는 Sh ine -Dalga mo 연속부분 을 제의하고도 상당히 긴 부분에 걸쳐 있어서 개시 코돈의 하류 부분까 지 포함된다. 그리고 목정한 위치에 어떤 특정한 영기가 절대적으로 요 구되는 것이 아니라 일정한 염기들 (A 또는 U) 을 선호한다는 것이 특 칭이다. 그러므로 mRNA 에의 리보솜의 결합은 보다 더 미묘한 추가적 인 요소들에 의해서 결정된다는 것을 알 수 있다. 수 년 전에 At ki n s (1979) 는 종결 코돈들 중 UAA 또는 UGA 가 개시 코돈 앞의 15 개의 누클레오티드로 된 연속부분 내에 자주 일어난다는 것을 관찰하였다(종 결 코돈 UAG 가 있는 경우는 전혀 없다). 그렇지만, 최근에 와서 리보 솜 결합자리들의 목록이 증가함에 따라서 (약 200 가지가 알려져 있음) A t k i ns 의 규칙에서 벗어나는 예의가 늘고 있다 (Gold 등, 1981). 그러
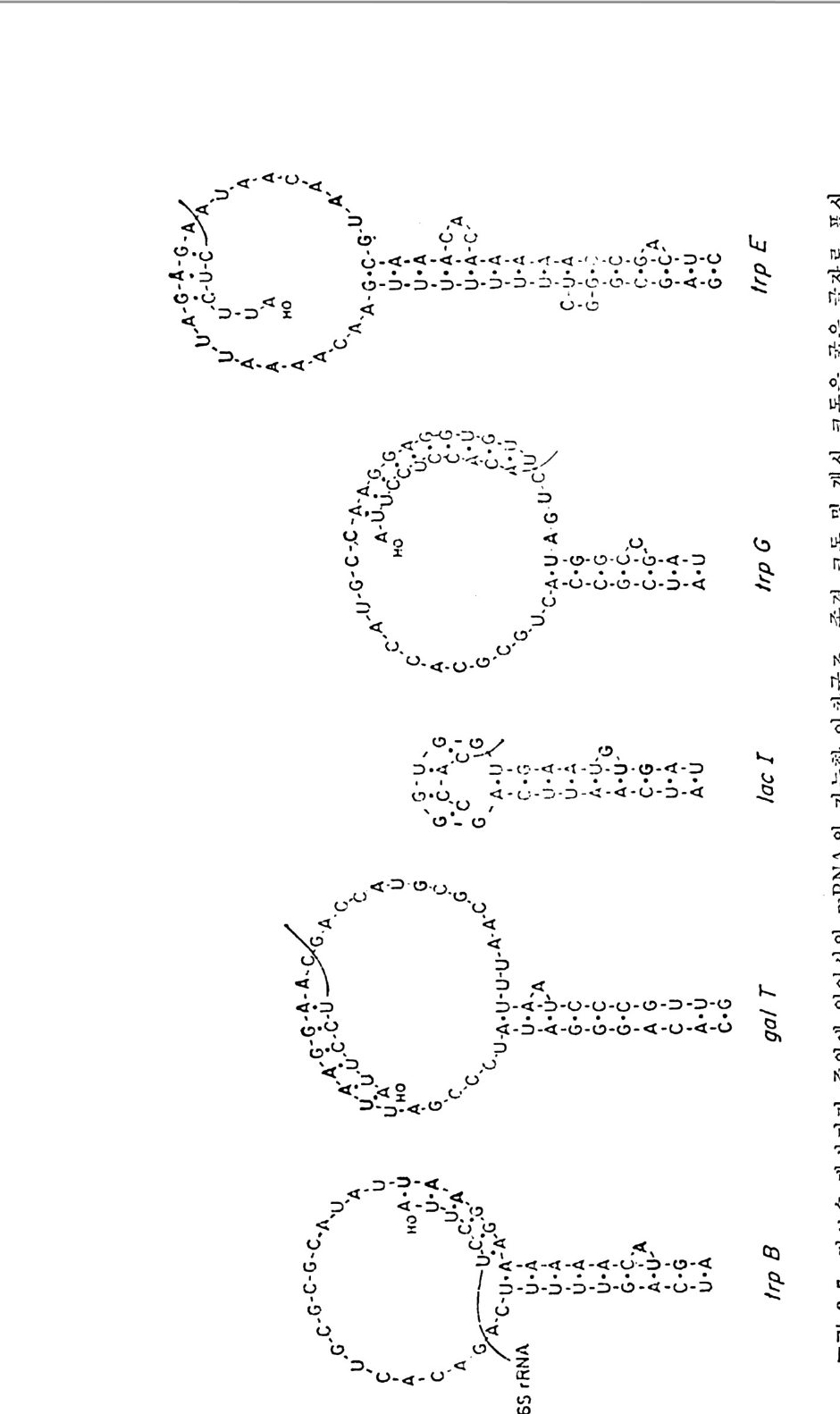 A•
A•
므로, 번역의 개시에는 종결신호들이 관계될 것이라는 종래의 견해는 앞 으로 더 많은 중거를 얻어서 확인해야 할 일이기는 하지만, 개시자리에 서의 누클레오티드 조성이 마구잡아로 이루어지지 않기 때문에 UAA 와 UAG 가 우세하게 존재하는 것이 우연한 일만은 아니라고 불 수 있다. 약간의 티보 송 결합자리들은 개시 코돈의 상류 쪽으로 머리핀 구조를 가지고 있다. 아 구조가 리보솜 에 대한 인석 요소의 역 할 을 하는 것으 트 가정 되 기 도 하 였 지 만 (Se l k er 와 Yanofs k y, 1979) , 모든 원 립 세 프의 개시 자리에 이 머리 핀 구조가 안 정한 구조로 존재하는 것은 아니다(그 림 3-3) . Sa/111011e //a typh in w rizm t 에 있 는 trp C -tr p B 접 속부븐이 즐기 - 고리 구조 물 형 성 할 수 있기는 하지단, E. co li의 trp 오페론의 상응하 는 부 분에서 는 이러 한 구조 형성에 필 요한 대칭성을 찾아 볼 수 없다 (Chris t i e 와 Platt , 198 0) . 문 리 파지 T4 의 r II B 유전 자 앞 에 있 는 머 리된 구조 물 제거하 여도 그 유전자의 표 현 에는 거의 아무런 영향을 미 치 지 않는다 (Si n g e r 등, 1981) . 지 금까지 의 증거 둘은 줄기 -고리 구조가 리브 송 의 결 합에 필 요한 인석 요소로서 작옹한다는 가설을 뒷받침해 주 지 듯하고 있다. 3.2 진핵세포에 있어서의 mRNA 의 구조와 기능 3.2. I 진핵세포의 mRNA 들은 단일시스트론성이다 진핵세포의 mRNA 는 언제나 단일시스트론성이며, mRNA 의 크기는 그 유전청보로 합성된 단백질의 크기에 비례한다. 비루스의 mRNA 들 중 에는 단일시스트론의 통례를 벗어나는 약간의 예의가 있지만, 대부분의 석뭉 및 동물 비루스들의 mRNA 들은 단일시스트론성이다(그림 3-6a). 상당한 수의 비루스 mRNA 들이 그립 3-6b 에 나타낸 형태를 가지고 있 다. 이 mRNA 둘은 구조적 으로 다시 스트론성 이 다. 이 러 한 mRl~A 둘은 둘 또는 그 이상의 중첩하지 않는 단백질들에 대한 정보를 내릴 수 있 다. 그러나 한 경우를 제의한 이러한 모든 경우들에 있어서 번역은 5' 말단에 가까운 시스트론에 한정된다. 한 가지 예의는 원숭이 비루스 40(SV40) 에 있어서의 후기 16S mRNA 인데, 여기에는 두 가지 단백질에 대한 유전정보가 들어 있다.
재 3 장 전령 RNA(mRNA) 의 구조와 기능 291
껍질 단백질 VPl 유전자의 상류에 62 개의 아미노산으로 구성되는 아그 노단백질에 대한 유전자가 있는데, 이 두 유전정보는 모두 번역된다(J ay 등, 1981). SV40 의 예의를 제의하면 구조적으로 다시스트론성인 mRNA 들은 기 능적으로 단일시스트론성을 가지고 있으므로 진핵세포들의 통례에서 벗 어나지 않는다. 소수의 진핵세포 mRNA 들은 그립 3-6c 에 나타낸 세번째의 부류를 (a) 구조적으로 또 기능적으 m'G-AUi. G UA A- (A ), 로 단일시스트론성인 것 세포에 있는 모든 mRNA, 레오비 루 스, 인-풍우엔자 비 우 스, 수포성 구내염비무스, 및 박시니아 비루스들웅 포함한 많은 동물 비우스 mRNA 들 (b) 구조적 으로 다시 스트론 m7 G -!도',UG1-UAA -~UG}, -UAA - (A ), 성이고 기능적으로 단일시 스트론성인 것 생리키 상립열 비루스 42S 게놈, 루 육종 비루스 게놈, 풀리오마 비우스 후기 19S mRNA, 브롬 모자이 크 비 두스, RNA-3, 담배 모자이 크 비 루스 게 놈, 아데 노비 무 스의 후기 rnRNA 들의 많은 것 들 (c)인 기것능 적으로 이시스트론성 m7G -AlUG1~-~UG 二1 -二U二A A-{A), 원숭이 비루스 40 의 후기 19S mRNA. 단순헤르페스 비르스의 티민 카나아재 rnRNA, 아데 노비 루스 Elb rnRNA 레 오비 우스 Sl rnRNA 그림 3-6 진핵세포의 mRNA 의 구조와 표현을 나타내는 도형. mRNA 를 칙선으로 나타내었고, 정보를 받아서 합성된 단백질을 파상선으로 나타내었 다. mRNA 들의 부류를 왼쪽에 지적하였고, 각각의 보기들을 오른쪽에 열 거하였다. 부류 a 의 mRNA 둘은 걷고 열린 시스트론 하나만을 가지고 있다. 부류 b 의 mRNA 들은 AUG1 과 AUG2 로 표시한 두 개의 시스트론을 가지 고 있다. 그러나 5' 끝에 제일 가까운 시스트론의 지령을 받는 단백질만이 생성된다. 부류 c 의 mRNA 들은 두 가지 단백질에 대한 지령을 낸다 . 부류 c 에 있어서의 mRNA 에 의해서 생기는 두번째 단백질은 SV40 의 VP2 와 VP3 에 있어서와 같이, 첫번째 단백질이 좀 짧아진 것에 지나지 않는 것일 수도 있다. 그러나 그밖의 경우에서는 두 개의 개시 코돈들이 별개의 시스 트론 내에 있게 됨으로써 아무 관련이 없는 단백질이 생성된다.
이루고 있다. 이 mRNA 둘은 두 단백질들에 대 한 정 보를 표현한다. 대 부분의 경우 이러한 표현은 첫번째 개시 코돈과 두번째 개시 코돈에서 개시가 일어남으로써 생긴다 . 이것은 대부분의 진핵세포의 mRNA 들에 서 5' 말단에 가까운 데 있는 AUG 만이 개 시 코돈으로 작용하는 것과 는 대조적인 일이다. 이 러한 mR NA 들은 아주 드 물게 존재하기 때문에 진핵세포의 mRNA 둘의 단일시스트론성 규칙에 큰 모순을 제기하지 는 않는다. 이러한 색다른 이 기능적 mR NA 들에 관해서는 아래에서 다시 곧 논의할 것 이다. 진핵세포에 있어서의 유전자 표현에 관한 단일시스트론 규칙은 단일 mR NA 가 단일 단백질의 합성을 지시한다는 것뿐 아니라 표현되는 단 백질은 51 끝에 제일 가까운 시스트론에 의해서 정보를 받는다는 것이 다. 이 규칙은 그립 3-6b 에 열거한 자연계에 존재하는 비루스의 mRNA 뿐 아니라 두 개의 인위적으르 구성한 두 개의 시스트론을 가지고 있는 mRNA 의 경우에도 적용한 다. 표현되는 시스트론이 5' 말 단에 한정되는 것은 진핵세포의 mRNA 의 구조에 기인하는 것이 아니라 진핵세포의 리 보솜둘의 성질에 의해 서 생기는 것이다. 이것은 밀 싹 으로부터의 리보 송과 박테 리 오파지 람다로부터 의 다시 스트론성 mR .'JA 를 항온반응시 켜 봄으로써 증명 되 었 다. E. coli 의 리 보송은 람다과지 의 mRNA 의 첫 째 와 둘째 시스트론들을 쉽게 번역하는 데 반하여, 밀 싹의 리보솜은 첫 째 시스트론만을 번역한다 (Rosenber g와 Patt er son, 1979). 하류에 있 는 시스트론을 번역 할 수 없다는 것은 리보송이 내부에 있는 개시자리를 직접 인식하지 못할 뿐 아니라, 상류에 있는 시스트론을 다 통과한 다 음에도 둘째 시스트론에서의 재개시를 할 수 없다는 것을 의미한다. ::::z.. 러므로, 진핵세포의 리보송은 원핵세포의 리보송과는 달라서 그 활동이 제약되고 있는 것이 분명하다. 진핵세포의 리보솜이 mRNA 의 안쪽에 있는 자리에서 개시반응을 일 으킬 능력이 없다는 것은 진핵세포돌은, 원핵세포의 경우와는 달라서, 단 하나의 전사의 촉진유전자 뒤 에 여 러 유전자들을 군집 하여 한 벌의 단백질들의 합성을 조정할수없음을 의미한다 . 원핵세포가 사용하는 주 요한 조절장치인 다시스트론성 전사물들이 진핵세포에서는 기능을 가지 지 않는다 . 그렇다면 유전자 표현을 조정하기 위해서 진핵세포들은 무 슨 장치를 사용하는가? 진핵세포에 있어서는 다시스트론성 mRNA 대 신에 몇 개의 유전자들이 융합하여 〈다단백질〉을 생성시킨다. 트립토판
제 3 장 전령 RNA(mRNA) 의 구조와 기능 293
합성효소가 그 한 예이다 . E. col i에 있어서는 별개의 유전자들의 지령 을 받아서 생성되 는 a 하위단위체 (분자량 28,727) 와 ,8 하위단위체 (분 자량 42, 756) 들이 S. cerevis i a e 에 서 는 옹합되 어 서 분자 량이 약 76, 000 되는 두 가지 기능을 가진 한 개의 단백질운 형성시킨다 ( Zalk i n 과 Yanofs k y, 1982) . 여 러 기 능 을 가진 단 백 질 에 대 한 정 보률 가진 융합된 유 전자등의 그밖의 예는 Neurospo r a 에 있어서의 arom 유 전자 군집체 이 다. 이 융합 유전자 에는 여러 고리 방향족 화합물의 대사과 정에 관 여하 는 5 가지 의 효소 들이 들어 있 다. 또한, s. ccrct’ isia c 의 lEs 4 유진 자는 세 가치 기능을 가진 단백질에 대한 정보 를 가지고 있다. 아다도 가장 인상적인 예는 포유동물에 있어 서 의 지방산 합성호소(분 자장 2-1 0 ,000) 인데, 이 효소는 E. col i에 있어서는 7 가 지의 별개의 단백 질들로 분리 되어 있다 (Ma tti ck 등, 1981). 유전자 옹합 에 대한 합리적인 실명은 아 칙은 추축에 불과한 것이지단, 유전자 들 의 옹합은 진핵세포의 리보솜이 다시스트론성 전사물을 번역하지 못하는 결합을 보상하기 위한 것이라 고 불 수 있다. 3.2.2 AUG 가 유일한 개시 코든이다 원핵세포와는 달라서, 진핵세포의 리보솜둘은 전적으로 AUG 코돈에 서 번역의 개시를 일으킨다. 진핵세포의 리보솜들이 GUG 에서 개시를 일으키지 못한다는 것은 Ste w art 등 (1971) 이 처음으로 알았다. 점돌연 변 이 로 AUG 개 시 코돈을 GUG 개 시 코돈으로 변 이 시 키 면 S. cerev is iae 의 이소 -1- 시토크롬 c 유전자의 번역이 일어나지 않음울 관찰하였다 (그림 3-7). 여러 가지 효모의 돌연변이체들을 보다 더 광범위하게 분 석해 본 결과 AUG 이의의 다른 코돈에서 이소 -1- 시토크롬 c 의 번역 이 개시되는 것을 불 수 없었다 (Sherman 등, 1980). 최근까지 밝혀진 200 가지 이상의 진핵세포의 mRNA 들의 티보솜 결합자리들을 살려 보 면 AUG 코돈 이의의 코돈에서 개시가 일어나는 경우는 하나도 볼 수 없 다고 한다 (Kozak, 1983) . 그러 나 개 시 코돈이 GUG (Je ff re ys 등, 19 82 ; Proudfo o t 와 Mania t is , 1980) 와 AUA (Gi vo l 등, 1981) 로 돌 연 변 이 한 몇 개의 사이비유전자들이 포유동물에서 알려져 있다. 그러나 이러 한 돌연변이로 인해서 유전자들의 표현이 불가능하게 되었다고 결론짓 기는 시기상조인 것으로 생각한다. 왜냐하면, 사이비 유전자와 기능을
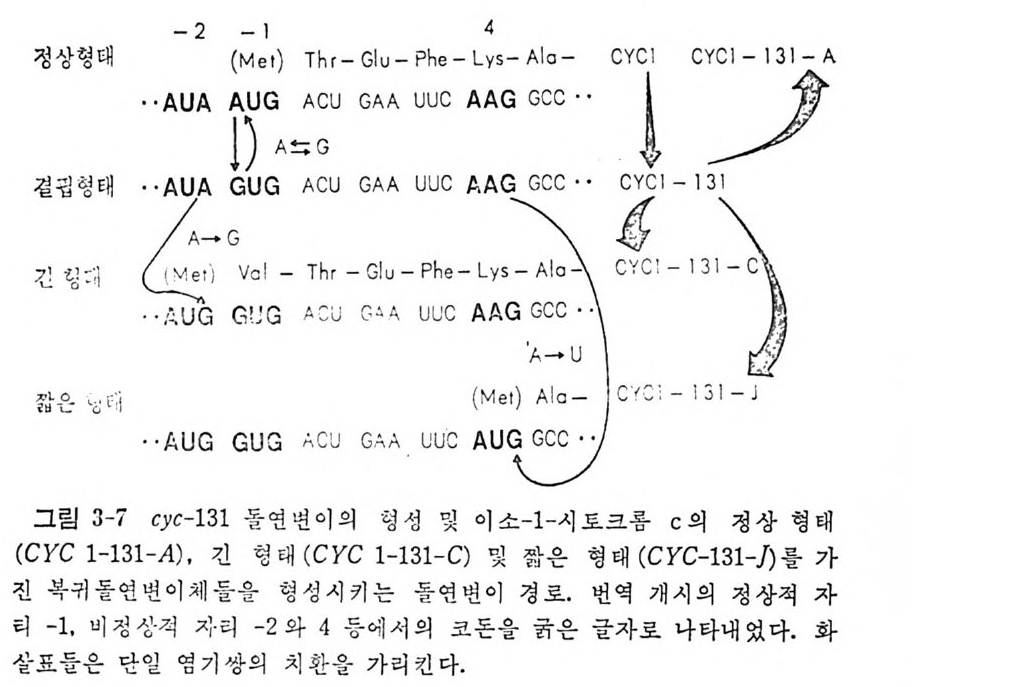 걸 립형 태 二- 2 l-\ 1; =A : U GAA UUC AA4 G GCC • • [CYC 1 -131 /
걸 립형 태 二- 2 l-\ 1; =A : U GAA UUC AA4 G GCC • • [CYC 1 -131 /
가진 유진자들 사이에는 일차구조에 있어서도 변화가 있기 때문이다• GUG 가 AUG 를 대신 할 수 없다는 것은 합성 울리고누클레오티드 또 는 풀리 누 클례 오티드 를 가지고 시 험관에서 한 실험으로도 확인이 되었 다 (Br own 과 Smi th, 1970 ; Kozak, 1981) . 생 쥐 의 복수 또는 밀 싹에 서 얻은 리보 솜둘은 GUG 가 대치되어 있을 때는 합성한 폴리누콜레오티드 들과 복합체를 형성하지 않는다. 그러나 이상한 것은 혼성 무세포계에 E. coli 의 티 보솜을 첨 가하면 효모의 Me t-記V A i AIe t 가 AUG 뿐 아니 라 GUG 를 개 시 코돈으로서 인식 한다 (RajB handary 와 Gosh, 1969) . 그렇 지만, 번역 장치의 성분들이 모두 진핵세포에서 유래된 것들일 경우에 는 번역의 개시 코돈으로 작용하는 것은 AUG 뿐이다. 3.2. 3 전사후 변형 진핵세포에서의 전사물은 핵으로부터 세포질로 수송되기 전에, 또는 수송되는 동안에 여러 가지 가공들을 받는다. 진핵세포에 있어서 성숙 한 m Ri\f A 를 생성시키는 데 관여하는 주된 변형은 5' 말단에 메틸화된
갓을 첨가하 는 일, 이어맞추기 및 3' 말단에 폴리 ( A) 꼬리를 첨가하 는 일 등이다 . 이러한 변형들의 하나가 결여된 mR NA 둘 이 예의적으로 존 재하기는 하지만 대다수의 진핵세포와 바루스의 mRNA 들은 위에서 말 한 세 가지 전사 후 변형을 받음으로써 일차 전사물로부터 성숙된 다. 가) 갓 갓은 mRNA 형성의 초기 단계에서 형성되며, 핵에서 형 성된 전사물을 세포질의 mRNA 로 가공하는 동안에 보존된다. 완전한 갓 구 조의 형성에는 4 가지 내지 6 가지의 효소들이 관여한다. 이것들을 아래 의 반응식들로 요약하였다. 1) pppN 1p N 2P· .. ➔ pppN ,pN 2 p· .. ➔ p1 또는 1') pN ,p N 2 p . .. + ATP ➔ ppN ,pN 2p ... + ADP 2) pppa G. + p;Jpa N ,pN _ 2 p . .. ➔ G_ '.5 'ipa p{ J p a 15 '1N 1 PN2p . . , + pp1 3) Ado:.-Iet + Gp ppN ,p N 2 p· .. ➔ m7G p ppN 1p N 2p · .. + Ado-S-homocys 4) Ado:-1et + rn1Gp ppN 1PN2p · .. ➔ rn7G p ppN 1mPN2 p· .. + Ado-S-homocy s 5) 만일 N,m=Am 이 면, Ado~1Ie t + rn7G p pprn 6A'p N 2p · .. ➔ rn7G p pprn 6A'p N 2 p· .. + Ado-S-homocy s 6) AdoAMdeot- S +-h ormn7Go cp yps p N 1'PN2p · .. ➔ 굶 G ppp N1mPN2mP··· +
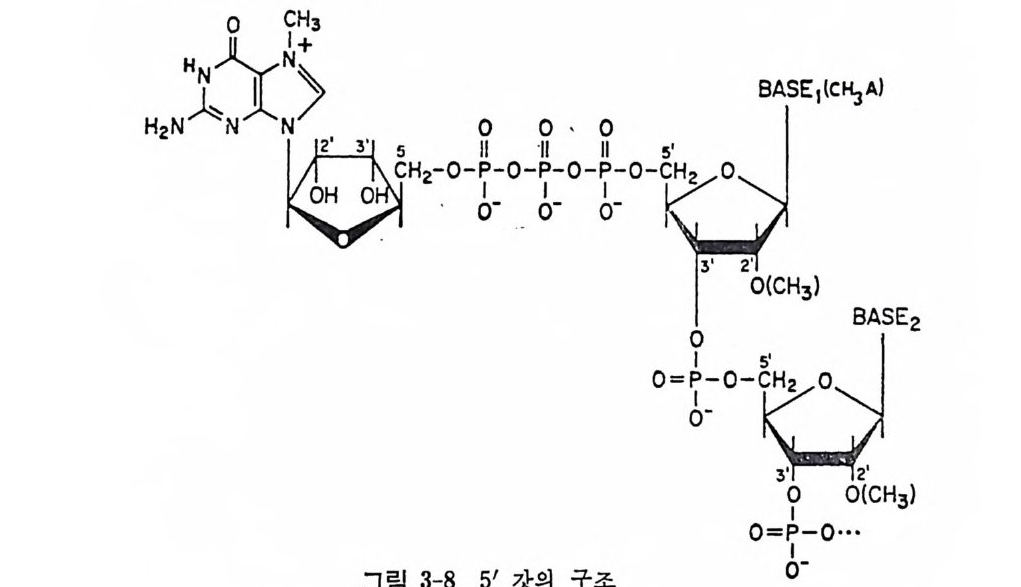 HN |_ N 。- --o 。 -)-。- - - 二i
HN |_ N 。- --o 。 -)-。- - - 二i
각 반응에 관여하는 효소는 (1) RNA 삼인산 탈인산가수분해효소, (1') RNA 5 ' -일인산 포스포키나아제, (2) mRNA 구아닐릴기 전달효소, (3) 7- 메 틸 구아노 신 매틸기 전달효소, (4) 및 (6) 2 ' -0- 메 틸기 전달효소, 1 에서 5 까지의 반 응들은 선구 mRNA 의 전사가 일어나는 동안 또는 그 것이 완성된 직후 핵 에서 일어난다. 반응 6 은 mRNA 가 폴리송으로 결 합된 다음에 세포질에 서 일어난다 ( Sha t k i n, 1976). 갓의 구조물 그림 3-8 에 주었다. 갓은 두 가지 기능을 가지고 있다. 첫째, 갓은 40S 하위단위체가 mRN A 에 결합하는 것을 활발하게 중진 시 킨 다 (Ba nerje e , 1980) . 둘째 , mRNA 를 안정 시 킨 다 (Furuic h i 둥, 19 77; Moy er , 1981) . 갓울 가지지 않 는 mRNA 가 기능을 가지는 예는 아 직 진 핵세포에서 는 알려져 있지 않다 . 그러나 갓이 없어도 기능을 발휘 하는 몇 가지 석물 및 동물 비루스의 mRNA 들이 있다. 자연적으로 갓 을 가지지 않는 바루 스의 mRNA 에 m 1 G 를 첨가하였을 때의 결과는 경 우에 따라서 다르다. 위성 담배 괴사 비루스 RNA 의 경우에는 갓을 침 가하여도 시험관 내에서의 번역에 별다른 영향을 미치지 않는다 (Sm it h 와 Clark, 1979). 그러나 진핵세포의 무세포 계에서 진핵세포의 리보솜 이 원핵세프의 mRNA 를 번역할 때와 같은 보다 인위적인 경우에 있어 서는 먼저 mRNA 에 갓을 붙임으로써 효과적인 번역을 일으킬 수 있다 (Pate r son 과 Rosenberg, 1979) . 자연 적 으로 갓울 가지 고 있 는 mRNA 로부터 m1G 를 제거하였을 때 생기는 결과는 쉽게 예견할 수 있다. 이 경우에는 언제나 번역의 효울이 크게 감소하지만, 어느 정도의 영향을 받는가는 무슨 mRNA 를 가지고 시험하였는지에 따라서, 또 무슨 무세 포 계에서 시험하였는지에 따라서 달라진다 (Lodd i sh 와 Rose, 1977; 'vV odnar-Fil lip o wi cz 등, 1978) . 메 틸 화된 갓이 번 역 의 효율에 미 치 는 영 향은, 갓 유사체가 무세포 계에서의 번역 효율에 미치는 방해효과를 분 석 함으르써 알 수 있 었 다 (Weber 등, 1978 ; Wi er in g a 등, 1981) . 말단 의 m1G 뿐 아니 라, 특히 고동진핵세포의 mRL\i A 에 있어서는 끝에서 두 번째와 세번째의 누클레오티드들, 즉, m7Gp ppN p N ' 구조에서 N 과 N' 이 메틸화되어 있는 경우가 혼히 있다 (Sha tki n , 1976). 이 위치들에서의 변 형이 방해되어도 생체 내에서의 mRL\ i A의 기능에는 거의 영향이 없다 {Dim o ck 와 Sto l tz f u s , 1979 ; Kaehler 등, 1979) . 나) 개입부분 많은 진핵세포의 유전자들은 단백질에 대한 유전정보를
내리는 연속부분이 하나 또는 그 이상의 개입부분들로 중단되어 있다. 중 단되지 않고 읽는 구조를 가진 성숙한 mRNA 가 생성되려연 일차 전사 물이 꼬아 이어져야 한다. 이어맞추기에 관해서는 다음의 문헌둘을 보라 Breath n ach 와 Chambon (19 81) , Lewi n (1980) , Sharp (19 8 1) , Padg e tt 등 (1984) , Hardy 등 (1984) . 여 기 서 는 최 근에 아데 노비 루 스의 후기 전 사물을 가지고 시험관에서 행한 실험결과에 기초하여 제안한 운가미식 이어맞추기 메카니즘을 그림 3-9 에 나타내었다 (Pad g e tt 등, 198 4). 진핵세포의 유전자의 경우 3' 쪽으로 있는, 정보 를 내리지 않는 부분 에 개입부분이 있는 예는 몇 개밖에 안되지만 (Lebow it z 와 \V eis s m ann , 등, 1979; Ng u en-Huu 등, 1979; Vi rt a n en 등, 1982) , 5' 독으 로 있 는
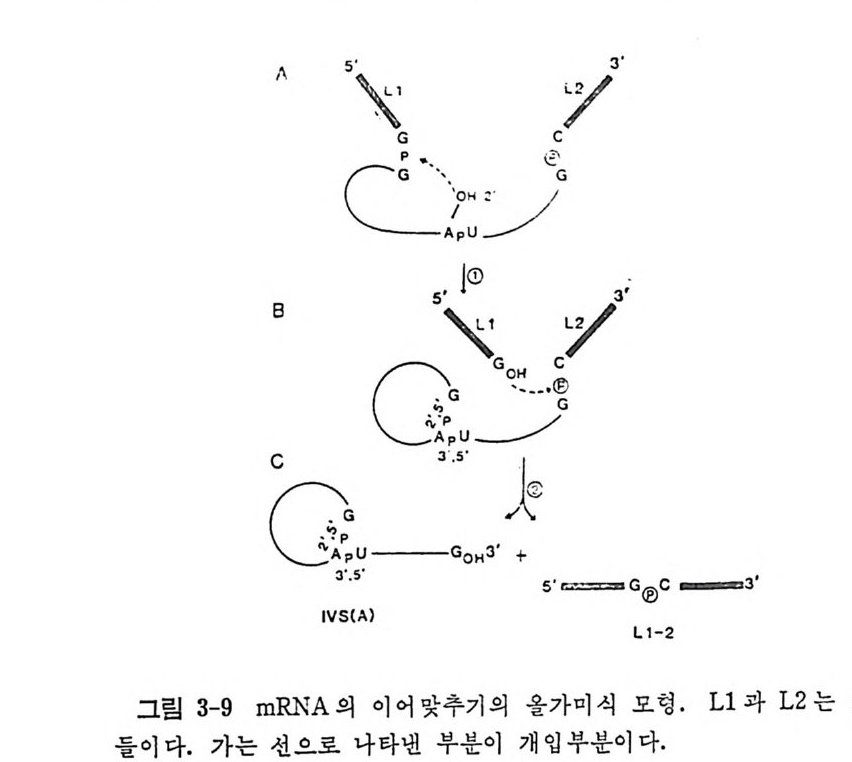 ^ \C/: /
^ \C/: /
정보를 내리지 않는 연속부분이 중단되어 있는 예는 비루스의 유전자 (Lebowi tz 와 \Veis s man, 1979 ; Wats o n 과 Vande vVoude, 1982 ; Zain 등, 1979) 와 세포성 유전자 (Amara 등, 1982; Catt er all 등, 1978; Fid d es 와 Goodman, 1981 ; Fornwald 등, 1982 ; Holmg r en 등, 1981 ; lVIeij lin k
동, 1981; Young 등, 198 1 ; Noda 등, 1982) 에서 많 이 불 수 있다. 유 전정보 를 내리는 부분에 있는 개입부분들을 일차 전사물로부터 제거하 지 않았을 경우에 번역 에 미치는 결과 는 자명한 일이지만, 5' 쪽에 있 는 번역되지 않는 부분의 개입부분을 제거하지 않았을 때 어떠한 결과 가 생길 것인지는 현재로서는 확실히 모르고 있다. 단백질 합성의 개시 메카니 즘 에 대하여 Kozak(1978) 가 제안한 주사 모형에 의하면, 번역되 지 안는 천 쪽 의 연속부분에 AUG 삼중체를 함유하고 있는 개입부분이 제거되지 않는다면 자연적인 개시자리에서보다는 개입부분에 있는 AUG 십중 제가 개 시 코돈으로 선택될 것이 예견된다(주사 모 형에 관해서는 제 4 강 에서 자세히 논의될 것 이다). DNA 구조을 재구성하여 시험한 결 과에 의 하면 , 쥐의 인슐린 II mRNA 에 있는 조그마한 개입부분의 일 부가 그 대로 남 아 있을 경우 , 하류 쪽으 로 있는 정상적인 AUG 코돈에 서의 개시가 전계되지는 않 았지만 철저하게 감소됨을 불 수 있었다 (Lo medic o 와 McAndrew, 198 2) . 아 데 노비 루스 mRNA 를 사용하면 보 다 더 자연적인 조건에서 시험 할 수 ’ 있다. 아데노비루스의 후기 전사물 들의 대다수는 i 선도 연속부분이라고 하는 부분이 이어맞추기로 제거되 는데, 가끔 이 i 선도 연속부분이 그대로 남아 있는 경우가 있다. i 선 도 연속부분을 보지하고 있는 mRNA 분자들에 있어서는 대다수의 후기 전사물에서 이용되는 하류 쪽의 AUG 삼중체에서가 아니라 i 선도 연속 부분에 들어 있는 AUG 삼중체에서 개시반응이 일어난다 (Akus j걸 r i와 Persson, 1981; Vi tra nen 등, 193 2). 이와 같이, 전사물의 5' 끝 부근에 서의 꼬아 잇기가 어떻게 일어났는가에 따라서 mRNA 의 기능아 크게 달라질 수 있다. 모두가 그러한 것은 아니지만, 대부분의 진핵세포의 세포질의 mRNA 들은 길이가 보통 50 내지 150 개의 누클레오티드로 되는 풀리 (A) 꼬리 몰 3' 말단예 부착하고 있다(폴리 (A) 연속부분의 합성과 대사에 관한 Brawerman(1981) 의 평론서를 참고하라). 번역에 있어서의 폴리 (A) 의 역할은 아칙 억측의 범주를 벗어나지 못하고 있다. 왜냐하면, 폴리 (A) 가 결여된 mRNA 가 여전히 번역되는 경우도 있기 때문이다 (Braw erman, 1981 ; Soreq 동, 1981, Zeevi 등, 1982) . 풀리 (A) 가 없 어 도 mRNA 들이 안정하기는 하지만, 풀리 (A) 가 있음으로써 약간의 mRl\lA 들의 안정도가 더 중전되는 것으로 보인다 (Huez 등, 1978; Huez 등, 1981 ; Zeevi 등, 1982) .
3. 2. 4 5' 끝에 있는 번역되지 않는 연속부분 진핵세포의 mRNA 둘의 5' 끝에 있는, 정보를 내리지 않는 연속부분 의 길이는 누클레오티드의 수가 3 에서 740 개까지 광범하게 다르다. MPCll 풀라스마시토마(골수종양의 일종) 제포에서 표현되는 카파 가벼 운 사슬에 대한 mRNA 는 갓과 개시 코돈 사이에 3 개의 누클레오티드 를 가지고 있다 (Kelle y 둥, 1982). 이와는 대조적으로, 풀리오비루스 RNA의 경우에는 5' 끝과 기능을 가진 AUG 코돈 사이에 740 개의 누 클레오티드가 있다 (K it amura 둥, 1981). 폴리오비루스의 5' 끝의 구조 는 대단히 색다르다(그림 3-10). 9 번에서 36 번까지 누클레티드의 연속 부분은 줄기-고리 구조를 하고 있다. 이것은 아마도 조절과 인식에 관 여할 것으로 생각되고 있다. 5' 말단의 우리딘은 게놈 단백질 VP g의 티 로신 찬기에 포스포디 에스테르 결합으로 연결되어 있다• 이 RNA 의 또 하나의 득칭은 기능을 가진 741 번 위치에 있는 개시 코돈 앞에 읽기 구
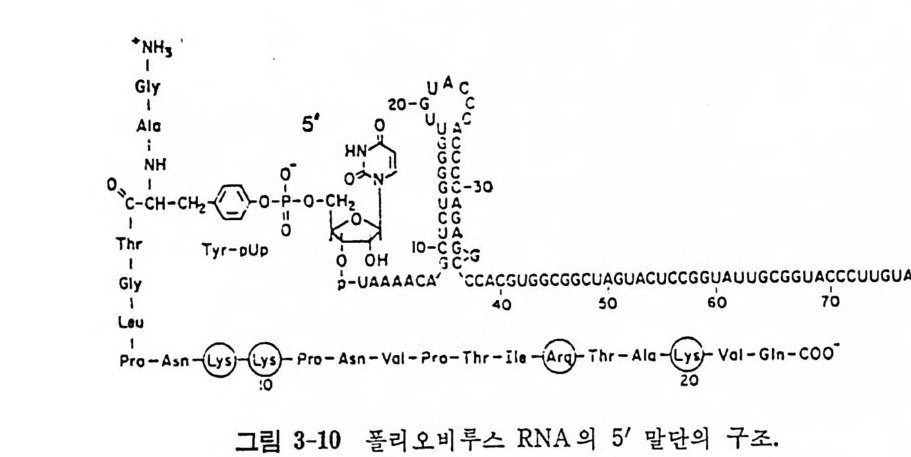 *GN,AH4_Cl-Y1IITOhA.'NrIHI CH-
*GN,AH4_Cl-Y1IITOhA.'NrIHI CH-
조와 상이 맞는 4 개의 AUG 삼중체들이 있는데 그들 뒤로는 얼마 멀지 않은 자리 에 종결 코돈들이 뒤 따르고 있다. 국단적으로 짧거나 기다란 번역되지 않는 연속부분들을 가진 mRNA 들은 드물며 보통은 비루스의 mRNA 들에서 볼 수 있다. 대부분의 세 포성 mRNA 둘은 5' 말단에 40 내지 80 개의 누클레오티드의 길이의 번 역되지 않는 연속부분울 가지고 있다 (Kozak, 1983) (표 3-3). 진핵세포
표 3-3 진핵세포의 전령 RNA 둘의 개시 자리의 목칭 전령 RNA 江근 접:성 鬪시작:한서다잇言기 汀 1 분麟 터 닭의 오 발 부민 65 그렇다 + ACCA .U. ·GG GC 닭의 콘 알부민 77 그렇다 AAC .. ·AA G 토끼의 a- 글로빈 37 그렇다 ACC···GUG 사람의 a- 글로빈 38 그렇다 ACC···GUG A 성취의 a- 알 부민 33 그렇다 ACC···G UG 토끼의 /3-알부민 54 그렇다 AGA· .. GUG 사람의 /3-알부민 51 그렇다 ACC· ··G U G 생 쥐 의 /3- 알 부탄 ( 주성 분) 53 그렇다 AUC···GUG 생쥐의 /3-알부민 ( 소성 분 ) 53 그렇다 AUC· .. GUG 닭의 /3-글로빈 ~52 그렇다 GCC· ··G UG 사람의 r- 글로빈 54 그렇다 GCC···GGU 누에의 피브로인 25 그렇다 AAG .. ·AGA 소쥐사닭의의의람 의프프프 레프레레 프 프프레 로로로프- 로 인부인 슐슐갑인린 숭싱린 린샘 호르몬 ~~~~516505083 그그그그렇렇렇렇다다다다 +++ AGAACUAACCCU . ·..·. ··· ··G·GG AC CCUCUCG 생쥐의 디히드로폴산 환 원 효 소 ~83 그렇다 AUC·· ·G UU SS굴.. 리pp11세11rr pp르 1111알r r aatt데 1 111s s 히 히히드 스스 -3몬돈- 인 HH산12 A 탈 수소효소 50~~ 1370내190지 그그그렇렇렇다다다 AAAAAuGcA .·· .··.·· GuG cCUuUU S. p11r p 11 ratu s 히 스몬 H2B ~79 그렇다 AUC···G C U S. p11r p 11r a t1 1 s 히 스돈 H3 ~56 그렇다 ACU···G CA S. p11r p 11 rat 11s 히 스톤 H4 ~68 그렇다 AUC···U C A P. mi lia r is ( 굳론 h22) 히 스톤 H1 ~39 그렇다 AAG .. ·ACU P. m i /i ar i s( 굳론 h22) 히 스돈 H2A ~75 그렇다 AUC···U CU P. m ili ar i s( 글론 h22) 히 스돈 H2B ~79 그렇다 ACC· .. P. m i li a l'i s( 굳론 h22) 히 스몬 H3 ~55 그렇다 ACC· ··G CA P. m il i ar i s( 글론 h22) 히 스돈 H4 ~62 그렇다 AUA .. ·UCA 사람의 섬유아세포 인터페론 ~73 그렇다 AAC .. ·ACC 사람의 백 혈 구 인터페론 ~57 그렇다 ACG· ··G C C Di ct y os t el i um 악단 클론 5 ~43 그렇다 AAA· ··G A C Dic t y o s t el i11 m 악틴, 클론 6 ~4 0 그렇다 AAA .. ·GA U Dic ty o st el iu m 악턴, 클론 8 ~4 2 그렇다 AAA···G A C
DDii cctt yy oo stet le il ui 1m1 1 1 1 디 스코이 던- I (L(\)V R 7) ~~7721 그그 렇렇다다 AAAAAA-··.·.U uCcUu 사람의 융모막성 생식생 자국호르몬 (a) ~51 그렇다 GCC···G A U 쥐의 프로락틴 ~52 그 렇다 ACC .. ·AAC 닭의 리소침 ~30 그렇다 AAA···AAG 생쥐의 a- 아밀라아제 (췌장의) 18 그 렇다 AAA···AAG II (타액의) 94 아니다 + AAA .. ·AAA 위성 담배 괴사 비루스 30 그 렇다 AAC· ··G CA 순무의 황색 비 루스-의 피 20 그 렇다 AAC· ··G A A 담베 모자이크 바루스 게놈 69 그 렇다 ACA· ··G CA 담배 모자이크 비루스 외피 단백질 10 그 렇다 .. \AC···U CU 브 롬 모자이크 비루스 RNA-4 ( 외피) 10 그 렇다 AUA… U CG 브롬 모자이 크 비 루스 RNA-3 92 그렇다 CCG· ··l ! CU 알팔과 모자이크 비 루스 RNA-4 (외 피 ) 37 그 렇다 AUC· ··A GU 레 오비 루스 (]2 단백 질 (s46) 19 그 렇 다 GU U… G CU 레 오비 루스 aNS 단백 질 (s45) 28 그 렇 다 ACU···G C U 레 오바 루스 u3 단백 질 (s54) 32 그렇다 GCA… G AG 레 오바 루스 µ1 단백 질 (m52) 30 그렇다 AAG···GGG 례 오비 루스 µNS 단백 질 (m44) 19 그 렇다 GUC···GCU 레 오비 루스 µ2 단백 질 (m36) 14 그렇다 GUC···GCU 레오비루스 큰 전령 14 그렇다 AGG· ··A A G 수포성 구내염 비루스 NS 단백질 11 그 렇 다 AUC···G AU 수포성 구내염 바루스 L 단백질 11 그렇다 AL 'C .. ·G. -\A 수포성 구내염 비두스 M 단백질 42 그렇다 AUC···AGU 수포성 구내염 비루스 G 단백질 30 그렇다 ACU···AAG 수포성 구내 염 비 루스 (India n a) N 단백 질 14 그렇다 AAA···U C U 수포성 구내 염 비 루스 (New J erse겁 ) ll. !J N 14 그렇다 AAA·00GCU 아데노비루스 헥손 단백질 질 240 그 렇다 + AAG .. ·GCU 아데노비루스 성유 단백질 203 그 렇다 + AAG···A AA 아데노비루스(후기) 폴리펜티드 lX 25 그렇다 GCC· ··AGC 아데 노비 루스 (초기 ) E7a mRNAs 62 그 렇다 AAA···A G A SV4 0 초기 mRNA 들 74 그렇다 AAG00·G..\U SV40 후기 16S mRNA (VPl) 239 아니다 + CUU···AAG S폴폴V리리4 0오오 후마마기 후 후1기기9 S 1169mSSR rmNnARR NN(VAAP ((2VV) PP2l)) 12220394783, ,1 1118551 0,, 그그아렇렇니다다다 +++/ - UAAACAACG ··.··.·· G·GGGCGUCA 폴리오마 후기 18S mRNA(VP3) 124260, 183, 그 렇 다 + AAU .. ·GCG
인인플플루루엔엔자자 ( A비/루ud스or i기 n/질72 ) 단H백A질 m RNA I 39~3494 그그 렇렇 다다 ++ 1AAACCG ··· ··AA AGGU 아데 노미 루 스 E76 부분. 15K 단백 질 13 그 텅 다 - CUC· ··G A G 루우 욱종 비루스 게놈 372 아 니다 - AGC… * AUG 코돈과 5' 말 단과의 근 접성은 m 7 G에 이 웃한 누쿨레오티드에서 개시 코돈의 A% 프합 시켜 계산하였다. 의 리보송들은 5' 말단에서 불과 세 개의 누쿨 레 오티드밖에 떨어지지 않 은 AUG 삼중체를 인식할 수 있기는 하지만, 이러한 mRNA 들에 있어 서는 번역의 개시는 5' 말단에서 가까운 AUG 코돈에 한정되는 것이 아 니 다. 예 를 들면 , m7Gp ppG AA !:._뜨~ CAU CAC ACC AGC AUG G 의 연속부분을 가진 임무노글로불린 mRNA 에 있어서 번역의 개시는 첫번 째와 두번째의 AUG 삼중체에서 일어난다 (Kelle y 등, 1982). 이와 같이, AUG 코돈 앞에 있는 연속부분이 너무 짧울 경우에는 번역의 정확성이 손상되는 것으로 보인다. 진핵세포의 리보솜이, m1G 에서 세 개보다적 은 누쿨레오티드만큼 떨어져 있는 AUG 코돈을 인식할 수 있는지 없 는지는 확실하지 않다. 예를 들면, Seml iki 삼림 비루스의 42S 게놈 RNA 는 m7Gp ppA UG 의 구조를 가지 고 있 으며 (Weng le r 등, 1979 ; Leh tov aara 등, 1982), 돼지의 가스트린의 mRNA 는 갓과 첫번째 AUG 코 돈 사아에 단 하나의 누클레오티드를 가지고 있다 (Yoo 등, 1982). Semlik i 삼립 비루스 RNA 와 가스트린 mRNA 의 두 경우에 있어서, Semlik i 삼림 비 루스 RNA: m7G ppp신:!9 ·GCG·GAU·UGU·GAC·AUA·CAC GAC • GCC ·AAA ·AGA ·UUU •U GU •U CC •A GC·UCC· UGC ·CAC •C UC •C GC· UAC· GCG •A GA • GAU •맘 포 •C CA ·CCC·ACG ·쓰::'..§-· GCC·… • • 가스트 린 mRNA : m;Gp ppG • A_U G • GAG •A AC •l .lliA •G GC • ACC •A GG •C CA • ACA·GCA • GCA ·CAC ·CUG·CCU •C CC ·AGC· UCU ·GCA· GUC•AAG ·쓰IQ· CAG····· .. 갓에 가까운 AUG 삼중체 뒤에는 읽기 구조와 상이 맞는 종결 코돈이 아주 가깝게 있으며, 하류 쪽으로 그리 멀지 않은 곳에 또 하나의 AUG 삼중체가 있다. 그러므로, 약간의 리보솜들은 갓에 가까운 AUG 코돈의 하류 쪽으로 있는 AUG 코돈에서 번역을 개시할 것이 확실하지만, 갓에 가까운 AUG 삼중체에서 개시가 일어나지 못한다고 증명되어 있지는 않 다. 설사 이 부분에서의 펩티드가 생긴다 해도 그 작은 펩티드를 검출한 다는 것은 매우 어려운 일일 것이다. 정반대가 되는 경우는 어떻게 되
는지 생각해 보자. 5' 끝 쪽에 있는 유전정보를 내리지 않는 연속부분 이 길면 번역이 중진된다는 견해를 가진 사람도 있지만, 아직 확실한 중 거는 없다 (Le g on, 1979). 5' 끝 쪽에 있는 번역되지 않는 부분이 길 경 우예는 번역에 해로운 효과를 나타낸다는 결과도 있다. 아마도 이러한 역효과는 길이 자체로 인해서 생기는 것이 아닌 것으로 생각된다. 예를 들면, 번역되지 않는 연속부분에 180 개의 누 클레 오티드 를 과외로 더 가 진 아데노바루스의 섬유 mRNA 는 시험관에서 그보다 더 짧 은 섬유 mRNA 와 꼭 같이 번역되는 경우도 있다 (Dunn 등, 1978). 그뿐 아니 라, Drosop hi l a 의 열 충격 mRNA 들은 111 개 내 지 253 개 의 누클레 오 티드를 가지는 매우 긴, 번역되지 않는 부분을 가지는 mRNA 인데, 이 열 충격 mRNA 둘은 그밖의 세포성 mRNA 들과 똑 갇온 효율로 번역 된 다 (Ing o lia 등, 1980 ; Ing o li a 와 Craig , 1981 ; Holmg r en 둥, 1981 ; H i cke y와 Weber, 1982). 5' 끝에 있는 번역되지 않는 연속부분의 길 이 그 자체가 번역의 효율을 저하시키는 것 같지는 않지만, 만일 번역 되지 않는 연속부분이 과도한 이차구조를 가지거나 AUG 삼중체들을 가 침으로써 리보솜이 하류 쪽으로 있는 진짜 개시 코돈에 잘 결합할 수 없 게 만든다면 번역에 해로운 효과를 주게 될 것이다. 예를 들면, 폴리오 비 루스 (Ki tam ura 등, 1981) , 루우 육종 비 루스 (Swanstr o m 등, 1982) , 원 숭이 비 루스 40 (Lebowi tz 와 Weis s mann, 1979) 및 Semlik i 삼 림 비 루스 (Leh t ovaara 등, 1982) 들에서의 길다란 번역되지 않는 5' 말단의 연속부분들에는 진짜 개시 코돈의 상류에 몇 개의 AUG 삼중체가 있다. 앞에서 말한 바와 같이 5' 쪽의 번역되지 않는 부분의 길이가 문제가 된 다면 이 비루스들의 mRNA 들은 효율적으로 번역되지 않을 것이다(적 어도 풀리오비루스와 Semlik i 삼림 비루스들의 경우는 실제로 그러하 다). 그리고 정상적인 5' 쪽의 번역되지 않는 연속부분을 가지지 않은 비표준형의 전사물들이 〈표준형태〉의 mRNA 들보다 더 효율적으로 번 역되어야 할 것이다. 그런데, 원숭이 비루스 40 의 후기 mRNA 들은 기 다란 번역되지 않는 연속부분이 있음에도 불구하고 효율적으로 번역됨 이 밝혀 졌다 (Cep ko 등, 1981) . 진핵세포의 rnRNA 둘의 5' 쪽에 있는 번역되지 않는 부분들은 그들 의 길이뿐 아니라 결합순서에 있어서도 상당한 차이를 가지고 있다. 서 로 유연관계에 있는 한 쌍의 진핵세포의 유전자들에서 조차도, 유전정 보를 내리는 연속부분들은 밀집하게 찰 보존되어 있지만, 유전정보를 내
리지 않는 5' 쪽의 연속부분들은 그 성질들어 매우 다른 것이 보통이다 (Montg o mery, 1980; Chin 등, 1981; Choe 등 , 1982; Karim 과 Ric h - ards, 1982). 그뿐 아니 라, 5' 쪽의 정 보를 내 리 지 않는 연속부분늘이 결실, 삽입, 또는 짝바꿈 동으로 달라지더라도 주어진 mR NA 의 번역 능은 교란되지 않는 것으로 보인다 (Kozak, 1981; Kozak, 1982) . 5' 쪽 의 번역되지 않는 연속부분들의 전체적인 이질성이 놀랄 정도로 콤에도 불구하고 다음과 같은 몇 가지 특징들이 보존되어 있음을 볼 수 있 다. (1) 진핵세포의 mR NA 둘 의 두드러 진 특징은 기능을 가전 코돈 앞에 는 보통 또 다른 AUG 삼중채가 없다는 것 이다. 현재까지 결합순서가 결정된 200 종의 진핵세포의 mRNA 들 중에서 기능을 가진 개시 자리 의 상류에 예의적으로 AUG 삼중체를 가진 것들은 18 가지뿐이다. 물 론 박테리아의 mRNA 들에서는 이 러한 경향을 볼 수 없 다. (2) 기능을 가진 개시 코돈둘은 mRNA 들에 있어서 어느 정도의 제 약을 받고 있는 연속부분 안에서 일어난다. AUG 개시 코돈둘 측면에 있는 염기들의 연속부분을 예비적으로 조사한 바에 의하면 두 자리에서 염기들이 보존되어 있음을 알 수 있다. 즉, AUG 앞쪽으로 3 번째 염기 (-3 번 염기)는 푸린(혼히 A) 이고, AUG 코돈 바로 뒤에는 푸린(흔히 표 3-4 진핵세포의 mRNA 들에 있어서의 AUG 삼중체 주위의 연속부분 아래와 같은 연속부분을 가진 mRNA 의 수 연속부분 a ;| 시능 을코 돈가진 I 깁능류 을쪽 의가 지A 지 U G않 T。 I 내AU 부G에 코있돈 는 ANN AUG G 74 1b 25 ANN AUG A 38 。 26 ANN AUG Y 29 。 27 GNN AUG G 18 2c 39 GNN AUG A 4 。 18 GNN AUG Y 4 4 38 YNN AUG G 11 4 25 YNN AUG A 1 7 23 YNN AUG Y 1 14 47 a) y는 괴리미딘이다. b) 이 연속부분을 축면에 가진 AUG 코돈은 루우 육종 비루스의 src mRNA 에 있는 기 능을 가진 개시 코돈 상류에 있다. c) 이 연속부분은 원숭이 비무스 40 의 후기 16S mRNA 에 있는 VPl 의 개시 코돈 상류 에 두 번 일어난다 .
G) 이 있다 (Kozak, 1982) (표 3-3 및 표 3-4 를 보라) . 표 3-4 는 -3 번 위치와 +4 번 위치의 누클레오티드에 대한 개시 및 비개시 ACG 삼중체 둘의 분포를 보여 준다. 대부분의 기능을 가진 개시 코돈둘은 이 표에 열 거한 보기들 중 위의 다섯 가지 연속부분들에 속한다. 다시 말하면, 개 시 코돈 주위 의 연 속부분은 ANN AUG N 또는 GNN AUG R 구조가 우 세하다 (R 는 푸린이다). 다른 한편, 위에서 말한 예외적인 mRNA 들의 5' 쪽의 번역되지 않는 연속부분에서 일어나는 기능을 가지지 않은 AUG 삼중체는 표 3-4 의 아래쪽으로 있는 네 종류에 속한다. 바꾸어 말하 면, 극소수의 진핵세포의 mRNA 에 있어서 기능을 가진 개시 자리의 상 류에 AUG 삼중체가 존재하지만, 상류에 있는 기능을 가지지 않는 AUG 삼중체 주위의 연속부분은 기능을 가진 개시 코돈 측 면에 있는 연속부 분과 다르다. mRNA 의 안쪽으로 있는 AUG 코돈들은 측면에 있는 누 클레오티드에 대해서 다소 마구잡이로 분포되어 있음을 알 수 있다. (3) 효모의 여러 가지 mRNA 둘의 개시 코돈으로부터 약 10 개의 누 클레 오티 드 정 도 상류 쪽으로 CACACA 연 속부분이 존재 한다 (Zalkin 과 Yanofs k y, 1982 ; Dobson 등, 1982) . S. cerevis ia e 의 어 떤 이 소 -1- 시 토 크롬 c 변종들을 분석한 결과에 근거하여, CACACA 요소가 효모의 리 보솜에 대한 인식 자리가 될 것이라고 가정한 사람도 있었다 (S ti les 동, 1981) . 그러 나 이 요소를 가지 지 않은 그밖의 효모의 유전자들과 고동 진핵세포의 유전자들을 S. cerevis iae 세포 안으로 도입하여도 그들은 효 율적으로 번역된다. 따라서 CACACA 요소의 중요성 에 대해서는 아직 은 의 심 의 여 지 가 있다 (Va lenzuela 등, 1982) . (4) 효모와 정균류들과 같은 하등진핵세포의 mRNA 에 있어서는 5' 쪽의 번역되지 않는 부분에 AU 를 많이 가지고 있는 것이 목징이다 (Gallwi tz 등, 1981 ; McKeown 과 Fir t e l , 1981 ; Poole 등, 1981 ; Ben- netz e n 과 Hall, 1982; Choe .등 , 1982). 약간의 선도 연속부분에 있어 서는 AU 함량이 90% 가 넘는다. 고동진핵세포들의 mRNA 들에 있어서 는 5' 쪽의 정보를 내리지 않는 부분의 조성이 어느 한쪽으로 기울어지 는 일이 덜하지만 G 찬기의 함량은 눈에 띄게 적다 (Kozak, 1981). 개 시 코돈 앞에 있는 G 함량이 적은 부분이 무슨 의미를 가지는지는 아 직 모른다. 이상하게도 그것은 원핵세포에서의 리보솜의 결합자리의 성 질을 연상시킨다. (5) m7G 갓에 인접한 연속부분들은 적어도 몇 가지 mRL~A 들에서는
보존되어 있다. 끝에서 두번째의 누클레오티드, 즉, m1G pp ;,N 에서 N 은 거의 언제나 푸린이며 대개의 경우 A 이다 (Baker 와 Zif f, 1981; Breat- hnach 와 Chambon, 1981 ; Shenk, 1981) . 그러 나, 예 외 적 으로 피 리 미 던으로 시 작하는 mRNA 들도 있다 (Gallwi tz 등, 1981; Muskavit ch 와 Rog ne ss, 1982). 유연관계를 가진 한 벌의 mRNA 들의 5' 말단 또는 말단 부근에서 더 광범한 상동성을 볼 수 있는 m Rt'.J A 들도 가끔 있다. 예 룹 들면 , Str o ng ylo centr o tu s pur pu r atu s 의 5 가지 의 히 스몬 mRNA 둘 은 모두 펜타누클레 오티드 AUUCR 로 시작하며, 그 뒤의 결합순서는 다양하게 달라진다 (Sures 등, 1980). 모든 포유동물의 글로빈의 8- 사슬 유전 자 들은 갓의 하류 쪽 으로 7 개 의 누클레 오티 드를 지 나서 CUUYUG 연 속부분이 존재 한다 (Ef st r a ti ad is 등, 1980) . 누예 나방의 장막 ( §斜模 ) 유전자 들은 모두 5' 말단에 공통되는 연속부분 RUCAUU 가 존재하며, Drosop h i la 의 각피 단백 질들에 대한 mRNA 들에서는 매우 비슷한 연속 부분 AUCAGU 가 있다 (Sn y der 등, 1982). 최근의 연구결과에 의하여 약간의 mR~A 들의 갓 자리 부근의 보존된 연속부분이 전사에 대한 촉 진유전자의 일부분을 이루고 있음이 알려졌다 (Talk i n gt on 과 Leder, 1982) . 3. 2. 5 3' 끝에 있는 번역 되지 않는 연속부분 번역의 종결 코돈과 폴리 (A) 꼬리 사이에는 유전청보를 내리지 않는 이질중합체 부분이 있는데, 어떤 mRNA 들의 경우에는 그길이가 1,000 개의 누클레오티드로 되는 경우도 있지만 보통은 50 내지 150 개의 누 클레오티드로 되어 있다 (Kak i dan i 등, 1982). 유연관계를 가진 유전자 들을 비교해 보면, 3' 쪽의 정보를 내리지 않는 연속부분들은 몇 가지 특별한 예의를 제의하고는 청보를 내리는 연속부분들에 비하면 훨씬 덜 보존되 어 있 다 (Efs tra ti ad is 등, 1980 ; Mi ch elson 과 Orki n, 1980 ; Mont go mery 등, 1980 ; Jag o d zin s ki 등, 1980 ; Poole 둥, 1981 ; Shani 등, 1981; Hennin g h ausen 등, 1982). 더 놀라운 것은 서로 다른 유전자들 의 3' 끝의 정보를 내리지 않는 연속부분이 상이한 것은 말할 나위 없 지만, 한 가지 단백질을 합성시키는 정보를 가진 mRNA 집단에 있어서 3' 끝의 정보를 내리지 않는 연속부분들이 이질적이라는 사실이다. 예 를 들면, 생쥐의 세포에서의 디히드로폴산 환원효소에 대한 mRNA 집
단을 적어도 네 가지 크기의 부류로 분획할 수 있는데, 그 안 쪽의 번 역되지 않는 부분들의 길이가 80 내지 930 개의 누클레오티드로 되어 있 다 (Se t zer 등, 1980). 길이가 다른 안 쪽의 번역되지 않는 연속부분들의 역할이 무엇인지는 아직 찰 모르고 있다. 디히드로폴산 환 원효소의 mRNA 집단의 각각은 동등한 효율로 번역되는 것으로 생각되고 있다. 3.3 세포소기관의 mRNA 여기서 세포소기관의 mRNA 라고 하는 것은 풀리솜을 형성하고 있는 전사뭉울 의 미 한다• 그러 나 세포소기 관의 mRNA 라고 추 측 되 는 mRNA 들이 지금까지 정제된 적도 없고, 그들을 사용하여 시험관 내에서의 번 역실험을 한 것도 없기 때문에, 그들의 기능은 앞으로 실험 적 으로 더 조사되어야 할 문제이다. Hela 세 포의 미 토콘드리 아의 추측상의 mRNA 들에 는 갓이 없 다 (Gro- hmann, 1978). 그들은 3' 말단의 폴리 (A) 꼬리 를 가지고 있다. 이 풀 리 (A) 꼬리 에 상응하는 유전정 보는 DNA 에 들어 있지 않다. 미 토콘드 리아에서는 mRNA 들과 rRNA 들이 모두 울리고아데닐화되어 있는 것 으로 미루어 보아, 아데닐화는 mRNA 기능에 필수적인 것이라기보다 는 전사의 종결 메카니즘의 자연적인 단계일 것으로 생각된다. 번역의 종결 코돈둘이 포유동물의 미토콘드리아의 유전자에 들어 있지 않는 경 우가 많다는 것은 주목할 만한 일이다. 미토콘드리아에서의 종결 코돈 UAA 는 폴리 (A) 꼬리가 첨가됨으로써 생기게 된다 (Anderson 등, 19 81 ; Anderson 등, 1982) . 포유동물의 미 토콘드리 아의 mRNA 둘은 번 역의 개시 메카니즘과 관계된 두 가지 색다른 특징을 가지고 있다. 첫 째로, 개시 코돈은 표준형의 AUG 대신에 흔히 AUA 또는 AUU 이다 (Bib b 동, 1981 ; Monta y a 등, 1981) . 둘째 로, AUN 개 시 코돈은 전 사 물의 바로 5' 끝에 또는 5' 끝에서 매우 가까운 곳에 있다 (A tt ard i 등, 1982) . 몇 가지 예 외 를 매 고, 포유동물의 미 토콘드리 아의 대 부분의 mRNA 둘은 단일시스트론성이다. 유전자에 상응하는 크기의 mRNA 둘 은 하나의 다시스트론성 선구체에서 절단에 의해 유도된다 (A tt ard i 등 1982). 효모의 미토콘드리아 mRl i A 둘은 몇 가지 중요한 점에 있어서 포유
동물의 미 토콘드리 아 mRNA 들과 다르다. 지 금까지 누쿨레 오티 드 결 합 순서가 결정된 효모의 유전자들을 보면 개시 코돈둘은 모두 AUG 이다. Aspe r gi llu s 미토콘드리아도 효모의 경우와 같은 규칙을 따르고 있지만, 예의가 하나 있다. 즉, 시토크 롬 산화효소의 하위단위체 3 의 유전자에 서 는 개 시 코돈이 GUG 이 다 (Netz k er 등, 1982 ) . 단백 질 에 대 한 유전 정 보 룹 내리는 연속부분 앞쪽으로 번역되지 않는, AU 가 풍부한 연속부 분이 있는데, 그 길이는 54 개 내지 940 개의 누클레오티드로 이루어져 있 다 (Co ruzzi 둥, 1981 ; Li 등, 1981) . 이 러 한 목징 은 하등진 핵 세 포들 의 경우에서 도 불 수 있었다 (3.2.4 절을 보라). 효모의 미토콘드리아 mRNA 가 지금까지 알려진 것 중에서 제일 긴, 5' 쪽의 번역되지 않는 연속부분을 가지고 있는 데 반하여 포유동물의 미토콘드리아의 mRNA 는 제일 짧은 것을 가지고 있다는 것은 매우 이상한 일이다. 효모와 곰 광이로부터의 미토콘드리아 mRNA 에 있는 5' 쪽의 번역되지 않는 부분 예 비기능성 AUG 삼중체가 존재하는 것은 드문 일이 아니다 (NIac i no 와 Tzag o loff , 1979; Brown i n g과 RajB h andary, 1932). 3' 말단에 있는 울 리그 (A) 는 약 8 개의 누클레오티드로 된 길이인데, 이 연속부분이 전사 된 것인지 또는 전사 후에 첨가된 것인지는 아직 참 모른다. 효모 미토 콘드리아의 약간의 유전자들은 개입부분으로 중단되어 있다. 이 개입부 분은 보기드문 꼬아 있기 메카니즘으로 제거된다. 죽, 개입부분 자체가 내리는 유전정보로 합성된 단백질이 개입부분을 제거하면서 양쪽으로 있는 표현부분들을 꼬아 잇는다. 그래서 개입부분 자체의 정보로 합성 되 는 단백 질 을 RNA 성 숙효소라고 도 한다 (Lewi n, 1980) . 엽록체의 mRNA 둘의 구조에 관해서는 거의 알려진 것이 없다. 영록 체의 mRNA 들은 3' 말단의 폴리 (A) 꼬리가 없으며, 아마도 5' 말단의 갓도 없는 것으로 생각되고 있다 (Sa g her 등, 1976). 지금까지 알려진 것 으로서 는 Eug l ena grac £ lis 엽 록체 의 리 불로오스 -1, 5- 이 인 산 카르복시 화효소의 큰 하위단위체에 대한 유전자가 개입부분을 함유하고 있다 (St ieg l e r 등, 1982) . 그러 나, 이 것 은 매 우 드문 보기 일 것 으로 생 각된 다. 엽록체는 여러 가지 성질들에 있어서 원핵세포와 아주 비슷함에도 불구하고 엽록체에서 이어맞추기가 일어난다는것은 매우기이한 일이다. 오늘날까지 연구된 엽록체의 mRNA 둘을 보면 5' 및 3' 말단에 정보를 내티지 않는 기다란 연속부분들을 가지고 있다. 번역의 개시의 관점에 서 아주 재미있는 것은 AUG 개시 코돈 앞쪽으로 16S rRNA 의 3' 말
단의 연속부분에 상보적인 푸린 염기가 많이 있는 연속부분이 있다는 것 이 다 (McInto s h 등, 1980 ; Zurawski 동, 1981 ; Krebbers 동, 1982) . 이러한 사실은 박테리아에 있어서의 개시 작용에 대하여 제안한 Shin e - Dal g arno 의 메카니즘이 엽록체에서도 일어날 것임을 암시해 준다. 3.4 mRNA 의 구조의 변형으로 생기는 결과 mRNA 의 구조를 교란시 킵 으로써 mRNA 의 리 보 솜 과의 상호작용이 달라지는 경우가 가끔 있다. 표 3-5 는 여러 가지 조작으로 mRNA 의 표 3-5 변형된 mRNA 구조가 리보솜 결합에 미 치 는 영 향 mRNA 구조의 변형 麟 서: 삽g ;ft]): 영리~t i 실麟广\:설\ 환상화 영향 없음 결합이 일어나지 않음 변성 리보송은 진짜 개시 자 mRNA 의 내부에 있는 리 이외에 가짜 개시 자리 자리에 리보솜이 칙집 결 제한 철단 |! 에자서연도적 개인시 를형 태일 으구킴성 으르 합가하는짜 일개은시 전자혀리 들없을음 많 보통은 제꺼져 있던 몇 개 이 활성화시킵 의 자리들만이 활성화됨 광범한 절단 (T1 또는 췌 16S rRNA 의 3' 끝에 상 18S rRNA 에 상보적 인 장의 리보핵산 가수분해효보적인 몇 개의 울리고누 올리고누클레오티드들의 소를 사용한 제 한 가수분 클레 오티 드들이 리 보솜에 선택적인 결합이 전혀 없 해) 정량적으로 결합함 다. 무의미 상중체들의 도입 무의미 코돈의 근방에 있 무의미 코돈의 하류 쪽 으로, 합성되는 단백질의 는 재개시 자리들이 활성 에 있는 참재적 개시 자리 종결이 너무 이르게 끝나화됨 둘의 활성화가 일어나지 게 할 때 않음 구조를 교란시켰을 때의 결과들을 요약한 것이다. 이 결과들에 대해서 는 단백질 합성의 개시에 관해서 논의할 때 (제 4 장) 다시 다루기로 하 겠다.
* 참고문현 Adhy a, S. , Gott es man, M. (19 78) , An11. Rev. Bi oc hem. 47, 967. Akusja r v i , G. , Persson, H. (19 81) , Natu r e 292 420. Amara, S. , Jon as, V. Rosenfe l d M. G. , Ong , E. S. , Evans, R. M. (19 82) , Natu r e 298, 240 . Anderso n , S., Ba nk ie r , A., Barrell, B.G ., de Bruij n, M., Coulson, A., Drouin , J., Ep er on, I., Ni er lic h , D. , Roe, B., Sang e r, F., Schreie r , P., Smi th, A. Sta d en, R. Young , I. (1981 ) , Natu r e 290, 457. Anderso n, S., de Bruij n, M., Coulso n , A., Ep er on, I., Sang er , F., Young , I. (19 82 ) , J Mo!. Bi ol . 156, 683. At ki n s , J.F . , Ste i t z, J. A. , Anderson, C. W. , Model, P. (1979) , Ce ll 18, 247. At tar di, G., Canta t o r e, P., Chomy n , A., Crews, S., Felfa n d, R., :tl'Ie rkel, C. Mont oy a , J., Oja l a, D. (19 82) , Mi toc ho11dria l ge nes (Ed. , P. Slonim ski) , p. 51, Cold Sp ri n g Harbor Laborat o r y, Cold Sp ri n g Harbor, New York. Ba ker , C. , Zif f, E. (19 8 1 ) , ]. Mo!. Bi ol. 149, 189. Ba ne rje e , A. K. (19 80) , Mi cr o bia l. Re v. 44, 175. Bennetz e n , J., Ha ll , B. (19 8 2) , ]. Bi ol . Che m. 257, 3018. Bib b , M. , Van Ett en , R. , Wrig h t, C. , Walberg, M. , Clay to n , D. (1981) , Cell 26, 167. Brawennan, G. (19 8 1) , Crit . R e v. Bi oc l1e m . 10, 138. Bre: it h nac h , R. , Chambon, P. , (19 81) , An11. Rev. Bi oc l1em . 50, 349 . Brow n , J. C. , Smi th, A. E. (19 70) , Na tu r e 226, 610. Brownin g , K. S. , RajB handa ry , U.L. (19 82) , ]. Bio l. Chem. 257, 5253. Ca tt er all , J.F ., O'M all ey , B.W ., Roberts o n , M.A., Sta d en, R., Tanaka, Y., Brownlee, G.G. (1978) , Natu r e 257, 510. Cep ko , C.L., Hansen, U. Handa, H. Sharp, P.A . (1981), Mo!. Ce ll. Bi ol . I, 919. Chin , W., Kronenberg, H., Dee, P., Maloof, F., Jab ener, J. (1981), Proc. Natl . Acad. Sci. 78, 5329. Choe, J., K olodrubetz , K., Grunste i n , M. (1982), Proc. Natl . Acad. Sci. 79, 1484. Chris t i e, G. E . , Platt , T. (1980) , J Mo!. Bi ol . 142, 519. Clark, B.F . C . , Marker, K.A . (1966), ]. Mo!. Bi ol . 17, 394. Coruzzi, G., Bonit z, S., Thalenfe l d, B., Tzag o loff , A. (1981), ]. Bi ol . Clzem. 256, 12780. Dim ocl< , K. , Sto l tz f u s (19 79) . J Bi ol . Chem. 254, 5591 . Dobson,~ 1. J ., Tuit e , M. Roberts , N., Ki ng sm an, A., Ki ng sm an, S., Perkin s ,
R. , Conroy, S. , Bunbar, B. , Foth e rgi ll, L. A. (1982) , Nucleic Acid s Res. IO, 2625. Dunn, A.R ., Math e ws, M.B ., Chow, L.T ., Sambrook, J., Keller, W. (1978), Cell 15, 511 . Dunn, J.J.. Stu d ie r , F.W . (1975) , ]. Mol. Bi ol . 99, 487. Dunn, R. , l'vlc Coy , J. , Sim sek , M. , Maju m dar, A. , Chang , S. H. , Ra jB h andary , U.L . , Khorana, H. G. (1981 ) , Proc. Natl . Acad. Sci. 78, 6744. Efs t r a ti ad is , A. , Posakony , J. W. , Mania t i s, T. , Lawn, R. M. , O'C o nnell, C. Sp ri t z, R.A . , DeRi el , J.K., Forge t, B.G., Weis s man, S.M., Slig h to m , J.L . , Blechl, A. E. , Smi thi e s , 0., Baral l e, F.E. , Shoulde rs , C.C ., ProudJo o t, N.J. (1980) Cell 21, 653. Fid d es, J.C ., Goodman, H.M. (19 81), ]. Mo/. Ap pl. G(/ il et . 1, 3. Fornwald, J.A ., Kunc io, G. Peng , I., Ordah l, C. (19 82), Nucleic Acid s Res. 10, 3!36 1. Furuic h i, Y., LaFia n dra, A., Shatk i n , A.J. (1977) , Natu r e 266, 235. Gallwi tz , D. , Perrin , F. , Seid e l, R. (1981) , Nu clei c Acid s Re s. 9, 6339. Gi vo l, D. , Zakut, R., Eff ro n, IC, Rechavi, G., Ram, D., Cohen, J.B . (19 81), Natu r e 292, 426. Godson, G. N ., Barrell, B.G. , Sta d en, R. Fid d es, J.C . (1978), Natu r e 276, 236. Gold, L., Prib n ow, D., Schneid e r, T. Shin e dlin g , S., Sin g e r, B.S ., Sto r mo, G. (1981) , A11m1. Rev. Mi cr obia l . 35, 365. Gop a lakrish na, Y., Lang le y , D., Sarkar, N. (1981), Nucleic Acid s Re s. 9, 3545. Gop a lakris h na, Y. , Sarkar, N. (1982) , Bi oc hemi st r y 21, 2724. Grohmann, K., Amalric , F. Crews, S., At tar di, G. (1978), Nucleic Acid s Res. 5, 637. Hardy , S.F., Grabowski, P.J ., Padg e tt , R.A., Sharp, P.A. (1984) , Na tu r e 308, 375. Hennig h ausen, L. , Sip pe l, A. , Hobbs, A, Rosen, J. , Nucleic Acid s Res. 10, 3733. Hi ck ey, E.D., Weber, L.A . (1982), Bi oc hemi st r y 21, 1513. Holmg ren , R., Corces, V., Morim oto , R., Blackman, R., Meselson, M. (1981). Proc, Natl . Acad. Sci. 78, 3775. Huez, G., Bruck, C., Cleute r , Y. (1981), Proc. Natl . Sci. 78, 908. Huez, G. , Marbaix , G. , Galjw i tz, D. , Wein b erg, E. , Devos, R. , Hubert, E Cleute r , Y, (1978) , Natt tre 271, 572. Ing o lia , T.D., Craig , E.A . (1981), Nucleic Acid s Res. 9, 1627. lng o li a, T.D., Craig , E.A ., McCarth y , J. (1980), Cell 21, 669. Jag o dzin s ki , L., Sarge nt, T. , Yang , M., Glackin , C., Bonner, J. (1981), Pro Natl . Acad. Sci. 78, 3521 .
Jay , G. , Nomura, S. , Anderson, C. \V. , Khoury, G. (19 8 1) , Natu r e 291, 346_. Jef f re ys , A.J. , Barrie , P. Harris , S. Fawcett , D. , Nug ~n t , Z. (19 82 ), ]. Mo/. Bio l . 156, 487 . Kaeh ler, M. , Coward, J., Rott m an, F. (19 79) , Nucleic Acid s Re s. 6, 1161 . Kakid a ni, H., Furuta n i, Y., Takahashi, H. Noda, M., Morim oto , Y. Hi ro se, T., Asai, M., Ina ya m a, S., Nakan is h i , S., Numa, S. (19 82) , Na tu r e 298, 245. Karin , i\J. , Ric h a rds, R. I . (19 82) , Nucleic Acid s Re s. 10, 3165. Ke ll ey , D., Colecloug h , Perry , R.P . (19 82) , Cell 29, 681 . Ki tam ura, N., Semler, B., Roth berg, P., Larsen , G., Adler, C., Dorner, A., Emi ni , E., Hanecak, R., Lee, J., van der Werf, S., A nderson, C.W., W im mer E. (19 8 1 ) , Natu r e 2lll, 547. Kozak, M. (19 7 8) , Ce ll, 15, 1109. Kozak, M. (19 81) , Nucleic Acid s Re s. 9, 5233. Kozak, ?\L (19 82) , Bi oc lzem. Soc. Sy m p . 47, 113. Kozak, M. (19 83) , Mi cr obi a l . Rev. 47, 1. Krebbers, E. T ., Larrin u a, I.lVI. , McInto s h, L., Bog o rad, L. (1982), Nucleic Acid s Re s. 10, 4985. Lebow i tz, P. , Weis s man, S. M . (1979) , Curr. Top. Mi cr obio l . lmmt m ol. 87, 43. Leg on , S. (19 79) , ]. Mo/. Bi o! . 134, 219. Lehto v a ara, P. , Soderlund, H. Keranen, S. Pett er sson, R. , Kaaria i n e n, L. (19 82) . Lewi n, B. (1980 ), Cell 22, 645. Li, M. , Tzag ol off , A. , Underbrin k -Ly on , K. Marti n, N. C. (1981) , ]. Bi ol . Che m . 257, 5921 . Lodis h , H.F., Rose , J.K . (1977), ]. Bi ol . Clzem. 252, 1181. Lome dic o , P. T. , McAndrew, S. (1982) , Natu r e 299, 221 . 1'Iac in o , G., Tzag o loff , A. (1979), ]. Bi ol . Clzem. 254, 4617. Matt ick , J., Ze h ner, Z., Calabro, M., Wak il, S. (1981), E11r. ]. Bi oc hem. 114, 643. McInto s h, L. , Poulsen, C. , Bog or ad, L. (1980) , Natu r e 288, 556. 1-Ic K eown, M. , Fir tel, R. A. (1981) , Cell 24, 799. Meij lin k , F., van het Schip , A., Amberg, A. , Wi er i ng a, B., Bruber, G. Ab, M. (1981) , ]. Bi ol . Chem. 256. 9668. Mi ch elson, A. , Orkin , S. H. (1980) , Cell 22, 371 . Mi n Jou , W., Haeg e man, G., Ysebaert, M., Fie r s, W. (1972), Natu r e 237, 82. Montg o mery, D., Leung , D., Smi th, M., Shali t, P., Fay e, G., Hall, B. (1980). Pr oc. Natl . Acad. Sci. 77, 541 . Monto y a, J. , Oja l a, D. , At tar di, G. (1981) , Natu re 290, 465. Moy er , S. A. (1981) , Viro log y 112, 157.
Muller, U.R ., Wells, R.D . (1980), ]. Mo/. Bio l . 141 . 25. Muskavit ch , M., Rog n ess, D. (1982). Cell 29, 1041 . Nakazato , H. , Venkate s an, S. , Edmonds, M. , Natu r e 256, 144. Netz k er, R., Kochel, H., Baszk, N., Ki int z e l, H. (1982), Nucleic Acid s Res. 10, 4783. Ng uyen -Huu, M., Str a tm ann, M., Groner, B., Wurtz , T., Land, H., Gie s ecke, K., Sip pe l, A., Schutz , G. (1979), Proc. Natl . Acad. Sci. 76, 76. Nic h ols, B. , van Cleemp u t, M. , Yanofs k y , C. (19 81) , ]. Mo!. Bi ol . 146, 45. Noda, M., Teranis h i, Y., Takahashi, H., Toy os ato , M. , Nota k e, M., Nakanis h S. , Numa, S. (1982) , Natu r a 297, 431 . Padg et t , R.A ., Konarska, M.M., Grabowski, P.J. , Hardy, S.F., Sharp, P.A. (1984) , Scie il c e 225, 898. Pate r son, B.M ., Rosenberg, M. Natu r e 279, 692. Pauza, C.D., Karels, M., Navre, M., Schachman, H.K . (1982) , Proc. Natl . Acad. Sci. 79, 4020. Pir r ott a, V. (1979) , Nucleic Ac ids Res. 6, 1495. Poole, S., Fir tel, R.A ., Lamar, E., Rowekamp , \\'. (1981), ]. Mo!. Bi ol 153, 273. Proudfo o t, N. , Mania t i s, T. (1980) , Cali 21, 537. Pta s hne, M. . Backman, K., Humay un , M., Jef f re y, A., Maurer, R., Mey er , B., Sauer. R. T. (1976) , Scie n ce 194, 156. RajB handary , U.L., Ghosh, H.P. (1969), ]. Bi ol . Clzem. 244, 1104. Rosenberg, M., Pate r son, B.M . (1979), Natu re 2i9 , 696. Sag h er, D. , Grosfe l d, H. , Edelman, M. (1976) , Proc. Natl . Acad. Sci. 73, 722. SaFngid ed r e, s,F .J, . CC. o, uHlsuontc, h Ais o. , n,F rCie. d mSlaoncno,m bTe,. APi. r, S mG.i ,t hB, arMre. ll,( 19B7.8G) .,, B].r oMwno/,. NB.iLo .!,. 125, 225. Scherer, G.F.E., Walkin s haw , M.W., Arnott , S. (1978), Nuclei c Acid s Res. 5, 3759. Scherer, G., Walkin s haw, M. Arnott , S. Moore, D.J. (1980), Nuclei c Acid . i Res. 8, 3895. Schii mp e rli, D., McKenney, K. Sobie s ki, D., Rosenberg, M. (1982) , Cell 30, 865. Selker, E., Yanofs k y, C. (1979), ]. Mo/. Bi ol . 130, 135. Setz e r, D.R . , McCrog a n, M., Nunberg, J., Schim ke, R.T. (1980), Call22, 361 . Shani, M., Nudel, U. Zevin - Sonkin , D., Zakut, R. Gi v l. , D., Katc o ff , D., Car- mon, Y., Reit er, J., Fris c hauf, A., Yaff e, D. (1981), Nucleic Acid s Res. 9, 579.
Sharp, P. A. (1981) , Cell 23, 6-1 3. Shatk i n , A.J. (19 76) , Cell 9, 645. Schenk, T. (19 81) , Curr. Top . 11,f icro bio l . !11111111110!. 93, 25. Sherman, F., McKnig h t, G., Ste w art, J.W . (19 80), Bi oc lzi m . Bi op h y s . Acta 609, 3:13 . Shin e , J. , Dalga r no, L. (19 74) , Proc. Xatl . Acad. Sci. 71, 1342. Sin g e r , B.S . Gold, L., Shin d li ng , S.T., Colkit t, M. Hunte r , L., Prib n ow, D., Nelson, M. (19 81) , ]. Mo!. Bi ol . H9, 405. Smi th, A. E. , Marcker, K. A. (19 68) , Bi oc lzemi st r y 18, 1366. Sny de r, l\1., Hunkap ille r, M. Yhen, D., Sil v ert, D. , Fris t r om , J., Davis o n, N. (1982) , Cell 29, 1027. Sti eg l e r, G., Matt he ws, H.M., Bin g h am, S.E., Hallic k , R. (1982), Nucleic Acid s Re s. 14, 3-1 2 7. Sti le s, J. , Szosta k , J. , Young , A. , Wu, R. , Consaul, S. , Sherman, F. (1981) , Ce ll 25, 277. Sto r mo, G. , Schneid e r, T. Gold, L. (19 82) , Nucleic Acid s Res. 10, 2971 . Sures, I., Lev y , S. Kedes, L.H . (19 80), Proc. Na tl . Acad. Sci. 77, 1625. Swanstr o m, R. , Varmus, H. E. , Bis h op, J. M. (1982) , ]. Vira l. 42, 535. Talkin g ton , C. A. , Leder, P. (19 82) , Na tu r e 298, 192. Thach, R.E., Sundararaja n , T.A., Dewey, K., Brown, J.C . , Doty , P. (1966), Cold Sp ri n g Harbor Sy m p . G11a11t . Bi ol . 31, 85. Valenzuela, P., Medin a , A., Rutt er , W., Ammerer, G., Hall, B. (1982), Natu r e 298, 347. Vir t a n en, A., Alestr o m, P., Persson, H., Katz e , M., Pett er sson, U. (1982), Nucleic Acid s Res. 10, 2539. Wats o n, J.C ., Surzy ck i, S.J . (1982), Proc. Natl . Acad. Sci. 79, 2264. Weber, L., Hi ck ey, E., Bag li o n i, C. (1978), ]. Bio l . Chem. 253, 178. Weng le r, G., Weng le r, G., Gross, H.J. (1979), Natu r e 282, 754. \Vier in g a, B., van der Zwaag -G errits e n, J., Mulder, j., Gruder, G. Ab., M. (19 81) , Eur. ]. Bi oc hem. lU, 635. \Vo dmar-Fil ip o wi cz , A., Szczesna, E., Zan-Kowalczewska, :!vi. , Muth u kris h nan, S., Szy b ia k , U., Lego cki, A., Fil ipo wi cz , W. (1978), Eur. ]. Bi oc hem. 92, 69. Yanofs k y, C. (1981) , Natu r e 289, 751 . Yoo, O.J. , Powell, C.T., Ag ar wal, K.L . (1982), Proc. Natl . Acad. Sci. 79, 1049. Young , R.A ., Hag e nbii ch le, 0., Schib l er, U. (1981), Cell 23, 451 . Zain , S., Sambrook, J., Roberts , R., Keller, W., Frie d , M., Dim m. A.R . (19 79) , Cell 16, 851:
Zalkin , H. , Yanofs k y, C. (1982) , j. Bi ol . Che m . 257, 1491 . Zeev i, M., Nevin s , J.R., Darnell, J.E ., Jr. (1982) , Mol. Ce ll . Bi ol . 2, 517. Zurawski, G., Perrot, B., Bott om ley, W., Whit feld , P.R. (1981), Nu clei c Acid s Res. 9, 3251 .
제 4 장 단백질 합성의 개시과정 전령 RNA(mRNA) 를 주형으로 사용하면서 리보솜의 매개로 일어나 고 있는 단백질 합성은 지구 상에 생존하는 생명체의 칭표의 하나이다. 단백질 합성의 메카니즘이 오랜 진화과정을 거쳐 오는 동안 거의 동일 하게 보존되어 있다는 것은 놀라운 일이 아니다. 제 2 장에서 본 바와 감이, 박테리아에서 포유동물에 이르기까지 리보솜둘은 그 전체적인 구 조가 거의 같다. 모든 유기체들에 있어서의 아미노아실-t RNA 의 결합, 뎁티드 결합의 형성, 그리고 리보솜의 자리옮김 등과 같은 과정들이 사 실상 동일하고, 리보송의 작은 하위단위체와 큰 하위단위체들이 분담 하고 있는 일들도 모든 종류의 리보솜들에서 동일하다. 그러므로, 원핵 세포와 진핵세포에 있어서의 개시과정들 사이에 두드러진 차이가 있다 는 것은 놀라운 일이 아닐 수 없다. 단백질 합성과정을 개시, 연장 및 종결 등 크게 세 단계로 나눌 수 있다. 이 세 단계들은 생리적으로도 구분된다. 죽, 특이한 단백질 인자 들이 각 단계에서 관여하기 때문에 세 단계들에서의 조절 메카니즘은 생리조건에 따라 구분된다. 이 장에서는 개시과정을 다루고, 연장 및 종결 과정들은 제 5 장과 제 6 장에서 다루기로 한다. 번역의 개시과정은 일련의 구분된 반옹둘로 이루어진다. 아 과정에서 리 보솜이 시 스트론의 출발점 인 개 시 코돈 AUG 를 함유하는 mRNA 의
특이한 자리에서 결합하게끔, 리보송의 하위단위체들이 mRN A 및 Met- tRN A 1M
전체적인 개시 반응을 다음 식으로 나타낼 수 있다. flVle t -tRN NM•• + mRNA + 30S + 50S + GTP IF-1, IF-2, IF-3 (fM et- tRN N~1•1 • 70S • mRNAJ + GDP + P; 제 가지 인자들은 모두 개 시 의 전체 과정 에 걸쳐 서 촉매 적 으로 작용한다. 70S 개시 복합체가 형성되면서 GTP 는 GDP 와 R 로 가수분해된다• 4.2 E. col i의 개시인자들의 성질 E. col i의 세 가지 개시인자들의 물리화학적 성질들에 관해서는 광범 하게 연구되어 있다. 그들의 몇 가지 주요한 성질들과 기능을 표 4-1 에 요약하였다. IF-2 는 IF-2a 와 IF-2b 두 가지 형 태 가 있다고 생 각된 적 도 있었으나 IF-2b 는 IF-2a 의 단리과정에서 생긴 인위적인 부분 가수 분해 물임 이 밝혀 졌다 (Kolakofs k y 등, 1969; Hershey 등, 1977) . IF-3 에 표 4-1 E. coli 의 개 시 인 자들의 성 질 과 기 능 갑자실 1 형태 분(k자da량l) 티폴 수드리 의펩기능 IF-1 8.8~ 9. 0 1 리보송 하위단위체들의 해리를 중 진. IF-2 와 IF-3 의 기능울 증진 IF-2 {IIFF --22ba 9802. .00~~1 1980.. 00 3 f활M동 et성- t RN A 'Me t 의 결 합, GTPase IF-3 21. 0~ 23. 5 1 mRNA 의 결합, 항회합 도 IF-3a, IF-3{3 등 여러 가지 형태가 있을 것으로 생각되었었지만 IF- 3 f3는 IF-3a 의 부분 가수분해물일 것으로 생각된다 (S p r i n g er 동, 1977). 세 인자들의 아미 노산 조성 들이 모두 결정 되 었으며 (Lee-Huang 둥, 1971 ; Hershey 등, 1977) , IF-1 은 결 정 체 로 얻 어 졌 다 (Lee- H uang 둥, 1971) .
4.3 70S 개시 복합체를 형성시키는 개개의 부분 반응들 30S 개시 복합 체라 는 중간체 를 거 쳐서 70S 개시 복합체 를 형성시키는 개개의 부분 반응들의 자세한 것들을 아래에 기술하였다. 약간의 단계 들은 아직 그 정 확 한 순서들이 밝 혀지지 않고 있다. 4. 3. l 70S 리보솜의 해리 70S 리보솜들은 mRNA 의 번역이 종결된 다음에 폴리솜 상태의 복 합 체로부터 떨어져 나와서 그들의 하위단위체 들 과 평 형을 유지하고 있다. 생리적 조건의 M g 狂 농도에서 해 리 속도는 느리고, 거 의 모든 리 보솜 둘 온 단단하게 결 합된 70S 로서 존재 한다 (Dav is , 1971 ; Noll 둥, 1973) . 단백질 합성의 개시는 30S 입자 상에서 시작 하 여 뒤에 50S 하위단위 체 와 결합하게 되므로, 리보솜의 하위단위체들을 공급하기 위해서 70S 리 보솜의 해리가 필요하게 된다. 이 해리과정은 IF-1 과 IF-3 둘의 합동작용으로 아래와 같이 매개된 다는 것이 밝혀졌다. 70S (I느F-= 1) 50S + 30S (I一IFF--31 ) 50S + 30S • IF-3 이 반옹에서 IF-3 은 70S 리보솜의 해리 속도 를 중진시키는 것이 아니 라, 오히 려 일차적 으로는 항회 합인자로서 작용한다 (Dott av io - M arti n 둥, 1979) . 자유 50S 와 자유 30S 하위 단위 체 들로의 해 리 속도 믈 중가시 킴 으 로써 해리과정이 일어날 수 있게 돕는 것은 개시인자 IF-1 이다 (Sabol -4 Ochoa, 1971 ; Sabol 등, 1973 ; Gott lie b 동, 1975 ; Godefr oy -C olburn 동, 1975 ; Naaktg e boren 등, 1977 ; Dott av io - M artin 동, 1979) . 한편 , IF-3 은 70S 리보솜의 해리로 생긴 자유 30S 하위단위체와 결합한다. 30S • IF-3 복합체는 50S 하위단위체와 재회합할 수 없다. 따라서, 평형은 자 · 유 하위단위체들이 생기는 쪽으로 이동된다.
4. 3. 2 30S·IF-1 • IF-2 • IF-3 복합체의 형성 30S 개시 복합체 형성의 첫번째 단계는 먼저 세 개시인자들이 30S 하 위 단위 체 에 협 동적 으로 결 합하여 30S • IF-1 • IF-2 • IF-3 입 자를 형 성 하 는 것 이 다. 그 다음에 이 복합체 에 mRNA 와 fM et- tRN NM 들이 결 합 하여 30S 개시 복합체를 형성 한다. IF-2 는 개시반응에 관련된 그밖의 모든 성분들 이 없을 때 30S 하위단위체와 특이하게 결합 한다. 이렇 게 생긴 회합체는 IF - 1 과 IF 전 들에 의해서 안정하게 된다 (Lockwood 등, 1972; Fakundin g 과 Hershey, 1973; Benne 등, 1973; Chu 와 Mazun- der, 1973). 이 조건에서 기능을 가전 매개의 30S 하위단위체는 한 분 자의 IF~2 를 결합한다. IF-3 도 역시 다른 인자들의 존재에는 무관하게 30S 하 위 단위체에 결합 한다. 그러나, 일단결합한다음에는 IF-1 과 IF-2 들에 의 해 서 안 정 하게 된 다 (Vermeer 등, 1973a ; Vermeer 등. 1973b) . IF-2 와 IF- 3 들 이 존재 할 때 IF-1 도 역 시 30S 에 안정 하개 결 합한다. 세 개시인자 들은 모두 70S 리보솜의 두 하위단위체들의 경계면에서, 30S 하위단위체의 16S rRNA 의 끝 이 있는 부근에서 서로 인접한 자리 또는 겹쳐 있는 자리에 서 서로 결합 한다(그립 2-37 및 그림 2-40 을 보라). 4. 3. 3 30S 개시 복합체의 형성 세 개시인자들이 30S 리보송에 결합한 다음에 f Me t-t RNNM et와 mR- NA 가 30S • IF-1 • IF-2 • IF-3 복합체 에 목이 하게 결 합한다. 그러 나, fM et- tRN An .ie1 와 mRNA 가 결 합하는 순서 는 아직 확실하지 않다. 그 렇지 만, 완전한 30S 개시 복합체의 형성 에 관한 실험을 시험관에서 한· 결과에 의하면 mRNA 가 f Me t-t RNNMe1 보다 먼저 결합하는 것으로 생 각된 다 (Vermeer 등, 1973a ; Vermeer 등, 1973b) . 30S • IF-3 • IF-2 • IF-1 복합체 는 개 시 코돈 AUG 또는 GUG 가 위 치 한 자리에서 mRNA 와 결합한다. 30S 리보솜 하위단위체가 자연의 mRNA 에 있는 시스트론의 개시 자리를 인식하는 일은 단백질 합성의 개시에 있어서 대단히 중요한 단계이다. 이에 관해서는 뒤에서 곧 다루 어질 것이다. 30S 개시 복합체의 형성과정을 다음과 같은 식으로 요약할 수 있다.
30S • IF-1 • IF-2 • IF-3 + mRNA + GTP + fM et- tRN A 'M ― ➔ (30S • IF-1 • IF-2 • mRNA • GTP • fM et- tRN A 'M•1 J + IF-3 이 30S 개시 복합체는 겔 거르기 또는 농도 기울기 원심분리 동으로 안정된 형태로 단리할 수 있다. 위의 식으로 나타낸 과정에서 GTP 는 입체적 효과물질로 작용함으로써, IF-2 가 비교적 낮은 농도에서도 30S 리보솜 하위단위체와 안정하게 회합할 수 있게 한다. 그러나, IF-2 가 과량으로 존재할 때는, GTP 가 없는 조건에서도 30S 개시 복합체가 형 성될 수 있다. GTP 는 이 단계에서 가수분해되 지 않은 채 30S 복합 체 에 결합되어 있다. 30S 개시 복합체에 . 결합한 1 몰의 IF-2 당 GTP 와 fM et- tRN A 'Mc1 가 각각 1 몰씩 결 합되 어 있다. 그러 므로, 30S 개 시 복 합체를 형성함에 있어서 IF-2 는 화학양론적으로 작용함을 알 수 있다 (Ve rmeer 등, 1973a; Vermeer 등, 1973b). fM et- tRN A 'M•• 가 결합할 때 30S 하위 단위 체 로부터 IF-3 이 떨 어 져 나오는 한편, IF-1 이 30S 복 합체에 결합한다. fM et- tRN A!Met 가 30S 리 보솜에 최 대 량으로 결 합하려 면 세 가지 개 시 인자들이 다 필요하지만, 30S 리보솜에 f Me t-t RN A' M•• 를 선택적으로 결 합시 킬 때 에는 IF-2 가 주요한 역 할을 한다. 즉, fM et- .tRN AIMe1 의 선 택에 있어서는 IF-2 가 절대적으로 필요한 인자이다. IF-3 의 기능은 30S 리보솜이 자연의 mRNA 에 있는 개시 자리의 선택을 돕는 데 있지 만, 30S 수준에서 의 IF-1 의 주되 는 역 할은, IF-2 가 30S 개 시 복합체 에 결합하는 것을 안정하게 만드는 데 있다. IF-2 가 30S 개시 복합체에 안 정하게 결합되어 있으면 30S 개시 복합체와 50S 하위단위체가 접합하여 70S 개시 복합체가 형성될 때 IF-2 는 GTPas~ 로서의 활동성을 가지게 됨으로써 GTP 를 70S 복합체로부터 제거할 수 있게 된다. 활동적인 70S 복합체가 형성되려면 GTP 가 제거되어야 한다는 것이 여러 실험들 로 증명 되 었 다 (Mazumder, 1971 ; Groner 와 Revel, 1971 ; Str i n g e r 동, 1977). 가) f Me t-t RNA!Me t의 특이한 인식작용에 있어서의 IF-2 의 역할 IF-2 는 개 시 t RNA 를 리보솜에 결합시키는 인자로 인정되고 있다• 그래서, IF-2 를 f Me t-t RNAlllle t의 인식 단백질이라고 불리기도 한다. 왜냐하면, AUG 룰 전 령 으로서 사용하였을 때 이 인자만 가지 고도 fM et- tRN A1M” 를
30S 하위단위체에 결합시킬 수 있기 때문이다. 이 과정과 관련된 단계 둘은 아직 밝혀지지 않았다. 아래와 같은 몇 가지 연구 결과들을 살펴 봄으로써 IF-2 의 기능을 침작할 수 있다. 고도로 정제된 IF-2 는 생리적 조건에서 개시 t RNA 가 없을 때 GTP 와 약한 상호작용을 하며 , GTP 가 없 을 때 는 fM et- tRN A '~1 와 약한 상 호작용을 할 수 있지만, 이 상호작용은 안정한 복합체를 형성할 정도로 강하지 는 않다 (Maju m dar 등, 1976; Pete r sen 둥, 1981) . 또한 Mg 2 + 이 온이 없 을 때 IF-2 는 GTP 의 존재 에 관계 없 이 fM et- tRN A 'Mct 와 이 성 분 복합체 물 형성한다 . 개시 메카니즘에 있어서의 이 복합체의 역할에 관해서는 아 직 잘 모르고 있지만, IF-2 는 자유 포르밀메티오닌 또는 f Me t-울리 고누 클레 오티 드와는 결 합하지 않지 만, 아미 노기 가 가리 어 진 메 티오닌과 공유결합으로 결합된 모든 t RNA 와 강하게 결합한다는 것 이 밝혀 졌 다 (Sundari 둥 , 1976) . 그뿐 아니 라, E. coli 의 개 시 tR NA 와 개지반응에 사용되지 않는 tRN AmM••, 구조적으로 많이 변형된 fM et- t RNA t Me t들, 아미노기가 가리어진 진핵세포의 개시 t RNA 둘이 모두 IF-2 에 강하게 결 합한다 . Clark 와 Marcker (1966) 는 리 보솜과의 결 합 에 있 어 서 는 tR NA 의 구조가 중요하다는 것 을 밝혔다. Mg 2+ 이 온의 농도가 매우 클 때는 Met- tRN A 'M 가 리 보솜의 P 자리 에 결합할 때 개시인자들 및 포르밀화가 필요 없다. 이 조건에서는 Me t_t RNA jf AIe t는 Met- tRN AmMc t 및 그밖의 모든 아미노아실-t RNA 들보다 훨씬 더 강하게 결합한다. 이것은 리보솜 자체가 아미노아실_t RNA 분자들의 tR NA 부 분에 대한 본성적인 목이성을 가지고 있다는 것을 나타내는 것이다. Mg 2+ 이온의 농도가 작을 경우(생리적 조건에 가까운 M g 2+ 의 농도)에 는, 개시 인자 없아도 일어날 수 있는 상호작용이 약화되며, 개시 tR NA 룰 포르밀화하면 리보솜에 대한 친화력을 가일충 감소시킨다 (Sunder i 등, 1976). 이와 같이, 생리적 조건에서, IF-2 가 없을 경우에는 f Me t-t記V A'Me t의 결합은 거의 일어나지 않는다. 이러한 결과들에서 리보솜의 개시 복합 체의 형성에 있어서 IF-2 가 하는 역할은 포르밀화된 개시 t RNA 와 리 보솜과의 상호작용을 안정하게 만드는 일이라는 것을 알 수 있다. Str e pt oc occus fae calis 및 E. col i의 어 떤 변종에서는 폴산이 전혀 들 어 있지 않은 배지에서도 자랄 수 있는데, 이러한 박테리아에서의 단백 질 합성의 개시는 Me t-t RN A' Mc1 의 포르밀화가 없어도 일어날 수 있다.
이러한 경우, t RNA'M” 의 고리 N 에 있는 GT 'f/J' C 의 리보티 미딘 (rT) 이 우리 던 으로 대 치 되 어 있 음이 밝혀 졌 다 (Samuel 과 Rabin o wi tz, 1974 ; Delk 와 R1bin o wi tz, 1975; Baumsta r k 등, 1977). 이것은 아마도 tR N- A'> 구조의 단 한 군데에서의 변화로 인하여 포르밀화되지 않은 Met- t RNA' ·'·' ’( 우리던 함유)가 풀산을 첨가한 세포에서 형성된, 포르밀화되 지 않은 Met- tRN A 'Me t (리 보티 미 딘 함유) 보다 개 시 코돈에 더 효과적 으 로 반응할 수 있게 됨으로써 생기는 일일 것이다. 나) 리보솜에 의한 자연의 mRNA 의 개시자리의 인식과 이 파정에 있어서의 개시인자들의 역할 30S 리보솜 하위단위체는 자연의 mRNA 에 있는 개 시 자리를 득이하게 인식하고 선택하는 데 필요한 독 성들을 가지고 있 으며, IF-3 은 30S 선택과정에서 이 하위단위체의 작용을 돕는 역할을 한다 (S t e it z 둥, 1977; Ste i t z, 1978). 개시 자리의 인식과 선택 에 있어서 가장 중요한 문제는, mRNA의 개시 부분에 있는 AUG 코돈과 mRNA 의 내부에 있는 AUG 코돈을 서로 식별할 수 있게 하는 mRNA 의 개 시 부분의 구조적인 특징이 무엇인가 하는 것이다. mRNA 분자에는 AUG 삼중체가 여기저기 있는데, 리보솜이 결합자 리는 왜 언제나 시스트론의 앞에 있는 AUG 이고, 이 코돈만이 개시코 돈으로 사용되 는 것 일 까 ? 초기 에는 mRNA (MS2 RNA) 의 이 차구조로 인해서 나사선 부분에 있는 AUG 삼중체는 개시코돈으로 작용 할 수 없 고, 고리 부분에 있는 노출된 AUG 삼중체만이 개시코돈으로 작용할 수 있을 것이라고 생각된 적도 있었다 (M i n- J ou 동, 1972) (그림 3-2 를 참조하라). 그러나 MS2 RNA 를 변성시켜서 펴면 리보솜이 결합할 수 있는 자리들이 더 노출되는 것은 사실이지만, RNA 를 여러 크기 들 의 조 각들로 절단하더라도 리보솜의 결합이 마구잡이로 중가하지 않는다. 이 사실은 이차구조가 파괴되더라도 대부분의 AUG 코돈둘은 여전히 개시 신호로서 이용되지 않는다는 것을 가리키는 것이다 (S t e it z , 1974). Shin e 과 Dalga mo, 그리 고 Ste i t z 와 그너 의 동료들은 모든 리 보솜-결 합자리는 시스트론의 개시코돈의 5' 의 상류쪽으로 거의 같은 위치에 AGGAGGU (3') 연 속부분 (이 것 을 Shin e -Dalga rno 연 속부분이 라고 부론 다) (또는 이와 매우 비슷한 유도체)을 가지고 있으며, 이 연속부분은 16S rRNA 의 3' 끝에 있는 피 리 미 단 이 많은 부분 (-GAUCACCUCCUU- AoH 3' )과 염기 짝짓기를 할 수 있다는 것을 알았다 (Sh i ne 과 Dalga r no,
1974 ; Ste i t z 와 Jak es, is;: i ; Ste i t z 등, 1977) (표 3-2 와 표 4-2 를 보 라). 이러한 염기 짝짓기는 개시 t RNA 의 역코돈과 개시 코돈 AUG 가 결합할 수 있게끔 자리를 잡아 준다. 위 에서 말한 mRNA • rRNA 염기 짝짓기가 E. co li의 리보솜에 의한 개시자리 선택에서 중요한 역할울 한다는 것을 뒷받침해 주는 많은 실 험적 증거들이 있다. 표 4-2 작은 하위단위체의 rRNA 둘의 3' 말단에서의 연속부분의 바교 출처 연속부분 고대 박테리아 Ha/o b acte r iu m /za /o b iu m 卜 •· NNUCUGCGGCUGGAUCACCUCCU 진성 박테리아 E. coli 『 ·AACCUGCGGUUGGAUCACCUCCUUA B. ste a rotl ze rmop/ zil11 s l· •· AAGGUGCGGCUGGAUCACCUCCUUUCUA 엽록체 Zea mays l···A AGGUGCGGCUGGAUCACCUCCUUU E11g /e na gra cil i s …A AGGUGUGGCUGGAACAACUCCC 미토효모콘 드리아 l··· AACCUGCGGUGGGCUUAUAAAUAUCUUA- AAUAUUCUUACA 밀 싹 …A ACCUGUGGCUGGAUUGAAUC (C) 사람 ···A AAGUGCACUUGGACGAAC 소 •• ·A AAGUGUGCUUGGAUAAAU 진핵세포의 세포질 :::류,밀개싹구리, 누에, I.:.:~::::::::::::: 問 (1) 지금까지 일차구조가 분석된 약 150 가지의 박테리아 및 비루스의 mRNA 들은 거의 모두 개시코돈 상류에 16S rRNA 의 3' 끝과 상보적 인 연속부분을 가지고 있다 (3. 1. 3 절의 표 3-2 및 표 4-3 을 보라). Shin e -Dalga mo 연속부분은 다시스트온성 mRNA 들에 있어서는 매 시스 트론 앞에 있다는 것 을 주목해 야 한다 (Post 와 Nomura, 1980; Pauza 등, 1982; Yanofs k y 둥, 1981). 자연의 mRNA 들 중에서 16S rRNA 에 대 한 상보성을 가지지 않는 것은 파지 람다 및 밀집한 유연관계를 가진 파 지 434 의 C1 억제인자 단백질에 대한 mRNA 만이 알려져 있다 (P t ashne
표 4-3 R17 리 보솜 결 합자리 연 속부분 및 16S rRNA 의 3' 말단과의 가능한 염기 짝짓기 박테리아 시R스1트7 론 리수말 보단있송과는 영결부기합분 자 짝리짓에기서를 5할' 가의영 기능쌍한수f펴과M과 2 진S 의R2리 ,N 보결RA또1솜합 7는둘, Esccohlei r iBc h ia 복A단 제 2효「 u 질소 (5ot't) AA cUuCi A~U U C 匠CU:C프C AIA luCU uYU (3 1' 6) SrRNA '내 ++ 외단피백 질 ACC| 露―|y「!~ I@ uuuG 3 (4) + Pseaeurd11ogm 1o1 1noassa I A단-백 질 (5oH')Ac uU j~ U C IC UG C U uC Yu (3' )1 6S rRNA 543++ 복제효소 UGl~IU UAC 외단피백 질 AC c|—G 더 이L 一 5 |uuu ( 4) + I 스 1 Baprcohi/ti1 h l 1ue 1 srs msto e -a - A단-백질 (o5u'A) UA CU CUC UU U~ 으C C므 U |YG( 3')1 6S rRNA >4 + 복제효소 ACAUG~ 건 U 4 + 걸걸니 AACCGG 鬪r uu 2 (1) A Cacurleosbcaecntte i rs A단-백질 (5o'a)UU CC UC UU| 詞U C 죠C U IYG (3')1 6S rRNA v4 42 복제효소 cAuGl~lu 외단피백 질 ACCGGT一l~ luu ,_1`` ,./
동, 1976 ; Pir o tt a, 1979) . pppA UG GAC ACA AAA AAG··· NH2Ser Thr Ly s Ly s· ·· 두 경우 다, AUG 개시 코돈이 mRNA 의 5' 끝에 아주 가깝게 있기 때 문에 Shin e -Dalga rno 연속부분이 있을 여지가 없다. 한편, E. col i의 dnaG 프리 마아제 와 박테 리 오파지 T4 의 단백 질 38 을 합성 하는 mRL'{A 둘은 동상 적 인 위 치 에 Shin e -Dalga r no 연 속부분을 가지 고 있지 않다. T4 의 단백 질 38 에 대 한 유전자의 경 우에는, Shin e -Dalga r no 연속부분이 개시 코돈에서 얼리 떨어져 있지만, 머리 핀 구조를 만듦으로써 Shin e - Dalga rno 연속부분이 개시 코돈에 가까와지는 것으로 생각되고 있다 (Gold 등, 198 1 ) (그 림 4-1) .
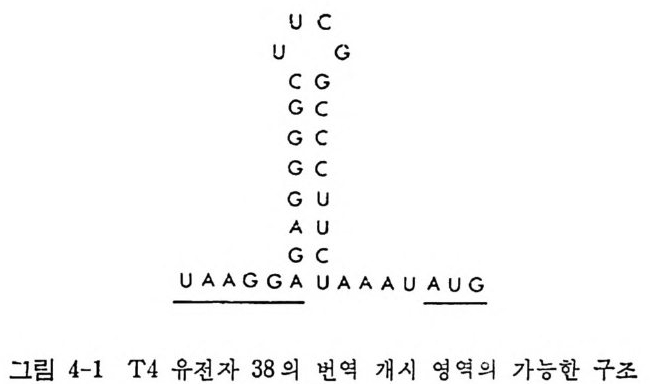 U C
U C
지금까지 일차구조가 분석된 mRNA 둘은 대부분 E. col i의 것들과 묘 co li와 밀접한 유연관계에 있는 박테리아의 것들이지만, 최근에 분석된 그람 양성 박데 리 아의 mRNA 둘의 일 차구조들도 16S rRNA 의 3' 끝에 대해서 광범한 상보성을 가지고 있다 (McLau g h li n 등, 1981; McLaug h lin 등, 1982; Murray 등, 1982) (표 3-2 를 보라) . 二러 나, 그람 양성 박 테리아로부터 더 많은 정보를 얻어야 이 박테리아들에 있어서의 Shin e - Dalga rno 상호작용의 중요성 을 평 가할 수 있을 것 이 다. (2) 16S rRNA 의 3' 끝이 개시반응에 관여하고 있다는 여러 가지 간 접적인 실험결과들이 있다. 2.5.4, 2.6.2, 및 2.6.3 절들에서 기술한 바와 갇이, 16S rRNA 의 3' 끝은 30S 리보솜의 플랫폼에 위치하고 있
으며, 개시 인자들도 플랫폼 부근에 있다(그림 2-35, 2-37, 및 2-40 들 올 보라). 16S rRNA 의 3' 끝에 있는 m26Am26 A 가 개시 반응의 강력 한 방해물질인 카수가다아신의 됴 적 이라 는 것 도 홍 미있는 증거 라고 생 각된다. (3) Ste i t z 와 Jak c (l9 75) 는 32p 르 표지 된 콜리 파지 R17 의 A- 단백 질 시스트는울 포함하는 개시 복합체 를 콜 리신 E3(16S rRNA 의 3' 끝에서 49 번째의 누클래티드에서 단일 절단을 일으키는 핵산 가수분해효소)로 처리하여 32P 로 표지된 mRNA 조각과 안정한 복합체 를 이루고 있는 16S rRNA 의 조각을 얻을 수 있었다. S t e it z 와 J akes 가 고안한 생화학 적 방법을 사용하여 여러 가지 mRNA 들 에 대해 서 비 슷한 실험둘 이 이 두어졌다. 얻어진 mRNA • rRNA 복합체에 있는 mRNA 조각들은 푸린 을 많이 가지고 있는 연속부분이 있었고 그 뒤쪽으로 개시 코 돈이 있었 다(그림 4-2).
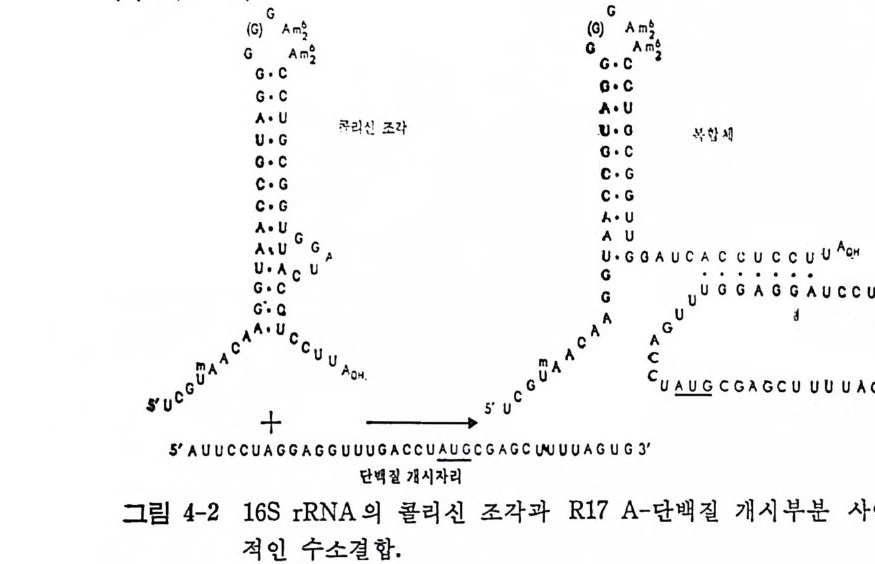 G(G ) 따Am ; 仰°c · AmCm·^2. 2
G(G ) 따Am ; 仰°c · AmCm·^2. 2
이러한 실험들 중에서 Sh ine -Dalga m o 상호작용의 원리를 뒷받침하는 중 요한 실험결과를 Jay 둥 (1980) 이 얻었다. 이들은 원핵세포의 mRNA 둘 의 결합자리에서 볼 수 있는 몇 가지 특징을 가진, 화학적으로 합성한 20 개의 누클레오티드로 된 울리그누클레티드가 dAATTC TI 莖으~ TC ATG(3')
IF-2 와 IF-3 이 존재하는 반응조건 에서 기능을 가 진 70S 개시 복합체를 독이하게 형성할 수 있음을 알 았 다. 이 가상적인 리보송 결합자 리의 특 칭은 다음과 같다. 첫 째, 3' 끝에 ATG 개시 코돈 을 가지 고 있다. 둘 째, 16S rRNA 의 풀리피리미딘 절 편 과 상호 작 용 할 수 있는 폴 리푸린 연 속부분 AGG A 를 가지고 있다. 세째, 많은 파 지 rnR N A 둘 의 리보솜 결 합자리 에서 흔 히 보는 RRUUU R R 에 상응하는 GATTTA A 연속부분을 가진다. 네째, ATG 개시 코돈의 5' 끝바로 옆에 피리미딘 ( C) 이 있다. RAUG 보다 YAUG 가 16S rRNA 에 더 찰 결합되는 것 이 알려져 있다 . 다섯째, 개시 코돈의 5' 쪽으로 〈 읽는 상 〉 에 맞지 않는 종 결 코돈 TAA 와 TAG 를 가지고 있다 . 종결 코돈둘의 이러한 배치는 이 자리들에서 번역이 방해되지 않을 것임을 확실히 해 두기 위해서였다. 같은 실험에 서, ATG 개시 코돈을 삭제하고, 나머지 결합순서는 위의 합성 울리고 누클레오티드와 동일한, 17 개의 누클레오티드로 된 것을 사용하였을 때 도 f Me t-t RNNM•1 가 리보솜과 안정하게 결합한다는 것을 알았다. 이 실 험 결 과는 fM et- tRN Af M e’ 에 의 한 정 확한 개 시 코돈의 선택 은, fM et- tR NAn .ie1 • 30S 리 보솜 복합체 가 개 시 자리 를 인식 하여 결 합한 다음에 일 어날 것 임 을 암 시해 주는 것이다. (4) 16S rRN A 의 3' 끝과 상보적 인 을리 고누클레 오티 드들은, mRNA 가 박테리아의 리보솜에 결합하는 것을 방해한다 (Tan igu c hi와 Weis s- mann, 1978 ; Eckhardt 와 Lii hr mann, 1979) . 이 방해 작용은 자연 의 mRNA 들 에 대해서 특이하게 작용한다. 그렇지만, AUG 또는 폴리 (U) 의 결합은 방해되지 않는다. (5) Shin e -Dalga r no 연속부분을 바꾸거나 결실시키는 돌연변이가 일 어 나면 원 핵 세 포의 mRNA 들의 번 역 이 크게 감소한다 (Dunn 등, 1978; Schwartz 둥, 1981 ; Sin g e r 등, 1981) . 개시 자리 연속부분들은 몇 가지 특징을 가지고 있다. 첫째로, 여러 가지 mRNA 들의 리보솜 결합 자리들과, 그들에 대해서 상보적이라고 추측되는 16S rRNA 의 3' 끝에 있는 부분과 비교해 보면 개시 자리들 의 구조가 이질적임을 볼 수 있다. 즉, 16S r Ri'l A 의 3' 말단의 울리고 누쿨레 오티 드 부분과 참된 Wats o n-Cric k 염 기 쌍을 이 룰 수 있는 누클 레오티드의 수는 mRNA 의 종류에 따라서 3 개 내지 9 개이다(표 3-2 및 표 4-3 둘을 보라). 16S rRNA 의 3' 끝과 염기 짝짓기를 할 수 있는 mRNA 의 리보솜 결합 자리에 있는 누클레오티드의 수가 많을수록 리
보솜이 개시 자리 에 결합하는 효율이 더 커지며, 개시 복합체 형성 에 있 어서의 IF-3 에 대한 의존도 더 작아진다. 또 하나의 두드러진 득칭은 개시 삼중체와 16S rRNA 와 염기 짝짓기 를 하는 mRNA 의 풀리푸린 부분 사이의 거리가 일정하지 않다는 것이 다. 이 거리도 mRNA- 리보솜 복합체의 형성과 안정도에 중요한 영향을 미치는 요인이 될 것으로 생각되고 있다. 개시 코돈과 개시 자리 사이 의 거리는 평균 7 士 2 개의 누클레오티드로 되는 길이이다(표 3-2). 16S rRNA 의 3' 끝 부분에 대해서 상보적인 mRNA 의 길이가 어떤 경우에는 3 개의 염기 쌍 정도의 짧은 길이밖에 되지 않을 메도 있기 때문에, 자연의 mRNA 는 3 개 내지 4 개의 염기쌍들로 된 푼리푸린 연 속부분 앞에 가짜 AUG 삼중체가 오는 경우가 있다. 이러한 참재적 〈가짜〉 개 시 자리 들이 실 제 로 MS2 RNA 에 서 발견 되 었다 (그립 3-2 에 서 중합효소 개 시 자리 앞으로 하나가 있다) (Fie r s 둥, 1976) . 보통 은 이 부분들이 RNA 의 이 차구조에 묻혀 있어 서 16S rRNA 또는 개 시 t RNA 와의 염기 짝짓기 에 사용되지 않는다(그립 3-2 및 그립 3-5). 리 보솜이 잠재적 리보솜 결합 자리에 있는 비기능적 AUG 삼중체를 인식 하지 못하도록 mRNA 는 이차구조와 삼차구조를 사용하는 것으로 보 인다. 개시반응의 인식 단계에서 작용하는 인자는 IF-3 만이 아니다. IF-2 와 IF-1 들도 30S 개 시 복합체 의 형 성 에 있어 서 16S rRNA 의 3' 끝 부 근에 결합한다. 16S rRNA 의 이 부분은 mRNA 의 개시 자리를 인식하 . 는 데 관여하고 있으므로 IF-3 과 몇 가지 리보솜 단백질들이 30S 개시 복합체 형성에 관여할 것으로 생각된다. 16S rRNA 의 3· 끝이 위치하 는 영 역 에는 작은 하위 단위 체 단백 질 S7, Sl, Sll, Sl2, S18, 및 S21 등이 자리 잡고 있다 (그림 2-26 및 그림 2-39 를 보라) . Dahlberg 와 Dahlberg (1975) 는 16S rRNA 와 mRNA 와의 인 식 작용에 관해서 다음과 같은 모형을 제안하였다. 30S 리보솜 하위단위체에서, 16S rRNA 의 피리미딘이 많이 있는 연속부분들의 대부분은 머리 핀 모 양의 구조를 가지 고 있음으로써 mRNA 의 〈리 보솜 결 합 자리 〉와의 염 기 짝지음에 이용할 수 없게 된다. IF-3 및 30S 하위단위체의 S1 이 이 부분에 결 합함으로써 16S rRNA 의 3' 끝의 이 차구조가 풀리 어 서 mRNA 의 리보솜 결합 자리와 수소결합을 할 수 있게 된다(그림 2-22 및 그림 2-34 를 보라). 실제로 단백질 Sl 은 단일 가닥으로 된 풀리누클레오드
가 치쌓인 구조 또는 나사선형의 구조들을푸는 작용을 한다는 것이 알 려 져 있다 (Ste i t z 동, 1977) . 또한, 70S 복합체 에 있어 서 는, 16S 및 23S rRNA 둘의 두 3' 끝둘이 서 로 짝지 어 져 있 다 (그 립 4-3) (Van Duin 둥, 1976 ; Branlant 등, 1976) . 이러한 상호작용이 70S 쌍에 있어서의 50S 와 30S 하위단체들의 회합의 분자적 근거 가 된다. IF-3 이 16S rRNA 의 3' 말단에 결합하면 이 두
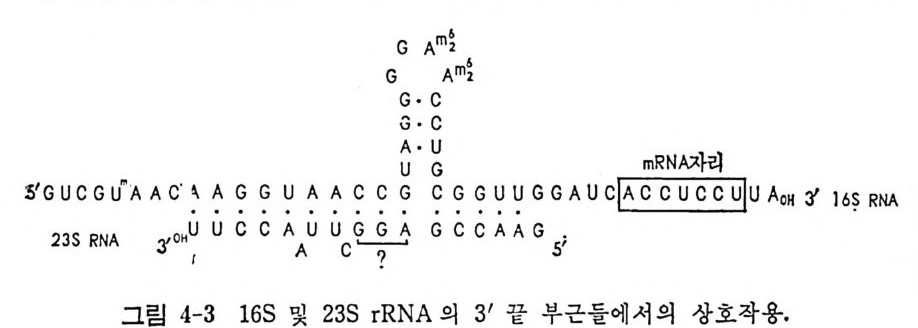 GG AmA•;m z‘
GG AmA•;m z‘
RNA 들 사이의 염기 짝짓기를 불안정하게 만듦으로써 자유 50S 하위단 위체와 30S-IF-3 입자의 형성이 증진된다. 4. 3.4 70S 개시 복합체의 형성파 IF-2 의 재이웅 위 에서 말한 바와 갇이, 완전한 30S 개시 복합체는 fM et- tRN A'Met' 완전한 GTP, mRNA , IF-2, 및 IF-1 들로 구성 된다. 30S 개 시 복합체 에 50S 하위단위체를 첨가하면 50S 하위단위체와 30S 개시 복합체가 집 합하여 fM et- tRN A '11•1 와 mRNA 를 1 : 1 의 몰 비 율로 함유하는 70S 개시 복합체가 형성된다. 50S 하위단위체의 결합이 일어나는 동안, 원 래 30S 개시 복합체에 있던 GTP 는 리보솜에 결합된 IF-2 에 의해서 GDP 와 P1 로 가수분해 된다. 이 때 IF-2, IF-1, GDP 및 P1 둘이 리 보 솜 복합체로부터 방출된다. 이 방출에 뒤아어서 70S 리보솜 복합체에 있 는 f Me t-t RNA ! Me t는 펩티드 결합의 형성 반응에 참여하게 된다. 펩티 드 결합 형성 반응성온 70S 에 결합한 f Me t-t RN A' 11 가 푸로마이신과 반응하는 능력으로 측정할 수 있다. 위에서 말한 것을 종합하여 하위단 위체들의 접합 반응을 다음과 같이 나타낼 수 있다. [30S · mRNA • IF-2 • IF-1 • fM et- tRN A '11•1 • GTPJ + 50S —+
(mRNA • 70S • fM et- tRN NM••J + IF-2 + GDP + P, + IF-1 가) GTP 가수분해의 역할 4. 4. 3 절 에서 언급한 바와 같이 , IF-2 는 70S 개시 복합체 형성에 있어서 화학양론적으로 작용하며, 복합체에 결 합된 채로 남아 있다. 30S 개시 복합체가 GTP- 의존적으로 형성될 때, IF-2 는 리보솜에서 떨어쳐 나온다. 그러므로, 개시 반응들에 있어서의 IF-2 의 작용은 촉매적이라는 것을 알 수 있다. 이와는 대조적으로, GTP 대신에 가수분해되지 않는 그의 유사체 GDPCP( 구아닐릴 메틸렌 이 인 산, GMP-P-CH2-P) 를 첨 가하면 IF-2 는 70S 리 보솜 복합체 에 결 합된 채 로 남아 있다 (Lelong 둥, 1970) . 다시 말하면 , IF-2 는 GTP 가 가수분해되어야 70S 개시 복합체에서 떨어쳐 나온다. 기능을 가진 70S 복합체 형성 에 GTP 가수분해의 에너지가 필요한지 를 알아보기 위 해 서 , Dubnoff 동 (1972) 은 30S 개 시 복합체 에 결 합되 어 있는 GTP 는 불안정하여서 37° 에서 15 분 항온처리한 후에 세파덱스 G-100 으로 겔 거르기를 하면 쉽게 제거된다는 사실을 이용하였다. 이 러 한 방법 으로 GTP 는 제 거 되 었지 만 fM et- tRN A 'M•1 를 함유하고 있는 30S 개시 복합체를 얻었다. GTP 를 가지지 않는 이러한 30S 복합체는 여전히 50S 하위단위체를 받아들여 펩티드기를 전달하는 능력을 가진 70S 복합체를 형성하였다. 복합체에서 제거한 GTP 는 아무 변화도 받 지 않고 있으므로, GTP 의 가수분해로 생기는 에너지가 70S 복합체의 형성 에 필요 없음을 확인할 수 있다. 그뿐 아니라, GDPCP 는 30S 개시 복합체에 있어서는 GTP 를 대신할 수 있지만, 여기에다 50S 하위단위체를 첨가하여 만든 70S 복합체는 펩 티드 결합의 형성 능력을 가지지 않는다. 그러나, 50S 하위단위체를 침 가하기 전에 GDPCP 를 30S 복합체로부터 제거하면, 형성되는 70S 복 합체는 펩티드 결합을 형성시키는 능력을 회복하게 된다. 이와 같이, GTP 또는 GDPCP 로써 형성한 복합체들의 행동은 동일하다. 어느 경 우에서 든, GTP 가 30S 개 시 복합체 에 계 속 남아 있으면 fM et- tRN A 'Me1 가 펭티드 결합 형성에 참여하지 못하게 방해한다. 이 누클레오티드가 제 거 됨 으로써 복합체 의 형 태 가 바뀌 어 서 fM et- tRN A 'M• ’ 가 반응할 수 있는 활동적 상태로 된다. 이와 같이, GTP 의 가수분해 에너지는 f Me t-t RN A' Me t가 70S 개시 복합체 상의 주개 자리 (P 자리)에서 올바른 위치를 잡도록 하는 데 필
요한 것이 아니라, 70S 복합체로부터 IF-2 및 〈결합된〉 GTP 룹 방출시 키는 데 사용되며, 이렇게 함으로써 펩티드 결합이 형성될 수 있게끔 fM et- tRN NM•• 를 활성 화시 킨 다. GTP 의 가수분해 와 IF-2 의 방출은 fM et 부분과 tR NA'M” 의 인 끝이 펩 티 덜 기 전달효소와 상호작용할 수 있도록 t RNA f Mc l 의 형태 변화를 유발하는 것으로 생각되고 있다. 나) IF-2 의 기능 IF-2 가 촉매로 재이용되려면 GTP 의 가수분해뿐 아 니 라 IF-1 이 요구된 다 (Chae 등, 1969 ; Str i n g er 등, 1977) . IF-1 아 없는 조건에 서는 , GTP 의존성 반응으로 형성된 70S 개시 복합체들은 GTP 가수분해가 일어난 뒤 에도 〈 결합된〉 IF-2 를 함유하고 있다. 이러 한 70S 복합체 에 IF-1 을 첨 가하면 IF-2 가 정 량적 으로 방출된다. 요컨대, 개시과 정 에서 GTP 가 하는 역할은 IF-2 가 30S 리보솜에 회 합할 수 있게 하는 입체 적 효과뭉질로서 작용하는 것으로 생각된다. GTP 의 가수분해는 한 입체 효과물질인 GTP 를 리보솜 복합체와의 친 화력이 약한 다른 입체 효과물질 GDP 로 전환시키는 데에 필요하다. GDP 는 리보솜으로부터 쉽게 해리하며, 이 결과로 IF-1 은 IF-2 를 결 합하고 있는 70S 리 보솜 복합 체 와의 단순한 상호작용만으로도 IF-2 를 방출시 킬 수 있 다. 다) ;L3 개시 복합체와 50S 하위단위체와의 결합에 필요한 개시 인자들 4. 5 절에서 곧 논의될 것이지만, 진핵세포의 개시 반응에 있어서는 60S 하 위단위체와 40S 개시 복합체의 결합에 특수한 단백질 인자 eIF-5 가 관· 여한다. 박테리아의 세포에 있어서도 하위단위체들의 결합에 개시 인자 둘이 있 어 야 하는지 물 알아 보기 위 해 서 Str i n g er 등 (1977) 은 풀리 (U, G) 를 mRl'-.rA 로서 사용하고 IF-3 과 IF-1 들이 없는 조건 에서 30S 개 시 복합체 를 만들었다. 그 다음에 이 복합체를 항온처리하여 IF-2 와 GTP 둘을 해리시켜 제거함으로써 f Me t-t RNA f Me t는 가지고 있지만 개시 인 자들과 GTP 둘을 가지고 있지 않는 30S 복합체를 만들었다. 이 복합책 는 50S 하위단위체와 결합하여 펩티딜 기의 전달 능력을 가지는 70S7m 시 복합체를 형성할 수 있다는 것을 알았다. 그러므로, 일단 fM et... :. tR NAfM et 가 30S 하위 단위 체 에 결 합되 면, 50S 하위 단위 체 들이 집 합하여 활동적인 70S 복합체를 만듦에 있어서 개시 안자들이나 GTP 가 불필요 하다는 것을 알 수 있다.
Str i n g er 등은 갇은 실험 에서 IF-2 와 GTP 가 밀접한 관계를 가지고 있음을 알았다. 죽, GTP 가 있는 조건에서 70S 복합체가 형성될 경우 에만 IF-2 가 30S 개시 복합체 에 계속해서 있을 필요가 있다는 것을 알 았다 . 생체 내에서는, GTP 를 제거할 수 있는 유일한 길은 70S- 의존성 IF-2-GTPase 활동성 에 의한 가수분해밖에 없으므로 30S 복합체와 50S 하위단위체가 집합할 메, IF-2 가 30S 복합 체 상에 꼭 있어야 한다. 따 라서, 30S 복합체 형성에 있어서의 IF-1 의 중 요한 역 할 이 무엇인지 를 침작할 수 있다. IF-1 은 IF-2 를 개시 반 웅 전체 를 동하여 30S 복합체 에 묶어 둠으로 써 IF-2 로 하여 금 GTP 들 가수분해 하게 하고, 활동적 70S 복합체가 쉽게 형성될 수 있게 돕는다. 4.4 원핵세포에 있어서의 개시 과정예 관한 결론 위 에서 기술한 여러 실험결과들을 종합함으로써 활동적 인 70S 개시 북 항체 형성에 있어서의 일련의 반응둘을 다음과 같은 순서로 나타낼 수 있다. +IF-3, IF-1 70S 一 50S + [30 • IF-3 • IF-1) [3 0S• IF-3 • IF-1) + IF-2 - [30S • IF-2 , IF-1 • IF-3) +mRNA ―一 [30 S• mRNA • IF-2 • IF-1 • IF-3] (30S • mRNA • IF-2 • IF-1 • IF-3) + fM et- tRN NM + GTP 一 [30 S• mRNA • IF- 2 • IF-1 • fM et- tRN NM•• • GTPJ (30S 개시 복합체) + IF-3 (30S • mRNA • IF-2 • IF-1 • fM et- tRN A '~1 • GT 円 + 50S 一 [m RNA • 70S • fM et- tRN A 'M J + IF-2 + GDP + P, (활동적 70S 개 시 복합체 ) + IF-1
4.5 진핵세포의 개시 복합체 형성과 관련된 성분들 단백 질 합성의 개시 과정은 진핵세포들과 원핵세포들에 있어서 똑같 은 기본 메카니즘에 따라서 일어난다. 개 시 t R NA 는 GTP- 의존성 반 웅으로 작은 리보솜 하위단위체에 결합되 어서 mRNA, GTP 및 개시 t RNA 둘을 합유하는 리보솜 하위단위체 복합체를 만 든다. 그 다음에 이 복합체는 큰 리보솜 하위단위체 와 결합하여, mR NA 를 번역 할 수 있는 개시 복합체 융 헝성한다 . 진핵세 포에서의 단백 질 합성 의 개시에 관해서 는 다음의 평 론서 들을 참고하라 . (Kozak, 1978; Mait ra 등, 1982; Her-shey , 198 2 ; Kozak, 198 3. ) 원핵세포와 진핵세포에 있어서의 개시 과정이 기본적으로 비슷한 것 은 사 실 이지 만 , 세부적인 면에서는 중요한 차이점들이 있다. 이것을 표 표 4-4 단백 질 합성의 개시에 있어서의 원핵세 포와 진핵세포 사이의 차이 원핵세포 1 진핵세포 • 리 보송은 작으며 덜 복잡하 다. • 크기 와 복잡도가 크다. · 개시 인자의 수 :3 개 .10 개 • 삼성분 복합체 : GTP • 개시-t RNA • I • GTP • 개시-t RNA • eIF2 IF2 •개시 t RNA 의 메티오닌 : 포르밀화되 •메티오닌의 NH2 기가 포르밀화 되어 어 있다. 있지 않다. • 개 시 코돈 : AUG, GUG I • AUG 뿐 .그람+, ATP?; 그람-, ATP 가 관여 •mRNA 결합에 ATP 가 필요하다. • 하다시지 스않트음론 성 (내 부에 서 개 시 가능) I• 단일 개 시 자리 .. 그람+ 와 그람- 에서, mRNA 를 선 • 번역의 목이성이 덜하다. 택적으로 식별 가능 •mRNA 의 개시 부분의 조각은 리보 •80S mRNA 개시 조각은 리보송에 재 송에 재결합할 수 있다. 결합하지 못한다. • 30S 와 70S 로 보호되 는 mRNA 부분 • 40S 는 BOS 가 보호하는 것보다 더 긴 이 갇다. 부분을 보호한다. •30S 개시 복합체 형성에 있어서의 •40S 개시 복합체 형성에 있어서는 fM et- tRN AM•’ 와 mRNA 의 결 합 순 Met- tRN AM•' 가 mRNA 보다 먼저 서 : 어느 것이 먼저 결합하여도 좋다 결합해야 한다.
4-4 에 요약하였다. 진핵세포의 단백질 생합성 계는 리보송이 크고 복잡 하다는 사 실 뿐 아니라 관여하는 개시 인자들이 많다는 점에서도 상당히 복잡하다. 개시 인자들로 인정되고 있는 것이 10 가지이지만 그 중 두 가지는 아직 정제되 지 않은 조참한 분획이다 . 개시 복합체 형성 에 있어 서 원핵세포의 경우와 다론 중요한 점은 mRNA 의 결합에 ATP 가수분 해가 필요하다는 것이다. 개시 과정에 있어서 가장 두드러진 차이들 은 원핵 세포와 진핵세포의 mRNA 들의 구조적인 차이에서 기인된다 . 원핵세포 의 경우와는 대조적 으로, 진핵세포에서의 번역의 개시는 시스트 론 의 일 부가 전사되자마자 곧 개시될 수 없다. 생성된 선구체 mRNA 는 먼저 핵 의 염색질에 있어 서의 합성 자리에서 세포질로 수송되어야 한 다 . mRNA 의 선구체는 꼬 아잇기와 · 갓형성 등과 같은 성숙 과정을 거쳐서 단일 시스트론성 mRNA 로 가공된다(제 3 장). 또 하나의 현저한 차이는 진핵세포의 리보솜은 mRNA 의 내부의 연 속부분에 결합할 수 없다는 것이다. 제 3 장에서 이미 기술한 바와 같이 진핵세포의 mRNA 는 기능적으로는 단일 시스트론성이며 (물론 구조적 으로도 단일 시스트론성이다), 리보솜은 5' 끝에 가까운 데 있는 개시 코돈만을 인식한다. 또 하나의 주목할 만한 차이는 원핵세포의 리보솜은 mRNA 식별능이 매우 큰 데 반하여 진핵세포의 mRNA 식별능은 작다는 것이다. 예를 들 면, 그람 양성인 박테리아의 리보솜은 그람 음성인 박테리아에 감염하 는 파지의 mRNA 를 번역할 수 없다. 이러한 특이성은 개시 반응에 관 련되는 인자들에 기인되는 것이 아니라 30S 하위단위체 자체에 기인된다 (Lod ish , 1970). 진핵세포의 리보솜은 광범한 종류의 원핵세포의 mRNA 를 번역할 수 있다. 다만 번역의 효율은 갓을 부착시킴으로써 많이 중 가한다 (Pate r son 과 Rosenberg, 1979 ; Rosenberg 와 Pate r son, 1979) . 예 를 들면, 5' 끝 쪽으로 era mRNA 를 가전 A 파지의 다시스트론성 mRNA 인 80S era mRNA 가 만일 갓 구조를 가지면 밀싹의 단백질 합 성 계에 의해 번역되어서 경상적인 단백질이 합성된다. 마지막으로, 또 하나의 중요한 차이점이 있다 . 진핵세포에 있어서는 40S 하위 단위 체 가 핵 산 가수분해 효소의 작용으로부터 보호하는 개 시 자 리의 결편들의 길이는 80S 리보솜이 보호하는 절편들의 길이보다 상당 히 길다. 이것은 E. co li의 30S 와 70S 리보솜으로 보호되는 개시 절편
들의 길이가 거의 같은 것과는 매우 대조 적 이다 . 80S 리보 송으로 보 호 된, 갓울 잃은(가수분해로 인해서) 개시 절편이 리보솜에 재결합하지 않는 데 반해 서 , 70S 리 보솜으로 보호된 컬 편은 70S 리 보솜과 효과적 으로 다시 결합할 수 있다. 진핵세포의 리보솜들과 개시 인자들의 구조적 차원에서의 복잡성이 큰 이유는 진핵세포에 있어서의 단백질 합성을 번역 수준에서 조종하는 데 필요한 구조적인 요소가 추가되기 때문일 것으로 추측된다. 일반적 으로 원핵세포에 있어서의 단백질 합성의 조철은 전사 수준에서 조종되 고 있다. 4. 5. 1. 개시 인자들 진핵세포의 단백질 합성의 개시 과정에 관한 연구에 제일 많이 이용 되는 계는 토끼의 망상 적혈구이며, 오늘날까지 적어도 8 가지의 개시 인자들이 분리되어 있다 (Ma it ra 등 (1982) 의 평론서를 보라). 토끼의 망 상 적혈구가 많이 이용되는 이유는 이 세포에는 핵이 없기 때문에 전사 수준에서의 조절의 영 향을 전혀 받지 않는 조건에서 번역의 개시 과정 을 연구할 수 있기 때문이 다. eIF-1, eIF-2, eIF-3, eIF-4A, eIF-4B, eIF-4C, eIF-4D, 및 eIF-5 둘은 자연의 mRNA( 예, 글로빈 mRNA) 의 번역을 촉진시키는 그들의 능력에 기초하여 염 용액으로 씻어서 얻은 리보솜 단백질들의 조잡한 혼합물에서 분리하였다. 번역 반응을 일으키 기 위해서 사용하는 계는 특정한 아미노아실-t RNA 둘, 두 연장인자들 (EF-1 과 EF-2, 제 5 장 참조) , ATP, 및 GTP 둘을 함유하는 찰 정 재 된 분획이다. 그 다음에는, 각 개시 인자가 방사성 Me t-t RNA1M et와 mRNA 의 작은 리보솜 하위단위체 (40S) 로의 순차적인 결합울 증진시카 는 능력, 그리고 큰 리보솜 하위단위체 (60S) 와의 결합으로 기능을 가진 80S 개시 복합체가 형성되는 것 둥을 조사한다. 개시 복합체를 형성하는 데 필요한 개시 인자들 수는 아직 확실하지 는 않지만, 적어도 8 가지의 인자들이 있을 것으로 생각되고 있다(표 4- 5). eIF-4B 를 제의한 다른 인자들은 정제되어 있다. 자연의 mRNA 를 사용할 때에는, eIF-2, eIF-3, 그리고 eIF-5 들만이 기능을 가진 BOS 개시 복합체의 형성에 절대적으로 필요한 것으로 보인다 (Schre i er 동, 1977; Trachsel 등, 1977; Benne 와 Hershey, 1978). eIF-1, eIF-4 A ,
표 4-5 토 끼 의 망 상 적혈 구로부터의 가용성 단백 질 인자 들 e개I F시- 2 인자| 麟1갭1505.. O o III !겁13 펩 (~2 ?) I Met- tRN AIMeI 기및 G능 TP 와 삼 성 분 eIF-1 mRNA 의 결합을 증진 시 킴 복합체 를 만 듦 eIF-3 약 700. 0 약 9 Me t- tRN Ai hI e1 및 mR NA 의 결합 을 eIF-4A 49. 0 1111m1R증N1진A시 의 킴 결; 합해을 리- 중진시킴 e!F - 4B 80.0 mRNA 의 결합운 중 진 시킴 e!F-4C 17.5 Met- tRN A ?1•1 의 전 합윤 중진 시 킴 e!F-4D 16.5 Me t무로 마 이 신 형성운 촉진함 eIF-5 150.0 80S 복합 체 형성에 필 요 합 Co-e!F-2 22.0 삼성분 복합체 형성웅 촉 진 함 갓백결질합 단 24.0 1 mRNA 의 갓 과 전합합 eIF-4B, eIF-4C, 및 eIF-4D 둘은 필 수적 인 것은 아니 지 만 복합체 형성 을 2~3 배로증진시킨다. 자연의 mR N A 대신에 A U G 를 주형으 로서 사 용하였을 때는 eIF-2 와 eIF-5 들만이 80S 개시 복 합체 형성 에 필 수적이 고 eIF-3 은 다만 개시 복합 체 의 형성을 2 배로 증진시키는 역 할 을 할 뿐 이다. 이러한 결과들에서, 자연의 mRNA 의 결합과 인식에는 eIF-3 과 ATP 의 가수분해가 필요하며 , eIF-4A , eIF-4B, eIF-4C 인자 들 이 촉진 제로서 작용한다는 것을 알 수 있다. 이것은 원핵세포의 경우 IF-3 이 자연의 mRNA 의 결합에는 꼭 필요하지만 합성 mRNA 또는 AUG 삼중 체의 결합에는 IF-3 이 필요치 않다는 것과 유사하다. 시 험 관 내에서의 진핵세포의 개시 반응은 다음과 같은 적어도 네 개의 단계 들 로 진행되 는 것으로 생각된다. (1) eIF-2 • GTP • Met- R NA1M 삼성 분 복합체 의 형 성 (2) 40S 리보솜 하위단위체로의 삼성분 복합체의 전달 (3) 40S 개시 복합체와 mRNA 와의 결합 (4) 40S 개시 복합체와 60S 하위단위체와의 결합 이 단계들을 그림 4-4 로 나타내었다. 이 도식은 개시 복합체가 조립 되는 경로와 각 단계에서 어떤 인자들이 관여하는지를 나타낸다. 시험
 따re IRlNFA 7- —2 GTP 二 !T:IF- 2 eIF-3 4—0S 리보송 하위막단는 위다제) .
따re IRlNFA 7- —2 GTP 二 !T:IF- 2 eIF-3 4—0S 리보송 하위막단는 위다제) .
관 내에서의 실험으로 얻은 분석결과들 중 아칙 문계가 되고 있는 것은 eIF-5 를 제의한 다른 인자들이 개시 반응에서 촉매적으로 작용하는지 에 대한 증거가 전혀 얻어지지 않고 있다는 것이다. 개시 반응과 같은 계의 필수적인 요건은 개시 인자들이 반응 회로로 다시 들어가서 재이 용되어야 하는 것인데, 오늘날까지의 시험관 내 (즉, 무세포 계)에서의 분석 결과로 볼 때 이러한 성질을 가진 어떤 성분(또는 성분들)이 한정 된 양으로 함유되어 있거나 아니면 결핍되어 있는 것으로 보인다. 앞으 로 이러한 인자들이 발견되어야 개시 반응의 순환성 본질과 경로가 밝
혀질 수 있을 것이다. 4. 5. 2 개시 인자들의 기능을 보조하는 인자들 위에서 말한 인자들 이의에도 개시 반응들에는 그밖의 인자들이 관여 한다는 실험결과들이 있다. 가) Co-e1F-2A, Co-elF-2B, 및 Co-elF-2C 이 단백 질 인 자들은 삼성 분 복합체들의 형성을 조종하는 역할을 하는 것 으로 알려져 있다. 분자량 20 kdal 인 Co-eIF-2A 는 삼성 분 복합체 를 안정 시 키 며 (Maju m dar 동, 1979) , Met- tRN A1M et 의 40S 리 보솜 하위 단위 체 와의 결 합 속도를 중가시 킨 다 (Dasg u p ta 등, 1978 ; Ghosh-Dasti da r 둥, 1980 ; Roy 둥, 1981) . 이 인자의 순수한 제조물에 대한 항혈청은 토끼의 망상 적혈구의 추출 물로 구성한 단백질 합성계에서 단백질 합성을 강력하게 방해한다. 12 내지 15 개의 폴리펩티드들로 이 루어진 분자량 450 kdal 의 큰 복 합체인 Co-eFI-2B 는 〈 삼성분 복합체 해리 인자〉이다. 이 인자는 삼성 분 복합체의 해리를 촉매할 뿐 아니라, AUG 의 존재 하에서 일어나는 Me t-t RNA?1” 의 40S 리보솜 하위단위 체 와의 결합에도 관여한다. 그러 므로 이 보조인자는 eIF-3 과 비슷한 역할을 하는 것으로 보인다 (Gu pt a 등, 1975 ; Maju m dar 등, 1977) . 망상 적혈구의 리보솜을 높은 농도의 염 용액으로 씻은 액에서 정제 한 단백질 분획인 Co-eIF-2C 는 M g 2+ 의 존재 하에서 elF-2 에 의한 삼 성분 복합체의 형성을 증진시키며, AUG 의 존재 하에서 eIF-2- 의존성 으로 일어나는 Me t-t RNA 전의 40S 리보솜과의 결합을 촉진한다 (Das 동, 1982). 나) elF-2- 촉진성 단백질 Arte m i a sa lin a( 새우의 일종)와 토끼의 망상 적혈구의 리보솜울 염 용액으로 씻어서 얻은 단백질 혼합물에는 eIF-2 의 삼성분 복합체 및 40S 복합체 형성 능력을 중진시키는 eIF-2- 촉진 성 단백질이라고 불리는 인자가 들어 있다 (de Haro 와 Ochoa, 1979). eIF-2- 촉진성 단백질은 eIF-2 와 GTP 로 이루어지는 이성분 복합체를 안정 시 키 며 , 이 복합체 에 Met- tRN A1M” 가 결합하여 삼성 분 복합체 가 형성될 때 이탈된다는 것이 중명되었다 (S i e ki erka 동, 1982). eIF-2- 촉
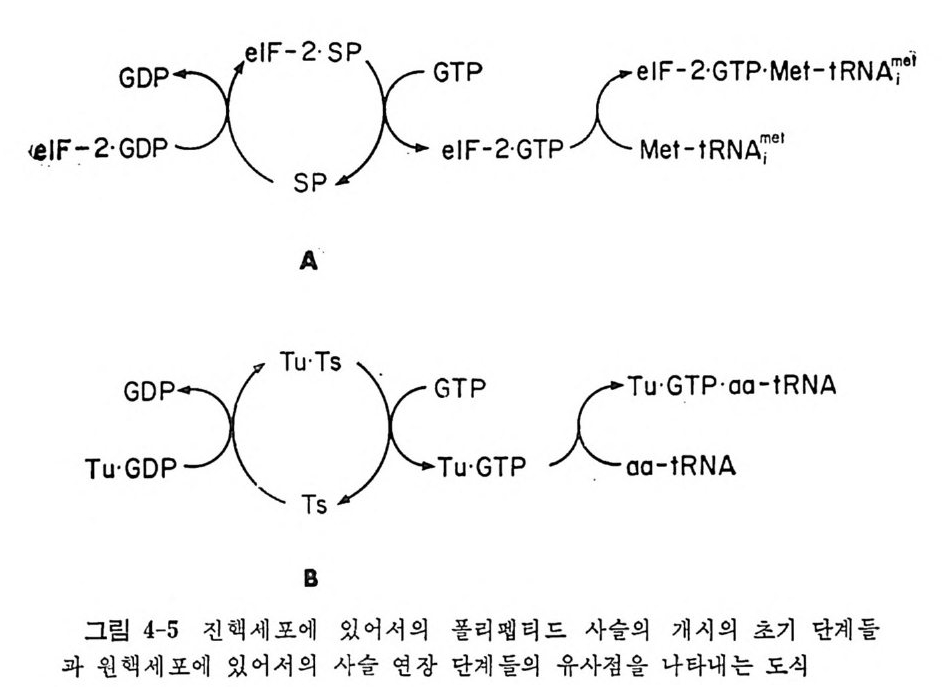 遣 IF-2 GGDDPP 二-..... 〈Fe.|.F -S-2PS -〉P \ 二,,..-- G eT|FP- 2GTP< .,....eMl Fet-- 2t·GRT NPA·M?'et - tRN A'mi Ci
遣 IF-2 GGDDPP 二-..... 〈Fe.|.F -S-2PS -〉P \ 二,,..-- G eT|FP- 2GTP< .,....eMl Fet-- 2t·GRT NPA·M?'et - tRN A'mi Ci
진성 단백질의 작용을 그림 4-5 에 나타내었다. 이 그림에서 알 수 있 듯이 , 진핵 세 포의 단백 질 합성 에서 삼성 분 복합체 eIF-2 • GTP • Met- t RNA i M e t가 형성되는 초기 단계들이 원핵 세포에 있어서 삼성분 복합 체 EF-Tu • GTP • aa- t RNA 가 형성되는 초기 연장 단계와 밀접한 유 사성을 가지고 있다는 것은 매우 홍미있는 일이다• 다) mRNA- 방해작용에 대한 반대작응을 하는 인자 mRNA 는 eIF-2 에 결 합하여 eIF_2 의 3 개의 하위단위체들을 해리시킴으로써 삼성분 복합체 의 형 성 을 강력 하게 방해 한다 (Barrie u x 와 Rosenfe ld , 1978; Chaudhuri 동, 1981) . 이 러 한 방해 작용을 막는 단백 질 분획 이 A. salin a (Malath i 와 Mazurnder, 1979) , 토끼 의 망상 적 혈구에서 분리 되 었다 (Roy 등, 1981). 토끼의 망상 적혈구에서 얻은 인자는 Co-eIF-2A 와 동일한 것으로 생 각되고 있다. 라) elF-6 밀 싹 (Russel 과 Sp re mulli, 1979) 과 소의 간 추출물 (Valen-zuella 등, 1981) 에서 분리 한 분자량 23. 0~25. 0 kdal 인 이 인자는 40S
및 60S 하위단위체들의 풀을 유지하는 역할을 하는 것으로 생각되고 있 다. 이 인자는 60S 리보솜 하위단위체와 결합하여 40S 하위단위체와의 회합을 막는 항해리 인자의 역할을 하고 있다. 그러나 이미 회합되어 있는 80S 리 보솜을 해 리 시 키 는 작용은 하지 않는다 (Valenzuela, 1981) . 4.6 개시 인자들의 물리적 성질들 eIF-2 와 eIF-3 千 인자들을 제외한 다른 개시 인자들은 모두 단일 풀 리펩티드 사슬로 이루어져 있다(표 4-5 를 보라). 그 분자량듄은 eIF-1 의 15. Okdal 에 서 eIF-5 의 150. Okdal 에 이 르기 까지 광범 하다. 토끼 의 망상 적 혈 구 에 서 얻 은 eIF-2 는 a (32~38 kdal) , {3 (48~52 kdal) , 및 r(50~57 kdal) 동 세 개의 하위 단위 체들이 1 : 1 : 1 의 화학양론적 관 계로 구성되어 있는 것으로 생각되고 있다 (Sa fe r 등, 1976; Llyo d 등, 1980) . 그러 나, Harbit z 와 Haug e (1979) 그리 고 Str i n g e r 동 (1980) 은 두 개 의 하위 단위 체 들 (분자량 48 kdal 및 38 kdal) 로 된 활동적 eIF-2 를 돼지의 간과 토끼의 망상 적혈구에서 정제하였다• 두 개의 하위단위체 로 된 eIF-2 를 다른 연 구진 에 서 도 얻 었 다 (Mi tsu i 등, 1981) . Hershty (1982) 도 두 개 의 하위 단위 체 로 된 eIF-2 를 얻 었 는데 f3 하위 단위 체 가 결핍된 것으로 생각하고 있다. 그러나, 두 하위단위체로 된 eIF-2 의 생 리적 역할에 대해서는 아칙 찰 모르고 있다. eIF-3 은 많은 폴리펩티드 하위단위체들로 구성되어 있으며 전체 분 자량은 500 kdal 이상이고 침강계수는 15S 와 18S 사이의 값을 가진다. elF-3 을 이루는 하위단위체들의 수와 그들의 화학양론적 관계는 아직 밝혀지지 않았다. 4.7 80S 개시 복합체의 조립에 관여하는 부분 반응둘 4.7.1 진핵세포의 리보솜 하위단위체 플의 생성 단백질 합성의 개시는 분리된 하위단위체들 상에서 일어나기 때문에 40S 와 60S 하위단위체들의 풀을 유지하기 위한 데카니즘, 또는 80S 러
보송들에서 이 하위단위체둘을 발생시키는 메카니즘 이 있어야 한다. 망 상 적혈구의 추출액 또는 복수 세포에서 분리한 eIF-3( 분자량 >500 kdal) 은 40S 리보솜 하위단위체들에 결합하여 40S 하위단위체들이 60S 하위 단위 체 들과 재 회 합하는 것 을 막는다. 즉, eIF-3 은 항회 합작용을 하는 것 으로 생 각되 고 있다 (Trachsel 과 Sta e helin , 1979) . 포유동물의 계 들에 서는 항회합작용을 하는 안자들의 기능에 있어서 아직 불분명한 데가 있 음에 반해 서 , 최 근 밀 싹 으로부터 항회 합작용을 하는. eIF-6 라는 작은 단 백질 (분자량 =23 kdal) 이 발견되었 는데, 이 인자는 60S 하위단위체에 결합함으로씨 이 하위단 위체가 40S 하위단위체와 재회합하는 것을 막는 戶 다는 것 이 밝혀 졌 다 (Russell 과 Sp re mulli, 1980) . 분자량이 25kdal 에 서 120kdal 되는 11 가지 풀 리 펩티 드들로 이루어지는 큰 단백질 복합체 인 밀싹의 e IF-3 은 하위단위체들의 재회합을 막거나, 80S 리보솜을 해 리 시 키 는 작용을 하지 않는다 (Checkley 등, 1981) . Checkley 둥의 결 과 와 일치하는 결과를 Valenzuel 등 (1981) 도 얻었다. 이 연구자들은 소 간 의 추출뭉에서 리보솜의 하위단위체의 재회합을 막는 활동성을 가진 분 자량 25.5 kdal 의 단일 단백질을 얻었다. 소 간에서 얻은 이 인자는 밀 싹에서 얻은 eIF-6 와 매우 바슷한 성질들을 가지고 있다. 리보솜 하위 단위체 항회합작용 또는 80S 리브송의 해리작용을 가진 그밖의 어떤 단 백질 인자가 소의 간 추출 물에 있다는 증거는 없다. 그러므로, 포유동 뭉에 있어서의 리보솜 항회합 활동성이 eIF-6 에 있을 것으로 추측할 수 있다. 고분자량의 eIF-3 에 리보솜 항회합 활동성이 있는 이유는 eIF-6 과 유사한 단백질이 eIF-3 과 회합되어 있는 데 기인될 수도 있겠지만. 아직 그러한 단백질을 eIF -3 에서 분리한 연구는 없다. 4. 7. 2 삼성분 복합체 형성 elF-2 는 GTP 의 존재 하에서 Me t-t RNA,M et와 특이하게 결합하여 삼 성 분 복합체 eIF-2 • GTP • Met- tRN A1M•' 를 형 성 한다• 이 복합체 에 서 의 GTP 와 Met- tRN A1M•t 의 몰 바 는 1 : 1 이 다 (Ranu 와 Wool, 1~76 ; Str i n - ge r 등, 1979 ; Str i n g e r 등, 1980) . GTP 의 비 가수분해 성 유사체 를 삼 성분 복합체 형성에서 GTP 대신에 쓸 수 있다. 이 사실은 삼성분 복합 체 형성에 있어서 GTP 가 하는 일은 다른자리 입체성 효과물질로서 작 용하는 것이며, 가수분해에서 발생하는 에너지를 공급하는 것이 아님을
알 수 있다 (Dett m an 과 Sta n ley, 1972) . 이 성 분 복합 재 eIF-2 • Met- tR NA1M 는 안정 하게 형 성 되 지 만 (Safe r 등, 1975) , eIF-2 와 GTP 사이 의 안정한 이성분 복합체는 형성되지 않음이 밝혀 졌다 ( Chaudhur i 등, 1981) . 그렇 지 만 elF-2 는 GTP 와는 강력 하게 결 합한다 (Walto n 과 Gil l, 1976; Str i n g er 등, 1977) . eIF-2 인자를 이 루는 3 개 의 하위 단위 체 들을 가지고 한 분석결과에 의하면 분자량 48 kdal 의 두 하위단위체들은 Me t-t RNA;M 와 mRNA 들과 결합하는 활동성을 가지고 있고, 작은 하 위단위체는 GDP 를 결합하는 활동성을 가지고 있다. 교차결합법에 의 해서도 큰 하위단위체가 Me t-t RNA1M 와 결합할 것이라는 결과를 얻었 다 (Ny ga rd 등, 1980) . 4. 7. 3 삼성분 복합체와 40S 하위단위 체와의 결합 개 시 반응의 다음 단계 는 삼성 분 복합체 eIF-2 • GTP • Met- tRN A1Mu 와 40S 리보솜 하위단위체와의 결합이다• 삼성분 복합체의 세 성분들은 모두 1 : 1 : 1 의 비로 하위단위체와 결합되어 있다 (Trachsel 과 Sta e he- lim , 1978 ; Pete r son 등, 1979) . 그러 나 삼성 분 복합체 가 40S 리 보솜 하 위단위체로 전달될 때 요구되는 목이한 조건들이 무엇인지는 아직 잘 모 르고 있다. eIF-2 와 GTP 의 존재 하에서 는 Met- tRN A1M•' 는 AUG 또 는 mRNA 가 없어도 40S 하위단위체와 결합할 수 있다. 이 결합은 eIF-3 과 eIF-1 에 의 해 서 더 안정 하게 된다 (Benne 와 Hershey, 1978; Pete r son 동, 1979) . eIF-3 와 삼성 분 복합체 eIF-2 • GTP • Met- tRN A,~!.' 는 모 두 서로의 존재에 무관하게 40S 하위단위체에 결합할 수 있으며, 서로 다른 성분의 결합을 증진시킨다. Me t-t RNA1M•’ 와 40S 하위단위체 와의 결합이 최대한으로 일어나려면 또 하나의 개시 인자 분획이 추가로 요 구될 것 이 라고 생 각하는 사람도 있다 (Maju m dar 등, 1977) . 그러 나, Maju m dar 등 (1979) 은 최 근 에 Met- tRN Ail ! et 와 40S 하위 단위 체 와의 결 합은 AUG 코돈에 의존해서 일어나는 것임을 발견하였는데 이것은 Str ing er 등 (1980) 에 의해서 확인되었다. 40S 개시 복합체 형성이 AUG 코돈 의 존성 이 라는 것은 Gup ta 등 (1975) 이 처 음으로 밝혔다.
4.7.4 mRNA 의 결합 mRNA 가 없어 도 l\tle t- tRN A1M 는 eIF-2 와 GTP 들과 함께 40S 하의 단위 체 에 결 합할 수 있다 . 이 사실은 Met- tR NA?'’ 와 40S 리 보 송 하위 단위체와의 결합은 그 다음에 일어나는 mRNA 의 결 합을 위한 필수조건 임을 암시해 준다. 이 메카니즘에 따르면, 다른 모든 개시 인자들이 존 재하더라도 Me t-t RNA1M• t가 없을 경우에는 mRNA 가 리보송에 결합할 수 없 을 것 이 다 (Darnbro11g h 등, 1973 ; Trachsel 등, 1978 ; Benne 등, 1978) . eIF-2 는 mRNA . rRNA . tR NA, 및 마이 너 스 가닥의 비 루스 RNA 들과 같은 여러 가지 RNA 들과 결합할 수 있는데, 그 중 천핵세포의 mRNA 들에 대한 천화력이 제일 크다. 그리고 eIF-2 와 mRNA 의 결합은 매우 큰 독이성을 가지고 있다. 이러한 관찰에서 eIF-2 는 mRNA 의 인식과 40S 하위단위체에의 결합에 중요한 역할을 할 것으로 믿어지지만, 아직 mRNA 의 리보솜과의 결합에서 eIF-2 가 하는 역할은 찰 모르고 있다 (Kaemp fer (1982) 의 평 론서 를 보라) . elF-3 은, 원핵세포에 있어서의 그의 상대물안 IF-3 과 마찬가지로, 자연의 mRNA 의 번역에 필수적인 인자이다. 이 인자는 ATP 와 GTP 등을 바롯한 그밖의 개시 인자들의 존재와는 무관하게 40S 하위단위체 에 결합할 수 있음이 밝혀졌다 (Benne 등, 1976; Thomp so n 등, 1977; Pete r son 등, 1979) . eIF-3 이 mRNA 의 번 역 을 촉진 시 키 는 메 카니 즘은 아직 밝혀져 있지 않지만, eIF-3 은 40S 하위단위체와 결합함으로써 mRNA 의 인식 자리와 결합 자리를 형성하는 것으로 생각되고 있다 (llan 과 llan, 1976) . 자연의 mRNA 는 광범위한 이차구조를 함유하고 있으며, 글로빈 mRNA 의 경우에는 염기들의 70% 가 염기 쌍을 이를 수 있도록 배열 되 어 있는 것으로 추산되고 있다(H older 와 Lin g rel, 1975). mRNA 의 이차구조는 큰 에너지 장벽을 가진 형태이기 때문에, 코돈들이 번역될 수 있게 노출되려면 이차구조가 풀리거나 이완되어야 한다. eIF-3 이 이 러한 풀림 과정에 관여한다는 중거가 있다(I Ian 과 Ilan, 1976). eIF-2 와 eIF-3 이 의 에 도, mRNA 의 결 합을 촉진 하는 eIF-4A, elF- 4B, 그리고 ATP 등 세 가지 인자들이 있다는 것이 알려쳐 있지만, 아
직 자세한 기능은 찰 모르고 있다. 이 인자 들 중의 어느 하나라도 빠지 면 결 합된 Met- tRN A;M•1 의 양은 전 혀 감소되 지 않지 만, mRNA 의 결 합이 상당히 감소된다. AUG 삼중체 또는 글로빈 mRNA 를 전령 RNA 로서 사용되었을 때 이 인자들은 메티오닐구 E 로마이신의 합성에는 거의 영 향을 미 치 지 않는다. 그러 나, eIF-4A, eIF-4B, 그리 고 eIF--1C 등을 단백질 합성 계에서 빼면 글로빈 합성이 상당 히 감소된다. 4. 7. 5 단백질 합성의 개시 파정에 있어서의 5' ~의 역할 진핵세포의 대부분의 mRNA 둘은 그들의 5' 끝에 갓 구조 (m 1 G ppp Xm p ) 를 가지고 있다 (3. 2. 3 절의 (가)항을 보라). 갓 구조가 개시 반응의 효 율을 증진시킨다는 것은 많은 연구들로 확인되었다. 두 가지 실험 예 들 울 들어 보자. 갓 형성 과정이 방해된 계에서 분리한 mRNA 의 5' 꾼 에 갓 구조를 효소적으로 첨가하면 mRNA 의 리보솜 하위단위체등에 대한 친 화도가 중가한다 (Muth ukris h nan. 1978) . m1GMP. m7 GD P. 그리 고 m7Gp ppN m 등과 같은 갓 구조 유사체 들은 갓 울 가진 mR: \IA 둘의 리 보솜 에의 결합을 방해할 뿐 아니라, 세포 추출액에 있어서의 갓울 쓴 mR'.'\A 의 번역을 방해한다 (Nakash i ma 등, 1979). 이 연구결과 들은 리보솜에 갓울 쓴 mRNA 를 인식하는 특이한 자리가 있거나, eIF-2 에 갓울 쓴 mRNA 를 인식하는 특이한 자리가 있어서 그 mRNA 믈 인식한 다음에 리보솜에 결합시킬 것임을 암시해 준다. 그렇지만, eIF-2 가 mRXA 를 인식하는 데 갓 구조가 꼭 필요한 것이 아닐 것이라는 실험결 과가 있 다. 멩고비루스 RNA 또는 STNV RNA 들은 갓을 쓰지 않고 있지만 굳 로빈 mRNA 보다 더 찰 eIF-2 에 결 합한다 (Perez-Bercoff . 1982) . 5' 갓은 mRNA 의 40S 리보솜 하위단위체와의 결합을 안정시키는 것 이 그의 중요한 역할일 것으로 생각된다. 4.3.3 절의 (나)항에서 기숭 한 바와 같이, 원핵세포에 있어서는 16S rRNA 의 3' 끝 부분이 mRNA 의 AUG 코돈의 상류 쪽으로 있는 폴리푸린 부분과 염기 짝지움을 한다 는 강력한 중거둘이 있다. 진핵세포들의 mRNA 와 rRNA 들의 분석결 과는 원핵세포에 있어서의 Shin e -Dalga rno 상호작용에 견줄 만한 상보 적인 연속부분들을 찾아내지 못하였다. 최근에 Nakashim a 등 (1980) 은 광화학적 교차 결 합법 을 사용하여 갓을 쓴 mRNA 의 5' 부분과 18S rRNA 의 3' 끝 부분이 40S 및 80S 개시 복합체들에서 상호작용한다는
결과를 얻었다. 그러나 그들은 같은 신험에서 18S rRNA 가 폴리 (U) 와 도 교차 결합되는 결과룹 얻었다. 그러므로, 그들의 실험결과 만으로는 진 핵 세 포에 서 도 Shin e -Dalga r no 상호작용이 있 다고 주장하기 는 어 렵 다. 최 근에 Sarga n 등 (1982) 은 18S rRNA 의 재 로운 아 차구조 모형 을 제 안 하였는데, 3' 끝의 머리 핀 구조 바로 옆에 있는 누클레오티드들이 여러 mRNA 둘의 개 시 코돈 앞에 오는 CCACC 연 속부분과 상호작용할 것 이 라고 가정하고 있다. 더 많은 18S( 또는 12S) rRNA 둘의 3' 끝의 구조 와 진핵세포의 mRNA 의 51 끝의 구조가 밝혀지기 전에는 진핵세포에 있어서의 mRNA • rRNA 상호작용의 가능성을 평가하기는 어려울 것이 다. 박태 리 아의 16S rRNA 의 3' 끝 부근에 있는 CCUCC 연속부분과 같 은 결정적인 연속부분이 진핵세포의 18S rRNA 에서는 발견되지 않기 때문에 (표 4-2 를 보라), 만일 진핵세포에서도 Shin e -Dalga rno 상호작용 이 있다 하더 라도 18S rRNA 의 다른 어 떤 연속 부분이 관련될 것으로 생각한다. 아마도 고동생물 세포들에 있어서의 갓 구조는 원핵세포들에 서 일어나는 mRNA : rRNA 상호작용의 역할을 대신하기 위해서 진화 되었는지도 모른다. 4.7.6 갓 결합 단백질 갓 구조는 진핵세포의 mRNA 에 있어서 공동되는 특칭이며, 그의 기 능은 mRNA 의 번역의 효율울 증진시키는 것으로 확인되었다. 따라서 개시 인자들 중의 어느 하나는 갓을 쓴 mRNA 을 특이하게 인식할 것 으로 생각된다. 화학적 교차 결합법을 사용하여 실제로 그러한 단백질 이 발견되었다. 이 단백질은 토끼의 망상 적혈구의 리보솜을 씻은 액에 서 m7GDP- 세파로오스 대롱 상에서 친화 크로마토그라피로 정제되었는 데 , 그 분자량은 24kdal 이 다 (Sonnenberg 등, 1979; Sonnenberg 등, 1980). 이렇게 정제한 단백질은 HeLa 세포의 추출물에서 갓울쓴 mRNA 의 번역을 촉진시키는 기능을 가지고 있다는 것이 확인되었다. 이러한 발견과 일치하게, 갓 결합 단백질에 대한 단일군집체성 항체가 갓을 쓴 mRNA 의 번역은 방해하지만 갓울 쓰지 않은 mRNA 의 번역에는 아 무런 영 향을 주지 않는다는 것이 관찰되 었다 (Sonnenber g 등, 1981). Sonnenberg 등 (1979) 은 갓 결 합 단백 질 에 관해 서 홍미 있는 모형 을 제 안 하였다. 이 모형에 의하면, 먼저 이 단백질은 mRNA 의 전 끝에 결합하
여 단백질 • mRNA 복합체룰 형성하며, 그 다음에 이 복합체는 갓 결합 단백질의 eIF-3 에 대한 친화력에 의하여 eIF-3 을 함유하고 있는 40S 리보솜 하위단위체에 결합한다(그림 4-6 을 보라). 안정한 복합체를 형 성한 다음에는 갓 결합 단백질은 이탈되고, elF-3 과 갓이 상호작용하
게 된다.
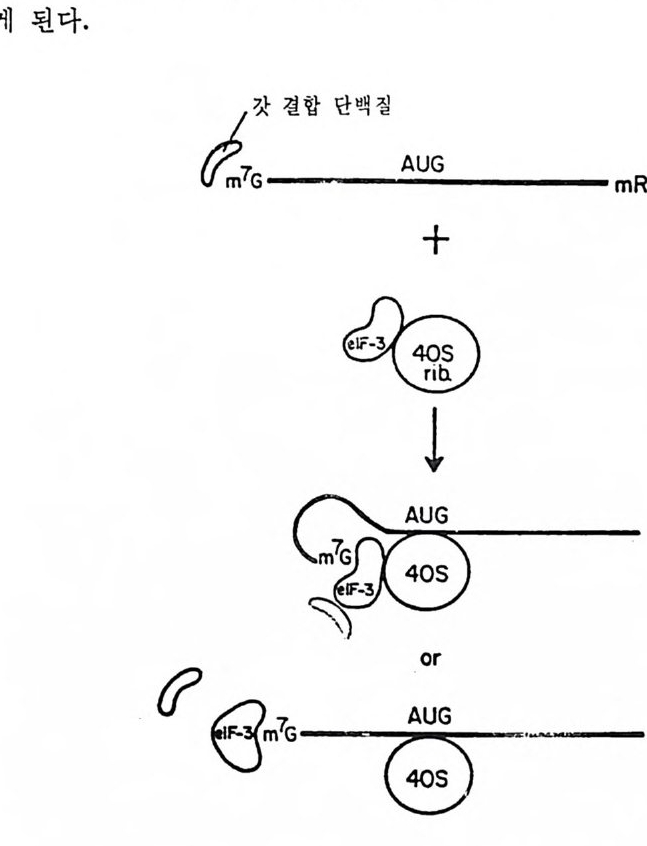 4갓 결합 단백 질
4갓 결합 단백 질
그림 4-6 번역의 개시 과정에 있어서의 갓과 갓 결합 단백질과의 상호 작용. 갓 결 합 단백 질 이 방출된 다음에 는 elF-3 이 갓과 상호작용한다. 4.7.7 40S 리보솜 하위단위체에 의한 진핵세포의 mRNA 의 AUG 코돈의 인식 앞의 절에서 기술한 바와 같이, 진핵세포에 있어서의 mRNA 의 인식 온 Sh ine -Dalga rno 상호작용으로 일 어 나지 않는다. Kozak (l978) 는 여 터 가지 실험결과들에 기초하여 진핵세포에 있어서의 AUG 코돈의 인식
에 대해서 〈주사 모형 ) 을 제안하였다. 최근애 수 정하 여 발 표한 새 모형 들에 대 해 서 는 Kozak (1981) , Kozak (1982) , 또는 Kozak (19 83) 등을 참 고하라. 이 가설에 의하면 40S 하위단위체는 mRNA 의 5' 끝에서 결합 한 다음에 AUG 코돈을 찾아서 이 동해 가다가 AUG 코돈에 이 르면 거 기서 멈추게 된다는 것이다(그립 4-7 을 보라). 다시 말하면 AUG 코돈 이 40S 하위단위체에 의한 mRNA 의 인식작용의 이른바 종결 코돈이 되는 셈이다. 많은 실험결과들이 이 가설을 뒷받침해 주고 있다. 몇 가· 지 증거문 알아 보자.
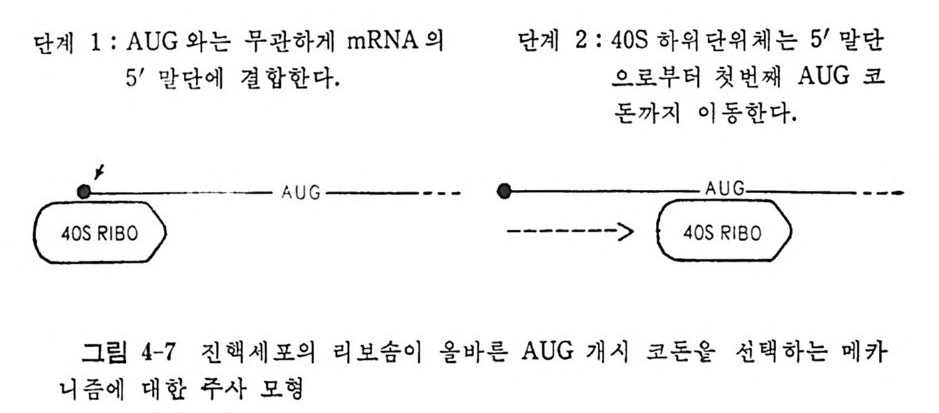 단계 1 : AUG 와는 무관하게 mRNA 의 단계 2 : 40S 하위 단위 체 는 5' 말단
단계 1 : AUG 와는 무관하게 mRNA 의 단계 2 : 40S 하위 단위 체 는 5' 말단
이 메카니즘은 40S 하위단위체가 결합하는 자리에 있는 m1G 의 촉진 효과를 합리적으로 설명할 수 있다. mRNA 의 5' 끝에 있는 갓이 시험 관 내에서의 번역을 촉진한다는 것은 이미 앞에서 기술하였다 (4.7.5. 절 을 브라). 5' 갓은 51 말단에서 수백 개의 누클레오티드 떨어진 곳에 AUG 코돈을 가진 mRNA 의 번역을 크게 증진시킨다 (Fre y ss i ne t. 1978; Frie d 동, 1981). 5' 갓이 번역을 증진시키는 것은 사실이지만 40S 하· 위단위체가 mRNA 와 결합하는 데 반드시 5' 갓이 있어야 하는 것은 아 니다 (4.7.5 절을 보라). 또한, 51 갓은 리보솜이 어디에 결합할 것인지 를 지시하는 인식 신호는 아니다. 왜냐하면, 말단의 m i G 가 존재하든 존재하지 않든간에, 리보솜이 번역을 개시하는 자리는 언제나 5' 말단 에 가까운 AUG 코돈이기 때문이다. 따라서, 리보솜의 결합에 필요한 일차적인 인식 자리가 되는 것은 mRNA 분자의 5' 끝 그 자체이며 m7G 갓이 아닌 것으로 보인다. 따라서, 갓이 있을 경우와 없을 경우에 개시 메카니즘이 다를 것으로 생각할 수는 없다.
3.4 절에서 기술한 바와 같이, mRNA 의 구조 율 환상화시키 면 리보 솜이 결합되지 않는다(표 3-5 를 보라). 갓을 쓰지 않은 많은 직 선형의 합성 폴리누클레오티드들은 시험관 내에서 밀싹 또는 망상 적혈구의 리 보솜과 결합하지만, 이 중합체를 RNA 연결효소로 완 상화시키면 리보 솜과의 결합능력이 상실된다. 이러한 관찰도 또한 리보솜의 전합 에 필 수적인 역할을 하는 것은 m7G 가 아니라 5' 끝 그 자체임을 층명해 주 는것이다. mRNA 가 완전한 것일 때는 그것을 광범하게 번성시켜도 내부 에 있 는 자리에는 리보솜이 결합하지 않지만, mRNA 를 여러 조각으로 가수 분해하면 mRNA 의 내부에서 유래되는 조각들에도 리보솜이 결합 한다 (F i ddes 와 Goodman, 1981). 이 실험둘로 RNA 분자 상에 있는 노출된 5' 끝이 리보솜 결합에 필요하고도 충분한 조전임 을 알 수 있다. 주사 모형이 옳다면 40S 하위단위체는 AUG 코돈이 없는 RNA 분자 물에도 결합할 수 있을 것으로 예상되는데, 실제로 그러하다는 것을 여 터 가지 합성 리 보폴리 머 들을 사용하여 증명 하였다 (Both 등 , 1976) . 주사 모형에 있어서 관건이 되는 가정은 40S 하위단위체가 5' 끝에서 첫번째 AUG 코돈까지 이동해 간다는 것이다. 여러 가지 방법들로 이 것이 중명되었냐 에데인 또는 팍타마이신 등과 같은 개시반응의 방해 물들을 첨가하거나 ITP 로 치환된 mRNA 를 주형으로 사용 함 으로써 Me t-t RNA i M et와 AUG 코돈 사이의 상호작용이 교란되었을 때, 40S 하 위단위체는 5' 끝에 가까운 AUG 를 넘어서 이동할 수 있다 (Kozak 와 Shatk i n , 1978 ; Kozal<, 1979 ; Kozak, 1980a) . 이 러 한 경 우 에 는 mRNA 는 10 개 내지 12 개의 40S 하위단위체를 가진 복합체로 축최되었 다. 아 마도 각 하위단위체는 5' 끝에 결합한 다음에 이동하고 있는 것들일 것 이다. 최근의 연구에서 밀싹의 40S 하위단위체가 이동하기 위해서는 ATP 가수분해 가 필 요하다는 것 이 밝혀 졌다 (Kozak, 1980b) . ATl? 를 제 거함으로써 이동이 방해되었을 경우에는, 단 한 개의 40S 하위단위체가 5' 끝 부근에 결합되어 있는 것을 불 수 있다. 이 실험은 주사 메카니 즘의 가장 중요한 단계를 확인하는 것이다. 여기서, 원핵세포에서는 단 백질 합성의 개시과정에서 ATP 가 전혀 필요치 않음을 상기하자. 주사 모형의 특징들 중의 하나는 5' 끝에 가까운 AUG 코돈에서 40S 하위단위체의 이동이 중지되며, 이 때 60S 하위단위체가 40S 하위단위 체와 회합한다는 것이다. 40S 하위단위체에 의한 AUG 코돈의 인식작
용의 효율은 AUG 코돈 양쪽 옆에 있는 누쿨례오티드 연속부분의 성질 에 따라서 결정되는 것으로 생각된다 . 설 NN~G 의 구조가 진핵세포 의 리보솜에 의한 개시에 가장 적합한 것 으로 생각되고 있다(표 3-3 과 표 3-4 를 보라). 이러한 연속부분이 5' 끝에 가까운 곳에 자리잡고 있 으면 그 자리에서만 개시가 일어날 것이지만, 첫번째 AUG 코돈이 덜 적합한 구조(예, GNNA—UGCu 또는 uCN NAUGG)에 들어 있다면 약간의 40S 하위단위체는 거기서 멈추어서 개시반응을 일으킬 것이고, 약간의 40S 하위단위체는 그 구조를 지나쳐서 더 하류에 있는 보다 적합한 개 시 코돈에서 개시반응을 일으키게 될 것이다. 주사 메카니즘에 있어서 의 이 특징은 홍미있는 융통성을 제공한다. 만일 첫번째 AUG 삼중체 가 준적합한 연속부분에 있으면, 약간의 리보솜은 하류에 있는 최적합 한 참재 적 AUG 삼중체 를 찾아서 이 동해 가고, 약간의 리 보솜은 준적 합한 개시 코돈에 머뭉게 될 것이므로, 한 개의 mRNA 가 두 가지 단 백질 합성에 대한 지령을 내리게 된다. 실제로 이러한 양식에 따르는 몇 가지 진핵세포의 mRNA 둘이 발견되었다. 이러한 mRNA 둘을 그림 3-6C 에서 열거하였다. 그 렇지만 진핵세포에 있어서는 이러한 이기능적 mRNA 둘은 드물게 존재한다. 대개의 경우 천 끝에 가까운 첫번째 AUG 삼중체가 있는 데가 보다 유리한, 즉 최적합한 구조를 구성하고 있다. 따라서, 정상적으로는 첫번째 AUG 코돈에서만 개시반응이 일어나며, mRNA 들은 한 가지 단백질만을 합성시키게 된다. 4. 7. 8 mRNA 결합에 있어서의 ATP 의 역할 진핵세포에 있어서의 개시반응에 ATP 가 요구된다는 것은 밀싹의 단백질 합성계에서 처음으로 밝혀졌다. ATP 를 대거나 ATP 대신에 그의 비가수분해성 유사체인 5' -아데닐릴 메틸렌 이인산 (ADPCP) 을 쓰 면 40S mRNA 의 리보송 하위단위체들과의 결합이 현처하게 감소된다 는 것이 알려졌다 (Trachsel 둥, 1977). 이 실험결과는 m Ri'.::f A 의 결합 에는 ATP 의 가수분해가 필수적이라는 것을 뒷받침해 준다 (4.7.7 절을 보라). 4.7.4 절에서 말한 바와 같이, 자연의 mRNA 는 광범위한 이차 구조를 함유하고 있으며, 번역이 일어나려면 이 이차구조가 이완되어야 한다. 이차구조의 풀립 과정은 에너지 장벽을 극복하여야 하므로 이 과 정을 촉진시키 기 위해서는 ATP 가 필요할 것이다. 풀립 과정과 관계가
있는 것으로 알려진 eIF-3 이 ATP 와 상호작용 할 것으로 기대되지만 아· 직 실험적 중거는 없다. 40S 리보솜이 mRNA 의 5' 끝에서 멀리 떨어져 있는 AUG 코돈까지 이등하는 데 ATP 가수분해에서 나오는 에너지를 이용할 것이라는 것은 4.7.7 절에서 이미 기술하였다. 4. 7. 9 80S 개시 복합체의 형성 40S 개시 복합체와 60S 리보솜 하위단위체의 결합은 80S 개시 복합체 를 형성한다. 원핵세포의 계와는 달라서, 이 회합 단계에서는 eIF-5: 라고 불리 는 특이 한 집 합 인자가 관여 한다 (Benne 등, 1978; Pete r son. 둥, 1979). 이 인자는 토끼의 망상 적혈구에서 처음으로 정제되었으며, 그 크기 는 125~160 kdal 이 고, 단일 펩 티 드 사슬임 이 밝혀 졌다. eIF-5 는 40S 개시 복합체의 형성 에는 아무 작용을 하지 않지만, 80S 복합체 의 형성에는 절대적으로 필요하다. eIF-5 로 촉 매되는 두 하위단위체의 결합반응은 GTP 의 가수분해를 필요로 한다. 5 ! -구아닐릴 메틸렌 이인 산 (GDPCP) 또는 상응하는 이미도 유도체 (GDPNP) 들과 갇온 GTP 의 비가수분해성 유사체들이 대치된 조건에서는 80S 개시 복합체가 형성되 지 않는다. 접합반응이 일어나는 동안, eIF-5 는 개시 인자 eIF-2 와 eIF-3 들이 40S 개 시 복합체 에 서 이 탈되 는 것 을 매 개 한다 (Pete r son 등, 1979a; Pete r son 등, 1979b) . 그러 나, 이 인자들의 이 탈이 60S 하위 단· 위체가 결합하기 전에 일어나는 것인지 결합과 동시적으로 일어나는 것 인지는 아직 찰 모르고 있다. 60S 리보솜 하위단위체가 없는 조건에서 는, eIF-5 는 40S 개 시 복합체 에 결 합된 Met- tRN A,M•t 의 양을 감소시 킨다. 40S 개시 복합체로부터 eIF-2 와 eIF-3 아 이탈되고 나면 Met- tRNA lMet 만을 함유하는 준안정 한 복합체 가 형 성 되 는데 , 이 복합체 가 60S 리보솜 하위단위체와 결합하여 80S 복합체를 형성하는 것으로 제안 되고있다. eIF~5 이 의 에도 두 가지 개 시 인자들, 즉, e!F -4 C 와 eIF-4D 들이 집 합반응에 관련되는 것으로 생각되고 있다. elF-4C 는 mRNA 가 결합되 지 않았을 때 Met- tRN A;M•t • 80S 복합체 의 형 성 에 부분적 으로 기 여 하 는 것으로 생각되고 있다. 또한, eIF-4C 는 60S 하위단위체와 상호작용 할 수 있도록 40S 하위단위체의 형태를 바꿈으로써 Met- tRN A/1•1 • 40S 복합체 를 안정 시 키 는 것으로 생 각되 고 있다 (Trachsel 동, 1977; Thomas
등, 1980). 왜냐하면, eIF-4D 가 메티오닐-푸로마이신 합성을 세 배나 중진시키지만 아미노아실-t RNA 와 Met- tRN Ai M c t 사이의 팹티 드 결합 형 성 에 는 필 요하지 않는 것 으로 미 루어 보아서 (Benne 와 He rshey , 1978 ; St ae heli n 둥, 1978) , eIF-4D 의 주요한 역 할은 Met- tRN Ai M cl 가 80S 개 시 복합체 상에서 올바른 위치에 자리잡게 해주는 것으로 생각할 수 있다. * 참고문현 Barrie u x, A., Rosenfe l d, M. (1978) , ]. Bi ol . Chem. 253, 6311 . Baumsta r k, B. R. , Sp r emulli, L. L. , RajB h andary , U. L . , Brown, G. M. (1977) , J. Bact. 129, 457. Benne, R. , Brown-Luedi, M. L. , Hershey, J. W. B. (1978) , J. Bio l . Chem. 253, 3070. Benne, R., Hershey, J.W .B. (1976) , Proc. Natl . Acad. Sci. 73, 3005. Benne, R., Hershey , J.W .B. (1978), J. Bi ol . Chem. 253, 3078. Benne, R., Naaktg e boren, N., Gubbens, J., Voorma, H.O. (1973). Eur J. Bi o- chem. 32, 372. Both , G.W :, Furuic h i, Y. , Muth u kris h nan, S., Shatk i n , A.J. (1976), ]. Mo/. Bi ol . 104, 637. Branlant, C., Sri W ida da, J., Krol, A., Evel,J. P . (1976), Nucleic Acid s Res. 3, 1671. Chaudhuri, A. , Str i n g e r, E. A. , Valenzuela, D. , Mait ra, U. (1981) , J. Bi ol . Che m . 256, 3988. Checkley, J.W ., Cooley, L., Ravel, J.M .•( 1981), J. Bio l. Chem. 256, 1582. Chu, J. , Mazumdar, R. (1974) , FEBS Lett . 40, 335. Clark, B.F.C . , Marcker, K.A . (1966), J. Mal. Bi ol . 17, 394. Dahlberg, A. E. , Dahlberg, J.E . (1975), Proc. Natl . Acad. Sci. 72, 2940. Darnbroug h , C. , Leg on , S. , Hunt, T. , Jac kson, R. (1973) , ]. Mo/. Bi ol . 76, 379. Das, A., Bag c hi, M., Roy , R., Ghosh-Dasti da r, P., Gup ta, N.K . (1982), Bi( )- chem. Bi op h y s . Res. Commun. 104, 89. Dasgu pta, A., Das, A., Roy, R., Ralsto n , R., Maju m dar, A., Gup ta, N.K . (1978) 讐 ]. Bio l . Chem. 253, 6054. Davis , B.D . (1971) , Meth o ds Enzym ol. 20, 248. Delk, A.S., Rabin w i ot z , J.C . (1975), Proc. Natl . Acad. Sci. 72, 528. Dott av io -M art in, D. , Sutt le, D.P., Ravel, J.M . (1979), FEBS Lett . 97, 105.
Dubnoff , J.S ., Lockwood, A.H., Mait ra , U. (1972), ]. Bi ol . Che m . 247, 2884. Dunn, J.J., Buzash-Pollert, E., Stu d ie r , F.W. (1978) , Proc. Natl . Acad. Sc i. 75, 2741 . Eckhardt, H., Lii hr mann, R. (1979) , ]. Bio l . Chem. 254, 11185. Fakundin g , J.L., Hershey, J.W .B. (1973), J Bio l . Chem. 248, 4206. Farbit z, I., Haug e, J.G . (1979), Meth o ds Enzym ol. 60, 240. Fid d es, J.C ., Goodman, H.M . , (1981), J. Mo/. Allp. Ge net. 1, 3. Fie r s, W. , Contr e ras, R. , Duerin c k, F. , Haeg e man, G. , Iserenta n t, D. , Merre- gae rt, J., Mi n- Jo u , W., Molemans, Raevmaekers, A., Van den Bergh e , A. Volckaert , G. , Ysebaert, M. (1976) , Natu r e 260. 500. Freys s in e t, G. (1978) , Exp . Cell Res. 115, 207. Fried , H.M., Pearson, N.J. , Ki m , C.H., Warner, J.R. (19 81) ,J . Bi ol . Chem. 256, 10176. Ghosh-Dasti da r, P., Gi bl i n, D., Yag hm ai, B., Das, A., Das, H.K ., Parkhurst, L., Gup ta, N.K. (1980), ]. Bi ol Che m . 255, 3826. Godefr oy - C obburn, T., Wolf e, A.D., Dondin , J., Grunberg- M anag o, M., Dessen, P., Panta l oni, D. (1975), ]. Mol Bio l . 94, 461 . Gold, M., Prib n ow, D,M Schneid e r, T., Shin e dli ng , S., Sin g e r, B.S ., Sto r mo, G. (1981) , km. Rev. Jvlicr obio l . 35, 365. Gott lieb , M., Davis , B.D ., Thomp so n, R.C . (1975), Proc. Natl . Acad. Sci. 72, 4238. Groner, Y., Revel, M. (1971), Eur. ]. Bi oc hem. 22, 144. Grunberg- M anago . M. , Gros. F. (1977) , Prog. N11cl, Acid , Res. Jvlo/. Bio l . Gup ta, N.K ., Chatt er je e , B., Chen, Y.C. , Maju m dar, A. (1975), ]. Bi ol . Chem. 250, 853. De Haro, C., Ochoa, S. (1979) , Proc. Natl . Acad. Sc i. 76, 2163. Hershey, J.W .B. (1982), Prote i 11 Bi os yn the sis i11 Eukaryo t e s (Ed., R. P~rez- Bercoff ) , p. 97, Plenum Press, New York. Hershey, J.W .B., Yanov, J., Joh nsto n , K., Fakundin g , J.L . (1977), Arch. Bio - chem Bio p / zys. 182, 626. Holder, J.W ., Lin g rel , J.B. (1975) , Bi oc hemi st r y 14, 4209. Ilan, J., Ilan, J. (1976) , ]. Bio l. Chem. 251, 5718. Jay , E., Seth , A.K., Jay , G. (1980), ]. Bio l Chem. 255, 3809. Kaemp he r, R. (1982) , Prote i n Bi os yn t h e sis in Eukaryo t e s (Ed. , Pfa e z-Bercoff ) , p. 223, Plenum Press, New York. Kozak, M. (1978) , Cell 15, 1109. Kozak, M. (1979) , ]. Bi ol . Chem. 254, 4731 . Kozak, M. (1980a) , Cell, 19, 79.
Kozak, M. (1980b) , Ce ll 22, 459. Kozak, M. (1981) , Nu clei c Acid s Re s. 9, 5233. Kozak, M. (1982) , Bi oc he m . Soc . Sy m p . 47, 113. Kozak, M. (1983) , Mi cr ob ia l . Re v. 47, 1. Kozak, M., Shatk in , A.J. (1978) , Cell 13, 2011 . Lloyd , M.A., Osborne, J.C ., Safe r , B., Powell G., Merric k , W.C. (1980), J. Bio l . Che m. 255, 1189. Lee-Huang , S., Sil lero , M.A.G., Ochoa, S. (1971) , E11r. ]. Bi oc he m . 18, 536. Lockwood, A.H., Sarkar, P., Mait ra, U. (1972), Proc. Natl . Acad. Sci. 69. 3602. Lodis h , H. F. (1970) , Natu r e 226, 705. Mait ra, U. , Str i n g er , E. A. , Chaudhuri, A. (1982) , A1111. Rev. Bi oc he m . 51, 869. Maju m da r, A., Bose, K.K., Gup ta, N.K ., Wabha, A.J. (1976), ]. Bi ol . Chem. 251, 137. Maju m dar, A., Dasgu pta, A., Chatt er je e , B., Das, H. K. , Gup ta, N. K. (1979), Meth o ds E11zy1 1 1ol. 60, 35. Maju m dar, A., Roy, R., Das, A. , Dasgu pta, A., Gup ta, N.K. (1977), Bio cl 1em. Bi op h y s . Re s. Commun. 78, 161 . Malath i , V. G. , Mazumder, R. (1979) , Bi oc hem. Bi op h y s . Re s. Commun. 89, 585. Mazumder, R. (1971) , FEES Lett . 18, 64. McLaug h li n, J., Chang , S.Y., Chang, S. (1982), Nucleic Acid s Res. IO, 3905. McLaug h li n, J., Murray, C., Rabin o wi tz, J.C . (1981), ]. Bio l . Che m . 256, 11283. Mi n- Jo u , W., Haege m an, G., Yaebaert , M., Fie r s, W. (1972), Natu r e 237, 82. Mi tsu i, K., Datt a, A., Ochoa, S. (1981), Proc. Natl . Acad. Sci. 78, 4128. Murray, C.L. , Rabin o wi tz, J.C . (1982), J Bi ol . Che m . 257, 1053. Naaktg e boren, N. , Roobol, K. , Boorma, H. 0. (1977) , E11r. ]. Bi oc l1e m . 72, 49. Naka sh im a, K., Darzy n dlewi cz, E., Shatk i n , A.J. (1980), Natu r e 286, 226. Noll, M., Hapk e , B., Schreie r , M.H., Noll, H. (1973), ]. Mo/. Bio l . 75, 281 . Ny ga rd, 0., Weste r mann, P., Hultin , T. (1980), FEES Lett . 113, 125. Pate r son, B. M. , Rosenberg, M. (1979) , Natu r e 279, 692. Pauza, C.K . , Karesis , M. , Navre, M., Schachman, H. K. (1982), Proc. Natl . Acad. Sc i. 79, 4020. Perez-Bercoff , R. (1982) , Prote i n Bio s yn t/ze si s in Eukaryo t e s (Ed. , R. Perez-Bercoff ) , p. 245, Plenum Press, New York. Pete r sen, H.U., Kruse, T.A., Worm-Leonhard, H. , Sib o ska, G.E., Clark, B.F . C., Bouto r i n, A., Remy , P., Eve!, J.P ., Dondon, J., Grunberg- M anago , M.
(1931) , FEBS Lett . 128, 161 . Pete r son, D.T . , Merric k , W.C., Safe r , B. (1979a), J Bi ol . Che m . 254, 2509. Pete r son, D. T. , Safe r , B. , Merric k , W. C. (1979b) , ]. Bi ol . Che m. 254, 7730. Pir o tt a, V. (1979) , Nucleic Acid s Res. 6, 1495. Post, L.E ., Nomura, M. (1980), J Bi ol . Chem. 255, 4660. Ranu, R.S ., Wool, LG. (1976), ]. Bi ol . Chem. 251, 1926. Revel, M. (1977) , Molecular Mechanis m s of Prote i n Bi ox y n tlt es is (Ed. , H. Weis s bach, S. Pestk a ) , Academi c Press, New York. Rosenberg, M. , Pate r son, B. M. (1979) , Natu r e 279, 696. Roy, R., Ghosh-D asti da r, P., Das, A., Yag h mai, B., Gup ta, N.K . (1981), ]. Bio l. Chem. 256, 4719. Russell, E.W ., Sp re mull i, L.L. (1980), Arch. Bio c lzem. Bi op l tys . 201, 518. Sabol, S. , Meie r , D. , Ochoa, S. (1973) , E11r. ]. Bi oc /z c m. 33, 332. Sabol, S. , Ochoa, S. (1970) , Natu re Netu Bi ol . 234, 233. Safe r , B., Adams, S.L . , Anderson, W.F., Merric k , W.C. (1975), ]. Bi ol . Chem. 250, 9076. Samuel, C.E . , Rabin o wi tz, J.C . (1974), ]. Bi ol . Che m . 249, 1198. Sarge n, D.R . Grego ry , S.P., Butt en vorth , P. (1982), FEBS let ! . 147, 133. Schreie r , M.H., Emi , B., Sta e helin , T. (1977), ]. Mo!. Bi ol . 116, 727. Sie k ie r ka, J., Mauser, L., Ochoa, S. (1982), Proc. Natl . Acad. Sci. 70, 2537. Sin g e r, B.S ., Gold, L., Shin e dli ng , S.T., Colkit t, M., Hunte r , L., Prib n ow, D. Nelson, M. (1981) , ]. Mol. Bio l . 149, 405. Sonenberg, N., Rup pr echt, K.M ., Hecht, S.M., Shatk i n , A.J. (1979), Proc Natl . Acad. Sci. 76, 4345. Sonenberg, N., Skup, D., Trachsel, H., Mi llwa rd, S. (1981), ]. Bio l. Che m 256, 4138. Sonenberg, N., Trachsel, H., Hecht, S.M., Shatk i n , A.J, (1980), Natu r e 285 331. Sp ring e r, M. , Graff e, M. , Hennecke, J. (1977) , Proc. Natl . Acad. Sci. 74 3970. Sta e helin , T., Emi , ch B., Seeir r , M. H. (1879, ) Meth o ds Enzym o/. 60, 139. Ste i tz , J. A . (1978) , Bio l og ica l Reg u lati on and Contr o l (Ed. , R. Holdberge r p. 349, Plenum Press, New York. Ste i t z, J.A., Jak es, K. (1975) . Proc. Natl . Acad. Sci. 72, 4734. Ste i t z, J.A., Sp ra gu e , K.U ., Ste e ge , D.A., Yuan, R.C ., Laug h rea, M., Moor P.B. , Wabhan, A.J. (1977), Nucleic Acid - Prote i n Recog n it ion (Ed., H Vog e l) , p. 491, Academi c Press, New York. Str ing e r, E.A., Chaudhuri, A., Mait ra, U. (1977), Bi oc lzem. Bi op /z ys. Ri
Commun. 76, 586. Str ing e r, E.A ., Chaudhuri, A., Mait ra, U. (19 79) , J. Bi ol Clze m . 254, 6845. Str ing e r, E.A., Chaudhuri, A, Valenzuela, D., Mait ra, U. (1980) , Proc. Natl . Acad. Sci. 77, 3356. Str ing e r, E. A. , Sarkar, P. , Mait ra , U. (1977) , ]. Bi ol Chem. 252, 1739. Sundari, R.M., Str i n g e r, E.A ., Schulman, L.H ., Mait ra, U. (1976), ]. Bi ol . Clzem. 251, 3338. · Tanig u chi, T., Weis s mann, C. (1979), 275, 770. Thomas, A., Goumans, H., Voorma, H.0., Benne, R. (1980), Eur. ]. Bio c hem. 107, 39. Thomp so n, H. A. , Sadnik , I. , Schein b uks, J. , Maldave, K. (1977) , Bi oc hemi st r y 16, 2221 . Trachsel, H., Erni, B., Schreie r , M.H., Sta e helin , T. (1977), J. Mal. Bio l. 116, 755. Trachsel, H. , Sta e heli n, T. (1978) , Proc Natl . Acad. Sci. 75, 204. Trachsel, H. , Sta e heli n, T. (1979) , Bi oc him . Bi op h y s . Acta 565, 305. Valenzuela, D., Chaudhuri, A., Mait ra, U. (1981), Fed. Proc. 40, 1749. Van Duin , J., Kurland, C.G . , Dondon, J., Grunberg- M anago , M., Branlant, C., Ebel, J. P. (1976) , FEES Lett . 62, 111 . Vermeer, C., Boon, J., Talens, A. , Bosch. L. (1973a), Eur. ]. Bi oc lzem. 40, 283. Venneer, C., deKi ev it , R.J., van Alph e n, W.J. , Bosch. L. (1973b), FEBS Lett . 31, 273. Walto n , G. M. , Gil l, G. N. (1976) , Bi oc lzim . Bi op !z ys. Acta 418, 195. Yanofs k y , C., Platt , T., Crawf ord , I., Ni ch ols, B., Chri sti e, G., Horowi tz, H., Van Cleemp ut , M., Wu, A.M. (1981), Nucleic Acid s Res. 9, 6647.
제 5 장 단백질 합성의 연장과정 단백질 합성의 개시과정에서 mRNA 의 개시 코돈 (AUG) 과 개시 tR NA (fM et- tRN AIMC' 또는 Met- tRN A;Mc') 가 리 보솜의 작은 하위 단위 체 (30S 또는 40S) 에 결합한 다음에 리보솜의 큰 하위단위체 (50S 또는 60S) 가 집합하여 70S( 또는 80S) 개시 복합체가 형성된다. 연장과정에서는 〈연 장 회로〉라는 반복성인 과정을 거쳐서 mRNA 의 코돈들이 지시하는 대 로 한 번에 한 개의 아미노산이 첨가되면서 폴리펩티드 사슬이 형성된 다. 이러한 연장회로는 완성된 풀리펩티가 방출인자들에 의해서 리보솜 에서 떨어져 나울 메까지 진행한다. 펩티드 결합의 연장이 일어나는 동안 · mRNA 와 리보솜은 상대적인 운등울 한다. 단백질 합성의 연장과정에 있어서의 활성화된 결합 상태들의 동적인 국면에 관해서는 아직은 아는· 것이 거의 없다. 연장과정의 여러 단계들의 정적인 국면들을 그림 5-1 로 요약하였다. 매 회로에서 일어나는 일들은 아미노아실-t RNA 의 리보 솜에의 결합, 펩티 드 결합형성, 자리옮김 등이다. 결합반응에 있어서, 아미 노아실-t RNA 분자는 리 보솜에 있는 아미 노아실 자리 (A 자리) 에 결 합한다• 어떠한 아미노아실-t RKA 가 결합할 것인지는 A 자리에 있는 mRNA 의 코돈에 의해서 결정된다. 아미노아실-t RNA 의 결합은 아마 노아실_t RN A, 연장인자(원핵세포의 경우에는 EF-Tu, 또는 진핵세포의 경우에는 EF-1). 및 GTP 들르 구성되는 삼성분 복합체에 의해서 매개 된다. 아미노아실-t RNA 가 결합된 다음에는 이미 펩티딜 자리 (P 자리〉
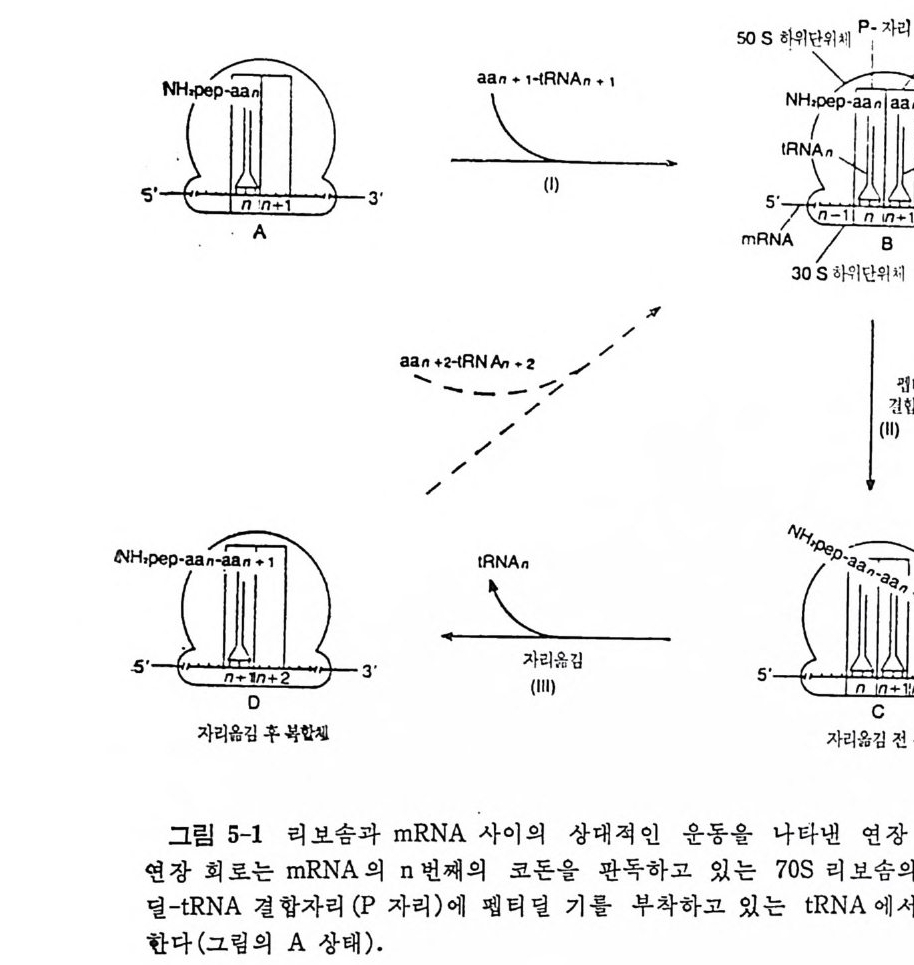 SO S B~] 단위세 p: 자리 k 洞
SO S B~] 단위세 p: 자리 k 洞
예 결합하고 있는 펩티릴-t RNA 의 펩티딜 부분이 A 자리에 있는 아미 노아실-t RNA 의 아미노산에 전달되어 펩티드 결합이 형성된다. 펩티딜 기 전달효소 활동성은 리보솜의 구조 자체에 있으며 가용성 단백질 인 자를 전혀 필요로 하지 않는다. 펩티딜 기 전달반응으로 A 자리에 결 합된 새 펩티딜-t RNA 가 만들어지며, 펩티딜 기는 그의 COOH 말단에 저 아미노산 찬기가 하나 더 늘어나게 되며, P 자리에서는 펩터딜 기 의 이탈반응이 일어난다. 연장 회로의 마지막 단계인 자리옮김에서는 티보솜이 mRNA 의 5' 에서 3' 방향으로 상중체 한 개만큼 이동하게 되며, 펩티딜-t RNA 는 A 자리에서 P 자리로 이동하고 펩터딜 기를 잃
은 t RNA 는 P 자리에서 방출된다. 이와 같이 자리옮김이 끝나면 다 음에 들어 오는 아미 노아실-t RNA 를 위 한 새 코돈이 A 자리 에 나타나 게 된다. 자리옮김은 다른 또 하나의 연장인자(원핵세포의 경우에는 EF-G, 그리고 진핵세포의 경우에는 EF-2) 와 GTP 에 의해서 촉진된다 . 단백질 합성 메카니즘과 풀리펩 티드 사슬의 연장에 관한 지식은 대부 분 박테리아에서 행한 실험결과로 얻었지만 진핵세포에 있어서의 단백 질 합성 계에서도 유사한 메카니즘으로 단백질이 합성되고 있다. 그러 나, 원핵세포와 진핵세포의 단백질 합성 메카니즘에는 다른 접들이 있다. 5.1 원핵세포의 연장인자들 원핵세포의 리보솜 상에서 일어나는 폴리펩티드 사슬의 연장에는 EF- Tu, EF-Ts, 및 EF-G 동 세 가지 연장인자들이 관여한다(표 5-1) (EF- Tu 와 EF-Ts 두 인자들의 회합으로 생기는 복합체를 EF-T 라고 부른 다) . 이 인 자들은 E. coli 에 서 처 음으로 단리 되 었 지 만 (Nath a ns 와 Lip - rnann, 1961 ; Allende 등, 1964 ; Nis h iz u ka 와 Lip m ann, 1966a) , 뒤 에 Bacil lu s ste a roth e rmop hi l u s (Beaud 와 Leng yel , 1971 ; Wi ttingh ofe r 와 Lebermann, 1976) 와 Pseudomonas fiuo rescens (Lucas-Lenard 와 Beres, 1974 ; Lucas-Lenard 와 Lippm an, 1966) 등에 서 도 단리 되 었다. 한 무제 포사술 연장계에 있어서의 연장인자들은 다른 박테리아의 연장인자들로 완전히 교체될 수 있다. EF-Tu 는 세포에서 제일 풍부하게 있는 단백질이다. 그 함량은 전체 단백 질 의 5. 5 % 를 이 루고 있다 (W itting h ofe r 둥, 1979) . 그렇 지 만, 연 장인자들의 양의 바율은 성장조건에 따라서 변한다. 예를 들면 신속히 자라고 있는 세포에서의 EF-Tu : EF-Ts : EF-G 의 비는 6 : 1 : 1 이다. 이렇게 EF-Tu 의 상대적인 함량이 큰 것은 세포에 있는 t RNA 의 수준 과 밀접한 관계가 있다 (Sk j old 동, 1973; Furano, 1975). 리보솜 한 개 에 대한 연장인자들의 몰 바를 보면, EF-Ts 와 EF-G 는 생리조건의 변 화에는 관계 없이 항상 1 : 1 이다 (Gordon, 1970). 다른 한편으로, 리보 송에 대한 EF-Tu 의 비는 리보솜 한 개 당 8 내지 14 분자이다.
표 5-1 원핵세포와 진핵세 포 에 있 어서의 연장인자들 원핵세포 진핵세포 반응 EF-Tu* EF-h1 아미 노아 실 -tR N A 의 리 보 솜에 의 결합 EF-Ts* 1 EF-1,2 GDP-GTP 교 환을 촉매한 다 펩티딜 기 전달효소 펜티덜 기 전달효소 펩티드 결합의 형성, 종결 EF-G I EF- 2 자리 옮 김 1. EF-la 또는 eEF-Tu 라고도 부른다. 2*. eEEFF-T-Tus- T라s고 복도합 체부 른운다 .E F-T 라고 부른다.
5.1.l 물리적 성질 박테리아의 모든 연장인자들이 균일하게 정제되었거나 결정상태로 얻 어 졌다 (Lucas-Lenard 와 Beres, 1974) . 분자량들은 연 장인자들을 얻은 생물종에 따라서, 또 측정법에 따라서 다르지만 큰 차이는 없다. EF- Tu 의 분자량은 39 kdal 내 지 51 kdal 이 고, EF-G 는 71 kdal 내 지 85 kdal 이 다. EF-Ts 의 경 우 에 는 보고된 값들이 19 kdal 에 서 71 kdal 까지 상당한 차이 를 보이 고 있다. EF-T 의 분자량은 약 65~68 kdal 이 다. 한 분자의 EF-T 복합체 는 EF-Tu 와 EF-Ts 를 각각 한 분자 씩 함유하고 있다. 박테리아의 모든 연장인자들은 환원된 SH 기들을 함유하며, 연장인 자들의 정상적인 기능에는 SH 기들의 존재가 꼭 필요하다. EF-Tu 는 세 개의 SH 기를 함유하고 있는데, 그 중 둘만이 EF-Tu 의 기능에 중요 하다. 둘 중 하나 (SH! )는 GTP 와 GDP 를 결합하는 데 필요하고, 다른 하나 (SH2) 는 아미노아실-t RNA 의 결합에 필요하다 (Hachmann 등, 19 71; Arai 동, 1974). ET-Ts 는 두 개의 SH 기를 함유하고 있으며, 그 중 하나는 EF-Tu•EF-Ts 복합체 형성 에 꼭 필요하다. EF-G 는 4 내지 6 개의 SH 기를 가지고 있으며, 그 중 하나는 구아닌 누클레오티드를 결 합하는 데 꼭 필요하다 (Marsh 등, 1975; Rohrbach 와 Bodley, 1976) . 5.1.2 EF-Tu 의 기능 EF-Tu 는 삼성분 복합체 아미노아실-t RNA·EF-Tu•GTP 의 형성을
거쳐서 아미노아 실 -t R NA 가 70S 리보솜에 결합하는 것을 증진시 킨다. 결합이 일어난 다음에 GTP 가 가수 분해되고 , 리보솜으로 부터 EF-Tu· GDP 가 방 출된 다(그림 5-2 를 보라). 가) EF-Tu 와 구아닌 누클레오티드를 합유하는 복합체둘의 형성 EF-Tu- c GDP, GTP, GMP-P (CH2 ) 2P, GMP-P (NH) P 들과 같은 구아닌 누쿨레 오티 드 들과 결 합 한다. EF-Tu 는 GDP 와 결 합하며 (20° C, 10 mM Mg H , pH 8 에서 Kd = 4 nM), 갇온 조건에서 GTP 와도 결합하지만 친화력 은 좀 작 다 (/(d = 0. 3 µM) (M ille r 와 \Veis s bach, 1970) . Mg 2+ 은 EF-
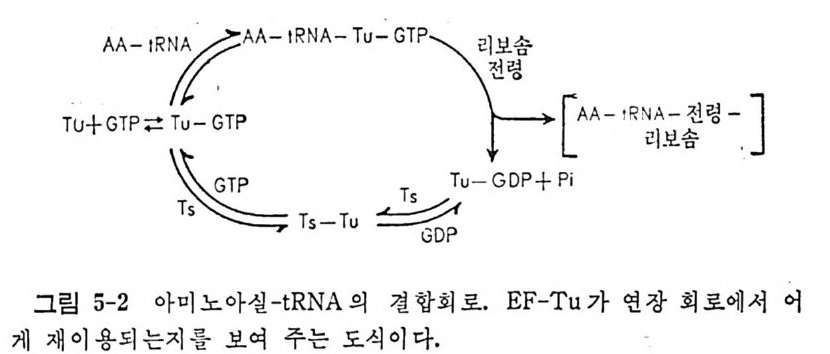 AA-tR ~AA-tR NA-T u-G TP
AA-tR ~AA-tR NA-T u-G TP
Tu·GDP 복합체의 안정 에 꼭 필요하다. Mg 2+ 이 없을 때의 Kd 값는 8 µM 이다. EF-Tu 의 한 분자 당 한 분자의 구아닌 누클레오티드가 결 합한다. EF-Tu-GTP 와 EF-Tu•GDP 사이에는 형태의 차이가 있움이 밝혀졌 다. EF-Tu 의 SH2 기의 반응성은 EF-Tu•GDP 에 있어서보다는 EF-Tu•GTP 에 있어서 더 크다 (EF-Tu 의 SH2 기는 아미노아실-t RNA 와 결합하는 작용기임울 상기하라). 나) EF-Tu·GTP· 아미노아실-t RNA 복합체의 형성 EF-Tu 는 연장 아미 노아실-t RNA 와 GTP 와 함께 삼성분 복합체를 형성한다 (Skoul t ch i 등, 1968; Ravel 등, 1968; Shorey 등, 1969; Weis s bach 등, 1969; Coop er 와 Gordon, 1969). 이 복합체 에 있어서 성분들의 몰 비는 1 : 1 : 1 이다. N- 아세틸아미노아실-t RNA 둘, 또는 포르밀 -Me t-t RNA0 1 , 또는 탈아 실화된 t RNA 들과 같이 NH2 기가 가리어진 t RNA 둘은 안정한 삼성분 복합체 형성 에 관여할 수 없는 것으로 미루어 보아서, EF-Tu 와 아미
노아실-t RNA 들과의 상호작용에는 변형되지 않은 아미노아 실 잔기의 존재 가 필 수적 인 것 으로 생 각된 다 (Ono 등, 1968 ; Weis s bach 등, 197 1 ; Lockwood 등, 1971) . 그렇 지 만, EF-Tu 는 a- 히 드 록 시 아미 노산 을 지 닌 t RNA 와의 삼성분 복합체를 형성할 수 있으며 그 것 이 리보송에 결 합하는 것을 중진시킨다 (Fahnens t ock 둥, 1972). tR NA 분자 의 CCA 끝 이 손상되지 않은 상태로 있는 것도 상성분 복합체 형성에 중요한 것으 로 밝혀져 있다. 아미노아실-t RNA 의 3' 말단에 CCA 연속부분을 가진 2' (3')-0- 아미 노아실 울리 고누클레 오티 드들은 EF-Tu • GTP 복합체 와 상 호작용한다 (R i n g er 와 Chladek, 1975). 다론 한편으로는, 효모의 tR NNh• 의 3' 말단의 리보오스를 2’ 과 3' 탄소 원자들 사이에서 분열시킨 것 , E. coli 의 tR NAV•I 의 5' 반분자를 제 거 한 것 , 또는 말단의 CCA 연 속 부분에 시티단 찬기를 하나 더 붙인 것 둥은 복합체의 형성을 방해한다 (Chen 과 Of en g a nd, 1970 ; Of en g a nd 와 Chen, 1972 ; Krauskop f 등, 1972; Thang 등, 1972). 역코돈 부분을 포함하여, tR NA 분자의 다른 부분에 있어서의 변형들은 복합체 형성에 영향을 미치지 않는다. 이러 한 사실에서, t RNA 의 역코돈 고리는 EF-Tu 와의 상호작용에는 직접 관계되지 않으며, 자유롭게 노출되어 있어서 리보솜의 A 자리에 있는 mRNA 의 해당하는 코돈에 의해서 인식될 수 있는 것으로 보인다. 삼성분 복합체의 형성은 이성분 복합체 EF-Tu•GTP 를 거쳐서 진행 한다. EF-Tu 는 GTP 를 가진 이성분 복합체에서만 삼성분 복합 체를 형성할 수 있는 적절한 형태를 가지고 있는 것으로 보인다. 왜냐하면 EF-Tu·GDP 는 아미노아실_t RNA 와 상호작용하지 않는다. EF-Tu 의 제 2 의 반응성 SH 기 (SH 시 가 아미 노아실-t RNA 를 결 합하는 데 관여 한 다. SH2 와 득이 하게 반응하는 L-1- 토실 아미 도 -2- 페 닐 에 틸 클로로메 틸 케돈은 EF-Tu 의 구아닌 누클레오티와의 상호작용에는 영향을 미치자 않지 만 EF-Tu 의 아미 노아실-t RNA 와의 상호작용을 방해 한다. 5. 1. 3 EF-Ts 의 기능 앞의 절 에서 언급한 바와 같이 , EF-Tu 는 GTP 보다는 GDP 에 대 한 친화력이 더 크지만, EF-Tu·GDP 복합체의 형태에서는 아미노아실 -tRN A 와만 상호작용할 수 있다. EF-Ts 의 기 능은 EF-Ts-EF-Tu 를 중간물질로 형성시키면서 EF-Tu·GDP 로부터 EF-Tu•GTP 를 재생시
키 는 것 이 다 (Weis s bach 등, 1970) . 또 한편으로는, 자유 EF-Tu 가 GTP 를 결합할 때는 EF-Ts 가 필요하지 않다. EF-Ts 는 EF-Tu•GDP ' 의 GDP 와 자유 GDP 또는 GTP 사이 의 교환반응을 촉진 시 킨 다 (Mi ller 와 Weis s bach, 1970) . EF-Tu 에 대 한 EF-Ts 와 GDP 의 친 화도는 거 의 비 숫하다. EF-Tu • EF-Ts 와 EF-Tu· GDP 의 해 리 상수는 각각 2 nM 과 3 nM 이 다. 그 러 므로, EF-Ts· EF-Tu 복합체 가 형 성 될 수 있다. EF- Ts 가 EF-Tu·GDP 로부터의 삼성분 복합체의 형성은 촉진시키지만, EF-Tu •G TP 또는 자유 EF-Tu 로부터 의 삼성 분 복합체 의 형 성 을 촉진 하지 않는다는 사 실 은 EF-Ts 의 기능 이 EF-Tu·GTP 의 재생을 일으키 는 것 임 을 뒷 받침 해 준다 (Wate r son 둥, 1970) . 5.1 .4 EF-G 의 기능 EF-G 는 리보솜이 존재하는 조건에서 GTP 를 신속히 가수분해하여 GDP 와 Pi 를 생 성 시 킨 다 (Ni sh iz u ka 와 Lip m ann, 1966b) . 이 반응은 리 보솜이 없는 조건에서는 일어나지 않는다. 폴리 (U) 와 아미노아실-t RNA 들은 EF-G 의 촌적 으로 일어 나는 리 보송의 GTPase 활동성 을 촉진한다. 시 험 관 내 에 서 의 연 구에 의 하면, 펩 티 딜-t RNA 가 70S 리 보솜의 A 자라 에서 P 자리로 이동하기 위해서는 EF-G 와 GTP 가 필요함이 밝혀졌 다. 삼성분 복합체 EF-G 러보솜 .GTP 는 GTPase 활동성에 있어서 중 간체의 역할울 한다. 리보솜의 50S 하위단위체는 GTP 의 가수분해를 부 분걱으로밖에 뒷받침하지 않으며, 30S 하위단위체는 아무런 작용을 하 지 않는다. 30S 하위단위체는 아마도 EF-G·GDP 복합체로부터 GDP 를 쉽게 방출되게 하는 역할을 하는 것으로 생각된다. 리보솜 상에서 GTP 가 가수분해된 다음에는 삼성분 복합체 EF-G· 리보솜 ·GDP 가 형성된다. 이 복합체 와 푸시 드산과 작용하면 이 복합체 가 안정 해 진다 (Bodley 동, 1969 ; Bodley 등, 1970) . 푸시드산은 단백질 합성을 방해하는 스테로이드 항생제이다. 이 항생 제는 EF-G 에 의해서 촉매되는 GTPase 의 작용울 방해한다 (Pes t ka, 1!) 68; Tanaka 둥, 1968) . 푸시 드산이 방해 하는 표적 물은 EF-G 이 지 라 보솜 단백질이 아니라는 것은 이 항생제에 대한 저항성을 가진 돌연변 이체를 얻음으로써 확인되었다. 야생형 세포에서 얻은 EF-G 는 푸시~ 산에 민감하지만, 돌연변이체에서 얻은 EF-G 는 저항성을 가지고 있다`
푸시 드산이 GTP 의 가수분해 를 방해 하는 작용을 자세 히 분석 해 보면 EF-G·GDP 복합체 물 리 보솜 상에 안정 하게 묶어 놓 기 때 문이 라는 것을 알 수 있다 (Mondolell 등, 1971a ; Mondolell 동, 1971b) . EF-G 가 리 보 솜 상에 묶여 있 게 되면 촉 매로서의 작용이 본 질 적 으로 방 해된 다 . EF-G·GDP 복합체가 리보송에 묶이기 때문에, 푸시드산은 자리 옮김 과 GTP 의 가수분해륭 한 차례씩만 일어나게 하고 더 이상 일어 나지 못하게 한 다. 삼성분 복합체가 형성되고 그 다음에 푸시드산이 반응하는 것을 아 래의 식으로 나타내었다. 1. EF-G + GTP (GDPCP) +± EF-G •G TP (GDPCP) 2. EF-G •G TP (GDPCP) +± EF-G-50 S •G TP 또는 EF-G •S OS • GDPCP 3. EF-G •5 0S • GTP ➔ EF-G •S OS • GDP + Pi 4. EF-G·50S·GDP ~푸시드산 EF-G·50S·GDP • 푸시드산 EF-G·GTP 복합체는 매우 불안정하므로 존재하지 않지만 GTP 의 유사 체 GDPCP 와의 복합체 EF-G·GDPCP 는 존재한다. 또한, 진핵세포의 EF-2 는 GTP 와 안정한 복합체를 형성한다 (5.4.1 절을 보라). EF-G· .50 S·GTP 복합체는 형성되자마자 EF-G-50S·GDP 로 가수분해되므로 단리할 수 없다• 그러나 EF-G-50S·GDPCP 는 안정하게 형성되므로 단 리할 수 있다. 푸시드산이 작용하는 메카니즘을 고려하면, 성장하고 있는 세포는 푸 시드산이 있는 데에서는 리보솜의 P 자리에 펩 티덜-t RNA 가 축지할 것 이라는 것을 예견할 수 있다. Bacil l us nze g a t er i tt m 의 원형전체 윤 푸시 드산으로 처리하면 단백질 합성이 즉시 중지되며, 푸로마이신에 의해서 갓 생긴 풀리펩티드 사슬의 약 80% 가 방출된다. 이것 은 단 백질 합성이 자리옮김이 일어난 다음에 중지되었다는 것을 증명해 준다 ( Ce l ma 등, 1972; Cundliff e, 1972) . 그러 므로, 푸시 드산은 자리 옮김 에 칙 접 적 으로 작용하는 방해물이 아니라 기능을 가진 아미노아실-t RNA 가 리보솜에 결합하는 것을 방해함으로써 단백질 합성을 방해한다는 결 론을 내릴 수 있다. 이것은 또한 EF-G·GDP • 리보솜 • 푸시드산 복합체가 EF-Tu 의 존적으로 일어나는 아미노아실-t RNA 의 리보송에의 결합을 방해하는 것 으로도 증명 된다 (Carber 등, 1972; Mi ller , 1972 ; Ric h man 과 Bodley, 1972). 이 결과는 EF-G 와 EF-Tu 가 리보솜 상에서 공통되는 자리 또
는 중첩하는 자리 에 결 합 한다는 것을 암시하며, 한 인자가 안정한 결합 을 이루게 되면 다른 인자가 리보솜과 상호작용하는 것이 방지됨으로써 이 인자가 일으키는 반응이 방해된다는 것을 암시한다. 50S 하위단위체와 바가역적으로 결합하는 항생제 티오스트 캡톤 과 시 오마이 신은 유사한 구조 를 가지 며 , 둘 다 EF-G 와 구아노신 누쿨 레 오 티드의 리보솜에의 결합을 막는다. 이 두 항생제가 EF-G 의존 적 으로 일어나는 GTP 의 가수분해를 방해하는 것은 푸시드산의 방해작용과 유 사하지만, 그 작용 메카니즘은 다르다. 티오스트랩돈은 자리옮김을 방 해하지만 푸시드산은 그렇지 않다 (MondoIell 등, 1971a; Mondolell 등, 1971b). EF-G 가 리보솜 상에서 결합하는 자리에 관해서는 이미 2.7.2 절의 (가)항에서 기술하였다. 삼성분 복합체 EF-G·50S-GMP-[C H2] P 상에 서 EF-G 가 교차결합하는 단백질들은 L7 과 L12 임이 확인되었다. 5.2 원핵세포의 리보솜 상에서의 연장 5.2.1 아미노아실-t RNA 의 리보솜에의 결합 EF-Tu•GTP· 아미노아실-t RNA 복합체가 적당한 코돈을 가지고 있는 리보솜과 작용하면, 복합체는 리보솜에 결합하며, GTP 는 가수분해되 며, EF-Tu•GDP 는 방출되며, 아미노아실-t RNA 는 리보솜의 A 자리에 결합하여 머무른다. 만일 P 자리에 또 다른 아미노아실-t RNA 가 이미 결합되었을 경우에는 즉시 펩티드 결합이 형성될 것이다. 이 반응은 GTP 의 가수분해가 뒤따를 때에는 0°C 에서도 매우 신속 하게 일 어 난다 (Weis s bach 둥, 1971) . 리보솜은 또한 상당히 빠른 속도로 EF-Tu•GTP 를 가수분해한다 (Mi ller, _19 72) . 리 보솜은 과량의 삼성 분 복합체 또는 EF-Tu• GTP 에 의속해도서를 계포화산될할 수수 있있다기. 때삼문성에분 복복합합체체들에의 대해한리 상값수들와을 가보수면분 K해m의 = 최 l대x G10T-6P M에 이대고 한, 값Vm들, x은 = K m1 2= p m 4o xl e1/0-m6 i nM/A 2이6 0고· 리V보m,솜. =인 데1. 8반 pm해 서ol,e/ mEi nF/A -T26u0•· 리보솜이다. 이 실험치들은 삼성분 복합체는 EF-Tu•GTP 보다 더 강
하게 결합하며 더 신속하게 가수분해된다는 것을 증명해 준다. 그러나, EF-Tu·GTP 복합체는 단독으로도 리보솜에 대한 찬화력이 상당히 있 는 것으로 생각되고 있다. GTP 의 가수분해는 코돈과 역코돈의 상보적인 관계가 없이는 일어나 지 않을 것이기 때문에, 삼성분 복합체의 상호작용의 자리로서 일차적 으로 생각할 것은 코돈이 된다. 그러므로 Phe-tR :-:A·EF-Tu·GTP 복 합체는 풀리아데닐산을 결합한 리보솜에 의해서는 벌로 가수분해되지 않 는다. 위 에서 말한 바와 같이, EF-Tu·GTP• 아미노아 실- t RNA 가 리보 솜에 결합하면 GTP 가 가수분해된다. GTP 가 가 수분해되면 EF-Tu· GDP 와 P i가 형성된다. 리보솜에 결합한 아미노아 실- t RNA 한 분자 당 GTP 한 분자가 가수분해 된 다 (Brot 둥, 1970) . GTP 대 신 에 GM P - P(CH2)P 를 사용하여 도 아미 노아실 -tRN A 가 리 브솜 에 결 합되 므로, 아 미노아실-t RNA 의 결합에는 GTP 의 가수분해 자체가 요구되는 것이 아 님 을 알 수 있다. GTP 의 가수분해 는 리 보솜에 결 합한 아미 노아실-t RNA 를 적당한 자리에 놓이게 하거나 EF-Tu 를 리보솜으로부터 방출시키는 데 필요한 것으로 생각되어 왔으나, GTP 의 가수분해는 EF-Tu 의 방 출과 그 다음에 일어나는 펩터드 결합 형성에 필요한 형태 변화를 일으 키는 것으로 생각되고 있다. GTP 가 분해되면 EF-Tu•GDP 의 아미노 아실-t RNA 와 리보솜에 대한 친화도가 감소됨으로써 EF-Tu•GDP 가 이탈한다 (Ara i 등, 1973; Kawakit a 등, 1974). EF-Tu•GDP 가 방출되 지 않으면 펩티딜 기 전달효소의 활동성이 방해된다. 5.2.2 펩티드 결합 형성 리보솜의 A 자리에 아미노아실-t RNA 가 결합한 다음에 리보송의 P 자리에 위치한 펩티딜-t RNA 의 펩티딜 찬기의 카르복시 기와 A 자리 에 있는 아미노아실-t RNA 의 아미노 기 사이에 결합이 이루어침으로써 펩티드 결합이 형성된다. 펩티딜 기의 전달은 리보솜의 큰 하위단위체 에 위치한 펩티딜 기 전달효소의 작용으로 촉매된다 (Monro 등, 1969) (그림 5-3). 펩티딜 기의 전달에는 가용성인 인자들이나 GTP 가 요구 되 지 않는다 (Ma den 등, 1968) . 술프히 드릴 기 에 작용하는 약품들은 전 달 반옹에 영향을 미치지 않는다. 펩티딜 기 전달효소의 활동은 아미노아실-t RNA 의 아미노아실-아데
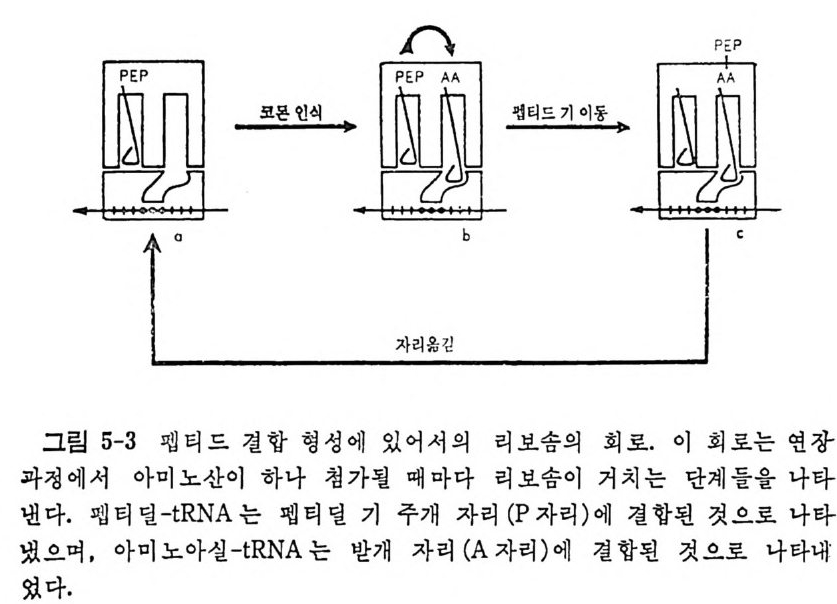 广三广r\ 一广PE P
广三广r\ 一广PE P
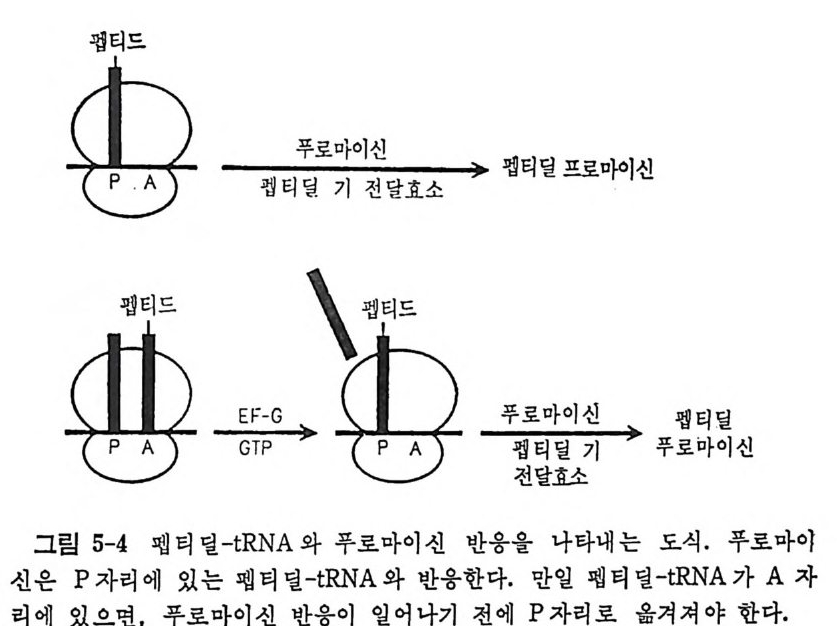 上十푸로마이신
上十푸로마이신
노신 말단의 유사체인 항생물질 푸로마이신을 사용하여 분석할 수 있다 (그림 5-4 및 그림 5-5 를 보라). 리보솜은 펩티릴-tRN A 유사체들인 풀 리페닐 알라닌-t RNA(Maden 등, 1968) 또는 울리고리실-tRN A(Go tt es-
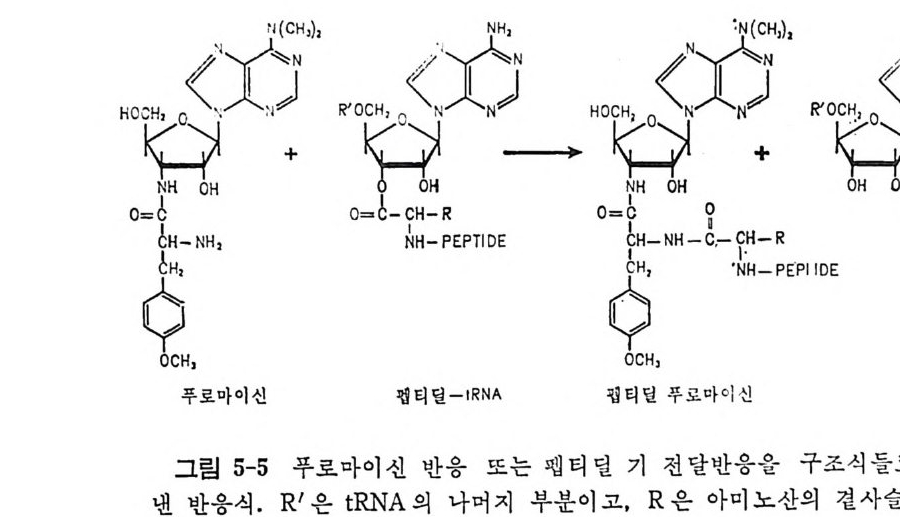 。= 〈抽OcFLJ N-H. I. ’ 。 n t CNIH -HR-E Pp T D E 。 =》안〈1CCH1IOC - NH I OgC ' NC卜 H -H_RE . PP 。E
。= 〈抽OcFLJ N-H. I. ’ 。 n t CNIH -HR-E Pp T D E 。 =》안〈1CCH1IOC - NH I OgC ' NC卜 H -H_RE . PP 。E
man, 196 7)로부터 펩티딜 기를 푸로마이신으로 전달한다. 푸르마이신 은 mRNA 및 펩티딜 기 전달효소 중심 이의의 리보솜 부분들과 상호작 용할 수 있는 아미 노아실-t RNA 의 구조적 요소들을 가지 지 않기 때 문 에 형성된 폴리페닐알라닌푸로마이신 또는 울리고리실푸로마이신은 리 보솜으로부터 방출된다. 펩티딜 기 전달효소에 관한 실험은 〈조각 반응 〉윤 기 웅하 여 할 수 있 다. 조각 반응이란 펩티딜-tR NA 대신에 NH2 가 가리어진 아미노산을 함유하는 울리 고누클레 오터 드 (예 , CACCA-AcPhe 또는 CAACCA-fM et 조각) 를 사용하여 50S 하위 단위 체 또는 70S 리 보솜 상에 서 푸로마이 신 과 결합시키는 것이다. 이 반응은 Mg 2+, K 리 및 알코올 들의 존 재하에 서 실시 한다 (Monro 와 Marcker, 1967 ; Maden 과 Monro, 1968) . 손상 되 지 않은 펩 티 딜-t RNA 분자들은 상응하는 〈조각〉들보다 더 반응성 이 큰 것으로 보아서, t RNA 가 리보솜에 효과적으로 결합하는 데에는 tR NA 분자의 CCA 말단 이의의 다른 부분들이 요구된다는 것을 알 수 있다. 정상적인 단백질 합성의 연장과정에 있어서는 자연의 펩티딜 t RNA 는 전체 연장과정에 걸쳐서 리보솜에서 떨어져 나오지 않는다. 펩티딜 기 전달효소 중심의 구조가 아미노아실-t RNA 또는 펩 티딜 tRN A 의 3' 말단에 상응하는 조각들을 사용한 친화표지법, 펩 티딜 기 전달효소를 방해하는 항생제물 사용한 친화표지법, 또는 리보솜의 재구
성 법 등으로 상당히 밝혀 져 있다. 이 것을 표 5-2 에 요약하였다. 50S 하 위단위체의 성분들의 약 반 정도가 펩티딜 기 전달효소 활동성과 관련 되어 있다. 표 5-2 에 실은 많은 단백질들이 펩티딜 기 전달효소의 활동 성에 직접적으로 관련되는 것은 아닐 것으로 생각된다. 펩티딜 기 전달 효소로 작용하는 한 단백질이 있고, 나머지 단백질들은 올바른 조립에
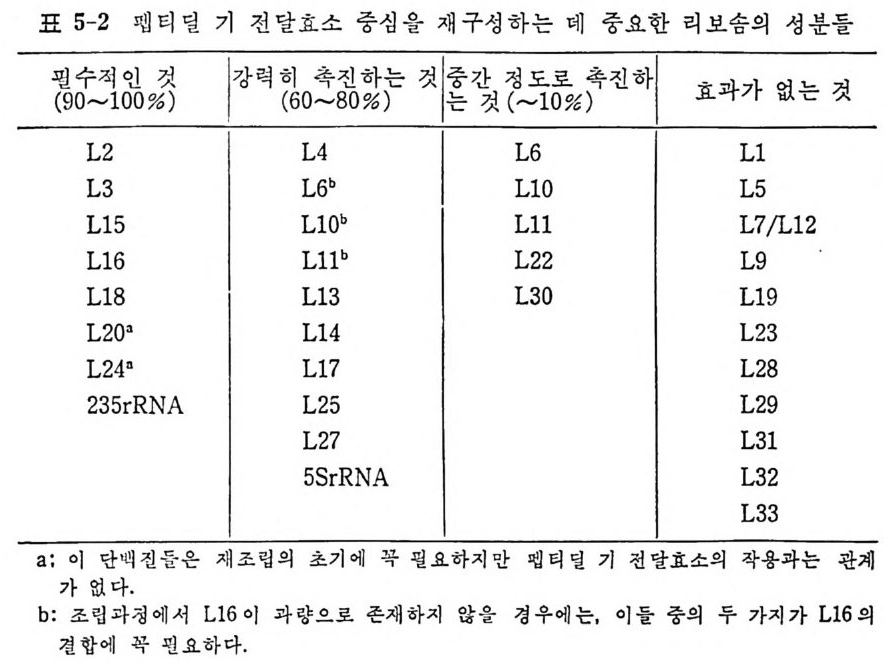 표 5-2 펩티딜 기 전달효소 중심을 재구성하는 데 중요한 리보송의 성분들
표 5-2 펩티딜 기 전달효소 중심을 재구성하는 데 중요한 리보송의 성분들
관여할 것으로 생각된다. L16 이 펩티딜 기 전달효소의 중심을 이루는 단백질로 생각되고 있다 (N i erhaus. 1980). 그런데 최근에 L16 은 tR NA 의 3' 끝을 결합하는 단백질이라는 것이 교차결합법으로 밝혀졌다(M a i mets 등, 1984). 따라서 Ll6 이 펩티딜 기 전달효소 중심의 일부분을 이루는 것은 거의 확실하지만 효소 그 자체는 아니라고 생각된다 (2.6.2 절을 참조하라). 이전에는 L11 이 펩티달 기 전달효소 중심으르 인정되 어 왔다 (Ni er haus 와. Monte j o . 1973) . 최근에 Schmi d 등 (1984) 은 진성박테리아, 고대 박테리아, 및 진핵세 포 등에서 분자량이 약 30,000 달돈 되는 리보솜 단백질들이 면역학적 인 교차반응울 한다는 것을 알았으며, 이 단백질이 E. co li의 L2 임을 확인하였다. 그러므로 L2 는 리보솜 단백질 중에서 제일 많이 보존된.것
으로 생각된다• 위에서 말한 바와 같이 (표 5-2), L2 는 팸티딜 기 전달 효소 중심의 한 성분이기 때문에 매우 홍미를 끄는 단백질이다. L2 에 상응하는 단백질들의 아미노산 결합순서를 분석해 봄으로써 리보솜의 진화에 대한 정보도 얻을 수 있을 것으로 생각된다. 펩티딜 기 전달효소 중심과 관계되는 단백질들의 상대적인 위치들을 그립 5-6 에 도형으로 나타내었다. A' 자리는 A 자리의 일부분으로서
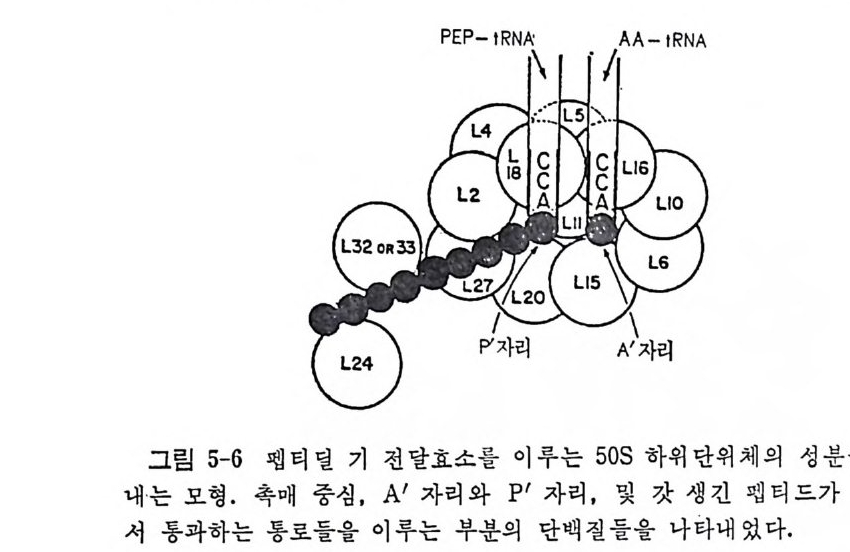 그립 5-6 펩티딜 기 전달효소를 이루는 50S 하위단위체의 성분들을 나타
그립 5-6 펩티딜 기 전달효소를 이루는 50S 하위단위체의 성분들을 나타
아미노아실-t RNA 의 CCA- 아미노산 부분이 결합되는 부분이고, P' 자리 는 P 자리의 일부분으로서 펩티틸-t RNA 의 CCA- 펩티드 부분이 결합되 는 자리이다. 펩티딜 기 전달효소의 작용에 23S rRNA 의 U2584 가 관여한다는 것은 이미 2.4.4 절의 (마)항에서 기술하였다. 펩티딜 기 전달효소 중심의 본질이 리보솜 단백질 성분들의 어느 것인지는 아칙 규명되지 않고 있 다. 그러나, 23S rRNA 의 영역 e 에 위치한 것만은 확실히 밝혀져 있 다 (그림 2-20 및 그림 2-21, 및 그림 2-38 올 참조하라) • 현재 로서 는 펩 터딜 기 전달효소의 가장 유력한 단백질 성분은 L11 과 L16 이다. 펩티딜 기 전달효소의 작용 메카니즘에 관한 자세한 점은 아직 찰 모 르고있다. A 자리에 결합한 받개 기질로서 아미노아실-울리고누클레오티드들을 사용하였을 때 3' OH 에 아실화된 것들만이 펩티딜 기를 받을 수 있다.
2' OH 에 아실화된 이성질체는 받개로서 반응하지 않는다 (Pozd y akov 동, 1972 ; Chladek 등, 1973 ; Rin g er 와 Chladek, 1974) . 그러 나 tR NA 의 2'-0- 아미 노아실 유사체 는 푸로마이 신 반응과 CACCA-Phe 의 티 보 솜에의 결합을 방해한다 (R i n g er 동, 1975). 따라서, 2'-0- 아미노아실 tR NA 유사체들은 A' 자리와 상호작용하고 펩티딜 기 전달효소에 의해 서 인식되기는 하지만 적절한 받개로서 작용할 수 있는 유리한 입체적 위 치 에 있지 않을 것으로 보인다. 그러 나, Phe-tR NAPh•-CCd3A 와 Phe- tRN APh•-CCAo,-red 둘은 느린 속도이 기 는 하지 만 AcPhe-tR N A 를 주개 로 사용하였을 때 그 것을 받을 수 있다 (Ch i nal i 등, 1974). 그러므로, 아미 노아실-t RNA 의 2' -이 성 질체 는 펩 티 딜 기 를 받아들일 수 있다. 펩티딜 기 전달반응에 있어서도 주개 기질의 입체화학적 특이성이 요 구되 고 있다. tR NA 의 2 '- 아미 노아실 유사체 들이 리 보솜의 P' 자리 에 결합되기는 하지만, 주개 기질로서는 이용되지 않는다. 따라서, 2'-0- AcPhe-tR NA-CCAo,-red (Hussain 과 Ofe n g an d, 1973 ; Chin a Ii 등, 1974) 와 2'-0-Phe-tR NA-CCdA (Sp ri n z l 과 Cramer, 1973 ; Chin a li 등, 1974) 는 펩티딜 기 주개로서 작용하지 않는다. 이 결과들은 3'-0- 펩티딜-t RNA 가 활동성인 주개 기질임을 암시하는 것아지만, 이성질화하지 않는 3'- 이성질체들을 얻어서 확인하기 전에는 이 결론은 결정적인 것이 못된다. 펩티딜 기를 전달하는 반응을 촉매하는 것 이의에도, 펩티딜 기 전달 효소는 펩티딜-t RNA 의 가수분해에도 관여한다. 여기에 관해서는 단백 질 합성의 종결을 논의할 때 다시 언급하기로 하겠다(제 6 장). 5. 2. 3 원핵세포에 있어서의 자리옮김 EF-G 와 GTP 가 자리옮김에 관여된다는 직접적인 증거들이 여러 가 지 실험둘로부터 얻어졌다. 앞에서도 언급한 바와 같이, 자리옮김 과 정에서는 (1) 아실화된 t RNA 의 A 자리로부터 P 자리로의 이동, (2) mRNA 의 이 동, (3) 리 보솜으로부터 의 탈아실화된 tR NA 의 방출 동 세 가지 반응이 일어난다. 자리옮김과 관련된 세 반응들 중 mRL~A 의 이동만이 실험적으로 증 명 되 었다. EF-G 와 GTP 와 함께 항온반옹시 킨 다음에 리 보솜에 의 해 서 보호되는 mRNA 조각의 길이는 3' 끝 쪽에서 세 개의 누클레오티드 만큼 더 길어진다 (Gu pt a 등, 1971; Thach 와 Thach, 1971). 자리옮김
이 일어나는 동안에 팹 티딜-t RNA 가 리보 솜 의 한 자리에서 다른 자리 로 이동하는 것에 대해서는 위 에서 말한 것과 비슷한 실험적 중거가 없 다. A 자리 에 팹 티 딜-t RNA 를 지닌 리보송을 EF-G 와 GTP 와 함께 항 온시키면 팸티덜-t RNA 가 푸로마이신과 반응 할 수 있는 상태로 변환된 다 (Lucas-Lenard , 1969) . 푸로마이신과의 반응성은 P 자리 에 있는 팹 티딜-t RNA 의 성질에 기인되는 것으로 생각하므로, mRNA 분자를 따 라서 일어나는 리보송의 이동은 펩 티딜-t RNA 의 P 자리로의 이동과 짝 지워져 있음을 알 수 있다. 이러한 실 험결과에서 티보 솜 에는 두 별개의 결합자리들이 있다는 생 각을 가지게 되었다 (S pir i n, 1969). mRNA 의 이동에는 tR NA 가 능동적으로 작 용 할 것으로 생각되고 있 다 (Lip m ann, 1969) . Lip m ann 은 tR NA 의 자리 옮김 과 mRNA 의 순차 적인 이동 사이의 짝짓기는 본질적으로 코돈-역코돈 상호 작 용에 기인될 것이라고 암시하였다. 코돈-역코돈 상호작용이 t RNA 의 자리옮김에서 중요한 역할을 할 것이라는 암시는 실제로 suf D 억압돌연변이체가 발 견됨으로써 뒷받침되었다. 이 돌연변이체는 h£s D 유전자리에서의 삽입 으로 생기는 읽기구조의 이동 돌연변이다. 이 돌연변이의 억압돌연변이 는 tR NAg ~G 에 대한 구조유전자에 있어서의 삽입 돌연변이라는 것이 밝 혀졌다. 억압 t RNA g~%의 역코돈은 CCC 대신에 네 개의 염기로 된 CC CC 이 다 (Ridd le 과 Carbon, 1973) . 코돈-역코돈 상호작용이 엄격히 유지되면서 t RNA 의 자리옮김이 일어 나는 데 대해서는 아직 실험적인 증거에 기초해서 설명할 수 있는 것은 아니지만 ,O f en g and 등 (1981) 은 다음과 갇은 모형을 제안하였다. 두 개
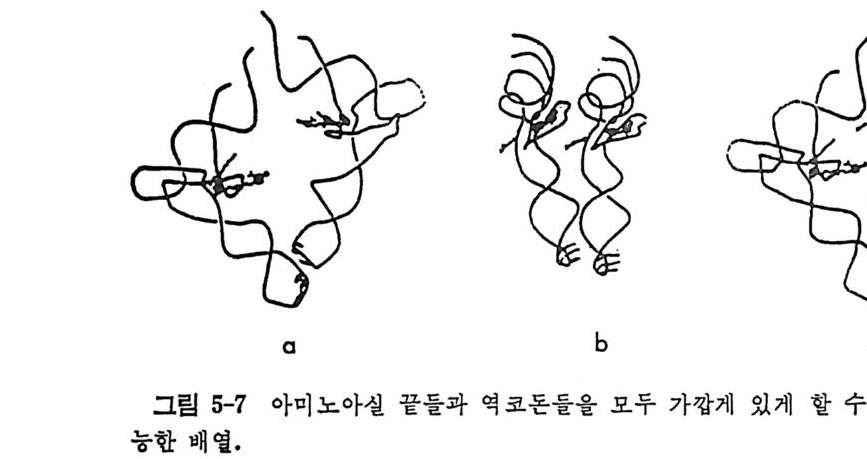 a b c
a b c
의 tR NA 분자가 리 보 솜 에서 배열 할 수 있는 방법 들을 그립 5 구 에 나타 내었다. 찬화표 지법 , 에 너지 전 달 에 의 한 거리 측 정 ( 자세한 것은 2.6.1 의 (나 ) 항 을 보라 )으 로 분석한 결 과에 의하면 그립 5-7 의 a 및 b 가 가장 그랄 듯한 배 열 이다. 이러한 배열에서 역코돈과 아미노산 끝 둘이 공히 나란 히 놓 일 수 있다. 펩티딜-t RNA 가 A 자리에서 P 자리로 이동 하는 것은 tR NA 부 분 에 있어서 L 구조의 중심부분에 해당하는 GT -we 부 분 이 크 게 회 전하면서 mRNA 를 이동시킬 것이라는 모형을 제안 한 사 람 도 있다 ( R i ch, 1974). GT-W C 부분의 희전은 리보솜의 형태 변 화로 유 발될 것으 로 생각된다. 자리 옮김과 동시에 탈아실화된 t RNA 가 리보송으로부터 방출된다 (Leder 등 , 1969). 자리 옮 김으로 촉진되는 탈아실화된 t RNA 의 방출이 일어나려 면 A 자리가 채워지는 것이 선결조건이다 (Lecas-Lenard 등, 1969 ; Ishit su ka 둥, 1970) . 다른 한편, 펩 티 딜 -tRN A 는 탈아실화된 tR NA 가 P 자리 에 없을 때 A 자리 에서 P 자리로 이동할 수 있다 (Tanaka 와 Kaji . 1972). 이것은 P 자리에 있는 탈아실화된 t RNA 는 펩티딜 tR NA 에 의해서 밀 러나간다는 것을 의미한다. 동적 계에 있어서의 EF-G 의 촉진으로 일어나는 자리옮김은 GTP 를 필요로 한다. EF-G 는 자리옮김 과정에 있어서 촉 매적으로 작용한다 (Chin a li 와 Parmeg gian i, 1973) . 자리 를 옮긴 펩 티 덜 -tRN A 한 분자 마 다 한 분자의 GTP 가 가수분해된다 C\1ondolell 등, 1973). GTP 의 가 수분해는 자리옮김 그 자체와는 칙접적인 관계가 없고 EF-G 가 촉매적 으로 연 장회 로 에 다시 이 용되 게 하는 역 할을 하고 있다 (Inoue-Yokosawa 등, 1974 ; Monta n aro 둥, 1976) . 그러 므로, 자리 옮김 은 일 차적 으로는 EF-G 의 리보솜에의 결합으로 매개되는 것으로 생각되며, GTP 는 EF -G 가 리보솜에 부착하는 것을 촉진하는 리간드의 역할을 하는 것으로 생각된다. 자리옮김이 일어난 다음에 일어나는 것으로 추축되고 있는 GTP 의 가수분해는 EF-G 또는 리보솜의 형태변화를 유발함으로써 EF-G 가 잘 방출되도록 하는 것으로 생각한다. 가용성 인자들과 GTP 가 없는 조건에서 일어나는 자리옮김 (비효소적 자리옮김)이 일어나는 것이 알려져 있다 (Gavr i lo v a 와 Sp irin , 1972; Gavrilo va 등, 1974) . 그러 므로, 자리 옮김 그 자체 는 리 보솜의 고유한 기능일 것이라고 생각되고 있다. 비효소적 자리옮김은 30S 하위단위처l 의 단백질인 S12 를 변형시키는 p -CIH g BzO~ 에 의한 처리로 촉진되며警
이 단백질을 30S 하위단위체에서 빼도 족전된다 (K i sha 둥, 1971; Brot 등, 1972). 그러므로, 이 단백질은 자리옮김에 대해서 제약적인 효과를 나타내는 메카니즘과 관련되어 있을 것으로 생 각된다. 5. 2. 4 GTPase 의 작용 및 연장에 있어서의 GTP 의 역할 한 회로의 연장과정이 작동할 때 두 분자의 GTP 가 가수 웁 해된다. 가수분해로부터 방출되는 에너지는 펩티드 결합의 형성 자체에는 필요 없는 것으로 보인다. P 자리에서의 펩티딜-t RNA 의 가수분해의 4G 0 은 -7 kcal/ 몰로 펩티드 결합의 형성 에 있어서의 -3 kcal/ 몰보다 훨씬 크 다 (Lip m ann, 1969). EF-Tu• GTP • 아미 노아실-t RNA 가 리 보 솜 에 결 합하 논 과정에서 한 분자의 GTP 가 필요하며, GTP 가수분해는 EF-Tu 가 리보솜으로부터 방출되는 데 필요한 것으로 보인다. 마찬 가지로 , GTP 가 없는 조건에서도 비효소적인 자리옮김이 일어나는 것으로 보아서, 자리옮김 과정에서 일어나는 GTP 의 가수분해는 일차적으로 리보솜으 로부터 EF-G 를 방출시키는 데 필요할 것으로 보인다. 이러한 결과들에 서 GTP 와 GDP 는 연장인자들과 리보솜에 대해서 다른 자리입체성 효 과물질로 작용할 것임을 암시한다. GTP 는 연장인자들이 리보솜에 결 합하는 것을 증진시키고, GDP 는 인자들의 리보솜에 대한 친화력을 감 소시킴으로써 방출을 증진시킬 것으로 생각된다. 5.3 진핵세포에 있어서의 연장인자들 진핵세포에 있어서의 연장 단계들은 원핵세포의 경우와 매우 유사하 다. 죽, 1) 코돈 특이성에 의한 아미노아실-t RNA 의 리보솜에의 결합, 2) 펩티드 결합의 형성, 3) 성장하고 있는 펩터드 사술의 A 자리에서 P 자리로의 이동 등 세 반응들이 단계적으로 반복한다. 이 세 반응둘 은 각각 연장인자 l(EF-1), 펩티 딜 기 전달효소, 및 연장인자 2(EF-2) 들에 의해서 촉매된다. 펩티딜 기 전달효소를 제외하고는 이 반응들에 관련되는 인자들은 가용성이며, 모두 고도로 정제되었으며, 그들의 작 용에 GTP 를 필요로 한다. 그렇지만, 펩티드 결합 형성에 관여하는 단 백질은 리보솜 단백질이며, 이 반응에는 의부로부터 가해 주는 고에너 지
화합물이 필요하지 않다 . 표 5-1 에서 진핵세포와 원핵세포의 연장과정 에 관여하는 인자들을 비교하였다 . 진핵세포에 있어서의 연장에 관해서 는 Brot (1982) 의 평 론서 를 보라. 5.3.1 물리적 성질 가) EF-1 EF-1 은 처음에 토끼의 망상적혈구에서 발견되으며 (Arlin g - haus 동, 1963), 그 후에 많은 동물조직들로부터 정제되었다. 여러 출처 들에서 단리한 EF-1 단백질의 분자량이 2,000 kdal 까지 되는 여러 가 지 크기 의 분자들의 응집 체 로 존재 한다는 것 이 특징 이 다 (Schneid e r 와 Moldave, 1968) (표 5-3) . EF-1 의 고분자량의 형 태 를 EF-1H 라고 부른 다. EF-1 의 여러 형태들이 분자량들의 큰 차이를 보이고 있지만, EF-1H 는 분자량이 50 kdal 정도인 가벼운 형태들로 이루어진 응집체이다 . 이 가벼 운 분자종들을 EF-1L 또는 EF-1. 라고 부른다. EF-1H 는 EF-1. 이 외에 적어도 다른 한 가지의 단백질을 더 가지고 있는데, 이 단백질을 EF-lp 라 고 부른다. 이 EF-lp 가 존재 해 야만 무거 운 형 태 EF-1H 로의 옹 집이 일어나는 것으로 생각되고 있다. 정제된 EF-lH 제조물에는 포스 포리피드와 콜레스테롤이 들어 있다 (Moon 등, 1973). 따라서 EF-1H 는 EF-h(EF-1.) 과 EF-l p(분자량 30 kdal 정도)의 하위단위체들로 이루어 지는 응집체이다. EF-1 의 무거운 형태의 생리적 역할에 대해서는 아칙 찰 모르고 있다. Arte m i a salin a 의 발육 과정 에 따라서 EF-1H 와 EF-h 의 상대 적 인 양 표 5-3 여러 출처에서 얻은 EF-1 의 분자량 출 처 응집체 단량체 kdal 누 어 1 200~600 60 망상적혈구 200~300 53 밀 싹 200~300 50 Krebs 복수 200~300 47 Arte m i a salin a 200~300 50 간 400~700 53 뇌 1,000~2,000 50
이 변 한다는 보고가 있 다 (Slobin 과 Moller, 1975) . 그리 고 엘 라스타아 재와 카르복시펩티다아제 등과 갇은 단백질 가수분해효소들이 EF-1H 를 EF-h 로 해 리 시 킨다는 것 이 관찰되 었다 (Twardowski 동, 1976; Twar- dowski 동, 1977). 아래에서 곧 기술하겠지만, EF-h 형태가 연장인자 로서 작용하기 때문에, EF-1H 형태는 이 인자의 저장형이라고 생각할 수 있 다 (Slobin 과 Moller, 1977) . 나) EF-2 EF-2 는 단일 폴리펩티드로 되어 있다. 이 인자도 토끼의 망상적혈구에서 발견되었다. 쥐의 간과 돼지 간으로부터의 EF-2 의 분 자량은 각각 110 kdal 과 100 kdal 으로 추정 되 고 있다. 밀 싹의 EF-2 의 분자량은 70 kdal 칭도이다. EF-2 의 독목한 성질은 디프테리아 독소와 NAD 가 있는 조건에서 ADP- 리보 실화컬 수 있다는 것이다 (H on j o 등, 1968). 뒤에서 곧 기술되겠지만, 이 반응은 그 목 이성이 매우 크다. 5. 3 . 2 EF-1 의 기능 EF-1 은 GTP 의존적으로 일어나는 아미노아실-t RNA 의 리보솜에의 결합을 증진시킨다. 아미노아실-t RNA 와 리보솜온 일정한 바율로 결합 하지만, EF-2 가 존재하는 조건, 죽 펩티드 결합이 형성되고 있는 조 건에서는 아미노아실-t RNA 의 결합은 촉매적인 성격을 가지게 된다. 원핵세포의 경우에서와 같이, 리보솜에의 결합에 앞서서 EF-1 은 GTP 및 아미노아실-t RNA 와 결합하여야 한다• 가) EF-1 의 구아노신 누클레오티 드 및 아미 노아실-t RNA 와의 상호작용 구 아노신 누클레오티드들은 EF-1 의 무거운 형과도 결합하고 가벼운 형과 도 결합한다. 이 반응은 oo 에서도 일어나고 37° 에서도 일어나며 2 분 이내에 반응이 완결된다. EF-1E 와 EF-1L 은 GTP 와의 결합이 좀더 강 하지 만, GTP 와도 결 합하고 GDP 와도 결 합한다 (Nag a ta 등, 1976; rvio o n 과 Weis s bach, 1972 ; Leg o ck i 등, 1974) . 이 것 은 원 핵 세 포의 경 우와 비 교하면 매우 대조적이다. 즉, 원핵세포의 EF-Tu•GDP 의 해리상수는 EF-Tu; GTP 의 것 보다 100 배 나 작다 (Mi ller 와 Weis s bach, 1970) 廳 돼 지 간의 EF-h 에 대 한 GTP 와 GDP 의 Km 값들은 각각 2. 0 X 1Q- 7 과 5. Ox 10-1 M 이 다 (Nag a ta 등, 1976) . Arte m i a ( Slobin 과 Moller, 1976)
와 소 뇌로부터의 EF-h 은 EF-1H 보다 GTP 를 결합하는 능력이 훨씬 더 크다. Arte m i a 의 EF-h 은 EF-1H 보다 10 배 나 더 많은 GTP 를 결 합하며, 소 뇌의 EF-h 은 EF-1H 보다 5 배나 더 많은 GTP 를 결합한 다. Arte m i a 의 EF-1H 에 서 EF-h •G TP (또는 GDP) 복합체 가 생 기 기 는 하지만, EF-h•GTP( 또는 GDP) 에 비하면 다소 불안정하다. 이성분 복합체 EF-h·GTP 는 아미노아실-t RNA 와 반응하여 삼성분 복합체를 형성한다. EF-h•GTP + 아미노아실-t RNA ➔ 아미노아실-t RNA·EF-h·GTP EF-ln·GTP 는 아미노아실-t RNA 와 거의 반응하지 않거나 전혀 반응 하지 않는다 (Moon 등, 1972 ; Slobin 과 Moller, 1976) . 이 러 한 결 과 에 서, EF-lu 는 아미노아실-t RNA 와 반응하는 동안에 EF-h 형태로 전환 되거나, 아니면 EF-1H 를 함유하는 삼성분 복합체가 불안정할 것임을 알 수 있다. 아직 증명되지는 않았지만, 삼성분 복합체가 형성되는 동 안에 EF-1 은 다음과 같은 전이과정을 밟는 것으로 생각된다. EF-h + GTP ~ EF-lu•GTP EF-h •G TP :;== EF-h· GTP EF-h·GTP + 아미노아실-t RNA ~ EF-h•GTP• 아미노아실 -tRN A 삼성분 복합체의 형성은 EF-h·GDP 와는 일어나지 않으며, 탈아실화된 tR NA 또는 NH2 기 가 가리 워 진 아미 노아실-t RNA 는 아미 노아실-tRt\T A 를 대신할 수 없다. 나) 삼성분 복합체와 리보솜의 상호작용 삼성분 복합체를 리보솜과 항온 반응시켰을 때, 삼성분 복합체의 성분들이 어떠한 변화를 받는지를 보 기 위 해 서 Weis s bach 등 (1973) 은 [3H ,r - 呼〕- ATP 와 “C-Phe -tRi';rA 들로 이루어진 표지된 삼성분 복합체를 만들었다• 이 복합체를 리보솜 및 풀리 (U) 와 함께 항온반응시키면 Ph e-t RNA 는 리보솜에 결합되고, GTP 는 가수분해되고, 이성분 복합체 EF-l·GDP 가 화학양론적으로 형 성하였다. 항온반응 혼합물에서 풀리 (U)를 삭제하였을 때는 원래의 삼 성분 복합체가 그대로 리보솜에 결합되어 있었으며, GTP 의 가수분해 는 전혀 일어나지 않았다. 그렇지만, 뒤에 풀리 (U)를 항온반옹 혼합물
에 첨가하면 GTP 가 재빨리 가수분해되었다. 이 결과는 삼성분 복합체 논 리보솜에 대해서 매우 큰 찬화력을 가지고 있지만, 폴리 (U) 가 존재 할 때만 올바른 자리를 잡게 되어서 GTP 가수분해가 일어난다는 것을 암시 해 준다. Slobin 과 Moller (1976) 는 Arte m i a 의 EF-1 을 리 보솜, Phe-tR l~A , 풀리 (U) , 및 GTP 들과 항온반응시 키 면 가수분해 되 는 GTP 의 양은 항온반응 혼합물에 존재 하는 EF-1 및 Phe-tR NA 의 양에 비 례 한다는 것 을 알았다. 가수분해 는 Phe-tR NA 뿐 아니 라 리 보솜의 두 하 위단위체들의 존재에 의존해서 일어난다. 위에서 본 일련의 반응들은 원핵세포의 연장인자들에 의해서 일어나 는 것들과 매우 유사하다 (5. 1. 2 및 5. 2.1 절들을 보라). 다) EF-1 의 순환식 재이웅 위에서 말한 바와 같이, 삼성분 복합체 아 미노아신-t RNA·EF-h•GTP 와 리보솜의 상호작용의 결과로서 EF-h· GDP 가 형성된다. 이 이성분 복합체는 아미노아실-t RNA 와 반응할 수 없으므로, EF-1 이 촉매적으로 기능을 발휘하기 위해서는 EF-h·GTP 로 전환되어야 한다. 원핵세포에 있어서는 EF-Tu•GTP 를 재생시키는 일은 연장인자 Ts 가 한다 (5. 1. 2 및 5.1 .3 절을 보라). a) EF-Tu •G DP + EF-Ts ~ EF-Tu• EF-Ts + GDP b) EF-Tu• EF-Ts + GTP ~ EF-Tu • GTP + EF-Ts EF-l·GDP 와 GTP 사이의 교환반응을 촉진하는 단백질은 EF-1, 임 이 밝혀쳐 있다 (5.3.1 전의 (가)항을 보라). a) EF-lL' GDP + EF-1, ~ EF-h • EF-1, + GDP b) EF-h•EF-1, + GTP ~=츠 EF-h•GTP + EF-1, Slob i n 과 M6ller(1978) 가 최근에 EF-h·EF-1,•GTP 복합체를 검출한 것은 의미있는 일이라고 생각된다• 0°C 에서만 안정한 것으로 알려진 이 복합체는 EF-1, 로 촉진되는 교환반응에 있어서의 가상적인 중간물질이 다. 구아노신 누클레 오티 드의 교환반옹을 촉매 할 뿐 아니 라, EF-1, 는 EF-1L 의존적으로 일어나는 아미노아실-t RNA 의 리보솜에의 결합과 EF-1 및 EF-2 의존적으로 일어나는 폴리페닐알라닌의 합성둘도 촉진 시킨다. 두 반옹의 이러한 촉진은 아마도 EF-h·GDP 를 EF-h•GTP 로 전환시키는 EF-1, 의 능력과 관계되는 것으로 생각된다. 요컨대, 여러 진핵세포들에 있어서 EF-1 의존적으로 일어나는 아마
노아실-t RNA 의 리브 솜에의 결합에 관련된 반 응둘은 원핵 세포 계 에서 볼 수 있는 상응하는 반응 들과 매우 유 사하다. 그 단 계들을 그림 5-8 에 나타내었다. 거의 모든 조직들에 존재하는 것으로 알려진 EF-1 의 우거 운 형 태 ( EF - 1 H) 는 GTP 와 반응하여 EF-h·GTP 를 형성시키 는 것으로 생각된다. 그 다음에 EF-h·GTP 와 아미노아 실 -t RNA 가 상호 작용합
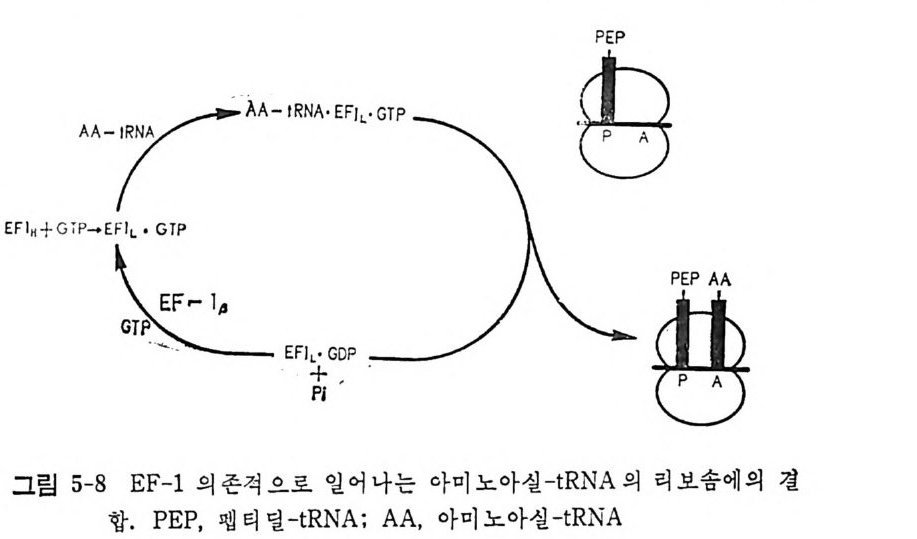 PEPL
PEPL
으로써 삼성분 복합체 아미노아 실 -t R NA ·EF-h·GTP 가 형성된다• 그 다음에 는 이 복합체 로부터 의 아미 노아 실 -t RNA 가 리 보송의 A 자리 에 결합된다. 이 과정에서 GTP 가 가수분해되고 리보솜으로부터 EF-h· GDP 가 방 출 된다. EF-h·GTP 의 재생은 EF-1, 에 의해서 촉매되는 GTP-GDP 교 환 반응으로 이 루어 진 다. 5. 3. 3 EF-2 의 기능 가) EF-2 의 구아노신 누클레오티드 및 리보솜파의 상호작용 원핵세포와 진 핵세포의 연장인자들 사이의 유사성은 EF-G 와 EF-2 들에 있어서도 볼 수 있다• 두 가지 인자들은 다 GTP, GDP 및 푸시드산들과 상호작용한 다. 쥐 간의 EF-2 가 리보솜에 결합하는 데에는 GTP 가 , 있어야 한다 는 것 은 Skog e rson 과 Moldave (1964) 가 처 음으로 발견하였 다. EF-2 와 GTP 를 함유하고 있는 항온반옹 혼합물에 서 분리 한 리 보솜은 추가로 첨
가하는 EF-2 가 없어도 단백질 합성을 할 수 있는 능력을 가지고 있다. 이 결과는 EF-2 가 리보솜에 결합된 채로 남아 있음을 가리킨다. 그 후 에 GDP 와 GDPCP 도 EF-2 의 리보솜에의 결합을 일으키게 한다는 것 이 알려 졌 다 (Skog e rson 과· Moldave, 1968) . 그러 나, 아미 노아실 -tRN A 의 리보솜에의 결합을 촉진할 수 있는 리보솜 ·EF-2 복합체는 GTP 에 의해서만 생길 수 있다. 이것은 EF-2 와 GTP 가 있는 조건에서 리보솜 의 A 자리에 있는 펩티딜-t RNA 가 EF-2 에 의해서 P 자리로 옮겨감 으 로써 리보솜의 A 자티가 아미노아 실 -t RNA 를 결합할 수 있게 된다는 것을 말해 준다. 정제된 EF-2 는 여러 가지 구아노신 누클레오티드들과 안정한 복합체 를 형성할 수 있다. 원핵세 포로부터는 안정한 EF-G· 구아노신 누큘례오 티드 복합체가 단리되지는 못하였지만, 그러한 복합체 형성이 일어난다 는 것이 평형두석법으로 밝혀졌다 (Ara i 등, 1977). 진핵세포의 경우에 는 여 러 생 물종들에 서 EF-2 •G TP 복합체 가 관찰되 어 있 다 (Bodley 와 Lin , 1972 ; Balig a 와 Munro, 1972 ; Chuang 과 Weis s bach, 1972 ; Mi z- umoto 등, 1974; Henrik s en 등, 1975a) . 마찬가지 로, GDP 와 GDPCP 도 EF-2 와 안정한 복합체를 형성한다. EF-2 와 GTP 를 리보솜이 있는 데서 항온반응시키면, EF-2, GDP, 및 리보솜이 1 : 1 : 1 로 함유된, 삼성분 복합체 리보솜 ·EF-2·GDP 가형 성 된 다 (Balig a 와 Munro, 1972 ; Mi zu moto 등, 1974 ; Henric k sen 등, 1975b). EF-2•GTP 복합체가 안정한 상태로 단리될 수 있기 메문에, 리보솜과 이 복합체의 상호작용은 GTP 를 가수분해시키는 결과가 된 다. 이러한 실험결과들에서 다음과 같은 일련의 반응이 일어나는 것으 로 생각되고 있다. a) EF-2 + GTP ~ EF-2 •G TP b) EF-2 • GTP + Rib ― ➔ Rib • EF-2 • GDP + Pi 그런데, GTP 대신에 GDP 또는 GDPCP 를 사용하여 삼성분 복합체가 생기므로, 이 반응이 GTP 의 가수분해를 필요로 하는 것은 아님을 알 수있다. A 자리에 펩티딜-t RNA 를 함유하고 있는 리보솜이 EF-2•GTP 와 상호작용하면 펩티딜-tR NA 가 P 자리로 옮겨가게 되며, 이와 동시에 GTP의 가수분해가 일어난다. 원래는 GTP 의 가수분해에서 방출되는
에너지가 자리옮김에 필요한 것으로 생각되었다. 그러나 EF-G 와 EF-2 들을 사용하여 연구한 바에 의하면 자리옮김은 GDP 의 존재 하에서는 일어나지 않지만 GTP 의 비가수분해성 유사체들의 존재 하에서도 일어 날 수 있음이 밝혀졌다. 이 결과들은 EF-2-GTP( 또는 GDPCP ) 의 리보 송과의 결합 자체가 자리옮김을 일으키는 데 충분하며, GTP 의 가수분 해는 EF-2 가 재이용될 수 있게 회전시키는 데 필요하다는 것을 암시해 준다. 푸시드산은 스테로이드 항생물질이며 원핵세포에 있어서 안정한 푸시드산 • 리보송 • EF-G·GDP 복합체를 형성하는 것으로 알려져 있다 (5.1 . 4. 절을 보라). 이 안정한 복합체가 형성됨으로써 EF-G 는 리보 송으로부터 떨어져 나울 수 없으며 따라서 촉매적으로 작용할 수 없게 된다. 이러한 관찰에서 푸시드산의 항생물질로서의 작용 메카니즘을 알 수 있다. 진핵세포에 있어서도 푸시드산의 방해작용의 메카니즘이 원핵 세포에서 관찰되는 것과 동일하다. 푸시드산은 리보솜에 결합된 EF-2 와 다음과 같은 일련의 반응으로 복합체를 형성한다. a) EF-2 + GTP ~ EF-2 • GTP b) EF-2·GTP + 리 보솜 - Ri b• EF-2-GDP + Pi c) Ri b· EF-2·GDP 그모프> 푸시드산 • Ri b· EF-2·GDP 단백질 합성이 일어나는 동안의 일련의 반응들을 보면, EF-2-GDP 는 자리옮김 반응에 뒤이어서 리보솜으로부터 떨어쳐 나울 것임을 암시해 준다. 유리된 EF-2-GDP 는 또다른 GTP 와 반옹함으로써 촉매적으로 기능을 발휘하게 된다. EF-l·GDP 와는 달라서 EF-2-GDP 는 추가적인 인자의 도움이 없이도 GTP 와 교환반응을 하여 EF-2·GTP 를 만들 수 있 다 (Mi zu moto 등, 1974) . 푸시 드산이 존재 하는 데 에 서 는 EF-2-GDP 가 리보솜에 포착되며, 그렇게 됨으로써 아미노아실-t RNA 가 결합되는 것을 방해한다. 왜냐하면, EF-1 은 EF-2 가 함유된 리보솜에는결합할 수 없 기 때 문이 다 (Bali ga 등, 1973 ; Nombela 와 Ochoa, 1973) . GTP 의 가수분해가 60S 리보솜 하위단위체에 40S 하위단위체를 첨가함으로써 다소 촉진되 기 는 하지 만, EF-2·GTP 복합체 의 리 보솜과의 상호작용 :::z. 리고 GTP 의 가수분해는 60S 하위단위체만이 필요한 것으로 보인다 (McKeehan, 1972). 이것 또한 원핵세포 계에서 관찰된 것과 매우 유 사하다.
나) 디프테리 아 독소에 의한 EF-2 의 활동성으 1 방해 Coryn e bacte r im n dip - h t hcr i ae 에 의해서 생성되는 디프테리아 독소는 분자량 62 kdal 정도 되 는 단일 폴리펩티드 사슬로 구성된 단백질이며, 독성이 매우 크다. 치 사량은 50-100ng /k g 정도이다. 득이한 펩티드 결합과 이황화결합에서 전단되면, 이 단백질은 두 조각으로 분해된다. 조각 A 는 독소의 아미 노 말단에서 생기며 분자량은 21 kdal 이다. 한편 카르복시 말단에서 생 기 는 조각 B 는 분자량이 약 40 kdal 이 다 (Pap pe nheim er, 1977) . 디 프 테리아 독소의 독성은 EF-2 를 비활성화시키는 능력과 관계가 있다는 것이 밝혀졌다. HeLa 세포를 이 독소에 노출시키면 두 시간 이내에 단 백 질 합성 이 득이 하게 방해 된다 (Str a uss 와 Hendee, 1959) . 현재 는 이 독소의 독성작용이 이단계 과정이라는 것이 알려져 있다. 초기단계는 독 소의 조각 B 부분이 막의 특이한 수용체에 결합하는 것이다. 그 다음에 는 조각 A 가 세포질 안으로 방출되며, 거기서 EF-2 의 비활성화를 촉 매한다. 디프테리아 독소의 작용에 대한 세포내 저항성은 이 독소가 세 포막에 결합하지 못하기 때문에 생기는 것으로 생각된다. 여러 연구진 돌의 연구결과로 EF-2 의 비활성화는 독소와 NAD 가 촉매한다는 것이 밝혀 졌다 (Coll ier, 1967; Goor 와 Papp e nheim er, 1967; Raeburn 등, 19' 68) . Honjo 등 (1968) 은 디 프테 리 아 독소의 방해 작용의 메 카니 즘은 NAD+ 의 아데노신 이인산 리보오스 부분이 다음과 갑은 반응으로 EF-2 에 전달되는 것임을 알았다. NAD+ + EF-2 혼츠 ADP- 리 보실 -EF-2 + 니 코틴 아미 드 + H+ pH 7 및 반응물질들의 생리적 농도들에서 이 반응은 본질적으로 비가 역적이다. 그렇지만, 만일 NAD+ 를 제거하고, p H 를 낮추고, 과량의 니 코틴 아미 드를 첨 가하면, 독소와 비 활동성 인 ADP- 리 보실화된 EF-2 의 존재에서 EF-2 의 활동성이 회복된다. EF-2 가 독소에 의해서 ADP- 리보실화되면, 폴리페닐알라닌 합성을 촉매하는 EF-2 의 능력과 리보솜 의존적으로 일어나는 GTP 가수분해 의 방해가 따르게 된다. 디프테리아 독소에 의해서 촉매되는 EF-2 의 ADP- 리보실화 반응은 식물과 효모를 포함한 광범한 진핵세포들로부터의 EF-2 에 대해서만 목 이 하게 일 어 난다 (Van Ness 등, 1978) . 박테 리 아 또는 미 토콘드리 로부 터 의 EF-G 는 이 독소의 영 향을 받지 않으며 , 포유동물의 추출물 중에
서 이 독소의 영향으로 ADP- 리보실화되는 기질은 EF-2 뿐이다. 여러 가지 진핵세포들로부터의 EF-2 가 비활성화된다는 것은 EF_2 단백질은 디프테리아 독소의 인식에 필수적인 독특한 성질이 있을 것임을 암시해 준다. 실 제 로, Robin s on 등 (1974) 은 ADP- 리 보싣 화된 EF-2 를 트립 신 으로 처리하여 얻은 펩티드들 중에서 다음과 같은 15 개의 아미노산 찬 기를 가진 펩티드가 독소의 인식 부분임을 밝혔다. Phe-Asp- V al-Hi s- Asp- V al-Thr-Leu-Hi s- Ala-Asp- Ala-lle-X-Arg ADP- 리 보오스는 이 드문 아미노산 찬기 (X) 에 결합된다. 최근에 이 아미노산의 화학적 본질이 NMR 분광법으로 밝혀졌다. 이 아미노산은 약한 염 기 성 을 가진 2-(3- 카르복시 아미 도 -3- (트리 메 틸 암모니 오) -프로필 히 스티 단으로 그 구조가 결정 되 었다 (Van Ness 등, 1980) (그립 5-9 를 보라)• 이 아미노산의 관용명은 디프타미드이다. 아직 이 드문 디프타미드 잔기가 무슨 기능을 가지고 있는지에 대해 서는 찰 모르고 있다. 이 아미노산 유도체가 모든 진핵세포로부터의 EF-2 에서 발견되기 때문에 이 단백질의 기능에 필수적인 것이라고 추측할 수 는 있다. 그러나, 이 아미노산 유도체를 가지지 않는 EF-2 를 가진 돌연 변이체가 단리되었는데, 단백질 합성에는 결함이 없는 것으로 알려져 있 다 (Moehrin g 등, 1980) . 그러 므로 펩 티 드의 일 부분으로서 의 티 프타미 드 가 EF-2 에서 하는 역할에 관해서는 앞으로 더 연구하여야 할 문제이다.
H尸 숙 -CHz-CH( NH2)-COQ H HN 了2 N CH2 CH3 CI (H')+ NI ~ CH3 o= CI CI H3 如 2 그림 5-9 디 프타미 드의 구조
5.4 진핵세포의 리보솜 상에서의 연장 5. 4. l 펩티드 결합의 형성 펩티드 결합의 형성은 단백질 합성에 있어서의 그밖의 모든 반응둘이 가용성 인자 를 필요로 하는 것과는 대조적으로 리보솜의 큰 하위단위체 의 구조적 성분인 단백질에 의해서 촉매 된다. 이것은 원핵세포 계와 진 핵세포 계에 있어서 공통적이다(그립 5-3 을 참조하라). 원핵세포 계에 서와 마찬가지로, 진핵세포 계에 있어서도 펩티드 결합의 형성은 펜디딜 기 전달효소의 촉매작용으로 리보솜의 P 자리에 결합된 펩티딜-t RNA 와 A 자리에 있는 아미노아실-t RNA 사이에서 일어난다. 이 반응에서 성장하고 있는 풀리펩티드 사슬이 아미노산 잔기 하나만큼 연장된다. 이 반응에는 추가적인 단백질 인자 또는 의부에서 가해 주는 에너지가 필요없다. 박테리아의 계에 있어서는 펩티드 결합 형성에 많은 리보송 단백질들 이 관여하는 것으로 알려져 있지만 (5.2.2 전의 표 5-2 를 참조하라), 진핵세포의 팹티드 결합 형성에 관여하는 단백질들에 관해서는 거의 알 려진 것이 없다. 촉매작용은 진핵세포의 리보솜의 60S 하위단위체에 있 으며, 린코마이신, 스과르소마이신, 아니소마이신들과 같은 항생물질들 뿐 아니라 그밖의 많은 화합물들에 의해서 방해된다(자세한 것은 제 7 장을 보라). 제 6 장에서 기술되겠지만, 펩티딜 기 전달효소는 단백질합 성의 종결반응에도 참여한다. 5.4.2 자리옮김 진핵세포에 있어서의 자리옮김은 원핵세포의 경우와 거의 갇은 메카 니즘으로 일어난다(그림 5-1 을 참조하라). 단백질 합성에 있어서 제일 찰 이해되지 않고 있는 과정은 리보솜이 mRNA 를 따라서 움직이는 과 정일 것이다. 각 아미노산이 첨가될 때마다 리보솜은 mRNA 의 5' 쪽 에서 3' 쪽으로 정확히 한 코돈(즉, 세 개의 염기)만큼 움직인다. 리보 솜의 A 자리 상에서 갓 생긴 펩티드 사슬은 자리옮김의 결과로 P 자리 로 옮겨가며, P 자리에 결합된 탈아실화된 t RNA 는 밀려나며, 리보 송은 mRNA 의 3' 끝 쪽으로 세 개의 염기만큼 이동한다. 이 결과로
A 자리에는 새로운 코돈이 오게 되고, 이 빈 A 자리에 새 아미노아살 -tRN A 가 결 합하게 된 다. 이 과정에서 작용하는 EF-2 의 기능에 관해서는 5.3.3 절을 보라. * 참고문헌 Allende, J.E . , Monro, R., Lipm ann, F. (1964), Proc. Natl . Acad. Sci. 51, 1211 . Arlin g h a us, R. , Favelukes, G. , Schweet, R. (1963) , Bio c /z e m. Bio p /z y s. Res. Co1111111111. 11, 92, Arai, N. , Arai, K. , Kazir o , Y. (1977) , ]. Bio c hem. 82, 687. Arai, K.I., Kawakit a, M., Kazir o , Y., Maeda, T., Ohnis h i, S. (1974), J Bio l . C/ze m . 249, 3311, Arai, K. I. , Ka w a ki t a, M. , Nakamura, S. , Ishik a wa, I. , Kazir o , Y. (1974) , ]. Bio c / w m. 76, 523, Balig a , B. S. , Munro, H. N. (19 72) , Bio c/zim . Bio p h y s . Acta 277, 368. Bali ga , B. S. , Schechtm an, M. G. , Munro, H. N . (1973) , Bio c / ze m . Bio p /z ys . Res. Co1111111111. 51, 406. Beaud, G. , Leng yel , P. (1971) , Bio c hemi st r y 10, 4899, Bodley, J. W. , Lin , L. (1970) , Natu re 227, 60. Bodlie y , J.W ., 'liev e, F.J. , Lin , L , Zie v e, S.T. (1969), Bio c lzem. Bio p h y s .. Res. Commun. 37, · 437. Bodley, J. W. , Zie v e, F.J . Lin , L. , Zie v e, S. T. (1970) , ]. Bio l . Chem. 245, 5656. Brot, R. (1982) , Prote i n Bio s yn th e sis in Eukaryo t e s (Ed. , R. Perez-B e rcoff ) , p. 253. Plenum Press. New York. Brot, N., Redfi el d, B., Weis s bach, H. (1970), Bio c /1 e 11 1 . Bio p /z ys. Res. Commun. 41, 1388, Brot, N., Yamasaki, E., Redfi el d, B., Weis s bach, H. (1972) , Arch. Bio c / 1e m. Bio p h y s . 148, 148. Chen, C. -M., Ofe n g an d, J. (1970) , Bio c lzem. Bio p / 1y s. Res. Commun. 41, 190. Chaung , D. M. , Weis s bach, H. (1972) , Arch. Bio c lzem. Bio p /z ys . 152, 114. Chladek, S., Rin g e r, D., Zeml ick a, J. (1973) , Bio c hemi st r y 12, 5135. Coll ier, R.J. (1975) , Bacte r ia l. Rev. 39, 54. Coll ier, R.J. (1976) , J Mo!. Bio l . 25, 83. Coop er , D. , Gordon, J. (1969) , Bio c he m is tr y 8, 4289. Fahnensto c k, S., Weis s bach, H., Ric h , A. (1972), Bio c / 1im . Bio p !z ys. Acta 269, 62.
Furano, A. V. (1975) , Proc. Natl . Acad. Sci. 72, 4780. Gavri lo va, L. , Kote l ia n sky , V. E. , Sp iri n , A. S. (1974) , FEES Le tt. 45, 324. Gavrilo va, L. P. , Sp iri n , A. S. (1972) , FEES Le tt. 22, 91, Goar. R. S. , Papp e nheim er, A. M. , Jr. (1967) , ]. Exp . Me d. 126, 899. Gordon, J. Weis s bach, (1970) , Bi oc hemi st r y 9, 4233, Gott es man, M.E. (1967), ]. Bi ol . Chem. 242, 5564. Gup ta, S.L. , Wate r son, J., S op o ri, M.L. , Weis s man, S.M. , Leng yel , P. (1971), Bi oc he m i st r y 10, 4410. Bachmann, I., Mi ller, D.L . , Weis s bach, H. (1971) , Arch. Bi oc lze m . Bi op l zy s. 147, 457, Harris, R. J. , Pestk a , S. (1977) , Molecular Meclza11is 11 1s of Prote i n Bio s y1 1t l1es is (Ed. H. Weis s bach, S. Pestk a ) , p. 413, Academi c Press, New York. Henrik s en, 0., Robin s on, E.A. , M axwell, E.S . (1975a), ]. Bi ol . Che 111 . 250, 720. Henrik s en, 0., Robin s on, E.A ., Maxwell, E.S. (1975b), ]. Bi ol . Che m . 250, Honjo , T., Nis h iz u ka, Y., Hay ai s h i, 0., Kato , I. (1968), ]. Bi ol . Che m . 243, 3553. Inoue -Y okosawa, N., Ishik a wa, C., Kazir o , Y. (1974), ]. Bi ol . Clze 111 . 249, 4327. Ishit su ka, H. Kurik i , Y., Kaji, A. (1970), ]. Bio l . Clzem. 245, 334 6. Kawakit a, M., Arai, K.I., Kazir o , Y. (1974) , ]. Bio c he m i st r y 76, 801 . Ki sh a, K. , Moller, W. , Sto e ff ler , G. (1971) , Na tu r e Ne w Bio l . 233, 62. Krauskp pf, M., Chen, C.- M ., Of en g an d, J., ]. Bio l . Clze m . 247, 842. Leder, P., Bernardi, A., Liv i n g s to n , D. Loy d, B., Roufa , D., Skog e rson, L. (19 69), Cold Sp ri n g Harbor Sy m p . Q11 a11t . Bi ol . 34, 411 . Lego ck i, A.B., Redfi eld , B., Weis s bach, H. (1974), Arclz. Bi oc hem. Bio p l zy s. 161, 709. Lipm ann, F. (1969) , Scie n ce 164, 1024. Lockwood, A.H., Hatt m ann, S., Dubnoff , J.S ., Mait ra, U. (1971), J Bio l. Chem. 246, 2936. Lucas- L enard, J., Beres, L. (1974), The E11zy m es(Ed., P.D. Boy er ), Academi c Press, New York. Lucas-Lenard, J., Lip m ann, F. (1966) , Proc. Natl . Acad. Sci. 55, 1562. Lucas-Lenard, J., Tao, P., Haenni, A. L. (1969), Cold Sp ri n g Harbor Sy m p . Qu ant. Bi ol . 34, 455. Maden, B.E .H., Monro, R.E. (1968), Eur. ]. Bi oc hem. 6, 309. Maden, B.E H., Traut, R.R., Monro, R.E . (1968), 35, 333. Maim ets , T., Remme, J., Vi llem s, R. (1984) , FEES lett . 166, 53. Marsh, R.C ., Chin a li, G., Parmeg gian i, A. (1975), ]. Bi ol . Chem. 250, 8344. McKeehan, W. (1972) , Bi oc lzem. Bio ph ys . Res. Commun. 48, 1117.
Mi lle r, D., Weis s bach, H. (19 70 ) , Arclz. Bi oc lze m. iJ . .)/ zy s . Hl, 26. M iller , D. , Weis s bach, H. (19 70) , Bio c lzem. Bi op h y s . Res. Com111w1. 38, 1016, M izu moto , K. , Iwasaki, K. , Kazir o , Y. (19 74) , ]. Bio c lze m . 76, 126 9 . Modole ll , J., Cabrer, B., Va zq u ez, D. (19 73) , ]. Bio l. C/z e m . 2,18 , 8356. Modole ll, J. , Vazq ue z, D. , Mon ro , R. E. (19 71a ) , Natu r e New Bi ol . 230, 109, Modolell, J. , Cabrer, B. , Pa rm eg gian i, A. , Vazq ue z, D. (1971b) , Proc. Natl . Acad. Sci. 68, 179 6. Monro, R.E ., Sta e helin , T., Celma, M.L., Vazq u ez, D. (1969). Cold Sp ri n g Harbor Sy m p . Qu a11t . Bio l . 34, 357, Monta n a o, L. , Sp er t i, S. , Testo n i, G. , Matt iol i, A. (1976) , Bi oc lze m . ]. 156, 15. Moon, H.M. , Redfi el d, B., Mi lla rd, S., Vane, F., Weis s bach, H. (1973) , Proc. Natl . Acad. Sci. 70, 3282. Moon, H. M. , Redfi el d, B. , \Ve is s bach, H. (1972) , Proc. Natl Acad. Sc i. 69, 1249. Moon, H. M. , Weis s bach, H. (1972) , Bi oc lzem. Bi op / zys. Res. Comm1111. 46, 254. Naga ta , S., Iwasaki, K., Kazir o , Y. (1976) , Arclz. Bi oc l1e111. Bi op h ys . 172, 168. Nath a ns, D. , Lip m ann, F. (19 61) , Proc. Natl . Acad. Sci. 47, 497. Ni er haus, K. H. (19 80) , Ri bo somes: Str u cure, Fzmcti o;z , and Geneti cs (Ed . , G. Chambliss , G.R . Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura), p. 267 Univ e rsit y Park Press, Baltim ore. Ni er haus, K. H. , Monte j o , V. (1973) , Proc. Natl . Acad. Sci. 70, 2224. Ni sh iz u ka, Y. , Lip m ann, F. (1966a) , Proc. Natl . Acad. Sc i. 55, 212. Nis h iz u ka, Y. , Lip m ann, F. (1966b) , Arch. Bio cl 1e111. Bio p h ys . 116, 344. Nombela, C. , Ochoa, S. (1973) , Proc. Natl . Acad. Sci. 70, 3556. Of en g a nd, J., C hen, C.-M. (19 72), J. Bi ol . Chem. 247, 2049. Of en g an d, J., L in , F.-L., Boublik , M. (1981) , Molecular Ap pro aches to Gene Exp re ssio n and Prote in Stm clllre(Ed., M.A.Q . Sid d iq u i, M. Krauskop h , H. Weis s bach) , p. l, Academi c Press, New York. Ono, Y. , Skoultc h i, A., Klein , A., Leng yel , P. (1968), Natu r e 220, 1304. Pap pe nheim er, A.M., Jr. (19 77), A11n. Rev. Bio c hem. 46, 69, Raeburn, S., Goor, R.S., Schneid e r, J.A ., Maxwell, E.S. (1968), Proc. Natl . Acad. Sci. 61, 1428. Ravel, J. M. , Shorey, R. L. , Froehner, S. , Shiv e , W. (1968) , Arc/1 . Bi oc hem. Bi op l zy s. 125, 514, Ri ch , A. (1974), Ri bo somes (Ed., M. Nomura, A. Ti ss ie r e, P. Leng yel ), p. 871, Cold Sp ri n g Harbor Laborato r y , Cold Sp ri n g Harbor, New York. Ri dd le, D. L. , Carbon, J. (1973) , Natu r e New Bi ol . 242, 230, Ri ng e r, D. , Chladek, S. (1975) , Proc. Natl . Acad. Sci. 72, 2950. Robin s on, E.A., Henrik s en, D., Maxwell, E.S. (1974), ]. Bi ol . Chem. 249,
5088. Rohrbach, M.S., Bodley , J.\V . (1976), J Bi ol . Clze m. 251, 930. Schmi d. G. , Str ob el, . 0. , Sti :iffier :M eil ick e, M. , Sto f f ier , G. , Bock, A. (1984) . FEBS Le tt. 177, 189. Schneir , l\L , Moldave, K. (1968) , Bi oc l1i 111 . Bi op l zy s. Acta 166, 58. Shorey, R., Ravel, J.M ., Garner, C.W ., Shiv e , \\'. (19 69), 244 , 4555. Skjo l d, A.C ., Jua rez, H., Hedg eo th , C. (1973), ]. Bacte r ia l . 115. 117. Skog e rson, L. , Moldave, K. (1967) , Bi oc hc111. Bi op l1y s. Res. Coii m lllil. 27, 568. Skog er son, L. , Moldave, K. (19 68) , ]. Bi ol . Chem. 243, 5354. Skoultc h i, A., Ono, Y., Moon, H.M., Leng ye l, P. (19 6 8) , Proc. Sall. Acad. Sci. 60, 675. Slobin , L. I. , Mi :ill er, W. (1975) , Natu r e 258, 252. Slobin , L. I. , Mi :ill er, W. (1976) , Eur. ]. Bi oc l1c ;;1 . 69, 367 . Slobin , L.I., Mi :ill er, W. (1977) , Bi oc hem . Bi op l tys. Res. Comi :1 11:1. 74, 356. Sp irin, A.S. (1969) , Cold Sp ri ;1 g Harbor Sy m p . Qu a; zt. Bi ol . 나 . 197 . Sp ri n z l, M. , Cramer, F. (1973) , Natu r e, New Bi ol . 2,1 3, 3 (1S 73 ) . Tanaka, S., Kaji , A. (1972) , Bi oc lzcm. Bi op hy s . Res. Com1111m. ,rn , 136. Tanaka, N. , Ki no shit a, T., Masukawa, H. (19 6 8) , Bi ocl ze111. Bi op l zys. Res. . Commwz. 30, 278. Tanaka, N., Ki on oshit a, T., l\'Ias ukawa, H. (1969) , ]. Bi oc hem i st r y 65, 459. Thach, S.S . , Thach, R.E. (1971), Proc. Natl . Acad. Sci. 68, 1791. Thang, M.N., Dondon, L., Thang , D. C., Reth e r, B. (1572) , REES Le tt . 26, 145. Twardowski, T., Hi ll, J., Weis s bach, H. (1977), Arch. Bi oc he m . Bi op hy s. 180. 444. Twardowski, T., Redfi eld , B., Kemp er , W.C., Weis s bach, H. (1976) , Bi ocl 1c111. Bi op h y s . Res. Comm1m. 71, 272. Van Ness, B.G ., Howard, J. B., Dodley, J.W . (1978), J Bi ol . Chem . 253, 8687' Wate r son, J., Beaud, G., Leng yel , P. (1970), Natu r e 227, 34. Weis s bach, H., Brot, N., Mi ller , D., Rosman, M., Erte l, R. (1969), Cold Sp ri n g - Harbor Sy m p . Qu ant. Bi ol . 34, 419. Weis s bach, H., Mi lle r, D.L ., Hachmann, J. (1970) , Arcl1. Bi oc lzcm. Bi op h y s . 137, 262. Weis s bach, H., Redfi eld , R., Brat, N. (1971), Arch. Bi oc hem. Bi op hy s . 145, 676. Weis sb ach, H., Redfi eld , B., Moon, H.M. (1973), Arch. Bi oc hem . Bi op h y s. 156, 267. W ittingh ofe r, Lebermann, R. (1976) , Eur. ]. Bi oc hem. 62, 373. Wi ttingh ofe r , A., Frank, R., Gast, W.H., Leberman, R. (1979), ]. Mo/. Bi ol . 132, 253.
제 6 장 단백질 합성의 종결과정 펩티드 사슬의 종결이 일어나면 멘 마지막으로 리보솜에 결합한t RNA 로부터 완성된 펩티드가 떨어져 나온다. 펩티드 사슬의 종결은 리보솜 상에서 일어나며 원핵세포와 진핵세포에서 모두 가용성인 단백질 인자 ` 둘을 필요로 한다. E. coli 세포에서 발견된 두 가지 단백질 인자들(방 출 인자, RF) 은 그들의 코돈 독이 성 이 서 로 다르다. 즉, RF-1 은 UAA 또는 UAG 를, RF-2 는 UAA 또는 UGA 를 인식 한다. 토끼 의 망상 적 혈구와 바다 새우 Arte m ia salin a 에서는 UAA , UAG, 및 UGA 코돈둘 울 인식하는 한 가지 RF 가 알려져 있다. 박테리아의 RF-1 과 RF-2 의 리보솜과의 결합 및 방출에는 제 3 의 단백질 인자, RF-3 이 관여하는 · 데, 이 인자는 GDP 및 GTP 와 상호작용한다. 망상 적혈구와 Arte m t .a sal in a 의 RF 는 GTP 에 의해서 촉진되며 리보솜-의존성 GTPase 의 작 용을 가지고 있다. 사술 종결 단계에서의 펩티딜-t RNA 의 가수분해는 리보솜에 결합되어 있는 효소인 펩티딜 기 전달효소를 필요로 한다. 6.1 종결 코돈 종결 코돈이 존재할 것이라는 것은 처음에 무의미 돌연변이들에 관한· 유전학적 연구로 예견되었다 (Garen, 1968). 무의미 돌연변이란 아미노.
산 코돈이 펩티드 종결 코돈으로 전환되는 것을 말한다. 무의미 코돈이 제일 잘 알려진 것은 박테리아이지만 진핵세포에서도 많이 알 려쳐 있다 (Ozeki 동, 1980 ; Pip e r, 1980 ; Late n 등, 1980 ; Kohli 둥, 1980) . 무 의미 돌연변이는 다음과 같은 여러 가지 효과와 목 징을 나타낸다. (1) 염기 변화를 일으키는 돌연변이 유발제들에 의한 복귀 돌 연변이가 일어 날 수 있다. (2) 야생종에서 볼 수 있는 표현형의 성질을 전혀 볼 수 없 다. (3) 〈유전자외 〉 억압돌연변이에 의해서 표 현 형의 성 질 이 달라질 수 있다. (4) 접속된 mRNA 에 있어서 (원핵세포의 경우) 돌연 변 이가 일어 난 위치로부터 먼 쪽으로 있는 시스트론들의 번역을 감소시킨다. (5) 조 숙된 펩티드 사슬 종결과 함께, 돌연변이된 유전자 산물의 아미노말단 조각들이 나타난다. 종결 코돈의 생화학적인 성질은 처음에 E. col i의 염기성 탈인산 가수 분해효소 유전자에서 일어나는 무의미 돌연변이에 관한 연구로 알게 되 었다(W e ig er t 등, 1966). 이러한 무의미 돌연변이체들은 유전자의 억압 유전자들에 의해서 유전적인 정정 (즉, 억압)을 받게 된다는 것이 밝혀 졌다. Garen 은 억압유전자의 독이성을 이용하여 무의미 돌연변이체들과 억 압유전자들을 암버 부류와 오크르 부류로 나누었다 (Garen 동, 1965;
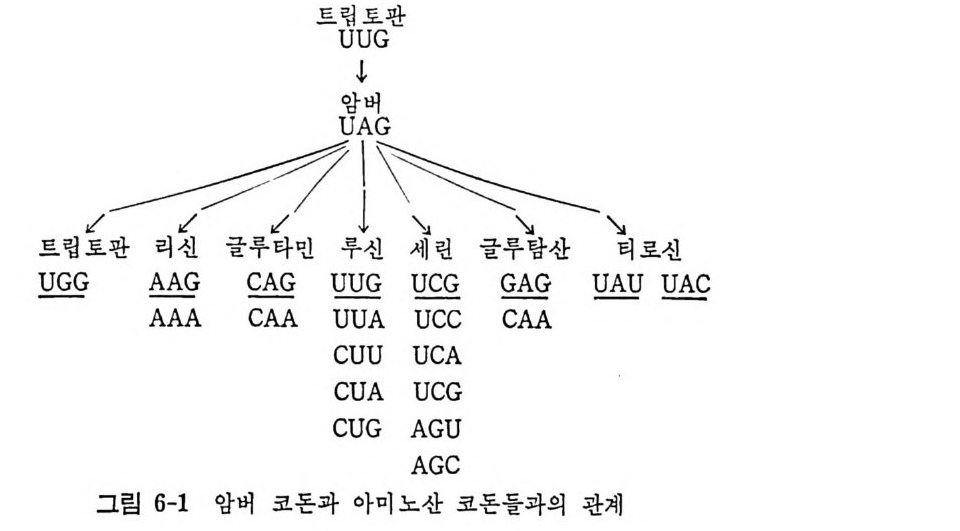 트U립U토G판
트U립U토G판
림 6-1) (Weig e rt 와 Garen, 1965) . 이 아미 노산들에 대 한 동의 코돈둘 중의 하나(그림 6-1 중에서 밑줄친 것)가 암버 코돈과 단 하나의 염기 변화로 달라졌다고 가정함으로써, 코돈 UAG 는 암버 코돈에 상응하는 트리누클레오티드라고 예견할 수 있었다. 바슷한 점근법으로 오크르 코 돈에 상응하는 트리 누클레 오티 드는 UAA 임 이 확인되 었다 (We ig e rt 등, 1967) . Brenner 등 (1967) 은 rl[ 돌연 변 이 체 를 사용하여 암버 또는 오크르 억 압유전자들로 정정되지 않는 또 하나의 무의미 돌연변이종들을 확인하 였다. 따라서 이 돌연변이는 UAA 또는 UAG 에 상응하지 않는 또 다 른 것임을 알 수 있었다. 이러한 결과에서 제 3 의 무의미 코돈이 있을 것임을 추측할 수 있었다. Sambrook 등 (1967) 은 UGA 에 특이한 억압 유전자를 얻어냈다. UGA 종결 코돈을 오팔 코돈이라고 한다. 이와 같 이 , 유전 학적 연 구들로 UAA, UAG, 및 UGA 들이 무의 미 코돈들입을 알았으며, 만일 이 무의미 코돈둘이 돌연변이체에서 일어나면 조숙한 펩티드 사슬의 종결이 일어난다. 1974 년대 초기에는 f2, R17, 및 MS2 둘과 같은 RNA 박테리오파지들 에 있어서의 RNA 둘의 시스트론과 시스트론 사이의 부분들의 누클레 오티드 결합순서가 부분적으로 결정되었다(Nic hols, 1970; N i chols 와 Roberts o n, 1971) (그림 6-2). 그림 6-2 에서 볼 수 있는 바와 같이, 의 피 단백 질의 C- 말단에 대 한 코돈 다음에 종결 코돈 두 개 (UA AUAG) 가
 입성효소 외피단디칼
입성효소 외피단디칼
나란히 있다. 이 RNA 들에 있어서는 UAA 에서 여덟 개의 코돈을지나 서 세번째의 종결 코돈이 있다. 아마도 이 세번째의 종결 코돈은 혹시 일어날지도 모르는 종결의 착오를 방지하는 역할을 하는지도 모른다. 최근에는 mRNA 의 단리법과 그 일차구조의 분석법이 많 이 발전되어 있기 때문에 원핵세포와 진핵세포의 mRNA 둘의 결합순서가 알려져 있 는 것이 매우 많다. 이러한 예들을 제 3 장의 그립 3-1,3-2 및 3-3 에 소개하였다• 이러한 예들에서 자연적으로 일어나는 종결 코돈이 UAA, UAG 및 UGA 둘이라는 것이 분명해졌다. 6.2 무의미 돌연변이의 억압 E, co li의 무의미 돌연변이는 UAG( 암버), UAA( 오크르), 및 UGA (오팔) 코돈 동에 의해서 일어나고 있다. 이 세 코돈들에 대한 t RNA 들 이 정상적인 세포에서는 존재하지 않기 때문에, 이 세 코돈둘은 아미노 산에 대한 정보를 가지지 못한다. 따라서 무의미 코돈에 대한 정보 독 이성을 변화시키는 돌연변이가 tRN A 유전자에서 일어난다면, 달라진 이 t RNA 는 번역이 일어나는 과정에서 특이한 아미노산을 삽입시킬 수 있게 됨으로써 다른 유전자들에서 일어난 무의미 돌연변이를 억압하게 될 것이다. 억압인자 유전자에 돌연변이가 일어난 경우에는, 돌연변이체는 보통 양성 (su+) 을 나타냄 으로써 정 상적 인 유전자들과 다르며 그의 대 립 유전 자인 야생형 유전자 (su- )에 대해서 우성이다. 따라서, 무의미 억압인자 유전자를 지닌 군주들의 검출이 비교적 쉽다. 실제로, 박테리아에서는
s11+1, s11+2, su+B, su+C 둥의 여 러 가지 무의 미 억 압인자 유전자들이 검출되었다. 이들은 염색체 상에서의 위치들과 삽입하는 아미노산들이 무엇인지에 의해서 구별된다. 앞에서 말 한 바와 같이, 무의미 억압인자 유전자들은 그들의 코돈 독 이성 에 따라서 분류된다. 즉, 암버 (UAG ), 오크르 (UAA), 및 오팔 (UGA) 억압인자 유전자들이 있다. 억압인자로 작용하는 몇 가지 t RNA 둘의 예를 들어 보자. 무의미 억 압인자 유전자가 tR NA 에 대한 구조 유전자라는 멘 처음의 결정적인 중거는 UAG 코돈에 대한 반응으로 티 로신을 삽입하는 su+3 에 관한 연 구에서 얻어졌다. 거의 모든 무의미 억압인자들은 억압인자로 작용하는 tR NA 에 있어서 누클레오티드 변화가 단 한 군데에서 일어난 것이다. 가) 티로신을 삽입하는 stt+ 3 암버 및 szi+ 4 오크르 억압인자 su+3 억 압인자 는 t RNA,T” 의 구조 유전자의 돌연변 이체의 하나이며 그의 역코돈에서 Q ➔ C 의 단일 영기 치환이 일어난 것이다(Q는 G 의 유도체이다). 그러 므로 이 t RNA 는 UAG 코돈이 있는 데서 티로신을 삽입할 수 있다. 오 크르 억압인자 유전자 su+4 는 같은 위치에서 Q ➔ U 돌연변이몰 한것이
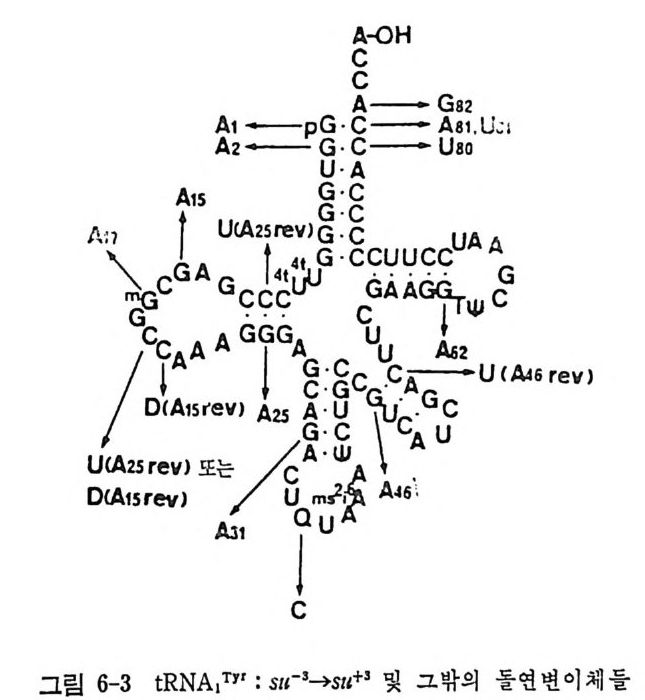 A`A'2 『-VG....G ACCCACCACUG三 야GGGG 8A28Uu138· l0
A`A'2 『-VG....G ACCCACCACUG三 야GGGG 8A28Uu138· l0
다. 따라서 UAA 또는 UAG 가 있는 데서 티로신을 삽입할 수 있다 (Smi th, 1972) . 나) 글루타민 또는 트립토판을 삽입하는 szt + 7 암버 및 sIt+ 8 오크르 억압인자 유전자들 su+? 은 t RNAT” 에 대한 구조 유전자의 역코돈 돌연변이체이 다(그립 6-5). t RNAT” 에서는 CCA ➔ CUA 의 역코돈 돌연변이가 일어 난다 (Soll, 1974; Yaniv 등, 1974). 억압인자 유전자 SI t +8 은 CCA(su-7) ➔ CUA(su+?) ➔ UUA(su+s) 과 같은 두 단계 돌연변이로 일어날 것으로 생각된다 (Yan i v 등, 1974). 이 역코돈을 가진 t RNA 는 글루타밀-t RNA 합성효소에 의해서 찰못된 아미노아실화가 일어난다. K 립--o 는연 이뎅오체 팔이 U GAkcC로X卜 G u전7c cL’억 c cG +인9K C } 는어 ’G t RG 대 N굽 CA TrCHp A1A A
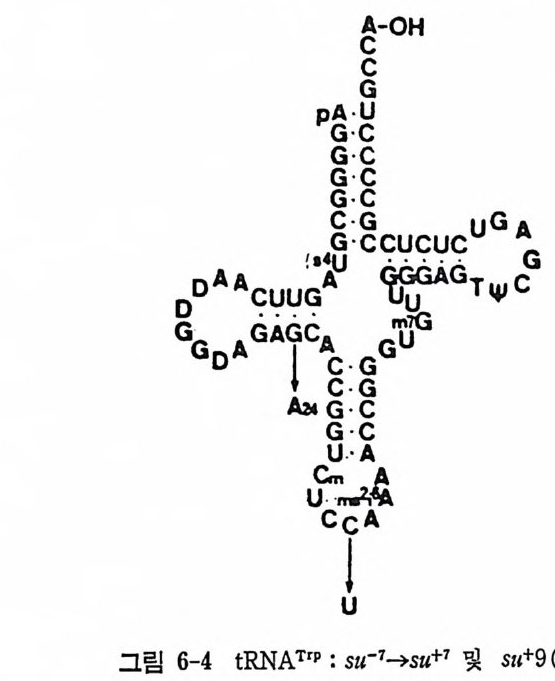 ..
..
대립적인 성질을 가진다. 그림 6-4 에 나타낸 바와 같이, 돌연변아 자 리는 역코돈에 있지 아니하고 24 번 위치 (D 줄기)에서 G ➔ A 로 달라진 것이다. UGA 에 대한 코돈 인식의 변화는 돌연변이체 t RNA 의 형태변
화로 일 어 나는 것 으로 추정 된 다 (Hirs h, 1971 ; Buckin g h an . Kurland~ 1980) . 라) 그밖의 굴루타민을 삽입하는 암버 및 오크르 억압인자들 su+2 및 su+B 여 압인자 tR NA 둘을 그림 6-5 에 나타내 었다 (Ozek i 등, 1980).
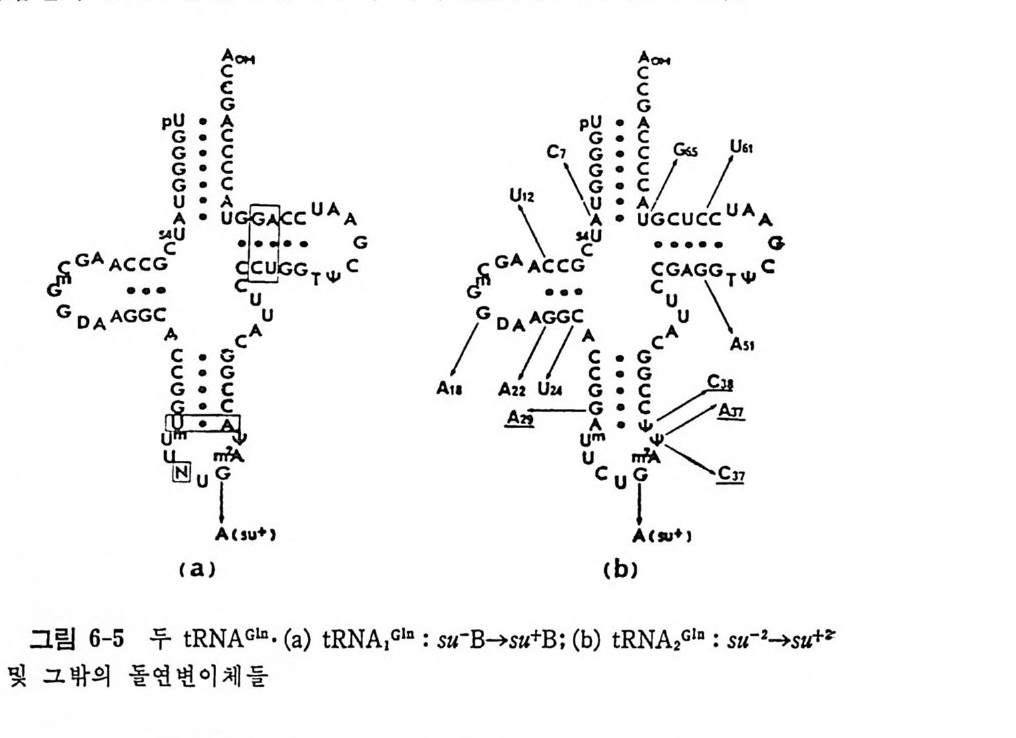 그.립FG- DG A6AA-A5G: G:C두:감p邑_A CGGGGU ( t aR:•••••• )N A I~CGtCCC言A(~ CSGU A:u i ♦ nu ,. (a :) :tCRN GA 1G1• : sAu -IB1S ➔1G csAUAnA뇨 u +1DB ;g5/2 U (겅b냅CGA·CAccGMUGP)GUc\UC( u ^tR •cN ^ G|'^)山_fA•GCCAAUCGC.CccCGGCCAC12 G:8U/C8c1죠%^/\ •: :• CsU——CuAn•-n I2U ➔c일 • sA u• + c2•. iA•Sutb
그.립FG- DG A6AA-A5G: G:C두:감p邑_A CGGGGU ( t aR:•••••• )N A I~CGtCCC言A(~ CSGU A:u i ♦ nu ,. (a :) :tCRN GA 1G1• : sAu -IB1S ➔1G csAUAnA뇨 u +1DB ;g5/2 U (겅b냅CGA·CAccGMUGP)GUc\UC( u ^tR •cN ^ G|'^)山_fA•GCCAAUCGC.CccCGGCCAC12 G:8U/C8c1죠%^/\ •: :• CsU——CuAn•-n I2U ➔c일 • sA u• + c2•. iA•Sutb
위에서 본 바와 감이, 원핵세포에 있어서의 정보전달의 억압현상은 유전암호와 단백질 생합성의 메카니즘을 해명하는 데 중요 한 역할을 하 였다. 진핵세포에 있어서의 무의미 돌연변이의 억압에 관한 연구는 효 ~ 모에서 제일 많이 이루어졌다(효모에 있어서의 억압인자 유전자의 돌연 변이의 종류에 관한 목록은 Mor tim er 와 Sc hi ld(1981) 를 보라). Saccharomy cescerev is ia e 에 있어서의 무의미 억압인자의 돌연변이체 ’ 들의 경우에도 UAA, UAG, 또는 UGA 등의 무의미 돌연변이에 상응하 는 것들이 알려쳐 있다• 이 돌연변이체들은 각각 UAA( 오크르), UAG - (암버), 그리고 UGA( 오판) 등의 무의미 코돈들 중의 한 코돈에서만 억 압을 일으킨다. UAA 와 UAG 억 압인자 유전자들은 이소 -l- 시토크롬 c 에 대한 구조 유전자 상에 오크르 또는 암버 돌연변이룰 받은 군주들-
(5. 2. 2 절을 보라)을 분석 함으로써 알 수 있었다 (Sherman 둥, 1973; Scherman 등, 1979) . 효모에 있어서의 무의미 억압현상이 원핵세포에서와 같 이 변형된 tR NA 분자들에 기 인된다는 것에 대한 중거는 원핵세포의 경우 와 마찬 가지 방법으로 얻어졌다 . 죽, 한 가지 방법으로는, 억압인자 유전자를 지닌 효모 균주에서 단리한 전 tR NA 혼합물을 시험관 내의 단백질 합 성계에 첨가하면 무의미 코돈에 반응하여 아미노산 을 삽입 할 수 있다. 또 한 가지 방법에서는 억압인자 유전자에 돌연변이가 일어나면 억압인 자로서 작용하는 tR NA 의 역 코돈에 서 염 기 변화가 일어 난다는 것을 누 쿨레오티드 결합순서 분석으로 알 수 있다.
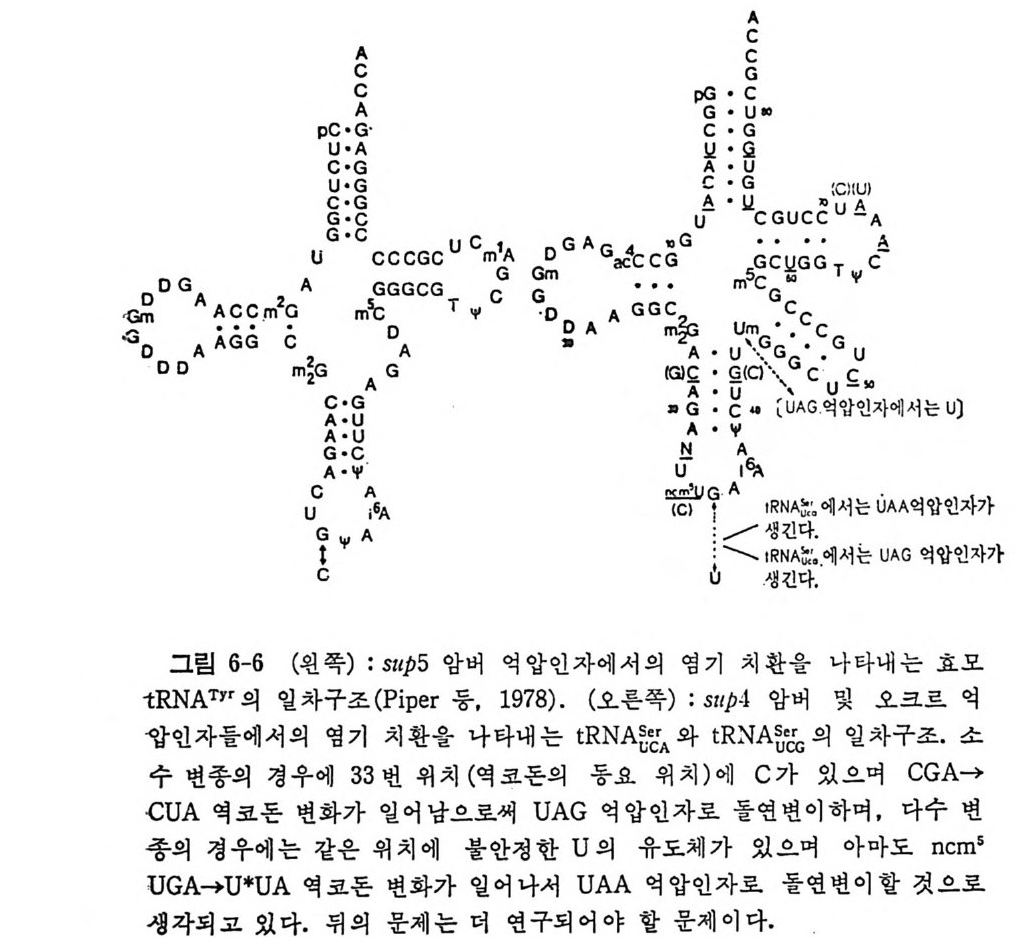 AccAGAGGGCcmGuucv AC
AccAGAGGGCcmGuucv AC
6.3 방출인자들 펩티드 사슬의 종결에 단백질 인자들이 관여할 것이라는 것은 처음에 Ganoza (1966) 에 의 해 서 제 안되 었 고, 뒤 에 Cap ec hi 와 Klein (1969) 에 의 해서 증명되었다. 시험관 내에서의 펩티드 사슬의 종결을 분석하는 방 법이 발달됨으로써 코돈에 특이한 두 개의 단백질 인자들을 E. co li에서 확인하는 데 성공하였다. 개시복합체 3H- f Me t-t RN A' ~1•AUG 터보솜을 펩티드 사슬 종결반응의 기질로 사용하여, 3H- f-메티오닌(펩티드의 유 사체로서)의 방출에는 단백질 인자들, 종결 코돈둘이 필요하다는 것이 밝혀졌으며, 어떤 조건에서는 구아닌 누클레오티드들이 필요하다. 코돈-독이한 두 가지 방출인자들이 E. col i로부터 정제되었다(표 6-1). RF-1 은 UAA 또는 UAG 에 목이 하고, RF-2 는 UAA 또는 UGA 에 득 이하다. 이 인자들은 울리고누클레오티드나 폴리누클레오티드를 전혀 가 지고 있지 않으므로 코돈 목이성은 단백질의 인식 메카니즘으로 생기 는 것이다 . 이 산성 단백질들은 그 물리적 성질들이 상당히 다른 데도 불구 하고 공통되는 면역학적 결 정 인자들을 가지고 있는 것으로 보아서 구조 적인 상동성이 상당히 있을 것으로 생각되고 있다 . Mi lm an 등 (1969) 은 세 번 째 의 인 자 RF-3 을 발견 하였 다 . RF-3 은 종 결 코돈이 있는 조건에서도 펩티드를 방출시키는 기능을 가지지 않지만 표 6-1 가용성 인 사숟 방충 인자들 인자 분K `r 량 ( .`d a ) 코돈 독-。 · 성 GT P 인 식 황 성리 등보G성 솜T 의aP 존eS E. coli RF-1 47• UAA 와 UAG 없음 없음 RF- 2 483, 35b UAA 와 UGA 없음 없음 RF-3 46a 없음 있음 있음 토끼의 망상적혈구 RF 56. 53, 1Q5 b U및 A UAGAA, UAAGA, 있음 있음 Arte m i a salin a RF 50b, 80C 있음 있음 a : SOS 전기이동법 b: 평형침강법 c: 세파덱스 겔 용리법
RF-1 과 RF-2 의 작용을 중진시 키 는 역 할울 한다. 이 단백 질 인자는 GTP 또는 GDP 와 상호작용하며 , RF-1 과 RF-2 의 리 보솜에 의 결 합과 리 보솜으로부터 의 방출을 촉진 한다 (Caskey 와 Camp b ell, 1979) . EF-Tu 도 같은 촉진작용울 한다는 것을 발견함으로 써 RF-3 와 EF-Tu 는 등일 한 물질 이 라고 주장되 기 도 하였지 만 (Cap ec chi 와 Kleim , 1969) , Caskey 의 연구실에서 RF-3 의 활동성을 EF-Tu 의 것과 분리시키는 데 성공하 였다 (Goldste i n 과 Caskey, 1970) . 그러 므로 RF-3 은 펩 티 드 사슬의 종 결에 특이하게 관여하는 인자이고 연장인자는 아니다. 진핵세포의 방출인자는 처음에 토끼의 망상적혈구에서 단리되었고 다 음으로 포유동물의 간과 곤충 세포들에서 단리되었다. 토끼의 망상적혈 구의 방출인자의 물리적 인 독성들을 표 6-1 에 주었다. 시험관에서의 실 험에서 단 한 가지의 단백질 인자가 테트라누클레오티드 UAAA , UAGA 또는 UGAA 둘의 존재 에 서 토끼 의 리 보솜 상의 기 질 인 [3 H]-fM et- t RNA;M•••AUG· 리 보솜으로부터 포르밀 〔 3H J-메 티 오닌의 방출을 촉진 시켰다. 테트라누클레티드의 3' 위치를 다른 염기들로 치환하여도 인식 작용에는 불리한 효과가 없는 것으로 보아서, 트리누클레오티드 보다는 테트라누클레오티드를 요구하는 것은 시험관 내의 분석에 있어서의 득징 이라고 생각된다. 그러므로 3' 말단의 염기는 인식작용의 일부분으로서 작용하는 것이 아니라 코돈 인식 복합체에서 하나의 안정 요소가 된다. 망상적 혈구의 RF 는 GTP 와 GDP 와 상호작용하며 리 보솜-의 존성 GTP ase 의 반응을 증진시 킨다 (Goldste i n 등, 1970) . 6.4 종결 코돈 인식 아미노산 코돈둘의 인식에 있어서와는 달리, 펩티드 사술 종결의 안 식은 핵산이 또 다른 핵산울 염기 짝지움으로 인식하는 원칙에서 벗어 나는 일이어서 상당한 관심의 대상이 되어 왔다. 리보솜 상에서의 펩티 드 사술 종결 코돈의 인식작용을 분석하기 위해서 3H 로 표지된 종결 코돈을 사용하여 방출인자 • 〔 3H] -종결 코돈 • 리 보솜 복합체 의 형 성 을 조사하였 다 (Scolnic k 와 Caskey, 1969) . 이 와 같은 실 험 에 서 , RF-1 은 UAA 및 UAG 에 옹하여 리 보솜에 결합하며 , 한편 RF-2 는 UAA 와 UGA 에 옹하여 리보솜에 결합한다• 리보솜의 부재 하에서의 방출인자
의 코돈 인식의 목이성이 절대적인 것이 아니지 만 방출인자 분자가 코 돈 인식에 관여된다는 것이 확인되었다 (Ca p ecch i ~-l- Klein , 1969) . 아주 최근에는 제한 핵산내부가수분해효소들과 같은 단백질들에 의한 DNA 의 특정한 누클레오티드 연속부분의 인식에 관한 연구들이 광범위하게 이루어지고 있다. 방출인자의 〈역코돈〉 부분의 분자구조에 관해서는 아직 잘 모르고 있 다. 그렇지만, 코돈 인식작용의 득이성을 m3UAG, m3UAA , m5UAG, m5UAA . brUAG, hUAG 및 UAI 등과 같은 변 형 된 트리 누클레 오티 드 들을 이용하여 간접적으로 연구한 바에 의하면, 이 트리누클레오티드들 의 방출인자에 대한 독이성은 Wa t son - Cr i ck 의 염기 짝지움과 코돈-역 코돈 염기 짝지움에 있어서의 동요현상과 상당히 유사하다는 것이 밝혀 졌 다 (Smrt 등, 1970) (표 6-2 와 6-3 을 보라) . 우라실의 N3 위치에 메딜 기를 결합시키면 RF-1 또는 RF-2 에 상% 하는 종결 코돈둘의 주형으로서의 활동성이 없어진다. 반면에 우라실와 Cs 위치에 브로모 또는 메딜 기를 부착시키면 종결 코돈의 주형으로서 의 활동성에 아무런 영향을 미치지 않는다. hUAG 는 RF-1 의 존재에 표 6-2 변형된 종결 코돈둘의 주형으로서의 작용 트리누클레오티드 포르밀 (면〕-메 티 오닌
RF-1 .dpm oles UAA 0.90 UAG 0.78 m5 UAG 0.00 m3UAA 0.01 m5UAG 。 •62 m5UAA 0.63 hUAG 0.47 brUAG 0.71 UAI 1.1 0 RF-2 UAA 0.37 UAI 0.00 msUAA 0.02 ro5UAA 0.68염표기 6-인3 식의종 결유 현코 돈| 갑염기\들麟의 인麟식서목이 성인 식되는 염기들 i 실식되지 않는 염기 I 첫 째 U, brU, 또는 m5U I m!U, hU, C, A, G II 둘째 또는 세 째 A, G (또는 I) I U, C 血 둘 째 또는 세 째 A I U, C, G (또는 I) 서 종결 코돈으로 작용하지 않는다. 이러한 실험결과들은 N3 위치의 수 소와 c4 위치의 카르복시 부분이 종전 코돈의 인식에 필 수적인 반면에 Cs 위치에 부착된 치환기들은 필수적이 아님을 가리킨다. 16S rRNA 의 3' 말단 부분에 있는 Shin e -Dalga rno 연 속부분이 mRNA 의 종결 코돈을 인식하는 데 관여한다는 것은 이마 2.4.4. 절의 ( 나)항 에 서 이 미 기 술하였 다. Dalga r no 와 Shin e (l973) 은 이 러 한 연 속부분의 말단에 UUAoH 가 있을뿐 아니라 이 연속부분의 8 개의 잔기 안에 UCA 가 있다는 것을 발견하였다. 이러한 삼중체들이 UAA , UAG , 그리고 UGA 들과 염기 짝지움을 할 수 있을 것이다. 종결 코돈의 인식에 있어 서 의 16S rRNA 의 3' 말단의 중요성 은 클로아신 DF13 이 라는 록 이 한 핵 산 가수분해효소를 사용한 연구결 과 에서 분명해 졌 다 (Caske y 동, 1977). 리 보솜에 있는 16S rRNA 의 3' 말단으로부터 49 개 의 누쿨레 오티 드를 찰 라내면 방출인자들에 의한 코돈 인식능을 없애버린다. 그러나 방출인자 의 매개로 일어나는 펩티딜-t RNA 의 가수분해반응은 그대로 일어난다. 코돈 인식에 미치는 핵산 가수분해효소의 이러한 영향이 리보솜 구조의 교란의 결과로 생기는지는 아직 확실히 모른다. Caskey 등 (1977) 은 또 한 E. col i의 방출인자에 의한 B. subti lis 리보솜 상의 코돈의 인식이, B. subti lis 의 16S rRNA 의 3' 말단이 종결 코돈들에 상보적 인 결 합순 서를 가지지 않더라도, 정상적으로는 아무 변화가 없다는 것을 관찰하 였다. 이러한 실험결과들에서 RF-1 과 RF-2 분자들이 종결 코돈을 직 정 인식한다는 것을 알 수 있다. 토끼의 망상적혈구 추출물에 있어서는 단 한 가지의 단백질 인자가 제 가지 종결 코돈 전부를 인식한다. 따라서 사정은 E. col i의 경우와 상당히 다르다. E. col i와 토끼의 망상 적혈구로부터의 방출인자들은 동족의 리 보솜들과만 작용한다 (Ko neck i 등 1977) .
6. 5 RF-3 및 GTP 가수분해 의 요구 단백질 인자 RF-3 은 방출작용은 없지만 RF-1 또는 RF-2 그리고 종 결 코돈들에 의해서 매개되는 f Me t의 방출을 촉진시킨다. E. col i의 RF-3 는 RF-1 과 RF-2 의 리 보송에 의 결 합과 리 보솜으로부터 의 방출을 중진 시 킨 다 (Goldste i n 과 Caskey, 1970) . RF-3 은 펩 티 딜 -tRN A 가수분 해의 Vmax 에는 영 향을 미치지 않으면서 종결 코돈들에 대한 RF-1 또는 RF-2 의 Km 을 5 내지 8 배만 큼 감소시킨다. 이 사실은 RF-3 이 작용 하는 단 계는 코돈을 인식 할 때(즉, 리보솜에 결합할 때)이지 펩티딜 -t RNA 의 가수 분해 단계가 아님을 의미한다 (M i lman 둥 1969). 실제로 RF-3 은 RF-1 또는 RF-2. 〔 3H J UAA· 리보송 중간체의 형성을 촉진한다. RF-3 의 존재 하에서 이러한 인식 복합체에 GDP 를 첨가하면 복합체들 이 신속히 해체하게 된다. RF-3 이 리보솜-의존성 GTPase 활동성을 가 지고 있는 것으로 알려져 있기는 하지만, RF-3 이 존재하는 조건에서 RF-1 또는 RF-2 의 리보솜에의 결합에 GTP 가 요구되는지는 아직 밝 혀져 있지 않다. 리보솜-의존성 GTPase 의 활동성을 가진 다른 단백질 인자 EF-G 가 RF-1 또는 RF-2 와 함께 리보솜에 동시에 결합할 수 없 을 것이라는 것은 명백한 일이다. 왜냐하면, Mccaug h an 등 (1984) 의 최 근의 연 구에 의 하면 RF-1, R-2 및 RF-3 들이 결 합하는 리 보솜 상의 위치는 L7/L12 줄기와 S2 및 S3 등이 아루는 경계면인데, 비교적 큰 RF-3 와 EF-G 가 동시에 같은 영역에 결합할 수는 없을 것이다 (6.7 절 참조). 따라서 RF-1 과 RF-2 의 결합과 방출은 RF-3 에 의해서 촉진되 며 GTP 와 그의 가수분해가 관여할 것임을 침작할 수 있다. 그러나 아 직 이 연속적인 순환과정에 대한 증거는 시험관 내에서의 실험으로는 증명이 되지 않고 있다. 망상적혈구와 RF 를 사용한 펩티드 사슬 종결에 있어서의 GTP 및 그의 가수분해 문제의 경우에는 사정이 명확하다. 진핵세포의 방출인 자는 리보솜-의존성 GTPase 의 활동성을 가지고 있으며, 이 활동성은 코돈들에 의 해 서 두드러 지 게 촉진된다 (Beaudet 와 Caskey, 1971) . RF 의 리 보솜에 의 결 합은 GTP 또는 그의 비 가수분해 성 유사체 인 GDPCP 들에 의해서는 촉진되지만, GDP 에 의해서는 촉진되지 않는다. 그렇지 만 RF 의 촉매로서의 행동을 촉진하는 것은 GDPCP 가 아니라 GTP 인
것으로 보아서, GTP 는 RF 의 리보솜에의 결합을 촉진하며, 그 후에는 곧 가수분해되는 것으로 생각된다. 가수분해가 일어난 다음에는 RF 와 GDP 를 리보솜으로부터 밀어낼 것이다(그립 6 구을 보라).
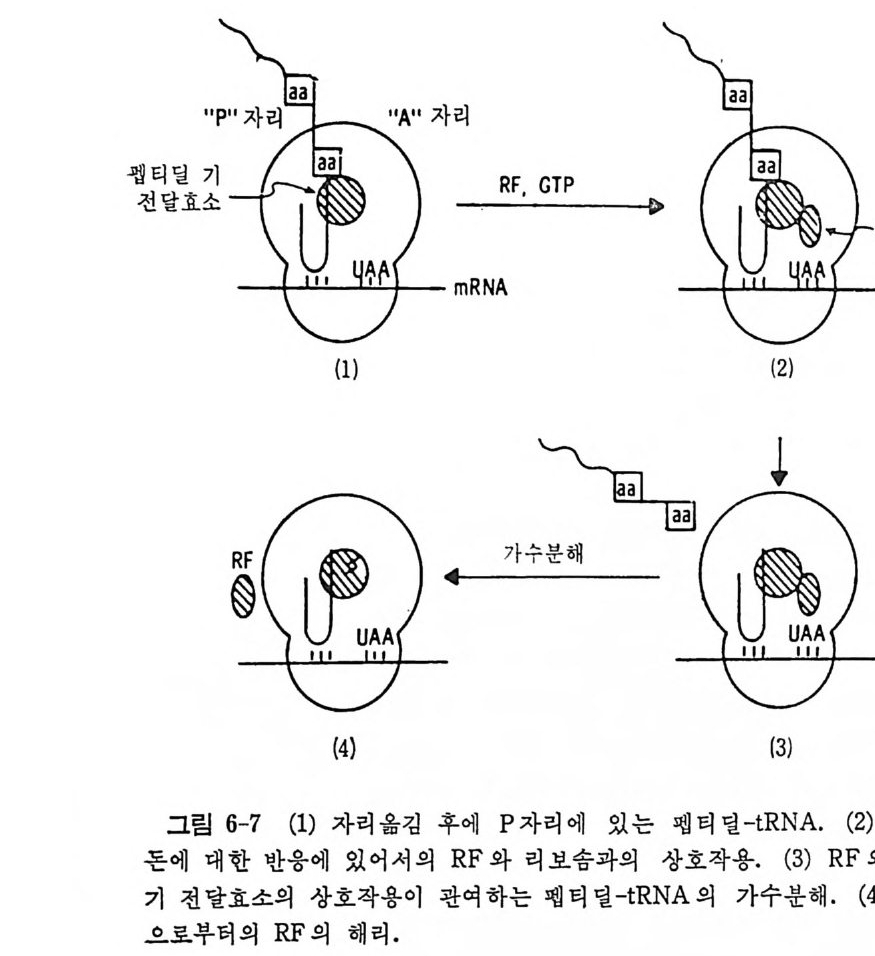 펩티딜 기 RF, GTP
펩티딜 기 RF, GTP
6.6 펩티 딜-t RNA 의 가수분해 팹티드 사술 종결에 있어서의 50S 리보솜 하위단체의 펭티 딜 기 전달 효소로서의 활동성의 역할은 처음에 펩티딜 기 전달효소의 작용과 사슬 종결의 펩 티 딜-t RNA 가수분해 단계 둘 다를 방해 하는 항생 제 들에 관한
연 구에 서 알게 되 었 다 (Beaudet 와 Caskey, 1971) (5. 2. 2 절 참조) . 만일 에탄을의 첨가로 RF 분자들을 리보솜에 결합시킬 수만 있으면, 펩티드 . 사슬 종결의 이 부분반응을 알아 볼 수 있을 것이다. 아미세틴, 린코신, 클로람페니콜, 그리고 스과르소마이신들과 같은 항생제들은 펩티딜 기 전달효소의 작용과 RF 로 매개되는 펩티딜_t RNA 의 가수분해 를 모두 다 방해한다. 이 항생제들은 코돈들에 대한 반응으르 일어나는 RF 의 리보솜에의 결합은 방해하지 않는다. 이것은 이 항생제들이 펩티드 사 술 종결의 독이한 부분반응을 방해한다는 것을 가리키는 것이다. 펩티딜 기 전달효소가 펩티딜-t RNA 의 가수분해 를 비롯해서 몇 가 지 촉매작용을 한다는 것은 시험관 내에서의 실험으로 증명할 수 있다 (Scolnic k 등, 1970). 아미노기가 친핵체로서 아미노아실-t RNA 의 에스 테르 결합을 공격할 때 이 효소는 펩티드 결합 형성을 촉매한다. 이 반 응은 보통 아미노아실-t RNA 에 의한 펩티드 사슬의 연장이 일어나는 동 안에 볼 수 있다. 또한, 친핵체가 알코울일 때는 펩티 딜 기 전달효소 중심이 에스테르 형성을 촉매할 것이고, 친핵체가 물일 때는 갓 생긴 펩티 딜-t RNA 의 가수분해 를 촉매한다 . RF 가 에스테르 가수분해효소로 서의 작용을 하지 않으며 펩티딜 기 전달효소가 펩티딜-t RNA 의 가수 분해에 요구되지 않는 것으로 보아서, RF 는 펩티딜 기 전달효소와 상 호작용함으로써 펩티릴-t RNA 의 가수분해를 촉진하는 것으로 보안다. 린코신 (E. col i의 리보솜의 경우)과 아니마이신(토끼의 망상적혈구의 경 우) 두 항생제들이 각각 상응하는 리보솜 상에서 펩티드 결합과 에스데 르의 형성 그리고 펩티딜-t RNA 의 가수분해를 일으키는 펩티딜 기 전 달효소에 미치는 영향이 차별적이라는 사실은 매우 홍미있는 일이다. 두 항생제는 각각 해당하는 리보솜 상에서 펩티드 결합과 에스데르 결합의 형성을 방해하는 한편 펩티딜-t RNA 의 가수분해를 현저하게 촉진한다 (Beaudet 와 Caskey, 1971) . 펩 터 딜 기 전 달효소의 특이 성 의 이 러 한 변 형은 린코신이나 아니소마이신이 아니라 RF 가 변형제로서 작용하면서 사술 종결 단계에서 일어날 것으로 추측된다. E. coli 의 리 보솜의 특정 한 단백 질들에 대 한 항체 들을 사용하여 Tate 등 (1975) 은 펩티딜 기 전달효소가 펩터드 사술의 종결에 참여한다는 중 거를 얻을 수 있었다. E. col i의 50S 리보솜 단백질들인 Lll 과 Ll6 에 대한 항체들은 RF- 의존적으로 일어나는 펩티딜-t RNA 가수분해에 영향 을 미침으로써 시험관 내의 실험에서의 종결을 방해한다. 그러나 이 항
체들은 RF 와 리보송의 상호작용에는 영향을 미치지 않는다• 최근에 펩 티딜 기 전달효소 중심을 이 루 는 단백질들로서 Lll 과 Ll6 임이 밝혀졌 다(자세한 것은 2.6.2, 철과 5.2.2, 철을 참고하라), 그러므로, Lll 과 Ll6 은 종결 단계에서 팹티딜-t RNA 의 에스페르 결합을 분해하는 반응 에서 중요한 역할을 할 가능성이 크다. 아직 확실 한 것은 아니지만 Lll 상에 있는 두 개의 다른 자리들이 펩티드 결합의 형성과 펩터딜-t RNA 의 가수분해에 따로따로 관여할 가능성도 있으며, 아니면 가수분해반 응에서는 RF 와 펩티딜 기 전달효소 사이의 상승작용이 관여할지도 모 른다. L16 은 클로람페니콜을 결합하는 단백질이며, 펩티딜 기 전달효 소가 이루는 A 자리 부분의 일부분을 이루는 것으로 추측되고 있다 (Ni er haus 와 Monte j o , 1973 ; 2. 6. 2 절 및 5. 2. 2 절 을 참고하라) . Ll6 에 대한 항체가 시험관 내에서의 종결 단계의 부분반응인 펩티딜-t RNA 의 가수분해를 방해한다는 것은, 이 가수분해가 일어날 때 RF 분자가 A 자리의 일부분을 차지할 것임을 암시한다. 왜냐하면 이 반응에 관여 하는 그밖에 알려진 성분들에 의해서 차지된 자리들(펜티딜-t RNA p자 리, 펩티 딜 기 전달효소 Lll) 이 콜로람페니콜에 의해 영향을 받지 않 기 때문이다. Ll6 과 Lll 은 펩티딜 기 전달효소 중심의 일부분을 이루 는 인접한 단백질들이므로, RF 와 펩티딜 기 전달효소는 기능적인 면에 서 상호작용할 것으로 추측할 수 있다. 6.7 RF 가 결합하는 리보솜의 자리 (1) 항생제, (2) 특정한 단백질들에 대한 항체, (3) 몇 가지 단백질 들을 제거한 리보솜들, (4) RF 와 리보솜 단백질과의 교차결합 등을 사 용하여 펩티드 사슬 종결에서 요구되는 리보솜 단백질들에 관한 연구를 하였다. 이러한 실험결과들을 종합해 보면 RF 의 결합자리는 리보송의 어떤 접촉 영역임을 가리키고 있다. 리보솜 단백질 S4 와 L4 가 펩티드 사슬의 종결에 관여하고 있다. 항 생제 스트랩토마이신과 에리트로마이신은 펩티드 사슬 종결의 방해물질 인데, 이들 두 단백질들 (S4 와 L4) 에 돌연변이가 일어나면 이 항생제들 에 대 해 서 저 항성 을 가지 게 된 다 (Beaudet 와 Caskey, 1971) . 리 보솜의 특정한 단백질들에 대해서 만들어진 항체들을 사용하여, L7/L12, S2,.
S3 들과 같은 단 백질들 이 RF 의 결합에 요 구 된 다는 것과 L16 과 L11 이 : 펩티딜-t RNA 의 가수분해에 영향을 미친다는 것이 밝혀져 있다 (Ta te' 등, 1975). 5. 2. 2 절에서 도 이미 언급한 바와 같이, 이 단백질들은 각 ` 각 팹 티 딜 기 전달효소 중심의 일부분과 주변 영역을 이루고 있다는 것 이 알려져 있다(표 5-2 를 보라). L16 과 Lll 은 둘 다 클로람페니콜의 결 합 에 요구되 고 있 다 (Ro th 와 Nie rh aus, 1975) . 17/112 가 제 거 된 리 보 솜은 RF 몰 결합할 수 없다. 이것은 항체물 사용하여 얻는 결과를 확 인 해 주 는 건과 이 다 . 리보솜에서 L1l 을 제거하여도 펩티딜 기 전달효 소의 완동성은 크게 영향을 받지 않으며 펩티드 사술 종결에 미치는 영 향도 거 의 없 다 (Ar mstr o ng 과 Tate , 1978) . 이 작용기 성 교차결 합제 를 사용한 실 험 에 서 RF 는 L2, L7/112, Lll, S17, S21, 및 S18 등과 o}- 주 가 깝게 접촉하 고 있다는 것이 밝혀졌다 (S t e ffl er 등, 1982). Pon g s 와 Rossner(1975 ) 는 종결 코돈 UGA 의 유도체를 친화표지 탐침으로 사용_ 하여 RF 가 코돈을 인식하였을 때 RF 가 S18 및 S14 들과 교차결합될 수 있음 을 알았다. EF-Tu 가 펩티딜 기 전달효소의 중심을 이루는 여 러 가지 단백질들 (A 자리의 단백질둘)과 접촉하기 때문에 종결 코돈을 인식할 RF 가 EF-Tu 와 상호작용하는 단백질들과 접촉하게 되는 것은 놀라운 일이 아니다(그립 5-6 을 보라). 6.8 펩티드 사슬 종결 단계에서의 조절 앞에서도 말한 바와 같이, 우의미 돌연변이는 조숙한 사슬 종결을 알 으키며 미완성된 단백질 조각들을 방출시킨다. 억압 tR NA 돌연변이돌 을 지닌 세포들에 있어서는 이러한 무의미 돌연변이들이 표현적으로는 t 억압된다. 억압돌연변이체에서의 아미노아실-t RNA 는 종결 코돈들을 인 식하여 그들을 번역한다. RF 와 억압 t RNA 가 종결 코돈을 놓고 경쟁 한다. 그러므로 억압돌연변이체에서의 유전자 표현의 조절은 종결(죽, . 무의미 코돈)과의 인식 단계에서 이룩된다. 단백질 사슬 종결을 방해하는 억압 t RNA 들이 있음이 알려짐으로써, 칭상적인 종결반응에서도 목수한 t RNA 가 종결 코돈을 인식할 것이라 는 집요한 가정이 오랫동안 계속되어 왔다. 그러나 오늘날에는 몇 가 지 방출인자들이 종결 코돈들을 인식한다는 개념이 정립되었다.
그러나 리보솜이라는 복잡한 기능적 구조가 해결되기 전에는 펩티드 사술 종결이 일어나는 과정에서의 펩티딜-t RNA 의 가수 분해 반응의 메 카니즘을 자세히 설명하기가 힘들 것이다. 방출인자들의 하나가 가수분 해작용에 참여하는 것은 거의 확실하지만, 리보송에 방출인자 가 결합하 는 것만으로는 펩티딜-t RNA 의 가수분해를 개시시킬 충분한 조전 이 되 지 않는다. 가수분해가 방출인자들과 리보솜의 한 성분과의 상호협동에 기인되는 것인지는 아직 명확하지 않다. 그러나 방출작용이 가능하러면 리보솜이 활동적인 형태로 있어야 하는 것만은 분명하다. 요컨대, 최근 까지의 지식을 집약하여 제안된 매력적인 이론은, 펩티딜 기 전 달효소 가 종결 코돈과 방출인자들에 의한 특별한 영향으로 합성이 아니라 가 수분해를 일으킵으로써 사슬 종결이 일어날 것이라는 것이다. 종결반응 은 앞으로 이 정립된 이론에 기초하여 설계된 접근법으로 연구되어야 할 것으로 생각된다. * 참고문헌 Armstr o ng , I. L, Tate , W. P. (1978) ) , J Mol. Bi ol . 120, 155. Beaudet, A.L., Caskey, C.T. (1971) , Proc. Natl . Acad. Sci. 68, 619. Brenner, S. , Barnett , L. , Katz , E. R. , Cric k , F. H. C. (1967) , Natu r e 213, 449. Buckin g h am, R. H. , Kurland, C.G. (1980) , Transfe r RNA: Bio l og ica l Aspe c ts (Ed. , D, Soll, J. N. Abelson, P, R, Schim mel) , p. 421, Cold Sp ri n g Harbor Laborato r y , Cold Spr i n g Harbor. 'Ca pe c chi, M. R. , Klein , H. A. (1969) , Cold Sp ri n g Harbor Sy m p . Qu ant. Bio l . 34, 469. Caskey, C.T., Bosch, L., Konecki , D.S. (1977) , ]. Bio l. C!z e m. 252, 4435. Caskey, C.T., Camp b ell, J.M . (1979), Nonsense muta t i on and tR NA supp r essors (Ed., J. E. Celis, J.D . Smi th) , p. 81, Academi c Press, New York. Dalga rno , L., Shin e , J. (1973), Natu r e New Bio l . 245, 261 . Gallucci , E. Garen, A. (1966) , ]. Mo!. Bio l . 15, 193. Ganoza, M. C. (1966) , Cold Sp ri n g Harbor Sy m p . Qu ant. Bi ol . 31, 273. Garen, A. (1968) , Scie n ce 160, 149. Garen, A., Garen, S., Wi lh elm, R.C. (1965), ]. Mol. Bi ol . 14, 167. Goldste i n , J. L. , Beaudet. A. , Caskey, C. T. (1970) , Proc. Natl . Acad. Sci. 67, 99. Goldste in , J. L., Caskey, C.T. (1970), Proc. Natl . Acad. Sc i. 67, 537.
Hi rs h, D. (1971) , ]. Mol. Bio l . 58, 439. Kohli, J., Altr ud a, F. Kwong , T., Rafa ls ki, A., Wetz e l, R., Soll, D., Wahl, G., Leup o ld, U. (1980), Transfe r RNA: Bio l og ica l Aspe c ts ( Ed., D. Soll, J.N Abelson, P.R. Schim mel), p. 407, Cold Sp r in g Harbor Laborato r y , Cold Sp ri n g Harbor. Konecki, D. , Aune, K.C ., Tate , W., Caskey, C.T. (1977), ]. Bio l . Chem. 13, 4514. Late n , H., Gorman, J.. Bock, R. M. (1980), Trans[er RNA: Bi ol og ica l Aspe c ts (Ed., D. Soll, J,N . Abelson, P.R. Schim mel) , p. 395, Cold Sp ri n g Harbor Laborato r y , Cold Sp ri n g Harbor. McCaug h an, K.K ., Ward, C. D., Trotm an, C.N.A., Tate , W.P. (1984), FEES Lett . 175, 90. Mi lm an, G. , Goldste i n , J., Scolnic k , E., Caskey, T. (1969), Proc. Natl . Acad. Sc i. 63, 183. Morti m er, R. K. , Schil d , D. (1981) , The Molecular Bio l og y of The Yeast Saccha- romy ce s: Li fe C y c le and Inherit an ce (Ed . , J. N. Str at h e rn, E. W. Jon es, J. R. Broach), p. 641, Cold Sp ri n g Harbor Laborato r y, Cold Sp ri n g Harbor. Ni ch ols, J. L. (1970) , Natu r e 225, 145. Ni ch ols, J.L . , Roberts o n, H. (1971) , Bio c lzim . Bio p h y s . Acta 228, 676. Ni er haus, K.H ., Monte j o , V. (1973), Proc. Natl . Acad. Sci. 70, 1931. Ozeki, H. , Inokuchi, H. , Yamao, H., Kodair a , M., Sakano, H., Ikemura, T., Shim ura, Y. (1980), Transfe r RNA : Bio l og ica l Aspe c ts ( Ed., D. Soll, J.N . Abelson, P.R. Schim mel), p. 341, Cold Sp r in g Harbor Laborato r y , Cold Sp ri n g Harbor. Pip e r, P. W. (1980) , Transfe r RNA: Bio l og ica l Aspe c ts ( Ed. , D. Soll, J. N. Abelson, P.R . Schim mel), p. 379, Cold Sp ri n g Harbor Laborato r y , Cold Sp ri n g Harbor. Pong s, 0., Rossner, E. (1975), Hop pe -Sey/ e r' s Z. Plzys i l. Chem. 356, 1297. Roth , H. E. , Ni er haus, K.H . (1975), ]. Mo/. Bio l . 94, 111 . Sambrook, J,F ., Fan, D.P., Brenner, S. (1967), Natu r e 214, 452. Scolnic k , E.M . , Caskey, C.T. (1969), Proc. Natl . Acad. Sci. 64, 1235. Scolnic k , E. Mi lm an, G., Rosman, M., Caskey, C.T. (1970), Natu re 225, 152. Sherman, F., Lie b man, S.W., Ste w art , J.W ., Jac kson, M. (1973), ]. Mo/. Bi ol . 78, 157. Sherman, F., Ono, B., Ste w art , J.W . (1979), Nonsense muta t i on s and tR NA supp re ssors(Ed., J.E . Celis, J.D . Smi th) , p.1 33, Academi c Press, New York. Smi th, J.D . (1972), Ann. Rev. Genet. 6, 235.· Smr t, J., Kemp er , W., Caskey, C.T., Nir e nberg, M. (1970), J Bi ol . Chem.
245, 2753. Soll, L. (1974) , ]. Mal. Bi ol . 86, 233. S t혀ffi er, G., Tate , W.P., Caskey, C.T . (1982), ]. Bio l . Clzam. 257, 4203. Tate , W.P., Caskey, C.T., S to f fi er , G. (1975) , ]. Mal. Bi ol . 93, 375. Weig e rt, M.G. , Garen, A. (1965) , Natu r a 206, 992. Weig e rt , M.G., Lanka, E., Garen, A. (1967), ]. Mal. Bio l . 23, 401 . Yaniv , M., Folk, W.R., Berg, P., Soll, L. (1974), ]. Mal. Bio l . 86, 245.
제 7 장 단백질 합성의 방해물질들 개요 단백 질 합성의 방해물질들은 번역과정의 전체 메카니즘과 개별적인 각 단 계 들의 메카니즘을 해명함에 있어서 매우 유용하게 사용되었다. 단백질 합성의 방해물질로 작용하는 것들로는 항생물질과 그밖의 물질 들이 있다. 단백질 합성계에는 적어도 두 가지 (원핵세포의 계와 진핵세 포의 계)가 있다. 그러나 이 두 계에는 많은 공통점들이 있다. 표 7-1 에서 볼 수 있는 바와 갇이, 단백질 합성의 방해물질에는 원핵세포에만 작용하는 것, 진핵세포에만 작용하는 것, 원핵세포와 진핵세포에 다 작 용하는 것들로 분류할 수 있다. 또한, 방해물질들은 작용하는 자리가 상 충 액인지, 작은 하위단위체 (30S, 40S) 인지 또는 큰 하위단위체인지 에 따라서 분류할 수 있다. 일반적으로 보면, 원핵세포 계들에 작용하 는 항생물질들은 박테리아, 남조류, 미토콘드리아 및 영록체 들에 영향 을 미치며, 진핵세포 계에 작용하는 것들은 80S 제포질성 리보솜을 가 진 고동생물의 세포에서만 작용한다. 리보솜에 두 가지 유형이 있다는 것을 처음에 알게 된 것은 클로람페니콜이 70S 리보솜에 결합하여 단백 질 합성을 방해하지만 80S 리보솜에는 결합하지 않는다는 사실을 알게 됨으로써 가능하였다 (Vazq uez, 1964). 방해물질들은 그들의 화학구조에 따라서 분류될 수도 있다. 표 7-2
표 7-1 단백질 합성의 방해뭉질들 상충액 30S(40S) 50S (60S) 원핵세포 폴산 길항뭉질 아미노글리코시드류 I 클로람페 니콜 L-1- 토실 아미 도 -2- 스트랩토마이신 페닐에틸클로로메틸 디히드로스트랩토마이신 I 마크롤리드류 케론 (TPCK) 파로모마이신 니다마이신 카르보마이신 키로마이신 네오마이신 스피라마이신 모시마이신 카나마이신 루코마이신 X-5108 겐타마이신 에리트로마이신 불루엔소마이신 칼코마이신 울레안도마이신 스펙티노마이신 란카마이신 메티마이신 카수가마이신 네가마이신 린코사미도류 에데인 셀레스토사미니드류 에데인 A 콜에리데신인 E3B I 스P트A랩 1토14그A라 민 A 군 오스트레오그라이신 스트랩토그라민 A 페난트렌 알칼로이드류 베르나마이신 A 크립토플레우린 미카마이신 A 틸로크레브린 틸로포린 | 스트랩토그라민 B 군 오스트레오그라이신 B PA114B 등 비리도그(에리타세마인0 1 신) 티오스트랩돈 군 티 오악(브스틴리)트아 랩마돈 이 신, 티 시오마이신 A 티오렌틴 B 물터오마이신
상충액 30S(40S) 50S (60 S) 스포란기오마이신 A-59 알티오마이신 미크로콕신 보트로마이신 A2 풀러 1 우로물틸린 원핵세포와 진핵세포 아구아미닐노 알-5킬' _ 메아틸데렌닐 산류 1 오팍린타마트이리신카 르복시산 푸아로미마노이아신실 올리고누쿨 이포스폰산 례티드류 4- 아미노핵소오스 피 리미딘 누쿨레오서 푸시드산 드류 구게로틴 아미세틴 불라스티시먼 S 풀리아세틴 바미세틴 히키지마이신 스과르소마이신 테트라시클린류 쿨로르테트라시클란 진핵세포 디프데리아 독소 글루티리미드류 시쿨로핵시미드(악티 디온) 아세목시시클로핵시 미드 스트랩토비타신 A 이페카크 알칼로이드류 에메틴 아니소마이신 트리코테센류 트리코테신 트리코데르봉 크로토신 니바렌울 T-2 독소 베루카린 A
상 충 액 30S( 40 S) 50S( 60 S) 테누아 존산 아브린 및 리 신 페데린 세 팔로탁 수 스 알칼 로이드 류 하링토닌 호 모하 링 토닌 이소하링 토 닌 MDMP Na F, KF MDMP 는 2-( 4 - 메틸 - 2, 6 - 디니트로아 닐리 노 ) -N- 메밀 프로피 온 아 미드의 약자 이다. 에서는 방해물질들 을 그들의 화 학 구조에 의거 해 서 분류하였다. 이 표에 는 분자량과 방해물 질 이 작용하는 자리 그리고 방 해되는 목 이한 자리들 에 관한 청보들을 실었다. 지금까지의 연구결과에 의하면, 거 의 모든 항생제들과 그밖의 방해물 질들은 리보송의 독정 한 한 성분과 독이하게 작용함으로써 단백질 합성 올 방해하는 것으로 밝혀져 있다. 따라서 항생제들이 작용하는 성분들 (리보솜 단백질 또는 리보솜 RNA) 그리고 이 성분 분자들 상에서 항 생제 분자가 부착하는 특이한 위치 (아미노산 찬기 또는 누 클 레오티드) 등을 알게 됨으로써, 각 항생제가 단백질 합성의 어느 단계 (개시, 연장, 및 종결)에서 방해작용을 하는지를 알 수 있냐 그러므로, 단백질 합성 의 방해물질들은 단백질 합성의 자세한 메카니즘뿐 아니라 단백질 합성 이 일어나고 있는 리보솜의 구조를 밝히는 생화학적인 도구로 이용될 수있다. 몇 가지 방해물질들의 화학구조를 그림 7-1 과 그림 7 - 2 에 나타내 었다. 단백질 합성의 방해물질들에 관해서는 몇 가지 훌 륭한 평론서들이 있 다. 자세한 것은 이 평론서들을 참고하기 바란다 (Cundl iff e, 1972b; -Va zqu e z, 1979 ; Pestk a , 1977 ; Cundli ffe, 1980 ; Vazqu e z 와 Jim enez, 1980).
부방해여포포세세·서주에1 주 에f물^+ + ++++ ++ ++ + + ++ + + + + + + + +++ + 방되해는 세포종 , I핵핵원진 진핵 진 핵진 핵핵진 원핵 )핵(진 핵진핵 진 핵 원핵 원핵 원핵 원핵 원핵 원방 되 응는반해되해방 계단는P TG해가 분수강,연개 시 김전딜팹 자()기 옮티,달 리 장연전, 옮달리) (팹단김터기 자 연장 달 옮 자 딘, 기(김펩리)티전장 ,시연결)개( 종팹옮딜)( 전 , 리자달김기디 장연 개Nt돈짝코,-a-a, RA기 시짓 종)장( 시연개, 전 종 결 김옮리자 연장 김옮리자 장연l lll.._. (( '~`',`A7A777 77,’ 77티종장연딜팹결빼) ,(달결전종 티딜맵연전장종. 종결() ` ,달전 |.(김 리)자옮달전 , 장연 딜티펩 .(김리자) 옮말전 , 장연 딜티팬 | .|.옮( 김리자)달전 . )시개(장인 딜티팬옮( 리김자)달전 , 장연 딜티팹 방의해분 량자 자리 E -uFT, 2.2 512,FG E- -F2I, l:E, F-!FE 니 . 35S7 69202S 3.36079 3 .1806S5 2 9 3.69330 S82 .38420 SF 2E-, 30006 E2-F00,2 045 0S.5640 55 S0 9.442 95??~Q 788 7379841 896995S5 00S5 0S5 ’ 0S5 진I
문2? -질백 단해방성의 합 표질물방해 틸구--5닐릴메렌'아 스산폰포이 류리루미글타드 A 신 트토랩스터비스랩티 돈미트미시시드클헥 로록클해드세 시로아시미시신이네마가 리독 디 전것(소테 아완프한) )A 독소데조프디 각리(아류드사미 코린코신린이 마린이클 마신다리 몰크마류드다이니마신 IA 코신루이 마ll I피스이 마라신A 리에마신로트 이여부포세충주 에A뭉 + + + + ++ + + + ++ + ++ + + 방해포세서에 + + ++ + + ++ + + + + + + ++ 는종 되 해방세포 원핵핵원핵원핵원원핵핵원핵원핵원핵원원핵원핵원핵원핵핵원핵원핵원- )))
김김김반옹 자 (옮리 옮(자리자 (옮리 결종)( (결) 종종( 결 ) 종)(결 종( )결) 종(결 ) 종(결 견 ) 종(해는되방달딜전 펩티기, 펩티딜기달, 전달기펩 티 딜 전,리자김 옮티 펩기달전딜 달 딜 ,전기펩 티 티 딜달기,전펩펩티달 ,딜 전기,팹전달 딜 기티, 달펩딜 기전티티팹딜 전 달 ,기티펩전 달딜 .기티,팹전 달딜 기자(옮 김리)옮김 리)(자 옮김 리)자( ))))))))계결결결결결결결결는 방단해되연 장장 연장연 장연 연 장종,시장(연개(시연장개,종(장연개종,시(장연개시종,(장연개종시,장개연종,(시시(장연개, 종(장연개,시종장 연연장 장 연 해겁問_50 S5 S05 0S50S 5 0S05S 0 5S0S 50S 50S 50S 550S 50S 5S0 50S 50S I량분자7.8688040.82191.40.83083538.62475.7455.612521.5615256.5215.6•52 .5.52615152.656.98686.9868.9 0~78. 질해물 신마이이신 A2 니류 드 세틴A 민류 리비먼A 신 A 이신M마아 이신 1M신마 이 A민 라그A오그 리신A B 민 류B 신 Ba 이 신리인 세방레울안도르마카보틸 로신이로마신토미사스셀스티레토라그랩세그오리미카마이베마르나비니르기스타로필스트랩토레오스트PA 114그렌라토마미이카나베마르도비리그트레트트보셀스스부여세포주충1 入에뭉 + + + ++ + + + + + + + + + + + “麟 +++++++++++++++
되는 종 진 핵))핵진 해방세포 핵원핵원핵원핵원麟 핵진핵진 (핵핵 (원핵원핵원핵핵원학원핵원원원 티 티 티펩팹펜 I 해방 반 응는되 김옮()자리리)(옮자김 리김(자옮)(리옮)자 김 티기종( ,)렌 결전 딜달 전딜 팹티달기-A aaR돈짝N짓t기-코 돈 달짓 기코a기AN딜R짝--ta 전 , 기N달코R짝a a-기t딜 짓 전A-돈, A결N t-합aR의a A 결RN t-a합a의 A 결N tR합-aa의 옮리 자김A- 기돈 N 달딜t짓R기 전짝-aa코, eMNRe'MA-ttf 결 의합t 계단 되해방 는 연장장 연장연 연장 종)(결 연장장연 연장 장 연장 연장시)종,결연개(장 연장시종,)개연결(장 연장 연시 개방의해리 자 5S0 5S0 S50 5S 05 00 S6S,60S 30S 85(030)S S530)0S( 30S 30S 30S 30S 8(3500) S30S } K량분 . _ 9318.2 6.896889 68.6 6.68983644 .1 265 1 .34 .671747.61 6 147.666 83.25 8585.58 585 1. .584 40.584 40.37938 클신누질물방 해S 신마필타 스이로 B트라토민랩그스 B리신스트레오오그 141-1P BA스파이르마 신소아소니이 마신드리시노미아코 글류C, 타신겐마 이B 오신네이 마C 오신이 마네스마이로토트드랩히디무마불 소이엔신마스 토랩이트신노티이신펙스마 나카신이마 수카이마가신 헥노스미아피미리 시단소뮤오드 오레
1 부여 세포Ig홉 ++++++++++++++++++ 방해麟 + + + + ++ + + + + + ++ ++ + 되해방는포종 세핵원진핵,,원핵진핵원,핵진핵진핵핵원,,핵핵원진원진,핵핵핵원,진핵해 진원핵 원핵 진핵 진핵 진핵 핵 원 진핵 진핵 진핵핵진 핵진 해는반 방되웅 딜티전기 달펩 전딜 기 펩티달팹 전티 달딜 기기딜티 팹달전 기티 전딜달팹 달전티기팹 달의의에Nm리 R솜 합A결보 펩덜전 달기티 -ETF u 의보으 리솜로의부터{그어 깁.$젊 셉』존 굽\F ETu-응 반.다이둘-을 기달 딜전티펩 ANRaa -t 합결 A결N tR -aa합의 시개 시개 시개기,결 종딜 티전펩달 ) ( 시개 단되계 는방해 연장장 연연장 장연 장연장 연연) 장(시 개장 연연장 장 연연장 장(연종 )결연장 개시 개시개시 연장 개시방의해 자리 0S5 0S 505 S50S S5 00 S5 3 0S4S,00S 0S 64,E u-TF- uETF06S 4,S, 03 0S)0S (5-TFEu 0S 60S 60S 60S 60S 6 량분자42443.6.0466422.5486961.95.1753.5558.4322574.377998.76101.8124. 19744.3445583. 1 2.132346.36152.50742.33034.262 질
물해방오 크. '1]]터 ]터-L 트
부해여방 . ..』:기1 에물 서+ + ++ + + + + + ++ + + + + + ++ ++ l. 託뀜핵 진핵 진핵 진진핵 진핵 핵원 핵원 핵원핵 원핵 원
김김김김김 옮 옮 옮 옮옮 방 응반는되해 전딜달 ( 펩티종기 ),결달전티 펩).종 딜(기 견결달전티기 )종펩딜. ( 시개시개 시합.수l하견분 i 가개 TG P ,A-aaN Rt리 의 결가분. 시i개수 합 민TG P, AR-aNa t 리의 .T결G 시개가. .분P수 합해A NRaa-t자 의리 하L결가 .분시 •개 합}수TG P ,ARN -aat리 의 합분히결i上 가 수. 시개TG P ,ARN-aa t리 의 계단 되는연장연장시개시개시개장연연장장연장연장연해방 방해의자분량 자리--- 60S .342052 6S0923.82643.S30 056.6S364 05046 0S4.20 4.1264 50S81~50 50S99171 5S0 1. 90.6461S5 001 2.7510S5 I 물해질방 코르데몰리트코리데르트 민리신트데코 T- 2 소독HT- 2 독소군몬트스렙 이티 물신마오오포신스이마기란 A신오시 이마랩오티돈트 스B랩오티틴트 스오티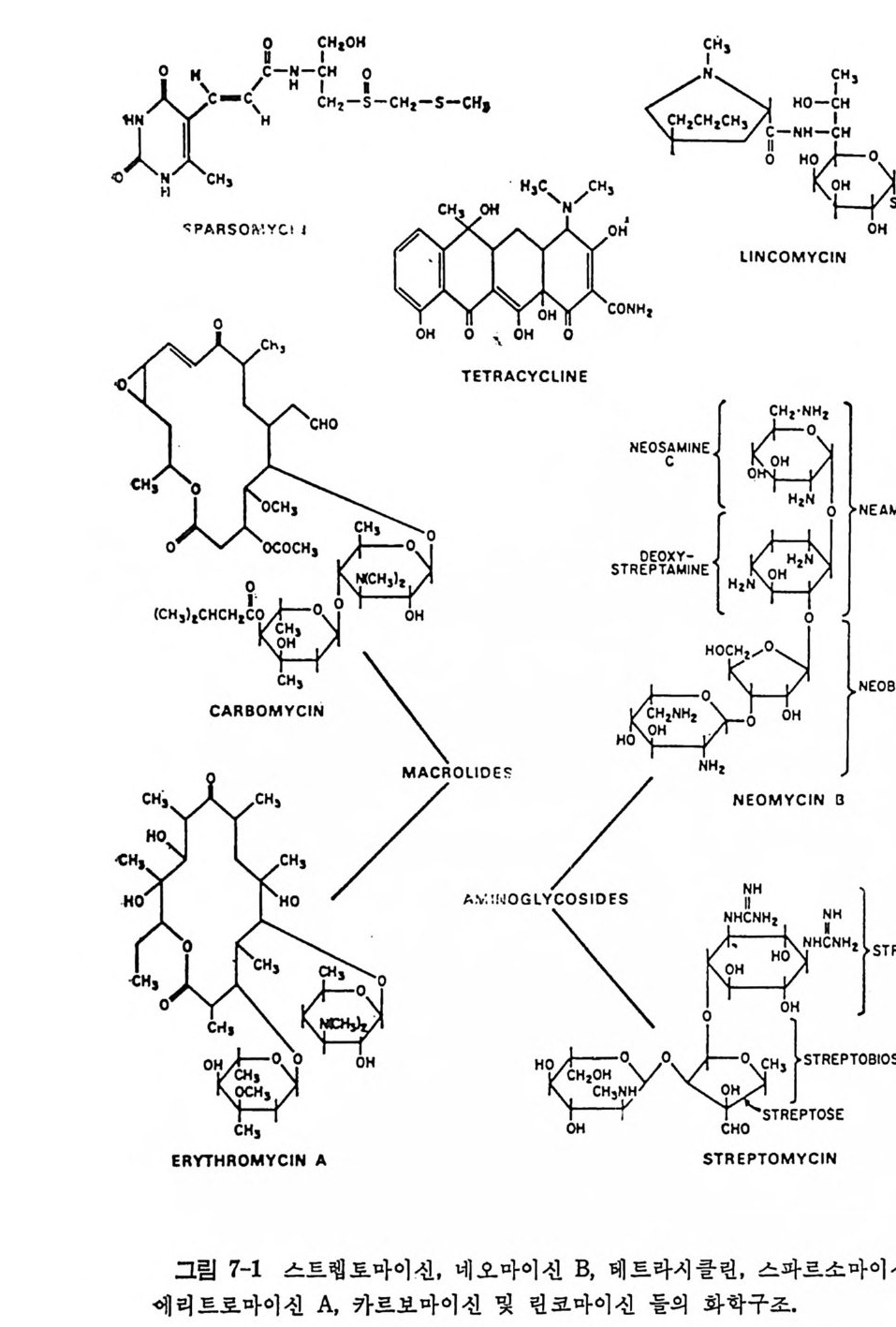 0DCHcHIo ,HC H-,
0DCHcHIo ,HC H-,
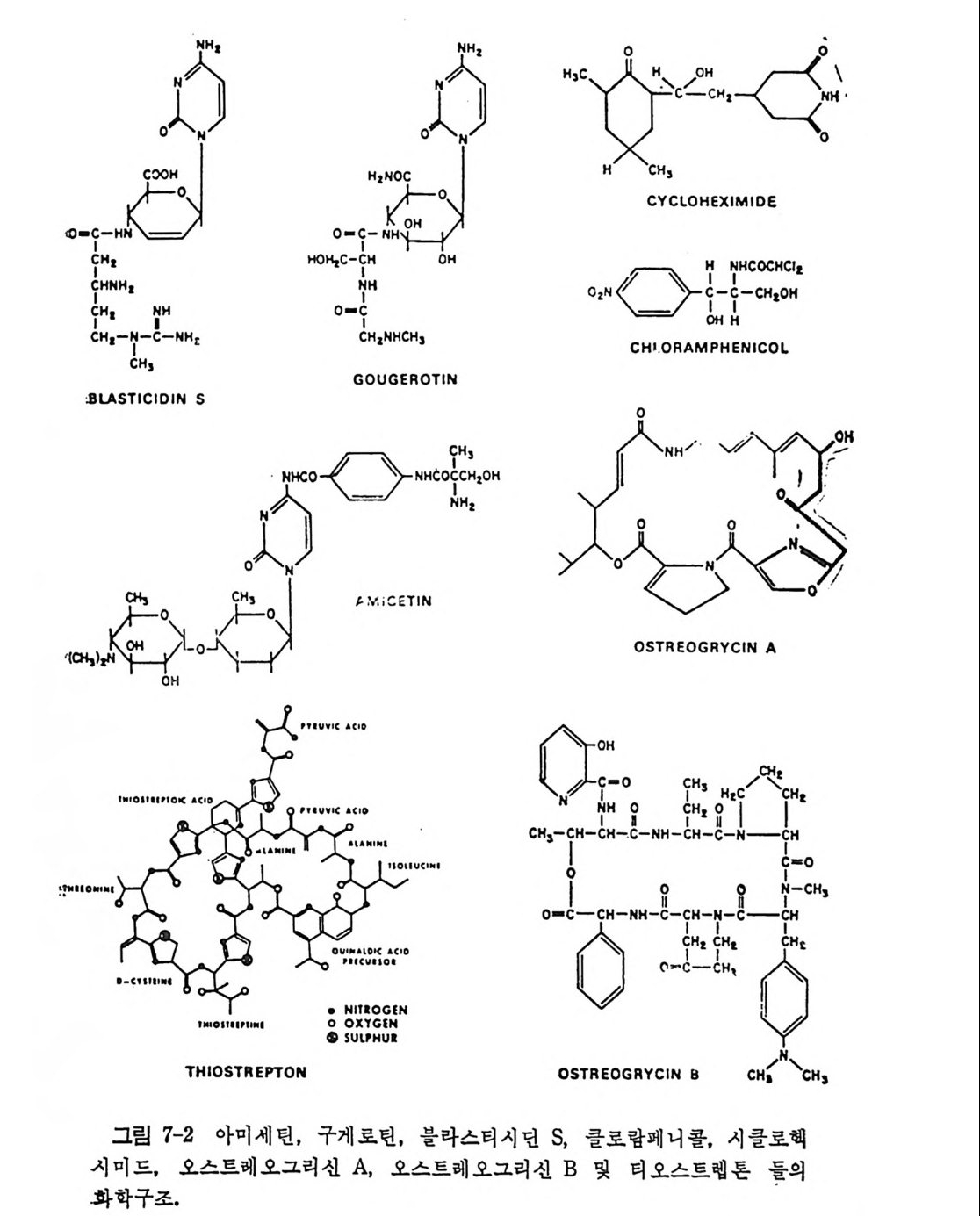 9 -C-IHCH IIHCNN'血〉〔〈ICNH HIIesH_CN“人HHNI BaI- 5 s HO foo- G COL-UII CHNGH I-ENc RHH :IO COT
9 -C-IHCH IIHCNN'血〉〔〈ICNH HIIesH_CN“人HHNI BaI- 5 s HO foo- G COL-UII CHNGH I-ENc RHH :IO COT
7.l 원핵세포에 대한 항생물질들의 작용방식 7. 1. 1 단백질 합성의 개시 및 종결에 미치는 영향 단백질 합성의 개시과정은 당연히 항생물질들에 의해서 목이하게 작 용을 받을 것으로 생각되지만, 이 과정을 득이하게 방해하는 항생물질 은 거 의 없 다. 카수가마이 신 이 fM et- tR NA! M ei 의 30S 하위 단위 체 와의 결합을 방해하는 것이 밝혀져 있어서, 개시과 정의 목 이한 방해물질이라 고 생각되고 있다 (Oku y ama 둥, 1974). 오린트 리카르복시산과 같은 트 리페닐메탄 염료류는 시험관 내 실험에 있어서 mRNA 의 30S 하위단위 체와의 결합을 방해하는데, 이 과정은 다른 항생물질들 에 의해서는 영 향을 받지 않는 것으로 알려져 있다. 시험관 내 실험에서 단백질 합성의 개시반응을 방해하는 또 다른 약제는 에데인이라는 것인데, 이 방해물 질은 원핵세포와 진핵세포의 단백질 합성계를 다 방해하는 것으로 알려 져 있으며, mRNA 또는 개시 t RNA 가 30S 또는 40S 하위단위체에 결 합하는 것을 막는 것으로 알려 져 있다 (Kur y lo-Boroska 와 Hi er owski, 1965 ; Szer 와 Kmy lo -Borowsk, 1972) . 진 핵 세 포의 추출물에 서 는 낮은 농도에서는 팍타마이신이 풀리펩티드 사슬의 개시반응의 방해물질로 ~ 용하지만 높은 농도에서는 사슬 연장을 방해한다. 그러나, 박테리아의 계에 있어서는 팍타마이신의 개시와 연장에 미치는 효과들은 겹쳐지기 때문에 개시반응의 특이한 방해물질로서는 이용할 수 없다 (S t ewar t와 ” Goldberg, 1973) . 풀리펩티드 사슬의 종결의 특이한 방해물질로서 알려진 것은 하나도 . 없다. 폴리펩티드의 방출반응에는 펩티딜 기 전달효소가 관여하는데, 이 반응은 이 효소에 작용하는 클로람페니콜과 스파르소마이신 등에 의해 서 방해된다. 그리고, 종결 코돈둘은 리보솜의 A 자리에서 방출인자들 · 에 의해서 인식되는데, 이 인식작용은 티오스트랩튼 또는 클로르테트라 시클린이 A 자리를 막음으로써 방해된다. 7.1.2 생체 내에서의 푸로마이신 반응에 미치는 항생물질들의 영향 여러 가지 항생물질들이 박테리아의 원형질체에서의 단백질 합성을
정지시키며 갓 생긴 펩티드 사슬을 크게 손실시킴이 없이 폴리솜을 〈동· 결 〉 시킨다. 이어서 이러한 계 에다 푸로마이신을 첨가해 봉으로써 그러 한 항생제들의 작용방식을 해명할 수 있다 . 약간의 항 생 물질들은 갓 생긴 펩티드가 푸로마이신에 의해서 리보솜 으로부터 방출되는 데에는 영향을 미치지 않으면서 생체내에서의 던맵 질 합성을 정 지시킨다. 이것은 이러한 항생물질들이 펩티딜 기 전달효 소에 의한 반응에도 영향을 미치지 않으며 자리옮김도 방해하지 않는다 는 것을 말한다. 왜냐하면 만일 이 두 반응이 영향을 받았다면 갓 생긴 패티드는 리보솜의 A 자리에 머물러 있게 될 것이므로 푸로마이신이 그 들을 방출시 킬 수 없을 것이다. 이러한 방식으로 작용하는 항생물질~ 에는 클로르데트라시클린, 팍타마이신, 보트로마이신, 티오스트랩튼 및 푸시 드산 등이 있다 . 이 방해뭉질들은 아미노아실-t RNA 가 리보솜의 A 자리 에 결 합하는 것 울 방해 한다 (Cundlif fe 와 McQ u il len , 1967 ; Cundliff e, 1971 ; Cundlif fe, 1972a) . 이 와는 대 조적 으로, 클로람페 니 콜, 스파르소 마이신 및 에리트로마이신은 생체 내에서 푸로마이신 반응을 방해한다. 그러므로, 이 방해물 질들은 펩티딜 기 전달효소에 작용하는 것으로 생 각되고 있다. 푸시드산은 EF-G 와 GDP 를 일시적으로 리보송 상에 붙잡아 둠으로 써 아미노아실-t RNA 가 A 자리에 결합하는 것을 막는다. 푸시드산 으 로 안정 화된 복합체 들은 무한정 하게 지 속하는 것 이 아니 다 . 푸시 드산으 로 처리한 원형질체에서는 결국에는 천천히 리보솜 회로가 다시 자리를 잡게 된다. 이 조건 하에서는 푸로마이신에 의한 갓 생긴 펩티드의 방 출이 스펙티노마이신, 린코마이신 및 셀레스티세틴 들에 의해서 방해된 다. 이러한 관찰은 이 방해물질들이 작용하는 단계는 펩티달 기 전달효 소이거나 자리옮김일 것임을 암시하는 것이다. 자리 옮김 반응에 관한 고전적 인 연구는 Haenni 와 Lucas-Lenard(1968) 에 의해서 처음으로 고안되었다. 그들은 A 자리에서 자리옮김 반응을 받을 수 있는 기질을 얻기 위해서 EF-G 가 없는 데서 N- 아세틸-dip h e tR NA 를 합성 한 다음에 EF-G 를 첨 가한 후에 N- 아세 틸 -d i p he- t RNA 가 푸로마이신과 반응할 수 있는 상태로 전환되는지를 추적하였다. 그` 이후로 비슷한 실험적 접근법이 설계되어 자리옮김에 관한 연구들이 이 루어졌다. 자리옮김을 방해하는 물질이라는 것이 처음으로 알려진 것은 에리트-
로마이 신 이 다. lga rashi 등 (1969) 은 이 항생 물질 이 EF-G 와 GTP 가 존 재해야만 일어나는 푸로마이신 반옹은 방해하지만 EF-G 와 GTP 에 의 존하지 않는 반응은 방해하지 않는다는 것을 알았다. 7. I. 3 리보솜의 GTPase 반응둘의 방해 EF-G 는 70S 리보솜 또는 50S 하위단위체와 함께 시험관 내에서 일어 나는 〈짝지워지지 않은〉 GTP 의 가수분해를 촉매한다. 이 반응은 티오스 트랩돈, 그리고 일정한 조건에서는 푸시드산에 의해서 방해 된 다 (Tanaka 등, 1968; Pestk a , 1970) . EF-G 는 자리 옮김 이 일 어 나는 도중에 작용하 프로, 이 두 항생물질들은 이 자리옮김 반응을 방해할 것이라고 널리 인 청하게 되었다. 실제로, 푸시드산에 저항성을 나타내는 E. coli 균주들 로부터 단리한 EF-G 는 이 항생물질들에 대해서 반응을 보이지 않는다 는 사실 이 그것 을 뒷 받침 하고 있 다 (Tocchin i - V alenti ni 와 Matt oc cia , 1968; Bernardi 와 Leder, 1970) . Bodley 동 (1970a) 은 푸시 드산이 리 보 송 •EF-G·GDP 복합체를 안정화시키기에 앞서서 한 차례의 GTP 의 가 수분해를 허용한다는 것을 증명하였다. 그러므로, 이 항생물질은 GTP 가 몰 당량 이상으로 과량으로 존재할 때만 짝지워지지 않은 GTPase 반옹을 방해 하게 된다• 그 다음에 Weis b lum 과 Demohn (1970) 그리 고 Bo dley 등 (1970b) 에 의해서 티오스트랩돈이 이러한 복합체들의 조립을 방해한다는 것이 밝혀졌다. 이 복합체는 시험관 내에서 GTP 나 GDP 로부터 형성될 수 있다. 거꾸로, 푸시드산이 존재하는 조건에서 EF-G 와 GDP 를 지니고 있는 리보솜은 티오스트랩돈에 의한 비가역적인 비 활성화로부터 보호된다는 것이 밝혀졌다(Hig hland 동, 1971). 이 관찰들은 생체 내에서 티오스트랩돈이 자리옮김에는 영향을 미침 이 없이 리보솜의 A 자리에로의 아미노아실-t RNA 의 결합을 방해한다 는 것이 알려침으로써 특별한 의미를 가지게 되었다. 이러한 관찰들과 일치 하는 결과둘이 Modolell 동 (1971) 과 Ki no shit a 등 (1971) 에 의 해 서 관찰되었다. 죽, 티오스트랩톤과 이와 관련된 화합물인 시오마이신과 터오펩티드는 시험관 내에서 EF-Tu 의존적으로 일어나는 아미노아실 -tRN A의 리보솜에의 결합과 리보솜과 EF-G 로 촉매되는 GTP 의 결 합 및 GTP 의 가수분해와 관련된 GTPase 의 작용을 동등한 세기로 방 해한다는 것이 밝혀졌다. 만일 리보솜이 그의 50S 하위단위체 상에 티
오스트렙톤에 대한 결합자리를 단 하나만 가진다고 한다면, 위에서 말 한 관찰들은 EF-Tu 와 EF-G 가 티오스트랩튼에 의해서 비활성화되는 50S 하위 단위 체 상의 단일
반하여 그밖의 아미노굴리코시드류는 〈무작위한 〉 오독을 일으킨다. 네 오마이신, 넓은 농도 범위에서 카나마이신 및 겐타마이신 동이 단백질 합성의 방해와 오독에 미치는 효과를 조사해 보면 그 효과가 다단계적 으로 나타난다. 예를 들면, 낮은 농도의 겐타마이신은 매우 근소한 오 독을 일으키면서 단백질 합성을 다소 방해하지만, 그 농도 를 중가시킴 으로써 오독이 더 중진되고 단백질 합성의 방해도 커지 기 시작한다. 겐 타마이신의 농도가 아주 높을 때는 단백질 합성의 방해가 매우 증가한 댜 이러한 효과로 보아서 이 항생물질들은 리보솜 상에 여러 결 합자리 들을 가지 는 것 으로 생 각된 다 (D av ie s 와 Davis , 1968) . 이 러 한 생 각은 실제로 이 항생제들에 대해서 저항성을 가진 여러 돌연변이체들이 발 견됨으로써 확인되었다. 이와는 대조적으로, 스트랩토마이신은 리보솜 의 단 한 자리에서만 결합하며, 단일 돌연변이체들을 쉽게 분리할 수 있다. 시험관 내에서 스트랩토마아신을 썼을 때 생기는 오독의 효과는 리보 송과의 비가 1 : 1 의 비일 때 최대의 수준으로 나타나며, 단백질 합성 의 방해의 수준과 비례한다 . 스트랩토마이신이 존재하는 조건에서 개시 반옹을 시작한 리보솜은 합성 속도가 낮고 오독 효과를 받는 상태이기 는 하지 만 mRNA 분자 를 따라서 계 속 이 동해 나아간다. 〈 스트랩 토마이 신-리 보솜〉 (비 가역 적 으로 영 향을 받은) 은 mRNA 로부터 이 탈된 다음에 도 무용한 존재로 있게 된다. 이 상태에서 〈스트랩토마이신-리보솜〉은 mRNA 및 f Me t-t RNNM• t와 불안정한 개시복합체를 반복해서 형성한 다. 이러한 복합체가 불안정하다는 것은 스트렌토마이신의 영향을 받은 리보솜이 한번 사용된 낡은 mRNA 에 억류되는 것이 아니라 계속해서 재이용된다는 것을 의미한다. 그러므로, 결합되지 않은 항생제를 제거 한 후에도, 〈스트랩토마이신-리보솜〉들은 재 mRNA 와 결합한 상태에 서도 새로 합성된 리보솜의 기능을 방해할 수 있다. 그렇기 때문에 스 트랩토마이신은 살균작용을 가지게 되는 것이다. 7.2 원핵세포의 리보솜에서의 항생물질의 결합자리 7.21 자연상태의 항생물질의 리보솜에의 결합 방사능으로 표지된 항생물질의 리보솜 또는 하위단위체들에의 결합은
여러 가지 방법으로 조사할 수 있다. 원심분리, 거르기, 침전 또는 추 출 등과 같은 방법들은 결합이 매우 단단해서 해리가 일어나지 않을 때 에만 응용할 수 있다. 활성탄소 또는 이온교환 수지 등으로, 결합하지 않은 항생제를 제거할 때도 유사한 고려를 해야 한다. 리보솜 또는 하 위단위체들에의 항생물질들의 결합에 대한 해리상수는 보통 5x10-1 M 내지 5x10-6 M 정도이다· 티오스트랩몬은 예의적이어서 매우 단단하게 50S 에 결합하기 때문에 해리상수를 측정할 수 없다• 대부분의 항생물 질들은 70S 리보솜과 1 : 1 의 비로 결합하며, 그 결합자리는 두 하위단 위체들 중 어느 하나에 있다. 그러나 농도가 클 때는 항생물질들은 〈이 차적인〉 결합을 할 수도 있다. 약간의 항생문질들은 2 : 1 의 1:l 1 로 각하 위단위체 상에서 강하게 결합하는데, 아마도 이러한 물질들은 리보솜에 이원적인 효과를 나타낼 것으로 생각된다 .• 리보송과의 결합자리에 대해서 경쟁적으로 작용하는 항생물질들도 많 이 있다. 이러한 항생물질들은 그들의 작용방식에 있어서 적어도 어떤 피상적인 상관관계가 있는 것으로 생각된다. 예컨대, 쿨로람페니콜, 린 코마이신 및 구게로틴 둘과 같이 펩티딜 기 전달효소의 작용을 방해하 는 물질들은 서로 경쟁적으로 작용하지만 티오스트랩튼이나 -자 리옮김 방 해물질인 네오마이신, 카나마이신, 겐타마이신, 비오마이신 및 두베르 악티노마이신 D 들과는 경쟁적으로 작용하지 않는다. 그러나 뒤에 말한 항생물질들끼리는 리보솜의 두 하위단위체 상에서의 결합에 대해서 서 로 경쟁한다. 7.2.2 항생물질의 친화표지 유사체의 리보솜에의 결합 항생물질들이 결합하는 리보솜의 특이한 자리들과 관련된 성분 단백 질들을 확인하기 위해서 친화표지 탐침이 많이 이용되고 있다. 이 문제 에 관해 서 는 Coop er man (1978) 의 평 론서 에 자세 히 기 술되 어 있다. 방사 능으로 표지된 탐침은 리보솜 상에서 항생물질이 결합하는 자리를 확인 하는 강력하고 직접적인 방법이 되고 있다. 일반적으로, 빛으로 활성화 될 수 있는 친화표지 탐침을 사용하는 것이 바람직하다. 왜냐하면 빛으 로 조사하기에 앞서서 탐침들이 리보솜과의 바공유결합성 상호작용의 득이성을 이물 수 있기 때문이다. 푸로마이신과 쿨로람페니콜의 몇 가 지 친화표지 유사체들을 그림 7-3 과 그림 7-4 에 나타내 었다.
제 7 장 단백질 합성의 방해뭉질들 427
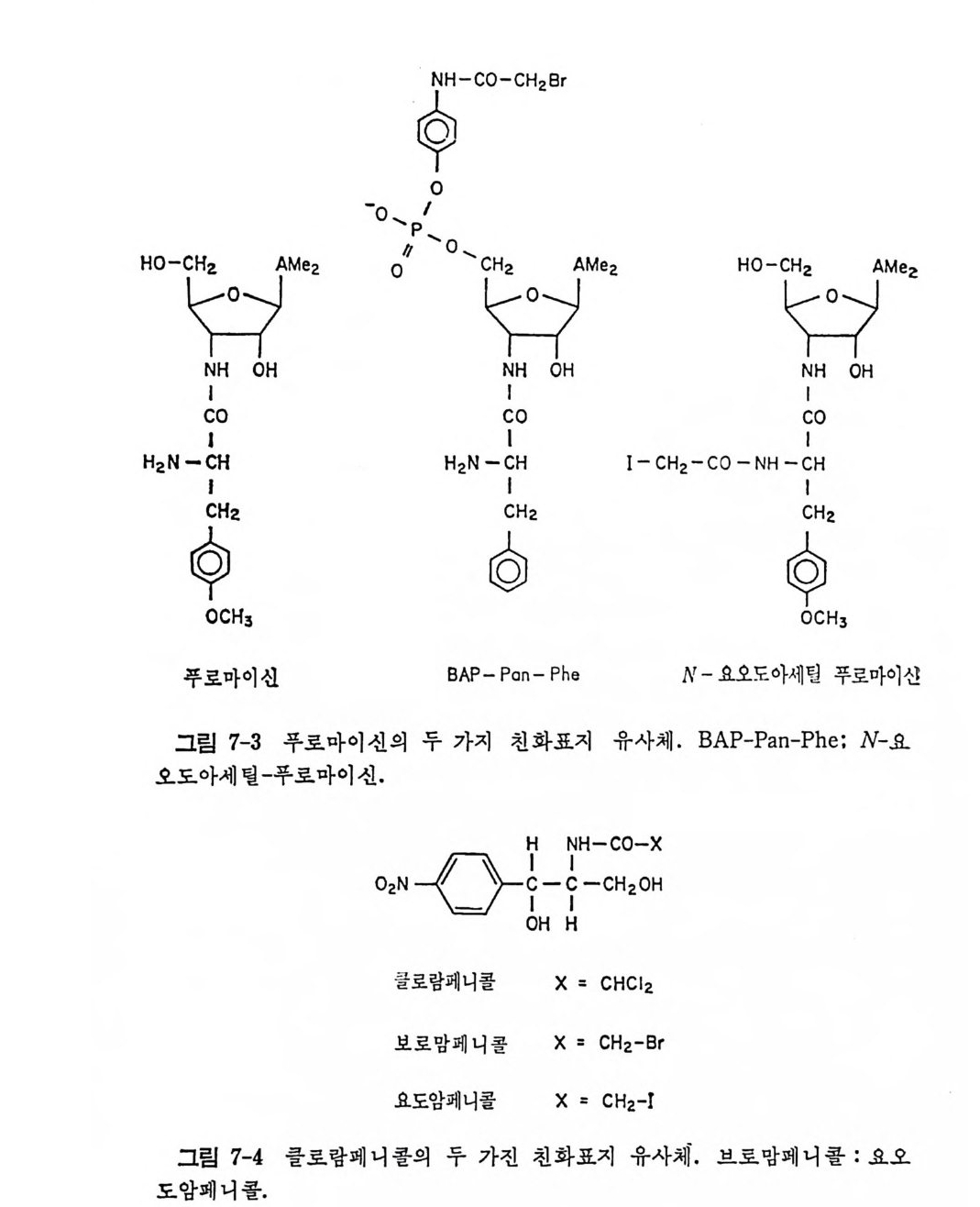 亨NH -c > '
亨NH -c > '
푸로마이신과 그의 유도체들을 사용하여 얻은 결과를 표 7-3 에 실 었다.
표 7-3 푸로마이신 및 그의 유사체들에 의해서 표지되는 리보솜 성분들 시약 표지된 리보솜 성분들 참고문헌 푸로마아신* L23 S14 RNA50 I Jay n e s 등 (1979) N- 에 틸 -2- 디 아조말로 S18 S14 Jay n es 동 (1978) 닐-푸로마이신* P- 아지 도 푸로마이 신* | L11 S18 (주성 분) 1 Ni ch ols 와 1S,32 S!,41 3 SL51 7 Ll8 L(27소 성 분) I Coop er man (1978> P- 아지도 푸로마이신* | L6 Ll3 L18 L22 L25 (주성분)| Krassnig g 등 (1978 〉 Lll L23 L27 L30 (소성 분) NB-At 요i오:신도n 아-P세he 틸 푸로 I L236S (R주N성A 분 ) , L2 (소성 분) || PGorenegn sw e등l1 ( 1동97 4(1) 974} * 빛으로 조사합 : RNA50 = 50S 하위단체로부터의 RNA. 그밖의 방해물질들의 친화표지 유사체들로 표지되는 예들을 들면 야 래와 같다. 스트랩토마이신의 아릴아지도 유도체 S7, S14 스트랩토마이신의 요오도아세틸 히드라촌 S4 클로람페니콜의 요오도아세틸 유도체 Ll6 클로람페니콜의 브로모아세틸 유도체 L2, L27 이러한 방법으로 앞으로 의미있는 결과들이 더 축적될 것으로 믿어자 지만 아직은 그 초기에 있는 실정이다. 7.2.3 리보솜의 부분적 재조립법에 의한 항생물질 결합자리의 조사 리보솜 내에서의 기능 자리들의 확인에 분할-재조립법이 사용되고 있 다는 것은 이미 제 2 장에서 기술하였다. 이 방법은 리보솜의 옹어리 입 자에다가 주어진 어떤 기능이 회복될 때까지 분할된 단백질들을 순차적 으로 첨가하여 성분 단백질의 기능을 추정하는 것이다• 비슷한 방법으 로, 항생물질의 결합자리를 생기게 하거나 완성시키는 데 필수적인 리 보솜 단백질들을 알아낼 수 있다. 이 방법은 항생물질이 실제로 결합하 는 리보솜 성분이 어느 것인지에 대해서 확실하게 알려 줄 수는 없지~ 친화표지 유사체들을 사용하여 얻는 정보를 보완할 수 있는 실험치들을-
계공해 준다. 재조립법은 N i erhaus 의 연구진에서 광범위하게 개발되었다. 그둘은 L16 이 클로람페니콜과 비르기니아마이신 S 가 E. col i의 50S 응어리 입 자에 결합하는 데 필수적 이 라는 것을 알았으며 (Ni er haus 와 Nie r haus, 1973 ; de Beth u ne 와 Nie r haus, 1978) , L15 와 함께 있 을 때 는 Ll6 이 예 리 트로마이 신과 결 합한다는 것 을 알았다 (Teraoka 와 Nie r haus, 1978) . 지금까지 알려져 있는 것으로서 리보솜에서 분리된 상태에서 항생물질 과 결합할 수 있는 단백질은 L15 인데 (Ll5 와의 결합에 있어서의 에리 트로마이신의 해리상수는 2X10-s M), L16 은 리보솜 내에서의 에리트로 마이신의 결합력을 증진시키는 것으로 생각된다 (70S 에 대한 에리트로마 이신의 해리상수 =10-8 M). 클로람페니콜이 펩티 딜 기 전달효소의 반옹 울 방해한다는 것은 앞에서 이미 말하였다. 그런데 이 항생물질이 Ll6 과 결합한다는 것은 Ll6 이 펩티딜 기 전달효소의 작용에 필수적이라는 것을 재확인해 주는것이다 (5.2.2 절을 보라). 항생물질과의 결합에 있 어서 이러한 방법으로 밝혀진 그밖의 단백질들은 티오스트랩톤에 대한 L11 과 디히드로스트랩토마이신에 대한 S3 또는 S5 이다. 23SrRNA 와 7 개의 단백질을 함유하고 있는 4M LiC l 응어리가 티오 스트랩튼을 게걸스럽게 결합한다는 것을 제일 먼저 안 사람은 Hig h land 등 (1975) 아었다. 최근에 티오스트랩톤과 결합하는 단백질아 L11 이며 이 단백질은 GTPase 의 작용과 · 관련된다는 것이 교차결합법으로 밝혀 겼 다 (Skold, 1983) . Str e p tom y ce s azures 에 서 는 L11 이 23S rRNA 의 A1067 과 결합하며, A1067 의 리보오스가 메틸화되면 티오스트랩돈에 대한 저항성을 가진다는 것은 이미 2.4.4 절에 언급하였다. 7.3 항생물질에 대한 원핵세포의 리보솜의 저항성 7. 3. I 리보솜 단백질들에 의해서 결정되는 저항성 항생물질에 대한 저항성을 가지고 있는 여러 가지 박테리아의 돌연변 이종들에 있어서 단 한 가지의 리보솜 단백질에 있어서의 돌연변이가 저 항의결정인자가 되는 경우가 많이 있다. 이것은 돌연변이체와 야생형 박테리아에서 유래되는 성분들을 함유하는 리보솜 하위단위체의 재구성
이 나 유 전학적 인 분석으 로 알 수 있 다 . 대표 칙 인 예 는 N omura 와 그의 공동연구자들의 스트랩 토마 이 신에 대 한 저항성에 관 한 것이다. E. coli 의 Str A 돌연변이체에서는 단백 질 S12 가 저항 성을 결정하는 인자가 되 고 있 다 (Ozaki 등, 1969) . 그밖에 도, S5 는 spc A 에 서 스펙 티 노마이 신 에 대한 저항성을 결정하 며, er y A에 서 의 L4 또는 ery B 에서의 L22 는 에리트로마이신에 대한 저항성을 결 정 한다 . 카수가마이신에 저항성인 ksgC 돌연변이체는 단백질 S2 가 변이되어 있다. 어떤 주어진 표현형은 리보 솜 성분들 중 어 떤 한 가지에 돌연변이가 일어남으로써만 얻을 수 있는 것 이 아니라 리보솜에 영향을 미치는 다 중성 돌연변이의 결과로서 얻을 수 있는 경우도 많 이 있다. 예컨대 eryA 균주 ( 단백질 L4 에 변 화 가 일어난 저항성 균주)는 s t rA( 단백질 S12) 또 는 s p cA( 단백질 S5) 돌연변이를 도입함으로써 에리트로마이신에 대해서 민감하게 된다 (Cundl iff e ( 1980) 에 인용됨). 국단적인 예를 둘어 보면. 단백질 S8 에 변이가 일어난 스트랩토마이신-의존성 균주는 리보솜 단 백질의 어느 것에서든 돌연변이가 일어남으로써 스트랩토마이신에 관계 없는 균주로 복귀한다. 마지막으로 한 가지 더 예를 들면, 변이된 리보 솜 단백질들을 가 진 돌연변이체들과는 대조적으로, Bacil lus meg a te r iu m 과 B. subti lis ( Cundli ffe, 1980) 는 E. coli 의 단백 질 Lll 에 해 당하는 단 백질을 상실함으로써 티오스트랩몬에 저항성을 가지게 되는 돌연변이체 들도 있다. 7.3.2 리보솜 RNA에 의해서 결정되는 저항성 Helser 동 (1971, 1972) 이 처 음으로 밝힌 바와 같이 , E. coli 의 ksg A 돌연변이체들에 있어 서 의 카수가마이신에 대한 저항성은 16S rRNA 의 3' 말단 가까이에 있는 A1518 과 A1519 의 아데닌에 메틸화가 일어나지 않음으로써 생긴다 (2.4.4 절의 (나)항을 보라). 야생형 균주에 존재하 는 메틸화효소는 ksg A 돌연변이체로부터의 30S 응어리에 작용할 수 있 다. 그래서 분리한 단백질들로써 재조립을 한 다음에는 리보솜(메틸화 된 30S 옹어리를 함유한 리보솜)은 카수가마이신에 대해서 민감하게 된 다. 메틸화효소는 16S rRNA 의 Al518 와 A1519 의 아데닌의 N6 위치 에서 디메틸화를 일으킨다는 것은 2.4.4 절에서 기술하였다 . 위의 경우와는 대조적으로, MLS 표현형 (마크롤리드류, 린코사미드
류 및 스트랩토그라민 B- 형 항생물질들에 대한 저항성)을 나타내는 Sta p h yl o coccus 또는 Str ep t oc occus 의 균주들은 야생 형 에 비 하여 과도하 게 메 틸화된 23S rRNA 를 가지 고 있음이 밝혀 져 있다 (Lai 와 Weis b lum, 1971). 이러한 균주들에 있어서, 마크롤리드류의 하나인 에리트로마이 신을 방해효과를 일으킬 수 있는 농도보다 적은 양을 첨가하면 풀라스 미 드의 정 보를 받아서 생 기 는 효소가 유발되 는데 이 효소는 23S rRNA 내에서 약 두 개의 N6,N6- 디메틸아데닌 찬기를 생성시킨다. 이 렇 게 메 틸화된 23S rRNA 를 함유하는 리보솜은 시험관 내에서 마크 롤 리드 류 에 대해서 저항성을 가진다. 에리트로마이신을 생산하는 Str e p t om y c es eryt hr eus 로부터 의 23S rRNA 에 N6, N6- 디 메 틸 아데 닌 이 존재 한다는 것 은 이 생체에서의 리보솜의 저항성도 비슷한 메카니즘으로 획득되는 것 으로 생각된다. 7. 3. 3 티오스트렙튼에 대한 저항성 E. coli 세 포는 티 오스트랩 돈을 받아둘이 지 않으므로 티 오스트랩 튼 에 대 한 저 항성 은 자생 적 으로 생 기 는 Bacil lu s meg a te r izm z 과 Bacil lu s sub tili s 의 돌연변이체들을 가지고 연구되었다. 이러한 돌연변이체 몇 가 지물 면역학적으로 조사해 봄으로써 E. col i의 단백질 L11 과 면역학적 으로 관계가 있는 또는 〈 BS-L11 〉이 돌연변이체들의 리보솜 에서 없어진 것으로 나타났다. B. subti lis 돌연변이체가 터오스트랩몬 민감성인 것으로 복귀됨으로써 BS-L11 과 형식적으로 유사한 단백질을 다시 가지게 된다. B. meg a te r iu m 돌연변이체들은 복귀돌연변이룰 하 지 않지만 단백질 BM-L11 로써 그들의 리보솜울 재구성하면 야생형의 성질이 회복된다. 이렇게 재구성된 리보솜은 시험관 내에서의 단백질 합 성의 활동성을 두 배로 촉진시킨다. 따라서 이러한 계는 BM-Lll 의 생 리적인 역할을 연구할 수 있는 좋은 길을 열어놓았다. 위에서 말한 돌 연변이체의 리보솜에 단백질 BM-L11 을 첨가하면 폴리펩티드 사슬의 연장과 관련된 부분 반옹둘 중의 하나, 죽, EF-G 의존적으로 일어나는 GTP 의 가수분해 반옹만이 촉진된다 (Cundl iff e, 1980). E. col i의 단백 질 L11 을 단백질 BM-L11 대신에 넣어도 비슷한효과를 낸다. 따라서, Lll 과 BM-Lll 은 기 능적 으로뿐 아니 라 면역 학적 으로도 유사한 관계 가 있음을 알 수 있다. 이 연구결과들은 단백 질 L11 이 EF-G 의 존적 안
GTPase 의 반응에 관여 할 것 이 라는 암시 를 뒷 받침 하는 것 이 다 (Schie r 와 Moller, 1975) . 어떤 생체들은 그들 자신이 생산하는 항생물질들에 대해서 방어해야 하는 문제 를 안고 있 다. 티 오스트랩 돈을 생 산하는 St re p tom y c es azureus 에서 이것을 볼 수 있다. 이 생체로부터의 리보솜들은 티오스트랩톤과 결합하지 못하며, 티오스트랩톤의 포화용액이 존재하는 시험관내 조건 에서도 기능을 완전하게 나타낸다• 이와는 대조적으로 그밖의 Str e p to- my ce s 균주들로부터 의 리 보솜들은 티 오스트랩 돈에 매 우 민 감하다. 서 로 다른 출처로부터의 RNA 와 단백질을 함유하는혼성 리보솜의 재구성방 법 으로 시 험 해 봄으로써 S. azureus 의 23S rRNA 가 터 오스트랩 본에 대 한 저항성을 결정한다는 것이 밝혀졌다 (Cundl iff e, 1978). 이 생체로부 터의 리보솜 단백질들은 E. col i의 단백질 Lll 에 상응하는 면역학적 유 사체를 함유하며, 티오스트랩돈에 대해서 큰 친화력을 가진 결합자리를 다른 생체로부터의 rRNA 을 사용하여 재구성할 수 있다. S. azureus 의 추출액 은 23S rRNA 의 1067 번 위 치 의 아데 노신울 메 틸화하여 2'-0- 메틸아데노신을 만드는 메틸화효소가 있다 (Thom p son 동, 1982). 완전한 리보솜 또는 50S 하위단위체는 이 메틸화효소의 기 질 이 되 지 않는다. 23S rRNA 를 메 틸 화한 다음에 Bacil lus ste a roth e r-
표 7-4 S. azure11s 로부터의 티오스트랩론-저항 메틸화효소의 23S rRNA 에의 작용 235 rRNA 의 출처 (처 리) I(p8 5m 경 o추l/ p갭m겁 ol의 • 입결 자 합) 재 _?T현HpSm ~'Ip :+gT:H}S, S. coel. (메 틸 화되 지 않음) 0.98 o.78 0. 02 S. coel. (메 틸화 됨) 0.07 。 •89 o. 92 E. coli . (메 틸 화되 지 않음) 1. 04 0.82 0.06 E. coli . (메 틸화 됨) 0. 08 0.77 0.76 S. azureus. 0.06 0.75 0.76 * S- 아데노실메터오닌이 있는 데서 그리고 없는 데서 RNA 를 S. azureus 메틸화효소 로 항온처 리 한다. 그 다음에 B. ste a roth e rmop h il u s 단백 질 들을 가지 고 혼성 50S 입 자를 · 재조립한다. 기능 재구성의 분석 : 푸시드산이 있는 조건에서의 재구성된 입자, EF-G 및 [.H] - GTP 둘 사이의 복합체 형성. 티오스트랩몬 (THS) (복합체 형성의 방해물)을 입자들보다 3 배의 ; 과량으로 사용하였다.
mop lzi lu s 로부터 의 리 보솜 단백 질 을 사용하여 혼성 50S 하위 단위 체 를 재 조립할 수 있다. 이렇게 조립된 입자들은 티오스트랩돈에 대해서 저항 성을 가진다(표 7-4 를 보라). 7.4 진핵세포에서의 개시반응의 방해물질들 풀리 펩 티 드 사슬의 개 시 과정 은 개 시 tR NA (Met- tRN A,M ct) 를 80S 리 보솜의 정확한 위치에 부착시키는 데 필요한 4 단계의 순차적인 반응들 로 일어난다. 이 네 단계의 반응은 (a) 40S 하위단위체에 의한 eIF-3 의 인식과 eIF-2•Met- tRN A;Mc t• GTP 복합체의 결합, (b) eIF-1, eIF- 4A, eIF-4B, eIF-4C 및 mRNA 의 개 시 코돈 인식 , (c1) 단계 b 에 서 형 성 된 개 시 복합체 에 의 60S 하위 단위 체 의 부착, (c2) Met- tRN A1M•1 의 3' 끝과 펜티딜 기 전달효소 중심의 주개 자리와의 상호작용 등이다(그 림 7-5B). 7.4.1 개시 t RNA 의 인식을 방해하는 물질들 진핵세포에서의 단계 (a) 는 다음과 같은 반응들로 일어난다. 40S 하 위 단위 체 와 eIF-3 과의 상호작용, eIF-2• Met- tRN A1M•1 • GTP 복합체 의 형성, 그리고 이 복합체와 40S 하위단위체 (elF-3 을 함유하고 있는)와 의 상호작용. 카수가마이신이 박테리아의 30S 하위단위체와 개시 t RNA 의 상호작 용을 방해하는 것은 많은 실험적인 증거로 알려져 있지만, 진핵세포의 경우에는 아직 실험적인 증거가 얻어지지 않고 있다. 쇼도마이신 (N- 에틸말레이미드의 유사체), 아드레노크롬 및 트리페닐 메탄 염료(오린트리카르복시산, 피로카테콜 보라, 아주르 파랑 B, 산성 및 염기성 푹신 등)은 eIF-2•Met- tRN A1Me t• GTP 복합체의 형성을 방해 한다. 번역 방해물질(행에 의해서 조종되는 억제물질)이라는 단백질은 eIF-2 키나아제이며, 이 효소는 무세포 계에서 eIF-2 의 작은 하위단위체를 인산화합으로써 eIF-2·Met- tRN A1M•1•GTP 복합체의 형성을 방해한다는 것이 밝혀져 있다. 최근에 토끼의 망상적혈구의 추출물에 elF-2 를 촉
진하는 단백질 ( ESP) 이 있다는 것 이 발견되었 으 며 , 이것은 eIF-2-Met- tR NAt M et • GTP 복합체의 형성에 앞서서 일어나는 eIF -2·GTP 복합체의 초기 형성에 필요하다는 것 이 알려졌다 . 그 러므로, 번 역 방해물질에 의 해서 eIF-2 의 작은 하위 단 위체 가 인산화되면 eIF-2 와 ESP 와의 상호 작용에 의 한 복합체 형 성 이 방해 된다 (Haro 와 Ochoa, 1979) . 그러 나 eIF-2 의 인산화는 무세포 계에서는 관찰되었지만 진핵세포내에서 일어 난다는 것 이 보고된 적은 없다. 이 중가닥의 RN A 는 eIF-2 의 작용을 방해 하고 단계 (a) 를 막음으로 써 세포의 mR NA 와 비루스의 mRNA 의 번역을 방해한다(그림 7-5). 이 효과는 무세포 계에 다 과량의 eIF-2 를 첨가함 으로 써 극복할 수 있 다 . 단백질 합성을 방해하는 이중가닥의 RNA 의 역 할 에 관해서는 아직 확 실 한 것 이 밝혀져 있지 않지만, 인터페론으로 처리한 세포의 추출액 에 이중가닥의 RNA 를 첨가 하면 리보 솜에 결합되어 있던 핵산 내부가 수분 해효소를 활성화 시키며, 이 효소가 mRNA 들을분해한다고 보고 있 다 (Le w i s 등, 1978; Bag li on i 등, 1978). 인터페론으로 처리 한 세포의 추출액에는 번역을 방해하는 물질이 들어있다는 관찰도 보고되어 있다 (Zi lb erste i n 동, 1978) . 인 터 페 론으로 처 리 한 세 포의 추출액 에 서 는 pppA (2'p 5 ' A ) • 의 합성 이 활발하며 , 이 울리 고누클레 오티 드가 핵 산 내 부가수 분해효소몰 활성화시키 는 것으로 추측되고 있다 (Lew i s 등, 1978). 7. 4. 2 mRNA 인식 (단계 b) 의 방해물질들 이 무리의 방해물질로서는 트리페닐메탄 유도체들(제일 찰 알려진 것 은 오린트리카르복시산이다), 몇 가지 아미노크롬류(제일 찰 알려진 것 은 아드레노크롬이다), 황산 풀리덱스트란 및 황산 폴리비닐 등이 있다. 이들은 모두 복잡한 작용방식을 가지고 있어서 한 가지 이상의 상호작 용과 한 가지 이상의 방해작용을 한다. 이 방해물질들은 모두 40S 하위 단위체와 상호작용하기 때문에 무세포 계에 있어서의 mRNA 인식을 방 해한다. 그러나 이들은 세포 안으로 두과할 수 없으므로 완전한 세포에 는 사용되지 않는다. 앞에서 말한 바와 같이, 이 화합물들은 삼성분 복. 합체 eIF-2 •M et- tRN A1M•1 • GTP 의 형 성 을 막음으로써 개 시 tR NA 의 인 식을 방해한다. 이 삼성분 복합체의 형성에는 리보솜이 관여하지 않는 다는 것은 4.2.2 절에서 이미 기술하였다.
 R中
R中
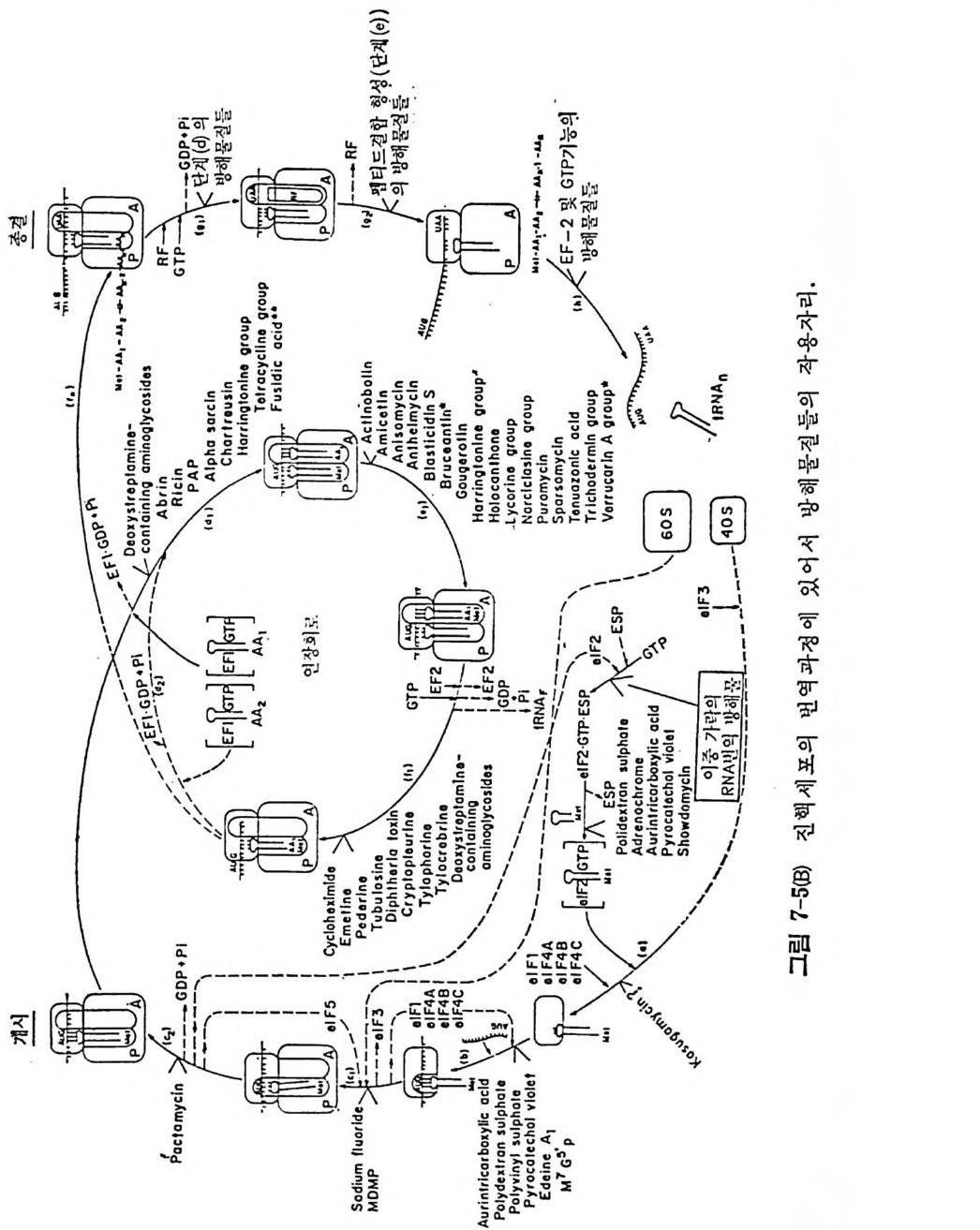 <홀좋>0· u lrJ • •
<홀좋>0· u lrJ • •
에데인 A1 은 작은 하위단위체와 상호작용함으로써 개시단계에서의 효 과적인 방해물질로 작용한다. 에데인 A1 이 기능을 가전 eIF-2·Met- tR NA?Ict• GTP•40S 복합체의 형성을 독이하게 방해한다는 것은 여러 생 물종들을 가지고 한 많은 실험들에 의해서 증명되었다. 이 항생물질은 밀 싹 (Hunte r 등, 1977) 과 토끼 의 망상적 혈 구 (Kozak, 1979) 에 서 , 40S 로부터의 표지된 mRNA 가 80S 리보솜으로 옮겨가는 것을 방해하며 례 오비루스 mRNA 의 AUG 코돈의 인식을 방해한다. 그뿐 아니라, 그밖 의 생물종에서도 에데인 A1 이 단계 (b) 를 직접 방해한다는 것이 확인 되 었다` (Odom 등, 1978) . m1G'' p (7- 메틸구아노신 -5' -일인산)은 5' 끝에 이미 m1G''pp p· .. 〈갓〉을 가진 mRNA 들의 번역을 방해한다는 것이 알려져 있다. 이 방해작용은 개시단계에서 일어나고 있으며 eIF-4B- 의존적으로 일어나는 mRNA 와 40S 하위 단위 체 의 상호작용을 막는다. 7.4.3 하위단위체의 결합(단계 C1) 의 방해물질들 NaF 와 KF, 그리고 2-(4- 메틸 -2,6- 디니트로아닐리노 )-N- 메틸-프로 피 온아미 드의 D- 입 체 이 성 질체 (D-MDMP) 들은 60S 하위 단위 체 가 40S 하위단위체 상에서 형성된 개시 복합체와 결합하는 것울 방해한다 (Weeks 와 Baxte r , 1972) . 7. 4. 4 개시 tR NA 가 주개 자리에 자리잡는 것을 방해하는 물질들 항생물질 팍타마이신은 낮은 농도에서 원핵세포와 진핵세포의 리보솜 의 작은 하위단위체에 작용하여 단계 C2 를 막음으로써 두 생물계들에 서의 풀리펩티드 사슬의 개시를 방해한다(그림 7-5). 높은 농도에서 이 항생물질은 큰 하위단위체와도 상호작용함으로써 연장에도 이차적인 효 과를 미친다. 7.5 연장반응의 방해물질들 진핵세포계들에서의 폴리펩티드 연장은 EF-1- 의존적으로 일어나는 아 미노아실-t RNA 의 결합(단계 d), 리보솜의 촉매작용으로 일어나는 펩
티 드 결합의 형성 (단계 e), 그리고 EF-2- 의존적 으로 일어나는 자리옮 김 (단계 f)들과 같은 순차적 으로 일어나는 세 단 계들 로 이 루 어지는 반 복되는 회로에 의해서 일어난다. 첫번 연장 회로에 있어서는 단 계 C2 에 서 형성되는 개시 복합체 이의에도 두 분자의 GTP, 특이한 아미노아 실 -t RNA 및 연장인자 EF-2 들이 필요하다. 5.2.1 절에서 기술한 바와 같이, GTP 와 EF-1- 의존적으로 일어나는 틀 아미노아 실- t RNA 의 리보솜의 A 자리에의 결합에 관해서는 많은 실험 적인 증거들이 알 려져 있다. 비효소적으로 일어나는 아미노아실-t RNA 의 A 자리에의 결합은 또한 EF-1 이 없는 데에서 무세포 계에서 연구 할 수 있다. 펩티드 결합 형성 (단 계 e) 는 60S 리보솜 하위단위체의 한 구성성분인 펩티딜 기 전달효소에 의해서 촉 매된다. 자리 옮김 (단계 f)은 EF-2 를 필요로 하며, 리보솜 상에서 mRNA 의 삼중체 하나가 이동 하 는 것과 짝 지어져서 펩티딜-t RNA 가 A 자리에서 P 자리로 이동한다. EF-2 의 방 출 에는 1 몰의 GTP 의 가수분해가 요. 구된다. 무세포 계에서는 자발적인 비효소적 자리옮김이 연장인자들과 GTP 가 없는 데에서 천천히 일어난다. 이 비효소적 자리옮김은 K+ 또 는 NH4+ 의 높은 농도에서는 상당히 촉진된다. GTP 와 복합체 를 이룬 두 연장인자들 (EF-1 과 EF-2) 은 리보솜의 큰 하위단위체의 공통되는 부위 또는 중첩되는 부위와 상호작용하는 것~ 로 보인다. 따라서 두 인자들이 등시에 리보솜과 상호작용할 수는 없고 서로 번갈아서만 리보솜과 상호작용할 수 있다. 그러므로, 두 연장인자 들 중의 하나는 다른 인자가 방출된 다음에야 리보솜과 상호작용할 수· 있다. 7. 5. 1 아미노아실-t RNA 인식 (단계 d) 을 방해하는 물질들 이 화합물들은 크게 두 종류로 나눌 수 있다. 그 하나는 EF-1- 의 존 · 적으로 일어나는 아미노아실-t RNA 의 결합울 방해하는것이고, 다른굴l 나는 아미노아실-t RNA 와 리보솜의 받개 자리 사이의 찰못된 상호작용 을 유발시킴으로써 단백질 합성을 방해하는 것들이다. 테트라시클린류의 항생물질들은 EF-1- 의존적으로 일어나는 아미노아 실-t RNA 의 결합의 무세포 계에 있어서 강력한 방해물질로 작용한다壘
이 항생물질들이 주로 작용하는 곳은 작은 하위단위체인 것으로 생각된 다. 진핵세포에 있어서의 데트라시클린의 활동성은 박테리아에 있어서 의 활동성에 비교하면 매우 작다. 그 이유는 박테리아에서만 이 항생물 질이 능동적으로 수송될 수 있기 때문이다. 실제로, 테트라시클린류에 대해서 정항성인 박테리아의 돌연변이체들의 대부분은 바깥 막의 단백 질들 중의 하나에 변형이 일어나 있다는 것이 밝혀졌다 (Ta it와 Boy er , 1978). 푸시드산을 과량으로 첨가하거나 무세포 계에다 EF-2 를 국소량 첨가 하면 푸시드산은 자리옮김의 단계를 방해한다. 그 이유는 GTP• 리보 솜·푸시드산 •EF-2 가 형성됨으로써 푸시드산이 모든 EF-2 를 억류해 버리기 때문이다. 그러나 이러한 계에 있어서의 이 항생물질의 효과는 EF-2 의 포화농도에 의해서 소멸된다. 그렇지만 완전한 세포와 단백질 합성을 위한 동합된 계에 있어서는 이 항생물질은 사실은 EF-1- 의존적 으로 일어나는 아미노아실-t RNA 의 결합에 대한 방해물질로 작용한다. 왜냐하면 이 반응은 리보솜·푸시드산 ·EF-2·GTP 복합체를 가지고는 일 어날 수 없기 때문이다. 이 복합체는 비교적 안정하며 GTP·EF-1· 아미 노아실-t RNA 복합체 EF-2-GTP 에 의해서 점유되고 있는 자리와 중첩 하는 리보솜의 자리와 상호작용할 수 없다. 진핵세포의 리보송의 60S 하위단위체를 촉매적으로 비활성화시킴으로 써 단백질 합성의 연장 회로를 막는 것으로 알려진 많은 단백질 독소들 이 있다. 리신과 아브린, 그리고 그밖의 몇 가지는 당단백질류이다. 알 과 사르신, 미토길린, 레스트릭토신들과 같은 세 화합물들은 60S 하위 단위 체 로부터 의 큰 rRNA (~28S rRNA) 의 3' 말단으로부터 320 개 의 누 클레오티드들을 찰라낸다는 것이 알려져 있다• 이러한 모든 경우에 있 어서 60S 하위단위체의 촉매적인 비활성화는 EF-1 과 EF-2 가 리보솜에 결합하는 천화력을 감소시키게 된다. 그러므로 이 독소들은 아미노아실 -tRN A 결 합 및 자리 옮김 을 방해 한다 (Olsnes 와 Refs n es, 1978) . 항생물질인 카르트레우신, 무코다당류인 헤파린, 아드레노크몸을 포 함한 아미노크롬류와 카테콜류의 많은 것들이 또한 EF-2- 의존적으로 일 어나는 아미노아실-t RNA의 80S 리보솜과의 결합을 방해한다. 박테리아의 무세포 계에서 오독을 유발하는 것으로 알려진 폴리아민 류, 스트랩타민을 함유하는 아미노글리코시드류, 몇 가지 유기용매 그 리고 고농도의 Mg 2+ 이온이 존재하는 데서 또 최적온도 이하에서 항온
반옹을 시켰을 때에도 진핵세포의 리보솜의 번역의 충실도가 매우 높다 는 것은 홍미있는 일이다. 그러나 데옥시스트렌타민 또는 데옥시스트 랩 타민의 몇 가지 유도체들은 박테리아와 진 핵 세포 그리고 무세포 계들에 있어서 오독을 일으키는 것이 알려져 있다. 7.5.2 펩티드 결합 형성의 방해물질둘 푸로마이신은 제일 보편적으로 사용되고 제일 찰 알려진 펩티드 결합 형성의 방해물질이다 . 이 항생물질은 원핵세포와 진핵세포의 리보솜의 큰 하위 단위 체 상에 있는 펩티딜 기 전달효 소 의 받개 자리에서 아미노 아 실 -t RN A 의 3' 끝(아미노아실-아데노신)의 유사체로서 작용한다는 것 이 잘 알 려져 있다. 푸로마이신은 펩티드 결합 형성 반응을 연구할 수 있는 간단한 방법을 제공한다. 이 푸로마이신 반응에서는 푸로마이신의 -NH2 기 가 주개 의 기 질 로서 fM et- tRN NMc t 또는 펩 티 달-t RNA 가 사 용될 때 해 당하는 아미 노산의 C- 말단과 결 합한다. 또는 〈조각반응〉에 서 는 fM et- 또 는 Ac-Phe- 또는 Ac-Leu- 울리 고누클레 오티 드의 아미 노산 의 C- 말단과 결합하게 된다. 푸로마이신의 구조와 작용에 관한 연구는 많이 이루어져 있으나 이 항생물질의 60S 하위단위체 상에서의 결합자 리에 관해서는 아직 명확한 결과를 얻지 못하고 있다. 요오도아세틸-푸 로마이신을 사용한 연구들에 의하면 L21, L26, L28, L29, L31 및 L36 둥 여러 단백질들이 상호작용하는 것으로 알려쳐 있다. 팹티드 결합 형성을 방해하는그밖의 물질들도 푸로마이신과 같이 60S 리보솜 상에서 작용한다. 이 방해물질들을 원핵세포와 진핵세포에 다 같이 작용하는 한 무리와 진핵세포에만 작용하는 또 한 무리로 나눌 수 있다• 첫째 무리에 속하는 아미세틴, 구게로던, 불라스티시단 s, 악티노 볼린, 안텔마이신 및 스파르소마이신 둥은 펩티딜 기 전달효소 중심의 받개 자리에서 작용한다. 그들은 리보솜 상의 결합자리에서 서로 배제 하며 또 푸로마이신 상호작용을 막지만, 푸로마이신과는 달라서 펩티드 결 합 형 성 에 있 어 서 받개 로서 작용하지 는 않는다 (Gonzalez 등, 1979) . 진핵세포의 리보솜 상에서의 펩티드 결합 형성을 선택적으로 방해하 는 물질들은 그들의 결합자리, 작용방식, 방해 범위 및 교차-저항성 등 이 서로 다르다. 예를 들면, 아니소마이신, 테누아존산, 브루세안틴, 나 르시클라신, 하르링토닌, 트리코더민, 베르루카린 A 및 리코린 등은
그들의 결합자리에서 서로 배제한다. 그렇지만, 브루세안틴, 하르링토 닌 및 베르루카린 A 등은 풀리솜 형성 이전에 일어나는 처음 몇 차례 의 펩티드 결합 형성만을 방해한다. 리코린류의 화합물들은 트리코더민 과의 교차-저항성을 가지고 있지 않으며, 테누아존산은 효모 리보송에 는 작용하지 않는다. 7. 5. 3 자리옮김 (단계 f) 의 방해물질둘 자리옮김 과정을 방해하는 물질들을 (1) 연장인자 EF-2 에 작용하는 것, (2) 40S 하위단위체에 작용 하는 것, 그리고 (3) 60S 하위단위체에 작용하는 것 둥 세 종류로 구분할 수 있다. Coryn ebacte r itt m dip lz t lz eria e ({3) 10•+ 와 Pseudomonas aert tgino sa 에 의 해서 각각 생산되는 디프테리아 독소와 PA 독소는 효소적으로 EF-2 믈 비활성화시킨다. 이 독소는 아래와 같은 반응으로 EF-2 몰 비활성화시 킨다. 디프테리아 독소의 방해작용에 관해서는 이미 5.3.3 절의 (나)항 에서 자세히 기술하였다. 데옥시스트렌타민을 함유하는 아미노글리코시드류의 항생물질, 그리 고 크리프토플례우린, 틸로크레브린, 에메틴 및 두불로신 들은 40S 하 위단위체와 작용함으로써 자리옮김을 방해하는 물질들이다. 데옥시스트 랩타민을 함유하는 아미노글리코시드류의 항생물질들은 자리옮김을 방 해할 뿐 아니라 정보의 오독을 유발시키기도 한다 (W i lhelm 등, 1978a; W ilhe lm 등, 1978b). 그뿐 아니라, 아미노글리코시드 항생물질들은 효 모 세포에 있어서 무의미 돌연변이를 표현적으로 억제할 수도 있다 (Palmer 등, 1979) . 페데린과 글루타리미드 군의 항생물질들은 60S 하위단위체와 상호작용 함으로써 자리옮김을 방해하는 물질들이다• 글루타리미드 군으로서 제 일 많이 연구된 것은 시클로핵시미드이다. 페데린과 시클로헥시미드는 모두 EF-2 의존적으로 일어나는 자리옮김뿐 아니라 I단 또는 NH4+ 의 다소 높은 농도에서 일어나는 비효소적인 자리옮김 (즉, EF-2 와 GTP 가 없는 데서 일어나는 자리옮김)도 막는다. 그러나 페데린은 시클로핵 지미드에 저항성이 있는 리보솜에도 작용하는데, 이것은 두 항생물질아 리보솜 상에서 똑 같은 자리와 상호작용하는 것이 아님을 의미한다•
7.6 진핵세포에서의 종결의 방해물질들 번 역 의 종결 단계 는 mRNA 의 사슬 종결 코돈 (무의 미 코돈) (UAA, UAG 또는 U GA) 이 인식되고 방출인자가 리보솜과 상호작용하도록 만듦 으로써 시작된다. 진핵세포의 계들에서는 단 한 가지의 방출인자 (RF) 가 단리되었으며, GTP 는 종결단계 g l 에서 필요하다• 방출인자가 인 식된 다음에는 큰 하위단위체의 펩티딜 기 전달효소는 그의 펩티딜 기 가수분해효소로의 작용성을 나타내어 펩티딜-t RNA 의 펩티딜 부분과 tR NA 부분 사이의 결합을 끊음으로써 펩티드 사슬이 방출되게 한다(단 계 g2) . 종 결이 완결되려면 자유 t RNA 가 방출되는 반응(단계 h) 이 추 가적으로 일어나야 한다. 진핵세포 계들에서는 아직 이 단계가 분리되 어 있지 않다. 종결 단계를 특이하게 막음으로써 단백질 합성을 방해하는 물질들은 아직 알려져 있지 않다. 그렇지만, 위에서 기술한 많은 방해물질들은 그들의 리보솜과의 상호작용의 결과로서 번역의 다른 단계들을 방해할 뿐 아니라 종결 단계도 방해한다. 예컨대, 테트라시클린류와 몇 가지 다 른 방해물질들은 단계 d 를 방해할뿐 아니라 종결 단계를 방해할 가능 성도 크다고 생각되고 있다. 펩티딜 기 전달효소는 펩티드 결합 형성에 관여할뿐 아니라 펜티딜 t RNA 의 가수분해 반응(단계 g 2) 에도 관여한다. 실제로, 펩티딜 기 전 달효소 를 방해하는 모든 물질들은 종결 단계도 방해한다. 그립 7-5 에 나타낸 바와 같이, 단계 h 에는 EF-2 와 GTP 가 필요할 것으로 보인다. 그러므로 EF-2 를 방해하는 물질과 GTP 의 어떤 유사 체는 또한 단계 h 를 방해할 것으로 생각된다. * 참고문현 Bag li on i, C., Mi nk s, M. A. , Maroney, P.A . (1978), Nalllre 273, 684. Bernardi, A., Leder, P. (1970), J. Bio l . Chem. 245, 4263. De Beth u ne, M. P. , Ni er haus, K. H . (1978), Eur. J. B i oc l1em. 86, 181. Bodley, J.W ., Lin , L., Hi gh land, J.H . (1970a), Bi oc hern. Bio f J !zys . Res. Commun. 41, 1406.
Bodley, J.W ., Zie v e, F.J. , Lin , L., Zie v e, S.T. (19 70b) , J. Bi ol . Che m . 245, 5656. Coop er man, B.S. (1978) , Bi o- orga nic Chemi st r y , vol. 4, p. 81, Academi c Press, New York. Cundliff e, E., McQ u il len , K. (1967) , f. Mo!. Bi ol . 30. 137. Cundliff e, E. (1971) , Bi oc hem. Bi op l zy s. Res. Commzm. 44, 912. Cundli ffe, E. (1972a) , Bio c / 1e1 11. Bi op h y s . Res. Com1111111. 46, 1794. Candli ffe, E. (1972b) , The Molecular Basis of Anti bio t i c Acti on , p. 278, Joh n W ile y & Sons, London. Cundliff e, E. (1978) , Natu re 272, 792. Cundliff e, E. (1980) , Ri bo somes: Str u ctu r e, F1111ct io11 , and Ge;1e ti c s (Ed. , G. Cham- bliss , G. R. Craven, J. Davie s , K. Davis , L. Kahan, M. Nomura), p. 555. Univ e rsit y Park Press, Baltim ore. Davie s , J., Davis , B.D . (1968), J. Bi ol . Chem. 243, 3312. • Fasano, 0., Bruns, W., Crechet, J-B ., Sander, G., Parmeg gian i, A. (1978) , Eur. J. Bi oc lzem. 89, 557. Gonzalez, A., Vazq ue z, D, Jim~ nez, A. (1979) , Bio c / 1i1 1 1 . Bi op l zy s. Acta 561, 403. Greenwell, P., Harris, R.J., Sy m ons, R.H . (1974), Eur. f. Bi oc / 1e m. 49, 539. Haenni, A.L ., Lucas-Lenard, J. (1968) , Proc. Natl . Acad. Sci. 61, 1363. Helser, T.L. , Davis , J.E ., Dahlberg, J.E . (1971), Natu r e New Ni ol . 233, 12. Helser, T.L., Davis , J.E ., Dahlberg, J.E . (1972), Natu r e Nez(/. Bi ol . 235, 6. High land, J.H ., Lin , L., Bodley, J.W , (1971), Bi oc hemi st r y 10, 4404. High land, J.H . , Howard, G. A ., Ochsner, E., Sto f fi er , G., Hasenbank, R., Gordon. J. (1975) , J. Bi ol . Chem. 250, 1141 . Hunte r , A., Jac kson, R., Hunt, T. (1977), Eur. J. Bi oc lzem. 75, 159. Iga r ashi, K., Ishit su ka, H., Kaji , A. (1969), Bi oc hem. Bio p l zy s. Res. Comm1111. 37, 499. Jay n es , E.N ., Grant, P.G., Gia n g ran de, G., W ied er, R., Coop er man, B.S. (1978) . Bio c hemi st r y 17, 561 . Ki no shi ta, T., Lio u , Y-F., Tanaka, N. (1971), Bi oc lzem. Bio p h y s . Res. Com1111111. 44, 859. Krassnig g, F., Erdmann, V.A ., Fasold, H. (1978) , Eur. f. Bi oc hem. 87, 439. Lai, C.J. , Weis b lum, B. (1971), Proc. Natl . Acad. Sci. 68, 856. Lewi s, J.A ., Falcoff , E., Falcoff , R. (1978), Eur. J. Bio c lzem. 86, 497. Modolell, J., Cabrer, B., Parmeg gian i, A., Vazqu e z, D. (1971), Proc. Natl . Acad. Sci. 68, 1796. NNii echr hoalsuosn, , DA.,. WN.i, e rC hoaoups ,e r mKa.Hn,. (B19.S7.3 ) ,( 19P7r8o)c .. FNEatEl .S ALceatdt. . 9S0c,i . 27003,. 2224.
Okuy am a, A., Yoshik a wa, M., Tanaka, N. (1970) , Bi oc hem. Bio p h ys. Res. Commun. 60, 1163. Olsnes, S. , Refs n es, K. (1978) , Eur. J. Bi oc lte m . 88, 7. Palmer, E., Wi lh elm, J.M ., Sherman, F. (1979), Natu r e. 277, 148. Pestk a , S. (1970) , Bi oc lt em . Bi op h y s . Res. Commlln. 40, 667. Pestk a , S. (1977) , Molec u lar Mechanis m s of Prote i a Bi os yn th e sis ( Ed. , H. Weis s -bach, S. Pestk a ) , p. 467, Academi c Press, New York. Pang s, 0., Nie r haus, K.H ., Erdmann, V.A., Wi ttm ann, H.G. (1974), 40, Sup pl. S28. Santo n , J.B., Sta n ley, W.M. (1978), Bi oc hem. Bi op h y s . Res. Commun. 84, 985. Skold, S. -E. (1983) , Nucleic Acid s Res. 11, 4923. Tait , R.C ., Boy er , H.W. (1978), Cell 13, 73. Tanaka, N., Ki no shit a, T., Masukawa, H. (1968), Bi oc lzem. Bi op l zy s. Res. Com- 1mm. 30, 278. Teraoka, H. , Ni er haus, K. H. (1978) , J. Mo!. Bi ol . 126, 185. Thomp so n, J., Schmi dt , F., Cundlif fe,E . (1982), J Bi ol . Chem. 257, 7915. Tocchin i - V alenti ni , G.P., Matt oc cia , E. (1968), Proc. Natl . Acad. Sci. 61, 146. Vazq ue z, D. (1979) , Ant ibio t i c Inhib i t or s of Prote i n Bi os yn tl ze sis , Sp ri n g e r- Verlag, Berlin . Weeks, D. P. , Baxte r , R. (1972) , Bi oc hemi st r y 11, 3060. Weis b lum, B., Demohn, V. (1970) , FEES Lett . 11, 149. W ihe lm, J. M., Jes sop, J. J., Pett it, S.E. (1978a), Bi oc hemi st r y , 14, 1149. W ilh elm, J.M . , Pett it, S.E., Jes sop, J.J. (1978b) , Bi oc hemi st r y 17, 1143. Zil b erste i n , A., Ki m chi, A., Schmi dt , A., Revel, M. (1978), Proc. Natl . Acad. Sci. 75, 4734.
색인
-1 갓 (ca p ) 갓을 결합하 는 단백질 구조 296 기 능 29-;, 346-8 형 성 29 6-7 개시과 정 , 원핵세포에 있어 서 개 시 인자 둥 319, 334 방해물 질들 415-9,435 30S 7 사 시 복합체 형 성 321, 334 30S·IF-1 •IF- 2• IF- 3 복합체 형 성 321 , 334 Shin e -Da lg a rno 연속 부분 인식 284-5, 290, 310, 324-31 GTP 가수분해 의 기 능 332-4 70S 개 시 복합체 형 성 331, 334 70S 티 보솜의 해 리 320, 334 개시과 정 , 진핵세포에 있어서 개시과 장의 단계들 33S-9 개시인자들 337-9 물 리 적 성질 342 개시자리 인식 324-31, 348-51 방 해 물질들 415-9, 436 보조개 시 인자들 340-42 40S 개 시 복합체 242 GTP 의 기 능 332, 334-45 개시인자들 원핵세포에 있어서 319, 334 진핵세포에 있어서 338-9 개시자리 인식 원 핵 세 포에 있 어 서 284-5, 290, 330, 324-31 진핵세포에 있어서 338-9, 349-51 개 시 코돈 13, 94-5, 283-5, 294, 317, 348-51 개 시 tR NA, tR NA 'Me f 결정구조 62-3
변형된 영기들 43-6 세포소기관에 있어서 90 역코돈 부분의 구조와 기능 8I 이차구조 64 입체구조 65 카수가마이 신의 방해 작용 I58 포르일메티오닐-t RN Af Me t 36- 7, Bo, 8I 화학적 변형 79 개 시 tR N A, tR NA;M•t 결칭구조 62 변형된 염기들 43-6 eIF-2 • GTP • Met- tRN Ai M •t 복합체 339 이차구조 63 tR NAm Met 와의 기 능적 차이 38 개 입 연 속부분 (int e r venin g seq ue nce) 297-9, 309 결합된 리보솜 253 계동수 228 고대 박테 리 아 134-40 과요오드산 산화 I9 교정 20-26 9S rRNA 137 E: 다단백질 293-4 다시 스트론성 (po lyc is t r o nic i t y) 279, 291-4 단백질-단백질 교차결합 I72-6 단일시스트론성 291-4 도킹 단백 질 206, 263 동요 현 상 (wobbli ng ) 14 변형된 염기들의 역할 53 확장 95 동종성 동족 복합체 (homolog ou s cog n ate comp le x) 74-8
동종성 비 동족 복합체 (ho molog o us noncog n ate comp le x) 74 -8 동수용성 tR NA (iso accep tor tR NA) 28,34,37 - 9 A'6 , N6- 디 메 틸 아르기 닌 216 디프타미드 385 디프테리아 독소 EF-2 의 ADP- 리보실화 384-5 2 렉틴 결합 249 리보솜 결합단백질 리보솜 수용체 257 리보포린 I 257 리보포린 II 257 막에 있는 2;6-7 리보송 단백질들, 원핵세포의 기능 246-8 단리 213 돌연변이 체 216-7 렉틴 결합 249 번역후 변형 249 산성 단백질 220-I 리보솜 단백질들, 세포소기관의 271-9 리보솜 단백질들, 원핵세포의 단리 108 돌연변이 I14-5 모양 123 변형 II3 삼차구조 I19-23 A 단백질 II2-3 이차구조 II5-8 일차구조 II0-1 종류와 수 107-9 티보솜 단백절들, 진핵세포의 기능 246-8 단리 213
돌연변이체 216- 7 렉틴 결합 249 번역후 변형 2I5_6 산성 단백질 220-1 인산화된 단백 질 2I9-20 일차구조 215 종 특이성 216-7 항생웅에 대한 처항 돌연변 이 216 리브송 단백 철 들의 공간배열 분석법 단백 질 -단백 질 교차결 합 17 2 -6 단백 질 복합쳐尺준의 형 성 176 면역전자현미경 사진법 16S-72 조립지도 172-82 중성 자 산란법 172-3 형광표지법 173 리보솜 단백질들의 성질 분석법 결정체 123 단백질 제한 가수분해 119-21 단백 질화학적 방법 !07 면역화학적 방법 !07 이차원 겔 전기이동법 107 리 보솜 RNA 들, 5S, 5. 8S, 9S, 12S, 16S, 18S, 23S, 28S rRNA 들을 보라 리보솜, 원핵세포의 결정체 !03 구조 102-5, I63-204 기 능 103-5 발견 102, 205 성질 IO2 St ef fle r 의 모형 187-94 진화 2II 리보솜, 진핵세포의 구조 209-12 Lake 의 모형 195-205 발견 205 성 질 102, 206-9 진화 21l, 217 학보송의 진화 21l, 217
리 보포린 I 2()6, 257 리 보포 린 II 206, 257 □ 막과 리 브송과의 결 합 256-63 도킹 단백 질 263 리브송 수 용체 259 신호 연속부분 259, 261 mRNA 의 역할 258 매듭 145 머 리 건 구조 282, 290 메 티 오닐 -tRN A/1'1 36-7 메 티 오닐 -tRN Am M et 38 면역전자현미경 사진법 168-72,243-6 e-N- 모노 메 틸 리 신 266 도노송 (m onosomc) 103, 210 무의 미 코든 (no nsense codon) 392-8 미토콘드리아에 있어서의 유전암호 94-5 동요현상의 확장 14,95 mt tR NA 의 구조 90-93 유전암호의 보편성 14,95 미토콘드리아의 rRNA 137, 143 미 토콘드리 아의 tR NA mt tR NA 를 보라 닙 반보존성 영 기 들 55-6 방출인자들 (release fac to r s) 분자량 399 GTPase 로서 의 작용 403 목이 성 39r, 399-402 방해물질들 구조식 420-21 도식 435-6 일람표 412-4, 4r5-9 방해물질들, 개시과정의 원핵세포에 있어서 4r5-9,435
오린트리카르복시산 422 에데인 422 카수가마이신 422 팍타마이신 422 진핵세포에 있어서 2-(4- 메 틸 -·2, 6- 디 니 트로아닐 리 노) -N- 메틸-프로괴오나미드 438 쇼도마이신 434 아드레노크룬 434 아미노크롬 437 에데인 A 438 NaF 438 m'G5'p 438 eIF-2 를 촉 진하는 단백 질 437 이중가닥 RNA 437 트리페닐메탄 염료 434 팍타마이신 438 풀리비닐 437 KF 438 황산 풀리덱스트란 437 방해물질들. 구조식 구게토닌 42I 네오마이신 B 420 린코마이신 420 불라스티시던 S 420 스트랩트마이신 420 스과르소마이신 420 시클로핵시미드 42I 아미세틴 421 에리트르마이신 420 오스트레오그리신 B 421 오스트케오그리신 A 42I 카르보마이신 420 클로람패니콜 421 테트라시클린 420 티오스트랩돈 42I 방해물질, 연장과정의 415-9, 435-6 레스트릭토신 440
리신 440 미트걷린 440 스트랩타민 440 아미노크롬류 440 아브린 440 카르트레우신 440 카데콜류 440 테트라시클린 439-4o 풀리 아민류 440 푸시 드산 440 헤파린 440 방해물질들 자리옮김의 415-9,435-6 진핵세포에 있어서 글루타리미드류 442 데 옥시 스트랩 타민 442 디프테리아 독소 442 시콜로핵시미드 442 에메틴 442 크리프토프레오린 442 두불로신 442 틸로크레브린 442 페데린 442 PA 득소 442 방해물질들, 펩티드 결합 형성 원핵세포와 진핵세포에 있어서 구게토닌 441 불라스티시단 441 스파르소마이신 441 아미세틴 441 악티노볼린 44I 안델마이신 441 푸로마이신 441 진핵세포에 있어서 나르시클라신 441 리코린 441 베르무카린 A 441 브루세안틴 441 아니소마이신 441
테누아존산 441 트리코더민 441 하르링토닌 441 3 - (4 - 벤 질 페 닐 )-프로피 오닐 -P he-tR ?\A 펩티 딜 기 전달효소 영역의 탐침으 로서 161 번역 후 변형 215-6, 219 변형된 누 클레 오시스듄 rRNA 125, 136, 222- 4, 225, 231 tR NA 46-53 보조개시인자듄 340-2 보존성 염기들 55-6 人 4oS 개 시 복합체 339 mRNA 의 AUG 인 식 348-51 주사 모형 348-51 40S 하위단위체의 모형 210,245 Shin e -Dalga rno 연속부분 284-5, 290, 310,324-31 30S 개시 복합체 318, 321, 334 개시인자들 3I9 IF-2 의 재 이 용 33 I fM et- tRN A 'Mc t 의 결합 32I-4 mRNA 의 결합 32I-3I GTP 가수분해 의 역 할 322 30S 하위 단위 체 (subunit ) 의 구조 귓 불 (lob e) 166 목 I66 몸통 166 머리 166 면역전자현미경사진법 170 조립지 도 I77-8 플랫폼 I66 30S 하위단위체의 기능 영역 개 시 인자들의 결 합자리 I89, I9l, I97 암호문 해독자리 I87 A 자리 I89
mRNA 의 결 합자리 189 tR NA 의 결합자리 188 P 자리 188, 197 삼중체 (tri p le t) 13 3' 끝에 있는 번역되지 않는 연속부분 307 3' -치 싸임 (st a c kin g ) 204- 5 선 도 연 속부분 (lea der seq ue nce) 299 I2S rRNA I43 16S rRNA 단백 질 들과의 결 합 I46-8 NG, NG- 디 메 틸 아데 노신 I85 매듭 145 미토콘드리아의 I4E2 변 형된 누쿨레오시드 I36 사차구조 145-8 삼차구조 I45-8 Shin e -Dalga rno 연속부분과의 상호 작용 157-8, 284, 288, 290, 324-31 제 기능 영역 I43-5 스위치 I62 IF-3 과의 결 합 157-8 A·G 영기쌍 145 50S 및 30S 하위 단위체들의 회 합 I59 에리트로마이신 저항성 161 코돈-역 코돈 상호작용의 자리 로서 160 과로모마이신 저항성 160 <1 6S와 같은〉 rRNA 137 1sS rRNA 리보오스의 메틸화 136, 222 분자 크기 223-4 mRNA 의 개 시 코돈 인식 251-2 원핵세포의 16S rRNA 와의 상등성 142, 22.5 이차구조 142 일차구조 139
<18 S와 갇은〉 rRNA 222-3 0 아답터 I3 아미노아실아데널산 I6-7 아미노아실-t RNA 구조 17-20 리보송에의 결합 367 2' -에스데르와 EF-Tu•GTP 와의 인 식작용 20-21 EF-Tu•GDP 에 대 한 친화성 363 가 형성 I6-7 아미 노아실-t RNA 합성 효소 구조 28-33 기 질 목이 성 19, 26, 33-4 복수성 28 세포소기관의 28 이영역 구조 86 이 종성 동족 복합체 (hete r olog o us cog n ate comp le x) 74-8 이 종성 비 동족 복합체 (hete r olog o us noncog n ate comp le x) 74-8 일차구조의 상동성 3I 하위단위체 30 합성효소들의 조직 34 아미노아실화반옹 I6-7 교정 20-26 기질 특이성 26 분석법 27 양이온 의존성 27 에 스데 르화의 초기 자리 I7-20 RNA 이 어 맞추기 156, 296, 297-9 암버 돌연변이 395, 397 암호문 해 독 (decodin g ) 187 ADP- 리 보실화반응 384-5 A 자리 105, 360, 367-75 A 자리의 확인 374 A' 자리 372
mRNA, 세 포소기 관의 개입부분 309 단일시스트론성 308 Shin e -Dalga rn o 연속부분 310 종결코돈의 형성 308 mRNA 의 이 동 373-4 mRNA, 원핵세포의 개시 복합체 321-2 개 시 자리 284-5, 290 개시코돈 283 다시 스트론성 279, 293-4 머 리 핀 구조 282, 290 Shin e -Dalga rno 연 속부분 284-5, 290, 310, 324-31 종결 코돈 280, 289 mRNA, 진핵세포의 갓 296-7 개시자리 300-7 개 시 자리 인식 335, 337, 339, 34.5 , 3.5 1 -2 개시코돈 294 개입부분 297-9 다단백질 293-4 단일 시 스트론성 291-4 1sS rRNA 와의 결 합 25I-2 이어맞추기 298 전사후 변형 29.5 - 9 풀리 A 꼬리 299 역 코돈 (anti co don) 14, .51 -3, 59 고리 43, 204-.5 연장과정, 원핵세포의 방해 뭉질들 415-9, 435 A 자리 3_60, 368-7.5 연장인자들 36I-7 연장회 로 201-2, 360 EF-G 의 존적 GTP 가수분해 366 코돈-역 코돈 상호작용 367-8 GTP 의 기능 375
티 오스트 랩 돈의 방 해 작용 194 팹티 딜 기 전달 360 푸시 드산 365-7, 435 P 자리 360, 368-5 연장과정, 진핵세포의 방해 물질들 415-9, 436 A 자리 382 연장인자들 362, 376-83 연장회로 3S6 EF-2 의 존적 GTP 가수분해 :;82 코돈-역 코돈 상호작용 382 GTP 의 기 능 382-3 펩 티 딜 기 전 달 382-3 푸시 드산 383, 436 P 자리 382 연장인자들, 원핵세포의 기능 362-7 둘리적 성질 362 종류 362 연장인자들, 진핵세포의 기능 378-83 디 프테 리 아 독소 384-5 물리적 성 질 377-8 종류 362, 377-8 염기-독이적 화학적 변형 67-8 영 록체 의 rRNA 137, 143 50S 하위단위체의 구조 동마루 167-8 면역전자현미경 사진법 171 5S rRNA 의 결합자리 171 왕관형 166-8 조립지도 179-80 줄기 167-8 초승달형 167-8 코 167-8 콩판형 167-8 50S 하위단위체의 기능 영역 암호문 해독 I87
IF-2 와의 결합 198 A 자리 189, 249-50 연장인자들과의 결합 198 팹티딜 기 전달효소 중심 193-5,200 P 가리 189, 249-50 5S rRNA 원핵 세 포의 계동수 228 고대 박테 리 아의 5S rRN..\ 134-5 기 능 128, 132 누 클레 오시드 잔기의 수 134 단 백 질 등 과의 결합 133 나 단 백 질 들에 의한 형태 번화 133 삼차구조 128-30 스위치 162 50S 하위 단위 체 와의 결 합 171, 186 이 차구조 124-34, 236 일차구조 124-34 5S rRNA, 진핵세포의 계통수 223 기 능 231, 249-50 단백질들과의 결합 235-7 누클레오티드 찬기의 수 134, 228 삼차구조 128-30 ATP 가수분해 249 이 차구조 124-34, 226-7 일 차구조 124-34, 226-7 P 자리 의 구성 성 분으로서 247-8, 249 5. 8S rRNA 기능 231, 250 단백질과의 결합 235-7 누클레오시드 잔기의 수 231 이차구조 233 일차구조 229-30 A 자리의 구성성분으로서 231 P 자리의 구성성분으로서 250 오크르 돌연변이 394-5, 397 오팔 돌연변이 394-5, 397
5' 끝에 있는 번역되지 않는 연속부분 300-7 5' 치 싸임 204-; 원 시 진 핵 체 (ur karyo te ) 140 원편광 이색분광범 JJ7 -8 유전암호 제포질에서의 I3 미토콘드리 아에서의 93-4 브편성 I3, 94-5 잘못 읽 기 를 항생 뭉질들 160, 425-6 60S 하위 단위 체의 모형 2J O 2- 이미노타올란 I74 이 소 -1- 시 토크롬 C .29 4-5, 306 23S rRNA 사차구조 및 삼차구조 185-6 스위치 I49 이차구조 I49-55 결제 I49 축소 I49 일차구조 I49-55 찬기의 수 I37 GTPase 작용 I6I-2 티오스트랩돈 I6I 저 항성 161, 432-4 GTPase 방해 I6I, 424-5 <23 S와 같은〉 rRNA 137, 149 2sS rRNA 메틸화된 연속부분 223 변형된 영기들 222-4 분자량 222 이 차구조 137, 225 일차구조 137, 225 <28 S와 같은〉 rRNA 222-3 이 어 맞추기 (sp lic i n g ) 156, 296, 297-9 이 중선 별 교정 (double-sie v e edit ing) 24 이중체교정 24
': 자리 옮김 (tra nslocati on ), 원핵세포에 있어서 방해물질들 415-9, 435 mRNA 의 이 등 373-4 EF-G 의 역할 373 정의 105 GTP 의 가수분해 375 t RNA 의 L 자 구조의 돌쩌귀의 역 할 375 자리옮김, 진핵세포에 있어서 디 프테 리 아 독소의 작용 384-5 방해 물질들 384, 415-9, 436 분자적 메 카니 즘 384-5 EF-2 의 역 할 381-3 자유 리보솜 253 작은 각 분산법 165-6 전달 RNA tR NA 를 보라 전령 RNA mRNA 를 보라 전사후 변형 295-9 전자현미경사진법 166-8, 243-6, 256 결제 (amp u ta t i on ) 149 조립 지 도 (assembly map) 30S 하위 단위 체 l77-8 50S 하위 단위 체 178-82 조립 반응조건 177, 179 조립 순서와 유전구조 사이의 상관 성 181-2 종결과정 무의미 코돈 392-8 암버 돌연변이 395, 397 억 압인자 80-82, 394-8 억압작용 394-8 오크르 돌연변이 394-5, 397 오판 돌연변이 395, 397 방층인자들 결합자리 406-7 분자량 399
종결코돈 인식 402 GTPa se 작 용 4o3 득이 성 391, 399- 40 2 종결인자들 방 출 인자들을 보라 종결 코돈 39r-7 주사 모형 (scannin g model) 갓의 기능 349-51 ATP 의 필 요성 350-52 중금속 이온 2+7 중성자 산란법 I72 -3 축소 (amp u ta t i on ) r+9 축퇴* 성 (deg e neracy ) q 천화표지 161, 190-5, 24S 70S 개 시 복 합체 의 형 성 333 IF-2 와 IF-1 의 역 할 334 70S 리 보송의 해 리 320 70S 입 자의 기 능 영 역 200 R 자리 202-4 A 자리 202 mRNA 의 결 합자리 195-8 tR NA 의 결합자리 203-5 tR NA 의 인식 메 카니 즘 202 궁 P 자리 202 = 코돈 개 시 코돈 13, 94-5, 283-5, 294-5, 317,348-51 동요현상 I4,95 제포질에서의 I3 미 토콘드리 아에 서 의 94-5 종결 코돈 I3, 94-5, 39I-7 축퇴성 I4 코돈요역 코돈 상호작용 14, 95, 367, 382 코브라 독액의 핵 산 가수분해 효소, RNase VI 83-5, 128
콜리 신 E3 157-8 클 로버 잎 모형 38-41 E tR NA 결정 구조 54-66 기능 36 tR NA 결정구조 54-66 기능 36 미 트콘드리 아 tR NA 90-93 발견 15, 36 번호매기기 39-41 변형된 누 클레 오시드 46-53 복 수 성 37 아미노아실화반응 16-7 억 압인자 tR NA 80-82, 394-8 역코돈 고리 39 염기의 보존성 43-6 이차구조 39-41 일차구조 39-4o 클 로버 잎 모형 38- 41 화학적 변형 67-9 tR NAA• P 결 정 구조, tR NA 의 결 칭 구조 를 보라 tR NAf \! et 견 칭 구조, tR NA 의 결정 구 조 를 보라 tR NAIMe t, 개 시 tR NA (원 핵 세 포) 를 보 라 tRN AGIY 결 정 구조, tR NA 의 결 정 구조 를 보라 tR NAi \1 e' 개시 t RNA( 진핵세포)를 보 라 tR NAmMet 37 tR NAPhe 결 정 구조 tR NA 의 결정 구조 를보라 mt tRN A 90-93 t RNA 의 결정구조
부머 랭형 67 스퍼틴의 역할 60 L 자형 54-8 역코돈 고리 59 tR NAA• P 65-7 tR NNMet 62-3 tR NAGIY 61-3 tR NAPh• 54-8 t RNA 의 형태분석, 용액에 있어서 상보적 인 올리 고누쿨레 오티 드의 결 합 70 -71 NMR 분광법 7I -3 화학적 변형 법 67-70 티오스트랩톤 결합력 194 구조식 42I 아미노아실-t RNA 의 리보송에의 결합 방해 I94 처 항성 I6L 432-4 펩티딜 기 전달효소 작용의 방 해 I94-5 .n: 80S 개 시 복합체 의 형 성 339, 352-3 리보송 하위단위체의 풀 342 80S 입자 막과의 결합 253-5 모형 2IO 물리적 성 질 206-8 재회합 254 크기 2IO 화학적 성질 209 펩티드 결합 형성 386 A 자리 368-75 A' 자리 372 펩티 딜 기 전달 368-73 펩티 딜 기 전달효소 368-73 P 자리 368-75
P' 자리 372 펩 티 딜 기 전 달 193-5, 360, 368-73 펩티 딜 기 전달효소 중심 368-73 구성 단백질 371 구성 rRNA 160-1, 372 모형 372 방해물질들 423 팹 티 딜-t RNA 368-73 펩 티 덜-t RNA 의 가수분해 방출인자의 역 할 405-6 펜티 딜 기 전달효소의 역할 404-6 포르밀메티오닐-t RNA 36-7 풀리 송 (po lys o me) 253-4 풀리송의 동결 423 풀리 (A) 꼬리 299 푸로마이 신 반옹 105, 369-70, 423 푸시 드산의 작용 365-7, 383, 436 프소랄렌 127, 183-4 플랫폼 (pla tf or m) 166 P 자리 105, 360, 367-75 , 381 P 자리의 확인 374 P' 자리 372 -lo 항생물질들에 대한 처항성 스트랩토마이신 432 에리트로마이신 161, 431 카수가마이신 I60, 43I
클로람페니콜 I60-I 티오스트렙톤 160,431-4 과로모마이신 I60 합성 효소-t RNA 복합체 등종성 동족 복합체 74-8 동종성 비 동족 복합체 74-8 이영역 구조 86-8 이종성 동족 복합체 74 -8 이 종성 비 동족 복합체 74-8 Vma 77-8 안정도 74 인단계 메카니즘 76-8 인식작용 79-80 tR NA 상의 변이가 복합체 형성에 미치는 영 향 80-82 형성의 이단계 메카니즘 76-7 형성의 엔탈피 75 형성의 엔트로피 75 형성의 분석법 75 광화학적 교차결 합법 82-3 절개 접근법 83 t RNA 의 돌연변이 80-82 핵산 가수분해효소에 의한 방법 83-5 합덴 I89 형광표지법 I73 혼성 무세 포계 (mi xe d cell-fr ee sys t e m ) 295
朴仁源 서울대학교 문리과대학 화학과 및 同대학원 졸업 벨기에 겐트대학교 졸업 (이학박사) 캐나다 국립연구원 연구 7석 원 미국 위스콘신대학교 분자생뭉학교실 방문교수 프랑스 국립보건의학연구원 연구원 현재 서울대학교 자연과학대학 화학과 교수 역서 『생화학』 대 우학술총서 자연과학 36 단백질생합성 1986 년 6 월 1 일 찍 음 1986 년 6 월 15 일 펴냄 지은이 朴仁源 펴낸이 朴孟浩 펴낸곳 民音社 우편대체계좌번호 010041-31-523282 110 서 울 종로구 관천동 44~1 734-4234•6110( 편집 부) 734-2000, 735-8524( 영 업 부) 춘판등록 1966.5.19 게 1-1 42 호 틀 과본은 바꾸어 드립 니 다. 값 9,.C O O 원
대 우학술총서 • 자연 과 학 l 소립자와게이지상로삭용 金鎖퓸 폼/값 3,600 원 2 動力學特論 李炳昊/값 5,400 원 3 질소고정 宋承達 폼/값 2,800 원 4 相轉移와臨界現象 김두절 물/값 2,800 원 5 觸媒作用 陳宗植 뭄 / 값 2. 800 원 6 뫼스 H 유어分光學 玉恒南 픕/길 2.800 원 7 국기량원소의 영양 昇正子 뭄 /~ 16.500 원 8 *秦{t를와 有禮틀慕{t合物 尹能民 물 / 값 5, 000 원 9 抗生物質의 全合成 姜錫久 폼 /~19.000 원 10 국소적 형태의 A tiy ah-S inge r 지표이론 지동표 뭄 / 값 2,800 원 11 Muco po l y sacchar i des 의 生{t릎 및 生物理릎 박준우 著 / 값 3. 800 원 12 AST~OPHYSICS ( 天體物理學 ) 洪承村 뭄 / 값 4. 7 00 원 13 프로스타굵堅 합성 숲 한표 뭄 / ~1 3. 600 원 14 천연물화학연구법 禹源植 쭙 / 값 7, 000 원 15 脂訪營養 金淑룡 픕 /값 6 .3 00 원 16 結晶化유리 金炳扇 픕 /;14 .500 원
