 金 炳盤
金 炳盤  金 炳盤
金 炳盤
저 자 는 일본 早岳 田 大學 응 용 화 학과 와 동 대 학 원 을 졸 업 하 고 , 박 사 학위를 취득했 다. 전공 은 無機合成과 유리 工學 이며, 현재 高麗大學校 工大 材料工學科 敎授로 재 직중 이다.
 結晶ft유리
結晶ft유리
 結晶化유리
結晶化유리
머리말 금세기 중반에 시작된 공업기술의 눈부신 발전에 따라 새로운 제 료가 계속 개발되었고, 이에 따라 공업기술도 더욱 전보되어 왔다. 그러나 기술이 진보함에 따라 재료의 품질에 대한 요구는 접접 가 ` 혹하게 되어 재료의 품질개량, 신재료의 개발이 더욱 강하게 요구 되고있다. Ceram i cs 는 내열성, 내화학성, 내마모성이 우수하며 이들 재료~ 는 매장량이 풍부한 천연자원을 사용하여 제조되고 있기 때문에 세 라믹스에 대한 기대와 관십도 더욱 깊어지고 있다. 結晶化유리는 유리를 재가열하여 유리 중에 미세한 결정의 집합 체를 성장시킨 재료이므로 造形性, 兩熱性, 爾化學性, 兩磨括性등 ~ 이 우수한 유리의 성질과 각종 전정의 특성을 겸비하게 되어 종래 의 유리에서는 기대하지 못했던 특성들을 가질 수 있기 때문에 새 로운 과학분야에서 광범위한 용도가 기대되는 재료라고할수있다• 結晶化유리논 他의 ceram i cs 와 비교하여 그 제조방법과 성질이 득이하기 때문에, 이 재료에 대한 올바론 이해가 앞으로의 연구, 개 발에 중요하다고 생 각된다. 本論著는 1 장 총론, 2,3 장은 결정화의 이론, 꾹尺은 제조, 5 장은 성질, 6 장은 응용, 7 장은 결정화유리의 중요성으로 구성되어 있다. 총론에서는 결정화유리가 어떤 재료인가를 이해하는데 도움이 되 도록 기술하였다. 2,3 장에서는, 유리 중에서 일어나는 결정화에 관한 이론을 정리 함으로써 결정화유리를 제조하기 위한 결정핵생성과 성장에 대한야
해를 돕고자 하였다. 4 장에서는, 결정화유리의 제조공정을 그 순서에 따라 설명함으로 써 유리의 열처리에 의한 분상, 핵생성, 결정성장 등의 각 과정을 이해할 수 있도록 하였다. 5 장은 각종 결정화유리의 물리적 및 화학적 성질을 미세구조적인 관접에서 實 例를 들어 설명하였다. 6 장은 독특한 성질을 가전 결정화유리가 전통적인 재료들과 어떻 게 대치될 수 있으며 최근의 기술적인 요구를 어떻게 만족시킬 수 있는가에 대해 實例몰 들어 설명하였다. 7 장은 결정화유리의 과학적 중요성을 기술함으로써 결정화유리의 미래상을 照明하여 보았다. 本論著는 P. W. McMi llan 의 Glass-Cerami cs 를 많이 참고하였으 나, 내용적으로는 더욱 충실하려고 노력하였다. 집필할 때의 의욕 과는 달리 이 논저를 완성한 후에 여러가지로 부족한 感 울 숨길 수 없다. 先學과 後學의 비판과 도움 가운데 이 책이 무기재료과학 분 야에서 조금이나마 제구실을 할 수 있기를 바란다. 끝으로 이 논저는 재단법인 대우재단의 지원으로 씌어졌으며, 이 에 깊은 감사를 드란다. I984 년 2 월 金炳尾
結晶化유리/차례
머리말 5 제 1 장 총론 1.1 결정화유리의 定義 • 11 1.2 결정화유리의 科學的 重要性 • 12 1.3 결정화유리의 技術的 重要性 • 13 제 2 장 結晶化 및 失透 2.1 유리狀態 • 15 2.1.1 유리의 生成條件 17 2.2 過冷却液體의 結晶化 • 33 2.1.1 結晶化過程 33 2.2.2 過冷却液體의 核生成과 結晶化 35 2.3 유리의 核生成과 結晶化 • 49 2.3.1 유리의 安定度를 決定하는 因子들 49 2.3.2 유리 중의 유리의 分相 50 2.3.3 유리의 失透 59 2.3.4 유리의 失透를 제어하기 위한 조건 68 제 3 장 結晶化를 제어하기 위한 結晶核 生成促進劑와 유리型 3.1 結晶核生成促進劑의 種類 • 73 3.1.1 金屬의 分離에 의한 核生成 73 3.1.2 酸化物의 分離에 의한 核生成 84 3.2 유리型의 選擇 • 100 3.2.1 熔融 및 成形時 유리의 擧動 1003.2.2 유리의 化學的 安定性 103
3.2.3 유리의 結晶化特性 104 3.2.4 결정화유리製造를 위한 유리組成 107 제 4 장 결정화유리의 製造工程 4.1 유리의 製造 • 112 4.1.1 유리製造用 原料 112 4.1.2 유리의 熔融 113 4.1.3 成形工程 114 4.2 徵細結晶인 세라믹의 生成 • 115 4.2.1 熱處理工程 115 4.2.2 熱處理工程의 硏究方法 128 4.2.3 결정화유리가 形成되는 條件과 結晶型 144 4.3 特殊결정화유리의 工程 • 153 4.3.1 感光性 결정화유리와 化學的 加工 153 4.3.2 유리의 表面結晶化 155 4.3.3 機械的 性質을 向上시킨 결정화유리 158 4.3.4 결정화유리의 複合物 159 4.3.5 切削用 결정화유리 160 4.3.6 配向性微細構造를 갖는 결정화유리 162 제 5 장 결정화유리의 性質 5.1 物理 및 化學的 性質 • 165 5.1.1 微細構造와 多孔度 165 5.1.2 密度 169 5.1.3 化學的 兩久性 171 5.2 機械的 性質 • 173 5.2.1 機械的 强度 173 5.2.2 彈性性質 1985.2.3 硬度 와 摩秏抵抗 205
5.3 電氣的 性質 • 208 5.3.1 電氣比抵抗 208 5.3.2 誘電性質 216 5.4 熱的 性質 • 231 5.4.1 熱膨脹 特性 231 5.4.2 耐火度 240 5.4.3 比熱 247 5.4.4 熱傳導率과 熱擴散率 248 5.4.5 耐熱性 249 제 6 장 결정화유리의 應用 6.1 一般 및 機械工學의 應用 • 257 6.1.1 日用品으로서의 應用 257 6.1.2 機械工學에서의 應用 258 6.2 電氣 및 電子工學에서의 應用 • 262 6.3 照明 및 光學的 應用 •275 6.4 航空―宇宙工學에서의 應用 • 277 6.5 核工學에서의 應用 • 279 6.6 醫學 및 관련분야에서의 應用 • 281 제 7 장 결정화유리의 연구 및 개발의 중요성 7.1 결정화유리의 硏究 • 283 7.2 工學 및 應用 • 287 색인 291제 1 장 총론 1.1 결정화유리의 定義 적당한 조성의 유리를 재가열함으로써 미제한 결정의 집합체 죽,. 磁器와 같은 多結晶體(p ol y c~ y s t a lli ne sol i d) 로 변화시킨 것을 結晶化 유리 (crys t a l l ize d gla ss, devit roc erami cs ) 또는 g lass-ceram ic s 라고 한 다. 결정화유리는 일반유리의 제조 및 열가공중에 발생하는 失透 (dev it r ifi ca ti on) 와는 달리, 유리의 조성 및 열처리를 제어하여 유리 를 결정화시킵으로써 우수한 성질을 가진 재료를 얻는다는 접이 종 래의 유리제조의 개념과는 다르다. 죽, 결정화유리는 유리를 출발 물질로 하여 그 대부분을 결정질로 변화시킨 것으로, 자기와 같이 결정성원료를 소성하여 그 일부를 유리화하여 소결시키는 생성과정 과는 정반대이다. 결정화유리가 발명되기 이전에는 유리 중의 결정석출은 모두失透 타고 하여 유리의 미관을 해치며 강도를 저하시키는 원인으로, ::L 방지에 힘써 왔다. 그러나 1950 年代 중반에 美國 Corn i n g社의 Sto - oke y l) 가 感光性貴金屬인 Au, Ag , ' Cu 둥을 結晶核形成粹 l 로 첨 가 하여 만든 感光性結晶化유리 (ph oto s ensit ive g lass-ceram ic s) 를 발명한 以來 결정화유리의 製造, 改善, 新種의 發明 등 응용면에서 많은 연구대상이 되어 왔을 분만 아니라, 유리의 結晶化過程율 동해 原
1) S. D. Sto o key, Ind. Eng . Chem. , 45, 115 (19 53).
유리 (moth er g lass) 의 본질을 규명하기 위한 기초적인 연구의 대상으 로도 취급되어 왔다. 成形이 용이하고 尉藥品性, 雨熱性이 좋은 유리의 목칭을 회생하 지 않고 유리의 缺點울 보충하는 것으로 기대되고 있는 것이 결정 화유리이나, 반드시 유리의 성능을 높이는 데 그치지 않고 종래의 유리에서 보지 못했던 새로운 성질을 결정화유리 중에 구비시키는 방향의 연구도 각 방면에서 연구되고 있다. 결정화유리의 一般特性은 다음과 같다 .2) a) 유리상태로 성형하기 때문에 복잡한 形狀의 것을 얻을 수 있 으며 空孔울 함유하지 않는다. b) 결정의 크기를 제어함으로써 0. 02~1µ 정도의 微晶集合體가 얻어질 수있어 기계적 강도가크다. 또 o.1µ 이하의 결정을약 70% 이상 석출시키면 透明한 것도 얻을 수 있다. c) 유리조성에 따라 석출결정의 종류를 결정할 수 있어 熱影服係 敷를 어느 정도 조철할 수 있다. 1.2 결정화유리의 科學的 重要性 결정화유리의 연구는 過冷却液體의 核形成 및 結晶化에 관한 연 구와 깊은 관계가 있다. 유리질 액체는 結度가 크기 때문에 핵형성 및 결정성장이 비교적 느리며 따라서 摘散過程과原子再配列과 같은 기초연구에 많이 이용되는 재료이다. 결정핵생성 및 성장과 無定形相의 분리에 관한 연구와는 깊은 관 계가 있어, 구조변화에 따른 유리성질의 修飾 및 이들의 기초적 현 상을 조사한다는 관점에서 매우 홍미있논 과제이다. 또한, 유리의 결정 화과정 에 서 최 초의 分相(p hase se p ara ti on) 은 결정 화유리 의 생 성 및 유리의 안정성에 중요한 영향을 미친다. 準安定 및 安定相, 固溶體 둥 각종 결정형이 제어된 조건하에서 연구되었다. 특히, 용융유리논 대부분의 산화물, 일정금속, 할로겐 화물의 일부 및 화합물에 대해 우수한 용매이기 때문에 이들 副成
2) 作花 濟夫, 齊藤肇· 『無機材料化學 I 』 ::i P 于社, p. 490977).
分의 촌재 가 결정 핵 생 성 (crys t a l nucleati on ) 및 성 장과정 에 어 떤 영 향 울 미치는 가를 연구할 수 있다. 이런 연구는 결정화유리의 미세구 조에 대 한 연구와도 관련된다. 결정화유리는 미세구조를 가질 수 있고 각종 결정형을 함유할 수 있기 때문에 脇性固體의 기계적 강도 및 파괴과정의 기초연구에 매 우 유용하다. 또한 같은 화학조성의 출발원료를 가지고 제조조건에 따라 無定形유리로부터 거의 완전한 결정화유리까지 結晶度를 변화 시킬 수 있기 때문에 기계적 파괴분만 아니라 이온전도도와 같은 확산과정에 따른 성질에 관한 연구도 가능하다. 결정화유리에 관한 연구는 유리제조기술의 응용분야를 넓혀 주었 울 분만 아니라 각종 유리의 조성과 안정도와의 상관관계를 알 수 있게 되었다. 예를 들면 일반세라믹제품의 분야에서도 결정질성분 과 물리적 성질과의 상관관계를 연구하는 데 도움이 되었다. 결정화유리의 연구는 槪知結晶의 異常組合物율 함유한 재료를 만 둘 수 있고 이상유리조성의 실두에 의해서는 만듈 수 없다고 생각 되었던 아주 새로운 결정질을 발달시킬 수 있기 때문에 지질학자들 에게도 홍미있는 분야이다. 1.3 결정화유리의 技術的重要性 결정화유리의 제조는 먼저 용융 또는 可塾性인 유리를 만드는 일 로부터 시작된다. 만들어전 유리기구는 제어된 열처리주기에 의해 여러가지 相의 핵형성 및 결정화 (cr y s t a lli za ti on) 가 일어나 多結晶質 제라믹인 최종제품이 얻어전다. 이와 같이, 결정화유리의 제조방법 온 古典的 세 라믹 (conventi on al cerami c) 인 일반제 라믹 제 품의 제 조방 법과는 매우 다르기 때문에 수많은 중요한 장접을 갖고 있다. 용융유리는 균질한 조건하에서 얻어질 수 있기 때문에 결정화유 리에서 화학조성이 균일한 것이 쉽게 얻어질 수 있다. 母유리를 제 어된 열처리에 의해 균질화하면 기공이 없고 아주 미세하고 군일한 구조를 갖는 결정화유리를 얻을 수 있다. 이것은 기계적 강도를 높 이고 우수한 전기철연특성을 나타내는 방법으로 좋다.
결정화유리의 제조공정에서 중요한 특칭은 유리조성과 열처리공 · 정을 변화시키면 각종 결정을 얻을 수 있기 때문에 결정화유리의 물리적 성질도 변화된다. 예를 들면, 결정화유리의 열팽창계수를 熱衝擊에 강한 低熱彬眼係數의 것으로부터 일반금속과 같이 매우 큰 열팽창계수를 갖는 것까지 만들 수 있다. 壓縮, 吹入, 引出 둥의 유리제조방법이 결정화유리의 제조에도 . 사용될 수 있으며, 특히 얇은 벽을 갖는 空洞기구 (hollow-ware) 둥은 · 깨지기 쉬우나, 결정화유리에서는 열처리에 의한 결정화 때문에 비 교적 강한 제품을 만들 수 있다. 유리로부터 결정화유리를 만들 때 치수의 변화가 일어나나, 아 변화는 매우 작고 제어할 수 있다, 일반요업제품은 건조와 소성과 정에서 비교적 큰 수축을 일으켜 비틀림 (d i s t o rti on) 이 생기며 결과적 으로 결정화유리보다 최종치수를 제어하기가 더 어렵다. 결정화유리는 본래 유리이기 때문에 용융상태의 유리의 젖음상 (we tti n g)을 이용하여 비교적 간단히 다른 재료와 결합시킬 수 있다. 죽, 母유리를 적당한 재료에 封着 (seal) 한 후 열처리를 하떤 유리는 결정화유리가 된다. 이 방법은 세라믹-금속의 봉착방법으로 매우 유용하다. 최근에는 유리 중에 配向性微細構造의 결정을 갖도록 함으로싸 切削用 (mach i nable) 결정화유리를 만들었다. 따라서 전공듀브 外皮, 우주항공공학의 레돔 (radome), 금속의 보호막 등 상업적으로중요한 · 제품으로 사용되고 있다. 결정화유리논 설계기술자에게도 유용한 재료이다. 결정화유리는 무기 및 비금속재료이므로 높은 화학적 안정성 및 부식저항을 · 갖고 있어 고온에서 널리 이용될 수 있으며 이와 갈은 독특한 성질은 득 수공학의 응용에 매우 홍미 있는 것이다.
제 2 장 結晶化 및 失透 결정화유리는 유리를 결정화시켜 만들며 결정화유리 중에는 유리 相이 존재하기 때문에 이 장에서는 유리의 각종 특성에 대해 설명 한 후 유리의 결정핵형성 및 성장에 대해 설명하겠다. 2.1 유리狀態 유리는 硬性 , 剛 性 및 脇性을 갖는 두명한 물질이나, 액체가 갖 는 목성을 많이 가지고 있어 유리를 매우 높은 접도를 갖는 액체로 분류한다. 유리의 定 義 는 많으나 ASTM 에 의해 제안된 정의는 〈유리는 무 기질의 瑢融體 를 냉각할 때 결정화하지 않고 단단한 상태로 과냉각 될 수 있는 물질 〉 이다. 위의 정의는 결정화되지 않고 단단한 상태 로 과냉 각되 는 glu cose, gly c erol 과 같은 유기 질유리 는 제 의 되 었 다. 앞의 유리에 대한 정의에는 용융체의 냉각방법 이외의 방법, 예 를 들면 眞 空 蒸着 法 (vacuum evap o rati on me t hod) 에 의해 얻어전 無 定形物質도 포함하고 있다. 여기서 무정형물질이란 원자배열의 長 範園規則이 10nm 以上 촌재하지 않는다는 것을 말하고 있다. 이와 같은 정의를 따른다면 10nm 보다 작은 결정질로 된 다결정질고체 는 cm 당 1019 의 鉛缺! 읽 을 갖는결정질고체이나무정형이라고 할 수 있다. 융용체의 냉각방법 이외의 방법으로 만들어진 무정형물질을 계어된 결정화에 의해 결정화유리를 만들 수 없다는 이유는 없으나
거의 사용되지 않고 있다. 유리의 구조를 명확히 이해하기 위해서는 고체와 액체상태의 상 호관계를 이해하는 것이 좋다. 액 체 의 X- 線回折은 1 개 이 상의 폭이 넓 고 불명 료한 回折環 (d iffu se hole) 을 나타내므로 액체상태도 어느 정도의 규칙성을 갖고 있다고 할수있다. 이것은고체상태와같은 분자의 배열 또는 集團(g rou pi n g) 의 일부가 액체에서도 촌재한다는 것을 의미한다. 원자 또는 분자 집단의 구조단위는 결정형고체나 액체에서도 같으나, 액체에서는 이들 단위가 규칙적인 방법으로 배열되어 있지 않다. 따라서 결정 형고체는 短範園 및 長範園規則을 모두 갖고 있으나 액체는 短範園 規則만을 갖고 있다. 순수한 물질의 楚融體룰 냉 각하면 一定疑固點에 서 固化 (so li d ifi ca ti on) 가 일어난다. 그러나 경우에 따라서는 결정화를 일으키지 않 고 옹고접 이하로 액체를 계속 냉각시킬 수 있으며 이때의 액체를 過冷却液體라고 하며 과냉각액체는 그 결정보다는 自由에너지가 높 으나 액 체 상태 의 자유에 너 지 보다는 낮기 때 문에 準安定狀態라고 한다. 유리상태 (gla ssy sta t e ) , 일반고체 및 액체상대간의 관계는 용융체 가 냉각되는 동안 일어난 현상을 근거로 이해할 수 있다. 결정화된 물질은 거의 일정온도에서 응고가 일어나며 이 온도에서 不連續的 인 체적변화가 일어난다. 또 응고가 일어날 때 열이 방출된다. 한 편, 유리상태로 냉각되는 물질은 불연속적인 체적변화가 나타나지 않고 액체상태로부터 고체상태로의 변화에 따른 발열효과도 볼 수 없다. 대신 융용체의 접도는 온도가 하강함에 따라 접차적으로 커 지며 결국에는 모든 실제적 목적으로 사용하기에 충분한 단단한 고 체와 같은 높은 접도를 갖는 물질이 된다. 따라서 유리상태는 액체 상태의 연장이며 일반액체상태와 다른 접은 높은 접도이다. 이런 이유 때문에 유리논 용융체가 액체와 같은 구조를 보유하면서 결정 화가 일어나는 온도영역을 지나 냉각되어지기 때문에 과냉각액체로 생각할 수 있다. 過冷却度가 증가함에 따라 평형고체와 액체상태 사이의 자유에너
지差가 커지나 온도하강에 따른 접도의 급격한 증가로 인해 결정화 에 필요한 구조적 再配列온 접차적으로 힘들어지게 된다. 다론 과` 냉각액체와 같이 유리는 준안정상태에 있는 물질이며 결정화가 일 어나면 더 낮은 자유에너지를 갖게 될 것이다. 그러나 유리는 상당 히 제한된 온도범위를 제의하고는 완전히 안정된 상태로 보인다. 유리의 많은 성질들은 유리가 액체와 같은 성질이라는 것을 확증 시키고 있다. 예를 들면, 유리의 두명성, 이것은 고체의 결정상태 에서보다는 액체상태에서 보통볼수있는 특성이라고 생각된다. 비 금속단결정에서는 종종 두명성이 나타나나 다결정질물질에서는 나 · 타나지 않는다. 유리의 두명성은 빛을 散亂하는 원인이 되는 粒界 (gr ain boundary) 또는 包接物 (inc lusio n ) 이 전연 없 기 때 문이 다. 유리 의 X- 선회철모양은 실제적으로 액체에서 나타나는 것과 구별할 수 없으며 이로부터 유리가 액체와 같은 성질을 갖고 있다고 확신할 수 있다. 유리는 等方性(i so t ro pi c) 이다. 유리의 성질들은 측정하는 방향에 따라 좌우되지 않는다. 이와 같은 둥방성도 결정구조보다는 액체구조에서 볼 수 있는 특성이다. 유리구조는 Na+ 와 같은 작은 입 자들을 두과시 킬 수 있 어 電解質傳導體 (elec tr ol yti c conduc t or) 로 가 동한다. 이것은 액체와 같은 開構造와 깊은 관계가 있다. 비슷한· 현상으로 수소 및 헬륨과 같은 보다 작은 기체원자들을 두과시키는 유리도 있다. 2.1.1 유리의 生成條件 (1) 構造的 考察 대부분의 산화물은 용융상대로부터 냉각시킬 때 결정화되나 일부 산화물들은 유리가 된다. 산화물이 유리를 생성하는 문제는 과학적 . 으로 홍미를 갖게 하며 유리생성을 좌우하는 기본원리를 이해하는 데 중요하다. 유리생성산화물에 대한 일반특성을 발견하기 위한 초기의 시도 중 다음과 같은 제 안들이 있 다. Goldschm i d t 1) 는 유리 를 생 성 하는 산
1) V. M. Goldschmi dt , Geochemi sc he Verte i l u ng sg e setz e der Elemente , vii i, Vi d. Akad. (19 26).
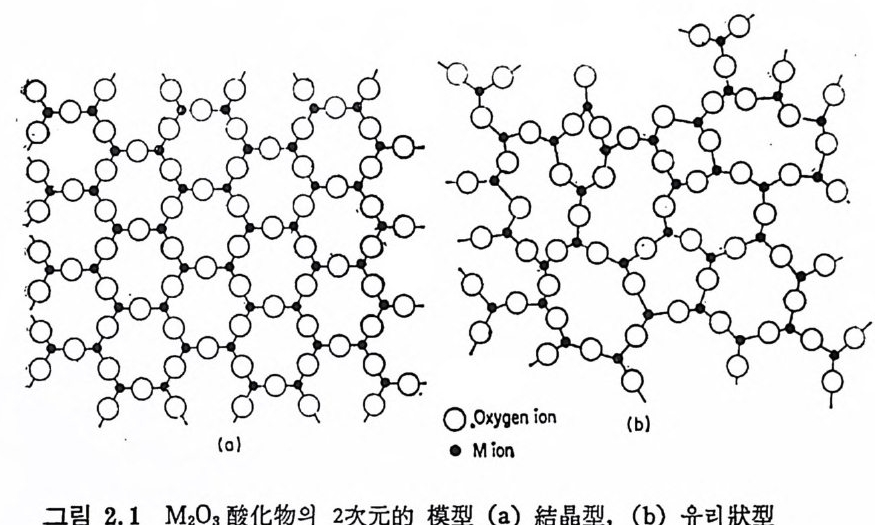
화물의 능력은 결정구조의 단위정을 형성하는 陽 이온주위의 산소이 온의 베열방법에 관계된다고 제안하였다. 죽, 안정된 결정구조에서 양이온주위에 인접된 음이온의 수(配位 數 )는 양이온과 음이온의 상 대적 크기에 의해 결정된다. 기하학적으로는 M x O y 의 산화물에 대 해 양이 온과 음이 온의 반경 비 RM/Ro 가 O. 225~o. 414 이 면 양이 온의 배 위 수는 4 가 되 며 산소가 중앙에 있 는 tet r a hedron 의 배 열 을 하게 된다. Goldschmi dt 는 Si0 2 , Ge02 및 P20s 와 같은 유리 생 성 산화물 에서 사면체배열은 결정상태에서 일어나며 이것이 유리生成能力 (gla ss-fo rm i ng abil it y ) 의 기 준아 된다고 생 각하였 다. 그러 나, Zachari ase n2) 은 사면체 배 열 을 형 성 하는 산화물의 능력 이 유리생성능력의 철대적 기준이 되지 않는다고 지적하였다. 그 이유는 예를 들면, BeO 의 이온반경비는 Be 이온주위에 산소이온이 사면체의 그룹들을 형성할 수 있지만 이런 산화물은 유리상태를 얻 울 수 없다. 따라서 Zacharlasen 은 유리 생 성 산화물들의 • 특성 에 대 해 더 상세히 조사한 결과 다음과 같은 유리구조의 不規則 網 目 構造 說 (random netw ork t heor y)을 제 안하게 되 었 다. 유리와 결정에서 원자상호간의 힘은본질적으로비슷하며 유리 중 의 원자들이 일정한 평형우1 치에서 전동한다는 기본원리로부터, 유 리에서도 결정체와 같이 원자들이 3 次元的 網目型으로 연결되어져 야 한다고 推理하였다. 또 유리에서의 網目은 규칙적이 아니며 유 리상태에 있는 물질의 에너지는 결정망목을 가전 물질의 에너지와 크게 다르지 않아야 한다고 제안하였다. 이것은 유리나 결정체에서 의 구조단위들이 실제적으로 同一하다는 것울 의미한다. 결정체에 서 이런 구조단위들은 규칙적인 格子(l a tti ce) 를 만들지만, 유리에서 는 불규칙망목구조로 인해 구조단위들이 非周期的으로 배열되어 結 合角이 비틀려진 모양이 된다. 그림 2.1 은 M2 아식으로 나타내는 산화물의 규칙적인 격자와 불 규칙망목구조와의 차이를 나타낸 것이다. 두 경우 모두 구조단위는 M03 삼각형이다. 유리는 산소가 상당히 규칙적인 多面 體 (p ol y hedra) 로 배열되어 있기 때문에 短範園規則울 갖지만 長範園規則온 없다.
2) W. H. Zacharia s en, J. Am. Ceram. Soc. , 54, 3841 (19 32).
 Q, Oxyg e ni on (bl
Q, Oxyg e ni on (bl
유리에 대한 이런 견해는 유리의 액체와 같은 성질과 완전히 일치 한다. 그러나 그림 2.1 의 (b) 에 나타낸 구조는 (a) 의 결정격자로부터 상당한 離脫을 나타내고 있다. x- 선과 中性子散亂의 결과를 설명 하기 위해서는 걷합각의 미소한 변화에 의해 장범위규칙이 상당히 부족한 구조인 비주기적 망목구조가 생기기에 충분하다고 생각할 수 있다. 예를 들면 유리질실리카 (v itr eous s ili ca) 에서 S i一 0 一 S i 결 합각의 변호R 즌 단지 土 10% 정도이다. Zachari~ s en 은 유리 를 형 성 하는 MxO, 산화물에 대 해 다음과 같 온 조건들을 제시하였다. a) 산소원자는 2 개 이상의 M 원자와 결합할 수 없다. b) M 원자주위의 산소원자들의 수는 작아야 한다. 죽, 양원자를 둘러 쌓는 酸素配位數는 3 또는 4 이 다. c) 陽原子를 중십으로 하는 酸素多面體는 서로 各 原點에서 연결 되며 邊 또는 面울 共有하지 않는다. d) 산소다면체 는 各各 적 어 도 2, 3 개 의 頂點 (corner) 을 인접 하는 다면체와 共有하며 M-0 ―M 의 결합으로 된 연속구조가 3 次元的
으로 형성된다. M20 와 MO 와 같은 산화물은 Zachari as en 에 의 해 제 시 된 조간 울 만족시킬 수 없다. M203 산화물은 산소가 각 M 원자주위에 삼각 형을 형성하면 위의 조건을 만족하며, M02 와 M2 아산화물들은 산 소원자가 각 M 원자 주위에 사면체를 형성하면 조전을 만족시킬 수 · 있다. 용융체를 냉각할 때 유리를 형성하는 산화물들은 3 차원적인 불 규칙망목구조를 형성하는 능력이 있기 때문에 유리形成 酸 化物 또는 網 目 形成酸化物 (N:et w ork Formi ng , NWF) 이 라고 하며 Si0 2 , B2 아, Ge- 02, P20s 및 As2 아 둥이 그 대표적인 예이다. 유리구조를 고려할 때 유리구조내의 기능에 따라 2 가지 형의 산 화물로 구벌할 필요가 있다. 즉, 網目修飾酸化物 (ne t work modif ying ox i de) 과 中間酸化物(i n t ermed i a t_ e ·
 王〔 + No20
王〔 + No20
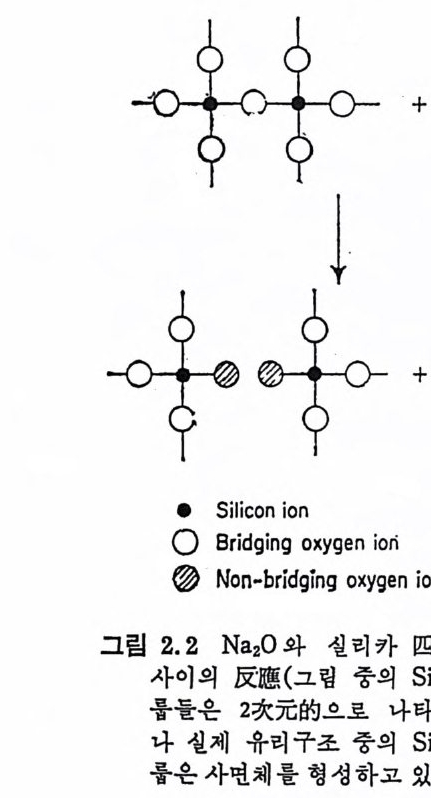
ox i de) 이 다. 망목수식산화물은 연속적인 망 목을만들수없는 것으로 유리의 망목상윤 약화시 키 며 Na20 가 ::::J.... 좋은 예 이 다. 중간산화물은 보통 _ 은 유리를 형성하는 능력이 없으 . 나 유리망목 중의 일부를 형성할 · 수 있는 것으로 AI2 아가 ::::J... 예이 , 다. 망목수식산화물의 여할을 알기 ’ 위해 Na20 를 실리카유리 중에 넣어 규산소오다유리 를 만들 때 그림 2.2 에 나타낸 것처럼 구조 .. 적 변화가 일어난다. Na20 와의 반응으로 2 개 의 Si0 4 , 사면체 사이를 연결하는 架橋酸 · 素이 온 (br i d gi ng oxy ge n ion ) 대 신 에 非架橋酸素가 생기며 이것들-
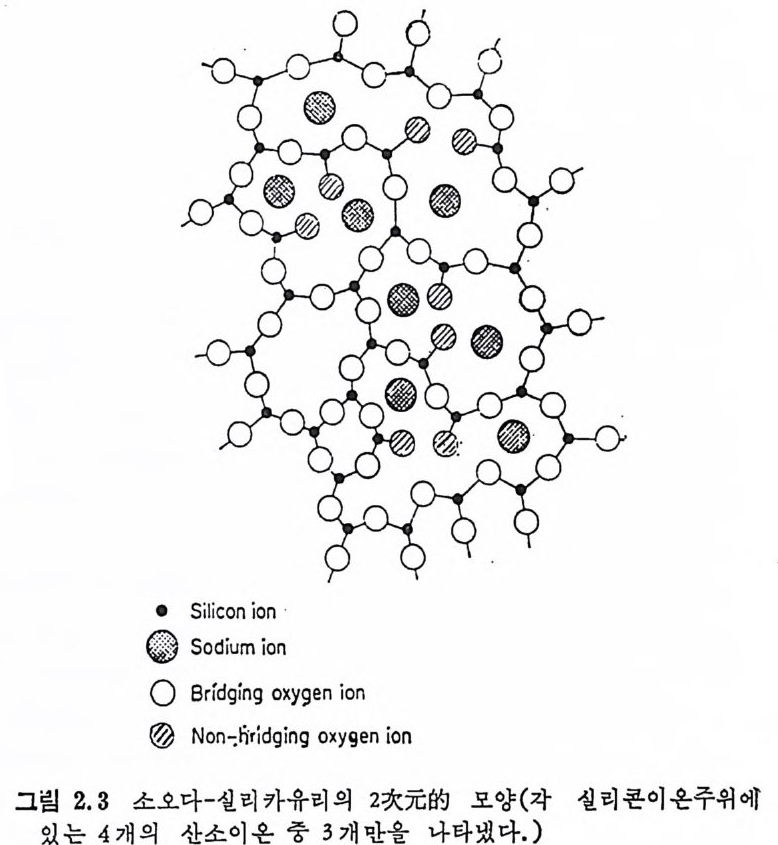
중 한 개의 산소는 Na20 로부터 도입된다. 따라서 Na20 의 도입~ 과는 연속적인 망목구조 중에 破裂部(g a p)문 만돈다. Na+ 는 아레 의 그림 2.3 에서 봉 수 있듯이 불규칙망목구조의 구멍 (hole) 이나 툼 새 (i n t ers tic es) 에 收容된다. 유리 중에 Na20 가 도입 되 면 유리 의 접 도가 감소를 하게 되고 열팽창계수가 중가를 하게 된다. 이들 영향 二 온 유리 망목구조 중의 걷합을 약하게 만든다.
 ®• SSioli dcio u n m i oion n
®• SSioli dcio u n m i oion n
다론 알칼리 금속산화를 죽, Li2 0 , K2~ 는 유사한 방법 으로 유랴 구조에 관여한다. Na+ 및 K+7} 커다란 구조적 름새에 수용되는것 에 비해 L i+은 보다 작은 구조적 듬새에 들어간다. Mg O , CaO 및 BaO 와 같은 알칼리 토류금속산화물도 유리 생 성능
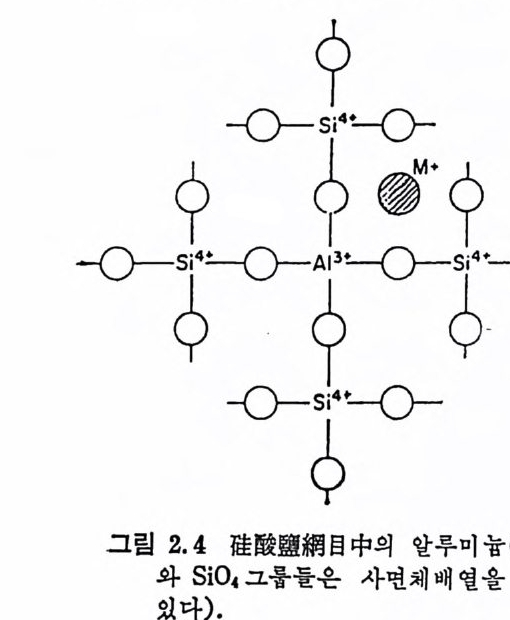
력을 갖고 있으며 금속양이온이 틈새에 위치하고 산소이온돌이 망 목형성이온들과 연결되어 유리를 형성한다. 2 價 陽 이온의 경우 1 개 의 양이온이 비가교산소이온들과 각각 쌍을 이루는 반면 1 價陽이 온에서는 2 개의 양이온이 비가교산소이온과 각각 쌍을 이룬다. 결정 또는 유리구조 중에서 알루미늄이온의 역할을 고려하여 보기 로하자. 결정체 중에서 알루미늄이온은 4 또는 6 개의 산소를 配位하므로 四面體 [AIO.J 또는 八面 體 [Al06] 의 그룹을 만든다. 사면체 그룹 온 그립 2.4 에서 나타낸 것처럼 규산영격자 중의 S i 04 사면체와 置換될 수 있다. 각 실리콘이온이 갖는 +4 의 電 荷에 비해 알루미 늄이온은 +3 의 전하를 갖고 있기 때문에 付加的으로 +1 의 전하 가 전기적 중성을 유지하기 위해 필요하다. Al04 사면체당 1 개의 알 칼리금속이온이 이런 요구를 만족시키기 위해 필요하며 알칼리이온 들은 사면체그룹 사이의 틈새에 수용된다.
이런型의구조배열은연 결된 Si0 4 와 Al04 그룹을 만드는 결정 인 長石(fe lds p· are) 과 :佛石 (zeo lit e) 과 같은 alumi no sil ica te 들에 서 볼 수있다. 다른 중간산화물로는 Be O(ber ylli a) 가 있 다. 유리 중 에서 이런 산화물은 Be04 사면체그룹을 형성함으로 써 불규칙 망목구조에 관여 한다. 이 경우 사면체당 2 개의 알칼리금속이온이 전 기적 중성을 유지하기 위 해 필요하다.
Ti0 2 나 ZrO 도 역 시 유리 망목구조에 관여 하는 중간산화물로 작 용하지만 망목구조를 형성하는 정확한 방법은 아직 규명이 되지 않
 亨
亨
고 있다. (2) 結合基準 유리형성 및 앞에서 설명한 유리구조 중의 산화물의 역할을 특성 화하는 기준은 본질적으로 기하학적인 것이었고 이온반경의 역할을 강조하였다. 그러나 양이온과 산소 사이의 결합독성도 기준의 역할 울 하고 있음이 분명하다. 산소와 높은 共有結合울 하는 산화물들 은 주로 이온결합을 하는 산화문보다 망목형성물의 역할을 한다고 생각할 수 있다. 양이온이 전자를 잡아 당기는 힘의 尺度 즉, 공유결합을 형성하 는 능력 은 이 온장강도(i on i c fiel d str e ng th) 인
 F=Z/ r2 (2-1)
F=Z/ r2 (2-1)
로 나타낼 수 있다. 여기서 Z 온 원자가이고 r 은이온반경이다. 표 2.1 에서와 같이, F 의 값은 Be2+ 이 망목형성이온의 분류一속어1 놓여지는 것을 제의하고는 유리구조 중의 각 산화물의 역할에 의해 분류할 수 있다. 이온장의 개념은 이온들이 단단한 球라고 가정하 고 있기 때문에 단순화된 견해를 나타낸다. 작은 전하를 갖는 큰 이온과 非 貴 金屬가스이온들은 변형될 수 있기 때문에 이런 개념은· 엄밀하게는 맞지 않는다. 그렇지만 이온장강도의 개념은 유리구조 중의 각종 이온둘의 역할을 이해하는 데 도움이 된다. 유리를 형성하는 능력에 따라 산화물들을 분류하는 또 다른 시 도가 있었다. S t anwo rt h” 는 결합의 공유-이온성질을 측정하기 위 해 양이 온과 산소 사이 의 電氣陰性度差를 계 산하였 다. Sun4) 은 生成熱로부터 單結合에너지를 계산하였고 Rawson” 은 이 개념을 확장하여 단결합에너지와 웅접 사이의 비를 계산하였다. 이와 같은 시도들은 쉽게 유리화 (v it reous) 상태를 얻을 수 있는 산화물과 그렇 지 못한 산화물 사이의 구벌을 할 수 있는 반면 유리생성문제를 아
3) •J . E. Sta n worth , Phys i c a l Prop e rti es of Glass, p. 215 Clarendon Press, Oxfo r d( l95 0). 4) . K. H. Sun, J. Am. Ceram. Soc. , 30, 없 70947). 5) H. Rawson, Proc. IV Int. Cong r . on Glass, Paris , 62, Imp ri m erie- Chaix , Paris ( l956).
표 2.1 유리 중에 존재하 는 腸 이온의 이온 場强度 : Ion Ionic ( Ara)i d u s sFtZri /ee rln 2dg h Strr oug lcleat su is rn a l B3+ 0.20 75.0 P5 + 0.34 43.2 Si• + 0.41 23.8 Netw orkfo r mi ng As5+ 0.4 7 22.6 IOns Ge.+ 0. 53 14 .2 Be2+ 0,31 20.8 AP+ 0. 50 12.0 Inte r media t e Ti H 0.68 8.7 IOi lS ZrH 0.80 6. 3 Mg 2+ 0.65 4. 7 Li+ 0, 6 0 2.78 Ca2+ 。 •99 2.04 Netw ork-m odif ying Na+ 0.95 1.11 IOns Ba2+ 1. 35 1.1 0 K+ 1. 33 0.57 해하는 데는 크게 기여하치 못했다. 앞으로 液體溶融物(liq u i d melt) 의 구조에 대한 더 깊은 이해와 결정화과정을 지배하는 動 力 學的 因子들 (k i ne ti c fa c t ors) 을 결정 하는 結合 및 原子配列에 관한 연구가 요망되고 있다. 불규칙망목구조이론은 유용한 개념이라는 것이 중명되었고 유리 의 구조와 성질 사이의 관계에 대한 개념을 발전시키는 데 중요한 기준이 되었다. 그러나 이 이론에도 한계가 있으며, 이 이론과 유 리 구조의 微晶說 (cr y s t a llit e hy po th esis ) 6) 의 이 론을 합성 시 킨 개 념 이 필요하다고 제안되어 왔다. 微晶說은, 유리는 일정한 화학조성을 갖는 매우 작은 무질서하게 배향된 결정들로 구성되어 있다고 가정 하고 있다. 이 이론은 확실히 너무 간략화시킨 것임에도 불구하고 유리구조는 그렇게 불규칙적이 아니기 때문에 불규칙망목구조설은
6) N. Valenkov and E. A. Porai- K oshit s, Z. Kris t . , S5, 195(1936) .
수정이 필요하다고 생각되었다. Jam es” 에 의 해 발표된 副顯微鏡的 相分離 (sub-m i crosco pi c ph ase se p ara ti on) 의 발견은 고사하고 Freeman 8) 둥에 의 한 高分解能電子 顯微鏡競察 로부터 유리와 비정질물질은 불규칙망목구조설에서 제시 된 것보다 더 높은 規則度를 갖고 있는 작은 區域이 있다는 사실이 일부 증거로 제 시되었다. 그러나 전자현미경으로부터 판단한다는 것은 논의의 여지가 많다는 사실을 명십하여야 한다. (3) 動 力 學 的 因子와 유리 형 성 위에서 논의된 것처럼, 주어전 산화물이 유리를 형성하는 능력은 그 산화물의 결정구조와 관계가 있다. 고체보다는 용융체의 구조와 성질이 유리형성의 支配因子가 된다는 것은 의문이 생간다. 그러나 대부분의 경우 액체 중의 단범위규칙은 고체에서와 같으며 산화물 용융체에서의 유리형성에는 단법위규칙을 갖는 특수형대의 것이 요 구되는 것 같다. 용융체와 결정질고체와의 차아는 주로 장범위규칙도의 차이에 따 라 결정된다. 따라서 결정화에는 장범위규칙이 결핍된 액체구조가 장범위규칙이 우세한 결정질구조로 변태되어야 한다. 유리형성을 일으키는 액체에서는 이런 변태 (t rans fo rma ti on) 는 비교적 어렵다. 액체가 결정으로 번대할 수 있는 속도는 다음과 같은 JM A ·O ohnson-Mehl-Avrami )9> 1°) 식으로 주어진다.
 X t =l-ex p(국 U3/t 4) (2-2)
X t =l-ex p(국 U3/t 4) (2-2)
여기서 X t는 t시간 후 결정화된 競積 分 率 , U는 결정성장속도, I 는 핵생성속도이다. 유리형성문제는 결정핵생성 및 성장속도를 지 배하는 인자들울 고려하여야 한다. 핵생성속도가 높으려면 결정핵 과 액 체 상(또는 유리 ) 사이 의 界面에 너 지 (int e r fa c ia l energy ) 값이 작 아야 하며 액체로부터 결정구조로 변태하는 데 따른 체적자유에너
7) P. F. Jam es, J. Mate r . Sci. , 10, 1802(1975). B) L, A. Freeman, A. Howi e, A. B. Mi str y and P. H. Gaskell, The Str u ctu r e of Non-C r ys t a l lin e Soli ds, r . 245. Talyo r and Franic s, London(l 'ifl7) . ].09)) MW.. AA. vJraomh ni s, oJn. aCndh emR., FP. hMys e. h, l, 70T2ra),n s1. 10A3I(1M 9 E39, ).1 35, 416(1 9 39).
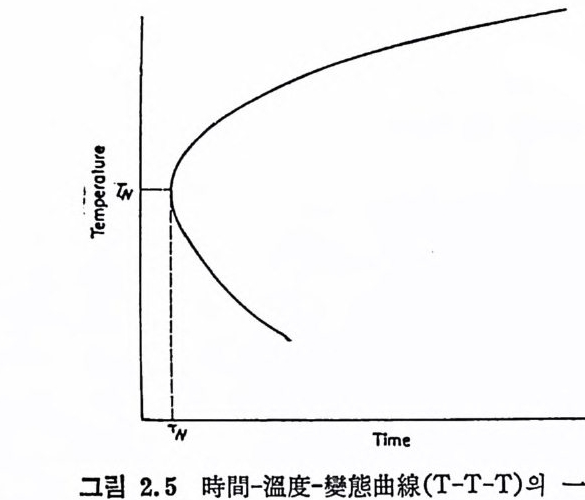
지의 변화가 큰 값이고 확산에 필요한 활성화에너지가 작은 값이어 야 한다. 유사하게 결정성장속도가 큘려면 결정질상태로 변태함으 로써 생기는 체적자유에너지의 값이 커야 하며 액체와 결정상 사이 의 계면을 가로지르는 원자들과 會 合하는 활성화에너지의 값이 작 아야한다. Uhlmann11) 은 유리 형 성 에 대 한 동력 학적 인자들의 영 향을 이 해 하기 위해 T-T-T(tim e-te m p er atu r e-tr a nsfo r mati o n ) 曲 線 을 사용하였 다. T-T-T 곡선에서, 일정한 체적분율을 결정화하는 데 필요한 시간을 過冷却度 4T 에 대해 취하면 그립 2.5 와 같은 모양이 된다.
 •m10,&eaL
•m10,&eaL
이 곡선에서 선덱된 체적분율이 결정화하는 데 필요한 시간 아 最小인 온도 TN 에 주시하자. 이 온도는 결정화가 일어나지 않는다 · 떤 臨界値를 나타낸다 .. Uhlmann 은 T-T - T 곡선상에서 체적분율이 X t =l0-6 값보다 작으면 결정을 感知할 수 없다고 제안하고 따라서 X《 10-6 인 재료는 유리狀이 된다고 결정하였다. 그는 핵생성속도 I 와 결정성장속도 U 의 측정값 또는 핵생성 및 결정성장속도석에 적합한 값들울 대입시킴으로써 계산된 값들을 사용하여 수많은 제i 료들에 대한 T-T-T 곡선을 유도하였다.
11) D. R. Uhlmann, J. Non-Crys t . Solid s , 1, 337(1 9 72).
유리생성능력을 평가할 수 있는 2 개의 양이 유도되었는데 이들 온 臨界冷却速度 Rc,
 &:::::JrN /T (2-3)
&:::::JrN /T (2-3)
로 주야지는 결정이 생기지 않고 냉각되는 재료의 臨界두께 (cr iti ca i thi c k ness), Ye 이다. 여기서 D 는 熱摘散率(t hermal d iff us i v ity)이다. 각종 재료들에 대해 얻어전 임계냉각속도 및 임계두께는 표 2.Z 와같다. 표 2. 2 유리 形成에 대 한 臨界冷却速度 Rc 및 臨界두께 ,c 의 값 Substa n ce (KsReCc 크) (cymc ) I I Sil ica 2Xl0 기 400 Germaniu m dio x id e 7X 10-2 7 Salo! 50 7X 10-2 Wate r 107 1o-4 Sil v er 1010 10-s (4) 유리의 化學組成 多成分系유리를 만들기 위해서는 유리狀의 조건을 갖추고 있는: 산화물이 필요하다. 가장 중요한 유리 형 성 산화물은 Si 02 , B2 야 및 P20 근]다. 일반유리의 조성온대부분 규산영이나붕규산염이다. 순· 수한 실리카유리는 낮은 열팽창계수와 높은 軟化點울 갖고 있어 열 충격 및 처항이 필요한 곳에 유용하게 사용될 수 있어 매우 가치있 는 재료이다. B203 와 P2°5 는 물에 의해 쉽게 침식되기 때문에 살 용적인 면에는 사용할 수 없으나 과학적인 관심을 끌고 있다. 다성분계유리에서는 촌재하여야 하는 유리형성산화물의 最低限界 比(l ower lim i ting p ro p or ti on) 가 있다. 가능한 유리조성의 型울 생각 하고 가능한 조성의 범위를 제한하는 因子들에 대한 연구는 흥미있 다. Si 02 , B203 또는 P20s 와 알칼리 금속산화물로 된 2 성 분계 유타 에서 가능한 알칼리금속산화물의 한계비가 촌재하며 이 한계비를·
넘은 용융체는 냉각중 결정화 또는 실두를 일으키게 된다. 限界組成의 촌재는 알칼리금속산화물의 양이 증가함에 다타 일어 나는 구조변화에 좌우된다. 비가교산소가 도입되면 점차 유리의 접 도는 낮아지며 결정핵생성과 성장속도를 증가시키게 된다. 또 비가 교산소가 군일하게 분포되어 있다면 S i 04 사면체당 평군가교산소의 수는 R20•S i 02(rne t as ili ca t e) 일 때 2 가 된다. 따라서 이 조성에서 Si 04 그룹의 고리 또는 무한히 긴 사슬이 되어 유리가 형성될 수 있다. 알칼리금속산화물의 양이 더 중가하면 사슬의 평군길이가 짧아지고 사슬이 파괴되어 쿵극적으로 망목형의 구조는 單一 S i 04 사면체가 존재하는 구조 (or t hos i l i ca t e 조성에서는 2R20·S i 02) 로 바뀌어 접차 유리 형 성 이 불가능하게 된다. 알칼리 금속산화물-실리 카계 에 서 Si0 4 그룹당 평 군가교산소수가 2 보다 작은 조성에서는 유리형성이 쉽게 일어나지 않는다는 사실온 홍미있는 일이다. 그러나 이와 같은 단순한 계산으로 용융물과 유 리의 구조를 엄밀하게 정의할 수는 없다. S i 04 그룹의 一團 (clus t er) 또는 사술들은 만일 고립 된 Si0 4 그룹이 존재 함으로써 각종 크기 의 음이온그룹을 갖는 구조를 가질 수 있다면 수식산화물의 양이 많은 조성의 유리도 존재할 수 있다 .12) 수식산화물의 도입에 따른 비가교산소의 역할이 고려되어 왔지만 첨가된 알칼리금속양이온의 성질도 중요하다. 높은 이온장강도를 가지며 작은 酸素配位數를 갖는 修飾陽이온들 온경 향보이다 더큰 크이다온고들 생보 다각할 주 수위 에있 다산. 소이이 런온 들경 을향 은질 서Li있20 게— S나i 02열 용시융키물는 이 다른 알칼리-실리카계보다 쉽게 실두된다는 사실로부터 증명된 다. L i 20 ― B2 아 계 에 서 는 R20 25mole%, . Na20 ― B2 아 계 에 서 는 33 ·m ole% 가 유리 형 성 한계 라는 결과가 2 성 분계 붕산영 에 서 관찰되 었 다. 비슷한 경향이 알칼리토류금속을 함유하는 2 성분계에서도볼수 있 으며 이것은 낮은 이온장강도의 이온들을 함유하는 용융체에서보다 마그네슘과 같이 이온장강도가 큰 이온들을 함유하는 용융체에서 실두가 더 찰 일어나기 때문이다.
12) H. L. Trap and J. M. Ste v ens, Phy s. Chem. Glasses, I, 107, 1810960) .
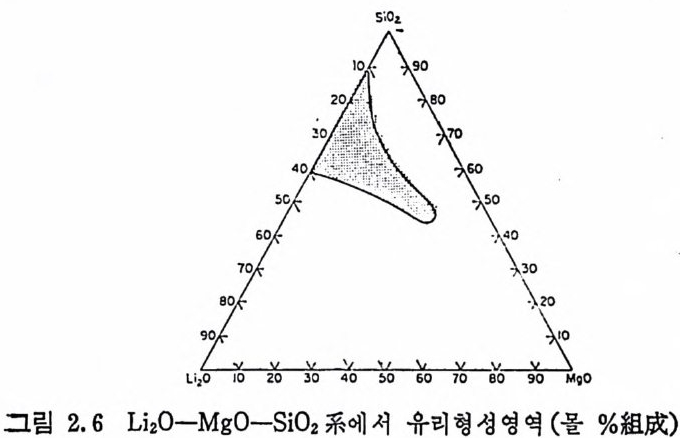
결정화유리로 변환될 수 있는 유리들을 고려할 때는 위에서 기술 한. 2 성분계보다 훨싼 더 복잡한 조성들에 대해 고찰을 하여야 한다. 그러나 다성분계들은 종종 3 성분계 중 비교적 한정된 수의 것을 수정한 것들과 같기 때문에 결정화유리조성의 기본을 이루는 몇 가 지 중요한 3 성분계를 고려하여 보자. 3 성분계의 복잡한 거동은 LL ii 22 00 ―— SNai0 22 0 ―또 는S i 아Na계2에0—서 S i볼0 2 계수 에 있 서으 보며다 이더 계많의은 유알리칼는리 금2 속성분산계화인물 울 함유하고 있다. 알칼리금속이온의 배위조건은 반경이 다른 이온 들이 혼합되어 있을 때 더 쉽게 만족될 수 있다. Li 20 ― M g O ― S i 02 의 3 성분계유리에서도 어느 정도 비슷한 결과 를볼수있다. 그림 2.6 에서와 같이, Li 20+M g O 의 全量온 55mole %까치 높일 수 있다. 이와 같은 유리형성한계조건에서는 L i+과 M g2+ 가 모두 망목수석 물로 톰새 에 들어 간다면 Si0 4 사면체 당 비 가 교산소이온의 평군수는 2.4 가 될 것이다. 이런 환경에서는 연속적 인 규산영망목구조는 촌재할 수 없으며 M g 2+ 의 일부는 망목형성물 의 역 할울 한다고 가정 하는 것 이 가능하다. 즉, Mg 2+ 이 Be2+ 과 비 슷한 거동을 한다면 사면체의 M g04 그룹에 관여하게 된다는 가능 성도 생각할 수 있다. Al2 아도 2 성분계규산염용융물이 실두되는경향을감소시킨다. 그 예는 그림 2. 7 에 나타낸 것과 같이, Li 20 ― S i아유리에서는 Li2 0 40
 -.,•o
-.,•o
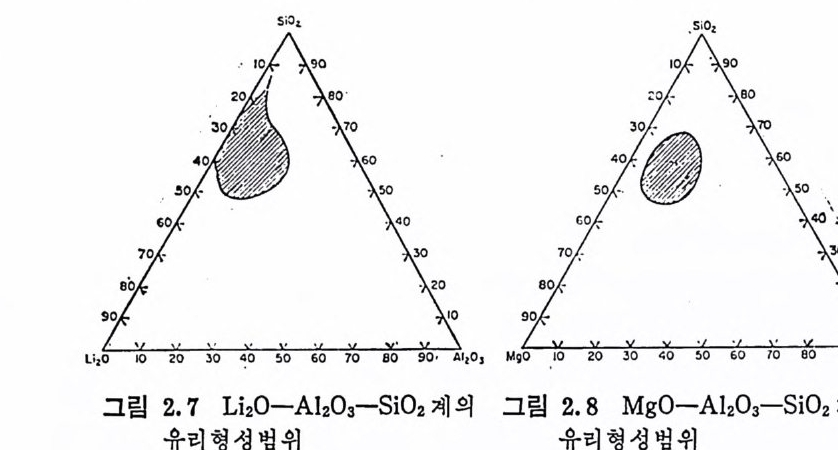
%가 유리 형 성 한계 인데 대 해 3 성 분계 L i 20 ― Al203 ― S i아 유리 에 서’ 는 Li 20 함량이 45% 까지 올라간다는 것을 알 수 있다. 이런 유리 에서 AI2 아의 比는 앞에서 논의한 전기적 중성조건을 만족시키기 위해 Al203 : L i 20 의 比가 1 : 1 를 넘을 수 없다는 조건에 의해 제 한을 받고 있 다. 또 다른 중요한 알루미 노규산염 은 M g O — Al2 아— S i 02 계로 그림 2.8 에 유리형성한계가 실려 있다.
 Si3 , .s;o ,
Si3 , .s;o ,
L i 20 ― ZnO ― S i O 며(그립 2.9) 에 대한 유리형성한계가 확장되어 있 는데, 이것은 ZnO 가 M g O 에서와 비슷하게 中間酸化物로 작용한댜
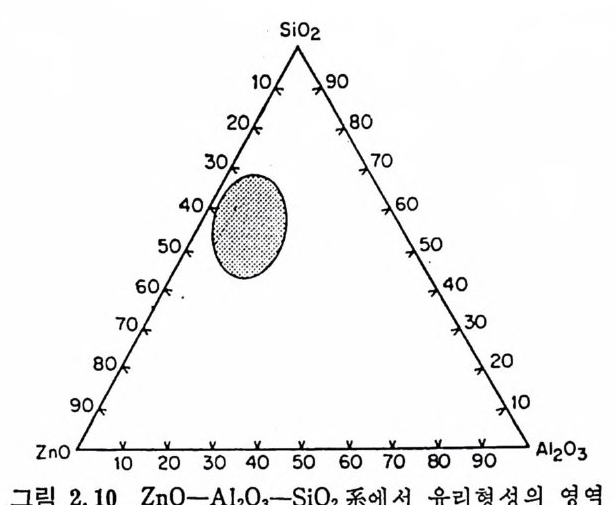
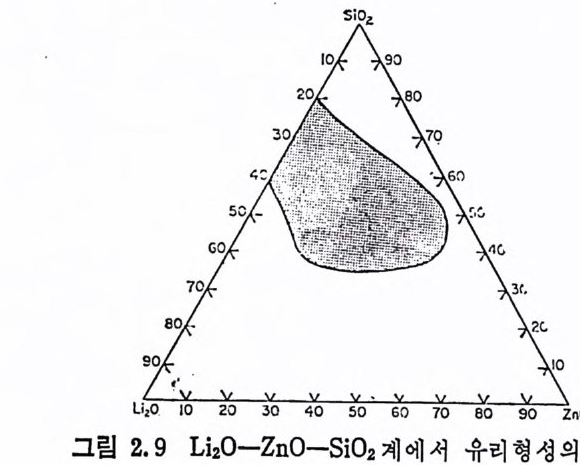 그립 2.9 L iz 0-Zn0-S i0 2 계에서 유리형성의 영 역
그립 2.9 L iz 0-Zn0-S i0 2 계에서 유리형성의 영 역
 Si0 2
Si0 2
논 것을 암시하고 있다. 유리Zn 형O 성와 영 M 역g 과O 의M g 類O 似— A한l 2역° 3 —할 은Si0 2Z n7'1O] ( ―그 A립l 2°2.3 8 ―) 의 S i것아 을계 (비그 교립 하2,면 10 ) 의알 수있다. 산화물계와 함께 CaO 와 PbO 를 함유하는 유리들은 결정화유리 분야에서 중요하다. 1700°C 以下의 온도와 약 29mole% 보다 적은 Ca0 량에서 용융물이 2 개의 不混和溶液(i mm i sci ble liq u i d) 을 만들기 때문에 CaO ― S i 02 계에서 2 성분유리조성의 법위는 제한을 받는다. Al2°3 와 같은 3 번째 성분을 첨가하면 유리조성범위가 매우 확장 되 어 Cao 와 Al2°3 가 매 우 높은 함량 (45mole%) 인 유리 가 얻어 진다. 특이하게 PbO 는 규산영과 붕산영유리 중에 매우 높은 비율 함유 되 어 도 유리 가 만들어 진다. PbO 가 77mole% 함유된 규산염 유리 가 얻어지며, 붕산영유리에서는 84mole% 까지 함유시킬 수 있다. 따 라서 규산영유리에서는 orth o sil ica te 조성 (2PbO~S i 02) 보다 PbO 함 량이 더 큰 유리도 만들 수 있으며 이런 유리에서는 S i 04 사면체의 연속망목구조는 촌재할 수 없다. 크게 分極할 수 있는 Pb2+ 들은 인 접된 S i 04 사면체 사이의 다리위치를 접유할 수 있으므로. 망목구조 가 형성될 수 있다. 여기서는 결정화유리분야에서 매우 중요한 계의 일부만을 소개하
였으나, 일반상업용 유리와 결정화유리제조용 유리의 형태가 어떻게` 다른가 하는 접을 알아야 하며 표 2.3 에 3 가지 중요한 유리의 화 학조성을 실었다. 이 유리들은 각종 공정에 따라 任意의 모양을 만 一 둘 수 있는 높은 加工性, 실두에 대한 높은 安定性 및 化學的 安定 : 性 등의 특성을 갖고 있다. :...i. 2. 3 商業用 유리 들의 組成( 重 :ill: %) Consti tue nt Soda-glil ma s es- sil i c a heBaotr-g or lesa sisli sis c t ai nte g Lead gla ss Si0 2 70~74 80.5 56~58 B2°3 0~0.2 12 Al2°3 0.5~2.0 2 0~1 PbO Mg O O~4 Cao 5~10 1 Na20 12~17 4.5 K20 12~13 (5) 유리 의 米占性-온도특성 유리는 명확한 웅접을 갖지 않는 과냉각액체이지만 점차 연화되 : 어 결국에는 온도상승에 따른 연속적인 접도감소로 인해 流動體 · (fl u i d) 가 된다, 유리에서 접성과 온도간의 관계는 여러 면에서 중 요하다. 예를 들면, 유리가 녹는 동안 접도가 낮아쳐 용융체를 동 해 氣泡가 빠른 속도로 상승하게 되어 기포가 없는 깨끗한 유리를 만들 수 있 다. 또 유리 의 徐冷 (annea li n g, 성 형 시 불군일한 냉 각으로 인 해 생긴 스트레인을 제거하기 위한 조작)은 유리를· 변형시키지 않고 웅• • 력을 제거시키기에 충분한 접도의 온도까지 유리를 어떻게 가열하 · 느냐에 따라 좌우된다. 신중하게 제어된 조건하에서 유리를 핵생성 및 결정화시키는 결정화유리제조에서는 최적열처리온도의 선정은 유리의 접성-온도특성에 의해 좌우된다. 유리의 접도(p o i se) 는 넓은 온도범위에 걸쳐 완만한 곡선을 나타 내나, 유리가 특정값의 접도를 나타내는 특정온도를 사용하여 접성-
온도의 관계를 정의하는 것이 더 편리하다. 이런 특정온도를 對應 하는 접도값과 함께 표 2.4 에 실었다. 표 2.4 유리의 特定溫度와 대응하는 祐度 tem Cph aerr aactut e rer i(s° tCi c) Vi sc osit y (po is e s) Fib r e soft en in g poi n t 101.6 Dil at o m etr i c soft en in g po in t or Mg poi n t 1011~1012 Anneali ng po in t 1013.4 Str a in poi n t 101u 유리 織 維(fi bre) 의 軟化點은, 직 경 o. 5~1mm 이 고 길이 22. ocm 인 섭유가 가열될 때 自重에 의해 그 길이가 1 mm/m in의 속도로 늘어나는 온도를 나타낸다. 示差彬服計에 의한 연화접은 축정시 結. 性流動이 열팽창을 中和시키는 온도이다. 따라서, 이 온도는 열팽 창곡선에서 얻어지는 최대접이 된다. 徐冷點은 유리내 ’ 의 내부응력 이 15 분이내로 완전히 제거되는 온도이다. 서냉범위에서 최처온 도를 나타내는 스트레인點 (s tr a i n p o i n t)은 유리를 상업적으로 16 시. 간이내로 서냉할 수 있는 온도이다. 2. 2 過冷却液體의 結晶化 2.2.1 結晶化過程 결정화 (cr y s talli za ti on) 는 규칙성이 적은 액체구조로부터 규칙격자 를 갖는 결정이 생성되는 과정이다. 가장 간단한 결정화는 단일의 순수한 원소나 화합물의 용융체가 냉각될 때 관찰되며 액체로부터 고체상태로의 변환은 일정압력하에서는 일정온도에서 일어난다. 이 온도를 疑固點 (fre ezin g poi n t ) 이 라고 한다. 모든 비율에서 균질액체를 형성하도록 용융될 수 있는 2 성분 A 와 B( 예, Na20 와 S i 02) 의 혼합물에서는 용매와 용질의 구분, 따라서 疑固點曲線과 溶解度曲線 사이를 구분한다는 것은 의미가 없다. 야
런 경우에는 液相線(liq u i dus curve) 으로 온도-조성관계를 정의하는 것이 보통이다. 이 곡선은 응고접곡선과 동일하며 任意組成의 용융 체를 천천히 냉각할 때 결정이 처음 나타나는 온도들을 p lo t하면 얻어진다. 이 곡선상의 모든 접들은 대응하는 조성의 液相溫度를 나타내며 이 액상온도에서 1 次相의 결정(初晶)이 용융물과 평형으 로 촌재할 수 있다. 결정들이 분리되지 않고 액상온도 이하로 냉각 되어지는 액체나 용융체를 過冷却液體 (su p ercooled liq u i d) 라고 한다. 과포화용액과 과냉각액체인 용융체의 결정화과정은 유사하며, 이 과정은 유리의 실두과정과 어느 정도 관계가 있다고 볼수있다. 냉 각하면 유리를 형성하는 용융체에서는 용액 중에 촌재하논 산화물이 많기 때 문에 결정화에 대 한 조건들은 복잡하다. 또한 cri sto b ali te 나
때문에 생기는 군질핵생성은 먼지 (dus t p ar ti cle) 와 같은 의부로부터 들어오는 핵을 배제해야 하는 문제 때문에 실험적으로 관찰하기는 어렵다. 보통 이런 형태의 핵생성은 °석상의 과포화도나 과냉각도가 높을 때 일어난다. 系와 관계없는 어떤 고체물질이 결정화를 촉진 시키는 경우도 있으며, 이 현상은 異質成分이 새로운 상의 핵들의 생성을 촉진시킨다는 것으로 설명되어 왔다. 다른 형의 이질성분 또는 핵생성촉진제는 결정화를 촉진시키는 능력에 따라 다르며 核 生成保進齊 l j (nuclea ti on ca t al y s t)의 능력은 촉진제의 원자구조가 핵생 성되는 상의 구조와 얼마만큼 비슷한가에 따라 결정된다. 2.2.2 過冷却液體으 I 核生成과 結晶化 (1) 均質核生成 이런 형태의 핵생성에는 모든 의부의 핵들이 배제되어야 한다는· 것 이 알려 져 왔으나 증명 하기 는 어 렵 다. Os t wald13 나근 정 밀한 실험 올 통해, 평군적으로 과포화용액의 수명은 과포화도에 반바례하며 이것으로부터 군질핵생성의 확률은 과포화도에 따라 중가한다는 일 반적인 효과를 확인하였고 만일 의부핵둘이 배제된다면 自發的으로 固相울 형성하지 않고 일부 과포화용액은 무한정으로 지속된다는 사실도 알았다. 이들 용액을 準安定溶液이라고 한다. 다른 과포화 용액 에 서는 限界時間(li m it ed ti me) 이 지나면 固相이 자발적으로 나 타나며 이런 용액을 不安定溶液이라고 한다. 농도가 증가하면 준안 정 용액 은 불안정 용액 으로 변하며 , 이 와 같은 轉移点 (tran sit ion po in t) 에서의 농도를 準安定限界 (me t as t able li m it)라고 한다. 준안정한계 이하의 농도에서는 결정핵들은 자발적으로 형성되지 않는다. 준안 정한계 근처의 용액에서는 압력, 온도, 또는 국부적인 증발에서의 변화와 같은 아주 작은 혼란효과에 의해 자발적인 결정의 석출이 일어날 수 있다. Tamman14) 은 핵생성과 결정화과정에 관한 이해에 큰 도움이 된
13) W. Ostw ald, Z. Phys . Chem. , 22, 289(1897). 14) G. Tamr rian , The Slate s of Ag gre g a ti on , D. Van Nostr a nd & Co. , New York(1 9 25),
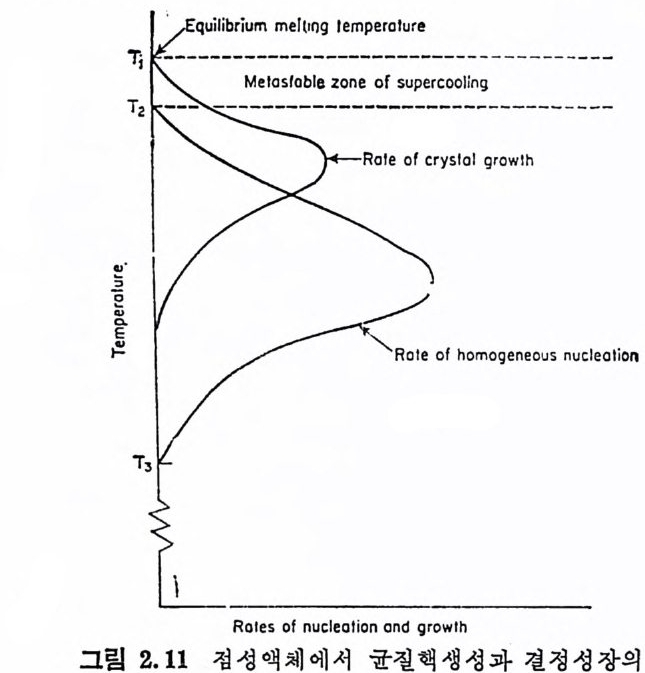
우기유리를 포함한 과냉각액체에서의 결정화에 관한 고전적인 연구 를 하였다. 그의 연구에 의하면, 平衡瑢融溫度 아래에 준안정영역이 라고 하는 溫度區間(t em p era tUi e i n t erval) 이 존재하며, 이 영 역 에서 는 感知할 수 있는 속도로 核이 형성되지 않으나 핵들이 공급되면 즉, 용융체에 種 (seed) 이나 茅(i nocula ti on) 가 공급된다면 결정들이 성 장할 수 있다. 이 영역 이하의 온도에서의 결정화과정은 핵생성속 一 도와 결정성장속도의 2 인자에 의해 지배된다. 냉각시키면 점도가 갑자기 커쳐 유리를 형성할 수 있는 용융체에서는 핵생성과 결정성 장속도에서 최대접이 나타나며, 그 이유는 최대접 이하의 더 낮은 온도에서의 높은 접도는 핵생성과 결정성장에 필요한 원자재배열과 확산과정을 방해하기 때문이다. 따라서 접성용융체의 핵생성속도와 결정성장속도에 대한 곡선은 그림 2. 11 과 같은 모양을 나타낸다.
 quil ib r iu m m•lt,o g lemp er alure
quil ib r iu m m•lt,o g lemp er alure
위 그림으로부터, 가장 많은 수의 작은 결정들을 만들려면 최대 ’ 핵생성속도가 일어나는 온도나 근처온도에서 핵생성을 일으켜야 한 다는 것율 알 수 있다. 뒷장에서 설명되겠지만, 最適核生成溫度를-
선덱하는 것은 결정화유리의 제조에 중요하다. 평형용융온도 이하에서 과냉각의 준안정영역 (T1-T2) 가 나타냐 며, 이것은 매우 작은 결정핵들의 웅접이 물질전체가 나타내는 웅 점보다 다소 낮기 대문이다. 바슷하게, 용액에서 과포화의 준안정 영역은 큰 결정립보다 작은 결정립의 용해도가 더 크기 때문에 생 간다. 그림 2.11 로부터, 용융체의 높은 접도 때문에 군질핵생성속 도가 O 이 되는 온도 T3 도 촌재한다. 과냉각액체의 핵생성에 대한 이론적인 연구는, 고상과 액상의 증 기압이 대기압과 비교할 때 무시할 수 있을 정도로 작은 擬縮系 (condensed s y s t em) 만을 대상으로 보통 다루고 있다. 母相內에서 새 로운 상( 핵 )을 형성하기 위해서는 계의 자유에너지는 증가하여야 하나, 이것은 핵생성의 장해물이 된다. G i bbs15) 는 이와 같은· 문제 를 연구하여 다음과 같은 식을 유도하였다 .
![]() W=161ra3/3(P-P')2 (2-5)
W=161ra3/3(P-P')2 (2-5)
여기서 W는 母相 A 內에 새로운 相, B 의 球狀物質울 형성하기 위한 일이며, a 는 面間張力(i n t er faci al ten sio n ), P’ 는 相 A 內의 압 력, P ” 는 相 B 內의 압력이다. 핵생성시 일어나는 자유에너지의 변화에 기여하는. 2 가지 현상이 있 다. 첫 번째 는 embryo 와 母相 사이 에 境界 (boundar y)나 표면이 형 성되어 떤간에너지 때문에 자유에너지를얻게 된다. 두번째는 emb ry o, 內의 원자배열이 :i 주위의 상에 있는 원자배열보다는 불규칙성이 낮기 때문에 계의 자유에너지가 감소하게 된다. 이와 같이 실질자 · 유에너지변화를 지배하는 2 가지 반대되는 인자들이 있으며, 이들 은 반경 r 의 球狀小集團 (s pher ic al i nclus i on) 에 대한 자유에너지변화 AF 로 주어지는 다음과 같은 형태로 나타낼 수 있다.
 t1 F= 스3군 t1f .+4 군t1f, (2-6)
t1 F= 스3군 t1f .+4 군t1f, (2-6)
여기서 A f.는 한 相으로부터 다른 相으로 전이할 때 생기는 단위 』
15) J. W. Gib b s, Collecte d Works, Vol. I , Long m ans, Green and Co. , New York( l928 ).
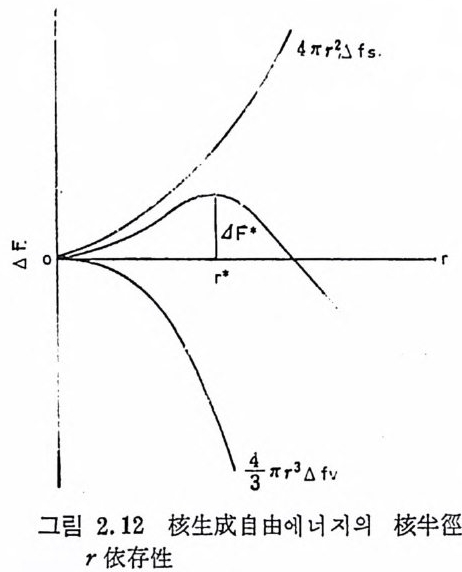
체적당의 자유에너지변화이고, 4 f s 는 2 상들사이의 단위표면적당의 에너지이다. 즉, 4 f 5 는 면간장력 a 와 같다고 할 수 있다. 어떤 환경하에서는 주위에 있는 상과 비교할 때 embryo 內의 원 자배열의 변화 때문에 생기는 스트레인에너지에 의한 에너지증가분 을 위 석의 오른 편에 1 항 더 포함시켜야 하나, 과냉용융체에서는 이런 효과는 보통 무시되어진다. 식 (2-6) 을 보면, r 이 작을 때는 면간에너지項이 우세하나 em- br y o 의 반경이 커지면 떤간에너지는 全에너지변화에 대한 분율이 더 작아진다. 일단 임계반경에 도달하면 체적자유에너지項이 우세 하게 되고 핵이 성장하떤 자유에너지는 더 작아지게 되어 더 안정 한 계가 된다. 임계반경보다 더 작은 영역에서는 핵이 형성되기 위 해 자유에너지가 중가하여야 하며 핵들은 연속적으로 형성되며 이 들은 계내에서 다시 용해될 것이다. 일부 embr y o 는 임계반경에 도 달하고 자유에너지의 감소와 함께 계속 성장하게 되어 안정한 핵들 이 형성되게 된다.* 임계반경 (r* )에서 자유에너지변화는 최대값을 갖게 되며 식 (2-6) 을 미분하면 임계반경이 얻어진다.
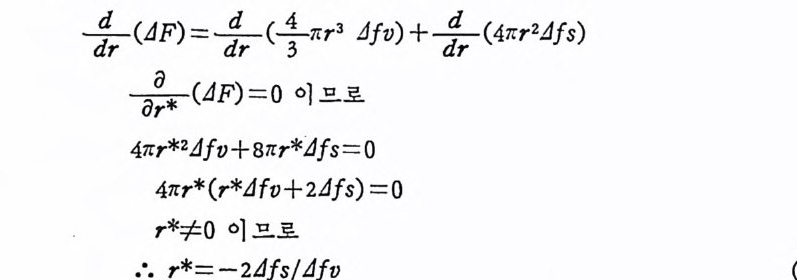 웅 (4F) = 옳냐硏 Llf v) + 꿈 (41rr2L1 f s)
웅 (4F) = 옳냐硏 Llf v) + 꿈 (41rr2L1 f s)
r* 는 최대자유에너지변화 4F* 와 대응한다. 식 (2-7) 을 식 (2-6) 에 대입하면,
![]() LIF*= 161r: (L1f s) 3/3 (Llfv ) 2 (2-8)
LIF*= 161r: (L1f s) 3/3 (Llfv ) 2 (2-8)
* r* 보다 각은 微小한 結晶에 가까운 集合狀態 7} 촌재 할 때 이 것 을 結晶의 embryo C 茅)라고 하며, 결정의 반경크기가 r* 보다 커지면 體積에 의한 자유에너지低下 가 界面에너지의 上昇보다 크게 되어 안정화된 茅가 된다. 이것을 結晶核 (nucl eus) 이라고 한다.
 I /< ,I I /4 m?A f s
I /< ,I I /4 m?A f s
이 식 은 Gi bb s 방정 식 (2 一 5) ) 와 비 슷하다. Becker 둥 16) 과 Frenkel17) 은 군질핵 생 성 속도 I 에 대한 석을 유도하기 위 해 통계역학을 이용했다. 이 식은 다음과 같다. I=A exp (-LlF*/kT) (2-9) 여기서 A 는 정수이고 L1F* 는 위에서 주어전 것과 같이 안정한 핵을 형성하기 위한 최대활성화에너지이다. 이 식은` 확산속도의 효과- 룰 무시하고 있으나 結性液
體에서는 相境界(p hase boundar y)를 지나는 분자들의 확산에 대한 활성 화에 너 지 는 핵 생 성 의 주요한 장벽 이 된다. 따라서 Becker1~) 에 의해 제안된 응축계내에서의 군질핵생성속도에 대한 일반식이 더 타당하다. 이 식은,
 /=Aexp [~] (2-10)
/=Aexp [~] (2-10)
여기서 Q는 상경계를 지나는 분자들의 확산에 대한 활성화에너지 . 이다. 이 이론은 대략적인 것이나 적어도 실험적 관찰에 대한 정성적인 . 설명을 해준다, 과냉각도가 작은 곳에서는 체적자유에너지변화 Ll f v· 의 값은 매우 작고 따라서 핵생성속도가 느리기 때문에 LlF* 는 크 다. 과냉각도가 커지면 4F* 가 Q의 크기와 비교될 수 있을 때까지 Ll f v 는 상당히 커진다, 즉, 이런 조건하에서 최대핵생성속도가 얻 어전다. 4F* 가 Q와 비교하여 무시되어질 때 과냉각도가 증가함-
16) R. Becker and W. Doerin g , Ann. Phy s. , f\1, 719(1935). 17) J. Frenkel, Ki ne ti c Theory of Liq u id s , Clarendon Press, Oxfo r d(l946). 18) R. Becker, Ann. Phys . , 32, 128(1 9 38).
예 따라 핵생성속도는 사라지게 된다. 일반적으로 측정할 수 있는 媒介變數(p arame t er) 들을 넣어 석 (2-9) 를 전개시킬 수 있으며 핵생성속도를 평가할 수 있다. 식 (2-7) 에 있는 체적자유에너지변화 4 f V 는, L1f v = L1H-T.:1 S v JfvT= -=J i= -HT mv — 에T서( J는H v!Tm) =L1Hv(Tm-T)/Tm= .:1 H。 •J T/Tm JH v=L!V 이므로 ,:1Jv = L.:1 T/ VTm (2- 1 1) 여 기 서 L 는 瑢融潛 熱 (lat e n t heat of fus io n ) , L1 T 는 액 상온도 Tm 이 하에 서 의 과냉 각도, V 는 결정 의 原子容(g ram ato m i c volume) 이 다. 식 (2-9) 의 지수항 앞에 있는 A 는 nv 와 같다. n 은 cm3 당 원자 수이고 v 는 核-液體의 面間에서의 전동수이다. 또, 상경계를 지나 · 논 분자들의 이동에 대한 확산계수 D 는 D=a51.1 exp (-Q/ kT) (2-12) 로 주어지며 ao 는 원자간거리이다. 따라서 식 (2-10) 을 정리하면, I=n1.1 exp (-i1F */kT) ·D/a51.1 =프a !t? -ex p(-i1 F* J kT) • 식 (2-8) 과 (2-11) 울 대 입 하면 .•. I= 言nD x p-16(7C(4f~ s) 3V)2T; (2-13) 만일 S t okes-E i ns t e i n 관계식이 다음과 같이 가정된다면, D=R T/N3 trTJ a 。 (2-14) 확산계수 D 는 접도 1J에반비례관계에 있다. 따라서, 식 (2-12) 중 의 a tJ,I의 효과는 용융온도가 액상온도 Tm 이하로 되면 핵생성이 갑
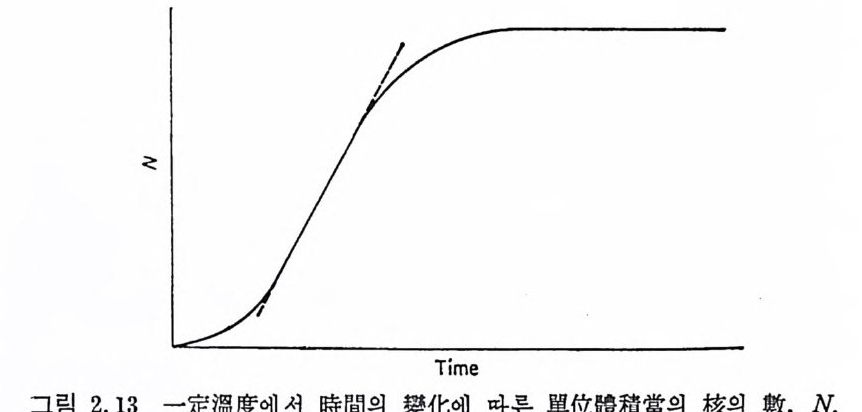
자기 떨어지는 원인이 될 것이다. 그러나, 동시에 지수항의 값은 과냉각도의 중가 때문에 커진다. 종합적인 결과는 실험적으로 관찰 된 것처럼 핵생성속도가 . 최대로 된다. 지금까지 다문 내용은 그림 2.13 에 나타낸 것처럼, 일정온도에서 시 간에 따른 핵 들의 수에 관한 곡선 중에 서 직 선부분인 定常狀態核 生成速度에 관한 것 이 다.
 /u4
/u4
그러나 핵생성속도가 0 이거나매우 작은동안에는初期期間(i n iti al 'P er i od) 이 있고 핵생성시간이 더 경과하면 단위체적당의 核의 數가 거의 일정하게 되는 곳에서 砲和女h 果가 생기게 된다. 포화효과가 중요하지 않은 영역에서는 시간 t가 경과한 후의 핵생성속도는 다 음과 같이 주어진다.
 l(t) =loexp (-r/t) (2-15)
l(t) =loexp (-r/t) (2-15)
여기서 t는 참복시간(i ncuba ti on ti me) 이고 k 는 정상상대핵생성속도 이다. (2) 不均質核生成 Vonneg u t1 9 ) 는 降雨를 유발시 키 는 구름들을 생 기 게 하는 방법 으 로 핵생성제가 되는 A g I 를 사용하였다. 왜냐하면 A g I 결정의 격자 상수는 얼음의 격자상수와 아주 비슷하기 때문이다. A g I 가 뿌려지
19) B. Vonnegu t , J. Ap pl. Phys . , 18, 593(1 9 47).
떤 수층기는 단지 4~6°C 의 과냉각도를 갖는 얼음절정을 석출한다~ 반면 내기 중의 먼지와 같은 물질들은 그 구조가 얼음구조와는 매 우 다르기 때문에 상변화를 일으키기 위해서는 20~30°c 의 과냉각 도가필요하다. Vonne gu t 20) 는 과냉금속용융체에 대해서도 연구하였다. 그는 금 속용융체를 小分 (subd i v i s i on) 하여 작은 방울(小萬 dro p le t)로 하는 실험에서 두 가지 십각한 난관을 극복해야 된다는 사실을 알았다. 첫째로, 핵들로 작용하는 의부입자들이 배제되어야 된다는 것, 두 번째로, 과냉액체는 일단 핵생성아 되면 결정성장은 매우 급격히 일어난다는 것이었다. 용융체가 小分되어 小商으로 될때 이들 小商· 中 단지 일부만이 핵생성입자를 함유하여 小商둘의 대부분은 군질 핵생성에 의해 固化될 것이다. 그는 기름필름으로 분리시킨 주석球 (tin s p here) 들은 110°c 의 과냉각도를 얻을 수 있는 반면 큰 금속 (bulk me t al) 에서는 20~30°c 이상의 과냉각도를 얻는 것이 불가능 · 하다는 것을 알았다. Holloman 둥과 m Turnbull 등은 22) 많은 금속들의 군질핵 생 성 온 도에 대한 값들을 얻었다. 군질핵생성 이전의 과냉각도의 범위는~ H g의 77°C 로부터 P t의 370°C 까지 매우 넓었다. 실제로 금속에 서 는 과냉 각도 4Tc 와 용융온도 Tm 사이 의 간단한 관계 는 Buckle23> 에 의 해 L1Tc/Tm~O. 18 로 주어 졌 다. 할로젠화알칼리 와 분자화합 물들과 같은 다른 물질들도 비슷한 경향을 나타내고 있다. Turnbull24) 은 H g방울들의 과냉 각에 대 한· 각종 표면코팅 (surfa c e· coa ti n g)의 효과를 실험 하였 다. 라우린산수은 (mercur y Iaura t e) 으로 구 코팅된 방울들은 77°C 의 과냉각도를 나타내어 코팅에 의한 촉전효 . 과를 볼 수 없었다(즉, 균질핵생성). H g 2l2 로 코팅된 방울들은 과냉 각도가 48° C 로 감소되 었으며 Hg 2 S 로 코팅 된 것들은 과냉 각도가- 12°c 로 핵생성이 촉진되었다는 것을 알았다. 핵생성촉진제로서《
20) B. Vonnegu t, J. Colloid Sci. , 3 563(1 9 48). 21) J. H. Holloman and D. Turnbull, Prog . Meta l Phys . , 4, 333(1 9 53). 22) D. Turnbull and R. E. Cech, J. Ap pl. Phys . , 21, 804(1 9 50). 23) E. R. Buckle, Natt ur e, Lond. , 186, 875(1 9 60). 24) D. Turnbull, J. Chem. Phys . , 20, 411(1 9 52).
Hg 2S 의 능 력 이 더 큰 것 은 Hg 2S 와 고체 Hg 사이 의 떤간격 (lat t ice s p a ci n g)이 비슷하기 때문이다. 이와 같은 결과는, 核生成保進劑 (nucleati on a g en t)의 능력은 촉진제입자의 구조와 핵생성되는 상의 구조간의 관계에 의촌한다는 것을 의미하고 있다. 이 접에 대한 더 확실한 증거는 알루미늄과 같은 금속들을 鑄造할 때 관찰되어지는 데, 다른 금속(예, T i)을 소량 첨가하면 주조금속의 입자크기가 매 우 精製된다. 효율적인 입자들의 정제는 핵생성촉진제와 금속의 유 · 사한 低指數面(l ow ind ex p lane) 들 사이의 d i sre gi st r y*가 10% 이하 일 때 일어난다는 것을 알았다.
* dis re gi st ry = l/o, o=L1a/a,, ,l a=( 핵생성촉진재의 격자상수―금속의 격자상 수), ao 는 금속의 격 자상수.
핵생성촉진제와 핵생성되는 상의 떤간격 사이에 허용되는 dis r e- gi s t r y에 대한 문제는 중요하며 配向重複成長 (e pit ax y or orie n te d overgr o wt h) 現象울 고려하는 것이 이 문제를 해결하는 길이 된다. 배향중복성장에서, 결정들은 일정한 방향을 갖는 의부결정의 표면 상에 형성되며 그 효과는 촉진제표면상의 배향된 핵생성으로부터 생긴다고 일반적으로 생각되어지고 있다. 대부분의 경우, 배향중복 성장이 일어나는 기준은 외부결정과 석출되는 결정의 類似한 低指 · 數面晶1 의 dis r eg ist r y 가 10~20% 를 넘 지 않을 때 이 다. 그러 나 대 부분의 경 우 배 향중복성 장은 더 큰 dis r eg ist r y 에 서 일어 나고 있 다. 과냉용융체나 과포화용액의 결정화에 대한 핵생성촉진제는 촉진제 와 핵생성되는 상의 처지수면의 떤간격에 대한 최대 d i sre gi s t r y가 · 15% 일 때 효과적이라는 것은 일반적으로 수긍이 가는 듯하다. 결 정격자의 不一致가 커질수록 과냉각도는 핵생성이 일어나기 전에 더 크게 생길 것이다. 과포화용액이나 과냉용융체에서 미리 촌재하는 표면(예, 콜로이드 . 함유물, 용기벽 등)의 효과는근 식 (2-8) 에서 나타낸 것과 같이, 면간 : 에너지 4 f 5 의 값이 감소함에 따라 군질핵생성에 대한 자유에너지 4F* 의 값이 감소하게 된다. 액상과 결정상간의 체적자유에너지변 화 4 f V 는 불군질핵생성에 의해 변화하지 않으며 확산에 대한 활성 화에너지 Q도 변하지 않는다. 불군질핵생성의 중요한 특칭은 異種 :
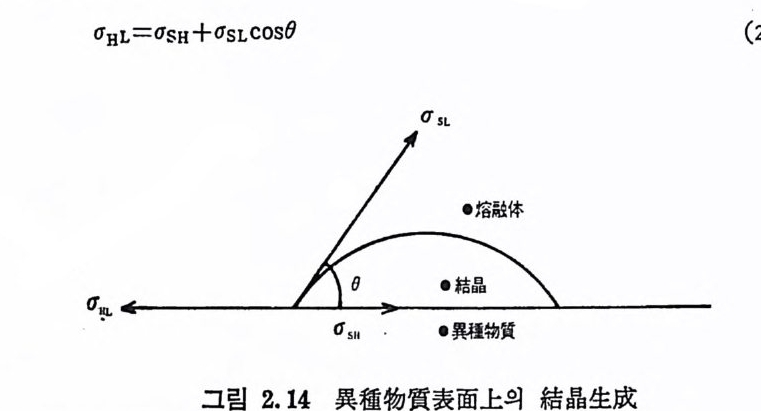
成分과 핵생성되는 상간의 面間張力이 작아야 한다. 따라서 핵생성 이 촉진되는 표면의 영향은 基板-楚 融體- 析出物의 接合 點 에서의 接 觸 角 0 에 의해 측정된다. 불군질핵생성의 활성화에너지는 다음과 같이 나타낸 수 있다. L1f 6 = L1F •f(O) (2-16) 여 기서 f(0 )=(2+cos8) (1-cos0)2/4 이 며 0<180° 일 때 f(0 )<1 이 고 4F*>4F; 가 된다. Turnbull 둥 25) 은 군질핵 생 성 속도석 을 불균질핵 생 성 속도석으로 수 정하였다. 죽, l.=A'exp (-L!F* f (0 )/kTJ (2-17) 그리고 S t ooke y에 의해 제안된 것처럼 확산에 대한 활성화에너지 가 포함된다면 위 석은 다음과 같이 된다. /,=A' exp [-(LlF*f( 8 ) +Q) /kT] (2-18) 따라서 불군질핵생성은 군질핵생성을 나타낼 수 있는 매개변수와 또. 하나의 변수()를사용하여 설명할수있다. 만일 핵 이 異種物質上에 球狀頭 (s p her i cal ca p)의 모양울 한다면 이종물질이 핵보다 크다고 할 수 있다. 그 각 ()는 표면장력의 평형 으로 측정된다. 죽,
25) D. Turnbull and B. Vonnegu t, Industr . Eng n g . Chem. , 44, 1292(1 9 52).
5SII : 異種物質 과 瑢融盤間의 연간자유에 너 지 (張力)
 태 =r f (B) (2~20)
태 =r f (B) (2~20)
여기서 T 는 순수한 유리(용융체)에 대한 참복시간이고 f (O) 는 다 음과같다.
 f(8 ) = (1 —co s8/2)-(cos28/2) (2-21)
f(8 ) = (1 —co s8/2)-(cos28/2) (2-21)
핵생성입자의 효율이 증가할수록참복시간은감소되며 핵생성촉진 하계여의 능N력a2 은0— 이P2야° 5 로유 리나 로타부낼터 수N 있aP 다0.3 의G ut걷z o 정w 화둥를 26 ) 은촉 진이하야 는률 수사많용 온 금속의 핵생성촉진제의 효율을 비교하였다. 이들 연구로부터 조사 된 금속촉진제들은 다음과 같이 능력이 커진다는 것을 알았 다. ` Au->Ag -> Re->Pd->Pt -> .I r 그러 나 격 자 dis r eg ist r y 와 결정 화의 효율 사이 에 는 어 떤 상관관계 도 없었다. 그렇지만 d i sre gi s t r y는 어떤 금속에서도 5% 를 초과하 지 않았고 따라서 이 인자는 배향중복성장을 허용할 수 있는 한계 내에 있다. 또 우선적으로 영향을 미치는인자로는 금속基板 (sub str .at e) 과 핵생성되는 결정상간의 접촉각 0 의 값이다. 실제로 f (O) 의 값들은 핵생성촉진제의 능력이 커지는 것과 같이 Au 의 o.125 로부 터 Ir 의 0. 007 까지 감소하였 다. 또 그들은 Na2B•01 유리 에 서 핵 생 성 촉진제의 효율은 Au-.Ir-.Pt 순으로 증가하며 이 경 우에도 역 시 격자 d i sre gi s t r y가 별로 중요하지 않다고 보고하고 있다.
26) I. Gutz o w and S. Toschev, Advances in Nucleati on and Crys t a lliz a ti on in Glasses, p. 10, Americ a n Cerami c Soc iet y (lr;nl).
불균질핵생성에 대한 고찰을 요약하면, 핵생성촉진제의 효율을 결정하는 2 가지 중요한 기준이 있다. a) 핵생성촉진제와 初晶相間의 面間張力은 작아야 한다. b) 低指數面上의 d i sre gi s t r y가 약 15% 이상 되지 않도록 결정구 · 조는 비슷하여야 한다. (3) 結晶成長 유리의 制御된 결정화에는 핵생성분만 아니라 결정성장도 포함된 다. 핵생성과정이 미세한 결정질의 결정화유리제조에 매우 중요한 반면, 결정성장과정은 제조된 재료의 형태를 결정하는 데 상당히 중요하다. 걷정성장은 2 가지 인자들에 의존한다. a) 불규칙유리구조가 성장결정 (gro wi ng cr y s t al) 의 주기적 격자로 재배열될 수 있는 속도. b) 상전이과정에서 방출되는 에너지가 제거될 수 있는 속도, 즉· 결정-유리의 면간으로부터 빠져나오는 열흐름의 속도. 구조적 전이과정윤 먼저 생각하여 보자. 결정구조내의 한 원자는 유리상에 있는 것과 같은 원자보다 결정화의 체적자유에너지 (bulk free energy ), L1G 만큼 자유에너지가 낮다. 또한 유리와 결정상간의 떤간을 지나는 한 원자는 활성화자유에너지 4G 에 대응하는 에너 지장벽을 넘어야 한다. 따라서 결정성장속도 U 는 다음과 같이 유 도된다.
![]() U=a 。 11e 쟈〔― .&G11/RT 〕(1 -ex p .&G/RT) (2-22)
U=a 。 11e 쟈〔― .&G11/RT 〕(1 -ex p .&G/RT) (2-22)
여기서 ao 는 원자간의 거리이고 v 는 결정-유리의 면간에서의 전동 수이다. 식 (2-22) 는 정상적인 결정성장을 나타내는 석이다. 이 식은 한 · 원자가 주어진 자리에 첨가되는 또는 제거되는 확률이 결정-액체의 떤간상의 모든 자리에서 같다는 가정에 기초를 두고 있으며 떤간의 크기는 원자 크기보다 훨씬 크다고 생각하여야 한다. 실제로 이오l 같은 가정은 일반적으로 사실과 다르다• 일반적으로 결정성장은 떤 간을 가로지르는 나선전위 (screw d i sloca ti on) 에 의 해 공급되 논 자리 ;
{ (s it e) 들을 원자듈이 에너지적으로 순조롭게 채워지는 機構에 의해 일어난다. 따라서 원자들이 채워질 수 있는 자리들의 총수의 분율 만이 결정성장에 이용될 수 있다. 이 분율은 다음과 같이 주어진다
![]() f::::;』 T / 21r 끄 (2-23)
f::::;』 T / 21r 끄 (2-23)
따라서 식 (2-22) 의 右邊은 f 로 곱해 야 된다. 작은 과냉 각도에 서 는 f값은 작으나 과냉각도가 커지면 f값은 중가한다. 표면핵성장으로 알려진 결정성장에 관한 또 다른 모델은, 먼저 面 間上에 2 차원적인 핵생성이 일어난 후 이 성장이 單層울 형성한다 는 것이다. 이 모델은 원자적으로 平擔한 面間울 의미하며 보통 이 런 형의 거동은 규산영과 유리에서는 볼 수 없다. 석 (2 - 22) 는 다음과 같이 전개 할 수 있 다. 확산계 수 D 는 다음과 같이 주어진다.
 D==a5vex p〔 _4G 미 Rm (2-24)
D==a5vex p〔 _4G 미 Rm (2-24)
이 식은 유리에서 결정성장속도를조정하는데 접도의 변화가상당 한 효과가 있다는 것을 명백히 하여 준다. 따라서 용융체가 °석상온 도 이하로 냉각될 때 처음에는 결정성장속도는 증가하지만 점도의 급격한 증가는 곧 결정성장속도를 떨어뜨리는 데 주된 영향을 미치 게 되어 그림 2.11 과 같은 전형적인 결정성장속도곡선이 그려지게 된다. 접도의 중요성을 또한 강조하고 있는 다른 시도에서는 결정성장 속도는 액체가 결정질구조로 재배열되는 데 필요한 단위험으로 결 정화에 필요한 縣動力 (dr i v i ng force) 을 나눈 刃配로 주어진다고 생 각하였다. 구동력의 구배는 체적자유에너지 4G 를 원자간거리 ao 로 나눈 것이다. 접도 7 인 媒質 (med i um) 를 지나 직경 d 인 입자가 이동하는 힘은
F= 3 r-:T Jd (2-27) 이다. 따라서 결정성장속도는 다음과 같 다. U= .d G/37l TJ a 。 d (2-28 ) 그리고 만일 a 。 zd 및 4G=4Hf 4T / T 근]라면 u= 4Hf4 T/ 3T C T ja 5 Tm (2-29 ) 따라서 U= Const. L1 TITJ (2-30) Na위20와— C같a은O — 관Si계0 2 는 형 의Si 0 2더 , P복2 잡야한 및 유G리e0 2에 와 서 같볼은 수많 은있 으유나리, 형 성과 냉물 과각 도가 작은 곳에서는 2 성분계알칼리규산영유리에는 적용되지 못한다. Doremus27) 가 지적한 것처럼, 결정성장속도를 제어하는 또 하나 의 인자는 열이 성장하는 결정으로부터 빠져나갈 수 있는 속도일지 도 모론다. 이런 경우에는 열흐름속도가 결정성장속도를 감소시키 는 값까지 결정-액체의 떤간온도의 증가를 방지하기에 불충분할 때 일어 난다. 보동 두 가지 인자가 중요하다. 죽 결정화의 몰열 (molar- heat) , L1Hr 와 결정을 둘러싼 액체의 연확산계수이다. 결정화동안 에 생 긴 熱流速 (hea tfl ux) 은 J= UAp L IHt !M (2-31) 여기서 U 는 1 차원적인 성장속도, A 는 떤간면적, p는 밀도그리고 M 은분자량이다. 또한 열속은 온도구배에 비례한다 J= AKdT/dx (2-32)· 여기서 K 는 熱傳導率(t hermal conduc ti v ity)이다. 따라서 dT/dx= Up ilH t /M K (2~33) 일부 규산영유리에서는 최대성장속도가 lµm/sec 를 초과하지 못
21) R. H . Doremus, Glass Scie n ce, p. 90 Joh n Wi ley & Sons, New York( l9 73).
한다. 이 값과 다른 매 개 변수들에 대 한 적 당한 값들을 식 (2-33) 에 넣 어 계 산하면 온도구배 의 값은 3°C/cm 가 된다. 따라서 규산영 유 리에서의 결정성장속도는 열흐름에 의해 큰 영향을 받지 못한다. 어떤 결정화유리계에서는 lOµm/sec 정도의 높은 결정성장속도가 관 ` 찰되어 결정-유리의 면간에서의 온도구배는 결정성장속도에 영향을 준다고 충분히 생각할 수 있다. 2. 3 유리 의 核生成과 結晶化 2. 3. 1 유리의 安定度룰 決定하는 因子믈 앞에서 본 것처럼, 모든 유리는 준안정물질이고 보통유리에서 살 온에 있는 평형상대는 결정질상태가 될 것이다. 유리를 용융온도로 부터 냉각하면 결정화 때문에 유리가 파괴되는 것은 과학적으로 상 당한 의문을 일으키며, 유리의 안정성을 지배하는 인자들을 고려하 는 것은 결정화유리에서도 적철하다. 과냉각용융체가 결정화할 때 파괴를 일으키는 이유는 두 가지로 생각할 수 있다. 핵생성속도가 매우 작거나 핵상의 결정성장속도 7 l 모든 온도에서 무시될 수 있을 정도일 대다. 이들 인자 중 어느 것 이 더 중요한가를 결정하기는 쉽지 않으며 핵생성속도와 성장속도 가 똑같이 중요할 수는 없다는 확실한 이유도 없다. 불균질핵생성은 보통유리들의 냉각중에는 일어나지 않는다고 일 반적으로 생각하고 있다. 왜냐하면 용융유리는 우연히 함유된 대부 분의 불순물 (d irt)에 대해 좋은 용매이기 때문이다. 이런 의견이 타 당한 것으로 간주하는 것은 결정질규산염을 형성하는 데 가장 효율 적인 핵생성촉진제는 결정구조가 규산영과 비슷한 물질들이며 따라 서 대부분의 경우 규산영 자신이 핵생성촉진제일 것이라는 이유 때 문이다. 물론 이들은 유리용융체에 의해 급히 용해된다. 불균질핵 생성온 의부입자들이 용해되지 않는 조건하에서 유리와 접촉하게 되면 유리의 실루를 일으키는 첫째 원인이 된다. 예를 들면, 그 후 에 재가열되는 유리 속에 떨어지는 먼지들은 불균질핵생성을 일으` 킨다.
유리를 형성하는액체의 군질핵생성도불가능할 것으로 생각될 것 이다. 왜냐하면 석 (2-10) 에서 확산의 활성화에너지는 고은에거는 비교적 높으나 온도가 내려가면 증가하기 대문이다. 이런 조건하에 서는 충분한 수의 안정한 핵둘 없이도 핵생성이 일어날 수 있는 危 險溫 度 領域 (dang erous tem p er atu re zone) 을 지 나 용융체 가 냉 각될 수 있냐 물론 유리가 임계온도영역에서 소바하는 시간이 핵생성을 일 으킬 수 있는가 없는가를 결정하는 데 중요하나, 보통 유리는 이 영 역을 지나 매우 급격히 냉각된다. 만일 결정성장속도가 유리의 안정도를 결정하는 데 중요한 인자 타란 군질핵생성이 일어날 수 있다고 가정하면 실두가 일어나지 않고 임계온도범위를 지나 유리를 냉각시킬 수 있을 것이다. 왜냐 하면 핵생성속도와 같이 결정성장속도는 결정성장을 제어하는 확산 과정울 방해할수 있을만큼접도가 커지는온도에서는 0 이 되기 때 문이다. 이 온도 이하에서 유리는 모돈 실제적 목적들에 대해 완전 히 안정하다. 이와 같이 핵생성속도나 결정성장속도가 유리의 안정성을 지배하 는 주요 인자타고 생각된다. 온도의 하강에 따른 점도의 급격한 증 대는 결정형성을 효과적으로 방해한다. 이런 이유 때문에 유용한 규 산영유리들은 0~ 상온도에서 높은 점성을 가지며 액상온도에서는 初 晶相 (pr im ary crys t a l l ine ph ase) 이 액 상유리 와 평 형 으로 존재 할 수 있다. 액상온도가 낮은 유리는 안정한 유리이며 시판용 소오다 - 석 회-규산유리들의 액상온도는 900~1000°c 이다. 이런 조성들은 dev- it r it e(Na20•3Ca0•6S i 02) 가 초정상으로 존재하는 相領域에 있고 만 족스러운 유리를 형성하기 위한 근본적인 조건은 물론 이 화합물이 냉각중 결정화를 일으키지 않아야 한다. 2.3.2 유리 중의 유리의 分相 유리는 微視的으로는 불균질하며 이 불군질성 때문에 유리의 强 度, 化學的 尉久性, 電氣的 性質 또는 유리 중에 도입된 微量成分의 거동 둥이 영향을 받게 된다. 이 미세한 不均質相發生의 중요한 원 인의 하나로서 分相 (ph ase sep a rati on , 單一相의 유리 가 2 以上위 유리 相
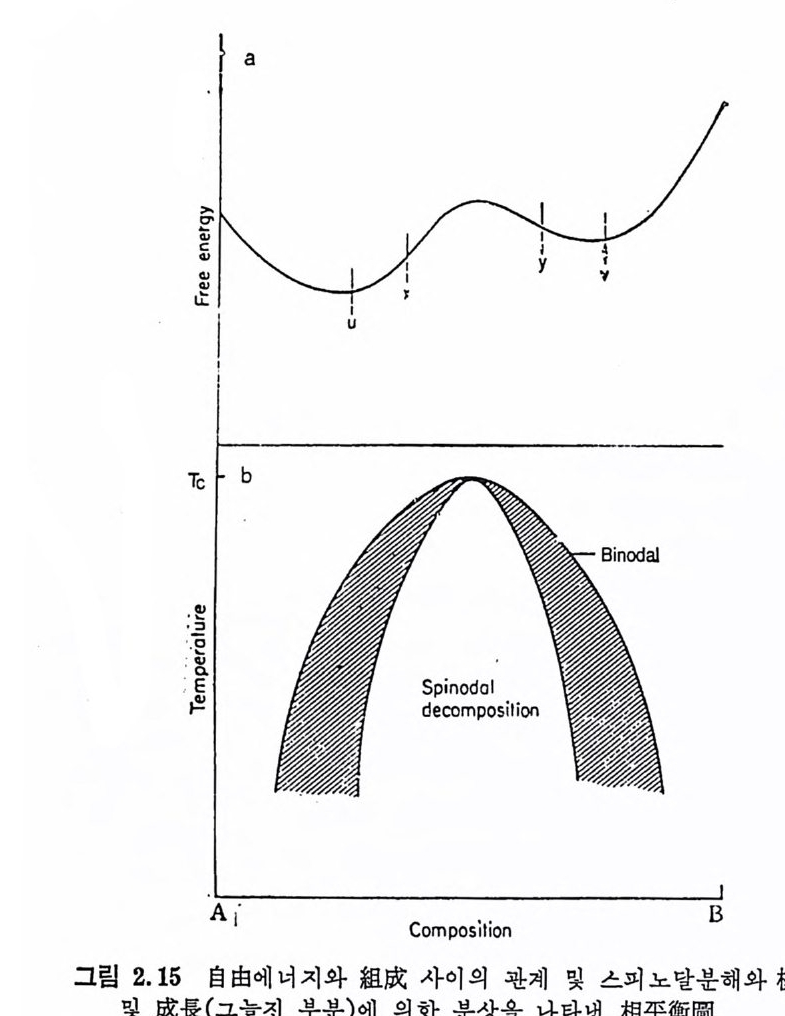
으로 分 離 하논 현 상)을 생 각할 수 있 다. 따 라서 분상현상을 이 해한다 논 것은 유리의 구조와 물성을 이해하기 위한 유력한 수단이 된다. 또 분상온 v y cor 유리의 제조에서 필수과정이며, 유리의 결정화에 서도 결정핵생성속도와 석출결정의 크기, 종류 둥에 영향을 주기 때문에 분상에 관한 지식은 매우 중요하다. (1) 일반적 고찰 유리의 分相에는 유리의 熱處理條件에 따라 2 가지로 나눠진다. 液相溫度 以上 즉, 용융체에서 일어나는 분상을 安定不混和 (s t able i mmsc i b ility)라고 하며 이때는 냉각에 의해 형성된 유리는 層 狀 構 造이거나 강한 乳白色울 며게 된다. 액상온도 이하에서 일어나는 분상을 準 安定不混和 (me t as t able im mi sc ib il ity or gla ss-in - gl a ss ph ase se p ara ti on) 라고 하며 결정화유리에서는 준안정불혼화가 더 중요하 다. 준안정불혼화에 의한 분상과정에는 핵생성과 성장과정에 의 한 분상과 스피 노달분해 (spi no dal decomp os it ion ) 에 의 한 분상이 있 다• 前者에 의한 분상에 관한 이론은 결정핵생성과 성장에 관한 이론과 거의 같으며, 스피노닫분해에 대한기초이론과유리에 기준을둔분 상에 관한 動力 學 的 硏究가 Cahn 둥 28)29) 에 의해 이루어졌다. 그림 2.15(a) 는 온도 T 에서 A 와 B 2 성분의 임의의 혼합물에서 자유에너지와 조성간의 관계를 나타낸 것이다. 이 자유에너지곡선 에서 최소접 U , V 사이에 있는 조성에서는 혼합물은 2 相으로 분리 된다• 온도가 낮을 때논 U 와 V 접이 서로 멀리 떨어지게 되나, 온 도가 높아지면 2 접은 서로 가까와전다. 그림 2.15(b) 의 im mi sc i bi l it y dome (b i nodal) 은 각 온도에서 자 유에너지의 최소접 u,v 접들을 추적하여 그린 곡선이다. 또 2 최소 접 U, V 가 한 접 에 서 만나는 온도가 Tc 이 며 臨界溫度 (cr iti cal tem p - eratu r e or upp e r consulate t em p.)라고 한다. 그립 2. 15(b) 의 imm i sc i- bil ity dome 에 는 2 개 의 다른 영 역 이 있 다. 첫 번째 영 역 은 sp ino dal decomp o sit ion 영 역 으로 자유에 너 지 곡선 의 변곡접 (d2F/dc2=0) 안 X,Y 점들이 모여 만들어진 곡선의 내부를
28) J. W. Cahn, J. Chem, Phys . , 42, 93(1961 ). 29) J. W. Cahn and R. J. Charles, Phys . Chem; Glasses. , 6, 181(1 9 65).
 }da
}da
나타낸다. X,Y 접 사이의 조성에서는 d2F/dc2
와 Y 사이의 조성에서는 &F/dc2>0 이다. 이들 조성 사이에서의 작 온 조성변화는 자유에너지의 증가에 기여하게 되므로 불안정하며 재용해하게 된다. 죽 임계크기 이상이 되지 않으면 핵의 성장이 생 기 지 않는다 . 따라서 sp ino dal 과 bin o dal 사이 의 영 역 에 서 는 핵 생 성과 성장과정에 의해 분상이 일어나게 된다. 이들과 2 과정에 의해 생기는 분상간의 기본적인 차이는 표 2.5 와 같이 요약할 수 있다. 표 2.5 核生成 과 成長 및 스피노말 분해에 의한 分相의 목 성 相特 組成性 | 一定溫核度生에成 서과 는 成長核 生成된 I| 組成은 스平피衡노에달 分도解달 할 때 相의 組成은 一定하다 . 까지 변화한다. 相間界面 1 全體가 완전히 확실하 다. 처음에는 散在하나 최종적 으로는 명확하게 된다. 核生成되는 相은 크기와 간 第 2 相은 보통 球狀이 아 形態學 격이 一定하지 않은 球狀 닌 실과 갈은 모양으로 一 粒子로 브동 나타나며 낮 定한 간격과 크기로 존재 온 相互連關性을 갖고 있다. 하며 · 높은 相互連 關 性윤 갖고 있다• 위와 같은 2 종류의 분상에 대해서는 아칙도 완전히 이해되고 있 지는 않지만 핵 생성과 성장에 의한 분상이 더 중요한 역할을 하고 . 있다. 핵생성과성장에 의한분상에서는분상된입자들은정확한조 . 성을 갖고 있으며 군질핵생성에 의한 결정화가 더 찰 일어난다. 한 · 편 주위의 유리상에서는 불균질핵생성에 의한 결정화도 일어날 수 · 있다. 그림 2. 15 로부터 , 不混和 境 界 以上의 온도 (Tc 이상의 온도)로부터 유리를 냉각하면 핵생성과 성장에 의한 분상의 영역을 가로지르게 된다• 따라서 정상적인 냉각속도를 사용하는 결정화유리에서는 분_ 상이 일어난다면 스피노탈분해보다는 핵생성과 성장에 의한 분상아 더 잘 일어날 것이다. 그림 2.16 은 30 Li 20·10S i 02 조성의 유리를 1 시간 550°c 에서 열처
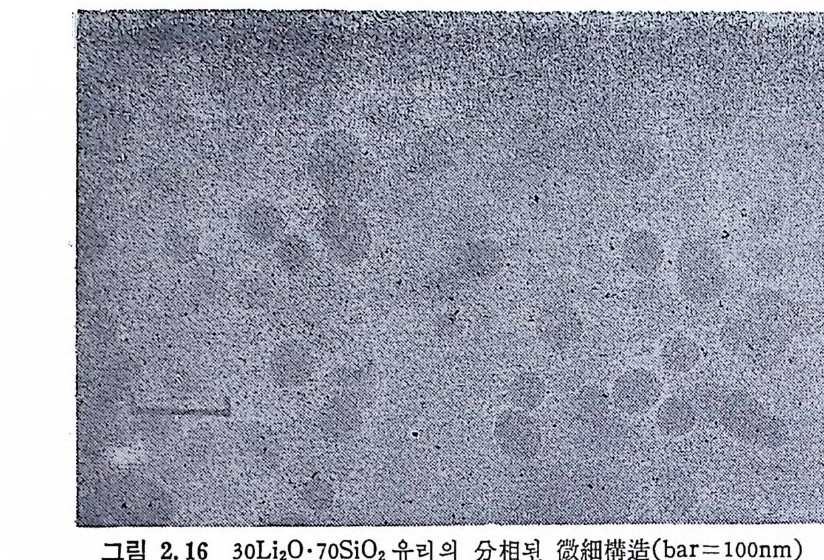 그립 2.16 30L iz 0·70S i아유리의 分相된 微細構造 (bar=100nm)
그립 2.16 30L iz 0·70S i아유리의 分相된 微細構造 (bar=100nm)
리 (분상)한 유리 의 전자현미 경 사진이 다. 이 경 우 第 2 相인 獨立球形 粒子들은 핵생성과 성장이 분상의 원인이 되었다고 할 수 있다. 그림 2.17 은· 분상된 붕규산유리의 미세구조이며 여기서는 兩相이 높은 相互連關性(i n t erconnec ti v ity)을 갖고 있어 스피노달분해와 일
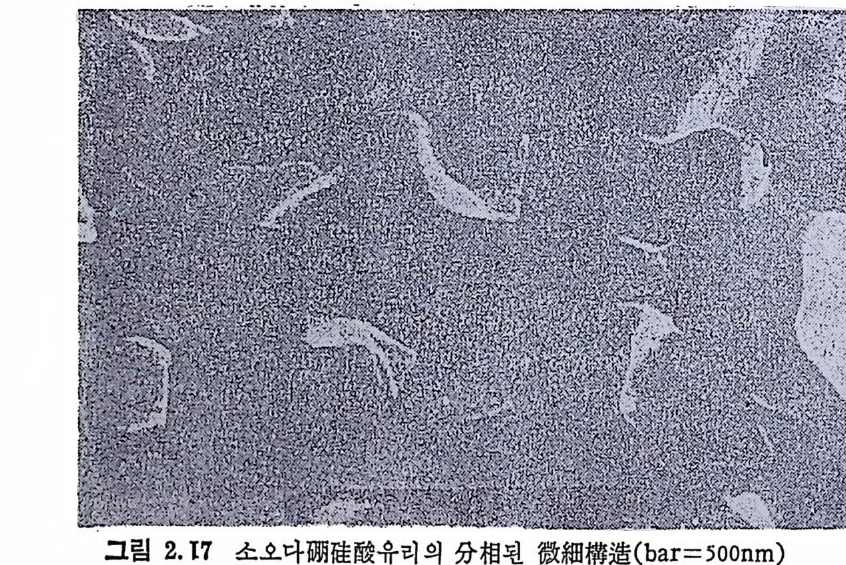 그립 2.17 소오다覇珪酸유리 의 分相된 微細構造 (bar= 500nm)
그립 2.17 소오다覇珪酸유리 의 分相된 微細構造 (bar= 500nm)
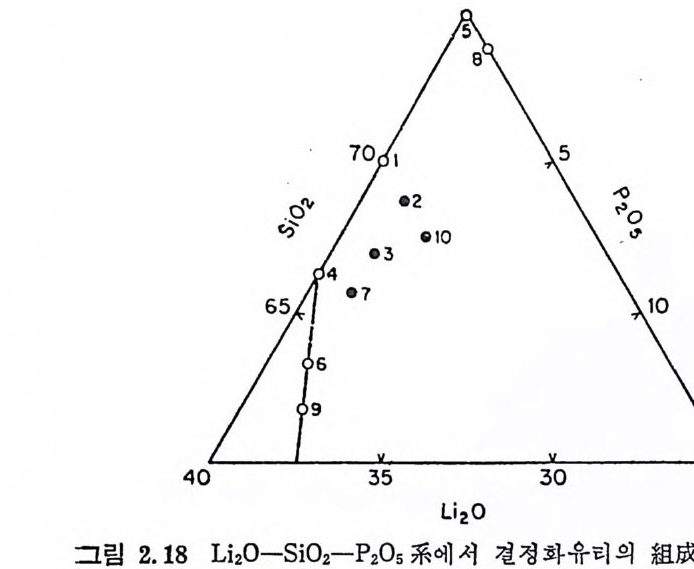
치하고 있다. 이와 같은 높은 상호연관성을 갖는 구조의 발생에는 - 2 개의 機構가 생각되며, 그 하나는 스피노달분해에 의한 경우, 또 . 다른 경우는 핵생성과 성장에 의한 분상에 의해 생성된 獨立球形粒 子듈이 서로 融合, 再配列하여 2 相이 상호연결된 상태로 되는 경우 가 있다 .30) (2) 結晶核生成과 成長에 대한 유리 중의 유리의 分相效果 Phil lips 둥 31) 은 Li 20 ― S i 02-P2 아 계 유리 에 서 의 결 정 화과정 울 전 자현미경 관찰과 전기전도도를 측정, 조사한 결과 핵생성과 성장 전에 분상이 일어나면 미립자의 미세구조가 생기는 것을 알았다. 이 이유는 성장하는 Li 2S i 2 야결정을 둘러싸는 경향이 있는 Si 02 71--- r i ch 한 분상된 영역의 존재로 인해 핵생성밀도가 증가하고 견정성 장B속u도rn가et t 감 둥소 32)하 은게 N되a 기20 -때B 문a0이— 다S.i 02 계 유리 에 서 상분리 가 먼저 일 어나면 결정성장속도가 감소한다는 것을 알았다. 이것은 분상된 입 자들이 결정성장하기 전에 機械的 防害를 하고 있기 때문이라고 설 명하Ha고rp e 있 r 으등나 33) 은지 지Li를20 —받 S지i 0 2 못-P하2고05 계있다 유. 리 들의 결 정 핵 생 성 과 성 장 · 과정에 관한 연구를 하였다. 열역학적 모델을 근거로 하여 그림 2. 18 에 나타낸 정선으로 표시된 일반식 x(Li2 0 ,2Si0 2 ) • (1-x)(Li 2 0•3P205) 의 조성에서는 單相이 촌재할 것이며, 이 접선의 오른편., S i 02 ― r ic h 한 조성에서는 2 相으로 분리될 것이라는 것을 예상하였 다. 실험결과는 예상과 잘 일치하였으며 그림 2.18 에 나타낸 조성 (접 1~10) 에서 P2 야를 포함하고 있건 없건 관계없이 單相 및 2 相유 리상에서의 결정화에 관한 연구를 할 수 있었다. 이들 유리는 핵생 성을 위해 soo°C/hr 의 열처리와 다음에 750°C/hr 의 결정화를 위 한 열처리를 하였다. 열처리한 유리들에서 결정의 평균반경을 光學 및 전자현미경으로 관찰하였다. 그 결과를 표 2.6 에 실었다. 또 열 역학모델로부터 계산한 S i 02 ― r i ch 인 球形相의 체적분율도 실었다.
30) W. Haller, J. Chem. Phys . , 42, 686(1965). 31) S. V. Phil lips and P. W. McMi llan , Glass Tee/mo/. , 7, 121(1 9 65). 3332)) HD.. GH.a rBpe u rr naentdt aPn. dW R. . MWc. MDi loluang ,l a sP, hPys h, yCs ,h eCmh.e mG. laGssleass,s e1s3, , 12r.r,7 C 1lr1.r77 2( 1 ).'. Yll).
 40 35 30 25
40 35 30 25
표 2. 6 Liz O -Si0 2 -P205 결 정 화유리 에 서 結 晶 의 平均半經고} sil ica -ri ch 相의 體積分率豫想値 No. Co\ mSp io0 s 2i t io!n (mLhoOl. %I) P20s Crys t a (l µdmia) m ete r Voolfu mSpei hO af zs-r era ic ct hi o n 1 70 30 126.5 0,124 2 69 30 1 11 . 7 0.183 3 67.5 31 . 5 1 42.8 0.130 4 66.7 33.3 340.0 。 5 75 25 188.0 0.298 6 64 35 1 65.1 。 7 66 33 1 53.1 o·. 0 7 5 8 74 25 1 0.37 0.353 9 61 .3 36.7 2 1.23 。 10 68 30 2 0.18 0,241 표 2.6 의 결과를 요약하면 다음과 같다. P2 야를 함유하지 않은 유리들(접 1,4,5) 에서는 租大한 미세구조를 갖는 多結晶質(죽, 핵생 · 성의 효과가 낮다)이 형성되고 핵생성과 성장이 일어나기 전에 유리
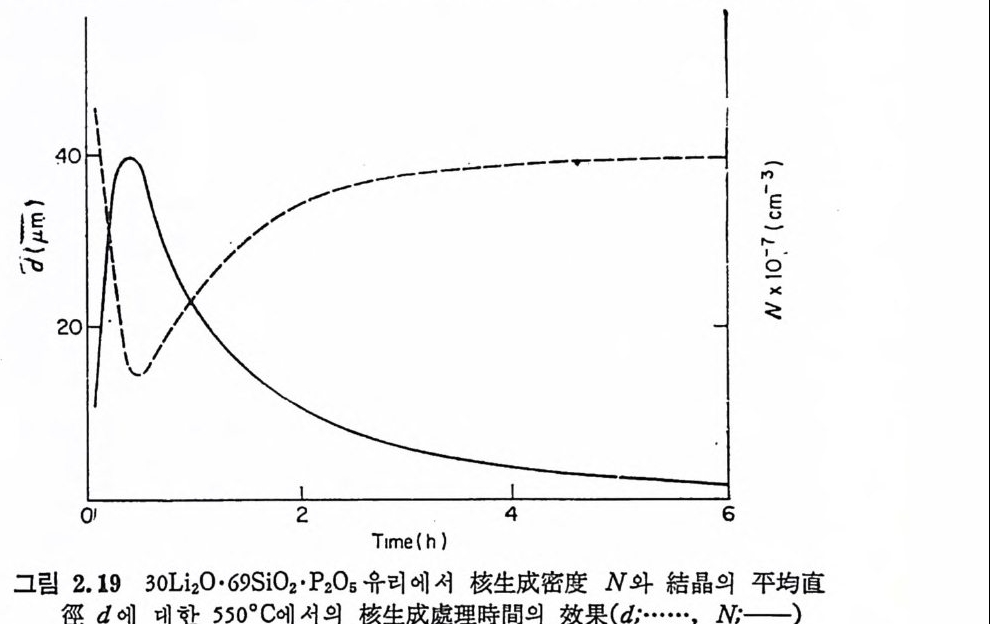
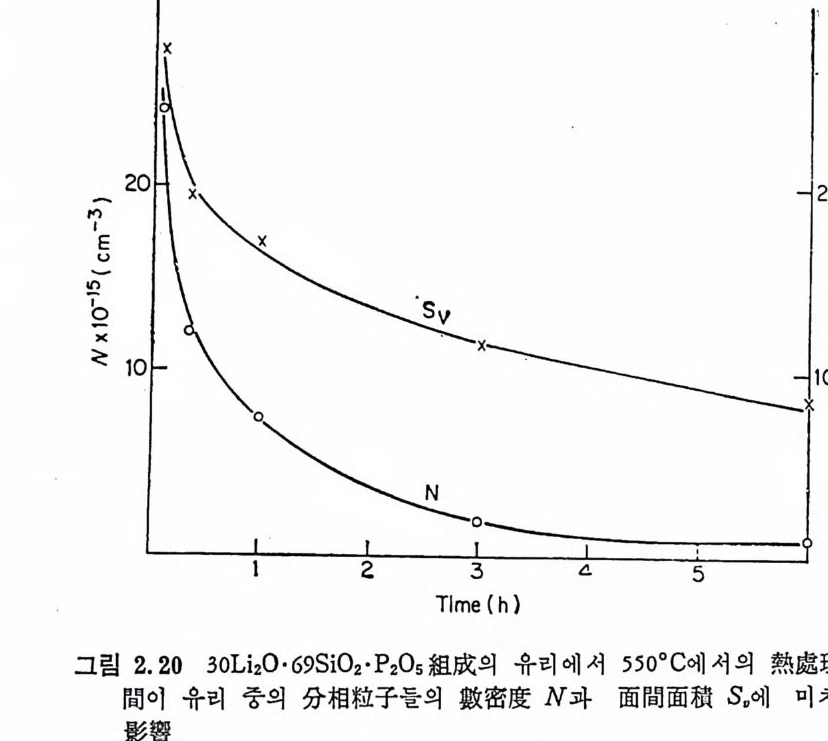
중에 유리의 분상이 생기면 핵생성밀도 (nuclea ti on dens ity)가 약간 증 가하게 되나 그 효과는 크지 않다. P2°5 를 함유하는 單相유리에서 는 P205 함량이 증가할수록 핵 생 성 밀도는 커 지 나(정 4, 6, 9), 가장 큰 핵생성효과는 P20s 를 함유하고 먼처 분상이 일어난 유리에서 얻어 진다(접 10). McM ill an34) 은 핵 생 성 효과와 분상의 형 태 학적 인 것 을 나타내 는, 예를 들면 단위부피 또는 面間面積當의 분상된 입자의 수와 같은 매개변수와의 사이에 직접적인 관련이 있는가를 조사하기 위해 30 L i 20·69S i 02·P20s 조성의 유리에 대한 결정화를 연구하였다. 550°C 에서 0.1~6 시간 핵생성시킨 후 750°C 에서 1 시간 표준결정화처리를 하였다. 이때 열처리시간의 변화에 따른 핵생성밀도, N 과 결정의 평군직경, d 의 변화를 그림 2.19 에 나타냈다. 그림에서 최대핵생성 효과는 550°C 에서 20 분의 열처리에 의해 얻어졌다. 그림 2.20 에서와 같이 분상된 입자들의 數密度 (number dens ity)와 面間面積(i n t er faci al area) 은 열처리시간이 경과함에 따라 감소하였기
 E / / / / / 一 -一 一 一 I_'E3T)L’o-xNl
E / / / / / 一 -一 一 一 I_'E3T)L’o-xNl
34) P. W. McMi llan , Proc, Xt h Int. Cong . on Glass, 14, 10974).
 x
x
때문에 핵생성효과와 분상된 미세구조와의 사이에는 간단한 상관관 계가 없었다. 이 결과는 분상된 입자들이 다음에 일어나는 결정화 ? 를 위한 핵 생 성 자리 (nucleati on s it e) 를 제 공한다는 개 념 과는 다르다. 그러나, 이 실험결과는 분상이 먼처 일어나면 결정핵생성속도를 증 전시킨다는 以前의 연구결과와 모순되기 때문에 이 모순을 조화시 키기 위해 McM ill an 은 새로운 제안을 하였다. 죽 핵생성을 위한 열처리중 2 相유리의 매트릭스상 (ma tri x p hase) 에서 결정핵이 생겨 처음에는 결정핵의 수가 증가하나 租大化過程 (coarsen i n g pro cess) 때 문에 결국에는 결정핵의 수가 감소하게 된다고 설명하고 있다. 유리에서 분상이 일어나면 확산의 활성화에너지를 증가시킬 수 · 있기 때문에 조대화과정을 방해한다. 따라서 분상온 핵을 보존하는 · 역할을 하므로 다음에 일어나는 결정성장단계에서 수많은 핵생성자 리로부터 결정성장이 일어나게 된다. 따라서 분상이 먼저 일어나서
핵생성밀도에 미치는 효과는 핵생성자리를 직접 공급한다기보다는 ` 간접적인 효과, 즉 핵생성자리를 보촌한다는 것이다. Harpe r33) 등은 Li 20 ― S i 02-P2 아 계 유리 의 600° C 에 서 의 결정 성 장속도를 측정하기 위해 誘電損失角 (d i elec tri c loss t an g en t)을 측정하 ’ 였다. 그 결과 먼저 일어난 분상은 기계적 방해효과에 의해 결정성 장속도를 감소시킨다는 결론을 얻었다. 이들 연구결과를 종합하면, 유리 중에서 유리를 먼저 분상시키면 유리의 결정화에 의해 생기는 미세구조에 상당한 영향을 준다. 죽 · 미제구조를 갖는 미립자를 만들기 위해서는 유효핵생성밀도의 증가 와 함께 결정성장속도를 감소시키는 것이 가장 중요하며 이들은 걷 정화유리의 제조에서도 같다. 2.3.3 유리의 失透 (1) -般的 要因 실두란 유리 중에 결정질의 성장을 뜻하는 것으로 보통 실제적안 유리제조공정에서는 실두를 방지하여야 한다. 만약 유리의 성형공· 정에서 실두가 일어난다면 유리성형기계의 작동울 방해하는 급격하 고 예기치 못한 점성의 변화가 일어날 수 있기 때문에 매우 좋지 않은 결과를 초래한다. 母유리와 열팽창계수가 매우 다른 결정상의 성장은 냉각과정에서 일어나는 수축률의 차이 때문에 유리에 매우 위험한 응력을 발생시키게 된다. 실두는 유리조성이 적당하지 않기 때문에 일어나는 것으로 실두를 방지하기 위해서는 유리의 조성을 조십해서 선택하여야 한다. 또 楚融遺의 停帶部分에서 내화벽돌과 장시간 접촉하거나 반응함으로써 局部的으로 조성이 변하여 실루가 · 일어날 수도 있다. 유리성형공정에서 결정성장이 일어날 수 있는 · 임계영역의 온도내에 유리를 장시간 放置하는 것은 피해야 한다. 또 실두에 대해 특히 불안정한 일부 유리에서는 사용할 수 있는 성 형조작이 제한되며 임계영역의 온도를 지나 급냉시킬 수 있는 조작 · 만을 사용하여야 된다. 결정화유리의 제조공정이 유리의 실두에 의해 이루어진다 할지라 도, 최종물질이 얻고자 하는 정확한 미제구조와 성질을 갖도록 하-
키 위해서는 그 공정이 찰 制御되어야 한다. 유리성형중 미리 일 어 나는 실두(p rema t ure dev itrifi ca ti on) 는 아주 바람칙 하지 못하며 피 해야 한다. 왜냐하면 이때 일어나는 결정성장은 원하는 微粒子構造 가 되지 못하고 비교적 약간 큰 결정으로 된 조대구조를 갖기 쉽게 되기 때문이다. 이런 재료들은 기계적으로 약하고 실용가치가 거 의 없다. 실두방지는 유리제조에서는 매우 중요한 것이지만 실험적인 어 려움 때문에 최근까지도 체계적인 연구가 거의 되어 있지 않은 실 정이다. 분리된 결정상은 관찰온도에서 가장 안정한 상은 아니기 때문에 더욱 어려움이 있다. 예를 들어 보면 S i아는 t r i d y m it e 가 안정 형으로 촌재하는 조전하에서 cris t o b ali te 로 종종 결정화 된다. 결정호H 즌 내부에서보다는 표면에서 매우 빨리 일어나고, 대부분 의 경우 표면에서 결정화가 시작되므로 표면온 보통유리의 실두에 중요한 역할을 한다• 결정화가 표면에서 일어나는 이유는 표면과 내부의 화학적 조성차이 둥 여러가지가 있다. 성형조작중 유리표 · 면으로부터 휘발성 성분의 손실이나 표면에너지를 낮추는 성분들이 표면에 농축되기 때문이다. 그러나 가장 중요한 요인은 결정핵생성 울 촉진시킬 수 있는 異物質이 표면에 존재하기 때문이다. 이 異物 質은 먼지 또는 작은 흠(fl aw) 들이다. 또 유리 내부에 가스기포나 의부입자들이 존재하면 주위의 유리에 더욱 빠른 실루를 가져오게 된다. 유리의 전체적인 불군질성 때문에 불안정한 조성을 갖는 영 역이 생겨도 실두의 원인이 된다. 결론적으로, 보통유리가 재가열되는 동안 생기는 실두는 핵생성 촉매 (nucleati on ca ta l y s t)로서 작용할 수 있는 의부입자들이 표면의 어떤 부위에 존재하느냐에 따라 달라지는 매우 제어하기 어려운 공 정이다. 이와 같은 방법으로 실두된 유리는 결정화과정이 종결된 후 독특한 구조를 갖게 된다. 유리표면으로부터 내부로 성장하는 결정들은 바늘모양으로 유리표면에 대해 90° 방향으로 배열되어 성 장한 결정의 두 끝이 유리 중십에서 만나게 된다. 결정들은 보통 크며 배향된 결정들은 재료의 기계적 성질을 약화시킨다.
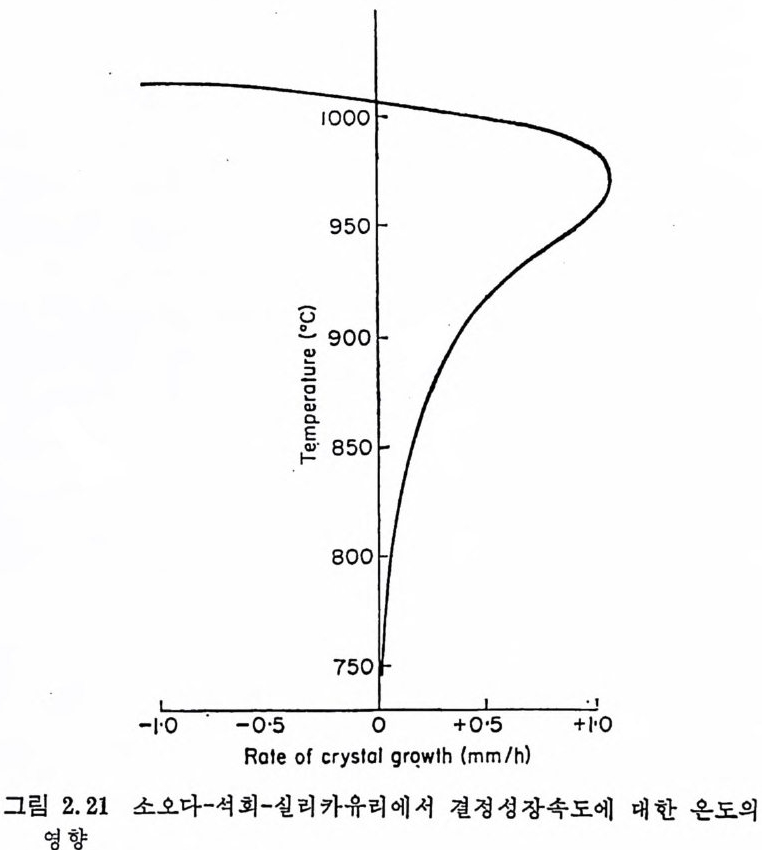
(2) 實驗 的 調査 일반적 으로 얻어 지 는 결정 성 장속도곡선의 모양은 Sw ift 35) 가 소오 다-석 회 -실리 카유리 의 결 정 화에 의 한 devit rit e ( Na20 • 3 CaO • 6 Si0 2 ) 에 대해 얻은 그립 2.21 과 거의 같다. 만약 결정성장을 위한활성화 에너지가 확산과정에 의해 제어된다면 결정성장의 최대속도는 유리 의 流動 度 (fl u i d ity)와 비 례 할 것 이 다. 위 의 사실은 결 정 상이 tri d y m i te 이 었 던 소오다-석 회 -실리 카계 유 리들에 대한 Litt le t on36) 의 실험결과와 거의 일치하였다. Presto n 37'
 950
950
35) H. R. Swi ft, J. Am. Ceram. Soc. , 30, 165(1 9 47). 36) J. T. Lit tleto n , ]. Soc. Glass Technol. , 15, 262(1 9 31 ). 37) E. Presto n , J. Soc. Glass Technol. , 15, 262(1 9 31 ).
온 최대성장속도의 온도 이하에서는 dev it r it e 결 정의 성장속도의 對 數(l o g)와 철대온도의 逆數 사이에는 어떤 관계가 있다는 것을 알았 다. 그리고 결정성장속도 1 에 대한 다음과 같은 경험식을 제시하 였다•
 I=K(TL-T)ITJ (2-34)
I=K(TL-T)ITJ (2-34)
여기서 TL 은 液狀溫度, T 는 결정성장속도 측정시의 온도, 7J는접 도, K 는 상수이다. 이 경험식은 물론 식 (2 - 30) 과 동일하다. S t anwor t h38) 는 Presto n 에 의 해 연구된 소오다 구4 회 -실리 카유리 에 대한 결정화과정의 활성화에너지는 전기전도도에 대한 활성화에 너지와 거의 같고 祐性流動 (v i scous fl ow) 에 대한 활성화에너지보다 는 매우 낮다고 지적하였다. 비슷한 결과가 규산영유리에서 cris t o - bal it e 의 결정화를 연구한 Cox 둥 39) 에 의해서도 얻어졌다. 이둘결 과는 실두과정을 제어하는 활성화에너지는 전기전도도로 측정되는 · 알칼리금속이온 (Na 하이 유리를 통해 확산하는 데 필요한 활성화에 너지와 거의 같다는 것을 의미한다. Sw ift 3” 는 0석 상온도 이상의 온도에서 결정을 과열시킬 수 있으며 0석 상온도 이하의 전정성장속도 곡선이 연장된 곳에 결정성장속도가 負인 마이너스成長 (ne g a ti ve g row t h) 의 영역이 있다는 흥미있는 특칭 울 例示하였다. CaO 가 일부 M g O 로 치환된 이 실험에서 그는 6% 까지 치환되는 M g O 는 액상온도를 낮추고 原유리 중에 결정상으로 나타나는 cr i s t oba lit e 와 dev it r it e 의 결정성장속도를 감소시킨다는 사실을 지적하였다. 이것은 액상온도의 강하가 실루에 대한 유리의 안정성을 증가시키기 때문에 실제로 중요하다. 이와 같은 이유 때 문에 일반 소오다-석회-실리카유리 중에는 M g O 가 일부 함유되어 있다. 그러나 M g O 함유량이 6% 를 넘으면 dio p si d e (CaO·Mg O ·Si0 2 ) 와 소오다 • 마그네슘·규산염 (Na20•2M g 0,S i 02) 이 새로운 상으로 냐 타나 유리의 안정도가 떨어진다. 또 原유리에 알루미나를 첨가시켰 울 경우에도 처음에는 결정성장속도가 감소되나 Al203 의 농도가 높
38) J. E . Sta n worth , Phys i c a l Prop er ti es of Glass, p. 215, Clarendon Press~ Oxfo rd ( l950 ). 39) S. M. Cox and P. L. Kir b y, Natu r e, Lond. , 159, 162(1 9 47).
 14 00
14 00
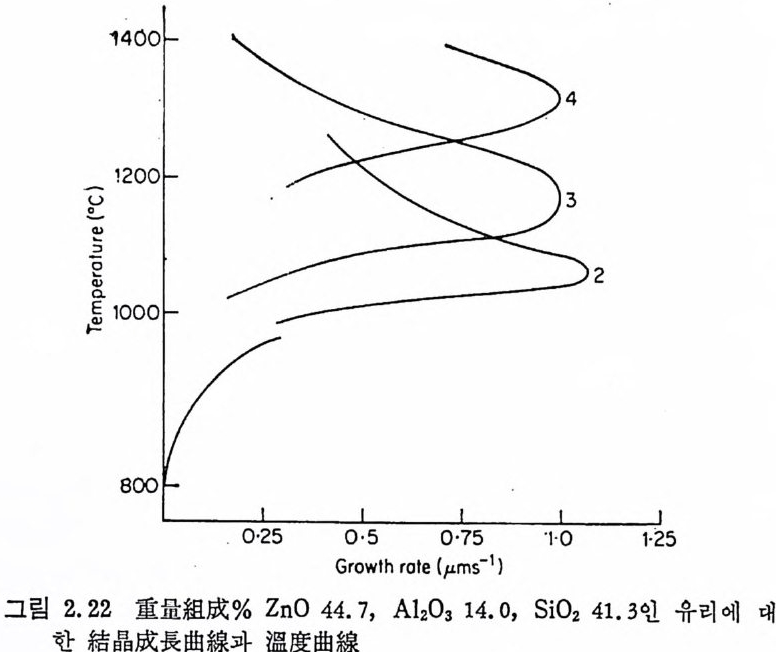
아지면 wollas t on it e(CaO•S i 02) 의 침전이 생겨 유리의 안정도가 떨 어진다. 이상의 모든 실험에서 결정성장은 표면으로부터 일어난다. McMi llan 둥 40) 은 ZnO ― Al203-S i 0 여 유리 에 관한 연구결과 다 성분계 유리에서의 실두과정은 더 복잡하다는 것을 강조하였다. 중 량조성 %로 ZnO; 44. 7, Al 2 0 어 14. o, Si0 2 ; 41. 3 인 유리를 高溫顯 微鏡 울 사용하여 결정성장속도를 측정한 결과는 그림 2.22 와 같다. 그림에서와 같이 4 개의 결정형이 나타난다. 初晶相은 800~950°c 에서 생기는 kea tit e(s ili ca - K) 이며 이것은 약 980°C 에서 zin c · or t hosU ic a t e(Zn2S i 04) 로 非可逆的으로 변환한다. 더 높은 온도에서 는 ZnA1204 와 cris t o b ali te 결 정 이 생 긴다. 原유리 에 알칼리 금속산화물이 나 B203, Ti0 2 , Zr02 또는 P2 0s 와 같은 알칼리토류 금속산화물을 1~3% 첨가하떤 결정화의 擧 動이 변화된다. L i 20 를 1% 첨가하면 800°C 에서의 kea tit e 상의 성장속도
40) P. W. McMi llan , G. Partr i d g e and J. G. Darrent, Phys . Chem. Glasses, 10, 1530969).
는 o. 067µm/sec 로부터 o. 75µm/sec 로 커 지 며 , Li20 를 3 %까지 첨 가하면 성장속도는 5.9µm/sec 로 커진다. 이와 같은 Li 20 의 큰 효 과는 soo°C 에서 原유리의 접도가 5.4x107 p o i se 인데 비해 Li20 3% 첨가시킨 유리는 3. 2x I04 p o i se 로 접도가 작아진 것이 主原因이 된 다. Na20 나 K20 를 I % 첨 가하면 keati te 상 을 억 제 하고 초정 상으 로 alb it e(NaAIS i 308) 와 w ill em it e(Zn2S i 04) 가 형성되는 다른 효과 를 나타낸다. 또다른 산화물의 첨가는결정성장속도에 약간 영향을 주며 이들의 유리접성에 대한 효과도 비교적 작다. 그러나 1% 內에 서 Mg O 와 CaO 의 2 산화물을 첨 가하면 keai:i te 상에 대 한 성 장속도 가 감소된다. Ma t us it a 둥 41) 은 25 Li 20 •75 S i 02•3R0n(ROn 은 망목형 성 양이온인 알 칼리 , 및 알칼리 토류 금속산화물)유리 의 실두에 관한 연구를 하였 다. 이 둘 유리에서 副液相不混和 (sub-l iq u i dus i mm i sc i b i l ity)가 관찰되었으며 混和溫度논 이온장강도가 커질수록 높아졌다. 죽 P2°5 와 같은 망 목형성산화물을 함유한 유리가 가장 혼화온도가 높았다. . 불혼화의 발생은 핵생성과 성장속도에 상당한 영향을 미치며 큰 핵생성은 2 유리상 사이의 떤간근처에서 일어날 것이라고 생각하였다. McM ill an 등은 35 Li 20(65-x)S i 02xROn(RO 표 Alz03, Ti 02 , V2 야, P2 아) 조성의 용융체에서 결정성장속도에 대한 작은 조성변화의 영 향을 조사하였다. 측정온도 범위인 800~1100°c 에서 나타나는 걷 정상은 Li 20•2S i 02 였다. 첨가물이 없는 35L i 20•65S i 02 인 기초조 성에서의 실험결과는 Hil lig and Turnbull42) 의 다음의 식과 잘 일 치한다는 것을 알았다.
![]() U= AIJ T l.15/TJ (2-35)
U= AIJ T l.15/TJ (2-35)
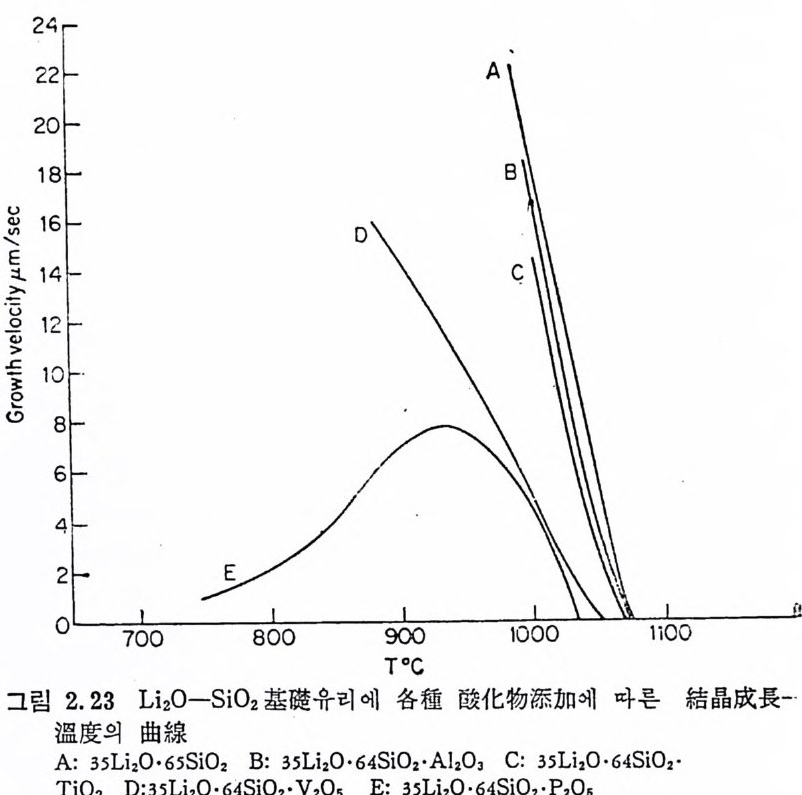
여기서 U 는 결정성장속도, T 는 접도, 4T 는 과냉각도, A 는정수 이다. 1% 내에서 각종 산화물을 첨가하였을 경우 결정성장속도의 변화 를 그림 2. 23 에 나타냈다.
41) K. Matu s it a, S. Sakka, T .. M uki and M. Tashir o, ]. ,M ate r. Sc i. , 10, 94 (19 75). 42) W. B. Hil lig and D. Turnbull, ]. Chem. Phys . , 24, 4(1 9 56).
 24~
24~
P2 야는 결정성장속도를 매우 감소시키며 V2°5 도 약간은 감소호 과가 있다. P2 아첨가에 의한 유리의 접성과 전기전도도의 변화는 거의 없었다. 이 결과로부터 結性流動 또논 리튬이온확산의 활성화 에너지변화에 기초를 둔 설명은 성립되지 않는 것 같다. P+5 와 V+ s. 둘은 성장하는 결정격자 중에 들어가 결정성장의 활성화에너지에 형향을 준다고 생각된다. Uhlmann11 ~ 은 유리형성계에서 결정성장에 대한 불순물의 효과를 논의하였다. 죽 많은 물질들에서는 불순물이 존재하면 결정화를 위 한 확산과정 때문에 또는 성장자리가 오염되기 때문에 결정화속도 논 감소되나 산화물유리의 경우 결정성장속도는 촉진될 수 있다
이 예로는 실리카유리에서의 H20, 아 및 Na, 유리狀붕소산화물에 서의 H20 이다. 以上을 요약하면 접도를 낮추는 조성의 변화는 유리의 결정화속 도를 증가시키나 결정성장에 대한 불순물의 영향도 고려하여야 된 다. 결정화의 동력학에 대한 소량의 물의 영향은 특히 홍미있다. 왜 냐하면 물은 불순물로 모든 산화물유리 중에 존재 하며 보통은 고 려되지 않는 영향을 유리의 실두에 관한 연구에서는 고려하기 때문 이다. (3) 結晶成長의 形態學 결정상의 성장에 대한 형태학 (mor p holo gy)은 유리의 결정화에서 중요한 한 분야이 다. Uhlmann43) 은 결 정 성 장에 서 첫 조직 을 결정 하는 결정 적 인 인자는 용융엔트로피 (entr op y of fus io n ) 이 라고 생 각하 였다. 용융엔트로피가 작은 물질들(.t! S1M>2R) 은 작은 접촉면이 없는 면간조직을 갖고 성장하며 성장속도는 거의 等方性이다. 용융 엔트로피가 큰 물질들(.t1 SrM<4~6R) 은 최밀충전면에서는 원자간에 平担한 떤간을 보이나 최밀충전이 아닌 면에서는 원자 크기로 볼 때 거천 면간을 나타내 작은 접촉면을 가전 조직으로 성장한다. 이 런 성질은 다른 방향 사이에 성장속도가 비등방성이기 때문에 일어 난다. 높은 용융엔트로피를 갖는 물질들은 과냉각도가 큰 상태에서 결 정화가 이루어지며 다른 방향을 갖는 새로운 결정의 핵생성은 결정 성장보다 먼저 일어나거나 동시에 일어난다. 이때 핵생성은 유리의 높은 접 도와 불순물의 존재 때 문에 낮은 分子移動度 (molecular mobi- Jity)에 의해 小球體成長 (s p herul itic g row t h) 을 하게 된다. 소구체성장은 결정화유리제조에서 중요한 장접이 된다. 소구체는 중십으로부터 放射되는 섬유상결정들로 되어 있어 기하학적 구형을 하고 있으나 다발모양을 할 수도 있다: 소구체는 유기고분자 중 겔 (g el) 의 결정화 중, 화성암 중 그리고 장시간 일정한 온도하에서 유 티가 실루를 일으켰을 때 상업용 유리 중(예, 유리탱크가마 중의 停帶
43) D. R. Uhlmann, Advances in Nucleato n and Crys t l l iz a ti on in Glasses, p. 91, Ame .rica n Cerami c Socie t y (l97 1 ).
領 域 )에서 생긴다. 결정화유리에서는 소구체생성은 혼히 일어나며 이것은 강한 기계적 강도를 얻는 데는 매우 좋지 않은 미세구조를 만든다. Ke it h 둥 44) 은 핵생성 다음 단계에서 결정의 分枝能力의 중요성을 강조한 소구체성장에 관한 이론을 제안하였다. 용융물에 촌재하는 불순물들이 분지능력의 전정적인 역할을 하며 이 불순물들이 떤간 에 농축되어 이미 느려진 성장속도를 더욱 느리게 한다. 결정성장 은 결정화되지 않은 유리의 영역에 의해 분리된 섬유상의 突出部에 의해 진행되나 결국은 느란 側面成長 (slow late r al g ro wt h) 에 의해 결 정화된다. 섬유의 分枝는 섬유표면상의 攝動(p er t urba ti on) 에 의해 일 어나며 과냉각도가 증가함에 따라 성장할 수 있는 섭동의 임계 크 기는 감소하기 때문에 분지되는 회수는 증가한다. 소구체 성 장의 동력 학은 Joh nson-Mehl-Avrami 식 을 사용하여 분 석할 수 있다.
 V 尸 1-ex p (-Kt ) (2-36)
V 尸 1-ex p (-Kt ) (2-36)
여기서 Vf 는 새로운 상의 체적분율, K 는 동력학상수, t는 시간, n 는 Avram i指數이다. 이 식은 석 (2-2) 로부터 나온 것으로 K= :n: /3 • U 얀 이 다. 지수 n 이 3 일 때는 새로운 핵의 생성 없이 일정한 속도로 放射 狀의 결정성장이 일어나며, n 이 4 일 때는 일정한 결정성장속도와 일은정 3한~4 핵이 생다.성 L속i도20 가— Si일0 2 어 , 난B다a.O ― S폴 i리아 에및틸 N렌a과20 -천P2연0고s 유무리의 들 n의 의 n 값의 값이 1~2 인 것은 이해하기 어렵다. 그러나 n 이 2 인 값은, 積層成 • 長(l am i nar gr o wt h) 은 한 충이 완전히 성 장한 후 다음 충이 성 장한다 논 것으로밖에 설명할 수가 없다. 실험적인 관찰과 일치되는 또 다 론 설명으로는 결정화과정은 새로운 섬유의 핵생성속도에 좌우된다 는 것이다. 성장속도가 일정하고 핵생성속도는 r2 에 비례한다고가 정할 수 있으므로 섬유의 밀도는 소구체성장이 진행될수록 작아질 것이다.
44) H. D. Keit h and F. J. Padden, J. Ap pl. Phy s. , 34, 2409(1 9 63).
소구체성장을 시킬 수 있는 온도보다 더 높은 온도에서 소구체를 형성하는 유리를 열처리하면 결정들을 쐐기 (l a t h) 나 針狀으로 변화 · 시킬 수 있다. 따라서 결정화유리 중에 바람직한 미세구조를 만들 수 있 다. 이 런 현상온 BaO-Si0 2 계 와 ZnO 一 Al2 아一 S i 02 계 에 서 관 찰되고 있다. 2.3.4 유리의 失透률 제어하기 위한 조건 결정화유리제조에 관한 연구의 목적은 경제적 및 보편적인 熱處· 理週期 (hea t trea tm ent c y cle) 를 사용하여 특별히 調製 된 유리 의 결정 화를 제어함으로써 다결정질제라믹재료를 만드는 것이다. 또, 우수한 기계적 성질을 나타내는 마립자로 된 미세구조의 생 ' 성, 독정한 열팽창계수와 같은 특정한 물리적 성질 둥을 갖는 결정 상의 생성 및 殘餘유리相의 체적분율과 조성을 조철하는 것 등도 . 연구의 중요한 목적 중의 하나이다. 이런 묵적틀들을 달성하기 위해 서는 많은 복잡한 인자들의 상호작용을 이해하여야만 하나 꼭 지켜 야 할 다음과 같은 일반원리가 있다. 첫째로, 바람직한 미세구조를 얻는다는 것은 유리내의 결정핵생 성속도를 높이는 것과 밀접한 관계가 있다. 槪知하는 바와 같이 全유리의 표면상에서의 결정핵생성에 의해서는 만족할 만한 물리적 성질을 갖는 결정화물질을 보통 생성할 수 없다. 그러나 일부 표면 . 결정화된 유리는 우수한 기계적 성질을 나타낼 수 있다• 만약 결정 화될 수 있는 유리를 미세분말로 한 다음 소결과정에 의해 큰 물잘 (bulk ma t er i al) 로 만들 때 유리 의 입 자표면에 충분한 수의 결정 핵 을 생성시킨다면 만족스러운 미세구조를 얻을 수 있다. 유리전체를 결정화시키기 위해서는 물질 내부에서 결정핵의 밀도 가 높도록 하여야 한다. 보통, 대부분의 유리에서는 군질핵생성이 일어날 수 없으나 어떤 限定組成範園(예 ; L i 20 합량이 많은 조성범위)` 에서는 군질핵생성이 일어나 결정화유리를 충분히 만들 수 있다. 미제입자로 된 결정화유리를 만들기 위한 최적 조건은 대부분의 결정상이 빠른 속도로 성장할 수 있는 온도 바로 아래의 온도에서 유리 중의 결정핵을 생성시키는 것이다. 서로 인접한 空間中心으로-
부터 계속적으로 결정율 성장시키기 위해서는 핵생성입자들의 말‘ 도를 높이고 분산을 군일하게 하여야 한다. 租大한 결정을 갖고 있 는 결정화유리는 결정의 방향이 제멋대로 (random) 라고 할지라도 徽 · 密한 미세입자로 된 구조를 갖는 결정화유리와 같이 만족스럽지는 一 못하다. 內部核生成자리 (int e r nal nucleati on s it e) 의 밀도를 높이 기 위해 유 리에 핵생성촉진제인 성분을 첨가하는 것이 결정화를 제어하는 수 一 단이 된다. 핵생성촉진제는 용융유리 중에서도 용해되지만 냉각중 · 또는 처음의 냉각된 유리를 재가열하는 동안에 유리의 구조변화에 참가하거나 증진시키기도 한다. 어떤 경우에는 핵생성촉진제는 군 질핵생성에 의해 찰 분산된 형태로 석출되기도 한다。 이런 방법으 로 형성된 핵들은 主結晶相이 불군질핵생성을 일으키도록 할 수도 있다. 이상과 같은 방법우로 기능을 발휘하는 핵생성축전제는 몇 가자 기본적인 조건을 만족하여야 한다. 즉 군질핵생성속도가 높아야 하_ 므로 핵생성을 위한 활성화에너지가 낮아야 한다. 다시 말하면 과 포화도가 높고 핵과 유리 사이의 떤간에너지가 낮아야 한다. 또 핵 울 형성하기 위한 원자나 이온들의 확산에 필요한 활성화에너지는 embr y o 가 안정한 크기로 성장할 수 있도록 낮아야 한다. 主相의 결정성장을 증진시키기 위한 핵생성입자의 능력은 핵생성 ! 입자와 결정화되는 相「버의 떤간에너지 및 핵과 석출상의 格子常數 : 사이의 類似性(構造의 類似性)과 같은 인자들에 의해 좌우된다. 위에서 논의된 것처럼, 핵생성촉진제가 직접 결정핵율 제공할 것 이라는 가능성 이외에도 또 다른 가능성이 있다. 죽 핵생성촉진제 는 0석 상온도 이하에서의 分相을 촉진시켜 결정핵생성의 동력학에 좋은 영향을 줄 것이라는 것이다. 결정핵생성과 성장 전에 일어나는 2 유리의 분상은 여러가지 방법 으로 재가열중 유리의 거동에 영향을 미친다. Uhlmann45) 이 지적하였던 것처럼 핵생성을 위한 구동력은 이전 보다 더 커지며, 핵생성자리로 작용할 수 있는 면간이 생기고 原子· 45) D. R. Uhlmann, Di sc ussio n remarks, Trans. Faraday Soc. , !IB( l97 0).
移動度가 증진되며 2 상간의 면간영역에서 국부적으로 핵생성에 대 한 큰 구동력 또는 큰 이동도를 가져오는 일부 성분이 많아지게 된 다. 이 런 인자들 중에 서 원자이 동도의 중가가 가장 중요하다고 Uhlmann 은 생 각하였 다. 유리의 분상결과 생긴 구조와 여러 原子種의 변화는 1 상 또는 2 상 모두에서 균질핵생성의 가능성울 증가시키며 이런 방법으로 생 건 핵들은 다른 결정상들이 불군질핵생성을 일으키도록 한다. 유리에의 첨가제가 결정화과정에 미치는 영향에 대해 이미 논의 하였던 몇 가지 機構 以外에도 다른 영향이 있다. 지금까지 기술하였 던 것처럼 석출상과 母相「1 31 의 떤간에너지는 석출상이 결정질일 때 는 특히 핵생성의 장벽이 된다. 만일 이 떤간에너지가 어떤 방법으 로 낮추1 질 수 있다면 핵생성은 쉬워질 것이다. 만약 표면활성성분 이 고체-액체의 떤간에서 농축된다면 표면자유에너지는 낮아질 것 이다. H illig 46) 는 이런 가능성을 연구하여 표면자유에너지가 낮아지 는 것은 2 相間境界의 확산에 의한 것이며 산소이온의 分極半(p olar i z ab ility)을 높이는 이온들(예 ; T i+ ◄ :)은 용융체-고체의 면간을 만드는 데 기여하는- 일을 낮춘다고 제안하였다. 이와 같은 영향을 실험적 으로 관찰하기는 어렵지만 촉매에 의한 결정화를 고려할 때는 무시 할수없다. 끝으로 결정화유리의 미세구조를 결정하는 결정성장속도의 역할 에 대해 언급하겠다. 결정성장은 취급하기 쉬운 방법 및 경제적인 시간에 全유리의 결정화에 적합한 속도로 진행되어야 하며 매우 빠 른 결정성장속도는 미세입자를 갖는 미세구조의 발달을 중전시키지 는 못한다. 이런 조건하에서 결정성장아 일단 한 핵생성자리에서 시작되떤 결정성장면이 너무 빨리 이동하여 인접자리에서의 結晶成 長開始를 방해하게 된다. 즉 급속한 결정성장은 작은 결정을 재분 해시키고 큰 결정은 더 커지는 미제구조의 租大化條件울 의미한다. 이 과정에서 결정과 유리상간의 全面間面積은복합재료(결정과 유리) 의 표면자유에너지를 낮추면 감소된다. 이런 근거로부터 알맞는 결
46) W. B. Hil lig, Sy m p os iu m on Nucleati on and Crys t a l liz a ti on of Glass, p. 77, Americ a n Cerami c Socie ty . (19 62).
정 성 장속도를 얻는 유리조성의 선택 및 결정성장을 여제하기 위한 성분의 첨가는 결정화과정윤 제어하는 중요한 인자들이다. 앞에서 논의된 내용은 생성되는 결정의 크기와 수를 제어하기 위 한 방법이었으나 이와 함께 핵생성촉매를 잘 선덱하면 생성되는 결 정모양을 어느 정도 조절할 수 있다. 다성분계 유리는 용액 중에서 둘 또는 그 이상의 결정상성분을 함유하며 그 중 일부 또는 全결 정상을 석출시킬 수 있다. 만약 핵생성촉진제의 구조가 어떤 한 상 의 구조와 비슷하다면 이 상은 연처리의 특정조건하에서 평형상이 아닐지라도 아주 쉽게 석출될 것이다. 한 결정상이 처음 생기면 찬 여유리의 조성이 변화되어 다론 상들의 석출을 가쳐오게 된다. 따 라서 핵생성촉진제의 선택은 결정화유리에서 생기는 결정상에 ~ 영향을 미찬다. 같은 결정화촉진제일지라도 열처리과정이 다르면 최종적으로 촌재하는 결정상의 성질 및 종류도 변하게 된다.
제 3 장 結晶化를 제어하기 위한 結晶核 生成保進劑와 유리型 실용재료로서 결정화유리의 성질은 主要析出結晶相과 微細構造에 의해 결정된다. 주요석출결정상은 유리의 기초조성에 의해 거의 걷 청되나 미세구조는 기초조성 이의에 유리를 軟化變形시키지 않고 미세한 결정입자의 집합체로 변화시키는 역할을 하는 微量添加物 즉 結晶核生成保進劑 (nuclea ti on ag en t)의 有無 및 景에 의해 영향을 받는다. 핵생성촉진제의 작용으로는 a) 유리의 分相保進, b) 不均 質結晶核生成울 일으키기 위한 異種結晶表面의 提供, c) 유리구조 의 변화에 의한 均質核生成의 保進 둥을 생각할 수 있으나 각종 결 정화유리에 대해 핵생성촉진작용이 어떤 기구에 의한 것인가는 아 직도 명확하지 않다. 따라서 以下에서는 결정핵생성촉진제의 종 류에 따라 결정화유리를 분류하여 설명하고 결정화유리를 만들기 위한 성질을 구비한 유리의 기초조성, 죽 유리型에 대하여 설명하 겠다. 3. 1 結晶核生成徒進濟 l 의 種類 표 3.1 에 결정핵생성촉진제로 사용되고 있는 성분과 그것에 적 함한 유리의 기초조성을 정리하여 나타냈다. 3. 1.1 金屬의 分離에 의한 核生成 결정화촉매 또는 핵생성촉진제에 대한 필수조건 가운데 하나는
표 3.1 結晶核生成徒進劑에 의 한 結晶化유리 의 分類 感結光晶性核貸生金成屬劑 | Li2 0基 — 礎A유l2리 °3의— S例i0 2 I 主L要i2 析0 ·S出i0 結2 晶相 I 紫外特線 照射徵 費Au金R,hA屈, gP ,dPC ,t uO (R s,u I, r) LLii22 00 —— ( -SMNig0 a2 O 2 —0 -AKl22 °30 ) LL/3-ii 22 S00 p•• o22 d SSuiim00 2e 2 n e 1 t學切削用 -Si0 2 ZTri0 02 2 LMLNiha2g 20OO 0 — — —- AAAAlhI2h20 0 O 033—3—J - —_SPSS S2iii000i 0 0 5 2 22 2 ¢BCNu-mo-e 石rpe石d h英ni英 eee ,lr, i in/t e e 3 i證 d2- 高勅低低絶彬强彬緣化眼眼抵用 抗 低損失 Si0 2 Li2 0 - Al2°3-Si0 2 /3-石英 低彭帳 一 B03 FCer220033 CL ai 2O0— -AMlg2 O 아 — -ASl 2i 00 23 Di op si d e , -Si0 2 Gelenit e V20s, Ni O L i :?. 0 一 Ah03 ― S i 02 s無FAP 2s 020s 3 PLLLLLN알iiibiia2222 2루 20O000 00 —미——-—- - A TSMS노AC1iiiIg020O실 2a 22 O° z° O 리—3 3— — ——-게S MASSSi이0h iigi 200 0O O 2트2 2 J r//풀L33i--ic z 로 SS h0 pp t오· e o o2 r d d르Si uutie m m0 2 ee nnee 易强高誘溶强融電度 性 Al203 PbTi0 3 Li2 ° _ Zn0— 一A Sh i0 032 W illem i te -Si0 2 그것이 콜로이드 (collo i d) 의 크기를 갖는 分散粒子로 유리내에 촌재 할 수 있어야 한다. 이런 금속들은 많으며 이런 조건을 구비한 금 속산화물들은 단지 열을 加하거나 환원분위기 중에서 용융시키면
쉽게 금속으로 분리된다.
(1) 유리 중에서 금속콜로이드의 形成 Cu 와 A g산화물은 환원분위기에서 용융하면 유리 중에 원소형태 로 얻어지는 대표적인 금속들이다. 또 Au 와 P t족 금속들도 유리 중에 서 쉽 게 금속이 된다. We y ll) 은 Ag , Au, Cu 와 같은 금속이 유리 중에서 콜로이드분산입자로 촌재하는가를 조사하고, 이들 금 속은 유리용융체 중에서 眞溶液*(tr ue solu ti on) 으로 얻어지며 용융유 리의 냉각을제어하돈가 냉각된 유리를 재가열하여 유리를 열처리하 떤 먼처 금속원자의 작은 집합체가 생성되어 이것이 결정성장의 핵 으로 작용하게 된다고 생각하였다. 이들 입자는 콜로이드 크기로 성장하며 어떤 경우에는 눈으로보이는결정과 같은크기로도 된다.
1) W. A Wey !, Coloured Glasses, Soc iet y of Glass Technolog y (19 51 ). * 眞溶液은 크기가 l0_,cm 보다 작은 溶質이 녹아 있는 溶液.
주석 산화물은 유리 중에서 금속분산물을 형 성 하는 중요한 역 할을 하며 유리용융물 중의 금속의 용해도를 높이는 역할도 일부 한다. Cu 는 유리 중에서 착색 또는 光學的勅果를 나타낸다. 즉, 콜로 이드 크기의 결정형으로 금속구리를 형성한 구리 - 루비유리 (co pp er ruby g lass) 를 형 성 한다. 만일 Cu 를 함유한 유리 가 산화조건하에 서 용융되면 구리는 靑色울 띠는 Cu2+ 로 주로 촌재하며 Cu+ 도 일부 촌재하게 된다. Cu+ 는 分光의 可視領域에서 흡수를 일으키지 않는 다. 還元度가 커질수록 Cu+ 의 바울이 큰 쪽으로 평형은 이동하여 나중에는 요원소가 생성된다. 따라서 유리 중의 Cu 상태는 용융조 전과 유리조성에 크게 좌우된다. SnO 는 특히 환원제로 적합하여 다음과 같은 반응을 한다. Sn 2+ +2Cu+ 一 Sn 1+ +2Cu (3-1) 이의에도 SnO 는 유리 중의 금속구리의 용해도를 높여 구리가 용` 웅유리 중에서 원자집합체와 같이 촌재하도록 한다. 이런 조건하에 서 Cu 는 가시영역의 흡수를 하지 않는다. Cu+ 과 구리원소를 함유 한 유리용융물을 급냉시키면 無色유리가 얻어진다. 만일 이 유리를· 충분히 높은 온도로 재가열하면 s t r i k i n g현상으로 알려진 질은 赤.
色의 구리-루비가 형성된다. Cu+ 은 다음의 반응에 의해 더 환원된 다. Cu++e_+Cu (3-2) 이 반응에 서 의 전자들은 Sn“ 나 Sb3+ 이 Sn4+ 나 Sb5+ 로 산화될 대 공급된다. 이 렇 게 형 성 된 Cu 원자들은 str i k i n g 온도에 서 확산되 어 핵생성과 성장과정에 의해 빛을 통과시키는 데 영향을 미칠 충 분한 크기의 Cu 입자가 성장된다. 구리유요비유리를 제조시 소오다 석회-실리카 조성의 유리도 사용할 수 있으나 금속구리에 대한 용 해도가 큰 高납유리가 주로 사용되고 있다. 着色을 완전히 하기 위 해 보통 구리 의 함유량은 0. 2~1 %이 다. 실두를 제어하키 위한 목적으로만 콜로이드상으로 분산된 구리를 사용할 때는 o.05% 정도의 낮은 함유량으로도 충분하다. 이 예로는 L i 20-Al203-S i O 검 Li 20 ― ZnO ― S i아 유리 가 있 다. 구리 콜로이 드 의 입자 크기가 작으면 착색효과는 나타나지 않으나 제어된 결정 화과정에서는 불군질핵으로 작용할 수 있다. 유리착색제로 콜로이드입자의 금속은도 사용되어 왔다. 응용분야 로는 유리를 황 또는 호박색으로 착색하는 데 사용된다• A g를 1% 이상 함유한 규산영유리에서는 Cu 보다 A g는 이온상태로 불안정하 여 산화조건하에서 용융시 A g의 침전이 생기나, 일부 인산영유리 에서는 10~15% 의 A 압 이 용액 중에 촌재할 수 있다. 산화조건하 에서 A g를 함유한 유리가 용융될 때 A g의 대부분은 A g+로 존재 하나 A g원자둔도 촌재한다. A g+은 유리구조 중에서 N 값에서와 같이 구조적 자리 (str uc tu r al s it e) 를 접 유하는 망목형 성 물로 작용한다. A 합은 착색효과를 갖지 않으며 A g원자도 무색이나 A g원자의 존 재는 유리가 자의선에 照射될 때 일어나는 강한 盛光에 의해 알 수 있 다. Ag + 오} Ag 원자간의 평 형 은 유리 뱃 지 (batc h ) 중의 산화제 나 환원제의 존재 또는 遺零園氣, 용융온도, 기초유리의 조성 둥에 의 해 결정된다. A g를 함유한 유리를 냉각하면 거의 무색안 유리가 얻어지나, 재가열을 하면 유리는 s t r i ke 되어 黃號泊色(y ellow amber -c olour) 이 된다. 이런 착색현상온 핵생성에 의해 A g원자의 집합체
까 형성되어 이것이 유리에 조사되는 빛을 선택적으로 흡수하기 때 문이 다. SnO 는 고온에 서 금속은의 용해 도를 높이 며 str ik i n g 중 A 압 을 Ag 원자로 환원시 키 기 때 문에 유용한 성 분이 다. Badg e r 등 2) 온 A g를 함유한 유리를 열처리하기 전에 紫外線照射를 하면 낮은 온도에서 s t r i ke 되기 때문에 자의선조사에 의해 핵생성이 강화된다 는 것을 알았다. 이 현상온 感光性유리 및 결정화유리의 제조에 매 우 중요하다. Au 도 유리착색제로 알려져 있으며 특히 미려한 루비유리를 만 드는 데 사용된다. 이 착색효과는 콜로이드 크기의 Au 입자 때문이 타고 생각된다 Au 는 보통 AuC13 로 유리 중에 첨가되며 고온에 서는 대부분 유리 중에 녹는 Au 원자를 만든다. 그러나 동시에 일 부 Au3+ 으로도 존재한다. 고납유리는 金色울 나타내는 데 좋으며 1/105 정도로도 흐린 淡紅色울 나타낼 수 있다. 전한赤色은 유리 중 에 1/103 정도의 Au 를 함유시켜야 한다. Au 는 Pb 가 없는 유리에 서는 용해도가 작기 때문에 같은 효과를 얻기 위해서는 SnO 를 첨 가하여야 된다. Sb2 아도 Au 의 콜로이드입자형성에 효과적이다. Au ― 루비유리의 형성에서 일어나는 과정은 다음과 같다. Au 는 .A u 와 Au3+ 의 금원자들의 평 형 혼합물로 존재 한다. 만일 유리 가 급 냉되면 Au 의 고온상태는凍結되어 유리는무색이 된다. 유리를徐 冷點 (annea li n g poi n t ) 以上의 온도에 서 재 가열하면 Au 원자들이 집 합되어 Au 의 핵을 형성하고 이들이 성장하여 5~50nm 크기로 되 어 빛을 선택적으로 흡수하게 된다• Au3+ 이 Au 원자로 환원되는 것은 재가열중 다음의 반응에 의해서도 일어날 수 있다. Au3++3e---+Au (3-3) 이 반응에서 필요한 전자들은 유리 중에 촌재하는 Sb 나 Sn 의 원 자가 상태의 변화에 의해 공급될 수 있다. Sb3+ 一 Sb5++2 e (3- 4) Sn2+ 一 Sn•++ 2e (3-5)
2) A. E. Badg er and F. A. Hummel, Phys , Rev. , 68, 231(1945).
유리 중에서 콜로이드입자를 이루는 P t는 단치 灰色만을띠기 때 문에 착색제로 사용되지 못하나 P t의 콜로이드입자는 유리 중에서 의 다른 過砲和相에 대해 핵생성자리로 작용할 수 있어 유리전체를 결정화하는 데 중요한 금속이 다. P t의 콜로이드입자를 형성하는 과정은 Cu, Ag , Au 와는 다르 다. 중요한 차이는 P t의 경우 재가열단계가 필요없다는 것이다. R i ndone3) 에 의하면 유리뱃지 중의 영화백금은 열에 의해 분해되어 유리용융체 중에서 콜로이드입자가 된다. 유리조성 중에 P t가 일 부 이온상태로 촌재할 수 있다는 것은 부정할 수 없다. 그러나 이 것은 P t가 일부 유리 중에서는 약간 녹는다는 사실을 보면 알 수 · 있다. 이 용해도는 불활성분위기나 진공하에서 용융울 하면 感知 할 수 있을 정도로 작으나, 공기나 산화분위기에서 용융을 하면 용 해도는 작으나 측정할 수 있다. 따라서 P t금속이 용융유리 중에서 不溶性인 반면 산소와 반응하여 생 긴 이 온성 Pt 는 溶解性이 있 다. P t의 이온상태가 유리용융체 중에 촌재한다면 용융체가 냉각중 계속해서 환원반응이 일어날 수 있으며 이것은 결정핵 및 성장과정 에 의해, 촌재하는 P t입자의 성장 또는 더 많은 입자들이 계속 석 출하도록한다. 앞서 기술한 4 가지 금속의 콜로이드입자 형성능력은 다음과같다. Cu>Ag > Au>Pt Cu 의 경우콜로이드입자형성은착색반응인 식 (3 一 2) 의 환원반응에 의해 알 수있다. Sn,Sb,As 와같이 원자가가변하는 이온들은콜로 이드형성에 중요한역할울한다. 동시에 Cu 원자가냉각된유리 중에 촌재할 수 있어 콜로이드형성에 필요한 확산과정에 참여케 된다. Pt 의 경 우순근 환원과 콜로이 드형 성 은 가열 만으로 가능하며 Cu 유리 의 str iki n g 에 해 당하는 저온에서 의 환원과정은 불필요하다. 비 슷 한 거 동은 Pt 족 (Ru, Rh, Pd, Os, Ir) 중의 다론 금속에 서 도 비 슷하다. A g의 경우, 환원과정은 콜로이드형성중에 일어나며 Sb2 아나- SnO 가 필요하다. Au 에서는 이온이 금속으로 환원되는 과정이 제
3) G. E. Rin d one, J. Am. Ceram. Soc. , 45, 7(1 9 62).
가열중에도 일 어나 A g나 Cu 보다는 산원과정이 콜로이드형성에 약간 더 중요하다. (2) 核生成保進 ~l j로서 金屬콜로이 드 영 국특허 No. 863569(1961) 에 의 하면 Ru, Rh, Pd, Os, Ir, Pt 금속들 울 2 가지 기초유리를 결정화시키기 위한 泥進齊 I J (ca t al y s t)로 0.001~ o.1% 사용하였다. 기초유리들 궁 첫번째는 R20 ― BaO ― S i 02 계로 0조~성10은, WK2 t0%; 로o ~S10i0 이2 ;다5.0 ~두85번, 째B a유O리; 3는~ 4L5 i , 20 —L i2A0l 2; 0 30—~ 2S5i 0, 2 계N a로20 조; 성 W t%는 Si0 2 ; 60~85, Al203;2~25, Li 20 ; 6~15, Na20/ K 20 ; 0~4 아 냐 이 런 유리 들은 용융시 유리 뱃 지 중의 Pt 족금속화합물은 산화분위기하에서도 분해되어 유리 중에 균일한 금속분산입자가 된 다. 이런 유리들을 처음에 580~650°C 로 가열하고 다음에 700~ 850 ° C 에서 가열하면 거의 완전히 결정화된다. 이런 방법으로 얻어 진 결정화유리들은 훌륭한 기계적 및 전기적 성질을 갖는다. R i ndone” 은 Li20 · 4 Si0 2 유리 에 Pt 를 핵 생 성 촉진제 로 사용하였 다. 소량의 P t는 결정화속도를 증가시킬 분만 아니라 작은 결정 (50nm 이하)이 매우 군일하게 분포되도록 하기 때문에 유리의 결정 화를 중전시킨다는 사실을 발견하였다. 또 600°C 와 650°C 에서 유 리의 결정화속도와 P t농도간의 관계를 X- 선회절분석에 의해 조사 하였다. 두온도에서 최대결정화를나타내는 P t의 최적농도가 촌재 하며 600° C 에 서 는 0. 04~o. oo7Pt% , 650° C 에 서 는 0. 008~·o . 011Pt %이었다. o.025P t%에서는 L i 20-2S i 02 의 결정화가 상당히 감소되 었으며, 그 이유는 결정형실리카가 고온수석물인 석영으로 석출되 기 때문이다. L i 20•2S i 02 의 결정화에 대한 활성화에너지는 P t의 농도가 0 으로부터 0.005% 로 증가할 때 최저값으로 급격히 감소되 었다. P t함유량을 약간 증가시키면 활성화에너지도 약간 증가하는 경향을 보였다. 그는 Li 20•2S i 02 를 핵생성시키는 P t의 능력은 Pt 결정의 (111) 면과 Li 20•2S i아의 (002) 면의 d i sre gis t r y가 거의 5% 이 타는 사실과 관계가 있을 것이라고 생각하였다. 이것은 Turnbull 등쩌 우수한 핵생성촉진제는 최대 d i sre gis t r y가 10~15% 內에 4) D. Turnbull and B. Vonneg u t, llldustr . Eng n g. Chem. , 44, 1292(1 9 52).
있다는 제안과 일치한다. 그는 또 P t核의 크기에 관해 연구하고 、 o.oo5P t%의 최적농도에서 5nm 의 핵의 크기가 결정화를 위한 많은 수의 자리 (s it e) 를 제 공하며 이 경 우 유리 l g당 1013 개 의 Pt 핵 이 존 재하게 된다는 결론을 얻었다. 이 값은 약 450nm 인 입자간의 평균 간격에 해당된다. Thakur” 는 示差熱分析을 사용하여 Li2 0 • 2S i아 유리 의 핵 생 성 에 는 유리 100g 중 Pt 가 8~32 x 10-5mole 또는 Ag 가 6~8 x 10-3mole- 필요하다는 것을 알았다. (3) 核生成徒進劑에 서 感光性反應 앞에서 유리를 열처리하기 전에 방사선을 照射하면 A g의 착색이 촉진된다는 것을 기술하였다. 이 효과 및 비슷한 현상들은 처음에 감광성유리를 만들고 후에 감광성으로 핵생성시키는 결정화유리의 기초가 된 Au 와 Cu 에서도 볼 수 있다. 최초의 감광성 유리 로는 Dal t on6) 이 활성 성분으로 Cu 률 사용하여 자 의선율 조사하면 더 낮은 온도나더 짧은시간에 착색유리가 된다는 빠 사실을 알았다. 만일 유리표면에 사전음화를 놓는다든가 하여 선덱 적 으로유리를 조사시킨 후적당한 열처리를하면 유리 중에 像(i ma g e) 이 생간다. 감광성 유리의 基本機構는자의선이나 방사선조사중에는 빠 숨은 상(l a t en t i ma g e) 이 생기고 열처리과정중 像이 생긴다는 것이다. 숨은 상의 형성은 식 (3-2) 에 의한 Cu 원자의 생성에 의한 것이다. 이 반응에 필요한 전자들은 다음의 반응에 의해 얻어진다. Cu++hv---+Cu2+ + e (3-6) 따라서, 유리의 조사된 부분은 조사되지 않은 부분보다 더 높은 농 따 도의 Cu 원자를 포함한다. 결과적으로 Cu 의 핵생성과 결정화는 조 사된 부분에서 더 쉽게 일어날 것이다. S t ooke y 7) 는 Ce02 의 소량 (0.05% 정도까지)을 첨가하면 감광성원소느 로 Cu 를 함유한 유리의 감광성이 촉진된다는 것을 알았다. Ce 은:
5) R. L. Thakur, Advances in Nucleati on and Crys t a l liz a ti on in Glasses, p.1 66. Americ a n Cerami c Soc iet y (19 71 ). 76)) SR.. DH.. SDtao lo t!o'e n y,, UB. rSit.. PPaatte en n t t NNoo. .2 643252644792 ((1199 4477))..
다음의 반응에 의해 이온가가 쉽게 변하여 감광성을 촉진한다. Ce3++hv-->Ce4++e (3-7)· 또는 Ce3+ + cu++hv_•Ce ◄ ++Cu (3-8) 이 후 Na20, Al2 아, BaO 또는 ZnO 를 함유한 규산영 유리 에 서 Ag 와 Au 도 감광성원소로 작용한다는 것을 알았다. Ce 아를 o.05% 까 지 또는 Sb203 를 O. I% 까지 함유한 유리 는 감광도를 증가시 킨다. 이 런 유리 에 자의 선을 조사하고 500~600°C 에 서 가열하면 금속이 석 출되 어 착색 된다. Sb203 으} Ce02 의 기 능은 Cu+, Ag +, Au+ 둥에 전자들을 꽁여하여 유리가 재가열될 때 집합될 수 있는 금속원지들 로 전환시키는 것이다. S t ooke y 8) 에 의해, 선택적 조사와 열처리에 의해 생간 불두명한 像이 Li 20-2S i 02 나 Ba0•2S i 02 결정으로 된 감광성유리가 만들어졌 ` 다. Cu, Au 또는 A g가 소량 존재하는 상태에서 자외선조사 후연 처리를 하면 콜로이드의 금속입자가 석출된다. 이들 입자가 규산염 . 의 결정화를 촉진시킨다. 이것은 유리로부터 결정화를 위한 핵생성 의 제어방법(불군질핵생성) 중 초기의 한 예로서 결정화유리의 발전 에 중요한 단계가 된다. S t ooke y”는 Si0 2 ; 60~85%, Li 20 ; 5. 5~15%, Al2 아; 2~25% 의 ’ 조성 인 유리 에 감광성귀금속으로 Au; o. 001~o. 003%, Ag C l; o. o, 01~o.3%, Cu20; o.001~1% 를 각각 첨가하고 자의선을 조사하였 다. 다음에 徐冷點(l o gT) =l3.4, 7/; 접도)과 軟化點(l o gr; =7.6) 사이의 ’ 온도인 500~540°c 에서 가열하면 금속원자가 집합되어 Cu, Ag 또 는 Au 의 미세한 결정이 형성된다. 이 입자들은 Li20 •Si0 2 (meta s ili - ca t e) 상의 결정화를 촉진시킨다. 유리가 L i 20 와 K20 를 다량 함유 하고 있다면 결정질은 거의 L i 20•S i 02 가 되나, 유리 중에 S i 02 가 다량 함유되어 있다면 L i 20•2S i 02 와 석영의 결정들이 생성된다.
8) S. D. Sto o key, U. S. Pate n t No. 2515275 (19 50). 9) S. D. Sto o key, Brit. Pate n t No. 752243 (19 56).
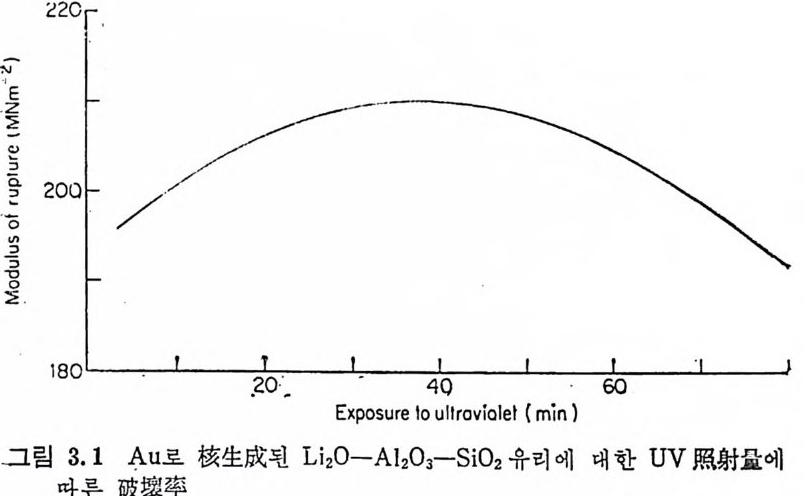
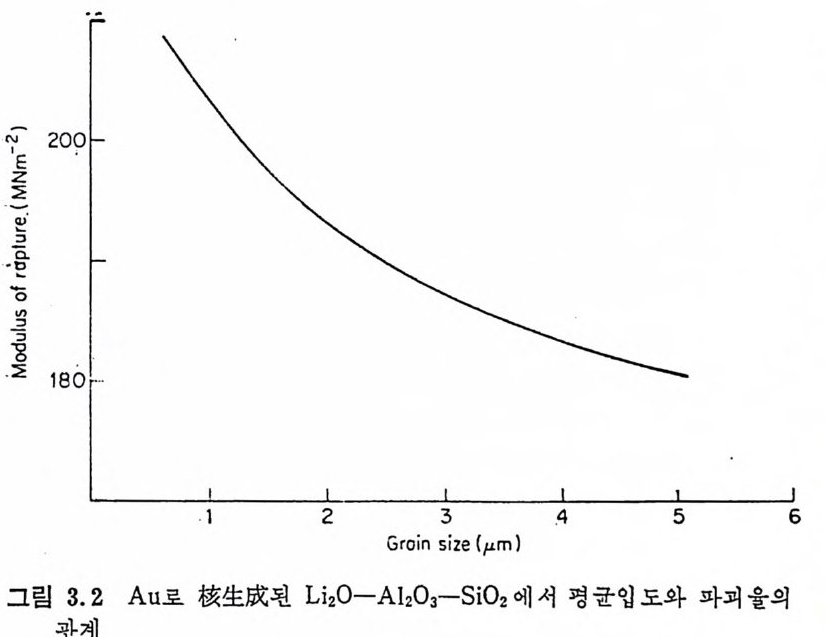
Al 요 가 많은 유리 에 서 는 /3-sp o dumene (Li2 0 • Al203 • 4Si 02 ) 이 나 /3 -s p odumene- 석 영 의 固溶體가 생 성 되 기 도 한다. 이 단계 에 서 유리 논 금속의 핵생성입자들 주위에 Li 20,2S i아나 다론 화합물의 얇은 결정들로 인해 거의 불두명하게 된다. 이들 결정 사이에는 유리가 남아 있다. 온도를 천천히 상승시키면 (5°C/m i n) 더욱 결정성장이 진행되고 생성된 결정들은 재료가 견고성을 갖도록 하며 온도가 상 승할 때 변형을 방지한다. 유리를 950°c 를 넘지 않는 上限溫度로 가열하고 약 1 시간 동안 유지하여 냉각시킨다. 열처리 결과 유리는 유리狀매트릭스가 약간 있는 다결정질고체로 된다. 이런 공정에 의 해 만들어진 결정화유리는 높은 기계적 강도, 우수한 전기적 성질 둥 수많은 바람직한 성질을 구비하게 된다. St oo key 등 10) 에 의 하면 光核生成反應에 의 해 생 성 된 금속결정 들 은 크기가 일정한 촉진제가 된다. Li 20,2S i 02 는 금속촉진제가 약 8nm 의 크기로 될 때까지는 결정화가 일어나지 않기 때문에 금속의 핵생성입자에는 임계 크기가 있다. S t ooke y 11) 는 금속의 핵생성촉 진제의 효력은 금속과 핵생성되는 상의 결정구조들 사이의 類似性 과 관계 가 있 다고 생 각하였 다. 따라서 NaF, Li2 S i 03 및 BaSi2 0 5 의 결정상들은 Au, Ag , Cu 또는 P t에 의해 핵생성될 수 있으며 각 결정상의 원자간거리는 적어도 금속결정의 원자간거리와 비슷하다 고 지적하고 있다. Mi les 등은 감광성 핵 형 성 된 Au 를 함유한 Li 20-Al 요― S i 02 결정화유리의 미제구조는 자의선조사량에 좌우된다는 것을 지적하 였다. 그림 3.1 은 자의선을 조사한 후 520°C 에서 1 시간, 620°C 에 서 1 시 간 그리 고 900° c 에 서 1 시 간 열 처 리 한 L i 20-Al203 一 S i 02 유 리의 자의선조사시간에 따른 破撲率 (modulus of ru pt ure) 의 변화를 나타낸 것이다. 平均粒度 (mean gra in s i ze) 와 기계적 강도와의 관계 를 나타낸 그림 3. 2 를 참고로 한다면, 약 230MNm-2 인 최 대 강도는 약 1µm 인 최소평군입도와 관계가 있다고 생각된다.
10) S. D. Sto ok ey and R. D. Maurer, Prog re ss in Cerami c Scie n ce, Vol. 2, p.7 7. Perga m on Press, New York (19 62). 11V) S0. 9D5. 9S).t o o key, G/aste c h Ber. V Inte r nati on al Glass Cong re ss, 32K, Heft
 22C 「
22C 「
 (,ZE 2 。。
(,ZE 2 。。
최적자의선조사량이 촌재한다는 사실은 다음과 같이 설명된다. 자외선조사되는 유리에서 생성되는 Au 원자의 수는 자의선조사량에 의해 좌우된다. s20°C 에서 열처리시 유리 중의 Au3+ 는 더욱 환원
되어 미리 촌재하고 있는 Au 원자에 의해 핵생성되고 Au 입자들의 ’ 성장이 일어난다. 이런 반응이 불균질핵생성에서 연속적으로 일어 나기 위해서는 Au 입자들은 최소임계반경을 가져야 한다. 그러나 자외선조사량이 너무 크면 모든 Au 입자가 최소임계반경으로 연속 적으로 성장하기에 불충분한 Au3 + 가 유리 중에 남게 된다 . 따라서 임계반경이 얻어지는 Au 입자의 최대농도를 언을 수 있는 최적자 의선조사량이 촌재하게 된다. 3. 1. 2 酸化物의 分離에 의한 核生成 규산영유리에 산화물을 첨가하였을 때 分相이 일어나는열역학적, 구조적 이유를 생각하고 그 예를 들겠다. (1) 酸化 物 系에 서 二相分離 2 장에서 설명한 것처럼, 분상의 열역학적 이유는 명확하지만, 구 조적 이유는 불확실하다. 핵생성제인 산화물을 첨가하면 분상이 일 어나며 이런 2 상분리는 제 2 상의 매트릭스내에 다론 한 상이 콜로 이드입자로 분상되어 있는 형태로 나타난다. 수많은 산화물들은 용 융유리를 냉각하거나 냉각된 유리를 재가열중에 유리내에서 위와 같은분상을 일으킨다. 2 상분리에 대한 구조적 이유를 생각하기 위해서는 網 目 修飾 이온 一 들로부터 網目形成 陽 이온의 분리효과를 고려하는 것이 편리하다. 여기서는 주로 규산영유리에서의 효과를 기술하겠다. 규산영유리의 망목은 S i 04 사면체로 이루어지며 이것이 異種構造 · 單 位(사면체나 삼각형)와 결합하여 複 合網目 楠 造가 된다. 侵 入 單 位 (intru siv e un it)의 농도가 낮을 때는 S i 04 구조는 안정하므로 單 相유 리가 만들어지며, 농도가 높을 때는 異種構造單 位의 방해효과 때문 에 Si0 2 가 ric h 한 상과 다른 상이 ric h 한 2 상으로 분리 된다. 만일 첨가한 산화물이 주성분을 이룰 정도로 농도가 더 커지면 S i 04 사면 체가 두번째 산화물의 망목 중에 용해되어 單 相系가 형성된다. 따 · 타서 2 망목형성산화물 사이에 구조적으로 不調和(i ncom p a ti bility)가 일부 생길 때 2 상분리가 일어나는 조성범위가 존재할 것이다. 서로 다른 형의 망목구조간에 부조화가 생기는 2 가지 기본적인
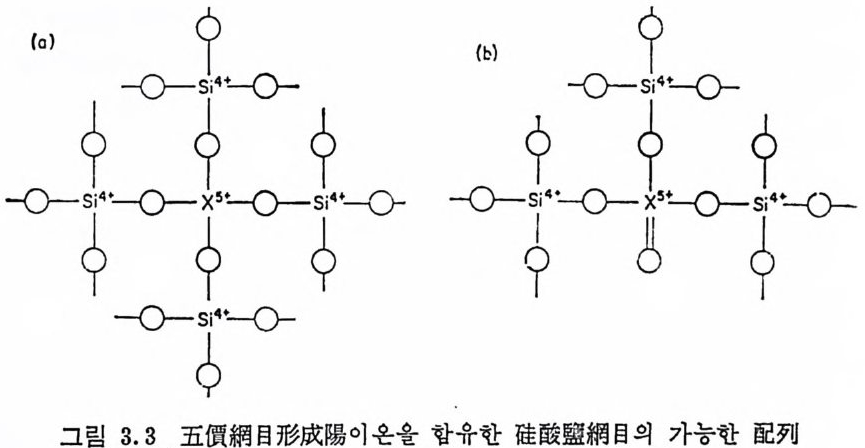
• 이유가 있다. 첫번째 이유는 기하학적 고찰에 근거를 둔다. 규산염 망목은 불규칙 적 구조를 하고 있으나 S i― 0 一 S i 의 結合角과 Si- - 0 거리는 평군값과 큰 차이가 없다. S i 04 단위크기와 큰 차이가 있는 이종망목형성단위가 도입되면 S i― 0 결합은 비들려질 것이며 이종 산화물의 농도가 임계한계를 넘으면 系의 전자유에너지를 낮추기 위해 2 상으로 분리될 것이다. 기하학적 효과에 의존하는 분상의 다 른 형태로는 첨가된 이온의 配位數가 변할 때이다. 많은 양이온둘 은 온도가 높아침에 따라 배위수가 작아진다. 이때 용융상태에서는 사면체를 이루어 규산염망목과 조화를 이루나, 냉각하면 평형배위 는 팔면체가 된다. 이런 경우 용융체를 냉각하거나 냉각된 유리를 재가열할 때 분상이 일어나게 된다. 두번째 이유는 기본적인 망목 형성이온 (S i 4+ )의 전하와 이종망목형성산화물이온의 전하가 다를 때 망목형성위치가 불안정하게 되기 때문이다. 예를 들면 中心陽이온 이 S i 보다 전하가 더 크다면 규산영망목에서 사면체단위는 收容 하기가 어렵게 된다. 이런 망목구조를 그림 3.3 에 실었다. 만일 이 와 같은 배열이 생긴다면 X5+ 주위의 망목영역에서 전기적 중성을 얻을 수 없기 때문에 이 배열은 매우 불안정할 것이다. 이런 구조 에서 각각의 X04 사면체는 과잉의 陽電荷를 가져야 하며 톰새이온 들(i n t ers titi al i ons) 이 負 電 荷률 가져야만 중성이 될 수 있다. 그림 3. 3(b) 에서와 같이 5 가이온 주위에 있는 산소이온 중의 하
 -0(o)- >亨S i 4 · —--Ooo—- - 亨 >亨 ssx,154• 주·느- 0 C 卜- - S:亨 i ―0- -0(bl -:亨si . - --00-- 古卓sx i 54 느조 -0- ¢」s;• •- o-
-0(o)- >亨S i 4 · —--Ooo—- - 亨 >亨 ssx,154• 주·느- 0 C 卜- - S:亨 i ―0- -0(bl -:亨si . - --00-- 古卓sx i 54 느조 -0- ¢」s;• •- o-
나가 중십양이온과 二重結合울 하여야 중성이 유지된다 .•그 러나, 5 가이온을 함유한 사면체단위에 바대칭성이 생기므로 이 배열은 국 히 불안정하며 사면체단위 주위의 영역에서는 규산염망목중의 결합 에 상당한 혼란이 생기게 된다. 따라서 2 상의 분리가 일어나게 된 다. 듬새 또는 수식양이온들도 2 상분리를 일으키기 때문에 이들의 효 과도 중요하다. 규산영유리의 구조는 연결된 S i 04 사면체 사이에 틍 새자리를 갖는 開放構造이드로 알카리나 알칼리토류이온들과 같은 수석양이온들을 수용할 수 있다. 유리구조 중의 각 양이온은 산소 와 최대배위를 하려고 한다. 일반적으로 실리콘이온은 산소이온의 全配列에 대해 俊位勅果를 나타내려고 하나 이온장강도에 따라서는 수식양이온이 평형배위상태에 도달하려고 배열에 영향을 미찬다. 따라서 유리용융체 중에서 이와 같은 경쟁이 일어나고 비교적 큰 이온장강도를 갖는 수석양이온들은 S i -0 의 망목에 혼란을 일으켜 논및系 의가R 는 O낮— T은Sai s0자 h2 i 유 r의o 1에2共) 너에婚 지의溫를 해度 갖 (c지도on 지s록o l되 u t2 e었 상 다의t e. m p분그 er리는a t 를u re 2) 성일 는 으분 키계수 게식인 양.된 R이다2.온0— 과이S i실0론 2 리콘 사이의 이온장강도의 차가클수복직선적으로 된다고 지적하였 다. 따라서 분상경향은 수식양이온의 이온장강도가 실리곤의 이온 장강도에 접근할수록 커진다. 2 상 중의 1 상은 실리카가 r i ch 하며 수식양이온의 농도는 작다. 두번째 상에서는 틈새이온이 많으며 이 둘이 구조전체에 현저한 영향을 미찬다. 비가교산소의 농도가 이상 에서는 높으며, 경우에 따라서는 응집된 규산염망목이 존재하지 않 울 정도로 망목구조가 약하게 된다. 2 성분계 규산영에서 不混和의 정도는 °석상곡선의 모양을 보면 알 수 있다. 2°석 상용융체로 된 계의 경우 °석상온도는 불혼화를 이루는 조성범위에서는 일정하다. 수평°석상선을 나타내지 않는 일부 계는 으S-로 型 생액 각상된곡다선.을 B a나O타 一내 S 며i 02 와이 들L은i2 0 대— 개S i0 2준 계안 의정 불°석혼 상화곡가선 은일 어뚜난렷 한것 s- 형 을 나타내 며 Na20-S i아 계 에 서 는 S- 형 이 확실치 않다. 이 들
12) M. Tashir o , Glass Industr y , 428 (19 66).
유리에서는 분상이 일어나는 것으로 알려져 있으며 L i 20-S i 02 우r 리에서의 분상은 이들 조성이 중요한 각종 결정화유리의 시초가 되 었기 때문에 매우 홍 미 있다. (2) 酸化物 核 生 成 保 進濟 l j의 實 例 a) Ti0 2 S t ooke y 13) 에 의 하면 각종 유리 조성 에 서 Ti0 2 2~20W t%가 핵 생 성 촉진제 로 효과적 으로 작용한다. Ti 0 2 는 용융유리 중에 찰 용해 되나 냉각중 또는 재가열시 많은 準 微細粒子 (subm i crosco pi c par t icle ) 로 석출되어 유리로부터 主結晶相이 생기는 것을 촉진한다. 미립자 로 된 바람직한 미세구조를 얻기 위해서는 유리의 徐冷点보다 약 50° C 높은 온도에서 유리를 가열하여 핵생성을 일으켜야 하며 이전 에 핵생성온도보다 100~300°C 낮은 온도에서 유리를 냉각하여 o.5 ~2 시간 유지하면 최적핵생성이 얻어전다는 것을 알았다. ru til e 결정이 먼저 석출하여 다른 상의 결정화를 위한 불군질핵으 로 작용한다는 · 생 각은 만족스럽 지 못하다. 왜 냐하면 ruti le 은 굴k 상 결정상으로 나타나지 않으며, 결정이 형성되더라도 다른 결정상 이 석출된 이후의 열처리단계에서 겁출될 분이기 때문이다. 그러나. • 결정화과정의 첫단계에서는 T i 02 가 r i ch 한 액상(유리)이 분산된 매 우 작은 小商모양으로 분리된다. 이 분상은 용융체를 냉각 중 시작 · 되지만 보통 이 단계에서 결정핵은 생성되지 않는다. T i아를 함유한 유리의 결정화를 제어하는 데 2 相液分離(tw o ph ase- l에iq u i의d 해se p확 ara인 ti 되on) 었 가 다 .중 요그한는 역T 할i아을 로 한 핵다 생는 성 된생 각M이g OM -aAurle2r0134—) 의S i0 연2 구유 리조성에서 미제구조의 변화를 光散亂 實 驗에 의해 조사하였다. 그 결과 용융유리를 냉각하는 초기단계에서는 乳濁液 (emuls i on) 모양의 2 상분리가 일어나며 그 다음의 열처리논 유타액모양의 형성에 대한 효과가 거의 없었다. 小流相 (dro p le t p hase) 의 결정화는 725~770°C 에서 시작되며 770°C 에서 더 오렌 시간 열처리를 하면 Mg O •Ti0 2 - 가 생겼다. 이와 같이 장시간 770°C 에서 열처리를 하면 입자크기 ,
13) S. D. Sto o key, Brit. Pate n t No. 829447 (19 60). 14) R. D. Maurer, J. Ap pl. Phys . , 33, 2132 (19 62).
가 2. 5nm 로부터 17. 5nm 로 변화된다는 것 을 알았다. Maurer 의 연 구결과 T i 02 는 순수한 화합물로 분리되지 않고 M g O•T i 02 로 분리 된다는것이 확인되었다. 다른유리에서도비슷한효과가 일어난다. 예를 들면, 어 떤 2 가금속산화물이 부가되 지 않는 한 Ti 0 2 는 Na20 ― AI2 야― S i아 유리 들에 서 는 좋은 핵 생 성 촉진제 로 작용하지 않는다. 이들 산화물은 T i아와 결합하여 i lmen it e 형의 조밀육방구조인 RO • Ti 02 가 된다. 적 합한 산화물로는 Fe, Co, Cd, Zn, Ni, Mn 및 Mg 가 있 다. Ti0 2 는 간단한 L i 20 ― S i아 유리 에 서 는 만족할 만한 핵 생성촉진제가 되지 못하나, M g O 나 AI203 를 함유한 더 복잡한 유 리에서는 만족한 효과를 나타낸다. 이런 사실로부터, 결정화유리에 서 T i아 는 다른 산화물과 화합물을 형 성 하고 이 화합물은 유리 중 에서의 유리분상을 포함한 과정에 의해 더 쉽게 핵생성을 하게 된 다고 생각된다. 분상자체의 과정은 T i 4+ 의 구조적 역할과 관계가 있다. 유리구 조에서 중간산화물로 취급되는 T i아는 T i 4+ 의 일부가 사면체망목 형 성 자리 를 접 유한다고 생 각된다. Ti 4+ 의 이 온반경 아 o. 068nm 이 므로 보통 6 중배위를 할 것으로 생각되며 대부분의 결정에서는 Ti4 + 는 이와 같은 자리를 차지하고 있다. We y P) 은고온에서 T i 4+ 논산 · 소와 4 중배위를 하며, 이 경우 T i -0 그룹은 구조적으로 규산염망 목과 조화를 이물 것으로 추정하였다. 냉각중에 T i”는 처온에서 의 平衡配位數 (6) 로 전환하려는 경향이 생겨 규산영망목으로부터 이탈될 것이다. 따라서 T i아는 2 가금속산화물과 결합하면 분상을 일으키게 된다고 생각된다. 일부 유리에서 T i 4+ 의 고온상태는 凍結 (疑結)되나 이 상태는 처온에서는 불안정하여 유리를 재가열하면 분 · 상이 일어나게 된다. Ti B0a2 r 로r y 핵등 생15 ) 성16) 된은 LiT2 0i —아 A가l2 0 표3—면 S활i0 성2 형제 로유 리작 둘용의한 결다정고 화 에생 각관하한였 실 다험. 결과를기초로 T i”가사면체망목에 참여하는능력에는 한계가 있기 때문에 T i”는 비가교산소이온을 끌어당기려고 하여 모든 산소이온 15) T. I. Barry, D. Cli nt o n , L. A. Lay, R. A. Mercer and R. P. Mi ller , ]. Mate r . Sc£ . , 4, 596 (19 69). 16) Ibid . , 5, 117(1 9 70).
이 가교되는 영역이 존재하며, 이 영역은 T i”와 결합된 비가교산소 에 의해 분리되어 유리 중에 磁區 (doma i n) 구조가 생길 것이라고 주장 하였다. Li+도 비가교산소와 연결되어 磁區境界에 농축되는 것으로 생 각하였 다. 이 磁區의 크기 는 2. 43nm 로 계 산되 었 다. Al04 그룹상 의 有勅負電荷는 磁區表面자리를차지하는것을 억제하여 모든 Al 따 는 磁區內部에 남게 된다. S i”는 磁區內部로부터 이동할 것이라고 제 안하였 다. 따라서 母유리 조성 에 따라 磁區形成을 내 포한 조성 의 變異 가 각종 상의 핵생성을 촉진하게 된다. 이상과 같은 결론은 많 은 假定 위에 기초를 두고 있으며 磁區形成에 대한 직접적안 중거가 없다고 지적되고 있다. b) Zr02 Sawa i 17) 에 의 해 Zr02 가 핵 생 성 촉진제 로 사용되 었 으나 규산영 용 웅체에서의 용해도가 3~ 4 % 로 작기 때문에 T i 02 보다 유용성이 없 었 다. 그러 나 Tash i ro18) 가 유리 중에 P2°5 를 함께 첨 가하면 Zr02 의 용해도가 상당히 증가한다는 사실을 발견하였다. 이 경우 ZrO~ 가 핵생성을 축전시키나 그 당시에는 P20s7} 핵생성촉진에 기여한 다고 생각하였다. c) P205 Partr i d g e 등 19) 에 의 해 P205 가 핵 생 성 촉진제 로 사용되 었 다 . p요는 핵생성촉진제의 성질을 갖는 망목형성물 (NWF) 이다. p5-t 는 사면체배위를 하여 기본망목형성이온인 S i”와 의부망목형성이 온인 P5+ 사이의 전하차이 때문에 분상이 생긴다. 그립 3. 3 에서 본 것과 같이, P ― 0 결합이 모두 單結合이라면 전기적 중성이 얻어지 지 않기 때문에 P04 사면체당 1 개의 P ― 0 결합이 2 중결합이 되어야 한다. 이때 규산영망목 중의 2 중결합된 산소이온은 규산염망목으로 부터 인산염그룹이 분리되는 조건을만든다. 이들 그룹은 P2°5 로 분리되지 않고 알칼리나 알칼리토류산화물과 결합되어 분리된다. 분리된 상은 결정질이나, 유리상과 매우 비슷하다. 인산염에 의해
17) I. Sawai, Glass Technol. , 2, 243(1 9 61 ). • 18) M. Tashir o and M. Wada, Advances in Glass Technolog y, Part 2, p. 191) 8G, . PlPenarutmr i d Pg er e sasn(dl 9P6. 3 W). ., McM illan , Glass Tech. , 4, 173(1963).
2 상분리된 유리의 전자현미경 관찰결과는 분리된 상내에 결정의 규 칙성을 나타내지 않으며 X- 선 분석결과에서도 규칙성을 볼 수 없 다. 극소량의 P20s 가 2 상분리 를 일으키 는 핵 생 성 촉진제로 효과적 이 며— A첨l2 0가 3—량 은Si0 2o ,. 5L~ i 260W- tM% g이 O 다 ―. S iM아c M및i l lanM g둥O 20-)A 은l 2금0속a-인S산i0 염2 계 이 로 부Li터20 제조된 각종 유리조성에서 결정화를 촉진시킨다고 설명하고 있다. 같은 핵 생 성 방법 이 L i 20 ― ZnO ― S i아 및 Li 20 ― PbO-S i아 유리 에 서 도효과적이다. 電子Jam顯 e微s 鏡등을 21) 22사) 은용 하분여상 과조 사결하 정였 핵 다 생. 성L i사 20 이— 의S i 0관 2 계형 룰유 리高 에分 L解 i a能P0透4 過를 · 생성하기 위해 P2 아를 소량 첨가하였다. 이때 30L i 20,70S i 02 인 유리를 550°c 에서 열처리하였을 때 Li 20 가 r ic h 한 매트릭스 중에 실리카가 r ic h 한 小液이 넓게 분상을 일으켰다(그럽 3.4). S i O 대신 P20s lmole% 를 치 환하면 분상의 형 태 가 변하여 단위체 적 당 입 자의 `
 나나죠,.., ;;,J i.,;. :덕
나나죠,.., ;;,J i.,;. :덕
20) P. W. McMi llan and G. Partr i d g e , Brit. Pate n t No. 924996 (19 63). 21) P. F. Jam es and P. W. McM illan , Phil . Mag . , 18, 863 (1968). 22) Ibid . , Phys . Chem. Glasses, 11, 59(1 9 70).
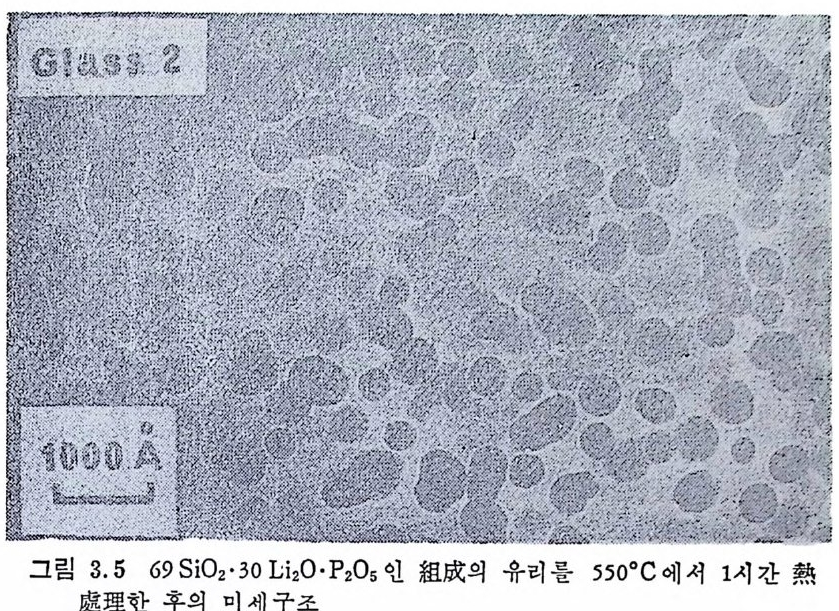 그림 3. 5 69 SiO z -30 L i 2 0·P 2 야 인 組成의 유리 를 550°C 에 서 1 시 간 熱
그림 3. 5 69 SiO z -30 L i 2 0·P 2 야 인 組成의 유리 를 550°C 에 서 1 시 간 熱
수가 증가하며 특수상의 체적분율도 약 2.5 배 커진다(그립 3.5). 소량의 P2 야가 큰 영향을 미치는 이유를 여러 가능한 모델로 설 명하고 있나. 분상된 상의 체적분율에 대한 계산량과 관찰량이 찰· 일치하는 모델은 母相이 Li 20•2S i 02 보다 L i 20 가 약간 더 r i ch 한 ` 조성을 갖는것이다. P 요 는 모상에 촌재 하여 Li20 와 결합함으로써 Li 20·3P2 야 가 된. 다고 생각된다. 분상된 유리의 유전상수를 측정한 결과는 이 모델 을 찰 설명하여 준다. 유리 중에 Li 20·3P20s 의 정확한 형태는 나타 나지 않으며 이 결 정이 촌재하더라도 10nm 보다 작다면 X - 선회철 모양에 나타나지 않을 것 이 다. Tomozowa23) 에 의 해 서 도 P20s 가 L i 20 ― S i아 유리 중에 서 분상을 일으킨다는 것이 확실해졌다. L i 20-S i아계 유리에 S i아대신 P20s 를 1% 치환하면 不混和溫度가 상승하고 不混和境界는 L i 20 함유량 이 더 많은 곳으로 이동한다. 비슷한 효과는 Na20-S i아계에서도 23) M. Tomozowa, Advances in Nucleati on and Crys t a l liz a ti on in Glasses ► p. 41. Americ a n Cerami c Socie t y (19 71 ).
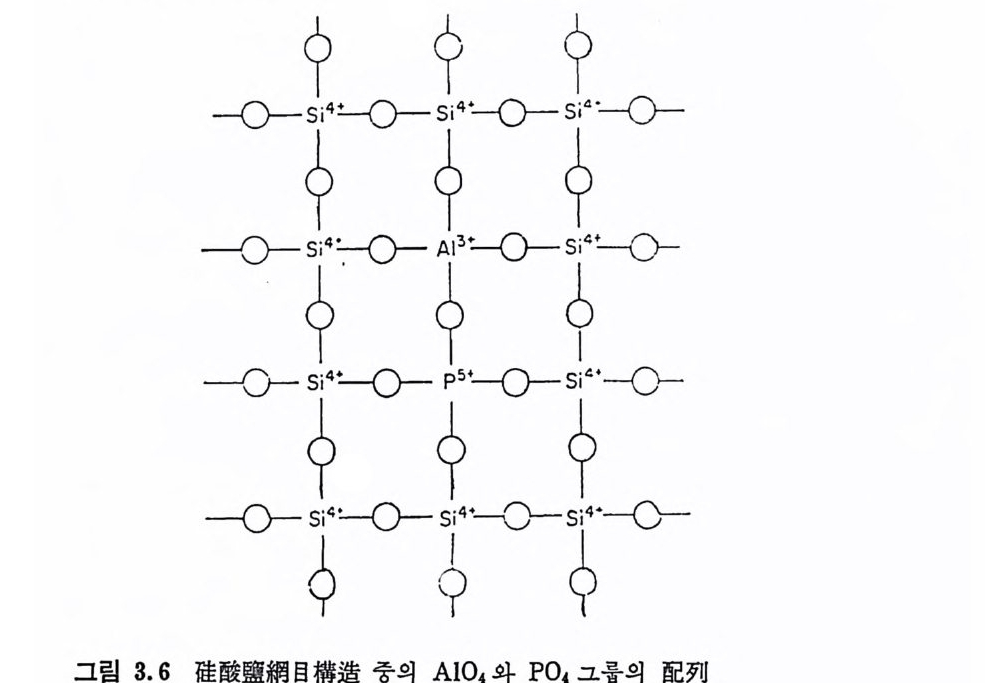
나타났다. Ma t us it a 둥 24) 은 Li 20 •3 Si0 2 조성의 유리에 각종 산화물 울 3mole% 이내로 첨가하여 분상과 결정화를 조사하였다. 이때 Ti 아는 불혼화온도를 약간 높이나 P2 야는 약 200°c 나 높였다. P20s 의 현처한 효과는 p s+ 의 높은 이온장강도에 의한 것으로 설명하고 있다. P20s 를 함유한 용융체나 유리 중에서 일어나는 2 상분리의 경향 온 Al203 가 높은 비율로 함유되면 감소된다. 이 효과는 유리구조 중의 Al3+ 와 P5+ 의 역할로 설명할 수 있다. Al3+ 는 유리망목 중에 참여하는 사면체 Al04 그룹의 중십을 접유하며 이 그룹들은 과잉의 負電荷를 1 개 가지고 있다. 대부분의 유리에서는 이 전하는 알칼리 나 알칼리 토류이 온들이 존재 함으로써 중성 이 되 나, 유리 중에 P 이 존재하면 그립 3.6 에서와 같이 Al04 그룹이 P04 그룹과 연결되어 전기적 중성을 얻게 된다. 이 배열에서 P04 그룹이 갖고 있는 과잉
 亨 亨 亨
亨 亨 亨
24) K. Matu s ita , S. Sakka, T. Muki and M. Tashir o , J. Mate r . Sci. , 10, 94(1 9 75).
전하 +1 은 Al04 그룹이 갖고 있는 과잉전하 -1 과 중성을 이룬다. 따라서 P 와 연결된 02 ~ 중의 하나가 중성을 유지하기 위해 2 중결합 율 할 팔요가 없게 된다. 또한 Al3+ 와 P5+ 의 반경은 각각 0.05 및 。 • 34n m 이므로, 이들 이온이 인접한 사면체그룹의 중심을 접유할 대 2 그룹의 全原子「1 31 距離는 중십이온인 S i4+가 반경 o.0 4 1nm 인 S i 0 4 그 룹들 간의 인접원자간거리와 매우 비슷하게 된다. 따라서 전 기적 중성과 망목구조에 관여하는 사면체그룹들의 크기를고려할때 A l0 4 와 P04 그룹이 연결되면 규산염망목내의 인산염사면체가 안 정하게 뮐 것이다. 이 접에 대한 또 하나의 증거는 결정질 AlP04 가 절정질 실리카인 cr i s t oba lit e 와 구조적으로 매우 비슷하여 규산 영 망목내에서의 AlP04-P04 그룹이 안정하게 된다고 추정할 수 있다. d) V205 V 2 0 s 는 져온 양으로 유리내에서 P2 야와 유사한 구조적 역할을 한다. V5+ 의 반경은 o.059nm 로, 산소와 결합하여 안정한 사면체 그룹을 만드는 이 온들보다는 크지 만 V2 야 는 유리 형 성 산화물이 며 각종 바나눔산유리 (vanadate g lass) 들이 제조되었다 • 이들 유리에서 配位多面體의 특성은 확실하게 얻어지지 않는다• 사면체는 형성되 나 결정질 산화물 중에 배위다면체는 매우 비들려진 팔면체이며 이 구조는 비틀려진 삼각형의 2 피라밋드板狀으로 되어 있다고 설명하 는 것이 가장 타당하다. 만일 V2 야가 규산영유리 중에서 망묵형성 여안 정할 하울여 한 다미 면세 한인 접분 상S을i4 + 와일 으비킨 교다할 . 때Li 2 V0 —5 +S 의i0 2 부형 가유된리 에陽 서電 荷P2는°5 불보 다는 덜 효과적이지만 V2°5 도 핵생성촉진제로 작용할 수 있다. F 와는 달리 V 는 유리 중에서 각종 원자가로 촌재할 수 있다. 실제 로 유리내의 V 는 전부 V5+ 로 존재하지는 않는다. 용융시 V4+ 및 V3+ 로 되면서 산소를 상실한다. 따라서 V 이 함유된 유리의 핵생 성과정을 조절하기는 어렵다. Wi lliam son 둥 25) 은 V2 야 와 V2 야 의 CaO ― M g O ― Al2 아― S i O 홉 리의 결정화에 대한 효과를 연구하였다. 이들 산화물은 내부 핵생 :i5) J. Wi lliam son, A. Tip ple and P. S. Rog er s, ]. Mate r . Sc i. , 4, 1069(1 9 69).
성을 벌로 촉진시키지 않으나, 표면핵생성된 anorth it e (Ca0•Al20:, •2S i 02) 와 wollas t on it e(CaO•S i 02) 의 결정성장속도에는 영 향을 미 찬다는 것을 알았다. 높은 이온장강도를 갖는 침입형이온이 평형배위수를 가지려고 함 으로써 규산염망목에 혼란이 일어난다. 따라서 이들 이온은 용융체 나 유리 중에서 2 상분리 또는 결정핵생성을 일으키게 된다. e) Cr 크롬은 높은 이 온장강도를 갖는 침 입 형 양이 온으로 유리 중에 촌 · 재할 수 있는 금속의 한 예이다. 산화분위기에서 용융된 유리 중에 크롬은 Cr3+ 과 Cr6+ 의 두 원자가상태 로 존재 할 수 있 다. 융융온도 를 높이거나 용융시간을 길게 하면 Cr3+ 형성이 有利하게 된다. 유 리 중에 알칼리 금속산화물이 촌재 하면 Cr6+ 의 형 성 이 有利하며 K20 는 L i 20 보다 Cr6+ 의 형성에 더 큰 영향을 미치며 Na20 는 중 간 정도의 영향을 미찬다. PbO 도 Cr6+ 형성에 좋다. Cr2+ 은 강한 환원분위기하에서 용융유리 중에 촌재할 수 있다. Cr6+ 은 높은 이온장강도 (Z/r2=17,2) 를 가지며 침입형자리를 점유 하기 때문에 주위에 있는 산소이온들이 규칙배열을 갖도록 規則勅 果 (order i ng e ff ec t)를 미 친다. 이 런 조건하에 서 Cr 이 ric h 한 상은 유리로부터 분리된다. 이런 방법으로 Cr 이 거동한다는 증거는 납 규산염柚藥에서 납크롬영결정이 석출되어 유약이 黃 또는 赤色울 떠게 되는것을보면 알수있다. Sawa i1”는 1~3% Cr2 아 를 사용하여 Li2 0 , K20, CaO 둥을 함 유한 알루미노규산영유리의 결정화를 촉진시키는 데 성공하였다. 죽 Cr203 률 사용함으로써 유리 중에 2 상분리가 일어나고 이어서 다 론 상들의 결정화가 일어 났다. 한편, Thakur 둥 26) 은 Cr203 는 Li20 • 2 Si 02 유리 의 容積結晶化 (bulk crys t a l liz a ti on ) 에 대 한 핵 생 성 촉진 제러 는나 그효과들적은이 K 2아0—니 M고 g O표 — 면C핵aO생 — 성A울l2 0중2-전Si시0 2 킨 형다 의고 복결합론다지성었 분다.계 그유 리 에 서 는 Fe203, Cr203 및 CaF2 를 포함한 핵 생 성 촉진제를 사용힘_ 으로써 결정화유리를 효과적으로 만들 수 있었다.
26) R. L. Thakur and S. Thia g a raja n , Glass and Cerami c B1' ll , , 13, 33 (1 966) 白
W illi amson27) 은 CaO-Mg O -Al203 -Si 02 -유리 에 서 Cr203 가 핵 생 성제로 효과적이 아니나, 유리 중의 Cr203 의 용해도가 o.6% 로 낮 다는 어 려 움아 있 다고 지 적 하고 있 다. Shelesta k 둥 28) 은 石油頁岩 (oil s hale) 을 용융시켜 결정화유리를 만들 때 母유리는 단지 표면결 정화를 일으킨다는 것을 알았다. 그러나 약 1% 의 Cr203 를 첨가하 떤 거의 90% 가 결정화되고 평군입도가 10µm 인 재료를 얻을 수 있 었다. 이 경우 생성된 핵들은 일반식이 (Mg ,F e) (Al,Fe,Cr)204 인 혼합스피넬형 (mi xe d spi ne ! typ e) 의 결정이 발견되었다. f) Mo 몰리브멘화합물에서는 o, +2, +3, +4, +5 및 . +6 인 6 개의 다른 산화상태가 존재할 수 있으며 산화물로는 원자가가 2 로부터 6 까지 촌재한다. 실제로는 Mo 아와 Mo03 만이 화합물로 확인되었다. 따 라서 Mo 은 유리 중에 Mo4+ 와 Mo6+ 로 존재할 수 있다. 반경이 · O.062nm 인 Mo6+ 는 높은 이온장강도 (Z/r2=15.6) 를 가지며 침입형 Mo6+ 가 주위 의 산소이 온에 강한 orderin g ef fec t 를 나타내 어 . Mo 이 r i ch 한 상이 유리로부터 쉽게 분리된다. 비교적 강한 이온장강 도를 갖는 W6+ 도 비슷한 성질을 나타낸다. 유리 중에 용해도가 3 ~ 4% 인 Mo03, W 아는 독정유리 중에 고정될 수 있다. 이 2 산화물 은 결정상을 분리하여 유리를 불투명하게 한다• 이 효과는 납산화 물을 다량 함유한 유리 위에 珉鄕 (enamel) 과 유리 狀의 색상을 만들 때 사용되어 왔다. Mo03, W 아는 이런 목적에 필요한특성을 일부 가지고 있기 때문에 핵생성촉진제로 사용되어 왔다. 이 산화물들 은 고온에서 유리용융체에 용해되며 어떤 유리조성에서는 냉각시 산화물이 용융체 중에 남는다. 이들 산화물을 함유한 유리 를 재가 열하면 유리의 軟 化溫度 範園 에서 미세한 결정질 침전이 생긴다. 그 후 이들 결정은 유리로부터 다른 과포화상의 결정화를 위한 핵생성 제로 사용될 수 있다. McMi llan 둥 29) 은 Li2 0 를 함유한 유리 나 고알루미 나유리 둥에
27) J. Wi lliam son, Mi ne r a log y, Mag . , 37, 759 (19 70). 28) L. J. Shelesta k , R. A. Chavez, J. D. Mackenzie and B. S. Dunn, J. Non• -29 C) rPy.s tW . . S oMlicdM s , i ll3a 7n, a8n3d(1 9G 7. 8)P. artid g e , French Pate n t No. 1328620 (•1 9 61 ).
MoO 과 W 아를 0,5~4% 첨가함으로써 결정화가 制御된다고 하였 다 유리를 示差彬眼計軟化點부근(l o gr; = 10 11 ~1012 po i se) 에서 열처리를 하면 핵생성되고 다음의 열처리에서 각종 화합물이 다량으로 결정 화된다. g) 鐵酸 化物 철산화물이 일부 결정화유리에서 유용한 핵생성촉진제로 작용한 다는 것 이 증명 되 었 다. W illiam son 둥 30) 은 Ca0-M g 0-Al203 一 S i 02 유리 로부터 anorth it e 와 wollasto n it e 의 성 장에 관한 동력 학은 재 료 중의 산화철에 의해 영향을 받는다는 것을 알았다. 결정성장속도 는 철산화물의 농도에 좌우되 나 FeO/Fe203 의 比도 중요하다. 이 들 이온은 결정성장과정에 중요한 영향을 미치나 내부핵생성에는 영 향을 나타내지 않는다. 내부핵생성에의 영향은 철산화물이 Fe203 로 5W t%를 넘을 때만 가능하다. Rog e rs 등 31) 도 같은 조성 의 유리 에 Fe203 나 Fe(C00) 2• 2 H20 (ferr ous oxala t e) 를 첨가하여 핵생성율 조사하였다. Fe2 야 7W t% 以 上 함유한 유리는 내부핵생성을 촉진하며 수많은 작은 樹枝狀의 결 정아 성장된다. 主結晶相은 dio p si d e [CaM g (S i 206) ]나 melili te[ Ca2 (Al, M g)[(A l, S i )201 J]이 다. meli lite 는 geh lenit e (2CaO•Al20:t ·S i 02) 와 akermanit e (2CaO•Mg O •Si0 2 ) 사이 의 固溶體이 다. 짧은 시간의 열처리에서는 d i o p s i de 가 우선적으로 결정화되며 낮은 온~ (950°C 이하), 장시간의 열처리에서는 me lilit e 가 성장된다. 결정화 유리에서는 스피벨상이 약간 함유되는 데 이것의 單位晶은 定常스 피 델 (normal spi ne l) 인 M gA l204 보다 약간 더 크다. 이 것 은 Al3+ 가 일부 Fe3+ 로 대치되기 때문이라고 생각된다. 격자상수를 측정한결 과, 母유리 의 Al 요 /Fe2 야 比보다 약 4 배 큰 12 : 1 을 나타냈다. 유리 중의 Fe3+ 는 대부분 사면체자리를 차지하고 이들은 Al3+ 와 치환되며 Al3+ 는 팔면체배위를 하여 스피넬핵생성을 더 촉진한다고 추정 하고 있 다. 이 들 핵 이 dio p si d e 와 melili te 건 정 의 성 장자리 를
30) J. Wi lliam son, A. J. Tip ple and P. S. Rog e rs, J. Iron Ste e l Inst. , 206, 898(1968). 31) P. S. Rog er s and J. Wi lliam son, Glass Tee/mot, , 10, 46(1969).
마련한다. 따라서 유리 중의 결정핵생성을 촉 진하는 Fe3+ 의 작용은 복잡하다. Fe3+ 의 작용에 관한 다른 예로는, Beall 등 32) 이 玄 武岩 (basal t)형 유리로부터 결정화유리를 생성한 연구가 있다. 여기서 핵생성을 제 어하는 가장 중요한 인자, 즉 현무암결정화유리의 미세구조를 얻 키 위해서는 Fe 의 산화상태라는 결과믈 얻었다. 4. 4 W t%의 Fe203 와 8. 4 W t % 의 FeO 를 함유한 현무암형 유리 를 용융시 평 형 은 Fe203 쪽으로 이동한다. 이 반응의 정도는 용융온도, 原 材 料 의 입자크기, 뱃 지 첨 가물 및 기포 등에 의해 결정된다. 예를 들면, 공기 중에서 4 시간, 1 40 0 ° C 에서 용융하면 Fe0/Fe203 의 比는 原 材料가 小粒인 경우 I.9 가 되나, 微粒 子인 경우에는 I.6 으로 떨어지며 NH4N03 를 4% 첨가하면 그 比는 o. 5 로 더 떨어진다. FeO/Fe2 아의 比가 o. 5 인 경우는 ma g ne tit e(Fe3 아)에서의 比와 거의 같게 된다. 핵생성효과에 대한 Fe 산화상태의 강한 영향은 환원제 (2% 설탕) 나 산화제 ( 4 % NH4N03) 를 현무암형 유리에 첨가하였을 때 결정화의 거동을 비교하면 알 수 있다. 환원된 유리를 열처리하면 유리매트 릭 스 중에 큰 小 球體 (~50µm) 인 單 斜 輝 石 (Cl i no py roxene, M 당 + (S i 03)2) 가 함유된 미제구조가 얻어진다. 이것은 열처리중 輝 石이 변형된 것이다. 산화된 유리는 미립자인 휘석결정화유리가 되며 결정 크기 는 100nm 이하가 된다. 650~700°C 에서 2 시간 핵생성처리를 한 결 과 ma g ne tit e 핵이 석출되고 900°C 에서 열처리를 하면 이들 핵 위 에 휘석결정이 석출된다. 따라서 유리를 산화하여야만 된다는 사실 이 확실하여졌다. 초기의 핵생성을 촉진시키기 위해서는 Fe3+/Fe2+ 의 比가 mag n eti te 에 서 의 比와 같아야 한다. 만일 Ti 02 를 현무암 형 유리에 첨가하면 환원된 유리로부터도 미립자로 된 미제구조의 결정화유리가 얻어진다는 사실은 주목하여야 한다 . 그 이유는 T i 0 2 가 FeO 와 결합하여 구조적 으로 mag n eti te 와 같고 따라서 핵 생 성 에 필요한 형태가 되는 스피델인 Fe2T i 04 를 형성하기 때문이다. 지금까지는 單成分이 핵생성촉진제로 사용되었지만 단독으로 사 용가능한 2 개의 산화물을 혼합하여 핵생성을 더욱 촉진시킬 수도
32) G. H. Beall and H. L. Rit tle r, Bull. Am. Ceram, Soc. , 55, 579(1 9 76).
있다. 핵생성제의 全 濃度 는 같으나 共 同作用 勅果 (s y n e rgi s ti c eff ec t) 가 일어나 단일 핵생성제를 사용하였을 때보다 핵의 밀도가 더 크 고 더 미 립 자로 된 미 세 구조가 얻 어 진다. S t eward 33 ) 는 전농도가 2.23 분자%인 T i 02 와 Zr02 의 혼합물은, 이들을 같은 농도로 각각 사용하였을 경우보다 더 미립자이며 기계적 강도가 큰 결정화유리 가 얻어진다고 보고하였다. 핵생성혼합물을 함유한 결정화유리는 열처리 주기의 변화에 덜 민감하다. h) 플르오르化物 소오다-석회-실리카형의 유리를 불투명하게 하기 위해 오래전부 터 플르오르화물을 첨 가하여 왔으며 , 이 런 목적으로 사용된 화합물 로는 NaF, Na3AlF6(crya li te) 및 Na2S i F6 가 있다. 1% 이하의 농도 에서는 F 가 유리구조 중에 수용되어 두명한 유리가 얻어지나, 더 큰 농도 (2~4% 이상)에서는 플르오르화물은 유리 냉 각시 용액 중에 석출되어 미제한 결정질 침전물을 형성하므로 유리가 불투명하게 된다. 유리 중의 플르오르화물의 양을 조절하면 냉 각시 두명 성 이 유지되나, 서냉온도범위보다 약간 더 높은 온도로 재가열하면 풀 르오르화물결정의 침전이 생긴다. 이것으로부터 유리의 결정화를 촉전시키는 방법으로 불투명한 유리를 만들기 위해 플르오르화물을 · 사용할 수 있으며, 이때 작은 풀르오르화물결정이 핵생성 중십으 로 작용한다. 영 화물도 유리 를 불투명 하게 하지 만 규산영 유리 중에 는 소량밖에 녹지 않기 때문에 실제적인 핵생성제로는 사용되지 않 고있다. F 가 규산영유리의 구조에 어떻게 참여하는가를 보자. F 적 반 경 은 o. 136nm 로, 02- 의 반경 0. 14nm 와 거 의 같기 때 문에 다른 이온들의 배열을 크게 방해하지 않고 유리망목 중의 02 一와 치환될 수 있다. 그러나 F 는 1 가로 유리내에서 全 置換 이 일어나려면 각 산소이온에 대해 2 개의 F_ 가 치환되어야 전기적 중성이 유지된다. F의 도입에 의한 효과는 강한 S i― 0-S i결합이 2 개의 S i -F 결합 에 의해 대치되어 유리망목구조가 약화되는 것이다. 이 효과는 용
33) D. R. Ste w ard, Advances in N11cleati on and Crys t a l liz a ti on Glasses, p, 83. Americ .a n Cerami c Socie t y (1971 ).
웅체의 접도감소를 가져오고 유리의 연팽창계수물 증가시키는 경향 울 나타낸다. 물론 규산영유리에서는 F 에 의한 0 의 완전한 치환 온 망목구조가 붕괴되어야 하므로 일어날 수 없다. 풀르오르화물이 유리의 컬 정화를 용이하게 하는 것은 유리망목구 조가 약화되는 데 있다. 비록 용융체를 두명한 유리가 연어지도록 냉각시키더라도 유리를 서냉온도범위나 조금 더 높은 온도에서 재 가열하면 원자재배열이 일어나 결정질 풀르오르화물의 핵이 생성된 다. 이 핵들은 플르오르화물결정의 성장속도가 낮은 온도에서 생 성되며 풀르오르화물은 수가 적고 큰 결정으로보다는 아주 미제한 많은 수의 결정으로 침전된다. Has 등외)은 유리의 결정화를 돕기 위해 금속플르오르화물을 사용 하였다. 여기서 유리는 알루미노_규산영형이고 각종 알칼리토류산 화물과 함께 알칼리 금속산화물 (Na20 와 K20) 을 함유하고 있 다. 플 르오르화물은 F 로 3~8% 첨가하고 결정화는 600~1000°c 에서 열 처리하여 얻어졌다. 풀르오르화물의 결정이 먼처 침전되며 이 침전 온 유리가 다결정질 결정화유리로 되도록 규산영결정의 성장에 필 요한 핵생성자리를 제공한다. 많은 금속황화물이 용융규산영유리 중에 용해되며 두명한 유리를 얻기 위해 냉각시킬 때도 용액 중에 금속황화물이 남을 수 있다. 이 유리를 上限徐冷 溫度 근처에서 재가열하면 s t r i k i n g과정에 의해 色이 나타난다. CdS 를 함유한 유리 는 이 효과가 찰 나타난다. 왜 냐하면 이 유리는 용융과 냉각 후에도 無 色이나 재가열을 하면 진 한 黃色울 며게 된다. 이 이유는 CdS 의 콜로이드 침전이 생성되기 때문이다. CdS 가 함유된 유리에 Se 을 첨가하면 황색은 처음에는 오렌지색으로 바뀌나 나중에는 Se ― rub y로 알려진 눈부신 赤色으 ·로와ph o바C— d뀐sSe다el .e7 n, }i 의d 이e s런각 라 종유고 리 혼할에합 서수결의정 있 으착 다로.색 제되는 어콜 있로 기이 드때크 문기에의 c a결dm정i이 um 며— CsudlS- 유리 중에 서 는 황화물과 sul p ho ― selen i de( 황제 렌화물)가 콜로이 드 침전물로 얻어질 수 있으므로 이 화합물들은 일부 유리조성에 대해
34) P. D. Has and L. N. Ste l ia n , Brit. Pate n t No. 848447 (19 60).
서는 미세결정의 결정화유리를 얻기 위한 핵생성 촉진제가된다~ u주m성- 분su으lp로h o —L is2e0l ,e nMid ge O 를 및 oA. 5l2~023 W둥t %이 함첨 유가시된 킴규 으산로영써 유 리미 에 세 c결a 정dm 의 i - 龜 결정화유리를 얻었다 .36) 즉 뱃지로부터 만들어전 유리를 연화온도 . 보다 약간 높은 온도에서 재가열하고 약 1 시간 유지하면 cadmi um . -sulph o-selenid e 가 str i k i n g 되 고 이 콜로이 드입 자는 리 듐규산영 과 다른 결정의 결정화를 촉진시킨다. 유리조성에 따라 800~1000° C 범위에서 온도를 올릴수록 유리의 결정화는 더욱 증진된다 . 이란 핵방 생법 으성 로촉 진기제계 적로 서강 c도ad가m큰i u미m —세 s결ul정p h 의 o- s결el정en화id 유e 리의 를결 얻접 을은 수su lp있h 다 o.- · selen i de 가 산화분위기에서 연소되지 않도록 찰 조절된 환원분위기 ., 에서 용융해야 된다는 접이다. 3.2 유리型의 選擇 결정화유리는 유리의 諸性質을 向上시켜 유리와 비슷한 用途에 사용하는 재료라고 생각할 수 있다. 결정화유리를 제조하기 위한 / 유리조성을 선택하기 위해서는 고려해야 할 중요한 因子둘이 많다. 이하에서는 이들 인자들에 대해 설명하겠다. 3.2.1 ~融 및 成形時 유리의 擧動 먼저 경제적인 방법으로 용융 및 성형될 수 있는 유리조성을 선 ? 택하여야 한다. 결정화유리의 제조에서는 이와 같은 인자들에 미치 는 유리조성의 영향에 대해 주의하여야 한다. (1) 楚融特性 유리의 용융온도는 너무 높아서는 안 된다. 보통 1600°C 가 실제 조업의 上限으로 생각되고 있다. 너무 높은 온도에서는 유리가마의 탉火物에 문제가 생기기 때문에 1400~1500°C 보다 높지 않은 온도 ‘ 에서 뱃지가 충분한 유동성을 가질 수 있는 유리조성을 선덱하여야 한다. 어떤 유리성분은 유리용융체의 접도가 낮아 용융과 淸澄 (re f-
35) P. W. McMi llan and G. Partr i d g e , Brit. Pate n t Ap pl, No. 8737/59(1 9 59) ~
i n i n g)을 신속하게 할 수 있 다. 알칼리 금속산화물은 이 런 효과를 갖 고 있어 용융공정에서 유용한 融劑(fl ux) 로 취급된다. Na20, K20 보다 Li20 논 용융체 의 접 도를 낮추는 효과가 더 크다. ZnO, PbO 와 같아 알칼리토류산화물도 융제효과를 나타낸다. B203 는신속하 게 용융 및 청칭하는 데 특히 유효하다. 이들 융제의 일부는 B203 와 같이 副成分으로 사용되나, 어떤 경우에는 결정화유리의 主成分 이 될 수도 있다. 수많은 유리계에서 유효한 핵생성촉진제로 작용 하는 T i 02 가 우수한 융제효과를 가지고 있으며 내화물을 부식시키 지 않고 경제적인 용융온도에서 유리를 용융시킨다는 것은 홍미있 는 사실이다. 용융특성에 유익한 효과를 주는 산화물 이의에 유리 의 접도를 높여 용융울 어렵게 하는 산화물이 있다. Al2037} 그예 로 Al2 아가 함유된 유리는 용융 및 청칭속도가 낮아전다. 유리에서의 화학조성변화도 중요하다. 용융시 유리뱃지로부터 휘 발성분의 손실 및 용웅유리와 접촉된 내화물의 용해에 의한 조성의 변화가 문제된다. 극소수의 경우에만 휘발에 의한 손실이 문제가 된다· 보통 용융온도에 서 Si0 2 , Al2 야, 알칼리 토류산화물은 중기 압이 낮으나 알칼리금속산화물은 휘발성이기 때문에 보통 약간의 손실이 생긴댜 내화물의 부식에 의한 조성변화는 매우 십각한 문 제이므로 비싼 내화물이나 P t로 내장된내화물을 사용하여야한다` . 알칼리 나 알칼리 토류산화물의 함유량이 많은 유리 는 부식 성 이 강 한 경우가 많고 Li 20 가 다량 함유된 용융체는 보통 내화물을 급속 히 부석 시 킨다. 용융체 중에 풀르오르화물이 함유되 면 F 가 Si0 2 와 반응하여 휘발성인 S i F4 를 형성하기 때문에 내화물의 溶出速度를 매우 증가시킨다. 유리용융체로부터 S i 02 의 손실도 같은 機 構 에 의 해 일어날 수 있다. 용융공정중 유리의 화학적 안정성에 관한 문제는 어떤 유리성분 이 臘零 園氣와 반응하여 환원될 수 있는 가능성이다. 이론적으로 유리조성은 遠內에서 용융시키기만 하면 되기 때문에 這분위기에 민 감하지 않을 것이나 PbO 와 같이 환원되는 산화물이 촌재할 때는 산화분위기하에서 용융하여야 한다. T i의 산화상태는 溶融遠의 분위기에 의해 영향을 받는다. 환원
조건하에서는 T i 3+ 가 되어 유리가 靑 色울 띠나, 산화조건에서 용 웅하면 T i아를 함유한 유리는 茶院 班色 (brown i s h-amber color) 을 며 게 된다. T i이 일부 환원되면 핵생성효과가 약해져 기계적 강도가 낮은 祖 大粒子의 결정화유리가 얻어진다. Fe, Mo, W 의 산화물과 같은 다른 핵생성촉진제도 용융로의 분위기에 만감하기 때문에 핵 생성을 제어하기 위해서는 산화상태를 조철하여야 한다. 한편 P20s 는 유리 중에서 p s+ 인 한 종류의 원자가상태로만 촌재하기 때문에 용융로의 분위기에 민감하지 않다. 따라서 P2°5 를 핵생성 촉진제 로 함유한 결정화유리의 조성은 迫 의 분위기를 조철할 필요없이 용 융시킬 수 있다. (2) 作 業 特性 유리의 작업특성은 어떤 성형공정을 사용할 수 있는가를 결정하 여 주기 때문에 실제적으로 매우 중요하다. 대부분의 유리성형공정 은 유리가 넓은 온도범위에 걸쳐 流 動 性 또는 塾 性인가에 좌우된다. 일반유리 의 작업 온도범 위 (workin g tem p er atu r e ran g e) 는 유리 의 접 도가 103~107 po is e 범 위 이 다. 결정화유리를 제조하기에 적합한유리의 작업온도범위는 일반유 리의 경우보다는 대개 좁다. 왜냐하면 보통유리의 조성과는 그 조 성이 다르며, 어떤 재료에 대한 성형조작이 급냉유리에는 적합치 않 키 때문이다. 유리 중에 알칼리금속산화물이 존재하면 작업범위가 넓어져 바람직하나, Cao 나 M g O 를 다량 함유한 유리에서는 작업 범위가 좁아져 바람칙하지 못하다. 다량의 Al203 를 함유한 유리는 접도가 커 성형조작의 온도가 높아져 좁은 작업범위를 갖는다. 이 런 유리들은 급냉시켜야 한다. ZnO 에 소량의 PbO 를 첨가하던 유 리의 작업특성이 개선된다. 최종적으로 얻어지는 . 결정화유리의 성질 을 개선시키기 위해서는 바람직한 화학조성들이 만들어질 수 있도 록 대부분의 경우 오히려 제한된 작업특성이 요구되고 있다. 작업특성 중 또 하나의 중요한 접은 성형조작시 냉각중의 실두 가능성이다. 결정화유리제조에서 기본적인 목적은 유리를 실두시키 는 것이지만 이 공정은 제어된 방법으로 행해져야 한다. 유리 냉각 중 군질핵생성에 의한 결정성장은 큰 결정을 만들며 촉진된 결정화
에 의한 미세결정구조는 얻어지지 않는다. 따라서 제어되지 않은 결정화는 제어된 성질을 구비한 고강도 걷정화유리를 만들 수 없게 된다. 또한 성형조작 중의 결정성장은 접도에 상당한 변화를 가져 오기 때문에 작업목성에 좋지 않은 영향을 미찬다. 또 생성된 큰 결정들은 유리제품이 깨지게 되는 바람직하지 못한 높은 응력을 발 생하게 된다. 유리를 냉각 또는 성형시 결정화가 일어나지 않도록 임계온도를 지나 냉각할 때 급냉시키는 유리성형기술을 사용하면 되지만, 유리조성을 선택할 때 위에서 기술한 인자들울 고려하여야 만 한다. 알칼리 금속산화물을 다량 함유한 유리 는 성형 조작시 오히 려 실두하기 쉬 우며 Li20 와 Mg O 는 특히 실두를 일으키 기 쉽 다. 다행히 이들 산화물을 극소량 첨가하면 냉각시 실두를 여제하여 작 업특성을 개선시킨다. 대부분의 경우 첨가되는 산화물의 효과는· 유 리가 성형되는 온도범위에서 실두가 일어나지 않도록 유리의 液相· 溫度를 낮추는 데 있 다. Al203 는 數%의 첨 가로 유리 성 형 시 실두를 여제하는 효과가 크다. ZnO 도 비슷하나 일부 유리에서는 큰 효과 가 없다. B2 아도 소량 첨가로 실두를 방지한다. Li20 를 함유한유 리 에 Na20 나 K20 를 소량 첨 가하면 좋은 효과를 발휘 한다. L i 20-S i아계 유리로부터 만들어지는 결정화 유리의 결정화를 억 제하기 위해 소량의 P205 를 첨가하면 작업온도범위에서 결정성장 이 감소된다. V20s 도 비슷한 효과가 기대되나 큰 효과는 없다. 3. 2. 2 유리의 化學的 安定性 여러 조건하에서 결정화유리의 화학적 안정성(兩化學性)은 매우 중요하며 母유리의 화학조성이 이 특성에 큰 영향을 미친다. 유리 의 화학적 안정성을 지배하는 인자들은 찰 알려져 있지만 결정화유 리에 관한 지식은 거의 없다. 결정화유리 중에는 여러 다른 결정질 화합물과 찬유유리상이 존재하며 물이나 다른 반응물의 침식에 의한 이들 상의 상대적 저항이 화학적 안정성을 결정한다. 찬유유리상의 화학적 안정성이 전결정화유리의 화학적 안정성을결정하는데 중요 한 역할을 할 것이다. 또 화학적 안정성이 약한 유리는 높은 안정 성을 갖는 결정화유리를 만들지 못할 것이다. 따라서 대개는 결정
화유리의 안정성을 지배하는 인자들은 유리의 화 학 적 안정 성 을 결 정하는 인자들과 같다고 할 수 있다. 이 원리를적 용 하면, Na 2 0 나 K20 를 다량 함유한 유리는 높은 안정성을 나타내지 못하기 때문에 피해야 된다. 또 찬유유리상에 Na20 나 K20 가 주성분이 된다면 결 정화유리의 화학적 내구성은 약해질 것이다. L i 20 는 다른 알칼리 금속산화물보다 화학적 내구성에 대한 나쁜 효과가 적기 대문에 결 정화유리의 유리상 중 주성분으로 촌재하여도 좋으나, 다량의 Li20 를 함유한 조성은 피해야 한다. 앞에서도 지적한 것과 같이 L i 20 보 다 알칼리금속산화물의 함유는 일부 결정화유리의 조성에서는 바람 직하다. 이런 경우에는 단독으로 알칼리금속산화물을 사용하는 것 보다 전체적으로 같은 농도인 2 개의 알칼러금속산화물의 혼합물을 사용함으로써 화학적 안정 성 을 더 높여 주는 mi xe d alkali eff ec t 를 이용하는 조성을 선택할 수도 있다. M g O 와 CaO 같은 알칼리토류산화물은 유리의 화학적 안정성을 중가시키므로 결정화유리에서는 가치있는 성분이다. Al203 와 ZnO 도 비슷한 효과가 있다. B203 의 소량을 첨가하면 이것이 찬유유리 상에 농축되어 안정성울 중전시킨다. 보통 B2 아는 유리상의 내화도 를 낮춰 열처리중 결정화유리를 변형시키기 때문에 첨가량은 2~3 %가 한계이다. 어떤 응용에서는, 결정화유리는 고온에서 환원가스 와 접촉하면 영향을 받지 않는다는 것은 중요하다. 이 경우 결정화 유리의 조성은, 쉽게 환원되어 금속이 되는 어떤 산화물도 함유하여 서는 안된다. 환원 또는 중성분위기에서 결정화유리를 열처리함으 로써 非化學量論的 結晶 (non·s t o i ch i ome t r i c cr y s t al) 이 생기는 것을 피 해야 된다. 예를 들면 비화학량론적 2 산화티탄이나 티탄산영은 전 기절연특성을 떨어뜨리게 된다. 3.2.3 유리의 結晶化特性 결정화유리제조를 위한 유리조성을 선덱할 때 가장 중요한 기준 온 아마도 쓸데없이 간 열처리를 하지 않고 결정화시키는 데 있을 것이다. 또요구되는특성을갖는 최종건정화유리가 얻어질 수 있도 록 결정형이 생성되기 위해서는유리의 성분과 그바울도 중요하다.
그러나 어떤 유리에서는 결정성장이 기대되는 온도에서 장시간 열처리하여도 실무를 일으킨다. 예를 들면 칼뮴-알루미노규산유리 특히 正長石 (K20•Al2 아 ·6S i 02) 을 용융시켜 만들어전 유리는 결정 화가 매우 어렵다. 이렇게 안정도가 높은 유리는 비록 핵생성촉진 제를 사용하면 실두가 일어나지만 열처리시간이 너무 길어 바경제 적이기 때문에 결정화유리를 제조하기 위한 출발원료로는 적합치 않다. 한편 실투가 쉽게 일어나 냉각 및 성형중 결정성장이 생기는 조성들도 바람직하지 않다. 유리의 냉각 및 성형중의 안정도에 필 요한 조건과 열처리중 신속히 결정화하는 데 필요한 조건은 일치 하지 않는다. 그러나 핵생성촉진제를 사용하면 이 불일치한 요구 조건은 일치하게 된다. 재가열공정중 비교적 쉽게 결정화가 일어나는 유리들은 많은 양 의 수석산화물울 함유하고 있다• 왜냐하면 이 수식산화물은 인접 S i 04 사면체와 연결되어 있는 架橋酸素이온 대신 비가교산소이온을 도입 함으로써 유리 망목을 약하게 하기 때 문이 다. 비 가교산소이 온 의 양이 증가하면 접차 망목구조가 약해져 결정화에 필요한 원자의 재배열이 접차 커지게 된다. 존재할 수 있는 수석산화물의 上限量 은 유리 가 용융체 나 준용융체 상태 (semi -m olte n s t a t e) 에 있 을 때 결정 화를 일으키지 않기 위한 조건들에 따라 좌우된다. 일반적으로 제여된 열처리공정중 유리의 절정화를 촉진시키는 데 유용한 수식산화물은 금속양이온의 크기와 전하에 의해 결정된 다. 높은 이온장강도를 갖는 작은 양이 온은 낮은 이온장강도를 갖는 큰 양이온보다 더 규칙적인 배열을 한 산소이온돌에 둘려싸이려는 . 경향이 있다. 따라서 작은 양이온을 가진 유리조성이 더 쉽게 규칙 적인 결정구조로 전이한다. 이런 이유로 L i 20 가 Na20 나 K20 보다 더 유용한 성분이며, 알칼리토류산화물 중에서는 M g O 의 M g 2+ 가 Ca2+ 나 Ba2+ 보다 이온장강도가 훨싼 더 크기 때문에 가장 유효할 것 이 다. 그러 나 Ca2+ 나 Ba” 이 고농도로 촌재 하면 실루를 촉진시 키는 경향이 있기 때문에 Cao 와 BaO 도 결정화유리의 주성분으로 사용될 수 있 다. ZnO 도 Zn2+ 의 이 온장강도가 상당히 커 Zn2+ 가 주위산소이온에 현저한 規則勅果 (order i n g e ffe c t)를 미칠 수 있기
때문에 유용한 성분이다. ZnO 를 다량 함유한 유리는 실 투 가능성이 : 증가된다. 유리구조에 대한 이 효과는 이온들을 剛球 로 취급 한 아 온장 강 도의 간단한 개념에 의해 예측되는 것보다 더 클 수 있다. 최 의 각전자를 18 개 갖는 Zn 2 도 은 稀 가스양이 온 (nobl e gas cati on ) 이 아니므로 주위의 음이온에 강한 변형 효 과를 나타낸다 . 예 를 들 면, ZnO 중의 Zn2+ 은 4 개 의 산 소 이 온에 둘러 싸여 있으나 Mg O 중의 M g 2+ 은 6 개의 산소이온에 싸 여 있 다. 따라서 Zn2 +7} 더 변 형시 키 표 3 . 2 市販 結晶 化유리 品 名 | 主 結 晶 相 | 特 徵 | 用 途 Cornin g 860 3 Lh O •S i0 2 , L ii O • Pho t oe t ch i n g可 流 體素 子 2Si0 2 能 II 9606 2Mg 0 • 2A h 0 3 · 5 Si 02 高周波絶緣性良 rado m e II 9608 /3 -s p odumene 固溶體 g久低l a彭 z性 e 服 하良, 化 學兩 食器 II 0303 Na20 • Alz 아 • 2S i0 2 여 强 化 食器 BaO · Alz 아 •2S i 0 2 I’I’II 990643513535 //-33m --ss upp l olidtoued um ImeIe nnee 固固溶溶證體 强으良 低度 低彭로大 彭服安, 財, 限定 風高 , 溫熱化 安的性 r熱建an材交g 換 e 機to p • • II High -K (Ba, Sr, Pb)Nb20 s 定 高誘電率 condense r GEenng elirsahl EEllee Rcc ettrr- Xii cc Lh 0 • 2S i0 2 金 屬 에 II封 着 可 能 bushin gI I N日 a 本 ru 電 m 氣 i N製 萌-陶 o 子 B- 石 英固溶體 低 彭服 , 透 明 尉熱窓 , 工 業材料 N- 11 P-s p odumene 固 溶體 低 彭服 , 不 透 明 食器 ,工 業 材 料 N-15 II 低 彭服 ,半 透 明 熱線透過雨熱窓 Owens·I ll in o is Cer v it C- 10 1 g-石英固 溶體 低 彭照 ,硏 磨性良 反射望遠鏡基體 C- 10 6 P-s p odumene 固 溶體 低彭服 , 半透明 熱源 cover NPhuacuedrilte eCr -126 알칼리 珪I I酸 鹽 鋼低 에 彭 服co a,ti 不ng 透 可明 能 化調 學 理機器器 , 加熱機 PPG Hercuvit 106 /3 -s p odumene 固 溶體 低 影眼 , 半 透 明 調 理 器 - 101 /3-石英固 溶體 透 明 高 溫 窓 u
는 힘이 크며 유리구조 중에서 주위의 산소이온들에 대한 Zn2+ 의 orderin g eff ec t 가 더 크게 된다. 3.2.4 결정화유리製造를 위한 유리組成 결정화유리의 조성은 보통 3 성분계 유리보다 더 복잡하다. 여기 서는 각종 산화물계로부터 만들어전 결정화유리의 質例를 들겠다. 표 3.2 에는 시관중인 결정화유리를 그 주결정상 및 특칭벌로 분류 하여 나타냈다. (1) Li 20 ― Al203 — S i O 홀로부터 의 製造 감광성핵생성된 결정화유리와 열팽창계수가 매우 작은 결정화유 · 리는 이 계로부터 만들어진다. 주성분 이의에 핵생성촉진제로 금 속, Ti0 2 , 금속인산영 등이 첨 가된다. 두번째 로 중요한 성 분이 용 융과 작업성질 또는 결정화목성을 개선시키기 위해 첨가되기도 한 다. 이 들 성 분에 는 알칼리 토류나 알칼리 금속산화물이 포함된다. 어 떤 경우에는 소량 첨가에 의해서도 결정화거동에 不均衡勅果를 나 타내기 때문에 매우 중요하다. K20 가 그 예로, 감광성핵생성된 결정 화유리 (ph oto s ensit ive ly nucleate d g lass-ceram i cs) 에 서 K20 는 Li 20 •2 Si0 2 보다 Li20 • Si0 2 (lithi u m me t as ili ca t e) 의 생 성 을 촉진한다. 또 결정질실리카의 생성에 강한 효과를 나타내기도 한다. 결정화유리의 조성과 첨가되는 성분의 성질에 대한 實例를 들겠 다. T i 02 로 핵생성된 L i 20-Al203 ― S i 02 계의 결정화유리는 열팽창 계수가 15XI0-7 보다 작으며 이 조성범위논 W t%로 Si0 2 ; 53~75, Ti Oz ; .3 ~7, Li 20 ; 2~15, Al2 아; 12~36 이다. 표 3.3 에 각종 결정 화유리의 조성을 실었다. (2) M g O ― Al203 ― S i O 홀로부터 의 製造 이들 결정화유리논 알칼리금속이온을 전혀 함유하지 않을 수 있 기 때문에 誘電損失이 작고 固有抵抗 (res i s ti v ity)이 큰 우수한 전기 적 특성을 떨 수 있다. 그러나 유리를 改質하기 위해 알칼리금속~ 화물과 다른 성분들을 소량 첨가하키도 한다. 이 유리의 주성분은 W t%로 Si0 2 ; 40~70, Al2 아; 9~35, Mg O ; s~12 범위이며 Ti 0 2; 7~15 또는 P20s; o.5~6 가 핵생성촉진제로첨가된다.
표 3. 3 결정 화유리 의 組成 伊U (*Glass re f erenc e 의 숫자는 본 문 중의 (1) (2) ... 1r e?e麟 : ~ce I Si0 2 j Ah0 3 I Mg O I CaO I BaO j ZnO I PbO (1) 73. 5 16.2 (1) 67.8 20.8 1. 0 1. 0 (1) 68. 0 21 . 0 (1) 63. 6 19.8 2.8 2.7 (1) 55.9 18.9 (2) 42.8 30 .2 14.0 (2) 45.2 29.5 10.4 (2) 46·7 28.9 13. 3 (2) 64.8 18. 5 9.3 (2) 52. 3 20.3 24.4 (2) 59.4 17.9 19. 7 (3) 73. 1 7.0 (3) 67.9 15.5 (3) 64.7 7.7 11 . 7 (4) 58.l 15,8 (4) 48 .2 39.2 (4) 44.4 48.1 (4) 37.2 50.5 (4) 59.2 13.1 14.0 (4) 47.8 11. 0 29.9 (5) 50.9 23.2 18.5 (5) 49.0 19.6 29. 4 ’ (5) 27.0 17.0 36.0 (5) 6.0 50. 0 (5) 6.0 5.0 50.0 (6) 53.4 17.7 17.8 (6) 66.7 15.5 6.7 (6) 48.2 17.6 21. 9 (6) 39.5 21 . 9 26.3 (6) 31 .1 15. 5 42. 3 (6) 15.6 4.4 68.9 (6) 27.3 27.3 (6) 44.7 22. 3
동에 기순된 걷정화 유리를 나타냄) 1_ CdO I Li2 0 I K20 I B203 I Ti0 2 I P20s I Zr02 I F I 4.3 6.0 3.9 5.5 4.0 1.0 6.0 8. 요 3.0 22,2 、- 3.0 13 .0 1. 8 10. 8 2.3 0.9 10.2 7.4 3.0 3.0 10.5 6.4 3.0 I 1123..69 33..00 23.1 3.0 9.6 3.0 4.5 3.0 9.3 3.0 9.0 2.0 2.7 7.3 1,6 2.4 7.4 2.0 16.0 4.0 40.0 4.0 39.0 11.1 11.1 12.3 12.3 11.1 11 .1 : 36.3 9.1 I -I 22 .3 10.7
(3) L i 20 ― M g O ― S i O 홀로부터 의 製造 이 계의 유리에는 결정화를 촉진시키기 위해 금속인산염이 사용 되며 유리의 조성은 W t%로 Si0 2 ; 51~88, Mg O ; 2~27, Li2 0 ; 9' ~27, P205; o. 5~6 범위이다. 이 계의 결정화유리는 열팽창계수가- 14(04X)1 0L-i72 이0 —상 Z으nO로 — 매Si우0 2 系높로다.부 터 의 製造 높은 기계적 강도를 갖는 결정화유리는 이 계의 유리로부터 만들 어진다. 적합한 핵생성촉진제로는 금속인산영이나 Cu, Ag , Au 와 같은 금속이다. 이들 유리는 금속핵생성 촉진제에 감광성을주기 위 한 방사선조사는 필요없다. 유리의 주성분은 W t%로 Si0 2 ; 34~81, ZnO; 10~59, Li2 0 ; 2~27 이며 이들 성분의 총량은 적어도 90% 이 상이어야 한다. 핵생성촉진제는 P20s; o.5~6, Au; o.02~o.03, A gCI 로 계산하여 0. 02~o. 03 의 Ag , Cu20 로 계산하여 Cu o. 5~1 범위이다. 이의에도 알칼리금속산화물 (Na20, CaO), 알칼리토류산 수 화물 (M g O, CaO, BaO), Al20a, B2 아, PbO 가 소량 첨가될 수 있다. 조성의 선덱에 따라서는 열팽창계수가 43X10-7~174X10-7 까지의 결정화유리를 만들 수 있어 융통성있는 재료이다. PbO 를 주성분으로 30% 까지 함유한 결정화유리도 만들어졌으며 이것은 열팽창계수가 크며 이와 같은 고납결정화유리는 유전손실특 성이 매우 좋다. (5) 알칼리가 없고 ZnO 를 多 墓 合有한 결정화유리 ZnO ― Al2°3 ― S i아 계 유리 에 T i아 를 핵 생 성 촉진제 로 첨 가시 킨 결정화유리가 있으며, 이 계의 유리에서 S i 02 의 일부 또는 전량을 B2 야로 치환시킨 결정화유리는 流動特性이 있어 특수코팅이나 封 着에 적합하다. (6) 알루미노-珪酸鹽系로부터의 製造 이 계의 유리에 T i 02 나 Zr02 등과 같은산화물을 핵생성촉진제로 . 사용하고 F 를 소량 첨가하면 강도가 콘 결정화유리가 얻어진다. 이상과 같이, 결정화유리는 각각 特定結晶相울 갖고 있기 때문에 넓은 법위의 각각 다론 물리적 독성을 갖는 재료들을 만들 수 있다*
제 4 장 결정화유리의 製造工程 결정화유리의 제조공정에는 a) 군절한 유리의 제조, b) 요구되는 形 狀 으로의 유리성형, c) 제어된 열처리공정에 의한 미제결정의 결정화유리제조 둥이 포함된다. 성형공정까지는 일반유리와 같으나 결정화유리의 조성은 일반적으로 용융온도가 높고 실루하기 쉬운 것이 문제이다. 따라서 제품의 품질에 영향을 주지 않는 범위에서 용융온도를 내리고 액상온도를 내리논 성분을 소량 첨가한다. 유리 의 성 형 온도는 성 형 방법 에 따라 다르나 대 개 103~107p o is e s 의 점도에 대응하는 온도로 되어 있다. 유리의 실두는 대개 °석상온도 이하에서 일어나나, 고온으로부터 차츰 온도를 내리는 경우에는 액 상온도 아하의 어느온도까지는 準 安定領域으로 실제로는실두가 일 어나기 어렵다. 따라서 실두를방지하기 위해서는가능한°석상온도를 낮 추] , 성형온도범위가 액상온도 이상 또는 준안정영역에 들어가도 록 하면 된다. 다시 말하면 액상온도에서의 접도가 높도록 하면 되 며 조성의 선택도 이 점을 주의하여야 한다. 단 실두가 일어나려면 시간이 필요하므로 성형을 신속히 하는 것도 실루를 방지하는 한 방법이다. 또한 용융시 용융로의 설계에 주의하여 용융유리가 실루 온도에 장시간 방치되지 않도록 하는 것도 중요하다. 성형 후의 유리의 결정화는 결정화유리의 特有한 공정이나, 이를 위한 열처리에서는 分相, 核生成, 結晶成長, 2 次結晶生成 둥이 일 어난다. 각각의 과정은 결정화유리에 따라 다르므로 가열온도와 시 간도 당연히 다르나, 분상과 핵생성이 충분히 일어나야 미세한 결
정입자를 석출할 수 있다. 以下에서는 미세결정의 결정화유리를 제조하기 위한 工程順에 따 타 상세히 설명하겠다. 4.1 유리의 製造 유리는 出發原料 (ba t ch) 의 혼합물을 충분히 높은 온도에서 가열하 여 원료들이 서로 반응하고 용융체로부터 가스기포가 飛散하도록 淸澄함으로써 만들어진다. 청칭공정이 완료되면 유리를 용융온도로 . 부터 더 높은 접도를 갖는 작업온도까지 냉각시킨다. 여기서 각종 성형방법이 적용된다. 4.1.1 유리製造用 原料 원료의 선택에서 가장 중요한 접은 純度이다. 즉, 유리조성을 찰 조철할 수 있도록 원료조성이 좁은 범위내에서 일정하여야 된다. 高價인 光學유리와 같은 高純度의 유리를 제조하는 경우, 또 값싼 유리에서 어느 정도 순도가 떨어지고 값싼 원료를 사용하는 경우 둥 경제적인 면에서도 원로선택은 중요하다. 결정화유리의 경우 소 량의 불순물도 유리의 결정화특성에 영향을 주기 때문에 고순도의 원료가사용된다. 유리 의 주성분은 S i O 군] 고 유리 뱃 지 중 Si0 2 의 주원료는 石英이 며 가장 좋은 모래는 S i아를 99.5% 이상 함유하고 있다. 소량의 Al2 아 가 함유되 기 도 하며 Fe2 야 는 반드시 촌재 한다. Fe2 야는 유리 , 에 녹색을 띠게 하나, 불두명 결정화유리에서는 나타나지 않는다. CaO 와 Mg O 의 원료로는 CaC03, Mg C 03 또는 dolomi te (CaCOa • M g C03) 가 사용된다. BaO 의 원료로는 BaC03 가 좋으며 Al2 아 로 는 Al20a•3 H20 또는 煥燒된 알루마 나가 사용되 기 도 한다. 일반식 이 R20·Al2 야 ·6S i 02 인 長石도 알루미 나源으로 사용된다. 물론 알루 미나源 이의에도 실리카와 알칼리산화물의 도입에도 장석이 사용된 다. 그러 나 Na20 源으로 가장 많이 사용되 는 것은 Na2COa 이 며 K20· 는 K2C03 로 도입된다. 유리 중의 알칼리성분의 일부는 空酸鹽으로-
도입되기도 한다. 질산염은 용융과 청칭을 축전시키며 산화제로 작 ` 용하기 때 문에 유용하다. Li 20 는 L i 2C03 로 도입 하는 것 이 편리 하나, 경 제 적 으로는 pet a l i te (LiA lSi4 0 10) 이 나 s p odumene[ Li Al(S i 2 아) ]와 같은 Li 울 함유한 원료를 사용하도록 권장하고 있 다. B2 아源으로 는 覇酸, 湖砂 (Na2B401·10H20) 가 많이 사용된다. As2 야 및 Sb203 는 淸澄劑 (re fi n i n g agen t)로 소량 사용되 며 CeO 는 산화제로 자주 사용된다. 사용목적에 따른 각종 원료는 전문서적 l l. 울 참조할 것. 4.1.2 유리의 瑢融 원료는 정확히 중량을 측정하고 충분히 혼합한 후 유리조성에 따 타 1250~1600°C 의 용융온도가 유지된 용융로에 두입한다. 정확한 조성 이 알려 진 破유리 (culle t)를 유리 調合物인 뱃 지 에 함유시 키 는 경 우가 있으나, 파유리는 유리의 용응과 군질화를 돕는다. 유리는 crusib l e 이 나 도가니 (po t)에 서 용융시 키 나, 다량의 유리 를 용융시 킬 때는 연속적으로 뱃지를 보충시킨다. 이런 용융로를 탱크가마라고 하며 이 進는 가스나 기름의 炎으로 가열하나 최근에는 용융유리 중에 고전류를 통과시키기도 한다. 내화물의 부식작용에 의한 유리 조성의 변화가 최소화되도록 용융유리의 容器를 築域하는 데 고급 내화물이 사용된다. 이 내 화물은 기 본적 으로는 mull ite( 3 Al203 • 2S i 02) 를 함유한 고순 도 내화접토나 s illi man it e(Al203·S i 02) 형 내화물이 사용되고 있다. 또 mu llit e-z i rcon 을 기 본조성 으로 한 電鑄兩火物 (electr oc ast refr ac to r y) 도 종종 사용되고 있다. 특수한 경우, 예를 들면 매우 높은 군질성 과 잘 제어도J. 성질을 필요로 하는 미사일의 radome 과 같은 결정화 소 유리를 만둘 때는 P t로 내장된 탱크가마가 유용할 때도 있다. 고온에서는용융로중에 십한 반응이 일어난다. 알칼리탄화물은 · 실리카와 반응하여 CO2 가 방출되며, 알칼리토류산화물도 분해되 어 이 산화물들은 용해되고 수산화물과 질화물도분해되어 珪酸溶融 體와 결합된 산화물이 얻어진다. 가스의 방출에 의해 용융유리는`
1) 金炳F@., [j'유리 工學』, P. 20, 淸文閣(1 978)
맹렬한교반이 일어나고 따라서 혼합이 촉진되며 고속도의 반응이 유 지된다. 또한 완전한 용해와 용융이 일어나고 용융체 중에서 기포가 없어지게 된다. 기포의 상승속도는기포칙경의 제곱에 비례하므로큰 키포는 작은 기포보다 빨리 상승한다. 이런 이유 때문에 청칭제를 뱃지 중에 첨가하여 용융공정의 최종단계에 가스가 방출되도록 한 다. 청 칭 제 로는 As203, Sb203 가 사용된다. 용융체 를 냉 각시 킬 때 기포가 재용해되어 유리 중에 CO2, 02, S 아와 같은 용해된 가스가 함유될 수도 있다. 청칭단계는 유리를 청칭온도 보다 數 百 度 아래 인 작업온도까지 냉각시킴으로써 일어난다. 탱크가마에서는 유리를 분리된 탱크가마의 냉각실로 보냄으로써 청칭과정이 이루어진다. 이곳에서 가능한 유리의 접도가 군일하도록 군일온도 를 유 치 한다. 4.1.3 成形工程 유리 細工技術者가 이 용하기 쉬 운 성 형 공정 은 鑄造法 (cas ti n g met- nod) 일 것이다. 이 공정은 간단하기 때문에 응용에는 한계가 있으 며 板이나얇은 環狀을 만들기에는제한을 받는다. 遠 心 鑄 造法 은 용 웅유리를 고속으로 회전하는 金型 (mold) 에 넣어 모양을 만드는 방 법이다. 마사일용 radome 의 원추형은 이 방법으로 만들어지는 예 이다. 주조법은 알칼리를 함유하지 않은 유리와 같이 작업온도 범 위가 좁은 유리에서 유용하다. 平板유리 는 탱 크가마로부터 유리 를 물로 냉 각시 킨 roll 사이 로 지 나게 하는 roll ing pro cess 에 의 해 만들어 지 며 薄板 유리 는 連續 引上 法 (con ti nuous-draw i n g p rocess) 에 의해 만들어진다. 棒 이나 듀브도 인 상법에 의해 만들어지나 용융유리를 回 轉 心 棒 (mandrel) 에 흘려 보내 고 연속적으로 봉이나 튜브를 만들기 위해 십봉의 끝으로겨부터 잡아 당간다. 적당한 금형을 사용하여 유리를 누르는 押型法(p ress i n g)은 렌즈나 접시모양의 기구를 만드는 데 사용되며 고속생산이 가능한 완전 자동압축기가 사용되고 있다. 각종 空洞유리제품들은 型吹法 (blow i n g)으로 만들며 역 시 완전 자동기 계 화되 어 있 다. 대부분의 결정화유리는 유리의 성형기술을 그대로 사용하여 성형 시킬 수 있기 때문에 유리의 융통성이 새로운 재료인 결정화유리에
서도 지속된다. 유리성형중 온도구배가 생겨 내부응력이 발생하며 이 응력은 徐 冷에 의해 제거해야 하며 이 응력은 유리기구의 파쇄를 가져온다. 서냉은 유리의 접도가 약 1012~1014 p o i se 인 서냉범위내에서 유리 를 균질한 온도로 하면 얻어진다. 내부응력은 結性流動에 의해 제 거된 후 큰 온도구배가 생기지 않도록 충분히 느린 속도로 냉각시 킨다. 냉각속도는 서냉되는 유리기구의 두께에 의해 결정된다. 얇 은 유리는 全工程이 1 시간내에 완결되나 두꺼운 유리는 數時間 또 는 며칠까지도 걸린다. 서냉은 중간가마(i n t erm itt en t k il n) 에서도 이 루어 지 나 연속가마인 lehr( 徐冷 黑 )가 가장 많이 사용되고 있 다. 4.2 微維結晶인 세라믹의 生成 4.2.1 熱處理工程 (1) 核生成 및 結晶化工程 열처리공정의 목적은 유리를 본래의 유리보다 우수한 성질을 구 비한 미세결정인 세라믹으로 轉換 시키는 데 있다. 특히 기계적 강도 가 큰 세라믹은 微粒化된 미세구조로부터 얻어지며 이것은 치밀하 게 결합된 미제한 결정들을 함유한 결정화유리를 만듦으로써 얻어 질 수 있다. 비교적 租大하고 數가 적은 결정보다 작고 수가 많은 결정을 제조하기 위해서는 유효한 핵생성이 팔요하다. 이것은 연처 리의 핵생성단계에서 신중한 제어를 해야 된다는 것을 의미한다. 핵생성된 유리는 核上에서 결정성정율- 일으키기 위해 더 온도를 높 여야 한다. 이 온도상승속도도 결정화유리의 변형을 피하기 위해 찰 제어되어야 한다. 가연속도가 너무 빠르면 결정성장속도가 충분 히 빠르지 못해 단단한 전정인 骨格 (skel t on) 이 모든 온도에서 존재 하지 않게 된다. 가열속도가 느리면 변형은 일어나지 않고 유리相 이 다량 존재하게 되나, 이것은 온도가 높아지면 접차 작아지게 된 다. 이 연처리단계를 동해 각종 결정이 석출되고 대부분의 경우 결정 화의 효과로 찬유유리상의 내화도가 높아지기 때문에 유리상의 조
성은 접차 변화될 것이다. 이 변화에 의한 바람직하지 못한 효과오T- 더불어 급속한 가열도 결정화유리의 군연을 가져오기 때문에 피해 야 한다. 이 현상은 생성된 결정의 밀도가 유리상의 밀도와 다르며 결정화에 따른 체적변화가 유리상과 결정상 중에 응력을 가져올 수 있기 때문에 일어난다. 천천히 가열울 하면 이들 응력은 유리상 의 점성유동에 의해 제거된다. 上限結晶化溫度 (u pp er crys t a l l iza ti on t em p.)에 도달하는 은도까지 계속해서 천천히 온도문 올린다. 이 上 限溫度에 서 는· 전·유유리 상의 軟化나 내 화도가 낮은 건 정 상의 용융 때문에 결정화유리가 변형되지 않고 결정화가 급속히 전행된다. 적당한 기간 동안 상한결정화온도에서 결정화유리를 유지하면 찬유 유리상이 극히 소량만 존재하는 거의 완전한 결정화가 얻어진다. 열처 리 공정의 여 러 단계는 그림 4. 1 을 참조하면 확실하다. 공정의 첫단계는 실온으로부터 핵생성온도까지 유리를 가열하는· 과정이다. 보통 여기서 사용되는 가열속도는 결정화공정에서와 같 이 까다롭지는 않다• 이 단계에서는 단지 유리기구내에 온도구배 가 생겨 군열의 원인이 되는 위험한 응력이 발생하지 않도록 주의 ;
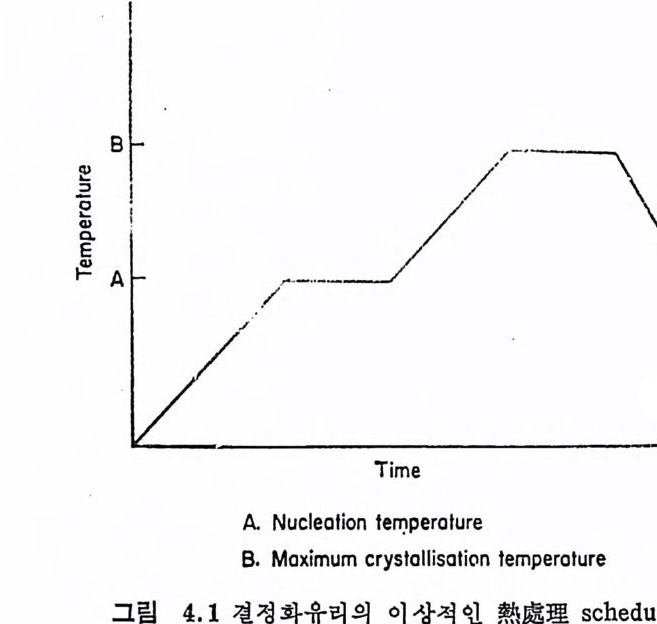 aJJaOd IO Ea L' ’~ 二 / . /
aJJaOd IO Ea L' ’~ 二 / . /
하면 된다. 유리기구는 곳에 따라?]는 열팽창계수가 큰 곳과 작은 곳이 있으나 가열속도는 유리기구의 두께에 의해 주로 결정된다. 얇은 유리는 10°C/m i n 인 높은 속도로 가열할 수 있으나 보통은 2 ~5° C / m i n 가 사용된다. 보통 최적핵생성온도는 접도가 1011~1012 p o i se 에 해당되는 온 도 범위내에 있다. 최적핵생성인 이 범위내의 온도는 실험에 의 해 결정된다. 최초의 近似質 驗 으로는 최적핵생성온도를 유리 轉移溫度 T g와 이보다 50° c 높은 온도 사이에 놓는다. 더 정확한 실험은 다음과 같다. 유리小摘의 온도를 정확히 또 신속히 측정할 수 있고 小 源 울 현미경 관찰할 수 있도록 장치한 小型 迫 에서 유리의 小 摘 울 용융 시킨다. 이 小 商 울 임의의 온도까지 냉각시키고 1 분 정도 그 온도에서 방 치한 후 가장 낮은 액상온도까지 재가열한다. 각종 결 정상이 실두에 의해 생성되면 대응하는 및 개의 액상온도를 얻게 된다. 가장 낮은 액상온도까지 재가열시 어떤 결정화도 일어나지 않는다면 유리 小商울 재 용융하고 前보다 약간 더 낮은 온도까지 냉 각하고 다시 재가열하여 결정생성을 관찰한다. 이 과정을 최대핵 생 성온도가 측정될 때까지 계속한다. 유리가 핵생성온도에서 유지되어야 하는 시간은 보통 o.5~2hr 이 다. 핵생성은 최적핵생성온도와 서냉점 사이의 온도에서도 일어날 수 있지만 핵생성온도가 낮으면 접도가 갑자기 커져 핵생성속도가 크게 떨어져 핵생성시간이 길어진다. 예를 들면 접도가 1013- 3 po is e 에 해당되는 서냉접에서 핵 생성촉진제로 T i 02 를 함유한 유리에 충분한 핵생성을 일으키려면 100hrs 가 질란다. 핵생성과정과 관련 하여 중요한 접은 최대강도의 결정화유리를 얻는 데 있다. 이것은 유리를 핵생성의 가열단계 전에 최대핵생성온도 이하로 냉각하면 된다. 이것은 유리가실온까지 냉각될 때 유리상태에서 냉각되고 . 핵생성온도 이하의 온도에서 서냉되기 때문에 종종 자연적인 과정 으로 일어난다. 그러나 어떤 경우에는 열처리에 의한 결정화과정이 유리기구의 성형 후 곧 뒤따르기 때문에 이때는 핵생성온도 이하 · 로 충분히 냉각시켜야 하며 경우에 따라서는 이 온도간격이 100~· 300°C 까지도 된다.
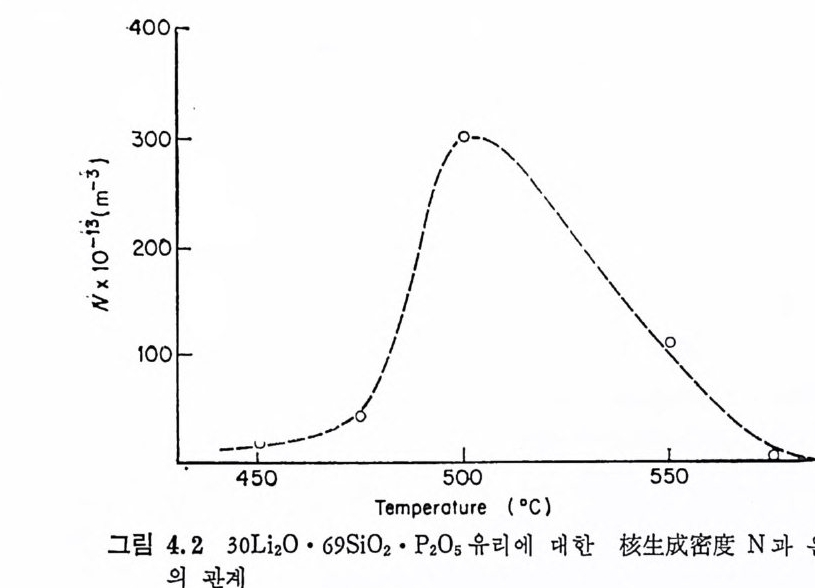 ·40 0
·40 0
앞에서 설명한 순서 대신 핵생성범위내의 각 온도에서 유리시편 · 울 일정시간 열처리한 후 결정성장온도에서 유지시켜 핵생성의 최 적온도를 결정할 수 있다. 미리 정해전 시간 후 迫 에서 유리시편을 빼내 충분히 냉각시켜 결정성장과정을 억제시킨다. 광학 및 전자 현미경을 사용하떤 성장한 결정핵의 수 및 걷정의 평군직경이 얻어 지며 이들은 사용된 핵생성 온도에 크게 좌우된다는 것을 알 수 있 다. 그림 4. 2 는 30 Li2 0 • 69 SiO z •Pz 야 의 결 정 화유리 에 대 한 Harpe r 둥 2) 의 연구결과를 요약한 것이다. 이 유리에서 최적핵생성온도는 약 500°C 임이 분명하다. P20s 의 핵생성촉진제로서의 역할은 그림 4.3 을 보면 확실하다. 이 그림에 서 각각의 유리는 500°C 에서 1 시간 핵생성 및 750°C 에서 1 시간 결정성장을 위한 열처리를 하였다. P20s 를 함유한 유리는 미립자 로 된 미제구조가 발달되어 있으며 이 유리의 核生成密度(核數 /m3) 및 平均粒度는 P2 야 가 함유되 지 않은 유리 의 1 x 1013m-3 및 60µm 에 대해 각각 3X1015m-3 및 5µm 이었다. 이들 핵생성 밀도는 간접
2) H. Harpe r, P. F. Jam es and P. W. McMi llan , Di sc uss. Faraday Soc. , 50, 206(1 9 79).
 그림 4.3 결정화유리의 미제구조
그림 4.3 결정화유리의 미제구조
법에 의해 결정되었다. 죽 광학 또는 전자현미경에 의해 핵의 수를 구하기 위해 결정을 성장시켜야 한다. 그러나 高分解能透過電子顯 ~ 微鏡을 사용하면 결정성장단계를 삭제할 수 있다. 전자현미경에 의 해서 분해된 결정들은 5~20nm 로 매우 작다. 以後 Hin g둥” 에 의한 똑같은 유리 30 Li 20·69S i 02·P20s 의 핵 생성에 대한 연구결과, 최적 핵생성온도는 Har p er 둥의 결과와같이 500°C 이나 500°C 에서의 핵생성밀도는 106 배나 더 크다는 사실을 알았다. 이 차이는 핵생성온도에서 발달된 결정질만큼이 결정성장 · 울 촉진시켰기 때문이라고 생각된다. 열처리중 정교하지 못한 공- 3) P. Hin g and P. W. McM illan , J . Mate r . Sc i. 8, 3400973).
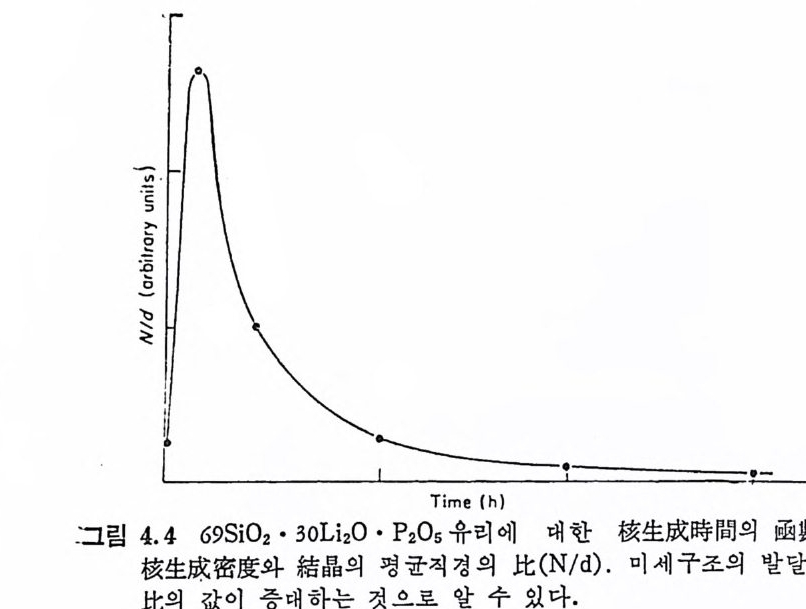 -' -Ti -m e (-h) -? •J -
-' -Ti -m e (-h) -? •J -
평(祖大化過程)이 핵둘을· 소멸시킨 것으로 생각된다. 이 와 같은 핵 들의 소멀 에 대 해 McM ill an4) 은 Li 20 ― S i 02-P20s 유 리를 550°c 에서 각 시간 열처리하여 핵생성효과를 조사하였다. 그 결과를 요약하면 그림 4.4 와 같다. 그림으로부터 가장 미세한 입 자로 된 미제구조를 갖는 결정화유리를 제조하기 위한 최적열처리 시간이 얻어졌다. 열처리시간의 변화가 미제구조에 큰 영향을 미 치며 최적핵생성시간 이후의 핵생성밀도의 감소는 租大化過程에 의 한 확산의 발생과 일치한다. 핵생성단계의 다음으로, 유리를 제어된 가열속도에서 충분히 느 리게 온도를 높이면 유리기구가 변형되지 않고 결정성장이 일어난 다. 주결정상의 °석상온도에 가까와지면 결정화가갑자기 커지나, 유 리相이 주성분일 때는 앞단계에서 변형울 방지하여야 하며 보통 가 열속도는 5°C/m i n 를 넘지 않는다. 허용되는 가열속도의 결정은 2 개의 칼날모양의 試驗支持台에 유리봉을 놓고 핵생성을 위한 열처 리단계에서 가열속도를 변화시키면서 실험을 하면 쉽게 얻어진다.
4) P. W. McM illan , Proc. Xt n Int. Cong . 011 Glass 14, 1(1 9 74).
즉 각종 가연속도에서 棒 의 중십이 伸長되는 것을 측정하여 가열속 도를 결정하면 된다. 결정화유리에 대한 上限結晶化溫度는 최대결정화가 유리의 현처 한 변형을 가져오지 않도록 하여 선덱된다. 최종제품아 상당한 변 형을 일으키는 온도는 主結晶相의 °석상온도에 해당한다. 왜냐하면 이 액상온도 이상으로 온도를 높이면 결정상이 다시 용해되기 대문 이다. 각종 결정질상의 °석상온도를 측정하는 한 방법으로는 수평방향으 로 온도구배가 존재하는 遠에서 미리 핵생성시킨 유리봉을 가열함으 로써 정확히 측정할 수 있다. 이 열처리 후 핵생성온도 이상의 온 도(그러나 최고액상온도 이하)에서 가열된 봉의 부분에 함유된 결정질 을 분석한다. 한편 최고액상온도 이상에서 가열된 봉의 부분은 결 정질이 없어 두명할 것이다. 봉의 결정질부분 중에는 각종 결정질상 이 각 지역에 분포되며 촌재하는 각상의 성질들은 가열온도에 따라 다를 것이다. 여러 지역에 존재하는 상들은 X- 선회철분석과현미경 관찰에 의해 同定된다. 최고액상온도를 결정하는 편리한 방법은 앞에서 기술한 小型 城 에 유리의 小商울 핵생성시킨 후 결정화를 일으키기 위해 재가열한 다. 그 후 모든 결정이 재용해하는 온도까지 더 가열을 한다. 앞의 방법에 의해 결정된 상한결정화온도는 적어도 1 시간 동안 · 유지시켜야 하나, 결정화유리 중에서 원하는 결정도를 얻기 위해서 는 더 오랜시간 유치시킬 수도 있다. 유지시간이 경과한 후에는 결 정화유리를 실온까지 냉각시킨다. 결정화유리논 기계적 강도가 높 기 때문에 매우 높은 온도구배에도 견달 수 있어 냉각은 급속히 하 여도 좋다. 열팽창계수가 큰 재료를 냉각할 때는 어느 정도 주의를 하여야 하나, 10°C/rn i n 보다 큰 냉각속도가 사용될 수 있다. 유리 와 달리 결정화유리는 永久스트레인(p ermanen t s tr a i n) 의 발생을 방 치하기 위한 서냉조작이 필요없다. 촌재하는 결정상의 일부는 어떤 온도영역에서는 구조변화를 일 으켜 밀도와 열팽창계수도 변화하게 된다. 일반제라믹에서는 이런 구조변화는 세라믹이 임계온도영역을 지나 천천히 냉각되지 않는
::: f 41 .표 의程過 化結分晶類EJ '二I :군成一核均生i() +, - 二드I댜i툴를1均成生核一i): ( i + , _ :广드〔::二凰I-广:I: ::: )(l ::C[g:〕1-~터 1도二: ―;:广+: :-1言(i )v 급
한 파손의 원인이 된다. 결정화유리에서는 매우 작은 크기의 결정 아 존재하여 체적변화에 의해 발생하는 응력이 작기 때문에 급냉처 리에 의한 파쇄가 일어나지 않는다. (2) 結晶化過程의 分類 유리와 같은 과냉각액체를 결정화하기 위해서는 핵생성, 결정성 장 이의에도 다성분계에서는 分相도 고려하여야 하므로 결정화과정 은 복잡하나, 이들 과정을 분류하면 표 4. 1 과 같다. 표 4. 1 중의 (i)의 경 우는 단일성 분 또는 화합물조성 으로 된 유리 를 가열할 때 볼 수 있다. 예를 들면 S i아유리 또는 L i 20,2S i아유 리 를 재 가열 하는 경 우 먼저 Si 02 결 정 5) (예 ; cris t o b ali te) 또는 Li2 0 • 2S i 02 결정의 핵이 생성되고 이것이 성장하여 관찰가능한 크기의 결정이 된다. 單一 또는 화합물의 성분이므로 분상은 일어나지 않 는다. 이 과정을 거치는 경우에는 결정핵생성이 유리표면에서 일 어나 이것이 차츰- 내부로 향해 성장하는 경우가 많다. 죽 엄밀히는 군일핵생성이라고 할 수 없다. 이와 같은 결정화물에서는 입자가 표면에 수칙으로 배향하며 결정입자의 크기가 커 기계적 강도가 작 고 얻어진 결정화유리를 실용화할 가능성은 작다. (ii)의 경우는 Au, Ag , Cu 를 함유한 感光性結晶化유리에서 볼 수 있다. W t%로 Si 02 ; s1, Li20 ; 12. 5, K20; 25, AI2 아; 4, Ce02; o. 03, Au; o. 027 의 유리 논 처 음에 는 Au( 그립 중의 M 에 해 당)를 이 온으로 함유하고 있다. 여기에 자의선을 照射한 후 가열하면 Au 결 정의 핵이 생성하고 6' 520°C 에서 Au 결정이 생간다. 더 가열하면 Au 콜로이드표면에 유리의 주성분인 결정핵 (그립 중의 A 결정핵)이 생 성하고 620°C 에서 이것이 성장하여 L i 2S i 03 결정이 생성된다.” Li2 S i 03 결정핵의 생성과정이 존재하는 것은 Au 결정생성 후 급속히 620°c 이상의 온도에서 가열하면 L i 2S i 03 의 결정생성의 수가 감~소 하는 것으로부터 추측할 수 있다. 그림에서는 A 유리가 그대로 A 결정으로 변화하는 것으로 적었으나, 실제로는 위의 예에서는 Liz :
5) F. E. Wag s ta f f , J. Am. Ceram. Soc. ,· 5 1, 섬 9(1968). 76)) 作田花代仁濟,夫 ,作 花表濟面,夫 ,7 , 《2黑2協7(誌1 》9 6,9 ).6 7, 263(1 9 59);68, 158(1 9 60).
: S i0 3 결정이 생성되어 본래의 유리조성과는 약간 다르다. 이 접은 확실하지 않으나 금속이 생성된 후 유리의 주성분 (A 유리)에 분상이 일어난다고 생각할 수 있다. (iii)의 경우는 실제의 결정화유리에서 多數의 예를 볼 수 있다. 强 誘電 性의 PbTi0 3 결정 을 주성 분으로 함유한 PbO-Ti0 2 -Al20 3-Si 아유리를 예로 들면, 가열에 의해 약 620°C 에서 분상이 발달한 유 리 는 PbO-Ti0 2 가 ric h 한 미 립 자상이 Si0 2 상이 ric h 한 매 트릭 스 상 중에 분산한 모양의 조직이 된다. 가열온도가 더 높아 지 면 PbO ― -T i 02 가 r i ch 한 상은 PbT i 03 결정으로 변화된다. (i v) 의 경우나=- (iii)과 다른 접은 분상이 일어나 한 쪽 의 유리상이 결정화한 상으로부터 다론 쪽의 유리상의 결정화가촉진된다는 것이 다. 이 과정을 지나 결정질이 얻어지는 것으로는 Li2 0 -AI203-Si 아계 ( 핵 생성촉진제 T i 0 2+ Zr02) 의 低彭 服 결정화유리가 있다. 이런 종 류의 결정화유리의 생성과정을 조사한 연구들을 8)9). 종합하면, 유리 는 가열에 의해 먼처 2~3 種 의 유리상으로 분상한다. 그 중 하나는 .으Zr로 02써, T이i 0 2 상 또은는 Z r이0 2,兩 Z 者r —가 T rii0 c4 h 또한는 상 으A로l2,0 3—약 T 7i0 520 °계 C 에결 서정 으가로열 변함 화한다. 다음에 이 결정의 표면에서 또 하나의 Li 2 0 一 Al20 3 ― S i 02 유리상(그립 중의 A 유리)으로부터 같은 조성의 결정핵이 생성되며 이 것이 성장하여 8 군 5 英固 溶體 가 된다. 실제로는 결정화과정은 더욱 복잡하여 결정성장시 조성의 변화 가 일어나 일부가 유리상태로 그대로 殘 存하던가 접하여 있는 다른 상 으로부터 일부 성분이 들어올 수도 있다. 특히 고용 체를 형 성하는 경우에는 복잡하다. 일단 결정화유리가 된 경우에도 머 높은 온도 로 가열하면 결정상의 轉 移나 다른 결정상과 반응이 일어나기도 한 다. 예를 들면 8- 석영고용체를 주결정상으로 하는 極低 彭張 결정화 유리를 900°C 이상의 고온에서 가열하면 주결정상은 /3- sp o dumene (/3 -L i 20•Al2 아 •4S i 02) 고용체로 된다. 결정화유리의 성질에 중요한 영향을 미치는 문제로 유리 體 의 표
8) 守 屋喜 郞, 《黑 協 誌》 , 76, 293(1 9 68). 9) W. Sack and H. Scheid l er, Glaste c l1 . Ber. , 39, 126(1 9 66) .
연과 내부에서 결정화과정이 다를 때가 있다는 것에 주의를 해야 된다. 현재까지 알려쳐 있는 표면의 영향을 열거하면 다음과 같다. a) 조성에 따라서는 표면근처에서만 결정핵생성이 일어나키 때문 에 결정이 표면으로부터 내부로 향해 성장한다.” 이 경우 결정의 配 向, 租大化, 표면충과 내부조직의 차이에 의해 강도의 감소가 일어 날수있다. b) 표면충의 성분이 변화하여 분상과 결정생성이 일어나기 어렵 다. 이 경우 결정화물은 유리의 얇은 충으로 덮혀져 강도에 영향을 미찬다. c) 표면충의 조성변화에 의해 내부와 다른 결정이 석출한다. 따 타서 강도에 영향을 미찬다. (3) 熱處理工程에 따른 物理的 特性의 愛化 출발물질인 유리와 제어된 실두에 의해 얻어진 결정화유리의 물 리적 성질을 비교함으로써 결정화유리의 有益性울 설명하겠다. 열처리에 의한 확실한 변화는 두명한 유리가불투명한다결정질재 료로 변환된다는 것이다. 결정화유리의 不透明度는 인접결정간 및 결정과 찬유유리상간의 面間에서 屈折指數가 다르기 때문에 빛의 散
亂이 일어나는 것이 원안이나, 절정이 작고 여러 상의 굴철지수가 비슷할 때는 두명하거나 반부명하다• 전자현미경관찰을 통해 열처리를 하면 둥근 결정립계와 경우에 따라서는 角이 전 결정으로 된 起伏이 있는 표면이 생성된다는 것 을 알 수 있다. 결정화유리의 표면이 유리보다 매끈하지는 않지만 실제응용에는 큰 문제가 되지 않는다. 더구나 결정화유리의 표면 은 柚 藥 을 바르지 않은 일반세라믹스의 표면보다는 훨씬 더 매끈 하다. 결정화유리의 비중은 열처리공정중 작은 체적변화가 일어나기 때문에 母유리의 비중과는 다르다. 이 변화는 약간의 수축이나 팽 창을 가쳐올 수 있으나 보통 3% 이상의 체적변화를 일으키지는 않 는다. 일반세라믹스가 건조 및 소성중 거의 40~50% 의 큰 체적변 화를 일으키는 것과는 대조적이다. 결정화유리에서의 체적변호R 큰 결정질상의 비중과 모유리의 비중과의 전체적인 차이 때문에 생기표 4.2 유리 및 대응하는 결정화유리의 밀도 Glass comp os it ion -weig h t pe r cent oDf e pnasi rte y - oDf e gnlsa ist ys Si0 2 I B203 IAh0.1 ZnO IMg O I BaO / Cd 이 L i 2 이 Ti 02 / Zr02 n(gt / cgmla 3s)s c(ge/rc amm3i c) 57.6 4.7 15.2 5.2 12.1 3.6 2.52 2.57 48.5 14.6 34.0 2.9 3.17 3.13 41 . 7 9.3 41 . 6 7.4 3.23 3.23 50.9 23.2 18,5 7.4 2.92 2.99 48.5 21.3 4.8 15.0 10.1 2.87 2.86 46.5 24.1 17.6 12.3 2.96 2. 96l 는 것이다. 생성된 결정의 밀도는, 결정화의 효과가 물질을 수축 또 는 팽창시키는가에 따라 더 커지거나 작아진다. 한 결정상의 생성 에 의한 수축이 다른 상의 생성에 의한 팽창과 균형을 이물 때 체 적변화가 0 이 되는 한정된 조성이 존재할 수도 있다. 실제적으로 일어날 수 있는 체적변화에 대해 유리와 결정화유리의 밀도에 관한 특칭 은 표 4. 2 에 실었 다. Ti 02 에 의 해 핵 생 성 된 ZnO-Al203-SiO z 유리의 밀도는 이들이 열처리중 +, o, _의 체적변화를 일으킬 가능성이 있기 때문에 매우 홍미있다. 열처리중 비교적 작은 치수변화는 기구들을 치수公差가 작게 생 산할 수 있기 때문에 일반세라믹의 제조공정보다는 결정화유리의 제조공정이 利點이 있다. 결정화유리의 열팽창계수는 보통 모유리와는 매우 다르다. 유리 의 실두는 형성되는 결정형에 따라 열팽창계수가 증가하거나 감소 한 결과이다. 예를 들면, cr i s t oba lit e 형성은 득히 20~200°c 에서 는 열팽창계수가 커지나, /3 -s p odumene[L i (A1S i 20 야이나 /3- eucry- ptite [A1L i (S i 04) ]와 같은 리튬-알루미노규산염형의 형성은 매우 작은 열팽창계수를 갖게 한다. 그림 4.5 에 주어전 유리와 결정화유 리에 대한 열팽창곡선으로부터 모유리는 매우 비슷한 열팽창계수를 가지나 다론 결정상을 형성하는 결정화유리의 열팽창계수는 매우 다르다는 것을 알 수 있다. 실두에 의한 다른 물리적 특성의 변화로는 재료의 兩火度가 증가-
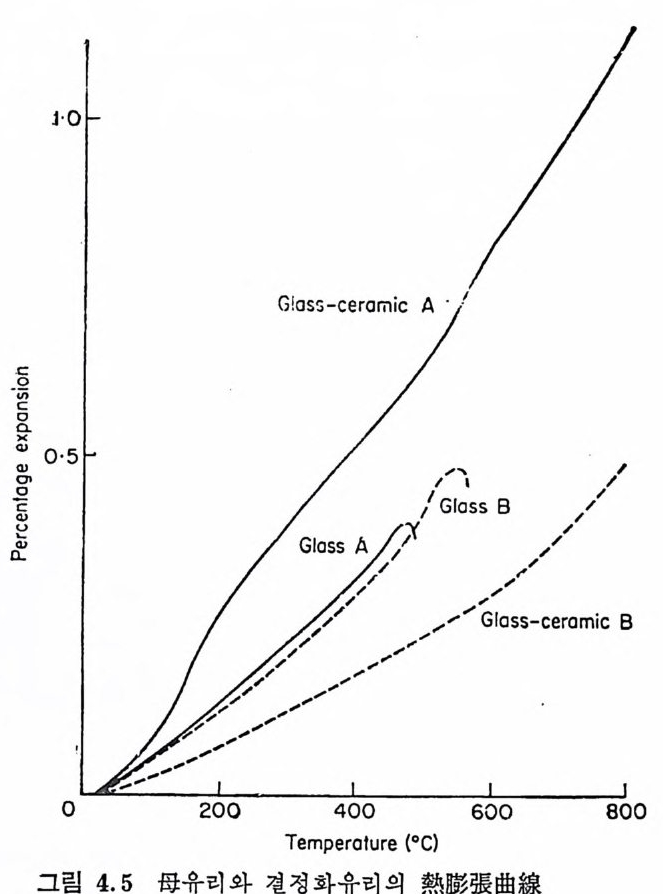 J·O
J·O
한다는 것이다. 이 특성을 정의하는 수많은 방법이 있으나 示差彭 張計軟化溫度에 의한 방법이 편리하다. 이 방법에 의한 결정화유리 와 이들의 모유리에 대한 표 4.3 에 주어진 데이터로부터 결정화공 정은 연화온도를 매우 높인다는 것을 알 수 있다. 결정화를 위한 열처리에 의한 가장 중요한 특성변화는 기계적 강 도의 증가일 것이다. 대부분 유리의 단면적 파괴강도 또는 파괴울 (modulus of ru pt ure) 은 직 경 5mm 인 棒에 서 는 10MNm-2(10000 Ibin - 2) 정도이나 결정화유리는 보통 200~2soMNm-2(30000~40000lb i n-2) 이 다.
표 4.3 유리 및 대응하는 결정화유리의 熱曲엇張係戱와 示差敷羽長i 1· i |M t溫度 ' Weig h t pe rcenta g e comp o sit ion * coe( 2ff T0~—h겁 1 ea4ernn0mst01s °ao Cx ln ) 1 07 Dteims l oapt f( oe t Oem C r na e) titun r gr ie c s Si0 2 I Lh 이 Mg o | Al2°3 | K2o |GIass leeGralamss1·c I Glass leeGralamss1-c 81 . 0 12. 5 4.0 2.5 84.3 113. 0 540 910 77. 5 12. 5 10.0 78. 0 50.3 530 930 62. 1 1. 9 17. 6 18.4 '12 . 0 50,3 790 1000 66.4 10.0 3.0 20. 6 63.4 ('. 7 640 1000 60.2 8.5 2.8 28.5 60.5 -42.4 720 1000 76.7 14. 7 8.6 92. 8 92. 5 525 890 62.4 12.4 25.2 78.8 74. 8 600 930 *N . B. The gla sses also conta i n a small pro p o rti on of P2 야 to act as a nucleati on cata l ys t . 일반적으로 결정화유리의 전기적 성질은 모유리보다 우수하며 특 히 電氣抵 抗率(또는 固有抵抗, electr ica l res i s ti v ity)은 더 높아지며 誘 電損 失은 작아진다. 이 성질의 改善은 견고하게 결합된 이온들, 특 히 불규칙적인 결정구조에 바해 규칙적인 결정격자들 중에 있는 알 칼리금속이온들의 寄與에 의한 것이 크다 . 4. 2. 2 熱處理工程의 硏究方法 열처리공정은 결정화유리를 제조하기 위한 중요한 단계이며, 요 구되는 形과 결정의 比 率 이 형성되도록 주의하여 制御하여야 한다. 따라서 최적열처리 schedule 율 적용시키기 위해서는 결정화공정을 연구하키 위한 정밀한 기술이 사용되어야 한다. 사용방빕둘은 유리 로부터 세라믹상태로 전환되는 동안 화학조성의 변화가 일어나지 않는 물리 적 방법 이 사용된다. (1) X- 線回折分析 결정질은 유리와 닫리 X - 선회철모양을 나타내기 때문에 유리와 결정화를 조사하는 데 훌륭한 수단이 된다. 그러나 X- 선회철모양 아 지금까지 알려지지 않은 결정형을 나타낸 경우도 있으며, 이때 : 는 X- 선회철 및 결정구조에 관한 연구를 계속해 나가야 된다. 더 i
복 잡한 것은 X 선모양이 알려져 있는 결정의 모양과 매우 비슷하 나 완전히 일치하지는 않는 경우이다. 이 이유로는 · 유리의 실두에 의해 생성된 결정이 완전히 순수하지 않고 결정구조 중에 있는 일 부 이 온들 이 크기와 전하가 비슷한 다른 이온들에 의해 부분적으로 치환되어 있기 때문이다. 또 어떤 결정들을 고용체를 쉽게 형성한 다. 예 를 들면 (3- spo dumene 과 석 영 은 全固溶體系를 형 성 할 수 있 으며 따라서 X- 선회절모양도 변형을 하게 된다. 열처리공정중 생기는 각종 결정을 同定하고 여러 상들이 형성되 는 온도와 시간의 조건을 측정하기 위해 유리시편을 열처리 sch- e dule 에 따라 처리하고 미리 정해진 시간간격에 따라 유리시편을 테 내 급냉 시칸다. 이들 각 시편을 X _ 선회절분석하면 핵생성단계로 . 부터 최종결정화 단계까지의 완전한 결정화공정을 얻을 수 있으며 다 몬 결정상의 분리는 열처리공정의 시간_온도 schedule 과 상호관 련지 을 수 있다. 그러나 이 방법도 연속적인 기록이 되지 못하기 때 문에 열 처 리 schedule 을 통해 특수상이 발달하는 것 을 연속적으 로 기 록할 수 있 도록 記錄回折計 (record i ng d iffr ac t ome t er) 와 연결된 高溫 X- 선 카메라를 사용하는 개량기술을 사용하는 것이 좋다. 이 기 술의 한계는 단지 한 상의 발달만을 쉽게 추적할 수 있다는 접이 다 . X - 선희철분석은 결정화유리 중에 촌재하는 각종 상의 양의 近 似値를 얻는 데도 사용할 수 있다. 이 방법은 同定할 수 있는 결정 들에만 적용된다. 經知의 결정과 유리의 분말을 각종 비율로 혼합 한 합성결정화유리들을 준비하여야 한다• X- 선산란효과가 합성흔 합물과 실체의 결정화유리 중에서 비슷하도록 혼합물 중에는 결정 화유리의 母유리를 사용하는 것이 현명하다. 露 出時間과 X- 선팔 름등의 같은 조건하에서 결정-유리의 혼합물과 결정화유리에 대한 X - 선회철스펙트럼을 얻는다. 합성혼합물에 대한 회철사진 중에서 강한 회철선의 光度測定을 함으로써 득정회철선의 강도와 결정상의 %와의 관계를 그어 檢量線을 작성한다. 이 곡선은 결정화유리에 대한 X_ 선회철사전의 측정을 통해 결정화유리 중에 있는 결정상 · 의 비율을 알 수 있게 한다 . 칼은 조작이 결정화유리 중의 각각 알
려진 상에 대해 실시된다. (2) 光學 및 電子顯微鏡 대부분의 결정화유리에서 홍미있는 구조적 득칭은 광학현미경의 分解能限界(li m it of resoluti on ) 以下인 경 우가 많다. 특히 완전히 발 달된 결정화유리의 미세구조 중에서 10nm 이하의 핵생성축전제 입자가 있는 경우에는 광학현미경을 사용하지 못한다. 따라서 보통 은 전자현미경이 결정화유리의 미세구조 연구에 더 유용하다. 그러 나 硏磨 및 腐仙面의 관찰에는 광학현미경을 사용할 수 있다. 결정화유리의 미제구조에 대한 조성변화의 영향을 조사하기 위한 광학현미 경 의 사용이 Harpe r 둥 10) 에 의 해 예 시 되 었 다. 기 본적 으로 는 Li2 0-Si0 2 %J 인 각종 조성 에 핵 생 성 촉진제 로 P205 를 소량 첨 가시켰다. 그립 4.6 에는 조성에 따라 租大한 小球體結晶으로부터 비교적 작은 결정을 함유한 미제구조까지가 나타나 있다. P2 아를 함유하면 바람직한 미립자로 된 미세구조가 성장하는 것을 알 수 있다. 광학현미경보다 더 큰 倍率이 요구되는 곳에는 走査電子顯微鏡 (SEM) 이 사용된다. 이것은 分解能이 약 20nm 라는 한계를 갖고 있 지만 결정화유리의 중요한 구조적 특칭을 대부분 밝힐 수 있다. 이 기숟은 시편준비가 비교적 간단하고 연마 및 약간 부식된 표면분만 아니타 파괴된 표면도 조사할 수 있다는 利点이 있다. 회석시킨 HF 중에서 약간 부식시키면 미세구조몰 더 자세히 관찰할 수 있다. 일 반적으로 주사전자현미경으로 결정화유리를 만족스럽게 관찰하려면 시편울 증발시킨 전기전도성팔름(예 ; Au-Pd) 으로 미리 피복시켜야 한다. 그렇지 않으면 시편이 帶電되어 像의 質울 나쁘게 하는 원인 이 된다. At k in s on 등 11) 은 결정화유리 의 미 세 구조를 조사하기 위해 陰極루미 네 센스 (ca t hodolum i nescence) 률 사용하였 다. 이 기 술은 전자 에 의해 충격을 받으면 일부 결정은 營光울 발생한다는 사실에 근 거를 두고 있다. 이 방법을 사용함으로써 미리 부식시키지 않고도 결정화유리의 미세현미경사전율 충분히 얻을 수 있었다.
10) H. Harpe r and P. W. McMi llan , Phys . Chem. Glasses, 13, 970972). 11) D. I. H. Atk i n s on and P. W. McMi llan , ]. Mate r . Sci. , 9, 6920974).
 L
L
분상이나 핵생성과정을 관찰하기 위해서는 높은 分 解 能울 갖는· 透過 電 子顯 微 鏡 (TEM) 이 유용하다. 이것을 사용하면 數 nm 크기의 구조도 구별할 수 있다. 얇은 시편과 정밀한 기술을 가지고 走査透 過 電 子顯微鏡 (STEM) 을 사용하면 더 높은 분해능을 얻을 수 있으 며, 數 A 크기의 구조목칭도 분해가능하다. 전자회철분석에 의한 각 결정의 同定 또는 X- 선에너지분산분석 (EDAX, energy dis p e r siv e analys i s of X-ra y)에 의 한 구조목칭 인 화학성 분의 起 源調査 도 가능 · 하게 되었다. 舊 式인 탄소 rep li c a 기술 대신 직접 TEM 을 사용하기 위해서는 매우 얇은 斷面 (100nm 정도)을 갖는 재료를 준비하여야 한다. 그러 나 간단히는미세한 분말로 된 재료를 준비하고 이것을 현미경내에 서 走査시 켜 전자광선이 두과하기 에 충분히 얇은 쐐 기 모양의 입 자 · 를 찾아낸다. 그러나 일반적으로는 제어된 조건하에서 결정화유리 의 얇은 箱울 준비하는 것이 더 유용하다. 吹迅法에 의해 준비된 유리필름을 열처리하여 결정화를 시키는 것은 수많은 불확실성을 · 가쳐오며 찰못된 설명을 할 가능성이 있다. 회석 HF 용액으로 부식 시켜 얻어지는 얇은 笛은 유리 중의 유리분상에 관한 연구에는 적 합하나, 결정상의 체적분율이 크면 결정상과 잔 유유리상 사이에 부 식속도의 차가 커쳐 시편이 깨진다. 가장 적합한 방법은 다이아몬 드돔과 같은 기계적 방법으로 먼처 얇은 단면을 준비하고 다음에 수십 µ의 두께로 la ppi n g시킨 후 최종 두께는 Ar 이온충격법을 사 용하여 조철한다. 최종방법은 비교적 느리지만 (1µ/hr 의 속도로 재 로 를 계거함), 바교적 큰 면적을 갖는 얇은 笛이 얻어질 수 있어 결정 화유리의 미세구조의 목성을 조사하는 데는 유용하다. 기계 적 방법 에 의해 얇은 細片을 만드는 방법에는 檢 鏡 用超 薄 片切 斷 器 (ul tr am i c ro t ome) 가 사용되나 아직은 널리 사용되고 있지 못하다. 결정화유리의 미제구조의 발달을 연구할 때 칙접 결정핵생성과 성장과정을 관찰하는 방법이 가장 좋으며 고온단계에서 전자현미경 울 사용할 수 있으나 이와 같은 방법으로 얻어전 정보는 기술적인 제약을 받는다. 왜냐하면 시편의 표면체적 비울이 매우 크기 때문 에 표면효과에 의해 결정핵생성과 성장은 여제되며 관찰된 과정은 7
全試料에서 일어나는 과정과는 다르기 때문이다. 이런 차이는 특히 현미경 중의 얇은 필름시편이 진공중에서 열처리될 때 핵생성과 성장의 동력학은 공기중에서와는 매우 다를 것이다. 이런 이유들 때문에 열처리공정의 각 단계에서 얻어전 시료를 급냉시킨 시편을 사용하는 것이 더 신뢰성이 있다. (3) 示差熱分析 결정질이나 유리질물질내에서의 화학반응 또는 구조변화는 열의 형태로 에너지의 방출 또는 吸收를 가쳐온다• 예를 들면, 물질이 결정화하면 규칙적인 결정격자의 자유에너지는 불규칙적인 액체상 태의 자유에너지보다 작기 때문에 발열효과를 일으킨다. 반대로 결 정이 용융되면 홉열효과를 일으킨다. 2 물질 사이의 화학반응도 홉 열 또는 발열효과를 일으킨다. 示差熱分析 (d iff eren ti al th ermal analy- s i s) 은 고온에서 물질의 반응이나 相轉移를 알수있는 수단이 된다‘ 이 방법은 미세한 분말로 한 시료를 P t나 다른 적당한 내연성금속 의 작은 셀 (cell 또는 ca p sule) 에 넣고 다른 셀에는 홉열이나 발열을 나타내 지 않는 a_AI2 아 를 넣 는다. 熱電對를 각각의 분말시 료 중에 집 어 넣 고 이 들의 em f(起電力)가 반대 로 되 도록 - 연결한다. 따라서 全 起 電 力은 시료분말과 알루미나분말 사이의 온도차를 나타낸다. 2 개의 셀이 함께 일정속도로 가열되면 횡축의 표준시료의 온도에 대해 종축에 시차온도가 그려진다. 발열효과는 얻어지는 곡선 위에 山形울, 홉열효과는 곡선의 아래에 谷를 만든다. 이 방법에서, 가열중 실두를 일으키는 유리는 적어도 하나의 발 열 p eak 가 나타나며 이것은 결정상의 분리에 해당된다. 따라서 시 차열분석은 유리의 결정화를 조사하고 다른 결정들이 형성되는 온 도를 결정하는 유용한 수단이 된다. 보통 유리의 결정화중 얻어지 논 DTA 곡선은 많은 특성을 나타내며 그 전형적인 곡선을 그림 4. 7 에 나타냈다. 온도가 상승하면 DTA 곡선에서 谷이 관찰되며, 이것은 유리가 서 냉접에 달하였을 때 일어나는 약간의 홉열에 의한 것이다. 온도가 · 더 높아지면 1 개 또는 더 많은 선명한 발열 peak 들이 관찰되며 이 둘은 각종 결정상이 생기기 때문이다. 더 높은 온도에서는 매우 큰
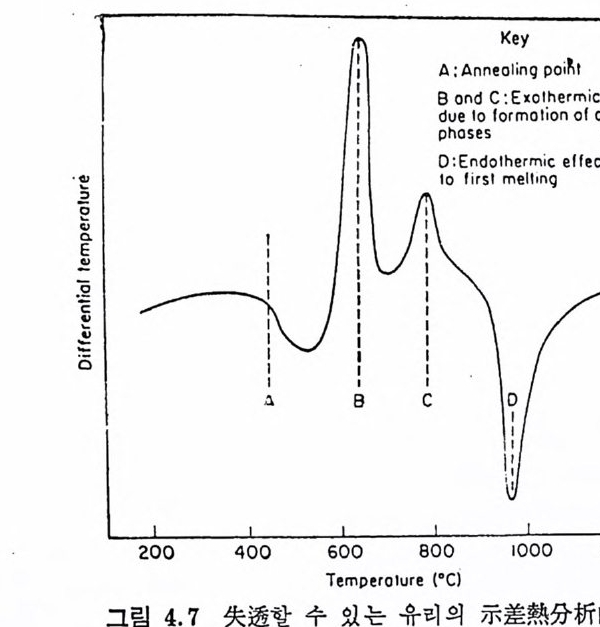 Key
Key
홍열효과가 나타나며, 이것은 결정상이 처음으로 용융되기 때문이 다. 따라서 DTA 곡선은 결정화유리에 대한 열처리 schedule 을 만 드는 데 매우 많은 유용한 정보를 제공한다. 죽 결정화가 일어나는 온도분만 아니라 결정상의 용융에 의한 변형을 일으키지 않고 결정 화유리가 가열될 수 있는 최대온도를 알 수 있다. DTA 곡선에서 발열 p eak 들은 각종 상의 결정화를 나타내며, 유리시편 을 이들 발 열 p eak 들에 해당하는 최대온도로 가열하고 X_ 선회철분석을 하면 어떤 결정상이 생기는가를 알 수 있다. S t ooke y둥 12) 은 목수형의 결정화유리에 대한 최적열처리를 얻기 위해 DTA 를 사용하였다. 이 재료들은높은 유전상수를 갖는 BaT i ` 아와 같은 强誘 電體 (fe rroelec tri c com p ound) 를 제조하기 위한 것이었 다. 이 들 재 료의 DTA 곡선은 500~700°C 에 서 제 1 홉열 pea k 를 나타내며 이것은 유리의 서냉범위에 해당된다. 서냉접보다 약 50~ 150°C 높은 온도에서는 初晶相으로 강유전체의 결정화에 해당되는 12) S. D. Sto o key and R. D. Maurer, Prog re ss in Cerami c Sc ien ce, Vol. 2, p. 77. Perga m on Press, New York(1 9 62) .
발열 p eak 가 나타났다. 다른 결정상의 분리도 조금 더 높은 온도 에 서 발열 pe ak 로 나타났다. 더 높은 온도(보통 1000~1300 ° C) 에 서 는 결정상의 첫 용융 때문에 홈열 p eak 가 관찰되었다. 강유전성결 정을 발달시키기 위한 최적열처리온도는 강유전성상에 의한 발열 pe ak 와 첫 용융에 의 한 홍열 pe ak 보다 약 50°C 아태 인 온도와의 중간 온도이다. Thakur 둥 1 3) 은 DTA 기 술을 이 용하여 핵 생 성 촉진제 의 효과에 관 - 한 정보를 얻었으며, 핵생성활성에너지 (En) 와 결정성장활성화에너 지 (E g)로부터의 기여에 의해 생긴 결정화의 복합활성화에너지 (E) 를 유도하였 다. 그들은 복합활성 화에 너 지를 DTA 의 발열 pe ak 의 온 도 (Tm) 와 관련지은 다음과 같은 식을 유도하였다.
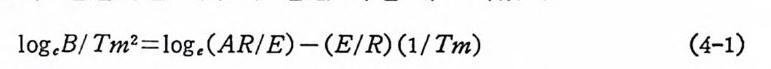 log ,B / Tm2 = 1 og , (AR/E) —(E lR) (1 / Tm) (4-1)
log ,B / Tm2 = 1 og , (AR/E) —(E lR) (1 / Tm) (4-1)
여기서 A 는 진동수인자(fr e q uenc y fa c t or) 이고 R 은 가스정수, B 는 ~ 가열속도이다. log B /Tm2 對 1/Tm 의 곡선을 그려 복합활성화에너 지를 유도할수 있냐 이 방법을사용하여 0~16x10-5mole Pt/ lO Og 유리 인 Pt 함유량울 함수로 Li2 0 •2 S i아 유리 에 대 한 복합활성 화에 너지의 변화를 측정하였다. 그 결과 가장 효과적인 핵생성(복합활성 화에너지가 가장 낮은)은 8X10-5mole P t /lOO g유리의 농도일 때라는 것을 알았다. 그들은 복합활성화에너지를 측정하기 위한 다른 방법도 제안하였 다. 표면핵생성이 우세한 유리에서 발열을 나타내는 결정화p eak 의 위치는 사용된 분말의 표면적에 크게 좌우된다. 미세한 분말에서는 발열 p eak 의 온도가 낮아졌다. 그러나 有勅容積核生成 (e ffici en t bulk . nuclea ti on) 이 일어 난다면 발열 pe ak 의 위치 에 대 한 입 자크기 의 영 향은 작아질 것이다. 표준의 미세 및 조대한 분말에 대한 발열 pe - ak 의 온도를 측정하면 유효용적핵생성을 판정할 수 있다. 그들은 p eak 의 온도차 4T 를 결정화를 위한 복합활성화에너지 E 와 관련: : 시켜 4T 가 커지면 E 도 증가한다는 것을 알았다.
13) R. L, Thakur and S. Thia g a raja n , Class and Cerami c Bui~ . , 13, 33, . Centr a l Glass and Cerami c Research Insti tut e , Calcutt a( l 96 6).
Br igg s 둥 M) 은 유리의 결정성장에 관한 동력학을 조사하기 위해 TITA 기 술을 발전시 켰 다. 연구된 유리 의 조성 은 CaO ― M g O 一 Al203 ― S i 02 형이며 DTA 의 결과를 고온에서의 현미경관찰과 비교하였 다. 그 결과 결정성장속도 V 는 다음의 식으로 나타낼 수 있었다.
![]() V=exp (s )exp (-q/ T) (4-2)
V=exp (s )exp (-q/ T) (4-2)
여기서 s 는 정수, q는 활성화에너지, T 는 철대온도이다. DTA 측정시 어떤 접에서 일어나는 온도차 4T 가 생성된 결정질 재료의 체적분율의 增加分 8a 와 비례한다고 가정하면 주어전 유리 에 대한 理論發 熱危울 유도할 수 있다. 이 값을 실험에서 얻은 발 열량과비교하면 가장 적합한 s 와 q값을 유도할 수 있으며 결정성 장속도도 槪算된다. 이 방법은 매우 편리하며 고온현미경관찰보다 도 시간이 철약된다. (4) 光散亂 광선이 유리와 같은 액체형 구조를 갖는 매개체에 들어가면 매개 체의 각 접에서의 굴철물이 다르기 때문에 入射光과는 다른 방향에 서 光散亂이 일어 난다. 산란중십은 밀도의 열적 변동(t hermal fluc tu a - ti on) 에 의 해 서 도 일어 나나, 산란중십은 광의 파장에 비 하면 작다. 그러나 입자들이 어느 정도 큰 직경을 갖는 매개체 중에 촌재한다 떤 산란광의 강도는 대우 증가할 것이다. 유리의 핵생성과 결정화 의 초기단계는 광산란이 일어나는 조건이 된다. 왜냐하면 대부분 의 유리와는 屈折率이 다른 작은 불연속적인 입자들이 석출하며 산 란광의 강도는 입자들의 수와 크기에 따라 변화될 것이다. 입사광 의 90° 방향에서 산란광의 강도를 측정하면 산란입자들의 촌재를 검출할 수 있으며 이것은 실험적으로 매우 간단하다. 여러 조건하 에서 열처리한 유리들을 비교실험함으로써 입자들의 농도도 알 수 있다. 정밀한 장치를 사용하면 산란입자의 크기 및 결정입자의 異方性 檢出과 같은 더 상세한·정보도 얻을 수 있다. 이런 특성을 실험하 키 위해 光散亂露出計(lig h t -sca tt er i ngp ho t ome t er) 가 Br ic e 둥 15) 에 의
14) J. Brig gs and T. G. Carruth e rs, Phys , Gli em . Glasses, 17, 30(1 9 76). 15) B. A. Bric e , M. Halwer and R. Sp ei s e r, J. Op t. Soc. Amer. , 40, 763(1950) .
해 사용되었다. 이 장치는 연마된 유리블럭시편(p ol i shed gla ss block s p e ci men) 이 비슷한 굴철울을 갖는 액체 중에 침지될 수 있는 특수 셀 (cell) 로 되 어 있 다. 적 당한 필터 를 사용하여 수은증기 램 프로부터 유도된 單 色光의 평행선을 시편에 照射하고 여러 角度에서 산탄광 의 강도를 光電增倍管(p ho t omul tipli er t ube) 을 사용하여 측정한다. 人 造偏光板(p olaro i d) 을 갖춘 분석기를 시편과 광전중배관 사이에 놓아 전기 벡 타 (vec t or) 가 수칙 또는 수평 이 되 도록 하여 復極 (de p olar i za ti on) 을 측정 할 수 있도록 한다. 이 실험 에 서 3 개 의 중요한 매 개 변수가 측정 된다. 죽 Ray le ig h 比, 非對稱 復極이다. Ray le ig h 比는 다음 식 에 의 해 주어 진다.
 Ru(9o) =l 규 /IoV (4-3)
Ru(9o) =l 규 /IoV (4-3)
여기서 I 는 입사광에 대해 90° 방향에서의 산란광의 강도이며, I 。 는 편광되 지 않은 입 사광의 강도, r 은 관찰하는 곳으로부터 산란체 까지의 거리, V 는 산란체의 체적이다. 非對稱은 45° 에서 산란된 광과 135° 에서 산란된 광의 强度比이 다 復極은. 90° 에서 산란된 수직 및 수평편광의 强度比이다. Maurer16) 는 중량%로 Si0 2 ; 49, M gO ; 10, Al203; 30, Ti 02 ; 9, Na20; 1.3, Asz 아; o.7 인 유리의 결정화에 대한 초기단계를 광산 란을 이용하여 연구하였다. 비교실험으로 다른 성분의 相對比는 같 고 T i아를 함유하지 않은 유리에 대해서도 같은 실험을 하였다. 연마한 불럭시편의 유리를 725~770°C 에서 열처리하고 실온까지의 냉각시간을 변화시켜 산란을 측정하였다. 이 실험에서 2 개의 중요 한 광산란의 매개변수는 굴철률의 공간변화에 의해 지배되는 산 란의 비대칭과 굴철률의 이방성을 나타내는 복광이다. 가장 낮은 열처리온도에서, 비대칭의 변화는 없고 단지 全散亂의 30% 만이 변화하며 복광은 6 배 증가하였다. 따라서 산란중십이 더 욱 이방성이 되는 동안에는 굴철율의 공간변화는 일정하게 유지된 다. 이 결과는 에 멀죤 (emuls i on) 과 같은 상이 결정화를 일으킨 것으
16) R. C. Maurer, J. Ap pl. Phys . , 33, 2132(1 9 62).
로 설명된다. 770°C 에서 더 장시간 열처리하면 확실한 X - 선 회절 모양이 얻어지며 형성된 결정상은 M g O•T i 02 이었다. Maurer 는 X - 선분석 으로부터 얻 어 전 결 정 의 체 적 농도와 Ray l- e ig h 比의 측정결과로부터 평군입자크기를 추산하였다. 결정성장 尸 과정 중 결정의 수가 일정하다고 가정하면 결정의 직경은 Ray le ig h 比의 1 /6 승에 비례한다. 실험에서는 최소입자는 직경이 2.5nm 이었 고 725°C 의 열처리에서는 평균입자크기가 7~9.4nm 로 커졌으며 770 ° C 의 열처리에서는 14.1~17. 5nm 로 커졌다. 비슷한 값이 X- 선 의 半値 幅 울 측정하여 얻어졌다. 열처리 전 유리 중에 에멀죤과 같은 상이 존재한다는 것은 광산 란의 측정에 의해 확인되었다. 죽 산란은 기초유리에서보다 Ti 02 를 함유한 유리가 3 배 더 컸다. 유리의 서냉은 산란에 큰 영향을 _ 미치지 못하며 산란에 해당하는 불군질성은 냉각의 초기단계에서 용융체의 2 상분리에 의한 것이라는 결론을 얻었다• T i아를 함유한 유리와 T i아를 함유하지 않은 기초유리의 거동 울 비교함으로써 분상과 결정화를 촉진하는 T i 02 의 중요성이 확인 되었다. T i 02 를 함유한 유리의 접도가 1.5x1012p o i se 에 대응하는 온도인 770°C(T i아를 함유하지 않은 기초유리에서는 812°C) 에서 25 시 간 열처리한 유리의 광산란은 105 배 변화하였으나 기초유리에서는 광산란의 변화가 검출되지 않았다. (5) 物理的 性質의 測定 유리구조가 다결정질세라믹으로 전환되면 물리적 성질이 현처하 게 변화된다는 것은 확실하다. 따라서 열처리기간중 또는 열처리 기간중 각 온도로부터 급냉시킨 시편에 대한 각종 성질을 측정하 기 위해서는 구조변화를 추적하기 위한 정밀하고 간편한 방법이 고 안되어야 한다. 비록 작지만, 열처리기간중 치수의 변화는 적당한 示差彬服計나· 다론 수단에 의 해 측정 할 수 있 다. McMi llan 등 17) 은 열처 리 공정 중 결정화유리의 섭유에 대한 길이의 변화를 관찰하였다. 그 건과- 17) P. W. McMi llan , B. P. Hodg so n and G. Partr i d g e, Glass Technol. , 7, 46(1 9 66).
결정 화 중에 약 1.67% 라는 상당한 길이의 수축이 생 겼 다. 또 전기적 성질을 측정하기 위해 구조적 변화를 검출하기 위~.l 매우 정밀한 방법이 사용되었고 X 겨 1 회철분석에 의해 결정상의 형 성을 검 출 할 수 있기 이전에 결정화가 시작된다는 것도 알 수 있었 다. 유리내에서는 전기전도를 담당하는 移 動性 陽 이온들(보 통 알칼리 금속이온 ) 은 결정상 중에 혼입되어 있어 유리가 결정화될 때 전기전 도도는 감소하며 誘電損 失 (d i elec t r ic loss t an g en t)도 감소하게 된다. 이것은 이온들이 운반되거나 진동운동을 하기 위해서 넘어야 할 에 너지장버이 규칙적인 결정격자에서보다는 불규칙적인 유리구조에서 더 작기 때문이다. 그림 4. 8 은 Li2 0-Si0 2 계 유리 를 450~600° C 에 서 열 처 리 한 시 편에 대 한 電氣 比抵抗울 측정한 결과이 다. 18) 이 결과는 550°c 에서 결정화가 일어 났다는 것을 나타내고 있으 나, 결정화는 유리를 600°C 에서 열처리할 때까지는 X- 선회절에 의
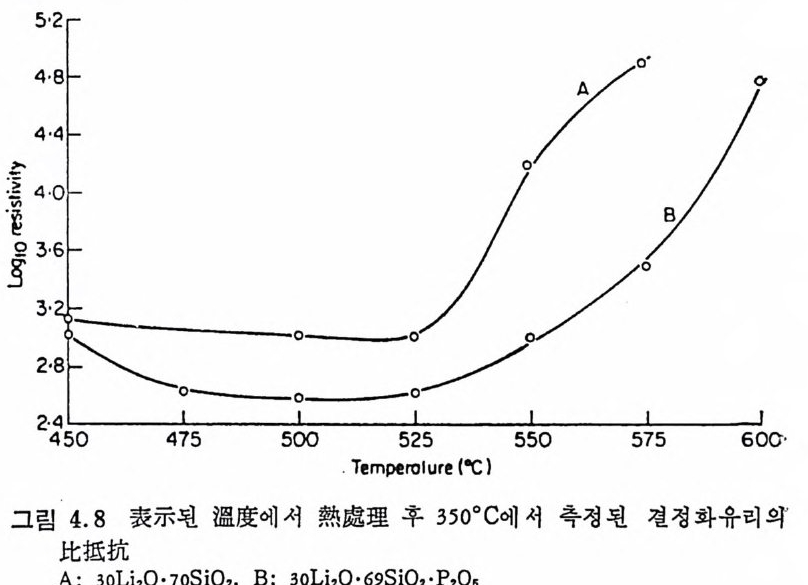 52
52
18) P. W. McMi llan , Advances in Nucleati cn and Crys t a l liz a ti on in Glasses-_ P. 224, Americ a n Cerami c Socie t y (l97 1 ).
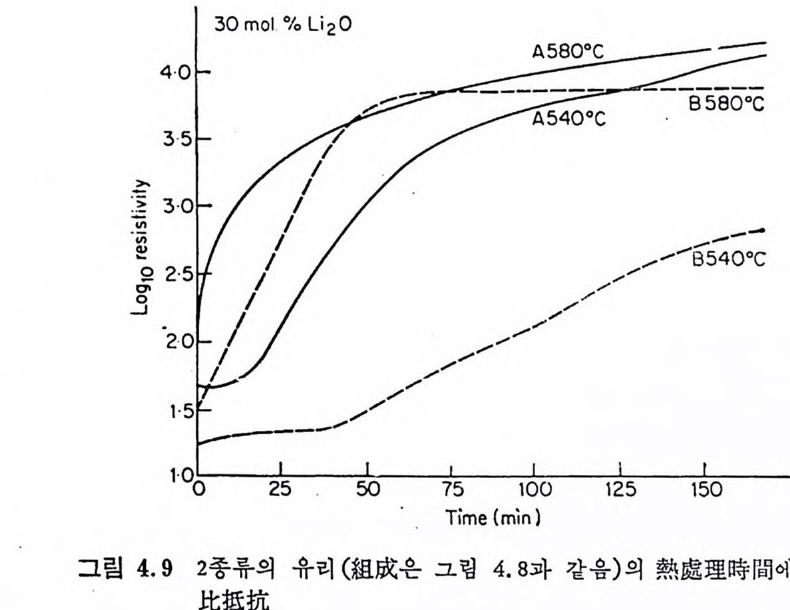 30mol % Li2 0
30mol % Li2 0
해 검출되지 않았다. 또 결정화는 P2 아를 함유한 유리에서 더 천 천히 일어나고 있다는 것을 나타내고 있으며 이것은 정량적인 X- 선회철분석에 의해서도 축정할 수 있으나 상당한 시간이 소도된다. 等溫熱處理에서 열처리시간에 따른 전기비처항의 변화를 측정한 결과를 그림 4.9 에 실었다 .19) . 2 종류의 유리에서 전기비처항은 시간에 따라 증가하나, 증가율은 점점 작아지며 툭히 540°C 의 낮은 열처리온도에서는 작으며 P20 , 를 함유한 유리논 결정화가 매우 느리다는 것을 나타내고 있다. Harpe r 둥 10) 은 Li 20 ― S i아 계 유리 의 유전손실을 측정 한 결과 - 600°C 이상에서 열처리한 시편들의 유전손실이 매우 감소한다는 사 실을 알았다(그립 4.10). 600°C 는 Li20 • 2 Si 02 결정 이 발달되 는 온도에 해 당한다. 등온조 건에서 유전손실을 측정한 결과, 결정질 L i 20•2S i 02 상 의 체적분율 Vf 는 시간 t후의 결정화유리의 유전손실 t an8 t를 결정상의 유전손
19) S. V. Phil lips and P. W. McMi llan , Glass Technol. , 7, 121(1 9 65).
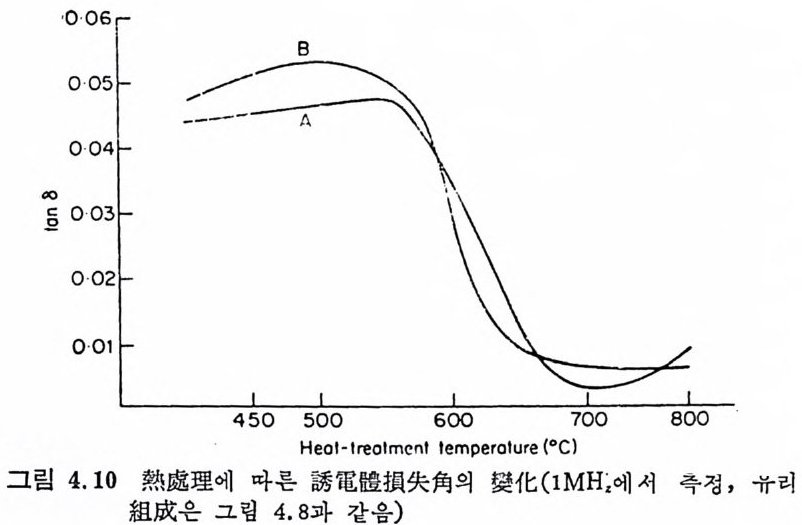 ·0· 0 6
·0· 0 6
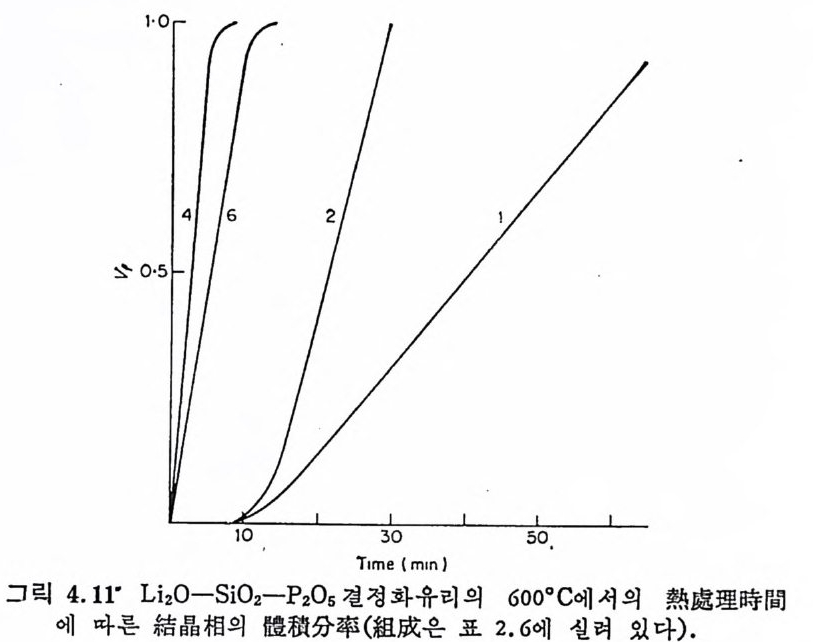 10 30 50.
10 30 50.
실 ta n 8cr 과 잔유유리 상의 유전손실 ta n og 의 加成函數 (add iti ve f unr ti on) 라고 가정 함으로써 推算된다. 그 식은 다음과 같다.
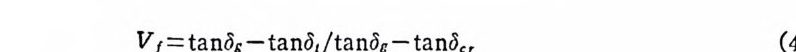 V, =t an oG-ta n o, /tan oc-ta n o,. (4-4)’
V, =t an oG-ta n o, /tan oc-ta n o,. (4-4)’
600°C 에서 등온처리한 4 개의 유리에 대한 Vr 의 결과를 그림 4_ 11 에 실었다. 2 개의 유리 (1 과 2) 는 결정화가 시작되기 전에 유도기간(i nduc ti on p er i od) 이 있으나, 다론 2 개의 유리는 600°C 에서 즉시 결정화가 시 작된다는 것은 매우 홍미있는 일이다. Vr 對 시간의 곡선이 직선인 것은 2 次元(平面) 또는 3 차원적인 결정성장이 각각 2 차 또는 3 차 종 속하기 때문에 섬유상성장을 한다는 것을 암시하고 있다. 유리 1 과 2 의 결정화속도는 다른 유리보다는 훨싼 느리다는 사실도 밝혀졌다. 이것은 1 과 2 의 유리논 2 상의 유리이고 나머지 유리들은 유리 중에 서 분상이 일어나지 않는다는 사실과 관련지을 수 있다. 유리의 결정화를 연구하기 위해 전기측정을 한 홍미있는 방법이 Baak20) 에 의해 발견되었다. ::::z..는 결정화될 수 있는 유리시편을 전 체가 결정화상태에 있는 같은 조성의 시편과 접촉시켜 열처리하면 결정화과정에 따라 2 시편 사이에 起電力 (em f)이 발생한다는 것을 알았다. 그는 그림 4.12 에서와 같이, 측정된 기전력과 결정질의 함-
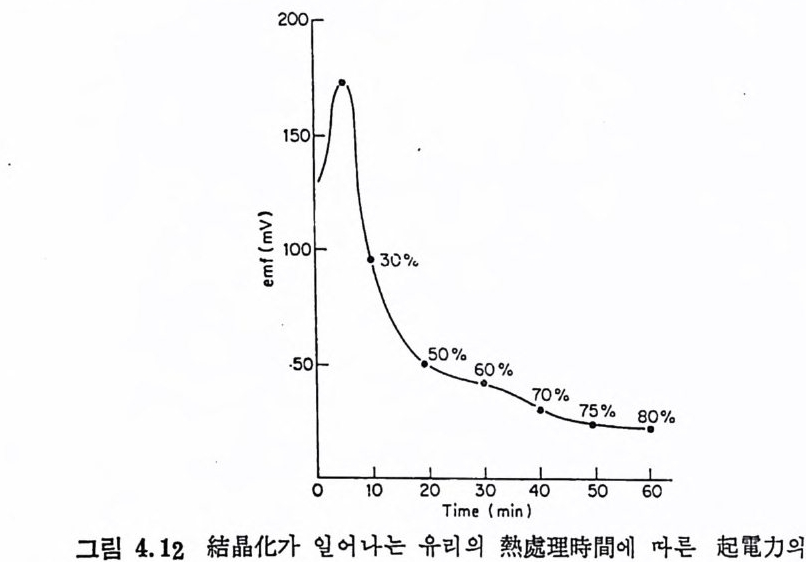 200
200
20) T. Baak, U. S. Pate n t No. 3295944(1 9 67).
량%를 상호관련지울 수 있었다. 따라서 이 방법은 결정화과정의 경과를 추적하는 데 유용하다. 그러나 이 방법은 결정절함유량의 체적분울이 작은 곳 (50 또는 60% 이하)에서는 더 민감하다. 그는 이 효과의 원인은 유리시편으로부터 결정화유리로 산소이온들이 이동 하기 때문이라고 생각하였다. 결정화에 따른 접도의 변화도 구조변화를 판단하는 수단이 된다. Lay ton 등 2 1) 은 Na20 ― Nb203 ― S i아 유리 들의 결정 화를 조사하기 위 해 접도축정울 하였다. 유리의 접도는 처음에는 감소하나, 유리조성 에 따라서는 어떤 온도 이상에서는 결정화 때문에 증가하게 된다. 그림 4.1 3 중의 곡선 1 과 2 가 이 효과를 예시하고 있다. 그들은 Na Nb03 결정 의 석 출에 따른 찬유유리 중의 S i아 함량의 증가는 접 도 를 높이는 데 크게 기여한다고 제안하였다. 또 접도는 분산된 결정 질입자에 의해서는 영향을 벌로 받지 않으나, 결정의 체적분율이 어 느 이상이 되면 이 가설도 벌로 믿을 수 없게 된다는 것을 지적하 였다. 그들은 매우 높은 온도까지도 결정화되지 않는 고실리카유리
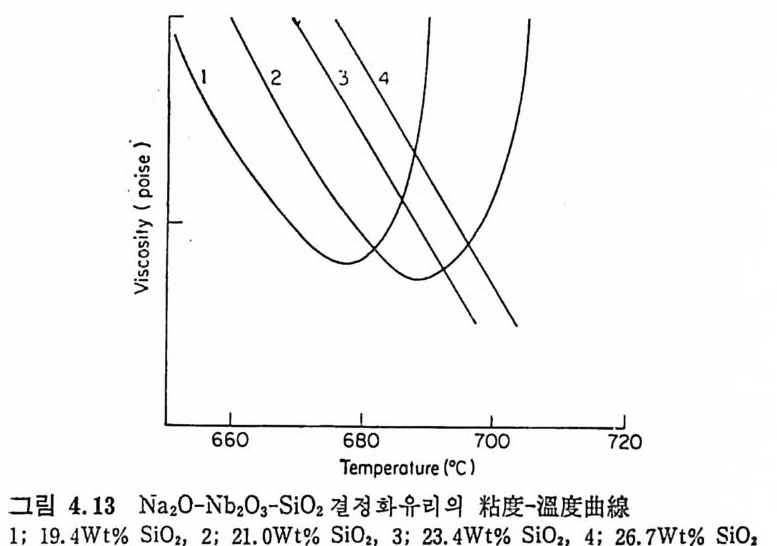 as1od
as1od
21 ) M. M. Lay t on and A. Herczog , I. Am. Ceram. Soc. , 50, 369(1 9 67).
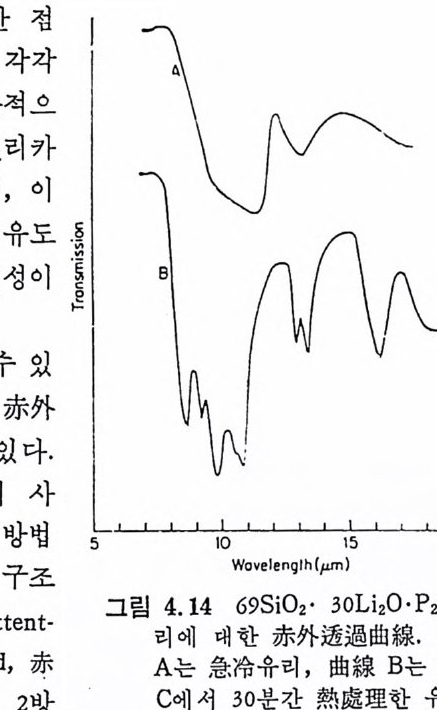 .§
.§
(그림 중의 곡선 3 과 4) 에 대한 점 도-온도곡선을 그림 으로써 각각 의 온도에서 가열하여 부분적으 로 결정화된 유리 중의 실리카 함량을 계산할 수 있었으며, 이 들 값과 밀도축정으로부터 유도 된 값 사이에는 상당한 일치성이 있었다. 유리의 결정화를 조사할 수 있 는 다른 물리적 방법으로는 赤外 分光(i n fr ared s p ec tr osco py)이 있 다 . 얇은 필름의 흡수스펙트럼이 사 용될 수 있으나 더 편리한 방법 은 全試片의 얇은 표면충의 구조 를 조사할 수 있는 ATR(At ten t· uate d Tota l Refl ec ta n ce meth o d, 赤 外反射스펙 트럼 의 일종)法이 다. 2 방
법들로부터 얻을 수 있는 내용들을 그림 4.14 와 4.15 에 실었다. 그림 4 .1 4 로부터 결정화에 의해 吸收 帶 가 날카로와졌을 분만 아 니라 새로운 帶도 나타났다. I6µm 에서의 흡수대의 강도는 550°c 에서의 열처리시간과 상호관련지워지기 때문에 결정화과정을 측정 할수있다. 같은 유리조성에 대한 ATR 스펙트럼으로부터 결정화된 유리(곡 선 . B) 를 연마하지 않은 시편에서는 기본적으로 급냉유리와 다른 득 성을 나타내나, 연마한 시편에서는 결정질의 특성이 없어져 결정화 되지 않은 유리 A 의 스펙트럼과 매우 비슷한 결과를 얻었다. 이것 은 표면결정화가 열처리조건하에서 일어났다는 것을 확실히 말해 주고있다. 4.2.3 결정화유리가 形成되는 條件파 結晶型 결정화유리를 제조하는 데 중요한 일부 산화물계에 대한 相平衡
~\ \ 그이림들이 상 출평판형되그어림 은왔 지임만반 안22)내23} · 는서에 비 율불을과 하정며확 하결게정 화추유궁리하 중에 촌재할 상들의 특성 또 기 위해서는 사용할 수 없다. e도접L \\ \ 리에가예 를카의나 영 하타들역면면날에 , 主 서것相어는으으떤 로로 상 t계기평 r의대 i d형되 y그 고m나립 i실,te 士s 결정질유리에서 결정질실리 카의 이런 형을 얻는다는 것 온 매 우 어 려 우며 cris t o b ali te 나 q ua rt z( 석 영 )가 주로 생 긴 5 10 15 20 다. 일반상평형그림은 결정 Wove l e 여 lh( p m) 화유리 공정에서는 이용될 그림 4.15 69S i 02·30LhO·P20s 유리에 수 없는 온도와 시간의 조건 대한 ATR 曲線 A 曲 線 은 急冷유리 하에서 측정한 것이므로 특 曲 線 B 는 550°c 에 서 30 분간 熱處 理한 유리, 曲線 C 는 B 에서와 갈 정 결정화유리조성 중에 촌- 이 熱處理한 후 粉粹, 硏磨한유리 재할 상들에 대한 정확한 지 ’ 침서로는 사용할 수 없다. 결정화를 위해 사용되는 열처리 schedule 이 다르면 같은 화학조성의· 재료에서도 존재하는 결정상이 다르기 때문에 특정 결정화유리계에 대한 포괄적인 상평형그림을 만들기 는 극히 어렵다. 최대결정화온도까지 도달하기 이전에 유리가 낮은 온도에서 경 과한 시간이 최후에 발달된 결정상의 성질에 큰 영향을 미칠 수 있 다. 또 조성의 미세한 변화가 결정화유리 중에 촌재하는 결정상에
22) E. M. Levin , H. F, McMurdie and F. P. Hall, Phase Di ag ra ms fo r Ceram- ist s , Americ a n Cerami c Soc iet y (l95 6). 23C) eEr.a Mmi. stL s ,e vAin m, eCr.i cR a .n RCoebrbaimn s i ca Snodc Hie .t Fy .( l9M6 4c)M. urdie , Ph• ase Di ag r a ms fo r
비례적인 효과를 나타내지 않을 때도 있다. 그러나 다른 결정상이 형성되는 조건을 포함한 유용한지침이 되는 원리도 일 부얻어 졌 다. 이와 같은 중요한 결정화유리계를 以下에 설명하겠다. L i 2 0 ― S i 02 계는 여러 중요한 결정화유리의 標準物質( p ro t o typ e) 이 다. 앞에서도 설명한 것처럼 X - 선회철측정에서는 비록 600°C 나 그 이상의 온도에서 결정화가 일어나는 것으로나타나지만, 이런 유 리의 전기비처항을 측정하면 550 ° c 부근에서 결정화가 시 작 된다는 것을 알 수 있다. H i n g둥 3) 은 選擇面電子回折 (selec t ed area electr on dif frac ti on , SEO) 과 高 分解能 電 子顯 微鏡 울 결합시켜 연구한 결과, 500°C 에서 열처 리한 후의 2 성분계 30L i 20·70S i아유리 중에서는 결정화가 나타나 지 않고 유리 중에 분상이 일어 난다는 것 을 알았다. 1mole% 의 Si 02 대신 P2 아를 치환하면 480°C 에서 결정화가 생겼다. 520°C 에서 1 시간 열처리를 하면 이 유리는 5~20nm 의 결정질을 함유하고, s . ED 에 의해 이 결정질은 L i 20·2S i아임이 확인되었다. 이 단계에서 는 X- 선회철에 의해서는 결정질을 겁출할 수 없다• 유리 중에 1 mole% 의 ZnO 를 첨가하면 유리 중에 租大하고 광범위한 분상이 일어나고 550°C 로 열처리하면 군열이 생겼다. 찬유유리상의 점도 를 낮추기 위해 1mole% 의 K20 를 더 첨가하면 군열의 발생을 괴할 수 있었다. 최종적으로 . 얻어전 물질은 미세결정형인 Li 20•2S i 02 를 함유하였다. 이 연구는 핵생성촉진제의 효과와 함께 결정화과정에 미치는 微成分의 영향을 나타내고 있다. Li 20 를 25~35mole% 함유한 L i 20 一 S i아 유리 의 결 정 화에 대 한 핵 생성촉진제의 영향이 연구되어 왔다. 사용된 핵생성촉진제는 p~ 05, T i아 및 금속 P t이다. 핵생성촉진제가 함유되지 않는 경우, 리튬규산염이 557~569°C 에서 열처리한 유리에서 검출된다• 2 차결 정상인 석영은 615~690·C 에서 발달된다. T i 02 의 첨가는 석영이 발달되는 온도에는 아무 영향도 주지 않으며, P2 야를 함께 넣으면 이 온도는 585~595°C 로 내려가며 P t도 온도를 내리나 효과는 크 치 않다. P20s 와 P t는 석영의 결정화를 촉진하나, T i 02 는 이 효 과가 없다. P20s 가 핵생성을 촉진하는 능력이 크다는 것은 P2 야를
함유한 조성의 결정화유리는 미제결정을 갖고 고강도이나, T i아를 함유하거나 핵생성촉진제를 함유하지 않는 조성의 결정화유리는 조대한 결정을 가지며 약하다는 사실로부터 알 수 있다. P t를 함유 한 결정화유리도 마제결정을 갖지만 P2 야의 것보다 강도가 작다. MacDowell 등 24) 에 의 해 Al 요 -S i아 계 결 정 화유리 가 연구되 었 다. 이 유리 중의 Al2 아함유량은 5~60mole% 이고 열처리온도는 900~1600°C 이 다. Alz 아 함량이 많아지 면 유리 는 안정 성 이 작아지 며 30mole% 이 상 의 함량에서는 유리질의 물질을 만들려면 급냉시켜야 된다. Alz03 조성이 60mole% 인 것을 제의한 모든 유리는 냉각시 준안정인 불혼 화를 나타내며 다음의 열처리중 2 상의 구조가 조대화된다. 어떤 경우에는 Al2 아가 r ic h 한 상은 냉각시 mu llit e 로 결정화된다. Na2 0, CaO 또는 BaO 와 같은 수식 산화물을 소량 첨 가하면 냉 각시 2 성 분리가 억제되며 Al; 아를 50mole% 까지 함유하는 용융체는 급냉시 키 면 군질한 유리 가 될 수 있 다. 망목형 성 양이 온(예 ; B3+, Ti 4+ , Ge4+) 울 함유하면 분상의 경향이 커지고 Al203 를 2omole% 보다 적게 함 유한 조성에서는 실두경향이 커졌다. Alz 야를 20% 보다 적게 함유 한 조성의 유리를 열처리하면 初晶으로 미세하게 분리된 mu llit e 가 발달된다. 예를 들면 Al203 를 15mole% 함유한 유리를 950°C 에서 10 시간 열처리하면 물질은 유리질로 두명하지만 mu llit e 의 X- 선희 철모양이 발달된다. 열팽창계수는 결정화되지 않은 유리에서는 13.4 x10-1rc 이나 1150°C 에서 연처리한 물질에서는 18.9x10-71°C 로 증가하며, 밀도가 커지는 것은 열처리온도가 높아침에 따라 mull ite 상의 양아 접차 중가하기 때문이다. 열처리온도가 1200°c 로 높아 치면 열팽창계수는 139.3X10-7 으로 매우 커지며 이것은 主相인 mull ite 에 cris t o b ali te 가 석 출되 기 때 문이 다. 이 온도에 서 열 처 리 한 후에도 결정화유리는 미세구조로 인해 透明性을 유지한다. 1500° C 로 열처 리 하면 主相으로 소구체 인 cri sto bali te 가 존재 하게 되 어 . 260X10-7 로 높은 열팽창계수를 갖게 된다. 이 결정화유리는 여전 히 미립자로 된 미제구조를 갖고 있으나 白色이며 不透明하다.
24) J. F. MacDowell and G. H. Beall, ]. Am. Ceram. Soc. , 52, 17(1969).
유리의 결정화거동은 다른 산화물을 첨가한 3 성분계에서도 연구 되 었 다. 예 를 들면 Al203 를 30mole% 함유한 유리 에 BaO 를 5mole % 첨가하면 950°c 열처리 후 mull it e 의 완전한 결정화가 나타나고 1200°c 이상의 열처리온도에서는 cr i s t obal it e 의 형성 이 억제된다. 다론 알칼리토류와 알칼리금속산화물을 소량 첨가하여도 비슷한 효 과가 나타났다. 이와 같은 연구는 유리의 결정화에 미치는 2 상분리 의 영향 및 소량의 산화물첨가가 가쳐오는 결정화거동의 현처한 도 변화를 조사하는 데 도움이 된다. L i 20-Al203-S i아 계 는 고알루미 나 영 역 에 서 는 열 팽 창계 수가 작 온 결정화유리를 만들 수 있기 때문에 중요하다. 또한 비교적 적은 Al 요함량의 조성에서는 감광성핵생성인 결정화유리의 기초가 된 다. E pp ler2” 는 이 계로부터 유리의 결정화에 내한 유용한 지석을 얻었다. 즉, Li20 20Wt % 이상을 함유한 유리만이 600°C 에서 열처 리할 때 결정화된다는 것을 알았다. S i아가 약 75% 이상일 때는 L i 20,2S i아가 형성되나 S i아함유량이 적을 때는 主相온 Li2 0 •Si0 2 이었다. S i아를 70~75% 보다 적게 함유한 조성에서는 /3-eu cryp tite- /q ua rt z 의 고용체도 생성된다• 700°C 이상의 열처리에서는 모든 조 ~ 성의 실제적인 主相인 L i 20•S i 02 가 생겼다. 이들 온도에서 고실리 카, 저 알루미 나조성 을 제 의 한 대 부분의 조성 에 서 /3_ sp o dumene/ q ua rt z 의 고용체도 나타났다• 이 고용체는 유리로부터 직접 결정화 에 의 한 것 이 라기 보다 /3- eucryp tite/ qu artz 의 재 결 정 화에 의 해 형 성된핵 생것 성이 촉라진고제 생로각 P된2 다야. 를 함유한 Li20 — Al2 0a-Si0 2 형 유리 에 서 , Al2 아를 약 10% 보다 적게 함유한 조성에서는 主相으로 Li20 •SiO z- 가 나타나고 Si0 2 7} 70~75% 이상 함유된 유리에서는 Li20 •2Si0 2 가, Si 아함량이 적은 유리에서는 L i 20,S i 02 가 나타난다. Si0 2 71-- r i ch 한 조성에서는 2 차 결정상으로 S i 02 의 각종 결정들이 종종 나 타나며 이 결정상은 미세한 성분, 특히 알칼리금속산화물의 촌재오1- 열처 리 조건에 따라 석 영 , cris t o b alite 또는 2 혼합물이 나타난다. 예를 들면 K20 가 1~2% 만 촌재하여도 석영의 생성에 큰 영향을
25) R. A. Epp le r, J. Am. Ceram. Soc. , 46, 97(1 9 63).
미치며 더 많은 양의 알칼리금속산화물은 더 큰 영향을 미찬다는 것이 확인되었다. 실제 사용되는 결정화유리에서는 cr i s t oba lit e 의 생성을 피하는 것이 좋다. 그 이유는 200°c 의 영역에서 a-/3 eris - t oba lit e 의 轉換(i nvers i on) 은 균열을 가져오는 큰 체적변화를 일으 키기 때문이다. S i 02 의 결정형들과 비슷한 구조를 갖는 알루미노규산영 결정들의 생성을 지배하는 기본원리가 Buer g er26) 에 의해 처음으로- 계통적으로 _ 연구되었다. 기본이 되는 것은 결정격자 중의 S i 04 그룹이 Al04 사 면체로 치환되고 전체의 전기적 중성을 유지하기 위해 1 가 또는 2 가양이 온이 틈새 자리 (int e r stit ial s it e) 에 收容된다는 것 이 다. Si0 2 의 결 정 질 변 태 인 석 영 , cris t o b alite , tri d y m i te 및 keati te (sil ica -K) 는 알루미 노규산염 을 同墓 갖는다. 이 들은 각각 crist o balite 와 tri d y m ite 의 구조를 갖는 carneg iei t e [ Na(A1S i 04)] 와 nep h elin e [KNa3(Al Si0 4 ) 4] 을 함유한다. /3- spo dumene 은 keati te 구 조를 가지 며 /3-eu c- r yptit e[L i (A1S i 04)] 는 (3-qu artz 의 誘導體이 다. /3- eucryp tite 의 겅 우, 틈새양이온은 Li이고 S i 04 그룹의 半온 Al04 그룹에 의해 치환 된다. 이 결정은 S i 04 와 全系列의 고용체를 형성할 수 있으며 /3- qu artz 와 類似構造이 다. g-석 영 고용체 도 M g 2+ 가 름새 자리 를 차지 하는 Mg O -Al20a-Si0 2 계로부터 형성될 수 있으며 한정된 양의 Zn2+ 도 듬새자리 (팔면체)와 · 사면체자리의 구조에 참여할 수 있다. 그러나 보통 Al203 가 부족 한 조성 에 서 는 Zn” 는 사면체 배 위만 한다고 생 각된다. Be2+ 도 Al2 03 가 부족하면 이 구조위치에 참여할 수 있다. 반대로 Al2 아가 과 · 잉으로 촌재하면 Al3+ 의 일부가 팔면체자리에 들어갈 수 있다. /3-석 영고용체는 고온에서 불안정하여 準固相 (sub-so li dus) 의 온도 에서 충분히 가열하면 파손되어 다른 상으로 된다. 생성물들에는 각종 sp ine !, sa pp h i r i ne( 碧石英), cris t o b ali te, mull ite, wi llem i te [Zn2(Si0 4 )], L i 20•S i 02 가 있다. 이들 생성물의 성질은 /3-석영조성 으로부터 제조된 결정화유리의 성질을 결정하는 데 중요하다. 중요 한 2 성질은 다음과 같다.
26) M. J. Buerge r, Am. Mi n eralog ist, 39, 600(1 9 54).
a) L i 20 를 2. sW t%보다 적게 함유한 Mg O -ZnO— Alz0 3— Si0 2 계의 경우, 파괴되어 생기는 생성물은 spi nel 과 규산질 8- 석영을 함유한다. 냉 각하면 8- 석 영 은 a- 석 영 으로 전환된다. 따라서 이 형 의 b결) 정Li화20 유를리 논2. sW열t팽 %창 보계다수 가많 이크 다함. 유한 Li2 0-Mg O — ZnO -Al203 S i아 계 의 조성 에 서 는 (3-석 영 형 결 정 이 주로 /3- spo duin e ne 으로 전 환되어 이 결정화유리논 열팽창계수가 작다. Doher ty둥 27) 은 W t%로 Si0 2 ; 69. 5, Al 요 ; 17:B, Mg O ; 2. s, Li2 0 ; 2. 5, Ti 02 ; 4. 75, Zr02; o. 25, ZnO; 1. o, Na20; o. 4, As2 03; 1.0 인 유리의 결정화에 관한 연구를 하였다. X- 선회철을 사용 한 결과 약 850°C 에서 처음 검출되는 결정상은 ,8 -eucr yptit e 이었 다. 975°C 이상으로 온도를 올리면 이 相의 바울은 급히 감소되고 온도를 1100° c 까지 올릴 경 우 /3- spo dumene 량이 증가하였 다. 농도가 1~2Vol. %이고 크기가 약 5nm 인 수많은 입자들이 825°C 근처 에 서 석 출되 는 것 이 透過電子顯微鏡에 나타났다 (죽, /3- eucry- ptit e 의 생성이 겁출되기 직전). 전자현미경을 통해 열처리온도를 1100°c 까지 접차 높일 때 미세구조의 변화를 관찰할 수 있었다 . .s 75°C 에 서 처 음으로 생 성 된 ,8- eucryp tite 의 크기 는 50~80nm 이 고 · 950°C 에서는 100nm 까지 커졌다. 1050°c 로 가열하면(/3 -eucr yptit e 一/3 -s p odumene 의 전이온도보다 높은 온도) 결정화유리의 90% 체적 분율에 평군크기가 600nm 인 결정이 석출되었다. 1100°c 까지 가열 하면 약간의 微相이 들어 있으나 크기가 lµm 로 큰 /3- spo dumene 결정으로 된 거의가 결정질인 물질이 얻어졌다. 이들 중에는 Ti0 2 가 2~3Vol% 촌재하는 것도 있다. {3- eucryp tite 生 成以前의 작은 입 자들을 조십 스럽 게 분석 하면 pyro chlore[ (Ca, Na)2 (Nb, Ta) 2 아 (O, OH, F) ]와 유사한 구조를 나 타냈고 아마도 Al2T i 2 아 (alum i n i um titan iu m py rochlore) 을 함유하고 있다고 생각된다. 미세하게 분산된 이 相이 {3 -eucr yptit e 의 결정화 에 불군질핵생성촉진제로 작용하는 것 같다.
27) P. E. Doherty , D. W. Lee and. R. S. Davis , J. Am. Ceram. Soc. , 50, 77(1 9 67).
L i 2 0 ― A l203 ― S i 02 형 결정화유리에 대한 유용한 다른 연구로는 W t%로 Li20 ; 17. 5~19. 5, Al20 어 13. 4~15. o, Si0 2 ; 55. 9~65. 7, Ti 02 ; o~11 인 유리 의 결정화에 관한 Barr y 28) 둥의 보고가 있다. DTA 에서, 유리전이온도 (T g)보다 100~200°c 높은 온도에서 큰 발열 pe ak 가 나타났다. 이 것 은 /3-e ucryp tite 와 Li20 •Si0 2 가 동시 에 결정화하기 때문이다. X- 선회철분석에서는 /3 -eucr yptit e 가 600~ 670°C 에서, Li 20•S i O 과 650~680°C 에 }1 성장됨을 나타냈다. Ti 02 를 함유한 유리에서는 L i 20,T i 02 도 성장된다. T i 02 가 최대농도 인 조성에서는 더 높은 온도가 필요하나 이 티탄산영의 성장을 위 해서는 700°C 의 열처리가 필요하다. 따라서 600°C 의 열처리도 이 티탄M산g O염 — 의A l2성 0장3-원Si인0 2이 형 의충 분결히정 화된다유.리 는 높은 기 계 적 강도와 중간 및 낮은 열팽창계수를 가지면서 전기철연목성을 겸비하고 있기 때 문에 중요하다. 이런 성질들은 이 형의 결정화유리 중에 基本相으 로 a- co rdie r i te( 2 Mg 0 •2 Al203•5 S i 02) 가 존재하기 때문이 다. 이 결 정은 유리를 형성하는 모든 조성들을 열처리하떤 나타난다. 촌재할 수 있 는 다른 상들로는, 고실리 카조성 에 서 crist o b ali te, 높은 Mg O 함량의 조성 에 서 cli no -ensta t i te ( Mg O •S i0 2 ) 또는 for ste r i te ( 2 Mg O • S i 0L 2i )2 가0 — 있Zn다O. — Si0 2 i-1] 중 일부 조성 범 위 에 서 는 지금까지 알려 처 있 지 않은 결정형아 성장했다. ZnO 함량이 약 20~35% 인 결정화유리 에서는 Li 20·ZnO·S i 02 의 상이, ZnO 함량이 약 30% 이상안 결정화 ~ 유리에서는 4 Li 20·1oZnO•7S i 02 가 성장했다. ZnO 45% 이상인 조성 에서는 wi llem i te (2 ZnO•S i 02) 가 때때로 생성된다. ZnO 가 약 10 % 미 만인 조성 에 서 는 기 본상으로 석 영 또는 cri sto b ali te 와 함께 L i 20•2S i 02 가 나타난다. 이 형의 조성을 열분석하면, 500~570°C 에서 L i 20•2S i 02 가 결정화하며, 이 유리 중에 P2 야를 첨가하여도 이 온도는 크게 변하지 않는다. P20s 가 없는 조성 에 서 Si0 2 는 720 ~740°C 에서 결정화하나 P20s 가 존재하면 670~700°C 에서 결정화 ’
28) T. I. Barry, C. Clin t o n , L. A. Lay , R. A. Mercer and R. P. Mi ller , J. Mate r . Sci . , 4, 596(1 9 69).
한다. P 요를 함유한 결정화유리는미세진정질이며 강 하나, P2 아믈 함유하지 않은 것은 매우 약하고 조대한 미세구조 를 갖는다. 따라 서 Li 20-ZnO-S i아 계 에 서 는 P2 야 는 유효한 핵 생 성 촉진제 가 된 다. Morell29) 에 의 하면 Li20 • 2S i아 가 석 출한 후 이 들 결 정 주위 의 유리는 Zn2+ 이 r i ch 해쳐 初晶과 유리결정의 面間相에 Zn2+ 울 함유 한 2 次相의 핵생성과 성장이 일어나는 조건이 생간다고 설명하고 있 다. 2 차상은 fi-Li20 • ZnO•Si0 2 이 며 이 침 전물은 Li20 를 접 차 고 갈시켜 ZnO•S i 02 와 S i 02 결정이 결정화되도록 한다. Burne tt둥 30) 은 찰 알려져 있지 않은 결정화유리계에 대한 연구 를 통해 유리의 결정화가 일어나는 복잡성을 상세히 설명하고 있다. 그들은 Na20 ― BaO ― S i아 계 의 유리 를 조사한 결과 처 음으로 검 출 되는 결정상은 나중에 안정한 低溫形으로 전이되는 고온형 Ba0•2 S i 02 이었다. 죽 처음에는 준안전상이 생성되고 다음에 안정상으로 전이된다. 또 고실리카유리에서 액체를 혼합하지 않으면 S i 02 가 r i ch 한 小摘이 생기며, 이 현상온 미제구조인 결정화유리를 성장시 킬 때 종종 볼수있다. Ba0,2S i 02 와 Na20,2S i아를 연결하는 선상에 있는 조성의 유리 를 열처리하면 Ba0,2S i 02 가 결정화되고 최종적으로 잔유유리상의 조성은 순수한 Na20•2 S i O 과 된다. 이 유리논 水中에서 용해된다. 일부 조성에서는 Ba0•2S i아침전이 찬유유리상의 조성을 不混和領 域으로 이 동시 켜 Si 02 가 ric h 한 小深은 再溶解되 어 유리 조성 은 고 실리카인 성분이 된다. 완전히 결정질인 결정화유리를 생성하기 위 · 해서는 1 차 결정질상이 결정화된 후 남은 찬유유리가 계의 유리형 성영역의 밖에 놓여쳐야 한다. Na20-Ba0 ― S i 02 계에서 이런 조 성은 60S i 02•30BaO•10Na20 이다. Ba0•2S i 02 의 침전 후 찬유유 리상의 결정화는 대부분이 결정질로 되지만 불행히도 공기 중의 순 . 기에 쉽게 침식되는 Na20•S i 02 결정이 생간다. 母유리의 조성에 따라 각종 결정형이 결정화유리 중에 성장된다. T i 02 를 핵생성제로 하는 알루미노-규산영의 조성에서 생성가능한
29) R. Moel! , •Ph. D. Thesis , • Univ e rsit y of Bris t o l (l 970 ). 30) C. G. Burnett and R. W. Doug la s, Phys . Chem. Glasses 12, 117(1971 ).
표 4.4 알루미노-규산영 의 걷 정 화 유리에서 生成되는 結 晶相 둘 Glass-cerami c type Crys t a l ph ases Ca 0 -A[z 0 3-Si0 2 -TiO z Anorth it e, CaO·Ah 야 ·2 Si0 2 Cris t o b ali te, Si0 2 Sp h ene, CaO •T i 02 • Si0 2 Trid y m i te, Si0 2 一BZna0전0 -_A Alb20 야안3 --SS ii 00 2 2 - --TTT iii 000 222 1II DG iab ha nriit ue m , Ztrni s0 i ·l Aic a] zt0e 3, 2 Ba0•3 Si0 2 Wille mi te, 2 ZnO·Si0 2 Cris t o b ali te, Si0 2 -- - ~- _.,. -- -· · - -···- -- - - Lead titan ate , PbOTi Oz Mn0-Alz03-Si0 2 -T i0 2 Py ro p h anit e, MnO • Ti 02 Cris t o b ali te, Si0 2 MMua2 nll Mgi taen n, 0e s•3e2 AcAhoizr 야d0 i3 e • • 2r Si t S eS,i i0 0 2 2 I Trid y m i te, Si0 2 Qu artz , Si0 2 결정상들율 표 4.4 에 실었다. 각 결정화유리형에 대해 인용된 결정상들은 주어진 조성에서 모 두 촌재할 필요는 없으나 2 개 또는 그 이상의 결정상들이 생성될 경 우가 많다. 이 들 상과 함께 Ti0 2 결정형 인 ruti le 이 나 anata s e 도 결정화유리 중에 존재할 수 있다. 4.3 特殊결정화유리의 工程 4.3.1 感光性 결정화유리와 化畢的 加工 감광성에 의해 핵생성되는 결정화유리들은 제어된 공정중에서 화 학적으로 부식시켜 정밀한 칫수를 갖는 물질로 만들 수 있다. 이 공정율 화학적 가공 (chem i cal mach i n i n g)이라고 하며 以下에 이들에
관해 설명하겠다. 화학적 가공공정 은 처 음에 S t ooke y 31) 에 의 해 감광성 유리 에 응용 되었다. 이 유리는 리뭄-알루미노-규산영형이며 감광성성분으로 Cu, Ag 또는 Au 가 소량 함유되어 있다. 이들 유리가자의선에 照 射되면 감광성금속의 원자들이 생성되어 유리 중에 潛 像(l a t en t im a- g e) 이 형성된다. 유리를 가열중 금속원자들은 집합되어 미세결정을 형성하고 이들은 L i 20•2S i 02 와 다른 결정들의 결정화문 촉진한다. 따라서 照射 및 열처리효과가 유리 중에 불두명한 상을 만든다. 중 요한 발견은, 유리의 불투명한 부분이 조사되지 않아 두명한 유리의 부분보다 희석 HF 에 적어도 10 배 더 찰 녹는다는 접이다. 따라서 두명한 부분을 비교적 변화시키지 않고 불두명한부분을재용해시킬 수 있냐 이 방법을 이용하면 복잡한 모양의 유리를 만들 수 있다. 결정화유리에 대한 화학적 가공공정은 上記공정의 초기단계와 매 우 비슷하다. S t ooke y 32) 는 Si0 2 ; 60~85%, Li20 ; 5. 5~15%, Al2 03; 2~25% 의 조성에 K20, Na20, ZnO 둥의 다론 산화물 그리고 Au; o. 001~o. 003%, Ag C l 로 계 산하여 Ag ; o. 001~o. 03%, Cu20 로 계산하여 Cu; o.001~1% 의 감광성금속을 첨가하였다. 보통 사용되는 기술로 이 조성의 원료를 용융 및 성형시켜 얻어 전 유리기구(보동은 평판)를 자의선조사하면 潛像이 생간다. 이 유 리 를 서 냉 접 (접 도 ; 1013·1 p o i se) 과 섬 유연화접 (접 도 ; 10;· 6p o i s e ) 사이 의 온도에서 가열하면 감광성금속원자들이 집합되어 작은 결정들이 된 다. 이들 결정은 보통 Li 20•S i 02 인 상의 결정화를 촉진한다. 앞에 서 기술한 감광성유리에서와 같이 유리의 불두명한 부분은 두명한 · 부분보다 희석 HF 중에 더 찰 녹기 때문에 자의선조사에 감광된 부분이 용해되어 유리기구는 이 단계에서 선택적으로 부식된다. 부 ` 석 후 유리기구는 자의선조사에 재감광시켜 앞에서 감광되지 않은 유리부분내의 감광성금속원자를 성장시킨다. 다시 열처리공정을 하 떤 금속결정이 성장하고 다음에 L i 20•S i 02 결정이 생성된다. 이 과 · 정은 500~540°c 의 열처리에 의해 이루어진다. 상승온도를 천천
31) S. D. Sto o key, U. S. Pate n t No. 2684911(1 9 54). 32) S. D. Sto o key, Brit. Pate n t No. 752243(1956).
히 하여 열처 리의 최고온도 (800~950 ° C) 에 도달하였을 때 유리가 충 분히 다 결정질세 라믹으로 변화된다. Li 20•S i 02 와 함께 고실리카 함 량의 유리 중에서는 Li 20•2S i 02 와 석영의 결정이 생성될 수 있다. 고알루미 나함량의 조성 에 서 는 /3- sp o dumene 이 나 /3- sp o dumene/qu a- rtz 고 용체 의 결정 들이 나타나기 도 한다. 이 공정은 결정화유리를 가공하는 데 매우 편리한 방법이며 복잡 한 모양의 구멍 을 갖는 板도 제 조가능하다. 감광된 유리 의 부식 속 도는 감광되지 않은 유리의 15 배나 되므로 작은 구멍도 만들 수 있 다. 1/ lOOO inc h 내 의 정 밀도로 직 경 이 I/4 inc h 인 구멍 , 1 inc h 平方 當 360 000 개의 미세한 구멍까지도 만들 수 있다. 4. 3. 2 유리의 表面結晶化 유리표면을 결정화시키는 목적은 유리의 광학적 두명성을 거의 처하시키지 않고 기계적 강도를 높이는 데 있다. 어떤 경우에는 유 리의 표면에 永久 壓縮應 力윤 발생시킵으로써 기계적 강도를 증가시 킬 수 있다. 유리 전체는 張力에는 비교적 약하나 압축강도는 상당 히 높다. 따라서 表 面壓縮層이 존재하면 기계적 강도는 증가한다. 표면에 높은 압축응력이 촌재할려면 유리 내부에 똑같은 장력옹력 이 존재하여야 한다. 유리의 표면결정화는 附加的 機構에 의해 더 높은 기계적 강도를 얻을 수 있다. 죽, 찬유유리매트릭스 중에 매우 작은 결정의 체적분 울을 높이면 응력발생의 원인이 되는 홈(fl aw) 을 엄격히 제한하게 될 것이다. 이 경우높은응력(압축)을만들지 않고도매우높은강 도를얻을수있다. 표면에 높은 압축응력을 발생시키려면 결정화되지 않는 내부유리 보다 열팽창계수가 더 작은 결정들을 생성시켜야 한다. Olco tt둥 33) , 온 L i 20 一 AI203 一 S i 02 형 인 유리 에 860~960° C 에 서 표면을 결 정 화 시켜 8 一석영과 同構造인 두명한 육각형결정의 표면충을 만들었다. 이 충은 열팽창계수가 매우 작고 따라서 냉각중 유리 중에 큰 압축 33P) leJn. Su.m OPlcreotsst , anNde wS. DY.o rSkt(o lo9 k6e2 y)., Adoances in Glass Technolog y, P. 400
응력이 발생되었다. 주산화물성분 이의에도 이 유리논 이 공정에 반대효과를 미치지 않는 부성분과 이 공정을 실제로 촉진하는 Ti0 2 가 소량 함유되어 있다. 표면결정화충에 대한 최적두께범위가 촌 재하며 그 두께는 60~80µm 이다. 장시간 열처리를 하면 표면충은 더 두꺼워서 냉각중 유리가 붕괴되기 쉬우며 한편 불충분한 열처리 는 표면충이 얇아 내마모성이 약해진다. 표면을 결정화시킨 유리의 마멸시 편의 파괴 율 (modulus of ru pt ure) 은 600~700MNm-2 (s1000~ 101500 lb i n-2) 으로 매우 높다. 이 재료는 결정과 찬유유리의 굴절울 이 매우 비슷하기 때문에 상당히 두명하다. Ti 약02 간 가 다5~른6 %공 정치 으환로된는 ,N a2G0a— r fAi nl 2k0e3l— 등 S 34i) 0 이2 형L i 2유0 리 를 에 소 표량면 결함 유정 화하고충 을 만들었 다. 이 유리 를 주로 Li 2S 아 아 나 Na2S04 도 함유한 용융염 의 욕조 중에서 처리하였다. 처리논 860~900°c 에서 5~10 분간이 며 그 결과 /3 - eucr yptit e 와 석영의 고용체를 함유한 표면결정충이 생성되었다. /3 eucr yptit e 결정은 열팽창계수가 매우 작아 약간의 收縮差가 생기므로 높은 표면압축응력이 발생한다. 유리 중에 Ti 02 가 존재하면 요구되는 상들의 결정화를 촉진시키는 중요한 역할을 한다고 생 각된다. 이 공정 에 의 해 sooMN ·2 (116000 Ib i n-2) 의 높은 강도를 갖는 두명한 표면결정화유리가 제조되었다. McMi llan 등 35) 은 간단한 조성의 유리도 표면결정화에 의해 강화 시킬 수 있다는 것을 알았다. 30L i 20•70S i 02 인 유리를 500~600° I C 에서 1 시간 열처리하면 강도가 커진다는 것을 알았다. 예를 들면 : 575°C 에서 열처리를 하떤 평군파괴울이 3soMNm-2 (55000 lb i n -2 ) 인 재료가 얻어진다. 그러나 기계적 강도를 측정하기 전에 시편을 마 멸시키면 표면의 결정화충이 매우 얇아져 강도가 매우 작아진다. 표면결정화공정을 여제하는 경향이 있는 P2 아를 1mole% 함유한 : L i 20 ― S i 02 유리에서도 약간의 표면강도중가가 있었다. 표면충에 존 재하는 결정의 同定은 X- 선회철분석이 매우 약한 모양을 보이기
34) H. M. Garfi nk el, D. L. Roth ermel and S. D. Sto okey, Advances in Glass Teclt no log y, P. 404. Plenum Press, New York( l96 2) . .35 ) P. W. McMi llan . B. P. Hodg s on and R. E. Booth , ]. Mate r . Sci. , 4, 1029(1 9 69).
때문에 매우 어렵다. 그러나 1 개의 강한 선과 확산된 및 개의 약한 선은 Li 20•2S i 02 의 결정과 일치하였다. 표면결정화유리의 강화는 표면충과 내부의 수축차에 의해 압축응 력 이 표면충에 생 기 는 것 으로 설명 할 수 있 다. 複屈折 (b i re fri n g ence) 울 측정하면 유리질의 중십은 스트레인이 나타나지 않으나 표면충 은 결정화되지 않은 유리보다 열팽창계수가 작기 때문에 응력이 발 생한다는 것을 알 수 있다. 결정화된 Li 20•2S i 02 의 열팽창계수는 · 96x10_71°C 이며 결정화되지 않은 유리는 87X10-71°C 이었다. 따 라서Pa r표tr 면i d g 압 e 축둥응 36)력 은을 표 발면생결시 정킬 화 공가정능 에성 에의서 해 벗Z어nO난— 다A.I 2 03-Si0 2 형 의 유리를 매우 강화시킬 수 있었다. 적합한 유리로는 W t%로 ZnO ; 44.7, Al 요; 14.o, Si 02 : 41.3 이고 S i아대신 다른 산화물울 치환 지킨 유리도 포함된다. 열처리는 보통 공기 중에서 700~800°C 이 며 시간은 대개 24 시간이나 어떤 경우에는 150 시간 처리하였다. 열 처리중 kea tit e 구조를 갖는 결정의 표면충이 생성되었다. 기초유 리에서 표면결정화충의 최적두께는 70µm 에서 최대기계적 강도를 나타내나, 첨가된 산화물의 성질에 따라 충의 최적두께는 30~160 µm 이었다. 열처리 전에 모래나 22omesh 의 S i C 로 약간 마멸시킨 유리는 강도가 커졌고 어떤 경우에는 표면-결정화유리의 透明性이 개선되었다. 미리 마멸시키는 효과를 조사하기 위해 현미경관찰을 한 결과, 마멀조작에 의해 표면결정화를 위한 핵생성자리의 밀도가 높아져 더 군일하고 더 미세한 입자로 된 미제구조가 생성된다는 것을 알았다. 대부분의 경우 미리 마떨조작을 하면 표면-결정화유 리의 평군 파괴울이 50% 증가하였다. 최적열처리조건을 사용하면 평군단면파괴강도가 630~830MNrn-2 ’(9 1000~120000 lb i n-2) 인 재료를 만들 수 있으며 光學透明性도 상당 히 좋게 된다. 이들 재료의 고강도에 대한 이유를 생각할 때 치밀 한 keati te 결 정 상이 구조적 으로 /3- spo dumene 과 비 슷하며 /3- spo du- mene 은 열팽창계수가 작다는 것에 주목하여야 한다. 따라서 고강 도의 일부는 표면결정충과 비결정인 유리중십과의 수축차에 의한
36) G. Partr i d g e and P. W. McM illa n, Glass Teclmol. , 15, 127(1974).
것이라는 것이 확실하다. 그러나 시편의 유리질 내부는 장력응력을 받고 複屈折測 定에 의한 응력의 크기는 큰 표면압축응력이 존재할 만큼 충분하지 않기 때문에 다른 인자들이 작용하는 것 같다. 표면 - 결정화충의 미세구조가 응력을 일으키는 홈의 크기를 제한 하기 때문에 강도가 증진된다고 생각된다. 본래 유리표면 중에 촌 재하는 홈은 핵생성자리로 작용한다고 생각되며 따라서 이것을 제 거하고 핵생성울 중전시키기 위해 미리 마멸시키면 더 기계적 강도 가 큰 미세구조가 생긴다는 의견이 지지를 받고 있다. 4. 3. 3 機械的 性質을 向上시킨 결정화유라 유리 표면 중의 알칼리 금속이 온들을 스트레 인접 (str a in poi n t ) 이 하 의 온도에서 더 큰 이온들과 이온交換시킴으로써 유리를 강화시킬 수 있다는 사실이 알려쳐 왔다 .37) 치환된 이온들은 더 큰 체적을 필요로 하기 때문에 냉각중 유리표면에 높은 압축응력이 발생한다. 비슷하게 표면압축응력을결정화유리 중에 발생시킬 수있으며 2 가 지 공정이 가능하다. 즉 간단한 고용체를 함유시키고 표면에 相 轉 移를 일으키는 것이다. Kars t e tt er 등 38) 은 첫번째 공정의 한 예를, 主相으로 fi -s p odumene 고용체를 함유한 결정화유리의 표면 중에 있 는 L i+울 N 감로 교환시켰다. 이온교환 후 결정화유리를 냉각중 큰 표면압축응력이 발생하여 마멸시킨 시편의 파괴울보다 3 배 증가한 · 다는 결과를 얻 었 다. Beall 등 39) 은 툼새 이 온으로 M g 2+ 울 함유한 沿 석영고용체 중의 M g 2+ 당 2 개의 L i+울 교환시켰다. 처음에 단위정의 체적이 증가하고 두번째는 L i의 열팽창계수가 본래의 결정보다 매 우 작다. 이 2 가지 효과가 결합되어 매우 강한 표면압축응력을 발 생시킨다. Duke 둥 40) 은 이온교환과 결정화유리의 표면에 상전이를 일으켜 압축응력 을 발생 시 켰다. 칼품영 의 욕조 중에 nep h eli ne 을 함유한 ·
37) S. S. Kiz t l e r, Bull, Am. Ceram. Soc. , 40, 231(1 9 61 ). 38) B. R. Karste t t er and R. O. Voss, J. Am. Ceram. Soc. , 50, 33(1 9 67). 39) G, H. Beall, B. R. Karste t t er and H. L. Rit tler , J. Am. Ceram. Soc. , 50, 181(1967). 40) D. A. Duke, J. F. MacDowell and B. R. Karste t t er , ]. Am. Ceram. Soc. ,. 50, 67(1967 ).
결정화유리를 넣어 표면충의 결정이 ka!s i l it e(KA1S i 04) 로 전이하도 록 하였다. 이 상전이는 10% 의 체적 증가를 가져와 매우 높은 표 떤 압축응력 을 발생 한다. 이 방법 에 의 해 파괴 울은 1400MNm-2 (200000 lb i n-2) 까지 높일 수 있 었 다. 4.3.4 결정화유리의 複合物 결정화유리논 보통 높은 기계적 강도를 가지나 破坡關性(fr ac t ure t oug hnes 하울 증진시키는 것도 요구된다. 이 방법의 하나는 결정화 유리의 매트릭스 중에 高强度의 섬유나 위스커 (wh i sker) 를 집어넣는 것이다. Avest on41) 은 C 나 SiC 의 섬 유로 cordie r it e [M g 2Al3(A1S i 5 야)] 형 결정화유리를 보강하였다. 30Vol% 의 탄소섬유로 보강된 것은 과 괴 윤이 550MNm-2 (soooo lb i n-2) 이 었다. 高溫壓縮法 (ho t p ress i n g)에 의해 S i C 섬유로 보강된 재료에서는 열팽창계수가 다르기 때문에 바 람직하지 못한 응력을 일으키는 /3 cord i er it e 의 생성을 피하기 위해 12so°C 이상의 온도에서 이 공정을 해야 된다는 것을 알았다. 최적 조건Sa을mb e사ll4용2H하3)면 등 평은군 L파20괴— 울A은l20 3G—s SoiMQ N2 m 형 - 의2( 99결00 0정l ~화 i n유-2리) 이 되중었에다 .불 규 칙적 배향울 한 탄소성유를 혼입하면 기계적 강도는 강소하나 파괴 인성이 매우 증가한다는 것을 알았다. 지금까지 기술한 복합물은 모두 취성성유를 혼입한 것이었으나 軟性섬 유를 사용하는 것 이 더 양호하다는 예 가 있 다. Donald 둥 44) 온 니첼섬유로 보강한 결정화유리를 만들었으며 그 曲强度는 180 MNm-2 (26000 lb i n-2) 으로 매우 컸다. 니젤로 보강한 결정화유리가 높은 파괴인성을 갖게 되는 이유로는 여러 원인이 있으나 주역할은 섬유라고 생각된다.
41) J. Avesto n , The Prop er tie s of Fib r e Comp os it es, P. 63. I. P. C. Scie n ce and Technolog y Press, London (1972). 42) R. A. J. Samb~l1, D. H. Bowen and D. C. Phil lips, J. Mate r . Sci. , 7, 663(1 9 72). 43) Ibid . , 676(1 9 72). •14) I. W. Donald and P. W. McMi llan . J. Mate r Sci. , 11, 949(1975).
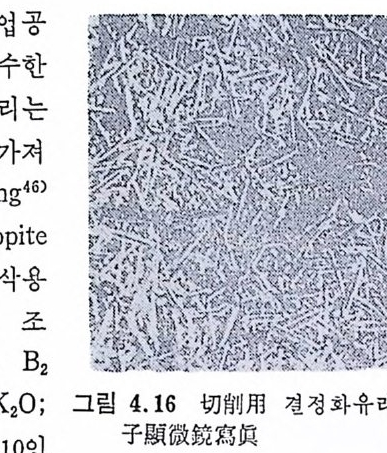 컴tf '찮..,
컴tf '찮..,
4. 3. 5 切削用 결정화유리 일반금속에서 사용되는 작업공 정 에 의해 가공이 가눙한 우수한 물리적 성질을갖는결정화유리논 재 료공학기 술에 큰 전전을 가져 다 주었 다. B e all 4 5) 과 Chy u ng 46 ) 등은 主結晶 相이 fluo rop h log o p ite m i ca(KM g 3AlS i 3010F2) 인 철식용 결정화유리들을 제조하였다. 조 성 이 Wt , %로 Si 02 ; 30~50, B2 0어 3~20, Al 요 ; 10~20, K20; 4~ 12, M gO ; 15~2 5 , F; 4~10 인
유리를 열처리하여 만들어졌다. 950~1oso ° C 에서 열처리하여 결정 화시킨 후의 미세구조는 그림 4 .16 에서와 같이 相互連結된 雲 母 의 결정이 발달되어 있다• 이 결정화유리는 열팽창계수가 50~115X 10-7/°C 로 크지만 탉熱衝擊性이 좋 으며 700°C 까‘ 지는 안정하나, 그 이상의 온도에서는 F2 가 손실되어 구조붕괴를 일으킨다. 그 강도 는 14~140MNm-2(2000~20000 lb i n -2 ) 이 며 강도는 雲母 片의 평 군직 경 에 반비례한다. 운모결정이 불규칙적 배향을 하며 상호연결되어 있 어 군열을 偏向시키며 약화시키기 때문에 파괴표면에너지는 높다. 운모-결정화유리의 독특한 미세구조 때문에 구멍뚫기 (drill ing ), 切斷 (saw i n g) 또는 旋削(l a t he t urn i n g)에 의해 公差에 가까운 加工이 가능하다. 이것은 雲 母片의 용이한 嬰開性 (cleava g e) 과 균열의 偏向 및 弱化의 機構가 함께 작용하여 가공성이 높아진 것이다. 미국의 Cornin g g lass 社가 제조, 판매하고 있는 切削用 (mach i na ble) 결정화유리의 하나인 macor( 商品名)를 소개하겠다 .4 7 ) 이 조성은 W t%로 Si0 2 ; 46, Al203; 16, K20; 10, M gO ; 17, F;.
45) G. H. Beall, Advances i11 Nucleati on and Crys t a l liz a to n in Glasses, P, 251 . Americ a n Cerami c Soc iet y (l97 1 ). 46) K. Chy u ng , G. H. Beall and D. C. Grossman, Proc. Xth Int. Cong . Glass, 14, 33(1 9 74) . 47) 岩田重雄, 『 工 業材料』, Vol. 28, 55(1980).
 그립 4.17 Macor 의 電子顯 微 鏡 寫 眞
그립 4.17 Macor 의 電子顯 微 鏡 寫 眞
4, B 요; 7 인 유리를 용융하여 형틀에 넣고 성형한 후연처리를 하 떤 유리 중에 合成 雲 母인 微結 晶이 불규칙하게 성장하여 유리와 세 라믹 으로 된 等方性의 복합재료인 macor 가 된다. macor 의 현미 경 사전을 그림 4. 17 에 실었 다. 현미경사전에서와 같이 母유리인 붕규산유리 중에 불규칙적으로. 상호연결된 운모결정이 macor 의 기계가공성을 높여 준다. 切斷時 에 는 공구날의 끝이 macor 중을 자르게 되 나, 운모결정 은 균열이 내부에까지 전행하는 것을 방지하며 군열을 철삭부분에만 그치도록· 한다. 따라서 매우 작은 균열이 절삭부분에만 집중하여 분말狀의 切 粉 울 만든다. 절삭에 의한 강도나 경도의 변화는 없으나 금속과 壘 는 달리 무리한 힘을 가하면 깨지는 경우가 있다. 표 4. 5 에 macor 와 다론 재료오벼 각종 성질을 비교하여 실었다 .. macor 는 광범위한 精 密加工이 가능하고 화학적으로도 안정한 人 . 畜無害 의 재료이며 _273~1000°c 에서 사용가능하다 .48) 斷熱性, 非磁性, 電 氣絶緣性이 우수하며 放射性에도 안정하다. 無孔性이므 로 眞空用 材料로도 좋다 .49> macor 는 形狀記憶注이 있는 有一한~ 48) G. K . Whit e, Cryo g e nic s Vol. 16, 487(1 9 76). 49()1 9V 7. 9O).. Alte m ose and A. R. Kacy o n, J. Vacuum Sci. _T ecll. , Vol. 16, 951
표 4. 5 Macor 와 다론재 료와의 목성 비 교 性 質 I Macor :,A lumi na (94%)IP-eotlh yy t lee t nr ae fl u oro 密 度 (g/c m3) 2.52 3.62 2.18 氣 孔 率(%) 。 。 0.01 Knoop hardness 250 2000 引張强度 (kg /c m2) 1000 2500 250 曲 强度 (kg /c m2) 1000 3500 壓楠强度 (kg /c m2) 3500 21000 120 機 械 加 工性 drill ing 0 X 。 saw.mg 0 X 。 lath e tur nin g 0 X 。 熱最高彭使服用係溫s亨e度c• \c;m(CO2 다C•) ) II 1000 II 1500 II 250 94X 10-7 nx10-1 438 X 10-7 熱傳導率( •cm。 c) 0.004 0.04 0.001 세라믹이다. 4.3.6 配向性微細溝造룰 갖는 결정화유리 결 정 화유리 중의 결정 의 배 향은, 動經配列 (rad i al alig nmen t)이 일 어나는 표면핵생성자리로부터의 결정성장윤 제의하고는 보통 불규 칙적이다. 만일 결정화유리의 전체에 평면 또는 축배열을 하는 針 狀結晶으로 된 미세구조를 생성시킬 수 있다면 기계적 강도와 파괴 인성에 좋은 효과를 기대할 수 있을 것이다. 또 정열된 미제구조를 갖는 결정화유리는 물리적 성질 중 有用한 異方性울 가질 것이라는 것도 기대된다. A t k i nson 둥 50) 은 결정화유리 중의 주결정상이 선택적인 방향으로 배향되도록 高溫抽出法 (ho t ex t rus i on) 을 사용하였다. 사용된 결정화 유리 의 조성온 mole% 로 Si0 2 ; 61. o~67. 5, Li20 ; 24. 5~30. 5, K2 O; • 1. 5, Al2 아; 1. o, P2 아; 1. o, B2 아; 5. 0 이 다. 직 접 추출기 술은 50) D. I. H. At ki n s on and P. W. McM illan , J. Mat. Sci. , 12, 443(1 9 77).
실린더 속에 유리片을 넣고 p lun g er 로 압축시켜 die a p era t ure 를 통해 결정화유리가 추출되어 나오도록 하였다. 추출시 유리봉을 d i e 에 놓고 局部結晶化가 일어나도록 일정온도에서 미리 정해진 시 간동안 열처리를 한다. 추출온도는 800~880°C 이고 작용된 荷 重 은 추출온도에 따라 2500~100k g으로 변화시켰다. 각 추출온도에서 유 리봉은 압력이 가해지기 전에 d i e 에서 30 분간 열처리되었다. 추출중 d i e 벽에서 마찰력 때문에 포물선분포의 속도 V 가 생간 다. 이 속도는 다음과 같이 나타낼 수 있다.
 V='1 P /4YJ l (r2-x2) (4-5)
V='1 P /4YJ l (r2-x2) (4-5)
여기서 .t1 P 는 d i e 의 입구와 출구 사이의 압력차, 7 는 접도, l 와 r 은 각각 d i e 의 길이와 반경, x 는 반경성분이다. 따라서 반경속도 구배가 추출중 결정들을 회전시켜 결정들의 長軸이 추출방향과 일 칙선이 되게 한다. 이상의 결정화유리에서 생성되는 결정상들은 針狀의 Li2 0 •2Si0 2 와 더 군질한 형의 t r i d y m it e 였다. Li 20•2S i 02 결정의 우수한 배열 아 얻어졌고 球狀에 가까운 t r i d y m it e 결정이 부분적으로 나타났다. 추출된 결정화유리의 走査電子顯微鏡寫眞이 그립 4.18 에 실려 있다. x- 선회절분석에 의해 추출된 결정화유리 중의 L i 20•2S i 02 결정의 결정학적 배향을 측정한 결과 (hkl) 反射의 강도는 (111) 面에 해당하 였다. 이것은 Li 20·2S i 02 결정이 抽出軸과 평행인 001 방향을 갖고
결정학적으로 배열되어 있고 tri - dy m i te 상 은 이 런 배 향을 나타내 지 않는다는 것을 의미하고 있 다• 추출법에 의해 제조된 결정화 유리의 성질은 같은 재료를 표준 방법으로 만든 결정화유리와는 다르다. 예를 들면 평균밀도는 추출결정화유리 가 약 10% 더 크 다. Knoop 경 도는 추출방향에
 그림 4.18 配向性微細構造를 갖는
그림 4.18 配向性微細構造를 갖는
90° 인 축에 i nden t er( 표식)를 배열시켰을 때 최대로 증가하였다. 연 마시킨 시편의 곡강도는 추출방향에 평행인 응력을 받았을 때 250 MNm-2(36000 Ib i n-2) 이고 이 값은 직 각방향의 2 배가 된다. 비슷한 異方性은 彈性率에서도 나타난다. 추출방향에서의 전기전도도 역시 직 각방향보다 2~40 배 더 높다. 배향성미제구조를 갖는 결정화유리의 섬유를 제조하는 방법이 Mar i es 둥 51) 에 의해 연구되었다. 조성이 W t%로 CaO; 30, ZnO ; 20, Si0 2 ; so 이며 직경이 거의 1mm 인 유리봉을 전기적으로 가열 시킨 P t코일을 통해 제어된 속도에서 引伸한다. 용융영역의 온도 는 액상온도 이상으로, 결정화는 Pt p robe( 際 本)를 최초의 용융체 에 도입함으로써 시작된다. 따라서 성장속도가 인신속도와 같은 위 치와 온도에서 안정한 성장면을 얻을 수 있었다. 성장된 결정상은 a 나 /3 -CaS i 03 이며 a 一 8 전이온도는 가열되는 최고온도(약 1soo° C ) 이 상이 다. 인신속도가 느리 면 (20 .u m/sec-1 보다 작은) a-CaSi0 3 의 핵 생 성 및 성 장을 일으키 고, ::L 속도가 빠르면 (50µmsec-1 이 상) 결 정 화되지 않은 유리봉이 된다. 중간인신속도에서는 /3 -CaS i 03 결정이 형성되고 이 결정화유리는 매우 우수한 축배향을 나타내며 전체가 봉의 단면적을 갖는 5µm 직경의 섬유를 형성한다는 것이 광학현 미경과 X- 선회철에 의해 확인되었다. 배향성 또는 섬유특성이 없 는 재료는 낮은 인신속도에 서 성장한 a - CaS i아 에 서 나타났다. 배 향성 을 갖는 /3- CaSi0 3 의 결정화유리 봉은 파괴 강도가 54oMNni- 2 (7800 !b i n 크)이고 탄성률이 124GNm-',(18X106lb i n-2) 으로 우수한 기 계적 성질을 갖고 있다. 배향성이 없는 a-CaS i 03 의 결정화유리에 , 서 는 파괴 강도가 320MNm-2(46ooo Ibin - 2), 탄성 률이 91GNm-2(13 x· 106lb i n-2) 이 었 다.
51) A. Maris and P. S. Rog er s; Natu r e, Land, 256, 401(1 9 75).
제 5 장 결정화유리의 性質 결정화에 의해 유리 중에 생긴 粒子는 結晶質이기 때문에 같은 조성의 유리와 전연 다른 성질을 나타내는 경우가 많다• 따라서 아 와 같은 結晶의 조성과 특성이 결정화유리의 성질을 결정적으로 지 배하며, 유리상태로는 비록 分相이 일어나도 얻을 수 없는 특수한 성질을 갖는 결정화유리를 얻을 수 있다. 이 장에서는 전기적으로 絶緣體이며 특수한 光學的 活性울 갖고 있지 않으나 熱的으로 우수 한 특성을 가지며 기계적 강도가 높기 때문에 유리나 종래의 磁器 · 대신으로 이용되고 있는 일반 결정화유리의 성질을 그 조성, 결정 성분 및 미세구조와 관련지어 설명하겠다. 표 5.1 은 시판되고 있는 · 결정화유리의 각종 성질을 시판유리와 비교한 것이다. 5.1 物理 및 化學的 性質 5.1.1 徵細構造와 多孔度 결정화유리의 주목할 만한 성질 중의 하나는 매우 미세한 결정립 으로 되어 있다는 것이며, 이것이 유용한 성질의 원인이 된다. 결 정화유리는 미제한 조직과 함께 거의 이상적인 多孔質構造를 하고 있으며 이 결정은 크기가 군일하며 불규칙적인 배향을 하고 있다. 일반적으로, 유용한 결정화유리에처 평군결정크기는 20~30nm 보다 작으나, 유리를 결정화시켜 만든 일부 재료들은 핵생성밀도가 작고 결정성장이 小球體化되어 기계적 강도가 좋지 않으며 평군입 一
질교미 성 리유와의리 시유화판정결 표 .51 ~1°,r a尸影]高 色白低色白I眼彭眼影透低明I 度- 유强化 高結(晶유리 晶結化 유 化리晶y結rx eP유 리板 유石英)리質硬級一( )s0022-多3i -S°A Nl2ii2아-0--B-2a22S3000220O-aCaLNi 2lAi0iLi 0 P(-00)L22L(i2S02S 組成礎基2i S0 溶0i,2Z02固삐r, T2s0 30B, 2P生劑成晶核結eunem 효益엷 - z /i3 iS220 . LO主晶相結 I I I I 陶色器隣磁色陶I)亨狀磁昌 I 光I)澤澤光透明 面I表面表明透 狀리I유 明透明透外觀 I— l l 3. 42.22 2524 ~. 47 . 2372.~. . 52245 .9~472. 42比重I 4519.9 474~ 851 46.11.. 145~9534 no.1 1. 折率屈 — 040 ~600~9I0 4030 0~070532度sr率ggkkco(en)强(硬/g度m(/2mc/ikkguc曲 0350180~015Y0VI 00 100~01I08 705405 407 0980~g3) 7001 m2m一重 g荷 X 5 5 7l5 . 0 0X5~8l0115.6 08X6X 5 017 X051X9~ 55) I 52 3 2~6~5 6 1~8 .7~43524_·791~(l°003~o° 0X 7loC係數眼彭熱 1~11 95 67~.1o °0080~ (2 0000517106~0 02~7011 2010 0 60 80990~95溫()O度C用度)C°(溫化最軟高使0100110~00 2010050 50 008 ~ 00 6X ~01 101 X118 110 10Xl 129015 X )C°001mc•.(抗U,氣電比抵03 1 1X 13 10 6X3 .74.436~. 81~2 7.~.4.47 6.~54 8.5~26.6 )3-52,cgMC0°率電誘9 34442~92 ~0 30103 4010~9 )1C°105- 2.(cM401 x 率體電誘23 3.004 .~0608. ~.90 1.~030. 9.20 9000.~2020. I ,a,g리mcoCN法,리表%m5칼間表c ( g알間l性m4m時2리/((時g,유,面H面 )%m'法a性칼水住雨 4 ,20c酸兩.003~7 143 .00.00 0.~010. 080. 3.10~0. 00 ) c0/99 5/ , C0° 알 蔚72o.410.~2 510. 00. 7.30~4.00) m2
266
도가 더 크다. 결정상과 함께 잔유유리상이 항상 촌재하며, 이 상은 노 결정형성이 일어나면 산화물들이 부족하게 되므로 母유리의 화학성 분과는 다르게 된다. 결정화유리의 일반특성인 미제구조와 바교하 여 소결알루미나의 평균결정크기는 10~20µ 정도이며 電氣磁器와 E 같이 광물울 기초로 한 세라믹은 40µ 정도의 크기이다. 앞 장의 미세구조에서 설명한 것과 같이, 결정질과 찬유유리상의 형태학과 그들의 체적분율에서 상당한 변화가 있다. 결정화유리의 성질을 설명하기 위해서는 결정질과 유리상의 체적분율 및 결정의 평군 크기에 대한 정확한 측정이 필요하다. 이 목적으로는 Dehoff 둥!)고} Underwood2) 가 설명 한 것 과 같이 , 點, 面 또는 線分析울 할 수 있는 電子顯微鏡觀察(예 ; SEM, EPMA) 이 유용하다. 만일 결정 상의 조성, 밀도 및 체적분율을 안다면 찬유유리상의 화학조성을 계산할 수 있다. 이들은 전기적 성질과 화학적 안정성을 조사하는 데 특히 중요하다. W illi am 홉”은 결정 상의 체 적 분율을 측정 하는 데 사용할 수 있 는 다른 방법들을 설명하고 있다. 한 방법은 X- 선회철로 결정상 울 同定한 후 결정질의 양을 pe ak 의 面積强度(i n t e g ra t ed int e n sit y) 로부터 정량적으로 측정하였다. 다른 방법은 결정질과 유리상을 분 리하는 각종 시약 중에서 용해도의 차이를 이용하였다. 그러나 이 방법은 상들을 충분히 구벌할 수 있는 용매를 항상 발견할 수 없기 때문에 널리 사용하지는 못한다. 저팽창 Li 20 ― A12°3 ― S i 02 형 결정 화유리에서는 0.1N ― HF 가 득히 유용하다는 것을 알았다. 이 반응 은 수분후 붕산을 약간 과잉 첨가하면 정지된다. 이런 형의 결정화 유리 에 서 는 결정 상이 /3- spo dumene 인 조건하에 서 는 용해 성 이 고 ru til e 과 알루미늄-티탄산영인 경우에는 불용성이다. 처팽창결정화 유리 중의 결정상의 체적분율은 o.86~o.9 이므로 찬유유리의 체적 분율은 o. 1 정 도가 된다. L i 20 ― A12°3 ― S i아 에 Mg O 와 B20a 7l- 철
1) R. T. Dehoff and F. N. Rhin e s, Qu anti tat i ve Mi cr oscop y, McGraw Hil l, New York (19 68). 2) E. E. Underwood, Qu anti tat i ve Ste r eology . Addis o n-Wesley, Readin g , Massachusett s( l 970 ) 3) J. P. Wi lliam s, G. B. Carrie r , H. J. Holland and F. J. Farmcomb, J. Mate r . Sci. , 2, 513(1967).
가된 더 복잡한 결정화유리에서는 찬유유리의 체적분율이 0.3 이므 로 결정화의 범위는 더 좁다. 기본결정상으로 mull it e 를 함유한 · BaO ― Al203-S i 02 결정화유리에서는 유리상의 체적분율이 약 0.6 으 로 상당히 높다. 결정상과 유리상의 바울이 상당히 변화하는 것은 결정화유리의 미세구조에서 볼 수 있으며 상들의 형태학도 마찬가치이다. 결정상 의 체적분율이 작을 때 (0.35~0.4 보다 작은)는 유리가 독립된 결정을 함유한 거의 연속적인 매트릭스를 형성하며, 이 결정화유리의 성질 은 유리상의 성질에 크게 좌우될 것이라는 것을 예측할 수 있다. 2 상의 체적분율이 거의 같을 때는 2 상온 서로 얽혀진 망목구조를 형 성하려는 경향이 있다. 결정상의 체적분율이 클 때는 유리는 인접 결정간에 얇은 충을 형성하며 어떤 경우에는 임계에 독립된 小空洞 (p ocke t)윤 형성하기도 한다. 그림 5.1 은 유리상의 체적분율이 비교 적 작은 전 정 화유리 의 미 세 구조이 다. cordie r ite ( 2 Mg O • 2 Al203 • 5 Si · 아)와 cris t o b ali te 그리 고 약간의 ruti le 의 혼합물을 함유한 결 정 들 의 평군크기는 0.5~1µ, 최대크기는 2µ 정도이다. 이런 미세구조는 높은 기계적 강도를 부여한다. · 정렬될 수 있는 응력이 보통 없는 조건하에서 결정화유리 중의 결정은 군질한 °각상(유리)으로부터 침전에 의해 형성되기 때문에 걷
정들은 불규칙적으로 배향된다. 배향성이 없다는 것은 결정화유 리의 성질이 등방성이라는 것을의미한다. 존재하는 결정의 일부가 비록 다른 결정학적 방향에서 다른 성질을 가지고 있다 하더라 도 이 성질은 유리 중에서 평군 화되어 나타난다. 일반기술에 의해 제조된 세타 믹의 겉보기기공물은 0 이고 진공 환경의 유지가 찰 되므로 거의 액체나 가스에 非透過性이나 閉
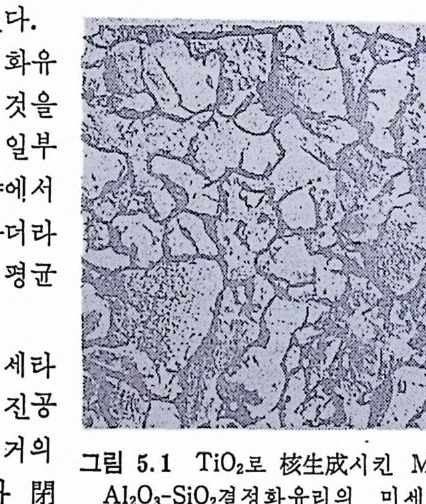 ~T·`
~T·`
氣 孔이 전연 없는 것은 드물다. 소결된 고알루미나세라믹에서 閉 氣 孔 率 은 보통 5~10% 정도이며 전기절연체로 사용되는 長石類磁器 논 약 10% 이다. 일반 세라믹스에 비해, 결정화유리는 어떤 형의 기공도 없다. 유 리로부터 세라믹상태로 전이할 때 全睦積裵化는 매우 작기 때문에 기공률이 커지지 않는다. 대부분의 체적변호H 큰 수축이나, 轉移 가 체 적중가를 가져올 때라도 이 체적중가는 原유리보다 밀도가 작은 결정이 생성되기 때문이며 재료의 내부에 空洞 (vo i d) 이 성장하지는 않는다. 전정화유리 중에 기공이 전연 없다면 매우 바람직한 성질 들을 구비하게 된다. 왜냐하면 기공은 재료의 유효단면적을 감소 시킬 분만 아니라 내부파괴를 일으킬 수 있는 홈으로 작용되기 때 문에 기계적 강도가 감소된다. 어떤 전기적 성질은 기공의 존재에 반대로 영향을 받는다. 죽 기공은 熱傳導率을 낮추며 이 성질은 재 료가 사용되는 곳에 따라 좋은 또는 나쁜 성질이 된다. 치밀하고 미세한 조직을 갖는 결정화유리는 일반 세라믹과는 구 별되어야 하고 이들 목수성질을 결정하는 원리를 알아야 하지만, 존재하는 결정상의 성질과 비율이 결정화유리의 각 목성을 결정하 는 데 가장 중요하다. 5.1.2 密度 결정화유리의 밀도는 표 5.2 에서 주어진 것과 같이 유리나 일반 세라믹스와 비슷한 범위에 있다. 결정화유리의 밀도는 존재하는 각종 결정과 유리밀도의 加成函數 가 된다. 유리상태로부터 결정화유리로 전이될 때 생기는 체적변화 는 보동 작기 대문에 결정화유리의 밀도에 대한 각종 산화물들의 영향은 일반 유리에서와 비슷하다. 유리의 밀도를 높이는 BaO 나 PbO 와 같은 산화물은 결정화유리의 밀도도 높이게 되므로 대개 加 成性이 성립된다. 비슷하게, 유리에서와같이 주성분으로 L i 20 를갖 는 결정화유리논 밀도가 작다. 결정화유리 중의 Al20a 나 Si0 2 대신 Mg O , CaO, ZnO, BaO 또는 PbO 의 바 울이 중가하면 밀도가 커 지 떠 BaO 와 PbO 의 효과가 가장 크다.
표 5.2 견정화유리, 유리 및 일반세라믹스의 밀도 Mate r ia l j Rang e of densit ies (g/ c m3) Glass-cerami cs Li2 0 — A'2 0 3— Si0 2 — Ti0 2 2.42 to 2.57 Mg O — Al2°3— Si0 2 — Ti 02 2.49 to 2.68 CaO-Ah 야 -S i 02-T i 02 2.48 to 2.80 Zn0-A}z 0 3-Si0 2- T i0 2 2. 99 to 3.13 BaO-A [z야― S i 02-T i 02 2.96 to 5.88 PbO— A '2 0 3-Si0 2 — Ti 02 I 3,50 to 5.76 Glasses I Fused sil i c a 2.20 Soda-lim e -sil ica 2.40 to 2.5 5 Low exp a nsio n borosil ica te 2.23 Pota s h-soda-l e ad-sil ica 2,85 to 4.00 High lead, alkali free 5.4 to 6.2 Cerami cs Hi gh ten sio n po rcelain 2.3 to 2.5 Ste a ti te cerami cs 2.5 to 2.7 Forste r it e cerami cs 2.7 to 2.8 Hi gh alumi na cerami cs 3.4 to 4. 0 결정화유리의 밀도는 대개 全化 學 組成에 의해 결정되지만, 존재하 는 결정 및 유리상의 구조가 결정화유리의 밀도를 결정한다. 예를 들면 실리 카는 유리 상의 한 성 분으로 cris t o bali te 나 석 영 , 또는 복 합규산영결정의 한 성분으로 촌재할 수 있으며, 결정화유리의 밀도 에 대한 실리카의 기여는 모든 형태에 따라 다르다. 예를 들면 석 영 의 밀도 (2. 65 g /cm3) 는 cr isto balit e (2. 32 g /cm3) 보다 훨싼 크기 때 문에 이들 2 결정의 상대량의 변화는 결정화유리의 밀도에 상당한 영 향을 준다. 열처 리 하여 실리 카가 전연 없고 cri sto bali te 나 석 영 또는 이들 결정이 半씩 함유된 결정화유리를 제조하기 위한 시도가 · 있 었 다. 실리 카가 완전히 crist o bali te 로 존재 할 때 는 결정 화유리 의 밀도는 2, 46g /c m3 이 나, 실리 카가 석 영 으로 촌재 할 때 는 2. 59g /c ms ;
으로 중가하였다. 이들 결정화유리는 같은 母유리로부터 제조되었 기 때문에 결정화과정중 생기는 체적변화는 상당한 영향을 받을 수 · 있다. 결정화유리의 밀도에 대한 열처리 schedule 의 영향도 (3- spo dum• ene 또는 (3- eucryp tite 를 主相으로 함유한 결정 화유리 들에 대 한 데 이타를 보면 알 수 있다. 열처리 최고온도를 800°C 로부터 900°C 로 또 1000°c 로부터 1200°c 로 변화시켰을 때 前者의 결정화유리의 밀 도는 약 1. 6%, 後者인 경 우는 2. 8% 변화가 일어 났다. 보동 고온 에 서 는 주결 정 상으로 (3- spo dumene, 처 온에 서 는 (3- eucryp tite 가 생 성되며 일정하지는 않지만 고온처리일수록 밀도가 낮다. 일부 결정화유리에서는 소량으로 촌재굴H 근 산화물이 주결정상의 예형 태를에 들 면영,향 Z을n O주 는기 L때i2문0 -에A l2밀0도a—에 S i0상 2 당형한 의 영P2향 야을 로 미핵칠 생 수 성도 된 있결다정. 화유리에서 Al2 아대신 ZnO 가 분자크기로 치환되기 때문에 ZnO 의 첫 첨 가에 서 는 밀도가 약간 증가하나, ZnO 의 분자비 율이 Al203 의 분자비울보다 커지면 밀도가 갑자기 증가하게 된다. 주결정상으로 석영이 촌재하기 때문이다. 5. 1. 3 化學的 尉久性 물 또는 다른 시약에 의한 화학적 침석에 대한 재료의 저항성은 실제적으로 매우 중요하다. 화학적 침식의 과정은 매우 복잡하며, 화학적 내구성을 축정하려면 보통 일정시험조건에 제어된 시료표면 울 침지시킨다. 종종 침식과정은 예상되는 사용조건과 비교하기 위 해 온도를 높이돈가 경우에 따라서는 압력을 높여 반응을 촉진시킨 다. 이와 같은 성질을 실험한 결과, 일반적으로 결정화유리는 우수 한 화학적 내구성을 갖고 있으며 다른 세라믹 재료들과 바교할 때 유용하다는 것을 알았다. 대부분의 경우, 결정화유리가 화학적으로 침식당할 때 첫 효과는 유리상에서 나타난다. 이것은 침식의 초기단계에는 H+ (또는 H3 아) 과 유리 중의 이동이온(보몽 알칼리금속이온) 사이에 이온교환이 일 어난다. 다음에 실리카의 망목구조가 水和過程에 의해 침식된다.
유리상 중의 알칼리금속이온의 이동도 (mob i l ity)가 결정상 중에 결 합되어 있는 비슷한 이온의 이동도보다 클 때는 유리상이 더 반응 도가 커져 화학침석에 대한 저항이 더 작아진다. 따라서 결정화유 리 중의 화학적 내구성을 높이기 위해서는 찬유유리상의 체적을 작 게 하고 이 상의 화학조성의 안정성을 높여야 한다. 유리상 중의 알칼리금속산화물의 농도를 높이지 않는 것이 화학적 내구성을 증 전시 키 는 데 도움이 된다. 알칼리 토류산화물과 함께 Al203 와 ZnO 를 함유한 설리카 r i ch 한유리상은우수한화학적 안 청 성을 갖는다. 이 일반적 효과는 Al2 아, M g O 와 ZnO 같은 산화물을 소량 (5% 정 도) 함유한 리튬-규산염을 기초조성으로 한 결정화유리에서 확인되 었다. 이 실험은 결정화유리 의 표준租粉(g r it)을 佛 騰 水 Eh 에서 2 시 간 침지시켜 중량강소를 측정함으로써 알 수 있다. 이 실험은 화학 척 침식에 노출되는 표면적이 크기 때문에 과격하다. L i 20 함량의 증가가 화학적 내구성에 가장 큰 ' 영향을 미찬다. 예를 들면 화학적 - 으로 침식되는 양온 L i 20 함량이 약 12W t%로부터 약 20W t%로 증 가하떤 14 배 커 진다. Li2 0 함량이 적 고 (2. sW t%) Mg O 와 Al203 가 치환된 복잡한 조성의 결정화유리는 L i 2O 를 12Wt % 함유한 결정화 유리에서의 중량강소보다 1/10 정도 작기 때문에 매우 내구성이 좋 다. Ka y등 4) 은 (3 - s p odumene 결정을 함유한 결정화유티의 내구성에 대해 보고하였다. 이 재료는 23°C 에서 물과 반응시킴으로써 응력 증진에 따른 강도의 감소에 약간의 반응성이 있었다. 이 결과는 유 리, 결정질산화물 및 다른 결정화유리에서 관찰된 결과와는 대조적 이다. 이것은 (3 s p odumene 결정화유리의 높은 안정도가 결정상의 낮은 반응성을 가져온 것이라고 생각된다. 물의 침식에 대한 결정 화결에 유정5리화00의유0 시 리간안에 정서노성출는에시 표켜관면 한의행 하연어여구떤는졌, 다退 .化시 도편이 을실볼 험 7수0 °후 C없 에L었서i다2 .0 1- 0Z0한n%O편 —相 NS對ia02 濕20 —度계 Cao ― S i아유리는 대우 風化되어 두꺼운 표면침전물이 생겼다. 理 1 t學容器로 사용되는 붕규산영유리는표면반사율이 떨어졌다 (surfa ce
4) J. F. Kay and R. H. Doremus, J. Am. Ceram. Soc. , 57, 480(1 9 74).
bloomi ng ). 이것은 약간의 風 化 (wea t her i n g)가 있었다는 것을 나타내 고 있다. 이와 같이 결정화유리의 화학적 저항은 우수한 화학안정 성이 요구되는 조건하에서 널리 사용되는 유리보다는 우수하다는 것을 알았다. 어떤 형의 결정화유리는 화학시약의 부식에 대해 우수한 저항성 울 갖고 있다. 리튬-알루미노규산영유리로부터 제조된 처팽창결정 화유리는 강산에 의한 침식에는 붕규산의 화학저항성유리보다는 M약g간 O —떨 A어l2지0 3지— 만Si 0 알2 조칼성리 용의 액유에리 로대부해터서 는제 조약된간 결 저정항 화성유이리 는더 크강다산.과 강알칼리의 침식에 대한 저항성은 화학저항성인 붕규산유리보다 약 간 떨어전다. 이 형의 결정화유리는농영산중에서 2 일간침지시켜도 크게 부석되지 않는다는 보고가 있다 .5) 또 HF 중기에 5~10 분간 노출시켜도 큰 부석이 일어나지 않았다. 고온에서도 어떤 결정화유리는 부식성 가스의 침식에 대해 처항 성을 갖는다. 예를 들면 중간적인 열팽창계수를 갖는 리튬 - 알루마 노 - 규산영결정화유리는 800°C, 6 시간 Cl2 나 HCI 가스에 노출시켜 도 큰 영향을 받지 않는다. 5.2 機械的 性質 5.2.1 機械的 强度 (1) 一般考察 재료의 기계적 강도는 특수응용에 대한 재료의 적응성을 결정하 는 主因子가 되기 때문에 가장 중요한 성질 중의 하나이다. 또 갑 작스런 온도변화에 파손되지 않고 견더는 재료의 능력과 같은 다른 중요한 성질도 기계적 강도에 의해 크게 영향을 받는다. 보통온도 에서 높은 기계적 강도를 가질 분만 아니라 고온에서도 견딜 수 있 는높은 강도를 갖는 것이 바람직하다. 이런 이유들 때문에 결정화 유리의 강도가 그 구조와 다론 인자들에 의해 얼마나 영향을 받는 가를 알 필요가 있다.
5) Briti sh Pate n t No. 903706(1 9 62).
결정화유리의 기계적 강도를 자세히 조사하기 전에 기계적 결함· 에 대한 일반개념을 고려하여야 한다. 보통유리나 세라믹스와 같이 결정화유리도 실온에서는 취성재료이다. 이것은 延性 또는 塾性領 域울 나타내지 않고 파손의 원인이 되는 하중 이하에서는 완전히 彈性擧動울 나타낸다는 것을 의미한다. 다론 취성고체와 같이 결정 화유리는 비교적 큰 탄성을 가지며 分枝破 康 (fo rked fr ac t ure) 가 일어 낱수있다. 유리는 시편의 크기에 따라 강도가 다르게 나타난다. 예를 듈면, 겉보기에 같은 유리시편에서의 실험결과의 偏差는 25~30% 가 된다. 한편 引伸시킨 유리섬유의 인장강도는 7000MNm-2(106lb i n-2) 이며, 더 큰 유리시편의 인장강도는 70MNm 一 2(104 lb i n-2) 을 넘지 못한다. 이 효과는 G riffit h6) 가 제 안한 가설에 의 해 설명 될 수 있 다. 즉 유 리시편은 각종 깊이의 균열이나 홈으로 요철두성이가 되어 있으며 이들 균열이 응력중폭제의 역할울 한다는 것이다. 기계적 강도에 영 향을 주는 正方向울 갖는 홍의 확률은 시편의 크기가 작을수록 작 아지며 따라서 유리섬유는 더 큰 시편보다 강도가 더 쿨 것이라고 . 기대된다. 비슷하게 일정시편에 대한 기계적 실험치의 변화는 시편 에 대한 임계방향에 흥이 존재하는지 않는지에 따라 좌우된다. 口J. 일 引伸된 유리봉이나 HF 에 약간 부식시킨 유리봉과 같이 홈이 작 다면 매우 큰 기계적 강도를 얻을 수 있으며 0.5cm 칙경의 유리봉 단면의 파괴 강도는 1400MNm-2 (200000 lbin - 2) 이 상이 었 다. 반대 로 유리표면을 마믿시켜 홈을 낸 유리는 기계적 강도가 떨어지나 동시 에 모든 시편이 비교적 깊은 홈을 많이 갖고 있기 때문에 실험결과 · 의 편차는 감소한다. 이런 이유 때문에 표준마털방법을 사용한 시 편을 가지고 기계적 강도를 실험하는 것이 좋다 . 일반유리에서 널리 사용되는 앞의 실험방법이 결정화유리의 연구 솔 에도 적철하다. 왜냐하면 결정화유리는 매우 미세한 미제구조~ 가지고 있으며 표면의 홈이 기계적 강도에 영향을 줄 것이라고 기 대되기 때문이다. 이것과 관련하여 전정화유리와 다론 재료와의 기 계적 강도를 비교할 때 실험조건을 고려하여야 한다. 종종 실험실
6) A. A. Grif fith, Ph il. Trans. A221, 163(1920).
에 따라 시편의 크기가 다론 것을 사용하고 어떤 사람은 표준마멸 수법을 사용하고 다른 사람은 마밀하지 않은 시편울 사용하기 때문 에 어렵지만 비록 각 실험값의 편차가 상당히 있더라도 실험전과가 재료의 실제, 강도에 더 근접하도록 하여야 한다. 유리에 대한 기계적 강도의 결과를 설명하는 데 가장 신뢰되고 있는 식은 Gr iffit h 에 의해 유도된 것이다.
 6=✓ 호7rC (5-1)
6=✓ 호7rC (5-1)
여기서 G 는 기계적 강도, E 는 탄성률, r 는 파괴표면에너지, c 는 임계홈(fl aw) 이 길이이다. 이 식으로부터 강도는 E 나 r 가 커지고 C 가 작아지면 중가한다는 것을 알 수 있다. 결정화유리의 기계적 강도에 대해서도 이들 매개변수의 상대적 중요성울 고려하면 된다. 그러나 이전에 실험적 증거를 재조사하는 것이 도움이 된다. 결정화유리의 강도에 영향을 주는 인자들을 종합하면 다음과 같 은 것이 있다. 내부구조에서는 結晶粒經, 열팽창, 결정량, 기공이 있으며 표면충의 구조에서는 유리층, 異種結晶, 配向이 있다. (2) 각종 결정화유리형의 機械的 强度 일반적으로 결정화유리의 강도는 일반유리와다론 형의 제라믹스 에 비해 높다. 표 5.3 에 주어진 데이타로부터 비교할 수 있으나 주 어전 재료에 대해 실제 얻어진 값은 시편의 표면조건에 따라 크게 영향을 받는다. 인용된 값들은 특수처리를 하지 않은 시편들에 대 표 5.3 결정화유리와 다론 재료들의 破壤率(이 값들은 0,5cm 직겅의棒 I 에 3 點M a荷te 重r ia에 l 의해 얻어진 것이다) I Rang e of values MNm-2 lb in- 2 Glasses 55-70 8000-10000 Glass-cerami cs 7700—- 3850 0 10000-50000 Electr i a l po rcelain ( ung la zed) 10000-12000 EHl 껑ect5 r ai pcl uae lmr pic noean r ct ec leAarihan mO ( g,i )cl a zed) 28000—- 134500 3102000000--5200000000
표 5.4 각종 결정화유리의 破裝率 LLLGiiiz 22lO00a —s—- sZ-SScniie00 Or22 a m-Si ci0 2s y st e m I 멀PPN짧22o 。0ni s5e ng 11M37106N0——M-m 533-o0249d80 u li Iof 12645000l000b000 —一-i n4 57-9 2800 00000 00 NZNCZMBLnn aaaia g2 OOO22O 0O00 —-—一— ———A MA AAlABAIlI2g 22al2l00 °2 O0 2°° 3333° -3— 3 ―—— 一—A — A SSS SSJ Sliii i 0i0i02 0i00 2202 °2 2 3 2 3 -_SSii00 22 TTTTTTZTriiiiiii 0 00 0000022222222 1161385199985218——-2--- 411016 21 03245131294 11118037660000000001010000200700 00 ———一一-00 100 19 1319 5068800000000000 0 00000 한 것이다. 표 5. 4 에는 각종 결정화유리계에 대해 발표된 값들을 실었다. 이 값들로부터, 결정화유리의 강도는 결정화유리계와 사용된 열처리주 기에 따라 상당히 다르다는 것을 알 수 있다. 표 5.4 의 값들로부터 다음과 같은 고찰을 할수있다. 첫째, 우수 한 기계적 강도를 얻기 위한 미제구조의 발달을 촉진시키는 핵생성 촉진제 의 중요성 은 데 이 타의 1 과 2 단에 서 나타난다. Li2 0-Si0 2 결 정화유리 중에 P2 야를 함유하면 강도가 7 배나 증가한다. 이 재료 중에는 주결정상으로 L i 20,2S i 02 가 존재하며 높은 강도를 얻을 수 있는 Li 20 ― ZnO ― S i아 계 의 결정화유리 중에 서 도 같다. 主相으로 cordie r it e 를 함유하는 M g O-Al203 ― S i아 계 의 결정화유리 도 높은 기계적 강도를 나타낸다. 이 이유 중의 하나는 결정상과 잔유유리 상의 열팽창계수의 차이가 작기 때문이라고 생간된다. 따라서 이 결정화유리 중의 미세응력은 비교적 작을 것이다. 리튬-알루미노규 산영재료는 열팽창계수가 작고 열충격처항이 크기 때문에 매우 홍드 미있는 재료이다. 이 재료의 기계적 강도는 cord i er it e 계 결정화유 리보다는 보통 작다. 이 작은 강도는 아마도 이 결정화유리 중위
상당한 내부응력의 존재 때문이라고 생각된다. 열팽창계수가 매우 작은 (3 - s p odumene 이 촌재하면 결정주위의 잔유유리상 중에 遠曲 引 張應 力 (cir c umf er enti al ten sile str e ss) 이 생 긴 다. 비 록 이 들 응력 이 미세군열의 원인은 되지 않더라도 이들은 결정화유리의 전체강도 를 낮추게 된다. 만일 (3- eucryp tite 가 主相으로 존재 한다면 다결 정 질 집합체의 형태로 이 결정은 높은 負의 열팽창계수를 갖기 때문에 강도가 더욱 나빠진다. S t ooke y”는 /3 -s p odumene 을 함유한 결정화유리의 曲强度는 129· ~143MNm-2(1sooo~20000 lb i n-2) 이고, /3 -eucr yptit e 를 함유한 것은 70~79MNm-2(10000~11000 lb i n-2) 이 라고 보고하고 있다. /3- eucryp - tit e 의 큰 異方性도 이 결정을 함유한 결정화유리의 강도를 낮추게 하는 것 같다. 매 우 작은 열팽 창계 수를 갖는 결정 이 발달되 지 않은 L i 20 一 A12°3 ― S i 02 형 결정화유리가 높은 기계적 강도를 가질 수 있다는 것에 주목하자. 이 런 재 료는 적 은 Al203 함량과 주결정상으로 보통 Li2 0 - • 2Si0 2 와 석 영 또는 cris t o b ali te 를 함유하고 있 다. McM ill an 등 8) 은 이런 형의 재료의 파괴율이 286MNm-2(4oooo lb i n-2) 이었다고 보고하 고 있다. 열팽창계수가 작은 상이 없다는 것은 결정화유리의 열팽 창계수가 102 X 10-7°C-l 인 것으로 확인되었다. 母유리의 조성을 변화시켜 결정화유리의 기계적 강도의 변화를 _ 조사한 연구가 있 다. mole% 조성 이 Si0 2 +Li2 0 +K20; 91. 5, P20s- ; 1.o, Al 요 ;(7.5-x), ZnO;x 인 유리의 Al2 아 대신 ZnO 의 치환 효과를 조사하였다. 그 결과는표 5.5 와 같으며, 결정화유리의 과과 울은 ZnO 의 함량이 증가함에 따라 매우 커진다는 것을 알 수 있 다. 처음의 ZnO 첨가에는 강도가 약간 커지나, ZnO 의 분자비율이 Al2· 야 의 분자비 율을 능가할 때 는 갑자기 강도가 커 진다. 이 효과는 ? 촌재하는 결정상의 형과 비울에서의 변화와 깊은 관계가 있다. Al::: 아함량이 ZnO 함량보다 큰 조성에서는 主相이 거의 Li 20•Al2 야 ·1C.
7) S. D. Sto o key, Aust. Pat. No. 46230(1959). 8) P. W. 1 •~M illan and B. P. Hodg so n, Eng 11 g , 196366(1963).
Mp표eo Zr lc n5eO.n5 t 결M p정Aoe r화llc 2°유en3리t 의 MM성Nro질mud-에up2 l t uulsbr 대 e/ i한no 2 f AlI 12 0아 4 와MM Neo(ZmIldnab-uOs2 /lt i함u in cs 2량 1 i) t0o y의 6f l b /영in 향2 [cex T5Xo 0ep h10afe 0nf°irc 7Csm1(i) oe2 aJnn0 l t - 。 7.5 138 20000 not mesaured 50.4 1. 5 6.0 152 22000 7.0 10.2 52.5 3.0 4.5 152 22000 9.7 14. 1 62.1 4.5 3.0 193 28000 9.8 14.2 108.6 6.0 1. 5 203 29500 12.1 17.6 118.4 7.5 。 272 39500. 14.9 21 .6 126.6 Si0 2 조성 인 실리 카 ric h 한 /3- spo dumene 고용체 이 다. Li2 0 • 2 S i아도 촌재 하며 AI2 아 함량이 감소하면 이 양은 중가한다. ZnO 함량이 AI2 03 함량보다 많아지면 /3 -s p odumene 은 더이상 겁출되지 않고 主相 이 석영이 되고 L i 20•2S i 02 의 비율도 커전다. 따라서 이런 형의 걷 정화유리에서는 주결정상으로 /3 -s p odumene 이 없어지고 석영이 나 타나는 것이 기계적 강도를 증가시키는 원인이 된다. 이런 재료에 서는 처팽창인 /3 -s p odumene 상이 바람직하지 못한 내부응력을 발 생하고 더 고팽창인 상이 대치됨으로써 기계적 강도가 증가하게 된 다고 결론내릴 수 있다. (3) 機械的 强度에 대 한 熱 處理 schedule 의 영 향 결정화유리의 미제구조와 광물학적 조직을 변환시키는 열처리주 기의 변화효과는 재료의 강도를 결정하는 인자들을 이해하는 기초 가 된다. 물론 이 경우 결정화유리의 화학조성은 변하지 않으나 결 정학적 조직은 크게 변할 수 있으며 강도와 같은 물리적 성 질 에 대 해 상당한 효과를 미 친다. L i 20-Al20a ― S i O 겨 울 기 본조성으로 하고 소량의 K20 를 함유하 며 금속銀을 핵 생 성 촉진제로 사용한 Wa t anabe 둥 9) 의 실험 결과는 기계적 강도가 열처리과정에 의해 크게 영향을 받는다는 사실을 나 타내고 있다. 열처리 전 마멸시킨 유리봉은 최대열처리온도를 500° 9) tMion. Wanadta Cn arybse t ,a l Rli. zVa.t i oCna po of r aGllia sasneds , RP. .E 2. 3,M Aoumlde,r icS ay n m Cp oesr iaum m i c Soonc ieN t yu (cll9e6a 2- ) .
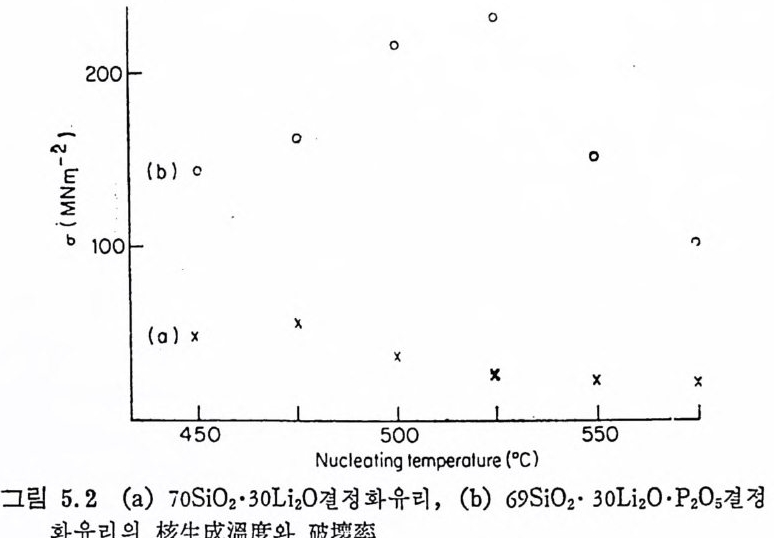 。
。
,c 로부터 900°C 까지 올릴 때 강도가 접 차 증가하였 다. 900°C 에 서 열처리한 시편의 강도는 모유리보다 2 배 커졌다. L i 20-S i 02 결정화유리의 기계적 성질에 대한 열처리의 영향이 McM ill an10) 에 의해 보고되었다. 그림 5. 2 는 450~575°C 에서 1 시 간 핵생성시키고 150°c 에서 1 시간 표준결정화처리를 한 마믿시킨 유리봉시편의 파괴율을 측정한 견과를 요약한 것이다. P 요를 함유한 유리는 모든 열처리에서 결정화유리를 강화자키 러, 이것은 P20s 가 함유되어 있지 않은 유리들의 미세구조(입도가 43~250 ,u m) 보다 더 미세한 미세구조(입도 8.5~50µm) 가 얻어지기 때 문이다. P2 야를 함유한 유리의 경우, 이 질과들은 최적기계적 강 도를 발달시키기 위해서는 핵생성처리가 중요하다는 것을 분명히 나타내고 있다. P2 아를 함유하지 않은 유리에서는 핵생성처리가 기계적 강도에 큰 영향을 미치지 않는다. McM ill an 둥 11) 은 22. 3 Li 20 •1 . 5K20·3. oZnO 72. 5 Si 02 o. 7P205 조
10) P. W. McMi llan , Advances in Nucleati on and Crys t a l li zat i on in Glas- ses, P. 224, Americ a n Cerami c Socie t y (l97 1). 11()1 9P6. 6W).. McMi llan , S. V. Phil lips and G. Partr i d g e, ]. Mate r . Sci. , 1, 269
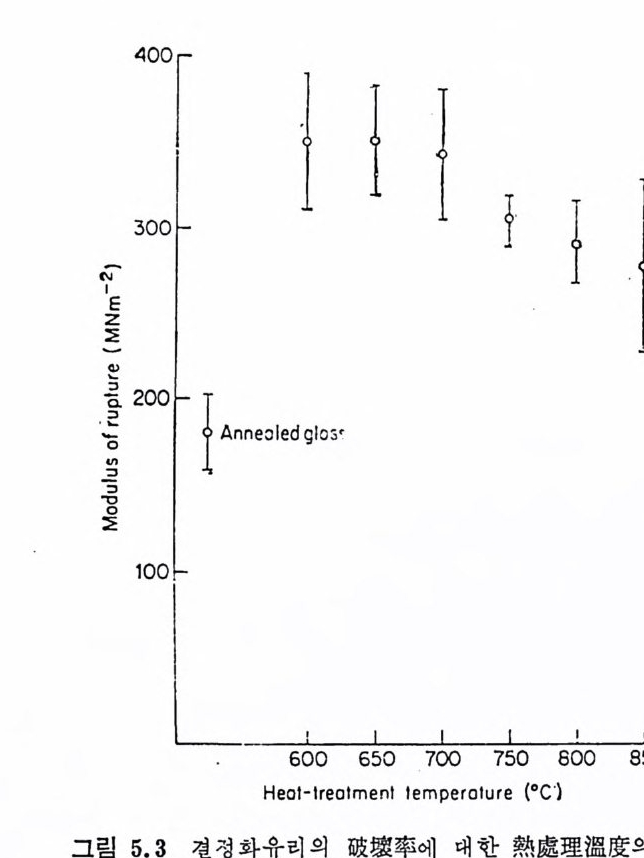 5 340000 「I I I I } I
5 340000 「I I I I } I
성의 유리를 열처리하여 L i 20•2S i 0 2 결 정을 발달시키면 상당한 강도. 의 증가를 가져온다는 것을 알았다. 이 유리시편은 500°C 에서 1 시 간 핵생성처리한 후 열처리를 600~s50°C, 1 시간 하였다 . 그 결과를 그림 5.3 에 요약하여 나타냈다. 600°C 의 열처리에 의해 기계적 강도는 실제적으로 2 배가 되었다 X- 선 회철분석과 전자현미경사전에 의하면 이 열처리에 의해 제조 된 결정화유리는 L i 20·2S i 02 와 결정화되지 않은 유리의 비율이 거 의 같았다. 700°C 에서 열처리 후는 결정질과 유리상의 비율이 여 전히 거의 비슷하지만 L i 20·2S i 02 의 樹枝狀이 확실히 나타났다. 700°C 이상의 열처리에서는 찬유유리가 결정화되고 결정질실리카 {보통 석영)의 비율이 접차 증가하며, 850°C 에서 열처리하면 Li2 0 h
2S i 02 와 결정질실리카의 비율이 거의 같고 잔유유리상은 약 5% 가 된다. 결정질실리카상의 생성은 결정화유리의 기계적 강도를 점차 감소 시킨다. 이 효과는 결정화유리 중에 바람직하지 못한 미세응력이 발달되는 것과 관련된다. 여기서 생기는 실리카의 결정형 (석영과 cr i s t obal it e) 들은 모두 L i 20•2S i 02 나 찬유유리상보다 열팽창계수가 훨씬 더 크다. 따라서 결정화유리를 냉각시 수축의 차이가 실리카 결정주위에 상당한 動經引張應力울 일으키게 한다. 극단적으로.는 · 미세군열이 생기며 바록 미세균열이 생기지 않더라도 높은 내부인 장응력이 촌재하면 대부분 결정화유리를 약화시키는 원인이 된다. 修飾된 Li 20-S i 02 형 결정화유리의 기계적 성질에 대한 유용한 연구가 Borom 둥 12) 에 의 해 이 루어 졌 다. 그들은 23. 7 Li2 0 • 2. 8 K20 • •2.sAl2 아 ·67.1S i 02•2.6B203•P2 야의 조성인 유리로부터 제조된 걷 정화유리의 과괴울에 대한 핵생성 및 성장처리의 변화효과를 조사 `. 하였다. 580°C 와 645°C 에서의 핵생성온도는 715~978°C 의 핵성 장온도범위와 연걷하여 행하여졌다. 645°C 에서 1 시간 핵생성처리하고 830°C 에서 168 시간 핵성장처 ' 리한 결정화유리 의 파괴울이 가장 큰 399MNm-2(55800lb i n-2) 이 었다. 각종 결정화유리 중의 결정질함량은정량 X- 선회철에 의해 계산되었 다. 모든 재 료는 L i 3P04 를 I. 5~5Wt % 함유하고 있 다. 그러 나 가장· 뚜렷한 특칭은 촌재하는 Li 20•S i 02 결정형의 변화이다. 낮은 결정성 장온도 및 짧은 성장시간에는 Li2 0 •Si0 z (lithi u m me t as ili ca t e) 는 상당 · 량 촌재 하나 높은 성 장온도에 서 는 Li2 0 • 2Si0 2 가 主相이 된다. Li2 0 • S i 02 상을 함유한 결정화유리는 L i 20•2S i 02 상을 함유한 것보다 매 우 약하다. 그들은 결정화유리의 强化機構는 탄성물의 증가에 의한 · 것이라고 단순화시킬 수 없다고 지적하였다. 매우 강한 재료(Li 20· 2S i 02 가 46W t%)는 모유리 보다 파괴 울이 3 배 크나, 탄성 울은 약 1. 3 배밖에 안된다. 이 이유는 일부 존재하는 L i 20•S i 02 와 찬유유리상 · 사이의 열팽창계수의 불일치가 매우 크기 때문이다. 여러 상들의. ,
12) M.P. Borom, A,M,Turkalo and R.H. ·Do remus, ].Am. Ceram. Soc., 58, 385(1975).
열팽창계수는 다음과 같다. 찬유유리상이 90X10-10c-1, Li 20 •2Si0 2 가 114X 10-10c-1, LhO•S i O 가 130X 10-7°C-I 이 다. 결정-유리 면간 의 動經引張應力윤 계산하면 L i 20•S i 02 결정화유리보다 3 배 더 크 다. 따라서 면간에 미세군열이 생길 가능성이 커지면 기계적 강도 는 감소된다. 결정화유리의 기계적 강도에 대한 미제구조의 영향을 H i n g둥 13) 이 연구하였다. 그들은 29L i 20•K20•ZnO•68S i 02·P2 아조성의 결정 화유리의 성질에 대한 열처리효과를 조사하였다. 이 시편들은 500° · C 에서 1 시간 핵생성처리를 한 후 550°c 에서 1~48 시간 절정호H 순 하였다. 발달된 결정상온 전부 L i 20•2S i 02 였다. 열처리시간을 1 시 간으로부터 24 시 간으로 걷게 하면 파괴 율이 176MNm-2(25500 lbin - 2) 으로부터 343MNm-2(49700 lb i n-2) 로 서 서 히 커 졌 다. 그후 강도의 감소가 일어나 48 시간 열처리한 시편의 파괴울은 239MNm- 2( 34 60 0 lb i n-2) 였다. 이 강도의 변화는 미제구조의 번화와 관련지을 수 있 다. 강도의 초기 증가는 Li 20 -2Si0 2 의 체 적 분율의 증가에 의 한 것 이다. 더 장시간 열처리에서는 체적분율이 약간 번하나 평군결정 크기가 커져 결국 租大化過程울 가져온다. 기계적 강도는 미제구조 의 매개변수인 찬유유리상의 평군자유행로 i의 변화를 사용하여 설 명할 수 있다. 이 매개변수는 다음과 같이 주어진다.
 J= d(1-V,)iV 1 (5-2)
J= d(1-V,)iV 1 (5-2)
여기서 d 는평군결정크기, V i는 결정상의 체적분율이다. 그립 5.4 에 나타난 관계가 존재한다는 것을 알 수 있다. 죽 i가 8µm 보다 작은 값에서는, 강도는 i l/2 에 반비례한다. i가 더 큰 곳 에서는 강도는 i의 변화와 무관하다. 이 결과는 찬유유리상 중의 L i 20•2S i 02 결정의 分散이 유리 중에 촌재할 수 있는 홈이 크기를 계한하기 때문이라고 설명할 수있다. 그러나 결정간평군간격이 비 결정질유리 중에 촌재하는 홍의 길이보다 클 때는 홍의 크기에 대 한 한계는 더 이상 없게 되고 강도는 입자간격과 무관하게 된다.
13) P, Hing and P. W. McMi llan , J. Mate r Sci, , 8, 1041(1 9 73). 14) S. W. Freim an and L. L. Hench, ]. Am. Ceram. Soc. , 55, 86(1 9 72).
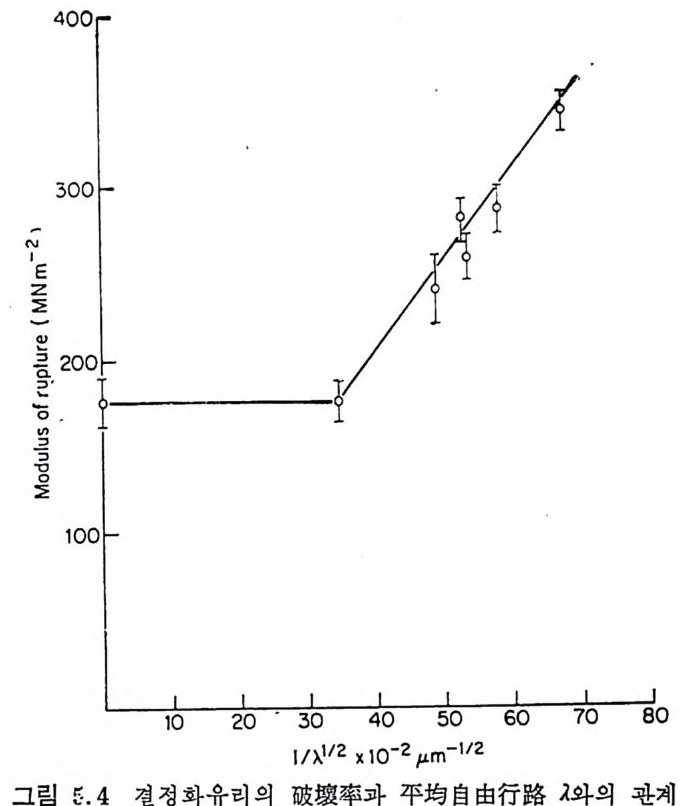 400
400
Fre i man 둥 14) 은 L i 20 ― S i O 여 결정화유리의 강도는 結晶間 間隔 이 감소할수록 중가한다고 보고하였다. 그러나 이들 재료는 광범위 한 미세군열을 나타내며 그 강도는 미제홈보다는 미제균열에 의해 더 좌우되는 것 같다. BaO•S i 02 계로부터 제조된 결정화유리의 기계적 성질에 관한 연 구가 Fre i man 둥 15) 에 의 해 이 루어 졌 다. 시 편들은 700°C 에 서 핵 생 성처리한 후 775~1300°C, 48 시간 내에서 열처리하였다. 열처리조 건에 따라 3 종류의 미제구조가 관찰되었다. 825°C 까지 온도를 올 리고 1 시간 결정화시키면 소구체화가 일어난다. 850°C 에서 더 간 시간 열처리를 하면 소구체의 가장자리 및 결정립 사이의 경계에 15) S.W. Freim an, G.y ; Onoda and A.G. Pin c us, ]. Am. Ceram. Soc.,. 57, 80974).,
있는 찬유유리에서 2 차결정화가 일어난다. 1000 ° c 이상의 열처리에 서는 가늘고 간 板 狀結晶 (l a t h-l i ke cr y s t al) 아 발달된다. 곡강도와 파 괴 에 너 지 를 2 重 canti le ver • beam 을 사용하여 측정 하였 다. 2 차 결 정 화가 일어날 때 기계적 강도가 중가함을 알았다. 평군곡강도가 161 MNm-2(23300 lb i n-2) 인 최 대 강도는 1000° c 에 서 2 4 시 간 열처 리 한 가 늘고 긴 板狀이 발달된 시펀에서 나타났다. 더 높은 온도에서 열처 리하면 강도가 매우 떨어지며 미제균열이 생기게 된다. 그들은 더 낮은 온도에서 열처리하여 강도가 증가된 것은 탄성율과 파괴에너 치가 증가하기 때문이라고 결론내렸다. 이 전론은 6 對 ✓ Er 의 p lo t가 原點을 지나는 직선관계에 있다는 것에 근거를 두고 있다. 이 결과는 Gr iffit h 식에서 군열의 길이 c 는 일정하게 남으며 미세 구조의 변화와는 무관하다는 것 을 의 미 한다. 직 선의 기 울기 로부터 홍의 크기는 54µm 임이 산 출 되었다. 이 결과가 일반적으로 결정화유리에 적용될 수 있는가를 고 려할 때, 시편준비시 사용된 마떨방법이 매우 중요하다는 것을 명심하여 야 한다. 취성재료에서는 만일 마멀처리가 아주 십하면 미세구조의 속박력을 없애는 표면미제군열이 생길 가능성이 존재하게 된다. 만 일 이 재료가 미세응력도 함유한다면 (BaO 一 S i O 거 결 정화유리에서 내 부미제군연의 생기는 것과 같이), 마텔중 십한 표면미세군열이 생기 께 된다. 그러나 십한 마떨조전 하에서는 표면미세균열은 거의 일 정한 깊이를 가지며 이 깊이는 실험되는 재료의 목성보다는 마털방 법의 특성에 더 좌우된다. BaO 一 S i 0 2 결정화유리의 경우, 연마처리 (po lish in g tr ea t men t)가 연삭조작중 도입 되 는 깊은 홈율 제 거 하는 데 · 적당하였다. (4) 機 械的 强度에 미치는 表面 條 件의 효과 지금까지는 결정화유리의 내부에서 기계적 강도에 영향을 마치는 - 인자들울 고려하였다. 그러나 재료의 내부구조오H 큰 직접 관계가 없 으나 기계적 강도에 상당한 영향을 미칠 수 있는 다른 인자들이 있 다. 기계적 강도에 대한 표면조건의 영향은 이미 설명하였으며 이 들 인자는 실험에 의해 증명되었다. 이 미 기 술한 연구에서 , Wa t anabe 둥”은 최 대 강도를 얻도록 열처
리한 결정화유리논 표준마텔처리에 의해 강도가 뗄어져, 마멀한 시 편의 강도는 마믿처리하지 않은 것의 81% 강도라는 것을 알았다. 그러나 같은 마멀처리 (abrasio n t rea t men t)에서 열처리하지 않은 유리 (결정화유리가 되기 이전)는· 강도가 매우 감소함을 알았다. 그. 이유 는 마멸한 시편의 강도는 마멸하지 않은 시편의 14% 에 지나지 않 았기 때문이다. 이 결과는 결정화유리가 유리보다 표면손상에 대해 민감치 않다는 것을 나타내며 이것이 결정화유리가 더 강도가 높다 는 이유가 될 수 있다. 그들은 만일 열처리 전의 유리에 표면손상을 피하도록 주의를 한 다면 결정화의 열처리효과가 강도를 오히려 감소시킨다는· 홍미있는 실험결과도 얻었다. 이 결과는 열처리 전에 마멸시킨 유리봉에서 관찰된 결과와는·정반대이다. 이것으로부터 결정화의 열처리는 유 리의 실용강도를 증가시키나(일반조건하에서는, 유리는 마밀이나 다른 이유 때문에 항상 표면손상을 입게 되기 때문에), 홈이 없는· 표모면을· 갖 는 유리에서 얻을 수 있는 강도보다는 큰 강도를 얻을 수 없다. 강도측정은 열처리하지 않고 각종 표면처리를 한 유리봉과 표준 결정화의 열처리를 한 시편을 가지고 행한다. 이들 실험결과를 표 5.6 에 실었다. 강도인자는 어떤 표면처리 및 결정화의 열처리도 하 지 않은 시편의 평군강도를 기준으로 각 시편의 강도를 비교하여 나타냈다. 표 5. 6 결정 화유리 의 强度에 대 한 結晶化 이 전의 ’ 表面處理左h 果 Gnroo.u p Surfa c e tre atm ent I hCearty- s ttr ae la l tizm a e tni otn Sftar ec tno gr t h 1 None give n None give n 1.0 2 None give n Normal schedule 2.4 3 Et ch ed in HF None give n 3.3 4 Et ch ed in HF Normal schedule 3.4 5 Abraded Normal schedule 1.4 이들 결과로부터 다음과 같은 결론을 내릴 수 있다. a) 열처리하지 않은 유리의 부식 (e t ch i n g)은 3 배 이상의 기계적 강 도를증가시킨다.
b) 부석시킨 유리를 열처리한 것이 연처리하지 않은 것보다 강도. 는 크게 증가되지 않으나, 부식시킨 유리로부터 제조된 결정화유리 가 부식시키지 않은 유리로부터 제조된 결정화유리보다 훨씬 강도 一 가 증가된다. c) 열처리 전에 유리를 마털처리한 결정화유리는 마멸처리하지 않은 결정화유리보다 강도가 상당히 감소된다. 이 실험은 한 종류의 결정화유리에 대한 것이기 때문에 모든 걷 정화유리에 적용될 수는 없으나 기계적 강도를 연구할 때 고려하여 야 하는 인자들이 어떤 것들인가를 제시하고 있다. Ka y둥 4 ) 의 연구에서는 표면조건에 영향을 주는 부가적인 정보를 ‘. 제시하고 있다. 이들은 주결정상이 /3 -s p odumene/s ili ca 고용체이고 一 소량의 ruti le 과 티 탄산염 을 함유한 Ti0 2 로 핵 생 성 된 Li2 0 -Al203. ― S i 02 형의 저팽창결정화유리에 대해 연구하였다. 4 접 하중의 파괴 울을 실온과 액체질소온도에서 측정하였다. 15µm S i C 종이를 사용하여 마믿을 제어하면 강도의 감소가 일어 나지 않는다는것은좀놀랄만한결과이다. 액체질소온도에서의 평 균강도는 약 8% 의 중가를 나타냈으며 이것은 중요한 의미를 가지 고 있다. 이 결과는 마털처리가 강도에 반대영향을 미치는 충을 결 정화유리의 표면으로부터 제거하기 때문이라고 설명할 수 있다. 全 근 材料보다 열팽창계수가 더 큰 표면충은 인장응력을 받으며 이 충이 제거되면 강도가 커진다. 이 효과는 다른 저팽창결정화유리에서도 관찰되었다. 또 4%HF 로 부식시킨 결정화유리가실온과액체질소온도에서 강 · 도가 매우 중가한다는 결과도 얻었다. 3~4µm 의 부식 깊이가 가장 강도가 컸으며, 이 결과로부터 부식되지 않은 결정화유리 중의 홈 의 깊이는 3µm 정도라고 생각된다. (5) 機械的 强度에 대한 온도효과 기계적 파손의 과정에서 중요한 변수는 온도이며, 결정화유리의 강도와 온도와의 관계를 안다는 것은 실용 및 기초적인 면에서 홍 鳳 미있는 일이다. 그립 5.5 는 일반용 결정화유리의 기계적 강도에 대 한 온도의 영향을 나타내고 있다.
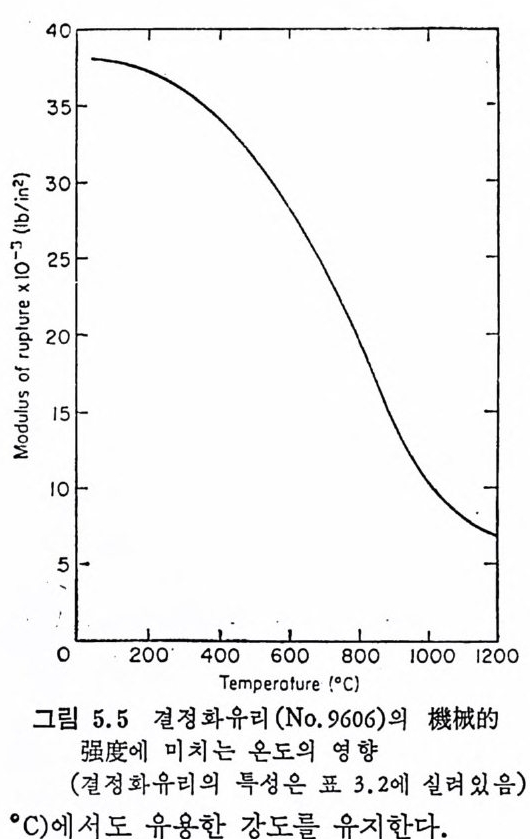 40
40
이 재료는 기초 조성 . 이 M g O ― Al203 ― S i O 려 고 핵생성촉진제로 Ti O z 믈 사용하였 다. cordie r -· it e 가 주결정상이고 실 리 카의 결 정 형 (cris t o b a- lit e) 도 촌재한다. 이 킹 도의 값들은 마멀처리한 후 화학강화처리를 한 결정화유리봉에 대한 것 들이다. 이 결정화유리 의 실온에서의 파괴율은 온도가 높아질수록 강도 가 떨어진다. 그러나 80 0°C 에서의 결정화유리의 강도도 실온에 서 의 대 부 분의 유리강도보다 훨씬 높다. 측정상한온도 (120 (1
그립 5.6 의 곡선 A 는 중간의 열팽창계수를 갖는 리튬-알루마노 규산영재료에 대한 것이다. 그러나 어떤 경우에는 강도의 초기 하강 이후 더 높은 온도에서는 강도가 회복된다. 이 효과는 곡선 B 의 조 . 성에서는 분명히 나타난다. 물론 더 높은 온도에서는 이 재료는 연 화, 용융까지도 일으켜 강도가 더 감소될 것이다. 비교실험으로 95- % 알루미나제라믹의 강도는 400~500°C 에서 최소값을 나타내며, Na20 ― CaO-S i아유리의 강도도 약 200°c 에서 최소값을 나타낸다. 유리의 경우, 최소강도의 촌재는 온도가 상승할 때 2 가지 반대효. 과 때문에 일어난다. 한 가지 효과는 원자결합력이 약해지기 때문 에 내부강도가 떨어지는 것이다. 그러나 동시에 유리표면에 존재하 · 는 홈들은 유리 중의 이 온들의 확산을 일으키 는 과정 (roundin g off_ pro cess) 때문에 약해지고 그 결과 강도가 증가하게 된다. 이 효과 7 1;-
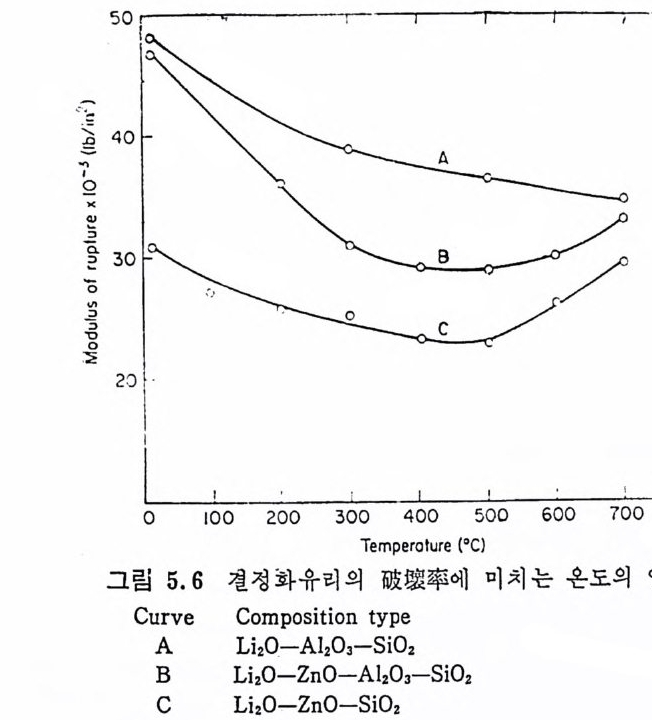 \\\
\\\
결합하여 일정온도에서 최소강도를 나타내게 된다. 이와 같은 설명이 결정화유리에도 적용될 수 있는지는 불확살하 머 더 많온 실험 연구가필요하다. 결정화유리와 같은 多相材料에서 는 결정질과 유리상 사이의 열팽창계수의 차이 때문에 생기는 응력 이 강도온도의 관계에 영향을 마치며 미세응력이 최대값을 갖는 온 도에Bo서ro m최16소) 은강 도주가결 정생 상간으다로고 L예i2 측0 •할 2 S i수0 2 를있다 함. 유한 Li20 — Al2° 3— Si 02 형의 2 종류의 결정화유리에 대한 강도의 온도의촌성을 연구하였 다. 2 재료는 모두 온도가 상승함에 따라 강도가 감소하였다. 한 재 료에서는 온도가 최고 550°C 로 상승할 때까지 강도가 계속 떨어 졌으나, 다른 결정화유리에서는 약 3so0c 에서 최소강도가 나타나 그 후의 온도상승에서는 강도가 약간 증가하였다. 그는 강도의 하 강은 온도상승에 따른 탄성율의 감소에 기여하지 못한다고 지저하
16) M.P. Borom, /. Am. Ceram. Soc., 60, 17(1 9 77) .
였다. 대상온도범위내에서 기계적 강도는 30~50% 감소하나 란성물 은 5% 이상 감소하지는 않는다. 강도의 감소는 결정과 유리상의 팽 창계 수의 차이 에 따론 내 부응력 (fav ourable int e r nal s t ress) 의 감소 에 의한 것이라고 생각된다. (6) 결정화유리 의 引張, 壓 楠 및 衝擊强度 결정화유리의 기계적 강도에 관한 논의는 파괴울의 측정값을 고 려한 것에 너무 한정시켜 왔다. 아 측정방법은 측정용 시편을 쉽게 준비할 수 있고 실험결과가 큰 편차없이 신용할 수 있는 평군값을 얻을 수 있기 때문에 널리 사용되어 왔다. 물론 인장강도, 압축강 도 및 충격강도와 같은 다른 강도들도 알 필요가 있다. 취성재료에 대한 안장강도의 측정은 아무리 조십하여도 시편들을 인장하중에 고정시키는 곳에서 응력집중이 일어나기 때문에 매우 어렵다. 따라서 결정화유리에 대한 인장강도의 측정값은 신용할 수 없다. 결정화유리의 인장강도는 高張力電氣磁器보다 대개 3 배 더 크다. 따라서 이들 재료의 인장강도는 파괴율에서와 같이 거의 같 은 비율을 나타낸다. 걷정화유리의 인장강도는 정확히 측정할 수 없기 때문에 압축강도는 벌로 의미가 없다. 압축강도를 측정하기 위해 설계된 어떤 실험에서도 인장력이 작용하는 동안 파손(fai lure) 이 생기며 작용하는 하중의 방법과 함께 시편의 모양과 크기가 파 괴에 펄요한 압축응력에 크게 영향을 미칠 것이다. 이런 이유 때문 에 인용되는 압축강도의 값은 종종 오해를 일으키게 된다. 그러나 직경이 3/8i nc h, 길이가 3/8 i nch 인 원통형 결정화유리의 끝면에 대 한 압축하중에 의한 압축강도 실험에서는 파괴울과 거의 비슷한 값 울얻을수있었다. 충격시 급격한 파손에 대한 재료의 처항성은 공학적 응용에서 유 용성을 결정하는 데 매우 중요하다. 그러나 충격강도는 기본량이 아니며 많은 다론 성질들에 의해 결정되는 복합적인 성질이다. 고 인장강도는 충격처항에 좋은 기여를 하나, 너무 단단한 재료는 에너 지홍수량이 작기 때문에 탄성울이 벌로 크지 않다. 파쇄가 시작되 떤 파쇄일은 커질 것이다. 죽 새로운 표면을 만드는 데 에너지가 신속히 소모되 고 파쇄 전파(fr ac t ure p rop a g a ti on) 는 갑자기 정 지 하게
된다. 어떤 경우에는 충격에 의한 파손은 실제의 충격접으로부터 약간 떨어전 곳에서 일어나기도 한다. 이것은 시편의 표면이 충격에 대 한 반발로 彈性波가 생기기 시작하기 때문이다. 예를 둘떤 직사각 형 유리판울고속액체방울로 충격울 주면 충격접에서의 국부손상 이 외에도 모서리 파손에 의한 손상을 입기도 한다. 충격파손의 복잡성 이의에도 충격파손에 대한 저항을 높이기 위 한 재료의 설계에 관한 해결책이 요구된다. 앞에서 논한 바와 같이 높은 안장강도를 얻기 위해서는 미립자로 된 미세구조가 요구되나 이런 구조가 충격처항에 가장 좋다고는 할 수 없다. 충격처항에는 높은 파괴인성이 필요하며 미세입자로 된 구조는 바람직하지 못하 다. 오히려 租大粒子로 된 구조가 유리-결정의 경계주위에서 파괴 를 偏向시키는 데 좋다. 탄성충격파를 약화시키는 데도 조대입자의 재료가 더 좋다. 이와 같이 불일치되는 요구에는 결정화유리의 매 트릭스와는 탄성성질이 매우 다른 섬유상으로 결정화유리를 강화시 키 는 방법 , 즉 複合材料 (com p os it e ma t er i al) 를 만드는 방법 이 가장 좋 을것이다. 충격과손의 복잡성 때문에 응용에 대한 재료의 현실적인 평가논 실제 사용조건 또는 가능한 사용조건에 가까운 조건하에서 실험하 도록 고려되고 있다. 그렇지만 충격파손을 지배하는 더 기본적인 성질들의 상호작용을 이해하기 위해 처음에는 표준시험에서 재료의 충격처항을 정량화하고 다음에 공학적 응용에서의 사용가능성을 기 . 준으로 재료들을 분류하는 것 이 좋다. 보통 사용되는 실험방법은 둥근 또는 직사각형인 단면을 갖는 시 편을 표준조건하에서 振子(p endulum) 로 충격을 가한다. 振子의 에 너지손실은 충격에 의해 흡수된 에너지에 해당하며 충격강도의 측 정 값이 된다. 직 경 1cm, 길이 8cm 이 며 홈이 파이 지 않은 (unno t ched) 결정화유리봉의 시편에 대해 char py시험을 한 결과 충격강도는 o. 54 ft•lb 를 얻었고 이 값은 95% 알루미나세라믹의 값보다 약 3 배이 다. 이 경 우 2 재료의 인장강도는 비 슷하며 파괴 에 요하는 일의 °ol::: 온 크게 다르지 않다고 생각된다. 따라서 알루미나세라믹의 성능자
하는 아마도 더 큰 탄성률에 기여하게 될 것이다(결정화 유리의 탄성 물 의 약 3 배) . 결정화유리의 충격강도는 300°C 에서는 o.4 8 ft •l b, 500 ° c 에서는 o.1s ft •lb 로 떨어진다. 이론적 및 실험적 관접으로부터 충격실험을 더 찰 이해하기 위한 시도가 McM ill an 둥 17) 에 의해 행하여졌다. 器械化된 振子와 컵퓨 터계산을 이용하여 시편에 유도되는 전동결과로 충격시 발생하는 복잡한 動的 勅果를 파악할 수 있었다. 유리, 결정화유리, 세라믹 스들에 대한 이들 결과의 일부를 표 5.7 에 나타냈다. 여기서 충겨 파손에 대한 저항은 振子의 에너지손실로 나타냈다. 표 5.7 직경 4mm 인 棒에 I대 한co nd衡it擊 io質n 驗의la b결s과8g :tmJ ) Mate r ia l Surfa c e M(orMdupuNltm uu sr-e•o )f Soda-li me -sil ica gla ss Abraded, dry 9. 3 (30) 42 (10) Soda-li m e-sil ica gla ss Abraded, wet 8, 4 (16) 37 (10) Glass-cerami c Ground 23 (20) 138 (8) 95% Alumi na cerami c Ground 21 (16) 208 (5) Electr i c a l por celain Ground 15.1 (6) 122 (5) ` 誌 : 광호내 의 숫자 들은 측정 값에 대 한 變動率 C%) 이 다. 표 5.7 로부터 결정화유리가 가장 큰 값을 나타내며 다음이 95% 알루미나세라믹이라는 것을 알 수 있다. 2 재료들은 유리보다는 훨 씬 충격저항이 크다. 비교하기 위해, 충격시 흡수되는 에너지 rI 와 파손이 일어나기 직전에 파괴울에서 저장되는 스트레인에너지 rs 와 의 比를 계산하였다. 스트레인에너지는 다음 식으로 주어졌다.
 rs =1 C6s2d 2I/48E (5-3)
rs =1 C6s2d 2I/48E (5-3)
여기서 아는 파괴율, E 는 Youn g울, d 는 시편의 직경, 2l 은 시편 支持 臺 사이의 거리이다. 유리시편에서 rI/r3 의 비는 약 4 로 거의 일정하였다. 결정화유리 의 이 比는 4.3, 전기자기는 3.2 였다. 그러나 알루미나세라믹에서 는 6.2 로 컸다. 이것은 알루미나세라믹의 탄성률이 커 평형이 되지
17) P. W. McMi llan and J. R. Tesh, ]. Mate r . Sc i. , 10, 6210975).
만 63 값이 나른 재료보다 훨씬 크기 때문에 좀놀랄만한 결과인 것 이다. 이것들의 견과는 알루미나세라믹이 다론 성질로부터 예측되 어온 것보다 충격시험에서는 찰 적용이 되지 않는다는 것을 의미 한다. 충격강도와 관계가 깊은 파괴인성은 파괴가 재료 중에서 曲經路 를 지나도록 한다면 커질 것이다. 이를 위해서는 입자를 관동하는 피펴보다는 결정간파괴가 요구된다. 파괴현상에는 2 인자가 영향을 미찬다• 첫째, 촌재하는 결정상이 일정한 勢開面 (cleava g e p lane) 들을 갖지 않는다던 유리-결정의 경계 에 도달하는 파괴는 쉽게 결정을 관통하여 전파될 것이다. 한편 찰 발달된 벽개면을 갖는 불규칙적인 배향을 한 결정들이 촌재하면 결 정들은 유리-결정의 경계를 가로지르는 군열전파에 대해 최적방향 으로 정렬하려고 하여 파괴확률은 낮아지고 따라서 파괴는 편향되 려고 한다. 따라서 이 경우에는 결정간파괴가 바람직하다. 主相으로 L i 20,2S i아와 석영을 함유한결정화유리에서, Li20 •2Si 02 결정에서는 파괴는 보통 粒界를 따라 일어나나, 석영의 경우 경 계를 가로질러 일어난다. 이것은 L i 20,2S i아에서는 찰 발달된 벽개 면이 촌재하나, 석영에서는 촌재하지 않기 때문이라고 생각된다. 다 론 예로는 운모를 함유한 결정화유리에서 볼 수 있다. 물론 이들 걷정은 아주 확실한 벽개방향을 갖고 있으며, 이것은 입자를 관통 하는 파괴보다 입자간파괴가 된다. 두번째 중요한 인자는, 유리-결정의 경계에 존재하는 응력과 관 계된다. 결정의 열팽창계수가 유리의 것보다 작은 곳에서는 兩相 에서의 動經方向應力 (rad i al s tr ess) 은 압축응력이 되고 周園應力 (circ umf ere nti al s tr ess) 은 유리에서는 인장, 결정에서는 압축응력이 된다. 따라서 결정에 접근하는 군열은 유리-결정의 면간에 수직인 응력이 압축이기 때문에 면간을 가로질러 전파될 것이다. 따라서 파괴는 입자간을 관통하게 된다(tr ans g ranular). 결정의 열팽창계수 가 더 큰 반대의 경우, 兩相의 動經方向의 응력은 압축이다. 주위 응력은 유리에서는 압축, 결정에서는 인장응력이다. 따라서 입자간 (inter gr a nular) 파괴 가 생 간다.
McCo lli s t er 둥 18) 은 비 슷한 기 하학적 미 세 구조를 갖는 2 가지 걷 정화유리에서의 파괴전파를 조사함으로써 이 이론을 확인하였다. L i 20 一 Al303 ― S i 02 형 결 정 화유리 에 서 주결정 상은 석 영 상보다 열팽 창계 수가 작다. 이 전 정 상의 열 팽 창계 수 (6 X 10-7°C - 1) 는 유리 상의 것 (41 X 10-7 0 c-1) 보다 훨씬 작으며 複屈折 (b i re fri ng ence) 에 의 한 유리 -걷 정의 떤간에서의 평군응력은 111MNm-2(11000 lb i n-2) 土 15% 이었다. 입자관통파괴가 우선적이라고 기대된다. 또 하나의 결정화유리는 유리매트릭스 중에 25µm 의 CaF2 결정이 촌재하며 CaF2 의 열팽창 계수 (195 X 10 구 Oc-l) 는 유리 (93X10-70c-l) 보다 훨씬 더 크다. 유리 걷정의 경계에서 인장응력은 29MNm-2(43000lb i n-2) 士 15% 이며 파괴 는 거의 입자간에 한정되었다. 이들 걷과는 찬유유리상의 열팽창계수가 결정상보다 큰 처팽창결 정 화유리 에 서 는 중 및 고팽 창 전정화유리 보다 파괴 인성 (frac tu r e tou g ~ hness) 이 작게 나타난다는 것 을 암시 하고 있 다. (7) 결정화유리의 靜的波勞 취성재료에 대한 기계적 강도를 연구하려고 할 때 주의하여야 할 ` 접은 정적 피로의 가능성이다. 규산영유리와 산화물계 제라믹스는 、 측정강도가 하중이 가해진 시간 또는 하중속도에 좌우되기 때문에 이 효과를 나타낸다. 이들 재료는 한정된 시간에서는 고옹력에 견 덜 수 있으나, 하중이 오랜 시간 가해진다면 상당히 낮은 응력에서 도 파손이 발생한다. 결과적으로 기계적 강도실험중 하중속도가 制御되어야 하며 보통 이 속도는 매우 낮다. 물론 정적 피로가 존 ` 재한다는 것은 세라믹에 대한 기계적 실험값을 안전하게 사용할 수· 있는 실제값으로 환산하기 위해서는 安全因子(보통 적 어도 3) 를 고려 해야 된다는 것을 의미한다. 결정화유리는 유리와 실용 제라믹스와` 깊은 관계가 있기 때문에 결정화유리가 정적 피로를 상당히 나타낸 다는 사실온 놀랄 일이 아니다. 정적 피로는 응력부식종 (s p e ci es of str es s corros i on) 을 함유하며 대 기 중의 수분이 중요한 역할울 한다는 유리에 대한 연구가 있다`
18)-H . L. McColl iste r and M. A. Conrad, Fractu r e of Glass-Cerami cs , • Presente d at Annual Meeti ng of Americ a n Cerami c Socie t y (l 966).
Charles 둥 19) 은 작용하는 응력 영 향하에 서 홍 끝(fl aw tip)의 부식 속 도가 촉진된다고 주장하고 있다. 이것은 홈끝윤 날카롭게 하면 촉 전되며 따라서 홈에 의해 응력이 倍加된다. 어떤 접에서는 홈끝의 국부응력은 유리의 파괴응력보다 커서 피로파손(fatig ue fail ure) 이 생 건다. 부석과정은먼처 유리중의 알칼리금속이온이 수소이온과 교환 된다고 추측된다. 즉, R+ (유리 )+H+( 물 )-+H+ (유리 )+R+( 물 ) 이 반 웅속도는 유리 중에서의 R+ 와 H+ 의 확산속도에 의해 제어되며 알 칼리이온의 이동도 (mob ility)에 의해 지배된다. 유리의 망목구조는 =Si— 0— S i= +H20 一 =S i -HO … HO ― S i= 과 같이 물에 의해 공격 을 받을 수도 있 다. 이 것 이 아마도 유리 의 지 연파손 (d e la yed fail· ure) 또는 정적 피로에 대한 타당한 이유일 것이다. 비록 용융실리 카유리는 실온에서 침식이 느리지만, 알칼리규산영유리에서는 매우 빠른 속도로 반응할 것이다. 유리와 접촉하는 용액의 p H 가 일정하 게 유지되더라도 반응이 빠른 속도로 진행되므로 알칼리용액이 형 성되기 때문이라고 간단히 결론지울 수는 없다. 알칼리금속이온이 결정상 중에 다량 함유된 결정화유리에서 비슷 한 반응이 일어날 수 있으나 정적 피로에 대한 민감성은 같은 조성 의 유리 에 서 보다는 작을 것 이 다. Wa t anabe 둥”은 리 튬 - 알루미 노 규산염의 결정화유리에 대한 정적 피로의 발생울 증명하였다. Kay 등 4) 은 주결 정 상으로 (3 sp o dl. l'ffie ne 을 함유한 결 정 화유리 의 거 동을 연구하였다. 정적 피로를 보통방법으로 측정하면, 액체질소온도에 서 관찰되는 파괴응력의 일부가 시편에 걸리고 파손이 생기기까지의 평균시간이 측정된다. 유리와 세라믹에서는 액체질소에서의 파손응 력의 o.7 배의 응력이 작용한다. 결정화유리의 경우, 어떤 시편도 104 초내에서 액체질소의 o.8 배 응력에서 파손이 생기지않았다. 이 연구결과, 결정화유리는 소오다 - 석회유리, 용융실리카 및 다 결정질 알루미나보다 정적 피로효과에 민감하지 못하다고 결론내릴 수 있다. 이 독특한 거동에 대해서는 결정화유리의 95% 를 차지하 는 /3- spo dumene 이 물에 대 한 반응성 이 낮기 때 문이 라고 설명 된다.
19) R. J. Charles and W. B. Hi'1Jig, Hi gh Str en g th Mate r ia l s, P. 682, Joh n W iley •& Sons, New York( l965 ) .
비록 Li+과 H 며 이온교환이 일어나지만 실리카충의 水和 룬 함유 한 2 차 반응이 작으며 따라서 응력 부식 효과에 대 한 크기 (sever ity)가 감소된다고 생각된다. (8) 결정화유리 의 强 度 에 대 한 微細 構 造的 基礎 결정화유리의 기계적 강도는 대다수의 실용제라믹스와 유리보다 크 다. 기공이 전연 없다는 것이 높은 강도를 주나, 측정된 강도에 대 한 충분한 설명이 되지논 않으며 많은 인자들이 결합되어 높은 강 도가 생긴다고 할 수 있다. 그 가능성들은 다음과 같다. a) 결 정 화유리 의 탄성 률 (8~15 x 104MNm-2) 은 유리 (6 x 104MNm-2) 보다 훨씬 크기 때문에 임계스트레인 개념에 기초를 둔 기계적 강 도의 이론은 결정화유리의 강도가 더 크다고 예측된다. 그러나 란 성률의 比보다 결정화유리는 유리보다 더 강하기 때문에 이 설명은 불충분하다. b) 결정화유리는 유리보다 더 단단하고 마텔처항이 더 커 강도를 잃게 되는 표면손상이 일정한 마밀조건에서는 덜 십각한 것 같다 . c) 열팽창계수가 다른 결정과 유리상의 결합은 높은 기계적 강도 룰 갖는 미세응력의 계를 갖게 한다. 결정이 주위의 유리보다 더 큰 열팽창계수를 가지면 유리 중의 動經 應 力온 인장이 되고, 周園 應 力은 압축이 된다. 결정이 작은 열팽창계수를 가질 때는 응력부 호는 반대가 된다. 저팽창 결정상을 함유한 결정화유리는 고팽창결 정울 함유한 결정화유리보다 약하기 때문에 경험상 2 次應力系는 바 람직하지 못하다. 異 方性 結 晶相이 존재하면 결정과 유리상 사이에 바람칙하지 못한 경 계 응력 (boundary str es s) 이 발생 하게 된다. 이 런 상들에 는 석 영 , /3 一 eucr yptrt e, corundum, 알루미 늄 티 탄산염 둥이 있 다. 표 5. 8 에 결정화유리 중에 생길 수 있는 결정들의 이방성의 크기를 나타냈다. 극단적으로, 발생된 응력은 기계적 강도를 급격히 감소시키는 원인 이 되는 각 결정립간의 분리와 군열을 일으키기에 충분하다. 경계 응력은 매우 작은 평군결정크기 때문에 최소화되나, 이 응력이 촌 재하면 입도에 대한 강도의 의존성에 대한 한 원인이 된다. d) 결정화유리 중에는 결정들이 촌재하기 때문에 偏向이 되고 破
표 5. 8 異方性結晶듄의 熱彭 服 係數 Crys ta l I Thermal exp a nsio n coeff icien ts • Qu artz 78 x 10-1 pa rallel to c axis I 144 x 10-1 pe rpe ndic u lar to c axis /3- Eucryp tite -176 x 10-7 pa rallel to c axis I 82. 1 x 10-7 pe rpe ndic u lar to c axis Corundum 66. 6 x 10-7 pa rallal to c axis I 50 x 10-1 pe rpe ndic u lar to c axis Alumi ni m um titan ate 118 x 10-7 pa rallel to a axis —19264 Xx 1100--7 1 ppaa rraalllleell ttoo bc aaxxiiss 壤先端이 둔감하게 된다. 따라서 파괴일은 중가하고 결정질이나 유 리상 사이의 경계면울 가로지르기 때문에 군열이 늦 어지거나 여제 되기도 한다. 한편 유리내에서는 파괴경로는 방해를 받지 않는다. 파괴는 보동 결정간의 입계를 따라 일어나므로 결정화유리의 파괴 면온 유리보다 더 거칠다. 파괴전파에 대한 이돌 미세구조적 효과 으 논 충격 파손에 중요한 것 같다. e) 결정화유리의 기계적 강도는 표면의 미세균열의 정도 및 분포 . 에 의해 제어되는 것 같다. 만일 미세균열이 결정 - 유리의 경계를 가로질러 전과된다면 유리 사이를 전파할 때보다 더 어려우며 따라 서 이들 인자들은 결정화유리의 표면미제구조에 의해 제어될 3 것이 다. 이 경우 미세균열의 길이는 결정상의 크기 및 체적분율과 관계 되며 최소평군 미세균열의 길이, 죽 최대기계적 강도를 가져오는 , 최적미세구조가 촌재할 것이다. U t suro i둥 20) 은 결정화유리의 기계적 강도 G 를 평군결정립적경 d· 와 다음과 같은 식으로 관련지었다. a=kd-> (5-4) 여기서 k 는 정수이다. 이 관계식은 Gr iffit h 식 (5-1) 중의 균열의 20) Y. Uts u mi , S. Sakka, J. Am. Ceram. Soc. , 53, 286(1970).
길이 C 가 결정립의 직경과 비례한다는 것을 의미한다. 그러나 비교 : 적 강한 결정질이 분산된 유리 - 결정의 복합재료에서는 破暖開始가 유리매트릭스 내에서 일어날 가능성도 있다. 분산상의 체적분율이 매우 큰 곳에서는 촌재할 수 있는 홈의 최대크기는 제한을 받는다 고 Hasselman 둥 21) 이 제 안하였 다. 제안된 기본성질은, 유리 중에 존재하는 홍은결정-유리의 경계에 서 정지되고 결정간의 평군거리, 죽 평군자유행로가 임계매개변수 가 될 것이타는 것이다. 평군자유행로 i는
 l=d(1-V,)/V1 (5-2)
l=d(1-V,)/V1 (5-2)
로 주어지며 여기서 Vf 는 결정상의 체저분율이다. 만일 결정화유리 중의 홍의 최대크기가 A 에 의해 제약을 받는다 떤 기계적 강도의 식은 다음과 같이 나타낼 수 있다.
![]() a=kl-½ (5-5)
a=kl-½ (5-5)
이 식 중의 k 의 값은 (2Er/1r)V2 로 주어진다. 만일 이 양이 미제구 조의 함수로서 비 교적 변화하지 않는다면 6 對 A - 1/2 의 plo t 는 i 의 . 값이 결정화되지 않은 유리 중의 임계홍의 크기보다 작을 때는 칙 선이 된다. 앞의 논의에서는 결정화유리 중의 미세응력효과에 대해 고려하지 않았으나, 기계적 강도에 대한 미세구조 변화의 영향을 고려할 때는 크게 영향울 미친다. 결정상의 열팽창계수가 잔유유리상보다 작을 경우 결정주위의 유리상 중에 周園張力應力과 動經壓縮應力이 촌재 ‘ 할 것이다. 팽창계수가 반대일 때는 응력부호도 반대가 된다. 따라 서 만일 결정상이 유리상 중의 홈의 크기를 제한한다면, 동경방향으 . 로 정렬된 主軸울 갖는 홈들은 결정상의 열팽창계수가 작은 곳에서 는 너 제약을 받을 것이며 홍의 길이는 결정간간격 A 에 의해 제어 될 것이다. 고열팽창계수의 결정들이 촌재하는 경우에는 周園方向 으로 정렬된 홈둘이 더 제약을 받을 것이다. 이런 홍둘의 길이는 결정 직 경 d 에 비 례 하며 따라서 강도는 A 一삼보다는 d- 岭의 함수가 된
21) D. P. H. Hasselman and R. M. Fulrath , ]. Am. Ceram. Soc. , 49, 68(1 9 66)_
다. 실용 결정화유리는 찬유유리상보다 작거나 큰 열팽창계수를 갖는 결정들의 혼합물을 함유하고 있어 강도의 미세구조에 대한 의 존성은 복잡하다. 기계적 강도에 대한 分散强化된 유리와 결정화유리에서의 응력효 과는 Borom16) 에 의해 연구되었다. 그는 Al2 아입자들을 함유함으로 써 강화된 유리 의 경 우, 강도의 증가는 분산상의 체 적 분율이 증가 할 때 탄성률이 증가하기 때문이라고 결론내렸다. 그러나 강도의 중가는 관찰된 탄성률의 중가로부터 예측한 것보다 작았다. 그는 갱Al 2각 아하입였자 다의. 인導산入염이 으홈로크 핵기 의생 성감 시소 킨보 다Li는2 0 — 증A가l20의 3 — 원Si인0 2이 결 되정 었화유다리고 의 기계적 성질에 관한 연구결과를 고려하여 결정화를 제어하면 란 성률을 증가시킵으로써 얻을 수 있는 강도보다 3~4 배 더 큰 강도 를 얻을 수 있다는 사실을 알았다. 이 사실을 설명하기 우]해 찬유 유리상이 압축응력을 갖도록 결정화유리 중에 바람직한 미세응력이 존재할 것을 제안하였다. 기본적으로는 유리상보다 결정상의 열팽 창계수가 큰 결정화유리에서는 결정주위의 유리상 중에 촌재하는 동경인장응력이 시편의 더 바깥 표면에서 O 로 감소하고 주위압축 응력은 감소하지 않을 것이다• 인접인자의 응력장 사이의 상호작용 은 동경응력성분의 부호를 반대로 하거나 감소시키는 원인이 될 수있다. 매트릭스인 유리보다 열팽창계수가 작은 결정을 함유한 결정화유 리에서는 母유리와 비교할때 界面應力이 결정화유리를 약화시킨다. 저팽창계수를 갖는결정상을 함유한결정화유리는 고팽창계수를갖 는 것보다 기계적 강도가 보통높지 않은 것이 사실이냐, 前者인 겅 우 같은 조성으로부터 제조된 유리보다는 훨씬 강도가 높다. 5.2.2 彌性性質 (1) 一般考察 재료의 탄성성질은 재료가 변형되는 조건에 놓여졌을 때 그 擧動 을 측정하는 데 매우 중요하다. 예를 들면 결정화유리가 온도구배 에 의해 변형된다면 탄성률은 발생되는 응력의 크기를 고정시킨다.
이것은 재료가 갑자기 가열되거나 냉각될 때 일어날 수 있으며, 이 ’ 경우에는 낮은 탄성률이 바람직하다. 비슷하게 결정화유리가 열팽 창계수가 다른 재료(예, 금속 )로 封着 된다면 주어전 스트레인에 대 해 응력이 낮게 되는 저탄성률이 유용하다. 물론 고탄성률이 바람 직한 경우도 있다. 이 경우는 플라스티울 강화하기 위해 섬유형으 로 유리를 사용할 때이다. 고체의 탄성상수에는, 탄성 물 (Youn g 품 ) ; E 剛性率 (Modulus of rig idi t y or tor sio n ) ; G 體積彈 性 率 (bulk modulus) ; K Pois s on 比 ; J.J 가있다. 等 方 體 에서는 이들 상수 사이에는 다음과 같은 관계가 있다.
 G=E/2(1+ )1) (5-6)
G=E/2(1+ )1) (5-6)
(2) 결정화유리의 彈性率 표 5.9 결정화유러와 다론 재료들의 탄성 물 Rang e of values of E Mate r ia l s 1 어 MNm-2 106 lb in- 2 Glass-cerami cs 8.3-13.8 12 一 20 Fused sili c a gla ss 7.2 10.5 Soda-l im e-sil ica gla ss 6.9 10.0 Borosil ic a te gla ss(Py re x) 6.6 9.5 Sin t e r ed pu re alumi ni a ( 5% po rosit y) 36.6 53 Hig h alumi na cerami cs 27.6-36.6 40-50 Sin t e r ed pu re mag n esia ( 5% po rosit y) 20.7 30 Sin t e r ed beryl l ia ( 5 % po rosit y) 31. 0 45 Electr i c a l hig h ten sio n po rcelain 6.6 9.6 Ste a ti te low loss cerami c I 6.9 l 10 I
표 5.10 20°c 에서 측정한 걷정화유리의 탄성 물 Consta n t Glass-cerami c 9606 I Glass-cerami c 9608 Meoldausltui cs it o yf, E 1(127. .0 4 X X 1 1어0 6M lbN min~- 22 ) 8(1.26.X 51 x 어 1 06M Nlbm i-n2- 2) Moridg uidlui ts y ,o f G 4(6. 8. 9 X x l 어10 6 MlbN min--2 2 ) Bulk modulus. K 7(1. 91 .X 4 l x0 41M06 Nlmb -2in - 2) Pois s on' s rati o 0.245 0.25 표 5.11 20°c 에서 측정한 결정화유리의 Youn g운 (E) Ty pe of gla ss-cerami c MmNmoYd-ou2u l|un sgl,b ' sEi n - 2 pr eMseanjo t r inc r ygsl a tas sl -cpeh raasmesi c L i 20 一 Alz03-S i 0 2 I 11004. 4X 11056. 1 X I /3- Sp o dmuemtea ns iel ,i cal itte h i u m LhO-Mg O -Si0 2 19. 5 X 10'1 섭 6 8 x / Qu artz , lit hi u m dis i l ic a te L((ii i)i 2) 0 L 一Hoi wZgnh ZOZn-OnSO ic 0oc 2no :tn e tne tn t 87..-37X X1 1004' 1111000266.. 66XX LCcsirirl it iishcs t a ti o uo t b emb a,a l,l( i iLt tdeeh,i, Os iq ,ll iiuc t Zaah rnti etu O z, m , Szi0 in2 c) Li 20 -ZnO-AI 2O a-Si0 2 l8 • 3 X 104I 11026. o x I sSo i!liu ct~1 -0 rn i :c hl_iPth 흐i pu mod ud '1!ls ~1~hec astoe l i d 결정화유리의 탄성울은 일반유리와 일부 실용제라믹스보다 높으 나, 표 5.9 의 데이타에서와 같이 소결한 순수한 산화물세라믹스의 탄성물보다는 낮다. 유리의 란성울 E 는 화학조성에 대개 加成關係를 나타내며 유리 조성으로부터 란성률을계산할수있다. 多相세라믹의 탄성율도결정 질과 유리 상의 각 란성 물의 加成函數가 되 며 이 것 이 Freim an 등 14) 에 의 해 확인되 었다. 산화물의 유리 상, 특히 CaO, Mg O , Al203 는 탄성률의 값을 높이지만 결정화유리의 탄성률은 주결정상의 탄성상 수들에 의해 거의 결정된다. 표 5.10 에 실린 데이타는 결정화유리의 탄성성질이 그들의 성분 예 따라 크게 차이가 생간다는 것을 나타내고 있다. 따라서 주절정
상으로 /3- sp o dumene/sili c a 의 고용체 를 함유한 결 정 화유리 (9608) 는 주결 정 상이 cordie r it e, cris t o b alit e 및 ruti le 인 결 정 화유리 (9606) 보 다 탄성물이 매우 작다. 결정화유리의 형에 따론 란성물의 의촌성에 대한 다른 예를 표 5.11 에 실었다. 각종 결정상과 찬유유리상의 체적분율을 알지 못하 떤 미제구조와 탄성성질 사이의 관계를 정확히 알 수 없다. 더 유 용한 방법은 조성과 미제구조의 系統的 變 化 (s y s t ema ti c var i a ti on) 를 고려하는 것이다. 표 5.5 는 이런 연구의 한 결과를 나타낸 것이다. ZnO 함량이 Al2 · 03 함량보다 많을 때 탄성률은 급격히 커지며 이것은 主相으로 석영 이 나타나고 /3- sp o dumene 이 사라지 기 때 문인 것 같다. 결정화유리의 열처리 schedule 을 변화시키면 결정상의 체적분율 이 달라지며 따라서 탄성성질에 대한 영향도 변화된다. McM ill an둥 22) 은 72. 5Si0 2 •22. 3L i20 · 1. 5K20·3ZnO•o. 7P205 조성 의 결정화유리에 대한 열처리효과를 조사하였다. 탄성물의 값 E 는 표 5.12 에 주어전 조건에서 열처리한 시편에 대해 측정하였다. 600 oc 에서 열처리함으로써 탄성률이 상당히 증가한 것은 L i 20•2S i 02 가 발달되었기 때문이다. 700°C 이상에서는 실리카는 최종물질로 석 영을 전정화시킨다. 이 相이 발달되면 최종적으로 탄성물이 약간 감소하게 된다. 표 5.12 열처리에 의한 탄성물의 변화 I E:MNm-2 I lb in- 2 Chil led gla ss as drawn 7,2X 104 10. 4X 106 Annealed at 450°C for 1 hr 7. 6X 10' 11 .0 X 106 500°C, 1 hr; 600°C, 1 hr 9.2X104 13.3Xl06 500°C, 1 hr; 100°C, 1 hr 9.6X 104 13.9Xl06 500°C, 1 hr; 100°C, 2 hr 9.8X104 14. 2 X 106 500°C, 1 hr; soo°C, 1 hr 9. ox 10• 13. 0X 106
22) P. W. McMi lla n, B. P. Hodg so n and G. Partr i d g e , Glass Technol. , 7, 1210966).
Borom 둥 12) 은 Li20 — Si 02 oJ] 유리 로부터 제 조된 결 정 화유리 의 탄 성률을 측정하였다. 35W t%의 Li 20•2S i 02 를 함유한 결정화유리의 단성 률은 母유리 의 7. O X 104MNm-2(10. 2 x 106 lb i n-2) 에 대 해 9. 0 X 104 MNm-2(13 x 106lb i n-2) 이 었 다. Li 20•2S i아를 29W t%, Li 20·S i 02 를 2 W t% 함유한 결정화유리 탄성률은 B. 6x 104MNm-2(12. 5x 106lbin - 2) 이고 Li 20 •Si0 2 20Wt % 그리고 L i 20-2S i 02 는 함유하지 않은 결정화 유리 의 탄성 률은 7. 9 x 104MNm-2(11 . 4 X 106 lb i n - 2) 이 었 다• 조성이 61.oSi0 2 •30. 5Li2 0 ·1. 5K20•Al203•P20s·5B203 인 유러를 사 용하여 At k in s on 둥 23) 은 단성 률에 대 한 600~900° C 범 위 에 서 의 열 처리효과를 조사하였다. 그 결과를 그림 5.7 에 요약하였으며, 탄성 률은 750°C 9-l 열처리온도에서 최대가 되었다. 이 온도범위에서 생성되는 주결정상은 L i 20-2S i아이며 미세구조 연구결과, 결정화유리 중의 결정상의 체적분율은 750°C 에서의 열처 리 후 최대였다. 그러나 란성률의 변화는 결정의 체적분율의 변화 · 만을 관찰하여 예측한 것보다는 약간 더 컸다. 약 820°C 이상으로 열처리하였을 때 탄성률의 중가도 촌재하는 결정상의 체적분율의 변화만울 가지고 단순히 설명하기는 어렵다.
(3) 彈性性質에 대 한 온 도의 영향 결정화유리의 탄성상수 에 대 한 온도의 효과는 어 떤 경우에는 일정결정상이 촌재함으로써 큰 영향을 나타낸다. 그림 5. 8 의 곡선들은 인 산염으로 핵생성시킨 각종 형의 결정화유리에 대한 탄성률을 나타낸 것이다. 이들 데이타 중 가장 콘 특칭은 200°c 의 온도부근
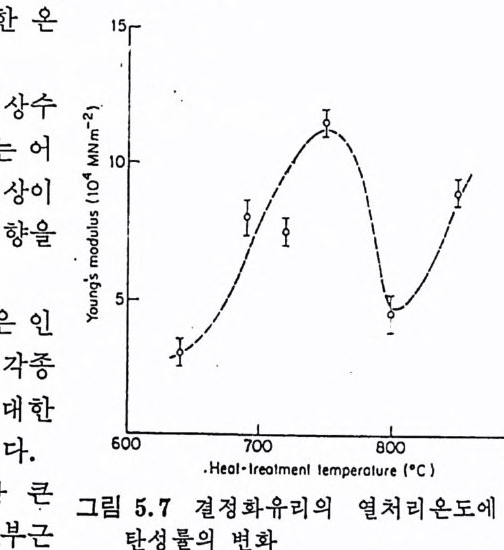 15 「
15 「
23) D. I. H. At ki n s on and P. W. McMi llan , J. Mate r . Sc i. , 11, 994(1 9 76).
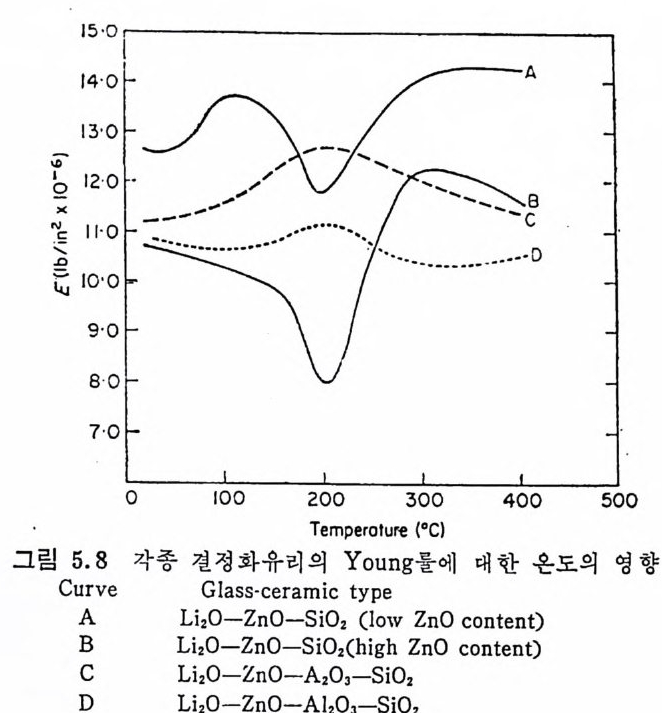 I 5D4 31211109
I 5D4 31211109
에서 A 와 B 의 조성인 결정화유리에서 탄성률이 최소접을 나타내며,. C 와 D 의 조성에서는 최소접이 없다는 것이다. • 이와 같은 반대결과는 다른 결정화유리 중의 결정함량과 관계되 며 A 와 B 조성 은 主相으로 cris t o b ali te 를 함유하며 이 결정 상은 C 와 D 조성에서는 존재하지 않는다. 약 200°c 에서 생기는 탄성률의 최소값은 cr i s t oba lit e 의 순도에 따라 220~270°C 범위에서 생기는 a-/3 cr i s t oba lit e 轉移 와 관계된다. 상전이를 나타내는 다른 결정들 도 결정화유리의 탄성률을 최소화한다. 예를 들면, 결정질석영은 V ig ore~ux 둥 24) 에 의해 주어전 데이타에 의하면 약 570°C 에서 탄 성률이 최소값을 나타냈다. a- /3석영전이는 573°C 에서 일어나며, 이 온도는 탄성률이 최소가 되는 온도와 매우 찰 일치한다. 따라서 주결정상으로 석영을 함유한 결정화유리에서는 탄성률군는도의 곡선 24) P. Vig o reaux and C. F, Booth , Qu artz Vi b rato r s and the ir Ap plica ti ons H. M. Sta t i on ary Of fice , London( l95 0).
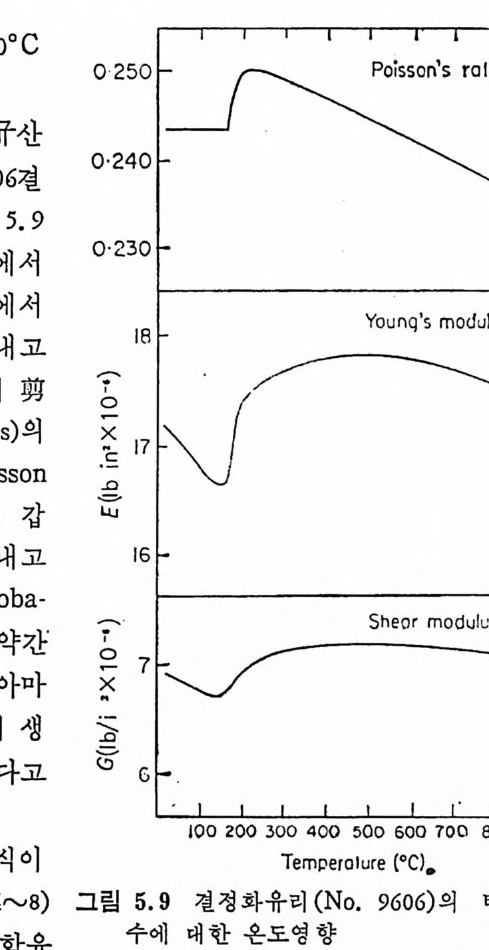 0 250 Pois s on's ra tio
0 250 Pois s on's ra tio
에서 최소값은 약 570°C 에서 생간다. 마그네슘-알루미노규산 영형 결정화유리인 9606 결 정화유리에 대한 그림 5.9 의 데이타는 약 160°C 에서 Youn g물/온도의 곡선에 서 현처한 최소값을 나타내고 있다. 비슷한 온도에서 前 斷彈性 率 (shear modulus) 의 최 소값이 생 기 고 Pois s on 比는 160~170°C 에서 갑 자기 증가함을 나타내고 있 다. 이 결 과가 cris t o b a- lite 전 이 온도보다는 약간 낮지만 이들 결과는 아마 도 견정화유리 중에서 생 기는 상전이와 관계된다고 생각된다. Muchow2” 는 일반식 이 Li2 0 •Al203•nSi0 z (n =4~8) 이 며 Keati te 고 용체 를 함유
한 결정화유리 의 탄성률변화를 20~800°C 범 위 에 서 온도의 함수로 서 조사하였다. n 이 4 인 재료(/3 -s p odumene 조성)는 20°c 에서 9.2X 104MNm-2 (13. 4 X 1061b i n-2) 로부터 800° C 에 서 의 9. 1 x 104MNm-2 ·(1 3.2X1061b i n-2) 로 서서히 탄성물이 감소되었다. n 이 더 큰 재료에 서 는 온도가 상승함에 따라 탄성률이 증가하는 異常畢動 (anomalous ;ii ehav i our) 을 나타냈고, n 이 10 인 재료에서 이 현상은 가장 컸다. n 이 10 인 경우 20°c 에서 7. 6X 104MNm-2(11 x 1061b i n-2) 로부터 800°C
25) G. M. Muchow, Advances in Nucleati on and Crys t a l liz a ti on in Glasses. P. 272, Americ a n Cerami c Soc iet y (l97 1) .
에 서 8. 3 x 104MNm-2(12 x 106 lb i n-2) 으로 란성 물이 중가하였 다. 이 재료는 異常熱影服崇動과 함께 異常等溫壓縮勅果도 나타낸다. 죽, 유이들한 결재료정는화 유열리팽가창 제異수常가熱 및작 거彈나性 性負質이을다 .나 타이 내k는ea ti것t e은 고 용Si-체 0를— 함 Si 결합길이와 결합각이 변화하기 때문이라고 생각된다. 5. 2. 3 硬度와 摩托抵抗 (1) 一般考察 경도는 재료의 기본적인 물리적 성질은 아니나 실험방법에 따라 탈리 나타나는 물리적 성질들의 복합함수이다. 따라서 재료의 경도 를 마모 또는 마텔처항과 같이 생각할 수 있으며, 이 성질은 사용시 재료의 尉久性울 결정하며 마모저항이 제일 중요한 목수응용에 대 한 재료의 적합성을 정하는 데 사용된다. 따라서 일정조건하에서 마모에 대한 재료의 처항은 경도의 척도가 된다. 다른 재료들에 의 한 scra t ch 저항은 강도의 다른 尺度이며, 일정조건 하에서 재료에 -py ram i d( 보통은 다이아몬드)의 하중에 의한 壓康의 깊이 (dep th of ii ene tr a ti on) 도 경도의 척도가 된다. 이들 실험방법은 재료를 경도의 척도로 분류할 수 있지만 모두 경험적인 것이며 경도의 크기는 사 용되는 방법에 따라 다르다. 이런 이유 때문에 가능한 실제조건에 가까운 실험방법을 선택하여야 한다. (2) 硬度實驗 scra t ch 경도는 그 결과가 종종 일정한 값을 나타내지 않지만 바 교적 간단한 실험 방법 이 라는 利點이 있 다. 다른 재 료들을 scratc h 하는 능력에 따라 재료를 분류하는 Mohs 척도가 널리 알려처 있다. 이 쳐 도는 上限이 다이 아몬드로 10 의 경 도, 下限이 滑石으로 1 의 경 도를 갖는다. 유리 의 Mohs 경 도는 보통 5~7 이 나, 다른 재료를 기준으로 각각의 유리를 분류하는 이 실험방법은 적합하지 않다. 이런 방법으로 결정화유리의 scra t ch 경도를측정하면 보통유리보 다 매우 큰 값을 나타낸다. Wa t anabe 등”은 리둠-알루미노규산영 형 결정화유리가 Mohs 경도 9 보다 작은 것으로는 상처가 나지 않는 다는 것을 확인하고 이 결정화유리의 Mohs 경도는 경도 9 인 Al203
(corundum) 나 9~9. 5 경도인 S i C 와 비슷하다고 지적하였다. 壓子(i nden t er) 에 의한 경도는 금속학분야에서 널리 사용되고 있으 며 이 방법도 유리와 이와 비슷한 재료에 이용되어 왔다. 적당한 조건하에 서 영 구압혼(p ermanen t i nden t a ti on) 을 제 거 시 킨 유리 표떤울 다이아몬드 피라밋의 끝으로 누른다. 惑康이 형성되는 기구는 복잡 하나 압자에 의한 유리의 탄성변형, 소성흐름, 압자 바로 아래에 있는 유리의 밀집상태의 효과가 함께 나타난다. . 각종 押入硬度(i nden t a ti on hardness) 실험 방법 이 이 용될 수 있 다. Knoop 경 도와 다이 아몬드 피 라밋 경 도 (D. P. H. )는 다른 모양의 압자 가 사용되지만 형성된 영구압혼의 크기를 측정하면 된다. Knoo p겅 도는 k g의 하중을 압혼의 mm2 으로 나눠 표시 하며 , D. P. H. (Vi ck ers hardness 와 같음)는 하중을 접촉면적으로 나눠 나타낸다. Rockwell 실험에서는 長圓維形의 다아아몬드압자를 150k g하중으로 누른다. 압자의 針入度는 시편의 경도를 나타낸다. 이들 방법들도 결정화유 리와 같이 연성이 아닌 재료의 경도를 측정하는 데 만족스럽지는 못하다. 그러나 이 측정방법들이 사용되어 왔고 이들의 한계를 숙 지한다면 관심을 가질 가치가있다. 표 5.13 유리 와M a결te 정r i a화 l 유리 의 押入硬度(IiT ensdt(e g nl) ot aa tdi oIn(H kKahgr na/dmor ndomenpse 2s s) s )( kDg. ,iPm . mH2. ) Glass-cerami c 9606 I 510000 661899 631 Glass-cerami c 9608 I 100 I 703 I 707 500 588 639 Glass 7900 100 I 532 I (96% sil ica gla ss) 500 477 Gl(alsos w 7 7e4x0p an sio n borosil ica te gla ss) 510000 481 I 44·2 Hig(h> 9a3lu%mAi hna 야 )c erami cs I 150000 I 11858300 I
표 5.13 에 유리와 결정화유리의 압자에 의한 경도를 실었 다. 결 정화유리의 경도는 고알루미나세라리보다는 작지만 유리보다는 매 우 크다. 이 경도값은 실험중 걸린 하중에 따라 어느 정도 좌우되 며 따라서 일정한 실험조건에서 경도를 비교하여야 한다는 접에 주 의하여야 한다. 결정화유리는 Knoo p경도 (SOO g 하중)가 180~300kg / mm 낀 회주철이나 150~2ook g /mm2 인 소둔한 스텐레스강보다 단 단하Li다2.0 — Si0 2 7 -l] 결정화유리의 열처리에 따른 압입경도의 변화에 관 한 연구가 A t k i nson 등 23) 에 의해 행하여졌다. 600°C 로부터 700°C 까지 의 열 처 리 에 따라 Vi ck ers 경 도에 약간의 중가가 보였 다. 900°C 까지의 열처리에 의해서는 경도가 약간 감소하였다. 최대경도는 확실하지는 않으나 결정화유리 중의 결정상이 최대체 적분율을 나타내는 것에 해당되며 미제구조효과가 경도에 영향을 준다고 생각된다. 결정상의 성질도 경도에 상당한 영향을 준다. 체 적분율이 작지만 존재하는 결정상의 일부가 경도를 매우 증가시킨 다고 할 수 있다. s pi nel 형의 상이 특히 효과적이다. (3) 摩託 및 摩滅 抵抗 결정화유리의 相對硬度를 조사할 때 더 실제적이고 신용할 수 있 논 방법은 표준조건하에서 결정화유리를 마모시켜 마멸된 양을 축 정 하는 것 이 다. 마모용 WC 로 하중을 걸고 재료의 평 면 (d i sc) 을 회 전시키도록 설계된 장치를 사용하여 비교실험을 한다. 이 실험에서 결마모정에화 유의리 해는 제높 거은 된 마재모 료저의항 을체 적나 을타 냈측다정. 한 시 결편과을, 5L0i02 00 0— 회 Z전nO시 — 킨S i0후 2 계 결정화유리는 18 젤스텐레스강보다 10 배 마모저항이 컸다. 미끄럼 (sl i d i n g)이나 회전에 의해 서로 접촉되어 제거되는 결정화 유리간에 일어나는 마텔 (wear) 의 가능성을 고려할 때 마찰이 일어 나는 정도가 중요하게 된다. 이런 이유 때문에 결정화유리 사이의 마찰계수를 알아야 한다. 표 5.14 에는 각종 결정화유리의 연마표면 사이에서 측정된 靜 및 動的 摩擦 係數를 실었다. 마찰계수의 차이는 결정화유리의 표면이 매끈하계 연마되었는가 에 따라서도 약간 달라진다.
표 5.14 결정화유리의 마찰계수 c0 efSf · IC i en t 。f f .ne ti。n Glass-cerami c type ta tic Dy nam.2 160714 Lit hi u m -zin c ·sil ica te ( l ow ZnO conte n t) 01090091 6 000 Lit hi u m ·zin c ·sil ica te ( hig h ZnO conte n t) Lit hi u m ·alumi no sil ica te 5.3 電氣的 性質 5.3. I 電氣比抵抗 (1) 一般考察 결정화유리가 전기철연체로 사용된다면 그 比抵抗 (res i s ti v ity)이 가능한 커야 한다. 대부분의 경우 절연체는 상온부근에서 사용되어 야 하나 어떤 장치에서는 고온에서 사용되어야 할 때도 있으며 고 온 사용시에는 온도에 따른 전기바처항의 변화가 중요하다. 傳導 (conduc ti on) 는 재료의 표면 또는 체적을 통해 일어나므로 전기절연을 定性的으로 평가하려면 표면비처항과 체적비처항 (volume res is ti vi t y) 울 알아야 한다. 표면비처항은 단위길이와 폭을 갖는 小片 表面 의 비저항으로 정의되며 단위는 ohm/cm 이다. 체적비저항은 단위단 면적을 갖는 군일한 봉의 단위길이당의 縱의 비저항으로, 단위는 ohm•cm 이다. (2) 表面比抵抗 전연체로 사용되는 재료에서는 표면을 지나는 漏電 (l eaka g e of curren t)이 체 적을 통과하는 누전보다 큘 경 우가 많기 때문에 표면비 저항은 중요하다. 이 효과는 多濕한 분위기의 실온에서는 특히 크 며, 표면전도는 분위기로부터의 습기흡착과 다른 재료들에 의해 크 게 영향을 받는다. 절연체의 표면이 젖으면 알칼리금속이온둘은 얇 온 물충에 용해되고 표면전도는 크게 증가한다. 이 효과는 소오다 석회유리나 비교적 알칼리함량이 많은 유리에서 득히 크다. 비슷하· 게 결정화유리에서도 표면비저항이 표면의 젖음과 알칼리금속이온~
울 함유한 물충의 형성에 의해 영향을 받을 것이다. 완전전조조건 하에서 측정한 표면비저항이 습기가 있는 조건하에서 측정한 값보 다 크기 때문에 실험조건이 중요하다. 결정화유리에 대한 표면비자 항의 측정은 별로 보고되 어 있지 않으나, 표 5. 15 에 L i 20 ― ZnO 一 S i 아계 결정화유리와 다른 재료들에 대한 표면비처항값들을 실었다. 표 5.15 20°C, 70% 相 對濕度 에 서 측정 한 각종 재 료의 표면비 저 항 Mate r ia l S(ouhrmfa sc ep erer ssisq t u i va ir tey) Glass-cerami c 1016 Borosili ca te electr i c a l gla ss 1011.1 Soda-lim e-sil ica -gl a ss 109.7 Glazed electr i c a l po rcelain 10” 결정화유리는 70% 습도하에서 높은 비저항을 갖고 있으며 유약 율 바론 전기자기 및 붕규산영전기용 유리보다 비처항이 높다는 것 을 알 수 있다. 물론 모든 결정화유리의 표면비처항이 높은 것은· 아니 며 결정 화유리 중의 잔유유리 상이 Na20 나 K20 와 같은 알칼리 금 속산화물을 다량 함유하면 낮아지나, 일반적으로 결정화유리는 전 기철연의 목적으로는 적합한 표면비처항을 갖고 있다. 고온표에면서비 처낮항은은 표 재면료누를전 을상 온필에요서로 사하용는할 경때우는가 있상다당.히 Li중2 0요-Z하n지0—만 S i O 레 결정화유리의 표면비처항을 700°C 까지 측정한 것이 표 5.16 이다. (3) 體積 比抵抗 표 5.16 L i 20-ZnO-S i 0 2 계 결 정 화유리 의 표면 비 저 항에 대 한 온도의 영향 Temp e ratu re (°C) S(ouhrmfa sc ep er er ssisq t ui va ri te y) 100°c 1015.4 300°c 1010 .2 500°c 108.1 700°C 101,3
일반적으로 결정화유리는 유리와 일반용 세라믹스에 비해 좋은 전기절연체이다. 이것은 800 ° C 까지의 전기비처항을 나타낸 표 5. I7 의 데이타로부터 알 수 있다. 죽 결정화유리는 다른 우수한 절연체 와 비숫한 비처항을 갖고 있다. 산화물유리 및 세라믹스의 체적전도도 (volume conduc ti v ity)는 보 동 재료를 통한 이동이온의 輸 送(t rans p o rt)에 의해 일어난다. 그러 나 유리, 제라믹스 및 결정화유리의 수송과정은 電 子 또는 正孔 (pos iti ve hole) 의 수송에 의한다. 결정화유리는 대부분 이온전도이므 로 이 과정에 대해 주로 설명하겠다. 유리와 세라믹스에서는 이동알칼리 양이온(예 ; Li+ , Na 기이 전도 과정에 크게 기여하며 유리의 전도도는 알칼리금속산화물 함량이 증가하면M a갑te자 r i기a l 커진다. I알칼2 0리°c금 I속 양2L0o0이g° 이온re 이sis4 i0t 0i전v°Ci t도 yI 도 a6t에 0 : 0° 이상 당8 。한。 。 c영 표 5.17 결정화유리와 다른 재료들의 電 氣比抵抗 I G(al)a saLs-tiect he triy ua pmm e·i aclsu mi no sil ic· 13. 7 8. 5 5.3 4.1 I (b) ctLyoipnt hte; ei un mlto -wz(c in. Z c5 n-%Osi )l ica te 15.5 11. 5 7.7 5. 0 3.7 (c) ctLyoiptn hete i : u n mht i-z갱in cZ -3ns0iO%l i c)a te 13. 8 6.7 4.7 4.2 (d) sLili it chai ut e m -zin c -lead 10,9 8.5 Glasfe s (a) Soda-li m e-sil ica gla ss 6.9 4.2 2.7 (b) gAlal ksas li -le ad-s i l ic a te 11. 0 6.9 3.9 2. 5 (c) Lboorwo siloli scsa tee l e gcltar si cs a l 9.8 6.8 4.4 Cerami cs (a) H(9i5g % h Aalluzm03i) n a cerami c 15. 3 11.9 9.3 7. 8 6.9 (b) Hig h ten sio n po rcelain 13. 7 8.6 5. 5 4.2
향을 미치는 것은 결정화유리에서도 마찬가지이다. 이온의 이동도 (mob ility)는 이온이 이동하는 구조에 크게 좌우된 댜 결정에서는 름새자리를 나온 이온이 더 낮은 에너지를 갖는 인 접자리에 들어가기 위해서는 높은 에너지를 갖는 중간 위치를 통과 하여야 한다. 일정 온도에서는 이 에너지장벽을 넘어 빈자리에 이 동하기에 충분한 열에너지를 갖는 이온들의 비율은 일정하다. 따타 서 이동이온돌은 제멋대로 움직이나 직류장이 작용하면 全移動은 직류장구배방향이 되어 전도가 일어난다. 유리에서는 유리구조의 불규칙성 때문에 에너지장벽이 일정값을 갖고 있지 않다는 차이 이의에는 비슷한 과정이 일어난다. 유리에 서의 평군에너지장벽은 더 큰 이동도를 갖는 알칼리금속이온으로 된 결정보다 낮아 같은 조성의 결정보다 전도도가 더 크다. 전도를 결정하는 중요한 인자들 중에서 이동도는 유리가 결정화 될 때 영향을 받는다. 보통 이동도는 유리가 결정화될 때 감소되며, 따라서 유리구조가 결정질상으로 전환될 때 전기바저항은 커진다. 결정화유리의 전도도에 영향을 주는 다른 인자로는 相境界의 존 재이다. 상경계는 이온의 운동울 방해하며 특히 경계응력이 존재하 떤 전도도는 더 작아진다. 유리와 결정에서 이온전도는 온도가 높아지면 급격히 커지며 전 도도의 온도의 존성은 다음과 같이 주어 진다.
 a=(] 。 ex p (-E/R T ) (5-9)
a=(] 。 ex p (-E/R T ) (5-9)
여기서 %는 온도에 크게 좌우되지 않는 항이며 E 는 전도의 활성 화에너지이다. 따라서 lo g a( 또는 log p, 비저항)對 철대온도의 역수를· p lo t하면 직선이 얻어지며 그 기울기가 E 가 된다. 이런 형의 곡선은 그림 5.10 에서, 유리로부터 결정화유리로의 전 환이 전기비처항을 감소시킨다(전기저항은 중가)는 사실을 확인시켜 준다(곡선 A 와 B). 결정화유리의 체적비저항은 20~400°C 에서는 母 유리보다 적어도 4 배 더 크다. 대부분의 결정화유리에서는 이와 같 이 母유리보다 철연성이 좋아전다. 결정화유리에 대한 전도의 활성 화에 너 지 (23. 3Kca l/ mole) 도 유리 (19. 3Kca l/ mole) 보다 더 크다.
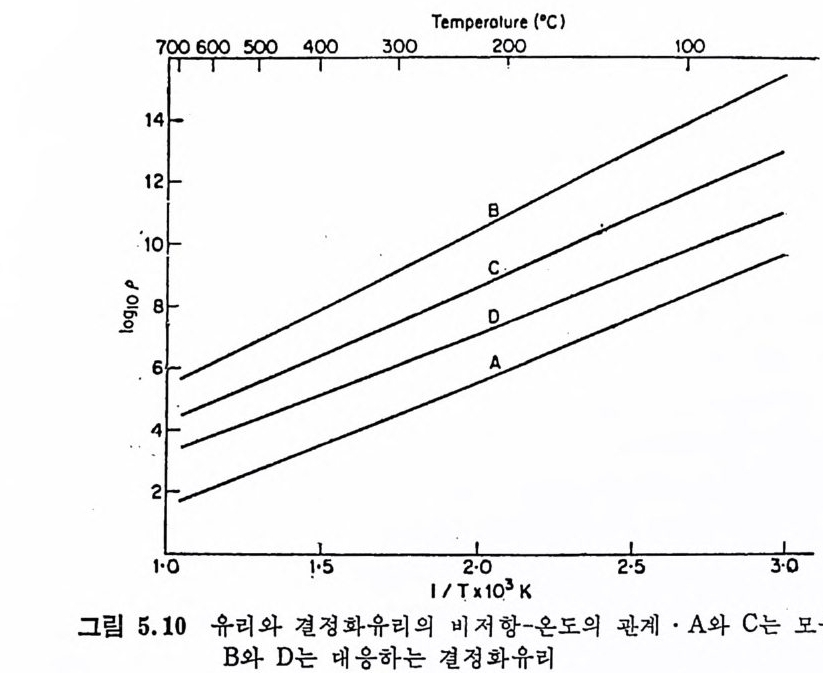 8 나广007 400 3?° Temp er a1t0u r0 e (•c ) 00T
8 나广007 400 3?° Temp er a1t0u r0 e (•c ) 00T
활성화에너지 E 의 증가가 비저항의 아주 큰 증가를 충분히 설당 하지는못한다. 온도와비처항 a 를 관계맺는 식에서 지수앞의 항인.
![]() (]= e2A2n 기 2kT (5-10)
(]= e2A2n 기 2kT (5-10)
이 석에서 i는 이온의 도약거리, n 는 단위체적당 원자의 수, IJ는 우물 (well) 안에 있는 이온의 전동수이다. 이동 Li+의 결정간 유리 상의 고갈(즉 n 의 감소)은· 지수 앞의 항의 증가에 해당된다. 이 결정 화유리에서는 강하게 결합되어 있는 리듐 석 규산영결정 중에 Li+ o ] 다 량 혼입되어 있어 전도도에 약간의 기여만을 한다. 전기전도도를 크게 증가시키는 것은 알칼리이온이 결정상 중에 혼입되어 있는 다론 결정화유리에서도 관찰된다. 그러나 알칼리이 온이 결정상 중에 고정되지 않는 경우에는, 결정화의 효과는 찬유유 리상 중의 알칼리금속이온의 농도를 증가시킨다. 이 경우 결정화유 리의 비저항은 모유리보다 작아진다. 그림 5.10 의 유리에 대한 곡-
선 C 와 대응하는 결정화유리에 대한 곡선 D 가 그 예이다. 이 결정 화유리 는 소량의 Na20 몰 함유한 ZnO ― Al203-S i 02 형 이 다. 이 경 우 결정화유리로의 전환에 대한 비저항의 감소는 전도의 활성화에너치 가 17.2 로부터 15.4Kcal/mole 로 감소된 데 그 원인이 있다. 왜냐 하면 지수항 앞의 %는 실제로 동일하기 때문이다. 이런 형의 거동 은 비교적 드물다. 즉, 더 일반적인 효과는 결정화유리의 비저항아 모유리보다 훨씬 더 크다. 화학조성과 존재하는 결정상의 성질에 따라 결정화유리의 전기비 처항은 크게 달라진다. 예를 들면 300°c 에서의 비처항은 106~1012- ohm•cm 범위에 있다. 그림 5.11 은 각종 결정화유리에 대한 비저항 n손it 도e (의 Zn Al관04계) 를와 나w타i ll낸em i것 te이 ( Z다n.2S i곡0 4 선) 인 AZ 는nO 주— 결Al성2 장03이-S i0약 2 간결의 정 화ga h운-
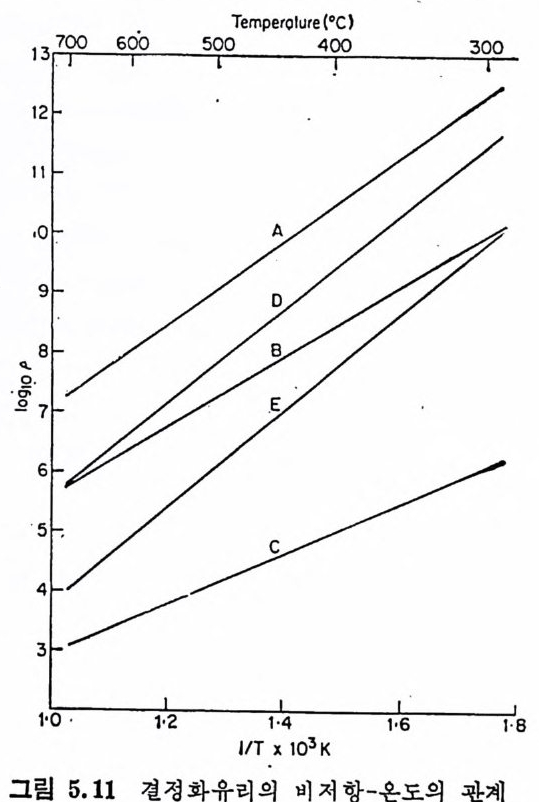 13 700 6OO 500T emp er olure4 (°0C0) 300
13 700 6OO 500T emp er olure4 (°0C0) 300
리이다. 300°C 에서 이 재료의 비저항 (2XI012chm•cm) 은 유리상실 리카 (I011ohm•cm) 보다 크기 때문에 매우 우수한 전기철연체이다. c저o r항d i을 er it갖 e 고형의 있 다알.칼 만리일가 소없량는의 결 N정a2화0유 가리 도Zn O비— 슷A하l2게0 3 — 높Si은0 2 전결 기정 비화 유리 중에 도입 된다면 Na20 를 각각 1 및 2Wt % 함유한 결정 화유리 에 대한 그림 5.11 의 B 및 C 곡선에서와 같이 비처항이 상당히 감 소한다. 이 경 우 Na+ 는 찬유유리 상 중에 농축되 어 있고 Na 2 0 의 소 량 첨가가 상당히 큰 효과를 준다고 생각된다. LI2O 를 다량 함유한 결정화유리는 예측한 것과 같이 비교적 낮은 전기비처항을 나타낸다. 그립 5.11 에서 D 곡선은 주결정상으로 (3- sp o dumene/sili ca 고용체 를 함유한 처 팽 창 결 정 화유리 에 대 한 것 이 며 300° C 에 서 의 비 저 항은 105ohm • cm 이 다. 주결 정 상으로 (3- eucryp tite 룰 함유한 결정화유리에 대한 J ohnson 둥 2 6) 의 연구에 의하면, 이 재 료는 비교적 높은 전기전도도를 갖고 · 있다. 300°C 에서 이 재료의 비처항은 l05ohm•cm 였다 . 이 결과는 유리상으로부터 전도도에 대 한기여는결정상으로부터의 기여보다 크며, 입계효과가 중요하다는 것을 나타내고 있다. 30mole% 의 L i 20 를 함유한 결정화유리에 대한 A t k i nson 둥 23) 의 연구에 의하면, 전기비처항은 사용된 열처리공정에 크게 좌우되었 다. 600~900°c 에서 결정화의 열처리를 하고 300°C 에서 전기비처 항을 측정한 결과 750°C 에서 열처리한 시편이 10Gohm•cm 로 최대 값을 나타냈고 전도의 활성화에너지도 제일 컸다. 미세구조의 분석 결과 750°C 부근에서 결정상의 체적분율도 최대였다. 지금까지 논의한 바와 같이, 대부분의 결정화유리에 대한 비저항 의 對數와 철대온도의 역수와의 관계를 나타내는 곡선들은 넓은 온 도범위에서 칙선에 가까와 1 개의 활성화에너지를 갖고 있다. 그러 나서 그2 직림선 이5. 12교 중차의한다 곡.선 Z Cn 는O 를 예 약의 이1다5.W t %곡 선함 유C 에한서 L는i2 02 —4 0Z~n2O5 —0 °SCi 0에 2 형 인 이 재 료는 주결정 상으로 cris t o b ali te 를 갖고 있으며 비 저 항-
26) R. T. Joh nson, B. Morosin , M. L. Knote k and R. M. Bie f e ld , Phys . Lett . , 54A, 403Clr:t l5) .
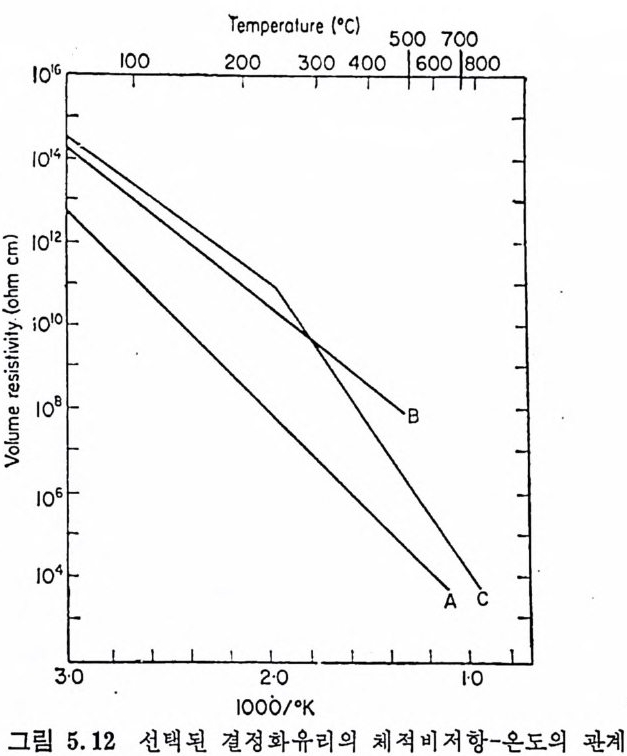 10'6 100 2T0eIm 0p er at3u r0e 0 ( °C4) 00 50| 06 0 이70 800 0
10'6 100 2T0eIm 0p er at3u r0e 0 ( °C4) 00 50| 06 0 이70 800 0
온도의 불연속은 220~270°C 사이에서 일어나는 a 꿉 c ri s t obal it e 전 이와 깊은 관계가 있는 것 같다. 전기전도도를 낮추기 위해서는 결정화유리 중에 알칼리금속이온 의 함량을 적게 하는 것이 필요하다고 강조하였지만, 어떤 경우에는 알칼리금속이온의 첨가를 피할 수 없을 때도 있다. 예를 들면 이들 의 존재는 ' 특정열팽창계수를 얻는 데 필요할 수도 있다(결정화유리가 금속에 봉착되는 경우). 이 경우, 母유리 중에 비교적 이동도가 나쁜 Pb2+ 이 나 Ba2+ 를 다량 첨 가하면 전기 비 저항이 상당히 증가할 수 있 다. 결정화유리 중의 찬유유리상에 농축되는 경향이 있는 이들 이 온은 알칼리금속이온의 이동을 방해하기 때문에 결과적으로 이온전 도도를 감소시 킨다. 그림 5. 11 중의 곡선 E 는 L i 2 0-를 약 25mole%, PbO 도 함유한 결정화유리에 대한 것으로 300°C 에서 3x109ohm•cm - 로. 비교적 높은 비저항을 나타낸다.
제어된 전기전도도를 필요로 할 경우에는 전극부근에서 이온을 · 운반하는 전류가 소모되어 分極이 생기기 때문에 이온전도를 하는 재료를 사용하는 것은 바람직하지 못하다. 물론 半導電性 결정화유 리는 이 현상을 나타내지 않는다. 이런 재료들은 그 자신이 반도체 인 적어도 1 개의 결정상을 함유하며 이 상은 결정화유리 전체에 연 속적인 망목을 형성하기에 충분한 높은 농도로 존재하여야 한다. 반도전성 결정화유리 가 12 %의 Fe203 를 함유한 칼슘붕규산유리 로 부터 제조되었다. 이 조성의 유리를 800°C 에서 열처리한 결과 실 온에서의 체적비처항이 106ohm•cm 로 크게 감소하였다. 이 높은 전기전도도는 Fe304 결정의 상호연결된 망목의 형성 때문이다. 어떤 경우에는 결정화유리 중에 반도성결정이 무의석중에 촌재 하며 기대하지 않은 높은 유전손실로 바람칙하지 못한 결과를 일으 키기도 한다. 5.3.2 誘電性質 (1) 誘電損失 ' 전기장이 유전체에 도달하면 전기에너지가 유전체내에 저장되고, 전기장을 제거하면 에너지가 전부 회수될 수 있으나 보통은 일부의 에너지만이 회수된다. 즉, 전기에너지의 일부는 열로 손실된다. 따 라서 교류장에서 철연체는 전력손실을 일으킨다. 전기에너지의 회 수할 수 없는 양과 회수할 수 있는 양의 비를 t ano( 損失因子) 또는 力率(p ower fac to r , cosO=cos(90°-o) )로 나타낸다 .. 유전손실은 재 료 · 의 誘電率(p erm itti v ity or die l ectr ic consta n t) K 에 좌우되며 誘電損 失率은 유전율과 손실인자룬 곱한 Kt ano 로 주어진다. 철연체가 고 주파철연에 사용된다면 낮은 유전손실이 필요하며, 이 목적으로는 온도상승에 따른 t ano 와 K 의 값이 크게 증가하지 않아야 . 한다. 물론 이 조건은 절연체를 고온에서 사용할 때 필요한 것이나, 보통 온도에서 사용할 때도 역시 필요하다. 왜냐하면 유전체의 열에 의 한 손실을 피할 수 없기 때문이다. 유리와 같은 유전체에서 에너지손실의 원인은 다음의 3 가지깃 L ql 다.
a) 이온이동손실 b) 공명형의 이온전동손실 c) 망목이나 격자의 변형과 관련된 변형손실 이들 중에서 이온이등손실은 전자공학에서 사용되는 주과수 범위 에서는 가장 중요하다. 이온전동손실과 변형손실온주과수가 1010 주 기 / 초 이하에서는 중요하치 않다. 유리에서 손실인자 t ano 와 전기 비처항 사이에 상호관계가 존재하며 이것은 유전손살이 이온이동과 정과 관련된다고 생각된다. 따라서 유리에서 중간 주과수범위에서 의 유전손실은 이동이온 (mob i le i on) 에 의한 것이 대부분이다. 이들 이온에는 알칼리금속이온이 있으며 다음과 같이 양이온의 이동도 에 따라 유전손실이 증가한다. Rb 七 ➔ K+-+Na~L i+ 이들 이온의 이동도는 유리의 망목구조에 의해서도 영향을 받으며, 구조가 더 개방적이고 약한 걷합의 망목으로 변화되면 유전손실은 증가하게 된다. 유전손실은 듬새자리를 점유하는 다른 修 飾 陽 이온 에 의해서도 영향을 받으며 특히 Ba2+, Pb+ 과 같이 큰 이온들은 이 동알칼리금속이온들의 운동을 방해하기 때문에 유전손실을 감소시 키는 효과가 있다. 결정화유리에서는 이 현상이 유리보다 복잡하며 각종 결정상과 화학조성이 확실치 않은 찬유유리상의 정확한 효과 를 파악하기 는 어 렵 다. 單結 晶의 유전손실은 작으며 주로 소량의 불순물에 의해 결정된다. 결정화유리 중의 유리상이 유전손실에 주 로 기여하는 것 같다. 이것은 찬유유리상의 양이 가능한 작아야만 유전손실이 작으며 유리상의 조성은 알칼리금속이온이 다량 존재하 지 않도록 제어되어야 한다는 것을 의미한다. 화학성분의 효과 이의에도 유리에서와 같이 결정화유리의 유전손 실은 측정되는 주파수와 온도에 따라 변화된다. 유전손실의 온도의 존성은 주파수보다 매우 작지만 온도가 상승하면 유전손실이 보통 증가한다. 알칼리금속이온이 결정상 중에 고정되는 경우, 유리의 결정화에 • 따른 손실인자의 현처한 감소는 3 장에서 이미 설명하였다. 이 효과
표 5.18 1MHz 에서 측정된 모유리와 결정화유리의 손실인자, tan o. Tem(p°eC ra)t ur e Power fac to r , tan o Parent gla ss I Glass·cerami c 25 0,0400 0,0018 50 0.0562 0.0039 70 0.0835 0.0071 100 0.1450 。 •0087 120 0.2050 0,0101 140 0.4250 0.0147 는결 정표 상 으5. 로18 에L i2실 0 린•2 Si데0 2이 를 타 를갖 는보 면Li 2 더0 - A찰I2 0알a —수 S i0있 2 다형. 이 이다 . 재L료i2 는0 - 2주Si 02 결정 중에 Li+ o ] 고정되 면 그 이 동도는 상당히 작아쳐 유전손실 . 에 대한 기여가 감소된다.
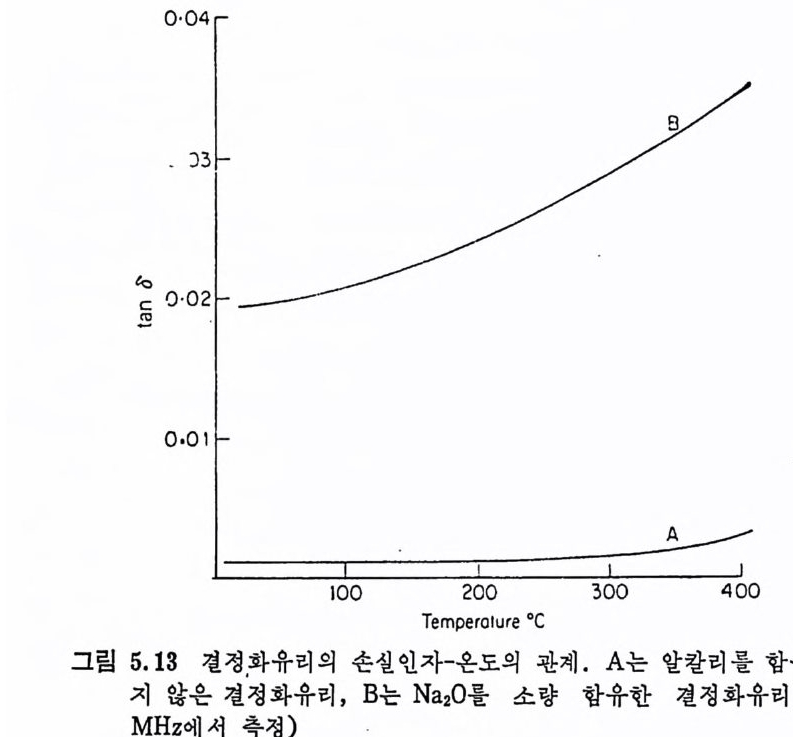 9~
9~
이동알칼리금속이온(예 ; Na+) 들이 결정상 중에 고정되지 않는 경 우에는 찬유유리상 중에 농축되어 결정화유리는 높은 유전손실을 · 나타내게 된다. 그립에 5.13 에 그 예를 나타냈다. 곡선 A 는 알칼리가 없는 ZnO 一 Al203 ― S i O 김정화유리에 대한 것 으로, 이것의 손실인자는 작으며 온도상승에 따른 영향이 크지 못 하다. 곡선 B 는 같은 조성과 같은 결정상 (w ill em it e 와 g ahn it e) 을 힘 유하나 Na20 가 2% 함유된 결정화유리에 대한 것이다. 이 경우에 는 손실인자가 거의 2 배 크며 온도상승에 따라 손실인자가 상당히 증가하고 있다. 표 5. 19 에는 각종 결정화유리와 다른 재료들의 유전성질에 대한 데이타를 실었다. 측정한 주파수에서 결정화유리의 유전손실률(l oss fa c t or) 은 낮은 유전손실물을 갖는 제라믹스와 비슷하다. 이 결정화 유리는 L i 20 를 거의 10Wt % 함유하고 있으며 다른 수식산화물이 촌 표 5.19 1MHz, 20°C 에서의 결정화유리와 다론 재료들의 유전성질 Mate r ia l I fPataocnw too e r r I P erm1•Kt t 1 •v itYI Kfa Ltcoa tnso sor Glass-Cerami c LLL iii 222 000 —— - A MZIn2gO O아— — - SSSi0i 0i 20 2 (2 c . 5%Zn0) 00o.,. 000000221328 655...604 o0o... 000111111599 L i 20 ― ZnO 一 S i 02(c.10% ZnO) 0.0013 6.0 0,0078 LLiiz2 0O — - ZZnnOO --PSbiO Oi (— c.S 3i0 o2 % Zn0) 00.,00006033 55..38 00..00031374 Glasses Fused sil ica 0.0002 3.78 0,0008 Borosili ca te low loss 0,0006 4.0 0.0024 Soda-li me -sil ica 0.0090 7.2 0.0648 Cerami cs High alumi ni a ( c. 95%Alz03) 0,0004 8.8 0.0 0 35 Ste a ti te type o. 0013 5.9 0.0077 Forste r it e type 0.0003 6.3 0.0019
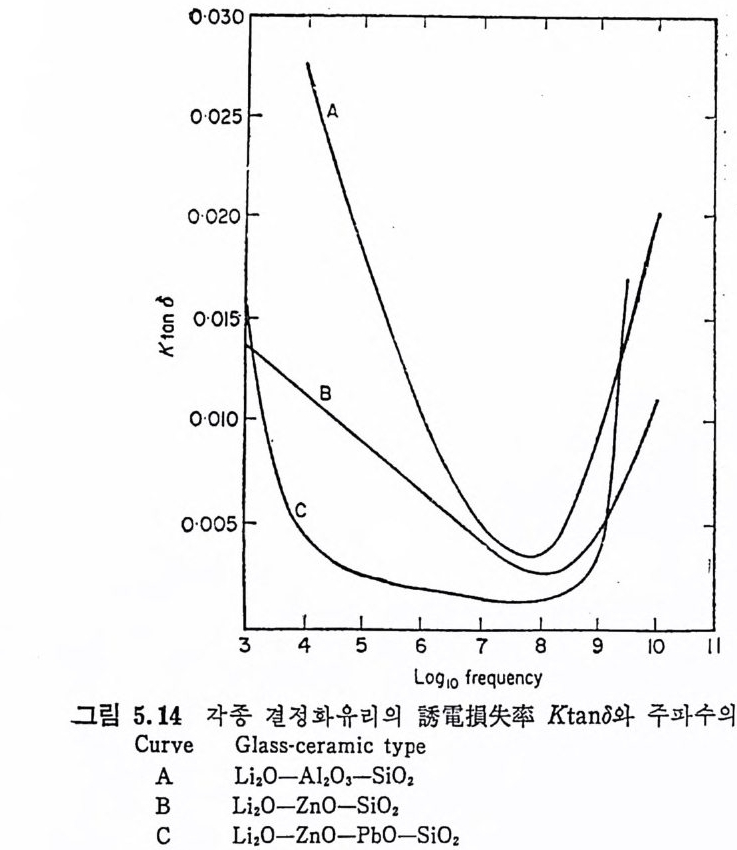 0·0 3 0
0·0 3 0
재하면 유전손실에 큰 영향을 준다는 것을 알 수 있다. 특히 PbO 가 함유되면 유전손실이 매우 감소되 며 이 것은 Pb2 + 이 찬유유리 상 중의 L i+의 전동운동을 방해하기 때문이 다. 알칼리금속이온들을 함유한 결정화유리의 유전손실은 그림 5.14 에 나타난 것과 같이 주파수에 크게 좌우된다. 여기서는 모든 재료 둘이 L i 20 를 거의 10Wt % 함유하고 있다. 모든 재료는 L i+운동에 기여할 수 있는 低周波數에서는 바교적 높은 유전손실물을 나타낸 다. 유전손실은 109Hz 이 상의 주파수에 서 상당히 증가한다는 것 도 . 확실하다. 모든 재료가 106~108Hz 에서 최소유전손실을 나타내나, PbO 를 함유한 조성(곡선 C) 은 104~109Hz 의 넓은 주파수범위에서 낮은 유전손실을 나타내고 있다는 것에 주목하여야 한다. 이 특성
은 유리상 중에 비교적 이동성이 아닌 Pb2+ 의 존재 대문이라고 생 각된다. 주파수에 따른 유전손실률의 변화는 이들 재료의 유전율 (K) 이 주 과수에 약간만 좌우되기 때문에 주로 tan o 의 변화 때문이라는 것 에 주의 하라. 따라서 곡선 B 로 나타낸 재 료에 서 104, 106 및 109Hz 의 주파수에 대한 유전율은 각각 5.2, 5.0 및 5.5 이다. McMi llan 둥 27) 은 ZnO 가 Cao, M gO 또는 BaO 로 일부 치 환된 ZnO ― Al203-S i 02 결정화유리의 유전성질을 조사하였다. BaO 를 함 유한 재 료는 105~ 1010Hz 의 주파수에 서 tan o 가 20 X 10-4 보다 작 은 값을 나타내어 특히 주목할 만한 것이다. 그러나 BaO 함량이 증 가하면 ta n o 對 주파수에서의 곡선 p eak 가 접차 처주과수 쪽으로 이등하였다 (BaO 를 함유하지 않은 재료의 101 · 2Hz 로부터 BaO 룹 10.6mole % 함유한 재로의 10MHz 까지). 이들 재료. 중의 찬유유리상이 유전손 실에 주로 기여하며 BaO 첨가에 대해 관찰된 효과는 저주파수에서 이온공명손실이 최대로 되기 때문이라고 생각되었다. 이것은 생성 된 결정상의 성질에 큰 변화가 검출되지 않았기 때문에 유리망목의 구조에 BaO 가 첨가된 결과가 원인이라고 생각된다. 결정상의 평군크기와 체적분율에 기준을 둔 결정화유리의 미세구 조가 유전손실의 크기를 결정하는 데 중요한가를 조사하는 것도 홍 미있는 일이다. Tash i ro28) 는 감광성핵생성 (Au) 유리, 득히 Li20 -Al2 03 ― S i 02 형에 대한 tan o 를 측정하였다. 그는 열처리전의 자의선방 사의 노출시간을 변화시켜 결정크기를 2 배로 변화시켜도 tan o 의 값은 영향을 받지 않는다는 것을 알았다. 이 유리는 동일한 열처리 를 받기 때문에 620°C 에서 열처리한 시편의 결정상 L i 20•S i 02 의 체적 분율은 일정 하다고 생 각된다. 비 슷한 결과는 /3- sp o dumene 과 /3- euc- r yptit e 결정상이 형성된 다른 결정화유리에서도 나타났다 .• 그러나 fi-e ucryp tite 결 정 울 주로 함유한 결 정 화유리 가 (3- spo dumene 결정 을 주로 함유한 것보다 유전손실이 크며 이들 재료에서는 유전손실 에 대한 결정상의 기여가 중요하다고 생각된다. 1MHz 주파수에서
27) P. W. McMi llan and G. Partr i d g e , J. Maler. Sc i. , 7, 847(1972). 28) M. Tashir o , Glass Industr y , 428(1 9 66).
/3_ eucry ptite 의 tan o 값은 /3- sp o dumene 보다 10 배 크며 이 것 은 /3·- eucryp tite 결 정 화유리 가 높은 유전손실을 갖고 있 다는 것 을 나타내 고 있다. 평군결정크기의 변화가 손실인자(t an o) 에 큰 영향을 주지 못한다 는 사실은 P2°5 로 핵생성된 L i 2 0 ― S i 02 결정화유리의 유전성질에 대 해 열처리주기를 변화시켜 조사한 Har p er 둥 29) 의 연구에 의해 확 인되었다. 결정의 평군크기를 5~2ooµm 로 변화시켰으나 손실인자 에 별 효과를 미치지 못했다. 이들 재료에서 결정상 Li2 0 •2Si0 2 의 체적분율은 모든 재료가 같은 결정화의 열처리를 받았기 때문에 거 의 일정하다. 죽 , 평군결정크기의 변화는 핵생성온도 를 변화시킵 으로써 얻어진다. 앞에서 기술한 바와 같이 결정상의 체적분율은 잔유유리상의 양 과 조성을 결정하기 때문에 유전손실에 중요한 인자가 된다는 것은 · 확실하다. 이 것 에 대 한 실험 적 확인은 At ki n s on 둥 23) 에 의 해 주어 졌다. 그들은 Li 20 를 함유한 결정화유리의 손실인자가 750 ° C 에서 열처리하였을 때 최소값을 가지며 이 온도는 결정상의 체적분율이 최대가 되는 때이다. 결정화유리의 유전손실에 대한 一 般機構 는 이온의 이동과 관련되 지만, 목일한 경우 다론 과정이 중요하게 된다. T i 02 를 약 20% 함 유한 유리 로부터 제 조된 결정 화유리 에 대 한 Monneray e 둥 30) 의 연 구가 있다. 결정화되지 않은 유리의 손실인자는 1MHz 주파수에서 20X10-4 보다 작았으나, 이 유리로부터 제조된 결정화유리의 손실 인자는 3000X 10-4 으로 매우 컸다. 이 높은 값은 결정화유리 중에 촌재하는 티탄산영 중의 산소부족으로 형성되는 非化 學量 論的인 半 導電 性 때문이다. 티탄산영 중에 3 가이온이 고정되어 전도도를 감 소시킨다는 것을 알았으며, 따라서 Cr203 (Cr3+ )를 소량 첨가시킨 효과가 조사되 었 다. Cr2 야를 o. 04mole% 만큼 적 게 함유하면 손실 인자가 3300 X 10-4 에 서 18 X 10-4 으로 감소되 었 다. Fe203 의 소량도.
29) H. Harpe r , P. F. Jam es and P. W. McMi llan , Di sc uss. Faraday Soc. , 50, 206(1970). 307) 0M(1 9. 6M8).o nneraye , J. Serin d at and C. Jou wersma, Glass Technol. , 9.
티탄산영걷정을 함유한 결정화유리의 손실인자를 감소시키는 비슷 한 효과가 있다. 이 성질에 대한 연구에서 비화학량론적 결정이 형 성될 수 있는 가능성이 있는 경우, 모유리의 산화상태를 조십스럽 게 제어할 필요가 있다. 유전손실은 온도가 상승하면 상당히 커질 수 있으며 알칼리금속 이온의 이동효과가 중요한 저주파수에서는 특히 영향이 크다. 고주 파수 (~1000MHz) 에서는 온도상승이 유전손실에 작은 효과밖에 주지 못한다. 각종 결정화유리에 대한 이들 특성을 그림 5.15, 16 및 17 에 예시하였다. 그림 5. 17 의 재료는 명 목상으로는 알칼리 가 없으나 불순물로 알 칼리 금속이 충분히 농축되 어 있 다고 추측된다. • 알칼리가 없는 일부 결정화유리는 10000MHz 주파수에서 손실인 자의 온도의 존성 이 대 우 작게 나타났다. 예 를 들떤 BaO 나 SrO 를
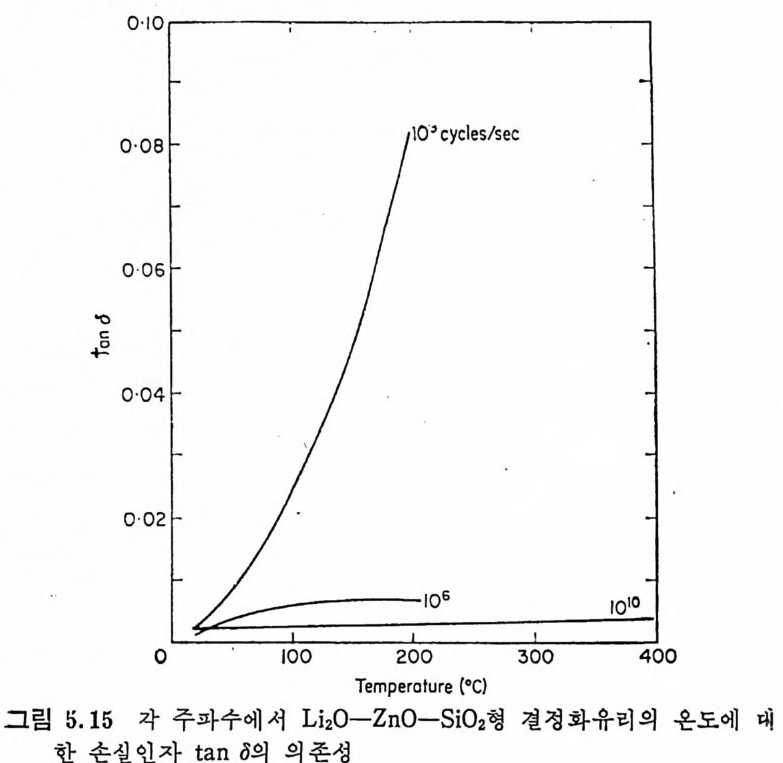 0·1 0
0·1 0
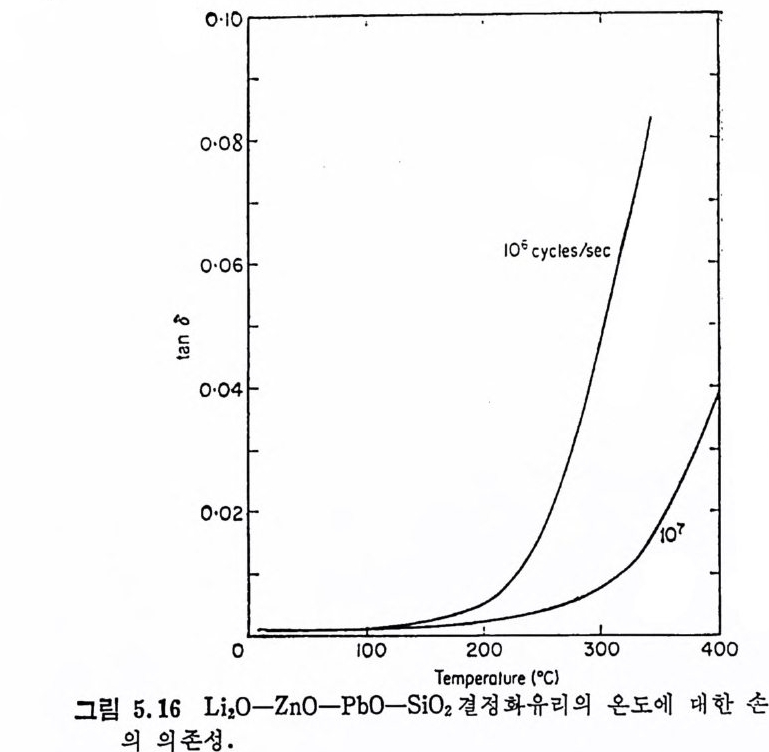 0·1 0
0·1 0
함유한 ZnO ― Al203 ― S i 02 형 결정화유리는 4009C 에서 손실인자가 단지 8X 10-4 이었다. (2) 誘電率 유전율 또는 유전상수는 유전체 중에서 생건 전기에너지와 전공 중의 전기에너지의 比를 나타낸다. 지금까지 본 것 같이, 실온에서 대부분의 결정화유리의 유전율 (K) 은 5~6 사이이며(표 5,19), 이 값 들은 측정된 주파수에 크게 영향을 받지 않는다. 처주과수에서는 유전율의 변화는 온도가 150°c 이상이 될 때까지는 벌로 변하지 않 지만, 온도가 더 높아지면 유전율이 증가한다. 매우 높은 주파수 (109~1010Hz) 에서는 유전울은, 온도가 400, 500°C 까지 상승하여도 . 거의 영향을 받지 않는다. 이 특성을 그림 5.18 과 19 에서 확인할 수있다. 재료가 고주파에서 철연체로 사용된다면 낮은 力率(p ower fac to r )
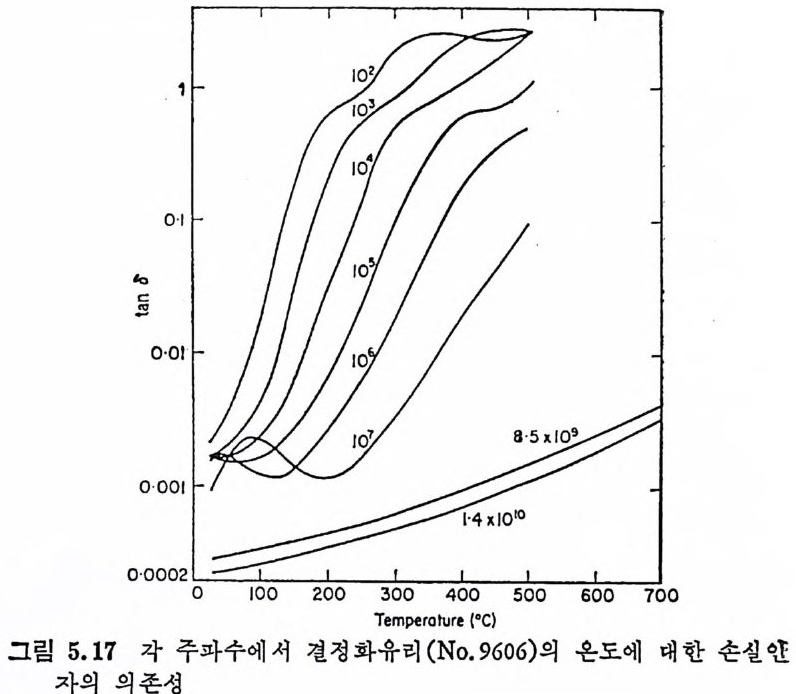 O·I
O·I
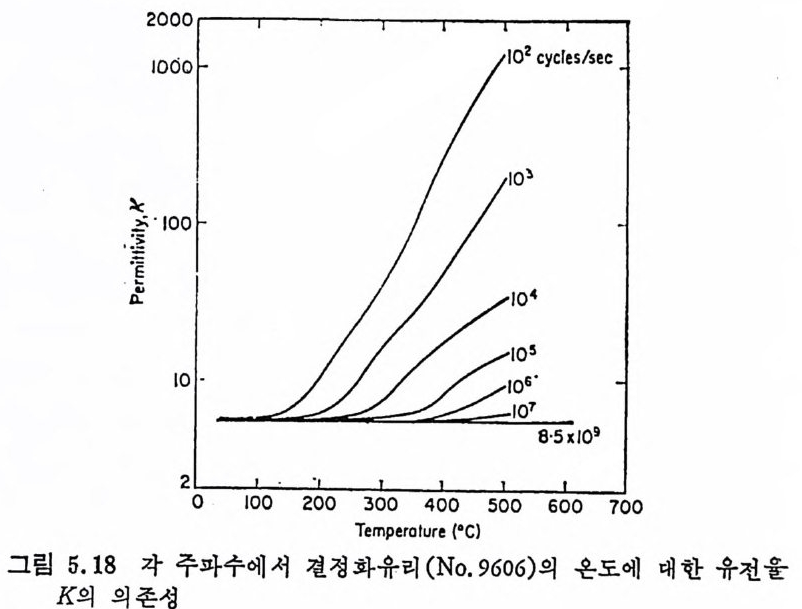 2000
2000
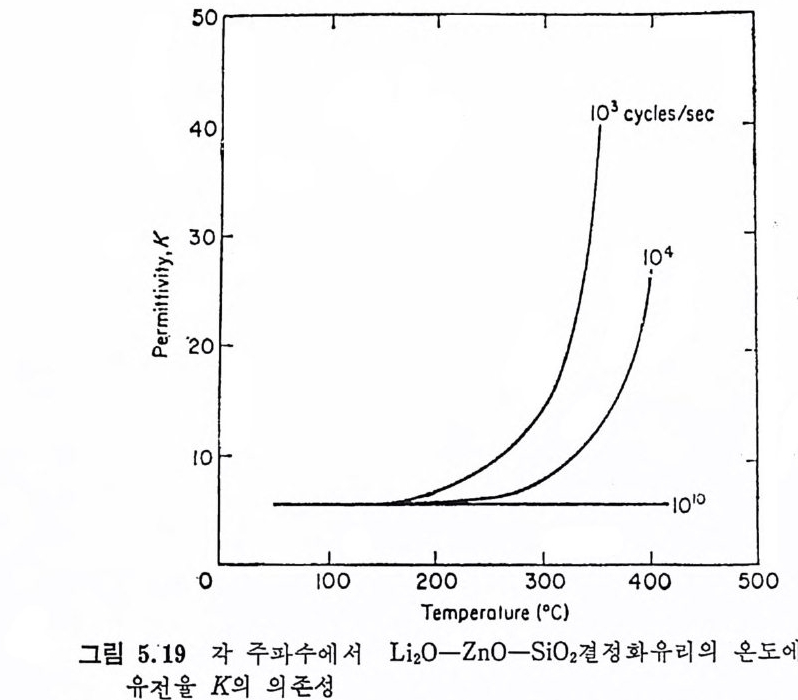 50
50
울 갖는 낮은 유전율이 필요하다. 어 떤 경 우에는 온도상승에 따라 가능한 유전율변화가 작은 것 이 요구된다. 처주파수에서 유전율의 증가는 이온이동도와 결정의 不完全移動 度(i m p erfec ti on mob i l ity)로부터의 기여의 증가와 관련된다. 또 고온 에서의 직류전도도 효과도 중요하다. 이들의 결합효과가 유전율을 급격히 증가시킨다. 온도에 따른 유전율의 변화에는 2 개의 인자가 작용하며 간단한 형태로 온도계수 4K 를 사용할 수 있다. 즉,
![]() L1K=Af ( K)+D tan o (5-11)
L1K=Af ( K)+D tan o (5-11)
여기서 K 는 유전울, D 는 상수, A 는 특정재료의 分極率(p olar i zab· ility)에 대한 온도의 영향을 나타내는 양이다. K<20 인 이온결정에 서 A 는 正이고 K>20 인 재료에서는 A 는 負이다. 유전율의 온도계수 4K 가 작은 결정화유리를 얻기 위해서는 tan 8 의 값이 작은 것이 필요하다. 또 A 가 負인 결정이 적당량 존재한
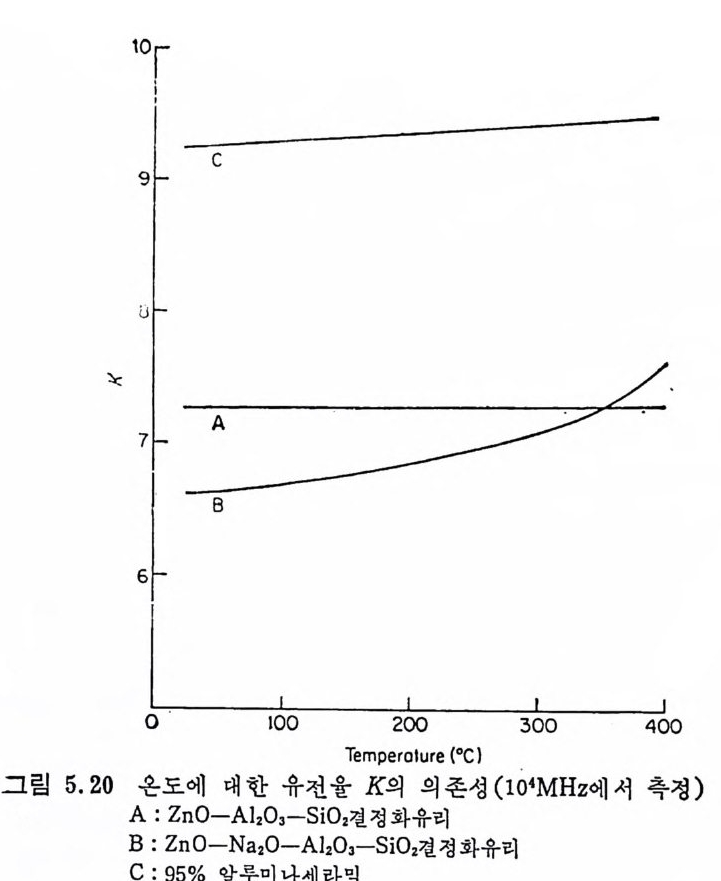 .' .。 r
.' .。 r
다면 Af (K)=D tan o 인 온도계수 O 를 갖는 재료를 얻을 수 있다. 그림 5. 20 중의 유전율국본도의 곡선은 10000MHz 주파수에 서 측 정한 것으로 t ano 값의 감소효과를 예시하고 있다. 곡선 A 와 B 는 기본적으로 같은 결정구조를 갖는 결정화유리에 대한 것이나, 곡선 A 로 나타낸 재료는 알칼리가 없고 困즌 Na20 를 2% 함유하고있다. 알칼리를 함유하지 않은 재료(곡선 A) 는 400°C 까지 유전율이 약 간밖에 증가하지 않으며 95% 알루미나제라믹이 유전율이 가장 크 다 . Na20 를 함유한 결정화유리 의 유전율이 작은 것 은 104MHz 에서 때알칼문리이가다 (1없50는X1 0-재4료).( t주 an결o=정18상X1으0로-4 )c 보or다 di e rti at en o를 의 함값유이한 훨M싼 gO — 크A기l2 03-S i 02 형 결정화유리에서 유전율에 대한 작은 온도계수가 언어질
수 있다. 104MHz 주파수 및 20~400°C 사이에서 유전윤의 변화는 4% 이 하이 다. BaO 를 함유한 ZnO ― Al203 ― S i 02 결 정 화유리 도 20~ 400 ° C 에서 유전율의 증가가 약 3% 밖에 되지 않기 때문에 작은 온 · 도계수를 나타낸다. 대부분의 결정화유리가 비교적 작은 유전율을 갖는다는 것이 薔 電器 (ca p a cit a t or) 를 제조하는 데 적합하다는 것을 의미하지는 않는 다. 그 이유는 고유전율을 갖는 특수결정화유리가 발전되어 왔기 때문이다. 고유전율, 낮은 역울, 고유전파괴강도 및 우수한 절연처항을 갖 는 결정화유리논 적당한 열처리기간중 强誘電性 相울 침전시킴으 . 로써 유리로부터 계조될 수 있다. 강유전성상(fe rroelec tri c p hase) 은 주로 일반식 이 AB03 인 pe rovskit e 형 이 다 . A 이 온은 주기 율표의 제 1,2,3 족으로부터 선덱하고, B 이온은 2~5 족 사이에서 선덱된다. BaTi0 3 이 의 에 이 형 의 중요한 화합물로는 NaNb03, CdTi0 3 및 다 론 니 옵산염 (nio b ate , xM20• y Nb2 야)이 있 다. 탄탈산염 과 지르콘 산영도 결정화유리 중에 강유전성 화합물로 촌재할 수 있다 . 이들 강유전성화합물의 산화물은 유리를 형성하지 않으므로 결정 화를 제어하지 전에 유리를 형성하는 다른 산화물을 함유하여야 한 、 다. 보통은 실리카 때로는 산화알루미늄인 유리성분을 가능한 소 량 첨가하여 강유전성상이 너무 희석되지 않도록 하여야 한다. 표 5.20 에는 고유전율 결정화유리의 성질 및 넓은 범위의 유전율 을 갖는 재료들의 예를 나타냈다. 표 5.20 25°C, 1KHz 에서 측정한 强誘電性 結晶相울 함유한 결정화유 리의 성질 Hi~ h pe rmi ttivi t y crys t a l ph ases | K P emit ti vti Y I t.aPn o woe(rp ef ar cc teo nr ,t ) SBoadriiuu m m ntiito ab na atte e, \.:admi um nio b ate 3307-52-059000 02. .15—- -42.. 04 Tung st i c oxid e 2100 120 SBoacdraiiduu mmm i uznm iiro c b ozanitrae c t,o e n, l aetlaee d a dn izo ibr ac oten ate , 216114 11..04
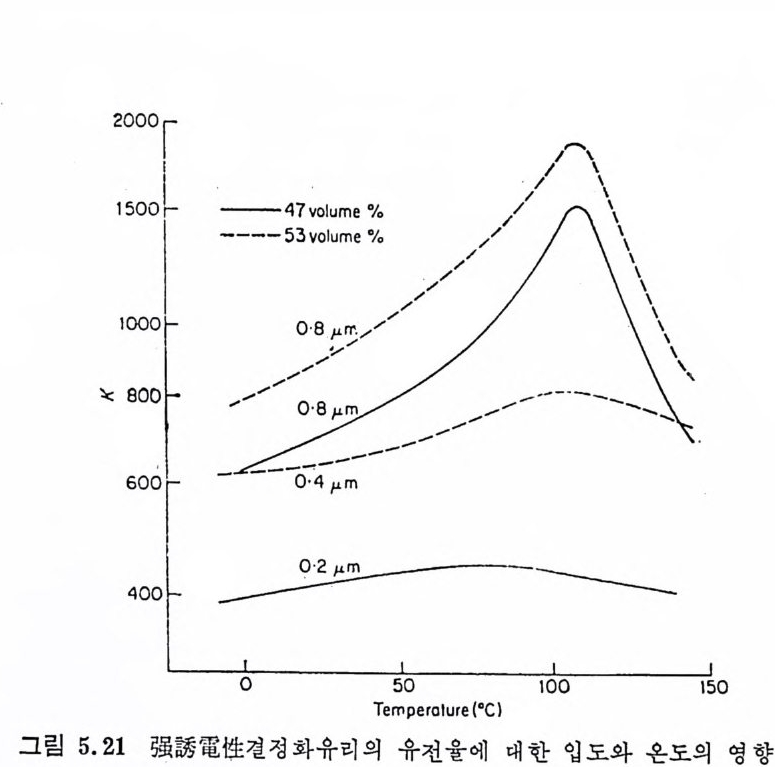 20010r5_0 0L 47volu m e % <
20010r5_0 0L 47volu m e % <
Layt on 둥 31) 은 이 들 재 료를 제 조하는 데 중요한 인자들에 대 해 기 술하였 다. 예 를 들면 Na20 — Nb203 ― S i 02 유리 에 서 S i아함량을 14 %로부터 2 7% 로 중가시키면 결정화유리의 粒度가 o.02µm 로부터 1µm 으로 점차 커졌다. Herczo g 32) 에 의 하면 BaT i O 퍼 결정화유리 는 입 도가 커 침 에 따라 유전율이 증가한다고 보고하고 있 다(그림 s. 21). 또 o. 2µm 의 입 도 에 서 , 유전율-온도의 곡선에 서 pe ak 가 사라지며 , 이 pe ak 는 强誘 電性 _ 常誘電性의 轉移點 울 나타낸다. 유전율에 영향울 주는 다른 안자는 강유전성상의 체적분율이다. 이 상의 체적분율이 60~80% 일 때는 결정화유리의 유전율은 순수 한 결정의 1/2~1/3 이 된다. 결정의 크기가 가시광선의 파장보다 작은 고유전율 결정화유리는 두명하다. 이런 재료에서의 결정들의 크기는 보통 5~50nm 이다.
31 ) M. M. Lay ton and A. Herczog , Glass Technol. , 10, 50(1969). 32) A. Herczog , J. Am. Ceram. Soc. , 41, 107(1 9 64).
Layt on 둥 m~ BaTi0 3 , NaNbOs 및 각종 1 및 2 가 양이 온을 함유 한 니옵산영 등을 함유한 강유전성 재료듈에 대해 보고하였다. Kokubo 둥 33) 은 강유전성 상으로 PbT i아를 함유한 두명 한 결정화유 리에 대해 연구하였다. 이들 두명한 고유전율결정화유리는 電場 이 작용하면 電氣一 光 學女力 果 (elec t roo pti cal eff ec t, 결정 의 굴철울이 전장에 의 해 변 화하는 현 상)를 나타내며 面-分極光線이 걷정화유리를 통과하면 분극면이 회전한 다. 보통 2 차전기-광학효과는 유도된 複 屈折 An 이 작용한 전장 E - 의 제곱에 비례한다.
 4n=2 4: -n3g K 2E2 (5-12)
4n=2 4: -n3g K 2E2 (5-12)
여기서 1 t은 굴철울, g는 전기-광학계수, K 는 결정화유리의 유전 울이다. (3). 誘 電 强度 전연체에 큰 전압구배가 걸린다면 터쳐(p unc t ure) 절연체는 파괴 될 것이다. 이 가능성이 고전압전연체의 설계시 중요한 인자가 된 다. 誘 電 破壤强度 (d i elec tri c break-down str en gt h) 도 에너지처장의 응 용에 사용되는 것과 같이 고전압에서 조작되는 축전기설계에 중요 - 하다. 철연체의 유전파괴는 2 가지 방법으로 일어난다. 첫째는 고유유전 파괴라는 것으로 電子가 원인이 되며, 두번째는 전기전도로 생기 는 국부과열에 의한 열파괴이다. 이 국부전도는 유전체에서 실제로 터침(p unc t ure) 이 생기는 곳에서 증가된다. 실제로는 이 두 효과를 분리하기는 매우어려우며 정밀한 실험기술을 갖고도얻어지는 값들 온 실제의 재료의 유전강도보다는 작다. 이 난접 이의에도 얻어지 는 실험값은 실험조건에 크게 좌우된다. 즉, 전극의 크기와 모양, 시편의 두께, 전압이 걸리논 속도 및 지속시간 등의 인자들이 영향 율미친다. 교류하에서 유전파괴강도가 측정된다면, 고주파에서는더 낮은 파
33) T. Kokubo and M. Tashir o , Bull. Inst. Chem. Res. , Ky o to - Univ . 54, 301(1976).
표 5.21 DIN 40685 에 의한 시편 을 사용하여 측정한 결정화유리와 일반 용 세라믹스의 誘電破城 强 度 ( 실 험주과수 50Hz, 온도 20°c) Mate r ia l I Dsite rl ee nctgr ti hc (bkreVa·k md mow) n Glass-Cerami cs Lit hi u m - zi n c ·sil ica te ( ZnO conte n t c. 5%) 47 Lit hi u m -zin c ·sil ica te ( ZnO conte n t c. 30%) 38 Lit hi u m -zin c -lead-sil ica te 28 Conventi on al cerami cs Hig h volta g e electr i c a l po rcelain 25 Hig h alumi na cerami cs (95 %A! i0, ) 14-23 괴강도가 관찰되기 때문에 주파수의 영향은 매우 크다. 따라서 실 험조건을 확실히 규정하고 표준설계의 시편을 사용하여야 한다. 코 . 로나放 電 (corona d i schar g e) 을 억제하기 위해 일정량의 기름 중에서 실험을 하며 보통 50 또는 60Hz 에서의 파괴강도를 조사한다. 결정화유리의 유전파괴강도는 일반용 세라믹스에 비해 크다. 이 예를 표 5.21 에 실었다. 이 결과들은 50Hz 주과수에서 독일표준 DI. N 4 0685 에서 주어전 치수의 시편에 대해 얻어전 것이다. 이 시편이 ASTM D 116-44 에서 제안된 다론 형의 시편보다 더 再現性있는 · 결과를 준다는 것이 알려져 있다. DIN 시편은 短絡(fl ashover) 을 방 一 지하도록 설계되었고 이 유전체의 두께는 1. 5mm이다. 결정화유리 의 유전강도가 일반용 세라믹스보다 큰 것은 일부 결정화유리 중에 閉 氣 孔이 전연 없기 때문이다. 기공률은 국부전장에 변화를 일으키 기 때문에 낮은 유전강도를 나타낸다. 매우 균질하며 微粒으로 된 결정화유리가 높은 파괴강도를 갖는 데 좋다. 5.4 熱的 性質 5.4.l 熱彰張 特性 (1) 一般考察 온도변화에 따라 생기는 치수변화는 여러가지 관점에서 매우 중 :
요하다. 예를 들면, 만일 결정화유리가 높은 열충격저항을 가지려 떤 재료내의 온도구배로부터 생기는 스트레인을 최소화하도록 열팽 창계수가 가능한 작아야 한다. 또 결정화유리가 다른 재료로 봉착 되거나 단단히 결합되려면 열팽창계수가 서로 아주 비슷하여 복합 된 부분이 가열되거나 냉각될 때 큰 응력이 발생하지 않도록 하여 야 한다. 어떤 응용에서는 온도변화에 따른 치수의 안정성이 중요 하며 이 경우에는 열팽창계수가 거의 0 인 결정화유리가 바람직하다. 결정화유리는 넓은 범위의 열팽창계수를 얻을 수 있기 때문에 좋 다. 국단적으로 負의 열팽창계수를 갖는재료가 얻어질 수있고, 다 른 조성의 것은 매우 높은 正의 열팽창계수를 갖기도 한다. 이들 2 극단적인 재료 사이에 열팽창계수가 실제로 0 인 결정화유리, 열팽 창계수가 보통유리, 제라믹스, 금속 또는 합금의 열팽창계수와 비 · 슷한 결정화유리들이 촌재한다. (2) 熱影眼係數에 미치는 化學成分 및 結晶型의 영향 결정화유리의 열팽창계수는 母유리의 열팽창계수와는 매우 다를 수 있다는 것을 앞에서 설명하였다. 결정화공정은 모유리의 열팽창 계수와는 보통 다른 열팽창계수를 갖는 상을 생성시키며 결정화유 리는 생성되는 결정상에 따라 더 크거나 작은 팽창계수를 갖게 된 다. 결정화유리는 複合材料이며 그 열팽창계수는 찬유유리상 및 촌 재하는 모든 상들의 열팽창계수와 탄성성질의 함수라는 것을 명십 하여야 한다. 따라서 결정장이 발달되면 보통 팽창계수에 큰 변화 가 생기고 결정화는 모유리의 조성으로부터 찬유유리상의 조성을 변화시키므로 결정화유리의 열팽창을 그 성분들과 관련지으려고 할 때는 이 접울 고려하여야 한다. 어떤 경우에는 찬유유리상의 조성 변화가 결정상의 발달에 의한 효과를 없앨청도로 큰 열팽창의 변 화를 가쳐온다. 그 결과 결정화유리와 모유리의 열팽창계수는 아주 비슷하게 된다. 이런 예는 매우 드물다. 더 일반적인 거동은 결정 화공정이 別個의 열팽창계수변화를 일으킨다. 결정화유리와 같은 복합재료는 열팽창계수에 대해 K i n g er y 34) 가 34) W. D. Ki ng er y, Intr o ducti on to Cerami cs , p. 478. Joh n W iley & Sons, New York (19 60) .
계 안한 熱擧動울 따른다고 생 각된다.
 으+으星+… ...
으+으星+… ...
여기서 ab 야는 열팽창계수, K1, K2 는 體積彈性率 (bulk modulus), -F1 , F2 는 성분의 중량분율이 다. 만일 Po i sson 比가 비슷하다면 체적란성률은 탄성률로 대치할 수 있다. 이 석은 각 성분의 수축이 全收縮 (overall con tr ac ti on) 과 같으 며 모돈 미세응력은 순수한 流體靜力學的 張力이나 壓縮 이라는 理 想擧動울 한다고 가정하고 있다. 결정상들의 체적분율과 그들의 물리적 성질을 알면 결정화유리의 열팽창계수를 추정하는 것이 가능하다. 한 가지 어려움은 잔유유리 상의 성질변화에 대한 적합한 허용치를 만드는 것이다. 그러나 결 정상의 체적분율을 전자현미경이나 정량회철분석을 통해서 상당히 정확하게 알게 된다면 찬유유리상의 조성을 추정할 수 있다. 이 정 보를 가지고 유리상의 近似性質울 加成關係式으로부터 유도할 수 있다. 결정화유리 중에 발달되는 결정들의 열팽창계수 를 표 5.22 에 실 었다. 이들 데이타는 대부분 S t u t zman 둥 35) 에 의해 주어전 것이다 이들 값은 異方性勅果를 평군화한 다결정질집합체에 대한 것이다. 결정화유리 . 중의 결정들은 보통 불규칙적으로 배향하기 때문에 주 어전 값들은 각종결정상들이 결정화유리의 열팽창계수에 기여한 것 으로 생각할 수 있다. 각종 결정형들에 의해 매우 넓은 범위의 열팽창계수를 나타내며 적당한 비율로 이들 상을 발달시킵으로써 제어된 열팽창계수를 갖 는 결정화유리를 만들 수있다. 따라서 저팽창결정화유리는 主相으 로 /3- eucryp tite, /3- spo dumene 또는 cordie r ite 를 함유하며 고팽 창
35) R. H. Stu t z m an, J. R. Salvagg i and H. P. Ki rc hner, An 'Inv esti ga ti on of the Theoreti ca l and Practi ca l Aspe c ts of the Thermal Exp an sio n of Cerami c Mate r ia l s, U. S. Dep t. of Commerce Of fice of Technic a l Serv· ice s (19 59).
표 5.22 결정화유리 중에 존재할 수 있는 結晶型 의 熱影服 係數 Crys t a l pha se Tchoeerfmf icaile ne xt( p° aC n-sIi)o n Liz O • A !z O JS i0 2 (Beta · eucryp tite) --6B46 Xx 1100--71 ((2200—- 110000 °0C°C) ) Ah03Ti0 2 (Alumi ni u m titan ate ) -19X 10-1 (25-1000°C) 2Mg 0 • 2Alz03 • 5Si0 2 (Cordie r it e) 6 X 10-7 (100-200°C) 26X 10-1 (25-700°C) Li2 0 •A I2 야 • 4Si 0 2 (Beta · sp o dumene) 9 X 10-1 (20-1000°C) • MCBaag OOO • • •A A S hhi0 O 야2 J •(• 2C2SSlii i0On 2o e((nCAsetnla sot iira t tne h ))i t e) 421B15 xXx 111 000---711 (((11200000-—1— 022000° 00C°°cc) )) Mg O •T i0 2 (Mag n esiu m titan ate ) 79x 10-1 (25-1000° C ) 2Mg O • Si0 2 (Forste r it e) 94 X 10-7 (100 一 20 9° C) CaO •S i0 2 (Wollasto n it e) 94 X 10-7 (100-200° C ) SLii00 2 • 2(SQi0u 2a r(tzL ) i t hi u m dis i l ica te ) 1ll1O2 X X 1100--17 ((220 0 —- 610000 °° C C )) 132 X 10-1 (20-300° C ) 237 X 10-1 (20- 600° C ) Si0 2 (Cris t o b ali te) 125 X 10-1 (20-100° C ) 500X 1 0-1 (20-300° C ) 271 X 10-1 (20-600° C ) Si0 2 (Trid y m i te) 175 X 10-7 (20-200° C ) 250 X 10-7 (20-200° C ) 144 X 10-7 (20-600° C ) 결 정 화유리 논 Li2 0 • 2Si0 2 , 석 영 또는 cris t o bali te 와 같은 결 정 을 다 량 함유하게 된다. 열팽창계수범위의 극단에 있는 결정상온 잔유유리상의 팽창계수 · 와 크게 불일치하게 된다는 접에 주의하여야 된다. 국단적인 열팽 창계수를 갖는 결정상을 덱하면 20°c 이상의 온도범위에서 負의 열 팽 창계 수를 갖는 유리 는 알려 쳐 있 지 않기 때 문에 /3- eucryp tite 는 · 찬유유리상과 팽창계수가 항상불일치하게 된다. 다론자팽창상에서 도 팽창계수의 불일치가 일어난다. 이들 불일치한 열팽창의 효과는 결정화유리 중에 미세응력을 일으키는 원인이 된다. 극단적인 경우 -
이들은 마세군연을 일으키므로 국부응력이 허용범위까지 제한되도 록 결정상의 크기를 보통 작게 하면 어느 정도 미세응력 발생을 약 화시킬 수 있다. 그렇지만 저팽창결정상을 함유한 결정화유리를 제 조시 찬유유리상 중에 농축되려는 그리고 열팽창계수를 높이는 성 분이 함유되 지 않도록 주의 하여 야 한다. 따라서 처팽창 L i 20•Al2 야 •S i 02 결정을 형성하는 데 필요한 Li20 의 과잉농도나 결정상 중에 참여하지 않는 다른 알칼리금속산화물 의 다량 존재는 보통 피해지고 있다. 비슷한 문제는 매우 높은 열 팽창계수를 갖는 결정이 발달 될 때 생긴다. 이 경우 찬유유리상은 · 결정상보다 열팽창계수가 거의 다 작다. 위에서 설명한 원리를 따 른다면, 찬유유리상의 조성은 열팽창의 불일치량을 최소화시킬 수 있어야 한다. 결정화유리의 열팽창에 대한 특정 결정상의 기여는 결정이 다론 결 정 상과 함께 고용체 로 들어 간다면 변화될 것 이 다. /3- eucry ptite 와 /3 - s p odumene 은 일련의 고용체를 형성할 수 있으며, 이들 고용 체의 열팽창계수는 두결정상의 중간값을갖게 된다. Li2 0 , Al2 야및 S i 02 의 비 가 1 : 1 : 4 인 /3- sp o dumene 도 실리 카와 고용체 를 형 성 할 수 있다. Hummel36) 에 의하면 순수한 /3 -s p odumene 의 열팽창계수 는 9X10-7 (25~100°c) 이고 1 : 1 : 6 인 고용체는 5X10-7, 1 : 1 : 8 인 고용체는 3X 10 라 1 : 1 : 10 인 고용체는 5X lo-7 이다. 실리카의 결정형은 측정온도에 따라 열팽창계수가 크게 변화된다 는 것에 주의하여야 한다. 이들 결정은특정 온도에서 열팽창계수의 변화와 함께 구조의 변화를 일으키기 때문이다. 결정화유리의 열펭 창특성에 대한 이들 상전이의 효과는 뒤에 더 자세히 설명하기로 하겠다. 표 5.23 에는 각종 결정화유리의 열팽창계수와 각종 결정상이 열 팽창계수에 미치는 영향을 例示하였다. 결정화유리 중에 촌재하는~ 독정 결정상의 체적분율이 물론 중요하며 같은 결정상을 함유한 결 정화유리가 다른 열팽창계수를 가질 수 있는 열팽창성질도 중요하 다. 따라서 일정한 열팽창계수를 갖는 결정화유리를 설계하기 위해
36) F. A. Hummel, J. Am. Ceram. Soc. , 34, 2350951 ).
tysh alCssrepa fitupi ytecEr· /3ir·tcty euEp /3pEecittur y- 3/,ui tedrSe·eueirtle donc irm,po rdeolrt,uiiieCre t /3eniS , e·teulrupdom giaoiatmatd rsuCmitrti ne,ne e otrer i etCieilu,rd ,te ioitlietrlrteisiour dabCcr e,gdmsui ,it tetrtia,aniemcoanreC euto ,ri t c leir s t il bag-oCcli emb teridnasto,,iiaeterr uset anaitit m / 3 nea ,u-ei,cmSm.uidlsi loth S.S pi me tacliisate iuliiuihtise ,l d attzcrmaQ eCr ,aiteuiilncialthtcibozislmtis I eaTrhlmn1 o.s it6pnfex of aec0Ine P2ic 10 7 X °C-I)(- 07.83 .39 8.一 1 1, 5 1. 41 1. 54 1. 2 62 .832 ..993 .605 336 ..507 5.4 201 0.3 541 0.3 7.2061 數眼係 0Ti 2 5 7..55 .48 .15 1 .45 .1111 .91 1.10 .91 .9
熱 彭2K 0.20 結는晶相 하과 i2LaN 200 .488 .3.5 5 2 6..09 .618 1.12 . 011 .09 재 에존 CaO •리유 중g MO .27 .125 17.8 191.2.2 205.1 73. 13 .7 5.23화걷정ZOn30 zAl 8.724 .12 • .453 181 .3 50. 21 0. 25 .3.562 8 .920 .o19 . 111 . 2 3 .9172. 표i S20 7.2 56.80 545.7 70. 55 .4 5 .56 .58425. 5 58 7.0 56.58. l56.7 87.5 28,3 9l52.u
서는 결정형뿐만 아니라 요구되는 성질을 얻 기 위해 결정형의 비율뻬 도 변화시켜야 된다. 검정화유리 중에서 결정상의 체계적인 변화의 효과를 그림 5.22 에 실었다. 이 재료 중의 Al 요를 ZnO 로 치환시키면 처음에는 열팽창계수에 비 교적 작은 효과밖에 미 치지 못하나, ZnO 의 分子比가 Al2 아 와 같 아지는 곳에서는 팽창계수가 갑자기 커지고 ZnO 함량이 더 증가하 면 접차 팽창계수가 커진다. 이들 효과는 결정화유리 중에 존재하 논 결정상의 변화에 기인한다. 죽, Al203 보다 ZnO 를 소량 함유한 재 료에 서 는 주결 정 상이 P-sp o dumene/sil ica 고용체 이 나, ZnO 의 함 량이 Al2 아함량보다 많을 때는 고용체의 상은 사라지고 고팽창상인 석영이 나타나게 된다. 석영의 양이 접차 중가하면 높은 ZnO 함량 과 함께 열팽창계수가 접차 커진다. 그림 5.22 에는 중요한 접이 내포되고 있다. ZnO/Al203 의 비가 약 1 인 영역에서 비교적 작은 조성의 변화가 열팽창계수를 크게 변화 시킨다는 것이다. 따라서 제여된 열팽창계수를· 갖는 결정화유리를 제조 한다는 실제적인 관접에서는 이런 조성은 적합하지 않다. 그러 나 한편 이 영역에서의 조성범위는 열팽창계수를 제어할 수 있다는 사실을 알 수 있다. 일반법칙으로 유리 중에서 조성의 작은 변화가 결정의 함량을 크게 변화시킬 수 있으며 따라서 결정화유티의 물리 적 성질의 변화를 피할 수 있다. (3) 熱影服特性에 대 한 熱處理 Schedule 의 효과 열처리 schedule 은 촌재하는 결정상의 비율과 성질을 결정하기 때문에 결정화유리의 열팽창독성은 ' 열처리 schedule 에 의해 크게 영향을 받는다. 즉 열처리 schedule 의 변화는 결정상의 체적분율도 바꿀 수 있어 결과적으로 결정화유리의 열팽창계수에 영향을 미천 다. 이 효과에 대해 각종 조건하에서 열처리한 인산영을 핵생성제 로 한 Li 20 ― ZnO-S i O 검정 화유리 의 열팽 창계 수를 측정 한 McMi llan 등 37) 의 연구가 있다. 그림 5.23 은 500°C 에서 1 시간 핵생성처리를 한 시편의 결정화열처리를 변화시킨 효과를 나타내고 있다. 37) P. W. McMi llan and B. P. Hodg son, Brit. Pate n t No. 10234800966).
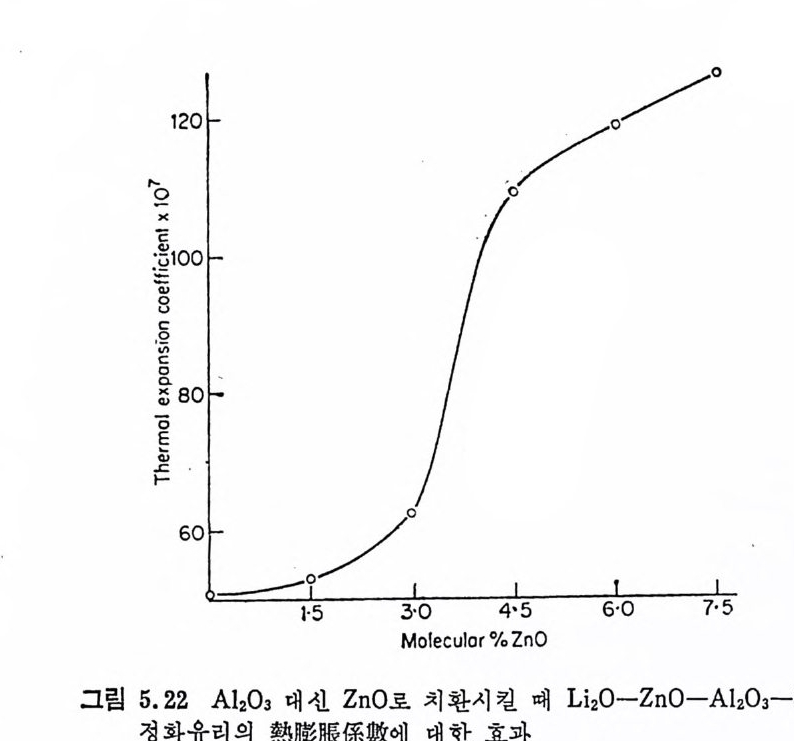 x 120 I /° o/0
x 120 I /° o/0
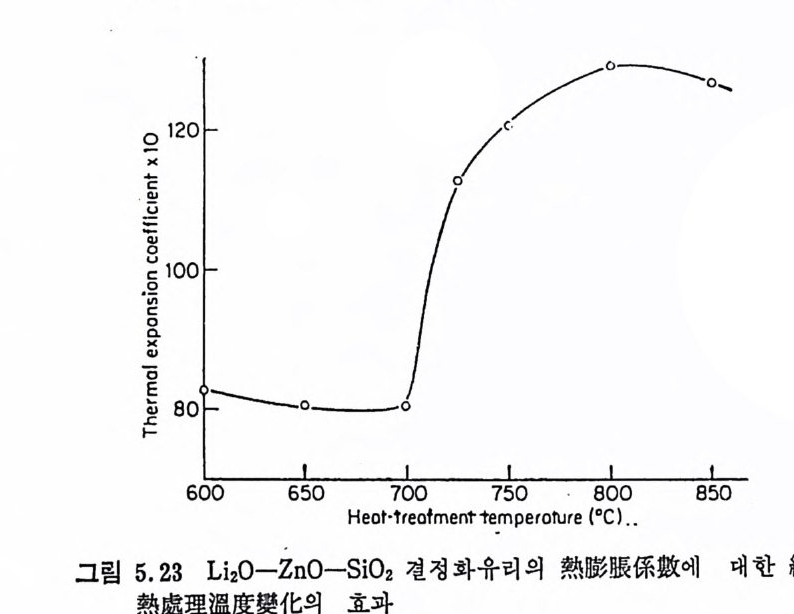 / 0 [°I
/ 0 [°I
처음에는 Li 20•2S i 02 결정이 침전되며, 700°C 에서 열처리한 시편 은 거 의 같은 체 적분율의 Li 20•2S i아 와 찬유유리 상을 함유한다. 700°C 까지 열처리를 하면, 비록 Li 20•2S i 02 결정의 열팽창계수가 母 유리의 열팽창계수 (83X10-7°C 크)보다 크지만 전체적으로 열팽창계 수는 약간 감소한다. 이것은 열팽창계수를 감소시키는 L i 20 유리상 의 소모에 의한 것이며, 이 결과 결정화유리의 열팽창계수는 전체 적으로 조금 감소한다. 700°C 이상의 열처리는 열팽창계수를 상당 히 중가시키며 이 원인은 고실리카유리상이 결정화되어 고열팽창계 수를 갖는 석영결정을 생성하기 때문이다. 1 시간 동안 800~850°C 에서 열처리한 재료는 거의 같은 양의 L i 20•2S i 02 와 석영 그리고 작은 체적분율(약 5% )의 찬유유리상을 함유하고 있다. 500°C 에서 1 시간 핵생성한 시편의 700°C 등온열처리의 결과를 그림 5.24 에 실었다. 1 시간 이상의 열처리시간에 의한 열팽창계수
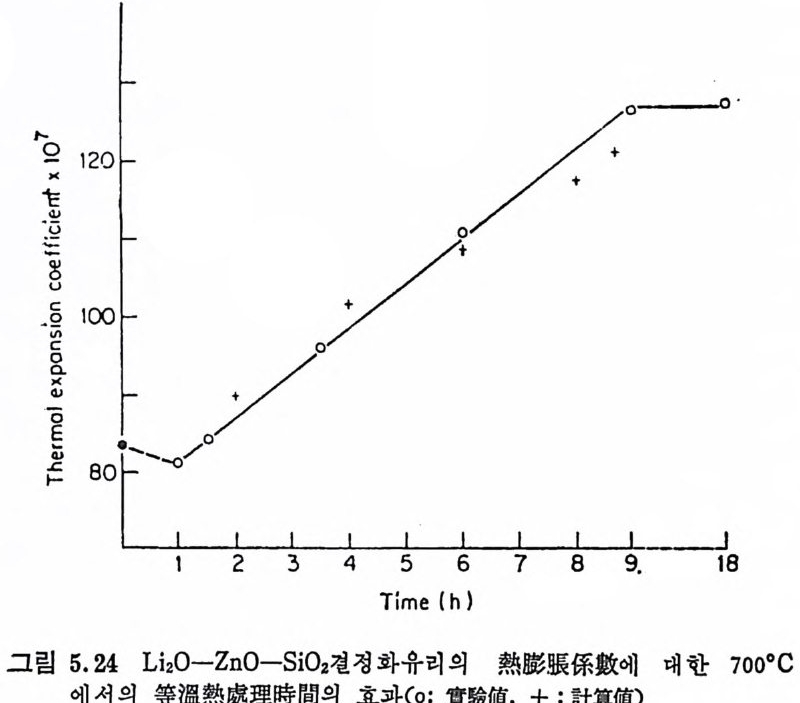 4p \。一
4p \。一
의 접차적인 중가는 석영상이 접차 발달하기 때문이다. 이 과정은 9 시간 열처리까지 완전히 나타난다. 1 시간 열처리한 재료가 50% 의 Li 20•2S i 02 와 50% 의 유리를 함유하고, 9 시간 열처리한 시료가 50% 의 L i 20,2S i아와 50% 의 석 영을 함유한다는 사실을 참고한다면, 각 종 열처리시간에서의 열팽창계수를 계산할 수 있다. 그림 5. 24 에서 와 같이, 계산에 의한 점들과 실험적으로 얻어진 곡선이 잘 일치하 며 따라서 결정화유리의 연팽창계수는 그들의 결정학적 성분을 알 면 추정할 수 있다고 생각된다 . .5 .4.2 尉火度 (1) 一般考察 만일 재료가 고온공정이나 조작이 요구된다면 결정화유리가 변형 울 나타내지 않고 가열될 수 있는 온도는 중요하다. 이런 이유 때 문에 결정화유리와 다론 세라믹형 재료들의 내화도를 비교하여야 하며 내화도특성을 결정화유리에 관련짓는 것도 유용하다. 결정화유리 시편이 변형될 때까지 가열되고 계속 가열된다면 ~ 론 시편은 녹울 것이다. 변형되는 온도는 가열속도, 시편을 지지한 방법 및 시편에 작용한 하중에 좌우된다. 따라서 실험조건을 표준 화하여야 한다. 한 방법은 막대시편을 일정거리 떨어진 칼날 위에 놓고 일정속도. 로 가열한다. 변형온도는 막대시편이 밑으로 늘어지기 시작할 때이 다. 매우 편리한 다른 방법은 열팽창곡선상의 최고접을 변형온도로 기록한다. 왜냐하면 이 최고접 이상의 온도에서는 연화가 일어나 기 때문에 시편은 더이상 팽창되지 않기 때문이다. 이 방법으로 측정되는 온도를 示差影眼計軟化溫度 (d i la t ome t r i c soft en in g tem p . )라 고한다, 제 어 된 조건하에 서 표준시 편의 크리 이 프 속도 (cree p ra t e) 를 측정 하는 것은 이 정보가 변형을 가쳐오는 공정의 기초를 포함한 推論 울 전개하는 데 유용하기 때문에 매우 중요하다. 결정화유리의 변형을 지배하는 인자들은 복잡하다. 왜냐하면 결 정 사이 oil 아마도 군일하게 분포되 어 있을 찬유유리 상과 함께 17a
이상의 결정상이 존재하기 때문이다. 존재하는 결정상의 대부분은 용융온도가 높기 때문에 유리상의 성질이 결정화유리의 내화도를 크게 지배한다. 존재하는 유리상의 비율이 결정화유리의 내화도에 크게 영향을 미치는 것이 확실하며 이런 관접으로부터 유리상의 비 울은 가능한 작은 것이 바람직하다. 유리상의 조성도 중요하며 유 리상의 軟 化溫度를 낮추는 산화물이 소량 존재하고 있는가를 확인 할 팔요가 있 다. 이 효과를 갖는 산화물로는 알칼리 금속산화물, 산 화붕소, 산화납이 있 다. 변형의 원인이 되는 유리상의 접성유동의 가능성 이의에도 온도 가 상승하면 결정상들이 재용해될 가능성도 있다. 충분히 높은 온 도 로 가열하면 물론 결정화유리는 최초의 액체 또는 유리와 같은 상태로 재전환된다. (2) 결정화유리형과 雨火度와의 관계 MacDowell 등 38) 에 의해 제조된 Al203 ― S i 02 형 결정화유리는 유 리를 결정화시켜 제조할 수 있는 재료 중 내화도가 높은 것의 대표 적인 것이다. 이 재료는 주결정상으로 mu llit e(3Al203•2S i 02) 를 함 유하고 있 다. 이 화합물의 높은 웅접 (1850°C) 은 주목할 만한 가치 가 있으나 이 재료 중의 찬유유리상의 높은 내화도 (re fr ac t or i ness) 도 고온에서의 치수안정성에 기여한다. 이 재료를 1500°C 에서 10 시간 · 열 처 리 하여 도 큰 비 들림 (d i s t o rti on) 이 나타나지 않는다. cordie r it e 를 주결 정 상으로 갖는 결정 화유리 에 M gO 를 첨 가하면 Al203-S i 02 형 결정 화유리 보다는 내 화도가 작으나 상당한 고온성 질 울 갖는 재료를 만들 수 있 다. 이 들은 AI203-Si0 2 결정화유리 보다 · 더 쉽게 제조 및 성형할 수 있는 이접이 있다. Al2 아함량에 따른- 1275~1370°c 에서의 이 재료의 번형온도가 S t ooke y 39) 에 의해 보고 、 되었다. 副成分이 이 재료의 내화도에 큰 영향을 마친다. 중량%로 Si0 2 ; 43. 5, Al2 아; 17. 4, Ti0 2 ; 8. 7, ZnO; 26. 1, RO (Mg O , CaO, BaO 또는 PbO) ; 4. 3 인 조성 의 결정 화유리 에 각종 산화물울 도입하여 변형온도를 측정한 결과를 표 5.24 에 실었다.
38) J. F. MacDowell and G. H. Beall, J. Am. Ceram. Soc. , 52, 17(1 9 69). 39) S. D. Sto o key, Brit. Pate n t No. 829447(1 9 60).
표 5.24 길정화유리의 변형온도에 대한 副 成分 (4.3W t. %)의 효과 Oxid e Defo rm ati on tem p er atu re(° C) Mg O 1125 CaO 1100 BaO 1025 PbO 875 반경이 큰 금속양이온이 도입될수록 변형온도가 더 크게 낮아전 다는 사실에 주목하여야 한다. 만일 치환량이 중량기준이 아니라 mole 기준으로 되었다면 이온반경 증가의 효과는 더 확실할 것이다. 유리 의 접 도를 낮추는 각종 산화물의 효과는, 가장 큰 효과를 나타 내는 산화납과 같은 모양을 나타낼 것이다. 이것은 결정화유리의 내화도에 대한 산화물의 효과는 찬유유리상 중에 산화물이 도입되 어 일어난다고 생각된다. 이 경우 PbO 는 가장 낮은 변형온도 플 가 쳐오지만, 이 산화물을 상당량함유한결정화유리는 대우 높은 변형 온도를가질 수있다. 예 를 들면, PbO ― Al203-S i 02 一 T i 02 조성 의 결 정 화유리 논 750~ 1150°C 범위의 변형온도를 갖는다고 S t ooke y 39) 가 보고하였다. 이들 조성 은 PbO 를 32~46% 함유하며 Al203 함량이 감소하면 내 화 도가 작아진다. 이 형 의 조성 에 서 높은 비 율의 PbO 는 PbT i아와 같이 결 정상 중에 고정된다. 표 5,25 에 실린 데이타는 각종 결정화유리의 시차팽창계연화접에 대한 효과를 나타낸 것이다. 1~5 번까지의 조성은 Au 를 소량 함유 하고 있으며, 6~11 까지의 조성은 핵생성촉진제로 금속인산영을 소 량 함유하고 있 다. 이 데 이 타로부터 Li2 0 — S i0 2 조성 중에 Al2 아 가 도입 되 면 내 화도가 증가하며 이 효과는 M g O 보다 더 효과적 이 다. 디론 효과로는, L i 20 함량은결정화유리의 내화도를 낮추며, Mg O - . Al2 아― S i 02 조성은 같은 분자량의 Li2 0 -Al203— Si0 2 조성 보다 상당 히 내화도를 높인다는 것을 알 수 있다. 일부 알루미노규산영유리의 연화온도가 800°C 이상이고 용융실리 : 카유리가 더 내화도가 높지만 일반 유리의 시차팽창계연화접은
표 5. 25 결정 화 유리 와 모유리 의 示差彬服計軟 化溫度 no. si02 M | oAlel2c0u3la| rZ pnOe r cIe nMt a gg 이 e Li2 O IIp Sao reftn etn ign lga s ste Im Gp laes rsacteu rr aems i c Comp o sit ion comp os it ion (°C) : l ;: I _6 1 二 I 二 1 :: I ::: I ::: 3456717718656976507601l7__5 75015006510l_ 05117011 702l3255002 0202040l9 50 6575 970 6 560 960 ―560 910 ―— 530 895 11 _一_- l40 655121500 >>11009002000 805 >1000 500~600°C 를 넘지 않기 때문에 결정화유리는 대부분의 실용유리 보다 내화도가 더 높다고 할수있다. 참고로 표 5.26 에 결정화유리 와 다른 재료들의 最 高安全使用溫度를 실었다. 표 5.26 결정화유리와 각종 재로의 最高安全使用溫度 Mate r ia l I up pe r safe ty tem p . (°C) T。 己] 370-480 軟 銅 430 Py re x 유리 560 低彭眼透明결정화유리, 700-800 Sp ine ! • Mull ite 두 명 결 정 화유리 1000 磁 器 1190 石 英 유 리 1200 雨熱性걷정화유리 1200 96% 알루마나 1700 Mull ite 1760 100% 알루미나 19.5 0 Zir c onia 2310
표 5. 26 으로부터 결정화유리 는 대 부분의 유리 보다 고온사용에 더 적합하다. 결정화유리에서 사용하는 방법과 내화도 측정방법이 다 르기 때문에 실용 제라믹스와 내화도를 비교하기는 쉽지 않다. 그 렇지만 정성적 비교는 가능하며, 결정화유리는 고알루미나세라믹 스보다 내화도가 떨어지며 결정화유리의 내화도를 높이기 위해서 알칼리금속산화물을 함유하지 않으면 s t ea tit e(3M g 0· 4 S i 02·H20) 냐 fo rs t er i t e(M g 2S i 04) 제 라믹 스와 비 슷한 변형 온도를 갖게 된다. (3) 祐性 變 形과 크리 이 프抵抗 고온의 應 力下에서 결정화유리의 변형은 열교환기, 가스터빈엔진 . 과 같은 공학적인 응용면에서 중요하다. 따라서 크리이프거동에 영 향울 주는 인자들을 아는 것이 기본이 된다. 전정화유리에서는 찬 유유리상이 접성변형을 하기 때문에 강한 영향을 나타낸다고 생각 ` 된다. 대부분의 재료에서는 변형-시간의 곡선은 3 단계로 확실히 분리된 다. 즉, a) 하중이 걸리는 순간에 시작되어 시간의 경과에 따라 감소되는 · 初期 크리 이 프(p r i mar y creep) . b) 일정기간동안 정상크리이프속도가 유지되는第 2 次크리이프 . (secondary creep) . c) 크리이프속도가 급속히 증가되어 시편에 파손을 일으키는 第 - 3 次 크리 이 프(t e rti ar y creep ). 제 2 차 크리이프는 일정한 내부크리이프 구조의 범위에 해당된다 고 생각된다. 만일 주어전 재료에서 이 크리이프형이 보이지 않는 · 다면 크리이프 구조는 全스트레인에 대해 연속적인 변화를 하며 평 형이 결코 얻어지지 않는다고 생각된다. 제 2 차 크리이프 속도는 } 개의 독립변수인 온도 T, 응력 6 및 구조인자 s 의 함수라고 생각 된다. 구조인자는 입도, 轉 位密度, 기공물과 같이 크리이프에 영향 : 울 주는 모돈 구조변수들을 포함하고 있다. 따라서 크리 이 프속도 e 는 다음과 같이 나타낼 수 있다. £ex: f( T)f( q)f(s) (5-14}
일정 온도에서 구조인자가 평형이라고 가정하면 ~ocf (a ) (5-15) 응력에 대한 크리이프속도의 의촌도는 직선적이 아니고 보통 다 음과 같은 관계가 있다. E=Aa (5-16) 여기서 A 는 상수이다. 응력치수의 값 n 은 변형기구의 독성을 나· 타낸다. n 의 값이 1 에 가까우면 변형과정은 접성유동이며, 3~4 의 큰 값을 갖는 경우에는 극한단계로서 비점성과정(예 ; 轉位 cl i mb) 아 존재한다고 해석하고 있다. 크리이프는 열적으로 활성화되기 때문에 온도함수는 다음과 같은 식이 된다. f( T) oc exp ( -L1H/R T) (5-17) 여기서 4H 는 크리이프의 활성화에너지이다. 다결정질세라믹에서는노 이 값이 보통 160~190Kca l/ mole 이며, 이들 높은 활성화에너지는 비접성크리이프(전위이동)에 해당되며 크리이프에 대한 낮은 활성화~ 에 너 지 (90~130Kca l/ mole) 는 접 성 유동기 구에 해 당된다. L i 20 ― ZnO ― S i 02 형 결 정 화유리 에 대 한 인장 및 압축크리 이 프거 동 의 연구가 Morell 등 40) 에 의해 이루어졌다. 촌재하는 결정상들은 Li20 • 2Si0 2 , L i 20·ZnO·S i아 및 석 영 이 다. 찬유유리 상은 결정 화유라 의 약 20Vol. %이고 이상의 중량% 조성은 20K20•s0S i아 였다. 이 유리상이 비교적 천천히 결정상 사이에 흘러 들어가도록 결정화속도. 를 제 어 한다면 결 정 화유리 논 뉴돈유체 (Newt on ia n fl u i d) 로서 거 동할 것이다. 크리이프의 3 가지 목성영역이 관찰되었다. 초기 크리이프는 유리 상의 結彈性擧勤에 의 해 제 어 된 결정상 중에 運延彈性 스트레 인 (de!-ay ed elasti c s t ra i n) 이 생기기 때문이라 생각된다. 제 3 차 크리이프는 표면으로부터의 파열 또는 군연발생에 의한 장력과 空洞 (vo i d) 형성 및 興斷破損 (shear fai lure) 에 의 한 압축이 원인이 된다. 제 2 차 크
40) R. Morell and K. H. G. Ashbee, J. Mate r . Sci. , B, 1253(1 9 73).
리이프 영역에서는 장력과 압축력에서의 활성화에너지가 같고 초기 크리 이 프의 활성 화에 너 지 (약 130~160Kcal/mole) 와도 같다. 이 결정화유리의 크리이프성질은 구조적 형태 및 유리상에 의해 제어된 속도에 의해 크게 영향을 받는다고 결론지었다. 결정의 소 성변형은 큰 영향을 미치지 못하나 순수한 접성유동은 낮은 응력에 서만 발생하수근 옹력지수 n 이 1 인 값을 갖는다. 더 높은 응력에서 는 n 의 값이 6 까지 변화된다. 이것은 고응력에서 높은 負의 유체 정력학적인 압력이 존재하기 때문이며 더이상 일정한 체적을 갖지 않고 변형이 일어나는 핵생성과 空洞의 성장이 생기기 때문이다. 공동의 생성은 작용하는 응력장의 성질에 따라 달라진다. 비불림 크리 이 프(t ors i onal cree p)에 서 는 응력 지수가 1. 4~1 . 7 범 위에 있으며 높은 응력 장에 서 는 크게 일어 나지 않는다는 것 이 Heuse 등 41) 에 의 해 보고되었다. 이들은 각종 결정화유리와 95% 알루마나세라믹울 정비 상교으 실로험 하Li였2 0다 •.2S i0 연2 구와된 석 재영 료을 중함 유가한장 저내 알화루도미가 나 인낮 은L i2재0 료-A는l2 0주3길— S i 02 조성이다. 이 재료는 750°C 의 실험조건하에서 상당한 변형을 나타내며 크리이프의 활성화에너지는 138~158Kca l/ mole 이었다. 같은 계로부터의 조성이나 알루미나함량이 더 많고 주결정상으로 /3- spo dumene 고용체 를 함유한 재료는 내 화도가 더 높다. 같은 변 K0형—c의 aAl / l온m20 o도 3l—e는 로S i 약0 큰2 와 1차0 0C이°Ca 가o 더— 없A높었l2았 다0다.3. -S 알i0그 칼2 러형리 나 를결 활정함성 화유화유하에리지너 는지않 내은는 화 B1도2aO0가~— 1Z5더4n 높았다. 후자의 경우, 1100°c 이상의 일정 하중에서만 큰 변형을 나타내기 시작하였다. 실제로 이 거동은 95% 알루미나세라믹의 거 동과매우 비슷하다. 핵생성 촉진제로 T i아를 3mole% 함유한 Li 20•Al2 아 ·4S i 02 결정 화유리의 인장크리이프에 대한 연구가 Bold 둥 42) 에 의해 행하여졌다. 上限熱處理를 1000°c 로 제한함으로써 기 본결정 상으로 /3-석 영 고용 체를 함유한 결정화유리가 제조되었다. 상한 열처리온도를 1200°c
4D E. M. Heuse and G. Partr i d g e , J. Mate r . Sci. , 9, 1255(1 9 74). 42) S. E. Bold and G. W. Groves, J. Mate r . Sci. , 13, 611(1 9 78) .
로 하면 결 정 상으로 (3- sp od umene 이 발달되 었 다. 2 재 료는 찬유유라 상이 약간밖에 없고 결정질이 대부분이다. ¢ _ 석영을 함유한 재료는 평 군입 도가 o. 14µm 이 고 {3- sp od umene 재 료는 I. Oµm 이 다. 兩材料 에 서 스트레 인속도를 지 배 하는 활성 화에 너 지 는 695K J mole - 1 이 고 옹 력지수 n 은 모두 1. 4 였다. 큰 크리이프 스트레인 이후의 재료의 미 제 구조 연구결과, 粒 界移 動 (g ra i n boundary sl i d i n g)을 함유한 크리 이 프기구는 임계확산에 따르게 된다. 파손 이전에 큰크리이프스트레 인이 일어나더라도 최종파괴는취성독성과같다는사실에 주의하라. 5.4.3 比熱 결정화유리의 비열은 조성에 따라 큰 변화를 나타내지 않으며 평 군비 열 (20~400°C) 은 보통 o. 22~o. 2acal•g -1 0°C-1 이 다. 따라서 이 값들은 유리와 세라믹스와는 너무나 다르다. 결정화유리의 비열과 · 조성 사이의 관계를 탐색하기 위한 데이타는 불충분하지만, 주성분 으로 L i 20 와 S i아를 함유한 결정화유리에서는 실리카성분이 감소할 수록 비열이 작아지는 실험결과를 나타낸다. 온도가 상승하면 결정 화유리의 비열은 커지며 이 2 매개변수 사이의 관계는 유리와 세타 -
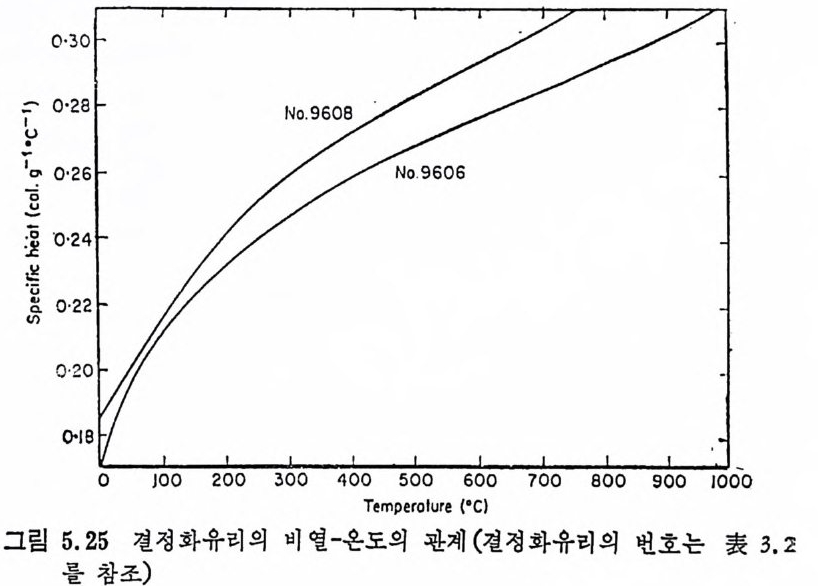 0·3 0
0·3 0
피스에서도 비슷하다. 그림 5.25 는 2 가지 결정화유리에 대한 비연 과 온도와의 관계를 나타내고 있다. 5.4.4 熱傳導率과 熱柄故率 (1) 熱傳導率 결정화유리는 熱導體 또는 熱不導體로의 사용이 요구되며 이들 응용에 대한 안정성은 주어진 온도구배하에서 건정화유리를 지나는 熱移動速度에 의해 대부분 결정된다. 예를들면, 요리기구에 결정화 유리를 사용한다면 상당히 높은 열전도울(t hermal conduc ti v ity)윤 갖 는 것이 바람칙하다. 한편 재료의 열충격처항도 열전도율에 의해 영향을 받는다. 결정화유리의 열전도울은 유리보다 약간 더 크나, 순수한 산화물 세라믹스보다는 작다. 이것은 표 5.27 에 실린 데이타로부터 알 수 있다. 열전도울에 대 한 온도의 • 영 향은 그림 5. 26 에 실었 다. No. 9606 결 표 5.27 100°C 에서의 결정화유리와 다른 재료들의 열전도울 Mate r ia l I T(chaelr •m seacl- Ic •o cnmd-uIc ' t0 i cv-i It } Glass-cerami cs LLLL iiii 2222 0000 ——一— ZZAZnnnlzOOO0 —3— - —SSA Sii 00l iz22O 0 z 3(((ccc-...S 352i0%00 %2% Z nZL0ni)zO O )) 000o.... 0000000176532070 Glasses Fused sil ica 0.0036 Low exp an sio n borosil ica te 0.004 Soda-li me -sili ca 0.0035-0.004 Cerami cs Pure alumi na 0.072 Pure mag n esia 0.090 l ‘‘ P95o rpceelr a icn e nt alumi na cerami c 00..005024
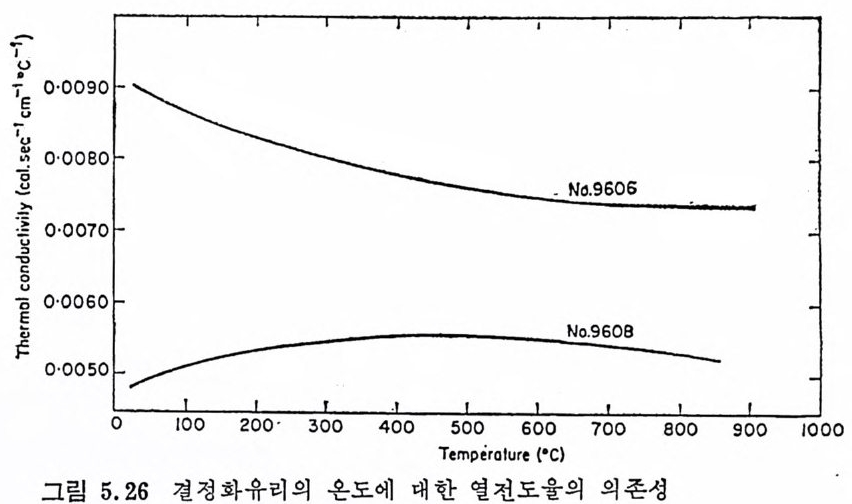 (
(
정화유리는 온도가 상승하면 열전도울이 조금씩 작아지며, 이 거동 은 온도가 상승할수록 열전도울이 조금씩 커지는 유리와는 반대 이다. 한편 견정질재료는 온도가 상승할수록 열전도울이 보통 작아지며 No. 9606 결정 화유리 의 거 동은 유리 상이 극소량만 함유된 높은 결정 질 미세구조와 일치한다. No.9608 결정화유리의 거동은 450~500°C 에서 열전도울이 최대값을 나타내기 때문에 이상하나 全溫度範園에 걸쳐 열전도율의 변화는 작다. (2) 熱摘散率 일시적인 열흐름(평형이 얻어지지 않고 열에너지가 물체의 온도를 높이 논 데 사용되어야 하는 경우)을 포함한 문계에서는 열확산량이 문제가 된다. 열 확산울 K= k/pC p (5-18) 여기서 k 는 열전도울, p는 밀도, C p는 眞比熱이다 • 그림 5.27 에 2 개의 상업용 결정화유리에 대한 열확산율(t hermal ,d iffu s i v ity)의 데 이 타를 실었 다.
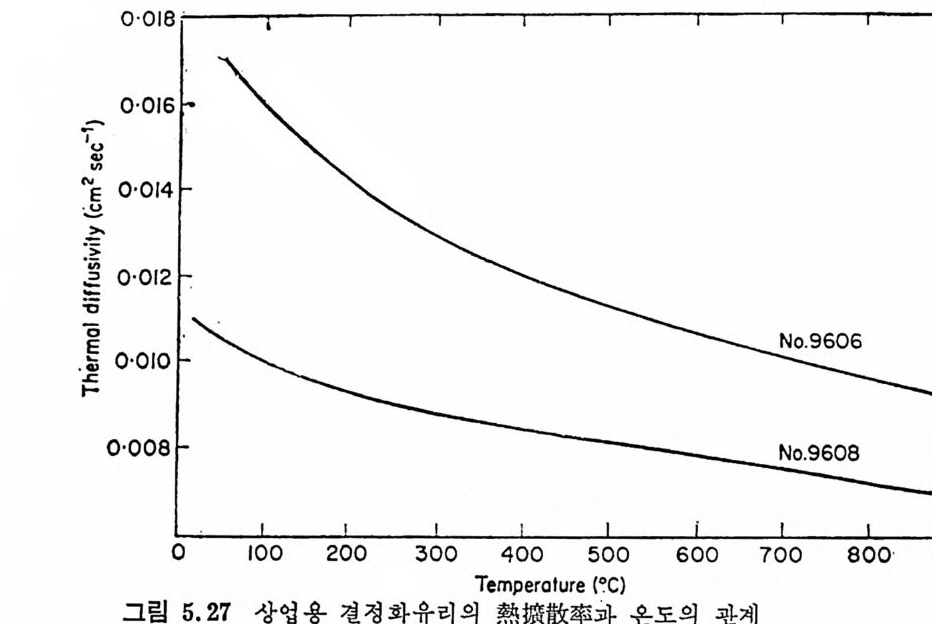 0·0 1 8
0·0 1 8
5.4.5 討熱性 (1) 一般考察 온도구배가 결정화유리와 같은 재료를 가로질러 생간다면 재료의 열팽창이 달라 스트레인이 생기기 때문에 내부응력이 발생한다. 板 에서 한 면이 가열되고 다른 면이 냉각되면, 뜨거운 면에는 압축옹 력, 차가운 면에는 인장응력이 생기게 된다. 이런 형의 정상상태하 鼻 에서 시편의 형상이나 의부적인 속박이 굽힘에 의한 응력제거를 방 · 지하는 곳에서는, 표면응력은 다음과 같이 주어진다.
![]() a=EaLlT/2(1-J.1) (5-19)
a=EaLlT/2(1-J.1) (5-19)
여기서, (1=표면응력 (압축 또는 인장), AT= 표면 사이의 온도차, . a= 선열팽창계수, ),1=P ois s on 比이다. 이 식은 시편의 두께방향에서의 온도구배가 균일하다고 가정하고 . 있으나, 실제 온도구배는 열전도도분만 아니라 재료의 두께에 따 라서도변화된다. 급격한 가열이나 냉각에 의해 발생된 응력은 정상상태의 조건어 L
서보다 더 크다. 왜냐하면 처음의 온도구배는 얇은 표면충에 국한 되고 표면응력은 정상상태 조건에서보다 2 배가 될 것이다. 급격궁i 가열은 표면압축응력을 발생시키나 급격한 냉각은 인장응력을 발생 한다. 장력하에서의 파손이 가장 보편적이며 발생된 응력이 재료의 파괴응력보다 클 때 파괴가 일어난다. 급격한 온도변화에 파괴되지 않고 재료가 견덜 수 있는 크기를 熱衝擊 抵抗(t hermal shock res i s t ance) 이라고 하며 이것은 재료가 파괴 되지 않고 급격히 냉각될 수 있는 최대온도 간격으로도 정의되고 있다. 급냉시의 파손이 더 일반적이기 때문에 급냉에 대한 저항이 가열 에 대한 처항보다 더 중요하나, 특별한 경우에는 가열에 대한 저항 도 알아야 한다. 시편의 모양은 열충격처항에 크게 영향을 미치기 때문에 열충격시험은 표준화된 조건에서 조십스럽게 행해쳐야 한 다. 또한 냉 각매 개 체 (cooli ng med i um) 의 성 질은 시 편의 표면으로부 터 열이 추출되는 속도에 영향을 주기 때문에 중요하다. 간단하고 편리한 방법으로는 각종 匠知의 온도로부터 急流인 표준온도의 水 檀 에 시편을 급냉시킨다. (2) 결정화유리의 熱衝擊抵抗 결정화유리의 열충격저항을 결정하는 중요한 인자들은 탄성률, 선팽창계수 및 기계적 강도이다. Po i sson 比는 결정화유리의 종류에 따라 크게 변하지 않기 때문에 2 차적으로 중요하다. 결정화유리의 기계적 강도는 우수한 열충격저항을 가질 것이라고 기대된다. 또한 매우 낮은 열팽창계수를 갖는 결정화유리가 제조가능하며, 이런 결 정화유리가 열충격에 매우 큰 저항을 나타낸다는 것은 당연하다. 주결정상으로 /3- s p odumene 을 함유하고 열팽창계수가 5~10X 10-7 인 결정화유리들은 깨지지 않고 700°C 로부터 0°C 로 냉각시킬 수 있었다• 높은 기계적 강도와 낮은 열팽창계수 이의에도 낮은 탄성률이 높 · 은 열충격 저항에 는 필요하다. 주결정상으로 /3- spo dumene 을 갖는 결정화유리는 적당히 낮은 Youn g률 (8.3~9.OX104MNm-2) 을 가지고 있다. 따라서 이런 형의 재료들은 높은 열충격처항을 나타내는 귄
표 5.28 결정화유리와 소오다-석회-실리카유리의 熱衝擊抵抗 Mate r ia l Tetimnof at (p e cOielra Cu rvuar) as etel u re (rMulb. op/ do ti ufun r 2l eu) s M(ellbaos/od tifuin cl 2 ui)t sy ecTxop(eh °afe Cfnjrc m기s1 i)0aen ln t Glass-cerami cs a 130 25,000 10.6Xl06 156.9X l 0-7 b 160 40,000 12, 6 X l06 127. 5 x 10-1 C 215 22,000 12.0Xl06 64. 9 X 10-7 d 285 28,000 ll. 2X l06 55.5x 1 0-1 Soda-lim e-sil ic a gla ss 140 16, 000 10. 0 X 106 92. 0 X 10-7 중한 성질들을 가지고 있다. 표 5.28 에 주어진 데이타는 열충격처항에 대한 각종 성질들의 영 향울 예시하고 있다. 이 실험은 각 온도로부터 20°c 의 물에 시편 봉을 급냉시켰다. 기계적 강도는 냉각된 시편에 대해 측정하였다. 열충격에 의한미세균열은 재료를 약화시키며, 급냉시키치 않은 재 료의 강도의 90% 로 강도가 낮아져 열충격에 의한 파손이 일어난 것을 나타내고 있다.
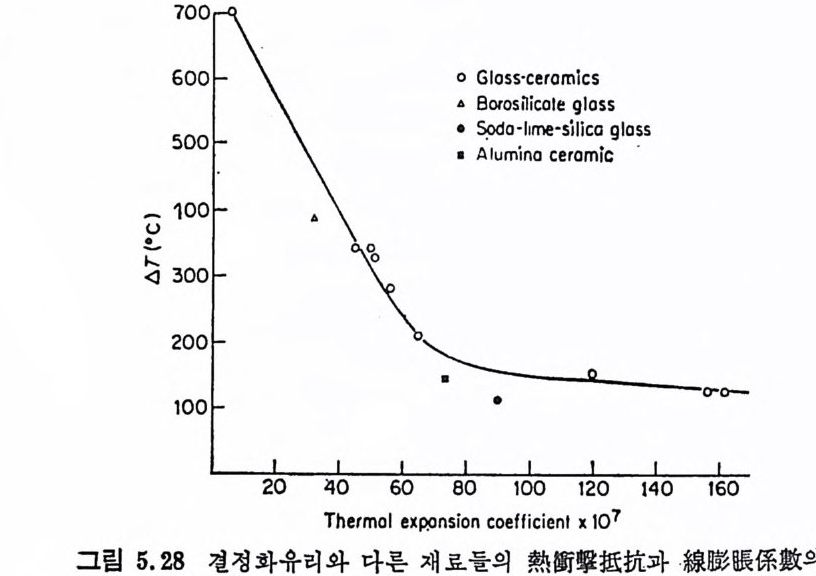 600 o Gloss·ceromlcs
600 o Gloss·ceromlcs
선팽창계수는 결정화유리의 相 對 的 열충격저항을 결정하는 가장 중요한 인자이다. 그림 5.28 에서 보는 바와 같이 열충격파손의 원 인이 되는 온도간격 4T 의 값을 열팽창계수에 대해 p lo t하면 접둘 은 완만한 곡선상에 놓인다(연충격저항이 열팽창계수에 반비례한다고 생 각한다면). 결정화유리의 탄성률은 그들의 열전도울과 매우 비슷하 다는 접에 주의하라. 결정화유리의 기계적 강도가 달라도 그 차이 는 4T 의 값을 크게 편향시키기에는 불충분하다. 그립 5.28 에서 소 오다-석회-실리카유리와 붕규산영유리의 4T 값은 모두 곡선 아래에 놓여 있으며 , 이것은 그들의 기계적 강도가 결정화유리에 비해 상 당히 낮기 때문일 것이다. 95% 알루미나세라믹의 L1T 의 값도 그 열팽창계수로부터 기대한 값보다 더 낮다는 것은 약간 의의이다. 이 세라믹의 더 높은 열전도울은 열팽창계수가 비슷한 결정화유리 보다 열충격저항이 더 좋다고 기대되나, 알루미나세라믹의 탄성률이 높기 때문에 기대한 것과는 다론 결과가 나오는 것 같다. 공기중에서 급냉하면 물속에서 급냉하는 것보다 십한 효과가 아 주 작게 나타나며 이 효과는 표 5.28 중의 결정화유리 b 에서 볼 수 있다. 각 온도로 유지된 가마로부터 시편봉을 빼내는 실험에서 700°C 로 부터의 급냉온 결정화유리의 강도에 큰 영향을 주지 않았다. 결정화유리논 급냉에 대한 열다충. 격급처열항 에이 대확 한실 히Li 2크0 -지A만l2,0 3급— 열Si의0 2 효과에 관한 데 이 타는 매 우 적 형 결정화유리의 처항을 축정한 결과는 표 5.29 와 같다. 실험은 직 경 5cm, 두께가 0. 5cm 인 시료관 (d i sc) 에 750°C, 300 ft /sec 의 가열 젯트 공기를 시로판의 한쪽 면에 부딪힌다. 이런 방법으로. 5 개의 표 5.29 急熱에 의한 열충격에 따른 재료들의 성질 ' 9G5l%caMes sara-tAcem elr ruii caam ml i in ca - (e77c2Tx52o0p(eh..o-1fa5e f5c nXirX-0 c sm71 0ii1 e) 00oa ° n- -nlC t77 )I r(Mulb.p 3o3/58o d t iu,,fu n 0r0 l2 0eu0)00 s I .m(Y13l5 5boo.. ud/10 inu nXXgl 2u '11)s s00 66 cco(Tamncth ad나 elu100 rc0..som00t e0ci51 c°va-23c -1li 1 t )y
II
擊의 抗低교비I I I I js 1국0 /l aEcXsck•e( k//aE aSESggI c(ckk( )mm2//))Cm°2 c 8103 0.75 5400.0 3.01 00301,0~25 87120 16,00 407321~159 04 .3C52(°) 6500250.003. 3 0 21 60.0 065620,00 6 226 5.66 .80C°25() 513 802 .892.00 0850321 c°00(1) 210041 3..080 7840227) C°25(007 2 470617.00o .7.549100260,0 0 207 5.3.735 1 370140.0 74 5. 1.666 070070.1104 5 3.50 衝료의재 熱라세믹10 xa 7 j° (0)21~0C50氐{ 5 7~0 彭2 C2 3(°)005~眼 20普3 2 0C5°3(2) ~0通33 ~ 5°C01(260彭75 0~5)C °(203眼06 28 高 88 彭 09 眼 종각 03 .5 결표정 리화유와 서z료 유석영리 (6m 리ra화低y유o)服彭r890ep결c 정 eiterc odri pyr ex리유 hpge rati p電e抵高(抗oycar氣r !i견m] -정 화?606 9 통기보자 tai etSet m aluAni 다석리오소유 회-542
결정화유리 시편을 실험하였으나 어떤 파손도 발생하지 않았으나, 95% 알루미나세라믹 5 개의 시편 중 2 개가 파손되었다. 이들 2 재료 의 열팽창계수와 탄성률은 비슷하며 알루미나세라믹의 더 높은 열 전도울은 더 작은 온도구배를 발생하여 더 작은 스트레인을 생성하 게 된다. 이런 이유들을 근거로 결정화유리가 더 높은 열충격저항 울 갖는 이유는 주어진 스트레인에서 응력이 더 작게 되는 작은 탄 성물에 그 원인이 있다고 생각된다. 이 인자 이의에도 공기흐름 (가연겟트공기)과 시편 사이의 열이동속도가 2 재료에서 차이가 있 어 다른 거동이 나타났다고 생각된다. 열충격저항은 같은 재료에서도 시편의 크기, 두께, 형상에 따라 변화되며 재로 사이의 비교는 다음 식에서 나타내는 R 또는 R’ 를 가지고 할 수 있다 .43)
 R=S/Ecr (5-20)
R=S/Ecr (5-20)
R 은 급냉조건이 급격한 경우, 예를들면 고온으로부터 수중급냉과 같이 열전달계수가 매우 큰 경우 열충격저항의 尺度가 되며, 강도 S 가 클수록 또 Youn g률 E 와 열팽창계수 a 가 작을수록 R 은 커 진다. R’ 는 공기중 냉각과 같이 열전달계수가 작을 때의 척도이며 재료의 열전도울 k 가 들어 있다. 표 5.30 은 결정화유리와 다른 세라믹재료의 열충격처항을 비교한 것이다 .44) 저팽창 결정화유리는 특히 급열급냉에 강해 800°C 로부터 수중에 두하 급냉시켜도 파괴되지 않는다. 팽창이 전연 없다면 R, R’ 는 계산상 무한대로, 급열급냉에 의한 파괴는 일어나치 않는다.
43) W. D. Ki ng e ry, J. Am. Ceram. Soc. , 38 3(1955). 44) 田代仁, 作花濟夫, 《金屈》, 31(5), 1(1961 ).
제 6 장 결정화유리의 應用 결정화유리의 독특한 성질은 더 低脈하며 발달된 성능이 요구되 는 응용면에서 전동적인 재료들과 代 置 될 수 있을 분만 아니라, 어 떤 재료도 기술적인 요구를 만족시키지 못하는 완전히 새로운 분야 에서의 응용을 가능하게 하고 있다. 이 장에서는 결정화유러의 성 질과 관련지어 결정화유리의 . 각종 실제적 및 참재적 응용에 대해 설 명하겠다. 6. 1 一般 및 機械工學의 應用 높은 기계적 강도, 우수한 치수안정성 및 마모저항은 결정화유타 가 기계공학에서의 수많은 응용에 적합하다는 것을 의미하고 있다` 기계적 성질이 이와 같은 응용에 결정화유리를 선택하는 기준이 되 지만 많은 경우 열 및 전기적 성질도 역시 중요한 기준이 된다. 6.1.1 日用品으로서의 應用 조리 기 구로는 접 시 , 냄 비 , tea -po t , coff ee -sip h on, jar 둥이 백 색 또는 두덩한 저팽창결정화유리로 만들어진다. 이것은 저팽창결정화 유리가 급열, 급냉에 매우 강하며 淸潔感울 준다는 접에 주목한 용 도이다. 熱器具材料로는 toa ste r , 전기 및 석 유스토브 둥의 니 크롬선보호 관, 가스 스 투 U , 석 유스토브의 chim ney 및 外意 가스 oven 의 外窓 ..
ga s-rang e cov e r 둥에 사용뇌 고 있 다. 전 열 선 또는 ga s-b u rner 를 완전히 처팽창결정화유리판으로 피복한 청소하기 편리한 rang e 가 붙은조리대도 고안되었다. 이들은저팽창 결 정화유리의 내 열충 격성, 미관, 높은 강도에 의한 것이다. 두명제품은 두시가능한 접이 유용 한 것은 물론이나 석영유리에 가까운 熱線透 過性울 갖 는 것도 용도 에 따라 중요하다. 이 이의에도 내마모성, 표떤의 平 滑性 , 높은 강도 를 이용한 것으 로 tile 동 가옥의 내 장품 및 의 장품, 낚시 대 용 gu id e ri n g 등에 고팽 창결정화유리를 사용할 수 있다. 6. 1. 2 機械工學에서의 應用 두명 또는 백색의 저팽창결정화유리는내열충격성, 내연성, 화학 적 내구성을 이용하여 熱交 換 器 및 hea t er 의 파이프, 적의선램프, 내열창 둥의 내열재료에 사용되어 금속이나 종래의 유리로는 이용 되지 못한 분야에서 응용되고 있다. 또한 우수한 가공성, 고강도, 내마모성, 표면의 平滑 性, 높은 전 기철연성을 이용하여 정밀기계재료( 軸 受石둥), 전기절연재료( 配還線 lin e spa ~ er, 碑 子), 전자공학재 료(抵抗 體基體 , 蒸着 用 및 pri n t 配線 用 絶 綠基 板 condenser 極板) 둥에 고팽 창성 및 저 팽 창성 결 정 화유리 가 이 용된다. 결정화유리는 급열, 급냉에 매우 강하기 때문에 종래의 유리나 급 냉 또는 이온교환에 의한 강화유리로는 미치지 못하는 우수한 성질 을 갖고 있으며, 용도에 따라서는 高 價 인 석영유리대신 사용할 수 있다. 강화유리는 基 體 유리의 열팽창계수가 크기 때문에 급열, 급 냉 에 는 그렇 게 강하지 못하며 400~600°C 에 서 강화의 효과가 없 어 진다. 고팽창결정화유리는 급열, 급냉에는 강하지 않으나 내마모성이 우수하고 강도가 높고 강화유리 보다 고온까지 사용할 수 있다. 한 판 결정화유리의 제조는 유리의 경우와 똑같은 성형법이 가능하 여 복잡한 형상의 제품도 쉽게 제작할 수가 있다는 장접을 갖고 있다.
(1) 베어 링 표면이 平滑한 결정화유리를 얻을 수 있다는 성질을 이용하여 특 수 목적의 베어 링 (bear i n g)에 이용할 수 있다. 95% 알루미나세라믹의 최고표면처리는 200~250nm 이나 결정화유리는 12.5nm 의 표면처 리가 가능하다. 컬정화유 리는 내부식성 및 산화되지 않는 성질 때 문에 대부분의 금속이 견달 수 없는 악조전하에서도 사용할 수 있 다. 최소량의 윤활유로도 조작이 가능하며 이 것은 보통 윤활유가 만 족할 만한 기능을 발휘하지 못하거 나 보통윤활유기 술로는 사용중 베 어 링 이 너무 접근(i naccess i b ility)하여 사용할 수 없는 조작조건(예 ; 항공기)에서의 利點이 있다. 일반용 베어 링에서 回轉子 (ro t or) 와 固定子 (s t a t or) 의 성분으로 서로 다른 금속을 사용할 때보다 결정화유리와 금속 또는 서로 다른 결 정화유리를 사용하면 마멀이 최소화될 수 있다. 결정화유리에서는 .ba ll, roller, jou rnal bear i n g(軸의 首베 어 링 )의 각종 모양이 제 조되 며 金屬軸과 가옥에 결정화유리를 피복하는 기술이 발전되고 있다. (2) 펌프, 밸브 및 파이프 결정화유리 의 강도와 우수한 마모처 항은 마모성 슬러 리 (abrasiv e · slurr y)의 조작에 사용되 는 펌 프, 벨브 및 파이 프를 조립 하는 데 사 용할 수 있다는 것을 암시하고 있다. 또한 대부분의 결정화유리는 우수한 화학적 내구성을 갖고 있기 때문에 대부분의 금속에서 바람 칙하지 못한 質의 低下 (de t er i ora ti on) 를 가져오는 조건하에서 부식성 액체와 접촉하는 곳에 결정화유리를 사용할 수 있다. 스테인레스강 도 일부 응용될 수 있으나 결정화유리의 마털처항이 더 우수하기 대 문에 유리하다. Pin c us1) 는 펌 프의 날개 (i m p ellor) 와 케 이 스 및 파이 프를 (3- sp od u- · mene/kea tit e 고용체를 함유한 저팽창결정화유리를 사용하여 만들 었다. 저팽창결정화유리논고온유체를조작하는데 적합한높은열충 격 저항을 준다. 금속에 이용되는 기술이 그대로 결정화유리에 적용 되며 마모저항성코팅을 한 금속들의 피복 (cladd i n g)도 설계상의 융통 1) A. G. Pin c us, Advances in Nucleati on and Crys t a l liz a ti on in Glasses, p. 210. Americ a n Cerami c Soc iet y (l97 1 ).
성을 갓게 한다. (3) 熱交換器 차량의 가스터빈 엔진에는 효율이 높은 열교환기가 필요 하 다. 페. 열을 회수하지 않으면 全勅率은 경제적으로 낮아진다. 순환공기가 ’ 연소실에 들어가기 전에 가열된 구조를 지나가도록 뜨거운 배출공 기가 먼처 축열실을 가열시키는 菩熱熱交 換器 (re g enera ti ve heat ex- chan g er) 의 설계를 하여 야 한다. 이 응용에는 높은 화학적 및 치수안 _ 정성을 갖고 또 열충격에 견딜 수 있는 재료가 요구된다. 열팽창계 수가 거의 0 에 가까운 결정화유리가 이들 요구를 만족시킨다. 열교환기의 최적설계는 뜨거운 가스와 차가운 공기가 반대방향으 로 흐를 수 있는 多孔質板(p orous d i sc) 으로 된다. 이 설계의 성공여 부는 다공질판과 가스 및 공기의 導管 사이의 효율적인 封着 (sea li n g) 에 의해 좌우된다. 이것은 가열과 냉각시 그 치수의 변화가 없는 一 재료를 사용하면 가장 좋다. 죽, 판의 재료는 열팽창계수가 거의 0 에 가까와야 한다. 이 응용에 결정화유리를 선택하는 다른 이유가 있다. 연교환기의 구조는 공기와 배출가스의 흐름에 비교적 장해를 주 지 않아야 될 분만 아니라 신속히 가열되어야 한다. 비열은 최대열 용량을 갖도록 가능한 커 야 한다는 것 이 분명 하다. Goss2) 는 열팽창계수가 매우 작은 (-2x10 - 1°C - 1) 결정화유리가 一 이 응용에 적합하다고 보고하였다. 이 재료는 치수안정성과 우수한 열충격저항을 갖고 있다. ’ 이것은 높은 비열도 갖고 있으며 화학적 으로 안정하여 1100°c 까지의 온도에서 장시간 운전에 적합하다. 열교환기는 용융 또는 소결에 의해 얇은 벽을 갖는 결정화유리의 튜브를 연속적으로 만들 수 있지만, Hollenbach” 가 고안한 공정에 의해 輕 量 構造를 만들 수 있다. 이 방법에서는 유연한 종이 擔體 가 一 결정화될 수 있는 유리분말의 현탁액으로 코팅된다. 코팅된 종이는 開벌집형 (op en honey comb- typ e) 을 만들기 위해 평평한 판을 모아 波 ? 型板으로 한다. 모아전 재료들은 열처리공정에 보내져 종이는 태워
2) C. L. Goss, Prod. Eng n g, 33, 52(1 9 62). 3) R. Z. Hollenbach, U. S. Pate n t No. 3112184(1963) .
버리고 유리는 소 걷 및 결칭 화 시켜 강하나 얇은 벽을 갖는 결정화 유리의 구조가 형성되도록 한다. 이런 방법으로 형성된 벌집모양의 재료 (cellular ma t er i al) 는 일반금속제 가공기 구로 자르거 나 구멍 뚫기 , 연마를 할 수 있다• 벌집모양의 결정화유리의 다론 응용으로는 적의선버너, 화학공학 에 이용되는 觸媒妃體 , 低溫 學 (cr y o g en i cs) 에 사용되는 열교환기가 포함된다. (4) 築 臘 유리를 용융시키는 대형가마(탱크가마로 알려쳐 있음)는 兩火벽돌로 만든다. 이 가마에 서 瑢融 鑄 造(fu s i on-cas t) 벽 돌은 용융유리 의 부식 에 대한 저항이 있지만, 용융주조벽돌 사이의 연결부가 부식되어 용융 유리의 침식을 피할 수 없는 문제가 생간다. 이와 같은 부식은 유 리의 質울 처하시킬 분만 아니라 植의 수명을 감소시킨다. 밀페에 요구되는 성질은 용융유리의 부식에 대한 저항, 遠의 작업온도에서 의 안정성, 벽돌재료와 매우 비슷한 열팽창계수, 작업온도범위에서 밀페 재 (sealan t)와 벽 돌 사이 의 연결부가 파괴 되 지 않고 작은 이 동이 가능한 약간의 가소성 이 필요하다. 이런 성질을 구비한 결정화유리의 시멘트에 대한 Ha y ward4) 의 연구가 있다. 분말이나 슬러리 (slurr y)로 한 재료를 這의 가열중 부· 분적으로 용융하여 내화벽돌에 찰 젖고 결합하도록 한다. 다음에 결정화시키면 결정화유리의 결합재가 생긴다. 대규모의 결정화유리 시멘트실험을 통해 상당히 부식문제가 감소된다는 사실이 확인되었 다. (5) 기타 應用 결정화유리의 화학적 안정성과 함께 우수한 마떨저항은 選鑛機 (jig) 및 電氣放電加工工程에서 요구되는 성분으로 이용할 · 수 있다. 다른 응용으로는 결정화유리의 兩久性울 이용하여 건축용 결정화 * 유리를 생산하고 있다. 미국과 일본에서는 건축용 결정화유리가 제 조되고 있으며, 생산품으로는 커텐벽, 건축용 블럭, lift와 같이 교
4) P. J. Hayw a rd, Glass Tech110I. , 19, 없(1 978).
동량이 많은 곳의 내장재 등이 있다. 약간 다른 취향으로는 海底 構 造物의 전설, 深海用 容器 가 있다. 높은화학적 안정성, 내부석성과 함께 매우 높은 압축강도는 이 분야의 응용에 매력 있는 목성을 갖 고있다. 결정화유리의 우수한 화학적 내구성을 이용한 다른 응용으로는 화학 및 식품가공업에서 사용되는 銅 으로 된 큰 용기의 내부코팅이 다. 이 목적으로는 오랫동안 유리狀 법랑코팅이 사용되었으나 미립 자로 된 결정화유리가 더 유리하다. 급격한 온도변화에 대한 우수 한 처항과 함께 코팅의 강도가 높기 때문에 허용되는 조작조건이 더 넓 다. Sandfo r d 등”은 유리 상법 랑코팅 보다 嗣 酸 性, 열 충격 저 항성 , 강도가 더 크기 때문에 이 응용에는 결정화유리의 조성이 좋다고 설 명하고있다. 결 정 화유리 는 汚染制御 (po lluti on contr ol ) 및 새 로운 에 너 지 源의 중 요한 분야에서의 응용이 개발되고 있다. 이런 예로는 자동차배기계 로질부 결터정 화탄유화수리를소 를사 용제한거다하.기 다위른한 예 再로 燃는裝 N置a (—a ftS e r밧bu 데rn리er의) 중封에 着 에다 아공 용되며 고온봉착이 잘되고 용융소오다와 접촉될 때 질 저하가 없는 - 물질로 결정화유리가 사용된다. 6.2 電機 및 電 子工學에서의 應用 (1) 金屬의 封 着 금속의 接合온 전기 공학, 마이 크로전자공학 및 전공튜브제조에 중요한 분야이다. 유리-금속봉착은 이들 기술분야에서 매우 중요한 위치를 접유하고 있으나 고온공정이나 조작이 요구되는 곳에서는 세라믹의 우수한 기계적 성질과 내화도가 더 유리하다. 결정화유리 는 유리와 세라믹의 유용한 성질들을 대부분 가지고 있어 장치들의 - 조립에 사용되는 금속들의 봉착에 사용되는 매우 중요한 재료이다.
5) E. A. Sandfo rd , D. H. Hall and G. P. K. Chu, U. S. Pate n t No. 3368712 (19 68) .
금속봉착용 결정화유리 를 선댁하는 기준은 미소수축에 의해 생가 는 위험한 고응력의 발생을 방지하기 위해 열팽창계수가 매우 비슷 하여야 한다. 그러나 실제 응용에 따라서는 다른 성질이 중요하기도 하다. 높은 기계적 강도가 요구되며, 고전압절연체에서는 높은 유 전파괴 강도도 요구된다. 진공튜브의 웅용에 서 는 고온의 가스배 출공 정에 견딜 수 있어야 하며 튜브가 고주파에 응용될 때는 낮은 散逸 因子 (d i ss ip a ti on fac t or) 도 요구된다. 금속봉착의 응용에서, 결정화유리의 多樣性 은 열팽창계수를 매우 넓은 범위에 걸쳐 변화시킬 수 있기 때문에 실제적으로 모든 금속과
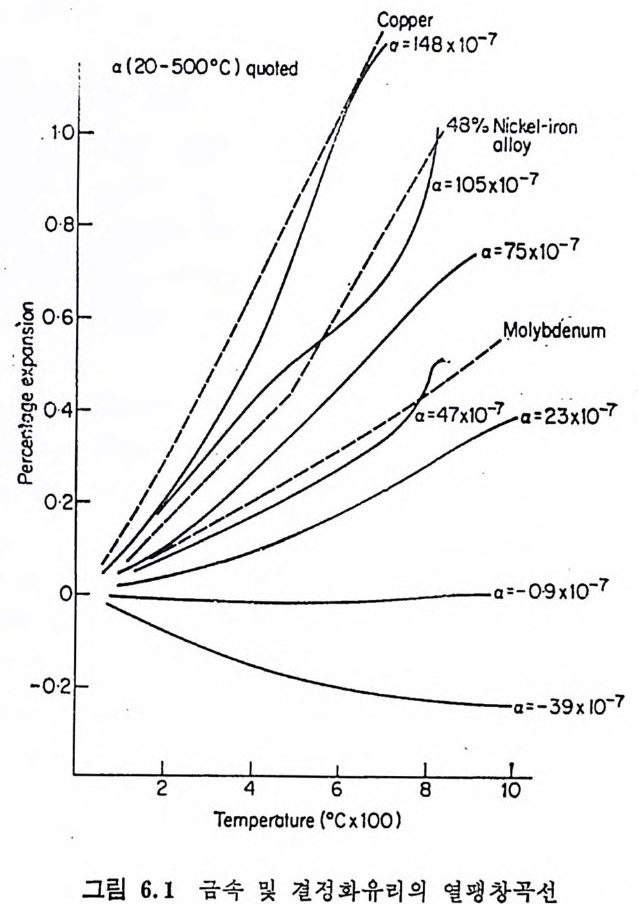 Cop pe r
Cop pe r
팽창계수를 일치시킬 수 있다는 사실에 근거를 두고 있다. 이 다양 성은 유리나 일반세라믹에서는 얻을 수없다. 그림 6.1 에 결정화유 리와 금속의 열팽창변화를 예시하였다. 금속에 결정화유리를 봉착시키는 데 2 가지 기본공정이 있다. 이 들 중의 하나는 세라믹(예 ; 알루미나)을 금속에 접합시키는 데 사용 하는 기숟과 매우 바슷하다. 보통 압축에 의해 결정화유리 성분이 성 형되며 결정화를 위한 열처리 후 요구되는 치수公差는 다이아몬드 연마로 이루어전다. 그후금속에의 봉착은 중간결합재를 사용한다. 다론 예로는 특수봉착용 유리 나 결정 화유리 의 薄層 또는 黃 銅 (braze) 의 금속충이다. 이것은 결정화유리 부분의 含金屬化(p reme t~lli za ti on) 나 T i과 같은 활성금속을 편입시킨 목수 황동충을 사용하여야 한 다. 중간결합재로 봉착한 예로는 M ill er 등 6) 에 의해 설명되었다. cor- - d i er it e 형 결정화유리가 매우 우수한유전성질과 함께 W, Mo 의 열 팽창계수와 매우 비슷하기 때문에 선택되었다. 또한 이 재료는 가 스두과율이 작다. 실제 듀브에서, 2 長方形의 압축성형물은 실투가능 한 solder 유리 에 의 해 端과 端이 봉착되 었 다. 텅 스덴리 드선 (lea d w ir e) 과 배 출구는 2 개 의 압축물 사이 의 봉착된 부분율 통과시 켜 듀 . 브화한다. 이런 방법으로 제조된 튜브는 5000 시간 이상의 사용기간, 400°C 에서의 연속조작능력 및 750°C 까지의 열주기에 견디는 능력을 가 진 우수한 특성을 나타냈다. 이들은 방사선노출과 塩噴霧 (sa lt spr a y ) 시험에 대한 처항성도 있다. McMi llan 둥”은 중간결합재를 사용한 금속에 대 한 결정화유리 의 봉착범위를 보고하였다. 사용된 금속은 Cu, Ni 및 軟鋼이고 결합 용 매질로는 유리, 결정화유리, 활성금속황동이다. 매우 우수한 기 계적 강도를 갖는 견고한 전공봉착이 언어질 수 있다는 사실을 알았
6) C. F. Mi ller and R. W. Shep ar d, Advances iii Elect ro n Tubes, (Ed. D. Slate r ), Perga m on Press, New York(1 9 61 ). 7) P. W. McMi llan , B. P. Hodg so n and G. Partr i d g e , Glass Technol. , 7, 46 (19 66) .
다. 결정화유리를 금속에 봉착하는 두번째 기본공정은 유리상태의 재 료를 봉착한 후, 이 유리를 열처리하여 고강도결정화유리로전환시 키는 결정화유리의 목성을 완전히 이용하는· 방법이다. 이 방법은 McMi llan 둥 8) 에 의 해 처 음으로 소개 되 었 다. 이 공정 에 서 는 다음과 같은 약간의 어려움이 있다. 먼처, 비교적 적은 경우이지만 母유리 와 결정화유리의 열팽창계수가 같을 때 결정화유리의 열팽창곡선과 금속의 열팽창곡선을 일치시켜야 하기 때문에 모유리가 금속에 봉 착될 때 큰 불일치가 생길 수 있다. 이 문제는 봉착시 유리가 결정 화유리로 완전히 전환될 때까지 유리의 스트레인접 이하로 냉각시 키지 않으면 극복된다. 이 방법에서는 미세한 열수축에 의한 응력 이 발생하는 것을 피해야 된다. 다음에 일어날 수 있는 문제는 유 리가 결정화유리로 전환될 때 일어나는 체적변화 때문에 일어난다. 금속에 봉착된 결정화유리에서는 이것은 약 1% 의 線 收縮에 해당된 다. 이와 같은 변형이 제거되지 않는다면 매우 큰 응력이 발생하여 봉착부분이 붕괴된다. 다행히 McM ill an 둥”에 의해 보여전 결정화 유리의 조성과 열처리주기를 적합하게 선덱하면 결정화유리가 접성 변형을 하는 온도범위에서 체적변화가 일어나 위험스러운 고옹력의 발생을 피할 수 있다. 결정화유리를 금속에 칙접 봉착하는 2 가지 기본방법이 있다. 첫 번째 는 豫熱 된 금속물을 형 들(金첼 mould) 에 넣고 용융유리 를 도입 한다. 최 종봉착조립 품(fi nal seal assembl y)은 압착이 나 원십 주조법 (centr ifu ga l cas ti n g)에 의해 성형된다. 봉착조립품은 결정화유리의 핵생성온도로 유지된 這 에 넣어 유리가 결정호H l 때까지 열처리주 기를 제어한다. 두번째 기술은 흑연형틀에서 금속물과 함께 조립되는 유리를 넣 는다. 조립품은 제어된 분위기(금속물의 산화와 흑연형를의 질저하를 방지하기 위해)에서 열처리주기를 따르게 한다. 열처리는, 유리가 금
8) P. W. McMi lla n and B. P. Hodg so n, Eng n g. , 196, 366(1 9 63) . .9) P. W . McMi llan , B. P. Hodg so n and G. Partr i d g e , Glass Technol. , 1, 121 (19 66).
속에 봉착하여 결정화되어 금속의 열팽창과 거의 일치하는 전정화 유리가 되도록 한다. 첫번째 봉착공정의 이접은 분리된 봉착공정을 사용할 때 결정화 유리가 정밀한 公差를 갖도록 미리 성형할 필요가 없다는 것이다. 이런 방법으로 수많은 금속을 적당한결정화유리에 봉착할 수있다. 이 금속들에는 각종 N i― Fe 합금, Cr ― Fe 합금, 수많은 鋼(값싼 軟 鋼 을 포함)들이 포함된다. 세라믹형 재료가 연강이나 구리에 봉착되 논 능력은 연강이 전기공학산업에서 구조재로 널리 사용되고 구리 는 도체로 가장 많이 사용되기 때문에 특히 가치가 있다. 그림 6.2 는 직접봉착공정에 의해 만들 수 있는 봉착조립품의 기.
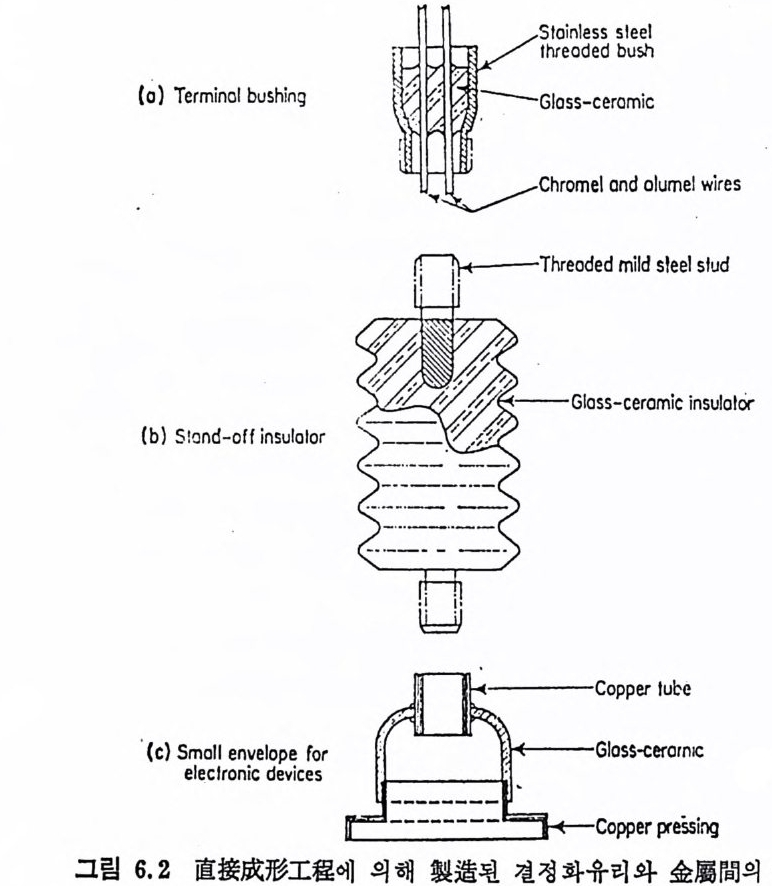 Slhtrae ino lde essd sbtue 삽 e l
Slhtrae ino lde essd sbtue 삽 e l
본 섣 계를 도시하였다. 전공 듀브 외피 (envelo p
 그림 6.3 眞空스위치用 결정화유리/金屈의 外皮
그림 6.3 眞空스위치用 결정화유리/金屈의 外皮
 그립 6.4 直接封着工程에 의해 導線이 封着物과 基板울 관통한
그립 6.4 直接封着工程에 의해 導線이 封着物과 基板울 관통한
금속봉착에 적합한 2 가지 결정화유리의 전기 및 다론 중요한 성; 질을 표 6.1 에 실었다. 연강에 봉착된 결정화유리 A 는 높은 유전 파괴강도를 갖고 있어 고전압철연체의 제조에 적당하다. 구리에 봉· 착된 결정화유리 B 는 낮은 유전손실독성을 가지고 있어 전자공학·
표 6.1 軟銅 (A) 및 구리 (B) 의 封着用 으로 개발한 진정화유리의 성질 Prop e rty and unit s A B Densit y(gc m-3) 2. 52 3. 14 Modulus of rup tu re(MNm- 2) 286 251 Young 's modulus(GNm- 2) 92 82 Thermal exp a nsio n coeff icien t 20 to 600°C, (°C-1) 140X l0-7 178X 10-7 Defo r mati on tem p er atu re(°C) 850 750 Die l ectr i c breakdown str e ng th (kVmm 기 447 30 Volume resis t i vi t y at 20°C (ohm cm) 3. 2 X 1015 1. 9X 1015 Permi ttivi t y(2 0°C) at: 1 MHz 5.0 5. 8 10 MHz 5. 8 100 MHz 5. 3 5. 8 1000 MHz 5.5 5. 9 Loss ang le , tan ~(20°C) at: 1 MHz 0,0023 0. 00032 10 MHz 0.00028 100 MHz 0.00050 0,00020 1000 MHz 0,00081 0.00053 의 응용에 적합하다. (2) 絶緣體 및 부성 (bushin g ) 견정화유리의 높은 유전파괴강도와 기계적 강도는 일반용 전기자 키와 비교할 때 더 얇은 단면으로도 사용될 수 있어 중량이 감소되 며 설계가 더 자유롭기 때문에 이접이 많다. 유약바름(g laz i n g)이 필요없는 平滑한 표면은 전기적 파괴의 원인 이 되는 表面汚染物質의 생성을 감소시키기 때문에 유익하다. 變 壓
器 bush i n g에서와 같이 절연체가 금속에 완전히 밀봉된 봉착이 필 · 요할 때가 많으며 금속에 결정화유리의 열팽창이 일치되는 능력은 연주기 중 발생하는 응력이 낮기 때문에 확실성 있는 접합을 얻을 수 있 다. 또 금속과 결정 화유리 의 봉착은 접 합부의 保全性(i n t e g r ity) 이 크다.,· (3) 高溫電氣絶緣材 결정화유리의 높은 전기비처항은 유기물의 철연체로는 걱합 하지 않은 원자반응기내의 熱電對 와 장치전선과 같이 고온에서 사용되는 전선이나 導體 의 철연체로 사용된다. McM ill an10) 은 이 응용을 위해 개발한 특수형 결정화유리를 제조 하였다. 이것은 규산영보다는 인산영조성이며 알칼리금속산화물은 함유하고 있지 않다. 이 형의 대표적인 결정화유리는 높은 체적바 처항 (300°C 에서 1012 ohm·cm, 500°C 에서 10 9 ohm·cm) 을 갖고 있다. 이 결정화유리는 연속코딩공정에 의해 각종 전선의 전선에 응용할 수 있 다. Chromelt 과 alumel* 熱電對 및 Pt 나 Pt 합금을 함유한 다른 전선에도 밀착된 코팅이 가능하다. 높은 전기비저항과 함께 결정화유리는 우수한 유전파괴강도를 갖고 있다. 25nm 두께의 결 정화유리로 코팅된 한 쌍의 감간 전선(t w i s t ed w i re) 은 파괴전압이 600 ~800V 이다. 결정화유리 철연재는 질저하를 가져오지 않고 700°C 의 높은 온도에서 안전하게 사용할 수 있다.
10) P. W. McM illan , J. Scie n ce and Technol. , 37, 25(1 9 70). t* aclhrumoemle 은! 은 N Ni ;i ;9 48%9. , 0%A,l ; 2C. r0 %; 9,. 8 S%i ,; lF. 0e% ; ,1 . F0%e ;, 0M. 5n% ;, 0M. 2n% ; 의 2 . 5合%金 의 合金
(4) 電 子工學의 應 用에서 豫備成形된 回路系 전자공학산업에서는 프란트된 회로로부터 더 복잡한 웅용과학까 지 각종 형 의 예 비 성 형 된 회 로계 (pr efo r med c i rcu ity)가 많이 사용 되고 있다. 결정화유리의 성질은 이들 형의 응용에 적합하다. 특히 우수한 전기득성과 치수안정성은 고온에서 아주 유이하다. 결정화 유리의 프란트 호 ]로판은 화학철삭형 감광성결정화유리이다. 이 판은 미세한 穴洞으로 된 정밀한 공간모양 (3 차원적)을 가질 수 있다. 프린트된 회로판의 다른 모양으로 Cu, Ag 또는 N i로 된 金屬 ?自 은 직접봉착공정에 의해 결정화유리판에 결합된다 .ll) 이 笛은 도체 모양을 만들기 위해 표준공정으로 부식조작 (e t ch i n g)을 할 수 있다. A g나 N i笛은 이들 금속이 산화에 대한 저항이 있기 때문에 고온에 서의 응용에 유리하다.
11 ) P. W. McMi llan and B. P. Hodg so n, _Fr ench Pate n t No. 1317042(1 9 61 ).
표면금속화된 결정화유리를 제조하기 위한 신기한 공정은 Mc M ill an 등 12) 에 의 해 처 음으로 개 발되 었 다. 이 것 은 o. 5~7. 5 W t%의 CuO 를 함유한 결정화유리가 환원분위기에서 가열되면 금속구리필 름의 밀착된 표면이 얻어진다는 사실을 발견한 것에 근거를 두고 ‘ 있다. 이 공청은 결정화유리의 내부로부터 표면에 구리이온들아 이 동하여 표면에서 금속구리로 환원되어 일정한 두께의 금속필름으로 석 출된다. 구리 필름은 표준방법 으로 부석 시 키 면 導體經路 ( conduc ti n g p a t h) 를 만들 수 있 다. 이 금속충은 모든 노출된 표면상에 서 생 성 되 기 때문에 금속코팅된 튜브와 각종 전자장치에 장래 응용가능성이 있는 다른 복잡한 형상들을 만들 수 있다. 실제로 Sek i 13) 는 이돌 가능성을 더 발전시켜 프린트된 회로판, 처항기 (resis to r ) 및 전자현 미경의 부품을 제조하기 위한 기술을 발전시켰다. B y er14) 는 높은 안정성의 회로를 제조하기 위한 홍미있는 기술에 대해 설명하였다. 이 공정은 결정화유리의 일부가 접촉부분에서 가 열되면 내부확산이 일어나 접촉부분은 完全 一體化된 물질로 전환 ·된다는 사실에 근거를 두고 있다결합은 보통 결정화주기 중이나 다 음의 조작에서 얻어진다. 회로제조에서, 결정화유리의 판은 溝(g roove 나 slo t)나 穴洞모양을 제조하는 4 장에서 설명한 공정을 사용하여 광화학적 기계가공을 한 다. 이 판을 결합시킬 때 도체모양은 溝둥의 배열에 의해 정해전 다. 도체는 결합온도(보통 약 850°C) 에서 용융하지 않는 비교적 내화 성인 금속이어야 한다. 이 경우 도체는 열처리 전에 도체 channel 중 ` 에 주입되거나 분산된다. 도체가 처융접의 금속이나 합금일 경우에 는 용융금속을 결합공정 후 결정화유리器具 중의 통로에 吸引方法 으로 引上시킨다. 이 공정은 마이크로전자공학에서 사용되는 습도, 압력, 온도의 영향과 같은 의부인자들로부터 완전히 차단된 多層回路의 제조가능 성을 제공하고 있다• 유기질판은 습기에 대해 완전히 불두과성이 야
12) P. W. McMi llan and B. P. Hodg so n, Brit. Pate n t No. 944571(1 9 63). 13) S. Seki, Proc. X Int. Cong r . on Glass, 14, 88(1 9 74). 14) M, By e r, U. S. Pate n t No. 3040213(1 9 62).
니므로 절연저항에 의한 질저하가 일어날 수 있기 때문에 이와 같 은 응용에는 결정화유리가 더 좋다. (5) 마이 크로電子工學用 基板 컴퓨터와 비슷한 장치를 제조시 매우 복잡한 확산과정에 의해 만 들어 지며, 전기적으로 절연성기판인 실리콘짚 (ch ip)을 수많은 장치 를 함유한 각 부분에 끼워야 하며 이렇게 함으로써 각종 활성성분 이 상호 연건되게 된다. 알루미나세라믹이 이 응용에 널리 사용되어 왔으나 결정화유리가 일부 유리한 접도 있다. 이들은 분산된 도체모양을 만들기 위한 공 정이 고안된다면 곧실용화될 것이다. 이들중 하나는 厚필름기술로 알려 진 것 으로, 전도성금속(보몽 금)을 함유한 pa ste 를 스크란프린 트법에 의해 요구되는 배열로 한다. 2 번째 방법은 도체모양울 도체 배열을 얻기 위한 mask 를 사용하는 전공증발법에 의해 침전시킨 다. 결정화유리는 각종 금속을 단단하게 결합시킬 수 있기 때문에 厚 필름기술에서는 유용하며 매우 平滑한 표면처리를 할 수 있기 때문 에 薄 필름기술에서는 특히 유익하다 • 기판설계에서는 桂能力(p lu g in ca pab il ity)을 갖는 단단하게 결합된 接緖用핀 (connec t or pi n) 이 삽 입되어야 한다. 이것은 앞에서 설명한 직접봉착기술로 결정화유리 를 사용하면 쉽게 얻어지며 봉착된 합금핀이 정밀하게 정렬된 기판 이 제조된다. 기판재료로서 결정화유리의 단접은 열전도도가 알루미나세라믹보 다는 상당히 낮을 가능성이 있다는 것이다 . 일부 반도체장치에서는 단위면적당 力의 散逸(p ower d i ss ip a ti on) 은 매우 크며 따라서 과열에 의한 장치의 손상을 방지하기 위해 열을 제거하여야 한다. 이 문제 를 해결하기 위해 McMi llan 둥 15) 은 底面에 일정두께의 구리판을 사 용하여 복합기판에서 열을 낮추는 방법율 제안하였다. 이 장치에서 결정화유리의 코팅이 구리판(약 3mm 두께)의 반대 면에 사용되었다. 판의 구멍을 구리선이 봉과하게 하고 철연성 결정화유리로 봉착시켜 15) P. W. McM illan , B. P. Hodg so n, J. D. Lale and S. E. Davie s , Brit. Pat· ent No. 1232621Cl970).
2 면 사이를 연결시켰다. 이 판들의 각면에 厚 필름회로를 붙이고 컬 정화유리코덩으로 덮으면 다론 회로충을 더 붙일 수 있어 多層 能力 을 갖게 된다. 이 판의 한 端의 인접영 역 은 강제적인 냉각 을 시키 기 위해 코팅하지 않은 채 로 남겨 둔다. 이런 형의 기판은 장치의 공간에 잘 맞고 매우 우수한 熱 散 逸特 性 을 갖고 있다. 이것은 고속노 작동이 가능한 컴 퓨터 에 중요하다. (6) 薔電 器 强 誘電 性 結 晶울 함유하고 높은 유전율을 갖는 목 수 결정화유리에 대해서는 이미 5 장에서 설명하였다. 높은 유전율의 세라믹스를 일 반기술로 제조할 수 있지만 결정화유리의 공정을 사용하면 利 點 이 있다. 기본적인 잇접의 하나는 결정화유리의 조성이 유리상태에서 연속공정에 의해 매우 얇은 필름으로 引上될 수 있다는 것이다. 일 반세라믹스의 매우 얇은 판을 제조한다는 것은 극히 어렵다. 따라 서 단위체적당 높은전기용량 (ca p ac it ance) 을갖는유전충의 제조는걸 정화유리에서 더 쉽게 얻어진다. 결정화유리의 축전기를 만드는 공정은, 얇은 유리판과 전도성금 ` 속 적층시킨 후 조립품을 가열하여 유리를 연화시키고 유리적충 물의 端울 녹인다. 더 가열하여 조립품 중에 강유전성화합물을 결 정화시킨다. 적합한 결정화유리는 유전손실이 비교적 작고 유전고卜 괴강도가 높으며 우수한 철연처항을 갖고 있기 때문에 이 응용을 위 , 한 유용한 부가적인 목성을 갖고 있다. (7) 封着材 및 結合材 전자공학용 부품을 제조시 용용, 비틀림 또는 다른 구조적 되화 · 를 일으키는 온도에서 이들 부품의 영향을 받지 않고 다른 재료의 부품과 접합될 수 있는 봉착재가 필요할 경우가 많다. 윽별히 형식 화된 결정화유리가 이런 응용과 유리 또는 세라믹부품, 금속듭윤 결합시키기 위해 제조되었으며 반도체가 완성될 수 있었다 . 유리 와 금속성 분을 결합시 키 기 위한 접 합용 유리 (solder g lass) 가 수 년 동안 알려져 왔다. 이 기술에서는 접합용 유리의 얇은 총이 유동 ` 화되어 장치의 주성분이 아칙 단단한 온도에서 봉착면을 적신다. 그러나 접합용 유리의 봉착은 다음의 공정과 조작온도가 접합용 유-
리의 연화를 피하도옥 세한을 받는다는 한계룹 갖게 된다. 접합용 유리가 결정화유리로 전환되는 것은 더 높은 공정온도에서 가능하 다. 접합용 결정화유리로 Wt % 조성이 Pbo ; 70~80, ZnO ; 10~15, B 요 : 6.S~10 및 부성분으로 Al2 아와 S i 02 가 함유된 납-아연-붕 산염 재 료에 대 한 Cla yp oole16; 의 보고가 있 다. 미 분말유리 를 유기 용 액 중에 분산시켜 봉착면에 얇은 필름으로 한다. 예비 코탕된 떤울 접촉면에 놓고 420~4so0c 에서 30 분간 가열한다. 유리는 유동상태 가 되어 봉착되나 내화성을 더 갖도록 실두시킨다. 납-아연방산영조성은 열팽창계수가 80~120X10-7°C - l 인 유리를 봉착하는 데 적합하며 중요한 상업용 응용으로는 칼라 TV 튜브제조. 시 원추에 面板(fa ce p la t e) 을 봉착하는 데 사용된다. 아연붕규산염형의 다론 조성은 30~SOX10-7°C-1 범위의 팽창계수 를 갖는 유리나 다른 재료를 봉착하는 데 유용하다. 이들 결정화유 리의 중량% 조성은 ZnO ; 60~.6 5 , B2 아 ; 20~25, Si0 2 ; 10~15 및 부성분이다. 실리콘과 같은 반도체 재료의 코팅이나 다론 재료의 기판 또는 다 른 재료와의 결합이 요구되는 응용들이 있다. 반도성의 질저하를 일 으키는 실리콘의 구조적 손상을 피하기 위해 걷합온도는 용용접 (1410°C) 이하이어야 한다. 수축차에 의해 생기는 응력도 구조적 절 함을 발생하기 때문에 작아야 한다. 한편 결합재는 확산과정이 일 A어의I 나2온°도3도— 록에S i 0 서충2 분형행 한의 하 내여결화 정진성다화.이유 리C있 a가O어 , 야이B a런하O 며 응또 용다는에론 B 2적조 야 합작 를하들 다은첨 는가 1 한20것 0°을Zcn 이OM내— c M ill an 등 17) 이 보고하였다. 30~40X 10-1°C-1 사이의 열팽창계수를 갖는 결정화유리는 실리콘의 결합에 적합하다. 이들 조성은 주결정 상으로 Zn2Si0 4 (zin c o rt hos ili ca t e) 와 ZnA1204(zin c alum i na t e) 를 함유 하고 있다. 이들 결정화유리의 전기비처항은 높고 500°C 에서 보통 108 ohm•cm 보다 크다.
16) S. A. Clayp o ole, Brit. Pate n t No. 822272(1959). 17) P. W. McMi llan and G. Partr id g e , Brit. Pate n t No. 1151860(1 9 69).
n- 형 실리콘을 코팅하기 위해서는 유리를 미분말로 분쇄하고 유 동코팅 법 (flow -coati ng t echn iq ue) 에 의 해 숟러 리 형 태 로 적 용시 킨다. 결정화유리의 성분이 실리콘에 확산되는 것을 방지하는 0.5 p m 두께 의 산화물충을 만들기 위해 실리콘을 미리 산화시켜야 된다. 이렇 게 함으로써 결정화유리를 용해하기 위한 소성온도가 1180°C 까지 로 제한된다. 이 온도에서는 밑에 있는 실리콘이 약간의 손상을 입는 다. 10~75µm 두께의 코팅이 가능하며 이들은 1100°c 의 내화도를 갖는다. 결정화유리의 코팅은 실리콘성분을 결합하는 데도 사용될 수있다. 비틀림을 방지하기 위해 충분히 낮은 온도에서 처팽창의 붕규산 영유리성분을 사용하여 봉착하는 데도 문제가 있다. 예를 들면 TV 카메라 튜브를 설계시 광학적 특성을 처하시키지 않고 광학적으로 平坦한 표면판을 튜브에 봉착시켜야 된다. McM ill an 둥 18) 은 負의 열팽창계수를 갖는 결정화유리와 저융접 · p b Q― ZnO ― B2 아 유리 를 섞 어 복합봉착재 를 개 발하였 다. 이 렇 게 만 들어전 복합재료는 열팽창계수가 30X 10-7°C-l 보다 작고 광학부품 의 비틀림을 피하기 위해 비교적 낮은 온도에서 봉착하는데 사용할 수있다. 같은 연구자들 19) 에 의해 할로겐울 함유시켜 매트릭스유리의 연화 점을 낮추고 더 낮은 유동접을 갖는 복합봉착재도 개발되었다. (8) 電氣-光學材料 강유전성 결정들을 함유한 고유전율 결정화유리는 결정들이 충분히 작도록 열처리제어를 하면 가시스펙트럼에서 두명한 형태로 제조된 · 다. 이런 조건을 만족시키기 위해서는 결정의 크기는 가시광의 파 장보다 작아야한다. 적 합한 재료로는 강유전성상으로 소오다니 옵산영 20)21) 과 납티 탄산 염 22) 을 함유한 것이 있다. 이들 결정화유리는 분국면에 電場이 45°
18) P. W. McMi llan , G. Partr i d g e , Brit. Pate n t No. 1205653(1 9 70). 19) P. W. McM illan and G. Partr i d g e , Brit. Pate n t No. 13J 6 727Cl973) . .20 ) N. F. Borell i, J. Ap pl. Phys , 38, 4243(1967) . .2I) N. F. Borell i and M. M. Lay ton , l. E. E. E. Trans 011 Electr o n Devic e s, ED- 16 , 5110969) .
22) T. Kokubo and M. Tashir o , /. Non-Crys t . Soli ds, 13, 328(1 9 73).
로 배향될 때 이 재료를 동과하는 분국광빔의 분국면에서 홍미있는 전기-광학효과 (elec t ro-o pti cal e ffe c t)를 나타낸다. 이 효과의 크가는 전장의 2 乘에 비례한다. 비슷한 형의 전기-광학거동은 常誘 電 狀態 에 있는 일부 강유전성 단결정에서도 발견되나, Bore lli는결정화된 유리에서 관갇된 활성도는 적어도 강유전상태가 일부 존재하기 때 문이며 이 현상은 작용한 전장하에서 磁區 (doma i n) 가 再配向하는 것 과 관련있다고 지적하였다. 6.3 照明및 光學的 應用 (1) 램프덮개 放 電 램프와 같은 고강도光源에서는 두명 또는 반두명성과 함께 수많은 성질들을 구비한 재료가 필요하다. 높은 기계적 강도가 요 구되며 램프의 효율은 조작온도가 높을수록 커지기 때문에 변형하 치 않고 고온에서 견딜 수 있는 재료의 능력도 중요하다. 이런 이 유 때문에 반두명의 알루미나세라믹스가 방전램프제조에 사용되어 왔다. 그러나 이런 세라믹스의 결접은 이들을 금속전극에 봉착하기 가비교적 어렵다는 접이다. 결정화유리를 금속에 봉착하는 것은 결접이 더 적기 때문에 두명 한 결정화유리가 이 응용에 적합하다고 생각하였다. 무명한 결정화 유리의 대부분은 매우 작거나 거의 0 인 열팽창계수를 갖고 있어 W 이나 Mo 과 같을 금속과는 열팽창계수가불일치하는문제가 생긴 다. 고급결정화유리를 사용하면 되나 비경제적이다. 그러나 Mo 및 W 의 열팽창계수와 매우 近似하며 내화성인 두명한 결정화유리의 제조가 가능하다는 것이 발견되어 이들 금속을 봉착할 수 있었다. S t r yj ak 등 23) 은 주결 정 상이 g ahn it e(ZnAI2 아) 인 이 런 형 의 결 정 화유 리를 제조하였다. 규산영유리를 기초로 한 결정화유리는 방전램프에서 사용되논 할 로젠증기에 대한 처항이 우수하나 이들은 Na 증기와 반응하여 재료
23) A. J. Str y j ak and P. W. McM illan , J. Mate r Sc i. , 13, 1275(1 9 78).
를 黑化시킨다. 따라서 이러한 결정화유리는 Na 증기방전램프의 덮 개 재료로는 부적합하다. Na 증기에 대한 저항성이 있는 실리카롤 · 함유하지 않은 결정 화유리 가 제 조될 수도 있으며 Plesslin g e r 둥 24) 은 · 이러한 형의 수식된 칼슘-알루미노붕산영조성의 결정화유리를 제조 소 하였다. 이들 결정화유리는 램프덮개, 금속전극에 Na 중기저항성 세라믹덮개를 결합시키는 봉착재로 적합하다고 설명하고 있다. (2) Laser 用 部品 가스 laser 의 안정 성 능은 laser 구조 중에 사용되 는 부품의 치 수 안정성을 필요로 한다. 이런 이유 때문에 外皮나 다른 부품의 제조 . 용으로 팽창계수가 0 인 결정화유리를 사용하는 것은 홍미로운일 이 다. 의피에 대한 다른 요구로는 채워진 가스 특히 He 에 대한 낮은 · 두과성이며 이런 접에서 결정화유리는 일반저팽창유리보다 보통 우 · 수하다. (3) 望遠鏡의 反射鏡 반사형의 天體大望遠鏡의 성능은 반사경에 사용되는 재료의 성잘 에 ' 크게 좌우된다. 물론 이 재료는 광학연마가 가능하여야 하며 피 , 할 수 없는 온도구배로 생기는 반사경의 비들립을 최소한 줄이기 위해 가능한 열팽창계수가 아주 작아야 한다. 이전에는 대망원경의 반사경은 처팽창 (30X10-70c-1) 인 붕규산영유리로 만들었다. 팽창계 수가 매우 작은 (5X10-70c 크) 용융실리카유리를 사용함으로써 치수 안정성이 크게 전전되었으나 이 유리윅 내화성 때문에 반사경의 조 . 립에서 십각한 기술적 문제가 생겼다. 광학적으로 연마가능하며 팽 창계수가 0 인 결정화유리의 出現으로 큰 반사형 망원경의 성능에 눈부신 발전을 하게 되었다. 이런 형의 반사경은 미국과 독일에서 제조되어 왔다. 무게가 약 1soook g이고 칙경이 4m 나 되는 반사경이 주조법 및 제어된 열처 리주기에 의해 제조되었다. 직경이 10m 인 반사경도 같은 공정에 . 의해 제조가능하다.
24) G. A. A. Plessli ng e r, F. Berth o ld and E. Roeder, U. S. Pate n t No. 392660:?; (1975).
6. 4 航空_宇宙工 學 에 서 의 應 用 고속비행기와 우주선의 발달은 가혹한 조건하에서 조작가능한 재 료 를 필요로 하 게 되 었 다. 결정화유리는 어려운 수많은 도전에 아 용될 수 있으며 이들 재료가 이 분야에서 홍미있는 중요한 역할을 할것이다. (1) 레돔 고속 비 행 하는 비 행 기 와 미 사일은 레 이 다무선용 (radar aeria l ) 레 돕 (radome) 으로 알려 진 보호외 피 가 필요하다. 미 사일용 레 돔은 보통 · 미사일의 先 端 울 형성하며 半球狀, 圓 維 또는 o gi val 모양을 하고 있다. 비행기용 레돔은 嗣 體 의 위나 아래에 설치되며 적합한 기체 역학적 모양을 하고 있다. 樹 脂로 보강된 유리섬유가 일부 레돔에 적당하나, 고속에서는 공기의 마찰열에 의한 품질저하가 문제가 된. 다. 어떤 재료들은 이런 결점이 나타나지 않기 때문에 레돔의 설계 시 채용되어 왔다. 고속용 비행에 응용될 수 있는 레돔용재료에 대한 조건은 다음과 · 같다. a) 레돔에 의한 레이다신호의 至曲울 최소화시키기 위해 유전성- 수의 同 質 性 및 均一性. b) 유전상수의 온도계 수가 작을 것 . c) 조작주파수(예 ; 10000 MHz) 에서 유전손실이 작을 것. d) 고온에서 지속될 수 있는 높은 기계적 강도. e) 미사일이 고밀도 대기권에 재돌입할 때는 급속히 가열되므로 열충격저항이 우수할 것. f) 雨水에 대한 침식저항이 우수할 것. 폭풍우춤귈 7 고속 비행하 · 는 비행기나 미사일은 비행중 빗방울과 충돌하기 때문에 매우 십~ 충격을 받는다. 고알루미나제라믹스는 위에서 요구하는 물리적 성질을 대부분 가 지고 있다. 레돔의 기하학적 모양온 外形과 벽두께의 정밀성을 요 ~ 구하나 정밀하게 제어된 치수를 갖는 알루미나제라믹의 레돔울 재 ·
조.한다는 것은 어렵다. 소성중 큰 수축은 종종 비틀림을 가져오기 때문에 요구되는 모양을 얻기 위해서는 상당한 연마를 하여야 한 다. 레돔제조에 걷정화유리를 사용하면 결정화공정에 따르는 치수변 화가 작기 때문에 정밀한 모양을 얻기 쉽다. 유전성질이 매우 높은 군질성과 함께 최소한의 연마로 레돔의 최종형상을 얻을 수 있다. 레돔제조에 적합한 결정화유리는 알칼리를 함유하지 않은 알루미 노규산염 형 이 다. 한 예 로는, 주결 정 상으로 cordie r it e 를 함유한 결 정화유리이며 이 형의 재료가 미국에서는 상당히 많이 사용되고 있 다. 이 결 정화유리 는 Ti0 2 로 핵 생 성 시 킨 Mg O — A l203— S i0 2 유리 로부터 제조되며 이 유리는 매우 높은 균질성과 재생성을 확보하기 위해 P t로 내장된 탱크가마 중에서 용융시킨다. (2) 赤外線透明物 적의선으로 활성화되는 誘導系, laser 빔을 사용하는 거리측정장 치 둥에는 각종 영역의 저의선스펙트럼에서 높은 강도, 우수한 雨 水澄勉抵抗 및 높은 두명도를 갖는 재료들이 팔요하다. 광학적으로 두명한 결정화유리는 4 장에서 설명하였으나, 가시영역에서 불투명 한 일부 결정화유리도 적의영역에서는 두명하다. 촌재하는 결정이 고려되는 광의 파장보다 작으면 광산란이 일어나지 않으며 결정화 유리는 광을 두과한다. 대부분의 결정화유리는 크기가 1µm 보다 작은 결정들을 함유하고 있어 더 큰 파장의 적의선은 산란을 일으 키지 않고 동과할 수 있다. 그러나 실리카롤 함유한 결정화유리에 서는 S i― 0 결합의 기본흡수대가 매우 크기 때문에 약 4.5µm 의 과 장은 투과되지 않는다. 따라서 1~4.5µm 과장범위의 적의투과에 유 용한 고강도 결정화유리의 사용이 가능하며 일부 응용되고 있다. 두명도가 더 큰 파장에서 요구되는 경우 실리카가 없는 재료나 더 짧은 파장에서 흡수를 일으키는다른 산화물을 사용하여야된다. 이 가능성은 우수한 적의두과성과 더 높아진 강도와 내화도를 겸바 한 chalcog e nid e 형 바산화물유리 를 결정 화시 킴 으로써 이 루어 졌 다. 불행히도 chalco gen i de 조성으로부터 석출된 결정들의 일부는 에너 겨 며 간격 (band g a p)이 l eV 인 전자반도체 이 다. 물론 이 것 은 1 µm
부근의 흡수를 일으키며 이 재료는 1µm 보다 큰 파장에서는 불두 명하다. (3) 熱 保 設 材로서 결정 화유리 의 應用 우수한 기계적 성질과 함께 처밀도인 결정화유리는 비행기구조의 정밀부품에 유용할 것으로 예측된다. 이런 예의 하나로는 마모열효 과가 큰 고속 비행기날개의 前緣(l ead i ng ed g e) 에 사용될 수 있다. 平 坦하고 부착력이 강한 결정화유리코팅과 함께 금속성분을 코팅하는 능력이 귀중한 가능성을 창조하며, 경량이며 線 性인 복합재료를 제 조하기 위해 금속섬유로 보강한 결정화유리는 비행기와 우주선에 사용하는 귀중한 재료로 기대되고 있다. 6.5 核工 學 에서의 應用 원자력 공학에서는 온도, 압력 및 방사선의 가혹한 조건에 서는 일 반 재료들은 적합하지 않기 때문에 많은 새로운 재료둘이 개발되어 야 한다. 결정화 유리의 가능성 있는 일부 응용에 관해서는 이미 기 술하였으나, 결정화유리에 사용되는 原材料는 대부분 풍부하고 바 교적 처형하기 때문에 공급부족인 原材料를 보존한다는 필요성에서 볼 때 결정화유리가 앞으로 더 홍미를 끌게 될 것이다. (1) 反應器制御棒用 材料 붕소를 함유한 銅 울 비롯한 수많은 재료들이 반응기제어용 봉으 로 사용될 수 있다. 그러나 이 경우 Cd 과 In 과 같은 熱中性子의 높은 捕 獲 斷面 (ca pt ure cross-sec ti on) 을 갖는 고농도의 붕소와 다른 원소듈이 결정 화유리 중에 도입 될 수 있 다. McM ill an 등 25) 은 이 런 형의 2 개의 결정화유리에 대해 설명하였다. 그 중 하나는 유리 형성제로 실리카를 함유하며 다른 것은 붕소산화물을 함유하고 있 다. 이 2 형의 재료들은 높은 비율의 산화카드뮴울 함유하고있으나, 붕소산화물이 높은 중성자 포획단면을 갖기 때문에 보통 그 양온 붕 산영조성보다는 적다. 산화인디움은 에너지의 넓은 범위에 걸쳐 열 25) P. W. McMi llan and B. P. Hodg so n, Brit. Pate n t No.1063291(1 9 67).
중성자를 흡수한다. 붕소를 함유한 전형적인 재료는 다음과 같은 중량% 조성이 다. Cd0;3o, In2 아 ;5, B2 아 ;35, K20; 15, Ti0 2 ; 15 이 며, 붕소가 없는 재료는 Cd0;6o, In2 아 ;5, Si0 2 ;25, Na20;5, ·C aF2;5, Au;o. 027 이 다. 2 계로부터 만들어전 결정화유리는 만족할 만한 기계적 강도를 갖 고 있다. 붕산염형 재료에서 열팽창계수는 105~148X 10- 7 °C-1(20~ 500°C) 이고 변형온도는 750~850°C 범위이다. 실리카롤 기초로 한 재료의 열팽창계수는 65~100X 10-1°C- 1 이고 변형온도는 850~ 1000°c 이다. 스데인레스강 중에 결정화유리의 氣 密化 (encap sula ti on) 는 결정화 유리의 우연한 파괴가 일어날 때 반응기의 被毒 울 방지하기 위해 반 웅기의 응용에 필요하다. 비교적 높은 열팽창계수를 갖는 결정화유 리는 全溫度에 걸쳐 스데인레스강의 外裝과 우수한 열적 접촉을 유 지할 수 있기 때문에 유용하다. 이것은 중성자 포획에 의해 결정화 유리 중에 발생하는 열을 효율적으로 제거할 수 있다. 제어봉으로 이들을 사용하는 것 이의에도 중성자흡수용 결정화유리는 생물학적 의장재로서 유용할 것이다. (2) 反應器用 封着 원자력설비의 조작에서는 반응기의 수많은 접에서 온도와 다른 중요한 매개 변수의 감시장치 (mon it or) 가 필요하다. 따라서 수많은 熱電對와 器具케 이 불이 반응기 의 제 안된 곳을 관통하여 밖으로 나 와야한다. 사용되는 케이불은 보통 스테인레스강으로 의포]되고 단열재로 ' M g O 분말을 압축시킨 무기질단연재를 사용한다. 단열저항을 매우 감소시키는 습기가 침입하는 것을 방지하기 위해 케이불의 끝을 봉 착하여야 한다. 납땜용 세라리봉착이 이 목적으로 사용되어 왔으나 충분히 작은 것을 만들기에는 어려움이 있다. 직접봉착공정으로 컬 정화유리를 사용하면 직경이 2.5mm 정도로 작은 꼬인 도선봉착도 가능하다. 케이블의 끝을 납벰한 봉착은 고전공을 유지하며 21kg --e m-2 의 가스압력이나 상온과 700°C 사이에서 20°C/m i n 의 열주기 에 놓여도 안전하다.
(3) 放射性 廢棄 物의 處理 핵분열 반응기로부터 연료봉을 소모하는 공정은 半減期 가 긴 放射 性 核種 (rad i onucl i de) 을 함유한 다량의 페 기 물을 발 생 한다. 高速增殖 盧 가 널리 사용되었다면 위험성이 높 은 방사성폐기물의 양이 크게 증가하였을 것이다. 현재 페기물은 용액 상 태로 처장되며 분명히 이것은 매우 간 처장 기간중 환경주위에 누출되지 않는다는 확신 을 하기가 어렵다는 관 접에서 매우 불만족스럽다. 이런 이유 때문에 원자력공학은 되1 기물 울 고형화시켜 안정하고 더 취급하기 쉬운 형태로 발전시켜야 한다 고 열망하고 있다. 여러 가능성 중 가장 유망한 것 같고 전세계적 으로 집중적 연구, 개발이 진행되고 있는 것은 방사성폐기물을 적 당한 산화물(예 ; Si0 2 와 B 2 야)과 결합시 켜 이 들을 화학적으로 안정한 유리로 전환시킨다는 것이다. 이 재료의 블럭둘은 적당히 기밀화시 켜 안전하게 제여된 조건하에서 저장할 수 있다. 이 개발연구에서 결정화유리의 기술은 중요한 역할을 할 수 있을 것 같다. 처장방법에서 한 가지 조건은 물과 우연히 접촉하였을 대 방사성성분(예 ; Cs 동위원소)의 누출을 방지하기 위해 매우 우수한 화학적 안정성이 요구된다. 물리적 안정성과 높은 강도도 요구된다. 또 재료 중에 함유된 동위원소의 방사성붕괴는 열을 발생하기 때문 에 우수한 온도안정성과 함께 블럭으로부터 충분히 열을 제거할 수 있을 만큼 가능한 열전도도가 높아야 한다. 이와 같은 접에서 저장 용 유리를 제어된 결정화를 하여 결정화유리로 전환시키는 것이 유 익할 것이라고 생각된다. 6.6 醫學 및 관련분야에서의 應用 높은 기계적 강도와 다른 우수한 물리적 성질과 함께 결정화유리 의 화학적 불활성은 生醫學分野에서 응용가능성에 대한 홍미를 일 으켜M ac왔C다ul.lo ch26) 는 Li2 0 — ZnO - Si02 결정화유리 로부터 人工齒를 제 26) W. T. MacCullocb, Brit. Dent. J. , 124, 361(1 9 68):
조하였다. 관련된 분야에서 결정화유리의 분말은 重 合複合材인 챠 과용 강력 충전재 (fi ller) 로서 사용되 었 다. 걷 정 화유리 의 충전재 는 '[:.J:- 단하고 우수한 마모처항을 가지고 있어 이 응용에 유용하다. 또 매 우 작은 또는 0 인 열팽창계수를 갖는 결정화유리를 사용함으로써 自然齒와 열괭창계수가 거의 비슷한 복합재료를 제조할 수 있다는 잇접이 있다. 이것은 齒와 충전물 사이의 결합을 완전하게 유지하는 데 유용하다. Mi llle r2” 는 복합치 과용 강력 제 에 사용하기 위해 전 단용 X- 선에 대한 높은 흡수를 갖는 특수 결정화유리를 개발하였 다. 적합한 이식수술에 의해 손상되거나 변질된 뼈와 대치할 수 있는 상당한 가능성이 있다. 사용되는 재료는 강도가 커야 하며 동시에 독성이 없고 체내에서 주위환경과 일치하여야 한다. 특수합금이 사 용되거나 일부 重合材가 사용되기도 하였다. 일부 응용에서는 높은 마텔처항이 필요하다. 예를 들면 십한 관철영으로 고통받는 환자에 사용되는 人工基節連結部 (h ip foi n t)가 있다. 지금까지 사용되어 온· 것보다 더 좋은 성질들을 갖는 재료들이 개발되고 있다. 결정화유리는 높은 강도, 우수한 마모처항 및 화학적 불활성 때 문에 이들 응용에 이용할 수 있다. 앞으로 유용한 화학적 및 물리 적 특성을 갖는 재료가 개발될 수 있는 가능성이 있다. 안산영유리 를 기초로 한 결정화유리논 규산영계로부터 만들어전 결정화유리보 다 더 적합하며 미세다공질 재료를 만들 가능성도 있다. 이 방법에 서 걷정화유리의 移植은 결정화유리의 주위와 내부에 천연뼈의 구 ~ 조성장을 허용할 것이라고 상상할 수 있다.
Zl) G. Mi ille r, /. Dent, Res. , 53, 1342(1974).
제 7 장 결정화유리의 연구 및 개발의 중요성 지난 수십년 동안 결정화유리에 관한 기초과학과 공학이 눈부신 발 전율 하였으나, 기본공정을 더 확실히 이해하여야 할 분야가 아칙 도 많다. 이것의 달성온 재료과학에서와 마찬가지로 중요하다. 왜 냐하면 유리의 제어된 결정화를 기초로 한 수많은 공정, 결정화유 · 리의 微細構造 와 물리적 성질의 상호관계는 다론 중요한 재료분야 : 에서도 거의 같기 때문이다. 또, 에너지와 原料믈 보촌하여야 된다 - · 는 최근의 필요성은 새롭고 더 효과적인 방법으로 재료들을 사용하 겠 다는 욕망을 돋보이게 하였다. 따라서 결정화유리의 장래의 역할에 대해 고찰한다는 것은 기초 연구의 論題 로서 또 기술상의 중요한 재료로서 가치가 있다고 생각 된다. 7.1 결정화유리의 硏究 결정핵생성과 성장과정은 처음의 무정형유리로부터 전정화유리의 미제구조를 발달시키는 데 매우 중요하다. 이 과제에 대해 최근 수 년간 많은 전전이 있었으나 더 이론적이고 실험적인 연구를 필요로 하는 미해결의 문제가 아직도 많다. 準液狀不混和性 (sub-l iq u i dus i mm i sci b ility)을 포함한 기 본개 념 과 핵 생성 및 성장과정 또는 스피노달분해에 의한 2 상 유리구조의 발달 에 관한 개념들이 좋은 성과를 거두었으나, 결정핵생성 및 성장과`
정에 대한 豫備 分相(p r i or pha .se se p:i ra ti on) 의 효과는 찰 이해되지 못 하고 있다. 많은 결정화유리에서는 초기에 발생하는 유리 중의 분 상이 요구되는 미세결정질구조를 발달시키는 기본단계이기 때문에 더 많은 연구가 필요한 분야아다. 결정핵생성 및 성장과정은 예비 분상에 의해 모두 영향을 받는다. 일반적으로 핵생성밀도는 증가하 고 결정성장속도는 감소한다. 이들 2 효과는 미립화된 미세구조를 발달시키는 데 좋다. 그러나 확산과정에 내한 분상의 상세한 영향 은 찰 알려쳐 있지 않으며 결정화에 대한 분상의 역할이 이해된다 떤 본질을 알 수 있게 될 것이다. 더 홍미있는 접은 핵생성과 성장에 의한 분상과 비교하여 스피노 달분해가 일어나는 유리의 결정화거동에서의 차이접이다. 2 상 사이 의 계면에서의 조성기울기를 기준으로 한 2 가지 분상 사이의 뚜럿 한 차이는 다른 거동을 가쳐운 것으로 기대된다. 그러나 스피노달 적으로 분해된 유리에서의 상의 계면은 장시간의 열처리 후 갑자기 생기므로 어떤 영향도 결정화의 초기단계에서만 관찰될 수 있다. 어 떤 유리 에 서 는 記憶勅果 (memor y e ffe c t)에 대 한 약간의 증거 가 있다. 즉, 결정화된 유리를 재용융한 후 다시 결정화시킬 때 열처 리중 더 쉽게 결정화되는 경향이 있다. 또한 어떤 조성에서는 핵생 성범위보다 높은 온도범위에서의 용융공정과 유리의 냉각속도는 그 다음의 결정화에 영향을 미찬다. 이런 효과들이 액체상태에서 보통 기대되는 것보다 더 높은 규칙도를 갖는 작은· 영역이 유리용융체 중에 촌재하는 것을 의미하는지를 조사하는 것은 매우 홍미있는 일 이다. 이런 영역들은 이전의 결정화에 의해 생성된 결정구조나 유 리를 만들기 위해 사용된 결정질재료의 잔여물 (remnan t)을 나타낼 수도 있다. 만일 이들이 촌재한다면, 이 영역의 검출은 1 次配位穀 이하의 거리에 있는 유리 중의 원자배열을 확인할 수 있는 기술의 발전에 좌우된다. 이것은 어려운 문제이나 EXAFS(Exte n ded X-ray :Ab sorp tion Fin e S t ruc t ure) 연구와 Raman 분광학과 같은 기술이 발전 되고 있다. 유리구조의 고전적인 불규칙 망목구조설에 의해 가정하 였던 것보다 더 복잡한 분자그룹이 붕산영유리 중에 촌재한다는 증 거가 Raman 분광학에 의해 이미 밝혀졌다. 따라서 유리와 용융체
의 구조를 포함한 개념의 발전은 유리의 결정화를 포함한 개념의 재조사 및 수정을 초래할지도 모른다. 결정화유리의 부성분들은 핵생성 및 결정화의 과정을 修飾 하는 데 매우 중요한 여할울 한다. 이들 중 대부분은 핵생성촉진제로 첨가 된 성분이며 이들 중 일부의 역할은 최근 몇 년 동안 부분적으로 이 해하게 되었다. 준 0식 상블혼화성에 대한 중요한 효과를 측정하기 위 한 핵생성촉진제의 연구, embr y o 와 유리상 사이의 계면에너지에 내한 효과, 다른 결정상들의 配向重復成長 (e pit ax i al g row t h) 을 위한 불균질핵을 만들기 위해 석출시키는 핵생성제 단독 또는 다른 산화 물과 결합 하고 있을 가능성 둥아직도 상당한연구분야가 남아있다. 2 개의 핵 생성재가 결합함 으로써 나타내는 協力勃果 (s y ner gi s ti c eff ec t ) 는 핵생성제의 어느 한 쪽만을 사용할 때보다 핵생성이 더 촉진된 다는 관찰결과는 매우 이상하다. 핵생성촉진제로는 보통 부성분들이 결정화유리의 미세구조에 큰 효과를 미찬다. 예를 들면, 기본성분이 Li 20 ― S i 02 인 결정화유리에 더 큰 알칼리 금속이 온둘을 소량 첨 가하면 바람직 하지 못한 cris t o b - : a lit e 보다 석영생성이 촉진되며, 이것은 실제로 중요하며 연구할 가치가 있다. 별로 생각하지 않았던 유리나 결정화유리 중의 다른 부성 분은 유리 구조 중에 결합된 수산기 (hy d roxy l i on) 로 형 성 된 물 이다. 이 형태의 물은 眞空炤融 이의의 방법으로는 용융유리로부터 제거하기는 매우 어려우며 유리의 결정화에 대한 이 효과는 문제가 될 수 있다. 수산기가 존재하면 유리의 접성이 낮아지며 따라서 결 정핵생성 및 성장에서의 확산과정은 더 쉽게 일어날 수 있다. 물은 鑛 化劑로 오랫동안 인정되어 왔으며 유리의 결정화에 대한 이 효과 의 상세한 연구가 매우 요망된다. 다른 부성분들도 유리의 접성을 증가시키거나 감소시키는 효과가 있기 때문에 결정화과정에 영향을 줄 수 있다. 주어진 성분이 母유 리 중에서의 농도로부터 예측되는 것보다 더 큰 효과를 나타낼 수 있다는 사실이 지적되어야 한다. 대상의 산화물이 결정상의 구조 중 에 침전되지 않는다면 결정성장 이전에 산화물의 농도는 증가할 것 이머 이 전과 유리접성에 매우 큰 영향을 미칠 것이다. 따라서 부
성분은 결정성장속도를 높이거나 낮추는 데 기대하지 않았던 큰 ~ 과를 나타내게 된다. 일부 부성분들은 성장하는 결정 중에서 고용 체를 형성함으로써 결정성장과정에 영향을 미칠 수 있다. 결과적으 로 얻어지는 격자공간의 변화는 결정성장 동력학에 영향을 미칠 것 이다. 이들 문제에 대한 더 깊은 연구가 필요하며 유리의 결정화 중 고 용체 및 준안정결정상들의 광법위한 생성에 대한 연구도 필요하다. 특히 흥미있는 것 중의 하나는 일부유리가 결정화중에 일으키는 小 球 體 成 長 (s p heru liti c g row t h) 이다. 점성액체 중에서 특히 일어나는 이 결정화생성은 유기고분자들의 결정화에서도 중요하며 재료과학과의 2 분야 사이에서의 상호작용을 연구할 필요가 있다. 더 광범위한 연구를 위한 매우 중요한 분야 그리고 일반적으로 다결정질제라믹에서 중요한 분야는 결정화유리의 미세구조와 광물 학적 성분 및 그들의 물리적 성질 사이의 상호관계이다. 귀중한 연 구가 이미 이런 방향에서 이루어지고 있으나 지금까지 얻어전 많은 정보는 정성적인 것이라고 할 수 있다. 더 깊은 연구가 필요하며, 예를 들면 결정화유리의 기계적 성질에 대한 相들의 성질과 이들의 형태학은 계통적인 방법으로 변화된다. 이런 연구는 ' 결정화유리의 파괴강도를 측정하는 데 홍의 한계, 파괴표면에너지 및 내부응력과 같은 비교적 중요한 인자들을 평가할 수 있기 때문에 매우 중요하 다. 다른 물리적 성질 및 물리적 성질이 미제구조변화에 의해 영향 울 받는 방법들에 관한 연구도 매우 유익하다. 특히 전기전도도냐 유전손실과 같은 이온이동이나 확산을 포함한 성질들에 대한 효과 에 대해 더 집중적인 연구가 팔요하다. 이들 성질은 결정화유리의 미세구조변화에 매우 민감한 것 같으며 따라서 미세구조를 측정하 기 위한 시 험장치가 필요하다. 적 합한 常磁性이 온둘로 dop ing 시킨 결정화유리에 ESR( 전자스핀공명)분광기를 사용하는 것은 미세구조 연구에 가치있는 수단이 될 수 있다. 이런 연구의 묵적은 미세구조와 특성 사이의 기본적인 상호관계 를 얻는 데 있으며, 이 결과는 기술상 매우 중요하다. 결정화유리 의 미제구조로부터 그 특성의 예측이 가능하여진다면 결정화유리위
공업적 이용가능성이 쉬워질 것이다. 7.2 工學 및 應用 영가인 원료로부터 제조되는 고강도 결정화유리에 대한 탐색이 계속되고 있는 것 같다. 玄武岩과 같은 천연적으로 생성되고 풍부 한 재료로부터 제조된 결정화유리가 이미 유럽에서는 우수한 마텔 처항이 요구되는 응용면에 이용되고 있다. 약간 다른 방향에서, 페 기물을 유용한 결정화유리로 전환시키는 가능성도 있다. 이런 분야 중의 하나는 영기성원료로 治金工程으로부터 얻어지는 鑛 ~ (sla g)의 사용이다. 또 다른 가능성온 석탄을 연소시키는 발전소에서 다량 . 생산되는 fly -ash 의 이용이다. 이들 利用面에서의 발달은 재료들의 보촌(폐기물의 재이용)에 공현할· 분만 아니라, 다른 분야에서는 이용 하기 어려운 다량의 페기물을 처분할 수 있기 때문에 가치가 있다. 또, 유리의 주성분이나 핵생성촉진제와 같은 비싼 성분의 사용을 최소한으로 억제하면서 더 보편적인 재료들을 기준으로 한 결정화 유리의 발전이 큰 이익을 가져올 것이다. 모유리를 제조하는 데 높 은 융접을 갖지 않는 조성들을 찾는 것이 중요하며 그럽으로써 域 에 사용되는 내화물의 부식문제가 감소된다. 또한 일반유리에서와 가능한 비슷한 접도-온도의 특성을 갖는 조성을 선덱하는 것이 바 람직하다. 왜냐하면 유리의 성형공정범위가 넓은 것이 기술적으로 는 바람직하기 때문이다. 저렴하면서 고강도인 결정화유리를 제조하는 것이 容器제조업자 들에게는 제일 주목되고 있다. 만일 더 높은 정적 및 충격강도를 갖 는 결정화유리를 사용한다면 그 두께, 따라서 용기의 중량을 감소 시킬 수 있으며 결국 매우 큰 에너지절약이 된다. 이런 응용에서 표면을 결정화시킨 고강도유리의 사용은 가능성이 높으며 이 경우 화학조성상 일반용기의 유리에 가까운 재료가 사용될 수 있으며 접 성유동독성이 얻어질 수 있다. 만일 용기에 고강도의 유리를 기초 로 한 재료를 사용할 수 있다면 부분적으로 금속깡통과 풀라스틱 용 기와 대체될 수 있기 때문에 포장기술에 상당한 충격을 줄 것이다.
풀라스틱과의 대체는 이들 원료가 보동 기름이며 이 원료의 보존이 매우 요망되기 때문에 특히 상당한 이익을 가쳐올 것이다. 기술적인 옹용분야에서 결정화유리의 더 큰 발전이 일어날 것 갇 다. 예를 들면 견정화유리의 미세구조에 방향성을 갖게 할 수 있~ 며 이것은 전기 (이온)전도성에서 상당한 異 方性울 띠게 한다. 이것 은 Na ― S 밧데리와 같은 새로운 형대의 축전지에 사용되는 전해질 에 필요한 성질은 높은 이온전도성이다. 이와 같은 고온형 밧데리에 필요한 조건은 용융알칼리금속에 대한 저항성을 갖는 고온용 봉착 재이며, 이런 목성을 갖는 결정화유리의 개발은 가능하다• 결정화유리는 軟鋼과 같은 금속의 보호코팅으로 이미 사용되고 있으나, 가스터빈회전자날개에 사용되는 고온용 합금을 위한 兩火 코팅도 요구되고 있다. 여기서의 목적은 연료 중에 존재하는 무기 오영물질에 비교적 불활성인 코팅을 하는 데 있다. 이 오영물질은 합금을 부석시키는 粒界의 원인이 되며 그 결과 수명을 단축시키게 된다. 고온용 불침두성 결정화유리의 코팅이 이 문제에 대한 해답이 될 수 있다. 터빈날개를 완전히 결정화유리로 만들 수 있는가 하는 것은 문제접이 있다. 이 재료는 강하나 아직은 취약하여 일단 인칭 강도를 넘으면 파멀적인 결함이 일어난다. 그러나 적당한 섬유 목 히 연성금속으로 결정화유티를 강화시키면 파괴안성이 매우 강화되 며, 복합재료를 기초로 한 결정화유리의 분야는 가스-터빈엔진과 같이 국십한 조건에서 사용되는 공업재료의 새로운 분야를 산출하 게 되었다. 회전자날개에 적합한 결정화유리를 만드는 문제는 어렵 지만 내화성 결정화유리를 엔진의 다른 부품에 사용하기 위한 연 T 가 발전해 나갈 것이라는 것은 의십의 여지가 없다. 더 높은 엔진 온도의 가능성이 생길 분만 아니라 금속 대선 세라믹형 재료로 대치 한다는 것은 더 높은 효율과 함께 항공기엔진에서는 분명히 총중량 이 감소되는 잇접이 있다. 결정화유리의 가치 있는독칭은 찬유유리상과 각종 결정상의 제어 된 양울 함유한 미세구조를 발달시킬 수 있다는 접이다. 따라서 열 팽창계수가 0 인 재료를 제조할 수 있으며 이런 재료들은 복잡 미 묘한 計器에서의 사용이 증가되고 있다. 또한 全溫度範園에서 다몬
물리적 성질이 실제로 번하지 않는 결정화유리의 제조도 가능하다_ 예를 둘탄 탄성률이 실제로 유용한 온도범위에서 무관한 재료들 이 알려쳐 있으며 이들은 새로운 형의 計器에 매우 유용하다. 다 · 론 예로는 유전율의 온도계수가 0 인 결정화유리를 개발하는 것이 다. 온도에 대한 이 성질의 불변성은 전자공학장치에 매우 가치있 는것이다. 앞으로의 컵퓨터개발에서는 결정화유리의 가치있는 성질이 많이 이용될 것이다. 더 계산속도를 높이는 것과 함께 컴퓨터회로판의 全치수를 작게 하는 노력이 상당히 확산되고 있다. 실리콘깊으로노 결합된 수많은 장치들을 상호연결하는 데 팔요한 복잡한 전기회로 를 생산하기 위한 厚팔름기술은 여러 방법으로 도체인 금속과 親和 性있는 基質材料를 필요로 한다. 이전에도 기술한 것과 같이, 결정 화유리는 금속과 찰 結 着 되는 우수한 성질을 가지고 있으며 이것은 매우 중요한 성질이다. 또한 기질재료의 전기적 성질은 회로의 성 능에 상당한 영향을 줄 수 있으며 제어된 절연 및 유전성질을 얻을 수 있는 능력은 매우 중요하다. 증발기술에 의한 도체의 증착을 기초로 한 薄필름기술은 더 높은` 밀도를 갖는 회로를 가능케 하고 있다. 이 기술에서는 도체선을 보 촌하는 데 영향을 줄 수 있는 요철이 없는 표면을 갖는 기질이 중 요하다. 결정화유리의 매우 미세한 입도는 이런 결합부에서 가치있 는 재료가 된다. 결정화유리의 공학면에서 미래의 가능한 개발분야를 요약하면 득· 수분야에 사용되는 재료의 유도 및 응용이라고 할수있다. 대부분 특이한 성질을 갖는 결정화유리는 큰 다양성을 내포하고 있으며 비 금속재료의 그룹으로서 필적하는 다론 재료의 그룹으로부터 얻을수 ` 있는 물리적 성질보다 더 큰 융통성을 갖고 있다고 할 수 있다. 따 라서 공학의 여러 분야가 발전함에 따라 생기는 많은 요구를 결정 화유리논 해결하여 줄 수 있으며 이들 분야에서 궁극적으로 결정화 유리가 가장 큰 공헌을 할 것이다.
색인
-, 가교산소이 온 20, 105 강성물 199 강유전성 상 228 결정 272 강유전체 고 34 건정 성 장 3-7 , 46. 결정핵 34 생성 I3 생성촉진체 73 겅계 37 응력 195 계면에너지 25 . 고온압출범 . I59 추 출 범 . 162 고유유전파괴 230 고화(固化) I6 · 공동 (vo i d) 169 공동작용효과 98 공용온도 86 과냉각도 16 액체 16, 24 · 구동력 47 구리-루비유리 75 구멍 (hole) 21 구상소집단 37 굴철지수 I25 규칙효과 94, IO5 금형 (mold) u4 -ca rneg iei t e. 149 gah nit e 213, 275 ·ge hlenit e 96
L 나선전우 l 46 내부핵생성자리 69 내화도 126, 240 니 옵산영 (nio b ate ) 228 Knoop 경도 163 nep he li ne 149, 158 E: 다결정질 56 다공도 I65 단법위규칙 I6, I8 단사휘석 97 동경방향응력 I92 동경응력 I95 devit rit e 50, 61 dio p si d e 96 dis r eg ist r y 43., 7 9 dolomi te u2 2 레돕 I4, 277 리 둠규산영 146, 207 리 듐-알루미 노규산영 I76, I87, x94, 205 lap ping 132 lehr u5 Ra y leig h 비 I37 ruti le 87, I53, I67, I86 Cl 마그네 슘-알루미 노규산영 . 204 마믿 207 마털처리 I85
마이너스성장 62 망목형성산화물 20 떤7J:면적 57 면적강도 I67 미정설(微晶說) 24 macor 161 mag ne ti te 97 meli lite 96 meta s il ica te 28, 81 mi xe d alkali eff ec t 104 mull ite u3, 147, 168, 241 Mohs 경도 205 t:I 바나늄산유리 93 방사성핵종 28I 배 향중복성 장 43, 285 벼개면 I92 벽 개 성 (cleavag e) 160 복굴절 (bir e fr ing en ce) 157, 193 복극 I37 복합재료 I9° 부조화 (inc omp at i bi l ity) 84 분국물 70 분상 I2, 50, III 분자이동도 66 분지 파괴 (fork ed frac tu r e) 174 분해능한계 I30 불규칙망목구조실 I8 불균질핵 생 성 34, 41, 49 불혼화용액 꼬 비가교산소 21,89 비 석 (zeoli te) 22 비들림크리이프 246
비화학량론적 결정 IO4 batc h 112 bin o dal 51 /3- cordie r ite 159 /3- eucry ptite 126, 148, 150, 156, 171,. 177, 195, 221, 235 /3- spo d umene 82, 124, 126, 129, 149,. 157, 167, 17l, l76l94, 2I4, 22I,` 235 B- 석영고용체 124 人 산일인자 (d i ss ip a ti on fac to r ) 263 : 상경계 39 상한결 정 화온도 I 16, 121 서 빙 (anneali ng ) 32, us 서 냉요 II5 서 냉 정 77, 81, 154 석 영 34, II2 선택전자회철 146 섬유연화접 154 소구체 97 결정 130 성장 66, 286 화 I83 수밀도 57 스트레 인 접 33, 158 스피노탈분해 51,53 시차열분석 I33 시차팽창계연화접 96 온도 127, 24<> sap ph ir i n e 149 sil lima nit e u3 sp ine l • 150, 207 sp o dumene u3
·ste a ti te 218, 244 !St r ik i n g 현상 75, 99 。 안정불혼화 5I 압임 경 도 205, 207 압형법 II4 맥상선 34 연마처리 I84 연속인상법 Il4 연화정 33,8I ·연교환기 260 연유속 (hea t flux ) 48 연전도울 뱌 열처리주기 68 연충격저항 250 연확산운 27,249 영구압축웅력 I55 영구압혼 206 영구스트레인 I2I 예비분상 284 용융참열 40_ 용적걷정화 94 운모 I60 원곡인장응력 177 원십주조법 265 위스커 .15 9 유도기간 I42 유리전이온도 (T g) I 유전성 124 · 유전손실 I39, 2I6 유전손실각 59 유전들 m6 운전파괴강도 230 유효용저핵성 I35
융제 IOI 음극루미네센스 I30 웅고정 33 응력부식종 I93 응축계 37 이 동도 (mobil ity) 172, 2n 이 상거 동 (anomalous behavio r ) 204 2 상 액분리 87 이온장강도 23 2 차견정성장 Ill 입계 17 입계이동 247 akermanit e 96 albit e 64 anata s e 153 anorth i t e 94, 96 ilme nit e 88 orth o sil ica te 28 wi llem i te 64, 149, 151, 213 wollasto n it e 63, 94, 96 x- 선에 너 지 분산분석 132 x- 선회절분석 I28 x: 자구(磁 區 ) 89 작업온도범위 I02 참복시간 4X 참상(潛像) x54 장법위규칙 I5,x8 장석 2 구 xm 저 팽 창결정 화유리 I24 져충성장 67 전기-광학효과 230,275 전기비저항 208
전기저 항 뮴 128 전단파손 245 전단랄성문 204 전이 34 전이접 35 전주내화물 II3 전해질전도체 17 철삭용결정화유리 I4, I60 정성유동 62 접합용유리 272 정 공(p os iti ve hole) 210 정상스피넬 96 정장석 IO5 것음성 14 조대 화과정 58, 120, 182 주결정 상 69, 87, 121 주조법 II4 주위응력 I92 준안정 불혼화 .51 준안정한계 35 중간가마 IZ5 중간산화물 20 지연탄성스트레인 245 지연파손 194 진용액 75 J MA 식 25 -K 청칭 100 체적 비저항 208 초정 34, 134, 152 최저탄성물 199 최적한계비 27 취입 법 132 측면성장 67
= 콜로이드 74 크리 이 프 (creep ) 244 chalcog en id e 278 cli no ·ensta t i te 151 ccori.rsd t ioe b r aitl eit e 1 5 9,3 41,6 680, ,1 6726,, 9138,7 ,1 22267, ,1 2474.z,. : I49, I70, 203, 2I4 crya l i te 98 kalsil ite 159 keali te 63, 149, 157, 204 E 탄성물 I99 두과전자현미경 I32 몸새 2I 이온 85 자리 I49 Ti0 2 146 T-T-T 곡선 26 고 파괴 울 I27, X56, I59 파괴 인성 I59, I93 파쇄전파 I89 파손 189 판상결정 184 평형배위수 88 표면바저항 208 표면압축충 I55 피로파손 I94 per ovskit e 228 pet a l i te u3 Pois s on 비 199, 204
pyro chlor e 150 P20 s 146 -Io 핵 생 성 III 밀도 57 자리 58 촉매 60 촉진 제 35, 43, I46
현무암 97 협 력 효과 (s y ner gi s ti c eff ec t) 285 형 취 법 (blowi ng ) 114 화학 적 내구성 I7I 혼 합스피 델형 95 홍 (fl aw) 60, 155, 175 fluo rop h log o p ite _m i ca 160 for ste r ite 151, 244 hip joi n t 282
金炳蕙 일본 早稱田大學 應用化學科 졸업. 同大學 석사, 박사 저서 『유리工學 』 논문 「이온교환성 다공질유리에 관한 연구」등 다수 현재 고려대학교 재료공학과 교수 「.II I . - - --一‘ ----· ···- • 結晶化유라 인 쇄 I984 년 7 월 25 ' 일 발 행 I984 년 8 월 10 일 저 츠 金炳扇 발행인 朴孟浩 발행처 民音社 출판등록 1969. 5.19 제 1-142 호 우편대제계좌번호 010041-31-523282 110 서 울 종로구 관철동 44-J:• * 파본은 교환72해4- 2드00립0니 • 다72.4- 42!>i4: f• 4 7,255-080' 2원 4 ;'
대우학술총서 • 자연과학 1 소립자와 게이지상호작용 金鎭義 著 • 값 3,60 0 원 2 動力學特論 3 질李소炳昊고 정著 • 값 5,400 원 4 相宋承轉達移 著와 臨• 값界 2現, 8 0 0象 원 5 觸김두媒칠作 著用 • 값 2,800 원 6 뫼陳宗스 植바著우 어• 分값 光2, 8學00 원 7 극玉恒미南량 著원 소• 의값 2,영80양 0 원 昇正子 著 • 값 6, 500 원 8 水素化覇素와 有機覇素化合物 9 草尹能物民 質著 의• 全값 合5,00成0 원 姜錫久 著 • 값 9,000 원 10 국소적 형태의 A tiy ah-S i n g er 지표이론 지 동표 著 • 값 2, 800 원 11 Muco po l y sacchar i des 의 生化學 및 生麟學 박준우 著 • 값 3,800 원 12 ASTROPH_Y S IC_S ( 天體物理學) 洪承樹 著 • 값 4, 700 원 13 천연물화학연구법 禹源植著 14 투무타글란딘합성 金聲珪 著 15 脂防營養 金淑喜 著 값 6, 500 원 16 結金炳晶壓化 著유 리• 값 4,500 원