
金淑喜 저자는 이화여자대학 교 가정학부 영 양학과를 졸업 하였으며 마 국 Te xas Women' s U n i v e r s i ty에 서 영 양학 전공으로 Ph. D . 를 획득하였다. 또한 미국 Joh ns Hop k in s Un iv e r s it y McColum 영 양학 연 구실에 서 Post docto r al Researcher 로서 연구하였으며, Univ . of M i nneso t a 에 방문교수로 재직한 바 있고, 현재 이화여자대학교 아시아 식품영양 연있다구.소 소장과 가정대학장직을 맡고

 脂朋營養
脂朋營養
 脂防營養
脂防營養
머리말 영양소를 분류하는 방법에는 여러가지가 있다. 그러나 그 중에 서 용액에 녹는 성질로 나누어 보면 지용성과 수용성으로 나누어질 수가 있다. 지방은 지용성 물질의 대표이다. 그런데 우리 신체는수 용액과 조칙이 서로 맞닿아 있는 상태로 형성되어 있어서 마치 조 직을 선으로 보면 수용액이라는 바다에 떠 있다고보아도과언이 아 니다. 그렇기 때문에 수용성의 물질은 신체내 대사에서 크게 문제 를 던져 주는 것 같지 않으나 지용성의 물질은 수용액의 환경 가운 데에서 대사되려면 여러가지 문제를 수용성의 물질에 비해서 던쳐 주누 것 같다. 요즈음 성인병으로 그 원인과 치료방법이 모호한 것은 모두 신체 내 치방대사와 관련이 되어 있지 않은 것이 없다. 보 지방영양 책에서는 지방이란 영양소를 놓고 주로 신체내 대사 의 인장에서 다루었기 때문에 지방영양 중에서 극히 일부를 다루었 다코 본다. 지방대사를 주르 지방조직 (adip o se ti ssue) 과 간조직 (hep at i c tiss nP. ) 그리고 혈액내에서 지단백질(lip op ro t e i n) 형태로의 대사를 7 주로 다루었기 때문에 이 책의 많은 부분이 중성지방과 콜레스테롤대사 를 다루었으며 인지방대사는 비교적 소홀히 다루어져 있다. 그리고 이들 대사와 관련된 효소작용에 대해서 기술되어 있다. 이 책은 지방대사에 관십있는 많은 분들에게 조그마한 도움이 되 고자 하는 마음에서 씌어졌다. 요즈음 광범위하게 발표되어 있는 이 분야의 연구논문 내용을 간추려서 쓴 책이기 때문에 득히 대학원과 정중에 있는 학생들에게 도움이 되었으면 하는 마음이다. 이 책이 나오기까지 원고 정리에 많은 도움을 준 이화여자대학교 식품영양학과 연구원인 윤지상과 박사과정중의 정혜경양에게 그리 고 이 원고 교정에 많은 도움을 준 장문정과 윤군 0 사양에게도 감사 를 표한다. 이 책을 쑬 수 있는 계기를 마련해 주시고 재정적인 뒷 받침을 해주신 대우재단에 십십한 감사를 표한다. 1984 년 5 월 김숙희
脂防營養 Lipid Metabolism/ 차례
머리말 5 서론 11 제 1 장 지방의 소화와 흡수 l 서론 15 2 식이지방의 물리화학적 분류 16 3 물과 지방의 상호작용 17 4 담즙산과 micelle 형성 18 (1) 담즙산 18 (2) micelle 형성 2I 5 지방의 소화 23 (1) 췌장에서 분비되는 지방분해효소 23 6 장내로부터의 지방흡수 29 7 장내막 세포에서의 지방대사 33 (1) 지방산의 활성화 33 (2) 장내 막에서의 중성지방의 생합성 35 (3) 중성지방 생합성의 조철 37 (4) chylomicron 형성 39 * 참고문헌 44 제 2 장 지방조직에서의 중성지방대사 l 지방조직의 지방세포 51 (1) 흰색지방제포 52 2 지방조직내의 중성지방대사 56 (1) Lipoprotein lipase 58 (2) 지방조직내의 중성 지방 합성 83 (3) 지방조직으로부터의 중성지방 이동 86 (4) 식사요인이 지방조직내 중성지방대사에 미치는 영향 97 * 참고문헌 98제 3 장 간에서의 지방대사
l 간의 구조와 간세포 I05 2 간과 지방대사 107 (1) glyceride 대사에 있어서의 간의 역할 108 (2) 간내 glyceride 합성과 간세포로부터의 이탈경로 109 (3) 간내의 지방 축적 118 (4) 간에서의 glycerolipid 합성효소 120 (5) 지방산의 활성화 122 (6) DiacyIglycerol의 생합성 123 (7) 중성지방의 생합성 I24 (s) phosphatidylcholine과 phosphatidylethanolamine 생합성 125 (9) 영양상태에 따른 간내 지방대사 I27 3 알코올의 신체내 대사과정 130 (1) 알코올대사에 관련된 효소 131 (2) 에탄올산화가 간과 신체대사에 미치는 직접적인 영향 135 (3) 간세포내에서 지방산화와 케톤체대사 154 * 참고문헌 l76 제 4 장 콜레스테롤대사 l 신체내 콜레스테롤의 동선 198 2 콜레스테롤의 신체내 pool 203 3 소장으로부터의 콜레스테롤 흡수 203 4 콜레스테롤의 생합성 205 (1) 콜레스테롤의 생합성 205 (2) HMG CoA reductase의 조절 208 5 담즙산의 생합성 220 (1) 담즙산의 생합성 220 (2) 담즙산 생합성의 조절기전 225 6 콜레스테롤 ester 형성 229 (1) 콜레스테롤 ester 229 (2) lecithin·cholesterolacyltransferase (LCAT) 230 (3) 혈장내 콜레스테롤 ester 234
* 참고문헌 236 제 5 장 Lipoprotein 1 역사적 고찰 243 2 혈장 lipoprotein의 분류 244 3 Lipoprotein의 구성성분 246 (1) Chylomicron 246 (2) VLDL 247 (3) LDL 248 (4) HDL 249 (5) Lipoprotein (a) 250 (6) Lipoprotein X 250 4 Apolipoprotein의 대사와 기능 251 (1) Apolipoprotein A 251 (2) Apolipoprotein B 258 (3) Apolipoprotein C 266 (4) Apolipoprotein E 274 (5) Apolipoprotein D 276 (6) 기타 Apolipoprotein 277 5 Lipoprotein 구조의 모델 277 (1) LDL 모델 277 (2) HDL 모델 280 (3) VLDL 모델 284 (4) Lipoprotein X 모델 287 6 Lipoprotein 대사 288 (1) Lipoprotein의 합성 289 (2) Lipoprotein의 분해 298 (3) Lipoprotein의 교환과 이동 298 7 Lipoprotein 대사에 관련된 효소 304 (1) LCAT 304 (2) LPL 314 (3) Hepatic lipase 33I 8 Lipoprotein의 상호전환대사 334 (1) VLDL 과 Chylomicron 대사 334 (2) HDL 대사 336 9 고지단백혈증 339 * 참고문현 339제 6 장 동맥경화증과 고지방혈증
1 서론 367 2 동맥벽의 구조 369 3 동맥경화중의 조직학적인 변화과정 370 4 동백경화증의 임상적인 증제 374 (1) 관상동맥경화증 374 (2) 뇌혈관병 376 (3) 대동맥경화증 377 (4) 신장혈관의 폐쇄 377 (5) 말초혈관 경화증 377 (6) 폐동맥 경화증 379 5 LDL과 동맥경화 379 (1) LDL의 성분과 특징 379 (2) 사람의 fibroblast 세포내에서의 LDL 결합부위와 대사경로 381 (3) 혈청 LDL 수준의 상승이 어떻게 동맥경화를 촉진하나 386 * 참고문헌 388 제 7 장 영양소로서의 지방 *참고문헌 399 색인 401서론 인체에 대한 호기십을 만족시키기 위해서 초기의 생리학자, 의학· 자, 영양학자들은 인체 구성성분의 분석에 관십울 가졌었다. 20 세기 에 들어서면서 영양학자들은 인체의 성분을 크게 안정된 요소 (elem ent cons t an t)와 변화하는 요소 (elemen t var i able) 로 구분하였 다. 이 의 안정된 요소로서 대표적인 요인은 주로 단백질을 의미하였으며 이 는 신체조직을 구성하고 있는 주요 물질로서 신체의 열량섭취상태 에 따라서 쉽게 그양이 변화하지 않는 것이다. 한편 번화하는 요소. 로서 대표적인 요인은 주로 지방질을 뜻하였으며 이는 신체내에 저 장된 에너지형태로서 신체의 열량섭취상태에 따라서 쉽게 그· 양이 변화하는 것으로 생각하였다• 그러므로 지방조직은 신체내에서 불 활성의 조직으로서 대사상의 기능으로 볼 때 활발하지 못한 저장의 뜻이 강조되었다. 실제로 지방은 우리 신체 구성성분 중에서 무게로 따져서 몸무게 의 4% 정도를 차지할 수도 있지만 섭취하는 에너지양이 증가되면 신체내에 여분으로 저축되는 에너지의 양이 증가되어서 몸무게의 5% 까지 축적될 수 있다고 본다. 이러한 견해에 근거해서 보면 20 세기 초기에는 이 분야의 연구가 활발하지 못하였던 이유로 설명이 될 수 있으리라고 본다. 지방은 선체내에 처장된 에너지원이고 지방조직은 불활성조직으로서 신체 내 장기의 쿠숀역할을 하며 또한 신체 체온유지를 위한 절연체의
역할을 하는 것으로 생각되어 왔다. 그러나 1929 년에 Burr & Burr 에 의해서 팔수지방산의 중요성이 강조되면서 이것의 결핍으로 인해 나타나는 성장 부진내지 숨진등의 결집중이 제시되면서 지방의 생리적 팔수성이 강조되기 시작하였 다. 한편 18 세기 후반에서부터 유럽지역에서 겪었던 산업 혁 명은 생 활의 변화를 가져왔으며 전원생활에서 근대 도시생 활 형대로 바귀면 서 구루병을 위시한 여러 가지 영양결핍울 초래하게 되 었 다. 이의 해결을 위한 연구가 전행되면서 지용성 비타민의 팔수성이 강조되 기 시작하였다. 그러면서 치방의 요구량으로 관십이 쏠리게 되었 다. 많은 초기의 연구자들은 지방이 단지 지용성 비타민 공급양을 만족하고 필수지방산 공급양이 만족되는 수준, 즉 전체 칼로리 섭취 량 중 2~3% 정도만 지방에서 섭 취하면 신체건강을 위해서 큰 지장 이 없을 것이라는 견해를 보였다. 아직까지도 지방의 요구량에 대 한 정확한 결정이 없으며 이에 대한 연구도 진행이 되어야 한다고 본다. 그러나 1945 년 제계 제 2 차대전 종료 후 미국을 위시해서 서구 여 러 국가들은 공업화가 급전적으로 이루어지면서 1910 년 이래로 허덕 이던 불황에서 벗어나 경제성장률의 증가를 초래하기 시작하였다. 그러면서 우리들 생활속에서 가장 예민하게 반영되는 식탁내용에도 변화가 오게 되었다. 물론 서구인의 식사내용이 동양인의 것에 비 해서 동물성식품 위주라는 것도 부인 못할 사실이다. 그러나 경제 성장은 식사내용을 접접 더 동물성 위주로 편중되게 하는 데 박차를 가하게 되었다. 급기야는 1950 년대에 이르러서 서구인에게서는 동 백경화증 발병률이 (특히 미국인) 일본을 비롯한 동양인에 미해서 월 등히 높다는 것이 연구자들에 의해 지적되게 되었다. 득히 쌀을 주 식으로 하는 일본과 한국의 경 우가 비 교군으로 등장하였 다. 그래 서 한대에 미국에서는 쌀을 위주로한식단이 동백경화 치료식으로 등 장된 때도 있어서 캠프너의 쌀식이 (Kemp e ner's Ri ce d i e t)가 제시되 기도 하였다. 그러나 쌀을치료식으로하여 동맥경화증환자를 치료해 보아도근 본적인 치료효과가 없었으며 일시적으로 혈청내 지방 구성성분의
번화만이 나타났었다. 동서양의 식사내용의 영양가 분석을 해보면 서양에서도 과거에 비해 탄수화물 섭취량이 감소하며 지방과 단백질양이 중가되는 것 으로 나타났으며 동양의 식사내용 영양가와 비교해 보아도세 가지 영양소의 섭취량에서 큰 차이를 빚어내고 있음이 지적되었다. 죽 동물성식품의 섭취량이 높은 서양에서 단백질과 지방섭취량이 높았 으며 곡유위주의 석사를 하는 등양에서는주로탄수화물 섭취가 높 아전 결과를 초래하였다. 한편 동양을 위시한 저개발국가 및 개발도상국가가 개발국가로 발전하는 데는 서구화가 되어 가는 경향이고 따라서 식탁의 내용도 서구화가 되어감을 주시하지 않을 수 없다• 서구사회에서 이미 많 은 사람들이 고민하고 있는 몸무게 과잉문제 및 동맥경화로 인한 십장성 질환의 발병률이 서서히 증가되고 있음울 주의하여야 한다 고본다. 단적으로 이야기해서 동물성식품의 섭취량이 증가되면 동백경화 우려가 높아전다고 볼 수 있다. 동물성식품 위주의 식사목칭은 고 단백, 고지방식이며, 저섬유식사로 인한 섬유질의 섭취량 저하로 콜레스테롤의 배설문제가 대두되었으며 콜레스테물의 체내합성은 담즙산 (b i le acid ) 합성과 분해경로를 통해서 연구가 진행되고 있다. 지방은 정의에서 가리키듯이 이질적인 물질로 모여진 하나의 군 으로서 아 물질들 사이의 공통접은 수용액에서 녹지 않고 유기용매 에 녹는 접이다. 그러므로 체내에 흡수되어서 이리저리 이동될 때 에 수용액 중에서 이동이 되어야하드로 지방이 수용액 중에 촌재하 논 물리적인 특칭과 구조 연구에 많은 관십이 모아졌다. 지방 중에서 문과 찬화력이 없는 중성지방도 있지만 수용액 중에 서 상호작용을 할 수 있 는 양성 을 지 닌 양성 물질 (Amp ho te r ic ) 인 인지 방이 있으며 유리 콜레스테불은 에스데르화된 콜레스테롤 (es t er ifi ed choles t erol) 에 비 해 서 알코올 형 태 그대 로 수용액 에 서 상호작용이 가 능하다. 지방이 수용액 중에 촌재하려면 반드시 구(球)를 형성하여 야 하며 이 구의 표면 중 수용액의 단면은 인지방과 유리 콜레스 테를이 싸고 있으며 내부 중십부에는 중성지방과 에스데르화된 콜
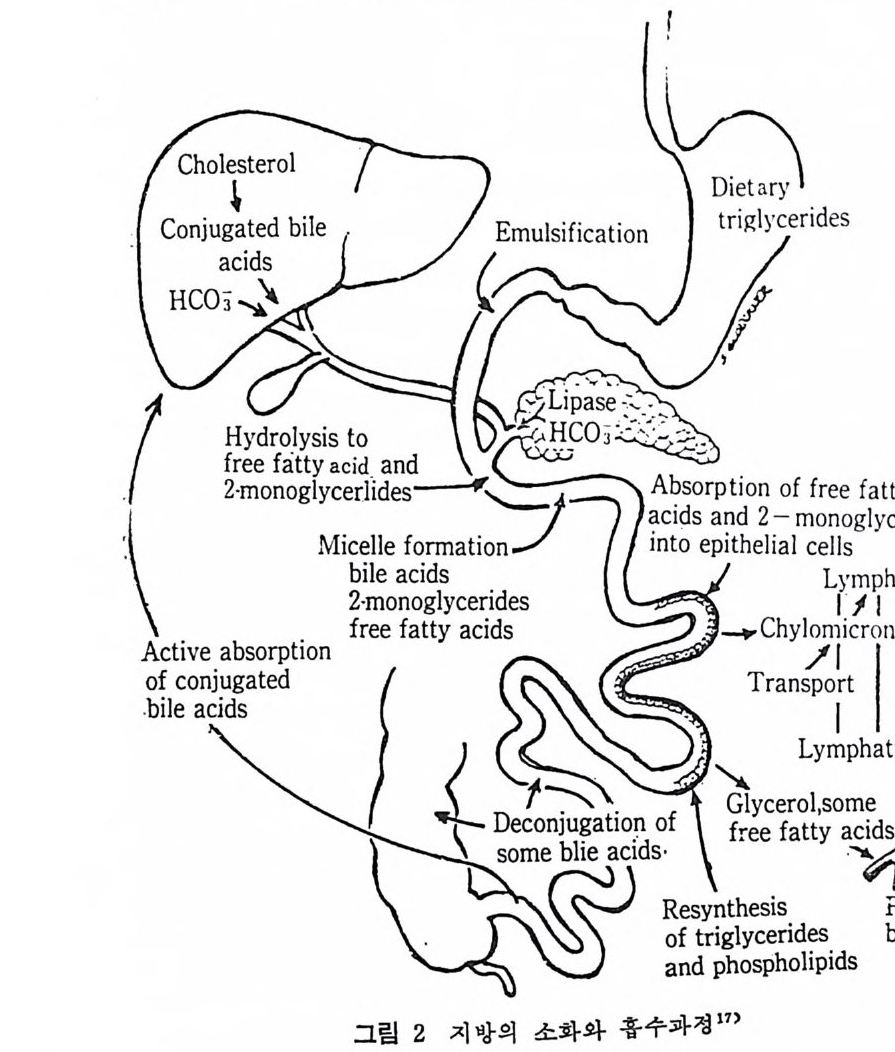
레스테롤이 위치하고 있다. 이에 부과해서 수용엑에서 상호작용 이 되는 단백질과 탄수화물 소량이 이 지방구의 표면물질로 융화되 어 소위 지단백질(Iip o p ro t e i n) 형태로 존재하계 된다. 그런데 지방 구가 신체내에서 혈액에 의해 여러 조직으로 이동되어 갈 때 조직 의 외면을 이루는 세포 표면막도 지방구의 표면물질과 유사한 구조 로 이루어졌음이 또한 홍미로운 일이다. 우리 신체내 지방조직내에는 중성지방이 축적되어 있으며, 지방 조직은 신체내의 여러 부위에 형성되어 있다. 과거의 개념으로 보면 지방조직은 신체내의 불활성 조직으로 간주되어 왔다. 그러나 식 사로부터 섭취된 지방은 소화과정을 거쳐서 일단 장내로부터 홍수 되면 간으로 이동되어서 간에서부터 신체 여러 조직으로 이동된다. 그러므로 혈청내 지방구성성분도 간에서 지방대사 여하에 따라 많 이 달라진다고 보지만 이의 근원을 찾아보면 섭취하는 석이지방의 종류에도 관련이 크다고 본다. 예로서 콜레스테롤을 식이로부터 많 온 양 섭취하면 혈청내 콜레스데몰 함량이 증가되고 있음이 여러 가 지 실험결과로 나타나고 있다. 혈청내 콜레스테롤의 함량에 관련된 영양소는 다양하다. 죽 섭취되는 총지방량 또는 지방의 종류, 탄수 화물중에서 2 당류, 죽 서당의 섭취량, 요츠음은 단백질의 과량 섭취 둥이 혈청 콜레스테롤의 함량을 높이는 원인이 되고 있음이 밝혀지 고 있다. 그러나 혈청 콜레스테롤의 함량조철은 주로 간에서 이루 어지고 있는 것도 사실이지만 한편 간은 지방조직과 관련하여서 대 사가 이루어지고 있다. 지방조직과 간 사이에서 밀접히 관련을 맺 고 있고 지방은 중성지방대사로서 중성지방이 지방조직으로부터 대 사되어서 이동되고 또한 간으로부터 이동되어서 저장되기도 한다. 이러한 견해로 볼 때 지방조직은 더이상 불활성의 조직이 아니며 이는 신체 지방대사를 조철해 주는 조직으로 간주되고 있다. 더 나아가서 우리 신체내의 열량 대사 및 혈청지방 구성성분의 조철, 나아가서 동백경화 유발과 밀접하게 관련되어 있다. 본문에서는 지방의 소화홉수, 지방조칙에서의 지방대사, 간에서 의 지방대사, 콜레스테롤 대사, 지단백질 대사, 동맥경화증과 지방 대사 순으로 다루었다•
제 1 장 지방의 소화와 흡수 1 서론 서구인의 석사내에는 1 일에 60~lOO g r 의 지방이 함유되어 있다. 이 양온 섭취하는 칼로리의 40~45% 가 지방으로 섭취된다는 것을 의미한다. 우리나라 사람의 식사내에는 지방 함유량이 지역적으로. 큰 차이를 보인다. 대도시의 중류 이상의 생활자들은 18~25 g r/1 일 의 지방섭취량을 나타내 보이고 있으며 농촌이나 도시의 변두리에 서는 6~lOg r 내의의 지방울 섭취하고 있는 실정이다. 여하돈 이들이 섭취하는 지방의 90% 이상이 중성지방이며 나머지 10% 는 콜레스테롤 에스텔, 식물성스테롤, 인지방이라고 생각한다. 서양인의 식사에 함유된 지방산의 종류로는 올레인산과 리놀레인 산이 각각 30% 와 19% 함유되어 있다.1) 탄소의 수가 C6~cl4 정 도의 중간 길이 의 지 방산이 소량으로 사 람들의 식사내에 함유되어 있다. 중간 길이의 지방산의 흡수는 비 교적 빠르게 그리고 효울적으로 흡수된다고 보고되어 있다. 이의 흡수는 단순한 확산에 의해서 이루어진다고 보고되었다 .2) 지방의 장내흡수는 지방대사를 연구하는 많은 사람들에게서 오랫 동안의 관십사가 되어 왔다. 소장의 흡수 부위인 내막이 수분으로 두껍 게 덮여 있는 수분충 (uns ti rred wate r la y er) 인데 지방의 효율적 인 흡수는 이를 지방구가 통과하는 속도에 의해서 좌우된다고 본
다. 그런데 지방구논 수용액에 거의 녹지 않거나 불 용성의 물질이 라는 데 문제가 있다. 지방의 소화는 화학적인 측면과 물리적인 측떤의 두 가지 현상운 모 두 내포하고 있다. 화학적인 측면온 lip ase 와 독 정치 않은 este r ase (non-spe c if ic este r ase) 에 의 해 서 지 방의 este rs 가 가수분해 되 는 것 이 고 물리적인 측면온 담즙영에 의해서 유화되거나 효소에 의해서 분 해된 분해산물의 mi ce llar 확산 현상이 다. 지방 중에서 어떤 지방, 즉 중성지방은 화학적인 가수분해가 팔 요하며 완전분해 산물은 수용액에 용해된다. 다른 불용의 지방, 즉 콜레스테롤과 같은 물질은 소화작용 동안에 변화되지는 않지만 그 러나 흡수를 위해서 m ic ellar 형태로 변화되어 용해상태로 되는 변 화가 요구된다. 장벽의 수분충은 장내물질의 빠른 흡수를 위해서는 방해장벽이 된다. 또한 어떤 영양소이돈 빠른 흡수를 위해서는 이 수분장벽을 빨리 통과하지 않으면 안된다. 그런데 탄수화물과 단백 질은 이 수 분장벽 을 통과하기 위해 서 특수한 운반체 (carr i er) 가 필요하지 않 다. 왜냐하면 이들의 소화된 마지막 산물은 수용성이기 때문이다. 여 하튼 또한 홍미 로운 접 은 이 들의 마지 막 소화산물이 monomer 만이 아니 타 dim er(I ac to s e, sucrose, mal t ose) 도 있으며 더 나아가 o lig omer (i soma! t ose) 와 여 러 종류의 펩 타이 드(p e pti de) 도 있 다. 이 들 온 수분장벽 동과 후에 장내 막의 brush border 에 도착해 서 거 기 에 촌재하는 소화효소에 의해서 가수분해가 이루어진다. 그러 나 지 방의 소화는 전적 으로 소장내 부벽 (i n t ralum i nal) 에 서 이 루어지며 담줍산, lip a se 그리고 지방이 참여하여서 이루어진다. 2 식이지방의 물리화학적인 분류 소장내 막에 서 의 지방의 소화는- brush border 근처 에 서 이 루어 지 며 몇 종류의 효소작용에 의 해 서 비 극성 (nonp olar) 의 불용성 지 방이 수용성의 홍수가능한 물질로 전환되는 것이다. 그런데 화학적으로
보면 지방은 상당히 다양한 물질로서 지방의 소화홍수 분야에서 이 의 물리화학적 특칭의 이해가 접차로 고조되어 가고 있다. Hoff m ann 과 Sma112-4) 은 지 방이 수분과 상호작용하는 현상에 기 초해서 지방의 분류를 다음과 같이 시도하였다. i) 비 국성 (nonp ol ar; hyd r ocarbons, ste r ol este r s, waxes, vit am i n este r s) : 물에 불용이 며 mi ce lle 형 성 등이 아주 처 조한 물질 . ii) 극성 (po lar ) ® 물에 불용성 이 며 부풀지 않은 양성 (amp ho te r ic ) 지 방으로 dia c y lg l y c erol (DG) , 중성 지 방, long chain fatty ac ids , 스테 롤, 지용성비타민이 여기에 속하며 m i celle 형성능력이 아주 처조하다. @ 불용이 지 만 부푸는 양성 지 방으로 인지 방, gly c oli pid, monoac y l g l y cerol(MG) 이 이에 속한다. 물에 약간 용해되며 용매와 담즙영 사이의 바례가 70 : 5 정도로 혼합 m i celle 형성 을한다. ® 용해성 양성의 지방으로 겁화된 LCFA 와 담즙영이 이에 속한다. 이 는 수용액 중에 서 mi ce lle 을 형 성 한다. 이 들은 혼 합 mi ce lle 의 담즙영 용액 이 다. 3 물과 지방의 상호작용 Mi ce lle 내에서는지방의 가수분해산물의 용해도에 의해서 지방흉 수가 영향을 받는다. 지방의 물리화학적 특칭은 지방분자내의 극성 (p olar) 과 비 극성 (nonp o lar) 부위 의 균형 에 의 존한다. 수용액 중에서 치방의 용해도는 용매의 농도, 온도, 이온화정도, pH , 분해 효용도 (pa rtit ion coeff ici e n t) 그리 고 극성 도 (po larity ) 에 의 하 여 좌우된다. 그런데 생체내에서는 p H 와 온도는 거의 고정되어 있 다. po larit y 는 지 방산의 탄소사슬길이 , 첨 가물질, 포화도에 의 ~ 된다. 5-6) 게 부분의 식 이 지 방은 분류 ii)-(!)에 속하는 찬수성지 방으로서 물 E
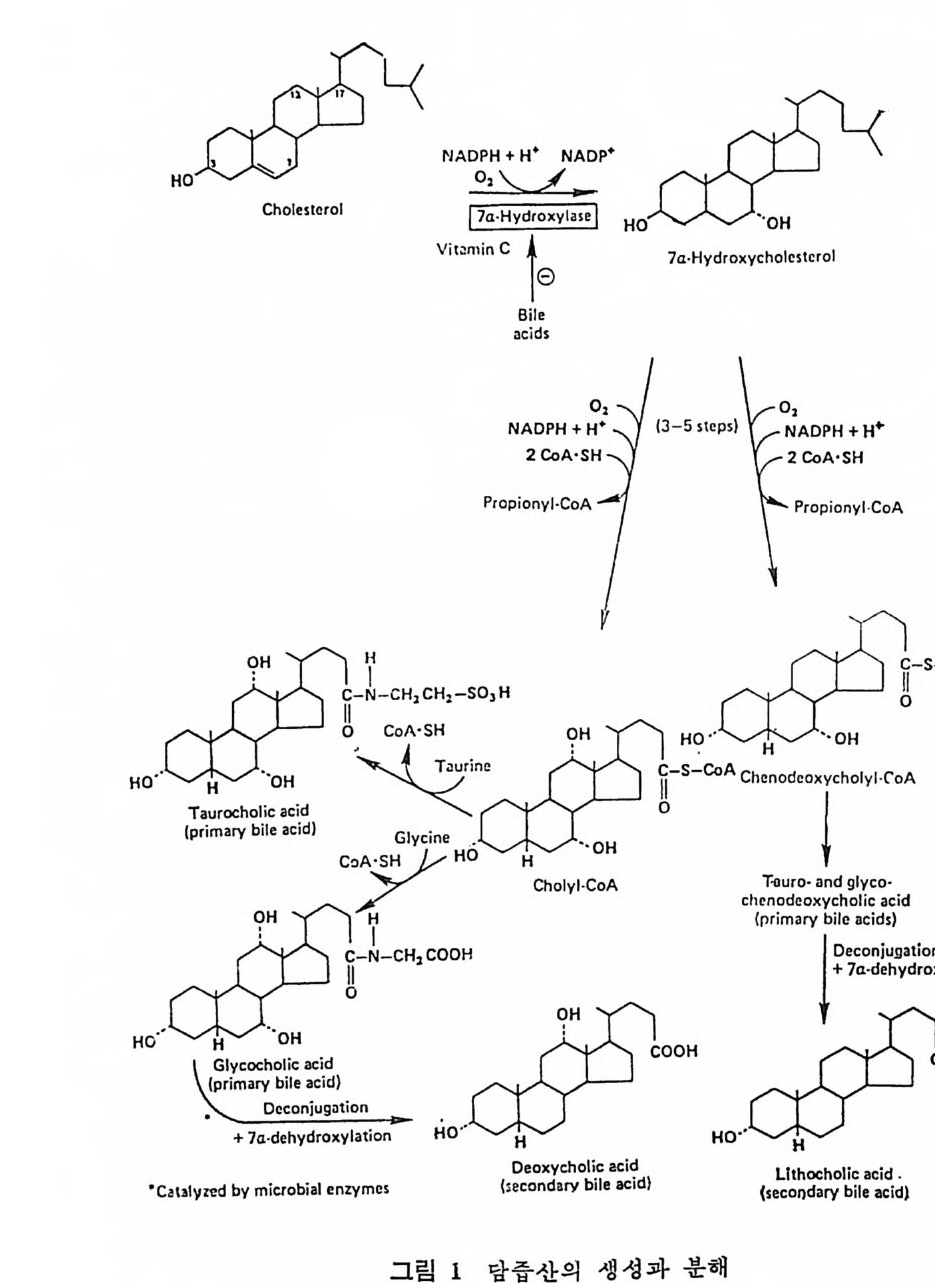
예 불용이며 부풀지 않은 양성으로서 대개 사 슬 이 간 지방산으로 형 성된 중성지방, 스테물과 지용성비타민이다. 이들은 물과 상호작용 을 하지 않으나 고체의 물질과는 구텔이 된다• 이의에도 식이지방은 분류 ii)_@에 속하는 극성지방으로서 물에 는 불용이 나 부푸는 양성 의 지 방으로 인지 방과 gly c olip id 의 다양한 양이 섭취된다. 이들은 물에는 불용이지만 이 지방의 분자내로 물이 스며들어서 이 치방의 극성부위(p olar head) 가 수분면으로 전열이 되어서 이들 정연한 결정구조 (cr y s t a lli ne) 가 부풀게 된다. 그러므로 부풀은 정연한 결정구조로 인해서 적어도 수분면의 한 면만이라도 규칙적인 배열에 의한 평면이 생기게 된다. 분류 ii)-@에 속하는 물질은 수용성의 양성지방으로 겁화된 영과 이온화된 담줍산으로서 한정된 분자수의 용해도가 있으며 따라서 몇 분자가 응집하는 득칭을 나타낸다. 이러한 응집으로 인해서 mi ce lle 이 형 성 되 며 비 교적 낮은 농도에 서 crit ica l mi ce llar concen- t ra ti on(CMC) 를 이 룬다. 1) 4 담줍산과 mi ce lle 형 성 '(1 ) 담줍산 모든 척추동물의 소화기 장내에는 담줍산과 이와 관련된 물질이 존재한다. 특히 사람의 소화기 장내에는 2 종류의 주요 담즙산이 있 으며 이는 간에서 콜레스테롤로부터 형성된다. 2 종류의 주요 담 줍산 중 하나는 1 차 담즙산이 라고도 불리 며 , 이 들은 3, 7, 12-tr i h y - droxy c holanic a ci d 로 일명 choli c a ci d 로 볼란다. 또 다른 1 차 담즙산은 3, 7-dih y d roxy c holanic aci d 로서 일명 chenodeoxy choli c . a ci d 로 불린다. 이들 1 차 담줍산 합성시에 첫번째 합성속도 조철과정은 콜레스데 몰의 7 번째 탄소에 a-hy d roxy la ti on 이 되는 과정 이 다(그립 1 참조). 이 러 한 7a-hy d roxy la ti on 작용은 간세 포의 mi cr osomal sys te m 에 의해서 촉진되며 이는 산소와 NADPH 를 요구한다. 그리고 이 작
용은 일산화탄소에 의해서 방해를 받는다. 바타민 C 가 결핍되면 ?a-hy d roxy la ti on 이 되 는 수준에 서 담즙산 형 성 에 방해 를 받으며 그 결과 콜레스데롤의 축적이 생겨서 동백경화까지 생기는 경우가 실험동물 gu in e a pig에서 나타났다. 두 종류의 2 차 담즙산이 있 다. 이 는 3, 12-dih y d roxy c holanic ac id 이 며 또 하나는 3-monohy d roxy c holanic ac id 로서 이 를 일명 deoxy - cholic ac id 와 lith o cholic acid 로 불란다. 이 2 종류의 2 차 담즙산은 1 차 담즙산으로부터 형성되는 것으로 장내 미생물에 의해서 7a- 부 위부터 OH 기를 유리시켜서 형성된다(그립 1 참조 ). 두· 종류의 2 차 당 즙산 중에 서 오로지 deoxy c holic acid 만이 재 흡수되 어 서 다시 소량 이 담관을 동해서 장내로 분비된다. 그리고 Iith o cholic ac i d 는 그. 대로 배설된다. 그러므로소장내에 촌재하는 담줍산, 즉 choli c acid chenodeoxy c holi c acid 그리 고 deoxy c holic acid 의 함량비 는 1 : 1 : o. 5 이 다. 간세 포내 mi cr osome 내 에 서 담즙산은 활성효소 (b il e aci d acti va ti ng enz y me) 에 의해서 담즙산 Co A 유도체로 전환된다. 그리고 활성화 된 담즙산 Co A 는 글리 신과 타우린과 결 합되 어 서 gly c ocholi c 또 는 gly c ochenodeoxy c holic acid s 와 tau rocholi c 또는 tau rochenodeox- yc holic a ci ds 로 된다• 이들 주요 담즙산의 글리신과 타우린과의 결합되는 비례는 정상안에게 있어서 3 : 1 이다. 탐즙산이 유리된 형태로 촌재하면 이들의 p Ka 치는 높은 6 인데 비 해 서 tau rin e 과 결 합되 면 pK a 는 2 로, gly c in 과 결 합하면 pK a 치 가 4 로 낮아전다. p Ka 치가 낮아침으로써 탁월한 유화제의 역할을 할 수 있다고 한다. 특히 장내 의 상황을 보면 장내 용 산도(p H) 논 5. 5~6. 5 인 약산이 며 온도는 약 37°C 이며, o.15mol~ 의 염의 농도가 있는 상황하에 서는 더구나 음담즙산은 영으로 침전되기가 쉽다. 이런 경우에 모든 담즙산에 수소이온이 첨가(p ro t ona t ed) 되어서 영아 생성되어 침전 된다.
 HO: 只 VFJ AtD
HO: 只 VFJ AtD
(2) mi ce lle 형 성 수용엑 중에서 담즙영은 분자내에 찬수성과 소수성의 양면적안 . 특 칭을 지니고 있기 때문에 분자들이 응집한다. 이 응집된 분자를 mi ce lle 이 라고 부른다. 이와같이 m i celle 이 형성될 수 있는 만큼의 담즙영의 농도를 crit ica l mi ce llar concen t ra ti on(CMC) 라고 한다. 담즙염 의 mi cel le 의 크기와 응집된 분자수는 용액내의 반대이온 농도인 Na+, K+ 둥 의 농도에 닫려 있으며 또한 온도, 사술의 길이 , pol ar gro up charge 와 담 즙 영 분자내의 OH 기 수이다. OH 기의 분자내 위치오H 근 큰 관 련이 없다고 본다. 수용액이나 저영농도용액내에서는 1 차적인 응집이 생긴다. 이는 t r i hy drox y-담즙영 유리 형 태 로써 이 루어 지 며 응집 되 는 분자수는· 적 어서 약 2~7 분자이다. hy d roxy 담즙영은 아주 희석된 영용액내에서 응집이 형성된다. 그러 나 용액 중의 반대 이 온 (coun t er ion ) 농도가 증가되 면 tri h y d roxy 담즙영 과 d i hy drox y - 담즙염 의 특칭 이 다르게 작용한다. tri h y ·· droxy 담즙영 은 응집 크기 가 약간 증가해 서 매 mi ce lle 당 9 분자 정 도가 되 나 dih y d roxy 담즙염 는 영 의 높은 농도가 증가되 면 그것 에 현저히 영향울 받아서 반대이온농도가 증가되는 것에 의해서 영향 이 크다. 이 때 응집 분자수는 60 분자 이 상이 되 며 온도 70° C, o. 8N 소금용 액 내 에 서 는 dih y d roxy 담즙영 으로 침 전되 고 만다. 그러 므로 OH 기 의 수는 형성되는 m i celle 형태에도 중요하지만 담줍영의 용해도에도 또한 중요하다 .1) Non-io n ic dete r ge nt 의 응집 분자수의 증가는 po lar gro up 의 탈수 (deh y dra ti on) 와 관련이 되 어 있 다. dih y d roxy 와 tri h y d roxy 담줍 염의 현저한 차이는 OH 기가 3 개보다는 2 개일 때 빨리 탈수될 수 있기 때문으로본다. 이에 부가해서 반대이온농도의 증가로 인해서 분자의 크기가 작
온 경우에 응집의 수가 증가되는 것은 다음의 몇 가 지 요인에 의해 서 영 향을 받거 나 charge d anio n ic po lar gro up 의 상호 반발과 분 자내 의 탄화수소 부분이 salt ing out 하는 것 이 다. 8) 생리학적인 견지에서 볼 때 담즙영의 찬수성과 소수성지방과의 상호작용은 매우 홍미로운 일이다. 담즙염은 콜레스테 롤 이나 지 방 산과 같은 비교적 소수성분자의 용해도를 약간 증가시키고 인지방 이나 췌액에 의해서 분해된 분해산물인 사슬이 긴 지방산이 결합된 mono g l y cer i de 나 지방산의 용해도를 대폭 증가시킨다. 사슬이 긴 지 방산이 결 합된 monog ly c erid e 는 지 방으1 분류 중에 서 볼용성 의 부푸는 양성 군에 속하며 담줍영 용액 내 에 서 mi ce lle 을 형 성 하는 분자의 비 율은 monog ly c erid e /b il e salts 가 1 보다 커 야 한 다. 9) 담즙영 용액 내 에 서 지 방산의 pK a 치 를 titra ti on curve 에 서 계 산 해 본 견과 6.4~6.6 이다 .0,10) 이 값은 소장윗부분의 내용물의 pH 에 가깝다. 그러므로 비이온화된 지방산이 이 조전하에서는 담줍염 지 방산 mi ce lle 용액 내 에 거 의 같은 양으로 존재 한다고 본다. 그러 떤 담즙영은 접점 지방산의 이온화를 억제할 것이며 따라서 mi ce lle soluti on 내 에 서 이 온화지 방산의 농도가 장내 이 pH 에 로 약간 증가 할 것으로본다. 간사슬 지방산의 담즙영 용액내에서의 용해도는 pH 5 이하에서 논 낮다. p H 가 증가되면 지방산의 용해도도 급하게 증가된다 .6) ' II) 담줍영은 LCFA 나 알코올을 용해시키는 데는 부실한 유화제이 다 .12) 그러나 중간 탄소 길이의 알코올이나 지방산에는 득출한 유 화제 이 며 12-3) 짧은 사슬길이 의 지 방산과 담즙영 과는 상호작용을 하 치 않는다 .11) 담줍영 은 콜레스테 롤을 용해시 키 지 못한다. 콜레 스데 폴은 mi ce llar 형 성 시 에 는 주로 po lyc y c li c nonp o lar hy d rocarbon 으로 작용한다. 1 분자의 콜레스테풀을 용해시키기 위해서 약 20 분자의 sodiu m ,de oxy c holate 가 요구되 거 나 130 분자의 sodiu m tau rocholate 가 요구 된다 .13) 담줍산은 섭취된 콜레스테를 es t er 의 가수분해에 영향을 미친다.
탐즙산은 콜레 스데 올 에 스 텔 과 상호작용하여 서 이 를 try p tic 단백 잘 분해효소에 의한 분해로부터 보호해 준다. 담 즙 산은 콜레스테롤과 같은 지방의 흡수에 없어서는 안되는 물 질이다. 왜냐하면 콜레스데를 자체가 물에 용해되지 않으며 이 물 질 이 m i celle 형성시에 수용액 면에 충분한 농도로 촌재하여야 되기 때 문 이다. 그러므로 콜레스테를 흡수를 위해서는 담즙산은 필수물 질로 간 주된다. 14- 6 ) 5 지방의 소화 섭취된 지방은 지방을 구성하고 있는 기본단위까지 화학적인 분 _ 해와 물리적인 변화가 이루어져야 한다. 이러한 화학적, 물리적인 변화는 소화기관의 여러 부위에서 이루어진다. 그럼으로써 섭취된 . 치 방은 먼저 담줍영 과 작용하여 서 mi ce lle 을 형 성한다. 또한 화학 인 과정은 특정한 효소 를 필요로 하며 이 효소가 보다 복잡한 지방 적 을 분 해 하여 서 mi ce lle 형 성 이 가능한 구성 성 분으로 전환시 킨다• (1) 췌 장에서 분비되는 지방분해효소 1 ) 췌 장지 방분해 효소 (pa ncreati c lipa ses) 와 Co-li pa se 춰넘 은 적 어 도 3 종류의 지 방분해효소와 한 종류의 조효소 (Co lip ase) 를 함유하고 있으며 이들은 지용성의 물질을 모두 가수분해시 킨다. 이들 효소는 첫째 췌 장지방분해효소(g l y cerol - es t er hy d rolase) 로서 이는 비교적 작은 특 수성을 지닌 효소로서 중성지방을 MG 와 지방산으로 분해시킨다. 그리고 담즙영이 촌재하면 효소의 작용이 상승된다. 둘째 콜레 스테 몰 este r ase(carboxy li c este r h y drolase) 로서 이는 carboxy lic es t er 를 분해시키며 이는 담즙영을 절대적으로 요 .. 구한다. 세 째 ph osph o lipa se A2 로서 체 액 내 에 zy m og e n 으로 존재 한다. 이 는 gly c erop h osph oli pid 의 2 번째 의 지 방산울 가수분해 시 키 며 이 역시 담줍염을 철대적으로 요구한다. 포유동물은 섭취된 중성지방을 그대로 이용할 수 없다. 이들 -
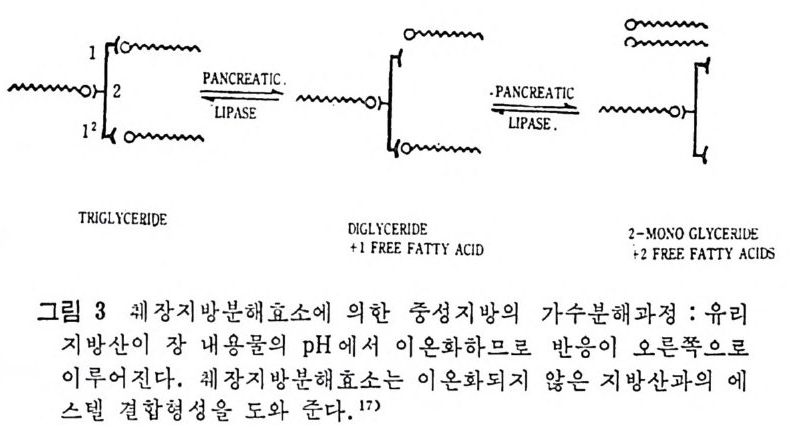
은 흡수되기 전에 반드시 가수분해되어야 한다. 췌장지방분해효소 (pa ncreati c lip ase) 는 여 러 종류의 수용성 이 아난 este r 률 가수분해 하는데 이들이 수분과 지방의 단면에 유화구로서 확산되어 있을 때 비로소 가수분해가 이루어질 수 있다 .18-9) 췌장지방분해효소의 작 용은 중성지방의 지방산의 위치에 내해서 대단히 특 수 (s pec ifi c) 하 다. 즉 중성지방의 Sn-1 과 Sn-3 위치에만 작용한다. 생리적인 기 질 (subs tr a t e) 로서는 사슬이 긴 지방산이 중성지방 Sn - 1 과 Sn-3 위치
 ulsif ica ti o trig ly c e rid e s
ulsif ica ti o trig ly c e rid e s
에 촌재할 때 이 효소가 작용하며(그립 3) 또한 이 위치에 사슬이 짧은 지 방산이 존재 할 때 도 작용한다는 보고도 있 다. 19)
 지T R방JG 며산L\' C이E al D El 장 l내 용g l一一문 의 pH [에 Ot IGi서 LF\ R 'CEETE T이 R F ID A 온ET TY화[ A하C ID 므l로 一一呼 반응이 2오F-~2 IOF른RSll 니 EOf쪽 . GFLA으YTCTEY로 인 A 及 C lE
지T R방JG 며산L\' C이E al D El 장 l내 용g l一一문 의 pH [에 Ot IGi서 LF\ R 'CEETE T이 R F ID A 온ET TY화[ A하C ID 므l로 一一呼 반응이 2오F-~2 IOF른RSll 니 EOf쪽 . GFLA으YTCTEY로 인 A 及 C lE
수용성의 이 효소는지방충을통과해 스며들어가지 못한다. 그런데 물과 기름단면에 중성지방 기질이 존재하면 이에 효소가 작용한다. 이 효소의 작용역 학 (enz y me acti on k i ne ti cs) 은 Benzonana 와 Desnelle 에 의해서 연구되어 있다. 많은 연구자들은 이 지방분해 효소의 지 방분해 작용에 있어서 기질 자체가 효소작용속도에 제한울 주는 요 인이 된다고 한다. 지방분해 작용속도는 이 효소에 노출되는 지방구 의 표면적 양에 의해서 조철된다고 본다. 죽 지방구는 작은 유화구 로서 촌재하여 이 효소에 노출시키는 표면적을 증가시킨다. 그러나 최근의 보고에서 보면 지방과 수용액의 단면 없이 기질이 그대로 용 해되어 있어도 지방분해효소(lip ase) 가 작용한다고 하였다. 그러나 이 효소는 특히 지방과 수용액 단면에서만 작용한다는 것이 찰 알 려진 목칭으로 되어 있다 .2 1) 지 방분해 효소는 콜레 스데 몰 este r ase 나 ph osph o lipa se A2 가 요 구하는 담즙영을 요구하지 않으며 이 효소가 작용하기 위한 적정 의 p H 는 8~9 정도이다 .22) 그러나 효소의 지방구오P ] 접촉작용면적 확보를 위해서는 적정량의 담즙영 농도가 요구된다. 이 적정량 이 상의 담즙영은 오히려 방해가 된다 .20),23-5) 효소 작용의 방해는 수용액단면과 기질접촉으로부터 수용액 떤울
유지시켜서 효소로 하여금 수용액에 불용인 기질과 물리적으로 분 리 되 게 하는 것 이 다. 26·· 8 ) 이 렇 게 방해 된 lipa se 의 작용은 Co-lip a se 가 촌재 함으로써 회 복된다. Co-li pa se 는 담즙영 이 없 어 도 lipa se 의 작용울 상승시 킬 수 있 다. 25> Borgs t r o m 과 Erlanson 은 담즙영 의 방해는 lip a se 기 질 외 곽에 dete r ge nt 단일막을 형 성 하여 서 효소가 기질에 접촉해 들어갈수없도록 하는데 있다고 하였다. 이때 같은 전극끼리 반발이 있을 수 있다고 하였다 .25) 또한 최근에 Nano 와 Savar y도 담 줍 영의 lipa se 작용에 관련해 서 단면의 표면장력과 관련이 있다고 하였다. 기질 단면의 표면장 력이 높으면 lip ase 가 빨리 흡착되며 따라서 빠른 지방분해가 이루 어진다. 그러나 담즙영은 기질의 표면장력을 감소시킵으로써 지방 분해를 제한시키는 결과를 초래한다고 생각한다 .29) Bor g s t rom 은 lip ase 의 담즙염에 의한 작용방해는 일반적으로 구 조나 전극의 전극화 (char g e) 에 의 한 것 보다도 담즙영 의 농도에 의 해서 더 많이 영향을 받는다고 하였다 .30-1) 담즙영의 방해효과는 담 즙영의 CMC 와 관련이 있다고 보며 CMC 범위에서는 방해작용이 없다고하였다. 또한 담즙영 의 방해 효과에 대 해 서 작용역 학 (k i ne ti c) 연구로부터 다른 기전이 제안되었다 .28) 이 연구자의 자료에 의하면 용액 중에서 효소와 담즙영 복합체는 담줍영으로 덮여진 기질에 용이하게 훈착 되지 못한다고하였다. Desnuelle 과 그의 동료도 32' Co-lip a se 는 l ip ase-Co- lip ase- 담즙영 인 3 자 mi ce lle 복합체 를 형 성 하는 것을 조정 한다고 하였 다. 이 복합체 형성은 담즙염이 촌재할 때의 지방분해작용의 초기 작용이라고 하 였다. Vandermeers 둥은 작용역학 분석결과 다음과 같은 사실을 제시 하였다. Co- lip ase 와 lip ase 는 담즙영이 촌재하면 기질에 차례로 홉 착이 되며 마치 Co- lip ase 가 l ip ase 결합을 위한 고리와 같은 역할을 · 한다고 하였 다. Co-lip a se 와 담즙영 과의 두 가지 mi ce lle 복합체 는 지방분해작용에 있어서 경쟁적인 방해물질이 된다. 그러므로 Co-· lip ase 는 lip ase 의 지방분해작용 속도를 최대로 하여 방해룩 받지 ,
않게 하려 면 lip a se 의 분자수가 Co-lip a se 분자수에 비 해 서 훨 싼 많 은 양이 존재해야 된다. 세제안 담줍영의 농도가 증가되면서 Co- lip a se 가 존재 하면 lip a se 의 활성 은 감소된다. 26l pa ncreati c lip a se 와 Co-lip a se 는 I : I 의 복합체 를 형 성 한다고 하였 다• 33) Co-lip a se 는 먼저 지 방구의 면을 동과해 들어 갈 수 있 으며 그렇 게 되 면 lip a se 는 Co-lip a se 가 제 공해 주는 고리 를 이 용해 서 지 방구를 통 과해 들어갈 수 있다》 4) Borgs t r o m 은 제 시 하기 를 Co-lip a se 는 Co-lip a se 와 세 제 사이 의 복 합체가 이루어지돈지 이루어지지 않든지간에 l ip ase 의 작용을 부활 시킨다고 하였다. 그러나 또 다른 해석은 Co-l ip ase 가 세제의 농도 . 가 증가되면 기질로부터 분리된다고 하였다. Co-l ip ase 와 세제는 기 질의 부착부위 (b i nd i n g s it e) 에 서로 경쟁적인 방해자라고 하였다. 그 런데 Co-l ip ase 는 l ip ase 가 기질에 부착할 수 있도록 고리와 같은 역할을 하지만 담줍영은 이러한 역할이 없다고 하였다 .30) Co-lip a se 와 lip a se 복합체 는 생 리 적 으로 중요하다. lip a se 의 활성 은 담즙영의 농도가 CMC 이상으로 존재하여 활성을 위한 (o pti mum) · p H 가 9 에서 6 으로 이동되면 절대로 방해를 받지 않는다 .30) 2) 콜레 스테 롤 este rase (carboxy li c este r hy d rolase) 섭취된 콜레스데몰 es t er 의 가수분해는 콜레스테롤 흡수를 위해서 중요하다. 식 사에 서 섭 취 된 choleste r y l este r 는 이 형 태 로는 흡수 가 되지 않는다 .35) 그러나 콜레스테롤을 콜레스테롤 es t er 형태로 、 공급했을 때 콜레 스테 롤 este r ase 의 가수분해 작용에 반발하여 국 히 소량이 흡수되는 경우도 있다 .36) 콜레 스테 롤 este r ase 는 콜레 스테 롤 este r 의 가수분해 분만이 아니 라 콜레스테롤과 유리지방산을 결합시켜서 콜레스테롤 es t er 의 합 성도 한다. 이 두 가지 기능 모두가 콜레스테롤의 흡수와 대사를 위 해서 중요하다. 콜레스테롤 es t er 의 합성은 콜레스테롤 흡수를 방 해할 것이다. 그러므로 소화기 장내에서의 콜레스테를 es t erase 의 소화작용에 있어서의 역할은 콜레스테몰 es t er 의 가수분해로 나타 나서 콜레스데몰 es t er 의 축적을 제한한다. 또한 장내에 함유된 범
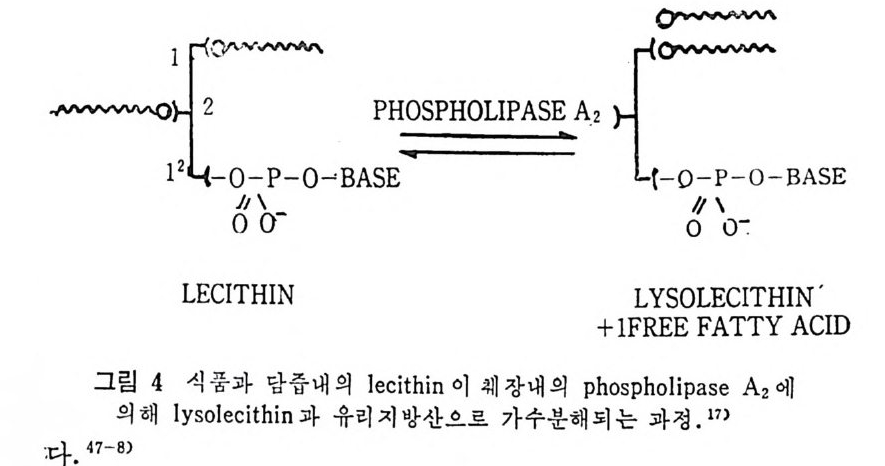
위의 담줍염 농도는 장내에서 콜레스테롤의 에스델화 를 방지하며 가수분해를 조장한다. 37) 그리 고 이 효소는 장내 의 단백 질 분해효 소로부터 의 파괴 를 방지해 준다. 38) 콜레 스데 몰 este r ase 는 dim er 로써 유리 되 어 있 으며 39) 분자량 은 136, 000 이 다. 또한 monomer 로도 유리 되 어 있으며 , 40) 분자량은 70,000 이며 이 효소가 작용하기 위해서는 담줍영이 필요하다 .4 1) 췌 장 este r ase 는 담즙산 mi ce lle 내 에 용해 되 어 있 는 carboxy li c este r , 스데 몰 este r s 와 불용성 este r 에 작용한다. 이 효소의 콜레 스데몰 es t er 의 가수분해를 위해서 적합한 p H 는 약 6.6~s. 5 사이 라고 한다. 가수분해작용을 위해서 흔히 문헌에 나타나는 가장 최 적의 p H 는 6.6 이다 .42 가) 또한 최근에는 넓은 폭의 최적 pH 6.5~ 8. 8 이 보고되 었 다. 28) 모든 지방분해효소에서 최적의 p H 는 그때그때의 기질상대에 따 라서 결정된다. 그러나 carboxy lic este r hy drolase 는 기질의 화학 적 구조에 대 해 서 덜 특수 (s p ec ifi c) 하게 반응한다. 45) 3) ph osph oli pa se ph osph olip a se 는 주요 세 포막의 구성 성 분인 인지 방을 가수분해 한 다. 체 액 내 에는 적 어 도 두 종류의 ph osp h olip a se 가 존재 하는데 하 나는 ph osph oli pa se A1 으로 이는 인지방의 글리세롤의 제 1 번 위치 의 es t er 결합를 분해한다. 그리고 또 다론 하나는 ph osph olip a se A2 인데 이는 인지방의 글리세돌의 제 2 번 위치의 es t er 결합을 분해 한다(그립 4 참조) . ph osph olip a se A2 는 체 액 중에 zy m o ge n 으로 존 재 하여 이 효소의 활성 을 위 해 서 try p s in 이 요구된다• 췌 장의 p hos p ho lip ase 는 이 효소의 작용을 위 해 칼슘이 온이 cofa c to r 로서 철대로 요구된다. 칼슘이온이 없으면 이 효소의 작용이 이루 어지지 않는다 .46) 인지방은 수용액중에 확산되면 얇은 충을 이루게 된다. 그러면 ph osph oli pa se 에 의 해 서 작용되 어 지 지 않는다. 작은 mi ce lle 로 확 산되는 것이 이 효소작용을 위해 중요하다. 담줍영이 이 가수분 해를 위해 철대적으로 필요하며, 십지어 co fac t or 라고까지 부른
 。-J^^^
。-J^^^
6 장내로부터의 지방 흡수 장내로부터 용해성의 분자를 내막세포내로 흡수하는 속도는 두 가 지의 장벽을 통과하는 울에 의해서 결정된다. 이 장벽은 첫째는, 수분충 (unsti rr ed wate r lay er ) 이 며 다음은 내 막세 포의 지 방충의 장내 막 (membrane) 이 다. 내막세포막 근처에 수분충이 있다는 사실은 과거 몇 년 동안 알 려 진 사실이 다. 그러 나 1960 년대 에 Wr ig h t 49) 와 Di amond50) 에 의 한 세포막을 꿰뚫어 통과하는 흡수과정 연구가 넓게 인정될 때까지는 구체적으로 많은 사람의 관심을 끌지 못했다. 소장내에 이러한 수분충이 촌재함으로인해서 소장의 공장 내막세 포에 의 한 용해성의 mi ce lle 로부터 담즙산과 지방산의 수동적 인 홉 수에 영향을 미치는 주요 결정적인 요인으로 간주하게 되었다. 지방의 흡수연구를 위해서 처음으로 m ic elle 을 형성해서 이의 이 용률을 확인해 내기 위한 시도는 J ohns t on 과 Bor g s t rom 에 의해서 이루어졌다 .S I) 이 연구에서 보여준 결과는 지방의 홉수는 지방이 m i celle 의 형태로 촌재할 때 다론 형태로 촌재할 때보다 빨리 흡수 된다고 하였다. 그런데 이 연구결과는 후에 많은 다른 연구자들에
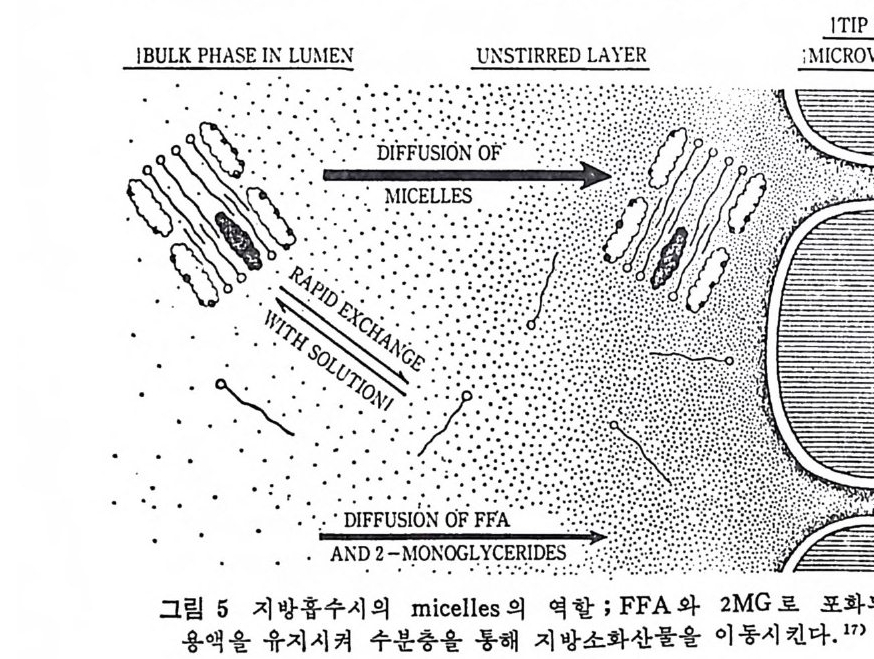
의해서 지지되었다. 52-5) 최근 Di e t sch y의 실험실에서 지방홈수과정에서 주요한 장버인 수 분충에 대한 과거의 개념을 보다 새롭게 소개하고 있다 .66) 지방홍수에는 수분충의 두께가 결정적으로 영향을 미찬다. 이론 적으로도 수분충의 두께 를 감소시 키 면 mi ce lle 형 태 의 지 방의 흡수율 은증가한다. 대조적으로 천수용액 (po lar solu t es) 의 흡수는 수분충이 흡수에 방 해장벽이 될 수 없으며 오히려 내막세포막이 주요 방해장녀이 된 다. 57) 안정 된 (unsti rr ed) 조건하에 서 수분충의 평 균 두께 는 공장과 회장이 각각 198 土 5µm 와 217 土 5µm 인 것으로 여덟 종류의 동물 에게서 자모가 수집되었다 58) (그림 5 참조). 분해된 지방물질이 m ic elle 형태에서 소장의 내막세포내로 이동되 는 과정에 대해서는 알려진 기전이 없다. 그러나 Gau g l 에 의해서 제안된 바에 의하면 장내 내막세포내에 사슬이 긴 지방산과 찬화력이 높은 원형질내에 존재하는 단백질이 있는 것으로 보고되었다 .59) 이 단백질의 지방산에 대한 찬화력은 -
 ITIPOF
ITIPOF
포화지방산일 때에 불포화지방산에 비해서 감소되며 지방산의 길이 가 중간 정도나 짧은 것일 때는 결합조차 일어나지 않는 것으로 관 찰되었다 .60) 이 단백 질을 지 방산절 합단백 질 (fatty aci d bin d in g pro te i n ) 이 라고 부른다. 지방산결합단백질은 소장의 기부(p rox i mal p o rti on) 에 촌재 하며 cryp tic cell 보다도 융털돌기 (v ill us) 의 끝부분(tip of cell) 에 더 많은 양 촌재한다고 본다. 고지방식사를 하면 이 단백질의 양이 중 가되기도 한다. 이와 유사한 단백질이 간, 지방세포, my o cardiu m , 신장에서 발견된다 .Gl - 2 ) 분 해 된 지 방산물은 넓 게 흡수가 일어 나나 tau rin 과 결합된 담즙 영은 공장에서는 흡수가 일어나지 않는다 .63) 동위 원소로 처 리 된 MG 와 지 방산이 함유된 mi ce !l ar 용액 을 사용 하여서 hams t er 의 소장 절편 (s li ce) 에서 홍수운을 관찰한 결과 MG 와 지방산 모두 빠른 홍수를 하였으며 곧 세포내에서 중성지방으로 융합되 었 음이 나타났다. 51) 소장세포에 의해서 두 물질의 흡수는 대사상 나타나는 방해물질, 열에 의한 불활성화, 저온부탄 등에 의해 아무런 영향을 받지 않았 다. 이 관찰결과 물질의 소장세포에 의한 흡수의 물리적 현상온 효 소의 작용이나 열량상태에 따라서 무관하며 흡수자체는 수동적 과 칭이라고 결론지었다. 지방산의 길이가 또한 지방산 흡수에 주요 결정인자이다. 대부분 의 짧은 사슬의 지 방산은 직 접 문맥 혈 (po rta l blood) 로 이 동이 되 며 알부민 (album i n) 과 지방산이 결합되어서 이동된다. 중간 사슬길이의 지방산은 혈액과 림프로 모두 이동된다. 이는 소장의 홍수세포내에 서 재에스텔화가 되어서 중성지방울 형성하돈가 아니면 문맥혈 순 환에 의해서 직접 이동된다. 사슬이 긴 지방산은 항상 흡수세포내에서 중성지방으로 재결합이 되어서 ch ylom ic ron 의 구성성분이 된다 .64) 굴리세몰은 수용성의 물질이므로 수분충을 단순한 확산에 의해서 통과한다. 그리고 흡수 세포막에서는 운반체의 포화기전에 의해서 중재된다. 농도가 낮은 상태에서는 글리세를의 상당량이 흡수되는데 이는 운반체기전에 의
해서 굳리세몰이 1mM 이상의 농도만 존재하면 흡수가 되기 때문 이다. 굳리 세 를의 운반체 기 전은 glu cose-ga lacto s e 운반체 기 전과는 다론 것 이 다. 소장의 끝부분에 는 충분한 농도의 굳리 세 몰 운반체 (carrie r ) 가 존재한다. 이 운반체에는 글리세몰분해효소가 포함되어 있으며 이는 굴리세를대사에 필요한 물질이다 .65) 담즙영도 사슬이 간 지방산과 MG 의 흡수를 상승시킨다. 장내에 서 담줍염이 촌재하지 않으면 흡수는 감소하지만 흡수가 전혀 일어 나지 않는 것은 아니다. 담줍영의 효과는 지방의 용해성을 증 가시 켜 서 장내 흡수부위 인 내 막세 포로부터 수분충륜 통과해 서 이 동을 · 빠르게 하는 것이다 .66) 중성지방홉수와는 대조적으로 콜레스테풀의 홍수도 제한되어 있 다. 콜레스데를의 섭취가 증가되면 흡수량은 증가되나 흡수울로 환 산하면 감소될 수도 있다. 그러나 콜레스테롤의 흡수는 섭취에 따 라서 그 울이 변화되는 것이지 고정된 양이 흡수되는 것은 아니다. 더구나 식사에서 섭취된 콜레스테롤의 흡수는 콜레스데몰과 함께 섭취한 다른 지방의 종류와 양에 따라서 좌우된다. 모든 콜레스테롤은 필수적으로 유리된 형태로 되어야만 흡수가 일어나고 지방산과의 es t er 형태로는 흡수되지 않는다. 그러므로 소 장내 에 서 작용하는 콜레 스테 롤 hy d rolase 의 작용은 콜레 스데 롤의 흡수를 위해서는 결정적으로 중요한 과정이다. 콜레스테롤은 결국 장내 의 mi ce llar 에 융합되 어 서 장내 막세 포로 흡수된다. 이 때 의 홈 수기전은 밝혀진 것이 벌로 없다. 장내막세포에 의해서 취해전 콜레스테를의 상당량이 사슬이 긴 지방산과 에스텔화를 한다. 이 작용을 촉진하는 효소는 콜레스테 롤 este r ase 로서 이 는 췌장 콜레 스테 롤 este r ase 와 그 득칭 이 유사 하다. 아마도 장내막세포에 촌재하는 이 효소는 췌장에서 기원된 것으로 생각할 수 있으며 67) 또 한편에서는 전연 다른 두 종류로 생각한다 .68) 장내막세포내에서의 콜레스데를 에스벨화기전은 찰 이해되어지 지 않았다. 에스텔화를 위해서는 지방산의 활성화가 필요하지 않나
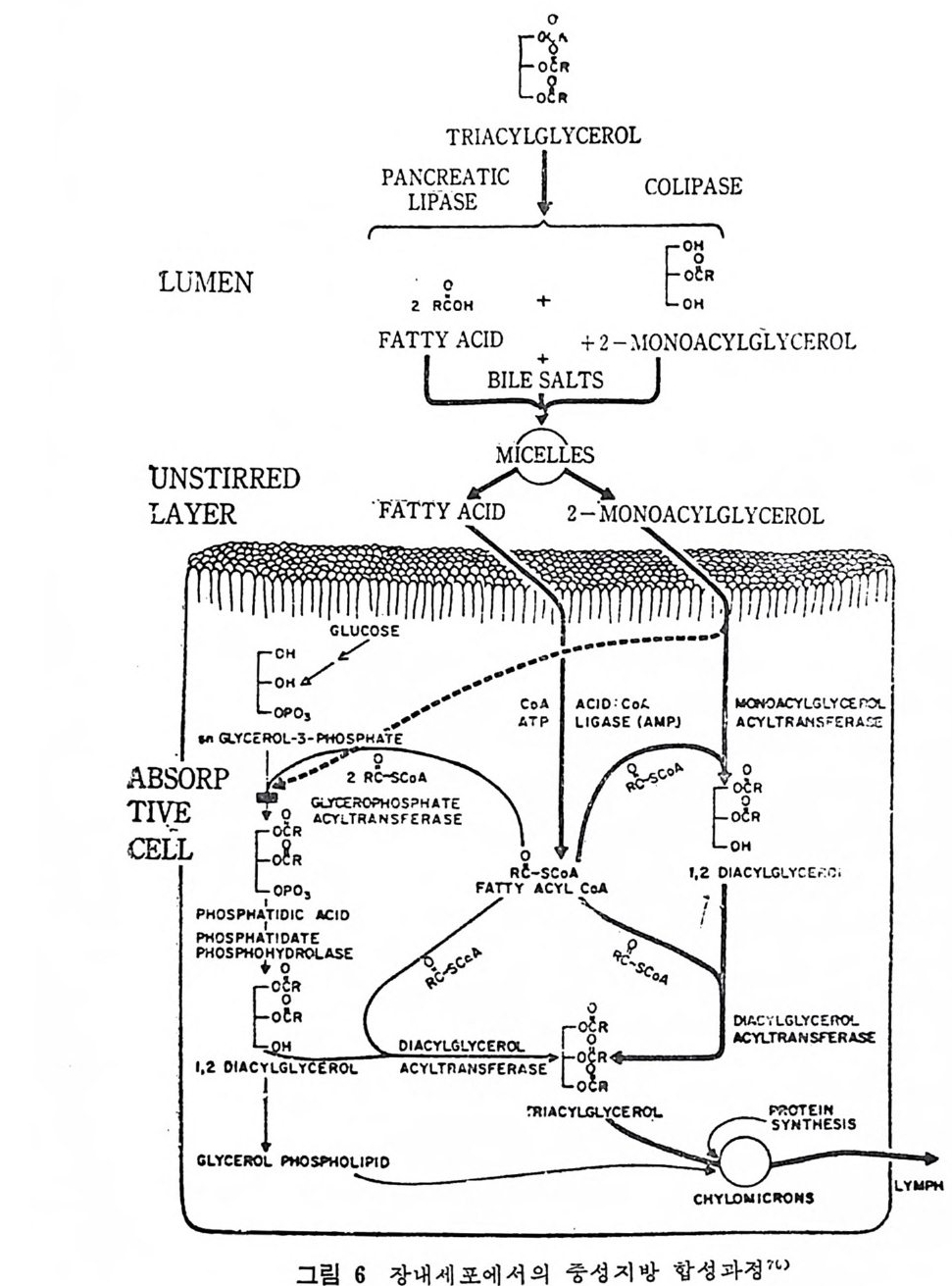
고 보고되었다 •36) 더구나 담즙영의 에스텔화를 위해서 요구되논 농 도는 장내막세포내에 존재하는 양보다 훨싼 높은 것으로 나타났다. 에스낼화의 기전이 무엇이든지간에 ch y lom i cron 에 융화되어 장 내막세포를 떠나는 콜레스테폴의 60~80% 가 에스텔화된 형태이 다. 59> chy lo mi cr on 내 에 는 콜레 스테 롤 este r 와 유리 콜레 스테 몰이 중성지방과 지단백질(Iip o p ro t e i n) 과 관련되어서 존재한다. 일단 흡수 된 콜레 스테 롤은 모두 tho racic duct lym p h 에 나타나며 문맥 정 멕 으로 이동되는 것은 없다. 7 장내막세포내에서의 지방대사 Mi cro vil lu s 막 (membrane) 을 통과해서 지방산걷합단백질에 의해 서 이 동되 어 전 지 방은 SER (smooth endop la smi c reti cu lum) 의 끝부위 (ter mi na l web) 밑 에 도착한다. 지 방의 흡수되 는 형 대 는 지 방산, MG 와 lys o p h osph ati de s 이 다. 이 들은 여 러 종류의 효소작용에 의 해 서 gly c erolip id 로 재 합성 되 어 chy lo mi cr on 을 형 성 하며 순환계 동을 거 노 쳐 서 신체 조직 으로 이 동된다(그림 6 참조). (1) 지방산의 활성화 지방산은 이용되기 위해서 사슬이 간 지방산은 각각 CoA 유도체 로 전환되지 않으면 안된다. 이 작용을 촉진하는 효소는 사슬이 긴 치 방산 CoA lip a se(l on g chain fatty acid CoA l ip ase) 라고 Kornberg· 와 Pr i cer71) 는 연구해내었다. 관찰되 어 졌 던 소장의 mi cr osomal 부위 (frac ti on ) 에 서 이 효소의 작 용이 모두 나타났다. 일반적으로 보면 이 효소의 작용은 지방산의 사슬의 길이가 길어질수록 증가된다고 본다. 그러나 소장내막내에 는 짧은 사슬길이나 중간 사슬길이 지방산의 활성을 위해서 팔요한 · 효소를 함유하고 있다고 본다 .72) 사슬이 간 지방산울 활성화시키 는 효소의 작용은 기아시에는 감소된다고 하였다 .73) 지 방산이 활성화되는 기 전을 보면 enzy m e-CoA 가 중간산물로 냐-
 臼;
臼;
타나며 74) 지방산과 ac y l 운반체 단백질이 복합체로 나타난다 .75 - 6) 그러나 보다 분명한 중간산물을 통해서 이 효소의 작용기전을 규명 하기 위한 연구가 더 진행되어야 한다고 본다. (2) 장내막에서의 중성지방의 생합성 장내막세포내에서 중성지방의 생합성기전은 3 가지로 구분지을 수 있 다. 첫 째 , Sn-gl y c erol-3-ph osp h ate 를 아 용하여 서 합성 하는 경 로 와 둘째 , dih y d roxy a ceto n e ph osph ate 를 acy l accep tor 로 이 용하여 서 합성하는 경로와 세번째는 MG 를 이용하여 합성하는 경로이다. 아들의 중성지방 합성경로는 그립 6 에 나타나 있다. 첫째, Sn- g l y cerol-3- p hos p ha t e 를 이용하여 합성하는 경로는 처음 으로 Weis s 와 Kenned y 77) 에 의 해 서 제 안되 었 으며 이 물질 이 장내 막에서 발견된 것은 50 년대 말 78) 이었다. Glyc erol-ph osp h ate 에 acy la ti on 되 기 위 한 지 방산의 특수성 에 대 해 서 연구자들이 장내 막에 서 연구하였 다. acy lg l y c erol 생 합성 을 위 해서는 사슬이 긴 지방산을 보다 호의적으로 이용한다는 증거를 제 시하였다 .79) 마에리스탄산과 팔미탄산이 보다 호의적으로 활성호臣] 며 g l y cerol- p hos p ha t e 에 결합되는 현상이 여러 종류의 동물에게서 나타났다. 79 -8 0) Br i ndle y는 여러 종류의 치방산을 이용했을 대 여러 형태의 글리 세몰이 합성되었음을 연구하였다. 여러 종류의 지방산과 이들의 유 도체 인 지 방산 CoA 가 촌재 할 때 labeled gly c erol-ph osp h ate 가 여 러 형태의 ac y l g l y cerol 로 결합되는 현상이 실험으로 보고되었다 .8 1) 이 실험으로서는 여러 가지 나타난 특정사실을 해석하기는 어려운 것 으로 본다. 왜 냐하면 다양한 과정 의 효소작용이 글리 세 몰 · 합성 과 정에서 나타나기 때문이다. 더 나아가서 포화지방산이 촌재할 때는 불포화지방산이 g l y cerol ipi d 생합성과정중에서 결합될 때, 현처한 영향을 미쳤기 때문이다. 보다더 이 현상을 복잡하게 하는 것은 불포화지 방산이 촌재 할 때 ph osph ati dic acid 가 중성 지 방으로 전환 되는데에 현저하게 영향을 미찬다는 Br i ndle y의 보고대문이다 .82)
장내 막세 포내 에 서 합성 된 ph osp h ati di c acid 도 endop la smi c reti - culum membrane 에 굳게 결 합되 어 있 다. 83 시) mi cr osome 에 결 합 되 어 있 는 ph osph ati di c acid 는 cy tos ol 에 촌재 하고 있 는 ph osp h a- tida te ph osph ohy d rolase 에 의 해서 Sn-1, 2-dia c y lg l y c erol 로 가수분 해된다 .85) 이 효소는 mi ce llar 에 존재 하는 ph osph ati di c acid 룬 기 질 로 사 용한다. 현재 까지의 증거 로 보면 이 cy tos ol 에 존재 하는 효소가 ac y l g l y cerol 생합성을 위해서 중요작용을 하는 것으로 생각된다. 이 에 부가해서 이 효소의 상등액 (su p erna t an t)은 acy lg l y c erol 생 합성을 자국하는 주요 인자로 관찰되었다. 이런 현상은 일찌기 195 7 년 에 간에서 관찰되었으며 86) 소장내막에서도 관찰되었다.i 2 ) 이때 생성 되는 d i ac y l g l y cerol 은 Sn-1,2 형대이며 8” 이 물질은 중성지방과 p hos p ho g l y cer i des 생합성을 위해서 사용된다. 둘째 , dih y d roxy a ceto n ep h osph ate 를 acy l accep tor 로 이 용하여 합 성하는 경로이다. 이 과정은 처음에 gu in e a pig의 간에서 실험되었 다. 87) Di hy d roxy a cto n eph osph ate 가 acy la te d 되 어 서 1-a cy l 유도체 를 형 성 하며 이 acy ld ih y d roxy a ceto n ep h osph ate 는 NADPH 에 의 해서 환원되 어 서 lys op h osph ati dic acid 로 전환된다• 이 lys o 물질 은 결 국 acy la te 되 어 서 참정 적 으로 ph osph ati di c acid 인 중간 대 사 산물을 만든다. 이대 생성된 ph osph ati dic a ci d 는 앞에서 언급한 대 로 endoth eli al reti cu lum membrane 에 결 합되 어 서 결 국 중성 지 방 과 ph osph og ly c eri de s 합성 에 이 용된다. 1970 년에 Rao 둥에 의 해 서 dih y d roxy a ceto n ep h osp h ate 경 로가 장 내막에 존재함이 다시 밝혀졌으나 이 경로를 통해서 합성되는 중성 지방의 양적안 공헌은 아직까지 밝혀지지 않고 있으며 88) 이들의 홈 수효과도 밝혀지지 않고 있다. 세 째 는 monoacy lg l y c erol 을 이 용하여 서 장내 막세 포내 에 서 중성 지방울 합성하는 경로이다. 중성지방의 장내에서 소화되고 난 최종 주요 산물은 monoacy l 유도체 이 다. 지 방흡수에 있 어 서 monoacy l- g l y cerol 이 관련이 있다고 처음으로 발표된 보고는 약 1 세기 전이 다. 89) 그리 고 소장내 에 monoacy lg l y c erol 이 존재 한다고 처 음으로
발표된 것은 1935 년이었다 .90) 이 후에 많은 연구자들의 monoacy lg l y c e rol 의 acy lg l y c erol 생 합 성의 중요성에 대해서 제시한 바가 많았다 .91-3 > 196I 년에 Clark & Hubscher 는 장내 막에 서 monoacy lg l y c erols 로부터 중성 지 방합성 의 직접적인 증거를 처음으로 제시하였다. 이 합성경로는 그림 6 에서 굵은 선으로 표시되었다 .94) 소장내막에서 중성지방의 생합성에 있 어 서 monoacy lg l y c erol 경 로가 주요 합성 경 로라는 것 이 쥐 , 행 스 터, 맑 돼지, 고양이, 기니아 돼지, 양, 말, 사람에게서 증명되었 다 . 70) Sn1 - ,2 一 그리고 3 - monoac y l g l y cerol 은 같은 효소에 의해 서 acy la te 되 며 rac -1- m onoacy lg l y c e rols 은 1, 3-di a c y lg l y c erols 로 acy la te 된다• 95) 결과적으로 보면 2-m onoacy lg l y c erol 은 특히 Sn-1 위치에 acy la te 되어서 Sn - I,2 - d i ac y l g l y cerols 을 형성한다 .8” 이 효소를 기 질로서 2-m onoacy lg l y c e rol 은 호의 적 으로 취 한다. 95) 이 효소작용의 Vmax 는 1 - 과 2-monoacy lg l y c erols 과 유사하다고 본 다. 그러 나 1 _ 이 성체 (i somer) 의 Km 치는 2 - 이 성체 (i somer) 보다 훨싼 큰 것으로 보고되어 있다 .9 6) 그러나 동물의 여러 종류에 따라서 이 효소가 작용하는 기질 이성체가 다르게 나타나는 것으로 밝혀졌 다 .9 7) (3) 중성지방 생합성의 조절 —지 방생 합성 에 있 어 서 Sn-gl y c erol-3- p h osp h ate 와 monoacy lg l y c erol 경 로의 조절과 이 들의 상호작용 1976 년에 Joh nsto n 에 의 해 서 중성 지 방 ph osph og ly c erid e 의 생 합 성조절에 있어 합성경로의 상호관련이 제시되었다 .98) 과거 에 도 Sn-gl y c erol-3-ph osph ate s 의 수준조절기 전에 대 한 결론은 지방산이 홉수되는 동안에는 또한 포도당 이용량이 증가되며 이때 에 Sn-gl y c erol-3-ph osph ate 의 po ol siz e 가 증가된다는 데 에 기 초 를 두었다 .99) 또한 행스터실험에서 기아 동안에는 지방산의 에스텔화가 현저 히 감소하는데 이 현상은 선행물질인 글리세롤 양이 현저히 감소
하였기 때 문이 라고 생 각한다. 100) 지 방산의 활 성 화 는 지 방흡수조 절 에 가장 기본적인 역할을 하는 것으로 생각한다. 왜냐하면 하 루 저 녁울 굶으면 지방산을 활성화시키는 효소의 활성이 감소된다 . 73 ) 어 떤 종류의 호르몬의 작용이 장내 막에 의 해 서 acy lg l y c erol 생 합 성에 영향을 미치는 역할이 있다고 제시되었다. 부신을 철단해 내 면 지 방산 CoA lip a se 와 monog ly c erol 과 dig ly c erolacy lt r a nsfe r ase 의 활성 이 감소됨 을 보여 주었 고 장내 막에 서 gly c erol-3 - p h osp h ate 의 에스텔화도 감소함을 보여주었다 .101-2) Brin d ley 와 Ferr i er103) 에 의 해 서 관찰되 어 전 바에 의 하면 장내 막 에서 지방산 CoA lip a se 에 의 해서 gly c erol-3 - p h osp h ate 가 acy la - tion 이 되는 작용이 바로 속도제한 단계 (rate lim i ting s t e p)라고 한 다. 장내막에서 중성지방의 합성은 만일에 monoacy lg l y cerols 이 존재 하면 기 본적 으로 먼저 monoacy lg l y c erol 경 로를 통해 서 이 루어 진 다. 104) Ki ne ti cs 실험 에 서 보면 monoacy lg l y c erol 에 p:ilm i toyl- CoA 가 acy la ti on 되 는 Km 치 는 gly c erol 3 -ph osp h ate 의 것 보다 낮다고 한 것으로 우1 의 사실이 더욱더 입증되었다 •105) 한편 monoacy lg l y c erol 경 로가 지 방조직 에 서 도 존재 함이 증명 되 었 다. 106) 이 과정 을 관찰하는 동안에 monoacy lg l y c erols 이 현저 하 게 gly c erol-3-ph osph ate 의 acy la ti on 에 영 향을 미 치 는 것 이 나타났 다. 106> monoacy lg l y c erols 이 gly c erol-3-ph osph ate 에 ac y la ti on 되 어서 중성지방이 합성되는 조절작용이 있음이 밝혀졌다 .107) 장내막 조직 편이 나 mi cr osome 은 monacy !gly c erols 를 가함으로써 gly c erol -3-ph osph ate acy la ti on 에 보다 예 민한 조철작용이 있 음이 나타 났다. monoacy lg l y c erol 이 gly c erol-3 -ph osph ate 의 acy la ti on 에 미 치는 영향은 직접적이며, ac y l-CoA 의 유용성에 대한 경쟁은 아 니 라는 사실이 gly c erol-3-ph osph ate 의 acy la ti on 이 Sn-3-mono- ac y l g l y cerol 의 유사물질인 Sn-3-e t her 에 의해 직접적으로 방해되 었던 사실로 미루어 밝혀졌다. 2-monoacy lg l y c erol 이 gly c erol-3-ph osph ate 의 acy la ti on 에 직
접적으로 영향을 미찬다는 사실이 간의 m i crosome 을 효소의 급원 으로 사용함으로써 관찰될 수 있 었 다. 108) 이 mi cr osome 내 에 서 중 성 지 방과 ph ci sp h og ly c erid e 는 gly c erol-3- p h osph ate 의 acy la ti on 에 의 해 서 만이 생 성 되 는데 이 때 monoacy lg l y c erol 이 존재 하면 이 합 성과정이 현저하게 나타나지 않는 것으로 관찰되었다. 이 결과는 monoacy lg l y c erols 의 gly c erol-3- ph osph ate 의 acy la ti on 에 대 한 효 과는 직접적인 방해효과임을 밝힌 것이며 acy l- CoA 기질과는 경쟁 에 의한 것이 아닌 것으로 나타났다 .70) 생리적인 조전하에서 중성지방대사는 그림 6 에 굵은 줄로 표시되 어 있 다. 즉 췌 장의 lip a se 에 의 해 서 형 성 된 monoacy lg l y c erols 과 치방산은내막세포내로들어간다. 이들의 흡수는주로장내막세포내 vil lu s 의 윗 부분에 서 일어 난다. 홍수되 어 전 MG 는 tri g ly c erol sy n t- he t ase 에 의해서 중성지방 생합성의 기질로써 사용되었다. (그립 6 의 굵은 선 표시 ) MG 는 또한 Sn- gl y c erol-3 - ph osph ate 경 로플 통한 중 성지방 생합성의 방해물질로써 기능한다 . 이 경로는 그립 6 에 접선 으로 표시되어 있다. 중성지방생합성에 MG 가 사용됨으로 인해서 세포내의 MG 의 함 유수준은 감소되 며 따라서 Sn-gl y c erol-3-ph osph ate 의 경 로를 통한 중성 지 방합성 의 MG 방해효과가 초 1 처 수준이 된다. 장내 막세 포의 세 포내 에 서 가장 효과적 인 기 전에 의 한 acy lg l y c erol 합성기질의 유용량이 문제이며 따라서 MG 가 존재하지 않은 상태 에서 중성지방의 생합성이 일어나는 기전으로 제안되고 있다 .70) (4) Chy lo mi cr on 형 성 장내막 세포내에서 흡수되어진 지방산과 MG 가 다시 중성지방으 로 합성이 되면 이 합성된 중성지방과 인지방, 콜레스테를 este r 및 유리 콜레스테롤은 서로 결합되어서 ch y lom i cron 을 형성한다. 이 때에 중성지방, 콜레스데몰 este r , 유리콜레스테롤 및 인지방을 지 칭 해 서 pre chy lo mi cr on 또는 신생 (nascent) chy lo mi cro n 의 기 질 이 라고 부른다.
Chy lo mi cr on 의 구의 크기 는 다양하다. 대 개 직 경 이 I OOmµ 으로부 터 500mµ 이 나 70mµ~lmµ 까지 작은 것 도 존재 한다. chy lo mi cr on 의 크기는 장내막 세포내에서 중성지방, 인지방 및 단백질의 합 성 률에 의해시 달라진다. 중성지방의 합성물은 MG 나 지방산의 유용 량이 풍부할 때 상승되 며 이 런 조건하에 서 는 chy lo mi cr on 의 구의 크기가 큰 것이 합성되는 경향이다. 사람과 쥐 의 림 프 chy lo mi cr on 의 화학적 구성 성 분은 다음 표 l 에서 보는 바와 같다.
 표 1 사람과 쥐 의 림 프 chy l omi cr on
표 1 사람과 쥐 의 림 프 chy l omi cr on
다음의 표 2 는 사람의 chy l- omi cr on 의 화학성 분 중에 서 인 지방의 성분을 세분화한 것이 다. Chy lo mi cr on 의 화학구성 성 분을 보면 글리세몰 결합치방 (gly c erid e ) 의 대 부분이 중성 지 방이며 인지방의 많은 양이 lec ithi n 이 다. 여 하튼 chy lo - mi cr on 구성 성 분 가운데 에 서 85% 내의가 중성지방이기 때 문에 생리적인 조건하에서 보 면 chy lo mi cr on 은 지 방흡수에
뜻이 크다.
 표 2 인지방의 구성성분 110 》
표 2 인지방의 구성성분 110 》
인지 방은 함유량이 소량이 치 만 ch- y lom ic ron 을 구성하고 있는 중요한 물질로서 최외각을 구성하는 물질이 다. ch ylom i cron 의 인지방과 함께 유 리콜레스테롤과 단백질은 이 chy lo m- i cron 의 외각을 구성 하고 있는 물질 이 다. chy lo mi cr on 구의 의 각구성 성 분인 인지방은 장내막세포내에서 de novo 합성을 하지만 정상적으로는 대 부분의 인지방아 장으로부터 흡수된
인지방이다. 장내의 인지방은 석이로부터 섭취된 것도 있지만 대 부분이 당관으로부터 분비 된 ph osph ati dy lc holin e 이 며 홍수된 ly solecit hi n 은 다시 :.ic y la ti on 되 어 서 chy lo mi cr on 표면물질로 사용 된다• 인지 방과 유사하게 chy lo mi cr on 의 콜레 스테 롤은 식 이 로부터 섭 취된 것도 있지만 장내에 존재하는 콜레스테롤도 있다 . 이들의 50 ~ 7 5 % 는 장내막세포내에서 에스텔화되어서 ch y lom i cron 형태로 분 비된다. Ch y lom i cron 내 단백질은 많은 흥미를 꿀고 있다 . 함유되어 있는 양으로 보면 비 록 소량이 지만 chy lo mi cr on 의 ap o p ro te i n 은 특칭 을 지 닌 목 수단백 질 이 다. 앞의 표는 사람과 쥐 의 chy lo mi cr on 에 서 지 방울 제 거 한 후에 SDS acryl a mi de ge ls 에 서 전동분석 해 낸 결과아 다. 사람과 쥐의 두종족간에 거의 유사한 단백질 분포와 형대를 가 쳤다는 것이 홍마로운 사실이다. 장내에서 특별히 지방이동에 중요한 단백질은 lip o pr ote i n ( Ap o -B) 이 다. 이 에 부과해 서 Ap o A-I 은 모든 종족의 동물의 순환하는 액 중에 서 hig h densit y lip o pr o te i n 의 주요 단백 질이 며 이 는 chy l- om i cron 의 구성성분으로서 중요하다. 양적으로 보면 사람의 경우 chy lo mi cr on 단백 질의 20%, 쥐의 경 우 40% 가 Ap o A-I 으로 구성 되어 있다. 사람에게서 새로 나타나는 ap o p ro t e i n 은 A p oA-N 로 서 쥐에게서도 유사한 물질이 나타나고 있지만 이의 기능에 대해서 는 좀더 연구되어야 한다. 분자량이 적 은 ap o pr ote i n 으로서 ap o lip o p ro te i n - C 가 lym p h ch ylom i cron 에서 발견된다. A p o-C 도 단독물질이 아닌 군(g rou p) 으로서 나타나며 이 들은 Ap o C-I , Ap o C-II , Ap o C-][ , Ap o C-N 등등으로 다음 표 3 에 나타난 바와 같다• 110) 이 중에 서 Ap o C-II 는 lipo pr ote i n lip a se 의 활성 제 (acti va to r ) 로서 작용하므로 chy lo mi cr on 이 분비 된 이 후에 분해 되 는 데 에 극히 중요 하다. 림 프 chy lo mi cr on 내 의 ap o lip o pr ote i n 은 상호관련 이 되 어 게있 으되나 었 어다.느 왜것 냐이하 면장 내a에po 서 lip o합 pr 성ot되e i n는 의 것장인내지 합에성 대 은한 c홍hy미 ! o가mi c많r o아n 지이
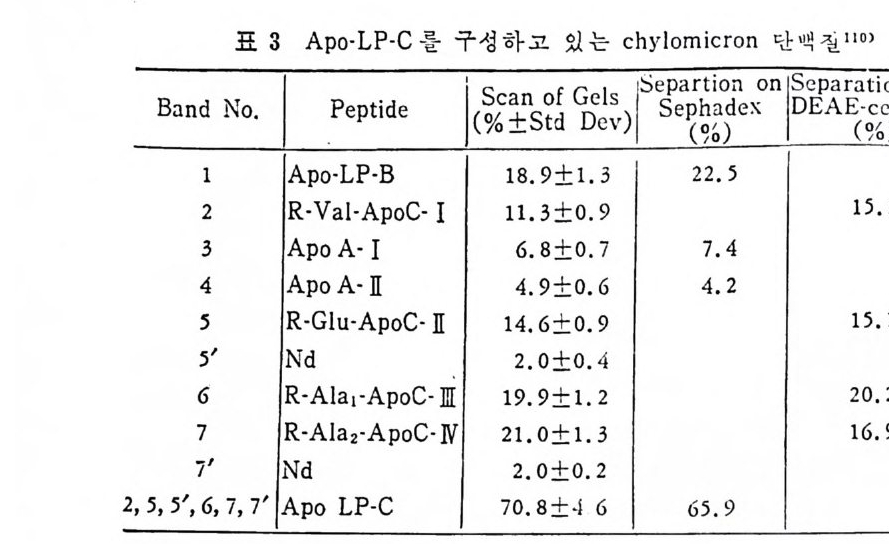 표 3 A p o·LP·C 룹 구성하고 있는 chy lo mi cr on 단백실 110)
표 3 A p o·LP·C 룹 구성하고 있는 chy lo mi cr on 단백실 110)
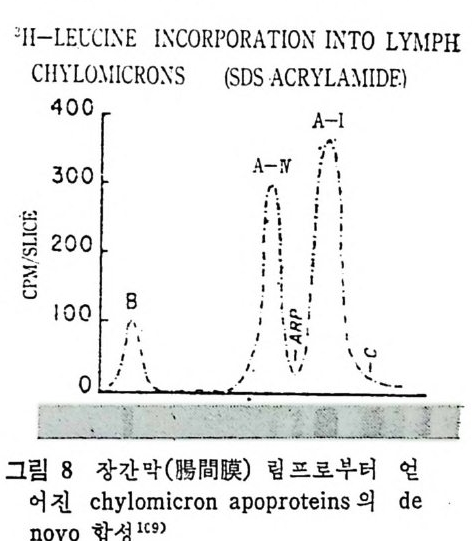
장내에서 합성되는 동안에 이루어지는 것이기 때문이다. 실험적으로 이 문제를 해결하기 위해서 접근해 본 방법이 있다. 즉 쥐에서 지방흡수 동안에 동위원소로 활성화된 (Rad i oac ti ve) 아미노 . 산을 사용하여 림 프에 서 여 러 종류의 chy lo mi cr on 내 에 ap o p ro te i n 으로 영합되는 것을 관찰하였다. 이 결과 그림 8 에 보여주는 바와 같으며 오로지 세 종류의 ap o p ro te i n 인, Ap o B, Ap o A-N 와 Ap o A-I 만이 chy lo mi cro n 이 합성 되 는 동안에 de novo 합성 됨 이 밝혀 졌다. 이 의 chy !o mi cro n ap o lip o p ro te i n 은 chy lo mi cr on 이 장내 막세 포로부터 분비 된 후에 다른 종류의 ap o li po p ro te i n 으로부터 전환되 는 것으로 밝혀졌다. 다음의 그립 9 는 18 시간 동안 굶은 다음에 abeta l ip o p ro te i n e mi a 환자의 장내 막을 생 겁 (b i o p s y)하여 서 보여 주는 현상이 다. 장내막은 커다란 지방구로 가득 차 있으며 이들은 대부분이 중성 지방임이 분석결과로 밝혀졌다. 굶은 상태에서 아턴 현상이 나타났 다는 것은 비정상이며 이는 중성지방 이동 기전에 손상이 왔다고 볼 수 있다. beta l i po p r ote i n s 결핍증이 란 회귀한 선천병으로 이는 중성지방이 많이 함유되어 있는 /3-lipo p ro te i n 합성능력이 없는 현
상이다. Ap ol ip o pr o te i n 은 chy lo mi cro n 구성 성 분중 에 소량 함유되 어 있 지 만 ap ol ip o pr o te i n 은 장내막을 통한 중성지방의 이동에 치명적으로 중요한 물질이다 .111-2) 단백질과 연량불량된 환자의 장내막은 생겁 하여서 나타나는현상도유사하나이 경우는단 백질 합성능력이 저조한 경우에 나타난다 .113) 실험동물이나 사람에게서 보여주듯이 굶은 상대 에 서 의 장내 막은 chy lo mi cro n apo l ip o p- rote i n 의 소량의 집 합량 (p ool) 을 함유하고 있 다고 한다. 114- 5) 이 집 합량은 chy lo mi cr on 형 성 초기단계에서는 급하게 없어졌다가 새로 운 ap ol ip o pr o te i n 합성 이 이 루어 지 면 계 속해 서 chy lo mi cro n 형 성 이 진행 된다. 116) 실험 적 으로 관찰해 보면 일단 이 집 합량이 없 어 지 면 단백 질의 합성 이 손상을 받으며 그러 면 장내 막세
 CHYLO M ICRON
CHYLO M ICRON
포내 에 중성 지 방이 축적 된 다 .117) 단백질 • 열량결핍 때에도 이와 비슷한 현상 이 나타나지만 아직까지 증 명되지는 않았다. Beta l ip op r o te i n s 결 핍 증 의 경 우에 만 apo l ip o pr o te i n 합성이 손상을 받아서 장 내 중성지방 흡수에 결핍 울 초래하게 된다. 이러한 환자의 장내막은 중성지방 으로 곽 차 있 으며 im mu-noreacti ve Ap o B 의 완전
 Jl l-LE CCI;;E !~CORPORATION INTO LYMPH
Jl l-LE CCI;;E !~CORPORATION INTO LYMPH
한 결핍이 나타난다. 그런데 다른 종류의 a p o lip o p ro t e i n 은 정상으.
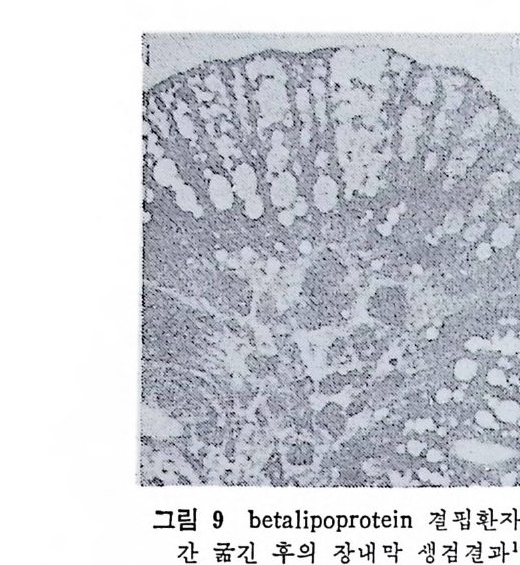 그립 9 beta l ip o pr o te i n 결 핍 환자분 18 시
그립 9 beta l ip o pr o te i n 결 핍 환자분 18 시
로 나타난다. 이러한 회귀 한 병울 통해서 관찰해 보 던 Ap o B 의 합성온 chy lo mi cr on 형성의 필수적인절 차 이며 만일 A p oB 의 합성 이 이 루어지지 않는다면 따 라서 chy lo mi cr on 형 성 도 전적으로 이루어지 지 않는 다. 그런데 Ap o A-I , Ap - oAW 의 합성불능이 원인 이 되는 사 람의 질병이 아 직까지 알려져 있지 않아 서 동물실험을 통해서 관
찰해 보면 이 러 한 ap o lip o p r ote i n 은 chy lo mi cr on 형 성 을 진행 시 키 기 위해서 철대적으로 필요한 것은 아닌 것으로 나타났다 .109)
* 참고문현 1) Frie d man, H. I. & Barbara, Ny b urd, Am. J. C/in . Nutr . , 33: 1108, 1980. 2) Cartie r , M. & J. Bazard, J. Cell. Bi ol . , 65 : 383, 1975. 3) Hof fm an, A. F. , D. S. Small, Ann. Rev. Med. , 18 : 333, 1967. 4) Small, D. S. , J. Am. Oi l Chem. Soc. , 45 : 108, 1968. ·5) Borgs tr o m, B. , Fat dig es ti on & absorp tion in Bi o membranes, 4B New York, Plenum Press, 1974 . pp. 555~620. <5) Sim monds, W. J. , T. J. Redg ra ve, R. L. S. W illi s , J. Clin . Inv· est. , 47:1015, 1968. 7) D. W. Marti n, P. A. May e s, V. W. Rodwell, Harpe r s Revie u , of Bi oc hemi st r y , 18t h edit ion , p. 529, Lang e. 1l) Small D. M. , The ph y si c a l chemi st r y of cholanic ac id: In the Bi le acid s, edit ed by P. Nair k & D. Krit ch evsky , New York, Pleum Press, 1971, vol. I , pp. 249~356, 1971 .
9) Hoff m an, A. F. , Bi oc hem. J. , 89 : 57, 1963. 10) Maki T. & N. Suzuki, J. Exp tl. Med. , 84:259, 1964 . 11 ) Borgs t r o m, B. , Acta Med. Scand. , 196 : I , 1974 . 12) Ekwall, 0. , A. Ste i n & A. Norman, Acta . Chem. Scand. , 10: 681 , 1956. 13) Carey, M. C. , D. M. Sma ll, Am. J. Med. , 45 : 590, 1970. 14) W ils on, F. A. , J. M. Die t s h y , Gastr o ente r o/og y, 61 : 911, 1971 . 15) Holt , P. R. , Di se a s e J. Jun e:3 1971. 16) Sip e rste i n , M. D. , I. L. Cha ik o ff , W. 0. Rein h art, J. Bi ol . Ch· em. , 198: 11 1, 1952. 17) Horace , W. Davenp or t, A dig es t of dig es ti on , ye ar book, Me· dic a l Publish ers, 197 8. 18) Be n zonana, G. , P. De snu elle, Bi oc him . Bi op h y s , A.: ta. , 105 : 121, 1965. 19) Entr e saug el es, B. , P. De sn uelle, Bi oc hi m . Bi op hy s. Acta . , 159 : 285, 1968. 20) Be nz onana, G. , P. De sn ue ll e, Bi oc hi m . Bi op h y s . Acta . , 164:47, 1968. 21) Brockman, H. L. , U. Do, J. Law & F. Kezdy , Fed. Proc. , 32 : 561, 1973. 22) Borgs t r o m. B. , Scand. J. Cli n. Lab. Invest. , 9:226, 1957, 23) Desnuelle, P. , Avdan. Enzym ol. , 23 : 129, 1961 . 24) Wi lls , E. D. , Bi oc hem. J. , 57: 109, 1954 . 25) Borgs t r o m, B. , C. E. rlanson, Europ ea n J. Bio c hem. , 37:60, 1973. 26) Vandermeers, A. , M. C. Vandermeerspi pe t, J. Ratu e & I. Chr· ist o p h e, Bi oc hem. Bi op h y s . Res. Commum. , 69:790, 1976. 27) Borgs t r o m B. , J. Lip id. Re s. , 16: 41 1, 1975. 28) Momsen, W. E. , H. L. Brockman, Bi oc him . Bi op hy s. Acta . , 486 : 103, 197 7. 29) Nano, J. L. , P. Savary, Bi oc lz im i c. , 58:917, 1976. 30) Borgs t r o m, B. , Bi oc h im. Bi op h s . Acta . , 488 : 381, 1977. 31) Canio n i, P. , R. Jul ie n , J. Poath e lot, L. Suvda, Bi oc hemi c. , 58: 751, 1976.
32) Charles, M. Sari, B. Entr e saug e! es, P. De sn uelle, Bi oc hem. Bi op h y s . Res. Commum. , 65:i4 0, 1975. 33) Donner, J. , C. H. Sp ink , B. Borgs t r o m, I. Sy o holms, Bi o che-mi st r y , 15 : 5413, 1976. 34) Verge r, R. , R. Rie t s c h, P. Desnuelle, J. Bi ol . Chem. , 252 : 4319, 1977 35) Shir a to ri, T. , D. S. Goo'.i m an, Bi oc hi m . Bi op hy s. Acta . , 106 : 625, 1965. 36) Treadwell, C. R. , G. V. Vahouny , Choleste r o' Absorp tion » In : Handbook of Phys i o l og y, edit ed by C. Code & \\'. Heid a !, Washi· gton D. C. , An Phy si o lo g ica l socie t y 1968. vol. 3, Sec6, pp. 140 7~38. 37) Kelley, L. , H. A. Newman, Bi oc hi m . Bi op ! tys. Acta , 231 : 558, 1971. 38) Vahouny , G. V. , S. Weersin g , C. R. Treadwell, Bi oc hem. Bi o- phy s. Res. Commum. , 15:224, 1964 . 39) Hy u n, J. H. Kot h ari, E. Henn, J. Morte n son, C. R. Trea d well & G. V. Vahouny , ]. Bi ol . Chem. , 244: 1937, 1969. 40) Vahouny , G. V. , S. Weersin g , C. R. , Treadwell, Bi oc hi m . Bi op - hy s. Acta . 98 : 607, 1965. 41) Matt so n, F. H. & R. A. Voldenhein , J. Lip id Res. 7: 536, 1966. 42) Swell, L., C.R. Treadwell, J. Bi o l. Chem., 212:14 1, 1955. 43) Swell, L. , J. E. By ro n, C. R. Treadwell, ]. Bi o l. Chem. , 186: 543, 1950. 44) Korsvovsky , M. , C. P. Walte r s, 0. A. Harvey , E. R. Dille r, Pr- oc. Soc. Exp tl. Bi ol . Med. , 105:303, 1960. 45) Erlanson, C. , Scand. , ]. Gastr o ente r ol. , 10:401, 1975. 46) Hug he s, R. H. , E. J. W im mer, ]. Bi ol . Chem. , 108 : 141, 1935. 47) DeHaas, G. H. , A. J. Slatb oom, P. D. M. Bonsen, L. L. M. Va-ndeenen, S. Muroux, A. Puig s erver, P. Desnuelle, Bi oc hi m . Bi - oph y s. Acta . , 221 : 31, 1970. 48) Borgs t r o m, B. , J. Donner, Bi oc hi m . Bi op hy s. Acta . , 352, 1976. 49) Wrig h t, E. , Natu r e, 212 : 189, 1966. 50) Diam ond, J. M. , ]. Zp hy s i o l . , 183 : 83, 1966.
·51) Joh nsto n , J. M. , B(I r gs t r o m, B. , Bio c hi m . Bi op h ys . Acta . , 84: 412, 1964. 52) Hoff m an, A. F. , Di ss erta t i on , Lund, 1964. 53) Gordon, S. G. , Kem, F. , Bi oc hi m . Bi op h y s. Acta , 152 : 372, 1968. 54) We b b, .T. P. W. , Hami lton , J. D. , Dawson, A. M. , Bi oc hi m . Bio p hy s. Acta , 187: 42 , 1969. 55) Hof fm an, N. E. , Sim monds, W. J. . Morga n , R. G. H. , Bi oc him Bi op hy s. Acta , 231 : 487, 1971, 56) West e r ga ard, H. , Diet s c hy . J. M. , ]. C/in , Invest, 58: 97, 1976. 57) Wi ls o n , F. A. , V. L. Salee, J. M. Die t s c hy , Sc ien ce, 174 : 1031, 1971 . 58) Wi ls o n , F. A. , J. M. Die t s c h y , Bi op h y s , Bio c hem. Acta , 363 : 112, 1974. 59) Gaug l, A. , Ockner, R. K. , Gastr o ente r o/og y, 68: 167, 1975. 60) Ockner, R. K. , Pit tm an, J. P. , Yag e r, J. L. , Gastr o ente r olog y, 62:981, 1972a. 61) Ockner, R. K. , Mannin g , J. M. , Pop pe nhausen, R. B. , Ho, W. K. L. , Sc ien ce, 177: 56, 1972b. 62) Mi sh esin , S. , Ste i n , L. , Gatm ait an , I. , Aria s , I. M. , Bi och em Bi op lzy s. Res. Comm11n. , 47 : 997, 1972. 63) Borgs t r o m, B, , B. G. Lundh, A. F. Hof fm an, Gastr o ente r olog y, 45 : 229, 1963. 64) Bezard, C. H. , Abst. Gastr o ente r ol. 70 : 460, 1976, 65) Rubin , A. , J. Daren, Gastr o ente r olog y, 66:378, 1974, 66) Watt , S. , W. J. Sim mons, Cli n. Exp t!. Pharmacol. Phy si o l , , 3 :305, 1976. 67) Hernandez, H. H. , Chaik o ff , I. L. , Kiy a su, J. Y. , Am. ]. Ph· ysi o l . , 181 : 523, 1955. 68)Murth y , S. K. , Mahadevan, S. , Gang ul y, J. , Arch. Bi oc hem. Bi op hy s, 95:176, 1961 . 69) Holt, P. , Arch. Ente r nal Med. , 130 : 574, 1972. 70) Joh nsto n , J. M. , Gastr o in t e s ti na l tiss ue, Lip id Me t abol i sm 靈i n Ma-mmals I, edit ed by Fred Sny d er, p. 151, Plenum Press: New Yo-
rk & London, 1977. 71) Kornberg, A. Pric e r. W. E. , ]. Bi ol . Chem. , 204 : 329, 1953. 72) Brin d ley , D. N. , Hil bs cher, G. , Bi oc h im. Bi op ! zys. Acta , 106: 495, 1965. 73} McManus, J. P. A. , Isselbacher, K. J. , Gastr o ente r o/og y, 59 : 214, 1970. 74) Bar-Tuna, J. , Shap irs , B. , Bi oc lzem. ]. , 1964 . 75) Rao, G. A. , Joh nsto n , J. M. , Bi oc lzem. Bi op lzy s. Re s. Comm1111. , 24:694, I966a. 76) Rao, G. A. , Joh nsto n , J. M. , Bi oc lzi m . Bi op lz y s. Acta , 144:25, 1967. 77) Weis s , S. B. , Kennedy , E. P. , J. Am. Chem. Soc. , 78:3550, 19.5 6 . 78) Joh nsto n , J. M. , ]. Bi ol . Chem. , 234: 1065, 1959. 79) Brin d ley , D. N. , Hi lbs cher, G. , Bi oc lzi m . Bi op h y s. Acta , 125:92, 1966. so) Bic k ersta f f e, B. , Annis o n, E. F. , Bi oc lzem. J. , 111 :419, 1969. 81) Mi tch ell, M. P. , Brin d ley , D. N. , Hi lbs cher, G. , Eur. J. Bi oc - hem. 18:214, 1971. 82) Brin d ley , D. N. , Bi om e m branes, 4B. :621, 1974. 83) Joh nsto n , J. M. , Rao, G. A. , Lome, P. A. , Schwarz, B. E. , Lip ids, 2:14, 1967a, 84 ) Smi th, M. E. , Sedg w ic k , B. , Brin d ley , D. N. , Hil bs cher, G. Eur. ]. Bi o chem. , 3:70, 1967. 85) Joh nsto n , J. M. , Polta u f, F. Schil le r, C. M. , Schultz , L. D. , Bi oc him . Bi op h y s. Acta , 218 : 124, 1970. 86) Ste i n , Y. , Ti et z , A. , Shap iro , B. , Bi oc hi m . Bi op h y s. Acta , 26 : 286, 19.5 7 . 87) Hajr a , A. K. , Ag ra noff , B. W. , J. Bi ol . Chem. , 243 : 3.54 2, 1968b. 88) Rao, G. A. , Sorrels, M. F. , Reis e r, R. , Lip ids , 5:762, 1970. 89) Frank, 0. Z. , Bi ol . , 36 : 568, 1898. 90) Arto m , C. , Realse, L. , Arch. Sci. Bi ol . Bolog n a. , 21:368, 1935 .. 91) Frazer, A. C. , Sammons, H. G. , Bt' oc hem. J. , 39 : 122, 1945.
92) Reis e r , R., Wi ll ia m s, M.C., ]. Bi o l. Chem., 202:s1s, 195 3 . 93) Skip s ki, V. P. , Morehouse, M. G. , Dene!, H. J. Jr. , Arch, Bi o- clzem. Bi op h y s . , 81 :93, 1959. 94) Clark, B. , Hil bs cher, G. , Bi oc hi m . Bi op lz y s. Acta , 46:479, 1961 95) Brown, J. L. , Joh nsto n , J. M. , Bi oc lz im . Bi op l zy s. Acta , 84: 264, 1964 a. 96) Ai lha n d, G. , Sammuel, D. , Lazdunski, M. , Desnuelle, P. , Bi- ochim . Bi op / zys. Acta , 84:643, 1964 . 97) Joh ns to n , J. M. , Rao. G. A. , Bi oc lzi m . Bi op h ys . Acta , 106: 1, 1965. 98) Joh nsto n , J. M. , Trig ly c erid e Bio s y n th esis in th e Inte s ti na l M- uco sa, pp. 38~-1 2, In K-Rommel(ed) Bi oc lzemi c al & clin ic a l Asp- eel s of lipid Absorp tion , Ti tise , F. K. Schata u er Verlag , St u g a rt, New York, 1976. 99) Hil bs c h er, G. , Glyc e rid e Meta b olis m , pp. 280~370, In S. J. Wakil (Ed) Lipid Meta b olis m , Academi c Press Inc. New York, 1970. 100) Ge lb , A. M. , David s on, M. I. , Kessler, J. I. , Am. J. Phy si o l . ,. 207: 12 07, 1964. 101 ) Essel b acher, K. J. , Fed. Proc. , 24: 16, 1965. 102) Rodg er s, J. B. , Ril e y , E. M. , Drumney, G. D. , Isselbacher, K. J. , Gastr o ent~ r olog y, 53 : 547, 1967. 103) Brin d ley, D. N. , Ferrie r , P. , Facto r aff ec ti ng acy l- CoA sy n th - eta s e & gly c erolip id syn th esis in Small Inte s ti ne •, pp. 219~29, In W. L. Burland & P. D. Samuel. (Eds), Transpo r t Acrosis & In- tes ti ne , Churchil ls, London. 104) Kem, F. , Borgs tr o m, B. , Bi oc him . Bi op h ys . Acta , 98:520, 1965. 105) Rao, G. A. , Joh nsto n , J. M. , Bi oc him . Bi op / zys. Acta , 125:465, 1966b. 106) Schult z, F. M. , Joh nsto n , J. M. , J. Lip id Res. , 12 : 132, 1971. 107 ) Polheim , D. , David , J. S. K. , Schult z, F. M. , W ylie, M. B. , Jo: hnsto n , J. M. , J. Lip id Res. , 14:415, 1973. 108) Palta u f, F. , Joh nsto n , J. M. , Bi o chim . Bi op h ys . Acta , 239: 47 , 1971 . 109) Glic k man, R. M. , Inte s ti na l fat absorpt ion s•, Nutr i t ion & Gast- -
roente r o/og y( Ed), M. W ini c k , p. 29, Jo hn Wi ley & Sons, New Yo rk, 1980. 110) G. Kostn er, A. Holosek, Bi o chemi st r y , 11 : 1217, 1972. ·111 ) Levy , R. I. , D. S. Frederic k son, & L. Laste r, J. Cl in. Invest. , 45:331, 1966. 112) Gli ck man, R. M. , Chy lo mi cr on for ma ti on by the Inste s ti ne , in K. Rommel & H. Goebe ll Eds. , Lip id absorp tion Bi oc he m i c al & Cli nic a l Aspe c ts , 1975. ·11 3) Theron, J. J. , W. Wi ttm ann, J. G. Prin s lon, Exp . Mo/. Patl z . 14: 18 4, 1971. ·11 4) Gli ck man, R. M. , J. Khorana, A. Kil go re, Sc ien c e, 193 : 1254 , 1976. 115) Glic k man, R. M. , P. H. R. Green, R. S. Le es , S. E. Lux, A. Ki· !go re, Gastr o ente r o/og y, 76 : 288, 197 9. 116) R. M. Gli ck man, K. Kir s ch, ]. C/in , Invest. , 2910, 1973. 117) R. M. Gli ck man, A. Ki lg o re, J. Khorana, ]. Lipid Res. , 19 : 260 , 1978.
제 2 장 지방조직에서의 중성지방대사 1 지방조직의 지방세포 약 4 5 년 전까지만 하여도 지방조직 (adip o se ti ssue) 은 대사적으로 볼 때 불활성의 조직으로 단순히 지방이 축적되는 곳이며 신체의 체온조철에 철연체의 역할을 하거나 몸의 일정 부위에 축적되어 쿠 숀의 역할울 한다고 생각했다. 그러나 요츠음에는 접차로 지방조직을 신체 에너지 대사조절에 철대적으로 필요한 조직으로 안정하고 있다. 지 방조직 은 느슨한 결 체 조직 (loo se connecti ve ti ssue) 으로서 지 방 중 중성지방이 처장되는 특별한 조직이다. 모든 동물은 계속해서 에너 지를 섭취하고 따라서 참정적으로 에너지의 저장이 신체에 꼭 팔요 하게 된다. 이 경우에 탄수화물이나 단백질보다도 지방이 저장되기 에 가장 적합한 물질이다. 왜냐하면 지방은 당이나 단백질보다 덜 무거우며 단위무개당 함유한 에너지량이 많기 때문이다. 그러므로 지방조직은 신체의 에너지 저장고로서 가장 포용력이 있는 조직이 다. 평군 성인 몸무게의 약 IO% 정도가 지방으로 이루어져 있으며 이 양은 40 일분의 에너지 저장량이 된다. 그러나 비만한 사람은 이 지방처장량이 1 년분의 에너지가 될 만큼까지도 정상적인 대사를 통 하여 저장할 수 있다. 지방은 석품의 과잉섭취 기간 동안에 저장되며 굶는 동안에는 지
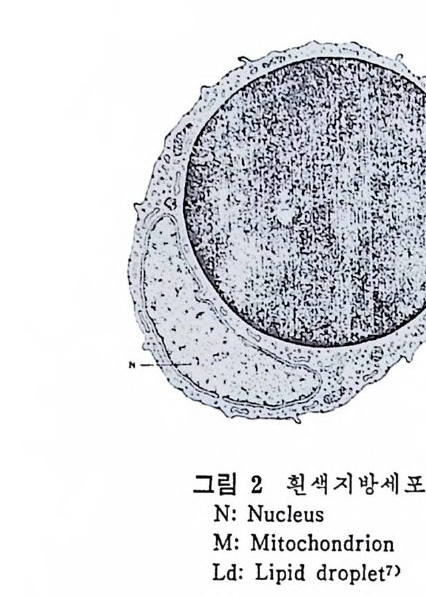
방산으로 유출되 어 나오는 작용을 동해 서 지 방조 직 이 신체 의 안청 된 에너지 공급을 위한 매우 중요한 역할을 한다. 그러므로 지방조직이 불활성의 조직이라는 생각에서 벗어나야만 지방조직의 세포는 당으로부터 지방울 합성하고 또한 신경 자극이 나 호르몬의 작용에 민감하게 반응하논 조직임을 인식하게 될 것이 다. 대부분의 포유동물에는 두 종류의 지방조직이 있는데 이 를 구성 하고 있는 지방세포의 크기, 수, 분포, 그리고 대사량이 모두 다르 다. 이중에 양적으로 많은 지방세포가 흰색지방세포 (wh it e adip o se cell) 로서 이 는 지 방조직 을 구성 하며 이 들은 피 하지 방 중 mesente rie s , omentu m , retr o p e rit on eal 부위 에 있 으며 대 개 느슨한 결 체 조직 에 서 지방세포가 분리된다. 또 다른 종류는 갈색 의 지 방세 포 (brown adip o se cell) 로서 이 는 양 적으로 흰색지방세포만큼은 많지 않지만 사람이나 원숭이와 같은 유인원에게는 비교적 제한된 소량의 갈색지방세포가 존재하고 동 면하는 동물의 체내에는 상당히 풍부한 양이 존재한다. (1) 흰색지방세포 1) 구조 지방조직은 지방세포로 구성되어 있으며 · 이것의 색깔은 흰색 내 지 질은 노란색으로 되어 있다. 지방조칙의 지방세포의 수는 인체내 지방조직을 치방세포 수로 나누어서 나온 숫자로 대개 21~43X 10 정도이다.1) 치방세포는 일 반적으로 청년기나 초기 성인기에 최고의 수에 도달하여 그 이후에 는 그대로 고정된 수로 신체내에 남아 있게 된다 .2) 그러나 한편 성안이 과잉의 칼로리섭취를 하는 초기에는 지방세 포분열의 촉진에 의한 수가 증가되며 이런 상태가 수년 동안 계속 하면 이에 부과해서 세포크기도 증가될 수 있다는 사실을 많은 사 람들이 수긍하고 있 다• 3) 어란이들을· 유아기에 과석시키면 지방세포의 수가 증가되며 이는 후에 비만중이 될 수 있는가능성을 부여해 준다. 왜냐하면 지방으
로 채워질 지방세포가 이미 형성되어 있기 때문이다 .4) 성인이 된 후에 조금 과석을 하면 이미 존재하고 있는 지방세포의 크기가 커지며 세포수에 는 두드러진 증가가 없다고 보는 견 해가 있다 .4 - 5) 지방세포의 크기는 다양하나 직겅 이 120 f.l 나 되는 크기의 것까지 촌재 한다. 지방세포는 전형적인 구상이며 다면 형대 이다. 왜냐하면 치방세포 개 개 가 뚜렷 한 형 태 를 지 니 지 못한 채 서 로 인접해 있으므로 인접된 부분이 면 으로 나타나기 때문이다(그립 1 참조 ). 지방세포의 내부는 한 방울의 지방이 세 포 대부분의 부피를 다 채운다. 그러드로 이러한 지방세포틀 갈색지
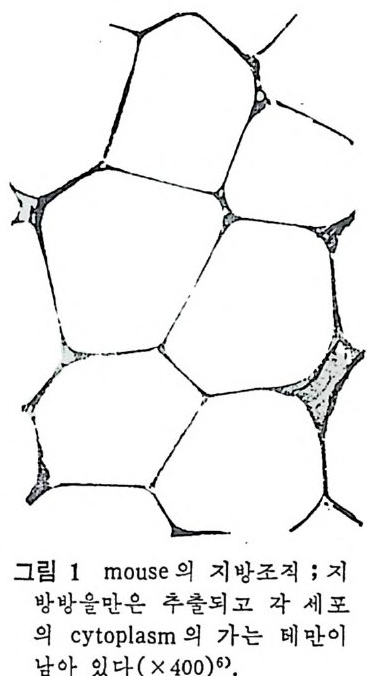
방세포와 구멀하기 위해서 un i locular 라고 하며, 갈색지방세포는 여 러 개의 지방구가 한 세포부피내에 분포되어 있어서 이를 multil oc - ular 라고 한다• 지방세포 내부에는 한 덩어리의 큰 지방구가 자리를 거의 다 메 우고 있는 형편이타서 핵은 한쪽 구석으로 밀려서 촌재하며 원형질 은 가늘게 세포 가장자리에 둘러 있으며 원형질 양은 세포 전체의 1/40 정도밖에 되지 않는다(그림 2 참 조). 치방세포의 핵은 지방구와 원형질 사이에 끼여서 찌그러져 있다. 지방세포문 조칙학적으로 분석해 보면 지방은모두녹아버려서 세포 자체는 마치도 가운데가 빈 반지모양만이 남아 있기 일쑤이다.제포 내부에 있는 모든 or g anelles 들은 세포의각막(p lasma membrane) 과 지 방구 사이에 끼여 있는 원형질내에 분산되어 있다. m it ochondr i a 는 구형 으로 내 부에 응집 된 물질을 가지고 있 으며 , 작은 go lgi comp le x 와 몇 개 의 짧은 roug h endop la smi c reti cu lum 과 유리 되 어 있 는 몇 개 의 rib o somes 들이 있 다. 세 포의 각막은 때 때 로 pino cy tot i c
 그립 2 흰색지방세포
그립 2 흰색지방세포
inv ag ina ti on 이 있 다. 지방세포내의 지방구가 따로 지방막 (membrane) 으로 싸여 있 느 냐 하는 데는 많은 의십 을 하고 있 다. Fawcett ( I 966) 8) 은 지 방세 포내 원형질 안에 지방이 축적될 때에는 원형질내에 축적이 되는 것이지 원형질내에 촌재하는 세 포내 orga nelle 내 에 축적 되 는 것 은 아니타고 하였으며 원형질내에 축적된 지방은 따로이 막과 연결 되 어 있 지 않은 것 같다고 하였 다. 지방세포내의 지방구와 원형 질 사이를 구텔짓는 농축된 내면
이 있기는 하지만 이 면이 어떠한 지단백 (lip o p ro t e i n) 막의 독성도 지 니고 있지 못하였다고 한다. 그리고 이것을 세포막이라고 부르기에 는 무리가 있다고 생각하였다. 전자현미경으로 지방세포를 관찰해 보아도 지방세포내의 지방구 를 둘러싼 막은 보이지가 않지만 항상 지방세포내에 함유된 lipa se 를 유리해 보면 지방과 함께 이 효소가 유리된다. 이는 지방세포내 의 지방구와 세포내에 촌재하는 lip ase 와는 구조상으로 밀접히 관 련이 있다고 보는 것이다. 그래서 Gal t on(I97I)” 은 lip ase 가 그대 로 지방구와 원형질 사이의 공유 영역에 존재할 것이라고 암시했으 며 이것이 사실이라면 이 효소가 부착되어 있어서 안정하게 존재하 기 위한 membrane 이 있을 것이라고 주장하였다. 그러나 아직까지 분명하게 이 지방구를 둘러싼 막은 관찰되지 못했다. 2) 지방조직의 체내분포 일찌기 Fremm i n g(1870)” 은 지방조직이란 보통의 결체조직으로 지방이 이 조직의 fi broblas t내에 처장된다는 견해를 피력한 바 있 다. 이 견해대로 된다면 신체내 모든 부위나 어떤 부위에서든지 결
체조직은 에너지의 과량 섭취시에는 모두 지방의 저장소이어야 한 다는 것이다. 그러나 결체조직은 신체내 여러 곳에 보편적으로 존 재하고 있지만, 비만한 사람들의 체내 지방 축적현상은 신체 골고 루 모두 축적되는 것이 아니라 어떤 독정한 부위에 먼저 축적이 일 어나고 다른 부위에는 혼적 정도의 지방이 촌재하는 현상을 나타내 고 있다. 예를 들어서 손등이나 발둥, 눈꺼풀, 코, 귀, scro t um 과 g en it al i a 에는 어지간한 상태가 아니고는 지방의 축적이 일어나지 못한다. 이 사실은 지방세포가 신체내 결체조직이 있는 어더에서나 나타난다는 사실을 증명해 주지 못하고 있다. 한편 Told t (1s70~1888)” 는 지 방조직 이 독정 한 지 방형 성 세 포인 Iip o blast 로부터 형 성 되 는 것 으로 이 lip o blast 는 생 이 시 작되 는 배 아 (embryo ) 당시에 초기저인 지방형성 장기내에서 따로이 형성된다고 하였다. 성인의 신체내에 지방이 분포되는 특징으로 미루어 보면 이 특정한 지방형성 세포가 어떤 신체부위에는 풍부히 분포되어 있다고 분 수 있 다. 요즈음에 와서 는 많은 연 구자들이 Toldt 의 lip o blast 와 mesenchy m al eel[ 울 특밀히 구일지 우려 고 하지 않는다. Hammor's(1895)” 는 위의 두 견해를 합찬 제 3 의 견해를 가지고 있었다. 그는 지방조직의 체내 형성 및 분포가 두가지 과정에 의해 서 이루어진다고 하였다. 첫째는 배아 당시에 1 차적인 지방형성 이 이루어진다. 이 과정 중에서 특정한 세포가 선처럼 정렬되어진 ep ithe li oid cell 내에 정렬되어지며 그 안에서 이 세포가 여러 개의 작은 지방구를 만든다. 후에 이 여러 개의 지방구가 합쳐져서 하나 의 큰 지방구를 이룬다. 이러한 1 차적인 지방형성에 부과해서 출생 이후 또는 대아 후반기에서도 특정하지 않은 결체조직 세포내에 지 방이 축적될 수 있다고 한다. 이룰 2 차 지방형성이라고 보고 1 차나 2 차 때 형성된 지방은 그 이후에 가지는 영양상태가 양호한 사람 에게서는 구별이 되지 않는다고 본다. 여하튼 흰색지방조직은 성인의 신체 전역에 존재하지만, 양적으 토 많이 존재하는 곳과 적게 촌재하는 곳의 차이가 있다. 지방조직의 신체내에 존재하는 부위를 지적해 보면 다음과 같다. i) 피부 밑에 촌재하는 지방조직으로서 이를 즉 피하지방 (subcu t a·
neouse fat)이 라고 부른다. ii) 복강내에 촌재하는 지방조칙은 여러 곳에 산재해 있다. G) omentu m : 위장의 아랫 부분 (9 ~esenta r y : 복막주변과 소장을 연결하는 주변, 복강의 뒷 면 @ pre renal tissu e : 신장을 둘러 싸고 있 는 것 iii) 근육내의 지방 iv) 골수내의 지방 v) 혈관주변의 지방 vi) • ep idi d y m al fat pa d 내 의 지 방 pa rametr i a l fat pa d 내 의 지 방 2 지방조직내의 중성지방대사 지방조직은 하나의 특정한 조직으로서 대사에너지의 처장기능을 가지고 있다. 지방세포내의 에너지는 지방산에 글리세를이 에스텔화 된 중성지방의 형태로 처장되어 있다. 처장되어 있는 중성지방이 다른 조직에서 요구하는 에너지원으로 사용되기 위해서는 무엇보다 도 먼저 유리지방산과 글리세를로 가수분해되어야 한다. 이러한 가 수분해 과정은 지방세포내에서 이루어치며 및 종류의 효소에 의해 축전되는 일련의 작용을 거찬댜 이에 관련된 지방분해효소(lip a se ) 는 중성 지 방 lip a se, dia c y lg l y c erol (DG) lipa se 그리 고 monoacy l- gly c erol (MG) lipa se 이 다. 이 때 유리 된 유리 지 방산은 혈 액 에 의 해 여러 다론 장기로 분산이 된다. 지방산은 및 종류의 장기, 즉 십장과 골격근육의 주요 열원이 되 는데 10- 2 ) 특히 십장근육은 유리 지 방산을 포도당보다 먼처 산화시 킨 다고 밝혀졌으며 유리지방산이 포도당의 이용을 방해할 수도 있다 고 하였다 .13-4) 지방조직내에서 중성지방 l ip ase 에 의해 첫번째 es t er 결합이 분 해되는 시작반웅이 바로 중성지방이 이 지방조직으로부터 유출되는 울을 조철하는 작용이 된다. 일단 중성지방(lip ase) 에 의해서 중성 지 방의 첫 번째 este r 결 합이 분해 되 면 DG lip a se 오1- MG lipa se 의 작
용력 이 대 단히 강하기 때문에 중성지방의 중간대사 산물인 DG 나 MG 의 축적이 방지된다. 중성지방 l ip ase 의 작용력은 및 개의 호르몬의 영향을 받아서 증가 될 수 있는데 여러 중류의 호르몬에 의해서 지방조직내의 중성지방 lip a se 가 활성 화되 는 생 화학적 조철기 전은 굳리 코겐 ph osp h oryl a se 작용 조절기전과 유사하다 .15) 이의 조절기전의 순서는 다음과 같 다 .16) i) hormone recep tor 와의 상호작용 ii) adeny la te cy c lase acti vi t y 의 증가 iii) 세 포내 의 cy c lic AMP 수준의 증가 iv ) 활성 단백 질 kin a se 수준의 증가 v) 활성 화된 중성 지 방 lipa se 양의 증가 vi) 중성지방의 가수분해양 증가 및 지방조직으로부터의 지방산
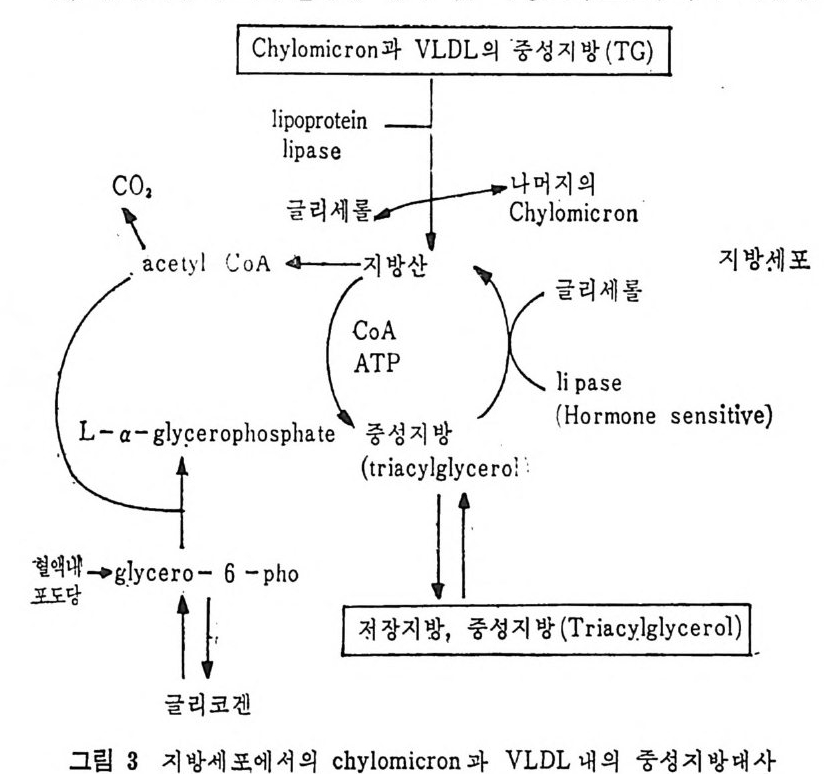 r-Chy lo mi c ron 과 VLDL 의 중 성 지 방 (TG) |
r-Chy lo mi c ron 과 VLDL 의 중 성 지 방 (TG) |
유리 vii ) 유리된 지방산은 알부민 (album i n e) 과 복합체를 이 루 어 혈 액에 의해 운반된다. 지 방조직 은 혈액 으로부터 chy lo mi cr on 과 VLDL 내 의 중성 지 방울 취해 조직내에서 재정비한 뒤 다시 중성지방으로 에스 텔화 하여 조 직내에 저장하기도 한다. 이 과정을 순서별로 보면 다음과 같 다. i) chy lo mi cr on 과 VLDL 의 중성 지 방이 lip o p ro te i n lipa se 에 의 해서 가수분해된다. ii) 중성지방으로 다시 에스텔화된다. iii) 처장지방인 중성지방형태로 조칙내에 처장이 된다. 이상의 관계를 도해해 보면 그림 3 과 같다. (1) Lip o p r ote in lipa se Lip o pr ote i n lipa se (LPL) 는 혈액내에 존재하는 물질로서 순환되 고 있는 l ip o p ro t e i n 내에 함유된 중성지방울 분해시킨다. 그러므로 지방섭취로 인해서 혼탁해진 혈액이 이 효소의 작용으로 다시 맑아 지게 된다. 그러므로 LPL 은 일명 혈액의 clearin g fa c t or 라고 부 른다. 보통 정상조건하의 혈액내에는 현저한 양의 LPL 이 존재하 지 않는다고 보며 hep a rin 을 정 맥 주사하면 LPL 이 혈류 속으로 유 리 된다. 17) hep a rin 을 0. 1 mg /k g B. W. 정 도의 적 은 양 주사하면 LPL 이 상당히 빠른 속도로 혈류내로 유리된다. 실험적으로 중성지방 현탁액 (emuls i on) 이나 chy lo mi cr on 현탁엑에 he p ar i n 이 가해전 혈청을 넣어 주면 뿌영게 혼탁되었던 혈청이 맑아 지논 현상을 볼 수 있다. 이는 중성지방이 LPL 에 의해 가수분해 되 어 나타난 현상으로 이 를
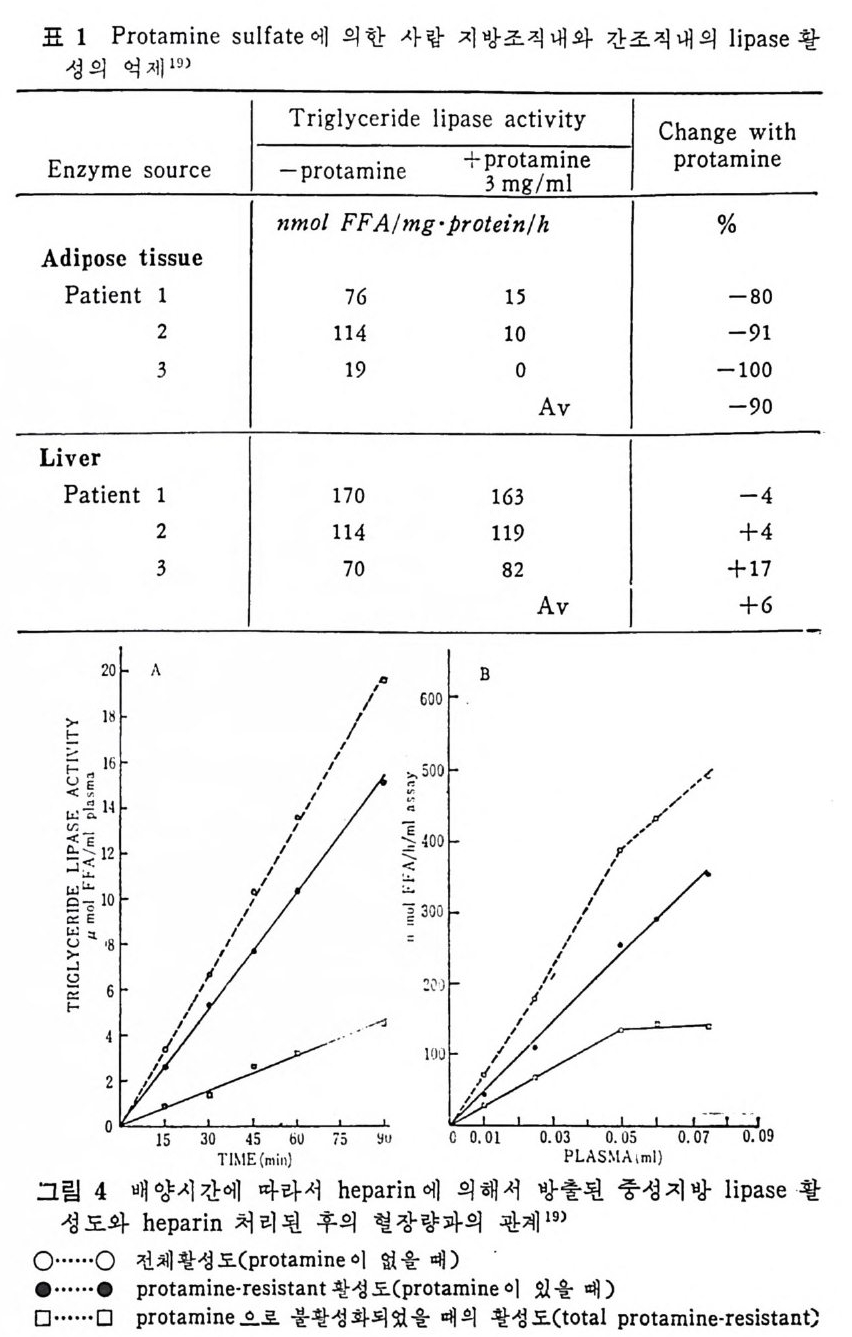 표 1 Prota m i n e sul fa te 에 의 한 사 람 지 방 조칙 내 와 간조직 내 의 lipa se 활
표 1 Prota m i n e sul fa te 에 의 한 사 람 지 방 조칙 내 와 간조직 내 의 lipa se 활
 ALI2A0I L3>3S
ALI2A0I L3>3S
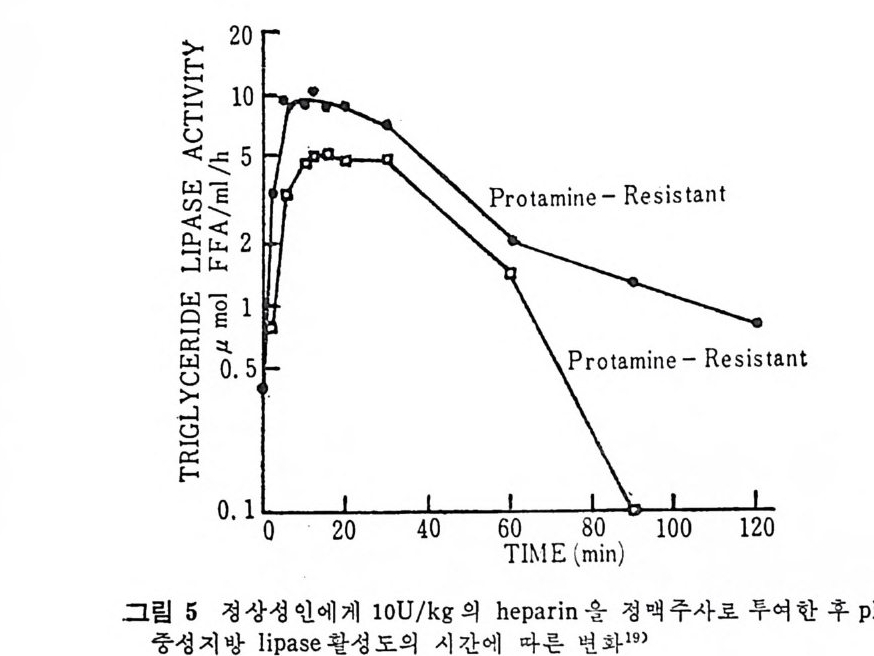
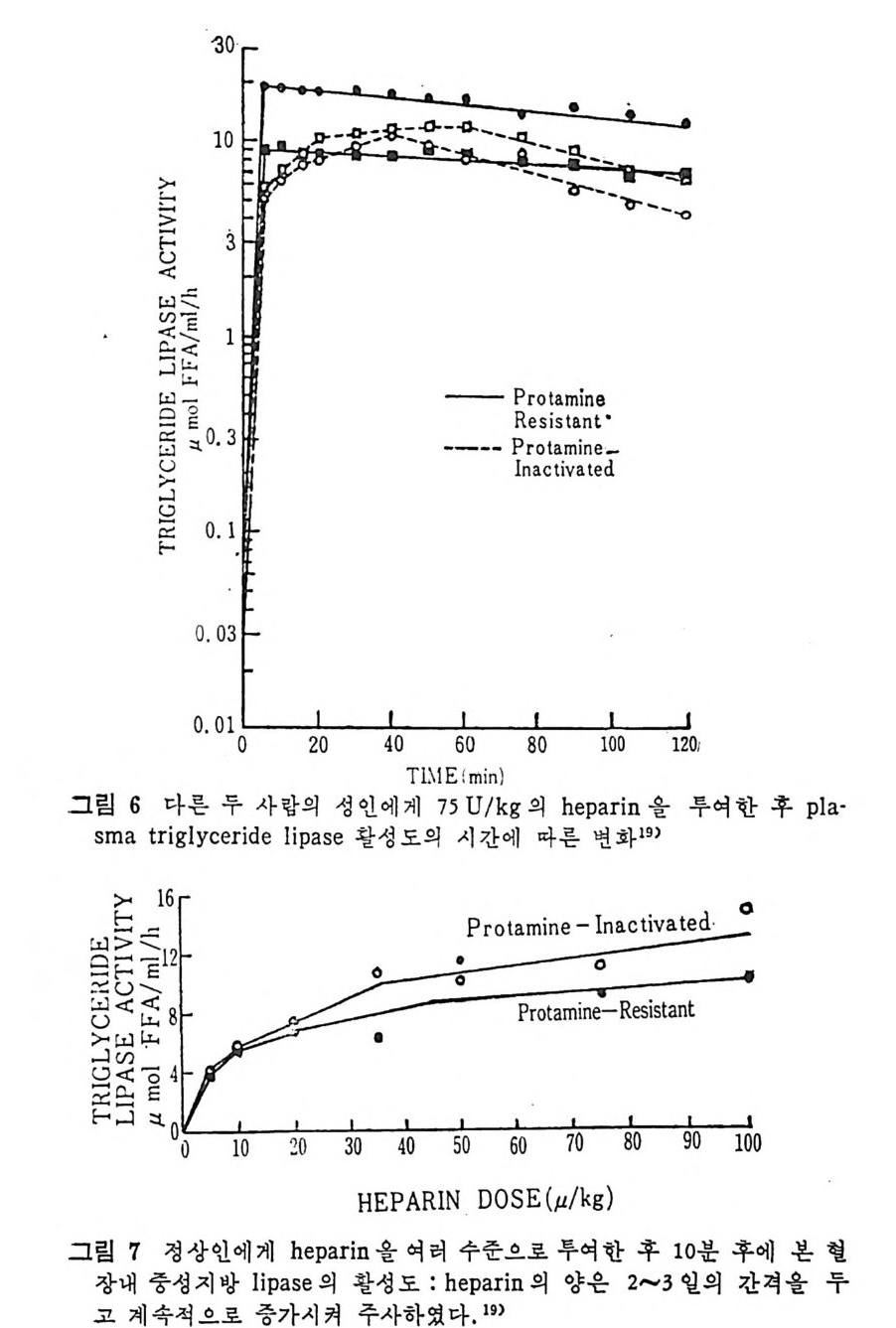
Q) hep a rin 에 의해서 활성이 되는 효소 ® 단백 질 조요소(p ro t e i n co fa c t or) 를 요구하는 효소 @ NaCl 이 나 pr ota m i ne 에 의 해 서 방해 되 는 효소이 다. 반대 로 Hep a ti c LPL 은 Q) he p a ri n 에 의해서 활성이 되지 않는 효소 ® 단백 질 조요소(p ro t e i n co fa c t or) 를 요구하지 않는 효소 @ NaCl 이 나 pr ota m i ne 에 의 해 서 방해 되 지 않는 효소이 다. 다음의 표 1 에서 보여주는 바와 같이 사람의 간과 지방조직내의 LPL 활성 도를 비 교해 보면 확실히 pro ta m i ne 에 의 해 서 간에 있 는 LPL 이 방해되지 않았음이 밝혀졌다 .19) 다음의 그림 4 와 그림 s, 6, 7 도 LPL 의 pro ta m i ne 에 의 한 효과를 비교해 놓은 것이다 .19) Lip o pr ote i n lipa se 활성 도는 hep a rin 처 리 후 지 방분해 활성 도 (po sth e p a rin Jipo !y tic acti vi t y) 의 전체 양을 축정 한 것 으로서 대 표하지 만 사실온 hep a rin 처 리 후의 지 방분해작용은 다양하다. 이 는 mon·
 'AM AI3 0 -~--zr.... __ '7----
'AM AI3 0 -~--zr.... __ '7----
oacy lg l y c erol h y drolase20 - 2) 와 p hos p ho lip ase23) 의 활 성 도 그리 고 십 지 어 는 hep a ti c 중성 지 방 lipa se acti vi t y 까지 포 함된 것 이 다. 그 러 나 hepa ti c 중성지방 l ip ase 는 기질의 목 칭이나 기타 다른 독 징에 의해 달라진다고 보고되고 있다》 - 9) 1) Hep a rin 의 지방대사에 있어서의 가능한 생리기능 He p ar i n 은 동물의 종족에 따라서 동일한 화학구조로 되어 있는 것인지, 아니면 종족에 따라서 화학적 구조가 조금씩 차이가 있는 지에 대해서는 아직 밝혀져 있지 않다. 여하돈 he p ar i n 의 화학적 구조는 그림 8 에 서 보는 바와 같다고 제 안되 어 왔다. 30) Hepa rin 은 uronic aci d 와 hexosami ne 이 교대 로 결 합되 어 있 는 he t ero p ol y sacchar i de 의 일종으로서 동석물계에 널리 분포가 되어 있 다. 31 ) He p ar i n 의 분자는 강한 산성으로서 음이온 (an i on) 의 분자내 밀도 가 아주 높은 물질로 정전기적 (elec tr os t a ti call y)으로 단백질과 작용할
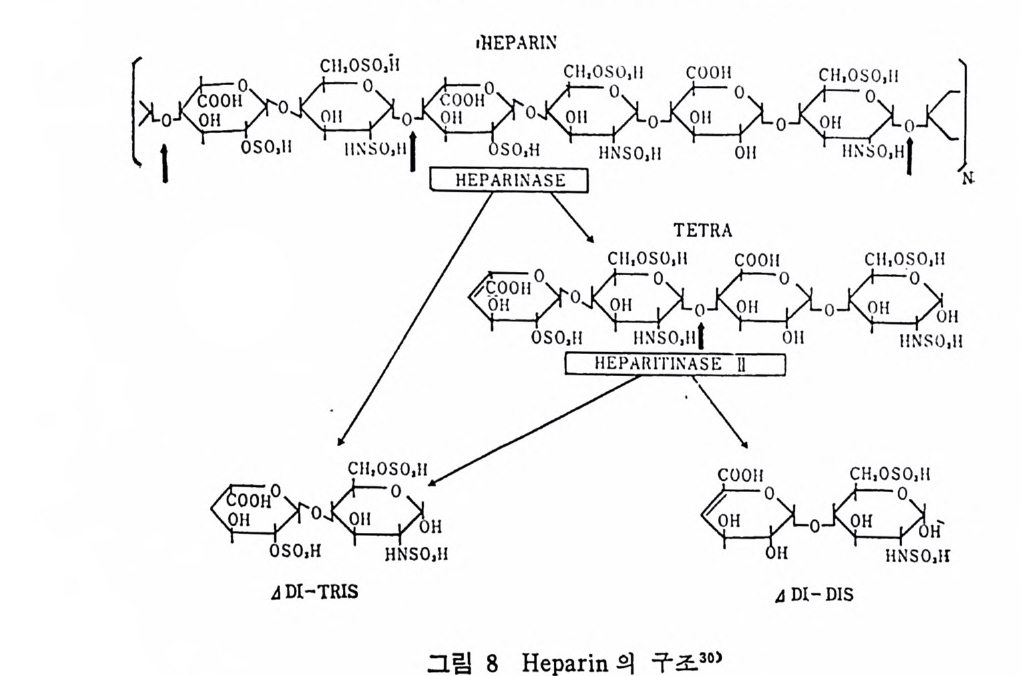 广 [>: 〔 ' 틀’ OII g: 011 。 三,o <`N ,
广 [>: 〔 ' 틀’ OII g: 011 。 三,o <`N ,
수 있다 •32) 이러한 작용은 간단한 영의 형성작용이고 형성된 영은 역으로 분해되어서 서로 분리되기도 한다 .33) He par i n 과 주어전 단백질 사이에서 일어나는 반응은 역학적으로 평형상태를 이루지만 또 다른 단백질, 죽 양이온 (ca ti on) 이 주어지면 쉽게 변화할 수도 있다. 그러므로 hep a rin 자체도 두 단백질 사이 에 서 이 들의 농도와 hep a rin 에 대 한 해 리 상수 (d i sso ci a ti on consta n t) 에 반응하면서 분산되어 있다 .34 ) 이 에 부과해 서 hep ar in 은 chargi ng 조전에 따라서 쉽 게 결 합 (bond ) 을 변화시킬 수 있는 능력이 있지만 이런 면의 he p ar i n 의 생리적인 독 칭 을 보면 hep a rin 에 단백 질 이 결합될 때 결합작용이 상승되 든지 또는 저해를 받든지간에 결합된 결합이 붕괴되고 나면 여기에 결합 되었던 단백질의 활성도나 기능은 원상대로 복구되어진다 .35) 이 사실로 he p ar i n 이 생리적으로 단백질과 상호작용을 할 때 조 철과 항상성 유지에 역할을 할 수 있는 기능아 있다고 볼 수 있다. 과거에는 he p ar i n 이 정상인의 혈액 속에 촌재하지 않는다고 믿 었기 때문에 he p ar i n 의 연구에 많은 지연을 가져오기도 하였다. 그 러나 he p ar i n 이 정상인의 혈액내에 존재하는 증거를 많은 사람이 보여주었다 .36 - 7) 정상인의 혈액내에 존재하는 he p ar i n 의 양은 100 ml 당 10~2 4 단위 (un it)로 발견되 었으며 평 군 100 ml 당 15. 3~17. 7 단위이다 •38) 또는 혈청내 l it er 당 1. 5~1.8m g의 he p a ri n 이 있다. He p ar i n 이 처음 발견된 것은 1916 년이고 35) 이 이후 계속해서 he p ar i n 의 기능은 혈액응고 기능과 관련해서 연구되어 왔다• hep a -rin 을 매 ml 당 0. 15 단위 만 혈청 에 첨 가해 주면 int r i n s ic pla sma thr ombop la sti n 형 성 을 방지 한다• 39) 한편 최근에 와서는 정상인의 혈청 0.8ml 내에 hep ar i n 을 0.01 단위 첨가해 주면 혈청내에 자연적으로 촌재하는 방해제에 의해 fac to r X 의 활성 도가 중화되 어 버 리 는 것 을 촉진한다고 하였 다. 40) 이와 같이 he p ar i n 의 혈액의 항응고기능에 대한 연구가 많이 진 행되고 있지만, 본문에서는 혈액으로부터 중성지방울 혈액 밖으로 이 동시 키 는 데 관련된 hep a rin 의 기 능을 주로 논하고자 한다. 1943 년에 개를 실험대상으로 지방식 섭취 후에 혈청이 우유빛으
로 된 식이성지방혈증 (al i men t ar y l ip em i a) 에 he p ar i n 을 첨가해 중으 로써 혈청이 맑아졌다는 실험결과가 발표되었다. 이 지방혈층에서 혈청이 맑아전 결과를 초래하게 된 기전을 살펴보면 다음과 같다. 혈액으로부터 중성지방이 사라지면서 동시에 혈액내에 존재해 있던 chy lo mi cro n 과 크기 가 큰 low densit y lip o p ro te i n (LDL) 이 없 어 졌 음을 발견하였다. 결국 이 연구에서 보여준 것은 중성지방이 가수분해되는 치방분 해가 일어남으로써 유리지방산과 글리세롤로 면화되었기 때문이며, 이 결과 보다 크기가 작고 밀도가 높은 l ip o p ro t e i n 이 나타났다는 것이다. 그리고 이때 유리된 지방산의 운반체로 안부민이 있다는 것도 밝혀졌다. 결국 이때 지방분해를 위해서 직접 작용했단 물질 은 쥐의 심장근육과 사람의 혈청내에서 he p ar i n 을 주사하기 전에 지방조직에서 발견되었던 물질이다. 이 물질은 l ip o p ro t e i n 의 특칭 을 지닌 것으로 밝혀졌으며, 보다 정확하게는 he par i n 에 의해서 활 성 화되 는 lipo p ro te i n lip a se 로 불리 게 되 었 다. 실제 로 lipo lyt ic ap o enzy m e 이 모세 관 혈 관버 (cap illar y wall) 에 촌 재하고 있다. he p ar i n 은 실제로 필수적인 조요소 (co fa c t or) 로 모세 관혈관벽에 약하게(l oosel y) 결합되어 있으면서 이곳에 결합되어 있 는 lipo p ro te i n lip a se 를 유지 시 켜 서 이 러 한 작용이 가능할 수 있 도 록 안정시켜 주는 역할을 하는 것이다. 직 접 또는 간접 의 증거 를 모두 종합해 보면 혈류 (c i rcula ti on) 로부 터 중성지방을 이동시켜 내는 것은 LPL 의 효소작용이라는 것이다. LPL 이의에는 어떤 물질 또는 효소도 이 작용을 진행시키는 것은 없다고 본다. 어떤 물질이든지 he p ar i n 작용의 방해인자이거나 LPL 작용을 손상시키는 물질이 있을 때 동물이나 사람의 혈청내에서 지 방혈증이 생간다. 고지 방식 사 후나 또는 동위 원소 처 리 된 low densit y lip o p ro te i n (LDL) 을 주사하고 난 후에 는 혈액 내 에 ch y lom i cron 이 나 보다 크기 가 큰 lipo p ro te i n 이 고농도의 중성 지 방울 함유하고 있 었는데 , 이 물질이 보다 크기 가 작은 저 농도의 중성 지 방을 함유한 lip o p ro te i n 으로 전환되는 것을 관찰해 볼 수 있다. 그리고 동시에 유리지방
산, monoacy lg l y c erol, dia c y lg l y c erol 의 농도가 증가되는 것을 볼 수 있 다 35) (그림 9, 10 참조). He p ar i n 은 모든 혈관의 내막 (endo t hel i um) 밑에 위치한 mast cell 내에 저장되어 있다. 이곳에서부터 hep ar i n 은 쉽게 혈류로 스며나 옹 수가 있다.
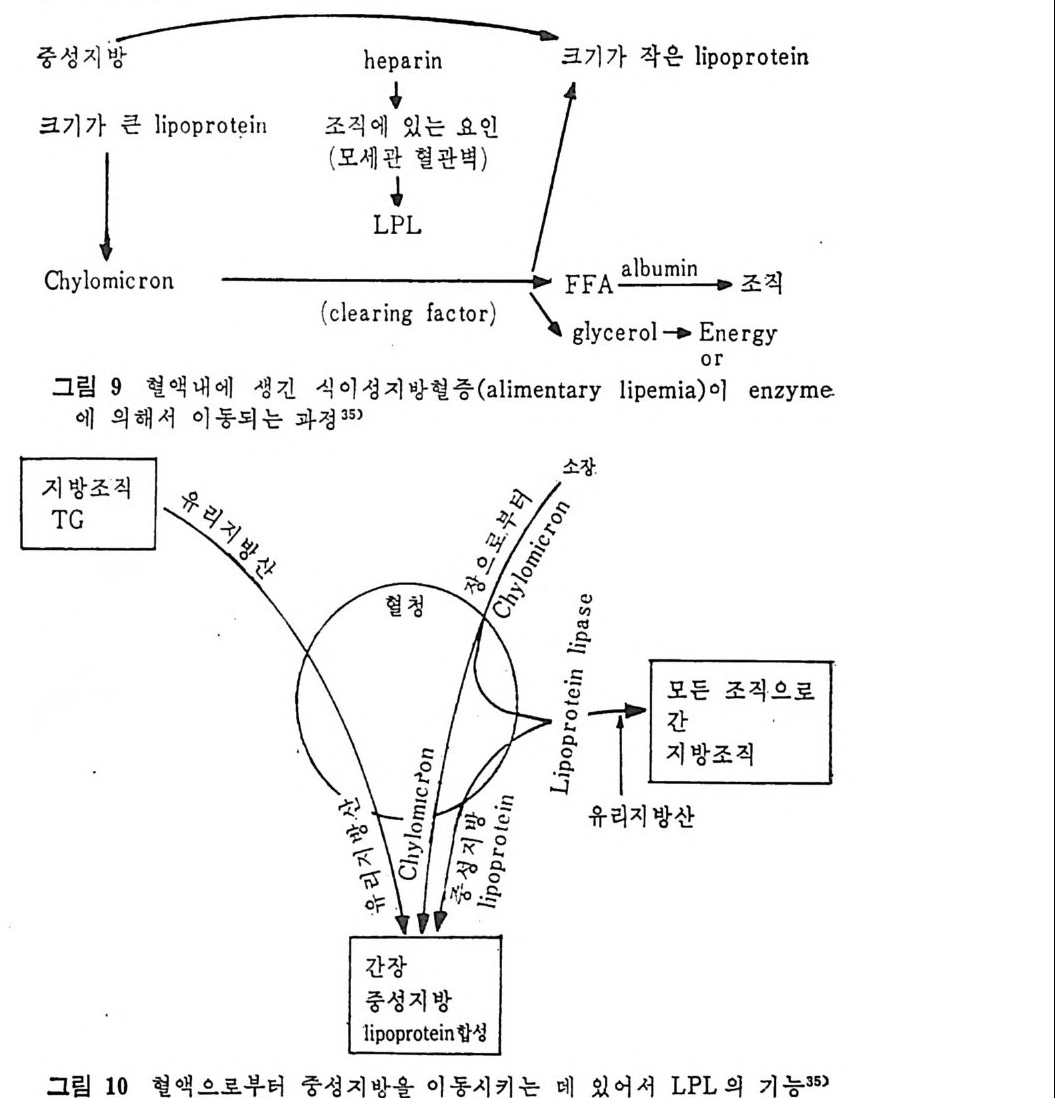 중그성 헉hC 림에 지 。방}글 m 9의 l.C큰해r혈 서액n 。내이 에동。 되· 생는긴 과정식(조(c 모아l3직e5 )세a성 h에re관지i‘ pn a g있방 r혈 는if혈n관a c 벽증 요to) 인(r a) l i men`L\|||| t a소`、,크rg y장7lyl 71 二-』iAFrep regn o zteey c. mnl e y rl
중그성 헉hC 림에 지 。방}글 m 9의 l.C큰해r혈 서액n 。내이 에동。 되· 생는긴 과정식(조(c 모아l3직e5 )세a성 h에re관지i‘ pn a g있방 r혈 는if혈n관a c 벽증 요to) 인(r a) l i men`L\|||| t a소`、,크rg y장7lyl 71 二-』iAFrep regn o zteey c. mnl e y rl
2) Hep a rin 과 lipo p ro te i n lipa se 와의 상호관계 Hep a rin 을 주사하면 적 어 도 두 종 류의 lip a se 가 혈 액 에 는 유지 된다. 26 ),41- 2) 하나는 고전적 인 lip o p ro te i n lip a se (LPL) 또는 ex tr a hep a ti c LPL 라고 부르는 것 이 다. 이 효소는 NaCl o. 3 M 이 상 의 농도에서 작용이 방해를 받으며 이 효소의 작용을 위해서 복 정한 ap o li po p r ote i n 을 요구한다. 17-8),43 ) in viV 0 연구에 서 보면 이 효소 는 모세 관의 endoth e liu m 에 서 중 성 지 방이 풍부한 lip o p ro te i n 에 작 용한다 . 4 4)
 e .SmE oht xaomtrte t1h rT . e tfeOh껍 nra lehho egp h ol.PtUHothhSuiS de ee. gIrUeSEaT n r a yuctP c e .gp lr.eOiAaoaES nprp. ' n .s0ett oSe dT r s. lelIIt lhCr dlfeo.L Cc rtPa oLP Cd .畑 tIa il :r oH msaf。 D cL hshCM S uRNOe \ 尸/\ ? @
e .SmE oht xaomtrte t1h rT . e tfeOh껍 nra lehho egp h ol.PtUHothhSuiS de ee. gIrUeSEaT n r a yuctP c e .gp lr.eOiAaoaES nprp. ' n .s0ett oSe dT r s. lelIIt lhCr dlfeo.L Cc rtPa oLP Cd .畑 tIa il :r oH msaf。 D cL hshCM S uRNOe \ 尸/\ ? @
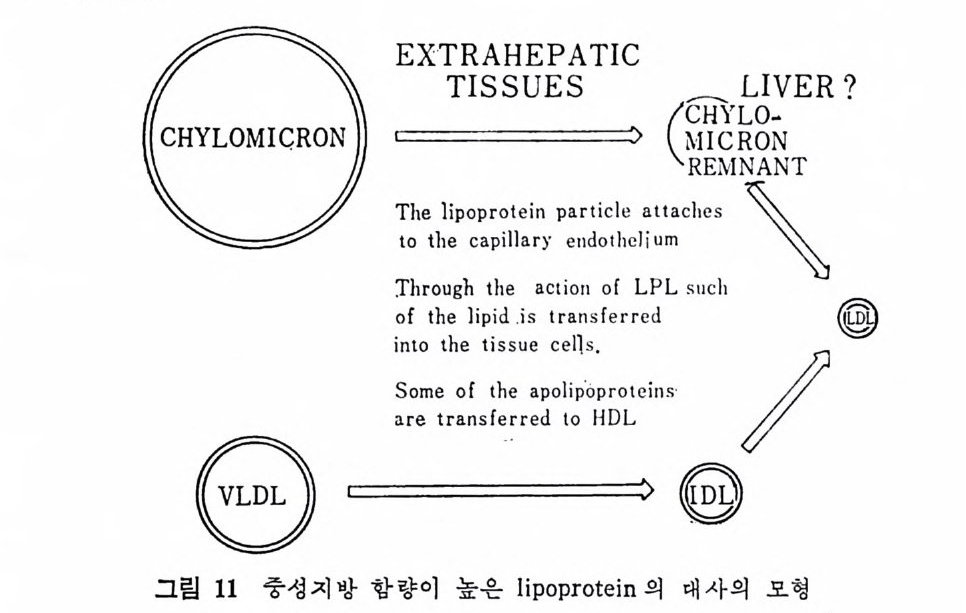
지 방산과 부분 gly c erid e s, 죽 MG 또는 DG 가 유리 되 며 이 들은 조직에 의해서 취해진다 .45) LPL 에 의해서 중성지방이 가수분해되어서 이동되어 나오면, 결 과적으로 이 효소와 작용하였 던 lipo p r ote i n 의 구의 크기 가 차차 감 소하며 이 lipo p ro te i n 내 의 구성 성 분에 번화가 온다. 죽 단백 질 의 양 이 증가하고 지방량이 감소하는 결과가 된다. 그래서 이 lip o p ro te i n 의 밀도가 변하게 된다 46-7) (그립 11 참조).
이러한 과정을 거치는 동안에 생기게 되는 l ip o p ro t e i n 은 이 LPL 예 더 좋은 기질이 되지 못한다 .48) 죽 중성지방 분해가 계속되어 서 VLDL 이 나 chy lo mi cr on 으로 시 작했 던 기 질 인 lip o p ro te i n 이 중성지방이 분해되어 나가서 IDL 에 도달하게 되면 LDL 은 더이상 IDL 을 기질로 하여 작용하지 않는다. VLDL 이 IDL 로 변형되는 과정 은 모세 관의 내 막 (endo t hel i um) 에 서 일어 난다. Extr a hep a ti c 조직 이 lip o p ro te i n 에 함유된 중성 지 방으로부터 지 방산을 취해 가려 면 lip o p ro te i n lip a se (LPL) 의 작용을 요구한다. 45) 모세 관 할 관벽 의 내 막에 lip o p ro te i n l ip ase(LPL) 가 활성 화되 어 있 으 떤 extr a hep a ti c 조직 도 lip o p ro te i n 의 중성 지 방으로부터 지 방산을 이용할 수 없다. 이러한 작용을 동한 변화룰 거치는 등안 혈청내의 lip o p r ote i n 으로부터 지 방산이 각각의 extr a hep a ti c 조 직 , 죽 지 방조 직 같은 곳으로 그 조직 의 팔요에 따라서 이 동된다. 예를 들어서 지방조직에서는 잘 먹었을 때 LPL 의 작용이나 중성 치방 이용률이 높으며 굶었을 때는 이들의 작용이 낮은 것을 볼 수 있 다. 49) 분만 직 후에 는 유선의 지 방 조직 내 에 서 lipo p r ote i n lip a se 의 작용과 혈액내의 중성지방 이용융이 현저하게 높아지고 있음을 볼 수 있다. 이는 젖지방의 합성을 위해서이다. He p ar i n 에 의해서 혈액내로 분비되는 또 다른 l ip ase 는 간으로 부터 유리 된 것 이 다 26-7),44 - 5),50 - 1) In vit ro 연구에서 보면 이 효소가 분명히 LPL 과 다른 것은 고농 도의 NaCl 에 도 그 작용에 방해를 받지 않으며 , LPL 작용에 필요하 다고 알려 진 ap o lip o p ro te i n s 에 의 해 서 도 그 작용이 중전되 지 않는 것 이 다. 이 lip a se 는 인지 방과 부분 gly c erid e 로 가수분해 작용을 하 고 있 다. 59) 그래 서 이 효소는 간세 포를 hep ar in 과 함께 배 양 (inc ub- a ti on) 했을 때 간세 포의 pla sma membrane 에 결합되 어 있는 ph osp- holip a se 라고 알려 진 효소와 같은 것 이 아닌가 하는 생 각을 하였 다. 52) 이 효소의 생리적 기능은 아직 분명히 밝혀져 있지는 않다고 본 다. 이 효소는 VLDL 이 나 chy lo mi cro n 내 에 있 는 중성 지 방울 효율 척 으로 가수분해 시 키 지 못한다. 그러 나 extr a hep a ti c 조직 에 서 LPL
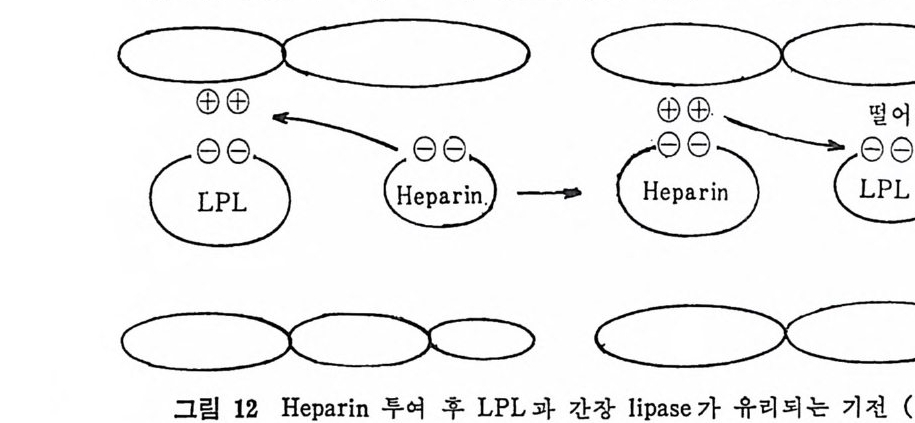
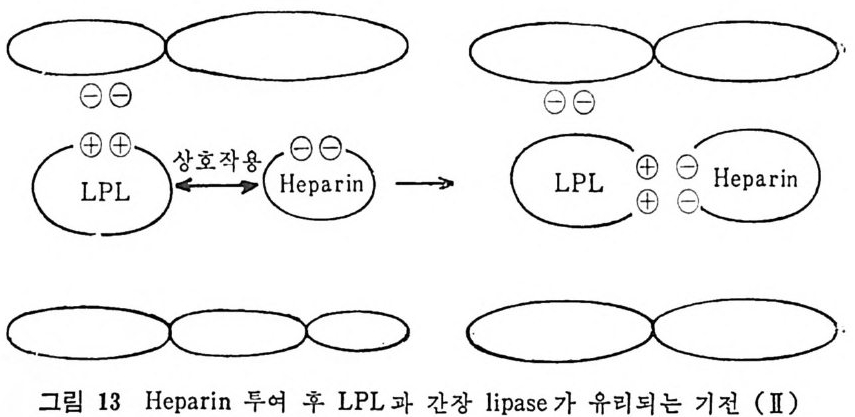
에 의해 분해되고도 남은 ch y lom i cron 의 나머지가 간에서 내사된 다고 하였 다. 53-4) 또한 in viv o 연구에 서 보면 다량의 chy lo mi cr on 을 주사하면 이 중의 얼마만큼은 간이 취해 가는 것을 볼 수 있다 .55) 또한 간장 lip a se 는 이 러 한 chy lo mi cr on 나머 지 와 LPL 의 작용의 결과로 extr a hep a ti c 조직 에 서 VLDL 에 서 생 성 된 IDL 에 작용하는 것으로 생각한다. 3) LPL 파 간장 lipa se 결합위치와 유리기전 Hep a ri n 울 주사하고 나면 LPL 과 간장 lip a se 가 혈 엑 으로 유리 되는데 이 유리되는 기전은 다음과 같이 설명되고 있다. he p ar i n 과 r 효소 사이에서 상호작용이 생긴다는 견해와 he p ar i n 이 모세혈관의 내막세포 (endo t hel i al cell) 표면 56) 과 간세포 (hep a t oc yt e) 표면, 즉 이 효소가 결합되어 있는 곳과 상호작용하는 것으로 생각한다. 모세 혈관벽 이 나 간세 포의 외 각막(p lasma membrane) 에 는 충분한 양 이온이 분포되어 있으며, 이곳에 LPL 이나 lipa se 분자내에 있는 음 一 이온과 정전기결합에 의해서 효소가 결합되어 있다. 그런데 분자내 에 음이 온 밀도가 높은 hep a rin 이 접 근해 오면 이 hep a rin 분자가 결합되어 있던 곳으로부터 효소를 유리시키고 그 자리에 hep a rin ion ic 결합에 의해서 상호관련을 갖게 된다(그립 12 참조). 또 다른 一 견해는 효소와 hep ar i n 이 상호작용을 한다고 보는 견해이다(그립
 - 〈二〉三三나옴
- 〈二〉三三나옴
 〈e〉e 二론〉一 三ee 二 三
〈e〉e 二론〉一 三ee 二 三
13 참조 ). 이 경우순근 LPL 과 he p ar i n 이 전기적으로 서로 천화력이 생겨서 이를 상호간에 알 수 있어서 LPL 과 he p ar i n 이 결합한다는 · 견해이다. Hepa rin 이 첨 가된 혈청 을 hep a rin - sep h arose 관을 동과시 키 면 . LPL 이 나 간장 lipa se 가 모두 이 관에 부착되 어 서 작용하고 있으며 이들은 sal t (NaCI) 에 의해 비중농도(g rad i en t) 차에 의해서 유리되어 나온다. 41 ),5 0) 위의 실험에서 보여주는 것은 두 가지 l ip ase 가 모두 생리 p H 에 서 hep a rin 과 강하게 결합될 수 있 으며 이 들은 NaCl 의 농도를 증 가시킵으로써 유리되어 나울수있다는 것이다. 여기서 보여준 결과 는 두 가지 lipa se 모두 hep a rin 과 결합할 수 있 는 lipid- sit e 가 있 다는 것 이 다. 모든 고등동물의 이 두 가지 lipa se 에 는 모두 hep a rin - lip id sit e 가 있 다고 추측한다. 4) Endot h eli al cell 표면에서 lipo p r ot ei n lipa se 의 결합상태 요즈음 증명되고 있는 것은 모돈 포유동물의 제포표면물질 중에 hep a ran sulf ate 가 있 다는 것 이 다. 57-8) 물론 endoth eli al cell 표면 에도 이 물질울 가지고 있어서 LPL 과 결합접이 되고 있다. 모델실험 결과에서 보여준 바와 같이 생리 p H 에서 LPL 과 hepa - ran sulfa te 는 고도의 찬화력 을 가지고 있으며 , 이 온결합력 (ion ic :
 그립 14 Endoth e lia l cell` -p• l' a -s 8·m ; 、 a、 \ 그·:림', 15 정모\세 관근 en d:鬪 oth e Iiu m 에 서
그립 14 Endoth e lia l cell` -p• l' a -s 8·m ; 、 a、 \ 그·:림', 15 정모\세 관근 en d:鬪 oth e Iiu m 에 서
Lip o p ro te i n 형 대 의 기 질 (substr a te ) 이 endoth e lia l cell surfa c e 에 결 합이 되 면 lip a se 분자가 막과 같은 평 면으로 움직 여 서 lip o p ro te i n 이 결합되도록 한다(그림 14 참조). 그림 15 에서 보면 이 다당류 (po lys accharid e ) 의 길이 는 20~50 µm 가 된다. 그러 므로 LPL 은 一 막에 서 좀 떨어 져 서 lipo p ro te i n 과 결합이 되 어 상호작용이 가능하 게 된다(그림 16 참조). 그러 므로 이 경 우에 는 LPL 이 다당류(p ol y sacchar i de) 에 부착되 어 작용하지만 endoth e li al 세포표면으로부터 분리된 용해성효소 (soluble enz y me) 인 LPL 이 기질에 작용하는 거와 비슷한 결과를 나타내게 된다. 59) 혈청이 he p ar i n 에 의해 처리된 후에 용해성효소인 모돈 LPL 은 chy lo mi cr on 이 나 유화된 중성 지 방과 결합한다. 60) 이 와는 대 조적 으 로 효소가 endo t hel i um 에 결합이 되어 있어서 이미 가수분해를 좀 진행 한 후에 이 endoth e liu m 에 서 떨어 져 나오면 단지 소량의 용해 성 효소만이 lip o p ro te i n 과 작용울 한다고 본다. 61 ) 그러 므로 LPL 효 소는 endoth e liu m 에 강하게 결 합되 어 있 다. 아마도 sulfa ted gly c - osami no g ly c an 과 enzy m e 과의 전기 적 (electr o sta t i c) 상호작용이 이 강한 결합을 유지시켜 주는 것으로 본다. Chy lo mi cr on 중성지방도 혈액으로부터 빨리 사라지는데 쥐의 chy lo mi cr on 의 반감기 (half life)는 4 분이 다. 55) 직 경 이 150 µm 되 는 전형 적 인 chy lo mi cr on 1 분자는 약 106 분자의 중성 지 방을 함유하고 있 다. 45) 그런데 Bovin e 것 의 LPL 에 의 한 중·
성 지 방 분해속도는 매 분당 40, 000 정도이고 he p ar i n 으로 처리한 혈 청으로부터 유리된 LPL 은 매분 당 약 30,000 정도이다 .62) 그러 므로 여 러 분자의 enzy m e 이 1 분자의 chy lo mi cr on 에 결합 되어서 작용한다는 것은 자명한 사실이 다. LPL 은 endoth e lia l cel1 에서 합성되는 것이 아니고 다른
 直 붙
直 붙
조칙, 지방조직의 지방세포 (ad ip ocyt es) 에서 합성된다. 63 4) 합성된 LPL 은 이 세 포로부터 subendoth e li al spa c e 로 분비 되 어 그곳에 서 hep a ran sulfa te 와 결 합이 된다. 이 결 합되 는 과정 이 그립 17 에 나 타나 있다. 5) LPL 의 acti vit y 와 C- a p o -pr ote i n 과의 관계 Hepa rin 이 두여 되 면 혈청 내 의 LPL 은 VLDL 과 chy lo mi cr on 과 상당히 찬화력이 있는 것으로 나타난다. 그리고 LPL 은 LDL 과 홈 착이 된다. 그런데 이 흡착은 ch y lom i cron 이나 중성지방유액 (emu- ls i on) 의 사이 면(i n t er fa ce) 에서 일어 난다(그립 18 참조). LPL 이 유화된 중성 지 방구나 또는 chy lo mi cr on 과 혼합된 것 을 원십분리해 보면, 그 멘 위충부분의 용액에서 중성지방유화구나 chy lo mi cr on 이 유리 된다. LPL 은 또한 VLDL 과 chy lo mi cr on 의 구성 성 분인 Ap o B 와 sul- fated 된 다당류인 pro te o g ly c an 과 상호 작용한다. 아마도 pro te o g ly - :ea n 이 측면에 서 스며 나와서 LPL 과 작용하도록 한다고 본다.
 from Gut Endoth e lium
from Gut Endoth e lium
그러나 LPL 은 활성됨 에 따라 중성지방기질을 요구하는 것이 없다. 그런데 의 활성화작용은 에 인 위적으로 현탁°바울 가해 주게 되 면 영향을 받는다. 이때 청내에 단백질 Ap o C- II CR-g lu ta m at 물가해 주면활성작용이 상당히 상승된다. Ap o C -II 는 chy lo mi cr on 이 ·vL DL 내 에 풍부한 존재한다. 그러나 만들어 전 신생 (nascen chy lo mi cro n 과 온 Ap o C-II 를 포함해 다른 C-pr o te i n 의 이 낮다. 그렇기 Ap o C-II pro te i n 은 개의 경우 LPL 이 내로 유동이 되기 하면 HDL 로부터 된다. 그래 서 chy lo m cron 이나 VLDL 내의 중 성 지 방의 가수분해 가 어 느만큼 진행 이 되 면 단
 1009027060504082010
1009027060504082010
백 질 인 Ap o C-II 는 다시 HDL 로 보내 지 게 되 며 chy lo mi cr on 나머 치 는 간으로 보내 진다. 65) 신생 chy lo mi cro n 이 LPL 과 결합될 때 도. HDL 이 C-pr o te i n 의 처장고로서 의 역 할울 한다고 본다.
 0o503o30o1 -
0o503o30o1 -
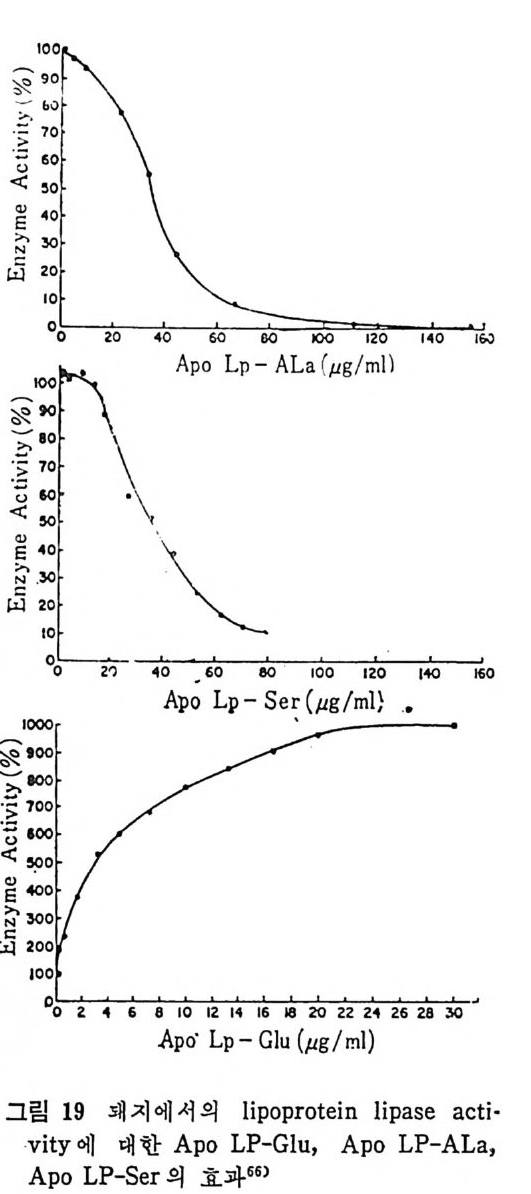
돼지의 지방조직 중 에서 여러 가지 종류 의 C- p ro te i n 을 유리 하여서 LPL 의 혈 청내 의 활 성도 를 측 정하였 다. 66 ) 그립 19 에서 보여주 는 바와 같이 Ap o - alanin e 인 Ap o C· IlI 나 A p o 一 ser i ne 인 Ap o C- 1 은 LPL 의 방해물 질로써 작용 을 하며
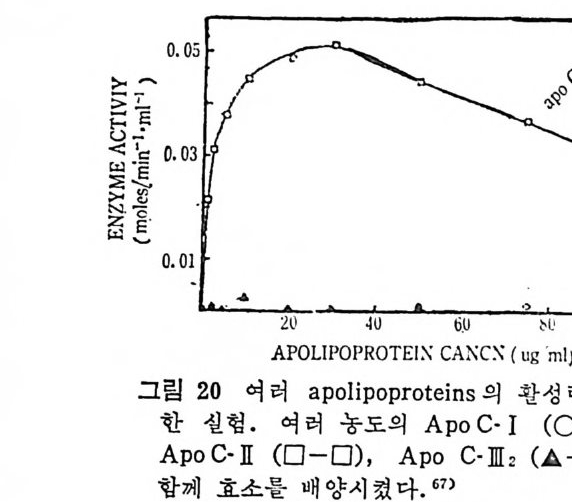
Ap o -gl u ta m ate 인 Ap o C-lI 만이 LPL 의 활 성 울 증가시 켰 다. 소것 (Bov i ne) 에 함유되어 있는 LPL 을 유리하여 여러 종류의 C- p ro t e i n 과 함께 배양시켰다 .67' LPL 이 A poC-Il 에 의해서 활 성화 되려면 적당량의 A p oC-Ill 가 있어야 한다고 하였다. 다음의 • 그림 20 은 LPL 을 Ap o C-Il , Ap o C- il l2( R·aia 1 )- si a l ic
 ;--
;--
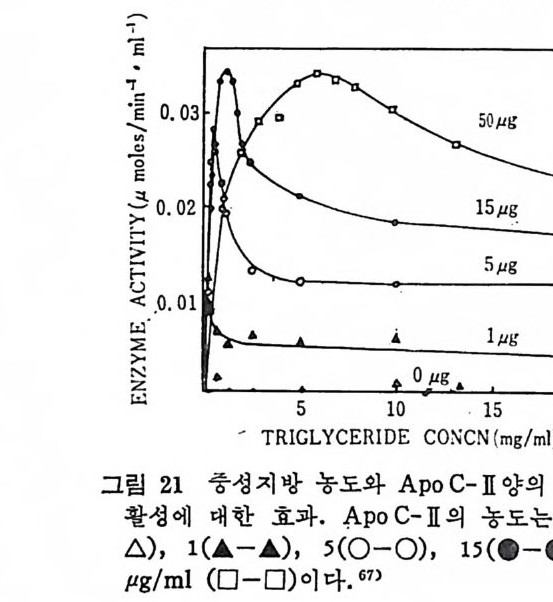
acid / mole, Ap o C-Ill2 (Ra-Ja 2 )-sia l i c a cid / m- ole 과 기 질농도도 2. 5. m g /m1 로 하여서 배 양시 켰더 니 Ap o C- II 에 의해 LPL 의 활 성 화되는 힘은 적당량의 A p oC-IlI 가 있을 때 이루어졌다고 하였다. 또 한편 중성 지 방농 - 도와 Ap o C 개 양의 LPL 의 활성에 대한관 계 를 보았다. Ap o C-lI 와 중성지방의 농도어t
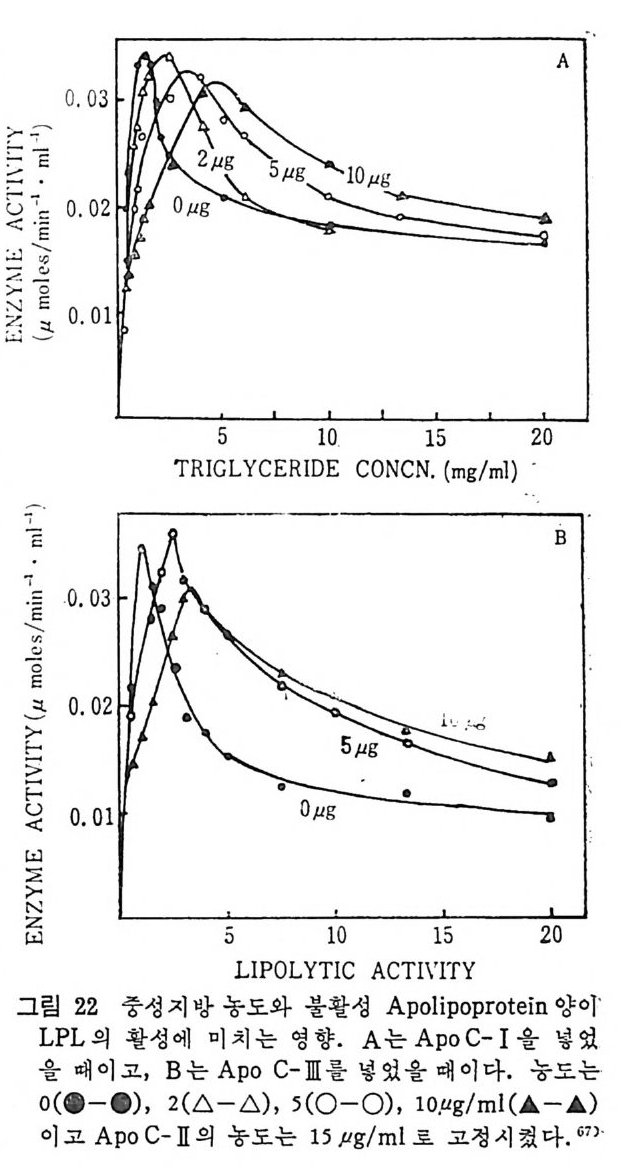
따라서 LPL 활성 에 영향를 미찬다 는 것이 다.즉 A p o C-II 와 중성지방의 가장 적합한 농도=는 10 2 A~중p 성1o0 지0C 라-방II고 하 였 다. 이는 무게 울 로 표 시되었다〈그립 21 참조). 다음의 그립 는 A p oC-II 의 농도는 15µ g으로고 청이 되어 있으면서 다른 C-p t e i n 을 첨가해 보았다. Ap o C-I A p oC 내 h 를 각각 다른 농도로 첨가했을 때도 이 둘이 LPL acti v ty에 전적인 방해 제라기보다는 중성지방농도와 비 례 해 서 LPL ac v ity에 영향을 미 치고 있음이 나타
 尸• .
尸• .
났다. 그리 고 Ap o C-1 , Ap o C-l[ 군} Ap o C-II 사이 에 서 농도에 비례해서 중성지방에 대해서 서로 경쟁이 있음이 나타났다. 여하튼· Ap o C-II 의 농도가 종가되 면 다른 C-pr o te i n 의 방해 작용은 문제 가 되지 않는 것으로 나타났다.
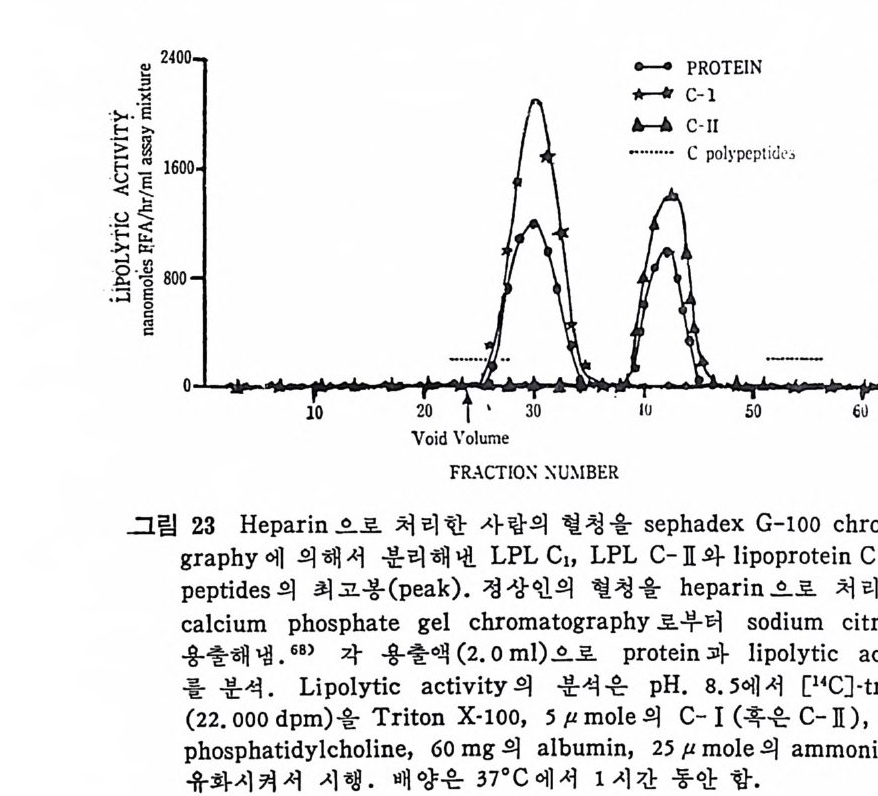
Ap o C - II 의 LPL 작용에 대한 역할은 이들이 1 : 1 의 비율로 결합 이 되 면 LPL 의 활성 부위 (acti ve s it e) 가 노 출 이 된다고 한다. Ap o C 내가 LPL 의 기질인 중성지방에 대한 찬화력을 증가시키지는 않 는다. 한편 A p oC 기이 첨가되면 중성지방의 적당량의 농도가 l 민 화 한 다. 이런 현상으로 보면 A p oC - I 이나 A p oC - III 모두 의 견상 의 활 성 제 (app a rent ac ti va t or) 라고 볼 수 있 다. Extr a hep a ti c L PL 은 hep a rin 에 의 해 서 유리될 때 두 가지 형 대 의 것이 유리된다고 한다 .68) 다음의 그림은 he p ar i n 으로 처리한 사람의 혈 청에서 LPL 을 분 리 했을 때 나타난 최고봉(p eak) 이 다. ~ep h adex G- 1 00 chromato g ra p h y 에 의 해 서 LPL Ci , LPL C- I I , 그리 고 lip o p r ote i n C po lyp e p tide
 24001600 800 60
24001600 800 60
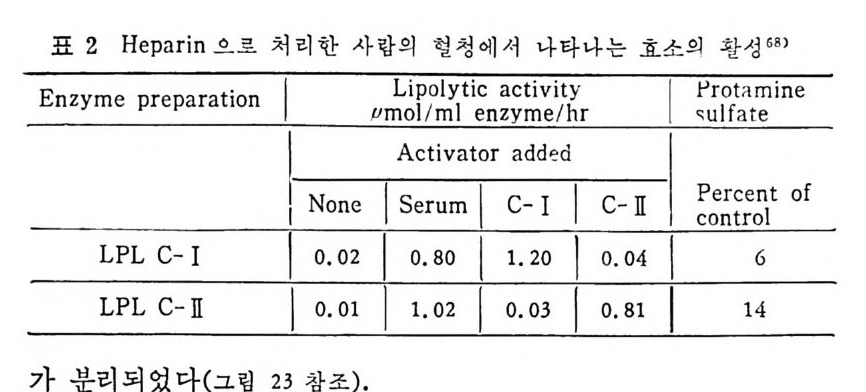 표 2 He par i n 으 르 처리한 사람의 헝청에서 나타나는 효소의 활성 68 )
표 2 He par i n 으 르 처리한 사람의 헝청에서 나타나는 효소의 활성 68 )
분리된이들의효소활 성 도 (enz y me acti vi t y) 를 비교하여 보았다 (표 2 참조). LPL C -I 은 pr ota - mi ne sulf at e 에 의 해 서 방해를 받으며 이 특성 은 extr a hep a ti c LPL 과 유사하다. 그 러나 LPL C- JI는 그 렇지 않음을 보여주고 있 으며 활성 제 (acti va - t or) 로 C-JI 를 첨 가했 을 때, LPL C- JI의 활 성 도 (ac ti v ity)는 증가 하는 것을 보여주었 다. 한편 쥐의 혈청을 hep a rin 으로 처 리 하 고 두 종류의 LPL 을 분리하였다. 찬화력이 낮은(l ow aff ini t y) -LP L
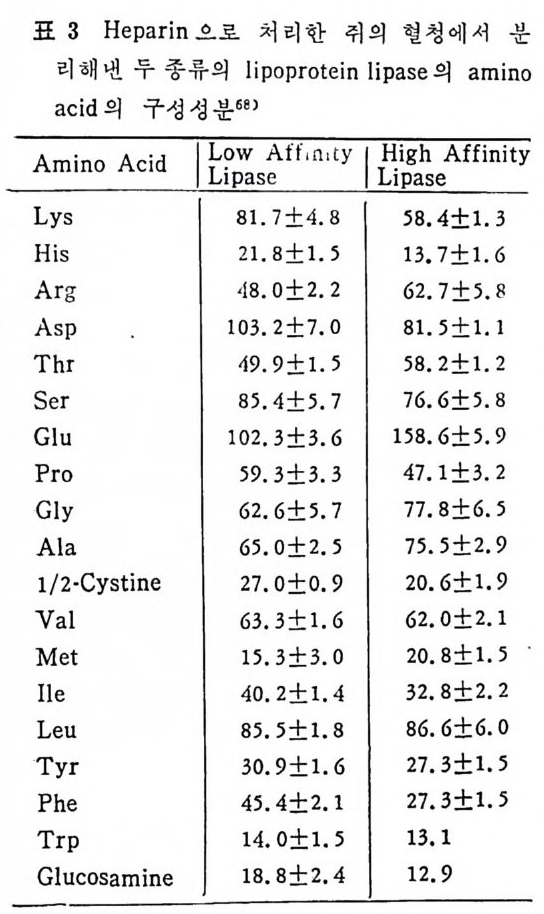 표 3 Hep a rin 으로 처 리 한 쥐 의 형 청 에 서 분
표 3 Hep a rin 으로 처 리 한 쥐 의 형 청 에 서 분
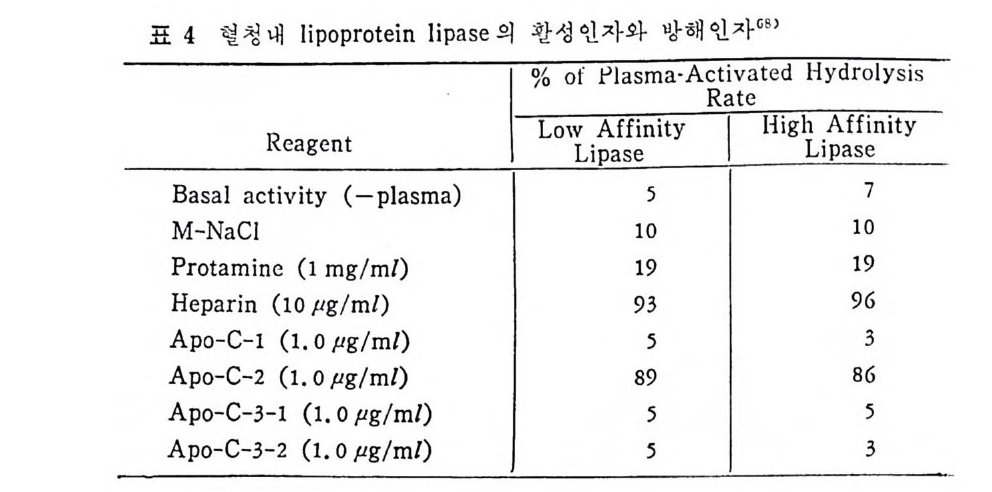 표 4 혈청 내 lip o pr o te i n lipa se 의I 활% 성o I인 P자la와s ma방 · 해A 효인\;자: t6 8 c ) d Hy d ro ly s i s
표 4 혈청 내 lip o pr o te i n lipa se 의I 활% 성o I인 P자la와s ma방 · 해A 효인\;자: t6 8 c ) d Hy d ro ly s i s
과 찬화력 이 높은 (h ig h aff ini t y) LPL 이 다. 이 들의 아미 노산 구성 은 다음 표에 나타나 있 다( 표 3 참조 ). 찬화력 이 낮은(l ow aff ini t y) LPL 은 분자량이 69, 250 으로 hep a rin seph arose aff ini t y chromato g ro p h y 에 의 해 유리 된 것 이 며 69) 찬화 력 이 높은 (h ig h aff ini t y) LPL 은 F i eld i ng e t al6 2 ) 에 의 해 서 분리 된 것 으로 분자량 37, 500 이 며 , ami no acid s 의 구성 성 분에 서 서 로 다론 구성 을 보이 고 있 다. 특히 lys in e , argi ni n e , glu ta m i c acid 와 ph e-
ny la lanin e 의 함유량에 차이 를 나타내 고 있 다. 위 의 표 4 에 나타난 바에 의 하면 LPL C-I 은 pro ta m i ne sulfa te- 에 의해서 방해를 받으며 이러한 득칭은 extr a hep a ti c typ e 의 LPL 과 유사하다고 본다. 그러 나 Ty pe ][에 서 나타난 바에 의 하면 low aff init y 나 hig h aff init y LPL 이 모두 pr ota m i ne 과 NaCl 에 의 해 서 pla sma 내 에 서 가수분해 능력 의 저하를 가쳐 오고 있으며 , Ap o · c - [ 에 의해서 가수분해능력의 상승을 가져오는 것으로 보면 이들 의 효소들이 같은 acti ve sit e 를 가졌 다고 볼 수 있 다. 이 듈 low 와 hig h aff init y enzy m e 의 cofa c to r 는 오직 Ap o C- [라고 볼 수 있으며 기타 다몬 종류의 A p o p ro t e i n 은 오히려 활 성을 감소시켰다. lipo p ro te i n lip ase 도 low 와 hig h aff ini t y LPL 모두 VLDL 보다 chy lo mi cro n 에 보다 큰 분해 력 을 가지 고 있 다 。 표. 5 혈 청 Jip o p ro te i n lipa ses 의 작용역 학 (kin e ti c) 상수 6 9 )
표. 5 혈 청 Jip o p ro te i n lipa ses 의 작용역 학 (kin e ti c) 상수 6 9 )
또한 표 5 에 나타난 것 처 럼 low af finit y LPL 이 hig h aff ini t y LPL 보다 높은 Km 치를 가지고 있어서 low aff ini t y LPL 보다 쉽게 해 리 (d i s s oc i.: ti on) 된다. 십 장조직 내 에 촌재 하고 있 는 hig h af fini t y LPL 은 언제 나 기 질 과 결합되 어서 기질은 포화 되어 있는 상태로 촌재한다고 한다 .70) 정제된 LPL 은 현저한 양의 he par i n 을 함유하지 않았다. 정제된 LPL 은 he p ar in 과 상호작용을 하지 않는 것 으로 본다. 그런데 crude LPL 은 hep ar i n 과 결합 이 되어 있다. 다 음의 표 6 에 서 보면 o. 02 µg hep a rin /mg 단백 질로 나타나
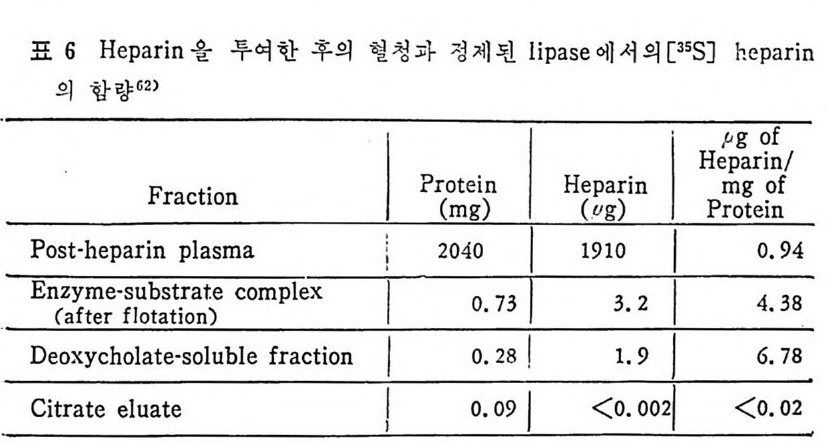 표 6 He p a rin 을 두여 한 후 의 혈 청 과 정 제 된 lip a se 에 서 의 [35S] hep a rin
표 6 He p a rin 을 두여 한 후 의 혈 청 과 정 제 된 lip a se 에 서 의 [35S] hep a rin
있 다. 이 는 1 molecular of hep a rin / 1000 LPL molecule 로 볼 수 있 다. 그러므로 he p ar i n 은 아마도 LPL 정제시에 분리되어서 나가 버 린 어떤 구성요소와 결합되어 있는지도 모른다고 한다. LPL 은 endoth e li al cell 에 서 합성 되 는 것 이 아니 고 지 방세 포에 서 합성 된다. 그리 고 LPL 은 go lgi vesic l e 에 서 유리 되 어 세 포내 int r - acellular spa c e 로 유리 되 는 과정 이 serum 내 hep a rin 에 의 해 서 이 루어 진다. mast cell 에 는 hep a rin 과 his t a m i ne 이 결 합된 상대 로 존재 한다고 본다. 그러 므로 유리 된 hep a rin 의 농도는 매 우 낮으며 다량이 거의 다 결합된 상태로 존재한다고 본다. 앞부분의 그림 17 은 LPL 이 지방세포에서 합성되어서 g ol gi내로 분비 되 어 서 endoth e lia l cell 내 로 이 전되 어 가논 과정 이 다. go lgi 에 서 유리되면 endoth e li al cell 로 la t eral 확산 (d iff us i on) 에 의해서 이 동된다고본다. 다음의 그립 24 는 ep idi d y m al fat pa d 를 collag e nase 로 처 리 하여
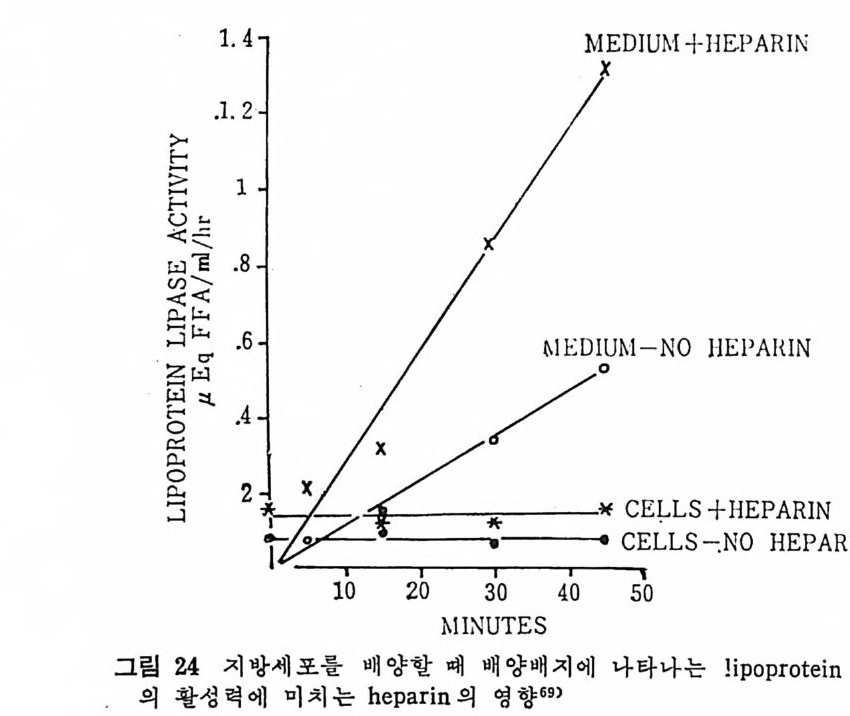 1. 4 MEDIUM -I-H E .P ARIN
1. 4 MEDIUM -I-H E .P ARIN
 A.LIALL. :2::5> >3SVdI1
A.LIALL. :2::5> >3SVdI1
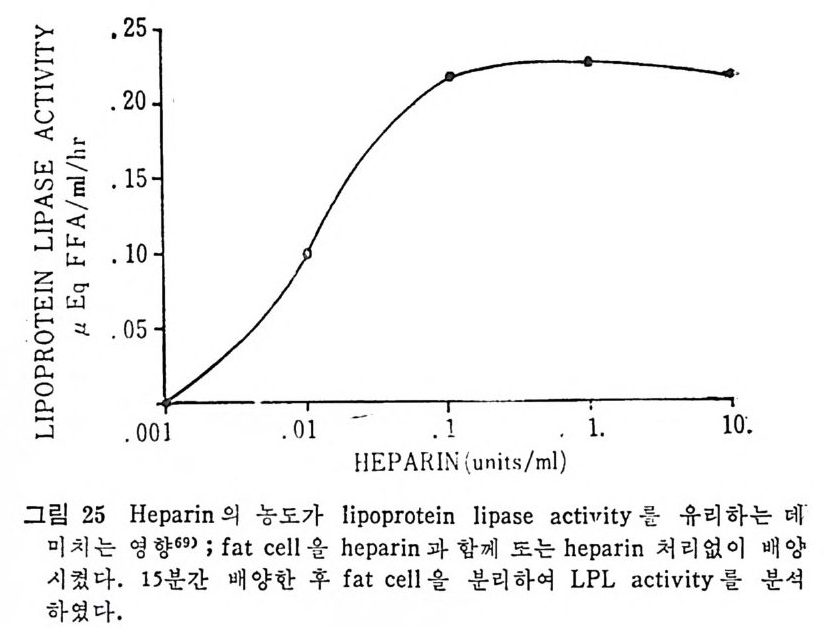
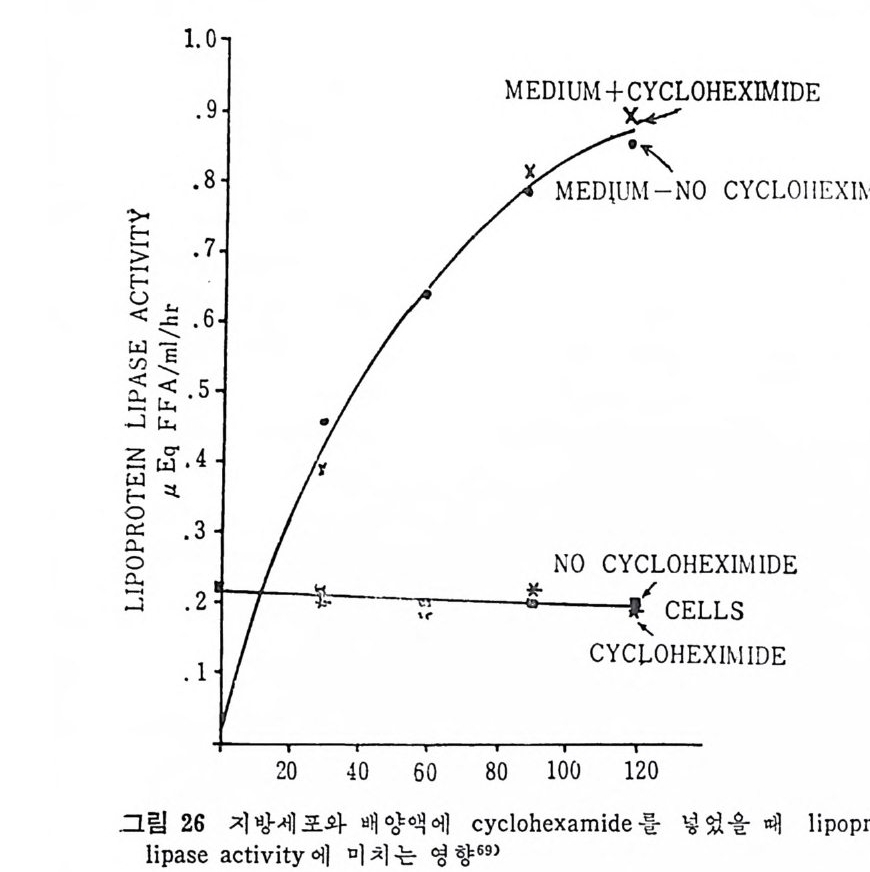
서 지방세포를 유리한 다음, 이곳에 he p ar i n 을 첨가하여서 LPL 의 작용상태를 유리지방산이 유리되는 양으로 측정한 그래프이다. 작 · 용용엑 내 에 hep a rin 을 첨 가함으로써 유리 되 는 유리 지 방산의 양이 증가됨을 볼 수 있다. 이는 LPL 의 유리되는 양이 증가되었다고 볼 수 있다. 다음의 그림 25 는 hepa rin 이 LPL 유리 에 미 치는 영 향을 나타낸 것 이 다. hep a rin 의 첨 가량이 증가함에 따라서 LPL 의 acti vi t y 가 무한정 증가되는 것은 아닌 것으로 나타났다. 어느 수준에서 최고 치에 달하고서는 그대로 그 수준을 유지하는 것으로 나타났다. 다음의 그림 26 은 cy c lohexami de 가 lip o p ro te i n lip a se acti vi t y· 에 미치는 영향을 관찰하였다. fat cell 과 함께 배지 (med i um) 내에 c y clohexam i de 를 첨가해서 LPL 과 함께 배양시켰더니 120 분 후에 LPL 의 acti vi t y 가 본래 세 포에 함유된 활성 의 5 배 나 증가되 었 다. 위의 모든 결과를 종합해 보면 분명히 LPL 은 지방세포에서 합 성되 어 서 hep a rin 에 의 해 그곳으로부터 유리 되 도록 자극을 받아서 :
 1. 0.9.8
1. 0.9.8
지방조직내의 모세관 혈청내로 이전되어서 중성지방의 지방산을 분 해시켜서 유리시킨다. 그렇기 때문에 배지 가운데 포도당과 인슈틴 이 함유되어 있으면 he p a ri n 에 의한 LPL 의 유리가 더욱더 증가 한다 .9 1) 인슈린으로 처리한 후에 LPL 의 활성이 지방조직내에서 증가되 는데 그 증가는 지방세포로부터 LPL 의 분비가 촉진되고 증가되어 서 나타나는 결과라고 하였다 .72) 또한 실험동물 쥐에서 보면 굶었 을 때보다 찰 먹인 동물에게서 LPL 의 지방세포로부터의 유리가 더 욱더 많다고 보고되기도 하였다 .73) 그러므로 LPL 이 유리되려면 대 사에 너 지 가 요구되 며 74) 또한 배 지 중에 포도당이 나 pot a s siu m ,
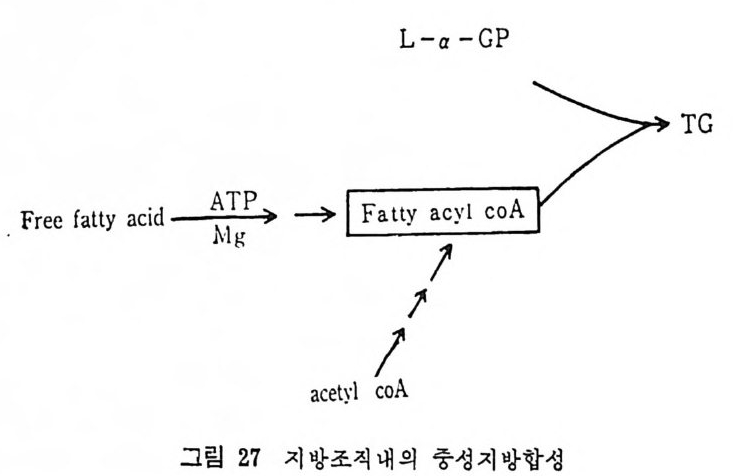
calciu m 이 온이 함께 배 양되 면 LPL 유리 에 영 향을 미 찬다고 하였 다 .75) 그 런 데 단백질합성을 차단시키는 c y clohexam i de 를 첨가했더 니 LPL 유리나 그의 활성 에 영향을 미치지 않음이 나타났다 .7 5) 단 백질합성이 방해를 받아도 LPL 의 활성이나 유리에는 전혀 영향을 미치 지 않 는 것으로 보면, he p ar i n 이 LPL 에 미치는 영향은 LPL 합성에 영향을 미치는 것이 아니라 LPL 의 활성화 증진에 영향을 미 찬 다고 볼 수 있다. (2) 지방조직내의 중성지방 합성 Chy lo mi cr on 이 나 VLDL 내 의 lip o p ro te i n 중성 지 방은 주변의 조 직들에 의해서 취해지지 못하고 우선 모세관의 endo t he li um 에 있 던 LPL 에 의해서 가수분해가 시작된다. 그러면 유리된 지방산이 유리되며 이 유리된 지방산의 일부도 지방조직내에서 다시 중성지 방 합성에 이용된다. 지방조직내에서의 중성지방의 합성은 유리된 지방산이 ATP 와 CoA 에 의 해 서 활성 화된 후에 acety l- C oA 와 작용하여 서 fatty .ac y l- CoA 를 합성 한다. 그러 면 L-a-gl y c erol pho sph ate 와 fatty .a c y l-CoA 와 결합하여서 중성지방이 합성된다(그립 27 참조).
 L-a -GP
L-a -GP
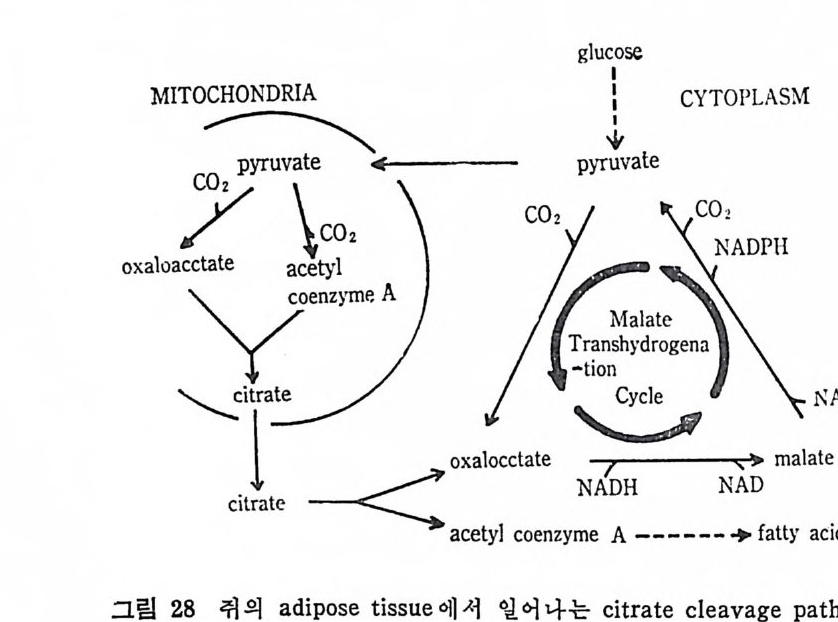
이와 같이 지방조직내에서의 중성지방의 합성은 유리된 지방산을· 이용한다는 듯이 있다. 한편 고당식사를 했을 경우 간에서 지방산의 de novo 합성이 이 루어지는 사실이 동물에게서 밝혀졌다. 지방산의 de novo 합성은 acety l CoA 가 mi toc hondria 막을 통과할 수 없 어 서 이 루어 지 는 것 이 며 동물내 에 서 는 득히 쥐 에 서 는 다른 citra te cleavag e enzy m e sys te m 이 모두 cy top la sm 내 에 촌재 하고 있 다. 다음 그림 28 은 cit ra te cleavag e pa th w ay 로 동물의 지 방조직 에서만 이루어지고 있고 사람의 지방조직내에서는 이루어지지 않는 다. 이 cit ra te cleavag e pa th way 를 동해 서 NADPH 가 합성 되 며 이는 지방산합성을 위해서 이용된다. 한편 malate tra nshy d rog e nati on cy c le 이 이 루어 쳐 서 cy top la sm 내의 NADH 가 존재할 경우 이 경로를 통해서 NADPH 합성울 한 다. 그래서 합성된 NADP 는 지방산합성하는데 이용될 수도 있다. 지 방조직 내 에 서 중성 지 방 합성 시 에 L-a-GP( g l y cerol-3- phosp ha t e) 의 합성은크게 두 가지 경로로 이루어진다. 첫째, g lucose 의 섭취가 충
 glu cose
glu cose
 p{? \\a\>::::
p{? \\a\>::::
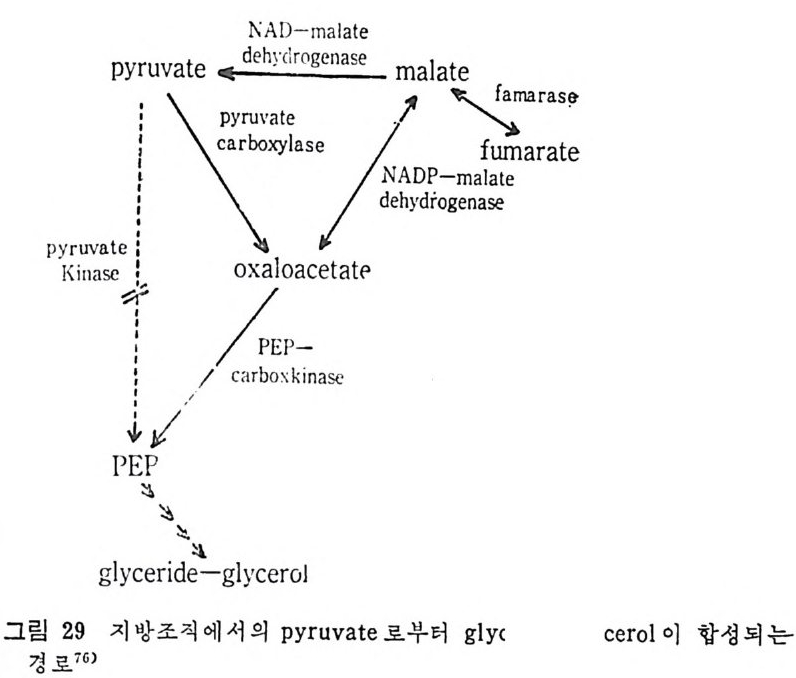
분히 된 상태 에 서 는 Embden-Mey e rhof pa t] 거 치 고 중간,I.J:- 물로 dih y d roxy a ceto n -ph osp h ate 가 L-cr-' l 환되 어 서 공급 된다. 그러나 g lucose 가 결핍된 상태에서i. r a t e 가 다음의 네 가지 단계 를 거 쳐 서 gly c erid e -g l y c erol 로 전조된다. 이 과정 중에 도 dic a rboxy li c ac id shutt le sy st e m 이 포함된다(그럽 29 참조 ). i) pyru vic acid 가 carboxy la ti on 이 되 어 서 oxaloaceta t e 로 전 환된다. ii) 탄소 4 개 의 대 사중간물질인 fum arate 가 포함되 어 탄소수 1 (C-1) 이나 탄소수 2(C-2) 를 임의로 선정하는 과정을 거찬다. iii) oxaloaceta t e 가 ph osph oenolpy ru vate - carboxy k in a se 에 의 해 서 decarboxy la ti on 된다. iv) ph osph o enolpy ru vate 가 gly c erid e -gl y c erol 로 전환이 된다. 간에서 denovo p a t hwa y에 의해서 지방산이 합성되면 이는 곧 중성지방으로 합성되어 혈액내로 배설되어 신체를 순환하게 되는데,.
순환되는 혈액내에서 VLDL 의 중성지방의 형대로 순환한다. 그러 면 이 중성지방은 LPL 에 의해서 분해되어 지방세포가 취해가면 치 방조직에서 중성지방합성에 쓰인다. 그런데 사람에서는 이 과정 이 일어나지 않는다고 한다. (3) 지방조직으로부터의 중성지방 이동 1) 서론 굶은 포유동물에게서는 지방산이 주요 대사물질이다. 굽은 동물 의 호흡계 수 (res pi ra t or y q uo ti e n t)가 가장 낮기 때 문에 이 를 중거 로 해 서 체내에서 지방산이 산화되고 있다고 믿을 수 있지만 과연 혈청 내의 유리지방산이 산화되는지 아니면 조직내에 존재하고 있는 내 적지방 (endo g enous l ipi d) 이 산화되는지에 대해서 구별할 길이 없다. 하여돈 굶는 기간이 연장이 되면 산화되는 모든 지방산의 근원은 치방조직의 저장지방이라고 본다. 왜냐하면 지방조직내에만 양적으 로 다량의 지방이 저장되어 있기 때문이다. 일단 지방조직으로부터 이동된 유리지방산은 및 가지의 운명이
 PLASMA COMPARTMENT
PLASMA COMPARTMENT
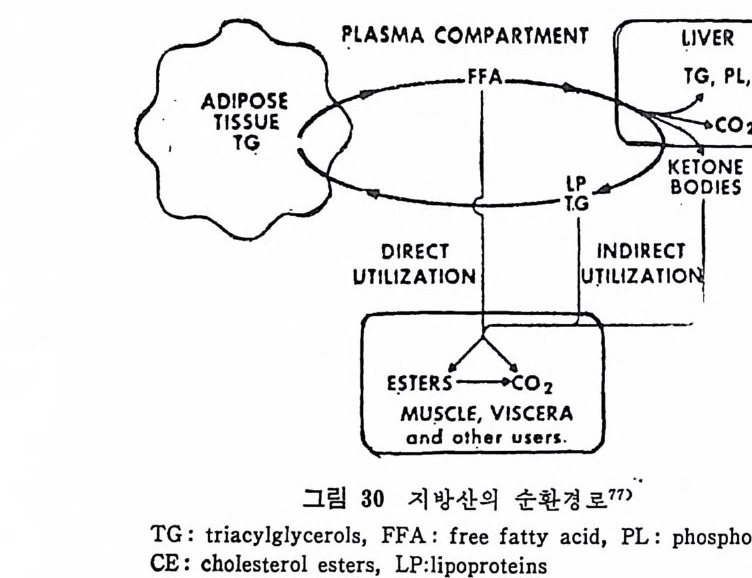
있다고 본다 .77) 혈청내의 유리지방산은 주로 간으로 이동된다. 간으로 이동되는 혈청 유리지방산의 양은 혈청내 전체 양의 30% 에 이른다 .78-9) 간에 의해서 취해진 유리지방의 총량 중 약 30~50% 가 완전히 산화되어 CO2 로 되며 나머지의 일부는 케톤체로 산화되어 결국은 말단조직으로 이동되어 산화된다. 아마도 이와 같이 간접적으로 산 화되는 양 또한 약 1/3 정도 된다고 보고되었다 .75) 나머지의 지방 산은 간에 서 lip id este r 로 전환된다. 족 중성 지 방, 인지 방, 콜레 스 테 롤 este r 로 전환된다• 이 러 한 lip id este r 들은 결 국 lip o p ro te i n 합 성시에 여기에 컬 합되며 다시 혈청으로 배설된다. 혈 청내에서 중성지방을 주로 이동시키는 수단은 VLDL 이다. 그 러면 VLDL 내의 중성치방은 LPL 의 작용을 받아서 분해되며, 분 해된 산물은 지방조직을 포함한 신체 각 부위 조직에서 취해간다. 이러한 경로를 통해서 지방조직에서 유리된 지방산이 혈청내로 유 리되어서 신체내를 순환하다가 근육, 지방조직 및 기타 조직으로 분산되어 가는 하나의 회전 (c y cle) 을 이룬다(그립 30 참조). 지방산이 지방조직에서 나와서 다시 치방조직으로 들어가는 이 능력이 바로 지방조직이 신체내의 지방산의 항상성 조철에 공헌하 · 는 기능이라고 볼 수 있다 .80) 치방조직으로부터 지방산이 유리되어 나오는 데는 섭세한 호르몬의 조철작용이 영향을 미치지만 유리된 지방산이 이용되는 데는 직접적으로 호르몬의 영향이 미치는지에 대 한 증거는 아직 없다고 본다. 결과적으로 말단조직들이 취해서 산 화시킬 수 있는 양보다 많은 양의 유리지방산이 이동되어 나온다. 그래서 이런 상태가 오랫동안 계속되면 지방간(fatty li ver) 이 생기는 경향을 보인다 .81) 이런 경우 간이 VLDL 분비를조철해서 다량의 지 방산이 지방조직으로 이동되도록 하여서 유리지방산의 순환율 못하 게 하는 균형을 맞추는 작용이 일어난다. 사실은 중추신경계통조직을 제의하고서는 모든 조직들이 혈청으 . 로부터 유리지방산을 취해갈 수 있다. 취해전 지방산은 말단조칙내 에서 직접 산화되어서 CO2 가 되든가 아니면 este r com p ound 로 전 환되어서 저장된다. 이 저장된 지방은 참정적으로 제한된 시간 동-
안에 에너지 공급원이 될 수 있다. 2) 지방조직내에서의 저장파 이동 지방조직은 혈청으로부터 이동되어 들어온 포도당, 유리아미노 산, 그리고 유리지방산 을 이용하여서 지 방 울 합 성하 고 주로 중성 지 방의 형태로 처장한다. 그리고 이 지방합 성 에 이 응되는 또 다 른 물 질로는 혈청내의 VLDL 내에 함유되어 있는 중성지방 으 로서 지방조 직내로 이동되어 들어가서 지방 합 성에 이 용된 다. 그러 나 V LD L 의 중성지방이 지방조직내로 이동되려면 힐청 내에 유동되고 있는 LP L 에 의해서 촉진된다 . 혈 청 LPL 은 지방조직 내에 존재하고 있 는 hormone sensit ive lip a se (HSL) 와는 다 른 효소 이 며 이 HSL 은 지 방 조직내에 처장되어 있는 중 성 지방의 분해 설- 촉진한다 . 82) 지방조직내에 저장된 지방의 이동은 HSL 의 작용 속도 에 따라서 처장된 중성지방으로부터 유리되는 지 방산의 이동에 의해 주로 이 루어지고 있으며 이때 생성된 굴리세 를 의 이동은 현 저 하게 나 타 나 지 않고 있다. 다음의 그림 31 과 같이 지방조직의 지방세 포 내에서는 계속해서 중성지방이 분해되며 한편으로는 중성지방이 재 합성 되는 동적상대 (dy n ami c s t a t e) 를 유지하고 있 다. 여 기 서 이 루어 지 는 중성 지 방 의 분 해와 합성의 두 과정은 완전히 독립된 두 체제 로 이 루 어 지 고 있 다. 중성지방분해로 인해서 유리된 지방산의 상당 량 이 지방 산 ac y l- ·Co A 유도체로 활 성화됨으로써 중성지방재합성에 이 용 되고 있음 이 밝혀졌으나 이때 유리된 글리세롤은 중성지방재 합 성에 이용된 흔적 이 보이지 않고 있다 . 7 7) 왜냐하면 정상 지방세 포 내에서는 굳리 세몹 울 활성화시키는 글리세를 k i nase 의 활 성이 아주 낮기 때문이다. 지방세포내의 유리지방산이 지방세포 로 부 터 유 출 되는 속도는 포 도당이 이용되기 쉬운 상태로 촌재하는 양 과 여러 종 류의 지방분해 촉진 호르몬(lip ol yti c hormone) 에 의 해 서 조철된다. 죽 포도당의 분 해과정 중간 산물인 글리 세 폴 aldehy d e 가 글리 세 롤 kin a se 에 의 해 서 활성화되어 글리세롤 p hos p ha t e 로 전환된 후 지방세포로 이동 되 는 양에 따라서 유리 지 방산의 재 este r ifi ca ti on 되 는 양이 조철된
다. 즉 재 este r if ica ti on 되 는 양이 증가되 면 반대 로 유리 지 방산의 유 출양은 감소된다. 또한 유리지방산의 이동은 여러 종류의 지방분해 촉진 호르몬에 의해서 자극됨이 in vit ro 실험에서 밝혀졌다 .77) 이들 호르몬은 ACTH, ep ine p h rin e , norep ine p h rin e , glu cag o n, vasop re ssin , seroto n in e , fat mobil izin g pitui t ar y pe p tide s, melanocy te sti - mulati ng hormone 둥둥이 다. 그러 나 이 들이 in viv o 실험 에 서 도 같은 견과를 나타내는지에 대한 확인은 아직 덜 되어 있다. 그러 나 이 러 한 호르몬의 작용 강도는 동물의 종류에 따라서 다르 게 나타나고 있 다. 즉 포유동물에 서 는 sy m p a th e ti c nerve-endin g 이 나 부신수질 에 서 분 비 되 는 cate c holami ne 계 통 호르몬이 지 방세 포로 부터의 지방산이동에 영향이 크다고 보나, 조류에서는 이와는 달리 g luca g on 이 더 큰 영 향 을 미치는 것으로 in viv o 연구에서 나타났 다. 포유동물의 지방세포내에서는 인슈린이 유리지방산의 이동을 가장 감소시키는 호르몬으로서 그 작용내용은 다음의 2 가지로 설 명된다. 첫째는 인슈란이 지방세포로 하여금 포도당을 취하도록 자 국하여 서 유리 지 방산의 재 este r if ica ti on 을 촉진시 킨다. 둘째 는 인 슈린이 ca t echolam i ne 에 의해서 HSL 이 활성화형태로 전환되는 것 울 방해 하는 항지 방분해 작용 (an ti-lip ol yti c ac ti v ity)을 한다. 83) 그러 나 조류에서는 인슈란이 유리지방산의 재 es t er ifi ca t i on 을 자극하나 항지 방분해작용에 는 영 향을 미 치 지 않는 것으로 나타났다. 84- 5 ) 또 한 p ros t a g land i n 이 인슈린과 마찬가지로 항지방분해효과가 있는데 이의 자세한 기전은 밝혀져 있지 않았다 .8 6-7) 3) 지방조직으로부터의 중성지방 유출기전 지방제포로부터 지방이 유출되는 속도는 HSL 에 의해서 중성지 방이 가수분해되는 속도에 의해서 결정된다. 그런데 지방조직에 촌 재 하는 HSL 은 4 가지 종류가 있 다. 이 들은 중성 지 방 hy d rolase, DG-hy d rolase, MG-hy d rolase 와 choleste r ol este r hy d rolase 이 다. 이 들은 모두 pro te i n kin a se 에 의 해 서 활성 화된다. 그러 므로 pr ote - in kin a se 방해 제 를 가해 주면 이 4 가지 종류의 hy d rolase 는 불활성
으로된다. 다음 그림 32 에는 쥐의 지방조직내에서 88) HSL 이 활성화되어 가 논 과정이 나타나 있다. 그러나 사람의 지방조직 89) 이나 닭의 지방 조칙 16) 에서는 거의 유사한 과정을 관찰하였다. HSL 의 활 성 화 되어 가는 과정은 그림 32 에서 보여주듯이 단계적으로 이루어 지고 있다.
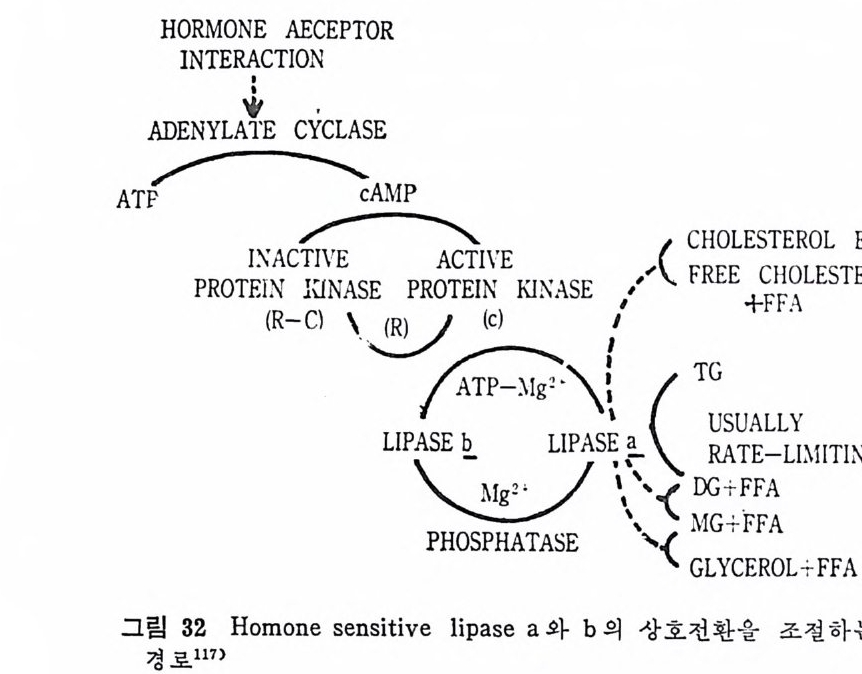 HORMONE AECEPTOR
HORMONE AECEPTOR
이 과정의 시작은 지방분해 촉진 호르몬이 지방세포막 표면의 recep tor 와 상호작용하여 서 adeny l cy c lase 를 활성 화시 키 는 작용 이 이루어지면서 시작된다. 이 작용이 시작되고 난 칙후에는 지방 세포내에 cy c li c A MP(cAMP) 의 양이 참정적으로 증가하고 있음 울볼 수 있다 .90) Adeny l cy c lase 는 c-AMP 합성 효소이 며 낮은 Km 치 를 가지 고 있 다. 또한 ph osph odie s te r ase(3, '5'-cyc lic AMP-ph o sph o die s te r ase) 는 cAMP 를 7 난분해하는 효소로서 이 두 가지 효소는 모두 세포 막에 결합되 어 있는 효소이 다. 91 > adeny l cyc lase 는 지 방세 포의
pla sma membrane 에 존재 하는 것 으로 알려 져 있 다. adrenalin 은 adeny l cyc lase 의 활성 을 높여 서 cAMP 양을 중가시 키 며 반대 로 인슈린은 감소시키고 있음은 잘 알려진 사실이다 .92) 한편 인슈란은 adeny l cy c lase 활성중가에는 벨로 효과는 없으나 ph osph odie s te r ase 의 활성 을 자극한다고 보고되 기 도 한다. 93- 7 ) Hormone recep tor 와 membrane enzy m e 사아 의 상호작용에 대 해서는 알려진 바가 거의 없다. 그러나 adeny l c y clase 의 활성화에 호르몬이 관여할 때 GTP 가 관여한다고 보고되어 있다 .98 - 9) 호르몬의 자국을 받고 지 방세 포내 에 cAMP 의 양이 증가되는 것 은 잠정적이며 최고치에 달했다가 떨어치게 되어 있다. 초기에 최고 치 에 탈했 다가 cAMP 의 양이 감소되 기 시 작하는 기 전은 lip o lyt ic ag e nts 에 의 해 서 ph osph odie s te r ase 의 작용이 증가되 거 나 100) 또는 adenosin 을 유리 함으로써 IOI) 또는 fee d back 조절에 의 해 서 102-3) 이루어진다고 보고되고 있다. 그러나 cAMP 의 양이 감소하는 것 과 인슈린 작용으로 인한 auto l ip o lyt ic ac ti on 과는 별개의 작용이 라고 보고되 어 있 다. 100) 또한 지 방조직 내 에 서 도 pro te i n kin a se 가 함유되 어 있 음이 보고뒤 었 다. 104) 그런데 이 것 은 간이 나 근육조직 내 에 함유되 어 있 는 pro te i n k i nase 와 여러 가지 점으로 미루어볼 때 유사한 것임이 밝혀졌 다. 104) Prote i n kin a se 는 복잡한 cata l yt ic un it (C) 와 Reg u lato r y unit (R ) 로 구성되어 있다. 그러므로 이 두 부위가 결합되어 (CR) 촌재하다 가 cAMP 농도가 지방세포내에서 증가되면 pro te i n k i nase(CR) 에 서 cata l yt ic unit 가 유리 되 며 105) 아 unit 가 hormone sensit ive enzy m e 을 ph osph oryl a ti on 시 켜 서 비 교적 불활성 형 (ina cti ve lipa se b) 에서 활성형 (acti ve lipa se a) 으로 전환시킨다 .106) HSL 은 네 가지 종류로 구성되어 있다고 앞에서 언급하였다. 죽 TG-hy d rolase, DG-hy d rolase, MG-hy d rolase, choleste r ol este r hy d rolase 이 다. 이 들 네 종류의 hy d rolase 가 닭이 나 쥐 의 지 방조 직에 모두 함유되어 있음이 보고되었다 .107) 그림 33 에 서 보여 주듯이 4 종류의 h y drolase 를 5mmole M g표 이 온
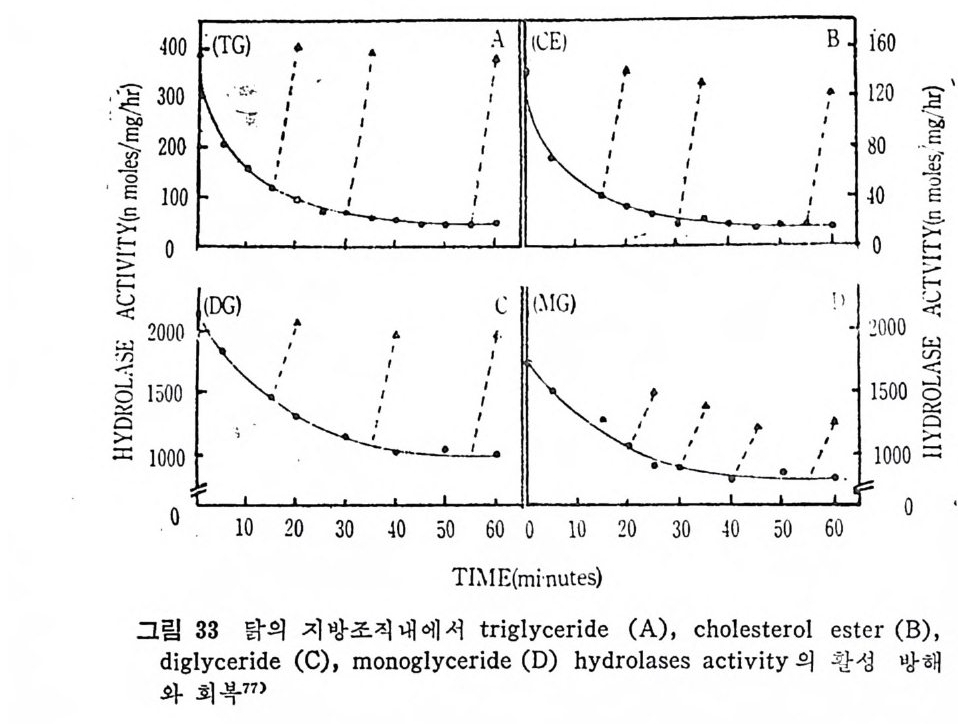 ' B
' B
과 배양시키면 이 효소들의 활성이 감소되며 이들을 ATP-M g표와 cAMP 와 함께 배양시키면 다시 활성이 증가된다. 그런데 이들 효 소들은 pro te i n k i nase 방해제 108) 에 의해서 그 작용이 방해를 받으 며 의 부에 서 충분한 양의 pro te i n kin a se 를 첨 가해 주떤 다시 그 활 성 이 회 복된다. 그런데 4 가지 의 hy d rolase 의 활성 이 회 복되 어 서 최 고치에 달하는 비 율은 각각 다르다• 그립 34 에 서 보여 주듯이 4 가지 hy d rolase 의 최 고치 의 활성 화된 바 울을 비 교해 보면 중성 지 방 hy d rolase 와 콜레 스테 롤 este r hy d rolase 가 가장 높으며 DG hy d rolase 와 MG hy d rolase 는 그것 들에 비 해 서 낮다. 같은 조건하에서 중성지방 hy drolase 는 30~50% 의 활성화가 되
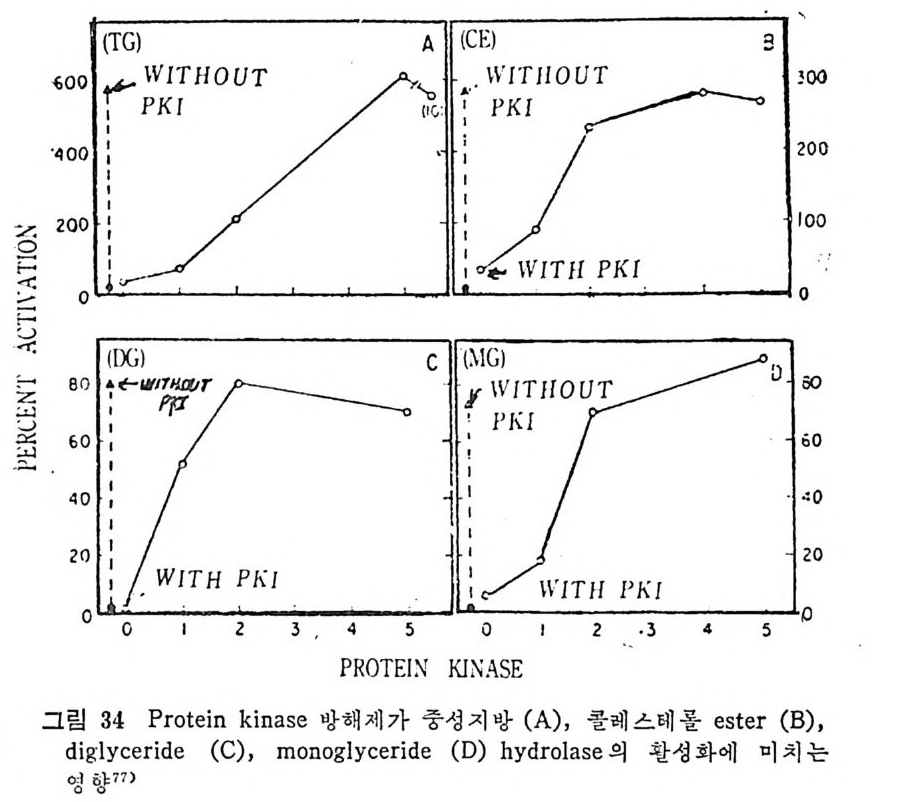 (TG) A (CE) >2 .
(TG) A (CE) >2 .
는대 비해서 DG hy drolase 의 칼성호낡근 크게 증가되지 않고 있다• 같은 조건하에서 활성화되는 법위는 중성지방 hy d rolase))DG hy d r· olase)) M G h y drolase 순으로 볼 수 있다. 그러나 절대활성도는 DG hy d rolase 나 MG hy d rolase 가 중성 지 방 hy d rolase 에 비 해 서 3~20 배나 크기 때문에 중성지방의 가수분해시에 첫번째 es t er 결합의 가 수분해가 속도제한단계 (rate - li m i ting s t e p)가 된다고 본다. 또한 4 개 의 hy d rolase 의 활성 은 ph osph ata s e 에 의 해 서 방해 를 받 을 수 있 다. M g++이 온이 단독으로 ph osph ata s e 불 활성 화시 켜 서 활 성 형 태 의 hy d rolase 에 서 dep h osph oryl a ti on 시 켜 서 불활성 hy d rolase 로 전환시키기도 한다.
4) 호르몬 recep tor 와 adeny l cy c lase 의 상호작용 지방분해를 촉진하는 호르몬이나 합성을 축전하는 호르몬이나 모 두 작용초기에는 지방세포의 외각막(p lasma membrane) 과 상호작용 울 시작한다. 이 상호작용은 처음에 외각막에 존재하고 있는 독 정 한 호르몬과 결합되는 독 정 단백질 (hormone spe c if ic p ro t e i n) 과 걷 합 한다. 이 단백 질은 recep tor sit e 라 고 생 각된다. 지 방세 포의 외 각막에 호르몬과 결 합될 수 있 는 recep tor sit e 는 한 가지 호르몬에 대해서 여러 곳이 있다는 것은 거의 명백해전 사 실이다 .109) 그러므로 외각막내의 독 정 단백질호르몬과 결합되는 곳, 즉 recep tor sit e 에 호르몬이 결 합되 지 않고서 는 adeny l cy c lase 와 외각막 사이에 거의 상호작용이 일어나지 않는다. 다른 말로 바꾸어 말하면 호르몬이 촌재 하지 않으면 호르몬 recep tor 와 adeny l cy c lase 와 의각막 사이에서의 결합이 일어나지 않는다. 다음의 그림 35 는 지방세포막(fat cell membrane) 과 adeny l cy c lase 사이의 상호작용이 일어나는 것을 가상 모델로 만들어 도해해 본 것이 다 .110) 호르몬이 세포막내의 특정 결합단백질과 결합되기 위해서 recep tor
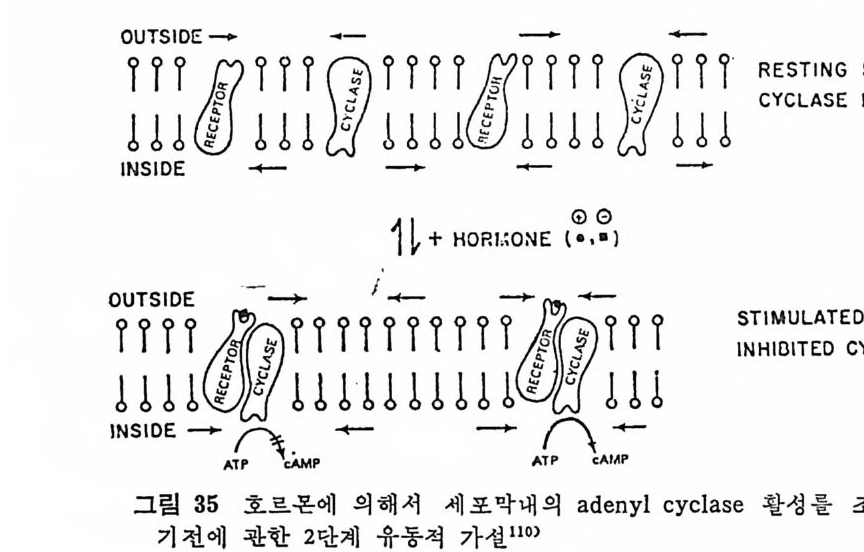 0I~具N冒u| T? fosf) ISIDE_fI DI' oI A 一iE ~m頁DE: - 〈걷O汀具―f L g_O f 0i! 'O _O .— l i.)_1Off,r一'~ l fo& _i+o0 l LIH oo blO| |RLf_o 凰tL |:'O _lN r l- E 一f f lA 麟 o: 0?^oi' | _lT_—?l
0I~具N冒u| T? fosf) ISIDE_fI DI' oI A 一iE ~m頁DE: - 〈걷O汀具―f L g_O f 0i! 'O _O .— l i.)_1Off,r一'~ l fo& _i+o0 l LIH oo blO| |RLf_o 凰tL |:'O _lN r l- E 一f f lA 麟 o: 0?^oi' | _lT_—?l
의 구조상의 (con fo r mati on al) 년화 가 온다고 본다. 그래 서 호르몬과 결합이 되면 비로소 adeny l c y clase 와 결합이 가능해진다. recep tor sit e 에 호르몬이 결합 되 고 여 기 에 adeny l cy c lase 가 결 합이 된 3 자 복합체 가 세포막내에 이루어지면 이를둘러싸고있는액체환경에 변 화 를 초래 하게 되며 따라서 작용하려 하는 분자와의 접촉 (coll i s i on) 이 생간다. 대 체 로 호르몬 recep tor sit e 는 세 포막의 외 각인 수용액 쪽으로 접 해 있 으며 adeny 1 cy c lase 의 acti ve sit e 는 세 포내 부로 면해 있 다. 그러므로 지방분해를 촉진하 는 호르몬과 결합하느냐 혹은 그 반대 의 호르몬과 결 합하느냐에 따라서 adeny l cy c lase 의 활성 에 영 향을 미치게 된다고 본다. 호르몬 recep tor s it e 와 adeny I c y clase 와의 결합체가 분해되는 경 우도 호르몬의 농도가 감소되 었 을 때 나타난다. 5) 지방조직으로부터 유리된 유리지방산의 이용 혈청 내의 유리지방산의 농도는 영양공급상태와 호르몬의 요소에 의해서 변화한다. 사람에 게서 유리지방산의 혈청내의 농도는 o.1~ o.2mM 이라고 한다. 그러나 하룻처넉 굶고난후의 농도는 o.4mM 로 증가한다. 또한 FFA 의 붕괴 울(t urnover ra t e) 은 빠르나 약 t 1/2 2~ 4 분 이다. 사람의 유리지방산의 붕괴윤은 t1 /2 3 분이며 유리지 방산의 전체 함유량은 약 4.5 g이다. 유리지방산의 12 시간 동안의 붕괴량은 약 53 g이나 된다. 쥐 에게 있어서 유리지방산의 혈 청내의 농도는 잘 먹인 상태(fe d , cond iti on) 에서 o. 3~o. 4 mM 이 며 굶온 상대 에서는 (1~2 일간) o. 6~ o.smM 이다. 다음의 그림 37,38 는 유리지방산이 이용되는 현상을 그림으로표 . 시한 것이다. 지방조직에서 유리된 지방산은 근육조직 세포내에서와 다론 조직 제포내에서 이용된다. 간세포내에서는 유리지방산이 중성지방으로 재결합되며 이 렇게 해서 생성된 중성지방은 l ip o p ro t e i n 내 중성지 방으로 구성된다. 그러면 대부분이 VLDL 의 중성지방으로 구성되
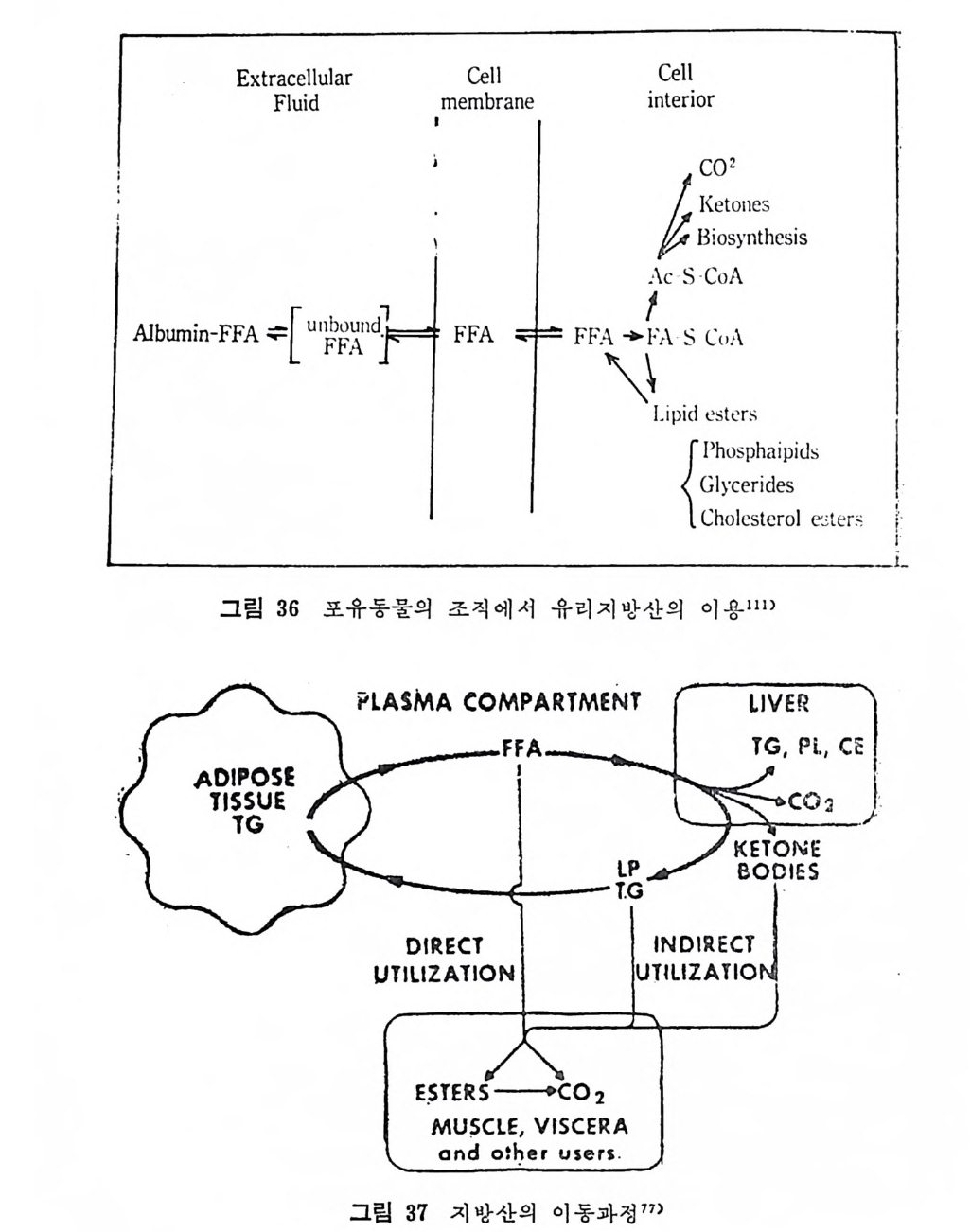 Extr Fa lcueildl u lar meCmebllr ane m. Ctee ln l. o r
Extr Fa lcueildl u lar meCmebllr ane m. Ctee ln l. o r
어서 혈액내에서 순환된다. 여분으로 생성된 VLDL 은 잠정적인 중 성지방 저장수단으로서 간세포내에 저장된다고 본다. 간세포는 지 방산으로부터 생성되는 케돈체 를 이용할 수 없으므로 이들은 다른 조직으로 산화되기 위해서 이동된다. 근육조직세포가 대부분의 케 돈체 를 이용한다. (4) 식사요인이 지방조칙내 중성지방대사에 미치는 영향 지방조직내에서의 중성지방대사를 논하고자 할 때 한 가지 조건 하에서만 논의될 수는 없다. 우리의 신체내에서 이루어지는 대사의 굴곡은 1 일을 기준으로 하여 보아도 일정한 곡선를 그리면서 지~ 가고 있다. 죽 공복시와 식사를 하고 난 직후와의 사이에서는 이때 작용되는 호르몬이나 효소의 작용이 서로 상반되는 현상을 보여주· 고있다. 특히 지방대사에서는 석사를하고난 후와 식사를 곧 하여야 하는 공복시의 지방조직내의 대사는 서로 다르게 이루어지고 있다. 첫째로 식서를 하고 난 직후, 죽 섭취된 영양소가 흡수되고 있는 동안에는 당연히 혈액내의 당의 농도가 증가하게 되어 있다. 그러
면 췌장의 fi -cell 에서 인슈란의 합성이 증가되며 따라서 분비가 증 가된다. 그러면 지방세포가 혈액으로부터 포도당을 취해내는 속도 가 증가된다. 죽 혈중 포도당이 지방세포로 빨리 이동되어 간다고 본다. 지방세포내로 포도당의 이동이 증가되면 지방세포내의 포도. 당이 L-a-gl y c erop h osph ate 로의 전환이 빨라지 며 따라서 거 기 에 존· 재하고 있던 유리지방산의 중성지방으로의 전환이 빨리 일어난다. 혈액내 의 인슈린양이 증가되면 반대로 cAMP 의 양이 감소되어서 , hormone sensit ive lipa se 의 활성 이 억 제 된다. 한편 혈 당량이 증가되 고 인슈란 양이 증가되 면 lip o p r ote i n lip a se (LPL) 의 생산, 분비활성이 증진되는 것으로 나타난다. 그러면 결 국 모세관 혈액내나 장내 조직세포내에 유리지방산양이 중가되며 이 지방산은 결국 지방세포내에서 중성지방합성에 이용되게 된다. 그. 래서 결과적으로 지방조칙내의 지방합성량이 증가되는 결과를 초레하게 된다. 둘째, 식사로부터 섭취된 모든 영양소가 홈수되고 난 후에도 접 차로 혈엑내 당의 농도가 감소하며 따라서 인슈린의 양도 감소된다. 그러 면 당연히 지 방세 포내 에 서 L 갔.g l y cero p hos p ha t e 합성 률 이 감소 되고 유리지방산과 재결합이 되어 형성되던 중성지방으로의 합성온 처지된다. 그러면 유리지방산은 혈류내로 들어가서 알부민과 복합 체를 이루어 신체내를 순환한다. 인슈린은 hormone sensit ive lipa se 의 활성 에 방해 효과 륜 나타 낸다. 그런데 인슈린의 혈액 내 양이 감소하면 hormone sen sit ive l ip ase 의 방해인자가 감소된 결과가 되므로 이 효소의 작용이 증가 되어 중성지방의 가수분해를 촉진시키는 결과를 초래한다. 이런 조 건하에 서는 한편 췌장으로부터 glu cag o n 의 분바 가 증가되 며 이 호 르몬 역 시 hormone sensit ive lip a se 의 활성 울 증진시 켜 준다. 한편 공복시에는 LPL 의 작용이 감소된다. 이 모든 작용이 종합 적으로 작용하여서 중성지방의 유리를 증가시키며 또한 유리지방산 을 c yt o plasm 내로 유리시켜서 알부민과 복합체를 이루는 것을 증 가시킨다.
* 참고문현 1) Sa!ans, L. B. , E. S. Horto n and E. A. H. Sim s, ]. Cli n. Inve· s. t, 50: 1005, 1971. 2) Hir s h, J. and J.L . Knit tle, Fed. Proc., 29:1516, 1970, 3) Knit tle, J. and J. Hi rs ch, Clin . Res. , 1s:323A, 1967. 4) Hir s ch, J. , J. L. Knit tle and L. B. Salans, ]. Cli n. Invest. , 45 : 1023 A, 1966. 5) Bj or nste i n , I. and L. Sjo s tr o m, Meta b oli sm , 20 : 703, 1971 . 6) Wi lliam Bloom, Don. W. Fawcett , A Textb o ok of Hi st o l og y, W. B. Saunders comp an y , p.1 66, 1969. 7) Ruth , L. Pik e , My rt l e , L. Brown, Nutr i t i(Jn Inte r gr ate d APP· roach 2nd Ed. , p. 708, 1975.
s) Fawcett , D. W. , The cell, Its orga nells and Inclusio n s, W. B. Saunders comp an y , Phil ad elph ia , 1966. 9) Galto n , D. J. , The Human Adip o se cell: A Model for Errors in Meta b olic Reg u lati on , Ap ple to n -Cent u ry- C roft s N. Y. , 1971 . 10) Deuto n, R. M. and P. J. Ra ud le, Natu re(London), 208:488, 1965. 11 ) Evans, J. R. , L. A. Op ie & J. C. Ship p, Am. ]. Phy si o l . , 205 : 766 I 1963. 12) Neely, J. R. & H. E. Morga n , Ann. Rev. Phy si o l . , 36:413, 1974. 13) Ne el y, J. R. , R. H. Bowman & H. E. Morge n , Am. J. Phys i o l . , 216:408, 1969. 14) Ship p, J. C. , L. H. Op ie and D. Chil lon er, Natu re (London) , 189 : 1018, 1961 . 15) Fis h er, E. H. , L. H. G. Heil m ey e r and R. J. Hoschke, Current Top . Cell Reg u l., 4:2ll,1971 . 16) Khoo, J. C. & D. Ste i n b erg, ]. Lipid Res. , 15:602, 1974. 17) Korn, E.D., ].Bi ol Chem., 215:1, 1955. 18) Korn, E. D. , J. Bi ol . Chem. , 215 : 15, 1955. 19) Krauss, R. M. , R. I. Levy and D. S. Fredric k son, ]. Cl in. Invest. , 54: 1101, 1974. 20) Grete n , H. , R. I. Levy and D. S. Fredric k son, ]. Lip id R es. , 10 : 326, 1969. 21) Bia l e, Y. , E. Shafr ir, Clin . Xhim . Acta , 23:413, 1969. 22) Vog el , W. C. , L. Zie v e, ]. Lipid Acta , 23:413, 1964. 23) Vog el , W. C. , E. L. Bie r man. ]. Lip id Res. , 8:46, 1967. 24) LaRosa, J. C . , R. I. Levy , H. G. Wi nd mueller and D. S. Fredric · kson, J. Lipid Res. , 13 : 356, 1972. 25) Fie l din g , C. J. , Bi oc him . Bi op h s. Acta , 280: 569, 1972. 26) Krauss, R. M. , H. G. Wi nd mueller, R. I. Levy and D. S. Fredric • kson, J. Lip id Res. , 14 : 286, 1973. 27) Assmann, G. , R. M. Krauss, D. S. Fredric k son and R. I. Levy , ]. Bi ol . Chem. , 248: 1992, 1973. 28) Krauss, R. M. , G. Assmann, H. G. Wi nd mueller, D. S. Fredric - kson and R. I. Levy , Ci rcu lati on , 48:Sup pl. IV. i12 (Abstr ), 1973.
29) Assmann, G. , R. M. Krauss, D. S. Fredric k son an d R. I. Le vy , ]. Bi ol . Chem. , 248:71 8 4 , 1973. 30) Sil v a, M. E. , C. D. De et ri c h , ]. Bi ol . Che m . , 17: 6841 , 1975. 31) Eng e lberg, H. , Hep a rin meta b oli sm , Phy s io l og y and clin ic a l ap p licat i on s, sp ing field II , Thoma s, 196 3. 32) Fis c her, A. , Bi oc he m . 2, 278:13 3, 1935. 33) Fis c her, A. , Bi o che m. 2, 278: 326, 1935. 34) Jac g u es, L. B. , Bi oc lze m . ]. , 37 : 189 , 194 3. 35) Eng e lberg, H. , Fed. Proc. , 36 : 70, 197 i. 36) Astr u p , F., Acta . ph armacol. Toxic o l., 3:1 6 5 ,1947 . 37) Eng e lberg, H. , A. Dudley , L. Freeman, ]. Lab. Clin . Med. , 46: 65 3 , 1 9SS. 38) Eng e lberg, H. , Ci rcu lati on , 23 : 578 , 1961 . 39) Big gs , R. , A. A. Doug la s, R. G. Macfa r lane, ]. Plzy s io l . (London), 122: SS4, 1953. 40) Yi n, E. T. , S. Wesslor, Bi oc lzi m . Bi op lz y s. , 201 : 387, 1970. 41) Hernell, 0. , T. Eg e lrud, T. Oliv e crona, Bi oc lt im. Bi op lz y s. Ac - ta, 381 : 233, 1975. 42)Shore, B. , V. G. Shore, Am. ]. Phy si o l. , 201 : 915, 1961 . 43) Havel, R. J. , C. J. Fie l din g , T. Ol ive crona, V. G. Shore, P. E. Fie l din g and T. Eg e lrud, Bi oc lt em . , 12 : 1s2s, 1973. 44) Oliv e crona, T. , G. Be ng so n, Fe d. Proc. , 36:60, 1977. 45) Scow, R. 0. , E. J. Blanchett e- M ackie and L. C. Smi th, Ci rc. Re s. , 39 : 149, 1976. 46) Eis e nberg, S. , D. Rachmi lew i tz, ]. Li p i d Res. , 16 : 341, 1975. 47) Mj ps , 0. D. , 0. Faerge man, R. L. Hami lton , R. J. Havel, J. Clin . Invest. , 56:603, 1975. 48) Higgins , J. M. , C. J. Fie l din g , Bi oc hem. , 14: 2288, 1975. 49) Bezman, A. , J. M. Felts , R. J. Havel, ]. Lip id Res. , 3 : 42 7, 1962. SO) Brown, W. V. , W. Shaw, M. Bag ins ky , J. Bobe rg , J. Aug u s- tin, Lipa ses and Lip o p r ote i n s ~, In: Lip op r ote i n Meta b oli sm , Hei- delberg: S p r in g e r-Verlag, p. 2, 1975.
51) Grete n , H. , B. Walte r, W. V. Brown, FEBS Lett . , 27:306, 1972. 52) Wait e, M. , P. Sis s on, ]. Bi ol . Chem. , 248:7201, 1973. 53) Noel, S. P. , P. J. Dolph in , D. Rubenste i n , Bi oc hem. Bi op hy s. Res. Commun. , 63:764 , 1975. 54) Redg ra v e, T. G. , ]. Cl in. Invest. , 49 :465, 1975. 55) Schotz , M. C. , B. Arnesjo , T. Oliv e crona, Bi o chim . Bi op h y s. Acta , 125 : 485, 1966. 56) Cleg g, R. A. , Bi oc him . Bi op h y s. Acta , 664: 397, 1981. 57) Kre.r ne r, P. M. , Bi oc he m . , 10 : 143 7 , 1971 58) Kr 때 mer, P. M. , Bi oc he m . , IO: 144 5 , 1971. 59) Fie l din g , C. J. , J. M. Hig gins , Bi o chem. , 13: 43 24, 1974. 60) Anfi ns en, C. B. , T. W. Qu ig le y , Ci rcu lati on , 8 :435, 1953. 61 ) Ro bin so n, D. S. , Adv. Lipid Res. , 1 : 133, 1963. 62) Fie lr lin g , P. E. , V. G. Shore, C. J. Fie l din g , Bi oc hem. , 13:4318, 197 4. 63) Robin s on, D. S. , D. R. Wi ng , Adip o se tissu e Reg 11 /at ion and me· tab olir fun cti on s, edit ed by B. Jea nrenaud and D. Hep p. , New York:A c ademi c, p. 41, 197 0. 64) Ste w art, J. E. , M. C. Schotz , ]. Bi ol . Chem. , 246: 5749, 1971. 65) Fie l din g ,, C. J. , R. J. Havel, Arch. Path o l. Lab. Med. , 101 : 225. 1977. 66) Andre Bensadoun, Chris t i an Ehnholm, Danie l Ste i n berg, W. Vi - rg il Brown, ]. Bi ol . Chem. , 249 : 2220, 197 4. 67) A·M Ostl un d Lin d q u is t , P. H. Iveriu s , Bi o chem. Bi op h y s. Re . Commum. , 65 : 1447, 1975. 68) Gansen, & Bass, FEBS lett er s, 53 : 1, 1975. 69) Ste w art and Schotz , ]. Bi o l. Chem. , 249:904, 1974 70) Fie l din g , P. E. et al, Bi oc lzem. , 16 : 1896, 1977. 71) Hallenberg, C. H. , Am. ]. Plzy si o /. , 197: 66 7, 1959. 72) Arlenes Garfi nk el, Pete r Ni lss on·Ehlf, Mi ch ael C. Schotz , Bi - och im. Bi op lzy s. Acta , 424: 264 , 197 6. 73) Pokraja c , N. , Lossow, W. J. , Chaik o ff , I. L. , Bi oc him . Bi op h y s. Acta , 139 : 123, 1969.
74) Ste w art, J. E. , Whelan, C. F. , Schotz , M. C, , Bi o chem. Bi op - hys . Res. Commun. , 34:376, 1969. 75) Ste w art, J. E. , Schotz , M. C, , ]. Bi ol . Chem. , 246 : 5749, 1971 . 76) Ballard, Hanson, ]. Lip id Res. , 8 : 736, 1967. 77) Danie l Ste i n berg, Joh n C. Khoo, Fed. Proc. , 36 : 1986, 1977. 78) Fin e , M. B. , R. E. Wi lliam , Am. ]. Phy si o l . , 199:403, 1960. 79) Havel, R. J. , J, P. Kane, E. V. Balasse, N. Seg a l and L. V. Ba• sso, ]. Cli n. Invest. , 49 : 2017, 1970. 80) Ste i n b erg, D. , meta b olis m , 13 : 1264 , 1 964. 81) Feig e lson, E. B. , W. W. Pfa ff, A. Karmen an d D. Ste i n b erg, ]. Clin . Invest. , 40:2171, 1961. 82) Khoo. J. C. , D. Ste i n b erg, J. J. Huang and P. R. Vag e los, ]. 8- io clzem. , 251 : 2882, 1976. 83) Ste i n b erg, D. , S. E. May e r, J. C. Khoo, E. A. Mi ller , R. E. Mi - lier , B. Fredholm, R. E. Eic h ner, Advance in cyc l ic Nucleot· id e Research, Edit ed by G, I. Drummond, P. Greeng a rd & G. A. Robin s on, New York Raven, Vol. 5. , p. 549, 1975. 84) Heald, P. J. , P. M. McLachlan and K. A. Boodkedg e, J. Endo-cri ·no l, 33 : 83, 1965. 85) Lang sl ow, D. R. , E. J. Butl e r, C. N. Hales and A, W. Pearson, ]. Endocrin ol. , 46 : 243, 1970. 86) Ste i n b erg, D, M. Vang h an, P. J. Neste l , 0, Str a ud, S. Bergs t - ron, ]. Cl in. Invest. , 43 : 1533, 1964. 87) Tay lo r, S. S. , C. Y. Lee, L. Swain , P. H. Sta f f or d, Anal. Bi o- chem. , 76:45, 1976. 88) Huff um en, J. K. , A. A. Aq ui n o , D. Ste i n b erg, Bi oc him . Bi op - hys . , Acta , 224:295, 1970. 89) Khoo, J. C. , A. A. Aq u in o , D. Ste i n berg, ]. Cli n. Invest. , 53 : 1124, 1974. 90) Khoo, J. C. , D. Ste in b erg, B. Thomp so n, S. E. May e r, ]. Bi- ol. Chem. , 248:3823, 1973. 91) Sid d le, K. , C. N. Hales, Proc. Nutr . Soc. , 34:233, 1975. 92) Robin s on, G. A. , Butc her, R. W. , Suth erland, E, W. , cyc l ic
AMP, ch. 6, p, 146 , ch. 8, p, 286, Academi c Press, 1971, 93) Lote n , E. G. , Suey d, J. G, T. , Bi oc he m . 2, 120 : 187, 197 0, 94 ) Schonhofe r , P. S. , Skid w are, I. F. , Kris h na, G, , Hormone Met· ab, Res. , 4:44 7 , 1972. 95) Mang an ie l lo, V. , Vang h an, M. , J. Bi ol . Chem. , 248:7 16 4 , 1973. 96) Sakai, T, , Thomp so n, W, J. , Lav is , V. K. , W illiam s, R. H. , Archs. Bi oi :h e m . Bi op h y s, , 162 : 331, 197 4. 97) Zin m a n, B. , Hollenberg, C. H. , ]. Bi ol . Chem. , 249:2182, 197 4. 98) Rodhcll, M. , Lin, M. C, , Salomon, Y. , Londos, C. , Harwood, J. P . , Marti n, B. R. , Reudell, M. , & Be rm nn, M. , Acta . Endoc. Cop e1 1 h. , 11: 11. , Sup pl. , 191 : 11, 1974. 99) Sie g el , M. J. , Cua tr e ca sas, P. , Mol. Cell. Endocr. , 1 : 89, 1974. 100) Pawlson, L. G. , Love ll ·Smi th, C. J. Mang a nie l lo, V. C. , Vang · han, M. , Proc. N11t r. Acad. Sci. U. S. A. , 71, 1639, 1974. 101) Fain , J. N. , Poin t e r , R. H. Ward, W. F, , J. Bi ol . Chem. , 247: 6686, 1972. 102) Ho, R. J. , Russell, T. and Asakawa, T. , Meta b oli sm , 24: 257, 1975, 103) Ho, R. J. , Sut h erland, E. W. , J. Bi o l. Chem. , 246:6822, 1971. 104 ) Cobin , J. D. , Co, D. Brostr o m, R. L. Alexander, and E. G. Kr· ebs, J. Bi ol . Chem. , 247 : 373 6, 1972. 105) Brostr o m, M. A. , E. M. Reim ann, D. A. Walsh, E. G. Krebs, Adv. Enzy m e Reg 11 l. , s: 191 , 1970. 106) Hut tum en, J. K. , D. Ste i n b e rg, S. E. May er , EJioc hem. Bi op lzy s. Res. Commun. , 41 : 1350, 1970. 107) Khoo, J. C. , D. Ste i n b erg, J. J. Huang , P. R. Vog el os, J. Bi ol . Chem. , 251:2882, 19i 6 . 108) Walsh, D. A. , C. D. Ashby , C. Gonzales, D. Calkin s , E. H. Fis h er, E. G. Krebs, J. Bi ol . Chem. , 246: 1977, 1971. 109) Sid d le, K. , C. N. Hales, Proc. Nutr . Soc. , 34: 233, 1975. 110) Cuatr e casas, Am. Rev. Bi o chem. , 43 : 169, 1974. 111) Sp ec to r , A, , Prog r . Baio chem. Pharmcol. , 6:130, 1971.
제 3 장 간에서의 지방대사 1 간의 구조와 간세포 간의 구조물 보면 다음 그림 에 서 보여 주듯이 lobus hep a ti s d exte r 와 left hep a ti c sin i s t e r 인 두 부분으로 이 루어 져 있 다. 이 두 부분 은 오른쪽과 왼쪽의 hep a ti c duc t로 연결이 되며 이 두 duc t는 common hep a ti c duct 로 합찬다. common hep a ti c duct 에 cys t i c duct 로써 ga llbladder 로 연 결 이 되 며 common duct 는 bil e duct 로 연결되어서 십이지장으로 연결된다. bil e duc t가 십이지장으로 연 결 되 는 부위 를 amp u lla of bil e duct 라고 하며 이 곳은 pa ncreati c duc t와 b il e . duc t가 한 데로 연결된 분위이다(그립 1,2 참조). 간의 구조는 간세포 (he p a t oc yt e) 의 다양한 기능에 의해서 이루어 진다. 개개의 세포는 외각막(p lasma membrane) 으로 구분지어지며 이 외 각 membrane 의 한 면온 sin u soid s 에 면해 있 으면서 정 맥 과 동백 을 모두 받는다. 그리 고 다론 한 면은 담줍 canalic u li 에 접 해 있으면서 간세포에 의해서 합성되는 담줍의 수집과 상호 교류를 한 다. 그러므로세포자체는한쪽은혈액과, 다론한쪽은 b il e 과의 사 이에서 좁은 벽을 형성하게 된다. 간의 구조는 그림 1 에서 보듯이 세포 하나 두께로 세포가 나열된 세 포벽 사이 사이 에 bil e canali cu li 와 sin u soid 가 존재 한다. 이 들 의 세포가 나열된 줄기는 대개 커브로 둥글게 구부러져서 서로 사
방에 뻗쳐 있지만 일정한 중심부로 모이게 되어 있다. blood sin u soid 에는 b i le 을 제외한 개개의 간세포가 합성한 합성산물이 모두 배달 되 며 , 담줍은 bil e canalic u li 로 배 달이 된다. 그러 므로 간세 포와 혈액 그리 고 담즙을 함유한 exocrin e duct 사이 에 밀접 한 왕래 가 있다• 이러한 방법에 의해서 하나의 장기로서의 간은 인체의 요구 에 빠르게 대응할 수 있다. 간으로 들어오는 전체 혈액 중에서 65~75% 는 문맥정맥(p or t al
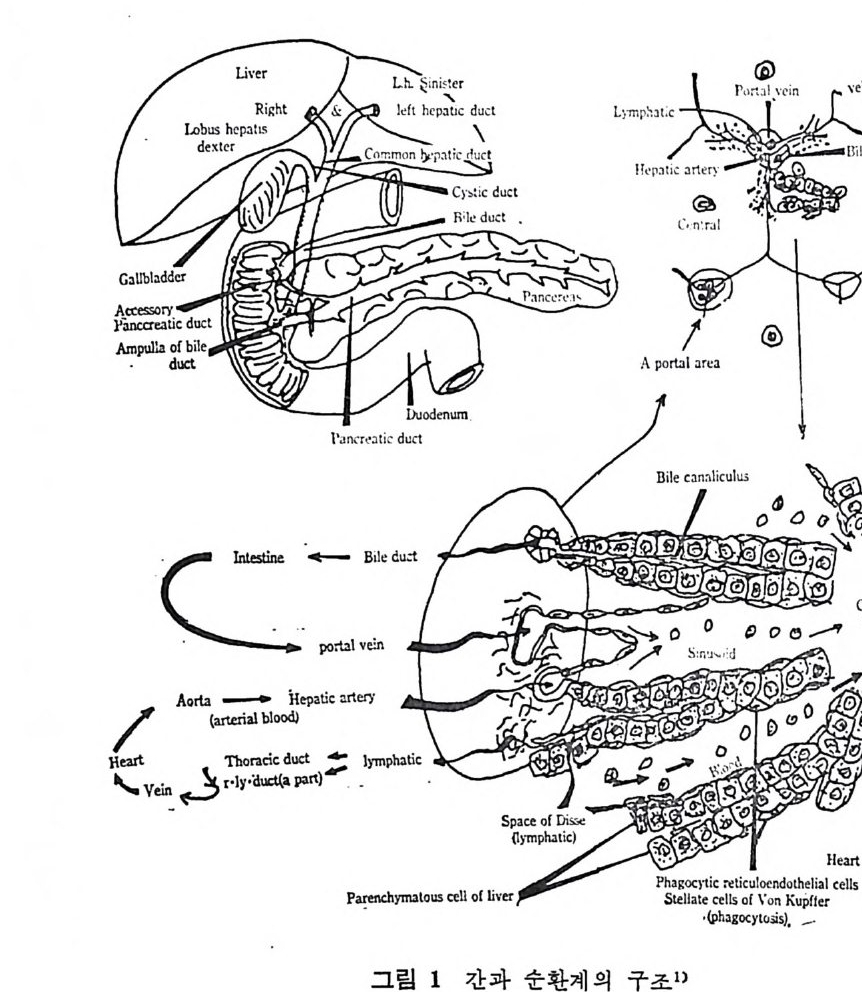 I ®
I ®
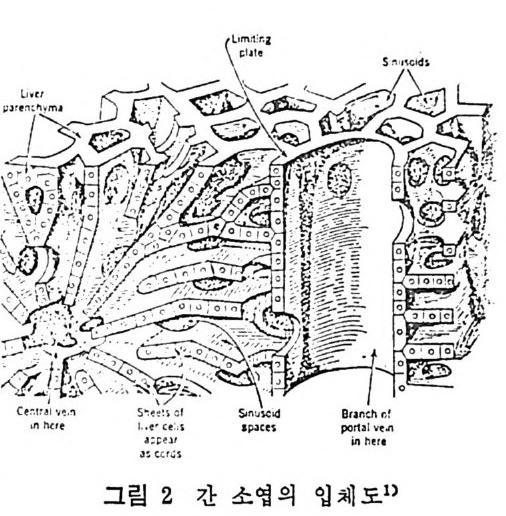 \L';;;' g따
\L';;;' g따
ve i n) 을 동해서 오는 것 으로 그 속에 소장으로 부터 흡수된 모든 영양소가 촌재한다. 그리고 나머지 25~35% 의 혈액 온 간동맥을 통해서 둘어오는 것이다. 여기에 논 소장으로부터 림프를 통해서 흡 수된 영양소가 동맥을 통 해서 간에 도착되는 것이다• 그러므로 liv e r sin u soid 는 자동적으로 동백혈을 가쳐
오드로 결과적으로 소장에서 홉수되는 모든 영양소를 간세포로 가 쳐오게 된다. 2 간과 지방대사 간은 포유동물의 치방대사에서 중추적인 역할을 하고 있다. 또한· 간은 신체내 다른 조직에서와 마찬가지로 혈액으로부터 취해진 지 방산이 에너지로 사용되기 위해서 물과 CO2 로 산화시키는 과정을 _ 수행하는 이외에, 독히 이 지방산을 케톤체로 전환시킬 수 있는 유』 일한 장기이다. 이 케본체는 특히 포도당의 공급이 제한된 조건하에서 간 이의의 조직내에서 에너지 공급원으로 이용된다. 또한 간은 간조직 자체 가 사용하기 위한 처장에너지 급원으로서, 또한 간제포막의 구성 성 분으로서 이 용하기 위해 서 중성 지 방과 ph osph og ly c erid e s 의 합성 을한다. 한편 간은 혈액내의 구성성분과 다론 조직의 구성성분으로 샤 용하기 위 해 서 중요한 gly c erolip id 를 lip o pr o te i n 형 태 로 수출한다-
칸은 순환하고 있 는 lipo p ro te i n 의 분해 를 위 해 서 도 주요 여 할을 하는 장기이다. 신체내의 콜레스테롤 항상성 유지를 위해 거의 전적으로 간이 그 역할을 담당하고 있다. 간은 콜레스데몰 합성의 주요 장기이며, 순 환되는 혈액 콜레스데를의 농도조철을 위한 주요 역할이 있다. 그 러므로 간은 콜레스테롤을 유리된 형태 또는 콜레스테롤 es t er 형대 로서 l ip o p ro t e i n 의 구성성분으로 하여 순환계에 배설하는 장기이 다. 또한 간은콜레스테롤을 담즙산으로전환시키는 유일한 신체 장 기 이 다. 그래 서 간은 이 담즙산과 함께 콜레 스테 몰과 ph osp h ati dy l- ,ch olin e 이 함께 담즙으로 분비 되 며 따라서 식 이 지 방 흡수 를 돕는 역할을 한다. 이와같이 간이 치방의 신체내 대사에 중추적인 역할을 하고 있음 은 자명한 사실이다. 그러므로 여러가지의 조철대사와 대사과정 (pa t hwa y)에 관련된 연구가 간을 중심으로 이루어지고 있다. 그렇 다고 이러한 조철대사나 대사과정이 다른 조직에서 일어나지 않는 것은 아니다. 그러므로 본 장에서는 간을 중십으로 중성지방 대사 와 지 방축적 , 케 돈체 합성 작용 (ke t o g enes i s) 과 콜레 스테 몰 대 사 및 .lipo p ro te i n 대사에 관련하여서 논하고자 한다. (1) gly c erid e 대 사에 있 어 서 의 간의 역 할 포유동물에 있어서 혈액내에서 순환하고 있는 지방과 관련된 물 질은 3 가지가 있다. 첫째는 유리지방산이고 둘째는 중성지방이며 마지막으로 케돈체이다. 간은 유리지방산을 이용하고 중성지방, 케 본체를 분비한다. 간세 포내 에 서 는 탄수화물과 아마 노산울 함유한 대 사 po ol 이 acety l CoA 로 전환되어 지방산으로 전환된다 (de novo 지방산 합성). 그러 나 이 과정의 반대과정은 일어나지 않는다. 모든 급원으로부터 전 환된 지 방산은 분해되 거 나 중성 지 방으로 또는 다론 형 태 의 gly c erid e 로 전환되어 그대로 자신이 이들을 이용하거나 간 밖으로 수출해 내보내기도한다.
간장내에서의 지방대사를 살펴보면 여러가지 다양한 경우의 생리 져 또는 병리적 상태에서 대사과정이 변화한다. 예로써 당뇨병과 다론 내분비장애, 혈관계통 질병, 신영, 영양불량, 소모성질환, 비 만증, 선천성질환, 간질환의 경우 등을 들 수 있다. 이러한 병리적 안 조건하에서는 g l y cer i de 의 체내 대사도 병리상태에서 이루어전 다는 것은 자명한 사실이나 이 경우 지방의 대사기전에 대해서도 거의 아는 바가 없으므로 이런 경우, 간장내의 정상 조건하에서 이 루어지는 지방대사 기전에 기초를두고설명을할 수밖에 없는 실정 이다. (2) 간내 gly c erid e 합성 과 간세 포로부터 의 이 탈경 로 간장내로 이동되는 지방은 크게 두 가지 경로를 거쳐 온다• 첫째 지 방세 포로부터 유출되 어 나온 지 방산과 둘째 chy lo mi cr on 나머 지 (remnant) 에 함유된 중성 지 방이 다. 또한 de novo 합성 에 의 해 서 생 성 된 지 방산의 공급도 가능하다. 간장내 의 지 방 (gly c e rid ~ ) 합성 은 gly c olys is , glu coneog en esis 또 는 혈액 내 글리 세 몰 로 공급되 어 전 활성 화된 글리 세 를의 Sn-gl y c erol 3-p h o sph a te 형 태 와 acety l CoA 와 더 불어 활성 화된 long chain 지 방산의 결합으로 생성된다. 다음의 그림은 간세포내에서의 gly c erid e 합성과 이로부터의 지방 의 이탈경로를 도해한 것이다(그림 3 참 조). Acy l CoA 형태로 활성화된 지방산은 간세포내에서 de novo 합성 에 의해서 공급되거나 또는 유리지방산으로부터 공급된다. 이때 유 리지방산은 혈청내에서 이동되는 단백질로부터 공급되거나 4 ) 또는 간세포내에서 지방분해에 의해서 공급된다. 간에 서 gly c erid e -fa tty acid 가 de novo 합성 되 는 데 에 는 여 러 종류의 선행물질아 관계된다. 사람에게서는 이들 선행물질의 목칭 이나 지방산의 de novo 합성관계가 분명히 확립되어 있지 않다. 그러나 동물실험에서 나타난 결과는 mouse 의 경우 글리코겐이나 유산(l ac t a t e) 도 gly c erid e 의 단소 급원으로 사용되 나 포도당은 이
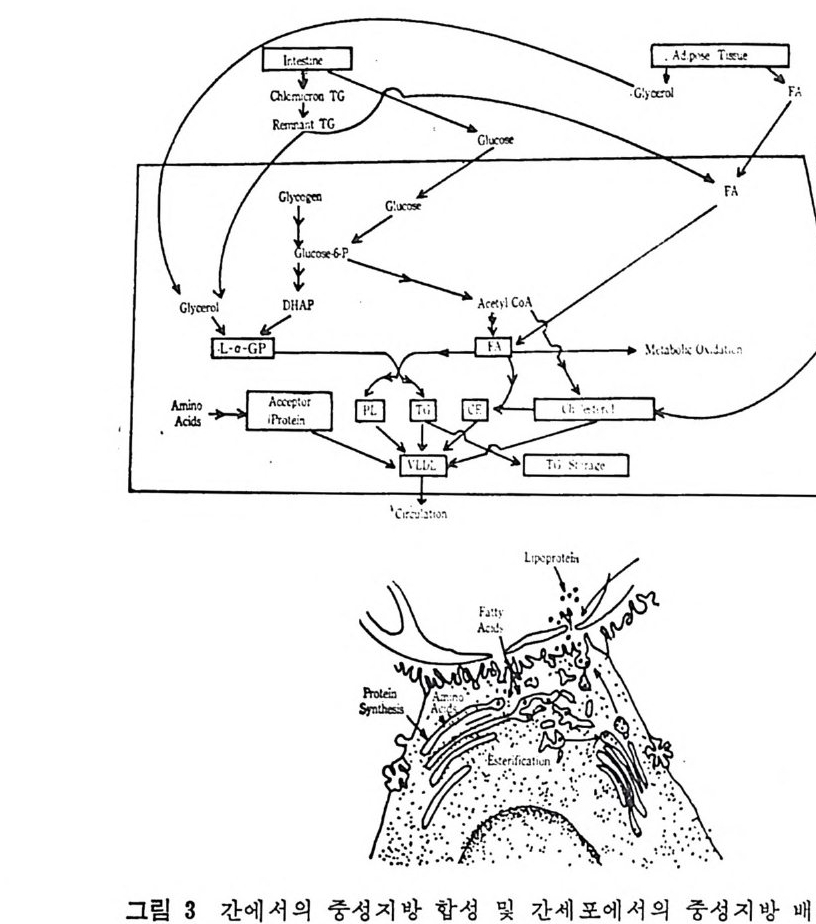 CIy ~. Lf ·G P l DI노t \ /~ 、, 1A ft d \ 'I 1- 、 . \:,:. ,!..I, U 나: .• ,
CIy ~. Lf ·G P l DI노t \ /~ 、, 1A ft d \ 'I 1- 、 . \:,:. ,!..I, U 나: .• ,
접에서 관련된 선행물질의 증거가 없는 것으로 pe rfu s ed live r5l 살 험에서나 in viv o 6l 실험에서 밝혀졌다. Mi toc hondria 밖에 서 de novo 합성 에 의 해 생 성 된 주요 지 방산 온 팔미틴산과 스테아린산의 A 형태이며” 이들은 곧 다른 종류의 지방산 acy l CoA 로 전환될 수 있다. 새로이 합성된 지방산은 간세포내에서 인지방과 함께 중성지방 구 합성에 주로 융합된다. 여러가지 경로를 통해서 8) 새로이 합성되는 지방산에 융합된 수소는 주로 NADPH 로 환원형태의 운반체에서 공급된다.
탄수화물 함량이 높은 식사 후라돈처 9) 비만한 m i ce 의 경우와 같 이 10) 지 방산의 합성 이 증가될 때 는 유리 된 NADP + 와 NADPH 의 비례도 증가한다• 포도당, 유산과 아마도 굴리코겐까지도 모두 지방합성작용을 자 국한다고 생 각한다. 이 들의 지 방합성 자국은 탄소의 공급원과는· 무 관하 게 5) 자국하는 것 으로 생 각되 며 오히 려 NADP + 와 NADPH 의 비례 변형 으로 기인된다고 본다. Glyc erid e 합성 에 있 어 서 중추적 인 역 할을 하는 효소는 . acy lt r a n- s fe ra se 로서 이는 기질 선택에 있어서 복잡함을 나타내며 또한 여 러가지 영향 을 미치는 인자에 대해서 반응하여서 11 - 7) 결과적으로 간 내의 g l y cer i de 형 대 조철에 매우 중요한 역할울 하게 된다. 예를 들 어서 옹레인산이 중성지방에 융합되고 다른 지방산에 이 어서 보다 먼저 독정한 경로를 동해서 융합되는 것이 보고되었 다. 18 9J Phosph ata s e 에 의 한 ph osp h ati di c acid 의 가수분해는 또한 중성 지방과 인 지방 생산에 결정적인 전환접이 되며 간에서 지방생 성을의 조철시에 이루어진다 . 20 ) 예를 들어 인지방 합성 때 영기이 동이 마지막 과정이라고 한다 . 2 1) 주 요 지 방산을 활성 화시 키 는 효소는 endop la smi c reti cu lum 과 mi toc hondria l 최 의 각 membrane 에 존재 하면서 22-4) 지 방산 대 사 울에는 일반적으로 영향을 미치지 않는다 .25) 그러므로 지방산 acy l CoA 가 gly c erid e 에 웅합되 기 위 해 서 이 에 관련된 물질은 mi toc hon- dria 밖에 촌재 한다. 결과적 으로 지 방산의 mi toc hondria 내 로의 이 동은 적 어 도 2 종류의 효소로 구성 되 어 있 다. 26) Carnit ine acy l- tra nsfe r ase 계 통에 의 해 서 이 루어 진다. 이 계 통의 효소들이 gly c - - er i de 의 간내 대사에 있어서 주요 조철작용울 한다 .27-8) 이계통 효 소의 방해 물질 인 ( +) decanoy l carnit ine 은 굶거 나 당뇨병 이 있 는 동물의 간으로부터 케 본체 합성 을 방해 하며 29) gly c erid e 합성 속도가 저조되었을 때 다시 정상으로 복원시킨다. 그러나 간에서 carnit ine 과는 독립 적 으로 지 방산울 산화할 수 있 다고 한다. 30) 그러 나 mi to- ,·ch ondria 자체 가 gly c erid e 합성 을 할 수 있 으며 특히 인지 방울 합성 히는 효소를 모두 소유했다고 한다. 31-2) 그러 나 mi toc hondr ia 밖
에 촌재 하는 합성 체 계 가 보다 광범 위 하 며 24' mi toc hondria 내 로 gly cerid e 몰 공급한다. 33) 사슬이 긴 지 방산의 acy l CoA 가 특정 한 gly c erid e 나 중 성 지 방 으로의 영 합은 주로 mi toc hondria 밖에 서 , 특 히 mi cr osomal enzy m e 에 의해서 이루어진다. 그런데 지 방산합 성을 위한 합 성 효소 (s y n• th eta s e) 복합체 는 subcellular 용 출 상동용액 에 나 타난 다. 이의에도 여러 종 류의 간 지 방이 존 재 하는데 그 중 에 서 주 요 한 것 온 floa ti ng fat, 34' mi cr osomal lipid, me m brane lip ids 그리 고 간 밖으로 이 동되 어 나가 기 위 해 기 다리 는 lip o p ro te i n 이 있 다. 이 들 지방은 여러 종류의 구조로 촌재하며 35) 그 기능은 분 명히 알 려 져 있지 않다. 간은 혈청 lip o p ro te i n -g l y c er i d e 의 공급 을 위한 주 요 장기 이 다. 그러나 간이 l ip o p ro t e i n 의 합 성 분해, 상호전 환 작용에 관련된 주요 역 할은 대 단히 복잡하다. 36 ) 간은 주로 간내의 지방을 간 밖으로 이동시 킬 때 VLDL 의 형태 로 한다. 간으로부터 유출되어 나가는 VLDL 은 혈 액내의 지 방산 구성 에 영 향을 미 찬다• 37 -9> VLDL 의 대 부분은 주로 go lgi comp le x 내 에 서 형 성 된다고 본다. 40> endop la smi c reti cu lum 에 서 합 성 된 성 숙된 gly c erid e 가 go lgi comp le x 로 가서 거 기 에 서 VLDL 형 성 에 이용된다. Bil ia r y gly c erid e s 의 주요 형 태 는 인치 방이 며 이 는 주로 endop l- asmi c reti cu lum 에 서 합성 된다• 41 ) 이 용가능한 ap o lip o p r ote i n 의 간내 함유량이 l ip o p ro t e i n 의 간으로부터의 유출에 커다란 영향 을 마 친다. 인지방과 중성지방이 구의 형태로 간으로부터 수출되어 나가며 이 지 방구에 함유된 지 방산으로부터 혈청 내 lip o pr o te i n 의 지 방산 공 급에 공헌울 한다. 42) 고도의 불포화지 방산이 VLDL 수출에 관련되 어 있다 .43) 1) 간세포내에서의 지방산파 gl yc erid e 사이의 상호관계 지방내에는 다양한 종류의 지방산이 존재하면서 지방의 기능수행
에 큰 여할을 한다. 마치도 단백질내의 아마노산과 같은 경우라고 생각한다. 간내에서는 지방산이 광범위하게 상호전환을 한다. 죽 지방산의 킬아연장이 그 예이다 .44 - 5) 지 방산의 길이 연장은 mi toc hondria 내 에 서 나 45 - 7> mi toc hondri:: . 밖에 서 나 4 6) 지 방산합성 효소들인 fatty acid sy n t h eta s e 복합체 의 일 반적인 한 바퀴작용과 관련이 있으며 이 작용은 기아상태에서 더욱 소 현저 해 진다 . '19> M itoc hondria 밖에 서 진행 되 는 작용이 불포화지 방산 의 여러 종류 사이의 전환에 주 요 역할을 한다. 지방산의 불포화작용은 널리 퍼져 있으며 비교적 복잡한 작용이 다 .50) 이 작용은 적어도 2 가지의 주요한 작용에 의해서 이루어진 다. 첫째로 포화지방산 acy l CoA 와 결합되어서 6. 9 에 c i s 형태의 불포화결합을 삽입하는 것과 둘째로 이미 6. 9 에 cis 불포화결합이 있는 지방산의 acy l CoA 는 6. 6 에 cis 불포화결합을 삽입하는 것 이다. 6. 9 - 불포화 효소는 pa lmi tyl 과 ste a ryl CoA 복합체 가 기 질로 사 용된다. 이 작용에 관여 하는 효 소는 cy toc hrome b 5 와 이 의 환원효 소 (reduc t ase) 와 산화효소 (ox i dase) 이 다. 51- 2 ) 즉 이 들의 산화환원 효 소가 유리 되 었 으며 53) 이 들의 조절작용이 었 음이 밝혀 졌 다. 54) 6_ 6- 불 포화효소도 고도의 불포화지 방산 사이 에 서 의 상호전환에 관여 한 다. 포유동물에 있어서는 단일불포화와 이중 불포화 사이의 상호전 환이 나 6_ 3 6_ 12 6_ 15 나 기 타 다른 위 치 의 불포호呂근 나타나지 않는다. 불포화작 용효소들은 diu r nal rhy thm 을 나타내 며 55) 기 아 대 나, 54) 56- 9) 당뇨병 때 에 감소된다. 60-1) 6_ 9- 불포화효소( 6. 9-desa t ura tr ase) 는 지 방산합성 효소 (FA s y n t he t ase) 와 같이 작용한다. 간장내 acy lg l y c erols 와 인지 방 사이 에 서 는 폭넓 은 상호전환이 이 루어 진다. 그러 므로 간에는 중성지 방 62) 과 인지 방 63) 을 분해 시 킬 수 있는 효소인 ly a ses 가 존재 한다고 본다. 간2) 세간포세에 포 로의부해서터 의합 성gl된 y c e중rid성 e 지 이방 탈은조 절lip o p rot e i n 복합체로서 혈청
내로 이동된다. 주로 VLDL 의 형대로 이동된다• 간세포내의 중성 지방에 함유된 지방산은 곧 VLDL 내로 이동되어서 존재하게 되며 VLDL 내의 중성지방의 선행물질이 된다 •64) 반대로 간세포내의 중 성지방은 혈청내 유리지방산이 중성지방합성에 이용되어서 간내로 이동되든가 또는 간세포내에서 합성된 건사슬 지방산으로부더 합 성된다. VLDL 내에는 중성지방, 인지방, 콜레스테롤 _ es t ers, 유리 콜레 스테 롤과 독정 한 ap o lip o p ro te i n 이 함유되 어 있 기 때 문에 이 . 를 형성하려면 많은 주요 대사과정이 이루어져야 한다. 그러므로 VLDL 을 형성하기 위한 대사과정중에 참정적이지만 조철기전이 있 음을 알 수 있다. 이것이 바로 VLDL 생산을 조전하게 된다. 간으로부터 VLDL 에 의 한 중성 치 방의 분비 가 증가되 면 smooth endop la smi c reti cu lum 에 위 치 한 작은 선행 물질 po ol 에 서 중성 지 방합성이 중가되는 결과를 가져온다. pe rfu s ed 간실험에서 보여준 바 에 의하면, VLDL 내에 있는 중성지방에 결합된 굴리세롤 지방산에 동위원소로 처리하여서 관찰한 결과 VLDL 내의 중성지방의 치방 산은 작은 유리지방산 p ool 에서 온 유리지방산으로 70% 가 점유되 어 있고 나머지 10% 는 fl oa ti ng - fat으로 온 유리지방산이 접유하고 있음이 나타났다 .65) 이 결과로 VLDL 내의 중성지방 선행물질은 오 히 려 floa ti ng fat 와 같은 크기 가 큰 po ol 의 지 방산보다는 크기 가 착은 p ool 의 유리지방산으로 생각할 수 있다(그립 4 참조). 14C 동위원소로 처리된 유리지방산인 olea t e 의 대사를 혈청내에 서 실험동물 쥐를 찰 먹였을 때와 굵겼을 때를 비교하였다 .67 8) 중 성 지 방의 분비 는 유리 지 방산의 농도가 증가함에 따라서 중가한다고 한다. 이 현상은 유리지방산의 에스텔화와 이들이 산화되어서 CO2 로 되는 것과 케돈체형성과 관련이 되어 있다. 유리지방산이 일정 한 농도에서는 찰 먹인 실험동물의 간은 굶간 동물의 간에서보다 지방산을 소량 산화시키고 에스텔화는 활발히 하며 VLDL 로 유리 된 지방산의 간 밖으로에의 수출량이 많아진다. 유리지방산을 소량 먹인 쥐의 간에서는 대부분의 섭취된 유리지방 산이 간으로 옮겨져서 에스텔화 되어서 VLDL 내의 중성지방으로 써 수출된다. 여하돈 유리지방산의 농도가 증가되면 산화되는 양이
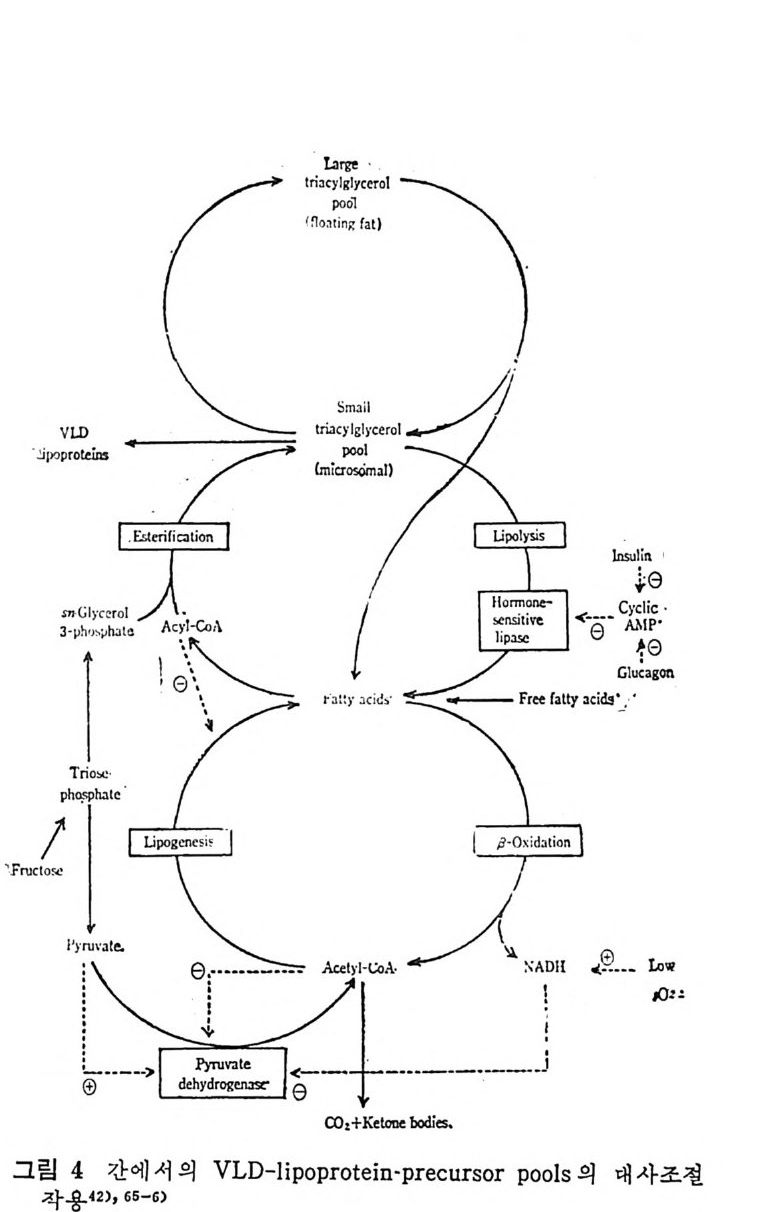 vw (.g·In J\己〔던, lO쩌 二\
vw (.g·In J\己〔던, lO쩌 二\
중가되며 에스텔화되는 양이 감소한다. 그러나 에스텔화된 전체양 은 증가된 셈이다. 그러나 굶긴 실험동물 쥐의 간에서는 에스텔 화되는 형태가 다르다. 죽 일정량의 지방산이 들어오며 이 양과는 무관하게 지방산은 산화되고 에스텔화된다.
그러나 에스텔화와 산화 사이를 조철하는 조철기전은 잘 알려처 있지 않다. 이용 가능한 Sn gly c erol 3 p hos p ha t e 양이 에스텔화를 조철하는 인자로 간주되기도 한다. 여하돈 잘 먹인 동물의 간 속 에 도 이 용 가능한 Sn - g l y cerol 급 - p hos pha t e 의 양이 많은 것 으로 지 적되었다 .67 - 8) 그래서 굶은 동물의 간에서는 찰 먹인 동물의 간에 서 이루어지는 에스텔화와 산화량을 도저히 따르지 못하는 것으로 나타났다. McGarry 둥은 29> (+) decanoy lc arnit ine 이 굶은 동물의 pe rfu s ed 간에서 간 사슬 지방산의 산화를 방지했다고 밝혔다. 그 · 래서 결과적으로 모든 지방산은 에스텔화된다고 하였다. 이 물질 은 carnit ine -p a lmi toy lt r a nsfe r ase 의 방해인자이 다. 이 신험 전과 로 굶온 취의 간도 정상량의 지방산을 에스델화시킬 수 있는 능력 이 있는 것으로 나타났다. 이 연구는 지방산의 산화 를 조절하는 것 은 carnit ine pa lmi toy lt r a nsfe r ase 라고 하였 다. 그러 나 이 접 에 대 해서는 분명한 증거가 나타나지 않았다. Vavrecka 둥은 69) 굶는 다는 것 이 acy l CoA-gl y c erol ph osph ate acy l tra nsfe ra se 의 활성 을 · 감소시키는 원인이 된다고 보고하였다. 그러나 이 효소 역시 정상 적으로 작용속도 제한 (ra t e-l i m iti n g)효소인지에 대해서는 그 중거가 없다. 유리왼 간편을 사용하여서 전혈(全血)을 통과시키면 CO2 가 13.3 k p a(lOOmmH g)에서 약 9. 3k p a(70mmH g)로 감소되지만 02 소비 량은 감소되지 않는다 .66) 이는 세포내의 산화환원 상태가 보다 더 환원상 태 로 되 었 기 때 문으로 생 각한다. 이 는 lacta t e / py ru vate 의 비 례 와 3--hy d roxy b uty ra te / aceto a ceta t e 의 비 례 를 측정 함으로써 나타난 사 실이다. 산화환원 상태가 보다 더 환원상태로 변화될수록 유리지방 산의 산화와 에스텔화 사이의 균형도 변하여서 산화되기 위한 호 조건으로 된다. 이런 상태에서는 VLDL 중성지방의 분비가 갑d:.. 되는 상태를 야기시킨다• 또한 in vit ro 연구에서 간에 혈액을 통과시켜서 CO2 를 변화시 키면 간으로부터 중성지방의 유출에 영향을 끼치게 된다. [NADHJ / [NAD 단의 비 례 가 증가되 면 pyru vate - dehy d rog e nase 가 불활성 으 로 되며 그러면 탄수화물 산화가 지방산의 에스텔화를 감소시키는-
결과가 된댜 굶간 동물과 먹인 동물의 간에서 〔 NADH J /[NAD 汀 의 비례가 변화되는 것을 에스텔화와 산화 사이의 균형의 변화로 되는 것을 비교 관찰해 보면, 먹인 동물의 간에 상당량의 지방산이 주입되었을 때 에스텔화와 산화의 비례가 변화되는 것을 관찰할 수 있다. Carboxy h emog lo bin 이 함유된 全血울 간으로 pe rfu s io n 시 키 면 0,. 소비 량과 중성지방의 배설량이 감소되고 유리지방산의 산화는 증가 되 는 것 으로 나타났다. 70) 동물이 굵은 상태 에 서 도 탄수화물의 acety l CoA 를 통한 간세 포 내의 지방 합성작용은 감소되며, 따라서 유리지방산이 VLDL 내에 존재하는 중성지방분자 내의 지방산의 주요 급원이 되고 있다. Wi nd mueller 와 Sp a eth 는 먹 인 쥐 의 pe rfu s ed 간으로부터 중성 지 방의 유리 는 지 방산합성 률과 고도로 상호관계 가 있 다고 밝혔다. 71 ) 여하튼 유리된 지방산의 농도가 증가될수록 지방합성작용(lyp o g en es i s) 은 접차로 방해를 받으며 새로이 합성된 지방산의 VLDL 의 중 성 지 방에 융합되 는 공헌은 감소된다고 한다. 72) 간에서 대사되는 간사술지방산의 종류가 그것에 의해서 형성되는 · VLDL 의 구성 성 분과 형 성 률에 영 향을 미 찬다고 본다. 73l Kohout 둥 은 pe rfu s ed 된 간에 서 중성 지 방의 배 설은 C18 지 방산의 불포화도에 따라서 감소된다고 하였고 지방산의 길이가 길어지면 증가된다고 하였다 .38) 또한 Heim berg 와 Wi llco x 는 oleate 로부터 합성 된 VLDL 은 pa lmi i:at e 로부터 합성 될 VLDL 에 비 해 서 크기 가 크며 콜레 스테 롤 과 중성지방 매 mole 당 인지방의 양이 적게 함유되어 있다고 하였 다,” 이 발견은 lip o p r ote i n 의 밀도가 <1 .0 06g /c m3 로 같지만 크 기가 큰 것이 작은 것에 비하여 혈류로부터 사라져 맑게 되는 시간 이 빠르다고 생각해 볼 수 있다. 존재하고 있는 탄수화물의 종류에 따라서 간세포로부터의 중성지 방 분비 윤이 변화한다고 본다. 과당의 주입 은 즉시로 pe rfu s ed 간으 로부터 중성지방의 분비를 증가시키며 65) 서당 (sucrese) 을 먹인 동 물의 간은 서서히 중성지방의 분비를 증가시키는 방향으로 적응하-
고 있는 것으로 나타났다 .74) 이상의 결과는 과당이 존재하면 혈청 내 유리지방산의 산화는 적어지고 많은 양이 에스낼화되어서 VLDL 에 융합되는 울이 높아진다고 볼 수 있다. Alloxan-dia b eti c 쥐 의 pe rfu s ed 된 간으로부터 중성 지 방의 분비 는 억제되었다고 보고하였다 .75) 찰 먹인 쥐의 간에 인슈란이 과량 함 유된 혈액을 p er fu sed 시키면 VLDL 에 함유된 중성지방의 분미가 상승되며 유리지방산의 산화는 감소되고 이들의 에스텔화는 증가 되 었 다. 65) 그러 나 glu cag o n 은 인슈린의 반대 역 할울 한다. glu - ca gon 은 간세포내에 c-A MP 농도를 증가시키며 인슈란은 그 반대 의 효과가 있 다고 하였 다. 65) 즉 c- A MP 는 Hormone sensit ive lip a se 를 활성 화시 켜 서 작은 선행 물질 po ol 에 촌재 하는 (small pr- •ecursor po ol) VLDL 에 함유된 중성 지 방에 작용하도록 한다. 인슈린은 혈청내 유리지방산에 대한 항지방분해효과에 대해서 길 항작용을 하며 새로이 합성된 지방산을 VLDL 의 구성원으로 포함 시 키 도록 하여 간으로부터 의 수출울 증가시 킨다. 76) 인슈린과 glu cago n77) 및 glu cocort ico id s 78) 둥이 간세 포내 의 중성 치방 분비를자극한다. 암컷 쥐 의 pe rfu s ed 간으로부터 중성 지 방의 분비 가 수컷 쥐 의 pe rfu s ed 한 간으로부터 보다 많다고 하였 으며 이 는 성 호르몬이 ' VLDL 생산에 영향을 미치는 것으로 생각할 수 있다고 하였다 .79) 한편 Chan 등은 80) in vivo 나 in vit ro 연 구에 서 닭 (cockerel) 을 실험동물로 하여 estr o g e n 이 VLDL 합성 에 미 치 는 영 향을 연구하였 다. VLDL 합성 시 estr o g e n 은 VLDL 의 주요 ap o p r ote i n 의 합성 을 위한 m-RNA 의 축적을 자국함으로써 결과적으로 VLDL 합성을 자 극한다고하였다. (3) 간내의 지방 축적 간장내의 중성지방 축적에 대한 연구를 위해서는 다양한 조건하 에서 지방대사의 견해를 고터하여야 한다. 간장내 지방축적이 생기는 일반적인 기전은 다음의 4 가지 경우로
구분지 울 수 있다. i) 과량의 중성 지 방이 지 방세 포로부터 유출되 거 나 식 사로부터 과량의 지방울 섭취함으로써 간세포가 과량의 지방산을 취하는 경우• ii) 간장세 포에 서 de novo 지 방산합성 이 증가되 어 서 궁극적 으로 중 성 지방합성이 증가되는 경우. iii) 간에 함유된 중성지방에 결합되어 있는 지방산 산화가 강 ` 소 되 는 경우. i'V) VLDL 합성 이 감소되 는 경 우이 다. 이 경 우는 유용하게 이 용 뮐 수 있는 VLDL 을 구성하는 단백질이나 인지방의 양이 적어 서 VLDL 합성이 감소되면 간에서의 지방분비가 궁극적으로 감 소된다. 반대로 혈 액으로부터 지방산이나 중성지방울 간이 과량 으로 취했을 경우이다. 기아나 당뇨병의 결 과 로 지방간이 생성되는 경우는 지방조직으로 부터 과량의 지방산이 유 출 되거나 또는 인지방합성이 여제되어 결 과 적 으 로 ph osph ati dy lc holin e 합성 이 저 조하여 간으로부터 중성 지 방의 지 방분비가 감소되는 경우이다 .8 1) 또 한 eth io n in e 을 두여 하면 Iip o p ro te i n 합성 이 여 제 되 어 서 간장 내에 지방이 축적되는 결과가 나타난다 .82) 독물질인 사영화탄소 (CC J 4) 나 83) 약으로 섭취한 p urom y c i n 은 혈청내의 lipo p ro te i n 수 준 을 감소시키므로 간에 지방축적이 생간다 .8 4 ) 또한 oroti c acid 는 간세 포내 에 서 nucleoti de 합성 을 억 제 시 키 므 _ 로 혈청 내 l ip o p ro t e i n 의 합성이 감소되어 간장내 지방이 축적된 다. 85 ) 지방간은 알코올음료를 급성 또는 만성적으로 두여시키면 그 결 과로 생 성 된다. 86) 알코올음료를 마십 으로써 에 탄올이 간을 손상시 키는데 이는 알코올섭취로 인한 저지방석사의 섭취에 기인한 것이 타고 본다. 에탄올 무여 후에 간에 지방의 축적이 생겼어도 lip o - p ro t e i n 의 혈액내로의 유출은 여전히 이루어진다. 그러나 이러한 적응기전이 간의 지방축적을 막을 수는 없다고 본다 .81) 쥐실험을 통해서 보면 쥐에게 중간 길이의 지방산이 함유된 중성지방울 먹야
떤 알코올로 인한 지방간형성이 간사슬의 지방산이 함유된 중성지 방울 먹 였을 때 보다 감소된다고 본다. 88) 지방간은 또한 필수지방산 결핍 때에도 생기며 이의 부분적인 이 유는 인지방합성이 처조한 때문이라고 설명할 수 있다. 또한 팔수 지방산이 결핍되면 간세포내의 콜레스데몰 축적이 비정상적으로 나 타난다 .89) (4) 간에 서 의 gly c eroli pid 합성 효소 gly c erolip id 생 합성 경 로는 20 여 년 전에 Kennedy 와 그의 동로에 의해서 밝혀졌지만 90) 여전히 이의 정확한 경로는 아직까지 밝혀지 지 않은 것이 남아 있다. 다음의 그림 5 는 Eukaryo te s 세 포내 에 서 의 gly c erolip id 생 합성 겅 로를 나타낸 것이며 이에 관련된 효소의 명칭이 명시되어 있다 .9 1) 현재에는 많은 연구자료에 의해서 여러 종류의 효소와 가능한 ' i soz y me 들에 대한 연구가 계속되고 있으며, 이들의 세포내에서의 기능이 규명되고 있는 중이다. 이 연구에서 가장 어려운 문제는 이 들 효소들이 endop la smi c reti cu lum 과 mi toc hondria l membrane 이 견고히 부착되어 있어서 효소들을용해해 내기가 어렵게 되어 있다논 접이다. 그러므로 현재에는 단지 및 종류 안 되는 효소만이 유리되 어 있 다. 현재 까지 의 연구에 서 도 gly c eroli pid 합성 효소의 활 성 이 서 술적으로만 규명되어 있으며, 이들의 조절작용에 대해서 이제 비로 소 규명하기 시작해서 그 결과가 발표되고 있는 중에 있다고 본다. 현재 분명 하게 명 시 되 고 있 는 중성 지 방, ph osph ati dy lc holin e , ·ph osph ati dy le th a nolami ne 의 생 합성 작용은 세 포의 원형 질표면의 -en dop la smi c reti cu lum 에 서 비 대 칭 적 으로 이 루어 지 고 있 다고 한 다 .91) 이러한 비대칭적인 합성은 현재 membrane 을 통과해서 이동 하는 현상의 연구와 endop la smi c re ti culum 내와 다른 세포 mem- brane 내 의 gly c eroli pid 를 종류 별로 분류하는 데 많은 관십 울 기 울 이게 하고 있다 .
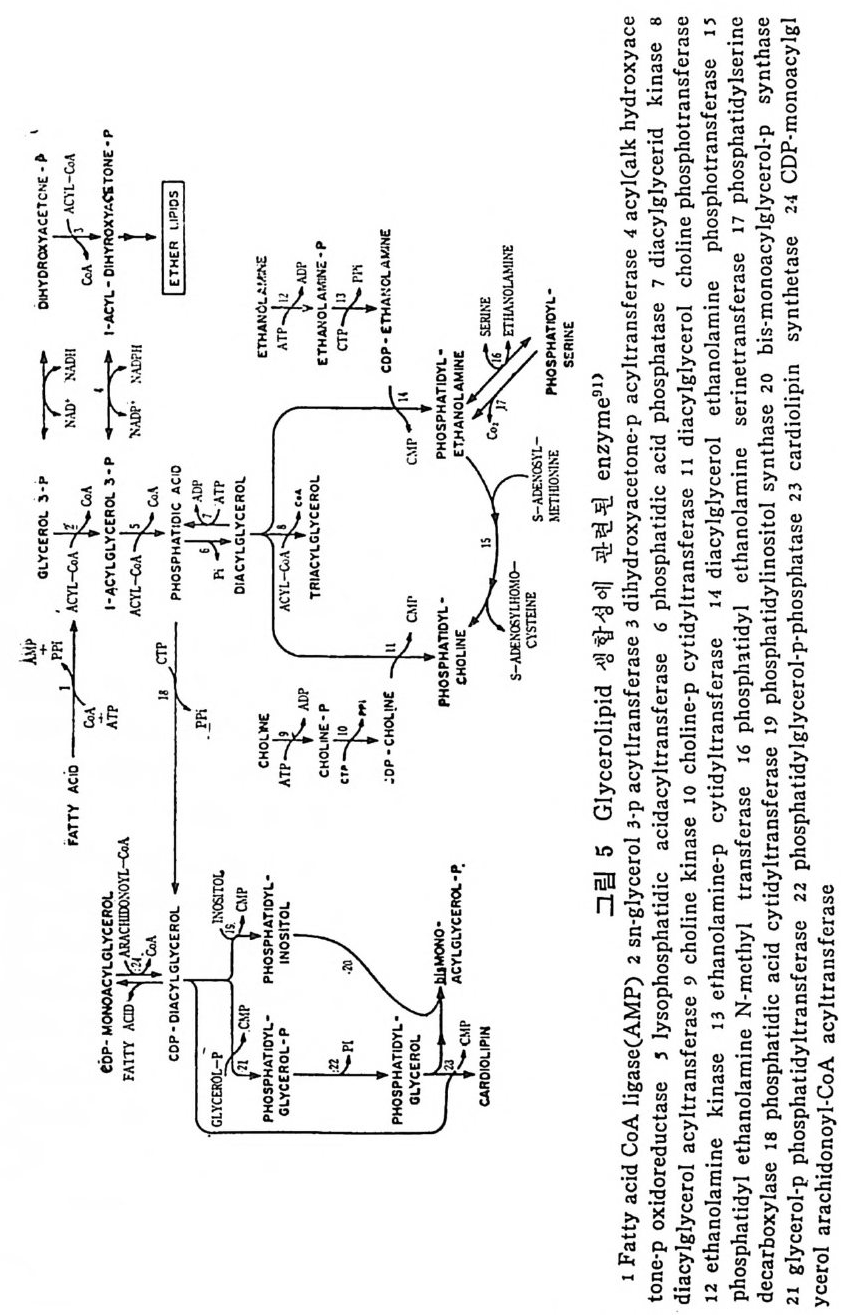 .NCpT.E如O(RYOYCA 7_군퉁 ' GLYL·O CRPE3 p.YTNLEO一·,LII나.:了pR:z.閑도: :홉다곤F::; OA卞i~―o\ CA-.· -+LA.m~ I'·NTYC TA.:cA.0,\f A 0:P CT CI ADICH~H~\TOPOSP OAEYLG LCO•YRLI~COCP 盆ki4pP . P!'i.• LCLLOA YCCIREYO .i--t- .ALN¢= :!E, E,-LHCOL•AIPI•YLD HTT< PSOIASYOHHTOHPP IRIGTN ·OPOCLOEYLLS L-CY`Ol‘AA TAPDPAAP DTPA •星C RELOAYGCLIYTRLC MPN O , LAANI•T-HEEIHOCLN p ~I서P mCTPT鼻卞C Plr ANLCAN E• D CP OHP-C;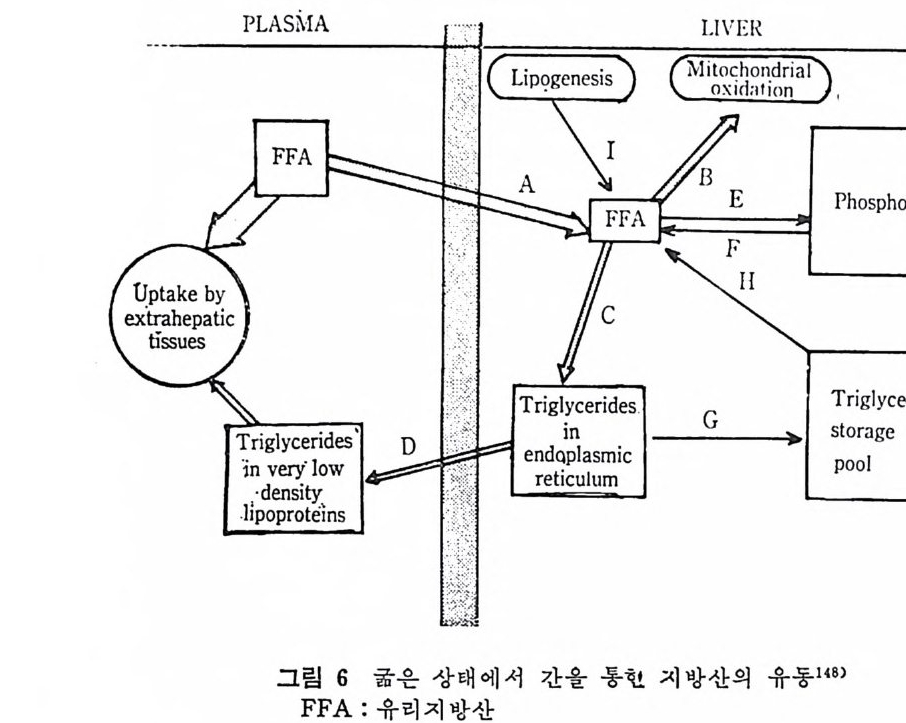 PLASMA
PLASMA
그림 7 에서 보여주듯이 고당, 저지방식사를 하고 난 후면 혈창 내 유리지방산의 농도는 최처로 감소된다(경로 A). 간세포내에서 도 섭 취 한 당의 대 사를 위한 gly c olys i s 가 활발히 진행 되 어 acety k
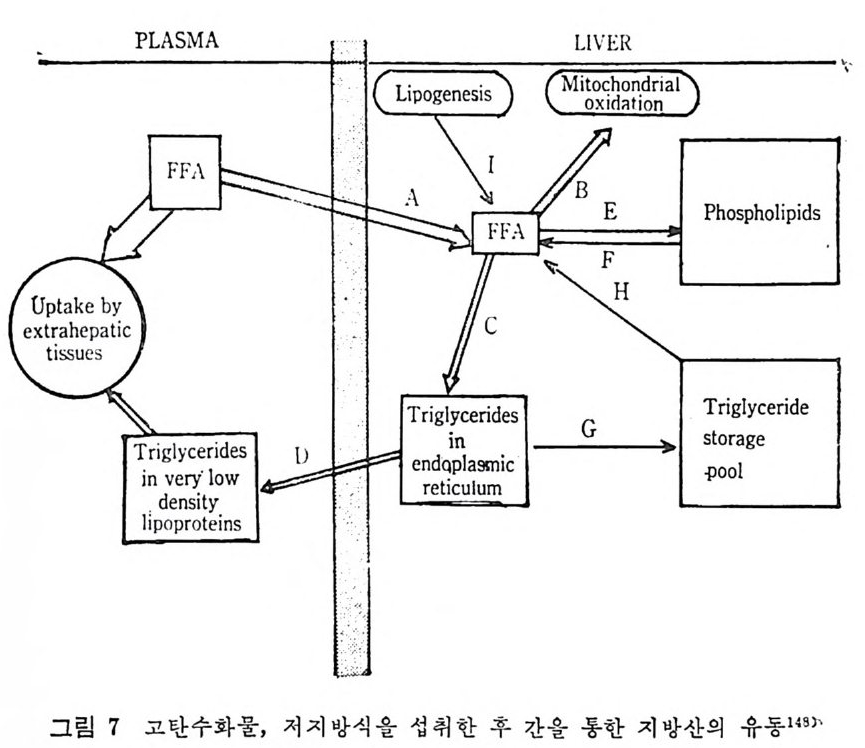 ,
,
CoA 의 공급량이 증가된다. 그러면 이를 기초로 하여 간세포내에 서는 지방산의 de novo 합성량이 증가되며 이때 합성된 유리지방 · 산은 중성지방울 합성한다. 이 경우에 유리지방산은 간세포내의 mi toc hondria 내에서 산호년기 위한 주요 급원이 아니고(경로 B) 혈 류로부터 간으로 들어 온 VLDL 내 의 중성 지방이 산화를 위한 주요 급원이 된다. 정상석이를 공급하면 즉 적당량의 탄수화물과 지방이 함유된 식 사를 하면 chy lo mi cr on 나머 지 에 함유된 중성 지 방으로부터 분리 된 지방산과 de novo 합성에 의해서 합성된 지방산이 간에서 주로 중 성지방합성을 위해서 이용된다. 그런데 고당식사를 하였을 때와 비 교해 보면 de novo 합성에 의해서 합성된 지방산의 간내 중성지방 합성의 이용물은 비교적 낮다고 본다•
굶었을 때와 먹었을 때를 그림 7 에서 비교해 보면 굶었을 때는 A 경로를 통해서 간조직 이외의 조직으로 유리지방산이 이동되고 며 었을 때는 D 경로를 통하고 있다. 한편 경로 I. C.B 가 먹었을 때와 굵었을 때 그 범위에 차이가 나타나고 있음을 보여주고 있다. 쥐 의 간세 포에 서 여 러 종류 호르몬의 작용이 간내 의 gly c erolip id 합성에 미치는 영향에 대해서 보았다• 닭의 간세포 배 양실험에 보 떤 인슈린은 정상적인 속도의 VLDL 합성을 유지시키고 있으나 glu cago n 이 나 cAMP 는 지 방산합성 을 방해 하고 간 세 포내 에 중성 지 방이 주가 된 세 포막으로 둘러 싼 지방구가 나타나 게 하였 다. 149) es t ro gen 울 주사한 닭에게서 실험한 결과 간에서 중 성지방합성에 관련된 효소들의 독정 한 작용에 벌로 변화가 없 다고 보고되 었 다. 150) 지방간의 형성온 알코올섭취로 인한 영양불량으로 생간다고 본 다. 알코올섭취로 인한 지방간 형성에 대해서는 뒤에 자세히 논하 고자 한다(제 3 장, 3 참조). 비만증은 열량대사장애로서 개발국가에서는 주요한 영양장애로 간주되어지고 있다. 선천적으로 비만한 생쥐는 간의 중성지방합성 이 증가되 며 간조직 밖으로 많은 양을 유출해 보낸다. 151 ) 이 현상 온 지방산의 de novo 합성이 증가된 결과라고 부분적으로 설명될 수 있다 .6) 또한 인슈란의 작용으로 비만중의 원인을 규명해 보려는 시도를 많이 해보지만 152) 비만증이 생김으로써 변화되는 모든 과정을 충분 히 설명할 수가 없다. 비만한 생쥐의 혈청내에서 유리지방산과 굳 리세롤의 이동은 증가되지만 153) 간세포내에서 케본체형성률은 갑 소되며 153) 따라서 혈액내의 유리지방산의 농도가 유지되지 못한 다 .154) 이러한 모든 현상은 사람의 비만증 상태와 유사하다고 생각 한다. 3 알코올의 신체내 대사과정 에탄올은 국소량이 신체내에서 생성되기도 하지만 그러나 의부
로부터 섭취되논 물질이다 . 섭취된 에탄운은 소화기관에서 홍수가 용이하게 일어난다. 섭취된 에탄옹의 20% 는 위장에서 홍 수되며 나머 지 80% 가 소장부위 에 서 홉수된다. 홍수된 에 탄올의 2~10% 만이 신장이나 페를 통해서 뇨나 내뿜는 호 흡 을 동해서 체의로 배 설된다. 그리고 섭취된 에탄올의 90% 이상이 빠른 속도로 대사된 다. 155) (1) 알코올 대 사에 관련된 효소 1) Alcohol dehy d rog e nase 섭취된 알코 올은 주로 간내에서 대사된다. 간내에서 주요 알코 올 대사과정은 alcohol deh y dro g enase(ADH) 에 의해서 이루어지며 이 효소는 세 포의 c yt os 이 내 에 존재 하면서 알코올을 aceta l dehy d e 로 전환시키는 것을 촉 진한다. 이때 수소이온이 에탄올로부터 cofa c to r 인 NAD+ 로 이 동되 어 NADH+H 인 환원형 태 를 이 루어 준 다. 이 결과로 에탄울이 산화됨으로서 간세포내에 환원형태인 NADH 의 과량이 생성되는 결과가 된다. 그러면 과량생성된 NADH 는 여 러 종류의 비정상대사를 초래하게 된다. 한편 ADH 는 다량의 알코올 산화를 정상상태에서 가능하게 하지 만 ADH 의 방해물질인 py razole 이 촌재하여도 여전히 간세포내에 서 in v i vo 나 in vit ro 연구에서 모두 알코올이 대사되고 있음을· 관 찰하였 다. 156- 9 ) 더 나아가서 pyra zole 이 존재 할 때 포도당에 동위 원소처리를 하여서 연구한 결과 c yt osol 에 촌재하는 ADH 와 무관한 다른 현처한 에탄울 대사과정이 있음을 발견하였다 .160) ADH 가 중재되지 않고서도이루어지는 알코올의 산화율은사용되 어지는 에탄올의 농도에 따라서 전체 에탄올 대사 수준의 20~25% 157-8),161 ) 내지 50% 또는 그 이상까지도 156),159) 도달할 수 있다고 한다. 또 다른 pyra zole 이 촌재하므로 ADH 와 무관하게 에 탄올이 대 사된다는 증거 는 cy tos ol 내 의 산화환원 상태 가 변화하지 않는 것 이 다. 162) 이 론적으로 두 가지 효소계 통이 ADH 와 무관하게 알코올을
대 사시 킨다고 보고 있 다. 그 하나는 mi cro somal eth a nol oxid i z i n g sy s te m (MEOS) 이 고 또 하나는 cata l ase 이 다. 163) 2) Mi cr osomal eth a nol oxid i z i n g sy s te m (MEOS) 에 탄을은 간세 포의 mi cr osomal 부위와 상호작용이 있 다는 사실 울 처음으로 관찰한 것은 실험쥐에게 에탄을을 먹여 놓고서 smooth endop la smi c re tic ulum(SER) 의 중식 이 되 는 형 태 학적 인 관찰에 서 부 터 시작되었다 .164 - 5) 이 경우에 SER 이 중석되는 이 현상은 에탄을 을 섭취하였을 때만이 아니라 여러 종류의 이물질을 섭취하였을 때 죽 여 러 가지 알려 진 7J- 독소물질 , 166) 여 러 가지 치 료용물질 167) 그리 고 식품첨가물 168) 등 이물질을 섭취했울 때 SER 이 증식되는 결과 가 관찰되었다. 에탄올이 섭취되면 SER 이 증식되는 것으로 미루어보아 cy tos ol 내에서 ADH 에 의해서 산화되는 것에 부과해서 에탄올은 mi cr o- some 에 의해 대사되는 것으로 본다. ADH 에 의해 에탄올이 산 화되는 율과 MEOS 에 의해서 산화되는율을 비교해 보면 MEOS 에 의해 산화되는 율이 ADH 에 의한 것보다 10 배나 높다고 보고되었 다 169) ADH 에 의한 것이 아닌 에탄울 대사는 에탄올 섭취량이 높을 때 ADH 의 Km 치와 MEOS 의 Km 치를 바교해 보면 각각 o.5~2mM 170-l) 과 8~9mM167) 로 보고되 었 다. 이 상의 Km 치 를 비 교해 볼 때 신체내에서 에탄올의 산화에 MEOS 가 크게 공헌하고 있음을 볼 수있다. 다음의 그림 8 은 간세포내에서의 에탄올대사를 지방간 형성 hy pe rlip e mi a, hy pe ruri ce mi a, hy pe rlacta c i de mi a, keto s is 와 관련 하여서 도해한 것이다. 3) Cata l ase In vit ro 연구에 서 cata l ase 는 H2 아 의 생 성 계 통이 촌재 하면 에 탄올 은 산화할 수 있다고 알려쳐 있다 172? (그립 9 의 C,D 참고). 그러나 cata l ase 에 의 해 에탄올이 산화되는 사실을 많은 사람들이 부정하
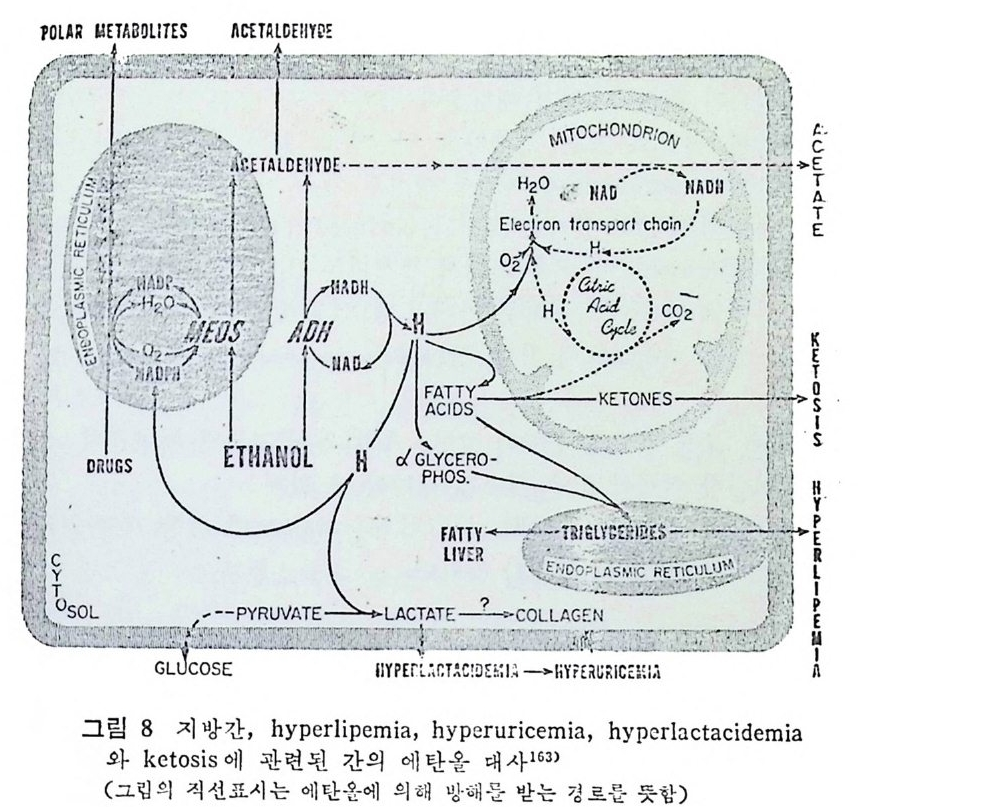 FOLAR METABOLITES AC {l~L OEIIY~E
FOLAR METABOLITES AC {l~L OEIIY~E
기도 했으니 .158), 173- 6 ) 일부 사 람들 은 긍정하기도 했다 .176-7) 일 반적 으로 cata l ase 에 의 한 에 탄을의 산화는 cata l ase 자체 의 ’ 양에 의 촌한다기 보다는 H202 의 합성 속도에 제한받아서 에 탄올의 산화량이 결정된다고 한다. 그러므로 간에서 ca t alase 가 예탄올 · 산화에 참여하는 역할은 간에서 H 2 02 의 합성속도에 의해 전적으로 제한을 받기 때문에 이것을 간접적이라고 말을 할 수 있다고 생각 한다. 간에서 생성되는 H202 의 생리적인 수준은 간조직 매 g r 당 1 시 간에 3~6µmole 의 H 요 가 생 성 된다. 178) 이 수준은 in viv o 연구에 서 몸무게 lOOg r 당 간의 무게를 3. 5 g r 으로 설정해 놓고 간 메
gr 당 1 시 간에 178µmole 의 에 탄올이 산화되 는 것 을 뜻하게 된다. 즉 약 2% 의 에탄올이 산화되는 윤이라고 볼 수 있다• 161 ) 그러나 간세포내에서 생성된 모든 H2 야가 모두 에탄울 산화에만 쓰이는 것은 아니기 때문에 2% 의 에탄을이 산화된다는 것은 사실보다 많 이 강조된 것으로 보는 견해라고 반박하고 있다 .179) 더 나아가서 간세포내의 m i crosome 에 의해서 생성된 H202 가 모두 에탄올 산 화에 쓰여 지 치 않고 있 다는 보고가 pe rfu s ed 7J -에 서 연구되 었 다• JOO ) 그런데 m i crosome 이 전체 간에서 생성되는 H2 야를 철반이나 공급 하고 있 다고 한다. 178) 여 하튼 간에 서 ADI -I 중재 로서 가 아닌 H202 와 관련이 있는 ca t alase 에 의한 산화량은 5~10% 미만으로 보고 . 있 다. 181 ) 이상의 모든 결과를 종합해 보면, ADH 와 무관하게 에탄올의 산 화에 현처한 역할이 없을 것으로 생각할 수 있다. 다음의 식 (그림 9) 은 ADH, MEOS 와 cata l ase 에 의 한 에 탄올의 산화과정을 수석으로 표시한 것이다.
A CH3CH20H+NAD+ ADH --+ CH3CHO+NADH+H + 1l CHaCH20H+NADPH+H ++ 02M~EO-S + CHaCHO+NADP 나 2H20 c +「 NADPH+ H+ +Oz 접O京xi詞d a -se + NADP++H202 I_H202+CH3CH20H— Ca—ta las-e + 2H20+CH3CHO D +「 HYPOXANTHINE+H20+0O~x 禪id ~a s-e - XANTHINE+H202 l___H2 02+CH3CH2C0atHa l ~as-e- > 2H20+CH3CHO 그림 9 ADH, NAD+, NADH(A), MEOS, NADPH, NADP+(B), N탄A올D P산H화(C과)정, xanth i n e oxid a se 와 ca t alase(D) 에 의 한 간내 에
(2) 에 탄올 산화가 간과 신체 대 사에 미 치 는 직 접 적 인 영 향 1) Ant idi u r eti c Horrnone(ADH) 대사과정에 의해 간내에 과량 생산된 NADH 의 영향 그림 8 과 그림 9 의 A 에서 보여주듯이 에탄운의 산화결과 수소 가 NAD+ 로 이 동되 어 서 NADH/NAD+ 의 비 율에 변화를 가져 오게 되 었 다. 그러 므로 NADH/NAD+ 의 비 율의 변화는 에 탄옹의 남용 으로 생기는 여러가지 비정상증을 초래하는 원인이 된다 •182) CD Hy pe rlacta c id e mi a, hy pe ruric e mi a 와 acid o sis NADH / NAD 떠 비 율 이 상승됨 으로써 lacta t e /py ru vate 율이 증가 되 면서 hy pe r! acta c id e mi a 가 생 간다. 183 > l2cta t e 나 pyr uvate 의 간 에 의한 이용물이 낮아지면서 lac t a t e 의 생성이 증가되기 때문이다. hy pe rla c ta c id e mi a 는 산독증 (a ci dos i s) 을 발생 시 키 며 신장으로 하 여 금 uric acid 배 설능력 을 감소시 켜 서 hy pe ruric e mi a 가 생 간다. 183) 알코올로 인해서 유도된 ke t os i s 가 또한 h yp erur i ccem i a 를 보다 더 상승시 키 기 도 한다. 이 와같이 알코올섭 취 로 인해 서 hy pe ruric e mi a 가 계속 생기면 신체내에 통풍(g ou t)이 생기게 된다. 죽 술을 장기 간 계속 마시면, 이 통풍증세 가 악화되거나 새로 생기게 된다 .184) 또한 lacta t e 가 과량으로 생 기 면 collag en 생 성 을 자국하게 되 고 마 라서 collag en pra lin e hy d roxy la se 의 활성 이 증가되 어 결과적 으로 collag en 이 축적 되 게 된다. lf 5 ) ® 지방합성의 증가와 치방산화의 감소 NADH/NAD+ 의 비 례 가 증가되 면 2-gl y c e rop ho sph ate 의 농도가 증가되어 186) 지방산이 남아 있게 되므로 간세포내에 중성지방의 축 적이 생간다. 이에 부과해서 NADH 의 과량 존재로 지방산의 합 성 ,187-8) 지방산 사슬길이의 연장 또한 NADP+ 로의 수소이온의 이 동둥이 증가된다. 이론적으로 보면 지방함량의 증가는 과량의 수소이온의 배치수· 단으로 고려 된다. 이 중 약간의 수소 equ i v a lents 둘은 여 러 종류의
〈 shu ttle 〉기 전에 의 해 서 mi toc hondria 내 로 이 동원 것 이 다. Krebs cy c le 의 활력 이 감소될 것 이 며 1s9- 9o > NAD+ 를 요구하는 부위 의 cy c le 내 의 작용속도는 부분적 으로 느려 질 것 이 다. mi toc hondria 는 지 방 산으로부터 유도된 2 개 의 탄소물질을 Krebs cy c le 을 동해 서 산화하 기 보다는 에 탄울로부터 유레 된 수소 eq u iv a lents 륜 이 용할 것 이 다. 그러므로 정상적으로는 지방산이 간의 주요 에너지 공급원이었던 것이 에탄올로 대치되는 현상이 나타난다. 간철편 연구에서, 188 ), 191) p er f us e d 7L 의 연구에서, 189 ) 유리된 간세 포 연구에서 ,1 92> in v i vo 연구에서 1 9 1) 보여준 바에 의 하면 , 에만 웅 은 지방산 산화를 감소시킨다고 한다. 이 결과는 유용한 식이지 방 이 존재하면 간에 축적될 것이며 또한 식 이지방이 없윤 메도 체 내 에서 합성된 지방산이 간에 축적될 것이다 .1 93 - 6 ) @ mi cr osomal 기 능과 에 탄을과의 상호관계 여러 종류의 약이 에탄 운 에 미치는 효과에 대한 상호관계는 년 리 알려져 있다. 술에 중독 이 되어 있는 사 람은 및 가지의 약 에 보 다 예민하다 .1 9” 이러한 여러 가지 효과는 , 알코운과 여러 종류 의 약 과의 상호관계가 중추신경계통에 영향을 미찬 것이다 • 계속적으로 술을 섭취하면 약의 대사효과가 느려진다 .1 9 8 ) 반대로 in v it ro 연구에서 보면 , 약은 간의 m ic rosome 에 서 ca t alase 와는 무 관하게 에 탄을의 산화를 방해 하고 !99) 또 어 떤 약은 AD H 릉 방해 한다 .200) 에탄을과 약 사이의 상호관계는 실제 로 많은 문재룹 야 기시킬 수 있다. 요츠음 많은 사람들이 전정재나 안 칭제룹 먹으면 서 음주를 하는데 이때는 알코올의 신체내 정상대사가 이루어지지 않기 때문에 혈 액내 알코올의 능도가 위험한 수준을 오래 유지하는 경우를 유발하게 된다. 그래서 사고낼 위험이 커전다. @ 에 탄올 산화로 인해 생 성 된 aceta l dehy d e 와 aceta t e 의 영 향 aceta l dehy d e 는 에 탄올이 산화되 어 서 생 성 된 주요 산물이 다. 알 코올의 만성 섭취자의 혈액내에는 알코올을 섭취하지 않은 사람보 다 aceta l dehy d e 함량이 높은 양 들어 있 음이 밝혀 졌 다. 163) 이 현상 은 아마도 mi toc hondria 에 상해 가 왔거 나 또는 MEOS 의 활성 이
높아진 것 으로 추측된 다. 201 ) Ace t aleh y de 의 정확한 대사과정은 아직 밝혀지지 않았지만 alde· hy d e dehy d rog e nase 에 의 해 서 alde h y d e 의 산화가 이 루어 지 는 것 으 로 대 개 이 해 되 어 지 고 있 다. 이 aldehy d e dehy d rog e nase 찰성 의 80% 가 m it ochondr i a 에 위치한다고 한다 .18 1) ,202) 에탄 웅 섭취로 인 한 aceta l d e h y d e dehy d rog e nase 활성 의 변화에 대 해 연 구한 결 과, 증가되 었 다는 보고 20 3 - 4) 와 변화가 없 었 다는 보고가 있 다. 205-6) Al de hy d e dehy d rog en ase 에 의 한 aceta l dehy d e 의 대 사는 NADH 몽 생 성 하는 킬 과 륭 나타내 므로 aceta l dehy d e 의 효과는 NADH 생 성효과라고 봉 수 있다 . 이는 에탄 운 이 산화되어서 생성된 NADH 의 효과와 다른 접 이 없는 것으로 본다 . Aceta l d e hy d e 자체 가 대 단히 왈 발한 물질 이 어 서 어 떤 독성 을 유 발할지는 모르지만 이것의 정확한 대사경로는 밝혀쳐야 될 것으로 본다 . In vit r o 연구에서 밝혀진 바로는 간은 ace t a t e 를 쉽게 이용하지 만 in viv o 연 구에 서 보면 대 부분의 aceta t e 는 말단조직 에 서 이 용 된다 . ~07> aceate 는 산체 내 에 시 치 방조직 에 높게 나타나며 여 기 서 ace t a t e 는 지방산의 유리문 감 소시 켜 서 유리지방산의 혈액내 농도 룰 감소시 킨 다. 208) 2) 지방간 형성에 미치는 알코올의 영향 알코운섭취로 . 인해서 간에 지 방 이 축적되는 것은 혼히 나타나는 증상이다. 알코 운 이 간에 손상을 입히는 첫째 단계는 조직학적으로 간에 지방이 고여 있는 상태이다. 이러한시작단계 를 일컬어서 알코 울성 지 방간이 라고 부른다. 알코울성 지 방간은 급성 혹은 만성 으로 알코 올 을 섭취하면 생길 수 있다. 알코올로 인한 지방간브다 복잡 한 간질환은 알코올성 간염 (he p a titi s) 으로서 간세포가 중성지방으로 포화되어서 간세포의 되화가 생긴 단계이다. 가장 심각한 간의 손 상이 온 것 이 알코올로 인한 경 변현상(ci rrhos i s) 이 다. 이 경 우는 손 상된 간세 포가 섬 유화된 결체 조직 (fibr oti c connecti ve ti ssue) 으로 대 치되어 있는 상태이다. 이때는 간장내의 혈유량과 세포의 수가 감
소되어서 결과적으로 간기능이 처하된다. 죽 혈청 단백 질 합성저하, bil i r u bin 합성 처 하 및 bil iru bin 의 간으로부터 의 이 동속도 저 하 둥도 을 주로 들 수 있다. ® 간장내 지방축적에 미치는 급성 알코올섭취효과 Mallov 와 Bloeh20” 는 알코올을 한꺼번에 많은 양( 동문의 몸무게 kg 당 4.2~6.2g ) 두·여하면 12~16 시간 후에 간에 현저한 중 성지방의 축적이 생긴다고 처음으로 보고하었다. 간장내 지방의 면화는 에 탄올의 산화와 부분적으로 관련이 있다. 죽 지방축적 정도는 에 탄올의 산화능력을 능가한 양의 알코올을 섭취함에 따라서 년하기 때문이다 .210) 또한 혈액내의 에탄울 함량을 감소시키기 위해서, 일 정량의 알코올울 일정시간 간격으로 섭취시키면 간의 지방 축 적은 사라진다 .211) 다른 종류의 간장 (str ess) 상대 에 서 도 마찬가지 로 알코운중독은 시 상 하부 (h yp o t halamus), 뇌 하수체 , adrenocoti ca l212-s) 그리 고 sy m p a th - adrenomedulla216- 7) 계 통을 자극한다. cate cholami ne 이 유리 되 는 것은 특별히 지방조직으로부터 유리지방산을 유리시키는 것을 증진 시키는 데 그 뜻이 크며, 따라서 간에 중성지방의 축적을 중전시키 는 결과가 된다. 218) 알코올울 루여 하기 전에 먼저 cate c holami ne 의 저 장을 처 하시 키 떤 급성적인 알코올성 지방간은 방지된다 .211) 이러한 급성적인 알 코올성 지방간현상은 만성적안 알코올 섭취에서는 관찰되어지지 않 논다. ® 간장내 지방축적에 미치는 만성 알코올섭취효과 만성적인 알코올의 섭취로 발생되는 지방간은 성장기 동물실험의 결과에 나타난 증거로서는 영양불량을 주요 원인으로 간주하여 왔 다. 죽 단백 질과 lip o tr o p ic 요 인 인 cholin e , meth i o n in e 의 결 핍 울 논하여 왔으며 에탄올의 독성에 대한 고려는 전연 되어 있지 않았 다. 2l9) 더구나 지방간으로부터 회복되고 있는 환자에게 알코올을 두여하 떤 간지방의 소멸이 방지되며 여러가지 해로운 효과가 나타남이 밝
혀졌다. 220-1 ) 이 연구에서는 두여했던 알코올의 양은 보통 알코올 중독자가 섭 취하는 양보다 적었으며 이는 알코올로부터의 칼로리 섭취량이 전 채 칼로리 섭취량 중 50% 내지 그이상되는 양이었다. 알코울 중독 자 들 이 섭 취 하는 양만큼의 알코올을 지 방간을 가진 환자에 게 주었 을 때는 간으로부터의 지방의 소멀은 방지되었다 .222) 실험주] 에게 에탄올을 마시는 물과 함께 주어 에탄올로부터 섭취 된 칸로리 의 양을 전체 섭취된 칼로리양의 10~25% 정도로 하였 울 대 에탄운은 간의 지방축적에 벨 영향을 미치지 않았다, 이와 바 슷한 양 을 유동식이로 주었을 때도 혈액내 에탄올의 농도는 무 시할 만한 양이었으며 지망간의 발생은 되지 않았다 .223) 필요한 영양소가 모두 함유된 석사에 물 대신 에탄올울 공급해 주면 에탄 울로 부터 섭취하 는 칼로리는 전체 섭취하는 칼로리의 36 %에 해당하며 이 문 사 람의 경우와 비교해 보면 중간 정도의 알코 올 섭취자에 해당한다• 식사내의 탄수화 물 에서 섭취하는 칼로리를 전부 알코올로부터의 칼로리로 대치해 보면 간세포내에서 5~10 배의 중성지방 함량을 관 찰할 수 있 다. 223- 5 ) 지방의 축적과정은 에탄울을 섭취시키는 첫번 달에 서서히 이루 어지며 226) 쥐의 경우는 1 년을 견디고 원숭이 (Baloon) 의 경우는 3 년 울 견디었다 . 에탄 울을 공급한 실험동물군에서 몸무게 증가는 없었고 탄수화물 로부터 얻는 칼로리보다 에탄올로부터 얻는 칼로리가 몸무게 증가 효율을 저하시 켰 다 • 227) 탄수화물로부터 섭 취 하던 칼로리 를 동량 지 방으로 대치한 식사 죽 무단수화물식사로 실험동물을 사육하여도 에탄 올 섭취시에 나타나던 효과가 재현되지 않았다. 이 결과로 지방간은 에탄올 때문에 나타나는 것이지 다론 종류의 열량소의 열량공급으로 나타나는 것은 아 니라고 생각된다 . 형태적 관찰에 의해서 간이 정상적인 사람에게(전에 지방간의 경험 이 있던가 없던가에 무관하게) 정상식사에 에탄을을· 첨가해서 공급하 거나 아니면 탄수화물 대신에 에탄올을 첨가하면 지방간이 발생한
다 86), 223), 22 8 ) 이때 생건 지방간은 형태학적으로도 분명하며 간조직 생 검 (B io p s y ) 에서 분석한 지방함 량을 보면 정 상간의 25 배나 되는 중성지 방이 합 유되어 있었다. 지방의 축 처은 에 탄·운 섭 취 후 며칠되지 않 아서 나 타나기 시 작하였 다. 228) 간내 지방중의 중 성 지 방 의 중가 는 물론 이 었고 다른 증류의 지 방 즉 인지 방 2 23 ) 과 콜레 스데 물의 축적 후) 이 에 단·운윤 만 성 지 으로 섬 우 ] 한 쥐에게서 나타 났다 . 이 때 나 타난 간 콜레스태운은 주로 에 스벨화 된 콜 레스테 롤 이며 유 리 콜레스태풀 은 미 세한 양이 ·중가더었다 . 22 · 1 J 팔 요한· 모든 영양소가 다 포함 되어 있 는 석사동 하면시 알고운운 섭취했을 때 섭 취 된 영양소의 홉.- 수 불량의 가능성을 고지하여야 한 다. 실제로 알코운움료 수정 도의 농도 가 섞 인 일·교·홍윤섭위했요- 데 도 소 장의 윗부분 (p rox i mal j e j unum ) 까지의 관강( 입요 )내 의 알 코 윤 농 도가 혈엑 내보다 비 교적 높다 는 것 이 발견되었다 .229) 소장의 관강내 (i n tr2. lum i n a l) 의 알코운농도가 높은 것 은 장 내 막 의 손상을 가쳐 와서 기 능의 손 상 까 지 초래 하게 된 다. 230) 또한 in viv o 와 in v it ro 연구결과에서 보여 준 바에 의하면 에 탄올 의 고농도 는 포도당, 아미 노산, 비 타민의 능등적 이 동 (ac t i ve t ran s p o r t) 을 방 해 한 다고 하였 다. 231 국) 영양이 충분한 식사와 함께 알코올을 섭취시킨 사 람과 동물 에서 는 변으로 비정상 칼로리급원, 질소 그리고 지방배 설 이 되지 않 았 다. 이 결과로 일부의 알코올중독자에게서 흡 수 분량 이 나타나 ·농 것 은 영 양불량에 기 인된 것으로 본다. 227 ),23 5-G) 그러나 한편 영양결핍의 상태에서일지라도 짧은 기간 동 안에는 알코운로 인한 지방간 발생이 잘 생기지 않는 것으로 보고되기도 하였다. 237-8) 사람이 아닌 원숭이에게 전체 칼로리 섭취량의 50% 를 알코올로 섭취시켜도 홍수불량이나 영양불량이 초래되지 않았다. 그러나 이 런 상태하에서논 알코올로 인한 간 질병, 지방간으로부터 간경번까 지 나타났다 .23U)
3) 알코울로 인한 지방간 생성에 영향을 미치는 인자들 ® 식이지방의 역할 알코운로 인해 서 생 성 된 간의 지 방증 (s t ea t os i s) 의 정 도는 식 이 내 의 함유된 치방의 양에 따라서 탈라진다. 전체 칼로리 섭취량의 25% 나 그 이하 물 - 지방으로부터 섭취할 때는 에탄올을 려인 쥐에게서 간에 지방의 축적량 이 감소함을 보여주고 있다 . 22 6) 그리 나 지 방의 섭 취 량을 아주 낮추어 서 오로지 팔수지 방산, lin - olea t c 요구량 충족 징 도로 먹여도 간에 지방의 축적이 완전히 방지 되지는 않 았다 . 226) 석사내의 지당함량 의 중 요 성을 다시 확 인하기 위해서, 자원한 사 람에게 일정항의 에탄을-울 섭취시킨 길 과 지방이 정상량 함유된 식 사 를 한 사 간 에게서 저지방식사를 한 사람보다 지방증 (s t ea t os i s) 이 많이 발생 하였 다 . 192 ) 또한 식 사내에 함유 된 지방의 양에 부과해서 지방의 종류에 따라 서 간에 처장되는 지방의 종류를 비교하였다. 식사내 지방을 사슬 이 긴 지방산으로 구성된 중성지방 대신에 중간 길이의 지방산으로 구성된 중성지망 으로 대치시칸 식사 를 하였더니 에탄을을 섭취하였 을 때 보다 간에 지 방 축적 량이 감소하였 다. 239) 이 효과는 아마도 중 간사 슬 길 이의 지방산은 에스 텔화 되는 것보다산화하여 분해되는양 이 더 만은 것 으로 볼 수 있다 .1 89 ) ® 단백 질과 lip o tr o p ic fac to r 의 역 할 사람에게서 단백질결핍이 간에 미치는 영향에 대해서는 확실한 결론이 아직까지 내려지지 않았다 . 그러나 동물에게서는 앞에서도 지적 했 듯이 성장기 쥐에서만이 단백질과 lip o tr o p ic fac to r 결핍으로 지방간이 형성되었다고 하였다. Kwashio r kor 어란이에게서는 단백질결핍으로 간에 지방증이 나 타났다고 한다. 또한 취의 실험에서도 칼로리의 4% 만을 단백질로 구성하고 칼슘이 결핍된 식사를 하면 에탄올로 인한 지방간이 생성 된다고. 한다. 195)
사람의 경우 과량의 단백질 (25% 칼로리 섭취)과 과량의 chol i ne 참 가 식이를 먹어도 알코올에 의해서 생성된 지방간을 방지해 주지는 못하였다고 했다 .228) 그러나 이 결과는 어느 의미에서는 당연하다 고 생각된다. 왜냐하면 사람에게서 chol i ne 결핍 식사가 아무런 해를 끼치지 않기 때문이다. 설치류의 간에서와는 달리 사람의 간에는 대단히 적은 양의 cholin e ox i dase 가 함유되어 있다. 이 사신은 chol i ne 의 결핍증은 동물의 종류에 따라서 다르게 나타난다고 생각 한다. Lip o t ro p ic fac t o r 의 결 핍 으로써 간에 손상이 온다는 선 험 은 원래 쥐에게서 시행되어졌으며 사람에서는 lip o t ro p ic fa c t or 가 안코운 로 인한 간의 손상에 약간의 관련이 있는 것으로 생각된다. 쥐실험 에서는 과량의 chol i ne 첨가가 알코울로 인해서 생간 간의 손상을 방 지 하지 못하였 다고 한다. 239) 더 나아가서 쥐 의 실험 에 서 보면 cholin e
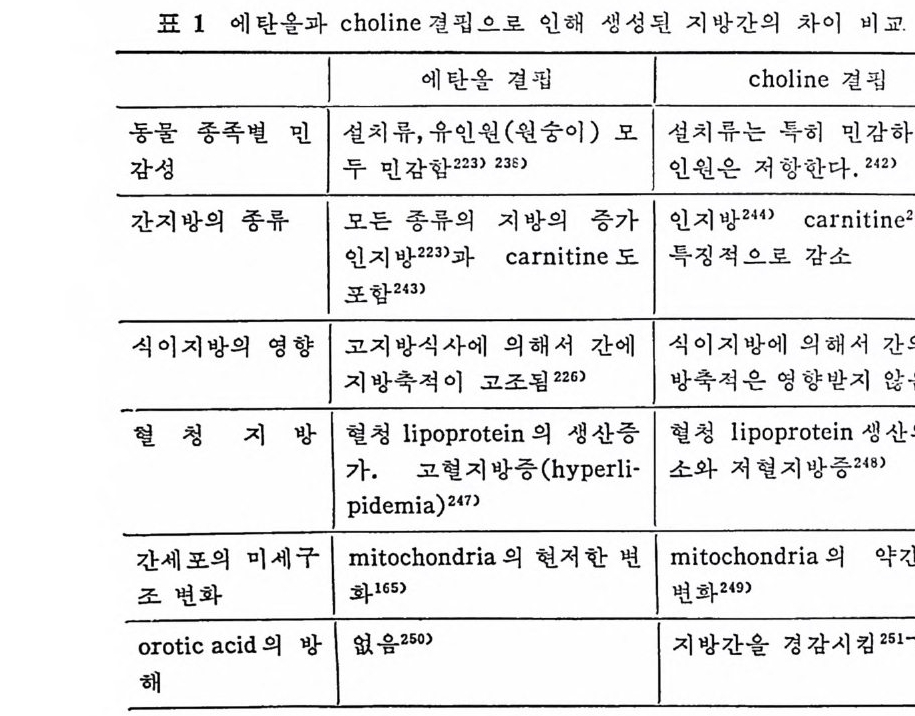 표 1 에탄올과 cho li ne 결핍으로 인해 생성된 지방간의 차이 비교
표 1 에탄올과 cho li ne 결핍으로 인해 생성된 지방간의 차이 비교
결 핍으로 인한 지방간과 알코올로 인해 생 긴 치방간에는 차이가 있 었다. 이 차이를 다음의 표 1 에 요약해 보았다. 두 원 인으로 인해서 생간 지방간 사이에는 유사접이 있으나 많은 차이를 보이고 있다. 그러나 두 경우 다 혈청 단백질 즉 알부민 이 240 - 1) 간으로부터 유 출 되는 것이 지 연되고 있고, 결국 간경변으로 이끌려 가고 있는 접이 동일하다. 4) 간내 알코올로 인해서 생기는 지방급원과 축적의 기전 지방간이 생기면 간내의 치방의 대사에만 변화가 오는 것으로 생 각하기 쉽지만 이에 부과해서 단백질대사에도 십각한 변화를 초래 하기 때문에 간아 지방을 대사하는 데 있어서 더욱더 불리한 여전 이 조성된다. 알코올로 인한 지방간 형성시 두 가지 이상이 생기는 데 하나는 지방의 축적이며 또 하나는 간장자체의 크기가 확대되는 것이다. 전동적으로 간 장기가 커지는 현상 (he p a t ome g al y)을 간조칙내에 치방이 축적되었기 때문으로 생각해 왔지만, 최근에 나타난 쥐의 실험결과에서 보면 알코올을 먹인 쥐의 증가된 간장 무게의 1/2 에 해당하는 양 정도의 지방이 축적된 것으로 보고되었다. 그리고 나머
지 증가량의 1/2 정도는 단백질양이 증가된 것으로 보고되었다 253) (그립 10). 이 증가된 단백질은 전체 간장내에 촌재하는 단백질의 농도가 증가된 것이거나 또는 간장의 젖은 무게와 마론 무게비 례 를 환산하여 봉으로써 단백 질의 축적에 따르는 비례적인수분의 보유가 증가된 것으로 생각한다. 이러한 지방, 단백 질, 수분의 증가가 모두 합쳐 쳐서 간세포 크기의 증가와 관
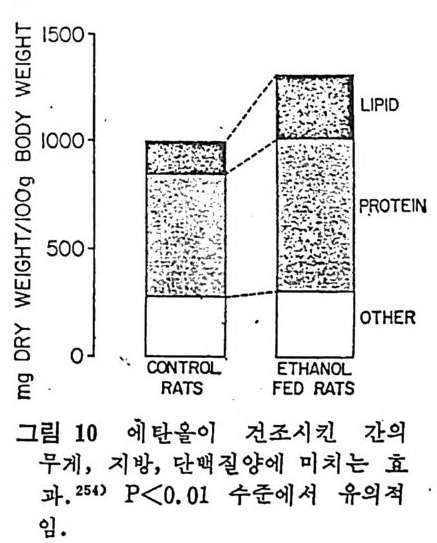 토 1500
토 1500
련이 있다고 한다 .254) 간내의 단백질의 보유는 부분적으로는 간으 로부터 분비되어야 하는 단백질아 그대로 간에 보유된 것이라 고 생 각된다. 241) 에탄올 자체가 산화해서 이 변화에 주요 원인이 되 었다 고 확신할 만한 증거는 없다. 그러나 단백질의 축적원인을 규명해 보기 위해 ADH 의 길항물질인 py razole 만의 효과 물 급성 알코운 섭취로 인한 지방간에서 실험하여 보았다. 그러나 결과는 여러가지로 나타나서 어먼 경우는 일부의 층 거만 이 나타나서 결론을 내랄 수 없었으며 어떤 경우는 완전히 단백질 축 적이 방지되기도 하였다 . 2 56 - 6) 그리고 어떤 경우 는 아무탄 효 과가 없 었 으며 257- 8 ) 어 떤 경 우는 두여 한 약의 양에 따라서 259 ) 또 는 동물 의 성 260 - 1) 의 차이 에 따라서 모두 다르게 나타났다. 이상과 같은 여러가지 실험결과는 급성 알코 운 섭취 로 인한 지방 간의 병인을 규명함에 있어 여러 종류의 스트레스에 대한 반 옹 이므 로 벨로 새로운 사실은 아니라고 본다. 만성적으로 알코올과 길항물잘울 함께 두여했을 때의 걷 과는 에탄올이 간세포의 영중과 괴사 (necro s i s) 를 유발하는 데 더욱 효과 가 컸다고 보고되었는데 262 - 3) 이 결과 를 해석하기란 매우 복잡하다. 즉 길항물질의 독성으로 나타난 것인지 2G· I ) 아니면 에탄옹의 산화 가 py razole 에 예민하지 않은 대사과정을 동해서 일어난 결 과인지 등으로 해석해 볼 수 있다 .264) 간에서의 에탄올 산화결과는 단백질과 지방의 변화가 일어난다 고 연관지어 볼 수 있지만 지방간이 나타날 때 생기는 탈수현상은 다음에 요약하였다. 앞장에서 에탄올의 신체내 대사(p .75 참조)에서 이미 언급 했 듯이 에탄올의 산회는 간에 많은 부담을 준다. 에탄올 자체는 고 열 당 물질 (7. 1Cal/ g)로서 소화기 장내 에 서 흡수가 용이 하며 주로 간에 서 산화된다. 그런데 간장의 특칭은 처장이 없으면 간장의 상태가 악 화되며 신체 각조칙 세포의 필요량을 충당시키고 또 그 제포로부를 터 물질을 취해오는 상호 fe ed-back 의 조철 관련을 한다. 그러므로 에탄올의 산화는 간장내의 대사에 있어 십각한 불균형을 초래하게 된다. ‘
간세포내에서 에탄운은 3 가지 대사과정에 의해서 산화된다고 하 였다. 그 중 ADH 에 의한 산화가 주요 기전이며 이 결과 aceta l de- h yde 가 생성되면서 에탄운에서 유리된 수소이온이 NAD+ 로 이동 되어서 왠·원된 NADH 를 생성한댜 한편 과량의 NADH 형성은 자 연히 수소이 온의 이 동으로 NADPH 를 생 성 하며 이 는 endop la smi c reti cu lum 에 존 재 한다. 15 7 ) 그러 나 만성 적 인 알코올의 섭 취 시 에 MEOS 의 왕 성 이 증가된다. 또 한 알코 운 섭 취 로 인해 간세 포의 endop la smi c reti cu lum 의 smooth - membrane 전제 단백 질과 전체 지 방의 함량이 증가한다고 보고하었다 .265) 이러한 변화가 일어나는 기전은 밝혀지지 않았으나 이와 같은 현상이 여러 종류의 약이나 이물질을 섭취해도 생간다. 에탄올의 산화 룹 바롯해서 이러한 약이나 이물질의 산화가 바로. mi cr osome 에 서 이 루어 진다고 생 각할 수 있 다. 또한 에탄올의 효과는 m ic rosome 의 기능과 관련이 있는 환원 등가 (reduc i ng e qu i valen t)의 증가이 다. 그러 므로 에 탄운을 만성 적 으 로 섭 취 하면 mi cr osomal 활성 이 중가한다• 또 다론 효과는· 에 탄올의 대 사산물이 aceta l dehy d e 와 aceta t e 에 의한 것이다. 마지막으로 대부분의 산화된 에탄올은 관정맥내에서 유리된 aceta t e 로서 나타난다. 266) 이 현상은 aceta l dehy d e 의 산화결 과로. acety l CoA 가 생성된 것인지 또는 유리된 ace t a t e 에서 생성된 것 인지에 대해서는 불분명하다. 그러나 유리된 ace t a t e 는 에탄운을 동 위원소로 처리하여서 대사시켰을때 지방산이나 콜레스테돌의 여러 종류의 대 사산물로써 이 용되 고 있 음이 나타났다. Aceta t e 도 in vit ro 연구에 서 보면 간세 포가 이 용을 찰 하지 만 in viv o 에 서 는 말단조직 이 이 용한다. 또한 에 탄올 산화시 에 aceta t e 의 간세 포내 의 산화량은 감소한다. 왜 냐하면 Krebs cy c le 의 작용이 방해 률 받기 때 문이 다. 여 하돈 간에 서 유리 된 aceta t e 의 과량합성 의 기전은 아직까지 모른다. 에탄올에 의해서 발생된 지방간은 지방의 공급이 증가된 결과라 고 본다. 간으로의 지방공급원은 다음의 3 가지로 간추려 볼 수
있다. 죽 식이지방, 지방조직의 지방 그리고 간 자체가 합성하는 지 방을 들 수 있다. 한편 지방의 산화, 지방의 분해 그리고 일 청으로 또는 담줍으로 지방의 배설 둥이 불충분하게 이루어져도 간에 지방 축적이 울 수 있다. 여러가지 실험에 의해서 간에 지방이 축 적되는 가능한 기전을 다음 그립으로 표시해 보았다(그립 11). ® 소장으로부터 지 방공급의 증가 특정한 지방이 함유된 식사와 함께 에탄올을 며칠동안 섭취하면 간에 지방이 축적되는 현상이 나타난다. 그란데 축적된 지방의 종 류는 식이지방에 의해 결정된다 .193 - 4),196) 급성으로 알코올윤 섭취 해서 지방이 생성될 때는 오히려 지방의 섭취가 상대 륜 악화시킨 다. 267) 앞에서도 지적했듯이 식사내의 지방을 전적으로 제한하여서 필수 치방산 요구량 충족 정도로 섭취하여도 만성적인 알코올섭취시에는 치 방간이 방지되 지 못하였 다. 226) 알코올을 주지 않았던 실험쥐에게 급성으로 알코올을 두여하면
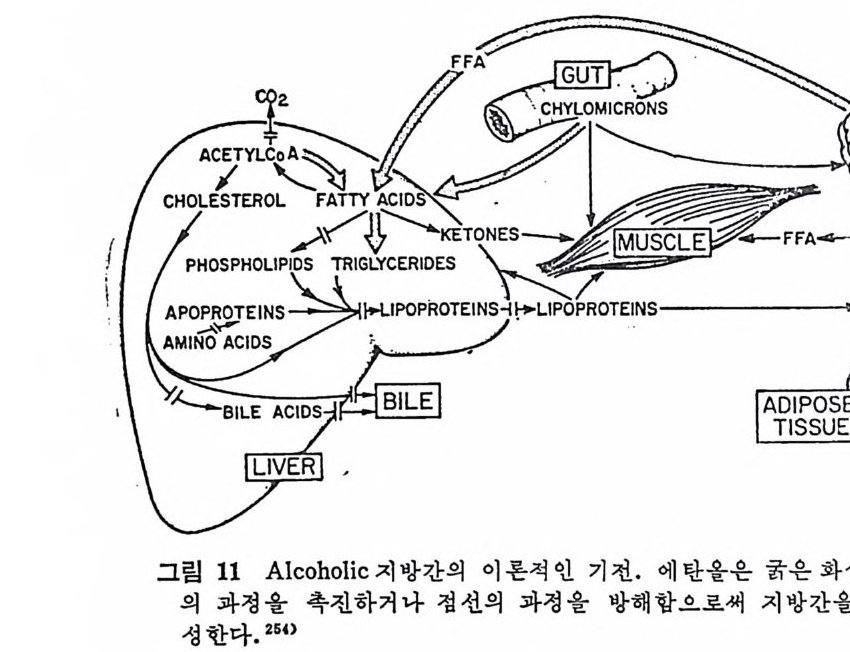 ,..'.J. \ l+-LI POPROTEINS
,..'.J. \ l+-LI POPROTEINS
장내의 림프 흐름이 증가되며 또한 석이지방 268) 과 식이지방 아닌 지방 269) 의 유출이 증가했다. 이런 현상의 결정적인 주요 요인은 에 탄올에 의 해 자극을 받아서 림 프 장내 순환 (s p lench i n i c circ ula- ti on)210 - 2) 과 장막간의 순환 (mesen t er i c lym p h fl ow) 이 활발해지기 때 문이 다. 268) 그러나 에탄운로 인한 림프물질의 증가 정도는 에탄올을 만성적 으로 먹인 취에게서는 감소되며 3~ 4 주일 동안 에탄운을 먹인 쥐에 게서의 림프지방의 유출량은 에탄올을 먹이지 않은 표준군과 크게 차이 가 나지 않았다는 보고도 있 다. 268) In v i vo 나 in v it ro 연구에서 림프지방 유출의 변화는 장내 지방 대사의 변화와 상호관련아 없는 것으로 본다 . 12~20 시간 동안 많 온 양의 알코올을 머였거나 또는 만성적으로 알코올울 먹인 쥐에게 서 는 소화장기 에 서 지 방산의 산화 273) 와 중성 지 방합성 273- 6 ) 그리 고 콜레스데몰 합성“이 모두 증가되었다. 그러나 이러한 증가는 림 프지방 유출의 증가오H 근 관련이 없는 것으로 본다. 그러나 이 결과와는 반대로 1~3 시간 동안 급성으로 에탄올을두 여하면 지방산의 산화나 지방산의 에스텔화가 소화장기에서 감소되 나 2 73) 여 전히 림 프지 방의 유출은 중가되 었 다. 268) 이상의 모든 결과를 종합해 보면 식이에 함유된 지방이 에탄올 로 인한 지방간형성과 어떤 관련이 있을 것으로도 보나 지방간형성 에 장내에서 흡수된 지방아나 소화장기에서 생성된 지방의 증가가 주요 원인이 될 수 없다고 생각한다. ® 지 방조직 으로부터 지 방산 유출의 증가 한 번에 많온 양의 에탄올을 두여했을 때는 간에 지방이 축적되는 현상과 유사한 현상이 지 방조직 에 도 나타난다. 194),278) 에 탄올이 혈청내 유리지방산 농도에 미치는 영향은 섭취된 에탄올의 양에 달려 있 다. 적 당량의 알코올을 사람이 마셨을 때 (0. 5~lg/ k g Body We ig h t /hr) 유리지방산의 혈청내 농도는 짧은 기간 동안 급하게 떨 어 진다 . 279) 그리 고 유리 지 방산의 분해 (tur nover) 량도 감소되 고 280) 참 정 적 으로 순환되는 글리 세몰 양도 감소된다. 281 ) 이 때 유라지 방산의
유출의 방해 는 acet at e 에 의 해 서 발생 된 것 으로 보며 이 acet at e 는 간에서 에란을이 산화되어 생성되는 주요 마지막 물질이다 .208) 이 현상과는 반대로 에탄올이 주어지는 양에 따라서도, 즉 혈엑 에탄 올의 수준이 200m g /100ml 가 되면 혈청내 유리지방산의 농도가 증 가된다. 282-3) 섭취하는 에탄올의 양에 따라서 지방조직으로부터 지방산의 유 출양상이 다르다고 본다. 죽 과음을 하면 치 방조직 으로부터 지 방산 의 유출이 증가되 며 이 는 cat h echolarnin e 의 유리 를 동해 서 생 긴다 고 생각된다. 그런데 적당한 양을 마시면 오히려 반대로 지방산의 유출이 감소되는 결과가 나타났다. 이 결과는 ace t a t e 생산을 통해 서 생기는 결과라고 본다. 그러므로 술을 마십으로써 생기는 지방 조직으로부터의 대사는 일률적으로 결론짓기는 어렵다. ® 간의 지방산 흡수력의 증가 적당량의 에탄을을 마시면 지방조직으로부터 유출되는 지방산의 양은 감소되 지 만 간에 의 해 서 흡수되 는 지 방산의 양은 중가된다. 284) 왜냐하면 알코올 섭취로 인해서 혈액의 흐몸이 증가하기 때문이 다. 285) 복강내 로 소량의 에 탄올을 주사해 주면 (o. 7g /k g Body Weig h t) 간 에 의해서 흡수되는 지방산의 양은 중가되며 따라서 간에 지방축적 이 생간다 .284) 그러나 만성적으로 알코올을 섭취할 때 치방간이 생기는 기전에 대해서는 더 규명해야 하는 과제로 남아 있다. @ 간에서 지방합성의 중가 처지방식사와 함께 알코올을 두여하면 간장내에 내자 (endo g enous) 지 방산합성 이 증가되 어 서 축적 된다. 93-5) 합성 된 지 방산의 선행 물질 온 섭 취 한 당과 에탄올로부터 공급되 었다고 본다. in vit ro 연구에 서 에탄올의 많은 부분의 탄소가 지방산을 구성하는 탄소로 영합 됨 이 밝혀졌 다. 286-7) In vit ro 연구에 서 는 에탄올로부터 의 대 사산물인 탄소 2 개 의 물 질은 간내 에서 이 용이 되 지만 이 들의 대 부분은 acet at e 로서 순환혈
액내로 분바되며 결국 말단조직에서 CO2 로 산화되어 버란다. 그 러므로 간장내에서 에탄올이 간지방으로 전환되는 가능성은 상당히 제한되어 있다. 한편 py ruva te187) 와 ace t a t e288) 가 간장내 에 서 지 방으로 영 합될 때 에탄올이 촌재하면 지방으로 전환되는 양이 증가된다. 에탄올이 아닌 다른 선행물질로부터 지방산이 합성되는 율은 번로 영향을 받 지 않거나 오히려 감소된다 .287 - 8), 2 90 - 1) 이 현상으로 미루어보면 aceta t e 의 간내 지 방산합성 에 서 의 공헌은 mi toc hondria 내 에 서 지 방산탄소사숟의 증가이 지 de novo 합성 에 참여 한 것은 아닌 것 으로 생각한다 .2 5 ~) 이 상 의 모든 증거를 종합해 보아도 에탄올로 인한 간지방 합성 의 증가와 따라서 지방축적이 증가되는 기전은 분명히 구벌되지 않 은 문제로 남아 있다고 생각한다. ® 간내에서 지방산 에스텔화의 증가 섭취된 에탄올의 산화가 ADH 에 의해서 이루어지떤 간세포내의 NADH/NAD+ 울이 중가한다. 이 런 조전하에 서 는 dih y d roxy :ice to n ph osph ate 로부터 a-gl y c erop h osph ate 의 생 성 이 유리 하게 된다. 186) a-gl y c erop h osph ate 의 생 성 이 증가되 는 상태 에 서 간세 포를 에 탄올 과 함께 부화시키면 중성지방과 인지방의 형성이 중가되는 여건이 된다 .19 2 ) 또한 in v i vo 연구에서 에탄올을 두여한 쥐에서 동위원소 처리된 글리세폴이 간세포 중성지방에 현저히 영합되고 있음이 밝혀졌고이 보다 좁은 법 위 도 ph osph ati dy !ch olin e 과 ph osph ati dy le th a nolami ne 으로 영합되고 있음이 보고되었다 .292) 이러한 중성지방합성의 중가의 기전율 규명하기 위해서 이 작용에 관련된 효소의 활성에 대해서 관십을 두고 관찰되었다. 실제로 에 탄올을 섭 취 하면 간세 포의 mi cr osome 내 에 서 L-a-gl y c erop h osph ate acy lt r a nsfe r ase 활성 이 증가되 었 음이 관찰되 었 고 293) mi cr osome 내 의 다른 ac y l t rans fe rase 활성도 증가되었다 .294) 그런데 후자의 효 소는 인지방 합성에 관계하는 효소로서 이의 활성은 에탄올과 함께
섭 취 된 지 방산에 따라서 좌우된다고 한다. 294) 이 상의 mi cr osome enz y me 활성의 증가도 만성적인 에탄올 섭취로 인해서 유발되는 endop la smi c reti cu lum 의 증석 과 관련 이 있 다고 생 각한다. @ 간내 콜레스테불합성 증가 만성적인 알코올섭취로 인한 m i crosome 내의 또 다른 번화 는 콜 레스테롤합성의 중가이다. 실제로 에탄올을 두여한 쥐의 간 절편에 서 동위원소 처리된 ace t a t e 가 콜레스테 롤 로의 영합이 중 가되었다. 그러 나 에 탄올 없 이 간 철편을 aceta t e 와 배 양시 켜 도 중 가하 였 다. 295) 한편 간내 의 콜레 스테 -문 합성 증가는 ph enobabeta l 과 같 은 약 을 두 여 했 을 때 도 생 기 는데 이 때 endop la smi c reti cu lum 이 층식 되 는 것 을 관찰할 수 있었다 .296) 그런데 이란 상대에서는 에탄 을- 투여 괘 와는 다르게 간장내 콜레스테롤의 축적이 일어나지 않았다. 그 런 대 에 탄올로 사육하면 choleste r yl este r 함량이 증가된다. 22~) 그러 나 콜레스테물의 에스 텔 화는 급성으로나 192) 만성으로 29 7) 에탄운을 두 여하여도 별다른 영향이 없음이 관찰되었다. 이 사실온 간세포내 에 에탄올로 인해서 생기는 콜레스데롤의 축적은 생산량의 증가보 다는 조직 밖의 조직으로 이동되는 양이 감소된 결과로 생각할 수 있다. ® 간내에서 지방산의 산화 감소 에 탄올로 인한 지 방산의 산화 감소는 in viv o 298' 연구에 서 간 철판이 나 282'•288> pe rfu s ed liv e r, 189' 유리 된 간세 포에 서 192) 나타났 다. 만성적인 에탄올 섭취로 인해서 지방산의 산화가 감소되면 간조 직내에 섭취된 식이지방의 축적이나 내자적인 (endo g enous) 합성에 의해 공급된 지방산의 축적이 일어날 것으로 설명한다. 지방산 산화는 간세포의 m it ochondr i a 에서 이루어진다. 그런데 지 방산 산화의 감소는 이 mi toc hondria 에 기 능적 , 구조적 변화가 온 것으로 볼 수 있다. 앞에서도 지적했듯이 환원동가와 ADH 에 의해 서 알코올이 산화되 떤 c yt os 이 내 에 서 환원이 증가되 며 환원등가는
여 러 가지 shutt le 기 전에 의 해 서 mi toc hondria 내 로 이 동된다. 또한 Krebs cy c le 의 활성 도 감소된다고 하였 다. 왜 냐하면 NAD 를 요구 하는 cy c le 내 의 반응이 감소함으로써 일어 나는 현상이 다. 또한 전 자 전달계 (electi on tra nspo r t cha i n) 는 환원등가를 에 탄울 산화르부터 생성된 것을 사용하는 것이지 지방산의 산화로 인해서 생성된 탄소 2 개로 구성된 물질이 Krebs c y cle 을 동해서 생성된 환원둥가를 사 용하치는 않는다. 정 상적 으로 간의 주요 에 너 지 공급원은 지 방산이 다• 299) 그런데 NADH/ N AD+ 의 비 례 가 에 탄올 산화결 과로 mi toc hondria 내 에 서 중 가되 면 /3- oxid a ti on 은 acy l CoA dehy d rog e nase 와 /3- hy d roxy a cy l CoA dehy d rog e nase 수준에 서 제 한울 받으며 이 결과 사슬이 간 지 방산의 acy l CoA 가 축적 된다. 실제 로 유리 된 간세 포와 에 탄을을 함께 부화시 키 연 /3- oxid a ti on 은 저 조해 진다. 192) 알코올 대사의 결과로 인해서 생기는 m it ochondr i a 의 기능적인 변화에 부과해서 만성적으로 알코올을 남용하여 중독이 된 사람들 에 게 서 세 포의 mi toc hondria 구조에 변화가 온 것 을 관찰하였 다. 죽 m it ochondr i a 가 부어 있었고 따라서 모양이 접혀 있지 않았으며 cris t a e 가 정 돈 되 어 있 지 않 았으며 mi toc hondria 내 부에 crys t a l in 이 생겨 있었음이 관찰되었다. 300-1) 이와 유사한 번화가 실험적으로 재현되었다. 영양적으로 충분한 식사 중 단지 탄수화물에서 섭취되는 칼로리만큼을 에탄올로대치시 칸 식 사물 쥐 , 165) 원숭이 (Baboon), 302> 사람에 게 주었을 때 mi toc hon- dr i a 구조가 위에 제시한 것과 유사한 변화를 나타내 보였다. 이 실 험에 참여했던 쥐, 원숭이, 사람을 모두 알코올중독의 과거가 있있 던 경 우와 86,303) 없 었 던 경 우 228) 의 2 가지 로 나누어 모두 실험 에 포함 시켰다. 그래서 나타난 결과는 영양불량 때문이라기보다는 에탄올 의 직접적인 영향으로 생각할 수 있게 하였다. 이러한 m it ochondr i a 구조의 국단적인 변화는 결과적으로 mi toc - hondria 의 구조를 약화시 켰고, 두과성 을 증가시 켰 다. 304-6) 그리 고 인지방 함유량이 감소되었고 307) 지방산 구성에 변화를 가져왔다 .3C8) Mi toc hondria 내 에 촌재 하는 효소인 glu ta m ate dehy d rog e nase 의
활성이 힐청내에 증가되는 것으로 알코올 중독자에게서 간의 괴사 정도를 알아내는 좋은 척도로 삼을 수 있다고 하였다 •309) Mi toc hondria membrane 이 어 떻 게 변화되 는지 에 대 한 기 전은 모 른다. 그러나 에탄올 섭취로 인해 m it ochondr i a 에서 합성되는 단 백질 합성률이 떨어지는 것에 기인할 수 있다고 지적하였다 •305) M it ochondr i a 의 구조가 극단적으로 변화됨으로써 이와 관련된 기 능에 놀라운 비 정 상중을 나타내 고 있 다. 이 렇 게 변화된 mi tor. h on- dria 는 cy toc hrome a 와 b 의 함량이 감소되 었으며 305) 그리 고 suc-cin y l dehy d rog e nase 활성 도 감소되 었 다. 305 대 10) 이 mi toc hondria 의 호흡능력 (respi ra to r y ca p a city)이 처 조해 지 면 311 - 4) 지 방산화로 생 산된 탄소수 2 개 물질의 산화까지 저 조해 진다. 315-6) 이 오H 근 대 조적 인 현 상으로 지 방산의 fi-o xid a ti on 율은 중가된다. 316) 그러 므로 acety l- CoA 의 축적이 생기며 케톤체 형성이 증가된다. 이런 현상은 만성 적 인 알코올섭 취 후에 나타난다. 사람이 알코올을 섭 취 하면 접 전적 으로 keto nuria 와 keto nemi a 가 발생하며, 이런 현상은 기아상태에서 나타나는 것과 같은 현상이 다. 그러나 혈액내에는 에탄올이 함유되어 있지 않다 .317) 에탄올을 먹인 동물에게서 m it ochondr i a 의 대사변화는 부분적으 로 재 현해 볼 수 있 다. 즉 정 상 mi toc hondria 와 aceta l dehy d e 를 함께 배양시켜 보면 위의 경우와 부분적으로 유사한 대사변화를 나 타낸다. 318) 그런데 aceta l dehy d e 는 에 탄올 대 사산물이 며 , 알코올을 먹 인 동물의 mi toc hondria 내 에 서 aceta l dehy d e 산화가 방해 를 받 고 있음이 나타났다 .319) 더구나 에탄올 과다섭취로 인해서 변화된 mi toc hondr ia 는 aldehy d e 가 손상을 끼 치 는 효과가 보다 더 많이 나 타나고 있 었다. 320) 그러므로 알코올섭취로 인한 손상은 부분적으로는 알코올 산화 로 인해 서 생 성 되 는 aceta l dehy d e 가 mi toc hondria 를 접 전적 으로 손상끼치게 되며 그 결과 지방산산화가 비정상으로 되는 것으로 생 각할수 있다. ® 간내에서 지방산 es t er 의 가수분해 감소
만성적인 알코운섭취로 인한 간장내에 중성지방, 인지방 그리고 choleste r yl este r 의 증가는 이 들 물질 의 가수분해 가 감소되 어 서 생 성되논 현상이다. 이들 물질들의 가수분해는 주로 l y sosome 의 acid lip a se 와 este r ase 에 의 해 서 이 루어 진다. 321- 3 ) Ly s osome 의 lip a se 방해 물질 즉 sulfo n y l ureas 도 간내 의 중성 지 방축적 을 증진시 킨다. 324) 에 탄올 두여 후의 lys o some lip a se 활성 에 대한 자세한 정보는 아직 없지만, 다른 l y sosome 효소를 에탄올의 급성적인 섭취 또는 짧은 기간동안 또 긴 기간동안 섭취할 때의 효 과는 다 다르다고 하였 다. 325- 8 ) 이 에 부과해 서 제 포내 다론 부위 에 존재하는 다른 l ip ase 와 este r ase 활성에 대한 연구도 있다. 이들 중에 는 chy lo mi cr on 이 나 lip o p ro te i n 일부에 포함되 어 있 는 중성 지방과 콜레스데풀을 가수분해하는 것도 있다. 그런데 쥐에게 만성 적 으로 알코올을 두여 하고 난 후에 는 콜레스테 롤 este r 의 가수분해 가 감소되었음이 발견되었다 .29 7) @ 간지방의 담줍으로의 배설 감소 담즙으로 배 설되 는 주요 간지 방은 인지 방(주로 pho sp ha ti dy lc holi ne ) 과 유리 콜레스테롤이다. 그런데 이들의 농도는 담줍내에서 에탄올 을 두여한 쥐에게서 변화되지 않았으나 329) 간장내의 pho sp ha ti dy l- <::holin e 과 este r if ied 콜레 스테 롤의 양은 중가되 었 다. 급성적으로 알코올을 두여했거나 또는 알코올을 만성적으로 쥐에 게 먹여서 혈액내의 알코올의 수준이 증가했을 때 담즙의 분비는 감소하였 다. 330-1) 그런데 이 와는 반대 로 쥐 에 게 알코올이 함유된 식 사를 2~4 주 먹인 후에 3~4 시간 동안 알코올을 먹이지 않았더니 담줍의 흐름이나 담줍영과 관련되었거나 관련되지 않은 담줍의 일 부 분바 가 증가되 었 다. 329,331 ) 그러 나 담줍영 분비 율의 증가는 확대 된 담줍의 p o 이 때 문으로 생 각된다. 왜냐하면 에탄올을 두여한 쥐에게 이 담줍의 분해율이나 <::holi c acid , chenodeoxy c holic ac id 의 분비 가 현저 히 감소되 었 다 .295) 더군다나 에탄올에 의한 사육은 담줍산의 정상적안 생산울 올 감소시키며 이 현상은 콜레스데롤을 먹이고 난 후에 나타난다.
이는 간장내 este r if ied choles t erol 의 농도가 상당히 증가했기 때문 이다 .29 5 ) 이 기전에 대해서는 규명된 것이 없다. 담줍산 분비를 감소시키는 것은 아마도 2 차적인 영 향 으 로 생 각할 수 있 다. 먼저 choleste r ol 7-a hy d roxy la se 의 활성 이 감소되 고 난 후에 나타난다고 지 적 한다. 332) 이 현상의 기 전은 콜 레 스데 롤 의 주 요 분해과정이 막힘으로써 간세포내에 콜레스테 롤 의 축 적이 생긴 것이라고 본다. ® 혈 청 lip o pr o te i n 의 분비 감소 간세 포내 에 서 의 lip o p ro te i n 합성 이 나 혈청 lip o p ro te i n 유리 의 방해 는 여러가지 독소에 의한 지방산 생성기전으로 제한되어 왔다. 즉 사영 화탄소 333) 에 티 오닌 334) oroti c acid 3 35> 그리 고 식 사내 cholin e 246) 이나 단백질 336-7) 의 결핍을 들 수 있다. 그란데 이 러 한 지 방간과는 반대 로 사람과 2 36), 262 ) 실험 동물 2 47),339) 에 게 서 만성 적 인 알코올의 섭 취 는 hy po lip e mi a 보다는 hy pe rlip e mi a 와 관련이 있다. 간이 손상되 기 시 작하는 단계 에 서 는 간장내 의 lip o p ro te i n 의 혈액 내 로의 유출이 증가되 어 서 serum hy pe rlip e mi a 가 생 성 된다. 그런 데 이 유출되는 통로가 막히는 것은 간의 지방중이 되는 초보 기전 으로 간주된다. 여 하튼 lip o p r ote i n 의 간내 의 보유는 생 산이 증가되 고 충분한 분 비가 되지 않을 때 생기는 증세이다. 에탄올은 간장내의 다른 수 출용 단백질의 분비를 방해한다. 이는 간장의 미제관 (m ic ro t ubules) 의 감소와 관련이 있 다. 241 ) 간조직 의 미 세 관의 변화는 colchic ine 둥의 다론 약 두여 에 의 해 서도 생기며 이렇게 되면 l ip o p ro t e i n 분만이 아니라 단백질의 분바 까지 방해 한다. 340-1) (3) 간세포내에서 지방산화와 케론체대사 사람은 하루를 지나는 중에 식사를 하여 음식을 취한 후 몇 시간
동안 굶다가 다시 섭취하는 것을 반복하게 됨에 따라서 간장은 탄 수화 물 을 이용하는 장기에서 지방산을 합성하는 장기로 전환하며 또한 지 방산을 산화하고 케론체를 생성하는 작용을 반복하게 된다. 이러한 복잡한 작용에 나타난 현저한 적응은 조직내에 존재하는 단 한 가지 물질 인 malony l CoA 의 농도에 의해서 이루어진다. 그리고 부수 적 으로 fatty acy l CoA 와 carnit ine 의 수준이 변화하는 것 에 의 해 서 영 향을 받는다. 이 러 한 생 화학적 인 변화는 인슈린과 glu ca- g on 의 주 요 역할에 기인한다. 최근에 이해되어지고 있는 이 조철기전의 필수현상은 다음과 같 다. 탄수 화물을 먹 인 상대 에 서 는 glu cag o n/in s ulin 의 바 울이 낮으며 간내 의 지 방산대 사방향은 합성 쪽으로 향하게 되 고, 지 방산의 산화 는 그치 게 된다. 왜 냐하면 조직 내 의 malony l CoA 의 수준이 높아 지 기 때 문이 다. malony l CoA 는 지 방산 산화의 시 작단계 를 촉진시 키 는 효 소인 carnit ine acy l- tr a nsfe r ase I 의 방해 인자로서 작용한 다. 반대로 g luca g on / i nsul i n 의 바가 높아지면 이는 keto t i c 상태에서 일어나며 이때는 malony l CoA 의 합성이 여제되며 참정적으로 지 방산의 산화와 케본체 합성작용의 활성이 높아진다. 자동적으로 간 세 포내 의 carnit ine 과 fatty acy l CoA 함량이 증가되 고 더 나아가 서 ;3- oxid a ti on 이 증가되 고 aceto aceta t e 와 3-hy d roxy b uty ric ac id 함량이 증가된다. 1) 케톤체 합성파 이용 ®합성 간에 서 지 방산 산화를 통해 서 생 성 된 acety l CoA 는 HMG-CoA c y cle 의 여러 반응을 통해서 케론체를 중가시킨다. 2 acety l CoA .=:e aceto a cety l CoA + CoA (i) aceto a cety l CoA+acety l CoA ---+ hy d roxy m eth y lg l u ta r yl CoA+CoA @ hy d roxy m eth y lg l u ta r yl CoA ---+ aceto a ceta t e + acety l CoA @
aceto a ceta t e + NADH+H+ ~ hy d roxy b uty ra te + N AD+ @ 위 의 ®~@까지 의 작용을 가능케 하는 효소는 aceto a cety I CoA th io l ase, HMG CoA sy n th a se, HMG CoA lya se 와 D-3 hy d roxy - buty ra te dehy d rog e nase 둥이 다. 342) 이 상의 4 가지 효소가 모두 간 조직 이의의 신장, 십장, 소장의 조직내에 모두 존재하나 이 전체 작용의 속도조철에 영 향력 이 강한 효소 (Ra t e- li m iti ng en z y m e ) 는 HMG CoA s y n t hase 인데 이를 간조직이 다량 함유하고 있어서 간장이 케 본체 합성 의 주요장기 라고 생 각하게 되 었 다. 343) 케 돈체 는 aceto a ceti c acid 와 3-hy d roxy b uty ri c acid 와 aceto n e 을 합쳐 서 말한다. 쥐 의 군절된 간조직에서 acety l CoA 를 포화상태로 첨가하고서 37°C 에 서 배 양시 키 면 간조직 매 gr 당 한 시 간에 200~250µmol 의 aceto - aeta t e 를 생 성 한다고 보고되 었 다. 344.、 이 상의 보고로 미 루어 보면 간 조직 의 aceto aceta t e 합성 능력 이 상당히 크다는 것 을 알 수 있 다. @이용 간에 의해서 생성된 케본체는 쉽게 혈액으로 스며나가서 간조직 밖으로 이 동된다. 그래 서 다시 케 론체 는 acety l CoA 로 전환이 되 며 이는 Krebs c y cle 의 여러가지 작용을 거쳐서 물과 CO2 로 완전 히 연소된다. 이러한 전환은 다음의 작용에 의해서 영향을 받는다 고 생각한다. 3-hy d roxy b uty ra te + NAD+ +± aceto a ceta t e + NADH+H+ @ aceto a ceta t e + succi ny l CoA +± aceto a cety l CoA+succi na te @ aceto a cety l CoA+CoA 구 2 acety l CoA cr) 위의 작용 ®와 ®은 케론체 생성과 이용과정으로 보편적으로 나 타나는 작용이 다. 이 에 관련된 효소는 D-3-hy d roxy b uty ra te dehy - drog e nase 와 aceto acety l- CoA th io l ase 로서 신체 내 모든 조직 에 년 리 분포되어 있다. 그런데 이 연속작용 ®~®의 속도를 제한해 주 는 작용은 @이 다. 이 작용은 3-oxoaci d CoA tra nsfe r ase 에 의 해 촉진되는데 이 효소는간조직을 제의한 신체 모돈조직내에 분포되어 있다. 그렇기 때문에 간조직은 케본체 대사를 못하는 장기이다 •342
쥐 의 조직 에 서 밝혀 진 바에 의 하면 aceto a cety l CoA th.i o l ase 는 2 가지의 i soz y me 으로 A 형과 B 형이 촌재한다 .346) 신체 모든 조직 울 조사해 본 결과, 거의 B 형을 함유하고 있는데 오로지 간조직만 은 A 형 이 높은 양 함유되 어 있 음이 나타났다. 그래 서 iso zy m e A 는 HMG-CoA 대사과정을 통해서 케돈체 합성과정에 관련되고 득 히 acety l CoA 로부터 aceto a cety 1 CoA 합성 을 촉진한다고 한다. 그 런 데 iso zy m e B 도 aceto a cety l CoA 를 thi o l ys is 해 서 acety l CoA 합성 을 촉진한다고 생 각한다. 이 작용은 /3- oxid a ti on 에 서 나 ace- to aceta t e 이 용시 에 흔히 일어 나는 과정 이 다. 2) 케톤체 합성조절 신체내에서 케돈체 과잉상대는 지방조직으로부터 지방산이 유출 되어 생기며, 이런 경우는 흔히 인슈란결핍의 결과로 나타난다고 알려 져 왔다. 또한 지 방산과 케 본체 와의 관계 는 pr ecursor 와 pro duc+ 의 관계로 알려져 왔다. 케돈체 과잉상태에 있는 동물의 혈액내에는 치방산과 케본체의 함량이 높다• 이런 경우에 케본체 합성률이 높 은 간으로 이동되는 지방산의 이동물에 의해서 주로 결정된다고 이 해 되 어 왔다. 299), 347-9 ) Scow 와 Chern i ck 는 250) 췌장절제로급성당뇨병이 생긴 쥐에게 준 키 아식 (semi sta r vati on d i e t)을 주어 봄으로써 keto s is 가 없어 지는 연 구결과를 발표하였다. 이는 지방조직내에 처장된 지방 죽 케돈체의 전구체가 없기 때문이라고 하였다. 이 결과와 관련하여 기아로 인 해서 생긴 가벼운 ke t os i s(2~5mM) 때는 혈액내의 지방산 함량수준 이 1mµ 을 능가하지 못하는데 29),351) 조철되지 않는 당뇨병의 경우 혈액내의 지방산함량이 2~4mM 로 증가되면서 최대치의 케론체 형 성 죽 농도가 2omM 에 달하는 경 우가 발생 하였 다. 352-3) 더 구나 alcoholi c k eto a cid o sis 의 증세 는 당뇨병 이 없는 사람에 게 서 나타났으며 ,354-5) 이 경우는 에탄올의 섭취로 인해서 지방조직 으로부터 지방분해과정이 강조되며 따라서 혈액내에 유리된 지방산 의 함량수준이 마치도 조절되 지 않은 당뇨병 대 나타나는 keto a ci - dosis 와 같은 수준으로 나타났다.
그런데 한편 신체내 케돈체의 생산층가 없이 혈액내에 유리지방 산의 함량이 증가될 수 있다는 결과가 in v i vo 연구에서 나타났 다 .356 - 8) 그리고 반대로 ke t os i s 가 사라쳐도 여전히 혈 엑내의 유리 지 방산의 함량은 중가된 채 로 유지되 었 다는 보고가 있 다• 359- 6 0) 이상의 결과를 함께 고려해 보면 간에 의한 케돈 체 의 생성은 간으 로 들어오는 지방산의 속도에만 오로지 의촌된다고 생각되 지 않~ 다. Perfu se d 된 쥐 의 간에 서 같은 수준으로 지 방산 을 공급하 였 어 도 간에 서 aceto a ceta t e 나 3-hy d roxy b uty ra te 가 생 성 되 는 양이 같 지 않았다. 이러한 차이는 지방산울공급받는 동 물 의 식이섭 취 후 여~ 와 당뇨병 존재 유무에 따라서 모두 다르게 나타났다. 67) ,36 1 - 4 ) 이 현 상은 동물의 간에 공급되어지는 유용한 기질의 양의 증가분 아니 라, 간자체의 기본적인 대사의 변화가 케본체합성에 팔수적으로 고上 련이 되어 있다고 생각한다. ® 케론체 합성조철부위 기 Acety l CoA 합성 과 이 용의 중요성 사슬이 건 지방산이 간세포내에 들어온 후의 주요 처리경로는 1 림 12 과 같다. 지 방산은 간세 포내 의 mi to c hondria 밖에 서 acy l CoA 유도체 로 활 성 화되 고 나면 두 경 로에 의 해 서 대 사된다. 그중의 한 길은 gly c erol- 3- pho p ha t e 가 에스텔화되어서 인지방이나 중성지방 합성을 할 때 쓰일 것 이 고 또 한 길은 그림 12 에 보여 주듯이 mi toc hondria 내 로 carnit ine acy lt r a nsfe r ase 의 영 향하에 서 이 동된다. mi toc hondria 내 에서논 acety l CoA 생산을 하면서 지방산이 참정적으로 산화된다. 생성된 acety l CoA 는 여러가지 대사과정을 동해서 대사된다. 즉 Krebs cy c le 을 통해 서 산화되든가 또는 지 방합성 작용에 쓰이 든가 아니 면 HMG CoA 의 작용에 의 해 서 단계 적 으로 작용해 서 aceto - aceta t e 와 3-hy d roxy b uty ric aci d 를 합성 한다. 간조직 내 의 aceto a ceta t e 합성 을 위한 최 대 활성 의 효소능력 때 문에 정 상 쥐 나 keto t i c 쥐 에 서 모두 aceto a cete 합성 은 같다고 본다. 344)J 3 ·4 6 >
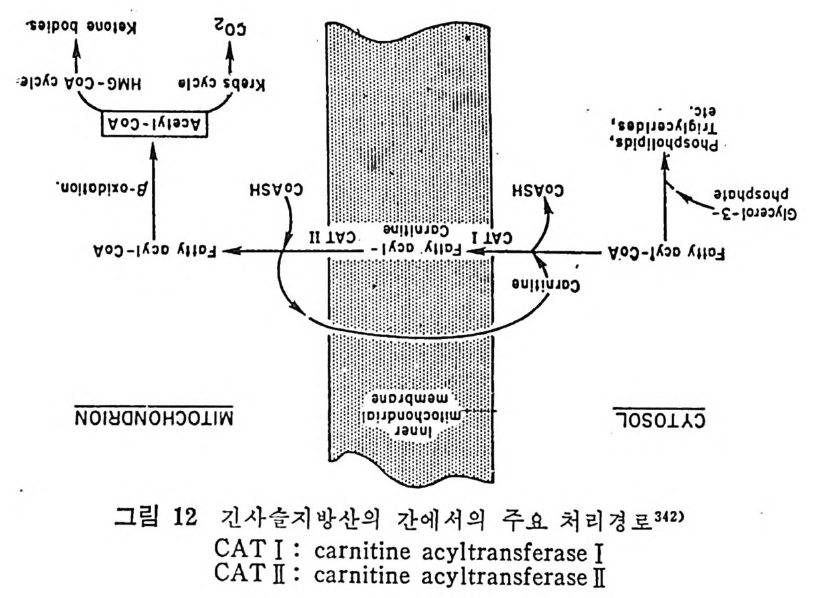 'apI Pk 3u ov二oqto 3 oV-u9OoH,3.-HxIK 3D A·I,O ,K。3』 % 노st q3 o 』H )IS VO3 \\;!三: l::\::!;::i: \ \i : v:o:3 :』갑::* ;0;?. :I;인업』?,}f 9
'apI Pk 3u ov二oqto 3 oV-u9OoH,3.-HxIK 3D A·I,O ,K。3』 % 노st q3 o 』H )IS VO3 \\;!三: l::\::!;::i: \ \i : v:o:3 :』갑::* ;0;?. :I;인업』?,}f 9
이 결과로 케톤체 형성물은 acety l CoA 농도에 좌우되거나 또는 합성부위의 acety l CoA : 유리 CoA 의 비례에 더 의촌된다고 본 다. 365- 7 ) 이상의 결과는 간세포내에서 주어전 지방산에 의한 케본체 생성 이 간내 에 서 의 acety l CoA 합성 능력 에 달려 있 다고 보며 나아가서 acety l CoA 가 케본체합성 대사과정 이외의 대사과정으로 처리되는 능력 또한 결과적으로 케톤체 생성에 영향을 미치게 된다. L Acety l CoA 의 이 용 Lehnin g e r 에 의 하면 368) 군질 된 취 의 간에 서 oxaloaceta t e 를 포함 해서 여러가지 전구체물질들을 중간 사슬길이의 지방산 산화를 위 해 작용시 켜 보았더 니 Krebs cy c le 의 중간대 사산물의 축적 과 더 불 어서 ace t oace t a t e 의 형성이 저조해지는 결과가 나타났다. 이 결과 룔 Krebs c y cle 의 활성과 in v i vo 에서의 케론체 형성 사이에는 찬 밀한 관계가 있는 것으로 설명하였다. Keto t i c 간에 서 특히 십 한 keto s is 때 관찰해 보면 oxaloaceta t e 의 쳐핍으로 Krebs c y cle 의 활성이 처조해 있는 조건이 바로 생성된
ke t os i s 의 원인으로 생각해 볼 수 있다고 지적하였다. 그런데 oxal-oaceta t e 함량의 감소 원인은 첫 째 , 세 포내 의 redox po te n ti al 이 증 가함으로 인해 서 malate 로 전환되 든가 369) 또는 glu coneog e nesis 가 중가해 서 포도당으로 전환되 기 때 문이 다. 370) 또한 cit ra te syn th ase 작용의 직 접 적 인 방해 가 Krebs cy c le 내 에 서 acety l CoA 산화를 감 소시키는 기전으로 제안되기도 했다 .371 - 2) 이상의 제시된 결과와는 다르게 쥐의 pe rfu s ed 간에서 케톤체합성이 중가되는 여러 상황에서 도 Krebs c y cle 은 저조해지지 않았다는 보고도 있다 .373 - 4) 그러나 케톤체합성이나 Krebs c y cle 의 활성은 모두 동물의 기본적인 조전 인 먹었을 때, 굶었을 때 또는 당뇨병이 있을 때에 따라서 밀접한 관련이 있다고 생각한다. 찰 먹인 동물의 간에서는 케돈체합성이나 Krebs c y cle 의 활성이 모두 증가되 면서 동시 에 octa n oate 의 농도도 증가된 것 으로 지 적 하 였 다. 342) 지 방산의 산화율이 대 단히 높을 때 만이 Krebs cy c le 이 저 조되 는 것 이 라고 생 각한다. 이 사실은 Krebs cy c le 활성 의 감소 가 지방산이 케본체로 전환이 되는 원인이 되기보다는 차라리 지 방산이 높은 수준으로 산화되기 때문에 생긴 결과라고 생각하는 편 이 타당할 것으로 본다. 이 상의 모돈 보고와 연구를 종합해 보면, acety l CoA 의 처 리 속도 가 바르 케론체 형성과정을 통하는 탄소의 흐름속도를 결정해 주는 것으로 생각할 수 있다. 죽 acety l CoA 의 이용률이 바로 케돈체 형성률과 관련이 있다고보며, Krebs c y cle 의 활성변화보다도 지방 산 합성속도의 변화가 더욱더 케본체합성에 영향을 미찬다고 생각 한다. c Acety l CoA 의 합성 Acety l CoA 의 처 리 보다는 acety l CoA 의 생 산이 케 톤체 생 성 조 철에 더 중요하다고 생각했다 .375) 이 연구자들은 전체 동물의 모든 간 절편에서 찰 먹인 상태에서의 동물이 굶거나 당뇨병이 있는 동 물에 비 해 팔미 트산의 /3- oxid a ti on 이 십 하게 제 한울 받고 있는 결 과를 보여주었다. 이 결과는 후에 May e s & Fe tt s 에 의해서 다시 확인되었는데 67).
굵은 쥐 의 pe rfu1 :;ed 된 간에 서 동위 원소로 처 리 된 oleate 가 중성 지방으로 영합되는 울은 거의 없으며 동시에 케톤체로의 산화도 중 가되었다는 보고를 하였다. 또 한편 케돈체 생성률이 잘 먹인 동물 의 간과 굶은 동물의 간에서 같지 않았다. 364),376) 위의 보고를 종합해 보면, 간세포 내 지방산의 산화와 또한 케돈 체합성 전과정의 주요 조철은 간 사슬 지방산의 에스텔화와 산화를 따로 구별해서 생각해야 될 것으로 본다. 그런데 에스텔화의 능 력이 오히려 이 접의 지방산 대사에 있어서 분기접이 된다고 보는 ~ 견해가 많이 있다. 또한 에스텔화는 전적으로 gly c erol-3-ph osph ate 의 이 용가능한 양에 의 촌한다고 한다. 67),299),377) 따라서 인슈란이 결핍된 상태에서 간세포내의 지방산 산화율의 중가는 이차적인 영향 으로 생 각된다. 죽, 지 방산 산화율의 중가는 gly c erol-3-ph osph ate 수준이 처하된 결과 에스번화의 능력이 없어지니까 일어나는 현 상으로 본다. 이 현상은 인슈린이 사술이 간 지방산으로부터의 케 본체형성을 방해하는 것은 호르몬이 중성지방 합성을 자극하는 눙 력 이 있 어 서 이 를· 자극한 결과라고 생 각한다. 또한 octa n oate 가 케 돈체 형 성 을 자극하는 것 은 에 스텔화를 지 나쳐 오히 려 p-o xid a ti on s y s t em 으로 들어가기 때문으로 설명할 수 있다. 이상의 관찰결과와 일치하지 않는 보고도 있다. 첫째 Wi lliam son 과 그의 동료는 쥐에게서 기아로 인해 생간 ke t os i s 를 복귀시킬 수 있 는 여 러 가지 물질들과 간내 의 gly c erol-3-ph osph ate 농도 사이 의 상호관계 가 없다고 주장하고 있 다. 359) 둘째 는 찰 먹 인 동물과 굶은 동물의 간내 의 gly c erol-3-ph osph ate 의 농도를 측정한 결과 오히려 굶은 동물에게서 높온 양을 보여주 고 있 다. 364),378) 반대 로 간의 gly c erol-3-ph osph ate 농도는 oleate 로 부터 케본체합성의 감소 없이 몇 배로 올릴 수 있다고 보고되었 다. 364) 세째로 굶온 동물의 간에서 oleic a ci d 의 산화는 (+)decanoy l- carn iti ne 에 의해서 방해되었을 때 지방산은 즉시로 중성지방이나 인지 방으로 영 합되 어 들어 간다. 29) 비 슷한 결과를 alloxan 당뇨로서 십한 ke t o ti c 상태에 있는 쥐의 간에서 얻었다 .379-80) 실제로 이러
한 상태하에 있는 동물의 간에서는 중성지방 합성을 위한 효소의 능력이 항전되어 있었다 .38 1) 네 째 , 실험 적 으로 dia b eti c keto a ci do sis 를 발생 시 킨 쥐 에 서 hy - p erke t onur i a 가 생겼는데 이 상태에서 간에 지방의 축적이 생겼 다 .352) 이렇게 기대치 않았던 결과가 발생한 것은 중성지방 합성 이 (3- oxid a ti on 이 포화상태 로 발생 함으로써 흘러 새 어 나온 치 방산 에 의해서 이루어진 것으로 본다. 이상의 여러가지 실험결과를 종합해 보건대, 간세포내에서의 지 방산 산화는 에스텔화와 산화 사이에서 산화쪽으로 이루어진다고 생각해 볼 수 있다. 그러나 에스벨화와 산화의 분기접은 동물이나 사람의 그 당시 신체의 상태 죽 먹었을 경우, 굶었을 경우 또는 당 뇨병 의 유무에 따라서 영 향을 받는다고 생 각하며 이 영 향은 acety l CoA 합성에까지 미치게 된다. ® Carnit ine acy lt r a nsfe ra se 의 역 할 Octa n oic aci d 는 먹 인 동물이 나 굶 7, 1 동물이 나 당뇨병 이 있 는 등 물의 간에 서 모두 유사한 울로 acety l CoA 로 산화되 는 것 이 관 찰되었다 .363) 이 사실온 간세포 내에서 사슬이 긴 지방산 산화율의 조절은 mi toc hondria 내 로 들어 갈 때 이 루어 진다는 증거 를 보여 준 것 이 다. octa n oate 는• mi toc hondri a 내 로 들어 갈 때 carnit ine 과 무 관하게 들어 가지 만 사슬이 간 지 방산은 득벌히 carnit ine acy lt r a n- sfe r ase 에 의 해 mi toc hondria 내 로 들어 간다. 이 는 동물의 상태 에 따라서 산화율이 다르게 나타나므로 사슬이 긴 지 방산의 산화조철 의 첫단계는 바로 이곳에서 이루어진다고 생각할 수 있다. 이 전부터 carnit ine acy lt r a nsfe ra se 가 유리 된 mi toc hondria 에 서 겨 방산산화율 조철을 위한 효소라고 생 각해 왔다. 299,365) 그러 나 쥐 간의 mi toc hondria 에 서 분리 해 낸 tra nsfe r ase 활성 온 분석 해 낸 /3- oxid a ti on 효소를 능가하였 다는 근거 에 서 이 결과가 도전을 받았 다 .382-3) 그러나 많은 연구자들에 의해서 이 도전에 대한 재도전 울 받았다. 384-5) 아직 까지 carnit ine a~y lt r a nsfe r ase 의 지 방산 산 화조철 작용에 대해서 일치된 의견을 . 보지 못하고 있지만 이 효소
가 지방산 산화의 조절에 영향을 미찬다고 보는 견해가 보다 농후 하다. ® 호르몬이 케돈체 합성조철에 미치는 영향 만일 에 위 에 서 지 적 했 듯이 carnit ine acy lt r a nsfe r ase 의 작용이 간내에서 지방산 산화의 조절접이 된다면, 이 효소의 작용을 활성 시켰다가 비활성시켰다가 하는 조절은 영양상태와 호르몬의 조철상 태에 따라서 관련이 큘 것으로 보인다. 쥐 의 간에 서 oleic acid 물 aceto a ceta t e 와 3-h y d roxy b uty ra te 로 산화시키는 능력이 증가되려면 쥐가 굶은지 6 시간 후라야 나타나며 곧 이어서 다시 반복해 보면 3 시간 정도의 빠른시간에 나타나는 적 웅이 있게 된다. 이러한 적응은 쉽게 반복이 된다 .29) 모든 ke t o ti c 상태에서는 순환되고 있는 인슈린의 양이 떨어지기 때문에 케본체합성이 활발해지 는 것이 이 호르몬 하나만의 변화로 이루어지는가 하는 의문이 제기될 수 있다. 그러나 인슈린 작용에 서로 길항(j 吉섭L ) 작용을 하는 g luca g on 조철이 있기 때문에 복잡하 다. 이 g luca gon 의 혈청 내 양은 인슈린의 양이 떨어졌을 때 중가 된다. 386- 8 ) 이 두 종류 호르몬의 역할을 관찰하기 위해 in v i vo 연구믈 하였 다. 며인 쥐에게 항인슈린 혈청으로 처리하였고, 또한 g luca g on 을 1~3 시간 동안 주입한 후에 여러가지 대사현상을 관찰하였다 .389) 항 인슈린 혈청으로 처리한 쥐에게서는 기대했던 대로의 대사현상이 나타났다. 죽 hy pe rgl y c emi a, 간장내 glu cag o n 의 감소, 혈청 내 유 리지방산과 케돈체 함량의 중가가 나타났다. 그러나 이와는 대조적 으로 g luca g on 을 주입한 동물에게서는 혈청내 포도당, 유리지방산 과 케본체에 대한 농도의 변화는 벌로 없으면서 항인슈란 혈청대 와 마찬가지로 간내의 g luca gon 변화를 가져왔다. 의심할 여지없이 항인슈린 혈청을 주입하였을 때는 간의 g luca g on 의 유출속도는 빠 르고 혈정내에 유출된 포도당은 말단조칙에 의해서 취해져야하는데 인슈린 결핍으로 취해지지 못하니까 혈청내에 h yp er g l y cem i a 가 생 간 것이다. 그런데 g luca g on 울 주사하면 자연히 췌장의 인슈란 분
비 가 촉진되 어 참정 적 인 hy pe rgl y c emi a 가 나타나며 시 간이 경 과 되면 곧 혈청내 포도당을 말단조직에서 취해 가서 대사될 것이다. 또한 인슈린이 지방조직으로부터 지방분해작용을 억제할 것이며 따 라서 지 방산 유출이 방지 될 것 이 다. 390-1 ) 항인슈린 혈청과 g luca g on 의 혈청내 케톤체 함량에 미치는 영 향이 서로 다른 결과로 나타나는 것은 지방조직으로부터 지방산 유 출 수준이 두 종류의 실험에서 서로 다르기 때문이라고 한다 .389) In v i vo 연구에서 인슈란과 g luca gon 은 케본체 형성시 서로 상호 군형을 이루면서 영향을 미치고 있음이 나타났다. 신체내 대사경향 은 케톤체 형성이 되지 않는 조건에서 케톤체 형성조전으로 기울어 질 때도 분명히 혈청내 〔g luca g o 띠 : 〔i nsu li띠의 함량바가 증가됨으 로써 시작된다. 또 한편 in v i vo 연구에서 ke t os i s 가 발생하려면 순 환하는 혈청내에서 완전히 인슈란이 사라져야 되며 이차적으로 케 론체 합성이 촉진되려면 처장지방으로부터 지방이 유출되어 유출된 지 방산이 간으로 가면 된다. 인슈린과 glu cag o n 의 특정 작용을 농도인 mole 대 mole 로 비 교해 보면 인슈린의 항지 방분해효과 (an tilip ol yti c e ff ec t)는 glu cag o n 의 지 방분해효과(lip ol yti c e ffe c t)보다 크며 또 한편 glu cag o n 의 간조직 으 로부터의 포도당의 유출을 자극하는 효과는 인슈린이 이를 억제하 는 효과보다 크다. 391 ) 이상과 같은 결과는 동물실험에서 나타난 것이지만 두 가지 호르 몬의 케본체 합성에 대한 영향은 사람에게도 유사한 효과를 나타 낸다고 지적하였다 .392-3) 위의 사람을 이용한 두 연구에서 밝힌 바 는 g luca g on 은 간에서 케돈체 합성작용을 항전시키지만 인슈린 온 유리지방산 죽 케론체 합성을 위한 선행물질을 간으로 공급하는 것을 조철한다고 본다. 이 관계는 다음의 그림 13 에서 설명이 되어 있다. 이 모델은 인슈린 결핍이 되면 지방조직으로부터 유리지방산이 유출되 어 서 간으로 들어 가는 것 이 고 〔g luca g o 따 : [i nsu li n] 의 비 례 가 증가됨으로써 간에서 지방산 산화와 케돈체 합성이 증가되는 것 이 다. 394)
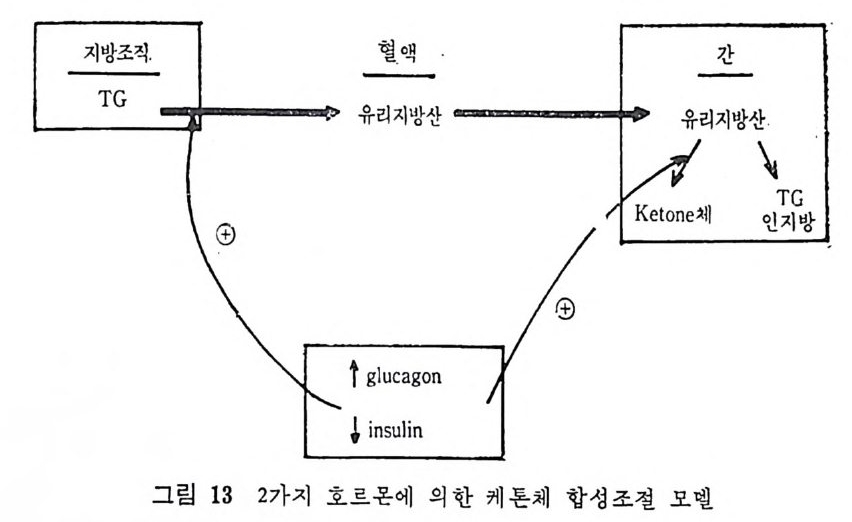 지방조칙 . 혈액 간
지방조칙 . 혈액 간
사 실상 간세포내에서의 케톤체 합성에 미치는 영향을 위시해서 간내 의 대 사는 어 느 한 호르몬작용보다는 〔 g luca go 띠 : [i nsul i n] 의 절대적인 함량 비례가 가장 중요하다고 본다. @ Carnit ine , 굳리코겐과 케톤체 합성에 미치는 호르몬의 영향 〔g luca g o 미 : 〔 i nsu li n ] 의 비 례 가 증가되 면 간세 포내 에 서 케 톤체 합성 이 시 작된다. 이 작용의 시 작은 carnit ine acy lt r a nsfe r ase 작용 이 활성화 되는 것이다. 그러 면 이 호르몬의 바 례 증가와 carnit ine acy lt r a nsfe r ase 활성 의 증가가 일어나는 두 현상이 어떻게 관련이 맺어지는 것인지에 대한 의문이 생긴댜 크게 두 가지 가능한 상황을 생각해 볼 수 있 댜 첫 째 는, 호르몬의 불군형 이 아마도 효소의 활성 물질 (acti va to r ) 울 합성할 수 있다는 생각과 둘째는, 호르몬의 불군형이 효소의 방 해물질(i nh i b it or) 의 손실을 초래할 수 있다고 생각할 수 있으며 구 태여 3 번째 가능성을 생각해 본다면 첫째와 둘째 가능성의 혼합된 작용으로 생각해 볼 수 있다 .342) 첫번째 가능성을 생각해 보면, 간에서 케돈체가 생성되는 모든 상태 죽 기아시, 조철되지 않은 당뇨병이 있을 때와 먹은 상태의 동물에게 항인슈린물질이나 g luca g on 으로 처리했을 때 간세포내에
서 carnit ine 의 생 성 이 증가된다. 그런데 이 c::rnit inc 은 carnit inc , acy lt ra nsfe r ase 의 기 질 이 다. 395) 이 사실을 보다 지원해 주는 실험결과가 나타났다. 잘 며인 쥐의 pe rfu s ed 간에 carnit ine 을 첨 가해 주었 더 니 ole :i te 로부터 의 케 본채 합성이 중가되었다 .395) 이 결과로 미루어 보면 간세포내에서 carnit ;n c 농도의 변동이 간세포에서는 케본체 합성과정이 증가되는 데 중요 한 역할을 한다고 생각한다. 그러나 수유중에 있는 동물에게서는 carnit inc 의 농도 변동만을 생 각하지 는 않는다 . :96) 새 끼 풀 춘산하 고 난 수일 후에 동물이 찰 먹은 수유기 동안에는 간세포내의 carni- ti r.요 함량 이 수유하지 않은 처 녀 쥐 에 미 해 서 2~ 3 배 로 높아전다. 그 L 러나 간에 olea t e 를 p er fu sed 해 주어도 수유중의 쥐에게서는 케돈 합성능력 이 중가되 지 않는다. 그러 나 이 동물 을~ 2.1 시 간 동안 굵기 면 간조직 내 에 carnit ine 의 함량이 소량 증가함에 도 불구하고 케 본체 합성능력이 증가된다• 이러한 현상은 아마도 찰 며인 수유중의 쥐 에 서 일어 나는 유일한 현상으로 보이 며 간내 의 굳리 코겐과 carnit i n e 이 함께 자동적으로 증가했다고 본다. 이상의 결과로 미루어보면 간조직내에 글리코겐 함량을 감소시키 고 carn iti ne 을 강화시키면 지방산을 최대로 산화시키는 조전이 된 다고 본다. 그러 므로 [glu cag o nJ : (i ns ul i n 〕의 비 례 가 층가되 면 간 조직내의 carn iti ne 함량의 증가되고, 방해물질울 이동시키게 되는 데 이 방해물질은 어느 면으로든지 간조직의 굳리코겐 농도와 관련 이 있 다고 본다. 397 ) ® 케돈체 합성조철에 있어서 malony l CoA 의 역할 간내의 지방산 산화와 탄수화물대사가 밀접하게 관련이 되어 있 다는 개념은 오래전부터 알려져 온 것이다. 사실상 간세포내의 굳 리코겐 함량과 케돈체 합성 사이에 상호관련이 있다는 사실은 이미 일찌기 연구자들에 의해서 보고되었다 .398-40 1) 이상의 개념이 50 년대 중반까지는 간세포내의 지방산 산화시 탄 수화물의
중간 대사산물로서, 이의 간조직내 농도는 지방산 합성률과 비례해 서 변동한다. 403-4) 균질된 간에 서 실험 해 보면 malony l CoA 는 oleic acid 산화룬 강 하게 방해하는 물질 이다 •405) 이 효과는 쉽게 전환이 되지만, 다론 종류의 Co A 에스텔둘, 예로서 acet y l CoA, pro p ion y l CoA 또는 meth y lm n lon y l CoA 에 의 해 서 는 이 효과가 나타나지 않는다. Malony l CoA 의 방해 기 전은 car n it ine acy lt r a nsfe r ase I 단계 라 는 사실이 취의 군질 된 간과 간의 mi toc hondria 부위에서 밝혀졌 다. malony l CoA 는 oleate , pa lmi tat e 그리 고 pa lmi toy l CoA 의 산화믈 모두 차단시 키 는데 이 들은 mi toc hondria 내 에 서 산화되 기 위 해 모두 tra nsfe r ase I 과 tra nsfo r ase II 룬 팔요로 하고 있 는 물질 둘이다. Transfe r ase I 는 octa n oate 나 octa n oy lc arnit ine , pa lmi toy l carni- ti ne 과 같은 물질의 산화에 영향을 주지 못한다 .405 구) 이 현상은 tra nsfe r ase 와 inn er mi toc hondria l membrane 과의 관계 에 서 그 기 전이 설명 될 수 있 다. 407 ) 즉 tra nsfe r ase I 은 mi toc hondria 의 inn er membrane 의 곁 에 느슨하 게 결 합되 어 있 고 tra nsfe r ase II 는 안쪽 의 깊은 곳에 결합되어 있다. 2 종류의 tra nsfe r ase 중에서 오로지 tra nsfe r ase I 만이 원형질 쪽에 면해 있으면서 malony l CoA 와 예민 하게 접 촉하게 된다. 그러 드로 malony l CoA 에 의 해 서 tra nsfe r ase 작용이 억제되면 사슬이 간 지방산의 산화도 억제되고 만다. 결국 malony l CoA 가 이 효소를 방해하는 생리적인 물질인 것이다. 그러 나 malony l CoA 가 긴 사슬의 지 방산 산화를 여 제하는 작용 온 간에서분만이 아니라 쥐의 십장과 선장근육에서도 일어날 수 있 다. 406) 그러나 성장이나 선장 근육세포의 m it ochondr i a 밖 원형질내 에서는 지방산 합성작용이 활발하계 일어나지 않으므로 영양상태에 관계 없 이 이 세 포내 에 는 tra nsfe r ase I 의 작용을 방해 할 만큼의 농도 로 .malon y l CoA 가 함유되어 있지 않다. Malony l CoA 의 carnit ine acy lt r a nsfe r ase I 에 대 한 방해 력 은 쥐의 7J- m it ochondr i a 내에서 낮다. 그리고 이 기전에 대해서는 분 명히 알려진 것이 없으나 가능한 기전온 다음과 같이 설명된다.
mi toc hondria membrane 의 자연 적 인 상태 에 서 는 carnit ine acy l- tra nsfe r ase I 이 유리된 상태로 있을 때와는 달리 둥각 (con fo rma ti onal s tat e) 상태 에 있 다. 그리 고 confo rm ati on al 상태 로 있 는 형 태 의 효소 만이 malony l CoA 에 예 민하다. 한편 malony l CoA 가 membrane 의 구성성분에 결합되면 긴 사술 지방산의 acy l CoA 가 효소에 결 합되는 결합특성이 간접적으로 변화한다. 또 다른 가능성 온 malony l CoA 가 지 방산 acy l CoA 가 결 합하는 carnit ine acy lt r a nafe r ase I 의 acti ve sit e 에 ste r ric hin d erance 를 일으킬 수 있는 가능성도 있다. 이와 같이 malony l CoA 의 방해효과 기전은 분명치 않으나 acy l CoA 가 ac y lcarn iti ne 으로 전환되는 방향에서 방해가 일어나 치 않 나 하는 규명연구가 고려되고 있다. Malony l CoA 의 독특한 독성 을 다음의 그립 1 4 에 서 표시 하였 다. 이 그림에서 간에서의 탄수화물과 지방대사의 잠정적인 관련이 찰 표시되어 있다. 고탄수화물식 이 로 사육하면 [g luca g o 띠 : [i nsu li n] 의 비 례 는 감 소하며 malony l CoA 수준이 증가되 어 지 방산합성 이 활발해 지 고 지방산 산화를 방해하는 과정은 모두 막히는 현저한 현상이 나타난
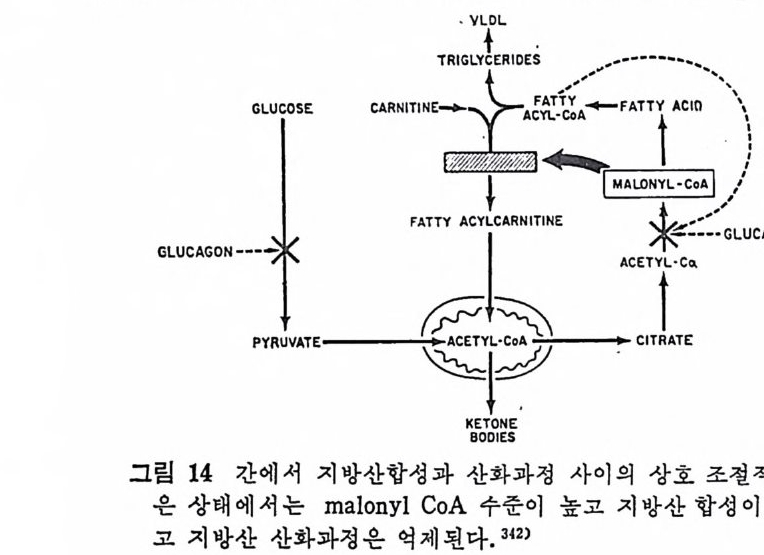 . YLOL
. YLOL
다. 이 러 한 조건하에 서 malony l CoA 의 생 리 적 인 역 할은 glu cose 로부터 온 탄소가 중성지방과 함께 VLDL 로 되는 한 가지 방향으 로 대 사가 이 루어 진다. 따라서 carnit ine acy lt r a nsfe r ase I 의 활성 온 억재되며 새로이 합성된 지방산의 재산화를 방지해 준다. keto t i c 상태 에 서 는 〔g luca g o 띠 : 〔 i nsul i n] 이 비 가 높아져 서 malony l CoA 수 준 이 떨어지고 지방합성작용 단계가 여제된다 .405) 지 방산의 산화와 케 돈체 합성 이 활발해 지 면 조직 내 의 carnit ine 의 농도도 동시에 증가된다. 조직내 carn iti ne 함량에 미치는 glu ca- go n 의 급성 적 인 자극효과와 또한 glu cag o n 의 지 방산합성 의 방해 효과는 malony l CoA 형성의 억제능력으로써 설명될 수 있다 .404-5) 요즈음 쥐의 유리된 간세포를 가지고 여러가지 종류의 실험이 행 해지고 있다 .408) 잘 먹인 쥐의 간세포를 이용해서 지방산합성이 여러 수준으로 이루어지도록 처리하여 이 조직내에서 계속적으로 malony l CoA 를 측정하며 지방산 산화 및 케론체 합성을 축정하 였다• 이 실험 에 서 지 방산 합성 의 최 대 율은 간세 포를 lacta t e 와 pyr uvate 와 함께 배양시켰을 때이고 최소울은 g luca g on 이 촌재할 때 나타 났다. 이 실험의 주요 발견은 g luca g on 이 지방산 대사의 방향을 합 성으로부터 산화방향으로 전환시켰다는 접이며, 지방산 합성작용에 는 glu cag o n 이 방해 는 하였 지 만 완전히 방지하지 는 못하고 lacta t e 와 pyr uvate 가 가해지 면 glu cag o n 작용이 정 지 된다는 것 이 다. 세 포 내 의 cit ra te 와 malony l CoA 수준의 변화는 glu cag o n 이 지 방산 합 성의 두 수준에서 방해를 하기 때문인데 첫째는 g l y col y s i s 를 막는 것 이 고 둘째 는 말단 단계 의 부분적 인 방해 로써 acety l CoA carbox- y lase 의 방해로 생각된다. Glucago n 의 항 gly c olys is 작 용은 의 십 없 이 pyr uvate kin a se 와 같 은 ph osph oryl a ti on 의 주요 효소몰 중재 하는 cAMP 에 근거 가 있 다고 보며 409-10) 또한 ph osph ofr uc to k in a se 와 관련이 있 다고 본 다. 410-11) 또한 이 와 유사한 기 전으로 glu cago n 에 의 해 서 기 인된 acety l CoA carboxy la se 의 방해 가 발표되 었 다. 412)
이러한 여러가지 효소의 관련에도 불구하고 여전히 지방산 합성 물은 malony l- C o A 농도와 양성적으로 관련이 크며 이 두 요인은 지방산 산화율에는 역으로 관련되어 있다. 대단히 중요한 것은 조 직 내 에 malony l CoA 농도의 변화이 다. 이 농도는 1~6mmol/g 으 로서 상당히 일정 하며 이 농도 안에 서 car n it ine acy lt r a nsfe r ase I 의 활성수준을 조절하는 역할을 수행한다 .34 2) 이러한 상황 아래서 g luca gon 의 케본체 합성작용은 두 영역으로 나뉘어져 수행된다. 첫 째 는 carnit ine acy lt r a nsfe r ase I 의 작용을 가로막고 있 는 malony l CoA 를 glu cag o n 이 이 동시 킵 으로써 p-o xid a ti on 을 자국하는 효과 라고 생각할 수 있다. 두번 째로, 첨가한 호르몬의 자국은 내원적으 로 oxaloaceta t e 합성을 억 제함으로써 gly c olys is 의 방해물 막아 주는 효과이 다 그러 드로 결 과적 으로 끼 치 는 영 향은 (3- oxid a ti on 의 율 을 촉진시 켜 acety l CoA 생 성 이 촉진되 며 많은 양의 acety l CoA 가 Krebs cy c le 로부터 케 돈체 합성 대 사로 옮겨 가게 하는 것 이 다(p. 602 참조). 그러나 이 제안에 대해서 Brass 와 Ho pp e l 이 의문을 제기하였 다. 413) 찰 먹 인 쥐 를 carnit ine 으로 처 리 함으로써 pla sma 내 에 케 돈체 와 간세 포내 의 사슬이 간 acy lc arnit ine 수준 사이 를 분리 하는 것을 기초로 해서 간세포내 지방산의 산화를 위한 조절기접으로 carnit ine acy lt r a nsfe r ase I 이 과연 중요한 것 인지 에 대 해 서 의 문의 이 제기되었다. 두번째의 비판은 Ben it e 와 W illi amson 에 의해서 표 시되었다 .414) 간에서 지방산의 합성과 산화의 상호관계 속에서 케 톤체 합성의 조철에 관련해서 기아 때문에 간세포의 케돈체 합성 능력이 굉장히 많이 증가된다는 것울 전제로 생각할 수 없지 않느 냐는 비판이다. 이런 바판하에 쥐의 유리된 간세포에 다음과 같 온 실험 이 수행 되 었 다. 415) 이 실험 에 서 포도당과 lacta t e 와 pyr uvate 를 혼합해 놓으면 최 대 수준의 malony l CoA 형 성 과 지 방합성 이 얻 어 진다. 이 때 에 이 과정 의 2 종류의 방해 물질로서 glu cag o n 과 RMI 14, 514(5-(te t r ad ecy lo xy ) -2-fu r oic a ci d) 를 사용하였 다. 4l6 ) 그리 고 이 방해 물질들이 CoA 유도체 로 전환된 이 후에 acety l CoA carboxy - lase 의 수준에서 방해작용울 한 것으로 믿었다 .4l7) 그리고 실험동
물은 먼처 carn iti ne 의 측정 실현물절인 동위원소 처리된 cl4-but - yro bet ai n 으로 처 리 하여 서 이 동물의 간세 포내 의 carnit ine po ol 이 모두 radio a cti ve 해지도록 하였다• 이러한 실험설계로서 세포내의 지방산 산화속도와 지방산 합성속도가 달라서 유도되는 여러가지 사정 에 관련된 간 사슬의 acy lc arnit ine 의 세 포내 수준변화를 비 교 적 정확하게 그리고 자동적으로 측정할 수 있다고 생각한 것이다. 그림 15 에서 보여주는 바와 같이 지방산의 합성률이 최고 수준이고 산화율이 최 저 수준인 경 우는 포도당, lacta t e 그리 고 pyru vat e 가 촌재할 때 언어진다. 이 반대의 결과가 g luca g on 과 RMI 14, 514 의 두 요소가 함께 작용할 때 최대로 지방산 합성을 억제했고 지방산 산화를 자극한 결과가 나타났다. 또한 조직 내 의 malony l CoA 수준 과 관련해서 지방산 합성률이 50 배의 범위내에서 양성적으로(+) ·
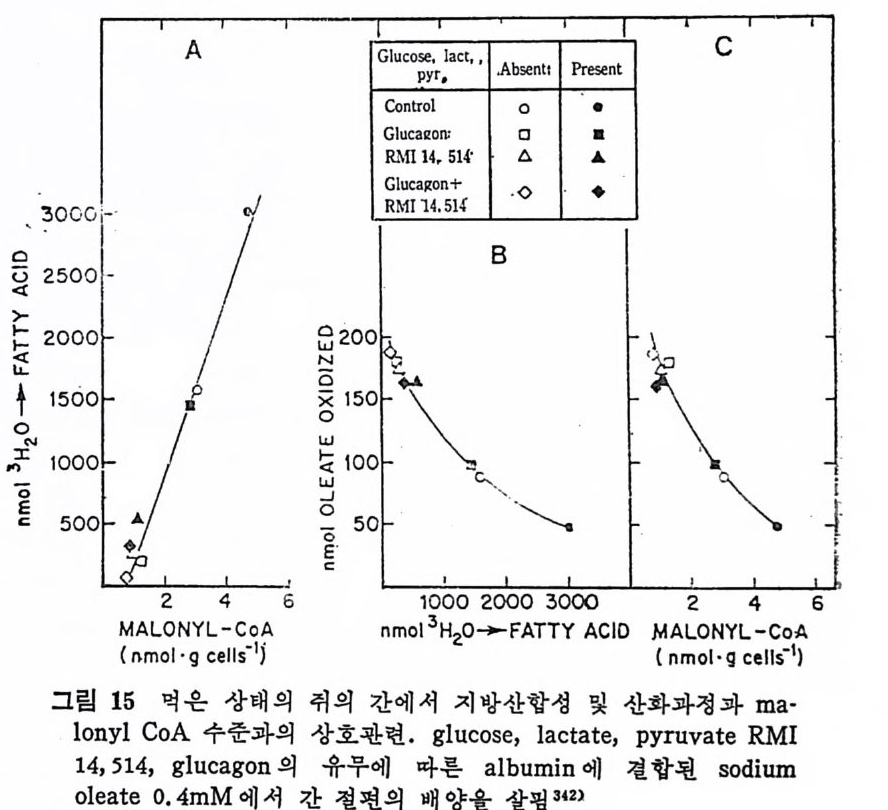 ’ A Glucopsey ,r .!a ct, , .Ab sent l Pros ,nt C
’ A Glucopsey ,r .!a ct, , .Ab sent l Pros ,nt C
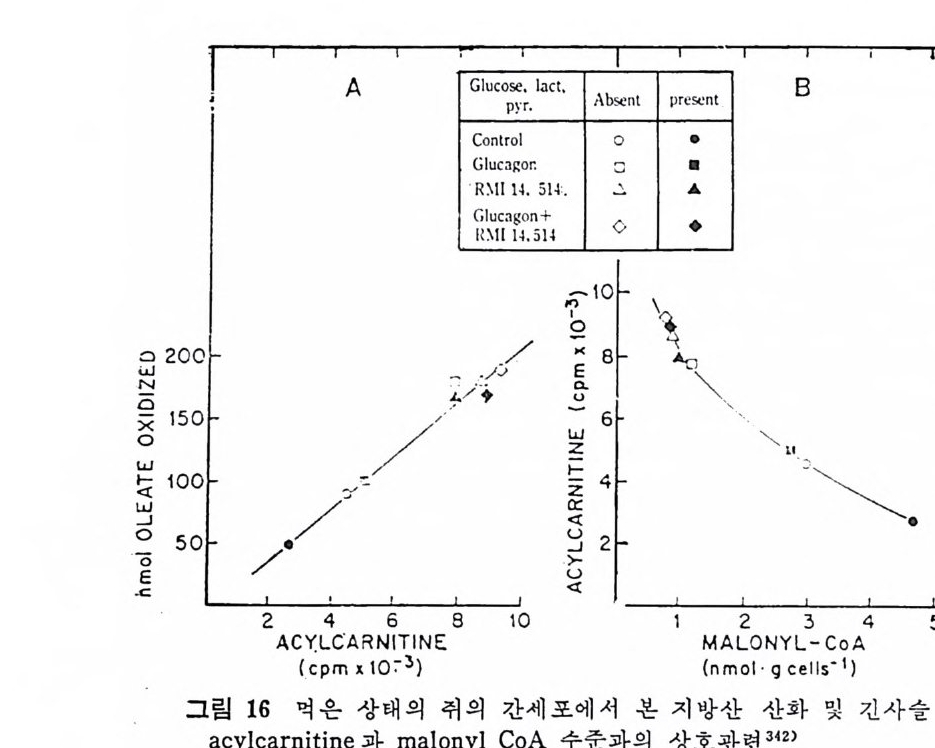 '|
'|
그리고 적선의 관련을 가지고 있음이 나타났다. 이미 기대 했던 대로 지방산의 산호H 즌 비슷한 형태로 음성적인(-) 관련을 갖고 있었다. 이 미 앞에 서 암시 했 던 바와 같이 carnit ine acy lt r a nsfe r ase I 를 방 해하는 rnalony l CoA 이용의 직접적인 결과로써 세포내부의 건 사슬 의 acy lc arnit ine 의 수준에 따른 지 방산 산화율은 직 접 적 으로 비 례 하며 rnalony l CoA 수준과 지 방산 합성률과는 역 으로 비 례 된다. 한편 잘 먹인 쥐의 간세포를 g luca g on 과 RMI 14 , 51 4 를 혼합한 물질에 노출시킨 후 포도당, lac t a t e 와 py ruva t e 만이 존재할 때 나 타났던 비율과 비교해 보니 지방산의 산화율과 케본체 합성물이 5.5 배에서 12.4 배까지 증가되었다(표 4 참조). 여 기 에 carnit ine 을 첨 가하였 더 니 rnalony l CoA 나 지 방산합성 수 준의 억제효과가 나타나지 않으나 지방산 산화와 케본체 합성의 자 국은 7.1 과 19.3 배로 각각 증가되었다. 다른 말로 바꾸떤 이 두 과
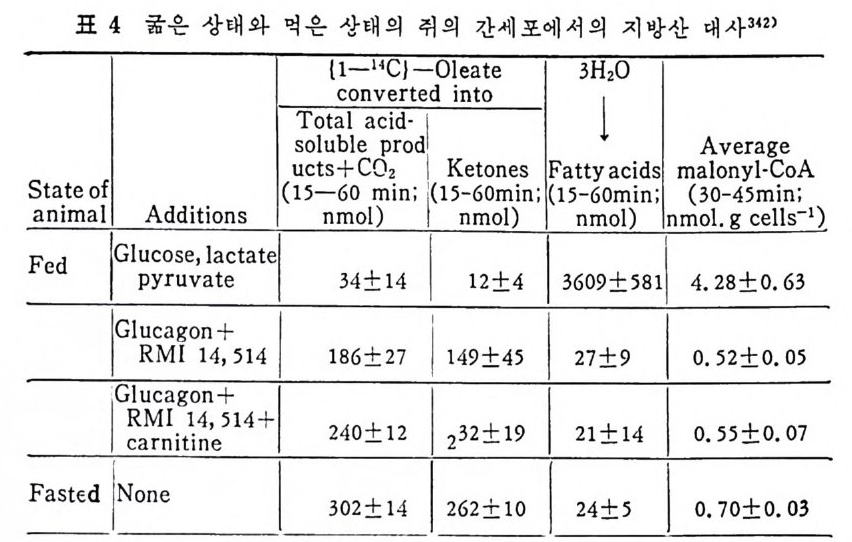 Satna it m e표 ao lf 4 A굼d은d it 상ion태 s 와 1(먹 •1u sT5co은o—tlnu s t lam+b6 1상 l 0l _oeC 태 aI lC m)cip)의 zCi ri d n o l · ;d — 취 I1\lI( O 의1K5 i ne -e a6m t간0to oem n세 l e) is 포n ; 에I\II( F 1서a5tn3-t의 6mHylT0 o2am 0 cl지 ) i i dn방s ; I\ l n산 mm ( a3oA대l0lo.v -사 ng4ey5 r 3c a4lm-2e gC)li e lnos A;- • )
Satna it m e표 ao lf 4 A굼d은d it 상ion태 s 와 1(먹 •1u sT5co은o—tlnu s t lam+b6 1상 l 0l _oeC 태 aI lC m)cip)의 zCi ri d n o l · ;d — 취 I1\lI( O 의1K5 i ne -e a6m t간0to oem n세 l e) is 포n ; 에I\II( F 1서a5tn3-t의 6mHylT0 o2am 0 cl지 ) i i dn방s ; I\ l n산 mm ( a3oA대l0lo.v -사 ng4ey5 r 3c a4lm-2e gC)li e lnos A;- • )
정에서 나타난 결과는 굶은 동물의 간세포에서 나타나는 정도였다. 즉, malony l CoA 치 와 지 방산합성 치 가 아주 낮은 기 초값 정 도를 나 타내 주 었다. 기대했던 대로 g luca g on 에 부과해서 RMI 14,514 를 첨 가한 후에 carnit ine 의 첨 가유무에 따라서 굵은 쥐 의 제 포에 서 측정 했 던 기준치들에 아무런 영향이 없었다는 것은 지방산 산화를 위한 조직은 malony l CoA 가 결합되고 carn iti ne 함량이 부과될 때 최대로 자극이 된다는 것이며 지방산 산화와 케돈체 합성조절에 malony l CoA, carnit ine 그리 고 carnit ine acy lt r a nsfe r ase I 이 중 십적인 역할을 한다고 생각할 수 있다 이상의 결과를 모두 종합해 보면 간장내에서 케돈체 합성에 직접 적으로 영향울 미치고 지방산 산화와 합성속도에도 영향을 미치논 인자 죽, glu cag o n, 인슈린, malony l CoA carnit ine , 및 carnit ine acy lt r a nsfe r ase 등이 안정 된 대 사작용을 유지 할 때 죽 homeosta t i c 범위내의 대사작용이 이루어질 때는 각 인자의 작용이 강조됨에 따 라서 지방산 산화나 합성을 촉진하게 된다. 그러나 실제로 우리 몸 은 이와 같은 안정된 대사 범위로만 계속 유지되기란 거의 불가능한 일이며 굶었다든지 음석섭취를한 상태라든지 질병으로 당뇨병이 있
다든지에 따라서 몸의 기본적인 대사상태가 달라지게 되며 이런 상 태에서도 기대치 않았던 복합작용이 일어나는 것이다. 그러브로 이 상에 제시된 모든 실험의 설계나 결과가 철대적이라고 주장하기에 는 너무 단순하다. 그러므로 보다 포괄적인 실험설계하에서 얻어진 결과 위에서 보다 많은 연구가 계속되어야 한다. @ 케돈체 합성조절에 있어서 석이지방산의 역할 쥐의 간세포에서 실험한 걷과 Cook 둥은 418) malony l CoA 의 세 포내 함량이 케돈체 합성물의 주요 결정요인이라고 하였다. 이와 유사한 결과로서 식사로부터 섭취된 사슬이 긴 지방산 자체가 세포 내 malony l CoA 수준을 낮추어 주는 결과 를 나타냈다고 보고하였 다 .419) 이 조건하에서는 지방산 합성물이 비례적으로 감소되는 기전 온 건 사슬의 지 방산 acy l CoA 에 의 해 서 acety l CoA carboxy la se 의 작용이 방해되었다는 것이다. 긴 사슬지방산 acy l CoA 는 car- box y lase 의 유력한 방해물질이며 이는 세포내 의원 (exog enou s ) 의 지 방산 함량이 증가함에 따라서 축적된다고 알려졌다 .420) 결과적으로 세포의 (ex t racellular) 의 지방산 농도가 높으면 간접적으로 malony l CoA 합성 과 지 방합성 작용의 fee dback inh ib i t ion 에 의 해 서 자신의 산화율울 증가시 킨다. 이 러 한 상황하에 서 glu cag o n 은 malony l CoA 합성을 방지하는 효과를 나타낼 것이며 차라리 의부의 지방산 농도 가 증가함에 따라서 지방산 산화율이나 . 합성률에는 작은 영향력을 미칠 것으로 본다. 3) 케톤체의 신체내 대사 조철하지 않은 당뇨병 상태와 관련하여서 케론체는 비정상 대사 물로서 본래 고려되어 왔지만, 케론체는 신체 생리적인 기능으로 볼 때 중요한 물질이타는 것이 밝혀졌다. 가장 중요한 기능중의 하나는 탄수화물로부터 열량공급이 부족되 거나 효율적으로 신체내에서 산화되지 못할 때 케본체는 열원 (en ergy source) 으로 사용된다. 특히 중추신경 계 통 조직 의 열 량공급원으 로 뜻이 크다. 왜냐하면 실제적으로 신체내 다른 부분의 조직과 달
타서 중추신경 조직은 포도당으로부터 열량공급이 되지 않을 때 지 방산이 열원으로 사용되지 못하기 때문이다. 사실상 장기간 동안의 기아상대가 계속될 때 노]조직의 호흡을 위해서 포도당 대신 케돈체 가 열 원으로 사용되 며 ·121 ) 이 에 부과해 서 glu coneog en esis 의 목적 으 로 발생하는 근육단백질의 분해를 최소로 감소시킨다. 죽, 케돈 체가 신체내 질소 의 음(一)의 군형으로 인해서 야기되는 몸의 해를 방자해 준다고 생 각할 수 있 다. 422) 케돈체는 대사적으르 적응할 수 있기 대문에 오로지 포도당 이 용능릭이 없어졌을 때만 이용되는 것이 아니고 케본체 자체가 근 육내 의 단백 질 분해작용을 지 접 적 으로 방해 한다고 한다. 423) 끝으로 ac0 w:1 c eta t e 와 3-hy d roxy b uty ra te 는 신생 아의 노] 조직 지 방합성 의 중요한 선행물질로 생각된다 .424) 이 상의 모든 유용한 기 능에 도 불구하고 십 각한 당뇨병 이 나 alco-holi c ke t oac i dos i s 때 혈액내에 과량의 케론체 축적은 심각한 건과 를 가져온다. 간내의 이러한 상대에서는 생리적이돈 병리적이돈간 에 케돈체 합성능력이 최대로 활성화 된다. 이와 같은 2 가지 상태에 서 즉 생리적으로든 병리적으로든 간으로 지방산울 공급해 주는 울 을 구 벨해 내는 일이 결정적으로 중요한 작용일 것이다. 다른 말로 하면 유리지방산의 유리 정도가 조철되지 못하면 케돈체 합성이 고 속도로 이루어져서 합성과 분해 사이의 군형이 깨어쳐 생명을 위협 할 것이라는 것이다. Wi lliam son 과 Hems · 12” 는 기 아로 인해 서 발생 되 는 keto s is 는 생 리적인 것이며, 케본체 자체가 지방세포에 직접적으로 영향을 미치 거나 췌장의 인슈란 분바의 자극을 통해서 케톤체 자체에 의한 과 잉의 치방분해 작용을 방지해 준다고 하였다. 그런데 병리적인 keto s is 대 는 이 러 한 조철 fee dback 의 능력 을 잃 어 버 리 게 된다. 케돈체의 신체대서수근 지방산의 산화와 합성이 밀접하게 관련이 되어 이의 조절이 곧 케톤체 체내조철이 된다고 본다. 간세포내의 지 방산 산화와 케 론체 합성 의 조철이 이 루어 지는 곳은 carn itine acy lt ra nsfe r ase I 작용이 라고 본문에 지적 되 었 다. 또한 케 본체 합 성은 포도당 생성과정에서와도 같이 인슈린의 부족이라는 한 가지
이 유만이 아니 라 동시 에 glu cag o n 의 과잉 으로도 이 루어 진다는 것' 이다. 고로 인슈란과 g luca g on 의 신체조칙내의 농도비례를 생각하 게 된다. 또한 간에서의 지방과 탄수화물대사를 각기 메어서 생각 할 수 없으며 서로 결부시켜서 생각해야 된다. 이러한 두 물질의 대사사이룰 연결하는데 있어서 malony l CoA 도 상당히 중요한 입 장에 있음을 제시하였다. 그러브로 간의 지방산 산화와 케본체 생 성의 조절에 탄수화물이 그 열쇠를 가졌다고 오랫동안 생각되어 왔 다.
* 참고문현 1) George , H. Bell, Textb o ok of Phy si o l og y, 10t h Ed. , Churchil l Li· vin g st o n e, p. 9 7, 1980. 2) Ruth , L. Pik e , & My rt l e, L. Brown, Nutr i t ion An in te g r ate d A- ppro ach, 2nd Ed. , p. 571, Wi ley , 1978. 3) D. W. Marti n, Harpe r 's Revie w of Bi oc hemi st r y , Korean Ed, , p, 231, 1981 . 4) Mi sh kin , S. L. , E. Gat m ait an , I. M. Aria s , Bi oc lt em . Bi op ! tys, Res. Commun. 47:997, 1972. 5) Salmon, D. M. W. , N. L. Bower, D. A. Hems, Bi oc hemi ca l ]. , 142 :611, 1974. 6) Hems, D. A, E. Rath , & T. Verrin d er, Bi oc hemi ca l ]. , 150 : 167, 1975. 7) Wadke, M. , H. Bruneng ra ber, J. M. Lowenste i n , J. J. Dolhun, G. P. Arsenault , Bi oc hemi st r y Easto n , 12 : 2619, 1973. 8) Rous S. , Adv. Lip id Res. , 9:73, 1971. 9) Kreb, S. H. A. , R. L. Veech, Adv. Enz. Reg u l. , 7 : 397, 1969. 10) Ell iot t , J. A. , E. Dade, D. M. W. Salmon, D. A. Hems, Bi oc him . Bi op h y s . Acta ., 344:307, 1974. 11) Lands, W. E. M. , An. Rev. Bi oc hem. , 34: 313, 1965. 12) Lamb, R. G. , H. J. Fallon, ]. Bi ol . chem. , 245 : 3075, 1970. 13) Fallon, H. J. , J. Barwi ck , P. G. Lamb, H. Van den Bosch, J.
Lip t'd Res. , 16 : 107, 1975. 14) Abou-Issa, H. M. , W. W. Clelland, Bi oc him . Bi op h ys . Acta , 176: 692, 1968. 15 ) Okuy am a, H. , K. Yamada, H. Ikeja w a, J. Bi ol . chem. , 250 : 1710, 1975. 16) Reit z, R. C. , W. E. M. Lands, W. W. Chris t i e, R. T. Holman, J. Bi ol . chem. 243 : 2242, 1968. 17) Yamashit a, S. , N. Nakay a, Y. Mi k i, S. Numa, Proc. Natn . Acad. Sci. U. S. A. , 72:600, 1975. 18) Akesson, B. , Bi oc hi m . Bi op h ys . Acta , 218 : 59, 1970. 19) Akesson, B. , J. Elouson, G. Arvid s on, Bi oc h im. Bi op h y s . Acta ~ 248: 1, 1970. 20) Mang iap a n e, E. H. , K. A. Lloy d -Davie s , D. N. Brin d ley, Bi o ch-em. ]. , 134:103, 1973. 21) Da w son, R. M. 0. , Essays in Bi oc hemi st r y , vol. 2, p. 69, London: Academi c Press, 1966. 22) Lip pe !, K. , J. Robin s on, E. Trams, Bi oc him . Bi op h ys . Acta , 206 : 173, 1970. 23) Groot, P. H. E. , C. M. I. Van Loon, W. C. Hulsman, Bi oc him . B- iop hy s . Acta , 337 : 1, 1974. 24) Van Golde, L. M. G. , J. Raben, J. J. Bate n burg, B. Fleis c her, F. Zambrano, S. Fleis c her, Bi oc him . Bi op h ys _. A cta , 360:179, 1974. 25) Lloy d -Davie s , M. , D. N. Brin d ley, Bi oc hem. Soc. Trans. , I :436, 1973. 26) Solberg, H. E. , Bi oc him . Bi op h ys . Acta , 360: 101, 1974. 27) McGarry, J. D. , D. W. Foste r , Meta b oli sm , 21 : 471, 1972. 28) McGarry, J. D. , D. W. Foste r , ]. Bi ol . Chem. , 249 : 7984, 1974. 2, ) McGarry, J. D. , J. M. Meie r , D. W. Foste r , ]. Bi ol . chem. , 248: 270, 1973 . .3O ) VanTol, A. , W. C. Hulsmann, Bi oc him . Bi op h ys . Acta , 223:416, 1970. 31) Sarzala, M. G. , L. M. G. Van Golde, de Krug ff B. , L. L. M. Van Deenen, Bi oc him . Bi op h ys , Acat, 202 : 106, 1970.
32) Sancehz, M. , G. D. Ni ch olls, D. N. Brin d ley , Bi oc lzem. ]. , 132 : 607, 1973. 33) Parkes, J. G. , W. Thomp so n, Bi oc h im . Bi op hy s. Acta , 306:4 0 3, 1973. 34) Di Aug es ti ne , R. P. , J. M. Schaefe r , J. R. Fouts . , Bi oc lzem. ]. , 132 : 323, 1973. 35) Sin c lair , A. J. , Li pids , 9:809, 1974. 36) Ste i n , Y. , & 0. Ste i n , Horm, Meta b . Res. Sup pl. , No 4 : 16, 1974. 37) Neste l , P. J. , D. Ste i n b erg, J. Lip id Res. , 4:461, 1963 . .3 8) Kohout, M. , B. Kohouto v a, M. Heim bey , J. Bi ol . Chem. , 246: 5067, 1971 . 39) Heim berg, M. , H. G. Wi lc ox, ]. Bi o l. Chem. , 247 : 875, 1972. 40) Champ m a n, M. J. , G. L. Mi lls, C. E. Tay la ur, Bi oc he m . ]. , 131 :177, 1973. 41) Greg o ry, D. H. , D. V!ahcevic , P. Schatz k i, L. Swell, ]. C/in . Invets . , 55: 105, 1975. 42) Bar-on H. , P. S. Roheim , 0. Ste i n , Y. Ste i n , Bi oc him . Bi op h y s. Acta , 248:1, 1971 . 43) Fukazawa, T. , 0. S. Priv e tt , Y. Takahashi, Lip ids , 6:388, 1971. 44) Senbert, W. , E. R. Padack, Mol. Cell Bi oc lzem. , 1 : 29, 1973. -45 ) Gurr, M. I. , in MTP Inte r nati on al revie w of Scie n ce, Vol. 4, Bio c hemi st r y of lip ids , p. 181, T. W. Goodwi n, Edit or , London, Butt er worth s. -46 ) Podack, E. R. , M. Lakomek, G. Saath o ff , W. Senbert, Ett r. ]. Bi ch em, , 45:13, 1974. -47 ) Hi ns ch, W. , W. Senbert, Eur. ]. Bi oc h em. , 53 : 437, 1975. 48) Landusci na , C. , G. V. Guoni, E. Qu ag liar ie l ls, Bi oc h im. Bi op • hys . Acta , 202:405, 1970. -49 ) Coneg lio, J. G. , D. L. Cate , ]. Bio l. Chem. , 232: 361, 1958. 50) Brett , D. , D. Howlin g , L. J. Morris , A. T. Jam es, Archs. Bi o· chem. Bi op h y s. , 143 : 535, 1971. 51 ) Joh n, P. D. , P. W. Holloway, R. 0. Peluff o, S. J. Wakil , J. Bi · ol. Chem, , 244: 744, 1969.
''5 2 ) Holloway, C. T. , P. W. Holloway , Archs. Bi oc hem. Bi op y h s. , 167:496, 1975. 53) Str i t tm att er , P. L. Sp a tz , D. Corcoran, M. J. Rog er s, B. Setl o w, R. Redli ne , Proc. Natu . Acad. Sci. U. S. A. , 71 : 456 5, 1974. 54) Oshin o , N. R. Sato , Archs. B io c hem. Bi op hy s . , 1<19 : 369, 1972. 55) Acti s- Dato , S. M. , A. Cata l a. , R. R. Brenner, Lipid 8: 1, 1972. 56) Elovson, J. , Bi oc him . Bi op h y s. Acta , 106: 291, 1965. 57) Inkp e n, C. A. , R. A. Harris , F. W. Qu ackeubush, ]. Lipid Res. , 10 : 277 I 1969. 58) De Gomes, Dumm I. N. T. , M. J. T. De Alaniz , R. R. Brenner, ]. Lipid Res. , 11:96, 1970. 59) Oshin o , N. , Bi oc him . Bi op h ys . Acta , 149 : 378, 1972. 60) Di! Thomas, M. E. , R. 0. Peluff o. , 0. Mercuri, Bi oc him . Bi o· phy s, Acta , 306 : 149, 1973 . . 61) Mercuri, D. , R. 0. Peluff o, De Thomas M. E. , Bi oc him . Bi o- phy s. Acta , 369 : 264, 1974. -62 ) Kap la u, A, M. H. Teng , ]. Lip id Res. , 12: 324, 1972. 63) Gott , S. , Y. Barenholz, Ann. Rev. Bi oc lzem. , 42:61, 1973. 64) Havel, R. J. , J. M. Felt s. , C. M. Van Duy n e, J. Lip id Res. , 3 : 297, 1962. -65 ) Top ping , D. L. , P. A. May es , Bi oc hem. J. , 126 : 295, 1972. 66) May e s, P. A. , J. M. Felts , Bi oc hem. ]. , 156 : 685, 1976. 67) May es , P. A. , J. M. Felt s, Natu re (London), 215:7 16, 1967a. ,68 ) May es , P. A. , in Adip o se tissu e Reg u lati on & meta b olic fun ct- ion s, Geanrenand, B. & Hep p, D. eds. , p. 186, Academi c Press, New York & London, 1970. -69 ) Vavrecka, M. , M. P. Mi tch ell, G. Hi ibs che r, Bi oc hem. J. , 115: 139, 1969. 70) Top ping , D. L. , Bi oc hemt 'ca l J. 152:425, 1975. 71) Wi nd mueller, H. G. , H. E. Sp ae th , Arch. Bi oc hem. Bi op hy s. , 122 :36 2, 1967. 72) May es , P. A. , D. L. Top ping , Bi oc hem. J. , 140 : 111, 1974. -73 ) May es , P. A. , Bi oc lzem. Soc. Trans. , 4 : 572, 1976.
14) Gardner, R. , P. A. May es , Bi oc hem. Soc. _T ra.11 s . , 2: 1127, 1974 .. 75) Heim berg, M. , A. Dunkerley , T. Brown, Bi oc hem. pha rnacol. , 14:890, 1965. 76) Top ping , D.L., P.A. May e s, Bi oc lzem. Soc. Trans., 4:717, 1976. 77) Klausuer, H. , M. Heim berg, Am. J. p!zysi o l . , 212: 1236, 196i. , 78) Kir k , C. J. , T. R. Verrin d er, D. A. Hems, Bi oc lzem. Soc. Trans, 3 : 515, 1975. 79) Watk im , M. L. , N. Fiz e tt e. , M. Heim berg, Bi o chem. Bi op y h s. Acta , 280:82, 1972. so) Chan, L. , L. R. Jac kson, W. B. O'Molley, A. R. Means, J. Cli1 1 . Invest. , 58 : 368, 1982. 81)Day, R.I. Levy , Bi oc hem. Med., 3:177,1969. 82) Oliv e crona, T. , Acta phy s i o l . Scand. , 54:287, 1962. 83) Ai ya r Fatt er pa ker Ste e niv a san, Bi oc hemi ca l J. , 90: 558, 1964. 84) Robin s on & Seakin s , Bi oc him . Bi op h ys . Acta , 60 : 163, 1962. 85) Creasey, Haukin s & Handschumaker, J. Bi ol . Chem. , 236 : 2064,. 1961. 86) Lie b er, C. S . , E. Rubin , Am. J. Med. , 44 : 200, 1968. 87) Goodhart, S. R. , M. E. Shil ls, Modern Nutr i t ion in Healt h & dis e ase, 6th Ed. , p. 128, Lea & Febig e r, Phil ad elph ia , 1980. 88) Lie b er, C. S. , Lip id Pharmacol. , 2: 183, 1976. 89) Al fin·S late r , Af ter go o d, Wells, Devel, Arch. Bi oc hem. Bi op ! zys. ,. 52:180, 1954. 90) Kennedy , E. P. , Fed. Proc. , 20:934, 1961. 91) Bell, R. M. , R. A. Coleman, Ann. Rev. Bi oc hem. , 49:459, 1980. 92) Groot, P. H. E. , H. R. Scholte , W. C. Hii ls mann, Adv. Lip id R•· es. , 14 : 75, 1976. 93) Bar Tana, J. , G. Rose, B. shap iro , Bi oc hem. ]. , 122 : 353, 1971. 94) Bar Tana, J. , G. Rose, Bi o chem. J. , 131 : 443, 1973. 95) Moes, E. , J. Bar Tana, Bt'o c him . Bi op h y s . Acta , 480 : 527, 197 7. 96) Tanaka. T. , K. Hosaka, M. Hoshim aru, S. Numa, Eur. l► Bi oc hem. , 98: 165, 1979.
C/7 ) Lloy d e·Davie s , K. A, D. N. Brin d ley , Bi oc hem. ]. , 152 : 39, 1975_ C/8 ) Jas on, C. J. , M. A. Polo·koff , R. M. Bell, ]. Bio l. chem. , 251 : 1488, 1976. C/C/) Kami ry o , T. , M. Mi sh in a , & S. I. Tashir o , S. Numa, Proc. Natt . Acad. Sci. U. S. A. , 74:4947, 1977. JO ()) Mi sh in a , M. , T. Kami ry o , S. I. Tashir o , S. Numa, Eur. ]. Bio c he m . , 82 : 347, 1978. 101) Mi sh i n a , M. , T. Kami ry o , S. I. Tashir o , T. Hay iba ra, A. Ta . naka, S. Fukui, M. Osumi , S. Numa, Eur. ]. Bi o chem. , 89:321, 1978. I 02) Hosaka, K. , M. Mi sh in a , T. Tanaka, T. Kami ry o , S. Numa, Eur. . ]. Bio c hem. , 93 : 197, 1979. 103) Gelsema, C. L. , D. J. Marri, ]. Bi o l. Chem. , 253 : 7960, 1978. 104 ) W ilg r a m, G. F. , E. P. Kennedy , J. Bi ol . chem. , 238:2615, 1963 .. 105) Hosaka, K. , S. Yamashit a, S. Numa, ]. Bi oc hem. , 77: 501, 1975_ 106) Kent, C. , P. R. Veg e lo, Bi oc h im. Bi op h y s . Acta , 436 : 377, 1976. 107) Coleman, R. , G. Hii bs cher, Bi oc him . Bi op h ys . Acta , 56:479,. 1962 . 108) Ag ra noff , B. W. , J. Lip id Res. 3 : 190, 1962. 109) Caras, J. , B. Shap iro , Bi oc him . Bi op h ys . Acta , 409:201, 1975. 110) Follon, H. J. , R. G. Lamb. , S. C. Jam dar, Bi oc hem. Soc. Tra- ns. , 5:37, 1977. 111) Brin d ley, D. N. , Reg u lati on of fat t y acid & gly c eroli pid meta b o- /ism , ed. , R. Dil s & J. Kundsen, pp. 31~40, Oxfo r d & New York,. Perga m on, 1978. 112) Coleman, R. , B. C. Reed, J. C. Mackall, A. K. Stu d ent, M. D. Lane, R. M. Bell, ]. Bi ol . Chem. , 253 : 7256, 1978. 113) Grim aldi, P. , R. Nig re l, G. Ai lha ud, Eur. ]. Bi oc hem. , 84:369, 1978. 114) Van Golde, L. M. G. , B. Fleis h cer, S. Fleis c her, Bi oc h im. Bi o- phy s. Acta , 249:318, 1971 . 115) Wi lgr am, G. F. , E. P. Kennedy , J. Bi ol . Chem. , 238:2615, 1963. 116) Coleman, R. , R. M. Bell, ]. Bio l . Chem. , 251 :4537, 1976. 117) Lin , C. Y. , S. Smi th, S. Abraham, J. Lip id Res. , 17:647. .
1976. 118) Holube, B. J. , J. Pie k arski, Can. ]. Bi oc hem. , 55 : 1186, 1977. 119) Hosaka, K.U .Schie l e, S. Numa, Eur. ]. Bi oc lt em .,76:113,1977. 120) Polakoff , M. A. , R. M. Bell, Bi oc lt em . Bi op ! tys. Acta , 1980. 121) Up re te , R. K. , G. G. Sanwal, P. S. Kris h man, Arch. Bi oc lt im. Bi op lzy s. , 174:658, 1976. 122) Brop h y , P. J. , P. C. Choy . , J. R. Toone, D. E. Vance, Eur. }. Bi oc hem. , 78:491, 1977. 123) Wein h old, P. A. , V. B. Reth y , Bi oc hemi st r y , 13 : 5135, 1974. 124) Infa n te , J. P. , J. E. Ki ns ella, Lipids , U : 727, 1976. 125) Wein h old, P. A. , R. S. Skin n er, R. D. Sta n ders, Bi oc lzi m . Bi o- ph y s. Acta , 326:43, 1973. 126) Schneid e r, W. C. , ]. Bi ol . Chem. , 238: 3572, 196 3. 127) Choy , P. C. , W. J. Schneid e r, D. E. Vance, Eur. ]. Bi oc lzem. , 85 : 189, 1978. 128) Choy , P. C. , D. E. Vance, ]. Bi ol . Chem. , 253 : 5163, 1978. 129) Infa n te , J. P. , Bi o chem. ]. , 167:847, 1977. 130) Sundler, R. , B. Akesson, ]. Bi ol . Chem. , 250:3359, 1975. 131) Sundler, R. , J. Bi ol . Chem. , 250:8585, 1975, 132) Coleman, R. , A. , R. M. Bell, J. Bi ol . Chem. , 252: 3050, 1977. 133) Kanoh, H. , K. Ohno, Bi oc him . Bi op h y s. Acta , 380 : 199, 1975 . .134 ) Morim oto , K. , H. Kanoh, ]. Bi ol . Chem. , 253 : 5056, 1978. 135) Holube, B. J. , J. Bi ol Chem. , 253 :691, 1978. 136) Morim oto , K. , H. Kanoh, Bi oc him . Bi op h y s. Acta , 531 : 16, 1978. 137) Radomi ns kap yre k, A. , M. Pil a ska, P. Zim ria k , Bi oc hem. Bi o phy s. Res. Commum. , 85 : 1074, 1978. ·13 8) Kanoh, H. , K. Ohno, Eur. ]. Bi oc hem. , 66 : 201, 1976. 139) Bremer, J. , D. M. Greenberg, Bi o chi m . Bi op h y s. Acta , 46 : 205, 1961. 140) Schneid e r, W. J. , D. E. Vance, Eur. ]. Bi oc hem. , 85 : 181, 1978 141) Schneid e r, W. J. , D. E. Vance, ]. Bi ol . Chem. , 254:3886, 1979. 142) Katy al , S. L. , B. Lambardi, Lip ids , 11 : 513, 1976. 143) Schonf el d, G. , B. Pf le g er , J. Li pid Res. , 12:614, 1971.
144) Park, C. E. , E. Marai, S. Mookerje a , Bi oc him . Bi op h y s . Acta , 270: 50, 1972. 145) Waddell, M. , H. J. Fallon, J. Cl in. Invest. , 52: 2725, 1973. 146) Olevsky , J. M. , J. W. Fargu har, G. M. Reaven, Am. J. Med. , 5,7 : 551, 1974. 147) Romsos, D. R. , G. A. Leveil li, Bi oc him . Bi op ! tys. Acta , 360: 1, 1974. 148) Robin s on, D. S. , The fun cti on of the pla sma tri g ly c erid e ~ in- fatty aci d tra nsp or t , Comp re hensiv e Bioc hemi st r y , Vol. 1 8, L iP 깝 Meta b oli sm , 1970. 149) Tarlow, D. M. , P. A. Watk ins , R. E. Reed, R. S. Mi ller , E. E. Ewerge l , M. D. Lane, J. Cell. Bi ol . , 73 : 332, 1977. 150) Coleman, R. A. , M. A. Polokoff , R. M. Bell, Meta b olis m , 26 : 1123, 1977. 151) Salmon, D. M. W. , D. A. Hems, Bi oc hem. J. , 136: 551, 1973. 152) Lote n , E. G. , A. Robin o wi tch , B. Jea nrenand, Di ab eto l og ia, 10· :45, 1974. 153) Ellio t t , J. A. , E. Dade, D. M. W. Salmon, D. A. Hems, Bi oc hi m . Bi op ! tys. Acta , 343 : 307, 1974. 154 ) Abraham, R. R. , E. Dade, J. A. Ellio t t , D. A. Hems, Di a- bete s , 20 : 535, 1971 . 155) Lie b er, C. S. , Gastr o ente r olog y, 59 : 930, 1970. 156) Grunnet, N, B. Qu is t o r f, H. I. D. Thie d en, Eur. J. Bi oc lt em . ,. 40 : 275, 1973. 157) Lie b er, C. S. , L. M. Decarli, J. Bi ol . Chem. , 245:2505, 1970. 158) Pap e nberg, J. , J. P. Von. Wartb urg, H. AEbi, Enzym ol. Bi ol .. Clin . , 11 : 237, 1970. 159) Thie d en, H. I. D. , Acta Chem. Sca1' d. , 25:3421, 1971 . 160) Rog n sta d , R. , D. G. Clark, Eur. J. Bi oc lzem. , 42: 51, 1974. 161) Lie b er, C. S. , L. M. Decarli, J. Pharmacol. Exp . Ther. , 181 : 279, 1972. 162) Grunnet, N. , H. I. D. Thie d en, Li fe S c i. (pa rt II') , 11 : 983, 1D72. 163) Lie b er, C. S. , R. Teschke, S. Hasumura, L. M. Decarili , Fed_
Proc. , 34: 2074, 1975. 164 ) Iseri, O. A. , L. S. Goti lieb , C. S. Lie b er, Fed. Proc. , 23 : 579 , 1964. 165) Iseri, 0. A. , C. S. Lie b er, L. S. Gott lieb , Am. ]. Patl z ol. , 48: 535, 1966. 166) Meldolesi, J. , J. Bi oc /z e m. P/z a rmacol. , 16 : 125, 1967. 167) Conney , A. H. , Phannacol. Re v. , 19 : 317, 1967. 168) Lane, B. P. , C. S. Lie b er, Lab. Invest. , 16 : 342 , 196 7 . 169) ORME-Jo h nson, W. H. , & D. M. Zie g le r, Bi oc lze m . Bi op lzy s. Re s. Commum., 21:78, 1965. 170) Makab, A. B. , G. J. Mannerin g , Bi oc lzem. Plzarmacol. , 19 : 2017, 1970. 171) Rey n ie r , M. , Acta Chem. Scand. , 23 : 1119, 1969. 172) Keil in, D. , E. F. Hartr e e, Bi oc lzemi ca l ]. , 39: 293 , 194 5 . 173) Bartl et t , G. R. , Q J. Stu d , Alcohol. , 13 : 583, 1952. 174 ) Fey trn ans, E. , F. Leig h to n , Bi oc /z e m. Pharmacol. , 23 : 34 9 , 1973. 175) Leste r , D. , G. D. Benson, Scie n ce, 169 : 282, 1970. 176) Oshin o , N. , B. Chance, H. Sie s , T. Bucher, Arch. Bi oc lze m . Bi op /z _ys . , 154:117, 1973. 177) Theorell, H. B. , B. Chance, T. Yoneta n i, N. Oshin o , Arch. Bi oc hem. Bi op h y s . , 151:434, 1974. 178) Boveris , A. , N. Oshin o , B. Chance, Bt o chem. ]. , 128:6 1 7, 1972. 179) Oshin o , N. , R. Oshin o , B. Chance, Bto c/z e m. ]. , 131 : 555, 1973. 180) Thurman, R. G. , R. Scholz, Drug . Meta b . Di sp o s . , 1 :44 1 , 1973. 181) Marja n en, L. , Bi o chem. ]. , 127:633, 1972. 182) Lie b er, C. S. , C. S. David s on, Am. ]. Afgd , , 33 : 319, 1962. 183) Lie b er, C. S. , D. P. Jon es, M. S. Lowsowsky , C. S. David s on, ]. Cl in. Invest. , 41 : 1863, 1962 184) Newcombe, D. S. , Meta / z o li sm , 21 : 1193, 1972. 185) Fein m an, L. , C. S. Lie b er, Sct e nce, 176: :795, 1972. 186) Ni kk il a, E. A. , K. Oja l a, Proc. Soc. Exp . Bi o l. Med: , 113 : 814, 1963. 187) Gordon, E. R. , Bt' oc hem. Pharmacol. , 21 : 2991, 1972 .
,188 ) Lieb e r, C. S. , R. Schmi d, J. Clin . Invest. , 40 : 394, 1961 . 189) Lieb er, C. S. , A. Lefe v re, N. Sp ri t z, I. Fein m an, I. M. Deca• rli, ]. Cli n. Invest. , 46 : 1451, 1967. 190) Forsander, 0. A. , P. H. Maenp aa , M. P. Sa!aspu ro, Acta . Ch· em. Scand. , 19: 1770, 1965. 191) Bio : n s tr a nd, R. , L. Kag er , 0. Lantt o, Li fe S ci, 13 : 1131, 1973. 192) Ont ko , J. A. , ]. Lip id Res. , 14:78, 1973. 193) Lie b er, C. S. , N. Sp ri t z, ]. Clin . Invest. , 45 : 1400, 1966. 194) Lie b er, C. S. , N. Sp ri t z, L. M. Decarli, ]. Clin . Invest. , 45 : 51, 1966. 195) Lie b er, C.S., N. Sp ri t z, L.M. Decarli, ].Lip id Res., 10:283, 1969. 196) Meudenhall, C. L. , ]. Lipid. Res. , 13 : 177, 1972. 197) Soehrin g , K. , V. Schop pe I, Dt sc h. Mzd. Wochenscher, 91 : 1892, 1966. 198) Rubin , E. , A. Gang , P. S . Mi sr a, C. S. Lie b er, Am. ]. Med. , 49 : so1, 1910. 199) Hil d ebrandt, A. G. , M. Sp ec k, I. Root s, Nouny n -Schmi ed eber· gs, Arclz. Pharmaco!. , 281:371, 1971 . 200) Suth e rland, V. C. , T. N. Burbrid g e , J. E. Adams, A. Sim on, ]. Ap pl. Phy si o l . , 15 : 189, 1960. 201) Karste n , M. , S. Mats u zaki, L. Fein m an, & C. S. Lie b er, New Eng l. ]. Med. , 292:386, 1974. 202) Grunnet, N., Eur. ]. Bi oc hem., 35:256,1973. 203) Daja n i, R. M. , J. Danie l ski, J. M. Orte n , ]. Nutr . , 80 : 196, 1963. 204 ) Horto n , A. A. , Bi oc h im. Bi op ! tys. Acta , 253:514, 1971. 205) Raskin , N. H. , L. Sokoloff , Natc tr e (London), 236 : 138, 1972. 206) Redmond, G. , G. Cohen, Scie n ce, 171 : 387, 1971. 207) Katz , J. , I. L. Chaik o ff , Bi oc hi m . Bi op h y s. Acta , 18:87, 1955. 208) Crouse, J. R. , C. D. Gerson, L. M. Decarli, C. S. Lie b er, ]. Li· pid Res. , 9 : 509, 1968. 209) Mallov, S. , J. L. Bloeh, Am. ]. Phy si o l . , 184:29, 1956. :21 0) Hornin g , M. G. , E. A. Wi lliam s, H. M. Mali ng , B. B. Brodie ,
W. M. Butl er Jr. , Bi oc hem. Bi op h y s. Re s. Commun. , 3 : 635, 1960 .. .21 1) Kalant, H. , J. M. Khanna, F. Sey m our, J. Lot h, Bio c lzem. Plzarmacol. , 24:431, 1975. 212) Forbes, J. C. , G. M. Duncan, Qu art. J. Stu d . Alcolzol, 12: 355, 1 951 . 213) Forbes, J. C. , G. M. Duncan, Qu art. J. Stu d. Alcohol, 14: 22, 1953. 214) Kis s in , B. , V. Schenker, A. C. Sche n ker, Am. J. Med. Sci. , 239 :690, 1960. 215) Ellis, F. W. , J. Pharmacol. Exp. Tlze ra p. , 153 : 121 , 1966. 216) Ki li n g m an, G. I. , C. M. Goodall, J. Pharma co l. Exp . The ra p. , 121 : 313, 1957. 217) Perman, E. S. , Acta Phys i o l . Scand. , 51:62 , 1 %1 . 218) Ferge lson, E. B. , W. W. Pfa ff, A. Karman, D. Ste lnberg, J. Cli n. Invest. , 40:2171, 1961 . 219) Best, C. H. , W. S. Hortr o ft , C. C. Lucas, J. H. Rid out, Br. Med. ]. , 2: 1001, 1949. 220) Volwi le e, W. , C. M. Jo nes, T. B. Mallory, Gastr o ente r olog y, 11 : 164, 1948. 221) Summerskil l, W. H. J. , S. J. Wolfe , C. S. Davis o n, Lancet, 1 : 335, 1957. 222) Mang h in i , G. , Bull. Acad. Swi ss . Sci. Med, , 16 : 36, 1960. 223) Lie b er, C. S. , D. P. Jon es, L. M. Decarli, J. Cli n. I nvest. , 44 : 1009, 1965. 224) Decarli, L. M. , C. S. Lie b er, J. Nutr . , 91 : 331, 1967. 225) Porta , E. A. , W. S. Hartr o ft , F. A. de la Igl e sia , Lab. Inves t . , 14: 1437, 1965. 226) Lie b er, C. S. , L. M. Decarli, Am. J. Clin . Nt,tr. 23 :474, 1970, 227) Pir o la, R. C. , C. S. Lie b er, Pharmacolog y, 7 : 185, 1972. 228) Rabin , E. , C. S. Lie b er, N. Eng . ]. Med. , 278 : 869, 1968. 229) Hakte d , C. H. , E. A. Robles, E. Mezey , Am. ]. Clin . Nutr . , 26 : 831, 1973. 230) Baraona, E. , R. C. Pir o la, C. S. Lie b er, Gastr o ente r ology , 66::
226 , 197 4. 231) Chang , T. , J. Lewi s, A. J. G!azko, Bi oc hi m . Bi op ! zys . Acta , 135 : 1000, 1967. 232) Isr ael, Y. , I. Salazar, E. Rosenmann, J. N11t r, , 96:49 9, 1968. 233 ) Isr ael, Y. , J. E. Valenzue la , I. Salazar, G. Ug a rte , J. Nutr . , 98: 222, 1969. 234 ) Ho y u mp a, A. M. , K. J. Br~z n, S. Schenker, F. A. W ilso n, J. Lab.Clin . Med. , 86:803,1975. 235) Ro:i ri g e , C. , C. Ante z ana, E. Baraona, J. N11t r. , 101 : 1307, 1971. 236) Lin d enbaum, J. , C. S. , Lie b er, Ann. N. Y, Acad. Sci. , 252:228, 1975. 237) W ieb e, A. , A. Lundq ui s t , P. Belfr ag e, J. Clin . Lab. Invest. ,. 27 : 33, 1971 . 238) Lie b er, C. S. , L. M. Decarli, J. Med. Prim . , 3 : 153, 1974. 239) Lie b er, C. S. , L. M. De ca rli, Gastr o ente r olog y, 50:316, 1966. 240 ) Oler, A. , B Lomb3rdi, J. Bi ol . Chem. , 245 : 12s2, 1970. 241) Baraona, E. , M. A. Leo, S. A. Borowsky , C. S. Lieb er, J_ Cli n. Invest. , 60 : 546, 1977. 242 ) Hof fba uer, F. W. , F. G. Zaki, Arch. Path o l. , 79:364, 1965. 243) Kondrup , J. , N. Grunnet, Bi oc hem. J. , 132:373, 1973. 244 ) Ashworth , C. T. , F. Wrig h ts m an, V. Butt ro m, Arch. Path o l. ,. 72:620, 1961 . 245) Corredor, C. , C. Mansbach, R. Bressler, Bi oc him . Bi op h ys , Acta , 144:366, 1967. 246 ) Iwamoto , A. , E. E. Helberste i n , D. M. Heg st e d , J. N11t r. , 79:· 488, 1963. 247) Baraona, E. , C. S. Lie b er, J. C/in . Invest. , 49 : 769, 1970. 248) Lombardi, B. P. , P. Pani, F. F. Schlunk, J. Lipid. Res. , 9:. 437, 1968. 249) Ami ck , C. J. , R. J. Ste n g er , Lab. Invest. , 13 : 128, 1964. 250) Edreir a , J. G. , R. L. Hir s ch, J. A. Kennedy , Qu art. J. Str e d. Alcoho l. , 35 : 20, 1974. 251) Porta , E. A. , C. Mannin g , W. S. Hartr o ft , Arch. Path o l. , 86:
217, 1968. 2.5 2 ) Sim on, J. B. , R. Scheig , G. Klats k in , Proc. Soc. Exp. Bi ol . Med. , 129:874, 1968. 253) Baraona, E. , M. A. Leo, S. A. Borowsky , C. S. Lie b er, Sc ie· nce, 190:794, 1975. 254) Baraona, E. , C. S. Lie b er, J. Lipid Res. , 20:292, 1979. 255) Morga n , J. C. , N. R. Dil uz io , Proc. Soc. Exp er . Bi ol . Med. , 134 : 462, 1970. 256) Blomstr a ud, R. , L. Forsell, Life S ci. , lO(pa rt JI ) : 523, l9i l. 257) Busto s , G. 0. , H. Kalant, J. M. Khanna, J. Lot h, Scie n ce, 168 : 1598, 1970. 258) Koff , R. S. , J. J. Fit ts, Bi o chem. Med. , 6 : 77, 1972. 259) Nordmann, R. , C. Rib i e r e, H. Ronach, J. Nordmann, Rev. Eur. Et ud es. Cli n. Bi ol . , 17 : 592, 1972. 260) Domankki, R. , D. Dif en beric k , F. Ste a ru s, R. M. Scorpi o, S. A. Narrod, Proc. Soc. Exp . Bi ol . Med. , 138: 18, 1971. 262) Lelbach, W. R, Exp er ie n t ia, 25:816, 1969. 263) Kalant, H. , J. M. Khanna, G. 0. Busto s , Bi oc hem. Plzarmacol. , 21:811, 1972. 264) Lie b er, C. S. , E. Rubin , L. M. Decarli, P. Mi sr a, H. Gang , Lab. Invest. , 22:615, 1970. 265) Ishii , H. , J. G. Jol y, C. S. Lieb er, Bi oc h im. Bio p lzy s, Acta , 291 :411, 1973 . .2 66) Lundq u is t , E. , N. Ty gs tr u p , K. Wi nk lee, K. Melleng a ard, S. Munch Pete r sen, J. Clin . Invest. , 41:955, 1962. 267) Ockner, R. K. , S. P. Mi st il is, R. B. Pop pe :1 :ia u sen, A. F. Sti eh l, Gastr o ente r ology , 64 : 603, 1973 . .2 68) Baraona, E. , C. S. , Lie b er, Gastr o ente r olog y, 68:495, 1975. 269) Mi st i lis, S.P., R.K. Ockner, J. Lab. Cli 11. Med., 80:34, 1972. 270) Medeloff , A. I. , J. Cli n. Invest. , 33 : 1298, 1954. . 271) Ste i n , S. W. , C. S. Lie b er, C. M. Leevy , G. R. Cherric k , W. H. Abelmann, Am. J. Cli n. Nutr . , 13:68, 1936. 272) Shaw, S. , E. Heller, H. Frie d man, E. Baraona, C. S. Lie b er,
F.ro c. Soc. Exp . Bi ol . Med. , 156 : 509, 1977 . .27 3) Baraona, E. , R. C. Pir o la, C. S. Lieb er, Bi o chi m . Bi op hy s. A eta , 388 : 19, 1975. 274) Carte r , E. A. , G. D. Drummey , K. J. Isselbacher, Sci e nce, 17 : 121 5, 1971. 27 5) Rodg er s, J. B. , R. J. O'Brie n , Am. J. Di ges t. Di s. , 20: 354, 1975. 276) Ga ng l, A. , R. K. Ockner, J. Clin . Invest. , 55 : 803, 1975. 277 ) Mi dd leto n , W. R. J. , E. A. Carte r , G. D. Drummey , K. J. Issel-bacher, Gastr o ente r olog y, 60 : 880, 1971. 278) Brodie , B. B. , W. M. But le r, M. G. Hornin g , R. P. Maic k el, H. M. Mali ng , Am. J. Cl in. Nutr . , 9:432, 1961. 279) Lieb er, C. S. , C. M. Leevy , S. W. Ste i n , W. S. George , G. R. Cherric k , W. H. Abelmann, C. S. David s on, ]. Lab. Cl in. Med. , 59:82 6, 1962. 280) Jon es, D. P. , E. S. Perman, C. S. Lieb er, J. Lab. Cl in. Med. , 66 : 804, 1965. 281) Fein man, L. , C. S. Lie b er, Am. J. Cl in. Nutr . , 20 : 400, 1967. 282) Lieb e r, C. S. , D. P. Jon es, J. Mendelson, L; M. Decarli, Tra- ns. Ass. Am. Phy si c ian s, 76:289,.1 9 63. 283) Schap iro , R. H. , R. L. Scheig , G. D. Drummey , J. H. Mendcls- on, K. J. Isselbacher, New Eng l. J. Med. , 272:610, 1965. 284) Abrams, M. A. , C. Coop e r, Bi o clzem. J. , 156:33, 1976. 285) Abrams, M. A. , C. Coop e r, Bi oc !z e m. J. , 156:47, 1976. 286) Sheig , R. , Gastr o er. ter olog y, 60 : 751, 1971. 287) Bruneng r aber, H. , M. Bout ry , L. Lowenste i n , J. M. Lowenste i n , The eff ec t of etl n nol on lip o ge nesis by the pe rfu s ed live r•, In Al-coho! and Aldehy d e Meta b oliz i n g Sy st e m s, R. C. Thurman, T. Yoneta n i, J. R. W illiam son, B. Chance, edit or s, Academi c Press, New York and Landon, 329~37, 1974 . 288) Lie b er, C. S. , R. Schmi d, J. Cl in. Invest. , 40 : 394, 1961. :28 9) Guy n n, R. W. , D. Veloso, R. L. Harris , J. W. R. Lawson, R. L. Yecch, Bi o chem. J. , 136 : 639, 1973.
290) Scholz, R. , A. Kalt ste i n , U. Schwabe, R. G. Thurman, Inhi• bit ion of fatty acid syn th e sis from carbohy d rate s in pe rfu s ed rat live r by eth a nol, 0 In Alcohol and Aldehy d e Meta b oliz i n g Sy s- etm s, R. G. Thurman, T. Yoneta n i, J. R. Wi lliam son, B. Chance, edit or s, Academi c Press, New York, 315~28, 1974. 291) Savolain e n, M. J. , J. K. Hil t u nen, I. E. Hassin e n, Bi o chem. J. , 164: 169, 1977. 292) Medenhall, C. L. , R. H. Bradfo r d, R. H. Furman, Bi oc hi m . Bi- oph y s . Acta , 187:501, 1969. 293) Jol y, J요 , L. Fein m an, H. Ishii , C. S. Lieb er, J. Lipid. Res. , 14:337, 1973. 294) Mendenhall, C. L. , R. H. Bradfo r d, R. H. Furman, Bi oc lz im . Bi op h y s . Acta , l.87 :510, 1969. 295) Lefe v re, A. F. , L. M. Decarli, C. S. Lie b er, J. Lip id Res. , 13 :48, 1972. 296) Jon es, A. L. , D. f. Armstr o ng , Proc. Soc. E 쟈 Bi ol . Med. , 119:1136, 1965. 297) Takenchi, N. , M. Ito, Y. Yamamura, Lzp ids , 9:353, 1974. 298) Blomstr a nd, R. , L. Kag e r, Li fe S ci. , 13 : 113, 1973. 299) Fritz , I. B. , Phy sf o l. Rev. , 41 : 52. 1961 . 300) Svoboda, D. J. , R. T. Mannin g , Am. J. Path o l. , 44:645, 1964. 301) Kie s sin g , K. H. , L. Pil s tr o m, Cy tob i o log ie, 4 : 339, 1971 . 302) Leib e r, C. S. , L. M. Deacrli, H. Gang , G. Walker, E. Rubin , Hepa ti c Eff ec ts of long te rm eth anol consump tion in pr im ate s , ,,. In Medic a l Prim ato l og y, E. I. Goldsmi th, and J. Moor-Ja n kowski, edit or s, S. Karge r Basal, 270~78, 1972. 303} Lane, B. P. , C. S. Lie b er, Am. J. Path ( )/. , 49: 593, 1966. 304) French, S. W. , Gastr o ente r olog y, 54: 1106, 1968. 305) Rubin , E. , D. S. Beatt ie, C. S. Lie b er, Lab. Invest. , 23 : 620, 1970. 306) French, S. W. , T. Todoroff , Arch. Path o l. , 89 : 329, 1970. 307) French, S. W. , T. J. , Ihrig , R. J. Morin , Qu art. J. Stu d , Ale-- ohol, 31:801, 1970.
'30 8) French, S. W. , T. J. Ihrig , G. P. Shaw, T. T. Tanaka, M. L. Norum, Res. Commum. Chem. Path o l. Pharmacol. , z: 567, 1971 . 309) Van Waes, L. , C. S. , Lieb er, Br. J. Med. , 2: 1soB, 1977. 310) Oudea, M. C. , A. N. Launay , S. Qu eneherve, P. Oudea, Rev. Eur. Et ud es. Cli n. Bi ol . , 15:748, 1970. 311) Pil s tr o m, L. , K. H. Kie s sli ng , Hi st o c hemi e, 32:329, 1972. 312) Kie s sli ng , K. H. , L. Pil st r o m, Qu art. J. St ud . Alcohol, 29:819, 1968. 313) Rubin , E. , D. S. Beatt ie, A. Toth , C. S. Lieb er, Fed. Proc. , 31 : 131, 1972. 314) Gordon, E. R. , J. Bi ol . Chem. 248:8271, 1973. 315) Toth , A. , C. S. Lie b er, A. I. Cederbaum, D. S. Beatt ie, E. Ru- bin , Gastr o ente r olog y, 64:198, 1973. 316) Cederbaum, A. I. , C. S. Lie b er, D. S. Beatt ie, E. Rubin , J. Bi ol . Chem. , 250: 5122, 1975. 317) Lefe v re, A. , H. Adler, C. S. Lieb er, ]. Cl in. Invest. , 49:1775, 1970. 318) Cederbaum, A. I. , C. S. Lieb er, E. Rubin , Arch. Bi oc hem. Bi op h y s. , 169: 29, 1975. 319) Hasumura, Y. , R. Teschke, C. S. Lie b er, Scie n ce, 189 : 727, 1975. 320) Mats u zaki, A. , C. S. Lie b er, Bi oc lzem. Bi op hy s. Res. Commu· m. 75: 1059, 1977. 321) Fowler, S. , Ce DeDuve, J. Bi ol . Chem. , 244:471, 1968. 322) Mahadevan, S. , A. L. Tap pe !, J. Bi ol . Chem. , 243 : 2819, 1968. 323) Hay a se, K. , A. L. Tapp e !, ]. Bi ol . Chem. , 245 : 160, 1969. 324) Debeer, L. J. , J. Thomas, G. Mannaerts , P. J. Deschep pe r, J. Cl in. nvest. , 59 : 185, 1977. 325) Platt , D. , U. Ste i n , H. Heis s mey er , Z. Klin . Chem. Kl in. Bi- ochem., 9:126,1971 . 326) Pil s tr o m, L. , E. Felleniu s , K. H. Ki es sli ng , Br. J. Nutr . , 29: 297, 1973. :32 7) Berg, T. , J. Morland, Acta . Plzarmacol. Toxic o l. , 33:409, 1973. 328) Mezey , E. , J. J. Pott er , R. A. Ammon, Bi oc hem. Plzarmacol. ,
25: 2663, 1976. • 329) Boy e r, J_. L. , Gastr o ente r olog y, 62: 294 , 1 972. 330) Schap iro , R. H. , G. D. Drummey , Y. Shim i zu , K. J. Isselbac-her, ]. Cl in. Invest. , 43 : 1338, 1964. 331) Maddrey , W. C. , J. L. Boy e r, ]. Lab. Clin . Med. , 82: 21s, 1973. 332) Lakshmanan, M. R. , R. L. Veech, J. Lipid Res. , 18 : 325, 19n. 333) Recknag el , R. 0. , Plzarmacol. Rev. , 19 : 145, 1967. 334) Farber, E. , Adv. Li pid. Res. , 5: 119, 1967. 335) W in dmueller, H. G. , R. I. Levy , ]. Bi ol . Che m . 242: 224 6, 1967. 336) Flores, H. , W. Sie r ralta , F. Monckeberg, ]. Nutr . , 100 : 375, 1970. 337) Seakin s , A. , J. C. Wate r low, Bi oc hem. ]. , 129 : 793, 1972. 338) Jon es, D. P. , M. S. Losowsky , C. S. David s on, C. S. Lie b er, ]. Lab. Cl in. Med. , 62: 67 5, 1963. 339) Baraona, E. , R. C. P_ir ola, C. S. Lieb er, ]. Cl in. Inve st . , 52: 296, 1973. 340) Le Marchand, Y. , A. Sin g h , F. Assim acop o ulos-Je a nnet, L. Orci , C. Rouil ler , B. Jea nrenaud, ]. Bi ol . Chem. , 248 : 6862, 1973. 341) Ste i n , 0. , Y. Ste i n , Bi oc hi m . Bi op h y s. Acta , 306: 142, 1973. 342) McGarry, J. D. , D. W. Foste r , Ann. Rev. Bt oc hem. , 49 : 395, 1980. 343) McGarry, J.D ., D.W. Foste r , ]. Bi ol . Chem., 244:4251, 1969. 344) W illiam son, D. H. , M. W. Bate s , H. A. Krebs, Bi oc hem. ]. 108: 353, 1968. 345) McGarry, J. D. , D. W. Foste r , Bi oc hi m . Bi op h ys . Acta , 77: 34, 1969. 346) Mi dd leto n , B. , In Bi o chemi ca l & Clin ic a l asp e cts of Keto n e body Meta b oli sm . , Eds. , H. D. Soli ng , C. D. Senfe r t, pp. 1~10, Stu t t ga rt: G eorg Thie m e, 269, 1978. 347) Hanson, P. G. , R. E. Joh nson, D. S. Eabarko, Meta b oli sm , 14: 1037, 1965. 348) Ontk o , J. A. , D. B. Eil ve rsin i t , Proc. Soc. Exp . Bi ol . Med. ,. 121 : 319, 1966. 349) Bewsher, P. D. , M. E. Tarrant, J. Ashmore, Di ab ete s , 15 : 346,.
1966. 350) Scow, R. 0. ,' S. S. : Chernic k , Recent Prog r . Hormone Res. , lo :49 7 , 1960. 351) Owen, 0. E. , P. Feli g, A. P. Morga n, J. Wahren, G. F. Ca-hil l. Jr. ·, ]. Clin . • Invest. , 48: 574, 1969. 352)M eie r , J. M. , J. D. , McGa rr y, G. R. Fooona, R. H. Ung e r, D. W. Fost e r , ]. Lipid Re s. , 13: 228, 1972. 353 ) Al ke rt i , K. G. M. M. , T. D. R. Hoc k alay , R. C. Te rn er, Lancet, 2: 515, 1973. 354 ) Le vy , L. J. , J. Dug a , M. Gir g is, E. E. Gordon; Ann. Int. Me- d, , 78: 213, 1973. 355 ) Coop e rman, M. T. , F. David o ff , R. S. Sp a rk, -J. Pallott a, Di a- bet e s . 23:433, 1974 . 356) Se y ffer t , W. A. Jr. , L. L. Madis o n, Di ab ete s ; 16 : 765, 1967. 357) W illm s, B. , M. Botc h e r, V. Wolte e , N. Sakamoto , H. D. Sol- ing , Di ab eto l ogt a, 5 : ss, 1969. 358 ) Gres p in, S. R. , W. B. Greenoug h III, D. Ste in b e rg , }. Cl in. Inve st . , 48:1934 , 1 969. 359) W ill ia m son, D. H. , D. Veloso, E. V. Ellin g ton , H. A. Krebs,. Bi oc he m . ]. , 114: 575, 1969. 360) Bie b erdorf, F. A. , S. S. Chemi ck , R. 0. Scow, ]. Cli n. Invest. ,. 49: 1685, 1970. 361) Van Harken, D. R. , C. W. Dixo n, M. Heim berg, ]. Bi ol . Che- m. , 244 :2278, 1969. 362 ) Kreb s, H. A. , R. Hems, Bi oc lie m . ]. , 119 : 525, 1969. 363) McGa rr y, J. D. , D. W. Foste r , ]. Bi ol . Chem. , 246:1149, 1971 •. 364 ) McGarry, J. b. , D. W. Foste r , ]. Bi ol . Chem. , 246: 62 47, 1971. 365) Shep h erd, D. , D. W. Yate s, P. B. Galand, Bi oc hem. ]. , 97: 380,.. 1966. 366) Sauer, F. , J. D. Er fle, J. Bi o l. Chem. , 241 : 30, 1966. 367) Bremer, J. , Scand. ]. Cl in. Lab. Invest. , 23:105, 1969. 368) Lehnin g e r, A. C. , J. Bi ol . Chem. , 164: 291, 1946. 369) W iel and, O. , L. Weis s , I. Eg e r-Neufe ld t, Adv. Enzym e Reg -
ul. , 2:85, 1964. 370) Krebs, H. A. , Adv. Enzym e Reg u l. , 4:339, 1966. 371) W iel and, 0. , L. Weis s , Bi oc lt em . Bi op hy s. Res. Commum. , 13 : 26, 1963. 372) Tubs, P. K. , P. B. Garland, Bi oc lU !m . ]. , 93:550, 1964 . .37 3) Reg e n, D. M. , E. D. Terrell, Bi oc ht m . Bi op h y s. Acta , 170:95, 1968. 374) Wi lliam son, J. R. , R. Scholz, E. T. Browi n g , ]. Bi o l. Chem. , 244:4617, 1969. 375) Lossow, W. J. , I. L. Chaik a ff , Arch. Bi o chem. Bi op ! zys . , 57: 23, 1954. 376) Lossow, W. J. , G. W. Brown, Jr. , I. L. Chaik o ff , ]. Bi ol . Ch- em. , 220:839, 1956 . .3 77) Tzur, R. , E. Ta!, B. Shap iro , Bi o chim . Bio ph ys , Acta , 84: 18, 1964 . .3 78) Veech, R. L. , L. Raii m an, H. A. Krebs, Bi o chem. ]. , 117 : 499, 1970. 379) McGarry, J, D. , D. W. Fo,;;te r, ]. Clt 'n. Invest. , 52: 877, 1973. 380) McGarry, J. D. , D. W. Foste r , Di ab ete s , 23:485, 1974. 381) Murth y , V. K. , J. C. Ship p, Di ab ete s , 28:472, 1979. 382) Van Toi, A. , W. C. Hulsmann, Boic h im . Bi op hy s . Acta , 189 : 342, 1969. 383) Ponde, S. V. , ]. Bi o l. Chem. , 246:5384, 1971 . 384) Aas, M. , L. N. W. Daae, Bio ch im. Bi op hy s. Acta , 239 : 208, 1971. 385) Harano, Y. , J. Kowal, R. Yamazaki, L. Lavin e , M. Mi el er, Arch. Bi o chem. Bi op h ys , , 153:426, 1972. 386) Heim berg, M. , I. Wein s te i n , M. Kohont, ]. Bi ol . Chem. , 244: 5131, 1969. '38 7) Menahan, L. A. , 0. Wi el and, Eur. ]. Bi o chem. , 9: 182, 1969. 388) Wein s te i n , I. , H. A. Klansner, M. Heim berg, Bi oc lt im. Bi op - hy s. Acta , 300 : 300, 1973. '38 9) McGarry, J. D. , P. H. Wrig h t, D. W. Foste r , ]. Cli n. Invest. , 55 : 1202, 1975.
390) Whit ty, A. J. , K. Shim a, M. Trubow, P. Foa, Pro. Soc. Exp. Bio l . Med. , 130 : 55, 1969. 391 ) Lilje n g u is t , J. E. , J. D. Bomboy , S. B. Lew i s, B. C. sin c lair · sm- ith, P. W. Felt z, W. W. Lavy , 0. B. Croff or d, G. W. Lind dle, J. Cli n. fov est. , 53 : 190, 1974. 392) Ge ri c h , J. E. , M. Lorenzi, D. M. Bie r , V. Schneid e r, E. Tsa- liki a n , J. H. Karam, P. H. Forsham, N. Eng l. ]. Med. , 292: 98 5, 1975. 393) Schade, D. S. , R. P. Eato n , J. Cli n, lllvest. , 56 : 1340, 1975. 394) Ung er , R. H. , Meta b oli sm , 23:281, 1974. 395) McGarry, J. D. , C. Robles-Valdes, D. W. Foste r , Proc. Natl . Acad. Sci. U. S. A. , 72:43 85, 1975. 396) Robles -Vald es, C. , J. D . McGarry, D. W. Foste r , J. Bio l . Chem. , 251 : 6007, 1976. 397) McGarry, J. D. , D. W. Foste r , Am. ]. Med. , 61 : 9, 1976. 398) Bli xe nkrone·Me f,l ler, N. , z. Phys i o l . Chem. , 252: 117, 1938. 399) Embden, G. F. Kalbarlah, Beit r. Chem. Phys i o l . Path o l. , s: 121, 1906. 400) Embden, G. , J. Wi rt h , Bi oc hem. Z. , 27: 1, 1910. 401) Mi rk y , I. A. , ]. Am. Med. Assoc. , 118:690, 1942. 402) Wein h ouse, S. , R. H. Mi lling ton , B Freedman, J. Bi ol . Chem. , 181 : 489, 1949. 403) Guy n n, R. W. , D. Veloso, R. L. , J. Bi ol . chem. , 247: 7325, 1972. 404) Cook, G. A. , M. R. Lakshmanan, R. L. Veech, Fed. Proc. , 36 : 672, 1977. 405) McGarry, J. D. , G. P. Mannaerts , D. W. Foste r , J. Cli n. Inv- est. , 60 : 265, 1977. 406) McGarry, J. D. , G. P. Mannaerts , D. W. Foste r , Bi'o c hi m . Bi- oph y s. Acta , 530 : 305, 1978. 407) McGarry, J. D. , G. P. Mannaerts , D. W. Foste r , ]. Bio l . Chem. , 253:4128, 1978. 408) McGarry, J. D. , Y. Takabay a shi, D. W. Foste r , ]. Bi ol . Chem. , 253 : 8294, 1978.
409) Felin , J. E. , L. Hue, H. G. Hers, Pro. Natl . Acad. Sci. U. S. A. , 73 : 2762, 1976. 410) Casta n o, J. G. , A. Nie t o , J. E. Feli n, J. Bi ol . chem. , 254: 5576, 1979. 411) Kag im oto , T. , K. Uy e da, J. Bi o l. Clzem. , 254: 5584, 1979. 412) Wi tter s, L. A. , D. Moria r ity , D. B. Marti n, J. Bi ol . Clzem. , 254:6644, 1979. 413) Brass, E. P. , C. L. Hop pe l, J. Bi o l. Clzem. , 253 : 5274, 1978. 414) Benit e, M. , Wi lliam son, D. H. , Bi oc hemi ca l. J. , 176: 33 1, 1978. 415) McGarry, J. D. , D. W. Foste r , J. Bi o l. Chem. , 254:8163, 1979. 416)_P ank, E. , G. A. Cook, N. W. Cornell, Lip id, 12:s14 , 1 977. 417) McCune, S. A. , Fed. Proc. , 38:649, 1979. 418) Cook, G. A. , M. T. Ki ng , R. L. Veech, J. Bi ol . Chem. , 253 : 2529, 1978. 419) McGarry, J. D. , D. W. Foste r , Di ab ete s , 1980. 420) Numa, S. , W. M. Bortz , F. Ly n en, Adv. Enzym e Reg u l. , 3 : 407, 1965. 421) Owen, 0. E. , A. P. Morga n , H. G. Kemp , J. M. Sull ina n, M. G. Herrera, G. F. Cahil l. Jr. , ]. Cl: 'n. Invest. , 46: 1589, 1967. 422) Cahil l, G. F. Jr. , T. T. Aoki, Trans. Amer. Cl in. C/im ato l . Assoc. , 82: 43 , 1970. 423) Sherwi n, R. , R. Hendler, P. Felig , ]. c/in. Invest. , 55 : 1382, 1975, 424) Webber, R.J. , J. Edmond, J. Bi ol . Chem. , 254:3912,1979. 425) Wi lliam son, D. H. , R. Hems, In: Essays in Cell meta b oli sm , ed. , W. Bartle y , H. L Kornberg, J. R. Qu ay le , pp. 257~81, London, Wi le y int e r sci en ce, 1970,
제 4 장 콜레스데물대사 콜레스데롤은 우리 신체내 세포를 구성하고 있는 주요 성분으로 서 우리 산체내 대부분의 조직에서 합성이 된다. 그러나 뇌조직만 은 예외의 조직으로 콜레스데몰 합성이 되지 않는다. 고콜레 스데 몰혈증 (h yp ercholes t erolem i a) 은 동맥 경 화로 일어 나는 여 러가지 혈관병의 가장 위험한 요소로 증명이 되었다 .l - “ 유전적인 요인들과 식이가혈청내 중성지방과콜레스데를농도 조철에 주요 역 할을 한다 .3-4) 역학과 대사연구에서 분명히 밝혀진 바에 의하면 혈청콜레스테롤 의 함량수준이 식이내 함유된 콜레스테롤의 양을 비롯해서 석이지 방의 종류와 양에 의해서 강하게 영향을 받는다고 한다. 고콜레스데몰혈증 환자의 석이 중 포화지방산 대신에 불포화지방 산을 부분적으로 대치함으로써 혈청콜레스테롤을 낮추는 데 효과가 있었다는 문헌은 광법위하게 많다. 또한 포화지방산을 섭취한 사람 이 콜레스테를중에 쉽게 결란다는· 문헌도 많이 있다 .3),5-8) 혈액내의 콜레스테롤의 수준을 저하시키기 위해서 자유로이 처하 요소를 적용하는 경우에 약 3~4 개월이 결렀다고 한다 .9) 콜레스데몰 저하석이의 기전은 아칙까지 분명치도 않고 여러가지 이견들이 있지만 Grund y와 Ahrens10) 에 의해서 제안된 바에 의하 떤 식사내 포화지방산을 불포화지방산으로 대치시키면 혈청과 조칙 의 콜레스테롤 Pool 사이에서 콜레스테롤을 재분산함으로써 혈청
콜레스데룬의 양을 저하시킨다고제안하였다. 또한 다른 및 개의 보 고에 의하면 콜레스테몰수준 저하식이를 먹고 있는 동안에 사람에 게서 변으로 중성 s t ero i d 와 담줍산 (b i le a ci ds) 의 배설이 증가되었다 고 하였다 .11-3) 이들 결과에서 제시하는 것은 콜레스테롤의 수준을 낮추는 기전 온 콜레 스테 롤의 배 설과 대 사울이 증가함으로써 이 루어 진다는 것 이다. 과거에는 식사 중에 함유된 콜레스테롤의 양이 혈청콜 레 스 데 룬 의 농도 결정에 벌로 중요하다고는 생각하지 않았으나 근래에 와서 사 람을대상으로 실험해 본 결과 식이콜레스테롤이 사 람 의 혈 청콜레스. 테를의 농도에 분명히 영향을 미친다고 하였다 .5 - 7) 혈청내 콜레스데몰 농도에 미치는 영향으로는 식이콜레스데몰 자 체에 부과해서 여러가지 영양소의 섭취량, 또 섭유소 섭취량에 이 르기까지 다양한 결과가 제시되고 있다. 이러한 영양 둘 은 대개 콜 레스테를의 장내 흡수를 감소시키고 배설은 증가시키는 것으로 생 각된다 .147) 1 신체내 콜레스테롤의 동선 (1) 식사로부터 섭취된 콜레스데몰. es t er( 그림 1 참조)는 소화되어 서 유리콜레스테롤로 된다. 또한 담줍에 섞여 분비된 콜레스테롤로 부터 보대어질 수도 있다. (2) 유리콜레스테롤은 장내막제포에 의해 흡수되어 장내악세포내 에 서 유리 콜레 스테 롤 또는 콜레 스테 롤 este r 로써 chy lo mi cr on 에 영 합된다. (3) 간세 포에 의 해 서 chy lo mi cro n(remnant ch y lom i cron) 으로부터 유리콜레스데롤과 콜레스데몰 es t er 가 취해진다. (4) 콜레 스데 몰 este r hy d rolase 에 의 해 서 콜레 스테 롤 este r 가 가 수분해된다. (5) 콜레스데를의 합성은 식이콜레스테롤에 의해서 방해될 수도 있 다. 죽 chy lo mi cro n 이 콜레 스테 롤이 합성 되 는 간세 포의 recep tor
에 결합되어서 콜레스테풀과 콜레스테롤 es t er 를 간세포에 보태 주 면 결과적으로 간에서의 콜레스테돌의 합성은 방해가 된다. 이 조 절기 전에 는 HMG-CoA reducta s e 가 관여 한다. (6) 간세 포내 의 유리 콜레 스테 롤은 lip o pr o te i n 의 구성 성 분으로 영 합되 어 순환계 로 이 동된다. 주로 유리 콜레 스테 롤은 Low Densit y L ip o p ro t e i n(LDL) 에 영 합된다. (7) 혈 청내 l ip o p ro t e i n 내의 유리콜레스테를은 적혈구내 콜레스데 몰 사이에서 빠른 교환이 일어난다. (8) 헐 청 콜레스테롤과 뇌조직세포의 콜레스테롤 사이에서의 교 환은 이루어지지 않는다. (9) 혈 청 내 lip o p ro te i n 내 의 콜레 스데 롤은 간조직 밖의 조직 , 죽 근육조직, 동백조직, 피부 둥을 포함한 조직내의 콜레스테롤과 교 환이 이루어전다. (10) 콜레스테롤합성이 간조직 이의에서 일어난다. 그러나 이 조 직 제 포의 recep tor 에 LDL 이 결 합되 고, 그리 고 endocy tos is 에 의 해서 LDL 이 취해지면 합성은 방해를 받는다. (11) 유리콜레스테롤은 간세포 이외의 조직세포내에서 콜레스데 몰 acy l- CoA acy lt r a nsfe r ase 에 의 해 에 스텔화가 일어 나서 콜레 스 테롤 es t er 로 된냐 이 조직세포들은 유리콜레스데롤을 보유할 수 있는 능력이 한정되어 있다. 과량의 유리콜레스테롤을 보유하고 있 으면 이 세포의 막 상태가 변하게 되어 정상적인 기능을 상실하게 된다. 그러 므로 과량의 유리 콜레 스테 롤이 존재 하면 콜레 스데 몰 este r 로 전환되어 지방구로되어 세포내에 존재하게 됨으로써 유리콜레스테롤 의 형태로 머무는 것을 방지한다. 한편 콜레스테몰 h y drolase 에 의 해서 콜레스테롤 es t er 의 가수분해가 일어난다. (12) 혈청내 콜레스테롤 es t er 와 간 밖의 조직에 존재하는 콜레스 테롤 este r 사이의 교환은 없다. 그러나 앞에서도 지적했듯이 간조 직 밖의 조직제포에 의해 혈청으로부터 이동되어 온 LDL 이 취해진 다. 그러면 간조직 이의의 조직제포에 존재하는 콜레스데풀의 처리 가 문제된다, 왜냐하면 간조직제포내에서만 콜레스테롤이 분해되고
이의의 조직에서는 콜레스데를의 분해가 일어날 수 없기 때문이다• 그러므로 간조직 밖의 조직에 촌재하고 있는 콜레스테롤은 반드시 간세포로 이동되어야 한다. 간조칙 밖의 조칙내에 · 촌재하는 콜레스데몰이 간세포내로 이동하 는경로는 그림 1 의 (9) 와 (6) 에 의해 이루어진다. 이 경로에 의하면 간조직 밖의 조직에서 LDL 이 힐청내로 이동되어 간으로 들어간다. 이의에도 경로 (9) 를 통해서 (13) 과 (14) 를 거쳐서 간으로 도착하 는 경로도 있다. 그립의 경로 (9) 는 대단히 천천히 이루어진다. 그 러나 계속적으로 이루어지는 경로이므로 간조직 이의의 조직의 콜 레스테를이 간조직으로 이동하는 것이 가능해진다. 경로 (10) 에 의 하면 간조직 이외의 조직제포내에서도 콜레스테롤합성이 되기도 한 다. 그 과정은 대단히 느리나 합성속도는 정확히 유지된다. 어느 철대량의 콜레스테롤이 간조직 이외의 조직으로부터 간으로 . 이동이 계속된다. (13) 이 경 로는 혈청 의 lipo p r ote i n 내 의 유리 콜레 스테 롤의 농도 를감소시키는데중요하다. 또한편간조직이의의조직으로부터 이 동되는 유리콜레스테롤을 보다 많이 혈청내에 보유할 수 있는 능력 을 부여 하기 도 한다. 이 작용은 lecit hi n c holeste r ol acy lt r a nsfe r ase (LCAT) 에 의해서 이루어진다. (14) 혈액내의 유리콜레스테를이 LCAT 에 의해서 콜레스데롤 es t er 로 전환되면 HDL 의 이동에 의해서 간세포로 이동된다. 그러 므로 간조직 이의의 조직에 존재하는 콜레스데를이 LDL 에 주로 영 합되어 촌재하는데 이의 분해에 의해서 나온 콜레스테룬의 처리에 HDL 이 중요한 역할을 한다고 생각할 수 있다. LDL 은 간조직 이 외의 조직내에 콜레스테롤을 저장해 주는 수단으로 생각할 수가 있 다. 그러므로 〈선질의 콜레스데폴(g oo :l. choles t erol) 〉이라는 별명이 불 은 것은 HDL 의 콜레스테롤이고 〈악질의 콜레스데몰 (bad choleste - roI) 〉은 LDL 콜레스테 롤을 뜻하기 도 한다. LDL 과 VLDL 의 인지방 : 유리콜레스데롤의 함량비가 1 : 1 분자 비인데 비해서 HDL 은 인지방 : 유리콜레스데풀의 비가 4 : 1~6 : 1 이다. 그러므로 HDL 만이 보다 많은 콜레스테롤을 취할수있는 여
유있는 인지방량을 함유하고 있다. (15), (16) 사람의 간세포내에는 콜레스테롤 acy l- CoA acy lt r a ns• fe rase 가 없을 가능성이 많기 때문에 이 경로는 사람에게는 불가능 하다고 보지 만 좌우간 세 포내 에 는 콜레 스테 몰 acy l- CoA acy ltra ns- fer ase 가 없 기 때 문에 유리 콜레 스데 를이 콜레 스테 롤 este r 로 전환 되어서 처분되기도 한다. (17) 콜레스테롤이 분해되는 주요 경로로서 콜레스테롤이 담즙산 으로 분해되어서 전환된다.
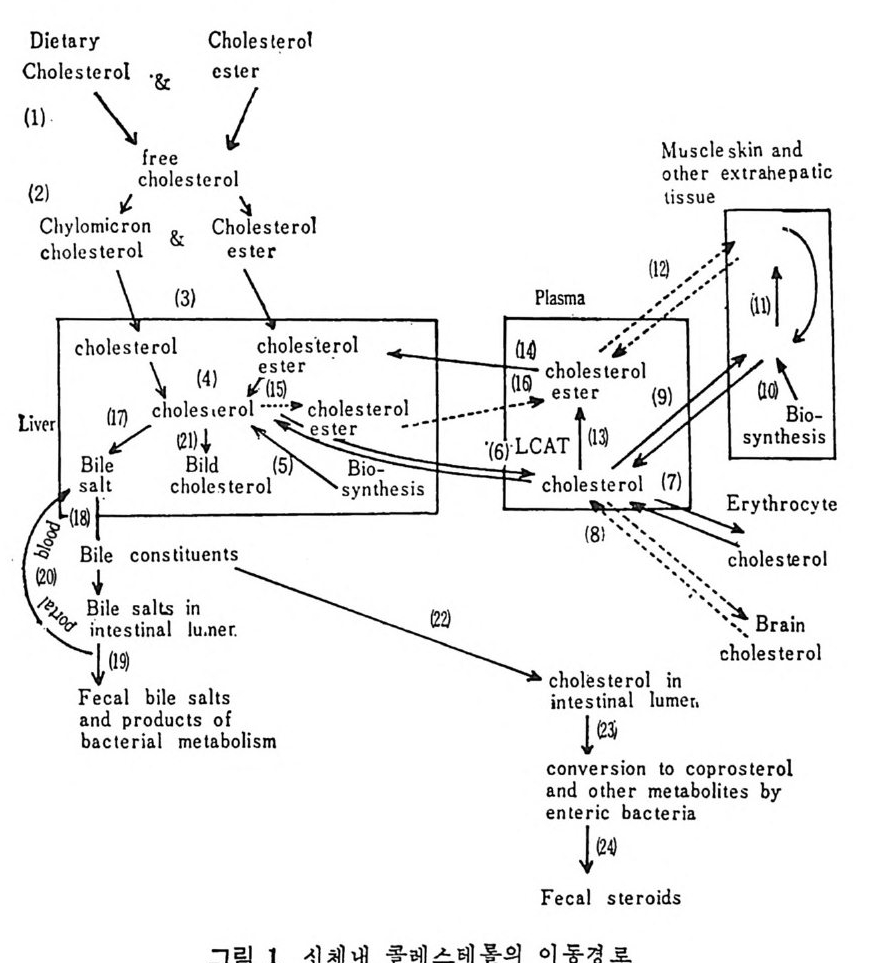 Di et a r y Choleste r ol
Di et a r y Choleste r ol
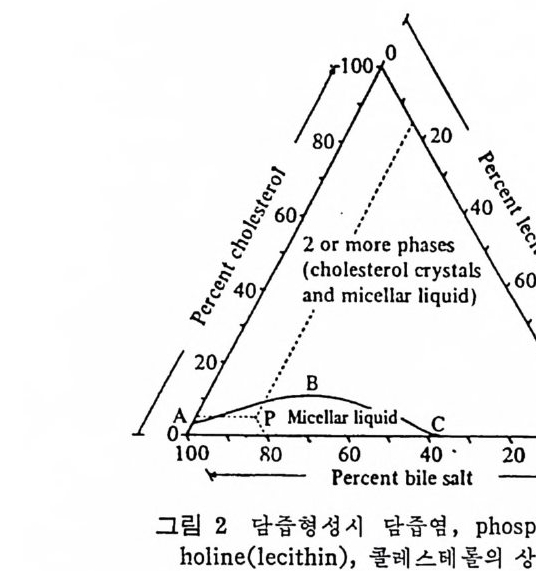 \
\
(18) 담줍산이 담즙영 으로 전환된다. (19) 담즙염 과 담줍의 생성물질들이 변으로 쉽 게 처리된다. 장내에 기 생하는미생물에 의해서 담즙영은 덜 국성을 가 전물질이 되며 수용액에 서의 용해력이 낮아져서 변으로 배설된다• (20) 일부는 이 곳에 서 문맥혈에 의 서 다시 간의 담즙영 으로. 이 동되 기 도 한다. 이 를 담즙영 의 장간순환
(ente r ohep a ti c ci rcula ti on) 이 라고 한다. (21) 콜레스테롤은 또한 간세포내에서 유리된 형태는 담즙의 구 성성분으로 처리될 수 있다. 그러므로 담줍 콜레스테롤, 인지방 그 리 고 담즙영 이 혼합 mi ce lle 형 태 로 촌재 한다. 이 들 각각의 함량에 따라서 m ic elle 의 용해도가 결정된다. 만일의 경 우 mi ce lle 내 의 콜레 스테 롤의 양이 증가되 고 담즙과 O,l 지방의 함량이 감소되면 콜레스테롤은 결정체로 변하여서 담석 (g alls t one) 이 생성된다(그림 2 참조). (22) 담줍내에 존재하는 콜레스데를은 소장내로 이동되어서 처분 된다. (23) 장내에서 콜레스테롤은 장내 미생물에 의해서 co p ros t erol 과 기타 다론 대사물질로 전환된다. (24) 변 스테 로이 드로 배 설된다. (25) 장내 내막에서 일부분의 콜레스테롤이 재흡수되어서 내막 세포내에서 ch y lom i cron 에 영합되어서 신체 순환계로 갇 수도 있 다.
2 콜레스테롤의 신체내 po ol 혈 청 내 콜레 스데 폴은 주로 Low Densit y Lipo p r ote i n s (LDL) 에 의 해 서 이 동된다. Goodman 과 Noble16) 은 동위 원소로 처 리 된 콜레 스 테 몰 을 사람에게 주사함으로써 신체내에서 콜레스테롤의 활성시간 울 이용하여서 산체내 콜레스데몰이 교환가능한 2 개의 주요 p ool 에 분 포되 어 있 음을 제 안했 다. 첫 번째 po ol 은 빠른 교환이 가능한 po ol 로서 주로 혈청내에서 이동되는 콜레스데롤과 혈구내의 콜레스테롤 그리고 간과 내장장기, 비장, 선장, 페, 소장에 함유된 콜레스테롤 로 구성되었다고 본다. 두번째 p ool 은 천천히 교환되는 p ool 로서 내 장장기 와 말단조직 과 골근육에 함유된 콜레 스테 몰울 말한다. 세 번째 p ool 을 굳이 구별을 짓자고 하면 이는 교환이 가능하지 않은 콜레스테몰로서 이는중추신경계동에 촌재하는 대부분의 콜레스테롤 을 구성하고 있다• 17) 이상에 언급된 신체내 p ool 내로 콜레스데풀의 공급은 장내막을 통해서 식이콜레스테 롤 의 흡수에 의해서 이루어지며 또 한편 간에 서 내원에 의해서 합성된 합성콜레스테롤, 죽 내자콜레스테롤 (end_ og e nous choleste r ol) 에 의 해 서 이 루어 진다. 이 po ol 로부터 의 콜레 스 테폴의 배출은 콜레스데몰이 담즙으로 배설이 되거나 또는 담줍 산으로 전환이 되는 것에 의해서 이루어진다(콜레스데풀의 체내증진 참조). 그리고 아주 소량의 콜레스테롤이 피부나 털이 붕괴될 때 제거 되며, 또 한편 스테로이드 호르몬으로의 전환에 의해서도 제거 된다. 3 소장으로부터 의 콜레 스테 를 흡수 식이콜레스테를은 간과 소장에 의해서 장내로 분비된 콜레스테롤 과 혼합된다. 소장내에서 콜레스데몰의 일부는 장내막을 통해서 혼 합된 mi ce lle 의 형 태 로서 흡수된다. 장내 막세포로 흡수된 콜레스테
롤은 장내막세포 자체에서 합성된 유리콜레스테롤과 혼합되며 이 중 일부는 콜레 스데 를 -es t er 로 전환되 어 chy lo mi cr on 으로 영 합된다. 이 chy lo mi cr on 은 lym p h ati c 과 tho racic 관을 통해 혈류로 이 동되 며 이는 곧 간으로 들어간다 .1 7) 간에서 콜레스테롤은 담즙으로 분비되 거나 담즙산으로 전환되거나 또는 혈청내로 분비된다. 담즙산의 대 부분이 담즙으로써 장내로 배설되면 다시 장간순환 (en t e rohe pa ti c ci rcula ti on) 을 통해 문백 정 맥 에 의 해 서 간으로 돌아간다. 그러 나 소 량은 변으로 배 설된다(그립 1 참조). 여 러 동물의 종족에 따라서 장 내에서 흡수될 수 있는 콜레스테롤의 양은 바교적 다양하다. 개는 석이콜레스테롤의 상당량을 흡수할 수 있다. 1 일에 3g r 정 도의 콜레스데를 섭취가 되면 이 양의 50% 까지 흡수되며 따라서 담 즙산의 형성과 배설이 증가되었음이 관찰되었다 .18) 쥐 또한 식이콜레스데를의 흡수능력이 크다. 1 일에 o. 5 g/ kg Body We ig h t까지 흡수된다 .19 - 20) 토끼는 식이콜레스테롤의 90% 까 지 흡수할 수 있는 능력이 있다 •19),21) 토끼도 콜레스테롤을 과량 섭취하면 혈장콜레스데롤의 농도가 2000m g /100ml 까지 증가된다 는 사실온 매우 찰 알려져 있다. 이와는 대조적으로 사람에게서 장내 콜레스테롤의 흡수량은 제한 되어 있다(표 1 참조). 섭취량에 따라 흡수윤은 폭이 넓은 차이를 보 여주고 있다. 1 일에 약 900m g /da y를 섭취할 경우 장내로부터의 흡수율은 약 45% 정도된다. 다음의 표 1 에서는 사람에서 콜레스테롤 섭취수준에 따르는 이의 흡수울을 나타낸 것 이 다. 사람의 경우도 1 일 몸무게 k g당으로 표시해서 흡수되는 콜레스 테롤을 m g으로 환산하여 보면 이를 앞에 설명된 동물의 효율과 비 교해 볼 때 약 1% 정도에 불과하다. 이 흡수율은 고콜레스데를혈증 (hyp e rchol~ste r olemi a) 환자에게서도 같다. 그리고 혈청내의 지방항 량이 정상인 사람에게서는 같은 양으로 흡수되는 능력을 가지고 있다 .22) 몇 가지의 요인들이 콜레스테를의 흡수되는 양에 영향을 미찬다. 콜레스테풀울 고지방식사와 함께 섭취하면 흡수가 보다 찰 되며 ,23)
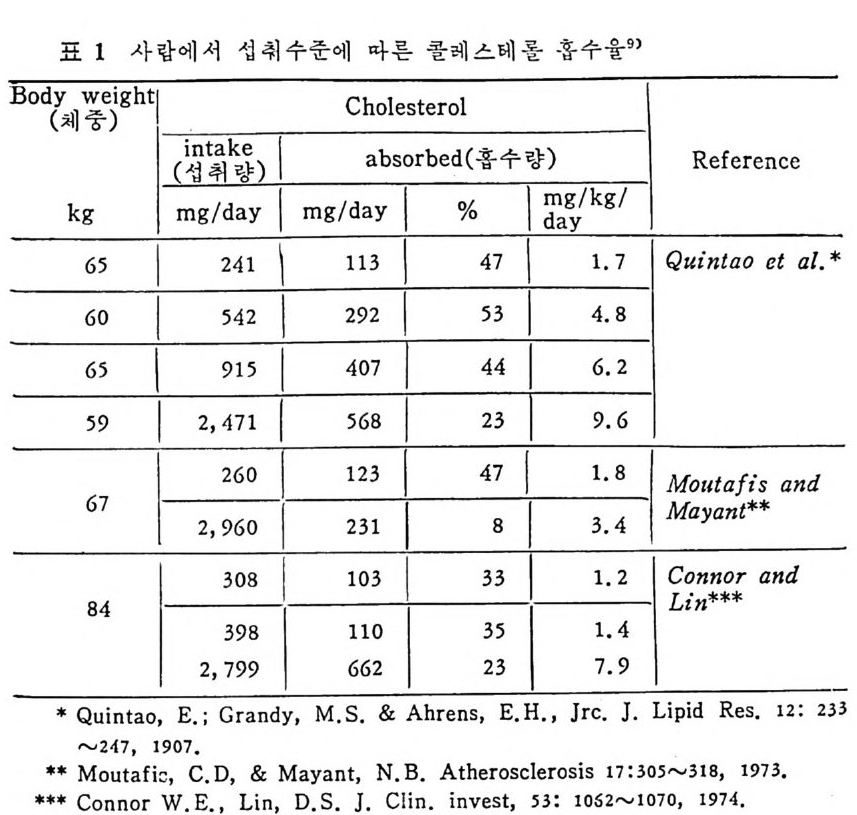 표 1 사람에서 섭취수준에 따른 콜레스테룬 홍수운 9 )
표 1 사람에서 섭취수준에 따른 콜레스테룬 홍수운 9 )
소장내 담즙산의 농도가 감소되는 경우와 관련된 상태에서는 흡수 가 처하된다 .24) 이러한 상황이란 담관이 막혔다든지 소장철단의 경 우, choles ty ram i ne 이나 neom y c i n 치료를 했을 때, 식물성 스테롤을 먹었을 때로서 콜레스테물의 흡수는 십하게 제한을 받든지 완전히 흡수되 지 않게 된다. 10) 4 콜레스테롤의 생합성 (1) 콜레스테롤의 생합성 대부분의 포유동물의 조칙은 콜레스데몰 합성능력이 있으나, 그
합성물은 다 다르다 •25) 쿨레스데몰 생합성과정을 연구한 노력의 댓가 로 노벨상 수상을 한 바 있는 L yn e n 과 Blooh 를 위시해서 많은 사 람들의 노력 으로 콜레 스데 룹의 합성 과정 은 정 확하게 밝혀 졌 다. 26- 7 ) 콜레스테돌의 생합성과정은 및 단계로 이끌어진다. 첫 째 로 acety l- C o A 는 aceto a cety l- C o A 를 동해 서 8-hy d roxy · 8 meth y l- gl u ta r yl - Co A (HMG-Co A) 로 전환되 고 HMG-Co A reduc- tas e 가 HMG-Co A 로부터 mevalonate 의 합성 을 축전한 다. 문헌 에 나타난 바에 의 하면 이 단계 가 aceta t e 로부터 콜레 스데 몰이 생 합성 될 때의 주요 조철단계라고 한다 .28) Mevalonate 가 mevalonate - 5-ph osph ate 와 5-p y ro p h osp h omeval-
onate 를 거 쳐 서 iso p e nte n y l pyro p h osp h ate 로 대 사되 며 이 는 3, 3- dim eth y l ally! pyro p h osph ate iso mer 로 된다( 표 2 참조) . 이 들 iso - mers 는 결과적 으로 iso p re ne unit s 를 구성 하게 되 며 스데 로이 드골 로의 구성단위이다.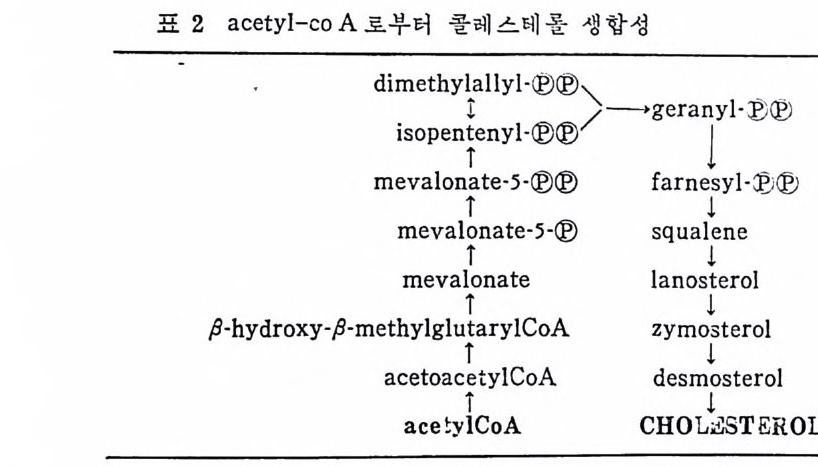 표 2 acety l- co A 로부터 콜레 스데 물 생 합성
표 2 acety l- co A 로부터 콜레 스데 물 생 합성
Gerany l pyro p h osph ate 는 iso p e nte n y l pyr op h osph ate 에 dim et- hy la llyl pyro p h osph ate 가 결 합되 어 서 생 기 는 물질 이 다. ge rany l- pyro p h osph ate 는 두번째 의 pe nte n y lp y ro p h osph ate 와 작용하여 서 far nesy l pyro p h osph ate 가 형 성 된다. far nesy l pyro p h osph ate 두 분자가 pyro p h osph ate 끝에 서 축함되 어 서 오로지 hy d rocarbon 으로
만 구성 된 squ alene 이 형 성 된다. 마지 막 단계 로 squ a ie n e 은 산화과정 과 cy c liz a ti on 에 의 해 서 Ian-oste r ol 로 년형 된다. 탄소수가 30 개 있는 lanoste r ol 은 결국 zy m - oste r ol 과 desmoste r ol 을 거 쳐 서 탄소수가 27 개 인 콜레 스테 몰로 전 환된다. 대부분의 포유동물의 조직에서는 이와 같은 콜레스테 를 합성이 가 능하다. 그러나 간이냐 소장조직이 콜레스테롤합성의 가장 주요 부 위라고 알려쳐 왔다 .29) 콜레 스데 몰 합성 전과정 중에 서 득벌히 중요한 단계 는 3-hy d roxy - meth y lg l u ta r yl - C oA (HMG-Co A) 가 mevalonate 로 전환되 는 작용 이 다. 이 작용은 HMG-CoA reducta s e 에 의 해 서 축전되 며 이 효소가 콜레스데 몰 생합성속도를 조철하는 조절효소로 · 알려져 있다. 이에 대한 여러 학자들의 견해를 수집해 놓은 많은 고찰문헌이 있다 .30-~) 여러 종류의 장기들 사이에서 콜레스데를 합성능력은 상당한 차 이를 나타낸다. 유리된 조직의 단위당 스데몰 합성률이 가장 높은 조직은 간, 회장(i leum) 조직이다 .17) 그러나 이 두 조직에서 합성되 는 콜레 스테 롤의 양도 동물의 종류에 따라 다르다. Die t s c hy 와 W i lson 은 다람쥐종류 (s qu i rrel monke y)와 사람에게서 콜레스테롤 합 성 률을 계 산하였 다. 29> squ ir r el monkey 는 간에 서 내 자 s t er 아 합성 의 82% 가 이루어지며 소화기장에서는 11% 밖에 이루어지지 않는 데 비해서 사람의 경우는 간과 소화기장내에서 거의 같은 양의 콜 레 스테 롤이 합성 된다고 한다. 17) 사람에게서 콜레스데롤의 합성률에 대한 연구는 대단히 복합적으 로 이루어지고 있다. 콜레스테롤 합성물을 연구하기 위해서 squ a lene 의 대 사를 연구하였 다. 간에 서 콜레 스데 롤의 합성 온 neg a ti ve -fe e d back 조철하에 있다고 한다. 이 조전작용에는 몇 가지의 요인이 관 계되며 쉽게 장기내에서 증거가 나타나지 않는다 .35) In vit ro 연구에 서 사람의 간조직 생 검 결과를 가지 고 연구한 결과 콜레스테롤을 섭취하면 콜레스데롤의 체내합성을 감소시킨다고 하 였다. 그러나 그 반대의 경우, 즉 콜레스테룹을 섭취하지 않으면 콜레스테몰 합성이 증가되어야 되는데 석사시에 콜레스테롤을 전연
함유하고 있지 않은 식사를 하여도 합성량의 중가는 이루어지지 않 는다. 이 현상은 아마도 내자 콜레스데몰이 소장으로 담즙과 함께 분비되어서 다시 재흡수를 하기 때문에 이러한상황하에서는 내자콜 레스테롤 양만으로 콜레스테롤의 체내 대사량이 비교적 충분하기 때 문에 합성이 억제된다고 본다. 사람에게 있어서 콜레스테롤합성의 neg a ti ve fee d back :조철의 확실한 중거 는 처 음으로 Grundy 둥 37) 에 의해서 제시되었다. 사람에게 식물성 s t erol 을 먹여서 장으로부터 콜레스데를의 흡수를 격감시킨 상태에서 콜레스데몰합성이 중가 되었음을 제시하였다. 이와 아주 유사한 fee dback 조철의 결과는 · Kudchodkar 둥에 의 해 서 도 발표되 었 다• 38) Nega ti ve fee d back 조철에 의 해 서 콜레 스테 롤의 합성 이 방해 되 어 지는 단계 는 HMG-Co A 로부터 mevalonate 로 전환되 는 곳이 며 , 이 작용은 HMG-CoA reducta s e 에 의 해 서 촉진이 된다. Brown 과 Goldste i n 에 의 해 서 입 증된 바에 의 하면 40) 세 포수준에 서 콜레스테롤의 생합성은 콜레스데를이 LDL 과 VLDL 내 콜레스 • 테롤로서 적어도 말단조직의 세포내로 들어가는 것과 밀접히 관련 되어 있다고 한다. 이 저자들에 의하면 ,40) 선덱되어진 세포표면에 있 는 recep tor 가 VLDL 과 LDL 의 Ap o p ro te i n B 와 강하게 서 로 결합되어야 비로소 VLDL 과 LDL 이 세포내로들어온다고하였다. 세포표면에 촌재하논 rece pt or 가 중재되어서 LDL 이나 VLDL이 결합될 때는 Ap op r o te i n B 가 분해되며 이렇게 되면 HMG-CoA reduc t ase 의 합성이 조철되어 결과적으로 콜레스테롤 생합성이 조 절된다. 39-40) 것산이 간에서 콜레스테롤의 합성을 감소시키는 역할이 있는데, 굶은 쥐 에 게 서 HMG-CoA reducta s e 의 활성 이 젖 산으로 인하여 감 소되 었음을 보고하였 다 .19) (2) HMG-CoA reducta s e 의 조절 1) HMG-CoA reducta s e 와 콜레스테롤 합성조절 HMG-CoA reduc tas e 활성 은 콜레 스테 를에 의 해 서 fee d back 조
철을 받는다. 일찌 기 1933 년에 이 미 Schoenheim er 와 Brensch41) 도 동물에게서 자신의 콜레스테롤합성에 의해 콜레스데롤의 대사가 조 절된다고 귀결하였다. 1950 년경에 Gould 와 Ta y lor42) 에 의해서 식이 내 콜레스테롤과 기아가 간으로부터의 콜레스테롤의 합성을 여제한 다고 보고하였 다. HMG-CoA reducta s e 는 이 러 한 조철기 전에 서 콜 레스테롤합성의 시작작용을 위한 주요 역할이 있다고 하였다• 그러나 콜레스테롤합성과 관련하여서 환원효소 (reduc t ase) 활성을 고려해 볼때 여러가지 조전에 의해서 영향을 받게 된다. 죽 동물실 험 에 서 보면 굶었 거 나 콜레 스데 롤을 먹 었 거 나 또는 cholesty ra mi ne 을 먹인 쥐에서 표준군에 비하여 이 효소의 활성이 크게 감소하고 있다. 콜레스데물의 합성능력은 여러가지 상태하에서 100 배나 증가될 수도 있고 1/100 로 감소될 수도 있는 넓은 폭을 가지고 있다. 이러 한 상황하에서 콜레스테롤의 합성능력과 환원효소활성과도 아주 현 저히 상호관련을 맺고 있다 .43) 여 하튼 HMG-CoA reducta s e 는 대 부분의 생 리 적 인 조건하에 서 는 간에 서 의 콜레 스테 롤합성 (choles t ero g enes i s) 에 중추적 인 효소이 다• 그 러 므로 콜레 스테 롤 합성 조철작용은 HMG-CoA reducta s e 자체 가 주 로 맡아서 한다. 30,44) 그러나 이에 이견을 가전 많은 연구보고가 있다. 죽 HMG-CoA reducta s e 가 콜레 스테 롤 합성 의 조절을 전적으로 담당한다는 것은 세 포내 부위 (int r a cellular com p ar t men t a ti on) 에 서 는 이 루어 지 지 않음을 밝혔 다. 32),45-6) 이 작용은 aceto a cety l- CoA th io l ase 와 HMG-CoA sy n th a se 에 의 해서 촉진되며 이 역할이 사실상 이 두 효소에 의해서 이루어진다 고 본다. 이들의 조철작용 측정도 많은 관십을 모으고 있다. 간내 에 는 mi toc hondria 내 의 에 모두 aceto acety l- CoA thi o l ase 와 HMG- CoA sy n th a se 가 촌재 한다. 전자의 효소는 케돈체합성에 관여하며 후자는 · 콜레스테롤합성에 관여 한다. mi toc hondria 밖에 존재 하는 thi o l ase 와 sy n t h ase 의 활 성 은 콜레 스테 롤을 먹 이 고 나면 감소된다. 47-51 )
그러나 이 사실은 모든 사람들에게서 공통적으로 관찰되어진 것 온 아니 고 48),51-2) 이 작용은 속도가 느리 고 불완전하다• 너 무 시 간 이 지연되면 이들 작용은 HMG-CoA 의 합성이 예민하계 여제되는 수준까지의 처수준으로 감소된다. 콜레스테롤식이로 사육 기간을 연장해서 계속적으로 먹이면 me- valonate 가 far nesyl pyro p h osph ate 로 그리 고 squ alene 으로의 전 환이 억 제 된다. 53) 이 들 효소들은 굽으면 감소하며 다시 재 사육을 하면 pyro p h osph o-mevalonate decarboxy la se, iso p e nte n y l pyro p - hosph ate iso merase, cia m eth y la llyl t r a nsfe r ase 와 squ alene syn th ase 의 활성은 중가된다. 54) 그러나 이들 효소들의 활성변화는 환원효소의 활성 이나 콜레스테 몰합성만큼이나 광법위하지도 않으며 빠르지도 않다. 그러느로 이 둘 효소에 의 한 조절은 HMG-CoA reducta s e 다음으로 중요한 것 으 로 생각된다 .55) 2) HMG-CoA reducta s e 의 분포 HMG-CoA reducta s e 는 모든 포유동물의 조직 중에 촌재 하지 만 이 효소의 합성은 간, 소장조칙, 피부, 순환하고 있는 백혈구내, 비 장내 lym p h ocy te, 발달단계 에 있 는 뇌 그리 고 간의 tu mor cell 에 서 가장 많이 발견된다. 그러나 대부분의 연구는 설치류를 실험동물로써 사용하여서 이루 어진 것이지만 이 환원효소활성은 사람의 피부내의 fibr oblast,5 6> 사 람의 백혈구내 ,57) 사람의 간조직편에서 58) 발견되었다. 포유동물의 세 포 homog e nate 에 서 보면 HMG-CoA reducta s e 는 대개 m i crosomal 막 부위에서 주로 발견된다. 환원효소의 80% 는 :SE R, go lgi a pp ara t us 의 막 부위에 관련이 되어 있으며 원형질막 과도 관련이 되어 있다 .59) 3) 포유동물 간내의 HMG -C oA reducta s e 의 Diur nal 리듬 쥐나 설치류를 실험동물로 사용하여서 환원효소의 d i urnal 리듬을 관찰하였다. 처음 이 효소의 리듬은 생쥐의 간에서 보고되었으며 60)
이후 얼마 되지 않아서 쥐의 간에서 61-2) 그리고 쥐의 소장 63) 에서 발 견되었다. 그러나 이의의 다른 동물아나 사람에게서는 이 환원효소 의 활성에 리듬이 있는지에 대해서는 아직 밝혀쳐 있지 않다. 지 금까지 밝혀 진 바에 의 하면 aceta t e 로부터 squ a lene 까지 전환 되 는 데 관여 하고 있 는 모돈 효소 중에 서 오로지 HMG-CoA reduc- tas e 만이 diu r nal 리 듬을 나타내 고 있 다. 54) 다른 효소로서 리 듬을 나타내 는 것 은 콜레 스테 롤 -7-a-h y drox y lase 분이 며 이 는 콜레 스데 몰 이 담즙산으로 붕괴 될 때 첫 번째 작용을 촉진한다. 64) 리듬의 현상은 낮과 밤 또는 빛과 어두움의 시간표에 따라서 효 소의 조절작용이 변화한다. 65) 쥐 에 게 사료를 임 의 로 먹 도록 공급하 고 정상적인 시간표에 의해서 빛과 어두움을 각각 12 시간으로 조절 해 놓으면 간에 서 의 HMG-CoA reducta s e 의 활성 이 간에 서 나 소 장조직에서나 모두 빛이 미칠 때 최소치에 달하며 어두어진 중간시 간에 가장 높은 치를 나타낸다. 그러나 그 최고치와 최소치의 차이 의 크기는 소장보다 간에서 더 크게 나타난다(그림 3 참조). 생 쥐 의 간에 서 도 HMG-CoA reducta s e 의 활성 이 질적 으로 봐서 쥐의 간에서와유사하게 변화하나활성이 가장높은 최고치에는빛이 비치고 있는 마지막 시간 쪽에서 나타났다. 죽 쥐의 간에서 나타났
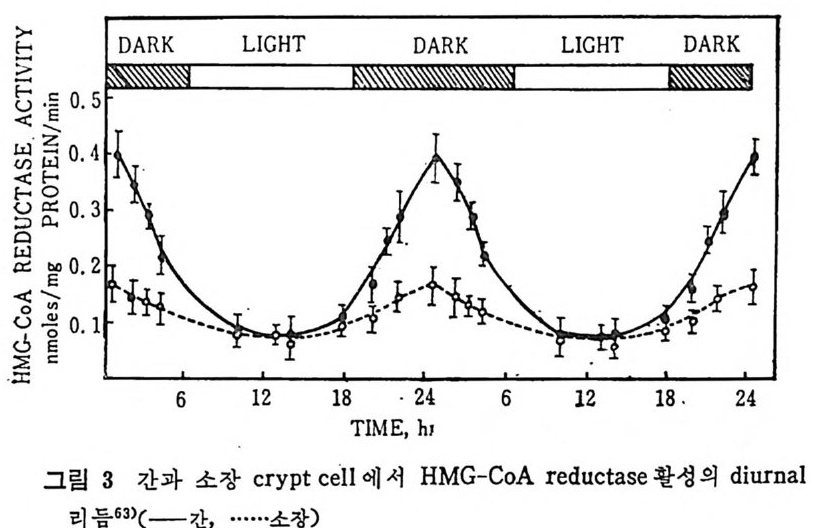 Al!A
Al!A
던 최고치의 고지(高地)보다 훨씬 먼처 나타나는 현상을 보여주었 다 .66) 그렇기 때문에 동물의 종족간의 차이를 알아보기 위해서 이 에 대한 관찰을 더하여야 할 것으로 본다. 쥐에게 임의의 식이를 공급하고 빛과 어두움의 조명시간을 달리 함으로써 리 듬의 현상을 변화시 킬 수 있 다. 65) 이 계동의 연구에서는 실험설계에 이 접을 고려하여서 설계한다. 그러나 또 다른 편법으로 식이공급시간을 조정함으로써 이 리듬의 현상을 조철하기 도 한다. 68) HMG-CoA reducta s e 의 활성 에 있 어 diu r nal 리 듬에 대 한 십 리 적인 특칭은 간 6 1) ,68) 에서나 소장 63),65) 에서나 모두 ace t a t e 로부터 여 러 종류의 스테롤들의 합성현상과 같은 리듬으로 나타났다( 그립 4 참조). 여기에 나타난 리듬은 스데몰합성이 mev alo nate 로부터 전환된 것을 관찰한 것은 아니다 .6 1)
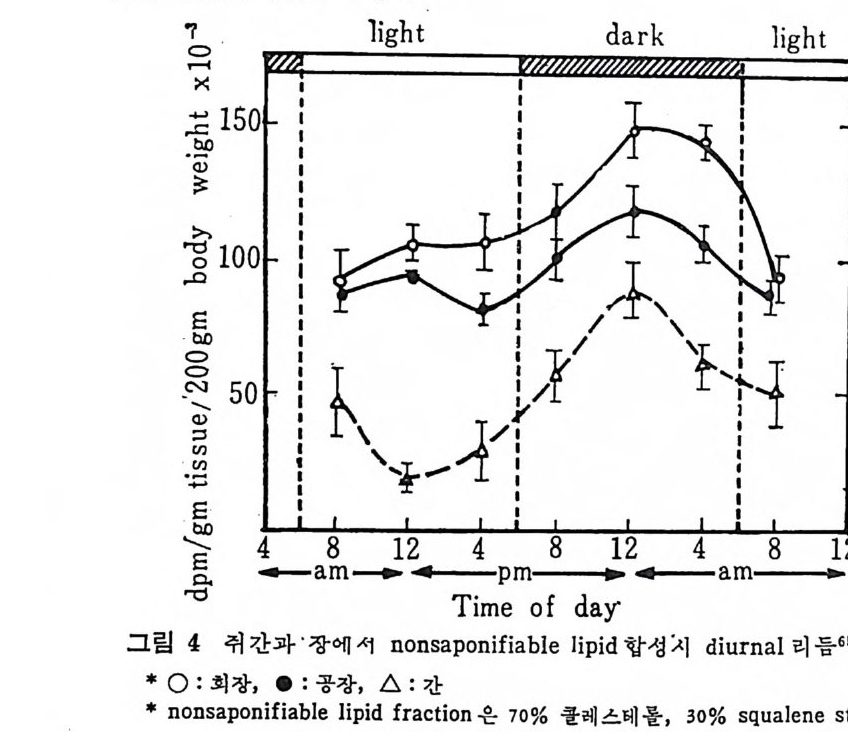 ?Ol lig h t dark ligh t
?Ol lig h t dark ligh t
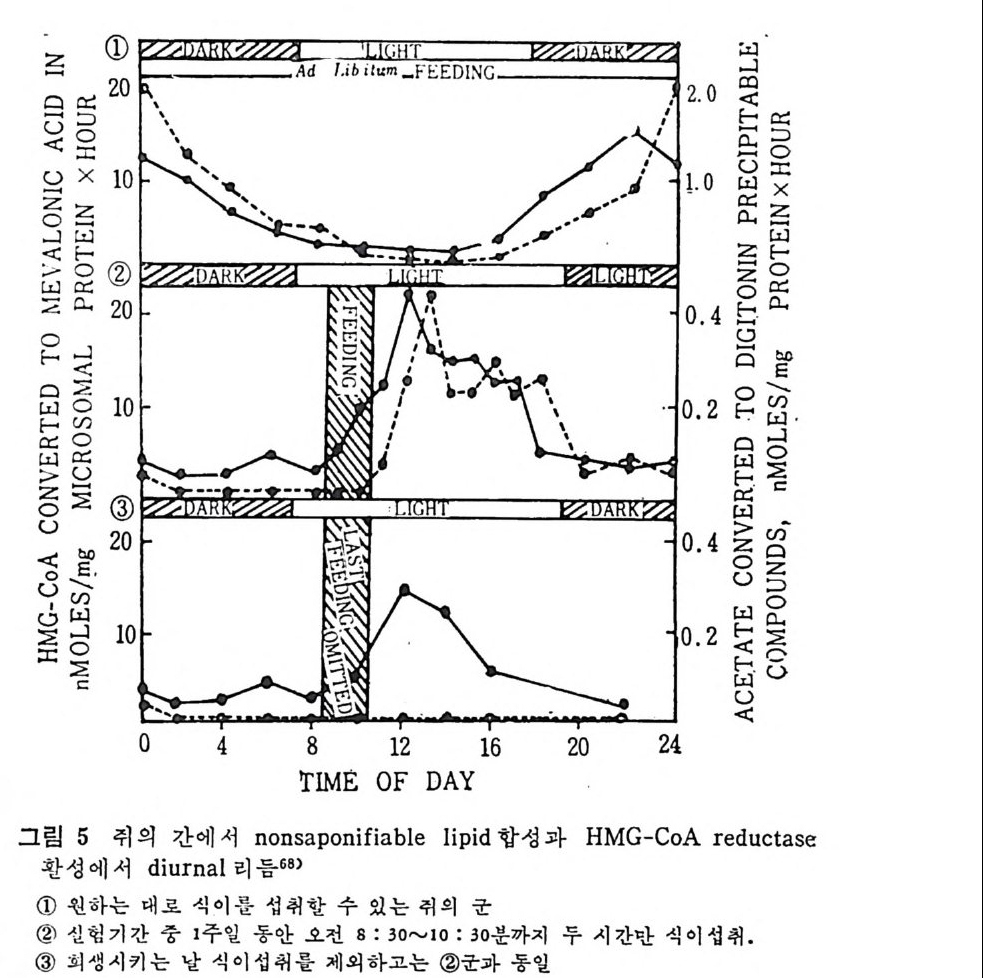 N, I ®2010 :!18>.. LidIJ3Hd
N, I ®2010 :!18>.. LidIJ3Hd
HMG-CoA 가 mevalonate 로 전환되 는 철대 울이 간에 서 콜레 스 테롤합성을 위한 속도조철의 기전이 된다고 고려한다면 콜레스테롤 합성 을 위한 리 듬으로서 도 HMG-CoA reducta s e 의 리 듬이 어 야 한 다고 본다. 그러 나 어 떤 조건하에 서 는 reducta s e 의 리 듬이 콜레 스 테롤합성 리듬과 같지 않다(그립 5 참조). 쥐에게 meal- fe ed i n g시키면 쥐는 이에 적응한다. 그러나 굶기면 스테 롤합성 의 리 듬은 깨 어 지 지 만 HMG-CoA reducta s e 에 대 한 리
듬은 그대로 있게 된다 70) (그립 5). 그렇다고 이 결과를 가지고 이 두 리듬 사이에서 원인이 되는 관계가 증명되지 않는다는 것은 아 니다. 다른 효소의 활성 의 변화 때 문에 reducta s e 가 더 이 상 합성 률에 제한울 가하는 효소가 아닐 수도 있 다. 그 예로 굶으면 mevalonate - 5-p yro p h osph ate - -+--+--+sq ua lene 으로 전환되 는 데 관계 하는 모든 효 소의 활성 이 감소한다. 64) 이 모든 효소의 활성감소는 콜레스데몰합성의 리듬의 표현이 방 해를 받고 오로지 reduc t ase 만이 이 리듬을 생성한 것으로 생각해 볼 수 있다(그립 5). 4) 리둠의 원인규명 콜레스데몰 자체, 호르몬 그리고 다른 여러 요소들을 두여하거 나 아니 면 억 제 하거 나에 따라서 간에 서 aceta t e 로부터 의 콜레 스테 롤 합성률에 현저한 변화가 온다는 것은 알려진 사실이다 .32) 이 변화는 결국 HMG-CoA 가 mevalona t e 로 전환되는 울이 변화 하기 때 문이 라고 생 각된다. 그러 므로 우선 HMG-CoA reducta s e 의 활성에 촉진을 가하거나 방해를 가함에 따라서 이 효소의 촉진작용 에 영향을 미찬다. 이 사실은 또한 HMG-CoA reducta s e 자체의 단백질합성아나 분 해에 따라서 리듬이 오르거나 떨어지는 현상이 나타난다고 해석해 볼 수 있 다. 그러 므로 HMG -C oA reducta s e 자체 의 단백 질합성 에 영 향을 미치는 여러가지 요인들을 생각하게 된다. Reducta s e 합성률이 중가되 면 현처한 간격 을 두고 이 효소의 활 성률이 증가되며 합성이 빠르면 약 6 시간 정도나 계속된다 .68) Dug a n 은 reducta s e 합성 의 증가울을 계 산하였 는데 diu r nal 리 듬 이 오르기 시 작하면 reducta s e 합성 물은 10 배 로 증가한다. 68) red- ucta s e 합성 의 증가가 diu r nal 중가 때 생 기 기 시 작하는 기 전은 이 전 에 먼저 de novo RNA 합성 물에 의 존된다. 70) Edwards 와 Gould 는 정상적으로 관찰되는 diu r nal 최고치가 나타나기 5~9 시간 전에 actin o my c in D 를 동물에 게 주사하면 reducta s e 활성 에 의 한 diu r nal
상승이 억 제 되 는 것 을 관찰하였 다. 그런데 acti no my c in D 의 주사 기간을 달리해서 diu r nal 최고치가 되기 15 시간 전이나 또는 1 시 간 전에 주사하면 reducta s e 활성 에 억 제 를 나타내 지 않아서 그대 로 diu r nal 최 고치 를 나타내 준다. Edwards 와 Gould 도 또한 acti no my c in D 가 식 품의 섭 취 와 대 사를 방해 한다고 하였 다. 70) 다음으로 reducta s e 단백질분해율이 diu r nal 리듬조철에 관계있 논지에 대해서도 아직 분명한 증거가 제시되지 않았다. 여하튼 정상 상태 에 서 reducta s e 활성 의 반감기 는 2~4 시 간으로 본다. 65),68-9),71 ) 부신 을 절제한 쥐에서도 이는 같다고 보고하였다 .72) 쥐 의 간에 서 reducta s e 활성 에 있 어 서 diu r nal 감소는 cy cl ohexa-mi de 의 주사에 대해서 두 가지 다른 견해가 보고되었다. Shap iro 와 Rodwell62) 은 완전히 활성 이 막힌 것 으로 보고하였 고 Edward 와 Gould6” 는 영향이 없는 것으로 보고하였다. 또한 이에 부과해서 acti no my c in D 를 주사함으로써 쥐 의 간에 서 reducta s e 활성 의 감 소에 영 향을 주지 않았다고 보고하였 다. 70) 이 상의 다양한 결과를 종 합해 보면 reducta s e 분해 의 조절이 diu r nal 리 듬에 어 떠 한 역 할이 있다고 결 론지을 수 없다 .55)
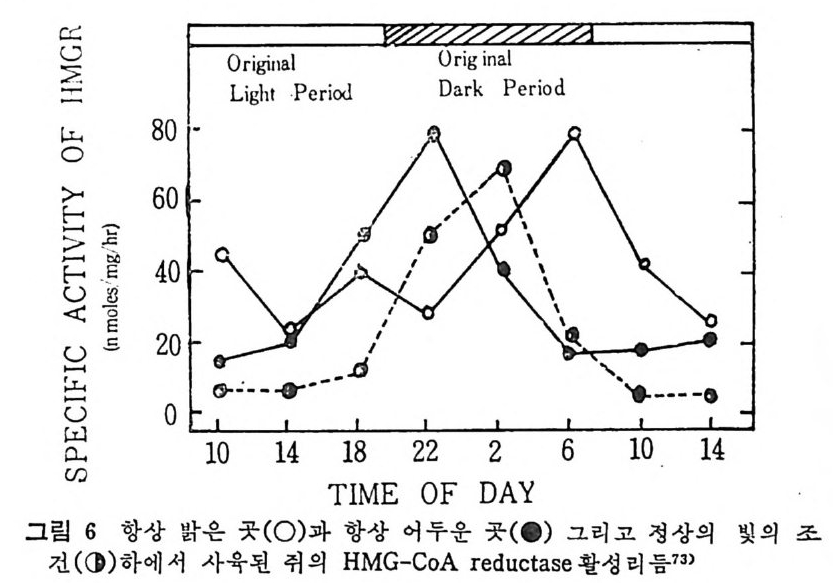 u
u
쥐 에 게 임 의 로 먹 이 거 나 (ad libi t ium ) 시 간표에 따라 먹 이 거 냐 (meal fe ed i n g)하는 것 또는 밥과 낮의 시 간조정 이 간내 의 HMG- C oA red- uc t ase 의 리듬을 결정한다고 생각한다. 그런데 정상쥐에게서 이 리 듬은 낮과 밥시간에 관계없이 계속됨이 나타났으며 72) ( 그립 8 참조 ), 그리고시간표에 의해서 먹이는쥐는사료 를 먹이기 직 전에 활 성이 중 가되기 시작하였다 6 8 ) (그 림 5 참 조). 빛의 c y cle 이나 식품의 섭취가 리듬을 야기시키는 원인이 되지 않는 것으로 보이며 내적인 요인, 죽 호르몬의 영 향 이 있 윤 것 으 로 본다. reduc t ase 합성과 콜레스테몰합성의 전반적인 조철에 관여하 여서 d i urnal 리듬을 유지하는 데 관여하는 호르몬은 인슈린, glu ca- go n, th y ro id 호르몬 그리 고 hy d rocorti so n 둥이 다. 인슈란과 th y r oid 호르몬은 reduc t ase 합성률을 증가시키거나 또 는 합성의 시작에 관여하여서 결과적으로 리듬의 고조된 부 분 을 유 지 시 키 는 득칭 이 있 으며 , 74-6) 한편 hy d rocorti so n 과 glu cag o n 은 되cA 어M P있 의 다 고영 향한다을. 7통4 )해,76 )서 reducta s e 합성 의 끝을 내 는 작용에 포함
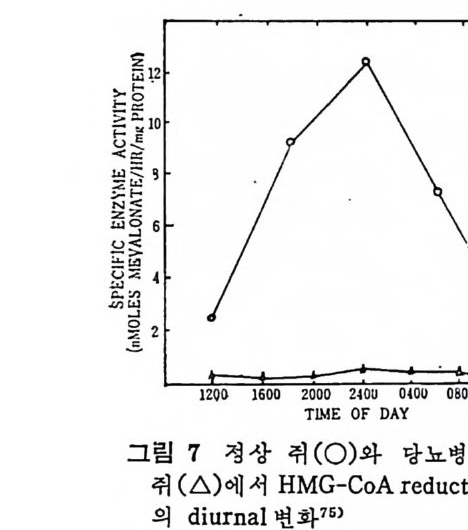 홍1 2
홍1 2
정상쥐에서도 혈 청내 인슈 란 수준은 diu r nal 변화와 같이 번화하며 이 현상은 참정 적 으로 HMG- C oA red-ucta s e 의 리 듬과 함께 한 다. 76) 그런데 str e p toz oto c in 에 의해서 유발된 당뇨병쥐 의 reducta s e 의 평 균 활 성 은 대 단히 낮다 76) (그 립 7 참조 ). 여하돈 정상쥐나 당뇨병의 쥐 모두 diu r nal 변화가 낮은 때에 많은 양의 인슐린을 한 꺼 번에 주사하면 reducta s e 의 활성은 정상 diu r nal 최고
치 의 수준까지 증가된다. 73-4)
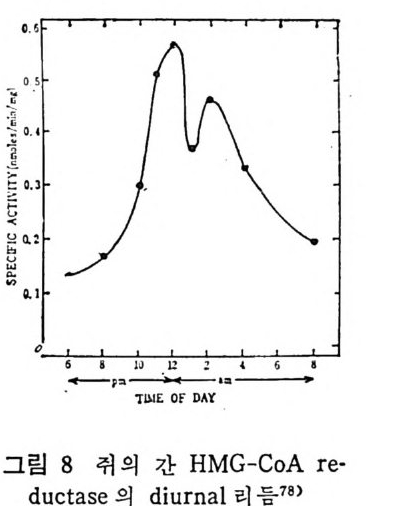 ..6
..6
Glucag o n 도 역 시 HMG-CoA-redu-cta s e 의 diu r nal 리 듬을 조철하는데 diu r nal 최 고치 에 달하기 3~4 시 간 전 에 glu cag o n 을 주사하면 diu r nal 중 가는 정상의 50% 밖에 증가시키지 못 한다 . 77) 인슈린을 주사하기 전에 먼 저 g luca g on 을 주사하면 인슈린 하 나만 주사했을 때 에 비 해 reducta s e 활 성의 빠른 증가가 억제된다 .77) 이 는 glu cag o n 이 인슈린의 reducta s e 에 대한 영향에 길항작용울 한다고 생 각한다. 앞에서도 언급했듯이 당뇨병이 있 는 쥐에게 인슈린을 두여하면 re-
ducta s e 활성 이 급하게 상승하며 정 상범 위 의 리 듬으로 된다. 76) 그러나 h yp o phy sec t om i zed 된 쥐에게서는 인슈린을 두여하여도 reducta s e 활성 이 증가되 지 않는다. 75) 이 현상은 th y r oid 호르몬이 reduc t ase 작용에 인슈린의 효과를 위해서 필요하다고 본다. 그리고 th y r oid 호르몬이 리듬표현에 요구되어진다고 본다 .75) Adrenal 호르몬의 효과에 대해서는 d i urnal 리듬의 조철에는 서로 상반되 는 결 과가 나타났다. adrenalecto m y 는 reducta s e 활성 에 있 어서 리듬의 범위가 감소하며 12) 간에서 콜레스데롤의 합성능력이 감소한다고 보는 반면 m reduc t ase 리듬에 영향이 없었다고 보고되 기도 하였다 .75-6) 이러한 상반된 결과에 대해서 아직까지 실마리가 해결되지 않은 채로 있다. 5) HMG-CoA reducta s e 활성 의 이 중최 고치 Shap iro 와 RodwelF8) 는 취 의 간에 있 는 HMG-Co A reducta s e 의 d i urnal 리듬에서 이중최고치를 관찰하였다(그립 8 참조). 이 현상에 대한 가능한 전망은 Rodwell55) 등이 하였다. 첫째는 HMG-CoA reducta s e 의 붕괴 시 에 특수한 대 사조칙 에 의 해 서 과도
기적으로 나타나는 것이라고 하였고, 둘째는 i soz y me 이 이중의 최 고치를 나타낼 수 있다고 하였다. 그리고 세째는 대사가 너무 지나 치게 이루어지기 때문이타는 것이며, 네째는 HMG-CoA reducta s e 의 주기적인 전동으로 생각해 볼 수 있다고 지적하였다. 이에 부과 해서 호르몬의 작용이 reducta s e 단백 질합성 을 조철할 수 있 다고 생 각한다 .55) 6) HMG-CoA reducta se 활성 에 관련된 기 타 인자들 (D Cy c lic AMP 3'5'-cyc lic AMP 를 동해 서 효소활성 에 영 향을 미 치 는 호르몬의 조철은 찰 알려진 사실이다 .79> HMG- C oA reducta s e 경우도 cAMP 와 많은 관련이 있다는 제안이 많이 있지만, 아직 확신할 수 있는 증거는 되지 못한다• 7J. -철 편이 나 간 homog e nate 에 cAMP 몰 첨 가하였 더 니 콜레 스데 롤의 합성 이 감소되 었 다. 80- 2 ) 또한 cAMP 로 처 리 된 mi cr osomes 의 homog e nate 에 서 도 reducta s e 의 활성 은 감소되 었 다고 보고하 였다. 81 ) In vit ro 연구에 서 Raskin 은 도전하기 를 소량의 cAMP 로서 red-ucta s e 활성 이 나 콜레 스테 롤 합성 의 방해가 막대 하게 나타난다고 하 였 다. 그러 나 pe rfu s ed 된 간에 서 glu cag o n 주입 에 의 해 서 cAMP 의 세포내 농도를 50 배로 증가시켜도 reducta s e 활성에 방해가 냐 타나지 않았다고 하였다 .80-1) @ Mg - ATP Reducta s e 활성 을 분석 하기 전에 유리 된 mi cr osome 을 Mg - ATP 와 함께 배 양시 켜 서 reducta s e 활성을 관찰해 본 결과 빠른 감소골 나타내 었 다 81),83) (그립 9 참조). M g++오l- ATP 가 첨 가되 고 여 기 에 부과해 서 EDTA 를 첨 가하면 reduc t ase 활성은 여전히 방해되었다. 그러나 원십분리에 의해서 처리되었던 m i crosomes 에서 M g -ATP 를 분리시켜서 이동시켜도 reduc t ase 의 불활성이 활성으로 전환되지도 않았다 .8 1) 그런데 cA-
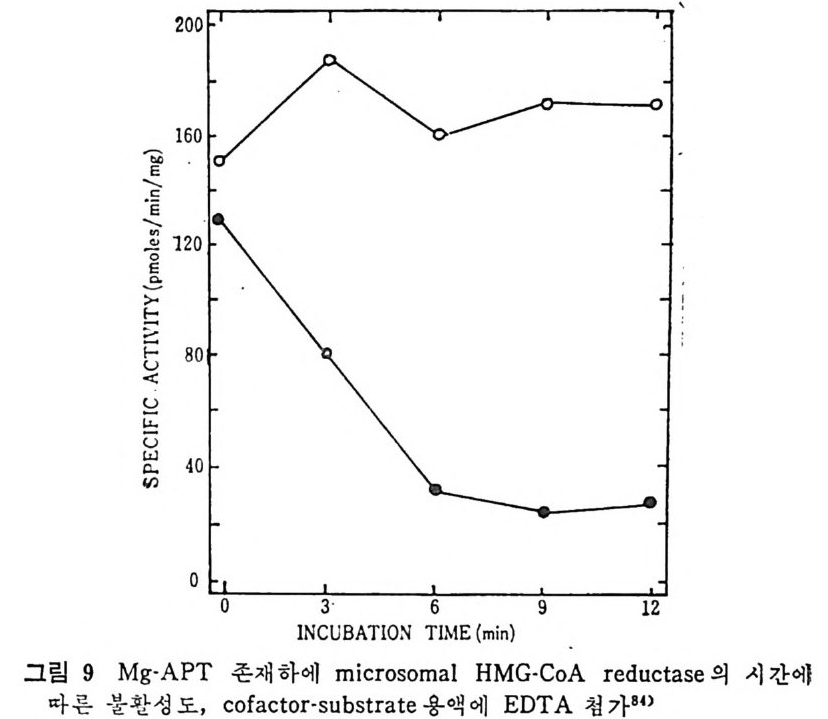 200
200
MP 는 Mg - ATP 에 의 해 서 reducta s e 의 불활성에 아무런 영향을 미 치 지 못한다고 보고하였 다. 83) ®기타요소 쥐의 담즙내에 함유되어 있는 단백질은 취의 간에서 ace t a t e 로 부터 콜레스테롤이 합성되는 것을 방해한다고 한다. 그런데 이 단 백 질은 mevalonate 로부터 의 합성 은 방해하지 않는다. 84) 그런데 후에 McNamara86) 의 관찰에 따르면 쥐 의 담줍이 쥐 의 간에서 의 mi cr osome 내 의 reducta s e 의 활성 울 방해하였 다고 하였 다. 그 밖 에 소의 담줍에서도 redu ct ase 의 활성을 방해하는 단백질이 있다 고 하였다 .87) 그러나 이들의 방해기전은 알려진 것이 없다. 이들 활성부위논 매우 유사하나 취나 소의 담줍으로부터 유리된 방해물질은 분자량
으로 비교해 보면 엄청나게 다르다. 쥐의 담즘에서 유리된 것은 분자량이 낮아서 19,000 정도인데 소 의 담줍에서 유리된 것은 밀도가 낮으나(/3=1. 024), 분자량은 높은 2 x 106 lip o pr o te i n 으로서 이 들의 지 방구성 은 혈청 의 /3- lip o p ro te i n 과 비슷하다. 이외에도 reduc t ase 의 방해물질이 쥐의 것, 소와 사항의 젖에서 보고된 바 있다 .88) 5 담줍산의 생합성 (1) 담즙산의 생합성 담즙산은 간에 서 콜레 스데 볼의 분해 최 종산물이 며 신체 로부터 스 테 를의 궁극적 인 배 설의 주요 수단이 다. 89- 9 1 ) 이에 부과해서 담줍산은 생리적으로 중요한 몇 가지 기능이 있다. 예로서 장내에서 담줍산은 식이로부터 섭취된 중성지방이 췌장의 lipa se 에 의 해 서 분해 된 마지 막 산물인 지 방산과 monoacy lg l y c erol 형 태 로 mi ce llar 용액 내 로 들어 오도록 하는 데 중요한 역 할이 있 다. 92) 그리 고 담줍산은 콜레스테물과 다른 스테 로이 드 호르몬의 소장으로 부터 의 흡수에 도 필요하다. 92-3) 담산은 장내막을 건너서 지용성물질의 이동을 증가시키는 것에 부과해서 몇 가지의 중요한 대사과정에 조절기전으로써 효과를 나 타내 고 있 다. 94) 예 로서 쥐 의 간에 서 담줍산은 aceta t e 로부터 콜레 스데 를의 합성 과 콜레스테 롤로부터 의 담줍산합성 시 의 fee d back 조 철에 중요한 역 할을 한다. 95-6) 또한 담즙산도 소장에 서 콜레 스데 몰 합성률을 변화시킨다고 본다 .29),97)
본장에서는 콜레스테롤의 합성과 분해와의 관계 측면에서 담줍 산의 역할을 논하고자 한다. 그러므로 담즙산의 합성과 이의 조 철은 곧 콜레스테롤의 대사와 직결이 되어 있으므로 이를 중접적 으로논의하고자한다. 담줍산의 생합성에 관련된 구체적인 정보는 주로 포유동물에 있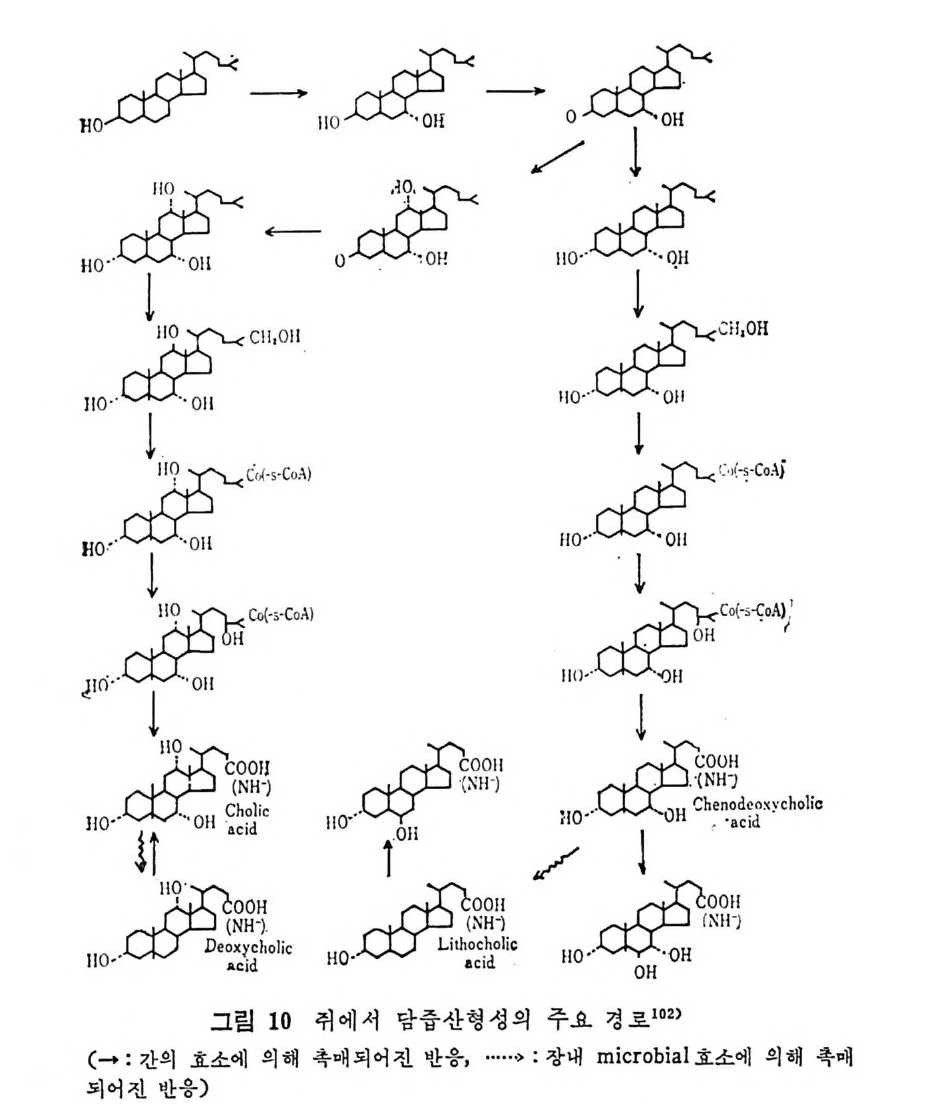 三一 II O : :一 。 」:
三一 II O : :一 。 」:
어서 쥐를 사용하여서 얻은 연구 결과이다 .98 - 10 1) 다음 그림 10 에 요약된 것은 쥐에게서 콜레스데몰이 담즙산 선행 물질 (pr im ary bile a ci ds) 인 cholic acid 와 chenodeoxy cholic acid 로 전환되는 대사과정이다. 콜레스테를로부터 담줍산이 합성되는 울은 choleste r ol 7a-hy d roxy la se 에 의 해 서 조철된다. 또한 콜레 스테 롤
합성 에 서 주요 속도조철효소인 HMG-CoA reduct:i .s e 는 담줍산 생 성에 유용하게 쓰인 콜레스테롤의 새로운 생성을 조절해 준다. 담줍내의 담즙산 구성은 부분적으로 2 종류의 효소에 의해서 결정 된다. 첫 째 로 12a-hy d roxy la se 이 며 또 다른 하나는 26- h y d roxy la se 로서 이 들은 모두 7a-hy d roxy c holest- 4 -en-3-one 혹은 5/3 - cholesta n e- 3a, 7a-dio l 에 작용한다. 간은 콜레스데몰 (그립 11-I )로부터 담즙산 선행물질인 chenode- oxy c holic acid (그립 11 ~ II) 와 cholic acid (그립 11-m) 로. 전환시키는 유일한 장기이다.
콜레 스데 몰로부터 cholic acid ' 의 합성 은 고리 (Ri ng ) 구조 변화 이 전에 sid e chain 의 분해 가 언 저 일어나야 한다. 콜레 스데 롤은 먼처 5/3 - choles- tan e-3a, 7a, 12a-tr i o l , 탄소수가 C21 인 bil e alcohol (그립 12- 벤)로 전환되 며 이 로부터 sid e chain 인 iso octy l 로부터 끝에 서 iso p ro p yl gro up 을 옮겨 냄 으로써 C24 bete aci d 인 cholic acid 를 형 성 한나 (그립 12 참조)• 그립 13 에서 보여주는 것은 choleste r ol 로부터 7a-hy d roxy c -holest- 4 -en-3-one 으로 전환되 는 과정이다.
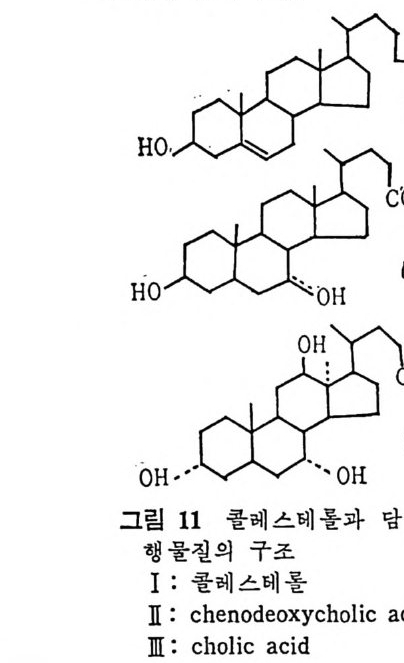 HO
HO
콜레 스테 롤로부터 cbolic aci d 와 cbenodeoxy c holi c acid 로 전 환 되는 주요 경로는 그림 13 에서 보여주는 바와 같다. 콜레스데 몰이 7a-hy d roxy c boleste r ol (N) 을 거 쳐 서 7a-hy d roxy c holest- 4 - en-3 - one (V) 로 전환되는 것이다. 불포화 케돈기를 가전 물질 (V) 은 결국 두 종류의 담줍산 선행물질의 공동 중간대사 산물이다. 이 물질은 5/3 - cbolesta n e-3a, 7a-dio l (vI)로 전환되어 서 결국 chenode-
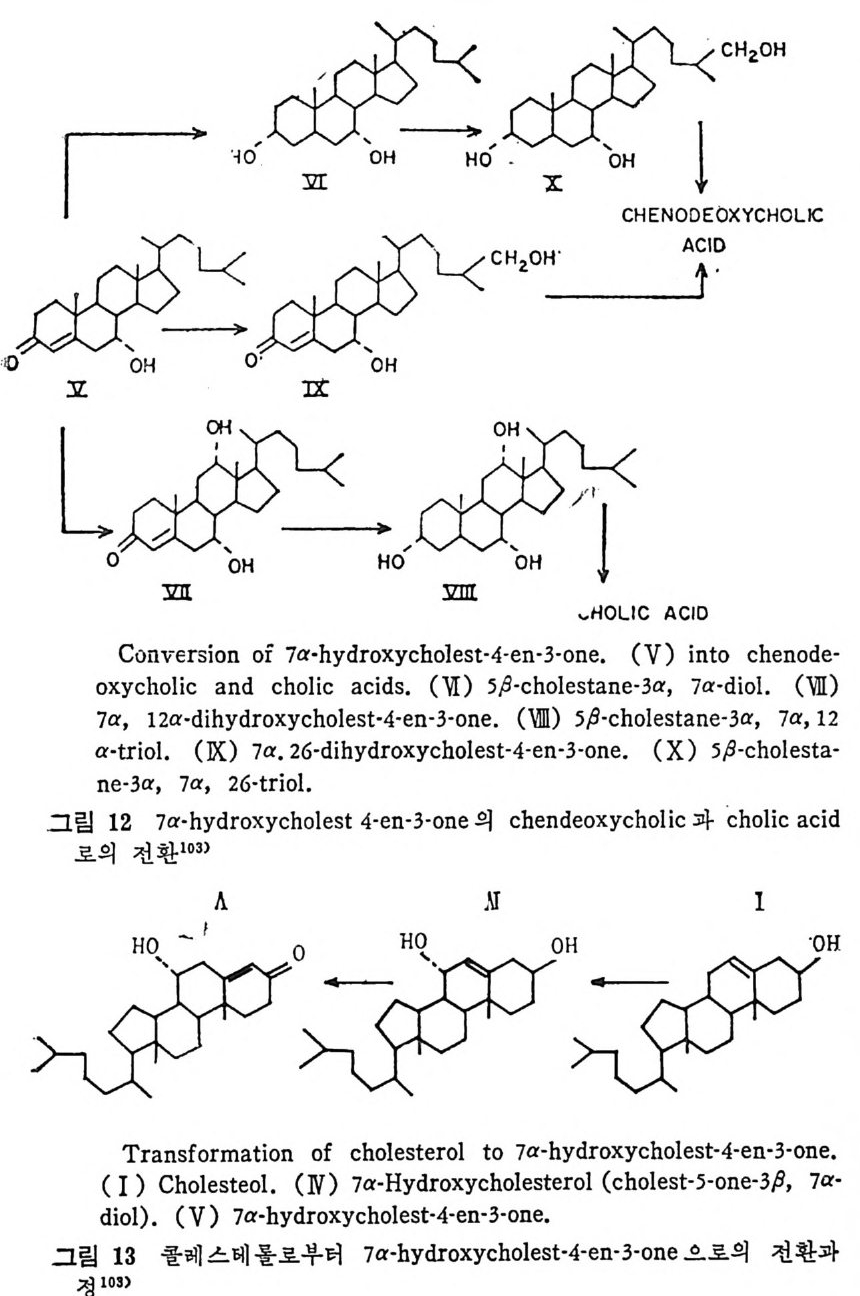 · 广 广 0广 \,广CH 20H
· 广 广 0广 \,广CH 20H
oxy c holic :i.cid 로 전환되 거 나 또는 12a-hy d roxy la ti on 을 거 쳐 서 3a,. 7a-dih y d roxy c holest- 4 - en -3-one (맨)으로 되 며 이 는 5(3 - cholesta n e- 3a, 7a, 12a-tr i o l 澤)을 거 쳐 서 cholic acid 로 전환된다. 3a, 7a· dih y d roxy c holest- 4 -en-3-one (넘)과 5/3 - cholesta n e-3a, 7a-dio l (\lfi) 의 sid e cha i n 의 분해로 26-hy d roxy la te d 된 중간산물(예 : X) 을 동 해 서 choli c acid 로 전환되 기 위 해 서 이 에 해 당하는 26-carboxy li c ac i d( 예 : 그림 14 의 XI~XIII) 로 전환된다. 5/3 - cholesta n oic acid (XI) 로 /3- oxid a ti on (XII, XIII) 을 거 쳐 서 C24 의 5/3 - cholanoic acid ( ll )와 pr op ion ic acid (XIV) 를 형 성 한다. 담즙산 합성 시 에 sid e chain 의 산화는 mi toc hondria 내 에 서 이 루 어 진다고 Sta p le 이 발표하였 다. 105) 이 어 서 1973 년에 Tanig u chi, Hoshit a 와 Okuta 에 의 해 서 26-hy d roxy la se 가 mi toc hondria 내 에
 HO 二 l0 〈C :〈 coon
HO 二 l0 〈C :〈 coon
존재 하고 있 음이 확인되 었 다. 26-hy d roxy la se 는 5/3 - cholesta n e-3a: ~ 7a :, 12a :-tri o l 에 작용하는 것 으로 밝혀 졌 다. 106) 그러 나 이 와는 대 조적 으로 쥐 의 간 mi cr osomes 에 서 5/3 - cholesta n e 3a: , 7a: , 12a :-tri o l 의 hy d roxy la ti on 이 C-23, C-24, C-25 와 C-26 에 서 일어 나며 득히 5/3 - cholesta n e 3a: , 7a: -d io l 은 주로 C-26 에 서 hy d r- oxy la ti on 이 일어 나며 소량은 C-25 에 서 도 생 긴다고 보고하였 다. 107 ) (2) 담즙산 생합성의 조절기전 1) 일반적인 기전 간에 서 합성 되 는 담즙산의 합성 률은 담즙산의 순환움과 poo l 내 의 담줍산의 구성성분에 의해서 조절된다고 본다 .103),108) 담즙산합성의 자세한 조절기전은 잘 알려져 있지 않지만 알려진 바에 의 하면 간의 mi cr osomal 효소인 콜레 스테 롤 7a-hy d roxy la se 가 쥐 , 108) 토끼 109) 와 사람 llO) 에 서 도 속도제 한효소로 밝혀 졌 다. 또 한· 편 콜레스테롤은 담즙산 생합성의 팔수선행물질이므로 콜레스데몰 생 합성 의 속도제 한효소인 간세 포내 의 HMG-CoA reducta s e 도 담줍 산합성 에 조절을 가하는 역 할이 있 다. 소장세 포에 서 나 111) 간세 포내 에 서 Hz) HMG-CoA reducta s e 의 수준은 순환하는 담즙산의 양에 의 해서 영향을 받는다고 하였다. 그러므로 HMG-CoA 는 새로이 생성 되는 콜레스데롤의 공급에 제한을 가하게 될 것이며, 그럼으로써 cholanoic acid 생 합성 에 제 한을 받게 될 것 이 다. 어 떤 조건하에 서 도 HMG-CoA reducta s e 와 choleste r ol 7a-hy d rorxy la se 의 담즙산 총생산량에 미치는 영향을 비교하여 보면 HMG-CoA reduc t ase 의 영 향이 더 큰 것 으로 나타났다. 한편 어 떤 경 우에 는 7a-hy d oxy c h-oleste r ol 로부터 형 성 되 는 담즙산의 양온 순환되 고 있 는 담즙산에 의해서 조철되지 않는 것 같다 .108),109) 그러나 그림 12 에서 보여주듯이 하나의 선행물질 7a-hy d roxy c h-olest- 4 -en-3-one 으로부터 chenodeoxy c holi c ac id 와 cholic ac id 로 전환되 므로 또한 담즙산 po ol 의 구성 성 분, 즉 choli c ac id 와 che·- nodeoxy c holic ac id 의 비 울에 따라서 두 종류의 효소의 상호작용이
영 향을 U士 을 것 으로 본다. 우선 7a-hy d roxy c holest- 4 -en-3-one 의 12 ao-xhyy l ad trio oxn y 이 la ti된 o다n .이 (N촉— 진DC되)l 고04) (그V-러VI I나), 또둘 째한로편 c이h ol물ic 질 a이cid 와26 -hchy edn r-- odeoxy c holi c aci d 의 비 례 를 결정 해 주는 주요 중간대 사산물 5g - cholesta n e-3a, 7a-d i ol(VI) 로서 이는 마치도 불포화 케톤물질과 마찬 가지로 12 나 26 위치에 hydrox y la ti on 이 될 수 있다 .(\ ·I --+X: orVI--+ 맨 ).113) 2) 콜레스테롤 7a-hy d roxy la se 콜레 스테 롤 7a-hy d roxy la se 의 활성 은 diu r nal 리 듬을 나타내 며 , 이 현상은 간세 포와 장내 세 포내 에 존재 하는 HMG-CoA reducta s e 의 활성과 거의 같은 현상을 보인다. 그래서 이 효소의 활성은 밥 에 최대의 활성을 나타낸다. 이 효소의 활성 은 장간순환 (en t erohe p a ti c c i rcula ti on) 이 어 떤 이 유 로든지 방해 를 받았을 때 , 죽 cho!esty ra mi ne 을 두여 하였 든가 아니 면 담관 (b ili ar y t rac t)에 변화가 생 겼을 때 증가된다. 담낭으로부터 의 콜레스테롤과 담즙산의 분비는 두 최고접을 나타낸다. 즉 새벽 1 시 와 아침 6 시 였 다. 이 러 한 최 고접 들은 HMG-CoA reducta s e 활성 의 2 중 최 고접 과 일치 한다고 본다. 79) 담낭으로부터 의 당줍산의 분비 와 아울러 서 콜레 스테 몰 7a-hy d r- oxy la se 의 활성 은 낮과 밤 또는 빛 과 어 두움의 cy c le 보다도 식 이 섭취량과 더 관계가 있는 것으로 본다. She fer 와 그의 동료들은 계 속해서 십이지장으로 식품을 주입해 줄 때 쥐의 담낭으로부터 담즙 산분비 에 어 떤 diu r nal 번화를 관찰하지 못하였 다. 103), 108) 개와 쥐에게서는 담즙산생산이 내자 콜레스테몰에 의해서 자국되 었다고 하였다. 그러나 토끼와 사람에게서는 이러한 현상이 나타나 지 아니하였다. 1% 콜레스테롤 식이를 쥐에게 섭취시키고 난 약 6 시 간 후에 콜레스테롤 7a-h y drox y lase 의 활성이 30% 정도 증가되었 다. 또한 고콜레스테롤 식이를 섭취한 6~7 일 후에도 이 효소의 활 성이 배로 증가되었다 .114) Mosbach 와 그의 동료들은 동위원소 영합방법에 의해서 콜레스
테롤 7a-h ydroxy lase 를 결정하였는데 2% 콜레스테롤 석이로 10~ 1 4 일간 사육한 결과 이 효소의 활성이 약 67% 정도 증가되었다. 그. 러나 첫 주일에는 중가됨을 관찰하지 못하였지만 담즙산의 배설이 중가되 었 다. 112),1 1 5) May a nt 와 그의 동료들은 지적하기 를 콜레 스데 몰 사육으로 인해서 증가된 7a-hy d roxy la se 의 활성 은 내 자 콜레 스데 몰에 의 해 서 mi cr - o s ome 의 콜 레스테 륭 p ool 이 증가되었기 때문이지 간에서의 효소 농도가 증가된 것 은 아니 라고 하였 다. 114' Shefe r 와 그의 동료도 동 위원소 영합방법을 사용하여서 HMG-CoA reduc t ase 의 활성을 관 찰 하였 다. 1 %의 tau rocholate 나 1 %의 tau rochenodeoxy c holate 가 함유된 사료식사로 7 일간 사육한 쥐에게서 간세포내의 HMG-CoA reduc t ase 의 활 성이 방해되었음이 나타났다. 이 결과와는 대조적으 로 콜레 스테 롤 7a-hy d roxy la se 의 활성 은 tau rucholate 를 먹 였 을 때 도 강하게 방해 를 받았는데 tau rochenodeoxy c holate 를 먹 였 을 때 는 그렇지 않았다 .112) 그러 나 Danie l son 에 의 하면 두 종류의 담줍산 선행물질을 3~7 일간 먹였을 때 7a-h y drox yJ ase 의 활성은 거의 같 온 정도로 방해하였다고 하였다 .116) 이 두 연구결과를 직접 비교해 볼 수는 없 다. 왜 냐하면 Danie l son 은 이 효소의 활성 을 diu r nal 리 듬의 최고치 때 측정하였고 She fe r 는 최저치 때 측정하였다. 한편 Ra i ch t는 쥐에게서 스테롤 균형연구를 했는데 담줍산 형성 온 tau rocholate 나 tau rochenodeoxy c holate 를 두여 하였 을 때 모두 같은 정 도로 방해 를 받았다고 하였 다. 117> HMG-CoA reducta s e 의 활성 이 방해 될 조건하에 서 는 콜레 스테 몰 7a-hy d roxy la se 의 활성 은 in v it ro 에서 결정할 수 있어도 이 결과가 반드시 in v i vo 에서 담 즙산 합성을 반영하지는 않는다. 콜레 스테 몰 7a-hy d roxy la se 의 활성 은 담관를 묶어 놓으면 담즙산 생산이 정상 이하로 되었을 때 증가되었다고 하였다 .118) 여하튼 이 모든 경 우를 종합해 보면 간세 포내 의 mi cr osome 의 콜레 스테 롤 7a-hy d roxy la se 는 활성 으로 모든 in viv o 에 서 의 생 합성 률을 반영 한다 고 말할 수 없다고 본다.
3) choli c a c id/ chenodeoxy c holi c a cid 의 비 율 간세 포의 mi cr osome 내 에 있 는 효소 7a-hy d roxy c holest- 4 - en -3- one-l2a-h y drox y lase( 그립 12 의 V-\ 'lI)는 전체 담줍산 합성을 위한 속도제한효소로서의 여할이 있다고 보기보다는 간에 의해서 담줍 내로 담즙산 선행물질의 분비량을 결정하는 데 주요 역할이 있다고 본다. 119),120) 그러 나 담즙 내 의 cholic acid 와 chenodeoxy c holic acid 의 함량마 례 는 어 떤 기 전에 의 해 서 유지되 는지 는 아직 모른다. 7a-hy d roxy c - holes t -4-en-3-one(V) 만이 오로지 12a-hy d roxy la se 의 기 질이 아니 다. Bjo r khem 과 Gus t a f sson113) 은 5p -c holcsta n e-3a, 7a-dio l nD 도 12a-hy d roxy la ti on 이 될 수 있 어 서 5(3 - cholesta n e-3a, 7a, 12a-tr i o l (멘)을 생산할 수 있다고 지적하였다. 그래서 결국 cholic ac i d 로 전환된다고 하였 다. 26-hy d roxy la ti on 이 이 루어 지 면 Ri ng sy s te m 의 hy d roxy a ti on 은 더 이 상 일어 나지 않는다고 하였 다. 아마도 12- 나 26-hy d roxy la ti on 의 비 율아 cholic ac id 와 chenode- oxy c holic acid 의 비 율을 결정 하게 되 는 것 으로 본다. mic r osomal IW-hy d rox~Jf \~ e act i vi t v mic r osomal 26u-hy d roxy la se acti v it y 의 울이 in v it ro 에서 결정되면 in v i vo 에서 담즙산 구성을 비교적 정확히 예견할 수 있다고 본다 .12 1) 이 처자들은 또한 쥐를 사용하여서 실험한 결과 갑상선 호르몬이 mi toc hondria 내 의 26-hy d roxy la se 활성 에 부차적 으로 영 향이 있 음 을 발표하였다. 그러므로 갑상선 호르몬이 담즙산합성에 관련이 있 다고 생각한다. 또한 mi cr osome 내 의 12a-hy d roxy la se 는 다른 종류의 담즙산울 두여 함으로써 나타나는 반응이 다르다고 하였 다. 이 론적 인 배 경 으로 본다면 cholic aci d 도 이 효소의 활성 을 방해 한다고 생 각할 수 있 으며 chenodeoxy c holi c ac id 도 자극한다고 생 각할 수 있 다. 그러 나
12a-hy d roxy la se 는 쥐 에 게 tau rocholate 나 또는 tau rochenodeox- y chola t e 을 먹였을 때 작은 범위내이긴 하지만 이 효소의 작용을 방해 한다고 하였 다• 116) 이 로 미 루어 보면 이 효소가 ?a-hy d roxy - cholest- 4 - en ·3-one 에 작용하면서 담줍산 po ol 내 의 구성 성 분 조철에 주요 역할이 있는지에 대해서는 분명치가 않다고 본다. 6 콜레 스테 롤 este r 형 성 (1) 콜레 스데를 este r 콜레 스데몰 es t er 는 신체내에서 두 가지 경로에 의해서 합성된다. 첫 째 는 신체 모든 조직 내 에 서 콜레 스테 롤 este r sy n th e ta s e 에 의 한 경로이다. 이 효소에 의한 경로로 에스텔화가 이루어지려면 두 단계를 거쳐야 된다. 먼처 지방산이 활성화되어서 지방산 acy l- CoA 를 형성해야 한다. 지방산이 활성화되려면 에너지급원으로써 ATP 를 사용한다. 이 과정은 지방산 활성효소(fatty aci d acti va ti ng enz y me) 에 의해서 중재된다. 활성화된 지방산, acy l- CoA th io e ste r 는 콜레 스테 롤과 작용하며 이 작용은 acy l- CoA choleste r ol acy l tra nsfe r ase (ACAT) 에 의해서 이루어진다 . acy l- CoA + 콜레 스데 몰 A―C一AT 콜레 스테 몰 -es t er + CoASH 이 과정이 주로 이루어지는 신체내 부위는 간, 소장, 부신피잘 이다. 두번째 콜레스데몰 es t er 합성경로는 혈청내에서 이루어지며 이는 효소 lecit hi n - choleste r ol acy lt r a nsfe r ase (LCAT) 에 의 해 서 중재 되 어 진다. 이 작용은 pb osp h ati dy lc holin e (l e cit h i n) 의 두번째 탄소 에 결합된 지방산이 칙접 콜레스테롤로 이전되는 것이다. 이 작용 은 지방산이나 또는 acy l- CoA 중간체를 거치지 않고 직접 콜레스 테롤로 이전된다.
(ph ospLh ea ctii dt hy il nc h +ol i콜 ne레 ) 스테 몰 L_C_A+ T 콜레 스데 (몰!y ―so eps h to ers p+ ha !tyi dso y ll ec ch iotlhii nn e ) 대부분의 혈청콜레스테롤 es t er 는 이 경로에 의해서 합성된다. 콜 레스데롤은 간에서 유리형태의 콜레스데를로 유리되며 이는 혈장내 에 서 lipo p ro te i n 의 구성 성 분으로서 촌재 한다. 그러 나 혈청 내 에 서 lip o pr ote i n 구성 성 분이 된 유리 콜레 스테 롤은 LCAT 에 의 해 서 절 과 적으로 에스텔화된다. (2) lecit hi n - choleste r ol acy ltra nsfe r ase (LCAT) 이 효소는 간에서 생성되며 혈장내로 분비되어서 혈장내에서 작 용한다. ap o li po p r ote i n C-I 은 이 효소 LCAT 를 활성 화시 킨다. LCAT 는 HDL 을 기 질로 하여 작용하며 특히 nascent HDL 은 더 욱더 호의 적으로 작용한다. 그 이 유는 nascent HDL 내 에 는 소량
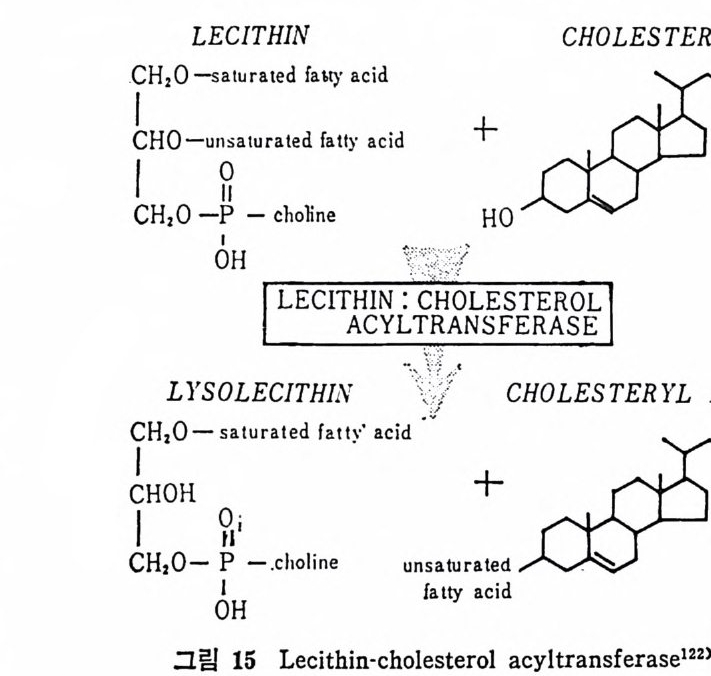 LECITHIN CHOLESTEROL
LECITHIN CHOLESTEROL
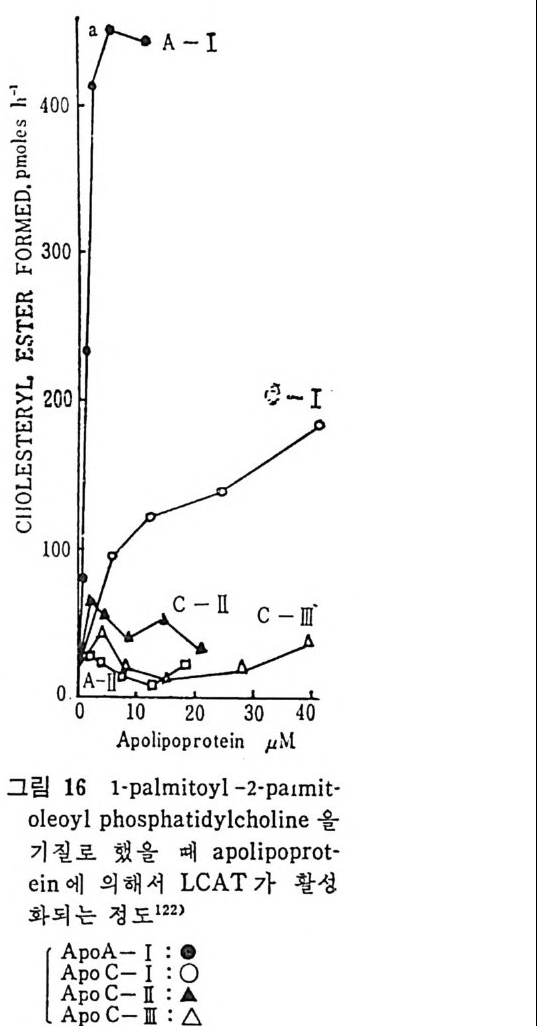 A-I
A-I
의 lecit hi n 이 함유되 어 있 으며 , 이 lecit hi n 은 LCAT 를 HDL 에 쉽 게 결 합되도 록 조장한다. Ap o C -I 이 LCAT 작용을 자국시 키는 것은 어떤 종류의 인지방울 기 질로 삼느냐에 따라서 달라진다. 다음 의 그 립 은 LCAT 의 활성 lip o pr o te i n 의 활성 을 그래프로 나타낸 것이다 ( 그 립 15- 7 참조 ). 콜 레 스테 롤 의 에 스텔 호H 근 콜레 스테 롤 이 lip o p ro te i n 내 에 결 합된 상태 로 혈 액내에 머무르게 하는 데 목적 이 있 다. 죽 콜 레스테 몰 이 lip o pr o te i n 내에 머무르게 되면 콜 레스테롤이 신 체내 다론 조 직 으로 이동되어 가는것 울 방 지 하는 결과가 된다. LCAT 의 활 성은 혈청내의 중 성지방이 증가될 대 최 고의 활성윤 보이며 123 - 4) 또한 실험식이로부터 지방울 재거하면 아 효소의 활성이 없어진다 .123) 이에 부 과해 서 혈청 내 chy lo mi cr on 과 VLDL 의 양이 증가되 면 지 방사육으로 인해 서 HDL 의 함유량도 변화된다. 지방식을 섭취한 후 12 시간 이후 까지도 HDL 과 안지방의 양이 증가
하는 데 비해서 콜레스테롤과 단백질은 증가하긴 하지만 HDL 이나 인지방만큼 지속적으로 증가되지는 않는다고 하였다 .125) 그런데 LCAT 의 활성은 지방석을 섭취한 후에 혈청내에 식이성지방혈증 (ali m enta r y lipe mi a) 이 거 의 사라질 무렵 에 나 비 로소 이 효소의 활성 이 증가됨 을 관찰하였 다. 126) 이 러 한 현상온 혈청 내 에 HDL2 와 HDL3 의 큰 변화와 관련이 있음을 지적한다. HDL 을 ultra centr ifuga l fra-
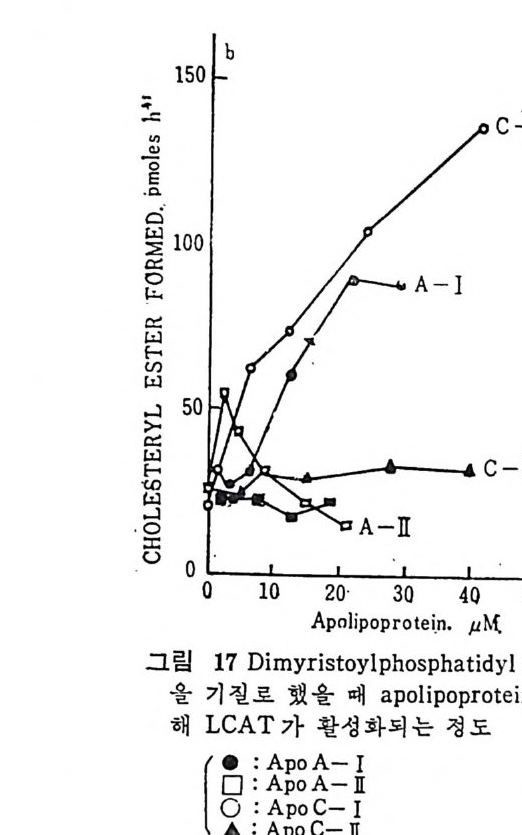 b
b
cti on ati on 을 하여 서 HDL2, HDL3 와 VHD 로 분리해 서 LCAT 활성과 관련시켜 보았다. 지방식을 섭취하면 HDL2 의 단백질과 인지방은 견 과적으로 증가되었으며 인 지 방 중 ph usp h ati dy lc h· olin e 이 강화되 는 것 으로 나타났다. 그런데 LCAT 효소의 주요기질이 함유되 어 있는 HDL3 의 중성지방 함량은 증가되며 콜레스데 몰 este r 의 함량은 감소되 었다. 그러나 이 두 물질 의 변화는 LCAT 의 활성 과 관련시켜서 관찰해 보 면 콜레스테롤 es t er 의 함 량은 부분적으로 중성지방 함량과 관련이 있음이 나
타났으며 LCAT 활성과는 오히려 관련이 적은 것으로 나타났다. 죽 콜레 스테 몰 este r 는 LCAT 반응에 역 으로 반응을 보이 고 있 음운 관 찰하였다. 그러나 각각의 지방구성성분과 LCAT 효소의 반응 사 이에는 부분적으로 상호관련이 되어 있음을 미루어볼 때 어떤 한 종류의 지방 성분도 이 효소작용의 조철원인으로 볼 수는 없다고 생각한다. F i eld ing등에 의 해 서 보고된 바에 의 하면 lec ithi n : 유리 콜레 스 테롤의 확산작용에 있어서 콜레스데를 es t er 를 첨가하였을 때 강하 게 방해작용이 일어나는 것으로 미루어보면 es t er 에 대한 이 효소 의 반응은 민감한 것으로 볼 수 있다 .127) 이렇게 효소의 작용이 콜 레스테를 es t er 에 의해서 방해되어 있는 상태에서 콜레스테롤 este r
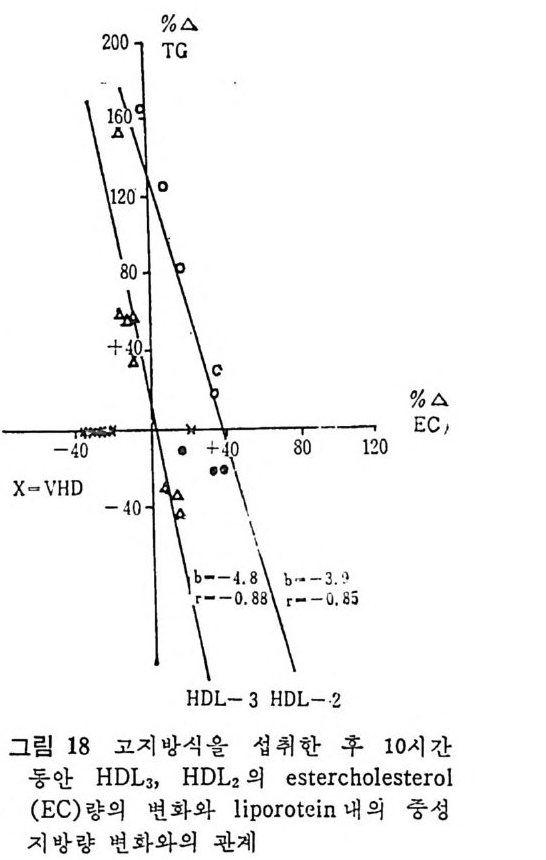 %A
%A
를 제거해 주면 다시 LCAT 의 활성이 회복됨을 관찰할 수 있다. 이 현상은 콜레스데 몰 este r 가 LCAT 활성 의 방해인자라는 가능성을 재시 해 준다. 그러나 이 가능성 은 LCAT 와의 상관관계 가만일에 HDL3 의 중성지방량이 일정하게 유지되면 결과적으로없어진다는사실때문에 지지를 못 받고 있다. 그립 18 에서 보여주듯이 HDL3 내의 콜 레스데를 es t er 의 함 유량은 중성지방함유량과 역 의 관계에 있기 때문이다. In v i vo 연구에서 보면 지 방혈중(Iip em i a) 때 VHD 내 의 콜레스테폴의 양은 감소되나 중성지방의 양온 측정할 수가 없었다. 홍미롭게도 VHD 내 의 lys o lec ithi n 의 양도 감
소되 었 다. 126) 이 결과는 in vit ro 배 양 연구에 서 개 의 chy lo mi cr on 의 인지 방이 HDL 로 빼 앗기 고 있 음이 나타났으며 또한 chy lo mi cr on 내 에 lys olec ithi n 양이 증가하고 있음을 관찰한 결과와 관련이 있 다고 본다. 129) 여 하튼 lys olecit hi n 은 LCAT 의 유용한 처 해 제 (inh ib i t or ) 로써 127) 주목되 고 있 다. 이 상의 결과를 종합해 보면 VHD 와 HDL3 구성 성분내 에 LCAT 의 가장 활발한 기질이 함유되어 있는 이상에는 VHD 와 HDL3 가 콜레스테를 es t er 를 VLDL 과 LDL 로 이전시키는 데에 관련이 있다 고 보며 이전기전은 효소에 의해서 되는 것이 아니고 괴차의 교환 에 의해서 이루어진다고 본다. 그러므로 es t er 의 이전에 가장 결정
적인 요인은 VLDL 의 수준이라고 생각된다. (3) 혈 장내 콜레 스테 롤 este r 혈장내의 콜레스테롤 es t er 는 l ip o p ro t e i n 내에 함유되어 있으며 이 는 lip o p r ote i n 의 비 중이 높아질수록 문레 스터나t este r 함량이 높 o} 전다. 다음의 표 3 은 정상 성인남자의 공복시의 총 콜레스테 몰 함량이 176 mg / 100ml 일 때 의 콜레 스테 롤의 lip o p r ote i n 내 의 분포상대 와 콜 레스테롤 es t er 의 분포상태를 나타낸 것이다. 사람에게서 혈청내의 총 콜레스테롤의 2 / 3(6 4 ~72% )가 에스텔화 된 콜레스테롤로 촌재하는 것이 보통의 예이다. 그리고 앞에서 지 적 했듯이 lip o p r ote i n 의 비 중이 높을수록 콜레 스테 롤 este r 의 함량 도 높아진다. 그런데 쥐에 있어서는 사람과 비교해 볼 때 콜레스테롤의 함량은 · 낮지만 상당히 동백경화현상에 저항적이다. 쥐에게서는 콜레스데몰 este r 는 주로 HDL 에 과량 함유되 어 있 다. 다음 표 4 는 콜레스테롤 es t er 의 지방산구성성분의 분포이다. 사 람의 경 우 VLDL, LDL, HDL 을 막론하고 지 방산 18 : 2 가 가장 많
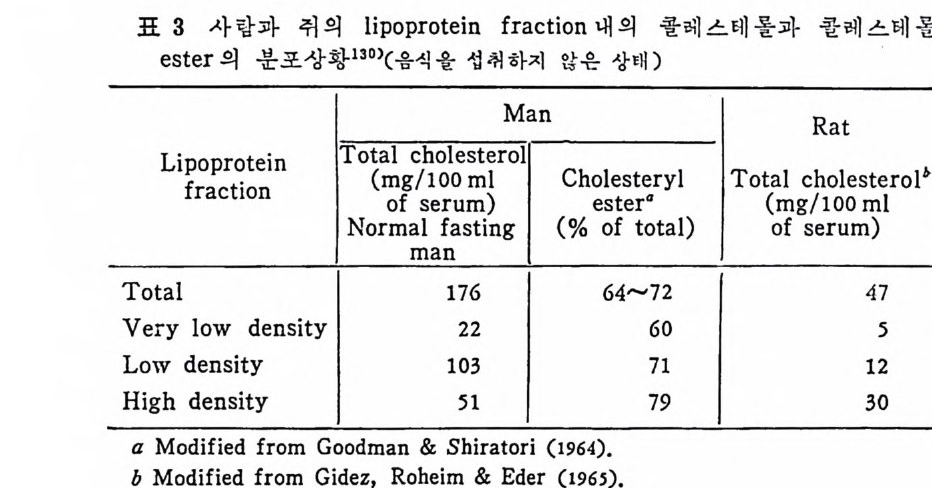 표 3 사 람과 취 의 lipo p ro te i n frac ti on 내 의 콜 레 스데 몽과 콜레 스테 몰
표 3 사 람과 취 의 lipo p ro te i n frac ti on 내 의 콜 레 스데 몽과 콜레 스테 몰
이 함유되어 있다. 그런데 사람의 간내에는 지방산 1s:1 이 비교적 과량함유되어 있다. 그런데 쥐의 경우 지방산 20:4 가 많이 함유되어 있으며, 지방산 18:2 는 HDL 과 LDL 에 비교적 높은 양 함유되어 있다. 그러나 쥐의 간내에는 지방산 1s:1 아 다량 함유되어 있으며 주로 VLDL 내에 함유되어 있다. 쥐의 간내에서는 콜레스테롤 acy l- CoA acy ltra nsfe r ase 에 의 해 서 콜레 스데 몰 este r 가 형 성 되 어 서 직 접 VLDL 형태로써 간세포 밖으로 이동되어 순환계로 들어간다. 그러 나 혈장 내 의 콜레 스데 몰 este r 는 chy lo mi cr on 을 제 의 하고는 lip o p ro t ei n 에 존재 하는 것 은 모두 LCAT 작용에 의 해 서 형 성 된 것 이다. 쥐에게 고콜레스테롤 식이를 섭취시키면 간내의 VLDL 내에 고농도의 1s : 1, W6(oleic a ci d) 가 나타난다.
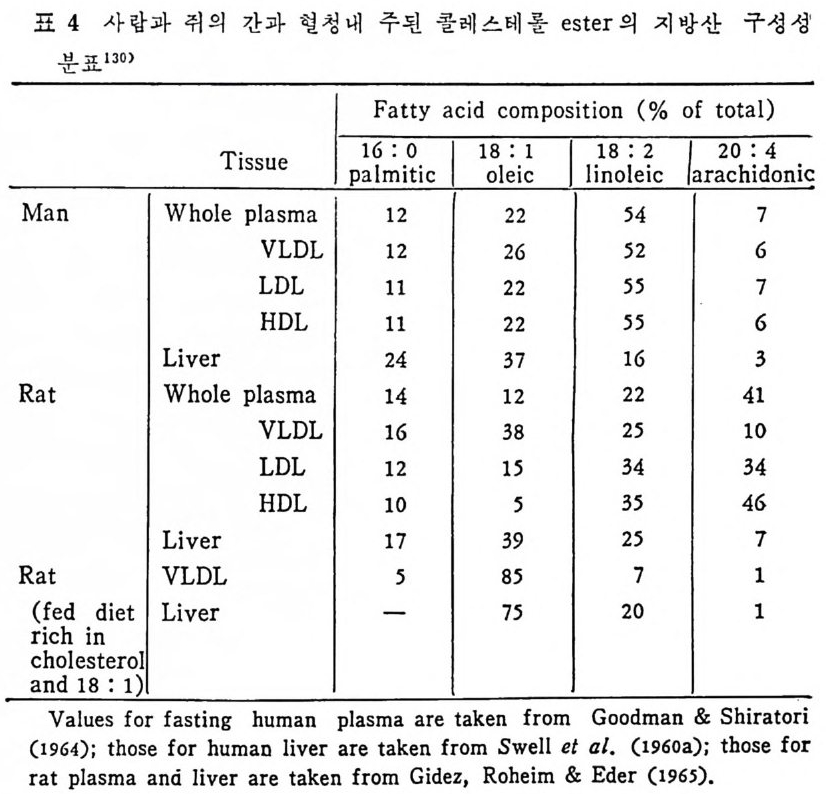 표 4 사람과 쥐의 간과 혈정내 주된 콜레스테몽 es t er 의 지방산 구성상
표 4 사람과 쥐의 간과 혈정내 주된 콜레스테몽 es t er 의 지방산 구성상
* 참고문헌 1) Carlson, L. A. & Bollig e r, L. E. , Lancet ii: 86~8, 197 2. 2) Kannel, W. B. , Caste l li, W. P. , Gordon, T. & McNamara, P. M. , Am. Int. Med. , 74:1~12, 1972. 3) Key , A., Cir cu lati on , 4:Sup pl, 1:1970. 4) Goldste i n , J. L . , Schrolt, H. G. , Hazzard, W. R. , Bie r m a n , E. L. , Motu l skey, A. G. , Comp b ell, E. D. , Levin s ky , M. J. , J. Cl in. Inves t, 52:1544~66, 1973. :;) Connor, W. E. , Hodg es , R. E, , Bleil e r, R. E. , J. Cl in. Invest. , 40:894~901, 1961, '6) Connor, W. E. , Sto n e, D. W. , Hodg es , R. E. , J. Cli n. Inves t . , 43 : 1691~9, 1964. 7) Key s, A. , Anderson, J. T. , Grande, F. , Meta b oli sm , 14:759~65, 1965. 8) Key s, A. , Grande, A. , Lancet ii : 959~66, 1957. 9) Manc ini , M. , Posti gli m & L. di Marin o , Nutr i t ion & Meta b olis m , 21 : 13~25, 1977. 10) Grundy , S. M. , Ahrens, E. H. J. , J. Clin . Invest. , 49 : 1136~52 , 1 970. 11) Lewi s, B. , Pil k in g ton , T. R. E. , Hodd, K. A. , Clin . Sci. , 20 : 249 ~ 54, 1961. 12) Moore, R. B. , Anderson, J. T. , Tay lo r, H. L. , Key , A. , Fran tz , I.D . Jr. , J. Cl in. Invest. , 47:1517~34,1968. 13) Neste l , P. J. , Hasenste i n , N. , Why te, H. M. , Scott , T. J. Cook, L. J. , N. Eng l. ]. Med. , 228: 279~382, 1973. 14) Americ a n Heart Associa t i on Nutr i t ion 's commi ttee :A H , A Comments on Diet a ry Fib e r C. V. D. ep ide m, Newslett er , 21 : 53, 1976. 15) D. W. , Marti n, P. A. , May e s, V. W. , Rodwell, Harpe r 's Revi ew of Bi oc hemi st r y , 10t h ed. p. 533, 1981. 16) Goodman, D. S. & Noble, P. R. , J. Cli n. Invest. , 47: 231~4 1, 1968, 17) Diet s c hy, J. M. , Wi lso n, J. D. , New Eng l, ]. Med. , 282: 1128~38, 1179~83, 1241~9, 1970 .
18) Perts e mlid i s , D. , Kir c hman, E. H. , Ahrens, E. J. Jr. , ]. Cl in. Invest. , 52: 2353~67, 1973. 19) Cook,R.P., Thomp so n, R.O.Q .,]. Exp. Phy si o l., 36:61~74,1951. 20) Tomkin s , G. M. , Chaik o ff , I. L. , ]. Bi ol . Chem. , 196:569~73, 1952. 21) Cook, R. P. , Klim an, A. , Fie s er, C. F. , Arc/t s: Bi oc hem. , 52:439 ~50, 1954. 22) Mancin i , M. , Orie n te , P. , Moro, C. 0. , Key s , A. G. , Arte r io s cl, 4: 247~53, 1966. 23) Ki m , K. S. , Ivy , A. C. , Am. ]. Plt ysi o l . , 171 : 302~18, 1952. 14) Sip e rste i n , M. D. , Chaik o ff , I. L. , Rein h ardt, W. 0. , ]. Bi ol . Chem. , 198:111~4, 1952. 25) Diet s c hy , J. M. , Sip e rste i n , M. D. , J. Lip id. Res. , 8: 93~104, 1967. 26) Bloch, K. , Scie n ce, 150: 19~28, 1965. 27) Frantz , I. D. , Schroep fer , G. J. , Ann. Rev. Bi oc hem. , 36 : 691~726, 1967. 28) Sip e rste i n , M. D. , Guest, M. J. , ]. Cl in. Invest. , 39:642~52, 1960. 29) Diet s c hy , S. J. , Wi ls on, J. D. , J. Cl in. I nvest. , 47: 166~81, 1968. 30) Sip e rste i n , M. D. , Curr. Top Cell Reg u l. , 2:65, 1970. 31) McNamara, D. J. , Rodwell, V. W. , In Bi oc hemi ca l Reg u lato ry Mee: hani sm s in Eukaryo t i c cells, (E. Kun & S, Gris o li a ed. ) p. 205, Wi ley , New York, 1972. 32) Rodwell, V. W, , In Current Trends in the Bi oc hemi st r y of Lip ids, (R. M. S. Smellie ed. ) p. 295, Academi c Press, New York, 1973. 33) Bortz , W. M, , Meta b . Cl in, Exp . , 22: 507, 1973. 34) Damp se y , M. E. , Ann. Rev. Bi oc hem. , 43:967, 1974. 35) McNamara, D. J. , Lin , G. C. K. , Ahrens, E. H. Jr. , Cir cu lati on , 52: sup pl 2, p. 81, 1975. 36) Bhatl at h i r y , E. P. M. , Sip e rste i n , M. D. , J. Cl in. Invest. , 42: 1613~ 8, 1963. ·37 ) Grundy , S. M. , Ahrens, E. H. Jr. , Danig n on, J; , J. Lip id. Res. , 10:304~15, 1969. ·.38 ) Kudchodkar, B. J. , Horlic k , L. , Sodhi, H. S. , At he rosclerosis , 23 : 239~48, 1976.
39) Brown, M. S. , Dana, S. E. , Goldste i n , J. L. , ]. Bio l . Chem, , 249; 789~96, 1974. 40) Brown, M. S, , Goldste i n , J. L. , Proc. Nat. Acad. Sci. U. S. A. ,. 71 : 788~92, 1974. 41 ) Schoenheim er, R. , Breusch, F. , ]. Bi ol . Chem. , 103 : 439, 1933. 42) Gould, R. G. , Tay lo r, C. B. , Fed. Proc. Fed. Amer. Soc. Exp . Bi o l. , 9;179, 1950. 43) Die t s c hy , J. M. , Brown, M. S. , ]. Lipid. Res. , 15: 508, 1974, 44) Bucher, N. L. , R. , Ouerath , P. , Ly n en F. , Bi oc lt im. Bi op ! tys . Acta , 40:491, 1961. 45) Decker, K. , Barth , C. , Mo/. Cell Bio c lt em . , 2 : 179, 1973. 46) Diet s c hy , J. M. , McGarry, J. D. , ]. Bi ol . Chem. , 249 : 52, 1974. 47) Whit e, L. W. , Rundney , H. , Bi oc hemi st r y , 9:2725, 1970, 48) Sug iya ma, T. , Cli nk enbeard, K. D. , Moss, J. , Lane, M. D. .. Bio c hem. Bio p ! tys. Res. Commun. , 48: 25 5, 1972. 49) Cli nk enbeard, K. D. , Reed, W. D. , Fed. Proc. Amer. Soc. Exp . Bi ol . , 33 : 1426 (abstr . No. 1144), 1974. 50) Beg , E. H. , Gib s on, D. M. , Fed. Proc. Fed. Amer. Soc. Exp. Bi ol . • 32:480A (abstr . No. 1456), 1973, 51) Clin k enbeard, K. D. , Sug iya ma, T. , Moss, J. , Reed, W. D. , Lane M. D. , ]. Bio l . Chem. , 248:2275, 1973. 52) Wi lliam son, D. H. , Bate s , N. W. , Krebs, H. A. , Bi oc hem. ]. , 108: 353, 1968. 53) Gould, R. G. , Swy r y d , E. A. , ]. Lip id Res. , 7 : 698, 1966, 54) Sia k ey , L. L. , C!aig , M. C. , Bey tia, E. , Brie d is , A. , Feldbruegg e , D. H. , Dug a n, R. E. , Qu reshi, A. A. , Subbaray a n, C. , Porte r , J. W. , ]. Bi ol . Chem. , 247:3014, 1972 55) Ro:l w ell, V. W. , Nordstr o m, J. L. , Mi tsc holen, J. J. , Adv. Lip icf Res. , 14:1~74, 1976. 56) Brown, M. S. , Dana, S. E. , Goldste i n , J. L . , Proc. Nat. Acad. Sc i. USA, 10:2162, 1973b. 57) Fog el man, A. M. , Edmond, J. , Seag er , J. , Pop jak , G. , ]. Bi o l. Chem. , 250:2045, 1975,
58) Ni co lay , G. , Shefe r , S. , Salen, G. , Mosbach, E. H. , J. Lipid Res. , 15:94 , 1 974 . 59) Goldfa r b, S. , FEBS Lett . , 24: 153, 1972. 60) Ka n duts c h, A. A. , Saucie r , S. E. , J. Bi ol . Chem. , 240: 22 99, 1969. 61) Ba ck, P. , Ha m p re cht, B. , Ly n en, F. , Arch. Bio ch em. Bi op h y s. , 133 : 11, 1969. 62) Shap iro , D. J. , Ro:l w ell, V. W. , Bi oc hem. Bi op h y s. Re s. Commun. 37:867, 1969. 63) Shefc r , S. , Hause r, S. , Lap a r, V. , Mosbach, E. H. , J. Lip id Res. , 13:571, 1972. 64) Da n ic l s s on , H. , Ste r oid s , 20:63, 1972. 65) Edwards, P. A. , Gould, R. G. , J. Bi o l. Chem. , 247: 1520, 1972. 66) Be rn t tel t , J. , Gaumert, R. , Lowel, M. , Hop pe -Seyl e r's Z Plt ysi o l . Clzem. , 353 : 1454, 1972. 67) Edwards, P. A. , Muroy a, H. , Gould, R. G. , J. Lipid Res. , 13 : 396, 1972. -6S ) Dug a n, R. E. , Slakey, L. L. , Brie d is , A. V. , Forte r , J. W. , Arch. Bi oc lzem. Bi op l zy s. , 152:21, 1972 ,69 ) Hig gins , M. , Kawachi, T. , Rudney , H. , Bi oc hem. Bi op hy s . Res. Commun. , 45: 138, 1971. 70) Edwards, P. A. , Gould, R. G. , J. Bi ol . Chem. , 249: 2891, 1974. 71) Hilk man, P. E. , Horto n , B. J. , Sabin e , J. R. , J. Lip id Res. , 13: 17, 1972. 72) Edwards, P. A. , J. Bi ol . Chem. , 248:2912, 1973. 73) Huber, J. , Guder, W. , Latz i n , S. , Hamp re cht, B. , Hopp e -S e yl e r's Z Plzy si o l. Chem. , 354: 795, 1973a. 74) Lakshmanan, M. R. , Nep o kroeff , C. M. , Ness, G. C. , Dug a n, R, E. , Porte r , J. W. , Bi o chem. Bi op hy s . Res. Commun. , 50 : 704, (1973). 75) Huber, J. , Guder, W. , Mi llier , 0. A. , Latz i n s , Ganser, H. , Ham· pre cht, B. , Hopp e -Seyl e r's Z Plzys i o l. Clzem. , 355:669, 1974. 76) Nep o kroeff , C. M. , Lakshm:1 .n an, M. R. , Ness, G. C. , Dug a n, R. E. , Porte r , J. W. , Arch. Bi oc lzem. Bi op l zy s. , 160 : 387, 1974. 77) Dug a n, R. E. , Ness, G. C. , Lakshmanan, M. R. , Nep o kroff , C. M. ,
Perte r J. W. , Arch. Bi oc hem. Bi op hy s. 161 :499, 1974. 78) Shap iro , D. J. , Rodwell, V. W. , Bi o chemi st r y . 11 : 1042, 1972. 79) Robin s on, G. A, , Butc h er, R. W. , Sut h erland, E. W. , cyc lic AMP ,. . Academi c Press, New York, 1971 . so) Brie k er, L. A. , Levey , G. S. , J. Bi ol . Chem. 247:4914, 1972. 81) Beg , E. H. , Allmann, D. W, , Gi bs on, D. M. , Bi o chem. Bi op l zy s. Res. Commun. 54:1362, 1973. 82) Raskin , P. , McGarry, J. D. , Foste r , D. W. , J. Bi o l. Chem. 249: 6029, 1974. 83) Brown, M. S. , Brunschede, G. Y. , Goldste i n , J. L. , J. Bi ol . Chem 250 : 2502, 1975. 84) Shap iro , D. J. , Nordstr o m J. L. , Mi tch elen, J. J. , Rodwell, V. W. , Schim ke, R. J. , Bi o chim . Bi op lz y s. Acta . 370 : 369, 1974. 85) Og ilv ie , J. W. , Kap la n, B. H. , J. Bi o l. Chem. 241:4722, 1966. 86) McNamara, D. J. , Qu ackenbush, F. W. , Rodwell, V. W. , J. Bi o l. Chem. 247 : 5805, 1972. 87) McNamara, D. J. , Rodwell, V. W. , Arch. Bi o chem. Bi op h y s, 168: 378, 1975. 88) Bog u slawski, W. , Wrobel, J.·, N atu re, (London) 247:210, 1974. 89) Sip e rste i n , M. D. , H. H. Hernandez, I. L. , Chaik o ff , Am. J. Phy si o l. 171 : 297, 1952; 90) Sip e rste i n , M. D. , . F. M. , Harold, I. L. , Chaik o ff , W. G. , Danben,. J. Bio l . Chem. 210:181, 1954. 91) W ilso n, J. D. , J. Lt'pids Res, 5:509, 1964. 92) Hof m ann A. F. , B. Borgs t r o m, J. Clin , Invest. 43 : 247, 1964. 93) Sip e lste i n M. D. , I. L. Chaik o ff , W. 0. Rein h ardt, J. Bi o l, Chem,. 198:111:1952. 94) Die t s c hy , J. M. , ·Fe d; Proc. 26:1589, 1967. 95) Bergs t r o m, S. , H. , Danie l sson, Acta . Phy si o l . Scand. 43 : 1, 1958. 96) May a nt, N. B. , H. A. , Eder, J. Lip id Res. 2:363, 1961. 97) Die t s c hy , J. M. , M. D. , Sip e rste i n , J. Clin , Invest. 44: 1311, 1965~ 98) Ell iott , W. H. , Hy d e, P. M. , Am. J. Med. 5 : 568, 1971. 99) Boy d , G. S. , Percy -R obb, I. W. , Am. J. Med. 51 : 580, 1971.
100) Danie l sson, H. , Mechanis m s of bil e acid bio s yn th esis , edit ed by P. P. Narr & D. Krit ch evsky : The bil e aci ds : Chemi st r y Phy si o l ogy , & Meta b oli sm # vol II , New York, Plenum Press, 1973, pp. 1~32, 305~6. 101) Bjo r khem, I. , Danie l sson, H. , Mot. Cell. Bi oc hem. , 4: 79, 1974. 102) Ing e mar, Bj or khem, Henry, Danie l sson, Bi os .vn th esis & Meta b oli sm . of Bi le acid s in man Prog r ess in Li v er Di se ase, p. 216. 103) Shefe r , S. , Hauser, S. , Bekersky , I. , Mosbach, E. H. , ]. Lipid Res. , 10 : 646~55, 1969. 104) Mosbach, E. H. , G. , Salen, Di ge sti ve dis e ase, Vol. 19, No. 10:920 ~9, 1974. 105) Sta p le , E. , Mechanis m of cleavag e of th e cholesta ne sid e chain : in bil e acid for mati on , a in Bi le salt s meta b oli sm , I. Schif f. , J. B. Corey , J. M . Die t s c hy (eds) spr i n g fiel d Charles C. Thomas, 1969, pp.1 27~39. 106) Tanig u chis , Hoshit a, N. Okuda, K. Eur. ]. Bi oc hem. , 40:607~ 17, 1973. 107) Cronholm, T. , Joh anson, G. , Eur. ]. Bi oc hem. , 16:373~81, 1970. 108) Shefe r , S. , Hauser, S. , Bekersky , I. , Mosbach, E. H. , ]. Lip id Res. , 11:404~11, 1970. 109) Mosbach, E. H. , Roth schie l d, M. A. , Berkersky , I. Oratz , M. • Mong e ll i, J. , ]. Cl in. Invest. , 50: 1720~30, 1971. 110) Ein arsson, K. , Hellstr o m, K. , Kallner, M. , Meta b olis m , 22: 1477~ 83, 1973. 111) Shefe r, S. , Hauser, S. , Lap ar , V. , Mosbach, E. H. , ]. Lip id Res. , 14:400~5, 1973. 112) Shefe r , S. , Hauser, S. , Lap ar , V. , Mosbach, E. H. , ]. Lip id Res. , 14:573~80, 1973. 113) Bjo rkhem, I. , Gusta f s s on, J. , Eur. ]. Bi oc hem. , 36 : 201~12, 1973. 114) Mi tro p ou los, K. A. , Balasubramania n , S. , May a nt, N. B. , Bi oc h im. Bi op h y s. Acta , 326:428~38, 1973. 115) Raic h t, R. F. , Cohen, B. I. , Shefe r, S. , Mosbach, E. H. , Bi oc lzim . Bi op lzy s. Acta , 1974.
116) Danie l sson, H. , Ste r oid s, 22: 667~75, 1973, 117) Raic h t, R. F. , Cohen, B. I. , Shefe r , S. , Mosbach, E. H. , Fed. Proc. , 33 : 689, 1974. (abstr a ct) 118) Danie l sson, H. , Ste r oid s, 22: 567~79, 1973. 119) Ein a rsson, K. , Eur. J. Bi oc lzem. , 15: 101~8, 1968. 120) Joh ansson, G. , Eur. J. Bi oc lzem. , 17: 292~5, 1970. 121) Bjo r khem, I. , Danie l sson, H. , Gusta fs s on, J. , FEES Lett . , 31: 20~2, 1973. 122) Souta r , et al, Bi oc lzem. , 14: 3057, 1975. 123) Rose, H. G. , J. Jul i an o, J. Lab. Clin . Me d. , 89: 524 ~ 32, 1977. 124) Wail en ti n, L. , 0. Vi kr ot, J. Cl i11. Lab. Inve st . , 36:4 7 3~9, 1976. 125) Havel, R. J. , J. Clin . Invest. , 36 : 848~54, 1957. 126) Rose, H. G. , J. Jul i an o, J. Lipid Res. , 20: 3 99~407, 1979. 127) Fie l din g , C. J. , V. G. Shore, P. E. Fie l din g , Bi oc him . Bi op h y s, Acta , 270:513-8, 1972. 128) Rose, H. G. , J. , Jul ia n o, J. Lipid Res. , 20 : 399, 1979. 129) Mi na ri, 0. , D. B. Zil v ersmi t, J. Lip id Res. , 4:424~36, 1963. 130) My aa nt, N. B. , The tra nsp or t and tu rnover of the pla sma c/z o leste ro' in pl asma lip op r ote i n edit ed by R. M. S. Smell ie, Academi c Press, New York, 1971.
제 5 장 혈 장 Lip o pr o te i n 1 역사적 고찰 1929 년에 Macheboeu f 1-2) 가 말의 혈청에서 처음으로 단백질과 결 합되어 있는 지방이 함유되었음울 기술하였다. 이 물질은 그 당시
종류의 lip o p ro te i n 의 분리 가 시 도되 었 다. 7> 1967 년에 Fredric k son 과 그의 동료에 의 해 서 혈장 lip o p ro te i n 의 구조적 그리 고 생 리 적 지 식에 대한 분명하고 알기 쉬운 조사결과가 발표되었으며 또한 다 섯 가지 형 태 에 따라서 분류되 는 hy pe rlip o p ro te i n e mi a 의 정 의 를 내리는 방법이 제시되었다 .8) 혈장 lipo p r ote i n 의 형 대 학적 인 (ph enoty pe ) 분류법 은 WHO 에 의 해서 준비된 여러 형태 정의법에 따라 온 세계가 널리 사용하고 있 다. 9) 그러나 최근에 와서는 형태학적인 분류가 반드시 유전적인 형대 (g ene· typ e) 를 나타내 주는 것은 아니라고 본다. Goldste i n 과 그의 동료들에 의 해 서 유전적 인 형 태 의 주류문 이 루 논 3 가지 형태가 기술되었다. 하나는 유전되어 내려온 가족력이 있 논 고콜레 스데 몰혈증 (b yp ercholes t erolem i a), 고중성 지 방혈증 (h yp er t r ig l yc erid e mi a) 그리 고 적 당히 복합된 고지 방혈증 (h yp erl ipi dem i a) 으로 분 리하였다. 그러나 이 연구에서 한 가지 l ip o p ro t e i n 형태에 의해서 유 전적인 장애가 기술되어진 것은 없다 .10-2) 최근에는 독정한 lip o p ro t e in의 결핍증 환자물 중심으로 이에 대 한 유전적인 영향 및 순환계 계통의 질병과의 관계문 방대하게 다 루고 있는 고찰문헌이 많이 있다 .13-24) 2 혈 장 lip o pr o te i n 의 분류 혈장 lip o p r ote i n 의 분류와 명 명 법 (no in encla t ure) 는 전동기 의 전 동운동에 기 초를 두거 나 또는 영 (sal t)용액 내 에 서 ultr a centr i f uga l fl o t a ti on 울에 의해서 정의한다. 이러한 척도에 기초를 두고서 분류 해 보면 정상인의 혈장 lip o p ro t e i n 은 전통적으로 네 가지 죽, chy lo mi cr on, VLDL (very low densit y lipo pr o te i n ) , LDL (low densit y lip op r o te i n ) , HDL (Hi gh densit y H p o p ro t e i n) 으로 분류한다. 이 혈장 lip o p r ote i n 의 분류와 구성 성 분은 다음 표 1 과 같다. 이 상의 네 가지 주요 분류 의 에 도 VHDL(very hig h densit y lipo p·
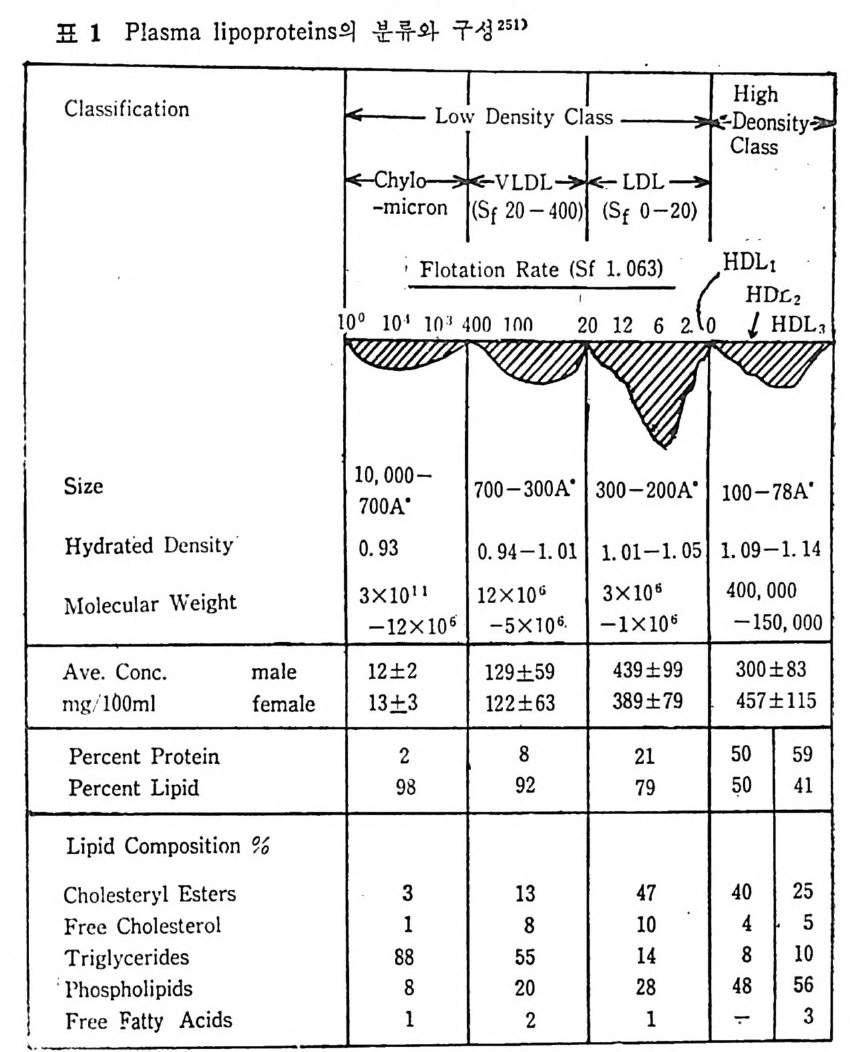 표 1 Plasma lip o p ro t e i n s 의 분류와 구성 251 )
표 1 Plasma lip o p ro t e i n s 의 분류와 구성 251 )
ro t e i n) 이 있으며 이는 densit y g /ml 가 1.210~1.250 사이의 lipo p - rote i 1 1 을 말한다. 이상의 분류를 가지고는 모든 임상적인 조건에서의 분류가 충분치 못하다. 즉 obstr u cti ve live r di se ase type ]I. d y s li po p r ote in e mi a, abeta li po p r ote in e mi a, Tang ier dis e ase, LCAT 결 핍 증세 의 혈장 lipo p r ote i n 은 또 다르다.
개개의 lip o p ro t e i n 종류들은 각각 다른 종류와 양의 단백질을 함 유하고 있 다. 현재 에 는 세 계 적 으로 수궁이 가는 ap o lip o p ro te i n 의 명 명 법 (nomencla t ure) 은 없다. Alanp o vie 과 그의 동료는 개 개 lip o p- rote i n 종류에 따라서 각각의 함유된 단백 질 , 죽 ap o lip o p ro te i n 의 명명법을 제안하였다 .26-8) 즉 Ap o A,B,C 등이 제안되었다. 다른 조사자들은 ap o lip o pr o te i n 의 _COOH 끝의 아미 노산을 사용하여 서 구벌하기 도 한다. 16),29) ScanU 와 그의 동료들은 30> chromato g ra - p h i c 분리에 의해서 frac ti on 1[』 V 와 V 로 구별하기도 하며 또 다 른 사람들은 ap o lip o pr o te i n 을 gly c ine -ric h ap o p ro te i n 또는 hig h ly po lar pro te i n 으로 분류하기 도 한다. 31 ) 또한 ap o pr o te i n D 와 ap o pr o te i n E 에 대 한 상호의 이 견 때 문에 이 들은 대 때 로 th in - li ne 단백 질 또는 argi ni n e -ric h 단백 질 로 사용되 기도 한다. 26-7) 3 Lip o p ro te i n 의 구성 성 분 (1) Chy lo mi cr on 혈장내 에 서 대 부분의 중성 지 방은 chy lo mi cr on 에 의 해 서 이 동된 다 .32-3) 섭취된 중성지방은 십이지장에서 다시 유리지방산과 2-M G 로 가수분해된다. 그리고 흡수된 후에 장내벽에서 중성지방으로 합 성 되 며 또한 chy lo mi cr on 으로 영 합된다. 지 방산 가운데 에 서 탄 소의 수가 10 개 내지 20 개 이하의 것은 직접 문맥정맥으로 흡수된 다. Chy lo mi cr on 도 림 프계 통 체 계 에 의 해 서 th oracic duct 로 이 동 된다. 그래서 거기서 신체전체 순환계통으로 영합된다. 림프로부터 유리된 ch ylom i cron 은 순환되는 혈액내에서 유리된 것보다 단백질 함량은 적 고 인지 방함량은 높다. 34) 림 프에 나타나는 chy lo mi cr on 의 크기는 다양해서 지름이 300~5000A 이다. 이들의 대부분은 주로 중성 지방울 함유하고 있으며 중성지 방함유량은 chy lo mi cr on 의 크 기에 달려 있다. chy lo mi cro n 도 무게로 계산해서 약. 8% 의 인지
방과 5 % 의 콜레 스테 롤을 함유하고 있 다. ph osp h ati dy lc holin e 과 sp h in g o my e lin 이 주요 인지방의 구성성분이 다. 35) 림 프 chy lo mi cr on 내 의 단백 질함량은 적 고 다양하다. th oracic duct 에 서 유리 한 사람의 림 프 chy lo mi cr on 내 에 도 VLDL 에 함유하 고 있 는 모든 종류의 ap o li po p ro te i n 이 함유되 어 있 다. 36- 7 ) 구성 성분 의 함유량은 ap o p ro te i n C 가 66%, ap o p ro te i n B 가 22%, ap o p r - o t e i nA 가 12% 이다. 그런데 홍미로운 접은 Ap o A-I 과 A p o A- II 가 거 의 동량으로 함유되어 있는데 사람의 혈장내의 HDL 내에도 약 3 : 1 의 비율로 함유되어 있는 접이다 .19) 또 한편 Gl i ckman 과 K i rsch 37) 도 chy lo mi cro n 의 입 자가 크면 클 수록 작은 것에 비해서 Ap o B 의 함량이 커진다고 하였다 .38) 더 나아가서 장내 chy lo mi cr on 을 혈장과 함께 배 양(i ncuba ti on) 시 키 면 Ap o C 는 얻어 지고 ap o lip o p ro te i n B(Ap o B) 는 손실된다고 하 였다. (2) VLDL(very low densit y lip o p r ote i n ) 사람에게서 VLDL 입자도 내자 (endo g enousl y)로 합성된 중성지방 울 이동시키는 주요 운반체이다 .3 5 ) VLDL 입자의 크기는 직경이 280~750 A 이며 이 입자의 크기도 중성지방함유량과 직접적으로 관련이 있다. 그리고 인지방과 단백질함량과 입자의 크기 사이에 는 역의 관련이 있다. VLDL 위 구성성분을 무게로 측정해 보면 단백질이 8~10% 이며 지방이 90~92% 이다 . 3 5 、 지방 중에서 중성지방이 가장 양적으로 많 은 것으로 56% 나 되며 인지방 평균함량은 19~21% 이고콜레스테롤 은 17 %이 냐 VLDL 내 의 este r if ied : uneste r if ied 콜레 스테 롤의 비 울은 거 의 1 : 1 이 다. ph osp h ati dy !ch olin e 과 sp h in g o my e lin 이 가장 많은 인지방이다. VLDL 은 ap o lip o p r ote i n 구성 성 분으로 보면 대 단히 다양한 물질 이 다. 39-4o, sodiu m decy l sulfa te 와 같은 dete r ge nt 가 존재 하면 지 방이 없는 VLDL 로 유리 용해될 수 있다. 그리고 sep h adex G-
100 으로 분별(fr ac ti ona ti on) 시킨다. 분리된 단백질은물리화학적 목 성 으로 보나 면역 학적 목성 으로 보나 LDL 의 주요 ap o lip c p r ote i n 인 Ap o B 와 같다 .4 1) 비중으로 측정해 보면 Ap o B 는 VLDL 총 단 백 질 중에 서 35 %를 접 한다고 한다. 42> Radio i m muno assay 에 의 해 정 량을 해 보면 Ap o B 는 VLDL 총단백 질 중 20~30% 를 점 하고 있 다고 한다. 43-4> sep h adex G - 100 에 의 해 서 분리 해 낸 마지 막 부분 에 argi ni n e ri ch 단백질과 Ap o C 가 함유되어 있다 . 4 0),4 5-6) 고지방혈증의 정도와 연령이 높아질수록 Ap o C 단백질의 비교중 가량은 개 인에 따라서 달라진다. 4o> VLDL 의 입 자크기 가 큘 수록 Ap o C 의 함량이 비교적 많으며 Ap o B 의 함량은 비교적 적다 •39) 면 역 화학적 (im munochemi ca l) 방법 에 의 해 서 분리 해 보면 VLDL 은 Ap o A 도 소량 함유하고 있음이 나타났으며 47) 그 함량은 VLDL 총 단백질 함량 중 1% 이하였다 .48) (3) LDL( low densit y lip o p r ote i n ) 정 상 미 국남자 공복시 의 평 군 LDL 농도는 400mg /1 00ml 이 며 여 자는 340m g /100ml 이다 .35> LDL 은 약 75% 가 지방이며 25% 가 단 백질이다 .35) 이 지방의 구성성분을 무게로 축정해 보면 콜레스테롤 es t er 가 50% 이며 인지방이 30%, unes t e rifi ed 콜레스테롤이 10% 이 며 중성 지 방이 10 %이 다. ph osp h ati dy !ch oli ne 과 sph in g o my e lin 은 전체 인지방함유량 중 각각 65% 와 25% 를 접유한다. LDL 지방중 lino leic acid 가 주요 지 방산이 다. LDL 의 입자는 거의 구형이며 크기도 거의 같은 크기이다. 혈액 내에 촌재하는 LDL 입자의 80% 가 그 직경이 210~250/\ 사이의 것 이 다. 49) 보고되 어 전 LDL 분자량은 2~3. 5 X 106 으로 알려 져 있 다. 50-3) LDL 의 소입 자 (sub fr a cit on) 가 밀도 (dens ity) 1. 019~ I. 063 g /ml 사이 에 서 유리되었다 .53-6) 이들 소입자의 분자량은 각각 다르지만 각각 LDL 입자내에 함유된 단백질의 양온 510,000 으로 일정하다. LDL 에 함유된 주요 ap o p ro te i n 은 Ap o B 이 다. 특정 한 면역 학적 분석 방 법에 의해서 측정해 본 결과 건강한 사람의 혈청내에는 Ap o B 가
90 土 2 4 m g / 100ml 정도 함유되어 있다 .57) Lee 와 Alan p ov i c58 - 60) 에 의 해 서 LDL 내 에 Ap o C 와 Ap o A 가 소량 함유되었음이 보고되었다. Ap o C 는 밀도 1.006~1 .0 19g /m l 사이 의 것 에 서 발견되 며 Ap o A 는 밀도 1. 050~1 . o63g / m l 사이 의 것 에 서 발견되 었 다. 이 에 부과해 서 Kos t ner 6 1) 도 HDL 입 자로서 밀도 가 1.073~1.125g /m l 사이의 것에서 오로지 Ap o B 만이 함유되었 음을 보고하였 다. LDL 은 사람이 아닌 다른 동물, 죽 쥐 , 62- 3) 닭, 64) 돼 지 , 65) 고래 66) 와 유인원 67 - 8) 에 서 유리 되 었 다. (4) HDL (hig h densit y lipo pr o te i n ) HDL 은 lip o pr o te i n 중에 서 입 자의 크기 가 가장 작은 것 으로 이 의 직 경은 90~120A 이다 . 4 9> HDL 구성성분 중 소량 함유된 HDL1 은 밀도 1. 050~1.0 6 0 g / ml 사이에서 유리되었으며 이는전동기상에 서나 면역화학적 독 성에 있어서 HDL2 와 유사하다 . HDL 은 이의 소립자로 다양한 방법에 의해서 분리해서 유리하였 다. 죽 초원십 분리 에 의 해 서 69' ge l elec t ro fo cuss i n g에 의 해 70- J) 분 리 하였 다. 그러 나 사람의 소립 자 각각의 HDL2, HDL3 의 생 리 적 톡 칭 은 아직 모른다. 그러 나 사람의 혈장내 의 HDL2 와 HDL3 의 함유 바울은 여러가지 생리적 그리고 병리적 측정기준으로 많아 이용된 다. 페경직전에 있는 여자는· 남자에 비해서 HDL2 의 혈액내 함량이 3 배 나 높으며 이 는 HDL2 오}- estr o g e n 함량 수준 사이 의 관계 를 나 타내 주고 있 다고 본다. 74-5) 무게로 보면 HDL 의 반이 지방으로 구성되어 있다. 지방 중에서 그 구성성분을 보면 인지방이 42~51% 이며 콜레스데몰이 32% 그 리고 중성지방이 10% 이다.J S) 인지방 중에서 보면 ph osph ati dy lc ho-lin e 이 총 인지 방 중 70~80% 이 며 sph in g o my e lin 이 12~14 % , ph os- ph ati dy ls erin e 과 ph osph ati dy li n o sit ol 은 소량 함유되 어 있 다. lino leic acid 가 콜레 스데 몰 este r 의 주요 지 방산으로 되 어 있 다. HDL 의 단백 질 부위 는 Ap o HDL 의 DEAE-cellulose chromato g - ra p hy 31) 에 의하거나 또는 sep h adex G- 20076) 에 의해서 분리해 보.
면 COOH 끝이 glu ta mi ne 인 두 종류의 단 백 질이 유리 된다. 이 두 종 류의 ap o p ro te i n 을 Ap o A-I 과 Ap o A- 1 1 로 기 술 했 다. Ap o A-I 과 Ap o A-11 의 함량은 HDL 의 소립자 사이에서 각각 다르다. Kostn er 와 그의 동료 4 7) 와 Borcet 와 Alad j em 7 ” 에 의 하면 Ap o A-I 과 Ap o A-11 의 함량비 는 HDL2 에 서 가 HDL3 에 서 보다 크다 고 하였 다. 이 에 부과해 서 HDL 은 소량의 Ap o C 와 thi n - l in e 단백 질과 argi ni n e ric h 단백질도 함유되어 있다. (5) Li po p ro te i n ( a) [L P(a)] LP(a) 는 LDL 과 많은 특칭이 유사하지만 이는 따로 분리해서 LP (a) 로 고려하여야 한다. LP(a) 는 혈장내에서 densit y 1.0 50~I.120 g/ ml 사이에서 유리되며 이의 분자량은 5 X 10 이며 a g arose 전기영 동 (elec t ro p hores i s) 에 서 pr e fi 운동을 나타내 었 다. 78- 9> LDL 과 LP(a) 의 지방구성성분은 유사하지만 이들의 단백질구성은 상당히 다르 다. LP(a) 에서 지방울 제거하면 Ap o B 가 65%, album i n 이 15% 그리고 Ap o LP(a) 라고 불리는 독특한 단백질이 함유되어 있다. 미국 사람에게서 LP(a) 는 평군농도 1 4 m g /100ml 정도로 존재한 다. 이 농도는 나이, 성, 지방농도 또는 십장동백병과도 일률적인 관련이 나타나지 않는다 .so 2> LP(a) 의 기능적 목 칭은 아직 모론다. 그러나 사람 이외의 다른 동물에게서는 분리되었다는 보고가 없다. (6) Lip o p r ote i n X 담관장애 (Bi liar y obs tr uc ti on) 나 LCAT 결 핍 환자에 게 서 비 정 상 lipo - pro te i n 인 LPX 가 나타난다. LP X 는 많은 양의 인지 방과 uneste r i- fied 콜레 스테 물을 함유하고 있 다. 83-5) 그러 나 LCAT 결핍 울 모든 사람의 담관장애와 관련해서 생긴 LP X 의 출현원인으로 볼 수는 없다. 86-9) Se i del 과 그의 동료도 LP X 는 Ap o A 가 결핍되어 있다고 지적 하였다 .90) 이 현상은 이러한 사람이 바정상으로 Ap o A 를 합성한 결과 나타나는 현상으로 이 비정상 lip o p ro t e i n 은 지방과 결합되지
가 않는다고 하였다. 4 A p o lip o p ro t e i n 의 대 사와 기 능 (1) Ap o lip o p r ote i n A I) 물리적 특징 Ap o A-I 과 Ap o A-II 가 HDL 의 주요 단백질 구성요소이다. 이들 A p o p ro t e i n 둘은 면역학적으로 구별되며 이들은 사람의 HDL 로부터 쉽 게 얻 어 진다. 그리 고 여 러 가지 의 chromato g ra p h y 방법 에 의해서 분리된다 .9 1) Ap o A 一 1 은 구조에 있어서 대부분이 나선구조 (hel i cal) 이다 .92} 이 단백 질은 glu ta m i ne 이 COOH 기 끝에 있 으며 NH 피 끝에 는 asp a r tic ac i d 가 있 으며 iso leucin e 은 함유되 어 있 지 않다. Ap o A-I 은 LCAT 의 활성제로 알려쳐 있다 .93' Ap o A-I 과 Ap o A - Il 의 야 미 노산 배 열 (se q uance) 도 알려 졌 다. 94- 8 )
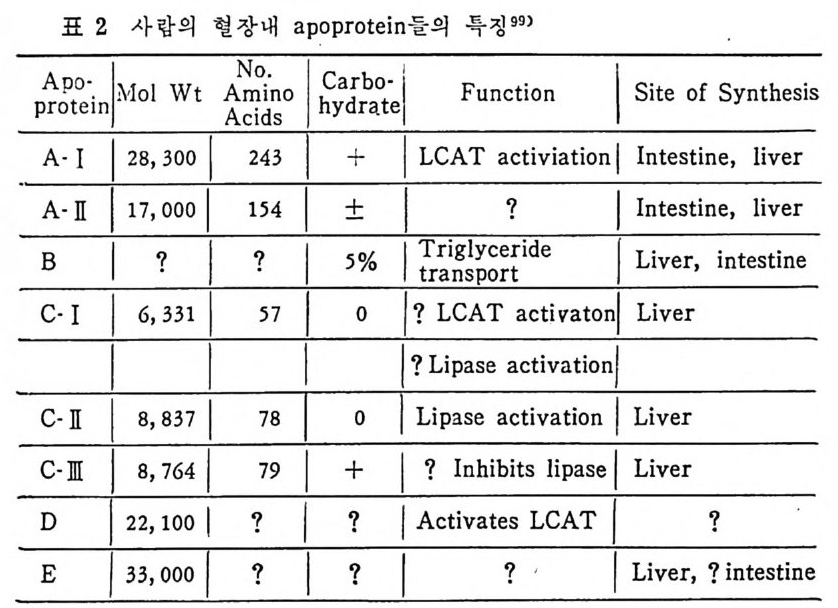 표 2 사 람의 혈 장내 a p o p ro t e i n 들의 목칭 99)
표 2 사 람의 혈 장내 a p o p ro t e i n 들의 목칭 99)
Ap o A-I 은 한 줄기 의 po l!pe p tide chain 으로서 2 4 3 개 의 아미 노산으로 구성되어 있다. 아미노산의 배열에 관해서 Breever 와 그 의 동료 97) 가 보고한 적 이 있 다. 이 보고내 용은 이 보다 앞서 보고한 내용과 비교해 보면 몇 군데의 아미노산의 배열이 다르게 되어 있다. Ap o A-I 은 DEAE 이 온교환 chromato g ra p h y 에 의 해 서 두 가지 다른 형태가 분리가 되나 이들의 아미노산 구성이나 배열로 보} 서 다를 것이 없으며 십지어 면역학적으로 같은 반응을 보이므로 이 두 물질의 차이가 어디에서 기인하는지에 대해서는 아직 모르고 있다. Ap o A-TI (sin g l e p ro t e i n) 는 단순한 단백 질로 분자질 량 (molecular mass) 이 17, ooo dalto n s 이 다. 이 는 하나의 S-S 결합을 환원시 킵 으 로써 2 가닥의 같은 pe p tide 로 분해 되 며 분자질 량이 s, 500 dalto n 이 다 .98),100) 이 p e pti des 는 77 개의 아미노산으로 구성되어 있으며 COOH 끝에 는 glu ta m i ne 이 있 고 NH2 끝에 는 pyrr olid o ne carboxy li c acid 가 있 다. 그리 고 이 두 pep tide s 들은 his t i din e , argi ni n e 그리 고 try ptop h an 이 결핍 되 어 있 다. Ap o A 와 지방과의 사이에서의 상호작용에 대해서 광범위하게 연 구되 어 왔다. 10D Ap o A-I 과 Ap o A-TI 는 ph osph ati dy lc holin e 과 결합되 어 서 단백 질-인지 방 복합체 로 존재 한다. 92) 밀도가 1. 063 ~1.2 lg/ m l 사이에 유리된 HDL 내에는무게로 계산해서 40% 의 단 백질이 함유되어 있는 인지방과의 복합체가 있으며 이 물질은 또한 콜레스데를 es t er 과 영합되어 있다. Ap o A-I 이 지 방과 복합될 때 Ap o A-I 의 2 차 구조 (secondar y s tru c t ure) 가 53% 에서 63% 로 증가된다. 이와 유사한 결과가 Ap o A-I 에서도 나타난다. 이 두 결과에 의하면 지방과 단백질의 상호 작용은 Ap o A 의 2 차 구조를 증가시 킨다고 볼 수 있 다. 102) 요즈음 보고된 바에 의 하면 Ap o A-I 과 Ap o A-TI 두 물질은 용이 하게 자신이 결 합되 어 서 self -as soci at e olig o mer 를 형 성 한다. 그리고 이 자신결합은 이들 단백질의 2 차와 4 차(t er ti ar y str uc tu r e) 구조에 주요한 변화를 초래 한다. 103 구) Ap o A 단백 질의 2 차 구조의 변화로 미 루어 보여 준 결과는 Ap o A
와 지방과의 재결합현상은 단백질과 단백질 상호작용만으로 기인된 다는 것을 암시해 준다. 2) Lip o p r ote i n 내 의 Ap o A Ap o A lip o p ro t e i n 은 혈장내에서 흔히 HDL 밀도의 법위내에서 발견 된다. HDL 질 량의 50% 가 단백 질이 며 30% 는 인지 방이 고 나머 지 20% 가 콜레스테롤이다. Phosph ati dy lc holin e 과 sph in g o my e lin 함량비 가 5 : 1 이 며 este r i- fi ed 와 유 리 콜 레스테롤 함량비가 3 : 1 이다. HDL 내에는 Ap o A 와 Ap o C 가 함께 발견된다. 그러나 Ap o A 가 전체 HDL 단백질의 90 %나 되며 Ap o A- I 과 Ap o A-II 의 무게당 함량비가 약 3 : 1 이 다. 91 ) HDL 은 습관적으로 두 종류의 밀도 (dens ity)로 나눈다. 죽 HDL2 (d:1. 063 ~1. 125 g / ml ) 와 HDL3 (d:1. 125~1. 21 g /ml) 이 다. HDL2 의 분자 질 량은 360 . ooo dalto n s 이 며 이 는 60% 가 단백 질이 고 4 0% 가 지 방이 다. 이 에 비 해서 HDL3 의 분자질량은 175, 000 dalt on s 이 며 약 55% 가 단백질료 되어 있다. Phosph ati dy lc holin e 과 sph in g om y e lin 의 함량비 와 유리 콜레 스테 몰 과 este r if ie d 콜레 스테 를의 비 례 는 HDL2 에 서 가 HDL3 에 서 보다 높 다. 108) 그런데 보고된 Ap o A- I 과 Ap o A-II 의 함량비 를 HDL2 와 HDL3 에서 비교해 보면 이는 대조적인 현상을 나타내는데 어떤 보고서 에 는 HDL2 가 높게 보고되 며 109-12) 다론 보고서 에 는 낮게 113) 그리고 같게 11 4 ) 보고된 것도 있다 . HDL 내에는 서너 개의 다론 단백질이 존재한다고보고되었다. 죽 Ap o A,B,C,D,E 둥이 보고되어 있다 .109 - 16) 이들에 대한 보다 많 은 연구가요구된다. HDL 모델이 화학적, 물리적 그리고 효소로서의 연구가 NMRS (nuclear mag ne ti c resonance s p ec tr osco py)를 사용하여 보고되 어 있 다. 117-119) 이 연 구보고에 의 하면 HDL 은 구상의 mi ce ll 이 며 직 경 이 90~120A 정 도이 고 인지 방의 극성 (po lar) gro up 이 이 mi ce ll 밖울 싸고 있 어 서 수용액 과 상호작용을 하여 , glo bular 단백 질인 Ap o A
ij ����� <�\� �� ��
�. 119) �1����� ��)��� ��i��¤Д���Ȕ��8֑ǩ%��@nj�1�X�� �t���. �\� Apo A- I �� Ap o A- Il ��D� X� ��8֑ǩ�@� HDL X� �Ƙ� �Xl �1�� ��Ҍ��� ����t �ǔ� ɔ�\� ��|�t��" ���xX� � ֥Ǵ���� 8%7 Apo A - I �� 90 %pA o -lA�IH D L �� � ���� p� ��ɷX �pAo A- I �� Apo A- Il � �x� lipoporeti n �� �� � � ����. 112) ����ɷX� Apo A �1���t� �ij 1.21 g /ml ��� �����. �� pAo A-I @�1% ,2 ApoA I-l � �9% � ����p� �������8 � X�t� `��]� t� ��@� �����. ������ ��t��Y<��\� ��� � � �ǔ� i(mumnaosasyable ) Apo A- I t� ���� �� ����� ���� �ǩ� ٳH��� HLD� �0� Ǭ � � � ��� .120) poA A � �� � X�� chylomicron �� � ij ��� �.�c hylomicron l� 1�X� 2% tǴ�� �1���t�p� � ch y lo mcirno �1��� �A p oAI�-� Ao p A- Il �ɷh@� }� 12 %\� t� ��t� thoracci dutc� � ��� � Ǭ� � ��.� 121-2) ̴֭�X� Apo A-I X� ���� �t�� � ����X� ��l����t� � �X�� �� p� t� X�@ �� �\� radio immunoassay ��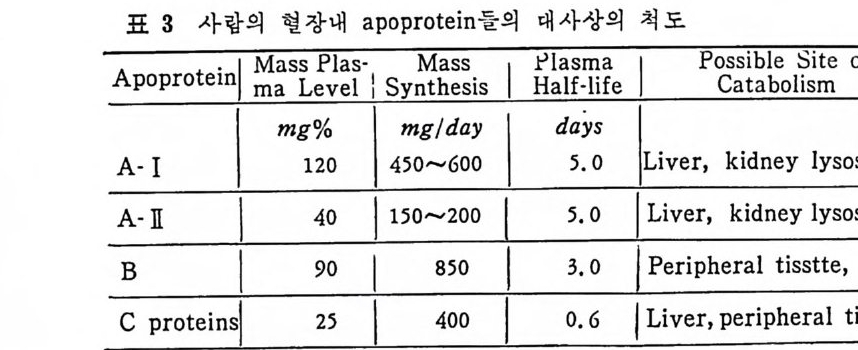 electroimmunoassay )���<�\� �ɷX���. �
electroimmunoassay )���<�\� �ɷX���. �
보고하였 으며 , 124) 또한 다론 보고자들은 거 의 같다고 보고한 사람 도 있 다. 111-2), 120), 123) LCAT 가 결핍된 환자는 Ap o A-I 과 Ap o A-Il 의 혈장내 함 량이 정상인의 30% 밖에 되지 않으며 h yp erch y lom i cronem i a 환자 에게서는 정상인의 25% 밖에 되지 않는다 .112) 또한 가족적인 유전 HDL 결핍환자 (Tan gi er d i sease) 는 Ap o A-I 의 혈장내 수준이 정상 인의 1% 미만이며 Ap o A - Il 는 정상인의 7% 정도로 낮다 •112) 나 25-6) 혈장내 Ap o A- I 과 Ap o A-Il 의 수준은 HDL 내의 콜레스테롤 수준과 상호관련이 있다 .III) 많은 대상자를 상대로 조사해 본 결과 HDL 내 의 콜레 스데 몰함량의 저하로 관상동백 중이 관련되 어 있 다 .127 ― 30) 이 결과는 HDL 이 콜레스데룬의 조직으로부터의 이동에 중요한 역 할이 있 음을 보여 준다. 131 ) 혈장내 콜레 스데 물의 수준은 장거 리 육상선수에 게 서 나, 132 ) 페경 직 전의 여 자에 게 서 , 133i estr o g e n 에 의 해 서 , 134) 또는 nic o ti ni c acid 두 여 에 의 해 서 135) 감소된다. 또한 고중성 지 방혈증 (h yp e rtrig l y cer i dem i a) 환자나 고당식사를 하는 사람에게서도 감소된다 .135),141) 3) 대사 Ap o A 단백질의 합성부위가 어디인지를 알아내는 것이 숙제로 남아 있 다. 쥐 의 pe rfu s ed ;;:&실험 에 서 보면 HDL 이 간으로부터 분 비된다. 그러나 이 HDL 은 혈장의 HDL 과 구성성분이 다르다. 죽 Ap o E 의 함량이 높고 Ap o A-I 의 함량이 대 단히 낮다. 137) 보다 최 근의 쥐 의 간 pe rfu s ed data 에 의 하면 간은 신생 원판상 의 HDL 입자를 분비하는데 이의 구성성분을 보면 Ap o E 와 Ap o A-I 의 함량비 가 10 : 1 인데 비 해 서 혈청 구상의 (sph eric a l) HDL 은 이 비 가 1 : 7 이 다. 138) 이상의 결과를 종합해 보면 간은 Ap o E 가 높고 A.po A-I 이 아주 적은 신생 HDL 을 생성한다고 본다. 이 신생 HDL 은 원판상 이며 LCAT의 작용을 방해하는 특별한 조전하에서 보면 유리콜 레스데풀의 함량이 높다. 그러나 Ap o A-I 이 소장에서 합성이 되며 여기서 합성된 Ap o
A-I 이 HDL 에 나타나는 것으로 보아 소장이 또한 HDL 의 합상 부위가 될 수 있다고 보고하고 있다. 묵벌 히 지방흡수가 일어나게 되 면 소장에 서 도 A po A-I 이 합성 된다. 139-40) 이 러 한 발견 은 이 전 에 보고된 A po A-I 의 주요 급원은 소장이라고 한 보고와 비교 . 된다 .137) 요즈음은 사람의 림 프 chy lo mi cr on 내 의 A po A-I 과 A po A - ll 는 혈장내 HDL A po A-ll 의 전구체 가 될 수 있 다고 본다. 122 ) 또 한편 쥐 의 실험 에 서 보면 소장이 Ap o A- I 함량이 높은 chy lo - m i cron 과 HDL 입자를 생성할 수 있다고 보고되었다 .l41) 이상의 것을 종합해 보면 소장으로부터 유리된 A po A-I 입자가 혈장내로 들어갈 수 있다는 개념은 거의 일정하게 확립되어 가고 있는 것으로 본다. 사람의 HDL 의 a p ol ip o p ro t e i n 대사에 관한 연구가 이루어지고 있 다. 혈장 HDL 의 ap o lip o p ro t e i n 의 반감기는 정상인에게서 3.5~ 5.8 일 135),142 - 4) 로 보고되었다. 이는 HDL 자체의 반감기와 유사하다 고 하였다 .1 43 ) 순수한 단백질을 신체내에 주사로 주입시키면 주입 된 단백질량의 90% 가 HDL 에서 발견된다. 이 결과는 혈장내에서 Ap o HDL 이 쉽게 HDL 과 재결합할 수 있다는 증거를 보여준 것 이 다 .143) 125I 로 동위원소처리된 HDL( l. 09~ 1. 21 g /ml) 을 가지고 정상인에게 서 kin e ti cs 를 연구했으며 특히 HDL 내 에 서 A po A-I 과 A po A - ll 의 특정한 활성에 대해서 정상인에게서 14 일간 연구하였다. 이 연구에 서 도 A po A-I 과 A po A-ll 의 붕괴 (ca t abol i s i s) 윤은 거 의 같은 것으로 나타났다 .135) 그러나 요즈음 HDL 과 결합되어 있는등 위 원소 iod i ne 으로 처 리 된 ap o lip o pr o te i n 의 주사 후에 관찰되 어 진 결과는 rad ioi o d in a te d 된 A po A-I 이 A po A 내 보다 빠르게 붕 괴된다고 보고하였다 .145) 그러나 이 연구자는 동위원소처리된 Ap o A-I 이 HDL 과 재결합된 것이 HDL 내의 동위원소처리된 A po , A-I 보다 빠른 속도로 붕괴 된다고 하였 다. 146) 이 현상의 차이 에 대 한 기전이 규명되어져야 할 것으로 본다. HDL 붕괴 속도는 사구체 영 환자, 142> hy pe rchy lo mi cr onemi a 환자로.
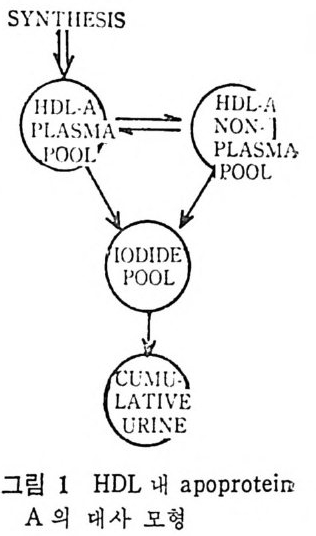 SYN TH E SI S
SYN TH E SI S
서 특히 고중성지 방혈증환자에 서 3) 빠르 다고 보고되어 있다. 도한 고당석사룰 하 는 사람과 1351 Tang ier 환자 147) 에 게 서 도 이 HDL 붕괴 속도가 빠르다고 보고되 어 있 다. HDL 의 붕괴속도가 혈장내 HDL 수준 조 철작용의 주요 역할을 하는 것으로 생각 한다. HDL 내 의 ap o pr o te i n A 의 기 본모형 을 그립 1 에서 보여주고 있다. 그래서 이의 대사 를 알아보기 위해서 SAAM 컵퓨터 프로그램을 이 용하 여서 연 구하였다 .135 ) 이 결과에 의하면 HDL(1. 0 9 ~1. 2l g / ml) 의 단백질합성률은 정상 인 8 인
의 평군치가 s.2om g / k g / 1 일이었다. 이때 이 8 인은 균형된 석사로 모두 같 은 양의 칼로리 를 섭취하였다 .135 ) 그러나 HDL 합성물은 정상인 8 인 중 4 인은 고당식사의 영향을 받 지 않는 것으로 나타났으며, 2 인에게서 nic o ti ni c ac i d 를 주었을 때 약간의 감소가 있었다. HDL 덩어티의 62% 가 혈장부위에 촌재하며 8% 가 다론 부위에 존재한다. HDL 혈장내 입자의 붕괴속도(fr ac ti onal cata b olic rate : FCR) 는 0.113/da y이며 이 속도는 혈장 이의에 존재하는 HDL 입자의 붕괴 속도, 즉 o. 122/day 와 유사하다. 또한 80% 탄수화물 식사를 섭 취하면 혈장내 HDL 입자 붕괴속도가 39.1% 나 증가된다. 그러나 nic o ti ni c a ci d 를 먹이면 붕괴속도가 4 2.2% 나 감소되었다. 혈장내의 HDL 붕괴속도와 혈장 밖의 HDL 붕괴속도는 서로 역의 관계에 있다. 또한 HDL (1. 09~ 1. 21 g / ml) 의 평군 단백질량이 20% 감소되면 콜레스테롤은 32% 나 감소된다고 보고되었다. 이 보고는 고당식사로 HDL 붕괴속도가 증가되었을 때 관찰되어전 것이다 .135) HDL 붕괴에 영향을 미치는 결정적인 인자를 규명하기 위해서는 더 연구되어져야 한다. 그러나 동물실험에서 지적된 바에 의하면 간과 신장조직 의 lys osomes 이 HDL 붕괴 에 주요 역 할울 한다고 하
였다 .148-50) 또한 간조직 이외의 조직이 HDL 붕괴에 지배적인 역할 이 있다고 했 다 .151 - 2) 또 한편 chy lo mi cr on 의 Ap o A 가 HDL Ap o A 의 선행 물질이 라고 보고되 었 다. 1 22 ) 그리 고 또한 Ap o A- I 과 Ap o A-Il 가 HDL 내에서 유사한 울로 붕괴된다고 하였다 .135) 이들에 대 한 보다 많은 연구가 진행되어야 한다. (2) Ap o lip o pr ote i n B 1) 물리적 특성 Ap o lip o p ro te i n B 는 혈장내 ap o lip o pr o te i n 중에 서 특 칭 이 가장 덜 알려 진 것 이 다. 153) 막단백 질과 유사하게 도 ap o lip o p ro te i n B((Ap o B) 는 수용액 중에 고농도의 dete rge nt 가 촌재 하지 않는 한 녹지 않 는다 .154) Lipo p ro te i n 입 자내 에 ap o p ro te i n B 의 분자수는 아직 모르며 또한 Ap o B 의 정확한 분자량에 대해 여러가지 이견이 있으나 보고 되 어 전 것은 10, 000~250, ooo dalto n s 으로 추정 된다. 153> ap op r o te i n B 의 아미 노산 구성 성 분은 다론 ap o lip o p ro te i n 과 유사하다. Ap o B 의 분자량 전체 의 5~6% 가 탄수화물이 며 , mannose, ga lacto s e, fruc to s e, glu cose, glu cosami ne 그리 고 sia l ic acid 를 포함하고 있 다. 153) Ap o B 의 glu cosid e sid e chain 하나의 배 열 이 보고되 어 있 다. 155) 2) Lip o p ro te i n 내 의 Ap o B Ap o 底 분명한 면역학적 특징이 있으며 면역학적 분석(i mmuno .a ssa y)에 의해서 양적으로 분리될 수 있다. 정상인의 혈장내의 Ap o B 의 농도는 70~100m g%로서 주로 LDL 내에 촌재한다 .156-9) Ap o B 는 세 종류의 lipo pr o te i n 죽 chy lo mi cr on, VLDL 과 LDL 에 촌재 하는 단백질의 구성성분으로 나타난다(표 4 참조). 혈장내 에 Ap o B 가 결 핍 된 A-Beta lipo pr o te i n e mi a 환자에 게 서 는 위 의 어 느 종류의 lipo p ro te i n 내 에 도 Ap o B 가 존재 하지 않는다. 160) 림 프, chy lo mi cr on, 혈장내 VLDL 과 LDL 내 에 함유되 어 있 는 단
표 4 Lip o p ro te i n 내 의 A pop ro t e i n 의 양 99) C%hy olof m ti oct ra o l n so•f lipoVp L rDo Lte 6i .n prLo Dtc L:bn I HDLb Ap op ro tc i n A· I 7. 4 Trac e 67 A· II 4.2 Trace 22 B 22. 5 36.9 98 Trace C·I 15 3.3 Trace 1-3 c-n 15 6.7 Trace 1 一 3 C-lll 36 39.9 Trace 3-3 D + E 13. 0 Trace + Tota l 100 100 100 100 a Ly m p h, b Plasma
백질내의 Ap o B 의 평군함량은 20%, 40% 그리고 98% 가 함유되 어 있다. Ap o B 와 용해성단백질 (A p o C 와 Ap o E) 사이의 질량비는 입자 의 s f울이 감소될수록 161) 또한 입자의 직경이 감소된 162) VLDL 입 자내에서 증가된다 . 3) Ap o B 의 대사 쥐의 실험견과에서 보여준 바에 의하면 Ap o B 는 간과 소장에서 합성 되 어 서 chy lo mi cr on 과 VLDL 에 영 합되 어 서 혈류내 로 들어 간 다 .137-8),163 - 4) 이 결과는 사람에게서도 같다고 본다. Ap o B 도 사람 의 장접막세포내에서 면역학적 분리방법에 의해서 촌재여부가 알려 졌 다. 165) Ap o B 는 간과 소장으로 중성 지 방 이 동시 에 필수물질로 나타난다. 혈장내 에 Ap o B 가 결핍 된 abeta l ip o p ro tc i n e mi a 환자의 경우 세포내에 다량의 중성지방이 촌재하는데도 불구하고 160) 중성 치방이 혈액내로 들어가지 않는다. VLDL 의 단백질 부위는 LDL 의 단백질 부위가 되는 선행물질로
이 용된다고 1950 년대 연구자 Volwi ler 166l 둥과 Git l i n1 42 l 둥에 의 해 보고되 었 다. 1960 년대 에 들어 와서 VLDL 의 단백 질 부위 에 12sr 동위원소를 이용하여 연구한 결과 153),1~, - 9> VLDL 의 Qpo pr o te i n B 가 LDL 로 대사되는 대사경로가 발표되었다. 사람의 혈청내의 VLDL 을 전할( 全血 ) 또는 유리된 다른 lip o pr o - tei n 과 배 양(i ncuba ti on) 시 켰을 때 VLDL 내 촌재 하는 ap o pr o te i n B 가 다른 lip o pr o te i n 내 의 ap o pr o te i n B 와 교환되 거 나 이 동되 지 않 은 것을 발견하였다. 그러나 12 안동위원소로 처리된 VLDL 을 사람 에 게 주사한 후에 는 모든 ap o pr o te i n B 의 활성 은 VLDL 내 에 서 발 견되었다. 그러 나 후에 Ap o B 의 활성 이 IDL(1. 006~1 . 09l g / ml) 에 서 더 나아 가서 LDL 에 나타난 것 으로 보면 VLDL - B 와 LDL- B 사이 가 선행 물질과 최종물질의 관계에 있음이 나타났다. LDL 내 의 동위 원소로 처 리 된 ap o p ro te i n B 를 사람에 게 주사하였 울 대 110> VLDL 내 에 LDL 의 ap o pr o te i n B 가 나타나지 않는 것 으 로 보아서 ap o pr o te i n B 의 VLDL 로부터 LDL 로의 이 동은 일방동 행 으로 보고 있 다. 이 러 한 lip o pr o te i n 의 상호전환은 lip o pr o te i n lipa se 에 의 해 서 진행 된다. hep a rin 을 주사하면 lipo pr o te i n lip ase 의 활성 은 크게 축전되 며 따라서 VLDL 입 자로부터 의 apo pr o te i n B 가 궁극적 으로 IDL 로 이 전된다. 153) , 167) 이 상의 결과로 마 루어 브딘 ID L 은 VLDL 이 lip o pr o te i n lipa se 와 작용하고 난 직후에 형성되는 중간산물이라고 볼 수 있다. 한편 VLDL 은 lip o pr o te i n lip a se 가 많이 함유되 어 있 고 hep a ri n 으로 처리된 혈청과 배양시키면 IDL 과 유사한 입자가 형성된다고 보고 되었다 .171-4) 또한 LDL 과 유사한 입자도 함께 생성되었다 .174) 이러한 in vit ro 실험의 결과는 생성된 IDL 에는 ap o pr o te i n C 의 함량은 거의 없으 며 VLDL 을 선행물질로 한 ap o pr o te i n B 가 거의 단백질의 전체를 접유하는 것으로 나타났다. Lipo pr ote i n lipa se 에 의 해 서 지 방이 분해 되 는 동안에 입 자는· 중성 지 방 및 인지 방 묵히 ph osph ati dy lc holi n 그리 고 유리 콜레 스테 롤을-
잃어버란다. 실험쥐의 ap o p ro te i n B 의 체내 대사과정은 125I 와 14C 동위원소를_ VLDL 에 부착시 켜 서 연구하였 다. 175 一 ” 이 연구의 결과는 사람과 유 사하다 고 생각한다. 쥐의 혈장내 VLDL 의 ap o p ro te i n B 는 쥐 혈 장 내 의 소 량의 IDL 내의 선행물질이다. 여하튼 VLDL 에 존재하는 ap o p ro ~cin B 의 소량인 약 10~30% 가 IDL 로 전환된다. 그리 고 VL DL 의 ap o p r ote i n B 는 순환하는 혈액으로부터 직접적으로 이등 되 어 나 아간 다. 즉 간이 VLDL 의 ap o p r ote i n B 를 분해시키는 주요 장기 카 된 다. 전자연 미 킹을 사용하여서 rad i oau t o g ra ph y에 의한 관찰 결과, l i p o pro t e ir. 은 상 호 전환되거나 분해되기 전에 앞서 간세포 표면막에 농 축되 어 있 음 이 발견되었다. 이 사실은 간세포 (he p a t oc yt e) 표면에 독정 한 rec ep tor sit e 가 있 을 가능성 을 지 적 해 준다. 178) 이상의 연구는 쥐에게서 혈장내 LDL 수준조철기전의 의십접을 설 명해 준다. 죽 VLDL 이 LDL 로 전환되기에 앞서 혈장내에 생성되 는 중간산물의 소실되는 속도 (clearance) 조철을 설명한다. 그러나 이 대사과정은 오로지 쥐에게서 나타난 것이지 사람을 포함한 다른 동 물에게서는 더 연구되어져야 한다. 125I ~ 동위원소로 처리된 VLDL 을 사람에게 사용하였을 때의 대사 과정이 및 및 연구자에 의해서 연구되었다. 정확한 ap o p ro te i n B 의 kin e ti cs 분해 과정 , 죽 VLDL-B->IDL-B-.LDL-B 로 상호전환 가능성 은 mul ti -com p ar t men t al 접근법을사용하여서 연구하였다. 이 연구는 1 4 인에게 행해졌다 .167-9)>179) 그 대사과정은 다음 그림에서 보여준 다(二 림 2 참조). 이 연구에 포함된 4 인은 정상인이었고 나머지는 Ty pe II b hy pe rlip o p ro te i n e mi a, Ty pe IlI hyp e rlip o p ro te i n e mi a, Ty pe N hy pe rlip o p ro te i n e mi a 환자였 다. C( 2 대사경로는 정상인에게서 ap o p ro te i n B 가 사라쳐 가는 경로를 표시한 것이다. /3-경로는 지방이 제거된 VLDL 을 여분으로 사용하 여서 VLDL-B 가 type II hy pe rlip o p r ote n emi a 환자에게서 연구되 었 다. 19- 경 로는 새로이 분비 된 VLDL 입 자로부터 보여 준 경 로이 다. 그러나 이 경로는 정상¢경로에서 지방을 제거한 과정을 따라서 메
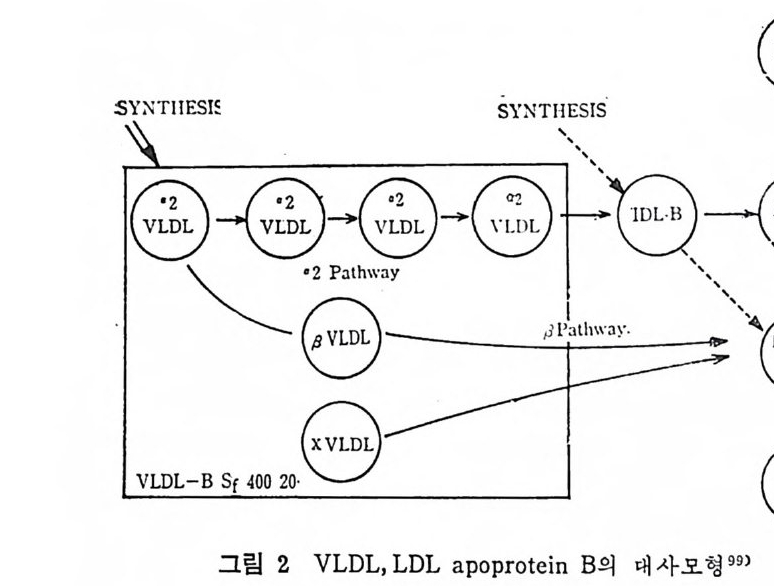 NLOI J NL ··l 1l
NLOI J NL ··l 1l
사된 마지막 단계에서 형성될지도 모른다고 생각한다. /3·경로를 따라서 이루어지는 VLDL-A p oB 입자의 독 특 한 대사과 정은 VLDL 과 IDL 밀도법위로부터 Ap o B 가 대단히 서서히 사타지 고 있으며 이 경로를 통해서 대사되는 VLDL 의 Ap o pr o te i n o p B 의 양은 약 1/8 정도이고나머지도 야경로를통해서 붕괴된다. g·경 로 로 붕괴 될 때 도 LDL 비 중범 위 의 lip o pr o te i n 은 지 나쳐 버 리 게 된 다. X-VLD 냐 동위원소처 리 된 VLDL 로써 이 는 ap o pr o te i n B 의 빠 론 붕괴 경 로를 따라서 붕괴 되 어 서 iod id e po ol 로 들어 간다. X-VLDL 이 정상 VLDL 비중범위의 것과 같은 것인지에 대해서는 이 연구 에 서 해결을 보지 못하였다 .179) IDL 내 의 ap o pr o te i n B 는 a-VLDL 입 자로부터 온 것 이 며 이 는 따 - 경 로의 직 접 적 인 산물이 다. IDL 내 의 apo pr o te i n B 는 두 경 로에 의 해서 붕괴된다. 첫째는 LDL 로 전환되는 것과 둘 째 는 혈액으로 부 터 직 접 적 으로 이 동되 어 나가는 것 이 다. a2-VLDL - B 의 IDL-B 로의 전 환율온 정 상인에 게 서 2. 8~2. 6/ 일 (입 자p ool/da y)이 며 hy pe rt rigly c e- .ri dem i a 환자에게서는 그 울이 낮아서 o.7~1.4/ 일이다. IDL - B 가
LDL - B 로의 전환율은 VLDL - B 에 서 IDL- B 로의 전환율과 유사하 다 .179) 정 상 인에게서의 A p oB 합성치는 1 일에 7.13~11.36mg / kg 사이 이 며 hy pe rIip o p ro te i n e mi a 환자에 게 서는 1 일에 4. 63~11. 40mg / kg 사이 로 보 고되었다. 그러나 환자의 경우 T yp ellI 와 중간사슬길이의 중성지 망 Ty pe I 환자는 제의되었다. 정상인의 모돈 ap o p ro te i n B 합성은 따 - VLDL 경로 를 통해서 이루어지며 환자의 경우도 Ty pe I 과 Ty pe I Ib 그리 고 T yp eN 환자도 마찬가지 경로를 통해서 이루어 진다 . 그 리 나 T yp e lli 환 자(치 로룹 하고 있든지 안하든지 모든 경우 포함)나 Ty pe I 환 자 (60 g / d a y 의 MCT 에 의촌하는 환자)에게서 ap o p ro te i n B 합 성의 2 차 주 요 경로 는 IDL 을 경 유해서 합성됨이 관찰되었다. Ty pe N 환자의 경 우는 ap o rpr o te i n B 합성 이 a2-VLDL 경 로를 동해 서 IDL 형 태 로 직 접 합 성 되 며 또한 (3- delip ida ti on 경 로를 통해 서 /3- V LDL 이 합성되므로 a p o p ro t e i nB 의 합성은 정상인의 2~3 배나 되는 높 온 양 을 합성하는 비정상적인 현상이 초래된다. 또한 VLDL 이나 IDL 법위내의 ap o p ro t e i nB의 분해속도도 T yp em 환자에게서 상당히 느리 다. Ty pe N 환자의 병 은 lip o p ro te i n 대 사에 장애 가 있 는 것 이 지 lip o p ro te i n 분자의 구조상에 이 상이 있는 것 은 아니 라고 본다. 또 한편 T yp eN 환자에게서 VLDL 내의 a p o p ro t e i nE 에 양적 • 질 적 변화가 있다는 보고도 있다 .180) 1 마 동위 원소 처 리 된 VLDL 내 의 ap op ro te i n B 의 합성 분해 율은 125I 동위원소 처리된 LDL 내의 a p o p ro t e i nB 와 바교한 결과가 다음표에 요약되어 있다. 이 표의 수치도 VLDL-B p ool 에서 추정한 것이 므로 미 교하는데 약간의 문제 접 이 있 다. 181-4) VLDL-B 의 분해 도 hy pe rlip o p ro t ei n e mi a 환자에 게 서 LDL-B 로 전환되 지 않고도 직 접 이 루어 질 수도 있 다고 하였 다. 181-2) 이 와는 반대 로 FH (fom i lial hyp e rcholeste r olemi a) Homozy go ts 에 서 상당량의 VLDL 과 무관한 ap o p ro te i n B 가 합성 된다고 하였 다. 이 ap o p ro t ei n B 는 LDL-B 합성 에 필수적 인 물질이 다. 184) LDL 합성 분해 울에 관한 kin e ti cs 연구가 여 러 연구자들에 의 해서 ;
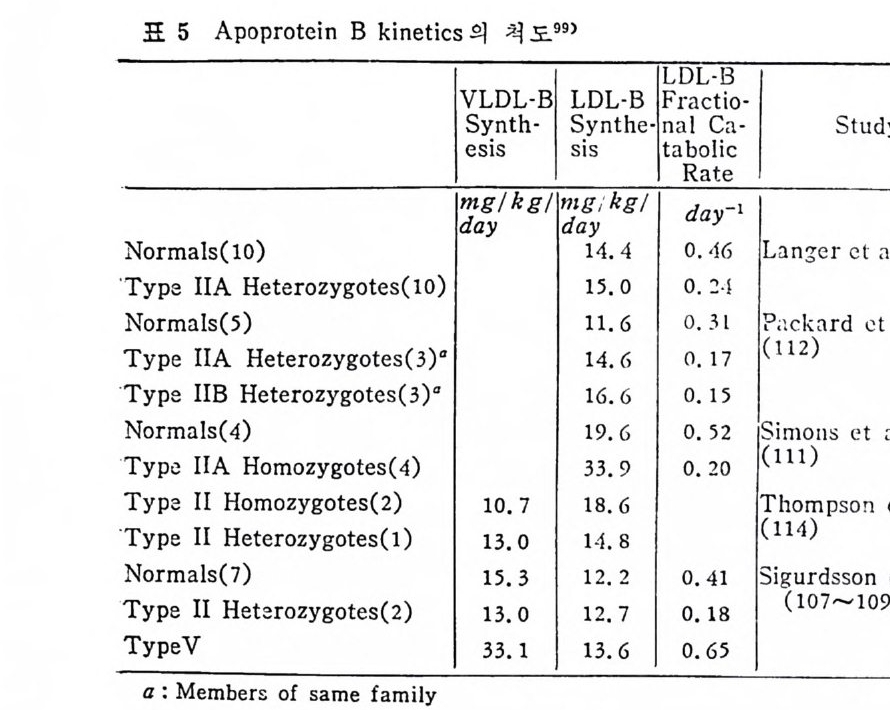 표 5 Ap o p ro te i n B kin e ti cs 의 쳐 도 99)
표 5 Ap o p ro te i n B kin e ti cs 의 쳐 도 99)
이 루어 졌 다. 142), 168), 170), 181- 90 ) 동위 원소로 처 리 된 LDL kin e ti cs 연 구 는 두 부위 (two comp artm enta l ) 모델연구에 서 잘 보여 주고 있 다. 이 두 부위는 혈장과 혈장 이외의 부위를 말한다(표 5 참조). 이 연구 에 대한 결과는 LDL-B 의 합성과 분해는 혈장부위에서 이루어지며 LDL-B 는 역으로 · 두 부위 사이에 분포되든가 아니면 교환된다고 앴 다. LDL-B 의 kin e ti cs 척 도(p arame t er) 도 표에 제 시 되 였 다. 이 표는 정 상인과 FH 환자에 서 12s1 동위원소로 처 리 된 LDL 을 사용하여 서 두 부위에서 연구되어전 것이다. FH 환자에게서 LDL-B 분해에 결 함이 있는 것 은 LDL po ol 크기 와 무관한 것 으로 본다. 181- a> LDL-B 의 합성 은 FH Homozy go te s 시 중가되 며 FH Hete r ozy go t e 에 서 는 약간 증가되든지 아니면 정상으로 유지된다 .168),180),1 8-1) Ni cot i nic ac id 는 LDL 합성 을 감소시 키 는 것 으로 나타났으며 187)
VLDL 과 LDL 을 차례 로 delip ida ti on 시 키 면 ap o p r ote l n B 가 이 들 입자에 나타난다. 이전 과정에서 이루어지는 것은 보나 입자의 크 기가 크고 가벼운 것으로부터 입자의 크기가 작고 무거운 것이 생 성되는 것이다. 이러한 상호전환과정에서 중요한 현상온 생 성된 각 각의 입 자내 에 는 ap o p r ote i n B 분자들이 선구체 로서 함유되 어 있 다 는 것 이 다. 그러 므로 lip o p r ote i n 의 입 자의 크기 가 작아질수록 이 들 은 ap o pr ote i n B 로 차차 강화되 어 가고 있 다. 평 군 크기 의 LDL 입 자내 에 함유된 ap o p ro te i n B 의 평 균 농도는 평균 크기의 VLDL 입자내에 보다 및 배 높은 양이 함유되어 있다. 아러한 a p o p ro t e i nB 의 농도중가 현상에 대한 생리적인 중요한 뜻 온 알려져 있지가 않다. 이 현상온 아마도 결과적인 분해에 영향을 미칠 수도 있다. 이 분해과정은 각 조직의 세포표면에나 또는 효소 에 lipo p ro te i n 의 recep tor 부위 와 lip o p ro te i n 사이 에 서 의 상호작용 이 포함되어 있다. 그러나 사람의 혈액은 조직으로 LDL 을 이동시키는 특정한 부위 로 알려 져 있 지 않다• 간을 갈라낸 (hepa l ecto m y ) 돼 지 에 게 서 LDL-B 의 분해가 지연되지 않았다 .191) 이 현상은 LDL-B 분해장소는 간 보다도 말단조직으로 생각해 볼 수 있다. 이 생각은 조직세포배양 에서 뒷받침된다. 조직배양시 및 종류의 세포표면에 recep tor sit e 가 있는 것으로 나타났으며 궁극적으로 LDL 이 분해되는 것으로 나 타났다. 192- 3 ) 또한 LDL 이 recep tor sit e 에 결합되면서 동시 에 그 부 위 의 fibr oblast 내 에 3-hy d roxy - 3-meth y lg l u ta ryl - CoA 효소활성 이 저하되었음이 관찰되었다. 그란데 FH 환자에게서는 LDL 의 recep tor s it e 에 고도의 찬화력 이 결핍되어 있거나 전연 없었다고 보고되었다 .192-3) 또한 FH 환 자에 게 서 LDL 이 recep tor sit e 에 결 합된 후에 fibr oblast 내 로 LDL 이 융화될 수 없다는 보고가 있으며 , 194> LDL recep tor 연구에 대 한 문현고찰도 발표되 었 다. 195) 이 상의 모돈 보고를 종합해 서 VLDL-LDL ap op r o te i n B 의 인체 내 에 서 의 주요 대 사경 로를 묘사하여 보았다. apo p r ote i n B 는 VLDL 에 영합되어서 혈액으로 듈어간다. 그래서 지방울 제거하는 과정
을 통해 서 LDL 로 전환된다. 그러 므로 LDL 은 VLDL 대 사과정 의 마 지 막 생 성 물질이 다. 혈액 으로부터 ap o pr o te i n B 의 재 거 는 LDL 형 태 의 입 자로서 이 루어 진다. 여 러 형 태 의 Iip o p ro te ine mi a 질 병 상대 에 서 는 여 러 양의 ap o pr o te i n B 가 IDL 이 나 LDL 에 결 합해 서 혈 액 으로 들어가며 또한 혈청으로부터 a p o p ro t c i nB의 재거는 VLDL 또는 IDL 의 비 중범 위 내 의 lip o p ro te i n 으로서 직 접 재 거 된다. (3) Ap o lip o p r ote i n C 1) 물리적 특성 A p oC 는 혈청 l ip o p ro t e i n 내에 촌제하는 분자량이 낮은 단백질 군이다. 사람에게서는 세 종류의 A p oC 가 존 재한다. 죽 Ap o C- I , Ap o C-II, A p oC - · l!I이다. 이 셰 종류의 아미노산 구성과 배영순 서 도 보고되 어 있 다. 196-9) 이 들 단백 질은 2mole, ! mole 의 sia l i c acid 를 각각 함유하고 있 으며 나머 지 한 종류는 sia l i c acid 를 함유 하고 있 지 않다. 이 세 종류의 ap o p ro te i n 은 수용액 에 녹는다. 아 둘 C-lip o pr o te i n 은 인지 방, ph osph ati dy lc holin e , sph in g o my e lin 또는 lys o p h osph ati dy lc holin e 과 결 합된 단백 질 지 방 복합체 로 촌 재한다. 10 1) ,200 내) Ap o C t:-J:백 질은 특히 중성 지 방을 많이 함유하고 있 고 lip o p ro tc i n 의 대사에 중요한 역할이 있다. 특히 A p oC-II 는 간세포 밖에 존재 하는 lipo pr o te i n lip a se 에 의 해 서 이 루어 지는 중성 지 방의 가수분해 를 위해서 필요한 특정한 조요소 (co fac t or) 로써 작용한다. 204- 6 ) 또 한 인지방은 지방의 원만한 분해를 위해서 필요하다고 본다. 또한 Ap o C-I 이 lipo p r ote i n lip a se 의 활성 을 위 해 필수물질 이 라고 보 고되 었다. 207-8) 또한 Ap o C-I 이 LCAT 를 활성 화시 킨다고 보고되 었고, 154) Ap o C-II 는 lip o pr o te i n lipa se 의 작용을 방해 한다고 보 고되었다 .211) 그러나 A p o 앉 1 모든 세 종류는 중성지방이 여분 으로 촌재할 때 중성지방의 가수분해를 부분적으로 방해한다고 한 다. Ap o C 의 lipo pr o te i n 대 사에 대 한 인상적 인 모든 역 할 때 문에 Ap o C 는 혈장 lipo pr o te i n 의 〈기 능적 인 (fun cti on al) n p o p ro t e i n 〉야
라고 때때로 불린다. 2) Lip o p ro te i n 내 의 Ap o C 정상 철청 내의 A p oC - II 와 Ap o C-lll 함유량은 각각 약 5mg /d l 와 I 4 m g / dl 이다 .2 0 8),210) 이 두 단백질의 혈장내 수준은 고중성지방 혈증 간자 에게서는 증가된다 . 그러나 VLDL 에 함유된 단백질 매 gr 팅 - Ap o C- II 의 양과 lip o pr o te i n lip a se 의 활 성 화되 는 양은 고중 성지 당 일 중환 자에게서 감소된다. 이 현상은 아마도 이러한 환자에 게서 VLDL 분해과정에 손상 이 온 것으로 생각해 봅 수 있다 .210.、 또한 고지방혈증환자에게서 이차적인 영향으로 A p oC - Il 의 전핍 증이 현저해졌다고 보고되었다 .211) A p oC 의 다양한 양이 모든 혈장내에 존재하는 lip opro t e i n 내에 서 발견된다. A p oC 는 ch y lom i cron 내의 총단백질 중 60% 를, VLDL 단백질 의 40~80% 를, HDL 단백질의 2~10% 를 접유하며 LDL 단백 질 에 는 흔적 량으로 존재 한다. 153) 여러 수준 의 비중 범위내 의 VLDL 단백질 중에 A p oB 에 바교한 Ap o C 의 함유량을 비 교해 보면 VLDU 니 입 자크기 가 작고 비 중이 높으면 입자의 크기가 큰 것과 입자가 가벼운 것에 비해서 Ap o C 의 함량이 비교적 적다. LDL 내에는 A p oB 에 비교해서 극히 소량 의 Ap o C 량이 존재 한다. 153) LDL 은 VLDL 로부터 전환되 는 것 이 므 로 대 부분의 LDL 내 의 Ap o C 는 VLDL 로부터 전환될 당시 에 이 동 된 것이다 . 사람이 기 아시 에 는 혈청 내 에 서 apo lip o pr o te i n C 는 주로 VLDL 과 HDL 내에서 발견되는데 주로 HDL2 (1. 063~ 1. 125 g / ml) 에서 발 견된다. 108) 그러 나 Ap o C 는 VLDL 단백 질의 50% 를 차지하며 HDL 단백질의 5% 밖에는 점유하지 않는다. 그러나 기아시에는 이 단백 질이 VLDL 과 HDL 사이에서 군등하게 분배된다. 기아시에 혈청내 에서 이러한 군등분배는 HDL 단백질질량이 VLDL 단백질질량에 비 해서 150m g%나 되며 VLDL 단백질질량은 단지 10m g%로 되기 때 문이다. 그러나 고중성지방혈증 환자에게서는 A p oC 단백질이 HDL 로부터 VLDL 로 재 분포된다. 210)
다양한 연구컬과가 VLDL 과 HDL 대사와 An oC 와 관련해서 전 행 되 었 다. 유도되 어 전 al: menta r y lip e mi a 때 에 Ap o C- II 는 HD L 에 서 chy lo mi cr on 으 로 이 동되 었 다. 이 때 에 Ap o C- II 는 !j p o pr · ote i n lip a se 의 활성 제 로 축정 되 었 다. 21 2 ) 또 한편 chy lo mi cr o n 이 사 라지는 것은 효소활 성제 단백질 (ac ti va t or p ro t e i n) 이 HDL 로 되둔 아 가논 현 상과 관련되었음이 관찰되었다. 또한 먼처 12 기 동위원소로 처리된 VLDL 을 혈청내에 주입시키고 그 혈청 에 he p ar i n 은 수 입 시 켜서 지방분해 문 시도해 보았을 대 VLDL 내의 중성지 망이 신속 히 감소되는 현상이 나타났으며 , 동위원소로 표 시 되 어 전 Ap o C- ll 와 A p oC- 1[가 HDL 로 이동되었다 . 그런데 6 시간 후에 새 로운 VLDL 이 혈액내로 주입되었을 때 A p oC - II 와 A p oC - IlI 도 다시 VLDL 로 이동되어 들어갔다 .167) 이 연구에서 제시해 주는 사실은 Ap o C 분자도 chy lo mi cr on 에 서 VLDL 을 거 쳐 서 HDL 로 이 등되 어 지 며 중성 지 방함량이 높은 lipo p ro te i n 의 분비 , 분해 동안에 다시 HDL 에서 VLDL 로 되돌아가는 여현상이 나타난다는 것이다. 3) A p oC 의 대사 A p oC 의 인체내에서의 대사과정에 대한 충분한 실험치가 없기 때문에 대사나 경로를 분명히 정리할 수가 없다. 그리고 A p oC 의 소립자, 죽 C- I , C-lI, C- ll[로 나누어전 대사경로는 더구나 알 려져 있지 않다. 그러므로 A p oC 를 묶어서 논의하기 로 한 다. 실험 쥐에게서 관찰되어전 바에 의하면 장내에서 새 로이 합성되 어 분비되는 A p oC 양은 극히 소량이거나 흔적량 정도라고 하였다 . 1 64 ) A p oC 는 분명히 간에 의해서 합성되고 분비되는 것으로 생각한 다. 164) 간 절편을 동위원소로 처 리 된 아미 노산으로 pe rfu s e 하면서 이 간에 서 VLDL 과 HDL 을 유리 하여 보면 이 lip o p ro t ei n 내 에 동 위원소를 포함한 A p oC 가 함유되어 있다. 그렇지만 이 결과로 는 A p oC 가 VLDL 이나 혹은 HDL 또는 둘 다 함께 간으로부터 분비되었는지에 대해서 분명하지가 않다. A p oC 는 abeta l i po p ro - ;te i n e mi a 환자나 HDL 결핍자, Tang ier dis e ase 환자의 혈장내 에 서 발견된다. 126),160) 이 관찰은 Ap o C 대 사가 Ap o B 와 Ap o A 대 사와
무관하다는 처 도를 보여 주고 있 다. 쥐 에 게 서 Ap o C 는 go lgi cist e r -nae 로 부터 유리 된 VLDL 입 자에 서 유리 되 었 다. 213) 이 현상은 분명 히 A p oC 가 합성되는 세포내의 부위와 g ol gi가 연결되어 있다고 보며 그래 서 go lg i 내 에 서 새 로이 탄생 되 는 lip o pr o te i n 과 Ap o C 가 관련이 있다고 생각된다. 1 25 1 동위원소 처리된 VLDL 을 혈청이나 HDL 과 함께 배 양시 키 면 VLDL 내 의 Ap o C 의 특 정 활 성 은 감소되 며 반면에 HDL 내의 묵 정 활 성은 증가되었다 .17 1) ,214) 이 렇 게 A p oC 의 VLDL 과 HDL 사이에서 상호교 환 되는 방법이나 기전에 대 해 서는 알 려진 바가 없다. 그전대 이러한 A p oC의 VLDL 과 HDL 사이에서의 상 호 교환현 상은 인지방과는 관련없이 이루어진다고 보지만이 교환이 적합하게 이루어지기 위해서는 인지방의 참여가 완전히 배제될 수는 없다 .214) 1251 동위 원 소 처 리 된 VLDL 과 lip o p ro te i n lipa se 함량이 높은 혈 장의 in v i t ro 연구에서 배양하는 동안에 VLDL 로부터 HDL 로 이 동되는 A p oC 의 양은 중 성지방 가수분해 양과 비례한다고 하였 다. 171) 배 양하는 동안에 VLDL 내 의 12s1 동위 원소로 처 리 된 Ap o C 의 독 정 활 성은 정상 혈청과 배양한 입자와 유사한 현상이 나타난 것 으 로 보아 VLDL 로부터 HDL 로의 A p oC 의 이등을 중성지방 가 수분해와 관련해서 살펴보면 이는 결과적으로 이동되어전 정량에 기인된다고 본다. VLDL 내 에 함유된 중성 지 방의 80% 를 가수분해하고 난 후, VLDL 입자내에 함유된 A p oC 불 화학적으로 측정해 본 결과 본래 입자 에 함 유된 양의 7% 밖에 남아 있지 않았다. 이 현상에 미루어 생 각해 보면 입자내에 포함된 A p oC 의 모든 양이 인지방이나 또는 전체 입자표면에 결합되어 촌재하며 그래서 A p oC 의 농드는 지방 가수분해로 인해서 입자가 작아지니까 표면적이 본레의 1/5 르 감소 되 므로 Ap o C 양도 따라서 감소된다고 추측해 볼 수 있 다. VLDL 내의 A p oB 는 지방분해 동안에 이동되는 것도 전연 없으므로 Ap o B 의 표면에 농도도 3 배로 증가되었다. 그러므로 지방분해과정 동 안에 VLDL 입자 표면적에 Ap o B : A p oC 의 농도비례를 비교해 보 떤 15 배 로 증가하였 다. 172)
Lip o pr o te i n 입 자내 의 Ap o B 와 Ap o C 는 각각 다른 대 사과 정 에 서 중요한 역 할이 있 다. 죽 조 직 세 포 와의 상호작용과 lipo p ro te i n lip a se 부위와의 상호작용을 각각 한다. 관 찰 되 어 전 바 와 갇 이 지 방 분해과정 동안에 l i p o p ro t e i n 표면의 A p oB 와 A p oC 의 함유량의 년 화 는 여러가지의 대사과정 윤 통 해서 결 과 적으로 l ip o p ro t e i n 의 붑 해를 전정해 주 게 된다. Lip o pr o te i n 내 에 존재 하는 Ap o C 의 전 합 상 대 와 분리 되 는 과정 또 는 교 환 되는 과 정 의 물리 화학적 목성은 아 직 찰 알려져 있지 않 다. A p o C 는 인지 방 과 안 정된 복합체를 이 루 지 만 이 러한 유사한 복 합체가 이들의 대사 동안에 l ip o p ro t e i n 내 에 생성되는지에 대해서 는 아 칙 까지 증명 되 지 않았다. Ap o C 의 subunit s 믈 유리 해 보는 시도가 이루어졌으며 또한 중 성 지 방 함 량이 높 은 l ip o p ro t e i n 분 자 로 부터 A p oC 가 유리되는 과정에 대한 실 험이 시도되었다. 12s1 동위 원소로 처 리 된 VLDL 입 자 를 혈 청 이 나 다른 lip o p ro te i n 이 없는 상태 에 서 정 제 된 lip o p ro te i n lip a se 와 함께 배 양시 켰 다. 17 3 ) 이 결 과 지방분해 정도와 관련을 지어 볼 때 VLDL 로부터 Ap o C 를 이동시키는 과정에는 배양체계내에 혈청 의 존재가 아무런 영 향을 미치지 못하였다. 그러므로 이 실험의 결과는 A p oC 의 분 리 는 오로지 부분적으로 가수분해된 입자의 상태에 의 존 하는 것 으 로 결론을 내릴 수 있다. album i n-bu ffe r 내에서 발 견되어전 A p oC 의 일부는 지방과 결합되었을 것으로 본다. 왜냐하면 이는 밀도가 I.04~ 1. 21 g /ml 범위내의 입자에서 유리되었기 때문이다. 그리고 나머지는 지방과 결합이 찰 되어 있지 않는 것으 로 보며 이는 밀도 가 1.21 g /ml 보다 큰 입자에서 발견되었다 .173) 또 다론 연구에서는 VLDL 입자가 합성될 때 여러 구성성분에 동 위원소 처리를 하였다. 죽 인지방에 32 p동위원소를 처리하였으며 콜레스데를에는 3H 를 부착시켰고 중성지방의 지방산에는 14C 을 부 착시켰다. 그리고 A p oC 에는 125I 를부착시켰다. 그결과 지방 분 해 가 시 작됨 에 따라서 지 방과 ap o p ro te i n 은 복합체 를 이 루는 운명 이 라는 것이 발견되었다. 인지방의 일부는 주로 ph osph ati dy lc holin e 온 lys o com p ound 로 가수분해되었고 이는 밀도 〉 I.2l g /ml 의 것에
저 albumi n buff er 입 자와 결 합 되 어 있 었 다. 또 다론 VLDL 부위 의 인 지 방, 주로 lecit hi n 과 sp h in g o my e li n 이 함유된 것 은 VLDL 밀 도법위로부터 이동되었으며 밀도범위가 1.04~1.21 g /ml 입자에서 발견되었다. 그리고 VLDL 입자내에 함유된 중성지방의 50% 가 가 수 본해 되었을 때 비로소 소량의 콜레스 데몰이 이동되었다. 지방의 분해 가 더 전행 됨 에 따라서 주로 unest e r if ied 콜레 스테 롤이 VLDL 로부터 밀도가 I.01~1.2I g / ml 범위내의 bu ff er 입자내로 이동되었 다. 이 연구에서 보여준 결과는 중성지방 함량이 높은 lip o p ro te i n 으로부터 A p oC 가 이동될 때는적어도부분적으로라도 밀도의 범위 가 1.0 4~ I. 2I g / ml 인 소량의 지방-단백질 복합체의 형태로 되어전 다고 본다. 혈청 이 존재할 대에는 VLDL 로부터 이동되어전 Ap o C 는 주로 HDL 과 함께 존재하는 것으로 발견되었다. 이는 아마도 단백 질과 lip o p ro te i n 사이 의 상호작용 때 문으로 본다. 215) 이상의 결과와 유사한 연구결과가 쥐의 십장을 대상으로 실험했 울 대 나타났다 .216) 이상의 모든 결과를 기초로해서 볼 때, lip o p r· o t e i n 입자들 사이에서 결합되었다, 분리되었다 하는 동적인 관계 (dy n ami c rela ti on) 에 있 는 것 으로 볼 수 있 는 Ap o C 는 분명 히 lip 0 · pro t e i n 입자에서 수용액 중으로 이동되는 것으로 미루어볼 수 있 으며, 이것은 A p oC 의 lip o p ro t e i n 내와 수용액내에 농도의 평형상 태 (eq ul ib r iu m s t a t e) 를 제 시 해 볼 수 있 다. 이 런 견지 에 서 보면 lipo · pro t ei n 의 표면 에 촌재 하는 지 방의 독수한 confi gu rati on 아 Ap o C 의 길 함평 형 (associa ti on con s t an t)을 결 정 해 준다고 본다. 중성 지 방 함량이 높은 !ipo p ro t ei n 은 Ap o C 분자에 대 한 고도의 찬 화력 이 있 으며 이 lip o p r ot e i 1 1 내 의 지 방의 분해 가 lip o rpo ',ein lipa s e 에 의 해 서 진행 됨 에 따라서 천화력 이 차차 감소되 다가 lipo p ro te i n 입자가 LDL 로 되면 이 친화력은 최소로 된다. A p oC 와 lipo p r ote i n 사이의 상호관련이 다음의 그림으로 표시되 었다(그림 3 참조 ). 사람의 혈청내의 Ap o C 의 대사의 k i ne ti cs 는 12 탄동위원소로 처 리 된 VLDL 을 사용하여 서 연 구되 었 다. 153), 167-9), 179) 다음 그림 에 서 보여 주듯이 multic o mp a rt m enta l 모델을 사용하여
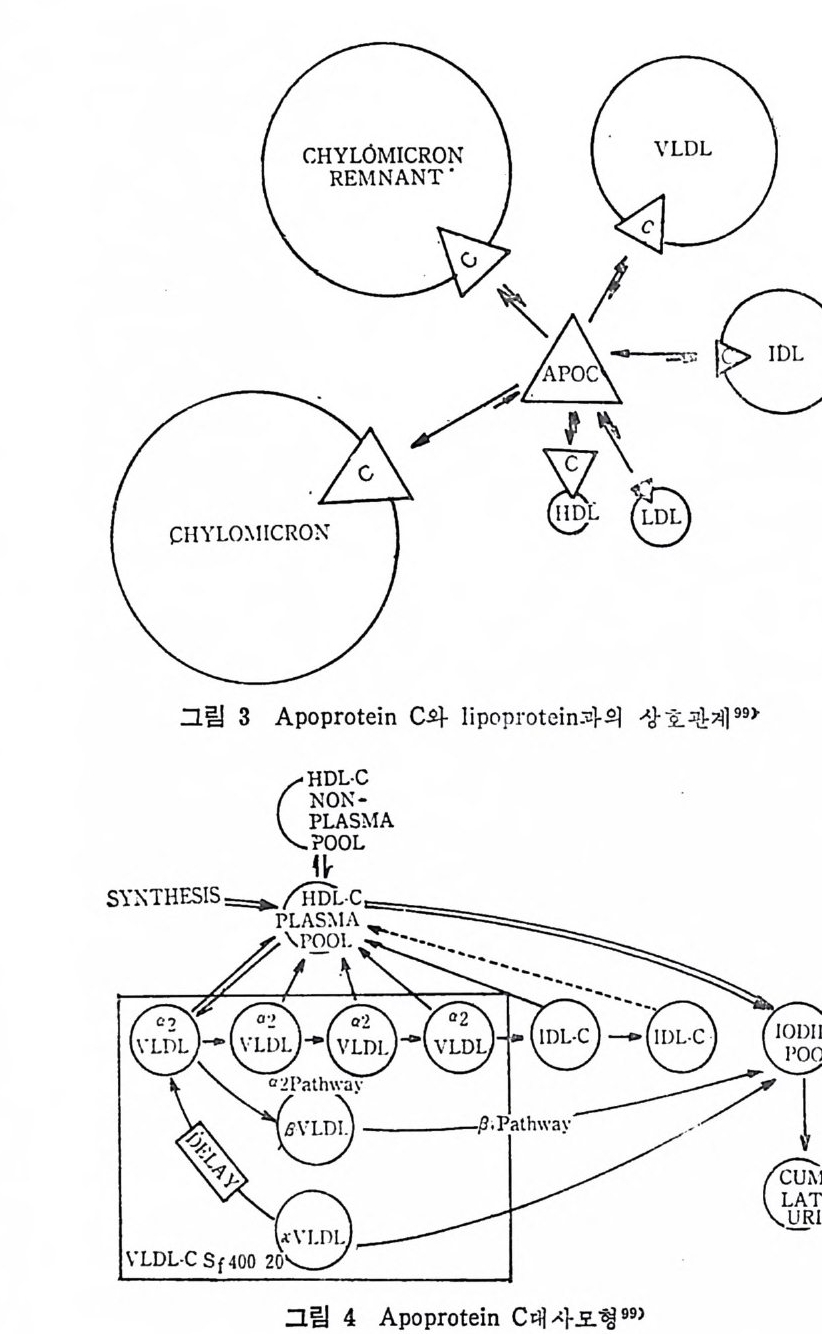 : I
: I
서 1251 로 처 리 된 VLDL 의 대 사과정 이 정 상인과 hy pe rlip o pr o te i n - em i a 환자에게서 연구되었다(그 립 4 참조 ). 이 연구 결과 혈청 내의 A p oC 입자의 분해율은 1.5~2.5/ 일이며 Ap o C 의 반감기 는 10~ 18 시 간 사이 였 다. 168-9), 179) 이의 합성률은 A p oC 가 VLDL 로 들어가면 10 0~400 m g /일 이며 만인에 HDL 로 둘 어가면 150~ 660 m g / 일이었다. 그리고 정상인이 나 hy pe rlip o p ro te i n e mi a 환자에 게 서 의 합성 이 나 분해 에 서 일정 한 차이 문 나타내 지 않 았다. 179) A p oC 의 분해 에 대해서 아는 바가 거의 없다. 그러나 중간 크 기 의 Iip o pr o te i n 분자 와 LDL 은 극히 소량의 Ap o C 를 함유하고 있 으며 이 두 종류의 l i p o p ro t e i n 은 순환하고 있는 혈액으로부터의 Ap o C 소멸 (clearance) 에 아주 작은 역 할이 있 다고 생 각한다. HDL 이 A p oC 소 멀 에 주요 운반체로서 작용한다. 그러나 정상인의 혈 액내 A p o C 의 반감기는 2 4 시간 이하이며 이와 비교해서 Ap o A-I 괴- A p oA - II 의 반감기는 5.0 시간이다 . 이와 같이 A p oA 와 Ap o C 의 반감기의 차이 를 설명해 줄 수 있는 가능성은 A p oC 가 수명이 짧은 HDL 입자와 호의적으로 결합되 기 때문이다. 그러나 아직까지 이 가설을 지 원해 줄 자료가 없다. 좀 다르게 설명해 보면 순환되는 혈액으로부터 A p oC 의 소털은순환되면서 이 루아지고 A p oB 와 A p oA 에 직접적으로 이루어진다. 이 가설에 의 하면 Ap o C 의 소털은 중성 지 방 함량이 높은 Iip o pr o te i n 과 HDL. 사이에시 이동되는 단계에서 이루어질 수도 있다고 보거나 또는 수 용성의 형태로 이루어질 수도 있다고 본다. 그러나 이 가설 역시 실업으로 증명 되지는 못하였다 /15)
A p oB 와는 대조적으로 A p oC 는 새로이 합성된 중성지방 함량이 높 은 lip o p ro te i n 과 HDL 사이 룰 쉽 게 이 동한다. 간은 A p oC 합성의 주요 장기이다 .16 4 ) A p oC 가 순환계로 들어갈 때 VLDL 과 또는 I-I DL 과 또는 둘 다와 함께 들어가는지에 대해 서는 분명히 결정되어야 한다. A p oC 가 분해되는 부위는 아직 모 론다 . 또한. Ap o C 의 소립자, 즉 C-I , c_II 가 각각 대사적으로 다른 것 이라고 상상해 보는 것은 무리가 아니다. 그러나 아직까자이에 대한 실험정보가 거의 없다. (4) Ap o lip o p r ote i n E 1) 울리적 톡성 및 lip o p r ote in 내의 Ap o E Argi ni n e 함유량이 높은 단백 질인 Ap o E 가 사람의 혈청 내 VLDl- 로부터 유리되었으며 이의 분자량은 약 33,ooo dal t cns 이 다 . ~17- 20) 전체 아미 노산의 약 10% 를 접 하는 217 - 20) 이 물질은 및 종 유 의 다른 형대로 촌재한다 .ISO),220) 그러나 여러 형태의 Ap o E 사이의 구 성이 나 구조적 차이는 아직까지 결정되지 않았다. Ap o E 의 정 상인의 혈청 내 수준을 전기 적 면역 방법 (ele ctr o im muno assn y)에 의 해 분리 해 보면 약 10mg % 이 다. 그리 고 아 양온 Ty pe I[ 과 Ty pe V h yp er lip o p ro t e i nem i a 환자에개 서 2 배 로 증가된다 . 116),22 1) A p oE 는 VLDL 과 . HDL 내에서 발견되며 사람의 VLDL 내의 단백 질 양의 약 13% 를 점유한다 .162) 또한쥐의 HDL 단백 질 의 20~25% 룬 접유한다. A p oE 는 원래 VLDL 과 결합되어 있으며 또한 작은 입자 162),222) 와 결합이 되어 있고 또 HDL/23) 와도 결합이 되어 있다. 쥐의 HDL 단백질 중 20~25% 가 A p oE 로 구성되어 있 다 . Ap o E 의 쥐 의 혈장내 수준은 radio i m muno assay 방법 에 의 해 서 측 정 되 엇 다• 138)'224) lipo p ro te i n 내 의 상당량의 Ap o E(3o~ · i O% )가 한 번 의 조 원십분리에 의해서 본래의 위치에서 분리되어 나오며 수 로 밀도가 . 〉 1 .2I g /ml2 23-4) 의 수용성 단백질과 함께 발견된다. VLDL 의 Ap o E 의 수준은 Ty pe I[ h yp erl ip o p ro t e : nem i a 1 ~ ) 환자 에게서 증가되며 또한 콜레스테롤 섭취로 인해서 비정상아 킨 lip o pr ote i n 내 에 도 증가되 어 있 다. 225) Ty pe III hy pe rlip o pr o te i n e m ; a 환자의 혈장내에서도 콜레스테몰 es t er 양은 풍부하며 중성지방 양 온 적 은 P-mobil it y 의 VLDL 입 자가 병 적 인 lip o pr o te i n 으로 발견 된 다. 219) 이 경 우 p-m obil ity 의 VLDL 내 에 단백 질 양의 20% 가 Ap o E 로 구성되어 있다. A p oE 의 정밀한 분석, 죽 Ap o E-I, Ap o E- I I, A p oE -· ill가 ,ele ctr ic foc usin g 에 의 해 분리 되 었 다. 180) Ty pc IlI 환자의 p-V LDL
내에는 A p oE - IlI 가 결핍되었는데 정상인의 VLDL 내에는 전체 Ap o E 양 중 39% 가 A p oE-Ill 라는 것은 홍미로운 일이다 .180) 2) 대사 pe rfu s ed 된 쥐 간으로부터 유리 된 신생 Iip o pr o te i n 내 에 는 Ap o E 가 전체 HDL 의 단백질 중 50% 이상이나 구성하고 있으며 또한 VLDL 내에도 상당량 발견된다 .131-a i, 163) LCAT 가 방해를 받으면 대 부분의 Ap o E 는 HDL 내 에 서 발견 이 된다. 163) 알코올성 간영 환자 나 LCAT 결핍 자에게 있어서 HDL 의 수준은 감소하나 HDL 내의 단백 질 의 ,J o % 정 도가 Ap o E 로 구성 되 어 있 다. 225 - 7) 한편 VLDL 내 에서는 A p oE 가 발견되지 않는다. LCAT 결핍환자로부터 온 혈청 윤 LCAT 와 함께 배 양시 키 면 Ap o E 는 HDL 로부터 VLDL 로 옮겨 진다. 이와비슷하게 알코올성 간염으로부터 치료된 후에도 HDL 단 낵질내의 A p oE 함량은 1% 로 떨어지며 칭상량의 A p oE 가 VLDL 에서 발견된다 . 226 ) VLDL 이 lip o pr o te i n lip a se 에 노출이 되 면 대 부분의 Ap o E 는 부분적으로 분해된 입자로 남아 있게 된다. A p oE 의 함량이 높은 단백질의 약 70% 가 지방분해가 이루어지고 난 후의 입자와 결합되 어 서 발견 된다. 171-2) 정 상인의 혈 청 내 pre -beta mobil it y 의 VLDL 에 서 는 Ap o E 양이 증가된다. 219),222) 그러 므로 Ap o E 는 중간 Iip o pr o te i n 의 ap o pr o te i n 함량에 현저한 공헌이 있을 것으로 본다. 그러나 아직까지 극히 소 량의 A p oE 가 LDL 내에서 발견된다. A p oE 는 LDL 을 형성하거 전에 중간 lip o pr o te i n 범 위 에 서 이 동되 거 나 또는 일부의 IDL 입 자내 에 다량 촌재하며 이는 순환혈액으로 소멀되어서 LDL 로 전환되는 지에 대해서는 알려져 있지 않다. 쥐에 있어서 12 인동위원소로 처리 된 VLDL 로부터 A p oE 를 HDL 로 이동시키는 것에 의해서 VLDL 이 분해되어진다 .1 7 5-6) 그러나 이동되어지는 양을 분석하기는 불가 능하다. 1 피동위원소 처리된 A p oE 가 다량 함유된 사람의 VLDL 의 단백질 부위를 사람의 혈청과 혼합해 보면 동위원소 활성의 20 %가 VLDL 에 서 발견되 며 50% 는 HDL 그리 고 30% 는 혈청 단백 질
〉1. 21 g /ml 범위 것에서 발견되는 것은 홍미로운사실이다 .169) 쥐의 실험걷과에서도 이와 유사한 실험을 했을 때 동위원소의 혈청 내 분 · 포는 15%, 30% 그리고 55% 가 VLDL, HDL 그리고 밀도가 1. 21g / ml 입 자에 서 각각 나타났다. 175) 사람에게서 연구되어진 바에 의하면 VLDL 내에서 A p oE 의 분 해 와 합성 물(t urnover ra t e) 은 Ap o C 의 것 과 유사하다고 하였 다. 228} 이상의 연구에서 종합해 보면 A p oE 는 신생 HDL 입자와 함 께 순환되어 혈액내로 들 어오며 콜레스테롤의 에스텔화과정 동안에 VLDL 로 이 동된다. 그러 면 Ap o E 는 다시 HDL 로 되 돌 아가서 결과적으로 A p oE 의 대사는 혈청내에서 결국 A p oC 와 유사하게 된다. A p oE 의 역할이 중성지방 함량이 높은 VLDL 이나 IDL 입자내 에서 무엇인지에 대해서도 결정되어야 할 분야로 남아 있다. 그리 고, A p oE 의 합성과 분해율에 대해서는 더 연구되어야 한다. (5) Ap ol i po p ro te i n D (Thin lin e pro te i n ) Ap o D 는 일명 thi n lin e 단백 질 이 타고 하며 이 는 HDL3 로부터 유 리 되 었고 이 의 분자량은 22, 700dalto n 이 다. 229> Ap o D 는 HDL 밀도 법위내에 존재하는 단백질 중에 소량의 단백질이다. A p oD 에 부과 해서 A p oA-][ 가 역시 HDL 로부터 유리된 th in li ne 단백질로 이 름지어전다 .230) 그러나 A p oA-][ 는 A p oD 와 다르다. A p oD 에는 아미노산인 c y s ti ne 이 결핍되어 있다. Kos t ner232) 는 사람의 Ap o HDL 에 서 sep h adex 와 DEAE cellulose 로 chromato g ra p h y 에 의 해 서 thi n lin e 단백 질을 유리 했 다. 이 는 glu coasmi ne 을 함유하고 있 으며 COOH 끝의 아마 노산은 serin e 으로 판명되었다. 그러나 Kos t ner 는 이를 A p oA-][ 로 정의하였다. 그 리고 Kos t ner 는 이 단백질이 LCAT 의 활성제라고 보고하였다. 233) 또한 이 단백질을 HDL 에서 LCAT 작용 후에 형성되는 lys olecit hi n e 의 특정한 이동체로 제시하였다 .234)
(6) 기 타 Ap o lip o p r ote i n 요츠음 새 로운 ap o li po p ro te i n F 71- HDL 내 에 촌재 한다고 보고되 었 으며 이 의 분자량은 26, 000~30, ooo dalto n 이 다• 2m Ap o F 와 지 방과의 결합상태는 HDL 내에서 연구되어져야 한다 .215) 5 Lipo p ro te i n 구조의 모델 L ip o p ro t c i n 입자내 구성단백질의 위치와 지방의 비교위치는 확 실히 모른다. 물리화학적인 문제는 수용액 중에서 물에 불용인 지 방이 비 국성 (non• p olar) 을 유지 하는 것 이 다. 중성 지 방 함량이 높은. . 입자, 즉 VLDL 이나 ch y lom ic ron 에 대해서 중성지방의 핵십체를 구상해 볼 수 있다. 이러한 모델에서 중성지방과 콜레스데몰 este r 는 중십부에 우1 치하며 인지방, 콜레스테를 그리고 단백질은 표면 에 위치하게 된다 .16),33>,23s-1) Gus t a fs en23s) 은 단백질, 인지방, 유리 콜레스데몰의 양온 그 lipo p r ote i n , 즉 VLDL 표면을 덮기에 충분한 양이 존재 한다고 하였 다. 한편 Adam239) 은 중성 지 방이 lip o p ro te i n 입 자로부터 lip o p r ote i n , l ip ase 의 작용에 의해서 이동되면 입자의 크기가 길어지고 따라서 표면적도 좁아지니까 LCAT 에 의해서 표면적 물질인 콜레스데몰 로 이동된다고 제시하였다. 또 한편 고지방식을 섭취함으로 인해서 지방이 축적되떤 중성지 방의 가수분해가 일어나게 되어 VLDL 과 HDL 사이에서 Ap o C 가· 이동됨으로써 중성지방 입자의 크기를 조철할 수도 있다고 본다. 이때에도 반드시 인지방이 동반하지 않을 수도 있다. (1) LDL 모델 LDL 의 모델구조도 다음의 여러가지 측정방법의 결과 만들어찬 것 이 다. small ang le X-ray scatt er in g , 240) NMR 측정 , 241) 전자현마,
경 관찰 49),242-3) 중성자 확산장치 (neutr o n scatt er in g tec hniq u e)244 > 그 리고 이론적인 고려 등에 의하여 제시되었다 .245) Mate u 와 그의 동료는 2 l0) LDL 입 자의 sm: 1!1 ang le scatt er in g 연 구 에서 다음과 같이 결론지었다. LDL 입자내에는 전자의 분포밀도상 태가 높은 곳과 낮은 곳이 있는데 이 두 전자일도는 중간 밀도 부 위에 의해서 구분지어진다고 하였다. 이 방법에 의하면 이 연구자 논 전자밀도가 높은 부위 안과 밖에 단백질이 존재한다고 하였다. 그래서 이 전자에 의해서 LDL 모델(그립 5B 참조)을 재시하였다. 즉 인지방입자에는 b i la y er 가 있으며 이는 콜레스대문 este r , 콜레스 테를 그리고 중성지방이 이 인지방 b i la y er 에 참여한다고 하었다. 그리고 이 b i la y er 는 단백질주위를 둘러싼다고 하였다. 그리고 이 들은 다시 LDL 입 자를 중성 자 확산장치 (neutr on -dif fra cti on tec hniq u e) 에 의해서 관찰하였는데 LDL 입자 중십부에는 주로 지방의 hy d ro- carbon 이 존재 한다고 하였 다. 244) 또 한편 Fin e r 와 그의 동료들은 NMR Sp e ctr o scop y 에 의 해 서 241 ) LDL 입자내의 지방과 단백질 존재부위에 대해서 연구하였다 .241) 이 결과 LDL 입자는 t r i la y er 구조를 가지고 있으며 이는 단백질 주년 울 둘러싸고 있다고 하였다(그립 5A 참조).
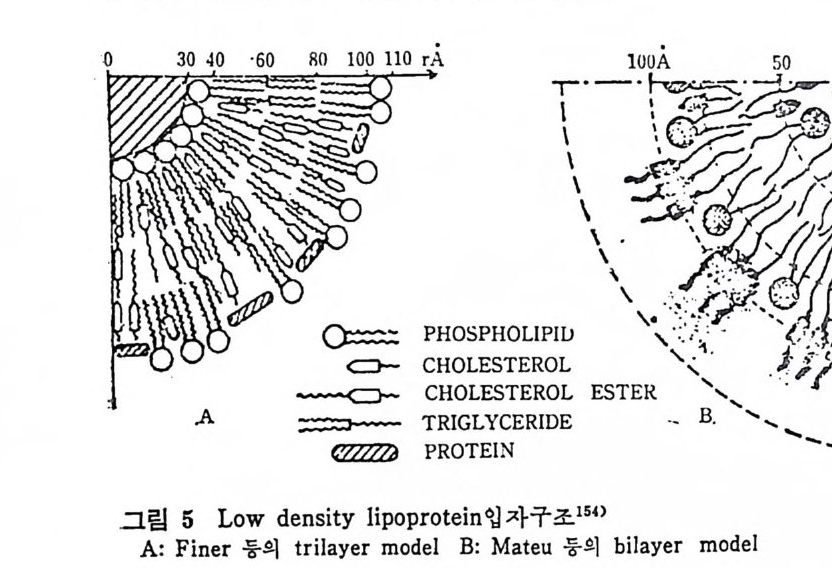 .A -=-=--
.A -=-=--
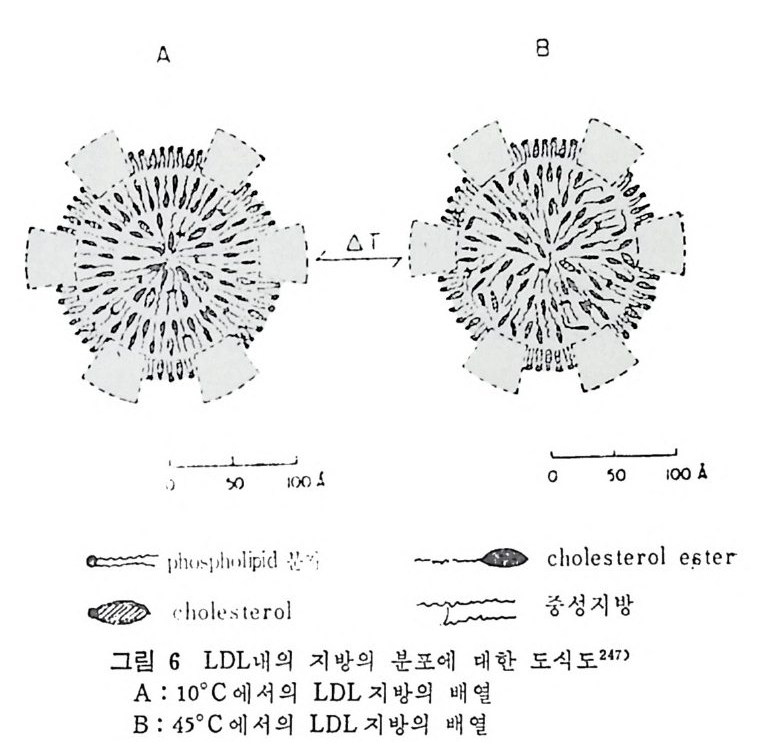 8
8
사 람 의 혈 장내의 LDL 입자구조와 치방의 상호작용에 대해서 tt7 mp e ratu re-dep e ndent tec hniq u e 에 의 하여 연구하였 다. 247) LDL 분 자는 온도변화에 따라서 분자내의 여러 구성성분의 배열상태가 달 타진다고 한다. 다음의 그림은 LDL 내의 지방의 분포현 황 이다(그림 6 참 조). 온도 가 10° c 이하에서는 LDL 분자내의 구성성분의 배열에 변화가 오지 않는다. 콜 레스테롤 es t er 그림에서 보여주듯이 약 36A 의 두께로 집중적으로 찰 배열되어 있다(그림 6A 참 조). 그러나 온도가 상승함 에 따라서 LDL 분자의 변질이 오며 분자내의 지방의 배열의 정연한 이 없어진다. 45°c 에서는 그립에서 보여주듯이 콜레스테롤 este r - 충이 무질서해졌으나(그립 6B 참조) 그러나 그 무질서의 정도에 있 어서는 지방분자의 온도에 어떤 제약이 있는 것으로 보인다. 그림 6A 와 6B 에서 보듯이 LDL 분자내에는 콜레스테롤 es t er 가 주요
치방구성성분이라고 볼 수 있다. LDL 지방의 약 18% 만이 유리콜레스데몰이며 LDL 의 중성지방의 대부분이 콜레스테롤 es t er 에 포함되어 있다. 대개의 인지방과 15% 의 유리 콜레 스데 몰이 LDL 분자의 바깥쪽에 존재 하면서 콜레 스테 롤 -es te r 주변을 둘러 싸고 있 다. 그러나 인지방과 유리콜레스테롤 두 성분이 모든 콜레스데푼 es- t er 의 외각을 둘러쌀 수는 없다. 그러므로 LDL 분자의 외각에는 .-apo pr ote i n B 와 국성 지 방이 상호작용하고 있 다고 할 수 있 다. 248-9) (2) HDL 모델 몇 종류의 HDL 모델이 알려 졌 다. low-ang le X-ray scatt er in g 에 의 해 서 HDL 입 자를 관찰해 보면 HDL2 와 HDL3 에 는 두 부분에 서 전 자밀도에 있어서 현저한 차이를 볼 수 있다 .250-4) HDL2 는 중심부위가 있고 이의 반경이 43A 이다. 그리고 의각을 둘러싼 부위가 있으며 이의 반경이 14A 이다. 이곳 의각에 수산화 된 인지방과 단백질이 있다. 인지방의 국성부위(p olar head) 의 넓이 가 약 11A 이며 255) 이 부위가 최의각에 촌재하는 것으로 보인다. 최 외 각에 존재하는 인지 방의 극성 (po lar) gro up 의 상호작용은 다음 그 립에 제시되었다(그립 7 참조). 다음의 그립 은 ap o lip o pr o te i n 과 ph osph ati dy lc holi ne 사이 의 상호 관련 기전을 개념적으로 도해한 것이다. 인지방 b i la y er 표면에는 양성 이 온 (zw itt er i on) 울 가전 국성 부위 군에 그 근처 에 있 던 전기 를
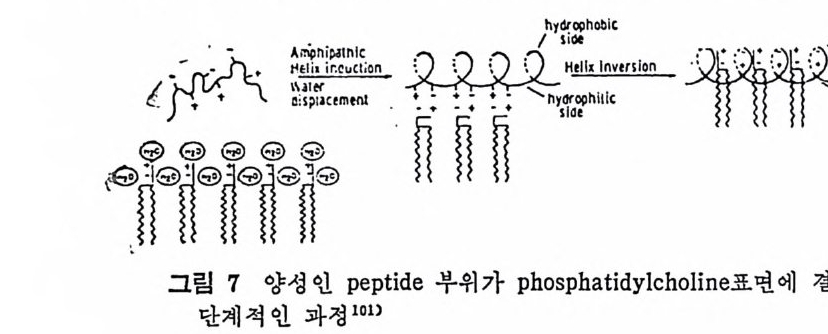 틀i『:0 『 『巴@ 三[드 [도 [ 門三'::
틀i『:0 『 『巴@ 三[드 [도 [ 門三'::
떤 (charge d) 아미 노산의 sid e chain 의 반대 이 온이 서 로 정 전기 적 인 접 근 (elec t ros t a ticall y a tt rac t)을 하게 된다. 이 러 한 접 근 (a tt rac ti on) 이 극성부위(p olar head) 에 존재하는 물분자를 이동시키며 따라서 반 대로 전기를 떤 a p o p ro t e i n 의 아미노산이 극성부위로 접근해 오면 서 he li x 를 형성한다. 그러면서 접접 강한 상호관련이 인지방의 극성부위군과 ap o p ro te i n 사이에서 생간다. 동시에 단백질의 helix 가 간 쪽을 축으로 회전하여서 지금까지 소수성 (h y dro p hob i c) 면이 밖으로 되 었 던 것 이 안쪽으로 그리 고 찬수성 (hy d rop h il ic) 떤이 밖으 로 면하게 된다. IOI ) Sto ff el 과 그의 동료들은 256-7) HDL 분자의 표면적 의 반이 단백 질 로 덮여 있고 나머지 반이 인지방의 극성부위 g rou p과 콜레스테롤 에 의 해 덮 여 서 단충 (monola y er) 으로 정 렬되 어 있는 model 율 제 시 하 고 있다(그립 8A 참조). 그리고 콜레스데몰 es t er 의 s t ero i d 핵은 입 자의 지방 부위에 존재한다. Assmann 과 그의 동료에 의 해 서 258-9) 또 다른 형 태 의 HDL 모델 이 제시되었다. 이는 지방물질이 존재하는 곳에 HDL의 단백질이
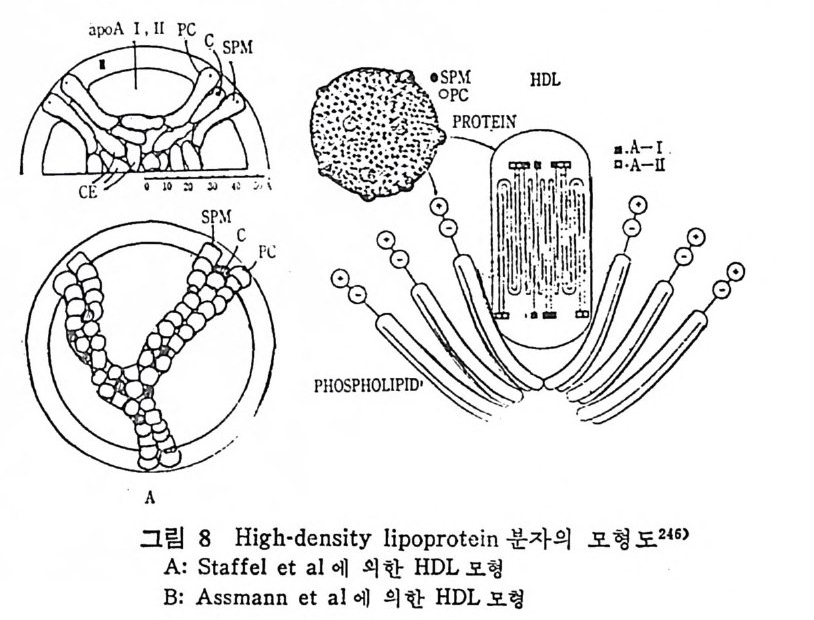 P~! HDL
P~! HDL
마치 둥둥 떠 있는 것과 같이 제시되었다. 마치도 막 (membrane) 구조의 액 체 모자이 크 모델 (mosaic model) 과 유사하게 제 시 되 었 다 260) (그립 8B 참조). 이 그림에서 보면 지방충이 있는 곳에 단백질이 표면적 껍데기에 11A 정도의 두께로 덮여 있다는 사실이 X-ray sca tt er i ng 측정 에서 나타났다. 그런데 이 모델에서 보면 단백질 입자가 지방충 내로 상 당히 깊숙이 존재한다. 앞에서도 설명하였지만 Ap o A 단백질은 인지방과 결합되면 서 a-helic a l 구조가 단백 질구조중에 서 중가된다. 76),261-5) 이 ap o p r ote i n 은 인지방 없이는 중성지방과 결합이 거의 이루어지지 않기 때문에 분자내 의 인지 방이 대 단히 중요한 역 할을 담당하는 것 으로본다. 266-9) 모델 빌 딩 (buil din g ) 구조연구에 기 초를 두어 a-helix confo r mati on 형 성 이 인지 방과 ap op ro te i n 과의 결합을 위한 기 본적 인 기 전이 된 다고 본다면 heli ca l 구조의 어 떤 묵정 부위 가 Ap o A 와 Ap o C 의 인 지 방과의 결합부위 라고 제 시 된다. 270)
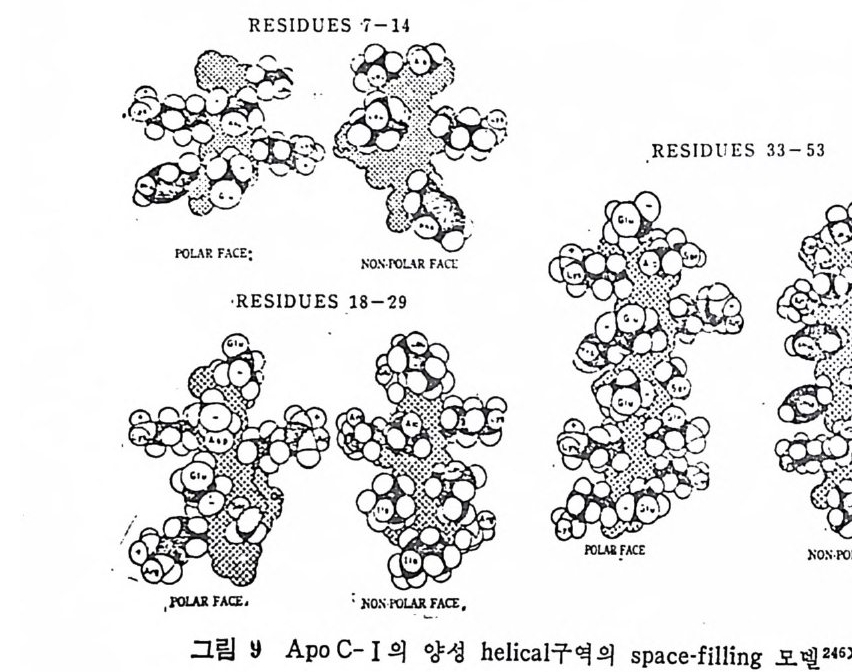 POLIR F.\ C E. 誕 숨〔E g닝홑品『?언_RESIDUES 33-53
POLIR F.\ C E. 誕 숨〔E g닝홑品『?언_RESIDUES 33-53
Hel i x 구조의 단백질은 국성면과 비극성 (non- p olar) 면, 즉 양면을 다 가지고 있다(그립 9 참조). 이 양성 (am phe p a t h ic) hel i x 의 극성면 에는 고도로 유별난 표면의 분포가 있다. 즉 전기를 떤 아미노산 인 glu ta m i n 과 asp a rt ic acid 가 국성 중십 에 존재 하며 한편 ( + ) charge 가 있 는 lys i n e 과 argi ni n e 은 국성 면과 비 극성 면 중간 위 치 의 분자 끝부분에 존재한다. 이러한 아미노산의 분포 상태가 인지 방과 단백 질 분자 사이 의 전기 상호결합 (elec t ros t a ti c a tt rac ti on) 을 유 발하게 된다. Jac kson 과 그의 동료는 amp h ip a th i c heli x the ory 에 기 초하여 서 HDL 모델을 재 안하였 다. 101 ) 이 모델에서 보면 단백질은 HDL 입자표면에 퍼져 있으며 인지방 의 국성부위 g rou p과 끊임없이 상호작용을 하고 있다. 이러한 종 류의 단백 질의 3 차구조(t er ti ar y str uc t ure) 는 ap o p ro te i n 이 구부러 져 서 HDL 입자 표면의 굽은 부위에 알맞도록 되어야 한다(그립 lOA 참조). HDL 의 주요 단백질인 A p oA-I 은 그 분자내 아미노산 나 열 중에 규칙 적 으로 단백 질이 64, 103, 124, 146, 168, 212 그리 고 223
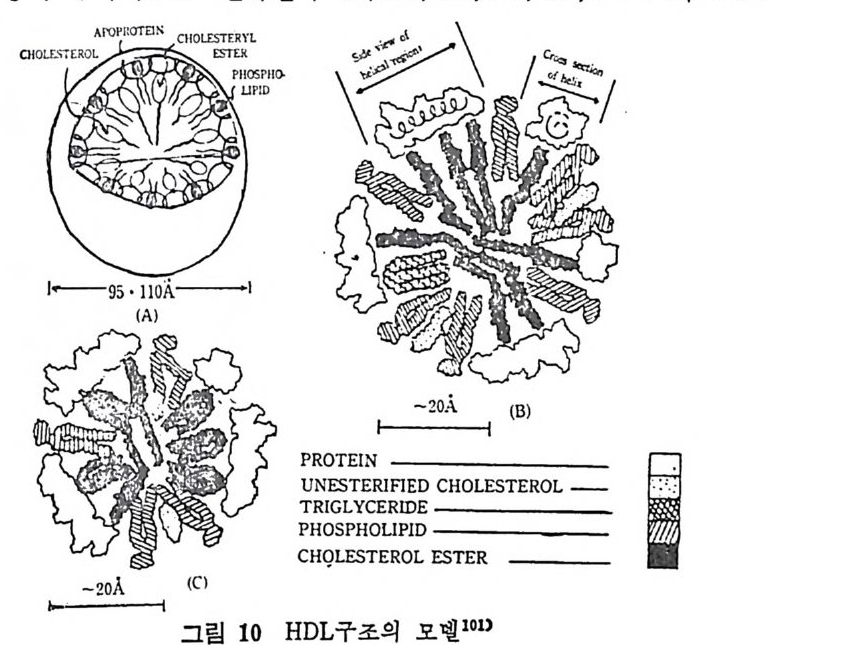 Ic— 95 • l lOA .- I
Ic— 95 • l lOA .- I
번째에 위치하고 있어서 po lyp e p tidy l cha i n271) 의 갑작스런 방향년 화에 충분한 적응이 될 수 있다고 본다. Verder y와 N i chols 2 72) 는 HDL2 와 HDL3 의 모델(그림 10 B,C 참조 ) 을 구상하였 다. 이 두 물질은 특 히 콜레 스데 몰 este r 의 분자구조 (con fo rma ti on) 에 주로 차이가 있다. 입자의 크기가 HDL3 에 비해서 큰 HDL2 는 콜레스테롤 es t er 가 길게 뻗어질 수 있는 공간의 여유 가 있으나(그립 10 B 참조) 아에 미해서 HDL3 는 공간의 여유가 제 한되어 있기 때문에 입자 중심부인 a p olar 부위에서 acy l cha i n 이 s t ero i d 핵 위에 차곡차곡 접혀져서 촌재하고 있다. 이 부분이 콜 레스테롤 es t er 의 주요 부위이다(그림 lOC 참조). (3) VLDL 모델 VLDL 입자내의 지방과 단백질이 어떤 형대로 결합되어서 촌재하 는지에 대해서는 아직까지 연구가 불충분하다. 여러가지 단백질과 지방과의 비교결합연구에서 제시된 바에 의하면 A p oC-][ 는 보다 국성 지 방과 상호작용을 하는데 묵히 ph osph ati dy !ch olin e 과 sph in g - oroy e li n 과 상호작용이 있으며 중성 지 방인 tri o l ein 이 콜레 스테 롤 oleate 오뚝 관련이 희 박하다. 273) VLDL 을 효소 neura mi n i dase 로 처리하면 입자에 함유된 95% 의 sia l ic aci d 가 유지 되 는 결과를 초래 한다. 274) 이 결 과로 VLDL 입 자내 에 ap o pr o te i n 의 당단백 질 (gly c o p ro t ei n ) 부위 가 지 방과 수용액 단면 근처에 촌재하고 있음이 제안되었다 .274) 또한 VLDL 입자내에 비교적 다량 함유된 단백질 약 10% 나 인지방 약 19% 는 입자의 최 외각 주변에 함께 촌재하며 내부에는 중성지방 함량의 약 50% 가 함유되어 있다 .275) 콜레스테롤 es t er 는 함량이 약 10% 정도이며 중 성지방이 촌재하는 부위에 무작위로 분포되어 있다. NMR da t a 에 의하면 275-n VLDL 입자내에는 콜레스데몰 es t er 가 LDL 입자내에서처럼 지방과 함께 나열되어 촌재하지 않는다. LDL 내 의 콜레 스테 를 este r 의 나열은 X-ray scatt er i ng 방법 에 의 해 서 연 구되 었 다(그립 11 참조).
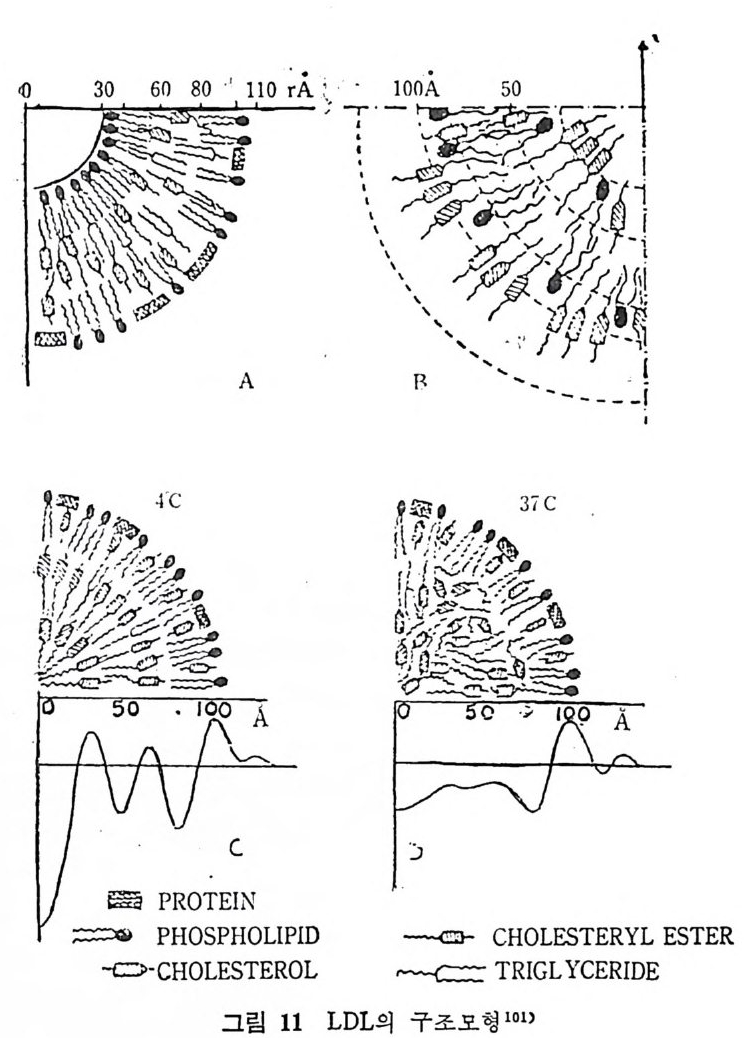 , ..‘‘. .
, ..‘‘. .
VLDL 입자내의 구성성분의 배열은 그림 12 에 요약되어 있다. 그림 에 서 나열 된 VLDL 구성 성 분의 분포로 미 루어 보면 `lip o p r o- tei n l ip ase 가 이의 활성제인 A p oC-Il 단백질에 쉽게 접근할 수 있 게 배 열 되 어 있 으며 , 또한 LCAT 가 ph osp h ati dy lc holi ne 에 쉽 게 접근할 수 있고, 또한 콜레스테롤의 분해가 쉽게 이루어질 수 있게
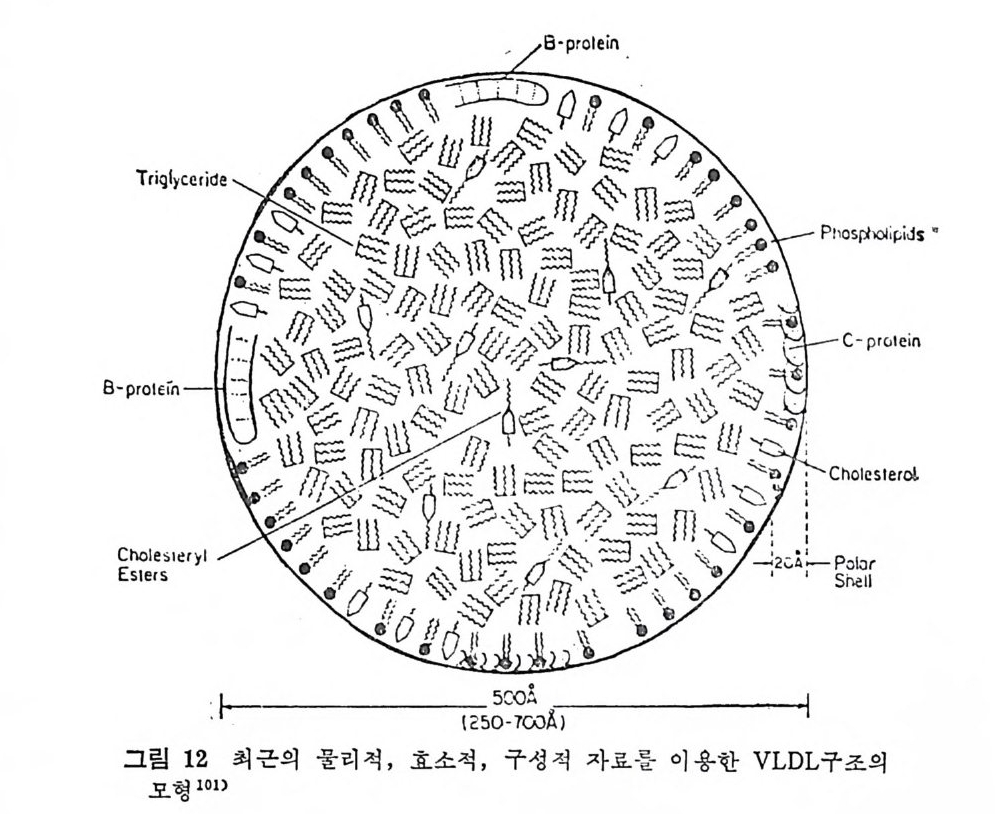 B -그pT 림모.cInge 형-l ye1c l 21l血ryr一e0I .E1I )S on최-/軒 근e의 rh I 言망《}s 물 f /B /&낱군리o f 적 ,를〉i 信% S 효令多冠r 소적I\〔:二〔2 5, 05- 7구®CA/성O/`¢ 홋A》를 적 -) g广언》〔广자 료 룹〈三llIl 炳 多 이 田출 巳용 \、 ~ 한`-7〈 如〈V L '포,':':솁D L 구c1P조o oSlOnel 이 -s lp의 cp 5 . 中lCer j.d야 CrIn s `I2 hsI
B -그pT 림모.cInge 형-l ye1c l 21l血ryr一e0I .E1I )S on최-/軒 근e의 rh I 言망《}s 물 f /B /&낱군리o f 적 ,를〉i 信% S 효令多冠r 소적I\〔:二〔2 5, 05- 7구®CA/성O/`¢ 홋A》를 적 -) g广언》〔广자 료 룹〈三llIl 炳 多 이 田출 巳용 \、 ~ 한`-7〈 如〈V L '포,':':솁D L 구c1P조o oSlOnel 이 -s lp의 cp 5 . 中lCer j.d야 CrIn s `I2 hsI
되어 있다. VLDL 입 자내 의 지 방의 유동화(fl u i d ity)현상은 TEMPO pa ramag - ne ti cresonance 방법에 의해서 연구되었는데 그 결과는 0 ° c 에서 40° C 사이에서는 유동화경향이 직선적으로 계속 증가현상을 보였으나 40°c 이상에서는 더이상의 증가가 없었다고 보고되었다 .278) VLDL 구성성분의 질적인 변화와 구성성분의 정렬상태를 섭취하 는 식 사내 의 지 방종류에 따라서 관찰하였 다. VLDL 입 자내 의 acy l cha i n 의 정렬 (order) 은 고도의 불포화지방산을 소량 섭취한 (P/X= 4.0) 사람의 입자가 고도의 포화지방산율 섭취한 (P/S=o.25) 사람 의 입자보다 덜 정렬이 되어 있다 .278) In v it ro 실험에서 VLDL 의 분해울은 입자의 유동화정도에 의존 된다고 하였 다. lipo p ro te i n lip a se 는 보다 유동화되 어 있 는 불포화-
지 방산을 함유한 중성 지 방보다 빠르게 분해한다고 제 시 하였 다• 278) 따라서 lip o p ro te i n lip a se 의 활성은 VLDL 과 같은 여러 종류의 lip id 가 섞여 있는 입자에 작용하여서 보다 고도의 불포화지방산을 유리 시 킨다고 한다. 그러 면 lip u pr o te i n lip a se 가 작용하고 난 후의 남 은 VLDL 입 자는 보다 높은 mi cr oscop ic 접 도를 함유하게 된다. (4 ) Lip o pr ote i n X 모델 t I F 감 상 lipo pr o te i n X 는 많은 흥 미 률 끌고 있 는 lip o p ro te i n 이 다. 이 lip o p ro te i n 은 lecit hi n cholest e r ol ac y l t rans fe rase(LCAT) 가 부 족된 사 람 이거나 또는 대사방해로 생기는 간명환자의 혈청에서 발 견 된다. 289) LP-X 는 다른 lip o pr o te i n 이 갖지 않은 독특한 단백 질을 및 층류 함유하고 있다 .281) 이의 지방구성을 보면 약 25% 가 전칙 으로 unes t er ifi ed 된 콜레스테롤이며 약 65% 가 인지방이고 6% 정도 가 단백 질로 단백 질의 함량은 비 교적 낮다. LP-X 의 ap op r o te i n 의 구성을 살펴보면 독특하여서 약 4 0% 가 album i n 으로 되어 있다. 그리고 나머지 60% 의 단백질은 대부분이 A p oC 이며 소량아 Ap o A 기 , Ap o D 그리 고 Ap o E 이 다. LP- X 내 의 anti ge nic 부위 인 al- bumi n, A p oC 게 그리고 A p oC - 1[는 정상적으로 덮여져 있다. 그 러나 부분적으로 덮여 있지 않은 곳이 있다 .2S2) 이와 대조적으로 anti ap o C- I 과 anti Ap o D 는 LP-X 와 쉽 게 작용한다. LP-X 구조의 대략의 모델은(그립 13 참조) 직경이 다양한 구형으 로 albumi n, Ap o C-II 와 Ap o C_ m는 내 부에 파묻혀 있 으며 한편 Ap o C-I 과 Ap o D 는 표면에 크게 노출되어 있다. 또한 인지방의 분포가 바대칭으로 분포되어 있는 b i la y er 에 대한 연 구도 되 어 있 다. small ang le X-ray scatt er in g 방법 에 의 해 서 LP -X 의 bil a y er 내 의 인지 방분포가 연구되 었 다• 283) Pa t sch 와 그의 동료는 대사방해로 발생된 간병환자의 혈청내에 서 LP-X 를 자세 히 분석 하여 284) 3 가지 종류의 LP-X 를 분리 하였 다. LP-X1(d=l . 038g /m l ), LP-Xz (d =l. 049 g /ml) 와 LP-X3(d=l . 058 g /ml) 가 초원십분리에 의해서 분리되었다. 이 세 종류 모두 인지방의 함량
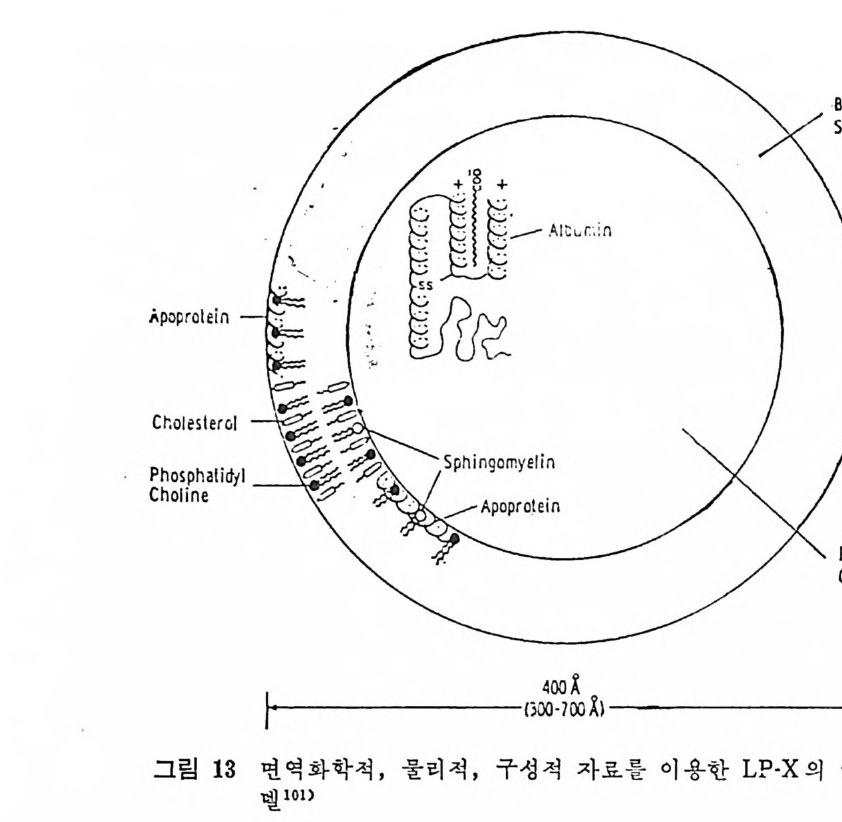 Bil Jy e t·
Bil Jy e t·
이 높고 (65%) 유리콜레스테몰도 높으나 (25%) 중성지방은 낮다 (~$ % 정도 ).LP-X1,2,3 모두에 함유되어 있는 단백질은 대부분이 a-helic a l 구조를 가진 것이며 (41~65%) 지방부분의 유동화 경향은 낮다 고 한 다. 이 세 종류 모두 albumi n 과 C-p e pt i d e 를 함유하였 지 만 LP-X1, 2 만이 A p oA-I 과 A p oE 를 함유하였다. 6 Lip o p ro te i n 대 사 혈청 lipo pr o te i n 은 지 방과 단백 질 복합체 로서 이 는 순환하는 혈 액 중에서 지방울 이동시키며 도한 지방의 합성과 분해를 조절한다. 다음의 표 6 은 사람의 혈청내 Iip o p ro t e i n 의 구성과 특성을 요약한· 것이다.
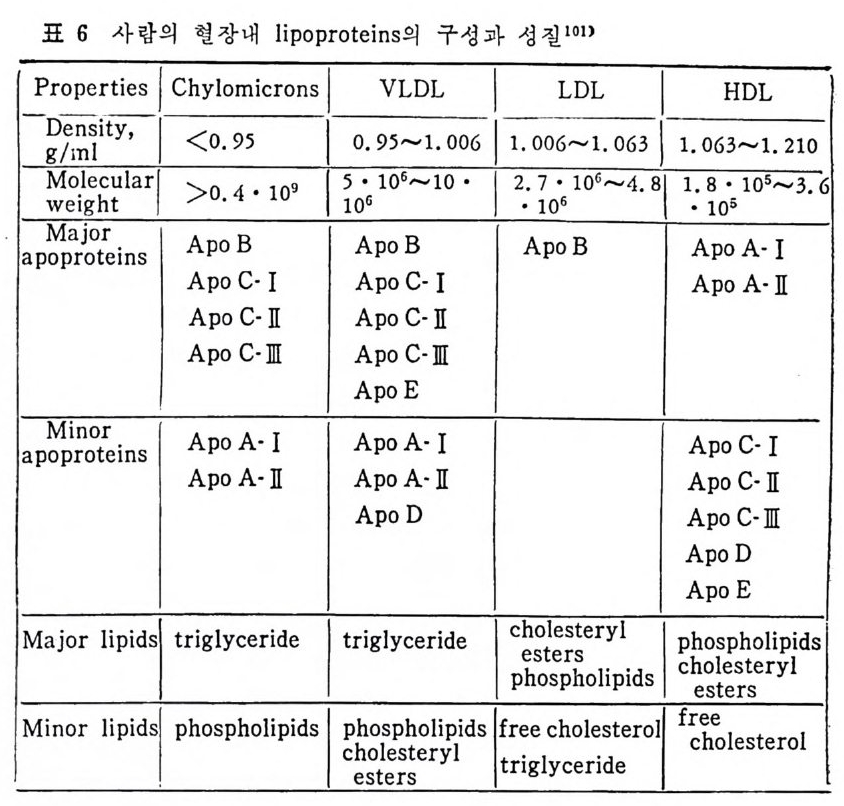 표 6 사람의 형장내 Iip o p ro t e i ns 의 구성과 성질 101)
표 6 사람의 형장내 Iip o p ro t e i ns 의 구성과 성질 101)
( 1 ) Lip o p ro t e i n 의 합성 1) Chy lo rnic r on 합성 1962 년에 Dole 과 Ham li n32) 이 chy lo mi cro n 대 사에 관하여 명 료하 게 발표하였다. 식이지방의 흡수는 주로 소장의 윗부위에서 일어나 며 장내용물이 회장(i leum) 에 도달하기 전에 설제적인 흡수는 끝난 다 .285) T ytg a t와 그의 동료에 의한 형태학적 또한 생화학적 연구 결과 사람의 ch y lom ic ron 합성부위는 공장접막(j e j una! mucosa) 이라 는 것 이 밝혀 졌 다. 286) 실험 적 으로 공장(j e j unum) 을 데 어 내 어 관찰해 보면 중성 지 방 este r yf ying 효소의 활성 이 회장에 서 감소되 어 있으 며 또한 fatty ac id CoA lipa se 와 acy l- CoA monog ly c eri de acy l-
tra nsfe r ase 도 감소되 어 있 다• 287) 중성지방의 흡수와 체내 이동에 관한 뒤어난 문헌고찰이 많이 있 다. 33),288- 90 ) 지 방의 장내 흡수 주요 경 로 는 다 음 과 같다. 식사에서 섭취한 중성지방은 위장내에서 부 분적 으 로 유화되어서 인지방과 혼합되어 하나의 작은 구 문 형성하며 담즙염 이 존 재함으 로써 가수분해된다. 위장내에서 지방이 부 분 적 으로 가 수분 해되는 것이 바로 식이 중성지방 홍 수의 첫단계이다 . 293 ) 소장 세 포 에 의해 서 중성지방이 취해지는 윤은 치방산의 사 슬건 이에 닫러 있 다 . 2 9 - I J 중간 사슬길이의 지방산을 함유한 중성 지 방이 긴 사슬 지 방산 함유 중성지방보다 장내막 세포에 의한 흡 수가 빠르다. 중 성 지 방에 길합 된 지방산의 탄소수가 10 개 이하인 중성지방은 지방산 분리 를 위한 가수분해 과정을 거치지 않고도 흡수된다. 사슬이 간 지방산을 함유한 중성지방은 철대로 흡 수가 그대로 이 루어지지 않으며, 중성지방의 1 과 3 번 위치의 지방 산 이 가수분해되 어 서 두 분자의 유리 지 방산과 2-mono g l y cer i de 가 되 어 야 홍 수가 일 어 난다. 결합되어전 담줍염 (conju g a t e d bile sal t)이 촌재하면 2-mono- gl yc erid e 는 mi ce llar 용엑 울 소장벽 에 서 만든다. mi ce llar 구가 소 장내막세포내로 스며들어가는 것은 단순한 확산에 의해서 이루어 진다 .295) 일단 장내막세포내로 들어갔으면 유리지방산과 2-mono 중 성 지 방은 다시 중성 지 방으로 Smooth Endop la smi c Reti cu lum(SER) 내 에 서 재 결 합된다. 295) 쥐 의 chy lo mi cr on 입 자내 의 인지 방에 결 합된 치방산은 섭취된 지방산의 종류에 따라서 다르지만 그러나 대부분 의 chy lo mi cr on 의 인지 방은 이 미 po ol 에 촌재 하던 장내 악세 포내 의 인지 방으로 구성 이 된다. 296) 전자현미 경 관찰에 서 밝힌 바와 같이 SER이 새로이 합성된 중성지방의 이동에 공헌하는 주요 세포부위 라고 하였 다. 그리 고 SER 내 에 서 chy lo mi cr on 합성 이 완성 된다고 제 시 하였 다. 295),29“ 유사하게 도 Ap o B 의 합성 과 기 타 림 프의 chy - !omi cro n 내 에 함유된 단백 질 합성 은 거 의 Roug h Endop la smi c Reti - culum(RER) 의 rib o some 에 서 이 루어 전다고 본다. Sabastin 과 Isselbacher298) 는 기 본적 인 연 구를 하였 다. 쥐 에 게 욱 수수 기름을 먹이면서 단백질 합성의 방해물질인 p urom y c i n 을 합
께 두여하였다. 그 결과 쥐의 장내막 세포내에 지방이 축적되어 있 으며 그리고 혈청내 에는 중성지방 함량이 감소되어 있었다. pu ro- my c in 두여 로 단백 질 생 합성 이 방해 를 받아서 chy lo mi cr on 합성 의 마지막 단계인 단백질과의 결합이 이루어지지 않아서 생간 현상이 라고 하였 다• 그러 나 Redg ra ne 과 Eil v ersmi t 299) 는 혈청 내 동위 원 소 처리된 중성지방 출현에는 표준군이나 p urom y c i n 으로처리된 군 이나 차이가 없었다고 지적하였다. 이 발견은 사실 p urom y c i n 두여 로 ch y lom i cron 형성에 아무런 지장이 없었던 것으로 보며 중성지 방의 축 걱이 오히려 p urom y c i n 으로 인해서 감소되었다고 하였다. 이 사실은 간세포내에서 내자 (endo g enous) 로서 지방합성에 영향을 미 찬 것 으로 본다. pu romy c in 이 위 내 용물이 위장을 비 우는 울(g as t r i c ·em p tying ra t e) 을 감소시 키 며 298) 그리 고 중성 지 방 흡수울을 감소시 킨 다고 하였다. 다른 연 구에 서 Redg ra ne 은 300> acti no my c in D 와 cy c lohexami de 도 지방홍수에 아무런 손상을 주지 않았으며 단지 두여된 약의 양 이 커 지 면 (300mg / ra t) 림 프의 흐름양을 감소시 키 거 나 흡수불능을 초 래하기 때문이라고 설명하였다. Glic k man 은 단백질 합성 방해물 질의 두여가 과연 지방흡수에 영향을 미치는지에 대해서 연구하였 다. 301) 그 결과 chy lo mi cro n 의 크기 가 신속하게 증가되 기 도 하고 한편 천천히 증가되 기 도 하는 현상이 동물에 게 aceto x y c y c lohexa- m i de 를 두여하고 난 후에 관찰되었다. 이 결과를 가지고 chy lo mi - cron 의 크기가 중가되면 표면적 물질의 철약이 된다고 해석하였다. 그래서 적은 양의 표면물질로 보다 많은 중성지방울 림프로 이동할 수 있게 한다는 것이다. 그러나 한편 장내막에서의 ap o p ro t e in생산 과 chy lo mi cr on 입 자의 크기 와의 관계 를 보면 상호관련이 없는 것 으로 나타났다. 그러 나 Glic k man 과 K i rsch302) 는 결국 aceto xy c y c lo- hexami de 를 쥐 에 게 두여 함으로 chy lo mi cr on 내 여 러 가지 ap o p ro - tei n 중 주요한 한 가지, 죽 Ap o A-I 의 합성이 저하되며 이 쥐에 게 서 다른 종류의 ap o p ro te i n 은 정 상량 촌재 하는 것 으로 보고하였 다. 그러 나 Ap o A-I 의 결핍 으로 chy lo mi cro n 의 크기 가 증가되 거나 또는 지방흡수가 감소되는지에 대한 의문은 아직까지 풀리지
않고 있다. 단백질합성 방해물질들이 또한 RER 과 g ol gi막에 영향을 끼찬 다고 한다 .297) 실형동물 쥐를 p urom yci n 으로 처리하면 장내세포내 에 큰 치방구가 축적되는 결과를 초래하며 세포 내부의 세부구조 (or g anells) 를 감소시킨다고 하였다. 일반적으로 지방흡수시에는 RE R 과 SER 의 보존이 잘 되며 아울러서 중성지방 재합성에 요구되 는 효소들의 활성 을 보촌한다. Red g rane303) 은 흡수세포로부터 지방이 유출되는 가능한 2 가지 기 전을 제시하였다. 첫째는 지방울 함유한 SER 구조가 원형질막에 영 합되 어 서 역 pino cy tos is 가 일어 나거 나 또는 exocy tos is 에 의 해 서 세포간질 공간으로 지방이 이동되는 것이다. 둘째는 막 channels 에 의해서 지방이 유출되는 것이다. 그런데 많은 연구자들은 첫번째 제안에 보다 많은 홍미를 보인다 .305-6) 첫번째 기전에서는 go lg i 막이 p rech y lom i cron 을 쌓아서 원형질막과 연합함으로써 chy lo m- i cron 이 세포 밖으로 이동된다고 본다. 이 연합과정에 관련된 효소 는 ph osp h olip a se A, ph osp h olip a se B 그리 고 중성 지 방 lipa se 로 서 이들은 g ol gi막에 존재한다 .306-7) 이들 효소의 조철기전은 찰 알려 져 있 지 않다. go lgi 구조내 에 서 ph osp h oli pa se 활성 의 감소라돈 지 또는 새로운 인지방의 합성은 ch y lom ic ron 의 크기가 커지는 요 인이 되 기 도 한다. 301) 일단 세 포로부터 유리 된 chy lo mi cr on 은 lac- tea l 로 이 동되 어 서 림 프 channel 에 모여 져 th oracic 관을 통해 서 순 환계로 들어간다. 2) VLDL 합성 간과 소장에서 동위원소로 처리된 아미노산이 VLDL 의 단백질 로 영합되고 있음이 알려졌다. 소장이 혈장내 VLDL 의 급원이라고 처 음으로 제 안한 사람은 Roheim 과 그의 동료 308) 이 며 그리 고 이 사 실이 몇 몇 실험 실에 서 확인되 었 다. 309-12) 또 한편 소장과 간 p er fu s i on 실험에서 동위원소로 처리된 아미노 산이 VLDL 과 HDL 에만 영합이 되고 LDL 에는 되지 않음아 밝혀 졌 다. 313-5> pe rfu s ed 된 소장과 림 프의 Ap o C 단백 질에 서 는 방사능
활성이 나타나지 않았다. 이 결과로 Ap o C 단백질은 소장에서 합성 되지 않고 간에서 합성됨이 밝혀졌다. 장내에서 합성이 완성되는 VLDL 의 Ap o C 의 공급원은 다른 lip o p ro te i n 으로부터 이 동되 어 서 쓰인다고 생각한다. Ap o B 의 소장내 합성 은 쥐 에 게 2% oroti c acid 를 함유한 석 사를 먹임으로써 증명되었다 .31 1) 실제로 이 동물에게서는 A p oB 가 혈장 내에 본래는 없었고 mesente r ic 림프에는 정상 수준의 A p oB 가 있 었다. A p oB 의 간세포에서의 생성이나 또는 중성지방의 순환계동 으로의 유리 는 orO(ic acid 처 리 로 인해 서 완전히 막혔 었 다. Oroti c acid 뭍 먹 인 쥐 에 게 서 나타나는 대 사상태 나 abeta l ip o p ro t- e i nem i a 에 있는 사람에게서의 대사상대가 어떤 유사함을 나타내었 다. 이 때 에 나타난 abeta l ip o p ro te i n e mi a 는 상당히 희 귀 한 경 우로 au t osome 이 휴식울 하고 작용하지 않는데서 생간 병이다. 이런 환 자를 30 여명 이상이나 발견하여서 그 증세에 대한 고찰을 하여 놓 은 문헌이 있 다. 317- 8) 이 환자에 게 서 는 지 방흡수불량중이 있 으며 건 사술의 지 방산이 문맥 정 맥 (po rt al vein ) 계 동으로 흡수된다. 이 환자 의 간세포내에는 큰 지방구가 촌재하며 g ol gi공포 (vacuoles) 가 거의 결핍되어 있고 SER 은 완전히 결핍되어 있다 .319) 이 환자의 chy lo - mi cro n, VLDL, 1D1320-2) 내 에 는 Ap o B 가 전혀 존재 하지 않는다. 혈청내의 중성지방과 콜레스테롤 수준은 극단적으로 낮다. 또한 HDL 농도도 비 정 상적 으로 낮다. 320-2) 또한 abeta l ip o p ro te i n e mi a 환 자에 게 서 는 LCAT 활성 이 감소되 어 있 다. 321-2) 한편 VLDL 과 chy lo mi cr on 의 여 러 가지 지 방구성 성 분은 두여 된 지 방산의 종류에 따라서 달라진다. 즉 십 이 지 장내 로 pa lmi tic acid 를 두여 하였 더 니 VLDL 과 chy lo mcir o n 내 에 중성 지 방과 콜레 스테 롤 의 농도가 증가되 었 다. 이 와는 대 조적 으로 불포화지 방산인 oleic acid 와 lin o leic acid 를 두여 하였 더 니 chy lo mi cr on 내 의 중성 지 방과 콜레스테풀의 양은 중가되었는데 VLDL 내의 콜레스데몰 양온 감소 하였고 중성지방양은 변화가 없었다. 이 결과를 보면 지방산의 포 화정 도에 따라서 장내 lip o p ro te i n 합성 에 영 향이 미 치 고 있 음을 알* 수 있다.
간과 소장은 VLDL 의 합성과 분비에서 어떤 공통접을 나타낸다. 분비 되 는 VLDL 의 입 자는 내 자와 의 자 급원의 (endog en ous & exog e- nous orig in) 유리지방산의 유용한 이용량 (ava i l ab ilty)에 의해서 영향 울 받는다. p er fu sed 된 쥐의 간에 의해서 중성지방의 축적 과 분비 는 유리지방산의 구조, 이의 농도 그리고 p er fu sed 된 시간에 의해 서 영 향을 받는다. 323-4) 그런데 acti no my c in D 는 유리 지 방산이 VLDL 내 의 중성지 방합성 을 유도하는 것 을 방지 한다고 하였 다. 323) Heim berg 와 W ilc ox 는 324 只귀 에 게 oleic acid 를 pe rfu s e 했 을 때 가 -pa lmi tic acid 를 pe rfu s e 했을 때 보다 VLDL 로부터 약 50% 나 더 많은 중성 지 방울 분비 하였 다고 하였 다. 따라서 pa lmi tic acid 를 p er fu se 했을 대 간에 의해서 분비되는 VLDL 입자내에는 olea t e 를 p er fu se 한 간에서 분비되는 VLDL 에 비해서 높은 양의 콜레스테몰 과 인지방이 높은 밀도로 함유되어 있었으며 중성지방의 양은 비교 적 낮았다. Olei c ac i d 에 의해서 콜레스테롤의 생합성이 자극되었음이 쥐의 -pe rfu s ed 7J -에 서 관찰되 었 다. 325) 이 는 VLDL 의 구성 성 분으로서 의 콜 레스데볼의 요구량에 반영이 되며 또한 간에 의해서 분비되는 중성 치 방양에 도 반영 된다고 지적 하였 다. 그런데 또 다론 연구자둘은 326-3 0) VLDL 의 콜레 스테 롤 este r 는 직 접 간으로부터 유리 되 어 서 공급된 다는 중거를 제시하였다. 그러나 HDL 의 경우는 이와 같지 않다고 치 적 하였 다. 326> in vit ro 연구에 서 보면 HDL 과 VLDL 사이 에 서 콜 레스테롤 es t er 의 교환이 일어나고 있다고 하였다. 한편 Chan 과 그의 동로는 estr o g e n 이 수닭에 게 서 VLDL 합성 을 자극한다는 결과를 보여 주었 다. 33D estr o g e n 은 Ap o VLDL-J I 문 전 이 (tr ansla ti on) 하는 m-RNA 의 양을 증가시켰으며 estr o g e n 이 전합 되RN논A 특p정o ly한m e결ra합se부 I위 과가 I급l 의하 게활 성증 이가 되증었가되다 고며 또하였한다 R.N A또 합 성이 이결 과시 작되 는 부위 (ini t iat i on s it e) 도 증가되 었 다. 332) 이 러 한 결 과는 estr o g e n 에 의 한 VLDL 합성 의 조철은 부분적 으로 유전인자의 전사(t ranscr ip 五 on) 수준에 있다고 보여진다. 간세포내에서의 VLDL이 합성되는 부 위 는 아직 까지 논쟁 중에 있 다. 333-4> Alexander 는 332) 중성 지 방과
인지방은 둘 다 SER 에서 합성되나 ap o p ro t e i n 은 독립적으로 RER 에서 합성된다고 하였다. Nestr u ck 과 Rubin s te i n 에 따르면 Ap o B 는 VLDL 입 자가 조립 될 때 첫단계로 지방과 결합한다고 하였다 .335) 이들의 견해에 의굴l 떤 Ap o C 는 우선 조립 되 고 있 는 VLDL 분자가 spa ce of dis s e 로 배설되는 동안 또는 후에 결과적으로 얻게 된다. g lucosam i ne 은 go lgi 를 동과하는 동안에 조립 되 고 있는 VLDL 분자에 영 합된다고 하였다. 336) 소장에서 유래된 VLDL 은 A p oA 를 함유하고 있는 반면에 간에 서 합성된 것은 함유하고 있지 않다고 보고되었다 . 3 37) 이를 기초로 해서 생각해 보면 VLDL 입자간에 단백질 교환이 있을 것으로 보인 다. 3) LDL 합성 LDL 의 합성과정은 VLDL 의 분해시에 자세히 논의하게 되므로 . 이 장에서는 압축해서 고찰하기로 한다. LDL 의 형성은 VLDL 이 간세포로부터 분바된 후에 형성된다고 본다. 그러나 약간의 LD L-은 간세포에서 직접 합성되기도 한다. 이 에 부과해서 ch y lom i cron 이 LPL 에 의해서 분해되고 난 후 나머지 가 LDL 의 한 가지 급원으로 생 각해 볼 수 있 다. chy lo mi cr on 내 의 Ap o B 의 함량이 o. 1~0. 5% 이 므로 이 것 이 또한 순환하고 있는 혈 액으로 들어오면 질량의 10~15% 가 A p oB 로 된다. 이러한 상황하에서는 순환하는 혈액의 IDL 입자수논 chy lo mi cro n . 형성에 달려 있다 .338> A p oC 는 VLDL 분해시에 빠르게 HDL 로 이동 되 나 Ap o B 는 이 런 이 동이 일어 나지 않는다. VLDL 에 서 LDL 로의 전환은 LPL 의 작용에 의해서 VLDL 내의 중성지방이 가수분해되며 또한 콜레스테롤과 인지방이 LDL 로부터 이동되어 버 립으로써 형성 된다고 본다. LDL 의 합성 률의 감소는 hy po beta l ip o p ro te i n e mi a 환자 339) 에 게 서 나타난다. 이런 개인에게서는 혈청내 HDL 의 농도가 낮아지며 콜레 스데 를이 정 상치 의 약 10% 정 도밖에 되 지 않는다. 317)
A p oB 는 동물의 VLDL 과 LDL 의 주요 단백질이다 .340) 사 람 에게 서 VLDL 내의 A p oB 는 LDL A p oB 로 이동되고 있는 사실이 거의 확실시되고 있다. 그리고 이와 같은 기전으로 다른 동물에게서도 이 동되 고 있 음이 밝혀 졌 다• 341-6> LDL-B 입 자가 VLDL-B 에 서 이 동 되어 오는 것 이의에 다른 급원으로부터 이동되어 오는 사실이 여 러가지 임상증세하에 있는 환자에게서 발견되었다. 그러나 정상인 에 게 서는 LDL-B 는 전적으로 VLDL-B 로부터 유도되 고 있 음이 밝 혀졌다 .347-50) 그러나 가족력이 있는 고콜레스데 몰혈 증 (h yp e rchole s t eroloem i a) 환자에게서는 LDL-B 의 상당량이 독립적으로 합성되고 있 음이 나타났다. 351-3) 그런데 쥐 에 게 서 는 LDL-B po ol 의 오 로 지 일 부, 죽 LDL1-B 가 VLDL-B 로부터 유도되 며 , LDL2-B 는 VLDL-B 로부터 전환되는 양이 거의 무시할 만큼 져온 양이었다 •354) 최 근에 Ghis e ll i G. 는 1251 동위 원소처 리 된 VLDL 과 IDL 을 토끼 에 계 주사하여 서 Ap o B 의 혈장내 특수활성을 관찰하였 다. Ap o B 의 특수활성 은 VLDL, IDL 에 서 관찰되 었으며 또한 LDL1 과 LDL2 에 서 도 관찰되었다. 그 결과 VLDL-B 도 (d 〈 1. 006 g /m l) 주로 혈 장내 IDL (d= l. 006~1 . Ol9 g /ml) 내 로 사라졌 으며 또한 소량의 주사된 VLDL-B 가 LDL1 (d=l.019~ 1. 040 g /ml) 과 LDL2 (d= 1. 04o~ 1. 06 3 g / ml) 입자 내에서 발견되었다. IDL-B 의 주요 분해산물이 LDL1-B 과 LDL2-B 에서 나타나며 이 양은 동물의 전체 혈장 LDL-B p ool 의 약 20% 밖에 되 지 못하였 다. 이 로 미 루어 서 LDL-B 는 VLDL-B 냐 IDL-B 로 부터 유도되는 것이 아니타 독립적으로 합성되는 것으로 결론지었 다 345) 4) HDL 합성 HDL 은 간 313),316) 과 소장 315) 에서 합성이 된다. 간에서 합성되는 . HDL 들은 A p oA 와 A p oC 를함유하고있다. 이에 비해서 장내 HDL 은 오로지 Ap o A 만을 함유하였 다. 315) 또 한편 Hami lton 과 그의 동료 350) 들은 per f us ed 된 쥐의 간에 서 새로이 분비 되 는 신생 HDL 울 유리하였다. 이는 평원모양으로 생겼으며 혈장내 HDL 과 바교했 울 때 함유된 구성성분에 차이가 있음을 지적하였다. 간세포에서 유
리된 신생 HDL 에 함유된 es t er ifi ed 콜레스데물의 함량이 혈청 HDL 에 함유된 양에 비해서 낮았다 ( 4 .3% : 23.8%). 그리고 ap o p r ote i n 구 성도 달랐다. 죽 Ap o E 의 양이 Ap o A-I 의 양보다 훨씬 많았다 .34 8) 이 평원모양의 HDL 은 고도로 활성화된 LCAT 의 기질이다 .350) Hep a to c y tes , go lgi ap pa ratu s 와 쥐 의 pe rfu s ate 간으로부터 유리 된 신생 HDL 의 성분을 화학적으로 분석해 보면 이는 단백질, 인 지방 그리고 콜레스테롤을 많이 함유하고 있으며 콜레스데몰 es t er 는 거의 함유하고 있지 않았다. 이 사실은 HDL 의 LCAT 에 의한 콜레 스테 롤의 este r if ica ti on HDL 이 순환계 로 이 동되 어 나간 후에 이루어진다는 견해물 증명해 주고 있다 .358) 정 상 생 성 조전하에 서 의 ap o p r ote i n 합성 의 중요성 과 HDL 내 로의 영 합은 가족력 이 있 는 HDL 결핍 환자, 죽 Tang ier dis e ase 환자를 동 해서 열거해 볼 수가 있다. 이 환자의 혈청내 HDL 과 LDL 의 수준 은 현저히 감소되어 있으며 혈청 중성지방의 양온 증가되어 있고 fas ti ng ch y lom i cronem i a 가 발생되어 있다. 또한 혈장의 전 콜레스 테 롤 함유농도는 30~70mg /m l 범 위 내 에 있 고 HDL2 함유농도는 정 상인의 것에 비해서 1~5% 밖에 되지 않는다. 이렇게 소량 존재하 는 HDL 도 전기영동기의 움직임으로 봐서 거의 HDLT 의 구성성분 에 가까울이 만큼 비 정 상적 인 성 분을 함유하고 있 다. 359)360) Lux 와 그의 동료들은 초원십 분리 에 의 해서 HDLT 를 유리 하여 서 ap o p ro te i n 의 함유성 분을 분석 하였 다. 360) HDLT 내 에 함유될 Ap o A- I : Ap o A-II 의 비례는 1 : 12 인 데 비해서 정상 HDL 내의 함 유비율은 3 : 1 이었다. 이 결과를 가지고 Lux 와 그의 동료들은 Ta- ng ier dis e ase 는 ap o p ro te i n 의 구성 비 에 변화가 옴으로써 HDL 의 분해를 항전시 킨다고 하였 다. Assmann 과 그의 동료들은 359) Tang - ier 병 은 HDL 입 자의 qu arte n ary 구조에 Ap o A-I 의 영 합이 되 지 않아서 생기는 결합 때문이타고 하였다. 또한 이러한 기본적인 결 합에 부과해서 Ap o A-I 의 결핍은 HDL 함량의 감소를 초래하였 으며 이는 정상인의 것에 2% 정도의 HDL 이 혈장내에 함유되어 있 는 반면에 조직내에 콜레스테롤 es t er 의 축적이 일어난다. 이러한 임상적인 발견으로 이 말단조직에 존재하는 콜레스데롤을 간으로
이동시키는 데에 중요한 역할아 있다고 제시하였다. 세포배양 연구결과에서 밝혀전 바에 의하면 HDL 과 ap o p ro te i n 이 인지방과 복합이 되면 배지로부터 세포 스데 문 의 유출을 상승시 킬 수 있 다고 하였 다. 361-3) Tang ier dis e ase 환자에 게 서 LCAT364-6) 와 lip o p ro te i n lip as e366> 의 수준에 대해서 여러 종류의 보고가 되어 있다. Gre t en 과 그의 동료들은 Tang ier dis e ase 환자에 게 서 po st hep a rin lip o lyt ic acti vi t y (PHLA) 의 결핍이 없었으며 또한 간세포내의 중성지방 l ip ase 의 활 성 에 변화가 없었 던 것 으로 보고하였 다. Grete n 과 그의 동료는 365) Tang ier 환자 혈청 내 에는 PHLA 의 작용이 충분할 수 있 을 정 도의 lipo p ro te i n l ip ase 의 활성제 및 A p oC - Il 의 양이 촌재한다고 하였 다. Tang ier 환자에 게 서 lip o p ro te i n 의 전환륜 측정 하고 또한 Ap o , A-I 과 A p oA-Il 의 구조적 목칭에 대해서 많은 연구가 이루어져 야 될 것으로 본다. (2) Lip o p r ote i n 의 분해 혈청 내 lipo p r ote i n 은 신체 내 에 서 동적 인 상태 (dy n ami c s t a t e) 에 있 다. 이 과정은 합성과 분해에 의해서 이루어진다. 주어전 시간에 혈청 내 어 떤 종류의 lipo p ro te i n 의 농도는 그 당시 의 분해 와 합성 률 에 의해서 결정된다. 혈청내의 lip o p ro t e i n 의 분해는 3 가지 별개의 과정에 의해서 이~ 어 진다. a) lipo p ro te i n 내 에 함유된 지 방과 ap o p ro te i n 구성 의 이 동 과 교환에 의 해서 이 루어 진다. b) LCAT 와 LPL 과 같은 효소에 의 한 lipo p r ote i n 의 성 분변화에 의 해 서 이 루어 진다. c) recep tor 가 중재 된 cellular up tak e 에 의 하거 나 또는 피 동적 인 endocy tos is 에 의해서 이루어진다. 다음의 표 7 에 개개의 분해과정이 요약되어 있다. (3) Lip o p r ote i n 의 교환과 이 동 중성지방이 VLDL 로부터 LDL 과 HDL 로 이동되는 것은 in vit re>
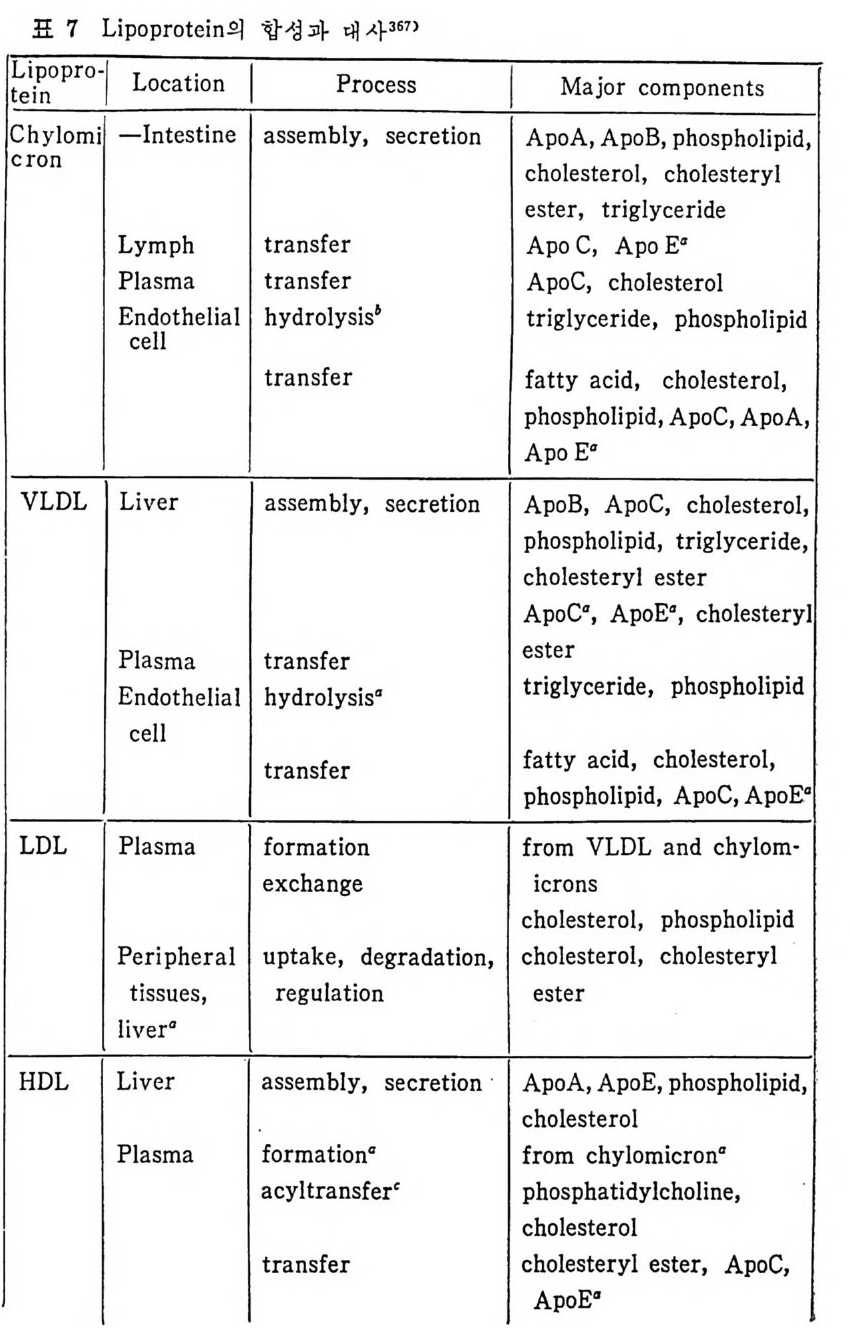 표 7 L ip o p ro t e i n 의 합성 과 대 사 367)
표 7 L ip o p ro t e i n 의 합성 과 대 사 367)
 exchang e I Ap o C, choleste r ol, ph osp·
exchang e I Ap o C, choleste r ol, ph osp·
실험을동해 혈장과수용액에서 모두 관찰되었다 .368 一 70) 이러한 이동 온 온도에 의촌되는 것으로 37°C 에서는 쉽게 찰 일어나지만 40°c 에서는 이동이 되지 않는다. 또한 VLDL 내의 중성지방이 HDL 의 콜레 스데 몰 este r 로 교환되 었 음이 관찰되 었 다• 369) Uneste r ified 콜레 스데 를은 in vi tro 나 in viv o 연 구에 서 모두 쉽 게 혈장내 각종의 lip o p r ote i n 사이 에 서 교환이 되 며 또한 Iipo p r ote i n 과 막 사이에서도 교환이 된다 .371-6) 이와 대조적으로 콜레스테롤 es t er 는 교환이 대단히 천천히 일어난다. 동위원소로 처리된 콜레 스테를 es t er 의 혈장과 적혈구 사이에서 균형이 이루어지는 데는 in v i vo 에서 8 시간이 질렀다. 이러한 교환은 온도에 따라서 그 속 도가 달라진다. 죽 37°C 에서는 10°c 대에 비해서 2 배나 빠르다. LDL 또는 HDL 로부터 적혈구로의 대부분의 콜레스테롤의 교환은 세 포막의 bil ay e r 와 관련이 있 다. 그런데 이러한 교환은 LCAT 처해제에 의해서 아주 막히지는 않 으며 아마도 피차의 마찰과 한꺼번에 비벼서 생기는 복합체 형성을 통해서 교환이 가능하다고 본다. 그러나 콜레스테를 교환의 생물학적인 현처한 면은 아직 모른다. 이 는 막의 액 성 (fl u i d ity)의 결과에 서 나타나는 역 할로 생 각해 볼 수 있다. Kunkel 과 Beam371) 은 일찌 기 Iipo p ro te i n 내 의 인지 방의 아 동에 관해서 관찰하였으며 이들은 LDL 에서 HDL 로 또는 그 반대로는 대 단히 빠른 이 동을 한다. 인지 방 교환의 유사한 현상이 토끼 378) 또 는 다람쥐 종류 (s q u i nal monke y )379) 로부터 유리 된 Iipo p r ote i n 사이 에
서도 일어난다. 그러나 이러한 교환은 단백질과는 무관하게 이루어지고 있다. L DL 과 HDL 사이 에 서 ph osp h ati dy lc holin e 과 sp h in g o my e lin 의 군 형 이 이루어지는 데는 4~5 시간이 걷렀다. ph osp h ati dy lc holin e 의 이동은 지방산의 포화에 의해서 영 향 을 받지 않는다. LCAT 의 방 해 로 ph osp h ati dy l cholin e 의 이 동은 완전히 차단되 는 것 은 아니 나 이 과정 에 참여 하는 sp h in g o my e lin 의 총량이 감소된다. 인지 방의 이 동은 혈장 lip o p ro te i n 과 적 혈구 ,380> mi toc hondria ,3 9D 7J : mi cro somes, 382) 간편 383) 그리 고 조직 배 양에 서 빠르게 분열 하는 세 포 384-5) 사이 에서 일어나고 있음을 보여주었다. Lekin 과 그의 동료는 386) 동물의 전신으로의 지 방의 영 합은 혈장 lipo p r ote i n 과 조직 사이 에 서 지 방의 계 속적 인 교환을 반영 한다고 하였다. Mi toc hondria 와 혈장 lip o p ro te i n 사이 의 인지 방의 교환은 〈인지 방 교환 단백질 〉 이라고 불리는 간 387) 으로부터의 105,000g 상등액에 있는 단백질의 작용에 의해서 2~3 배가 자국된다. Reed 와 그의 동료는 사람과 개에게서 혈장 l ip o p ro t e i n 과 적혈구 사이에서 인지방의 교환율을 결정하였다 .380> s p h i ng om y el i n 과 ph osph ati dy lc holin e 은 12 시 간 동안의 입 자전환이 13~14% 이 다. 그란데 적 혈구내 의 ph osp h ati dy ls erin e 과- pb osp h ati dy le th a nolami ne 은 이 교환에 관계하지 않았다. 이러한 발견은 적혈구 막이 비대칭 이 라는 것 을 제 시 하며 ph osp h ati dy ls erin e 과 ph osp h ati dy le th a nola- m i ne 은 막의 안쪽에 위치하고 있다고 하였다. A p oC 는 in v it ro 연구에서 VLDL 과 HDLJ 8 9- 91 ) 사이에서 이동된 다. 이러한 이동은 쌍방으로 이루어지므로 오히려 이 현상온 교환 으로 생 각한다. 그런데 LDL 은 이 이 동에 참여 하지 않는다. VLDL 과 HDL 사이의 A p oC 단백질의 분포는 in v it ro 연구에서 혈장내의 여 러 종류의 ap o p ro te i n 의 농도에 비 례 한다. 그런데 in v it ro 연구에서는 A p oC 의 분포는 혈장 중성 지방농도 에 의해서 기본적인 것이 결정된다. 죽 중성지방의 농도가 높으면 많은 양의 ap o p r ote i n 이 중성 지 방양이 높은 lip o p ro te i n 으로 이 동
된다. 사람에 게 서 고지 방식 을 섭 취 한 후에 alim enta ry lip e mi a 가 생 기 면 이 때 에 는 Ap o C 의 이 동이 HDL 에 서 chy lo mi cr on 으로 그리 고 VLDL 로 된다. 392) 그런데 이 ap op ro te i n 이 단독으로 이 동되 는 지 에 대 해 서 는 모른다. 그런데 Rub i ns t e i n390) 은 후자의 경 우를 더 생각한다. 다음의 그립 14 는 여 러 종류의 Iip o p r ote in 둘의 기 능적 그리 고 대 사적 상호관련을 표시한 것이다. 간세포내 (1) 간 세포로부터 VLDL 의 형성과 분비 운 표시하였다. (2) VLDL 이 지방조직, 근육 그리고 다른 간 밖의 조칙의 모세관운 통해 서 동과해 나가는 경로이다. (3) 모든 간 밖의 조직 내 에 존재 하는 extr a hep a ti c lip a se 에 의 한 중성 지 방과 VLDL 이 가수분해되어서 IDL 로 전환된다• (1') 간세포에서 신생 HDL 의 생성과 분비과정이다. (2') 유리 콜레 스테 롤이 콜레 스데 올로 LCAT 에 의 해 서 전환되 며 따라서 lecit hin 이 lys o lec ithi n 으로 전환된다. (3') 콜레스테롤 es t er 가 HDL 로 영합되는 과정이다. (a) Ap o C 의 HDL 로부터 VLDL 로 이 동된 다. (b) extr ah ep a ti c LPL 에 의 해 서 lec ithi n 과 콜레 스테 롤이 이 동된다. 이 때 LCAT 의 작용이 개 입 되 어 서 lec ithi n 이 lys o lec ithi n 으로 전환된 다. (c, d, e, f, g) hepa t i c LPL 에 의 해 서 VLDL 은 HDL 로 이 전 시 킨다. 이 때에 중성지방의 분해와 콜레스데롤, lecit hi n , A p oC 의 이동이 있으 며 소량의 콜레스테롤 es t er 와 중성지방의 이동이 있다. (4) hep at i c LPL 에 의 해 서 IDL 이 LDL 로 전환된다. (5) LDL 은 모든 조직 의 LDL 분해 sit e 로 이 동된다. 소장내 세포 굶었을 때는 ch y lom i cron 의 합성은 이루어지지 않거나 소량 이루어진다. 왜냐하면 지방산의 공급부족 때문이다.따라서 VLDL 의 합성도 소량 이루 어진다. 이때에는 내자지방을 이용해서 VLDL 을 합성한다. 이때 이용되는 내 자지 방은 3 가지 급원으로 나눈다. 첫 째 , 담줍 lec ithi n 으로 이 lecit hi n 은 지방산과 l y sole cit h in으로 분해되며 지방산이 중성지방합성에 공헌한다. 둘
 I Liv e r Parenchy m aI CeIls |
I Liv e r Parenchy m aI CeIls |
째, 립프로부터 이동되는 FA-albumi n 복합체에서 지방산이 유용해진 다. 재 째로 지방산이 장내막세포에서 합성 원 수도 있다고 본다.장내에서도 HDL 이 합성된다고 본다. 7 L ip o p ro t e i n 대 사에 관련된 효소 (1) LCAT(Lecit hi n - Choleste r ol Acy lt r n '1 s fe r ase) LCAT 는 혈장내에서 순환히는 효 소이 다 . 요즈음 및및 연구팀에 의해서 사람의 혈청으로부터 LCAT 가 유리되 었고 그 목성 이 알려 쳤 다. sedim enta t i on equ il ibr lu m 방법 에 의 해 서 결 정 된 분자량은 59, 000393) 이 고 이 보다 조금 높은 양의 분자량 (65, 000~70, 000) 이 SDS po lya cryl a mi de ge l elec t o p hores i s6H4>23>39% )에 의 해 보고되 었 다. 그리고 효소 LCAT 는 높은 양의 당을 함유하고 있어서 무게로 약 24% 에 달한다. LCAT 는 용엑에 monomer 로서 317),393) 존재하며 이는 glu cosam: n~ 울 함유하며 g alac t osam i ne 은 함유되 어 있 지 않다. 이 효소의 아마 노산 구성성분은 여러 가지 기술에 따라서 분리되었으며 23),393 -4) 이 둘은 상호 유사한 결과를 보여주고 있다. LCAT 는 p hosp ha ti d y lcho li ne 의 C-2' 위 치 에 부착되 어 있 는 지 나 산을 콜레스테롤로 이동시키는 것을 촉진하여 혈청내 대부 분 의 콜 레스테몰 es t er 를 형성한다 394-7) (그립 15 참조). 그리 고 ph osph ati dy lc holin e 에 부착되 어 있 는 지 방산이 불포화되 었을 때가 포화되었을 때보다 LCAT 의 더 좋은 기질이 된다 .398) LCAT 작용을 위한 콜레 스테 몰과 ph osph ati dy c holin e 의 주요 급 원은 HDL 과 LDL 이다. 부분적으로 정제된 LCAT 의 활 성은 Ap o A-I 의 촌재 로 크게 상승된다. 399-400) 특히 인지 방의 지 방산이 불 포화지방산일 때 이 효소의 작용은 A p oA-I 에 의해서 크게 상 승된다. 또한 Ap ·o C -Il 도 인지 방의 지 방산 구성 에 따라서 활성 화 될 수 있 다. •oo, Ap o A-I 은 계 란의 ph osph ati dl yl c holin e 을 기 질 로 취할 때 LCAT 의 활성제 역할을 가장 크게 해준다. 또한
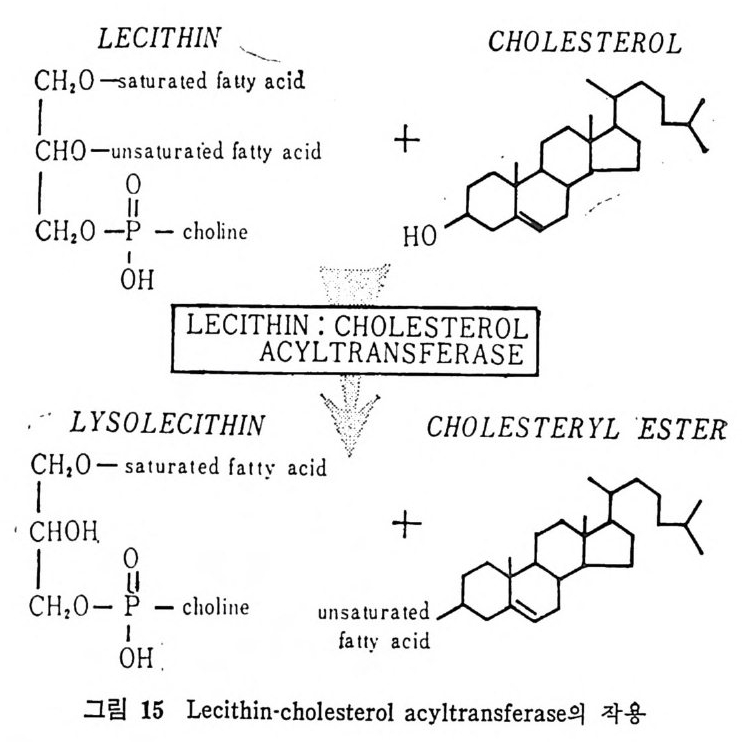 CCI HH1O0-L-u sEnaCst a uItTr u aH r tae Idt Ne d f afta、t y`tt `y`a— c a icd i d + CHOLESTEROL
CCI HH1O0-L-u sEnaCst a uItTr u aH r tae Idt Ne d f afta、t y`tt `y`a— c a icd i d + CHOLESTEROL
Ap o C-I 은 dim y risto y l ph osph ati dl yl c holin e 을 기 질 로 취 할 때 가장 유력한 활성제의 역할을 한다 400) (그립 16 참조). Ap o A-I 에 의 한 LCAT 의 작용은 Ap o C-I 에 의 해 서 작용하 는 울의 4 배나 높다고 하며 Ap o C-I 은 인지방의 지방산이 불포 화나 포화나 같이 작용한다. 401) 또 한편 Ap o D 는 LCAT 작용률을 높 인다고 하였다 .402) 또 한편 Ap o A-II 은 LCAT 를 활성 화시 키 지 않으며 오히 려 Ap e A-I 첨 가로 생 성 된 활성 을 감소시 킨다. 399-400) 정 상인의 혈장내 에 서 는 HDL (d : 1. 063~1 . 210) 이 나 HDL3 (d : 1.125~1. 210) 을 첨 가했 을 때 LCAT 활성에 아무런 효과가 없었다. 그러나 HDL2 (d=l. 06 3- ~1.125) 의 첨가로 효소의 작용이 방해되었다 .403) 이와는 대조적으 로 ch ylom ic ron 이 나 VLDL 의 첨 가로 전체 혈장내 에 서 LCAT 작용률
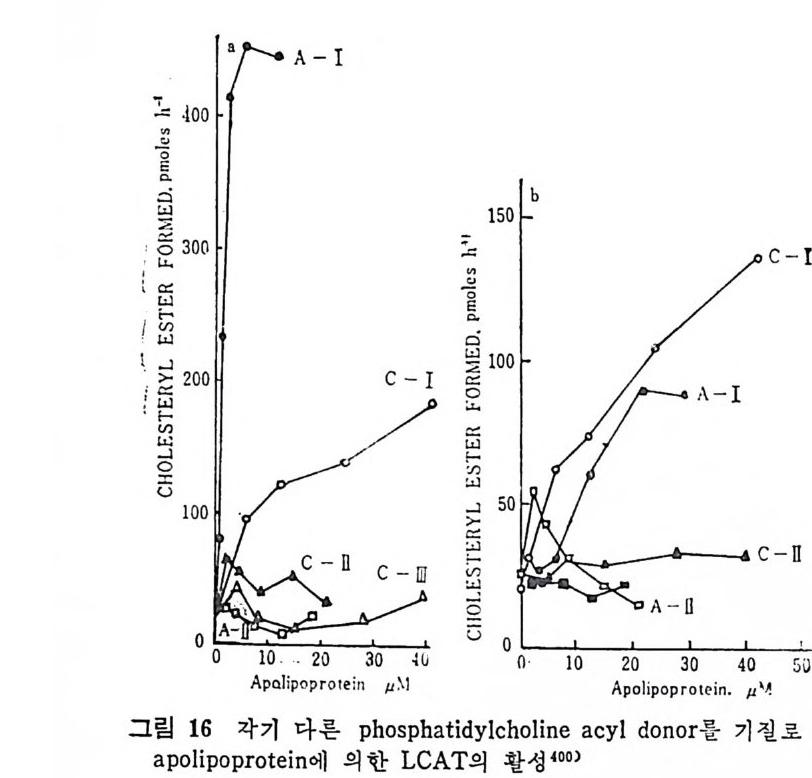 A-I
A-I
을 자극하였 다. 389) Soute r 와 그의 동료는 LCAT 활성 에 있 어 서 인지 방의 물리 적 상 태의 효과에 대해서 연구하였다 .404> LCAT 에 의해서 촉진되는 tra · nsacy la ti on 을 위 한 활성 에 너 지 는 ph osph ati dy lc holin e acy l donor 의 전환이 온도에 따라서 급격한 증가를 보여주었다. 이 연구자들 온 효소와 ph osph ati dy lc holin e 과의 상호작용이 전반적 인 촉진작용 에 있 어 서 속도제 한 단계 이 며 (rate - lim i ting ste p ) 인지 방이 ge l 형 태 에 서 용액 형 태 로 전환되 는 온도 이 상으로 유지될 때 효소와 ph osp h a- tidy lc holi ne 과의 상호작용이 가장 호조건하에 서 이 루어 진다고 하였 다. 그러나 LCAT의 작용률에 영향을 미치는 여러 효소에 대한 연구 는 아직도 분명히 이루어질 수 없는데 그 이유는 LCAT 를 완전히
정제해 낼 수 없기 때문이다. Albe rt”는 LCAT 를 고순도로 정제 해 보려고 노력하였으나 이 물질의 안정된 형대를 알아내지는 못 했고 이 물질의 비교적 정확 한 분자량은 약 68,000 이라고 보고하 였다. Glomset 과 그의 동료들은 LCAT 작용 동안에 HDL 로부터 VLDL 로 콜레스테롤 este r 이동의 가능한 기전을 다음 그림 17, 그림 18 과 같이 도해하였다. 간은 혈청 내 LCAT의 주요 급원이다 .407-8) 그러나 장내에서도 합 성된다고 하며 1 09) 이는 혈청내에서 순환한다. LCAT 수준은 여자보 다 남자에게서 더 높다 .410) LCAT 의 기본적인 결핍증이 1967 년에 처음으로 노르웨이에 사는 여자 3 형제들에게서 회귀한 유전질환으 로 발견되었다 .41D Norum 과 그의 동료 412) 그리고 G j one413) 은 LCAT
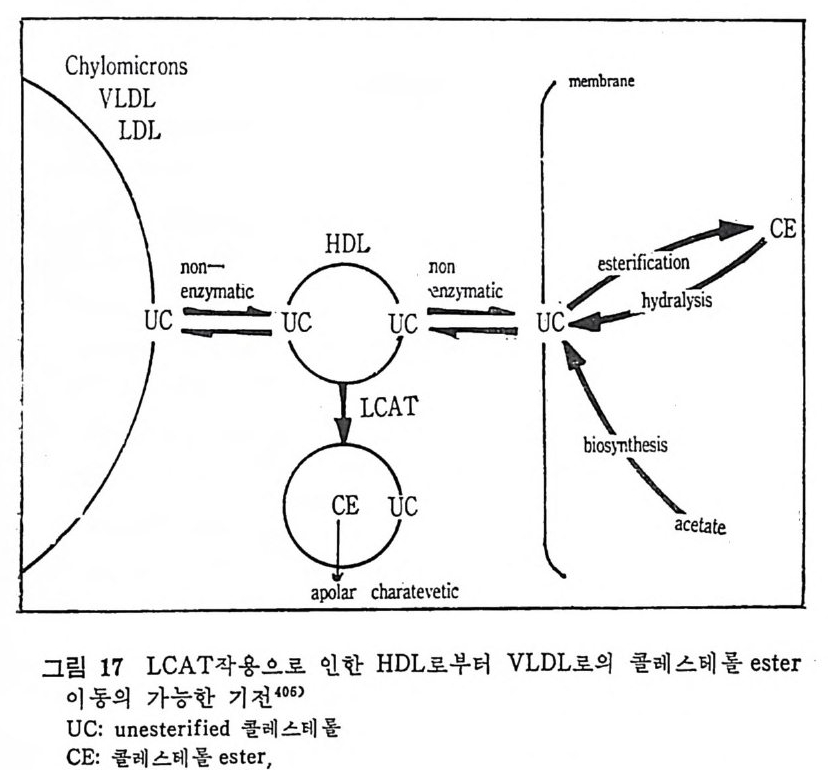 ( membrane
( membrane
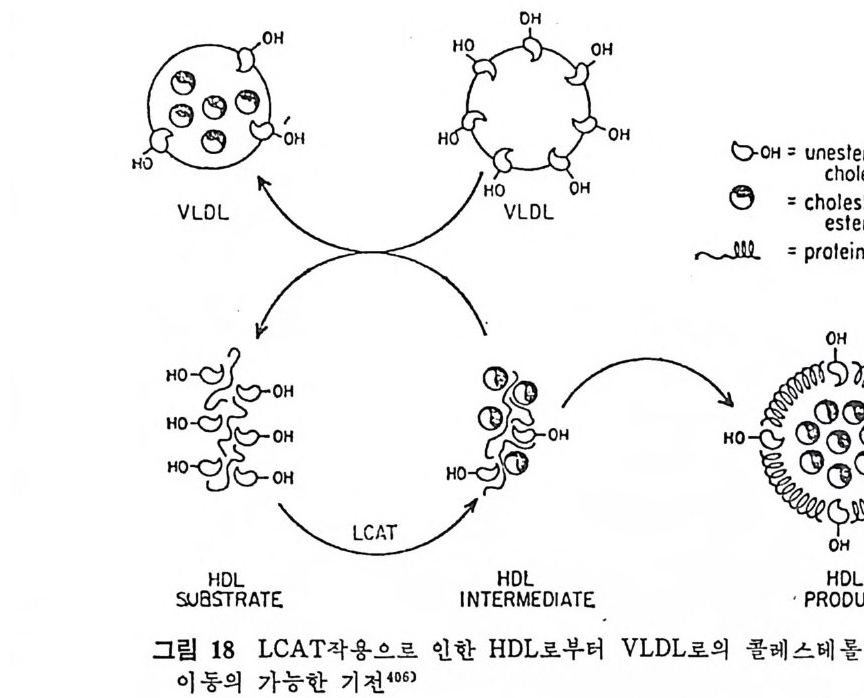 도VLDL H 二 1b9o H == uchnceoehlsseolleselerrts ei frt i e yerl c of r
도VLDL H 二 1b9o H == uchnceoehlsseolleselerrts ei frt i e yerl c of r
결핍증의 광범위한 임상적인 증세에 대해서 고찰하였다. 임상적인 증세를 개괄적으로 살펴보면 작은 회색입자에 의한 눈의 망막침착 증, 적혈구 수명감소를 동반하는 빈혈, 단백뇨, 혈뇨, urin a ry red cell casts 와 Renal ins u fficien cy 등이 었 다. LCAT 가 결 핍 된 모든 사람들은 콜레스테불과 p hos p ha ti d y!c ho li ne 의 혈청내 농도가 증가 되 며 ly s op h osp h ati dy lc holi ne 과 콜레 스테 롤 est e r 의 수준은 감소 되었다. 또한 LCAT 활성은 그들의 혈청내에서 발견될 수 없었다. 적혈구내의 치방의 구성성분은 비정상적이었다. unes t er ifi ed 콜레~ 테를 농도가 약 2 배로 증가되었다 .414) 다음의 표 8 은 Glomset 이 가족력 이 있 는 LCAT 결핍 세 환자의 혈청내 지방농도를 측정한 것이다. Este r i fied 콜레 스테 몰의 농도와 lys olecit hi n 의 농도가 감소되 었 음이 나타났다. LCAT 가 결핍된 환자에게 정상인의 혈청을 주입시 키면 접차로 콜레스테를 es t er 의 양이 증가되어서 4~6 일에 최고차
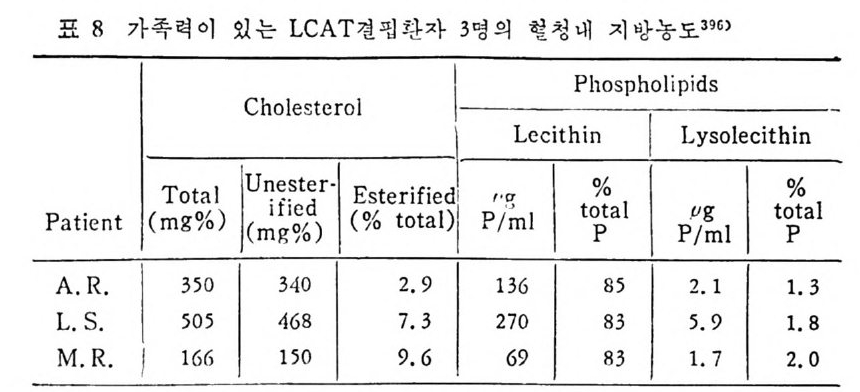 표 8 가족력이 있는 LCAT 전핍칸자 3 명의 형청 내 지 방농 도 3 9 6)
표 8 가족력이 있는 LCAT 전핍칸자 3 명의 형청 내 지 방농 도 3 9 6)
에 도단한다 . 415) LCAT 결 핍 환자의 혈 청 내 에 정 상인의 lip o p ro te i n 과 ap o lip o pr o- tei n 의 종류가 다 존재 한다고 할지 라도 H6-7) 이 들의 철대 구성 성 분 과 혈청 lip o p ro te i n 의 구조에 획 기 적 인 변화가 온다. 이 중 가장 현 저 한 번화는 LPX, /3- electr o p h oreti c 울 동에 의 한 VLDL 입 자와 두 ~ 종류의 비정상 HDL 입자가 촌재하며, Ap o A, Ap o B 그리고 thi n line 단백 질농도의 감소가 나타난다 . 418-22) 이러한 변화는 LCAT 결핍으로 아마도 대사의 순서에 변화가 오 므로 나타나는 결과로 생각된다 . LCAT 결핍환자로부터 얻은 VLD L 입자들은 중성지방과 단백질함량에 비해서 비정상적으로 높은 함량 의 uneste r if ied 콜레 스테 풀과 인지 방이 함유되 어 있 다. 420) 그런데 in v i vo 연구에서 LCAT 결핍환자에게 LCAT 를 첨가해주면 혈장내 의 콜레스데몰 es t er 의 수준이 정상으로 되며 VLDL 의 전기영동이 정 상으로 된다. 423) LCAT 결핍환자로부터 얻은 LDL 입자듣도 정상인의 것에 바해서 그 크기 가 다양하다. 2 % ag a rose ge l 을 이 용한 chromato g r ap h y 에 의 해 서 3 가지 종류의 입 자가 분리 되 었 다 . 420) 하나는 void volume 에 서 정제했으며 이는 정상 LDL 의 구성성분에 비해서 콜레스테롤 : 단백 질 그리 고 ph osph ati dy lc holin e : 단백 질 비 율이 4~6 배 높았다 (표 9 참조). 또한 nega ti ve ly sta i n 해보니 까 이 입 자는 크기 가 크며 전자현미,
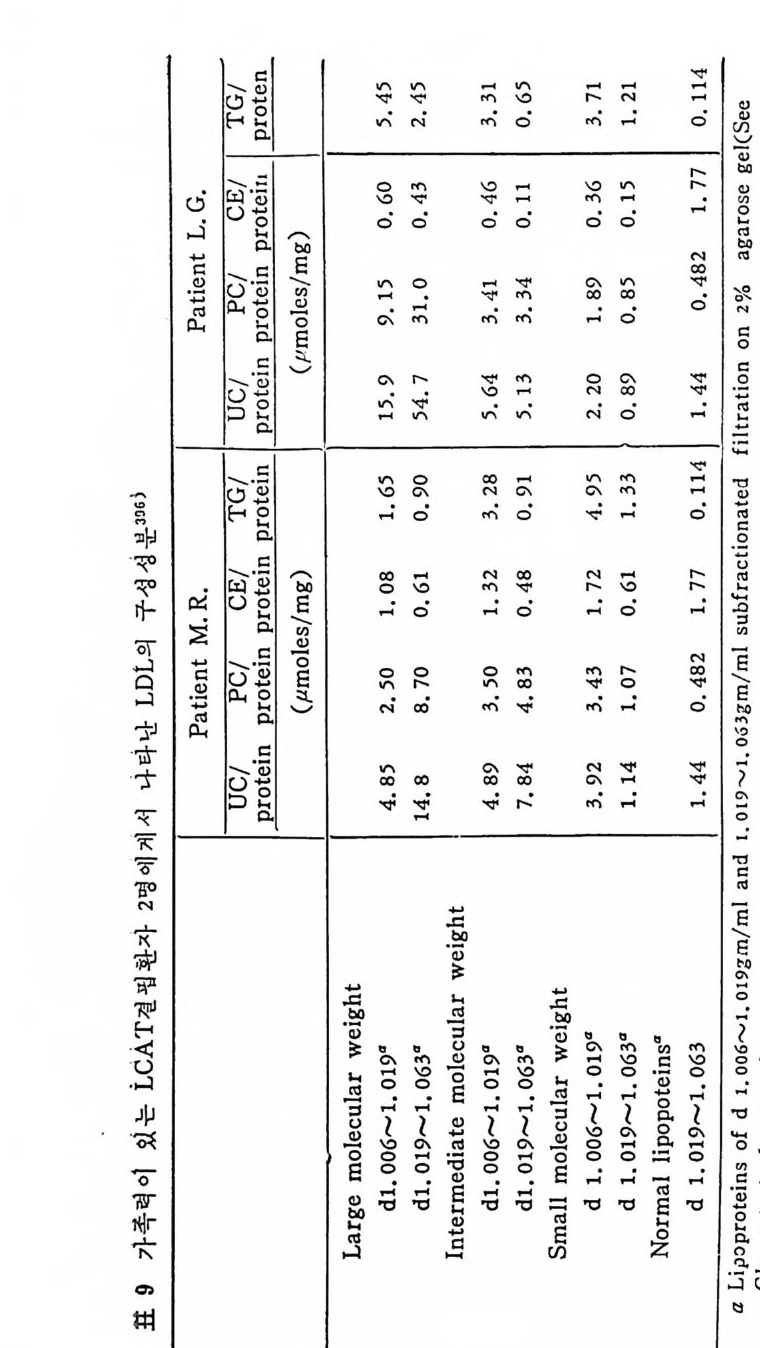
경 으 로 관찰안 절 과 편 편한 구조 로 직 경 이 900 ~20 0 A 이 다. 420) 이 를 0 s 0 루 고 정시켜 절단 (sec ti on i n g)해서 보았을 때 이 입자의 표면온 밀집된 전자로 덮여 있으나 electr o n core 는 벌로 없었다. Glomse t 420) 은 이 큰 입 자도 VLDL 로부터 분해 되 어 나오는 중간 입자라고 하였다. 이러한 비정상적으로 큰 입자가 생성되어 나오는 순서는 다음과 같다. 중성지방이 가수분해에 의해서 이동되어 나오 떤 과량의 인지방과 유리 콜 레스테롤이 LCAT 결핍으로 인해서 부 분적 으로 분 리 되 거 나 또는 VLDL 이 분해 되 어 서 VLDL 입 자의 bil a · y er 를 형성한다. 그러면 이 b i la y er 는 응집되어서 큰 입자로 되며 바정상적으로 된다. LCAT 결핍환자의 혈장에 정상인의 혈장을 첨 가해 주고 배양시키면 이렇게 바정상적으로 큰 입자 형성이 감소된 다. 세번 째 입자는 정상 인의 LDL 과 같은 volume 의 column 에서 떠 오른다. 이는 정상 LDL 입자와 유사하나 그 구성성분을 보면 정상 인의 것에 비해서 1.5~3 배의 더 많은 unes t er ifi ed 콜레스데풀과 ph osp h ati dy lc holin e 이 함유되 었 고 13 배 나 더 되 는 중성 지 방이 함유 되어 있다. 이러한 특징이 이 입자의 바중을 LDL 에 비해서 낮게, 부유율 (floa ta t io n ra t e) 은 높게 한다. LCAT 결 핍환자의 혈청에서 유리한 HDL의 비정상중은 다른 종류 의 lip o p r ote i n 보다 현저 하다. HDL 비 중범 위 에 서 유리 된 lip o p ro te i n 입자는 크기가 다양하며 정상인의 HDL 에 비해서 unes t er ifi ed 콜레 스데 롤은 12 배 , ph osp h ati dy lc holin e 은 5 배 를 함유하고 있 다. sep h • adex G200 chromato g r ap h y 에 의 해 서 분리 된 420-1) 주요 미 립 자는 4oA 두께 의 원판모양으로 반경 이 150~200A 정 도로서 돌돌 말려 있 다 419),424) (그림 19 참조). 이러한 비정상 HDL이 촌재하는 혈청내에 부분적으로 정제된 LCAT 를 첨가하니까 정상인의 HDL 형태로 되었 다. 그러 나 sep h adex column 에 남아 있 는 부차적 인 입 자를 전기 연 등에 걷어 보면 pr ealbumi n 부위 근처 에 서 나타나며 이 는 정 상 HDL 보다 약간 많은 uneste r i fied 콜레 스테 롤과 ph osph ati dy lc holin ~ 을 함유하고 있 다. 이 입 자의 직 경 은 45~60A 으로서 원판모양이 나 돌 돌 말려 있지는 않고 LCAT 의 기질로 작용이 된다 .396) Glomse t과
 그립 19 정계한 LCAT 문 LCAT 걷핍환자의 형청과 배양하기 전후의
그립 19 정계한 LCAT 문 LCAT 걷핍환자의 형청과 배양하기 전후의
Norum3 96 ) 그리 고 Ham ilt on358) 은 이 입 자도 간으로부터 나온 신생 HDL이 라고 말하고 있 다. 이 입 자 들 은 주로 Ap o A- I 과 소량의 Ap o A- I l 를 함유하고 Ap o C 는 함유하고 있 지 않다. 422) 그런데 이 러 한 환자 에 게 서 유리 된 LP-X 는 Ap o A-I , Ap o A- I l , Ap o C- I , Ap o C- I l , Ap o C- Il I , th in - l in e 단백 질 그리 고 알부민을 함유하고 있다 425 - 6 ) ((3) 「 L ip op ro t e i n 구 성성분 J 중 lip o pr o te i n X 참조 ). 이는 장 애 성 (ob st r uc ti ve ) 간질 환 환 자 의 LP-X 에 는 Ap o A- I 이 전연 부재 한 다는 사실 과 대조적인 현 상을 보 여 준 다 . 9 0) 다 음의 그 립 2 0 은 Glomse t이 제 안한 LCAT 결핍 환 자에게서 비정 상 LDL 과 HDL 형 성기전 을 도 해 한 것이다.
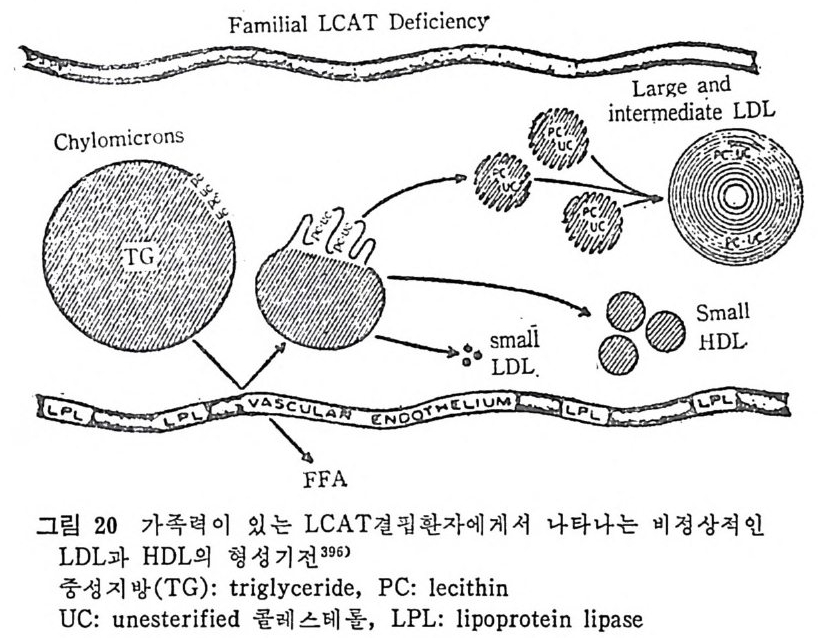 Fa m il ia l LCAT De fic ien c y
Fa m il ia l LCAT De fic ien c y
다음의 표 10 은 LCAT 결핍환자의 혈청 중에 함유된 LP-X 의 합 량 비교이다. LCAT 의 lip o p r ote i n 대사에 있어서의 주요 여할은 정의되어 야 한다. 장내 chy lo mi cro n 내 에 Ap o A-I 이 촌재 한다는 사실은 427) LCAT 가 HDL 구성 성 분들 죽 ph osp h ati dy lc holin e (PC), 콜레 스데
 표 10 LCAT 걷팝환자의 혈청내 lipo p ro te i n X 의 함량비교 41 6 )
표 10 LCAT 걷팝환자의 혈청내 lipo p ro te i n X 의 함량비교 41 6 )
몰, A p oA-I 둥의 구성과정에 중요 역할이 있음을 암시해 준다. 그런데 HDL 구성성분들은 분해하는 동안에 ch y lom i cron 으로부터 유래되어 온 것들이다 .428) LCAT 결핍환자에게서 식후에 얻은 혈장 내 의 HDL, 비 중범 위 내 의 lipo p r ote i n 내 에 는 콜레 스데 몰 este r 가 결 핍 되 어 있 음을 보고하였 다. 429-31 ) LCAT 는 세포막에 의해서 융화되는 양 만큼의 콜레스테풀과 PC 를 이동시킨다. LCAT 의 작용은 이마 촌재하고 있는 HDL 내로 기 질과 A p oA 를 이동시키는 것일 것이다. 또는 바꾸어서 생각해 보 면 p er fu sed 간체계에서 연구한 바에 의하면 LCAT 작용에 의해서 신생 lipo p ro te i n 이 유리 되 도록 하며 이 로부터 HDL35” 이 형 성 된다 고본다. LCAT 에 의해서 형성된 콜레스데몰 es t er 의 이동을 위한 주요 경로는 간에서 HDL 에 의해서 취해지는 것으로 본다 .432) (2) LPL(Li po p r ote i n s lipa se) 1) LPL 의 물리 • 화학적 성질 LPL(lip o p ro te i n lip ase) 는 효소의 일종으로서 또는 밀접히 관련 이 있는 효소군으로서 일반적으로 영에 의해서 방해를 받으며 alkali ne p H 에 서 최 적 의 상태 를 나타내 며 조요소로서 Ap o C 一 ]I 의 가 장 호조건의 분해작용을 유지하기 위해 필요한 것이다. 여러 급원으로부터 유리된 LPL 은 위의 일반적인 독칭을 나타낸
다. 그러나 화학적으로 그리고 효소작용 독칭에서 차이가 나타나며 면역학적인 목 칭, 호르몬과 대사조철에 있어서 차이를 나타내므로 여러 급원으로부터 유리된 LPL 이 과연 같은 단백질인가에 대한 의 문을 일으키게 된다. 여 러 급원으로부터 분리 된 LPL 은 무게 로 보아서 3~10% 의 탄수 화물 함량을 가전 당단백 질 (g l y co p ro t e i n) 이 다. 432-4) 분자량은 일반적 으로 SDS 가 존재 하는 po lya cryl a mi de ge l 전기 영 동 (elec tr o p hores i s) 에 의해서 결정된 바에 의하면 대개 60,000~72,000 법위내이다. 이 범위내에서 속하는 LPL 은 다음의 여러 급원에서 분리하였다. hep - ar i n 으로 처리된 후의 쥐의 혈청 ,435) 쥐 십장 ,436) 돼지 십장 ,437) 돼 지 지 방조직 438) 육류, 439- 4 0) 닭지 방 조직 438) 그리 고 사람의 hep a rin 으로 처리하고 난 후의 혈장 432),442) 둥이다. 또한 쥐의 십장근육과 433}
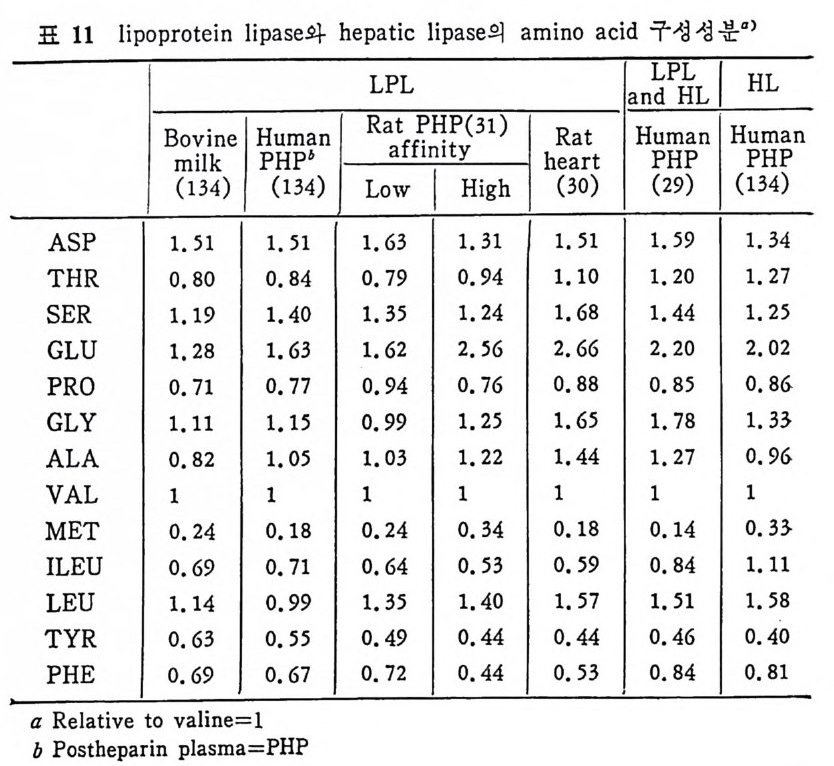 표 11 lip o pr o te i n lip ase 와 hep a ti c lip ase 의 ami no aci d 구성 성 분•>
표 11 lip o pr o te i n lip ase 와 hep a ti c lip ase 의 ami no aci d 구성 성 분•>
쥐의 he p ar i n 으로 처리하고 난 후의 혈청 443) 에서 분자 량 이 낮은 (3 4 ,000 과 37,5oo)LPL 이 유리정제되었다. 그러나 이 두 저분자량의 LPL 의 아미노산 구성성분에도 차이가 크게 난다( 표 11 참조 ). 위의 표 11 은 6 가지 급원으로부터 유리 된 LPL 의 아미 노산 구 성 이며 이로 미루어보면 이들은 같은 단백질이 아니라는 것 이 증 명 뮌 다. 그러나 면역학적 연구에서 보면 다른 급원에서 유 리된 LPL 의 유사접 울 보여 준다. 쥐 의 십장 4) 과 닭의 지 방조직 44 1) 으 로부터 유리 된 LPL 을 상대 로 준비 된 anti se rum 는 같은 종 족 의 동물 에 있 어 서 여러 부위의 조직으로부터 효소의 활성을 방해하 였 다. 이 사실은 한 종류의 동물체 내 에 서 는 한 가지 anti ge nic 결 정 요 소 와 반 응 하는 사실이 증명되었다. 우유 LPL 을 상대로 한 an ti serum 은 사 람 의 젖 LPL 과 사람 혈청 LPL 에 상호작용하였다 .4 4 6) 그러나 한 편 동물 의 종족이 다른 경우 쥐의 십장 근육의 LPL 을 상대로 나타나는 항 체는 쥐, 토끼, 돼지, 소 등의 십장으로부터 유리된 LPL 의 작용을 방해하는 능력이 없음울 증명하였다 . 44 4) 여러가지 급원으로부터 유리된 LPL 의 효소로서의 특칭은 기질선 덱에 있어서나 조요소를 요구하는 사실로 미루어 보 면 일반적으로 유사하다. LP L-은 기 질의 화학적 구조와 물리 화학적 특 칭 을 고려 해 볼 때 비교적 낮은 독수성을 가지고 있다. 예로서 in v it ro 에서 여 러 가지 다른 상태 하에 서 우유로부터 정 제 된 LPL 은 tri o l ea t e , tri o - ctan oate , monooleate , tw een 20 그리 고 p-n it ro p he ny la ceta t e 4 4 7 ) 둥 울 가수분해시킨다. hep a ri n 으로 처리된 후의 혈장내의 LPL 은 부 차적 인 ph osph olip a se 활성 을 가지 고 있 으며 433) c 귀 의 십 장으로부터 정 제 된 LPL 은 dig ly c eid e 와 중성 지 방 monolay e r 를 가수분해 하고 433) 그리고 m ic ell 이나 알부민과 결합되어 있는 momo g l y cer i de 로 가수 분해한다 .448) Ap o C-II 는 조요소로서 중성 지방 가수분해할 때 에 효소의 작용운 울최고치로 증가시키고 다론 기질에 작용할때는 영향이 없다 .447-8) 영에 의해서 방해를 당하거나 조요소인 A p oC-II 의 의촌도는 같으 나 기질에 대해서 찬화력이 다른 두 종류의 효소가 취의 hep a rin 처리된 혈청에서 정제되었고 이와 비슷한 효소들이 쥐의 십장과 지
방조칙 으로부터 도 각각 정 제 되 었 다. 434) 분자량이 다르고 아미 노산 구성이 다르다는 사실온( 표 11 참조 ) 같은 단백 질 이라고 볼 수 없다. He par i n 으로 처리된 사람의 혈청 으로부터 다른 종류의 LPL 이 정 제되었으며 이 들 은 Ap o C- I 에 의 해서 선택적으로 효소의 작용을 상승시 킨다고 보고되 었 다. 449) 이 사실은 아직 확인되 지는 못하였 다. 여 러 연 구로부터 LPL 이 Ap o C- I 에 의 해 서 방해 되 고 있 음이 보 고되었다 .430), 45 0 - 2) 여러 조직내에 존재하는 LPL 의 작용조철기전 이 다르다고 반드시 종류가 다른 LPL 이라고 볼 수는 없다. 효소의 활 성 은 차라리 조직 내 의 특 수한 liga nd 와 호르몬의 recep tor 와 상 호작용함으로써 조절된다고 본다. 45 3) 2) LPL 의 생리적인 역할 LPL 의 목성 과 생리적인 역할을 두 가지 견해에서 논의하고자 한 다. 첫째는 LPL 이 중성지방 지방산대사에 미치는 역할이고 다음은 혈장 내의 l i p o p ro t e i n 종류의 혈 장내 농도조철 역할이다.
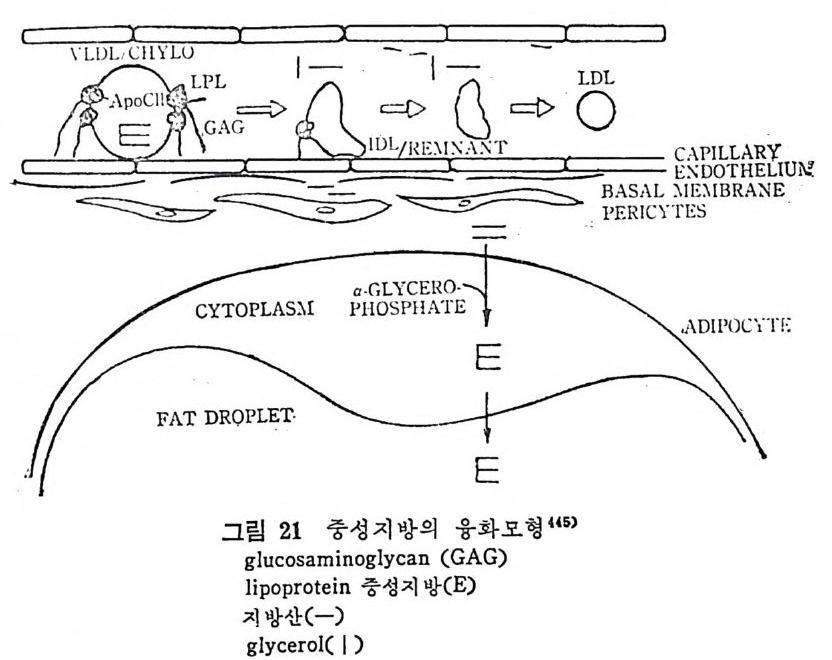 -기 一 LDL
-기 一 LDL
CD LPL 이 중성지방 지방산대사에 미치는 영향 형태학적, 화학적 그리고 면역학적인 실험방법에 의해서 언어진 결과률 종합해 보면 다음 그림 21 에서 보여주듯이 중성지방으로서 의 지방산은 저장과 산화물 위해서 세포에 의해서 취해진다는 일반 一 적인 견해에 수긍이 간다. 순환하고 있는 VLDL 과 ch y lom i cron 은 모세관혈관벽에 부착이 되는데 거기는 생리적으로 활성인 LPL 입자가 endo t hel i al 의 내막 표면에 glu cosami no g ly c an 고리 에 걸려 서 촌재 하는 곳이 다. 454) 이 곳에 효소가 결합하는 현상은 Ap o C- II 가 lip o p ro te i n 입 자와 LPL 사이 에 서 목수한 상호작용이 발생 함으로씨 이 루어 진다고 본다• 456) 이 에 부과해 서 glu cosami no g ly c an chain 과 lip o p ro te i n 표면 구조사 이 의 상호작용과 그리 고 효소와 lip o p ro te i n 내 지 방 사이 의 상호작용 一 이 Iip o p r ote i n 입 자로 하여 금 움직 이 지 못하게 한다고 보고되 었 다. VLDL 의 Ap o B 부위와 IDL 사이 의 관계 와 IDL 과 LDL 사이 의 관계 를 선행물질과 최종물질 관계로 보는 견지에 기초해서 보면 중성지 방의 가수분해는 LPL 이 endoth e liu m 을 따라서 여 러 부위 에 부착되 었다가 다시 떨어졌다가 하는 동안에 이루어진다고 제시하였다 .456) VLDL 입자내에는 36 분자의 Ap o C 개가 포함되어 있음이 계산되 었 다. 457-8) 이 분자수는 lip o p ro te i n 중성 지 방을 최 대 로 가수분해 하 는 데 필요한 LPL 분자수와 거의 일치하며 433) 한 효소에 한 조요소 A p o 단백질 사이의 상호작용 가능성을 in v i vo 에서 제시한 것이다. VLDL 과 chy !o mi cro n 내 에 존재 하는 중성 지 방 모두 거 의 구의 중 십부에 위치하며 이를 국성표면구성물질이 의검으로 싸고 있다. 이 런 형 태 에 서 Ap o C-II 는 VLDL 이 나 chy lo mi cro n 입 자표면에 LPL 이 부착되도록 한 후에 이 입자의 외겹 표면막을 뚫고 들어가는 효 소작용이 아닌 그대로의 침두작용을 중재한다. 또 하나의 기능은 LPL 이 phosp ho lip ase 작용이 있으므로 LPL 이 입자표면의 인지방울 제거하여서 입자 중십부로 쉽게 파고들어가게 할 수 있는 가능성도 있다고 본나 .459) In v it ro 실험에서 VLDL 입자와 정제된 LPL 을 같이 배양시키니까 VLDL 인지방이 40% 까지 분해되었다 .460) 이 사실은 득히 lipo p r ote i n
분해에 현저한 공헌이 될 수 있다는 것을 보여준다. 중심부와 표면의 여러 종류의 지방 용해도에 기초해서 Small458) 은 그 입자에 존재하는 것 중 무게로 10% 의 중성지방이 표면에 존재 한다고 예견하였다. 이러한 상황하에서는 LPL 은 극성표면을 뚫고 들어가지 않고도 쉽게 중십부로 들어갈 수 있다고 생각한다. 그렇 다면 이란 상황하에서는 A p oC-IT 의 역할은 LPL 과 VLDL 또는 chy lo mi cr on 입 자사이 의 결합에 만 작용하는 것 으로 볼 수 있 다. 효소와 중성지방아 접하기만 하면 지방산이 빠르게 생산된다. 이 중의 일부의 지 방산은 순환계 로 나타난다. 462) 그러 나 대 부분의 지 방산은 endoth e lia l 충을 동과해 서 조직 세 포내 로 포화되 어 서 다시 중 성지방으로 재조정되거나 또는 산화된다. 그러나 지방산의 이동기 전은 알려져 있지가 않다. Scow 와 그의 동료는 지 방분해 산물이 모세 관벽 을 측면에 서 스며 나옴으로써 세 포막내 로 이 등되 어 들어 간다고 하였 다. 463) 우유에 서 정 제 된 LPL 과 tri o l ey lg l y c erol 의 의 검 을 사용하여 연 구한 결과, 지 방분 해 산물인 지방산과 MG 는 album i n 과 접할 수 있는 부위로 측면을 동해서 이동되어 나가며 거기서 표면으로부터 흡수된다고하였다 .467) 중성지방함량이 높은 l ip o p ro t e i n 의 분해과정은 인지방, 중성지방 DG, 그리고 MG 의 순서로 이루어질 것으로 본다. 이러한 단계적으. 로 분해되어 가는 과정마다 LPL 의 역할을 살펴보면 중성지방의 분 해시작은 LPL 에 의해서 이루어지고 있음이 Kom pi an g과 그의 동료 에 의해서 제시되었다 .441) 이들은 LPL 에 대항하는 an ti serum 을 닭 의 힐청내에 주사함으로써 중성지방의 이동을 완전히 차단하였다. 유사한 실험 으로 쥐 의 십 장근육에 서 유리 된 LPL 에 항체 를 pe rfu s e 하니 까 chy lo mi cro n 중성 지 방의 up tak e 가 완전히 차단되 었 다. 444) 또 한 LPL 이 결핍된 사람의 혈장내에서 매우 과량의 중성지방이 축적 되 는 현상을 볼 수 있 다. 이 때 에 중성 지 방 함량이 높은 lipo pr o te i n 입자는 LPL 결핍환자에게서 중성지방 가수분해기전이 아닌 것에 의 해서 465-7) 순환혈로부터 이동된다고 하였다. 그러나 정상인에게서는 중성지방 이동의 시초단계는 중성지방분해가 LPL 에 의해서 이루어 쳐야함은 필수단계이므로 아직 LPL 결핍환자의 경우를결론지울수
가 없다. DG 니. MG 가수분해에 LPL 이 관여하는 지는 덜 분명하다. 그러나 DG 나 MG 의 가수분해에 LPL 이 관여하고 있음은 일반적으로 수궁 이 되는 사실이다. in v it ro 에서 LPL 은 I(3) - 위치의 es t er 에 목수 성을 나타내며 둑- 히 l - 위치 에 입체적인 목수성을 나타내므로 465 - 6) 이 사실온 대부분의 실험전과 2 - mono g l y cer i de 문 축적시킨다 . 이러 한 체계 속에서는 효소작용은 아니지만 비교적 속도가 느린 2-m on-og ly c erid e 가 iso meriz a ti on 이 되 어 서 I (3) 지 성 체 로 전환되 는 것 이 속도제 한 단계 (rate - li m i ting ste p ) 라고 일 반적 으로 이 야기 한다. 그러나 MG 가 조직이나 혈장내에 축적되지 않는다는 증거가 in v i vo 실험에서 제시되었다. 최근에 MG hy drolase 활성 이 사람의 혈 장내 혈소판에 서 나타난 사실이 증명 되 었 다. 46” 이 효소는 LPL 에 의해서 생성된 MG 를 더 대사시키는 데 중요한 역할 이 있음을 보여 주었다 .47 1) 지방조직내에서 축출된 he p a ri n 에 의해서 유리되지 않는 MG h y drolase 가 정제되고 그 특성이 연구되었다 .163) 이 효소는 2-MG 에 대해서 높은 촉진작용이 있으며 저장지방의 가수분해에 참여한 다고 한다. 요즈음 이 효소가 gly c erid e 지 방산을 취 해 가는 것 을 돕 는다고 한다. 죽 LPL 에 의해서 생성된 2-MG 를 분해함으로써 중성 지 방으로 동화되 는 동안에 MG 의 축적 을 방지한다. 473) 또한 이 효 소는 in vit ro 에 서 보다는 in viv o 에 서 높은 속도로 모세 관 표면에 서 2-MG 의 iso meriz a ti on 을 가능케 한다. 474) 그러 므로 LPL 중성 지 방 분해시에 MG 의 축적 없이 분해가 이루어지도록 하는 것이다. ® Lip o p r ote i n 의 변형 Chy lo mi cr on 과 VLDL 은 LPL 의 목칭 적 인 기 질이 다. 그러 나 중 성 지 방 함량이 풍부한 lipo p ro te i n 으로부터 LDL 형 성 에 이 르기 까지 전과정 지방분해에 LPL 이 작용하는 것인지 또는 다른 지방분해과 정이 여기에 개입되는지에 대해서 논란이 있다. Hep a ti c lip a se 는 IDL 이 나 chy lo mi cr on remnant 를 LDL 로 변형 시 키 는 것을 촉진함으로써 중성지 방이 풍부한 lip o p ro te i n 분해 의 마솔 지막 단계를 중재한다는 사실을 반복적으로 제시하였다.
현재 제시된 중거에 따르면 LPL 은 전체 분해과정을 담당한다고 본다. 첫째로 우유에서 정제된 LPL 은 in v it ro 연구에서 보면 VLDL 로부터 460),475- 7 ) LDL 비중에 속하는 입자를 생산할 수 있다고 본다. 그런데 이때 생성되는 LDL 의 구성성분은 정상 혈장에서 발견되는 LDL 의 구성성분과 약간 다르다고 한다. 둘째는 쥐의 실험에서 보 면 간을 순환계 통으로부터 제의 해 놓고도 in viv o 연구에 서 VLDL 에서 LDL 로 대사시킬 수 있다는 것은 간 이외의 조직에서 이루어 집을 침작할 수 있다 .478) 마지막으로 간질환이 있는 사람의 IDL 아 나 LDL 내의 중성지방 농도는 he p ar i n 으로 처리되고 난 후의 혈 청내 LPL 활 성과 현저한 상관관계를 보인다 .479) 이 현상온 지방 분 해 전 과정 동안에 중성지방 가수분해에 LPL 의 두드러진 역할을 증명해 준다. VLDL 과 ch y lom i cron 의 분해가 이루어지는 동안에 표면물질인 인지 방, uneste r if ied 콜레 스테 롤 그리 고 apo lip o pr o te i n 이 HDL 로. 이동된다 427),476),480) 이들의 정확한 이동기전은 아직 분명하지가 않 다. 한겁충으로 이루어져 있는 VLDL 과 ch ylom ic ron 의 표면충 구 성물질은 같지 않기 때문에 역시 이들의 이동과정도 질적으로 볼 때 간과 장내에서 각각 다르다. in v it ro 연구에서 HDL3 촌재하에 LPL 에 의한 VLDL 의 지방분해결과 HDL2 가 형성되었다 .475) 이 결 과는 HDL3 와 HDL 과이 의 상호대 사가 관련이 되 어 있음을 보여 주 고 있다. 죽 HDL2 소립자 일부는 VLDL 의 표면충 구성물질이 HDLa- 로 이동됨으로써 생성된 결과라고 보며 이로 미루어보면 LDL 은 혈 장내 의 VLDL 분 아니 라 HDL2 의 농도까지 조철한다고 볼 수 있 다. 많은 연구자들에 의해서 in v i vo 실험에서 VLDL 과 HDL 의 농도 사이에 서로 역의 관계가 있다는 사실이 증명되고 난 후에도 ,481-2) 죽 VLDL 의 농도가 증가되면 HDL 의 농도는 감소되고 그 반대 현 상도 사실인 것을 고려해 볼 때 HDL 의 어떤 종류가 바로 VLDL 의 분해산물이라는 생각을 할수있다. 예로서 만성적인 알코올중독 환자에 서 hep a rin 처 리 된 후의 혈장에 서 나 지 방조직 내 에 서 모두 483) LPL 의 활성 이 증가되 면서 이와 관련해서 HDL2 의 농도가 선택 적으 로 중가되고 있음이 나타났다. 이 사실온 in vi vo 연구와 in vitro
연구에서 Pa t sch 와 그의 동료 475) 에 의해서 연구되어전 사실과 평행 된 da t a 를 보여주고 있다. 앞에 서 논의 된 바에 의 하면 chy lo mi cr on 과 VLDL 이 대 사적 으로 변형되는 것은 유사한 현상으로 취급되어 왔다. 그러나 위에 지 적 했듯이 VLDL 과 chy lo mi cr on 표면충의 구성 성 분 대 사산물은 같 은 산물을 생 성하지 않는다. 4sn VLDL 과는 대 조적으로 새 로이 생 성 된 림 프 chy lo mi cro n 은 상당량의 Ap o A-I 이 함유되 어 있 다. 485) 이러한 ap o p ro t e i n 의 합성과 분바는 장내세포의 배양실험에서도 증명되었다 .486) 중성지방이 존재하는 중십부위에 지방분해과정동안 에 chy lo mi cro n 으로부터 의 표면 껍 질충의 구성 성 분은 Ap o A- I 과 Ap o C 를 함유한 인지 방-콜레 스데 롤의 복합체 구성 의 결과라고 생 각한다. 이러한 입자는 LCAT 에 의해서 혈장내의 구형의 HDL 입자 로 변형된다고 제시되었다 .484) 이러한 표면충 구성물질의 변형과 대사에 대한 LCAT의 정확한 역할은 요츠음 흥미있는 연구분야이다. LCAT 의 작용은 비교적 느 리 다고 지 적 되 고 있 다. 중성 지 방이 풍부한 lipo p ro te i n 의 표면충으 로부터 유출되어 나오는 유리 콜레스데를이 참정적으로 RBC 의 원 형질막에 영합되는 사실을 하나의 완충작용으로 본다. 왜냐하면 이 작용이 바로 chy lo mi cro n 의 분해 로 인해 서 빠른 속도로 유출되 어 나오는 유리콜레스테롤의 참정적인 처리작용이 되기 때문이다 .476) @ LPL 의 조철 혈장에 의해서 이동되는 3 가지 주요 에너지원은 주로 포도당, 지 방산 그리 고 lipo p r ote i n 내 의 중성지 방으로서 상호 호르몬의 기 전 에 의해서 관련이 있으며 이들은 고도로 섬세한 기능이다. 조철작용은 여 러 단계 에 서 이 루어 지 며 lipo p ro te i n 중성 지 방대 사의 가장 중요한 조절작용이 이루어지는 부위는 혈청내 중성지방이 조 직 으로 동화되 어 가는 기 전이 다. lipo pr o te i n 중성 지 방의 가수분해 율 이 혈장 중성지방울 조직이 취해가는 데 있어서 가장 제한울 주는 작용이라는 증거가 있다. 이 가수분해율에 영향을 미치는 기전이 2 가지 있으며 이들은 상호작용을 이루고 있다. 첫째는 혈청내 중성 지방농도에 영향을 미치는 중성지방이동의 피동적 조철이며, 둘째
는 lip o p r ote i n lip a se 활성 에 의 한 능동적 조철이 다. 기 중성지방 이등의 피동적인 조절 사람에 게 서 식 이 chy lo mi cr on 중성 지 방을 간헐적 으로 순환계 로 보 내 주는양은 1 일에 50~100 g정도이다. 또한간으로부터 · VLDL 의 형 태로서 24 시간 동안에 20~50 g의 중성지방을 순환계 혈액으로 보내 준 다. 안정된 상태하에서도 혈장으로부터 중성지방의 이동량은 약 70~150 g으로서 혈청 내로 들어오는 양과 같은 양이 된다. 그러므로 힐장내 중성지방의 p ool 의 크기는 비교적 작아서 2~5 g정도이다. 그러나 할청으로부터 의 중성지방 이동기전에 아주 부수적인 손상도 중성지방 p o 이크기에 영향을 미찬다. 그래서 중성지방의 이동량이 중 가된다. in viv o 에 서 보면 중성 지 방의 이 동기 전에 서 LPL 작용이 충분히 포화되 지 는 않는다고 본다. 487-8) 혈장내로 들어가는 중성지방량이 증가되면 혈장내 중성지방의 농 도는 증가되며 따라서 매시간당 혈장으로부터 이등되는 중성지방 의 양도 중가된다. 이동량이 최고치에 달했을 때도 이미 혈장내의 중성지방함량은 정상 수준을 넘어선 수준이다 .489) 중성지방 이동률 의 차이는 LPL 활성의 변화없이도 이루어진다. 중성지방 이동에 있어서 피동적 조철기전의 기초적인 현상은 위 에 제시했듯이 각각 다른 조직들이 다른 울로써 중성지방울 취해 간 다논 현상을 고려해 넣지 아니한 것이다. 그 조직에 특수한 LPL 의 종류는 lipo p ro te i n 중성 지 방 기 질에 대 해 서 각기 다른 찬화력 이 있 다는 것도 생각해 보아야 할 문제라고 본다 .490) Fie l din g 과 그의 동료는 434) 쥐 로부터 2 종류의 lip o p r ote i n lip a se 를 유리해 내어 이들의 분자구조와 효소로서의 특칭을 규명하였다. 한 종류의 효소는 십 장에 촌재 하는 것 으로 chy lo mi cr on 중성 지 방에 고도의 찬화력이 있으며 또 다른 종류의 효소는 지방조직내에 촌재 하는 것으로 이 기질에 대해서 비교적 낮은 찬화력을 가지고 있다. 이들의 Km 치는 각각 o.07mM 이고 o.7omM 이다. 이 K 근]로 미 루어보면 혈청내에 정상 중성지방수준으로써 십장근육에 촌재하는 LPL 은 기질과 포화될 수 있지만 지방조직에 촌재하는 LPL 은 그렇 치 못한 것으로 본다.
석사를 하지 않는 시간에는 혈청내 중성지방 수준은 낮다. 그러 므로 지방조직으로 중성지방울 취해 가는 양도 낮다. 그러나 한편 십장근육내 LPL 의 중성지방에 대한 찬화력이 높기 때문에 십장근 육내로 중성지방이 취해쳐 가는 양온 비교적 높은 울을 유지한다. 식사 직후에는 혈장내 중성지방농도가 증가되며 지방조직은 LPL 이 포화되지 않았으므로 중성지방울 취 해 가는 양이 증가된다. 그러나 십창근육은 여전히 중성지방울 취해 가는 양이 증가되지 않고 일정 한 수준을 유지 한다. 왜 냐하면 LPL 이 포화되 었 기 때 문 이 다. 이 두 종류의 LPL 은 각각의 조직에서 요구하는 에너지양에 따라 서 지속적으로 그리고 피동적으로 작용한다 . 45 1) 묵텔 히 이 기전은 영양상태에 관계없이 십장근육내로 중성지방 지방산의 일정량을 공 급하는 데 의의가 크며 또한 지방조직내에 여분의 중성지방울 저칭 _ 하는 데도 뜻이 있다. 노 LPL 활성의 능동적인 조절 피동적인 조철과는 대조적으로 능동적인 조절은 효소 활 성에 현처 한 변화를 가져오는 특 칭이 있다. 예를 들어서 식이섭취 후 동물의 지방조칙내에는 굶은 동물의 지방조직내에 바해 LPL 활 성이 높다. 그런데 십장근육내에서는이와반대현상이 나타난다. 이러한효소활 성의 변화는 아마도 호르몬의 영향을 받는 것으로 본다. 인슈란, ACTH, pr olacti n, ep ine p h rin e 의 지 방조직 내 LPL 활성 에 관련 된 영향은 잘 알려져 있으나 심장근육내에 존재하는 LPL 의 활 성에 대 한 호르몬의 영 향은 아직 분명 하지 않다. 45 2) LPL 은 간세포에서 합성되는 것으로 보며 세포내에서 변형되어 (그립 22 참조) 분비되어 모세혈관 endo t he li um 으로 이동된다. 거기 서 lum i nal 표면에 결합된다. 이러한 체계의 대부분을 지원해 주는 자료는 쥐의 지방조칙으로부터 유도된 것이며 쥐의 십장근육으로부 터는 제한된 자료밖에 없다. 세포내의 활성화된 효소의 p ool 의 크기는 비교적 일정하며 이의 반감기 는 4 시 간이 다. 493) 먹 인 동물과 굶긴 동물의 지 방세 포를 유리 해 서 494-5) 굶간 동물의 지 방세 포를 인슈린으로 처 리 해 보니 까 496) 여 전히 동량의 활성화된 LPL 이 함유되어 있었다. 먹인 동물과 인슈
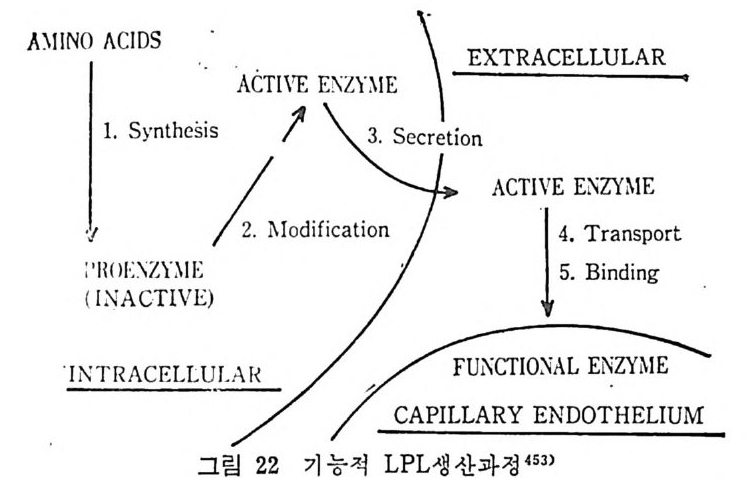 A\IINO AC IDS At m ; ';'.'ZrnE \ EXTRACELLULAR
A\IINO AC IDS At m ; ';'.'ZrnE \ EXTRACELLULAR
란으 로 처리된 동물의 지방조직에서 증가된 효소의 활성은 전적으 ` 로 세포 밖 (ex t rncelIular y)에 촌재하는 효소의 활성 때문인 것으로 ` 본다. 그러나 식이룬 섭취시킨 후나 인슈란으로 처리된 동물에게 서 LPL 의 활성이 증가되는 것은 새로운 단백질의 합성 때문인 것 인지 아니떤 이미 촌재하는 단백질의 변형 때문인 것인지에 대한 질문이 생간다. 그런데 요즈음 많이 보아는 면역적정(i mmuno titr a ti on) 방법에 의해 서 굶간 쥐와 먹인 쥐의 지방조직으로부터 유리된 효소의 특정활성 을 측정해 본 결과 효소의 활성과 효소단백질의 율은 같았으나 전 체 활성은 3 배나 달랐다. 그러나 대부분의 LPL 의 활성이 굵은 쥐 에게서는 지방세포내에 촌재하며 며인 쥐에게서는 세포 밖에 존재하 기 때문에 4 9 4-6) 면역적정 실험의 결과에서 보여준 바는 LPL 활성상 태가 지방조직내나 세포 밖이나 갈은 수준이었다고 생각할 수 있 다. 이미 촌재하고 있는 활성화되어 있는 효소에 변형이 나타나서 세포내에 효소활성의 증가가 나타난 층거는 보여주지 아니하였다. Ashby 와 그의 동료는 굽은 쥐 의 지 방조직 내 LPL 의 활성은 포도 당, 인슈란, 아마노산 그리고 c y clohex i m i de 와 함께 배양했을 때 2 시간 내에 2~3 배로 증가되었으나 단백질생합성의 94% 가 방해되 었다고 보고하였다. 이 연구견과는 아미 합성되어 있는 pro enzym e
이 지방세포내에서 활성화 되는 것으로 설명하고 있다. 또 한편 지방세포의 원형질막이 LPL 의 조철부위라고 치적하였 다 (그립 22 ste p 3 참조). 인슈란으로 처 리 한 취 의 지 방세 포에 서 의 LPL 의 분비율은 대조군에 비해서 건과적으로 크다 .496) 쥐에게 포도당 을 위장내 로 주입 시 키 고 난 후에 hep a rin 으로 pe rfu s ed 된 십 장으 로부터 유리되는 LPL 의 활성 은 원래 값 (value) 의 I / IO 로 감소되었 다. 그러 나 십장근육내 LPL 의 함유수준에 는 변화가 없 었 다. 494) 아 마도 hep ar i n 에 의해서 유리되는 LPL 의 활성은 그립 22 의 4 와 5 단계와 관련이 있다고 본다. 쥐 의 심 장내 에 촌재 하는 모세 관 endoth e liu m 내 기 능적 효소의 정 상 전환시간(t urnover ti me) 을 약 2 시간으로 볼 대i 93),498) 이 부위는 세포로부터 효소의 분비에 의해서 새로와지는 윤이 조직에 의한 중 성지방 섭취에 영향을 빨리 나타낼 수 있다. 십장에서 LPL 의 활성적인 조절이 혈액내의 중성지방이 풍부한 l ip o p ro t e i n 의 농도에 의해서 이루어진다는 두 연구가 제시되었다. 혈청 VLDL 이나 또는 먹인 동물의 혈청을 신생 십장세포 배양에 첨 가한 결과 LPL 의 활성이 50% 나 감소되었다 . ·199 ) 이러한 감소현상 온 배양 위치에 유리지방산울 첨가하여도나타난다. 이 결과는 중성 지방가수분해로 유리되는유리지방산이 LPL 활성에 영향을 미칠 수 있다는 것을 보여주었다. 그런데 in v i vo 연구에서 4-ami no p yra zole- [3, 4- 선-py r i m i d i ne 을 사용하면 순환하는 VLDL 양이 감소되 며 쥐 의 심장근육내의 LPL 의 활성이 증가되는 것이 관찰되었다. 그런데 VLDL 을 주사하니 까 22 시 간 후에 이 현상이 반대 로 바뀌 었 다. 500) 가수분해 가 진행 되 고 있 는 동안에 는 LPL 분자가 chy lo mi cr on 이 나 VLDL 에 부착되 어 있으며 endoth e liu m 에 서 떨어 져 나와서 순환 중의 혈액 내 에 존재 하계 된다. 이 때 에 부분적 으로 분해 된 lip o p ro - te in 입 자와 함께 촌재 한다. LPL 분자가 lip o p r ote i n 분자에 결 합되 어 서 촌재 하고 있는 상태 가 바로 lip o p ro te i n 이 분해되 고 남은 분자 (remnan t)를 간으로 하여 금 취 해 가라는 자국이 될 수 있 다고 하였 다. 501 ) 분명히 LPL 은 순환계로부터 빠른 속도로 이동되기 때문에 단지
대단히 낮은 LPL 의 활성량이 정상적인 혈액 중에 남아 있게 된다. 동위원소로 처리된 우유 LPL 을 쥐에게 주사했더니 첫번 반감기가 1 분이었으며 동위원소 7 0% 가 10 분만에 간에서 모두 발견되었다 .502) LPL 은 간조직에 의해서 효율적으로 이동되며 이 현상은 순환하고 있는 LPL 의 수준을 낮게 유지시켰다. 앞에서 논의한 증거에 의하면 요즈음 LPL 조절연구는 주르 LPL 합성과정, 이동과정 그리고 이의 활성에 관한 연구에 촛접이 모아 치고 있다. 여러 종류의 호르몬과 LPL 작용과의 관계는 지방조직, 십장, 유선 503) 둥에서 서술적으로 연구되어 있다. 앞으로 여러가지 호르몬과 LPL 과의 상호작용에 관련된 연구가 여러 조직에서 이루 어져야 한다. 지금까지 논의되어 온 많은 연구는 주로 쥐의 지방조칙에서 실험 되어진 것이다 .192),495),501) 그러나 십장근육, 유선 둥에서도 유사한 - LPL 체계가 존재한다는 것이 밝혀지고 있다• 하나의 기본적인 현상 은 LPL 은 간세 포에 서 합성 되 어 서 endoth e lia l 세 포에 서 작용한다. 이 endoth e lia l 세 포는 LPL 을 합성 하거 나 분비 하지 않고 오로지 LPL 을 아 세포에 결합시킨다. 3) LPL 의 활성파 Lip o p r ote i n 구성성분과의 관계 In vit ro 연 구에 서 몇 종류의 lip o p ro te i n 의 구성 성 분이 LPL 활성 에 영향을 미치고 있음이 증명되었다. 중성지방 함량이 풍부한 lip o - pr ote i n 의 지 방제 거 과정 중에 지 방과 ap o !i po p r ote i n 의 함량비 가 변 화한다. 아마도 중성지방 가수분해와 합성작용에 의한 여러 종류의 lip o p r ote i n 구성 성 분의 농도가 조철기 전의 역 할을 할 가능성 이 농후 하다고 본다. Ap o C-II 는 in vit ro 실 험 에 서 LPL 활성 을 크게 중가시 킨다. 이 러한 현상은 여러 종류의 급원으로부터 유리된 효소에서 증명되었 다. 이 조요소 (co fa c t or) 는 효소와 기질 사이의 찬화력울 증가시키 논 것은 아니고 유화된 중성지방의 기질과 작용할 때 최고의 작용 윤을 나타낸다. LPL과 Ap o C-II 는 상호작용함으로써 대 단히 안정 된 복합물을
만든다. LPL 과 Ap o C-II 복합체 의 분리 계 수 (d i ssoc i a ti on cons t an t)는 〈 10~8M507) 이고 또 다른 실험실에서는 3X 10 -3M5 06) 로 나타났다. LPL 의 가수분해 율은 Ap o C-II 의 농도에 의 촌된다. Ap o C-II 의 농 도가 증가하면 따라서 이 효소의 가수분해울도 중 가하며 효소와 A p oC-II 의 비례가 I : I 일 때 최고울에 달한다 .505) 그러 나 Ap o C-II 에 의 한 이 효소활성 은 ap o lip o p r ote i n 이 기 질 과 작용함으로써 비 롯된 결과인지 또는 효소와 Ap o C- JI 가 작용한 결 과인지 에 대 한 현상온 불분명 하다. 507 ) Gackson 과 그의 동료들에 의 한 Ap o C-II 분자내 의 아미 노산 배 열의 결정 은 508> Ki nn unen 과 그의 동료들이 509) 우유 속에 존재 하는 LPL 의 활성에 팔요한 아미노산의 최소 범위의 배열을 인지해내는 데에 결정적인 정보제공을 하였다고 본다(그립 23 참조). CNBr(cya noge n bromi de ) 입 자가 Ap o C-II 분자의 아미 노산 배 열 의 1~9 번과 10~59 번째에 관련있는데 이 부위는 적어도 A p oC-II 의 활성에 능력이 없음이 나타났다. 그러나 COOH 끝의 CNBr 부위와, Ap o C-II 분자내의 아미노산 60~78 번째와 같은 배열의 합성팹타 이드가 가수분해울을 3 배에서 4 배로 증가시킨 데 비해서 같은 농도 의 Ap o C-II 는 가수분해율을 9 배로 증가시켰다. 이 결과와는 대조
 Thr·Glu-Gln·Pro-Gln-Gln-Asp· G lu·Met· P ro-Ser·Pro·Thr·Phe-L e u-
Thr·Glu-Gln·Pro-Gln-Gln-Asp· G lu·Met· P ro-Ser·Pro·Thr·Phe-L e u-
적으로 합성된 펩타이드부위, 죽 아미노산 배열부위 55 년째로부터 78 번째는 Ap o C-II 에 의해서 나타나는 효소활성량의 IO% 내의의 활성량을 실험적으로 나타내 주었다. 그러나 합성된 펩타이드 55~66 번째는 효소의 활성을 나타내지 않았다. 그리고 60~78 번째 부위에 존재하는 g l y-g lu- g lu 의 COOH 기를 CNBr 과 작용시켜서 COOH 기의 특성을 상실하게 하면 이 펩 타이드로 효소의 활성은 오히려 없어전다. 다시 말하면 55~78 번째 의 아미노산은 효소를 활성시키나 이 중에서 66~78 번째를 따로 데어서 실험해 보니까 효소의 활성이 나타나지 않았다. 그러면 효 소의 활성부위 는 분명히 55~66 번째 사이에 촌재하며 60~66 번째 사이 에 존재 한다고 추리 되 고 두 분자의 포도당-포도당의 COOH 가 효소활성 에 팔요하다고 볼 수 있 다. 이 연구를 요약해 보면 A p oC-II 단백질의 LPL 활성에 팔요한 최 소 부위논 아미노산 55 번과 78 번째 사이라고 본다. 그리고 이 부 위 중 55~65 번째 에 존재 하는 2 분자의 COOH 기 에 의 해 서 LPL 과 Ap o C- II 사이의 상호작용이 이루어지며 이 결과 효소의 작용률이 상승된다고 본다• 그리 고 Ap o C-II 의 49 번째 아미 노산에 존재 하 는 ― NH2 기 에 의 해 서 인지 방과의 상호작용이 이 루어 전다. 510) Ap o C 내 분자의 NH2 끝부위는 양성 의 heli ca l 구조를 가지 고 있 으나 COOH 끝부분은 이 러 한 특징 을 보여 주지 않는다. 511) 그런데 Ap o C-II 의 NH2 끝부분은 인지 방과 결합하는 데 사용되 며 COOH 끝부위는 LPL 을 활성화시키는 데에만 역할이 있으며 기질을 결합 하는 데는 사용되지 않는다. LPL 의 활성은 MG 나 수용성 기질에 대해서는 A p oC-Il 에 의해서 상승되지 않는다 .447-8) 이 사실온 수 용액과 지방의 단면이 A p oC-II 에 의한 LPL 의 활성화에 참여한 다고볼수있다. Perfu s ed 십 장근육에 서 modif ied chy lo mi cr on 을 가지 고 한 연구 에 서 정 상 chy lo mi cr on 에 함유된 Ap o C-II 의 함량은 chy lo mi cr on, 중성지방의 정상 가수분해를 진행하는 데 필요한 양 이상으로 촌재 하고 있다고 보고하였다 .512-3) 한편 A p oC-II 가 전적으로 결핍되면 고중성지방혈증을 유발하는데 이는 정상혈청을 두입하면 극적으로
감소함을 보인다 .514) 여하튼 현재까지 제시된 중거로 미루어 보면 A p oC-11 는 중성지방 가수분해에 팔요한 물질이나 정상적으로도 중 성 지 방이 풍부한 lip o p ro te i n 의 분해 에 속도제 한 요인이 될 수 없 다 (A p oC- JI와 LPL 과의 좀더 자세한 내용은 지방조칙의 지방대사의 LPL1 i/- 분 참조). Ap o C-I 447-9) 과 C-Ill435-44) 그리 고 E452)71- in vit ro 에 서 LPL 활 성을 방해한다고 증명되었다. 방해하는 범위는 독정한 실험조전 과 515) 효소의 급원 그리 고 순도에 따라서 다르다• pe rfu s ed 쥐 의 심 장근육에 서 Ap o C-I 과 Ap o C-I[ 가 chy lo mi cr on 가수분해 에 아무 런 영향이 없었음이 밝혀졌다. 이 사실온 in v i vo 에서 이들 ap - o p ro t e i n 들아 중성지방 합성대사에 영향을 미치지 않는 것으로 본 다. 513) . 이 러 한 ap o lip o pr o te i n 에 부과해 서 중성 지 방함량이 높은 lip o p ro - tei n 의 표면충 구성지 방이 LPL 활성 의 조철요소로서 지 적 되 었 다. 어 떤 in vitro 연구에 서 중성 지 방의 가수분해 는 lys o p h osp h ati dy lc ho- lin e 이 존재함으로 인해 서 크게 자국을 받으며 기 타 다른 인지 방의 촌재에 의해서도 정도는 좀 낮지만 자극을 받는다 .440),513),514) 그러 나 in vitro 연구에 서 chy lo mi cr on 의 표면충에 서 ph osp h ati dy k ho- l i ne 을 제거해도 LPL 에 의한 중성지방 가수분해가 영향을 받는 것 같이 보이 지 않았다. 459> uneste r i fied 콜레 스테 롤이 in vit ro 에 서 LPL 활성에 크게 영향을 미찬 것으로 나타났다. 죽 유리콜레스데몰 의 농도가 낮은 수준에서는 중성지방 가수분해도 국적으로 감소하는 원인이 되었음이 나타났다 .442),5l8) 그러나 p erfu sed 십장연구에서 각 각 다른 수준의 콜레 스테 몰의 함량 수준에 서 도 chy lo mi cr on 의 가 수분해율에 영향이 미치지 않았음이 나타났다 .459) 이 상의 모든 결과를 종합해 보면 중성 지 방 함량이 높은 lip o p r ote i n 의 표면충을 구성하고 있는 지방들이 콜레스테롤 이동에 조전요소 로서의 역할이 있는 것으로 생각한다. 4) LPL 활성에 영향을 미치는 기타 요인 LPL 이 endoth e li al 세 포에 결 합되 는 데 는 hep a rin 과 같은 물질의
역 할이 있 으며 이 에 부과해 서 hep a rin 은 LPL 작용을 조철할 수 있 고 따라서 중성지방울 대사시키는 역할이 있다고 본다• LPL 은 hep a rin sulfa te po lym er 와 전극적 으로 안정 되 게 결 합되 어 서 endoth e lia l 세 포표면에 부착되 어 있 으며 부착된 형 태 로 혈관 내 부에 서 endoth e lia l 세 포표면으로부터 20~50nm 정 도로 뻗쳐 있 다. 519 ) Hep a rin 이 LPL 활성 에 영 향이 있 다는 것 은 in vit ro 연구를 통해 서 이 견해에 기초 를 이룬다. 대부분의 연구는 he p ar i n 의 농도가 낮은 수준에 서 도 효소의 작용을 상승시 키 며 농도가 높은 수준에 서 도 방해 물 한다고 증명하고 있다 .520) 그러 나 한편 고도로 정 제 된 효소는 hep a rin 에 덜 예 민하다. 521 ) 또한 glu cosami no g ly c an 의 구조가 LPL 과의 상호작용에 영 향을 미 치 는 것 으로 보인다. 522) 다양한 분자량을 가전 hep a rin 입 자가 LPL 작용에 각기 다른 영 향을 미 찬다고 하며 또한 hep a ri n dep o lym er- ase523> 조철기능을 가졌다고 제안되기도 하였다. 그러나 아직까지 in viv o 실 험 에 서 hep a rin 이 나 다른 glu cosami no g ly c an 이 LPL 조철 에 있어서 어떤 역할이 있다는 증거는 없다. 그러나 acid pla sma gly c op r ote i n 인 orosomucoid 가 LPL 의 조요소로서 의 기 능을 하므 로 중성지방이동에 참여한다고 제시되기도 하였다 .524) 그러나 이에 대한 연구는 더 전행되어야 한다고 본다. (3) Hep at ic lipa se Chy lo mi cr on 과 VLDL 의 기 초적 인 가수분해 가 말단조직 의 모재 관에서 LPL 에 의해 이루어진다고 생각하며 더 나아가서 LPL 입자 는 간에서 생성된다고 본다. 그러나 간에서 생성되는 l ip ase 는 여러 종류의 기질, 죽 MG, DG, 중성지방 그리고 인지방까지도 가수분 해시킬 수 있는 능력이 있다고 i n vit ro 연구에서 밝혀졌으며 43 7) 525-6) 요즈음은 이 효소가 in viv o 연구에 서 Iipo p ro te i n 대 사에 관련된 기 능울 가지고 있는지에 대해서 연구가 진행되고 있다. LPL 이나 마 찬가지로 간에서 합성되는 중성지방 lip ase 는 중성지방 가수분해시
에 최 적 의 p H 가 8~9 이 나 LPL 과 다론 접 은 ap o lip o p r ote i n 활성 제 를 요구하지 않으며 또 고농도의 NaCl 이 나 pro ta m i ne 에 432) 의 해 서 작용에 방해를 받지 않는다. 이 효 소의 분자량은 쥐의 간으로부터 정 제 된 것 으로 62, 500 이 다. 526) 정 제 된 hep a ti c lip a se 와 hep a rin 으로 처리되기 전 사람의 혈청으로부터 청제한 LPL 은 같은 아미노산 구성을 가졌고 펩타이드 지도(p e pti de ma p)도 같았으나 오로지 다론 것은 탄수화물 부분이 있는 것이라고 보고되었다 .43 2) 그러나 보다 고도로 정제해 보면 이 두 효소는 면역학적으로 차 이가 있으며 따라서 아미노산 구성이 다르다는 것 이 증명되었다 527 ) (표 11 참조 ). J ansen 과 그의 동료에 의해서 in v it ro 연구에서 보고 된 바에 의하면 이 효소 활성량의 80% 이상이 쥐의 간에 hep a rin 울 p erfu se 했을 때 유리되었다고 보고하였다. 이와 같 이 hep a ti c lip a se 의 빠른 분비 는 이 효소가 세 포 밖에 존재 한다는 사실을 암 시한다. 간조직 세포를 쥐의 혈청이 포함된 배지에서 배양시켰더니 그 배 지에서 시간에 따라서 l ip ase 활성이 증가되는 결과가 나타났으며 이 결과로 간세포가 hep a ti c l ip ase 합성부위라는 것이 제시된다 .528) 이 러한 견지에서 보면 간도 지방조직이나 마찬가지로 한 종류의 세포 가 LPL 을합성하고분비하며 그후분비된 LPL 은다른세포에 걷 합이 되며 거기서 대사활동이 전개된다• Anti se rum 을 사용하여 서 얻 어 진 hep a ti c lip a se 의 세 포밖에 위 치 하는 증거가 제시되었으며 이 결과 간에서 endo t he li al 세포 포면 이 이 효소의 작용부위라는 사실이 명 확해졌 다. 529) Hep a ti c lipa se 는 in vitro 실 험 에 서 보면 lip o pr o te i n 과 작용하였 을 때 그 분해작용이 낮았다. 그리고 in v i vo 연구에서 보여준 바는 hep a ti c lipa se 의 활성 과 lipo p ro te i n 내 의 중성 지 방 농도 사이 에 현 처한 관련이 없음이 나타났다. 이 결과는 hep a ti c lip ase 가 혈청 으 로부터의 중성지방이동속도 조철요인으로 작용하지 않음을 제시해 준다. 그러 나 hepa ti c lipa se 의 활성 아 아주 낮으면 이 는 차라리 간 세 포 손상의 반영 으로 본다고 하였 다. 530' Ni kk il a 와 그의 동료에 의 해 서 연구되 어 진 바에 의 하면 531' hep a ti c lip a se 에 길항하는 항체
룬 주]에게 주사하였더니 헐 청내 LDL 과 HDL 내의 콜레스데몰과 인 지방의 현저한 축적이 이루어졌음이 나타났다. 그러나 anti se rum 은 l ip o p ro t e i n 내의 콜레스데롤농도에 아무런 영향을 미치지 않았으 며 또한 LDL 의 단백질농도에도 영향 을 미치지 않았다. 이 결과로 볼 때 hep a ti c lip a se 의 한 가지 기 능은 he p a ti c lip a se 가 간을 동과 하는 동안에 LDL 과 HDL 입자로부터 콜레스데폼과 인지방울 이동 시킨다는 것 이다. 한편 hep a ti c lip a se 가 중성 지 방과 MG 의 분해 작용에 참여 하는지 에 대 한 확 신이 서 있 지 않으며 526) 중성 지 방 가수분해 작용과 ph osp- holip a se A 의 작용에 이 효소의 작용이 있 다는 증거 가 hep a rin 을 함유한 쥐의 간 p er fu sa t e 526) 와 he p ar i n 처리한 혈청을 사용하여서 실험 한 결과 나타났다. 526) Wait e 와 그의 동료들 은 MG 가수분해 작용아 간세 포의 원형 질막에 서 이 루어 진다고 하였 다. 532> in viv o 에 서 원숭이 의 ch y lom i crons 과 VLDL 을 동위 원소로 처 리 하여 이 에 정 제 된 우유 lip o p r ote i n lipa se 몰 사용하여서 MG 를 in v it ro 에서 준비하였다. 쥐 간에서 유리된 간 세포를 MG 에 작용시키니까 MG 불 분해하였고 그리고 나머지 MG 는 album i n 과 LDL 또는 HDL 에 결 합되 었 으며 chy lo mi cr on 의 중성지방에는 결합되지 않았다. 이 결 과 MG acy l h y drolase 가 hep a ti c lip a se 와 같은 효소가 아닌가 하는 추측도 하였 다. 또한 colla g enase 로 처리하니까 중성지방 가수분해작용이 선덱적 으로 이루어지지 않았으며 이는 아마도 중성지방 결합부위가 분리 된 것 으로 본다. 533) 반대 로 MG acy l hy d rolase 를 dete rge nt 로 처 리 하니 까 중성 지 방 가수분해 작옹이 오히 려 aff ini t y chromato g ra p h y 에 의해서 유도되었다 .534) 그런데 사실상 간에 의해서 남아 있는 입 자, 죽 MG 의 아 동시 에 monoacy lg l y c erol hy d rolase 의 역 할의 model 은 제 안된 hep a ti c lip a se 의 기 능과 유사하다고 본다. 536) 이 는 지 방분해효소로서 간세 포 표면의 chy lo mi cr on 과 VLDL remant recep tor 부위 에 서 작용한다고 본다. 이 지 방분해효소에 의 해서 입자에 있는 기질인 MG 와 중성지방이 가수분해됨으로써 간세포 rece pt or 에 의해서 인지될 수 있는 결합부위가 노출되게 된다. 그러
면 이 rece pt or 부위에 전체 입자가 걷함될 수 있으며 결합되고 난 후에 endocy tos is 에 의 해 서 취 해 지 며 마지 막으로 lys osomal 분해 문 거치게 된다. 8 L ip o p ro t e i n 의 상호전환대 사 사람과 쥐에 있어서 l ip o p ro t e i n 은 간과 소장에 의해서 합성되며 혈청 내 로 신생 입 자 (nascen t p ar ti cle) 로써 분비 된다. 536) 정 상인의 혈 청내에서는 이와 같이 분비된 입자의 반감기가 대단히 짧기 메문에 쉽게 발전이 되지 않는다. 효소에 의한 분해작용과 효소가 개입되 지 않은 이동현상의 복합작용에 의해 이 기본입자는 힐청내 VLDL 과 HDL 내로 빠르게 이동된다. 신생입자가 할청내로 분비되어서 혈청내 l ip o p ro t e i n 으로 변형되는 현상에 대한 문헌이 요즈음 관찰 되었다. 537-8) (1) VLDL 과 Ch ylom i cron 대 사 ―중성 지 방이 풍부한 Lipo pr o te i n s 중성지방 이동의 기본적인 기능은 지방산으로서 처장과 산화 를 위 해서 여러 조직으로 공급해 주는 것이다. 사람에게 있어서 24 시간 동안에 소장과 간으로부터 말단조직으로 70~150 g의 내자와 의자 중 성지방이 분산되고 있다. 이러한 l ip o p ro t e i n 체계의 조기능 (aux ili ar y) 의 중요성은 말단조칙세포로 콜레스테풀을 공급하여서 세포막과 호 르몬을 합성하는 것이다. 중성지방이 풍부한 입자는 간에서 합성되 거나 장내에서 합성된 ch y lom i cron 둥 모든 것은 유사한 대사경로 를 통해서 대사된다(그립 14 참조). HDL 입 자로부터 LPL 을 활성 화시 키 는 ap o lip o p ro te i n 인 Ap o C-II 가 VLDL 이 나 chy lo mi cr on 으로 이 동된 후에 이 입 자의 중십 부 의 중성지방은 LPL 에 의해서 가수분해된다. LPL 은 여러 조직 가 운데 에 존재 하며 이 의 작용 부위 는 모제 관의 endoth e li um 이 다. 대 부분 분해되어서 유리된 중성지방, 지방산은 산화와 처장을 위해서
조직 으 로 옮겨 진다. VLDL 과 chy lo mi cr on 의 접 차적 인 지 방제 거 작용은 중간 바중법위의 lip o p ro te i n , 즉 IDL 과 chy lo mi cr on 나머지 (remnan t)를 각각 형성하여서 결국 LDL 을 형성 하는 방향으로 대 사된다. '15 6) 이 LDL입 자는 결 국 순간계 몽에 서 말단조칙 으로 endoc- ytos i s 에 의 해 서 제 거 된다. endocy tos is 과정 은 recep to r 가 중재 되 어서 이루어지는 과정이다 .539) 요즈음 돼지에게 MC- 서당 LDL 을 주 사하고 난 후의 14C 의 체 조직 분포상황을 조사한 결과 간, 부신, 지방조직이 in v i vo 에서 LDL 이 이동되어가는 가장 활발한 부위라 는 것 을 알아냈다. 540) 중성 지 방이 풍부히 들어 있 는 lip o p ro te i n 의 단계 적 인 지 방제 거 의 기 본적 인 현상은 신속한 것 이 다. 사람에 게 서 chy lo mi cr on 의 중성 지 방이 순환계 로부터 반감기 가 5 분 이 내 로 이 동된다. 모든 lip o p· ro t e i n 은 복합체이므로 지방과 단백질 구성성분의 교환이나 또는 혈청 으로부터 떠 나가는 속도는 다 다르다. 456),540) 또한 Iip o p ro te i n 의 종류에 따라서 그 구성성분이 사라지는 시간과 사라지는 방식은 다 다르다. 정상인에게 있어서 VLDL 입자의 지방제거 경로를 따라 서 분해되어 나가면서 이 입자가 혈청내에 머무르는 시간은 약 6 시 간이다 .456) 그런데 VLDL 비중범위의 입자내에 있는 A p oB 의 반 감기는 사람에게서는 2~4 시간이며 쥐는 5~10 분 정도이다. 한편 VLDL, HDL 그리고 IDL 사이에서 교환되고 있는 A p oC 의 순환하 는 시간의 반감기는 사람에게서 15~20 시간이며 쥐에게서는 8~10 시간이다. 간은 IDL 과 나머지 입자를 순환계로부터 이동시킬 수 있는 능력 이 있는 것으로 나타났다. 그러나 동물의 중류에 따라서 이 경로의 이용도에 차이가 현저히 있는 것으로 나타났다. 예로서 쥐에게서 chy lo mi cr on 나머 지 와 IDL 의 주요 부분이 간에 의 해 서 이 동될 때 456) 아마도 독정 한 recep tor 와 상호작용에 의 해 서 이 루어 전다. 541-3) 사 람에게 있어서 간에 의해 IDL 과 나머지 입자가 취해지는 경로는무 시 되 어 도 좋을 만큼 소량이 며 VLDL 과 chy lo mi cr on 전구체 각 입 자 사이에서 관계를 맺으며 또한 LDL 같온 산물로 된다 .456) 이러한 전구체 각 입자 사이의 연구는 주로 동위원소로 처리된 VLDL 의
A p oB 부위를 가지고 연구한다. (2) HDL 대사 HDL 의 대 사경 로와 기 능은 대 단히 복잡하고 성 세 하다. pe rfu s ed 된 쥐의 간에서 연구되어전 바에 의하면 평원판 형대의 신생 HDL 입자도 간과 소장에서 분비되어서 혈청 으로 들어간다 . 그래서 혈청 내에서 혈청구성성분에 의해서 구형의 HDL 입자로 변형된다 .5 3 8) 이 러한 변형의 가장 중요한 현상은 LCAT 촉진에 의해서 생성된 산 물 인 양성 (amp h ip a th i c ) 인지 방과 유리 콜레 스데 몰로부터 생 성 된 소수 성 (hy dr op ho bic ) 콜레 스테 롤 este r 의 생 성 이 다. 혈 청 HDL 을 원십 분리에 의해서 분해시키면 HDL2 와 HDL3 로 분리된다. HDL3 입자의 크기는 HDL2 에 비해서 작으며 콜레스테롤 es t er 함량과 Ap o A- I /A p oA-Il 의 바례도 HDL2 에 비해서 낮다 .545) 이러한 소립자의 특성과 대사관계는 아직까지 잘 알려져 있지 않다. 정상인에게서 51I 로 처 리 된 HDL 의 반감기 는 순환계 내 에 서 3~6 일이 며 545) HDL 의 a p o lip o p ro t e i n 의 반감기도 이와· 유사했다. 동물실험에서 나타난 바 에 의 하면 소장, 546) 간과 신장“이 HDL 을 취 해 가는 주요 장기 라 고하였다. HDL 의 일부는 중성 지 방이 풍부한 lip o pr o te i n 으로부터 전환된다. LPL 의 작용에 의 해서 VLDL 과 chy lo mi cr on 중십 부의 지 방분해 가 이루어쳐서 이들 입자에서 지방이 제거되면 따라서 표면충 물질의 함유농도가 입자내에서 높아지면서 이들 물질이 불안정해진다. 그. 러 면 콜레 스데 롤과 인지 방이 HDL 비 중범 위 46 0 )4 75)480) 의 입 자로 이 동 되어 들어가며 거기서 콜레스테롤은 에스텔화되고 인지방은 LCAT 에 의해서 가수분해된다(그립 1 참조). 생성된 콜레스테몰 es t er 는 다시 LDL 이 나 VLDL 로 되돌아오기 도 한다. LDL 중십 부의 콜레 스테롤 es t er 의 일부는 VLDL 과 ch ylom i cron 의 표면충 구성물질인 콜레스테롤로부터 유도된 것이다. 콜레스테롤과 인지방이 HDL 비중범위내 입자로 이동되면 이 결과 ‘ 새로운 HDL 입자가 형성되는 것인지 또는 이미 형성되어 있던 HDL
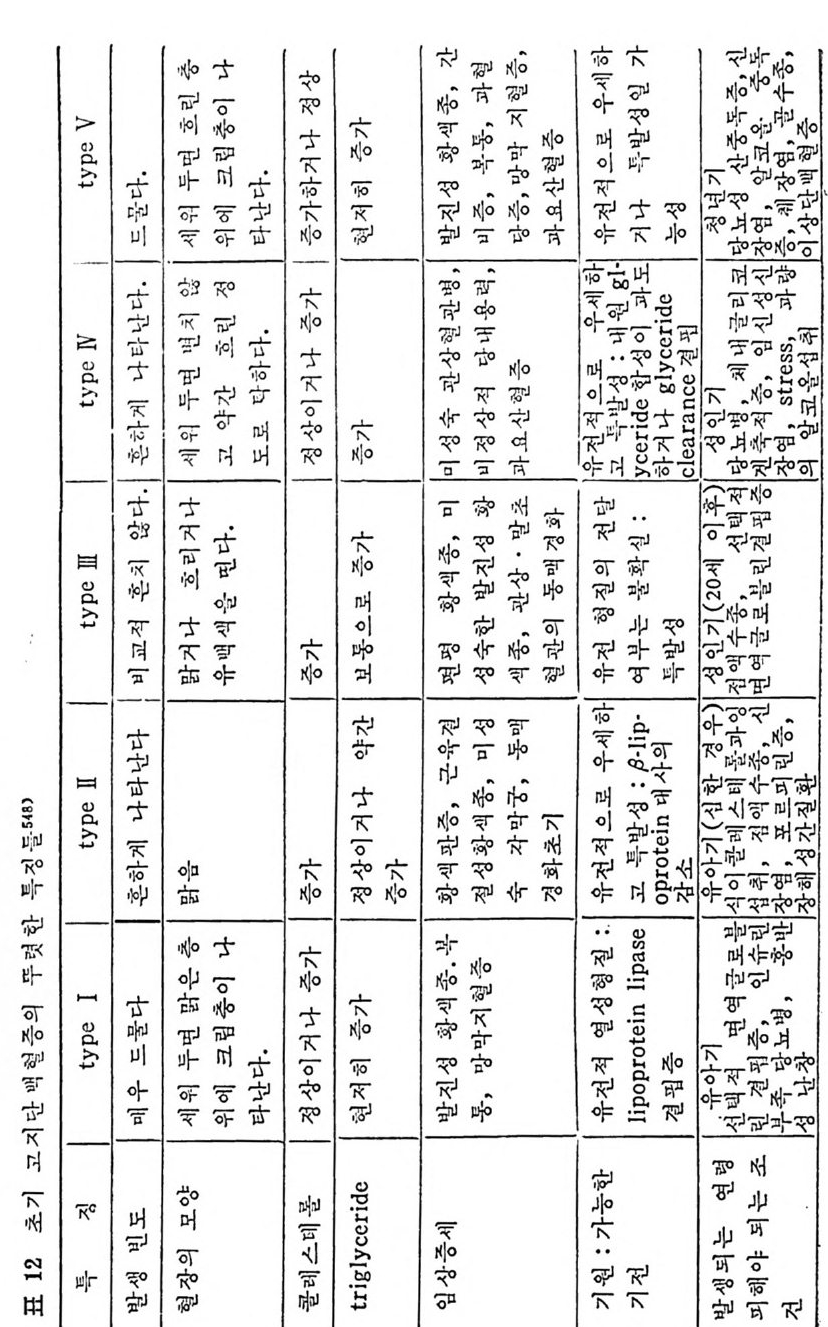
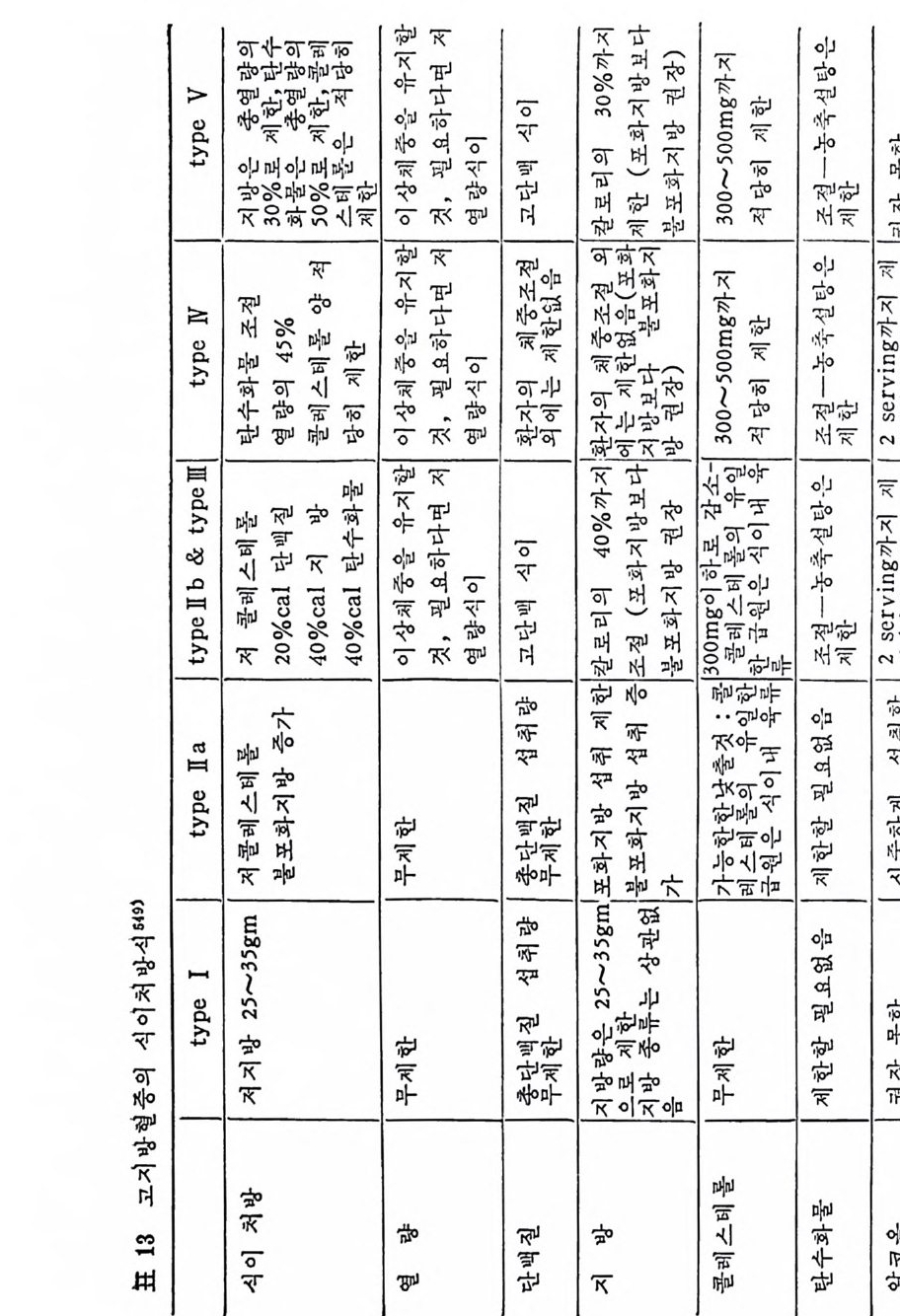
업자내로 이동되는지에 대해서는 연구가 진행중 이다. 중성지방이 풍부히 함유된 lip o p ro te i n 의 표면충 구성 성 분의 대 사에 대 한 기 능 이 외 에 HDL 은 또한 LPL 작용에 팔 수 조요소안 Ap o C-II 를 공급 한다. HDL 은 여 러 말단조직 으로부터 콜레 스테 롤을 수집 해서 간으 로 이동시켜서 신체 밖으로 배 설 시킨다 . 476> HDL 의 이 기능에 대해 서 요즈음 많은 사람들의 관십이 모아지고 있으며 이로 인해서 HDL 이 항동맥 경 화 효과를 가진 lipo p r ote i n 이 라고 생 각하기 도 한다 477) (LDL 의 대사는 7. 동맥 겅화증 과 고지 방혈증의 LDL 부분을 참조하시오). 9 고지단백혈증 고지단백혈증 (h yp erl ip o p ro t e i nem i a) 는 1 차적으로 가족력에 의해서 나타나며 2 차적으로는 여러 가지 질병, 죽 간질환, 신장질환 그리 고 알코 올중독 등에 의 해 서 도 생 간다. hy pe rlip o p ro te i n e mi a 는 다 음 표 12 에 보여주듯이 5 가지 typ e 으로 나눈다. 표 12 에서는 hy pe - rl ip o p ro t e i nem i a 의 형태와 종류, 혈청구성성분의 변화, 관상십장 병의 위험도와 치료석이에 대해서 요약하였다. 표 13 은 hy pe rlip o p ro te i n e mi a 치 료를 위 해 서 행 해 저 야 할 석 이 요 법의 원칙을 요약하였다.
* 참고문현 1) Macheboeuf, M. , Bull. Soc. Chi m . Bi ol . , 11:268, 1929. 2) Macheboeuf, M. , Bull. Soc. Clzim . Bi ol . , 11:485, 1929. 3) Gof m an, J. W. , F. T. Lin d g re n, H. Ell iot t , J. Bio l . Chem. , 179 : 973, 1949. 4) Dang e rfie l d, W. G. , E. B. Smi th, J. Cli n. Path o l. , 8: 132, 1955. 5) Gof m an, J. W. , F. Glazie r , A. Tamp lin, B. Str iso wer, 0. De Lalla, Phys i o l. Rev. , 34: 589, 1954. 6) Fredric k son, D. S. , R. S. Gordon, Phys i o l . Rev. , 38 : 585, 1958. 1) Lees, R. S. , F. T. Hatc h , J. Lab, Clin . Med, , 61 : 518, 1963,
8) Fredric lc son, D. S. , R. I. Levy , R. S. Lees, Ne w Erg! . ]. Med. , 9) B27e6a:u3m4o~n4t4, , J9. 4L~. 1, 0L3., A1. 48C~a5r6ls,o n2, 15G~2. 5R,. 2C7o3o~p8 e1 r,, 19z6.7 . Fejf ar , D. S. Fredric k son, T. Str a sser, World. Healt h. Orga n. , 43:891, 1970. 10) Goldste i n , J. L. , W. R. Hazzard, H. G. Schrott , E. L. Bie r ma n , A. G. Mot u lsky , ]. Clin . Invest. , 52:1533,1973. 11) Goldste i n , J. L. , H. G. schrott , W. R. Hazzard, E. L. Bie r man, A. G. Mot ul sky , ]. Clin . Invest. , 52: 1544, 1973. 12) Hazzard, W. R. , J. L. Goldste i n , H. G. Schrott , A. G. Mot ul sk y , E. L. Bie r man, ]. Clin . Invest. , 52 : 1569, 1973. 13) Eis e nberg, S. , R. I. Levy ,, Adva11. Lipid Re s. , 13 : I , 1975. 14) Fredric k son, D. S. , Harvey Lect1 1 rcs, 68: 185, 19i 2 , 1973. 15) Fredric k son, D. S. , S. E. Lux, P. N. Herbert, Advan. Exp tl. Med. Bi o l. , 26 : 25, 1972. 16) Holdsworth , G. , J. B. Fin e an, Chem, Phy s. Li pids , 9: 217, 1972. 17) Levy , R. I. , S. Eis e nberg, Ann. Bi o l. Clin . , 32: I, 1974. 18) Morris e tt , J. D. , R. L. Jac kson, A. M. Got to, Ann. Rev. Bi oc /z e m . • 44: 183, 1975. 19) Scanu, A. M. , Bi oc lt em . Bi op lzy s. Acta , 265 :471, 1972. 20) Scanu, A. M. , L. Vi tell o, S. Deg an ello, Rev. Bi oc hem. , 2: 175, 1974. 21) Scanu, A.M., C. Wi sd om, Ann. Rev. Bi o clzem., 41:703,1972. 22) Schumaker, V. N. , G. H. Adams, Ann. Rev. Bi oc /z e m. , 38: 113, 1969. 23) Fredric k son, D. S. , Proc. Natl . Acad. Sc i. US. , 64 : 1107, 1969. 24) Scanu, A. M. , Ann, N. Y. Acad. Sci. , 195 : 390, 1972. 25) Onclcy, Brain Lip ids and lipo pr ote i n s and tlz e Lecodys t r o p h ie s , Elsevie r Press, p. 1, 1963. 26) Alaup o vic , P. , At he rosclerosis , 13 : 141, 1971. 27) Alaup o vic , P. , Proti de s. Bi ol . Fluid s . Proc. Co/l og . 19t h, 1971, p. 9. 28) Gusta fs o n, A. , P. Alaup ov ic , R. H. Furman, Bi oc lzcmi st r y , 5:632, 1966. 29) Shore, V. G. , B. Shore, Blood Lipids and Lip op r ote i n s Qu anti ta- tion Comp o sit ion Meta b olis m , edit ed by G. J. Nelson, N. J. W iley 1972, p. 789. 30) Beg, Z. H. , D. W. Allmann, D. M. Gib s on, Bi oc hem. Bi op l tys. Res. Commi m . , 54: 1362, 1973. 31) Shore, B. , V. G. Shore, Bi oc hemi st r y , 8:4510, 1969.
32) Dole, U. P. , J. T. Haml in, P!z y si o l . Rev. , 42:67 4, 1962. 33) Zil v ersm i t, D. B. , Fe d. Proc . , 26 : 1599, 1967. 34) Bie r m a n, E. L. , D. Porte , Jr. , D. D. O'Ha ra, M. Schwartz , F. C_ Wood, Jr. ,J. Clin . Invest. , 44:261,1965. 35) Skip s ki, V. P. , Blood Lipids and Lip o pr ote i n s Qu anti tat i on Comp o ~ sit ion and Meta b oli s m , edit ed by G. J. Nelson, N. Y. W ile y , 1972, p. 471 , 36) Kos tn er, G. , Hop pe -S e yl e r ' s, Z. Phy si o l . Che m . , 353 : 1863, 1972. 37) Ko stn er , G. , A. Holas ek, Bi o c/z e mi st r y , 11 : 1217, 1972. 38) Glic k man, R. M. , K. Kir s c h , Bi oc him . Bi op / zys. Acta , 371 : 255, 1974. 39) Eis e nberg, S. , D. W. Bil h e im er, F. Lin d g re n, R. I. Levy , Bi oc /z im . Bi op lzy s. Acta , 260 : 329, 1972. 40) Shore, V. G. , B, Shore, Bi o chemi st r y , 12 : 502, 1973. 41) Got to, A. M. , W. V. Brown, R. I. Levy , M. E. Bir ba umer, D. S_ Fredric k son, ]. Clin . Inve st . , 51 : 1486, 1972. 42) Brown, W. V. , R, I. Levy , D. S. Fredric k son, Bt oc him . Bi op h y s . Acta , 200 : 573, 1970. 43) Schonfe l d, G. , C. Bir g e , J. P. Mi ller , G. Kessler, J. Santi ag o, Di ab - ete s , 23 : 827, 1974. 44) Schonfe l d, G, , R. S. Lees, P. K. George , B. Pfl eg e r , J. Cl in. Inve st, , 53 : 1458, 1974. 45) Brown, W. V. , R. I. Levy , D. S. Fredric k son, J. Bi ol . Chem. , 244:· 5687, 1969. 46) Albers, J. J. , A. M. Scanu, Bi oc him . Bi op l z y s . Acta , 236 : 29, 1971 . 47) Kost n er, G. M. , J. R. Pats c h , S. Sail er , H. Braunste r ner, A_ Holasek, Europ ea n J. Bi o chem. , 45:611, 1974. 48) Ka n e , J. P. , Anal. Bi oc /z e m . , 53 : 350, 1973. 49) Forte , T. , A. V, Nic h ols, A.d van. Lip id Res. , 10: 1, 19i2 . 50) Adams, G. H. , V. N. Schuma ker, Anal. Bi oc lze m. , 29 : 117, 1969. 51) Fis h er, W. R. , M. E. Grana de , J. L. Mauldin , Bi oc hemi st r y , 10: 1622, 1971. 52) Fis h e r , W. R. , M. G. Hammond, G. L. Warmke, Bi oc hemi st r y , 11: 519, 1972. 53) Lin d g re n, F. T. , L. C. Jen sen, R. D. W ills, G. R. Ste v ens, Lip id,s : . . 7 : 194 , 1 972.
54) Fis h er, W. R. , Ann. Cl i11. Lab. Sci. , 2: 198, 1972. 55) Hammond, M. G. , W. G. Fis h e r, ]. Bi ol . Chem. , 246 : 545 4 , 1971, 56) Schumaker, V. N. , Acco1111t s Chem. Re s. , 6 : 398, 1973. 57) Bauto v ic h , G. J. , L. A. Sim ons, P. F. W illi a m s, J. R. Turtl e , At h• erosclerosis , 21 : 211, 1975. 58) Lee, D. M. , P. Alaup ov ic , Bi oc hemi st r y , 9 : 2244, 1970. 59) Lee, D. M. , P. Alaup ov ic , Bi oc hcm. ]. 137: 155, 197 4. 60) Lee, D. M. , P. Alaup ov ic , At he rosclerosis , 19 : 501, 1974 . 61) Kastn er, G. , Bi oc hem. ]. , 130:913, 197 2. 62) Bersot, T. P. , W. V. Brown, R. I. Lev y , H. G. W ind mueller, D. S. Fredric k son, V.S. LeQ u ir e , Bi oc he m i st r y , 9:3 427, 1970. 63) Kog a, S. , L. Bolis, A. M. Scanu, Bi oc hem. Bi op hy s . Acta , 236: 416, 1971 . •64 ) Hi llya rd, L. A. , H. M. Whit e, S. A. Pang b urn, Bi oc hemi st r y , 11 : 511, 1972. •65 ) Jac kson, R. L. , 0. D. Taunt on , R. Seg u ra, J. G. Gallag h e r, H. F. Hoff , A. M. Got to, Comp . Bi oc hem. Phy si o l . , In pre ss. ,66 ) Pup pion e, D. L. , T. Forte , A. V. Ni ch ols, Comp . Bi oc hem. Phy s· iol, 39B: 673, 1971. -67 ) Fless, G. M. , A. M. Scanu, Bi oc hemi st r y , 14; 1783, 1975. 68) Lee, J. A. , M. D. Morris , Bi oc hem. Med. , to : 245, 1974. ,69 ) Pats c h, J. R. , S. Sail er , G. Kastn er, F. Landhofe e , A. Holasek, H. Braunste i n e r, J. Lip id Res. , 15:356, 1974. 70) Mackenzie , S. L. , G. S. Sundaram, H. S. Sodhi, Clin . chim . Acta , 43 : 223, 1973. 71) Robin s on, D. S. , Comp . Bi oc hem. , 18 : 51, 1970. 72) Sundaram, G. S. , S. L. , Mackenzie , H. S. Sodhi, Bi oc hi m . Bi op • hy s, Acta , 337: 196, 1974. 73) Sundaram, G. S. , H. S. Sodhi, S. L. Mackenzie , Proc. Soc. Exp tl. Bi ol . Med. , 141:842, 1972. 74) Ewi ng , A. M. , N. K. Freeman, F. T. Lin d g re n, Advan. Lip id Res. , 3:25, 1965. 75) Kostn er, G. , P. Alaup ov ic , Bi oc hemi st r y , 11 : 3419, 1972. 76) Scanu, A. , J. Toth , C. Edelste i n , S. Kog a, E. Sti ller , Bi oc hemi · str y , 8: 3309, 1969. 77) Borut, T. C. , F. Aladje m , Immunochemi st r y , 8:851~63, 1971 .
78) Ehnholm, C. , H. Garoff , K. Sim ons, H. Aro, Bi oc lzi m . Bi op h ys ~ Acta , 236:431, 1971. 79) Sim ons, K. C. , Ehnholm, 0. , Re n konen, B. , Blot h, A. , Acta . P· ath o l. Mi cr obia l . Scand. Se ct . B. , 78:45 9, 1970, 80) Albers, J. J. , W. R. Hazzard, Lipids , 9: 15, 1974. 81) Berg, K. , G. Da h len, M. H. Fric k , Cl in. Genet. , 6: 230, 1974. 82) Walto n , K. W. , J. Hi tch ens, H. N. Mag n ani, M. Khan, At h eroscl· ero sis , 20 : 323, 1974 . 83) Seid e l, D. , P. Alaup ov ic , R. H. Furman, ]. Clin . Invest. , 48: 1211,. 1969. 84 ) Seid e l, D. , P. Alaup ov ic , R. H. Furman, W. J. McConath y , J~ Clin . I11v est. , 49: 2396, 1970. 85) Swi tze r , S. , L. Sate n ste i n , J. Clin . Invest. , 46: 1855, 1967. 86) Kep a y, D. L. , R. Poon, J. B . Sim on, ]. Lab. Cl in. Med. , 81 : 172,.. 1973. 87) Ri tla n d, M. C. and M. E. Demp se y , Bi oc he m . Bi op ! zys. Res. Com•· mun. , 38:9 21 , 1970. 88) Weng el er, H. , H. Grete n , and D. Seid e l, Europ ea n ]. Clin . Invest. ,. 2:372, 1972. 89) Weng el er, H. , and D. Seid e l, Cl in. Chi m . Acta , 45:429~32, 1973. 90) Seid e l, D, H. Grete n , H. P. Geis e n, H. Weng le r, H. Wi el and,. Europ ea n ]. Clin . Inve st. , 2 : 359, 1972. 91) Levy , R. I. , C. B. Blum, and F. J. Schaefe r , The Comp o sit ion , str u ctu re and meta b olism of hig h densit y lip o pr ote i n s » In Lip op r o· tei n Meta b olis m 11, Grete n edit or , Sp r in g e r-Verlag , Berli n, 56, 1976. 92) Lux, S. E. , R. V. Hi rz, R. I. Shrag er , A. M. Gott o, Jr. , ]. Bi oc • hem. , 247: 2598, 1972. 93) Fie l din g , C. J. , V. G. Shore, P. E. Fie l din g , Bi oc hem. Bi op h y s . Res,. Commun. , 46 : 1493, 1972. 94) Baker, H. N. , A. M. Got to, Jr. , R. L. Jac kson, ]. Bi ol . Chem. , 250 ~ 2725, 1975. 95) Baker, H. N. , R. L. Jac kson, A. M. Got to, Jr. , ]. Bi oc hemi st r y , . 12: 3866, 1973. 96) Delabunty , T. , H. N. Baker, A. M. Gott o, Jr. , R. L. Jac kson, ]. Bi ol . Chem. , 250: 2718, 1975. 97) Brewer, H. B. , Jr, T. Fair w ell, A. Larue, R. Ronan, A. Houser,..
T. Bronzert, Bi oc lzem. Bi op ! iys. Re s. Commun. , 80:623, 1978. '98 ) Brewer, H. B. , Jr. , S. E. Lux, R. Ronan, K. M. Joh n, Pro,;, Nat. Acad. Sc i. USA. , 69: 1304, 1972. 99) Schaefe r , E. J. , S. Eis e nberg, R. I. Levy , ]. Lipid Res. , 19, 1978. 100) Jac kson, R. L. , A. M. Got to, Jr. , Bi o chi m . Bi op l z y . Ac ta, 285 : 36, 1972. 101) Morris e tt , J. D. , R. L. Jac kson, A. M. Got to, Jr. , Bi oc lz im . Bi op h y s Acta , 472: 93, 1977. 102) Ste i n , Y. , V. Ebin , H. Bar·on, 0. Ste i n , Bi oc lzi m . Bi op l z y s. Acta , 486:486, 1977. 103) Osborne, J. C. , Jr. , H. B. Brewer, Jr. , Adv. Prote i n Che m . , 31 : 253, 197 7. 104) Vi tell o, L., A.M. Scanu, ]. Bi ol . Chem., 251:1131,1976. 105) Osborne, J. C. , G. Palumbo, H. B. Brewer, Jr. , H. Ede lh och, Bi o· chemi st r y , 14: 3741, 1975. 106) Sto ne, W. L. , J. A. Rey n olds, ]. Bi ol . Clzem. , 250:8045~8, 1975. 107) Formi sa no, S. H. , B. Brewer, Jr. , J. C. Osborne, Jr. , ]. Bi o l. che m , 253:354,1978. 108) Kostn er, G. M. , J. R. Pats c h, S. Sail e r, H. Braunste i n e r, A. Holasek, Eur. ]. Bi o chem. , 15:611, 1974. 109) Kostn er, G. M. , P. Alaup ov ic , Bz' oc hemi st r y , 11 : 3419, 1972. 110) Borut, T. C. , F. Aladje m , Immunochemi st r y , s:ss1, 1971 . 111) Cheung , M. C. , J. J. Albers, J. Clin . Invest. , 60 : 43, 1977. 1.1 2) Curry, M. D. , P. Alaup o vic , C. A. Suenram, C/in . Chem. , 22: 325, 1976. 113) Albers, J.J., F. Aladje m , Bi o chemi st r y , 10:3436,1971 . 114) Frie d berg, S. , J. A. Rey n olds, ]. Bi ol . Chem. , 251 :4oos, 1976. 115) McConath y , W.J ., P. Alaup o vic , Bi oc hemi st r y , 15:515,1976. 116) Curry, M. D. , W. J. McConath y , P. Alaup o vic , J. H. Ledfo r d, .M. Pop o vic , Bio c him . Bi op h ys . Acta , 439:413, 1976. 117) Sto f f el, W. , 0. Zie r enberg, B. Tung ga l, E. Schreib e r, Proc. Nat. Acad. Sci. U. S. A. , 71 : 3696, 1974. 118) Seg re st, J. P. , R. L. Jac kson, J. D. Morris e tt , A. M. Got to, Jr, FEES Lett . , 38: 247, 1974. 119) Assman, G. , H. B. Brewer, Jr. , Proc. N,야 Acad. Sci. U. S. A. , 71:153, 1974 .
120) Fain a r u , M. , M. C. Glang e aud, S. Eis e nberg, Bi oc hi m . Bi op h ys . Acta , 386:4 3 2, 1975. 121) Kastn er, G. , A. Holasek, Bi o chemi st r y, 11 : 1217, 1972. 122) Schaefe r , E. J. , L. L. Jen kin s , H. B. Brewer, Jr. , Bi oc hem. Bi op • Jzys . Res. Commun. , 80:4 0 5, 1978. i23 ) Schor feld , G. , B. Pf leg e r , ]. Cl in. Invest. , 54: 236~46, 1974. 124) Karli n, J. B. , D. J. Juh n, J. L . Sta r r, A. M. Scanu, A. H. Rubens· tei n , ]. Lip id Res. , 17 : 30, 1976. 125) Assman, G. , E. Smootz , K. Adler, A. Cap u rso, K. Dett e, J. Cl in. Inve st. , 59 : 565, 1977. 126) Assman, G, P. N. Herbert, D. S. Fredric k son, T. Forte , ]. Cl in. In!/est. , 60 : 242, 1977. 127) Rhoads, G. , C. I. Gulbrandsen, A. Kag an , N. Eng l. ]. Med. , 294 : 293, 1976. 128) Caste l l i, W. , J. T. Doy le , T. Gordon, C. G. Hames, H. Hj or tl a nd, S. B. Hulley , A. Kag an , W. J. Zurkel, Ci rcu lati on , 55 : 767, 1977. 129) Mi lle r, N. E. , D. S. Thelle, O. H. Forde, O. D. Mj os , Lancet, 1 : 965, 1977. 130) Gordon, T. , M. Caste ll i, M. Hj or tl a nd, W. B. Kannel, T. Dawber, Amer. ]. Med. , 62 : 707, 1977. 131) Carew, T. E. , S. B. Hay e s, T. Kochin s ky , D. Ste i n b erg, Lancet, 1:1315, 1976. 132) Wood, P. D. , W. Haskell, H. Klein , S. Lewi s, M. P. Ste r n, J. W. Farqu har, Meta b olis m , 25: 1249, 1976. 133) Fredric k son, D. S. , R. I. Levy , The Meta b oli c Basis of in herit ed Di se ase, J. B. St am bury, J. B. Wy n g aa rden, 0. S. Fredric k son, edit or s, McGraw·hil l, N. Y. 545, 1972. 134) Schaefe r, E. J. , R. I. Levy , L. L. Jen kin s , H. B. Brewer, Jr. , Six t h Inte r nati on al sym p o siu m on Drug s aff ec ti ng lipid meta b olis m , 1977. 135) Blum, C. B. , R. I. Levy , S. Eis e nberg, M. Hall, R. H. Goebel, M. Berman, J. Cli n. Invest. , 60: 795, 1977. 136) Levy . R. I. , R. S. Lees, D. S. Fredric k son, J. Cl in. Invest. , 45:63, 1966. 137) Marsh, J. , J. Lip id Res. , 17:85, 1976. 138) Felker, T. E. , M. Fain a ru, R. L. Hami lton , R. J. Havel, J. Lip id Res. , 18:465, 1977.
139) Glic k man, R. M. , P. H. R. Green, Proc. Nat. Acad. Sci. U. S. A .• 74: 2569, 1977. 140) Imaiz u mi , K. , M. Fain a ru, R. J. Havel, Ci rcu lati on , 54(sup pl) : u ~134 (abstr a ct) , 1976. 141) Green, P. H. R. , A. R. Tall, R. M. Gli ck man, ]. Cl in. Invest. , 61'. 528, 1978. 142) Git lin, D. , D. G. Cornwell, D. Nakasato , J. I. Onc !ey , W. L. Hug h es, Jr. , C. A. Jan eway , J. Cl 玩 Invest. , 37: 172, 1958. 143) Furman, R. H. , S. S. Sanbar, P. Alaup o v1c, R. H. Bradfo r d, R. P. Howard, J. Lab. Cli n. Med., 63:193,1964 144) Scanu, A. , W. L. Hug h es, J. Clin . Invest. , 41: 1681, 1962. 145) Shep h erd, J. , C. Packard, J. Pats c h, A. M. Got to, Cir cu lati on , 56(Sup pl) : ][-5 ( abstr a ct) , 1977. 146) Sheph erd, J. , A. M. Got to, 0. D. Taunto n , M. J. Clake, E. Faris h , B£ oc h£ m . Bio p h y . Acta , 489:486, 1977. 147) Schaefe r , E. J. , C. B. Blum, R. I. Levy , R. Goebel, H. B. Brewer, M. Berman, Cf rcu /ati o11 , 54(sup pl):1 1~27 (abstr a ct) , 1976. 148) Nakai, T. , T. F. Whay n e, J. Lab. Cli n. Med. , 88:63, 1976. 149) Eis e nberg, S. , H. G Wi nd mueller, R. I. Levy , J. Lip id Res. , 14 : 446, 1973. 150) Rachmi lew i tz, P. , 0. Ste i n , P. S. Roheim , Y. Ste i n , Bi oc hi m . Bi op h y s . Acta , 270 : 414, 1972. 151) Mi ller , N. E. , D. B. Wein s te i n , D. Ste i n b erg, J. Lip id Res. , 18: 438, 1977. 152) Carew, T. E. , R. P. Sack, K. H. Joh ansen, C. A. Dennis , D. Ste i - nberg, J. L£p id Res. , 17:441, 1976. 153) Eis e nberg, S. , R. I. Revy , Adv. Lip id Res. , 13:1, 1957. 154) Jac kson, R. L. , J. D. Morrise tt , A. M. Got to, Jr. , Phy si o l . Rev. ~ 56 : 259, 1976. 155) Swami nt h an, N. , F. Aladje m , Bi oc hemi st r y , 15: 1516, 1976. 156) Bedfo r d, D. K. , J. Sheph erd, H. G. Morga n, Cli n. Chem. Acta , 70 ~ 267, 1976. 157) Albers, J. J. , V. G. Cabana, W. R. Hazzard, Meta b . Cl in. Exp. , 24: 1339, 1975. 158) Schonfe ld , G. , R. S. Lees, P. K. George , B. Pf leg e r , J. Clin . Invest. , 53:1458, 1974.
159) Durrin g ton , P. N. , J. T. Whic h er , C. Warren, C. H. Bot ton , M. Harto g , Clin . Chi m . Acta , 71 : 95, 1976. 160) Got to, A. M. , Jr. , R. I. Levy , K. Joh n, D. S. Fredric k son, N. Eng l. ]. Med. , 284:813, 1971 . 161) Eis e nberg, S. , D. Bil h e im er, F. Lind g r en, R. I. Levy , Bi o chim . Bi op hy s . Acta , 260 : 329, 1972. 162) Kane, J. P. , T. Sata , R. L. Hami lt o n, R. J. Havel, ]. C/in . Invest. , 56 : 1622, 1975. 163) Ha m i lt o n , R. L. , M. C. W illi a m s, C. J. Fie l din g , R. J. Havel, J. Cl in. Invest. , 58: 667, 1976. 164) Wi nd mueller, H. G. , P. N. Herbert, R. I. Levy , ]. Lip id Res. , 14:215, 1973. 165) Gli ck ma n, R. M. , J. Khorana, A. Kil go re, Sc ien ce, 193: 1254, 1976. 166) Vo!wi le r , W. P. , P. D. Goldsworth y , M. P. MacMarti n, P. A. Wood, I. R. Mackey , G. Fremont- S mi th, ]. Cli n. Invest. '. 34: 1126, 1955, 167) Eis e nberg, S. D. , W. Bil he im er, R. I. Levy , Bi o chi m . Bi op h y s. Acta , 326 : 361, 1973, 168) Bil he im er, D. W. , S. Eis e nberg, R. I. Levy , Bi oc li im. Bi op hy s . Acta , 260:212, 1972. 169) Eis e nberg, S. D. , W. Bil he im er, R. I. Lev y, Bi oc hi m . Bi op h ys . Acta , 280:94, 1972. 170) Lang er , T. , W. St ro ber, R. I. Levy , ]. Clt n . Invest. 171) Eis e nberg, S. , D. Rachmi le wi tz, ]. Lt Ptd Res. , 16:341, 1975. 172) Eis e nberg, S. , Lt po pr ote t n Meta b olt s m, H. Grete n , edit or Sp ri n g e r-Verlag, Berli n, 32, 1976. 173) Glang e aud, M. C. , S. Eis e nberg, T. Oliv ecrona, Bi o clzim . , Bt op- hy s. Acta , 486: 23, 1977. 174) Deckelbaum, R. , S. Eis e nberg, Y. Barenholz, T. Oliv e crona, Ci rcu /att o n(Sup pl ), 56: 111~56(abstr a ct) , 1977. 175) Eis e nberg, S. , D. Rachmi le wi tz, Bi o clzt m . Bt oph ys . Acta , 326: 378, 1973. 176) Eis e nberg, S. , D. Rachmi lew i tz, Bi o clz im . Bt oplz y s. Acta , 326: 391, 1973. 177) Faerge man, 0. , T. Sata , J. P. Kane, R. J. Havel, ]. Clt n . Invest. •
56:1396, 1975. 178) Ste i n , 0. , D. Rachmi le wi tz, L. Sang e r, S. Eis e nberg, Y. Ste i n , Bi oc lzi m . Bi op h ys . Acta , 360 : 205, 1974. 179) Berman, M. , M. Hall, R. I. Levy , S. Eis e nberg, D. W. Bil he im er, R. D. Phair , R. H. Goe be l, ]. Lipid Res. , 19 : 38, 1978. 180) Ut e rmann, G. , M. Jae schke, J. Menzel, FEES. Lett . , 56 : 352, 1975. 181) Sig u rdsson, G. , A. Nic o ll, B. Lewi s, Eur. ]. Clin . Invest. , 6 : 167, 1976. 182) Sig u rdsson, G. , A. Nic o ll, B. Lewi s, E11r. ]. Cl in. Invest. , 6 : 151, 1976. 183) Sig u rdsson, G. , A. Nic o ll, B. Lewi s, ]. Cli 11. Invest. , 56: 1481, 1975. 184) Souta r, A. K. , N. B. My a nt, G. R. Thomp so n, At h erosclerosis , 28 : 247, 1977. 185) Sim ons, L. A. , D. Reic h ), N. B. My an t, M. Manc ini , At l1er oscle- rosis , 21 : 283, 1975. 186) Packard, C. J. , J. L. H. C. Thir d , J. Shep h erd, A. R. Loumer, H. G. Morga n, T. D. V. Lawrie , Meta b oli sm , 25 : 995, 1976. 187) Lang e r, T, R. I. Levy , Meta b olic eff ect s of Ni co t inz' c acid and its Deriv ati ve s, K. F. Gey , and L. A. Carlson, edit or s, Huber, Bern 641, 1970. 188) Thomp s on, G. R. , T. Sp ink s, A. Ranic a r, N. B. My a nt, Cl in. Sci. Mo!. Med. , 52: 361, 1977. 189) Bil he im er, D. W. , J. I. , Goldste i n , S. M. Grundy , M. 요 Brown, J. Clin . Invest. , 56: 142 0 , 1975. 190) Levy , R. I. , T. Lang e r, Pharmacolog ica l contr o l of Li pid Me ta b , oli sm , W. L. Holmes, R. Paolett i, D. Krit ch evsky ,· e dit or s, Plen u m, New York, p. 155~3, 1972. 191) Snid e rman, A. D. , T. E. Carew, J. G . Chandler, D. Ste i n b erg, Scie nce, 183 : 526, 1974. 192) Goldste i n , J. L. , M. S. Brown, Proc. Nat. Acad. Sci. USA, 70: 2804, 1973. 193) Goldste i n , J. L. , M. S. Brown, Amer. ]. Med. , 58: 147, 1975. 194) Goldste i n , J. L. , M. S. Brown, N. J. Sto n e, Cell, 12:629, 1977, 195) Goldste i n , J. L. , M. S. Brown, Ann. Rev. Bt' oc lzem. , 46:897, 1977. 196) Shulman, R. S. , P. N. Herbert, K. Wehrly, D. Fredric k son, ].
Bi ol . chem. , 255 : 182, 1975. 197) Jac kson, R. L. , J. T. Sp a rrow, H. N. Baker, J. D. Morris e tt , O. D. Thaut on , A. M. Got to, Jr. , J. Bi ol . Chem. , 249: 5308, 1974. 198) Jac ks on , R. L. , H. N. Baker, E. B. Gi ll ia m , A. M. Got to, Jr. , Proc. Nat. Acad. Sci. USA, 74: 19 4 2,1 977. 199) Brewer, H. B. , Jr. , R. Shulman, P. He rb ert, R. Ronan, K. Weh• 200) rFloyr, te J, . TB, i, o l.E . CGheomng. , , A24. 9V:4. 97N5i, c 1h 9o7ls4,. Bi o chi m . Bi op hy s . Acta , 337: 169, 1974 . 201) Jac kson, R. L. , J. D. Morris e tt , J. T. Sp ar row, J. P. Seg re st, H. J. Pownall, L. C. Smi th, H. F. Hoff , A. M. Got ts, Jr. , J. Bi ol . Che m . , 249 : 5314, 1974. 202) Morris e tt , J. D . , J. S. K. David , H. J. Pownall, A. M. Got to, Jr. Bi o chemi st r y , 12: 1290, 1973. 203) Hof f, H. F. , J. D. Morris e tt , A. M. Got to, Jr. , Bi o chi m . Bi op h y s. Acta , 296:653, 1973. 204) La Rosa, J. C. , R. I. Levy , P. N. Herbert, S. E. Lux, D. S. Fred• ric k so n , Bi oc lt em . Bi oc p !iys. Res. Commun. , 41 : 57, 1970. 205) Havel, R. J. , V. G. Shore, B. Shore, D. M. Bio u , Ci rc. Res. , 27: 595, 1970. 206) Havel. R. J. , C. J. Fil e din g , T. Oliv e crona, V. G. Shore, P. F. Fie l din g , T. Eg el rud, Bi o chemi st r y , 12: 1828, 1973. 207) Ganesan, D. , H. B. Bass, FEBS. Lett . , 53 : 1, 1975. 208) Ga nesan , D. , R, H. Bradfo r d, Bi o chem. Bi op hy s . Res. Commun. , 43:544, 1971. 209) Brown, W, V. , M. L. Bag ins ky , Bi o chem. Bi op hy s . Res. Commun. , 46 : 375, 197 2. 210) Kashy a p , M. L. , L. S. Sriv a sta v a, C. Y. Chen, G. Persutt i, M. Gamp b ell, R. F. Lut n er, C. J. Gluec, J. Cl in. Invest. , 60:171, 1977. 211) Breckenid g e , W. C. , J. A. Lit tle, G. Ste i n e r, A. Cho, M. Poap st , Ci rcu lati on , 54 (Sup pl) : 11~25(abstr a ct) , 1976. 212) Havel, R. J. , J. P. Kane, M. L. Kashy a p, J. Clin . Invest. , 52: 32, 1973. 213) Mahley, 1 R. W. , .T . P. Bersot, V. S. Leq u ir e, Scie n ce, 163 : 380, 1970. 214) Eis e nberg, S. , J. Li pid Res. , 19 : 229, 1978. 215) Schaefe r , E. J. , S. Eis e nberg, L. I. Levy , J. Lipid Res. , 19:667,
1978. 216) Mj ¢s , 0. D. , 0. Faerge man, R. L. Hami lt o n , R. J. Havel, J. Clin . 1nvest. , 56:603, 1975. 217) Shore, B. , V. G. Shore, Bi oc lzem. Bi op l zy s. R1t s . Commu. , 58: 107, 1974. 218) Shore, V. G. , B. Shore, Bi o chemi st r y , 12: 502, 1973. 219) Havel, R. J. , J. P. Kane, Proc. Nat. Acad. Sci. USA, 70: 2015, 1973. 220) Shelburne, F. A. , S. H. Qu arfo r dt, J. Bi ol . Chem. 249 : 1428, 1974. 221) Kushwaha, R. S. , W. R. Hazzard, P. W. Wahl, J. Hoover, A11n. Inte r n. Med. , 87: 509, 1977. 222) Pagn an, A. , R. J. Havel, J. P. Kane, L. Kot ite, J. Lipid Res. • 18 : 613, 1977. 223) Fain a rce, M. , R. J. Havel, K. Imaiz u mi , Bi o chem. Med. , 17: 347, 1977. 224) Fain a ru, M. R. , R. J. Havel, K. Imaiz u mi , Bi oc lz im . Bi op h ys . Acta , 490: 144, 1978. 225) Mahley, R. W. , K. H. Weis g r a ber, T. Innerarit y, H. Brewer, Jr. • G. Assman, Bi oc hemi st r y , 14:2817, 1975. 226) Rag la nd, J. B. , H. L. Hawkin s , S. M. Sabesin , Ci rcu lati on , 54 (Sup - pl, 1) : 11, 27 (abstr a ct) , 1976. 227) Rag la nd, J. B. , P. D. Bertr a m, S. M. Sabesin , Bi oc lzem. Bi op hy s . Res. Commu~. , 80:81, 1978. 228) Qu arfo r dt, S. , Bi oc him . Bi op h ys . Acta , 489:477, 1977 229) McConath y , W. J. , P. Alaup o vic , FEBS Lett . , 37: 178, 1973. 230) Kostn e r, G. M. , Bi oc lz im . Bi op l zy s. Acta , 336 : 383, 1974. 231) Olofs so n, S. , W. McConath y, P. Alaup ov ic , Cir cu lati on , 56(Sup - pl):1 11~56, 1977. 232) Kostn er, G. M. , Bi oc hi m . Bi op h ys , Acta , 336 : 383, 1974. 233) Kostn er, G. , Scand. J. Cli n. Lab. Invest. , 33(Sup pl.1 37) : 19, 1974. 234) OLof ss on, S. O. , A. Gusta f s o n, Scand. J. c/in. Lab. Invest. , 33(Sup - pl. 137) : 57, 1974. 235) Sata , T. , D. L. Estr i c h , P. D. S. Wood, L. W. Ki ns ell, J. Lip id Res. , 11 : 231, 1970. 236) Sata , T. , R. J. Havel, A. L. Jon es, J. Lip id Res. , 13 : 757, 1972. 237) Schneid e r, H. , R. S. Morrod, J. R. Colvin , N. H. Tatt rie , Chem. Phys . Lip ids, 10 : 328, 1973,
238) Gusta f s o n, A. , Acta . M 교. Scand. , 179, (Sup pl. , 446) : 1, 1966. 239) Schumaker, V. N. , G. H. Achms, ]. Theoret. Bi o l. , 26:89, 1970. 240) Mate l l, L. , A. Tardie u , V. Luzzati , I. Ag ge rbeck, A. M. Scanu, J. Mo/. Bi o l., 70:105, 1972. 241) Fin e r, E. G. , R. Henry, R. B. Lesli e, R. N. Roberts o n, Bi oc ht m . Bt oph y s. Acta , 380:320, 1975. 2'12 ) Pollard, H. B. , S. K. Devi, Bi o chem. Bi op hy s. Res. Commun. , 44: 593, 1971 . 243) Puo. lsla. r,d , H. , A. M. Scanu, E. W. Tay lo r, Proc. Natl . Acad. Sc i'. 64:304, 1969. 244) Stu hrmann, H. B. , A. Tardie u , L. Mate u , C. Sardet, U. Luzzati , L. Ag g e rbeck, A. M. Scanu, Proc. Natl . Acad. Set. U. S. , 72: 2270, 1975. 245) Da y, C. E. , R. S. Levy , J. Theoret. Bi o l. , 23:387, 1969. 246) Deckelb3. u m, R. J. , G. G. Ship le y, D. M. Small, Scte nce, 190:392, 1975. 247) De ck elblu:n , R. J. , G. G. Ship le y, D. M. Small, J. Bi o l. Chem. , 252, No. 2: 744, 1977. 248) Sm1ll, D. M. , J. Up id Res. , 8:551, 1967. 249) Sfr oe ve, P. , I. Mi ller , Bi oc hi m . Bi op hy s. Acta , 401 : 157, 1975. 250) At k in s on, D. , M. A. F. Davis , R. B. Lesli e, Proc. Roy . Soc. London Ser. B. , 186: 165, 1974. 251) Lag gn er, P. , 0. Kratk y , G. Kostn e r, J. Satt ler , A. Holasek, Fed. Europ ea n Bio c hem. Soc. Lett er s, 27: 53, 1972. 252) L3 .ggn er, P. , K. Muller, 0. Kratk y , G. Kostn er, A. Holasek, Fed. Europ ea n Bi oc hem. Soc. Lett er s, 33:77, 1973. 253) Muller, K. , P. Lagg n er, 0. Kratk y , G; Kostn e r, A. Holasek, 0. Glatt er , Fed. Europ ea n Bi oc hem. Soc. Lett er s, 40:213, 1974. 254) Ship le y, G. G. , D. At k in s on, A. M. Sc3.n u, J. Sup ra mol. Str u ct. , 1:9s, 1972. 255) Phil lips, M. C. , E. G. Fin e r, H. Hauser, Bi oc h im. Bi op hy s. Acta , 290 : 397, 1972. 256) Sto f f el, W. , 0. Zie r enberg, B. Tung ga l, E. Schreib e r, Proc. Natl . 257) SAtco af df e. l, ScWi.. , U0. .S . Z, ie 7r 1e:n3b6e9r6g, , 1B9.7 4D.. Tung ga l, E. Schreib e r, Hop pe• Sey le r's Z. Phy si o l. Chem. , 355 : 1381, 1974.
258) Assmann, G. , H. B. Brewer, Jr. , Proc. Natl . Acad. Sci. U. S .• 71 : 1534, 1974. 259) Assmann, G. , R. J. Hig h et, E. A. Sokoloski, H. B. Brewer, Jr. , Proc. Natl . Acad. Sci. US, 71:3701, 1974. 260) Sin g er , S. J. , G. L. Nic o lson, Scie nce, 175:no, 1972. 261) Assmann, G. , H. B. Brewer, Jr. , Proc. Natl . Acad. Sci. US, 17 989, 1974. 262) Jac kson, R. L. , A. M. Gott o, Jr. S. E. Lux, K. M. Joh n, S. Fleis · cher, ]. Bi o l. Chem. , 248:8449, 1973. 263) Jac kson, R. L. , J. D. Morrise tt , H. J. Pownall, A. M. Gott o, Jr. , ]. Bi o l. Chem., 248:5218, 1973. 264) Jac kson, R. L. , J. D. Morrise tt , J. T. Sp a rrow, J. P. Se gr e st , H. J. Pownall, L. C. Smi th, H. F. Hoff , A. M. Gott o, Jr. , ]. Bi o l. Clzem. , 249:5314, 1974. 265) Lux, S. E. , R. Hirz , R. I. Shrag er , A. M. Gott o, J. Bi o l. Clze m ... 247:2598, 1972. 266) Camejo , G. , E. M. Suarez, V. Munoz, Bi oc lzi m . Bi op h ys . Acta , 218: 155, 1970. 267) Gia n g ea ud, M. C. , D. Pasti er , M. Ay r aultj ar rie r , J. Polonovski, Bi o chim i e, 56 : 245, 1974. 268) Scanu, A. , J. Bi o l. Chem. , 242:711, 1967. 269) Sodhi, H. S. , R. G. Gould, J. Bi o l. Clzem. , 242: 1205, 1967. 270) Segr e st, J. P. , R. L. Jac kson, J. D. Morrise tt , A. M. Gott o, Jr. , Fe d. Europ ea n Bi oc hem. Soc. Lett er s, 38:247, 1974. 271) Baker, N. H. , Delahunty , T. , Gott o, A. M. , Jac kson, R. L, Proc. Natl . Acad. Sci. U.S ., 71:3631, 1974. 272) Verdery, R. B. , A. V. Nic h ols, C!zem. Plzy s. Lipids , 14: 123, 1975. 273) Morrise tt , J. D. , Pownall, H. J. , Sp ar row, T. Jac kson, R. L. , Go- tto, A. M. , Lip ids Lip o p r ote i n s and Drug s (Kritc h evsky , D. Paolett i, R. Holmes, W. L. eds. ), pp. 7~35, Plenum Press, New York, 1975. 274) Van der Bij l, P. , and Reman, F. C. , C/ in. Clzem. Acta , 60: 191, 1975. 275) Sata , T. , Havel, R. J. , Jon es, A. L. , ]. Lipid Res. , 13 : 757, 1972. 276) Hami lton , J. A. , Op pe nheim er, N. P. , Addleman, R. , Clouse, A. 0. , Cordes, E. H. , Ste i n e r, P. M. , Glueck, C. J. , Scie n ce, 194: 1424, 1976.
277) Ha m i lton , J. A. , Op pe nheim er, N. , Cordes, E. H. , J. Bi o l. Chem. • in the Presss, 1977. 278) Morrise tt , J. D. , Pownall, H. J. , Jac kso n , R. L. , Seg u ra, R. , Gott o, A. M. , Ta un to n , 0. D. , Polyu nsa tu r ate d Fatt y acid s Am. oil Chem. Soc .. Monog ra p h, No. 4. (Ha m i lto n , R. T. , Kunau, W. H. eds. ), 139 ~61, Am. Oi l Chem. Soc. , Publi sh e rs Ca m p a ig n , 1977. 279) Smi th, L. C. , Mi lle r, A. L. , Ta u nto n , 0. D. , Hu, A. S. , Pownall, H. J. , Ci rcu lati on \떠~넬 Sup pl. N, Abstr . , p. 445, 1973. 280) Glomsct, J. A. , Norum, K. R. , Advances in Lipid Research(Pao- ett i, R. Kritc h evsky , D. eds. ), vol. Il , pp. 1~65, Academi c Press. New York. 281) Neubeck, W. , Seid e l, D. , Cl in. Chi m . , 21:853, 1975. 282) Mag n ani, H. , Alaup o vic , P. , Seid e l, D. , Confe r ence on Serum. Li po pr ote i n s Graz. Oct. 21~23, Abstr . , B. p. 16, 1973. • 283) Hami lto n , R. L. , Havel, R. J. , Kane, J. P. , Blaurock, A. E. , Sata . T. , Scie n ce, 172:475, 1971. 284) Pats h , J. R. , Aune, K. C. , Gott o, A. M. , Jr. , Morrise tt , J. D. , J. Bi ol . Chem. , 252: 2113, 1977. 285) Jer shil d , R. A. , Jr. , R. T. Chay ton , Am. J. Anat. , 131:481, 1971. 286) Ty tga t, G. N. , C. E. Rubin , D. R. Saunders, J. Cl in. Invest. , 50: 2065, 1971 . 287) Rog e rs, J. B. , Jr. , W. Bochenek, Bi o chi m . Bi op h ys . Acta , 202:426, 1970. 288) Rubin , C. E. , Gastr o ente r olog y, 50 : 65, 1966. 289) Senio r , J. R. , J. Li pid Res. , 5 : 495, 1964. 290) Sim monds, W. J. , Fat absorpt ion and Chy lo mi cr on for mati on In: Blood Lip ids and Lip op r ote t n s Qu anti tat i on Comp o sit ion and. Meta b olis m , edit ed by G. J. Nelson, New York, W ile y , p. 705, 1972. 291) Carey, M. C. , D. M. Small, Arch. Inte r nal. Med. , 130:506, 1972. 292) Holt, P. R. , Arch. Inte r nal. Med. , 130 : 574, 1972. 293) Hamosh, M. , R. 0. Scow, J. Cli n. Invest. , 52:88, 1973. 294) Kay d en, H. J. , M. Medic k , Bi o chi m . Bi op h y s. Acta , 176 : 37, 1969. 295) Cardell, R. R. , Jr. , S. Badenhausen, K. R. Porte r , J. Cell Bi o l .• 34: 123, 1967. 296) Arvid s on, G. A. E. , A. Nil s son, Li pids , 7:344, 1972. 297) Frie d man, H. I. , R. R. Cardell, Jr. , J. Cell Bi o l. , 52: 15, 1972.
298) Sa be sti n, S. M. , K. J. Iss; il b a ch er , Scie nce, 147: 114 9, 1965. 299) Re dg ra ve, T. G. , D. B. Zil v e rsmi t, Am. J. Plt ys io l. , 217 : 3 36, 1969. 300) Re :l5 r ave, T. G. , Proc. Soc. Exp tl. Bi o l. Me d. , 130 : 776, 196 9. 301) Glic k m 3 .n , R. M. , K. I\oir s ch, K. J. Isse lb achc r, J. Cli 11. Invest. , 51: 35 6, 1972. 302) Gli ck man, R. M. , K. Kir s ch, J. Cl in. Inve st . , 52 : 291 0, 197 3. 303) Redg ra ve, T. G. , Austr a li an J. Exp tl. Bi o l. Me d. Sci. , 49 : 209 , 1971. 304) Frie d man, H. I. , R. R. Ci r dell, Jr. , Exp tl. Ce ll Re s. , 75 : 57, 1972. 305) O!ed zka·S l otw in s ka, H. , V. J. De se t , Hi st o c lze m i e. , 28: 195, 1971. 306) Redg ra ve, T. G. , Austr a li an J. Exp tl. Bi o l. Med. Sci. , 51 : 427 , 1973. 307) Subbraia h , P. V. , J. Ga ng u ly, Bi o chem. J. , 118 : 233, 1970. 308) Roheim , P. S. , L. I. Gid e z . , H. A. Eder, J. Clin . Invest. , 45 : 297, 1966. 309) Ockner, R. K. , K. J. Bio : :k, K. J. Ihsel b a ch er , Scie n ce, 162: 1285. , 1968. 310) O::kner, R. K. , F. B. Hug h es, K. J. Ihsel ba cher, J. Cl in. Invest. , 48:2367, 1969. 311) Wi nd mueller, H. G. , R. I. Levy , J. Bi o l. Chem. , 243:48 78 , 1968. 312) Wi nd mueller, H. G. , F. T. Lin d g re n, W. J. Lossow, R. I. Levy , Bi oc li im. Bi op/zys . Acta , 202: 507, 1970. 313) Noel, S. P. , D. Rubin s te i n , J. Li pid Re s. , 15: 300, 1974. 314) Wi nd mueller, H. G. , P. N. Herbert, R. I. Levy , J. Lipzd. Res. , 14: 215, 1973. 315) Wi nd mueller, H. G. , A. E. Sp a eth , J. Lipid Re s. , 13 : 92, 1972. 316) Marsh, J. B. , J. Lip id Res. , 15 : 544, 1974. 317) Fredric k son, D. S. , A. M. Gott o, R. I. Levy , Fami lial Lip o pr o te i n defi cie n cy (abe ta l ip o pr o te i n e mi a, hy po beta l ip o pr o te i n e mi a and Tan· gier dis e ase)• In: The Meta b olic Basis of Inherit ed Di se ase, edit ed by J. B. Sta n bury, J. B. Wy n g a arden, D. S. Fredric k son, New York, McGraw·Hi ll, pp. 493~530, 1972. :31 8) Kay d en, H. J. , Ann. Rev. Med. , 23 : 285, 1972. 319) Parti n, J. S. , J. C. Parti n, W. K. Schubert, A. J. McAda m s, Gast· roente r olog y, 67: 107, 1974. 320) Gott o, A. M. , R. I. Levy , K. Joh n, D. S. Fredric k son, New Eng l .
]. Med., 284:813, 1971. 321) Kostn er, G. , A. Holasek, H. G. Bohlmann, H. Thie d ~, Clin . Sci. Mo!. Med. , 46:457, 1974. 322) Scanu, A. M. , L. P. Ag ge rbeck, A. W. Kruski, C. T. Lim , H. J. Kay d en, ]. Clin . Invest. , 53 : 440, 1974. 323) Alci nd or, L. G. , R. Infa n te , C. Soler·argi la g a , A. Rais o nneir , J. Polonovski, J. Caroli , Bi o chi m . Bi op h y s. Acta , 210:483, 1970. 324) Heim berg, M. , H. G. Wi lc ox, ]. Bi o l. Chem. , 247:875, 1972. 325) Grete n , H. , A. D. Snid e rman, J. G. Chandler, D. S t z i:l b 따 r g, W. V. Brown, Fed. Europ ea n Bi o chem. Soc. Lett er s, 42: 157, 1974. 326) Gi de z, L. I. , P. S. Roheim , H. A. Eder, ]. Lip id R es. , 6: 377, 1965. 327) Barte r , P. J. , ]. Lip id Res. , 15: 11, 1974. 328) Barte r , P. J. , ]. Lip id Res. , 15: 234, 1974. 329) Illin g w orth , D. R. , 0. W. Portm an, L. E. Whip ple , Bi o ch im . Bi o · phy s. Acta , 369:304, 1974. 330) Rudel, L. L. , M. D. Morris, J. M. Felts , ]. Clin . Invest. , 51 : 2686, 197 2. 331) Chan, L. , Jac kson, K. L. , O'Malley, B. W. , Means, A. R. , ]. Clin . Invest. , 58 : 368, 1976. 332) Jac kson, R. L. , Ch1n, L. , Snow, L. D. , Means, A. R. , Fed. Proc. , 1978. 333) Gi au mann, H. , Be rs tr a nd, A. , Eric s son, J. L. E. , ]. Cell Bi o l. , 6-l: 356, 1975. 33-1 ) Alexander, C. A. , Hami lton , R. L. , Havel, R. J. , ]. Cell Bi o l. , 69: 241, 1976. 335) Nestr u ck, A. C. , Rubin s te i n , D. , Can. ]. Bi o clzem. , 54:617, 1976. 336) Dolph in , P. J. , Rubin s t.z i n , D. , Can. ]. Bi o clt em . , 55: 83, 1976. 337) Jac k s'.)n, R. L. , Morrisz tt , J. D. , Got to, A. M. , Jr. , P!z ys io l. Rev. , 56 : 259, 1976. 338) Fellin , R. , B. Ag o sti ni , W. Rost, D. Seid e l, Clin . Cli im. Acta , 54: 325, 1974. 339) Levy , R. I. , T. Lang e r, A. M. Gott o, D. S. Fredric k son, Cl in. Res. , 18: 539, 1970. 340) a) Goldstz i n , S. , Ch1p :n1 n, M. J. , Mi lls , G. L. , At he rosclerosis , 28: 93, 197 7. b) Ch3. pm an, M. S. , ]. Li pid Res. , 21:789, 1980. 341) Faerge men, 0. , Slta , T. , Kane, J. P. , Havel, R. J. , ]. Cl in.
Invest. , 56 : 1396, 1975. 334432)) SFuid rgi ,e , B .N S.. H, . ,T aProgn, lisM, . PE.. ,, ].R oLbiipn s iodn , ReDs.. S, . ,1 9B : i3 4o2cl, ze1m9 」78.. , 178:455, 1979. 344) Weech, P. K. , Mi lls , G. L. , Bi oc lzem. ]. , 175 : 413, 1978. 345) Maro!, Y. L. , Nestr u k, A. C. , Bergs e th , M. , Bid a llie r , M. , Robin - son, W. T. , Jef f ries , D. , Can. ]. Bi o chem. , 56:963, 1978. 346) Illin g w orth , D. R. , Bi o clzem. Bi o p hy s. Acta , 388: 38, 1975. 347) Sig u rdsson, G. , Nic o ll, A. , Lewi s, B. , J. Cli1 1 . Invest. , 56: 1481, 1975. 348) Reardon, M. F. , Fid g e, N. H. , Neste l , P. J. , J. Cl in. Invest. , 61 : 850, 1978. 349) Le, N. A. , Melish , J. S. , Roach, B. C. , Gin s berg, H. N. , Brown, W. V. , ]. Lip id. Res. , 19 : 578, 1978 . 350) Berman, M. , Hall, M. ILL, Le vy , R. l. , Eis e nberg, S. , Bil h eim er, D. W. , Phair , R. D. , Goebel, R. H. , ]. Lipid Res. , 19:38, 1978. 351) Berman, M. , Hall, M. ILL, Levy , R. I. , Eis e nberg, S. , Bil h eim er, D.W. , Phair , R.D., Goebel, R.H.,J . Lip id Res., 19:38, 1978. 352) Soete r , A. K. , My a nt, N. B. , Thomp so n, G. R. , At he rosclerosis , 32 : 315, 1979. 353) Jak os, E. 0. , Nic o ll, A. , Woott on , R. , Turner, P. R. , Mag ill, P. J. , Lewi s, B. , Eur. ]. Cl i11. Invest. , 10 : 149, 1980, 354) Fid g e, N. H. , Pouli s, P. , J. Lip id Res. , 19 : 342, 1978. 355) Ghis e ll i, G. , Bio c h im. Bi op hy s. Acta , 711 : 311, 1982. 356) Hami lton , R. L. , Wi lliam s, M. C. 1 Fie l in g , C. J. , Havel, R. J. , ]. Clin . Invest. , 58: 667, 1976. 357) March, J. B. , ]. Lip id Res. , 17:85, 1976. 358) Hami lto n , R. L. , Advan. Exp tl. Med. Bi o l. , 26:7, 1972. 359) Assmann, G. , D. Fre:l ri c k son, P. Herbert, T. Forte , R. Hein e n, Ci rcu latt o n, 49 : 50, Sup pl. ][ , abstr . , 1000, 1974. 360) Lux, S. E. , R. I. Levy , A. M. Got to, D. S. Fredric k son, ]. Cl in. Invest. , 51: 2505, 1972. 361) Bail ey , J. M. , J. Butl er , Arch. Bio c hem. Bi op hy s. , 159 : 580, 1973. 362) Bate s , S. R. , G. H. Roth b lat, Bi oc him . Bi op l z y s. Acta , 360 : 38, 1974. 363) Ste i n , 0. , Y. Ste i n , Bi o ch im. Bi op hy s. Acta , 326 : 232, 1973. 364) Cli fton -Bl igh , P. , P. J. Neste l , H. M. Why te. , New Eng l. ]. Med.
286 : 567, 1972. 365) Grete n , H. , T. Hannemann, W. Gusek, 0. Vi ve !!. , New Eng l. J. Med. , 291:548, 1974 . 366) Scherer, R. , G. Ruhenstr o uth ·Bauer, Klin . Wochsche. , 51 : 1059, 367) L19o7u3is. , L. s. , H. J. PownaIl, A. M. Gott o, Jr. , Ann. Reu. Bi o chi m . , 47:751, 1978; 368) Ni ch ols, A. V. , E. L. Cog giol a, L. C. Jen sen, E. H. Yokoy a ma, Bi oc h im. Bi op hy s. Acta , 168: 87, 1968. 369) Nic h ols, A. V. , L. Smi th, J. Li pid Res. , 6 : 206, 1965. 370) Qu arfo d t, S. H. , F. Bosto n , H. Hild erman, Bi oc h im. Bi op hy s . Acta , 231 : 290, 1971 . 371) Ba sf o r d, J. M. , J. Glover, C. Green, Bi o chi m . Bi op h y s. Acta , 84:764 , 1964 . 372) Be ll, F. P. , Exp tl. Mo/. Path o l. , 19 : 263, 1973. 373) Be ll, F. P. , C. J. Schwa rt z , Bi co hi m . Bi op h y s. Acta , 231 : 553, 1971 . 374 ) Be ll, F. P. , J. B. Somer, I. H. Craig , C. J. Schwartz , Path o log y, 4 : 2os, 1972. 375) Bj or nson, L. K. , C. Gn\ew kowski, H. J. Kay d en, J. Lipid Res. , 16:39, 1975. 376) Bruckdorfe r , K. R. , C. Green, Bi o chem. J. , 104:270, 1967. 377) Kunkel, H. G. , A. G. Bearn, Proc. Soc. Exp tl. Bi o l. Med. , 86: 887, 1954 . 378) Illin g w orth , D. R. , 0. W. Portm an, Bi oc hi m . Bi op h y s. Acta , 280: 281, 1972. 379) Illin g w orth , D. R. , 0. W. Portm an, J. Lip id Res. , 13 : 220, 1972. 380) Reed, C. F. , M. Murph y, G. Roberts , J. Cl in. Invest. , 47:749, 1968. 381) W irt z , K. W. A. , D. B. Zil v ersmi t, Bi oc hem. Bi' oph y s. Acta , 193: 105, 1969. 382) Zil v ersmi t, D. B. , J. Li pid. Res, 12 : 36, 1971 . 383) Kook, A. I. , D. Rubin s te i n , Bi oc h im. Bt' oph y s. Acta , 202:396, 384) Illin g w orth , D. R. , 0. W. Portm an, A. L. Roberts o n, Jr. , W. A. Mag ya r, Bio ch i m . Bi op hy s. Acta , 306:422, 1973. 385) Pete r son, J. A. , H. Rubin , Exp tl. Cell Res. , 58: 365, 1969. 386) Lekim , D. , H. Betz i n g , W. Sto e ff el, Hop pe -Seyl e r's Z. Phy st o l .
Chem. , 353 : 9-49 , 1972. 388) W irt z , K. W. A. , Bi oc lzi m . Bi o p lz y s. Acta , 3H : 95, I 974. 389) Eis e nberg, S. , D. W. Bil he im er, R. I. Levy , Bi oc h im . Bi op ! zys. Acta , 280:94, 1972. 390) Rubin s te i n , B., D. Rubin s te i n , J. Lip id Re s., 13:317, 1972. 391) Rubin s te i n , B. , D. Rubin s te i n , J. Li pid Re s. , 14: 357, 1973. 392) Havel, R. J. , J. P. Kane, M. L. Kashy a p, J. Cl in. Invest. , 52 : 32, 1973. 393) Fosbrooke, A. , S. Choksey, B. Wharto n , Arclz. Di se a se s Clz ild lzood, 48 : 729, 1973. 394) Fredric k son, D: S. , P. H. Al tro cchi, L. V. Avio l , A1111. Inte r n al Med. , 55 : 1016, 1961 . 395) a) Gj on e E. , Scand. J. Cl in. Lab. Invest. , 33- Su p pl. 137, 1974. b) Glomset J. A. , J. Li pid Res, 9: 155, 1968. c) Glomset, J. A. , Blood Li pids and Lip o p r ote i n s: Qu ant itat i on Comp o sit ion and Meta b olis m , edit ed by G. J. Nelson, New York, Wi ley , p. 745~87, 1972. 396) Glomset, J. A. , K. R. Norum, Advan. Lipid Re s. , 11 : 1, 1973. 397) Norum, K. R. , Ann. Bi o l. Cl in. , 31 : 123, 1973. 398) Sg ou t as , D. S. , Bi o chemi st r y , 11 : 293, 1972. 399) Fie l din g , C. J. , V. G. Shore, P. E. Fie l din g , Bi o chem. Bi op h y s. Res. Commun. , 46 : 149 3, 1972. 400) Souta r , A. , C. Garner, H. N. Baker, J. T. Sp ; 1r row, R. L. Jac kson, A.M. Gott o, L. C. Smi th, Bi o chemi st r y , 14:3057, 1975. 401) Kostn e r, G. , Scand. J. Clin . Lab. Invest. , 33, Sup pl, 137, p. 19, 1974. 402) Marcel, Y. L. , C. Vezin a , Bi oc lzi m . Bi op !1 y s . Acta , 306:<197, 1973. 403) Souta r , A. K. , H. J. Pownall, A, S. Hu, L. 0. Smi th, Bi o chemi s· try , 13:2828, 1974. 404) Albert, J. J. , Canbana, V. G. , Sta h l, Y. D. D. , Bi oc he mi st r y , 15 : 1084, 1976. 405) Osug a, T. , O. W. Portm a n, Am. J. Phy si o l. , 220 : 735, 1971 . 406) Glomset, J. A. , et al. , Sca11d. ]. C/in . Lab. Invest. , 33: 165, 1974. 407) Sim on, J. B. , J. L. Boy e r, Bi o chi m . Bi op ltys. Acta , 218: 549, 1971 . 408) Clark, S. B. , Norum, K. R. , J. Lipid. Res. , 18: 293, 1977. 409) Marcel, Y. L. , C. Vezin a , Bi oc hlm. Bi op hy s. Acta , 306:497, 1973.
410) Norum, K. R. , E. Gj on e, Scand. ]. C/i1 1 . Lab. Invest. , 20: :Bl, 1967. 411) Norum, K. R. , J. A. Glomset, E. Gj on e, The Meta b oli c Basis of Inherit ed Di se ase, edit ed by J. B. Sta n bury, J. B. W yn g a arden, D. S. Fredric k son, New York, McGraw- H i ll, pp. 531~45, 1972. 412) Gj on e, E. , Scand. ]. Clin . Invest. , 33, Sup pl, 137: 73, 1974. 413) Norum, K. R. , E. Gj on e, Scand. J. Cl in. Lab. Invest. , 22: 94, 1968. 414) Norum, K. R. , E. Gj on e, Scand. J. Cl in. Lab. Invest. , 22: 339, 1968. 415) Alaup o vic , P. , W. J. McConath y, M. D. Curry, H. N. Mag n ani, H. Torsvik , K. Berg, E. Gj on e, Scand, J. Clin . Lab. Invest. , 33, Sup pl, 137: 83, 1974. 416) McConath y, W. J. , P. Alaup o vic , M. D. Curry, H. N. Mag n ani, H. Torsvik , K. Berg, E. Gj on e, Bi o chi m . Bi op lzy s. Acta , 326:406, 1973. 417) Forte , T. , A. V. Ni ch ols, J. A. Glomset, K. Norum, Scand. J. Lab. Cl in. Invest. , 33, Sup pl, 137: 121, 1974. 418) Forte , T. , K. R. Norum, J. A. Glomset, A. V. Ni ch ols, J. Cl in. Invest. , 50:1141, 1971 . 419) Glomset, J. A. , A. V. Nic h ols, K. R. Norum, W. Ki ng , T. Forte , J. C/ in. Invest. , 52: 1078, 1973. 420) Norum, K. R. , J. A. Glomset, A. V. Ni ch ols, T. Forte , J. Clin . Invest. , 50: 1131, 1971 . 421) Torsvik , H. , C/ in. Gene!. , 3 : 188, 1972. 422) Norum, K. R. , J. A. Glomset, W. Ki ng , Europ ea n J. C/ in. Invest. , t:3 86, 94. abs, 1971. 423) Forte , T. M. , A. V. Ni ch ols, E. L. Gong , S. Lux, R. I. Levy , Bi o · chim . Bio h p ys. Acta , 248: 318, 1971 . 424) Torsvik , H. , K. Berg, H. N. Mag n ani, W. J. Mcconath y , P. Alaup ov ic , Fed. Europ ea n Bt' oc hem. Soc. Lett er s, 24: I65, 1972. 425) Kostn er, G. , Holosek, A. , Bi o chemi st y , 11 : 1217~23, 1973. 426) Gli ck man, R. M. , Green, P. H. R. , Proc. Nati . Acad. Sci U. S. A. , 74: 2569, 1977. 427) La Ross, J. C. ,_ Levy , R. I. , Brown, W. V. , Fredric k son, D. S. , Am. J. Phy si o l. , 220: 785, 1971 . 428) Glomset, J. A. , Norum, K. R. , Ni ch ols, A. V. , Ki ng , W. C. , Mi tc·
hell, C. D. , Ap ple g a te , K. R. , Gong , E. J. , Gjo n e, E. , Scand. J. Cl in. Lab. Invest. , 35, Sup pl, 142, pp. 3~30, 1975. 429) Van Berke!, T. J. C. , Kostn er, J. F. , Hulsmann, W. C. , Bi oc lz im . B£ oplz y si c s Acta , 486 : 586, 1977. 430) Nakai, T. , Ott o, P. S. , Kennedy , D. L. , Whay n e, T. F. , J. Bi o l. Clzem. , 251:4914, 1976. 431) Drevon, C. A. , Berg, T. , Norum, K. R. , Bi oc lzi m . Bi op hy s ic s Acta , 487: 122, 1977. 432) Aug u sti n, J. , Freeze, H. , Teja d a, P. , Brown, W. V. , J. Bi o l. Chem. , 253:2_9 1 2, 1978. 433) Chung , J. , Scanu, A. M. , ]. Bi o l. Che m . , 252:4 2 02, 1977. 434) Fie l din g , P. E. , Shore, V. G. , Fie l d in g , C. J. , Bi o chemi st r y , 16: 1896, 1977. 435) Fie l din g , C. J. , Bi oc h im. Bi op hy s. Acta , 178: 499 , 1969. 436) Twu, J. S. , Garfi nk el, A. S. , Schotz , 1\1. C. , At lter o sclerosis , 22: 463, 1975. 437) Ehnholm, C. , Shaw, W. , Grete n , H. , Brnwn, W. V. , J. Bi o l. Chem. , 250:6756, 1975. 438) Bensadoun, A. , Ehnholm, C. , Ste i n b erg, D. , Brown, W. V. , J. Bi o l. Chem. , 249 : 2220, 1974 . 439) Eg el rud, T. , Oliv e crona, T, J. Bi ol . Chem. , 247 : 6212, 1972. 440) Iveriu s , P. H. , Ostl u nd-Lin d g v is t , A. M. , J. Bi ol . Chem. , 251 : 7791, 1976. 441) Komp ian g , I. P. , Bensadoun, A. , Yang , M. W. W. , J. Lip id Res. , 17:498, 1976. 442) Fie l din g , C. J. , Bi oc him . Bio ph y s. Acta , 218: 221, 1970. 443) Fie l din g , P. E. , Shore, V. G. , Fie l din g , C. J. , Bi o chemi st r y , 13 : 4318, 1974. 444) Schotz , M. C. , Twu, J. S. , Pedersen , M. E. , Chen, C. H. , Garfi- nkel, A. S. , Borenszta j n , J. , Bi oc hi m . Bi op hy s . Acta , 489 : 214, 1977. 445) Pete r Ni lss on-Ehle, Ai len e S. Garfi nk el, Mi ch ael C. Scholz, Ann. Rev. Bi o chem. , 49:674, 1980. 446) Hernell, 0. , Eg e lrud, T. , Oli ve crona, T. , Bi oc hi m . Bi op hy s. Acta , 382:233, 1975. 447) Eg el rud, T. ; Oli ve crona, T. , Bi oc him . Bi op hy s . Acta , 306: 115, 1973. 448) Twu, J. S. , Ni lsso n-Ehle, P. , Schotz , M. C. , Bi oc hemi st r y , 15 :
1904, 1976. 449) Ganesan , D. , Bass, H. B. , FEBS. Lett . , 53: 1, 1975. 450) H:i v el, R. J. , Fie l d i ng , C. J. , Oli ve cr ona, T. , Shore, V. G. , Fie l din g , P. E. , Eg el rud, T. , Bi o chemi st r y, 12: 1828, 1973. 451) Twu, J. S. , Garfi nk el, A. S. , Schotz , M. C. , At h erosclerosis , 22: 463, 1975. •15 2) Ekma n, R. , Ni lss on -Ehle, P. , Cl in. Chem. Acta , 63:29~35, 1975. -l53 ) Ni ls son-Ehle, P. , Garfi nk el, A. S. , Schotz , M. C. , Ann. Rev. Bi o• chem. , 49 : 67, 1980. 45 4) Oliv ecrona, T. , B~ ng tss on, G. , At h erosclerosis N, ed. G. Schet- tier , Y. Goto , Y. Ha t:1 , G. Klose, pp. 325~8, Berlin , Sp r in g e r, p. 797, 1977. 455) Mi ller , A. L. , Smi th, L. C. , J. Bi o l. Chem. , 248:3359, 1973. 456) Eis e nberg, S. , Prog . Bi oc lt em . Pharm. , 15 : 139, 1979. 457) Eis e nberg, S. , Rachmi le wi tz, D. , J. Lip id. Res, 16 : 451, 1973. 458) Eis e nberg, S. , At h erosclerosis Revi ew s, ed. R. Paolett i, A. M. Got to, Jr. , 1 : 32~60, New York, Raven, p. 275, 1976. 459) Scow, R. 0. , Eg el rud, T. , Bi o chi m . Bi op h y s. Acta , 431 : 538, 1976. 460) Eis e nberg, S. , Oli ve crona, T. , J. Li pid Res. , 20:614~23, 1979. 461) Small, D. M. , Proc. Int. Conf. Bi o l. Membr. , ed. K. Bloch, L. Boli o, D. C. Toste n , In Press, 1980. 462) Smi th, L. C. , Scow, R. 0. , Prog . Bi o chem. Plt ar m. , 15:109, 1979. 463) Scow, R. 0. , Blanchett e- Mackie , E. J. , Smi th, L. C. , Gi re. Res. , 39:149, 1976. 464 ) Scow, R. 0. , Desnuelle, P. , Verge r, R. , J. Bi o l. Chem. , 254:6456, 1979. 465) Havel, R. J. , Kane, J. P. , Fed. Proc. , 34: 2250~7, 1975. 466) Howard, B. V. , J. Lip id Res. , 18: 561, 1977. 467) Brennem3 .n , D. E. , Sp ec to r , A. A. , J. Lip id Res. , 15:309, 1974. 468) Morley, N. H. , Kuksis , A. , Buchnea, D. , My the r, J. J. , J. Bi o l. Chem. , 250 : 3414, 1975. 469) Somerharju , P. , Kuusi, T. , Palt au f, F. , Ki nn unen, P. K. J. , FE BS. Lett . , 96: 170, 1978. 470) Bry; K. , Andersson, L. 0. , Kuusi, T. , Kin n unen, P. K. J. , Bi oc him . Bi op hy s . Acta , 575 : 121, 1979. 471) Bry, K. , Kuusi, T. , Andersson, L. C. , Ki nn unen, P. K. J. , FEBS.
Lett . , 106: 111, 1979. 472) Tornq u is t , H. , Belfr ag e , P. , J. Bi o l. Chem. , 239:401, 1976, 473) Tornq u is t , H. , Ni lss on-Ehle, P. , Belfr ag e , P. , Bi oc lzi m . Bi op lz y s. Acta , 530:474, 1978. 474) DeGroot, W. T. M. , Lipids , 7:626, 1971. 475) Pats c h, J. R. , Gott o, A. M. , Jr. , Ol ive crona, T. , Eis e nberg, S. , Proc. Natl . Acad. Sci. USA, 75:4519, 1978. 476) Glomset, J. A. , Prag. Bi o chem. Plzarm. , 15 : 41~66, 1979. 477) Mi lle r, N. E. , Lipids , 13 : 914, 1978. 478) Suri, B. S. , Targ, M. E. , Robin s on, D. S. , Bi o clzcm, ]. , 178:455, 1979. 479) Sauar, J. , Holme, R. , Blomhoff , J. P. , Cl in. Chem. Acta , 87: 327, 1978, 480) Chaje k , T. , Eis e nberg, S. , ]. C/in . Invest. , 61 : 1654, 1978. 481) Wi lso n, D. E. , Lees, R. S. , ]. Cii 11. Invest. , 51 : 1051, 1972. 482) Belfr ag e, P. , Berg, B. , Hag e rstr a nd, I. , Ni lss on-Ehle, P. , Tornq - uis t , H. , Wi eb e, T. , Eur. ]. C/ in, Invest, , 7: 127, 1977. 483) Ekman, R. , Fex, G. , Joh ansson, B. G. , Ni ls son-Ehle, P. , Wads· eti n, J. , Scand. ]. Cl in. Lab. Invest. , 1980, 484) Tall, A. R. , Small, D. M. , N. Eng . ]. Med. , 299: 1232, 1978. 485) Gli ck man, R. M. , Green, P. H. R. , Proc. Natl . Acad, Sci. U. S. A. , 74:2569, 1977, 486) Rachmi lew i tz, D. , Fain a ru, M. , Meta b olis m , 28 : 739, 1979. 487) Hallberg, D. , Acta . Phy si o l. Scand. , 65, Sup pl. 254, p. 22, 1965, 488) Brunzell, J. D. , Hazzard, W. R. , Porte , D. , Bie r man, E. L. , ]. Clin . Invest. , 52: 1578, 1973. 489) Robin s on, D. S, , Comp , Bt' oc hem. , 18 : 51, 1970. 490) Fie l din g , C. J. , Bi o chemi sr y, 15 : 879, 1976. 491) Fie l din g , C, J. , Havel, R. J. , Arch. Path ol. Lab. Med. , 101 :225, 1977 492) Crye r, A. , Davie s , P. , Robin s on, D. S. , Blood and Arte ria l Wall t'n At he rog e nesis and Arte r ia l Thrombosis , ed. J, G. A. J. Haut· vast, R. J. J. Hormus, F. Vandenhaar, pp. 102~10. Leid e n: Brill p.1 50, 1975, 493) Borenszta j n , J. , Rone, M. S. , Sandros, T. , Bi o chim . Bi op h y s, Acta , 398:394, 1975. 494) Cunnin g h am, V. J. , ·Ro bin s on, D. S. , Bi o clzem. ]. , 112 : 203, 1969.
495) Ni lss on-Ehle, P. , Garfi nk el, A. S. , Schotz , M. C. , Bi/ 'Jc hi .. ,. Bi op - ltys. Acta , 431 : 147, 1976. 496) Garfi nk el, A. S. , Ni lss on-Ehle, P. , Schotz , M. C. , Bi o chi m . Bi op h y s. Acta , 424: 264, 1976. 497) Pe de rsen, M. E. , Schotz , M. C. , /. Nutr . , 110: 48 1, 1980. 498) Chaje k , T. , Ste i n , 0. , Ste i n , Y. , Bi o chi m . Bi op h y s. Acta , 388: 260, 1975. 499) Frie d m'. ln , G. , Ste i n , 0. , Ste i n , Y. , Bi oc hi m . Bi op h y s. Acta , 573: 521~34, 1979. 500) Frie d m an, G. , Ste i n , 0. , Ste i n , Y. , FEBS Lett . , 100:371~3, 1979. 501) Felts , J. M. , It:1k ura, H. , Crane, R. T. , Bi o chzm. Bi op hy s. Res. Commun. , 66: 1467~75, 1975. 502) Wall ind er, L. , Beng tss on, G. , Oli ve crona, T. , Bi oc hi m . Bi op h y s . . Acta , 49: 166, 1979. 503) Borenszta j n , J. , Bi o chi m . Bi op h y s. Acta , 6: 231, 1979. 504) Ashby , P. , Bennett , D. P. , Sp e ncer, I. M. , Robin 3 on, D. S. , Bi oc ·· lzem. J. , 176:865, 1978. 505) Chung , J. , Scanu, A. M. , /. Bi o l. Chem. , 232:4202, 1977. 506) Fie l din g , C. J. , Fie l din g , P. E. , Choleste r ol Meta b oli sm and Lip o l- ytic Enzy m ~s, ed. J. Polonovski, pp. 165~72, New York: Masson, USA. p. 211, 1977. 507) Tan, M. H. , S:1 ta, T. , Havel, R. J. , J. Li pid Res. , 18: 363, 1977. 508) Jac kson, R. L. , Bi k er, H. N. , Gil liam , E. B. , Gott o, A. M. , Jr. , Proc_ N. lti. Acad. Sci. USA, 74: 1942, 1975. 509) Ki nn unen, P. K. J. , Jac kson, R. L. , Smi th, L. C. , Gott o, A. M. , Jr . .. Sp irro ,v, J. T. , Proc. Natl . Acad. Sci. USA. , 74:4848, 1977. 510) S:n ith, L. C. , Pownall, H. J. , Gott o, A. M. , Jr. , A 、 m. Rev. Bi o chem. , 47:751, 1978. 511) M1nt ul i n, W. W. , G::>t to, A. M. , Jr. , Int. C?.> tf . on At he roscler, ed. L. A. Ci rlso n, R. Paolett i, C. R. Sir tor i, G. Weber, pp. 57~69,. New York: Raven, p. 762, 1977. 512) Fie l din g , C. J. , Fie l din g , P. E. , /. Li pid Res. , 17:419, 1976. 513) Lukens, T. W. , Borenszta j n , J. , Bi o chem, J. , 175: 1143, 1978. 514) Breckenrid g e, W. C. , Lit tle, J. A. , Ste i n e r, G. , ·ch ow, A. , Poaps t ,,. M. , N. Eng l. J. Med. , 298: 1265, 1978. 515) Ostl u nd-Li nd q u is t , A. M. , Iveriu s , P. H. , Bi o chem. Bi op hy s. Res,
Commun. , 65: 1447, 1975. -,1 6) Chung , J. , Scanu, A. M. , Reman, F. , Bi o chi m . Bi o p hy s, Acta , 296: 116, 1973. 517) Bia t o n , V. , Vandamme, D. , Peete r s, H. , FEES. Lett . , 44: 185, 1974. 518) Rossner, S. , Vessby , B. , Nutr . Meta b . , 21 : 342, 1977. 519) Oliv e crona, T. , Beng tso n, G. , l\far klund, S. E. , Hind ahl, H. , Hook, M. , Fed. Proc. , 36:60, 1977. 520) Elkeles, R. S. , Harm. Meta b . Res. , 6: 151, 1974. 521) Iveriu s , P. H. , Lin d ahl, U. , Eg e lrud, T. , Oli ve crona, T. , ]. Bi o l, Chem. , 247:6610, 1972. 522) Oli ve crona, T. , Beng tss on, G. , Hook, M. , Lin d ahl, U. , Lipo p r· ote i n Meta b oli sm , ed. H. Crete n , p. 13, Berli n: Sp r in g e r, p. 160, 1976. 523) Horner, A. A. , Proc. Natl . Acad. Sci. USA. , 69: 3469, 1972. 524) Sta p ra ns, J. , Felts , J. M. , Bi o chem. Bi op hy s. Res. Commun. , 79:1272, 1977. 525) Crete n , H. , Levy , R. I. , Fales, H. , Fredric k son, D. S. , Bi o chi m , Bi op hy s. Acta , 210:39, 1970. 52 6) Kuusi, T. , Ki nn unen, P. K. J. , Ehnholm, C. , Ni kk il a, E. A. , FEES Lett . , 98:314 , 1979. 527) Ostl u nd-Lin d q ui s t , A. M. , Bi o chem. ]. , 179 : 555, 1979. ·52 8) Jan sen, H. , Kalkman, C. , Zonneveld, A. J. , Hi ilsm ann, W. C. , FEES Lett . , 98:299, 1979. 529) Kuusi, T. , Ni kk il a, E. A. , Vi rt a n en, I. , Ki nn unen, P. K. J. , Bi o clzem, ]. , 181 : 245, 1979. 530) Sauar, J. , Sto kke, K. T. , Cl in. Chem. Acta , 92: 101, 1979. 531) Kuusi, T. , Ki nn unen, P. K. J. , Ni kk il a, E. A. , FEES. Lett . , 104: 384, 1979. 532) E!-Mag h rabi, M. R. , Wait e, M. , Rudel, L. L. , Ki ng , V. L. , Bi o chi m . Bi op hy s . Acta , 572: 52, 1979. 533) Kuusi, T. , Bry, K. , Ni kk il a, E. A. , Ki nn unen R. K. J. , Med. Bi o l. , 57:192, 1979. 534) Wait e, M. , Sis s on, P. , El-Mag h rabi, R. , Bi o clz im . Bi op hy s. Acta , 530 : 292, 1978. 535) Chaje k , T. , Frledman, G. , Ste i n , 0. , Ste i n , Y. , Bi o chi m . Bi op hy s,
Acta , 488:270, I977. '53 6) Hami lton , R. L. , Kay d en, H. J. , The Li v er:Normal and abnormal fun cti on s, ed, . F. F. Becker, pp. 531~72. , New York, Dekker, p. 572, 1974. 537) Getz , G. S. , Hay , R. V. , Bi o chemi st r y of At he rosclerosis , ed. , A. M. Scanu, R. W. W iss ler, G. S. Getz , pp. 151~88, New York: Dek· ker, p. 548 . 538) Hami lto n , R. L. , Di st u rbances in Lip id and Lip o p r ote i n Meta b o· /ism , ed. , J. M. Die t s c hy , A. M. Gott o, Jr. , J. A . Ont ko . , p.1 55, Balti m ore: Waverly, p. 295. 539) Goldste i n , J. L. , Brown, M. S. , Ann. Rev. Bi o chem. , 46 : 897, 1977. 540) Ste i n b erg, D. , Prog . Bi o chem. Pharm. , 15: 166, 1979. 541 ) Floren , C. H. , Ni ls son, A. , Bi o chem. J. , 174:827, 1978. 542 ) Carrella, M. , Coop e r, A. D. , Proc. Natl . Acad. Sci. USA. , 76: 338, 1979. 543) Coop e r, A. D. , Yu, P. Y. S. , J. Lipid Res. , 19:635, 1978. 544 ) Sherrill , B. C. , Die t s c hy , J. :M. , J. Bi o l. Chem. , 253 : 1859, 1978, 545) Schaefe r , E. J. , Levy , R. I. , Prog . Bi o chem. Pharm. , 25 : 200, 1979. 546 ) Roheim , P. S. , Rachmi le w i tz , D. , Ste i n , 0. , Ste i n , Y. , Bi o chi m . Bi op hy s. Acta , 248: 315, 1971 . 547) Nakai, T. , Whay n e, T. F. , J. Lab. Clin . Med. , 88 : 63. , 1976. 548) Ernst, Nancy and Robert I. Levy , Di et , Hy pe rlip ide mi a and At h er· osclerosis , Goodhart, Shil ls , Mordern Nutr i t ion in Healt h and Di se ase, 6th ed. , ,Le a & Febig e r, p. 1059, 1980. 'S4 9) Ernst, Nancy and Robert I. Levy , Diet Hy pe rlip ide mi a and At h ero· sclerosis , Goo:l ha rt, Shil ls, Modern Nutr i t ion in Healt h and Di s· ease, 6th , ed. Lea & Febig e r, p. 1065, 1980 ..
제 6 장 동맥경화증과 고지방혈중 1 서론 동백 경 화증의 현상은 동맥 내 벽 에 다량의 콜레 스테 롤 este r (est- -eri f ied choleste r ol) 의 축적 으로 형 성 되 는 ath ~romato u s 의 덩 어 리 (표면에 말라붙어 있는)이다. a t heroma 라는 것은 그 이름 자체가 회 람어에서 유래된 것으로 〈 죽 〉 이라는 것이다. 이 단어는 18 세기에 병리학자에 의해서 처음으로 씌어졌으며 그 부분을 쪼개 보면 노란 색의 죽 같은 지방이 나오며 요즈음은 이 물질의 대부분이 콜레스 테 푼 es t er 라고 알려 져 있 다• !) 흡연, 고혈압, 당뇨병 , 고지 방혈증 과 같 이 여 러 가지 이 유로 사람의 혈관벽 에 ath eroma 가 생 기 는데 2-4) 이 각각의 경우를 병리학적으로 분석해 보면 놀랍게도 증상내용 이 비슷하다. 이는 대부분이 동백벽의 가장 중간총인 med i a 와 i n ti ma 에 덩어리 같은 것이 붙어서 두꺼워져 있다. 이렇게 동백벽 의 중간충이 두꺼 위 지 는 이 유는 대 개 collag e n, elasti n, glu cosa-mi no g ly c ans 그리 고 fibr in 이 포함된 동백 벅 중간물질에 의 해 서 둘 러싸인 smooth muscle 세포의 증식에 의해서 축적되는 결과이 다. 5-7) 그러 나 ath eroma 내 부에 포함된 물질은 지 방 특히 콜레 스테를 -es te r 로서 smooth muscle 세 포로 둘러 싸여 있 는 세 포 사이 사이 의 공간과 smooth muscle 세 포내 자체 에 까지 도 다량 축적 되 어 있 다.
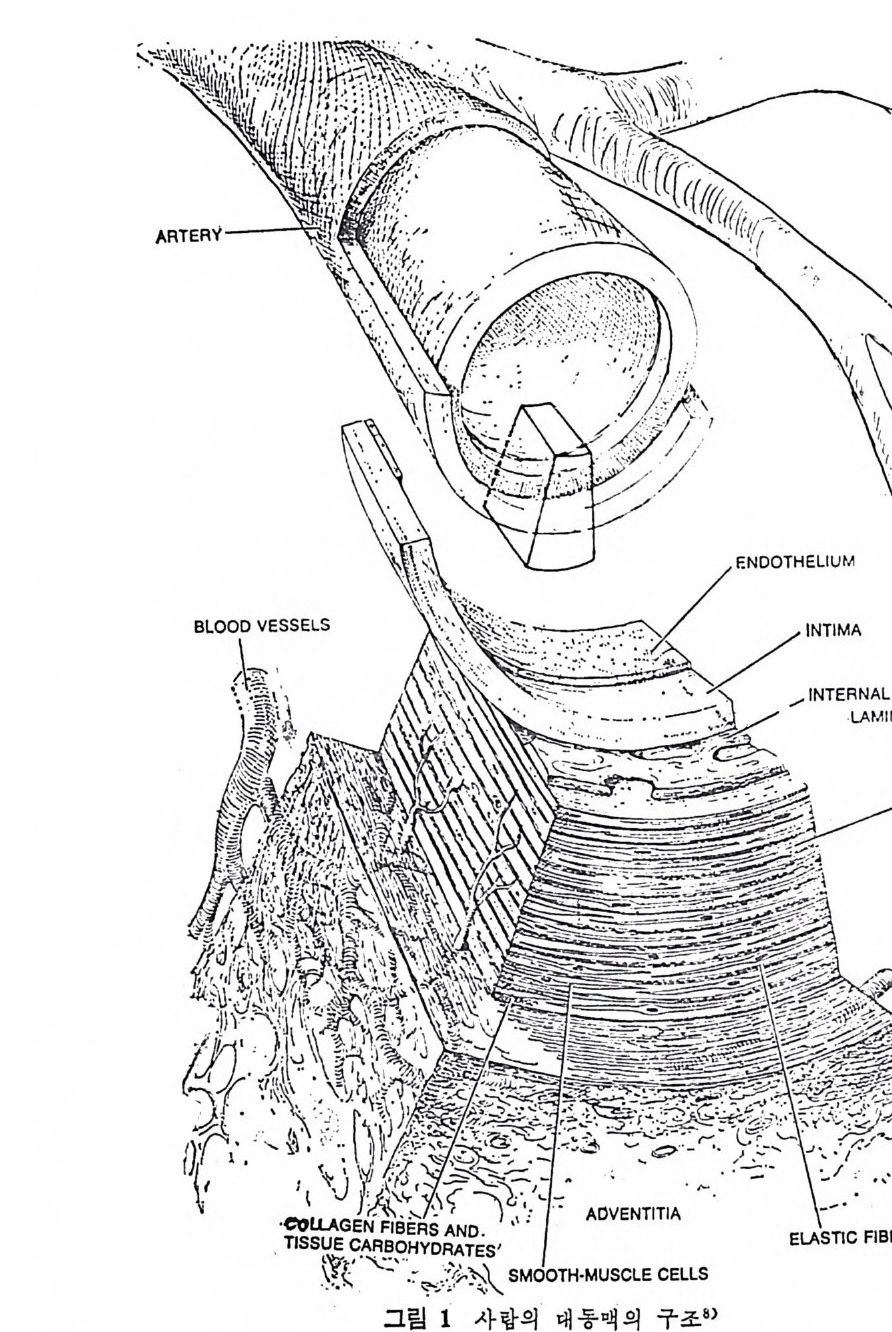 INTERNAL ELASTIC·
INTERNAL ELASTIC·
2 동맥벽의 구조 동맥은 득수한 구조로 이루어져 있으며 세포구성 성분도 특수하 다. 동맥벽은 3 컵으로 이루어져 있는데 가장 내면이 int i m a, 중간 충이 med i a 아고 초]의각충이 adven titi a 이다(그림 1 참조). In ti ma 의 최내부는 한겸의 endo t hel i al 세포로 나열되어 있으며 이들은 동맥내의 혈구세포를 갖고 있고 혈청으로부터 물과 기타 다 론 물질을 조직으로 통과시키는 것을 조절한다. 그리고 나머지 i n ti ma 충은 결체조직충으로서 내부의 탄력있는 세포막이다. 이 충 은 선체내 어느 부위의 동맥이냐, 또는 그 개인의 나이와 성별에 따라서 다르다. 십장동맥 의 int i m a 는 여 자보다 남자가 좀더 두 껍고 이 두께와 세포의 수는 양성 모두 나이가 증가됨에 따라서 중 가된다. 동맥 경 화증이 나타나는 충은 바로 이 int i m a 충이 다 탄력있는 조직으로 눈에 띄는 부위는 i n ti ma 와 분리된 부위, 죽 중간충인 med i a 이다. 이 부위는 동맥벽충중에서 가장 두껍고 동백 조직을 가장 지지하는 충이다. 이 충은 colla g en 의 섭유가 얽혀있 논 속에 자리 잡고 있 는 smooth muscle 세 포로써 이 루어 쳐 있 으며 이 세 포는 fibr ous 단백 질 인 elasti n 과 collag e n 과 그리 고 탄수화물 (g l y cosam i no g l y cans) 을 분비 한다, 동백 벽 의 가장 바깥충은 adventi tia 인데 이 충은 fibr oblast 세 포로써 구성 되 어 있 으며 이 들은 세 포간질에 촌재 하는 collag e n 과 gly c osami no g ly c ans 과 결 합되 어 있 다. adventi tia 충 은 혈관이 통하 고 있어서 이 혈관으로부터 공급되는 영양소를 동해 이 충의 영양 공급이 아루어진다. 또한 이 충은 주변 조직에 동맥이 정착하도록 부착시키는 역할울 한다• 신체내 다론 조직과 마찬가지로 동백조직에도 여러가지 질병이 나타나 전행될 수 있다. 마치 어떤 손상에 의한 상해와 치료, 감 영, 영중, 기타 종양 등이 나타날 수 있다. 그러나 이러한 질병 진행과정은 분류해 볼 수가 없다. 왜냐하면 모돈 병이 마지막 단계 에 가서는 유사하게 보이며 또한 혈관내부를 관찰하기가 어렵기 때
문에 자세한 분류가 아직까지 이루어지지 못하고 있다. 3 동백경화증의 조직학적인 변화과정 부겁 (au t o p s y)때 관찰된 동맥 경 화가 진행 된 부위 는 다음 사건에 서 보여주듯이 둥굳게 솟아오른 부위이다(그립 2 참조). 이들의 표 . 면에는 영중이 생겨 있지는 않지만 그대로 위로 솟아올라 있고 이 들의 색깔은 회색에서 황회색을 띠고 있다. 동백혈관 단면을 보면 내면 직경이 좁아져 있으며 동맥벽이 두꺼 워져 있다(그립 3 참조). 그림 4 는 혈관내부에 혈전(t hrombus) 이 생 겨서 혈류와 함께 이동되고 있는 상태이다. 다음의 그립 5 는 혈관벽 의 단면을 동백 경 화가 전전됨 에 따라서 도해한것이다. 그림 5_A 는 대동맥이나 심장대동맥의 정상적인 3 검의 동맥벽을 나타낸 것 으로 int i m a, media 그리 고 adventi tia 아 다. 그림 5-B
 그립 2 동맥경화가 생긴 동맥을 절개했을 때의 내부표면의 단면
그립 2 동맥경화가 생긴 동맥을 절개했을 때의 내부표면의 단면
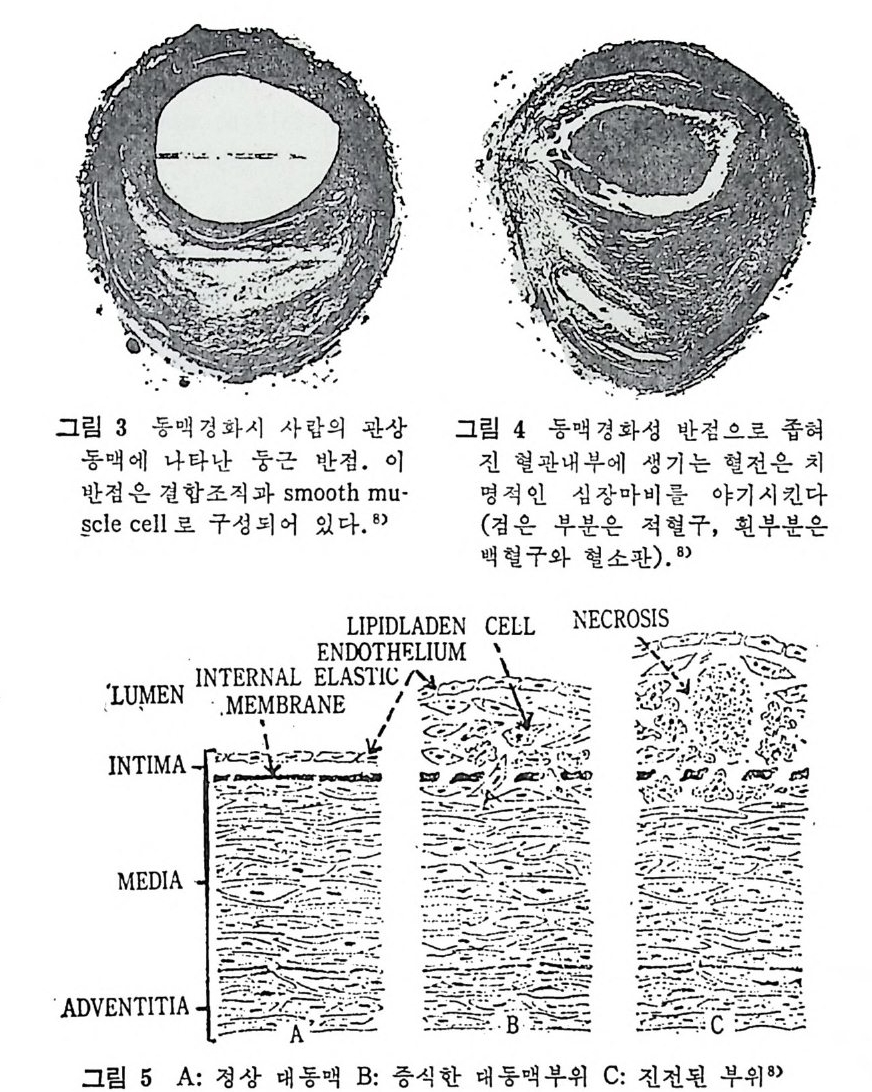 그립 3 동맥정화시 사람의 관상 그립 4 동맥 경화성 반접으로 좁혀
그립 3 동맥정화시 사람의 관상 그립 4 동맥 경화성 반접으로 좁혀
논 증식 되 고 있 는 부위 로서 int i m a 공간 안에 smooth muscle cell 이 축적되고 있는 것이다. 그림 5 C 는 전전된 부위로서 괴사부위가 생겼으며 혈전(t hrombus), 궤양이 생겼고 출혈 및 석화까지 생겼다. 동백 경 화는 혈청 내 의 lip o p ro te i n 이 나 또는 다른 구성 성 분이 동맥 벅내로 스며들어서 생성된다는 설이 있다. 이 설은 독일의 병리학
자 Rudolf Veic h ow 가 19 세 기 에 주장한 데 서 기 원된다. 8) 이 런 현 상은 고혈 압일 때 , endoth e lia l 세 포결 합에 상처 가 있 을 때 , 또는 hy pe rlip o pr ote i n e mi a 시 에 더 욱더 많이 일어 나는데 이 때 동백 벽 의
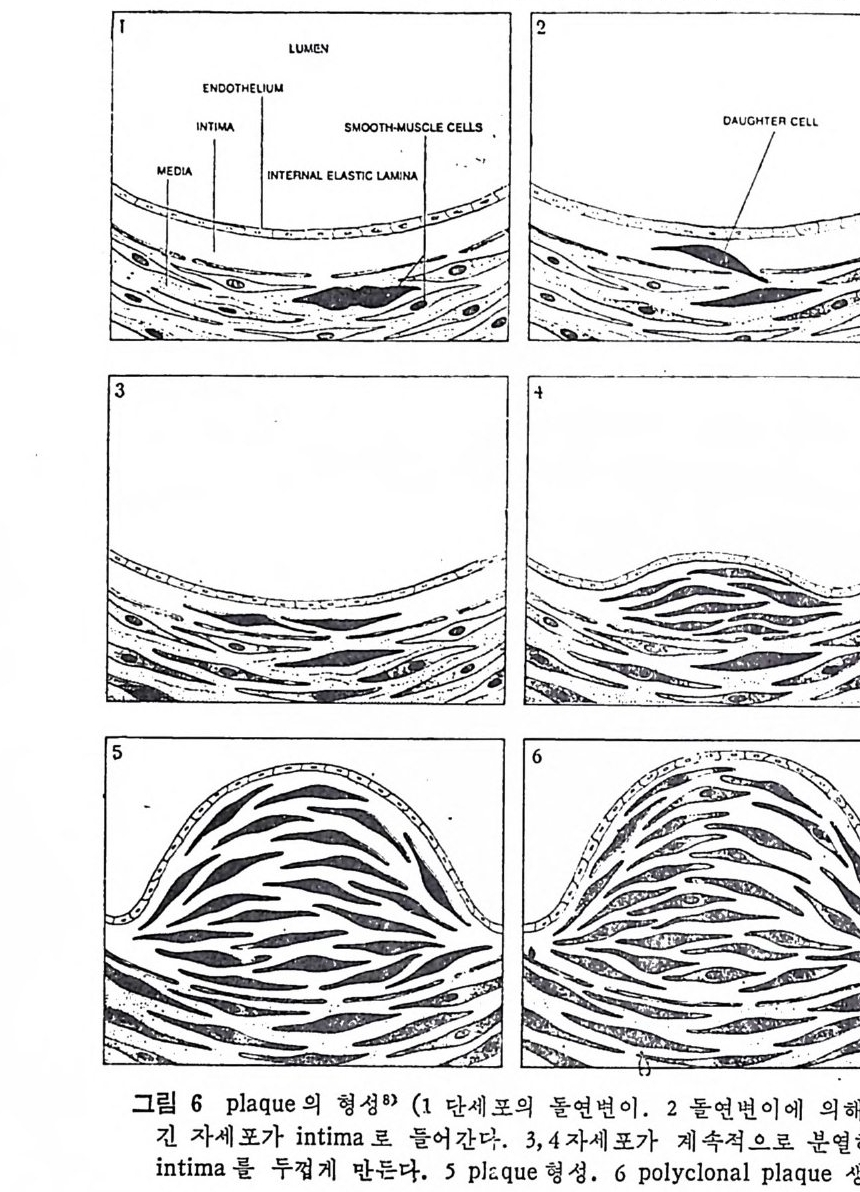 c~.
c~.
int i m a 공간에 혈청 lipo p r ote i n 이 나 다른 구성 물질이 스며 들여 가 논 윤이 상승되어 동백경화현상은 더욱 촉진된다. 요즈음 관찰된 바에 의 하면 동맥 경 화는 smooth muscle 세 포가 int i m al spa c e 로 증식 되 어 올라와서 축적 되 기 때 문에 생 긴다고 한다. 이 경 우에 여 분의 LDL 과 VLDL 을 smooth muscle cell 이 취 해 감 으로써 이 세포내에 콜레스테롤농도가 증가되며 콜레스테롤의 대사 울은 저하된다. 그러므로 이 세포내에 콜레스테를과 콜레스테롤 es t er 의 축적이 증가되고 그 결과 smooth muscle 세포의 변질이 온다. 따라서 성유화되고 지방이 축적되어서 뭉그렇게 뒤어 오르는 ath eroma pla q ue 가 생 긴다(그립 6 참조). 그림 6 은 p la q ue 가 생성되는 과정을 도해한 것이며 그림 7 은 생 성된 p la que 에 궤양이 생겨서 혈관벽이 터지고 세포가 변질되는 과 정이다. 그리고 p la q ue 내부에 콜레스데몰 결정이 생기고 지방이 축廳 적되어 있다. p la q ue 형성의 시작은 내부 med i a 에서 시작된다. 그 림에서 보여주듯이 두 종류의 세포가 존재한다. 하나로 겁게 나타 난 것은 단세포 (s i ng le cell) 이며 이는 돌연변이를 한다. 그래서 선 택적으로 유익을 끼치는데 어떤 자극은 변이에 의해서 생간 세포를 분열하도록 하는 원인이 된다(그립 6-1). 그래서 자세포 (dau gh t er cell) 는 int i m a 로 이 동해 간다(그림 6-2). 돌연변이 (mu t a ti on) 에 의 해 서 생긴 자세포는 중석을 자유로이 할 수 있는 능력이 생겨 계속 적 으로 분열한다. 고로 int i m a 를 두껍 게 만들어 (그립 6-3, 6-4) 결 는과 적본으래로의 불세쑥포 로튀부어터오 른변 이p l에a q u의e 를해서 생 생성긴한 다자(세그포립이 6며-5 ()그. 림모 6든— 5세) 결포 국 po lyc l onal pla q u e 가 생 성 되 며 두 종류의 세 포로부터 이 동되 고 중석되는 현상이 나타난다. 그림 7 은 monoclonal pla q u e 의 전전된 모습으로 endoth eli al 표 면 에 퀘 양이 생 기 며 smooth muscle cell 이 죽는 현상이 나타난다. 내부는 지방덩어리로 차있으며 결과로 세포가 죽거나 변질된다. 그 러 면 콜레 스테 롤과 lipo p r ote i n 이 pla q u e 내 로 이 동되 어 서 나간다. 때로는 동맥이 완전히 막히는 십한 경우도 나타난다. 위에서 말 한 p la q ue 가 계속해서 커지든가 또는 p la q ue 위에 혈액응고 덩어라
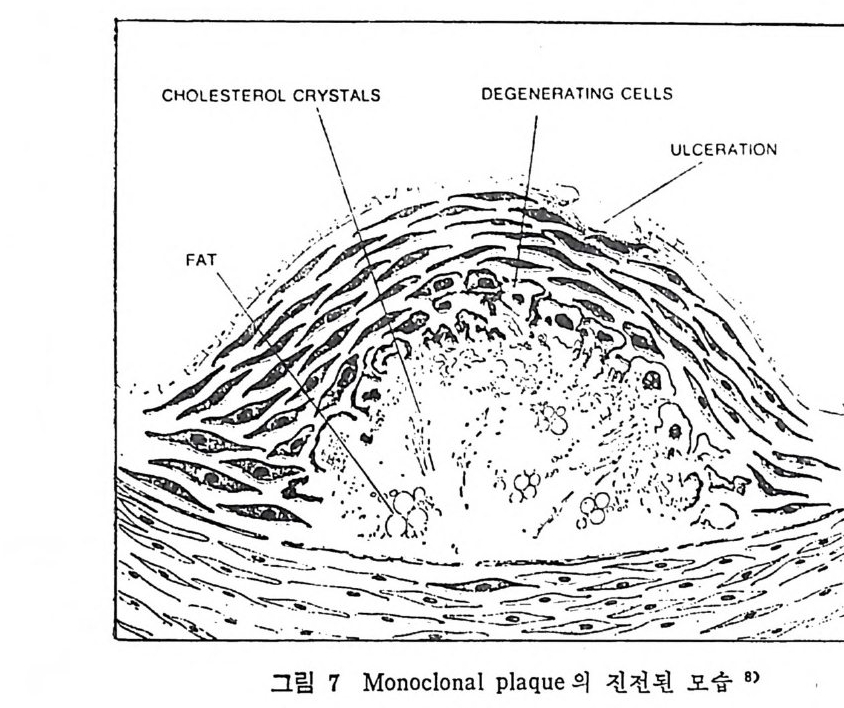 CHO L ESTEROL CRYSTALS DEGENERA T ING CE LLS
CHO L ESTEROL CRYSTALS DEGENERA T ING CE LLS
(t hrombus) 가 생기게 된다. 그러면 혈액의 소통이 미세해지는 부위 가 생기게 되며 결과적으로 혈관이 터지는 중상을 초래한다. 4 동백경화중의 임상적인 증세 (1) 관상동백 겅 화증 (coronar y ath erosclerosis ) 이 를 또한 동백 경 화성 (ath e roscleroti c) 또는 동맥 경 화성 십 장 질 환 (ath e roscleroti c heart d i sease) 이 라고 부르기 도 하고 관상동백 십 장절 환 (coronary hea rt dis e ase) 이 라고 부르기 도 한다, 1) Ang ina Pecto r is 관상동맥 (coronary art er y ) 내 면적 이 너 무 좁아져 서 십 장근육에 혈
액순환이 순조롭지 못한 혈저해중(i schem i a) 이 발생하며 결과적으로 가슴이 아프고 답답한 층세 가 나타난다. 이 런 단계 를 ang ina pec to r is 라고 하며 이 증세는 항상 그런 것이 아니고 육체적인 운동을 하돈 지 혹은 감정적인 스트레스를 받을 때 참정적으로 오는 층세이다. Ang ina pec to r is 는 안정 되 게 만 생 활하면 오래 살 수 있 다. 그리 고 어떤 a tt ack 이 와도 가볍게 넘길 수도 있다. 그러나 어떤 계기에 스 트레스나 운동이 십하게 되면 갑자기 사망할 수도 있다. 죽 불안정 해지면 심장동백에 혈전이 생겨서 동맥이 막히는 결과를 초래하여 죽음으로 이끈다. 2) 급성 심 근경 색 증 (acute my o cardia l in f ar cti on ) 십장으로 혈액을 공급하는 대동맥 중의 하나가 혈전으로 인해서 곽 막히면 이 걷과 심장에 혈액공급이 원활히 되지 않는다. 이런 증세 를 십 근경 색 증 (m y ocard i al i n fa rc ti on) 이 타고 하며 대 개 급성 으로 나타난다. 이때에는 십장근육이 죽으며 이런 현상을 혼히 〈십장마 비 (heart a tt ack) 〉라고 부른다. 대개 십장마비가 일어나기 몇 시간 전 이나 길어서 1 일 정도 전에 가슴에 통증이 있거나 압박감을 느낀다. 이러한 가슴의 통증이 새로 생긴 경우도 있고 이미 존재하고 있는· ang ina pe cto ris 의 가슴 통증이 자주 생 겨 서 나타나기 도 한다. 그 러 나 이 경 우 통증의 증상은 ang ina pe cto ris 때 보다 훨씬 십 하다. 3) 급사 급사를 하는 사람들의 50~65% 가 관상동백 십장병 (coron 효y hea rt dis e ase) 경 우라고 한다. 죽 십장병 으로 갑자기 사망하거 나 통증이 있다가 24 시간 내에 사망하는 경우를 말한다. 이러한 십장동맥경화로 인해서 오는 급사는 다음과 같은 경우에 나타난다. i) 아전에 어떤 증세가 있었던 사람 ii) 안정된 ang ina pec to ris 의 경 우로 가슴에 통증이 없 었 던 경 우 iii) ang ina pec to ris 의 경우는 아니지만 과거에 십장혈관의 혈전증세를가졌던사람 iv ) 급성 심장혈관 혈전중제로 고통이 온지 1 시간 정도된사람등이다. 대개 급사의 경우는 십장근육에 혈액공급이 되지 않는 혈저해중
(i schem i a) 의 경우로 혈전증을 반드시 동반하지는 않는다. 혈처해중 이 생기면 십장의 리듬이 깨진다. (2) 뇌 혈관병 (cerebrovascular dis e ase) 동백경화증은 뇌가 다른 혈관으로부터 혈액의 공급을 받고 있는 한 뇌에서는 어떤 증세도 나타나지 않는다. 또한 어떤 경우도 동맥 경화로 인해서 혈관이 완전히 막히거나 십하게 좁아져 있어도 이 과정이 갑자기 이루어지지 않고 서서히 이루어지면 아무런 증상이 나타나지 않는다. 죽 혈류량이 감소하여 뇌조직내에 혈 엑공급이 치 명적인 수준으로 감소되거나 혈관이 막히면 혈관이 터지거나 뇌조 직의 혈처해(i schem i a) 가 생기며 출혈이 생긴다. 뇌조직 어느부위냐 에 따라서 증세가 다룰 수 있다. 1) 잠정적인 중추신경계통 혈저해성 충격 노]조직내로 운반되는 혈액의 공급량이 갑자기 감소되는 상대를 〈중추신경계통 혈처해성충격〉이라고 한다. 이런 때는 혼히 뇌의 주 요 동맥, 죽 추골 (ve rt ebral) 중 하나가 막힌다. 만일에 추골 (ver t ebra l) 과 뇌 저 (basila r ) 또는 경 동맥 (caroti d ar t er i a) 의 혈류가 막히 면 이 는 뇌 수 (bra i n s t em) 로 혈액 공급을 하는 동맥 이 막히 는 것 으로써 이 런 경우에는 어지러운 증세를 보이고 몸의 균형이 깨지며 귀에서 소리 가 나며 시야가 이중으로 보이며 말을 더듬고 무엇을 삼키기가 곤 란해지는 증세가 나타난다. 만약 caroti d 동맥이 막히면 혈액공급이 안 되는 혈저해성충격이 오는데 이때에는 얼굴의 2/3 가 약해지며 손가락, 손, 팔, 다리 등이 혼들혼들 그대로 달려 있는 것처럼 약해진다. 또한 참정적으로 말을 잃어버리며 이해가 되지 않고 눈이 보이지 않게도 된다. 2) 뇌 졸증 (str o ke) 대개 뇌졸증은 2 가지로 나눈다. i) 동백혈관이 좁아져서 나타나 는 2 차 중세로 노]조직에 손상이 오거나 i schem i a 가 생기는 것과 ii)
동맥이 터져서 뇌출혈이 생기는 것이다. 전자의 경우는 대개 동백경화와 관련이 있지만 후자의 경우는 고 혈압과 관련이 있고 십한 동백경화와는 관련이 있기도 하고 없기도 하다. (3) 대동맥경화중 대동맥 (aor t a) 의 윗부분(t hora ci c a c. r t a) 의 동백경화는 혼히 나타나지 만 임상적인 증세는 혼하지 않고, 아랫부분의 대동맥 (abdomi na l aort a) 온 임상적 증세로 인해서 알려지게 되었다. 동맥 경 화로 인한 th oracic aorta 의 aneurys m 은 때 때 로 그 인접 부근에 압박을 초래한다. 증세로는 가슴의 통증, 무호흡중, 성대의 마비로 인한 언어곤란, 대정맥 (vena cava) 위쪽의 압박 신호가 오는 데 치명적일 수도 있다. 복강동맥 (abdomi na l aor t a) 의 ancurys m 은 신동백 (renal ar t er y)의 밑에서부터 유래된다. 배가 몹시 아프며 특히 요추(l umbar) 나 골반 (pe lvic ) 부위가 아프다. 때로는 혈관이 터지며 통증과 더불어서 출 혈이 있고 쇼크가 온다. (4) 신장혈 관의 페 쇄 (renalvascular occluio n ) 신장동맥의 동맥경화로 인한 페쇄는 신장부위의 기능무력증을 유발한다. 부분적으로 한쪽 신장동맥이 막히거나 또는 양쪽이 부분 적 으로 막히 면 고혈 압 (h yp e rt ens i on) 을 유발한다. (5) 말초혈관 경화중 복부동맥이 말초혈관(지체 혈관)으로 갈라지는부위에 경화가 와서 폐쇄되면 두 다리는 종아리로 내려가면서 십한 경련과 통증이 나타 난다. 그러나 편안히 쉼으로 해서 통증이 좀 가라앉을 수도 있다.
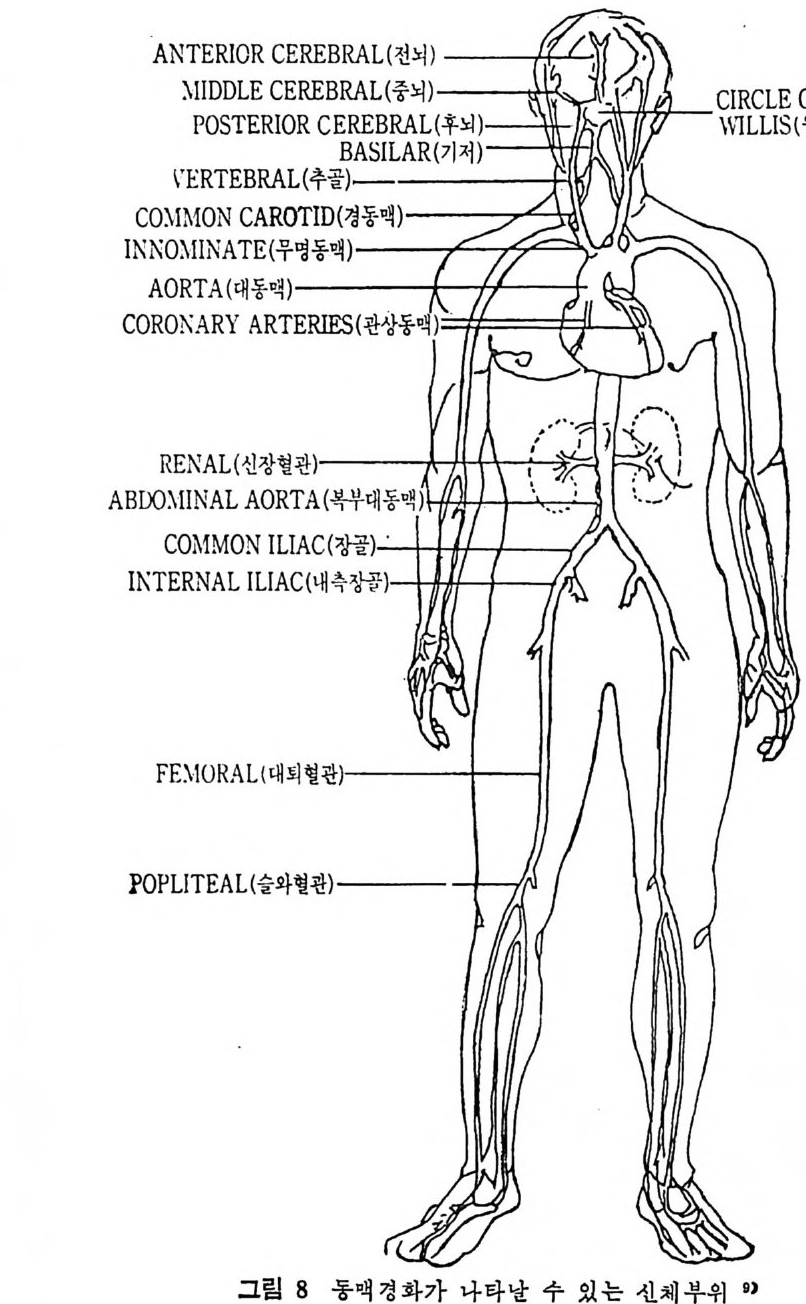 ANTERIOR CEREBRAL( 전뇌)
ANTERIOR CEREBRAL( 전뇌)
(6) 켜 1 동맥 경화중 페로 공급되는 동맥 한 은 말초부위로 가는 혈액과 다르다. 즉 페 동맥은 그 압력이 낮으며 또한 혈액에 함유된 산소의 농도도 낮다 .. 이 접과 관련해서 페동맥의 경화는 신체 다른부위로 순환하는 동맥 에 비 해 서 문제가 적을 수 있다. 그러나 이러한 경우는 페동맥의 압 력 이 높을 때에 일어난다. 그 원인은 십장의 왼쪽 십방에 병이 있거나 아니면 페 자체에 병이 있을 때 또는 아직까지 알려지지 않 은 이유로 일어난다. 앞 의 그립 8 은 동백경화가 발생할 수 있는 신 체의 각 부위 를 표시한 것이다. 5 LDL 과 동맥경화 (1) LDL 의 성분과 특칭 LDL 은 lip o p ro te i n 일종으로 1950 년대 에 이 미 Gof m an 에 의 해 서 이것의 함량이 혈청내에서 증가되면 동백경화가 생길 수 있는 확~ 이 현저해진다고 하였다 .10- 1) 사람의 혈청으로부터 유리된 LDL 입자를 초원십분리하면 그 비 중범위는 1.019~1.063 g /ml 이며 원자량은 약 2~3.5X106 정도이고 입 자의 크기 에 있 어 서 그 직 경 은 200~250°Am-3) 정 도로 다양하다. 이와같이 LDL 의 분자량이나 크기가다른 것은 이 입자내부중십부 에 함유되어 있는 지방량이 다르기 때문이며 단백질 구성성분의 차 이 때문은 아닌 것으로 알려져 있다 .12) 또한 LDL 은 전기영동시 p. 부위 에 나타나므로 /3- lip o p ro te i n 이 라는 명 칭 이 있 다. 일반적으로 LDL 의 지방구성은 전체 질량의 75% 를, 단백질은 25 %l4) 를 접유한다. 단백질은 모두 ap o lip o p ro t e i nB(A p oB) 로서 그 양이 LDL 매 입 자마다 500, ooo dalto n 정 도 함유되 어 있 다. 12-3> LDL 에서 지방울 제거하면 A p oB 는 강한 세제가 촌재하여도 불용성이
된다. A p oB 의 불용성 성질이 구조상에서 독수한 독성을 나타내는 데 분자량이 8,000 에서 250,000 범위 정도의 소단위 ( s ubun it)의 물질 로 구성되어 있다. 흔히 이 소단위물질의 분자량이 25,000 정도의 것 이 문헌에 나타난다. 12> Ap o B 의 5~9% 가 탄수화물이 며 주로 ga lacto s e, mannose, glu cosami ne , sia l ic acid 둥이 함유되 어 있 다• LDL 의 지방구성성분으로도비극성 중십부에 중성지방이 주로 함 유되어 있으며 대부분 콜레스테롤 es t er 이 많이 함유되어 있 다 .l4) a p olar 중십부 주변을 싸고 있는 지방은 인지방과 유리콜레스테 몰 이 다. Ap o -B 도 소단위 입 자로 구(g lobules) 형 태 로서 이 중 일부는 지 방중십부에 묻혀 있고 일부는 수면에 노출되어 있다 .1 2> LDL 입자내 전체 지방중에서 콜레스데몰이 약 60% 접유하며 이중 80% 가 콜레 스데 롤 es t er 로서 중십 부에 존재 한다. LDL 의 콜레 스테 롤 este r 에 부착된 주요 지 방산으로는 lin o leate 가 약 50% 이 며 oleate 와 pa lm- t a t e 가 각각 20% 와 15% 를 접유한다. 그리고 나머지 15% 중 에 ste a ric acid , pa lmi tola te , arachid o nate 가 분포되 어 있 다• 14- 5 ) LDL 전체에 함유되어 있는 지방중에서 30% 를 접유하는 지방은 인 지방이며 인지방 중에서 양적으로 많은 양이 함유된 것이 ph osp i hati dy lc holin e 으로 65 % 나 되 며 sp h in g o my e lin 이 2 5 % 이 다. 14) 그 리 고 LDL 은 적 어 도 다섯 종류의 gly c osp h in g o li pids 가 함유되 어 있다고 본다 .16) 혈청내 LDL 의 Ap o B 구성성분의 급원에 대해서 많은 연구가 전 행되고 있는데 간과 소장조직에서 합성되고 있음이 알려졌다 .17 - 8) Ap o B 는 중성 지 방함량이 풍부한 lip o pr ote i n 입 자 VLDL 의 일부성 분으로서 간에 의해 혈청내로 분비된다. 그런데 VLDL 은 기타 다 론 여러가지 종류의 단백질을함유하고 있다 .17 - 9) 간에 의해서 혈청 내에 분비된 VLDL 입자는 지방조직으로 이동되며 거기에서 lipo p r - o t e i n lip ase(LPL) 의 작용에 의 해 서 중성 지 방이 입 자로부터 이 동되 어 나간다 .19) 중성지방이 이동됨과 관련해서 A p oB 이의의 모든펩타이 드는 VLDL 입 자로부터 이 동되 어 나간다. 그리 고 나머 지 VLDL 입 자내에는 콜레스데몰 es t er 의 함량이 증가된다. 이 증가된 콜레스 테롤 es t er 는 필경 HDL 로부터 공급되는 유리콜레스테롤에 혈청
효소인 LCAT 의 작용에 의해서 형성된다고 본다. Glomse t의 연구에서 제시된 바에 의하면 HDL 은 모든 유리 콜레 스데몰의 급원이 되며 이 유리콜레스데롤은 에스텔화되어서 LDL 의 콜레 스테 롤 este r 의 급원이 된다고 하였 다. 20> VLDL 입 자로부터 대부분의 중성지방이 이동되고 입자내에 콜레스데몰 es t er 의 함량 이 충분히 증가되 면 VLDL 이 LDL 입 자로 된다. l9) 125I 동위원소로 처리된 l ip o p ro t e i n 을 이용한 연구에서 제시된 바 에 의하면 정상인의 간에서는 LDL 이 직접적으로 혈청내로 분비되 지 않으며 혈청 LDL 은 위에 제시된 기전에 의해서 VLDL 로부터 유도됨이 밝혀졌다 .21-2) 그러나 최근에 토끼를 대상으로 실형된 바 에 의 하면 LDL1 (d=l . 019~1 . 040 g /ml) 와 LDL2 B(d=l. 040~1 . 063g / ml) 가 혈청 LDL-B p ool 의 20% 를 접유한다고 본다. 그러나 이들은 VLDL 이나 IDL 에서 유도되어 오는 것 같지 않고 독립적으로 생 성되는 것이 아닌가 하고 생각한다 .23) 사람의 혈청 LDL 이 분해되는 조직이 어느 것인지에 대해서 분명 히 알려 진 바가 없 다. 그러 나 St ei n b erg 와 그의 동료들에 의 해서 최근에 실험되어전 바에 의하면 쥐의 경우 간, adrenal, 난소 (ovary) , 지라 (s p leen) 의 순서로 LDL 분해가 양적으로 많이 이루어지 논 조직 이 라고 지 적 하였 다. 24) 이 들은 14C-sucrose 를 추적 자(tr acer) 로서 이용하여서 LDL 이 분해되는 조직을 찾아내는 실험을 하였고 그 결과는 다음 표와 같다. 위 결과로 미루어 보면 LDL 의 분해가 이루어지는 조직은 간 이 외의 조직에서도 이루어지고 있음이 나타났다. (2) 사 람의 fibr oblast 세 포내 에 서 의 LDL 결합부위 와 대사경로 모든 포유동물의 세포는 그 세포막의 구성성분으로 유리콜레스 테롤을 요구한다. 최근에 포유동물 세포 배양실험에서도 의부에서 콜레스테롤을 가해 주거나 아니면 콜레스테롤을 체내에서 합성하도 록 해주지 않으면 세포가 생존하지 못하는 결과를 보여주었다 .25-6)
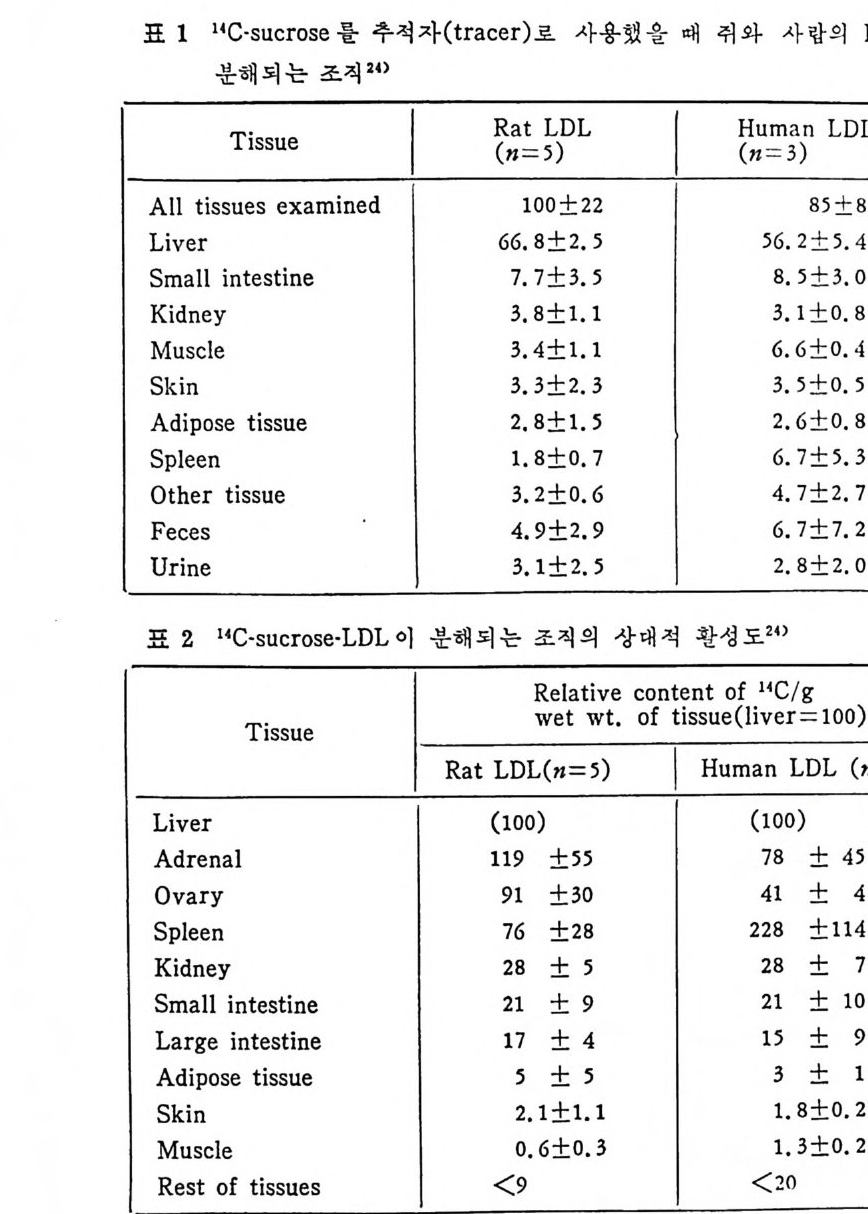 표 1 14C·sucrose 를 추적자(t racer) 로 사용했 을 때 쥐와 사람의 LDL 이
표 1 14C·sucrose 를 추적자(t racer) 로 사용했 을 때 쥐와 사람의 LDL 이
거의 모든 유리콜레스테롤은 세포의 원형질막에서 발견이 되며 이 들은 인지방분자와 관련되어 있다. 그리고 세포막을 형성하고 남은
여분의 콜레스데롤은 에스텔화된 형태로 세포내에 액체 결정체로서 처장된다 •27' LDL 대사에 있어 특정한 구성요소는 혈청 LDL 이 걷 합되 는 세 포표면 의 목정 결 합부위 (recep tor s it e) 이 다. 28-31 ) LDL 결합부위는 gly c op r ote i n 계통의 단백질로 구성되었을 것으 로 본다 . LDL recep tor sit e 의 다양한 특칭 에 대 해 서 연구가 진행 되 어 있 다. 다음의 표 는 LDL recep tor sit e 에 대 한 둑칭 을 요약한 표이다.
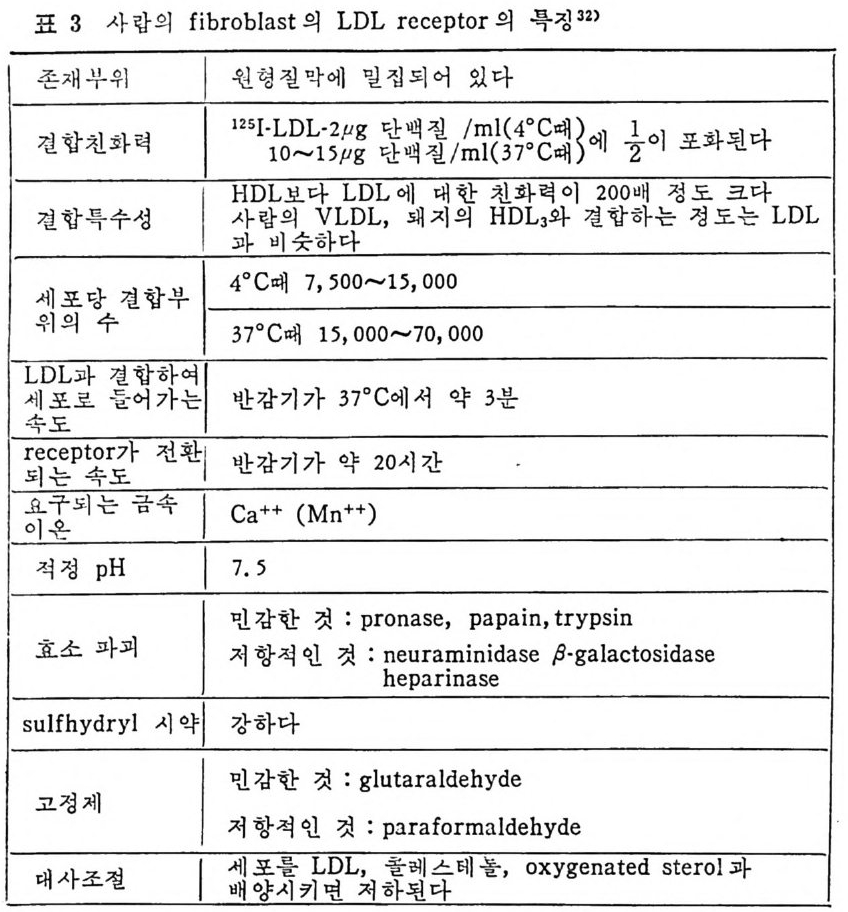 표 3 사 람의 fibr oblast 의 LDL recep tor 의 복칭 32)
표 3 사 람의 fibr oblast 의 LDL recep tor 의 복칭 32)
다음의 그림 은 LDL 이 LDL 결 합부위 (recep tor s it e) 에 서 결 합되 어
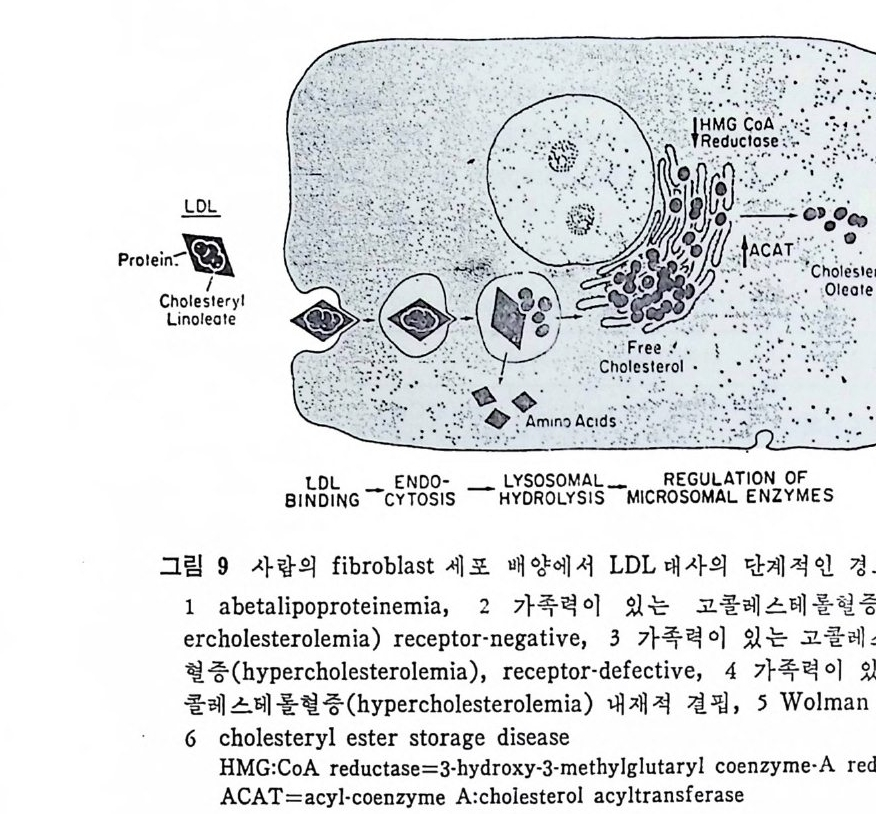 뿌
뿌
서 단계적으로 대사되어가는 경로를 사람의 fibr oblast 세포배양 실 현결과 표시한 것이다. 위의 그림 에서 제시된 숫자는 돌연변이 (mu t a ti on) 가 일어 난 부위 를 표시한 것이다. 대부분의 인체 세포는 계속해서 LDL 을 접하게 되므로 33 -4 > in viv o 연구에서 이들의 대사형태는 다음 그림에서 보여주는 바와 같 다 .35) 죽 LDL 이 촌재함으로 해서 평형의 상태가 유지된다. 그립 10 은 사람의 fibr oblast 세포배양시 배양배지에 LDL 을 포 함시키지 않았을 때와 포함시켰을 때에 콜레스테를 대사변화 cy c le 이 다. LDL recep tor , HMG CoA reducta s e, 콜레 스테 롤 ACAT 및
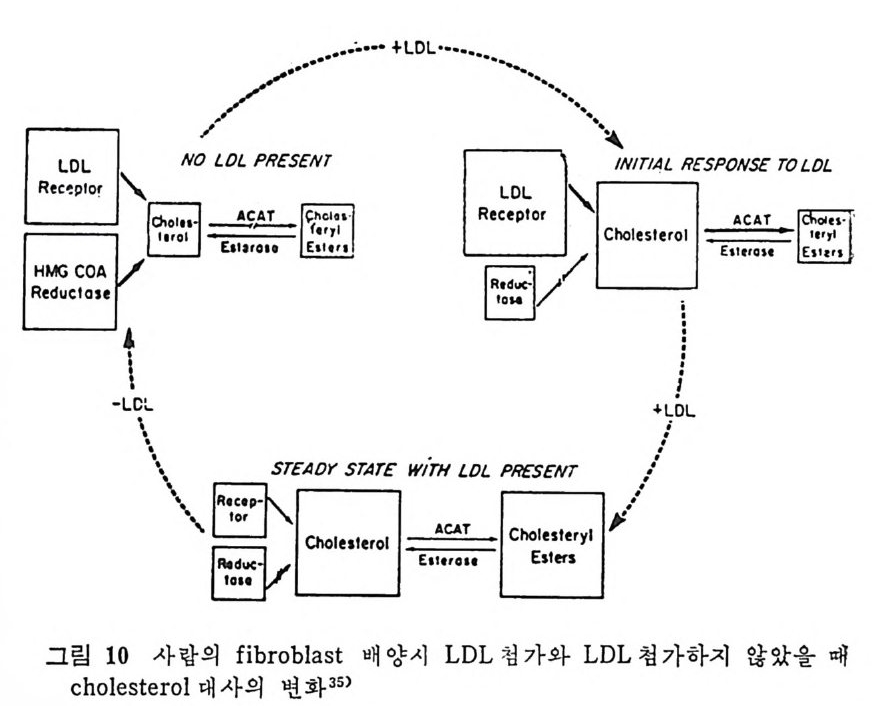 /'/ •••••••·•~•-+L DL••••-• ··•-.... .•••. ..• · ..· ··~
/'/ •••••••·•~•-+L DL••••-• ··•-.... .•••. ..• · ..· ··~
콜레스데몰 est e r 사이의 바교농도 수준은 4 각형의 크기로 표시하 였다. 35) LDL 이 정 상량으로 촌재 하고 콜레 스테 롤과 콜레 스데 몰 est e r 0J = 이 정 상적 으로 존재 하면 recep tor si te 는 LDL 과 결합이 일어 나며 따라서 HMG CoA reduct as e 의 활성은 처 하된다. 그러 므로 새 로이 합성되는 콜레스데를 양은 처하된다. LDL 이 배양배지에 첨가되 면 즉시 로 HMG CoA reduct as e 활성 이 저 하되 는 현상을 관찰하였 다. 36-7) 그런데 LDL 이 배양배지로부터 제거되면 LDL 결합부위의 수는 증가되 며 LDL 과의 천화력 은 커 지고 따라서 HMG CoA reduc tas e 의 활성이 커진다. 그러나 콜레스테롤과 콜레스데몰 es t er 의 양온·
갑소된다. 배지에 LDL 양을 접차증가시키면 LDL 결합부위는 LDL 에 기본적으로 결합되려고 반응하며 콜레스데룬의 농도가 높아진다. 그러 나 HMG CoA reducta s e 의 활성 은 낮다. 또한 신선하게 유리된 사람의 l y m p hoc yt es 가 LDL 과 결합되어 서 recep tor 기 전에 의 해 서 세 포내 로 취 해 지 면 HMG CoA reducta s e 활성이 처하되며 콜레스테 롤 este r 형성은 자국되고 또한 LDL rec- e pt or 의 합성이 억제되는 fee d back 의 관계 물 보이기도 한다 고 보 고되 었 다. 38-9) 그런데 유리 된 사 람의 lym p h ocy te 나 배 양된 fibr o-blast 가 LDL recep tor 에 있 어 서 도 다 같다고 본다. 40) 요츠음 동물을 대상으로 하는 연구에서 l ip o p ro t e i n 이 관련된 콜 레스데몰 대사조절 연구가 진행되고 있다 .4 1) 이 방법은 Henderson 에 의해서 시도되었으며 42) 다론 연구자들에 의해서 확인되었다 . 4 3-4) 4-a m i no p yra zol-py r im i di n e 인 adenin e ` 유사물질 이 간으로부터 lip o - pr ote i n 유리를 억제시키는데 이를 동물에게 두여했을 때 쥐의 할 청내 콜레스테롤의 수준이 떨어지면서 반면에 HMG CoA reduc- t ase 활성은 증가되었다. 그러면서 간세포 이의의 조직세포, 신장과 페에서 콜레스데를의 합성이 증가되었다 .4 1) 그런데 요즈음 다시 같 온 처리를 하였을 때 소장과 난소에서도 콜레스데를의 합성이 증가 되었음이 보고되었다 .45) LDL 의 대 서순곤 먼처 세 포표면의 LDL recep tor 부위 의 수와 찬화 력이 관련이 있으며 LDL 이 세포내로 들어가면 콜레스데를과 콜레 스테롤 este r 합성에 분명히 관련을 미치게 된다. 결과적으르 혈청 내에 총 콜레스데를과 콜레스테롤 este r 양 조절에 LDL 의 중재역 할은 현저하며 이런 기초에서 볼 때 LDL 대사는 동백경화 유발에 관련이 있다고 본다. (3) 혈청 LDL 수준의 상승이 어떻게 동백경화를 촉진하냐 동백경화증 유발은 나이가 증가함에 따라 비례적으로 증가하며 따라서 노인들의 사망원인으로 가장 큰 비율을 차지하는 것이 요 츠음 선진국의 경향이다. 그러나 동백경화의 병리학적 원인은 충분
히 규명되어 있지 않은 상태로 있으며 혈청 콜레스태 물 과 LDL 의 증 가가 가장 주요한 원인으로 지적되고 있다. 그런데 사람의 혈청내 콜레스데롤의 농도가 나이 중가와 더불어서 거의 직선적으로 증가 되고 있음은 찰 알려진 사실이며 이는 동맥경화의 위험을 항상 동 반한다 .48) LDL 의 혈청 내 수준이 상승되 는 기 본적 인 기 전은 LDL recep tor 부위에 LDL 이 결합되지 못하여 LDL 이 혈청내에 유리됨으로써 생 기는 결과이다. 그러므로 LDL 의 혈청내 수준이 증가되는 것은 고 콜레스테 롤 혈증 (h yp ercholes t erolem i a) 의 가족력 이 있어서 유전적으로 LDL rece pt or 부위 전핍이 생기거나 또는 다른 유전적인 요인이나 환경적 요인으로 인해서 생기며 그 결과 동맥벽에 콜레스테롤 este r 가 축적되어 결국에 가서는 동맥경화가 발생한다 .49) 그런데 늙은 fibr oblast 에 서 는 LDL 결 합능에 차이 가 나타나며 나이 증가에 따라 세 포막에 recep tor 부위 수의 감소가 차차 나타날 수 있 다고 생 각한다. SO) 한편 LDL 로부터 유도되 는 콜레 스데 몰 este r 의 축적 기전에 대해서는 알려진 것이 없다. 요즈음 확실하게 설명되는 것 은 동맥 경 화가 lip o p ro te i n 을 포함한 혈청 구성 성 분이 손상이 있 는 endoth eliu m 을 동해 서 동맥 벽 으로 스며 들어 가는 데 서 시 작된다 고 하였다 .51 一 2) 면역화학적 방법 (im munochemi ca l t echn iq ue) 을 사용해서 연구된 바 에 의 하면 사실상 많은 양의 lip o p r ote i n 과 다른 혈청 단백 질이 동맥 경 화부위 에 축적 되 어 있 는 것 으로 나타났다. 5-7) , 52-4) 그런데 이 러 한 이물질이 동맥벽에 존재하게 되면 동백벽의 중간총 med iai료부 터 온 smooth muscle cell 의 증석 이 촉진되 며 이 세 포들이 int i m a 로 이동해서 들어가게 되는데 이물질을 배제하기 위한 식군작용의 결 과로 이 런 현상이 나타난다. 55) 그러 면 smooth muscle cell 에 의 해서 먹히고 난 후에도 이 이물질은 lys osome 내에서 가수분해되어 서 작고 용해성이 있는 물질, 죽 아미노산, 지방산, 또는 단당으로 전환되며 또한 이동되어서 동백벽 밖으로 나간다. 그러나 LDL 7} 수분해에 의해서 유리된 콜레스테롤은 이를 용해시켜서 혈청내로 이 동시 킬 수 있는 운반체 가 촌재 하지 않는 한 smooth muscle cell 을
떠 나지 못한다. 그러 므로 smoot h muscle cell 밖으로의 콜레 스데 몰 · 이 동속도는 느리 며 따라서 스데 몰이 축적 된다. smooth muscle cell 내에 콜레스테롤이 축적되어 분비되지 못하면 세포내에서 일부가 에 스텔화되 어 콜레 스테 몰 este r 로서 축적 된다. 그런데 최 근에 LDL 생성과 분해가 혈청 콜레스테몰 수준에 영향을 미찬다고 보고하였 다. 특히 LDL 분해보다는 LDL 합성률에 의해서 혈청 콜레스데롤의 수준이 비교적 낮았던 사람에게서 조금 증가시켜 주는 걷과를 초래 하였 다고 보고되 었 다. 56) 여하튼 사람의 동백경화부위에 접차적으로 콜레스테롤 es t er 가 축적되고 있음이 Smi th & Sm it h 에 의해서 정리 보고되었다.” 가 족력이 있는 고콜레스데몰혈증 (h yp ercholes t erolem i a) 의 층세도 LDL 의 recep tor 수가 감소하면 이 를 보상하기 위한 작용으로 혈청 내 LDL- 콜레스테몰의 수준이 중가하는 것은 명백해졌으며 57) 이러한 · 사람은 동맥경화의 초기 증세를 보이고 있음이 관찰되었다. 최초의 LDL 과 콜레스테롤 수준 및 동백경화 유발관계의 연구는 주로 세 포표면막에 LDL-recep tor 수와 관련된 결합능력 및 찬화력의 차아 가 동맥경화 유발에 미치는 영향 둥으로 연구가 진행되고 있다.
* 참고문현 1) Schwartz , C. J. , Mi tch ell, J. R. , A. Postg r ad, Med. J. , 38:25, 1962. 2) Nati on al Insti tut e s of Health , Arte r io sclerosis , A Rep o rt by- the Nati on al Heart and Lung Insti tut e tas k for ce on Arte r io s c• lerosis , HEW, Pub!. No(NIH) 1971. 3) Ep st e i n , F. H. , Ostr a nder, L. D. Jr. , Prog . Cardio v asc. Di s. , 13:324, 1971. 4) Kannel, W. B. , Caste l l i, W. P. , Gordon, T. , McNamara, P. M. ,. Ann. Inte r n. Med. , 74: 1, 1971. 5) Wi ss ler, R. W. , in the My o cardiu m: Fail u re and Inf ar cti on , ed. E. Braunwald, pp, 155~66, New York: H. P. Pub!. Co. , 1973 ►
6) Haust, M. D. , Hum. Patl z ol. , 2:1 . 1971 . 7) Smi th, E. B. , Smi th, R. H. , In At he rosclerosis Revie w s, ed. R. Paolett i, A. M. Gott o. J r. , 1 : 119~36 , New York, Raven. B) Benedit t, E. P. , Sc i. Am. , 236 : 74, 1977. 9) DHEW. Publi ca t i o n No. (NIH) 72~ 13 7. JO ) Gof m an, J. W. , DeLalla, 0. , Glazie r , F. , Freeman, N. K. , Lin - dgr e n F. T. , Ni ch ols, A. V. , Str i s o we r. B. , Tamp li n , A. R. , p/a smati clz e 2:41 3 , 1954. 11) Gof m a n, J. W. , Rubin , L. , McGi nl ey , J. P. , Jon es, H. B. , Am. J_ Med. , 17: 514, 1954 . 12) Jac kso n , R. L. , Morris e tt , J. D. , Got to, A. M. Jr. , Phys i o l .. Re v. , 56 : 259, 1976. 13) Alaup o vic P. , Lee, D. M. , McConath y , W. J. , Bi oc him . Bi op h ys _ Acta . , 260:689, 1972. 14) Skip s ki, V. P. , In Blood Lipids and Lipo pr ote i n s : Qu anti tat i on , Comp o sit ion and Meta b olis m , ed. G. J. Nelson, pp, 471~583,. New York:W iley -I nte r -Scie n c e, 1972. 15) Goodman, D.S., Plzy si o l . Rev., 45: 74 7. 1965. 16) Dawson, G. , Kruski, A. W. , Scanu A. M. , J. Lip id Res. , 17;- 125, 1976. 17) Ha m i lt o n , R. L. , Adv. Exp. Med. Bi ol . , 26:7, 1972. 18) Fredric k son, D. S. , Got to, A. M. Jr. , Levy , R. I. , In The· Meta b olic Basis of Inherit ed dis e ase, ed. J. B. Sta n bury, J. B. Wy n g aa rden, D. S. Fredric k son, New York: McGraw Hi ll, pp. 493~530. 3rd, ed. 19) Havel R.J ., Adv. Exp . Med. Bi o l., 63: 37, 1975. 20) Glomset , J. A. , J. Lip id Res. , 9:155, 1968. 21) Bil h eim er, D. W. , Eis e nberg S. , Levy R. I. , Bi oc him . Bi op h ys . . Acta . , 260:212, 1972. 22) Levy , R. I. , Bil h e im er, D. W. , Eis e nberg S. , In Plasma Lip o - pro te i n s , ed. R. M. S. Smel! ie, pp, 3~17, New York: Academi c, 1971 . 23) Ghis e ll i, G. , Bi oc him . , Bi op h y s. Acta , 711:311, 1982.
24) Pit tm an, R. C. , At tie, A. D. , Carew, T. , Ste i n b erg, D. , Bi o c- him. Bi op l zy s. Acta , 710:7, 1982. 25) Brown, M. S. , Goldste i n , J. L. , ]. Bi ol . chem. , 249 : 7306, 1974. 26) Chen, H. W. , Kanduts c h, A. A. , Way m outh , C. , Natu r e, 251 : 419, 1974. :27 ) Brown, M. S. , Faust, J. R. , Goldste i n , J. L. , J. Clin . Inves t. , 55: 783, 1975. 28) Goldste i n , J. L. , Brown, M. S. , J. Bi ol . Chem. , 249: 5153. 1974. 29) Brown. M. S. , Goldste i n , J. L. , Proc. Natl . Acad. Sc i. USA, 71 : 788, 1974. 30) Goldste i n , J. L. , Basu, S. K. , Brunschede, G. Y. , Brown, M. S. , Cell. , 7:85, 1976. 31) Anderson, R. G. W. , Goldste i n , J. L. , Brown, M. S. , Proc. Natl . Acad. , Sci. USA. , 73 : 2434, 1976. 32) Goldste i n , J. L. , Brown, M. S. , Ann. Rev. Bi oc lzem. , 47: 908, 1977 . .3 3) Reic h l. D. , Sim ons, L. A. , My an t, N. B. , Pfl ug , J. J. , Mi lls, G. L. , Clin . Sci. Mo/. Med. , 45:313, 1973 . .3 4) Reic h l, D. , Posti gli o n e, A. , My an t, N. B. , Pfl ug , J. J. , Press, M. , Clin . Sci. Mo/. Med. , 49:419, 1975 .35 ) Brown, M. S. , Goldste i n , J. L. , Scie n ce, 191 : 150, 1976 . .3 6) Wi lliam s, C. D. , Avig a n J. , Bi oc hi m . Bi op h y s . Acta . , 260 : 41 3, 1972. 37) Hig gins , M. J. P. , Lecamwasam, D. S. , Galto n , D. J. , Lancet, 2:737, 1975. 38) Ho, Y. K. , Brown, M. S. , Bil he im er, D. W. , Goldste i n J. L. , ]. Cli n. Invest. , 58 : 1465, 1976 . .3 9) Ho, Y. K. , Faust, J. R. , Bil h eim er, D. W. , Brown, M. S. , Gol- dste i n , J. L. , J. Exp. Med. , In Press, 1977. 40) Goldste i n , J. L. , Brown, M. S. , Ann. Rev. Bi oc hem. , 46 : 897, 197 7. -41 ) Balasubramania m , S. , Goldste i n , J. L. , Faust, J. R. , Brown, M. S. , Proc. Natl . Acad. Sci. USA. , 73 : 2564, 197G •
42) Henderson, J. F. , ]. Lipid Res. , 4:68, 1963. 43) Shif f, T. S. , Roheim , P. S. , Eder, H. A. , ]. Lipid Res. , 12: 596~ 1971 . 44) Mj os , 0. D. , Faerge man, 0. , Hami lton , R. L. , Havel, R. J. , ]. Clin . Invest. , 56;603, I975. 45) Ande rs on, J. M. , Die t s c hy , J. M. , Sc ien ce, 193 : 903, 1976. 46) Egg e n, D. A. , Solberg, L. A. , Lab. Invest. , 18: 571, 1968. 47) Heis s , G. , Tami r, L. , Davis , C. E. , Ty ro ler, H. A. , Rif ki n d , B. M. , Schonfe l d, G. , Jac obs, D. , Frantz , I. D. , Cir cu lati on , 61:302, 1980, 48) Jen kin s , P. J. , Harpe r, R. W. , Neste l , P. J. , Br. Med. ]. , 2.— 388, 1978. 49) Wi ss ler, R. W. , Vesselin o vit ch , D. , Getz , G. S. , Prog Cardi- ovasc Di s. , 18 : 341, 1976. 50) Lee, Hon chi, Paz, M. A. , Gallop , P. M. , J. Bi o. Chem. ,. 757(No 15):8912, 1982. 51) Dock, W. , Ci rcu lati on , 50:647, 1974. 52) Walto n , K. W. , Am. ]. Cardio l . , 35 : 542, 1975. 53) Smi th, E. B. , Slate r , R. S. , Hunte r , J. A. , At he rosclerosis , 18: 479, 1973. 54) Hoff , H. F. , Heid e man, C. L. , Jac kson, R. L. , Bay ar ds, R. J. ,. Kim , H. S. , Got to, A. M. Jr. , Gir e. Res. , 37:72, 1975. 55) Ross, R. , Glomset, J. A. , N. Eng l. ]. Med. , 295 : 369, 1976. 56) Kesanie n i, Y. A. , Grundy , S. M. , J. Cli n. Invest. , 70: 13,. 1982, 57) Goldste i n J. L. , Morrise tt , J. D. , Got to, A. M. Jr. , Phys i o l .. Rev., 56:259, 1976.
제 7 장 영양소로서의 지방 서구인의 지방 섭취량은 1 일에 60~100g 정도 된다. 이는 전체 칼 로리 섭취향의 40~45% 에 해당하는 것이다. 아에 비해서 한국인의 치방 섭취량은 1 일에 약 20~60g 정도로 이는 총칼로리 섭취량의 7~20% 정도에 해당하는 것이다. 서구인의 식사에서나 한국인의 식사에서 지방급원의 90% 는 중성 치방이며 나머지 IO% 정도가 콜레스테롤 este r , 식물성 스데몰 그. 리고 인지질이다. 서구인이나 한국인의 식사내에 들어 있는 지방산의 대부분은 탄소 수가 14 개 이상되는 사슬이 간 것으로 포화지방산과 불포화지방산 으로 이루어져 있다. 사람이 먹 는 지 방 중에 서 주요지 방산은 oleic ac id 와 lino leic acid 로 이는 생산된 총식용지방의 19~34% 에 해당된다 .1) 중간사슬지방 산 (MCFA) (C 의 수 6~14 개 )은 대 개 pa lm oil , nutm eg , seed o i ls 과 같은 식물성 기름에서 발견되는 것으로 동물성 지방에서는 동물의 유지방 구성 중에 비교적 소량 함유되어 있다. 중간사슬지방산은 간사술지 방산 (LCFA) 과는 달리 수동적 확산(p ass i ve d iff us i on) 에 의 해 서 문맥 체 계 (po rt al s y s t em) 로 쉽 고 빠르게 흡수된다. 2) 지방이 식사의 주요 구성요소로서 생각되어지는 것은 지방이 고 열량물질이기도 하지만 지용성 비타민과 팔수지방산이 우리가 섭 취하는 지방내에 함유되어 있기 때문이다. 신체내에서 지방은 효율
성이 높은 에너지 궁원으로 사용되는데 이때 에너지 급원으로 직잡 사용되 기 도 하지 만 처 장지 방조직 (adip o se ti ssue) 에 저 장되 었 다가 사 용되는 간접 사용의 길도 있다. 지방은 또한 체내의 피하지방충 ( s ubcu t aneous ti ssue) 이나 일정 장기 룬 둘러싸고 있는 지방충을 통해서 온도 절연체로써 작용하며 또한 m ye lin a te d nerve 를 따라서 비 국성 화 (de p olar i za ti on) 과장이 빨 리 퍼 쳐나갈 수 있도록 전기적 절연체의 역할도 한다. 신경조 직 내의 지 방함량은 특히 높다. 지 방과 단백 질 의 걷 합체 인 lip o p r ote i n 은 세 포 구성성분으로 중요한 물질이며 이 물질은 세 포막 과 세포 원형진 내의 m it ochondr i a 내에 포함되어 있다. 또한 혈엑내에도 이 물질 이 함유되어 있으며, 이는 체내에서 지방의 이동수단으로 사용되어지 고 있다. 이상과 같이 지방의 신체내의 기능은 다른 영양소와 함께 매우중요하다. 그러나 요즈음 식사를 통한 지방의 섭취량과 종류 죽 동물성 지 방과 식물성 지방의 식이내 함유 비율에 따라서 동맥경화의 유발반 도에 크게 영향을 미치고 있다고 발표되고 있다. 특히 혈청내의 콜 레스테롤 양이 관상십장질환 (coronar y heart d i sease) 을 일으키는 위 험요소라는 사실은 이미 널리 알려져 있고 많은 학자들도 그 렇게 믿 고 있다 .3) 관상십 장질환 (coronar y hea rt d i sease) 을 유발시 키 는 데 관련된 여 러 가지 위험요인들은 다양하지만 그중에서 비교적 수긍이 가는 보다 정확한 지침이 되는 요인은 사람의 혈청내 콜레스테롤 함량이다.그 러므로 혈청콜레스테롤의 함량을 하나의 지표(i nd i ca t or) 로서 사용한 다. 물론 여기서 뜻하는 위험요인들이란 주로 통계적인 뜻으로 간 주된 것이지 의학적인 전단에 의해서 되어진 것은 아니다. 과거의 연구도 그러한 경향을 떠고 현재의 연구경향도 별로 크게 달라전 것이 없는데 그 내용을 간추려 보면, 결국 동맥경화증 (a t her oscleros i s) 의 발병과 혈청콜레스테몰 수준을 동일시해 보려는 노력 또 ` 는 식이지방 섭취량과 혈청콜레스데를의 수준을 동일시해 보려는 노력이었다. 만일에 우리가 미국인의 식사내용과 한국인의 석사내용의 변화경.
향을 간추려 보면 좀 홍미로운 면울 찾 아 볼 수 있다• 한국인의 것 보다도 미국인의 것에서 석사내용이 변화된 경향이 뚜렷한 것을 볼 수 있으며, 현재 한국의 일부 계충에서 그와같은 변화 를 하고 있음 울 엿분 수 있다. 다 음 표 에서 보여주듯이 미국인의 1909 년에서 1972 년에 이르기까
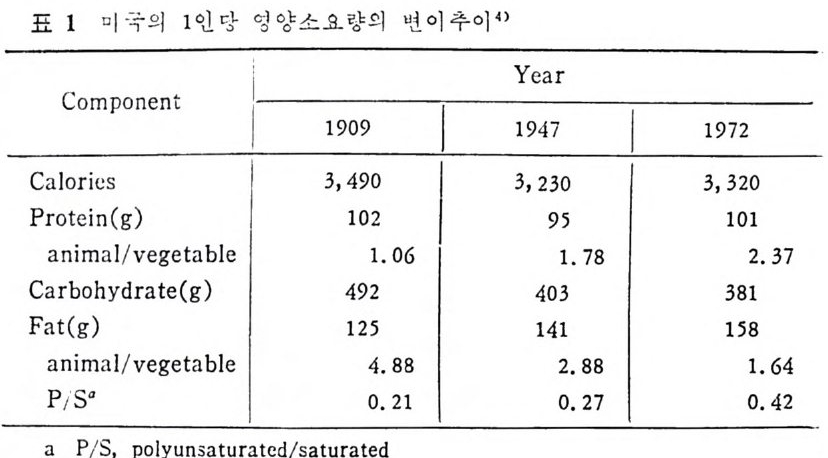 표 1 미국의 1 인당 영양소요량의 년아추이 4 )
표 1 미국의 1 인당 영양소요량의 년아추이 4 )
지 영양 소요량의 변화추이를 간추려 보면 섭취할 수 있는 칼로리의 양에는 변화가 없었다. 그러나 동물성 단백질과 식물성단백질의 섭 취비율은 배로 증가되었으며 섭취할 수 있었던 탄수화물의 양은 一 21% 가 감소되었고 섭취가능한 지방의 총량은 26% 가 증가되었다. 그러나 동물성지방과 식물성지방의 비율은 4.9% 에서 I.6% 로 오 히려 감소를 보였다. 콜레스테롤 섭취가능량을 보면 1909~1913 년 사이에서는 1 인당 509m g아었던 것이 1957~1959 년 사이에서는 578 m g으로 증가되었다. 한편 1900~1960 년대 사이 에 십 장병 으로 사망한 사람수를 보면 1,30/1000 명 ~3.55/1000 명으로 약 3 배의 증가를 보이고 있다 5-7) 위 에 인용된 조사자료와 유사한 것 으로 Kahn, 9> He g s t ed10) 와 Ke y 11) 에 의해서 제안된 공식에 의해서 미국인의 콜레스테롤 수준 울 예견해서 계산해 본 결과, 전체국민 혈청콜레스테롤양의 수준이 평 군 4mg /d l 정 도 증가하였 다.
1957 년에 Yerushahny 와 Hil leb ee 는 1 2) 지 방과 십 장병 사이 의 가설 올 설정 하기 위 해 서 WHO, Annual Ep ide mi ol og ica l & Vi tal s t a ti s t 一 ic s 의 1951~1953 년의 자료를 정리해 보았다. 그리고 걷본을 내리 기를 지방과 십장병의 관계는 표 24) 에서 보여주는 바와 같이 원인 과 결과의 관계가 되기에는 충분하지 못하다는 결론을 내렸다.
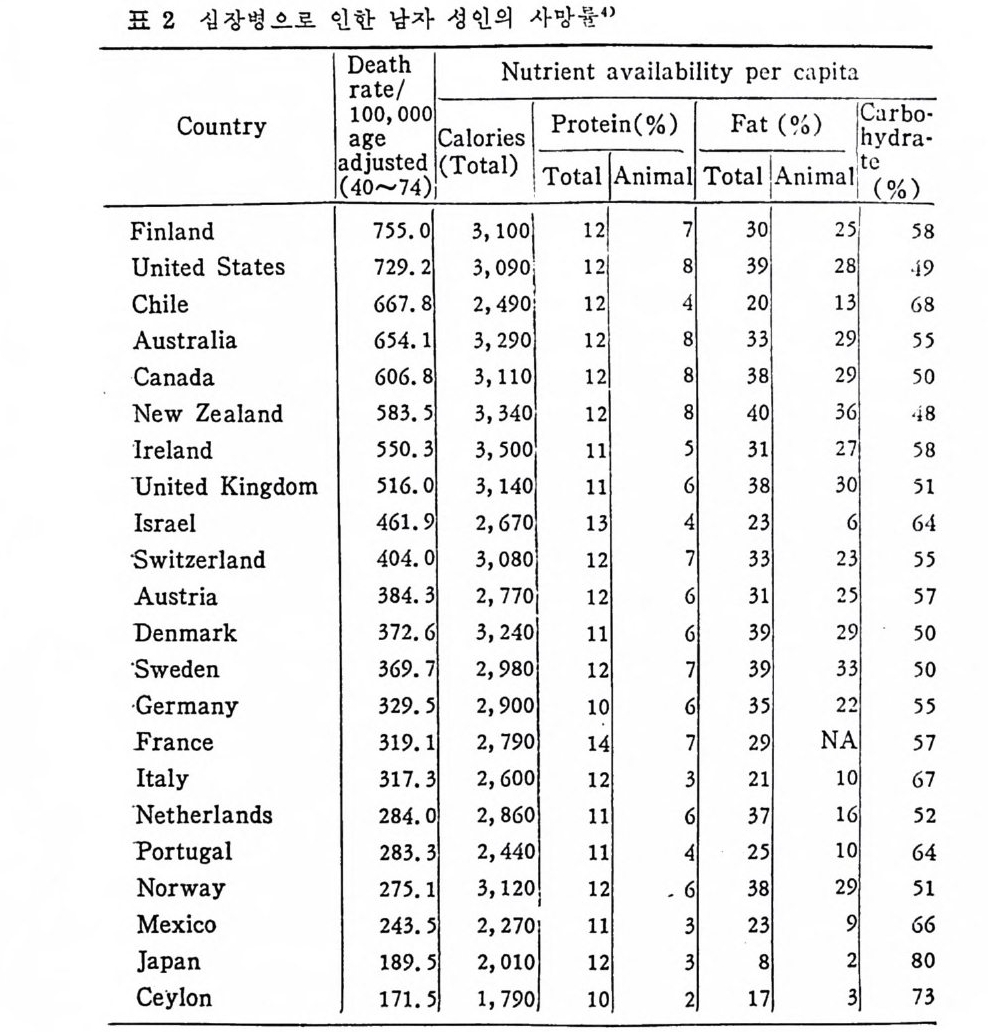 표 2 심장병으로 인한 남자 성인의 사망윤 4)
표 2 심장병으로 인한 남자 성인의 사망윤 4)
Mas i rom4) 은 1970 년의 십장병으로 인한 사망율을 1955~1965 년 서이의 실대와 비교하였다. 역시 위에서 지적한 건과와 같이 섭취 하는 영양소와는 어떤 뚜렷한 관계가 나타나지 않았음을 보여주고 있다. 유고슬라비아에서는 십장병으로 인한 사망률이 355% 나 대폭 증 가하였는데도 포화지방의 섭취량은 26% 나 갑소되었고 오히려 설탕 의 섭취량은 3 배로 중가하였다고 한다. 한편 미국이나 스위스에서 는 십장병으로 사망하는 울이 4~6% 가 증가했는데 미국은 오히려 7% 의 포화지방산 섭취량이 감소되었으며, 스위스는 28% 나 증가하 였다. 그러므로 이러한 모든 조사자료를 종합해 보면 십장병의 발병이 나 사망률에 영향을 미치는 식사내용의 구성성분은 어떤 한 가지 의 구성성분이 아니라 복합된 여러가지 성분이라고 생각할 수밖에 없다 • 그러나 동맥경화증의 발병에 가장 밀접한 관계가 있다고 밝혀진 것은 신체내 대사물질 중 지방이며 이중에서 특히 콜레스테롤과 관 련이 있다고 할 수 있다. 물론 식사에서 섭취하는 콜레스테몰로 인 해 체내 콜레스데몰 p ool 에 양적인 증가가 생기지만, 또 한편 상당 량의 콜레스데문이 체내의 장기내에서 합성된다. 콜레스테롤이 합 성되는 장기는 주로 간과 소장벽이다. 식사로부터 콜레스테를의 섭 추 1 량이 중가되면 신체내의 장기로부터의 콜레스테를의 합성량이 감 소되며 이와 반대현상도 사실로서 알려져 있다. 콜레스테롤이 신체내에서 합성될 때 선행물질로 사용되는 것은 calorig e nic substa n ce 라고 밝혀 졌 다. 13) 여 하튼 동백 경 화증 (a t herosc· Ieros i s) 은 과량의 콜레스테롤의 축적으로 일어나며 득히 혈청내 콜레 스데 문의 농도가 크게 주목을 받아 오고 있 다. 또한 포화지 방산의 섭 취가 콜레스데돌의 혈청내 농도를 증가시킨다는 현상은 이미 찰 알 려진 사실이지만 최근에 와서는 불포화지방산의 섭취 역시 혈청내 콜레스테를의 농도와 관련이 있는 것으로 생각되어 이 접에 많은 관 십울 모으고 있음도 사실이다. 혈청콜레스데롤의 양을 감소시키려면 식사로부터 콜레스데롤의
섭취량을 감소시키는 것도 한 가지 방법으로 생각하고 있지만 섭취 하는 총지방량도 크게 문제가 되고 있다. 高 H) 정 둥 15) 의 동물 실험결과에 의하면 흰 쥐의 겅우 지방의 종 류, 죽 동물성지방인 우지와 식물성지방인 면실유를 각각 사료의 지 방으로 하고 식이내에 함유된 지방의 양을 총칼로리 섭취향의 45% 에서 3% 까지 2% 간격으로 구분하여서 사육한 결과, 혈청의 콜레 스테롤의 양은 지방의 종류보다도 섭취지방의 총량과 오히려 관련 이 더 큰 결과를 보여주었다. 죽 식이내 지방의 종류가 동물성이전 석물성이전 관계없이 지방 섭취량이 9% 이하이면 혈청콜레스테롤의 양과 할 청 총지방의 양은 낮았으며 총 식이내 지방함량이 9% 이상 45% 이하이면 그중 어느 수준을 섭취하든지 혈청내 총지방량과 콜레스테롤의 양은 크게 차이 를 보이지 않고 높았던 결과를 보였다. 이상의 결과에서 보여준 것은 혈청콜레스테롤의 양은 섭취하는 지방의 총량이 높으면 따라서 혈청콜레스데롤의 양도 증가하는 경 향이라고 말할 수 있다. 우리나라의 식이섭취실대에 나타난 결과는 지방의 총섭취량이 증 가하고 있는 것 을 보여 준다. 16) 특히 우리나라는 지역별로 볼 때 도시와 기타 지역에서 지방섭취 량에 크게 차이가 나타나고 있지만 그러나 지방 총섭취량은 서구의 섭취량에 비교하면 낮은 양이다. 그러나 도시의 일부 계층에서는 생활수준이 접접 윤택해침에 따 라서 지방의 섭취량이 중가되고 있으며 한편 동물성식품의 섭취량 도 증가되고 있다. 이에 따라서 고혈압으로 인해 생겨나는 스트레 스를 받는 계충의 인구가 접접 증가해 가는 경향으로 생각해 볼 수 있다(표 3 참조). 영양소로서의 지방은 신체내에서 여러가지 기능아 있지만 반면에 지방의 과잉섭취로 인해 금세기의 많은 사람들이 고민하고 있고 뚜 렷한 해결책이 없는 성인병의 한 요인이 되고 있다는 접에서 주목 을 받고 있음에 틀림이 없다.
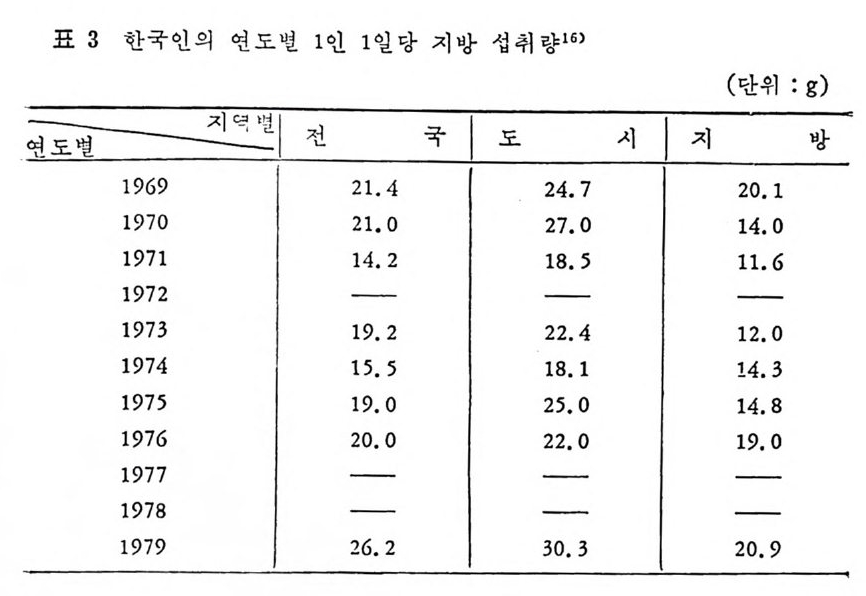 표 3 한 국 인의 연도벌 1 인 1 일 당 지방 섭취량 16)
표 3 한 국 인의 연도벌 1 인 1 일 당 지방 섭취량 16)
* 참고문헌 I) Braveorman, J. B. S. , Lip ids , An Intr o ducti on to the bio c hemi s- try of foo ds, New York, Elsevie r pu bli sh in g Co. pp. 234~51, 1963. 2) Carlie r , M. , J. Bazard. , J. Cell Bi ol . 65:383, 1975. 3) Kannel, W. B. , T. B. Dawber, A. Kag a n, N. Revots k ie , J. Sto k es. , Ann. Inte r n. Med. 55:33, 1961. 4) Masir o m. R. , Di et a ry fac to rs & Coronary heart dis e ase, Bull. WHO. 42:103, 1970. 5) Frie u d, B. , Am. J. Cl in. Nutr . 20:907. 1967. 6) Gortn e r, W. A. , Cancer Res. 35:324 6, 1975. 7) Pag e, L. , B. Frie u d. , aLevels of use of sug ar s in the U. S. ,, In Sug a rs in Nutr i t ion, ed. by , H. L. Sip ple , K. W. McNutt , pp. 93~107. Academi c Press, New York, 1974. ~) Riz e k, R. L. , B. Frie u d. , L. Pag e. , J. Am. Oi l. Clzem. Soc. 51 : 244, 1974.
9) Kohn, H. A. , Am. ]. Clin . Nutr . 23 :879, 1970. 10) Hegs t e d . , Am. ]. Clin , Nutr . 17:2s1. 11) Key, A. , Meta b oli sm , 14:776. 12) Yerushahny , J. , H. E. Hi lleb ee, ]. Med, 57 : 2343, 1957. 13) Marti n, D. W. , P. A. May es , V. W. Rodwell, Harpe r 's Revic 1 c. of Bi oc hemi st r y , 18th Edit ion , p. 239, 1981 . 14) 고성숙 「식이내 합유된 지방의 수준이 흰 취의 체중 층 가에 미치는 영향」 이화여자대학교 식품영양학과 석사논문, 1980. 15) 정덕순 (I ), 이동희 (Il): 「식이내 함유된 동 • 식물성 지방 의 수 준이 흰취의 체내대사에 미치는 영향」 이 화 여자대학교 식 품 영양 학 과 석사논문, 1980. 16) 보건사회부 「국민영 양조사보고」 1969~1979.
한쿨색인
-l 간 68, 137, 14 1, 259, 339 간의 구조 IO5 찬색지방세포 52-3 갑상선 호르몬 228 걷정 구조 crys ta l lin e ,s 전합 평형 상대 27I 겅동맥 376 고단백 I21 280 고당식 사 .25 5, 257 고 중성 지 방영증 244, 248, 255, 257, 267 고지단백 현중 337-9 고지 방식 12, 280, 302 고지 방형 중 244, 267, 367 고콜레 스데 몰혈증 197, 244, 296, 387-8 고탄수화물식이 I68 고혈압 377, 398 관상동백 경 화증 255, 374 관상동맥 심장병 375 관상십장질환 394 국성 po lar 17, 253 국—성—지방pkhi n oa s2sp 8eh 0 a t8e 8 88 굴리 세 룬 31, 35, 56, 64, 88, 130 굴리신 I9 굴리코겐 I66 급사 375 급성 십근경색층 375 기 능적 ap op r o te i n 266
기 질 71, 79 L- 내막세포 68 내자콜레스데몰 203 내적지방 S6 뇌수 376 뇌저 376 뇌졸증 376 뇌혈관명 376 E: 다당류 사슬 70 단백질 143,277 단백질 함량 246-7 단백질 합성물 257 단세포 374 담관장애 250 담줍 153 담즙 lec ithi n 30 그 담줍산 12, 18, 108, 19S, 220 1 차담즙산 18 2 차담줍산 19 담줍산 CoA 19 당뇨병 157, 162, 173, 175, 216 대등맥겅화증 377 돌연변이 374, 384 동맥겅화성 십장질환 374 동맥 겅 화증 12, 197, 367, 377, 379, 386 ,~ 387, 394, 397
동백 벽 369 등위 원소 203, 256 동적인 관계 27I 둥각상태 x68 E: 리놀레인산 I5 림프장내순환 I47 림 프지방 I47 口 마에리스탄산 35 말초혈관 경화증 377 면역 적 정 im munoti tra ti on 325 면 역 학적 분석 방법 248, 254, 258 면역화학적 방법 387 문맥 정 맥 204, 293 문맥체계 393 문백혈 3I,202 t:I 반감기 256,273 반대 이 온 counte r ion 21 핀스테로이드 202 변화하는 요소 element varia b le II 부.,.(J. 25 부착부위 bin d in g sit e 27 분해 효용도 par t ition coeff icien t X7 불용성 16-7, 283 불포화지 방산 35, 286, 397
불활성 조칙 II, l3 붕괴속도 256-7 바 극성 non po lar 16-71 277, 283 비 극성화 394 비만중 130 人 사구체영 환자 256 사슬의 길이 2I 사슬이 긴 지 방산 CoA lipa se 33 사영화탄소 II9, X54 산도p H 19 산독증 135 상동액 sup e rnata n t 36 생 검 bio p s y 42 섬유질 I2 소수성 21,336 소장 256,259 소장내 부벽 int r a lumi na l 16 소장의 기 부 pro xim al po rti on 31 속도제 한단계 rate -lim i ting ste p _ 38 수동져 확산 pa ssiv e dif fus io n 393 수분충 unsti rr ed wate r lay e r 15, 2<; 수용성 수용액 I2 식물성 스테롤 205 식이성 지방혈충 64,231 식이지방 16 신장질환 339 신장혈관의 폐쇄 377
십근경색증 375 심장마미 375 십장성 질환 12 o 안정 된 요소 clement consta n t 11 안부민 했 알코—홉- 1 30, 137 알코운성지 망간염간 113377 , 275 알코운중독 138, 339 액 체 모자이 크 모델 282 양성물질 I2, I7 양성이온 280 양성인지방 336 양이온 63,68 에너지원 II 에 스텔화 32, 37, 56, 58, 199 에스덴화된 콜레스데룬 12,39 에 만운 II9, l3I, I36, I43, X46 에티오닌 I54 영의 형성작용 62 운데인산 I5 용해도 2I 용해성 단백질 259 용해성 효소 7I 운반체 carrie r 16, 31 유동화 fluid i t y 286 유리 지 방산 27, 56, 64, 81, 86-7, 95, 108, 114, 118, 127, 130, 138, 163,
246 유리 지 방산의 재 este r if ica ti on 89 유리 콜레 스테 롤 12, 39, 198, 255, 280, 380 유화제 19, 22 웅털 둔기 31 음이온 요 ,68 이 온걷합력 69 인슈란 82, 89-91, 97-8, us, 122, 130, 163,216,3 자 인지 방 12, 28, 39-40, 87, 158, 161, 200, 246-50, 266, 277, 280 츠 장간순환 202 장내 막 세포 35, 42, 198 장막간 순환 I47 장애성 간질환 313 저성유 식사 I2 저장지방조칙 394 전기적 상호작용 7I 全血 I16, 260 철연체 II 정전기적 결합 68 정전기적 상호작용 70 것산 208 조효소 Co lipa se 23 준기아식 I57 중간사술 지방산 393 중성 자 확산장치 277-8
중성 지 방 12-3, 15, 35, 40, 42, 56, 58, 64, 71-5, 86-7, 95, 108, 114 군 30, ———158hl이i,yp1 동d a6 rs1의 oe,l 2 a활4피s6e성-동 7화 적829 인6 기6 -전7조, 철25 9730 2 3-4 중성 지 방 lipa se 56, 292 __- 유액 72 중추신경계동 혈저해성 충격 376 지단백막 54 지단백질 13,33 지방 II 지 방간 87, 130, 137, 140, 143 지 방과 십 장병 396-7 지—방——―단C활a백oc성Ay 질 l 도 l iCp 복oa As합6e0 체 2 122922 71 지 방분해 촉진 호르몬 88-90 지 방산 56, 148, 322 _ 결합 단백질 31,33 지 방산의 de novo 합성 84, 129-30 지방산의 활성화 33, 38 지방산 활성효소 229 지방섭취량 I5 지방세포 54,72 지방조직 51-5 지방합성작용 117 云:
초원십 분리 249, 254 추골 376 췌장 지방분해효소 23 찬수성 I7,2I 찬수용엑 30 = 케 돈체 S;, 107-S, II.J, 130, 159, 163, —166,이 1 용74 156-7 -— 합합성 성 조1철55 -61 57 램 프너 의 쌀 식 이 Kemp n er's Ric e Diet 12 콜레————— 스테7eaees-scs at롤tty eee - lr hr r a yCss21 deyo72 r An,,o 8t 2 x 2h727yea ,, lct1aa4 y0s1s 8lee,t, r 1 22a0 2nu2892,s,, 9f 22e1 325r 210a,,,s e221425 684 ,, 197, 247, 249, 255, 277, 386, 394 I99 277-80,300,367,380 콜레스데풀과 동백경화증 397 드: 타우란 19,31 통증 376-7 봉풍 135 독정 결합부위 recep tor sit e 383
끄 팔미탄산 35 펩 타이드 I6 팹 타이 드 지 도 pe p tide map 332 평형상태 271 례동맥 깅 화중 379 포도당 82,3 22 포화지 방산 35, 197, 286, 397 피하지방 55 피하지방충 394 팔수지 방산 I2, I20, I 7 항지방 분해작용 89
해리상수 63 ; 혈장 lipo pr o te i n 244 혈 저해증 375-6 호르몬 recep tor sit e 95 확산 I5, 3I 환원등가 I45, I50 활성 단백 질 kin a se 57 활성효소 I9 회장 207 효소의 작용역 학 enzy m e acti on kin e ti cs 25 효소활성 계 단백 질 268 흰색지방제포 52,55
영문색인
Abeta l i po p ro te i n e mi a 42, 245, 258-9, 268, 293 aceta l dehy d e 136, 145, 152 ace—ta t e Co1A36 , 1t4h5i ,o 1l a4s8e- 502, 029 1 9 aceto a ceta t e 155, 159, 175 aceto a cety l CoA 206 aceto a cy l CoA th io l ase 157 aceto x y c y c lohexami de 291 acety l CoA 83, 109, 117, 129 , 158, 160, 162, 206 -carboxy la se 169 ac ido sis 135 ACTH S9 acti no my cin D 214, 291 acti va to r 41 acti ve lip a se a 91 acute my o ca rd ia l inf a r cti on 375 acy la ti on 35 ac———y l CosmsAyyo n nn c tto hhh ge oe lttly eaa css s eteee rri IoIdl le aa11c2c2y22y l l t r a nsfe r - tra nsfe r ase(ACAT) 229 -dehy d rog e nase 151 ase 289 一 thi o e ste r 229 acy lg l y c erol 35, u3 acy lt h io e ste r 122, 124 acy lt r an sfe r ase ur, 149 adeny la te c y c lase acti vi t y 57 adeny lc y la se 90-1, 95 adip o se tiss ue 394
adip o sit e 72 adrenal hormone 217 adrenalecto m y 217 adrenali n 91 adventi tia 369 albumi n 58, 250 alcohol dehy d rog en ase (A DH) 131, 134, 143, 150 alcoholic keto a cid o s is 157, 175 alde h y d e dehy d rog e n a se 137 alim enta r y lip e mi a 6-t , 231, 268 , 3°2 alloxan dia b eti c me ll it us 161 4-ami no p yra zole-py r im i di n e 386 -1- ami no p yra zole-[3 , 4 -d 坪y r i m i d i;i e 326 amp h ote r ic 13, 283 amp u lla of bil e duct 105 ang ina pe cto r is 374-5 an io n 62 anti di u r ecti c hormone(ADH) 135 anti ge nic 316 anti lipo lyt ic acti vi t y 89 anurys m 377 ap— ol ar 28 4 ————a—p :> lip ABAAAA'.l -p ---W r ]Io2I [I 2 0 t 48e 6i, 4242n-2 78I14 4 6,,7 46 ,22 1-542,8 3752,1 ,04 ,2226 5525, 05502,2,- 5 ,521 22,8, 5252248,88 ,72 192,, 663 57,9 291, 297, 305 269, 280
———· CC -I2 464 -18, , 752, 6263-19, , 26267, 3310 52, 7371,7 282, 287, 293, 295-6, 301 -———DCCF -- NIl22 777 6 44, 11 2 ,8 773, ,3 7055 -6, 78, 266-8, 285, 2S7 - c-血 41, 75, 266-7, 284, 287 - E 255, 263, 274 -5, 287, 297 ap pa rent acti va to r 76 aarragci. nh.i i n d e o na2t5e 2 , 237840 argi ni n e -ric h pro te i n 246, 248 , 250 aspa r t i c ac id 251 associa t i on consta n t 271 ath eroma 367 ath e rosclerosis 394, 397 ath e roscleroti c heart dis e ase 374-5 ATP 83, 229 auto ! i po lyt ic acti on 91 Beta lipo pr o te i n ( /3-lipo p ro te i n ) 42,379 fl-——o xid a datciu ocind t 111350,15 , 1 91585 bil a y e r 278 bil e 106 bil iar y obstr uc ti on 250 bil iru bin 138 bin d in g sit e 27 brain ste m 376
brush border 16 Burr & Burr 12 Ca————nalic uaapa lcccai y y!y m lll ttt 1irrr t0 a a a o 5nnny sss !fffteeer arrr naaasssseeefe rII al 1 seu1 1,66 7u7u, 5 16,7 0, carboxy lic este r hy d rolase 23, 27 carnit ine 155, 165, 170 158,162-5 l75 caroti d arte r ia 376 cata l ase 132, 134 cate c holami ne 89, 138, 148 cerebrovascular dis e ase 376 charge d anio n ic po lar gro up 22 chenodeoxy cholic ac id 18, 153, 221 크, 228 ch—oleste 7r o-ag e hn ye dsi rso xy2 0la9 s e 154 choleste r ol este r hy d rolase 89 一 este r 150 cholesty ra mi ne 205, 226, 264 cholic ac id 18, 153, 221-2, 228 ch———oli ne ppohxh1o oi4d ss2 pap ,sh h 1e oa 5 tt4re 1a c4n 2ys. ftie dr ya !ster a n1s2f6e r ase -kin a se 125 125 chy lo mi cr on 丸 31, 58, 64, 71, 78> 83, 198, 244, 246, 254, 277, 289>
299, 320 desmoste r ol 207 cciiat—rm a tee t h csy ly le n a atvhl laa ygs l e et r eann1 6zs0yf e mr ae se 842 10 dia—- b e ti cal i cpkyea tls toe ra ac n i5sd6fo e sri as s e 162x 24 cirr ohosis 137 dia c y lg l y c e rol(DG) 17, 36, 64 clearin g fac to r 58 dic a rboxy lica c id shutt le sys te m 85 coli pa se 23, 26 dih y d roxy a ceto n e ph osph ate 35, 85, collag en 135, 367, 369 149 collag en ase 80, 333 3, 7-dih y d roxy c holanic ac id 18 collage n pro li ne hy d roxy la se 135 3, 12-dih y d roxy c holanic aci d 19 com——monaa trhht eee pr ryo a st ic3 cl7 e4 dr ouscits 13o754 dd3ii,s u 3sr o-ndcaiilam t rei hotnhy y tch l om na sltlany n !3 t , 2p61y30r ,o 2p2 h6 o sp h ate cop ro ste r ol 202 iso mer 206 coronary heart dis e ase 374, 394 dim y r is t o y l ph osph ati dy lc holi ne 30; criti ca l mi ce llar concentr at i on dy n ami c reacti on 271 (CMC) 18, 21, 26 type ]ll dy s lip o pr o te i n e mi a 245 cryp tic cell 31 ccyy cc lloich exAaMmPi d(e c ABMxP, 8)3 , 25175, , 29901, 130, El—asti n v a3r6i7a, b 3 l6e9 II 169, 216, 218 electr os ta t i c int e r acti on 70-1 cy a nog en bromi de (CNBr) 328 element consta n t xx cy s ti c duct 105 emulsio n 58 cy tos ol 36 EM pat h w ay 85 endocy tos is 199, 298, 334-5 Dehy d rati on 21 endoth e li al cell 68-9, 72, So, 3691 (+) decanoy l carnit ine n1, n6, 372, 387 161 ente r ohep a ti c circ ulati on 202 fi-d eli pida ti on .26 3 epi di d y m al fat pa d 56, So de novo syn th e sis 84, 109 ep ine p h rin e 89 deoxy c holi c acid 19 ep ithe li od cell 55 dep o lariz a ti on 394 este r if ied choleste r ol 13 .19 desatu rat a s e 113 estr o g e n us, 130, 249, 255, 294
eth—— io n i nppe hh oossIppI hh9 oa tter a cnys tfied r ya lster a n1s2f6e r ase et h anolami ne kin a se 125 126 cxocy tos is 292 Fami lial hy pe rcholeste r olemi a horn· ozy go te ( FH) 263-5 far nesy l pyro p h osp h ate 206 fas ti ng chy lo mi cr onemi a 297 fa—t mobbil iin z: i: n I ing g p iptruo i tt ea ir n y p3e 1p tide s 89 fatty ac id acti va ti ng enzy m e 229 -CoA lipa se 289 一 sy n th e ta s e u3 fatty acy l CoA 83, 155 fatty live r 87 fee d back 91, 157, 386 fee d back inh ib i t ion 174 fibr in 367 fibr oblast 54, 265, 381 fibr oti c connecti ve tiss ue 137 frac ti on al cata b oli c rate ( FCR) 257 frac ti on ati on 247 fruc to s e 258 fun cti on al ap o p r ote i n 266 Galacto s e 258, 380 ga llbladder 105 ga llsto n e 202 ga str i c emp tying rate 291 ge l electr o fo c ussin g 249
ge rany l pyro p h osp h ate 20S glu cag o n 89, 98, IIB, 130, 163, 165, 169, 176, 216 gI ucocorti co id s IIS gIu co:i eo g e nesis 175 glu cosami ne 258, 276, 380 glu cosami no g ly c an 函 glu cose 166, 169, 258 glu ta m ate dehy d rog e nase 151 glu ta m i ne 250-2 gly c erol-este r hy d rolase 23 gly c eroli pid 120, 123, 130 gly c erol ph osp h ate 35, 38, 135, 149 gly c erol-3-ph osp h ate 158, 161 Sn-gl y c erol-3-ph osp h ate 35, 109, u6 L-a-gl y c erol ph osp h ate 83-4, 97 gly c erop h osp h oli pid 23 gly c in 19 gly c in -ric h pro te i n 246 gly c ocheno:i eo xy c holi c acid 19 gly c o choli c ac id 19 gly c oli pid 17, 107 gglly y cc oolsyps h i is n g o1 2li.8 p .id 380 HDL 73, 200, 231, 234, 244-7, 277, 296-9, 314, 380 HDL2 249-50, 253, 280, 284, 321 HDL meta b oli sm 336-9 HDL sy n t he sis 296-8 Heart att ac k 375 hep a ran sulfa te 69-70, 72 hep a rin 58, 60-62, 66, 69, Sr, 260, 316
hep a rin eff ec ts on LPL acti vi t y 330-1 hep a ti c lipa se 320, 331-4 hep a ti tis 137 hep a to c y te 68, 105, 26x: hep a to m eg a ly 143 hexosami ne 62 his t a m i ne So hormone recep tor 57 _ sensit ive lip a se(HSL) 88- 91, 97-8, us spe cif ic pro te i n 94 hy d rocorti so ne 216 hy d roxy a cy l CoA dehy dr og en ase 15x: D-3-hy d roxy b uty ra te dehy d rog en - ase 156 3-hy d roxy b uty ri c acid 155, 175 hy —d— roxyrl leya dat usi oecn t a s1 e518 6 199, 3S4-5 hy d roxy m eth y l gl u ta r yl CoA 155, 206 一 syn th ase 156, 209 hy pe rcholeste r olemi a 197, 244, 387 hy pe rgl y c emi a 163 hy pe rketo n uria 162 hy pe rlacta c i de mi a 135 hy pe rlip e mi a 154 hy pe rlip ide mi a 244 hy pe rlip o pr o te i n e mi a 263-741 338-9,372 hy pe rt en sio n 377
hyp e ruric e mi a 135 hy po beta l ip o pr ote i n e mi a 295 hy po lip e mi a 154 IDL 68, 260, 29;, 318, 335 IDL B 퍄 IDL1-B 296 IDL2-B 296 ile um 207 im munoassay 254, 258 im munochemi ca l tec hniq u e 387 im munoreacti ve ap o p ro te i n B 43 ina cti ve lipa se b 91 int i m a 367, 387 int r i n s ic pla sma thr ombop la sti n 63 iod id e po ol 262 ion ic str en g th 70 isc hemi a 375 iso p e nte n y l pyr op h osph ate 206 iso p e nte n y l pyro p h osph -ate iso mera• se 210 iso zy m e 218 Kemp n er's ric e die t 12 keto a cid o sis 157 keto n emi a 152 keto nuria 152 keto s is 135, 157, 164, 175 Km value 37 Krebs cy c le 145, 156-8, 160 Lacta t e 135 lanoste r ol 207
late r al dif fus io n Bo LCAT de fi ci e n cy 245, 250, 255, 275, 308, 314 lec ithi n 229, 27 1 lec i t hi n - choleste r ol acy ltra nsfe r ase (LCAT) 200, 277, 285, 304-14, 381 LDL B 260-4 LDL for mati on 335 LDL recep tor 38 4 , 388 lino leate 141, 380 lino lei c aci d 248-9 lip a se 16, 54, 220 lipi: I este r 87 lip o blast 55 lipo g e nesis 117 lip o lyt ic ag e nt 91 lip o ly tic ap o enzy m e 64 lip————— —o lyt icaXxXCX ( 13 2hL oP72 r22286m 888 7 a-777o7 ) n e 25808 lip o pr o te i n 14, 64, 71, 95, 154, 199, 243, 288- 9 , 298-304, 394 - C-I[ 76 一 lipa se (LPL) 64, 66, 7_1 , 74, 79, 97, 260, 314-34 lipo tr o p ic fac to r 141 lit—ho choClio cA a cli ipda se1 9 33 long chain fatty ac id 17, 22
loose connecti ve tiss ue 51 low densit y lip o pr o te i n ( LDL) 64, 199, 234, 244, 248, 266-7, 278-80, 295-304, 380 lym p h ocy te 386 lys o p ho sph a ti de s 33 lys op h osph ati dy l choli ne 266 !yso somal degr a dati on 334 lumber 377 Malate 160 malate tra nshy d rog e nati on cy c le 84 malony l CoA 155, 166, 176 mannose 258, 380 mast cell 65 meal fee din g 216 media 367, 387 melanocy te 89 messenchy m al cell 55 messente ric lym p h flow 147 messente r ie s 52 mevalonate 206 mi ce llar 16_- 7 , 290 mi ce lle 21, 30, 20_2 , ~53, mi cr osomal eth anol oxid i z i n g sys . tem I3I, I34 mi cr osomal sys t e m 18 mi cr ovil lus 33 fl-m obil ity 274 pr—e -/3 mhoyb d ir lo itlays e 27652 , 89, 320, 333 monoacy l gly c erol 17, 38, 64, 220 - lipa se 56
monoclonal pla q ue 374 rnonog ly c e rid e 22 2-monog ly c erid e 246 .;-monohy d rexy ch olanic ac id 19 monomer 16 mosaic model 282 multi -c omp a rtm enta l ap pr oach 퍄 muta t i on 374, 384 my o cardia l inf a r cti on 375 my o cardiu m 31 NAD I3I, I35, I45 NADH 135, 137, 145 NA—DP H8D4L 230 NADPH 145 nascent chy lo mi cr on 39 nega t i ve fee dback contr ol 207 neomy cin 205 neurami ni d a se 284 nic o ti ni c acid 255, 257, 264 p-n it rop h eny l ph osp h ate 123 non-io n ic dete r ge n t 21 non-po lar 17, 277 non spe c if ic este r ase 16 norep ine ph rin e 89 Obstr uc ti ve liv e r dis e ase 245 oleate 161 oleic ac id 235 oli go mer 16 omentu m 52, 56 orosomucoid 331
oroti c ac id 119, 1H, 293 oxaloaceta t e 159 3-oxoacid CoA tra ns fe r a se 156 oxta n oic acid 162 Palmi tat e 293, 380 pa lmi tol ate 380 pa—l mi toly i pl aC seo A 233 S pa ncreati c duct 105 par ametr i a l fat pad 56 pe lvic 377 ph enobabeta l 150 pho sp ha ta s e 111 ph osp h ati da te ph osp h ohy d rolase 36 ph osp h ati di c acid 35, 123 ——-p ho sp h ata se(PAP) 123 ph osp h ati dy l cholin e 41, 108, 123, 125, 149, 229, 232, 247-9, 266, 285 —301,30N4- ,m38e0t h y ltra nsfe r ase 127 ph osph ati dy l eth a nolami ne 125, 149 ph osp h ati dy l ino sit ol 249 ph osph ati dy l serin e 249 ph osp h odie s te r ase 91 ph——— osph o BAAf2r 1 uc2 92t2o2 83 k ,,26in9 2a2 s e 169 ph osph oli pa se 28 pino cy tos is 292 pla q ue 373 po lar 17
po lar head 280 po lar gro up 253 po larit y 17 po lyc lonal pla q u e 374 po lys accharid e chain 70 po rta l blood 31 po st h e p a rin lip o ly tic acti vi t y 6o pr echy lo mi cr on 39 pr eren al tiss u e 56 pro p ion ic acid 224 pro sta g la ndin 89 pro ta m i n sulfa te 59, 77-S pro te i n kin a se 69, 91 pro te o g ly c an 70, 72 pro to n ate d 19 pro xim al po rti on 31 pu romy cin u9, 290 pyra sole 131, 144 pyrr oli do ne carboxy li c acid 252 pyr uvate 84, 135, 149 一 dehy d rog e nase u6 Rate lim i ting ste p 38, 93, 360 recep tor sit e 94, 261, 383 reduc ing eq u iv a lent 145 remnant chy lo mi cr on 198 renal arte ry 377 一 vascular occlusio n 377 retr o p e rit on eal 52 RMI 14, 514-(te t r a decy lo xy ) -2-fu r · oic acid x70 RNA po lym erase I 294 - Il 294
Salti ng out 22 self associa t e oli go mer 252 semi sta r vati on die t 157 serin e 276 seroto n in 89 sia l ic acid 258, 266, 284, 380 sin g le cell 374 —sin u sdoeiod xs y c1 h0o5l ate 22 smooth muscle cell 369, 374, 387 sodiu m decy l sulfa te 247 _—tau rocholate 22 soluble enzy m e 71 sp h in g o my e li n 247-9, 266, 271, 3011 380 spl e nchin i c circ ulati on 147 squ alene 206 一 sy n th a se 210 ste a ric ac id 380 ste a to s is 141 str ep toz oto c in 216 subcuta n eous fat 56 - tissu e 394 sulfa ted gly c osami no g ly c an 71 sulfo n y l ureas 153 sup e rnata n t 36 sy m p a th e ic nerve endin g 89 Tang ier dis e ase 245, 255, 257, 268, 297-8 tau nne 19, 31 tau rochenodeoxy ch olate 227, 229 tau rochenodeoxy c holi c acid 19
tau rocholate .22 7, .2.29 Vasop re ssin 89 tau rocholi c ac id 19 vert eb ral 376 th in line pro te i n .24 6, .25 0, .27 6 very hig h densit y lip o pr o te i n th io l ase 156 (VHDL) .24 4 th oracic duct .24 6, .25 4 very low densit y lipo pr o te i n ( VLDL) th rombus 370, 374 58, 68, 7.2 , 78, 83, 87, 97, 112-4, 169, thy ro id hormone .21 6 .20 0, .23 1, 234, 244, 247, .26 5, .27 4, .27 7 3, 7, 1.2 -tri h y d roxy c holanic acid 18 .29 9, 318, 380 tri l ay e r 278 VLDL syn th e sis 292-5 tryps in .28 VLDL B .26 0 try p top h an .25 .2 a-VLDL .26 2 x-VLDL 26.2 Uneste r ifi ed choleste r ol .24 7-8, .25 0 vesenta r y 56 unil oc ular 53 vil lus 31 unsti rr ed wate r lay e r 15, 29 urin a ry red cell casts 308 Zy m og e n 23, 28 uronic aci d 62 zym oste r ol 207 zwi tter ion 280
金淑喜 이화여자대학교 가정학부 졸업 Texas Women's Univ ersit y 에 서 영 양학 Ph. D. Jho ns Hop ki n s Univ e rsit y McColum 영양학 연구실에서 연구 현재 이화여자대학교 가정대학장 - t
一 脂防營養· 1984 년 7 월 I5 김 인쇄 1984 년 7 월 30 일 발행 저 자 金淑喜 발행인 朴孟浩 발행처 民音社 우편대 체계 좌번호 010041-31-523282 IIO 서 울 종로구 관천동 44-I 724-2000 • 724-4234 • 725-85 석 출판등록 1966. 5.19 제 I-I42 호 * 파본은 바구어 드립니다. 값 6,300 원 .대우학술총서 • 자연과학 1 소립자와 게이지상호작용 2 動金鎭力義學 著特 論• 값 3 600 원 3 질李소炳昊고 정著 • 값 5, 400 원 4 相宋承轉達移 著와 臨• 값界 2現, 80象0 원 5 觸김媒두철作 著用 •값 2, 800 원 6 뫼陳 宗스 植바 著우 어• 分값 光2, 8學00 원 7 극玉恒미南량 著원 소• 의값 2,영8 0양~ 昇正子 著 • 값 6500 원 8 水素化覇素와 有機覇素化合物 尹能民著 9 麟物質의全合成 姜錫久 著 • 값 8,000 원 10 국소저 형태의 A tiy ah-S ing er 지표이론 지동표 著 • 값 2,800 원 11 Muco po l y sacchar i des 의 生化學 및 生麟學 박준우 著 • 값 3,800 원 12 ASTROPHYSICS (天體物理學) 洪承樹 著 • 값 4, 700 원 13 천연물화학연구법 14 도禹源무植타著 글란딘합성 金馨표 著 15 脂防營養 金淑喜 著 •값 6,~o 원 16 麟뱌:유리 金邑著