

저자는 독일 G i essen 의 Jus tu s Lie b ig Univ e rsit iit 영 양학과를 졸업하고 同 대학원에서 석사 및 박사학위를 받 았다. 그리고 Mi ich en 의과대학 생화 학과에서 연구원으로 재직했으며 同 대 학교임상영양연구소에서 연구실장으 . 로근무한후 현재는 숙명여자대학교 식품영양학과 교수이다.
 국미량원소의영양
국미량원소의영양
 극미량원소의 영양
극미량원소의 영양
머 리 말 생체에 있어서 극미량원소는에너지원은 아니지만, 생물체를 구성 하는 성분이며, 비타민과 같이 생명에 관계되는 여러 생리 작용에 관여하므로, 우리가 생촌하는데 철대적으로 필요한 영양소이다. 오 늘날, 영양학에 대한 관십이 지대해침으로써, 국미량원소에 대한연 구도 급전적 발전을 보아고 있다. 이에 처자는 물일듯아 쏟아져 나오는 새로운 지석을 간추려 엮기 위하여, 국내의의 극미량원소에 관한 설험 및 학술 문헌의 최신 정보를 입수하여 이 책을 집필하게 되었다. 이 책은 영향학적 측면에서 극미량원소가 생체 내에 미치는 영향, 필요량, 다른 영양소와 국미량원소들과의 상호 작용을 살펴보았으 며, 독성, 결핍 둥으로 인한 생화학적, 생리학적인 변화에 중접을 두었다. 아 책의 미바한 접은 앞으로노 판아 거듭됨에 따라, 수정, 보완이 될 것이며, 여러 선배님들의 조언과 비평을 바랄 분이다. 본 연구 는 대우재단의 학술연구조성비 지원으로 수행되었으며, 이에 감사 드리고, 끝으로 이 책을 출판하는 데 있어, 직접 • 간접으로 협조해 주선 여러분들께 십십한 사의를 표하는 바이다.
1983 년 6 월 昇正子
극미량원소의 영양/차례
머리말 - 31 서론 • 111.1 trace elements의 정의 121.2 trace elements의 영양학적 의의 131.3 trace elements의 종류와 체내분포 141.4 trace elements의 필수성과 결핍 161.5 trace elements의 독성 191.6 trace elements의 화학결합과 효소로서의 기능 201.7 trace elements의 대사 23참고문헌 242 철 (Iron, Fe) •262.1 체내 함량과 분포 262.2 주요 기능 282.3 대사 302.4 권장량 482.5 결핍증 502.6 Fe의 대사장애에서 오는 질병과 기타 질병과의 관계 522.7 독성 542.8 함유식품과 강화식품 55참고문헌 663 구리 (Copper, Cu) •723.1 체내 함량과 분포 723.2 주요 기능 743.3 대사 76
3.4 권장량 843.5 Cu 결핍증과 Cu 대사장애에서 오는 여러 가지 질병 863.6 함유식품 923.7 독성 943.8 Cu와 다른 미량원소와의 상호작용 95참고문헌 1224 아연 (Zinc, Zn) •1404.1 체내 함량과 분포 1404.2 주요 기능 1424.3 대사 1454.4 Zn의 필요량 1504.5 Zn 결핍증과 대사장애에서 오는 질병 1554.6 함유식품 1834.7 독성 184참고문헌 1855 몰리브덴(Molybdenum, Mo) •2005.1 체내 함량과 분포 2005.2 주요 기능 2015.3 대사 2015.4 필요량 2035.5 결핍증 2035.6 함유식품 2045.7 독성 204참고문헌 2066 망간 (Manganese, Mn) •2086.1 체내 함량과 분포 2086.2 주요 기능 209
6.3 대사 2116.4 섭취량과 필요량 2116.5 결핍증 2126.6 함유식품 2136.7 독성 214참고문헌 2157 크롬 (Chromium, Cr) •2187.1 체내 함량과 분포 2187.2 주요 기능 2197.3 대사 2207.4 결핍증 2217.5 섭취량과 필요량 2227.6 함유식품 2237.7 독성 224참고문헌 2258 셀레늄 (Selenium, Se) •2298.1 체내 함량과 분포 2308.2 주요기능과 결핍증 2338.3 대사 2368.4 섭취량과 필요량 2398.5 함유식품 2408.6 독성 242참고문헌 2449 니켈(Nickel, Ni) •2489.1 체내 함량과 분포 2489.2 주요 기능 2499.3 대사 2499.4 섭취량과 필요량 250
9.5 결핍증 2519.6 함유식품 2549.7 독성 255참고문헌 25610 코발트(Cobalt, Co) •25910.1 체내 함량과 분포 25910.2 주요기능과 결핍증 26010.3 대사 26210.4 섭취량 26310.5 함유식품 26410.6 독성 264참고문헌 26611 요오드(Iodine, I) •26811.1 체내 함량과 분포 26911.2 주요 기능 27011.3 대사 27111.4 섭취량과 필요량 27411.5 결핍증 27411.6 함유식품 27611.7 독성 277참고문헌 27812 불소(Fluorine, F) •28012.1 체내 함량과 분포 28012.2 주요 기능과 결핍증 28112.3 대사 28412.4 섭취량과 필요량 28912.5 강화식품 290
12.6 독성 290참고문헌 29113 규소(Silicon, Si) •29413.1 체내 함량과 분포 29413.2 주요 기능과 결핍증 29513.3 대사 29713.4 섭취량과 필요량 29813.5 함유식품 29813.6 독성 298참고문헌 29914 바나디움(Vanadium, V) •30114.1 체내 함량과 분포 30114.2 주요기능과 결핍증 30214.3 대사 30214.4 섭취량과 필요량 30314.5 함유식품 30314.6 독성 304참고문헌 30515 비소(Arsenic, As) •30715.1 체내 함량과 분포 30715.2 주요 기능과 결핍증 30715.3 대사 30815.4 섭취량과 필요량 그리고 함유식품 30915.5 독성 310참고문헌 31116 주석(Tin, Sn) •313
참고문헌 31517 카드뮴(Cadmium, Cd) •31717.1 체재 함량과 분포 31717.2 주요 기능 31817.3 대사 31917.4 섭취량과 필요량 32017.5 함유식품 32117.6 독성 321참고문헌 32318 납(Lead, Pb) •32618.1 체냐 함량과 분포 32618.2 주요 기능과 결핍증 32713.8 대사 32918.4 섭취량과 필요량 33018.5 함유식품 33118.6 독성 332참고문헌 33319 수은(Mercury, Hg) •33519.1 체내 함량과 분포 33519.2 대사 33619.3 섭취량과 허용량 33719.4 함유식품 33719.5 독성 339참고문헌 34020 알루미늄(Aluminium, Al)•342참고문헌 34521 리티움(Lithium, Li) •347
참고문헌 34822 스트론튬 (Strontium, Sr) • 349참고문헌 35323 붕소 (Boron, B) • 355참고문헌 35724 특수환경에서의 trace elements • 35924.1 포유동물의 임신과 수유시 필수 trace elements 359 24.2 임신과 수유시 trace elements -36224.3 인체의 태반과 trace elements와의 관계 -36324.4 신생아와 trace elements -36424.5 유아영양과 trace elements와의 관계 ——— 36724.6 Parenteral nutritiondml의 trace elements 一 37224.7 상처가 심한 의식불명환자의 혈청과 뇨의 Cr, Mn, Co, Ni, Cu, Zn 함량 375참고문헌 37825 기타 비필수 미량원소 • 38226 각 식품에 함유된 trace elements • 383참고문헌 39327 결론 • 394색인 3961 서 론 Trace elemen t s 는 생체 내에 국미 량 촌재하지만 인체에 미치는 영 향은 매 우 크다. 식 이 tra ce elements 는 약 300 년 전부터 이 따금씩 연구되어져 오다가 최근 여러 가지 특수한 미량원소 분석범의 발달 과 생화학, 영양학 및 의학 등의 급전적인 발달로 영양적인 면과 그 작용기전에 관한 관십이 더욱 깊어졌고, 이에 관한 연구도 활발 해졌다. 1857 년 Bernard1) 와 1885 년 Mac Munn2) 은 세 포호흡 과정 에 있 어서 철 (Fe) 의 산화과정을 연구함으로써 후에 meta l lo enzy m es 촉 매 와 meta l loenzy m es 에 대 한 밑 받침 이 되 어 조직 내 에 서 의 tra ce elements 의 존재 와 기 능의 중요성 에 대 한 인식 을 높였 고, 1869 년 Rau li n3) 은 aspe rgi llus nig a r 의 영 양에 아연 (Zn) 이 필수적 임 을 밝 혀 냈으며 , 프랑스 식 물학자인 Cha ti n (l 850~1854)4) 은 흙, 물, 식 품 으로부터 얻어지는 요오드(I)가 g o it er 에 미치는 영향에 대해서 연 구함으로써 tra ce elements 의 중요성 에 대 해 더 욱 관심 을 가지게 하였다. 근래에 와서 selen i um(Se) 이 v it am i nE 와 함께 항산화작용에 관 여 하여 glu ta t h io n e pe roxid a se 의 구성 요소가 됨 이 밝혀 졌고, 5)6) s ili con(S i)은 걷체조직의 cross li nk ing요소”로서의 역할이 접차 뚜렷해지고 있으며 특히 S i와 동맥경화중 8) 과의 연관성온 매우 홍 미있는 사실로 받아들여지고 있다.
또한 근래에 물의를 일으키고 있는 환경오영에서 오는 공해병과 tra ce elemen t s 와의 관계는 연구되어져야 할 매우 시급한 과제라 고 생 각된다. 9)10)11) 현재 까지 사람이 나 동물의 건강에 중요하다고 알려 진 tra ce ele- men t s 는 15 종 정도이며 인체의 필요량이 정확히 알려진 것들은 철 (Fe), 요오드(I), 아연 (Zn) 분이 다. 12) 몇몇 미량원소에 대한 결핍증은 실험동물에서만 입증이 되고 인 체에 마치는 영향에 대해서는 아직 확실하지 않은 사실들이 많이 있으므로 앞으로 계속 연구 규명되어쳐야 할 주요과제라고 생각한 다. 특히 tra ce elements 의 필요성 과 독성 이 함께 강조되 면서 이 들 에 대한 보다 서대하고 지속적인 연구가 철실히 요구되어진다고 하 겠다. J. J Trace elements 의 정 의 무기질은 인체를 구성하고 있는 요소로서 체내에서 유기물질이 완전히 산화된 후에 남게 되는 생물체의 구성성분이다. 이러한 무 기 질은 체 내 에 존재 하는 양과 하루 필요량에 의 해 서 macro elem-ents 와 mi cro elements 로 분류된다. Mi cr o elements , 죽 tra ce elements 는 성 인의 체 내 에 서 평 군 약 lOg 정도 존재한다고 한다. 그러나 최근 그 범위를 넓혀서 인간과 동물에 촌재 하는 모든 무기 물로서 체 내 존재 량이 50mg / kg 체 중 이 하이 면 tra ce elements 라고 정 의 를 내 리 기 도 한다. 예의로 Fe 은 체내에 50mg / kg 체중 이상 촌재할 수도 있으나 trac e elemen ts 라 하기도 하는데 Fe 은 효소의 활성인자로서 호르 몬, 비타민의 주요 구성인자이며 또한 핵산대사에서의 주요기능이 trac e elements 의 기 능과 같기 때 문이 다. Co t z i as1” 는 tra ce elements 에 대해 다음과 같이 정의를 내리고 있다. 1) 모든 생체내 건강한 조칙에 촌재한다. 2) 항상 일정한 농도를 유지한다. 3) 결핍시에는 종류에 관계없이 동일한 생리적, 구조적 이상을
유발한다. 4) 첨가시 비정상 상태에서 정상상태로 회복되거나 바정상상태의 예방이 가능하다. 5) 결핍되었을 때 비정상상태의 생화학적인 변화를 수반한다. 6) 이때의 생화학적인 변화들은 결핍증이 참재해 있거나 발생되 었을 때 예방 또는 치료되어질 수 있어야 한다. 대 부분의 tra ce elements 의 함량은 mg / kg 또는 µg/g(µg= 10- 6g )' ppm ( pa rt pe r m illi on) 으로 표시하나 그 중의 vanadiu m (Va), chrome(Cr), cobalt (C o), nic k el(Ni ), molyb den(Mo), iod in e (!) 둥은 신체에 국미량 촌재하기 때문에 n g/g (n g =l0-9 g)으로 표시하 기도한다. 1. 2 Trace elements 의 영 양학적 의 의 요오드(I)의 결핍은 갑상선종을 초래하고 철 (Fe) 의 부족은 영양 성빈혈을 유발시키며 충치예방에는 적당량의 불소가 효과적임은 이 미 알려진 사실이다. 최 근에 는 병 인식 이 나 정 맥 투입 법 (pa rente r al nu triti on) 에 서 사용하 는 特 定 食 , 죽 유전적 대사장애에서 기인되는 질병, 또는 십한화상 전염 병 , 돌발적 인 사고로 인한 장애 둥에 tra ce elements 섭 취 의 중 요성이 강조되고 있다 •14) 이 이 의 에 도 역 학적 연 구 (e pi dem i olo gi c s t ud y)에 서 음료수나 식 품 에 함유된 tra ce elements 의 섭 취 증가는 (예 ; Se) 암이 나 순환계 질환의 사망률을 감소시켰다고 한다 .9)15) 또한 급전적인 공업기술의 발달로 인한 공장페수, 대기오염에서 오는 공해질환의 급증은 날로 매우 십각한 문제가 되고 있다. :::L 예 로는 모내 기 물에 다량 함유된 카드뮴 (Cd) 으로 인한 lta i - Itai 라고 하는 카드뮴 (Cd) 의 독성과 수은 ( H g)으로 오염된 바다에서 자란 생 선 둥을 먹고 십한 수은중독에 걸린 사실 둥을 들 수 있다 .l4) 이 와 같이 tra ce elements 의 영 양학적 인 중요성 은 최 근 의 학, 생 화학 둥의 연구와 함께 이 분야에 대한 관십이 철실히 요구되며 보
다 나은 인류의 건강과 번영을 위해서도 매우 시급한 과제라 생각 한다. 1. 3 Trace elements 의 종류와 체 내 분포 인체에 촌재하는 tra ce elemen t s 의 종류와 체내함유량, 1 일 섭취 량, 뇨로 배설되는 양, 그리고 혈장 내의 평군 함유량은 표 1. 1 과 같다.
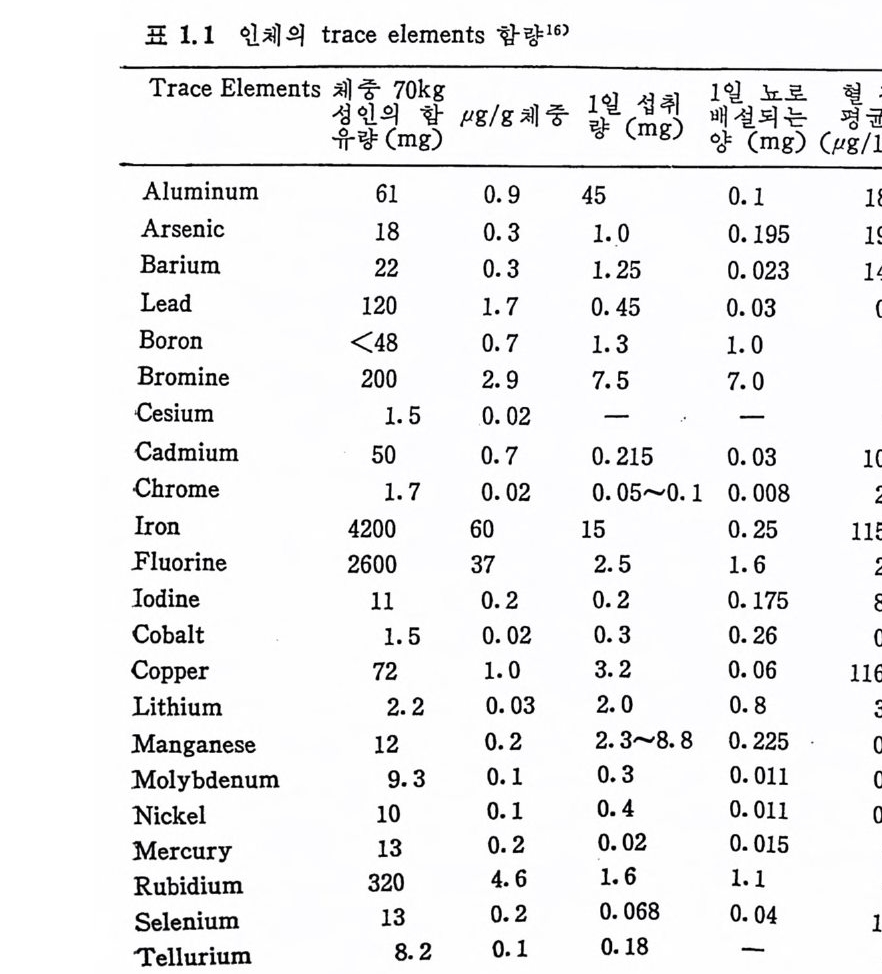 표 1.1 인체의 tra ce elements 함량 16)
표 1.1 인체의 tra ce elements 함량 16)
 Ti tan iu m 9 o. 1
Ti tan iu m 9 o. 1
Trace elements 의 함량은 가 기 관과 조직 마다 그 차이 가 크게 나 타나며 극미량 있는 것이 많다. 표 1. 2 는 필수 tra ce elements 의 체 내 분포상황을 나타내 고 있 다.
 표 1. 2 팔수 tra ce elements 의 체 내 분포 상황 17)
표 1. 2 팔수 tra ce elements 의 체 내 분포 상황 17)
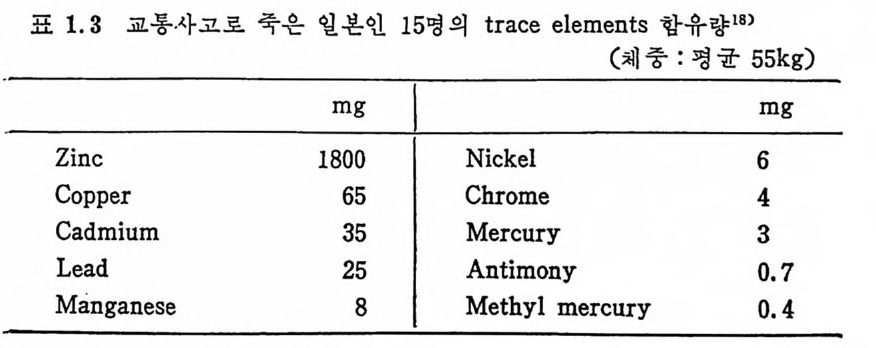 표 1. 3 교통사고로 죽은 일본인 15 명 의 tra ce elements 함유량 18)
표 1. 3 교통사고로 죽은 일본인 15 명 의 tra ce elements 함유량 18)
표 I. 3 은 교동사고로 죽은 일본인 15 명의 tra ce elemen t s 의 함유 량을 나타낸 것이다. l. 4 Trace eleim ents 의 필수성 과 결 핍 tra ce elemen t s 의 필수성은 체내 각 기관에서의 특정한 기능과 대사에서 볼 수 있다. Trace elemen t s 는 체내의 뼈나 조직에서 호 . 르몬, 효소, 비타민의 일부분이 되거나 이것들과 같이 결합하여 광 범위한 기능을 발휘하고 있다. Trace elemen t s 의 결핍은소화기, 피부, 뇨 배설기관울 경유하면 서 tra ce elemen t s 가 손실되는 경우와 이 원소들을 석이로부터 부 적당하게 섭취하는 경우에 나타난다. 부적당한 석이의 예로서, 도 정한 밀가루는 밀 자체보다 철 (Fe), 아연 (Zn) 의 양이 적으며 or- ang e jui c e , wi ppe d cream 같은 가공식품도 가공하기 전보다 많은 양의 tra ce elements 가 손실되 게 된다. 1957 년까지 만 해 도 7 개 의 tra ce elements 가 인간과 동물에 중요 하다고 알려져 왔으나 그 후 그 수가 2 배로 중가했다. 표 1. 4 는 필 수와 필수가능한 tra ce elemen ts 의 발견년도와 이 발견에 공헌한 사람들을 나타낸 표이 다.
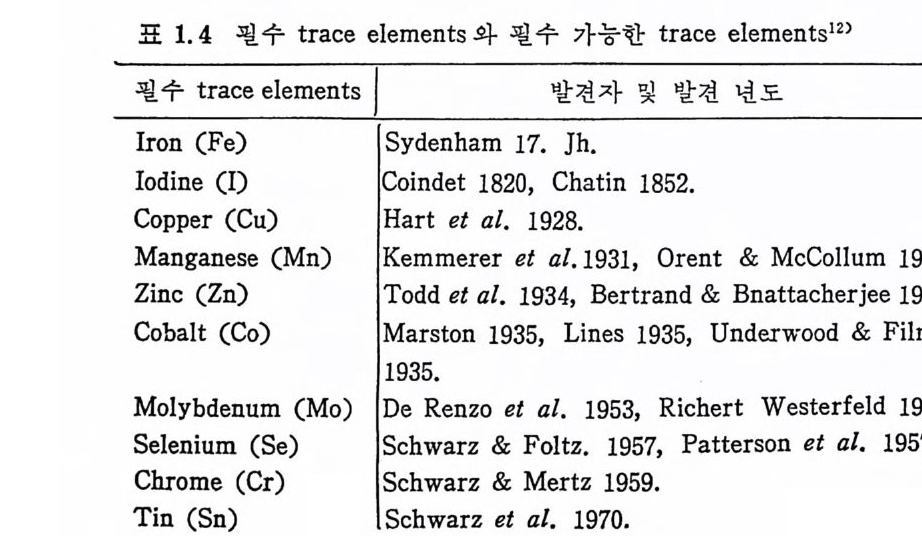 표 1. 4 필수 tra ce elements 와 필수 가능한 tra ce elements 1 2 >
표 1. 4 필수 tra ce elements 와 필수 가능한 tra ce elements 1 2 >
 Vanadiu m (V) Hop k in s & Mohr 1971 .
Vanadiu m (V) Hop k in s & Mohr 1971 .
Trace elements 각각에 대 한 기 능과 함유식 품을 정 리 해 보면 표 1. 5 와 같다.
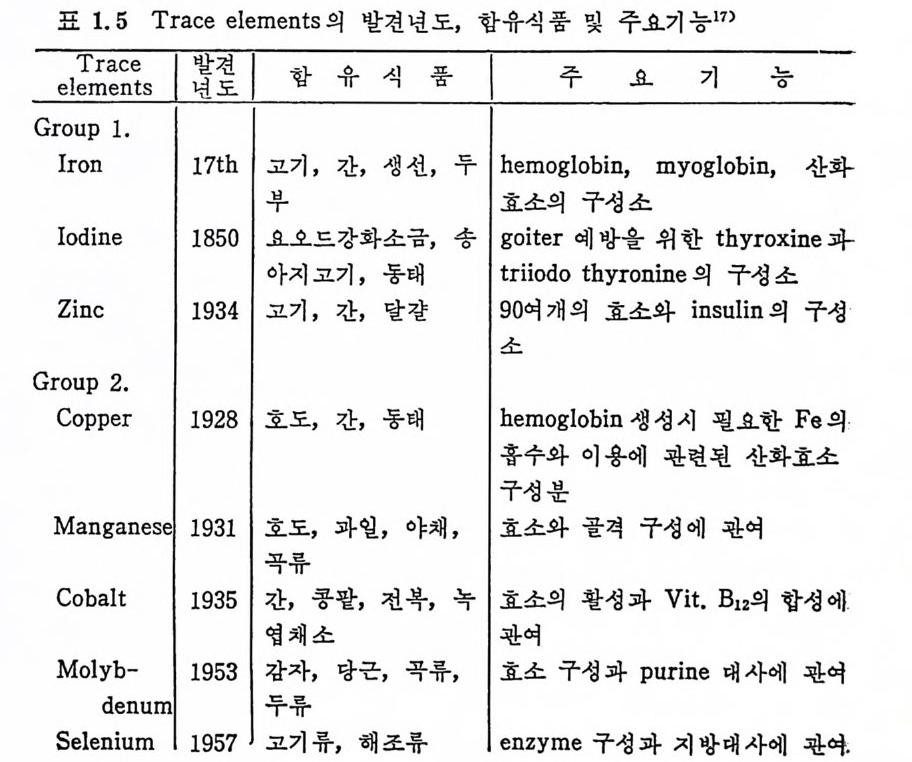 표 1.5 Trace elemen t s 의 발견년도, 함유식품 및 주요기능 17)
표 1.5 Trace elemen t s 의 발견년도, 함유식품 및 주요기능 17)
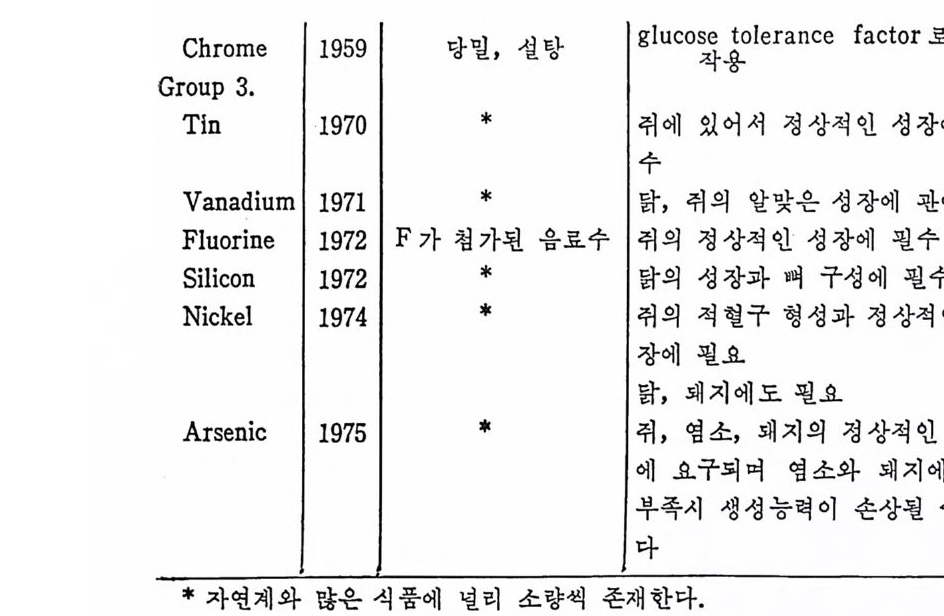 Chrome 119591 당밀, 설탕 | glu cos작e 용to lerance fac to r 로서 의
Chrome 119591 당밀, 설탕 | glu cos작e 용to lerance fac to r 로서 의
식 이 tra ce elements 는 3 gro up 으로 분류할 수 있 다. Group 1 은 인체 요구량이 규명된 tra ce elements 이며 Group 2 는 인체 에 필요하지 만 체 내 요구량이 규명 되 지 않은 tra ce elemen t s 이고 Group 3 은 인체에서의 필요 여부에 대해서는 아직 알려쳐 있지 않으나 다른 동물에 있 어 서 는 필수적 인 tra ce elements 이다. 이 가운데 식 이 tra ce elements 의 가장 대 표적 인 결핍 은 gro up 1 에 속하는 Fe 이 라 할 수 있 다. Fe 은 hemog lo bin 과 my o g lo bin 의 주성분으로 결핍시 빈혈을 초래한다. Group 2 에서 결핍되기 쉬운 것은 구리 (Cu) 로서 구리는 체내 산 화반응에 매우 중요한 역할을 하며 부족시 빈혈과 골격구성에 손상 울 주며 어떤 동물에 있어서는 melan i n 색소의 전이가 안되어 모발 의 탈색 원인이 되기도 한다. Group 3 은 1970~1975 년 사이에 발견된 원소들로 아직 인체에 대한 필수성은 밝혀지지 않고 있다. 이 상을 종합하여 tra ce elements 의 주요기 능을 살펴 보면 신체 구
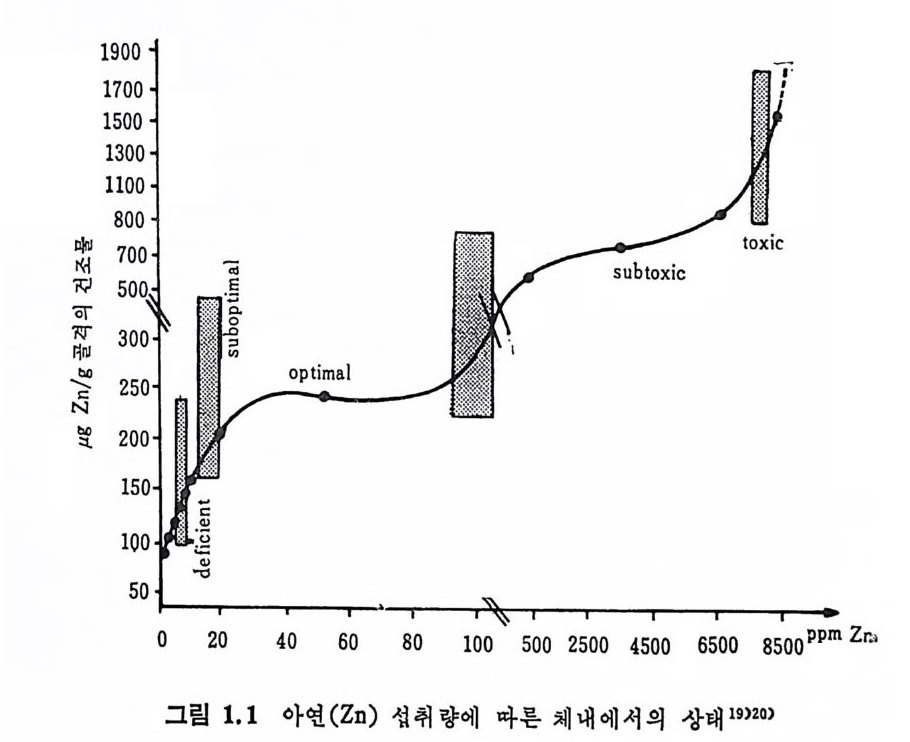
성분이 되며 신체 조철성분으로서 산―알카리평형과 수분평형을 유 노 지시켜주고 몇몇 효소의 기능에 팔수적이며, 신경자극의 전이작용 ` 이 있다고 할 수 있다. 1. 5 Trace elements 의 독성 (tox ic ity) Trace elements 는 체 내 에 서 여 러 가지 대 사작용에 기 여 하나 과잉 섭 취 할 경 우 독성 을· 일으킬 수 있 다. 그러 나 subop tim al, opt ima l, t ox i c 까지의 경계선은 각 tra ce elemen t s 마다 현저한 차이가 있기 때 문에 각 tra ce elements 둘의 tol erance 는 현재 까지 완전히 규명 되지 못한 상태에 있다. 그림 1. 1 은 아연 (Zn) 의 섭취량에 따른 체내에서의 상태를 나타 낸 것이다.
 1900
1900
Mn, Fe, Co, Zn, Ni 은 다른 tra ce elements 에 비 해 서 비 교적 많은 양을 섭취해도 빨리 독성상태에 이르지 않는 반면 Cu, Se, Va, As 는 미량이라도 과잉섭취하면 즉시 독성상태에 이르게 된 다. 얼 마 전까지 만 해 도 많은 tra ce elements 의 정 확한 작용기 전이 불확실했기 때문에 무조건 유독하다고 알려쳐 왔다. 그러나 최근에 와서 는 Cd 이 나 Pb 둥을 완전정 제 석 이 (pu rif ied d i e t)에 서 국미 량 섭취하면 오히려 성장 발육에 도움을 준다는 것이 동물실험을 통해 서 입층되고 있다 .2 1) Trace elements 의 독성 은 식 품에 함유된 양에 의 해 서 라기 보다는 화학적 결합형태에 의해서 독성의 강도가 달라진다. 예를 들어 유 기 H g의 경우 alk y l 형태의 H g과 ar y l 형태의 H g이 sal t형태의 Hg 보다 몇 배 나 강한 독성 을 나타낸다. 또한 tra ce elements 들의 상호작용 (homeos t a ti c re g ula ti on) 에 의 해 서 독성 의 강도가 더 강화되 거나 약화되어질 수도 있다. 특히 체내의 흡수와 배설의 상호작용 에 의한 독성온 Zn, Mn 둥에서 보여지는데 이들은 조직내에 장기 간 축적되어 독성을 초래하기도 한다. Cu 의 경우 5 pp m 정도에서도 박테리아와 작용을 할 수 있으며 이 박테리아를 Cu 와 함께 섭취했을 경우 장의 미생물과 함께 작용하 여 독성을 일으키기도 한다. 또한 아래와 같이 간접적인 방법에 의해서도 독성이 일어난다. 1) 식품에 부착되어 있는 농약 2) 식품 가공시 사용하는 첨가물 3) 식품을 포장하는 재료 위와 같은 원인에 의해서는 특히 As, Pb, Hg , Se 둥의 독성이 문제시된다. 1. 6 Trace elements 의 화학결 합과 효소로서 의 기 능 표 1. 6 은 원소 주기 율표에 서 의 팔수 및 비 필수 tra ce elements 의 분포도인데 다음과 같은 특성을 찾아볼 수 있다 ..
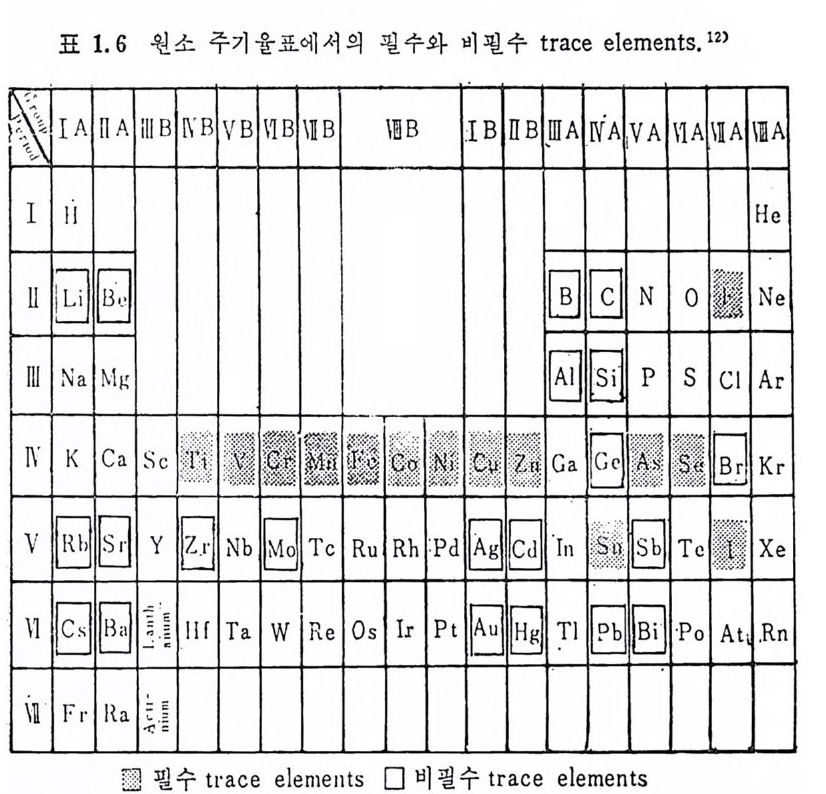 표 1. 6 원소 주기 융표에 서 의 팔수와 비 팔 수 tra ce ele m e nt s . 12 >
표 1. 6 원소 주기 융표에 서 의 팔수와 비 팔 수 tra ce ele m e nt s . 12 >
대 다수의 필수 tra ce elements 는 양이 온이 며 그 중 몇 몇 은 음이 온으로 촌재 한다 . Trac e element s 중 I, B 를 제 의 하고는 met a l 로 서 세 포에 서 효소의 촉매 작용울 한다. 대 략 30% 의 효소가 met al ion 으로 구 성 되 어 있으며 그들은 산 (ac i d) 의 촉매 기 능을 갖는다. 이 들 효소들은 met al lo enzy m es 고~ met al acti ve enzy m e 의 두 종 류로 분류한다. 이 분류는 met al i on 과 결합되는 단백질의 종류에 의하여 질적이기보다는 양적인 성격으로 분류한다. met a l i on 이 enzy m e p ro t e i n 의 어떤 부분에 연결되어쳐 있는가 또 몇 개의 met a l ion 이 연결 되 어 져 있 는가에 따라서 그의 촉매 작용이 달라진 다. 어 떤 상 황 에 서 는 met a l ion 이 없는 ap o enzy m e 에 met a l ion 울 넣어 줌으로써 그의 본연의 활성작용을 할 수 있게 된다. met a l 과 효소의 상호 교체 는 목수작용에 의 한 것 이 다. 많은 met al lo enzy - mes 은 Fe(]I l), Cu(I[ ), Zn(I[ ), Mn( I[)과 같은 me t al 로 안정한
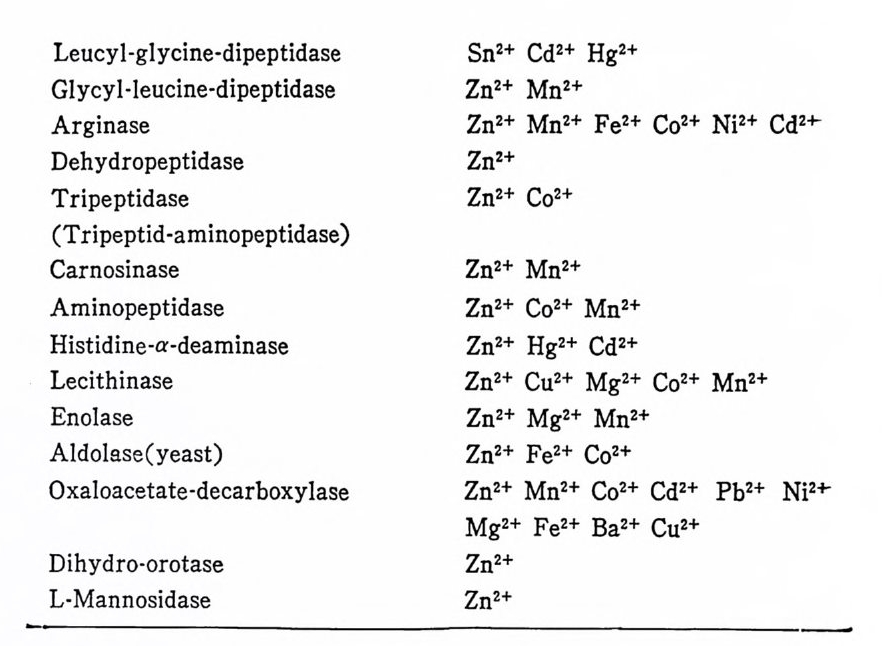
chelate 를 형 성 한다. 표 I. 7 은 meta l lo enzy m es, 표 1. 8 은 meta l acti ve enzy m es 을 나타낸 것이다.
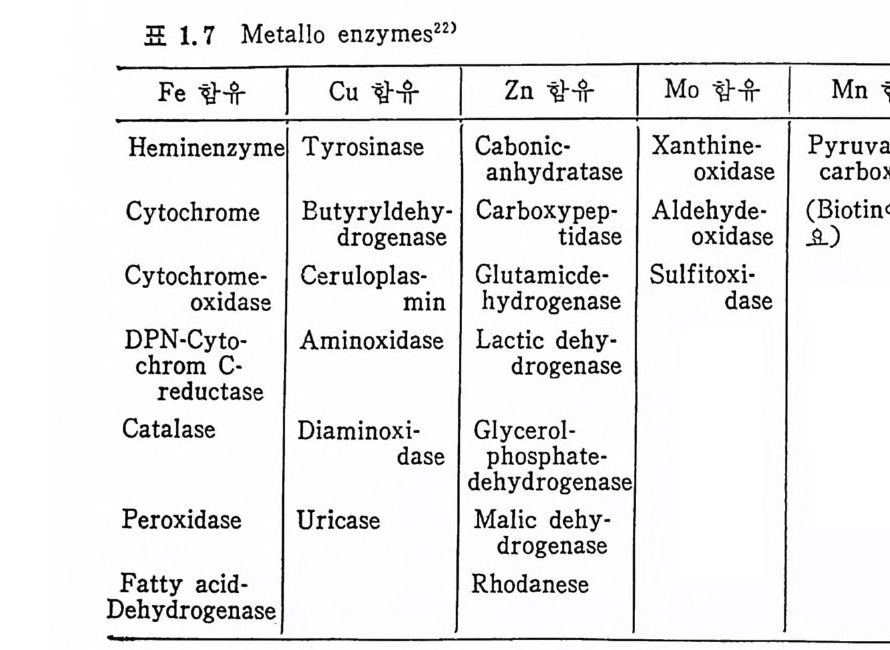 표 1. 7 Meta l lo enzy m es22 >
표 1. 7 Meta l lo enzy m es22 >
효소들마다 각기 다른 meta l 을 사용하는데 Cu 는 주로 oxid a se 에 , Zn 은 다량의 dehy d rog en ase 와 hy d rolase 에 , fer rop ro to p o r-- ph y r in 은 많은 electr o n tra nsfe r enzy m es 과 oxy ge nase 에 쓰인다. Meta l acti ve enz y mes 은 me t al 과 효소가 아주 느슨하게 연결되 어 있는 상태 이 며 이 meta l acti ve enzy m es 으로부터 meta l 을 분리 시 켰 을 때 에 도 meta l free enzy m es 으로서 그의 본연의 활성 도를 거 의 잃지 않는다. Meta l acti ve enzy m es 에 주로 쓰이 는 meta l 로는 Fe, Cu, Zn, Mn, Mo, Co 등을 들 수 있 다.
 표 1. 8 Meta l acti ve enzy m es17>
표 1. 8 Meta l acti ve enzy m es17>
 Leucy l- gl y c ine -dip e pt ida se Sn2+ Cd2+ Hg 2+
Leucy l- gl y c ine -dip e pt ida se Sn2+ Cd2+ Hg 2+
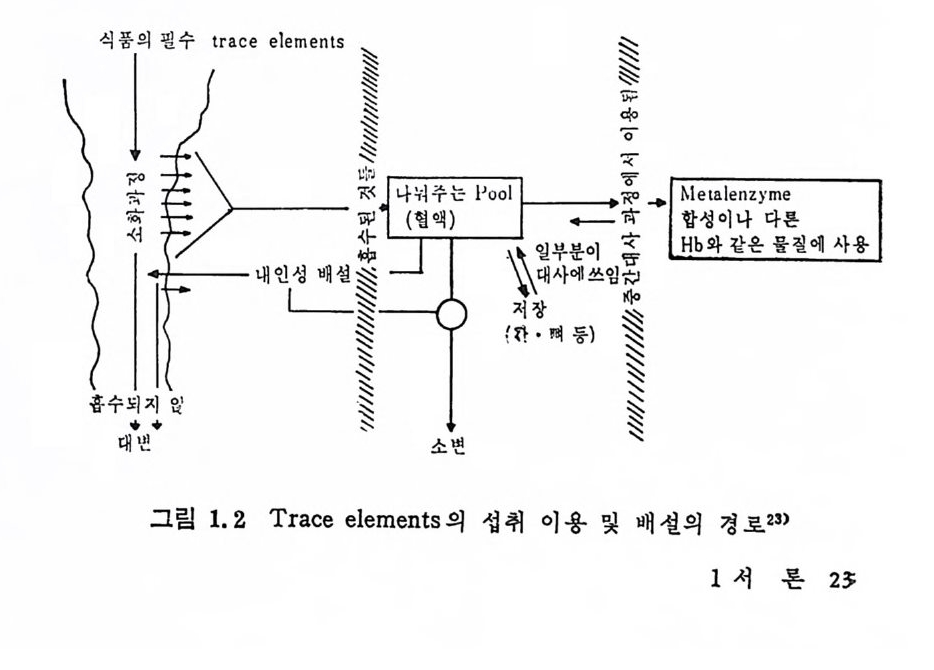
1. 7 Trace elements 대 사 Trace elements 의 주요 대 사는 체 내 의 항상성 유지 에 있 으며 이
 식 풍 의필 수 r ac e e le m g충\`l`h言中
식 풍 의필 수 r ac e e le m g충\`l`h言中
는 각 기관의 조직이나 식품과의 상호관계에 의하여 영향을 받는 다. 그림 I. 2 는 tra ce elements 의 체 내 대 사와 이 용도를 나타낸 것 이다. Trace elements 의 대 사경 로에 따라 다음과 같이 3 가지 로 분류할 수있다. 1) 흡수와 배 설을 통하여 조철작용이 가능한 것 (예 : Fe). 2) 장에 완전히 흡수되며 단지 배설에 의해서만 그의 조절이 가 능한것. 3) 흡수와 그 중간대사과정의 이용도에 의하여 조철이 가능한 것 -(ol] : Zn, Cu, Mn). *참고문현 1) Bernard, C. , Le~ons sur eff ects des substa n ces tox iq u es et mi d i· .ca mente u ses Bail lier e, Paris, 1857. 2) Mac Munn, C. A. , Phil . Trans. R. Soc. London, 177, 267, 1885. 3) Raulin , J. , Ann. Sci. Nat. , Bot. Bi ol . Veg . [2 )11, 93, 1869. 4) Chati n, A. , C. R. Acd. Sci '. 30, 1850~1854. 5) Omaye . S. T. and A. L. Tapp e !, J. Nutr . 104, 666, 1974. 6) Ganth e r, H. E. , Hafe m an, D. G. , Lawrence, R. A. , Serfa s s, R. E. and Hoekstr , W. G. , in Prasad, A. S. , Trace element in human healt h and dis e ase Vol. Il , p. 165, Academi c Press, New York, 1976. 7) Charlis le , E. M. , Fed. Proc. 33, 1758, 1974. 8) Schwartz , K. , Lancet 1977. 9) Luckey, T. D. and B. Venng op a l, Phys i o lo g ica l and chemi ca l basi s for meta l tox i ci ty , Plenum Press, New · York and London, 1977. 10) Patt y, F. A. , Industr i a l hy gien e in Toxic o log y, Inte r sie n ce Publi sh ers New York and London, 1962.
11) Petr i , H. and A. Grohmann, Di e ge sundheit liclz e Bedeutu n g des Zi nk s als Umwelt fakt o r des Menschen Sp ez ie l l in der Trin k wasser Ve rs org u ng , WaBo Lu-Beric h t 7, 1971 . 12) Kric h g e ssner, M. , E. Weig i!nd , A. Schnegg , E. Grossmann, F. J. Schwarz and H. -P. Roth , in Cremer, H. -D. , D. Hotz e ! and J. Kii hn au, Bi oc hemi e und Phys i o l og ie der Ernti hr zmg , Band I. Ti el I, Georg Thie m e Verlag, p. 30, 1980. 13) Cotz i a s , G. C. , Trace Subst . Envir on . Healt hp ro c. Univ . Mc. Annu. Conf. , 1st, p. 5, 1967. 14) Petr i d e s, P. E. and G. Loff ler, in Loff ler Petr i d e s Weis s and Harpe r Phys i o l og ich e Chemi e Sp ri n g e r-Verlag, Berlin Heid e lberg New York, p. 531, 1979. 15) Coop er , W. Ch. , J. R. Grover, in Zin g ar o, R. A. , and W. Ch. , Cooder, Seleniu m , Van Nostr a nd Rie n bold Comp an y , 1974. 16) Schroeder, H. A. c:n d A. D. Nason, Clin . Chem. 11, 461, 191. 17) Ki rc hg e ssner, E. Weig a nd, A. Schnegg , E. Grassmann, F. J. Schwarz and H. -P. Roth , in Cremer, H. -D. , D. Hotz e ! and J. Ki ihn au Bioc hemi e und Phy si o l og ie der Ern!i hr ung . Band I, Teil 2, Georg Thie m e Verlag p. 276, 1980. 18) Sumi no , K. , K. Hay ak awa, T. Shib a ta and S. Ki tam ura, Arch . .En vir . Healt h 30, 487, 1975. 19) Pallauf, . J. and Kir c hg e ssner, M. , Z. Tie r ph y s i o l Ti er ernii hr , Futt er mi ttelk d. 30, 193, 1972. 20) Ansari, M. S. , W. J. Mi ller , M. W. Neath e ary, J. W. Lassit er , R. P. Gentr y and. R. L. Ki nc aid , Pro. Soc. Exp . Bi ol . Med. 152, 192, 1976. 21) Schwarz, K. and D. B. Mi lne , Bio i n org Chem. 1, 331, 1972. 22) Lang . K. , Bi oc hemi e der Ernii hr ung 4. Aufl ag e D. R. Die· ,tri c h Ste i n k off Verlag p. 333, 1979. 23) Ki rch g e ssner, M. , H. L. Muller, E. Weig a nd, E. Grassman, F. J. Schwarz, J. Pallauf and H. -P. Roth , Z. Ti er ph y s i o l Ti er ernii hr . Futt er mi ttel Kde. 34, 3, 1974.
2 철 (Iro n, Fe) 지구표면에 약 5% 정도로 촌재하는 Fe 은 17 세기경 영국의 의사 S y denharn (l 624 一 1689)1) 에 의해서 빈혈 치료에 효과가 있음이 밝혀 쳤고, 그 후 접차적으로 체조직에서도 혈액의 주요 성분임이 명백해 쳤다F.e 의 필요량과 분포에 관해 서 도 화학자인 Boussin g a ult( l802 — 1887) 에 의 해서 연구되 었 다. 2) 1889 년 독일의 생리학자 Bun g e 는 정상적인 영양 섭취에서도 빈 혈을 초래할 수 있으며 특 히 유아와 이유기에 있는 어린아이의 경 우우유 영양만으로는 Fe 의 섭취가 충분하지 못하다고 발표했다 .2) 이 와 때 를 같이 해 서 의 사인 Hoess li n (l 882) 는 Fe 부족에 서 오는 여러 가지 결핍증에 관하여 연구하였다 .2) 최근엔 Fe 이 적혈구 형성의 필수 구성요소 역할 이외에도 여러 종류의 효소의 구성 성분이라는 것이 많은 생화학자들을 통해서 입 증되어지고 있다 .3)4)5)6)” Fe 은 체내에 비교적 져온 양이 존재하나 · 미량원소 중에서 가장 찰 알려쳐 있고 많은 연구가 되어전 원소이 , 다 .8) 2.1 체내 함량과 분포 인체의 Fe 함유량은 체중의 0.004% 정도이며 연령, 성별, 영양 ..
건강상태, 신체의 Fe 저장상태에 따라 다르다. 태아의 체내에는약 3 00m g정도가 함유되어 있으나 접차 증가하여 성인에 있어서는 약 3~5 g이 함유되어 있다. Fe 은 체조직 내에 널리 분포되어 있으며 특히 혈액 내에는 다른 조직의 약 20 배 가량 분포되어 있다. 성 인 남자는 체 중 1kg 당 50mg , 여 자는 35mg 정도를 함유한다. 그 중 60~70% 가 hemo g lob i n 에 함유되어 있고 3% 정도가 my o - glo bin 속 에 촌재 한다. My o gl o bin 은 구조나 기 능이 혈액 에 있는 hemog lo bin 과 비 슷하나 전신을 순환하지 않고 근육조직 내 에 고정 되어 있다(체내 Fe 함량은 남자보다 여자가 더 적은데 이것은 혈 액 hemog lo bin 과 근육 my o gl o bin 의 농도가 낮고 Fe 의 체 내 보유 가 적기 때문이다). 약 2% 는 산소와 함께 작용하는 효소로 cy to- chrome, dio x y ge nase, hy d roxy la se 와 H2 아 와 함께 작용하는 pe roxid a se, . cata l ase 둥에 존재 한다. 현재 약 10% 정 도가 완전히 알려져 있지 않은 상태이나 po rph y r in 형태가 아닌 pe p tide 결합에 연결되어 있는 enzy m e p ro t e i n 인 것으로 추축되어지고 있다• 나머 지 는 간, 비 장, 골수 등에 fer riti n 과 hemosid e rin 형 태 로 처 장되 어 있다. Fe 은 혈액 속에 1. 0~1. 7mg %, 혈장 속에 0. 08~0. 07%, he- mog lo bin 속에 약 0.33% 들어 있다. 표 2.1 은 Fe 의 체내 분포도이며, 표 2.2 는 성인과 신생아, 그리
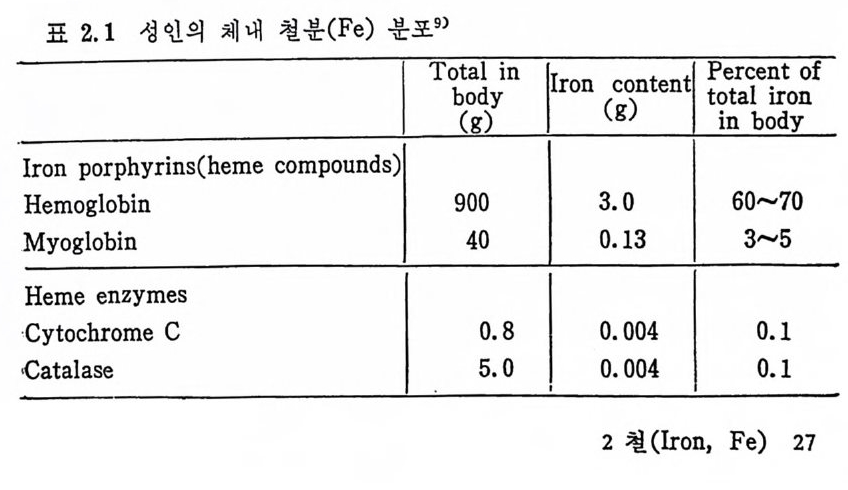 표 2.1 성 인의 체 내 철분 (Fe) 분포 9 )
표 2.1 성 인의 체 내 철분 (Fe) 분포 9 )
 Ot he r cy toc hromes
Ot he r cy toc hromes
 표 2. 2 성 인, 신생 아, 동물의 철분 (Fe) 함량 10)11)12)
표 2. 2 성 인, 신생 아, 동물의 철분 (Fe) 함량 10)11)12)
고 동물의 Fe 함유량을 표시한 것이다. 2.2 주요 기능 1) 적혈구는 Fe 이 들어 있는 색소 heme 과 단백질인 g lob i n 이 결합되어 이루어전 것으로 이 가운데 Fe 은 혈색소의 약 1% 에 지 나지 않지만 이것이 없으면 혈색소가 합성되지 못한다. Heme 에 있 는 po rph y ri n 은 아미 노산인 gly c ine 과 Krebs 회 로의 중간산물이 결합된 것이며 여기에 g lob i n 이 결합되어 합성된 것이 다. 적혈구 (er yt hroc yt e) 는 처음 형성될 때는 세포핵을 소유하며 비교 져 큰 형 태 로 존재 한다. 이 상태 의 적 혈구를 eryt hr oblasts 라고 하 며 접 접 성 숙함에 따라 주로 Fe 을 함유한 혈색 소인 hemog lo bin 에 의 해 구성 된다. 이 상태 의 적 혈구를 reti cu locy tes 라고 한다. Re tic uloc yt es 는 혈류로 이동되며 이때의 적혈구는 핵을 손실하여
성숙하게 되는데 이 과정에 Cu 가 관여하게 된다. 성숙한 핵이 없 는 상대의 적혈구는 산소를 각 세포충에 운반하고 생성된 탄산가스 를 체외로 방출하는 기능울 한다. 이때 혈색소는 산소와 연결되는 데 (chelati on ) 이 것 을 산화형 혈색 소 (ox y hemo g lob i n) 라 하고 조직 으로 이동되어 산소를 데어 놓은 것을 환원형 혈색소 (reduced hemog lo bin } 라고한다. 적혈구의 수명은 약 120 일 정도로 대단히 짧은데 이는 세포핵을 소유하지 않으며 자기생존을 위해 효소를 합성할 능력이 없기 때문 인 것으로 보여진다. 수명이 오래된 적혈구일수록 깨어지고 부서지 기 쉽다. 우리 체내에는 약 2,000 억 개의 적혈구가 있으므로 매분마다 1 억 5,000 만 개의 적혈구가 파괴되며 또 생성되는 셈이다. 기능이 소멀 된 적 혈구는 파괴 되 어 Fe 은 간과 비 장에 hemosid e rin 과 fer riti n 상대 로 처 장되 거 나 골수에 둘어 간 다음에 새 로운 hemog lo bin 을 형 성하는 데 재이용된다. 정상 성인의 경우 혈액의 양을 5,000m! hemog lo bin 농도를 15g /1 00ml 로 보면 총혈액 량에 대 한 hemog lo bin 함량은 750g 이 되 고 hemog lo bin Fe 은 750 X 0. 34% =2. 55 g이 된 다. 적혈구의 수명은 약 120 일 정도이므로 2.55-;-120=21mg 정도 의 Fe 이 hemo g lob i n 합성에 쓰이는 것이 된다. 정상적인 기능을 하는 골수는 hemog lo bin 의 적 혈구세 포의 생 산을 6 배 정 도 중가시 키 는 효과가 있으므로 최 대 한 1 일 100mg ~ 125mg 의 Fe 이 hemo- glo bin 합성 에 쓰이 게 된다. 2) 근육조직 내 의 Fe 은 근육의 색 소인 my Qglo bin 에 들어 있으 며 hemog lo bin 과 비 슷한 역 할울 한다. My o g lo bin 한 분자당 한 개 의 Fe 이 들어 있는데 이 는 hemog lo bin 에 서 산소의 공급을 받아 근 육내에 저장되었다가 근육내에서 ATP 가 형성될 때 사용된다. ATP 는 근육의 수축, 단백질, 지방, 당질 및 기타물질의 합성과정 둥 에너지를 필요로 하는 반응에 사용된다. 3) Fe 은 세 포내 mi toc hondria 에 서 산화환원 작용에 관여 하는 효. 소인 c yt ochrome 의 구성요소로서 산소와 결합하지 않고 호홉 연 쇄 에 서 전자를 전달하여 Fe2+~Fe3+ 로 산화 • 환원한다.
4) Peroxid a se 와 cata l ase 의 구성 요소로서 체 내 에 서 생 성 된 H202 를 제거하는 역할울 한다. 5) Fe 은 oxy ge nase 와 tra nsfe r ase 의 구성 요소이 다. 이 효소들 은 ph eny !a lanin e 과 tyro sin e 이 homog e nti sin i c acid 로 전환될 때 사용되 며 또한 try ptop h an 이 for my lk y n urenin e 으로 대 사될 때 Fe 이 필요하게 된다. 6) Hy d roxy la se(mono ox yg enase) 의 구성 요소로서 cy toc hrome p45 0 과 같이 해독작용을 한다. 7) Flavin enz ym e 의 구성 요소이 며 succi no dehy d rog e nase, aid e -hy d roxid a se, xanth i n oxid a se, choli no xid a se 둥이 여 기 에 속한다. 8) /3- carote n e 이 Vi tam i n A 로 전환되 는 과정 과 핵 산의 일부인 pu rin e 합성 과정 둥에 Fe 은 촉매 작용을 한다.
 2.3 대 사
2.3 대 사
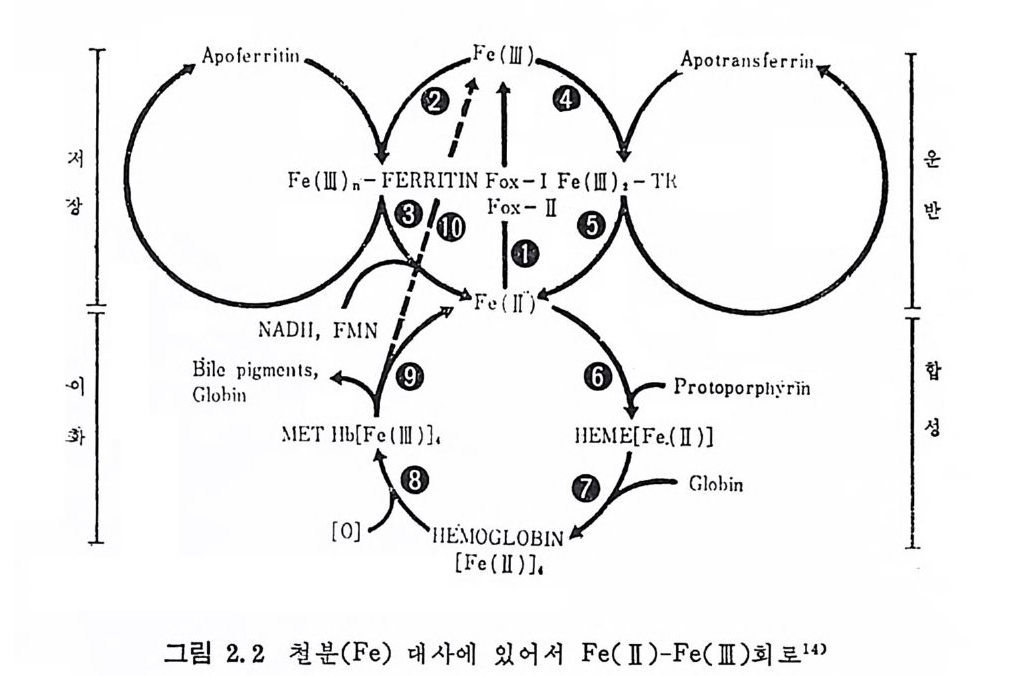
수있다. 그림 2.2 는 Fe 대사에 있어서 Fe(II)-Fe( JlI)회로이다.
 Ap o k r rIIV I ,tF cIIll ) 겹 VA p o I ra Is fe r
Ap o k r rIIV I ,tF cIIll ) 겹 VA p o I ra Is fe r
1) Cerulop la smi n( fe r roxid a se I )과 다몬 fer roxid a se 에 의 해 Fe2+ 이 Fe3+ 로 산화된다. 2) 처장; Fe 의 처장형태인 fe rr iti n 과 hemos i der in은 출혈에 의 한 갑작스런 Fe 의 손실을 방지하기 위하여 내부 Fe 처장물로 작용 한다. Fer riti n 은 소장분만 아니라 간장(약 700mg ), 비장, 그리고 골수에서도 발견된다. Fe 을 정 맥 으로 두여 하면 간장에 hemosid e rin 형 태 로 축적 되 어 있 는 것을 현미경으로 관찰할 수 있는데, 이것은 단백질과 공존하는 colloid 상 Fe 산화물 형 태 이 다. Hemosid e rin 의 Fe 함량은 중량의 35% 이다. Ferr iti n 은 Fe 을 가용형태로 처장하며 Fe 에 대한 찬화성이 각가 다론 g rou p의 분자로 되어 있기 때문에 단기간이나 장기간 동안 Fe 의 처정물로작용한다.
3) NADH 와 FMN 울 필요로 하는 fer riti n reducta s e s y s t em 에 의 해 Fe3+ 이 fer riti n 에 서 방출되 어 Fe2+ 로 환원된다. 성 인에 있어 서 혈청 Fe 의 약 0. 2~0. 4% 가 혈청 fer riti n 으 로 촌 재한다. 혈청 fe rr iti n 의 농도는 체내에 처장된 Fe 의 가장 민감한 척도가 된다. 4) 운반; Fe” 이 Fe3+ 으로 산화되는 반응이 혈청에서 일어나면, Fe3+ 은 tra nsfe r rin 과 복합체 를 형 성 하여 운반된다. 5) 적혈구나 그의 Fe 을 필요로 하는 물질에 Fe 을 Fe2+ 의 상대로 보급한다. 6) 합성 ; Hemog lo bin 이 나 my o g lo bin 의 합성 을 위해 Fe 은 Fe2+ 상대 로 pro to p o rph y r in 과 결합하여 heme(pr o to h eme X) 을 형 성 한 다. 7) Heme 과 단백 질 부분인 glo bin 이 결 합하여 hemog lo bin 을 형 성 한다. 체 내 Fe 의 2/3 는 hemog lo bin 에 존재 한다. 8) 이 화 작용 ; Hemog lo bin 분자는 활성 울 가전 단백 질이 라고 할 수 있으며 안정되어서 적혈구 생존기간 동안 활성을 갖고 산소의 운반에 사용된다. 적혈구의 생명이 다 되면 Hb 는 산화되어 Fe3+ 형태를 함유한 me t -Rb 로 전환된다. 2.3.1 홉 수 Fe 의 흡수 • 조절기전은 그 자체가 매우 복잡하기 때문에 아직까 지 명확히 알려쳐 있지는 않지만 주로 위와 소장 상부에서 이루어 진다. 음식으로 섭취된 Fe 은 약 10% 가 흡수되고 신체의 요구량 에 따라서 40% 까지 상승하기도 한다. 한때 많은 실험을 동해서 흡수기전에 대하여 옳지 않은 판단을 내렸었는데 그 원인은 생리적인 Fe 의 섭취가 아닌 과량의 약용의 함량을 석품에 사용하였으며 Fe2+ 과 Fe3+ 의 흡수기전이 완전히 다 르다는 것을 고려하지 않았기 때문이다. 또한, 음식물로 매일 섭취할 수 있는 Fe 량은 매우 소량이기 때 문에 장에서 얼마든지 환원된다는 사실도 입증되었다 .15 )1 6) Hahn17) 과 Gran i ck18) 이 내 세 운 〈점 막장애 (mucosablocks)> 가설은
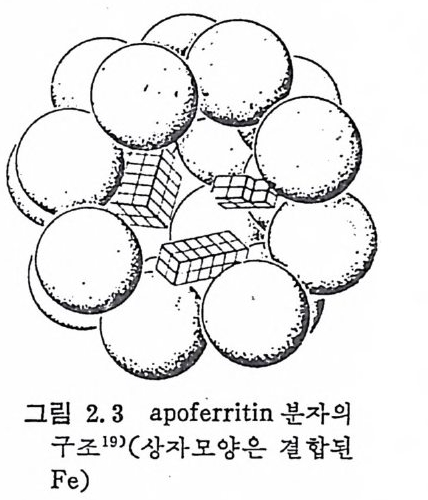
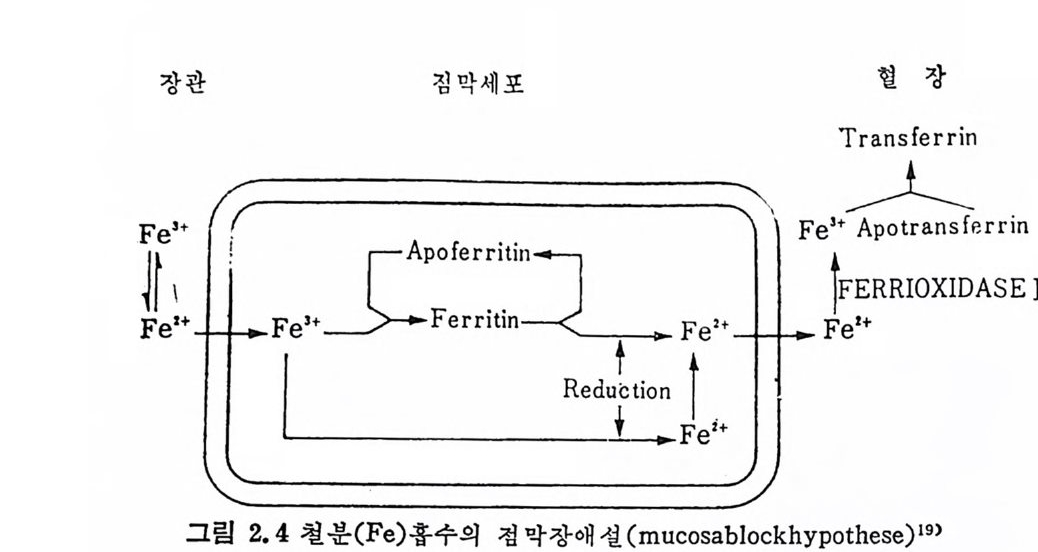
Fe 의 흡수기전으로 받아들여져 왔기 때문에 그 이의의 연구는 대 단히 부전했었다. 1940 년에 세 워 진 〈접 막장애 (mucosablocks) 〉가설이 란 그림 2. 4 에 서 보듯이 소장 상피세포에서 Fe2+ 이 단백질과 결합하여 Fe 결합 단백 질인 ap o fe r riti n 을 생 성 하고 아 ap o fe r rit in 의 홉수 조철인자 로 중요시 여 겨 졌 다. 이 ap o fe r riti n 은 그림 2. 3 에 서 보듯이 24 개
의 단백질과 5,000 개의 Fe 원자가 결합되어 있으며 전자현미경으로 이 구조를 볼 수 있다. 일단 접막세포에 들어간 Fe2+ 이 세 포막에 서 Fe3+ 로 산화되 면서 ap · ofe r rit in 과 결합함으로써 Fe 함유 단백질인 fe rr iti n 을 형성한다. 혈관막에서 Fe 은 산화 • 환원작 용에 의하여 Fe2+ 울 형성하여 혈 액 속으로 확산되 어 들어 가서 Fe3+ 로 산화되 어 tra nsfe r ri tin 과 결 합 된다. 이 가설에서는 Fe 에 대한
ap o fe rrit in 의 결합능력 이 Fe 의 그 다음 흡수를 제 한하고 Fe 과 포 합된 상태에서는 그 이상의 Fe 의 흡수는 일어나지 않는 것으로 생 각되어진다(그림 2.4). 또 한 가지, 신체 요구량에 따라 Fe 의 흡수가 중가하는 것은 산. 화 • 환원이 감소되었을 때에도 Fe2+ 이 Fe3+ 으로 산화과정을 거치 지 않고 직접 세포내로 흡수되어전다고 주장하였다. 이 가설을 위한 실험으로는 개에게 과량의 Fe 을 음석으로 섭취 케 한 후 홉수가 다 된 몇 시간 후에 방사선 동위원소로 된 Fe 을 섭취시켰는데 결과로는 더 이상 Fe 이 흡수되지 않은 것으로 나타 나 이 가설을 입증하게 했다 .17) 그러나 fe rr iti n 이 Fe 흡수의 조철인자로 관여한다는 가설은 다음 과 같은 여러 요인들이 입증되지 않는 한 받아들이기에는 불가능하 다는 것이 최근의 보고이다.
 그립 2. 3 apo f e r riti n 분자의
그립 2. 3 apo f e r riti n 분자의
 장관 침막세포 힐 장
장관 침막세포 힐 장
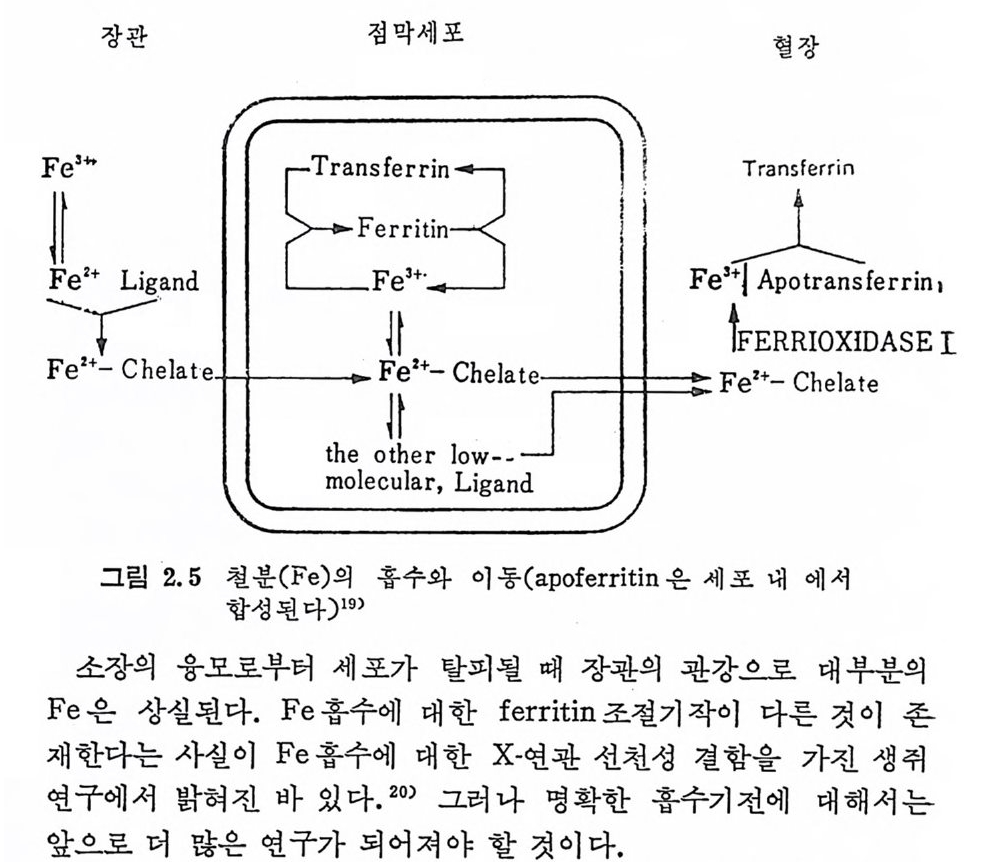
® Fe 이 Fe2+ 형태로 상피세포를 통과한다는사실을 실험을 동해 입증하지 못했다. ® 소장접막과 혈관에서 일어나는 산화 • 환원작용을 입증하지 못 했다. ® Fe 의 흡수는 과량의 fer riti n 를 두여 했을 때 감소되 거 나 중량 되지 않았다. @ 식품으로 몇 십 배의 Fe 을 두여했을 때에도 Fe 의 흡수는 계 속되고 가설대로 ap o ferr itin이 조철인자 기능을 수행하지 못하고 흡수가 멈추지 않았다. 근태에 Fe 의 홉수기전에 관해서 새로운 연구 실험결과가 발표되 고 있다 .14) Fe 은 먼처 장벽에서 에너지에 관계없이 접막세포에 홉수되고 혈 장으로 이동된다(그립 2.5). 이때의 Fe 이 이온의 형태인지 미립자 인지 혹은 음석이나 소화액에 연결된 chelate 형태인지는 아칙까지 완전히 규명되어 있지 않다• 접막세포에 들어간 Fe 은 접막 세포로부터 혈액으로 Fe 이동을 조철하는 1 개 또는 그 이상의 특이 운반체와 결합된다(운반체에 결합될 수 있는것 이상으로세포내에 들어가는 Fe 은 fe rr itin에 도 쉽될 수 있을 것이다). 그러므로 소장 fe rr itin은 홍수의 조철물이
아니 라 처장물로 작용하는 것으로 보여 진다. 취를 이용한 실험에서 보면 접막세포에 의하여 흡수된 Fe 은 일 부분만이 혈액으로 이동된다.
 장관 점막세포 혈장
장관 점막세포 혈장
1972 년 B j orn-Rasmussen15) 과 그의 동료들이 발표한 Two-Pool- Model 은 전체적인 Fe 흡수를 입증해 주는 좋은 실험이다. 이는 두 po ol 중에 서 한 po ol 에 는 Fe 이 무기 물과 결합되 어 , 다론 po ol 에 서는 Fe 이 유기물과 결합되어 있다고 선명하여 무기물과 결합된 Fe 은 i on 형대로 장 안에서 여러 흡수조건과 인자들에 의해서 흡수가 수행된다. 반면에 유기물과 결합된 Fe 은 p H 와 밀접한 관계가 있을 분 다 론 흡수조건 인자들과는 무관하다. 이것을 실험으로 입증하기 위해
저 두 방사선동위원소인 59Fe 과 55Fe 을 닭의 혈액에 섞어 옴석불과 함께 섭취하게 함으로써 각 p ool 의 흡수율도 관찰할 수 있으며 두 p ool 에서 흡수된 Fe 로써 총 Fe 의 흡수량도 알아낼 수 있었다. 또한 이 실험에서 Fe 의 섭취논 Fe 함유식품을 단독으로 섭취하 는 것보다 일반식이에서와 같이 여러 가지 식품이 혼합된 식이와 함 께 섭취할 때가 훨씬 흡수가 좋다는 결론도 얻었다. 다음은 Fe 의 흡수에 영향을 미치는 인자들이다. 〈 Fe 의 홍수를 증진시키는 인자〉 1) 신체의 Fe 필요량 혈액내에 Fe 를 결합하지 않은 t rans ferr i n 의 양이 증가되면 다량 의 Fe 이 혈액에서 처장 Fe 로 이동되었음을 암시하며 동시에 Fe 의 흡수율이 증가되어 혈액 내의 Fe 량을 일정하게 유지하려고 한 다. 일반적으로 hemo g lob i n 의 양이 정상치인 경우에는 섭취하는 Fe 의 2~10% 만 흡수하나 hemog lo bin 의 양이 극히 저 하되 었 을 때 에 는 Fe 의 흡수율이 증가되어 섭취량의 60% 까지 흡수된다. Fe 의 흡수율을 보기 위하여 방사선 동위원소 59Fe 을 사용하여 신체의 r-ac ti v ity를 측정한 결과 건강한 성인남자는 6.1 土 5.2% 의 Fe 흡수율을 보였고 Fe 이 결핍된 부인에게서는 78 土 9% 의 흡수율 울 보였다 .21) 그러므로 성장기의 어란이, 월경기의 여자, 임신부, Fe 결핍성 빈혈환자, 그리고 pyri d o xin 결핍시에는 건강한 성인남 자보다 훨씬 Fe 흡수율이 높아진다(표 2. 3). 2) 위 및 소장내의 상태와 Fe 의 형태 소장의 상부, 죽 십이지장에서 대부분의 Fe 이 흡수되는데 그것 온 누 가지 형 태 로서 제 1 철(fe rrous, Fe2+ ) 및 제 2 철(fe rr i c Fe3+) 이 모두 홉수되기는 하나 제 2 철의 형태에서 제 1 철의 형태로 환원되 었을 때 Fe 은 소장에서 최대한으로 흡수된다. 계 2 철은 위의 산도와 소장의 상부가 계속 산성을 유지하고 있을 때에 제 1 철로 쉽게 환원되며 산성용액은 제 1 철을 용해하여 홉수 불 돕는 작용울 한다. 위액에서는 Fe 과 결합한 분자량이 560,000
인 g l y co p ro t e i n( gas t ro f err i n) 을 볼 수 있 었 다. 22) 사 람에 있 어 서 Fe 과 위액이 결합된 양은 1 1. 3m g /100ml 로 측정되었다 .23) 3) Ascorbic ac id 함량 소화기관 내의 산성용액분만 아니라 식품 내에 함유되어 있는 -as corbic ac id 도 제 1 철로 환원되 는 것 을 도와 Fe 흡수를 축전시 킨 다. Fe 흡수에 관한 여러 실험결과에 의하면 Fe 결핍성 빈혈환자에 게 Fe 섭 취 를 증가시 키 는 것 보다 ascorbic ac id 의 양을 중가시 킬 때 Fe 홉수가 더 효과적이었다. 그러므로 빈혈치료에는 Fe 두여와 동시 에 ascorbic ac id 를 같이 섭 취 하도록 권장하고 있 다. 음식물을 과일쥬스와 함께 섭취했을 때 Fe 의 흡수가 증가됨을 보였 는데 24)25) 이 는 쥬스의 ascorbic ac id 의 함량 때 문인 것 으로 생 각된다.
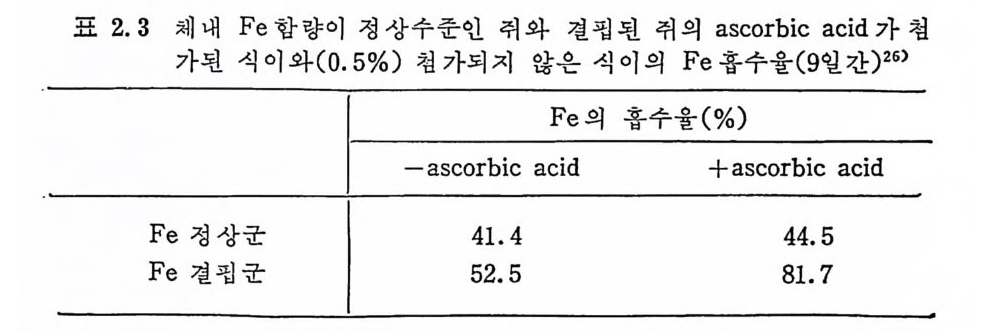 표 2.3 체내 Fe 함량이 정상수준인 쥐와 결핍된 취의 ascorbic a ci d 가첨
표 2.3 체내 Fe 함량이 정상수준인 쥐와 결핍된 취의 ascorbic a ci d 가첨
체내 Fe 함량이 정상인 쥐와 결핍된 쥐에게 ascorbic a ci d 를 식 이 (0.5% )로 섭취시켰을 때와 시키지 않았을 때의 Fe 흡수율은 ascorbic acid 의 섭 취 군의 흡수율이 섭 취 시 키 지 않은 군보다 높았 으며 체내 Fe 함량이 정상인 쥐보다 결핍된 쥐의 Fe 홉수율이 현처 히 증가했다(표 2. 3). 4) 유기산 함량 Cit ric ac id, lacti c ac id, pyru vic ac id, succ ini c ac id 와 같은 유 기 산도 Fe 의 흡수를 중전시 킨다. 5) 급원석품 동물성 석품에 함유되어 있는 Fe 은 10~30% 까지 흡수율을 보이 는 한편 식물성 식품내에 함유되어 있는 Fe 은 2~10% 의 흡수율을
보이고 있다. 표 2.4 에서는 고기 섭취 가 각 석품의 Fe 흡수에 미치 : 는 영향을 나타냈다.
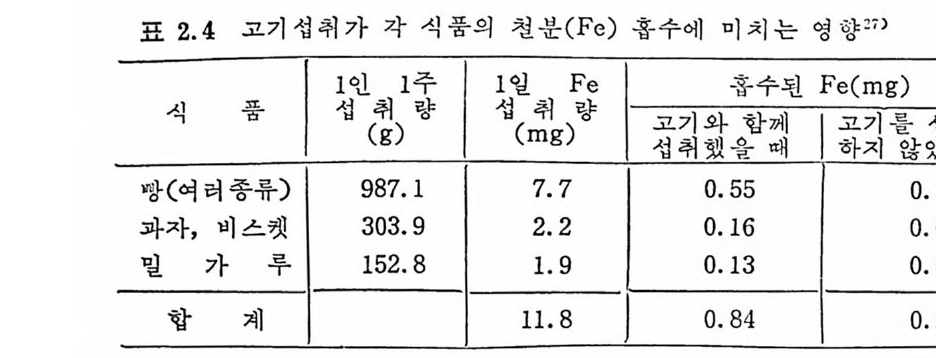 표 2.4 고기 섭취가 각 식품의 천분 ( F e) 흡수에 미 치는 영 향 2; )
표 2.4 고기 섭취가 각 식품의 천분 ( F e) 흡수에 미 치는 영 향 2; )
동식물성 식품을 같이 섭취하면 식물성 식품 중의 Fe 의 홉수 가 증가되는데 이는 단백질에서 분해된 아미노산 특히 c y s t e i ne 이 Fe 울 효과적으로 용해하여 흡수를 촉진시키기 때문이다. 그 이외의 Fe 의 좋은 섭취 방법의 한 예로서 곡류와 동물내장과
 겁홉의 Fe 2m싼g 시2금mg치 3검-4정m공g 식 2옥전-·4수성m수 g 식 I품-무I 7우m g 2 겨밈 m g 3-4·m。 g Fe3rm r git i n 송3m아g 자간 동 산선l-성산2 생m식산g 중 3gI I1- t-.. J).. bm 4 imo I1 - g 3숭 섬-모4아 기 지l : 합계
겁홉의 Fe 2m싼g 시2금mg치 3검-4정m공g 식 2옥전-·4수성m수 g 식 I품-무I 7우m g 2 겨밈 m g 3-4·m。 g Fe3rm r git i n 송3m아g 자간 동 산선l-성산2 생m식산g 중 3gI I1- t-.. J).. bm 4 imo I1 - g 3숭 섬-모4아 기 지l : 합계
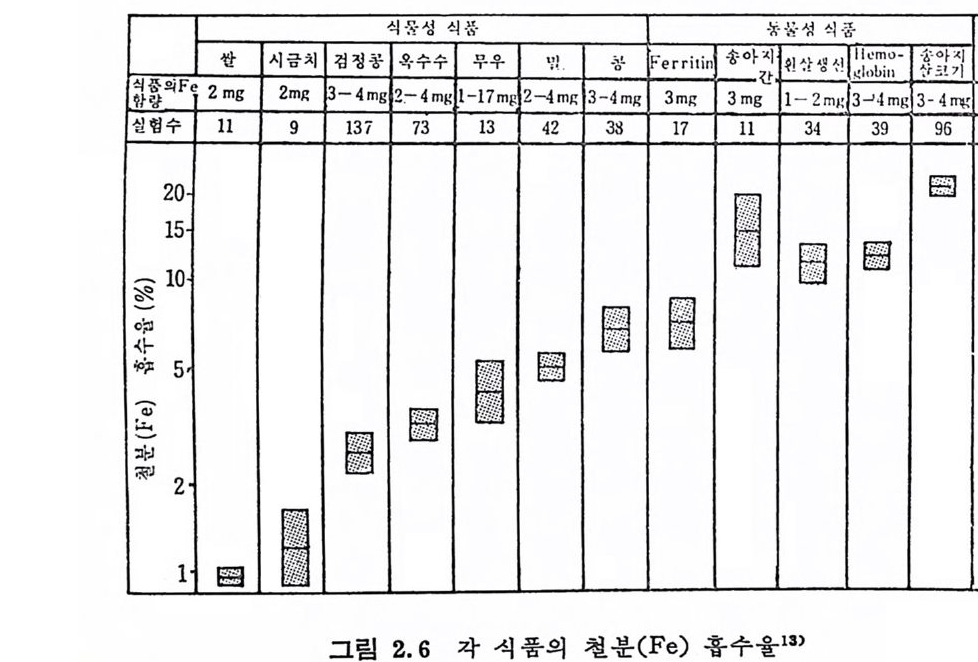
Fe 을 함께 섭취하는 것을 들 수 있다. 또한 육류 생선 과일이 함 유된 일반적인 석사는 nonheme Fe 의 이용에 현처한 효과를 보이 고 있다. 그림 2.6 은 각 식품의 Fe 흡수율이다. 6) 섭취량 식사내에 함유된 Fe 량이 높울수록홍수율은 저하되며 Fe 흡수율 은 Fe 섭취량에 반바례한다 .49) 그러므로 Fe 의 흡수를 위해서는 소 량씩 여러 번으로 나누어 섭취하는 것이 효과적이다. 7) Vi tam i n 함량 Ni ac in, pa nto t h enic ac id 둥의 vit am i n 은 Fe 의 흡수를 증진시 킨다. 8) 아미노산 함량 Hi st i di n e , lys in e , cy s te i n e , argi ni n e , try p top h an 은 Fe 의 흡수 를중전시킨다. 9) Fe 의 형태 Heme-Fe 은 무기 Fe 에 바 해 흡수가 좋다. 〈 Fe 의 흡수를 저해하는 인자〉 1) 신체의 Fe 필요량 Trans f err i n 과 Fe 결합이 포화상태가 되면 이는 체조직에서 Fe 의 필요가 감소되었음을 의미하는 것이 되고, 따라서 Fe 의 흡수율도 감소된다. 2) 위와 소장내의 상태 노안과 무산중의 악성 빈혈 환자에게는 흔히 Fe 흡수가 다;,; P0 '(c') . 볼수있다. 3) Diet a ry fibe r 의 함량 Diet a r y fibe r 를 많이 함유하고 있 는 석 사를 하면 Fe 의 흡수융 이 저하된다고 한다. 그 예로 밀기울울 음석에 첨가시켜 인체에 섭 취시킨 결과흡수율이 감소했다. 그러나 많은 감소울은 아니었다 .26) 4) Phy tic ac id, oxali c aci d, tan nin 곡류 중에 ph y tic a ci d 는 m y o i nos it ol 핵에 인산이 결합된 유기산 으로 Fe 과 결합하여 불용해성인 ph y tic a ci d 의 복합체를 형성하
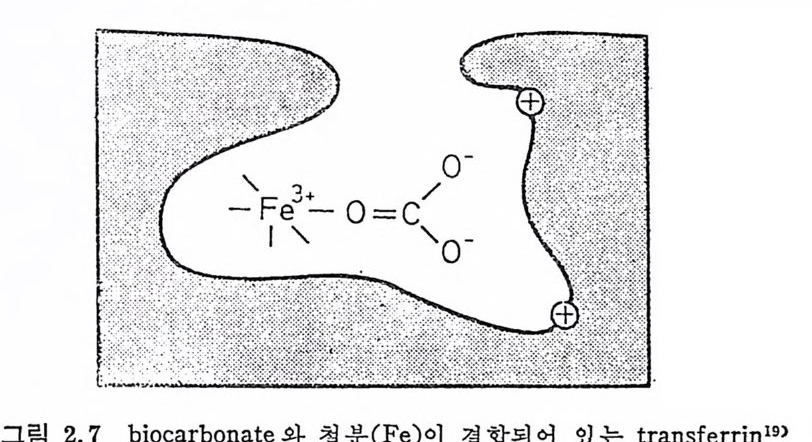
여 Fe 홍수의 장애를 일으킨다. 정상적인 군형식에 함유되어 있는 ph y tic a ci d 의 양은 Fe 흡수에 큰 지장을 초래하지는 않으나, 몽밀, 귀리 둥 cellulose 가 많은 식 품으로 식사가 구성되어 있을 때는 ph y tic a ci d 로 인해 Fe 흡수의 지장을 받게 된다. 시 금치 에 들어 있 는 oxalic ac id 나 차에 들어 있 는 tan nin 도 Fe 과 불용해성인 복합체를 형성하여 홉수를 저해시킨다 .50)5 1) 5) 지 방변 증 (s t ea t orrhea) 변내에 비정상적으로 다량의 지방이 배설되는 중세가 있을 때에 는 Fe 흡수에 지창이 있다. 6) 무기질 함량 인 (P) 과 칼슘 (Ca) 은 Fe 과 결합하여 불용성 침 전물을 만들어 Fe 의 홍수를 나쁘게 한다. 그러나 Ca 이 공촌하면 P 과 Fe 이 결합하 기 전에 P 과 Ca 이 결합하므로 Fe 의 흡수롤 간접적으로 향상시키 게 된다. 또한 많은 양의 Co, Zn, Cd, Cu, Mn 은 Fe 와 경쟁적인 작용을 하여 흡수를 억 제한다 20)59)62)(3. 8.1 참조. ). 7) 당질 함량 당질은 흡수를 저해시키는 인자로서 lacto se, sucrose, glu cose, ·sta rch 순으로 처 해 한다. 29) 그러 나 sta rch 와 sucrose 가 Fe 흡수에 아무런 영향을 미치지 않는다는 설도 있다 .30) 8) 달걀 달걀은 Fe 의 흡수를 감소시 킨다. 1968 년 Elwood 는 빵에 달걀울 첨가한 결과 Fe 홍수율이 14% 에서 l% 로 감소했음을 밝혔다 .31) 2.3.2 혈장내 이동 접막세포로부터 방출된 대개의 Fe 은 주로 Fe2+ 형태로 문백혈로 들어간다. 혈장에 있어서 Fe 따온 신속히 Fe3+ 형태로 산화되어 특 수 Fe 과 결합, 단백질인 t rans fe rr i n 으로 도입된다. 이 단백질은 단백 질 1 분자당 2 원자의 Fe3+ 와 결합하여 적 색 의 Fe3+ 단백 질 복합 물을 형성할 수 있다.
Trans f err i n(s i dero p h ili n) 은 분자량이 77, 000 이 며 5. 3 %의 단백 질 을 함유하고 있는 당단백질이다. 이 당질은 그 말단이 N-acety ln - ,eu ami ni c ac id( sia l ic a ci d) 의 분자로 끝나는 동일 한 2 개 의 분자 곁 가 치를 갖는다 .32) 당단백질인 t rans t err i n 은 전자현미경에서 /3i-g lobu li n 과 함께 결 합된 20 여 종을 볼 수 있 다. 각 tra nsfe r rin 분자는 1 개 의 bic a rbon-ate 이 온과 Fe3+ 이 결합되 어 있 다(그립 2. 7). 점 막세 포로부터 Fe 방출은 Fe 에 의 한 tra nsfe r rin 포화도가 낮을 때 촉진된다. Cu 결 합 단백 질 인 cerulop la smi n 은 혈장에 있 어 서 Fe2+ 울 Fe3+ 로 전환시 키 는 촉매 활성 을 갖고 있으며 따라서 tra nsfe r rin 에 의 한 Fe 도입 속도를 촉진시 킨다.
 /o-
/o-
인체 혈장은 또한 Fe 의 산화를 촉매 하는 황색 의 cup ro p ro te i n {ferr oxid a se II )을 함유한다. 33) 정 상적 인 상황에 서 tra nsfe r rin 에 결합된 거 의 모든 Fe 은 골수 에서 재빨리 흡수된다. Transfe rrin 에 결부된 Fe3+ 울 이 용할 수 있는 것은 망상적 혈구 분이지만 망상적혈구와 성숙적혈구는 다 같이 유리상태의 Fe3+ 울 흡수할 수 있 다. 그러 므로 tra nsfe r rin 은 혈장 Fe 을 hemog lo bin 이 활발하게 만들어지는 세포내로 돌려준다.
혈 액 의 tra nsfe r rin 의 농도는 200~ 300mg /1 00ml 이 며 성 인의 t rans f err i n 의 총량은 7~15g 이 다. Transfe r rin 은 운반자 기 능 이 의 에 도 신체 조직 에 유독한 영 향을 끼 칠 수 있는 free Fe 이 온을 완충작용을 하므로서 보호해 주며 Fe 이 뇨 속에 섞여서 배설되는 것을 막아 주는 작용울 한다. Trans· ferr i n 은 많은 양이 간에서 생성되어 혈액의 회로를 지나며, 그 반 감기는 8~10 일이다. 남성 의 혈장에 서 단백 질과 결합된 Fe(PBI, Prote i n - Bi nd in g Iron) 의 정 상 함량은 90~l80µg /1 00ml 이 고 여 성 의 경 우 70~150µg / 1 00ml 이다. 혈액의 Fe 량은 3~4m g이다. 그러 나 Fe 을 결 합할 수 있 는 전체 능력 (TIBC, Tota l Iron-Bi nd in g Ca pac ity)은 남녀 의 경 우 동일하며 300~360µg /1 00ml 이 다. 이 것 은 정상적으로 혈청의 Fe 결합능력의 30~40% 만이 Fe 이동에 사용 되 고 Fe 이 붙지 않은 sid e rop h il in, 즉 불포화 Fe 결합능력 (UIBC,.
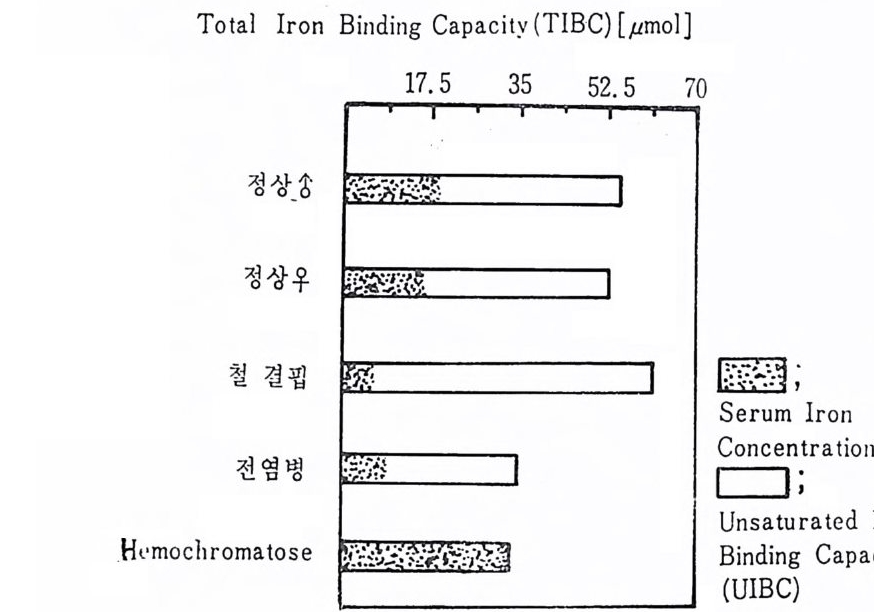 Tota l Iron Bin d in g Cap ac it y (TI BC) [µmol]
Tota l Iron Bin d in g Cap ac it y (TI BC) [µmol]
그립 2.8 정상인과 질병에 걷란 환자들의 혈청 철분 (Fe) 의 불포화 철분 결합능력 (Unsatu rate d Iron Bin d in g Ca p a city)과 전체 철분 결 합능력 (Tota l Iron Bin d in g Cap a c ity) 19'
'l.Jm atu r ate j Iron Bin d in g Ca p ac ity)은 전체 의 60~70% 이 라는 것을 지사한다. 혈장에서 결합된 Fe 의 양은 주 • 야간 변호H 층 나타내어 24 시간 동 안 60µ g /100ml 로 보고되었다. 그 최저치는 저녁 취침 후 2 시간 경 에 그리고 그 최고치는 이로부터 5~7 시간 후, 죽 아침에 나타나 게 된다 .9) Fe 결핍성 빈혈에서 혈장의 단백질에 결합된 Fe 은 낮은 데 비하 여 전체 Fe 결합능력은 상승하는 경향이 있고 불포화 Fe 결합능력 이 정상치보다 더 높게 된다. 간장 질환에서는 결합된 Fe 과 혈장의 전체 Fe 결합능력의 비율
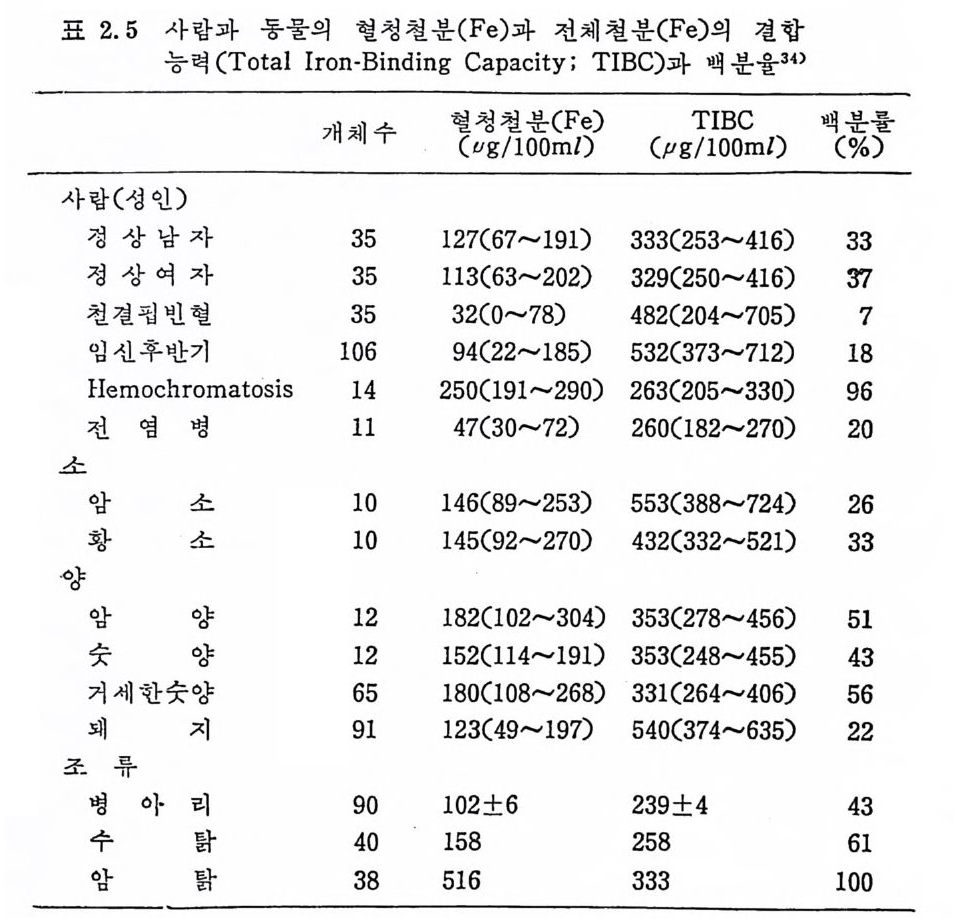 표 2. 5 사람과 동물의 혈청철분 (Fe) 과 전체철분 (Fe) 의 결합
표 2. 5 사람과 동물의 혈청철분 (Fe) 과 전체철분 (Fe) 의 결합
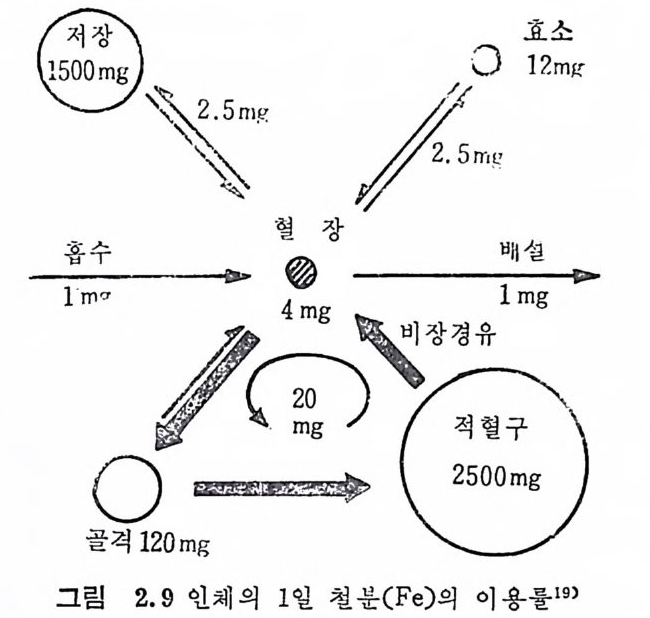
은 청상치와 벌로 차이가 없다. Hemochromato s e(hemosid e rin 침 착증)에 서 는 현저 한 차이 를 보인 다(그립 2.8). 비장 등에서 적혈구논 결국 파괴되어 g lobu li n 은 아미노산으로, pro to p o rph y r in 은 담즙색 소로 바뀌 게 되 고 Fe3+ 은 Fe2+ 형 태 로 전 환된 후 재 이 용되 어 hemog lo bin 회 로를 완성 하게 된다. Fe 을 재이용한 Fe 은 약 27m g이 하루에 쓰여지는데 이중 75% 는 hemog lo bin 의 형 성 에 사용된다. 그 중 약 20mg 은 적 혈구의 분 해로부터 얻어치며 극소량은 새로 흡수된 Fe 이고 나머지는 저장된 Fe 에서 조달된다. 정상적인 상태에서는 혈장 Fe 과 처장 Fe 의 교 환은 비교적 느리게 진행되며, 급성출혈이 있은 후에는 혈장내 Fe 함량이 수주간 낮게 유지되는데 이는 저장분으로부터 Fe 의 동 · 원이 느리다는 것을 시사한다. Me t -Hb 에서 풀려나온 Fe3+ 는 Fe2+ 의 형태를 거치지 않고 직접 fer riti n 형성에 쓰인다. 사람과 동물의 혈청 Fe 와 전체 Fe 결합능 · 력을 나타낸 것은 표 2.5 이다. 2.3.3 이 용 Transfe r rin 과 결 합된 약 70 一 90 %정 도의 Fe 은 hemog lo bin 을 합 성하기 위하여 골수의 적혈구 안에서 사용되며 그 나머지는 효소, 조효소의 생합성에 쓰이고 일부는 저장된다. 처음에 세 포핵 을 소유하여 비 교적 큰 형 대 로 존재 하는 basop h il en e eryt br o blast 에 서 적 혈 구가 핵 을 소실하고 reti cu locy te 형 태 로 되 면서 Fe 을 사용하는 정확한 기전은 아직 알려져 있지 않다. Fe 은 아주 중요한 tra ce elements 로서 수명 이 다 된 hemog lo bin · 으로부터 유리된 Fe 은 모두 배설되지 않고 그 대부분은 신체내에 서 재이용되는데 그 좋은 예로 인체 실험에서 Fe 방사선 동위원소 를 정맥으로 투여한 후 12 년 후에도 Fe 방사선 동위원소를 발견할 수 있었다 .35) 그림 2.9 에서 보듯이 신체는 1m g의 Fe 을 흡수 • 배설함으로써 철 분대사의 평형을 유지할 수 있다. 혈장 Fe 은 4m g으로써 Fe 전체
태자의 중심부 역할을 한다.
 二\\〈 /// 3 : m麟g
二\\〈 /// 3 : m麟g
정상 조건 하에서 적혈구의 수명은 120 일로 회전하는 적혈구는 미 창에서 0.8% 정도 기능이 소멸되고 골수에서 새로 합성된다. Hemo g lob i n 과 결합된 Fe 함량은 lml 혈액이 0.5m g이타고 할 때 전체 혈액 인중에 Fe 은 정상 조건하에서 성인의 2.5 g이다 그러므 로 Fe 2. 5g 의 0. 8% 즉 20mg 이 매 일 hemog lo bin 회 로에 사용된 다. 또한 5m g의 효소와 저장 Fe 도 함께 계산된다면 매일 25mg 이 이용된다고 보겠다. 혈장내 Fe 수준은 동적 평형의 결과이며, 혈장으로부터의 Fe 는 · 몇 개의 대사 회로에서 재분비되었다가 각 회로는 Fe 을 혈장 Fe p ool 로 되돌려보냅으로서 끝을 맺게 된다. 양적으로 가장 중요한 회로로 Fe 은 hemo g lob i n 합성에 쓰여지는 데 혈장 Fe 은골수, 적혈구, 노쇠한 적혈구, 그리고 다시 혈장으로 이전된다. 이것을 〈 hemo g lob i n 회로〉라고도 한다. 2.3.4 처 장 Hemo g lob i n 과 활성을 가전 단백질에 쓰이지 않는 Fe 은 제일 먼
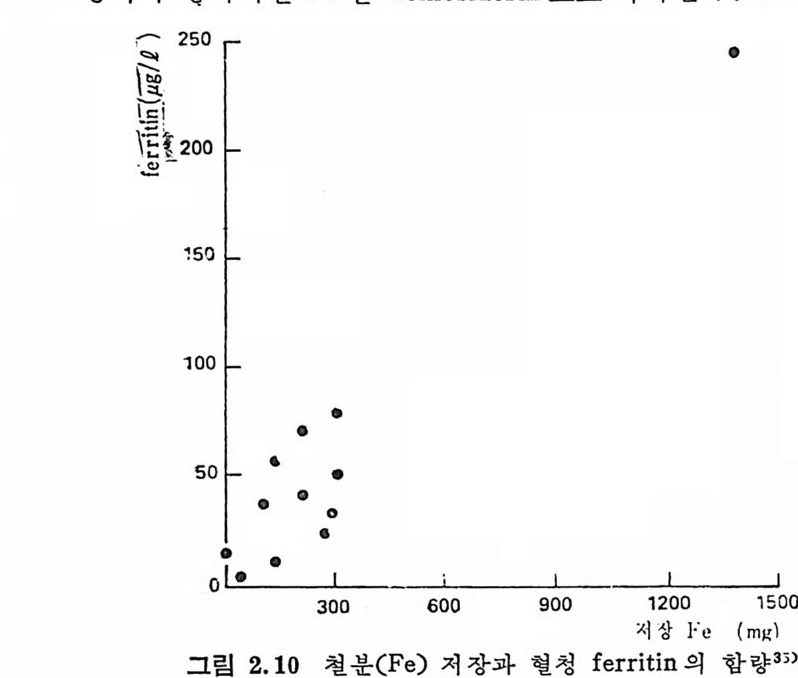
처 fer riti n( Fe 전체 무게의 25% 차지)의 형태로 처장되고 Fe 처장 능 력 이 궁 가되 면 Fe 은 hemosid e rin 으로 축적 된다(그립 2. 10).
 ' (u늄 250200 •
' (u늄 250200 •
처장장소는 주로 간의 pa renchy m 세 포, 골수, 비 장과, 간의 re tic uloendo t he li al 의 세포이다. 이 처장 Fe 은 출혈시나 적혈구 형성시에 운반 이용된다. 건강한 성인은 1. 5 g의 Fe 을 저장하며 ·fe r riti n 에 서 Fe 방출은 효소작용에 의 한다. 몇 년 전만 해 도 pu rin e 대 사의 효소 xanth in e oxid a se 에 의 해 서 fer riti n 의 Fe 이 방출된다고 생 각했는데 , 요즈음은 NADH 와 FMN 을 팔요로 하는 fer riti n reducta s e sy s te m 에 의 해 Fe 이 fer riti n 에 서 방출된다고 한다(그 림 2. 11). 처장 Fe 을 측정하는 데는 여러 가지 방법이 있는데 가장 정확한 방법은 여러 차례의 혈액검사를 하는 것이다. 혈액에는 전체의 저 장 Fe 의 형태가 전부 모여 있기 때문이다. 그러나 병원에서 손쉽 게 측정하기에는 여러 가지 어려운 접이 많다. 병원에서 측정하는 방법이 있으나 고도의 숙련된 기술이 필요하다.
최근 뇨에서 저장 Fe 검사를 하고 있으나, 이 방법도 한 가지 형 태의 저장 Fe 만 볼 수 있다는 단점이 있기 때문에 방사선 동위원소 를 정맥으로 주사하여 측정하는 방법도 시도되고 있다.
 Sllll Ce ll Fe ” 三H Feme jo srtiidt ie n r in F투 三〈M:y o g: lo bin ) ? me
Sllll Ce ll Fe ” 三H Feme jo srtiidt ie n r in F투 三〈M:y o g: lo bin ) ? me
2.3.5 배 설 사람은 한정된 범위 내에서 Fe 을 흡수 배설하는데 이것은 혈장내 의 Fe 이 사구체에 의하여 여과되기 어려운 단백질 결합물질로 촌 재하기 때문일 것이다. 그러나 다량의 Fe 이 오줌으로 배설되는 것 온 ,::.J:-백뇨 중에서 일어날 수가 있다. 성인 남녀가 정상적인 조전 하에서 배설하는 Fe 은매일 0.5~1mg 인데 대 변으로 0. 5mg , 오줌으로 0.1mg , 그리 고 담줍과 땅으로 0.3~0.4m g이 배설된다. 대변으로 배설되는 Fe 은 소장 융모로부 터 세포가 탈피될 때 상실되는 것과 흡수된 Fe 이 문백혈로 보내 지기 전의(엄격한 의미에서는 흡수만 되고 체내에서 사용하지 못했 던) Fe 을 포함한다. 다량의 Fe 손실온 출혈에 의해서 hemo g lob in을 손실할 때라 할 수 있 다. Hemog lo bin 1mg 은 3. 4µg Fe 윤 함유하며 , lml 혈액 은
150mg 의 hemog lo bin 을 함유하고, 0. 5mg Fe 을 함유한다. 월경 사 는 25~60ml 정도의 혈액 손실로 한 달에 약 12.5~30m g의 Fe 을 배설한다고 하겠다. 임신기간 동안 모체가 태아에게 주는 Fe 은 300mg 정도이다. 출 산시 손실과 수유기간 동안의 모체로부터의 손실은 매일 0.5mg 정 도이다. 그러나 이 기간 동안의 Fe 손실은 임신기간과 출산후 수 개월간 정지된 월경에서 보충할 수 있다. 2.4 권장량 하루에 필요한 Fe 의 양은체의로손실되는 Fe 의 양을 식사중의 Fe 이 어느 정도 대치할 수 있는가 하는 것을 측정함으로써 결정된다. 일반적으로 건강한 성인남자와 페경기의 여자가 하루에 배변하는 Fe 의 양은 1. 0m g이다. 월경으로 인하여 손실되는 Fe 의 양이 하 루평군 0.5~1mg 정도이므로 가임연령의 여자는 남자나 페경기의 여자보다 많은 양의 Fe 이 필요하다. 수유부인 경우는 수유로 인한 Fe 손실도 고려하여 보충해야 한다. 의상에 의한 출혈 후 적혈구의 hemolys is 등이 있는 경우, 임신 후반기, 성장이 왕성한 유아, 사 춘기의 남 • 녀 및 가임기간의 여자에서는 필요량이 보충되어지지 않으면 Fe 결핍성빈혈이 나타난다고 보고되었다. 보건사회부의 국민 영양 섭취 실태조사에 의하면 우리나라는 곡 류를 주석으로 하여 총 섭취 에너지의 80% 이상이 당질이며 또한 섭취된 Fe 의 대부분이 식물성식품에서 얻어지는 실정이므로 ph y - t a t e 와 같은 화합물에 의한 Fe 흡수의 처해가 큰 것으로 추정된다. 일반적으로 건강한 성인 남자와 페경기의 여자가 하루에 체의로 배설하는 Fe 의 양온 약 1. 0m g이며 식사중에 포함되어 있는 Fe 의 흡수율은약 10% 로추정하여 하루에 10m g의 Fe 을섭취하도록권 장한다. 1975 년에 우리나라의 FAO 에서 제정한 Fe 권장량은 월경으로 안 한 Fe 손실을 13 세부터 고려하여 정했으나 실제로 초경을 11~13 세 사이에 시작한 여학생이 대상중에 약 15% 나 된다는 보고가 있으므 .
로 이번에는 더욱 안전한 범위를 정하기 위하여 10~1~] 여자에셔 부터 Fe 18mg 을 섭 취 하도록 권장량을 개 정 하였 다. 37) 또한 13~15 세 남자는 성 장이 왕성 하고 정 상적 인 hemog lo bin 양 울 유지하기 위해서 이 기간 동안 적절한 Fe 저장을 할 수 있도록 Fe 18m g을 섭취하도록 개정하였다•
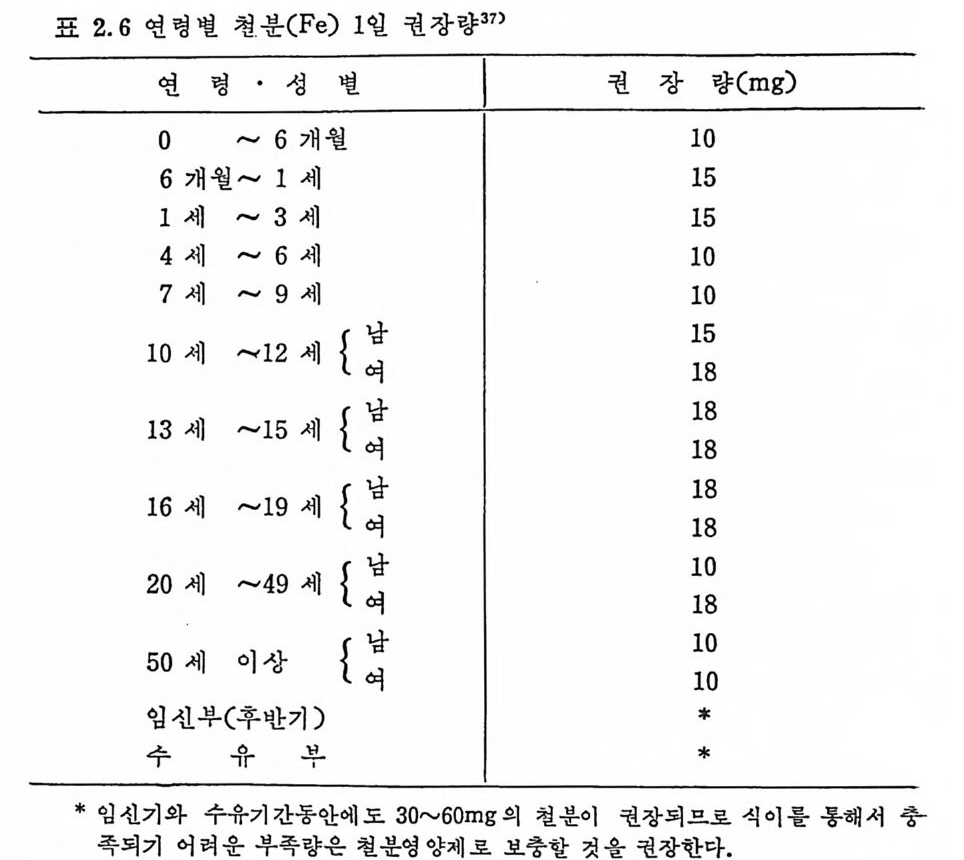 표 2.6 연령별 천분 (Fe) I 일 권장량 37)
표 2.6 연령별 천분 (Fe) I 일 권장량 37)
특히 임신부의 경우는 기초적인 Fe 의 생리적 손실분 아니라 임 신에 의한 적혈구의 증가와 태아 및 태반에 필요한 Fe 분만시의 출혈 둥에 의 한 Fe 의 손실동을 고려 하여 하루평 군 Fe 2. O~4. 0mg 이 필요하므로 특히 임 신 후반기 와 수유부는 하루 30~60mg 의 Fe 율 섭취할 것을 권장한다 .37) 물론 이 권장량은 섭취하는 식품으로. 는 충족되기 어려우므로 Fe 을 함유한 영양제로 보충함이 좋다.
2.5 결핍증 2.5.1 Fe 결핍성 빈혈 Fe 결핍성 빈혈은 처개발국, 개발도상국, 공업국에서도 찾아볼 수 있는 질환으로 전세계 인구의 20% 정도이다. Fe 결핍성 빈혈증 온 처색소성 소적혈구형이다. Fe 결핍성 빈혈이라고 진단하는 데 는 여러 가지 겁사결과에 의거한다. 빈혈의 중제 중 Fe 결핍으로 인한 것은 Fe 결핍성 빈혈 또는 nutr i - -tion al anemi a 라고 한다. 1968 년에 world health stu dy gr oup 은 38) 혈 액 내 hemog lo bin 치 로서 남자의 hemog lo bin 량이 혈액 100ml 당 13g , 임 신하지 않은 여자는 혈액 100ml 당 12g 이하가 되면 이것은 빈혈의 기준으로 삼 았다. 처 hemo g lob i n 치는 비단 Fe 결핍분만 아니라 기타 영양소의 부족으로도 기인된다. 그러므로적혈구의 크기와 모양 및 수, color in dex, 그리고 저장 Fe 의 측정결과에 의해 Fe 결핍성 빈혈을 평가 할수있다. 건강한 남녀의 평균 hemog lo bin 량과 적혈구의 수는 표 2.7 에 표 시한 바와 같다.
 표 2.7 정 상인의 hemog lo bin 양과 적 혈구의 수 38)
표 2.7 정 상인의 hemog lo bin 양과 적 혈구의 수 38)
Color ind ex 역시 빈혈 판정에 효과적으로 사용되는데, color in dex 는 다음 방정식에 표시한 바와 같이 정상치와 비교한 hemo- g lob in의 백분율을 역시 정상치와 비교한 적혈구 수의 백분율로 나 타낸 것이다.
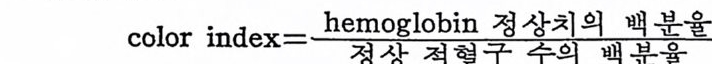 color ind ex he정m상og lo 적bi혈n 구정 상수치의 의백 백분 분율율
color ind ex he정m상og lo 적bi혈n 구정 상수치의 의백 백분 분율율
정 상적 인 사람의 color ind ex 는 거 의 1 이 며 , color ind ex 가 1 보 다 쿨 때 는 hemog lo bin 은 정 상이 나 적 혈구 수가 미 달이 고 color ind ex 가 1 보다 작을 때 는 적 혈구의 수는 정 상이 나 hemog lo bin 의 양 이 저하됨을 나타낸다. Fe 이 결핍된 쥐에 대한 실험에서 빈혈이 일어나지 않아도 cy to· chrome C 수준이 감소되었음이 밝혀졌다. 이것은 빈혈에 있어서 일부 증후는 hemog lo bin 치 가 낮아서 가 아니 라 세 포내 효소의 활 성 감소 때 문임 을 시 사한다. 39)40) Fe 결핍성 빈혈의 증세는 기타 빈혈과 같이 혈액이 세포충의 호 _ 홈에 필요한 산소의 공급을 불충분하게 하여 주므로 창백 한 피부, 기력감되, 찾은 호흡, 식욕부전, 의욕상실증을 수반한다. 빈혈현 상이 극심한 상태로 오래 지속되면 사망에 이르는 경우도 있다. Fe 결핍성 빈혈은 주로 Fe 부족의 식사를 오래 지속하거나 다량 의 출 혈(월경 또는 상해에 의한 출혈), 기생충에 의한 출혈, 위퀘 양 출혈, 암, 그리고 Fe 흡수에 지장이 있는 질환에 처해 있을 때 일어난다. 또한 Fe 결핍성 빈혈을 사춘기 소녀들 사이에서 흔히 볼 수 있는데 이둘 소녀들은 대부분 Fe 섭취가 불충분한 데 비해 월경 으로 인해 매월 다량의 출혈로 Fe 의 손실이 많기 때문이다. 임신 후반기 임부들 사이에서도 흔히 빈혈중세를 발견하게 되는 데 임신 후반기에는 대아가 출생 후 6 개월 동안 충분한 Fe 을 간과 혈액에 처장하려는 데 비해서 모체에 공급하는 Fe 의 양이 불충분 하기 때문이다. 최근 어머니의 Fe 결핍증이 영아에게 빈혈의 원인을 주는 범위는 논쟁의 대상이 되어 있다. 영국의 조사에 의하면 Fe 을 보충한 어머 니의 석사가 그렇지 않은 대조군의 그룹에 비하여 6, 12, 18 개월 된 어린이의 적혈구 수의 변화에 아무런 영향이 미치지 않는다는 보고 도있다. 1974 년 Guth ri e 둥 41) 은 어 미 의 Fe 결핍 이 어 미 자신과 그 새 끼 의 혈청지질에 미치는 영향을 연구 발표했다. 그는어미 자신의 혈청지 질에 는 아무런 영 향이 없 었으나 그 새 끼 들에 게 는 tri g lice rid e , choles- ter ol, ph osp h olip id 가 증가되 었 음을 보고하였으나 그 기 전은 밝혀
겨지 않았다. 과거의 연구자들은 52) Fe 결핍시 헐청이나 조직의 일 부에 서 lipo p ro te i n lipa se 활성 이 감소되 어 고지 혈증을 일으켰 다고 해석하기도 했다. 그러나 이런 실험이 확실하게 입증될 때까지는 사춘기 소녀와 임 신 후반기 에 는 충분한 양의 Fe 공급이 요구될다고 보겠 다. 그러 므 로 흡수가 찰 될 수 있는 조건 조성과 FeS04 를 매일 석이에 첨가 해 주면 Fe 부족형으로 인한 빈혈은 치료되어질 것이다. 경구두여 한 Fe 을 홍수하지 못하는 환자에 게 는 근육주사용 Fe 제 품 (Fe dex- t ran) 이 개발되어 있으며, Fe 의 비경구 두여시는 조직내 과포화 가 능성 과 이 로부터 유래 되 는 hemosid e rin 침 착증의 유발에 대 하여 유 의하여야 한다. 최근 Fe 결핍중 측정방법으로 hemog lo bin 이의에 조직의 효소 측 정율 하고 있다. 그러나 현재까지의 Fe 결핍증의 판단기준치와 증 상들이 과연 옳은 것인지 아닌지에 대해서 많은 문제접들이 대두되 고 있다. 왜냐하면 Fe 결핍증의 경중과 hemo g lob i n 치가 바례하지 않는다는 것이 인체 실태조사에서 입증되고 있기 때문이다 .41 )4 2)43) 효소측정 결 과 Krebs cy c le 에 있 는 aconit as e, cy toc hrome C- by d rog e nase, succi na te - dehy d rog e nase 둥의 측정 치 는 정 상이 었 다 44)45)46) ‘ 그러나 이런 보고들은 현재로서 조심스럽게 받아들여져야 하며 앞으로 더 많은 실험이 계속될 때 정확한 판단 기준이 성립될 수 있을 것이다. 2.6 Fe 의 대사장애에서 오는 질병과 기타 질병과의 관계 2. 6. 1 hemosid e rin 침 착중 Fe 에 대한 배설경로가 명확하지 않고 또 적은 양이 배설되기 때 문에 조직 내에 과잉량이 축적될 수 있다. 이것은 수년간에 걸쳐 많 은 수혈을 받은 처혈성 또는 용혈성 빈혈, 간경변증, 알코올 중독 증 환자에게서 관찰된다. 수혈시 500ml 의 혈액에는 250m g의 Fe 이 함유되어 있다. 또한 소장으로부터 Fe 을 흡수하는 데 과잉능력을
가전 일부 개체가 촌재한다는 것이 39 Fe 에 의한 실험에서 입증되었 다. 이러한 개제는 표시된 Fe 투여량의 20~45% 를 홉수하 나 정 상 개체는 1. 5~6.5% 롤 흡수한다 .17) Fe 흡수의 비정상성은 선천적일 수 있는데 그러한 환자에서 과안 량의 Fe(40~50g)이 수년 후에 조직 내 에 축적 된다. 이 hemosid e rin 침 착증에 는 피 부의 갈색 화 (hemochroma t os i s) 와 조직 내 에 서 결합되 지 않는 Fe 의 독성으로 말미암아 간경변증, 당뇨 및 췌장섬유증의 칭 후를 나타내는 간장장해가 뒤따 를 수 있다. 예 기 되 는 바와 같이 혈색 중 (hemochroma t os i s) 환자의 혈청 내 불포화 Fe 결합능력은 매우 낮다. 그러므로 정상 개체 혈청의 Fe 결합 단 백질은 약 30% 만이 포화된 데 반하여 아들 환자에 있어서는 소장으 로부터의 Fe 과잉흡수로 말미암아 약 90% 가 포화되어 있다. 정 상인의 전체 Fe 함량이 3~5g 인 데 반하여 혈색 증 (hemochro· ma t os i s) 환자는 20~40g 까지 의 높은 수치 를 보인다. 정 상개 체 는 매 일 1~2m g을 흡수하는데 비해 선천적인 결함을가전 환자는 매일 2 배 의 양을 흡수 축적한다. 이런 경우 치료법으로는 Fe 의 양을 적게 하기 위 하여 동맥 에 서 피 를 뺀다든지 혹은 desfe r rio x ami n 을 복 용시켜 인체 내에 촌재하는 Fe 을 chela t e 로 결합시켜 배설하도록 하 여 야 한다. 표 2. 8 은 골수 hemosid e rin 침 착증에 서 fe rriti n 의 함량 울 볼 수 있다.
 표 2.8 혈청 fer riti n 과 골수 hemosid e rin 과의 관계 4B)
표 2.8 혈청 fer riti n 과 골수 hemosid e rin 과의 관계 4B)
2. 6. 2 장티 푸스와 chelate d Fe 과의 관계 Sm it h 둥의 53) 연구에 의 하면 쥐 에 게 salmonella typ h i mur i um 을 접종시켜 장티푸스에 질리게 한 후 군형석이에 chelate d Fe 을 첨가 해서 생촌기간을 관찰했다. FeS04 나 FeCI3 가 첨가된 식이군은생촌기간이 변화되지 않는데 비 해 서 Fe-EDTA(fe r ric sodiu m eth y le ne dia m i ne tet r a ace t a t e) 에 의 해 서 는 생 촌기 간이 현처 하게 짧아지 고 Fe NTA(fe r ric nit ri lo t r i a c eta t e ) 에 의해서는 생촌기간이 약간 연장되었다 .54) Chr i s t o p her 둥이 발표한 in vit ro 에서의 실험은 Fe-EDTA 의 대 사에서 흡수와 이용이 아주 느린 반면 Fe NTA 는 빨리 흡수되고 곧 t rans f err i n 과 함께 작용하여 빈혈이나 전영병에 사용되기 때문 이 라고 보고했 다. 55) 2.7 독 성 장기간의 동물실험에서 Fe 은 독성이 비교적 적었음이 밝혀졌다. 4~7 년동안 개에게 매일 체중 1kg 당 500~1000m g의 Fe 을 섭취시 켰던 결과 목별한 중상은 나타나지 않았다 .56) 그러나 어린이의 겅 우 900m g의 Fe 섭취는 죽음을 초래했다. 일부 Afric a Bantu s 족의 Bantu s Sid e rosis 와 Et h io p ia 의 경 우를 보면 전자의 경우는 200mg Fe/1 일 섭취하는 그들의 식습관에서 나 타난 kaff ier beer 의 Fe 양은 120mg Fe/l 이 었으며 인체 에 흡수된 Fe 양은 2~3m g /l 일이었다. 후자는 곡류, 가공, 처장, 조리시 오 영된 Fe 에 의해 470m g /I 일까지 측정되었는데 이 중 3/4 이 오영 에 의한 Fe 양이었다. 이 Fe 의 거의가 흡수 불가능한 Fe 이었다. 그러나 동물실험의 정상적인 영양 조건하에서는 조칙철혈중 (T i ssu e sid e rosis ) 중상이 나타나지 않았다. 57) 조직 철혈중 (T i ssue s i deros i s) 은 과량의 옥수수와 Fe 을 함께 섭 취 , 했을 때 나타나는 것으로 판명되었다. 취에 있어서 과량의 Fe 섭취 는 간의 m it ochondr i a 에 Fe 을 축적하고 지방의 과잉산화가 일야 난다.
성안남자에게 Fe 을 50m g /1 일 58) , 또 다른 실험에서는 25~75mg f 1 일 59) 섭취시켰던 결과 안전했으나 개인에 따라서 t olerance 의 범 위가 조금씩 다른 것 같다. 흡수 가능성과 독성효과를 내는 최소량과 안전량 그리고 최대량 에 대해서는 Fe 과 다른 원소들의 상호작용에 의한 효과와 더불어 많이 연구되 어 지 고 있 다. 59)60)61)62)63) 참재 적 인 독성 을 갖는 tra ce elements 의 안전한 식 이 섭 취 량은 보유하고 있는 양과 흡수에 영 향 을 미치는 다른 원소의 양에 의해 결정되는 것과 같다. 2.8 함유식품과 강화식품 2.8.1 함유식품 Fe 의 우수한급원으로는 간·심장등의 내장과 난황, 녹두, 완 두콩 등이고 중간 정도 함유식품은 육류, 어류, 밤, 팥, 코코아, 김, 미역, 굴, 조개, 파래, 참깨, 찻, 버섯, 들껫잎, 무우청 둥을 들 수 있다. 표 2.9 는 Fe 의 급원식품을 나타내며 표 2.10 은 10mg 과 18mg 섭취가능한 표준 석단이다. Fe 의 함량이 비교적 적은 식품으로는 우유와 유제품, 과일, 근 채류 및 정백한 곡류 등을 들 수 있다. 우유에는 계절에 관계없이 Fe 이 75µg /l OOml 함유되 어 있으며 , 모유에 는 수유시 작 때 130~ l50µ g /lOOml 이 함유되어 있으며, 수유가 계속되면서 Fe 의 함량이 감소되며 우유와 비슷해진다. 우유의 Fe 은 약 40% 가 지방입자에 함유되어 있다. 그러므로 탈 지유는 전유보다 훨씬 적은 양의 Fe 이 함유되어 있는 셈이다. 참 ` 고로 끓는 물에서 야채 중의 Fe 은 20% 가 감소될 수 있다는 보고도 있다. 65) 이씨조선 중기 허준이 편찬한 동의보감을 토대로 한 李와 蔡 둥 3 7). 의 연구에 의 하면 동의 보감에 수록된 곡류, 알류, 조류, 수육류, 과실류에 있 어 서 조혈에 좋은 식 품의 Fe 함량은 100g 당 8. 6, 5. 0, 6. 5, 3. 4, 2.12mg 등으로 나타났다. 죽 곡류, 알류, 수육류, 과살 류에서는 조혈 빈혈에 관계되는 경험적인 한방식품이 기타군보다
 식표 2. 9품 석 풍의명 천l 분분 ( Fe량) :함량: 64)김 i I 식 품 명 1 분 량— 1갭 虹
식표 2. 9품 석 풍의명 천l 분분 ( Fe량) :함량: 64)김 i I 식 품 명 1 분 량— 1갭 虹
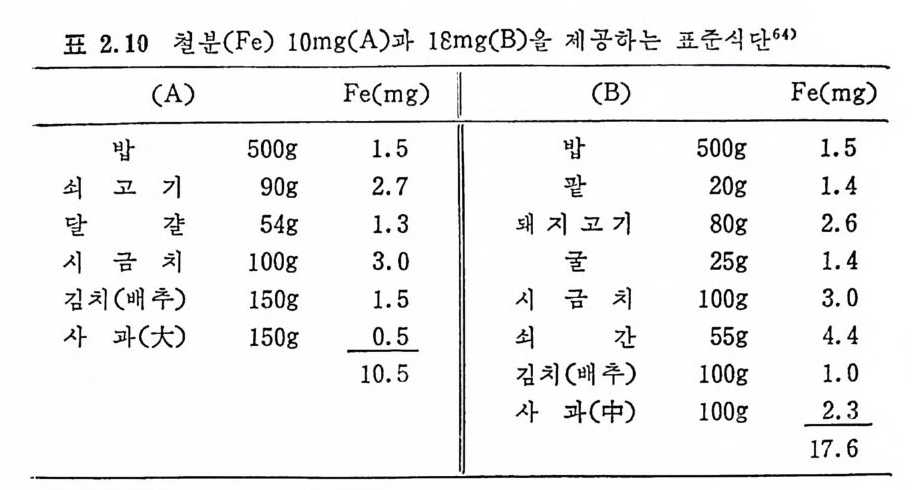 표 2.10 철분 (Fe) !Om g (A) 과 18m g (B) 을 제 공하는 표준식 단)
표 2.10 철분 (Fe) !Om g (A) 과 18m g (B) 을 제 공하는 표준식 단)
Fe 함량이 높은 것으로 나타났으며 채소류, 어류에서는 기타군보다 낮은 것으로 나타났다. 다음의 표 2.11 은 곡류, 알류, 육류, 어류, 과실류, 채소류에 함 유된 Fe 함량을 보여 준다. 66)
 표 2.11 빈혈과 조혈에 권장되고 있는 식품과 기타 대조식품군의
표 2.11 빈혈과 조혈에 권장되고 있는 식품과 기타 대조식품군의
 토 란 0.5 A。 1] 70l- 1.1
토 란 0.5 A。 1] 70l- 1.1
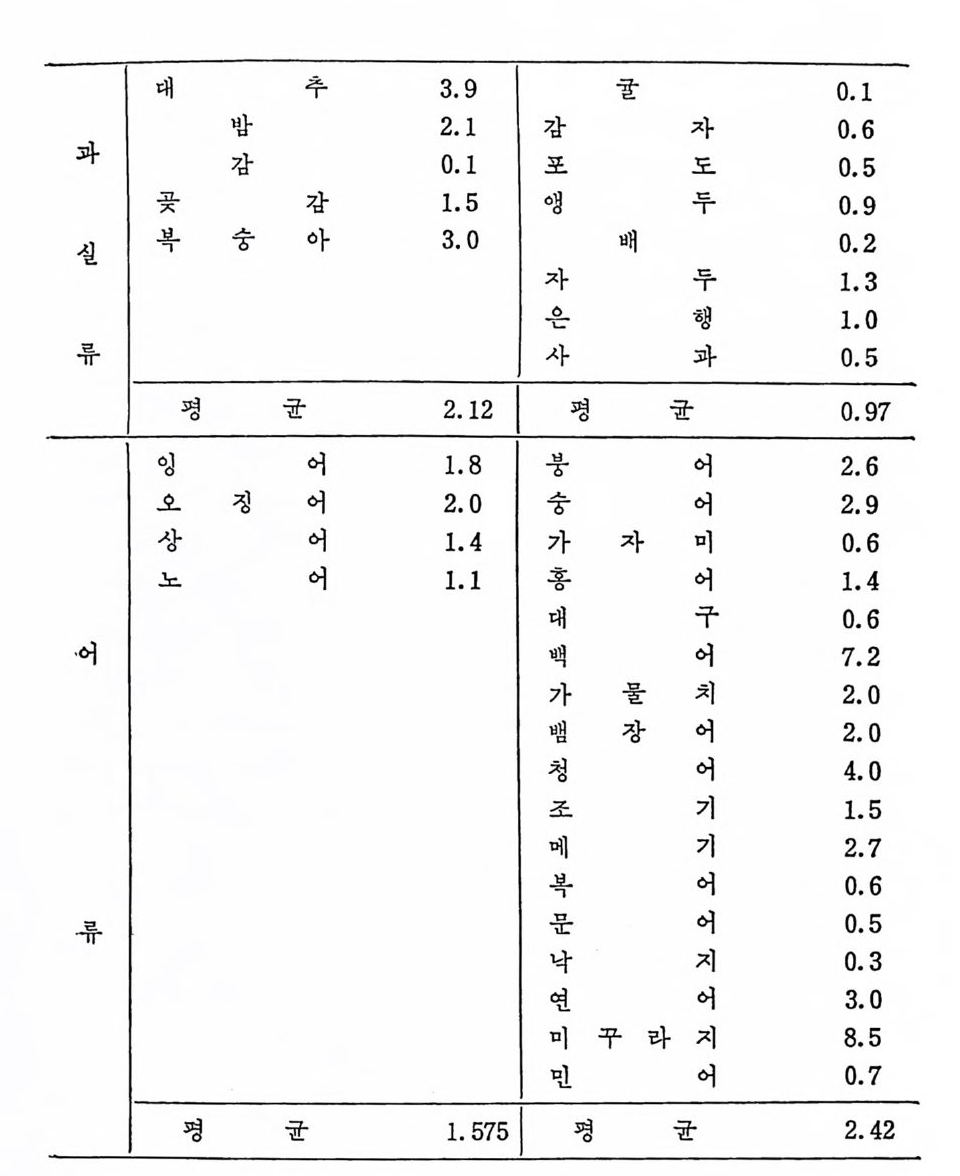 대 추 3.9 굴 0.1
대 추 3.9 굴 0.1
죽, 한방의학 특히 동의보감의 湯液編울 중십으로 하여 빈혈 또 는 조혈석 품군의 Fe 함량이 같은 종류, 유사 기 타군보다 비 교적 높 온 것은 현대 영양학, 의학적인 면에서도 매우 의의가 있다고 불 수 있으며 채소류, 어류 등에서 약간의 예외가 있음은 조혈기능에 Fe 분만 아니라 단백질, vit am i n B 군 둥 여러 가지가 동시에 영향
을 미찬다는 것을 고려하면 더욱 광범위한 연구가 필요하다. 2.8.2 강화식품 Fe 강화석 품으로는 밀가루, 빵, 국수류, 쌀 등이 며 주로 fer rum reductu m, Fe-2-sulfa te, Fe-ascorbate , Fe-p y ro p h osph ate 등을 사용한다. Vi tam i n C 와 함께 강화하면 흡수가 더 좋다고 한다. 67 } 밀가루의 강화에 는 fer rum reductu m 을 주로 사용하고 있으며 표 2.12 는 세계 각 나라에서 강화하고 있는 밀가루의 Fe 량을 나타_ 낸 것이다.
 표 2.12 밀가루에 강화된 철분 (Fe)(m g/kg 밀가루 ) 6E )
표 2.12 밀가루에 강화된 철분 (Fe)(m g/kg 밀가루 ) 6E )
쌀의 강화는 도미니크 공화국, 일본, 콜럼비아, 쿠바, 필리핀 ,.. 태국, 미국, 베네주엘라 둥에서 실행하고 있다. 특히 쌀 강화는 씰:
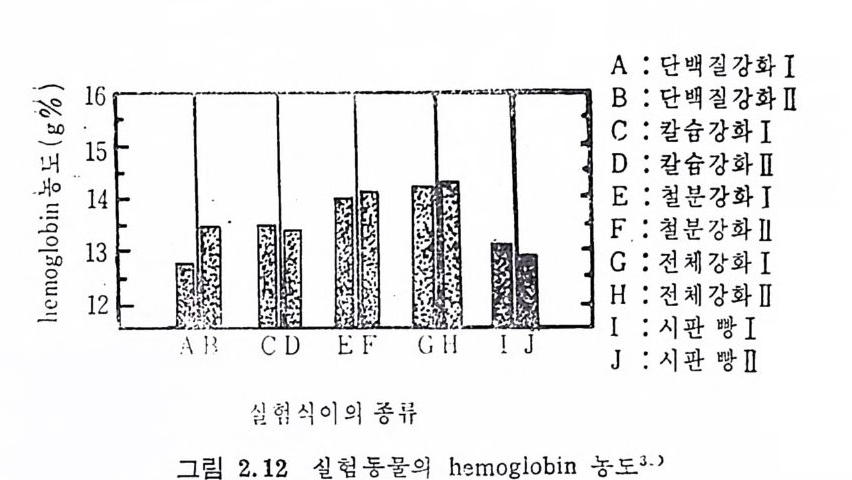
을 씻어서 밥을 지을 때까지 강화된 영양소가 씻겨 나가지 않아야 하며 독정한 맛이 나지 않아야 한다. 이 렇게 하기 위해서 먼처 강화 하고자 하는 비타민을 분무기 형식으로 쌀 위에 뿌린 다음 그 위에 Fe-py ro p h osph ate 가루를 묻힌 후 말란 다움 그 위 에 abie t i c aci d, pa lmi tic ac id 그리 고 zein 과 용해 된 eth anol 은 쌀 위 에 필름처 럼 씌워서 말리면 냄새, 맛, 색깔이 전혀 없고 뜨거운 물에만 용해되 는 〈강화미 〉 를 만들게 된다. 이 〈 강화미 〉를 1 : 199 의 비 율로 많은 분량의 다른 쌀에 섞 어 찰 혼합하여 사용한다. 1kg 의 혼합된 쌀에 는 28.5m g의 Fe 이 함유되어 있다 .69) 1958 년에 대만에서 만들어 낸 〈 강화마〉에는 1kg 당 5,740m g와 Fe 이 강화되어 있었다. 옥수수 가루에 는 1kg 당 29~35mg 의 Fe 을 그리 고 국수류에 는 100g 에 2. 9~3. 6g m g 의 Fe 을 강화한다. 70) 미국에서는 밀가루에 Fe 을 강화하게 하였으나 보다 철저한 현촌 영양섭취 상태와 과량의 Fe 섭취가 문제접으로 드러났다 .68) Beal 과 그의 연구팀은 71) 미국에서 유아석품에 Fe 을 대규모로 강 화하는 대 대하여 문제접을 제기하였다. 그들은 Fe 을지나치거] 처장 하는 것은 Fe 의 결핍증보다더 큰 문제를 유발한다고 말하고있다. 미국에서는 Fe 을 강화한 유아용 조제유에 lqu arte r 당 (40 컵) 8~ 12m g의 Fe 을 함유하고 있다. 따라서 이러한 처방식은 체중 4kg 의 유아에게 1 일 6m g의 권장량으로 하였을 때 첫 2 개월 동안 Fe 의 주요 급원으로 많이 장려되고 있다. 1968 년 Lee 와 Lim 12) 이 조사한 우리 나라 농촌의 이 유석 으로 강 화하는 석품에 함유된 Fe 의 합계는 다음 표 2.13 과 같다. 1969 년 李 39) 등이 조사한 쥐실험에서 시판된 빵을 섭취한 군과 빵 에 Fe 과 단백 질 및 Ca 을 강화한 군의 hemog lo bin 농도를 비 교한 결과 시판빵을 주재료로한 식이군은 13.1, 12.9% 였고 강화한 빵의 섭 취 군은 14. 3, 14. 2% 로 강화한 빵의 식 이 군의 hemog lo bin 농도가 높았다. 그러나 실제적으로 사람에게 이용할 수 있는 강화빵을 만 든다는 것은 앞으로 큰 연구과제로 남게 될 것이다(그립 2.12).
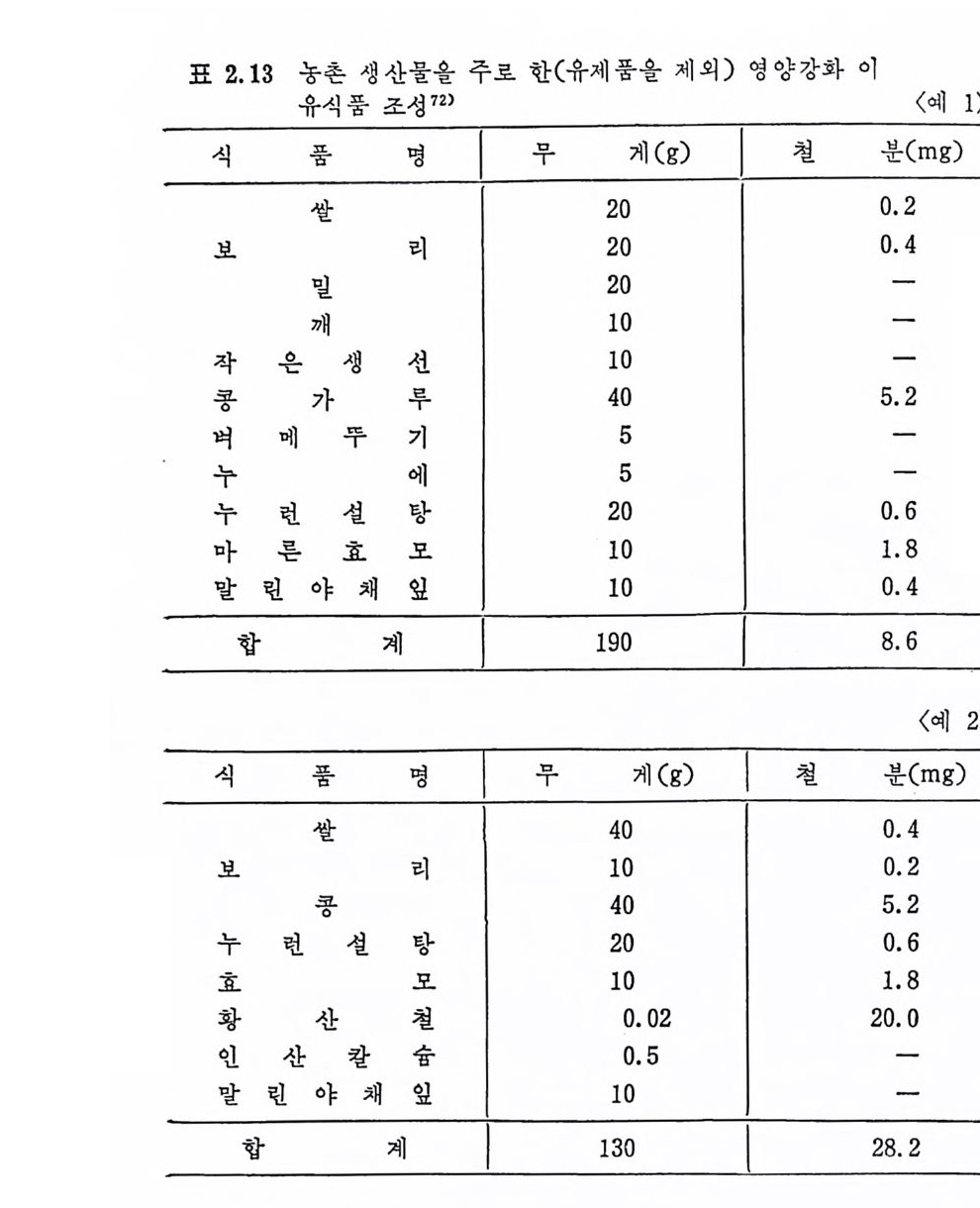 표 2.13 농촌 생산물울 주로 한(유재품을 제외) 영 양강화 이
표 2.13 농촌 생산물울 주로 한(유재품을 제외) 영 양강화 이
2.8.3 우리나라의 Fe 연구 우리나라의 Fe 결핍으로 인한 영양성빈혈의 빈도 추이를 살펴보 떤 m 1960 년대 초반기에는 농촌의 경우 6% 정도이다가 1960 년대 후 반기에는 약 15% 로 증가되었으며 1970 년대에 들어와서는 약 10%
 lu'ootu혼(g)l !~버11 q1J .11162 5 14广13_||\_빠l _ HAJGIFBcDE : ::::::::: 전전철칼단시칼단철시백체판체분슘백슘분판 강강강질강강질강땅빵 화화화화강화화강 III 화화 IlIII1IlI 11I
lu'ootu혼(g)l !~버11 q1J .11162 5 14广13_||\_빠l _ HAJGIFBcDE : ::::::::: 전전철칼단시칼단철시백체판체분슘백슘분판 강강강질강강질강땅빵 화화화화강화화강 III 화화 IlIII1IlI 11I
로 나타나 아직도 그 해 결책 이 하나의 큰 과제로 남아 있다 . 74 ) 1972 년 李 등 7 5) 의 각 지 역 별 10~12 세 (4~5 학년) 국민학교 아동의 도시락 영양가 조사에 의하면 4 개 지역의 Fe 평균치는 권장량보다 낮 으며, 농촌은 남녀 학생 모두 부족한 섭취상태를 보이고 있으며, 산 촌 아동은 녹색채소 를 다량으로 이용하고 있어서 다른 지역보다 좋 은 상태이다. 1959 년 Fe 결핍성 빈 혈 에 대한 세계보건기구 (WHO) 전문위원회 의 보고 80) 에 의하면 6 개월에서 4 세 사이의 소아의 혈색소량, hema- to crit 치 , M. C. H. C. (Mean Corpu scular Hemog lo bin Concen t ra ti on) 은 각각 10.8g /1 00ml 미만, 32% 미만, 33% 미만일 때를 Fe 결핍성 빈혈이라 정하였고, 5 세에서 9 세 사이의 혈색소량, hema t ocr it치, M. C. H. C. 를 각각 11 . 5g /1 00ml 미 만, 33% 미 만, 34% 미 만의 경 우를 Fe 결핍성 빈 혈 이라 보고하였는데 1968 년 WHO 의 영양성 빈 혈 전문위원회의 보고 8l) 어1 서는 6 개월에서 6 세 사이의 소아에서는 혈 색 소량, hemato c rit 치 를 각각 llg/l OOml 미 만, 32 % 미 만의 경 우 를 빈혈상태로 진단하였다. 혈청 Fe 은 체내 Fe 의 상태를 조기에 알아넬 수 있는 측정방 법 으로 여 러 연 구자에 의 하여 측정 되 었 다. 82)53)54) TIBC (Tota l Iron Bin d in g Ca pac ity)는 감영으로 인한 빈혈과 Fe 결핍성 빈혈을 구분하 는데 도움이 되는데 Fe 이 결핍되면 TIBC 는 450µg /l OOml 수준으
로 중가하며 혈청 Fe 은 50µg /1 00m! 미만으로 감소되고 tra nsfe rrin · sa t ura ti on 은 10% 이하로 감소되며, 감영으로 인한 빈혈의 경우에 는 혈청 Fe 과 TIBC 가 전부 감소된다. 82)83)84)85) 또한 Fe 이 결핍 되 떤 혈색 소를 생 성 할 만큼 Fe 의 이 용이 충분하지 못하여 hy po chromi c mi cr ocy tic anemi a 가 발생 되 며 , 이 증세 는 Fe 결핍 증의 특수한 빈 혈로 혈청 Fe 량은 50µg / l00ml 미 만으로 감소되 고, TIBC 는 450~ 650ml 로 중가된다. Bain t o n 둥은 86) tra nsfe r rin satu rati on 이 Fe 결 핍 성 빈 혈 검 사 에서 16% 이하가 되면 골수에 운반되는 Fe 이 부적당함을 나타낸 다고 한다. 그리고 정상 혈청내에 Fe 과 결핍되는 포화정도는 보통 ~ 25~50% 범위에 있으며 평군치는 30~40% 사이에 있다 .87) 정 상 혈청 Fe 량, TIBC, tra nsfe r rin satu rati on 은 각각 50~180 µg/l OOml, 300~450µg /l OOml, 30~45% 이 고, Fe 결핍 성 의 기 준은 혈청 Fe 량이 50µg /l OOml 미 만, TIBC 가 450µg /1 00ml 이 하, tra ns- fer rin satu rati on 이 15 % 이 하로 정 하고 있 다. 표 2. 14 는 정 상 혈 청 철분 (Fe) 량과 TIBC 그리 고 tra nsfe r rin satu rati on 이 다. 88)
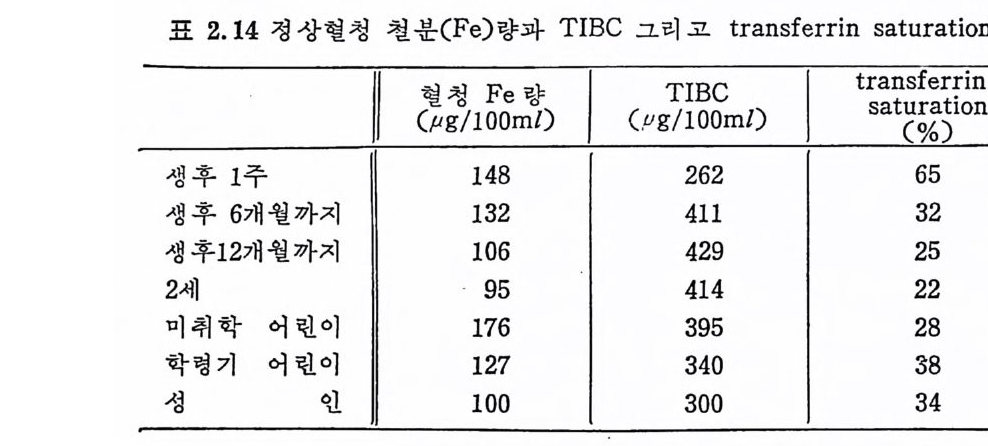 표 2.14 정 상혈청 l1 천분麟 (Fe)二 량과 TIBlC (그u g리 尻고問 m tlra) n sfe1 r rin ssaatt(u` u% r 'r a-a)다tt i io onn 8 8>
표 2.14 정 상혈청 l1 천분麟 (Fe)二 량과 TIBlC (그u g리 尻고問 m tlra) n sfe1 r rin ssaatt(u` u% r 'r a-a)다tt i io onn 8 8>
蔡와 李둥 76) 의 농촌 미취학 아동의 빈혈 특히 Fe 결핍성 빈혈에 관한 연구에 의하면 만 1 세 ~6 세의 미취학 아동 92 명(남 : 47, 여 : 45) 의 혈색소량의 평군치는 11 . 0 士1. 57g / 100ml 이고 그 중 38% 가 빈 혈해 당치 인 11 . Og /l OOml 미 만에 속하고 있 으며 60 %가 전국 체 중-
표준치에 미달되었다. Hemato c rit 치 의 빈혈해 당치 는 32% 미 만이 27. 5% 였 고 M. C. H. C (Mean Corpu scular Hemog lo bin Concen t ra ti on) 의 빈혈해 당치 (33% 미 만) 는 28% 로서 미취학 아동의 빈혈의 빈도는 높았으며 이것은 처색 소성 빈혈 (h yp ochrom i c anem i a) 로 판단되 었다. 또한 혈청 Fe 량이 50mg / 10 0ml 미 만의 예는 37. 9% 이 고 TIBC(Tota l Iron Bin d in g Cap a- c ity)가 400µg /l OOml 이 상인 예는 31% 이 다. Transfe r rin satu rati on 은 15% 미만인 예가 48.3% 였다. 그러므로 Fe 결핍성 빈혈의 빈 도가 높음이 나타났다. 농촌의 성장기 아동의 Fe 상태에 대한 연구가 1973 년에 행하여졌 는데 1 ” 이에 의하면 평군 혈색소량은 1 1. 3 g%(土 0.94 g%)로서 68.4% 의 아동이 빈혈해당치 (5 세 이전 : Ilg% 미 만, 6 세 이후 : 12g % 미만) 이 내에 속해 있었으며 평군 hema t ocr it치는 36.1%( 土 2.36% )로서 29.8% 가 빈혈해당자 (5 세 이전 : 33% 마만, 6 세 이후 : 36% 미만)였고 평군 M.C. H. C 는 3 1. 3%( 士1. 71%) 로서 34% 이상 해당자는 3.5% 에 불과했다. 이같은 결과는 위에 기술한 1968 년에 행해진 연구오1- 마찬가지로 농촌아동의 빈혈의 발생빈도, 독히 저혈색소성 평군 혈 청 Fe 량은 78.2µ g%(士 29.Bµ g%)로서 5Q µg% 미만인 예는 5.6% 였 으나, TIBC 에서는 4 1. 8% 가 450µg % 이상에 속했다. 한편 tra ns- fer rin sa t ura ti on 은 15% 미만인 예가 학령전 아동기에는 71 .4 %, 학령기아동에서는 28.6%, 전체 아동에서는 43% 로서 학령전 아동 · 에서 특히 낮은 상대를 나타냈다. 이같은 결과로서 Fe 결핍성 빈 혈의 높은 빈도와 함께 Fe 의 영양상태가 벨로 좋지 않은 것으로 생각된다. 이 밖에도 1974 년 曺 와 蔡 78) 의 도시 영세민 미취학 아동과 정상 건강인, 칙업적 給血者를 대상으로 한 연구를 참고로 해보면 마취 학 아동의 혈색 소 농도의 평 군치 는 11. 3g /1 00ml 로 전체 의 36. 5%. 가 빈혈해당치에 속해 있음을 보여주었고 일반적으로 남자보다 여 자가 빈혈의 빈도가 높았고 연령이 증가함에 따라 낮아졌다. 이들` 의 적혈구 p ro t o p or p h y r i n 의 평군농도는 Fe 결핍성 빈혈의 빈도가 높은 1~3 세에서 유의하게 높았다.
정 상적 인 남자의 적 혈구 pro to p o rph y ri n 농도의 평 균치 는 47. 5µg / 100ml 이 고 tra nsfe r rin satu rati on 은 35. 2% 이 었 다. 칙 입 적 급혈자 의 평 군 혈색 소 농도는 11 . 9g /1 00ml 이 며 12g /1 00ml 미 만은 전체 의 46% 였 다. Transfe r rin satu rato n 이 15% 미 만인 예 는 47. 4%이 러 이 들의 혈청 Fe 의 평 군치 는 27. lµg /l OOml 이 었 다. 이상을 종합해 보면 한국 영세민 미취학 아동의 각종 신체 계측 치는 대체로 낮았으며 빈혈의 빈도는 높았다. 특 히 l~3 세의 유아 기에는 Fe 결핍성 빈혈의 빈도가 높은 것을 볼 수 있었다. 참고로 蔡 79) 의 건강인 혈청 Fe, Fe 결합기능 및 tra nsfe r rin satu rati on 측정 에 관한 보고를 보면 건 강한 남자의 tra nsfe r rin satu rati on 평 군치 는 35. 6 土 12. 8 %, 건 강한 여 자의 tra nsfe r rin sa- tu rati on 평군치는 25,4 土 12.4% 로 여자의 혈청 Fe 측정치가 남자의 것보다 낮았다. 혈청 Fe 의 빈혈해당치인 50µg / lO Oml 이하에 드는 예는 남자에는 없으나 여자는 5.5% 가 해당되었다. 또한 혈청결합기능이 400µg /l OOml 이상인 남자는 10.2% 였으나 여자는 44.5% 가 해당되었다. 혈청 tra nsfe r rin sa t ura ti on 이 15% 이하에 해당되는 남자는 없고 여자의 경우 5.6% 가 해당되었다. *참고문헌 1) Todhunte r , E. N. , Fed. Proc. , 36, 2504, 1977. 2) Marcuse, J. , Di iitet i k in Al ter ttt m , Enke, Stu t t ga rt, 1899. 3) Grassmann, E. and M. Ki rc hg e ssner, Zbl. Vet. Med. , A 20, 481 1.9 73. 4) Theonell, H. , M. Benznak, R. Bonnic h sen, K. G. Paul and A. Akeson, Acta Chem. Scand. , 5, 445, 1951. 5) Grassman, E. , S. V. Krziw anek and M. Kir c hg e ssner, Arch. Ti e rernii hr ung , 28, 45, 1978. 6) Kir c hg e ssner, M. and D. Heis e ke, Z. Ti e rph ys io l . and Ti er ern-
ahrg, u. Futt er mi ttel kde 39, 272, 1977. 7) Beutl e r, E. and R. K. Blais d ell, Blood, 15, 30, 1960. 8) Kir c hg eB ner, H. , E. Weig a nd, A. Schneg g, E. Gra/3 m ann, F. J_ Schwarz and H. -P. Roth , in Cremer. H. -D, D. Hotz e !, und J. Kii hn au,. Bi oc hemt e und Phy si o l og ie der Erni h rung Band I. Teil I, 29, 1980. 9) Happ e r, H. A. , V. W. Rodwell and P. A. May es , Revie w of Phy - sio l og ica l Chemi st r y , 17th Edit ion , Lang e medic a l Publi ca ti on , 602,. 1979. 10) Wi dd owson, E. M. , Natu re, London, 166, 626, 1950. 11) Sp ra y, C. U. and E. M. Wi dd owson, Br. ]. Nutr . , 4, 332, 1951. 12) Wi dd owson, E. U. and C. M. Sp ra y, Arch. Di s. Chil d . , 26, 205,. 1951. 13) Beutl e r, E. , in R. S. Goodhart, U. E. Shil s, Modern Nutr i t ion • t, n Healt h and Di se ase, 6th Ed. Lea & Febig e r 325, 1980. 14) Fried en, E. , Nutr . Rev. , 31, 41, 1973. 15) Bj or n-Rasmussen, E. , L. Halberg and R. B. Walker, A. ]. Cli n. Nutr . , 25, 317, 1972. 16) Forth , W. and W. Rummel. , Phys i o l . Rev. , 53, 724, 1973. 17) Hahn, P. F. , W. F. Bale, J. F. Ross, N. M. Balfo u r and G, H_ Whip ple , J. Exp . Med. , 78, 169, 1943. 18) Granic k , S. , J. Bi ol . Chem. , 164, 737, 1946. 19) Loff ler , G. and P. E. Petr i d e s, in Loff ler , G. , P. E. Petr i d e s,. L. Weis s , H. A. Harpe r. , Phy si o l og isch e Ckemt e, Zweit Aufl ag e ,. Sp ri n g e r Verlag, 539, 1979. 20) Kir c hg es sner, M. and U. Weser, Z. T£e rph y si o l . Ti e rernii hr . . Fu2t1t )e r mHei itnt e rlikc hd ,, H18. ,C . 1,8 1E,. E1.9 6G3.a bbe, R Mein k e and D. H. Schang , Kl in. Wschr. , 44, 827, 1966. 22) Davis , R. S. , J. S. Multa n i, C. P. Cap u rneek and P. Saltm ann,. Bi oc hem. bio p hy s. Res. Commum. , 37. 532, 1969. 23) Jac obs, A. and P. M. Mi les, Cl in. Ck im . Acta . , 24, 87, 1969. 24) Moore, C. V. and R. Dubach, Trans. Assoc. Am. Phy si c ian s. ,.
•64 , 245, 1951. 25) Callender, S. T. and G. T. Warner, Am. J. Cli n. Nutr . , 21, 1170, 1968. 26) Van Camp en , D. Fed. Proc. , Fed. Am. Soc. Exp . Bi ol . , 33, 100, 1974. 27) Callender, S. T. , in Do Hollin g s w orth and M. Russell, Nutr i t ion al Problems £n a Chang t'ng World. Ap pl. Sc i. Puhl. , London, 205, 1973. 28) Elwood, D. C. , D. New t on , J. D. Eakin s and D. A. Brown, Nutr . , 21, 1162, 1968. 29) Ami ne , E. K. and D. M. Heg st e d , J. Nutr . , 101, 927, 1971. 30) Garrets o n, F. D. and M. E. Conrad, Proc. Soc. Exp . Bi ol . Med. , 126, 304, 1967. 31) Elwood, P. C. , D. Newt on , J. D. Eakin s and D. A. Brown, Am . .]. Cl in. Nutr . , 21, 1162, 1968. 32) Jam i es on, G. A. , M. Jet t and S. L. BeBernardos, J. Bi ol . Chem. 246, 3686, 1971. 33) Top ha m, R. W. and E. Fried em, J. Bz'oc hem. , 245 , 6698, ·19 10. 34) Underwood, E. J. , Trace Elements in Human and Anim al Nutr i t i'on , Academi c Press Inc. New York and London, 17, . 20, ·19 77. 35) Walte r s, G. 0. , F. M. _M i ller and M. J. Worwood. , Cli n. Path o l. , .26 , 770, 1973. 36) Cric h to m , R. R, FEBS. Lett er s, 34, 125, 1973. 37) FAO 한국협회, 《한국인 영양 권장량〉〉, 제 3 개정판, 37, 1980. 38) WHO, Technic a l Rep or ts Serie s Nr. , 383, Genf, 1968. 39) Dagg , J. H. , J. M. Jac kson, B. Curry and A. Goldberg, Br. ] . .H aemato l . , 12, 331, 1966. 40) Dagg , J. H. , J. J. Morrow, B. Mac Farland and A. Goldberg, -G. ]. Med. ]. , 36, 600, 1967. 41 ) Guth rie , H. A. , M. Froozani, A. R. Sherman, and G. P. Barron. J. Nutr . , 104, 1273, 1974.
42) Wood, M. M. and P. C. Elwood, Br. J. Prev. Soc. Med. , 20, 건 17, 1966. 43) Elwood, P. C. , Proc. Nutr . Soc. , 27, 14, 1968. 44) Beutl e r, E. , J CUn. Invest. , 38, 1605, 1959. -45 ) Beutl e r, E. and R. K. Blais d ell, Blood 15, 30, 1960. 46) Jac obs, A. , Lancet 2, 1331, 1961. 47) Lang . K. , Bz' oc hemz 'e der Ernii. h rung , Dr. Die t r i c h Ste i n k off -Ve rlag, Darmsta d t 337, 1979. 48) Lip s chit z, D. A. , J. D. Cook and C. A. Fin c h, N. Eng l. ]. Med. , 290, 1213, 1944. 49) Smi th, M. D. and I. M. Pannaci ul l i, Br. ]. Haemato l . , 4, 428, 1958. 50) Cook, J. D. and E. R. Monsen, Am. ]. Cli n. Nutr . , 29, 859, 1976. 51) Cook, J. D. and E. R. Monsen, Am. ]. Clz 'n. Nutr . , 28, 1289, 1975. 52) Lewi s, M. and R. M. Lammarin o , ]. Lab. Clin . Med. , 78, 546, 1971. 53) Smi th, M. D. and Mallet, B. , ]. Cli nt'. Sc i. , 16, 23, 1957. 54) Smi th, I. M. and R. Hil l, in M. Kir c hg e ssner, Trace Elements Meta b olz 'sm z'n Man and Anz'm als, 3, 383, 1978. 55) Chris t o p h er, J. P. , J. C. Heg e nauer and P. D. Saltm an, in Hoe· ·ks tr a , W. G. , J. W. Sutt ie, H. E. Ganth e r and W. Mertz eds. Trace Element Meta b ol£ s m z'n Anz'm al. 2, 133, Univ e rsit y Park Press, ·.Ba ltim ore, 1974. 56) Brown, E. B. jr. , D. E. Smi th, R. Dubach and C. V. Moore. , ]. Lab. CUn. Med. , 53, 591, 1969. 57) Gil lma n, J. , P. A. S. Canham and M. Harth o rn, Lancet ][ , 557, 1958. 58) Monsen, E. R. , J. Nutr . Educ. , 2, 152, 1971. 59) Hart, E. B. , H. Ste e nbock, J. Waddell and C. A. Elvehie m , ]. Bi ol . Chem. , 77, 797, 1928. 60) Bunn, C. and G. Matr o ne, ]. Nutr . , 90, 395, 1966.
GI) Sourkes, T. L. , K. Lloy d and H. Bir n baum, Can. J. Bt o chem. ,. 46, 267, 1968. 62) Marsto n , H. R. , S. H. Allen and S. L. Swaby , Br. J. Nutr . , 25,. 15, 1971. 63) Tomp so n, H. J. and J. L. Evans, Nutr . Rep . Int. , 15, 279, 1977 ► 64) 이 기 열 , 문수재 , 『기 초영 양학』, 수학사, 188, 1980. 65) Skeets , 0. , E. Frazie r and D. Dick in s , Mt s s. Ag r fr . Exp . St n . Bull. , 291, 1931. 66) 이 은경 . 채 범 석 , 〈( 한국 영 양학회 지 >, 10, 2, 54, 1977. 67) McCurdy , P. R. and R. J. Derm, Ame r. J. Cl in. Nut~ . , 21, 284, 1968. 68) Menden, E. , in Cremer, H. -D. and D. Hotz e !, Ang e wa~dte · Ernii lzr ung s lehre Band DI, Georg Thie m e Verlag , 361, 1974. 69) Furto r, M. F. , Int. , Z. Vt ta mt n f or sclmng , 23, 324, 1952. 70) Todd, W. R. , J. Ag rt'c. Food Chem. , 7, 166, 1959. 71) Beal, V. A. , A. J. Mey e rs and R. W. Mc Cammon. , Pedia tr t 'e s 30, 518, 1962. 72) Lee, K. Y. and S. C. Lim , J. Colleg e of Home Ee. , Yonsei Univ . . 1968. 73) 이기열, 유계완, 김정자, 박정자, 《한국 영양학회지》, 2, 29, 1969. 74) 이 기 열 , 이 양자, 《한국 영 양학회 지 >, 10, 2, 59, 1977. 75) 이 기 열 , 김 명 호, 이 성 관, 김 영 우, 《한국 영 양학회 지 >, 5 , 2, 27, 1972 .. 76) 채 법 석 , 이 효은, 《한국 영 양학회 지 >, 3, 3, 4, 149, 1970. 77) 정 영 진, 이 혜 수, 강길원, 채 범 석 , 《한국 영 양학회 지 >, 7, 4, 202, 1974 .. 78) 조경 환, 채 법 석 , 《한국 영 양학회 지 >, 7, 3, 121, 1974. 79) 채 범 석 , 《한국 영 양학회 지 >, 3, 3, 4, 141, 1970. 80) WHO, Technic al Rep o rts servie s, Nr. , 182, 1959. 81) WHO, Techni'c a l Rep o rts servt'e s , Nr. , 405, 1968. 82) Beuth er, E. , Robson, M. J. and Butt en weis e r, E. , Annals of Inte rnal. Med. , 48, 60, 1958. 83) David s ohn, I. and Nelson, D. A. , The Blood, in cli nic al di a g n ost's c by Laborato ry Meth ods, p. 212, chap, 5, 14th ed. , W. B Saunders Co . ., pb il ad elph ia 1969.
84) Ressler, N. and Zak, B. , Am. J. Clin . Path . , 30, 87, 1958. 85) Moore, C. V. in Goodhart and Shil s , Modern Nurit ion in Healt k and Di se ase, Lea and Febig e r, 6th , ed. , p. 324, 1980. 86) Bain t o n , D. F. and Fin c h, C. A. , Am. J. Med. , 38, 62, 1964. 87) Ramsey , W. N. M. , Plasma Iron z'n Advances t'n Cl inic a l Che- mi st r y I . p. 19, Academi c pre ss Inc. New York, 1958. 88) Kug e lmass, I. N. , Bi o chemt 'st r y of Blood in Healt h and Dz 's ease, Sp r in g field Illin o is , U. S. A. Charle C. Thomas, Publi sh er, 1959. 89) Both well and Fin c h, Iron Meta b olz 'sm . Bosto n , Lit tle, Brown, and Co. , 1962. 90) Fair b anks, Fahey and Beutl e r, Clin ic a l Di so rders of Iron Me- tab oli sm , 2nd ed. New York, Grune and Str a tt on , 1971.
3 구 리 (Cop pe r, Cu) Cu 는 선사시대 (B.C. 8000 년대)부터 도구로 사용되어 왔으나 식 물과 동물조직에서 Cu 가 영양학적인 필수 요소임이 밝혀지기 시작 한 것은 1920 년대였다 .1) Ha rt와 그의 공동연구자들은 1928 년 미국의 W isc onsin 주립대학 에서 우유만을 먹인 쥐의 빈혈방지에 Fe 의 보충만으로는 효과가 없었으나 간이나 상치와 같은 Cu 함유석품을 첨가함으로써 치료되 었으며 , 또한 Fe 과 함께 hemog lo bin 합성 에 필수적 인 요소임 을 밝 혀냈다 .2) 3.1 체내함량과 분포 Cu 의 체내함유량은 성별, 연령, 건강상대에 따라서 달라진다. 성인의 체내에는 100~150m g의 Cu 가 함유되어 있는데 약 64mg 이 근육에서, 23m g이 골격에서, 18m g이 간장에 함유되어 있으며 간장은 다른 기 관에 비 해 많은 양의 Cu 를 함유한다. 다음은 Lang 이 조사한 Cu 함량인데(pp m/we t weig h t) 뇌에는 6.3, 간장에는 5.1, 십장에는 3.0, 신장에는 2.0, 그리고기타다론기관에는 0.5~ 1. 5 로 나타났다. 3) 또한 Hami lton 과 그의 동료들 4) 은 성 인에게 서 각기 관의 €u 함량을 다음과 갈이 측정 하였 다(µg/g wet weig h t) . 간 14.7 土 3.9, 뇌 5.6 士 0.2, 허파 2.2 士 o.2, 신장 2.1 土 o.4, 난
소 1. 2 士 0. 3, 고환 0. 8 士 0. 2, 림 프.고fr 0. 8 士 0. 06, 근육 0. 7 士 0. 02 로 나타났다. 특히, 태아의 간에는 성인과 비교할 때 5~15 배 가량 많은 Cu 가 들어 있 다고 하는데 성 인의 함량은 0. 6~0. 8mg /1 00g 이 며 태 아는 -1. 5~25mg /1 00g 정 도 함유하고 있 다. 신생 아는 비 지 방조직 (fat free tiss ue) 1, OOOg 당 평 군 4. 7mg 의 Cu 를 함유하고 있고 성인은 1. 7m g의 Cu 를 처장하고 있다. 신생아의 세포핵에는 전체 Cu 량의 80% 가 들어 있고 20% 는 다른 세포 부분에 들어 있으나 성인이 되면서 세포핵의 Cu 는 40% 로 감 소된다. 전체 Cu 의 6% 가 혈액 중의 Cu 로 혈장이나 혈구에 각각 1/2 정도씩 함유되어 있으며 혈청의 평군 Cu 함량은 여자가 남자보 다 약간 높아 성 인 남자는 llOµg /l OOml, 여 자는 120µg /1 00ml 정 도 였다.1) 건강한 사람과 동물의 혈액 에 함유된 Cu 의 농도가 표 3.1 에 표 시되어 있다.1)
 표 3.1 사람과 동물의 혈 액 에 함유된 구리 (Cu) 농도!)
표 3.1 사람과 동물의 혈 액 에 함유된 구리 (Cu) 농도!)
적혈구의 Cu 함량은 일정한 데 비하여 혈청의 Cu 는 흡수량과 밀 접한 관계를 가지고 있다. 또한 임신 후반기에는 혈청 중의 Cu 가 증가한다. 그러나 신생아
의 혈청에는 많이 들어 있지 않다. 표 3.2 는 쥐의 간과 소의 뇌에 함유되어 있는 Cu 의 양이다.
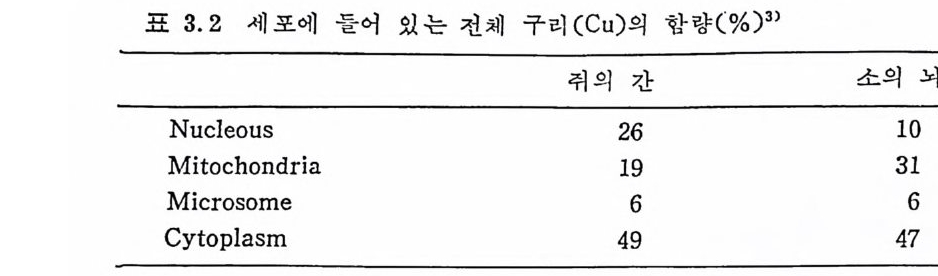 표 3.2 세포에 들어 있는 전체 구리 (Cu) 의 함량 (%)3>
표 3.2 세포에 들어 있는 전체 구리 (Cu) 의 함량 (%)3>
N i elsen6) 은 31 명의 임산부를 대상으로 혈청의 Cu 의 양을 측정하 였 던 바 임 산 3 개 월부터 중가추세 를 보였 고 약 270µg /1 00ml 로 나 타났다. Hambid g e 와 Dro gmuelle” 은 혈장의 Cu 를 측정 했 는데 16 주가 된 건강한 임산부는 162.4 士 6.lµ g /lOOml 인 데 비해서 38 주경에는 192.1 士 5.4µ g으츠브 상승했는데 출산 1 주일 후에는 다시 정상으로 되 둘아왔다. Ni xo n 과 그의 동료들은 인체 의 치 아에 1. 3~9. 5µg /g 정 도의 Cu 가 들어 있다고 보고했다 .8) 그 후 Losee 둥 295) 은 사람의 치아의 Cu 함량은 일정하지 않아 0. 07~2. OBµg /g 의 차이 를 보이 며 표준치 는 대 강 6. 8 土 4. Oµg /g 이 라고보고했다. 머 리 카락에 함유된 Cu 의 양은 0.13~0. 63mole/kg 으로 나타났으 며 Bower 는 머리카락의 Cu 함량이 연령과 세척비누, 머리색 그리 고 성별에 따라서 탈라진다고 하였으나 Moeller” 는 그들의 차이를 볼 수 없었다고 주장했다. 다만 난장이의 경우 머리의 Cu 함량이 , 정상인에 비해서 현처하게 낮다고 보고되었다. 3.2 주요 기능 Cu 는 자연계에 존재하는 일부 색소의 필수적인 구성성분이며 체 내 에 서 는 주로 redox sy s te m 으로서 촉매 적 인 역 할을 하며 hemo-
g lob i n 합성, 정상적인 골격형성 및 신경계내의 수소에 대하여 팔 수인자로 작용한다. 일부 무척추동물의 혈 액에서 발견되는 hemo- -cy a nin 은 Cu- 단백 질 복합 물 로서 산소운반체 인 hemog lo bin 과 같은 기능을 갖는다. 이 지 구상에 서 생 물이 소모하는 산소의 약 90% 이 상이 cy toc hrome oxid a se 에 의 해 환원되 는데 Cu 는 완전 환원에 관여 하는 효소인 sup e roxid e dis m uta se 와 cata lase 라는 2 개 의 key enzy m e 의 보결 분자로 촌 재 한다. Sup e roxid e dis m uta se 는 분자량이 32, 000 이 며 , 2 개의 동 일한 분 자단위로 구성되어 있고 분자 단위당 1 개의 Cu2+ 와 1 개 의 Zn2+ 를 함 유하며 , to ) cy tos ol 에 서 cy toc hrome C oxid a se 와 호기 성 대 사과정 중에 발생 되 는 독성 유리 기 인 02-(sup e roxid e rad i cal) 이온을 촉매 적으로 제거해서 H202+ 아를 생성하면 cata l ase 는 H 요 를 H2 0 와 아 로 전환시 켜 완전환원을 돕는다. Sup e roxid e dis m uta se 는 ami no acid 의 수가 다르고 Cu 와 Zn 이 결합된 대 AJ . Mn 을 함유하며 cy tos ol 에 위치 하지 않고 mito- -ch ondria 의 matr i x 에 촌재 하는 것 도 있 다. 이 와 같 이 성 질 이 다른 sup e roxid e dis m uta se 가 어 떤 부분에 촌 재하느냐에 따라서 적혈구에는 eryt hr ocup r ein , 간장에는 hep a to - -cu p r ein , 그리 고 뇌 에 는 cerebrocup r ein 이 라는 명 칭 이 부여 되 어 있 으나 그것의 정확한 효소로서의 기능에 대해서는 아직 찰 알려져 있 지 않다. Cu 는 적혈구의 성숙에 철대적으로 필요하며 이것이 부족할 때에 는 적 혈 구의 수가 현저히 감소된다. 조혈 (hema t o p o i es i s) 에서의 Cu 기능은 여러 가지 생리적인 면에서 관심 을 갖게 했는데 Cu 의 작용기 전은 hemog lo bin 합성 에 앞서 Fe 의 홍수와 이 용에 있 다고 한다. 11) Fe2+ 이 온이 tran sfo r m 인 Fe3+ 이 온으로 전환되 는 것 도 Cu dep e ndent enzy m e 인 fer roxid a se 에 의해 이루어진다고 한다 .11) 적혈구세포에 존재하는 Cu 의 약 80% 는 sup e roxid e dis m uta s e 인 eryt hr ocup r ein 이 다. Cu 는 혈장내에서 두가지 형태로 결합되어 있는데 하나는 Cu 와 복합단백질인 cerulo p lasm i n 과 밀착하여 결합되어 있고 다론 하나
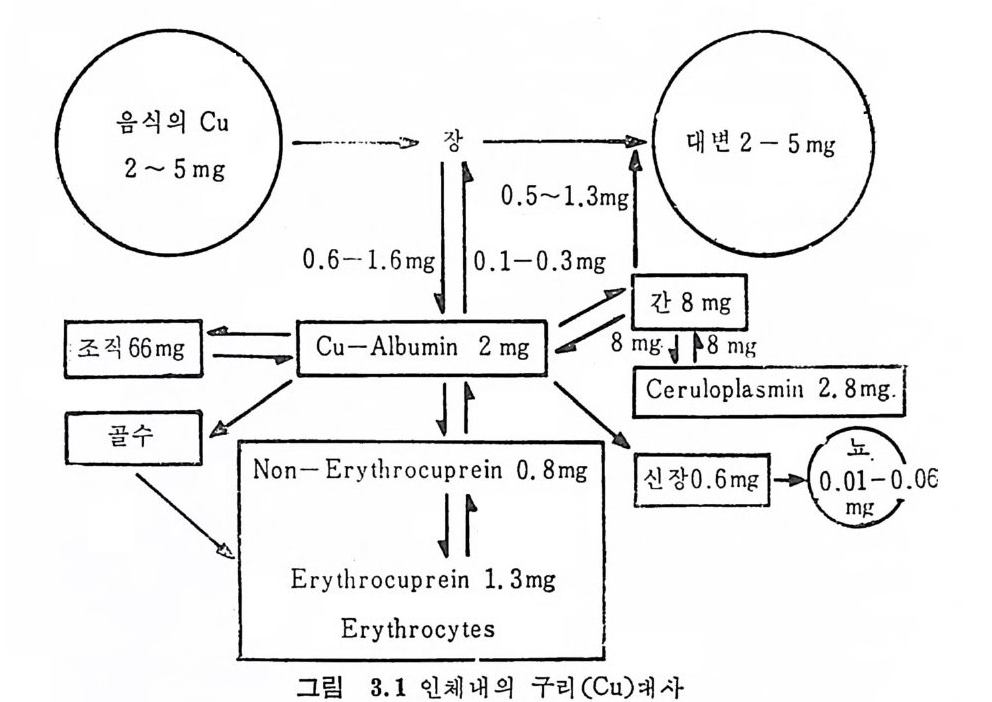
는 Cu 와 albumi n 이 느슨하게 결합되 어 있 다. 인체는 전체혈장의 80~95% 가 cerulo plasm i n 으로 되어 있고 약 151, 000 의 분자량을 갖고 있으며 blue p ro t e i n 과 0. 34% 의 Cu 또는 mol 당 8 개 의 Cu 원자를 가지 고 있 다. 12) 쥐 에 있 어 서 는 cerulo- p lasm i n 이 99%, 개는 88%, 그리고 돼지는 58% 로 나타났다. 사람의 정 상적 인 혈장은 100ml 당 약 30mg 의 cerulop la smi n 을 함유하나 임신기간이나 호르몬 치료, 혹은 피임약 복용, 또는 전염 병 에 질 렀 을 경 우 cerulop la smi n 이 상승한다. 13) Cerulop la smi n 은 단백질과 결합되어 있기 때문에 단백질 섭취, 체내합성과 밀접한 E 관계를 갖고 있다. 그러므로 단백질이 부족된 영양상태인 kwashio - rkor 나 Fe 결핍 시 에 는 cerulo p lasm i 、 n 의 감소현상이 나타난다. 그 러나 marasmus 에서는 감소현상이 거의 나타나지 않는다. Cerulop la smi n 의 가장 중요한 기 능으로는 Fe2+ 이 산화과정 에 서 촉매 역 할울 하는 것 으로 fer roxid a se I 이 라고도 한다. 이 효소는 Fe 을 운반해 주고 hemog lo bin 합성 을 가능하게 해 준다. Album in과 느슨하게 결합된 Cu 는 〈직접반응〉울 한다고 알려졌 으며 이 것 은 Cu 와 복합된 시 약 (d it h i zon, die t h y ld it hi o c arbonate ) 과 자유롭게 반응하며 체 내 에 서 는 Cu-albumi n 으로 알려 처 있으며 노란색 효소로서 fer roxid a se II 라고도 한다. 14) 이 두 형 태 가 합쳐 진 전체 혈장의 Cu 함량은 정 상적 인 조건 하에 서 는 80~150µg /1 00mf 이다. 3.3 대 사 정상인의 Cu 대사는 장관에서 흡수되어 간에 저장되며 간에서 특 수 단백질과 결합한 후 cerulo p lasm i n 으로 이동되어 대변으로 배 설된다고 한다 .15) 그림 3.1 은 구리 (Cu) 대사의 경로이다 .16) 대사과정을 보기 위해 방사선 동위원소 “Cu 를 사용했는데 섭취 칙후 주로 혈장의 albumi n, 분획과 결합되어 발견되었다. 혈장의 “Cu 는 album i n 에 연결된 Cu 가 간장과 기타 조직에서 Cu 단백질로 분배됨에 따라 감소하었
 드二\코/=尸巴- 0 6---_--三 ·l- - 6- 三.:m>' g J三j장 r「 0 1 三0 .8\m \g/ ;g~l I간 鬪 B대 m 변: 三 l2 g - 5 mg
드二\코/=尸巴- 0 6---_--三 ·l- - 6- 三.:m>' g J三j장 r「 0 1 三0 .8\m \g/ ;g~l I간 鬪 B대 m 변: 三 l2 g - 5 mg
다가 간장의 cerulo p lasm i n 에 도입된 Cu 가 혈액으로 방출됨에 따 라 정차로 상승하였다. 3.3.1 홍 수 Cu 의 흡수는 소장의 공장 부분에서 가장 찰 이루어지는 것으로 보이나 정확한 홈수기전에 대해서는 아직 잘 알려져 있지 않고 다 만 가설에 의하면 일부 음석으로 섭취된 Cu 는 Cu-ami no ac i ds 복 합체를 형성하여 이 복합체가 Cu 의 흡수와 밀접한 관계가 있다고 한다. 17 ) 특히 Cu-ami no ac ids 복합체 중에 서 도 L-ami no ac ids 가 D-ami no ac ids 보다 더 흡수가 찰된다고 한다. Harr i s 등은 Cu 가 신체 조직 의 세 포막을 통하여 운반된다는 것 을 입증하였다 .18) Cu 가 소장접막에 운반될 때 몇몇의 세포질에 있는 단백질이 작 용한다고 본다. 여기에는 두 종류의 단백질로 하나는 sup e roxid e - dis m uta s e 와 다른 하나는 meta l loth io n ein 이 다.
Meta l loth io n ein 은 sulf hy d ry l gro up pro te i n 으로 meta l 과 연 걷되 어 있 으며 흡수시 다른 meta ll ion e 과 상호작용에 의 해 서 이 루 어진다고 볼 수 있다 .19) Meta l lth io n ein 이 합성 될 때 는 고농도의 Zn, Cu, Cd 이 그의 합성 윤 높여 주며 또한 Cu 흡수시 항상성 (homeos t as i s) 의 기능을 갖는다. 〈 Cu 의 흡수를 촉진시키는 인자〉 1) Cu 는 Zn 과 마찬가지 로 항상성 (homeosta s is ) 조절작용에 의 해 저 음석으로 소량 섭취했을 때에는 많은 양이 흡수되며 음식으로 많은 양의 Cu 를 섭취했을 때에는 홉수량이 감소된다 .20) 2) 임 신기 간 동안에 는 Cu 홍수가 촉진된다. 3) Ami no ac ids , fum arate , oxalate 와 EDTA 가 Cu 와 복합 체 를 형 성 할 때 흡수를 촉진시 켜 준다. 또 ami no ac id 의 중합(p ol y mer i za ti on) 의 정 도에 의 해 서 흡수가 다르다. 21) 표 3. 3 은 mono-, di- , 그리 고 tet r a -ami ne g ly c ine 의 흡수율이 다. 22)
 표 3. 3 Mono-, di- , t e t ra-am i neg l y c i ne 의 흡수율 22)
표 3. 3 Mono-, di- , t e t ra-am i neg l y c i ne 의 흡수율 22)
4) 섭취 하는 음식 물에 함유된 Cu 는 필수아미 노산 흡수를 촉진시 키 나 ami no acid 의 축합 (condensa ti on) 에 따라서 그 효과가 감소된 다. 5) 위의 HCI 은 섭취 석품에 함유된 Cu 복합체를 파괴하여 cu- io n 으로 전환시 켜 흡수를 촉진시 킨다. 그 예로 위 철제수술을 한 환자의 간장에서 Cu 함량이 감소되는 것을둘수 있다. 〈 Cu 의 흡수를 저해시키는 인자〉 1) 음식물에 들어 있는 ph y tic a ci d 는 Cu2+ 와 결합되어 영을 형
성 하여 흡수를 감소시 킨다. 2) Ascorbic ac id 도 홍수를 감소시 킨다. 23) 3) 높은 농도의 Ca, Zn, Cd, S, Mo 도 흡수를 처해한다. Ca 은 위와 장의 PH 를 변화시키며 Cu 와 함께 Cu(OH)2 를 형성 하여 흡수를 감소시키는 것을 소의 실험에서 볼 수 있었으며 24) Tom p se tt 25) 는 1940 년에 쥐 실험 을 통하여 Ca 이 Cu-Ca 영 을 형 성 하여 흡수를 감소시키는 것을 증명하였다. Mo 은 Cu 흡수를 방해 하거 나 변경 시 킨다고 알려 져 있 다. 1)2 6)27)28) Cu, Mo의 과량섭취시 Cu-Mo-S 복합체가 형성되어 쉽게 이용되 지 못한다고 한다. 그러나 M illi s 둥은 Cu 복합체도 흡수가 가능하다는 것을 실험을 통해 밝힌 바 있다 .29) Cu 의 섭취가 1. 5~3m g/일이라고 할 때 흡수는 1~60% 까지 넓 은 폭을 보인다 . 30)31) 또한 식 품으로 섭 취 하는 Cu 가 2~5mg 일 때 0.6~1 .6 mg 정도 흡수된다고 알려져 있다. 가장 흡수가찰되는 연 령충은 어란이와 청년기이다. CaveIl 과 W idd owson 은 젖 먹 이 들의 Cu balance 를 겁 사한 결과 중간 정 도의 Cu 섭 취 량 lOOµg /k g /1 일에 중간 정 도의 보유량 9µg / k g /1 일을 보였으며 5~10 개의 balance 는 배설량이 섭취 량보다 많 았다 .32) 1974 년 Alexander 와 그의 동료들의 보고에 의 하면 중간 정 도의 섭취 량인 Cu 35µ g /k g /1 일에 보유량은 4.6µ g /kg /1 일로서 약 13% 로 중간 정도임을 보고하였다. 그리고 3 개의 balance 는 neg a ti ve (-)balance 를 보였다. 33) Cu 의 흡수율과 보유율을 알아내기 위하여 다음의 여러 연구자들 이 사람과 동물을 통해 서 balance 겁 사를 하였 다. 32)33)34)35)36)37) 1942 년에 Macy 는 8~12 세 의 7 명 의 어 린이 들로부터 72 Cu-balance 를측정했다. 1979 년 Z i e g ler 는 태 어 난 지 78~727 일된 8 명 의 건강한 어 린이 들 로부터 80 Cu 一 balance 실험 을 하였 다. 36) 1 개 의 balance 는 72 시 간이 걸리 는 Fomon35) 의 방법 으로 오영 을
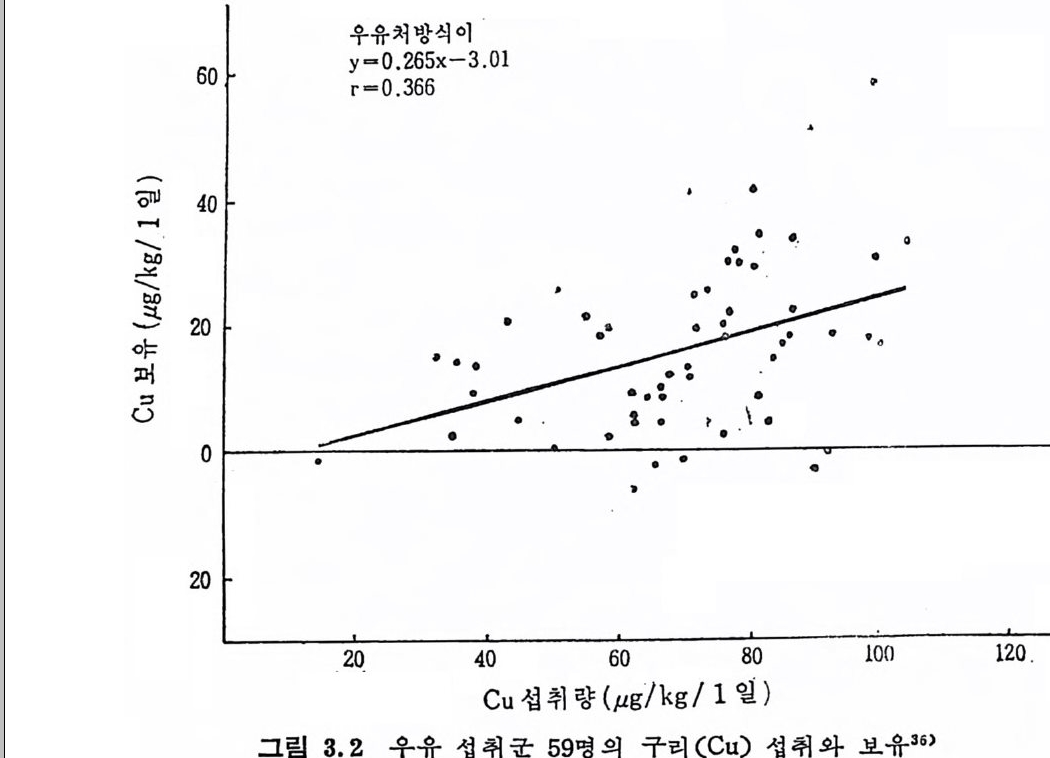
방지하기 위해서 뇨와 변의 채취시 청결히 다루었으며 득 델히 제조 된 Boros ili ca tg las 를 용기로 사용했다. 실험이 시작되기 11 일 전부 노 터 d i e t를 주기 시작해서 우유와 이유식으로서 섭취하는 군은 0.06 ~0.47m g Cu// 의 Cu 를 섭취시켰고, 두유를 섭취하는 군은 0.88~ 1. 16mg Cu// 의 Cu 를 섭 취 시 켰 다. 우유 섭 취 군의 59 개 의 balance 는 Cu 를 평군 70. 6µg / kg/ 1 일 섭취시켰으며 뇨를 통한 배설은 1.2 9· µg/ kg /1 일로 높은 po sit ive cr=o. 724 ; p< o. 001) balance 로 Cu 섭 취 와 비례했다. 흡수율은 평군 17.lµ g /k g /l 일로 섭취량의 23.9% 였 으며 평군 체내보유량은 15.7µ g /k g /l 일로서 섭취량의 2 1. 9% 이며 유의적 차이 cr=o.360; P
 60 y우r=- 유0 0. 치2.3 6방6 56식 x -이 3 .0 l
60 y우r=- 유0 0. 치2.3 6방6 56식 x -이 3 .0 l
Phy tic ac id 가 함유된 두유 섭 취 군의 13 개 의 balance 는 Cu 섭 취 137. 4µ g/kg /1 일에 서 흡수는 17. 8µ g/kg /1 일로 12. 6% 의 흡수율을 보였고 보유는 15 . 5µ g /k g /1 일로 10.8% 의 보유율을 보였다. 우유 에 비 하여 낮은 홍수율과 보유율을 나타낸 이 유는 ph y tic aci d 가 · Cu 의 흡수를 저해하기 때문일 것이다. 그러나 일반적으로 사람이 식품으로 섭취하는 Cu 가 2~5m g일 때 0. 6~1. 6mg 정 도를 흡수한다고 알려 쳐 있 다. 31)296)297 )29 8)299)300) 사람의 Cu 평형 실험에서는 섭취된 Cu 가 2mg 이상일 때 po sit ive - (+)balance 를 보였다 .36) 많은 양의 Cu 를 섭취하게 되면 기관에 처장되는데 제일 먼저 간에 처장된다. 정상보다 10~20 배 정도가 · 간에 처장되어도 독성을 일으키지 않는다. 표 3. 4 는 Cu 의 balance 와 동화작용을 정 상상태 의 소와 임 신한 소를 대상으로 Cu 를 p os iti ve(+ )로 섭취시킨 군과 부족하게 섭취 시킨 군과를 비교했다. 임선한 군은 Cu 를 부족하게 섭취시켰음에 . 도 불구하고 balance %는 정 상군과 펄 차이 가 없었다.
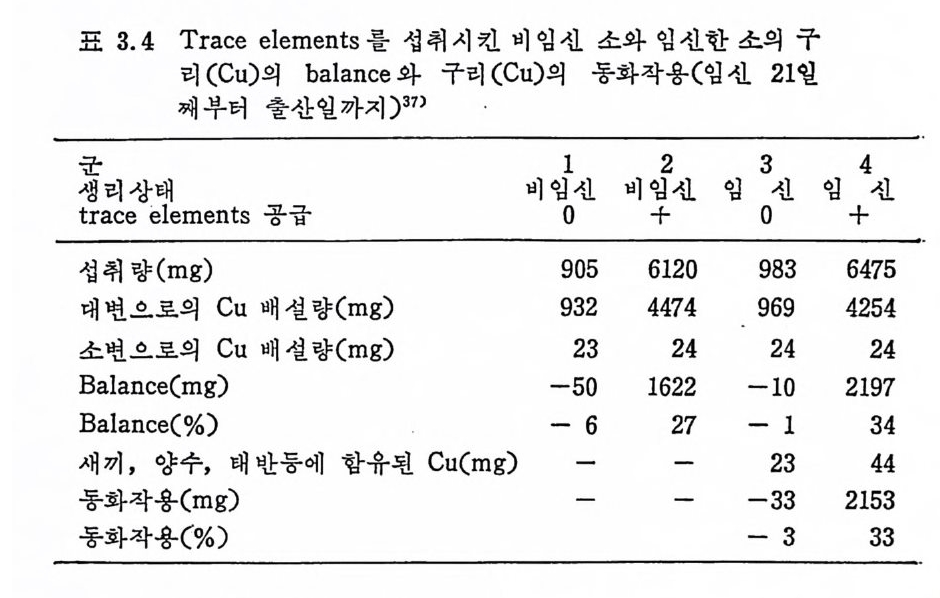 표 3. 4 Trace elements 를 섭 취 시 킨 비 임 신 소와 임 신한 소의 구
표 3. 4 Trace elements 를 섭 취 시 킨 비 임 신 소와 임 신한 소의 구
Cu 를 충분히 섭취한 임신 군은 매일 24m g을 체내에 보유했 으며 도합 2.2g 정도였다. 그러나 정상군도 1. 6 g의 Cu 를 보유왔
으며 매일 18m g의 Cu 를 보유한 셈이다. 표 3.4 에서 보듯이 비임신한 0 군이 Cu 를 -6% 보유한 반면 비 임 신한 +군은 27% 입 신한 0 군은 -1% 이 고 임 신한 +군은 34% 의 Cu 를 보유하였다. Cu 의 동화작용을 보면 임신한 +군은 매일 33% 인 데 비해서 0 군은 -3% 의 낮은 수준을 나타냈다 .37) 새끼, 양수, 태반 둥에 함 유된 Cu 량은 임 신한 0 군이 23mg , 임 신한 +군이 44mg 이 었 다. 완전히 규명되어 있지는 않으나 호르몬 (ACTH, cortic o id e , 갑상 선호르몬, 성선호르몬)이 Cu 대 사에 영 향을 준다는 보고도 있 다. 301 ) 3.3.2 저 장 섭취된 Cu 는 간에 처장되는데 간장의 Cu 저장률을 보기 위해서 · Cu 가 결핍된 쥐에게 Cu-ami no ac ids 복합체 혼합식이를 주었다• 표 3. 5 에 서 보듯이 Cu-asp a rag ine , Cu-th reonin e 을 제 외 하고는 나 머 지 Cu-lys in e , Cu-vali ne , Cu-is o leuc ine 과 ph eny la lanin e 은 대 조군 CuS04 와 비교할 때 처장과 흡수율이 약 30% 정도 중가되었 다(p
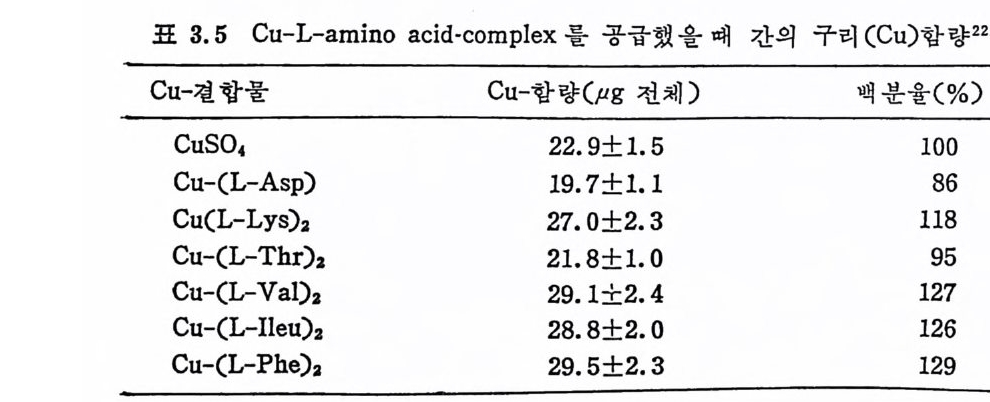 표 3. 5 Cu-L-ami no aci d- comp le x 를 공급했 을 때 간의 구리 (Cu) 함량 22)
표 3. 5 Cu-L-ami no aci d- comp le x 를 공급했 을 때 간의 구리 (Cu) 함량 22)
반대 로 표 3. 6 에 서 는 alanin e 과 leucin e 은 그의 중합(p ol y mer i:i.-i tion ) 정 도가 중가함에 따라서 간장에 저 장되 는 Cu 가 감소되 는 것 을 보여주고 있다 .40)
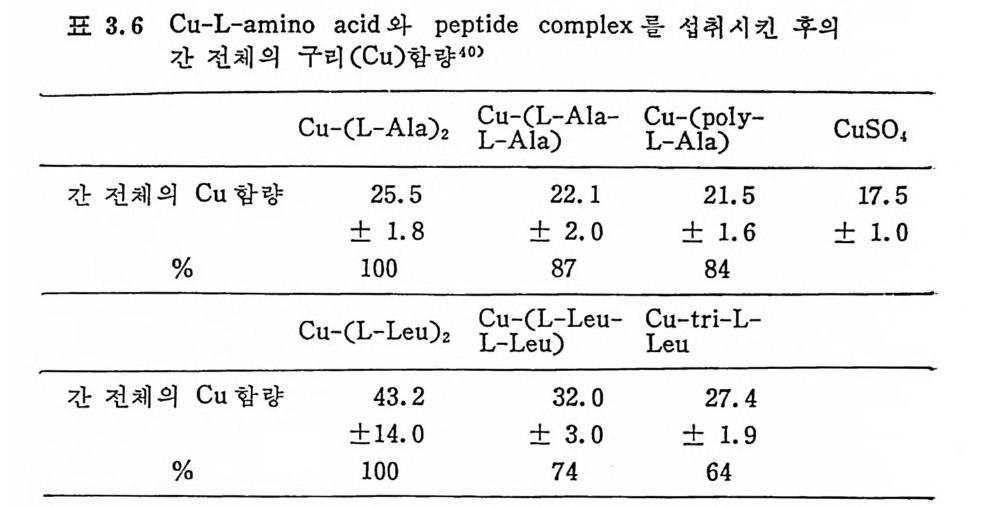 표 3. 6 Cu-L-ami no acid 와 pe p tide comp le x 를 섭 취 시 킨 후의
표 3. 6 Cu-L-ami no acid 와 pe p tide comp le x 를 섭 취 시 킨 후의
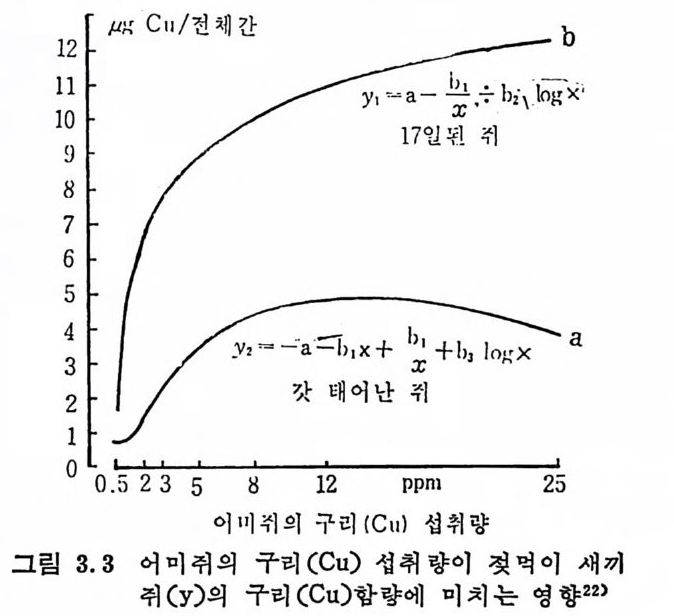
K i rch g essn P. r22) 는 어미쥐의 Cu 섭취량을 젖을 먹는 새끼취의 간
 2. µi.: C11/ 전체간 b
2. µi.: C11/ 전체간 b
장에 저장되는 Cu 양과 비교했는데 그럽 3.3 에서와 같이 갓 태어난 쥐는 어미취의 Cu 섭취량과 간장의 Cu 처장량과의 관계를 갖지 않 는 데 비해서 (a) 17 일 동안 젖을 먹던 새끼취의 간장의 Cu 처장량 은 어미쥐의 Cu 섭취량과 밀접한 관계를 보여주었다 (b). 3.3.3 배 섣 Cu 의 배설은 담낭울 통해서 이루어지는데 거의 대부분이 Cu 와 p ro t e i n 으로 연결되어 있으며 일부는 담즙산과 ami no acid , 그리고 짧은 p e pti de 사술과도 연결되어 있어 쉽게 오줌으로 배설되지 않 는다. 그 대부분은 담줍을 동하여 소장으로 배설되었다가 대변으로 제 거된다. Cu 는 ente r ohep a ti c c y cle 에 중요한 역할을 하지는 못한 다 .41) Cu 의 배설은 Cu 의 영양상태와 밀접한 관계가 있으며 또한 ·Cu 항상성 (homeos t as i s) 과 연관성 을 갖는다. 최근의 실험 보고에 의하면 사람은 하루 평군 I.7m g 정도의 Cu 를 담낭울 통해서 배설한다고 한다 .42) 또한 Cu 는 장벼울 동해서 장관으로 간다. 보통 오줌으로 배설되 는 양은 하루 5~50µ g으로 아주 적다. 그러나 홉수를 저해하는 복 합체를 형성하는 인자를 섭취했을 때와(예 ; Mo, S 등) 대사에 장 애가 생겼을 때에는 배설이 많아지게 된다. 땅과 월경으로는 극미 량 (0. 1mg ) 배 설된다. 44) Cartw rig h t 는 0. 5~1. 2mg 이 담낭을 동하여 , 0. 1~0. 3mg 이 장 으로 그리 고 0. 01~0. 06mg 이 신장으로 배 설된다고 발표하였 다. 43) Cu 의 배설을 추적하기 위하여 방사선동위원소 “Cu 를 사람에게 주사한 결과 거의 전부가 담낭을 통하지 않고 직접 장으로 배설되 었고 아주 저온 양이 신장으로 배설되었다. 쥐에 있어서는 99% 가 장으로 그리고 1% 가 신장으로 배설되었다. 3.4 권장량 우리나라에서는 아칙까지 필요량과 권장량이 결정되어 있지 않으
나 평형실험을 동하 여 미국이나 유럽에서는 안정선까지 고려해서 다음과 같이 Cu 를 권장하고 있 다. 어 린이 (6 세 이 하) ; 80µg / kg 체 중 어 린이 (6~10 세) ; 40µg / kg 체중 성 인 ; 30µg / kg 체중 1 일 권장량은 어 린이 (6 세 이 하) ; 1. 5mg 까지 /1 일 어 란이 (6~10 세 ) ; 1. 2m g /1 일 성 인 ; 2. 2m g /I 일 미 국의 1980 년도 RDA(Recommended Dail y Allowances) 에 서 는 Cu 를 하루 다음과 같아 권장하고 있다 .306)
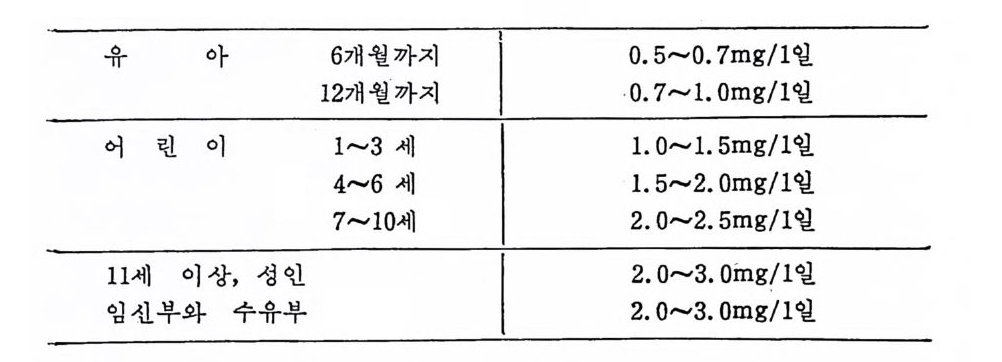 유아 6 개월까지 0. 5~0. 7m g /l 일
유아 6 개월까지 0. 5~0. 7m g /l 일
임신기간 동안에는 태아의 Cu 처장과 자궁의 Cu 축적에 근거를 두고 정 상보다 더 많은 양의 Cu 를 권장한다. 44) 사람의 경우에도 임신한 여성은 비임신 기간보다 2 배의 Cu 가 필 요하다는 것을 시사했는데 46) 이는 cerulo plasm i n 과 결합된 Cu 의 필요성 때문이라고 결론지을 수 있다. 또한 Henken 과 그의 동료 둘 46) 은 난포 홀몬의 상승 때문이라고 보고하기도 하였다. 모유에는 평군 50µg /lOOkcal 의 Cu 가 함유되어 있고 2/3 우유에 는 18~26µg /1 OOkcal 지 방이 adap tat i on 된 우유에 는 17~30µg /1 00 kcal, 완전 모유화된 우유에 는 10~20µg /l 00kcal 정 도밖에 들어 있지 않다. 1980 년 FAO/WHO 에 서 임 시 로 채 덱 했 던 유아의 Cu 권장량 (60µ g
Cu/IOOkcal) 에 대 하여 많은 학자들이 이 의 를 표명 했 다. 47)48) 우유만 섭 취 하는 유아에 게 Cu 권장량 6Q µg/ lOOkcal 은 너 무 높으 며 실천하기에도 비현실적이고 또한 모유나 우유를 섭취하고 있는 유아에게서 Cu 의 결핍증세률 발견하지도 못하였다는 것이다. 서양인의 Cu 섭취는 음석의 종류에 따라 다르지만 성인은 보통 · 2~4m g /1 일으로 보고되어 있다 .49) 미국의 경우는 1. 5m g /1 일로 . subop tim al 의 선이 라고 한다. 50) 3.5 Cu 결핍중과 Cu 대사장애에서 오는 여러 가지 질병 3.5.1 결핍증 토양에 Cu 가 부족되었을 때 그 지역의 가축에서 Cu 의 결핍울 · 볼 수 있었으며1) 저 Cu 식이를 실험식이로 주었을 때도 병아리와 · 취에서 Cu 결핍증세를 볼 수 있었다 .51)52) Cu 결핍시에는 점막세포에 의해 Fe 의 흡수는 영향을 받지 않으- · 나 혈장내의 Fe 방출은 처하된다• 이로 인하여 cerulo p lasm i n 의 합성이 감소되고 따라서 fer rit in 처장물로부터 혈장으로 이동되는 · Fe 이 감소되며 Fe 의 흡수와 이용이 감소되어 처 Fe 혈중이 발생 한다. 그 결과 heme 의 합성이 감소되고 이 결핍이 심하거나 장기 간 계속되면 사람과 동물에서 빈혈이 일어나게 된다. 양울 대상으로 실험한 결과 산화 • 환원에 관여하는 cy toc hrome· ox i dase 의 활성이 낮아졌는데 이는 대사의 신합성 부족을 초래하 · 는 1 차적인 장애이다. 호기성대사의 억제로 일어나는 내인성 ATP 합성의 감소는 어린 동물과 어란이들의 수초형성 (me y e li na ti on) 에 소요되는 인지질합성을 · 여제하는 현상이 나타났다. 골격 과 십 장 백 관 장애 는 ami ne oxid a se 인 lys y lo xid a se 활성 의 감소에 기인한다. Ly s y lo xid a se 는 Cu 를 가전 lys in e 과 hy d roxy ly s in e 의 탈아미 노 . 반응의 효소로 이 효소가 억 제되 었을 때 po lyp e p tide 사순간의 교 차연결 에 장애를 초래 하고 collag e n 과 동맥 elasti n 의 안정 성 과 강 -
도의 약화롤 초래 한다. 54) 또한 Cu 걷 핍 시 에 는 털 과 양모의 dis u lf ide bond 형 성 이 부족되 어 kerati n 형 성 이 찰 되 지 않는 것 을 들 수 있 다. D55) Trosin a se 활 성의 감소로 인하여 melan i n 색소의 부족현상이 일어나며 골격의 무기질감소와 성장부전, 순환기 계통의 장애 등을 초래한다. Bunch 등은 동물에서 신생아운동실조중, 생석능력감되와 소화기관 이상 등을 보였 다고 발표하였 다. 302) 쥐 실험결과 Cu 결핍시 (0.5 pp m 의 Cu 식이 때) 죽어서 태어난 쥐 와 낳아서 곧 죽는 쥐가 많았다. 표 3.7 은 0.5 pp m 의 Cu 식이와 25 pp m 의 Cu 식이와의 차이를 보여준다.
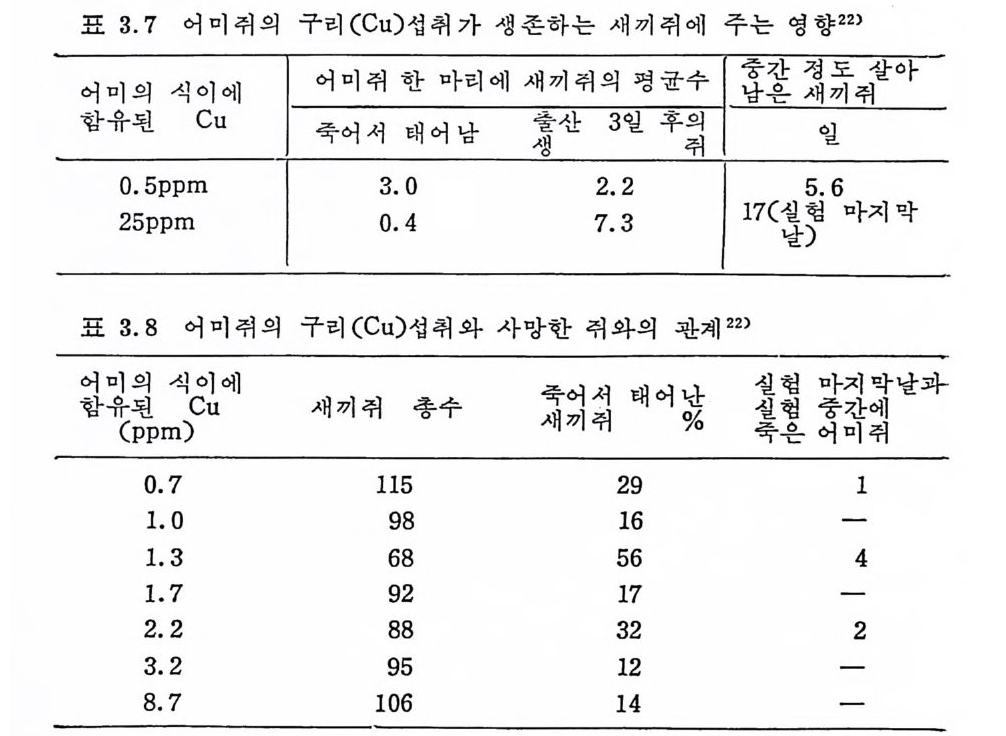 함표 유3된.7 어C미u 취의 구二리 (Cu )二 섭취가1 에생 촌^하;는: :새:끼:쥐:에; 1주 蠶는 영 :향〔 2尸2)취 살아
함표 유3된.7 어C미u 취의 구二리 (Cu )二 섭취가1 에생 촌^하;는: :새:끼:쥐:에; 1주 蠶는 영 :향〔 2尸2)취 살아
표 3.8 에서 보듯이 0.7~8.7 pp m 의 CU 석이 섭취와의 사이의 생 촌율을 보면 많은 편차가 있으나 3.2~8.7pp m Cu 식이 때가 월동· 히 사망율이 낮았음을 알 수 있다.
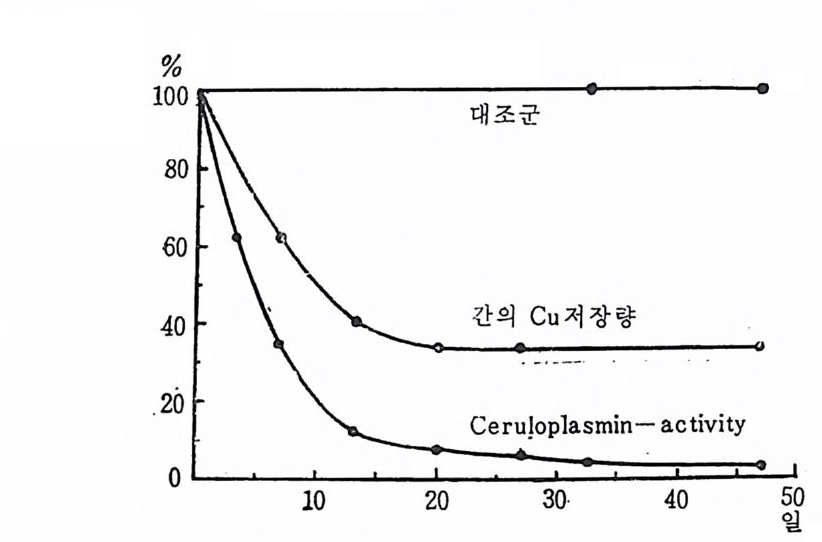
Cu 결핍 여부 를 알 아내기 위 해 서 cy to c h romoxid a se, 56 ) mono- -am i no xid a se, 57) 그리 고 cerulop la smi n( CP) 둥 5 8) 의 효 소 들 을 측정 했 다. Cerulop la smi n 의 감소는 Cu 의 결핍 울 측 정 하는 데 가장 정 확 한 척 도라고 할 때 S9)6o)GDG2 ) monoami no xid a se 와 cy toc hromoxi- dase 의 측정은 정 확 성이 결여됐다고 하겠다 .63)6 4 ) 정확성이 적은 이유로는 체내대사에서 어느정 도 의 유동성에 의해 서 Cu 결핍증이 심한 경우에만 두 효소의 변화치 를 볼 수 있으며 또 한 이는 신체기관마다 조금씩 민감도가 서로 다르기 때문이라고 한 다. 그러므로 위의 두 효소는 Cu 결핍중이 심한 경우에만 검사를한 다. 거기에 비해서 cerulo p lasm i n 은 사람과 동물의 종류에 따라 다 르나 혈장 중에 55~99% 까지 cerulop la smi n 형태로 들어 있다. 이 것 은 장에 서 albumi n 과 느슨하게 결합되 어 있 고 일부는 ami no .ac id 와 함께 문정 맥 을 통하여 간에 운반되 어 여 기 에 서 cerulop - 1asmi n 으로 배 치 된다. 65)66)67)66) Cerulo p las ini n 의 반감기는 약 5 일 69) 이기 때문에 Cu 의 섭취가 부 족될 경 우 아주 민감하게 반응한다(그립 3. 4).
 %
%
그립 3.4 구리 (Cu) 결핍시에 감소되는 간의 구리 (Cu) 저장량과 열 장의 cerulop la sm ac ti v ity(실형 동물 취 : 100)70'
Cerulop la smi n 은 Cu 걷 핍 증이 십 한 경 우는 물론 가벼 운 subop · :t i mal 일 경우에도 그것의 감소를 감지할 수 있다. 쥐 실험에서 Cu 식이룰 20µg /g 주었을 때 효소의 활성은 24 시간 이내에 80% 를 회복할 수 있었으며 4µg /g 섭취시켰을 때에는 효소 의 활성이 정상군과 같아지기까지에는 12 일이 결렀다 .70) 위와 같이 효소의 실험은 결핍증과 회복도 그리고 필요량을 측정 하는 데 좋은 지 침 이 되 고 있 다. 그러 나 ceruloi, la smi n 활성 온 음 식의 Cu 함량에만 있는 것이 아니고 또 다론 요인 등에 의하여 영 향을 받는다. 예를 들면 단백질이나 Fe 의 섭취상태 ,71)72)73) 7'1) 그리고 생리적인 상태 죽 나이 , 임신, str e ss 둥을 들 수 있다 .75) Cu 결핍증에 있어서 다음의 대사회로는 영향을 받지 않았다. 호홉 연쇄작용과 TCA 회로 중의 산화되는 부분, 지방산과 아 미 노산의 산화작용중의 cata l ase, cy toc hrome-c reduc tas e, tra ns • meth y la se, choli ne oxid a se 와 iso c itri c dehy d rog e nase 둥이 다. 또한 뇌 에 서 glu cose 와 pyr uvate oxid a ti on 도 영 향을 받지 않았 으며 혈액의 혈장단백질, Na, K, Mg , Ca, 그리고 무기인 (P) 역시 변화하지 않았다. 뇨로 배 설되 는 ami no ac id 는 정 상이 지 만 요산과 allanto i n 은 더 많이 배설되었는데 요산과 allan t o i n 의 비율은 요산이 훨씬 높게 나 타났다. 그러나 Cu 의 결핍증이 극한 상태에 이를 때에는 간의 iso c itri c dehy d rog e nase 가 상승되 었 고, cy toc hrome-c-reducta s e 는 감소했으며 TCA 회 로의 oxid a ti on 을 하는 부분은 거 의 측정 할 수 없었다. Cu 결핍 초기 단계 에 cy toc hrome oxid a se 는 4 주 이 내 에 40~70 % 까지 감소되 며 이 차적 으로는 succ ina te oxid a se sy s te m 도 감소되 었 다. 또한 전체 Fe 의 농도가 감소되 었 으며 76) 간의 mi toc hondria 추출시 빨리 변화되는 것을 볼 수 있었다. 간과립체의 fatty ac id- dehy d rase 의 활성 도 또한 감소되 었 다. 77) Cu 결핍 시 long chain fatty ac id 와 RNS 의 합성 에 는 변화가 없 었 다. 그 반대 로 간 mi toc hondria 의 ph osp h ati de 는 감소되 었 다.
또 acy l- C oA 와 a- gl y c erop h osph ate 의 축함반응이 처 해 를 받는 다. 또한 C14- g l y c i ne 의 실험에서 heme 합성이 감소되며 그로 인해 빈혈증상을 볼 수 있었다. 단백질 합성과 혈장 단백질은 Cu 결핍임 에도 정상인 것을 C1C gJy c i ne 을 통해서 입증하였으나 몇몇의 경우 감소된 것도 들 수 있다 .78) 동·식물 ` 조직 중의 Cu 의 형대에 대하여는 거의 알려져 있지 않다. Cu 는 Fe 과 마찬가지로 그 결합 상태에 따라서 효용에 차이가 있 다. Schul t ze5) 에 의하면, 밀의 씨눈, 알파파, 양조효모, 심장 및 간 장의 Cu, cy s ti ne 의 제 I Cu, meth y l cap tide , Cu- as p a rta t e , Cu- citra te , Cu-ph osp h orate 등의 Cu 는 중중의 빈혈인 흰 쥐에 유효 . 하지만 Cu - p or p hr i n 과 sur fe rous - Cu 는 별로 이용되지 않는다고 . 한다. 3. 5. 2 Morbus Wi ls on 씨 질 병 (Hepa t o l enti cu lene deg en erati on ) 1912 년 영 국의 정 신과 의 사 Ki nn er Wi ls on 이 발견한 Cu 대 사의 장애 에 서 바 롯되 는 질 병 (
거나 약간만 감소된 것으로 나타날 수 있다. 간장에 Cu 가 지나치게 축적되면 경변종이 발생하고 선장에 축적 되 면 세 뇨관에 장애 를 유발시 키 며 그 결과로 요산, ami no aci d pe p tide 와 포도당이 소변을 통하여 증가 배 설되 게 된다(표 3. 9). 눈의 descenet- m embrane 에 Cu 가 축적 되 면 각막 (cornea) 에 황금색 노랑 혹은 초록색 의 환 (r i n g)이 생 기 는데 이 것 을
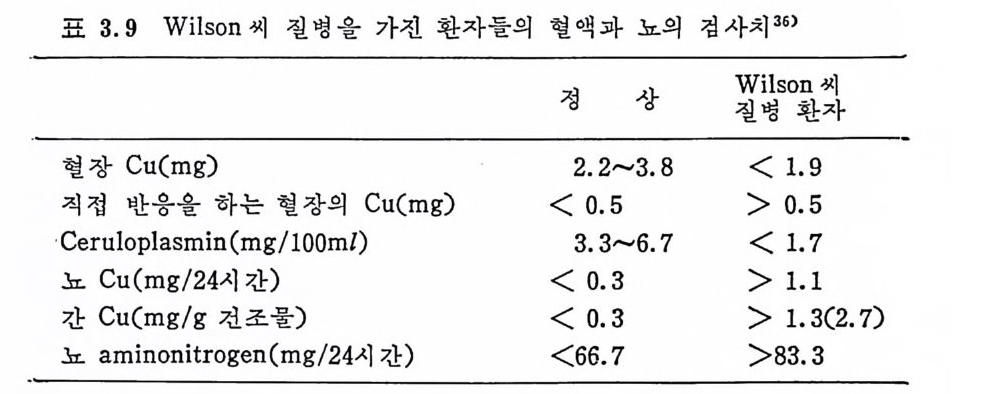 표 3.9 W i lson 씨 질병을 가전 환자들의 혈액과 뇨의 검사치 36)
표 3.9 W i lson 씨 질병을 가전 환자들의 혈액과 뇨의 검사치 36)
Danks 는 Cu 항상성 (homeos t as i s) 은 Cu 의 담즙배설에 의하여 조 절되어 이 과정이 W i lson 씨 질병을 처해한다고 했다. Cu 의 과잉축적 현상온 황달인 경우 의부의 황달현상이 없어져도 간 의부의 담즙 페쇄를 수술로 교정한 생촌자 가운데 6 명 중 5 명 정 도로 볼 수 있었으며 오렌 기간 동안의 Cu 의 축적은 간을 손상시킬 우려가 있다. 그 치 료로는 pe nic illam i ne 이 Cu 와 복합체 를 형 성 하여 Cu 를 배 선하므로 효과를 볼 수 있었다 .80) 3. 5. 3 Cu 과다혈증 (h yp ercu p rem i a) 사람은 미생물로부터 급성과 만성감염에 의해 이 질병이 발생하게 되는데 그 원인으로는 간장에서 cerulo p lasm in합성을 촉진해 주는
 백혈구의 내인성 작용물에 기인하는 것으로 보인다.
백혈구의 내인성 작용물에 기인하는 것으로 보인다.
풀에 비 해 서 우유의 Cu 함량은 1/2 에 불과했다.8 2) 분만후 2~3 개 월된 모유는 lOOg 당 약 35mg 의 Cu 가 함유되 어 있 고 성 숙유에 는 lOOg 당 15~40mg 이 들어 있 다. 초유에 는 lOOg 당 52~77mg 의 Cu 가 함유되 어 있 다• . 8 3)84) 우유에 는 100g 당 2~30mg 으로 평 군 10mg 의 Cu 가 함유되 야 있어 모유보다 적게 함유되어 있다 .85)
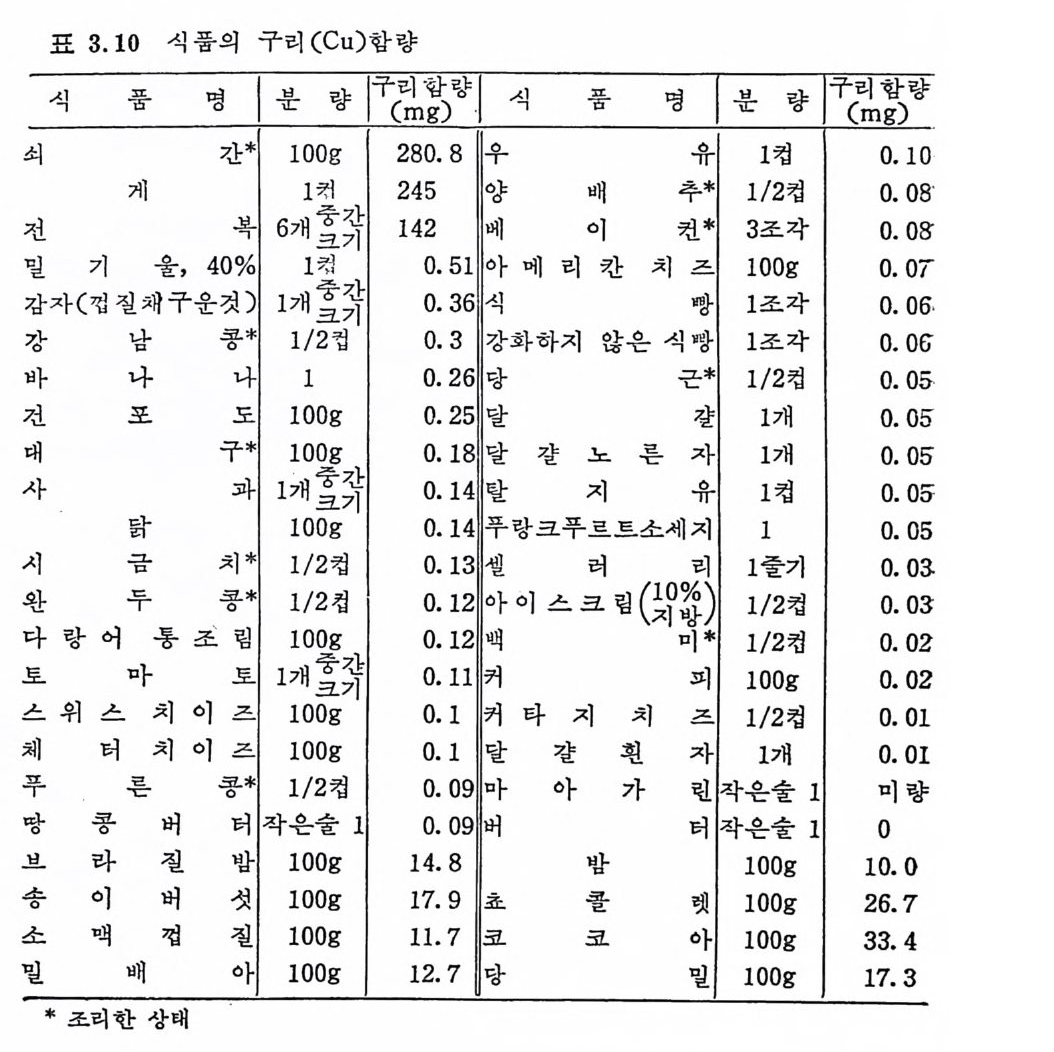 표 3.10 식 품의 구리 (Cu) 함량
표 3.10 식 품의 구리 (Cu) 함량
洪이 조사한 우리 나라의 곡류와 두류의 미 량원소 측정 에 서 Cu 는 쌀과 보리 종류에 따라 2pp m 내의였으며 밀은 7pp m 정도를 함유 하고 있다고 하였다 .305) 두류는 Cu 를 매우 많이 함유하고 있어 9p pm 정 도이 며 팥류는 8pp m 함유하고 있 다고 하였 다. 그리 고 깨 류는 9.5p pm 내외로 역시 그 함량이 많았다. 3.7 독 성 Cu 에 대하여는 많이 연구되어져 왔지만 지금까지 인체의 독성에 대한 실험은 거의 없고 주물공장에서 작업을 하는 사람에게서만 Cu 의 독성이 나타나게 되었다고 한다. 그러나 최근 연구에 의하면 alcohol 중독증에서부터 갑상선기능 항전증 (h yp er t h y ro i d i sm) 에 이 르기 까지 많은 질 병 들이 hy pe rcup re -mi a 를 동반한다고 한다. 87) 또한 동물은 높은 Cu 량에 아주 예민하게 작용한다는 것도 알 려져 있다. 쥐는 25mg CuS04/kg 상태에서 성장이 정지되고 양은 5~9% 의 CuS 이를 함유한 소금덩어리를 장기간 lOm g /k g /1 일 핥 아먹 으면 죽는다는 보고가 있 다. 88)89) 동물의 먹 이 에 200~300p pm 의 Cu 가 함유되 었 을 때 hy pe rth y - roid i s m 과 po rph y r ia 증상 (heme 합성 이 상증)이 나타났다. 3) 독성 의 증세 로는 위장관의 자극, hemoli tic anemi a, 황달 및 간 창과 신장의 되화를 둘 수 있다. Energy 대 사 이 상과 Fe, Mn, Mo, 그리 고 Zn 의 상호작용과도 밀접한 영향이 있다는 보고가 있다 .90)9 1) 92) Cu 가 조직에 과량 축적되면 독성을 나타내는데 그 중상으로는 빈혈 hemoli tic anemi a 둥이 대 표적 이 다. 1 일 10~15mg 이 상의 장 기 두여는 구토, 설사 둥이 나타나고 한꺼번에 20 g의 CuS 아를 섭 취 하면 hemoli tic anemi a 를 초래 한다고 한다. 1) 복잡한 대사와 상호작용 때문에 동물 독성실험에서 얻은 결과를 사람과 연관지운다는 것은 가장 어려운 문제 중의 하나라고 하 겠다. 그러므로 Cu 의 결핍증 치료시에도 필요량 약 2.5mg /70 kg
· (35µ g / k g)을 지표로 삼고 독성에 관한 많은 문제접을 고려해야 할 것이다. 3. 8 Cu 와 다른 미 량원소와의 상호작용
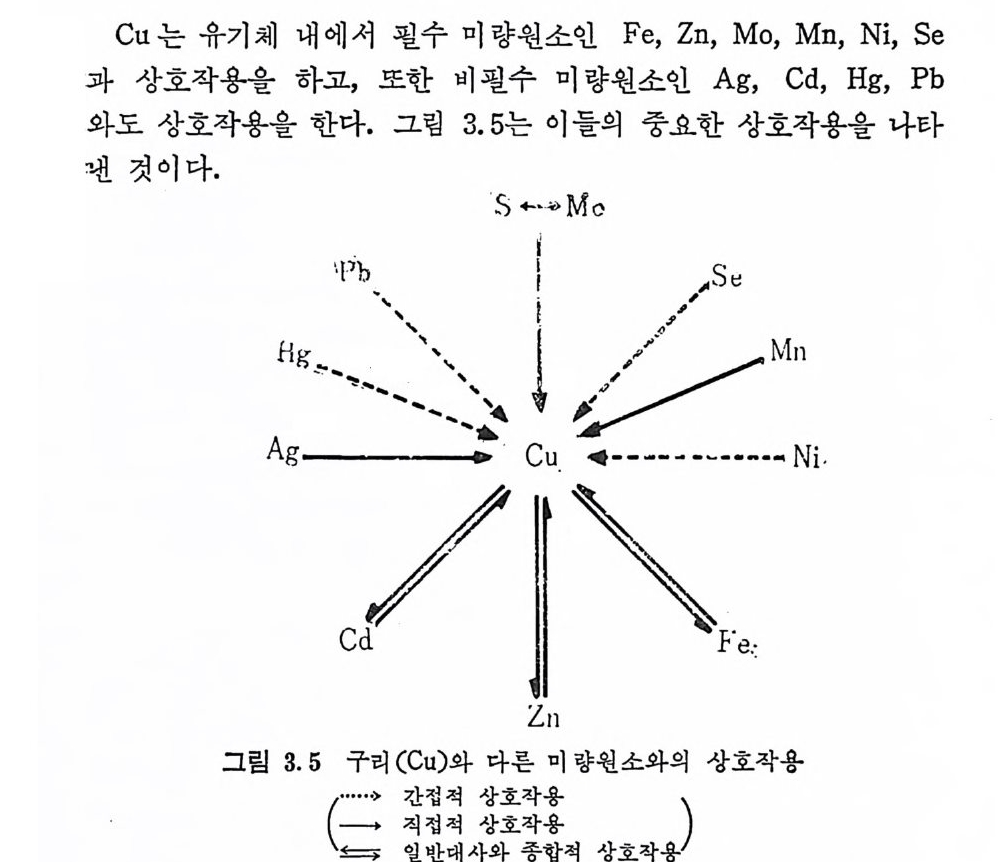 Cu 는 유기 체 내 에 서 필수 미 량원소인 Fe, Zn, Mo, Mn, Ni , Se
Cu 는 유기 체 내 에 서 필수 미 량원소인 Fe, Zn, Mo, Mn, Ni , Se
그러나 다른 미량원소와의 상호작용의 기전에 대하여는 정확하게 규명되어 있지 않다. 화살표는 Cu 가 다른 원소에 의해 영향을 받 는지 혹은 다른 미량원소에 영향을 미치는지에 대한 것을 나타내고 있다. 이 상호작용은 p os iti ve(+)이 거 나 ne g a ti ve(- )로 작용할 수 있 다. 음성적 상호작용은 하나 또는 그 이상의 미량원소가 비교적 과
다하여 Cu 대사기능에 방해를 하게 될 때를 뜻하며, 양성적 상호 작용은 그와 반대로 Cu 가 정상적인 대사 효율을 위해 하나 또는 그 이상의 미량원소를 필요로 할 때이다 .92) 미량원소 사이의 상호작용을 〈상승작용〉과 〈길항작용〉으로 설명 할 수 있는데 이러한 상호작용이 미량원소 대사에서 어떤 기능에 관련되어 있는지에 대해서는 아직 확실하게 알려져 있지 않다. 상호작용은 경쟁적 반응에 있어 배위자(lig and) 식 위치에 있을 때 직접적으로 나타난다. Dav i es92) 는 이 상호작용을 〈경 쟁 적 (com p e titi ve) 〉과 〈비 경 쟁 적 (noncom p e titi ve) 〉이 라는 용어 를 사용했 다. 상호작용은 소화, 흡수와 중간대사에 모두 영향을 준다. Cu 와 다른 미량원소의 직접적안 상 호작용은 Cu 가 다른 미량 원소에 의해 그 복합체로부터 치환되었 을 때나, Cu 가 그들의 복합체로부터 다른 미량원소를 치환시킬 때 발생 한다. 이 상호작용은 열 역 학(t hermod y nam ic s) 과 목별한 복합체 의 운동 안정성 (k i ne ti c s t ab ility)에 의해 설명된다. 복합체의 안정성 온 주로 미량원소의 전자배치와 배위자의 종류에 의하나 금속이온 의 전하 범위와 반응 환경 등이 또한 관여한다. 표 3.11 은 여러 가 지 복합체둘의 열역학적 안정성을 나타낸 것이다.
 표 3. 11 Meta l locarboxy pe p tida se 와 chelate s 의 안정 성 39)
표 3. 11 Meta l locarboxy pe p tida se 와 chelate s 의 안정 성 39)
Cu2+ 이온은 다론 배위자에서와 같이 단백질과 함께 매우 안정된 복합체를 형성하기 때문에, 복합체로부터의 치환은 다른 과량의 미 량원소가함께 촌재할 때만 발생하는 것 같다. 그러나 반대로, Cu2+ 이 온은 그들의 복합체 로부터 미 량원소를 제 거 하기 도 한다. 전자1--
배치와 이온 반경의 유사성 때문에, Zn 오1- Cu 사이의 상호작용이 특 히 강할 것으로 추측되며, 이것은 또한 배위자로써 단백질을 가 지고 있는 복합체에서 Cu2+ 와 Zn2+ 의 유사한 안정성 계수로서 명 확해진다. 그래서 몇몇의 금속효소에서는 Cu2+ 대신 Zn2+ 울 치환 하는 것이 가능하다. 그러나 가끔 이 치환으로 인하여 그들의 생리 적 활성을 잃는 경우도 있다. 또한 장내의 금속 결합작용에서 경쟁적 반응에 의하여 흡수 도중 Zn 와 Cu 사이에 상호작용이 일어날 수도 있다. Zn 의 과량 섭취는 Cu 의 홍수를 방해하며 반대로, Cu 의 과량 섭취는 Zn 의 흡수를 방해 하는 작용을 한다. 91) Cu 와 Ca 사이 의 상호작용은 생 리 적 환경 에 의해 조정된 상호작용의 한 예로 둘 수 있다. 반추 동물의 사 료에 Ca 의 양을 증가시켰을 때, Cu 의 흡수가 저하되었으며 95) 돼 치 96) 와 병 아리 97)98) 의 경 우에 있 어 서 는 Ca 의 흡수량이 사료에 포함 된 Ca 양의 중가에 의해 크계 영향을 받지 않았다. 이 결과로 미 루어 보아 단위 동물에서는 생체 내에 Cu 가 침전되는 것울 방해 하는 산이 충분히 촌재하는 데 반하여, 반추 동물에서는 소량의 Ca 보충이 되 씹 는 식 이 (rumi na l con t en t s) 의 pH 값을 증가시 켜 주고, 이로. 인하여 흡수가 적게 되어질 것이라는 가설에 의해 설명될 수 있다. Cu 와 다론 미량원소의 상호작용은 또한 단백질 특히 효소의 구 조를 안정시키는 키능과 관계가 있다. p e p s i n 은 Ca 의 첨가에 따 라 in v it ro 에서 활성화되거나 여제된다 -99 )1 00) 또한 Cu 와 다른 미 량원소와의 상호작용은 세 가지 형태로 알려졌는데, 그것은 부가 작용 (add iti ve eff ec t) , 경 쟁 작용 (com p e titi ve eff ec t) , 중립 작용(i nd if fer ent e ff ec t)이 라 할 수 있 다. 101) 부가작용은 Cu2+ 와 Fe2+ 사이 의 상호작용에서 Cu2+ 와 Fe2+ 이 분리되었다가 다시 결합할 때 사용 된다. Cu2+ 와 N i 2+ 울 동시에 부가시킬 경우, 그 작용은 경쟁적이 다. Cu2+-Ni 2+ 결합에 대 한 교체 율 곡선(t urnover-ra t e curve) 은 Cu2+ 나 Ni 2+ 하나만 부가하여 얻어전 곡선의 중간을 나타냈다. 반대로, Cu2+ 울 가지고 있는 배양기에 Zn2+ 울 동시에 부가시키는 것은 Cu2+ 을 독접적으로 부가하여 얻어전 p e p s i n 의 활성에 영향을 주지
못했 다. 용액 에 서 pe p s in 의 자동 촉매 작용의 가수분해 (auto c ata l yt ic ' h y drol y s i s) 는 결합 위치가 같거나(경쟁 혹은 중립 작용), 결합 위치 가 다른 작용(부가작용) 모두를 포함하여 , 금속 복합체 형 성 에 의 해 뚜렷하게 분해속도가 늦추어졌다. 지금까지 Cu 와 다른 미량원소의 상호작용에 대한 기술이 대체 로 화학적 원쳐율 적용시켜 설명되어졌지만, 가끔 생리적 상호작용 에서 화학적 원칙을 벗어날 경우도 있다. 그러므로 상호작용에 대 한 광범위한 연구가 앞으로도 계속되어쳐야 한다. 가장 깊이 연구 된 상호작용은 in v i vo 에서의 Cu 와 Fe 의 상호작용으로 볼 수 있 디-. 3.8.1 . Cu 와 Fe 의 상호작용 Cu 와 Fe 사이의 상호작용은 Hart 둥 2) 에 의해 젖먹이 쥐의 빈 혈에 있어서 Fe 와 함께 Cu 가 공급되어졌을 때만 치료가 가능했 · 다는 보고에서 알려지게 되었다. Fe 과 Cu 의 이러한 상호작용은 형태학적으로 구분할 수 없는 혈색소가 감소된 적혈구성 빈혈 (h yp o- -ch romi c mi cr ocy tic anem i a) 이 생 기 기 때 문인 것 으로, 불충분한 Cu 의 공급은 Fe 이용에 영향을 준다는 것을 보여준다. 이와 관련하 여 다론 동물의 빈혈 형태에 대해서도 많이 알려졌고, 그에 대하 여 논의 되 고 있 다. 102) 그러 나 혈액 학적 변수(p arame t er) 가 변화되 · 고, Cu 를 많이 복용시켰을 때는 소적혈구성 빈혈과 용혈 현상의 빈 혈이 발생하였다 .5) 사람과 동물의 영양에 있어서 Cu 와- Fe 사이의 상호 관계의 중요 성 때문에, 많은 연구자들의 관십이 이들 두 미량원소의 상호작 용에 집중되었으며, 처음에는 Fe 대사에서 Cu 가 주는 영향에 관한 것이었으나 반대로의 연구에서 Cu 대사에 Fe 가 주는 영향에 관십 이 증대되고 있다. 3.8.1. 1 Fe 대사에 대한 Cu 의 영향 Elvehje m 동 103) 의 연구 이래로, Cu 의 결핍이 Fe 보유에 미치는 영향이 알려졌다. Cu 의 결핍은 간과 지라에서 Fe 의 축적을 상승 지 킨다고 하는데 이 반옹은 쥐 104) 10 5)106)107 )6 3), 양 108), 소 109) 의 연구
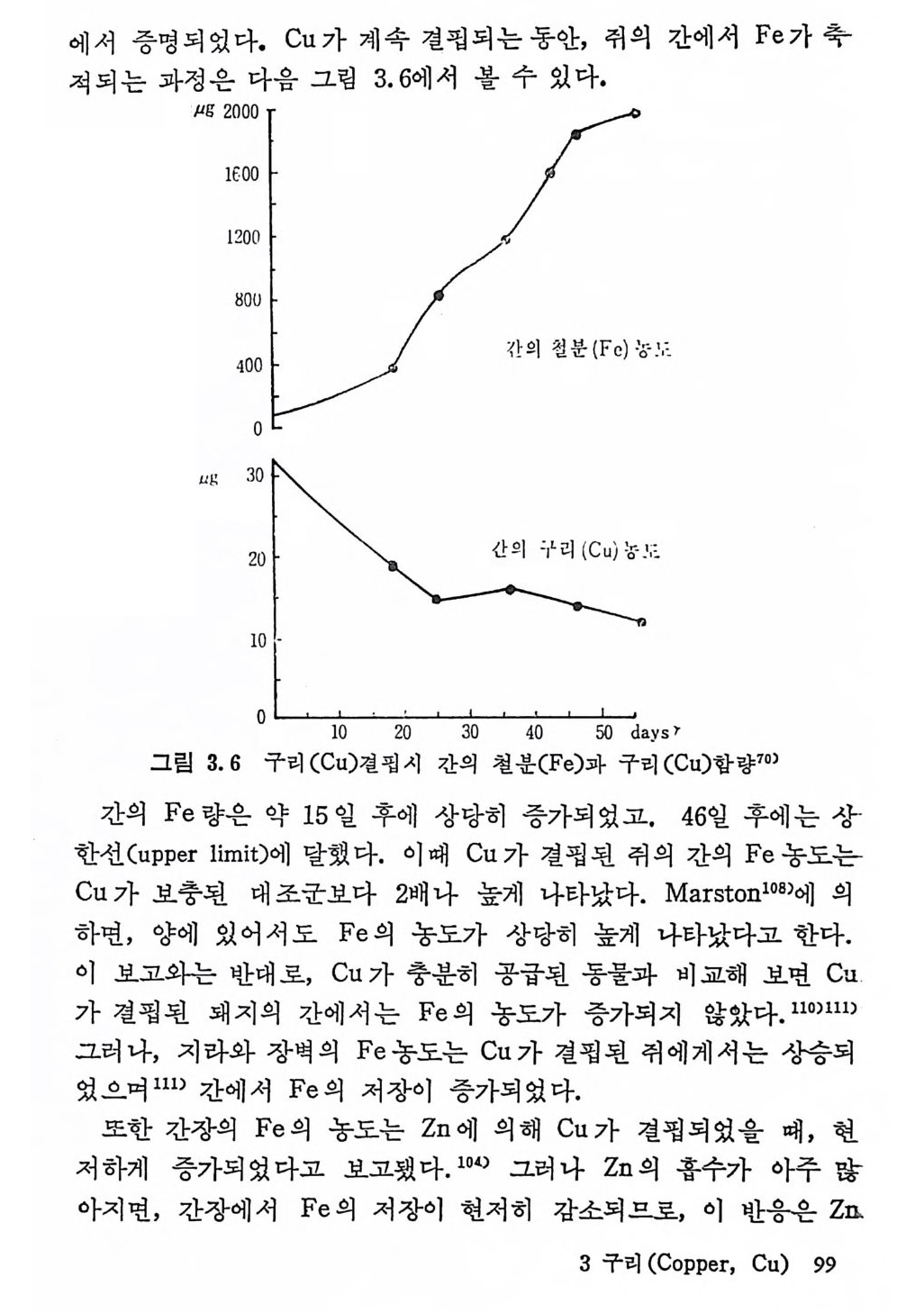 적에서되 는증 명과되정µ었g은 다210 82000. 다0U0 음C u그 가림 계3속.6 에결서핍 되볼는/ 수동 안 있,다 .쥐 의 간에서 Fe 가 축
적에서되 는증 명과되정µ었g은 다210 82000. 다0U0 음C u그 가림 계3속.6 에결서핍 되볼는/ 수동 안 있,다 .쥐 의 간에서 Fe 가 축
복용량의 영 향을 받는다고 하겠다. 112)113) Cu 결핍 식 이 나, Zn 에 의한 Cu 결핍은 Cu 의 보충식이로 인해 Fe 의 축적 현상이 다시 정 상으로 되 었 다 114 )1 06) 고 한다. 그러 나 이 미 상승된 Fe 의 감소는 많 온 시 간을 필요로 한다. 쥐 실험 에 서 , CuS04 로서 3. 2mg / kg 을 사료에 보충시키면 14 일 후에는 Fe 이 축적되었으며 Fe 의 축적률 온 Cu 의 복용량에 영 향을 받았다. 70) Evans 와 Abraham115) 도 35p pm 의 Cu 로서 충분한 양의 식 이 를 공급했울 때 , 2 일 후에 간장의 Fe 이 30% 가량 감소했고, 5 일 후에 는 정상치 이하로 내려가는 것을 알아냈다. 또한 Marsto n 둥은 106) 다른 기 관 상호간에 Fe 교환력 의 차이 가 있다고 보고하였다. Cu 결핍과 Fe 축적 이의에도 Cu 과잉 섭취와 Fe 축적에 대한 연구도 중요시되고 있다. 여러 연구자들은 Cu 를 주입시키거나 사료에 Cu 의 양을 접차 중 가시 켜 서 , 간의 Fe 농도의 감소에 대 해 연구하였 다. 114)116)117)1 0 6) K i nnamon118) 은 Cu 식 이 를 200mg / kg 섭 취 시 는 Fe 의 변화에 반응 이 없 다고 밝혔 으며 Ki rc hg e ssner 와 vVeser11” 는 ' 균형 시 험 (balance t r i als) 에 서 , 125~250mg / kg 의 Cu 가 강화된 사료를 섭 취 한 성 장기 의 돼지는 대조군보다 더 많은 Fe 을 함유하고 있다고 보고하였다. 여러 기관에서 Fe 의 저장이 증가되었음에도 불구하고, Cu 가 결 핍 되 어 있 는 동안에 는 hemo g lob i n(Hb) 의 농도, hemoto crit ~l, 적 혈구 수와 같은 혈액의 변수는 접차적으로 감소되었다. 이 현저한 효과는 쥐 70)105)115) 와 돼 지 76)120) 에 게 서 관찰되 었 다. Hemog lo bin 량의 감소는 Cu 공급과 함께 Fe 의 공급을 동시 에 관련시 켜 관찰하는 데 쥐 를 이 용한 연구에 서 명 백 하게 나타났다. 70)71 )10 5) Gubler 둥 76) 에 의 하면, 근육의 my o g lo bin 농도는 Fe 결펑 에 의 해 서 현저히 감소되며, Cu 가 결핍된 동안에는 영향을 겨 받지 않았다고 한다. Cy toc hrome 에 관하여 , Cohen 과 Elveh j em121) 은 Fe 과 Cu 가 부 족하게 공급된 쥐의 심장이나 간 조칙에서 이들 효소가 약간 감소 되 었음을 관찰했 다. Cy toc hrome 의 양은 이 두 미 량원소의 동시
복용에 의해서만 중가되었다. 여러 연구에 의하면, c yt ochrome 은 Cu 의 부족보다 Fe 의 부족에 더 민감하게 반응하는 것으로 보여전 다. 그러 나 Cu 를 함유한 cy toc hrome oxid e 는 cy toc hrome 중에 서 예의가 된다. 실험을 한 여러 조직에서, cy toc hrome ox i dase 는 Cu 의 불충분한 공급에 의 해 주로 영 향을 받으며 102)1 2 2) 12 3) 또한 Zn 에 의 한 Cu 의 결핍 시 에 유효한 것 으로 보여 진다. 112)1 2 4)125)126) Cu 가 결핍되었을 때, 산화효소의 활성변화는 Fe 보유의 중가와 관련된 Fe 이용효율의 감소를 초래하였다. 쥐실험에서 혈액의 산화 효소의 활성은 Cu 가 충분히 공급된 대조군에 비해 Cu 가 결핍된 쥐군 (7 주 후)에서 더 낮게 나타났다 .70) 그러나 단기간의 다른 실험에서는 71) 이 산화효소의 활성이 영향을 받지 않았다. 이와 비슷한 실험이 Zn 에 의해 Cu 가 결핍된 동안에 도 관찰되 었 다. 125) 또한 Schult ze 등 127) 도 쥐 의 신장, 간, 혈액 에 서 의 산화효소 활성 이 현저히 감소되었음울 알아냈지만, 사료에 Fe 과 Cu 의 보충이 둘 다 적었기 때문에, 그들의 연구에서는 명확한 관계를 찾아내지 못했다. Lahey 둥 120) 은 돼지의 적혈구에서 산화효소의 활성이 감소되었음 울 알아냈으며 그후 이 연구팀 76) 은 간에서도 산화효소의 활성이 감 소됨을 보고했다. Theorell 등 128) 과 M ill er129) 의 연 구에 의 하면 , 산화효소 형 성 과 Hb 의 heme 부분의 생합성온 같은 방법을 취한다고 하였다. 그렇 지 만 이 두 Fe 금속 단백 질 (iro n me t allo p ro t e i n) 의 결 핍 과 충분했 을 때 의 반응 곡선은 이 미 1941 년에 Schultz e 둥 127) 에 의 해 언급되 었 던 것처럼 확실한 평행선은 아니었다. 위의 연구를 종합 검토하여 Ma t rone102) 은 산화효소의 활성은 부 가적 요인에 의해 영향을 받으며, Cu, Fe 의 상호작용 연구에 효소 둘의 측정은 한정되어 있을 것이타고 추측했다. 이 가정의 도움으로, 이 효소의 활성에 대한 식이 단백질의 양과 질의 영향에 대한 연구가 시작되었다 .130) Fe 의 흡수과정 131)110)120) 중간 대 사과정 과 적 혈구 조혈과정 둥
의 132) 13 3>102) 12 0> Fe 대 사에 있 어 서 Cu 가 어떠한 영향을 주는가는 다 - 음과 같이 연구 되었다. Cerulop la smi n 이 fer roxid a se 로서 작용한다는 것 이 알려침으로 써 134)135), Fe 이용에 대한 Cu 의 영향은 확실한 것으로 단정할수 있 다. 136)137138) 13 9) Cerulop la smi n 은 2 가 이 온을 3 가 이 온으로 산화시 키 며 , 그로 인 하여 tra nsfe r rin 으로의 이 동이 가능하게 된다. 140) Cerulop la smi n 은 Cu 의 영 양 상태 에 민감하게 반응하기 때 문 에 68)59)70 )1 41)142) (그림 3. 7), 간장과 다론 처 장 기 관에 서 Fe 의 보유와 - 동원도 같은 속도로 영향을 받는다는 것을 알 수 있다.
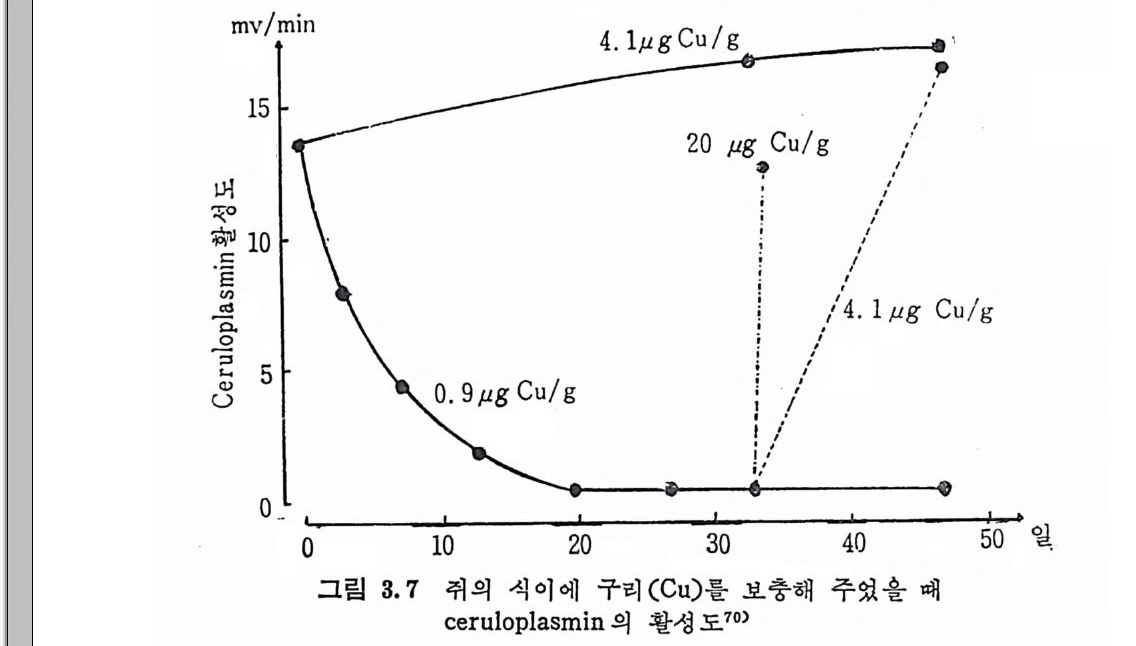 mv/mi n .' ?c
mv/mi n .' ?c
Fe 동원에 대한 효과는 혈장의 Fe 과 Fe me t allo p ro t e in의 농도 의 차이로써 설명할 수 있다. 여기서 Cu 가 불충분하게 공급되는 동 · 안, Cu-Fe 의 상호작용이 일어나게 된다. 중간대사에서도 Cu-Fe· 상호작용은 Fe 홉수에 영향을 미친다. Cu 가 결핍된 동안, 장접 막의 Fe 의 함량은 상승되었으며, 장벽의 Fe 농도의 현처한 중가 에 대한 반웅으로 Fe 의 흡수가 낮아졌다 .143) 그러므로 Cu 의 잘
핍은 Fe 의 흡수를 감소시킨다고 할 수 있다 .144 )1 45)102)111) Cu 의 과량 공급에 서 오는 간의 Fe 농도의 변호H 즌 fe rroxid a se 의 작용에 의해서만 설명되어질 수 없으며 또한, 장관 내부와 중간 대 사 등에서 발생하는 치환작용은 i nv it ro 에서의 연구결과와두 미량 원소의 복잡한 분석과정울 기초로 하여 생각되어질 수 있다 .119) Cu 와 Fe 의 상호 작용은 Fe 의 대사과정에서 Cu 의 영향과 반대 로 Cu 의 대사과정에 있어서도 Fe 의 부족량이나 과량의 Fe 공급에 대하여 연구될 수 있다. Cu 의 이용률과 Fe 공급의 결핍이 어떠한 영향이 있는가는 돼지를 이용한 Lahey 둥 120) 의 연구에서 시작되었 다. 이 실험에서 Fe 의 정상적인 공급시에 간의 Cu 의 양이 몇 배 로 증가되었다. 또한 쥐의 경우에도, 간의 Cu 의 양은 Fe 두여 8 주 이 후에 매 우 중가되 었 다. 63) 10 5) 다른 연구 71)72)146) 에서, Cu 의 축적은 Fe 의 공급이 불충분한 3 주 후에 이 미 나타났다. 그러 나 몇 몇 의 연구에 서 는, 147)148)149) Cu 보유와 Fe 공급에 대한 효과는, 간에서 발견되지 않았다고 하는데 이 모순된 결과는 Fe 의 한정 된 공급량과, 148) 실험 기 간, 그리 고 동 물의 성장률에 관계가 있는 것으로 보여진다. Fe 이 결핍된 동안 몇몇 기관들의 Cu 저장상태가 다르게 나타났 는데 , 이 는 Fe 공급이 여 러 가지 Cu met al lop ro t ei n 의 활성 에 차이 가 있기 때문인 것으로 보여지며, 체내 Cu 의 반응이 상승됨에도 불구 하고 Fe 의 결핍 약 3 주 후에 는 간에 서 cerulop la smi n 의 활성 이 현저 히 감소된 것 으로 나타났다. 71)72) 이 는 또한 cerulop la smi n 의 합성 감소나 Cu 결핍에서 기인되는 Fe 동원의 감소와바슷한 현상이 며 Fe 이 불충분하게 공급되는 동안 Cu 이용의 대사적 효율의 감소 로서 설명되어질 수 있다. 그 이의에도 Fe 결핍시에 나타나는 간장 의 m itoc hondria 에 촌재 하는 monoami ne ox i dase63) 와 cy toc hrome ox i dase150) 의 활성 감소도 이 런 방법 으로 설명 되 어 질 수 있 다. 확실 히 Fe 이 결핍된 동안 전체적인 대사율이 낮아침을 알 수 있다. 6~7g % 이하의 Hb 충은 여러 가지 종 (s p e ci es) 의 성장 지연과 관계 가 있다 .72)15 1) 152)153) 이러한 효소 활성의 감소는 체내의 대사물잘 의 합성 률이 처 하되 기 때 문이 라고 생 각하는데 74) 13 0) 예 를 들어 ce-
rulop la smi n 은 주로 단백 질을 합성 하는 동안에 형 성 된다. 15 4)155) 59) Cu 와 Fe 의 상호작용에서 Cu 의 흡수는 Fe 과는 달리 Fe 의 결 핍시에도 중가하지 않았다 .145)156) Fe 을 과잉 공급하면 간의 Cu 처 장과 분포에 영향을 받는다는 몇몇의 연구가 있다 .157) Di ck15” 은 동물에게 매일 5.2 g의 Fe 을 홍수시켰을 때 Cu 농도가 현처히 감소됨을 밝혔다. 그는 황산 Fe 이 약간의 Mo 과 함께 음이 온으로서 감소 효과의 원인이 된다는 것을 제시했다. 또한 Fe 의 과량 복용은 소의 간에서 Cu 의 결핍울 일으켰으며 158) 이는 Fe 의 공급증가로써 Cu 과잉 복용의 유독상태를경감시킬 수 있었다는 연구 159) 와 유사한 것으로 설명할 수 있다. 3.8.2 Cu 와 Zn 의 상호작용 Cu 와 Zn 사이의 상호작용은 서로 길항적이라고 생각된다. Cu 는 Zn 대사에 영향을 주며, 또한 Zn 은 Cu 의 대사에 영향 을 준다. 한 원소의 과잉 복용에서 오는 역효과는 다른 원소의 공급을 증가 시켜 줌으로써 억제된다. 체내대사의 정상기능을 유지하기 위하여 가장 중요한 접은 원소가 식이 내에 촌재하는 비율이다. 또한 석이 로 섭취하는 양은 흡수량과는 관계가적은데 그 이유는 위장관내에 서 그 원소의 화학적 결 합 형 태 die t a r y lig a nd, 무기 질 이 나 미 량원 소 등이 두 원소의 상호작용을 더 낮추거나 증가시키기 때문이다. 그러므로 Cu 와 Zn 의 상호작용에 대한 많은 연구둘은 흡수되기 쉬운 Cu 와 Zn 의 특정 비율에 관하여 연구되어지고 있다. 대사과정에서 Cu 와 Zn 의 상호관계는 Zn 공급이 충분하여도 Cu 가 부족되거나 혹은 과량 복용되면 방해를 받는다. 그러므로 Cu 의 공급이 적을 때 Zn 은 Cu 에 비하여 비교적 많은 양이 촌재 하며, Zn 의 영양상태는 영향을 받지 않는다. 간이나 골격에서 Zn 보유가 약간 증가되는 것은 Cu 가 정상적으로 공급된 대조군보다 Cu 가 결핍 된 동물군에 서 나타났다. 160)1 6 1 ) 또한 최 초의 연구 162) 에 서 Cu 가 결핍된 쥐의 골격, 간, 혈청의 Zn 보유량은 약 5~10% 증가되 는 것 으로 나타났다. 200~250mg / kg 의 Cu 가 성 장 촉진제 로써 성장하는 돼지에게 복용시켰을 때 163) Cu 의 흡수는 Zn 의 공급
조전에 따라 달라졌다. 돼 지 의 착각화중(p arakera t os i s) 에 최 적 량의 Zn 이 나 과량의 Ca, 혹은 ph y tat e 를 사료에 125~300mg / kg 의 Cu 와 함께 공급하였 을 때 착각화증과 피부장애를 완화시키거나 완전히 회복시켰고, Zn 공급시 의 효과와 거 의 동등하게 나타났다. 114) 16 5)166)1 6 6)167) 그 이 의 에 병아리의 콩 단백 석이에 Cu 를 첨가하면 Zn 의 유용도를 증 가시켜 주는 것으로 보여졌다 .168) 두석 실험 (dia l ys i s ex p er iP.J en t)에 서 는 Cu 이 온이 낮은 천화력 으로 결합되어 있으면 Zn 의 흡수가 용이하게 될 수 있게 하기 위하여, 그들의 화합물로부터 Cu 를 다론 금속과 치 환시 켜 줌으로써 효과를 얻는다. Cu 를 과량 섭취시켰을 때 간의 Zn 보유가 증가되는 것은 Zn 홉 수에 대한 가설을 증명해 준다고 할 수 있다. 또한 O'Hara 둥 171) 과 Sutt le 둥 159),170) 은 간의 Zn 농도가 상승되 어 있는 상태에서도 Cu 의 과잉복용은 임상적인 Zn 결핍증세를 더 욱 십하게 하였다고 보고하고 있다. 식이의 Cu:Zn 의 비율을 변화시키는 데 있어 혈청의 Zn 과 Cu 함 량의 정반대적인 반응은 이 연구를 뒷받침한다. 따라서, Cu 의 과 량섭취에 기인하는 Cu 와 Zn 사이의 상호 관계는 장관 내의 중간대 사 과정에서 발생되는 것으로 보여진다. 또한 보급형태에 관계없이 식이의 성분에 차이가 있는 것으로 보여진다. Zn 이 결핍된 석사에서 Cu 와 Zn 의 적당한 비율을 얻기 위하여 2mg / kg 의 Zn 과 12~2COmg / kg 의 Cu 를 이 용하여 , Pallauf 둥 172) 과 O'Dell173) 은 in v it ro 에서 Zn 의 기능을 추정할 수 있는 연구를 했다. 그러나 Zn 대신 사용되는 Cu 의 대체효과가 명확하지 못하기 때 문에 Zn 의 결핍된 쥐의 체중과 Zn 의 변화에 대한 영향은 변하기 가 쉬운 것으로 보여진다. Cu 의 공급이 적당하게 계속되는 동안 Zn 의 공급이 번화되면 불군형을 초래하게 된다. Zn 이 결핍되면 Cu 를 많이 보유하게 되고 Zn 이 과량으로 복용되면 Cu 가 감소된 다. Cu 의 대사에서 Zn 의 결핍은 별개의 것으로 목수화되어처야한
다. 여 러 연구자들 20)174 )1 75)176 )1 7” 은 Cu 가 결핍된 동물과 대 조군의 동 - 물 사이에서 여러 기관과 조직의 Cu 의 양에는 차이가 없다고 하 였 으나, 178)179)180)181)182)183) Zn 의 농도가 감소됨 에 따라 간과 골격 에 서 Cu 의 양이 증가되었다고 보고한 연구자들도 있다(표 3.12).
 표 3.12 아연 (Zn) 결핍시 간장과 골격 의 구리 (Cu) 와 아연 (Zn)
표 3.12 아연 (Zn) 결핍시 간장과 골격 의 구리 (Cu) 와 아연 (Zn)
이 두 미량원소는 Zn 이 매우 결핍된 것소의 젖, 배설물 등에서 는 반대 반응을 나타냈다. 184) 그러 나 이 확실한 상호작용은 급식 실험 (pa ir - fe d or ad l i b it um) 이 나 사료의 Cu 량의 차이 때문이다. 또한 Cu 의 보충시 원소의 농 도변화는 각 기관 사이에서 일정하지 않았다. 그래서 신장과 십 장의 Cu 량은 Zn 이 결핍된 식이를 공급받는 동안 매우 감소되었 다. 마찬가지로 혈청과 혈액의 Cu 농도는 Zn 농도와 비슷하게 감 소되 는 경 향이 있 었 다. 20)180)181) 또한 Cu 의 공급이 일정한 농도로 유지되는 동안 Zn 의 공급이 매우 중가되면, Cu 는 상대적인 최소값으로 떨어진다. 그래서 Cu 농도의 영향은 Cu 결핍 정도에 따라 변화하고, cerulo plasm i n 과 cy toc hrome oxid a se 와 같은 Cu-meta l loenzy m e 의 활성 에 서 나타 나다며 . ,112 )1간13,) 1 26신) 1장27,)1 85)혈 186청) 1에87)서188의) 18 9) C19u0) 1농91)도 감소에 의해서도 증명되고 있 그러 나, 유효한 Zn 의 복용 농도는 건조물 식 이 100~lOOOmg / kg:
이상에까지 매우 넓은 범위에 걸쳐 다양하다. 그것은 석이의 내용 에 따라 Zn 의 흡수력에 영향을 주고, 그로 말미암아 Cu 대사에도 영향을 주기 때문인 것으로 보여진다. 또한, 동물의 종류에 따라 차이가 있는데 석이에 Cu 의 함량이 적을 때, 그 상호작용은 더욱 명확해진다 .192) Cu 의 농도에 따른 변화는 Zn : Cu 의 비율을 좁게 하기 위하여, ·Cu 공급을 증가시 킴 으로써 전환될 수 있다 . 같은 방식 으로, Cu 의 흡수가 과도한 동안, Zn 의 공급을 중가시 키면 Cu 중독증을 없앨 수 있다. 그래서 약물학적으로, Cu 를 과량섭취시킨 돼지에게 Zn 을 부가 적 으로 급식 시 키 는 것 은 간의 Cu 보유를 낮추어 주며 114)159)1 7 0), 혈 청 의 asp a rta te 와 ami no tr a nsfe r ase 활성 도 감소되 었 다. 159)1 7 0) 유 사한 현상이 반추 동물, 특히 양에게도 적용되었는데, 비교적 적은 양의 Cu 복용도 독성 효과를 나타내기에 충분했다. 이와 같이 상호 착용을 이용할 때, Zn 의 공급은 Cu 의 독성을 막는 효과가 있는 것 으로 보여 진다. 193) Cu 와 Zn 의 상호작용은 기관과 조직에 나타난 Cu 와 Zn 의 함량 이나 섭취식이의 Cu 와 Zn 의 체내 보유량의 변화에서 찾아볼 수 있 다. Cu 와 Zn 의 상호작용을 설명할 수 있는 생리학적인 결과는 각 기관과조직에서 이 두원소의 결합이나, 배설, - 흡수 과정 등에서 나타난다. Van Cam p en 과 그 연구자들 194) 은 Cu 와 Zn 은 서로 장내의 흡수 를 방해한다는 것을 입증했다. 섭이지장내의 Zn 의 과량 두여는 Cu 의 흡수를 매우 감소시켰고, 반대로, Cu 의 과량 두여는 Zn 의 흡 · 수를 감소시 켰 다(표 3.13). 이와는 달리 복강내에서는 각각의 원소 투여가 흡수에 영향을 주지 못했다. 마찬가지로, 공복상태에 있는 쥐에게 Zn 을 매우 많 이 두여한 5 주 후에도, 십이지장내로 주입한 Cu 의 흡수는 Zn 의 두여 량에 의 해 영 향을 받지 않았다. 112) Evans 등에 의하떤 ,19s) Cu 가 과량일 때, Zn 흡수 저하는 필요 량의 Zn 을 공급받는 쥐에게서만 나타났으며 Zn 과 Cu 의 흡수는
 Zn 이 결핍되었을 때만 좋아진다는 것이 몇몇 연구에 의해 나타났
Zn 이 결핍되었을 때만 좋아진다는 것이 몇몇 연구에 의해 나타났
 표 3.13 과량의 아연 (Zn) 과 구리 (Cu) 두여 시 아연 (Zn) 과
표 3.13 과량의 아연 (Zn) 과 구리 (Cu) 두여 시 아연 (Zn) 과
 표 3.14 아연 (Zn) 이나 구리 (Cu) 부 족 시 장관내의 아연 (Zn) 과
표 3.14 아연 (Zn) 이나 구리 (Cu) 부 족 시 장관내의 아연 (Zn) 과
 Zn 의 흡 수 증가가 Cu 의 결핍에 의한 것으로 알려졌으나, 활성
Zn 의 흡 수 증가가 Cu 의 결핍에 의한 것으로 알려졌으나, 활성
을 필요로 한다는 것을 추정할 수 있으며, 이러한 상황 하에서, 살 제로 Zn 의 홍수 증가몰 기대할 수 있으나 흡수 장소에 따라 Cu 와 Zn 의 상호작용의 기전에 대한 충분한 연구가 현재까지 제공되지 못하고 있다. Cu 의 in v it ro 에서의 장내 Zn 결합에 대한 실제적인 실험의 결과는 상당히 다르게 나타났다 .195 )1 97)198) 죽 Cu : Zn 의 비 율이 국도로 높아졌을 때, 반대로 Zn 의 결합이 낮게 나타났으며, 따라서 실질적인 세포 수송 과정에서는 영향을 받는 것 같다. 이와 관련하여, 여러 연구자들은 유리된 접막의 Cu 결합 단백질과 Zn 결 합 단백 질 인 199>200> meta l loth io n ein 에 서 의 201)202) 상호 치 환 작용 은 고려되어야 한다고 주장하고 있다. Cu 와 Zn 의 배설시의 상호영향은 흡수시에 나타낸 영향과 비교 해 볼 때 그다지 중요하지 는 않다. Parente ral Cu 의 중가량은 내 인성의 Zn 배설에 영향을 주지는 않으며 ,203>204> Cu 의 결핍도 내인 성의 Zn 배설에 영향을 주지 않는다 .196) 그러나 Zn 을 과량 공급 할 때는 소변으로 배설되는 Cu 의 양이 증가되었다 .112)124) 또한 대 변으로 배설되는 Cu 와 비교할 때 소변으로의 손실은 적은 것으로 나타났다. Cu 와 Zn 의 상호작용의 또 다론 과정은 세포내의 운반과 ,203) 체 내 중간 대 사 과정 중 ami no ac id, pe p tide 나 pr ote i n 과의 결합 192) 으 로부터 얻어진다. 그러므로 여러 가지 Cu 결합 단백질과 Zn 결합 단백질은 간과 신장의 군동질 (homo g ena t e) 에서 용해되기 쉬운 분류 · 법 (fr ac ti ona ti on) 에 의 해 나타난다. Bremner 둥의 연구를 비 롯한 몇 몇 의 연구 206)207)208)209) 결과는 Cu 와 Zn 이 대 체 로 분자량이 65, 000 에 서 75, 000, 약 35, 000~75, 000, 8, 000~12, 000 인 3 개 의 주요한 fr ac ti on 의 단백질과 관련되어 있는 것으로 나타났다고 밝혔다. 분 자량이 35, 000 인 frac ti on 의 Cu 와 Zn 의 양은 목수한 Cu 와 Zn 의 공급 상태와는 비교적 관계가 없었다 .206) 이와는 대조적으로, 낮은 분자량을 가진 fr act i on( 약 10, 000) 과 높은 분자량을 가전 frac ti on (약 70, 000) 의 Cu 와 Zn 의 농도는 이 미 량원소의 공급 보충 상태 에 따라 변했 다. 206)210) 분자량이 낮은 frac ti on (8, 000~12, 000) 은 Cu-th io n ein 과 Zn-th io n ein 을 가지 고 있 으며 , 201)210)211 )2 12)213)214) 이
둘은 금속의 상호작용에 서 중요한 여 할을 하는 것 으로 보여 진다. 결 합상태 에 서 의 상호치 환작용과 206>210> Zn 이 th io n ein 의 생 합 성 을 활발하게 하고 201 )21 1) 그들의 안정 성 을 중가시 키 며 , 그들의 분해 를 감소시 키 는 것 으로 보아 2os,209> th io n ein 에 서 Cu 와 Zn 사 이에 상호작용이 있는 것으로 보여진다. Zn 이 결핍된 동안 분자 량이 8, 000~12, 000 의 범 위 에 있 는 Zn-bin d in g pro te i n 과 Cu-bin - ,di ng p ro t e i n 을 함유한 fr ac ti on 은 비교적 작다. 반면에, 높은 분자 량을 가전 fr ac ti on 에 의한 결합 특히 Cu 의 결합이 필요하게 된 다. 206)210) Zn 의 공급이 적당하고 Cu 의 공급이 대단히 높을 때, 비슷한 효과가 나타났으나, 206)210) 양, 송아지 , 돼 지 , 쥐 사이 에 는 종에 따 라 차이 가 있 었 다. 207 )2 08) . Cu-th io n ein 과 Zn- th io n ein 의 기 능은 여 러 가지 조건과 산화전위 {redox p o t en ti al) 의 효과적인 이용 및 에너지 전달 과정과 함께 논의되 어져야 하지만, t h i one i n 은 금속의 처장이나 해독 과정에서 중요한 역할을 담당하는 것으로 생각된다. 이 기능은 Cu 의 과잉공급에 의 해 일어난 상대적인 Zn 의 결핍이나 영양적으로 Zn 결핍에 대한 €u 의 보유량 증가에 관련되어진다. 여기에서, t h i one i n 이 매우 짧 은 반감기 를 갖고 있 다는 것 은 홍미 로운 일 이 다. 202)207 )2 08) 그러 므 로 중간 대사에서 금속의 빠른 이용률을 조정할 수 있는 것으로 생 각된다 .211) 3. 8. 3 Cu, Mo, S 과의 상호작용 Fergu son 등 215) 은 처 음으로, 영 국에 서 Mo 이 많은 토양의 목초로 인하여 질병이 발생되었다고 보고했다. 〈 Tear t〉라고불리논 이 병은 설사와 쇠약증세를 나타냈으며, 그 목초는 정상적인 목초의 Mo 의 양인 3. 5mg / kg 에 비 해 20~lOOmg / kg 의 Mo 을 함유했 다. 이 때 ·Cu SO4 용액을 목초에 뿌리거나 동물에게 먹임으로써, 이 중상을 치료하거나 방지했다 .216) 따라서, Mo 과 Cu 의 상호작용에 원인 이 있다는 것이 분명해졌으며, 과량의 Mo 에 의해 발생된 Cu 의 결 핍도 관련되어 연구되었다 .21 7) 218) 이러한 현상온미국 ,219) 뉴우질랜
드, 220) 캐 나다, 221 ) 스웨 덴 둥의 소에 게 서 도 유사한 증세 가 나타났 다. 양을 이 용한 연구에 서 Dic k 은 223)224)225) 식 이 중의 S 의 양이 Cu 오} Mo 의 상호작용에 영향을 준다는 것을 입증했다. 이러한 많 은 원소들의 상호작용에 있어서는 종에 따른 차이가 분명히 있기 때문에, 실험적 연구는 각종 동물에 따라 각각 다르게 설명되어질 수있다. Cu 대사에 있어서 Mo, S 의 영향은 이 원소들의 공급 정도에 따 라 다른 결과가 나타나기 때문에, 특히 Cu, Mo, S 사이의 비율 은 대단히 중요하다. 식이의 S 의 양이 일정하게 유지되는 동안 Mo 의 공급 변화에 대 한 간에 있어서의 Cu 의 양의 변화는 그림 3.8 에 나타나 있다.
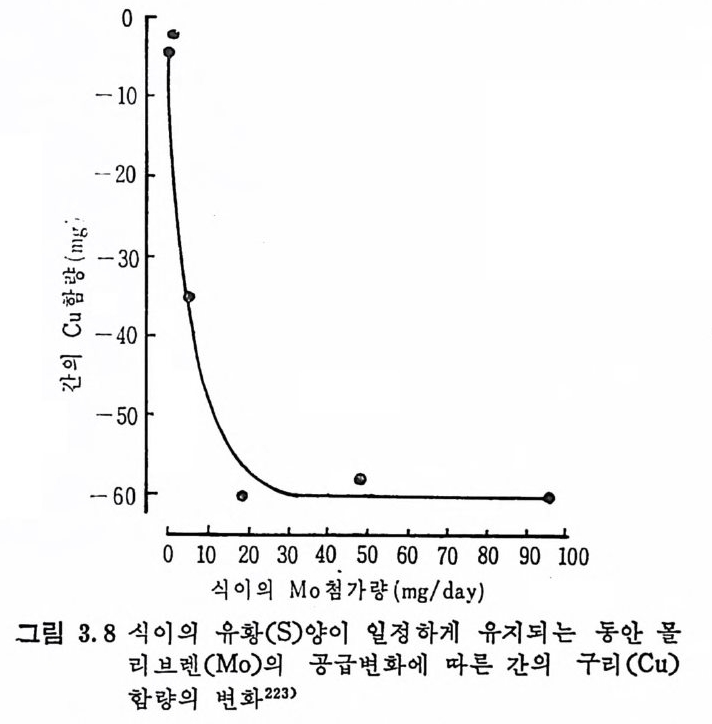 。 •
。 •
반면에 그림 3.9 는 S 의 공급이 변화되고, Mo 의 양이 일정할 때 의 관계를 나타낸 것이다 .223) 간에 Cu 가 다량 축적되면 Mo 와 S 의 흡수율이 처하된다.
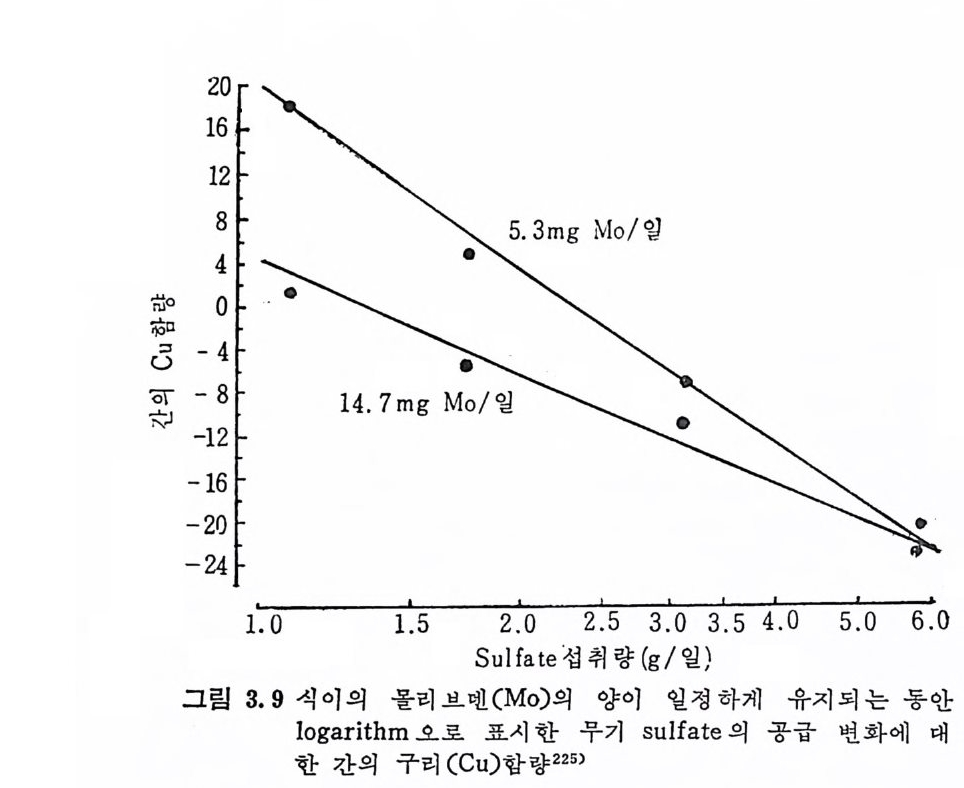 20-'_16 128404
20-'_16 128404
이 제 인자 (S, Cu, Mo) 의 상호관계와 양(羊)의 간에 있어서약 Cu 의 저장에 대한 연구결과를 표 3.15 에서 명확하게 나타내고 있 다. 226) Mo 과 S04 의 보충은 간의 Cu 의 보유와 축적 을 감소시 킨다. Mo 과 S04 의 보충에 대 한 간의 Cu 의 축적 의 정 합반응 (ma t ch i n g · res p onse) 은 W yn ne 등 227) 에 의 해 서 도 보고되 었 다. 그러나 많은 연구에 있어서는, 단독으로 또는 혼합하여 M.0 과 S 울 보충했을 때 Cu 의 상태에 영향을 주지 않는 것으로. 나타났 다 228)229)230)231) 지금까지 연구된 상호작용의 결과는 Mo 과 S 의 양이나, 그비율 · 에 관계가 많은 것으로 보여진다. 식 이 의 0. 03% 의 S 와 Mo 의 중가량이 (2. 4~9. 2mg / kg ) 간과 혈 장의 Cu 의 양에 영향을 주지 못한 데 반하여, 석이에 0.55% 의 s. 를 증가시켰을 때는 간과 혈장의 Cu 의 양을 감소시켰다 .232) Di ck , 1m225) Marcil ese , 233) Pi er son & Aanes, 234) Sutt le & Fi el d 둥도 간
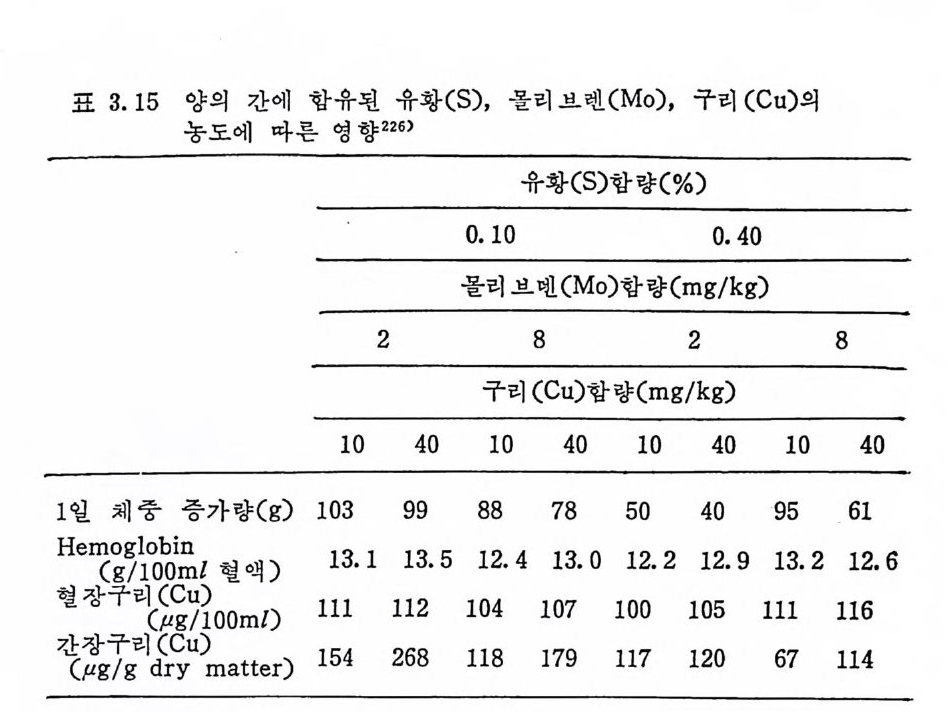 표 3. 15 양의 간에 함유된 유황 cs) , 문 리 브렌 (Mo), 구리 (Cu) 의
표 3. 15 양의 간에 함유된 유황 cs) , 문 리 브렌 (Mo), 구리 (Cu) 의
에서 유사한 결과 를 발견하였는데 과잉의 Mo 과 S 의 흡수는 Cu 의 이용과 대사 효능을 감소시키며, 그 결과 Cu 의 결핍울 야기시키게 된다는 것이 추정되었다. 방사성 동위원소를 이용한 Cu 실험에서 Marcil e se 등 233) 은 Mo 과 S 의 보충은 간과 cerulop la smi n 의 합성 에 Cu 의 결합을 감소시킨다는 것을 입증했다. 반대로 Cu 의 과잉 복용은 Mo 과 S 의 작용을 방해하는 것 으로 보여 진다. M ills 등 63) · 온 Mo 이 많이 함유된 목초를 먹은 송아지에게 CuSo4 의 주입은성 장을 좋게 했다고 보고했으며, 소에서도 이와 비슷한 결과가 Poole 2 36) 에 의해 설명되어졌다. 이러한 관계는 임신 기간중 어미에게 Mo 과 S 울 보충시킴으로써 야기된 Cu 결핍 증상(신생아 운동 실조, swa y back) 이 있는 어 린 양에게서도 나타났다. 237)238)239) CU 와 M o- 사이의 상호작용은 S 이나 다른 S 화합물에 의해서도 영향을 받는 다. D i ck240) 은 염소에게서 Cu 이용에 대한 Mo 과 S 의 역효과는 식 이의 M g 량을 높임으로써 역전될 수 있으며, 이것은 아마도 Mo 과 S 의 제한작용을 방해하기 때문인 것으로 생각했다. 그러나 My l- r ea232) 는 숫송아지 에 있어 서 M g 의 과량 흡수에 서 그런 효과를 발
견할 수 없었다고 보고했다. 단위 동물들의 Mo 과 S 고} Cu 와의 상호작용에 관한 대 부분의 연구에서 식이의 Mo 량은 반추 동물에서 보다 더 많이 쓰여졌다. 이 과량 보충 (800~1, OOOm g /k g)은 쥐 의 성 장을 현처 하게 감소시 켰 고, 241 )2 42)243)244)245) 그 결과 또한 빈혈과 설사를 유발시 켰다. Cu 가 부족하게 공급되는 동안에는 Mo 의 양을 더 감소시킨 경우에도 같은 중상이 나타났다 (20~140m g /k g). 246> Cu 의 보충은 빈혈과 설사를 경감시켰고, 성장 지연을 부분적으 로 회복시켰다 .244) 또한 Mo 이 과량으로 섭취된 돼지에서 두드러 진 성장 지연은 사료에 0.4% 의 S 울 추가시킴으로써 다시 회복되 었다는 것이 입증되었다 .24 7) 사료에 과량의 Cu 의 공급과, 적당량, 그리고 비교적 낮은 양의 Mo(20~50m g)과 S(o.1~0. 4% )의 공급은 동물의 성 장을 감소시 키 지 는 않았다. 248)249)250)251) 몇몇의 연구에서는 Cu 의 보유가 Mo 이나 S 의 보충에 의해 중가 되 었 다고 한다. 242)247)251)252) 그러 나 대 변에 서 Cu 배 설의 감소는 내 인 성 요인이 영향을 주므로, 단적으로 Cu 흡수만의 변화에서 생간다 고 추정할 수는 없다. 돼지 실험에 있어서는 Mo 이나 S, Mo 과 S 의 보충에 대하여 아 무런 영향도 발견되지 않았고, 간에서의 Cu 의 양의 감소도 발견되 치 않았다. 247)248)251 )25 2) 이와 같이 각각의 연구들은 필수적으로 Cu 와 S 의 양과 관련되 어 있으며, 또한 사료의 다른 S 화합물과도 관련되어 있음을 나타 내고, 따라서 sul fate 는 Cu 의 이용도를 현처하게 낮추는 것으로 보여 진다. 253)254)255)256) cu 의 대 사는 또한 Mo 과 S 의 상호작용에 의해 달라진다. 예를 들면 위에 기술된 작용으로 Cu 정화치 (clearance) 와 cerulop la smi n 의 활성 에 있 어 서 의 차이 가 Dale 둥 25 1) 과 St an dis h 등 247) 에 의 해 설명 되 었 다. 그러 나 Dowdy 둥 257)258)259) 은 cerulop la smi n 의 활성 감소가 2CuMo04(0H)2 로서 식 이 에 첨 가 되었으나, 이용할 수 없는 Cu 와 Mo 화합물의 형성 때문이라고 하 였다.
Mo 과 S 의 상호효과는 그 동물의 Cu 의 농도와, 식이에서의 아 제 원소의 비율에 의한다. 따라서 적은 양의 Cu 를 흡수한 쥐에게 . Mo 을 낮게 보충(l Om g /k g)시키는 것은 Cu 의 결핍을 유발시키기어·1 충분했다. S 울 동시에 첨가했을 때, 악화된 증상은 Cu 첨가에 의 하여 지연될 수 있다. 충분한 Cu 를 흡수한 경우 높은 Mo 의 보충 온 Cu 의 결핍을 일으킨다 .220) 또한 p H 값, 또 다른 미량 원소의 촌재(예를 들면 Mg , S) 의 산화 상태도 중요하다. 단위 동물에 비 하여 , 반추 동물은 desulfo v ib r io bacte r ia 의 작 용 때 문에 , 전위 에 서 261) 대 부분 sulfa te 를 sulfi te 로 환원시 킬 수 있 다. 이것은 Huis i n g h 등 262) 에 의하여 되새김질한 음식에서 처음으 로 발견되었다. 양의 전위에서 배출된 배양군에 Cu 를 첨가하면 sulfa te 가 sulfi te 로 환원되 는 것 이 약간 지 연되 었 으나, Mo 의 부 가는 낮은 농도에서 더욱 효과적이었다. Cu 와 Mo 이 함께 배양군의 배양기에 부가되었을 때, 후자의 원 소의 효과는 감소되었다 . 이것은 Mo 이 효과가 덜한 Cu-Mo 화합 물을 형 성 하기 때 문인 것 같다. Huis i n g h 둥 262) 에 따르면 Mo 은 황의 환원에 관여 하는 주된 효소, 즉 ATP-sulfu r y la se 의 역 행 을 막는다. 전위에서 형성된 황화물은 간에서 흡수되고 해독되며, sulf ur - ami no acid 에 혼합되 거 나, 무거 운 금속 황화물로써 침 전된다. 또 한 Cu 는 전위에서 S 과 함께 불용성의 CuS 를 형성하기 때문에 Cu 의 흡수가 감소된다. 253) M0 은 sulf at e 가 sulf ite 로 환원되 는 과정 올 방해 하며 Mo 섭 취 중가는 Cu 의 흡수를 증가시 킨다. Gomez- Gar ci a263) 에 의한 실험결과에서는 Mo 은 시료에 S 함유 ami no ac id 가 함유되어 있지 않을 때에도 sul fat e 가 S 의 유일한 급원으로서 소변의 N 와 함께 Cu 의 결핍증세를 완화시켰다고 보고했다. 그러 나 M i lls253) 과 Hear t man264) 은 만약 pro te i n - holdin g rati on 이 sul- fat e 와 Mo 을 함유하면 전위의 sulf ite 량이 증가되었다고 보고하 였다. Huis i n g h 둥 265) 은 위 의 실험 결과에 서 sulf ite 의 증가는, 전위 에 있 는 sulfa te 를 함유한 ami no ac id 로부터 유래 된다고 하였 다. Mo
은 sul fat e 가 su lfit e 로 생성되는 것을 방해하는 동안 전위의 총 sul fit e 의 생성은 석이에 함유된 유기물의 S 과 sul fat e 의 비율에 따르기 때 문에 , S 울 함유한 ami no ac id 로부터 의 sulfi te 유출을 활 성화한다. 전위에서 sul fit e 의 흡수가 Mo 에 의해 감소되는 것에 대 한 연구는 Gawt h rone 둥 266) 에 의 해 논의 되 어 졌 는데 , 그들은 su lfit e 의 새로운 합성이 Mo 의 보충에 의해 현저히 낮아지는 동안 척새김 유체 (rumi na l fl u i d) 의 sulf ite 량 이 높아졌다는 것을 발견하 였다. 이러한 결과들은 반추 동물과 단위 동물 사이에서 몇 개의 차이 접 을 나타내 준다. Huis i n g h 와 Ma t rone261)261) 의 보고와는 탈리 Su ttl e268) 는 meth io n in e , cy s te i n 그리 고 sulfa te 의 S, Cu-Mo-S 상 호작용에서 비슷한 역할을 한다는 것을 발견했다. 모든 S 의 급원은 Mo이 있을 때 Cu 대사의 역반응에 다같이 효과가 있 다. 그러 나 sulf ite 의 생 성 온 Mo 의 농도에 따라 달라지 는데 268) 이 연구에 서 사용되 어 전 4mg / kg 의 Mo 양은 매 우 낮았다. Huis i n g h 와 Matr o ne 은 소변과 S-ami no ac id 및 sulfa te 를 이 용 하여 N 와 S 울 정확하게 조철한 식이를 사용하기도 했다. 전위에서 생산된 su lfit e 는 부분적으로 전위 벼울 통하여 매우 급 속히 흡수되었고 간에서 sulfat e 로 산화되었으며 소변에서 sulfa te 형 태 로 배 설되 었 다. 267) Sulfa te 의 sulf ite 로 의 산화와 관련 있 는 sulf ite oxid a se 의 활성 은 간에 서 이 용될 수 있 는 Cu 의 양에 달려 있 는 것 으로 보여 진다. Cu 가 sulfi te oxid a se 의 활성 을 증가시 키 는 반떤 Mo 은 반대로 활성을 감소시켜 준다 .270) 감소된 sulfi te oxid a se 는 간에 서 sulfi te 를 축적 시 키 고 이 로 인 하여 이용할 수 없는 불용해성의 CuS 의 형태로 Cu 를 침전시키 게 된다. 245)269)271) 이 영 향은 Mo 의 농도가 간에 서 sulfi te oxid a se 의 활성을 조철하기 때문에 흡수할 수 있는 Mo 의 양에 의해 결 정된다. D ic k212)224)24o) 은 황산영 이 Mo 의 흡수를 변화시 킨다고 주장했으 며 그 후 Card ian273) 과 Huis i n g h 267) 의 하여 in vi tro 실험 에 서 sul- fit e 가 과잉으로 존재할 때 Mo 의 흡수가 감소되었다는 것이 명백
해 졌 다. 전위 의 bacte r ia 에 의 하여 su lfa te 가 sulf ite 로 환원되 기 때문에, 단위 동물에 비해서 반추 동 물 의 장관에서 일반적으로 sul fat e 의 흡수가 적게 되므로 결국 은 더 많은 Mo 이 반추 동물에 의하여 흡수된다. Cu 와 Mo의 상호작용을 설명하기 위하여 부차적인 가능성으로 서 , Dav i s93) 는 Cu- M o 화합물의 생 성 에 대 하여 검 토하였 다. Dowdy 와 Ma t rone25 7 ) 2 58) 은 Cu- M o 은 복합체 로서 흡수는 아주 찰되 나 이 복합체로서 Cu 가 이용되기는 어렵다고 했다. Hu i s i n g h 267 ) 에 의 해 연 구된 Electr o n Paramag n eti c Resonance (EPR) 은 이 복합체가 혈청내에서 안정치 못하다는 중거를 제공했 으나 전위의 상태 하에서는 안정한 것으로 나타났다. EPR 연구를 토 대로 하여,
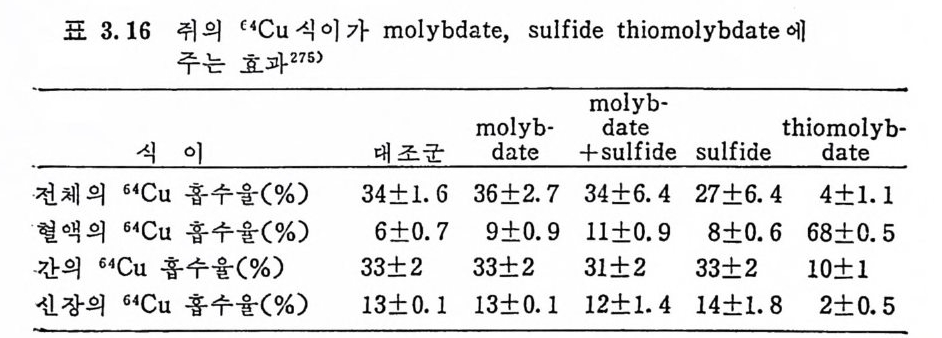 표 3. 16 쥐 의 Cu 식 이 가 molyb date , sulfi de thi o m olyb date 에
표 3. 16 쥐 의 Cu 식 이 가 molyb date , sulfi de thi o m olyb date 에
흡수된 th io m olyb date 는 급속히 albumi n 에 결 합된다. Thio m olyb - da t e 가 반추 동물과 단위 동물의 다른 여러 가지 혈장 단백질에 결 합된다는 증거 도 있 다. 이 th io m olyb date - pr o te i n 혼합체 는 Cu 이 온 一 에 대하여 역반응을 증가시켰다. 이런 실험적 상태 하에서 Cu 가~ 단백질의 TCA 침전에 의해 유리되지 않는 것은 혈장에 단단히 결 합되 어 있 기 때 문이 다. 275)276) 이 연 구에 서 , th io m olyb date 를 장기 간에 걸쳐, 음식에 2m g /k g의 Mo 을 섭취시킨 쥐는 높은 Mo 보충 과 S 을 먹 인 반추 동물의 Cu-Mo-S 의 상호작용의 것 과 유사한 증상을 나타냈다. 이 증상으로 혈장의 Cu 의 농도가 중가되었고, cerulo p lasm i n 의 활성이 감소되었으며, 간의 Cu 의 함량이 낮아지 게 되었다. 반추 동물과 단위 동물의 Cu-Mo-S 의 상호작용에 있 어 각각의 효과는 소화계의 차이 에 따라 3 과정 으로 나뉜다. 첫째 과정에서는 전위(fo res t omach) 에서의 미생물의 활성은 S 울 함유한 ami no a ci d 의 분해에서 생산되는 sul fit e 는 물론이거니와 Sulfa te 의 환원작용에 서 생 성 되 는 sulfi te 와 더 많은 관계 를 갖는다. Sulfit e 는 용해가 찰되 지 않고 흡수도 되 지 않는 Cu, sulf ite 형 성 울 위하여 Cu 와 반응한다. 단위 동물에서도 발생하는 두번째 과정 온 su lf a t e 의 아주 적은 양이 반추 동물의 장으로 통과하는 것이다. sul fat e 는 mol ybda t e 의 흡수를 방해하고, 이로 인해 아주 적은 양 의 Mo 이 단위 동물의 간에 도달하게 된다. 세번째는, 단위 동물 보다 반추 동물의 간에 sulf ite 가 더 많이 축적 되 므로, Mo 은 sulf ite 산화작용을 방해한다. 또한 sulfi te 는 sulf ite 의 축적 을 위 하여 간 에서 Cu 와 반응하기 때문에 반추 동물의 체내에서 대사에 이용할 수 있는 Cu 의 양은 감소된다. Sulf ite 는 또한 Cu-th io m olyb date 복합체 의 합성 에 필요하다. sulfi te 는 단위 동물보다 반추 동물이 더 많이 함유하는데 이는 Cu 가 충분하게 이용될 수 없는 Cu- th io m olyb date 복합체 로 촌재 하기 때 문이 다. 그 결과 반추 동물에 서 의 Cu 의 결핍울 악화시킨다. 일반적으로, Cu-mol ybda t e 와 Cu_ molyb denum 의 합성 은 단위 동물과 반추 동물에 따라 달라진다.
3. 8. 4 Cu 와 Mn, Ni , Se 의 상호작용 Cu 와 필수 미 량원소인 Mn, Ni과 Se 사이의 상호작용에 대한 몇 개의 보고가 있다. Cu 를 과잉 복용한 돼지의 Mn 보유의 증 가 270) 는 복합 화합물의 장관내 치환작용에 기인하며, 이로 인하여 Mn 의 흡수상태가중전된다. 다론한편으로는, 극십한 Mn 의 결핍은간, 신장, 비장, 췌장에서의 Cu 의 농도가 현처히 감소되는 것과 관계 가 있다 .277) 동시에 Fe 의 농도는 간에서는 중가되었고, 골격에서 는 감소되 었 다. 49) 또한 hemog lo bin 과 hemato c rit 치 는 이 원소를 정상적으로 공급한 대조 동물에서 보다 Mn 이 결핍된 동물에서 더 낮게 나타났다 .27 7 ) Fe 과 혈액 변수의 반응은 또한 Cu 가 결핍되는 동안 계속적으로 나타났다. 그래서, Cu-Mn 의 상호 작용은 1 차적 으로 고려 하여 야 한다. Fe 빈혈의 중상은 Mn 과잉 복용에 서 유발된 다. 278 )27 9 )28 0) 득히 , Vohra 와 He i l281) 은 요구량을 초과한 Cu 와 Zn 를 복용하면 간이나 신장에 Mn의 축적이 감소되는 것을 발견하였 다. 이 발견은 Zn 과 Mn 이 같은 방법으로 반응하기 때문에, Zn 과 의 상호작용을 나타내기 위한 것으로 설명되어질 수 있다 .49 )1 83) Schne gg와 K i rch g essner282'28” 는 또한 국십한 Ni 결핍에서 쥐의 성장과 N i의 양, 그리고 여러 기관의 Fe,. C u, Zn 의 양이 매우 감 소함을 발견했다. 또한 미량원소의 농도에도 변화가 나타났다. 따 라서 정상적으로 섭취시킨 대조군과 비교했을 때, N i이 결핍된 숫 쥐의 간에서 Cu 의 농도가 현저히 중가되었다. 그러나, N i이 결핍 된 모든 쥐 는 뚜렷 하게 빈혈을 나타냈다. 284)285) 따라서 Ni 과 Cl[ 사이의 상호작용은, 특히 Fe 빈혈 동물의 간에서 Cu 의 농도가 증 가된다는 여러 보고를 토대로, 제 2 의 효과가 될 수 있다 .70)7 1) 105)120) Cu 가 결핍 된 취 의 사료에 20mg /k g 의 Ni 을 보충시 켰을 때 286) 성 장 중전, cerulop la smi n 활성 의 중가, hemog lo bin 과 he- ma t ocr it치의 상승 여부는 Fe 대사의 증진에 기인될 수 있다. Godwi n 동 287) 은 Cu 대 사에 대 한 Se 결핍 의 민감성 이 현저 하게 증 가되었다는 것을 알아냈다. 그러나 부족한 Se 흡수의 첫번째 결과· 가 적혈구막의 약화를 증진시키기 때문에, Cu 의 유독성은 적혈구
막의 손상이 층가된 것을 강조하게 된다 . 따라서 이 상호작용~ 이 두 미량원소 사이에서 직접 존재하는 것이 아니라 결핍으로 인 한 악화의 한 현상으로서 생각될 수 있다. 3. 8. 5 Cu Cd, Ag , Hg 과 Pb 의 상호작용 Cu 와 Cd 사이 의 상호작용이 가금류, 반추 동물과 단위 동물에 서 관찰되었다. Hi ll 등 192) 은 Cd 이 병아리의 Cu 이용률을 매우 감 소시킨다고 보고하였다. 병아리의 사망률은 사료의 Cd 의 함량을 높였을 때 극단적으로 증가되었다 . Bunn 과 Ma t rone104) 은 쥐에게서 유사한 효과를 발견했으며 이 동물분만이 아니라 염소에서도 간과 다른 조칙의 Cu 의 농도가 감 소된 것 을 보고했 다. 더 우기 Whan g er18” 는 cerulop la smi n 의 활 성이 매우 감소됨을 관찰했다. Cd 과 Cu 사이의 상호작용은 Cd 공급의 양에 의 하여 영 향을 받는다. Camp b ell 동 288) 은 Cu 와 Cd 의 상호작용은 특히 적은 양의 Cu 가 흉수되는 동안 뚜렷해졌다고 지 적했다. Cu 의 섭취가 충분했을 때 Cd 에 의한 영향이 없는데 반하 여, 식이의 Cu 량이 낮을 때 약 6m g/k g의 Cd 부가에 대해 쥐의 혈 장속의 Cu 량이 약 50% 까지 낮아졌다. Cd 이 Zn 과 강하게 반응하고 Cu 대사가 Zn 영양 공급과 · 매우 밀접하게 관련되어 있기 때문에, Cu 이용에 대한 Cd 의 영향은 식이의 Zn 량과 관련되어 고려되어쳐 야 한다. 190)288)289) 6_ lmg / kg 의 Cd 식 이 가 lOOOmg / kg 의 Zn 식 이 만큼 cerulop la smi n 의 활성 을 감소시 킨 표 3. 17 의 자료에 서 더
 표 3. 17 쥐 에 게 카드뮴 (Cd), 아연 (Zn), 구리 (Cu) 를 섭 취 시 켰
표 3. 17 쥐 에 게 카드뮴 (Cd), 아연 (Zn), 구리 (Cu) 를 섭 취 시 켰
욱 확실해전다. 따라서, Cd 은 Zn 과 같이 Cu 의 이용도에 영향을 미찬다는 것을 알 수 있다. 그러나 석이 중 적온 양의 Cd 도 위와 칼은 효과를 낸다. . Hi ll 등, 192) 과 Van Cam p en290) 과 Camp b ell 둥 288) 의 연 구에 서 는 상호작용이 흡수 도중에 일어난다는 것이 확실해졌다. Camp b ell 동 288) 은 17. 6mg / kg 의 Cd 식 이 는 소량으로 Cu 가 공급된 쥐 에 게 서 약 45% 까지 Cu 의 흡수를 감소시켰다고 밝혔다. 적은 양의 Cd 은 oxid a ti ve ph osp h oryl a ti on 에 의 해 유지 되 고 장벽 을 통과한 미 량 원소의 수송은 energy 에 의 존하기 때 문에 292)293) 이 것 의 부족은 홈 수 감소의 원인이 된다. 290) 흡수 도중의 상호작용은 두 미 량원소 를 동시에 복용하였을 때에만 발생한다 .290) 그러므로 장내의 결 합이나 수송의 위치에서 치환 작용이 중요시되고 있다. 장내의 meta l loth io n ein 의 작용은 간과 신장의 meta l loth io n ein 의 생 성 과 이 단백질들의 Cu 와 Cd 의 결합에 있으며 또한 중간 대사 과정에 서 상호작용을 일으키는 것들이다. Whang e r 와 Weswi g 189) 에 의 하면 Ag 은 Cu 에 대 하여 가장 강 한 길항작용을 한다고 하였 다. Hi ll 둥 294) 은 100~200mg / kg 의 Ag 석이가 Cu 를 적게 공급받은 병아리의 Cu 결핍증상을 악화시켰다 는 것을 알아냈다. A g의 함량이 높은 사료 (900m g /k g)에 의해 나 타난 결과는 칠면조 새끼와 169) 병아리의 경우 39) 50m g /k g의 Cu 를 공급시 킵 으로써 부분적 으로 회 복될 수 있 었 다. Van Camp e n290) 에 의하면 Cu 의 흡수는 A g에 의해 영향을 받지 않는다. Cu 와 A g은 특히 대사과정에서 상호작용이 일어난다. SH 기에 대한 Ag 의 강한 찬화력 은 th io n ein 이 나 200) 혹은 다른 SH 함유 단백 질에 서 나타난다. Cu 와 A g의 상호작용과는 현저히 달라서 Cu 와 Hg 사이에는 칙 접 적 인 상호작용은 없는 것 으로 보여 진다. Hil l 등 294) 에 의 하면 ‘ Cu 가 결핍된 병아리의 성장은 25m g /k g의 Cu 석이 섭취 후 병아 리의 성장이 십하게 감퇴되었음에 반하여 과량의 H g섭취시는 영 향을 받지 않았다고 한다. 400m g /k g의 H g식이의 섭취는 cerulo JPl asmi n 의 활성 에 변화를 주지 않았다. 189) 또한 Van Camp e n 도 290)
Cu 흡수에 대한 H g의 영향을 발견하지 못했으며, Cu 대사에 대한 H g의 효과는 기관의 일반적인 손상 때문에 나타나는 것으로 보여 진다. 정상적인 Cu 와 Mo 의 홍수에도 불구하고 어미가 Pb 이 많은 목 초를 먹었을 때, 새끼양은 신생아 운동실조중에 길렀다 .53) Allo- wa y 53) 에 의하면 이 병의 발병은 Pb 이 야기시킨 Cu 의 결핍 때문 이라고 한다. 쥐에게서 2.5m g /k g의 Cu 첨가식이를 주었을 때 Pb 의 과잉 섭취 (0. 5%) 는 혈장의 Cu 의 양과 cerulop la smi n 의 활성을 감소시 켰 다. 식 이 의 Cu 량이 O. Smg /k g 으로 낮추어 졌 을 때 hemato - crit 와 hemog lo bin 은 현처 하게 감소되 었 다. 93) 또한 이 연구자들은 양에 있어서 성장 감소, 간과 신장의 Pb 의 보유량, 적혈구의 Pb 의 양은 식이의 Cu 의 양에 반비례한다는 것을 알아냈다. 이 견과 둘을 재 검 토하여 Klauder 둥 93) 은 Cu 는 Pb 의 유독성 을 낮추고, 반대로 Pb 은 Cu 의 결핍을 유발시킨다고 결론지었다. *참고문현 1) Underwood, E. J. , Trace Elements in Human and Ani m al Nutr i - tion, Academi c Press Inc. , New York and London, p. 56 1977. 2) Hart, E. B. , H, Ste e nbokk, J. Waddel and C. A. Elvehje m , J. Bi ol . Chem. 77, 792, 1928. 3) Lang . K. Bi o chemi e der Ernii hr ung 4 Auf la g e , Dr. Di et r i c h St ei n k of f Verlag . p. 343, 1979. 4) Hami lton , E. I. Mi ns ki, M. J. and Cleary, J. J. , Sci. Tota l En- vir on . 1, 341, 1972~1973. 5) Schltz e , M. 0. , Elvehje m , C. A. and Hart, E. B. , J. Bi ol . Chem. ,. 115, 453, 1936, 16, 93 and 107, 1936. 6) Ni el sen, A. L. , Acta Med. Scand. 118, 87 and p. 2, 1944. 7) Hambid g e, K. M. and Droeg e mueller, Wo Obste t . Gy n ecol. , 44 .. 666, 1974.
8) Ni xo n, G. S. , Smi th, H. and Liv i n g s to n e, H. D. , in Sy m p os iu m ,on Nuclea r Ac tiva ti on Techniq u es in th~ Li fe Scie n ces, IAEA, Vi en na, 1967. 9) Moeller, H. , G. W ilk in Gladtk e . E, G. Heim ann and I. • Eckert, .Sp u renelemente , Georg Thie m e Verlag St u tt ga rt p. 171, 1979. 10) Frid o vic h I, Annu. Rev. Pharmacol. 15, 259, 1975. 11) Frid e n, E. , Nutr . Rev. , 31, 41, 1973. 12) Frie d en, E. and H. S. Hsie h , Advances Enzy m ol. 44, 187, 1976. 13) Evans, G. W. , Phy si o l. Rev. 53, 535, 1973. 14) Top :1 :1 m , R. W. and Frie d en, E. , J. Bi o l. Chem. 245, 6698, 1970. 15) Van Camp e n, D. R. , in Skoryn a, S. C. and Waldron Edwards, D. , Inte s ti na l Absorp U on of Meta l Ions, Trace Elements and Radio .nu clid es, p. 211, Perga mon Press, Oxfo r d, 1971. 16) Petr i d e s P. E. , Loff ler , G. L. Weis s and H. A. Harpe r , .Ph y si o l og isch e Cherne. , Zweit Aufl ag e , Sp ri n g e r-Verlag p. 531, 19 79. 17) Ki rc hg e ssner, M. and Gra/3 m ann, E. , in Mi lls, C. F. , Trace Element Meta b oli sm in Anim als, p. 277, Liv i n g s to n , Edin b urg u. London, 1970. 18) Harris , D. J. M. and Sass-Korts a k, A. , J. Clin . Inverst. 46, 659, 1967. 19) Ki rc hg e ssner, M. , Schwarz, F. J. , Grassmann, E. and Ste i n h art, H. in Nria g u , J. 0. , Cop pe r in th e Envir o nment, Part ]I , p. 433, Jo hnwi ley &, Sons, New York, 1979. 20) Schwarz, F. J. an:i Ki rc hg e ssner, M. , Int. Z. Vi tam i nf o rsch. , 44, 116, 1974. 21 ) Schwarz, F. J. , E. Grassmann and M. Ki rc hg es sner, Z. Ti e rP• Jiys io l and Ti e rern!i hr g, u. Futt er mi ttelk de, 31, 98, 1973. 22) Ki rc hg e ssner, J. Pallauf, F. J. Schwarz and H. P. Roth , in Betk e, K. , F. , Bin :i li n g m aie r , Frank, Sp u renelemente in der Entw i ck lung .von Mensch and Ti e r, Urban & Schwarzenberg, p. 39, 1975. 23) Van Cam;>en, D. and Gross, E. , J. Nutr . , 95, 617, 1968.
24) Ki rc hg e ssner, M. , z. Ti e rpl tysi o l, Ti e rernii ltrg . u. Futt er mi ttelk de,. 14, 278, 1959. 25) Tomp s ett , S. L. , Bi o chem. J. , 34, 961, 1940. 26) Burch, R. F. , H. K. J. Hahn and J. F. Sulliv an. , Cl in. Chem 니 · 21, 501, 1975. 27) Seeli ng , M. S. , Am. ]. Cl in. Nutr . , 25, 1022, 1972. 28) Seeli ng , M. S. , Am. J. Clin . Nutr . , 26, 657, 1973. 29) Mi lis, C. F. , Bi o chem. J. , 63, 190, 1956. 30) Cartw rig h t, G. E. , in McElroy , W. D. Glass, B. , Cop pe r Me•· tab oli sm , p. 274, Joh ns-Hop k in s Press, Balti m ore 1950. 31) Greg e r, J. L. Bennet, 0. A. , Buckley , S. , Bali ga r, P. , in Ki rc h•· ge ssner, M. Trace Element Meta b oli sm in Man and Ani m als-3, p. 300, ATW , Freis i n g - Weih e nste p h an, 1978. 32) Cavell, P. A. and E. M. W idd owson, Arch. Di s. Chi ld h._ , 39, . 496, 1964. 33) Alexander, F. W. , B. E. Clay ton and H. T. Delves, Qu art. I. Med. , 43, 89, 1974. 34) Macy , I. G. , Vol. l, Evali tat i on . Ch. C. Thomas, Sp r in g fiel d,. 1942. 35) Fomon, S. T. , Inf an t Nutr i t ion, 2nd Ed. , W. B. Saunders Co. ,. Phil ad elph ia , p. 549, 1974. 36) Zie g le r, E. E. , B. B. Edwards, R. L. Jen sen and S. J. Fomon, in · E. Gladtk e, G. Heim ann und I. Eckert, Sp u renelemente , Georg Thie m · everlag e St u tt ga rt p. 61, 1979. 37) Ki rc hg e ssner, M. , D. A. Roth -Maie r and R. Sp o rl, Arch. Ti e r-· ernii hr ung . Bd. 31. H. 1, p. 21, 1981 . 38) Grassrri an n, E. , A. Wetz s te i n and M. Ki rc hg e ssner, Z. Ti e rp - hy si o l. , Ti e rern!i hr ung u. Futt er mi ttelk de. 28, 1971. 39) Pete r son, R. P. and Jen sen, L. S. , Poult . Sci. , 54, 771, 1975. 40) Ki rc hg e ssner, M. , U. Weser and H. L. Muller, Ti er Plzy s io l. ,.. Ti e rernti kr g. u. Futt er mi ttel kde, 22, 76. 41) Mi st i lis, S. P. , Farrer, P. A. and Scand ]. Gastr o ente rol. 3. . 586, 1968.
42) Van Berge Heneg o uwen, G. P. , Tang e dahl, T. N. , Hof m ann, A. F. and North fi eld , N. F. , La Russo, N. F. , McCall, ]. T. , Bi liary ,. Gastr o ente rolog y, 72, 1228, 1977. 43) Cartw rig h t. G. E. and M. N. W int r o be, Am. ]. Clin . Nutr i t . ,. 14, 224, 1964. 44) Ki rc hg e ssner, M. , Sp oe rl, R. and Schneid e r, U. A. , in Ki rc hg e s-sner, M. , Trace Element Meta b oli sm in Man and Anim als-3, p. 4 40, ATW , Freis i n g -W eih e nste p h an, 1978. 45) Sp o erl, R. M. , and Ki rc hg e ssner, Z. Ti e rph y si o l, Ti e rernti hr g . . u. Futt er mi ttelk de, 35, 113, 1975. 46) Henkin , R. I. , J. R. Marshall and S, Meret, Mate r nal-fe ta l ,. Ame,:. ]. Ohstt r. Gy n ecol. , 1·10 , 131, 1971 . 47) Codex Alim enta riu s Commi ss io n FAO/WHO Joi n t Of fice , Rom,. ALINORM 76/7 6 A Ap pe ndix Il . 1976. 48) Pahlke, G. , L. Kl ing e bie l , H. P. Lenk, E. Gladtk e, G. Heim anrr. and I. Eckert, Sp ur enelemente , Georg Thie m e Verlag , Stu tt ga rt p. 113,. 1979. 49) Kir c hg e ssner,· M. , and Heis e ke, D. , Int. Z. Vi tam i n f o rsch. 48, 75, 1978. 50) Klevay , L. M. in Ki rc hg e ssner, M. , Trace Element Meta b oli sm in Man and Anim als-3. p. 307, ATW, Freis i n g -W eih e nste p h an 19- 78. 51) Hi ll, C. H. and G. Matr o ne, J. Nutr . , 73, 425, 1961. 52) Mi ln e, D. B. and P. H. Weswi g, J. Nutr . , 95, 429. 1968. 53) Alloway, B. J. , Ph. D. Thesis , Univ e rsit y of Waler, Aberys - tw y th, Chap e r 13, The Soil s a nd Veg e ta t i on of Arear Af fect e d by Mi n i n g for Nonf e rrous Meta l lif erro us Ores, wi th Sp ec ta l Ref e rence to Cadmi u m, Cop pe r Cead and Zi n c, p. 627, 1969. 54) Carnes W. H. , Fed. Proc. , 30, 995, 1971. 55) Guth rie , H. A. , Intr o ducto ry Nutr i t ion, 3rd ed. The C. V. Mosb}' Comany , 1975. 56) Mi lls , C. F. , R. B. Wi lliam s and D. B. Poole, Proc. Bi o chem. Soc. , Bi o chem. ]. , 87, 104, 1969.
57) Blaschko, H. , F. Buff on i, N. Weis s man, W. H. Z. Carnes and E. F. Coulson. Bi o chem. ]. , 96, 40, 1965. 58) Ki rc hg e ssner, M. and E. Grassmann, Z. Ti e rp! tys io l . Ti e rern- 퍄 r g, u. Fi .tter mi ttel kde. 26, 340, 1970. 59) Gomez-Garcia , G. G. and G. Matr o ne, J. Nutr . , 92, 237, 1967. 60) Ki rc hg e ssner, M. and E. Grassmann, in Mi lls, C. F. ed. , Trace Element Meta b oli om in anim als, Liv i n g s to n e, Edin b urg and London, 277, 1970. 61) Mi ln e, D. B. and Weswi g, P. H. J. Nutr . , 104, 14. 58, 1968. 62) St ar cher, B. , G. Matr o ne and C. H. Hi ll, Fed. Proc. 23, I, 133, 1964. 63) Sy m es, A. L. , T. L. Sourkes, M. B. H. Youdim , G. Greg o ria d is and H. Bir n baum. Can. J. Bi oc hem. , 47, 999, 1969. 64) Mi lls, C. F. and A. C. Dalga rno, in Mi lls, C. F. , ed, Trace Element Meta b oli sm in anim als, Liv i n g s to n e, Edin b urg and London, 456, 1970. 65) Lang , N. and H. E. Renschler, Z. Ges. Exp . Med. , 130, 203, 1958. 66) Neif ak h, S. A. , N. K. Monakhov, A. M. Shap o shnik o v and Y. N. Zubzhit sk i, Exp er ie n t ia 25, 337, 1969. 67) Owen, C. A. , Jr. Am. J. Phy si o l. , 209, 900, 1965. 68) Neumann, P. Z. , A. Sass·Korts a k, J. Cl in. Invest. , 46, 646, 1967. 69) Kekki, M. , P. Koskelo and E. A. Ni kk jl o , Natu re 209, 1252, J.9 66. 70) Grassmann, E. and M. Ki rc hg e ssner. , Arch. Ti e rernti hr ung 23, ·26 1, 271, 1973. 71) Grassmann. E. and M. Ki rc hg e ssner, Z. Ti e rhp ysi o l. , Ti e r- 아 rnih g, u. Futt er mi ttelk de. 31, 38, 113, 1973. 72) Grassmann, E. and M. Ki rc hg e ssner, Z. Ti e rpy si o l. Ti e rern- .jjhr g, u. Futt er mi ttelk de. 31, 38, 113, 1973. 73) Ki rc hg e ssner, M. , S. V. Krziw anek and E. Grassmann, Z. Ti e rp- Jzys io l , Ti e rern!i hr g. u. Futt er mi ttelk de. 38, 273, 1977.
74) Grassm1nn, E. S. V. Krziw anek and M. Ki rc hg es sner, Arch. Ti e rernli hr ung 28, 451, 1978. 75) Evans, G. W. , D. R. My ro n, N. F. Cornatz e r and W. E. Cornatz e r, Am. ]. Phy si o l. , 218, 298, 1970. 76) Gubler, C. J. , G. E. Cartw rig h t and M. M. Wi nt r o be, J. Bi ol . Chem. , 224, 533, 1957. 77) Wahle, K. W. J. and N. T. Davis , Brit . J. Nutr . , 34, 105, 19 75. 78) Gallag h er, C. H. , J. D. Jud ah and K. K. Rees, Proc. Roy . Soc. London Ser. B. , 145, 134, 195, 1956. 79) Evans G. W. , Dubois R. S. and Hambid g e K. M. , Scie n ce 181, 1175, 1973. 80) Kir c hg e ssner, M. , Trace Element Meta b olis m in Man and Ani· mals-3, Technis ~ he Univ e rsit at Mi lch en Freis i n g -W eih e nste p h an, p. 370, 1978. 81) Danks D. M. , in Ki rc hg e ssner M. , Trace Element Meta b oli sm in Man and Anim 2ls-3, Mi lnc hen Freis i n g -W eshenste p h an, p. 401, 1978. 82) Ki er meie r , F. an:l H. Ste g er , Ti e rph y s io l . Ti'er ernti hr g. 16, .25 0, 1961, Z. Lebensmi ttelu nte r s. 115, 410, 1961. 83) St ol ley , H. W. Droese an:l I. Rewents , in Betk e , K. F. Bin d lin g - maie r , Sp u renelement in der Entw i ck lung von Mensch und Ti e r, Urban & Schwarzenberg, Mi lnc hen-Berlin - W ien , 113, 1975. 84) Schletl w .e in , Gsell, D. and S. Mommsen-Str a ub, Beih elf Inte r nat .z. Vi tam i n- u nd Ern'i hr ung s fo r schug Nr. B. , Hans Huber, Bern, St u tt ga rt, W ien , 1973. 85) Souci , W. , W. Fachmann and H. Kraut, Di e Zusammensetz u ng ,der Lebensmi ttel, W iss enschaft lich e Verlag s ge sellschaft moH. Stu ttga rt , 1973. 86) Pennin g ton , J. T. and D. H. Calloway, J. Am. Di et . Associ. , ,63 , 143, 1973. 87) Adelste i n , S. J. an::I B. L. Vallee, Cop pe r, in Mi n eral Meta b ol· .i'sm . Academi c Press, New York, London, 1962.
88) Hap ke , H. J. Toxik o log ie Jiir Vete r i n f rm e d i zi n er, Ferdin a rd Enke Verlag e St u tt ga rt, 1975. 89) Patt y, F. A. , Industr i a lhy gien e in Toxfr ol og y. Inte r scie n ce Publis h ers, New York-London, 1962. 90) Sutt le, N. F. , Proc. Nutr . Soc. , 33, 299, 1974. 91) Mi lls, C. F. , in Hoekstv a Ph. D. et al. , Trace Element Meta b o· lis m in Anim als-2, Univ e rsit y Park Press, Balti m ore, 1979, 1974. 92) Davie s , N. T. , Proc. Nutr . Soc. , 33, 293, 298, 1974. 93) Davis , N. and T. , Proc. Nutr . Soc. , 33, 293, 1974. 94) Van Camp en , D. R. and Scaif e, P. U. , J. Nutr . , 91, 473, 19· 67. 95) Ki rc hg e ssner, M. , Z. Ti e rph y s io l , Ti e rernii hr , Futt er mi ttel kd. , 14, 278, 1959. 96) Ki rc hg es sner, M. , Munz, W. and Oelschlag er , W. , Arch. Ti e r- ernti hr , 10, 1, 1960. 97) Hamp el , G. and Ki rc hg es sner, M. , Arch. Gef lu g e lk d . , 34, 181,. 1970. 98) Grassmann, E. , Ki rc hg es sner, M. , Hamp el , G. and Rot h -Maie r ,. D. A. , Arch. Gef lu g e lkd. 35, 67, 1971. 99) Bey e r, M. G. , Ki rc hg e ssner, M. and Ste i n h art, H. , Landwf rtsc h. Forsch. 29, 53, 1976. 100) Ki rc hg es sner, M. , Bey e r, M. G. and Ste i n h art, H. , Br. J .. Nutr . , 36, 15, 1976. IOI ) Ste i n h art, H. , Ki rc hg es sner, M. and Bey e r, M. G. , Arch .. Ti e rernii hr . 26, 629, 1976. 102) Matr o ne, G. , Fed. Proc. , 19, 659, 1960. 103) Elvehje m , C. A. and Sherman, W . C. , J. Bi ol . Chem. , 98, 309,. 1932. 104) Bunn, C. and Matr o ne, G. , J. Nutr . , 90, 395, 1966. 105) Sourkes, T. L. , Lloy d , K. and Bir n baum, H. , Can. J. •· Bio c hem. , 46, 267, 1968. 106) Marsto n , H. R. , Allen, S. H. and Swaby , S. L. , Br. ]. Nutr , ► 25, 15, 1971.
107) Thomp so n, H. J. and Evans, J. L. , Nutr . Rep. Int. , 15, 287 .. 1977. 108) Marsto n , H. R. , Phy si o l . Res. , 32, 66, 1952. 109) Chap m an, H. L. , Jr. and Ki dd er, R. W. , Fla. Ag r ic . Exp. Sta . Bull. , 674, 1964. llO) Gubler, C. J. , Lahey, M. E. , Chase, M. S. , Cartw rig h t, G. E. and Wi nt r o be, M. M. , Blood, 7, 1075, 1952. lll) Lee, G. R. , Nacht, S. , Lukens, J. N. and Cart w rig h t, G. E. , J. Cl in. Invest. , 47, 2058, 1968. ll2) Mag ee , A. C. and Matr o ne, G. , J. Nutr . , 72, 233, 1960. 113) Lee, D. , Jr. and Matr o ne, G. , Proc. Soc. Exp. Bio l. Med. ,. 130, 1190, 1969. ll4) Rit ch ie , H. D. , Luecke, R. W. , Baltz e r, B. Ve. Mi ller , E. R. Ullrey, D. E. and Hoefe r , J. A. , J. Nutr . , 79, 117, 1963. 115) Evans, J. L. and Abraham, P. A. , J. Nutr . , 103, 196, 1973. 116) Cassid y , J. and Eva, J. K. , Proc. Nutr . Soc. , 17, XXXI, 1958. ll7) Ruszczy c, Z. and Gacek, K. , Rocz. Nauk. Roln. B 81, 563,. 1963. ll8) Kin n amon, K. E. , J. Nutr . , 90, 315, 1966. ll9) Kir c hg e ssner, M. and Weser, U. , Z. Ti e rph y si o l , Ti e rernii hr . Futt er mi ttelk d. , 18, 181, 1963. 120) Lahey, M. E. , Gubler, C. J. , Chase, M. S. , Cartw rig h t. G. E. and Wi nt r o be, M. M. , Blood, 7, 1053, 1952. 121 ) Cohen, E. and Elvehje m , C. A. , J. Bi o l. Chem. , 107, 97, 1934. 122) Schultz e , M. 0. , J. Bi ol . Chem. , 129, 729, 1939/138, 219,. 1941 . 123) Gallag h er, C. H. , Austr . Vet. J. , 33, 311, 1957. 124) Ducan, G. D. , Gray , L. F. and Danie l , L. , J. Proc. Soc. Exp . Bi ol . Med. , 83, 625, 1953. 125) Van Reen, R. Arch. Bi o chem. Bi op h y s. , 46, 337, 1953. 126) Grant- F rost, D. R. and Underwood, E. , J. Austr . J. Exp . Bi o l.
~~ed. Sc i. , 36, 339, 1958. 127) Schultz e , M. 0. and Kuik e n, K. A. , J. Bi ol . Chem. , 137, 727, 1941 . 128) Theorell, H. , Benzak. M. , Bonnic h sen, R. , Paul, K. G. , and Akeson, A. , Acta Chem. Scand, 5, 445, 1951. 129) Mi ller , H. , Bi oc lzcm. ]. , 68, 275, 1958, 130) Ki rc hg e ssner, M. and Heis e ke, D. , Z. Ti e rph y si o l. Ti e rernii hr . Futt er mi ttelk d. 39, 272, 1977. 131) Bush, J. A. , Jen sen, W. N. , At he ns, J. W. , Ashenbrucker, H. , ·Ca rtw rig h t, G. E. and Wi nt r o be, M. M. , ]. Exp. Med. , 103, 701, 1956. 132) Lee, G. R. , Cartw rig h t, G. E. and Wi nt r o be, M. M. , Proc . .S oc. Exp . Bi o l. Med. , 127, 977, 1968 b. 133) Dunlap, W. M. , Jam es, G. W . and Hume, D. M. Ann. Inte rn. A-fed . , 80, 470, 1974. 134) Osaki, S. , Joh nson, D. A and Frie d en, E. , J. Bz ol . Chem. , :24 1, 2746, 1966. 135) Osaki, S. and Joh nson, D. A. , ]. Bi o l. Chem. , 244, 5757, 1969. 136) Lee, G. R. , Raga n, H. A. , Nacht, S. and Cartw rig h t, G. E. , -Cl in . Res. , 17, 152, 1969. 137) Rag a n, H. A. , Nacht, S. , Lee, G. R. , Bis h op , C. R. and Cart- wrig h t, G. E. , Am. J. ph y si o l . , 211, 1320, 1969. 138) Frie d en, E. , Nutr . Rev. , 28, 87, 1970. 139) Roeser, H. P. , Lee, G. R. , Nacht, S. and Cartw rig h t, G. E. , ]. ·Cl in. Invest. , 49, 2408, 1970. 140) Rein h old, J. G. , Cl in. Chem. , 21, 476, 1975. 141) Sta r cher, B. C. , Matr o ne, G. and Hi ll, C. H. , Feed. Proc. , 23, I, 133, 1964. 142) Mi lne , D. B. and Weswi g, P. H. , J. Nutr . , 95, 429, 1968. 143) Forth , W. and Rummel, W. , Phy s io l . Rev. , 53, 724, 1973. 144) Chase, M. S. , Gubler, C. J. , Cartw rig h t, G. E. , and Wi n tr o be, M. M. , J. Bi ol . Chem. , 199, 757, 1952.
145) Schwarz, F. J. and Ki rc hg e ssner, M. , Int. J. Vit u,m . Nutr _ Res. , 44, 116, 1974. 146) Grasmann, E. , Zbl. Vet, Med. , A23, 292, 1976. 147) Gubler, C. J. , Cartw rig h t, G. E. , and Wi nt r o be, M. M. , J. Bi ol . Chem. , 224, .53 3. 148) Grassmann, E. , Zbl. Vet. Med. , A24, 817, 1977. 149) Tomp so n, H. J. and Evans, J. L. , Nutr . Rep. Int. , 1.5, 279, 1977. 150) Dagg , J. H. , Jac kson, J. M. , Curry, B. and Goldberg. A. , Br. J. Haemato l . , 12, 331, 1966. 151 ) Kir c hg e ssner, M. , Grassmann, E. , Krip pl, J. and Mi llier , H. L. ,. Zuch tun g s kunde, 43, 336, 1971. 152) Grassmann, E. and Ki rc hg es sner, M. Zbl. Vel. Med. , A20, 481, 1973. 153) Ki rc hg es sner, M. and Weig a nd, E. , Z. Ti er ph y si o l . , Ti e rer- nii hr . Futt er mi ttel kd. , 34, 205, 1975. 154) Greg o ria d is , G. and Sourkes, T. L. , Natu re, 218, 290, 1968. 155) Evans, G. W. , My ro n, D. R. and Wi ed eranders, R. E. , Am. J_ Phys i o l. , 216, 340, 1969. 156) Schwarz, F. J. and Ki rc hg e ssner, M. , Z. Ti e rph y si o l . , Ti er - ernii hr . Fute r mi ttel kd. , 31, 91, 1973. 157) Dick , A. T. , Austr . J. Ag r ic . Res. , 5, .51 1, 19.54 . 158) Sta n dis h , J. F. , Ammeric a n, C. B. , Sim p so n, C. F. , Neal, F. C_ and Palmer, A. Z. , J. Anim . Sc i. , 29, 496. 159) Sutt le, N. F. and Mi lls, C. F. , Br. J. Nutr , 20, 13.5 , 1966. 160) Alfa r o, B. and Heato n , F. W. , Br. J. Nutr . , 29, 73, 1973. 161) Gip p, W. F. , Pond, W. G. , Tasker, J. , Van Camp e n, D. , Krook,. L. and Vi se k, W. J. , J. Nutr . , 103, 713, 1973. 162) Schwarz. , F. J. and Kir c hg e ssner, M. , Int. J. Vi tam . Nutr _ Res. , 44, 2.58 , 1974 a. 163) Braude, R. , 'Wo rld Rev. Ani m . Prod. 3, 69, 1967. 164) Hoefe r , J. A. , Mi ller, E. R. , Ullrey , D. E. , Ri tch ie , H. D_ and Luecke, R. W. , J. Anim . Sci. , 19, 249, 1960.
165) Wallace, H. D. , McCall, J. T. , Bass, B. and Combs, G. E. , J. Ant'm . Se t'. , 19, 1153, 1960. 166) Ri tch ie , H. D. , Mi lle r, E. R. , Luecke R. W. , Ullrey , D. E. and Hoefe r , J. A. , ]. Anim . Se t'. , 20, 950, 1961 . 167) De Goey , L. W. , Wahlstr o m, R. C. and Emeric k , R. J. , ]. Anim . Sci. , 33, 52, 1971. 168) Ni el sen, F. H. , Sunde, M. L. and Hoekstr a , W G. , ]. Nutr , 89, 14, 1966. 169) Jen sen, L. S. , Pete r son, R. P. and Falen, L. , Poult . Sci. , 53, 57, 1974. 170) Sutt le, N. F. and Mi lls, C. F. , Br. ]. Nutr . , 20, 149, 1966. 171) O'Hara, P. J. , Newman, A. P. and Jak son, R. , Austr . Vet. J. , 36, 225, 1960. 172) Pallauf, J. and Ki rc hg e ssner, M. , Zhl. Vet. Med. , A21, 562, 1974. 173) O'Dell, B. L. and Camp b ell, B. J. , Trace Elements Meta h olt 'sm and Meta h olt 'c Functt 'on in M. Florkin and E. H. Sto tz eds. , Meta h olt 'sm of Vt' tam t 'ns and Trace Elements , vol. 21, Elsevie r , Amste r da_m, p. 203. 1971 . 174) Prasad, A. S. , Oberleas, D. , Wolf . P. and Horwi tz, J. P. , ]. Cl t'n. Invest. 46, 549, 1967. 175) Rein h old, J. G. , Kf ou ry, G. A. and Thomas, T. A. , J. Nutr . , 92, 173, 1967. 176) Cox, D. H. , Chu, R. C. and Schlic k er, 요 A. , ]. Nutr . , 98, -44 9, 1969. 177) Chu, R. C. , Schli ck er, S. A. and Cox, D. H. , Nutr . Rep. Int. , 1, 11, 1970. 178) Moses, H. A. and Parker, H. E. , Fed. Pro. , 23, 132, 1964. 179) Prasad, A. S. , Oberleas, D. , Wolf , P. , Horwi tz, J. P. , Mi ller , E. R. and Luecke, R. W. , Am. ]. Cl in. Nutr . , 22, 628, 1969. 180) Pete rin g , H. G. , Joh nson, M. A. and Horwi tz, J. P. , Arch. Envt' ron . Healt h. 23, 93, 1971. 181) Burch, R. E. , W illiam s, R. V. , Hahn, H. K. J. , Jet t on , M. M.
and Sull ira n, J. F. Ci in. Che m . , 21, 568 , 1975. 182) Mag ee , A. C. , Jac kson, M. Y. and Wade, W. , Fed. Proc. , 34, 906, 1975. 183) Roth , H. P. and Ki rc hg es sner, M. , Zbl. Vet. Med. , A24, 177, .19 77. 184) Ki rc hg e ss n e r, M. , Schwarz, F. J. , Roth , H. -P. and Schwarz, -W. A. , Arch. Ti er e r n ti hr . , 28, 723, 723, 1978. 185) Sutt on , W. R. and Nelson, V. E. , Proc. Soc. Exp . Bi ol . Med. , .36 , 211, 1937. 186 ) Smi th, S. E. and Larson, E. J. , J. Bi ol . Chem. , 163, 29, 19 -46 . 187) Cox, D. H. and Harris , D. L. , J. Nutr . , 70, 514, 1960. 188) Schli ck er, S. and Cox, D. H. , J. Nutr . , 95, 287, 1968. 189) Whang e r, P. D. and Weswi g, P. H. , J. Nutr . , 100, 341, l.97 0. 190) Camp b ell, J. K. and Mi lls, C. F. , Proc. Nutr . Soc. , 33, 15A- 1.1 A, 1974. 191) Lantz s ch, H. and J. Ubers. , Ti e rernti hr . , 1, 57, 1973. 192) Hil l, C. H. , Matr o ne, G. , Pay n e, W. L. and Barber, C. W. , J . .Nu tr . , 80, 227, 1963. 193) Bremner, I. , Br. ]. Nutr . , 35, 245, 1976. 194) Van Camp en , D. R. , ]. Nutr . , 97, 104, 1969. 195) Evans, G. W. , Grace, C. I. and Hahn, C. , Bi oi n org. Chem. , 3, 115, 1974. 196) Schwarz, F. J. and Ki rc hg e ssner, M. , Z. Ti e rph y si o l . , Ti er er- .nt i hr . Futt er mi ttelk d. 197) Oberleas, D. , Muhrer, M. E. and O'Dell, B. L. , J. Nutr . , 90, '56 , 1966. 198) Pearson, W. N. , Schwi nk , T. and Reic h , M. , in A. S. Prasad, --e d. , Zi nc Meta b olis m , Thomas, Sp ri n g field , III, p23 9, 1966. 199) Sta r cher, B. C. , J. Nutr . , 97, 321, 1969. 200) Evans, G. W. , Majo r s, P. F. and Cornatz e r, W. E. , Bi o chem . .Biop h y s. Res. Commun. , 40. 1142, 1970.
201) Ri ch ards, M. P. and Cousin s , R. J. , J. Nutr . , 106, 1591, 19' 76. 202) Cousin s , R. J. , in Ki rc hg es sner, M. ed. , Trace Element Me- tab olis m in Man and Anim als-3, ATW. Weih enste p h an Germany , p. 57, 1978. 203) Cotz i a c , G. C. , Borg, D. C. and Selleck, B. , Am. J. ph y si o l. ,. 202, 359, 1962. 204) Ki nn amon, K. E. and Bunce, G. E. , J. Nutr . , 86, 225, 1965. 205) Owen, C. A. , Di ck son, E. R. , Goldste i n , N. P. , Bag ge nsto s s,.. A. W. and McCall, J. T. , Mayo . Cl in. Proc. , 52, 73, 1977. 206) Bremner, I. and Marshall, R. B. , J. Nutr . , 32, 283, 1974. 207) Bremner, I. , Br. ]. Nutr . , 35, 245, 1976. 208) Bremner, I. and Davie s , N. T. , Br. J. Nutr . , 36, 101, 1976. 209) Bremner. I. , Wi lliam s, R. B. and Young , B. W. , Br. J. Nutr _ 382, 1807) , B1r9e7m7n. er, L and Marshall, R. B. , Br. ]. Nutr . , 32, 293, 1974. 211) Bremner, I. and Davie s , N. T. , Bi o chem. J. , 149, 733, 1975. 212) Bremner, I. and Young , B. W. , Bi oc hem. J. , 155, 631, 1976. 213) Bremner, I. and Young , B. W. , Bi o chem. J. , 157, 517, 1976. 214) Rup p, H. and Weser, U. , Bi o chem. Bi op h y s. Acta . 533, 209, 1978. 215) Fergu son, W. S. , Lewi s, A. H. and Wats o n, S. J. , Natu re,. 141, 553, 1938. 216) Fergu s on, W. S. , Lewi s, A. H. and Wats o n, S. J. , J. Ag r ic .. Sci. , 33, 44, 1943. 217) Mi ltm ore, J. E. and Mason, J. L. , Can. J. Ani m . Sc i. , 51,. 193, 1971. 218) Alloway , B. J. , J. Ag r ic . Sci. , 80, 521, 1973. 219) Br itton , J. W. and Goss, H. , J. Am. Vet. Med. Assoc. , 108,. 176, 1946. 220) Cunnin g h am, I. J. , in McElroy W. D. and B. Glass, eds. , Copp e r Meta b oli sm , Jo hn Hop k in s Press Balti m ore, Md. , p. 246, 를
1950. 221 ) Cunnin g h am, I. J. , Brown, J. M. and Edie , A. E. , Can. 1- .Agr ic . Sci. , 33, 254, 1953. 222) Hallgr e n. W. , Karlsson, K. and Weamby , G. , Nord. Vet- Med. , 6, 469, 1954. 223) Dic k , A. T. , Austr . Vet. ]. , 29, 18, 1953. 224) Dic k , A. T. , Austr . Vet. ]. , 29, 233, 1953. 225) Dick , A. T.- , Austr . Vet. ]. , 30, 196, 1954. 226) Goodric h , R. D. and Ti llm an, A. D. , J. Nutr . , 90, 76, 1966 .. 227) W yn ne, K. N. and McClym ont, G. L. , Austr . ]. Arg ie. Res. ,.. 7, 45, 1956. 228) Allcroft , R. and Lewi s, G. , Landbouwkd, Ti jdsc hr. , 68, 711,- 1956. 229) Butl e r, E. J. and Barlow, R. M. , ]. Comp . Path o l. , 73, 208,. 1963. 230) Butl e r, E. J. , Barlow, R. M. and Smi th, B. S. W. , J. Comp ,_ Path ol. , 74, 419, 1964. 231) Hog a n, K. G. , Ri s, D. R. and Hutc h is o n, A. J. , N. Z. ]. Ar gi e ► Res. , 9, 691, 1966. 232) My lr ea, P. J. , Austr . J. Arg ie. Res. , 9, 373, 1958. 233) Marci le se, N. A. , Ammerman, C. B. , Valsecchis , R. M. , Duna- vant, B. G. and Davis , G. K. , ]. Nutr . , 99, 177, 183, 1969. 234) Pie r son, R. E. and Aanes, W. A. , J. Am. Vet. ,~ed. Assoc. ,- 133, 307, 1958. 235) Sutt le, N. F. and Fie l d, A. C. , J. Comp . Path ol. 78, 351, 19- 68. 236) Poole, D. B. R. , in Mi lls, C. F. ed. , Trace Element Meta b olis m · in Anim als, Liv in g s to n e, Edin b urgh , 465, 1970. 237) _M i lls, C. F. and Fell, B. F. , Natu r e, 185, 20, 1960. 238) Fell, B. F. , Mi lls, C. F. and Boy n e, R. , Res. Vet. Sci. , 6,- 170, 1965. 239) Sutt le, N. F. and Fie l d, A. C. , J. Comp . Path ol. , 78, 363,. 1968.
240) Dic k , A. T. , in McElroy W. D. and R. Glass, eds. , Inorga ni c 1'/itr o g e n Meta b oli sm , Joh n Hop k in s Press, Balti m ore, Md. , p. 44 5 , 1956. 241) Gray , L. F. and Ell is, G. H. , J. Nutr . , 40, 441, 1950. 242) Kulwi ch , R. , Hansard, S. L. , Comar, C. L. and Davis , G. K. , J. Anim . Sci. , 10, 1052, 1951. 243) Kulwi ch , R. , Hansard, S. L. , Comar, C. L. and Davis , G. K. , Proc. Soc. Exp . Bi ol . Med. , 84, 487, 1953. 244) Gray , L. F. and Danie l , L. J. , J. Nt ttr. , 53, 43, 195.4 . 245) Halverson, A. W. , Phif er, J. H. and Monty , K. J. , J. Nutr . , 71, 95, 1960. 246) Jet e r , M. A. and Davis , G. K. , J. Anim . Sc£ . , 9, 660, 1950. 247) Sta n dis h , J. F. , Ammerman, C. B. , Wallace, H. D. and Gombs, -G. E. , J. Anim . Sci. , 40, 509, 1975. 248) Gip p, W. F. , Pond, W. G. and Smi th, S. E. , J. Anim . Sci. , 26, 727, 1967. 249) Hay s, V. W. and Klin e , R. D. , Feedstu f fs, 41 (44) 18, 1969. 250) Klin e , R. D. , Hay s, V. W. and Cromwell, G. L. , J. Anim . Sc i. , 33, 771, · 1971. 251) Dale, S. E. , Ewan, R. C. , Sp e er, V. C. and Zim merman, D. R. , J. Anim . Sci. 37, 913, 1973. 252) Comp e re, R. , Burney, A. , Francois , E. and Vanuy tre cht, S. , .Bu l, Inst. Ag r onom. Gemblouy . 33, 102, 1965. 253) Mi lls, C. F. , Proc. Nutr . Soc. , 19, 162, 1960. 254) Hamp el , G. and Kir c hg es sner, M. , Arch. Gef lu g c lkd. , 34, 18 1, 1970. 255) Marsto n , H. R. , Allen, S. H. and Swaby , S. L. , Br. J. Nutr . , :25 , 15, 1971. 256) Kl ine , R. D. , Corzo, M. A. , Hay s , V. W. and Cromwell, G. L. , J. Anim . Sci. , 37, 936, 1973. 257) Dowdy , R. P. and Matr o ne, G. , J. Nutr . , 95, 191, 1968. 258) Dowdy , R. P. a!!:l Matr o ne, G. , J. Nutr . , 95, 197, 1968. 259) Dowdy , R. P. , Kunz, G. A. and Sauberlic h , H. E. , J. Nutt . ,
'99 , 491, 1969. 260) Gray , L. F. and Danie l , L. J. , J. Nutr . , 84, 31, 1964. 261) Huis i n g h , J. and Matr o ne, G. , Proc. Soc. Exp. Bi ol . Med. 1 189, 518, 1972. 262) Huis i n g h , J. , McNeil l, J. J. and Martr o ne, G. , . Ap pl. Mi cr osc. , 28, 489, 1974. 263) Gomez-Garcia , G. G. , Investi ga ti on of th e Bz 'ol og ica l Inte r acti on s .of Cop pe r, Molyb date and Sulfa te , Ph. D. the sis , North Caroli na Sta t e . Univ e rsit y, 1972. 264) Hartm ans, J. and Bosman, M. S. M. , in Mi lls, C. F. ed. , Trace Element Meta b olis m in Anim als, E. and S. Livi n g s to n e, London. 1). 362, 1970. 265) Huis i n g h . J. , Mi lho lland, D. C. and Matr o ne, G. , ]. Nutr . , 105, 1199, 1975. 266) Gawt h orne, J. M. and Nader, C. J. , Br. ]. Nutr . , 35, 11, 1976. 267) Huis i n g h , J. and Matr o ne G. , Chap ter . 12, in W. R. Chapp e ll and K. K. Pete r sen, eds. , Molyb denum in th e Envir on ment, vol. 1, Marcel. Dekker, New York, 1976. 268) Sutt le, N. F. Br. ]. Nutr . , 34, 411, 1975. 227609)) SViae ng e lR, eeLn. , MR.. , anAdr cMh.o nBty i ,o c hKe. mJ. . ,B i] o.p hNyu s.t r, . ,5 3,7 4,7 7,1 6719, 541.9 61. 271) Sp a is , A. G. , Lazarid i s , T. K. and Ag ian nid i s , A. K. , Res. -Ve t. Sci. 9, 337, 1968. 272) Dic k , A. T. , Soli . Sci. , 81, 229, 1956. 273) Cardin , C. J. and Mason, J. , Bi o chem. Bi op hy s. Acta , 394, 46, 1975. 274) Dick , A. T. , Dewey , D. W. and Gawt ho rne, J. M. , J. Ag r ic . Se t'. , 85, 567, 1975. 275) Mi lls, C. F. , Bremner, I. , El-Gallad, T. T. , Dalga rno, A. C. and Young , B. W. , in Ki rc hg es sner M. ed. , Trace Element Me• tab oli sm in Man and Anim als-3, ATW, Weih e nste p h an, Germany , :p. 150, 1978. 276) Bremner, I. and Young , B. W. , Br. ]. Nutr . , 39, 325, 1978.
277) Kir c hg e ssner, M. and Heis e ke, D. , Z. Ti e rph y s io l. , Ti e rernii hr ~ Futt er mi ttelk d. , 39, 272, 1977. 278) Gubler, C. J. , Lahey, M. E. , Chase, M. S. , Cartw rig h t, G. E. and W int r o be, M. M. , Proc. . S oc. Exp. Bi o l. Med. , 86, 223, 1954. 279) Hartm an, R. H. , Matr o ne, G. and W ise , G. H. , ]. Nutr . , 57, 429, 1955. 280) Matr o ne, G. , Hartm an, R. H. and Clawson, A. J. , ]. Nutr . ,. 67, 309, 1959. 281) Vohra, P. and Heil J. R. , Poult . Se t'. , 48, 1686, 1969. 282) Schneg g, A. and Ki rc hg e ssner, M. , Z. Ti e rph y si o l. , Ti e renahr. Fu2t8t e3r) mSi cthtenlek gd g. ,, 3A6., a6n3,d 19K7i5 r.c hg e ssner, M. , Arch. Ti e rernahr. , 26,. 543, 1976. 284) Schneg g, A. and Ki rc hg e nner, M. , Nt ttr. Meta b ol. , 19, 268,. 1975, 285) Schneg g, A. and Ki rc hg e ssner, M. , Int. ]. Vi tam . Nutr . Res. ,. 46, 96, 1976. 286) Sp e ars, J. W. , Hatf ield , E. E. and Forbes, R. M. , Fed. Proc. ,. 36, 1106, 1977. 287) Godwi n, K. 0. , Parti ck , E. J. and Fuss, C. N. , in Ki rc hg e ssner,. M. ed. , Trace Element Meta b oli sm in Man and Anim als-3. ATW ' Wei! ten ste p h an, Germany 185, 1978. 288) Camobell, J. K. , Davie s , N. T. and Mi lls, C. F. , in Ki rc h-· ge ssner, M. ed. , Trace Element Meta b olis m in Man and Ani m als-3. ATW Weih e nste p h an, Germany , p. _5 5 3, 1978. 289) Pete rin g , H. G. , in Hoekstr a , W . G. J. W. Sutt ie, H. E. Ganth er- and W. Mertz , eds. ; Trace Element Meta b olis m in An i mals 一 2 · Univ e rsit y Press, Balt im ore, Md. , 311, 1974. 290) Van Camp en , D. R. , J. Nutr . , 88, 125, 1966. 291) Jac obs, E. E. , Jac ob. M. , Sanadi, D. R. and Bradley , L. B. ,. J. Bi o l. Chem. 223, 147, 1956. 292) Cramp ton , R. F. , Matt he ws, D. M. , and Pois n er, R. , J. Ph- ysi o l . , 178, 111, 1965.
293) Huta g a lung , R. I. , Schwarz, F. J. and Ki rc hg e ssner, M. , .Ar ch. Ti er enahr. , 27, 347, 1977. 294) Hil l. C. H. , Sta r cher, B. and Matr o ne, G. , J. Nutr . , 80, 227, 1964. 295) Losee, F. , Cutr e ss, T. W. and Brown, R. , Trace Subst. Envir on . Healt h. 7, 1973. 296) Hami lt o n , E. I. and Mi ns ki, M. T. , Sci. Tota l Envir on I, 375, ·19 72~1973. 297) Van Camp en , D. , ]. Nutr . , 88, 125, 1966. 298) Leverto n , R. M. and Bin k ley, E. S, ]. Nutr . , 27, 43, 1944, 299) David s on, L. S. P. Fullerto n , H. W. , Howi e, J. W. Croll, J. M, ·Or r, J. B. and Godden W. M. , Br. Med. ]. , 2, 685, 1933. 300) De H. N. , India n ]. Med. Res. , 37, 301, 1949. 301) Henkin , R. I, in Hoekstr a et al. , eds. , Trace Element meta b olis m .tn Anim als, vol. 2, p. 647 Univ . Park Press, Balt imo re, Maryl a nd, 1974. 302) Bunch, R. J, Sp e ers, V. C, Hay s, V. M. and Mccall, J. J. , J . .An im . Sc i. , 22, 56, 1963. 303) Lin d ow, C. W, Pete r son, W. H. and Ste e nbock, H. , ]. Bi ol . Chem. , 84, 419, 1929. 304) W. H. 0, Tech, Rep. Ser. , 532, 1973. 305) 홍영숙, 선정래, 《한국영양학회지》, 8, 1, 39, 1976. 306) Nati on al Research Counc il, Nati on al Academy of Scie n ces, Was- liing ton , D. C. 99, 1974.
4 아 연 (Zin c , Zn) 박테리아 및 석물에 대한 Zn 의 필요성은오래전부터 언급되어 왔 으며 I) 생 체 내 Zn 에 관한 연구는 1877 년 Lecharti er 와 Raoult , Bre t on” 에 의 해 사람의 간에 서 Zn 을 발견함으로써 시 작되 었 고 19 34 년에 Todd3) 와 1934 년에 Ber t rand14) 는 쥐 의 성 장과 발육에 있 어 Zn 이 필수적 인 원소라고 보고하였 다. 1940 년 Keil in 과 Mann4) 은 소의 적 혈구에 서 Zn 과 결 합된 carbonic · a. nhy drase 를 발견, 분리하고 Zn 이 적혈구의 주요한 구성 성분으 로 촌재한다는 것을 보고하였으며 이것은 Zn 의 생체내 기능을 섣 명하는 첫 연구가 되었다. Zn 은 동물의 정상적인 성장, 번식 및 조직 보유와 상처 치유의 효과를 준다. 그러나 Zn 의 생리적 및 임상적 중요성에 관한 연구 가 본격적으로 시작된 것은 극히 최근의 일이며 Fe, Cu 와 함께 많 이 연구되고 있는 tra ce element 중의 하나타고 하겠다. 4.1 체내 함량과 분포 인간과 동물은 전채 무게의 20~30p pm 정도의 Zn 을 함유하며 : 따라서 Fe 다음으로 많이 들어 있 는 tra ce element 이 다. 75kg 의 성 인은 1. 5~2.3 g의 Zn 을 함유하는 것으로 추정된다. Zn 은 체내와 여러 조직에 널리 분포되어 있다. 표 4.1 은 조직의 Zn 농도이다 .1 ),
 표 4.1 정상적인 조 직 의 아연 (Zn) 함량 ' y y ) . ) : )
표 4.1 정상적인 조 직 의 아연 (Zn) 함량 ' y y ) . ) : )
그 이외에도 체조직 중에서도 Zn 함량이 가장 많다고 알려진 곳 · 이 눈으로서 사람의 홍채 에 는 5, 000p pm 까지 , 망막에 는 500~1, 000. ppm 까지 가 Zn 복합체 형 태 로 melanin 에 함유되 어 있 다. 238) 골격의 Zn 함량은 연령이나 환경에 관계없이 사람의 갈비려에서 181 土 70 pp m 으로 나타났다. 23 8 ) Sm it h239) 는 사람의 손톱과 발톱에 292~93 pp m 의 함유량이 있음을 측정했다. 여러 사람들에 의하여 성인의 머리카락의 Zn 함량을 측정했는데 338 에 서 92p pm 정 도였 다. 49)233)239)2 4 0) 췌 장의 /3- cell 에 는 100~1 , OOOp pm 의 Zn 이 함유되 어 있 어 Zn 이 많이 함유된 조직에 속하는 반면 반대로 췌장의 exocrin 부분에는 20~30p pm 으로 아주 적 온 양이 들어 있 다. 12) ins uli n 의 Zn 함유량은 0. 15~3% 이 상까지 큰 차이 를 보아 고 있 으며 in suli n 은 Zn 과 복합체 를 형 성 하고 있 다. 238) 체내 전체 Zn 의 약 20% 가 피부에 들어 있으며 약 1~2% 정도. 가 혈액에 촌재한다. 혈액의 75~88% 가 적혈구에, 12~20% 가 혈 장에, 그리고 3% 정도가 백혈구에 존재한다. 혈장의 Zn 농도는 평 군 1. lµg /m l(O. e~1. 4µg /mE 이 며 혈청온 1. 0~1. 2µg / ml 그리 고 적 혈구에 는 14µg / ml 로서 Zn 이 결합된
carbonic anhy d rase 의 효소로 촌재 한다. 신생 아 적 혈 구의 Zn 량은 성인과 비교했 을 때 약 3.8µ g /ml 로 적은 양 울 함유하며 6~11 세에 이 르러 성인과 같아진다 .10) 혈장의 Zn 은 30~40% 가 a2- m acrog lo blin 과 tra nsfe r rin 과 견 고하게 결 합되 어 있 으며 60~70 % 정 도가 album i n 과 느슨하게 결합되어 있고 pH 4 이상에서 용해된다. 음식물 섭취가 부족할 때나, 24 시간 전석시 성 인의 혈 장 Zn 상대 는 0. 4~0. 6µg /m l 로 감소되 었 다 . 11) 임 신기 간 동안에 도 역 시 혈장 Zn 이 0.8µ g /ml 로 감소되었으나 적혈구의 Zn 함량에는 변화가 없 었다. 백혈구에 80% 정도 함유되어 있는 Zn p ro t e i n 의 결 합은 찰 연구되어 있지 않다. 4.2 주요 기능 Zn 은 여러 효소들의 구성원소 및 조효소로 알려져 왔다 .13) 표 4. 2 는 인 간과 동물의 Zn- - me t alloenz y me41> 을 나타내 고 있 다. 표 4. 2 의 효소 이 의 에 도 try ptop h an, desmolase, pyri d i n e nucleoti de -dep e ndent meta l lo dehy d rog e nase 둥에 도 Zn 이 관여 한다고 알려져 있다 .3) Zn 은 또한 혈장의 albumi n, 15> tra nsfe r rin , 15> meta l lo th io n ein , 17> nucleop r ote i n , his t i di n e 및 cy s te i n e 과 복합체 18) 를 형 성 한다. Zn 이 결핍된 세포는 초기의 장애로 RNA 형성이 파괴되어 그로 인한 단백질, 총질소, DNA 의 합성이 감소되는 것을 볼 수 있어 19)20) 단백질 대사에 Zn 의 역할이 중요함을 알 수 있다. Eckhert 등은 Zn th y m i di n - kin a se 활성 에 관여 하여 이 효소는 DNA 합성 과 세 포 의 분열 과정에도 필수적이며 Zn 결핍시에 성장 정지 현상을 보여 주며 성장중의 태아기여)의 중추신경계를 조철해 주기도 한다고 보고되었다 .2 1) Zn 은 po rph y r in 대사와도 관련을 가지며 소변과 대변의 po rph y - 1.in 은 Zn 복합체 로서 po rph y r in 의 배 설을 중가시 켜 해독작용에 기여한다고 한다. Zn 은 몇 가지 hormone 과도 상호관련성이 있는 폐 20) 췌장에 Zn 함량이 높으면 ins ulin 의 생 리 적 기 능을 중가시 켜
 표 4. 2 동 물 과 인 체 조칙 의 아연 (Zn) meta l loenzy m es4 >
표 4. 2 동 물 과 인 체 조칙 의 아연 (Zn) meta l loenzy m es4 >
준다고 하며 Zn 결핍시 endog e nuis ACTH 생성이 여제되는 것으 로 보여 진다 . ins uli n 은 Zn 과 복합체 를 형 성 하는데 이 것 은 ins uli n 정체 과정중 결정형 Zn i nsul i n 을 만들 수 있게 하며 ins ulin 분자 에 달라붙은 Zn 은 체 내 에 주입 할 때 ins ulin 의 작용기 간을 증가시 킨다. Dav i es 2 2) 는 췌장의 /3세포에서 i nsu li n 을 저장하고 방출하는 데 Zn 이 작용한다고 시사했다. Landes2” 는 Zn 이 당질대사 작용에도 참여하고 있다고 보고했는 데 쥐의 실험에서 석이 내 당질은 Zn 상태에 영향을 주는데 전분은· 다른 당질인 서당, 포도당, 과당보다 간에 Zn 을 더 많이 축적시켰 다고 하였다. Zn 은 골격의 유기 물질에 대해 특수한 효과를 보이 고 있는데 석 회화를 유도하는 과정 및 hormone 과 효소 sy s te m 에 저 Zn 이 석회화과정을 촉매한다고 한다 .20)
Zn 은 취의 태아기 허파발달에 주요한 원소라고 하며 ,24) Zn 이 결 ’_ 핍된 취의 장 내에서는 중성지방의 흡수가 현저히 감소되었다고 한 다. 25) 최 근 Zn 의 주요 기 능으로 장접 막에 서 chy lo mi cro n 의 형 성 에 영향을 준다는 보고가 있으며 Zn 이 결핍된 쥐는 접막에 있는 chy lo mi cro n 을 둘러 싸고 있는 단백 질이 부족되 어 지 방이 축적 되 게 되고 그 결과 흡수가 지연된다고 한다. Me t allo t h i one i n(MTN) 은 Zn2+ homeosta s is 에 관여 하며 Zn2+ 상 태에 따라 MTN 의 합성과파괴가 달라진다고 한다 .26) Zn 대사에서 MTN 의 합성은 과량의 Zn 의 독성 방지 및 과량의 Zn 이온의 축적 을 방지해 주며, 필요시 Zn 을 효과적으로 재활용하도록 작용한 · 다 .27) Aceta z olami de 는 효소 분자에 촌재 하는 Zn 과 결 합함으로써 car-· bonic anhy d rase 활성 을 억 제 하였 다. 망막은 Zn 금속효소인 re- tine ne reducta s e 를 함유하며 이 효소는 rhodop s in 호] 로에 서 reti ne nc (vit am i n A aldeh y de) 의 재 생 에 쓰이 게 된다. Reti ne ne reducta s e 는 간장의 탈수소효소와 동일한 기능을 갖는다. Zn 은 혈장에서 vi- ta mi n A 의 정상적인 농도를 유지하는 데 필요하며 간장으로부터 혈장으로 vit am i n A 가 이 동되 는 데 Zn 이 소요된다고 지적 했다. 28) 그러 므로 혈장 내 의 vit am i n A 농도가 정 상보다 낮고 vit am i n A 무 여로서 치유되지 않을 경우 Zn 을 보충하는 것이 필요하다. 백혈병 환자의 경우, 백혈구의 Zn 함량은 정상치의 약 10% 로 김~ 소되어 있으며 이 병의 일시적인 치유효과에서 세포의 Zn 함량이 정상수준으로 중가하는 것을 관찰할 수 있었다. 백혈구에 의하여 생 성 되 는 sup e roxid e ion 은 살균작용을 하며 29) Zn 을 함유하는 sup e roxid e dis m uta se 는 이 들 세 포에 서 sup e roxid e 생 성 을 조절 하는 기능울 가졌다고 한다. 또한 Zn 은 상처 치유에 아주 효과적. 이라고 한다 .30)
4.3 대 사 4.3.1 홍 수 Zn 은 거의 전부가 소장에서 흡수되며 위장과 대장에서는 거의 흡수되지 않는다. 십이지장과 소장부분에서도 말단부분보다 근위 부분에 서 흡수가 찰된다. 31) 장에 서 Zn 이 흡수되 고 운반될 때 흡수 제 포에 서 energ y 를 필요로 한다고 한다. 32) 이 때 에 Zn 은 장관내 의 저 분자 liga nd 에 결합하여 세 포로 흡수된다. 췌장과 pro sta g la n-din E2 에 서 모유의 Zn 과 결 합된 배 위 자(iig and)238) 는 개 개 의 ami no , a ci d 에 의해서 Zn 의 홉수가 증가된다 .34) 여러 과정을 거쳐 추출된 장접 막 균등질은 분자의 Zn 단백 질 복합체 (Zn-b i nd i ng - p ro t e i n) 로서 Zn 을 세포로 운반해 주는 역할울 한다. Zn 에 의해서 합성되는 장 臺 의 Zn meta l loth i o n ein 은 평 형 조철 (homeos t as i s) 의 Zn 흡 수에 도 중 요하다. Zn 의 흡 수율은 신체의 Zn 의 상태에 의하여 영향을 받는 다. 그러므로 Zn 결핍시에는 Zn 이 정상치일 때 보다 더 많은 Zn 이 홉 수된다 .35) 그림 4.1 은 취에게 단계적으로 Zn 섭취량을 높여 주었을 때 체내 항상성을 유지하기 위하여 달라지는 전정 흡수량과 겉보기 흡수량 및 내인성 Zn 배설량을 보여준다. 그림 4.1 에서 보듯이 Zn 이 결핍된 식이에서는 100%, subop tim al 섭취시에는 90%, 그리고. Zn 섭취가 o pti mal 일 때는 30~40% 의 홉 수율을 보여준다. 임신 기간이나 어린이의 경우 생리적으로 Zn 을 많이 필요로 하 므로 그에 따라 흡수율도 중가한다. 36) 또한 Zn 의 흡수는 식 이 에 함유된 화학 성분과 장관내의 상호작용에 의해서 영향을 받는다. 동물성 식품의 Zn 흡수율이 식물성 식품보다 현저하게 높다고 한 다 .37) 병 아리에 있어서 EDTA 와 결합된 Zn chela t e 는 Zn 의 흡수 를 증가시 켰 다. Lan t zsch38) 는 곡식 과 두류의 Zn 의 이 용도를 측정 하였는데 ph yta t e 의 함량이 흡수율과 일정한 관계가 있다는 것을 입증했다. ph y tic ac i d 는 Zn 과 복합체를 형성하고 용해되지 않가
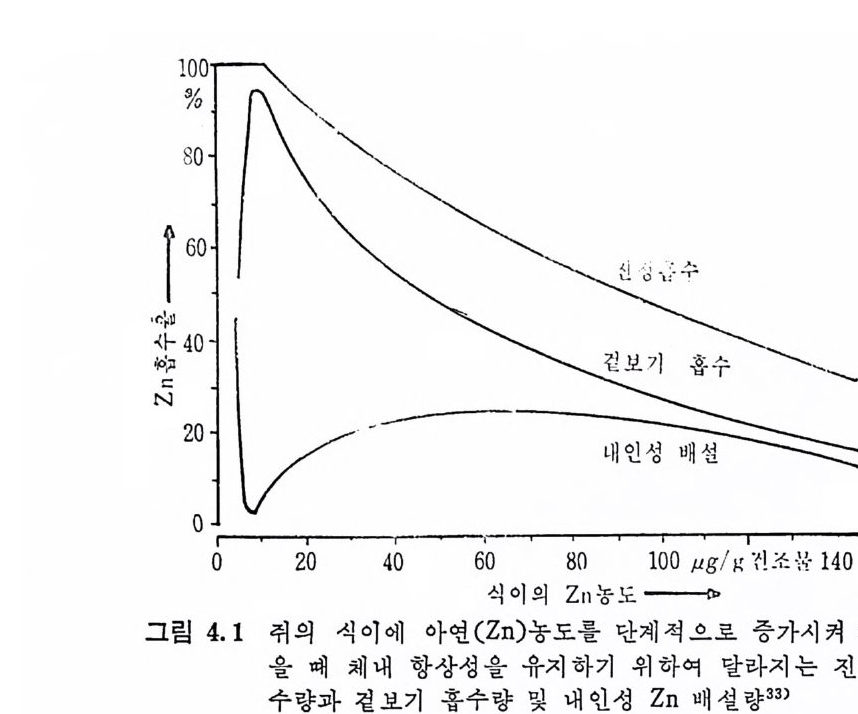 100
100
때문에 흡수율을 감소시키며 체내 Zn 의 생리적 수명을 감소시켜 . Zn 의 손실을 증가시킨다. 보리빵(전곡으로 만든)을 우유나 유제품 과 함께 섭취하떤 흡수율의 감소를 다소 여제할 수 있다 .39)
 표 4.3 식이 섬유소가 아연 (Zn) 평형에 주는 영향 40)
표 4.3 식이 섬유소가 아연 (Zn) 평형에 주는 영향 40)
표 4.3 은 섬유소와 Zn 의 평형 관계를 보여준다. 복합체를 형성 할 수 있 는 단백 질 인 his t i din e 과 cy s te i n e 은 장관내 에 서 Zn 의 홉 수를 중가시킨다. 식아에 함유되어 있는 과량의 Cu 는 Zn 의 흡수 를 처해하는데 이는 Cu 의 경쟁적인 흡수기전이 그 원인이라고 한
다. P, Cd, Cu 도 Zn 결핍을 십하게 하는 요소가 되며 섬유소도 역시 Zn 이용을 감소시킨다고 한다. Zn 의 정확한 흡수율을 축정한 다는 것은 섭취상대와 석이의 함유요소가 다르기 때문에 상당한 어 려움이 있다고 하겠다. Zn 의 평형실험에서 어란 아이들과 청소년들의 겉보기 흡수는 고 기와 유재품의 섭취시 20~50% 가량 되며, 성인의 혼합식에서는 10% 로 추정되었다. 전정 흡수율은 훨싼 더 높은데 이는 내인성 Zn 울 장에 보내 주기 때문이다 .4 1) 4.3.2 저 장 Zn 의 가장 빠른 축적과 교체는 연조직 특히 췌장, 간장, 콩팥, 비장에서 일어난다. 간장의 세포질은 me t allo t h i one i n 과 동일하거 나 또는 유사한 Zn 및 Cu 결합 단백질을 함유하며, 이 단백질은세 포 내의 중금속 해독 기능 이의에도 Fe 처장시의 ferr itin과 같이 Zn 의 저장 단백질로 작용하기도 한다. 골격은 비교적 많은 양의 Zn 을 저장하지만 이들 저장분은 개체의 다론 부위와 재빠르게 평 형을 이루지는 못한다. 생물학적으로 이용이 가능한 Zn 의 체내 p ool 은 작으며, 단지 빠른 교체율을 가진 것으로만 알려졌다. 방사성 동위원소 65Zn 을 두입했을 때 빠른 속도로 혈장에서 벗어 나 많은 양이 간장과 췌장, 신장, 이자 등에 저장되었으며 이 기관 불은 Zn 교체윤이 빠른 반면에 골격과 적혈구는 Zn 을 천천히 받아 들이지만 오렌 기간 동안 찰 저장하였다. Zn 의 보유는 vit am i n D 를많이 섭취했을 때 중가했다. 사람에게 두입한 65Zn 은 1 주일 이내에 투입량의 3.4~26% 가 대 변으로, 그리고 2 주 내에 3.3~11% 가 소변으로 배설되었다고 한 다. 42) 이 결과로 미루어보아 많은 양의 Zn 이 체내에 보유되는 것을 알 수 있다. 이온의 형태로 된 6szn 을 쥐에게 투입시킨 결과, 24 시 간 이 내 에 투입 량의 17% 를 배 설했는데 그 중 1/3 이 소변으로, 2/3 는 대변으로 배설되었다 .42) 반대 로 Co 복합체 와 결 합된 66Zn(Zin c eth y le ne dia m i ne tet r a acetic -
ac i d) 를 두입한 결과 24 시간 이내에 투입량의 70% 가 배설되었는데 그 중 9/10 가 신장을 동하여 배설되었다 .43) balance 실험에서 정 상적으로 음식물로 섭취하는 Zn 은 매일 6~22m g으로서 Zn 의 상 태가 평형이거나 p os iti ve 이었다고 한다. 신생아의 Zn 함유량은 약 60m g으로 매일 우유에서 1.0 ~1. 5 mg / kg Zn 을 섭취하며 거의 전 부를 보유한다고 했 다. 10) 4~6 세 의 Zn 보유는 0. 1~0. 2mg / kg /1 일 라고 하였다 .45) 초유에는 Zn 이 현처하게 많이 함유되어 있으므로 0.14~0. 6mg /l 00g 46 ) 생 리 학적 으로 큰 의 의 가 있 다고 하겠 다. 정상인의 머리카락의 Zn 량은 119.4 士 5.5µ g/g체중이다 .47) 머리 카락의 Zn 량이 70µg /g 체중으로 낮은 어란아이들은 신장과 체중 이 Iowa-gr owt h- chart s 에 비 해 서 10% 가량 적 었 다고 한다.
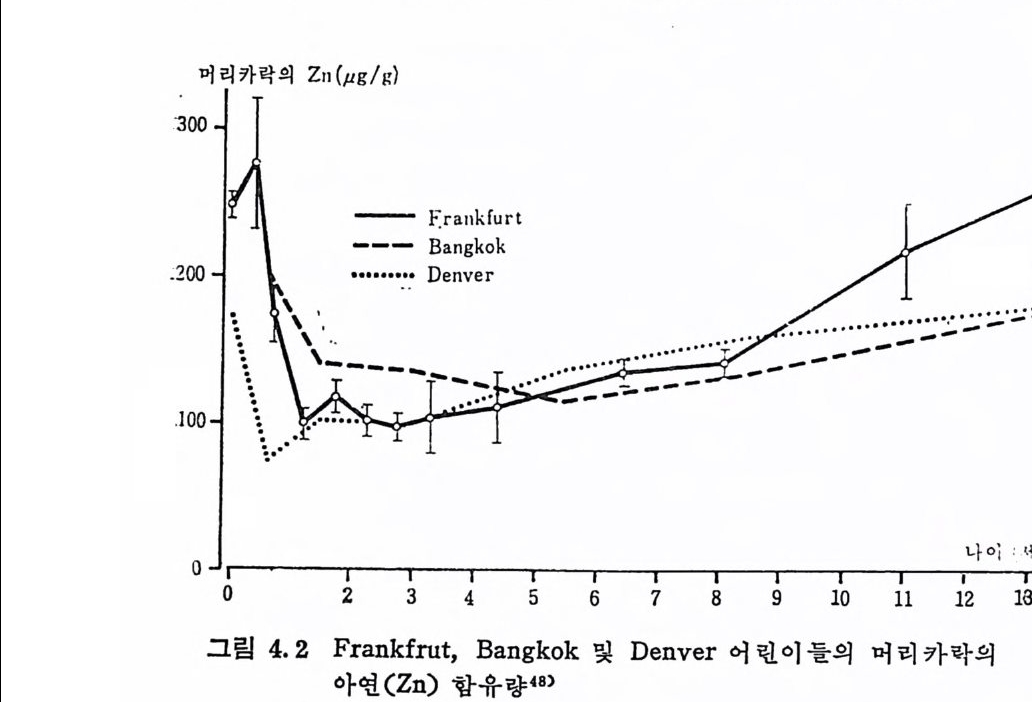 -
-
그립 4. 2 는 Frank fur t , Denver 와 Bang k ok 의 어 린이 들의 머 리 카락의 Zn 농도이다. 그립 4.3 은 머리카락의 Zn 의 농도와 성장과는 상관관계가 있다
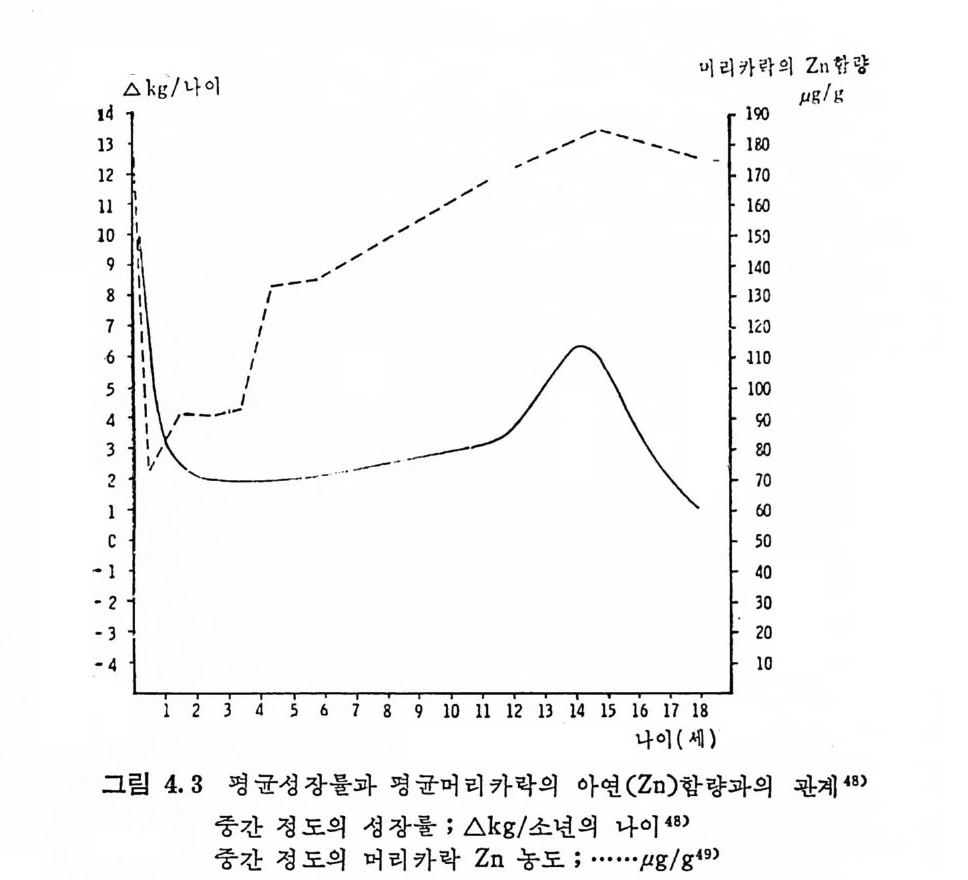 미리카락의 Zn 함량
미리카락의 Zn 함량
논 것을 보여준다. Zn 농도가 높으면 성장이 빠르고 Zn 농도가 낮 으면 성장이 늦다고 한다 .78> Zn 도 Fe 과 마찬가지로 출생시의 처 장량이 빠른 성장에 의해서 소모되어 버리기 때문에 나이에 따라서 Zn 의 감소 현상을 머 리 카락에 서 볼 수 있 었 다고 한다. so> Hellweg e 는 0~12 제까지 혈청의 Zn 을 겁사한 결과, 출생 후 4 세 이전까지 는 감소 현상을 보이다가 4 세 이후부터 접차 증가 현상을 보였음을 보고하였다 .44) 4.3.3 배 설 가장 많은 Zn 량이 대변을 동해서 배설된다. 대변으로 배설되는 Zn 은 식품에서 흡수가 되지 않은 것이거나 내인성 Zn 으로 배설된
것들이다. 내안성 Zn 분비는 제일 먼저 소장 접막에서 이루어지며 일부분은 체장액에 의해서 배설되고 대장이나 담즙을 통해서는 소 량이 배설된다. 내인성 Zn 분비는 섭취하는 Zn 의 양에 따라서 달 라지며 항상성에 의해서 결정된다. 그러므로 내인성 Zn 분비량은 흡수와 마찬가지로 변화한다. 신장으로 배설되는 성인의 Zn 은 약 0. 3~0.6m g /l 일로 아주 적다. 이것은 Zn 의 섭취 상태와 상관관 계가 없다. 단지 Zn 의 결핍이 극십한 경우에는 소변으로 배설되는 Zn 의 양이 감소된다. 반대로 여러 가지 질병의 경우(네프로제, 여러 종류의 간장 질환 화상 동) 수술 후 철식 기 간 동안 pa rente r al nutr i t ion 혹은 chelate 형성물을 섭취했을 때는 베설이 대폭적으로 중가된다. 땅으로 배설 되는 Zn 의 양은 약 1. 2µ g /ml 이라고 한다 .51) 여자들의 월경 기간 중 손실되 는 양은 0. 4~0. 5mg 이 라고 한다. sz) Hess 와 그의 동료 등 53) 은 젊은 여자들에 있어서 Zn 이 부족된 식이에서 불가피하게 손실되는 Zn 은 하루 약 1. 6m g으로 추정하였다. 4.4 Zn 의 필요량 1 일 Zn 필요량은 여러 요인에 영향을 받는데 예를 들어 석품, 기 후, str e ss, 수술 후, 전염병, 다본 질병동에 의한다. 현재 우리 냐 라에서는 권장량이 결정되어 있지 않고, 미국의 경우 RDA 에서 하 루 최처 Zn 섭취량을 다음과 같이 정했다 .89)
 1 세 이하 3~5mg
1 세 이하 3~5mg
위의 권장량은 건강한 상태에서 흡수와 배설 등의 대사가 정상적 인 경우이다. 또한 음식의 섭취 형태가 혼합식으로 동식물의 식품, 생선류, 내장 동을 섭취할 때를 기준으로 한 것이다. 내장은 Zn 이
많이 함유되어 있어서 좋은 Zn 급원이며 우유나 유제품 그 자채는 Zn 함량이 적으나 양질의 단백질로서 Zn 의 흡수물 촉진시켜 주 기 때문에 좋 다고 한다. 녹색채소와 전곡은 Zn 의 함량이 많으나 체 내 흡수량 이 적다. 채식주의자들은 단백질 섭취가 충분하지 못하기 때 문에 석품 에 충분한 양의 Zn 이 들 어 있음에도 불구하고 흡수와 이 용률이 낮아 Zn 결핍 현상이 나타난다. 단백질 섭취가 충분할 경우 에는 체내 Zn 의 상태도 좋으며 공업 국가에서는 매일 성인 이 12~ 15mg 정도의 Zn 을 섭취하고 있다. 각 나라벌로 Zn 섭취 량을 보면 다음과 같다 .
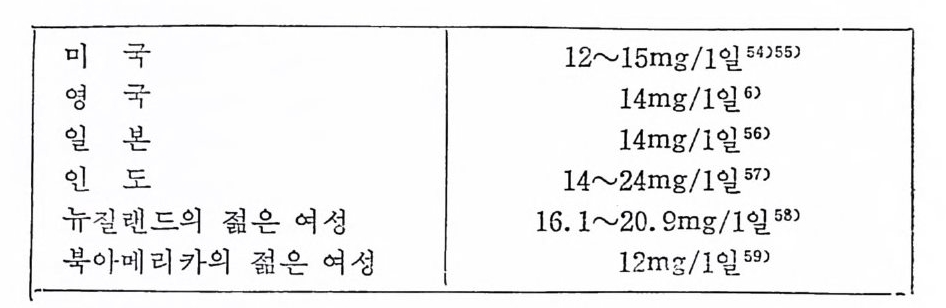 미 국 1 2 ~15m g /1 일 터 )55)
미 국 1 2 ~15m g /1 일 터 )55)
또한 사춘기의 소녀들이 4 .6~9.3m g/1일일 때 노 르웨 이의 3~9 세의 어린이는 5~7m g /1 일, 10~13 세는 9~13m g /1 일로 보고되었 다. 60) 생 후 1 주 일된 건강한 신생 아가 모유를 먹 을 때 Zn balance 는 neg a ti ve 로 나타났으며 , Zn 섭 취 량은 0. 2~1. 2mg / kg 이 었 다고 한 다. 61) 미 국의 병 원석 에 서 는 4. 7mg ~ 18. lm g /1 일을 섭 취 한다고 한 다. 54>55> Codex A li men t ar i us62) 에 서 는 Zn 의 임 시 권장량을 0. 5mg /lOOKcal 로 실험했는데 조사된 유아 석품의 Zn 함유량은 0.19~o. 55mg / 100Kcal 로서 6“ 모유화된 우유에 본래 의 우유보다 Zn 의 함량 이 현처히 낮기 때문에 알맞은 Zn 권장량 설정이 문제시되고 있다. 표 4. 4 는 World Health Or gan i za ti on(WHO) 에 서 임 시 권장량으로 만둘어전 Zn 필요량과 체내 Zn 의 배설과 이용률을 설명하고 있다 .6 4) 표 4. 4 는 fat-free -ti ssu e 의 Zn 이 약 30µg /g 이 들어 있 고 그리 고 lean body mass 의 측정에서 성인 남자의 연조직에는 Zn 이
2.Og , 성인 여자의 연조직에는 1. 2 g인 것에 기초를 두었다. 나이 에 따른 lean body mass 의 측정 으로 Zn 의 필요량을 결정 하였 다. 뼈의 Zn 함량은 측정하지 않은 상태에서 체내 Zn 함량과 비교했다. 땅 배설량은 ll 의 땅에 1m g의 Zn 이 함유되어 있는 데 근거를두었 다. 수유부는 l l 모유에 5m g의 Zn 이 함유되 어 있 으며 하루 650ml 를 수유한다는 전제 하에 결정되었다. 뇨 배설량은 여러 조사 결과 의 평 균값을 사용하였 다. 64)
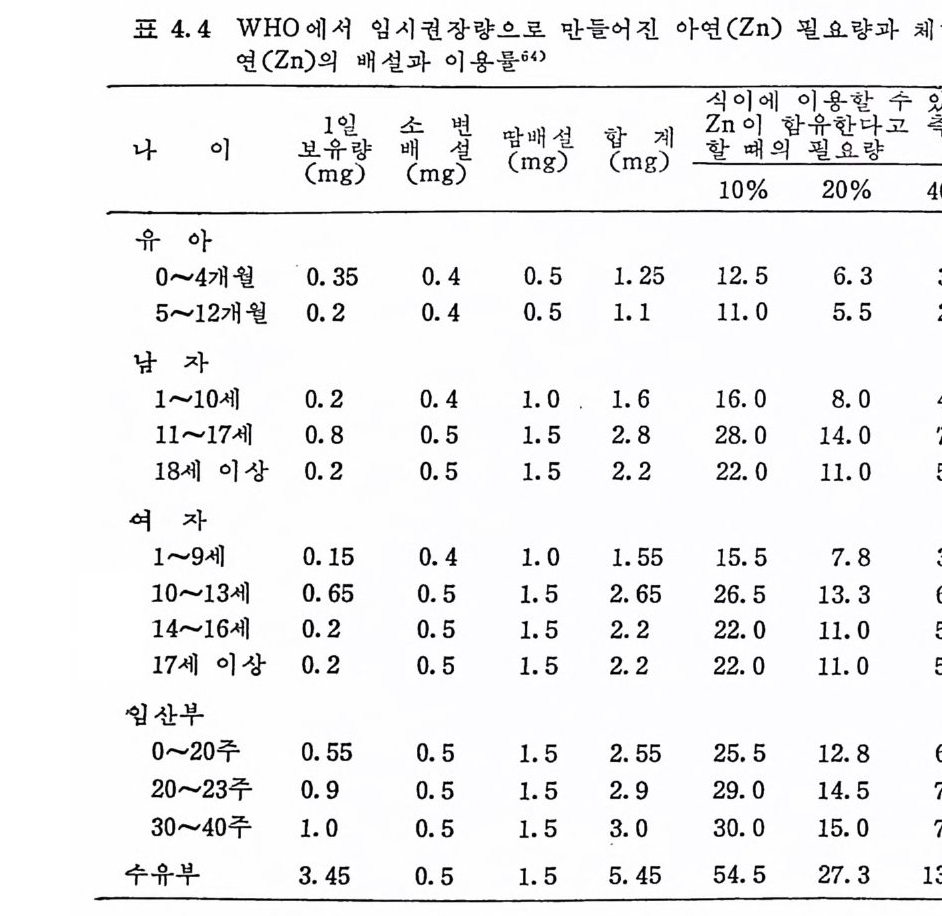 표 4.4 WHO 에서 입시권장량으로 만들어전 아연 (Zn) 필요량과 체내 아
표 4.4 WHO 에서 입시권장량으로 만들어전 아연 (Zn) 필요량과 체내 아
그립 4.4 는 여러 연구자들이 실험한 식이의 Zn 함량과 Zn 의 체 대 이용률에 의해서 영향을 받는 Zn 의 필요량을 나타낸 것이다.
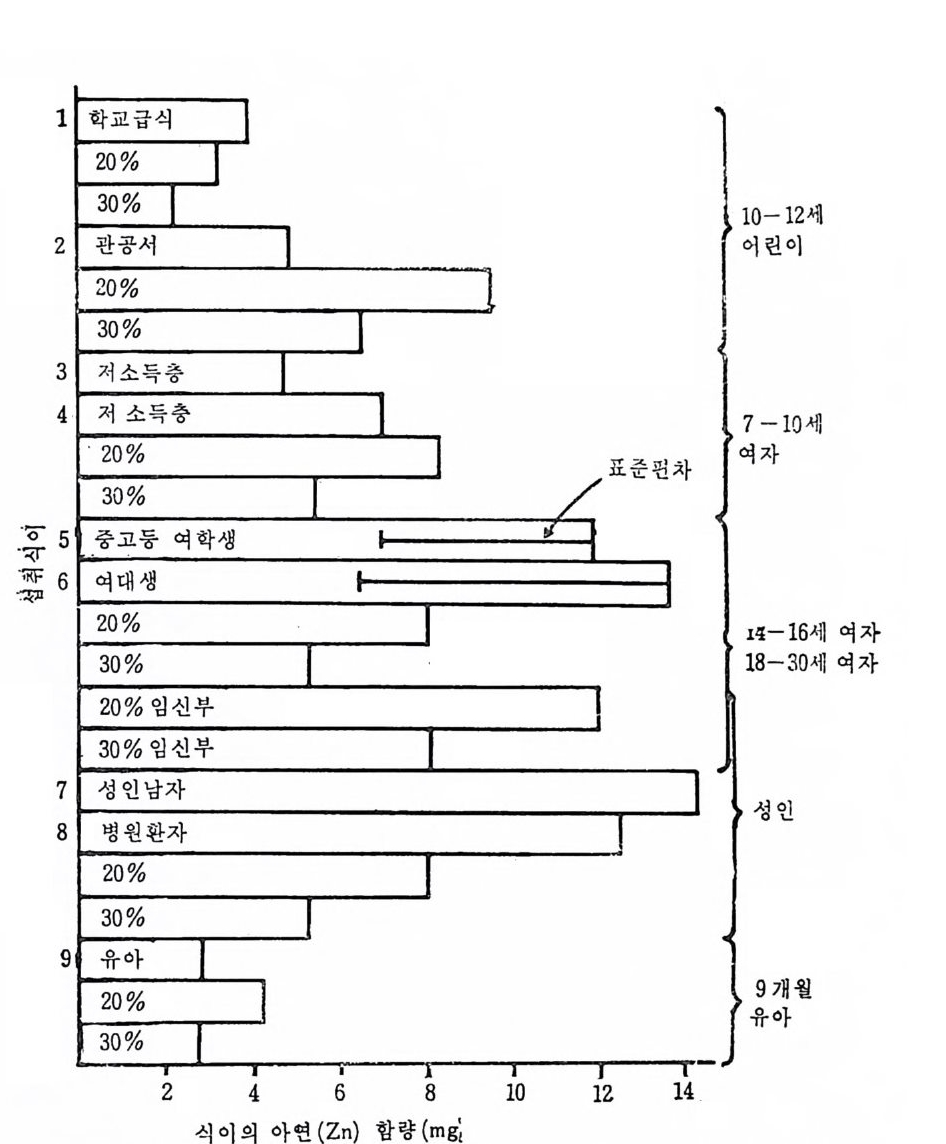 11 학교급식
11 학교급식
그립 4.4 식이의 아연 (Zn) 합량과 아연 (Zn) 의 체내이용물에 의해 서 영 향을 받는 아연 (Zn) 의 필요량 40) 20% ; 체내 아연 (Zn) 흡수율이 20% 일 때의 필요량 30% ; 체내 아연 (Zn) 홉수율이 30% 일 대의 필요량 1 ; Murph y 동의 연 구 66' 2 ; Murph y 등의 연 구 67) 3, 4 ; Pric e 등의 연 구 68' 5, 6 ; Whit e 등의 연 구 69) 7 ; Ti pton 등의 연 구 70> 8 ; Sp e ncer 등의 연 구 71) 9 ; Proudfi t 등의 연 구 7 2 ) 와 Schroeder 등의 연 구 73)
표 4.5 는 유아의 Zn 필요량을 추정한 것이다 .48)
 표 4. 5 유아의 아연 (Zn) 필 요량 4 8 )
표 4. 5 유아의 아연 (Zn) 필 요량 4 8 )
邸] 까지 의 유아의 Zn 권장량은 표 4. 6 에 서 보듯이 fat free dry subs t ance(FFD) 의 Zn 함량에 의 해 서 계 산해 낸 것 이 다.
 표 4. 6 나이 에 따론 신체 의 아연 (Zn) 함량 7 4)
표 4. 6 나이 에 따론 신체 의 아연 (Zn) 함량 7 4)
왜 냐하면 출생 시 108mg FFD/kg 은 성 인이 되 어 도 97mg FFD/kg 으로 거의 변화하지 않기 때문이다. 불가피한 손실은 Prasad 등 51) 과 Underwood1) 의 발표에 의 하여 추정 되 었 다. 1 세 까지 의 땅을 통한 배 설 량은 13 Q m g /1 일 , l~3 세 까지 는 180mg / 1 일로 보고 있다 .76) 뇨의 Zn 배설은 체세포 면적에 의해서 계산하 게되는데 1 제까지 체표면적은 0.36m2 이며 1~3 제는 0.55m2 이기 때 문에 1~3 세까지의 뇨 배설량은 0.08m g /1 일, 성인은 0.I3m g /1 일 이라고한다.
Ber g mann 은 40 ) 표 4.7 에서 여 러 저자들의 결 과 를 한데 모아서 Zn 의 필요량, 권장량 그리고 섭취량 을 추정하였다.
 표 4.7 성장과정에 있논 어린이 들 의 아연 (Zn) 필 요량, 권장량과
표 4.7 성장과정에 있논 어린이 들 의 아연 (Zn) 필 요량, 권장량과
4.5 결핍증과 대사장애에서 오는 질병 4.5.1 결핍중 생쥐의 Zn 결핍중 세로 제일 먼저 나타나는 현상이 성장감소와식 욕감되이다. 성장감소는 Zn 의 이용률 감소와 식욕감퇴에서 기인될 수 있다. 결핍증이 십해지면 3~4 일에 성장감소 현상이 일어난다고 한다. 장기간의 Zn 결핍시에는 탈모, 피부장애, 피부영 그리고 판, 다리, 입, 눈, 아래턱에 부종현상이 일어났다고한다. 숫쥐에게서 는 성기관에 at ro p h ie , 암쥐에게서는 임신능력 감되 현상이 일어났 다고한다. 임신한 쥐는 결핍 증상이 오면 Zn 홉수율이 매우 높아지며 임신 3 주 때의 결핍은 출산 후 새끼쥐에 있어서 지적능력 감소와 공격적 인 현상을 보였 다고 한다. 82) 사람의 Zn 결핍 은 1861 년 Prasad83) 에 의 해 처 음으로 이 란과 아 집트에서 보고되었다. 중세로는 빈혈, 간과 비장의 중량감소, 식욕
감되, 성장정지, 성부전중 둥이 나타났다. 최근 십한 Zn 결핍상대 는 선탄피부영, 장질병, 식욕감되, 피부장애, 성기능부전, 전염병 의 저항력 감되 둥을 대표적인 임상적 현상으로 설명하고 있다. 사 람의 Zn 결핍증은 당뇨병, 악성빈혈, 암, 동맥경화중 및 피임약 복 용 여성에게서도 나타났다 .24) 표 4.8 은 결핍 중상을 동물과 사람을 비교한 것이다.
 표 4.8 현재까지 알려진 아연 (Zn) 결핍증세 74)
표 4.8 현재까지 알려진 아연 (Zn) 결핍증세 74)
또한 alcohol 과음, 간경 변증, 화상, 영 중, 수술 후 정 맥 을 통한 영 양두입 (pa rente ral nutr i t ion ) 그리 고 임 신한 경 우에 도 Zn 결 핍 현 상이 나타났다 .84) 또한 쥐와 붉은 털 원숭이의 두뇌 발달에 중요 소 한 시기에 Zn 이 결핍되면 두뇌의 성숙과 영양상태에 영향을 미치 는 것 으로 나타났다. 85) 결핍증은 구강으로 Zn 복용시 1~2 주 이내에 치유되었다. Zn 견 핍증을 실험적으로 야기시켰을 때 사람은 미각과 시각을 상실했으 며 Zn 복용시 곧 회복되었다고 한다 .86) 정상인의 타액에서 Zn 을 · 함유한 단백질 〈g us ti n 〉을 추출했는데 분자량이 37,000 이며 이것이 미각에 영향을 준다고 한다 .76) Zn 결핍증을 판정하기 위해서 다음 과같은겁사를한다. 혈장, 혈청, 적혈구, 머리카락, 타액의 Zn 합
량과 혈 청 의 alkalin ph osp h ata se 의 활성 은 적 혈구의 65Zn 섭 취 량 으로 측정한다 .87) 표 4.9 는 농도가 다론 Zn 섭취시 성장하는 취의 혈청에 들어 있 는 alkalin ph osp h ata se 의 활성 을 나타내 고 있 다(정 맥 두입 량 0. 8mg / 취).
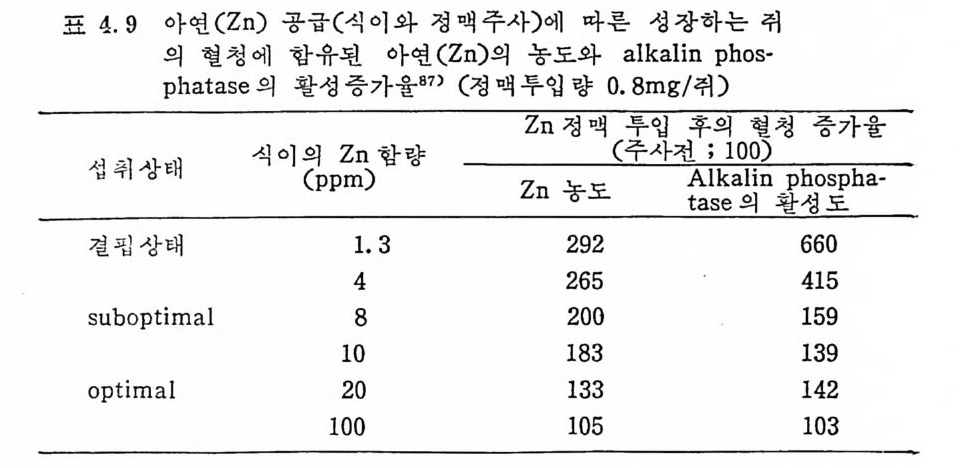 표 4.9 아연 (Zn) 공급(석 이 와 정 맥 주사)에 따른 성 장하는 취
표 4.9 아연 (Zn) 공급(석 이 와 정 맥 주사)에 따른 성 장하는 취
Zn 섭취상태가 정상일 때는 혈청의 Zn 농도와 alkali n ph osp h ate 활성에 변화가 없는데 비해서 결핍상태일 때에는 혈청의 Zn 농도오1- alkali n ph osp h ata s e 활성 이 둘 다 중가하였 으나 특히 alkali n ph os- p ha t ase 의 활성이 현처히 증가했다. 그러므로 결핍증을 측정하는데 alkalin ph osp h ata se 의 활성 을 가장 많이 사용한다. 88) 표 4. 10 은 alkali n ph osp h ata se 이 의 에 도 Zn meta l lo enzy m e 의 결핍증을 나타내고 있음울 보여준다 .90)9 1) 그 이의에도 적혈구의 carbonic anh y drase 와 췌장의 carboxy p- ep tida se A 와 B 둥을 측정할 수 있다. Zn 결핍시엔 DNA 와 RNA 의 합성이 감소되고 단백질의 합성이 감소된다 .92)93) 머리카 락의 Zn 량 감소는 Zn 결핍시 정확한 척도가 되나 61) 다시 충분한 Zn 섭취를 시켰을 때에도 머리카락의 Zn 량은 보충한 Zn 량만큼 중 가하지 않는다고 한다 .94) 또한 Zn 결핍중이 극십한 경우에는오히려 머리카락의 Zn 함량이 정상이었다는 보고도 있으며 ,95> subop tima l
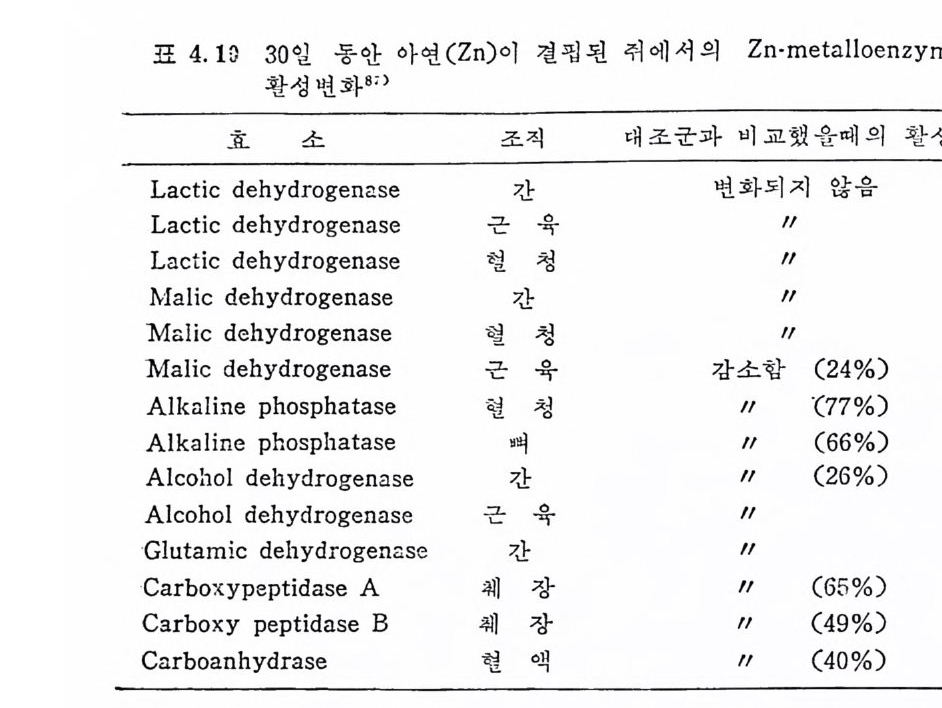 표 4. rn 30 일 동안 아연 (Zn) 이 결 핍 된 취 에 서 의 Zn-meta l loenzy m es 의
표 4. rn 30 일 동안 아연 (Zn) 이 결 핍 된 취 에 서 의 Zn-meta l loenzy m es 의
상태일 때 Zn 함량과 확실한 상관 관계가 있다는 것이 판명되었 다. 94) 표 4.11 은 Z n 의 영양상대를판정하기 위해서 사용되는변수들 이 다 . 77) 사람에게서 가벼운 Zn 결핍상태시의 체내대사의 변화를 관찰한 결과 96) 몇 주 동안 Zn 섭취를 재한시키면 혈장, 적혈구 세포, 소변 의 Zn 농도가 감소되 었 다 . alkalin e ph osp h t as e, lacta t e dehy d - To g enase 와 RNase 와 갇이 혈장에 있는 효소의 활성도는 식사의 Zn 섭취상태와 밀접한 관계를 가졌다 . 77) 2 명 의 실 험 자에 게 서 Zn 결 핍 이 sp o n g e con necti ve tissu e 의 총단 백 질 , 총 coll ag e n, RNA/DNA 와 de o x y t h y m i di n e kin a se 의 활성 도에 영향을 주었다. 새로운 사실은 Zn 제한 기간 동안 혈장에서 암모니아치가 상승했다는 접이다. 그러나 그기전은 아직 찰 알려지 지 않았다 . 이 기간동안 Zn 평형실험에서 체중감소가 었었는데 감소 성분은 50% 지방, 30% 수분 , 20% 는 기타의 것으로 설명된다 . 7 7)
 표 4.11 아연 (Zn) 섭취상태-문 조사하는 데 팔요한 변수)
표 4.11 아연 (Zn) 섭취상태-문 조사하는 데 팔요한 변수)
동물 실험에서 Zn 결핍과 i nsu li n 과의 관계를 살펴보면 ,9 7) 포도 덩·울 섭취시켰을 때 p ro i nsul in의 양은 변화되지 않았으나 glu cose t olerance 는 감소되었고 포도당을 자극하는 혈청 ins ulin 함유량도 낮아졌으나 전체 i nsu li ne 의 활성은 상승했다. 또한 혈청과 혈장의 유리지방산 농도도 상승했다. Zn 결핍 동물의 췌장 Zn 량은 60% 로 감소되었으나 glu cose to lerance 실험에서는 증가했고 간장에는 변화가 없었다. 그러므로 Zn 결핍이 i nsu li n 대사와 활성에 영향을 준다는 것은 확실하다고 보겠다. 4. 5. 2 Zn 결핍 증에 있 어 서 체 내 의 호르몬과 meta l loenzy m e 의 생화학적 변화 Zn 과 호르몬 사이 의 관계 는 ins ulin 분만 아니 라 glu cag o n, 성 장 호르몬과 성 호르몬과 같은 다론 호르몬에 대해서도 알려졌다. 남성의 성장과 성적 발달에 대한 Zn 보유상태의 중요성은 인간을 포함한 여 러 동물을 동해 증명 되 었 다. 1)54 ) 미 량원소는 분비 나 결합
조직 둥의 다양한 작용 위치에서 호르몬에 영향을 주며 반대로 분 비와 수송 동의 다양한 위치에서 호르몬이 미량원소의 대사에 영향 울미친다. 췌장 호르몬은 비교적 Zn 의 농도가 높다. 췌장은 Zn 대사에 매우 민감한 조직 중의 하나로, 급속한 축적과 보유를 나타낸다. 따라서, 이 조직은 식사의 Zn 결핍과 격심한 Zn 손실에 재빨리 반응하고, 99) 거 기 서 합성 된 소화효소, 특히 carboxy pe p tida se A 오1- B 의 활성 이 감소된다. 91 ) Sco tt 100) 가 결정 형 (crys ta l l ine ) ins ulin 이 상당한 양의 Zn 을 함유 ~ 하고 있다는 것을 발견한 이래로, Zn 과 i nsul i n 의 기능상, 형대학 상의 면밀한 관계가 수많은 연구에서 확인되었다. 당질, 지질과 단 백질 대사의 조철을 위한 i nsul in의 중요성은 오래전부터 알려쳐 왔 었다. 이와같어 내분비선 장애의 원인에 대하여 광범위하게 연구되어처 왔지만, 식이의 Zn 량과 식이의 요인들이 호르몬의 체내 대사에 주 는 영향과의 관련 여부에 대한 연구는 소수에 불과하다. 동물의 Zn. 상태의 변화는 체내대사의 합성, 축적, 분비, 그리고 i nsul i n 의 호 르몬으로서의 활성에 영향을 주는 것 같다. insu li n 에 대 하여 가장 찰 알려 진 기 능 중의 하나는 혈 당을 낮춘 · 다는 것이다. 1937 년에는 이미 Hove 둥 101) 이 Zn 이 결핍된 취의 내 당성 (Glucose t olerance) 에 대하여 그들의 첫 연구를 발표했다. 구 · 강으로 포도당을 복용시킨 후에, 그들은 Zn 이 결핍된 쥐와 ad li b it um 으로 섭취시킨 대조군 사이의 내당성 곡선에서 별로 차이가 없음을 알아냈다. Hendric k s 와 Mahone y 10” 는 구강으로 복용시 킨 포도당을 흡수시 키는 능력에 있어서 Zn 이 견핍된 쥐와 Zn 을 보충시킨 쥐 사이에 차이가 없다는 것을 발견했다. 그러 나, Qu arte r man 둥 103) 은 오랫 동안 석 이 치 료를 받은 후, 하 룻밥 동안 철석시킨 쥐의 복강내로 포도당을 주입시켰을 때, Zn . 이 결핍된 동물의 당내성은 pa ir -fed 대조군보다 낮았다. 이와 갇 은 결과는 발견은 Bo q u i s t와 Lernmark104) 의 연구와 Hendr ic ks 와
Mahone y 102) 와 Huber 와 Gersho ff 106) 에 의 해 재 확인되 었 다. 그림 4. 5 는 Rot h 둥 107) 에 의 해 Zn 이 결핍 된 쥐 와 pa ir - fe d 와 ad libit um -fe d 대 조군과 비 교해 서 얻은 당내 성 곡선이 다.
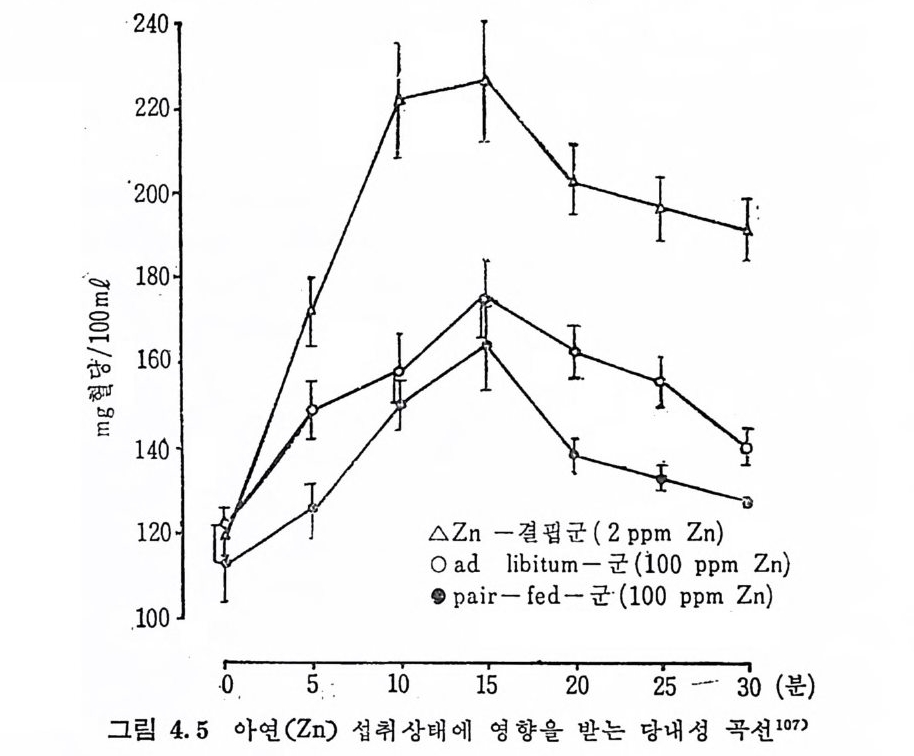 240
240
이들 연구에서 34 일 동안 쥐에게 Zn 이 적게 함유된 casein 반합성 석이 (2p pm Zn) 를 공급하여 Zn 결핍울 초래케 한 후 2 었]간 동안철 식시키고 체중 IOOg 당 80m g의 포도당을 근육내로 주입하였다. 초 기 의 혈 당농도가 pa ir - fe d 와 ad libi t um -fe d 대 조군이 같은 정 도였 던 쥐가 Zn 이 결핍된 후 당내성이 둘 다 감소했으나 p a i r- fe d 군이 ad lib i t um fed 군보다 당내 성 이 좀더 높았기 때 문에 Zn 이 결핍 된 쥐 의 당내성이 낮아진 것을 영양실조 때문이라고 단정짓기는 어려웠다. Zn 결핍시 복막내로 포도당을 주입했을 때 당내성에 영향을 미치는 것 을 논증할 수 없 었 던 Macap inl ac 둥 108) 의 연구와 meal-fe d 를 계 속 적 으로 pa ir - fe d 한 대 조군을 이 용했 던 Qn arte r men 과 Florence109) 에
의한 연구와는 다르다고 생각한다. Meal-fe d pa ir - mate s 는 오히 려 단시 간에 하루 허 용량을 먹 는 데 반하여 Zn 이 결핍된 동물들은 천천히 하루 종일 계속해서 먹기 때 문에 Zn 이 결핍된 쥐의 당내성의 감소는 석품 흡수에 있어서 다론 형 대 의 결 과라고 Qu arte rman 과 Florence10 2 ) 가 주장했 다. 그래 서 이 관계자들은 당내성 실험에 앞서 결정적인 요소가 되는 그날 소 비된 석품의 양을 고려하였다. 구강 섭취 후와 복강 내와 정맥 내 주입 후의 조사에서 구강으로 섭취된 포도당에 의한 i nsu li n 분비와 당내성에 대한 모순된 결과가 얻어졌다 .ll0)11D zn 이 결핍된 쥐와 pa ir - fe d 대조군에게 복강내로 포도당을 주입 시 킨 후, 10~15 분 이 내 에 pa ir - fe d 군의 혈청 Zn 농 도는 초기 농도보다 현저 하게 증가하였 다. 112) Zn 의 농도가 최고치일 때 혈당치가 최고치로 측 정되었다. 20 분 후에, 혈청의 Zn 량은 정상으로 돌아왔다. 결핍된 동물의 혈청의 Zn 농도는 pa ir - fe d 대 조군에 비 교할 때 약 1/2 만큼 감소되 었 고, 포도당 주입 때문에 별로 변화되지 않은 채 보유되었다. 반대로, 취에게 i nsu li n 을 복용시키면 소뇌, 다리, 체장과 그 밖의 다론 조직 들의 Zn 함량이 상승하였 다. 113) . 혈청의 Cr 함량도 Zn 에서처럼 pa ir - fe d 대조군의 경우에서는 당 내성을 시험하는 동안에, 10 분 후 최대에 탈하는 완만한 증가를 보 였다 .112) 그러나 결핍 동물의 경우에는 특히 당내성 시험 말경에 혈청의 Cr 함량이 증가했다. Zn 결핍쥐의 혈청의 Cr 함량이 일반적 으로 대조군보다 어느 정도 낮았다. Qu art er man 등 114) 은 Zn 이 걷펍 된 쥐 가 pa ir - fe d 대 조군과 비 교했 을 때 혈장의 ins uli n 의 농도가 낮아졌음을 증명 하였 다· 포도당에 대한 in sul in의 분비율은 Zn 결핍시 감소되었다. 또한 Zn 이 결핍된 동물은 비록 혈당농도의 차이는 없을지라도 용해 될 수 있는 Zn-fr ee ins ulin 이 복막내 로 주입 되 었 을 때 혼수와 경련에 민감하지 못했다고 한다. 마찬가지로, Huber 와 Gersho ff 106) 는 Zn 이 결핍된 쥐의 혈청은 백 libit um 대 조군보다 ins uli n 을 함유하는 면 역 물질이 적 음울 보고
하였다. 그러나 pa ir - fe d 대조군과 비교했을 때 차이는 없었다. in v it ro 에서 지방조직 분석에 의해 측정된 총 혈청 i nsu li n 은 활성이 p a i r- f ed 와 ad lib i t um 대조군에서보다 Zn 이 결핍된 군에서 현저히 낮았다. Huber 와 Gersho ff 10G) 는 in vit ro 에 서 자극물로서 포도당 을 배양시킨 Zn 이 결핍된 쥐의 췌장은 ins uli n 활성은 물론 면역반 응이 부족한 ins ulin 을 방출한다는 것 을 증명 하였 다. Qu arte rman 과 Florence10” 는 Zn 첨 가는 지 방조직 에 의 해 포도당 을 흡수시킬 때, i nsul i n 의 효능을 향상시키는 것을 설명하였다. 이상의 실험에서 Q uar t erman 과 Florence10” 는 Zn 이 결핍된 쥐 와 Zn 이 보급된, 죽 계 속적 으로 먹 었 거 나 meal-fe d pa ir - mate s 사 이에서는 혈장의 ins uli n 농도의 차이가 없음을 밝혔다. 마찬가지 로, Roth 와 K i rch g essner99) 에 의 해 행 해 전 4 개 의 실험 에 서 도 혈청 이 나 혈장의 ins uli n 농도는 Zn 이 결핍 된 취 와 pa ir -fed 쥐 사이 에 단 한 번의 차이 가 있 었 다. 비 록 그들이 ad lib i t um -fe d ; 대조군보다 계속 낮았지만 최근의 연구에서 ,115) 면역반웅이 있는혈 청 ins ulin 의 기 본 ins ulin 농도는 Zn 이 결핍 된 동물과 pa ir - fe d 대 조군 사이 에 차이 가 없 었 다. 복막내 로 포도당을 주입 한 후, pa ir -fed 대조군에서 내당성을 시험하는 동안, Zn 이 결핍된 동물에서는 변 화되지 않은 채 유지됨에 반하여 혈청의 ins uli n 농도는 매우 높야 졌다. 그러나 포도당울 주입한 후, 10~15 분, 죽 혈당치가 가장 ~ 아졌율 때, 총 ins uli n 활성은 대조동물에서보다 Zn 이 결핍된 쥐의 혈청 에 서 더 높았다. 116) 혈청 의 pro in s ulin 의 양은 포도당을 주입 하 기 전이나 후 모두 실험군 사이에서 차이가 없었다. 한편 성장하는 동물이 Zn 이 결핍되면 식욕감되를 초래하고, 식 품 섭취를 적게 하거나 전혀 먹지 않음으로써 낮아진, 혹은 전혀 식품을 섭취하지 않음으로써 i nsu li n 농도를 감소시키기 때문에 감 소된 혈청 ins uli n 양이 근본적으로 Zn 의 결핍에 의한 것인지, 낮 아전 석품 섭취 때문인지를 결정하기가 어려웠다. 그러나 성숙한 젖소의 실험에서 Zn 의 결핍 증상이 완연하였을 때에도 사료의 섭 취량은 · 감소되지 않았으나 i nsu li n 의 농도는 현처히 낮았다. 이때 충분한 Zn 보충식이로 결핍증을 회복하고 i nsu li n 농도도 다시 증가-
했다. 이 실험결과로서 Zn 의 결핍이 i nsul i n 농도 처하에 영향을 준다는 것 을 알 수 있 었 다. l) Zn 이 결핍 된 쥐 는 간장의 glu ta th io n e 이 중가되 었 는데 glu ta - th io n e 은 glu ta t h io n e-in s ulin tra nshy d rog enase 의 보조효소이 고 ins uli n 분자의 분해를 촉진시 키 는 효소이 거 때문에, Zn 의 결핍은 쥐에게서 p ro i nsul i n 이 i nsul i n 으로 되 는 대 사를 감소시 킨다. ll7) Boq u is t 와 Lernmark104) 는 당내 성 이 감 소되었음을 관찰했지만, Zn 이 결핍된 hams t ers( 쥐의 일종)에게 glu cose 를 정 맥 내 로 주입 시 키 기 전이 나 후의 ins uli n 농 도가 감소됨 을 알아내지 못했다. 당내성에서 유사한감소가췌장철제 수술 ll8) 후에 alloxan 의 복용 후 ll9) 발견 되 었 기 때 문에 Boq u is t 와 Lernmark104) 는 Zn 의 결핍 온 당뇨병 의 전기 (pre dia b eti c) 상태 를 유발시 킨다고 믿 었다. 또한 전자현미 경 에 서 의 연구는 췌장의 (3- cell 의 과립 이 감소되 고 또한 ins ulin 의 양이 감소되 었 다는 것 을 보여 주었 다. alloxan 이 주입되었거나 d it h i zone 이 주입된 당뇨병을 가진 토끼에게서, 섭조 칙 (isla nd ti ssue) 의 Zn 농도가 정 상적 인 대 조 동물보다도 현처 하게 낮 았다 .120) Eng e lhart 와 K i e f l2l) 는 쥐 에 있 어 서 ins ulin 분비 의 격 심 한 자극 온 췌장의 (3- cell 에 서 Zn 량을 감소시 킨다는 것 을 알아냈다. Zn 이 /3- cell 에 서 ins uli n 의 합성 과 처 장에 관여 한다는 것 을 추정 할 수 있 기 때문에, Zn 이 결핍된 동안 축적된 in su li n 의 양은 더 낮을 것으 로 사료된다. 평 형 두석 방법 (equ il ibr iu m d i al y s i s) 을 이 용하여 Coombs 둥 12” 은 po rcin e ins uli n 이 mol 당 mol 의 Zn2+ 과 결 합하고 용액 으 로부터 침 전시 키 는 반면에 po rci ne pr oin suli n 은 mol 당 5mol 의 Zn2+ 과 결합함으로써 용해되기 쉬운 종합체가 되게 한다는 것을 증 명했다. 그래서 in v i vo 에서 Zn 은 i nsul i n 의 빈약한 용해도에 중 요하고, 그것으로서 방출기전 기능을 담당할 수 있다는 것을 추정 할 수 있 다. Zn 은 ins ulin 이 ins uli n- Zn 복합체 로부터 방출되 기 전 에 분리되어야 한다. 이 접에 있어서 활성화된 (3 -cell 의 대사산물 죽 Zn 과 결합한 강한 물질인 구연산, 수산이나 유기인화합물도 한 몫을 담당할 수 었 다. L23)
Hendric k s 오l- Mahone y 102) 는 Zn 이 결핍 된 동물의 당내 성 의 감소 는 ins ulin 분해의 비율 중가에 의해 야기된다고 주장했다. 이것은 또한 Qu arte rman 동 114) 에 의 해 관측된 Zn 이 결 핍 된 쥐 의 ins uli n 처항력의 중가로 설명될 수 있는 것이다. Zn 결핍과 i nsu li n 사이의 관계를 분명하게 하기 위하여, i nsu li n 의 합성과 분해기능, 그리고 활성도에 대해 더 많은 연구가 행해져야 한다. Homan 동 105) 은 Zn 영 의 첨 가는 cortic o tr o p in 제 제 의 생 리 학상의 효력을 연장시키고, 증가시킨다는 것을 증명하였다. in v it ro 에서 인간의 세포 배양군의 연구에서 glu cocorti co id 활성을 가전 부신의 st e roid 호르몬은 Zn2+ 의 흡수력 울 중가시 켰 다. 109) Flyn n 둥 12 4 ) 에 의 한 cortic o ste r one 합성 의 촉진에 대 한 in vit ro 에서의 Zn 의 효과는 분리된 부신으로부터 연구되었다. ACTH( 부 신피 질 자극흐르몬)은 부화 매 체 (inc ubati on med i um) 에 서 Zn-chelat- ing ag e nt 에 대 하여 corti co ste r one 합성 을 자극하지 않는다고 밝혀 졌 다. 그러 나 만약 Zn 이 chelati ng ag e nt 에 과도하게 첨 가되 었 다 떤, ACTH 의 활성은 부활된다. 아 관찰 결과는 ACTH 는 기능적으로 Zn 에 의한다는 것을 나타 낸다. 만약 동물에 있어서 ACTH 합성을 세포 의의 Zn 에 의촌한다 떤 Zn 이 결핍 된 쥐 에 게 서 감소된 corti co ste r one 의 합성 은 분명 해 진다. 이집트에 있는 Zn 결핍 환자에게서, 뇌하수체 전영의 기능에 대 한 정확한 분석은, 이들이 부분적으로 최적 이하였다는 것을 나타 냈으며 54) 왜소 발육중을 포함한 성장감되와 성기능부전중은 가장 · 뚜렷한 득칭이었다. Zn 이 결핍된 난장이의 1/2 이상이 감소된 hy po p h y s eal ACTH reverse 를 나타냈고 ACTH 가 주입 된 신장부 에 서 17-hy d roxy s te roid 의 배 출물이 비 정 상적 으로 늦게 반응했 다. Zn 으로 장기 간 치 료한 후, 이 들 환자들은 신장의 ste r oid 의 배 설 이 정상이 되었다. 그러나 이것은 또한 Zn 식이가 일반적으로 환자 의 건강을 중전시킴으로 인한 Zn 의 간접적 효과가 될 수 있다. Henk i n12$ )등과 Lifsc hit z 와 Henk in 1 _2 6) 은 또한 adrenocort ico tr o p in 대사에 있어서 환자들의 Zn 대사 변화에 대하여 보고하였다. 성장
호르몬이 결핍된 낮은 혈장 성장호르몬을 갖는 환자들은 대조군보 다 높은 혈청 Zn 농도를 나타냈고, 부산의 Zn 배설량이 더 적었 다 .12 7) 의인성 성장 호르몬으로 치료한 후에는 혈청의 Zn 농도는 다시 떨어졌고, 반떤에 신장부의 Zn 배설은 높아졌다. 반대로 순환 하는 성장호르몬의 농도 중가는 치료되지 않은 선단비대증 (acrome g al y)에서처럼 혈청 Zn 의 감소와 신장부의 Zn 배설량의 상승을 유 발시킨다 .12” 이들 환자들은 수술로 뇌하수체를 철제하거나, X-ray 치료는 순환하는 성장호르몬농도의 감소와 혈청의 Zn 농도의 중 가와 신장의 Zn 배설을 감소시킨다. 부신절제나 뇌하수체률 절제시 킨 고양이 128) 와 쥐 129) 에 있 어 서 혈청 의 Zn 농도는 신장의 Zn 배 설 이 감소된 기간 동안에는 중가되었다. 이러한 결과들은 혈장에서의 성장호르몬 농도가 혈청의 Zn 의 양 에 반비례하고 신장의 Zn 배설에 정비례한다는 것을 말해 준다. 소 분자 배위자에 의해 결합된 Zn 은 신장 내의 배설에 영향을 받으며 이러한 변화들은, 혈액에서 거대분자와 소분자의 배위자와 Zn 의 결합에 의한 직접 혹은 간접적 영향의 결과일 것으로 보여진다 .130) , 18)1 3 1) 순환하는 Zn 이 온은 주요한 거 대 분자의 배 위 자인 albumi n 의 his t i din e 찬류물에 결 합한다. 주요한 소분자의 배 위 자인 his t i din e - 의 농도가 중가할 때 Zn 은 albumi n 에 서 단백 질 his t i din e 으로 이 동한다. 이 러 한 현상은 albumi n 의 크기 메 문에 정 상적 으로 통과 할 수 없음에도 불구하고 신장의 사구체막을 루과한다. 이러한 견 해는 h i s ti d in e 을 포함한 뇨 단백질과 혈청의 증가된 양과 더 높아 · 전 세포 교체율을 일으킨 순환하는 성장호르몬의 양이 상승된 실험 에 의해 입증된다. 따라서 부신피질은 순환하는 Zn 의 농도를 정 상적으로 유지시키고 신체의 Zn 저장소를 유통시키기 위해 요구된 . 다. 132) 그러 나 Zn 이 결핍 된 쥐 에 서 Reeves 둥 133) 은 혈청 의 corti co ste r -- one 농도가 식 사의 Zn 양이 나 동물의 Zn 상태 에 의 촌하지 않는다고 . 밝혔다. 이 결과에서 Zn 이 결핍된 동물들이 Zn 을 섭취한다 해도 변화가 없었으며 더우기 Zn 의 결핍은 ACTH- ind uced serum. cort ico ste r one 농도에 도 영 향을 미 치 지 않았다. 그러 므로 결핍 된 -
동물들에 게 단기 간의 Zn 보충은 혈청 의 corti co ste rone 농도에 영 향울 주지 못한다는 사실을 알 수 있었다. 동물에 Zn 이 적당량 공 급이 되든 그렇지 못하든 간에 ACTH 의 복용은 혈청의 Zn 농도에 아무런 영향을 주지 못한다. 또한 소의 성장호르몬으로 Zn 이 결핍 된 쥐를 치료하였을 때에도 체중을 증가시키지 못했다 .108) Ku134) 의 실험결과에서도 Zn 아 결핍된 쥐에게 주어진 성장호르몬 은 성장과 식품의 홉수를돕지 못했고, 그들의 혈청 Zn 농도나, 혈청 alkalin e ph osp h ata se 의 활성 , 착각화중 장애 (pa rakerato t i c les i on) 에 도 영향을 주지 못했다고 한다. Zn 이 결핍된 뇌하수체에 이상이 없는 쥐에게 Zn 의 보충은 성장율을 크게 중가 시켰음에 반하여, 소의 성장호르몬의 복용은 성장을 향상시키지 못했다. 그러나 뇌 수하체가 철제된 쥐의 성장율은 Zn 보유상태에 관계없이 호르몬과 Zn 보 충 에 따라 반응했다. 뇌하수체가 철제되었거나 성적으로미성숙한 쥐에게 Zn 영이 뇌하노 수체 전영 의 추출물에 부과되 어 졌 을 때 , 난포호르몬 (FSH) 과 항체 호르. 몬 (LH) 의 활성 이 중가된다는 것 이 B i scho ff 13s)136) 와 Maxwell137) 에 의 해 알려 졌 다. Gonadot ro p in 과 te sto ste rone 은 Zn 이 결핍 되 었을 때 부수적인 성기관의 성장윤 자극했다. 그러나 고환의 세뇨관 위 축은 예방하치 못했다. 이것은 전형적인 Zn 결핍 중상으로 생각된 다 .13 8.) 쥐에게 es t ro g en 을 복용시켰을 때, 혈청이나 소변의 Zn 농도에 얼마간의 감소가 있었으며, 혈청의 Zn 농도는 pr og e ste r one 복용 후에 도 감소되 었 다. 139) Brig gs 둥 140) 은 여 성 에 게 estr o g e n 요법 을 행 한 후 혈청 의 Zn 이 감소됨 을 밝혔 다. 다른 많은 관계 자들은 140)141)142)143)144)145) 경 구파 임약 사용에 있어서 혈장이나 혈청의 Zn 농도에 대하여 유사한 반응 을 보고하였다. A pg arl46) 는 pr og e ste r one 과 estr o g e n 을 복용시 킴 으로써 , Zn 야 결핍된 쥐의 약 50% 의 임신을 유지시킬 수 있었다. Porie s 둥 147) 에 의 한 연 구에 따르면 pr og e ste r one 은 조직 의 Zn 대 사에 영향을 미치는 요인으로 간주되어진다. 그들은 임신한 여성위
혈청 Zn 량이 증가하고 출산 후에는 감소한다는 것을 알아냈다‘ 이 것 은 pro g e ste r one 의 활성 에 의 하는 것 같다. 148) 또한 임 신기 간 동 안 estr o g e n 의 효과는 혈청 의 Zn 량에 영 향을 미 치 는 요인으로 간 주되어진다. 그러나 임신과 수유기간 동안 혈청과 기관의 Zn 량의 변화는 Zn 공급에 따라 달라진다. 149) 15 0) Gombe 등 151) 은 Zn 이 결핍된 암쥐의 뇌하수체의 황채호르몬 (LH) 의 양은 pa ir - fe d 와 ad libit um -fe d 대 조군과 같았다고 보고하였 다. 그러 나 LH 와 pro g e ste r one 의 농도를 ad libi t um -fe d 대 조군과 비 교할 때 Zn 이 결핍된 동물과 res t r i c t ed- fe d 군의 혈장에서 감소되 었 다. Zn 이 결핍 된 취 와 restr i c ted -fe d mate s 의 낮아전 혈장의 LH 농도는 LH- 방출인자가 부족해서 일어나는 것 같지 않다. 그러나 그 농도는 세 군 모두에서 대조적으로 나타났다. 석품 소비가 적고 실험적으로 Zn 이 결핍된 수유기의 젖소들과 영양상태가 좋은 동물 과 비교할 때 그들의 혈청의 황체형성호르몬 (LH) 과 난포자극호 르몬 (FSH) 은 변하지 않고 기본농도를 유지하였다 .98) 또한 혈청의 Zn 량에 따라 선정된 급혈자에게서 혈청의 t es t os t erone 은 단지 36 세에서 60 세 사이에서만 혈청의 Zn 양과 관계가 있고 FSH 와 LH 와는 관계가 없음을 알 수 있었다. 과거 의 연구와는 반대 로 소량의 Zn 결핍 은 뇌 하수체 의 go nadotr o p in 을감소시키지 않고고환의 내용물에 영향을미치는것이 확실해졌다. Lei 둥 152) 은 혈청 의 tes to s te r one 반응은 먹 이 에 제 한을 둔 대 조동 물과 비교할 때 감소된 반면 Zn 이 결핍된 쥐에게 LH 방출인자를 정맥내로 주입시킴으로써 혈청의 LH 와 FSH 의 반응이 중가되었다 는 것 을 알아냈다. 이 것 은 또한 male repr o ducti ve sy s te m 에 서 Zn 의 역할은 주로 고환의 위치와 관계가 있다는 것을 암시한다. 부분적으로 Zn 결핍으로 고통받는 겸상적혈구 빈혈환자에게서 혈 청 의 tes to s te r one 과 dehy d rote s to s te r one, androte s te r one 의 평 군 치 가 정 상인 보다 더 낮게 나타났다. 153> go nadotr o p in- releasin g hor- mone(Gn-R H)으로 자극한 후, Gn-RH 에 대 한 te sto s te r one 의 반응 은 완만한 데 반하여 15 4) 혈청의 LH 와 FSH 증가는 겸상적혈구 빈 철환자에게서 높게 나타났다. 혈청의 기본적 LH 와 FSH 값은 대조
· 군의 환자에 비해 더 높게 나타났다. 점상적혈구 빈혈환자에 있어 서 목칭 적 인 중상인 androg e n 결핍 은 hy po p h y s eal atr o p h y 보다 고 환의 영향인 것으로 보인다. 반대로 고환 내에서 andro g en 의 분해 는 Zn 이 결핍된 동안 증가된다고 추정할 수 있다. 고환의 기능처 하는 아직도 충분히 해명되지 못하고 있는 실정이다. 보통 영 색 체 의 열 성 형 질 병 (auto s ornal recessiv e d i sease) 인 장성 선 단 피 부영 (acrodermati tis en t ero pu t h i a) 은 필수지 방산의 비 정 상적 인 대 사에 의 해 155)156)157) 그리 고 Zn 의 흡수 장해 에 의 해 서 158)1 5 9)160) 생 간다. Evans 둥 161) 은 정 상적 인 Zn 흡수에 필수적 인 처 분자 Zn-bin d in g liga nd 를 모유에 서 발견 했 다. 이 배 위 자(lig and) 는 pr osta g l andin 임 이 Son g과 Adham162) 에 의해 확인되었다. 우유에서는 이 Zn-pr os- ta g la ndin 복합체는 검출되지 않았다. 장성선단 피부영을 가지고 있 는 환자의 혈청 에 서 발견된 arachid o nic ac id 양의 감소는 155 )1 56)15 7) pr osta g la ndin 합성에 이용됨을 나타냈다. 그 이유는 arachid o nic .-a c id 는 pr osta g la ndin 의 전조로서 소용되 기 때 문이 다. 163)1 6 4) 취 에 대 한 연 구에 서 나타났듯이 , Zn 흡수에 있 어 서 pr osta g la ndin E2 의 필수적 인 역 할은 Zn 의 chelati on 분만 아니 라, 장내 의 접 막울 가로 질러 Zn 수송에 있 어 서 더 중요하다. 162)1 6 5) 이 견과들은 장성 선단 피 부영 에 서 는 장내 Zn 흡수를 자극하는 pr osta g la ndin 을 합성 할 수 있는 능력이 없음으로 인해 생간다. Zn 의 결핍 에 서 나타난 것 과 유사한 중상아 임 신기 중에 asp irin 울 투여 한 쥐 에 게 나타났다. Asp iri n 은 여 러 조직 에 서 pr osta g la ndin 의 생합성울 방해한다. 그러므로 쥐의 Zn 홍수가 감소된다. 임신한 쥐에게서, Zn 결핍과 As pi r i n 에 의해 일어날 수 있는 결함 때문에 Zn 이 pr osta g l andin 의 기 능이 나 생 합성 에 관여 한다는 것 을 추측할 수 있다 .166) 그러나 Zn 과 p ros t a g land i n 이 저해되었을 때 병적으 로 유사한 증상을 초래하는 대사경로에 관계가 있는지 없는지를 보 여주기 위해 더 많은 연구가 필요하다. 호르몬대사에 있어서 Zn 의 역할, 득히 합성에 있어서의 기능과 여러 가지 호르몬의 분바에 관 찬 더 많은 연구가 요구된다. 특별히 요구되는 것은 호르몬들의 생
활참재력에 대한 Zn 의 관련여부에 관한 연구이다. 4. 5. 2. 1 meta l loenzy m es 에 서 의 Zn 의 기 능 Zn 은 수많은 meta l loenzy m es 의 필요 인자로서 , 또한 특수한 Zn-· dep e ndent enzy m e 활성 을 조철하는 보조인자로서 대 단히 중요하 다. 따라서 세포에 있어서 Zn 의 농도는 많은 대사과정, 특히 Zn-· dep e ndent enzy m e 의 활성 작용이 나 조철을 동하여 , 핵 산의 합성 이 나 분해, 당질, 지질, 단백질 대사를 좌우할 수 있다. Zn 결핍 식이시 목수한 효소의 활성감소는 Zn 양이온이 단백질에 얼마나 단단하게 결합되어 있는가, 혹은 lig ands( 배위자)의 교환율 · 이 얼마나 빠른가에 달려 있다. 이것들은 또한 이미 알고 있는 몇 개 의 Zn me t alloenz y mes( 표 4. 2) 이 Zn 공급에 민감하게 , 그리 고 급 속하게 반응하기 때문으로 보여 진다. 몇 몇 의 meta l loenzy m es 은 촉매 로 작용하고 구조적 안정 성 에 필 요한 금속결합 위치를 갖는다. 예를 들면, 대장군 (Esher i ch i a col i)에서 얻은 alkali ne ph osp h ata s e· 는 mol 당 4 g원자의 Zn 을 함유하는데 , 2g 원자 /mol 은 촉매 적 활 성에 필수적이다 .167) 반면에 부가적인 2 g원자 /mol 은 단백질 구조 를 안정 시 킨다. 168) 따라서 alkalin e ph osph ata s e 는 Zn 이 결 핍 될 때 활성을 급격히 감소시킨다. Roth 와 Kir c hg e ssner 는 90) 쥐 의 혈청 에 서 alkalin e ph osp h ata s e· 의 활성이 식이의 Zn 결핍 2 일 후에는 25% 까지, 4 일 후에는 50% 까지 감소됨을 밝혔다. 활성의 감소는 감소된 석품섭취에 기인하는 것은 아니며, 이 효소의 활성은 성장과 식품 섭취가 현저하게 감소. 되기 전에 이미 감소현상을 보인다• 또한 실험기간 동안 계속하여 제한된 석이로 사육된 군과 ad. libit um -fe d 대조군 사이에는 활성에 있어서 차이가 없었다. 혈청의 alkali n~ ph osph ata s e 의 활성 은 Zn 이 식 사에 첨 가되 거 나 주입 된 3 일 이내에 정상으로 회복되었다 169)90) (그립 4.6). in v it ro 에서 Zn 이 결핍된 쥐에게 Zn 을 첨가한 걷과 alkali ne · ph osph ata s e 의 활성 은 높였지 만 활성 도가 Zn 부가에 의 해 지속되 어지기 때문에 대조군의 혈청의 Zn 농도에는 미치지 못했다• Zn0[
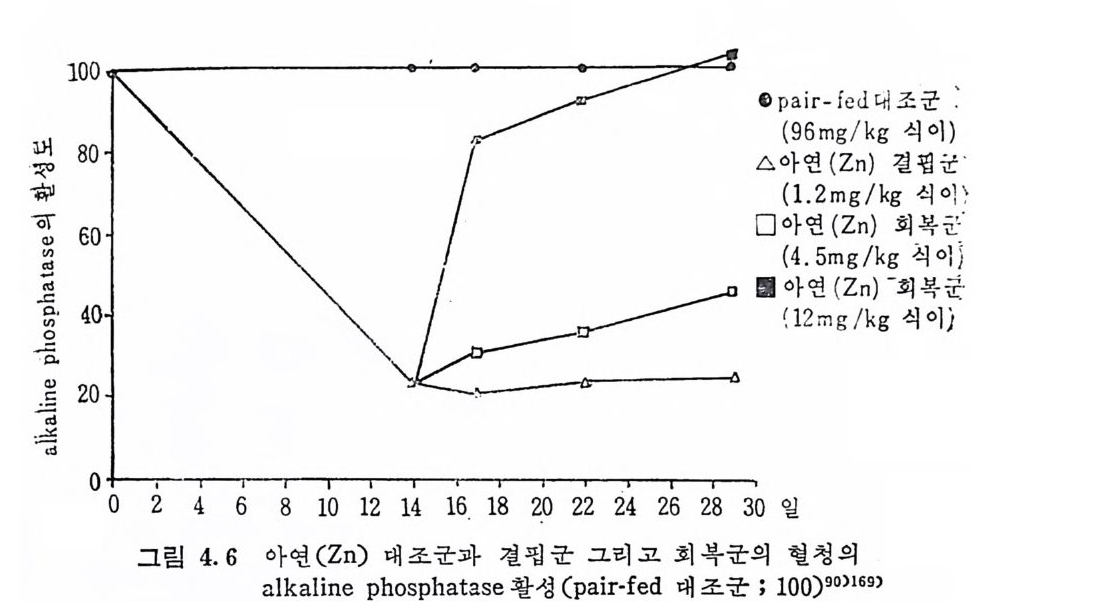 ;古z머로4o으”‘caU =>그 , 108640000 -I II스eD p(('o a} (15연92m연z記玩만o ( fzgg} zze g g(!m 4 do / ggk대kk}( 떠식 g희gm식결조1n 핍식식복복 군 °0 l0 /l l군이1 _` J 군 rT n.` .'/ .. ..`, . , l /ln lk
;古z머로4o으”‘caU =>그 , 108640000 -I II스eD p(('o a} (15연92m연z記玩만o ( fzgg} zze g g(!m 4 do / ggk대kk}( 떠식 g희gm식결조1n 핍식식복복 군 °0 l0 /l l군이1 _` J 군 rT n.` .'/ .. ..`, . , l /ln lk
부족한 상태 에 서 alkali ne ph osp h ata se 의 감소는 감소된 효소 활성 이나 높아전 감성에 의해 생긴 효소의 낮은 농도에 기인된다 .169) 따 타서 조철된 실험 상태하에서 alkali ne phosp ha t ase 의 활성온 Zn 공급 상태 의 좋은 지표가 된다. 그러 나 현 상태 하에 서 alkalin e ·-ph osp h ata se 의 활성 은 각각의 영 양상태 변화와 다른 많은 영 향을 받기 때문에 어느 정도가 적량인가에 관한 문제는 Zn 결핍의 치료 에 대한 연구에서는 밝히기가 어렵다. Henkie n 둥 131) 은 Zn 결핍 중상으로 미 각과 후각 장애 가 있 는 106 명 의 환자의 백 혈구에 서 alkali ne ph osp h ata se 의 활성 이 정 상치 이 하에 있다는 것을 밝혔다. 마찬가지로, 처음으로 인간 실험에서 가 벼운 Zn 결핍이 실험적으로 나타난 사람에게서, 혈청의 alkalin e pho sp h ata s e 의 활성 이 Zn 제 한 후에 천천히 감소되 었 음을 알게 되 었다. Zn 제한 식이에서 다시 Zn 을 첨가해 주었을 때 alkalin e p hos p ha t ase 의 활성은 8 주 이내에 2 배가 되었다. 이것은 또한 효 소 활성에 있어서의 생화학적 변화가 유일하게 Zn 결핍에 의한다는· 것울 증명한다. Zn 흡수 장애에서 기인하는 장성선단피부영이 있는 환자에게서 혈장과 피부에 있는 Zn 량 의에 신장의 Zn 배설량과 혈
청 의 alkali ne ph osp h ata s e 의 활성 이 또한 감소되 었 으며 17 0 ) 159) 아 것은 Zn 이 십하게 결핍되었음을 나타낸다. 하루에 두 번씩 22~ 44m g의 Zn 을 경 구 복용한 4 명 의 환자는 2 주 내 에 급속하고, 완전 한 병상의 차도를 보였고 혈장의 Zn량, 신장의 Zn 배설, 그리고 혈 청 의 alkalin e ph osp h ata s e 의 활성 등 생 화학적 지 수가 정 상치 로 회복되 었다 .159)
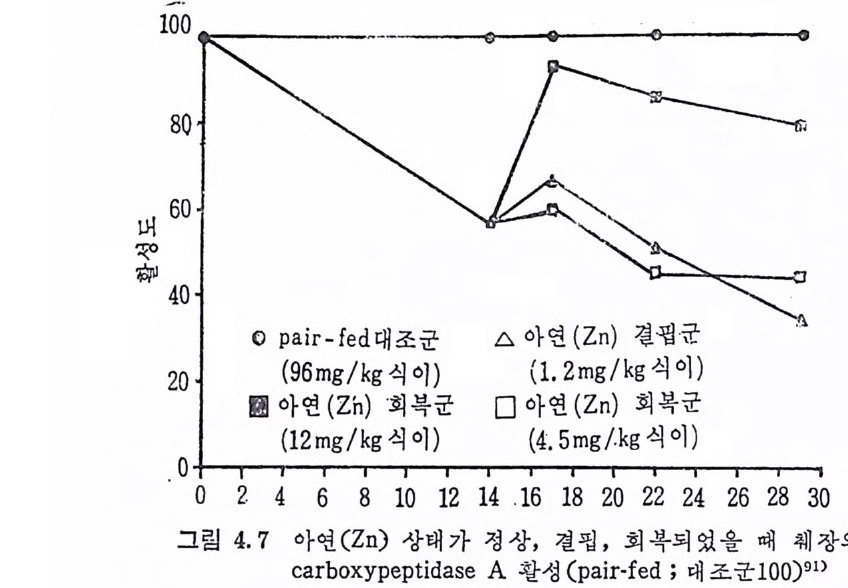 100
100
Zn 요법의 임상적인 효과는 피부장애, 설사, 식욕감되, 정서작 의기소침 둥에 아주 효과적이다. Zn 공급상태의 생화학적 매개 변 수(p arame t ers) 가 충분히 정 상으로 되 기 전에 Zn 요법 에 대 한 즉각 적인 임상적 반응은 Zn 보충에 따른 효과가 과잉된 Zn 의 약리학적 영향이 아니라 Zn 결핍의 경감에 의한다는 것을 나타낸다 .170) 비경구적 영양 공급으로 10 명의 환자가 장성선단피부영에서 나타 · 난 것과 비슷한 피부 장애를 나타냈고, 혈청의 Zn 농도가 낮게 나 타났으며 , 혈청 에 서 alkali ne ph osph ata s e 의 활성 이 감소되 었 다. 171) 장성선단피부영을 가진 사람의 증상과 유사한 증상을 가전 병인 edema dis e ase 를 가진 Frie s ia n 송아지 혈청 Zn 량이 정 상 이 하였
으며 , alkalin e pl:os p h ata s e 의 활 성 이 감소되 었 고, Zn 요법 후에 는 다시 중가되 었 다. 164)172)1 7 3) 원인이 찰 알려 지 지 않은 병 인 류마티 스성 관철영 에 서 도 Zn 결핍 상태 가 나타났다. 174) 헐 청 의 Zn 량이 alkali ne ph osph ata s e 의 활성 과 밀접 하계 관련되 어 경구적으로 황산아연 요법을 12 주 동안 계속했을 때 혈청의 alk alin e ph osp h ata se 의 활 성 이 매 우 증가되 었 다. 점 상 적혈구 빈혈을 가지고 있는 환자에 대한 최근의 연구는 Zrs 은 이 질병에서 중요한 역할을 하며 이 환자들이 얼마 7J Zn 결핍으 로 고통받는다는 사실이 밝혀져 Zn 요법의 효과가 재삼 증명되었다 .. 국동에서 식사에 Zn 을 보충한 결과 왜소중을 나타내는 Zn 결핍 인 사람들의 혈청에서 alkali ne p hos p ha t ase 의 활성이 중가되었다. 그래서 Zn 을 공급하기 전과 후에 혈청과 혈장에서의 alkali ne p hos p ha t ase 의 활성이 사람에게서 Zn 결핍 치료에 유용한 측정도 가 되었다 .169) 적 혈 구의 탄산탈수소효소 (carbon i c anh y drase) 는 또한 생 리 학상의 기능 때문에 Zn 을 필요로 한다. Keil in 과 Mann l 7 5 H 7 6) 에 의 해 탐지 된 첫 번째 Zn meta lloenzy m e· 은 mo1 당 l g원자의 Zn 을 함유한다. Carbonic anh y drase 의 활성은 쥐에게 Zn 이 결핍된 식이를 먹인 후 2 일과 4 일 내 에 각각 약 20%, 40% 까지 감소되 었다 17 4 ) 그러 나 ‘ 30 일의 실험 끝에, 결핍된 동물과 대조동물의 활성에 있어서 차이가 · 없었다. 이때 혈액 1/1,OOOm3 당 적혈구의 숫자는 40% 까지 증가되 었다. 신체는 혈액에서 적혈구의 농도를 높임으로써 이 필수적인 효소 의 활성을 유지하기 위해 노력한다고 볼 수 있다. 그 활성이 적혈 구 단위 당 표시 될 때 , 혈액 내 carbonic anhy d rase 의 활성 의 감소 논 Zn 의 결핍이 시작된 직후와 나중에 극십한 Zn 결핍의 단계에서 증명된다 .178) 또한 Zn 이 결 핍 된 쥐 의 장과 위의 carbonic anhy d rase 는 각각 33%, 47% 까지 감소되었다 .179) 점상 적혈구 빈혈환자의 적혈구에 있는 carbonic anhy drase 의 활성온 Zn 의 양과 밀접하게 관련되어
있다 .182) 단백 질 소화에 서 중요한 2 개 의 특별한 Zn meta l loenzy m e 은 췌 장의 carboxy pe p tida se A 와 B 이 다. 이 들은 각각 lg 원자 /mol 을 함유하며 , 분자량은 약 34, 000 이 다. Zn 결핍 에 대 한 연구에 서 carboxy pe p tida se A 는 쥐 91 )92 ) 18 0) 18 1) 와 돼지 180) 의 췌장에서 활성의 감소를 나타냈다. 이 효소의 활성 은 Zn 이 결핍된 2 일 후에 쥐의 췌장에서 약 25% 가 낮아졌다 .91) ·Ca rboxy pe p tida se A 의 활성온 Zn 을 보충시킨 후 3 일 이내에 거의 청 상값으로 회 복되 었다(그립 4. 7 참조). 또한 췌 장의 carboxy pe p tida se B 의 경 우, pa ir - fe d 와 ad lib i t um - .fe d 대조군과 바교했을 때, Zn 이 결핍된 쥐는 활성이 대략 50% 가 감소되었다 .9 1) Lacta t e , malate , alcohol, glu ta mate , dehy d rog e nase 는 Zn 의 g 분자량에 차이 가 있는 다론 Zn meta l loenzy m e 이 다. 사람과 동물 온 조직에 따라, Zn 결핍에 대해서 변화되지 않거나 약간만 감소된 활성 을 나타낸다. 183) 사람의 Zn 결핍 실험에서 96) 모든 실험 대상자의 혈장에 있는 lacta t e dehy d rog e nase 의 활성 은 Zn 제 한의 단계 와 Zn 을 다시 보 충해 주었을 때와관련되어 있다. Zn 이 제한된 동안 lacta t e dehy d -• :rog e nase 의 활성 은 감소되 었 다. Zn 을 보충하는 동안 활성 은 매 우 높게 나타났다. 1959 년에 Wacker 와 Valle65)184) 은 Zn 이 핵 산 대 사와 단백 질 합 성에서 역할을 담당하고 있는지의 여부를 조사하기 위해 많은 실험 져 연구가 행해졌다. Zn 은 DNA-dep e ndent, RNA po lym erase 의 필수 성 분으로서 알 려 졌 다. 대 장군 (Escher i ch i a co li)으로부터 DNA-dep e ndent RNA po lym erase 를 정 제 시 킨 제 법 을 이 용하여 Scruto n 등 185) 은 Zn 함량 올 효소의 mol 당 2g 원자로서 측정 했다. 균질의 DNA po lym erase 가 대 장균 (E. Col i)과 섭 게 (sea urch i ns) 로부터 Slate r 둥에 의 해 분 리되었고, 효소는 mol 당 2'4g 원자의 Zn 을 함유한다는 것을 밝 혀 내 었 다. 대 장군에 서 분리 된 DNA po lym erase 가 meta l loenzy m e
이 라는 것 은 Sy r in g ga te 둥 186)18 7 ) 에 의 해 확실하게 증명 되 었 다. RNA-dep e ndent DNA po lym erase 죽 reverse tra nscrip tas e 는 또한 Zn meta l loenzy m e 이 고 188)189) 수많은 병 원체 속에 서 발생 된 다. 전사효소(t ranscr ipti on enz y me) 는 핵 산 대 사에 서 주요한 위 치 에 있으며, 따라서 단백질 생합성에도 중요하다. Lie b erman 과 Ove190) 는 in vit ro 에 서 쥐 의 신장세 포를 이 용한 실 험에서 Zn 이온이 DNA 합성에 필수적이라는 것을 밝혔다. 배양기 에 서 Zn 의 제 거 는 DNA 합성 과 DNA po lym erase 와 th y m i di n e kin a se 의 활성 에 장해 를 초래 한다. Terhune 과 Sands t ead191) 는 Zn 이 결 핍 된 모체 에 서 태 어 난 젖 먹 이 쥐 의 간세 포의 핵 (nucle i)에 서 DNA-dep e ndent RNA po lym erase 의 활성에 대한 Zn 결핍의 영향을 연구했다. Zn 은 포유 동물에 있 어 서 세 포핵 의 DNA-dep e ndent RNA po lym erase 의 활성 에 필수 적이라는 것이 증명되었기 때문에, 이 효소의 활성은 생후 10 일부 터 계속 감소되었다. Zn 이 결핍된 신생쥐의 두뇌에 대한 유사한 연구에서, 크기가 더 작아전 두뇌와 DNA 합성 감소 이의에도 또한 RNA po lym erase 가 감소되 었 다. 192) 또한 DNA p ol ymerase 의 활성은 임신 9 일에서 12 일째의 대조군 의 태아보다 Zn 이 결핍된 신생쥐가 더 낮게 나타났다. 이 관찰을 토대로 하여, Zn 이 결핍되면 생물체들의 핵산 합성이 감소된다는 것을 추정할 수 있다. Zn 이 결핍된 동안에, 일어나는 단백질 합성 결함 원인에 대한 정확한 기전은 아직 확실히 규명되어 있지 않으 며 이는 또한 핵산 합성을 감소시키는 것으로도 나타났다. Fernandez-Madrid 둥 193) 과 Somers 와 Underwood19) 는 RNA 분 해가 낮아져서 Zn2+ 이 r i bonuclease 를 방해할 수 있다는 견해를표 명했다. 또한 이 효소의 높아진 활성은 Zn 이 부족한 실험 동물의 조직에서 관찰되었다 .194) RNA 분해율은 조직의 Zn 농도에 의하므로 세포에서 Zn 량은 rib o nuclease 의 활성 을 조절한다. 그래 서 Zn 이 결핍 된 취 의 고환 온 한충 적은 양의 Zn, RNA, DNA 와 단백질을 함유했으나 반면, .:ribo nuclease 의 활성 은 증가되 었 다. 19) 주목할 만한 결합은 rib o -
nuclease 의 활성의 증가인데, 이것은 단백질의 분해작용을 증가사 킨다. 유사한 실험 으로서 194) rib o nuclease 와 deoxy r ib o nuclease 의 활성 이 Zn 이 결핍된 쥐의 흉선, 골격, 신장, 고환에서 연구되었다. Deoxy r ib o nuclease 의 활성 이 Zn 이 결핍 된 쥐 와 pa ir - fe d 대 조군 사 이에서는 차이가 없었으나 r i bonuclease 의 활성은 Zn 이 결핍된 조 . 직에서 상승되었다. 연구자들은 상승된 r i bonuclease 의 활성은 인 간을 포함한 모돈 종 (s p e ci es) 에 게 서 관찰된 성 장 처 하와 낮아진 단 백질 합성은 물론 Zn 이 결핍된 쥐를 이용한 예전의 연구에서 관측 된 180) RNA/DNA 비율의 처하의 원인이 된다고 믿고 있다. 겸상 적혈구 빈혈이 있는 환자의 혈장에서 Zn 의 농도가 감소되 고 rib o nuclease 의 활성 이 상승됨 은 이 실험 대 상자들이 Zn 이 결 핍된 상태라는 중거를 제공함으로써 증명되었다 .1s2) Zn 치료 후 혈 장의 Zn 의 함량은 증가되었고, 혈장의 r i bonuclease 의 활성은 감 소되었다. 또한 장성선단피부영을 가지고 있는어란이에게서, Ham- bid g e 등 95) 은 vit am i n A 의 감소 외 에 혈청 에 서 rib o nuclease 의 활성 이 높아졌 으며 , Zn 치 료가 시 작된 후, rib o nuclease 의 활성 과 혈청에서의 vit am i n A 의 양이 정상으로 회복되었음을 알아냈다. 가벼운 Zn 결핍이 나타난 지원자를 대상으로 실험한 결과 혈장의 rib o nuclease 의 활성 은 Zn 이 제 한된 동안이 Zn 이 충분한 동안의 2 배 가까이 되었음이 밝혀졌다 .96) 이 결과들은 Zn 이 결핍된 쥐 를 이용한 실험에서 언어전 결과와 유사하다 .195) 그래서 혈장의 rib o nuclease 처 럼 Zn-dep e ndent enzy m e 의 활성 도는 인 간의 Zn 상 태의 평가와 치료를 위해 특별히 유용한 매개변수가 될 수 있다. 이 결과는 Zn 이 결핍 된 쥐 의 고환과 선장, 간장에 서 rib o nuclease- 의 활성 과 총 rib o nuclease 농도와 free rib o nuclease 억 제 인자의 농도가 pa ir - fe d 대조군과 비교할 때 변하지 않았다고 밝힌 Cheste r s. 와 W i ll196) 의 결과에 상반되 었 다. 그들은 조직 의 rib o nuclease 의 활 성에 대한 식사의 Zn 결핍의 영향이 효소계에 주는 Zn 의 직접적인 영향이기보다는 오히려 번화된 성장률에 대한 일반적인 반응이라· 고 할 수 있다.
최근의 연구에서, Zn 은 DNA 합성에 필수적인 효소인 th y m i di n e k i nase 의 활성에 필요하며 또한 세포분열에도 필요하다고 밝혀졌 다. 그러므로 th y m i di n e k i nase 는 초기 Zn 결핍 증상의 원인이 되 는 효소가 될 수 있다. Lieb erman 둥 65 ) 은 Zn 이 결 핍 된 포유동물의 세 포는 in vit ro 에 서 사육 후에 대 조 세 포군보다 th y m i di n e kin a se 의 활성 이 더 낮았다 고 했다. Zn 이 결핍된 쥐에서 빨리 재생성되는 결합조직에 있는 thy m i di n e kin a se 의 활 성 은 Zn 이 결 핍 된 영 양공급 6 일 후에 pa ir - fed 나 ad libi t um 대 조군보다 훨싼 감소되 었 다. 195) Zn 의 결핍 , 13 일, 17 일 후에도 비슷한 결과가 얻어졌고, th y m i di n e k i nase 는 더 이 상 발견되 지 않게 되 었 다. 결합조직 의 DNA 에 “C-th y m i di n e 의 결합은 Zn 이 결핍된 석이 6 일 후에 또한 감소되었다. Duncan 과 Dreos ti1 9” 는 수술 후에 Zn 이 결핍 된 식 이 가 주어 진, 간의 병소를 철제한 쥐는 DNA 와 단백질 합성의 감소가 일어나기 전에, 대조동물과 비교했을 때 th y m i di n e k i nase 의 활성이 감소되 었다는 것을 알아냈다. 수술 후 Zn 결핍에서 단백질의 합성이 48 사 간 후에 , DNA 합성 이 18 시 간 후 에 감소되 었 음에 반하여 , th y ro id i n e - kin a se 의 활성 은 단지 10 시 간 후에 감소되 었 다. 마찬가지 로, pa ir - fed 대조군과 비교했을 때 Zn 이 결핍된 쥐의 12 일된 태아에게서 th y m i di n e kin a se 의 활 성 이 현저 히 감소되 었 다. 198) Thy ro id i n e ki- nase 의 활성의 감소는 임신한 쥐에게서 단지 임신 9 일 ~12 일째에 Zn 결핍 식이가 주어졌을 때 명백해졌다. 이 러 한 결과는 th y m i di n e kin a se 의 활성 에 필수적 인 생 화학적 과 정아나 Zn 결핍에 극도로 민감하다는 것을 나타낸다• 대사 과정에 서 이 효소의 활성은 DNA 중합 반응과 세포 분열 전에 작용한다. 효소 활성의 지연된 반응이나 활성의 감소는 가장 빠르고, 민감한 대사 변화의 하나로서, Zn 이 결핍된 실험 대상자들의 성장율의 급 속한 감소, 식욕 감되, 지연된 상처 회복 등의 원인이 됨을 증명히 였 다. 199)200) 여기에서 나타난 연구 결과는 Zn meta l loenzy m es 중에서도 특정 한 것만이 활성이 변화되며, 일부 조직에서 일어나는 것으로 밝혀,
쳤다. 그러므로 Zn 부족에 민감하게 반응하는 조직, 예를 들면 혈 청, 골격, 췌장, 장접막에서 생화학적 반응을 측정할 가능성이 가 장 높다 .l80) Zn 과 관계되는 효소들이 Zn 이 결핍된 동물의 조직에 서 같은 정도로 영향을 미찬다고는 생각할 수 없다. 효소의 예민한 정 도는 여 러 가지 Zn meta l loenzy m es 의 Zn-lig a nd 찬화력 과 이 환된 조직 세포에서의 교체율의 차이 때문이다 .180) 그래서 매우 높은 찬 화력으로 Zn 과 결합하는 Zn me t alloenz y mes 은 Zn 결핍이 극십한 상태에서도 여전히 활성을 나타낸다. Swenerto n , 20D Swenerto n 과 Hurley, 202> Swenerto n 둥 203) 은 Zn 이 결 핍 된 쥐 의 간장에 서 lacta t e , glu ta m ate 그리 고 alcohol dehy - drog e nase 의 활성 이 감소됨 을 알아내 지 못했 다. 그리 고 조직 의 손 상을 보인 고환에 서 malate 와 lacta t e dehy d rog e nase 의 활성 이 감 소되지도 않았다. 그래서 그들은 효소 활성의 감소는 Zn 이 결핍된 동물에게서 발견된 극십한 생리학적, 형태학적 변화의 원인이 된다 는 가설에 동의하지 않았다. 국십한 Zn 결핍 증상이 표면으로 나타 났을 때에도 효소 활성작용의 전반적인 감소가 적은 것은 이 효소 에 대한 Zn 의 찬화력이 높고 조직에서의 교체율이 변화되지 않은 상대로 유지된다는 결과를 토대로 설명되어질 수 있다. 아직까지 Zn 이 생화학적 반응에서 산화되었거나, 환원되었다는 증거 가 없 다. 205) Co 는 활성 meta l loenzy m e 을 형 성 할 때 , Zn 울 대 신할 수 있다. 그리고 몇몇의 경우에서 이 Co 유도체는 천연의 Zn 효소보다 더 활성적이다 .204) 그러므로 몇몇 효소의 활성이 Zn 결핍으로 변경되지 않은 또 다른 이유가 될 수 있다. 따라서 만약 활성이 유일한 기준이라면 특별한 효소에 대한 Zn 결핍의 영향을 증명하기 어렵다. 그러나 Zn 이 다른 양이온으로 대치될 가능성은 Zn 결핍에서 대단히 감소된 활성을 보인 효소에서 제의된다. Zn 걷 핍시, Zn 의에 다른 필수 미량원소의 조직 농도는 현저히 영향을 받는다. 149)206)207) Burch 둥 206) 은 Zn 결핍 시 조직 의 미 량원소가 변 화되 는 양은 meta l loenzy m e 이 나, Zn 과는 관계 없 는 meta l acti va te d enz y me 의 활성의 변화를 초래한다. Zn 의 결핍증상은 또한 Zn 걷 핍에 의해 야기된 다른 미량원소의 함량에 영향을 준다.
많은 효소들이 그들의 생리학적 기능을 위한 Zn 을 필요로 하가 때문에 극십한 Zn 결핍 증상의 표시는 수많은 Zn 함유 효소의 감 소된 활성과 관계가 있다. 조직들은 서로 다론 천화력으로 Zn 과 결합하기 때문에, 석사의 Zn 의 결핍은 특히 어떤 조직에서의 불안 정한 Zn 의 결핍을 초래하고, 특별한 Zn me t alloenz y me 의 활성에 서 대응하는 손실을 유도한다. 충분한 Zn 보충은 이 결핍울 빨리 극복하고, Zn meta l loenzy m e 의 활성 을 정 상적 으로 유도한다. me- tal loenzy m e 이 그 활성 을 잃는 정 도는 또한 효소의 구조를 유지 할 때 Zn 의 기 능적 역 할에 의 한다, 몇 개 의 Zn-dep e ndent enzy m e, 예 롤 들면 alkalin e p hos p ha t ase 로 Zn 의 결핍은 분해를 위한 변화를 중가시키는 구조적 변화를 야기시키는 것 같다. 결과적으로 효소의 교체 율이 높아졌 고, 조직 에 서 효소의 활성 이 높아졌 다. 20s> Mi lls, 209> Prasad 와 Oberleas210> Prasad180) 는 생화학적 변화가 Zn 전핍에 대 응하여 일어나며, 다시 보충된 후에 사라지는속도는 Zn 의 대사기 능의 주요 위치를 확인하는 데 도움이 된다고 제시했다. 이 연구에 서 석사의 Zn 결핍, 효소 활성의 초기 변화를 응용하는 것은 Zn 의 주요한 역할이 극도로 높은 교체율을 가지고 있는 조직성분과 관계 되어 있다는 것과 Zn 이 자유롭게 교체될 수 있는 위치에서 필수적 이라는 것을 제시한다. Prasad129>21D 둥에 따르면 , 많은 대 사과정 이 그들의 합성 과 활성 의 조철에 유용한 Zn 의 조직 농도의 Zn meta l loenzy m e 에 의 해 조 절된다고 한다. 또한 Zn meta l loenzy m e 은 특별히 단백 질 합성 의 여러 단계와 세포 분해 전 초기 핵산 합성을 조절하기 때문에 본질 적으로 많은 세포 내의 생화학적 기전에 관련된다 .212} 이미 알려진 . Zn 의 결핍 중상과 효소 변화 사이의 관계는 더 밀접하게 고려되어 쳐 야 한다. 단백 질 소화에 영 향울 주는 두 효소는 췌장의 carboxy -- pe p tida se A 와 B 이다. 이 두 효소의 활성은 Zn 이 결핍될 때 췌 장의 carboxy pe p tida se A 는 2 일 이 내 에 그 활성 의 약 1/4 이 감소 되 었 다. 213) 그러 나 식 사의 건조물과 조단백 질 (crude p ro t e i n) 의 소화 능력은 pa ir - fe d 대조군과 비교했을 때 Zn 이 결핍된 어린 쥐에게서 약간 감소되 었 다 214) (각각 1. 5 와 3%). 다른 한편으로는, 일반적 으로-
Zn 결핍 때 사육능력과 성장률의 감소가 관측되었다. 그래서 Ki r` chg es sner213> 둥과 Weig a nd21 5> 둥은 대 조군에 서 보다 Zn 이 결핍 된 쥐에게서 3:7 횟수의 비율로체중증가를위한식품소비가더 많 았다고 밝혔다. Zn 결핍에 대한 현저한 효과는 장관과 체조직에서 세포의 생물학적 과정만큼 많이 연구되지 못했다. Carboxy pe p tida se A 와 B 의 에 alkali ne ph osp h ata s e 는 Zn 결핍 에 의 해 야기 된 많은 장애와 관련되어 있다. 이 Zn 을 함유한 me t alloenz y me 은 정상적 인 골격 형 성 의 수많은 생 화학적 과정 에 중요하다. 216)217)218) 혈청 속에 서 alkalin e ph osp h ata s e 가 여 러 조직 에 서 생 겼 기 때 문에 , Zn 결핍에 대한 혈청효소의 감소는 조직 효소의 감소의 결과이다. 골 격 은 혈청 의 alkali ne ph osp h ata se 의 주요 급원이 기 때 문에 , 219)218) 혈청 의 alkalin e ph osp h ata s e 가 감소하여 Zn 이 결핍 된 쥐 에 게 서 대 되 골의 alkali ne ph osp h ata s e 가 pa ir - fe d 대 조군과 비 교했 을 때 . 2/3 까지 감소되 었 다. 220> Westm oreland 둥 221)222) 은 Zn 이 결 핍 된 병아리의 다리가 비정상적으로 골격의 석회가 일어나며 성장을 위 해 alkalin e ph osp h ata s e 가 감소되 었 음을 보고했 다. 털순환과정 (hair c y cle) 과 동시 에 모포 (ha i r folli cles) 의 감소 때 문에 , Zn 견 핍 은 털 결 손 (ha i r de fec t)과 쥐 의 피 부의 alkali ne ph osp h ata s e 의 감소를 유발시킨다 .219) 또한 미뢰(t as t e buds) 의 막에서 높은 농도로 발견되 는 alkalin e ph osph ata s e 의 활성 의 감소는 Zn 이 결핍 되 었 을 때 맛 감각이 무더지는 원인이 될 수 있다. 223) 이 연구들은 alkali ne ph os- -p ha t ase 의 변화가 Zn 이 결핍되었을 때 나타나는 많은 결함의 원 인이 될 수 있다는 것을 증명한다. 그래서 Zn 이 결핍된 쥐에게 ·al kalin e ph osph ata se 를 주입 시 킴 으로써 성 장을· 촉진시 킬 수 있 다 .115) 그러나 성장의 결손은 단지 부분적으로만 회복되어질 수 있 다. 인간이나 동물의 Zn 결핍증상은 찰 알려져 있지만, 그것의 원인이 되는 대사적, 생화학적 결함은 찰 알려져 있지 않은 실정 이다. Zn 이 결핍되었을 때 가강 찰 규명된 생화학적 변화는 Zn meta l loenzy m e 의 활성 의 변화이 다. 224> Alkali ne ph osph ata s e 는 신 체에 널리 기여하는 Zn me t alloenz y me 이다. 그것은 많은 생화학 척인 과정에 참여하고, 동물과 인간의 조직에서 Zn 결핍에 대하여
활성의 감소 를 보인다 . 2 24) Zn 에 대한 이 효소의 관계는 Zn 의 걷 핍시 몇몇의 국십한 결핍을 설 명할 때 중요하고 Zn 의 생물학적 기 능을 이해하는 데 중요하다. 그래서 성장률과 식품 섭취가 감소되 기 전에 췌 장에 서 carboxy pe p tida se A 와 B 의 활성 이 감소되 었 고 9 1) 십 이 지 장에 서 alkali ne ph osp h ata s e 의 활성 이 감소되 었 다. 225) 식품 홍 수량은 이 효소의 활성 에 영향을 주지 않는다. 그들의 활 성의 감소는 이 활성을 유지하기 위한 충분한 Zn 의 부족에 의해 유발되는 것이 아니고, 오히려 효소 자신들의 양이 감소된 효소 합 성이나 분해의 중 가 때문에 감소되었다. 따라서 대조동물과 비교했 울 때 Zn 이 결 핍 된 동물의 alkali ne ph osp h ata s e 의 합성 에 Zn 의 첨 가가 활성 효과를 가져 오지 못했 다고 한다. 225)22 6 )227 ) 그러 나 Zn 이 결핍 된 쥐 의 위 와 장관의 기 능에 대 한 alkali ne ph osp h ata s e 와 carboxy pe p tida se 의 감소된 활성 의 관계 는 불분명 하다. 이 효소들 의 활성은 Zn 이 결핍된 영양공급의 시작부터, 죽 Zn 결핍 초기단계 동안, 식품 홍수의 변화가 없고 성장률이 정상이며 그리고 소화홉 수가 여전히 정상일 때에도 현저하게 곧 감소되어 있었다 .92)225> Zn 이 결 핍 된 공급석 이 5 일 후에 carboxy pe p tida se 와 장내 의 alkalin e p hos p ha t ase 의 활성은 식품 소비의 직접적인 감소에 의해 그들 본 래 값의 반으로 떨어졌다 .92)225) 이것은 사실상의 결함이 석품의 대 사나 흡수에서 일어난다는 것을 나타낸다. Zn 의 결핍 후기 상태에 서는 평군 매일 섭취량은 에너지 평형을 유지하는 데 충분했다. 그 래서 이것은 전형적인 Zn 이 결핍된 석이에서 식품 흡수가 열량 요 구량을 초과했을 때, 소화 흡수는 영향을 받지 않으나, 과대한 에 너지 축적이 Zn 결핍 때문에 감소되는 것 같다 .225> Zn 이 결핍된 동 안 th y m i ne kin a se 와 po lym erase 의 활성 의 감소는 RNA 와 DNA 합성과 이로 인한 제포분열, 단백질 합성, 정상적인 성장을 위한 조전 둥이 방해를 받는다. 따라서 부수적으로 식품 홍수도 방해되 기 때문에 쥐에서 Zn 이 결핍된 후 곧 발생하는 홍수의 억제 현상 은 성 장 지 연을 가져 온다. Weig a nd 와 K i rch g essner228) 는 Zn 결핍 식이를 준 쥐의 성장률은 석품 흡수가 영향을 받기 전에 감소되었 다고 밝혔다. Zn 이 결핍되었을 때 변화된 식품 전환율은 식이의
단백질이 체중 증가 과정에 낮아진 단백질 이용울만큼 음식의 열량 으로서 이 용되 지 못한다. Zn 의 생화학적, 생물학적인 면을 더 찰 이해하기 위하여는 전반 · 적으로 인간과 동물에서 Zn 결핍증상의 원인이 되는 기본적인 과정 울 설명하기 위한 더 많은 연구가 요구된다. 4.5.3 암과 Zn 과의 관계 Ma t hur229) 는 취에게 구강암을 실험적으로 발생시킨 후 석이 중의 Zn 과의 관계를 보았는데, Zn 함량이 적은 식이에서는 암의 발생을 · 촉진하는 반면 Zn 함유가 적당한 식이에서는 암의 발생을 저지해 주나 과량의 Zn 함유석이는 종양 성장을 촉진시켜 주기도 한다고 보고하였다. 4.5.4 Zn 대사 이상에서 오는 질병 선단피부장영은 소장에서 Zn 홍수를 부분적으로 저해하는 유전적 결핍의 특이한 현상이다 이 환자는 Zn 을 다량 배설하고 국십한 Zn. 결핍현상을 나타낸다. 또한 이 질병은 일차적으로 Cu 대사, 그리고 이 차적 으로 fatty ac id 대 사 장애 를 초래 한다. 230) Zn 보충물과 dio d oq u in 의 구강두여 는 Zn 배 설을 역 전시 킬 수 있 다. Diod oq u in 은 Zn 에 대 한 지 질막의 투과성 을 높여 주어 흡수를 · 촉진시 켜 준다고 하였 다. 231 ) 송아지 에 oxy c hin o li ne s 을 구강투여 하 · 여도 소장에서 Zn 흡수를 중가시켜 주고 혈청 Zn 를 정상으로 되찾 게 했다. in vit ro 실험 에 서 a-macrog lo blin 에 대 한 oxy c hin o li ne zin c _· comp le x 의 천화력 이 증명 되 었 다. 수송기 작에 서 oxy c hin o li ne 은 소 장의 barr i er 를 통해 수송을 증가시킬지도 모르지만 혈청의 Zn 은 Zn oxy c hin o lin e comp le x 가 아닌 형 태 로 전달되 어 진다고 한다. 232) 이러한 임상 실험을 통해서 또 다른 Zn 의 생리적 주요기능이 입증 되었다. 예를 들어 각질 형성, 상피의 통합성, 신체적 성장, 뇌기 눙, 생식력, 눈의 통찰력 백혈구 기능과 지질 대사에서의 중요 기 능둥을둘수 있다.
4.6 함유식품 Zn 의 함유량이 가장 많은 식 품은 굴로 1, OOOp pm 의 Zn 이 함유 되 어 있고, 그 다음이 해 산물과 살코기 , 호도 등으로 30~50p pm 정도 함유되어 있다. Zn 함량이 적은 식품으로는 근채류, 동물성 지방, 설탕과 설탕으 .
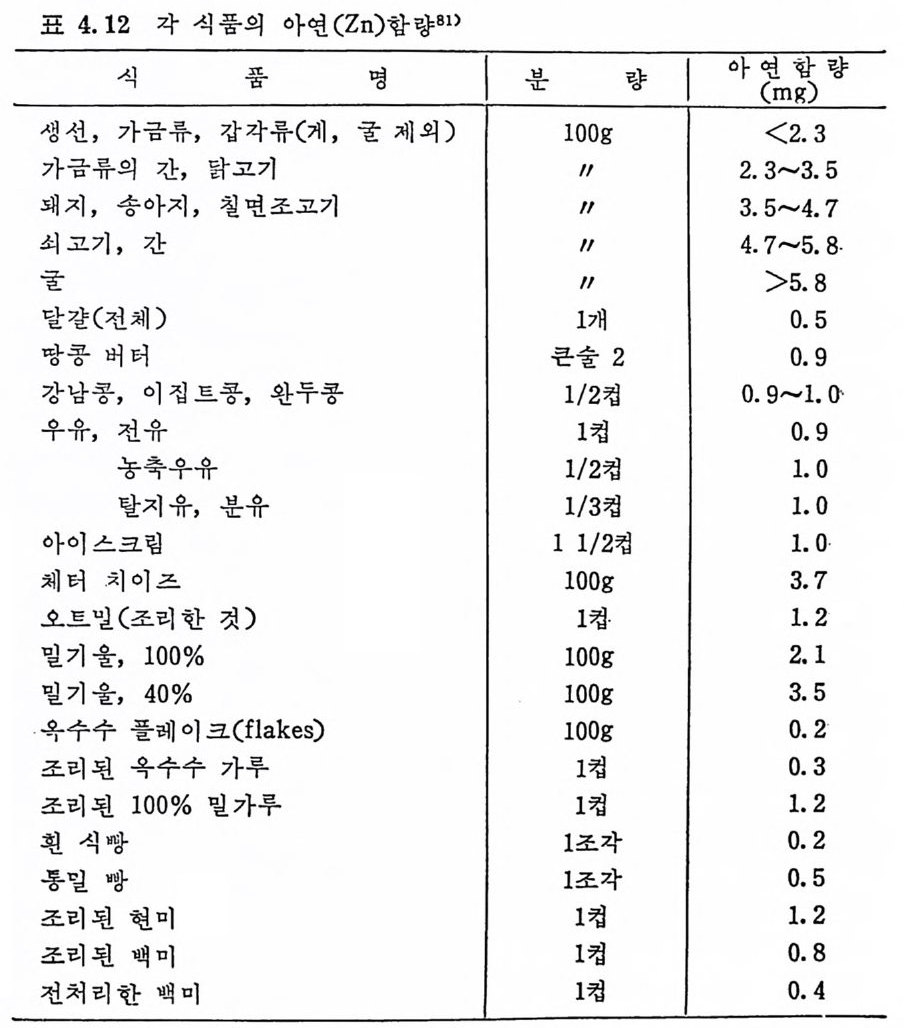 표 4.12 각 식 품의 아연 (Zn) 함량 8 1)
표 4.12 각 식 품의 아연 (Zn) 함량 8 1)
로 만든 제품과 흰 밀가루로 lpp m 이하의 Zn 이 함유되어 있다. 표 4.12 는 각종 석품의 Zn 함유량을 나타낸 것이다. 4.7 독 성 다른 tra ce elements 에 비 해 서 Zn 은 독성 이 적 다. 과량의 Zn 섭 취는 구토를초래하며 이 작용을이용하여 병원에서는 2 g의 ZnS04 를 구토제로 사용하기도 한다. 또한 Zn 용기에 신 음료수나 음식을 담 아서 섭취했을 때(예를 들어 감자 salad 를 Zn 그릇에 담은 단체 급 식 둥) 급성, 독성 현상으로 구토, 설사등을 듈 수 있다. 독성의 증 상을 보면 사람의 경우 발열, 허약, 구토, 복통, 두통, 타액감소, 어 지럼증, 탈수 전해질 불균형 등을 나타낸다. ZnS04 의 치사량은 45g 이 었다 .41) 겸상 적혈구 빈혈환자에게 1 년 동안 매일 660m g의 ZnS0 4 를 구 강으로 섭취시켰으나 부작용이 전혀 없었으며, 상처 치료에 2mg / kg 체중을 구강으로 섭취시켰으나 부작용이 없었다. 과량의 Zn 은 간의 Fe 와 요량을 감소시키는데 이는 Zn 의 독성에 의해서 Fe 와 Cu 의 체내 이용률을 저해하고 또한 많은 배설을 하게 한다 .234) 간 으] xanth io n xid a se 의 활성 도도 감소되 었 으며 체 내 의 Mo 함량은 변 하지 않았다 .235) 쥐의 사료에 0.5~1% 의 Zn 이 함유되었을 때는 성장정지, 빈혈, 간의 cata l ase chromoxid a se 의 생 성 과 활성 도가 감소되 었 다. 또한 쥐 실험에서 과량의 Zn 은 Ca 과 P 의 대사를 방해하고 그로 인해 서 골격의 Ca 과 P 의 감소를 가져오는데 원인은 Ca 과 P 이온 의 흡수가 저해되었기 때문이다. 돼지에 나타나는 Zn 의 독성은 식욕감되, 뒷발 부분의 마비, 7J:- 경변증과 골격의 변화 등이다. 쥐에 Zn 을 구강으로 장기간 섭취시켰을 때 Na 의 농도는 1.8 ~ 125mg Zn2+/kg 체 중이 었 으며 250mg Zn2+/kg 체 중에 서 성 장정 지 , 빈혈, 비임신중, 췌장섬유중 동의 현상이 나타났다 .236)237) 음료수에 30 pp m 의 Zn2+ 함량 (0.8m g /k g 체중)은 국민 건강을 해
치 지 않았다• 그러 나 음료수나 청 량음료에 7~8µg /g 의 Zn 이 함유 되었을 메는 쓴 맛이 난다. *참고문현 1) Underwood, E. J. , Trace Elements in Human and Anim al Nutr i- .ti o n, Academmi c Press Inc. New York and London, 1977. 2) Raoult, F. , Breto n , H. and C. R. Acad. Sci. , 85, 40, 1877. 3) Todd, W. R. , Elvehje m , C. A. and Hart, E. G. , Am. ]. Phys i o l . , 107, 146, 1934. 4) Keil in, D. and Mann, T. , Bz'oc hem. ]. , 34, 1163, 1940. 5) Ti pton , I. H. and Cook, M. J. , . Healt h Phys . , 9, 103, 1963. 6) Hami lt o n , E. I. , Mi ns ki, M. J. and Cleary, J. J. Sci. , Tota l En· -:viron . 1, 341, 1972/1973. 7) Macap inl ac, M. P. , Pearson; W. N. , Barney, G. H. and Darby , W. J. , J. Nut. , 93, 511, 1967/95, 569, 1968. 8) Gil be rt, I. G. F. and Tay lo r, D. M. , Bi oc hem. Bi op h y s. Acta . , 21, 54 6, 1956. 9) Mawson, C. A. and Fis c her, M. I. , Bi oc hem. ]. 55, 696, 1953, ,Ca n. ]. Med. Sci. , 30, 336, 1952. 10) Berfe n sta m , R. , Acta Ped£a tr. , 41, Sup ple mentu m 87, 1952. 11) Henry, M. W. und M. E. Elmes. Brit. Med. ]. , 1975, 625. 12) Weit ze l, G. , F. J. Str e cker U. Roeste r , A. M. Fretz d orf and E. .:Bu ddecke, Hopp e -seyl e rsz. Phy si o l . Chem. , 295, 83, 1953. 13) Vallee, B. L. , Bi oc hemi st r y , Phys i o l . Rev. , 39, 443, 1959. 14) Bertr a nd, G. , Bhatt ac herje e , R. C. and C. R. Acad. Sci. , 198, 1823, 1934. 15) Paris i , A. F. and B. L. Vallee, Am. ]. Cli n. Nutr . , 22, 1222, ·19 69. 16) Evans, G. W. and T. W. Wi nt e r , Bi oc hem. Bi op h y s, Res. Com- .mu n. , 66, 1218, 1975.
17) Nordberg, G. F. , M. Nordberg, M. Pis c ato r and 0. Veste r her,. Bi o che m . ]. , 126, 491, 1972. 18) Henkin , R. I. , Adv. Exp . Med. Bi o l. , 14, 299, 1974. 19) Somers, M. and E. J. Underwood, Aust. ]. Bi o l. Sci. , 22, 12 77, 1969. 20) Prasad, A. S. , Fed. Proc. , 26, 172, 1967. 21) Eckhert, C. D. and L. C. Hurley , ]. Nut. , 107, 855, 1977. 22) Davie s N. T, The CUnic al Sig n if ican ce of th e Essent ial Bl ol og ica l' Meta l s. , 1972. 23) Landes, D. R. , Proc. Exp. Blot. Med. , 150, 686, 1975. 24) Prasad, A. S. , Am. ]. Dls. Chi ld . , 130, 359, 1976. 25) Vojn i k , C. and L. S. , ]. Nutr . , 107, 862, 1977. 26) Ric h ards, M. P. and R. J. Cousin s , ]. Nutr . , 106, 1591, 1976. 27) Cheria n , M. G. , J. Nutr . , 107, 965, 1977. 28) Carney , S. M. , B. A. Underwood and J. D. Loerch, ]. Nutr . , 106,. 1773, 1976. 29) Bahio r B, Ki pn es R. and Curnutt e J. , ]. CUn. Inve st . , 52, 741,. 1971. 30) Porie s , W. J. , Henzel, J. H. , Rob, C. G. and St ra in , W. H. ,. Lancet 1, 121, 1967/Ann Surg. 165, 432, 1967. 31) Schwarz, F. J. and Ki rc hg eB ner, M. , Nutr . Meta h . , 18, 157~ 1975. 32) Huta g a lung , R. I. , Schwarz, F. J. and Ki rc hg e f n er, M. , Arch. Ti e renalzr. , 27, 347, 1977. 33) Evans, G. W. and Joh nson, P. E. , in Ki rc hg e /3 n er, M. , Trace- Element Meta h ollsm in Man and Anlmals-3, p9 8, A TW, Frezsin g - Weih enste p h an, 1978. 34) -Sc hwarz, F. J. and Ki rc hg e Bner, M. , Z. Tlerph y sz o l . , Tz'erern- 햐 r. Futt er mltte l kde. , 39, 68, 1977. 35) Schwarz, F. J. and Ki rc hg e Bner, M. , Int. Z. V£ tam £nf o rsch. 44, 116, 1974. 36) Weig a nd, E. and Ki rc hg e Bner, M. , Blol. Trace Element Res. , 19' 79, in pr in t i ng .
37) O'Dell, B. L. and Burpo , C. E. , J. Nutr . , 102, 653, 1972. 38) Lantz s ch, H, J. , H. Schenkel and I. Ni ck er! , in Ki rc hg e ssner, 11. Trace Element Meta b olis m in Man and Ani m als-3, Technis c he Un i vers it죠t Mi inc hen Freis i n g ·W eih e nste p h an, p. 460, 1978. 39) Sandstr o m, D. and Arvid s son, B. , Bj or n-Rasmussen, E. , Ced· derblad, A. , in Ki rc hg el 3ner, M. , Trace Element Meta b oli sm in Man and Ani m als-3, p.1 29, ATW, Freis i n g · Weih enste p h a n, 1978. 40) Gladtk e , E. , G. Heim ann and I. Eckert, Sp ur enelemente , Georg Thie m e Verlag St u tt ga rt, p. 105, 1979. 41) Ki rc hg e l3ner, M. E. Weig a nd, A. Schneg g, E. GraB m ann, F. J. Schwarz and H. -P. Roth . in Cremer, H. ·D. and D. Hotz e !, J. Ki ihn au Bi oc hemi e und Phy st 'o lo g ie der Ernti hr ung , Band I, Ti el 2, Georg Thie m e Verlag p. 275, 1980. 42) Graig , F. A. and E. Sie g e l, Proc. Soc. Exp. Bi ol . Med. , 104, 391, 1960. 43) Sta n d, F. , B. Rosoff , G. L. Wi lliam s and H. Sp en cer, J. Plzar· macol. Exp . Therap, 138, 399, 1962. 44) Hellweg e, H. H. , Mschr. Ki n derheil k . , 119, 37, 1971. 45) Ste r n, A. , M. Nalder and I. G. Macy , J. Nutr i t . , 21, 8, 1941. 46) Ni sh im ura, H. , J. Nutr i t . 49, 79, 1953. 47) Clevag , L. M. , Am. J. Clin , Nutr . , 22, 284, 1970. 48) Bergm ann, K. E. , W. Ste g n er, A. Klarl, G. Makosch, K. H. ·Te ws and R. L. Bergm ann, in Gladtk e , E. , Heim ann und I. Eckert, Sp u renelemente , Georg Thie m e Verlag St u tt ga rt, p. 95, 1979. 49) Hambid g e, K. M. , C. Hambid g e, M. Jac obs and J. D. Baum, Pedia t. Res. , 6, 868, 1972. 50) Str a in , W. H. , A. Lascari and W. J. , Porie s , Proc. VII. Int. ·Co 깐g r. Nutr . , 5, 759, 1966. 51 ) Prasad, A. S. , Schulert, A. R. , Sandste a d, H. H. , Mi al e, A. and ·Fa rid , Z. , J. Lab. Clin . Med. , 62, 84, 1963. 52) Greg e r, J. L. , Bennet, 0. A. , Buckley, S. and Bali ga r, P. , in M. Ki rc hege B ner, Trace Element Meta b oli sm in Man and Anim als-3, -;p. 300, ATW, Freis i n g ·W eih e nste r han 1 1978.
53) Hess, F. M. , Ki ng , _C. and Marge n, S. , J. Nt ttr. , 107, 1610,. 1977. 54) Sandstr e ad, H. H. , Prasad, A. S. , Schulert, A. S. , Farid , Z. , 一 Mi al e, A. , Bassil y , S. and Darby , T. W. , Am. J. C!t n . Nutr . , 20,_ 422, 1967. 55) Schroeder, H. A. , Nason, A. P. , Ti pton , I. H. and Balassa, J. J. ,. J. Chroni c Di s. , 20, 179, 1967. 56) Yamag a ta , N. and Iwashim a, K. , Bull. Inst. Poult . Se t. , 37, .. 1100, 1958. 57) Soman, S. D. , Panday, V. K. , Jos ep h , K. T. and Raut, S. J. , Healt h Phys . , 17, 35, 1969. 58) Robin s on, M. F. , Mckenzie , J. M. , Thomson, C. D. and Van- Ri j, A. L. , Br. J. Nutr . , 30, 195, 1973. 59) Trib b le, H. M. and Scouldr, F. I. , J. Nutr . , 52, 209, 1954. 60) Schlag e , C. and Wortb erg, B. , Acta Paedia tr . Scand. , 61, 425,. 1972. 61) Schwarz, W. A. and M. Kir c hg e Bner, Dt sc h. Tt e rarztl . Wschr. , 82, 137, 1975. 62) Codex Al ime nta r iu s Commi ss io n FAO/WHO Joi n t Of fice , Rom. ,. A.L INORM 76/26 A Ap pe ndt'x II. 63) Pahlke, G. , L. Kl ing e bie l , H. P. Lenk, in E. Gladtk e, G. He- im ann and I. Eckert , Sp u renelemente , Georg Thie m e Verlag, St u t- tga rt, p. 113, 1979. 64) Darby , W. J. (Chair m an) et al. , World Heath Orga nt'z a tt o n Te- chnt ca l Rep or t Serles 532, 9, Geneva, 1973. 65) Lie b ermann, Z. , Abrams, R. , Hunt, N. and Ove, P. , J. Br ol .. Chem. , 238, 3955~62. 66) Murph y , E. W. , L. Page and B. K. Watt , J. Am. Dt e te t . Assoc. ~- 58, 115, 1971. 67) Murth y , G. K. , V. Rhea and J. J. Peeler, Envfr on . Se t. Tech. ,, 55, 436, 1971. 68) Price , N. O. , G. E. Bunce and R. W. Eng le , Am. J. Cl in. Nutr . ,. 23, 258, 1970.
69) Whit e, H. S. , ]. Am. Di et . Ass. , 55, 38, 1969. 70) Ti pton , I. H. and P. L. Ste wart, in Hemp h il l, D. D. Trace Subs tan ces in Envir on menta l Healt h- III, Univ e rsit y of Mi ss ouri Press, Mi ss ouri, p. 305, 1969. 71) Sp e ncer, H. , D. Osis , L. Kramer and C. Norris , in Trace. Elements in Human Healt h and Di se ase I, Zi n c and Cop pe r, A. S. Prasad, edit or , Academi c Press, New York 345, 1976. 72) Proudfi t, F. T. and C. H. Robin s on, Normal and Therap eu ti c· Nutr i t ion, 12th Edit ion . Macmi llan , New York, 254, 1964. 73) Schroeder, H. A. , Am. ]. C/in . Nutr . , 24, 562, 1971. 74) Bergm ann, K. E. , and Renate L. Bergm an, in Betk e , K. & F. Bin d li ng M aie r , Sp ur ene/emente in der Entw i ck /ung von Mensch te nd' Ti e r, Urban & Schwarzenberg, p. 217, 1975. 75) Henkin , R. I. , E. Lippo ldt, J. Bil sta d and H. Edelhoch, Proc. Nat. Acad. Sci. , USA, 72, 488, 1975. 76) Bergm ann, K. E. and S. J. Fomon, in S. J. Fomon, Inf an t Nutr i - - tto n, 2nd, W. B. Saunders, Phil ad elph ia , p. 245, 320, 1975. 77) Bergm ann, K. E. and R. L. Bergm ann, In. Betk e K. und F. Bid ! - in g maie r (Hrg. ), Sp m ·e n elemente in der Entw i ck /ung von Mense 따 Ti e r. p, 217, Urban & Schwarzenberg, Mi inc hen, Berlin , Wi en , 19 75. 78) Sto lley , H. , W. Droese and I. Rewerts , In, K. Betk e und F. Bid l in g m aie r (Hrsg. ), Sp ur enelemente in der Entw i ck /ung von Mensch: und Ti er . p. 113 Urban & Schwarzenberg, Mi inc hen, Berlin , Wie n , 1975. 79) Vorobeva, A. I. and N. A. Bolsanin a , Nutr i t ion Abstr a cts and Revi ew s 35, 460, 1965. 80) Schlag e , C. and B. Wortb e rg, Mediz i n und Ernahrung 12,- 217, 1971. 81) Murph y , E. W. , B. W. W illis and B. K. Watt , J. Am. Di e te t _ Asso. , 66, 345, 1975. 82) Sandste a d, H. H. , Fosmi re , G. J. , Halas, E, S. and Jac ob, R. A. Terato l og y 16, 229, 1977.
83) Prasad, A. S. , J. A. Halste d , and M. Nandim i , Am. ]. Med. , 31, 532, 1961 . 84) Sandste a d, H. H. , Vo·Khactu , K. P. and Solomons, N. , in Prasad, A. S. , Trace Elements zn Human Healt h and Dz s ease, vol. I. , p. 33, Academi c Press, New York, 1976. 85) Sandste a d, G. Fosmi re , E. Halas, D. Str o bel and J. Duerre in M. Ki rc hg e ssner, Trace Element Meta o ol£ s m zn Man and Ant m als-3, Technis c he Un i vers it죠t M ilnc hen Freis i n g - Weih enste p h an, p. 203, 1978. 86) Henkin , R. J. , in Ki rc hg e Bner, M. , Trace Element Meta o olt s m in Man and Anz m als-3, p. 190, ATW, Freis i n g Weih e nste p h an, 19 78. 87) Ki rc hg e Ener, M. , Schwarz, F. J. , Graemann, E. , Roth , H. P. and Schneg g, A. , in Gladtk e, E. , Heim ann, G. , Eckert, I. , Sp ur en- .el emente , p. 68, Georg Thie m e, St u tt ga rt, 1979. 88) Roth , H. P. and Ki rc hg e fo e r, M. , Res. Exp. Med. , Berlin 17 4, 283, 1979. 89) Nati on al Research Counc il Food and Nutr i t ion Board, Recommed Di e ta ry Allowances, Nat£ on al Academy of Sz e nces, Washin g ton , D. C. 'J). 178, 1980. 90) Roth , H. -P. and M. Ki rc hg e Bner, Z. Tz e rph y s zo l. Tz e renahrg. :u. Ft ttter ml ttelk de. , 32, 289, 1974. 91) Roth , H. ·P. and M. Ki rc hg e £ner, Z. Tz e rph y sz o l Tz e rernahrg. -u. Futt er mz ttel kde. , 33, 1, 57, 62, 1974. 92) Mi lls, C. F. , J. Qu arte r man, R. B. W illiam s, A. C. Dalga rno and :'.B. Panic , Bz ochem. , ]. , 102, 1967. 93) Theuer, R. C. and W. G. Hoekstr a , J. Nutr . , 89, 448, 1966. 94) Pallauf, J. and M. Ki rc hg e Bner, Zol. Vet. Med. , A. 20, 100, 1.97 3. 95) Hambid g e, K. M. , Ped. Clz n . North Amerfr a. , 24, 95, 1977. 96) Prasad. A. S. , P. Rabbani, A. Abbasi, E. Bowersox and M. R. S. , ·in Ki rc hg e ssner, M. Trace Element Meta o ol£ s m £n Man and Anz mals- ..3, Technis c he Univ e rsit at Mi lnc hen, Freis i n g - Weih enste p h an, p. 280. ,
:19 78. 97) Roth , H. P. and M. Ki rc hg e ssner, Bi o log tca l Trace element Rese· .. ar ch 3, 13, 1981. 98) Ki rc hg e ssner, M. Roth , H. -P. and Schwarz, F. J. Z. Ti e rph y si o l, Ti er ernii hr , Futt er mi ttelk de. , 36, 175, 1976. 99) Roth , H. -P. and Ki rc hg e ssner, M. , Int. Z. Vi t. Ern. Forsch. , -45 , 201, 1975. 100) Scott , D. A. , Bi o chem. ]. , 28, 1592, 1934. 101) Move, E. , Elvehje m , C. A. and Hart, E. B. , Am. J. Phys i o l. , ·11 9, 768, 1937. 102) Hendric k s, D. G. and Mahoney , A. W. , J. Nutr . , 102, 1079, 1972. 103) Qu arte r man, J. and Florence, E. , Br. ]. Nutr . 28, 75, 1972. 104) Boq u is t , L. and Lernmark, A. , Acta Path o l. Mi cr obio l . Scand. , 76, 215, 1969. 105) Homan, J. D. H. , Overbeck, G. A. , Neute l i ng s, J. P. J. , Booiy , :L. J. and Van Der Vi es , J. , Lancet 2, 541, 1954. 106) Huber, A. M. and Gershoff , S. N. , J. Nutr . , 103, 1739, 19 ·73 _ 107) Roth , H. -P. , Schneid e r, U. and Ki rc hg :s sner, M. , Arch, Ti e- :rer nii hr . 25, 545, 1975. 108) Macap inl ac, M. P. , Pearson, W. N. and Darby , W. J. , in ·Pr asad, A. S. ed. , Zi n ce. Meta b olis m , Chales C. Thomas, Sp r in g fiel d, .II I. , p. 142, 1966. 109) Cox, R. P. and Ruckenste i n , A. , J. Cell. Phys i o l. , 77, 71, 1.97 1. llO) McInty re , N. , Holdswort h, C. D. and Turner, D. S. , J. Clin . .E ndocrin ol Meta b . , 25, 1317, 1965. Ill) Fasel, J. , Hadji kh ani, M. D. H. and Felber, J, F. , Gastr o en- .te rolog y. 59, 109, 1970. ll2) Roth , H. -P. and Ki rc hg e ssner, M. , Z. Ti e rph y si o l . , Ti er ernii hr . .Fu tte r mi ttelk d. , 43, in pre ss, 1979. ll3) Rib a s, B. , LopP .z -Calderon, A. , Culebras, J. M. and Dean, M. ,
In Ki rc hg es sner, M. ed. , Trace Element lvfe ta b olis m in Man and An-- im al-3, ATW. Freis i n g -W eih e nste p h an, p. 378, 1978. 114) Qu arte r man, J. , Mi lls, C. F. and Hump h rie s , W. R. , Bi o chem. Bi op h y s. Res. Commun. , 25, 354, 1966. 115) Roth , H. -P. and Ki rc hg e ssner, M. , Zbl. Vet. Med. , A23, 578, 1976. 116) Roth , H. -P. and Kric h g e ssner, M. , Z. Ti e rph y si o l. , Ti e re·· rnii hr . Futt er mi ttelk d. , 43, in pre ss, 1979. 117) Hsu, J. M. , in A. S. Prasad, ed. , Trace Elements in Humane and Di se ase, Academi c Press, New York, p. 295, 1976. 118) Boq u is t , L. , Acta Soc. Med. Up sa l. , 72, 358, 1967. 119) Bog u is t , L. , Vi rch ows Arch. , BI, 157, 1968. 120) Lazari s, Y. A. , Lop in, V. I. and Palmi na , T. V. , Vop . Med. . Khim . , 17, 621, 1971. • 121) Eng el hart, K. and Ki ef , H. , Vi rch ows Arch. , B4, 294, 1970 .. 122) Coombs, T. L. , Grant, P. T. and Frank, B. H. , Bi o chem. ]. , 125, 62, 1971. 123) Maske, H. , in -R. H. Wi lliam s, ed. , Di ab ete s , Haeber, New· York, p. 46, 1960. 124) Flyn n, A. , Str a in , W. H. and Porie s , W. J. , Bi o chem. Bi op h y s, . Res. Commun. , 46, 113, 1972. 125) Henkin , R. I, , Meret, S. and Jac obs, J. B. , J. Clin . Invest . . 48, 38, 1969. 126) Lif sc hit z, M. D. and Henkin , R. I. , J. Ap pl. Phys i o l. , 31, 88,.- 1971. 127) Henkin , R. I. , in W. G. Hoekstr a , J. W. Sutt ie, H. E. Ganth er, . and W. Mert z. , ed. , Trace Element Meta b oli sm in Ani m als-2. Univ e rsit y Park Press, Balt imo re p. 652, 1974. 128) Henkin , R. I. , in W. G. Hoekstr a , J. W. Sutt ie, H. E. Ganth er and W. Mert z, eds. , Trace Element Meta b olis m in Anim als-2, Uni- · versit y Park Press, Balti m ore, p. 647. 1974. 129) Prasad, A. S. , Oberleas, D. , Wolf . , P. and Horwi tz, J. P. , ] •. Lab. Clin . Med. , 73, 486, 1969.
130) Gir o ux, E. L. and Henkin , R. I. , Bi o chem. Bi op h y s. Actc . , 273,.. 64, 1972. 131) Henkin , R. I. , Med. Clt 'n, N. Am. , 60, 779, 1976. 132) Flyn n, A. , Porie s , W. J. , Str a in , W. H. and Hi ll, O. A. , Jr. , Lancet 2, 2.3 5 , 1972. 133) Reeves, P. G. , Fris s ell, S. G. and O'Dell, B. L. , Proc. Soc .. Exp. Bi ol . Med. 156, 500, 1977. 134) Ku, P. K. , Di ss . Abstr . Int. , B.3 2 , 6717, 1971. 135) Bisc hoff , F. , Am. J. Phys i o l . , 117, 182, 1946. 136) Bis c hoff , F. , Am. J. Phy si o l. 121, 765, _ 1938. 137) Maxwell, L. C. , Am. J. Phys i o l. , 110, 458, 19.3 4 . 138) Mi llar , M. J. , Elcoate , P. V. , Fis c her, M. I. and Mawson,. C. A. , Can. J. Bi oc hem. Phy si o l . , .38 , 1457, 1960. 139) Sato , N. and Henkin , R. I. , Am. ]. Phy si o l . , 225, 508, 19- 73. 140) Brig gs , M. H. , Brig gs , M. and Austi n, J. Natu r e, 232, 480, 1971. 141) Halste d , J. A. , Hackley, B. M. and Smi th, J. C. , Lancet 2,. 278, 1968. 142) Halste d , J. A. and Smi th, J. C, Jr. , Lancet 1, .32 2, 1970. 143) Schenker, J. G. , Pali sh uk, W. Z. and Jun g re is , E. , Ferti l. , 22, 229, 1971. 144) Prasad, A. S. , Oberleas, D. , Lei, K. Y. , Mog h is s i, K. S. and, Str y k er, , J. C, Am. J. Cl in. Nutr . , 28, .37 7, 1975. 145) McBean, L. D. , Smi th, J. C. , Jr. and Halste d , J. A. , Proc. Soc. Exp. Bi o l. Med. , 137, 54.3 , 1971. 146) Ap ga r, J. , J. Nutr . , 100, 47q , 1970. 147) Porie s , W. J. , Mansour, E. G. , Flecha, F. R. , Flyn n, A. and Str a in , W. H. , in Prasad, A. S. ed. , Trace Elements in Human Health and Di e sease, Academi c Press, New York, p.1 15, 1976. 148) Flyn n, A. , Porie s , W. J. , Str a in , W. H. and Weil an d, F. L. , Natu rwi ss enschaft en , 60, 162, 197.3 . 149) Ki rc hg e ssner, M. and Schneid e r, U. A. , Arch. Ti e rernii hr . ..
28 , 211, 1978. 150) Schneid e r, U. A. and Ki rc hg e ssner, M. , Nutr . Meta b . , in pr ess, 19 78. 151) Gombe, S. , Ap ga r, J. and Hansel, W. , Bi o l. Rep ro d. , 9, 41 ·5, 1973. 152) Lei, K. Y. , Abbasi, A. and Prasad, A. S. , Am. ]. Phys i o l. , 230, 1730, 1976. 153) Abbasi, A. A. , Prasad, A. S. and Orte g a , J. , Ann. Inte r n. Med. , 85, 601, 1976. 154) Prasad, A. S. , Abbasi, A. and Orte g a , J. , in G. J. Brewer and .A. S. Prasad, eds, Zi n c Meta b olis m , Current Asp ec ts in Healt h and Di se ase, Alan R. Li ss , New York, p. 211, 1977. 155) Neldner, K. H. , Hag le r, L. , W ise , W. R. , Sti fel, F. B. , Lufk in , :E. G. and Herman, R. H. , Arch. Dermato l . , 110, 711, 1974. 156) Cash, R. and Berge r, C. K. , J. Pedia tr . , 74, 717, 1969. 157) Whit e, H. B. and Monta l vo, J. M. , J. Pedia t r . , 83, 999, 19 73. 158) Moy n ahan, E. J. , Lancet, 1, 399, 1974. 159) Neldner K. H. and Hambid g e , K. M. , New Eng l. ]. Med. , 29 :2, 879, 1975. 160) Lombeck, J. , Schnip pe rin g , H. G. Kaspa rek, K. , Ri tzl, F. , Kastn er, H. , Fein e ndeg e n, L. E. and Bremer, H. J. , Z. Ki n derheil k d. , 120, 181, 1975. 161) Evans, G. W. , Grace, C. I. and Vota v a, H. J. , Am. ]. Phy si o l. , 228, 501, 1975. 162) Song , M. K. and Adham, N. F. , Fed. Proc. , 36, 4583, 1977. 163) Evans, G. W. and Joh nson, P. E. , Lancet, 2, 52, 1977. 164) Weis m ann, K. and Flag s ta d , T. , Acta Derm. Venerol. , 56, 151, 1976. 165) Song , M. K. and Adham, N. F. , Am. J. Phy s io l. , 234, E99, 1978. 166) O'Dell, B. L. , Rey n olds, G. and Reeves, P. G. , J. Nutr . , 107, 1222, 1977.
167) Placke, D. J. , Levin t h al, C. and Vallee, B. L. , Bio c hemi st r y , . 1, 373, 1962. 168) Sim p so n, R. T. and Vallee, B. L. , Bi o chemi st r y , 7, 4343, 19- 68. 169) Roth , H. -P. and Ki rc hg e ssner, M. , Res. Exp. Med. , in pre ss, 1978. 170) Hambid g e, K. M. , Walravens, P. A. and Neldner, K. H. , in G. J. Brewer and A. S. Prasad, Eds. , Zi n c Meta b ol£ s m, Current Asp ec ts - £n Healt h and Di se ase, Alan R. Lis s , New York, p. 329, 1977. 171) Van Vlote n , W. A. and Bos L. P. , Dermato / og ica , 156, 175,. 1978. 172) Kroneman, J. , Mey , G. J. W. and Helder, A. , Zbl. Vet. Med. , A22, 201, 1975. 173) St o ber, M. , Dt sc h. Ti e riir zt l . Wochenschr. , 78, 257, 1971. 174) Sim kin , P. A. , Lanc~t, 2, 539, 1976. 175) Keil i n , D. and Mann, T. , Bi oc hem. J. , 34, 1163, 1940. 176) Keil in, D. and Mann, T. , Natu re, 145, 304. 177) Roth , H. -P. and Ki rc hg es sner, Z. Ti e rph y si o l . , Ti er enii hr . Futt er mi ttelk d. , 32, 296, 1974. 178) Ki rc hg e ssner, M. , Sta d ler, A. E. and Roth , H. -P. , Chem. , 5,. 33, 1975. 179) Igb al, M. , Enzy m e, 12, 33, 1971. 180) Prasad, A. S. and Oberleas, D. , J. Ap pl. Phys i o l . , 31, 842,. 1971. 181 ) Hsu, J. M. , Anil a ne, J. K. and Scanlan, D. E. , Sc te nce, 153,. 882, 1666. 182) Prasad, A. S. , Schoemaker, E. B. , Orte g a , J. , Brewer, G. J. , Oberleas, D. and Oelshleg e l, F. J. , Jr. , Cl in. Chem. , 21, 582, l!l- 75. 183) Ki rc hg e ssner, M. , Roth , H. P and Weig a nd, E. in A. S ► Prasad, ed, Trace Elements in Human Healt h and Di se ase, vol. i.. Academi c Press, New York, p. 189, 1976. 184) Wacker, W. E. C. , Bi oc hemi st r y , 1, 859, 1962.
185) Scrutt on , M. C. , Wu, C. W. and Goldt h wait , D. A. , Proc, Natl . Acad. Sci. , 68, 2497, 1971 . 186) Sp r in g ga te , C. F. , Mi ld van, A. S. and Loeb, L. A. , Fed. Proc. Fed. Am. Soc. Exp. Bi o l. , 32, 1973. 187) Sp ri n g ga te , C. F. , Mi ld van, A. S. and Abramson, R. , ]. Bi o l. ·Ch em. , 248, 5987, 1973. 188) Auld, D. S. , Kawag u chi, H. , Liv i n g st o n , D. M. and Vallee, B. L. , Bi o chem. Bi op hy s. Res. Commun. , 57, 967, 1974. 189) Auld, D. S. , Kawag u chi, H. , Liv in g st o n , D. M. and Vallee, B. L. , Proc. Natl . Acad. Sci. , 71, 2091, 1974. 190) Lie b erman, I. and Ove, P. , J. Bi o l. Chem. , 237, 1634, 19 -62 . 191 ) Terhune, M. W. and Sandste a d, H. H. , Sc ien ce, 177, 68, 19 72. 192) Sandste a d, H. H. , Gil le sp ie, D. D. and Brady , R. N. , Pedia tr . Res. , 6, 119, 197~. 193) Fernandez-Madrid , F. , Prasad, A. S. and Oberleas, D. , J. ·Cl in . Med. , 82, 951, 1973. 194) Prasad, A. S. and Oberleas, D. , J. Lab. CUn. Med. , 82, 461, 1973. 195) Prasad, A. S. , Schoomaker, E. B. , Orte g a , J. , Brewer, G. J. , -Ob erleas, D. and Oelshleg e l, F. J. , Jr. , in Abstr a ct of Fi rst Nati on al Sy m p os iu m on Si ck le Cell Di se ase, p. 33, 1974. 196) Cheste r s, J. K. and W ill, M. , Br. J. Nutr . , 39, 375, 1978. 197) Duncun, J. R. and Dreosti , I. E. , J. Comp . Patl zol . , 86, 81, 1976. 198) Dreosti , I. E. and Hurley , L. S. , Proc. Soc. Exp. Bi o l. Med. , 150, 161, 1975. 199) Oberleas, D. and Prasad, A. S. , in W. G. Hoekstr a , J. W. Sutt ie ·H. E. Ganth er, and W. Mertz , eds. , Trace Element Meta b oli sm in Anim als-2, Univ e rsit y Park Press, Balti m ore, p. 730, 1974. 2011) Prasad, A. S. , in A. S. Prasad, ed. , Trace Elements in Human .an d Di se ase, vol. 1. Academi c Press, New York, p. 1, 1974.
201 ) Swenerto n , H. R. , Di ss . Abstr . Int. Bi o chem. , 31, 1971. 202) Swenerto n, H. R. and Hurley , L. S. , J. Nutr . , 95, 1968. 203) Swenerto n , H. R. , Shrader, R. and Hurley , L. S. , Proc. Soc. Exp. Med. , 141, 283, 1972. 204) Ri or dan, J. F. , Med. Clin . N. Am. , 60, 661, 1976. 205) Vallee, B. L. , Cancer Enzy m ol. 12, 159, Mt a mi Wi n te r Sy • mp os ta , 1976. 206) Bruch, R. E. , W illiam s, R. V. , Hahn, H. K. J. , Clin . Chem. , 21, 568, 1975. 207) Roth , H. -P. and Ki rc hg es sner, M. , Zbl. Vet. Med. , A24, 17 7, 1977. 208) Rein h old, J. G. and Kf ou ry, G. A. , Am. J. Clin . Nutr . , 22, :12 50, 1969. 209) Mi ll s, C. F. , Qu arte rman, J. , Cheste r s, J. K. , Wi lliam s, R. B. and Dalga rno, A. C. , Am. J. C!t n . Nutr . , 22, 1240, 1969. 210) Prasad, A. S. and Oberleas, D. , Ann. Inte r n. Med. , _ 73, 631, 1970. 211) Prasad, A. S. , Oberleas, D. , Wolf. P. , Horwi tz, J. P. , Mi ller .E. R. and Luecke, R. W. , Am. J. Clin . Nutr . , 22, 628. 212) Fell, G. S. and Burns, R. R. , Proc. R. Soc. Med. , 69, 474, 1976. 213) Ki rc hg e ssner, M. and Roth , H. ·P. , Zbl. Vet. , Med. , A22, 14, 1975. 214) Pallauf, J. and Ki rc hg e ssner, M. , Arch, Tzerent'i hr . , 26, 457, 19 76. 215) Weig a nd, E. and Ki rc hg e ssner, M. , Z. Ti e rph y si o l. , Ti e renii hr . Futt er mt ttel kd. , 39, 16, 1977. 216) Ellul-Mi ca llef, R. , Galdes, A. and Fenech, F. F. , Postg r ad. .M ed. J. , 52, 148, 1976. 217) Bourne, G. H. , in G. H. Bourne, ed. , The Bi o chemi st r y and Phys z o log y of Bone, Academi c Press, New York, p. 177. 218) Thawley , D. G. and W illou g h by , R. A. , Can. J. Comp . Med. , -41 , 84, 1977.
219) Lin , C. W. , Di ss , Abstr . Int. Bi oc lzem. , 32, 515B, 1970. 220) Rot h , H. -P. and Ki rc hg e ssner, M. , Z. Ti e rph y s io l. , Ti e rern- iihr . Futt er mi ttel kd. 33, 57, 1974. 221) Westm oreland, N. P. , Di ss . Abstr . Int. Bi o chem. , 30, 63B,. 1969. 222) Westm oreland, N. P. , Fed. Proc. , 30, 1001, 1971 . 223) Cata l anott o, F. A. and Nanrla, R. ]. Oral. Patl z ol. , 6, 211,. 1977. 224) Ki rc hg e ssner, M. , Roth H. -P. and Weig a nd, E. , in A. S,. Prasad, ed. , Trace Elements in Human Healt h and Di se ase, vol. 1,. Academi c Press, New York, p. 189, 1976. 225) W illiam s, R. B. , Br. ]. Nutr . , 27, 121, 1972. 226) Davie s , M. I. and Motz o k, I. , Comp . Bi o clzem Plzy s io l. , 40B,. 129, 1971. 227) Roth , H. -P. and Ki rc hg e ssner, M. , Zbl. Vet. Med. , in pre ss, 1979. 228) Weig a nd, E. and Ki rc hg e ssner, M. , Z. Ti e rph y s io l. , Ti e rern-· tikr . Futt er mi ttelk d. , 39, 16, 1977. 229) Ki rc hg e ssner, M. , Trace Element Meta b olz s m in Man and' Anim als-3, Technis c he Un i vers it죠t Mi inc hen Freis i n g - Weih enste p h an, p. 359, 1978, 230) Hambid g e , K. M. , P. A. Walravens, K. H. Neldner and N. A. Daug h erty , tµ Ki rc hg e ssner, M. , Trace Element Meta b oUsm in Man· and Anim als-3, Technis c he Univ ersit at Mi inc hen. Freis i n g - Weih e n-- ste p h an, p. 413, 1978. 231) Ag ge tt , P. J. , D. J. At h erto n , H. T. Delves, J. M. Thorn, A. Bang h am, B. E. Clay ton and J. T. Harrie s , in Ki rc hg e ssner, M. , Trace Element Meta b olz s m in Man and Anim als-3, Technis c he, Un i vers it죠t Mi inc hen Freis i n g - Weih e nste p h an, p. 418, 1978. 232) Flags ta d , T. , in Ki rc hg e ssner, M. , Trace Element Meta b oli sm · in Man and Anim als-3, Technis c he Univ e rsit at Mi inc hen Freis i n g - Weih enste p h an, p. 423, 1978. 233) Str ai n , W. H. , Ste a dman, L. T. , Lankau, C. A. , Berlin e r, W. P. ►
and Porie s , W. P. , ]. Lao. Cl in. Med. , 68, 244 , 1666. 234) Mag e e, A. C. und G. Matr o ne, Nutr i t . , 72, 233, 1960. 235) Cox, D. H. und D. L. Harris , ]. Nutr i t . , 78, 415, 1962. 236) Vallee, B. L. , Phys i o l. Rev. , 39, 443, 1959. 237) Vallee, B. L. , Zin e in Comar, C. L. and F. Bronner Mi n eral Meta b ol ism , Academi c Press, New York-London, 1962. 238) Hurley , L. S. , Duncan, J. R. , Eckhert, C. :0. , Sloan, M. V. , in Ki rc hg e Bner, M. , Trace Element Meta b oli sm in Man and Ani m als-3, p, 449, ATW, Freis i n g ·W eih enste p h an, 1978. 239) Smi th, H. , J. Forensic Sci. Soc. , 7, 97, 1967. 240) Schroeder, H. A. and Nason, A. P. , Invest. Dermato l . , 53, 71,. 1969.
5 몰리 브덴 (Molyb denum, Mo) 1953 년 W isc onsin 대 학의 Weste r fi eld 는 18) M0 이 등문 영 양에 중 요한 역할을 한다고 하였다. Mo 은 조직 내 의 flav op ro te i n enzy m e 과 xanth in oxid a se nit ra te reducta s e 의 구성 요소가 되 며 위의 효소들의 활성 도는 Cu 이 온에 의해 영향을 받게 된다는 보고는 있으나 아직 인간의 영양과의 작 용에 대해서는 많이 연구되어 있지 않은 신정이다. 5.1 체내 함량과 분포 사람은 체내에 약 8~10m g의 Mo 울 함유하고 있으며 혈액의 Mo 은 0.3~7.2µ g /lOOml 로 넓은 폭을 보이며 사람에 따라서는 ·0. lµg /l OOml 까지 도 측정 되 었 다. 혈장에 는 0. 5~3. 4µg /l OOml 의 Mo 이 함유되어 있고 Mo- 먼지를 끼얹었을 때는 36.5µ g /lOOml 까 지 상승하는 것을 볼 수 있었다 .2) Mo 은 주위의 환경에 많은 영향을 받는 것 같다. 그러나 간장은 Mo 이 2.7~4.9µ g/g으로 큰 차이가 없었다. 신장에서도 Mo 함량이 높은 것으로 발견되었다. 세포 안의 분포 는 아직 많이 알려져 있지 않으며 혈액에는 루과할 수 있는 Mo042+ 의 형태로 촌재한다 .3) 표 5.1 은 사람과 동물의 각 기관에 함유되어 있는 Mo 농도이다 .1)
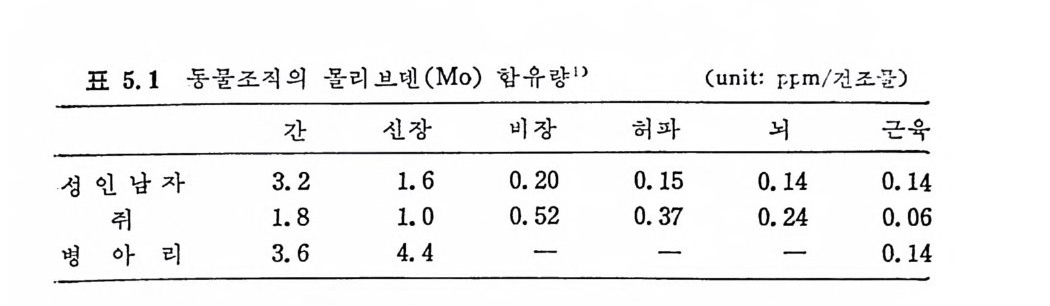 표 5.1 동물조칙의 몰리브멘 (Mo) 함유 량 I ) (unit : r,i: m / 건 조 군 )
표 5.1 동물조칙의 몰리브멘 (Mo) 함유 량 I ) (unit : r,i: m / 건 조 군 )
5.2 주요 기능 Mo 은 flav op r ote i n 인 xanth in e oxid a se 와 aldehy d e oxid a se 의 구성 요소로서 pu rin e 대 사에 관여 하여 hy po xanth in e 과 xanth in e 에 서 uric ac i d 의 형성에 중요한 역할을 한다. 또한 heme 단백질인 sulfi te oxid a se 의 필 수 구성 성 분이 며 S 아 를 해 독시 키 고 아황산영 을 황산으로 전환시 키 는 데 촉매 작용을 한다. Mo 은 식 물의 nit ra te reducta s e 와 nit ro g e nase 에 도 촌재 하며 이 생물에 의해서 공기 중의 질소몰 고정하여 질소고정 암모니아로 전 환되는데 이것은 산화 • 환원작용에 관여한다. Mo 은 F 와 함께 결 합되 어 충치 를 예 방하기 도 한다. Seeli ng 은 Mo 이 fer riti n 의 안 팎에 서 Fe 의 수용과 방출작용에 관여 한다고 하었 다. 4) 5.3 대 사 5.3.1 흡수와 배설 사람의 Mo 흡수와 배설에 대해서는 찰 알려져 있지 않다. 정 · 상적인 석이 상태에서 사람은 Mo 울 하루 0.3mg 섭취하여 빠른속 도로 쉽게 흡수한다. 그러나 토양과 물 그리고 섭취하는 음석물에 따라서 0.05mg ~ ·O. 35mg 까지 의 큰 차이 를 보인다. Sodiu m molyh date 나 ammo· •.n ium molyb date 등은 수용성 이 며 Mn 야 나 CaMo04 등은 불용성 인 형태인데도 토끼, 모르모트 등의 동물은 흡수를 찰 한다고 한다 `
Molyb den su lfit e 는 흡수가 찰 안되는데 그 원인은 S 함유 ami n o , ac i d 와 과량의 텅스텐 CW) 때문이라고 본다 .3) Mo 의 이용에 관계하는 요소를 보면 식이내 무기 sulfa te 상대가 Mo의 홉수 및 처장 배설 등에 영향을 준다. Sulfa te 함량이 높은 식이는 뇨로 Mo 이 배설하는 것을 증가시켜 준다. 양을 대상으로 한 실험에서 sul fat e 가 Mo 의 흡수를 감소시키고 배설을 증가시켜 주며 체내 보유량을 제한한다고 밝혀졌다. 아직 확실한 기전에 대 해서 완전히 밝혀져 있지 않으나 무기 sul fat e 가 Mo이 세포막으 로 이동되는 것울 방해한다는 설도 있다 .4)6) Mo 은 주로신장을통 해서 배설된다. 국민학교 학생들의 뇨로 배설되는 Mo 의 양은 평 군 3. 3µg / l00ml 이 며 Mo 섭 취 상태 가 좋아지 면 5. 7µg / 100ml 까지 배설된다. 성인에게 Mo 을 과량 섭취시킨 견과 평군 0.2~23µg / 100ml 에서 4.5~llOµ g /lOOml 까지 중가했다. 방사선 동위원소 99Mo 을 정 맥 투입 하여 분포도를 살폈 을 때 99Mo 이 간장과 선장으 로 많이 이동되고 내분비선 중에서도 갑상선에 Mo 이 많이 저장되 었다. 뇌와지방조직은 Mo 을 저장해 두지 않았고, 48 시간 이후에야 Mo 이 간 신장골격을제의한다른 모든 기관에 분포되었다. 99Mo 을 정맥주사한 10 일 후에 그 가운데 21~29% 가 뇨로, 그리고 1~7% 가 대변으로 배설되었다. 혈액에는 Mo 이 두과할 수 있는 음이온형태 로서 (Mo04++) 촌재 한다고 추정 되 고 있 으며 뇨에 는 molyb date 형 태로 촌재한다. 동물의 Cu 영양상태는 Cu 의 섭취와 Mo sulfa te 섭취 사이의 관 계에 따라 달라지는데 양에게 과량의 Mo sul fat e 를 섭취시키면 Cu 의 배설이 증가되는 것이 아니라 소화기관의 Cu 의 용해성을 감 소시켜 Cu 의 이용을 제한한다는 기전이 밝혀졌다 .4)6) 이와 같이 Mo 은 요 함유 효소의 활성울 방해하거나 조직 내에서 Cu 가 이용 될 수 없는 형태로 막아 주어 전반적으로 Cu 대사의 장애를 초래한 다고 했다. 반대로 Cu 는. Mo 의 체내 이동에 영향을 주지 못했다. 그 이의에도 과량의 Mn 섭취는 Mo이 Cu 보유에 미치는 영향을 제한하는 것을 막아 준다. Mo 과 Cu 의 상호작용은 매우 복잡한 관 계를 나타내고 Mo 을 과량 섭취하면 Cu 결핍증을 유발할 수 있다.
5.4 필요량 사람의 Mo 필요량에 대해서는 아직까지 알려져 있지 않다. 그러 므로 일반적인 식이상태로 섭취하고 있는 양이 충분할 것이라고 추 측하는 정도에 불과하다. 확실히 신뢰할 수 있는 연구라고는 할 수 없으나 balance 연구에서 2 세 정도의 어린이들에게서 얻은 자료로 는 메일 2µg / kg 체중 정도로 평형이 유지되었으며 가벼운 po sit ive 현상을 나타냈다고 한다. 5) 또한 6~10 세 사이의 여자 아이들은 하루 lOOµg Mo 을 섭취했을 페 Mo balance 가 po sit ive 였 다고 한다. Balance 연구에 서 사람의 일일 섭취량이 0.1~0.15m g일 때 얼마간 보유되었다. Cu 의 섭취 가 정상 상태일 때는 하루 0.15~0.5m g정도 Mo 섭취를 권장할 수 있으며 8) 이 양은 정상적인 혼합 식이에서 쉽게 섭취할 수 있는 것 으로 보인다. RDA 에 서 19) 하루권장량은 다음과 같다.
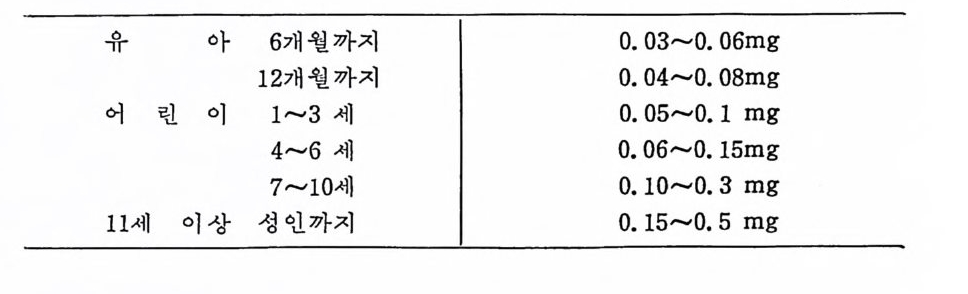 유 아 6 개월까지 0. 0 3~0. 06mg
유 아 6 개월까지 0. 0 3~0. 06mg
5.5 결핍증 아직까지 사람에게서 Mo 결핍증은 관찰되어 있지 않다. Mo 은 극히 적은 양을 필요로 하기 때문에 실험적으로 결핍증을 유발한다 는 것은 어려운 일이다. 최근 동물 식이에 하루 0.05p pm 이하의 M0 을 섭취시켰을 때 가벼운 결핍증세가 나타났다.
실험상으로 Mo 에 텅스덴 cw) 을 첨가했을때 그의 상호작용에 의 해서 결핍증이 유발되며 이때 성장 장애, 체조직의 Mo 함량 및 간 장의 xanth in e oxid a se 가 감소되 고 xanth in e 이 uric acid 로 산화 되는 정도가 낮아졌다. 또한 Mo 이 결핍된 쥐에게서 추출해 낸 간 h omog e nate 에 서 meth anol 이 fo rmaldehy d e 로 산화되 는 능력 의 감소”와 해 독작용을 하는 sulfi te oxid a se 의 감소가 나타났다. 10) 반정제된 식이로 유지된 어린 양의 석이에 0.36 pp m 의 Mo 올 보 충했을 때 좋은 성장반응을 보였는데 이는 Mo이 반추위 내 미생물 에 의한 섬유소 분해를 촉진하기 때문일 것으로 보여진다. 5.6 함유석품 동물의 내 장, 전곡 (whole gr ain ) , 두류 등에 는 Mo 이 많이 함유 되어 있고, 고기, 우유, 과일 그리고 근채류에는 Mo 이 적게 들어 있다. 5.7 독 성 사람의 Mo 독성에 대하여는 아직까지 알려져 있지 않다. 아르마 · 니 아 지 역 은 하루 Mo 섭 취 량이 10~15mg 으로 Mo 의 xanth in e -· oxid a se 의 촉진 기 능으로 인하여 통풍이 발생 하였 다. 11) 매 일 약 1. 5m g의 Mo 섭취는 요산대사에 영향울 주지 못했으나 Cu 대사가 현처히 증가하였다고 한다 .12) 동물 실험에서 과량의 Cu 섭취는 간 장의 Cu 결핍울 유발시키는 원인이 되었으며 sul fate 는 이 중상을 더욱 더 십화시켰다. 그러므로 과량의 Mo 섭취는 Cu 결핍울 야기 시킨다고 할 수 있다. 동물에게 0.1m g의 Mo 을 섭취시켰을 때 이러한 결핍 현상이 일 어 났으며 balance 가 neg a ti ve 였 다. 과량의 Mo 은 Cu 와 Cu moly- • bdate 나 Cu-th io m olyb date 복합체 를 형 성 하여 Cu 의 홉수와 대 사 과정에서의 이용울 방해하였다. • 취에게 500m g의 Mo 석이를 섭취시켰을 때 약 1 주일 후에 사망
했다. Balance 실험에서 하루 약간 높온 양인 0.54mg Mo 을 섭취했 을 때 Cu 의 배설이 현저히 증가하였다. 그 이의에도 간장 sulf ide - ox i dase 의 장애가 오는데 이는 Cu 의 이용율과 관계가 있는 것으 _ 로 알려졌다. M o 의 결 핍 증 세로는 성장감되 빈혈 둥이 나타났으며 이칙까지 독 성을 일으키는 수준은 확립되어 있지 않다. 쥐에게 250 pp m 의 Mo 식이를 섭취시켰 을 때 (mol y bda t e 형태로) 성장 감되와 설사를 일으켰으며 간장에 Mo 이 과잉 축적되면 xanth in ox i dase 의 활성 이 약화되 었으며 간 homog e nate 에 서 는 산소의 소비 가 감소되 었 다. 식이에 0.3% 의 me t h i on i ne 을 첨가했을 때에는 독성효과가 적어 쳤 다. 또한 sulfa te 를 첨 가하여 도 같은 효과를 가져 왔다. 영국, 미국의 캘리포니아 그리고 뉴질랜드의 몇몇 지역에는 토양 에 Mo이 많 이 함유되어 있어서 이 지역의 동물은 〈t ea rt〉라는 Mo 독성증을 일으키는데 cachex i a 와 설사를 수반한다. 독성의 증세는 Mo의 섭취량과 바례했다. 이 지역의 풀의 Mo 량 은 20~IOOµ g / 건조물 g이었다. 소련의 일부 지역에서는 하루 10~、 15m g의 Mo 을 섭취하는데 이곳 주민들은 통풍과 비슷한 중세와 혈액의 Mo xanth in oxid a se 그리고 뇨산의 증가를 나타냈다. 또한 혈 액의 Mo 상승 뿐 만 아니라 동시에 Cu 도 중가했다 .13) 식이 100g 당 8~14mg Mo 의 섭취는 성장지연과 생식 능력 불능을 나타냈 다 .l 4 ) 이때 Cu 의 섭취로 Mo 의 독성을 막을 수 있었는대 식이에 2mg Cu / 석 이 IOO g이 첨 가되 었을 때 40mg Mo/ 석 이 100g 의 독성 효과를 감소시켰다. Cu 이의의 다른 tra ce elemen t s 는 위와 같은 효과를 보이지 않았 다. 가장 국심한 독성 증상은 식이중 0.1% 의 Mo 을 섭취한 토끼 에게서 관 찰 되었다 .1 5 ) 이 토끼는 식욕감되, 체중감소, 탈모, 피부 장애, 빈혈 둥으로 곧 사망했으나 O.02% Cu 를 식이에 보충해 주 었을 때는 Mo 의 독성이 Cu 섭취량만큼 감소하였다. 그러나 병아 리에 있어서는 Mo 독성에서 오는 성장지연이 Cu 의 보충식이로서 일부만 해소되었다 .16) 쥐에게서 Mo 과 Zn 의 혼합식이는 Mo 단독석이의 섭취 때보다
현저한 성장지연을 초래했다. 소와 양에게서 자주 볼 수 있는 Mo 의 독성 중세 로 골다공증을 들 수 있 는데 이 는 Mo 을 함유한 alkali ne · p hosp ha t e 의 십한 기능 장해와 관계가 있다. 쥐도 과량의 Mo 을 섭취시켰을 때 간에서 alkali ne ph osp h ata s e 가 현자하게 상승되었다고 한다 .17) *참고문현 I) Underwood, E. J. , Trace Elements in Human and Ani m al Nutr i · tion, Academi c Press Inc. New York and London, 1977. 2) Walrarens, R. A. , Moure, R. , Solomons, C. C. , Chap pe ll, W. R. and Bentl e y , G. in Ki rc hg e l.: n er, M. , Trace Element Meta b olt 'sm in ..1\1a n and Ani m als-3, p. 577, ATW, Freis i n g - Weih enste p h an, 1978. 3) Losee, F, Cutr e ss, T. W. and Brown, R. , Trace Subst. , Envfr on . , Healt h- 7. Proc. Un£. Mo. Annu. , Conf. , 7th 1973, p. 19, 1973. 4) See: lin g , M. S. , Revie w , Am. J. Cl in. Nutr . , 25, 1022 , 19 72 . 5) Ki rc hg e Ener. M. N. -P. Rot h , F. J. Schwarz, E. GraE m ann, A. -Sc hneg g and E. Weig a nd. in Cremer, H. -D. and Hot z el, J. Ki lhn au, Bi o chemi e und p!tysi o log ie der Erni.i hr ung Band I, Tei! 2, Georg· ~hie m e Verlag, p. 29, 1980. 6) Dowdy , R. P. , G. A. Kunz and H. E. Sanberlic h , J. Nutr . , 99, 4 91, 1969. 7) Eng e l, R. W. , N. 0. Pric e and R. F. Mi ller , J. Nutr . , 92, 197, 1967. 8) Mert z, W. in Gladtk e, E. , Hein e mann, G. and Eckert, I. , Sp u - :ren elemente . p. 153, Georg Thie m e, Sutt ga rt, 1979. 9) Koiv u salo, M. , Acta Phys i o l. Scand. , 45, 109, 1959. 10) Cohen, H. J. , R. T. , Drew, J. L .. Joh nson and K. P. Raja g o p o lan, Proc. Nat. Acad. Sci. , USA 70, 3655, 1973. 11) Kovalsky , V. V. , Vorotn it sk ay a , I. E. and Tsoi, G. G. , in Hoe-
1<.s tr a , W. G. , Sutt ie, J. W. , Ganth e r, H. E. and Mertz , W. , Trace Element Meta o olt s m tn An tm als-2, p. 161, Univ e rsit y Park Press, Baltim ore, 1974. 12) Deosta h le, Y. and Gop a lam, C. , Br. J. Nutr . , 31, 351, 1974. 13) Kovalskij , V. V. , G. A. Jar ovay a and D. M. Shmavonja n , Z. -Oo sc. Bt ol . 22, 179, 1961. 14) Jet e r , M. A. and G. K. Davis , J. Nutr t t. , 54, 215, 1954. 15) Arrin g ton , L. R. and G. K. Davis , J. Nutr t 't . , 51, 295, 1953, 16) Kratz e r, F. H. , Proc. Soc. Exp. Bt ol . Med. , 80, 483, 1952. 17) Reen, R. Van. , Arch. Bt o. Chem. , 53, 77, 1954. 18) Weste r fe ld , W. W. and Ri ch ert, D. A. , J. Nutr . , 51, 85, 1953. 19) Food and Nutr i t ion Board, Nati on al Research Counc il, Recommende Dt e ta r y Allowences. 9th ed. , Nati on al Academy of Scie n ces, Washin g ton , p, 174, 1980.
6 망간 (Man g anese, Mn) 수년 전부터 Mn 은 동석물의 조직에서 발견되었으며 1931 년 Kem fn er 는 동물의 성장에 Mn 이 필요하다고 발 표 하였다. 그 후 McCollum 은 쥐 의 고환의 발육부전 방지와 정 상적 인 난소기 능의 유지 에 Mn 이 필요하다고 보고하였 다. 4) 그 후 접차 결핍중을 동하여 Mn 이 필수 tra ce elemen ts 의 한 요 소임이 입증되었으나 지금까지 Mn의 생화학적 대사 실험은 거의 in v it ro 에서만 이루어졌다. 6.1 체내함량과분포 인체의 Mn 의 총 함량은 Cu 나 Zn 과 비교할 때 Cu 의 1/5 정도 이며, Zn 의 1/100 정도이다. 따라서 사람의 체중이 70k g일 때의 Mn 함량은 12~20mg 정 도이 며 농도로 표시 하면 0. 17~0. 28p pm 이 다. 2) 그러 나 Lang 은 성 인의 Mn 함유량을 10~40mg 으로 보고하기 도 하였다 .3) Mn 은 뼈에 가장 많이 함유되어 있으며, 다음은 간, 유선, 췌장 그리고 신장 순으로 함유되어 있고 근육조직에는 적은 양이 함유되 어 있다. 표 6.1 은 사람과 동물조직에 들어 있는 Mn 농도이다. 세포에는 mi toc ondr ia 에 Mn 이 많이 있 고 그 이 외 의 기 관과 cy top la sma 에 `
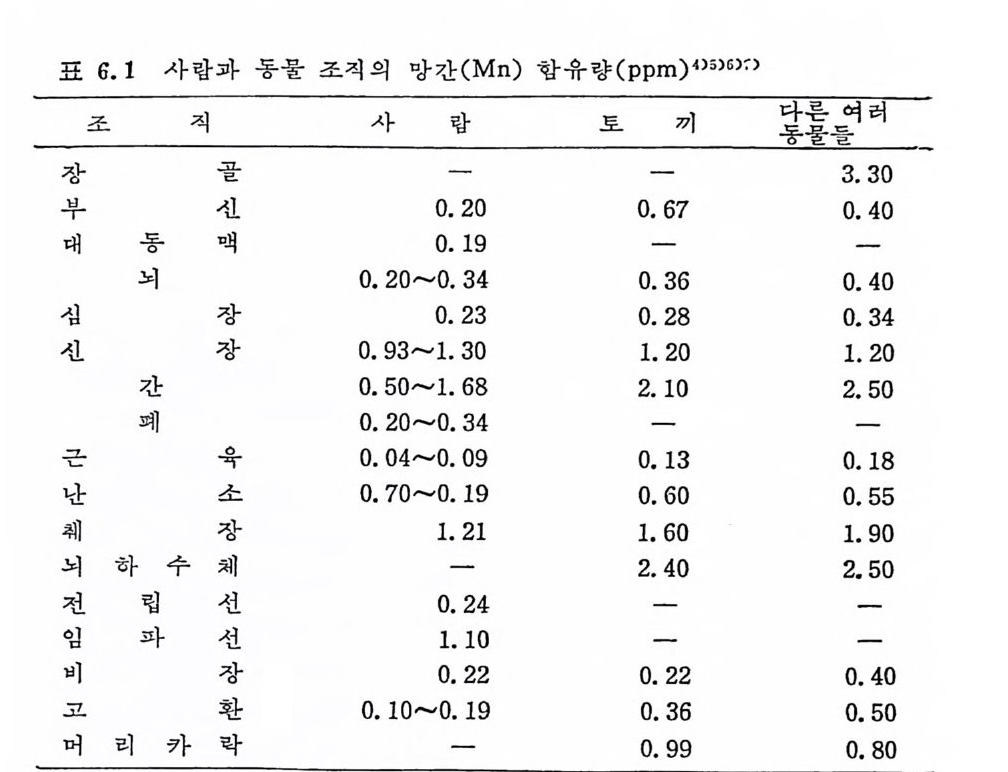 표 6.1 사람과 동물 조칙 의 망간 (Mn) 함유량(pp m) ◄> 5 )G)~>
표 6.1 사람과 동물 조칙 의 망간 (Mn) 함유량(pp m) ◄> 5 )G)~>
는 적게 함유되어 있다. 간에 Fe 과 Cu 가 많이 저장된 데 비해서 Mn 의 축적 은 많지 않다. 동물에 게 I, OOOp pm 정 도의 다량의 Mn 을 식이로 섭취시켰을 때 간의 Mn 저장분은 상승하지 않았다 .8) ::::z.. 러나 임신기간 중에는 간의 Mn 농도가 상승하였다.” Cu 와 같이 신생아의 Mn 처장은 볼 수 없었다. 모유에 는 Mn 이 적 게 함유되 어 있 으며 (1. 5µg /I OOml) 우유에 는 모 유의 약 두 배 가 들어 있 고 초유에 는 다른 tra ce elements 와 함께 Mn 도 다량 함유되 어 있 다. 사람의 혈청 에 는 0. 057 土 0. 013mg / 100ml 의 Mn 이 함유되어 있다 .10) 혈청에는 /3-g lobu li n 과 연결되어 있으 며 /3-g lobul in 11) 은 tra nsfe r rin 과 같다고 추측되 고 있 다. 6.2 주요 기능 Mn 은 성장과 정상적인 골격구조 형성, 생식기능 및 중추신경의
정상적인 기능에 팔수적이다. in v it ro 에서 여러 효소가 Mn 에 의 해 활 성화되었는데 이 기능은 다른 2 가의 양이온들도 담당할 수 있 는 것 이 었 다. Mn2+ 은 당단백 질 (예 ; p ro t hromb i n) 의 합성 에 관 여 하는 gly c osyl tra nsfe r ase 의 활성 화에 도 개 입 한다· 포도당의 해 당과정과 Kreb's c y cle 에 Mn 이 관여하며 포도당 생합성에 관여 하는 pyru vate carboxy la se 와 mi toc hondria 의 membrane matr i x 공간에 존재 하는 sup er oxid e dis m uta s e 는 Mn 과 견고하계 결 합되 어 촌재 한다. Argi na se 는 특이 적 으로 Mn2+ 에 의 하여 활성 화된다. in vit ro 에 서 Mn2+ 과 M g 2 드온 iso c:tr a te 탈수소효소와 몇 개 의 인 산기 전이효소롤 활성화시키며 Mn2+ 은 지질의 과산화 반응을 강 력하게 억제한다. Pe pti dase 를 활성화하며 단백질을 분해한다. Leucin e 과 같은 아미 노산울 분리 시 키 는 데 Mn 이 필요하다. Mn 은 지 방산과 choleste r ol 의 합성 에 관여 하는 효소들의 구성 요소인 동 시에 촉매역할울 한다. 에너지 방출에도 필수적인 요소로서 세포내 의 mi toc hondria 의 구성 과 기 능에 Mn 이 관여 한다. 질소 배 설과 지방의 방출을 위한 뇨형성에도 Mn 이 개입한다. Mn 관여 효소로 는 혈 액 , 뼈 및 간에 촌재 하는 ph osph ata s e, argi na se, carboxy la se, cholin e ste r ase 등이 있 다. Mi toc ondria 에 서 Mn 은 주요 세 포 내 인 자로서 또한 이와 관련된 호흡효소계에서 Mn의 역할이 중요시되 고 있다 .12) Mn 의 득이 적 인 기 능으로는 연골의 mucop o lys accharid e pr ote in com p lex( p ro t ea g l y kane) 를 생 합성 하는 것 이 다. 이 때 Mn 은 효 소를 활성 화하여 UDP-N-acety ga lacto sami n 과 UDP-g lu curonate po lys accharid e 로 전환되 는데 촉매 작용을 하게 도와 주며 ga lacto - tran sfe r ase 가 g alac t ase(UDP- g alac t ose) 에 서 두 개 의 ga lacto sy l 과 1 개 의 xy lo sy l 찬기 로부터 tri s a ccharid e 를 합성 하며 이 합성 된 po lys accharid e 와 pro te i n 이 결합하여 복합체 를 이 루는데 Mn 이 관 여한다. Skin n er 는 hemog lo bin 생 성 에 Fe, Cu 이 외 에 Mn 이 있 으면 더 좋은 효과가 있다고 했는데 이것은 Mn 이 Cu 의 작용을 돕는 보조 인자라는 것을 시사한다. Mn 의 대시는 s t ress 에 의해 영향을 받으
며 glu cocorti co id 조직 내 Mn 분포에 영 향을 준다고 한다. 13) Mn meta l loenzy m es 은 제 한되 어 있 으나 glu coneog e nesis 와 glu - cose 의 이 용에 관여 한다고 한다. 14) 6.3 대 사 6.3.1 흡수와 배설 Mn 은 소장에서 흡수되며 정상적인 조건 하에서 흡수율은 약 3~ 4% 정도이다. 음식물로 섭취된 대부분의 Mn 은 다시 대변으로 배 설된다. Mn 은 쉽게 흡수되지 않으며 혈액에서 t ransman g an in이 란 득수 Mn 이동단백질과 결합된다. 결합 상태에서는 흡수가 중가 된다. 과량의 Cu 와 P 은 Mn 의 흡수를 감소시킨다. Mn 은 주로 간과 담낭을 통해 장으로 가서 대변으로 배설되는데 이때 담당이 주요 배 설경 로가 된다. 담당의 Mn 함량은 bil iru bin 의 농도와 밀접 한 관계가 있다. 수술로 담당에 구멍을 만든 쥐에게서 식이 Mn 합 량의 농도 중가에 의해서 담즙이 10 배까지 상승하는 것을 관찰할 수 있 었 으며 이 는 bil iru bin 의 농도와 비 례 하는 것 으로 보여 진다. 16) 흡수된 Mn 의 50~70% 가 담즙에 의하여 운반된다. 이와 같은 항 상성을 수행하는 데는 신생아는 어느 정도의 시일이 길리며 생취~ 약 17 일이 걸렸다 . 16) 담당 이의에 췌장도 Mn 배설에 관여한다. 성 인은 Mn 을 뇨로 매일 약 0.04~0.07mg 정도밖에 배설하지 않는 다 . 방사선 동위원소를 이용한 연구에서 닭과 흰취는 구강으로 섭 취한 Mn 이 뼈 속에 나타나지 않으며 이것은 뼈에서 Mn의 필요성 이 적다는 것을 시사한다. 사람과 개를 사용한 실험에서는 간장과 췌장이 Mn 대사에 중요한 역할울 한다고 알려져 있다 .2) 6.4 섭취량과 팔요량 성인의 balance 실험에서는 1 일 3.7~5.8m g의 Mn 을 섭취했을 때 평형을 유지했다. 하루 동안 음식물로부터 섭취되는 Mn 은 2~ 3mg 정도로 추산되었으며 채식주의자는 7mg 정도였다. 이 결과
예 의해서 사람은 하루 2~3mg 정도가 필요량이라고 추측하고 있 다. 3) 또한 Schornmuller 는 0. 02~o. d3mg / kg 체 중을 팔요량이 라 고 추정했다 .17) 그러나 Mn 의 필요량은 아직 정해져 있지 않고 있다. 전체 열량 의 40~50% 를 흰 밀가루로 섭취한 성인은 1 일 2.2~2.7m g의 Mn 울 섭취한 셈이 된다 .18) 영국사람은 겨울에 7m g /1 일률 섭취하는데 그 중 3. 3m g /1 일 홍차를 자주 마시 는 습관에 서 온다고 한다. 19) 미국의 여대생들은 3.7mg Mn 을 하루 섭취하며 그 중 0.05~0. -4 6m g /1 일 보유되었다 .20) 영국 성인의 1 일 평군 섭취량은 2.7 土 0. 85m g /1 일이며 일본인은 2.7~2.9m g /1 일이라고 보고되어 있다 .21) Schroeder 와 그의 동료동은 22) Mn 섭취가 식품의 종류와 밀접한 관계가 있으며 2,300kcal 의 고기, 생선, 유제품, 빵, 지방과 설탕 이 함유된 식이에서는 0.5mg 정도가 섭취된다고 한다. 6 개월까지의 유아는 Mn 을 2.5~7.Sm g /1 일/체중 kg Mn 을 섭취 했는데 이는 유아의 섭취석품이 우유 혹은 다른 유아식인가에 따라 사달라지 며 나이 에 따라서 도 차이 가 있 었 다. Mcleod 와 Robin s on23) 은 우유가 모유보다 2 배의 Mn 을 함유하고 크림, 탈지분유, 곡류 와 채소와 유아식에도 Mn 이 많이 함유되어 있다고 한다. 그러나 Mn 의 이용률과 체내 흡수율 등에 관하여는 정확한 연구가 없다. RDA 에 서 는 28) Mn 권장량은 아래 와 같다.
 T。 아 6 개월까지 o. 5~0. 7m g /l 일
T。 아 6 개월까지 o. 5~0. 7m g /l 일
6.5 결핍증 Mn 의 결핍중세로는 동물에게서 대개 성장부전과 골격이상, 생
직능력 처하 등을 들 수 있으며 신생아에게서는 운동실조중등을 볼 수 있다 .4) 사람의 Mn 결핍은 거의 보고되어 있지 않으나 Schroeder 와 그의 동료 22) 등은 임 신기 간중에 Mn 의 섭 취 가 적 었 을 경우 태어난 어린이들이 신경질적이었으며 성인에게서는 뼈와 연골 의 변화와 일종의 생식감되 증상이 나타났다고 한다. Mn 결핍시에 태어난 새끼는 어미젖을 빠는 능력이 부족해짐으로써 곧 사망했다. 하루 쥐 한마리당 30m g Mn 을 4 세대 동안 섭취시킨쥐는 운동실조 증과 군형장애증을 일으켰으나 해부실험으로도 그 원인을 규명해 내지 못했다. 젖먹이 동물보다 닭은 Mn 결핍시 뼈의 발육장애에 휠싼 큰 영향을 미쳤다고 하며 날개와 다리가 짧았으며 뼈의 회분 함량이 감소되었다고 한다. Mn 이 결핍된 닭이 낳은 달걀에서 부 화된 병아리는 연곧 장애현상이 나타났다. Mn 결핍시에는 골격의 유기 물질 의 mucop o lys accharid e 함량이 감소되 었 다고 한다. 25) 6.6 함유식품 전곡, 호두, 땅콩 등의 견과류, 녹색 채 소(평 군 20~30p pm 정 도) 특 히 차에 Mn 이 많이 함유되어 있고 동물성 식품 죽 고기, 생선, 우 유, 찰 정제된 전분(평균 0.2~0.5p pm ) 그리고 설탕제품 둥에는 Mn 이 적게 함유되어 있다. Mn 은 식품에 촌재하는 활성화되지 않은 효소를 활성화시켜 반응을 촉진하기도 한다. Mn 을 저장하는 박테 리아는 Fe 과 같이 수도관에 찌꺼기를 만들기도 한다. Mn 영은 식 수의 맛을 처하시키며 세탁시 얼룩을 만들기도 한다. Mn 은 양질의 달걀껍질 형성과 Ca 의 함량에 영향을 준다고 한 다 .21> Mn 을 암탉의 석이에 lOOmg / kg 체중으로 과량 주었을 때 달걀껍질에 Ca 이 높은 농도로 들어 있었고 질이 좋아졌다. 또한 이 암탉의 간, 난소세포, 경골에 Mn 이 가장 많이 함유되어 있었 다. 이와 같은 사실로 미루어 보아 식이에 Mn 을 첨가하면 OJ -닭이 달걀울 많이 생산할 수 있도록 하는 데 이롭다는 것을 추축해 낸 수 있다. 표 6.2 는 식품의 Mn 함유량이다.
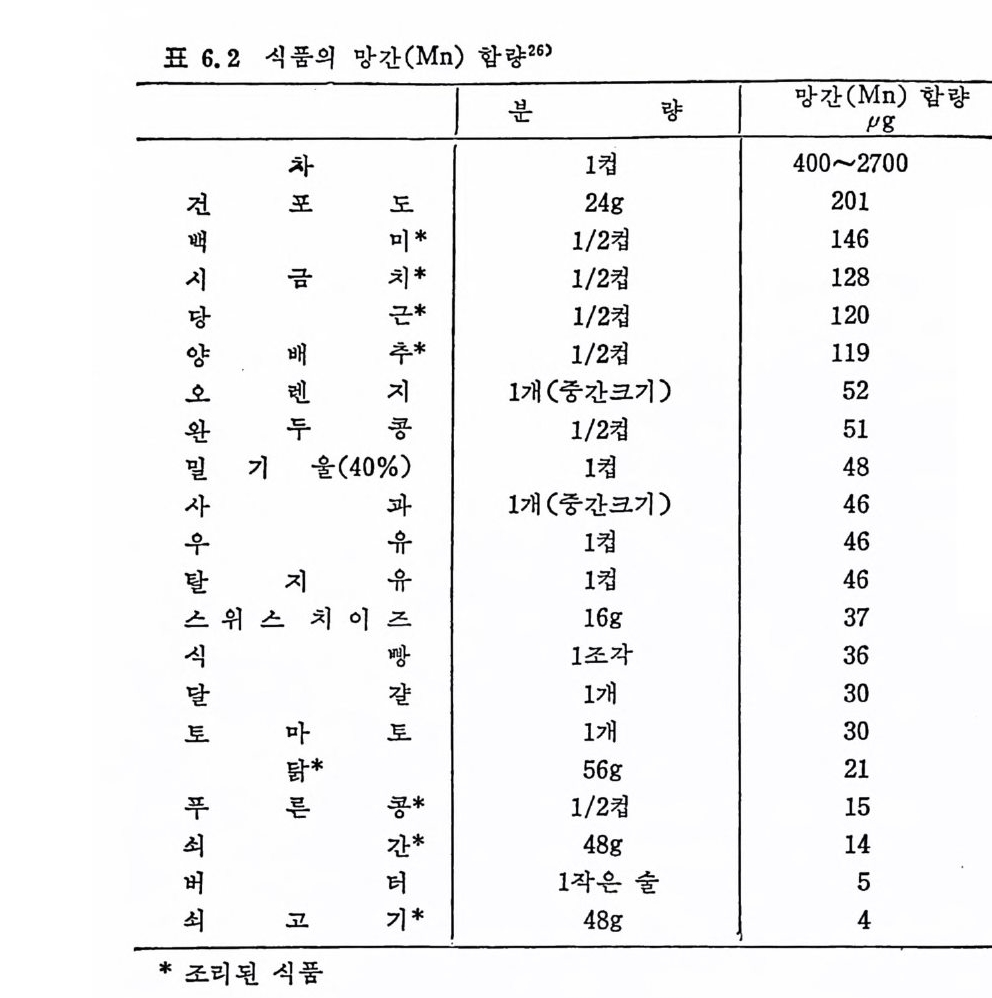 표 6. 2 식품의 망간 (Mn) 함량 26)
표 6. 2 식품의 망간 (Mn) 함량 26)
6.7 독 성 장기간 동안 과량의 Mn 을 섭취하며 높은 산 위에서 일을 하던 사람들에게서 십한 정신 이상중과 Parkin s on 질병과 같이 계속 떠 논 증상이 나타났다고 한다 .1) 이 독성은 중추신경 장애와 dop a mi n: 결핍에서 오는 이상으로 비정상적인 웃음, 울음, 기여력 상실과 언 어장애 등의 층상도 일어났다. ::::z.. 원인은 Mn 이 do p am i n 과 sero- t on in의 합성과정에 필요한 성분울 방해하는 데 있을 것이라고 추-
 측된다. Mn 은 항상성의 기능이 강하며 장기 독성은 조칙의 Mn 약
측된다. Mn 은 항상성의 기능이 강하며 장기 독성은 조칙의 Mn 약
ATW. Freis i n g -W eih e nste p h an 1978. 10) Versie c k, J. F. Barbie r , A. , Sp e eke and J. Hoste , Acta Endoc-rin ol. 76, 783, 1974. 11) Haneock, R. G. V. , D. J. R. Evans and K. Frit ze , Bi o chi m . Bi op h y s. Acta 320, 486, 1973. 12)Costa , D. and S. Mott a, Mi ne rals in Albanes A. A. ed. Newer Meth o ds of Nutr i o nal Bi o chemi st r y I, Academi c Press, New York and .l o ndon, 1963. 13) Hug h , E. R. and G. C. Cotz i a s , Am. ]. Phy si o l. , 206, 1061, 1961 . 14) Evenson, G. J. and R. E. Sharder, J. Nutr . , 94, 89, 1968. lfi) Mertz , W. , in Betk e , K. and Bidl i ng sm aie r , F. , Sp u rene/emt e in der Entw i ck lung von Mensch und Ti e r, p. 187, Urban und Sch- warzenberg, Mi lnc hen 1975. 16) Mi ller , S. T. , Cotz i a s , G. C. and Event, H. A. , Am. J. ph y si o e l. , 229, 1080, 1975. 17) Schormi llle r J. , Lehrbuch der Lebensmi ttel chemi e, zweit Aufl ag e, :Spr in g er , p. 118, 1974. 18) Kent, N. L. , and Mc Cance, R. A. , Bi o chem. J. , 35, 877, 19 45. 19) Monie r -Wi lliam s, G. W. , Trace Elements in Foods, Chap m an .an d Hall, London 1949. 20) McLeod, B. E. , and Robin s on, M. T. , Br. J. Nutr . 27, 221, 1972. 21) Murakami , Y. , Suzuki, Y. and Yamag a ta , T. , J. Radia l, Res. -6, 105, 1965. 22) Schroeder, H. A. , Balassa, J. J. and Ti pton , J. H. , J. Chron. Di s. , 19, 545, 1966. 23) Mcleod, B. E. and Robin s on, M. F. , Br. J. Nutr . , 27, 229, 1972. 24) Hi ll, R. C. and I. L. Chaik o ff , Proc. Soc. Exp, Bi o l. Med. , 91, 265, 1956. 25) Leach, R. M. jr. and A. M. Muenste r, J. Nutr i t . , 78, 51, 1962,
26) Patr i c i a , A and Kreutl e r, Nutr i t ion in per sp ec ti ve , Prenti ce Hall inc . , p, 357, 1980. 27) Panic , B. , N, Ap o sto l ow and Jav anka Knezevic , in Ki nc hg l3 ner -M. , Trace Element Meta b olis m in Man and Anim als-3, Technic h e Univ e rsit at Mi lnc hen Freis i n g ·W eih e nste p h an p. 511, 1978. 28) Food and Nutr i t ion Board, Nati on al Research Counc il, Recom mended Di et a r y Allowences. 9th ed. , Nati on al Academy of Scie n ces, Washin g ton , p. 178, 1980.
7 크롬 (Chromi um , Cr) Cr 이 쥐의 당질대사에 팔수적이라는 것은 1959 년 Schwarz 와 · Mer t z 에 의해서 보고되었다 .26) 사람에 있 어 서 는 중세 가 가벼 운 당뇨병 환자들에 게 Cr 이 glu cose· to lerance fac to r 로서 활발한 기 능이 보고된 이 후 Cr 의 생 리 적 기 능에 관십을 갖게 되었다. 7.1 체내 함량과 분포 Cr 은 극히 미량이긴 하지만 조직 내에 널리 분포되어 있다. 얼마 전까지만 해도 너무 미량이기 때문에 분석방법에 오차가 너무 커서 확실한 Cr 의 측정이 불가능했다. 최근 새로운 분석방법으로 조직과 기관 죽 간, 신장, 십장, 췌장 _ 근육에 Cr 함량은 20~30µg / kg 가량 들어 있 음이 밝혀 졌 다. 그러나 사람의 체내 Cr 함량은 주거하는 지역과 밀접한 관계가 있으며 1)2) 또한 연령이 중가함에 따라서 조칙 속에 Cr 함량이 감 소되는 것으로 나타났다.“ 동남아인은 158µg , 미국의 경우 32µ g으 로 보고되었다. 최근의 측정에서 가장 변화가 십한 것은 혈청의 Cr 함량으로 1971 년 Hamb i d g e4) 는 건강한 성 인의 혈청 에 서 Cr 을 1. 3~1. 7µg /l OOml 를 측정 하였 고 1976 년 Dois y 와 그의 동료들 5), 은 혈청 의 Cr 을 0. 16~O. l3µg /l OOml 로 보고하였 다.
3 가인 Cr 은 혈장에 서 tra nsfe r rin 인 /3-glo blin frac tion 과 결합 하여 촌재 하고, 일부는 glu cose to lerance fac to r 로 촌재 한다. 혈액의 Cr 은 조직내에 처장된 Cr 과 평형상태로 촌재하지 않기 페문에 Cr 상태 측정에 적합하지 않다. 모유의 Cr 함량은 Iµg /l OOml 로 우유의 함량과 바 슷하다. 석물의 조직에는 약 1 pp m 의 Cr 이 그리고 동물의 조직에는 1pp m 보다 적은 양이 들어 있는 것으로 보고되었다. 7.2 주요 기능 Cr 결핍시 동물의 성장이 처하되고 당질, 지질, 단백질 대사 장 애로 빨리 사망하게 되는 것을 볼 수 있다. 생화학적인 기능에 대하여는 아직까지 많이 알려져 있지 않다. Cr 의 가장 중요한 기 능은 glu cose to lerance fac to r 로서 의 작용 이다; 여기에서 3 가의 Cr 은 산화과정에 작용하여 포도당의 이용을 증진시 키 는데 ins ulin 과 함께 작용을 한다. Cr 결핍 으로 나타나는 가벼 운 giuc ose to lerance 는 구강으로 섭 취 시 킨 glu cose to lerance fa c t or 로서 다시 정상화되었다. 여기에 사용한 석품으로는 맥주 효 모, 간 그리고 콩팥이었다• in vit ro 실험 에 서 glu cose to lerance fac to r 가 ins ulin 의 최 대 효 과를 위 해 서 ins uli n sensit ive 조직 에 필요하다고 하였 다. 쥐 의 결핍 증의 하나는 glu cose to lerance 장애 였 으며 , Cr 이 in- .su li n 의 조직 반응을 용이 하게 해 주는 조직 의 ins ulin recep tor 들과 ins uli n 과 함께 세 가지 요소가 복합체 를 형 성 해 준다고 생 각했다. 6) 또한 Cr 은 ins ulin 작용을 위하여 세 포막에 있는 그의 rece ptor 의 필수보조인자라는 것도 알려쳐 있다. 그러나 Cr 의 결핍이 ins uli n 의 합성과 대사에는 지장을 주지 않았다. Cr 자체 는 ins uli n 과 같은 작용을 하지 는 않으며 ins ulin 을 대 신 해주는 물질로 생각해서는 안된다. 그 이유로는 Cr 은 내인성과 의인성 i nsu li n 이 존재하는 곳에만 작용할 수 있기 때문이다. Cr 의 작용부위로는 동물의 말초조직 을 들 수 있으며 , ins ulin 의
존재 하에 포도당의 탄소를 지 방과 탄산가스로 전환시 키 는 데 작용 하고 포도당이 세포 내로 들어가는 곳과 초산이 형성되는 곳에 Cr 의 활 성부위가 있음을 제시하였다 .3) 최 근 모르모트 실험 에 서 glu cose to lerance 와 혈 청 choleste r ol 에 영향을 주는 식이에 보충된 Cr 의 역할은 체중증가였으며 glu cose to lerance, 혈청 choleste r ol 농도에 는 큰 영 향을 주지 는 못 하였다. 입신기간 동안의 모르모트 생존에는 좋은 영향을 주었다 고 한다. 그러 나 Sta u b 동 8) 과 Schroeder 둥”은 쥐 의 hy pe rcholeste rolemi a 에 서 Cr 이 혈청 choleste r ol 을 감소시 켰 다고 서 로 상반된 견해를 보이기도 했다. 요르단과 나이지리아의 유아 영양불량중에 Cr 을 식아와 함께 섭 취 시 켰 더 니 glu cose to lerance 장애 가 치 료되 었 다. 10) 이 결과로서 Cr 이 첨가된 식이의 주요 효과는 Cr 결핍상태에서 , 초래되는 당질대사 장애를 방지하는 기능을 갖는다고 하겠다. 7.3 대 사 7.3.1 흡수와 배설 쥐의 Cr 의 주요 흡수 부위는 공장이며 그 다음이 회장과 심야 지장이고 극히 소량의 Cr 이 소화기관에서 흡수된다. Cr 은 두 가지 형태로 흡수되는데 하나는 간단한 무기물과 Cr 의 결합으로(예 ; aq u o, chloro 와 ace t o 오臣] 결합) 생리적으로 비중이 적으며 사람은 0.5~1 .0 % 정도 흡수한다. 그러나 이 양은 신장으로 배설되는 Cr 을 감안할 때 충분하지 못 하다. 이 무기 Cr 은 항상성의 조절에 관계하지 않으며 태반을 통 과하지 않는다. Insuli n 윤 필요로 하는 당뇨병 환자는 Cr 의 흡수율이 높았다. 또 다른 형 태 로는 glu cose to lerance fac to r 에 속하며 , 이 는 하나 또는 여러 개의 유사한 Cr 복합체로서 촌재하며 Cr 원자 하나에 두 개 의 nic o ti nic a cid 분자, 혹은 1 분자의 cy s te i n e , gly c in e 과 glu ta m i c ac i d 로 구성되었다 .11) 이 형태의 복합체는 Cr 을 10~25% 정도 홉-
수하며 태반에서 태아에게까지도 운반한다. Cr 은 Fe 의 운반단백 질 인 sid e rop h il in 과 혈 액 내 에 서 강하게 걷 합하여 이동되는 것으로 보이며, 조직으로의 Cr 흡수는 매우 빠르 . 고 주로 신장을 통해 배설된다고 한다 .3) 대변으로 배설되는 Cr 은 주로 홍수되지 못한 부분이 다. 매 일 배 설되 는 Cr 은 3~15µg 이 며 lµg /l OOml 뇨로 배 설한다. 최근 조사된 젊은 여성의 뇨의 Cr 양은 5.9~lOµ g /1 일이었다. Cr 과 Fe 사이 에 sid e rop h il in 에 결합하는 경 쟁 이 있 어 Cr-Fe 의 상호 관련성 연구도 아주 중요하다고 하겠다. 7.4 결핍증 Cr 은 홍수 가 찰 안되며 사용할 수 있는 양이 적고 석품에 소량 존재하기 때문에 결핍증에 걸리기가 쉽다. 특히 정제된 설탕 섭취 는 neg a ti ve balance 가 되 었 다. 사람은 극십한 Cr 결핍증으로부터 체중감소, glu cose to lerance 로 인한 말초신경 이상 증세와 당뇨병과 비슷한 증상까지도 나타낸 다. 이 중상의 원인은 말초조직의 i nsul i n 에 대한 기능감소로 보 인다. Cr 보충으로 조칙 의 ins uli n 작용울 중가시 킬 수 있 었 다. 어린이 당뇨병은 i nsu li n 의 이동이 Cr 대사의 장애로 인하여 찰 되지 않기 때문이다. Cr 의 상대를 판정하기 위해서 i nsul in이나 설탕을 섭취시킨 후 혈청이나 혈장의 Cr 을 측정했을 때 Cr 치가 급격히 상승하는 것을 보고 알 수있다. Insul i n 이 작용을 하기 위해서 체내에서는 말초조직에 Cr 공급을 높여 준다. 그 이외에 일부의 Cr 은 뇨로배설되기 때문에 설탕투여 후에 겁사를 한다. 또한 머리카락의 Cr 함량은 Cr 의 상태를 알려주는 데 좋은 지표 가된다. 임신기간중의 Cr 결핍 여성은 머리카락의 Cr 량이 750 ppb 에서
220p pb 로 감소되 었 고 임 신 36 주 후에 glu cose int o lerance 현상 이 나타났으며 대아는 모체에 처장된 Cr 을 이용한다고 했다 .l2) 신생아의 머리카락의 Cr 량은 900 pp b 이며, 2~3 세 때 그. 절반으 로 떨어진다 .l3) 요르단과 나이제리아의 영양불량중 유아에게 식이로 Cr 을 보충 해 주었 을 때 glu cose to lerance 장애 가 치 료되 었 다고 한다. 10) Cr 의 결핍증은 토끼 14), 원숭이 15> 를 대상으로 연구되었는데 쥐의 Cr 결핍 증세 로는 glu cose to lerance 장애 , 성 장장애 , 철식 에 서 오 는 저 혈 당중, 혈청 choleste r ol 농도의 중가둥을 들고 있 고 16> Cr 결 핍증의 쥐에게 5 pp m 의 Cr 을 식이에 보충한 견과 성장은 중전되 었으나 사망률 감소에는 영향을 주지 못했다. 5 pp m 의 Cr 이 함유된 식수의 실험에서 쥐의 사망률에 Cr 이 전 혀 영 향을 주지 못한 데 반하여 Pb, Cd, Ni , Ti 등은 사망률에 영 향울 주었다. l 실험적으로 Cr 결핍증을 연구하기 위하여 인위적 으로 결핍중을 야기시키기 위하여 주로 식이에 많은 양의 서당과 to rula ye ast 를 사용했다(예 ; 50% 서 당, 30% to rula ye ast, 15% 돼지기름, 5% 무기염 혼합+비타민 ).18) 7.5 섭취량과 팔요량 Cr 의 생리학적 작용에 대해서는 많이 연구되어졌으나 6) 사람에 있어서의 필요량과 식품에 함유되어 있는 Cr 의 체내에서의 대사작 용과 Cr 의 형태오더 관계에 대해서는 아직까지 확실하게 알려쳐 있지 않다. 식품에 존재하는 Cr 의 흡수율은 일정하지 않고 또한 당질에 의 해서 많이 영향을 받기 때문에 매일 Cr 의 필요량은 수십에서 수백 µg까지 나타났다. 11) 식품에 함유되어 섭취되는 Cr 의 양은 하루 5~200µ g까지 차이가 있으며 생리적 이용률은 식품에 함유된 Cr 의 양과는 관계가 적다. 철대적으로 성인에게 필요하고 흡수되는 Cr 의 양은 10~15µ g이며 도한 이것은 하루의 배설량이다 .19)
J ee j eebho y는 정맥으로 1 일 20µ g의 Cr 을 두여한 결과 Cr 의 상 테는 만족스러웠다고 보고하고 있다 .27) Cr 흡수율은 CrC13 • 6H20 의 형태일 때가 Cr 원소 형태보다 1% 정 도 적 게 흡수가 되 었 으며 glu cose to lerance factor (G. T. F. )는 10 ~25% 였다. 그러 므로 Cr 의 필요량은 Cr chlorid e 형 태 로면 lOOµg 이 고 Cr 원 소의 형 태 로는 40~lOOµg 정 도로 본다. 모든 접 을 고려 한다면 Cr 의 섭취는 식이의 형태에 따라서 영향을 받기 때문에 5~400µ g /l 일 로 달라진다. WHO 의 연구에 따르면 32) 사람에게 0.002mg / kg 체중의 Cr 을 섭 취 시 켰 을 때 Cr 이 얼마간 보유되 었 다고 하며 En g el33) 과 Robin s onm 의 연구에서는 성인에게 0.1mg Cr 을 섭취시켰을때 neg a ti ve ba- lance 가 관찰되 었 다. 이 와 같은 결과에 서 1980 년도 RDA35) 에 서 는 1 일 Cr 울 다음과 같이 권장하고 있다.
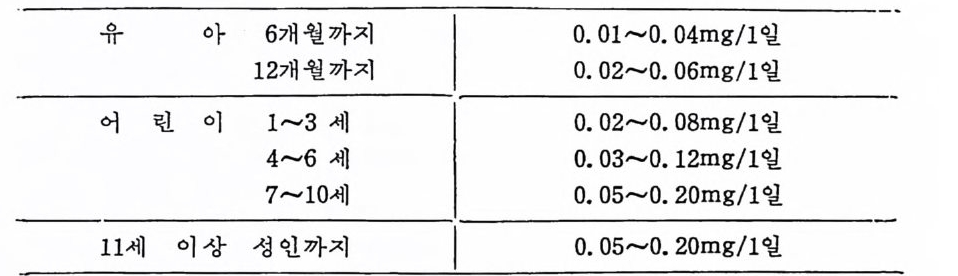 기。 아 6 개월까지 0. 01~0. 04m g /I 일
기。 아 6 개월까지 0. 01~0. 04m g /I 일
그러나 정확한 Cr 의 필요량 결정은 G.T.F 와 정확한 분석방법 이 연구되었을 때 가능할 것이다. 7.6 함유식품 육류, 달걀, 버 터 , 치 츠 그리 고 마아가린은 약 100~300µg / kg 을 함유하며 Cr 의 함유량은 지역에 따라 큰 차이가 있다. 또한 맥주 ye ast, 송아지 간, 엿기름과 꿀에는 Cr 이 많이 들어 있고 생선, 버섯, 닭고기, 우유와 빵에는 Cr 이 적게 들어 있다.
녹색식물에 함유된 Cr 은 생리적으로 활성화되지 못하여 설탕은 Cr 을 아주 적게 함유할 분 아니라 이용하기 어려운 형태이다. 표 7.1 은 식 품의 Cr 함량을 나타내 고 있 다. 28)29)30)31 )
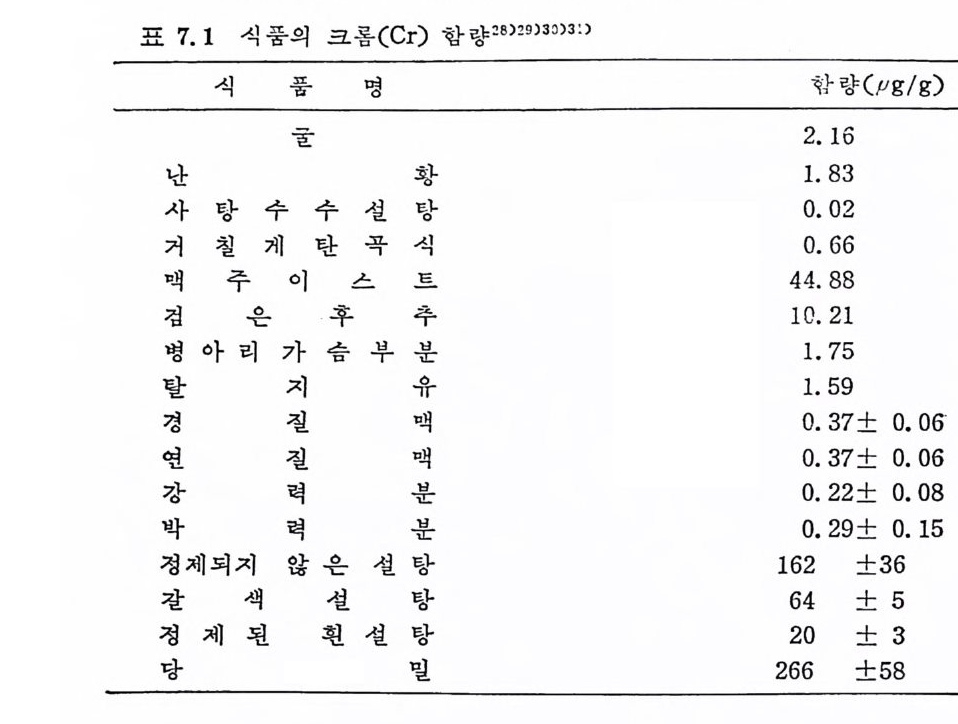 표 7.1 식 품의 크롬 (Cr) 함량 28)2 9 )3 3 )3 : )
표 7.1 식 품의 크롬 (Cr) 함량 28)2 9 )3 3 )3 : )
7.7 독 入J 독성 문제가 되는 것은 6 가의 Cr 이며 3 가의 Cr 은 거의 흡수되자 않기 때문에 독성이 문제시되지 않는다. 동물실험에서 장기간 석이 1k g당 2 g의 Cr 아를 섭취시켰으나홉· 수가 찰되지 않아서 독성이 없었으며 1000mg Cr3+/1 일은 고양이 에게서 역시 독성의 효과를 보지 못했다 .32) 그詩 반대로 쥐에게 50 pp m 의 Cr 을 chroma t e 형태로 섭취시 켰을 때 성장정지와 간과 신장의 장애 그리고 페암현상 둥이 일어 났다. 36)37 ) 정 백 두입 한 쥐 의 LD50( 반 치 사량)은 0. 01~O. 03µg / kg;
체 중으로 나타났다. 38) 또 다른 실험에서도 쥐에게 Cr3+ 로 장기 독성실험을 하였을 때 쥐의 각 기관은 Cr 이 10 배로 상승했다(간 3.2, 뼈 8.7, 신장 10. 5 그리 고 비 장은 25. 5p pm /fr es h weig h t 21 )). 개 에 게 4 년에 걸쳐 음료수에 l l. 2 pp m 의 Cr 을 섭취시켰으나 독성이 없었다 .22) 그러나 사람의 경우는 약 30 년 전부터 chromate -worker 들에게 호흡기 암이 자주 발병 하는 것 을 볼 수 있 었 다. 23) 그러 므로 chromate 는 조직 암의 발병원인으로 보고 있으며 쥐에게 chroma t e 로서 암 울 발병케 하려고 시도했으나 성공하지는 못한 단계이다 .24) 그러나 다른 금속과 마찬가지로 Cr 이 암의 직접적인 원인여부에 대해서는 아직 확실하게 규명되지 않았다 .25) Cr 의 급성 독성현상온 산화로부터 발생한다. 사람에 있어서 급 · 성독성을 유발하는 양은 약 lg 정도이다. 급성과 만성의 독성에서는 간장기관의 퀘양이나 변성의 증상을 나타낸다. 특히 간과 신장과 같은 유조직에 독성중상이 나타난다. 장기 간 chromate 를 식 수에 첨 가했을 때 실현 동물의 no eff ect level. 은 0. 15~lmg / kg 체 중이 었 다. 이 양은 안전요소 1/100 을 사람에 게 적 용시 키 면 매 일 2. 5~IOµg Cr6+/kg 체중이 허용될 수 있는 양이며 1 일 실제 섭취량의 2 배 이다. 이와 같은 결과는 국민건강의 안전성을 위하여 대략 정해 놓은 것 이며 위의 결과로 Cr 을 치료제로 사용할 때는 하루의 필요량보다 훨씬 더 많은 양이 사용된다는 것을 알 수 있다. *참고문헌 1) Tip ton , I. H. and M. J. _Co ok, Trace Elements in Human Ti ss ues II. Healt h, Phys . , 9, 103, 1963. 2) Ti pton , I. H. , H. A. Schreder, H. M. Perry and M. J. Cook, Trace-
-i!le ments in Human Ti ss ues IV. Healt h. Plzy s. , 11, 403, 1965. 3) Mertz , W. , Bi o log ica l Role of Clzromi ttm , Fed. Proc. , 26, i8 6, 1966. 4) Hambid g e, K. M. , in Mertz , W. and Cornatz e , W. E. , Newer Trace Elements in Nutr i t ion, p. 169, Dekker, New York, 1917. 5) Dais y , R. J. , Str e ete n , D. H. P. , Freib e rg, J. M. and Schneid e r. .A . J. , in Presad, A. S. , Trace Elements in Human Heath and Di se ase, Vol. Il, p. 79, Academi c Press, New York, 1976. 6) Mertz , W. , E. W. Toep fer, E. E. Rog ins ki and M. M. Polansky , Present Knowledg e of tlz e Role of Chromi u m, Fed. Proc. 33, 2275, 1974. 7) Presto n, A. M. , R. P. Dowdy , M. A. Presto n and J. N. Freeman, J. Nutr . , 106, 1391, 1976. 8) Sta u b, H. W. , G. Reussner and R. Thie s sen, Scie n ce, 166, 746, 1969. 9) Schroeder, H. A. , A. P. Nason and I. H. Ti ption , ]. Chrom. D1'.s. , ·23 , 123, 1970. 10) Gli ns mam, W. H. and W. Mertz , Ef feet of Triv alent, Cl in. Exp. , 15, 510, 1966. 11) Mert z, W. , in Betk e, K. and Bid l i ng s maie r , F. , Sp u renelemente .,.n der Entw i c klung von Mensch und Ti e r, p. 187, Urban und Sch- 'Wa rzenberg, Mi lnc hen. 1975. 12) Burt, R. L. and I. W. F. David s on, Acta Di ah et. Lat. , 10, 770, 1973. 13) Hambid g e, K. M. and Baum, J. D. , Am. ]. Cl in. Nutr . , 25, .37 6, 1972. 14) Mertz , W. , E. E. Rog ins ki and H. A. Schoreader, J. Nutr . , 86, ]07, 1965. 15) David s on, I. W. F. and W. L. -B lackwall, Proc. Soc. Exp . Bi ol . Med. , 121, 66, 1968. 16) Schroeder, H. A. , Am. ]. Cl in. Nutr . , 21, 230, 1968. 17) Barkhan, P. and A. Bellas, Natu re, 200, 141, 1963. 18) Schwarz, K. and W. Mertz , Arch. Bi o chem. Bi op h y s. , 85, 292,
1959. 19) Mertz W. , in E. Gladtk e , G. Heim ann and I. Eckert, Sp u ren- elements , Georg Ti h eme Verlag, St u tt ga rt. 1979. 20) Underwood, E. J. , Trace Elements in Human and Ani m al Nutr i - tion , 4th ed. , Acadmi c Press Inc. , New York and London, 1972. an2d1 )R .M Fa. ckLeannzgi eh ,a mR,. DA. r,c hR.. UIn. dBusyter r. ruHme,a lt Ch. F18. , D2e3c2,k e1r,9 58C. . A. Hop pe rt 22) Al fers , D. H. , S. W. Lee and L. V. Avio l i, Gastr o ente r ol. 62, 559, 1972. 23) Baetj er , A. M. , Arch. Industr . Hy g. 2, 487, 1950. 24) Huep e r, W. C. and W. W. Pay n e, Arch. Envir o nm. Healt h, 5, 1962, 445. 25) Luckey , T. D. and B. Venng o p a l, Plenum Press, New York ana London, 1977. 26) Schwarz, K. and Metz , W. Arch. Bi o clt em . Bi op h y s. , 85, 292, 1959. 27) Jee je e bhoy , K. N. Sub, R. Marlis s, E. B. , Greenburg, G. R. and· Bruce-Roberts o n. A. , Cl in. Res. , 23, 636A, 1975. 28) Zook, E. G. , Greene, F. E. and Morris , E. R. , Cereal Chem. , 47, 720, 1970. 29) Welch, R. M. and Canry, E. E, Ag r ic . Food Chem. , 23, 479,. 1975. 30) Masir o ni, R. , Wolf, W. and Mertz , W. , Bull, WHO 49, 322, 1973. 31 ) Gl ins mana, W. H, Feldmann, F. J. and Mertz , W. , Scie n ce 152,. 1243, 1966. 32) WHO, Rep o rt of a WHO Exp e rt Comi ttee , WHO Tech. Rept . Ser. No. 532, WHO, Geneva, p. 65, 1973. 33) Eng e l, R. W. , N. 0. Pric e and R. E. Mi ller , J. Nutr . , 92, 197, 1967. 34) Robin son M. F. , J. M. Mckenzie , C. D. Thomson and A. L. Van, Ri j, Br. J. Nr ttr. 30, 195, 1973. 35) Food and Nutr i t ion Board, Nati on al Research Council , Recommende< l
.Dieta r y Allomances, 9th ed. Nati on al Academy of Scie n ce, Washin g ton , D. C. , p. 164, 1980. 36) Brin t o n , H. P. , Frais e r, E. S. and Koven, A. L. , Publi c Healt h Rep. , 67, 835, 1952. 37) Ki rk p at r i c k , D. C. and Coff in, D. E. , ]. Sci. Food Ag r ic . , 26, ·99 , 1975. 38) Ki rc hg e Bner, M. , E. Weig a nd, A. Schneg g, E. GraBmann, F. J. Schwarz and H. -P. Roth , in Cremer, H. D. , D. Hotz e ! and J. Kuhnau, Bi oc lzemi e und Plzy si o l osie der Ernii hr rmg , Bd. I, Tei! . 2, p. 288, 1980.
8 셀레 늄 (Selen i um, Se) Se 은 1817 년 Bercel i us 에 의해서 발견되었으며 자연계에 유황과 함께 존재하는데 Se:S 의 비율은 1 : 6000 으로서 무기물로서는 아주 져온 양이다 .1) 대기중의 Se 평균치는 0.09 pp m 이며안 석물의 Se 함유량은 식 물의 종류와 토양에 따라 영 향을 받는다 (0. 007~10000 ppm ). 특수한 식물은 성장과정중에 특히 Se 을 필요로 하는데 Se 이 축 적되면 이것을 섭취하는 가축이 독성현상을 일으키기도 한다. 1930 년 미국의 대초원 지대의 가축들이
8.1 체내 함량과 분포 인체 는 Se 을 10~15mg 함유하는데 이 양온 약 0. 15~0. 2pp m- 이다. 간과 신장에 가장 많은 양이 촌재하며 혈액, 근육, 뼈에는 ` 소량 함유되어 있다. 그러나 각 기관마다의 함유량에는 차이가 있 는데 그 원인으로는 대기 속에 함유된 Se 의 양에 영향을 받기 때 문이다. 혈청과 혈액의 Se 농도는 연령과 관계가 있는데 동일한 양 울 섭취하여도 연령이 중가할수록 Se 농도는 중가한다 .6) 혈청의 Se 량은 신생 아는 5µg /1 00ml, 유아는 3. 4µg /1 00ml 의 낮은 수치 이 나 성 인이 되 면 10. 2µg /1 00ml 로 상승한다. 6) Lombeck 은 건강한 어린이의 Se 농도가 나이에 따라 달라침을 보고하였다.” Se 함유량이 가장 낮을 때는 유아 3 개월까지였으 며 적 혈구의 glu ta t h io n e pe roxid a se 의 활성 도 낮았다. 시 중에 서 판매되고 있는 모유화된 분유를 섭취한 유아는 모유를 섭취하는 유 아와 비교할 때 Se 함유량이 33% 정도에 불과하였다. Pheny lk eto nuria 와 map le sy r up urin e dis e ase 의 환자에 게 Se. 석이로 치료를 시켰을 때 10~12 주 후의 혈청 Se 함량은 정상보다 20% 낮았으며 적혈구의 glu ta th io n e p erox i dase 의 활성은 정상보 다 50% 낮았다. 전체 혈액과 머리카락의 Se 함유량도 역시 정상보 . 다 20% 낮았다. 그림 8.1 은 건강한 어 린이 들의 혈청 Se 농도이 다. 7) 태아기 혈액의 혈청 Se 농도는 50X10-9 g /ml 로서 성인의 50% 이 며 (성 인은 102 X IQ- 9g /m l ), 유아기 때 는 58 X 10-9g /m l, 유치 원 어 린이의 경우 82X10-9g / ml, 학생은 92X10-9 g /ml 로 접접 증가한 다. 가장 낮을 때는 생후 4 개월경으로 34X10-9 g /ml 를 나타낸다. 그림 8. 2 는 건강한 어 린이 와 식 이 로 치 료한 ph eny lk eto nuria . (PKU) 또는 map le sy r up urin e dis e ase (MSUD) 환자들의 적 혈구 에 있는 glu ta t h io n e pe roxid a se 활성 이 다. Pheny lk eto nuria , 췌장암, 위암, 장암, 그리고 간경변증, 간염, mapl e sy r up ur ine dis e ase 는 혈액 의 Se 함유량이 0. 2µg / ml 까지 ;
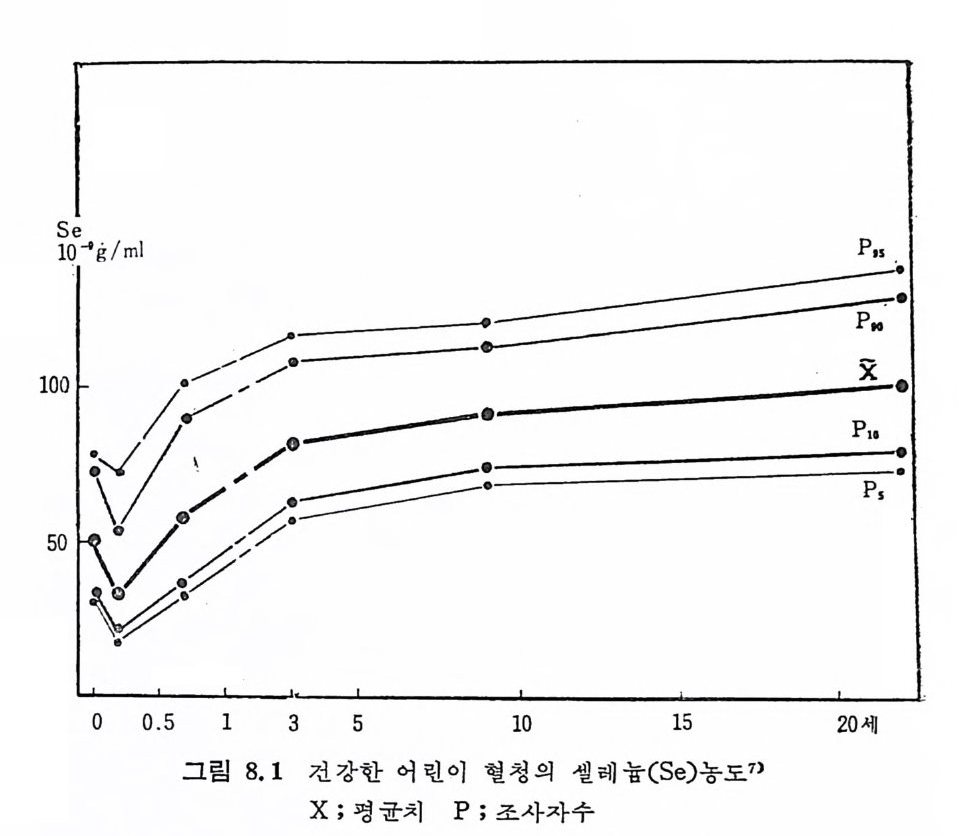 1S0e - tg / m l P,J
1S0e - tg / m l P,J
감소됨 을 알 수 있 다. 5> Map le sy ru p urin e dis e ase 를 갖고 있 는 환자 의 혈청 Se 함유량은 식이요법이 10~12 주 동안 실시될 때는 정상보 다 20% 정도 감소되었으며 전체 혈액의 Se 함량과 머리카락의 Se 함량도 감소되었고 혈청의 Se 함량이 제일 현저하게 감소되었다 .9) · 임선한 쥐오1- 수유하는 쥐의 Se 함유량은 임신 20 일째에 피와 간 에서 줄어들었고 수유 25 일째에는 신장, 비장, 간, 흉선에서 감소 되었다. 특히 임신 때보다는 수유시에 새끼에게 더 많이 전달되었 다 .10) Robin s on 은 뉴질랜드 사람의 전체 Se 함유량이 6mg (4 . 7~8. 7mg } 이며, 미국인은 13~20m g이라고 했다 .6) 표 8. 1 은 뉴질 랜드인의 혈 액 의 Se 농도와 glu ta t h io n e pe roxid a se.
 U._ 1 /H• 안\o b i•
U._ 1 /H• 안\o b i•
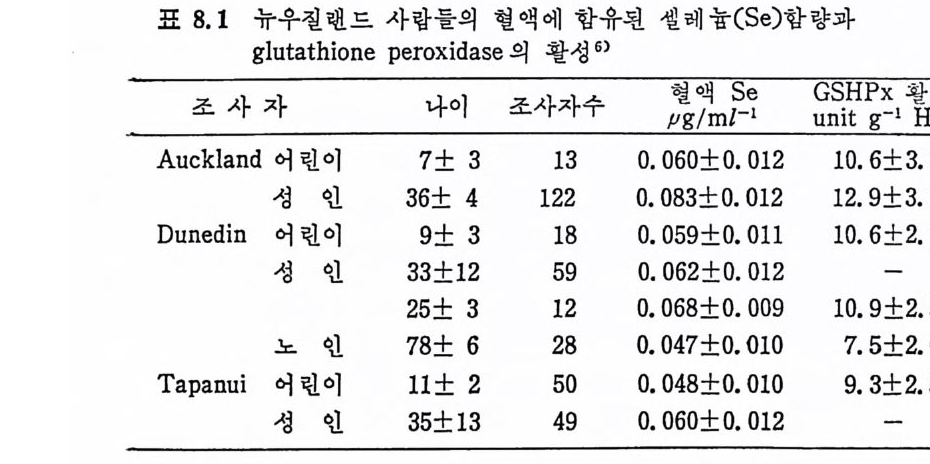 표 8.1 뉴우질렌드 사람들의 혈액에 합유된 셀레늄 (Se) 함량과
표 8.1 뉴우질렌드 사람들의 혈액에 합유된 셀레늄 (Se) 함량과
활성을 나타낸 것이다. Se 이 부족한 뉴우질렌드와 북아대리카 성인들의 Se 식이 섭취량 과 혈액과의 관계를 살펴보면 하루 56µ g /l 일 ll) Se 을 섭취하는 뉴 우질렌드 성인들의 혈액 Se 함유량은 6.8µ g /100ml 이었으며 12) 캐나 다의 13) Se 1 일 섭 취 량이 113~219µg 일 때 혈액 의 Se 함유량은 18. 2µg /l OOml 였다 .14) 타일랜드 15) 오} 과데 말라 16) 의 kwashio r kor 환 자들에게서도 혈액의 Se 농도 감소중세가 나타났다. 8.2 주요 기능과 결핍증 Se 결핍은 지금까지 동물에게서 많이 찾아볼 수 있었는데 성장 장애, 임신장애, 간경변증, 근육장애, 만성 간기능장애, 닭과 칠면 조의 삼출성질병, 혹은 Se 과 vit am i n E 의 부족이 병행되었을 때 나타났다. Se 결핍증은 동물의 종류에 따라 크게 차이가 있음이 알려졌다 .1 7) 쥐가 Se 결핍시 간경변증으로 22 일 만에 사망한 데 비해서 양, 송 아지, 말 둥은 근육장애롤 일으켰다 .4) Se 결핍시 어린동물들이 영향 을 받았으며 소류는 단백질 결핍증과 근육장애 현상을 나타냈다. 양 은· 불임중에 결렀으며 어린 돼지의 경우 그 어미에게 Se 이 결핍된 식이를 섭취시켰을 때 1 주일만에 사망했다. 득히 Se 이 부족한 토 양의 지역(뉴질렌드, 스칸디나비아 반도)에서는 가축들의 사망률이 높았는데 원인이 Se 부족 때문인 것을 밝혀내고 Se 을 보충시켜 주었을 때 사망률이 감소되었다. 원숭이에게서는 Se 이 부족된 식. 이에 vit am i n E 를 충분히 섭취시켰음에도 불구하고 Se 결핍증이 나타났다. 중상으로는 초기에는 불안정한 느낌을 주며 체중 감소, 원형탈모증을 나타냈다. 그 후 간의 손상과 근육장애, 십장과 근육 에도 이상을 초래하였다 .18) 이와 같은 중상온 많은 동물에게서 관 찰되었으나 사람에 관한 결핍증상은 아직 알려져 있지 않으며 Se 측 정결과도 아주 미비한 실정이다. 단백질 결핍증인 어린아이들에게 Se 을 보충해 주었을 때 성장이 축전되었으며 적혈구내에 있는 Se 의 양도 역시 중가했다. 최근에
는 Se 은 항암제로서 연구되어지고 있다. 그러나 항암제로서의 Se 의 ’ 효과는 Se 결핍이나 화학적, 세포학적 원인에 의해서 작용하는 것 이 아니고 암 초기 단계에 항암작용을 촉진시켜 주는 데 있다고 알 려졌다 .19) 조직의 Se 은 단백질과 관련되어 있는데 사람에 있어서는 he- mo g lob in과 혈장단백질의 결합형태로 촌재한다. 또한 Se 은 무기 물과 함께 단백질에 들어 있는 것도 있다. 그러므로 암환자에게 selen it e 를 주사한 후 몇 시간 경과 후에 Se 이 혈장 지단백질의 합 성에 사용된다는 것을 알 수 있었다 .8) 양의 심장과 근육에서 Se 과 결합된 분자량이 10,000 인 단백질을 추출해 냈는데 이 결합물은 Se 결핍시는 찾아볼 수가 없었다 .20) Se 의 가장 중요한 기능은 효소의 구성 성분이다. Se 은 사람과· 동물의 적혈구 안에 있는 glu ta t h io n e p erox i dase(GSH) 의 구성 성분 임이 밝혀졌다 .21) Se 결핍시 이 효소의 활성도가 급격히 감소하는 현상이 나타났다. 이 효소는 적혈구의 막과 제포막을 과산화물로부 터 보호해 주기 때문에 이 효소의 부족시는 세포막의 장애를 초래 한다; 면양의 적혈구 세포로부터 분리된 glu ta t h io n e p erox i dase 는 · 약 84, 000 의 분자량을 가졌 다. 이 효소는 그 분자량이 대 략 21, 000 인 단백 질 분자 단위 당 1 원자의 Se 울 함유한다 (0. 34% 의 Se). 또한 이 효소는 환원된 glu ta t h io n e 을 산화형 으로 전환시 키 는 것 을 촉매 한다. 2GSH( 환원된 glu ta t h i o n e) + ROOH--+GSSG( 산화된 glu ta t h io n e) + ROH +H20 산화된 glu ta th io ne 은 glu ta th io ne reducta se 의 활성 에 의 하 · 여 재생된다.
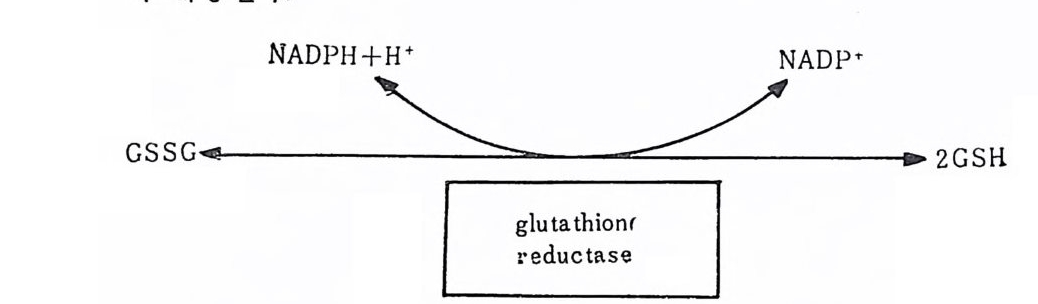 GSSG ◄ NADPH-+W \/NA DP• •ZGSH
GSSG ◄ NADPH-+W \/NA DP• •ZGSH
Se 은 면 역 기 작, ubiq u in o ne 생 합성 및 mi toc hondria 의 ATP 생 합성을 포함한 여러 가지 기타 중요한 생물학적 과정에 쓰여지는 것 이 근래 에 알려 졌 다. 22) Glut a th io n e pe roxid a se 이 의 에 동물조직 온 함유황 ami no ac id 와 유사한 Se 단백 질을 함유한다. 어 란 동물 에게 Se 이 충분한 식이로부터 결핍된 석이로 교체시키면 조직으로 부터 Se 의 급격 한 손실 과 조직 내 glu t a th io n e pe roxid ase 활성 의 급격한 감소를 초래한다. 석이적으로 유발된 동물 질병의 일부는 Se 또는 vi tam i n E 에 민 감하기 때문에 이들 두 개의 영양소간에 밀접한 관계가 있음을 시 사해 준다. 그러나 일부 질병은 이들이 2 개가 아니라 1 개의 영 양소에 득이적으로 반응하는 결과에서 초래된다. 또한 Schwarz 와 .Fo ltz 는 간경 변증에 cy st i ne (Facto r 1), vi tam i n E(Facto r 2), 및 Se ·(F acto r 3) 의 세 가지가 함께 작용하는 것을 알게 되었다. 대부분 초 기 연구에서는 s9) Se 이 vit am i n E 의 절약작용을 한다고 알려졌으 러 Se 과 a - t oco p herol 의 작용이 어떤 유사성이 있다고 믿었다. 그 러나 그 후 1974 년에 Oma y e23) 는 지질의 과산화작용의 방지에 glu - ·ta t h i o n e pe roxid a se sy s te m 이 관여 하며 vi tam i n E 와 Se 의 지 질 의 항산화 작용의 서로 다론 기전율 보여주었다(그립 8.3).
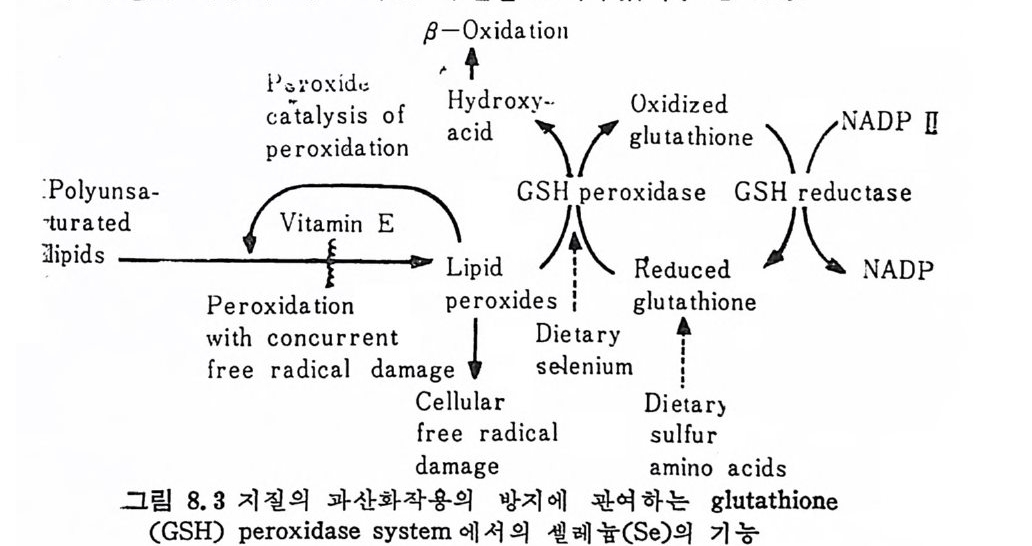 길Ilola `oo1yx x Iisdd I`a s; t I:: g—t aH CO4yl x ;id ra oti onx \/ gO1XU Idt a \\\:ne \ (NADP I!
길Ilola `oo1yx x Iisdd I`a s; t I:: g—t aH CO4yl x ;id ra oti onx \/ gO1XU Idt a \\\:ne \ (NADP I!
Vi tam i n E 가 세 포내 불포화 지 방산의 pe roxid a ti on 에 서 chain : reacti on 을 방지 하여 pe roxid e 형 성 을 처 지 하는 역 할을 하는 데 비 해 서 Se 은 GSH-pe roxid a se 의 구성 요소로서 이 미 형 성 되 어 진 지 질 의 과산화물을 제거해 주는 과정에 관여한다고 한다. Combes 와 Sco tt 24) 는 병 아리 에 대 한 Se 과 a-to cop h erol 기 능이 미 치 는 eth oxy qu in i n , &scorbic ac id, vit am i n A 의 역 할을 연구 하였는데 이 들 항산화제 들은 a-to cop h erol 결핍 인 병 아리 의 사망률 과 상출성 소질 (exudati ve d i a t hes i s) 의 방지 및 성 장에 필요한 Se 량 울감소해 주었다. 쥐 의 소화기 관에 서 GSH-p e roxid a se 에 대 한 Se 과 vit am i n E 의 식이내 p erox i dase 의 관계를 보면, Se 과 vit am i n E 가 적당량 공 급된 식이에 산화된 옥수수 기름을 첨가해 주었을 때 쥐의 위장에 있는 장접막에 GSH- p erox i dase 의 활성도를 증가시켜 주었다 .25),26) 쥐에 있어서 성장과 식이 이용률에 미치는 Se 의 영향은 Se 보충으 로 성장이 빨라지고 그와 비례해서 섭취량도 많아져서 열량도 중가 했다. 또한 Se 의 섭취량의 중가에 따라서 단백질 질소의 소화율도 . 중가되었다고 한다. Se 결핍시 식이섭취처하, 성장속도감소, 조 칙의 합성 및 성장호르몬 합성의 제한이 나타났으며 Se 보충시 위 의 중상등이 다시 정상으로 되거나 또는 촉진되었다고 한다. 그러 므로 Se 은 식욕조철과 단백질 소화율, 죽 단백질 소화효소의 생 성을 유지시키는 기능이 있음을 알려주었다. Se 은 Hg 와 Pb 의 독성 을 감소시 켜 준다고 한다. 27)28) 반대 로 . Se 결핍시 Pb 의 첨가는 Se 결핍을 더욱 악화시켰으며 더우기 Se 조 직의 분포에 영향을 주었다 .29) 양에게 Se 결핍울 야기시킨 후 식이에 30~60p pm 정도 Se 을 첨 가시켰을 때 (Sod i um selen it e) 이 결핍중상을 치료하는 데 효과적이었 다 .30) 8.3 대 사 Se 은 십이지장에서 홉수되는데 Se 의 형태에 따라서 영향을 받는-
다. Selenometh io n in e 은 meth io n in e 과 유사하게 흡수된다. Se 독성 실험 에 서 석 품에 함유된 Se- 영 은 흡수 속도가 빠르며 selenid e 는 아주 적게 홈수된다. 사람의 Se 흡수기작에 대해서는 거의 연구가 되어 있지 않은 상태이며 최근 selen it e 가 쥐와 마찬가지로 90% 정 도가 홈수된다고 보고되어졌다 .31) 그러나 과거의 실험에서는 사람 의 Se 흡수량은 아주 적다고했다. Se 는 그의 절반이 신장을 통해 서 배설되며 나머지의 양온 담당, 췌장 그리고 장의 내인성 분비선 에 의해 배설된다. 쥐 의 소변에 서 는 tri m eth y ls elenQ n iu m i on 의 형 태 를 가장 많이 볼 수 있 고 Se-meth io n in e 의 대 사산물과 아직 까지 그 형 태 가 규명 되 지 않은 또 다른 구조물이 함유되어 있음을 알 수 있다. 항상성 대사조철은 뇨의 배설에 의해서 수행되어진다고 생각되고 있다. 과량의 Se 을 섭취했을 경우 d i me t h y lselen i de 로서 허파로 배 설된다. AS 는 Se 이 담낭에 배설되는데 축전제 역할울 한다. 대 사회 로를 보기 위해 서 방사성 동위원소 75Se-S e nit e 를 주사한 결과 흡수된 75Se 은 제일 먼저 album i n 과 결합되었으며 그 다음 /3-와 7- g lobu li n 과 결합되었다. 그의 섭취와 기관의 분포는 to co- p herol 의 섭취와는 관계가 없었다 .32) 쥐 에 게 75Se-Selenit e 를 주사한 48 시 간 후에 65. 5% 가 뇨, 10. 5% 가 대변, 그리고 7.5% 가 호흡으로 전체 83.5% 가 배설되었다 .33) 기관으로서 쥐의 간에는 주사 24 시간 후에 2.7% 가 세포핵에, 31 . 0% 가 mi toc hondria 에 , 8. 9% 가 mi cro some 에 그리 고 54. 6% 가 피하조직에서 발견되었다 .34) Se 은 주사 후 제일 먼저 mi cr osome 에 운반되고 다시 단백질과 결합되어 다론 세포조직에 운반되어전 다. 35) Se 은 두 종류로 배 설되 는데 그 중 하나는
흡수율은 44~70% 였으며 첫주에 14~20% 정도 홉수했던 Se 이 뇨로 배설되었다. 호훈으로서의 배출량은 극미량이었으며 피부를 동한 배출은 볼 수가 없었다. 체내 75Se 의 반감기는 96~114 일이었다. 가장 빨리 75Se 농도가 감소되는 곳은 간, 십장, 그리고 혈장이었으며 근육과 골격이 그 . 속도가 가장느렸다. Se 은 체 내 에 서 유황대 신 cy s ti ne 이 나 meth io n in e 에 합성 되 었 으 며 단백 질 , 지 단백 질 , cy toc hrome 둥과 mercap tur ic acid ( bromben- -z ol) 을 섭취시켰을 때에도 결합되었다. Se 과 결합되어 있는 효소 (예 ; aldolase) 와 my o sin 은 위 의 pr ote i n 의 생 리 학적 활성 도에 영 향을 받지 않았다. 38) Se 은 머리카락에도 처장되는데 Se 의 섭취량과 머리카락의 Se 함유량과는 바 례 하지 않았다. 쥐 의 간세 포에 는 3 가지 형 태 의 Se 이 촌재 하는데 selenid e , sele- 11i te 그리 고 selenate 였 다. Selenid e 가 acti ve fo rm39) 이 며 이 는 to- cop herol 의 섭취상태와 전체 Se 의 양에 의해서 영향을 받는다. 쥐 에 서 A 압 은 toc op h erol 이 부족시 독성 현상을 초래 하는데 간의 전 체 Se 량과 selenid e 의 양을 감소시 킨다. 75Se-selenit e, 75Se-m eth i o n in e 의 형 태 로 섭 취 된 40~60% Se 은 (CH3)2Se 형 태 로 호흡기 로 배 설되 었 다. 40) 뇨에 서 는 tri m eth y ls eleni-
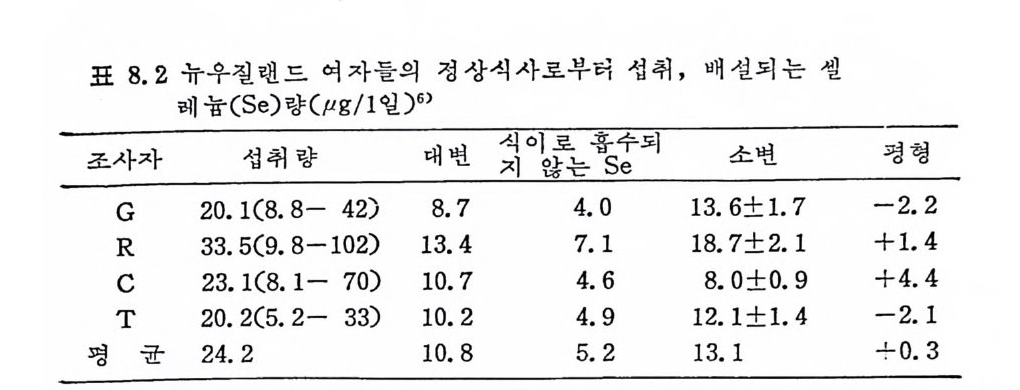 표 8.2 뉴우질랜드 여자 들 의 정상식사로부터 섭취, 배 설 되는 셀
표 8.2 뉴우질랜드 여자 들 의 정상식사로부터 섭취, 배 설 되는 셀
Theodora4” 는 미 국의 콜로라도에 서 음료수에 Se 함량과 그 음료 · 수를 섭취하는 사람들의 뇨로 배설되는 Se 의 양을 측정했다. Se 이 많이 함유된 음료수는 50~I25µg / l 이 었으며 Se 이 적 게 들어 있는 지 역 은 l7µg / l 이 었 다. 평 군 뇨의 배 설 량은 77 土 4lµg / I(l O~ 23lµg /l ) 였다. Se 이 많이 함유된 음료수를 마시는 군은 뇨로 배설하는 Se 의 양도 많았으며 반대로 Se 이 적은 음료수를 섭취할 때는 뇨의 배 설량도적었다. 8.4 섭취량과 필요량 사람의 Se 섭취량은 5~220µ g /1 일이며 지역에 따라서 크게 달라 진다. 캐나다에서는 1 일 Se 섭취량을 113~220µ g으로 보고하고 있 으며 13) 뉴질렌드 사람들은 1 일 5~102µ g의 Se 을 섭 취 한다고 한다. 6) 그리고 미국의 성인들의 1 일 Se 섭취량은 50~200µg 정도이다. RDA 에 서 의 권장량은 다음과 같다. 36)
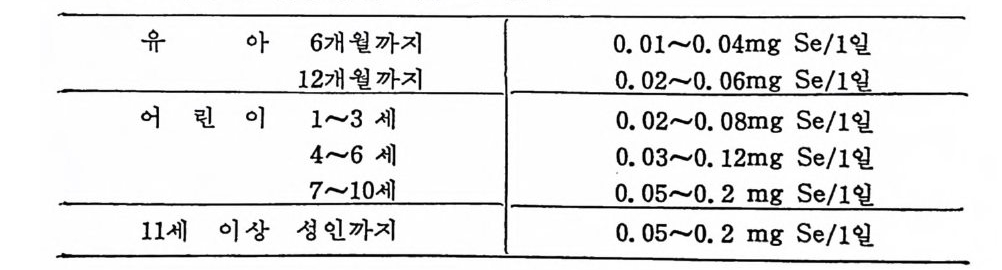 유 아 6 개월까지 0. 01~0. 04mg Se/I 일
유 아 6 개월까지 0. 01~0. 04mg Se/I 일
식이내 Se 함유량은 식품이 생산되는 토양의 식물과 동물에 의해
서 영향을 받는다. 석습관도 관계가 있는데 고기와 생선은 Se 악 함유량이 높고 과일과 야채는 Se 함유량이 낮다. 또한 곡류나 밀 가루 둥 정제과정과도 밀접한 관계가 있으며 곡류가 사람의 1 일 섭 취량의 철반을 차지한다 .44) 사람에 있어서 Se 결핍증은 아직 완전히 규명되어 있지 않다. 사` 람과 동물에 있어서 최처 섭취량은 0.04~0.Img / kg 식이로 보고 있다. 포유 동물에서는 식이에 함유되어 있는 Se 농도가 O.l pp m 이면 충분하다고 한다. 성인의 경우에는 하루 50~75µ g을 섭취했을 때 충분하다고 한다. 뉴질렌드에서는 Se 을 너무 적은 양 섭취했을 때 에 GSH pe roxid a se 의 활성 도가 낮아졌 다. 6) 생 선, 간, 콩팥울 함유하는 식이에는 250µg 이상 Se 을 함유하며 일본에서는 이런 식 이를 계속했을 때 독성중상이 없었고 유해하지도 않았다고 한다. Se 의 1 일 권장량을 추정해 보면 50~200µ g /I 일이라고 할 수 있 다 .45) 이 양온 정상적인 혼합석에서 손쉽게 섭취할 수 있다. 그러 나 Se 이 부족한 지역에서 사는 사람들은 생선, 간, 콩팥 둥의 섭 취를 많이 할 것을 권장한다. 8.5 함유석품 간, 콩팥, 생선, 달걀 둥에 Se 이 많이 함유되어 있으며 곡류는 중간 정도 과일과 야채에는 적게 함유되어 있다. 표 8. 3 은 46)60) ,식 품 속에 함유된 셀레 늄 (Se) 의 함유량이 다. 또한 · Gana p a t hy 46) 가 조사한 조리 된 것 과 조리 되 지 않은 석 품과의 Se 함 유량을 비교해볼 때 325°F 에서 25 분간 기름에 튀겼을 때 쇠고기의 Se 함량은 10%, 그리고 콩팥온 33% 가 감소되었으며 생선은 31% 감소했다. 325°F 에서 26 분 동안 오본에 구워냈을 때 생선은 15%. 가 감소되었다. 지방이 적게 함유된 고기나 생선은 조리시 Se 감소 ` 울이 크고 지방이 많이 함유된 고기나 생선은 Se 감소울이 적었 다.
 표 8. 3 식 품에 합유된 셀 레 늄 (Se) ◄ 6>6o>
표 8. 3 식 품에 합유된 셀 레 늄 (Se) ◄ 6>6o>
8.6 독 성 Se 의 독성중상에 관한 연구는 많이 보고되었는데 괴사 (necros i s), 출혈소 (hemorrha gi n) 중상에서 산소의 결핍으로 인한 사망을 초레 하기도 한다. 만성독성으로는 간경변증과 탈모, 심근의 허약 둥이 나타났다. 독성현상을 나타내는 Se 의 최처량은석이에 3~4 pp m 이 포함되어 있을때이며, 동물에서의 l pp m 의 Se 이 충치를 중전시켜 중을 시사했다. 석아내 Se 이 5~15 pp m 의 농도로 촌재할 때 Se 이 풍부한토양의 목초지에서 키운 반추동물에서와같이 동물에 특히 유 독하다. 또한 3p pm 이하일 때 Se 은 성장을 증진시키며 및 가지 동 물의 질병을예방하는데 효과적이라는 보고도 있다. 토양의 분포에 따라 어떤 지역에는 60 pp m 의 Se 울함유하는 곳도 있는데 예를 들어 South -Dakata 와 Nebraska 가 이 경 우이 며 그곳에 사는 주민들에 게서 치아의 비정상, 충치, 소화기관장애, 황달과 간장병 중상이 현저히 나타났다. 조직의 독성현상은 조직마다 조금씩 다르다. 홉 입에 의해서 나타나는 Se 의 급성 독성 중상온 흥분, 신경조직마비 경련과 호홉불능 증상이 나타난다. 만성 독성때는 간의 독성중상 과 비장의 팽대와 빈혈이 수반된다. 이 병에 걸린 사람은 냉담하며 -di m eth y ls elenit e 에 의 해 서 호흡할 때 마늘냄 새 가 난다. 몇 몇 의 보 고에서는 Se 의 독성이 기형을 초래한다고도 한다. Se 의 독성온 그 의 결합구조에 의 해서 달라지는데 selenit e 가 가장 독성 이 강하고 Se 을 함유한 토양에서 자란 석물에 촌재하는유기물과 결합되어 있 는 Se 도 독성이 있다. 반면에 원소형태의 Se 은 구강으로 섭취시 흡수율이 적기 때문에 독성이 없다. 지금까지의 결과는 대강의 보고에 지나지 않으며 Se 독성은 Se 의 형태, 섭취량과 식이의 배합율에 의해서 영향을 받는다. Meth - ion in e , vit am i n E 그리 고 arsenic 은 Se 의 배 설을 촉진시 켜 준다. -Cd , Cu, Hg 과 용해 되 기 어 려 운 selenid e 는 Se 의 독성 을 감소시 켜 준다. 또한 고단백식이는 Se 의 독성을 감소시키는 데 효과가 있다고 하였다 .47)
Se 은 오래 전부터 효모의 주정 발효를 여 제하고 필수적 인 효소의 SH 기와 복합물을 형성함으로써 호흡연쇄의 일부 효소의 활성을 · 여제하는 것으로 알려졌다. 조류의 암 발생은 Se 의 무기 유기 화합물의 섭취로부터 나타났 다. 장기간 0.2mg / kg 체중 두여는 간암을 유발시켰다. 또 다른 연 구자들은 Se 아 암울 발생시키는 다른 인자들에게 암울 보호해 주는 역 할을· 한다고도 알려 졌 다. 48)4 9 ) 1 일 섭 취 량은 1~2µg / kg 체 중 11)12)50) 으로 독성 을 일으킬 수 있 는 양은 그것 의 100 배 이 다. 2p pm 의 Se 이 selenit e 형 태 로 음료 수에 함유되어 있을 때 이것을 섭취한 후 독성을 유발했으나 생쥐 에게서는 독성현상이 일어나지 않았다 . 5 1) 사료에 4.8 pp m 의 Se 의 장기 섭취시에 쥐에서 처음 증상으로 체중증가 지연현상이 나타났 으며 6. 4p pm 때 는 간장 장애 , 4 주 동안 8p pm 섭 취 시 는 사망했다. 52) 독성의 원인은 Se 이 기관에 계속 축적 중가되기 때문이다. Selenit e- 와 selenate 의 독성 의 작용에 대 해서 는 서 로 상반된 결과가 나오고 수 있 다. 음료수에 첨 가한 selenit e 와 selenate 의 독성 은 거 의 같다고 . 한다. 53) ~귀 에 게 구강으로 lOµg selenocy s ti ne /kg 체 중을 섭 취 케 하 였 을 때 체 내 세 포와 lym p h osarcoma cell 에 서 의 L-cy s te in e 의 합 성을 처해한다. in vi tro 에 서 lOµg Se 은 간 단백 질 인 “C-leuc ine 합성 을 방해 했 다. 54) 또한 in vi tro 에 서 beta i n e 의 meth y lt r a nsfe rs 와 homocy - ste i n e 의 choli ne 합성 이 처 해 되 었 다. 55) Se 의 독성은 su lf a t e 를 섭취시킵으로써 감소되었다. 5 pp m 의 selena t e 와 2% 의 Na2S04 를 쥐의 사료에 보충시켰을 때 뇨로 Se 배설이 증가되었다 .56) 소량의 Se 은 암울 유발시키는 원인이 된다는 보고도 있다 .57) 취 에 게 3 주 동안 50µg selen it e/I 일 섭 취 케 하거 나 60 일 동안 금속 Se 을 lOOµg /1 일로 섭취시켰을 때 암울 유발했다. 또한 Se 이 함유 ? 된 크림약을 발라 주었을 때도 암이 유발됐다 .58) 식물 중에는 Se 을 다른 식물보다 1000 배 정도 많이 함유하는 것 이 있 는데 (예 ; astr a g al us bis u lcatu s ) 이 런 석 물을 침 승들이 섭 취
했을 때
1{irc hg e ssner, M. , Trace Element Meta b oli sm in Man and ·An i m als·3, ·Te chnis c he Univ e rsit at Mi inc hen Freis i n g - Weih e nste p h an, p. 44, 1978. 11) Watk in s on, J. H. , N. Z. Med. J. 523, 202, 1974. 12) Grif fiths , N. M. and Ch. D. Thomson, New Z. J. Med. , so, 199, 1974. 13) Thomp so n, J. N. , P. Erdy and D. C. Smi th, J. Nutr . , 105, 274, 1975. 14) Dick son, R. C. and R. H. Toml ins on, Clin . Chi m . Acta . , 16, 311, 1967. 15) Levin e , R. J. and R. E. Olsen, Proc. Soc. Exp t. Bi ol . Med. , 13 -4, _10 30, 1970. 16) Burk, R. F. , W. N. Pearson, R. P. Wood and F. Vi ter i, Amer. J. Clin . Nutr . , 20, 723, 1967. 17) Heatl e y , W. J. and A. B. , Grant, Fed. Proc. , 20, 679, 1961. 18) Muth , 0. H. , P. H. Weswi g, P. Whang e r and J. E. Oldfi eld , Amer. J. Res. , 32, 1603, 1971. 19) Schrauzer, G. N. , Whit e, D. A. and Schneid e r, C. J. , in Ki rch g e- Bner, M. , Trace Element Meta b oli sm in Man and, Anim als-3, p. 38 7, ATW, Freis i n g -W eih e nste p h an, 1978. 20) Whang e r, P. D. , Pederson, N. D. and Weswi g, P. H. Bi o chem. Bi op h y s. Res. Commun. , 53, 1973. 21 ) Awasth , Y. C, Beutl er , E. and Sriv asta v a, S. K. , J. Bi ol. Chem. , 250, 5144, 1975. 22) Frost, DV. and Lis h , PM. , Annu. Rev. Pharmacol. , 15, 259, 1975. 23) Omay e, S. T. and A. L. Tapp e !, J. Nutr . , • 104, 666, . 1974. 24) Combs, G. F. and M. L. Scott , J. Nutr . , 104, 1297, 1974. 25) Vi la s, N. N. , R. R. Bell and H. H. Drap e r, J. Nutr . , 106, 589, 1976. 26) Reddy , K. and A. L. Tapp e l, J. Nutr . , 104, 1069, 1974. 27) Frie d en, E. , Nutr . Rev. , 31, 41, 1973. 28) Floria n , L. , C. Cerklewski and R. M. Forbes, J. Nutr . , 106, 178, 1976. 29) Bell, M. C. , J. A. Baan, G. R. Bratt on and J. E. W ilki n s on, in
Ki rc hg e ssner M. , Trace Element Meta b olis m in Man and 4ni m als·3. . Technis c he Univ e rsit at Mi inc hen Freis i n g -W eih e nste p h an, 604, 1978. 30) Ullrey, D. E. M. R. Lig h t, P. S. Brady , P. A. Whett er , J. E. Ti lt o n , H. A. ·He nneman and W. T. Mag e e, in Ki rc hg e ssner, M. , Trace· Element Meta o oUsm in Man and Anim als-3, Technis c he Univ ersit at , Mi inc hen, Freis i n g ·W eih enste p h an, p. 530, 1978. 31 ) Tomson, C. D. , E, N. Z. Med. J. , so, 164, 1974. 32) Yoshid a , A. , A. E. Harpe r and C. A. Elerehje m , ]. Nutr . , 66, 217, 1958. 33) Hein ric h , M. Jr. and F. E. Kelsey , J. , Pharmacol, Exp . Tlzerap. ,. 14, 28, 1955. 34) Cavall in, D. , C. de Marco and B. Mondovi, ]. Bi o l. Chem .. 230, 26, 1958. 35) McConnell, K. P. and D. M. Roth , Bi oc lzi m . Bi op h y s, Acta 62,. 503, 1962. 36) Ewan, R. C; , A. L. Pop e and C. A. Baumann, ]. Nutr . , 91, 547,. 1967. 37) Thomsen, C. D. and R. D. H. Ste w art, Brit . J. Nutr . , 32, 47, 1974 .. 38) McConnell, K. P. and D. M. Roth , Proc. Soc. Exp . Bi o l. Med. ,. 120, 88, 1965. 39) Diplo ck, T. A. , H. Bauer and J. A. Lucy , Bi o clzem. ]. , 123,. 721, 1971. 40) Ganth e r, H. E. , 0. A. Levander and C. A. Baumann, J. Nutr . ,. 88, 55, 1966. 41 ) Palmer, I. S. , D. D. Fis c her, A. W. Halworson and 0. E. Olsen,. Bi o chem, Bi op h y s. Acta . , 180, 336, 1969. 42) McConell, K. P. , J. Argr tc . Food Chem. , 11, 385, 1963. 43) Theodora A, Tsong a s and S. W. Fergu s on, in Ki rc hg e ssner, M .. Trace Element Meta b oli sm in Man and Ani m als-3, Technis c he Un- iv ersit at, Mi inc hen, Freis i n g - Weih e nste p h an, 320, 1978. 44) Thorn, J. , Roberts o n, J. and Buss, D. H. , Br. J. Nutr . , 39, 391, 1978. 45) Mertz , W. , in Gladtk e, E. G. Heim ann und I. Eckert, Sp u ren-
elemente , Georg Thie m e Verlag, St u tt ~a rt, 153, 1979. 46) Ganap a th y . S. N. , B. T. Joy n er, D. R. Sawy e r and K. M. H 죠fn er~ in Ki rc hg e ssner, M. , Trace Element Meta b olis m in Man and Ani m a• /s·3, Technis c he Univ e rsit at , M ilnc hen, Freis i n g ·W eih e nste p h an, 322,. 1978. 47) Coop e r, W. C. , Seleniu m Toxic i t y in Man. , Ari Publis h in g Co. p. 203. 48) Tscherkes, L. A. , et al. , Acta Uni o. Inc. Contr . Cancrum. , 19, 632, 1963. 49) Frost, D. V. , CRC Crit ical Re~i ew in Toxic o log y 1, 467, 1972. 50) Sakurai, H. and K. Tsushij a, Envir on m. Phy si o l. Bi o chem. , 5~ 107 , 1975. 51) Schroeder, H. A. , J. Nutr . 92, 334, 1967. 52) Halverson, A. W. , I. S. Palmer and P. L. Guss, Toxic o l. Ap pt Pharmacol. 9, 477, 1966. 53) Palmer, I. S. and 0. E. Olsen, J. Nutr . , 104, 306, 1974. 54) Everett , G. A. and R. W. Holley , Bi o chem. Bi op h y s. Acta . , 46,. 390, 1961. 55) Rosenfe ld , I. , Proc. Soc. Exp. Bi o l. Med. , 109, 624, 1962. 56) Hallden, N. A. , J. M. Fis e nne and J. H. Harby , Scie n ce, 140 .. 1327, 1963. 57) Hadji ma rkos, D. M. , Natu re, 193, 173, 1962. 58) Sunderman, F. W. Jr. , Food Cosm. Toxic o l. , 9, 105, 1971. 59) Schrif t, A, Natu r e, 201, 1304, 1964. 60) Lane, H. W. , B. Tayl o r, ·E. Sto o l, D. Servance and D. C. Warren .. The Am. Di et . Asso. , 82, 1, 24, 1983.
9 니 켈 (Ni ck el, Ni ) 식물과 동물조칙에 N i이 촌재한다는 것은 오래전부터 알려쳐 왔 으며, 1920 년대에는 혈액의 합성에 N i이 관여한다는 추 측도 있었 다. 35) 1960 년대 에 와서 Ni 이 토양과 식 물에 Co 보다 많이 촌재 한다는 것이 밝혀졌다. 얼마전까지만 해도 N i의 생리적인 기능에 대해서 뚜렷한 실험 결과가 없었으며. 다만 간접적인 결과를 갖고 추측하 는 정도였는데 최근에는 일부 동물에게는 필수적이라는 것이 직접 적인 증거둘로 입증되고 있으며 또한 Ni 결핍시 여러 효소의 활성 이 감소된다는 것도 보고되고 있다 .22) N i이 양의 Co 결핍 치료시 부분적으로 Co 와 대치가 가능하다는 것과 in v it ro 에서 여러 효소들을 활성화하며, 다른 금속과 같이 RNA 와 DNA 에 촌재 한다는 것 이 알려 졌 다. 36)37 ) 38)39) 9.1 체내 함량과 분포 인체에는 약 10m g의 N i이 존재하며 중정도의 농도는 약 O.lpp m 이다. 허파, 췌장, 뇌, 뼈, 신장 그리고 피부에 N i이 많이 함유되 어 있으며 근육조직과 혈액에는 아주 소량 들어 있다. 최근 인체의 혈청의 Ni 합유량은 0.2~0.5µ g /lOOml 로 보고되고 있다 .1)
N i울 가장 많이 함유하는 시기는 대아기에는 12~25 주이며 그후 출 산에서 유아기까지 계속 함유량이 감소한다. 9.2 주요 기능 사람에 있어서 N i이 효소의 필수 구성 성분이라는 것은 찰 알려 겨 있 지 않다. 또한 Ni 울 함유한 혈청 의 a2-macrog lo buli n 의 기 능 도 완전히 규명되어 있지 않다 .2) 최근의 연구 결과에서 Ni 결핍시 여러 효소의 활성도와 기질 농 도가 감소된다고 보고되 었 다. 3) N i의 주요 기능으로서는 Fe 의 체내 이용에 관여하는 것이다. Ni 결핍 시 에 는 Fe 의 이 용률이 감소되 며 그 결과 적 혈구 수, hemato c ri t 치 , hemog lo bin 량이 감소되 었 다. 2)3) 간의 glu cose-6-ph osp h ate -dehy d rog e nase(G-6-P DH) 가 Ni 결핍 시 적은 양의 NADPH 를 방출한다. 그 결과, 에너지 운반이 감소 되며, 또한 Ni 결핍시 췌장의 a-am y lase 의 활성도 감소로 전분의 분해가 감소된다 .3) 또 다른 연구자들은, N i이 생체대사에 중요한 역할을 하며, mi - -toc hondria , 세 포막의 구성 성 분이 된다고 한다. 4) Ni 은 inh ib i t or -pe p tide 의 구성 성 분으로 pro lacti n 호르몬과, vi· -tam i n B12 의 합성 에 필요하다고 하는데 Ni 은 pe p tide 의 N 말단 :m eth y le ne 기 의 comp le x-fi xa ti on 을 활성 화한다. 5) 9.3 대 사 식이로 섭취된 N i은 소장에서 l~10% 정도가 홉수된다. N i의 홉수는 섭취하는 식이에 함유된 N i의 양에 의해 영향을 받는다. 표 9.1 은 취의 식이에 함유된 N i이 각 조직의 N i농도에 끼치는 영 향이 다. 6)7)8) 사람의 Ni 흡수와 배설은 극히 소량으로 건강한 성인의 뇨겁사에
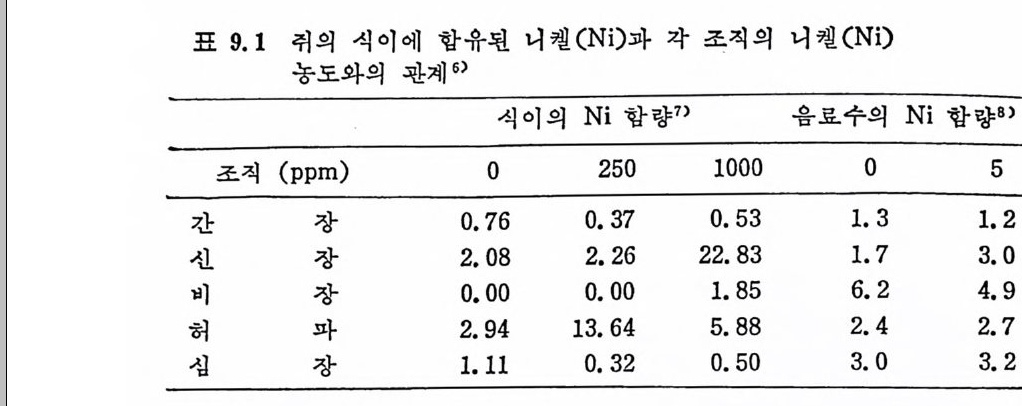 표 9.1 취의 식이에 합유된 니켈 (N i)과 각 조칙의 니첼 (N i)
표 9.1 취의 식이에 합유된 니켈 (N i)과 각 조칙의 니첼 (N i)
서 10~70µg / l 정도의 N i을 함유하고 1 일 뇨배설은 30µg 정도라고 . 하며 Sunderman36) 은 1 일 20µ g으로 보고했다. 대부분의 N i은 대 변으로 배설되는데 10 명의 건강한 성인의 3 일간의 대변검사에서는 · N i이 lg 건조물에 14.2µg 함유되어 있었으며 1 일 배설량은 258 土 126µg Ni 로서 뇨에 비 하여 20 배 정 도가 높았다. 9) 노인 남자들의 대변겁사에서도 N i을 1 일 258 士 230µ g 배설한다고 보고하고 있다 .15) K i rch g e .13 ner11) 에 따르면 식 품으로 섭취된 N i의 약 3%, 죽 l0µg /1 일 정도가 뇨로 배설된다고 한다. 땅으로는 약 50µg /l 가 분비 된 다.” 일부는 뼈에 축적된다. 혈장의 Ni 은 대 부분이 a-macrog lo buli n 으 로
리고 석물성 식품을 적게 함유한 혼합 식이에는 N i이 3~lOµg /1 일 함유되어 있다고 한다• 또한이 양은 사람의 필요량을충족시켜 주지 못한다고 했다. 그러나, 같은 열량과 단백가로서 처지방, 많은 양 의 전곡류의 식 품과 채 소류, 굴 둥이 혼합된 식 이 는 700~900µg /1 일을 함유한다. 성인(서양)들이 일상 섭취하는 혼합 식이는 300 ~500µg /1 일을 함유하고 있 다. 13)14)15)16) 취와 병아리의 석이내 Ni 적당량은 50~80µg / kg 식이로 추산된 다 .17) 곡류와 야채 종류가 N i의 좋은 급원이 된다고 알려쳐 있으며 ,18) N i의 함량이 높은 곡류는 p h yti n 함량이 높아 ph y tic ac i d 와 안정 한 복합체를 형성할 수 있으므로 장내 흡수가 감소된다. 9.5 결핍증 Ni 결핍시 쥐의 성장이 감소되고, N i이 결핍된 어미의 새끼는 사 망 률 이 높다. N i의 결핍은 기관과 조칙의 Ni 감소분만 아니라 모 유의 Ni 함량도 감소시켰다. N i의 결핍은 Fe 결핍성 빈혈을 초래 했으나 적혈구의 산화효소는 감소되지 않았으며, glu cose 분해, 'TC A cy c le 과 ami no ac id 대 사에 영 향을 주었 다. 19) 가장 많은 영 향을 끼 찬 효소들은 lacta t e dehy d rog e nase(LDH), 'iso c itra te dehy d rog e nase(I CD H), malate dehy d rog e nase(M DH), ·g l y cer - aldeh y de- p hos p ha t e-deh y dro g enase(GPDH) 와 glu ta mate oxa-}aceta t e dehy d rog e nase(GOT), glu ta m ate dehy d rog e nase(GLDH ) 로서 현처한 활성감소를 볼 수 있었다. 기질도 감소현상을 보였는데 간의 포도당과 gly c og e n, 혈청의 중 성지방과 포도당 등이었으며 소변도 감소되었다. 성장기의 쥐에게 N i울 15µg /lOOg 식이를 섭취케 하여 비축된 양울 전부 사용한 후 결핍증세를 인위적으로 야기시켰을 때 ,19) 취 의 체중은 N i결핍으로 35% 가 감소되었다. 또한 다른미량원소, 독 히 Fe, Cu, Zn 과의 상호작용이 일어 났다. N i결핍은 정상적인 Fe 홉수를 손상시켜 빈혈을 초래했다.
Hb 과 관련된 혈액치, 적혈구, hema t ocr it는 Ni 결핍시 44% 나· 감소되었다. N i의 필요성에 대한 생화학적 판정기준을 통해 간의 효소합성이 측정되었다. 30 일된 Ni 결핍의 쥐는 전체 deh y drogenase 의 활성도가 29~ 82% 나 낮게 측정되었다. Ami no aci d 대사에 관계되는 GLDH, GOT 와 GPT 등의 효소는 약 45% 가 감소되었다. 총 p ro t ease 의 활성은 Ni 결핍에 의해 영향을 받지 않으므로간 의 효소의 활성저하는 식사의 단백질 흡수를 감소시키지 않았다. 단지 a-am y lase 만 57% 감소되었으며 이때 혈청이나 간의 포도 당과 gly c og e n 그리고 중성지방의 농도도 현처히 낮아졌다. N i과 Fe 결핍에서 초래되는 빈헬의 원인이 두 가지 중 어느 것에 서 기인하는가를 알아내기 위해서 효소의 활성도와 대사산물의 농 도를 분석한 결과 Ni 결핍시엔 간의 효소 G6P-DH, ICDH, GOT 와 GPT 의 활성만이 감소되었으며, Fe 의 결핍시에는 간과 혈액완
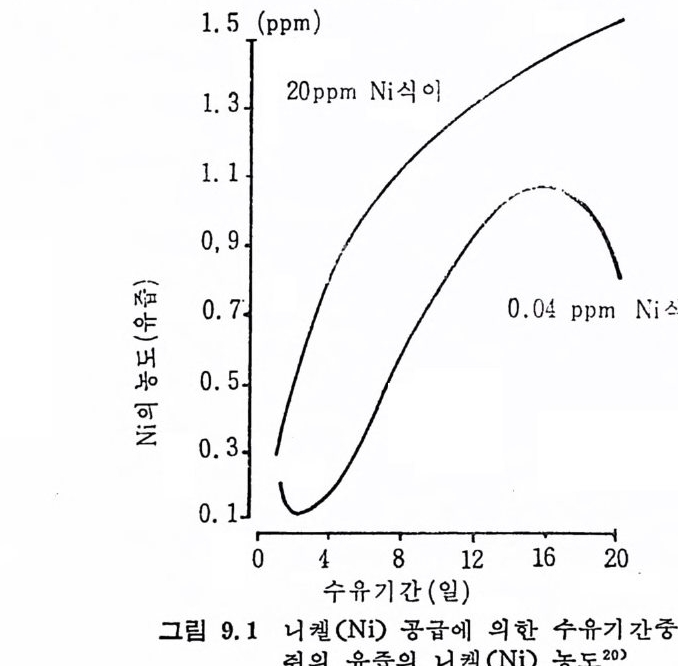 1. 5 (ppm )
1. 5 (ppm )
alkali ne ph osp h ata s e 의 활성 만이 감소되 었 다. 또한 대사 산물로서는 포도당, g l y co g en 이 Ni 결핍시 현처하게 감소되는 데 비해서, Fe 결핍시엔 변화가 없었다. 취에 있어서 N i이 결핍된 쥐의 어미는 정상보다 N i이 평군 30% 적게 들어 있는 우유를 새끼에게 주었다. (그림 9.1 ) 그립 9.1 은 수 유기간동안 Ni 섭취상태에 따라 달라지는 쥐의 유즙의 함량을 ~ 타낸 것이다 .27) 표 9.2 는 N i의 섭취 상태에 따라 달라지는 36 일된 취의 체내 각 기관의 Ni 함유량이다.
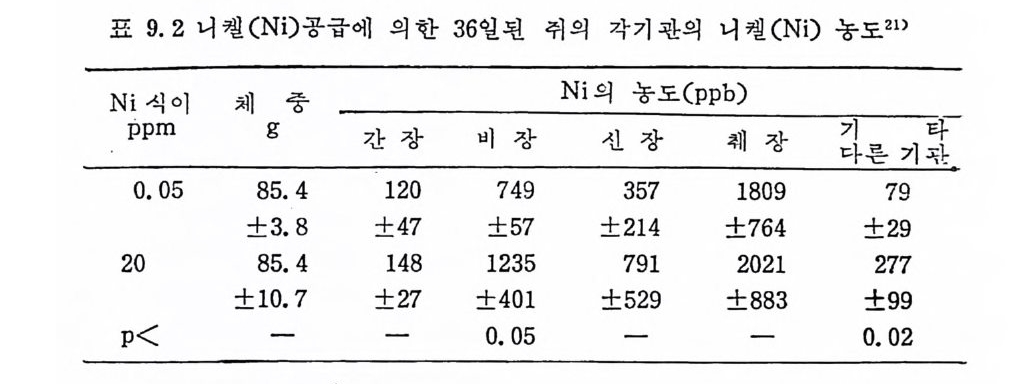 표 9. 2 니 펠 (N i)공급에 의 한 36 일된 취 의 각기 관의 니 켈 (Ni ) 농도 21)
표 9. 2 니 펠 (N i)공급에 의 한 36 일된 취 의 각기 관의 니 켈 (Ni ) 농도 21)
생 후 1 일 될 병 아리 에 게 4 주간 o. 3~0. 4µg /lOOg 석 이 를 먹 인 후, tra ce elemen t를 충분히 섭취시킨 대조군과 비교했을 때 생화 학적 인 차이 가 나타났다. 22)23) a-gl y c erop h osp h ate 가 존재 할 때 간의 hemog lo bin 에 의 한 소 비가 감소되었고, 간의 총 지방 함량이 증가되었으며 간의 ph os- ph oli pid 와 choleste r ol 도 중가되 었 다. 또한 간세 포에 서 는 ultr a str u ctu ral 장애 를 나타냈다고 한다. 야 러 한 장애 는 roug h endop la smi c reti cu lum 의 cist e r n 의 팽 창과, mi toc hondria 의 팽 대 둥이 있 다. Mi toc hondria 의 팽 대 는 matr i x 의 일부에서 일어났으며 cr i s t ae 의 분리와 관련이 있었다. 쥐에 대한 Ni 실험시 태아기, 신생아기 및 수유를 하는동안 Ni 결핍의 경우 생석에 큰 영향을 받는데, 제 1 세대시 Ni 결핍인 암 쥐는 15% 의 사망률울 보이고 이 사망률은 제 2 세대에서 더 크게
나타났다. Ni 견핍의 쥐는 대조군보다 체중이 적었다 .22)23) 수유기간 동안 N i이 결핍된 쥐는 털이 거칠어지고 활 발하지 못 했다. 쥐의 결핍은 병아리와 같이 간에 여러 가지 변화를 초래했는 데 정 상이 던 간의 red brown color 가 결 핍 시 엔 muddy brown 으 로 변화했다. 간에 서 는 a-gl y c erop h osp h ate 가 존재 할 때 산화 활 성 이 감소되 었 다. 또한 핵 의 RNA po lym erase 활 성 과 alkalin e RNAase/ pr ote i n 이 증가되 었 다. 위의 결과에서 N i이 대사에 중요한 기능을 가지며 주로 간에서 일어난다는 것을 알 수 있다. 간경변증 환자와 만성적인 요독증 환 자에서 혈장의 Ni 농도가 감소됨을 볼 수 있었는데 2~ ) 이는 Ni 대 사 이상으로 오는 것이며 이 경우 땅으로 많은 양 의 N i이 분비된 다 (49µg /l 땅). 9.6 함유식품 식품의 Ni 함량에 대한 자료는 아주 적다. 약 50 년 전에 Bertr a nd 와 Macheboeu f 25) 는 녹색 채 소에 Ni 이 1. 5~3. O pp m 이 며 과일류, 견과류 그리 고 곡류에 는 0. 15~0. 35p pm 이 함유되어 있다고 했다. 그 후 Schroeder 둥 26) 에 의 해 서 동물성 식 품, 고기 , 우유 둥에 Ni 이 소량 함유되어 있다고 발표했다. Zook 등 27) 은 북아메 리 카에 서 생 산된 곡류에 서 Ni 의 함량을 조사 했다(표 9.3). 이 밀가루들은 빵을 만드는 과정에서 N i의 양이 중 가하는 것으로 나타났다. 그 후 Welch 와 Care y 28) 는 북아메 리 카의 12 지 역 에 서 곡류알을 모아서 Ni 을 축정 해 본 질과 0. 08~0. 35p pm 으로 평군치는 0.18 pp m 이었다 . 동물성식품에는 N i이 적게 함유되어 있다.
 표 9.3 식품의 니첼 (N i) 함유량
표 9.3 식품의 니첼 (N i) 함유량
9.7 독 성 N i의 결핍중은 N i의 독성이 알려진 이후부터 연구되어졌다(특히 -nick el te tr a carbony l 의 독성 ) . N i정제소의 노.동자들은 호홉시에 N i이 축적되고 호흡기에 이상 이 일어났다. 또한 Ni울 다루는 사람들에게서 피부영, 습전, 알레 르기 , 가려 움중 등이 나타났다. 29) 이 증상들은 Ni 을 적 게 함유한 식이를 섭취했을 때 다시 정상으로 되돌아왔다 .30) 식이에 함유된 N i의 독성은 사람에게는 아직 알려져 있지 않다. 성장이 끝난 쥐는 lOOO pp m 까지 N i을 섭취했을 때 전혀 이상이 없었다. 돼지에 있어서는 250 pp m 의 Ni 첨가가 설사, 탈모, 구토, 무반 웅 둥의 독성중세를 나타냈다 .31) 성장과정의 쥐에게 lOOO pp m 의 Ni 을 섭 취 시 켰 을 때 적 혈구, hemog lo bin , hemato crit 치 , 그리 고 혈청의 Ni 함량이 중가되었다 .37) 이 와 상반된 다른 보고로는 쥐 에 게 100~lOOOp pm 의 Ni 을 섭 취 시켰을 때 성장정지, hemog lo bin 감소, 간, 혈장의 alky l ph os- ph ata s e 의 감소, 그리 고 십 장과 간장의 cy toc hromoxid a se 감소현상 이 나타났다고 한다. 또한 신장의 Ni 함량은 중가했고 간은 4p pm , 신장은 40p pm 이 상에 도달했다. 32) 쥐 에 게 N i울 4~5mg /kg 을 복강 내 로 한 번에 주사했을 때 nep h . :rop a th ia , ami no aci du ria , pr ote i n u ria 등의 독성 증상이 일 어 났다. 33) 5 pp m 의 N i이 함유된 음료수를 장기간 섭취한 취에게서 독성이
발견되지 않았으며 체내의 축적도 일어나지 않았다. 그러나 Ni 삽 취 는 다른 tra ce elements 이 용에 영 향을 주었 는데 , 허 파에 서 는 Cu 와 Zn 이 감소되었고 십장에서는 Cr 이 중가되었으며 신장에서는 Mn 이 증가되었고 비장에서는 Cu 오} Mn 이 감소되었으며, Cr 은 중 가하는 현상을 보여 주었 다. 34) *참고문현 i) Sunderman, F. W. Jr. , Nomoto , S. , Pradhan, A. M. Levin e , H. ,. Bernste i n and S. H. , Hi rs h, R. , N. Eng l . ]. Med. , 283, 896, 1970. 2) Nomoto , S. , McNeely, M. D. and Sunderman Jr, F. W, Bt o ckem- ist r y 10, 1647, 1971. 3) Ki rch g eB ner, M. and Schneg g, A. , in Nrta g u , ]. 0. , Nt ck el tw th e Envt ro nment, W iley Inte rscie n ce, New York, 1980. 4) Ni el sen, F. H. , in Mertz , W. and Cornatz e r, W. E. , Newer Trace- Elements tn Nutr t t to n p. 125, Marcel Dekker Inc, New York, 1971. 5) Fuji ok a, M. , Nakao, Y. and Nakahara, A. , Bull Chem. Soc. Jpn . > 49, 477, 1976. 6) Underwood, E. J. Trace Elements tn Human and Antm al Nutr t · - lto n, 4th ed. , Academi c Press Inc. New York, London, 160, 1977. 7) O'Dell, D. G. , Mi ller , W. J. , Moore, S. L. , Ki n g , W. A. , Ellers,. J. C. and Jur ecei. , H. , J. Antm . Se t'. , 32, 769, 1971. 8) Schroeder, H. A. , Mi tch ener, M. and Nason, A. P. , ]. Ni1 tr. ,. 104, 239, 1974. 9) Horak, E. and F. W. Sunderman, Cl in. Chem. , 19, 361, 429,. 1973. 10) Lang , K. , Bt oc kemt e der Ernakrung 4, Aufl ag e Dr. Diet r i c h , . Ste i n k off VP ,r lag. p. 355. 1979. 11) Ki rch g e .6 n er M. , E, Weig a nd, A. Schneg g, E. Graemann, E. J. Schwarz, and H. P. Roth , in H. -D. Cremer, D. Hotz e ! and J. Ki ihn a\h
Bi o chemi e und Phys io log ie der Ernahrung Band I, Tei! 21 p. 275 .. Georg Thie m e Verlag , p. 289, 1980. 12) Schroeder, H. A. , Balassa, J. J. and Ti pton , J. H. , J. Ckron,. Di s. , 19, 545, 1966. 13) Hami lt o n , E. I. and Mi ns ki, M. J. , Sci. Tota l . Envir on . , I, 37 5, 1972/1973. 14) Kent, N. L. and McCance, R. A. , Bi o chem. J. , 35, 837, and: 887, 1941. 15) Nody a , P. L. , Hy g. Sanit . , (USSR) 37, 108, 1972. 16) Schroeder, H. A. , Balassa, J. J. and Ti pton , I. H. , J. Chronic • . Di s. , 15, 51, 1961. 17) Ni el sen, F. H. and Sanste a d, H. H. , Am. J. Clin . Nutr . , 27,. 515, 1974. 18) Schroeder, H. A. , J. J. Balassa and I. H. Ti pton , J. Chronic . Di s. , 15, 51, 1962. 19) Schneg g, A. and Ki rc hg e Bner, M. , in Ki rc hg e Bner, M. , Trace- Element Meta b olis m in Man and Anim als-3, p. 236, ATW, Freis i n g- Weih e nste p h an, 1978. 20) Gladtk e, E. , G. Heim ann and I. Eckert Sp u renelemente , Georg- Thie m e Verlag St u tt ga rt, p. 72, 1979. 21 ) Schneg g, A. and M. Ki rc hg e ssner, Zbl. Vet. Med. A. 24, 394 ,. 1977. 22) Ni el sen, F. H. and D. A. Olleric h , Ni ck el, Fed. Proc. 33, 1974 ► 23) Ni el sen, F. H. , in Hoekstr a , W. G. , Sutt ie, J. W. , Ganth er, H. E. and Mertz , W. eds, Trace Element Meta b olis m in Anim als-2, Un_ iv ersit y Park Press, Boltim ore, 381, 1974. 24) McNeely, M. D. , F. W. Sunderman, M. W. Nechay and H. Lev- ine , Chem. , 17, 1123, 1971. 2/5 ) Bert ran d, G. and Macheboeuf, M. , C. R. Hebd Seances Acad ► Sci. , 180, 1380 and 1993, 1925, 182, 1504, 1504, 1926, 183, 5. 1926 ► 26) Consolazio , C. F. , Nelson, R. A. Meto u sch, L. O. , Hug h es, R. C ► and Vrone, P. , U. S. , Army Med. Res. Nutr . Lab. , Rep. , 284 , 1. . 1964.
27) Zook, E. G. , Greene, F. E. and Morris , E. R. , Cereal Chem. , 47, 720, 1970. 28) Welch, R. M. and Carry, E. E. , Ag r ic . Food Chem. , 23, 497, ·19 75_ 29) Lunn, J. A. , Practi tion er 220, 312, 1978. 30) Kaaber, K. , Veie n , N. K. and Tj el l, T. C. , Br. J. Dermato l . , 98, 197, 1978. 31 ) Ki rc hg eB ner, M. , Roth , F. X. , Z. Ti e rph y si o l. Ti e rernii hr . .F ult er mi ttelk de. , 39, 227, 1977. 32) Whang e r. P. D. , Toxic ol. Ap pl. Pharmacol. 25, 323, 1973. 33) Gi tlitz, P. H. , F. W. , Sunderman Jr. and P. J. Goldblatt , Toxi co l. Ap pl. Plzarmacol. , 34, 430, 1975. 34) Schroeder, H. A. , M. Mi tch ner and A. P. Nason, J. Nutr . , 104, 239, 1974. 35) Ki rch g e Bner, M. E. Weig a nd, A. Schneg g, E. GraBmann F. J. ·Sc hwarz and H. -P. Roth , in H. D. Cremer, D. Hotz e ! and J. Ki ihn au, Bi o chemi e and Phys rolog ie d er Ernii hr ung , Band I Tei/ . 2. p. 289, 1980. 36) Food and Nutr i t ion Board, Nati on al Research Council , Recom· mended Di e ta ry Allowances, 9th ed. , Nati on al Academy of Scie n ces, Washin g ton , p. 162, 1980.
10 코발트 (Cobal t, Co) Co 가 식물과 동물조칙에서 발견된 지는 오래전이나 1935 년에야 비로소 동물식이의 필수 성분임이 밝혀졌다 .. l) 호주에 서 자라는 가축에 서 볼 수 있 었 던 coast dis e ase 나 wasti ng d i sease 의 치료에서 Co 영을 두여했을 때 가축둘의 질환이 방지됐 다고 한다. 20)21 ) 이 연구과정에서 실시된 전체 간의 항 악성빈혈 효과의 분석결과 간에 어 떤
간, 골수, 그리고 신장에는 Co 의 농도가 다른 부위에 비해서 약 간 높게 함유되어 있다. 사람의 혈액 중 C 여근 0.2~l5µ g /l 로서 사람에 따라 큰 차이를 보이나 그 자체가 너무 소량이기 때문에 분석의 불확실성도 있는 것 같다. 10.2 주요 기능과 결핍증
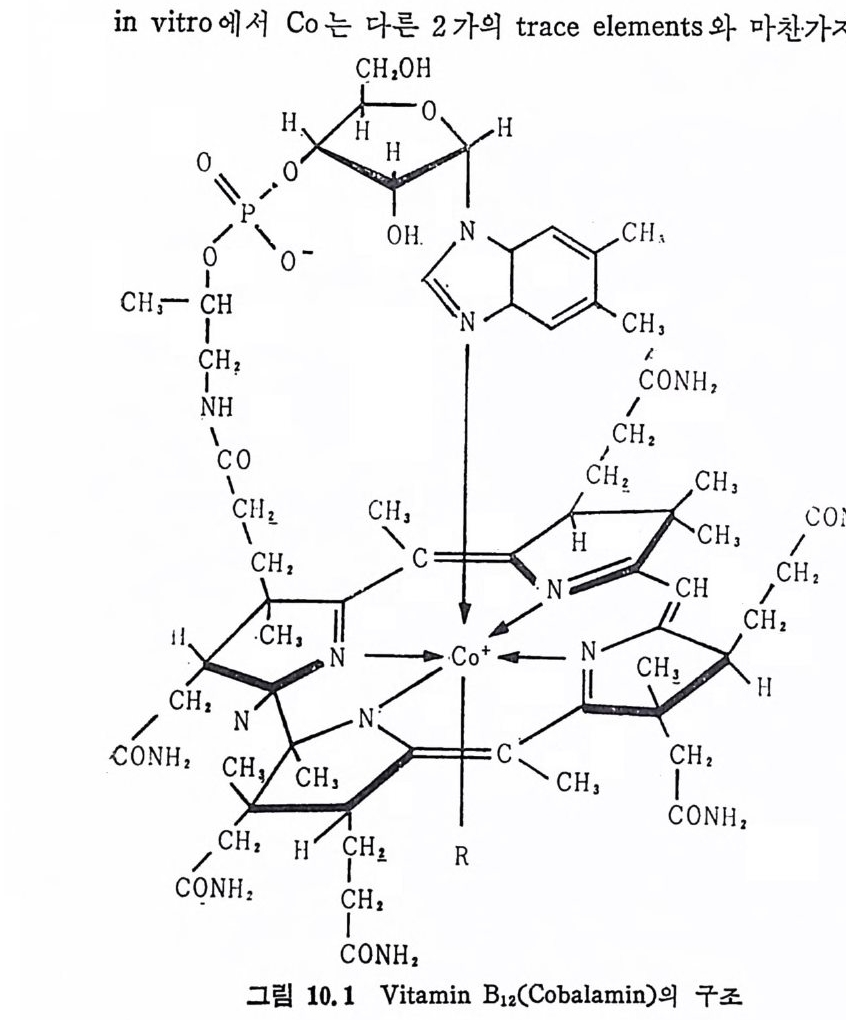 in vit roo 에 서/ C\o 는. 다l른: <2 가의I -{t ra c\ e el eCmHen ts 와 마찬가지 로 수
in vit roo 에 서/ C\o 는. 다l른: <2 가의I -{t ra c\ e el eCmHen ts 와 마찬가지 로 수
많은 효소의 활성에 사용된다. in v i vo 에서도 마찬가지 현상을 보 인다. Meth y lm alony l- Co A muta s e, meth y lt e t r a hy d rofo la te oxid - --or edueta se, hemocy s te i n e meth y lt r a nsfe r ase 와 rib o nucleoti de -red ucta s e 둥은 그의 활성 화에 vit am i n B12 를 필요로 한다. Co 는 vit ai m i n B12 의 구성성분으로 corr i nr i n g에 연결되어 있으 터 (그립 10. 1)3> vit am i n B12 는 4. 34% 의 Co 를 함유한다. 사람이 vit am i n B12 를 충분히 섭취하면 Co 의 결핍증은 나타나지 않는다. 사람에 있 어 서 Vi tam i n B12 의 결 핍 증은 pe rnic ios e anemi a 와 신경 조직 의 이 상을 나타낸다. vit am i n B12 결핍 에 서 기 인하는 악성 빈혈환자의 뇨 속에 다량의 meth y lm alonic a ci d 를 배설하는 폐 이는 muta se 반응의 결함 때문이다. 동물실험에서는 성장정지, 유전변형과 기형중상이 나타난다. 가 장 중요한 vit am i n B12 의 기 능은 pr op ion ic acid 대 사, DNA 합성 그리고 me t hy l 기의 이전을 들 수 있다. 소는 미 생 물을 통해 서 위장에 서 Co 를 함유하는 vit am i n B12 를 합성하여 소장에서 흡수된다. 석 물은 Co 를 흙에 서 흡수하며 반추동물은 Co 가 함유된 풀을 섭취한다. Co 가 부족한 지역에서 소와 떤양에 나타나는 영양성 빈 혈은 Co 로 잘 치유된다. 이들 동물의 반추위 내 미생물은 vit am i n .B 12 를 합성하는 데 Co 를 이용한다. 무기 Co 영의 약물학적 용량은 인체를 포함한 여러 동물의 체내에 서 적혈구 생산을 중가(다혈구 혈중)시킨다. 이러한 반응을 유발하 는데 소요되는 과량의 Co 가 가전 독성 영향 때문에 인체의 빈혈치 로에 Co 의 사용은 제한을 받는다. 사람이나 기타 동물은 소나 양의 수육과 육줍울 섭취함으로써 -vitam i n B12 를 공급받게 된다. 사람의 소화기 내 에 서 식 하는 bac- -ter ia 는 Co 를 이 용하여 vit am i n B12 를 합성 한다. 그러 나 그 흡수 울이 너 무 낮기 때 문에 vit am i n B12 의 섭 취 로는 충분치 못하다.
10.3 대 사 사람과 동물의 최근 실험에서 Co 의 흡수율은 20~90% 이며 평군 70% 이다. 식이에 함유된 Co 의 양온 홍수율과 비례하며 또한 그의 흡수량과 신장으로의 배설량도 비례한다. 배설 경로로는 일부가 담당으로 그리고 칙접 장벽을 통해서 내인 성으로 배설된다. 그러므로 대변을 겁사했을 때 대부분이 홉수되지 않는 Co 로써 발견된다. Co 와 Fe 의 흡수와는 밀접한 관계가 있는데 Fe 결핍시엔 Co 와 · Fe 의 홉수가 현처히 중가한다. Pollack 등 4) 과, Forth 둥”은 Co 의 섭 취 중가는 Fe 의 홉수를 처 해한다고 하였다. 반대로 Fe 의 섭취가 중가하면 Co 의 흡수를 처 해한다고한다. 그림 10.2 는 사람의 Fe 섭취 량에 따라서 변화되는 Co 의 섭취와-
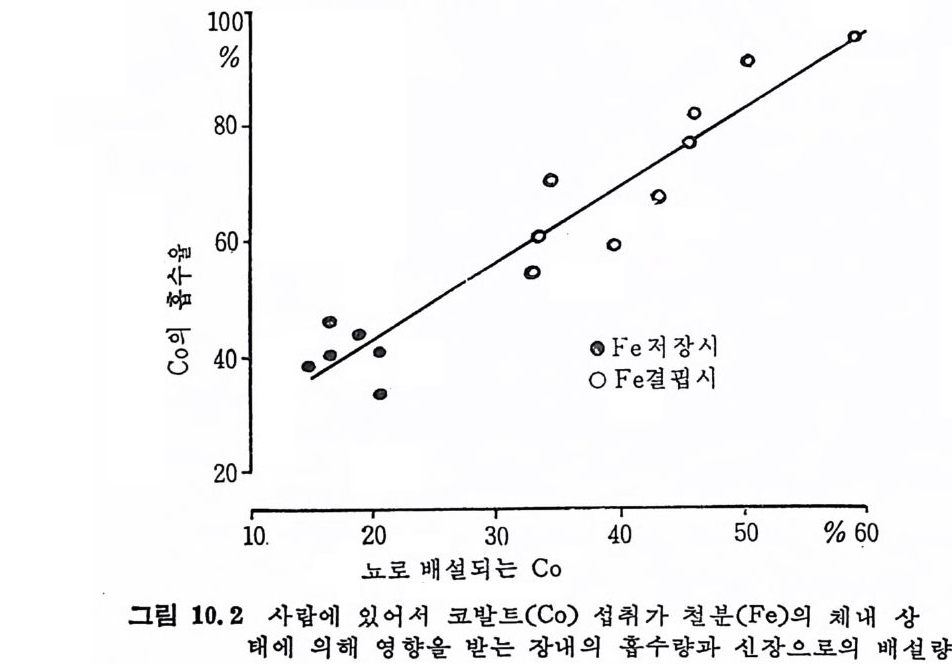 100
100
배설량이다. Co 는 Co2+ 형 태 로 흡수된다. 부인들이 섭취하는 일반석이에 함유된 5.6~7.8µ g의 Co 섭취에 서 po sit ive balance 를 보였 다. 7) 식 이 에 함유된 Co 는 73~97% 정 도 홉수되었다. 그러나 주사로 두여한 Co 는 60% 가 뇨로 그리고 , 나머지는 대변으로 배설되었다. 방사성 동위원소 69Co 는 주사 후 제일 먼처 간과 췌장에 일정기 간 동안 처장이 되었다. 24 시간 후에 각 기관의 Co 함량은 골고루 분포되었다. 장기간 처 장되는 기관은 부신, 골수, 흉선 둥이었다. 10.4 섭취 량 인체는 vit am i n B12 가 충분할 때에는 Co 가 필요치 않다. 식이로서 하루 섭취되는 Co 의 양은 전혀 조사되어 있지 않다. 그 ; 러나 섭취경향을 살펴보면 식이로 섭취되는 양온 5~600µ g일 것으 로 생각된다. 이와같은 큰차이는 분석에서 오는 오차가 아니고 지 역에 따라 토양, 석물과 식이 둥이 각각 다르기 때문인 것으로 보 안다. 하루 약 8µg Co 의 섭취가 군형적임울 보여주었다 .8) Co 는 vit am i n B12 의 구성 성분으로서 vit am i n B12 합성을 위해 장내 미생물의 작용을 받게 되는데 사람과 동물 등은 반드시 co- balami n( vit am i n B12) 의 형 태 로 공급되 어 쳐 야 한다. 이 들은 식 이 에 서 직접 vit am i n B12 를 합성할 수 없다. Schroeder 동”은 사람이 매 일 최 소한 lµg 의 vit am i n B12 를 섭 취하여야한다고 했다. Vi tam i n B12 는 4.34% 의 Co 를 함유하고있으며 사람의 Co 최처 요구량은 약 0. 0434µg 으로 규정 하고 있 다. 소의 먹 이 에 Co 를 0. 08~O.lµg /g 을 첨 가했을 때 충분한 양이 었 으며” 정맥으로 두여한 Co 는 결핍시에 변화를 주지 않았다. '구강 으로 섭취시킨 Co 영으로 CoC03 및 CoS04 는 효과가 있었다. 이 결과로 미루어보아 소는 구강으로 섭취한 Co 를 장내 박테라
아에 의 해서 vit am i n B12 합성 에 사용한다는 것 이 가장 중요한 사 실로 받아들여진다. 충분한 Co 를 섭취한 양이 Co 결핍인 양보다 양유의 Co 함량이 높았다. 쥐의 하루 Co 필요량은 0.03µ g이다 •10) 토끼는 Co 를 적게 필요 로 하며 실험으로서도 Co 결핍을 야기시킬 수 없었다. 10.5 함유 석품 Co 의 공급원은 간, 콩팥, 굴과 녹영채소가 되는데 녹영채소의 · Co 함량은 0.2~0.6p pm 정도이다. 무우에는 300µg % 완두콩에는 .38 0µg % Co 를 함유한다. 10.6 독 성 Co 는 tra ce element 중에 서 도 독성 이 적 은 원소 중의 하나이 다. 메일 25~30mg 이상의 Co 를 섭취했을 때 독성중상이 나타난다. 그 증상으로는 식욕감되, 체중감소, 갑상선의 h yp er p las i a 를 수 반하는 po lyc y the mi a, my x edema, 심 장기 능부전 둥이 다. 동물의 체중 1k g당 4mg 이상의 Co 섭취는 체중감소, 빈혈을 유 발하고 십하면 죽음에까지 이른다. 이 경우에 생기는 빈혈은 과량 의 Co 섭취에서 기인되는 Fe 의 흡수처해가 원인이 된다고 한다 .1 1) 쥐 에 게 200~250p pm Co 를 먹 이 면 골격 장애 와 reti cu locy tos is 의 by pe rpl a sia 를 수반하는 po lyc y the mi a 를 일으키 고, 혈액 의 양이 증가되 었 다. 또한 Co 는 eryt hr op o ie t i n 의 생 산울 촉진하는 반면 Co-po lyc y the mi a 는 체 내 의 vit am i n B12 농도를 증가시 켜 주지 않 았다. 다만 대변에 vit am i n B12 의 배설이 증가했을 분인데 이는 장내에 있는 미생물에 의한 vit am i n B12 의 합성에서 오는 것으로 보여진다. Co-po lyc y the mi a 의 경 우 cy s te i n e 이 나 his t i din e 을 섭 취 시 키 면 Co 와 복합체 를 형 성 한다. Vi tam i n C 도 같은 효과를 갖는다. 개 에 게 서 po lyc y the mi a 를 발생 하게 하는 최 저 량은 5mg / kg 체 중
ICo 였다 .12) Co2+ 농도가 25p pm 이 상일 때 세 포의 호흡작용을 저 해 한다고 했 고 추출된 간의 mi toc hondria 에 서 a-keto a c id 의 oxid a ti ve decar- boxy la ti on 을 공격 하여 lip o ic ac id 합성 을 저 해 한다. 13) 영 아에 게 매 일 Co 영 을 150mg 정 도 주게 되 면 p·o ly c y the mi a 가 발생 한다고 한다. 특히 임 신부에 서 Fe 와 함께 Co 에 대 한 hemop o ie t i c 반응은 상당한 문제로 지적되고 있다. 이 의 에 도 th y r oid hy pe rpl a sia , my x edema 및 유아의 충혈성 심 부전 등을 관찰할 수 있다 .14) 소련에서는 Co 와 Mn 은 쥐의 갑상선호르몬의 합성에 필요한 요 소타고 발표하였 다. 11) Co- p ol y c yt hem i a 의 발생기전에 대해서는 확실하게 규명되어 있 지 않으나 실험을 통한 가설에 의하면 방사성 동위원소의 실험에서 · Co 는 hemo g lob i n 을 합성하기 위한 Fe 의 이용률을 높여 준다고 한다• 그러 나 최 근의 실험 보고에 서 는 두약으로서 의 Co 양이 ery thr op o ie - i:in 합성 이 나 분해 에 영 향을 주지 않는다고도 한다. 15) in vit ro 에 서 는 10-6M C0 농도는 14C-g ly c ocoll 이 heme 의 합성 에 사용되는 것을 저해하며 g lob i n 의 합성을 촉진시켜 준다 .16) - 또한 vit am i n B12 를 장기간 복용했지만 po lyc y the mi a 증상은 나 타나지 않았다. 석이내 요오드와 Co 함량이 낮울 경우에 적당량의 Co 두여는 내 분비선의 무게에 영향을 주지는 않았으나 상피세포의 크기와 중가 등의 조직학적인 변화를 일으켰으며 I 와 Co 의 함량이 낮은 지역에 서 내분바선의 기능장애는 그 요소의 함량과 이 요소들의 비율에도 관계되며 g o it er 의 빈도와 Co 농도 사이엔 반비례적인 관계가 있다 고 지적하고 있다 .17 )1 8) 토양에 Co 가 많이 함유된 여러 지역에서 갑상선 기능 항전증 환 자의 발생 빈도가 높았다. 이 결과로서 Co 와 I 의 상호작용에 대 한 연구가 앞으로 많이 이루어쳐야 할 것이다. 석 습관이 불규칙 하고 맥 주의 과음으로 인한 소량의 Co 와 alcohol
의 섭취도 십장병 발생의 원인이 된다고 하는데 19) 이 결과는 맥주 에 거품을 내기 위해서 사용되었던 Co 영의 첨가에서 많이 관찰되 었다。 *참고문헌 I) Underwood, E. J. , Trace Elements in Human and Ani m al Nutr i • - tion , Academi c Press Inc. New York and London, 1977. 2) Schroeder, H. A. , A. P. Nason and I. H. Ti pton , Essent ial Trace-Meta l s in Man, Cobalt , ]. Chron. Di s. , 20, 869, 1967. 3) Loff ler , G. and P. E. Petr ide s, in Weis s , L. and H. A. Harpe r,'. Phys io l og ich e Chemi e, Zweit Aufl ag e , Sp r in g e r Verlag, 578, 1979. 4) Pollack, S. , Georg, J. N. , Reg a , R. C. , Kauf m ann, R. M. and : Crosby , W. H. , J. Clin . Invest. , 44, 1470, 1965. 5) Forth , W. , Rummel, W. and Becker, P. J. , Med. Pharmacol. . Exp. , 15, 179, 1966. 6) Valberg, L. S. , in Skoryn a, S. C. and Waldron-Edward D. , Trace • Elements and Radio nuclid es, p. 257, Perga mon P~ess, Oxfo r d, 1971. 7) Harp, M. J. and F. I. Scouler, J. Nutr i t . , 47, 67, 1952. 8) Eng el , R. W. , Pric e , N. O. and Mi ller, R. F. , J. Nutr . , 92, 197,. 1967. 9) Marsto n , H. R. , Phy s io l . Rev. , 32, 66, 1952. IO) Houk, A. E. H. , A. W. Thomad and H. C. Sherman, J. Nutr i t . ,. 31, 609, 1946. 11) Underwood, E. J. , Nutr . Rev. , 33, 65, 1975. 12) Brewer, G. , Amer. J. Phys i o l. , 128, 345, 1940. 13) Ding le , J. T. , J. C. Health , M. Webb and N. Danie l , Bi o chem_ Bi op h y s. Acta . 65, 34, 1962. 14 ) Sederholm, T. , K. Kouvalain e n, and B. A. Lamberg, Acta , Med_ Scandin a, 184, V, 301, 1968.
15) Lang , K. , Bi o chemi e der Ernahrung 4 Aufl ag e , Dr. Di et r i c h 'Stei n k off Verlag, p. 351, 1979. 16) Morell, H. , J. C. Savoie and I. M. London, J. Bio l Chem. , 233, ·92 3, 1958. 17) Wi ls on, E. D. , K. H. Fis h er. and M. E. Fug u a, Prin cip le s of Nutr i t ion, Jo hn W iley and Sons Inc. 1975. 18) Guth rie , H. A. , Intr o ducto ry Nutr i t ion 3rd ed, The C. V. Mosby Comp a ny , 1975. 19) Ki rc hg e Bner, H. , E. Weig a nd, A. Schneg g, E. GraBmann, F. J. Schwarz and H. -P. Rot h, in Cremer, H. D. Hotz e !, J. Ki ihn au, Bi o - chemi e und phy sl olog ie d er Ernahrung Ba.n d I, Tei! 2, Georg Thie m e Verlag 29, 1980. 20) Mansto n , H. R. , Lee, H. J. and McDonald, I. W. , J. Ag r ic . Sc i. , 38, 222, 1948. 21) Underwood, E. J. and Harvey, R. J. , Aust. Vet. J. , 14, 183, 1938. 22) O'Halloran, M. W. and Skerman, K. D. , Br. J. Nutr . , 15, 99, ·19 61. 23) Andrews, E. D. , N. Z. Vet. J. , 13, 101, 1965. 24) Becker, D. E. , Smi th, S. E. J. and Loosli, J. K. , Scie n ce, 110, 71, 1949. 25) Ibbots o n, R. N. , Allen, S. H. and Gurney , C. W. , At st . J. Exp. Bi o l. Med. Sci. , 48, 161, 1970. 26) Marsto n , H. R. and Lee, H. J. , Natu r e, 170, 791, 1952. 27) Phil lipso n, A. T. and Mi tch ell, R. L. , Br. J. Nutr . , 6, 176, ·19 52. 28) Lee. C. C. and Wolte r in k , L. F. , Am. J. Phy si o l . 188, 173, 1955, Poult . Sci. , 34, 764, 1955.
11 요오드 (Iodin e , I) 갑상선이 비대해집으로써 생기는 갑상선중(g o it er) 은 기원전 30001 년경에 이미 중국에서 발견되었으며 이것은 해조류를 복용하면 치 유될 수 있다고 전해져 왔다. 1811 년 Couto i s 가 I 를 발견하고, 1820 년 스위스의 의 사 Coin d et 는 U) 당시 처음 발견된 I 가 해조류나 해면에 함유되어 있으며, 이 물질이 g o it er 를 치료하는 데 효과적이라고 지적하였다 .1 4) 같은 해에 Humbold t는 콜롬비아의 인디언들이 소금산에서 나오 는 소금이 go it er 에 효과가 있 다는 것 을 발표했고 Rumbolt 의 발표 에 의 해서 1822 년 프랑스의 과학자 Boussin g a ult 는 남미 를 여 행 하 ‘ 면서 I 를 함유한 소금을 사용하는 주민듄 사이 에 서 는 go it er 를 보 지 못한데 비해 보통 섬영을 사용하는 주만들간에는 g o it er 가 성행 하는 것을 발견하였다. 그는 이 접을 고려 하면서 go it er 방지에 I 가 중요한 요소라는 것을 지적하고 극히 소량이간 하나 I 가 필수적이 타고하였다. 1852 년 프랑스의 식 물학자 Chati n 은 I 결핍 이 go it er 와 관계 가 있다고 하였으며 1896 년 독일의 화학자 Baumann 은 갑상선에서 I 를 발견했다 .15) . 1899 년 Oswald 는 I 를 함유하고 있 는 교질상 (collo i d 狀)의 pr ote i n 인 thy r og lo bulin 에 대 하여 발표하였 다. 16) 1915 년 Kendall 은 m th y r oxin 호르몬을 추출하는 데 성공했고
1952 년 Gross18) 는 3. 5. 3' -trii od oth y r osin e 을 발견했다. 갑상선에 촌재하는 90% 의 I 는 유기물과 결합되어 있는 th y r o- glo bulin 으로서 분자량은 67, 000 이 고 0. 2~0. 9%의 I 를 함유한다 e Thy r og lo buli n 내 에 있 는 수용체 tyro sin e 도 I 를 함유한다. 그것 의 분해 산물로는 monoio d oty ro sin e (I T y r) 과 dii od oty ro sin e CI2 Ty r ) 그 리 고 이 들에 게 서 형 성 되 는 두 호르몬인 t e t ra i odo t h y ron i ne(T4) 과 trii odo t hy ron i ne(T3) 이 있 다. 갑상선 내에 있는 유기 1 의 분포는 다음과 같다. I Ty r : 17~28% T3 : 5~8% !2 Ty r : 24~42% T4 : 35% Thy r og lo buli n 내 의 tyro sin e 의 찬기 에 약 20 %의 I 가 함유되 어 있다. 위의 화학 구조석은 그림 11.1 과 같다 .l}
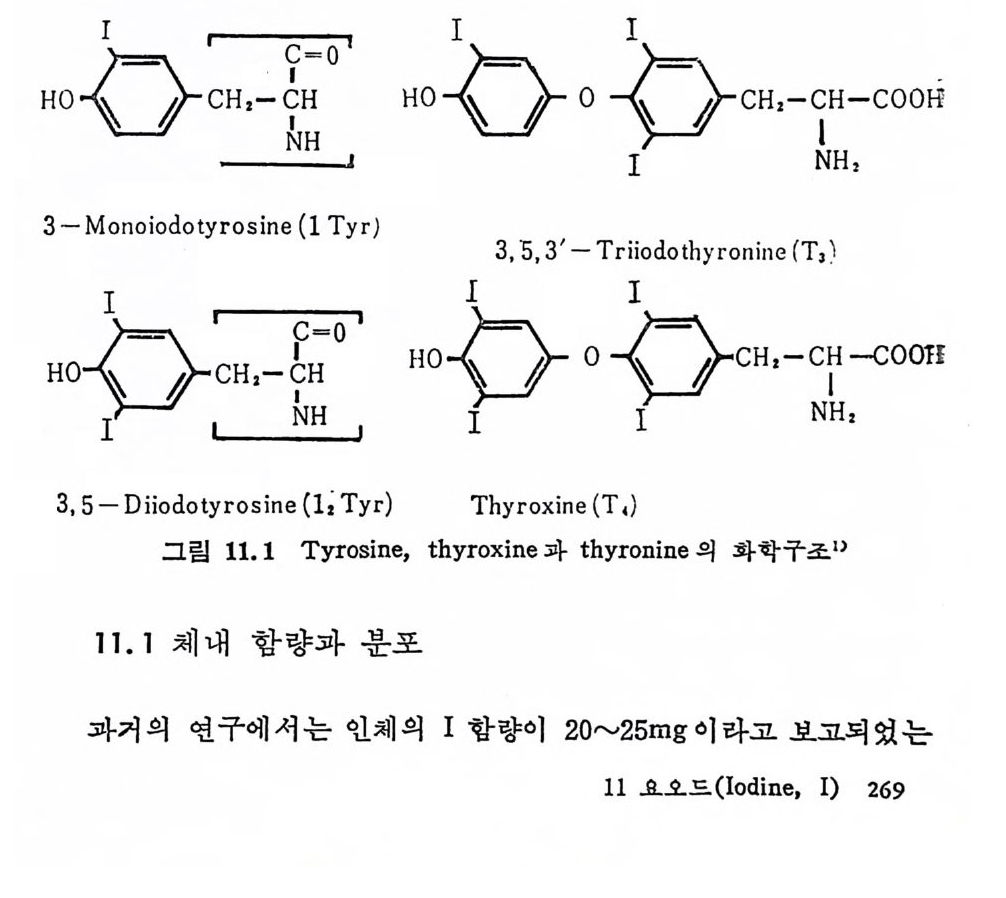 HOIO_C H' 2-{Hc=O I HIO O 。 七I >-cH, 가 H-COOH
HOIO_C H' 2-{Hc=O I HIO O 。 七I >-cH, 가 H-COOH
데 최 근 발표된 미 량원소의 분석 결과로는 그 함량이 10~15m g 2) 이 며 그 중 70~80% 가 갑상선에 농축되어 있고 그것의 전조물은 o.2 ~0.5% 의 I 를 함유한다고 한다. 그러나 I 의 함량은 1 의 섭취량, 나이 그리고 갑상선의 활성에 따라 영향을 받는다. 갑상선 이 외 의 조직 과 기 관은 0. 01~0. 02µg /g 정 도로 소량의 I 를 함유하며 간, 의분비선, 난소와 대반에는 그보다 몇 배 높은 양의 I 가 촌재한다. 혈장의 1 함량은 :::z.. 섭취상태와 깊은 관계를 가지며 보통 1~6µg / l 이다. 조칙과 혈액에는 유기물과 결합되어 존재하며, 혈액의 혈장 단백 질 인 T4 는 a-gl o buli n 과 pre albumi n 이 결 합된 상태 로 되 어 있다. 혈청 의 T4 농도는 40~l20µg / l 이 고 L 은 1~1. 5µg / l 인데 그 중 에서 0.03~0.3% 는 결합되어 있지 않은 상태이다. 식품 중에서 우유는 소가 섭취하는 사료의 I 함량과 밀접한 관계 가 있 다. 정 상적 인 성 숙유는 40 ~80µg /t 룹 , 초유는 50~240µg / l 룰 함유한다. 11 .2 주요 기능 I 의 가장 중요한 필요성온 갑상선호르몬의 구성성분이 된다는접 이다. I 의 체내 대사작용은 갑상선 호르몬의 합성과 분해, 그리 고 아 호르몬의 재이용과 I 의 분비에 있다. 갑상선의 I 이온은 능동적 수송에 의해서 I- p um p로서 혈액을 통하여 운반되 고 처장된다. 단백 질 결합체 인 th y r og lo buli n 안에 수 없 이 존재 하는 th y r osin e 분자는 요오드화하여 3-monoio d oty ro s- ine 과 다량의 3, 5-dii od oty ro sin e 이 생 성 된다. 갑상선 호르몬은 단백 질 분해에 의 해 서 th y r og lo buli n 을 만들며 필요에 따라 혈액으로 이동한다. 반면 갑상선에서 생성된 iod ot- yr osin e 은 탈요오드화하여 여 기 에 서 얻어 진 I 는 다시 호르몬합성 에 이용된다. 또한 I 는 갑상선, 뇌하수체, 시상하부 호르몬에 의해 저도 회전하며 체내에서 정상적인 형액의 호르몬농도를 유지하기
위한 작용을 한다. 뇌하수체 전영에서 분비되는 th y r otr o p in 호르몬은 T4 함량의 감 소와 hy po th alamus(TSH-releasin g fa c t or) 의 새 로운 분비 액 에 의 해 서 자극을 받는다. 회 전하는 th y r otr o p in 은 갑상선 호르몬의 생 성 과 -th y r og o lbuli n 의 분해 를 촉진한다. 갑상선 이외의 다론 조직에서는 대부분의 I 가 갑상선 대사 과정 을 동하여 특정한 탈 요오드효소에 의하여 생성되며 이것은 다시 체내의 I- p ool 로 흘러들어간다(I회로). 인체의 I 반감기는 평균 , 64 일이 다 .3) 1 가의 음이 온인 p~ rchlorate , rhodanid e 와 nit ra te 는 갑상선의 I 축적 에 영 향을 준다. 다론 th y r osta t i ca 는 요오드화하는 것 을 방 해 한다. 여 기 에 는 자연에 촌재 하는 식 물의 thi o g ly c osid e , 그 중에 서 도 brassic a 종류의 L-5-vin y l -a-th io o xali do n 이 다. 갑상선은 두 영으로 구성되어 있고 기관을 횡단한 막과 연결되 어 목 아래쪽 가까이에 자리잡고 있다. 이 기관은 대단히 작으며 성인의 갑상선은 약 25g 정도이다. 이 갑상선 조직 내에서 th y ro- - x i ne 을 형성하는 I 는 세포 내에서 일어나고 있는 열량대사를 조절 하는 기 능을 갖고 있 다. 그러 므로 정 상적 인 th y r oxin e 의 공급은 신 체와 지능발달을 순조롭게 할 분만 아니라, 신경과 근육조직, 순환 기 관 그리 고 모든 영 양소의 대 사기 능을 원활하게 조철한다. 11 .3 대 사 식이에서 섭취된 요오드는 i od i de 형태로 소장벽을 통하여 홉수되 나 일부는 위에서 직접 혈류로 홍수되기도 한다. 이외에도 내분비 선과 의분비선의 소화기관에서도 갑상선과 마찬가지로 높은 농도로. 흡수된다. 다른 iod ate 는 iod id e 형 태 로 환원되 어 서 흡수된다. I 의 흡수속도는 대 단히 빨라서 섭취 후 3~6 분이 면 흡수된다. I 의 흡수는 능동적 으로 energy 가 필요하며 I-Na pu mp 에 의 해 저 이 동된다. 에 너 지 를 요구하는 홍수는 cy a nid e , din i t ro p h enol 또 는 ouaba i n 에 의하여 여제되기도 한다.
그립 11.2 에서 보는 바와 같이 세포내 1 화합 물 은 2 개의 p ool 로 . 촌재한다. 그 중 하나는 혈액의 I 화합물과 자유로운 교환이 가능한 것이고, 다른 또 하나는 이용되지 않은 i odo ty ros i ne 에서 I 를 제거 할 때 합성 된다. Thio c y a nate , pe rchlorate 및 pe nte c hneta t e 는 I 화 · 합물과 흡수기작에서 서로 경쟁적이며 갑상선에서 교환이 가능한 I 의 급속한 배출을 초래한다. 갑상선 내에 있는 I 화 합 물 은 산화된 후 heme 함유인자에 연결되어 있는 p erox i dase 에 의하여 tyro sin e - 으로 이 전된다. 이 작용에 산소의 급원으로 H2 야 가 요구되 는데 H2 아는 cy toc h r ome C reduc t ase 와 NADPH 의촌형 효소에 의하
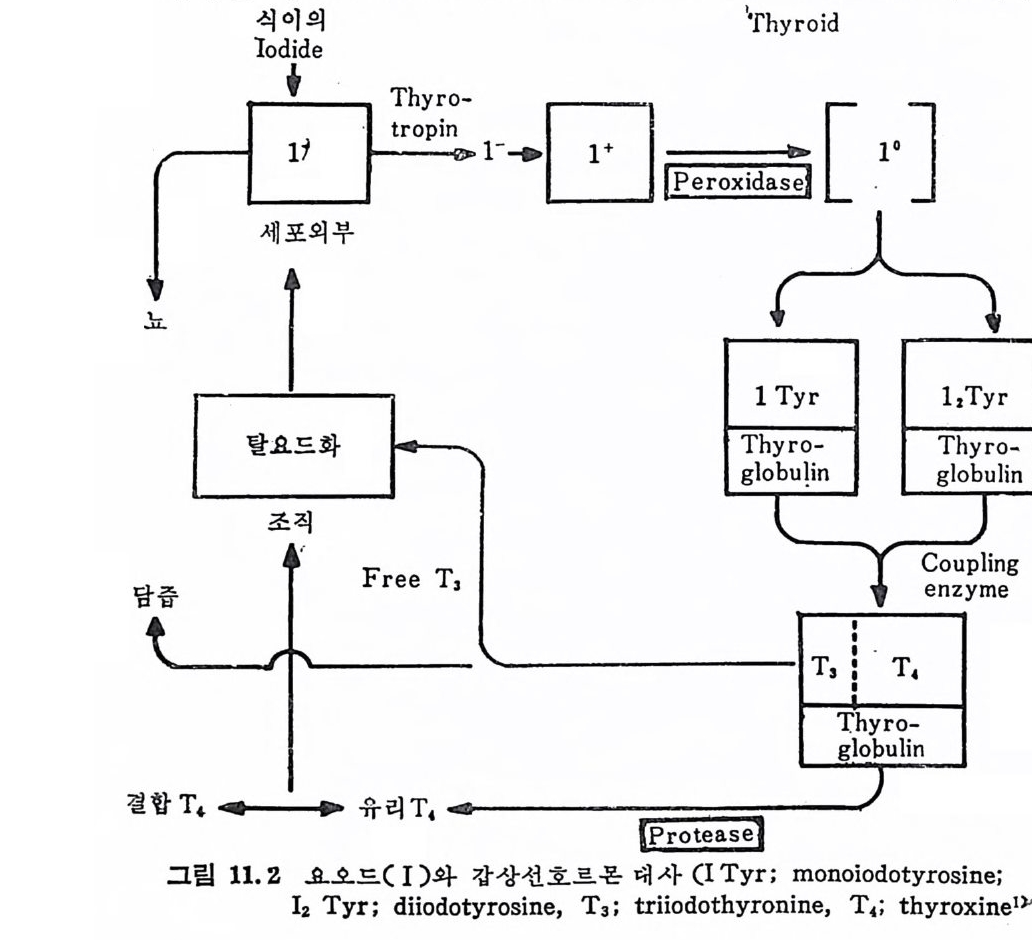 I식od이ii d의 e Thy ro -1 -. . .. 曰二百'三fhy 〔ro id I' 〕
I식od이ii d의 e Thy ro -1 -. . .. 曰二百'三fhy 〔ro id I' 〕
여 생성된다. 유리 I 는 pe roxid a se 반응에서 I 를 공급할 수 없고 :::z.. 대신 t h y rox i ne 과 I 의 유리기가 효소의 활성부위에서 결합되고 t h y ro t ro pi n(TSH) 은 이 반응의 자극에서 활성화된다. 수용성 ty ros i ne 은 당단백질인 th y r og lo buli n 내에 존재하며 분 자량이 660, 000 이 고 115 개 의 tyro sin e 찬기 를 함유한다. 홍수된 대부분의 I 는 갑상선 조직으로 유도되며 갑상선 조직 내 I 의 함량은 혈액 내의 1 치보다 약 25 배나 더 농축되어 촌재한다. I 의 흡수율은 갑상선 호르몬의 양에 직접적으로 영향을 받고 있다. 1 가 혈류롤 따라 이동될 때에는 유리상태와, 단백질과 결합된 (pro te i n bin d in g iod in e , PBI) 두 가지 상태 이 다. 단백 질과 결합된 I 는 갑상선기능 상태에 직접적으로 영향을 받는다. PBI 치는 임산이~ 갑상선기능이 항전되면 상승되고, 반면에 갑상선기능이 처하되면 PBI 치도 낮아진다. 그러므로 PBI 치를 측정한다는 것은 갑상선 기능 여하를 시험하기 위해 사용하는 기초대사량을 측정하는 것보 다 더 효과적이다. 대변으로 배설되는 I 는 체내의 I- p ool 에서 T4 와 간에서 I 의 분 해산물인 glu curonic a ci d 는 어느 정도의 sul fat e 와도 결합하여 담 즙을 거쳐 장으로 배설된다. 일부의 T4 는 다시 재홉수된다 (en t e rohep a ti c cy c le). 성인의 정상적인 I 배설은 대변을 통하여 되고 5~ 20µ g /1 일 혹은 그 이상이며 뇨몰 통해서는 io did e 만이 배설된다. 죽, 위에서 말한 대변과 소변이 I 의 중요 배설로이다. Fo lli s” 는 뇨로 배 설되 는 I 의 양이 5~10 살까지는 정상보다 낮은 35µg /g creati nine 이 고, 청 년들은 50µg /g, 성 인은 75µg /g 이 라고 한다. 콩팥의 I 는 보통 지 속적 인 clearance 로 약 30~40ml/ 분을 제거해 주며 혈장의 I 는 농도에 따라서 배설량도 달라지고, 이~ 또한 갑상선의 활성과 I 섭취에 의하여 영향을 받는다. 뇨로 배설되는 I 는 간접적으로 혈장의 I 함량과 I 상태를 나타내 준다. 홉수된 I 는 빠른 속도로 체내의 내인성 I - p ool 과 교대된다. 땅으로 배 설되 는 I 의 양온 5~l2µg / l 로서 아주 져온 양이 분뱌 된다. 수유기에는 혼히 I 가 유줍을 동해 분비되기도 한다.
11 .4 섭취 량과 필요량 Sche gfe r10) 와 Colem 둥에 의 하면 인체 에 있 어 서 의 I 섭 취 량이 44~162µ g /1 일일 때에 po sit ive balance 이거나 또는 평형이었다고 한다. 보통 I 의 필요량은 100~200µ g /1 일로 되 어 있 는데 1~9 세 어 린 이 들은 다소 낮은 편이 며 임 신부, 수유부는 많은 양을 필요로 한다. 독일의 Deuts c he Gesellschaft fur Ernahrun g 12) 에 서 는 어 린이 들 의 하루 섭 취 량을 50µg , 청 년과 성 인은 150µg 을 권장하고 있 다. 직물성 식품을 주로 섭취하고 g o it er 에 걸릴 요인이 있는 사람은 I 를 더 많이 팔요로 한다고 했다. I 결핍증이 유행되는 지역을 보 떤 음료수의 I 함량이 0. 2~2µg / l 로서 아주 낮은 인체 필요량을 충즉시키기에는 너무 적은 양이다• 동석물 식품의 I 함량은 지배되는 환경과 제조과정에 따라 다르 다. 예를 들어 I 가 함유된 토양과 물, 되비(밑거름), 동물의 I 섭 취상태, 제조과정, 조리과정은 밀접한 관계가 있다. 그러나 동식물 식품의 I 함량만으로는 필요량을 충족시키기엔 충분치 못하다.최 근· 독일에서도 갑상선종이 많이 발생하는데 북쪽에서 남쪽으로 내 려 갈수록 이 중상이 많이 나타난다고 한다. 4)5) 효과적 인 예 방 방법 으로는 소금에 I 를 강화하여 섭취하는 것안데, 5~lOµg /g po ta s - .siu m iod in ide 나 po ta s siu m iod in a te 형 태 로 강화된다. 11 .5 결핍증 I 섭취가 부족할 때 갑상선에서 호르몬을 충분히 합성하지 못하 므로 감상선종 (s i m p le go it er , endemi c g o it er) 에 걸 릴 우려 가 크다. 뇌하수체 에 서 의 th y r otr o p in 과다분바 는 갑상선을 비 대 하게 한다. I 섭 취 는 충분하나 T4- 합성 이 th y r osta t i ca 의 영 향을 받을 때 도 역 지 갑상선이 비대해진다. I 결핍울 타액에 들어 있는 I 를 방사선 동위원소로 측정할 수 있
듯이 혈장의 단백질과 결합된 형대의 I 로 갑상선의 기능을 측정하 게 된다. WHO 에서는 I 결핍증을 뇨의 I 배설량을 동해서 3 둥급으로 분리 했다. 제 1 등급은 go it er 가 유행 하는 지 역 으로 50µg /g creati ni n e 을 배 설했을 때이고, 제 2 등급은 I 배설이 25~50µg /g creati ni n e 배설 로 h yp o t h y reos i s 의 위험성을 갖고 있다. 제 3 등급은 더 져온 양이 뇨로 배 설되 는 지 역 만들에 게 지 방변성 creati ni s m 이 나타나는 것 이다. Sim p le go it er 는 기 초대 사량도 정 상을 유지 하는 등 갑상선이 바 대해지는 것 외에는 별다론중세가보이지 않는다. 그러므로 sim p le · go it er 환자는 기형적인 외모의 불편을 느끼면서도 생활할 수 있으 나 접차로 비대해진 갑상선조직의 중량이 기관에 압력울 가하여 호 홉에 곤란을 가져 오게 된다. 치료에 있어서는 비록 I 로서 g o it er 는 치료되었다 해도 이미 비 대해전 갑상선은 조직의 일부를 철단수술하거나 갑상선으로 통한 혈관을 동여 맴 (lig a ti n g)으로써 갑상선조직 의 증식 을 조철하여 sim p le - g o it er 를 치료한다. Creati nis m 은 청 년기 와 계 속되 는 I 부족중 임 신부에 서 출산한 어 란이에게서 혼히 볼 수 있는 현상이다. Crea tini sm 의 어란이는 십 한 hy po th y r oid i s m 으로 고충이 십하며 신체 적으로는 성 장부진으 로 복부만 비대한 난장이와 같은 인상울 주고, 지능은 극도로 되화 되어 마치 백치처럼 된다. 특히 crea tini sm 에 걸려 있논 어린이는 원숭이의 일종인 a p e 와 같은 인상이 특칭이다. 출생 후에 죽시 치 료하면 완쾌되나 그렇지 못할 경우 일생 동안 치유되지 못한다. 성 장 과정에서도 h yp o t hy ro i d i sm 의 증세를 지닌 채로 지내고 성인이 되 면 접 액 수종 (m y xoedema) 에 의 하여 얼굴과 손에 부종이 생 기 고 피 부는 건조하고 두꺼워진다. 감기 같은 질병에 대해서도 처항력이 약해지며 음성은 쉰 듯한 소리를 내게 된다. 이 의 에 도 갑상선 기 능 항전중 (h yp o t hy ro i d i sm), 혹은 안구 돌출성 갑상선종 (exo p h t halm i c g o it er) 이 있는데 그것 의 원인은 아직 완전하
규명되어 있지 않다. 이 경우에는 때때로 기초대사율이 100% 나 증 가하기도 한다. 치료로는 비대해전 갑상선을 수술로 제거하는 방법 과 약물치료, 또는 방사선 동위원소 I131 을 복용함으로써 갑상선의 기능을 여제한다. I 가 갑상선 조칙에서 t hy rox i n 을 형성하는 데 방해하는 물질을 go it ro g e n 이 라고 하며 이 는 겨 자류의 종자, 양배 추, 무우청 , cau- liflow er, 벨기 에 산 양배 추와 같은 채 소에 많이 함유되 어 있 다. 그 러므로 이런 생채소를 장기적으로 다량 섭취하면 go it er 중세가 나 타나게 된다. 생채소 내에 함유되어 있는 g o it ro g en 은 가열함으로써 그 기능을- 상실한다. Thio u racil 과 sulfa 제 는 th y r oxin e 형 성 을 저 지 하여 go it er 를 발 생케할 우려가 있으므로 이런 약품을 복용할때에는 충분한 I 를 섭 취해야한다. 11 .6 함유 식품 일반적으로 해조류를 포함한 해산물에 I 가 풍부히 함유되어 있 다. 그러나 같은 종류의 식품이라 할지라도 생산지 재배조건에 따 라 I 의 함량에 큰 차이가 생기게 된다. 표 1 1. 1 은 1 의 급원 석품이다.
 표 11. 1 요오드 CI ) 급원 식 품 6)
표 11. 1 요오드 CI ) 급원 식 품 6)
-V ou g h t가 대사 연구에 사용한 식품에 함유된 I 함량은 표 11.2
이 다 •7)
 표 11.2 lOOµg 요오드 Cl) 를 섭취하기 위해서 팔요로 하는 식
표 11.2 lOOµg 요오드 Cl) 를 섭취하기 위해서 팔요로 하는 식
표 1 1. 3 은 여러 나라의 석영에 강화된 I 함량이다 .7)
 표 11. 3 요오드 CI ) 를 강 화 한 요오드 CI )영 7)
표 11. 3 요오드 CI ) 를 강 화 한 요오드 CI )영 7)
미국을 포함한 세계 여러 나라에서는 식영에 I 를 첨가한 I 강화염 을 사용할 것을 권장하고 있다. I 는 go it er 가 많이 발생 하는 곳의 음료수에 0.1~2. Oµg / l 함유되 어 있고 발생하지 않는 곳은 2~15µ g /l 가 함유되어 있는것으로나 타났다. 11.7 독 AJ Wol ff 13) 는 I 를 2m g /1 일 섭 취 시 인체 에 유독하다고 했는데 이 는 갑 상선에 서 hy pe rth r eose 가 나타나기 때문이 다. 건강한 갑상선을 갖 은 사람들은 많은 양의 I 도 찰 받아들이는 데 비해 I 결핍에서 오
는 go it er 환자들은 I 를 하루 SOOµ g /1 일 이 상 섭 취 시 켰 을 때 th y r o, to xic o sis 가 발생한다. 5) 이 증상은 먼저 각 관절의 중생 (hy pe r pla sia ) 혹은 전체 내 분비 선의 촉진현상 (I - basedow) 을 나타낸다. 쥐를 대상으로 한 실험에 있어 과량의 I 를 사용하면 성장부전, 불임중, 수유장애가 일어났다. 500 pp m 의 I 를 시료에 첨가했을 때 수유에 장애를 받았으며 새끼들의 사망률이 높았다. 2,500 pp m 의 I 첨가시에는 새끼들이 모두 사망했다. 2,500 pp m 의 I 를 실험쥐에 ` 게 섭취시켰을 때는 생식능력이 감퇴되었다 .8) *참고문헌 I) Harpe r, H. A. , V. W. Rodwell and P. A. May e s, Revi ew oJ Phy s to log ica l Chemi st r y , 17t h ed. , Lang e medic a l pu bli ca ti on s, 527, 1979. 2) Ri ggs , D. S. , Pharmacol. Rev. , 4, 284, 1952. 3) Hein r ic h , H. C. and Gabbe, E. E. , !Gi n . Woche ns clzr. , 42, 1248, 1964. 4) Hazel, D. , Pie t r z ik , K. and Thomas, M. , Ernii hr . Umsch. , 23, 244, 1976. 5) Horn, K. , Habermann, J. and Scrib a, · P. C. , in Gladtk e, E. and· Hein e mann, G. , Eckert, I. , Sp u renelemente p. 174, Georg Thie m e, St u tt ga rt, 1979. 6) 이 기 열, 문수재 , Ii'기 초영 양학』, 수학사, 194, 1979. 7) Lang , K. , Bi o chemi e der Ernii hr ung , 4, Aufl ag e Di et r i c h Ste · - ink ohof f Verlag, p. 367, 1979. 8) Ammermann, C. B. , L. R. Arrin g ton , A. C. , Warnic k , J. L. Ed- wards, R. L. Shir l ey and G. K. Davis , J. Nutr i t . , 84, 107, 1964. 9) Foll is, R. H. , Am. J. Cl in. Nutr . , 14, 253, 1963. IO) Sceff er , L. , Bi o chem. Z. , 259, 11, 1933. 11) Cole, V. V. and Curti s, G. M. , • J. Nutr . , 10, 493, 1935.
12) DGE, Emp feh lung e n fu r di e Ni ihr sto f fzuf uh r der Deuts c hen Gesellschaft fu r Ernii hr ung , 3, Aufl . Umschau Verlag, Frankfu r t M. 1975. 13) Wolff , J. , Am. J. Med. , 47, 101, 1969. 14) Coin d et, M. , Ann. Chin . Phy s. , 15, 49, 1820. 15) Chati n, A. C. R. , Acad. Sc i. , 34, 14 and 51, 1852. 16) Osward, A. , Z. Phy si o l, Chem. , 27, 14, 1899. 17) Kendall, E. C. , Trans. Assoc. Am, ph y si c ia-n s 30, 420, 1915 。 18) Gross. J. and Pi tt-R i ve rs, R. , Lancet I, 439, 1952.
12 불 소 (Fluor i ne, F) F 는 18 세기경에 fluo rin e 정제가 사람의 충치예방에 유효한 것이 라고 이 야기 되 었으나 학문적 으로는 1938 년 미 국의 치 과의 사 Dean25) 이 음료수에 함유된 F 와 충치오回 관계 를 발표한 이 후부터 활발하 게 연구되 기 시 작하였 다. 1945 년부터 미 국과 캐 나다는 음료수에 lmg // F 를 첨가해 줌으로써 청소년들의 충치 발병률을 50~60% 까지 감소시킬 수 있었다. 최근에는 세계 여러 나라의 국민들이 F 가 첨가된 음료수 섭취로 청소년분만 아니라 성인들에게도 충치예방 에 좋은 효과를 보여 주고 있 다고 한다. 4}8)21)22) 1960 년대 골다공중과 23)24)29) 다른 무기 질 감소중 환자에 게 sodiu m ·fl uo rid e 로 치 료한 결과 back pa in , bone densit y, Ca balance 에 좋은 효과를 주었다고 했으며, 일부 F 함량이 높은 지역에서는 골 다공증이 적었다고 했다. F 는 치아의 건강뿐만 아니라 어른의 정 성적인 골격유지에도 매우 중요한 효과를 보였다고 한다.1) 12.1 체내함량과 분포 성 인은 골격 에 2~6g 의 FC200~600p pm fat free bone) 롤 함유하며 치아에도 같거나 약간 적은 양이 함유되어 있다. 체내의 F 는 전체 의 95% 가 골격에 함유되어 있다. 골격에는 뼈의 치밀질보다 뼈의 해면질에 F 가 많이 함유되어 있다. 치아내에서도 부분에 따라서 F
의 함유량이 다르다. 가장 많이 함유되어 있는 곳이 치아의 백악질 부분이다. 나이가 들어감에 따라서 치아의 F 함량은 F 섭취와 밀 접한 관계를 갖는다. 연조직의 견고질에는 나이와 관계없이 lpp m 이하의 F 를 함유한다. 예를 들어 태반아나 동맥에 높은 농도의 F 가 촌재하는 것은 조직의 석회화 때문이다. 사람의 혈장에는 0.1~ 0. 2p pm 의 F 가 두석 (d i al y s i s) 이 될 수 없는 형 태 로 존재 하며 그의 일부만 유리 혈청 의 F 로 (0. 01~0. 02p pm ) 존재 한다. F 섭 취 시 일시 적으로 혈장의 F 가 상승하면 몇 시간 이내에 F 농도는 정상으로 되돌아온다 .2) 다른 체액, 죽 체액, 타액, 담즙 둥의 F 함량은 혈 장의 F 함량과 비슷하다. 또한 모유의 F 함량도 마찬가지이다. 12.2 주요기능과 결핍증 1972 년 Schwarz 와 M ili ne19) 이 F 를 첨가한 고도로 정제된 석이 를 격리되어 있는 쥐에게 섭취시켰을 때 성장이 촉진되었다는 보 고에 서 부터 F 가 tra ce element 의 필수 요소임 을 입 증시 켜 주었다. 미량의 F 는치아와골격형성에 중요하다. 충치에 대한 F 화합물 의 보호작용은 많은 연구결과에서 3)4)2 1) 22) 확증되어졌다. 치아 발 생에서도 충치예방의 기전과 같이 F 의 보호 효과는 유년시철에 가 장 중요한데 이 시철은 치아를 형성하는 시기이기 때문이다. 그립 12.1 은 학생들의 음료수에 첨가된 F 섭취와 충치발생과 그 리고 불소침착증 발생과의 관계를 나타냈다. 충치 에 대 한 F 의 효과는 물리 화학적 작용에 의 하여 enamel 층을 견고히 해주고 구강내 박테리아가 생산한 산에 의해 부석되는 현상 울 방지하는데 있다고 한다 .4) 죽 충치가 발생하는 것은 치아의 -enamel 층에 p la q ue 가 형성되기 때문이다. 이 p la q ue 는 고농도의 dex t ran 이 축적된 것이며 여기에 산을 생성하는 박테리아가 촌재 하기 때 문이 다. Dextr a n 은 서 당, 포도당, 과당으로 구성 된 이 당류 제 서 anerobe str e p toc occus 에 의 해 서 합성 된다. 또 다론 원인은 저 분자 당질 인 서 당이 str e p toc occus 이 나 lacto bacil lus 에 의 해 서 형기적 해당과정을 거쳐 p la q ue 를 생성하기 때문이다. 산의 형성으
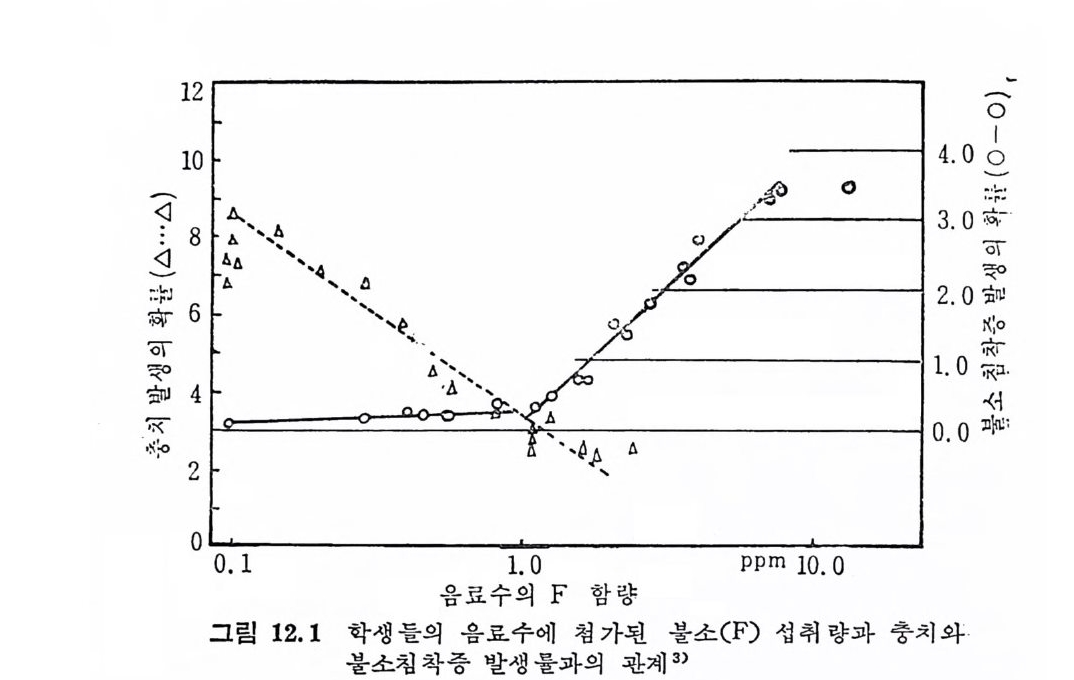 1210 』
1210 』
로 인해서 p H 가 낮아지고 enamel 충에 무기질 감소중이 일어난다 .. 그로 인해서 치골과 백악질 부위에는 박데리아에 의해서 단백질 분 해현상이 일어난다. 이때에 F 는 박테리아의 형기적 해당과정의 endolase 작용을 방해하여 유산생성을 막는다. 그러나 어떤 생화학 적 기작에 의해서 dextr a n 형성이 저해되는지는 완전히 규명되지 못한 상태이다. 그러나 충치예방과 치료의 F 효과는 한번에 섭취하 는 F 정제나 식품보다는 음료수에 함유된 F 로 자주 치아를 씻 어 내는 것이 훨씬 효과적이라는 것이 발표되었다 .2) 또한 F 의 물리 화학적 작용의 효과는 치아와 려의 무기질 부분 에 서 일부의 hy d roxy la p a ti ts 의 수산기 가 F - 인회 석 으로 합성 되 는 · 데 있을 것이라고 추측하고 있다. 최근 F 에 대한 관심은 F 가 정상적인 hema t oc rit의 농도와 번식 및 성장에 필요하다고 한 몇몇 보고에 의해서 더 고조되었다. 쥐의 임신기간 동안 낮은 F 섭취는 쥐에게 he ~ a t ocr it의 농도를 감소 시켜 주었으며 5) 번석의 감소를 초래했다. 이러한 조건들은 음료수 Iml 당 50µ g의 F 를 섭취했을 때 방지되었으며 이 양은 사람과 설 치류 둥의 실험에서 독성의 효과가 없었다.
골격 에 는 F 의 섭 취 시 cit ra te 와 carbonate 함량이 감소되 었 다. 이와 같이 소량의 F 가 내사과정이나 효소의 작용을 저해하는 기능 도 갖고 있 다(표 12. 1).
 표 12.1 효소와 대사작용에 저해를 할 수 있는 불소 (F) 의 양 6)
표 12.1 효소와 대사작용에 저해를 할 수 있는 불소 (F) 의 양 6)
노년 특히 페겅 후의 여성에게 일어나는 골격 구조 유지의 결함 인 골다공중 발생에 대하여 F 가 보호작용을 가졌다는 것도 보고된 바 있 다. Fuchs20) 는 골다공증을 치 료하기 위해 서 3 가지 종류 캅셀 의 효과를 27~28 세의 전은 여성을 대상으로 측정했는데 캅셀 A 는 natr i u m fl uoro 로서 18.2mg F 가 첨가되어 있으며 소장에서 용해 가 되 며 B 는 natr i u m fluo ro p hos p ha t e(Na2FP03) 로서 20mg F 가 첨 가되 어 있 고 C 는 Na2FPOa 와 calciu m g lu conate 가 혼합된 것 으 로 17. 85mg 의 F 와 31. 9mg calciu m 이 첨 가되 어 있 는 것 이 었 다. 그림 12.2 는 골다공증 치료를 위해서 3 가지 종류의 캅셀을 섭취 시킨 후의 흡수속도와 혈장 F 의 농도를 나타낸 것이다. 캅셀 A 의 흡수는 80.5%, B 는 100%, C 는 91% 였으며 이 질병의 치료효과 · 논 F 가 흡수된 후 오랫동안 신체에(특히 뼈부분에) 정체하는 데 있기 때문에 캅셀 C 가 Ca 함유 때문에 더욱 효과적이라고 한다. 그의에도 수도물의 F 첨가는 여러 가지 질병 예방에 효과가 있다
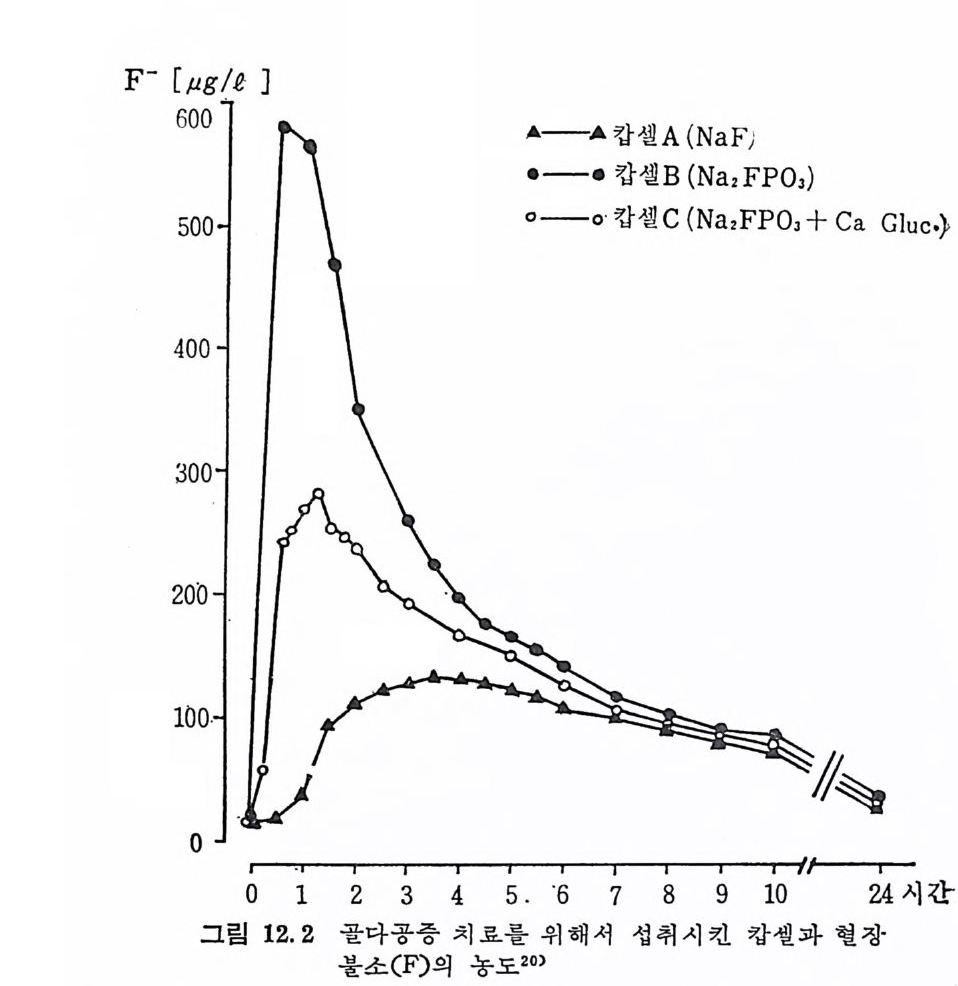 F-[6 µ00 g ../. t ] ..._ 쇼 캅셀 A (NaF;
F-[6 µ00 g ../. t ] ..._ 쇼 캅셀 A (NaF;
논 것이 동물과 사람의 실험에서 입증되었다 .7) 12.3 대 사 영양 생리학적으로 중요한 F 는 유기 F- 화합물로서 체내에서 F 가 유리된다. F- 유기화합물은 사람의 음식에 촌재하지 않는다. 음 빠 식과 음료수에 함유된 F 는 장과 위에서 확산에 의해서 80~100%, 흡수된다. 쉽게 용해되는 F 는 빠른 속도로 흡수되며 공복일 떄 는 고농도의 F 도 거의 전부 흡수된다. 쉽게 용해되지 않는 F( 예 ;.
fluo roap a t ite 나 식 품에 함유된 CaF2) 의 흡수속도는 느리 며 2/3 장 도밖에 흡수되 지 못한다. 8) 음료수의 가용성 F 화합물은 영 소와 동 일하게 분포되며 그 대부분은 세포 외액에 촌재한다. 미국의 영양 섭취 연구에서 성인남자의 매일 F 섭취량은 약 4m g 이었으며 섭취량의 철반이 음료수에서 섭취되었고 겉보기 흡수율와
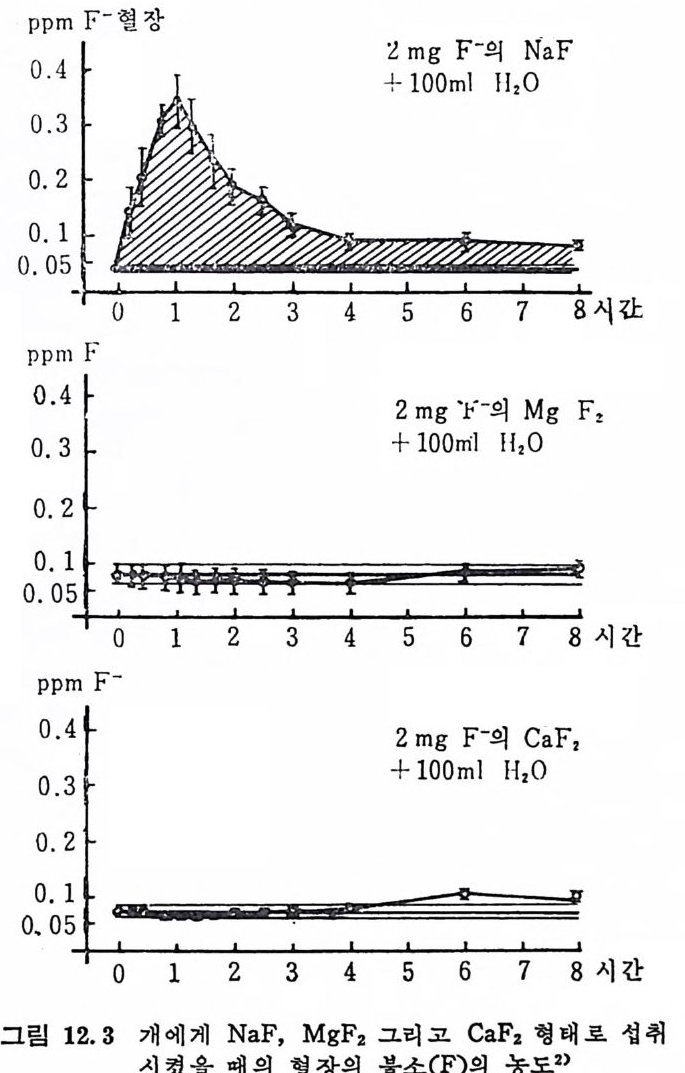 pp m F - 혈장
pp m F - 혈장
:9 0% 가 식품의 F 에서 섭취되었다고 한다. 높은 양의 Ca, Mg , Al 은 F 의 홍수를 감소시켰다. 그립 12. 3 은 개 에 게 NaF, M gF 2 그리 고 CaF2 를 구강으로 섭 취 지 켰 을 때 의 F 량이 다. 2) 그림 12.4 는 개에게 F 를 섭취시켰을 때 같은 양의 NaF(2m g)이
 p0p.m4 F ~ 혈 장 +2 1m0g0 mF l - 의1 1,N0 aF
p0p.m4 F ~ 혈 장 +2 1m0g0 mF l - 의1 1,N0 aF
타도 NaF+lOOml H20 때가 흡수율이 가장 좋고 NaF 와우유 그리 고 NaF+ 유아분유일 때는 혈장의 F 가 적게 흡수되는 것을 보여준 다. 사람에 있어서도 조반 후 혈장의 F 농도가 감소되는 것을 볼 수 있는데 그 원인이 느린 흡수 속도에서 오는지 혹은 적게 흡수되 는지에 대해서는 연구되고 있다 .10) 혈장의 F 농도는 0.1~0.2pp m 정도로 일정하게 유지되며 과량의 F 는 뼈의 F- 인회석으로서 처장되어지고 또는 뇨로 배설된다고 한 다. 뼈와 치아의 F 는 100~600p pm 정도로 나타나 있고 나이가 많아짐 에 따라서 려 의 F 함량이 중가된다고 한다. 11) 태아와 신생아에서 척추와 갈비뼈는 5~150p pm F 를 보유하며 F 농도가 낮은 지역에서도 태아의 뼈에는 40~47 pp m 의 F 가 함유되 어 있어 태반이 F 의 축적 및 이동을 조철하고 있다고 본다 .12) 여 러 가지 F 함유 화합물을 보면 F 나 fluo rop yru vate 와 같은 것 은 성장과정이나 Fe 대사에서도 이용될 것이라고 하며 hexafl uo - -ros il ic a te 와 monofl uo rop h osph ate 는 쥐 에 게 쉽 게 이 용되 지 않는 다고 한다 .13) 사람의 혈청에는 F 의 대부분이 유기화합물로 촌재하 러 F 함유 화합물은 단백질이 아니라 지용성 유기산이다 .14) 식품으로부터 F 를 충분히 섭취하면 대변으로 보통 1 일 0.2m g이 하를 배설한다. 그 중 일부는 내인성 F- p ool 에서 배설된다• F 의 주요 배설로는 신장이다. 뇨의 F 배설량은 섭취한 . F 와 흡수된 F 와 밀접한 관계가 있다. F 의 섭취상태의 변화는 장기간 동안 천천 히 나타나는데 그 원인은 높은 F 섭취시 F 를 항상 뼈에 저장해 놓 기 때문에 부족시 뼈에 저장된 F 를 이동해 주기 때문이다. 또한 소량은 땅으로 배 설되 기 도 한다 (0. 3~O. 6µg /m l). 그림 12.5 는 성인의 F 대사를 나타내고 있다 .15) 청 소년의 F balance 는 po sit ive 로서 섭 취 F 의 50% 를 보유한다. 성인이 되면서 뼈의 F 농도는 섭취량에 영향을 받는다. 성인은 F 의 섭취가 부족될 때 높은 양의 F 를 섭취시키면 몇 주 안으로 섭취 와 배설이 균형을 취하게 되고 계속 하루 팔요량을 섭취하게 되면 일정량이 뼈에 보유된다. 그 후부터는 섭취, 보유, 배설 그리고 뼈에서의 이동이 평형을
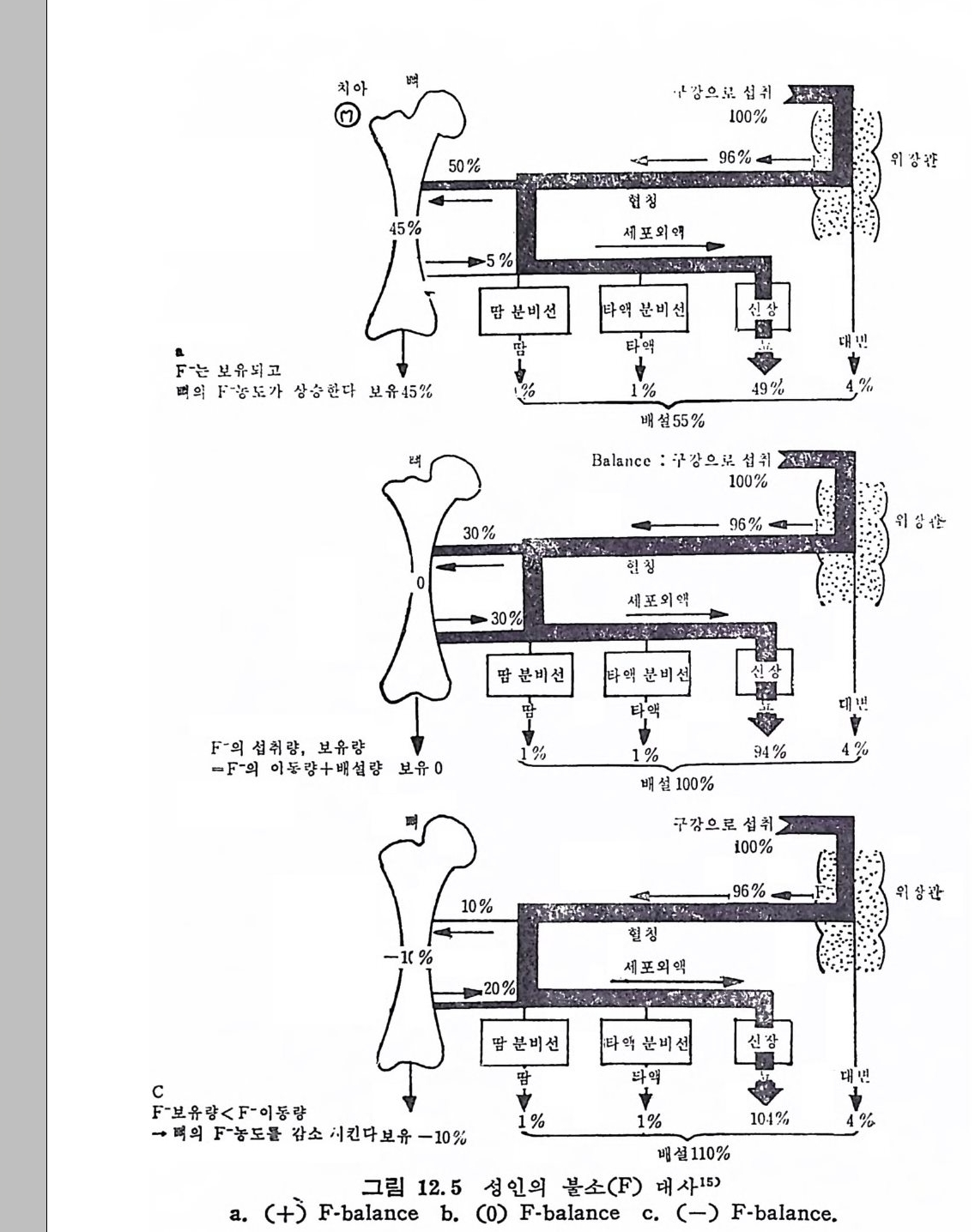 @病 떠 -<)--I l -· 상- 으9보 61% 0십0 %쉬 .,.1.....4 . 길 . . o, 4°., .t. '
@病 떠 -<)--I l -· 상- 으9보 61% 0십0 %쉬 .,.1.....4 . 길 . . o, 4°., .t. '
이루게 된다. 만약 F 섭취가 부족되면 뼈에 보유된 F 가 혈액으로. 이 동되 어 F-balance 는 neg at i ve 가 된다. 12.4 섭취량과 팔요량 독일의 Deuts c he Gesellschaft fu r Enn 걸 hrun g 에 서 는 매 일 F 의 : 섭 취 를 다음과 같이 권장한다. 16) 12 개월까지의 어란이들에게는 0.25m g /1 일 1~3 세 어 린이 0. 25~0. 50m g /1 일 4 세 부터 ~9세 0. 75m g /1 일 10 세 이 상에 서 성 인까지 1. Om g /1 일 1980 년 RDA 에 서 는 30) 다음과 같이 F 의 권장량을 정 하였 다.
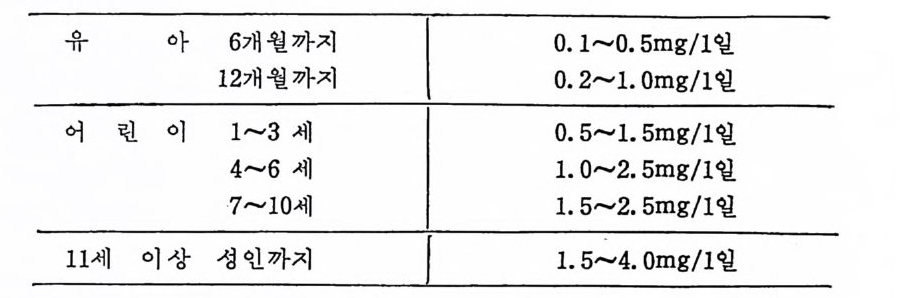 유 아 6 개월까 지 0. 1~0. 5m g /l 일
유 아 6 개월까 지 0. 1~0. 5m g /l 일
음식물로의 F 섭취 이외에 음료수의 F 섭취는 하루 F 섭취량에 중요한 위치를 차지한다. 그러나 음료수의 F 는 하루 섭취하는 식 수의 양과 그 안에 들어 있는 F 에 의하여 영향을 받는다. 음료수 의 F 량은 다론 식품에도 영향을 주게 된다. 식품에 함유된 F 의 함량은 lpp m 이하이며 바다 생선은 약간 많은 F 를 함유하고 있 다. 혼합 식이에서는 성인이(음료수를 제의하고) 0.5~1mg 정도의 F 를 섭취한다. F 의 요구량은 식이의 Ca, P. M g의 농도에 의해 영향을 받으며 규산영은 F 의 이용을 방해한다고 한다 .13) 취의 성 장에 팔요한 F 량은 2. 5p pm 정 도로 나타났다고 한다.
12.5 강화식품 식품 내의 F 함량은 지역적으로 크게 차이가 있으나 동식물계에 펄리 분포되어 있다. 식 품의 F 함량은 다음과 같다 17)( 표 12. 2).
 표 12. 2 석 풍의 분소 (F) 의 함량 17)
표 12. 2 석 풍의 분소 (F) 의 함량 17)
차에 F 가 가장 많이 함유되어 있고 해산물에도 F 가 많이 함유 되어 있다. 음료수에 는 0.14~0. 19p pm 코카콜라에 는 500µg / l 정 도의 F 가 함 유되어 있다. 미 국에 서는 전국적으로 음료수에 F 를 lp pm 첨 가하도록 권장하 고 있다. 12.6 독 성 과량의 F 를 섭취하면 이것이 뼈에 처장되며 뇨로 배설된다. 장기 간 계속 과량의 F 를 섭취했을 때는 뼈에 이상을 초래한다. 어린아 이들에게서는 세계의 여러 나라에서 연구된 불소화된 음료수 섭취에 서 보았듯이 치아에 F 가 축적된 현상이 나타난다. 더 십해지면 치 아의 enamel 층에 탈색 과 반접 이 생 기 고 hy po p la sti c 장애 가 온다. 충치예방을 위해서 첨가된 l pp m 의 F 에서도 약간의 F 축적 현상이 -e namel 층에 나타났다. 그러나 위의 양온 하루 음료수 섭취량과 관
계가 있다. 영국 학생들의 하루 음료수 섭취량은 0.2~3l 로 보고되 었으며 섭취된 F 의 양에 따라서 신장으로 배설된 F 량이 달라진다. F 의 축적은 영구치보다 어린이들의 유치에서 더 많이 나타난다. 태반과 유선은 대아가 모찬의 F 섭취에서 과잉되지 않도록 보호 해 주는 역할을 하는 것으로 알려졌다. 다론 건강장애는 아직 보고 되지 않고 있다. 장기간 계속 8mg 이상의 F 를 매일 섭취했을 때 골다공증이 나 타나고 더욱 심할 때는 골격 장애와 그 중에서도 척추와 골반의 마 비중상과 신경조직의 이상이 왔다. 이때에는 골격조직에 높은 F 농 도가 농축되 어 있 었 다 (9~13m g/g). F 침 착증은 물속에 비 정 상적 으로 높은 F 화합물이 자연적 으로 . 함유된(I O~45 pp m) 지역에서만 일어나며, 상수도의 불소화에 대한 적철한 조철시설을 가전 지역사회에서는 일어나지 않았다. F 화합물이 과잉일 때는 그 독성이 높은데 유년기에는 0.5g 정도 ` 의 양도 치사량이지만 사람에 따라 몇 배 높은 양도 꼭 치사적이라 고는 할 수 없다. F 화합물은 해당과정의 효소인 endolase 를 포함 한 인산염 대사에 개입하는 몇 개의 M g활성화 효소의 강력한 여제 물이다. Fluoroaceta te 는 대 사상 fluo roc itra te 로 전환된 후 〈치 사적 인 합 성 > aconit as e 활성 을 억 제 함으로써 Krebs 회 로의 강력 한 억 제 물로 작용한다. 최근 미국에서 상수도물의 불소화에서 초래되는 암의 발병에 관 한 보고는 찰못된 실험 결과의 보고였으며 26) 암의 발생과 음료수에 첨가한 F 의 섭취와는 아무런 관계도 없다고 하며 chromosom 의 변화나 그 밖의 muta g e n 의 작용도 찾아볼 수 없었다 .18)27)28) *참고문협 1) Underwood, E. J. , Trace Elements in Human and Anim al Nutr i -
tion, Academi c Press Inc. New York and London, p. 347, 1977. 2) Henschler, D. and Patz , J. in Gladtk e, E. Hein emann, G. and Ekkert, I. , Sp ur enelemente , p. 131, Georg Thie m e, Stu tt ga rt, 1979. 3) Hodg e , H. C. , J. Am. Deit . Assoc. , 40, 436, 1950. 4) Jen kin s , G. N. , Venkate s warlu, P. and Zip k in , I. , WHO Monog r . Ser. , No. 59, 163, 1970. 5) Messer, H. H. , K. Wong , M. Weg n er, L. Sin g e r and W. D. Arm- st ro ng , Natu re, 240, 218, 1972. 6) World Health Orga niz a ti on , Fluorid es and Human Healt h, Genf, 1970. 7) Ni el sen, F. H. and H. H. Sandste a d, Am. J. C/in . Nutr . , 27, 515, 1974. 8) Cremer, H. -D. and Dutt ne r, W. , WHO Monog r . Ser. , No. j9 , 75, 1970. 9) Sp e ncer, H. , Osis , D. , Kramer, L. W iat r o wski, E. and Norris , C. , J. Nutr . , 105, 733, 1975. 10) Patz , J. , D. Henschler and H. Fic k enscher. Dt sc h. Zahnii rz tl . Zschr. , 32, 482, 1977. 11) Turner, D. C. and T. C. Sta dtm an, Arch. Bi o chem. Bi op h y s. , 154, 366, 1973. 12) Gedali a, I. , W. H. 0. Monog r aph , 59, 1970. 13) Mi ln e, D. B. and K. Schwarz, Trace Element Meta b olis m in Anim als II, Baltim ore Univ e rsit y Park Press, p. 710, 1974. 14) Rotr u k, J. T. , W. G. Hoekstr a , A. L. Pop e , H. Ganth er, A. B. .Sw anson and D. G. Hafe m ar, Fed. Proc. , 31, 691, 1972. 15) Butt ne r, W. , Dt sc h. Zahnii rz tl . Z. 23, 123, 1968. 16) D. G. E. , Emp feh lung e n fu r di e Ni ihr sto f fzuf u hr der Dett tsc hen ,Ge sellschaft Ernii hr ung , 3, Aufl , Umschau Verlag , Frankfu r t/ M . , 1975. 17) Lang , K. , Bzochemi e der Ernii hr ung , 4, Aufl ag e Dr. Diet r i c h :Stei n kof f Verlag, 1979. 18) Leonard, Toxic ol og y 7, 239, 1977. 19) Schwarz, K. and Mi lne , D. B. , Bi o in org. Chem. , 1, 331, 1972.
20) Fuchs, C. , G. Heim ann, P. Heid e mann, H. -H. Pete rs, in E. G!adtk e, G. Heim ann and 1. Eckert, Sup re nelemente , p. 141, Georg Thie m e Verlag, St u tt ga rt, 1979. 21) Bi ittne r, W. , D. Henschler and J. Patz , Dt sc h. Med. Wschr. , 98, 751, 1973. 22) Abou, E. L. , J. Eis c h, V. Eis e nreic h , E. Fay and H. Rog e nhofe r , o·ste r r. Ap ot h e kerze£tu ng 11, 205, 1977. 23) Dambacher, M. A. and H. G. Has, Dt sc h. Med. Wschr. , 10(1), 504, 1976. 24) Fuchs, C. , D. Dorn, C. Hauswaldt, H. V. Hennin g , J. Kobberlin g , J. Kubasch C. Mc itos ch, K. 0. Ung e r and F. Scheler, Verh. Dt sc h, Ges. f. Inn. Med. , 82, 910, 1976. 25) Dean, H. F. , in Moulto n, F. R. ed. , Fluor ine and Denta i Healt h p. 6. and 23 Am. Assac. Adv. Se t. , Washin g ton . , D. C. 1942. 26) Yi am ouia n nis , T. , Lancet II, 296, 1977. 27) Hoover, R. N. , F. W. Mckay , J. F. and Fraumeni Jr. , J. Natl . Cancer Inst. , 57, 757, 1976. 28) Doll, R. L. Ki nl en, Lancet I, 1300, 1977. 29) Fuchs, D. , D. Dorn, C. A. , Fuchs, H. V. Henin g , C. Mcin t o sh and .F. Scheler, CUn. Ch tm . Acta 60, 157, 1975. 30) Food and Nutr i t ion Board, Nati on al Research Council , Recom· .m ended Dt 'et a ry Allowences. 9th ed. , Nati on al Academy of Scie n ces, :W ashin g ton , p. 156, 1980.
13 규 소 (Sil ic o n Si) S i는 산소 다움으로 지구상에 풍부하며 토양, 식물, 대기 중에 널리 분포되어 있고 탄소와 화학적으로 비슷한 성질을 갖는다. 최근에 와서 S i가 뼈와 결체조직 형성에 필요한 것으로 알려지게 되 었다. 1)2) 17)18)19) 50 년 전부터 동물조직 내의 S i가 측정되기 시작했으나 초기엔 주 로 S i의 해로운 면만 많이 알려졌었다. 자연의 S i는 주로 Si0 2 형 태로 촌재하며, 기타 H2S i 03 를 형성한다 • S i (OH)4 는 대표적인 용 · 해 형태이다 .8) 13.1 체내 함량과 분포 체내의 조직과 기관의 명확한 S i함량은 최근 발달된 분석 기술에 의해서 가능하게 되었다. 성인의 체내 S i함량은 약 1. 5 g이며 대부분이 뼈에 촌재한다. 뼈 의 Si 함량은 lOOp pm 이 고 연조직 에 는 10~450p pm 그리 고 고환에 는 3p pm 정도로 낮온 양이 존재하며 임파철에서는 450 pp m 으로 많은 양의 S i가 함유되어 있다. 임파절에서는 S i를 함유하는 작은 S i 02 이 발견되기도한다. 뇌, 신장, 간, 허파그리고 근육조직에는 ` 20~60p pm 의 Si 가 함유되 어 있 다.
상피 조직 과 결 체 조직 에 도 그의 구성 요소인 mucop o lys accharid e 와 함께 많온 양의 S i가 함유되어 있다 .1) 또한 뎃줄에서도 330~ 550 pp m 의 S i가 발견되었다 .2) 연골에 는 57~19lpp m 정 도의 Si 를 함유하는데 collag e n 분자의 각 단백 질 a-chain 에 는 3~6 원자의 Si 가 있 는 것 으로써 Si 함량아 계산되었다. 많은 양의 S i식이를 섭취시켜도 혈액에는 항상 약 lµg /ml 로 일 정함을 보여주었다. 표 13. l 은 사람과 동물의 각 기 관의 Si 함량이 다. 3) 4) 5)
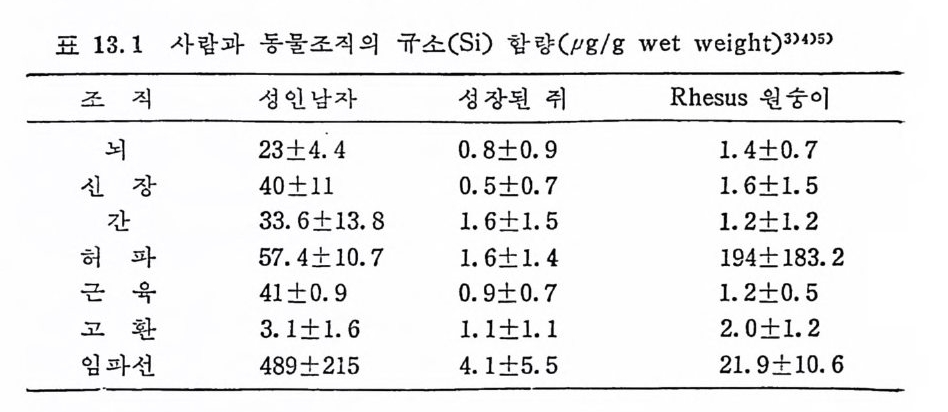 표 13. 1 사람과 동물조직 의 규소 (S i) 함량(µg/g wet weig h t) 3 >05>
표 13. 1 사람과 동물조직 의 규소 (S i) 함량(µg/g wet weig h t) 3 >05>
13.2 주요 기능과 결핍증 S i의 기능으로는 S i가 성장과정에 있는 뼈에도 촌재하므로 vi- tam i n D 와 관계없이 뼈의 형성과 석회화 과정에 중요한 역할을한 다. 1)11) S i는 Ca 과 마찬가지로 뼈의 광화작용의 증가에 따라 그 양이 많 아지며 S i의 축적량에 따라서 광화작용의 속도가 달라진다. 활성 화되 는 것 은 gly c osami ng lu can-pr ote i n 복합체 의 기 본 물질 이라고 본다. in vi tro 실험에서는 성장과정에 있는 뼈에서 석회~ 작용의 위치에 S i가 존재함을 알았으며 뼈의 석회화의 첫단계는 Ca 과의 결합인데 이 과정에 S i가 Ca 과 연관을 갖고 일부 기능을 담
당하고 있다고 보고 있다. 1)1 8)19) 또한 S i결핍시에 관절의 연골에서 muco p ol y sacchar i des 의 비율 이 현저히 감소하고 그로 인해 colla g en 형성도 감소됨을 볼 수 있 었다 .1) Si 는 mucop o lys accharid e 에 서 po lys accharid e matr i x 와 C-0- Si este r 결합으로 연결되 어 있 다. Polys accharid e -Si este r 연결은 다른 생물체의 조칙에도 촌재하기 때문에 뼈, 연골조직, 결체조직 형 성 이 의 에 도 다른 mucop o lys accharid e 가 관여 하는 과정 , 죽 대 아성장, 상처회복 등에서도 중요한 역할을 하리라고 본다 .6) in viv o 실험에서 이유기의 쥐의 뼈 형성에 S i와 Ca 과의 관계 를 보면 처 Ca 섭취시에도 식이내 S i의 첨가는 광화작용의 속도 를 중가시켜 주었다고 한다. 병아리에서도 뼈의 형성과 Si, Ca, M g, F 사이의 상호관계가 제시되었다. S i는 colla g en 의 구성 요 소로써 S i가 결핍된 병아리는 colla g en 량이 감소되었으며 1974 년 Schwartz 는 1 > in vit ro 실험 에 서 도 Si 와 collag e n 의 관계 를 보여 주 었다. 결 체 조직 에 서 Si 는 po lys accharid e chain 과 pr ote i n 그리 고 po - lys accharid e chain 사이를 연결해 주는 다리 역할을 하며 crossli n- ki ng ag e nt 작용을 한다. 그러 므로 Si 는 결 체 조칙 의 fibr ous ele- men t의 발달에 기여하고 구조의 강도를 제공해 주는 역할을 한다. 최 근 연구에 서 는 뼈 의 세 포인 oste o blast 의 mi toc hondria 에 Si 가 농축되 어 있 고 Ca 이 촌재 하고 있 는 mi toc hondria 에 Si 의 축적 은 세포 의부에서 화골작용이 일어나기 전에 수행된다고 한다. S i의 결핍증은 쥐와 닭에서도 발견되었다. S i가 완전히 제거된 식이를 섭취했을 때는 S i가 함유된 석이에 비해 체중중가율이 50% 밖에 되지 않았다. 1972 년 Car li sle 의 보고 9) 에 의하면, Si 결핍상 태에 S i를 첨가하면 정상적인 성장이 유지되었다고 하며, sodiu m meta s il ica te 로서 Si 가 식 이 에 첨 가되 면 병 아리 에 있 어 50 % 정 도 의 성장률이 증가되었다. S i가 결핍된 병아리에서는 성장부전 및 기관의 기능되쇠, 그리고 피부와 접막이 다소 영향을 받았다. 또한 결핍된 병아리는 근육 발달이 처지되고 다리뼈의 유동성이 작아졌
옴울 보여주었다 .8) 쥐의 S i결핍은 성장부진과 두골변형을 초래했다고 한다 .10) 일반적으로 식이에 있어 100 g의 식사에 50m g의 S i를 첨가했을 때 25~34% 로 성장율이 중가되었다. 또한 Schwarz11) 가 발표한 Si 와 섭 유소 그리 고 동백 경 화증과의 관계에서는 S i부족이 동맥경화증의 중요한 병인요소가 된다고강조 했다. 동맥내막에는 S i가많이 함유되어 있다. 동맥경화증에 여러가 지 섬유소식이를섭취하면 동백경화증도 예방하는 효과가있음이 밝 혀졌는데 이러한 섬유소 함량이 많은 석품은 분석 결과 S i함량이 많 은 것으로 나타났다. 이 결과에서 S ili ca t e-S i는 동백경화중 치료에 영향을 주는 식아 섬유소에서 활성요소가 됨을 알 수 있으며 선전 국에 비해서 후진국에 동맥경화증 빈도가 낮은 것은 석이 S i의 이 용과 관련이 있음을 시사해 주었다 .12) 13. 3 대 사 S i는 식품에 monomer 나 p ol y mer 의 Si 형태로 유기물과 결합하 여 pe cti n 이 나 동물조직 그리 고 mucop o lys accharid e 둥에 함유되 어 있다. 주로 monosil icic acid 형 태 로 흡수되 며 일부의 po lym er Si 는 장 에서 가수분해된다. 사람과 동물이 식품으로 섭취한 S i의 약 0.1% 정도는 뇨로 배출되는데 S i를 많이 섭취했을 때는 뇨의 배출량이 2.8% 가 중가되었다. 체내 보유량에 있어서는 대변과 소변으로 섭 취된 양의 99% 가 배설되므로 극히 미량이다• 그리고 젖소의 석이에 S i를 첨가했을 때 우유의 Si 함량에는거 의 영향이 없었으며 혈액에는 무기 S i농도보다는 유기형의 농도가 훨싼 더 높았다. 식품과 음료수내의 H2S i 03 는 소화관 벽에서 찰 흡수되고뇨로빨 리 배 설된다. 신장의 여 과속도는 약 lOOml/mi n 이 고 사람의 뇨로. 애 출되 는 Si 량은 10~60mg / l 일이 다•
13.4 섭취량과 팔요량 S i함량은 동물성 식품이 석불성 식품에 비해 적게 함유되어 있 다. 그러나 동물성 식품에 함유된 S i의 이용률이 식물성 석품의 이 용률보다 높다고 하며, 식물성 식품에 존재하는 po lym er 결정의 , sil ica te 는 양적 으로는 많으나 이 용률이 적 다. 혼합석에서 섭취되는 하루의 S i량은 1. 2 g /1 일로 계산한다. Schwarz 와 M il ne13) 의 실험 에 서 는 쥐 에 게 Si 50µg /g 식 이 를 섭 취시켰을 때 정상적인 성장과 뼈의 발육에 좋은 효과를 보였다. Car li sle” 은 병 아리 의 Si 요구량은 sodiu m sil ica te 로써 100~200 µg/g 식 이 로. 측정 하였 으며 , 7) 쥐 의 경 우는 Na2Si 03 • 9H20 로서 50· mg /l OOml 정 도로 밝혀 졌 다. 13.5 함유석품 동물성 식품에는 0.3~4mg /1 00g S i아이 함유되어 있으며 곡류가 · 주요 sil ic ic ac id 섭취의 급원이며 석물성 식품에는 일반적으로 많 이 함유되 어 있 다. 4)21)22) 13. 6 독 성 과잉 의 Si 섭 취 는 sil ico sis 를 발생 하는데 Si 가 lys osome 에 홍수 되어 세포막을 통과하는 단백질을 방해한다. 과량의 S i섭취는 갈비뼈와 복강내 종양을 생성하는데 14) 이와같 은 암 증상은 S i아 제조업에 종사하는 노동자에게서 일어났다. 취 의 경 우 높은 농도의 S i [IOm g /lOO g체 중 C= l. 67 • 10-3m)] 섭 취 는 monosili cic ac id 세 포대 사를 방해 한다. 15)16) 취 의 mi toc hondria 에서 S i는 인산화 과정과 NAD 와 관계되는 과정을 방해하는데 그 . 의 원인은 H3PO4 가 H4S04 로 대치되는 데서 오는 것으로 보인다. In vit ro 실험의 용엑에서 이와 같은 대치작용을 관찰할 수가 있 었다•
*참고문현 1) Carlis l e, E. M. , Fed. Proc. , 33, 1758, 1974. 2) Schwarz, K. , Proc. Natl . Acad. Sci. , USA 70, 1608, 1973. 3) Underwood, E. J. , Trace _Ele ments in human and Anim al Nutr i - tion 4t h ed. , Academi c Press Inc. , New York and London, p. 399, 1977. 4) Hami lt o n, E. I. , Mi ns ki, M. J. and Cleary, J. J. , Sc i. Tota l En· vir on . , 1, 341, 1972, 1973. 5) Levie r , R. R. , Bi oi n org. Chem. , 4,_ 109, 1975. 6) Schroeder, H. A. , J. J. Balassa and I. H. Ti pton , Essenti al Trace Meta ls in Man, Molyb denum J. Chron. Di s. , 23, 481, 1970. 7) Schwartz , K. , Fed. Proc. , 33, 1748, 1974. 8) Carlis l e, E. M. , Nutr . Rev. , 33, 257, 1975. 9) Carlis le , E. M. , Fed. Proc. , 31, 700, 1972. 10) Schwartz , K. and D. B. Mi lne , Natu r e, 239, 333, 1972. 11) Schwartz , K. , Lancet, 1977. 12) 이 양자, 손경 회 , 『가정 학 연구의 최 신정 보』, 신광출판사, p. 50, 1977. 13) Schwarz, K. and Mi ln e, D. B. , Natu r e, London, 239, 333, 1972. 14) Wag n er, C. , Perug ia Q u adrenn, Int. Conf. Cancer 3, 589, 1966. 15) Kerste n , W. , K. Kris c h and Hj . Sta u din g e r, Hopp e -Sey le rs Z. l'hy s i o l. Chem. , 313, 109, 1958. 16) Kerste n, W. and Hj . Sta u din g e r, Natu rwi ss . 43, 68, 1956. 17) Carlis le , E. M. , Fed. Proc. , Fed. Am. Soc. Exp. Bi ol . , 28, 374, 1969. 18) Carlis le , E. M. , Scie n ce, 167, 279, 1970. 19) Carlis le , E. M. , Fed. Proc. Fed. Am. Soc. Exp. Bi ol . , 29, 565, 1970. 20) Carlis le , E. M. , in K i rch g죠 ner M. , Trace Element Meta b oli sm
in Man and Anim als-3, ATW, Freis i n g -W eih e tn s ep h an, p. 253, 1978, 21) Bezeau, L. M. , Jah rsto n , A. and Smoli ak , S. , Can. J. Plant Sci, 46, 625, 1966. 22) Baker, G. , Jon es, L. H. P. and Wardrop , I. D. , Aust. ]. Ag r ic . Res. , R. 426, 1961.
14 바나더 움 CVanadiu m , './) V 이 동물에 서 필수요소라는 것 은 Hop k in s 와 Mohn1) 에 의 해서 . , 처음 보고되었다. 14.1 체내 함량과 분포 사람은 체내에 평군 43m g의 V 울 함유하고 있다. V 온 미량이 ’ 체내 각 기관에 분포되어 있으며 사람의 허파에 0.6p pm 정도로 가 장 많이 함유되어 있으며 간, 비장, 췌장, 고환 그리고 갑상선에는 - 0. 02~0. 03p pm 정 도가 분포되 어 있 다고 한다. 19) 그 후 Hami lt o n 20) 등은 성 인의 각 기 관의 V 함유량을 뇌에 0. 03 土 o. 008µg /g, 근육에 0. 01 土 0. 003µg /g, 간에 0. 04 土 0. Olµg /g, 고환에 0.20 土 0.08µ g/g, 허파에 0.10 士 0.02µ g/g, 그리고 임파선에 0.40 士 O. 2µg /g wet weig h t 로 측정 했 다. 또한 Losee2>21) 는 사람의 치 아의 enamel 층에 서 O.lµg /g 의 낮은 농도의 V 을 측정했다. Allaway 22 > 둥은 미 국사람들의 혈액 의 V 함량을 1~2µg /l OOml 로 측정했으며 다른 연구자들은 18)23)24) 좀더 높은 측정치를 발표했다. 예 를 들어 Nozdryu kin a 둥 24) 은 회 복 직 후의 십장병 환자들에 게 서 4. 6µg /l OOml 가 측정 되 었으며 70 일 후쯤에 는 1. 96 土 0. 5µg /l OOml 정도로 감소되었다고 보고했다.
14.2 주요 기능과 결핍증 lOm g/g이하의 V 식이를 먹인 병아리는 날개와 깃털의 성장이 현 처히 증가하였다. 취에게 V 울 lOOm g/g이하로 식이를 준 후 0.5 pg/g을 섭취한 대 조군과 비교했을 때 성장의 감소와 혈액공급제포의 양이 중가되었 고 혈액과 뼈의 Fe 함량이 역시 중가되었다.” V 은 지질대사에 영 향을 미찬다고 하는데1) V 이 결핍된 병아리는 처음에는 혈장의 -c holes t erol 량이 감소되다가 결핍증상이 오래 계속되면 혈장의 cho· Je ste r ol 이 증가되 었 다고 한다. 1974 년 Hop k in s 둥 4) 은 V 결핍 된 병 아리에서 혈장의 t r yg l y cer i de 가 현저히 감소된 것을 지적하였다. 취는 V 결핍시 생식 능력에 장애를 받는다고 한다. 병아리는 V 결 핍시 며의 발달에 좋지 않은 영향을 주며 조직에는 경골세포들이 파괴되어 세포의 크기가 감소되었고 핵이 납작하게 되었으며 그 결 과 다리조직의 발달에 이상을 초래했다고 한다. V 은 동물실험에서 충치치료에 좋은 효과를 보여주었다. V 은 치아와 뼈의 석회화를 촉진시켜 주었다. 취에게 충치를 야기시킨 후 음료수에 첨가된 0.02 ~0.9 pp m 의 V 온 충치를 감소시켰다. 그러나 음료수에 V 을 첨가 했을 때 충치예방에 아무런 효과가 없었다는 보고도 있다 .5) 이와 칼이 동물실험의 결과에서 V 온 고둥동물에게서 필수 영양소임이 입증되게 되었다. 그러나 사람에 대한 V 의 연구는 아직까지 보고 되어 있지 않다. 14.3 대 사 방사선 동위원소 48V 울 투여했을 때 간에 즉시 분포되었으며 거 의 같은 양, 죽 37~46% 정 도가 세 포핵 과 mi toc hondria 에 홉수되 었고 m ic rosome 과 48V 투여 24 시간 후에 4 1. 5 土 0.58% 가 뇨로, 그 리고 1. 5 士 0. 38% 가 대변으로 배설되었다. V 은 체내에서 vanadate (Na3VO -t)형 태 로서 가장 찰 이 용되 었 다. 사람은 1 일 0~8µg 의 적 은
양의 V 을 대변으로 배설하였다 .6) 7) 배설량은 구강으로 과잉 V 울 섭취했을 때 현처히 증가했다 .7)8) 사람은 100m g의 가용성 dia m • moniu m oxy tar ta rovanadate 로 섭 취 했을 때 0. 1~1. 0% 흡수되 었 다. 다론 연구결과는 흡수된 V 의 60% 가 24 시간 후에 배설되었으 며 나머지는 간과 뼈에 축적되었다.” 뼈의 V 온 간에 있는 V 보다 천천히 이 동되 고 배 설된다. Soremark 와 Ullberg 는 10) 귀 에 게 48V 울 주사 후 뼈와 치아에 높은 V 보유량을 지적했고 Ha t cock11) 등은병 아리에게서 뼈와 신장에 V 의 높은보유량을 지적했다. 또한 vana- , da t e 와 chromate 음이온의 상호작용에 대해서도 연구되고 있다. 14.4 섭취량과 필요량 체중 75 g의 쥐의 경우 V 은 1 일 1~2µg 섭취시켰을 때 체중 1kg 당 12.5~25µg 정도의 V 이 보유됨이 추산되었다. 이 수치를 사람 에게 적응시켜 본다면 약 1~2m g /1 일을 필요로 한다고 보겠다 .12) 제한된 지론이건 하나 병아리의 경우 실험식이 l g당 100m g의 V · 이 적당하다고 추산되어졌다. 대개 석품들은 lOOmg /g 이하의 V 울 함유한다고 알려 져 있 다. Schroeder 둥”은 1 일 V 의 필요량을 1. 2 m g으로 보며 군형적 상태를 유지하기 위해서는 1~4m g으로 추산 했다. V 의 섭취는 지방의 섭취와 밀접한 관계가 있다. 식물성 불 포화 지방산에는 동물성 포화 지방산보다 많은 양의 V 이 함유되어 있다. Welch 와 Cary 13) 가 10 종류의 식물성유를 분석해 본 결과 위 와 같은 톡벌한 유사성은 찾아내지 못했다. 유지의 V 함유량은 14 ~139 pp b 이었다. 그러나 사람에 대한 연구 결과는 대단히 미약한 형편이다. 14.5 함유식품 자연식품내의 자제한 분석치는 아직 많지는 않으나 Soremark 의 분석 결과 14) 에서는 무우에 52mg /g 이 함유되어 있고 간, 생선, 육류 예 는 lOmg /g 이 들어 있 다고 한다. 북미 의 12, ;<] 역 에 서 34 종류 곡물
로 V 울 분석 했을 때 그것 의 함량이 6. 5p pb ~20p pb 까지 보고되 었 다. 9) 밀 알, 보리 , 납작보리 , 콩 둥에 는 28~55p pb 의 V 이 함유되 어 있었다. 혹설탕에는 V 이 0.4µg /g 함유되어 있는 반면 백설탕 에 는 0. 002µg /g 이 함유되 어 있 다고 한다. 25) 14. 6 독 성 V 의 독성은 Se 과 비슷한 현상을 나타낸다. V 의 독성은 화학작 구조에 따라서 달라진다. 쥐의 식이에 25 pp m 의 V 울 첨가했을 때 독성을 일으켰다. V 의 과잉 섭취는 (50 pp m) 동물에게 설사를 초 래 하고 사망에 까지 이 르게 하였 으나 16)26) EDTACeth y le ne dia m i ne - tet r aa ceti c ac i d) 와 같은 복합체 형성 물질과 함께 섭취했을 때 독성 증상이 감소되 었 다. 17) 쥐 에 게 5p pm 의 V 울 vanady ls ulfa te 형 태 로 섭취시켰으나 독성중상이 나타나지 않았다. 쥐에 있어서 과잉의 V 섭 취 는 coenzy m e A27) 와 coenzy m e Q 28) 의 양을 감소시 켰 고 monoami ne - ox i dase 의 활성을 중가시켰고 인산화 과정을 방해했다 .29) 그러나 · 석이로서 과잉의 V 섭취는 거의 불가능하다. 몇 년 전 Franke 와 Moxon15) 은 쥐 에 게 25p pm 의 V 과 As, Mo, Fe 그리 고 Se 를 증가 시켰을 때 독성을 초래했다고 보고했다. 30p pm V 온 병아리에서도 독성 을 초래 했 다. 병 아리 에 30p pm 을 calci um vanadate 로 첨 가시 켰을 때 체중이 감소되고 200 pp m 일 때는 높은치사율을 보였다 .16) Nelson 과 ::::z...의 동료들은 17) 병 아리 는 20~25p pm 의 V 에 적 응할 수 있으며 그 이상 초과되었을 때 성장 감소 현상이 나타난다고 지적 했다. 인체의 독성 실험 결과로는 V 은 사람에게 독성을 일으키지 않는 것 으로 알려 졌 다. Dim ond 둥 8) 은 ammoniu m vanady l ta rt_ rate 를 6 사람에 게 6~10 주 동안 1 일 4. 5~18mg 을 섭 취 시 켰 을 때 독성 현상이 나타나지 않았으며 몇몇 사람에게서는 높은 양을 섭취 시켰을 때 설사가 수반되었다. Schroeder 둥”은 환자들에게 1 일 4. 5mg 를 oxy tar ta rovanadate 로 16 개 월 동안 섭 취 시 켰으나 현처 한 증상은 나타나지 않았고 뇨륜 동한 V 의 배설만이 중가했다고한다솔
*참고문현 l) Hop k in s , L. L. and H. E. Mohr, Fed. Proc. , 30, 462, 1971, 2) Curzon, M. E. , F. L. Losee, R. Brown and H. E. Tay lo r. Arch. Oral. Bi o l. , 19, 1161, 1974. 3) Str a sia , C. A. , Vanadiu m Essent iali ty and Toxic t'ty in the labo· rato ry Rat. Mi ch ig a n Univ e rsit y, 1971. 4) Hop k in s , L. L. and H. E. , Fed. Proc. , 33, 1974. 5) Ki rc hg e Bner, M. E. Weig a nd, A. Schneg g, E. GroBmann, F. J. Schwarz and H. ·P. Roth , in Cremer, H. -D. , D. Hotz e l and J. Kil hn au, Bi o chemi e und Phy s io l og ie der Ernii hr ung Band I, Tei! 2, Georg Thie m e Verlag, p. 275, 1980. 6) Perry, H. M. , Jr. and Perry, E. F. , J. Clin . Invest. , 38, 1452,. 1959. 7) Schroeder, H. A. , Balassa, J. J. and Ti pton , I. H. , J. Chronic Di s. ,. 16, 1047, 1963. 8) Diam ond, E. G. , Caravaca, J. and Brchim ol, A. , Am. ]. Clin . Nutr . , 12, 49, 1963. 9) Talvit ie, N. A. and Wag n er, W. D. , Arch. Ind. Hy g. , 9, 414,. 1954. 10) Soremark, R. a~d Ullberg, S. , in Frie d , M. ed. Use of Ra- dio iso to p es in Ani m al Bi ol og y and the Medtc a l Scie n ce, Vol. 2,- Academi c Press, New York, 1962. 11) Hath c ock, J. N. , Hi ll, C. H. and Matr o ne, G. , J. Nutr . 82,. 106, 1964. 12) Lang , K. Bi oc hemi e der Ernii hr ung 4 Aufl ag e, Dr. Di et r ich · St ei n k off Verlag, p. 330, 1979. 13) Welch, R. M. and Cary, E. E. , Ag r ic . Food Chem. , 23, 479,-1975. 14) Soremark, R. , J. Nutr . , 92, 183, 1967. 15) Franke, K. W. and Moxon, A. L. , J. Pharmacol. Exp. Ther. , 61, 89, 1937. 16) Romoser, G. L. , Dudley , W. A. , Machli n, L. J. and Roveless, L ...
.Po ult ry Sd. , 40, 1171, 1961 . 17) Nelson, T. S. , Gil l is , M. B. and Peeler, H. T. , Poult ry Sd. , 41, 51 9, 1962. 18) Schroeder, H. A. , Balassa, J. J. and Ti pton , I. H. , J. Chroni c Di s. 16, 1047, 1963. 19) Ti pton , I. H. and Cook, M. J. , Healt h Pit y. , 9, 103, 1963. 20) Hami lton . E. I. , Mi ns ki, M. J. and Cleary, J. J. , Tota l Envir on . , 1, 341, 1972/1973. 21) Losee, F. , Cutr e ss, T. W. and Brown, R. , Trace Subst. Envi- .ro n. Healt lt-7 , Proc. Univ . Mo. Annu. Conf. , 7th , 1973, p, 192, 1973. 22) Allaway , W. H. , Kubota , J. , Losee, F. and Rot h s, M. , Arch. Envir on . Healt h 16, 342, 1968. 23) Butt , E. M. , Nusbaum, R. E. , Gil m our, T. C. , Di D io , S. L. and Maria n o, S. , Arch. Envir on . Healt h 8, 52, 1964. 24) Nozdryu kin a , L. R. , Grin kevic h , N. I. and Grib o vs Kay a , I. F. Trace Subst. Envfr on . Healt h- 7, Proc. Uni v . Mo. Annu. Conf. , _7th , 1973, p. 353, 1973. 25) Hami lton , E. I. and Mi ns ki, M. J. , Sd. Tota l Envfr on . , 1, 375, 1972/1973. 26) Hi ll , C. H. , in Prased, A. S. ed. , Trace Elements and Human .Dte sease Vol. 2, p, 281, Academi c Press, New York, 1975. 27) Mascit ell i-C oria n doli , E. and Cit ter io , C. , Natu re, London, 183, 1527, 1959. 28) Ai yar , A. S. and Sreeniv a son, A. , Proc. Soc. Exp. Bi o l. Med. , 107, 914, 1961. 29) Perry, H. M. , Jr. Ti et e l baum, S. and Schwartz , P. L. , Fed. .Pro c. Fed. Am. Soc. Exp. Bt' ol . , 14, 113, 1955 .
15 비 소 (Arsen i c, As) 15.1 체내 함량과 분포 사람의 체내에는 소량의 As 가 분포되어 있다. 체내 전체 함량은 0. 04~O. l pp m/ 건조물로서 대 부분이 머 리 카락, 손톱과 발톱 그리 고 피부에 함유되어 있다. 구강으로 As 의 섭취를 증가시켰을 때 체내의 As 함유량도 함께 증가하였다. Smi th 가 20)21) 조사한 사람의 머 리 카락의 As 함량은 0. 03~74pp - m 으로 평 군은 0. 81p pm 정 도였 으며 남자의 머 리 카락에 함유된 As - 는 0.62 pp m 으로서 여자의 0.37 pp m 에 비해서 훨씬 높았다. 혈액의 As 함량은 매우 큰 차이를 보여주며 일반적으로 0.1~0.2. µg/m l 정도이다. 그 중에서도 80% 가 적혈구에 존재한다.1) 15.2 주요 기능과 결핍증 과거의 실험에 의하면 쥐에게 정제된 식이에 As 를 2µ g /1 일을 섭 취 시 켰을 때 성 장과 hemog lo bin 농도, 적 혈구 수의 증가둥에 좋은 결과를 가쳐오지 못했다 .1)22)23) Schroeder 는 As 를 쥐의 식이에 극히 소량을 장기간 동안 보충 시켜 주었을 때 성장이 촉진되었다고 했다 .10)
Ni el sen 과 그의 동료들 2 ) 은 쥐 에 있 어 서 As 는 필수 tra ce ele- ment 라고 말하고 있 다. 대기오영을 격리시킨 동물실험실에서 정제된 식이에 As 를 30p pb 정도 섭취시킨 쥐는 털이 엉성하고 성장이 감소되었으며 대조군은 4.5p pm As 를 sodiu m arsena t e(4 pp m) 와 sodiu m arseonit e( 0.5p pm ) 형태로 섭취시켰을 때 암컷의 취에게서는 결핍 증세가 현처히 나타 났으며 hema t ocr it의 Fe 과 비장의 Fe 이 50% 이상 파괴되어 있었 다. 결핍된 암컷의 쥐의 비장은 비대해졌고 손상된 적혈구가 증가되 어 있었다. 돼지, 조류에서도 As 가 성장 건강상에 중요하다는 것이 실험으 로 입증되었다 .3 )4) 위 의 실 험 에 사용한 As 로는 arsanil ic a cid , 4-nit ro p h eny la rsonic ac id, 3-nit ro -4-hy d roxy ph eny la rsonic acid 그리 고 arsenobenzene (p hen y larsenox i de) 으로 그 눙. ph eny la rsenoxid e 가 성 장에 효과가 있 논지는 아직 규명되어 있지 않으며 arsonic a ci d 는 돼지와 조류의 성장만을 촉진시키는 것으로 알려졌다. 동물에 있어서 As 가 결핍되면 불임종이 증가했으며 사망울도 높 게 나타났다 .5) 수유기의 어린 동물들은 그 어미의 As 결핍시 수유하는 동안에 일부가 사망했으며 나머지도 성장이 지연되고 체내 단백질이 제대 로 합성되지 않았다. 15.3 대 사 As 흡수와 배설은 As 의 화학결합에 의해서 영향을 받는다. 유기 결합물은 흡수가 잘되고 그의 대부분이 뇨로 배설된다. As 는 주로 선장으로 배설되고 배설량은 섭취량과 밀접한 관계를 갖는다. 그러므로 뇨로 배설되는 As 량은 독성 측정에 사용되기도 한다. 정상적 인 조건에서 사람은 뇨로 200~300µ g /l 일을 배설한다. 돼 지와 닭의 성 장에 유용한 arsanil ic ac id 는 조직 으로 흡수된 후
다시 대변으로 배설되기 6) 때문에 체내에 축적될 가능성은 없다. 15.4 섭취량과 필요량 및 함유식품 사람은 매일 음식물로 약 1~2mg 정도의 As 를 섭취한다• 생선과 해산물 특히 새우 종류에 As 가 많으며 우유에는 0.03~ · o.06 pp m 이 함유 7)8 )1) 되어 있으며 환경이 오영된 뉴우질랜드에서 는 1. 5p pm 정 도라고도 한다. 9) 사람이 섭취하는 식품의 As 함량은 거의 0.5p pm 이하아다 .10) Hami lt o n 과 M i nsk i 8) 가 nuclear acti va ti on tec hniq u e 로 분석 한 과일, 채소, 곡류 그리고 육류의 As 함량은 표 15.1 과 같다.
 표 15.1 과일, 채 소, 곡류, 육류의 바 소 (As) 함량 8).
표 15.1 과일, 채 소, 곡류, 육류의 바 소 (As) 함량 8).
바다 생 선과 해 산물의 As 함량은 표 15. 29..} 같다. 10)24)26)26)27 )2 8)
 표 15. 2 바다생 선과 해 산물의 비 소 (AS) 함량 I0)24)25)26)27)28)
표 15. 2 바다생 선과 해 산물의 비 소 (AS) 함량 I0)24)25)26)27)28)
1 일 섭취량은 섭취하는 음식물의 종류에 따라서 달라지게 된다. 일반 음식물 섭취로는 As 를 1 일 0.4m g을 섭취하며 미국사람들의 섭취량은 1 일 0.9mg lO ) 정도, 일본사람들의 1 일 As 섭취량은 0.07~ -0. 17mg 정 도이 다. 11) K i rch g e .l.3 ner 는 1 일 As 섭취량을 약 1~2mg 정도로추정했다 .12)
15.5 독 성 사람에 있어서 As 의 급성 독성 중상으로는 메스끼움, 구토, 섣 사, 복통 둥이며 이는 무기 -As 결합으로 특히 arsen it e 를 섭취했을 때 주로 일어났다. 소량의 As 섭취시의 만성 중상으로는 두통, 피 곤 그리고 피부에 이상이 오고 모세관의 삼두압 감소와 산화, 환원 효소의 기능처해 둥을듈수있다. 사람을 사망시킬 수 있는 As 량은 60~120mg arsen i ca ci d(As2 야) · 이다. WHO 에서 허용하는 성인의 As 양은 1 일 3.5m g이다 .13) 과수원에서 일하는 사람들이 농약에 의해서 1 일 6.8m g의 As 을 섭취했으나 독성현상이 나타나지 않았다는 보고도 있다 .29) 칠면조는 0.04%(400p pm ) arsanil ic a ci d 를 석이로 섭취했을 때 체중이 감소되 었다. 그러 나 0. 05~0. 06% sodiu m arsanil at e 를 4 번에 걸쳐서 주었을 때는 성장이 촉진되었다 .14) 그의 두 배의 양을 어란 칠면조가 28 일 동안 섭취했을 때는 사망율이 높았다. 취에게 50p pm As2 야를 주었을 때 독성 현상이 나타나지 않았다. 그러나 200 pp m 을 주었을 때에는 확실히 성장이 저해되었다 .15) 생 쥐 에 게 sodiu m arseonit e 를 음료수에 5mg / ml 로 섭 취 시 킨 후 성 장, 건강, 적혈구, 조직의 As 축적 둥에 전혀 변화가 없이 자연적 으로 사망한 보고도 있으며 또한 암의 발병도 나타나지 않았다고 한다 .16)17) 음료수에 lO pp m 의 As 을 15 개월 동안 함유시킨 결과 종양이 감소되 었 다고 한다. 18) 과잉의 As 는 취에게 g o it er 를 발생시킨다 15) 고 하며 사람에게서 는 arsenic - th y r oid anta g o nis m 이 나타났다. 19> Goit er 가 많이 발병 하는 지 역 의 사람들이 마시 는 음료수에 는 1. 4mg // 의 높은 양의 As :: 가 함유되어 있었다 .19) 위의 양은 보통 음료수보다 2 배 혹은 그 야 상 높은 양이다.
*참고문현 1) Hove, E. , Elvehje m , C. A. and Hart, E. B. , Am. J. Phy si o ! . , 124,. 205, 1938. 2) Nie l sen, F. H. , Giv a nd, S. H. and My ro n, D. R. , Fed. Proc. Fed. Am. Soc. Exp. Bi o l. , 34, 923, abstr . , 1975. 3) Frost, D. V. , Fed. Proc. , Fed. Am. Soc. Exp. Bi ol . , 26, 194,.. 1967. 4) Frost, D. V. , Overby , L. R. and Sp ru th , H. C. , J. Ag r ic . Food. Chem. , 3, 235, 1955. 5) Anke, M. , Hennin g , A: , Griin , M. Pants c hefe ld , M. , Grop pe l,. P. and Lil dk e, H. , Arch. Ti e rnti hr . , 26, 742, 1976. 6) Overby , L. R. and Frost, D. V. , Toxic o l. Ap pl. pha rmacol. , 4,. 38, 1962. 7) Archib a ld, J. G. , Dair y Sci. Abstr . , 20, 712, 1958. 8) Hami lt o n , E. I. and Mi ns ki, M. J. , Sci. Tota l Envir on . , I, 375 .. 1972/1973. 9) Grim mett , R. E. R. , N. Z. J. Ag r z'c . , 58, 383, 1939. 10) Schroeder, H. A. and Balassa, J. J. , J. Chronic Di s. , 19, 85,.. 1966. 11) Nakao, M. , Osaka Shir ttzu Daik a ku Ig a ku Zasshi 9, 541, 1960. 12) Ki rc hg e Bner, M. , E. Weig a nd, A. Schneg g, E. GraBmann, F. J. Schwarz and H. -P. Roth , in Cremer, H. -D. D. Hotz e l, and J. Ki ihn au Bi o chemi e and ph y si o log ie der Ernii hr ung Band I, Tei/ 2, Georg. Thie m e Verlag, 1980. 13) WHO, WHO. Tech. Rep. Ser. Nr. , 532, p. 38, 1973. 14) Sull iva n, T. W. and Al-Tim i m i , A. A. , Poult ry Sci. 50. 1635 .. 1971. 15) Sharpl e ss, G. R. and Metz g e r. M. , J. Nutr . , 21, 341, 1941, 16) Schroeder, H. A. and Balassa, J. J. , J. Nutr . , 92, 245, 1967. 17) Schroeder, H. A. , Kanis a wa, M. , Frost, D. V. and Mi tch enero M. , J. Nutr . , 96, 37, 1968. 18) Schrauzer, G. N. and Ishmael, D. , Ann. Cl in Lab. Sci. , 소
441, 1974. 19) Scott , M. , Trans Int. Goit re Conf. , 3rd, p. 34, 1938. 20) Schmi th, H. , J. , Forensic Se t. Soc. , 4, 192, 1964. 21) Schmi th. , H. , J. , Forensic Sc i. Soc. , 7, 97, 1967. 22) Skin n er, J. T. and Mc Hargu e, J. S. , Am. J. ph y sz o l. , 143, 85, 1945. 23) Skin n er. J. T. and McHargu e, J. S. , Am. J. ph y si o l. , 145, 500, •.1 9 46. 24) Chap m an, A. C. , Analys t, 51, 548, 1926. 25) Con, H. E. , Analys t , 50, 3, 1925. 26) Cox, H. E. , Analys t , 51, 132, 1926. 27) Coulson, E. J. , Remi ng ton , R. E. and Ly n ch, K. M. , J. Nutr . , 10, 255, 1935. 28) Lunde, G. , J. Se t. Food Ag r ic . , 19, 432, 1968. 29) Lang , K. , Bt oc hemt e der Ernti hr ung , 4. Auf! ag e Dr. Di et r i c h St ei n k off Verlag , 1979.
]6 주 석 (Tin , Sn) Sn 은 사람의 조칙에 널리 분포되어 있으나 신생아에게서는 거의 발견되지 않았다 .5) Sn 은 식품의 성분으로서보다는 환경오염 물질로 더 많이 알려져 있다. 1970 년에 Sn 공급이 제한된 환경에서 순수한 단백질 식이만을 공 급받게 한 쥐의 성장에 필수적이라는 것이 발표되었다(표 16.1).3> 연 령 이 중가함에 따라서 Sn 의 함량은 중가되 며 근육에 O.lpp m , 신장과 장에 0. 2p pm , 그리 고 뼈 에 0. 8p pm 이 존재 한다. 6) Ham ilt on 둥”은 성인의 각 기관의 Sn 함량을 근육에 0.07 土 0.Olµ g /g, 신장에 0. 2 士 o. 04µg /g, 뇌에 0. 3 士 0. 04µg /g, 고환에 0. 3 士 0.1 _µg /g, 난소에 0. 32 土 0.19µ g/g, 간에 0. 4 土 . 0. 08µg /g, 허파에 0. 8 土 ·O. 2µg /g, 그리고 입과선에 1. 5 土ci .6µ g/g wet we ig h t로 측정했으 며 혈 액 에 는 아주 낮은 농도로 0. 009 士 0. 02µg /g 이 었 다. Losee 등 8) 온 사람의 치 아의 enamel 층에 함유된 Sn 을 0. 03~7.lOµg /g dry weig h t 정도의 넓은 폭으로 측정했다. 정상적인 성장에 식이 lg 당 sta r nic sulfa te 로서 lµg 의 Sn 이 필요했 다. 그러 나 이 양이 확 실하게 인정되어 있지는 않다 .1)2) Sn 은 생리적 기능이 있는 것으로 생각되며 4 가의 Sn 은 단백질 의 제 4 구조에 기여하거나 다른 생리적 중요성이 있는 요소에 기 여할 것이라고도 추측되고 있다 .3) 또한 Sn 은 생체 내에서 산화 완
원 과정에 관여할 것으로 추측된다.
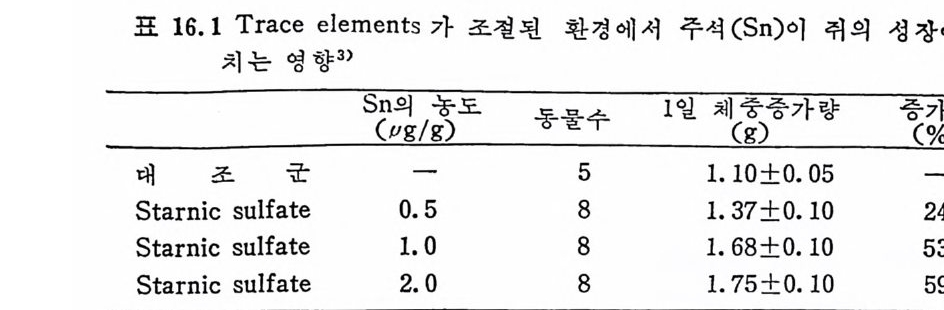 표 16. 1 Trace elements 가 조철 된 환경에서 주석 (Sn) 아 취의 성장에 마`
표 16. 1 Trace elements 가 조철 된 환경에서 주석 (Sn) 아 취의 성장에 마`
몇 몇 의 인체 실험 결과에 의 하면 9)10)11) Sn 은 아주 적 은 양이 흡 수되고 보유되며 배설은 주로 대변을 동해서 이루어진다. 뇨로는 약 10~20µ g /1 일을 배 설한다. 미 국사람의 1 일 Sn 섭 취 량은 1. 5 mg , 12> 3. 5mg , 13) 그리 고 17mg 까지 이 며 10) 영 국사람은 0. 187mg 1 4> 으로 추산되어진다. 그러나 통조림 석품 섭취시에는 높은 양의 Sn 을 섭취하게 된다. 1973 년 WHO 에서 발표한 통조림으로 섭취해도 무방한 섭 취 허 용량은 250m g/체 중 kg 이 다. 4) 고기, 곡류, 야채에는 l pp m 이하의 Sn 이 함유되어 있으며 구강 으로 섭취하는 양은 lm g /1 일 정도이다. 통조림에 든 채소, 과일 쥬 스 그리고 생선율 섭취했을 때는 38m g /1 일 정도이다. 곡류의 Sn 함유량은 표 16. 2 와 같다. 15)
 표 16.2 석 품 중의 주석 (Sn) 함유량 15)
표 16.2 석 품 중의 주석 (Sn) 함유량 15)
식품 중에서 Sn 의 함량이 높은식품은토마토스으프과토마토 케 찹 (l pp m 정도)이며 성성한 토마토에는 0.02 pp m 의 Sn 이 함유되어 있다 .16) Sn 의 독성은 그의 흡수량과 보유량이 적기 때문에 그다지 십각
하지 는 않다. 인체 실험 의 결과에 서 는 Sn 을 하루에 350~500mg m 섭취했을 때 독성 중상이 시작되었다. 그러나 Sn 의 독성은 Sn 의 화학구조와 Fe 의 섭 취 상태 에 따라서 달라진다. 가장 독성 이 강한 것은 Sn- 유기화합물로서 섭취시 성장 정지와 빈혈을 초래한다 .18)5 명 의 환자가 통조림 과일쥬스에 함유된 Sn 을 498p pm , 540p pm 혹 온 740p pm 섭취했을 때에도 독성중상이 나타나지 않았고 1370p pm 이상의 Sn 을 섭취했을 때 위장장애가 나타났다 .17) *참고문현 I) Schwartz , K. , Fed. Proc. , 33, 1748, 1974. 2) Ni el sen, F. H. and Sandste a d, H. H. , Am. J. Clin . Nutr . , 27, 515, ~974. 3) Schwarz, K. Mi lne , D. B. and Vi ny a rd, E. , Bi oc hem. Bi op hy s. Res. Commun. , 40, 22, 1970. 4) WHO, Trace Elements in -H uman Nutr i t ion, WHO. Tech. Rep . .S er. Nr. , 542, p. 38, U. 49, 1973. 5) Schroeder, H. A. and Mi tch ener, M. , J. Nutr . , 105, 421 and 452, 1975. 6) Kehoe, R. A. , Holak, J. and Sto r ey , R. V. , J. Nutr . , 19, 579, 1940. 7) Hami lt o n , E. I. , Mi ns ki, M. J and Cleary, J. J. , . Sci. Tota l Envi· .ro n. , 1, 341, 1972/1973. 8) Losee, F. , Cutr e ss, T. W. and Brown, R. , Trace Subst. Envir on . Healt h- 7, Proc. Univ . Mo. Annu. Con!. , 7th, 1973, p. 19, 1974. 9) Perry, H. M. , Jr. and Perry, E. F. , J. Cl in. Invest. , 38, 1452, ~959. 10) Kehoe, R. A. , Cholak, J. and Sto r ey, R. V. , J. Nutr , , 19, 579, 1940. 11) Ti pton , I, H. and Cook, M. J. , Healt h Phys . , 9, 103, 1963. 12) Ti pton , I. H. , Ste w art, P. L. and Marti n, P. G. , Healt h Phys . , :a 2, 1683, 1966.
13) Schreader, H. A. , Balassa, J. J. and Ti pton , I. H. , J. Chronic · Di s. , 17, 483, 1964. 14) Hami lton , E. I. and Mi n ski, M. J. , Sc i. Tota l Envir on . , 1, 375, 1972/1973. 15) Zook, E. G. , Green, F. E. and Morris , E. R. , Cereal Chem. , 47, 720, 1970. 16) Goeij , J. J. M. , de and Kroon, J. J. , IAEA/FAO/ WHO Sy m p o- · siu m on Nuclear Techniq u es in Comp er ati ve St u die s of Food and En·· vir on menta l Conta m i n ati on , Ot a nie m i , Fi n land, 1973, IAEA, Vi en - na. 17) Benoy , C. J. , P. A. Hoop e r and R. Schneid e r, Food Cosmeti c T o- xic o l. , 9, 645, 1971 . 18) Groot, A. P. , de, Food Cosmeti c Toxic ol. , 11, 955, 1973.
17 카드뮴 (Cad1n i um, Cd)* Cd 은 출생시 인체에는 거의 존재하지 않지만 연령이 증가함에 따라 접차적으로 체내에 축적된다 •31) 17.1 체내 함량과 분포 Cd 과 직접적인 관계를 갖지 않는 곳에서 일하는 50 세 가량된사 란은 인체전체에 약 20~30m g의 Cd 을 함유하며 上2 이나 으3 정도 가 간과 산장에 존재한다 .3l)32) Cd 은 의학적으로 독성이 있다고 알 려쳐 있으며 최근에는 환경오영에서 오는 Cd 에 많은 관십을 쏟고 있다 .l)2) 주변에 공장이 없는 지역의 사람의 혈액에는 1~7µg / 100ml 의 Cd 이 측정됐다. 담배를 많이 피우는 곳에 있을 때는 혈 액 의 Cd 량이 상승한다. 33) 뇌 , 허 파, 십 장, 근육은 1~45µg /1 00g fres h weig h t 를 함유한다. Fresh weig h t 100g 중에 10~390µg Cd 이 간장에 그리 고 120~1500µg Cd 이 신장에 함유되 어 있 었 다. 3) Hami lton 등의 연구에 서 도 이 와 비 슷한 함유량을 측정 할 수 있 었다.
* 지금까지는 과잉섭취 이의에는 독성이 나타나지 않고 필수 영양소로서 중요한 위 치문 차지하는 trac e elemen t s 둘울 주로 많이 서술했으나 17,18,19 장에서는 독성 의 겅향이 질고 영양소로서의 그 중요성이 완전히 규명되어 있지 않은 몇 가자 tra ce elements 문 알아보기 로 하겠 다.
Cd 의 체내 함유량은 섭취량과 밀접한 관계를 갖는데 특히 Cd 섭 취량이 중가하면 간과 신장의 Cd 량이 증가하는 반면, 체지방, 근 육, 그리고 피부는 벨로 영향을 받지 않는다. 또한 산장은 Cd 의 상승에 따라서 Zn 의 양도 같이 증가했다 .4)
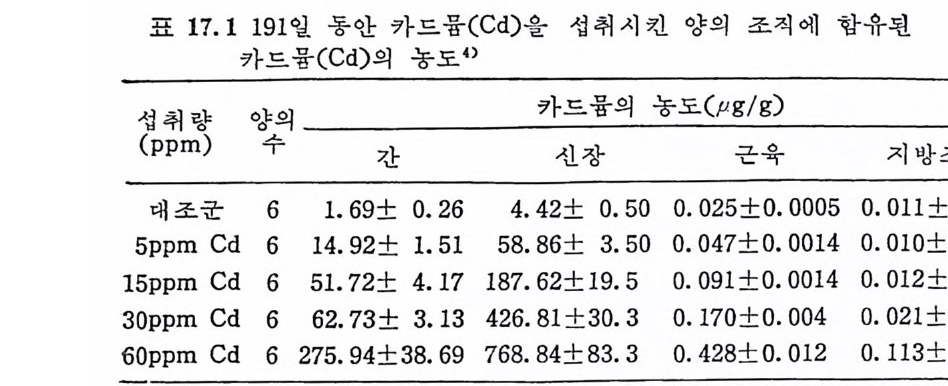 표 17.1 191 일 동안 카드뮴 (Cd) 을 섭 취 시 킨 양의 조칙 에 함유된
표 17.1 191 일 동안 카드뮴 (Cd) 을 섭 취 시 킨 양의 조칙 에 함유된
표 17.1 은 양에게 191 일 동안 Cd 의 농도를 다르게 섭취시킨 후 체내 각 기관의 Cd 함량을 측정한 것이다 .4) 17.2 주요 기능 Cd 은 화학적 성질이 Zn 과 흡사하다. 동물실험에 의하면 Cd 과 Zn 은 상호 길항작용을 하는 것으로 알려졌고 Cd, Fe, 그리고 Cu 간에도 중요한 상호작용이 있음이 밝혀졌다 .34)35) Cd 은 취의 혈압 을 상승시켰으며 Zn 을 공급하면 혈압이 다시 정상으로 되돌아 갔 다고 한다 .5)31) Cd 울 함유한 meta l lo enzy m e 에 대 해 서 는 아직 까지 보고되 지 않 고 있다. 다만 사람의 간과 신장에서는 Cd, Cu, 그리고 Zn 과 결 합된 복합단백 질을 볼 수 있 었 다. 이 분자는 26 sulfh y d ryl 기 를
가지고 있다. Cd 이온은 단백질과 함께 me t allo t h i one i n 을 합성하 고 특히 이 meta l loth io n ein 은 과잉 의 Cd 과 결합한다고 알려 졌 다. 독성이 있는 Cd 은 me t allo t h i one in에 결합되어 천천히 배설되 기 때문에 간의 해독작용과 관련이 있다고 추축된다•Meta l loth io n ein 은 체 내 에 서 비 단 Cd 뿐만 아니 라 Hg 그 이 외 에 도 2 가인 금속물 즉 Zn, Cu, Ag , Sn 의 독성을 감소시키는 작용 울 할 것 으로 추측하고 있 다. 39)40) Meta lloth io n ein 은 분자량이 10, 000 이 며 5. 9% 의 Cd 울 함유한 다. 6) 혈청 의 a.- 2 mi cr og lo buli n 은 Cd 분만이 아니 라 Zn 과도 결 합한다. Cd 은 leucin e dip e p tida se, his t i din e dia m i na se, oxali c ac id di- --ca rboxy l ase, argi na se, carboxy pe p tida se 와 같은 효소를 활성 화 하기도 한다 .4l) Schroeder 와 그의 동료들”은 쥐 와 생 쥐 들의 생 존율과 Cd 과의 관계 를 보기 위 한 연구에 서 이 동물들에게 다론 tra ce elements 는 전혀 들어 있지 않고 5 pp m 의 Cd 만 첨가한 음료수를 주었을 때 생촌율이 시간이 지남에 따라서 현처히 감소했음을 알아냈다. 표 17.2 는 쥐의 생촌율과 Cd 과의 관계를 나타냈다 .7)
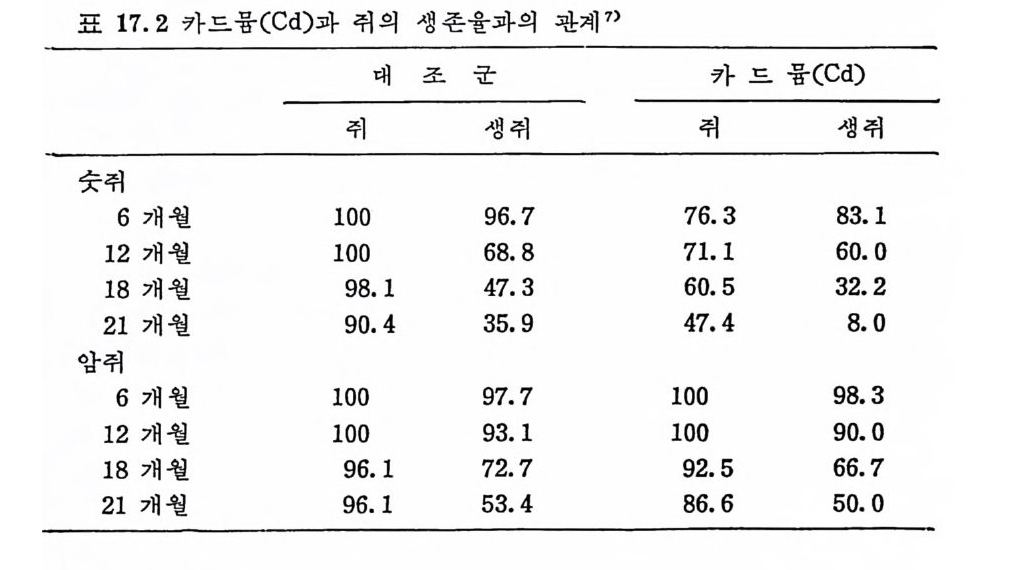 표 17. 2 카드뮴 (Cd) 과 취 의 생 촌울과의 관계
표 17. 2 카드뮴 (Cd) 과 취 의 생 촌울과의 관계
17. 3 대 사 .C d 의 흡수율은 3~8% 로 아주 낮으며 8) 대부분 식품에서 섭취된
Cd 은 대변으로 배설되고 약 lOµ g /l 의 Cd 은 뇨로 배설된다 .9) 7J - 과 신장에 는, Cd 이 특수 단백 질 인 meta l lot h io n ein 과 결 합되 어 있 다. 방사선 동위원소 115Cd 을 개에게 주사했을 때 그의 생리적 반 · 감기는 약 10 년이었다. 흡수된 Cd 의 배설률은 약 0.01% 이며 체 내의 축적량도 아주 적다. 또 체내의 Cd 반감기는 13~37 년의 긴 반감기 를 갖는다. 10) 식이에서는 Ca 과 P 을 다량 두여하여도 115Cd 흡수에 영향을 주 처 않았다 .11) 해조 다당류가 Cd 의 장내 홉수에 미치는 영향을 흰 쥐를 통하여 알아본 결과 5p pm 수준의 Cd 으로 오영된 식이에 5%, 혹은 10% 의 argi ni c a ci d 를 첨가했을 때, Cd 의 장내 흡수 억 제 효과가 있었으나 1% argi ni c ac id, 혹은 10% 미 역의 첨가는 효과가 없었다 •12) 17.4 섭취량과 필요량 사람의 1 일 Cd 섭취량은 30~70µg 정도이며, 동물과 석물성 삭 품에는 Cd 이 동량 함유되어 있다. 1 일 섭취량은 동식물의 혼합식 이와· 환경오염된 곳에서의 호흡에서 흡수되는 Cd 양을 합한 것이 되며, Cd 의 과량 함유는 Zn 을 주재료로 지은 집에서 발생되기도 _ 하는데 그 이유는 Cd 은 언제나 Zn 과 함께 촌재하기 때문이다. WHO 에 서 발표한 Cd to lerance 양은 70µ g /1 일로 발표되 었 다. 13)- 독일사람은 하루 약 50µ g의 Cd 울 14) 영국사람은 60 士 30µ g를 섭취 하는 것으로추정되고 있다. Rob i nson 등 16) 은 뉴질랜드의 젊은 여성 들의 1 일 Cd 섭 취 량을 60~92µg 으로 추정 하였 고, Murth y 와 동료들 은 17) 어린아이들이 27~64µg Cd 을 섭취한다고 보고했다. Dug ga n 과 L ip scomb18) 은 미 국의 어 린이 들이 하루 26µg 의 Cd 울 섭 취 한다 고 했다. 캐 나다의 1970~1971 년 조사에 서 는 식 품분석 에 의 거 해 서 、 1 일 67µg 정 도의 Cd 이 섭 취 된다고 보고했다.
17.5 함유석품 독일의 식 품에 함유하는 Cd 은 0. 1~150µg /1 00g fres h weig h t 이 다. 고기 에 는 100g 의 fres h weig h t 당 15~20µg , 과일과 채 소에 는 5~28µg , 두류에 는 15~30µg , 그리 고 음료수에 는 15~28µg 정도 함유되어 있다고 측정됐다. Lin m an 둥은 Cd 함량이 0. 05p pm 이 스웨 멘 밀에 , 0. 033p pm 이 밀가루에, 그리고 0.148 pp m 이 뇌에 함유되어 있다고 한다. Zook. 등 20) 은 밀과 밀가루 종류에 따라 Cd 의 함량을 다음과 같이 측정했 다(표 17.3).
 표 17.3 밀 의 종류에 따른 카드뮴 (Cd) 함유 량 20)21)22)23)
표 17.3 밀 의 종류에 따른 카드뮴 (Cd) 함유 량 20)21)22)23)
그 이의에 쌀과 옥수수에는 0. 055 土 0. 032µg /g 로 보고되았 다 21 )22 )23) 盧 등 28) 은 시료 버섯 중에 함유된 Cd 은 극히 미량이므로 측정할 수 없었다고 하며, 朴 둥 29) 은 해조류인 녹조류에 0.11mg %, 갈조 류에 0.12mg %, 홍조류에 0. 29mg % 함유되 어 있다고 하며 , 특히 ge li diu m amansii 중에 함유된 Cd 은 0.87m g%의 제일 높은 함유 량을 보이고 costa ria costa t a 중에 함유된 Cd 은 0.02m g%로 함유 량이 가장 낮았다고 보고되었다. 17.6 독 Aj 과잉의 Cd 은 단백뇨, 위장장애, 피곤 그리고혈액량의 감소를 나 타낸다. 단백뇨는 작은 입자로 된 단백질의 재흡수작용때문에 일야
나며 , 세 뇨관의 흡수장해 에 의 하여 신장의 Cd 의 농도가 200µg / g fres h weig h t 까지 도달하기 도 한다. 10 ) Cd 은 심 장과 혈 액 순환에 도 영 향을 준다 . Schroeder3 7 ) 는 Cd 섭 취 에 기인하는 고혈압증을 관찰할 수 있 었 는데 Cd 이 많이 오영된 환경에서는 고혈압 동 순환기 계통의 환자들이 많이 사망한다는 것 이 지적되었다. 또한 빈혈도 초래되는데 이는 Cd 이 다론 2 가 이 온인 Cu, Zn, Fe 의 흡수를 방해 하기 때 문일 것 으로 보여 진다. 42) 그 이의에도 유산, 사산 그리고 기형아 출산 둥을 들 수 있다. 1950 년도 말경에 일본에서는 골격의 무기질 감소중과 장애를 가쳐 오는 itai- itai 병 이 유행 하였 다 . 43)4 4 ) 그 원인은 탄광에 서 Cd 영 이 휼 러 들어 간 강물을 음료수로 사용한 것 으로서 대 개 의 음료수는 보통 0. 0005p pm 의 Cd 울 함유하는 데 반해 , 이 오염 된 음료수에 는 0. 18 pp m 의 Cd 이 함유되어 있었고 여기서 자란 조개와 생선 등에는 lOO pp m 의 Cd 이 함유되어 있었다. 식품위생 법규에 의하면 15p pm 의 Cd 이 독성 을 일으킨다고 한다. 24) Ita i - itai 병 으로 알려 진 Cd 독 성중은 Cd 이 Ca 과 교차되어 머에 이상을 초래하게 되고골격이 위 축된다. Cd 의 흡수경로를 살펴보면 Cd 에 오영된 달걀, 과일쥬스, 그릇, 조리기구와 장식품에도 Cd 을 사용하는데 이때 윤기가 나게 하기 위해서 발라 놓은 칠이 조리중에 벗겨지면서 Cd 이 음식에 들어가 고 이는 위의 영산에 의해서 CdC12 로 전환되어 체내에 흡수된다. 그 이외에도 인산을 함유한 비료에도 Cd 이 함유되어 있어 농작물 울 통하여 섭취된다. Cd 과잉 섭취시에는 Cd 의 독성을 적게 하기 위해 서 meta l loth io n ein 이 중요한 역 할을 한다. 쥐에게 lO pp m 의 Cd 율 포함한 음료수를 1 년 동안 계속 섭취시켰 으나 독성중상이 나타나지 않았으며 ,25) 5~lO pp m 의 Cd 울 aceta t e 형태로 생쥐에게 섭취시킨 결과 몇 주 후에 머의 citra te 량이 감소 되 는 것 으로 나타났다. 26) 50p pm 의 Cd 울 음료수에 첨 가했을 때 는 성 장지 연과 mi cro cy te anemi a 중상이 나타났다 .25) 한 번에 과량의 Cd 을 주사했을 때는 동물과 태 반에 necrose 현상이 나타났다.
최 근 뇨 중의 /32 -m i cr o glo bulin 방사선 면 역 평 가 분석 이 Cd 에 의한 초기 신세뇨관 손상을 측정하는 데 민감한 전단 방법이라는 것이 밝혀졌다 .27) *참고문현 1) Essin g , H. G. , K. H. Schaller, P. Szadkowski and G. Lehnert ,- Arch. Hy g. , 153, 490, 1969. 2) Flic k , D. F. , H. F. Kray b il l and J. M. Dim i trof f , Envir on . Res. , 4,. 71, 1971. 3) Lang , K. , Bi oc hemi e der Ernahrung 4 Aufl ag e De. Diet r icm Ste i n k off Verlag, 1979. 4) Doy le , J. J. , Pfa n der, W. H. , Grebin g , S. E. and Pie r ce, J. 0. , J. Nutr . , 104, 160, 1974. 5) Ferm. V. H. and Carpe n te r , S. J. , Lab. Invest. , 18, 429, 1968. 6) Kag i, J. H. R. and B. L. Vallee, J. Bi o l. Chem. , 235, 340, 1960,. 236, . 2435, 1961 . 7) Schroeder, H. A. , W. H. Vi nt o n Jr. and J. H. Balassa, J. Nutr i t . ,. 80, 39, 48, 1963, 83, 239, 1964, 86, 51, 1965. 8) Chem, R. , Hoekstr a , W. G. and Ganth er, H. E. , Fed. Proc. , 32,. 929, 1973. 9) Puli do , P. K. Fuwa and B. L. Vallee, Anal. Bt' oc hem. , 14, 393,-1966. 10) Frib e rg, L. , Pis c ato r , M. , Nordberg, G. F. and Kj el lstr om , T ... Cadmi u m in the Envir on ment 2, Aufl . p. 124, CRC Press, Cleveland, Ohio , 1974. 11) Sasser, L. B. , R. J. , Cherto k , M. F. Callaham and G. E. Jar boe,. in Ki rc hg es sner M. , Trace Element Meta b oli sm in Man and Anim als- 3, Technis c he Un i vers it죠t Mi lnc hen Freis i n g -W eih e nste p h an, p. 562 .. 1980, 12) 김영배, 강영회, 이서태, 《한국영양학회지》, 10, 1, 18, 1977.
13) WHO. Trace Elements z'n Human Nutr z ' tion , WHO. Tech. Rep. Ser. Nr. , 532, p. 38, 49, 1973. 14) Deuts c he Gesellschaft fiir Ernahrung . Ernakrung s berz'c k t 1972. Frankfu r t/ M ain 1973. 15) Hami lton , E. J. , M. J. Mi n ski and J. J. Cleary, Sci. Tot. Envir . , 1, 341, 1972/73. 16) Robin s on, M. F. , Mckenzie , J. M. , Thomson, C. D and Van Ri j, A. L. , Br. J. Nutr . , 30, 195, 1930. 17) Murth y , G. K. , Rhea, U. and Peeler, ]. J. Envir on . Se t'. Tecknol. , 5, 436, 1971. 18) Dug ga n, R. E. and Lips comb, G. Q. Pestz 'c. Monit . J. , 2, 153, 1969. 19) Lin m an, L. , Andersson, A. and Ni lss on, K. 0. , Arch. Envir on . Healt h 27, 45, 1973. 20) Zook. E. G. , Greene, F. E. and Morris , E. R. , Cereal Chem. , -41 1, 720, 1970. 21 ) W illiam s, C. H. and David , D. J. , Aust. J. Soz l Res. , 11, 43, 1.9 73. 22) Tsuy a g a wa, H. and Ohno, S. , Bull. Natl . Feeds & Fertz' l. , In- .sp ec t. Of f. , Toky o No. 3, p. 128, 1973. 23) Garcia , W. J. and Ing le tt , G. E. , Cereal Chem. , 51, 788, 1974. 24) Underwood, E. J. , Trace Elements in Human and Anz'm al Nutr i - -Uo n, New York. , Academi c Press, p. 243, 1977. 25) Decker, L. E. , R. U. By e rrum, C. F. Decker, C. A. Hop pe rt and R. F. Lang h am, Arch. Induct. Healt h 18, 228, 1958. 26) Weber, C. W. and B. L. Reid , Toxic ol. Ap pl. Pharmacol. , 14, 420, 1969. 27) Kj el lstr o m T. , in Ki rc hg e ssner, M. Trace Element Meta b oUsm i n Man and Anim als-3, Technis c he Univ ersit at Mi inc hen Freis i n g - Weih e nste p h an, p. 573 1978. 28) 노일협 , 《숙명 여 자대 학교 논문집 >, 제 21 집 , p. 141, 1981. 29) 朴贊杰, 《건국대 학교 논문집 >, 6, p. 217, 1977. 30) Anke, M. and Schneid e r, H. J. , Arch. Exp. Vete r in aermed, 25,
805, 1971. 31) Perry. H. M. , Jr. and Yunic e . A. , Proc. Soc. Exp. Bio l. Med. , 120, 805, 1965. 32) Schroeder, H. A. and Balassa, J. J. , J. Chronic Di s. , 14, 2.36 , 1961. 33) Lewi s, G. P. , Jus ko, W. J. , Coug h li n, L. L. and Hartz , S. , Lancet, 1, 291, 1972. 34) Berson. S. A. , Am. J. Med. , 20, 653, 1956. 35) Harden R. McG. , Mason, D. K. and Alexander, W. D. , Q. J. Exp. Phy si o l. Cong n . Med. Sci. , 51, 130, 1966. 36) Cump b ell, J. K. , Davie s , N. T. and Mi lls. C. F. , in Ki rc hg e ssner, M. ed. , Trace Element Meta b ol£ s m in Man and Anim als-3, ATW. Weih e nste p h an, p. 553, 1978. 37) Schroeder, H. A. , J. Chron. Dt 's. , 18, 647, 1965. 38) Ki rc hg e l3ner, M. E. Weig a nd A. Schneg g, E. GraBmann, F. J. -Sc hwarz and H. ·P. Rot h , Weih e nste p h an in Cremer. H. ·D. D. Hotz e l .an d J. Ki ihn au, Bio c hemt 'e und ph y s io lo g ie der Ernii. h r-un g Ba1: d I, Tet l 2, Georg Thie m e Verlag, p. 299, 1980. 39) Umweltb undesamt , Luft qu aUt ii.ts Krit er t'e n fu r Cadmt 'um , Be: .--rt 'ch te , 4/77, Berli n, 1977. 40) Okunik i, K. , Adv. Enym ol. , 23, 29, 1961. 41 ) Vallee, B. L. , Phy st 'o l. Rev. , 39, 443, 1959. 42) Decker, L. E. , R. U. By e rrum, E. F. , Decker, C. A. Hop pe rt and :R. F. Long h am, Arch. Indust, Healt h 18, 228, 1958, 43) Kobay a shi, J. , Morii, F. , Muramoto , S. and Nakashim a, S. , Jpn . ]. Hy g. , 25, 364, 1970. 44) Murata . I. , Hi ro no, T. , Saeki, Y. and Nakag a wa. S. , Bull. .So c. Int. Chfr . , 29, 34, 1969.
18 납 (Lead, Pb) Pb 은 식물과 토양에 많이 촌재한다. 사람은 거의 음식물과 대기 i 중에서 Pb 울 섭취하게 된다. 18.1 체내 함량과 분포 사람의 Pb 함량은 90~400mg 으로 90 %가 골격 에 촌재 하며 1)27)28), 혈 액 에 는 2> 15~40µg /l OOml 정 도이 다. Goldwate r 와 Hoover” 는 건 강한 성 인의 혈액 의 평 균 Pb 함량을 l7µg /l OOml 로 보고하였 으며 이 양은 환경오영과 밀접한 관계가 있을 것으로 생각된다. 표 18.1 은 사람의 Pb 함유량이다 .4) 이 수치는 46 명의 시체 해부 、 에서 얻어진 결과이다. 독일에 서 자동차가 많이 다니 지 않는 곳의 공기 는 0. 03~O.lµg / m 며 Pb 울 함유하고 보통 도시 에 는 0. 5~4µg /m 3, 그리 고 자동차 가 많이 다니 는 곳의 공기 는 l511 ,g/ m3 의 Pb 울 함유한다고 한다. 2)- 독일의 식 수에 는 0. 01~0. 03mg / l 의 Pb 이 함유되 어 있 었 으며 수도 관의 물을 오래 틀어 놓으면 0. 2mg / l 의 Pb 을 함유한다. 1871 년~ 1923 년에 실시했던 사람의 머리카락의 Pb 함량이 최근 자동차연갸 에 의해 오영된 환경의 머리카락에 함유된 Pb 량보다 더 높았다는 것은 대단히 홍미로운 결과이다 .6)
 표 18. 1 사람의 납 (Pb) 함유량 4)
표 18. 1 사람의 납 (Pb) 함유량 4)
18.2 주요 기능과 결핍증 사람에게 있어서의 Pb 의 결핍증이나 주요 기능에 대해서는 아칙 알려 지 지 않 았다. 1980 년 Reic h lmay r -Lais 와 K i rch g essne 한가 쥐 에 게 석이로서 Pb 의 결핍울 야기시킨 후 성장을 관찰했다. 이 Pb 결 핍 식이군에는 18 士 5 pp m Pb 이 대조군에는 l pp m 의 Pb 이 함유되 어 있었다. 이때 Pb 이 결핍된 어미쥐의 다음 세대에서 성장지연 현 상이 나타났다. 수유기의 마지막 단계에서는 정상군보다 생촌윤이 11% 나 줄어 들었다. 이 동물에게 Pb 결핍식이를 계속 주었을 때는 성장지연율 이 대조군에 비해서 22% 나 낮게 나타났다. 제 2 세대에서도 Pb 의 결핍 식이로서 성장지연을 다시 야기시킬 수 있었다. 이 시기에 Pb 울 정상으로 섭취시키면 성장이 다시 장 상으로 회복되는 현상을 보였다. Pb 이 결핍된 쥐와 정상쥐를 교배 시켰을 때 임신 기간 동안에 Pb 이 결핍된 쥐에는 체내 대사 장애 가 초래됨을.불 수 있었다. 위의 실험을 통하여 Pb 은 영양소로서 성칭에 주요한 기능을· 갖 고 있는 것을 증명할 수 있었으며 성장실험을 몇 번이나 반복했을 때도 같은 결과가 나다났다. 식이에 18 pp b 의 Pb 을 섭취시켜 결핍 증을 야기시킨 쥐에게서 태어난 여러 세대의 hema t ocr it치, 평군 혈 구량, hemog lo bin , 그리고 평균 혈구 hemo g lob in의 양울 대조군 과 비교했다. l pp m 의 Pb 을 섭취한 대조군과 비교해 볼 때 제 1서}
대로부터 태어난지 3 일된 숫쥐는 hema t ocr it치가 22%, hemog lo bin 이 25%, 평균 혈구량 23% 그리고 평군 혈구 hemo g lob i n 양 28% 정도가 각각 감소했다. 또 38 일간 계속 결핍된 식이를 섭취시킨 암 쥐는 더욱 더 현처한 감소현상을 보였는데 hemo t ocr it치가 14%, 해모굳로빈이 32%, 평군 혈구량이 29%, 평군 혈구 hemo g lob i n 이 37%, 그리고 평군 혈구 hemog le bin 농도는 12% 가 각각 감소했다. F2 제 2 세대에서도 Pb 이 결핍되었던 군이 대조군에 비해서 상당히 감소되었음이 나타났다. 또한 Pb 이 결핍된 쥐에게 Pb 을 섭취시킨 결과 감소된 hemog lo bin , hemato c rit, 혈구량, 혈구 hemog lo bin 둥이 다시 정상화 되었다. 위의 실험을 동해 Pb 은 성장, 혈액의 앙, 농도둥에 많은 영향울주는 필수 영양소임울 증명할 수있었다.
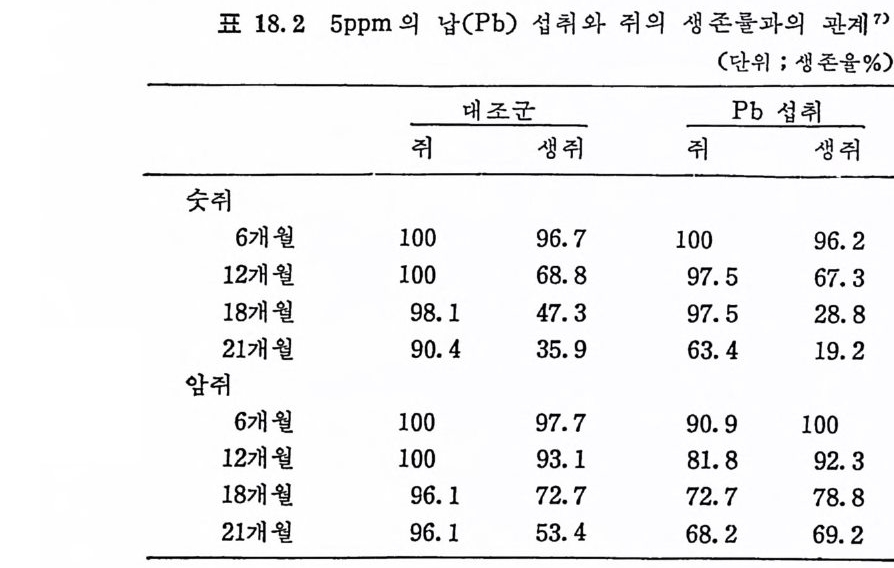 표 18.2 5 pp m 의 납 (Pb) 섭취와 쥐의 생존 률 과의 관계
표 18.2 5 pp m 의 납 (Pb) 섭취와 쥐의 생존 률 과의 관계
Schroeder 등”은 실험동물인 쥐와 생쥐의 생촌율과의 관계를 보 기 위해서 이 동물들에게 다른 일체의 tra ce elemen t s 는 식이에서 계한하고 5 pp m 의 Pb 만을 음료수로 섭취케 하였을 때 생촌울이 시 간의 흐름에 따라 접차 감소되는 것을 볼 수 있었다. 표 18.2 는 !Spp m 의 Pb 섭취와 생촌울과의 관계이다 .7)
1R. 3 대 사 Pb 은 적은 양의 흡수에도 독성을 일으킬 가능성이 큰 원소로서 흡수된 Pb 은 머와 근육조직을 동하여 간으로 이동되며 간에서 담 당을 동해 배 설된다. 정 상적 인 뇨의 Pb 농도는 3. 5µg /1 0Q m / 아 다. 음석으로 섭취된 과잉되지 않은 Pb 은 주로 대변으로 배설된다• 식 품에 아주 적은 양의 Pb 이 함유되어 있으면 체내에 흡수되어 거의 전부가 빠른 속도로 배설된다. 그러나 과량의 Pb 은 흡수량보다 배 선량이 훨씬 적으므로 그로 인해서 뼈와 조직에 Pb 이 축적되게 된 다 .l) 식품으로 섭취하는 Pb 의 흡수율은 6~IO% 정도이다. 사람의 하루 Pb 섭 취 량은 식 수, 공기 , 음식 으로서 0. 3~o. 6m g /I 일로 계 산 했을 때 체내에는 하루에 약 8 Qµg이 보유되며 24 시간 뇨로 배설되 는 Pb 의 함유량은 약 80µ g이다 .2) Ca 과 Fe 을 음식물로 많이 섭취하였을 때는 Pb 의 흡수율이 감 소되었다. 호홈으로 흡입된 30~40% 의 Pb 이 신체에 축적되는데 ·이는 Pb 입자의 크기에 따라서 흡입률이 달라진다. 쥐는 Zn 섭취 가 높을 때(시료에 200p pm ) Pb 의 흡수가 저해되었으며 그로 인해 서 Pb 의 독성이 감소되었다 .8) 과잉량의 Ca 섭취도 역시 Pb 의 홉 수를 저해하였다 .9) 어린이들이 섭취할 수 있는 Pb 의 허용량은 하루 30Q µg 정도이며 이는 1~3 세까지도 허용되는데 10) 이 허용량은 Pb 흡수율이 10% 정 도라고 생 각될 때 의 허 용량이 다. Alexander11) 논 평 군 Pb 이 1 일 10. 6 µg/ kg 체중이라고 할 때 흡수는 53% 정도이며 보유는 18% 정도라 고 보고했다. 쥐를 대상으로 한 실험에서 어린 쥐가 나이가 많은 취 보다 보유율이 높다고 한다. 12)13) Z i e g lerl4) 가 조사한 89 개 의 Pb- balance 실험에서 하루에 Pb 울 5µg / kg 체중으로 섭취시켰을 때 42 %의 흡수율과 32% 의 보유율을 보였다. Pb 의 섭취량이 증가함에 따라서 뇨와 변으로의 Pb 배설이 중가되었으며 흡수율도 섭취량에 따라 비례했다. 그립 18.1 은 Pb 섭취량과 보유량이다. 두 살 이하의 어린이듄은 성인에 비해서 Pb 의 흡수와 보유가 더
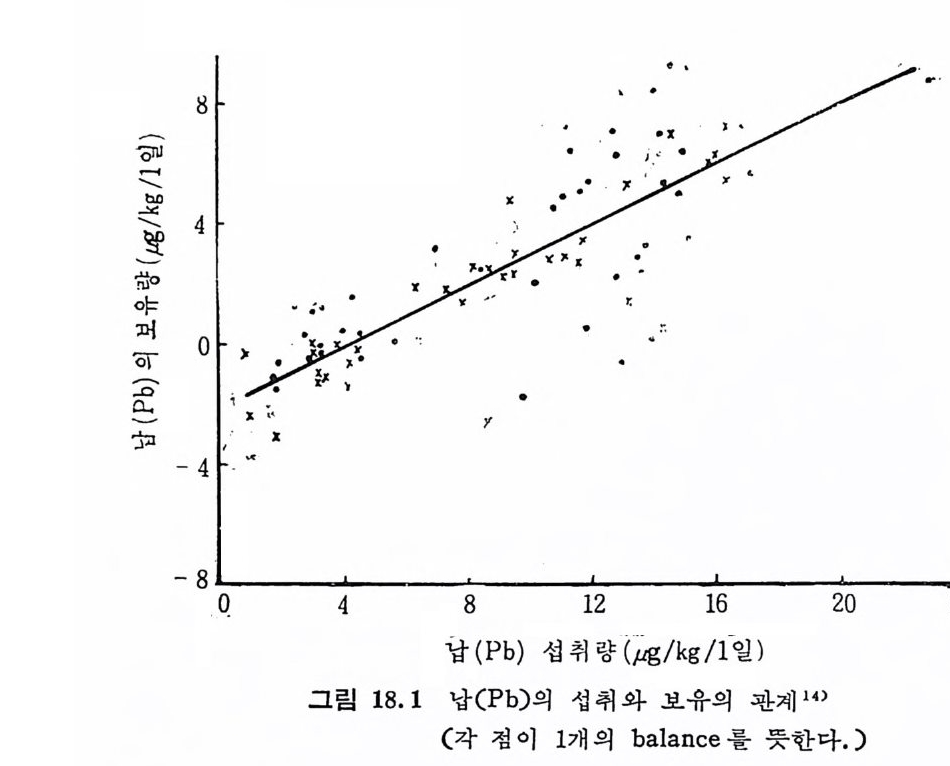 8 . • `
8 . • `
컸다. 18.4 섭취량과 필요량 Lehnert 등 26) 은 독일 사람들이 식 품으로 섭 취 하는 Pb 의 양을 518µg : 정도로 추정 했다. Bo pp el27 년겨사람의 Pb 섭 취 량을 조사한 결과 1 일 73~236µg 로 평 군 1 일 12lµg 이 었 다. 미 국인의 경 우 하루 Pb 섭 취 량을 200~300µg 로 추정 하고 있 다. 15) 오스트리 아 사람은 1 일 약 400µg Pb 이 고 16) 일본 사람들은 239~318µg , m 그리 고 네 덜란드 사람 은 105µg Pb 으로 나타났다. 식품 이의에도자동차에서 내뿜는 산화 과정 에 서 생 산된 Pb-alky l 의 흡입 량은 40µg 정 도이 다. FAO/WHO· 분과 위원회의 보고에 의하면 사람의 최대 Pb 섭취량은 1 주일에 3mg - 혹은 체중 1k g당 0.05m g으로 추산되어졌다 .18)
18.5 함유석품 최근 자동차에서 내뿜는 Pb 이 도로에서 50m 떨어전 밭에서 자 라는 농산물들의 Pb 의 양울 증가시키고 있으며 도로 결이 아난 곳 에서 자란 농산물보다 2~10 배의 Pb 이 더 함유되어 있었다고 한 다. 2) 표 18. 3 은 독일 식 품의 Pb 함유량이 다. 2)
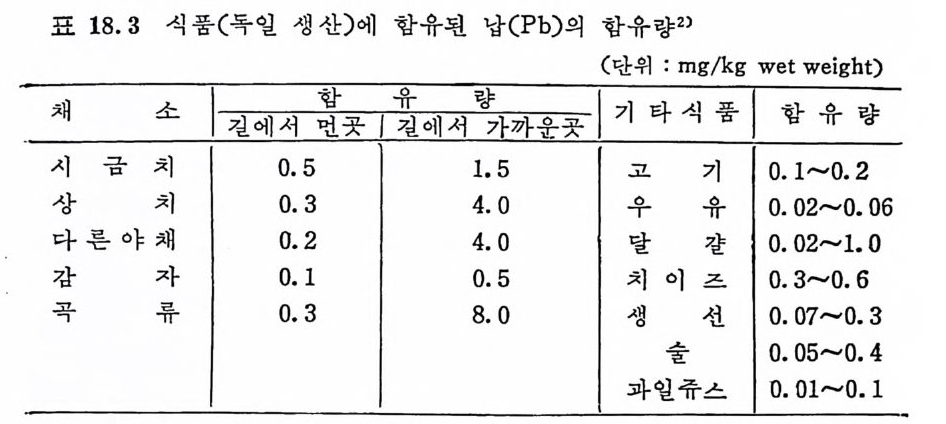 표 18. 3 식 품(독일 생 산)에 함유된 납 (Pb) 의 함유량 2)
표 18. 3 식 품(독일 생 산)에 함유된 납 (Pb) 의 함유량 2)
영국과 캐나다 19) 그리고 미국의 20) 식품에 함유된 Pb 량은 표 18.4 오卜 같다.
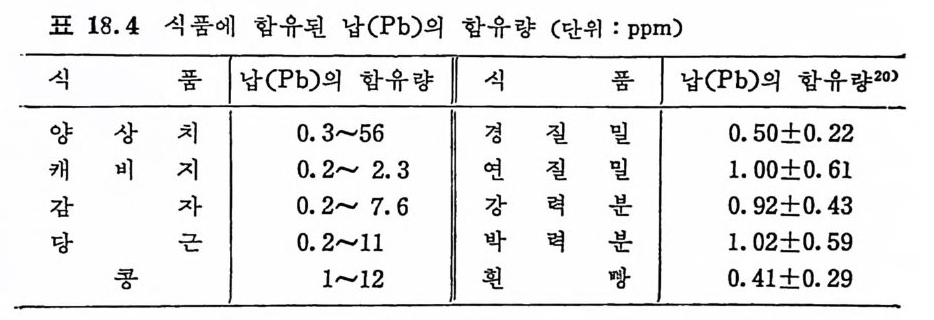 식표 18. 4 식품 품 에 납함 (유Pb된) 의 납함 (P유b)량 의 l함 .유.<,1 량 (단위 T:x zp pm )납 (P b) 의 함유량 20)
식표 18. 4 식품 품 에 납함 (유Pb된) 의 납함 (P유b)량 의 l함 .유.<,1 량 (단위 T:x zp pm )납 (P b) 의 함유량 20)
Mi tch ell 과 Aldous21) 는 Can 에 저 장된 유아식 에 는 과량의 Pb 이 함유되어 있다고 경고했다. Can 에 들어 있는 분유에는 Pb 의 양이 :20 2µg / l 로서 전유위 40µg / l 와 비 교했을 때 많은 양울 함유하고 있
었다. 256 개의 유아석인 과일쥬스 중에서 금속 can 에 보촌된 것은` 그중 62% 의 평균 Pb 의 양이 lOOµ g /l 였으며 37% 가 200µ g /l 그리고 1 %가 400µg / l 와 그 이 상으로 나타났다. 유리 와 알루미 늄 용기 롤 사 ~ 용한 유아식 의 1% 정 도가 200µg / l 의 Pb 을 함유했 다. 영 국의 168 개 의 과일동조림에는 Pb 의 양이 0.02~8.16 pp m 로 많은 격차를 보이 며 평군량은 0.94 pp m 정도였다 .22) 한국의 시료 버섯 중 Pb 함유 범위 는 0. 01~0. 07m g%이 며 해 조류에 는 Pb 함량의 평 균값이 녹조류에 53mg % 갇조류에 0.5mg % 홍조류에 0.25m g%가 함유되어 있다 .23) 高둥 24) 에 의하면 한국산 쌀의 Pb 평군 함량은 0.02mg %, 보리는 평군 0.03mg , 옥수수는 평군 0.06mg %, 야채류는 평군 0.003mg % . 이라고 보고하고 있다. 18.6 독 성 독성을 나타낼 수 있는 Pb 함량은 SH- 효소를 방해하는데 그중에 서 도 po rph y r in 생 합성 , ATP-ase 와 lipo ami de dehy d rog e nase 를 방해 한다• Pb 독성 의 지 표로서 &ami no levuli n ac id 가 Pb 과 함께 뇨로 배설되는 것을 축정할 수 있다. 표 18.5 는 Pb 의 독성을 측정 하기 위해서 병원에서 겁사한 Pb 함량이다 .25)
 표 18.5 병원에서 겁사하는 납 (Pb) 의 함량과 독성과의 관계 25)
표 18.5 병원에서 겁사하는 납 (Pb) 의 함량과 독성과의 관계 25)
Pb 의 급성 독성 증상으로는 hemog lo bin 결핍으로 인한 빈혈, 산 통, 뇌 손상마비, 신장장애 둥이 있으며 만성인 경우에는 창백한· 피부, 두통, 식욕감되를 들 수 있다. 독성 치료는 Pb 과 복합체를 · 형성시켜 뇨의 베설량을 늘리게 해야 한다. 그 의에도 장기간 cor- tiso n 치료시 많은 양의 Pb 울 뼈로부터 이동시켜 주어 그 결과 독 · 성을 초래하기도 했다 .
*참고문현 I) Schroeder, H. A. and Ti pton , I. H. , Arch. Envir on . Healt h 17,. 965, 1968. 2) Lang , K. , Bi oc hemi e der Ernti hr ung 4, Auf! ag e Dr. Diet r i c h Ste i n k off Verlag , p. 379, 1979. 3) Goldwate r . L. J. and Hoover, A. W. , Arch. Envir on . Healt h 15, 60, 1967. 4) Gross, S. B. , E. A. , Peit ze r, D. W. Yeag e r and R. A. Kehoe. , To-xic o l. Ap pl. Pharmacol. , 32, 638, 1975. 5) Weis s , D. B. Whit ten and D. Leddy . Scie n ce, 178, 69, 1972. 6) Reic h lmay r- Lais , Ki rc hg e ssner, Zeit ch rif t fu r Phy si o l og ie, Ti e - renti hr ung und Futt er mi ttell kunde Band 46, Heft 1~2 p.1 , 1981. 7) Schroeder, H. A. , W. H. , Vi nt o n Jr. and J. H. Balassa, J. Nutr i t , ,. 80, 39, 48, 1963, 83, 239, 1964, 86, 51, 1965. 8) Cerklewski, F. L. and R. M. Forbes, J. Nutr . , 106, 689, 1976. 9) Meredit h, P. A. , et al. , Bi oc hem, J. , 166, 531, 1977. 10) Ki ng , B. G. , Amer. J. Di s. Chil d . , 122, 337, 1971. 11) Alexander, F. W. , B. E. Clay ton and H. T. Delves, Qu art. Jr Med. , 43, 89, 1974. 12) Kosti al, K. , I. , Sim onovic and M. Pis o nic , Natu r e, 233, 564,. 1971. 13) Forbes, G. B. and J. C. Rein a , J. Nutr . , 102, 647, 1972. 14) Zie g le r, E. E. , B. B. Edwards, R. L. Jen sen, L. T. Fil er Jr. ancf S. T. Fomon, in Ki rc hg e ssner, M. ed. Proceedin g s of the 3rd Inte r - nati on al Sy m p os i'u m on Trace Element Meta b olt 'sm in Man and Ant' - mals, Munic h , p, 292, 1978. 15) Nati on al Academy of Sc ien ces, Nati on al Research Council , Ai r~ born lead in Perspe c ti ve, W a.s hin g ton , D. C, , 1971. 16) Woedic h , H. , et al, , Di e Nahrung 21, 685, 1977. 17) Horiu c hi, K. , Osaka Cit y Med. J. , 11, 265, 1965.
18) World Health Orga niz a ti on , Technic al Rep o rt Serie s Nr. , 505, -Gcnf 1972. 19) Warren, H. V. and Delavault, R. E. , Mem. Geo!. Soc. Am. , 123, .19 71. 20) Zook, E. G. , Greene, F. E. and Morris E. R. , Cereal Chem. , 47, 720, 1970. 21) Mi tch ell, D. G. and Aldous, K. M. , Envir on . Healt h Perspe c t . .Ex p . , Issue 7, 59, 1974. 22) Thomas, B. , Edmunds, J. W . and Curry, S. J. , J. Sci. Food .Agr i c. , 26, 1, 1975. 23) 朴贊杰 《전국대 학교 논문집》, 6, 217, 1977. 24) 고인석 外, 『희 갑기 념 논문집 』, p. 40, p. 58, 1978. 25) Haas. Th. , Schaller, K. H. and Valenti n, H. , Dt sc h. Arte o l. , 69, 1803, 1972. 26) Lehnert, G. G. , St a delmann, K. J. Schaller and D. Szadkowski, .Ar ch. Hy g. , 153, 403, 1969. 27) Kehoe, R. A. , U. S. Publi c H ealt h Serv. Puol. , 1440, 54, 1966. 28) Monie r · Wi lliam s, G. W. , Trace Elements in Food, Chap m an & :Ha ll, London, 1949.
19 수 은 (Mercur y, Hg ) H g은 환경오영과의 관계에 의해 관십이 증대되기 시작하였다. 자연에서 H g의 일부는 Hg 원자 상태로, 또는 무기물과 결합된 Hg C l2 나 Hg S 의 형 태 로 그리 고 나머 지 는 유기 물과 결합된 alky l - Hg 결합물과 aryl - Hg 결합물로서 존재한다. 사람에게 가장 위험한 독성 형태는 me t hy l-H g ((CH3)2H g]이며 아 는 식품을 통해서 섭취했을 때 많이 발생한다. H g과 me t hy l 기와의 결합은 주로 미생물에 의해서 이루어진다• 사람은 주로 해산물인 생선, 조개, 새우 둥에 의하여 H g을 섭취 하게 된다. 독일의 경우 공장 페수가 바다로 흘러가는 양은 1 년에 약 10,000 본 이상이 넘는다고 한다 .1) 바다에 서 나오는 생 선과 해 산물 중 약 80% 가 meth y l- Hg 을 함유 한다. 이들은 해처에 있논 공장페수가 호르는 곳에서 자라는 조 류나 pl ancto n 을 섭 취 하고 이 로 인해 서 meth y l- Hg 량이 증가하게 된다. 19.1 체내 함량과 분포 사람의 조직에는 정상적인 건강상태에서 약 0.5~2.5 pp m/ 건조 물로 Hg 이 존재 한다. 20)21)
혈액의 H g농도는 약 0.5µg /l 00g 정도로 아주 적게 촌재하지만 H g 섭취 량에 따라서 혈액의 H g 농도가 변한다. 22 )23 ) 70k g의 성인에게 H g 을 하루에 4µg / k g 체중을 섭취시켰을 때 혈 엑의 H g은 20µg /lOO g이었으며 14µ g / k g체중을 섭취시켰을 때는 80µg /I OOg 이 었 다. 혈액 의 Hg 이 20µg / l0 0g 일때 머 리 카락의 Hg 은 약 60µg /g 이 었 다. 1) 생선을 먹지 않는 사람들의 경우 적혈구의 H g함량은 0.4~0.5µg /lOO g이었으며 머리카락에는 2.5µ g/g보다 적게 함유되어 있었다. 석 탄도 약간의 Hg 울 함유하며 충치 의 구멍 을 막는 amalga m 그 티고 살군작용을 하는 크림에도 H g이 함유되어 있다. 표 19.1 은 사람의 각 기관의 H g함량이다 .2)
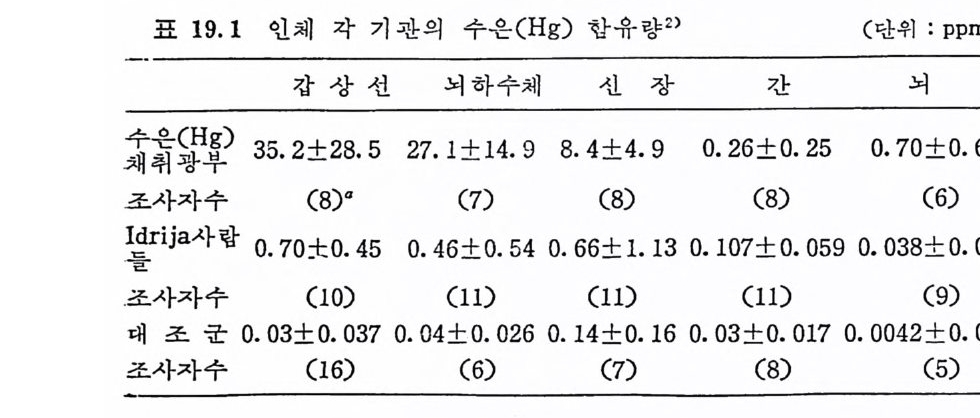 표 19. 1 인체 각 기 관의 수은 (H g) 합유량 2 ) ( 단위 : ppm )
표 19. 1 인체 각 기 관의 수은 (H g) 합유량 2 ) ( 단위 : ppm )
19.2 대 사 H g Cl2 은 사람에 있어서 약 2% 가 흡수되며 ph eny l H g은 약 5% 가 그리고 me t h y l-H g은 90% 이상이 홉수된다. 방사선 동위원소 인 203H g (CCH3)2 는 섭취 후 곧바로 적혈구에 이동된다. 흡수량 가 운데 약 50% 는 간으로 이동되고 나머지 약 10% 는 뇌로 이동된다. 뇨로 배 설되 는 Hg 은 · 0. 001~O. lµg / ml 로 보고 있 다. Me t hy l-H g의 생리적 반감기는 70~74 일인데 장율 통하여 섭취 후 1 일에는 약 3~4% 가 배설되며 그 후에 약 1% 가 배설된다. 신
장에서는 섭취 1 일 후에 약 0.1% 가 배설되었다. H g은 머리카락에 저장되기도 하는데 머리카락의 H g함량은 체내 의 Hg 상태를 측 정하는 데 도움이 된다. 유기화합물의 H g-결합물 은 적은 양이 간과 선장의 세포핵에서 분리되어진다 .3) 나이가 많아 침에 따라서 H g의 축적현상은 찰 관찰되지 않았다. 19.3 섭취 량과 허용량 독일 Karsruhe 의 연구소 조사에 의하면 일반 식사에서 Hg 섭 취St o량c k은h o1l 주m 일에간 서의 의 H조g 사 섭에 취 서 량8은. 203 ~士l 32 . µ5 5g µ/ 1g 일/1 l일” 이이 었었 으다.며 4) 스웨 덴의 또한 캐나다에서는 평군 13µ g /1 일로 계산되었다 .18) FAO/WHO 분과위원회에서는 최근 Hg 섭취의 최대 허용량을 0. 3m g l 주일로 결정 하고 이 중 0. 2mg 이 상이 meth y l- Hg 의 형 대 로 섭취되어서는 얀 된다고 지적하고 있다 .5) 19.4 함유식품 다음 표 19.2 는 식품에 함유된 H g의 함량이다 .6) 분석 된 생 선 중 99% 가 0. 5mg / kg 의 Hg 을 함유하는데 이 양은 아직까지 안전하다고 할 수 있다. 우리나라의 경우 콩나물 중에 없어야 할 H g이 존재한다는 것은 콩나물 성장의 촉진제로서 수은제 농약을 사용하는 데 서 기 인한다고 볼 수 있다. 朴둥”이 조사한 물에 의하여 재배되는 우리나라의 콩 나물 가운데 0. 06p pm ~0. 55p pm 정 도의 Hg 이 함유되 어 있 는 것 이 있는데 이러한 콩나물의 Hg 오영 현상은 큰 문제로 대두되고 있다. 朴둥”이 조사한 콩나물 중에 수은 정 량의 결과는 총 36 개 중 0, 1.. ppm 이 하가 8 개 , O. lpp m ~0. 5pp m 사이 가 8 개 , 0. 5p pm 이 상이 2 개 로서 검출되지 않은 것이 36 개 중 18 개로서 전체의 50% 가 H g이 검출되었으며 검출된 수은의 함량은 일본의 상치에 0.009p pm 시금 치 에 0. Olpp m 이 겁 출된 양에 비 하여 월등히 높았다.
 표 19. 2 식 품에 함유된 수은 (H g )6>
표 19. 2 식 품에 함유된 수은 (H g )6>
1974 년 盧둥 8)9) 의 보고에 의 하면 우리 나라의 딸기 에 Pb 이 0. 025~· 0. 037p pm , 마늘에 0. 059p pm , 상치 에 0. 034p pm , 쑥갓에 0. Ollpp m , 시 금치 에 0. 027p pm , 양배 추에 0. 062p pm 이 들어 있 는 것 으로 분 석되었다. 우리나라에서는 아직도 식품 중의 중금속류의 유해성 한 계치가 설정되어 있지 않으므로 그 기준이 모호하다. 일본의 식품 위생법규에 따른 기준을보면 청량음료는 H g 0.4p pm 이 기준으로 되어 있고 야채, 과실류에는 H g이 없는 것으로 나와 · 있다 .10) 그러나 일본에서도 상치 속에 H g이 0.009p pm , 시금치 속 에 0.01p pm 정도가 함유되어 있는 것으로 보고되어 있다 .11) 洪등 12) 이 보고한 바에 의 하면 한국산 계 란을 대 상으로 산지 , 종 류, 부위별 및 조리 방법벌에 따라 H g함량이 차이가 있었다고 보 고하고 있다. 계란의 산지별 Hg 함량은 표 19.3 과 같다. 공업시설이 많은 대도시에서 생산된 달갈에 수은 함량이 많은 것 으로 나타나고 있다. 계란의 종류별로는 레그혼이 0.087 pp m 으로. 수은 함량아 많았고 재 래 종은 0. 03lpp m 으로 적 은 함량을 나타내 었다. 계란의 부위별로는 전체 H g함량의 약 87% 가 난황에 들어 있으며 약 0.064p pm 정도이고 난백에는 전체 Hg 함량의 13% 정 도가 들어 있다. 계란의 조리 방법별로 보면 반숙된 계란이 0.OOT ppm 정도로 다론 조리방법에 비해 약 10 배가 감소되었으며 후라
 표 19.3 지 역 별로 본 달걀의 수은 (H g) 함량(레 그혼 )12)
표 19.3 지 역 별로 본 달걀의 수은 (H g) 함량(레 그혼 )12)
이는 0.015 pp m 으로 역시 다론 조리방법보다 많이 감소되었다. 19.5 독 Aj Hg 결합물의 독성 은 SH 와 S-gr oup 이 단백 질과 작용하고 더 나 •아 가서 는 pu rin , pyr im i di n e , nucleic acid , nucleoti de 와 작용하여 독성이 나타나는 것으로 보인다 . H g결 합물은 muta g e n 이 나 te rato g e n 으로 작용한다. 호흡기 관으로 흡입 되 는 Hg 은 공기 의 농도가 0. lmg /m 3 이 상일 때 독성 을 나타낸다. 70kg 의 성 인에 게 Hg 14µ g /k g /l 일을 섭 취 시 켰 울 때 독성중상이 나타나지 않았다. H g의 독성을 일으키는 형태는 meth y l- Hg 이 다. Hg 이 O. Smg / kg 체 중일 때 독성 증상이 나타나는 초기였으며 4m g /k g체중 이상이 되면 사망했다. 임신시 H g을 섭취하면 대반에서 H g을 조철해 주지 못하기 때문 · 에 태아에게 이동되며 또한 모유로도 이동된다 .13) 위험중상을 축정하기 위해서 혈액겁사를 하는 데 0.02µg /g 정도 가 알맞고 이 농도는 0.04µ g/g의 적혈구이다 .14) 스웨멘에서 조사한 바에 의하면 생선으로부터 섭취한 H g의 양과 H g의 혈액치는 비례했다. 이 생선에는 H g함량이 O.Sm g /k g이었 으며 지금까지의 결과로 미루어보아 이 생선에 함유된 Hg 양온 안 정하다. Blacksto ne 둥 15) 이 조사한 gu in e a pig 실험 결과에 서 는 8mg / kg
의 H g을 섭취했을 때 각 기관에 함유한 ascorbic ac i d 를 감소시켰다 고 하며 높은 양의 ascorbic a ci d(5m g /k g)는 Hg 에 서 기 인된 부신 피질의 득성을 막아 주었다고 한다. 그러나 다른 독성 증상에는 영 향을 미치지 못했다. 쥐 에 게 5p pm 의 selenit e 를 사료로 섭 취 시 켰 을 때 meth y l- Hg 의 독성증상을 감소시켜 주었다 .16> Hg 독성 현상으로 큰 물의를 일으 킨 곳은 일본으로 2 회 에 걷쳐 많은 주민들이 독성 을 일으켰 었 다. 19)26) M ina muto 에 서 는 24) 121 명 이 독성 을 일으켰 고 그 중 46 명 이 사망 했으며 Ni iga ta 에 서 는 46 명 중 6 명 이 사망했다. 그 원인은 meth y l- Hg 이 많이 함유된 생선을 섭취한 데서 비롯된 것으로 보인다 (100 , ppm H g까지 함유되어 있었다). 독성 증상으로는 장님이 되거나 중추신경의 이상에서 오는 말더 듬, 운동기능마비, 정산이상 등 뇌의 손상으로 인한 마비등의 많은 중상을 나타낸다. *참고문현 1) Lang, K. , Bi o chemi e der Ernii hr ung 4, Aufl ag e Dr. Diet r i c h , Ste i n k off Verl~g , p. 330, 1979. 2) Bate , L. C. and Dy e r, F. F. , Nt tcl eonic s 23, 74, 1965. 3) Fang , S. C. and E. Falin , Gli em . Bi ol . Inte r act. , 9, 57, 1974. 4) Schelenz, R. and J. F. Die h l, Z. Lebensm. Unte r such-Forsch. , 153,. 151, 1973. 5) World Health Orga n iz a ti on , Technic al Rep or t Serie s , Nr. , 505,. Genf 1972. 6) Sunart, N. A. , Res, Rev. , 23, 1, 1968. 7) Jae Hong Park and Hy u n Keun Nam, K. ]. N. , 10, 3, 1977. 8) 盧晶培 外 4 人, Rep or t of NIH, Korea 11, 171, 1974. 9) 盧晶培 外 6 人, ~~po rt of NIH, Korea 11, 161, 1974. 10) 未永泉二, 「有害性金屬의 試驗法과 許容濃度限界」, 《藥局〉〉, 25, 10., 1974.
11) 田中之 雄 外 3 人, 『日食衛 法』 , 15, 5, 390, 1974. 12) 洪永淑 , 幸正來, 《 한국영양학회지 》 , 4, 4, 69, 1971. 13) Ami n- Zaki, L. Elhassani, S. Maje e d, M. A. Clarkson, T. W. Do- herty R. A. and Greewood, M. R. , J. Pe d ia tr . , 85 , 81, 1974. 14) World Health Orga niz a ti on , Techni ca l Rep or t Serie s Nr. , 532, Ge n f 1973. 15) Blacksto n e, S. R. J. Hurley and R. E. Hug h es, Food Cosm . Tax i- col., 12, 511, 1974. 16) Pott er, S. and G. Mazone, J. Nutr . , 104, 638, 1974. 17) Weste r , P. 0. , At h er o scler o sis , 20, 207, 1974. 18) Somers, E. , J. Food Sci. , 39, 215, 1974. 19) Takeuchi, T. in Ranti ng , B. and Dinm an, B. D. eds, Scie n ce- Pub!. Inc. , Ann Arbor. Mi ch ig a n, p. 247, 1972. 20) Howi e, R. A. and Smi th, H. , J. Forensic Sci. Soc. , 7, 90, 1967. 21) Lenih a n, J. M. and Smi th, H. , in Nuclear Acti va ti on Techni- qu es in the life s cie n ces. IAEA. Vi en na, 1967. 22) Kellershohn, C. , Comar, D. and Lop o ec, C. , J. Lab. Cl in. M ed . , 66, 168, 1965. ·2 3) Dennis , C. A. R. and Fehr. F. , Sc i. Tota l Envir on . , 3, 267 and 27 5 , 1960. 24) Kurland, L. T. , Faro, S. N. and Sie d ler, H. S. , World Neurol. r 1, 320, 1960.
20 알루미 늄 (Alum i num, Al)* 인체의 각 기관에서는 미량의 Al 이 발견되는데 사람의 전체 Al 함량은 50~150mg 이 며 연령 이 증가함에 따라서 Al 의 함량도 함 께 증가한다. 식물, 동물, 그리고 미생물의 필수적인 기능에 관계한다는 뚜렷 한 증거는 아직까지 없다. 실험쥐의 경우 Al 이 함유되어 있지 않은 식이로사육했을 때 ,(Al 섭취량은 한 마리당 lµ g /1 일) Al 이 첨가된 식이로 자란 쥐와 성장 면에서 차이접이 없었으며 번식률에도 차이가 없었다 .14) 지구상에는 7~8% 의 Al 이 존재하지만 동석불에는 미량이 존재 한다. Al 의 체내 각기관의 함량은극히 미량이기 때문에 함량의 분석에 있어 큰 차이를 나타낸다. 그 이유로는, 1) 옛날의 분석 방법이 확실하지 못했다는 접 2) 환경오영에서 오는 식품의 분석치가 다르고 분석시에 먼지와 공기에 촌재하는 Al 도 큰 몫을 하기 때문이다. 동식 물의 Al 함량은 0. 5~5. Op pm /fr es h weig h t 이 고 음료수의 Al 함량은 0. Olpp m ~5pp m 정 도이 다. 탄산음료는 lOOp pm 의 높은 Al 함량을 보인다 .15)16 )17) Al 과의 접촉된 부분의 함량이 월둥히 높다는 것이 감자의 껍질
* Nonessenti al trac e elements ( 20, 21, 22, 23 장). 여 기 에 속하는 tra ce elements 는 생리적으로 그다지 중요성이 없거나 아칙 규명되어 있지 않은 것을 둘고 있다.
에 서 2, OOOp pm , 무우의 껍 질에 서 300p pm 까지 , 그리 고 사과의 껍 질 에서 20 pp m 으로 지적되었다 .20) 사람의 기관에는 9)19) 평군 0.5p pm 보다 저게 함유되어 있으며 간 온 30p pm 으로 약간 높다. 뼈 에 는 2. 5~5pp m , 허 파에 는 60p pm 이상으로 가장 많은 양의 Al 을 함유하는데 이는 Al 을 먼지나 공 기로 흡입하기 때문인 것으로 보인다. Al 은 뇨로 하루 0.1m g이 배설된다. 사람과 동물은 섭취한 AI 의 97~100% 를 이용하지 못한 채 뇨와변으로 배설시킨다. Al 은 장에 서 용해되 지 않는 Al-ph osph ate 를 만들어 서 장에 서 홉 수가 거의 되지 않는다. In vit ro 실험에서 Al 이 동물의 세포막을 찰 통과하지 못한다는 것이 알려졌다. 이 와 같은 이 유에 서 Al 의 국소량만이 유즙으로 이 동된다. 우유의 Al 농도는 lpp m 이 하로 아주 낮다. 위 산을 중화하기 위 해 서 사용되 는 alumi nu m-ph osph ate - ge l 의 형 태로 1. 6 g의 Al 을 수유부에게 섭취시켰을 때 모유에서 0.02p pm 의 Al 이 0.05~0.15 pp m 까지 증가하는 것을 관찰할 수 있었으며 이와 비슷한 실험이 영소와 소에서도 재입증되었다 .23) Al 영은 그 흡수율이 너무 낮기 때문에 독성이 없다• 토끼 에 게 Al 을 경 구 섭 취 시 켰 을 때 치 사량(L D100) 은 Al-chlorid e 형 태 로 1~3g /k g 체 중, Al-aceta t e 로 5~15g / kg 체 중 그리 고 수분 이 없는 natr i u m alumi na te 형 태 로 2g / kg 체 중으로 보고되 었 다. 1)2) 118 일 동안 사람에 게 1 일 970mg Al 을 경 구로 복용시 켰을 때 홉 수율에 변화가 없었으며 혈액의 Al 농도도 증가되지 않았고 다른 이상한 중상도 나타나지 않고 정상을 유지했다 .1) 위 산울 중화하기 위해 서 위 궤 양에 복용하는 alumi nu mhy d roxy -ge l 과 alum i num phosp ha t e- g el 은 약 2g / I 일로 사람에게 장기간 복용 시킬 수 있었다. 그러나 만성적으로 복용할 때 체내의 Al 과 ph os• p ha t e 가 결합되어 ph osph ate 결핍중을 초래한다는 설도 있다 .20) 그러 나 My e rs 와 MuU3>24) 이 과량의 Al 을 KA14(S04) 의 형 태 로 4 세대에 걸쳐 동물에게 섭취시켰으나 아무런 독성 증상이 나타나지 않았다고 한다. 이 동물들은 성장, 번식, 건강 상태, 생촌율, 그리
고 세포조직의 검사에서도 정상인 동물들과 바교하여 아무런 이상 을 나타내지 않았다. 더욱더 주목할 사실은 이 동물들이 살아 있는 會 동안 Al- 영은 첨가해서 섭취시켰으나 각 기관의 Al 함량이나 전체 Al 함량이 증가하지 않았다. 이와 똑같은 실험이 개에게서도 재현되었는데 Al 을 529m g /I 일로 (hy d roxy 형 태 로서 ) 1 년에 서 15 개 월까지 섭 취 시 켰으나 아무런 변화가 없었다 .4)5) 생 체 내 에 존재 하는 Al 은(l o-6 ; 27p pm Al ) 세 포내 대 사에 아무런 영향도 끼치지 못했다 .6) 과거의 실험에서는 많은 연구가들이 Al 이 대사과정에 촉진과 처 해작용울 한다는 상반된 결과를 보고했다. 그러 나 최 근 B 죠 ssler 와 그의 동료들 18) 에 의하면 과거의 실험 결과는 실험 방법의 찰못으로 찰못 희석하여 측정한 결과로 단정되었다. 최 근 요독증의 투석 환자들에 게 장기 간 ph osp h ate 와 결합하는 Al- g el 로 치료시켰을 때 혈액의 Al 양과 뇌, 근육, 그리고 뼈의 Al 양 이 증가되었음이 관찰되었다 .7) 여 러 실험 결과에 의 하면 D8)9) Al 의 하루 섭 취 량을 5~10mg 로 측정되는데 이 양은 조리기구나 포장동 Al 과 접촉을 하지 않았을 ` 때의 값이다 .8) Kehoe9) 는 28 일 동안 성인이 섭취하는 Al 양을 측정했던 결과 평 군 35.4m g /1 일이었으며 Camp b ell 등 1) 은 15 주일 동안 조사한 결과 식품으로 섭취하는 Al 의 평군치는 1 일 17.3m g이었다. 여러 연구에서 10)11) Al 솥에 물이나 중성 식품을 끓일 때는 극히 소량의 Al 이 유출된다. 산성 식품은 알카리 식품에 비해서 Al 의 유출을 더 많이 일으키고 물은 우유보다 Al 을 더 많이 용해시킨다. 감자, 야채, 우유, 국수류, 고기 둥을 Al 솥에 꿇였을 때는 식품 에 약 5p pm 정도의 Al 이 증가한다. 일반적으로는 끓이는 식품에는 1 pp m 정도의 Al 이 증가하는 것으 로 보인다. 모든 음식물을 Al 솔에 끓였을 때는 사람의 하루의 Al 섭취량이 약 10mg 정도가 된다. Hadorn10> 온 음석 물의 조리 과정 중 Al 솥과 그릇, 기 구 둥의 사용 ·
에 따라서 사람의 하루 Al 섭취량이 0.1~8m g까지 차이가 생지며 Ho g l 은 11) 1~10m g으로 추산했다. 이 조사의 결과는 솥이나그릇, 기구 등의 Al 유출에 의한 Al 섭취량은 그다지 중요하지 않으며 석 품에 함유된 Al 양에 따라서 달라진다고 판정했다. 죽 솔, 취사도 구 둥에 의한 하루 Al 섭취량은 너무 차이가 십해서 식품에 함유된 Al 양에 따라서 섭취량이 결정지어진다고 한다. Fle i sch12) 는 우유, 야채 , 과일 등의 조리 시 ascorbic ac id 의 파괴 울이 다른 금속으로 만든 솥에 비해서 Al 솥 사용시 가장 작었다고 보고했다. Ascorbic ac id 의 파괴 율이 가장 작은 경 우는 Al 으로 된 압력 솥울 사용했을 때이다. 그러나고기를 끓이거나후라이를 하거나빵을 구 위 낼 때 비 타민 중 th ia m i n, rib o fl av in 그리 고 nia c in 의 손실온 Al 솥이 나 후라이 펜이 다른 금속으로 만든 솥이 나 후라이 팬과 비 교했 을 때와 거의 비슷했다고 한다. Al 통조립에 들어 있는 기름으로 처장한 생선은 오랫동안 처장하 여도 vit . A 와 D 의 손실이 없었다고 한다 .13) *참고문현 I) Camp h ell, I. R. , J. S. Cass, J. Cholak. and R. A. Kehoe, AMA Arch, Industr . Healt h, 15, 359, 1957. 2) Lewi s, S. J. , Bi oc lt em . J. 25, 2162, 1931 . 3) My e rs, V. C. and J. W. Mull, J. Bi ol . Chem. , 78, 605, 625, 1928. 4) Underhil l, F. P. and F. I. Pete r man, Amer. J. Phys i o l. , 90, 15,. 1929. 5) W ilhr er, J. , Bi oc hem. , Z. , 265, 169, 1933. 6) Avery, G. D. , E. F. Cavie s and R. F. Broden, Drug s , 4, 7, 1972 ► 7) Nutr i t on s Revie w s, 34, 166, 1976. 8) Kay se r, J. , J. Neumann and J. Lavollay, C. R. Acad. Sci. , 262. 2063, 1966.
'9) Kehoe, R. A. J. Cholak and R. V. Sto r y, ]. Nutr . , 19, 579, 194 0 . 10) Hadorn, H. , Mi ttlg. LelJe nsmi ttelu nte r s. , 38, 314, 1947. 11) Hog !, 0. , Chi m i a 5, 239, 1951. 12) Fleis c h, H. , Chim i a, 5, 238, 1951, Z. Vi tam i n fo r sch. 12, 86, 1.9 4 2. 13) Lunde, G. , Vi tam i n e in Jri s c hen und Konservie r t e n Nahrung s · mi tteln , 2, Aufl , Berlin , 1939. 14) Hove, E, Elvehje m , C. A. and Hart, E. B. , Am. J. Phy si o l . , '12 3, 640, 1938, 15) Hop k in s , H. and Eis e n, J. , J. Ag r ic . Food Chem. , 7, 633, 1959. 16) Zook, E. G. and Lehmann, J. , J. Am. Di et . , Assoc. , 25, 225, 1968. 17) Schroeder, H. A. and Mi tch ener, M. , J. Nutr . , 105, 42 1, and -42 5, 1975. 18) Bassler, K. H. and V. Unbehauen, Arzneim i ttelf o r sch. , 12, 124 , 1962. 19) Ti pton , I. H. and Cook, M. J. , He al t hp hy s. , 9, 103, 1963. 20) Lang . K. , Bi o chemi e de r Ernahrung , 4, Aufl ag e , Dr. D. Ste i n - kop ff Verlag, Darmsta d t, p. 3~70, 1979. 21) Kir c hsessner, M. , Merz, G. and Oelschlag er , W . , Arch, Ti e rer- -ni i hr . , 10, 414, 1960. 22) Archib a ld, J. G . , J. Dair y Sci. , 38, 19, 1955. 23) Aria e y -N eja d , M. R. and W. N. Pearson, J. Nutr . , 95, 206, 1968. 24) My e rs V. C. and J. W. Mull, J. Bi o l, Che m . , 78, 605, 625, 1928.
21 리 티 움 (Lit hiu m , Li) Li 은 필수 tra ce element 는 아니 며 그의 화학적 성 질은 Na 과 비슷하다. 하루에 식품으로 섭취하는 L i은 1~2.5mg 정도이다. 체내의 L i의 함량과 분포는 Na 과 비슷하다》 사람의 임파선에는 0.2 士 o.07µ g/g, 허파에는 0.06 土 O.Olµ g/g,. 간에는 0. 007 土 0. 003µg /g, 근육에는 0. 005 土 o. 002µg /g, 뇌에는 0. 004 土 0.OOlµ g/g, 고환에는 0.003 土 O.OOlµ g/g 그리고 난소에는 0. 002 土 0. 004µg /g Li 함량을 축정 하였으며 혈액 에 는 0. 006 士 0. 002µg /g L i이 함유되어 있다 .6) Bowen8) 은 사람의 L i의 1 일 섭취량은 2m g으로 보고했는데 Ha- mi lton 훈은 영국사람들의 식사에서 1 일 107 士 53µ g으로측정했다. 사람은 매일 장으로 약 20µg 정도가 흡수된다고 한다. L i은 장으 로 흡수된 만큼 뇨로 배설된다. Li의 섭취는 혈장의 M g과 Ca 의 양을 중가시킨다는 보고도 있다 .7) 간에 는 약 4pp m 의 Li 울 함유하고 있다. Li은 정신질환의 치료에 사용이 되고 있다 (3m g 이상 L i이온 /k g체 중 /1 일) . 1) 2)” 이 Li 치 료시 혈액 의 Li 치 가 0. 6mEq /l 이 상일 경 우 어 지럼증, 근육 경련, 식욕 부전, 설사, 그리고 구토 등의 독성 증세 가 나타났다. 10)11) 12 ) 도한 사람의 동맥경화증 치료에도 유효하다는 보고도 있는데 Li.
이 혈청 choleste r ol 과 tri g ly c erid e 의 농도를 감소시 킨다고 한 다. 3)4)13) 과거에는 NaCl 대신에 Li울 사용할 수 있다고 생각했으나 독성 때문에 사용하지 않고 있다. *참고문현 1) Cade, J. F. J. , Med. ]. Aust. , 1, 684, 1975. 2) Gershon, S. , Annu. Rev. Med. , 23, 439, 1972. 3) Correa, P. and Str o ng , J. P. , Ann. N. Y. Acad. Sci. , 199. , 217, 1972. 4) Voors, A. W. , Lancet 2, 1337, 1969, Am. ]. Ep ide mi o l. , 93, 259, 1971. 5) Robin s on, W. 0. , Ste i n k oenig , L. A. and Mi ller , C. F. , U. S. Dep . .Agr ic . Bull. , No. 600, Washin g ton , D. C. , 1971. 6) Hami lton , E. I. , Mi ns ki, _M . J. and Cleany , J. J. , Sci. Tota l En- .vir on . , I, 341, 1972/1973. 7) Lang .. K, Bi oc hemt 'e der Ernti hr ung 4, Autl a g e , Dr. D. St ei n - -ko p ff Verlag, Darmsta d t, p. 370, 1979. 8) Bowen, H. J. M. , Trace Element in Bi o chemi st r y , Academi c .Pr ess, New York, 1966. 9) Schou, M. , Pharmacol. Rev. , 9, 17, 1957. 10) Py b us, G. and Bowers, G. N. , Jr. , Clin . Chem. , 16, 139, 1970. 11) Amdis e n, A. and Scand, J. , Clin . Lao. Invest. , 20, 104, 1967. 12) Coats , D. A. , Trautn e r, E. M. , and Gershon, S. , Austr a las. Ann. Med. , 6, 11, 1957. 13) Fleis c hman, A. I. , Lenz, P. H. and Bie r enbaurm, M. L. , J. Nutr . , 104, 1242, 1974.
22 스트론튬 (Str o nti um , Sr) Sr 은 ina cti ve 한 Sr 과 sta b le 한 Sr 으로 분리 되 어 있 다. Inacti ve 한 Sr 은 Ca 과 함께 지구상에 소량 촌재하며 생체 내에도존재한다. Inac ti ve 한 Sr 은 천연의 것으로 동위원소 SlSr, 84Sr, sssr, 87Sr 둥이 여 기 에 속하며 sta b le 한 Sr 은 방사선 동위원소 90Sr 둥이 촌 재한다. 사람의 각 기 관의 Sr 함유량은 표 22.1 과 같다. 7)1 3 )
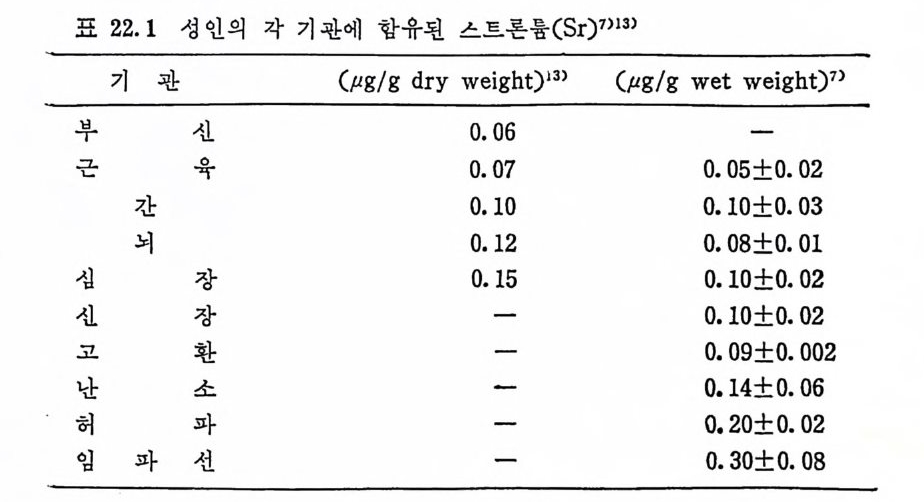 표 22.1 성 인의 각 기 관에 함유된 스트론움 (Sr)1)13)
표 22.1 성 인의 각 기 관에 함유된 스트론움 (Sr)1)13)
Sr 은 대사 활동면에서 Ca 과 비슷하며 인체의 Sr 의 총합유량은
뼈에 함유된 Sr 은 뼈의 회분 l g에 80~330µg 정도 함유되어 있 다 .7)8) 뼈의 Sr 함량은 사람의 나이와 주거지역과 밀접한 관계가 · 있는데 동양의 성인은 190p pm , 어린이는 320 pp m 이며 미국의 성 인은 llOp pm , 어 란이 는 96p pm 이 다. 6) 그 원인은 동양인의 저 Ca 섭취에서 기인하는지 또는 Sr 섭취를 많이 한 때문인지는 아직 규명 되어 있지 않다. 그러나 이스라엘의 태아들이 뼈와 치아의 Sr 함량 이 다른 것은 음료수에 함유된 Sr 에 영향을 받는다고 보고하였 다. 9) 10 ) 미 국인의 치 아 enamel 층의 Sr 함량은 평 군 121 土 llµg /g dry weig h t 이 다. 11) 치아는 지역에 따라 Sr 이 많은 경우 50~350 pp m 까지 차이를 보 이며 이 원소는 치아의 각 부위에 골고루 분포되어 있으며 식수에 함유된 F 는 치아와 뼈의 Sr 함유량에 아무런 영향을 미치지 못한 다. 12) 식 수는 지 역 마다 다르지 만 0. 02~0. 06mg // 로 보고되 고 있 다 .6) 식품의 Sr 함유량은 지역에 따라서 큰 차이가 있다. 석품에 존재 , 하는 천연 Sr 은 표 22.2 에 있다 .5)
 표 22.2 석 품에 함유된 스트론듐 (Sr) 의 양
표 22.2 석 품에 함유된 스트론듐 (Sr) 의 양
우유에 는 140~420µg /g Ca 으로 함유되 어 있 다. 8) 1 일 성 인이 섭 취 하는 Sr 은 1. 5~3. 0mg 이 며 14)15) 대 변으로는 1 일 0. 81~1. 58mg , 소변으로는 0. 24~0. 42mg 정 도 배 설한다. l4)l6)
성인이 되면서 섭취량과 체내의 함유량은 평형을 이루며 뼈에 함 유된 Sr 양은 조철된다. Bedfo r d 둥 16) 은 어 린 이 의 나이 에 따라서 1 일 0. 67~3. 57m·g 의 Sr 을 섭취하고 거의가 대변으로 배선된다고 한다. 또한 인도사람 둘 1 7 ) 은 1 일 3.1~4.7m g의 Sr 을 섭취한다고 하며 영국의 석이에서 는 1 일 0.858 士 0.144m g Sr 그리고 미국의 병원 석이에서는 1 일 각각 1. 2~2. 9m g 1) 과 2. 1~2. 4m g 6) 으로 보고되 고 있 다. Sr 의 대사에 있어서 천연으로 촌재하는. Sr 이 최근에 관십거리가 되었는데 그 이유는 체내의 동위원소는 방사선 동위원소인 90Sr 과 구벨되지 않으며 전부 90Sr 으로 기능을 수행했기 때문이다. 생체 내에서는 Ca 과 Sr 이 서로 비슷한 기능을 갖고 있는데 경쟁 작용으로 인하여 Ca 이 우선적으로 선덱되므로 체내에 Sr 이 Ca 보 다 소량 함유된다. 희석 윤=〔 Sr/Ca] 체내 (독히 뼈 )/[Sr/Ca] 식 이 위 와 같은 공식 을 통하여 sta b le 한 Sr 과 radio acti ve 한 Sr 은 0.20~0.25 정도의 희석울을 나타냈다 .8) 그림 22.1 은 Sr 함량이 나이 에 따라서 다름을 나타낸 표이 다. 2)
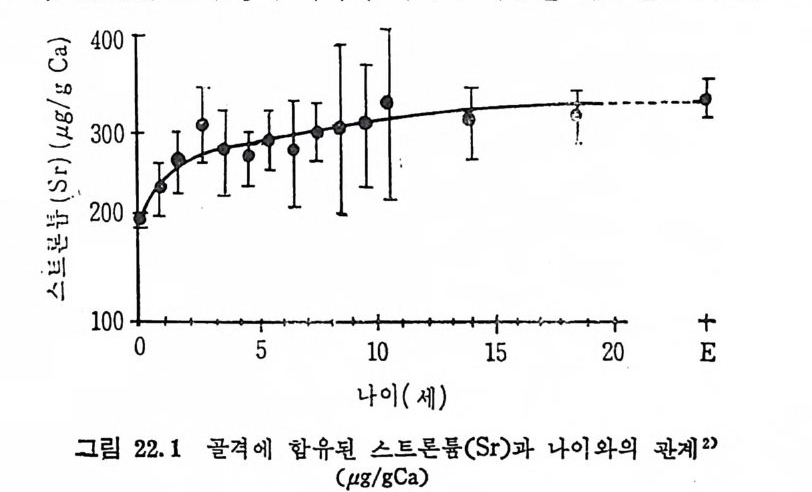 400300
400300
생후 6 개월까지는 우유만으로 영양을 섭취하기 때문에 Sr 농도가 일정하며 그 이후 갑자기 상승하는데 이는 식물성 식품에서 기인한
것이다 .2) 방사선 동위원소 90Sr 의 오영에 대비하기 위하여 Sr 을 섭취시켜 체내의 Sr 을 회석하게 하고 또 다론 방법으로는 많은 양의 Sr 을 섭취시킴으로써 뼈에 s t able 한 Sr 을 흡수토록 하여 방사선 동위원 소 9DSr 이 흡수되지 못하도록 방해하는 방법을 연구하고 있다. 그러나 위와같은 방법에는 실제 사용상에 있어서 문제접이 있다. 과량의 Sr 을 섭취시키면 그의 독성 현상으로 머의 석회화를 방 · 해하여 S t ron ti um- 구루병에 걸리게 된다는 것이 동물실험을 동하 여 여러 연구자들에 의해서 입증되었다 .3 )1 8)19)20) 이 S t ron ti um- 구루병 은 Ca 의 흡수를 처 해 하는 vit am i n D 의 활 성 형 태 인 1. 25-dih y d roxy c alcif ero l 의 작용으로 장접 막의 단백 질과 Ca 의 결합이 찰되지 않기 때문에 생기게 된다. 이때에 Sr 의 섭취를 중단시켰으나 Ca 의 흡수는 일부만 정상 상 · 태를 되찾았다 .3) Sr 은 뼈의 석회화에 관여하는 Ca, P, vit am i n D 의 섭취를 처 해하는 작용이 있다. 이 처해 현상은 뼈가 Ca, P, vit am i n D 대신 에 Sr 으로 완전히 대치되었을 때 발생된다. Lang m uir - ga s -absorpt ion sis o th erme 에 서 볼 수 있 듯이 Sr 은 아 주 선속히 흡수된다. 뼈 의 Sr 의 포화 현상은 Sr 이 125p pm 에 도 달했을 때였다. 이 신속한 흡수는 주로 뼈의 의부 흡수이며 접차적 으로 Ca+ +과 Sr 이온의 교차가 진행된다. 이 Ca+ +온 전체 뼈의 Ca++ 의 6% 를 차지한다 .4) 정상섭취량의 10 배 정도가 되는 40p pm 정도의 Sr 섭취는 쥐의 성장울 방해했다 .2 1) 포화농도는 연령과 밀접한 관계를 갖는데 쥐둥 미성숙 동물은 성숙취에 비해서 5 배 정도 농도가 높게 나타난다. Sr 의 저장속도 논 Sr 의 농도에 영향을 받는다. 쥐의 포화농도는 1.5 • 10-2Sr : ICa 일 때다. 식이의 Sr : Ca 의 비 울이 1 : 1 일 때 뼈는 12~14 일만에 포화되었으며 비율이 1 : 2 일 때 는 3~4 주일만에 포화현상을 나타냈다. 8) Sr 의 처장 속도는 대단히 빠르지만 그 분해 속도는 그에 비해서 ; 느리다.
지금까지 Sr 의 생리적이며 세포학적인 연구가 진행되고 있으나· 완전치 못하므로 그의 전반적인 대사작용에 대해서는 더 많은 연구 가 계속되어야 할 것이다. *참고문현 1) Gormi ca n, A. , ]. Am. Di et . Assoc. , 58, 397, 1970. 2) Brya n t, F. J. and J. F. Louti t, Proc. Roy . Soc. Ser. B. , 159, 449,. 1964. 3) Corradin o , R. A. , J. G. Ebel, P. H. Craig , A. N. Tayl o r and R. Wassermann, Calc. Ti ss . Res. , 7, 81, 93, 1971. 4) McDonald, N. S. , F. Ezmi rl ia n , P. Sp ai n and C. McArth ur, J. Bio l . Chem. , 189, 387, 1951. 5) Brya nt F. J. , A. C. Chamberlain , G. S. Sp ice r and M. S. Webb, Brit. Med. J. , 137, 1958. 6) Schroeder, H. A. , Tip ton , I. H. and Nason, A. P. , ]. Chronic - Di s. , 25, 491, 1972. 7) Hami lton , E. I. , Mi ns ki, M. J. and Cleary. J. J. , Sci. Tota l Envir o n. , 1, 341, 1972/1973. 8) Lang . K. , Bi oc hemi e der Erna'hrung , Dr. D. Ste i n k off Ver-larg, Darmsta d t, p. 358, 1979. 9) Gedalia , I. , Yariv , S. , Nay o t. H. and Eid e lman. , E. , in Hoeks- tra , W. G. et al. eds. Trace Element Meta b oli sm Ani m als-2, , p. 461, univ . pa rk, Press. Balt m ore, Maryl a nd, 1974. 10) Wolf , N. , Gedali a, I. , Yariv , S. and Zuckerman, H. , Arch, Oral Bi ol . , 18, 233, 1973. 11) Losee, F. , Cutr e ss, T. W. and Brown, R. , Trace Subst. Envir on . Healt h. 7, Proc. Uni v. Mo. Annu. Conf. , 7th 1973. p. 19, 1974. 12) Ste a dman, L. T. , Brudevold, F. and Smi th, F. A. , J. Am. Dent. Assoc. , 57, 340, 1958. 13) Tip ton , I. H. and Cook, M. J. , Healt h Phy s. , 9, 103, 1963.
14) Harris o n, G. E. , Ray m ond, W. H. A. and Treth eway , H. C. , Cl in• :Sc i. , 14, 681, 1955. 15) Tip ton , I. H. , Ste w art, P. L. and Marti n, P. G. , Healt h Phy s. , 12, 1683. 1966. 16) Bedfo r d, J. , Harris o n, G. E. , Ray m ond, W. H. A. and Sutt on , .A. , Br. Med. ]. , 1, 589, 1960. 17) Soman, S. D. , Panday , V. K. , Jos ep h , K. T. and Raut, S. J. , Healt h Phys . , 17, 35, 1969. 18) Weber, C. W. , Doberenz, A. R. and Reid , B. L. , Poutr y Sc i. , 47, 1731, 1968. 19) Weber, C. W. , Doberenz, A. R. , Wy c koff , R. W. G. and Reid , .B. L. , Poutr y Sc i. , 47, 1318, 1968. 20) Bartl e y , J. C. and Reber, E. F. , ]. Nutr . , 75, 21, 1961.
23 붕소 (Boron, B) B 는 사람과 동물에 분포되어 있는데 지금까지의 견해로는 B 가 생물체에 필수영양소가 아니라고 알려져 있었다. Hove 둥 1) 이 조사한 B 의 광범위한 연구에서 만약 B 를 필수 영 양소라고 단정한다면 그 양이 아주 적다고 하였다. 쥐의 경우 하루 0.8µ g이 팔요하다고 한다. 표 23.1 은 인체 각 기관의 B 함유량인데 입증이 될 만한 B 의 필 수성과 결핍증에 대해서는 완전히 규명이 되어 있지 않는 상태어}
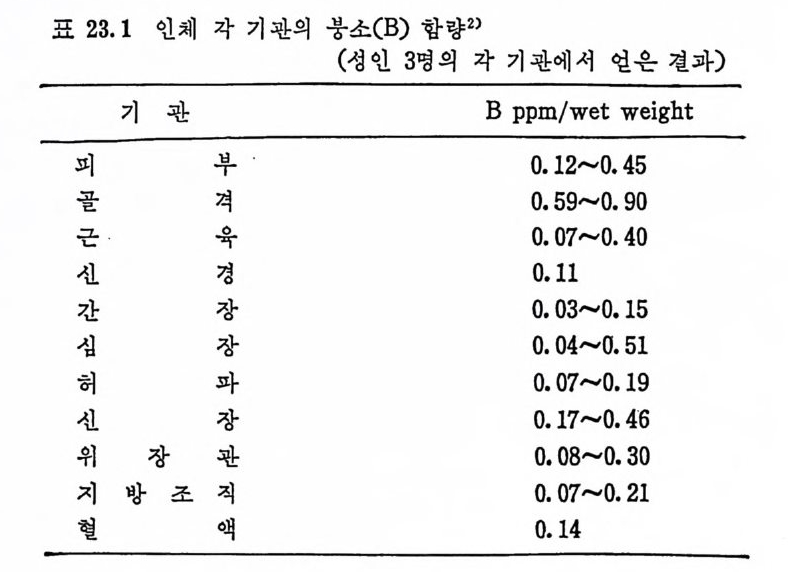 표 23.1 인체 각 기 관의 붕소 CB) 함량 2)
표 23.1 인체 각 기 관의 붕소 CB) 함량 2)
있다 .2) B 는 신체 각 기관에 골고루 분포되어 있으며 뼈에 약간 높은 함 량이 함유되어 있다. Alexander 와 그의 동료들”은 사람뼈 의 회 분에 서 16~138p pm 의 B 가 함유된 것을 발견했다. B 는 빠른속도로 완전히 흡수되어 세포외액과 세포내액에 골고루 분포되어 있으며 섭취된 B 는 거의 전부가 뇨로 배설된다 .7)8)9) 과일에 는 B 가 5~30pp m /fr es h weig h t, 채 소에 는 0. 5~2pp m /fr es h -we ig h t, 곡류에 는 0. 5~3pp m /fr es h weig h t, 달갈에 는 O. lpp m / fres h weig h t, 그리 고 우유에 는 0. 1~O. 2pp m /fr es h weig h t 가 함 유되어 있다 .6) Plo q u i n4) 은 사람의 B 섭 취 량이 매 일 5~15mg 으로 평 군 7mg 정 도 라고 한다. 여기에다 술로 B 가 첨가 섭취될 수 있다. 술에 함유된 B 는 IOmg / l 정도이며 종류에 따라서 큰 차이가 있다. B 의 급성 독성 증상은 거의 없으나, 쥐에 있어서 LD s o 은 0.73g /k g을 구강으로 섭취했을 때이다 . 4 ) B 의 만성 독성은 장기간 71m g /k g을 섭취시켰을 때 쥐에게는 쇠 약중 현상이 나타났으며 쥐 의 B 함량도 정 상보다 15 배 로 중가되 었 다 .4) B 는 특히 지방조칙과 중추신경계에 축적되며 2 년 동안 계속 borax 의 형태로 복용시킨 쥐와 개에게서 350p pm 까지도 독성이 나타나지 않았다 .5) 식 이 내 의 1170p pm 의 B 량은 동물에 서 atr o p ie 증상과 불임 중을 나타냈다 .10) 따라서 과거에는 boric a ci d 를 보조 효소로 사용했지 만 최근에는 그의 독성 때문에 보조 효소로서의 사용을 금지했 다. 사고 또는 화상의 붕산치료 기간 중 많은 양의 섭취를 하게 되면 과량의 B 가 일시적으로 축적됨으로써 특히 뇌조직에서 십한 독성 현상을나타넬 수있다. 소량의 B 가 함유된 식이 약 5p pm 정도로 생육한 쥐의 성장은 정상적이었다 .11)
*참고문현 I) Hove, E. L. , C. A. Elvehje m and E. B. Hart, Amer. ]. Phys i o l. , 127, 689, 1939. 2) Forbes, R. M. , A. R. Coop er and H. H. Mi tch ell, J. Bi ol . Chem. , 209, 857, 1954 . Forbes, R. N. , H. H. Mi tch ell and A. R. Coop er , J. Bi ol . Chem. , 22 3, 969, 1956. 3) Alexander, G. V. , R. E. Nusbaum and N. S. McDonald, J. Bi ol . -Ch em. , 192, 489, 1951 . 4) Plog u in , J. Ann. , Nutr . , 2, 149, 1967. 5) Weir , R. J. and R. S. Fis h er, Toxic o l. Ap pl. Pharmacol. , 23, 351, 1972. 6) Beeson, K. C. , U. S. Dep. Ag r ic . Mi sc . Pub/. , 369, 1941. 7) Kent N. L. and McCance, R. A. , Bi oc lt em . J. , 35, 837 and 877, 1941 . 8) Dwen, E. C. , ]. Dair y Res. , 243, 1944. 9) Ti pton . I. H. , Ste w art, P. L. and Marti n, P. G. , Healt h Phy s. , 12, ·16 83, 1966. 10) Lang , K. Owen, E. C. , J. Dair y Res. , 13, 243, 1944. 11) Schroeder, H. A. and Mi tch ener, M. , J. Nutr . , 105, 421, and 452, 1975. 12) Ste u dman, L. T. , Brudevold, F. and Smi th, F. A. , J. Am. Di et . .As soc. , 57, 340, 1958. 13) Tip ton , I. H. and Cook, M. J. , Healt h Phy s. , 9, 103, 1963. 14) Harriso n, G. E. , Howells, G. R. , Pollard, J. , Kasti al, K. and Manit as evic , R. , Br. J. Nutr . , 20, 561, 1966. 15) Tip ton , I. H. , Ste w art, P. L. and Marti n, P. G. , Healt h Phy s. R. , 1683, 1966. 16) Bedfo r d. J. , Harriso n, G. E. , Ray m ond, W. A. and Sutt on . A. , .Br . Med. ]. , 1, 589, 1960. 17) Soman, S. D. , Panday, V. K. , Jos ep b , K. T. and Raut, S. J. ,
He al t h Phy s. , 17, 35, 1969. 18) Weber, C. W. , Doberenz, A. R. , Wy c koff , R. W. G. and Reid r B. L. , Poult ry Sci. , 47, 1318, 1968. 19) Barnes, D. W. H. , Bis h op, M. , Harris o n, G. E. and Sutt on , A .... Int. ]. Radia t . Bi ol . , 3, 637, 1961 . 20) Forbes, R. M. and Mi tch ell, H. H. , AMA Arch. Ind. Healt h~ 16, 489, 1957. 21) Forbes, G. B. and Rein a , J. C. , ]. N11t r. , 102, 64 7 , 1972.
24 특수환경 에 서 의 tra ce elements 24. l 포유동물의 임 신과 수유시 의 필수 tra ce elements 임 신과 수유기 동안에 는 모든 대 사가 항전되 고 따라서 tra ce ele- ments 의 필요성 도 강조되 게 된다. 표 24.1 에서 보듯이 방사선 동위원소를 사용한 실험에서 쥐는 임 신기 간 동안 tra ce elements 를 골격 에 축적 했다가 수유기 간 동안에 접차사용하게 된다.
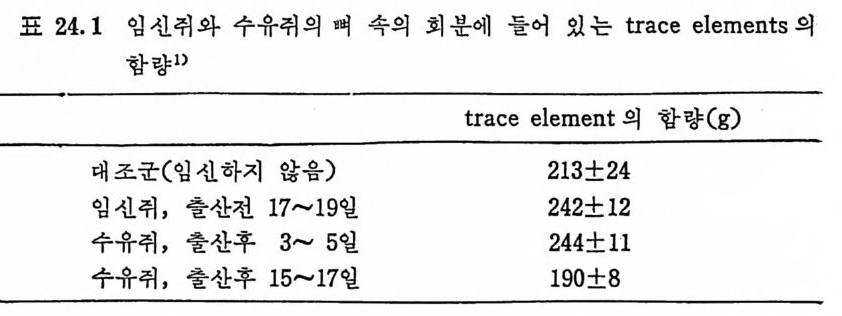 표 24.1 임 신취 와 수유쥐 의 뼈 속의 회 분에 둘어 있 는 trac e elements 의
표 24.1 임 신취 와 수유쥐 의 뼈 속의 회 분에 둘어 있 는 trac e elements 의
축적된 tra ce elemen ts 는 어란 새끼들을 위해서 쓰여지는데 생리 적 기 능이 찰 알려 쳐 있지 않은 Sr 도 이 경 우에 아주 적 은 양이 배 설되 는 것 을 관찰할 수 있 었 다. 2)3)4 ) 5)6) 표 24. 2 는 정 상쥐 의 주요 기 관의 tra ce elements 의 분포도이 다.
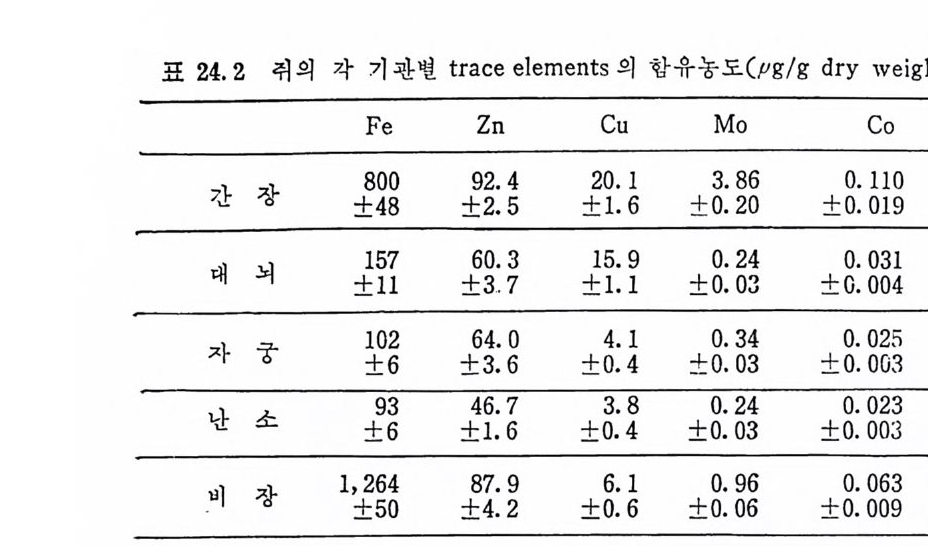 표 24. 2 취 의 각 기 관펄 tra ce elements 의 함유농도@g/g dry weig h t )”
표 24. 2 취 의 각 기 관펄 tra ce elements 의 함유농도@g/g dry weig h t )”
이 기 관 중에 서 도 특히 간에 tra ce elements 가 가장 많이 함유되 어 있다.7)
 표 24. 3 성 숙한 취 , 태 아기 쥐 , 새 끼 취 의 간에 함유된 tra ce elements 의
표 24. 3 성 숙한 취 , 태 아기 쥐 , 새 끼 취 의 간에 함유된 tra ce elements 의
표 24.3 은 성숙한 쥐, 태아기의 쥐, 그리고 새끼쥐에 들어 있는 tra ce elemen t s 의 함유량이다. 새끼쥐의 Cu, Fe, Zn 의 농도가 증 가되었다는 것은 여러 연구에 의해서 입증되었다 .9 )1 0)11 )1 2)13)14)15) Co 의 농도가 성숙한 쥐에 비해서 태아기에 약간 감소하는 것을 볼 수 있었으며 5 일된 새끼취는 다시 Co 의 양이 성인쥐와 비슷한 수 준이 되었다. Mo 의 농도는 태아기의 쥐와 새끼쥐가 성숙한 쥐에 비해서 낮았다 .8)
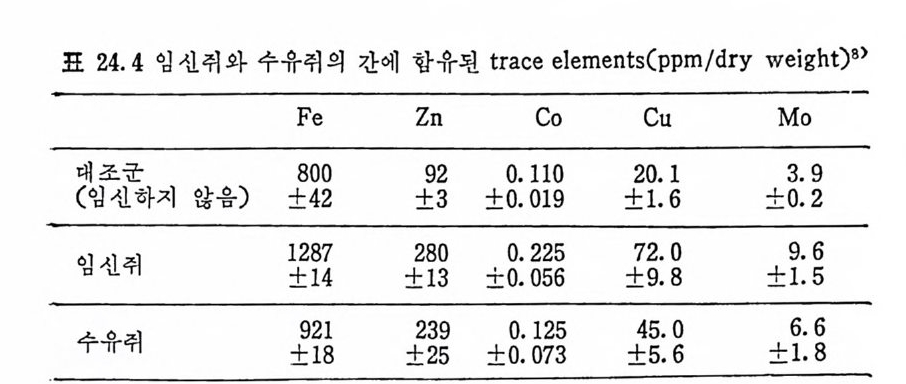 표 24. 4 임 신쥐 와 수유쥐 의 간에 함유된 tra ce elements ( pp m /dry weig h t) 8 >
표 24. 4 임 신쥐 와 수유쥐 의 간에 함유된 tra ce elements ( pp m /dry weig h t) 8 >
표 24.4 는 비임신쥐, 임신쥐 그리고 수유쥐의 간에 함유된 tra ce ,el ements 이 다. 8) 비임신쥐에 비해서 임신쥐의 Fe, Zn, Co, Cu, 그리고 Mo의 농 도가 상승했고 수유쥐의 Fe, Co, Mo, 농도는 비임신쥐와 다시 같 아졌다. 그러나 Zn, Cu 농도는 임신 때보다 더 적어졌다.
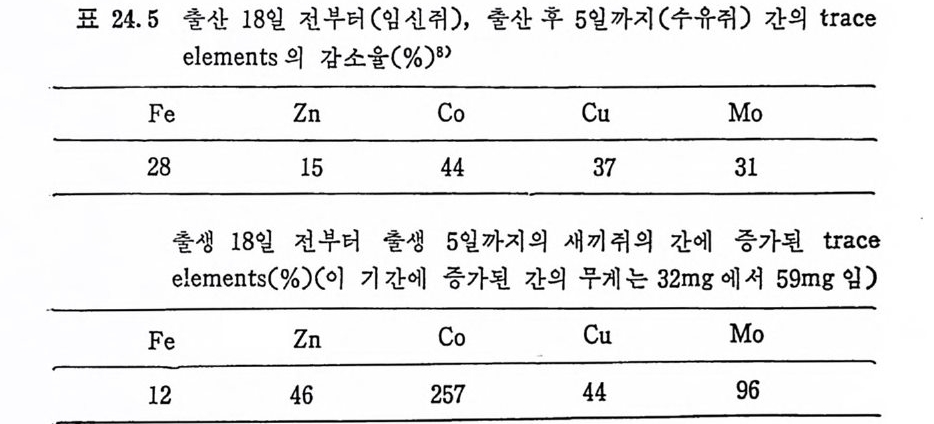 표 24. 5 출산 18 일 전부터 (임 신쥐), 출산 후 5 일까지 (수유취) 간의 tra ce
표 24. 5 출산 18 일 전부터 (임 신쥐), 출산 후 5 일까지 (수유취) 간의 tra ce
표 24. 5 는 간의 tra ce elements 가 임 신 기 간에 서 수유 기 간까지 감소된 것을 %로 나타냈다 .8) 이 기간 중에 가장 많이 감소된것은 Co 로서 44% 나 감소된 것으로 나타났다. 반면에 새끼 쥐에게서는 간의 무게가 32m g에서 59m g으로 증가되었을 때 Co 가 257% 로서 천처히 증가된 것으로 나타났다.
24.2 임신과 수유시 인체의 tra ce elements 이 기 간 동안에 현저 한 변화 를 갖는 tra ce elements 에 는 Cu, Zn 과 Cr 둥을 들 수 있 다. 16)17) 또한 성 호르몬의 영 향을 받는 tra ce elemen t s 에는 Se 이 관여됨을 알 수 있다 .18) 피임 약을 복용하는 여 자들의 머리카락을 Se 대사의 지침물로 사용하였는데 19) 3 개월간 복 용시 Se 의 농도가 11.8 pp m 에서 10.! pp m 으로 감소 했 다. 또한 쥐 에 게 성 호르몬과 Se 대 사를 보기 위해 서 estr o g e n 과 pro g e ste r one 을 섭취시킨 후 혈청의 Se 농도를 측정했다. 그림 24.I 은 임신쥐의 혈청 Se 의농도이다 .18)
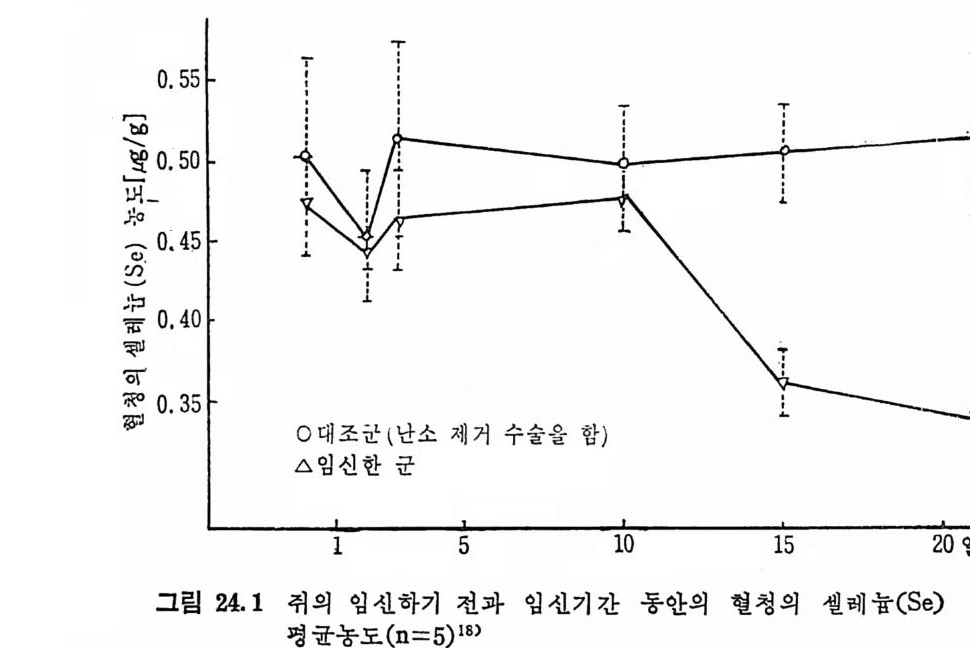 0.55 ';:T''' ..... .
0.55 ';:T''' ..... .
22 일 동안 호르몬을 두여 받은 쥐 는 정 상군보다 낮은 Se 농도를 보 였다. 임신쥐에서는 호르몬을 두여받은 암쥐보다 Se 의 농도가 현 처히 낮았다. 필수 trac e elements 의 농도는 태 아와 태 반과의 사이 에 차이 가 있
는 데 비해서 미필수 tra ce elemen t s 의 농도에는 차이가 없었다. Fe 과 Zn 은 능동적 수송을 하는 데 비해서 Co, Se 은 수동적 수송운 한다. 농도가 다르다는 것은 tra ce elemen t s 마다 다르게 태반으로 수송이 된다는 것을 의미한다 .20) 24 . 3 인 체 의 대 반과 tra ce elements 와의 관계 Th i eme21) 는 인체 의 태 반을 지 역 적 으로 자동차와 공장이 많은 lvii inc hen, 공기 가맑고 산이 많은 Al tot ti ng , 광산이 많은 Bay e ris c hen Wald (Furth in Wald) 등으로 구분해 서 채 취 했 다. Bay e ris c hen Wald 의 물에는 Pb 이 7µg /l 가 함유되어전 데 비해서 다른 두 지역은
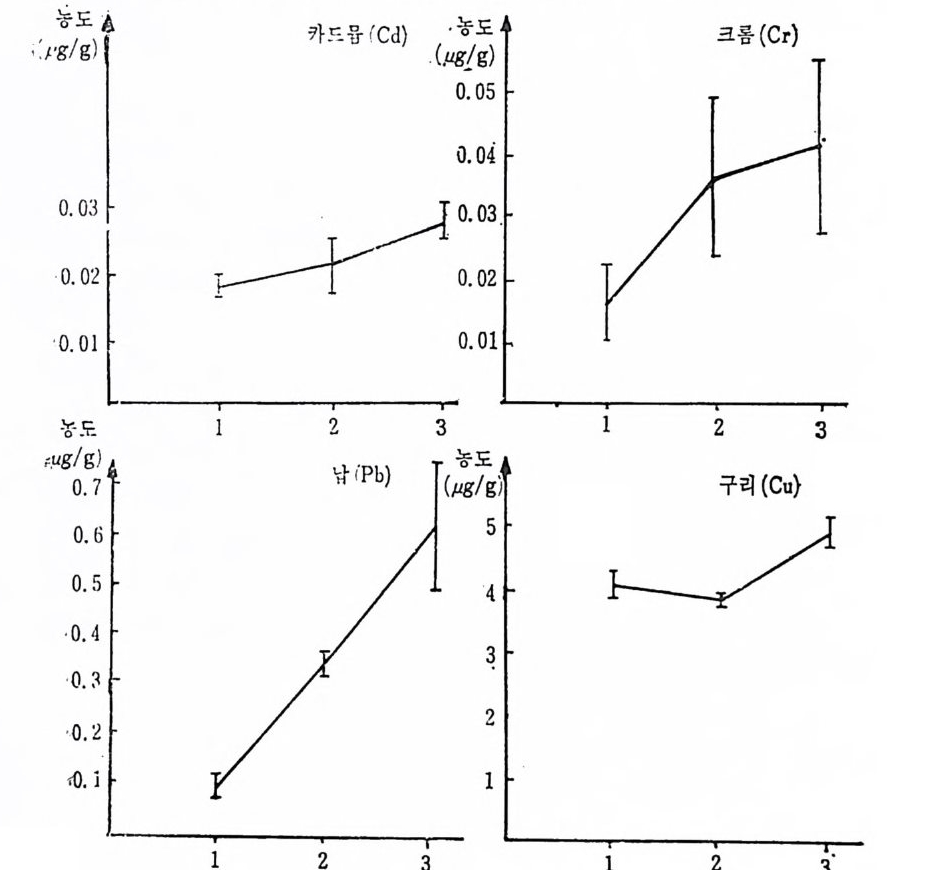 `:r 농g/ 도g ) A 카드뮴 ! C d) (.u농 g도jg) 크 롬 (Cr)
`:r 농g/ 도g ) A 카드뮴 ! C d) (.u농 g도jg) 크 롬 (Cr)
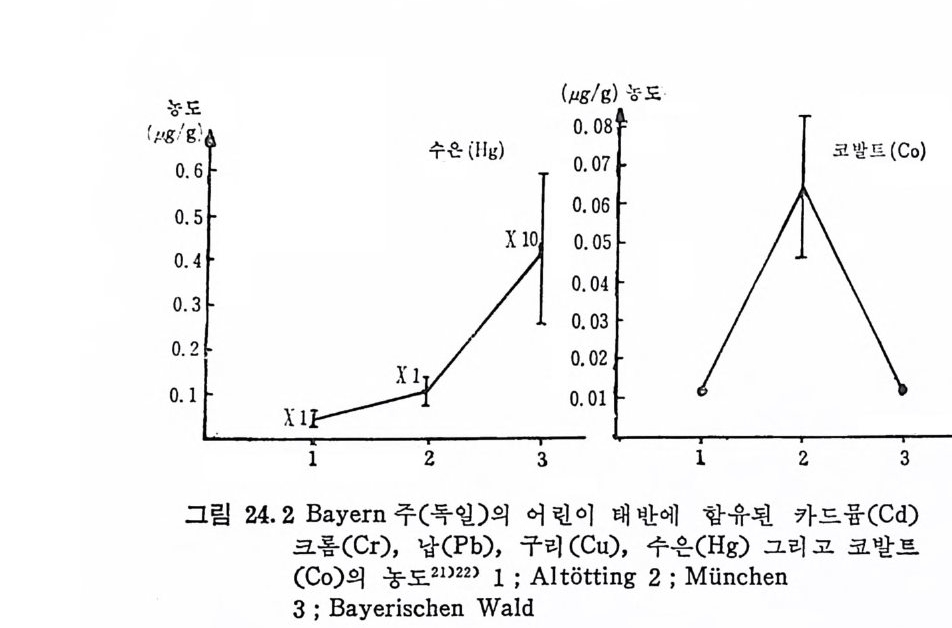 r;g 농 ;'도|• • ` (µ0g.0/ g8 ) 농 도
r;g 농 ;'도|• • ` (µ0g.0/ g8 ) 농 도
lµ g /l 의 Pb 이 함유되었다. 그림 24. 2 는 독일 3 개 도시 의 어 린이 태 반에 함유된 tra ce elements , 이 다. mm Cd, Cr, Pb 함량은 Alto tting , Munchen, Bay e ris c hen Wald 순위 로 높았고, Cu 는 Munchen 이 가장 낮았으며 Co 는 Mu-nchen 이 가장 높았다. Mi inc hen 어린이들의 태반에서 Co 가 높은 것은 대기오염에서 기 인되는 것으로 생각되며 Bay e r • Wald 에서 H g농도가 상승하는 것 온 그곳의 무기질에 의한 것으로 생각된다 .. 지금까지 태반의 tra ce elemen t s 에 대해서는 많이 연구되어 있지 않으나 Po p escu2” 는 Pb( II )가 사람의 태 반에 침 두될 수 있 다고 보 고하였다 .24> Pb 은모유 를 통해서 유아도 섭취할 수 있다고 한다 .25) 위의 실험 결과에서도 볼 수 있듯이 타)반의 tra ce elemen ts 함량은 환경 및 지역과 밀접한 관계가 있다고 본다 . 24. 4 신생 아의 tra ce elements Chr. Pan t el i ad i s26) 는 신생 아의 총혈액 , 혈청 , 적 혈구 그리 고 뇨
의 tra ce elements 를 표 24. 6 과 같이 측정 했 다.
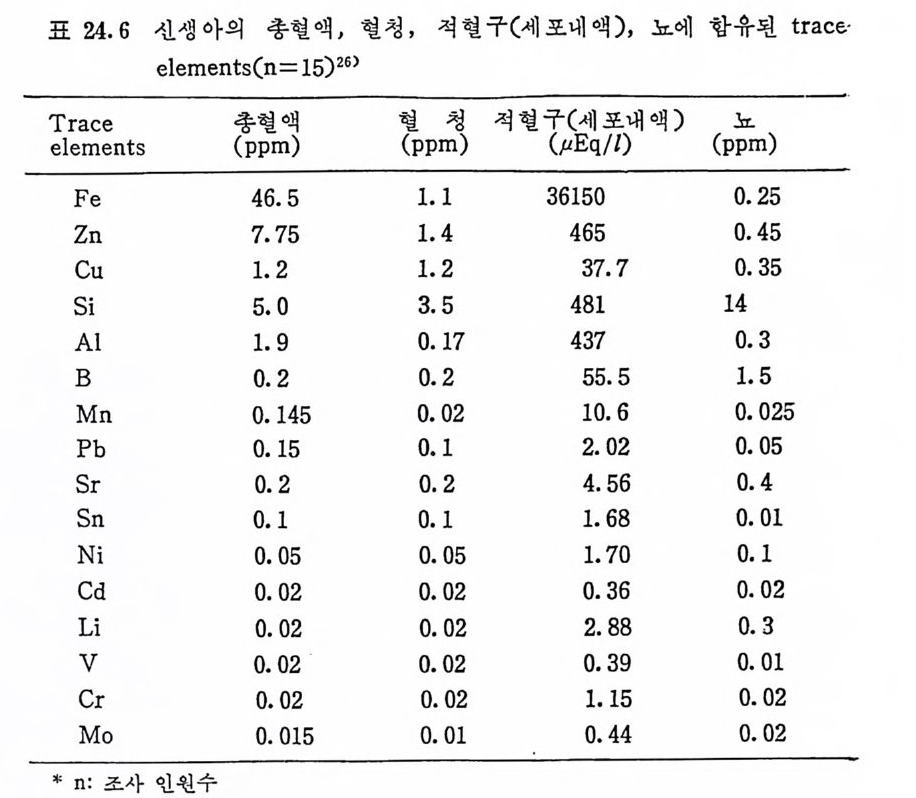 표 24.6 산생아의 총혈액, 혈청, 져혈구(세포내°석), 뇨에 함유된 tra ce·
표 24.6 산생아의 총혈액, 혈청, 져혈구(세포내°석), 뇨에 함유된 tra ce·
15 명 의 신생 아의 나아 는 34~57 시 간이 고 체 중은 2180~4640g , 섭 취 량은 5Xl0~5X20ml 의 분유였으며 뇨는 24 시간 동안 뇨채취 용기 에 모은 것이었다. 15 명의 출산은 정상이었으며 모두 건강하였다. 표 24. 7 은 성 인의 총혈액 , 혈청 , 그리 고 적 혈구의 tra ce elements 를 %로 표시 했다. 26) 신생 아의 적 혈구의 Zn, Fe, Cu, Sn, Al, Pb, Mn, V, 그리 고 Cr 은 성인과 비교할 때 현저히 달랐으며 총혈액의 Zn, Cu, Fe, Pb . 과 Cr 도 성인과 비교할 때 현처히 다르게 나타났다. 신생아의 혈청 에서는 Fe 과 Sn 만이 성인과 차이가 있었으며 Zn 이 성인보다 신생 아의 체내에 중요한 기능을 갖는다는 것은 중요한 사실이다.
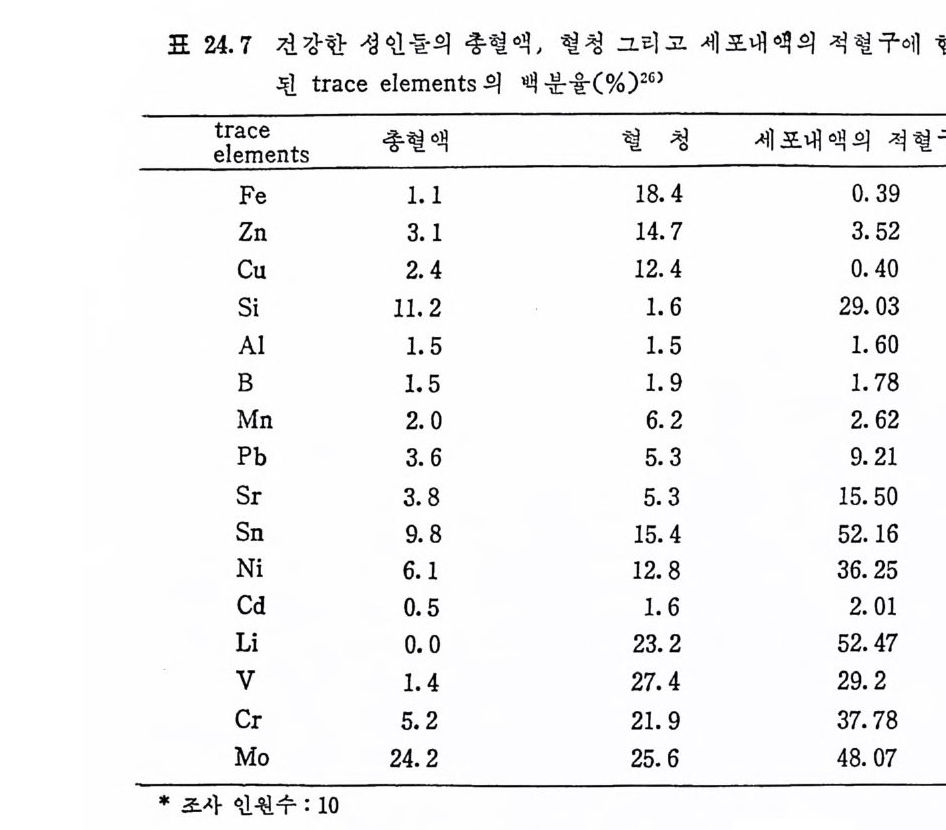 표 끽 .7 건강한 성인둘의 총혈액i 혈청 그리고 세포내액의 적 혈 구에 함유
표 끽 .7 건강한 성인둘의 총혈액i 혈청 그리고 세포내액의 적 혈 구에 함유
Zn 은 RNA, DNA 합성에 중요한 역할을 하며 부족시 여러 가지 결 핍증이 나타나는 것을 볼 수 있었다. Hol t me i er2” 는 임신부의 혈청 Zn 농도가 임신 초기부터 말기까지 계속 감소되는 것을 관찰하였 다. 태아기는 모체에서부터 계속 저장된 Zn 울 공급받기 때문에 Zn 결핍증과 더불어 저단백혈증을 일으키기 쉬운데 이때 Zn-DL-aspa r- ta te 를 찰 조철해 주어 야 한다. 28)29) Chr. Pan t e li ad i s26) 도 선생 아에 게 서 Zn 이 적 혈 구와 (전체 혈 액 Zn 의 85% 가 적혈구에 있음) 전체 혈액에서 아주 낮은 것을 관찰할 수 있었다. 그러므로 임신부에게 충분한 Zn 의 급여가 중요하다고 생각한다. 그 이의에도 임신부는 Cu 를 아주 적게 함유하고 있는데 Cu 는 태 아의 간에 처 장이 되 어 있으며 Fe 의 흡수와 hemog lo bin 합성 에
능동적으로 영향을 준다. Cu 는 약 93% 가 혈액의 원형질에 존재하 며 대반에는 동과가 되지 않는다. 그러므로 신생아와 장기 정백두 입을 받는 어린이에게는 하루 100~500µ g의 Cu 를 섭취시키는 것 이 좋다. 24. 5 유아 영 양과 tra ce elements 와 의 관계 사산아의 tra ce elemen t s 측정치는 조사 대상이 된 어린아이에 따 타 많은 차이를 보여주었다 .14) 신생아에서 성인까지 Cu, Fe 그리 고 Cr 이 측정 되 었 다. 30)31 ) 무지방 체조직에서는 Cu, Fe, Cr 이 신생아에서 성인으로 갈수 독 감소된다. 현재 까지 유아의 trac e elements 의 섭 취 량, 흡수량, 보유량이 아직 완전히 연구되어 있지 않은 상태이다 .32)33) 모유와 우유의 tra ce elements 의 함량도 측정 자에 따라서 다르게 나타났다 .34) 표 24. 8 은 소의 초유와 성 숙유의 trac e elements 의 평 균치 이 다. ”)
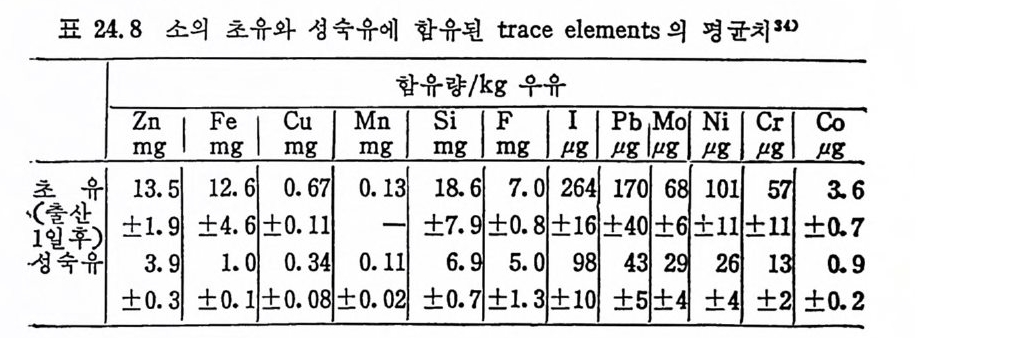 鬪표 2I 4.: 8益l ;;소 1: 의 \i;초1 1유 와:닙; ;성; 숙±『유:에: 함 I 함유:입유~량된니 /~k gt노 r~a우c e유| 1e kleI;m:3en:t:s : 1의 ;말평Jh 균치냐~ 냐:g
鬪표 2I 4.: 8益l ;;소 1: 의 \i;초1 1유 와:닙; ;성; 숙±『유:에: 함 I 함유:입유~량된니 /~k gt노 r~a우c e유| 1e kleI;m:3en:t:s : 1의 ;말평Jh 균치냐~ 냐:g
그립 24.3 은 소에 있어서 출생 1 주일 후 수유기간에 갑소되는 Zn 의 양이다.외) 신생아의 lOOOg 무지방 조칙에서의 평군 Zn 합량은 19m g이며 성 인은 28mg 이 다. 31) 표 24. 9 는 모유와 우유 그리 고 무지 방 조칙 의 tra ce elements 의 함량을 나타낸 것이다 .35) 2~3 개월 된 모유의 Zn 함량은 196 土 58µ g
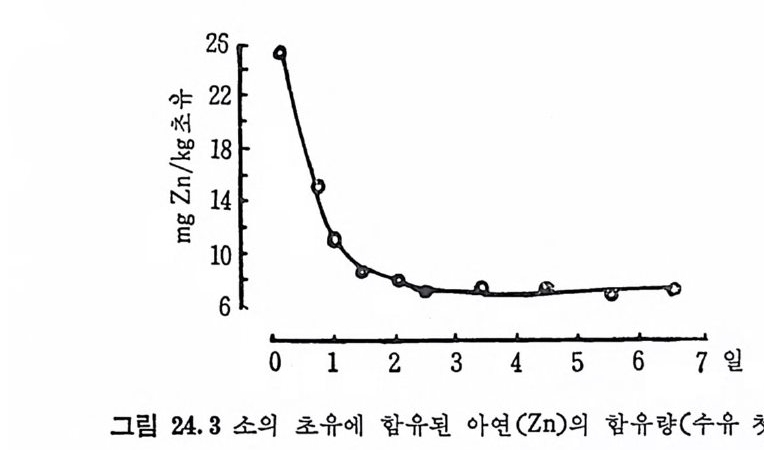 25
25
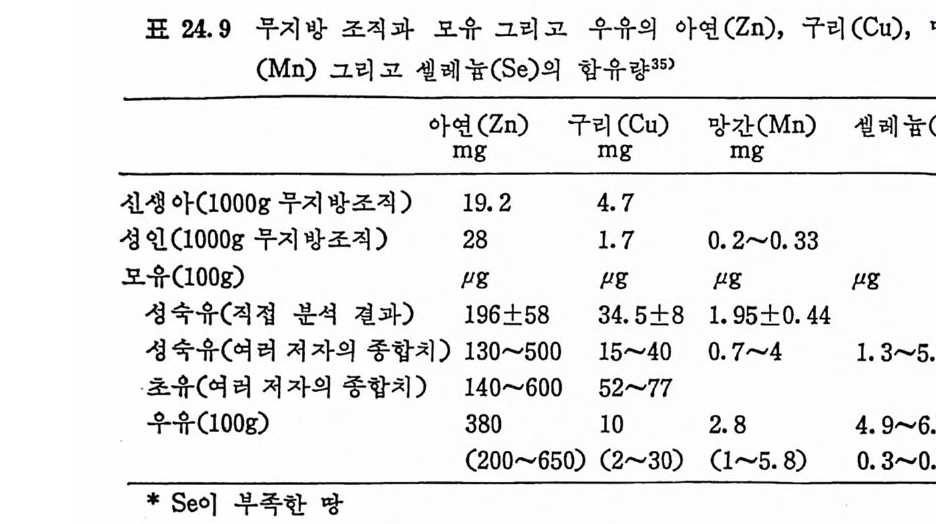 표 24. 9 무지 방 조칙 과 모유 그리 고 우유의 아연 (Zn), 구리 (Cu), 망간 -
표 24. 9 무지 방 조칙 과 모유 그리 고 우유의 아연 (Zn), 구리 (Cu), 망간 -
100g 이 며 성 숙유에 는 lOOg 당 500~lOOOµg Zn 이 함유된 것 으로 느 나타났으며 개 개 인마다 조금씩 다르다고 한다. 26)33)36) 우유에 는 380- µg lOOg 으로 200~600µg 의 차이 가 있 다고 한다. 신생 아의 Cu 함량은 4. 7mg /1 000g , 성 인은 1. 7mg /l OQ O g 무지 방 조칙이다. 연령이 증가함에 따라서 Cu 의 농도가 감소된다. 신생야 는 Fe 과 Cu 가 저장된 상태로 출생된다. 우유는 모유보다 Cu 가 적게 함유되어 있다 .37) 신생아의 Mn 의 함유량에 대하여서는 아직 알려쳐 있지 않았으나 신생아의 간에는-
성인의 간에 비해서 아주 소량의 Mn 을 함유하거나 38) 혹은 전혀 33), 함유하지 않는다고 한다. 표 24.10 은 800g 의 모유, 우유 그리 고 분유에 함유되 어 있는 tra ce elements 양이 다. 35)
 표 24.10 800g 의 모유, 우유 및 시 판되 는 분유의 아연 (Zn), 구리 (Cu),.
표 24.10 800g 의 모유, 우유 및 시 판되 는 분유의 아연 (Zn), 구리 (Cu),.
800ml 는 신생아가하루 섭취할 수있는 양이며 하루 모유 섭취서 는 1.6 mg Zn 을 그리고우유 1 : 1 의 회석유는 설탕도 포함해서 1.5 mg Zn 그리 고 15~20g 의 당질을 800ml 우유에 첨 가했을 때 는 1. 7 ~2. 5mg Zn 를 섭 취 하게 된다고 한다. 유아는 800ml 의 모유 섭취시 280µg Cu 를 하루 섭취하게 되며 1 : 1 회석우유에서는 40µg Cu 를 섭취한다. 분유에서는 48, 64, 88µg Cu 를 섭취하게 된다. Mn 과 Se 도 표 24.10 에서 볼 수 있다 .35) 표 24.11 는 시중에서 시판되고 있는 이유식의 Zn, Cu 그리고 Mn 의 함유량이다 .35)
 표 24.11 유아 이유식에 합유된 Zn, Cu, Mn의 함유량 35)
표 24.11 유아 이유식에 합유된 Zn, Cu, Mn의 함유량 35)
과일, 채소쥬스 등으로 Zn 의 섭취량은 많이 중가되어질 수있다 e Cu 는 과일과 야채죽 둥에 우유 음식보다 더 많이 함유되어 있다. 표 24.l~} 표 24. 13 은 Pahlke 둥 3 9) 이 조사한 유아 분유의 Cu 와 Zn 함량이 다. 표 24.12 는 2/3 우유를 기 초로 한 분유지 방을 모유화한 분유 그리 고 완전히 모유화한 분유의 Cu 함량 39) 이 다. 표 24 . 13 은 2/3 우유불 기 초로 한 분유, 지 방을 모유화한 분유, 그리 고 완전히 모유화한 분유의 Zn 함량 39) 이 다.
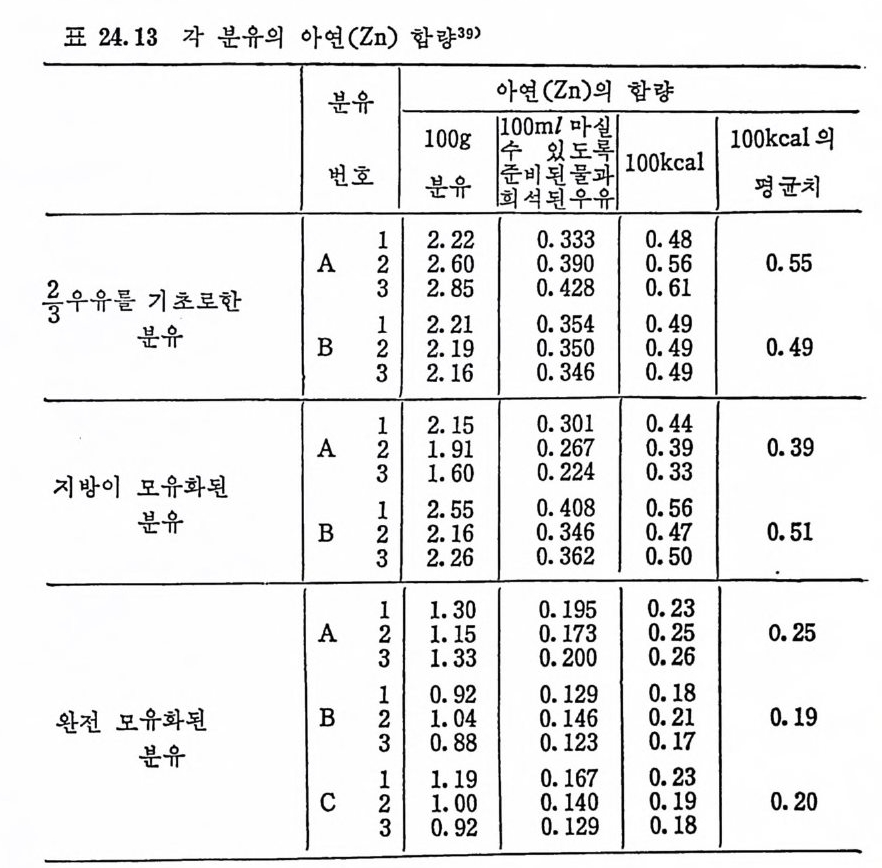 표 24.13 각 분유의 아연T번` r 3(호0TZ n ) 함l분O량O유 3g 9 ) :회10석비0m \l ;! lOOkcal lOO평kc군a치l 의
표 24.13 각 분유의 아연T번` r 3(호0TZ n ) 함l분O량O유 3g 9 ) :회10석비0m \l ;! lOOkcal lOO평kc군a치l 의
위 의 여 러 표에 서 보듯이 WHO 와 FAO 의 분과위원회 (alim e nta · r i us)40) 에 서 는 유아에 게 적 어 도 Cu 를 60µg /1 00 kcal 그리 고 Zn 0. 5- mg /l OO kcal 로 결정 단계 에 있지 만 실제 로 모유에 는 Cu 가 50µg /1 00
kcal 가 들어 있으며 모유에는 Zn 0. 3Img / IO Okcal 들어 있는 실정에 서 위와 같은 높은 권장량을 결정한다는 것은 실현시키기에 부적당 하다고 생각하며 이 분야에 대한 더 많은 연구가 있어야 되겠다 .39) 다음은 음료수와 분유를 혼합하여 유아가 섭취한 우유의 tra ce elements 를 분석 했는데 이 때 음료수에 함유된 tra ce elements 와 도 밀접한 관계가 있었다 .40) 표 24. 14 는 수도물을 들어 놓는 시 간에 따라 탈라지 는 음료수의 Cu 와 Zn 함유량이다 .41) 이 표에서 보듯이 음식을 준비하거나분유 를 희석하여 만들 때 수도물을 틀어 놓는 시간에 따라서 Cu 와 Zn 의 함량이 다르다.
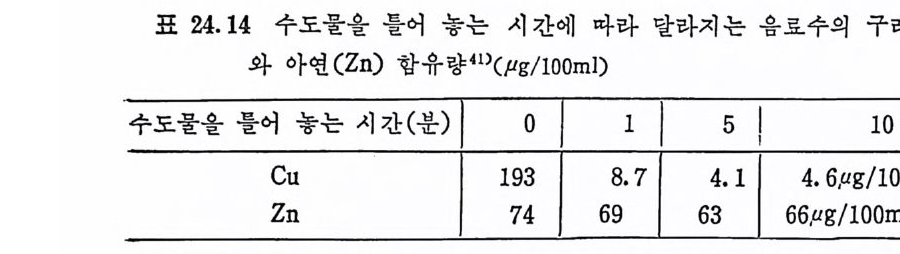 표 24.14 수도문을 틀어 놓는 시 간에 따라 달라지 는 음료수의 구리 (Cu)
표 24.14 수도문을 틀어 놓는 시 간에 따라 달라지 는 음료수의 구리 (Cu)
표 24.15 는 독일의 Tubin g e n 의 음료수로 준비 한, 유아가 섭 취 하는 Humana 0 의 tra ce elements 함유량이 다. 5 분 동안 음료수를 흘려 보내 고 나서 만든 분유의 Cu 함량이 제 일 적 당하다고 한다.
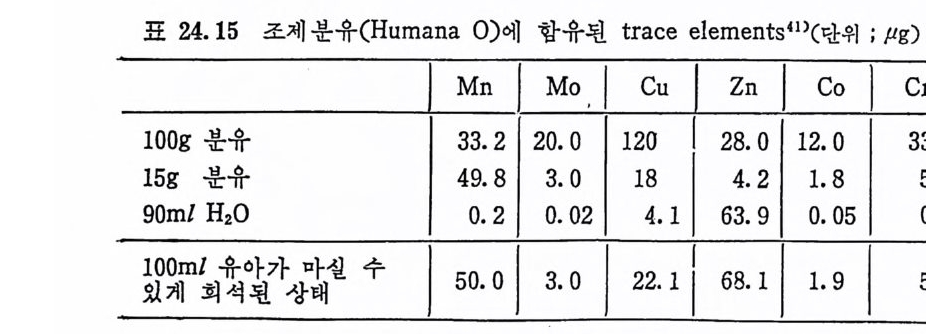 표 24. 15 조제 분유 (Humana 0) 에 함유된 tra ce elemen t s11) (단위 ; µg)
표 24. 15 조제 분유 (Humana 0) 에 함유된 tra ce elemen t s11) (단위 ; µg)
24. 6 Parente ral nutr i t ion 의 tra ce elements 제 계 여 러 나라와 우리 나라에 서 도 par ente r al nutr i t ion 이 증가하
고 있 으며 특히 장기 간의 정 맥 투입 시 는 tra ce elements 의 영 양이 중요하다. 그러나 여기에 대한 연구조사는 많지 않으나 다음의 연 구들을 알아보고자 한다. Moellg 와 W i lk41) 는 pa rente r al nutr i t ion 의 tra ce elements 를 축 정했다. Va, Ni, S i과 Sn 은 그의 필수성이 사람에 있어서 완전히 규명되지 않았고 F, I, Se 은 축정방법의 어려움 때문에 측정을 하지 못했다. Cr, Mn, Co, Cu, Zn, 그리고 Mo 을 축정했으며 여 기에 Mg을 더 첨가했다. 표 24.16 은 병원에서 사용하고 있는 R i n g er~석 에 함유되어 있는 tr ace elements 이 다. 41)
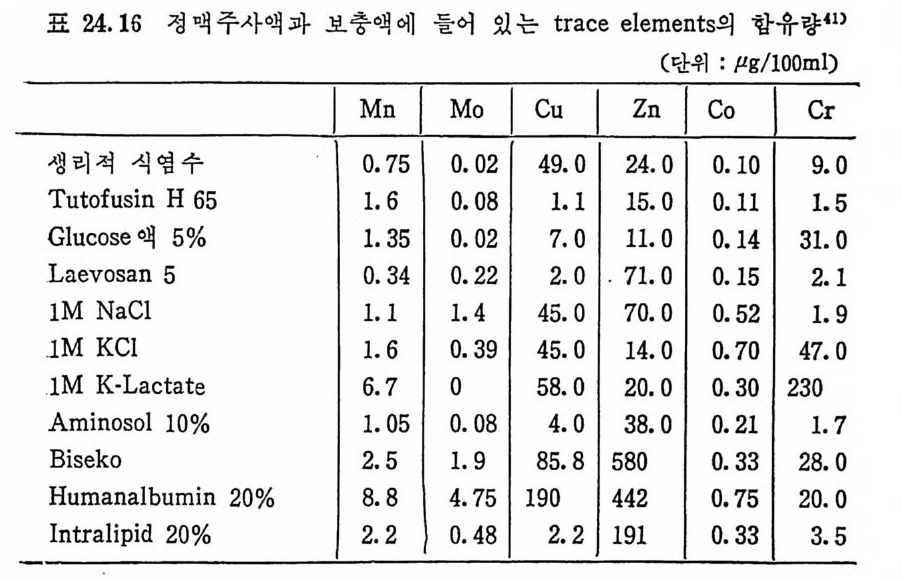 표 24. 16 정 맥 주사액 과 보충액 에 들어 있 는 tra ce elemen ts 의 함유량 4 1)
표 24. 16 정 맥 주사액 과 보충액 에 들어 있 는 tra ce elemen ts 의 함유량 4 1)
모든 Ri ng e r ~석 에 는 tra ce el~ments 가 함유되 어 있으며 단지 1M ·po ta s siu m lacta t e 에 만 Mo 이 함유되 어 있 지 않았다(표 24. 16). 단백질이 함유된 정맥 주사액 album i n 은 사람 혈청의 tra ce ele- men t s 의 함유량과 같았다. 그러나 정맥 주사액은 5 배의 Zn 이 강화 되었고 20% 의 인체 album i n 에는 Zn 과 Cu 가 첨가되어 있었다. 사람의 혈청에는 36µg % Zn 이 album i n 과 결합되어 있다 .42) 그 러므로 20% album i n 에는 약 lOOµ g%의 Zn 이 함유되어 있어야 하
Jµ데 442µg % Zn 이 함유되어 있었다. Cu 는 20 배 가량으로 혈칭에 5µ g %43) 가 함유되어 있는데 비해서 album i n 에는 l90µ g%가 함유되 어 있었다. 단백 질 이 아닌 glu cose 와 NaCl 의 용액 등에 도 다른 tra ce elements 가 많이 포함되어 있었다. NaCl 에는 Cu 와 Cr 이 상당량 들어 있 는데 체중 10k g인 어린이가 하루 정맥으로 두여받는 5% 의 포도당 IM NaCl, 그리고 IM pot a s siu m lacta t e 용액을 계산했을 때 표 24.17 과 같다 .4 1)
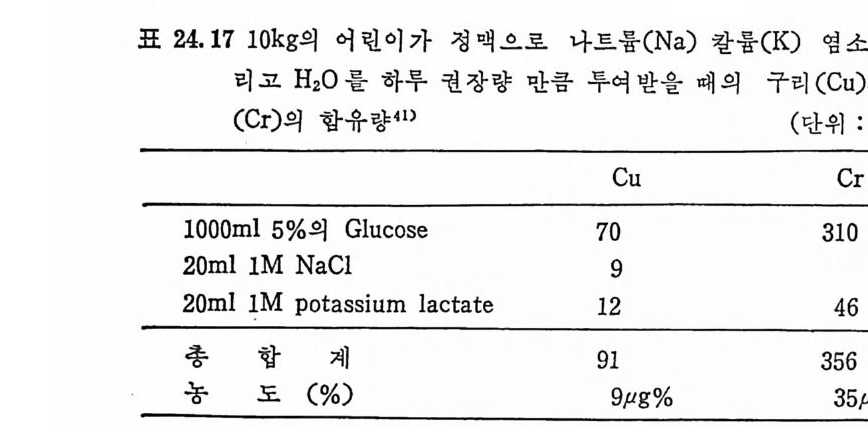 표 24.17 10k g의 어 린이 가 정 맥 으로 나트뮴 (Na) 칼룹 (K) 영 소 (CI) 그
표 24.17 10k g의 어 린이 가 정 맥 으로 나트뮴 (Na) 칼룹 (K) 영 소 (CI) 그
WHO 에서는 음료수로 Cu 오} Cr 을 5µ g%이상 섭취하지 못하도록 하고 있는데 44)45) 이 어린이가 정맥으로 두여받은 하루의 Cu 의 양 은 9µ g%이며 Cr 은 35µ g%이기 때문에 앞으로 많은 관십과 연구가 계 속되 어 쳐 야 할 것 같다. 또한 음료수의 tra ce elements 는 전부가 흡수될 수 있는 형태가 아닌데 비해서 정맥으로 두여받은 tra ce ele- men ts 는 곧 정맥에서 이용될 수 있기 때문에 위험윤은 더 크다고 생각한다. 그러나 Zn 은 필요량보다 적은 양이 섭취되는 것 같다. Fodor46) 는 수술 후 악성 종양 간질환혹은 설사때 Zn 의 결핍증이 나타나며 이때는 상처의 치료를 위해서도 0.1~0.2mg kg 체중을 권장하는 데 10kg 어린아이에게 정맥으로 두입되는 양은 0.13mg ; Zn 이기 때문에 약 1m g을 더 첨가해 주어야 한다고 한다 .41)
24.7 상처가 심한 의석불명 환자의 혈청과 뇨의 Cr, Mn,. Co, Ni, Cu, Zn 함량 48) 정맥으로 영양을 공급받게 되는 의석불명의 환자들의 혈청과 뇨. 의 tra ce elements 를 8~10 일동안 At om i c absorpt ion s spe c tro p h o- t ome t er 로 측정했다. Cr, Mn, Co 그리고 N i은 혈청과 뇨에서 급 격히 증가되었다. 그 원인이 정맥 두여액에 의한 것인지 아닌지에 대해서는 많은 논쟁이 되고 있다. Cr, Mn, Co, 그리고 N i의 혈청 에 서 의 급격 한 중가는 효소와 tra ce elements 그리 고 단백 질과 결합 되어 있는 모든 효소들이 이화작용에 의하여 분해되면서 상승된다
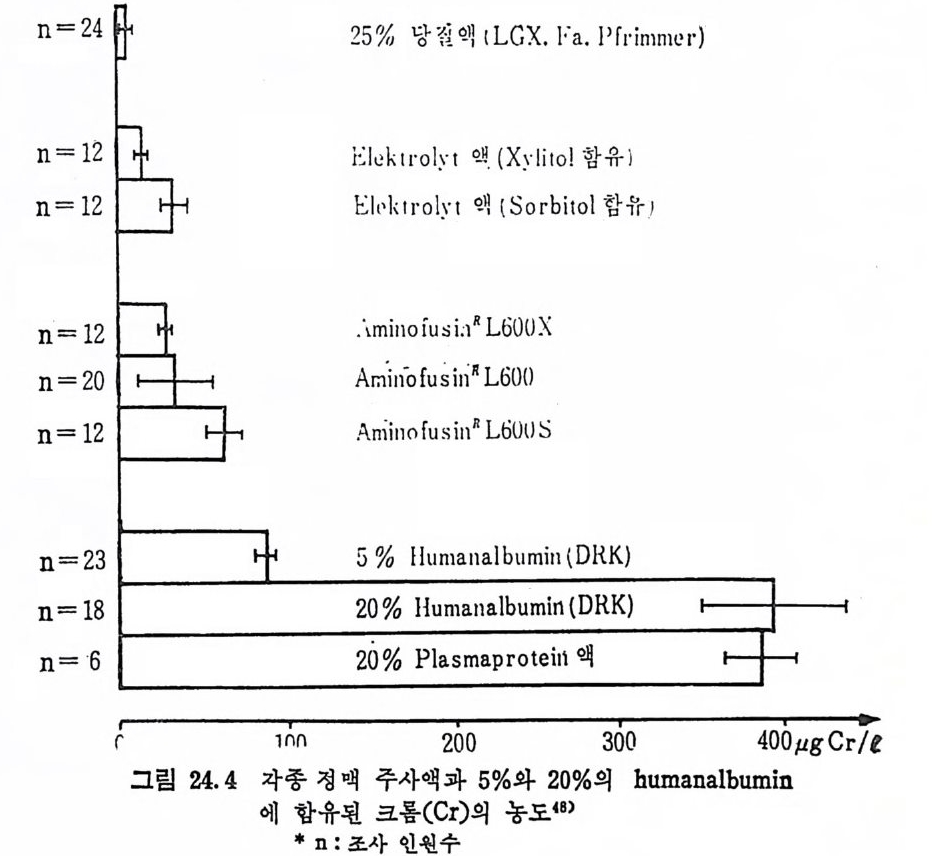 n=24 25% 당접액 tL GX. Fa.l' frim mer)
n=24 25% 당접액 tL GX. Fa.l' frim mer)
고 생 각되 기 도 한다. 48) 많은 tra ce elements 가 체 내 에 서 단독으로 어떤 기능을 갖기보다는 다른 효소와 결합됨으로써 그의 임무를 수 행할 수 있기 때문이다 .47 )49) 그림 24. 4 는 Rin g e r 액 에 함유된 Cr 이 다. 48) 그림 24. 5 는 Rin g e r ~석 에 함유된 Ni 이 다. 48)
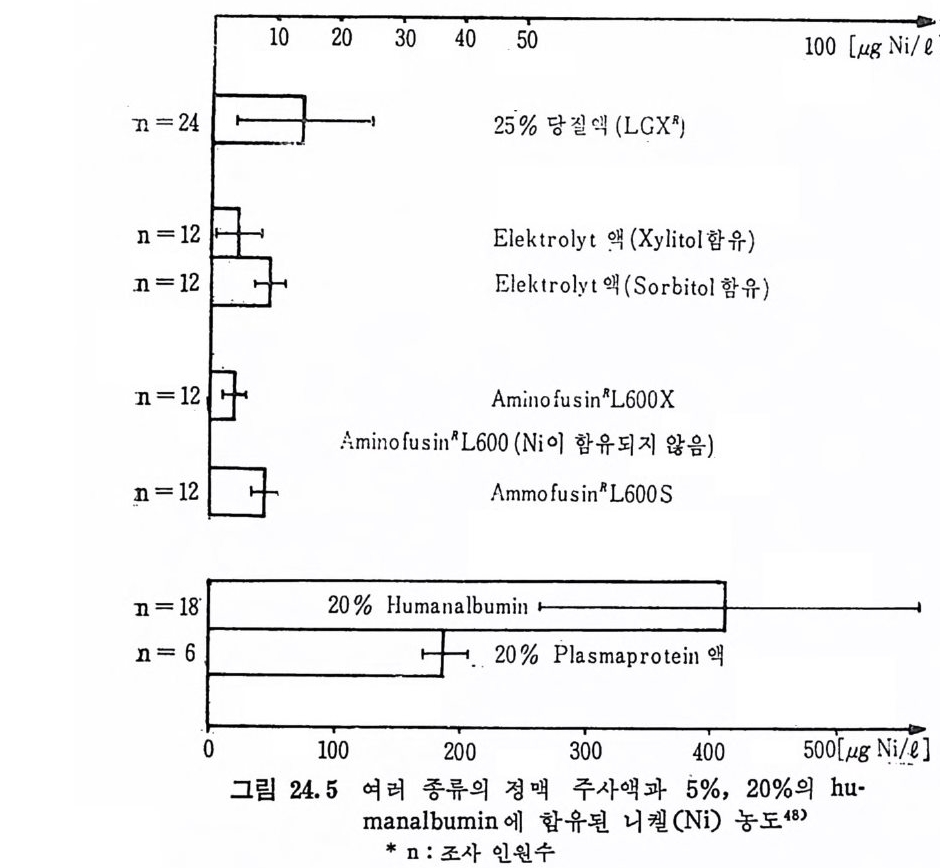 10 20 3I0 4I0 5I0 100 [µg Ni/• e l.
10 20 3I0 4I0 5I0 100 [µg Ni/• e l.
그림 24. 6 은 Rin g e r 액 에 함유된 Mn 이 다. 48) 혈청의 Cu 농도는 정상치 이하였으며 뇨로 많이 배설되었다. 정 맥 주사약에도 적은 양의 Cu 가 들어 있었다. Zn 의 양은 다른 실험과 같이 처음에는 혈청의 Zn 이 아주 낮아 쳤다가 치료에 의하여 접접 정상으로 되돌아왔다. 그러나 뇨로 배
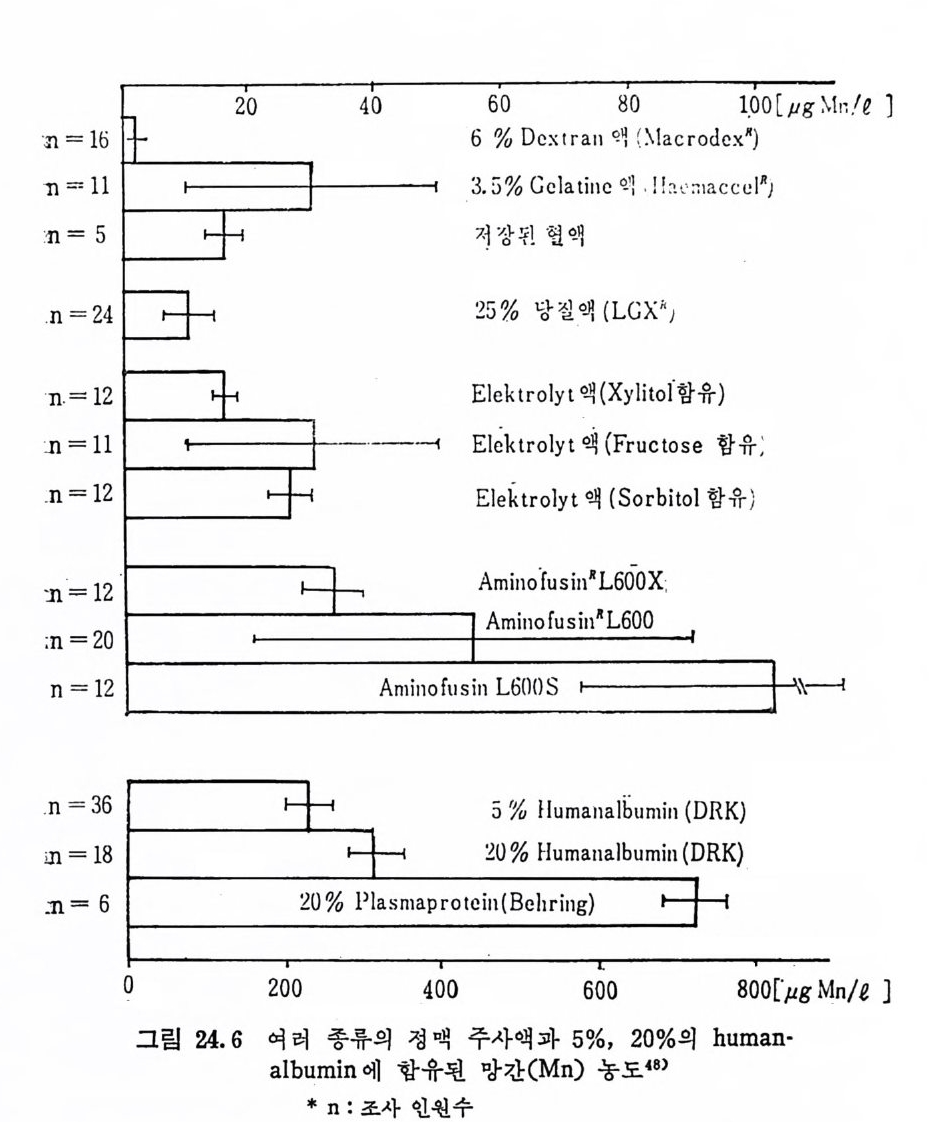 .n = l6 t 20 40 6 6%0 DcxEa,, e8!0 { Macrodcx1 사0 o [ µg :...1i1,1e J
.n = l6 t 20 40 6 6%0 DcxEa,, e8!0 { Macrodcx1 사0 o [ µg :...1i1,1e J
설된 Zn 의 양은 정상보다 10 배나 높았다. 그러므로 이와 갇온 증 장에는 되도록 빨리 Zn 을 보강해야 한다고 생각된다.
*참고문현 1) Kollmer, W. E. and H. Krie g e l , Int. ]. Radia t . Bi ol . , 9, 369,, 1965. 2) Kollmer, W. E. , Zbl. Vet. Med. , Beih e ft , 11, 181, 1970, 3) Kollmer, W. E. , Int. ]. Radia t . Bi ol . , 19, 183, 1971. 4) Kollmer, W. E. , Berg, ATKE 15/62. 303, 1970. 5) Kollmer, W. E. and H. Krie g e l , Int. ]. Radia t. Bi ol . , 9, 369, 1965·. 6) Kollmer, W. E. and H. Krie g e l , Natu r e, 205, 196, 1965. 7) Kollmer, W. E. , P. Schramel and K. Samsahl, Phy s. Med. Bi ol . ,. 17, 1972. 8) Kollmer, W. E. , in Betk e , Klaus & Bin d li ng Maie r , Frank, Ent; .. wi ck lung von Mensch und Tt' er , Urban & Schwarzenberg, p. 69, 1975. 9) Berge ! , F. , J. L. Everett , J. B. Marti n, J. S. Webband J. Pharm .. Pharmacol. , 9, 522, 1957. 10) Evans, G. W. , Phy si o l . Rev. , 53, 535, 1973. 11) Parr, R. M. and D. M. Tayl o r, Bi oc hem. ]. , 91, 428, 1964. 12) Sass-Korts a k A. , Cl in. Chem. , 8, 15, 1965. 13) Underwood. E. J. , Trace ·elements in human and anim al nutr i - tion , Academi c Press, p. 57, 1977. 14) Wi dd owson, E. M. and J. W. T. Di ck erson, Mi n eral meta b oli sm , Academi c Press 2A p. 1, 1964. 15) Wi dd owson, E. M. and C. M. Sp ra y , Arch. Di s. Chi ldh. , 26, '!05, 1951 . 16) Hambid g e , K. M. , in Dekker, Newer Trace Elements in Nutr i - tion, New York 1971. 17) Henkin , R. I. , in Dekker Newer Trace Ei em ents in Nutr i t ion , New York, 1971. 18) Behne, D. , in Betk e , Klaus and Bin d li ng Maie r , Frank, Sp ur en-elemente in der Entw i ck lung von Mensch und Ti' e r, Urban & Schwa- rzenberg, p. 77, 1975.
19) Behne, D. , in Prin t i ng . 20) Hock, A. , K. Kaspe rek, H, R. Scholz and L. E. Fein e ndeg en , in Betk e , Klaus & Bin d li ng Maie r , Frank, Sp ur enelemente in der En· 1wi ck lung von Mensch und Ti er , Urban & Schwarzenberg, p, 89, 1975. 21 ) Thie m e, R. , in Betk e , Klaus & Bin d lin g Maie r , Frank, Sp ur en· -el emente in der Entw i ck lung von Mensch und Ti er , Urban & Schwa· rzenberg, · p. 97, 1975. 22) Thie m e, R. , P. Schramel, B. J. klaus and E. Waid ! , Sp ur enele· ment unte r s uchung e n an der menschlic h en Plazenta , Geburts h il fe and Frauenheil k unde, in Prin t i ng . 23) Pope s cu, I. and G. Zachia , Chem. Abstr . , 53, 8445, 1959. 24) de Francis c i s, P. , F. Boccolate , Natu r e, 193, 989, 1962. 25) Brandt, H. H. , Z. ge s. inn . Med. , 12, 7, 1957. 26) Pante l ia d is , Chr. , in Betk e , Klaus & Bin d li ng Maie r , Frank, :Spu renelemente in der Entw i ck lung :.,on Mensch und Ti er , Urban & Schwarzenberg, p. 103, 1975. 27) Holtm eie r , H. J. and M. Kuhn, Therap iew oche, 22, 51, 4536, 1972. 28) Fodor, L. , F. W. Ahnefe ld and R. Dolp, Inf us io n sth e rap ie, Son· derheft 2, 5, 1973. 29) Fodor, L, , J. Eschner and W. Dic k , F. W. , Anaesth e s,·st 21, 456, 1972. 30) Hambid g e , K. M. , in W. Mert z, W. E. Cornatz e r, ed. Newer Trace Elements in Nutr i t ion, Marcel Dekker, Inc. , New York, 1971. 31 ) Wi dd owson, E. M. , in Barltro p , D. , W. L. Burland. , ed. Mi ne ral Meta b olis m in Pedia t r i c s , Blackwell Scie n ti fic Publi ca ti on s, Oxfo r d and Edin b urgh , 1969. 32) Mert z, W. , in W. E. Cornatz e r, Newer Trace Elements in Nutr · 다.ti on, Marcel Dekker Inc, New York, 1971. 33) Underwood, E. I. , Trace Elements i11 Human and Anim al Nu• tri t ion, 4th ed. , Academi c Press, New York und London, 1977. 34) Kir c hg e. Bn er, M. , J. Pallau f, F. J. Schwarz and H. -P. Roth , in Eetk e , Klaus & Bin d li ng Maie r , Frank, Sp ur enelemente in der Entw ,·c-
klung von Mensch und Ti er , Urban & Schwarzenberg, p. 39, 1975, 35) Sto l lei, H. , W. Droese and I. Rewerts , in Betk e , Klaus & Bin - dli ng Maie r , Frank, Sp ur enelemente in der Entw i ck lung von Mensch- und Ti er , Urban & Schwarzenberg, p. 113, 1975. 36) Schlett w ein - Gsell, D. and S. Mommsenstr a ub, Beih eft Inte r nal. Z. Vi tam i n und Ernahrung s fo rsch. Nr. B. , Hans Huber, Bern·S t u t t - ga rt- W ien , 1973. 37) Souci , W. , W. Fachmann and H. Kraut, Di e Zusammensetz u ng · der Lebensmi ttel, Wi ss enschaft lich e, Verlag e sellschaft , mbH, Stu tt ga rt, 1973. 38) Ramage , H. , I. H. Sheldon and W. Scheldon, Proc. , Roy. Soc .. B. , 113, 308, 1933. 39) Pahlte , G. , L. Klin g e bie l and H. P. Lenk, in Gladtk e , E. G. Heim ann and I. Eckert, Sp ur enelemente , Georg Thie m e Verlag Stu tt -- ga rt, p. 113, 1979. 40) Codex Al im enta riu s Commi ss io n FAO/WHO Joi n t Of fice , Rom. Al inor m. 76/26A Ap pe ndix II. 41) Moeller, H. and G. Wi lk, in Betk e , Klaus & Bin d li ng Maie r , Frank, Sp re nelemente in der Entw i ck lung von Mensch und Ti er , Ur-- ban & Schwarzenberg, 137, 1975. 42) Hellweg e, H. H. , Mschr. Ki n derheil k . , 19, 37, 1971. 43) Gubler, C. J. and M. E. Wi nt r o be, J. Cli n. Invest. , 32, 405, 1953. 44) World Health Orga niz a ti on , Europ ea n Sta n dards of Drin k in g · Wate r , Genf. , 1961. 45) World Health Orga niz a ti on , Inte r nati on al Sta n dards of Drin k in g · Wate r . Genf. , 1963. 46) Fodor, L. , R. Dolp, J. Eschner and F. Ahnef~ ld, •A naesth e sis t , 22, 393, 1973. 47) Dubin , T. L. and W. A. Leonow, Usp. Sovr. Bi ol . , 66, 453, 1968 .. 48) Seeli ng , W. , F. W. Ahnefe ld , W. Dick , R. Dolp, L. Foder, E. Schmi tz and R. Hohage , in Betk e , Klaus and Bin d lin g Maie r . Frank,,. Sp ur enelemente in der Entw i ck iu n g von Mensch und Ti e r Urban &
Schwarzenberg, p.1 59, 1975. 49) Gii nt h e r, T. , B. Ruhe, J. Schmalbeck and N. Tehrani, Z~ Klin . Chem. Kl in. Bi oc hem. , 12, 327, 1974.
25 기타 비필수 미 량원소 앞서 고찰한 원소 이의에 기타 다수의 비필수 미량원소가 동물 조직 에 다양한 농도로 촌재 한다. 이 에 는 Anti m ony , Bromi ne , Ger-maniu m , Rubid i u m , Sil ve r, Ti tan iu m , Zir c oniu m 등이 포함된다. 최근 환경오영이 된 식품과 식수 둥에, 그리고 공업과 농업의 발 달 둥에 의해서 몇 가지의 원소가 증가되었다. 그러나 아직 그의 작 용이 확실히 규명되어 있지 않으므로 여기서는 생략하기로 한다.
26 각 식 품에 함유된 tra ce elements 식 품에 함유된 tra ce element 는 다음과 같다. 표 26. 1 은 홍 1) 이 조사한 우리 나라의 곡류 중에 함유된 tra ce ele- :m en t s 의 함량을 표시한 것이다. 곡물 22 종 104 건을 원자 홉광 분석 법 으로 측정 하여 다음과 같은 결론을 얻었다. 1) Mn 과 Fe 함량은 깨류가 가장 높은 수치를 나타내며 다음이 豆 類 이며 가장 낮은 수치를 나타내는 것은 米類이다. 2) Cr 함량은 전반적으로 매우 적으며 그 중 깨류 및 두류가 :::z.. 함량아 많으며, 米類 및 麥類 는 그 함량이 비슷하며 적게 함유하고 있다. 3) Cu 및 Ni 함량은 두류 및 깨류가 가장 많으며 미류, 맥류는 그 함량이 비슷하며 적게 함유하고 있다. 4) Zn 함량은 깨류가 가장 높은 수치를 보이며 다음이 두류이 고, 미류는 맥류보다 적게 함유하고 있다. 5) Sn 함량은 두류가 가장 많고 그 다음이 깨류이며 미류와 맥류 는 적게 함유하고 있다. 6) Pb 는 각 곡물이 비슷하게 함유하고 있으며 Cd 합량은 두류 및 깨류가 가장 많고, 미류 및 맥류는 그 합량이 비슷하다. 표 26. 2 는 우리 나타 식 물성 식 품에 서 측정 된 trac e elements 의 함
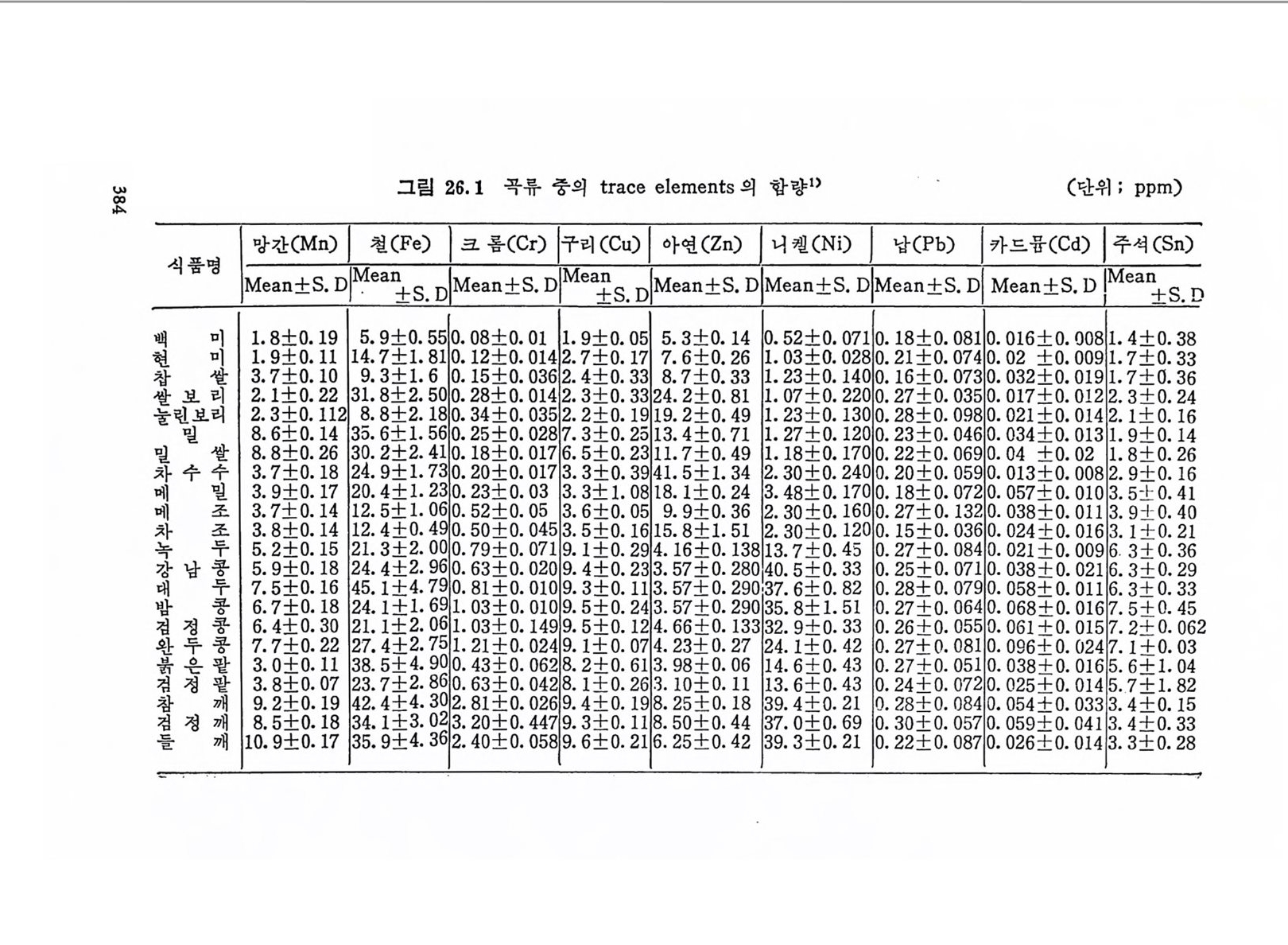 납 e 1 2 1 2 2 2 2 2 1 2 1 2 2 2 2 2 2 2 2 2 3 2
납 e 1 2 1 2 2 2 2 2 1 2 1 2 2 2 2 2 2 2 2 2 3 2
 표 26. 2 우리 나라 식 물성 식 품에 서 측정 된 tra ce elements 의 합량 2)~8)
표 26. 2 우리 나라 식 물성 식 품에 서 측정 된 tra ce elements 의 합량 2)~8)
량이 다. 2)8) Fe 의 함량은 1. 53~10. 76m g%이 며 , 송이 버 섯 , 싸리 버 섯 , 표고 버섯 등에 많이 함유되어 있고 느타리버섯, 석이버섯, 팽나무버섯 양송이버섯, 들버섯의 순으로 많이 함유하고 있다. 솜먹물버섯, 나도팽나무버섯, 목이버섯 그리고 흰목이 버섯에서는 겁출되지 않 았다. 해조류의 Fe 함량 평군치는 7 Q m g %3H) 이다.
시료 버섯 중 Cu 의 함량 범위는 1. 82~6.18m g%이며 송이버섯,양송이버섯, 목이버섯, 흰목이버섯, 싸리버섯, 표고버섯, 들버섯, 솜먹물버섯, 석이버섯, 느타리버섯, 팽나무버섯에 가장 적게 함유 되어 있다. Cu 함량은 곡류 2) 가 0.2~1m g%이고 백삼이 2m g으로 Cu 를 가장 많이 함유하고 있 으며 그 다음이 미 삼, 수삼의 순우] 5) 로 함유되어 있다. 시료 버섯 중 Mn 의 함량 범위는 0.70~2.82m g%이며, 송이버 섯, 흰목이버섯, 솜먹물버섯, 석이버섯, 싸리버섯, 느타리버섯, 나 도팽나무버섯, 양송이, 표고버섯, 들버섯의 함량 순위이고 묵이버 섯에서는 겁출되지 않았다. 시로 버섯 중 Pb 의 함량 범위는 0.Olm g %~0.07m g%이며, 양 송이버섯, 목이버섯, 들버섯, 나도팽나무버섯, 흰목이버섯, 팽나무 버섯, 송이버섯, 표고버섯, 솜먹물버섯, 석이버섯, 느타리버섯의 함 량 순위이고 싸리버섯에서는 겁출되지 않았다. 끝으로 국내 식품 제조 회사에서 상용하는 식품첨가물 10 그룹 39 종을 수집하여 원자홉광도로 분석한 결과 tra ce elemen t함량율 표 26. 3 과 같이 보고하였 다. 9)
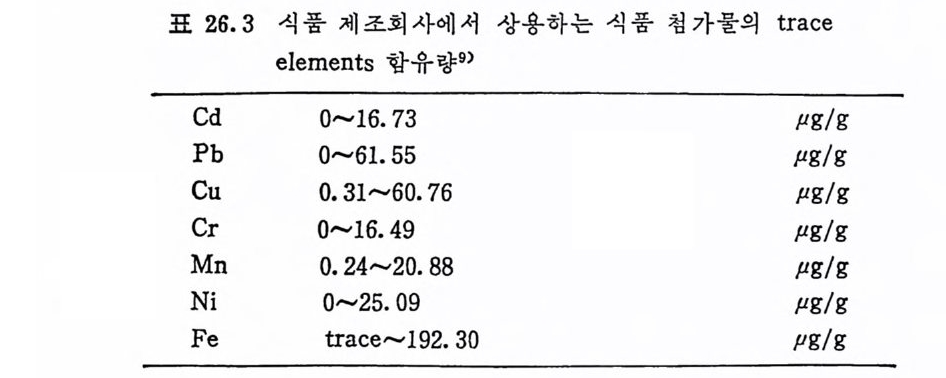 표 26.3 식품 제조회사에서 상용하는 식품 첨 가물의 tra ce
표 26.3 식품 제조회사에서 상용하는 식품 첨 가물의 tra ce
착향료는 레몬향과 지 방산이 다른 착향료보다 금속원소의 함량이 높았고 쵸콜렛향은 Ni, Fe 을 제의하고는 금속원소의 함량이 가장 낮다. 식품 첨가물 중 가장 문제시되고 있는 착색료에서는 전반적으로 각 금속 합량이 높다. 특히 Cd, Pb, Cr 의 함량이 높은 것 은 주시
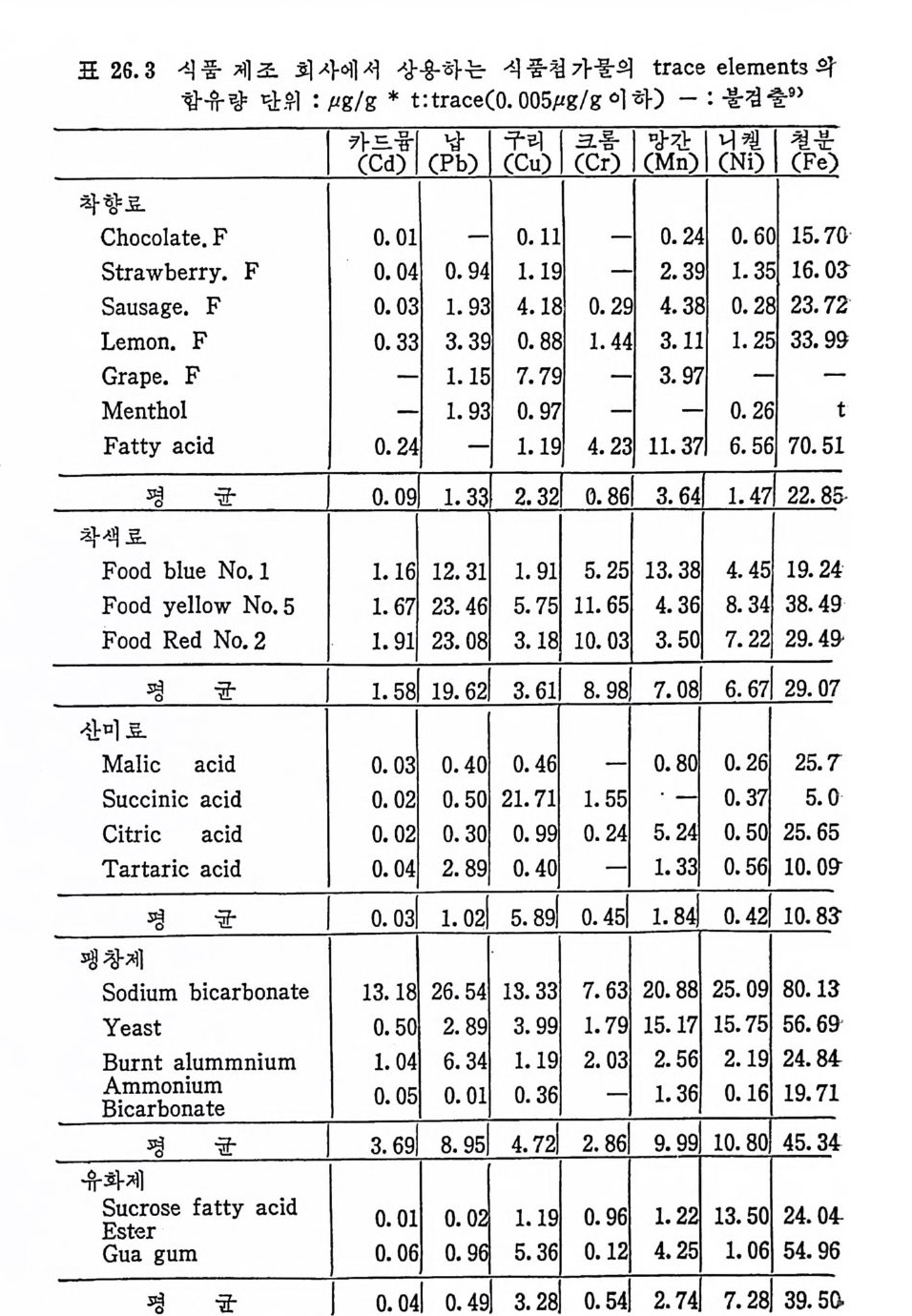 표 26. 3 식 품 제 조 회 사에 서 상용하는 식 품첨 가물의 tra ce elements 와
표 26. 3 식 품 제 조 회 사에 서 상용하는 식 품첨 가물의 tra ce elements 와
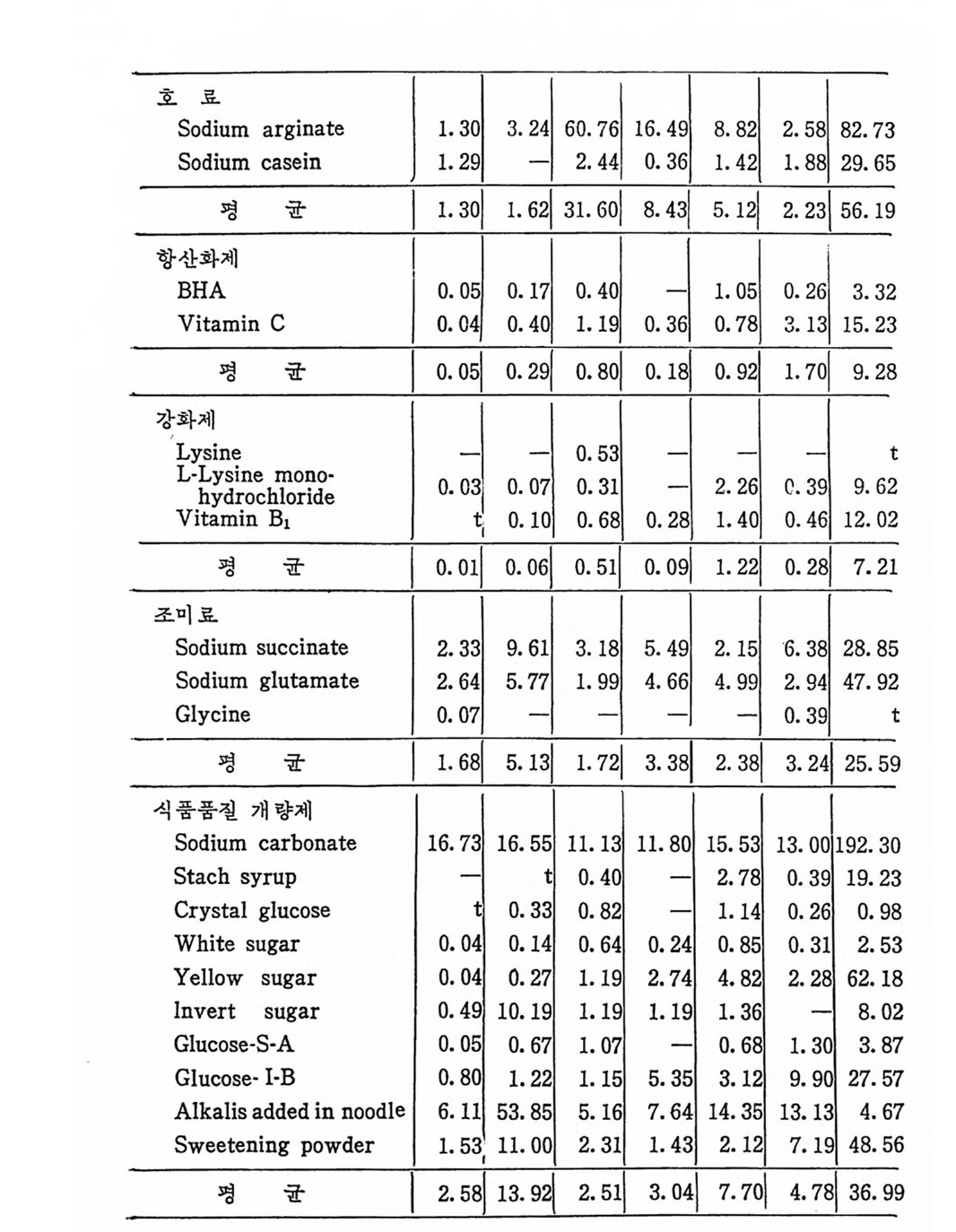 항호산 BVSSooHi화 d로dtAaii제u um mm i n c aCarsg ei nin a te ll0—3l5000234니9.1- 32—; _40010 1 561 20言 .. 74 06411 16。0..0 . 43」96 018.1482217一05 2021O 3.... 58 21883—2.06111 1 8213295.... 20 76323523 .11l 2.4
항호산 BVSSooHi화 d로dtAaii제u um mm i n c aCarsg ei nin a te ll0—3l5000234니9.1- 32—; _40010 1 561 20言 .. 74 06411 16。0..0 . 43」96 018.1482217一05 2021O 3.... 58 21883—2.06111 1 8213295.... 20 76323523 .11l 2.4
할 만하다(표 26. 4). Food ye llow No. 5 가 Mn 을 제 의 한 각 금속 원소의 함량이 가장 높고, foo d blue No. 1 은 Mn 을 재 의 한 각 금속 원소의 함량이 다 론 식용색소에 비하여 가장 낮다. 산미 료에 서 는 succi ni c aci d 의 Cu : 21. 7µg /g, Cr : 1. 55µg /g 을 제 의 하면 금속원소의 함량이 다른 gro up 에 비 해 득히 낮다. 팽 창제 에 서 는 sodiu m bic a rbonate 가 금속 원소의 함량이 가장 높 고, 특히 Cd : 13. 18µg /g 은 주시 할 만한 수치 인 데 비 해 ammo-niu m bic a rbonate 는 O. 05, Cd : 0. 65µg /g, Pb : 0. Olµg /g 등으로 각 금속원소별 함량이 낮다. 유화제 에 서 는 sucrose, fatty acid este r 는 gu a-gu m 보다 Cr, Ni 이 약 10 배 가량 함량이 많으나 그 외 의 금속원소는 gu a-g u m 에 더 많다 . 호료에 서 는 sodiu m argi na te 가 sodiu m casein 보다 각 금속 원 소의 함량이 높다. 항산화제에 서 vit am i n C 가 BHA 보다 Cd 율 제 의한 금속의 함량아 높지만 항산화제 그룹은 대체로 각 금속원소 의 함량이 낮아 안전한 g rou p에 속한다. 강화제에서는 대체로 각 금속 원소의 함량이 낮으며 l y s i ne 에서 는 Cu 를 제 의 한 기 타 금속 원소가 겁 출되 지 않았고 L-lys in e mono- hy d rochlorid e , vit am i n B1 의 금속 원소의 함량이 낮아 안전한 g rou p에 속한다. 조미 료에 서 는 sodiu m succi na te , sodiu m · glu ta m ate 가 금속원 소의 함량이 비 교적 높은 데 비 해 gly c in e 은 Cd : 0. 07µg /g, Ni : 0. 3 9µg /g, Pb, Cu, Cr, Mn 둥은 불검 출됨 으로써 다론 조미 료보 다 금속원소의 함량이 낮다. 식 품품질 개 량제 에 서 는 sodiu m carbonate 가 각 금속 함량이 현 처히 높고 물엿이 Cd, Cr 이 불겁출되고 Fe 이 19.23µ g/g으로 각 금속 원소의 함량이 낮다. 표 26. 4 와는 미 국의 식 품에 합유된 각종 tra ce elements 의 함량 율 표시한 것이다.11)
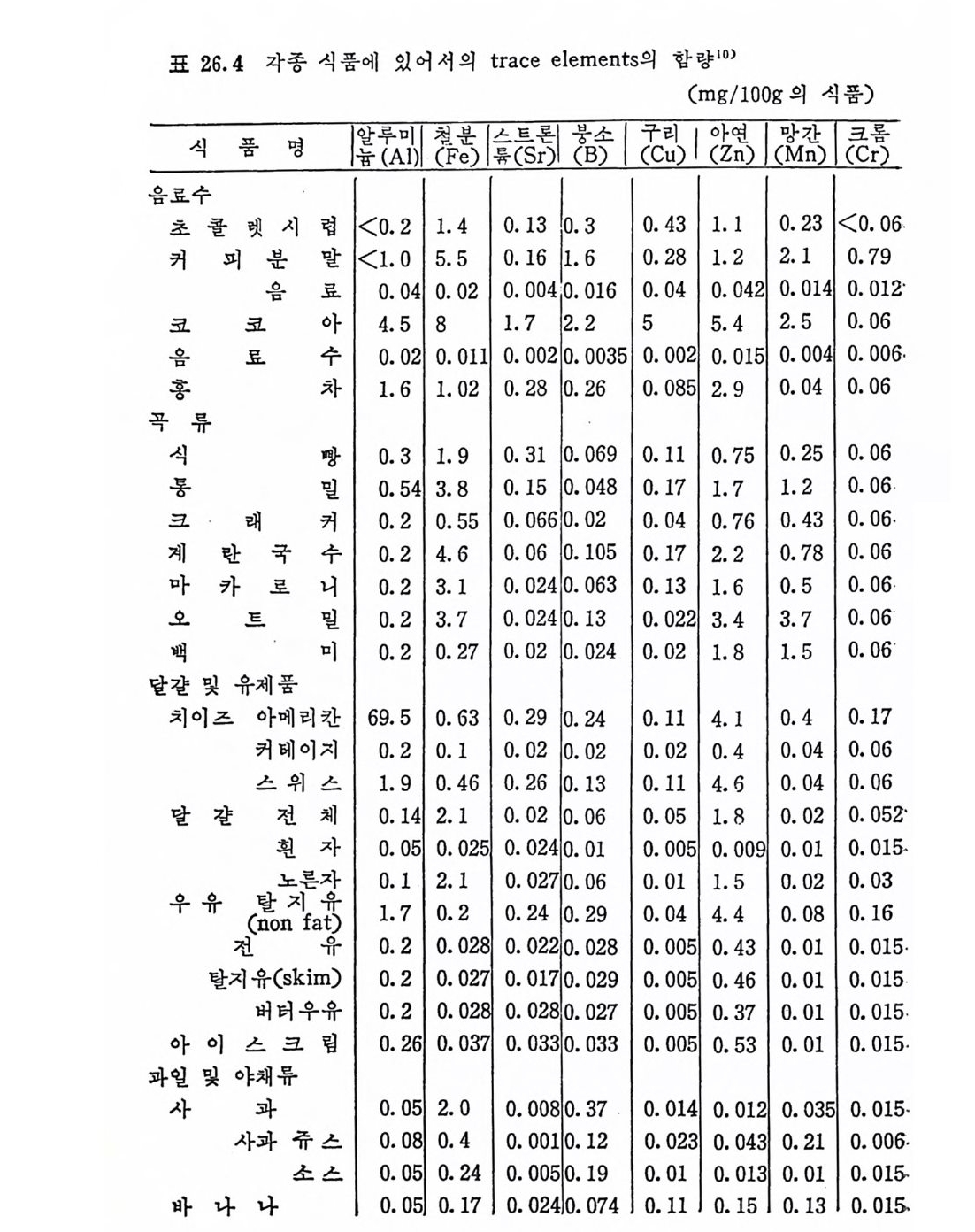 표 26. 4 각종 식 품 에 있 어 서 의 tra ce elemen t s 의 함 량 10 )
표 26. 4 각종 식 품 에 있 어 서 의 tra ce elemen t s 의 함 량 10 )
 포도o. 05I 1. 1 I o. 064I o. 45 JO . 035 r o. 035I o. 0651 o. 015
포도o. 05I 1. 1 I o. 064I o. 45 JO . 035 r o. 035I o. 0651 o. 015
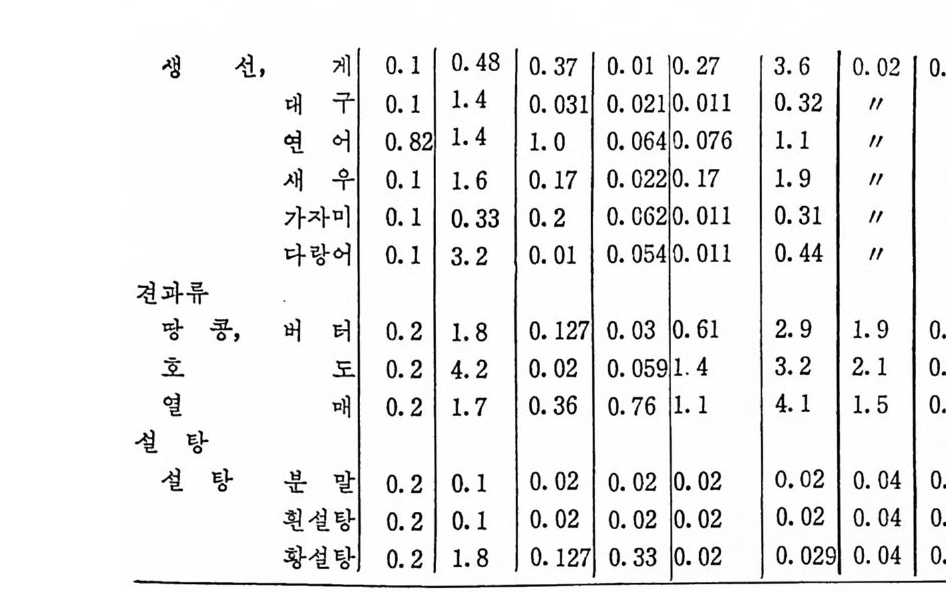 ^j 선, 거] o. 1 o. 48 0.37 o. 01 0.27 3. 6 0.02 o. 03
^j 선, 거] o. 1 o. 48 0.37 o. 01 0.27 3. 6 0.02 o. 03
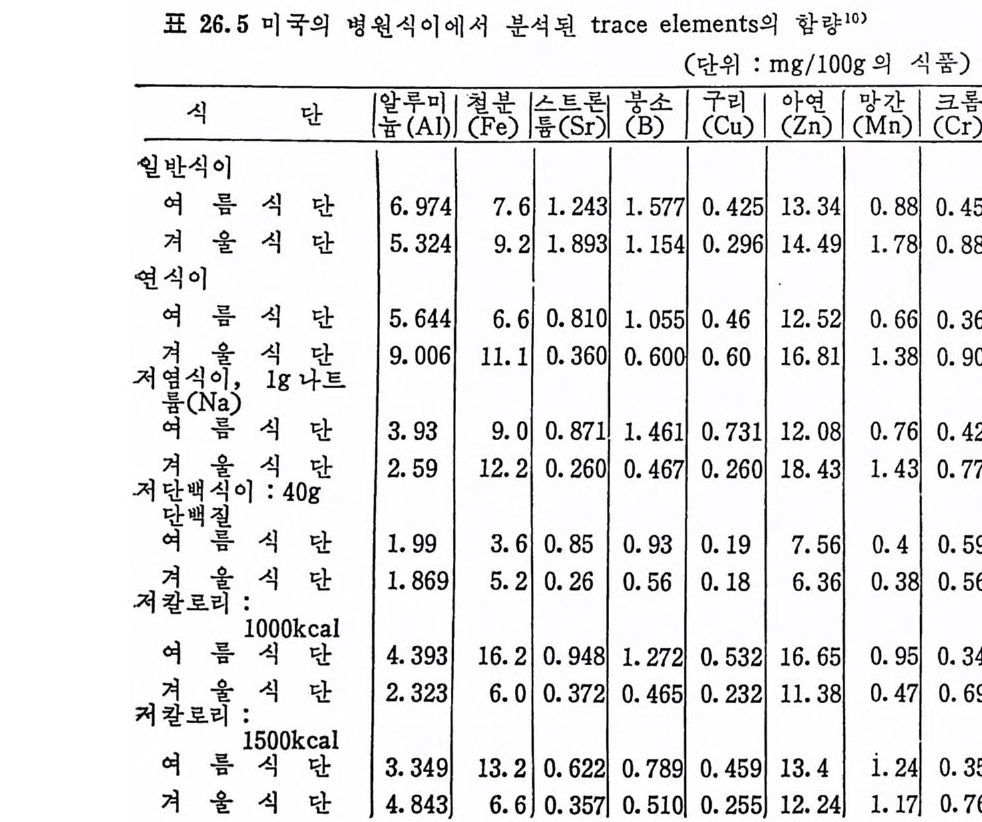 표 26. 5 미 국의 병 원식 이 에 서 분석 된 tra ce elemen ts 의 합량 10)
표 26. 5 미 국의 병 원식 이 에 서 분석 된 tra ce elemen ts 의 합량 10)
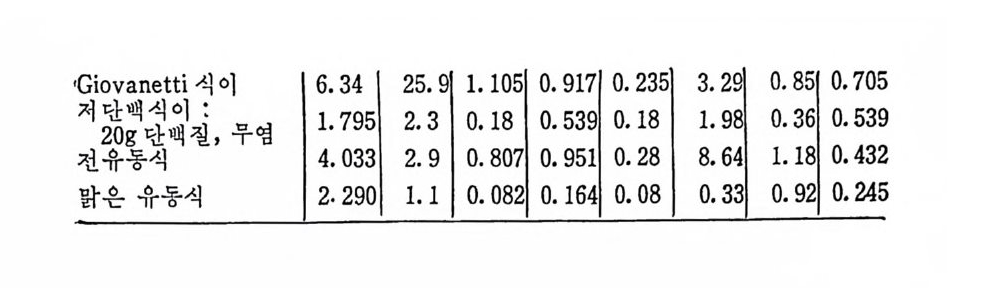 •Gi ov anett i 식 이 6. 34 I 25. 91 1. 1051 0. 9171 0. 235 0. 851 o.705
•Gi ov anett i 식 이 6. 34 I 25. 91 1. 1051 0. 9171 0. 235 0. 851 o.705
*참고문현 l) 홍영 숙, 신정 래 , 《한국 영 양학회 지 >, Vol. 8, Ko. 1, 39, 1975. 2) 노일협, 《 숙명여자대학교 논문집 》 , 21, 141, 1981 . 3) 전세 열 外, 《 인 간과학》, 3~4, 79, 1979. 4) Soeh, J. H. et. al. , ]. Kor. Soc. Food Nut. , 3, 17, 1974. 5) 조한옥 의, 《한국 식품과학회지》, 8~2, 95, 1979. 6) 농촌진흥청 편, 《식 품분석 표》, 22, 1970. 7) 朴貸杰, 《건국대 학교 논문집 )), 6, 217, 1977. 8) 고인석 外, 『희 갑기 념 논문집 』, 40, 58, 1978. 9) 문범수 등, 「식품의 제조가공용 화학적 합성품의 국내 소비실태에 관한 연구」, 《 국립 보건원보》, p. 229, 1973. 10) Krause and Mahan, Food, Nutr i t ion and Di et Therap hy , W. B. :Sa unders Co. Phil ad elph ia . London. Toronto , p. 828, 1978.
27 걷 론
Trace elemen t s 에 대한 연구는 앞에서 기술하였듯이 과거와 현제 를 통하여 많이 행하여지고 있다. 무엇보다 중요한 것은 각 tra ce- elements 연구에 기 초가 되 는 분석 방법 이 라고 생 각된다. 현재 까지 만족할 만한 분석 결과는 Cu, Fe, Zn 둥에서 얻어졌고, Hg , Mn, Se 는 연구 과정에 있으며, 그 의의 As, Cd, Co, Cr, Mo, Ni, Pb, Sb 등의 tra ce elemen ts 는 그 분석 방법이 아직도 계속 연구되어지 고 있는 실정이다. 또한 I, F, Si, V 과 같은 tra ce elemen t s 는 찰 알려쳐 있으나 국제적으로 인정받을 만한 연구 결과와 표준이 없고 분석방법에 대한 정확한 결과가 미약하다. 따라서 필자는 앞으로의 tra ce elements 에 관한 연구에 서 질적 으 로 향상된 정확한 분석방법이 요구된다고 생각되며, 실험이나 연 구과정에 있어 다음과 같은 면이 보충되어야 할 것으로 사료된다. 1) 생화학적 측면에서의 tra ce elements 대사의 연구 Trace elements 대 사는 결합된 배 위자와 함께 작용하기 때 문에 , 동화작용과 이 화작용에 서 의 tra ce elements 의 단독 특수 기 능을 규 명하는 데 난점이 많으므로, 새로운 연구 분석이 요구된다. 2) 생 리 적 측면에 서 의 tra ce elements 의 연子 지금까지 알려진 필수 tra ce elemen t s 의 생체내에서의 이용과 기 문] 대한 깊은 연구가 되어져야겠으며, 아직도 완전히 규명되지 않은 몇 개 의 tra ce elements 의 필수성 에 대 해 서 도 많은 연구가 필요-하다. 또한 tra ce elements 의 화학 구조의 규명 과 효소와 meta l lo- •or ga nic comp o und 와의 상호관계 도 고려 되 어 야 할 것 이 다. 생체내 대사에 있어서도 세포 내에서의 tra ce elemen t s 의 대사과 정의 정확한 분석이 요구된다. 3) 임 상효과에 관한 tra ce elements 의 연구 근래에 들어 문제시되고 있는 암 (cancer) 이나 바루스성 질병의 치 로요법 으로 tra ce elements 의 역 할에 대 한 연구가 전행 되 고 있 으나, 앞으로는 인체를 중심으로한 실험에 의해 분명한 임상효과를 연구 해야 할 것이다. 4) Trace elements 의 독성 에 관한 연구 환경오영이 날로 증가되고 있는 현시점에서 참재적인 독성물질에 관한 많은 조사가 행해지고 있다. 예를 들어, Cd, Zn, Cu, Hg 등 의 독성현상은 매우 심각하다. 그러나 독성중상은 개개인의 흡수량 이나 연령, 성벌 둥에 따라서 많은 차이룰 보이기 때문에 계속 상 품화되고 있는 유독물질에 대한 정확한 분석이 요구되며, 허용량, 최저량 등의 범위가 인체 실험을 통하여 더욱 확고해져야 할 것이 다. 또한 체 내 에 서 의 tra ce elements 의 상호작용과 hormone 과의 관계에 대한 연구는 독성문제를 해결하는 데 좋은 밀받침이 될 것이 다. 5) 유전성 과 tra ce elements 에 관한 연구 Trace elements 영 양과 유전적 인 면에 서 의 관계 는 아직 연구되 어 있지 않으나 이러한 관계의 정확한 분석 결과는 대단히 중요한 것 으로생각된다. 6) Trace elements 의 동물사육 증가에 관한 연구 동물의 사육시 tra ce elements 의 첨 가는 여 러 가지 결핍 증상을 없 애 주고, 성장에 현처한 효과를 보인다는 접에서 각 tra ce elements 가 어떤 과정에 관여하는지에 대한 연구와 적정량에 대한 정확한 분석이 요구된다.
색인
국문색인
-, 간경변증 235 갑상선 270 곡류의 마 량원소 함량 384 골다—공증과 다2 혈83 증 9
구리 결핍증 I8,86 I ―,망간, 니첼, 셀레늄의 상호 작용 II9 —, 몰리 브덴, 황의 상호작용 IIO —와 아연의 상호작용 104 ―와 철의 대사작용 98 —, 카드뮴, 은, 수은, 납의 상호작용 120 ―의 권장량 84 -의 독성 94 ―의 배선 14,84 ―의 섭취량 14 ―의 저장 82 —의 주요기능 74 .― 의 체 내 함유량 l4, 72 —의 합유효소 꾸 ―의 함유식 품 17, 92, 384, 390 ―의 흡수 78 규소 결핍증 295 — 합유식품 298 ―와 동맥 경 화증 11, 297 —의 독성 298 ―의 배설 297 _의 섭취량 14,298 -―-의 주요기 능 18, 295 —의 체내함량 294 __- 의 필요량 298―의 흡수 297 L 납 걷핍증 327 ―의 독성 20,332 一의 배설 329 —의 보유 330 ―의 섭취량 330 ―의 주요기능 327 _의 체내함량 326 ―의 필요량 330 _의 함유식품 331,384: —의 흡수 329 뉴질—렌드함인량의 혈23중1 셀레늄 섭취 량 238 니첼 걷핍증 251 ―의 독성 255 ―의 배설 250 ―의 섭취량 250 ―의 주요기능 249 ―의 체내함량 248 ―의 필요량 251 —의 흡수 249 E: 당내능 인자 2I9 동백 경 화증 297, 348 E 리티움과 동백경화증 34S __- 과 정 신질환 347 ―의 독성 347 _의 배설 347
―의 체내함량 347 ―의 흡수 347 口 망간 함유식 품 17, 213, 384, 390 ―의 결핍증 2I2 ―의 독성 2I4 ―의 배설 2II ―의 섭취량 2II ―의 주요기능 :?09 ―의 체내 함유량 208 ―의 팔요량 2II ―의 함유효소 22 一의 혈청 함유량 2Il ―의 흡수 2II 머 리 카락의 아연함량 I48 모유의 구리함량 93 ,95 ―의 망간함량 209 몰—_리_브- 덴의평 형결아 핍연 증함20 량3, 20I5I 一의 크롬함량 2I9 203 5 — 함유식품 204 __- 함유효소 22 ―과 크산틴 산화효소 204 —과 통풍 204 ―― · 의 독성 204 ―의 배설 201 ―의 섭취량 203 ―의 주요기능 20l ―의 체내함유량 200 ―의 팔요량 203 ―의 흡수 20l 미량원소의 대사 뀌
―의 독성 I9 —의 발견연도 I6,I7 ―의 배설량 I4 ―의 섭취량 I4 ―의 주요기능 I7 —의 체 내 분포 I4, I5, 36o ―의 팔수성 I6 ―의 함량표시 I3 ―의 함유식 품 17, 383, 390• —의 혈장농도 14 ―의 효소로서의 기능 20 l:f 바나디 움의 결핍 증 302 —의 독성 304 ―의 배설 302 ―의 섭취량 303 ―의 주요기 능 18, 302 —의 체내합량 301 ―의 팔요량 303 ―의 홍수 302 ―의 함유석품 303 버섯—의 침미 착량증원 소 2합81량, 2 90385 분유의 미 량원소 함량 369, 37% 불소 강화식품 290
―의 결합능력 42 —의 결핍증 281 ―의 독성 290 ―의 배설 287 ―의 섭취량 289 ―의 주요기능 I8,28I ―의 체내합량 15,280 ―의 팔요량 289__- 의 흡수 284 붕소의 독성 356 ― · 의 체내함량 355 ―의 함유식 품 356, 390 비소 결핍증 307 ―의 독성 20,310 ―의 배설 308 . -의 섭취량 309 —의 주요기 능 18, 307 ―의 체내함량 307 -의 필요량 3o9 _의 흡수 308 비필수 미량원소 382 빈혈 94, II4, 119, 252 人 산화형 혈색소 29 상처가 십한 의석불명환자의 미량원소 함량 375 성인— 혈청반내감기의 셀2레38늄 함유량 230 셀레늄 걷핍증 233 ―과 암발생 243 ―의 독성 20,242 ―의 섭취량 239 ―의 주요기능 18,233 ―의 필요량 239 ―의 합유량 20 ―의 합유석풍 240 소의 초유와 성 숙유의 미 량원소 367 수유시 의 미 량원소 359 수은의 독성 20, 339 —의 배설 336 ―의 섭취량 337
—의 체내함량 335 _의 함유식품 337 —의 허용량 337 -의 흡수 336 스트론룹과 구루병 352 ―의 배설 350 -의 섭취 350 _의 체내합량 349 _의 함유식 품 350, 390 석 풍에 함유된 미 량원소 383, 390 식 품첨 가물의 미 량원소 386 신생아 머리카락의 크롬함량 222 신생 아의 미 량원소 364 ―의 혈청내의 셀레늄 함유량 230 。 아연———— 함유황섭암백식 취체혈 병 상호품18 태 르2 몬l148조4 3사 , 13변8648수, 3 901 59 _과 난포호르몬 167 ―의 걷핍증 106,155 —의 권장량 152, 155 ―의 · 독성 184 ―의 배 설 152, 154 —의 임상적 효과 172 ―의 저장 147 ―의 주요기능 142 ―의 체내 이용물 153 __- 의 체내함량 140 ―의 평형 146 -의 필요량 150, 152
—— 합흡유 수효 소I45 22 알루미늄의 독성 344 —의 배설 14,343 ―의 섭취량 I4,344 ―의 체내합량 342 ―의 함유식품 390 요오드 결핍 증 I3, 274 ―영 277 ―의 독성 277 ―의 배설 273 —의 섭취량 14,274 ―의 주요기 능 17, 270 ―의 체내함량 269 ―의 팔요량 274 ―의 흡수 27l 요오드 함유식 품 I 7, 276 우유의 미량원소 368 ―의 아연함량 I48 ―의 요오드 함량 270 유아영 양과 미 량원소 367 ―이유식의 아연, 구리, 망간 함유량 370 유아 혈청내의 셀레늄 함유량 230 임신시 구리 함량 85 ―의 미 량원소 359, 366 ? 장티프스와 철 54 적 혈 구 44, 65, 230, 365 전사효소 I75 접막장애 32,33 정 맥 주사액 의 미 량원소 13, 373, 375 조제 분유의 미 량원소 372
조칙 철혈증 54 주석의 독성 3l5 —의 체내함량 3l3 —의 함유식 품 314, 384 天 착각화증 105 철 강화식품 60 철 결핍성 빈혈 43,51,62,65,50 철 결핍증 50 __- 전체결합능력 42 — 함유식 품 17, 55, 384, 390 _ 함유효소 22 ―의 권장량 48 ―의 독성 54 —의 배설 30,47 ―의 이동 30,40 ―의 이용 44 ―의 저장 31, 45,46 ―의 주요기능 28 ―의 함량 27,56 ―의 흡수 30,32 충치 281-2 = 카드뮴의 독성 13, 321 —의 배설 320 —의 섭취량 320 —의 주요기능 318 ―의 체내합량 14,317 —의 필요량 320 —의 합유식 품 321, 384 ―의 흡수 319 코발트 결핍증 260
―와 철의 상호작용 262 ―의 독성 264 ―의 배설 262 —의 섭취량 263 ―의 주요기 능 17, 260 -의 체내 함량 259 ―의 합유식품 17,264 _의 흡수 262 크롬 결핍증 22I —과 링게르액 376 -―의 독성 224 一의 배설 220 -_-의 섭취량 222 -의 주요기능 I8,2I9 -의 체내분포 2I8 -의 필요량 222
一의 합유식 품 18, 223, 384, 390 —의 흡수 220 E 태반의 미량원소 364 두석 실험 IO5, 28I 득수환경에서의 미 량원소 359 -lo 항암제 .23 4 해 마토크리 치 63, n9, 249, .25 2, 3.2 7 헤 모글로빈 침 착증 44, 5.2 헤 모글로빈 함량 .29 , 50, 100, .24 9, .25 5, 3.2 7 환원형 혈색소 .29
영문색인
A ACTH 165 alkali dis e ase 244 alkalin ph osp h ata s e 157, 170, 171, 173,180,206 alumi ni u m hy ro xy ·ge l 343 alumi ni u m pho sp h ate - g el 343 ap o fe r riti n 33 B bli nd sta g ge r 244 C -ca rbonic anhy d rase 22, 140, 141, 171 carboxy pe p tida se A& B 174, 179 cerulop la smi n 22, 76, 88, 102 -co balami n 263 corti co t ro p in 165 -cr eati ni s m 275 cu-balance 80, 100 -cu ·th io n ein uo cy toc hrom 22, 100 D -dia l ys is exp e rim ent 105, 281 dis m uta s e 75 'DN A (deoxy r ib o nucleic aci d) 142, 158, 174, 248, 366 E -el ectr o n pa ramag n eti c resonance (EPR) n7 eryt hr ocup re in 75
eryt hr op o ie t i n 264 estr o g en 167 F fer riti n 27, 31, 53, 147, 201 FSH 167 G ga str o fe r rin 37 glu cose tol erance fac to r 219 glu ta t h i o n e per oxid a se 230, 232, 234 gly c o p ro te i n 37 goi t er u, 265, 275, 310 gon adotr o p in 167 gu sti n 156 H hemato c rit 63, u9, 249, 252, 327 hemochromato s e 27, 31, 44, 52 hemog lo bin 27, 29, 32, 44, 47, 50, 75, 100, 249, 252, 255, 327, 366 hemosid e rin 27, 31, 44, 52 human albumi n 376 human albumi n Ni 376 hy pe rcup re mi a 91 I I-po o l 273 ins ulin I4I, X43, I59, 2I9, 22I itai· itai dis e ase 13, 322 M mapl e syr u p urin e dise ase 230 MCHC( Me an Corp u scular
Hemog lo bin Concentr a ti on ) 63 menkes's dis e ase 92 meta l acti ve enzy m es 22 meta l loenzym es 22 meta l locarboxy pe p tida se 96 meta l loth i o n ein 78, 109, 121, 147, 318,322 Mo & xanth in e oxid a se 204 morbus wi ls on's dis e ase 90 mucosablock hyp o th e sis 32 my o g lo bin 27, 29 N nic k el pla smi n 250 nonessenti al tra ce elements 342 P pa rakerato s is 105 pa rente r al nutr i t ion and tra ce elements 150, 372 pe roxid a se 22 ph eny lk eto nuria 230 ph y tic ac id 39, 251 po lyc y the mi a 264 pro g es te r op. e x 67 pro lacti n hormone 249 pro sta g la ndin 145, 169 pro to p o rph rin 65
R reduced hemog lo bin 29 reti cu locy tes 28, 44 Rin g e r soluti on 373, 376 RNA(rib o nucleic acid ) 142, 158, 174,248,366s selenid e 237 selenit e 237 seleniu m ( Iab il e , fix) 237 seleniu m & map le sy ru p urin e dis e ase 230 seleniu m & ph eny lk eto n uria 230 , seleniu m & Vit . E u, 230 sid e rop h il in 221 sid e rosis 54 sulfa te u5 sulfi te u5 sulfi t oxid a se u6, 204 sup er oxid e dis m uta s e 75 T tea rt 205 tes to s te r one 函 th io m olyb date 117 thy m i di n e kin a se 177, 181 thy ro g lo buli n 269 thy ro nin e 269 thy r oxin e 269 thy ro sta t i ca 274 TIBC(Tota l Iron-Bi nd in g Cap a c ity) 42, 63 tissu e sid e rosis 54 tra nscrip tion enzy m e 175 tra nsfe r rin (sid e rop h il in) 33, 41,. 44, 64, 209 tw o-po ol model 35 tyro sin a se 22 tyro sin e 269
u UIBC(Unsatu rate d Iron Bi nd in g Cap a cit y) 42 V vit am i n A 176 vit am i n B12 249, 261 vit am i n E 235 X xanth i n oxid a se 22, 204 z Zn-c o rti co tr o p in 165
Zn-meta l loenzy m e 142, 158i 170, I74,I78 Zn-meta l loth i o n ein 145 Zn & ACTH 海 Zn & DNA 142, 158, 174 Zn & estr o g en 函 Zn & FSH 168 Zn & gon adotr o p in 167 Zn & LH 168 Zn & por ph y ri n meta b oli sm 142- Zn & pro g es te r on 函 Zn & pro sta g la ndin 169 Zn & RNA 142, 158, 174 Zn & tes to s te r one 167 Zn & Vi t. A 176
昇正子 독일 기센의 유스무스 리비히대학교 영양학과 졸업 同대학원 석사 및 박사 논문 Uber die Reg u lie r ung der a·Keto g l u ta r at -Dehyd rog en ase beim Huhn. 讐 Das Ernahrung s Beratu n g s Sy st e m EBS. 廳 의 30 여편 현재 숙명여자대학교 식품영양학과 교수 극미량원소의 영양 1984 년 3 월 20 일 인쇄 1984 년 3 월 30 일 발행 著 者 昇 正 子 發行人朴孟浩 發行處民音社 우편대 체 계 좌번호 010041-31-523282 , 누 IIO 서을 종로구 관철동 44 의 1 724-2000 • 724-4234 • 725-8524 출판등록 1966. 5. 19 1-142 값 6, 500 원 파본은 교환해 드립 니 다.
대_우학 술총서 자연과학 1 소립자와게이지 상호작용 김진의 2 動力 學特論 이병호 3 室素固定 송승달 4 相轉 移와臨界現象 키口 T亡처 己 5 觸媒作用 진종식 6 뫼스바우어分光 學 옥항남 7 극미량원소의 영양 승정자 8 水 素化湖素와 有機湖素化合物 윤능민 9 抗 生物質 의 全合成 강석구 10 국소적 형태의 Ati ya h_-S in g e r 지표이론 지동표 11 Mucop ol ys a ccharid e s 의 生化學 및 生物理學 빅l-준우 12 Astr o p hy s ic s 홍승수 13 天然物化學硏究法 우원식