 陳宗植
陳宗植  陳宗植
陳宗植
저자는 연세대학교 화학과 및 동대 학원을 졸업 하고, Clarkson Colleg e of Technolo gy에서 박사 학위를 받았다. 그리고 Univ ersit y of M i ch ig an 에서 연구원으로 재직했으며, 현재 서강대학교 화학과 교수이다.
 觸媒作用
觸媒作用
 觸媒作用
觸媒作用
머리말 가용성 전이 금속 착화합물(유기 금속 화합물 포함) 촉매 에 의 한 유 기화합물 합성온 현재 실험실이나 공장에서 활발히 전행되고 있다. 가용성 촉매에 의해서 일어나는 군 .일 촉매작용 (homo g eneous cata l ys i s ) 울 이용하여 생산되는 유기화합물은 양적으로 보아서 불균일촉매작 용 (he t ero g eneous ca t al y s i s) 에 의 해 서 생 산되 는 양보다 훨 싼 적 다. 그 러나 군일촉매작용의 중요성은 양적인 것보다는 다른 면에서 찾아 볼 수 있다. 군일촉매작용을 응용하는 유기화합물합성의 특성은역 시 선덱성 (selec ti v ity)을 충분히 활용한다는 접이다• 죽 높은 순도의 화합물을 높은 수율로 얻을 수 있다는 사실이다. 이러한 북성은 화 합물의 높은 순도가 필수적 으로 요구되는 제 약 또는 중합중간체 (po lym er i n t ermed i a t e) 제 둥에 중요하게 응용된다. 군일촉매작용은 단일상 죽 액체상에서 일어나므로 고체표면에서 일어나는 불군일촉매작용에 비교하여 쉽게 반응조건(온도 및 혼합 등)을 조절할 수 있을 분 아니라 실제촉매 (ac t ual ca t al y s t)를 분리, 확인하기가 비교적 용이하다. 따라서 군일촉매작용에 관한 화학은 불균일촉매에 관한 것보다 자세히 연구되어 왔다. 많은 경우에 상 세한 반응메카니즘이 알려졌으며, 현재도 활발히 연구되고 있다. 이어서 새로운 균일촉매계의 개발도 체계적으로 진행되고 있으며 앞 으로의 큰 발전이 기대되고 있다. 군일촉매작용의 연구로부터 얻은 결과가 불군일촉매작용의 이해, 발전 및 개발에 응용됨으로써 촉매 작용은 일반적으로 체계화될 수 있을 것으로 기대된다. 최근 발간되는 학부 고급학년 또는 초급 대학원생을 위한 고급무 기화학 책들은 대부분 전이금속 배위화합물(유기금속 화합물 포함) 촉매를 이용하는 군일촉매작용을 상당히 다루고 있다. 본 모노그래 프는 대학원생을 위하여 균일촉매작용의 이해를 위한 기초적인 베
위화학, 배위화합물의 반응, 그리고 군일촉매작 용 의 소개 및 그에 따른 알려진 반응메카니즘, 나아가서는· 현재 활발히 전행되고 있는 분야를 소개 하고자 하였 다. 군일촉매작용에 의한 유기화합물의 합성 이의에도 일산화탄소의 제거 목적으로 연구되는 〈일산화탄소의 산화반응〉, 에너지문제와직 결 되 는 〈수소생 산을 위 한 물분해 (wate r s plitti n g)반응〉, 수성 가스이 동 반응 (wa t er g as shif t reacti on ), 연료 제 조과정 으로 알려 진 Fis c her- Trop sc h 합성과정 둥 학술적인 면에서분 아니라 공업적인 면에서도 중요한 반응들을 알려전 반응메카니즘을 통하여 소개하고자 하였다. 본 모노그래프는 大宇財團의 학술연구비 지원을 받아 씌어전 것 이다. 처자는 大宇財團에 깊이 감사를 도리는 바이다. 1983. 2. 처 자
觸媒作用 차례
머리말 2제1장 觸媒作用과 관련되는 轉移金屬錯物의 化學1. 觸媒用에 이용되는 轉移金屬 92. 代表的인 리간드들 14(1) 시그마전자주게리간드 (σ-donor ligand) 14(2) 금속과 파이 錯物(π-complex) 을 형성하는 리간드 163. 金屬과 리간드의 상호작용 174. 轉移金屬錯物의 代表的인 반응들 27(1) 삽입반응(insertion reaction) 27(2) β-수소전달반응(β-hydrogen transfer) 30(3) 산화성첨가반응 (oxidative adddition)과 환원성 제거반응 (reductive elimination) 32(4) 리간드해리 및 상호교환반응(ligand dissociation and ligand exchange) 36(5) 산화 및 환원 (oxidation and reduction) 38제2장 올레핀의 반응들1. 올레핀의 配位 412. 수소화반응 (hydrogenation) 43(1) 二水素 (dihydrogen, H2)의 均衡分離(homolytic splitting) 反應메카니즘 49
(2) 二水素 (dihydrogen, H2)의 不均衡分離(heterolytic splitting) 反應메카니즘 57(3) 選擇性 및 立體特異性 (selectivity and stereospecificity) 633. 異性質化反應(isomorization) 68(1) 알킬금속 中間體를 통하여 일어나는 二重結合의 移動 69(2) 파이 -알릴금속 (π-allylmetal) 中間體를 통하여 일어나는 二重結合의 移動 71(3) 시스-트란스 異性質化反應 74(4) 炭素骨格 異性質化反應 (carbon skeletal isomerization) 754. 二合反應 (dimerization), 小重合反應 (oligomerization) 重合反應(polymerization) 76(1) 二合反應 (dlimerization) 78(2) 小重合反應 (oligomerization), 重合反應(polymerization) 855. 酸化反應 (oxidation) 93(1) Wacker 공정 93(2) 히드로과산화물에 의한 올레핀의 에폭시화반응 976. 올레핀의 상호교환반응 (metathesis) 99(1) 觸媒系 101(2) 熱力學的인 考察 102(3) 상호교환반응의 立體特異性 104(4) 반응메카니즘 (reaction mechanism) 105제3장 一酸化炭素를 包含하는 反應들
1. 酸化炭素의 配位 1132. 히드로포르밀화반응 (hydroformylation) 117(1) 反應조건 및 觸媒 117(2) 反應메카니즘 121(3) 디엔類 (dienes) 의 히드로포르밀화반응 129(4) 치환기가 있는 올레핀의 히드로포르밀화반응 131(5) 非對稱性 히드로포르밀화반응 (asymmetric hydroformylation) 1333. 카르보닐화반응 (carbonylation) 136(1) 메탄올의 카르보닐화반응 138(2) 올레핀의 카르복시화반응 1414. 탈카르보닐화反應 (decarbonylation) 146제4장 二室素 (dinitrogen, N2) 의 活性化1. 생물학적(미생물에 의한) 二登素의 活性化 151(1) 질소를 고정하는 미생물의 종류 152(2) 질소고정의 생성물 154(3) 질소고정에 필요한 조건 156(4) 질소고정의 메카니즘 1592. 轉移金屬 物에 의한 二 素의 活性 166(1) 二室素의 配位 169(2) 配位된 二室素의 反應 179제5장 기타 중요한 반응들
1. 일산화탄소의 산화반응 189(1) 일산화탄소의 활성화 (activation of carbon monoxide) 190(2) 일산화탄소와 산소의 반응, CO+½O2→촉매 CO2 192(3) 일산화탄소와 산화질소의 반응, CO+2NO→CO2+N2O 196(4) 일산화탄소와 물의 반응, CO+H2O→촉매CO2+S 2102. 일산화탄소의 수소화반응 2223. 물분해에 의한 수소발생 237제6장 전이금속 착물에 의한 균일촉매 작용의 경향1. 새로운 공급물질(feedstock) 2502. 선택성의 향상 (enhanced selectivity) 2543. 혼성 촉매 (hybrid catalyst) 2584. 새로운 촉매화학 262* 찾아보기 267
제 1 장 觸媒作用과 관련되는 轉移金屬 結物의 化學 대 부분의 均一觸 媒反應 순화과정 (homog e neous cata l yt ic reacti on c y cle) 은 유기금속화학이나 配位화학에서 찰 알려진 반응들이 적철히 합쳐진 것이다. 대표적인 반응들을 보면 다음과 같은 것이 있다. 죽, 리 간드의 배 위 (coordin a ti on ) 및 해 리 (dis s oc iat i on ), 산화성 첨 가받 옹 (ox i da ti ve addit ion ), 환원성제거 반응 (reduc ti ve eli m i n ati on ), 삽입 반 옹(i nser ti on reacti on ), 베 타수소 전달반응(/3 -h y d t o g en tra nsfe r ) 및 산 화一환원 (oxid a ti on and reducti on ) 등이 다. 이 장에 서 는 상기 반웅들 및 관련되는 화학결합 둥을 간단히 기술하고자 한다. 좀더 자세한 내 용은 대부분의 고급무기교재에서 다루고 있다 .1) 1. 觸媒作用에 이용되는 轉移金屬 이 책에서 취급하고자 하는 均一觸媒作用은 可溶性 전이금속착물 에 의한 촉매반응들이다. 이렇게 사용되는 전이금속은 부분적으로, 최 소한 하나의 산화상태 에서 , 전자들이 채 워진 d 구止 E 요함수를 갖고 있으며 이러한 d 국i]도함수는 에너지적으로 보아서 적은 분자들(예 를 들면 CH2=CH2, CO, N2, 02) 의 분자궤도함수들과 큰 차이를
1) a) F. A. Cott en , Advanced Inorga nic Chemi st r y , 4th Ed. , Wi ley -I nte r -sci en ce, 1980, p.1 049, b) R. P. Houg h to n , Meta l Comp le xes in Orga nic Che-mi st r y , Cambrid g e Univ e rsit y Press, 1979, p. 73.
갖고 있지 않다. 또한 d- 궤도함수의 수 ( 5 개) 또는 형태로 보아서 전이금속화합물의 다양한 반응성은 예측될 수 있다. 전이금속원자(f-궤도함수를 갖는 원자는 여기서 제의)는 1 개의 S 대]도함수, 3 개의 p-퀘도함수 그리고 5 개의 d- 궤도함수를 갖고 있 다. 이들 9 개의 궤도함수는 기하학적인 형태나 에너지적으로 보아 서 화학결합에 적합하여 1 개의 전이금속원자는 최고로 9 개의 리간 드와 결합할 수 있다. 예를 들면 레늄화합물, ReH1(PE t 2Ph)2( 여기 서 PEt 2P h 는 P(C2Hs)2(C2H s )2 이 다 ) 은 7 개 의 Re 一 H 결합과 2 개 의 Re_p 결합을 갖는 9 配位 착물이다 .2) 여기서 레늄이 갖고 있는 7 개 의 원자가전자 (valence elec t ron) 는 7 개 의 궤 도함수에 각각 1 개 씩 배치되어 7 개의 水 素 에서 내어 놓는 7 개의 전자와 함께 7 개의 Re ― H 共有結合울 형성한다. 2 개의 Re-P 결합은 2 개의 P 가 각 각 한쌍의 전자를 내어놓아형성되는 配位 結 合으로 설명된다. 이 레 늄착물은 예외적으로 높은 配位數를 갖고는 있지만 금속이온(또는 중성원자)이 리간드와 공유결합을 할 수 있으며 동시에 배위결합도 할 수 있음을 보여 준다. 이러한 접이 轉移金屬이 촉매로 자용될 수 있다는 長點이다. 전이금속에 배위됨으로써 리간드(예를 들면 일산 화탄소, 울레판 기타 여러 유기화합물)의 전자 분포는 달라지제 되 며 따라서 배위된 리간드는 화학적 활성을 갖게 되고 따라서 전이 금속에 리간드가 배위되는 과정을 리간드의 활성화 (ac ti va t i on) 라고 도한다. 전이금속의 배위화합물의 安定度 (s t ab ility)를 예측하기 위하여 사 용되는 간단한 규칙이 있다. 하나의 전이금속이 9 개의 의각궤도함 수 (ou t er orb it al) 를 갖고 18 개 의 전자를 수용할 수 있 다는 사실로부 터 소위 18 전 자규칙 (18 electr o n rµle) 또는 불합성 기 체 규칙 (ine rt gas rule) 이 유도되고, 이 규칙으로부터 금속착물의 안정도가 논의될 수 있다. 다시 말하면 금속의 원자가전자와 리간드가 제공하는(금 속과 배위결합을 하기 위하여) 전자수의 합이 18 이 되면 그 금속착 물은 안정하다는 규칙이다• Cr(C0)6 를 예로 들어 본다면, Cr(O) 운 6 개의 전자를, 그리고 6 개의 CO 는 12 개의 전자를 제공하게 되
—~ffey , J. Ch em. Soc. , A, 1963 (1969).
므로 모두 18 개의 전자가 Cr 원자 주위에 있게 된다. 여기에 Cr 가 내 각궤 도함수(i nner orb it al) 에 갖고 있 는 18 개 의 전자 (1s2 2s2 2p 6 3s2 3 p 6) 를 더한다 면 Cr 은 모두 36 게 의 전자를 주위에 갖게 되는 셈이 다. 이는 원 자번호 36 번인 안정한 불 활 성 기체 Kr 의 전자배치 (con fig ura t i o n ) 와 같게 되 는 것 이 다. 많은 경 우에 금속의 내 각전자의 수를 계산 하 지 않고 의각궤도 함 수를 채 우는 전자의 수만 논의된다. 즉, 광법위한 뷸앙 성기체 규 칙 보다는 l S 전자규칙으로 적용되는 경우 가 많다. 이 간단한 규칙 은 많은 單核 (rnononuclear) 또는 二核 (din u clear) 금속一카르보닐 (meta l carbon y l) 화 합 물의 안정 도룰 예 측하 는데 유용하다. 17 전자화합물인 V(CO)s 는 예외로 생각되어질 수 도 있지만 V ( C0)5 가 쉽게 환원되어 더욱 안정한 V(C0) 5 - 이온이 된다는 사 실 은 18 진자규칙을 지지하는예가된다. 이 규칙은 금속一 카르보닐 화 합물분만 아니 라 일반적 인 유기 금속화합물 (or g anome t a lli c com p ound) 에도 적용시킬 수 있다. 그 렇 게 하기 위하여서는 다음과 같은 일반적인 규칙이 필요하다. 단순한 共有결합을 이루는 클로로 (Cl ), 메틸 (CH3), 히드리도 (H) 와 같은 리간드는 1 개의 전자를 제공 하는 것으로 간주하고 한편, 아민 (am i ne), 일산화탄소 (CO), 포스핀 (ph osph in e), 니 트릴 (nltr i l e ) 및 올레 핀 (ole fi n) 등 配位결합을 하는 리 간드는 2 개의 전자를 제공하는 것으로 계산된다. 기타 리간드들은 다음과 감이 전자제 공능력 에 따라 정 한다. 죽 파이 -알릴 (rr- a llyl ) 및 니 트로실 (n it ros y l) 은 3 개 , 디 엔 (d i ene) 은 4 개 , 파이 -시 클로펜타 디 에 닐 ( n: -c y clo p en t ad i eny l) 은 5 개 , 그리 고 과이 一아렌 (rr-arene) 은 6 개의 전자를 제공하는 리간드로 간주된다. 화합물의 형식전하(fo r mal char g e) 는 총 전자수에서 빼어 준다. 예를 들면 V(CO)s- 에서 V 는 5 개의 원자가전자를 가지고 있고, 6 개의 co 가 12 개의 전자를 제공하여 17 개의 전자가 되는데 이 화합물은 하나의 음(_)의 형식 전하를 갖고 있기 때문에 11_ (一 1)=18 죽 18 전자화합물로 간주 될 수 있 다. NH4+ 또는 PF6- 동과 같은 반대 이 온 (coun t er i on) 은 금 속원자에 共有결합 또는 配位결합되어 있지 않기 때문에 전자수계 산에서 고려되지 않는다. 여러 다른 종류의 리간드를 포함하고 있는 착물에 관하여 전자수
의 계산과 그것의 안정도를 실례로 들어 보자. 히드로포르밀화반응 (h y dro fo rm y la ti on) 의 촉매 역할을 하는 것으로 알려진 RhH(CO)(Ph3 P)3 중에서 Rh 은 9 개의 원자가전자를 갖고 있고, CO 는 2 개의 전 자, 3 개의 Ph3P 는 6 개의 전자, 그리고 수소원자는 1 개의 전자를 각각 제공하므로 총 18 개의 전자가 Rh 주위에 있게 되므로 18 전자 규칙에 의하여 RhH(CO)(Ph3P)3 는 안정도를 갖는 착물로 예상된 다. 실제 이 화합물은 질소하에서 녹는 접 (172~174°C) 까지 가열하 여도 분해되지 않는다. 여기서 예상되는 안정도라 함은 중십금속에 관한 것이다. 대부분의 有機金昴化合物이 그러하듯이 로듐수소화물 은 수소를 칙 접 공격 할 수 있 는 찬전자체 (elec t ro p h il e) 나 자유라디 칼 (free radic a l) 등과 반응할 가능성 은 크다. 18 전자규칙은 실험적으뇨 얻어진 규칙이지만 이론적으로도 다음 과 같이 설명된다. 만일 금속이 가지고 있는 9 개의 결합궤도함~ (bondin g orb it al) 가 모두 채워졌다면 이 경우에 錢物은 배위적으로 포화되 었 다 (coord i na ti vel y sa t ura t ed) 고 한다. 이 러 한 착물에 천핵 체 (nucleo ph i le) 가 공격 한다떤 새 로 들어 오는 찬핵 체 의 전자는 에 너 지 가 높은 금속의 궤도함수에 아니면 反結合性分子軌道函數 (an ti bond ing molecular orb it al) 에 채 워 지 게 되 므로 반응은 일 어 나기 어 려 울 것 이다. 따라서 리간드 치환반응은 일반적으로 혼히 유기화학 반응에 서 논의되는 SNI 메카니즘과 같은 과정을 거쳐 일어난다. 죽 하나 의 리 간드가 먼처 해 리 되 어 배 위 결 핍 (coord i na ti on-de fici en t)착물을 형 성리하 간고드 이의 배해위 리 결一핍회착 합물 (d은 i ss o쉽c i a게 ti on다-a론sso 리ci a간 ti o드n) 와과 정반 으응로하게부 터된 다16.— 18 전 자규칙(1 6-18 electr o n rule) 이 생겨나게 되었다. 이 16-18 전자규칙 은 전이 금속착물의 反應性 (reac ti v ity)에 관한 규칙 이 며 , 이 규칙 은도 均一觸媒作用 (homog en eous ca t al y s i s) 의 반응경 로를 논의 하는 데 대 단 히 유용하다. 물론 예의적인 경우도 많이 있다. 자세한 내용은 이 책 전권을 통하여 종종 기술될 것이다. 16 ― 18 전자규칙은 근본적으로 다음과 같이 설명될 수 있다. 죽 하나의 촉매반응은 연속적으로 일어나는 리간드의 해리-회합의 ~ 정 으로 얻어 지는 중간체 (i n t ermed i a t e) 들을 갖게 되 는데 이 들 중간재
둘은 16 전자(해리과정으로 얻어지는 중간체) 또는 18 전자(회합과 정으로 얻어지는 중간체) 화합물들이라는 것이다. 간단한 예를 들 어 보자. Cr(C0)6 중의 2 개의 co 가 2 개의 Ph3P( 트리페닐포스핀)에 의 하여 치 환되 는 다음의 반응 (식 1. 1) 에 서 18-16 一 18-16 一 18 진 자착물의 형성을 볼 수 있다 .3)
 Cr(CO)s ——CO-+ Cr (C0)5—P h3-P+ C r(C0)5(Ph3P)
Cr(CO)s ——CO-+ Cr (C0)5—P h3-P+ C r(C0)5(Ph3P)
마지막으로 16 ― 18 전자규칙에 예의적인 예를 들어 보면 사각평 떤형 (sq u are pla nar) 로듐( I), 백금(]I) 및 금 (Ill) 착물을 들 수 있 다. 이 상의 전이 금속착물은 많은 경 우에 안정 한 (k i ne ti call y sta b le) 16 전자착물을 형성할 분만 아니라 리간드의 해리에 의하여 얻어지는 반응성 이 높은 14 전자착물도 생 성 시 킨다. 그 좋은 예 가 Wi lk in s on 촉매 라고 널리 알려 진 16 전자착물 RhCl(Ph3P)3 이 다. 이 착물에 서 Rh 과 3 개의 P 그리고 Cl 은 동일한 평면에 있음이 밝혀졌다 .4) Rh 과 Cl 사이에는 단순한 共有결합이 있고, Rh 과 P 사이에는 P 로 부터 제 공되 는 한 쌍의 전자에 의 한 配位결합이 있 다. Wi lki n s on 촉 매 의 높은 반응성 은 주로 RhCl(Ph3P)3 에 서 하나의 Ph3P 가 해 리 되 어 14 전자착물인 RhCl(Ph3P)2 가 쉽게 얻어질 수 있다는 접에 기 인된다 .5)
3) a) J. R. Graham and R. J. Ang el ic i, Inorg, Chem. 6, 2082 (1967). b) R. N. Perutz , J. J. Turner, et al. , J. Am. Chem. Soc. , 97, 4791, 4805 (19 75). 4) a) M. J. Bennett and R. B. Donaldson, Inorg. Chem. 16, 655 (1977). b) J. Reed and P. Eis e nberg, Chem. Commun. , 628 (19 77). 5) a) J. Halpe r n and C. S. Wong , Chem. Commun. , 629 (1973). b) C. A. Tolman, P. Z. Meakin , D. L. Lin d ner, and J. P. Jes son, J. Am. Chem. Soc. , 96, 2762 (19 74).
2. 代表的인 리간드들 리간드를 분류하는 방법은 여러 가지 있을 수 있으나 여기서는 금 속과 리간드 사이의 결합형태에 따라 리간드를 분류 설명하고자 한 다. 특히 이 책 2 장 ~5 장에서 인용될 리간드들의 성질을 살펴 보고 자 한다. 시 그마전자주게 리 간드 (a-donor l ig and) 와 금속과 파이 착물 ( 1r -com p lex) 을 형 성 하는 리 간드의 두 종류로 크게 나누어 기 술한다. (1) 시그마전자주게리간드 (a - donor liga nd) 배위되지 않은 상태에서 리간드는 결합에 참여하지 않는 하나 이 상의 전자쌍을 가지고 있으며, 이 전자쌍의 퀘도함수가 금속의 빈 궤 도함수 (em pty orb it al) 와 겹 침 (overla p)으로써 금속과 리 간드 사이 에 결 합을 형성할 수 있다면, 이러한 리간드는 시그마전자주게리간드 (6· donor lig and) 라 불리운다. 시그마전자주게리간드는 다음의 제 가지 로 다시 세 분된다. 죽 단순 시 그마전자주게 리 간드 (11-donor only) , 시 그마전자주게 겸 파이 전자주게 리 간드 (11-donor and ;r-d onor) 및 시 그 마전자주게 겸 파아 전자받게 리 간드 (11-donor and ;r -acce pt or) 로 세 분된 다 .6) 1) 단순 시 그마전자주게 리 간드 (a-donor only) NH3 및 H- 동과 같이 파이결합 형성에 필요한 궤도함수를 갖고 . 있지 않아서 금속과 결합할 때 오칙 시그마결합만 할 수 있는 리간 드를 단순 시그마전자주게리간드라고 한다. 각종 아민유도체 (R1Rz R3N) 또는 알킬카르보음이 온 (alky l carbanio n ) 둥과 같이 결합에 참 · 여하지 않는 한쌍의 전자를 갖고 있는 리간드들이 이에 속한다. 금 속과 리간드 사이에 오칙 한 개의 시그마결합이 이루어지므로 금속 -리간드 결합에 미치는 영향도 비교적 간단히 논의된다.
6) R. P. Houg ton , Meta l Comp le xes in Orga n ic C!t em i st r y , Cambrid g e Univ - ersit y Press, 1979, p, 3.
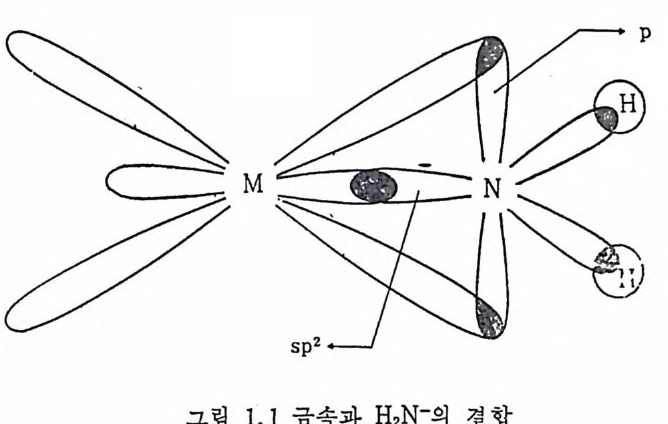
2) 시 그마전자주계 검 파이 전자주게 리 간드 (a-donor and rr-donor) 리간드가 전자쌍을 제공하여 금속과 리간드 사이에 시그마配位결 합을 형성할 분 아니라, 금속과 리간드 사이에 형성되는 파이결합 에 필요한 전자까지도 리간드가 제공하는 경우 이러한 리간드를 시 그마전자주게 겸 파이 전자주게 리 간드라고 한다. 예 를 들면 H2N- 가 금속에 배위될 때 시그마전자주게겸 파이전자주게로 작용한다. 混 成궤도함수를 이용하여 간단히 설명해 보면 다음과 같다. H2N- 온 그림 I. I 과 같이 두개의 궤도함수 sp2 및 p에 각각 한 쌍 씩 의 결합 에 참여 하지 않은 전자쌍을 가지 고 있다. H2N- 는 sp2 궤 도함수에 있는 한 쌍의 전자를 제공하여 금속과 시그마 配 位결합을 형성하고, p체도함수에 있는 한쌍의 전자를 제공하여 금속의 비어 있는 d- 퀘 도함수(또는 p예]도함수)와 파이결합을 형성한다(그립 1.1 ).
 p
p
리간드 내의 한 원자가 결합에 참여하지 않는 원자가전자를 두 쌍 이상 갖고 있는 리간드는 원칙적으로 시그마전자주게겸 파이전자주 게로 작용할 수 있다. 그러나 실제 위의 성질을 갖는 대부분의 리 간드들도 단순 시 그마전자주게 리 간드로 작용한다. 3) 시 그마전자주게 겸 파이 전자받게 리 간드 (a-donor and n:-a ccep - tor ) 리간드가 전자쌍울 제공하여 금속과 시그마配位결합을 형성하며,
동시 에 리 간드는 채 워 진 금속의 궤 도함수로부터 전자를 받아들여 리 간드와 금속 사이에 파이결합을 형성하면 이러한 리간드는 시그마 전자주게겸 파이전자받게리간드라고불리운다. CO 는대표적인시그 마전자주게겸 파이전자받게리간드이다. CO 는 탄소가 가지고 있는 결합에 참여하지 않는 전자쌍을 제공하여 금속과 시그마결합을 형 성하고, 금속의 d- 궤도함수로부터 전자를 받아들여 (CO 의 反結合 分子 淵 道函數 (an ti bond i n g molecular orb it al) 을 동하여 )금속과 파이 걸 합을 하므로 시 그마영 기 점 파이 산 (1e-a ci d) 이 라고도 불리 운다. 이 러 한 성질을갖는 CO 는이 책에서 가장많이 다루어질리간드중의 하나이 다. 다음철(제 1 장 3 철)에서 CO- 금속의 결합 및 그에 따론중요한 문제접 둥이 논의될 것이다. 일반적으로시그마전자주게이면서 파이 결합을 형성할 수 있는 빈 궤도함수를 갖고 있는 리간드이면 시그 마전자주게겸 파이 전자받게 리 간드로서 작용할 수 있 다. 예를 들면 N2, 02, P(CsHs)3( 트리페닐포스핀) 및 CsHsN( 피리단)등과 같이 금속 과 시그마配位결합을 할 수 있는 전자쌍도 가치고 있지만, 빈 反結 合分子軌道函數도 가지고 있어서 채워진 금속의 d- 궤도로부터 전자 를 받아 금속과 파이결합도 할 수 있는 리간드는 시그마전자주게겹 과이 전자받게 로 작용한다. 물론 결합되 는 금속의 酸化狀態 (ox i da ti on sta t e ) , 궤도함수의 對稱性 (s y mme t r y) 및 에너지상태 둥에 따라 리 간드의 파이전자받게 역할의 정도가 달라진다. 예를 들어 금속의 전 자밀도가 낮다면, 즉 酸化數 (ox i da ti on number) 가 높다면 리간드의 과이전자받게로서의 작용이 적어지게 된다. (2) 금속과 파이鑄物 (1r-com p lex) 을 형성하는 리간드 不胞和炭化水素 (unsa t ura t ed h y drocarbon) 는 불포화된 두 개 의 탄소 에 비 편재 화된 (deloca li zed) 파이 전자를 이 용하여 금속과 결합윤 형 성 한다. 여기서 금속은 결과적으로 두개의 탄소(때로는 그 이상의 탄 소〉와 결합하게 되는 셈이다. 리간드는 파이결합에 사용된 전자를 이용하여 금속과 결합하므로 이렇게 하여 생성된 銀物울 파이鉛物 이라고 하고 이러한 리간드를 파이銀物울 형성하는 리간드라고 한 다. 모돈 알켄 (alkene), 알킨 (alk y ne), 그리고 알릴음이온 (all y! anio n )
및 걸러 이중결합이 있는 리간드 (con j ug a t ed die n e), 방향족화합물 (aromati c comp o und), 시 클로펜타디 에 닐음이 온 (c y clo p en t ad i en y l anio n ) 둥이 이 부류에 속한다. 금속-올레핀의 결합은 시그마결합과 파이결합의 두 성분이 있다 고 설명된다. 즉 탄소-탄소의 이중결합을 형성하는 채워진 파이걷 합궤 도함수 (1r-bond i n g orb it al) 와 금속의 빈 궤 도함수가 겹 침 으로 생 기는 시그마결합과, 채워진 d 레]도함수와 빈 올레핀의 파이反 結 合 軌道函數 오려 겹침에 의한 과이결합이다. 이러한 접에서 보면 올레 핀은 시그마전자주게겸 파이전자받게의 역할을 하지만 올레판은 시 그마결합을 하기 위하여 파이전자를 제공한다는 접이 시그마전자주 게겸 파이전자받게리간드와 다른 접이다. CO 와 마찬가지로 올레편도 이 책 전권을 통하여 중요하게 다루 어질 것이므로 금속과 올레핀의 결합에 관하여서는 다음(제 1 장 3) 에 서 자세히 설명하고자 한다. 3. 金屬과 리 간드의 상호작용 촉매작용에 전이금속착물이 유용함은 전이금속이 5 개의 d 구!]도 함수를 갖고 있을 분 아니라 d- 궤도함수는 그 對稱性도 또한 다양 하기 때문이다. d 데도함수는 금속과 리간드원자간의 軸 (ax i s) 과 방 향이 같을 수도 있 고(예 를 들어 df- y’ 및 d,’), 금속과 리 간드원자 간의 軸 과 軸 사이 의 (예 를 들어 d,,,, d” 및 d,,) 방향을 가질 수도 있다. 분만 아니라 5 개의 d 대1 도함수와 3 개의 p구]도함수와 1 개 의 s 레]도함수가 이루는 混成 軌 道函 數 는 더욱 다양한 모양과 다양 한 방향을 제공한다. 이렇게 다양한 금속의 퀘도함수는 여러 종류 의 리간드와 여러 가지 방법으로 작용하기 때문에 전이금속은 다양 한 반응성을 갖고 있으며 또한 촉매작용을 하게 된다. 금속원자와 알킬기 , 수소 및 할로겐과 같은 리 간드 사이 의 共有 (covalen t)결합은 유기화합물에서 혼히 보는 공유결합과 같게 취급되 므로 더 이상 자세히 논의될 필요가 없다. 그러나 리간드의 分子軌 道函數 (molecular orb it al) 와 금속의 原子軌道函數 (a t om i c orbit al ) 사이
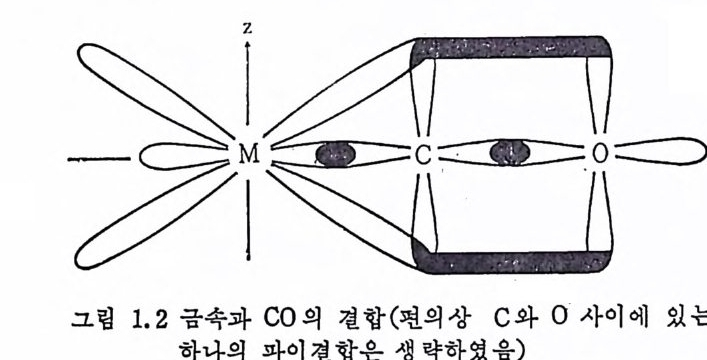
의 配位결합은 유기화합물의 공유전합과는 커다란 차이가 있다. 이 러한 접둘을 금속과 CO 와의 결합, 금속과 N2 와의 결합 그리고 금 속과 올레핀의 결합을 예로 들어 자세히 설명하고자 한다. 먼저 금 속 -co 의 작용을 살펴본다. 많은 수의 전이금속一 co 화합물이 지 금까지 알려진 반면, 主族 (ma i n g rou p)금속의 co 화합물은 하나도 알려쳐 있지 않다. 그 이유는 co 가 파이전자받게리간드로 작용하 여 소위 逆結合 (back bond i n g)을 할 수 있 다는 접 이 다• 전이 금속은· CO 와 시그마결합을 할 수 있을 분 아니라 체위전 d- 궤도함수를통 해서 co 의 퀘도함수와 파이결합을 형성할 수 있다. 그러나 主族금 속 은 파이결합을 할 수 있는 d- 전자를 갖고 있지 않다. co 가 한개의 금속에 배위되어 있을 경우에 (2 개 또는 3 개의 금 ` 속사이에 다리 리간드로 작용하는 경우는 약간 다를 수도 있음),금 속과 co 간의 파이결합은 금속의 d- 궤도함수와 co 의 反結合分子軌 하道지函 數만, ( ”an t原i bo子nd價 i n結g 合mo理le論cu l(avra loernbc iet a l)b 의on d겹 침t h e(oorv yer)la으 p로) 으도로시 설 하명면되 기그 림도 I. 2 에서 보여주는바와 같이 co 리간드에서 이미 C 와 0 사이에 파 이결합을 하고 있는 C 의 2 p예]도함수와 금속의 d- 궤도함수의 겹침 으로 금속 -co 간의 파이결합이 일어난다. 금속과 co 사이의 시그마결합과 파이결합은 상호보강작용 (s y ner gist i c i n t erac ti on) 을 하게 된다. 예를 들어 시그마결합은 파이결합에
 ZeM
ZeM
7) F.A. Cott en and G. Wi lki n s on, Basic Inorga nic Chemi st r y , Wi ley - I nte r - scie n ce 1'51 6 , p. 479.
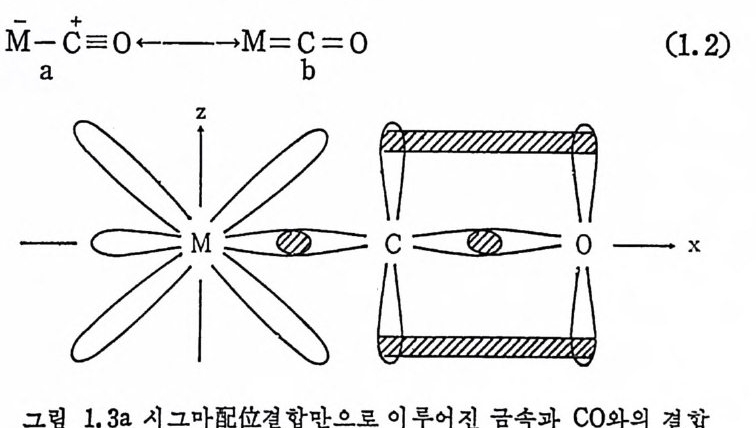
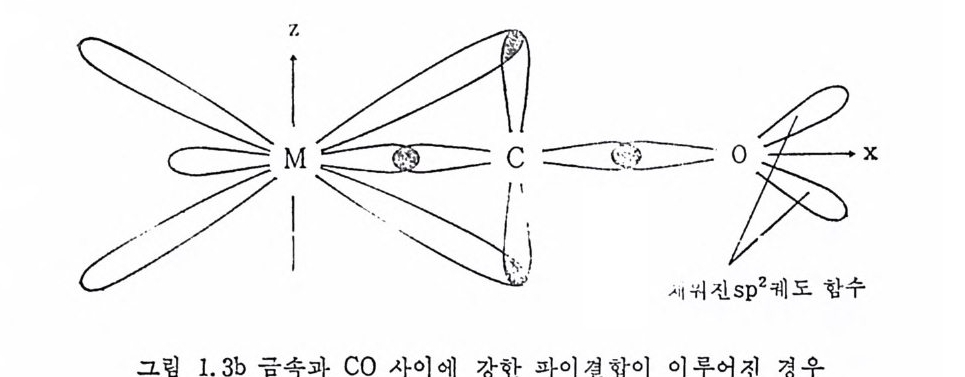
의해서 보강된다. 왜냐하면 시그마결합은 co 가 전자를 제공하여 이루어지는 配位결합이므로 co 의 전자밀도가 높을수록 강해질 것 이며, 한편 파이결합은 금속에서 CO 로 逆提供 (back dona ti on) 되는 전자에 의한 결합이므로 파이결합이 형성되면 co 의 전자밀도는 높 아지게 되기 때문이다. 같은 이유로 금속 -co 의 시그마결합은 금 속 -co 의 파이 견합을 보강하게 된다. 다시 말하면 금속 -co 간의 총결합의 강도는시그마결합이나파이결합이 각각따로 존재할때 그 것들의 합보다도세다는 뜻이다. co 보다 더욱센과이전자받게로서 는 PF3 와 CS 등을 들 수 있으나 co 보다는 널리 연구활용되지 않 고 있다. 그림 1. 2 에서 보여 준바와같이 금속카르보닐화합물 (M co) 에서 금속과 co 간의 과이결합은 탄소의 p케]도함수를 사용하 므로 금속과 co 간의 파이결합에 의해서 co 의 결합은 약해질 수 밖에 없다. 따라서 逆結合 (back bond i n g)의 정도가 증가할수록 탄소 와 산소의 결합은 약화되어 結合次數 (bond order) 는 3 에서부터 2 로 감림 소1.될 3 a 수는도 금 속있다과. c그o 국사단이적에인 파 예이를결 합그이림 형1.성 3 되에지서 보않여은 그준다림.이 며그 그림 1. 3b 는 금속과 co 사이의 파이결합이 강하게 형성되면서 CO 중의 탄소와 산소간에 있었던 파이결합이 꿇어전 그림이다. 이상 의 내 용은 다음과 같은 共鳴構造 (resonance str u ctu re) (식 1. 2) 로서 표현될 수도 있다. 여기서 CO 와 결합 전의 금속 M 의 산화수는 0 (zero valen t)이 다. 공명 구조 a 는 금속
 M- a- C+ 三 O+ ---—- M= Cb = O (1. 2)
M- a- C+ 三 O+ ---—- M= Cb = O (1. 2)
 z
z
과 co 사이에 시그마配位결합만 형성되었을 경우이며 그림 1. 3a 에 해당되는구조이다. 공명구조 b 는 금속과 co 사이에 파이결합이 강 하게 촌재할 때이며 그림 1. 3b 에 해당되는 구조이다. 逆結合이 전자밀도의 변화를 가져오기 때문에 配位된 리간드의 반 응성에 변화를 가져오게 된다. 따라서 금속착물에서 역결합의 정도 에 영향을 주는 것들을 살펴볼 필요가 있다. 금속과 CO 사이에 형 성되는 파이걷합의 정도는 위에서 언급한 바와 같이 C-O 사이의 c結o合 의次 數신 (축bo전nd동 i n수 g o(rs dt reer t) c 를h i n g 살fr펴e q 보 ue면nc y알)는 수 2 1있55 다c.m 一 즉1 인 데배 위배 되위 지된 않 C은O 의 신축전동수는 얼마나 감소되었는가에 따라 금속 -co 간의 逆結 合의 정도가 논의된다(여기서 주의해야 할 접은 금속 -co 간의 과 이결합 이의에 CO 의 신축전동수에 영향을 줄 수 있는 것들도 조십 스럽게 고려되어야 한다).지금까지 알려진 바에 의하면 逆結 合의 정 도에 영 향울 주는 인자들은 금속의 전자배 치 (electr o nic confi gu rati on ), 금속의 산화상태 (oxid a ti on sta t e ) 및 금속에 배 위 되 어 있 는 다론 리 간드의 성 질 (전자적 및 입 체 화학적 (ste r eochemi ca l)) 둥이 다. 일 반적 으로 금속이 음전하 (ne g a ti ve char g e) 를 가지고 있으면 逆결합은 중 가하고 co 의 신축전동수는 감소한다. 어 떤 하나의 금속에 관하여 보면 산화상태가 가장 낮을 때 逆 結 合의 정도는 가장 높을 것이 다.
같은 전자배치를 갖는 금속들에 관하여 보면 착물의 음전하가 증가 함에 따라 逆緖 合도 중가한다. 예를 들면 dlO 의 전자배치를 갖는 다 음의 착물들의 co 신축전동수로부터 위의 사실을 볼 수 있다. 또한
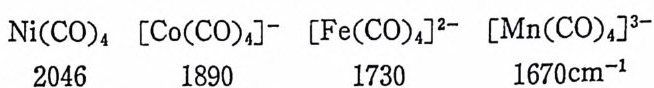 Ni (C 0)4 〔 Co(CO) 』- 〔 Fe(CO) 』 2- [Mn(CO) 』 3-
Ni (C 0)4 〔 Co(CO) 』- 〔 Fe(CO) 』 2- [Mn(CO) 』 3-
금속의 전자밀도를 증가시키는 리간드가 금속에 배위되면 금속 -CO 간의 逆 結合의 정도가 중가될 것이다. 예를 들면 co 가 co 보다 센 시그마전자주게이며 동시에 co 보다 약한 과이전자받게인 리간 드로 치환되면 逆結合의 정도가 증가할 것이다(아태의 예들을 참조 할 것). 비슷한 이유로 할로겐의 리간드가 촌재할 때 逆결합은 시
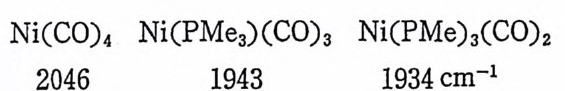 Ni (C 0)4 Ni( P Me3)(C0)3 Ni( P Me)3(C0)2
Ni (C 0)4 Ni( P Me3)(C0)3 Ni( P Me)3(C0)2
그마전자주게 의 세 기 에 영 향을 받는다. 예 를 들면 PtX (CO)(dip yri - d y l) 에서 X 가 Cl, Br, 및 I 일 때 co 의 신축전동수는 각각 2145, 2132 및 2120 cm-1 으로 알려 졌 다. 물론 금속의 전자밀도를 감소시키는 파이전자받게리간드가 금속 에 배위되어 있으면 금속― co 간의 逆結合의 정도는 감소하게 된다. 특히 CO 와 트란스위치에 파이전자받게리간드가 배위되면 그립 1.4
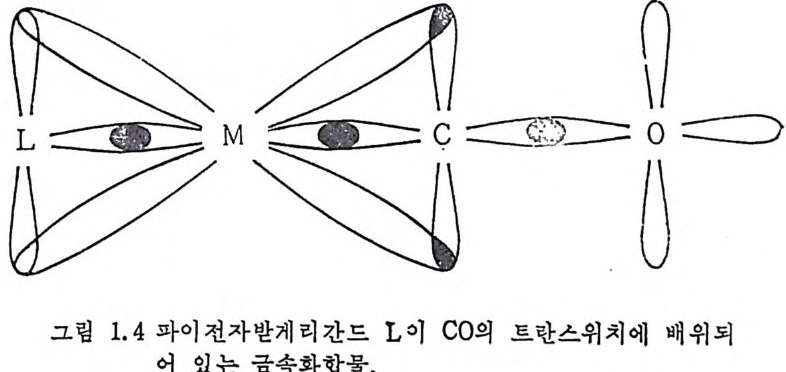 그림 1.4 파이전자받게리간드 L 이 co 의 트란스위치에 배위되
그림 1.4 파이전자받게리간드 L 이 co 의 트란스위치에 배위되
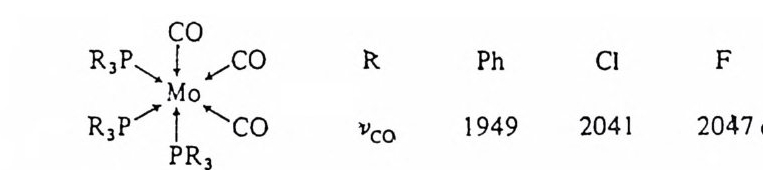 R3P'-... c!o ✓ co R Ph Cl F
R3P'-... c!o ✓ co R Ph Cl F
와 같이 CO 와 파이결합을 하게 되는 금속의 d- 궤도함수는 파이전 자받게리간드 L 과도 파이결합을 하게 되므로 금속의 해당 d 구i]도 함수를 통한 CO 로의 逆結合의 정도는 감소하게 된다. 예를 들면 위의 6 배위체 Mo(O) 鎔物에서 3 개의 CO 는 모두 포스핀에 대하여 트란스위치에 배위되어 있다. 포스핀의 P 는 빈 3d 궤도함수를 갖고 있어서 포스핀은 파이 전자받게 리 간드로 작용한다. 포스핀의 파이 전 자받게리간드의 강도는 R 의 전기음성도에 영향을 받게 된다. 죽 전 기 음성 도의 순서 (Ph
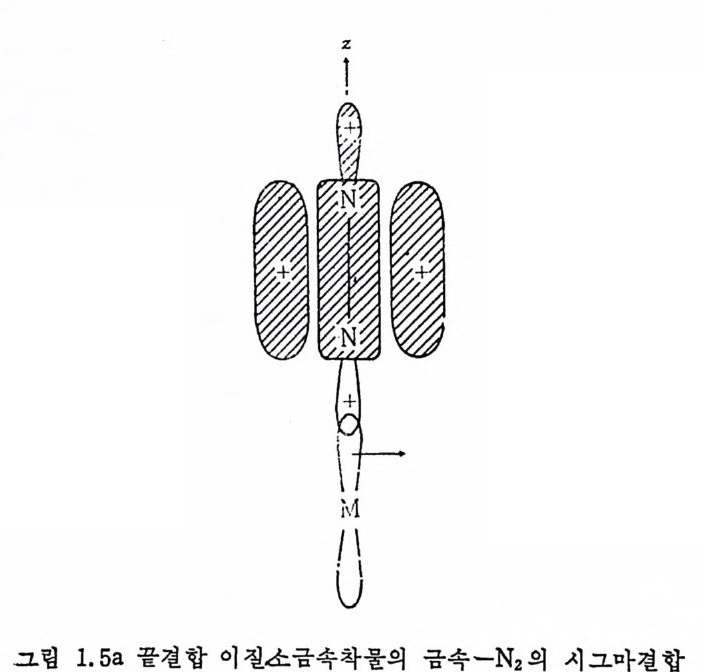
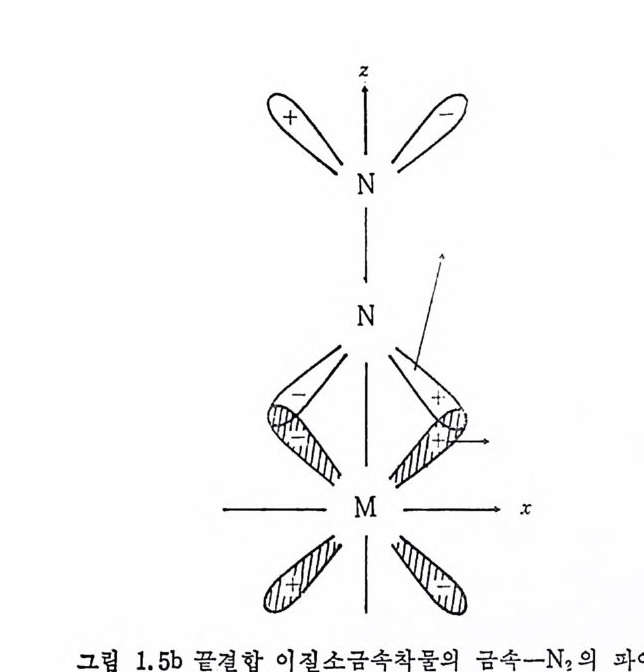
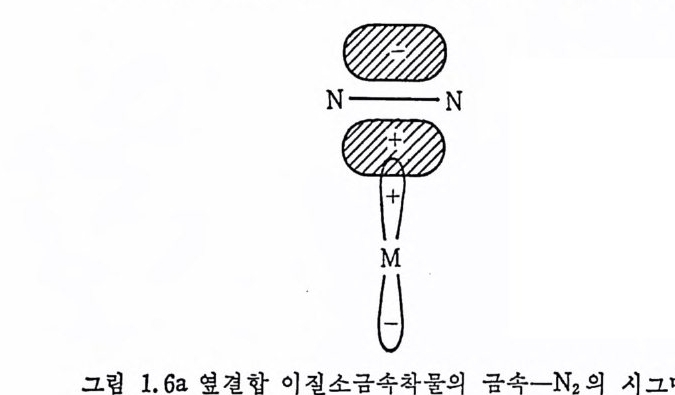
어 있는 co 보다 높은 신축전동수를 보여 준다는 사실은 P(OR)a 가 PR3 보다 더욱 강한 과이전자받게이기 때문이 아니고 PR3 가 P(OR)3 보다 더욱 효과적인 시그마전자주게라는 이유로 설명된 다. 질소분자는 일반적으로 非活性기체로 알려쳐 있으나 최근에는 많 온 안정 한 이 질소 (d i n it ro gen) 금속화합물이 합성 되 었 다. N2 가 금속에 배위되는 방법은 하나의 N 원자를 통하여 형성되는 끝결합 (end-on .b ond i n g)과 두 개의 N 원자가 모두 결합에 참여하는 옆결합 (s i de-on bond i n g)으로 나누어 진다. 끝결합 이 질소금속화합물의 경 우 그림 1. 5a 에서 보여 주는 바와 같이 빈 금속궤도함수는 채워진 N2 의 퀘도 함수로부터 전자를 받아서 시그마결합을 하게 되며, 그림 1.5b 에 서 보는 바와 같이 N2 의 反結合軌道函數(검 CP ) 는 채 워 진 금속의 d- 퀘 도함수로부터 전자를 받아 파이결합울 하는 것은 금속 -co 의 경우 와 비슷하다. 옆결합 이질소금속화합물의 경우 그림 1. 6a 에서 보는 바와같이 금속의 빈 궤도함수는 N2 의 채워진 파이궤도함수로부터
 z1
z1
 \Z-N/
\Z-N/
 른
른
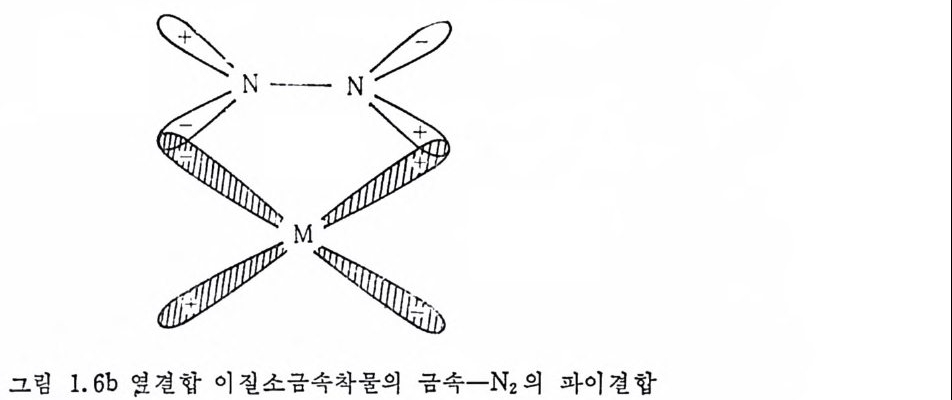
전자를 받아 사그마결합을 하고 그림 1. 6h 에서 보는 바와같이 반 N 거 反結合軌道函數는 채 워진 금속의 d 퀘도함수로부터 전자를 逆 提供받아 파이견합울 한다. 끝결합 이질소금속착물의 구조는 X- 선 회철을 이용한 結晶구조 조사에서 밝혀져 있지만 ,8) 옆결합 이질소금 속착물은 현재까지 여러 번 논의된 바 있으나 실제 X- 선 회절에 의 6) D. Thorn, T.H. Tuli p and J.A . lbers, J. Chem. Soc., Dalt on . 2022 (19 79).
 /\
/\
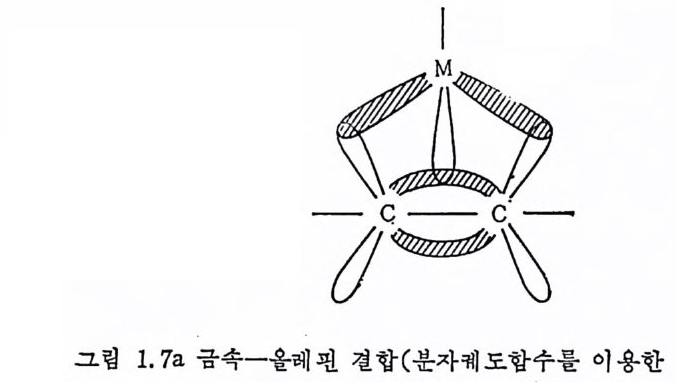
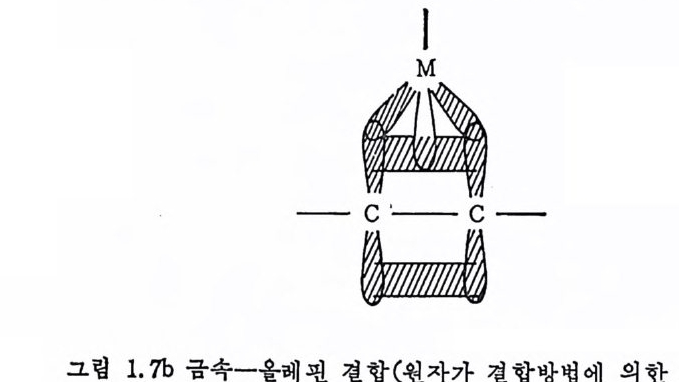
한 구조결정이 발표된 적은 없다. 이질소는 끝전합을 할 때나 옆결합을 할 때나 모두 co 처럼 시 1 마전자주게겸 과이전자받게로 작용한다. 따라서 금속一 N2 의 결합은 금속― CO 와 비 슷하게 다루어 진다. 같은 이 유로 금속-알킨 (alk y ne) 결합도 비슷하게 다루어진다. 마지막으로 금속과 올레핀의 결합을 살펴본다. 금속-울레핀 결 합도 금속― CO 및 금속 _N2 결합과 동일하게 시그마결합과 과이걷 합으로 설명된다. 그림 1. 7a 에서 보는 바와 같이 C 와 C 간의 채 위진 파이결합 퀘도함수와 금속의 빈 궤도함수가 겹침으로 시그마 결합이 형성되고, 금속의 채워진 궤도함수와 올레핀의 反結合分子 軌道函數가 겁침으로 파이결합이 이루어진다. 그림 1. 7b 는 원자가· 결합방법 (valence bond me t hod) 으로 금속一올레 핀의 결합을 표현한 것이다. 여기서는 빈 금속의 궤도함수가 두 개의 C 사이에 파이결 합을 이루는 2 p궤도함수와 겹침으로 금속一올레펀 사이의 결합 이 형성됨을 보여 준다. 그림 1. 7b 에서 금속의 d 궤도함수와 C 의 2p 퀘도함수의 겹침이 증가할수록 C 와 C 사이의 과이결합은 약화됨을 E 볼 수 있다. 이러한 이유로 다음과같온 두개의 공명구조(식 1. 3) 로 금속一올레핀의 결합을 표현할 수 있다. 즉 올레핀이 금속에 배위 되므로 올레핀의 C 와 C 사이의 결합은 약해지고 거리는 멀어지게 된다. 이러한 현상온 그림 1. 7a 로서도 설명될 수 있다. 죽 올레핀 의 反結合分子軌道函數가 금속으로부터 전자를 많이 받을수록 올레
 M.. -\|`Ic / M \/\c|, /',’? (1. 3)
M.. -\|`Ic / M \/\c|, /',’? (1. 3)
핀의 C ― C 결합은 약해져서 C ― C 거리가 멀어지고 두 탄소의 혼성 궤도는 s p 2 로부터 s 균에 가깝게 된다. 일반적으로 금속-울레핀착 물의 逆結合의 정도가 증가하여 C ― C 간의 결합이 약해지는 경우는 다음과 같다. 즉 금속의 상화상태 (oxid a ti on s t a t e) 가 낮을 때 , 금속 에 강한 시그마전자주게이며 약한 파이전자받게리간드가 배위되어 있을 때, 그리고 올레핀에 전자를 끄는 (elec tr on · w it hdraw i n g) 치환기 가 있을 때 등이다.
 d
d
 —白皇 —
—白皇 —
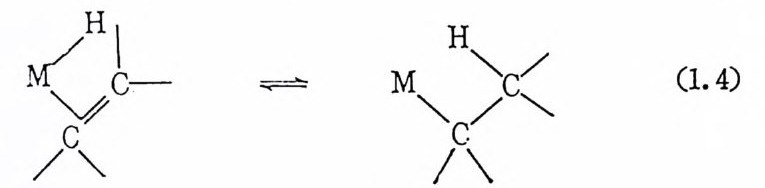
4. 轉移金屬鎖物의 代表的인 반웅들 전이 금속착물에 의 한 균일촉매 작용의 순환과정 (cata l yt ic c y cle) 은 갇 알려진 유기금속화합물(또는 전이금속의 배위화합물)의 여러 반 웅들이 합쳐진 것이다. 따라서 실제 촉매작용의 메카니즘을· 논의하 기 전에 찰 알려 진 반응들을 우선 고찰하고자 한다. (1) 삽입 반응(i nser ti on reacti on ) 삽입 반웅(i nser ti on reac ti on) 은 올레 핀의 촉매 화학에 서 가장 널리 인용되는 반응이다. 대표적인 예를 들면 아래 식 (1. 4) 과 같이 금
 二/'(_ 4 F M.\ ICH/ \- c\~ (1. 4)
二/'(_ 4 F M.\ ICH/ \- c\~ (1. 4)
속-수소결합에 올레핀이 삽입되는 반응이다. 삽입이타고 표현하기 보다는 수소의 이동 (m ig ra ti on) (금속으로부터 탄소로)이 더욱 적철한 표현이 다. 이 반응의 逆 反 應 (reverse reac ti on) 은 ¢一누소제 거 반응(fi· hy d rog e n eli mi na ti on ) (또는 B- 수소전달반응, ft-h y d rog e n tr ans fe r) 으 로 다음(제 1 장 4, (2) )에 서 기 술된다. 지금까지 알려 진 모든 삽입 반응 은 올레판, co 등 불포화된 기질 (subs tr a t e) 이 먼처 금속에 배위되고 난다음 일어난다.” 이동되어 가는 H-, R_, 또는 OH- 등도대부분 의 경우에 금속에 우선 배위된 다음 이동되어 가지만 반드시 배위될 필요는 없다. 올레핀의 삽입반응은 위에서 보여 준 것처럼 금속一·수소결합에 삽 입되는 반응이 가장 찰 연구되어졌고, 다음으로는 금속―탄소결합 에 올레핀이 삽입되는 반응으로서 올레핀의 중합반응에서 중요시되 고 있는 반웅이다. CO 의 삽입반응은 금속一탄소결합에 대하여 찰
9) F. Calderazzo, Ang e w . Chem. Int. Ed. , 16, 299 (19 77).
일어나지만 금속-수소결합에 삽입되는 예는 알려져 있지 않다. 금 · 속―탄소결합에 co 가 삽입되는 반응은 그 반응메카니즘도 찰 알려 쳐 있다. 예를 들면 메틸카르보닐망간착물의 삽입반응에서 아래 식 (1. 5) 과 같이 생성물 중의 아세틸기는 최초에 co 가 배위되어 있던
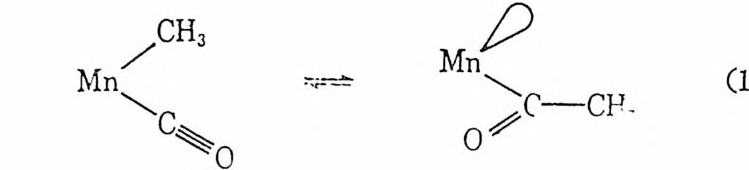 Mn \/ CH3 ,:;--~ Mn /\ )C -CP- (1. 5)
Mn \/ CH3 ,:;--~ Mn /\ )C -CP- (1. 5)
위치에 배위되어 있음이 알려졌다 .9),10) 다시 말하면 메틸기는 배우 I 된 co 의 탄소로 이동되어간 것이다. 逆反 應 에서는 배위된 아세틸 기로부터 메틸기는 떨어쳐 나가 먼저 배위되었었던 빈 자리로 둘 ~ 아가는 것 이 알려 졌 다. 9),10) 그러면 여기서 올레핀의 삽입반응의 메카니즘을 먼저 살펴보고이 어서 co 의 삽입반응을 살펴 본다. 올레핀의 삽입반응은 금속―탄소결합에 삽입되는 단계와 금속― 수소결합에 삽입되는 단계로 나누어진다. 이 두 단계는 예를 듈 어 이 합반응 (d i mer i za ti on) 이 나 중합반응(p ol y mer i za ti on) 에 서 아래 (식 1. 6) 와 같은 차례로 일어난다. 죽 M-H 에 C=C 의 삽입이 먼
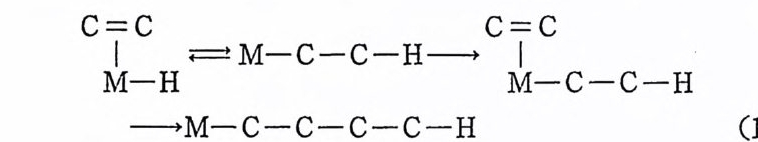 C=I C .=t M-C 一 C ― H 一 C=I C
C=I C .=t M-C 一 C ― H 一 C=I C
처 일어나고 이어서 M-C 에 C=C 의 삽입이 일어나며 C=C 의 삽입은 계속되어진다. 올레핀의 삽입반응은 군일촉매작용에서 중요함에도 불구하고 그 도 반응메카니즘에 관하여서는 찰 알려져 있지 않다. 지금까지 알려 Xi 실험결과와 최근에 보고된 分子軌道계산 11) 에 의하면 다음과 같은서-
10) K. Noack and F. Calderazzo, J. Orga nomet. Chem. , 10, 101 (1967). ID D. L. Thorne and R. Hof fm an, J . Ani. Chem. Soc. , 100, 2079 (19 78).
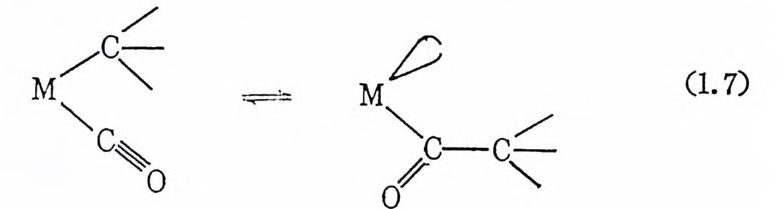
실을 추측할 수 있다. 첫째로, 삽입반응은 금속에 배위된 H 또는 C( 예를 들면 알컬기)가 C=C 의 한쪽 C 에 이동되는 과정이다. 따 라서 이 반응은 이 동적 인 삽입 반응 (m ig ra t or y i nser ti on) 이 라고 표현 하는 것이 적절하다. 물론 이상의 사실을 증명하려면 올레핀의 삽 입에 의해서 형성되는 금속―알킬 중의 알킬기의 위치가 처음에 울 레핀이 금속에 베우]되었던 위치와 같음을 보여 주어야 하지만 현재 까지 분명히 밝혀진 적은 없다. 둘째로, 올레핀은 삽입반응이 일어 나기 전에 일단 금속에 배위된다. 묵히 금속―수소결합의 시스 위 치에 배위된다. 몇몇 올레핀의 중합반응의 메카니즘에서는 올레핀 이 금속에 배위될 필요 없이 직접 금속―단소결합에 삽입된다고 제 시된 적도 있다. 세째로, 울레핀의 삽입반응은 쉬운 可逆反應이 다. 죽 금속에 배 위 된 알킬기 로부터 /3-수소의 전달반응(/3 -h y dro g en t rans fe r) 이 쉽 게 일어 난다(알킬기 의 전달반응은 비 교적 드물다). /3- 수소의 전달반응이 비교적 용이하다는 사실은 금속―알킬착물이 불 안정하다는 뜻이다. 따라서 /3-수소를 갖지 않는 금속-메탈, 금속 -벤질 (benzy l) 또는 금속—네 오펜털 (neo p en ty l) 착물은 금속―에 틸착 물보다는 안정하다 . . co 의 삽입반응도 아래의 석 (1. 7) 에서 보는 바와 같이 알킬기의
 M\ /cc`E° 겨 •• M。\/ / > c ― c\ 乙 (1.7 )
M\ /cc`E° 겨 •• M。\/ / > c ― c\ 乙 (1.7 )
이동반응이라고 표현하는 것이 더욱 적절하다. 이 반응의 逆反應은 脫카르보널반응 (decarbon y la ti on) 이 라고 불리 운다. 이 逆反應은, ~ 알킬 기가 있던 자리에 배위될 또다론 리간드가 촌재하지 않는 한, 쉽게 진행된다. co 의 삽입반응은 상당히 반응성이 큰 불안정한 중간생 성물의 형성과정을 거쳐 일어나기 때문에 자세한 메카니즘 연구에 는 상당한 난접이 있는 것으로 알려쳐 있다. 자세하게 연구된 실례 로는 앞에서 소개했던 메틸펜타카르보널망간 (I)(CH3Mn(CO)s) 의 반응을 들 수 있다 .9),10) 이 정팔면체 망간 CI) 착물은 13C0 과 다음
(식 1. 8) 과 같이 반응한다. 과량의 13co 존재하에서도 아세틸기는
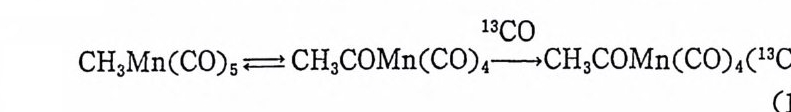 13CO
13CO
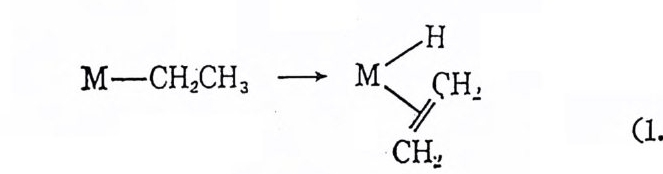
13CO 를 포함하지 않는다. 이 실험의 결과로부터 메틸기는 금속에 이미 배위되어 있는 co 에 이동됨을 알 수 있다. 즉 “co 가 CH3- Mn 결합에 삽입되는 것은 아니가 최초로 생성되는 아세틸펜타카르 보닐망간( I ) CH3C0Mn(CO)l13CO) 에 서 아세 틸기 는 13co 의 시 스 위치에 있다. 이 사실로부터 메틸기가 배위되었던 위치는 13C0 이 배 위되기 전에는 비어 있었던 것을 알 수 있다. 최초로 생성된 시스 아세탈펜타카르보닐망간 CI )착물은 co 의 해리 (dis s oc iat i on ) 및 再會 合 (reasso ci a ti on) 에 의한 이 성 질화반웅(i somer i za ti on) 에 의 해서 일부 분 트란스 이성질체로 바뀐다. 이와 같은 CH3 및 co 의 삽입 및 이 동반응은 分子軌道函數계산법에 의해서도 예측된 바 있다 .11) (2) p-수소전달반응(p -h y dro g en tra nsfe r) }수소전달반응은 g-수소제 거 반응 (P-h y dro g en el i m i na ti on) 이 라고 도 불리 운다. 앞에 서 (제 1 장 4(2)) P- 수소전달반응은 올레 핀 삽입 반응 (M-H 에 삽입되는 반응)의 逆反應이 됨은 이미 기술한 바 있 다 .• g-탄소에 수소를 가지고 있는 유기리간드를 배위하고 있는 전이 금속착물은 아래 식 (1. 9) 과 같이 B- 탄소의 C-H 결합이 끊어 지고 M -H 결합과 올레핀이 생성되는 반응을 일으킨다• 이러한 B- 수소전달 반옹은 대부분 可逆反應이다. 배위과정을 거치는중합반응 (coord i n~ tive p ol y mer i za ti on) 에 서 는 p-수소전달반응이 중합체 의 분자량을 걷
 M-CH2CH3 一 M /\eCHHH '-
M-CH2CH3 一 M /\eCHHH '-
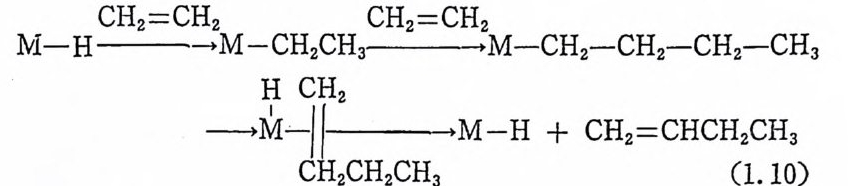
정한다. 예를 들여· 아래의 식(1. 10) 과 같이 두 개의 올레핀이 삽입 된 다음 B- 수소전달반응이 일어 나면 울레 핀의 二合盤 (d i mer) 가 생 성 된다. 금속아 ¢―수소를 끌어 당기 는 정 도는 금속의 종류, 금속의 산 화상태 및 리 간드의 종류에 따라 다르다. 12)
 CH2=CH2 CH2=CH2
CH2=CH2 CH2=CH2
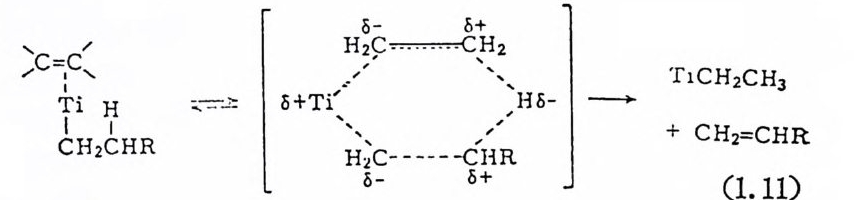
8- 수소전달반응은 금속의 配位圈 (coord i n ijti on s p here) 내에 새로운 리간드가 배위될 수 있는 빈 자리 (vacant s it e) 가 있는 경우에만 일어 난다. 이러한 사실은 식(1. 9) 에서 보여 준 것과 같은 고리형 전이성 태 (tra nsit ion s t a t e) 의 형 성 을 지 지 해 준다. 과량의 울레 핀이 존재 할 때 식 (I. 9) 와는 다른 반응메카니 즘이 제 시된 바 있다. 예를 들면 티탄착물을 촉매로 하는 에틸렌의 소중합 반응 (ol ig omer i za ti o p.)연구에 서 8- 수소전달반응은 二分子過程 (b i mole cular p rocess) 을 거 찬다고 제 시 하였 다. 13) 즉 식 (1. 11) 과 같이 금~
 /, ' C_=TC_,’IC H i /\ 2HCI H R :..:-=:...!: 5+Ti/ . HH.` / `’52 i` C¢- -· ·-· ·-·- ··-··-CC8 +/`HH /` `2’R ’` H 5- ) +T 1CCHH22C=HC3H R
/, ' C_=TC_,’IC H i /\ 2HCI H R :..:-=:...!: 5+Ti/ . HH.` / `’52 i` C¢- -· ·-· ·-·- ··-··-CC8 +/`HH /` `2’R ’` H 5- ) +T 1CCHH22C=HC3H R
-알킬과 올레핀 한 분자가 반응하여 6 원자고리 화합물과 같은 건 이상태를 거쳐 금속―알킬과 올레핀을 형성한다고 제시된 바 있다. 이 반응의 메카니즘에 따르면 중간체로서 금속-수소화물은 생성되 지 않고 수소는 올레편으로 전달되었고 새로운 금속―알킬 착물이 생성되었다. 전이상태에 관한 이론적인 연구에서는 식(1. 11) 에서 제
12) G. Henric i -O l ive /Ol ive , Coordin a ti on and Ccti .ly s i s , Verlag Chemi e· Wein h eim , 1977, p.1 27. 13()1 9G 7. 4)H. enric i -O l ive and S. Oli ve , J. Polym . Sci . , Poly. Lett . Edit . , 12, 39
시된 전이상대가 에너지적으로 보아서 식(1. 9) 에서 제시된 전이상 대 보다 용이 하리 라고 보고하였 다. l4) (3) 산화성첩가반응 (ox i da ti ve add itio n) 파 환원성제거반응 (reducti ve eli mi na ti on ) 산화성 첨 가반응이 란 중성 (neu t ral) 분자 XY 가 전이 금속에 첨 가되 는 반응을 일컫는다. 이 반응에서 XY 분자는 환원되면서 해리되어 두개의 음이온성 리간드 X-및 Y- 를 생성하고 동시에 금속은 산화 된다. 아래와 같이 Vaska 촉매로 알려진 4 배위 사각평면형 이리듐
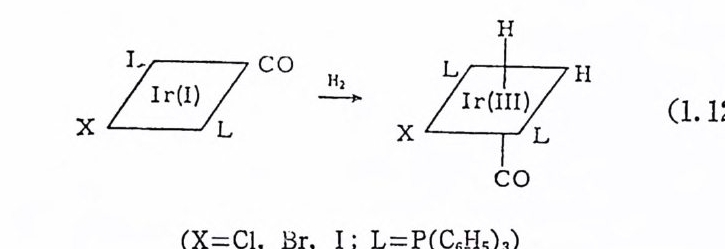 H
H
( I )착물이 수소분자와 반응하여 6 배위 이수소화 (d i hy dr i do) 이리듐 (IlI) 착물을 생성하는 반응울 예로 들 수 있다 .15) 실제 새로 형성된 금속―수소 결합은 共有 시그마결합이다. 그러나 일반적으로 통용 되는 법칙에 따르면 금속과리간드가 한 쌍의 전자를 共有하면 해당 전자쌍은 리간드에 속하는 것으로 간주하고, 전이금속의 산화수 {oxid a ti on number) 는 금속에 남아 있 는 전하 (char g e) 로서 정 의 된다. IrX(CO)L2 에 서 Ir-X 결 합은 한 쌍의 전자를 공유하지 만, 나머 지 결 합은 모두 배위결합이다. 배위결합에 제공된 전자들은 처음부터 리 간드의 전자이므로 배위된 뒤에도 리간드의 전자로 취급된다. 따라 서 IrX(CO)L2 중의 Ir 의 산화수는 I 이다. 한편 생성물 IrH2X(CO) L2 에서는 배위결합을 제의하고 3 쌍의 전자를 이리듐과리간드가共 有한다. 죽 한개의 IrX, 그리고두개의 Ir-H 결합에서 이리듐과리
14) 0. Novaro, S. Chow and P. Mag n ouat, ]. Polym , Sc i., Poly. Lett . Edit . , 13, 761 (19 75). 15) L. Vaska and J. W. DiLu zio , ]. Am. Chem. Soc. , 84, 679 (19 62).
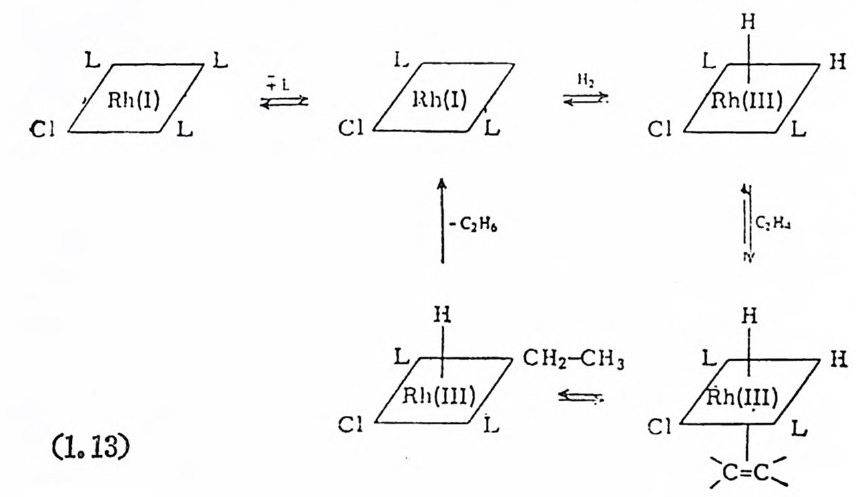
간드는 共 有결합을 하고 있다. 따라서 IrH2X ( CO ; L2 에서 이리듐의 산화수는 IlI 이 다. 산화성 첨 가반응의 독징 은 금속의 산화수 증가가 배위수의 증가를 동반하는 것이다. 평면사각형 d8 착물에서 혼히 볼 수 있는 반응으로서 두 개의 리간드가 첨가되어 6 배위, 18 전자 착물을 형성한다. 산화성 첨가되는 분자 XY 는 수소분자, 할로겐 분자, 16> RCOCl, 11> RCOOH, 18) 및 RI16),19) 둥이 다. 중성분자 (neu t- ral) 를 전이금속에 산화성 첨가시킨다는 사실은 그 분자를 活性化 (ac ti va ti on) 시 키 는 것 과 같다. 예 를 들면 수소분자를 전이 금속에 산 화성 첨가시킵으로써 얻어지는 금속-수소착물은 많은 경우에 수소 가 필요한 반응(예를 들면 올레핀의 수소화반응 또는 히드로포르밀 화반응)에 촉매적 역할을 한다. 많은 경우예 산화성첨가반응은 可 逆반응이다. 산화성첨가반응의 逆反應은 환원성제거반응이라고 부 른다. 촉매작용에서는 많은 경우에 산화성첨가반응 다음에 또 하나 의 반응단계가 있고(예를 들면 올레핀의 삽입반응 같은) 마지막으 로 환원성제거반응이 일어나며 금속착물은 원래의 閉媒 種으로 들아
 Cl 三 L J_; L+ • C1> th(l )/ =11, Cl 三H H
Cl 三 L J_; L+ • C1> th(l )/ =11, Cl 三H H
16) J. Hal;ie r n, Acc. Chem. Res. , 3, 386 (19 7(J ). 17) M. ·Ku bota and D. M. Blake, ]. Am. Chem. Soc. , 63, 1368 (19 71). 18) D. M. Blake, S. Shie l ds and L. W y四 n, Inorg, Chem. , 13, 1595 (19 74). 19) R. G. Pearson and W. R. Muir , J. Am. Chem. Soc. , 92, 5519 (1970).
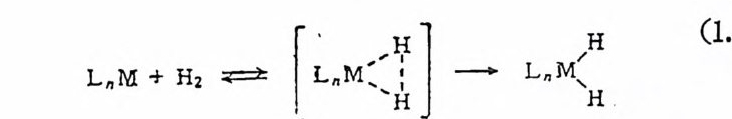
가며 생 성 물을 생 산한다(식 1.1 3 참조)• 20, 산화성 첨 가반응에 서 첨 가되 는 위 치 는 立體特異性 (s t ereos p e ci{icity} 이 있다. 즉 첨가되는 리간드가 시스 또는 트란스 위치를 차지하게 되는데 이는 첨가되는 분자 XY의 성질, 금속의 성질 또는 금속주 위에 배위되어 있는 리간드에 따라 결정된다 .19) 산화성 첨가반응의 메카니즘에 관한 연구를 동해서 리간드가 첨가되는 위치를 예측 설 명할 수 있다. 예를 들면 H2 가 첨가될 때 다음 식(1. 14) 과 같이 同
 L.M + H, = 仁 w〈 :] 一 LnM、/ `H H (1.1 4)
L.M + H, = 仁 w〈 :] 一 LnM、/ `H H (1.1 4)
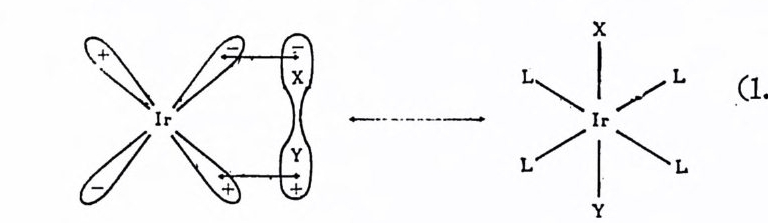
時三中心 (conce rt ed t hree-cen t ered) 과정에서 H2 의 결합분열과 M-H 결합의 형성이 동시에 이루어진다고 생각된다. 따라서 協同메카니 즘 (conce rt ed mechan i sm) 을 통한 첨 가반응은 시 스 첨 가생 성 물을 생 성하리라고 예상된다. 그러나 協同메카니즘을 통한 산화성첨가받옹 · 이라도 트란스 첨가생성물을 생성시킬 수도 있다. 예를 들떤, 다음 식(1. 15) 에서와 같이 채워진 금속의 dx y(조는 d y,)와 첨가되는 타
 \[-一〉! 〈 (1.1 5)
\[-一〉! 〈 (1.1 5)
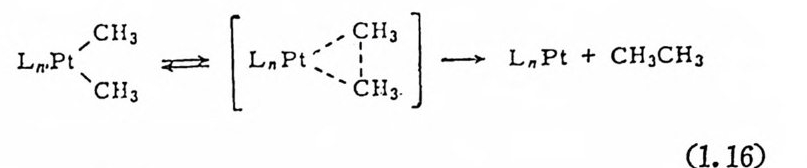
간드 XY의 反結合軌道函數의 겹침은 트란스 생성물을 형성할 것아 ! 다 19), 또다론 예 를 돈다면 Pt X (CH3)aCCC6H5)z P(CH2)2P(C5Hs)z) (X==Cl, Br) 의 환원성 제거반응은에탄을 생성한다. 이 반응의 메카 니즘 연구에 의하면 식(1. 16) 과 같은 協同메카니즘일 것으로 보고-
20) F. A. Cott en all
 L,,<::: ,= [ L,Pt ': `/二 ] 一 L,Pt + CH,CH,
L,,<::: ,= [ L,Pt ': `/二 ] 一 L,Pt + CH,CH,
누었다 .•1 』 한편 할로겐화 알킬이 Pt (O ) 및 Pd(O) 착물에 산화성 참 가될 때의 메카니즘은 라디칼 連 鎖 과정으로 진행되는 것으로 보고 노 된 바 있다 .22) 배위적으로 不胞和 (coord i na t i vel y unsa t ura t ed) 된 전이금속의 산화 성첨가반응은 금속이온 자신분 아니라 배위되어 있는 리간드에 영 향을 받는다. 전자주게 리간도는 산화성첨가반응을돕는다. 예를들 E 면 다음 식 (1. 17) 에 서 평 형 상수 K 의 값은 L 이 P(CsHs)3 일 때 보다·
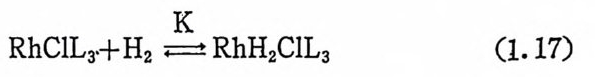 K
K
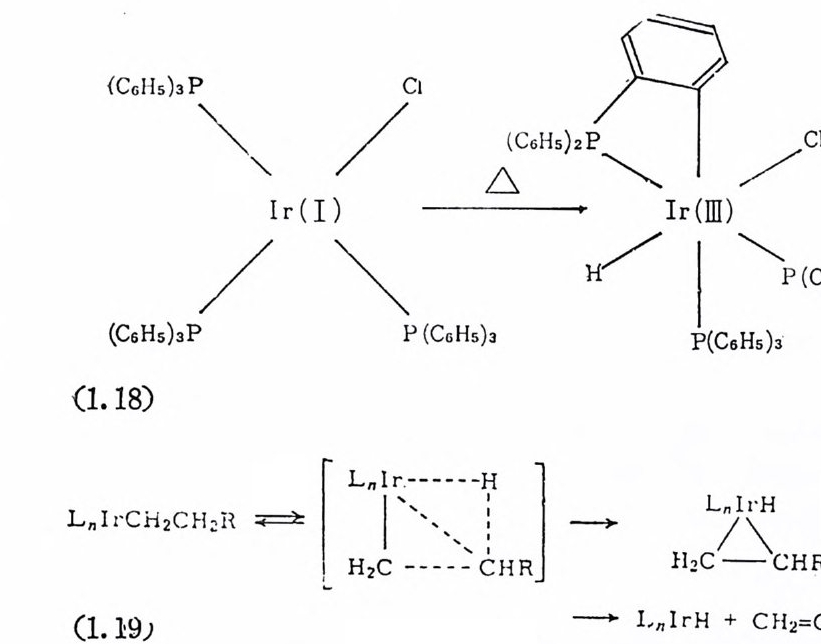
P( p -CHa-C 晶 )3 일 때 큰 값을 갖는다. 금속에 전자밀도가 높으면 산화성 첨가반응은 쉽게 일어난다. 예를 들면 Rhl(CO)L2(L=As cc 品 )3 또는 Sb(C6H5)3) 보다 [Rh l2(CO)L] _이 훨씬 빠르게 CH3I 와 산화성 첨 가반응을 일으킨다. 23) 산화성 첨가반응을 일으키기 쉬운 d8- 사각평면형 착물은 C - H 결~ 울 끊으면서 分子內 (i n tr amolecular) 의 첨 가반응을 일으킨다. 예 를 들 면 식(1. 18) 에서 보는 바와 IrCl(P(CsHs)3)s 의 용액을 가열하면 정 팔면체형 Ir(][ )착물을 얻는다. 24) 마자막으로 최근에 발표된 바에 의하면 /3-수소전달반응도 산화성 첨 가반응으로 선명 하였 다. 죽 식 (1. 19) 에서 보는 바와 같이 C-H 걷 합에 금속이 삽입되는 과정을 포함하는 메카니즘에서 중간체형성을-
21) M. P. Brown, R. J. Puddeph att and C. E. E. Up ton , J. Chem. Soc. , Dal- ton Trans. , 2457 (19 74). 22) A. V. Kq m er, J. A. Labin g e r, J. S. Bradly and J. A. Osborn, J. Am. Ch,e m . Soc. , 96, 7145 (19 74'.). 23) D. Forste r , J. Am. Chem. Soc. , 97, 95, l (19 75). 24) M.A. Bennett a.nd D.L . Mi lne r, J. Am. Chem. Soc,, 91, 6983 (19 69).
 (CG Hs )J P \ \
(CG Hs )J P \ \
산화성 첨 가반응으로 간주하였 다. 25) (4) 리 간드해 리 및 상호교환반응 (liga nd dis s ocia t i on and ligan d exchang e ) 촉매적 활성이 있는 전이금속착물은 때때로 리간드해리반응에 의 해서 생성된다. 죽 리간드가 해리되므로 촉매작용에 필요한 배위자 리가 금속 주위에 생겨나게 된다. 예를 둘면 이미 칙(1. 13) 에서 보 여 준 것과 같이 W il k i nson 촉매, RhCl(P(C6H 야 )3 가 용액 중에서 리 간드해리반응을 일으켜서 촉매적 활 성이 매우 큰 RhCl((C6Hs )3 )2 를 생성한다. 한편 이와 같은 종류의 화합물인 IrCl(P(C6Hs)3)3 는 P (C6H5)3 를 상당히 단단하게 붙들고 있기 때문에 리간드해리는 일어 나지 않는 것으로 알려졌다. 따라서 상기 이리듐착물은 수소분자의 산화성 첨가반응에는 活性 (ac ti v ity)이 크지만 울레핀의 수소화반응에 는 활성이 없다. 다시 말하면 수소의 산화성 첨가반응에서 생성되는
25) J. Evans, J. Schwartz and P.W. Urqu hart, J. Orga nomet. Che m . 81, 137 (1974).
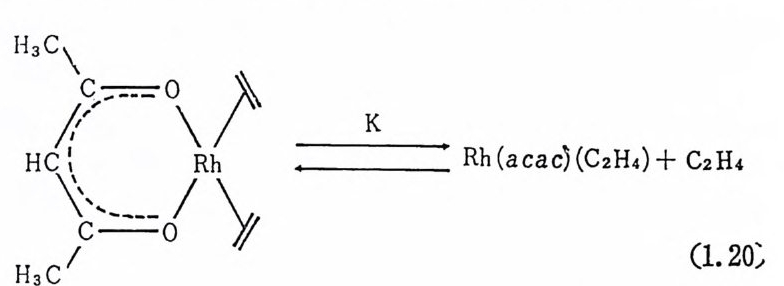
6 배 위 아 수소 (d i h y d r i do) 착 물, IrClHz (P (C6 H s )3 )3 은 용액 중에 서 도 P(C 晶 )3 리간드해리반응을- 일으키지 않기 때문에 올레 펜의 배 위에 팔요한 배위자리가 없기 때문이다 .26) 또 하나의 중요한 예를 돈다 떤, l60°C 이상에서 수소화반응의 촉매로 작용하는 펜타카르보닐철 (Fe(C0)5) 의 리간드해리반응 을 들 수 있다. 이 착물은 상기 고온에 서 CO 를 해리시켜 수소분자의 산화성첨가반응과 올레핀 배위에 필 요한 배위자리를 제공하는 것으로 보고되었다 . 27 ) 리간드 상호교환반응은, 용액 중에 리간드가 과량으로존재할때, 쉽게 일어나는 것으로 알려졌다. 리간드가 포스판류 2 8) 또는 올레핀 류 29 ) 일 때 특히 용이하다. 예를 들면 Rh(acac)(C2H 4 )2(acac= 두자 리 리간드, (CH3COCHCOCH3)-) 는 매우 안정한 화합물이다. 즉 80° C 정도에서도 과량의 에틸렌이 존재하지 않는한 리간드의 해리 반응은 일어 나지 않는다. 다시 말하면 아래 의 평 형 (식 1. 20) 은 거
 13 C\C/H4—rC/\'o{3\c'\`R}/h c _ / \入/o = =K= = Rh(acac}(C2H4)+ C2H,
13 C\C/H4—rC/\'o{3\c'\`R}/h c _ / \入/o = =K= = Rh(acac}(C2H4)+ C2H,
의 완전히 왼쪽으로 이동되어 있다고 볼 수 있다. 그러나 과량의 에틸렌의 촌재하에서는 매우 빠른 에틸렌의 상호교환반응이 일어난 다. 에틸렌의 상호교환반응은 -58°C 에서도 일어날분 아니라 25°c 에 서 는 배 위 된 에 탈 렌의 壽 命(life ti me) 은 10-4 秒) 정 도이 다. 죽 10-4 초 내에 에탈렌 리간드의 해리가 일어난다. 이러한 리간드 상호교 환반응의 메카니즘은 크게 나누어 두 가지로 나눌 수 있다. 죽 해리 적 메카니즘 (d i ssoc i a ti ve mechan i sm) 과 회합적 메카니즘 (assoc i a ti ve mechan i sm) 으로 나누어 진다.
26) M. A. Bennet and D. L. Mi lne r, J. Am. Chem. Soc. , 91, 6983 (19 69). 27) J. P. Collman, Acc. Chem. Res. , l, 136 (19 68). 2298)) RM.. WCr. amAedrl,a rJd. aAndm .G .C hSeomcr. atSe os ,c . C, h8e9m, . 21C7o m(1m96u4n).. , 17 (19 72).
해리메카니즘은 두 개의 과정으로 나누어진다. 첫번 과정은 느란 一分子과정 (unim olecular pro cess) . < ' 금속으로부터 리 간드가 해 리 되 는 과칭이며, 두번째 과정은 빠는 과정으로 새로운 리간드가 금속 에 회합되는 과정이다(식 1.2 1). 식(1. 21) 에서 금속의 배위수가 감 소되 는 첫 과정 은 速度決定단계 (rate dete r mi ni n g s t e p)가 되 며 , 一次 反應速 度式(fi rs t order k i ne ti cs) 이 예상된다(식 1.2 2). 죽 속도식은 새로 들어오는 리간드의 농도에 무관함이 예상된다.
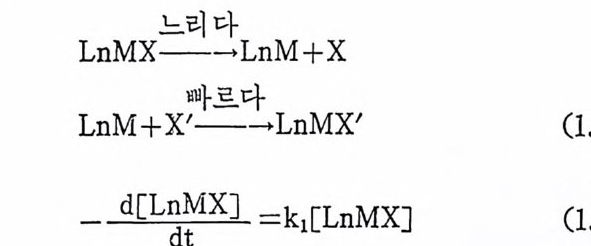 느리다
느리다
회 합메 카니 즘의 速度決定단계 는 二分子과정 (bim olecular p rocess) 이 된다. 轉移狀態(t rans iti on s t a t e) 에서 해리되는 리간드와 회합되는리 간드가 동사에 금속에 약하게나마 결합되어 있어서 금속의 배위수 논 하나 중가하게 되 고(식 1. 23), 속도식 은 식 0. 24) 과 같이 예 상된 다. 많은 경우에 해리메카니즘인지 회합메카니좀인지 분별이 뚜렷 하지 L못nM하X다+ .X3'0) 一〔 Ln M: … X' 〕一 LnMX'+X (1. 2.3) _ d 땝 ~=k2[LnMX J [X' J (1.2 4) (5) 산화 및 환원 (ox i da ti on and reducti on ) 많은 중요한 均一觸媒反應은 가용성 금속착물에 의 한 유기 화합물 의 산화반응이다. 많은 경우의 이러한 산화반응에서 전이금속은 비 교적 안정한 두개의 산화상태를 번갈아 갖게 된다. 예를 들면 코발
30) T. W. Swaddle, Coord. Chem. Rev. , 14, 217 (19- 7 4).
트(JI)와 코발트(]I[), 그리고 백금 (0) 와 백금(JI)의 짝을 둘 수 있 다. 코발트 CII) 와 코발트(]I[)의 경우처럼 산화-환원과정에서 한 개 의 전자를 주고받는 과정, 그리고 백금 (0) 에서 백금 CII) 의 경우처 럼 두 개의 전자를 주고받는 과정 둥이 있다. 몇몇의 一電子酸化 (one-electr o n ox i da ti on) 반응에 서 는 금속이 온과 유기 기 질 사이 에 단순 한 전자이동이 일어날 분아지만, 대부분의 一電子酸化반응 및 二電 子酸化반응에 서 전자의 이 동은 리 간도의 이 동을 동반한다. 예 를 들· 떤 석(1. 25 써서 보는 바와 같이 코발트(JI)는 코발트(]I[)으로 산 화되면RC서O OCHo+-COoH2 결+—합 이R O생 성· +된[다q.+ -O여H기J서 2+ 0-0 결합은 한(개1. 의25 ) 전자 를 코발트로부터 받아 RO· 오} OH- 울 생성한다. 끝으로 단순히 전
자의 이동만(리간드의 이동을 동반하지 않는) 존재하는 예를 들어 보면 다음석(1. 26) 에서 아세탈 라디칼은 한개의 전자를구리 (II) 에 게 주어서 구리(I)이 되게 한다. 리간드의 이동과정 및 전자의 이
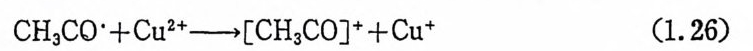 CH3CO • +Cu2+ 一 [CH3CO]+ +cu+ (1. 26)
CH3CO • +Cu2+ 一 [CH3CO]+ +cu+ (1. 26)
동과정 은 모두 탄화수소의 산화작용에 중요한 반응돌이 다. * 참고문헌 I) P. J. D.avid s on, M. F. Lapp e rt and R. Pearce, Meta l 11-Hy d rocar· lJo ny ls , Chem. Rev. , 76, 219 (19 76). 2) }. P. Collman, Patt em s of Orga nometa l lic Reacti on s Relate d to Homog e neous Cata l ys i s , Acc. Chem. Res. , 1, 136 (1968). 3) L. Vaska1 Reversi.b k Ac t'iva ti on of Covalent Molecules by Tran-sit ion Meta l Comp le xes, Acc. C.h e m. Res. , 1, 335 (1968). 4) J. Halpe rn, Oxid a ti ve -Addit fon Reacti on s of Transit ion Meta l Comp le 1es, Acc. Chem. R~s. , 3, 386 (19 7t >). 5) G. Henric i·O liv .e and S. Oli ve , TRe Acti ve Sp ec ie s in Homog e n·
eous Zie g l er-Natt a Cata l ys t s fo r the Polym er iz a ti on of Et hy l en e, A11g e w. Che m . Intc r nat. Edtt . , 6, 790 (19 67). 6) G. Henric i-O l iv e and S. Oliv e , Olef i n Inserti on in Transit ion Meta l Carbonyl s , Top ics Cu rr . Chem. , 67, 1 (19 76). 7) R. F. Heck, Orga notr a nsit i on Me ta l Chq m i st r y , Academi c Press, 1974. 8) F. Basolo and R. G. Pearson, Mechanis m of Inorg a nic Reacti on s, 2nd Ed. , Wi ley -I nte r scie n ce, 1967. 9) G. Henric i-O liv e and S. Oliv e , • Coordin ati on and Cata l ys i s , Ver-lag Chemi e, 1976. 10) B. L. Shaw and N. I. Tucker, Org a notr a nsit ion Meta l Comp ou nds and Relate d Asp ec t s of Homog e neous Cata l ys i s , Perga m on Press, 1975. 11) E. L. Muett er ti es , Transit ion Meta l Hy d rid e s, Marcel Dekker, 1971 . 12) J. K. Kochi, Orga nometa l lic Mechan is m s and Cata l ys i s , Academi c Press, 1978.
제 2 장 올레판의 반웅들 군일촉매반응에서 가장 다양하게 응용되는 반응은 올레핀을 포항 하는 반응이다. 그 중에서도 올레핀의 중합반응, 산화반응 및 히드 로포르밀화반응 둥은 공업적으로 대규모 생산에 응용된다. 기타 여 러 반응들도 실험실 제법으로 많은 합성 화학자들의 관십거리가 되 고 있다. 거의 대부분의 반응에서(공장에서 응용되는 반응과 실험 실 제법으로 응용되는 반응 모두 포함해서) 올레핀은 可溶性금속착 물에 의해서 活性化되고 있다. 제 2 장에서는 금속착물에 의한 올레 핀의 반응에 관하여 근본적인 원리 및 알려진 메카니즘을 취급하고 자 한다. 이 장에서는 군일촉매작용을 하는 전이금속 자체에 관한 화학을 주로 다루려고 한다. 죽 금속의 배위권 내에서 일어나는 과 정들을 포함하는 메카니즘등을 중접적으로 고찰한다. 여기에서 인 용되는 예들은 특별히 선택된 것들이냐 죽 어떤 하나의 메카니즘 울 설명하기 위하여 특별히 선택한 것들이다. 그러나 어떤 특별한 예로 들었다고 하더라도 일반화되어 응용될 수 있는 것들이다. 많 은 경우에 근본적안 메카니즘은 같고 그때그때의 조건에 따라 llJ:- 웅경로에 약간씩의 차이는 있을 수 있다. 1. 울레핀의 配位 올레편과 금속과의 결합은 이미 제 1 장 3 철에서 자세히 고찰한
바 있다. 건이금속―올레핀 착물은 가장 오레된 有 機 金屬환물 중의 하나다. 최초의 합성은 1827 년 덴마크의 학자 Ze i se 에 의하여 이루어졌다. Zeis e 의 鹽 (Ze i se's sa lt)이 타고 불리 우는 K[P t CllC2H4) ]는 백 금( 1I ) 의 착물로 에틸렌을 배위하고 있다. 1950 년까지는 올레판금속착물 은 벌로 흥미 를 끌지 못했으나 1951 년에 DewarD 그리 고 1953 년에 Chatt 2) 등에 의 한 연구보고가 기 접 이 되 어 그후 연구가 활발히 진 행되어오고 있다. 거의 모든 전이금속에 관하여 울레핀착물이 합성된 바 있다. 일 반적 으로 올레 핀금속착물 중의 금속은 낮은 산화상태를 갖는다. 예 를 들면 Pt 0( C2H4)3 및 〔 P~Cl JC C 晶)〕- 둥 백 금 (0) 및 백 금( 1I )착 물은 찰 알려쳐 있지만 안정한 백금 (N) ―올레핀착물은 아직 알 려 져 있 지 않다. 아마도 금속의 형 석 산화상태 (for mal oxid a ti on sta t e ) 가 중십금속의 실제 전자밀도보다는 중요하지 않을것이다. 예를들 면 Zeis e 의 鹽에 서 금속과 리 간드의 상호작용 때 문에 금속이 온은 거 의 전기 적 으로 중성 (elec t roneu t ral) 에 가깝다. 올레핀착물의 안정도는 올레핀의 종류, 금속의 산화상태 및 종류 그리고 금속주위에 배위된 리간드의 종류에 영향을 받는다. 일반적 으로 올레핀의 알킬기가길게 되면 형성되는 올레핀착물의 안정도는 강소한다. 예를 둘떤 〔 PdC13(ole fi n)] 제서 올레핀이 에 틸렌, 푸로 팔렌, 1 부젠으로 알킬기 가 층가할 때 다음식 (2.1) 의 평 형 상수는 각각 17. 4, 14. 5, 11 . 2 로 감소한다. 착물의 안정 도가 감소하는 이 유 주로 리간드와 금속간의 입체적인 작용으로 설명된다. 배위되 지 않은 올레핀 자체의 스트레인이 크면(예를 들어 시클로옥덴) 금 속과 올레핀의 결합은 강해진다. 그 이유로는 올레핀이 금속에 배 위됨에 따라 C=C 간의 거리가 길어지고 울레핀 자체의 스트레인이 감소되기 때문이다.
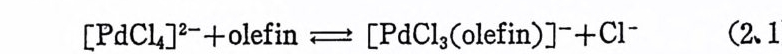 [PdCt. J2 -+olefi n .== [PdCl3(olefi n) J- + Cl- (2, 1)3'
[PdCt. J2 -+olefi n .== [PdCl3(olefi n) J- + Cl- (2, 1)3'
1) M. J. S. Dewar, Bui! . S oc. Chim . France, 18, C79 (19 51 ). 2) J, Chatt and L.A. Duncat s on, J. Glie m . Soc. , 2939 (1953). 3) P. M . Henry, ]. Am. CherJ. Soc. , 88, 1595 (1966).
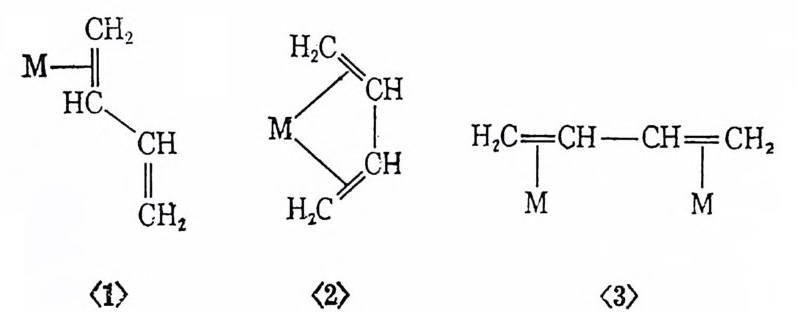
컨쥬게이션이 있는 디엔 (d i ene), 예를 들어 1, 3--¥- 타디엔, 은금 속과 다음과 같은 3 가지 방법으로 결합함이 찰 알려져 있다. 화합 물 〈 3 〉에 서 디 엔 (d i ene) 은 두 개 의 금속과 결 합하여 二核 (b i nuclear) 착 물을 형성한다 . 이러한 二核배위 착물은 可溶性 금속착물이 아닌 固 體금속표면 (meta l l ic sur fa ce) 에 의 한 촉매 반응에 서 형 성 되 는 것 으로 알려 져 있 다. 可溶性 금속착물에 의 한 촉매 작용에 서 는 〈3 〉과 같은 형의 二核착물은 거의 논의되지 않고 · 있다. 한편 〈 1 〉에서처럼 한 자리 리 간드 (monoden t a t e) 로 그리 고 〈 2 〉에 서 처 럼 킬레 이 트 리 간드
 CH2
CH2
로 금속과 결합한다. 착물 〈 1 〉과 〈 2 〉중 어 떤 모양으로 올레핀이 금 속과 배위하느냐가 상당히 중요한 문제이다. 왜냐하면 배우1 방법에 따라 촉매반응의 생성물이 결정되기 때문이다. 이 접은 제 2 장 4 철에서 예를 들어 고찰될 것이다. 2. 수소화반응 (h y dro g ena ti on) 많은 可溶性 전이금속착물이 보통의 실험조건 (1 기압, 25°C) 에서 수소화반응의 촉매적 여할을 함이 이미 알려져 있다. J ames 는 그 의 저서 『군일 수소화반응』 4) 에 서 수소화반응의 자세한 반응메카니 즘, 촉매의 제법, 실험방법 둥을 광범위하게 다루었다. 대부분의 수소화반응의 촉매는 산화수가 낮은 그리고전자밀도가 높은 VIII 族 금속착물아다. 많은 경우에 금속착물 촉매는 强한 場 4) B. R. Jam es, Homog e neous Hy d rog e nati on , Joh n Wi ley and Sons, 1 鄧 3.
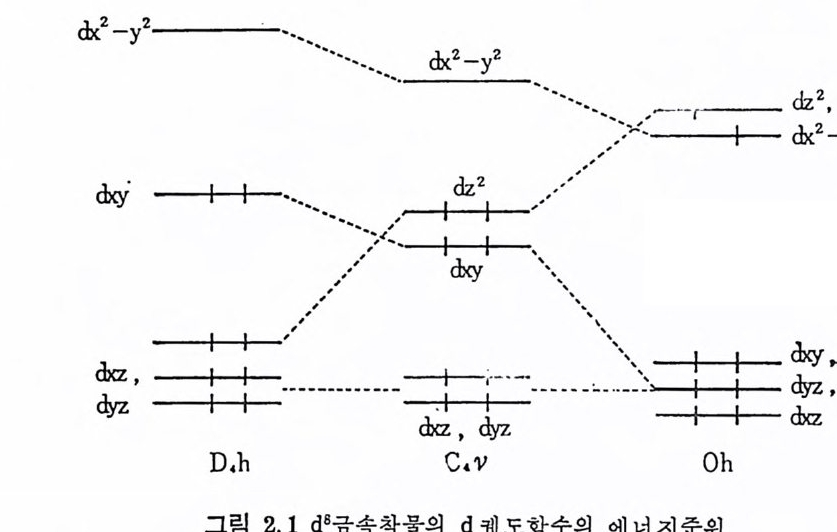
(str o ng fiel d) 리 간드(예 를 들면 CO, CN-, 및 포스판 類 )를 배 위 하 고 있 다. 따라서 금속의 d 전자들의 갈라침 (s plitti n g)이 크고 낮온 스 핀 착물(l ow spi n com p lex) 이 생성하게 된다. 만일 금속이 가지고 있 는 전자의 수가 여섯이 념으면, 6 배위 금속착물은 리간드場안정 화에 너 지 (liga nd field sta b il iza ti on ener gy)의 감소에 따라 안정 도가 감 소하게 되며 낮은 배위수(즉 4 및 5) 를 갖는 금속착물의 생성이 가 능하게 된다. 그리하여 금속에 있는 빈 배위자리는 수소분자를 活 性化시키는 데에 이용된다. 그리고 이어서 금속은 배위된 수소를 배위된 올레판에 이동시켜 줌으로써 촉매적 활성을 보이게 된다(:::z.. 림 2.1 참조). 예를 들어 사각평면형착물, RhCl(P(CsHs)3)3 이 접근 되 어 오는 수소분자와의 작용을 생 각해 보자. 수소분자의 접 근 방
 dx.2 -y 2--.. `` ```` `--_ `.. dx2-y2 -·-- --.·_- -- . -- -- 기-~ dz 라
dx.2 -y 2--.. `` ```` `--_ `.. dx2-y2 -·-- --.·_- -- . -- -- 기-~ dz 라
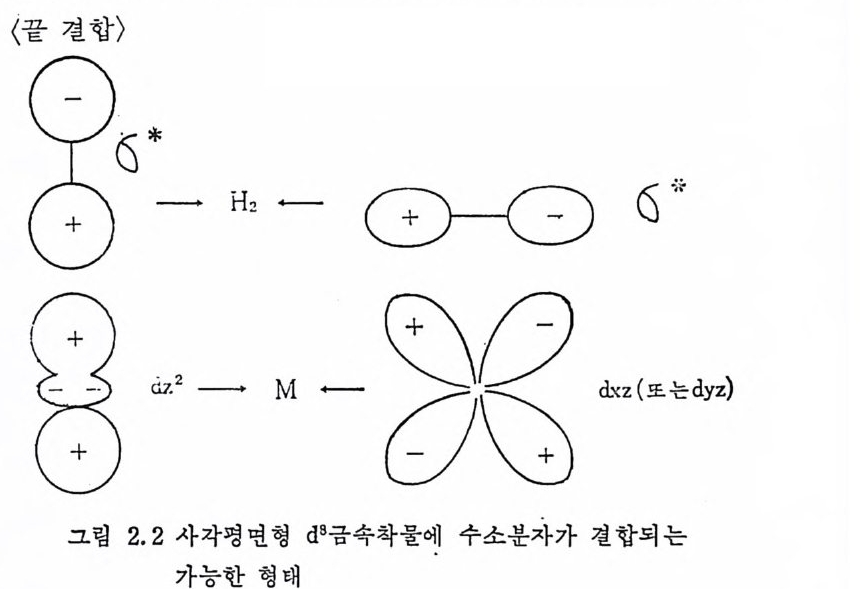
향은 z 방향이 될 것이다. 왜냐하면 水平 (e q ua t or i al) 방향의 x y平面 은 이미 다론 리간드들에 의해서 차지되어 있기 때문이다. X y平面 上下에 걸쳐 있는 금속의 d;, dn, dy, 궤 도함수는 채 워 진 함수이 므로 접근하는 수소분자는 빈 反結合分子軌道函數 (an ti bond i n g mole-cular orb it al) 와 결합할 수밖에 없다. 따라서 금속과 수소의 결합은 그림 2. 2 와 같이 끝결합 (end-on) 과 옆결합 (ed g e-on) 이 가능하다. 끝 걷합은 금속의 d· 태도함수와 수소분자의 a* 궤도함수의 작용으로.
이루어질 수 있고, 옆결합은 금속의 dxz 또는 d y z 궤도함수와 수소 분자의 간궤도함수가 1C_ 결합과 같은 모양으로 작용하는 것이다. 위 의 두 결합형태 중 어떤 경우타도 금속의 전자밀도는 H 려 反結合分 子軌道函數에 이동되어 H-H 의 결합이 약화되고 수소분자의 活性 化는 일어난다. 이의에도 금속의 빈 (n+ l) s 및 (n+ J)p퀘도함수와 수소분자의 채워진 結合分子軌道函數 (bond i n g molecular orb it al) 의 상
 〈끝 결합 〉
〈끝 결합 〉
호작용도 있으리라고 이론적으로 생각할 수 있다. 그러나 이제까지 알려진 실험적 결과로는 수소분자로부터 금속으로 이동되는 전자밀 도는 별로 중요할 정도가 못된다고 밝혀졌다. 위의 두 접근 형대 중에서 어느 방법으로 수소가 금속에 접근하는 지 정확히는 알려져 있지 않다. 그러나최종 생성물은알려져 있다. 즉 금속의 산화성 첨가반응 생성물(제 1 장 4 철 (3) 참조)에서 두개의 수소는 시스 위치에 결합되어 있고 금속과 수소는 시그마 결합을 하고 있다. 따라서 수소가 금속에 접근하는 방법은 옆결합 (ed g e-on) 으로 설명되어지고 있다(그립 2.2 참조). 여기서 수소화반응의 몇몇 실례를 들고 각 촉매반웅의 특성 및 촉 애를 살펴 보자.
루테 늄 c n) 착물 RuHCl(P(C5Hs)3)3 는 가장 活 性 이 높은 수소화만 웅의 촉매 로 알려 쳐 있 다. 6) 末 端 올레 핀 (ter mi na l ole fi n) 문만 아니 라 內部올레판(i n t ernal olefi n) 및 시클로알켄의 수소화반응에도 촉매적 활성을 보이고 있다. W ilki n s on 촉매 로 알려 진 RhCl(P(C 晶 )3)3 또한 상당한 活性울 가지고 있다. 이 촉매는 상온, 상압하에서 알킨 (alk y ne) 의 수소화반 응에도 활성을 가지고 있다. 컨쥬게이션이 있는 올레핀의 수소화반 옹은 상당히 어렵지만 예를 들어 1,3- 부타디엔의 수소화반응은 수 · 소압력이 60 기압 정도에서 W il k i nson 촉매에 의해서 일어난다 6). 그 이 유는 강한 킬레 이 트 리 간드로서 부타디 엔 분자는 수소의 活性化 에 필요한 배위자리를 차지하고 있기 때문이타고 설명된다. 환원될 가능성 이 있는 여 러 作用基(fu nc ti onal g rou p)를 갖고 있는 분자의 수 소화반응에 서 Wi lkin s on 촉매 는 선택 성 (selec ti v ity)윤 보여 준다. 예 를 들면 a, /3-불포화 카르보닐화합물의 수소화반응으로부터 포화 카 르보닐화합물을 생성 시 키 고, a, /3-불포화 니 트로화합물 그리 고 a, g 볼포화 니트릴화합물의 수소화반응에서도 포화 니트로화합물 그리 고 포화 니트릴화합물을 각각 생성시킨다.7) 일반적으로 로듐착물은 비슷한 이리듐착물보다 수소화반응의 촉 매로서 활성이 크다. 많은 경우에 포스핀 리간드가 중십 금속으로 부터 해리되어 수소 및 올레핀이 배위될 수 있는 자리를 만들어 주 어야 촉매적 수소화반웅이 가능하게 된다. 그런데 이리듐착물은 비 슷한 로듐착물보다 포스판 리 간드를 더 욱 강하게 붙들고 있어 서 ::L. 촉매 적 활성 이 낮다. 8) 죽 Vaska 착물로 알려 진 IrCl(CO) (Ph3P)2 는 수소와 반응하여 첨가성 산화생성물 (IrH2Cl(CO)(Ph3P)2) 을 생성하 · 는 최초의 화합물로 알려졌다. 그러나 25°C 에서는 올레판의 수소 . 화반응에 효과적인 촉매가 되지 못하고 고온 (80°C 이상)에서 촉메
5) P. S. Hallman, B. R. McGarvey and G, W ilki n s on, ]. Chem. Soc. , A, 3143 (19 68) . 6) F.H. Jar din e , J.A . Osborn and G. Wi lki n s on, J. Chem. Soc., A, 1574- (19 67). 7) R,E. Harmen, J.L . Parsons, D.W. Cooke, S,K, kup ta and J. Schoolen- berg, J. Org, , Chem. , 34, 3684 (1969).
여할울 한다 .8) 다른 금속착물의 예를 들어 보자. 사각평면형 팔라 듐 (II) 착물은 그 촉매적 수소화반응의 메카니쯤이 자연계에 촌재하 는 수소화반웅의 효소 (h y drog enase ) 와 바 슷하므로 효소의 모델화합 물로 연구된 바도 있 다. 9) 물에 可 溶 性인 코발트착물(〔 Co(CN)5 J 3-) 은 컨쥬게이션이 있는 올레핀의 수소화반응에 촉매적 역할을 하는 것 으로 알려 져 있 다. 4) 몇 몇 二 核 카르보닐화합물 (d i nuclear carbony l) (예를 들어 Re2( C 0) 10 4) 또는 Mn 2( C0 ) 1010) )도 수소화반응의 촉매 로 사용되었으나 반응조건이 高莖 및 高 溫이므로 아마도 실제 촉메 종 (ac t ual cata l yt ic s p ec i es) 은 初期물질 이 아니 고 분해 된 화학종일 것 으로 추정되기도 하였다. 지방족의 二 重 결합이나 三 重 결합의 수소 화반응분 아니 라, 방향족의 수소화반응도 Zie g le r 촉매 계 에 의 해서 일어남이 발표되었다 .4) 상기 Zie g le r 촉매계는 高 壓 및 高溫에서 촉매역할을 하지만, 벤첸에 可 溶 性인 코발트착물 Co(C3H5)(P(OC H3)3)3 은 방향족 화합물의 수소화반응을 低壓 및 低溫에서 일으킨 다 11). 마지막으로 해태로원자로 이루어전 불포화결합(예를 들어 카 르보널, 니트릴, 이만 등)도 . 高 壓 , 高溫하에서는 비교적 효과적으 로 수소화된다 .4) 많은 경우에 可溶性 전이금속착물에 의한 수소화 반응 과정 에서 불포화 有機物의 이 성 질화반응(i somer i za ti on) 도 함께 일어난다. 1- 알켄의 수소화반응 과정에서 2_ 시스알켄 또는 2- 트란 스알켄둥이성질체가생성되며 이렇게 하여 생성된 이성질체들의 수 소화반응은 l- 알켄의 수소화반응보다 느리게 일어나므로 전체적인 수소화반응의 속도가 감소된다. 예를 들면 이리듐과 로듐착물들에 의 한 수소화반웅은 항상 이 성 질화 반응을 동반한다. 12) 그러 나 위에 서 소개한 수소화반응에 대 한 촉매적 활성 이 가장 큰 RuHCI(P(C6 Hs)3)3 은 1 一알켄의 이성질화반응을 동반하지 않는다 .s)W ilkin son 촉 매에 의한 수소화반응은 벤젠 및 기타 탄화수소 용액에서는 이성질 화반응을 동반하지 않지만 벤젠과 에탄올 혼합물 용액에서는 이성
8) W. Str o b. eim er, Top ics in Current Chem. , 25, 71 (19 72). 9) G. Henric i-O l ive and S. Oli ve J. Mol. Cata l . , 1, 121 (1976). 10) G. Henric i-O l ive and S. Oli ve , J. Orga nomet. Chem. , 책 3Cll (1971 ). 11) E. L. Muett er tie s and F. J. Hire kom, J. Am. Chem. Soc .• 96, 4063(1 9 74). 12) W. Str oh eim er, R. Fleis c hman and W. Rehdr-Sti m welss , J. Orga nome· tal . Chem. , 47, C~ (1973 ).
질화반응이 성당히 일어 난다. 13) 현재까지 수소화반응의 메카니즘에 관하여 상당히 자세하게 연구 되어 왔다. 메카니즘연구 자체도 중요하지만 촉매적 활성이 더욱 크거나 또는 더욱 선덱성이 있는 촉매계를 찾는 방향으로 연구도 활발하게 진행되고 있다. 여 기 서 는 수소분자의 均 街 分 離 (homol yti c spl i tt ing ) 및 不均 衡 分離 (hete r olyt ic s p l itti n g)에 의한 반응메카니즘으로 각각 나누어 고찰하 고자 한다. 균형분리에 의한 반응은 금속의 산화수를 중가시킨다. 다시 말하면 수소원자는 금속의 原子價 般 (valence shell ) 으로부터 전 자를 받아서 6 결합을 한다. 따라서 아래 의 석 (2. 2) 와 석 (2. 3) 으로 표현된다. 식 (2.2) 는 중십금속에 수소분자가 산화성 첨가되는 과정
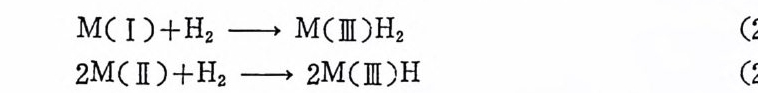 MC I )+H2 一 M(][)H2 (2.2)
MC I )+H2 一 M(][)H2 (2.2)
이고(산화성첨가반응은 제 1 장 4(3) 참조), 석 (2.3) 의 예로는 d7 착물인 [Co(CN) 간-울 들 수 있 다 .14) 한편 수소의 不均 衡 分 離 에 의 한 반응은 금속의 形式酸化 數( fo rmal oxid a ti on number) 에 변화를 동반하지 않는다. 일반적으로 음이온성 리 간드 A-가 히 드리 드 (h y dr i de, H-) 이 온에 의 하여 치 환된다(식 (2.4) 참조).
![]() MA+H2 一 MH+H++A- (2.4)
MA+H2 一 MH+H++A- (2.4)
일반적으로 수소분자와 올레핀은 동시에 금속의 配位 圈 (coord i na t1o n sph ere) 내에 존재하여야만 올레핀의 수소화반응아 쉽게 일어나 리라고 알려져 있다. 수소와 울레핀 중에서 먼저 금속의 배위권으. 로 들어오는 순서는 두가지인데 두경우모두 알려쳐 있다. 죽중십 금속에 서 수소분자의 活性化가 일어 나는 금속 - 수소화물 (me t al-h y dr i de) 경로를 거치는 경우는 다움 식 (2.5) 과 같이 표현된다. 즉 촉매와 수소분자가 먼저 반응하여 금속-수소화물 (MH2) 을 형성하고 난 다
13) R. L. Aug us ti ne and J. F. Van Pepp e n, Chem. Commun. , 495 (1970). 14) ]. Halpe rn, Acc. Clzem. Res. , 3, 386 (1'5'10 ).
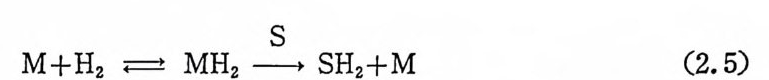 s
s
음 기질(올레핀, S) 과 반응하여 수소화된 생성물 (SH2) 을 생성하고 금속착물 (M) 을재생하게 된다. 한편을테핀배위 경로는 다음식 (2.6) 과 같이 먼처 금속착물촉매에 올레핀이 배위되고 배위된 올레핀과 수소분자가 반응하여 포화된 생성물을 생성시키고 금속착물촉매가 재생되는 과정이다.
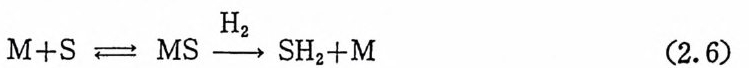 M+S ~ MS 一H2 SH2+M (2.6)
M+S ~ MS 一H2 SH2+M (2.6)
대부분의 경우, 총괄반응 (overall reac ti on) 에 관한 반응속도를 측 정하여 얻은 견과로부터 메카니즘을 추정, 제시한다. 따라서 복잡 한 여 러 반응단계 (multi s t e p)를 포함하는 촉매 작용에 대 한 구체 적 인 메카니즘은 상당한 불충분한 접을 갖고 있다. . 가능한 경우에는 각 단계를 별도로 연구조사함으로 총괄반응의 메카니즘 규명에 도움이 된 경우도 있다 .15) 중간체(i n t ermed i a t e) 의 분리확인, 동위원소에 의 한 상호교환반응 실험 , 반응속도에 미 치 는 동위원소의 영 향 (k i ne ti c iso to p e eff ec t) 및 리 간드가 반응에 미 치 는 영 향동도 반응메 카니 즘의 연구에 큰 도움을 주었다. 그 실례들을 들어서 자세히 고찰하여 보 자. (1) 二水素 (d i hy dro g en, H2) 의 均衡分離 (homol ytic sp litting ) 反應머 I’| 니즘 반응메카니즘에 관하여 가장 자세히 연구된 올레핀의 수소화반응 온 역 시 W ilkin s on 촉매 (RhCl(P(C 晶 )3)3) 에 의 한 시 클로핵 센 및 스티 렌의 수소화반응이 다. W ilkin s on 둥은 1966 년에 최 초로 상기 반응의 총괄반응의 속도를 측정하였으며, 그때 이미 트리페닐포스 핀 리간드 한개가 해리되는 과정이 포함되어 있을것이라고제시하
15) a) J. Halpe r n, in: Y. Ishii and M. Tsuts u , Eds. , Or g ano t rans iti on - M.따 Chemi st r y Plenum Pub!. , (1975). Cb)h eCm. . AS.o cT. ,o lm96a, n2, 76P2. Z0. 97M4e)a. kin , D. L. Lin d ner and J. P. Jes son, ]. Am.
였 다. 16) 그리 고 식 (2. 5) 와 같은 금속 - 수소화물 경 로와 동시 에 삭 (2:6) 과 같은 올레판의 배위 경로 동을 거쳐 수소화반응이 일어날 것 이 라고 제 시 하였 다. 16) 그후 Hal p ern15) 과 Tolman15b) 등은 각각 찰 계획되고 실험된 반응속도 축정을 동하여 복잡한 여러 과정 ~ 에서 각 과정에 관한 보고를 할 수 있었다. 여기서는 Hal p ern 의 연 구결과를 좀더 자세히 살펴보고자 한다. 왜냐하면 아직까지 발표된 연구 중에서, 특히 금속착물 촉매에 의한 울레핀의 수소화 반응 중 에서 Hal p ern 의 연구가 가장 찰된 연구의 하나로 항상 논의되기 때문이다. 우선 W ilkin s on 착물 RhCl(P(C&Hs)3)3 는 배위 능력 이 벌로 없는 용매(예를 들면 벤젠)에서 올레핀이나 수소 CH2) 가 共存하지 않을 시는 어떻게 되는가 알아 보자. 한개의 트리페닐포스핀이 해리되어 3 배위착물 RhCl(P(C&Hs)a)2 이 되고 이어서 이 3 배위 착물은 二合 반응 (d i mer i za ti on) 을 일으켜 Rh2Cl2(P(CGHs)3)4 를 생 성 한다(석 (2. 7) 및 (2.8) 참조). 중간체 RhCl(P(C6Hs)a)2 의 농도는 극히 낮고 Rh2Clz 0P(C 晶 )3)4 의 생성속도가 매우 파르기 때문에 실제 스팩트럼 변화·
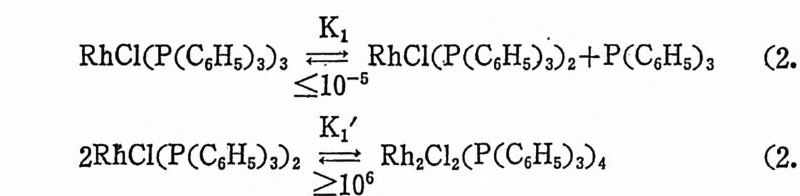 RhCl(P(C 晶 )a)3 ~K1 RhCl(P(C6H 야 )2+P(C 晶 )3 (2. 7)
RhCl(P(C 晶 )a)3 ~K1 RhCl(P(C6H 야 )2+P(C 晶 )3 (2. 7)
의 측정요로부터 얻을 수 있는 것은 식 (2.9) 의 평형분이다. 이렇게 스펙트럼 데이타에 의해서 구한 평형상수의 값이 약 10 -4 mol 크 (25° · C 에서)이다. 한편 이합체 Rh2Cl2(P(C&Hs)3)4 는 순수하게 合成될
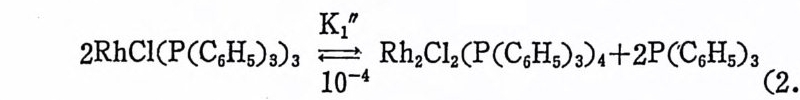 K1f1
K1f1
수 있을 분 아니라 16) 붉은 이합체의 용액에서라도 단위체 RhCI; (P (C 晶 )3)2 의 농도는 무시할 칭도이다. 이러한 사실을 근거로 해 16S) oJc.. , AA. , O1s7b1o1r n(1, 9F 6.6 ).H . Jar din e , J. F. Young and G. Wi lki n s on, J. Chem_
서 식 (2. 8) 의 평 형 상수를 약 1061 mo1-1 로 하고 식 (2. 7) 의 평 형 상 수를 K1 척 o-smol1-1=(K i /K1') o.s로 구하였다. 이상의 평형상수 들로부터 RhCI(P(C G Hs) 닝)3 를 벤젠에 녹였 을 때 용액 중에 촌재 하 는 대부분의 로듐은 제개의 트리페널포스핀을 배위하고 있는 RhCl (P(C6Hs)3) 3 로 간주된다. 다음으로 W ilkin s on 촉매 가 수소 CH2) 와 반응하여 6 배 위 착물 RhCl H2(P(C 晶 )3)3 를 형성하는 반응을 살펴보자. 용액의 31P-NMR::!:::.. 펙 트럼 측정 에 의 하면 RhClHi (P( C5Hs)3)3 에 서 두 개 의 수소 CH) 는 시 스 위 치 에 있 음이 밝혀 졌 다. 15b ) 수소 CH2) 와 RhCI(P(C6Hs)3)3 의 반응속도 측정은 470nm 에서 흡수도의 변화를 측정함으로써 가능하 다. 식 (2. 9) 에 의 한 Rh2Cli( P( C6Hs)3)4 의 생 성 을 막기 위 하여 과량 의 트리페널포스핀을 가하고 반응속도를 측정한 견과 과량의 수소 (H2) 촌재 하에 서 RhCI( P- (C i Hs) 야 와 H2 의 반응온 다음 속도석 에 따른다 ( 식 (2.10)) . 그러나 실제 측정 가능한 kobs 는 가해준 트리페 닐포스핀의 농도와 수소 CH2) 의 압력 에 따라 변한다. 따라서 RhCl (P(C6H5)3)3 와 H2 가 적 접 반응하여 RhCIH2(P(C5Hs)3)a 를 생 성 하
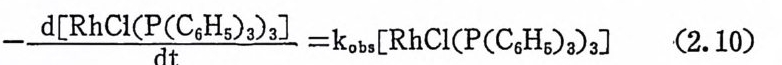 d[RhCl(dPt~ 晶 )3) 』 =kobs[RhC J (P(C 晶 )3)3] (2.10)
d[RhCl(dPt~ 晶 )3) 』 =kobs[RhC J (P(C 晶 )3)3] (2.10)
논 과정(식 (2.11) ) 이외에 트리페닐포스핀의 해리(식 (2.7) )에 따라서 일어나는 과정(식 (2.12)-(2.7)-(2.13) )들을 고려해야 할 것이다. 상 기 식 들울 고려 하면 Wi lkin s on 착물과 수소 CH2) 오回 반응의 총괄속 도식 은 식 (2.14) 와 같다.
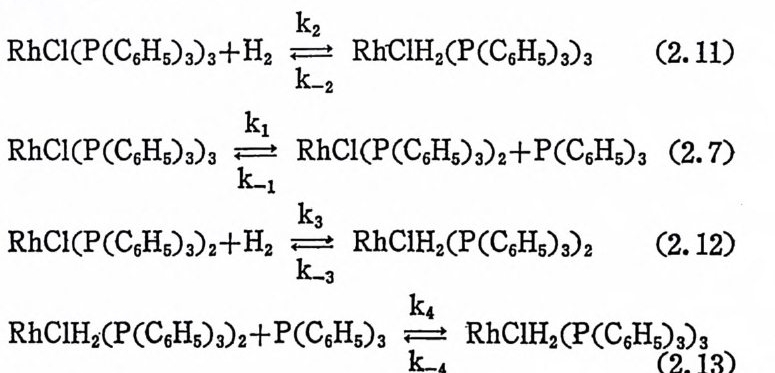 k2
k2
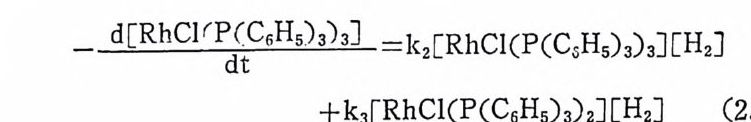 一 ~=k2dt [ RhCl(P(C 晶 )3) 나 [H 』
一 ~=k2dt [ RhCl(P(C 晶 )3) 나 [H 』
중간체 RhCl(P(C5 H s)3)2 에 대 하여 정 류상대 근사법 (ste a dy sta t e a pp rox i ma ti on) 을 적 용하떤 식 (2. 7) 및 식 (2. 12) 에 서 부터 아래 의 식 (2.15) 및 석 (2.16) 을 얻 게 된다. 이 어 서 식 (2. 10) 과 식 (2.16) 을 비교함으로써 식 (2.17) 을 얻게 된다. 일정한 〔 P(CGHs) 니에서 [H2J -1
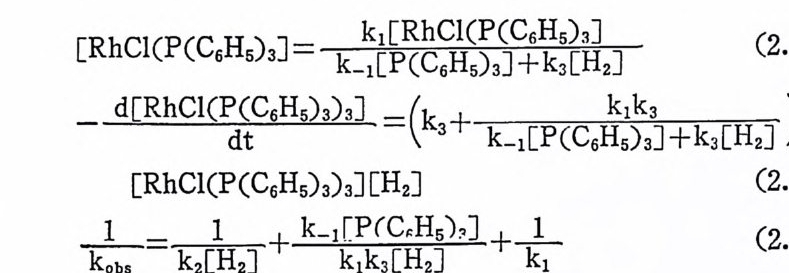 [RhCl(P(C5Hs)3J = ~k 키〔P 晶( C6H5) )니 +k3 〔 .H』 』 (2.15)
[RhCl(P(C5Hs)3J = ~k 키〔P 晶( C6H5) )니 +k3 〔 .H』 』 (2.15)
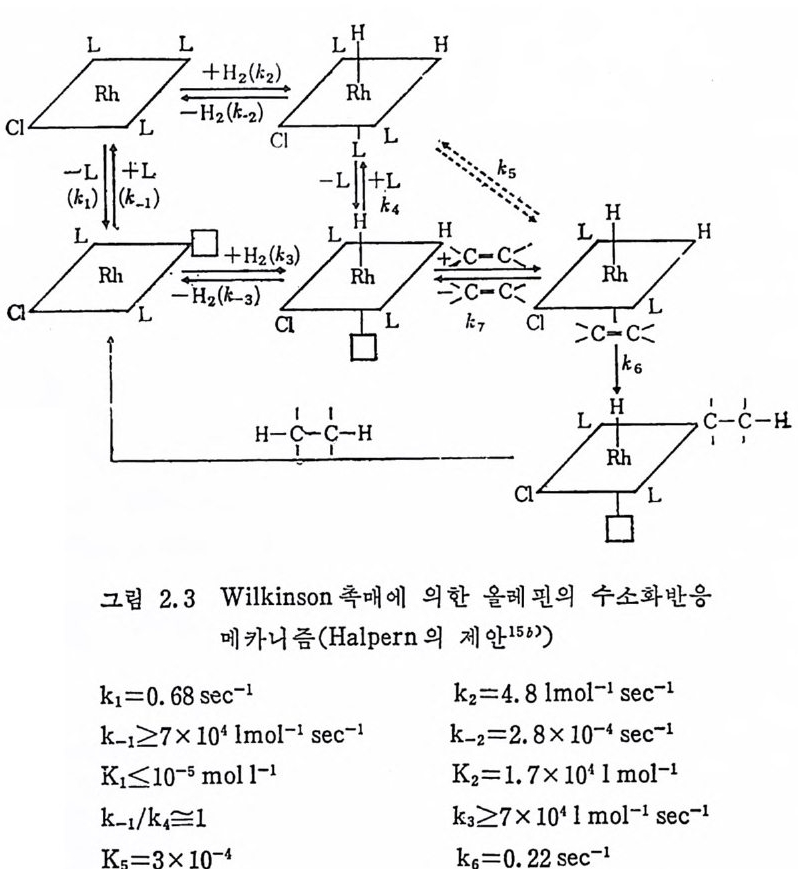
과 k 갑S 울 도시하여 얻어지는 직선의 철편은 k_1 이 된다. 한편 〔 H 』를 일정하게 유지하고 얻어지는 kobs 의 역수 (k 감.)와 [P(C6 Hs)3 J울 도시하면 얻어지는 직선의 기울기 및 철편은 k: 巨 및 k_1/k3 가 된다. 또한 K1~ 이미 정하여졌으므로 K =k1/k-1 을 이용하여 k1 을 결정할 수 있게 된다. 계속해서 비슷한 방법으로 얻은 속도상 수 및 평형상수를 그림 2.3 의 반응과정도시에 실었다. k2 와 k3 값 을 비 교하면 RhCl(P(C 晶 )3)2 가 최 소한 104 배 이 상 RhCl(P(C6 Hs)3)3 보다 빠르게 H2 와 반응함을 알 수 있 다. 용액 중에 과량으로 P(C5Hs)3 및 H2 가 존재 하게 되 면 이 합체 인 Rh2Cl2CP(C5Hs)3)4 는 일체 생성되지 못하게 된다. 따라서 올레핀이 촌재하지 않는다면 가 장 안정 한 화합물은 RhCIH2(P(CsHs)3)3 이 된다. 마지막으로 올레핀의 수소화과정을 살펴보자. 대부분의 실험조건 에 서 첫 단계 인 RhCl(P(C6Hs) 야 가 수소 CH2) 와 반응하여 RhCIH2 (P(C6Hs)3)3 로 되는 과정이 올레핀의 수소화반응 보다는 훨싼 빠 론 것 으로 나타났다. 따라서 RhCIH2CP(CsHs)3)3 생 성 이 후의 어 떤 과정이 총괄반응의 속도결정단계가 될 것이다. 이 접을 규명하기
 二二――Q〕7 § _¢-H.
二二――Q〕7 § _¢-H.
위하여 수소가 과량으로 촌재하지 않는 조건(죽 非촉매적 조건) 하 에 서 , 그리 고 과량의 포스핀이 존재 하는 조건에 서 , RhCIH2CP(Cs Hs)3)3 와 올레,;JJ.의 반응에 관하여 반응속도 및 평형상수를 측정하 였 다. RhCIHi (P( CsHs)3)3 중의 P(C6Hs)3 리 간드 한 개 가 올레 .;lJ.에 의 해서 치환되는 반응은 두 단계로서 5 배위 착물 RhCIH2(P(CsHs)3)2 를 거쳐 일어나지만 평형상수 Ks 로도 표현된다(그립 2.3 참조). 다음 과정은 그림 2.3 의 k6 과정으로 Rh-H 결합에 삽입되며, 이 어서 환원성제거반응 (reduc ti ve e li m i na ti on) 으로 알칸이 제거되고 로 듐착물은 다시 촉매순환과정으로 돌아가게 된다. 이 환원성제거반 응은 대단히 빠른 과정으로 생각된다. 왜냐하면 여러 가지 실험방
법으로(광학적 홉광도 측정 또는 NMR 동의 방법으로) 접출을 시 도하였으나 충분한 농도의 알키로듐착물을 측정하지 못했기 때문이 다. 따라서 유기질(울레편) S 의 수소화 반응속도 rH 는 식 (2.18) 이 되며, 여기서 RhCIH2(P(CGHs)3)3 와 RhCIH2(P(C6H5)3)S 는 평형석 (2.19) 의 관계에 있다. 위에서 기술한 비촉매적 조건에서 다음식
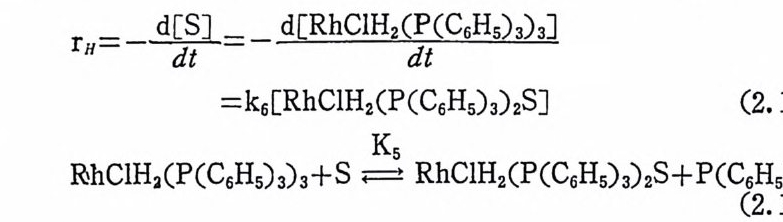 rH=-d d隣t〕 =• -d 〔 RhCIH2(Pd(t C 6Hs)3) 』
rH=-d d隣t〕 =• -d 〔 RhCIH2(Pd(t C 6Hs)3) 』
(2. 20) 은 반응초기 에 만 성 립 되 지 만, 촉매 적 조건(수소 CH2) 가 과량으 로 존재 하는 조건)에 서 는 RhCl(P(C6Hs)3)2 및 RhCl(P(C6Hs)a)3 의 수소화 반응이 매우 빠르기 때문에 식 (2.20) 은적철한가정이 된다.
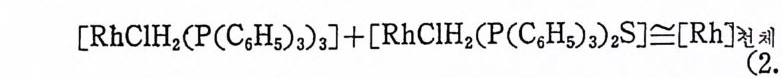 [RhC1H2(P(C 晶 )3) 급 + 〔 RhClH z( P(C 晶 )3)2S]::::[Rh] 천 체
[RhC1H2(P(C 晶 )3) 급 + 〔 RhClH z( P(C 晶 )3)2S]::::[Rh] 천 체
따라서 식 (2.19) 로부터 석 (2. 21) 을 얻 게 되 고, 석 (2. 20) 및 (2. 21 ) 로부터 석 (2.22) 을 얻게 되다.
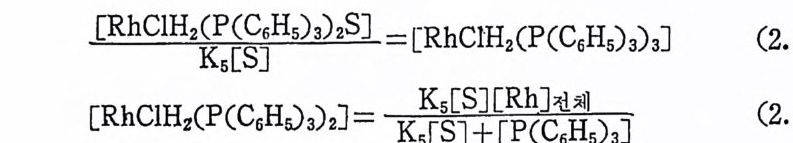 [R hClH2(P(C6 助 )2 언 = [RhClH2CPCCs 助)나 (2. 21 )
[R hClH2(P(C6 助 )2 언 = [RhClH2CPCCs 助)나 (2. 21 )
식 (2. 22) 와 식 (2.18) 에 서 부터 기 질 (올레 편) S 의 수소화반응 속 도 rH 에 관한 식 (2.23) 을 얻게 된다. rH 는 속도상수 및 평형상수 로 표현되는 샘이라고 볼 수도 있다. 다시 말하면 〔 Rh] 전체는 어 느 실험조건에서도 일정하게 . 볼 수 있으며, 〔 S] 와 [L 〕은 각실험에 서 과량으로 일정하게 유지시킬 수 있기 때문이다. 실험적으로 [H2 J =O 이며 〔 P(CdHs) 』=일정(과량)일 때 [RhCl( P. (C6Hs)3) 』三
 rH= k6K5[S][Rh] 전제 (2.23)
rH= k6K5[S][Rh] 전제 (2.23)
[Rh] 전체 이기 때문에, 과량이면서 일정하게 유지할 수 있는 S 의
농도를 변화시키면서 초기 반응속도를 측정하여 rH 를 얻은 다음 r? 와 [S] -틀 도시하여 얻은 직선의 절편과 기울기에서부터 k6 및 K5 를얻을수있다(식 (2.23) 의 역수식 (2.24) 참조).
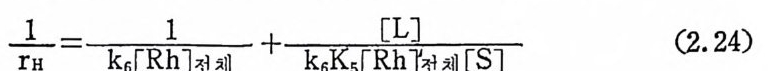 士 \[R\] 전제 + k6K 詞晶전체 [S] (2.2 4)
士 \[R\] 전제 + k6K 詞晶전체 [S] (2.2 4)
이 제 까자 살펴 본 것 은 주로 식 (2. 5) 로 표현된 끔속一수소화물 (me t al b y dr i de) 경 로에 따른 메 카니즘이 었 다. 이 제 부터 는 식 (2. 6) 으로 표현 되는 울레핀배위경로에 관하여 고찰하여 보자. 죽 RhCl(P(C6Hs)3) (또는 RhCl(P(CGHs)3)2:) 가 올레 핀과 반응하여 RhCl( 울레 편 )(P(Cs Hs)3)2 를 형 성 하는 과정 을 금속一수소화물경 로와 비 교해 본다. 아태 의 식 (2.25) 에서 보는 바와 같이 평형상수 K8 은 평형상수 K2Ck~/ k-2= 1. 7X104lmol-1) 보다 매우 적어서 올레핀배위경로는 열역학적오 로 금속-수소화물경로보다 상당히 불리한 경로이다.
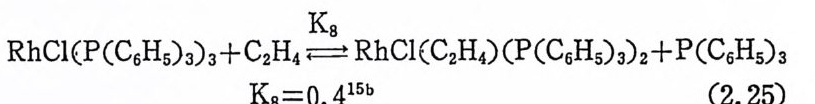 K8
K8
한 개의 금속―수소 결합을 갖고 있는 RhH(CO)(P(CsHs)3)3 및 RuHCl(P(C6Hs)3)3 둥을 촉매로 사용하는 경우에는 일반적으로 울레 핀배위경로(식 (2.6) )가 적용된다. RhH(CO)(P(CsHs)3)3 를 예로 물어 보자. 여기서도 최초의 단계는 포스편리간드 한개가해리되는과정 이다. 버訖간용액에서 리간드 P(C6H5)3 의 해리는 트란스―사각평면 형착물 RhH(CO)(P(C6H 야 )2 를 생성시키며, 4 배위착물 RhH(CO) (P(CsHs)3)2 는 붉은 용액에서 또 하나의 리간드를 해리시켜 3 배위 착물 RhH(CO)(P(C 晶 )9 를 생 성 한다(식 (2. 26) 참조). 착물의 농도 가 10-3M 정도일 때는 4 배위착물 RhH(CO)(P(CsHs)3)2 로 대부분 존재한다 .1 7) 다음의 실험적 결과에 의하면 RhH(CO)(PCCsHs)3)3 에 의한 울레 판의 수소화반응은 올레핀배위경로를 거쳐 일어날 것이라고 추정된 다. 4),1 7) ~ilkin s on, J. Chem. So c. A, 2665 (1968).
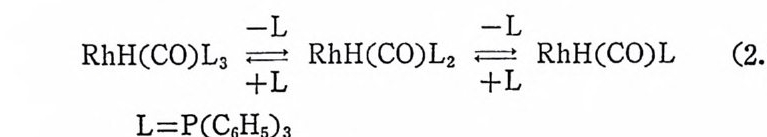 RhH(CO)L3 -~L RhH(CO)L2 ~-L RhH(CO)L (2. 26)
RhH(CO)L3 -~L RhH(CO)L2 ~-L RhH(CO)L (2. 26)
첫째, 올레핀이 촌재하지 않으면 촉매는수소와반응하지 않는다. 즉 석 (2.27) 과 같은 반응의 평형은 거의 완전하게 왼쪽으로 치우쳐 있다.
![]() RhH(CO)(P(C5Hs)3)2+H2 .=:t RhH3(CO)(P(C5Hs)3)2 (2. 27)
RhH(CO)(P(C5Hs)3)2+H2 .=:t RhH3(CO)(P(C5Hs)3)2 (2. 27)
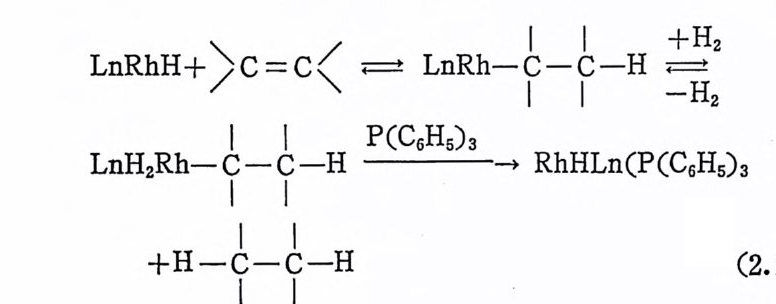
둘째, 4 배위착물 RhH(CO)(P(C6Hs)3)2 는 CF2=CF2 와 반응하여 안정 한 사각평 면형 착물 트란스 _Rh(-CF2CF2H) (CO) (P(C6H5)3)z 를 생성한다. 이 착물은 과량의 P(C6Hs) J의 존재하에서, 50°C 에서, 수소 (PH2=70 기압)와 반응하여 C2F4H2 를 생성하고 최초의 5 배위 착물 RhH(CO)(P(C6H5)3)3 로 돌아간다(식 (2. 28) 참조). 세 째 , RhH(CO)(P ( C6H5)3)3 는 Wi lkin s on 촉매 RhCl(P(C5Hs)3):i- 오뜹 다르게 l- 울레핀의 이성질화반응을 상당한 속도로 진행시킨 다. 이 실험적 결과로부터 울레핀의 삽입반응(식 (2.28) 의 첫단계)이 가역학적으로 일어남을 알 수 있다. 네째, 올레핀의 수소화반응 속도는 수소압력 증가에 따라 비례적
 LnRhH+\ )C=C(,\/ _ .=:t LnRh— c|| — C|1 — H =-+ HH2 2
LnRhH+\ )C=C(,\/ _ .=:t LnRh— c|| — C|1 — H =-+ HH2 2
으로 증가한다. 위에서 살펴본 W il k i nson 촉매 RhCl(P(C6H 야 )3 에 의한 올레핀의 수소화반응의 속도는 식 (2.23) 에서 보여준 바와 같 이 수소의 압력 (농도)에 무관하였 다. 따라서 RhH(CO)(P(C6H 야 )3 와 RhCl(P(C 晶 )3)3 에 의 한 올레핀의 수소화 반응은 서 로 다른 메 카니즘으로 진행된다고 볼 수 있다. 즉 RhH(CO)(P(C6Hs)3)s 에 의
한 반응은 울리 1 핀경로를 거쳐 일어나며, 석 (2.28) 의 둘째번 단계인 수소 CH2 ) 의 산화성 첨 가반응 단계 가 율속과정 이 된다. 실제로 RhH(CO)(P(C6Hs)3)3 에 의한 울레핀의 수소화반응은 아 직 까지 W ilk in s on 촉매 에 의 한 올레 핀의 수소화반응처 럼 자세 하게 연구되어 있지 못하다. 그러나 착물 RhH(CO)(P(C6Hs) 3 )3 가 말단 올레핀기에 대하여 매우 선택성이 높은 수소화반응을 일으킨다는 사실은 이미 발표된 바 있다 .8) (2) 二水素 (d i h y dro g en, H2) 의 不均 衡 分 ~( he t erol yti c sp li t tin g ) 反 應 메카니즘 몇몇의 촉매적 수소화반응에서 수소분자가 불군형분리되어 하나 의 금속一수소 결합과 하나의 양성자가 생성되는 과정이 제시되었 다(식 (2.29) 참조 ).4),18) 이러한 반응과정은 특히 극성용매에서 가능
 M+H2 —-. MH+H+ (2.29)
M+H2 —-. MH+H+ (2.29)
할 것이다. 많은 경우에 금속에 배위되어 있는 음이온성 리간드가 수소의 불군형 분리 에 의 해 서 생 성 되 는 수소화이 온 (h y dr i de i on) 에 의 해 서 치 환된다(식 (2. 30) 참조).
 MX 述一 MH+H++x- (2.30)
MX 述一 MH+H++x- (2.30)
수소 CH2) 와 重水素 化된 (deu t ra t ed) 용매(예를 들면 물 또는 알코 올) 사이에 일어나는 상호교환반응은 수소의 불균형분리반응의 좋 은 예가 된다. 죽 식 (2.29) 에 이어서 (2.31) 그리고 식 (2.32) 에 의 한 水素一重水 素 교환반응을 들 수 있다. 이와같은상호교환반응실 험에서는 D2 의 생성도 발견되는데, D2 의 생성은 아래의 식 (2.33)
 H++D20 一 D++HDO (2. 31 )
H++D20 一 D++HDO (2. 31 )
과 식 (2.34) 로 설명된다. 그러나 금속-수소의 결합을 M8+ ― H5- 로 생각하면, 석 (2.33) 보다는 식(2 .35) 에 의한 파생성이 가능할 것이
18) G. Henric i-O l i ve /Ol ive , Coordin ati on and Cata l ys i s (Monog r ap h i1i Modern Chemi st r y Serie s ), Verlag Chemi e• W ein h eim , N. Y. 1977. p.1 73.
다. 즉 석 (2.29), 식 (2.3 1) 그리고 식 (2.32) 에 의해서 생성된 HD
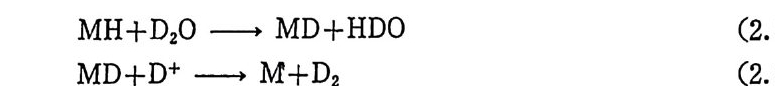 MH+D20 --+ MD+HDO (2.33)
MH+D20 --+ MD+HDO (2.33)
는 금속의 배 위 권 (coordin a ti on s p here) 을 떠 나기 전에 다시 분리 틱 어 이번에는 MD 와 H+ 를 생성하게 되고 이어서 식 (2.34) 에 의해서 D2 가 생성될 것이다 .9) 자연계 에 손재 하는 수소활성 화효소 (h y drogenase) 도 수소의 불군형
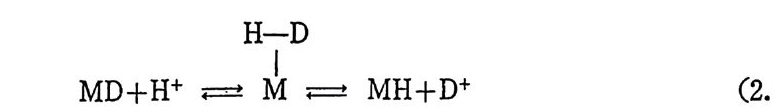 H-D
H-D
분리반응을 일으키는 것으로 알려져 있다 .4) 효소의 일부분인 전이 금속에 의하여 수소의 불군형분리가 일어나고, 생성된 양성자는 효 소의 다른 한 부분인 영기성 자리 B 에 결합되는 것으로 알려져 있 다(식 (2. 36) 참조). 산성 용액 에 서 수소의 불군형 분리 는 감소될 것 이
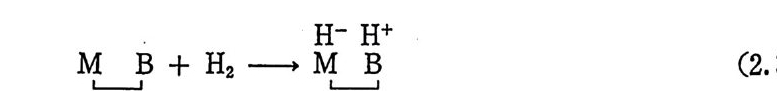 H-H +
H-H +
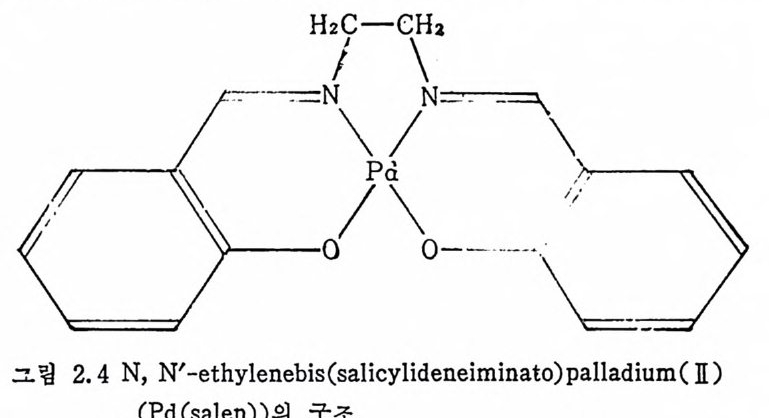
다. 왜냐하면 낮은 p H 에서는 영기성자리 B 는 이미 중화되어 더이 상의 양성자를 받을 수가 없기 때문이다. 실제로 자연계에 촌재하는 효소의 활성자리 (acti ve s it e) 에 관하여 알려진 것은 별로 없으며, 또한 효소주위에 결합되어 있는 거대한 단백질 때문에 연구에도 많은 난접이 있다. 그러나 자연계에서 발 견되는 전이금속화합물은 많은 경우에 4 자리 평면형 리간드(포르 피린 또는 프탈로시아닌 등)의 착물임이 이미 알려졌다. 따라서 최 근에는 수소활성화효소의 모델화합물로 Pd(1I)-Sh iff염기 착물이 합성, 연구된 바 있다.” 이 착물 Pd(salen) (그립 2.4 참조)은 자연 계의 수소활성화효소의 성질과 매우 비슷한 성질을 보여준다. 죽 Pd(salen) 은 H/D 상호교환반응, 기 질 (subs t ra te)의 수소화반응에 관한 반옹속도, 그리 고 반웅활성 도에 대 한 pH 의 영 향 등에 서 Pd(salen) 과 자연계에서 발견되는 수소활성화효소는 상당히 비슷한결과를보
여준다”· Pd(salen) 의 C2H50D 서 스펜션은 H2 와 C2HsOD 사이 에 H/D 상호
 H2I9 一 C\H 2
H2I9 一 C\H 2
교환반응을 일으키게 하며, Pd(salen) 의 DMF( 디메틸포름아미드)용 액은 올레판기질의 수소화반응을 일으키게 한다. 산성용액에서 올 레핀의 수소화 반응은 완전히 중지되는 한편 NaOH 를 가하면 [Na OH]:=O. IM 에 서 수소화반응의 속도는 최 대 로 중가한다. Pd(salen) 의 DMF 용액에서 l- 핵센의 수소화반응의 속도를 측정한 결과 다음 (식 (2.36)~(2.38) )의 속도식을 얻었다. 여기서 rH 는 수소화반옹의 속도이며 S 는 기질(올레편)이고, a,a',b 및 b’ 는 상수이다. 이와 동일한 속도식을 자연계에서 추출된 수소활성화효소의 연구에서도 이미 얻은 바 있—다 .19) -—rrHlH= a=a+'+-[ —SPb H J 2 (2. 36) l bI (2.37) 7H~[Pd] 。 (2. 38) ([Pd] 。온 최초에 넣어준 Pd 착물의 전농도) 이상의 속도식을 반응과정에 적용시키기 전에 우선 가능한 반응 예카니즘을 생각해보자. C2HsOD 의 서스펜션에서는(즉 고체상태에
19) D. klein e r and R. H. Burris. Bio c him . Bio p h y s , Acta , 212, 417 (1970).
서는) 팔라듐 금속은 동일 평면상에서 2 개의 산소 및 2 개의 질소 원자들에 의해서 싸여져 있다. 팔라듐평면 상하에는 또다른 팔라듐 울 포함하는 평면이 있게 된다. 용액 중에서는 배위능력이 강한 용 매 DMF 가 팔라듐을 포함하는 평면의 상하 중에서 최소한 하나의 축방향을 차지하게 될 것이다. 따라서 고체상태이거나또는용액 중 에서 수소와 올레판이 동시에 배위가능한 배위자리가 없다. 따라서 리간드의 해리가 불가피하게 된다. 위에서 기술한 바와 같이 Pd (salen) 이 자연계의 수소활성화효소와 매우 흡사한 성질을 보인다 논 접, 특히 수소화반응에 대한 p H의 영향울 고려하면, H2 의 붙군 형분해반응과 Pd(salen) 중 한 개의 배위자리에서 Pd 와 리간드사이 의 결합이 끊어지는 반응이 동시에 일어날 것으로 보인다(그립 2.5 참조). 여기서 한 개의 페녹시배위자리는 페놀기가 되고 동시에 금속 ―수소 화합물이 생성된다. 죽 리간드의 도움에 힘입어 수소분자의 불군형분리반응이 일어나게 되었다. 이제二는 H그'— 림 ~H2. 5 :의 〈_ 2 〉가- 보_여: _ 주는: 바-와 같l이 :올H레 <핀2>의 배위 에 그립 2. 5 Pd(sa i en) 에 의 한 H2 의 불균형 분리 반웅, O--N--N--0 는 salen, L 은 Pd 또는 DMF( 용매 )이 다. 필요한 빈 배위자타가 있다. 이렇게 하여 배위된 올레핀은 Pd-H 사 이에 삽입반응을 일으켜 Pd- 알킬형의 착물을 형성하게 되고, 배위 된 알킬기는 같은 분자내의 페놀기와 반응하여 알칸을생성하며 동 시에 초기의 금속착물을 생성하게 된다. 지금까지 기술한 Pd(salen) 을 상기한 효소와 비교한다면 다음과 같다. 죽 효소의 영기성자리 B 는 Pd(salen) 의 페녹시기와 비교된 `
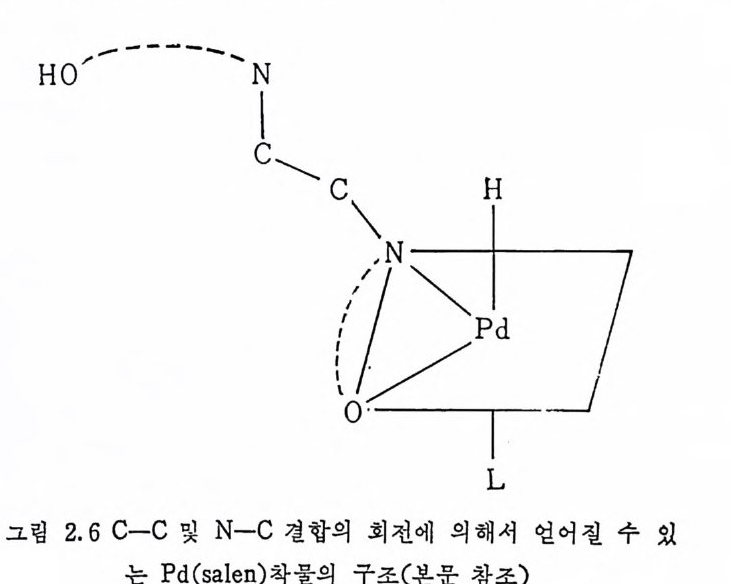
다. 왜냐하면 페녹시기는 양성자를 받으면서 금속의 배위자리를 떠 나지만 아직도 착물의 일부이기 때문이나. 여기서 알칸의 생성은 Pd -알킬 착물의 一次 분해반응에 의한 것이다. 죽 알칸의 생성반응은 용매 중에 촌재하는 수소이온이 참여하는 반응이 아니고 분자 내의 배위자리에 결합되어 있는 양성자와 배위되어 있는 알킬기의 반응 이다. 그림 2.5 의 〈 2 〉가 갖는 빈 자리가 올레.si:J.의 배위에 충분하지 못할 경우에는 페녹시기에 이웃하는 中性 질소배위자리 (neutr a l nit ro g en lig and) 가 동시에 금속으로부터 멀리 떨어져 나가면서 충분한 배위 자리 리되 를기 내위 줄해 서수도는 있C -다C( 그및림 N2.— 6 C참 조사) .이 의질 소시자그리마 결가합 금(속그림으 로2부.6터 참 조멀) 의는 실회험전적이 결있과어로야 한보다아.서 P실d(s제al로en )C 이— C올 레및 판 N에- C대 한사 이선의택 성시이그 마낮걷다
 HO' ------... N '_lC
HO' ------... N '_lC
합의 회전이 일어나고, Pd-N 결합이 꿇어져서(그립 2.6 참조) 울레 핀의 배위에 충분한 자리가 확보되어 올레핀에 대한 선택성이 낮은 것으로 판단되기도 한다. 이상의 반응메카니즘을 기초로 하여 식 (2.39)~(2.41) 을 세울 수
있다. 여기서 Pd 는 수소 또는 올레편과 반응하지 않은 팔라듐착물 ' (Pd(salen) 또는 Pd(salen) (용매))이며 PdH(OH) 는 수소 CH2) 와 반 응하여 생 성 되 는 그림 2. 5 의 〈 2 〉와 같은 화합물, 그리 고 Pd( 알킬) (OH!) 는 PdH(OH) 가 올레 핀과 반응하여 생 성 된 Pd- 알킬 화합물아 다. 식 (2.39) ― (2.41) 을 다시 살펴보면, 식 (2.39) 에 의해서 수소는
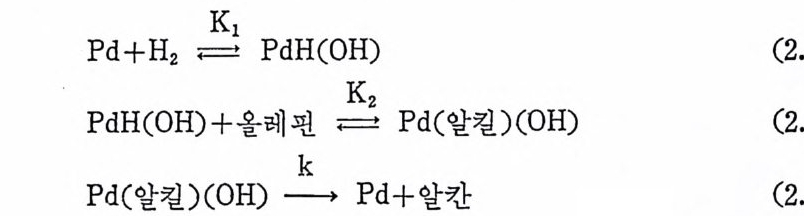 Pd+H2 .=K:1! PdH(OH) (2.39)
Pd+H2 .=K:1! PdH(OH) (2.39)
불군형분리되고, 식 (2.40) 에 의해서 착물 Pd(salen) 이 올레핀의 이 성질화 반응에 촉매적 역할을 함을 설명할 수 있고 식 (2.41) 에 의 해서 알칸이 생성되고 4 자리 리간드 salen 이 다시 팔라듐 주위에 평면을 이루어 초기 착물 Pd(salen) 을 재생한다는 것이 설명된다. 알칸의 생성속도는 식 (2.42) 이 된다. 최초의 Pd 착물의 농도를 [Pd 〕。 라고 하면 식 (2. 43) 이 성 립 되 고 식 (2. 44) 부터 석 (2. 46 ;) 을 얻 게 된다. 반응초기에는
 rH=d[ 알칸 ]/d t =k[Pd( 알킬 )(OH)] (2. 42)
rH=d[ 알칸 ]/d t =k[Pd( 알킬 )(OH)] (2. 42)
[울레핀]三[올레편]。([올레포tlJ o 은 반응최초의 올레핀의 농도)이라 고 볼 수 있으므로 식 (2.47) 을 얻는다.
 rH= 1 +kKKl1[KH2 니[H + 』K [1PKd2][ 。H[ 니올 [레 올_;i레:J ]팬。 ]。 (2.47)
rH= 1 +kKKl1[KH2 니[H + 』K [1PKd2][ 。H[ 니올 [레 올_;i레:J ]팬。 ]。 (2.47)
이렇게 하여 얻은 식 (2.47) 은 실험으로부터 얻은 속도식 (2.36),.. (2.37) 및 (2.38) 과 비교하면 일치됨을 알 수 있다. 따라서 각 단· 계의 속도상수 및 평형상수 k, K1 및 K2 를 쉽게 구할 수 있다.
실제로 식 (2.40) 은 지나치개 간단히 표현된 것일 수도 있다. 다 시 말하면 반응속도측정 으로는 구별하기 힘 든 식 (2. 48 ) 과 같은 평 형이 있을 수 있기 때문이다. 그렇다면 실험에서 구한 K2 값은 설 제는 K z' K2 의 값일 수도 있다.
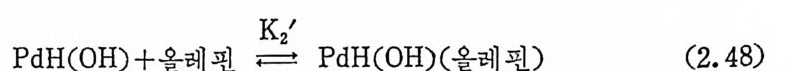 K2I
K2I
이제까지 고찰한 Pd(salen) 에 관한 것들을 종합하면 Pd(salen) 은 수소활성화효소와 매우 흡사한 성질을 갖고 있다. 전이금속이온울 갖고 있는 다른 효소들도 이제까지 논의된 메카니즘과 바슷한 메카 니즘으로그기능을 할 것이타고제시된 바도 있다尸 또한 Pd(salen) 에 의하여 활성화되는 작은 공유결합 분자 CO2, N2 등)들 그리고 C -N, C-H 및 C ― C 결합들도 이제까지 고찰된 수소 CH2) 의 불균형 분리메카니즘과 유사한 경로를 거쳐서 활성화될 것이라고제시된 바 있다 .9) (3) 選擇性 및 立睦特異性 (selec ti v ity and ste r eospe c if icity) 착물 RhH(CO)(P(CsHs)3)3 및 RuH(Cl)(P(C6Hs)3)3 이 말탄 올레 핀 (ter mi na l ole fi n) 에 대 하여 높은 선택 성 을 보여 주는 이 유는 주로 입체적인 것으로 알려졌다. 예를 들면, 아래식 (2.49) 에서 보여주는 바와 같이 두 개의 커다란 트리페닐포스핀은 결과적으로 알킬기의 시스 위치에 있게 되므로 R’ 이 큰 경우에 로듐―알킬 착물의 형성 이 어렵게 된다. Wi lki n s on 촉매 RhCl(P(C 晶 )3)3 에 의 한 올레 핀의 수소화반응도. 5 배 위 착물 중간체 인 RhClH2(P(CsHs)s)2( 그립 2. 3 참조)의 생 성 과정 에 우}와 비슷한 영향을 받게 될 것으로 추측된다. 그러나 RhCl(P(C6 H5)3)3 는 실제로 내부 올레핀 On t ernal ole fi n) 이나 고리형 올레핀 (c y clic ole fi n) 의 수소화 반응도 찰 일으킨다. 이같은 실험적 결과흘 설 명하기 위하여서는 Rh 과 P 간의 결합길이가 논의될 수도 있고, 두 ` 개의 P(C 晶 )3 의 상대적 위치가 논위될 수도 있다. 죽 예를 들어 서 6 배위 올레펀 착물 RhClH2C 〉 C=C 〈)(P (C 晶 )3)2( 그립 2.3 참 조)에 서 Rh-P 거 리 가 상당히 멀어 진다거 나, 또는 두 개 의 P(C6H5)3
 c ' ~_/;�h< /~oP P�P� RH3Rh P. ,H , ,,-.P:._P__,_ 'c -h \ 0r Po -c ,/ H/Rh h 03,RH'CI,
c ' ~_/;�h< /~oP P�P� RH3Rh P. ,H , ,,-.P:._P__,_ 'c -h \ 0r Po -c ,/ H/Rh h 03,RH'CI,
������ �t� �¤� �X��� ��<�t�� ���@�X� �����Q�D
 �
�
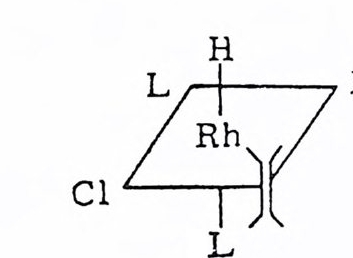
� J�D� �ij ���. H C Hl L�� �� �� �� ଽ� � t� ɰ�i� (isolated double bond) t� tȬ� X�p� ٳ�� �� ��t�ɰ�i�tǘ� ��ɰ�i�t� ��D� L
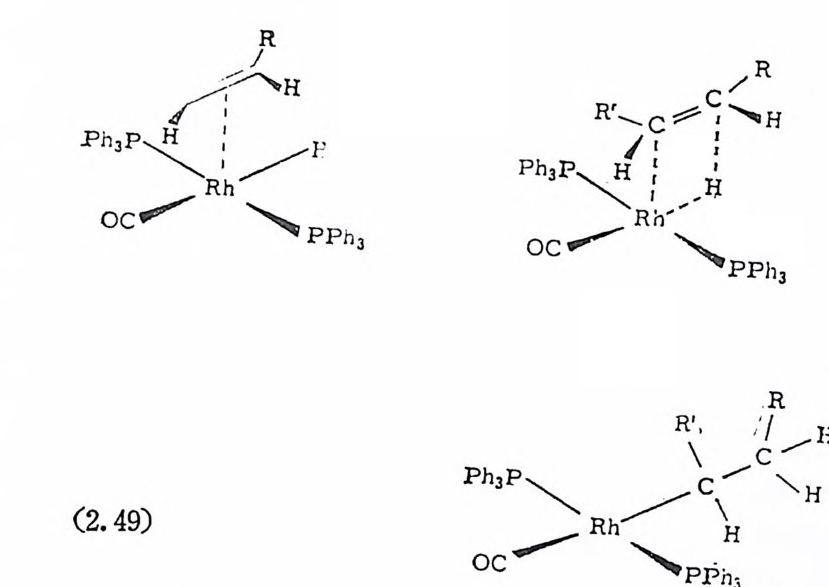
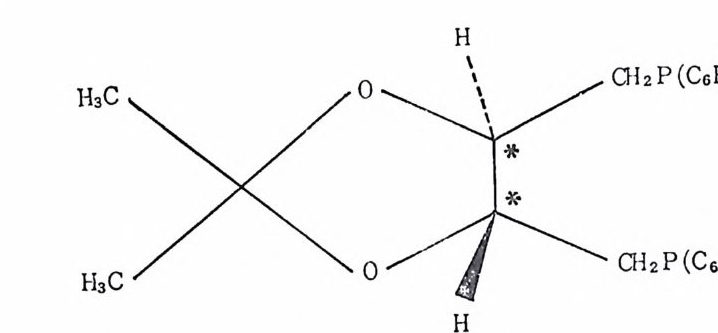
� ��t�ɰ�i�tǘ� ��� ��� ��i�̹ �q��<�\� ��T¤�Д� �|���Ĭ�� ��t � ��� �\�� � ��� 2.) �0L �@� �T���QX� �Ǵ�ݴt�1�, �҈� D��m��1 �T��Q�DǴ� 20)퍼 본다. Wi lk in s on 촉매 중에 P(C6Hs)3 를 P(C6Hs)(CH3)(C3H1) 으 로 바꾼 로듐착물을 촉매로 사용하여 광학적 불활성인 기질을 광학 적 활성의 물질로 수소화시킨 연구가 보고된 바 있다(석 (2.50) 참 조). 21) 식 (2. 50) 의 광학적 수운 (o pti cal yi eld) 은 5~15% 에 지 나지 않
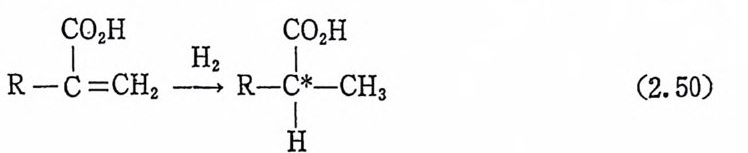 R -CC0 =2CHH 2 一 R— CC\*0 —2 HC H3 (2.50)
R -CC0 =2CHH 2 一 R— CC\*0 —2 HC H3 (2.50)
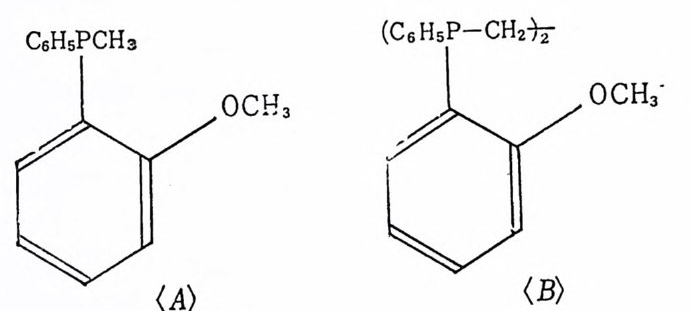
는다. 21) 그러 나 다음과 같은(아태 그립 〈 A 〉와 )두 개 의 비 대 칭 성 리간드를 사용하여 알파一아세트아미도아크릴산의 바대칭성 수 소화반응의 광학적 수울을 80~96% 로 올렸다 .22)
 CsHsPCH3 (CsHsP-CH2 늄
CsHsPCH3 (CsHsP-CH2 늄
아래 그림 과 같은 키 탈 디 포스핀 (chir a l d ip hosp h i ne) 리 간드를 포함 하는 로듐착물을 사용한 비대칭성 수소화반응도 비교적 높은 광학 적 수율울 주었 다. 23) 디 엔 (d i ene) 과 트리 엔 (t r i ene) 을 모노올레 핀 (monoole fi n) 으로 수소화 시키는 반응은 공업적인 면에서 응용되고 있다. 여러 곳에 불포화기 가 있 는 식 물성 기 름(p ol y unsa t ura t ed veg et a b le o i l) 을 선택 적 으로 수소 화시 키 는 데 공업 적 으로 사용되 는 촉매 는 주로 볼군일 (hete r og en eous)
21 ) W. S. Knowles and M. J. Sabacky, Chem. Comm1111. , 1445 (19 68). 22) a) W. S. knowles, M. J. Sabacky, B. D. Vi ne y ar d, Chem. Commun. , 10 (19 72). b) W.S. knowles, M.J. Sabacky , B.D. Vi ne y a rd and D.J. Wein · kauff , J. Am. Chem. Soc. , 97, 2567 (1! ?75). 23) a) T. P. Dang and H. B. kag an , Chem. Comm11n. , 481 (1971 ). b) W. Du· mont, J. C. Pouli n, T. P. Dang and H. B. Kag an , .T. Am. Chem. Soc. , 95, 8295 (19 73) .
 H\
H\
촉매이다. 한편 고도의 선택성이 요구되는 반응에서는불군일촉매겨l 보다는 군일촉매 계를 이 용한다. 하나의 예 를 돈다면 1, 5, 9- 시 클로도 데 카트리 엔을 시 클로도데 켄 (c y clododecene) 으로 만드는 수소화반응을 들 수 있 다. 상기 반응의 촉매 로는 (Co(CO)J( P (C4Hg )3 )2)2 또는 Ni I2: (P(C 晶 )3)2 가 사용되었다. 24) 또 하나의 예를 돈다면, [C o(CN)5] 3- · 및 Cr(CO)3(me t hy lbenzoa t e) 는 I, 3, 7- 옥타트리 엔을 수소화시 켜 1, 6- 옥타디엔과 I,5- 옥타디엔의 혼합물을 생성한다 .25) 이렇게 하여 생 성된 짝이중결합이 없는 (uncon juga t ed) 디엔은 결국 다시 천천히 수소 화된다. 짝이중결합이 있는 디엔 (con j u ga t ed d i ene) 을 수소화시킬 수 있는 ` 촉매로서는 Cr(CO)626) 및 (Cr(C0)2CCsHs)2)2m 등을 둘 수 있다. 특기 할 만한 접은, 상기 한 〔 Co(CN) 나 3- 및 Cr(C0)3(meth y lb enzoate ) 는 올레 핀의 이 성 질화반응을 일으킬 수 있지 만, Cr(C0)6 및 (Cr (C0)2(C5Hs)2)2 는 올레핀의 이성질화반웅에 촉매적 활성이 없다는 ` 접이다.
Cr(C0)6 에 의한 짝이중결합물질의 수소화반응을 살펴본다. 아래 의 식 (2.51) 과 같이 디엔은 시스형으로 금속에 배위되어 1, 4- 위차 에 수소첨 가반응을 일으키 는 반응으로 발표되 었 다. 26a) Cr(CO)6 대24) A. Mi so no and I. Og at a , Bull. Chem. Soc. Jap an , 40, 2718 (1967). 25) a) J. C. B 척 ]ar, Plat. Met. Rev. , 15, 2 (19 71). b) J. C. Bail ar , J. Am. 260) £a1 )C Ahe. mR. ejSo oa cn. , an4d7 , M4.7 5 C(a1is 蜀, )P.r og re ss in Coordin a ti on Chemi st r y , Else• vier , 1968, p. 32. b) M. S. Wrig h to n and M. A. Schroeder, J. Am. Chem. Soc. , 95, 5764 (1<: r!3 ). 'J:l) A. Mi ya ke and H. Kondo, Ang e w. Chem. Int. Ed. , 7, 631 (1968).
신에 Cr(C0)3(arene) 을 사용하여도 같은 실험적 결과를 얻는다. 이 사Cr실 (C로O부) 6 터 n 一리 2 C간o드 •a re(n, e(C} 이CO r)\ 4해 H리一-되C어O 금9H-속:(-C-C O주r-):3-위H 에_ 一세 /개 의1(CC Or빈) 3 \ 배 위 (2. 51)
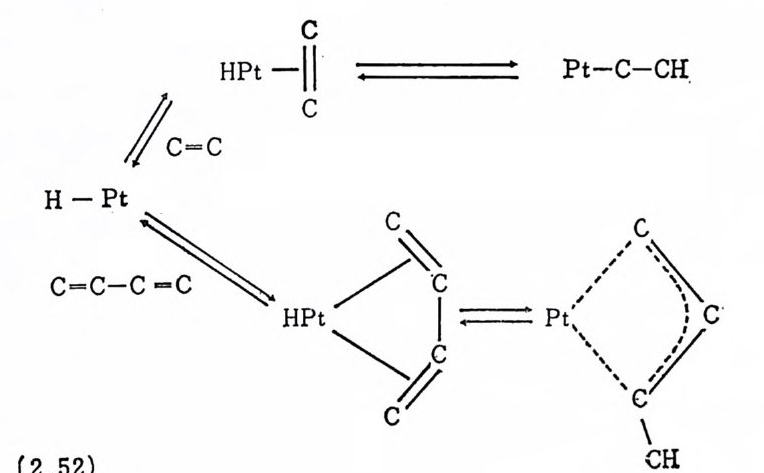
자리를 내어 놓으므로 Cr(C0)3( ci s-monoole fi n) 이 형성될 것이 추측 된다. Cr(C0)6 에 의한 반응은 또한 co 압력하에서는, 죽 용액에 배위되지 않은 co 가 과량으로 촌재하면, 그 속도가 감소하고 광화 학적 으로(p ho t ochem i call y) 배 위된 co 리 간드를 금속으로부터 메 어 놓으면 그 속도가 증가한다 .26b) 이러한 실험적 결과들도 식(2 .51) 의 반응경로를 지지해준다. 모노올레핀의 촌재하에서 일어나는 디엔의 선택적 수소화반웅의 예를 들어보자. 이러한 반응은 중간체로 생성되는 파이-알릴 (1r all y l) 착물의 안정도로 설명된다. 수소 (H2) 의 분리가 어떤 메카니즘 으로 일어나는지에 관계없이 M-H 와 짝이중결합의 반응은 파이― 알릴 중간체를 생성하는 것으로 알려져 있다. 예를 들면 디엔, 모
 HPt - 11C ~ Pt -C -CII.
HPt - 11C ~ Pt -C -CII.
노올레 핀 그리 고 백 금一주석 염 화물을 포함하는 촉매제는 다음 식 (2.52) 에서 보여주는 바와 같이 두 과정이 경쟁적으로 일어난다고 보고된 바 있다 .28) 또 다른 형의 선덱적 수소화반응을 하는 촉매계 의 예를 돈다면 짝이중결합이 없는 디엔이나 트리엔을 짝이중결합 이 있는 화합물로 만들기 위해서 이중결합의 이동을 일으킬 수 있 논 촉매계이다. 이러한 반웅들은 제 2 장 (4) 철에서 자세히 논의될 것이다. 3. 異性質化反應(i somer i za ti on) 거의 모든 전이금속의 착물이 울레판의 이성질화반응(이중결합의 이동 및 시스-트란스 이성질화반응)에 촉매적 활성을 보여준다. 에틸렌은 로듐촉매에 의해서 이합반응 (d i mer i za ti on) 을 일으킨다 .29) 이 반응의 주생성물은 1- 부텐이다. 일반적으로 이성질화반응은 이 합반응보다 빠르게 진행되기 때문에 이합반응에 의해서 생성되는 1- 부덴은 생성되는대로 2- 부텐으로 전환된다. 이합반응이 50% 정 도 진행되었을 때 용액 중에 1- 부맨은 40% 정도 존재하지만 충분한 시간을 가지고 1- 부탠과 2- 부텐이 평형을 이룬 다음에는 1 一부덴은 4% 정도밖에 존재하지 않는다. 이상의 실험적 결과는 열역학적인 면에서 고찰되어진다. 죽 에틸렌은 1- 부텐보다 약 1, 000 배 가량 안정한 로듐착물을 형성한다. 다시 말하면, 로듐에 에틸렌이 배위 되는 단계의 평형상수는 같은 로듐착물에 1- 부텐이 배위되는 단계 의 평형상수보다 약 1,000 배 가량 크다. 따라서 선덱적으로 일어 나는 올레핀의 배위가 전체반응에 크게 영향을 미치는 것 같다. 한 편 티탄착물 촉매에 의해서 2- 부텐의 중합반응이 일어나며, 여기서 생성되는 2- 부텐의 중합체의 구조는 같은 반응 조건에서 생성되는 l- 부텐의 중합체의 구조와 동일함이 보고된 바 있다 .30) 이러한 사 실은 동일한 촉매가 1- 부텐의 이성질화반응도 일으켜 2---¥- t반을 생
28) G. W. Parshall, J. Am. Chem. Soc. , 94, f!11 6 (1972). 29) R. Cramer, Acc. Chem. Res. , 1, 186 (19 69). 30) T. Ots u and M. Imoto , J. Polym er Sc£. , 4, 1579(1 9 66).
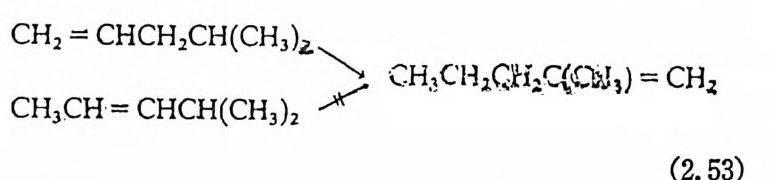
성하고, 2- 부텐의 중합반응도 일으킨다고 해석된다. 이 상과 같은 단순 이 성 질화반응도 일어 나지 만, 한편 다중 (mul tip le) 이성질화반응도 일어난다. 단순 이성질화반응이 일어날 것인가 또 는 다중 이성질화반응이 일어날 것인가는 이성질화반응의 속도와 배위된 올레핀의 해리 속도에 의해서 결정되는 것으로 추측된다. 예 를 들면 철착물에 의한 4- 메탈 -1- 펜텐의 이성질화반응과 4- 메탈 -2- 펜텐의 이 성 질화반응이 다. 31) 위 두 반응의 주생 성 물은 2- 메 탈 -1- 펜 텐이다. 한편같은 실험조건에서 4- 메탈 -2- 퍼바덴의 이성질화반응은 4- 메틸 -l 책J텐의 이성질화반응보다 훨싼 느리게 진행된다 .31)( 식 (2.53) 참조). 이상의 실험적 견과는 다음과 같이 설명된다. 다중 이성질화 반응, CH2=CHCH2CH(CH3)2 _-CH 2=C(CH3)CH2-CH2-CH3 은 올레판이 금속에서 떨어져나가기 전에 일어나며, 4- 메탈 -2 홉신덴~
 CH2 = CHCH2CH(CH3) 乙
CH2 = CHCH2CH(CH3) 乙
올레핀기가 내부에 있기 때문에 금속에 배위하기가 힘들고 따라서 이성질화반응이 찰 일어나지 않는다. 한편 커다란 리간드를 배위하고 있는 RuCl2(P(C6H5)3)3 는 선택 적으로 올레핀의 단순 이성질화반응을 일으킬 수 있는 착물로 알려 쳐 있다 32)• 이중결합의 이동반응에는 두 개의 대표적인 메카니즘이 현재까지 제시되어 왔다. 죽 알킬_금속과 파이_알 길 一금속착물 중간체를 각각 포함하는 두 개의 메카니즘이 여러가지 실험적 결과를 설명해 주 3L 있다. (1) 알킬금속 中間體률 통하여 일어나는 二重結合의 移動 이 메카니즘은 금속一수소 (me t al hy dr i de) 화합물을 포함하는 반응
3312)) TJ. .E A. . LMy oa nnsu, el], . JO. rOg.r gC. hCemhe.m , . 3, 6,2 72, 49379 401 9(7119 ) 6.2 ) .
과정이다. 금속-수소결합에 올레핀의 삽입반응이 일어나고, 이어 서 또다른 탄소원자로부터 금속원자로 베 타―수소 이 동반응이 일어 나고, 새로운 이성질체를 생성시키는 반응이다( 식 ( 2.54) 참조 ). 이러 한 반응에 서 금속의 산화상태 는 변하지 않는다. 석 (2. 54) 에 서 보는
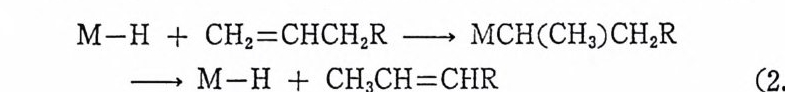 M 갤 + CH2=CHCH2R —-+ MCH(CH3)CH2R
M 갤 + CH2=CHCH2R —-+ MCH(CH3)CH2R
바와 같이 말단(t erm i nal) 올레핀의 이성질화반응은 反 -Markown i ko ff 형태로 올레핀의 삽입반응을 일으켜야 한다. (금4;=--수소 결합에 일어 나는 올레 판 삽입 반응은 많은 경 우에 Markownik o f f 법 칙 에 반 대되는 방향으로 일어난다. 죽 금속은 수소를 적게 결합하고 있는 탄소를 공격 한다. 이 러 한 반응을 反 -Markown i ko ff 방법 이 라고 한 다.) 반응에 필요한 금속―수소 화합물 촉매로는 별도로 합성된 RhH (CO)(P(C 晶 )3)3 와 같은 금속―수소 결합을 갖는 착물을 사용할 수도 있고, 특별한 실험조건에서 용액 중에서만 존재하는 금속―수 소화물을 유도하여 사용할 수도 있다. 금속―수소 화합물은 여 러 가 지 방법으로 생성된다. 예를 들면 식 (2.55)~(2.57) 에서 보여 주는 것 과 같이 산화성 첨 가반응(식 (2. 55), (2. 56)) 또는 수소분자의 불 균형 분리 반응(석 (2. 57) )에 의 하여 금속-수소 화합물은 생 성 된다.
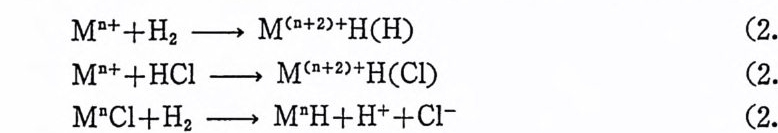 M0++H2 一 M(D+2)+H(H) (2.55)
M0++H2 一 M(D+2)+H(H) (2.55)
식 (2.54) 의 메카니즘을 살펴보기 위하여 하나의 예를 들어 본다. 즉 팔라듐착물 촉매 가 존재 하는 용액 에 서 , 삼중수소로 치 환된 l- 욱 텐 (CH2=CHCHT(CH2)4CH3) 과 치환되지 않은 l- 핵센 (CH2=CH(C H2)3CHs) 의 혼합물을 이성질화반응시킨 결과, 두 올레핀의 이성질 화반응도 각각 일어났지만 약 49% 의 삼중수소가 핵센의 수소와 상 호교환반옹을 일으킨 것을 발견하였다 .33) 죽 약 49% 의 핵센이 삼 33) F. Asin g e r, B. Fell and P. Kin g s , Tetr a hedron Lett . , 633 (1966).
중수소 하나를 갖고 있 다. 위에서 말단(t erm i nal) 울레핀의 이성질화반응이 일어나려떤 反 kown i ko ff형태의 올레핀삽입반응이 일어나야 한다고 기술하였다. Mar. 그러 나 금속과 리 간드의 종류에 따라 Markownik o f f 의 법 칙 에 맞는 올레펜의 첨가반응도 일어난다. 예로써 로듐착물에 의한 1- 부텐의 이 성 질화반응을 들 수 있 다. 29) 용액 내 에 서 로듐 CI )착물과 DCl (실제로는 CH30D 용매에 HCl 을 사용하였음)이 반응하여 산화 성첨 가생성물 Rh( Il[ )Cl(D) 를 생성한다. 이 렇게 하여 생성된 Rh-D 착물을 촉매로 하여 l- 부텐의 이성질화반응을 시도하여 본 결과, 반 옹혼합물 내에 CH2=CDC2Hs 가 촌재함을 발견하였다. 이러한 실험 척 사실은 식 (2. 58) 과 같이 Markownik o ff 법 칙 에 따르는 올레 핀의 삽입 반응의 결과라고 추측된다. 식 (2. 58) 과 같은 반옹과정 은 물론
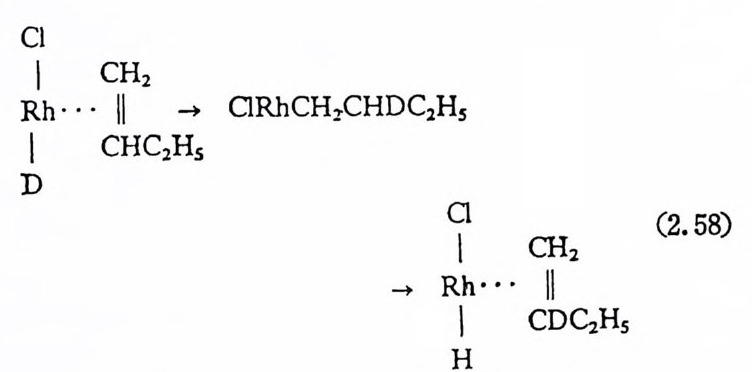 Cl
Cl
빠른 HCI/DCI 및 Rh-H/Rh-D 의 상호교환반응을 포함할 것 이 다. (2) 파이-알릴금속(ir -all y lme t al) 中問體룰 통하여 일어나는 二重結合의 移動 많은 전이 금속착물은 석 (2. 59) 와 갇이 파이 ―알릴 (;r-a Il y l) 금속착물 중간체 (i n t ermed i a t e) 를 거 쳐 서 1, 3- 수소이 동(1, 3-hy d rog en sh ift)반 옹을 일으킨다. 이 반응메카니즘은 산화성첨가반응과 환원성제거반 옹의 순환과정을 포함한다. 이 메카니즘을 지지하여 주는 예로는
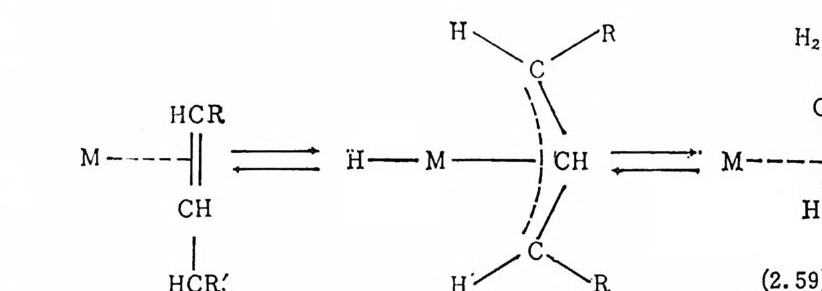 H\ /R H2CR
H\ /R H2CR
1H-NMR 분광범 으로 조사된 식 (2. 60) 과 같은 평 형 을 들 수 있 다 34)·
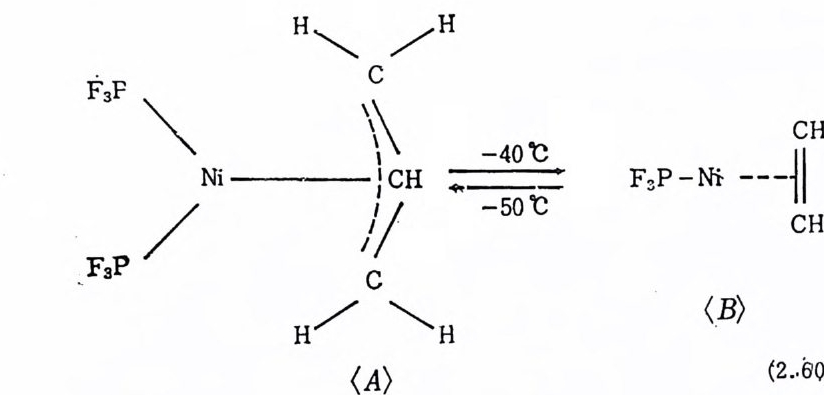 F탸3p \/ N i—--HH- ―/'-一\C( C}\i \ /CiHH \' A H... -- 5400'~C _ F3P-N< i-B > - -- ~CI HCH3
F탸3p \/ N i—--HH- ―/'-一\C( C}\i \ /CiHH \' A H... -- 5400'~C _ F3P-N< i-B > - -- ~CI HCH3
파이-알릴히드리도니첼 CII) 착물〈 A 〉는 一 130°c 에서 합성되어 분리 되었다. 이 착물은 -50°C 까지는 안정하며, 이 착물의 면 -NMR 은 파이-알릴기의 시그날윤 보여준다. 2~3 시간에 결쳐 _40°c 올려 주면 새로운 3 개의 시그날이 나타난다. 이 3 개의 시그날은 배위된 푸로팬에 의한 것이다. 이 반응은 식 (2.60) 에 표시된 것처럼 가역 반응이다. 식 (2.60) 에서 보여주는 것과 같이 대칭성을 갖는 파이一 알릴기를 배위한 금속-수소 화합물〈 A 〉은 수소가 금속으로부터 1 번 또는 3 번 어느 탄소에 이동되어도 같은 올레핀(펜벤)을 생성하 게 된다. 실제로 이성질화반응이 원할하게 일어나려면 수소가 금속 으로부터 1 번 또는 3 번 어느 탄소에도 모두 찰 아동되어쳐야 한
34) H. Boenemann, Ang e w. Chem. Inte r nat. Edit . , 9, 736 (1~0).
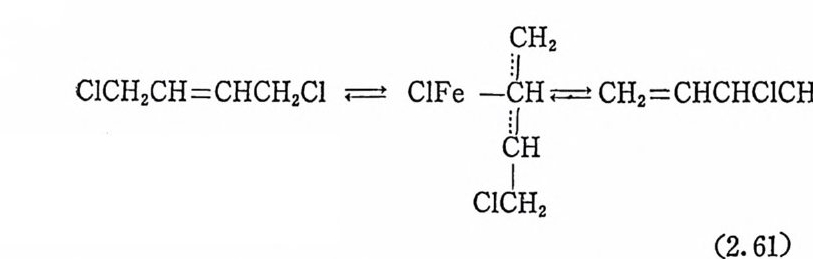
다(식 (2.59) 참조). 예를 들면 비대칭성 파이—알릴로듐 CI) 착물에 HCI 을 반응시키면, -75°C 에서는 Rh(Ill)H(Cl)(rr-all y l) 로 존재하 고, 실온에서는 수소가 알릴기에 이동되어 올레핀이 생성되는 것이 NMR 분광법에 의해서 확인되었다 .35) 알탈기가 메틸알탈(식 (2.59) 에서 R=CH3, R'=H) 또는 l- 메틸 -3- 에탈알릴(식 (2.59) 에서 R= C2H5, R'=CH3) 금속착물로부터 는 각각의 경 우에 1 : 1 비 율의 올레 핀혼합 물 을얻었다. 즉메탈알릴금속착물로부터는 1:1 비율로 C H3CH2CH=CH 포l- CH3CH=CHCH3 를 얻었고 1- 메탈 -3- 에틸알릴금 속착 물 로부터 는 C2H5 -C H2-CH=CHCH3 와 C 2 H5-CH=CH 一 CH i -CH3 를 1 : 1 로 얻었다. 그러나 입체적으로 장애를 받는 1, 1 - 디메 틸알탈기와 같은 경우에는 입체장애를 적게 받는 탄소로 수소이동 이 쉽게 일어난다. 철 (0) 착물 Fe J( C0)1 2 에 의한 3- 에탈 -1- 괜텐의 이성질화반응도 파이-알릴히드리도금속착물 형성매카니즘으로 진행되는 것으로 알 려 쳐 있 다. 36) 重 水 素 로 치 환된 이 성 질체 를 이 용한 실험 에 의 하면 1, 3 -수소이동의 반응이 일어난다. 이 반응에서 동위원소효과(i so t o p e e ff ec t ) 가 측정되지 않았으므로, C 一 H 결합이 꿇어지면서 파이―알 릴히드리도금속착물 (FeH( 11: -all y l)) 이 생성하는 과정은 속도결정단계 는 아니 다. 따라서 가장 느란 단계 는 Fe(C0)4(olefi n) 생 성 과정 또는 생성된 Fe(C0)4(ole fi n) 으로부터 co 가 해리되어 4 배위착물 Fe(C O) J( ole fi n) 의 생 성 과정 으로 추측된다. Fe(CO) J( ole fi n) 으로부터 Fe H(rr-all y l)(C0 ) 3 로 전환되면서 Fe 의 산화상태는 0 에서 2 로 되어 천은 산화된다. 철착물에 의 한 1, 4- 디 클로로 -2- 부텐의 이 성 질화반응은 3, 4- 디 클 로로 -l- 부덴을 생성한다 3 7). 죽 이중결합의 이동과 동시에 1,3- 염소 이동 (1,3 - chlor i ne sh ift)반응이 일어난다. 따라서 아래의 식 (2.61) 과 같은 파이―알릴클로로금속착물을 포함하는 반응메카니즘으로 추정 된다.
35) J. F. Ni xo n and B. Wi lkin s , ]. Orga nomet. Chem. , 44, C25 (1972). 36) C. P. Case y and C. R. Cyr , ]. Amer. Chem. Soc. , 95, 2248 (1973). '37) G. Henric i -Q live and S. Oli ve , J. Orga nomet. Chem. , 29, 307 (1971 ).
 『 H2
『 H2
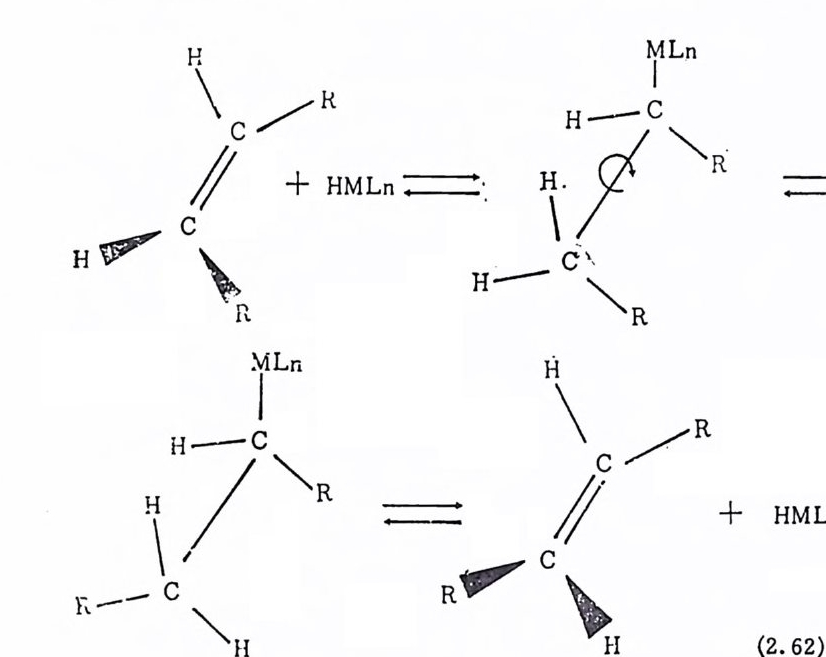
(3) 시스-트란스 異性質化反應 많은 전이금속착물 촉매에 의한 이성질화반응에서 다음과같은설 험적 결과를 얻었다 .38) 죽 이중결합 이동에 의한 1- 알켄의 이성질 화반응은 최초에는 주로 시스 -2- 알켄울 생성하지만 충분한 시간이 경과되면 시스一트란스의 평형(열역학적으로 예상되는)이 이루어전 다. 일반적 으로 내 부올레 편 (int e r nal ole fi n) 의 시 스-트란스 이 성 질화
 MnL| \
MnL| \
38) a) R. Cramer and R.V. Lin s ey, J. Am. Chem. Soc., 88, 3534 0966). b) H. Kanai, Chem. Commun. , 203 (1972). c) D. Bin g h am, D. E. Webste r and P. B. Well, J. Chem, Soc. , Dalt on Trans. , 1928 (1'5!2) .
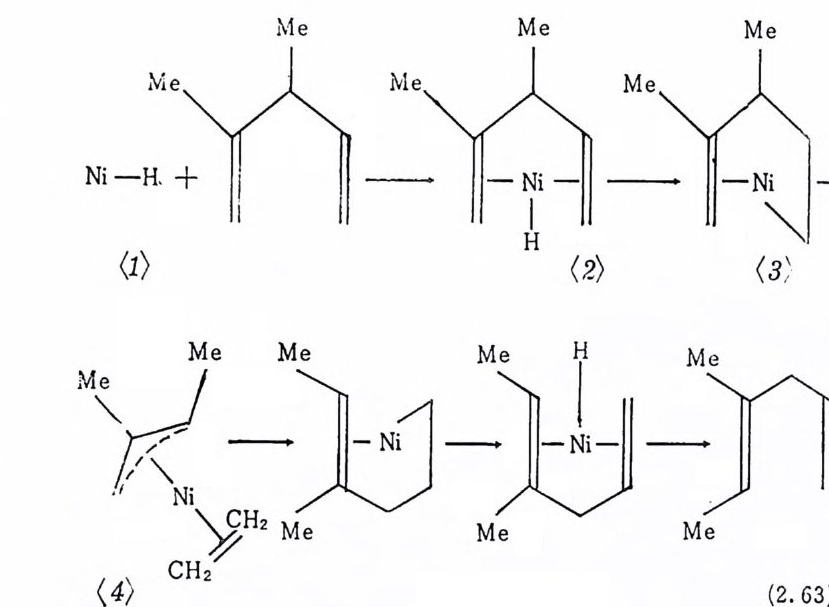
반응은 끝울레판(t erm i nal ole fi n) 의 이중결합이 이동되는 이성질화반 옹보다 느리게 일어난다. 이상의 현상은 말단 울레핀이 상대적으로 내부울레핀보다 쉽게 금속에 배위될 수 있다는 사실과 관련지울 수 있다. 예의적으로 빠른 시스―트란스 이성질화반응이 발표된 바 있 으나, 이 경우에 반응은 금속촉매에 의해서 진행되는 것이 아니고 强 酸 에 의해서 일어나는 반응으로 제시되기도 하였다 .39) 금속―수소화합물촉매에 의한 시스―트란스 이성질화반응은 올레 핀의 삽입 과 베 타-수소제 거 반응( (3 -h y dro g en e li m i na ti on) 을· 포함하는 것 으로 제 시 된 바 있 다(식 (2. 62) 참조 ). 40) (4) 炭素骨格 異性質化反應 (carbon skeleta l iso meriz a ti on ) 탄소와 탄소의 결합이 끊어지는 과정이 포함되는 울레핀의 자리 옮김반응은 공업적으로 중요한 반응이다. 니첼-수소화 착물에 의 해서 일어나는 탄소골격 아성질화반응을 예로 들어본다. 니 켈 (0) 착물 Ni (P (OC1H1)3)3 은 양성 자첨 가반응(p ro t ona ti on) 에 의 해 서 N i H(P(OC 晶 )3)3 을 생 성 하여 니 첼-수소화 착물은 디 엔 (die n e) 의 탄소골격 자리 옮김 반응에 촉매 적 역 할을 한다. 41 ) 이 착물에 의 하여 시스 -1,4 책사디엔은 상온에서 매우 빠르게 트란스 _2- 메틸_ 1,3- 펜타디엔과 2,4 책사디엔을 생성한다. 트란스 -2- 메틸 -1,3- 펜 타디엔의 생성을 설명하기 위하여 베타-탄소제거반응(/3 -carbon · el i m i na ti on) 이 제시되었다(석 (2.63) 참조). (베타―탄소제거반응은 식 (2.54) 에서 소개된 베 E l-수소제거반응과 비슷한 반응이다.) 석 -(2.63) 은 니겔―수소(화) 착물을 촉매로 하는 2,3- 디메틸 -1,4- 펜타 디엔의 탄소골격 이성질화반응에 제시된 메카니즘이다.(베 E l-수소 제거반응과정에 의해서 생기는 착물〈 4 〉(식 (2.63) 은 에틸렌과 이소푸 렌 (i so p rene) 으로부터 디 엔 (d i ene) 화합물을 만드는 과정 의 중간체 로 이 미 제 시된 바 있다 42)) . 반웅개시는 디엔이 니첼―수소 착물에 배위되므
39) P. M. Mait lis, The Orga nic Chemi st r y of Palladiu m , Academi c Press, N. Y. , l
로 일어난다(〈 1 〉一〈 2 〉). 이어서 배위된 한 개의 올레핀기가 Ni -H 결합에 삽입되어 착물 〈 3 〉을 생성한다. 이렇게 하여 생성된 디메
 Me Me Me
Me Me Me
틸 -4 궁신덴닐착물 3 은 베 E l-탄소제거반응(베타-단소와 감마―탄소 사 이의 결합이 끊어진다)을 일으켜 에틸렌(디메틸-파이-알릴)니첼 착물 〈 4 〉을 생성한다. 배위된 에틸렌은분자내의 과이―알릴기와 반응하 여 4- 메틸 -4- 핵센닐니첼착물〈 5 〉을 생성하고 이어서 베타수소제거 반응이 일어나 착물〈 6 〉이 된다. 착물〈 6 〉은 4- 메틸 -1,4- 핵사더엔을 , 생 성 하고 초기 의 착물〈 1 〉로 돌아온다. 4. 二合反應 (d i mer i za ti on) , 小重合反應 (o lig ome riz a ti on ) 重合反應 (Pol y mer i za ti on) 이 합반웅, 소중합반웅 및 중합반응의 촉매순환과정은 오직 두 형 태의 반응단계를 포함한다. 첫째로 금속과 알킬(또는 수소) 결합 사 이에 올레핀이 삽입되는 과정(식 (2.64) )과 둘째로 베타수소의 전달
반응(식 (2. 65) )이 포함된다 .두 반응의 상대 적 인 속도에 따라 생 성
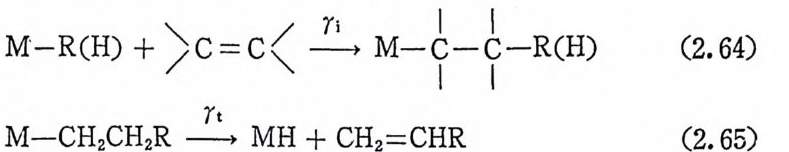 MM 一-R C(HH2C)H +2R > —Cr-t= > C M< H +느 CH M2=C-~HIR - ~I- R(H) ((22..6645))
MM 一-R C(HH2C)H +2R > —Cr-t= > C M< H +느 CH M2=C-~HIR - ~I- R(H) ((22..6645))
물의 분자량이 정해진다. 죽 올레핀의 삽입반응(식 (2.64) )의 속도 (r i)가 베 타-수소전달반응(식 (2. 65) )의 속도 (r t)보다 빠르면 생 성 되는 중합체의 분자량은 커지고 그 반대로 r t »r i이면 생성물은 주 로 이합체가 되며, r t::::::: r 거떤 생성물온 소중합체가생성될 것이다• 반복되는 올레핀의 삽입반응에 의해서 중합체의 사슬 (cha i n) 이 길 어 지 므로 울레 핀의 삽입 반응은 사술전파단계 (chain p ro p a ga ti on) 라고 도 부른다. 사술전파단계 와 베 타―수소전달의 상대 적 속도에 영 향 울 주는 것들을 살펴보면 다음과 같다. 실험적 결과에 의하면 일 반적 으로 전자주게 리 간드는 ri/r t 값 을 증가시 키 고 전자받게 리 간드 는 rl/r t값을 감소시키는 경향이 있다. 그러나 r J r t값은 리간드의 성질보다는 금속자체의 성질에 의해서 더욱 큰 영향을 받는 것 같 다. 일반적으로 넵族 전이금속착물은 비교적 베타―수소 전달반응 울 쉽게 일으켜서 이합반응의 촉매로 사용된다. 한편 N~VI 族전 이금속착물에 의한 반응은 주로 중합체를 생성한다. 예의적인 실험 결과들이 물론 많이 발표되고 있다. 실제로 올레핀의 이합반응, 소 중합반응 및 중합반응을 모두 일으키는 촉매겨}는 많다. 올레판의 이 합, 소중합 또는 중합반응에 촉매적 역할을 하려면 금속착물은 올 레핀이 배위할 수 있는 빈 배위자리를 갖고 있어야 하지만 분자 내 에 활성 이 있는 금속―알킬(또는 수소 )(M-R(H)) 결합을 갖고 있 어야 한다. 올레핀이 금속에 배위되는 반응속도는 올레핀의 종류에 따라 달라진다. 따라서 에틸렌 및 한 개의 수소가 치환된 에틸렌유 도체 (CH2=CHR) 등은 비 교적 쉽 게 중합반응(이 합반응, 소중합반 응도 포함)을 일으킬 것이다. 한편 시클로헥센이나 시클로옥덴과 같은 고리계 올레핀 (c y c li c ole fi n) 의 중합반응은 느리게 일어나며, 내 부 올레 핀 (int e r nal olefi n) 또는 두 개 의 수소가 치 환된 에 탈 렌유 도체 (CHR=CHR) 의 중합반응은 거의 일어나지 않는다. 푸로필렌
과 같은 비 대 칭 성 올레 핀은 단위 체 (monomer) 의 삽입 반응이 Mar- kownik o f f 법 칙 또는 反 -Markown i ko ff 형 태 로 일어 나는가에 따라 각각 다른 두 개 의 생 성 물이 얻어 질 것 이 다. 삼차포스핀 (ter t i ar y ph o- s p h i ne) 과 같은 커다란 리간드를 이용함으로써 반응의 선택성을 높 여 특정한 이성질체의 생성을 촉진시킬 수도 있다. 광학적으로 활 · 성이 있는 리간드를 이용함으로써 광학적 활성이 없는 단위체의 이 , 합반응을 통하여 비 대 칭 성 (as y mme t r i c) 물질 합성 도 가능하다. (1) 二 合 反應 (dim eriz a ti on ) 많은촉매계가에틸렌, 푸로필렌및탄소수가많은말단올레판각 ' 각의 이 합반응이 나 상호이 합반응 (cod i mer i za ti on) 에 활성 을 보여 준다. 예를 들면 코발트 (I) 一아세틸아세톤착물과 르리에틸알루미늄의 혼 · 합물과 같은 Zie g le r 촉매 형 43) 또는 로듐(I )착물에 HCl 을 산화성 첨가반응시켜 얻은 촉매계 29) 등을 둘 수 있다. 많은 경우에 촉 매계 의 생성방법은 알려져 있으나 실제로 촉매계가 어떤 물질을 포함하 · 고 있는지에 관하여서는 모르는 접이 많다. 현재까지 알려진 바에 의하면 에틸렌 및 푸로필렌의 이합반응에 가장 활성이 높은 촉 매계 는 할로겐화 파이―알릴니첼 착물계이다 .44) 이 촉매계는 할로겐화 파이-알랄니벨 착물과 할로젠화 알루미늄화합물 또는 할로젠화 알 킬알루미늄과 같은 Lew i s 의 산으로 구성되어 있다. 할로겐화 파이 ―알릴니첼 착물 하나만으로도 高溫, 高 惡 하에서 촉매반응은 일어 난다. 그러나 위와 같은 Lew i s 의 산을 가함으로써 반응은 매우 빠 · 르게 진행될 분만 아니타 _30~_40°c 에서도 반응은 진행된다 .. 할로젠화 파이-니첼착물은 염소를 다리로 하고 있는 이합체이다. 여기에 Lew i s 의 산을 가하여 촉매계를 더욱 활성화시킨다. 이때 ’ Lew i s 의 산이 이합체의 다리를 꿇고 니첼에 배위된 염소는 알루미 늄과 한 쌍의 전자를 공유하는 착물을 형성하는 것으로 보고되었다 (식 (2.66) 참조 ).44) 이렇게 하여 생성되는 착물은 중심금속원자 니첼
43) G. Hata , Chem. Ind. , 223 (1965). 44) a) B. Bog da nov ic, B. Henc, H. G. Karman, H. G. Nii ss el, D. Walte r and; G. Wi lke, Ind. Eng , Chem. , 62, 34 (1'570 ). b) B. Bog d anovic , Ang e w. Chem. Inte r nat. E.i it. , 12, 954 (1'573 ).
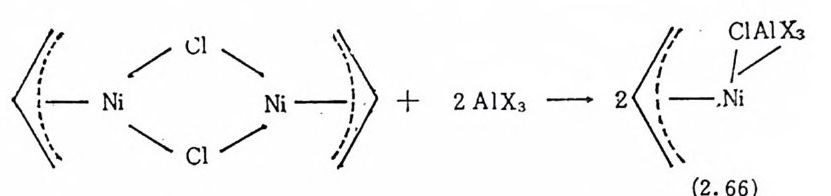 ii-', ' Ni / C1 \ N i一'\ \1 + 2AIX, 一 2 ,, 一· . {CIA/\X : J
ii-', ' Ni / C1 \ N i一'\ \1 + 2AIX, 一 2 ,, 一· . {CIA/\X : J
주위에 빈 배우1 자리가 생기게 된다. 이 빈 자리는 co 등과 같은 전 자받게리간드에 의해서 쉽게 접유되며, 득히 두개의 co 가 니젤에 배위되면 전체 촉매계는 활성을 잃게 된다. 그러나 한 개의 포스핀 (p hos p h i ne) 리간드만 배위되면 촉매계는 계속해서 활성을 갖는다· 포 스핀의 종류에 따라 촉매 반응이 영 향을 받게 된다. 파이―알릴, 할로겐 및 포스핀이 니첼에 배위되어 있고 Lew i s 의 산인 이영화메탈 알루미늄의 분자가 니첼에 배위되어 있는 할로겐 에 결합되어 있는 실제 촉 매의 구조는 X 국i 結晶 구조 결정법에 의 해서 밝혀진 바 있다 .44a) 연구보고에 의하면 44 b) 반응초기에서 파이―알릴기는시그마―알릴 기로 전환되고 이어서 배위된 울레판이 니첼―시그마―알릴 결합에 삽입된 다음 마지막으로 베타―수소전달반응을 일으키면서 니첼― 수소착물과 1, 4 점신타디 엔을 생 성한다(식 (2. 67) 참조).
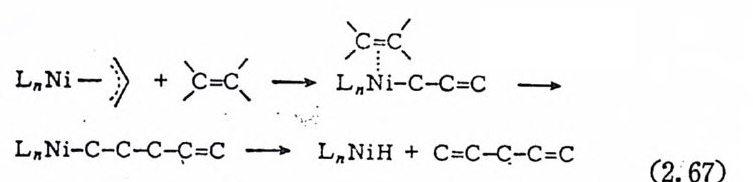 L,.Ni - >+ :c=C < - L\/ 파C=C -/ \ c -C=C •
L,.Ni - >+ :c=C < - L\/ 파C=C -/ \ c -C=C •
이렇게 해서 생성된 니첼―수소착물에 올레,;1J. 단위체(에틸렌 또 는 푸로팔렌)가 삽입반응을 일으킨다. 이어서 일어나는 또 하나의 올레판 삽입반응과 베타―수소이동 반응은 올레핀의 이합체 및 니 첼-수소화합물을 다시 생성시킴으로써 촉매순환과정을 이룬다(식 (2. 68) 참조). 석 (2. 68) 에 의 한 이 합반웅의 주 생 성 물은 1 --4덴이 다. 그러나 이합반응의 촉매는 이성질화반응에도 촉매져 활성이 있으므 로 실제는 1- 부덴과 2 --.1伊尸의 열역학적 평형혼합물을 얻게 된다.
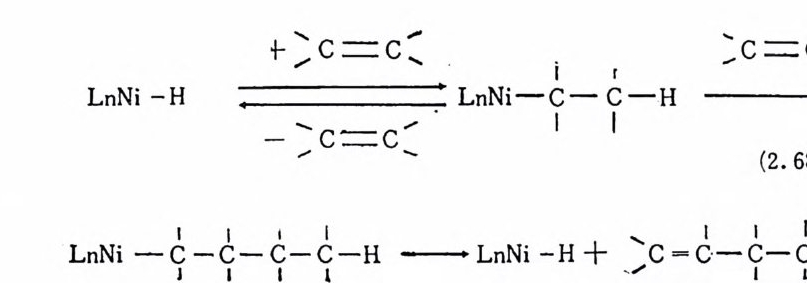 t-`/ C=c`/ i r 」`. C=c ,..,.,.
t-`/ C=c`/ i r 」`. C=c ,..,.,.
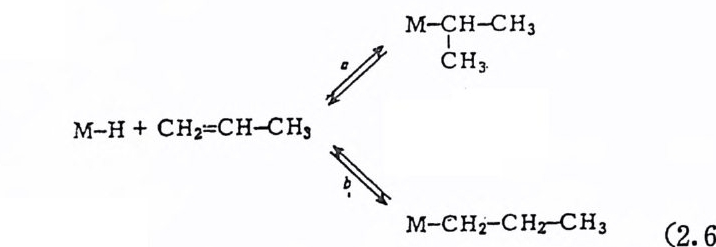
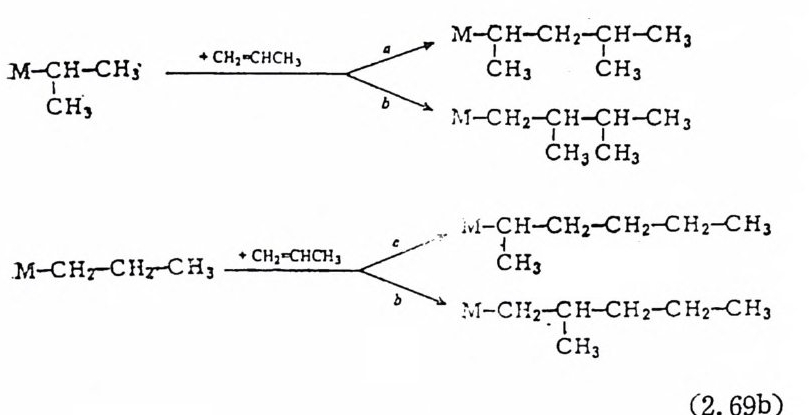
많은 경우에 올레핀이 M-H 결합에 삽입되는 반응이 M ― R 에 삽 입되는 반응보다 훨싼 빠르게 일어난다 .29) 따라서 전체반응의 속도 결정단계는 두번째의 올레편단위체가 M ― R 에 삽입되는 과정이다. 전이금속착물에 의해서 일어나는 푸로팔렌의 이합반응을 살펴보 자. 푸로필렌 단위체의 삽입방법에 따라서 아래에 보여주는 4 개의 반응경 로가 가능하게 된다(식 (2. 69) 참조). 식 (2. 69) 에 서 aa 과정 을 거쳐 베타-수소전달반응이 일어나면 4- 메틸 -2 궁신덴(또는 4- 메탈 -1 -펜덴)이 생성되는데 생성된 4- 메틸 _2- 펜렌은 이성질화반응을 거쳐 쉽게 2- 메틸 -2- 펜텐으로 전환될 것이다. ab 과정을 거치면 베타-수
 M -c H 조 H3
M -c H 조 H3
소전달반응에 의해서 2,3- 디메틸부텐둘이 생성될 것이다. 한편 ba 과정과 베 E l--수소전달반응을 거치면 線型 헥센둘이 생성될 것이고 bb 과정을 거치면 2- 메틸 -1- 펜덴이 생성될 것이나 2- 메틸 -l- 펜렌은 이성질화반응을 일으켜 2- 메틸 -l- 펜텐으로 전환될 것이다. 따라서 2- 메틸 2- (또는 l)- 펜텐, 2,3- 디메철 -l( 또는 2) 부텐, 線型 헥샌들
및 2 - 메틸 -1- 펜텐의 촌재를 확인함으로써 어떤 경로를 거쳐서 이합 반응이 일어났는가를 알 수 있다. 그러나 2 _ 메탈 - 2 - 펜텐의 생성은 두 경로 (aa 경로 또는 bb 경로)를 거쳐 생성될 수 있기 때문에 그 경로를 구별하기 힘들다.
 M y H -CH 국 H -C H3
M y H -CH 국 H -C H3
보고된 안구에 의 하면 식 (2. 66)~(2. 68) 에 서 기 술된 착물과 비 슷 한 니첼착물에 의한 푸로필렌의 이합반응은 주로 aa 경로를 거쳐 4 -메 탈펜텐을 생 성 한다. 45) 첫 번 올레 핀이 삽입 되 는 단계 (석 (2. 69a)) 에 서 a 과정 은 反 -Markown i ko ff 형 태 (제 2 장 3 의 (l) 참조)의 반응 으로 電 子的인 면으로 보아서, b 과정보다는 유리한 과정이다. 죽 푸로필렌의 파이 전자밀도분포는 다음과 같이 가운데 탄소의 전자밀 도가 비교적 낮아서, 전자밀도가 높고 산화수가 낮온 맨族 전이금 속은 푸로필렌의 가운데 탄소를 공격하는 a 과정으로 반응이 일어 날 가능성이 높다. 그 반대로 산화수가 낮은 N 族 전이금속을 사용 하였을 경우에는 b 과정으로 반응이 일어날 가능성이 크다. 표 2.1
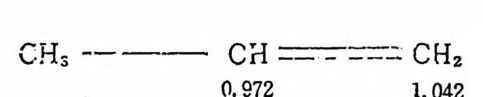 CH3 --—— oC. 9H72 ===.:. 1C. H0422
CH3 --—— oC. 9H72 ===.:. 1C. H0422
은 이상의 고찰을 지지해 주는 실험적 절과들이다. 표 2.1 에서 보
45) J. Ewers, Ang ew . Chem. Inte r nat Edit . , !'i. Se4 (19 66).
는 바와 같이 Ti — R 결 합에 삽입 되 는 반응은 Markownik o f f 법 칙 에 따라 일어 난다. 한편 낮은 산화수 를 갖는 벤 族 금속의 착물은 反 Markownik o f 과정 으로 울레 핀을 삽입 시 킨다. 여 기 에 도 예 의 는 있 다. 예를 들면 푸로필렌이 트란스 -PtH CI(P(C2Hs)s)2 중의 Pt — H 에 삽입 되 는 반응은 Markownik o f f 법 칙 에 따라 일어 나 Pt — CH2— CH2— CH3 단위 (mo i e ty)를 생 성 한다. 50) 이 경 우에 두개 의 커 다란 표 2.1 올레펀삽입반응경로 M-Ra 올레펜 삽입반웅경로 b 참고문헌 Ti( JJI)— R pro p yle ne bb 46) Ti (N )— R !-bute n e bb 47) Ti (N )-R 1-pe n te n e bb 47) Ni (Il)— H pro p yle ne a 44a) Co(I )-H pro p yle ne a 48) Pd-R pro p yle ne a 49) 0 R=H, 알킬 또는 아릴 (ar y l). b a= 反 -Markown i ko ff 법 칙 , b=Markownik o f f 법 칙 . P(C2H5)3 가 P t一 CH(CH3)CH3 의 생성을 어렵게 했을 가능성도 있 다. 리간드의 크기에 따론 입체적인 이유 때문에 푸로필렌의 이합반 응의 생성물이 결정되는 예를 들어 보면 아래와 같다. 파이-알릴 니켈촉매계(식 (2.66)~(2.68) 참조)에 의한 푸로필렌이합반응은, 포스 펀 리 간드가 P(C2Hs) (t-C 4H9)z 또는 P(i-C 3H7)3 와 같이 매 우 클 때 , ab 경로를 거쳐 약 70% 의 2,3- 메틸부텐울 생성한다 .44” 한편 포스 핀이 P Ci -CaH1)2C t -C4H9) 일 경우에는 선택성은 더욱 높아져서 96% 의 2,3_ 디메틸부텐을 생성한다. 위에서 기술된 것처럼 첫째 푸로필
46) P. Lang i, Z. Mazzani, A. ~og ge ro and A. M. Lachi, Makromol. Chem. , 61, 63 (19 63). 47) H. Besti an and K. Clauss, Ang ew . Chem. Inte r nal. Edit . , 2, 704 (1963). 48) P. Tay lo r and M. Orchin , J. Am. Chem. Soc. , 93, 6504 (1971). 49) R. F. Heck, J. Am. Chem. Soc. , 91, 6707 (19 69). 50) J. Chatt , R. S. Cof fey , A. Goug h and D. T. Thomson, J. Clzem. Soc. (A), 190 (19 68).
렌의 삽입반응이 a 경로를 통하여 일어나는 이유는 전자적으로 유 리하기 때문이며, 두번째 푸로필렌이 b 경로를 거치는 이유는 니첼 에 배위되어 있는 커다란 포스핀리간드와이소―푸로필기의 영향때 문으로 추측된다. 이렇게 해서 생성되는 2,3 _ 디메탈부맨은 좋은 노 킹억제 성격을 갖는 2,3 _ 디메틸부탄으로 수소화될 수도 있으며, 중 합반응둥에 많이 쓰여 지는 2, 3- 부타디 엔으로 탈수소화될 수도 있 다. 높은 선덱성을 보이면서 ba 경로를 거치는 예를 들면 아태와 같 다. 아세탈아세토나토팔라듐 (II) 에 알킬알루미늄과 포스판을 가하 여 얻어지는 촉매계는 푸로필렌의 이합반응을 일으켜 주로 線型 핵 센 (line ar hexene) 을 생 성 시 킨다 51). 특이 한 경 로 ba 를 거 치 는 이 합 반응을 일으킨다는 사실은 입체적인 이유에 기인된다고 설명된다. 왜냐하면 전자적인 이유에 의해서 식 (2.69a) 단계에서 b 경로를 거 쳤다면 석 (2.69b) 단계에서도 b 경로를 거칠 것으로 예상되기 때문 이다. 그러나 실제로 제 2 단계 (2.69b) 에서 a 경로플 거쳤다는 사실 은 입체적인 이유로 추측된다. 표 2.2 에서 보는 바와 같이 트리부 틸포스핀과 트리페닐포스핀을 가하여 얻은 촉매계는 각각 주로 線 型 헥센을 생성한다. 트리부틸포스핀과 트리페닐포스핀은 서로 매 우 다른 전자주게 성질을 갖고 있지만 비슷한 정도의 線型 혜센을 표 2.?. Pd ― Al-PR3( 조는 P(OR)3) 촉매계에 의한 푸로필렌의 이합반 웅, [Pd(acac) 』 =2X 10-3M; [C2H5A1Clz]=22X 10-3M; (P J /[Pd]=2; 온 도 =20 ° C; 시 간 =3 시 간. 51b) PRJ ( P(OR)J) 반웅뮬 선형핵센 메틸괜텐 디메탈부텐 P(n— CiH 9)3 4% 95.1% 4.9% P(C6H5 )3 4% 81 .8 % 18.2% P(OC6H5)3 12% 23.6% 68.2% 8.2% 생성한다. 따라서 전자적인 영향보다는 입체적인 영향이 큰 것으로
51) a) M. G. Barlow, M. J. Brya nt, R. N. Hasezeldin e and A. G. Mackie , ]. Orga no/1 r e/al, Chem. , 21, 215 (l<:!10 ). b) G. Henric i -O l ive and S. Oliv e , Ang ew . Chem. Inte r nal. Edit . , 14, 104 Cl<:!1 5 ).
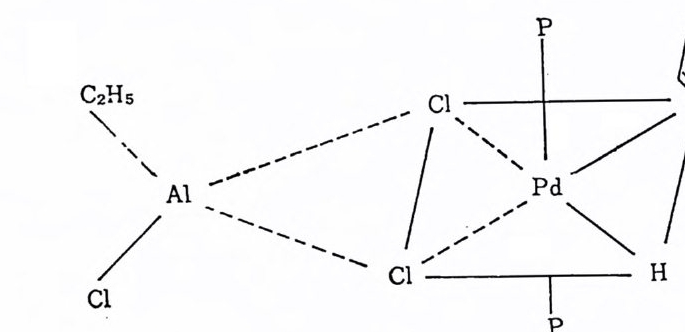
추측된다. 포스핀 대신에 (P(OC5H s )3( 포스핀-금속착물 중의 금속 주위 보다 P(OC6H5)3 — 금속착물 중의 금속주위 가 더 욱 복잡하다)를 사 용하면 線型 헥센의 생성은 줄고, 메탈펜텐 및 디메탈부텐의 생성 이 증가한다(표 2.2 참조). 포스핀을 포함하는 촉매계에 의한 반응의 속도가 P(OC5Hs)3 율 포함하는 촉매 겨 1 에 의 한 반응속도보다 느린 이유도 여시 입체적인 것으로 해석된다(표 2.2 참조). 촉매겨 1 가 포함하고 있는 P/Pd 비율도 매우 중요한 영향을 미찬 다. 예를 들면 P/Pd=2 일 때 반응은 매우 잘 진행되지만 P/Pd<2 일 때는 검은 p ao 가 생성되며 반응이 중지된다. ~/Pd:2 :5 일 때는 촉매적 활성을 잃는다. 촉매적 활성을 잃는 이유는 올레핀 배위자 리가 리간드 P 에 의해서 접령당하기 때문일 것이다. A l,' Pd 비율은 비교적 높아야 한다. 이 사실로부터 실제촉매는 가 역만웅(죽 평형)에 의해서 생성된다고 할 수 있다. Al /Pd =5~25 법위에서 촉매계는 활성율 브여주는데 Al/Pd=20 정도에서 가장 높 은활성을보여준다. 이상의 여러가지 실험적 결과와 분광법에 의한 데이타와 그리고 Zie g l e r 형 촉매 와의 유사성 등을 비 교하여 실제 촉매 종은 아래 와 같 다고 제시된 바 있다 .5lb)C 이 착물의 생성과정에 관하여서는 참고문헌 51 b) 를 참조할 것.)
 C' \; Al `.,.:\-\-`_`_ _ ...c. -!二 一p一 H
C' \; Al `.,.:\-\-`_`_ _ ...c. -!二 一p一 H
촉매계에 의해서 일어나는 올레핀의 아합반응 중에서 근래에 주 목을 끄는 반응의 한 예를 들면 아래와 같다. 식(2 .66) 에서 기술한 것과 비슷한 니첼착물(키탈 (ch i ral) 탄소를 갖는 포스핀을 가하여 얻
은)은 노르보르넨 (norbornene) (또는 노르보르나디 엔 (norbornadie n e)) 과 에 틸렌의 상호이합반응 (cod i mer i za ti on) 에 촉매직 활 성을 갖고 있 다 .44b) 이 촉매반응은 새로운 C-C 걷합을 생성시키는 비대칭합성 (asym metr ic syn th e s i s ) 반응으로 흥미 를 끌었 다. 석 (2. 70) 과 같이 노 르보르벤은 에 탈렌과 반응하여 주로 광학적 활성을 갖는 外向-(+) -2- 비 닐노르보르난 (exo-(+)-2-v i ny lnorbornane) 을 생 성 한다. 이 반응 에서 에틸렌은 노르보르넨의 C=C 이중결합에 첨가될 때 입체적 ,;coL 애가 적은 쪽을 공격하였다. 생성물의 일부는 이성질화반응을 일으 켜 2- 에 틸 일리 덴노르보르난으로 전환된다(식 (2. 70) 참조). 노르보르덴의 이중결합은 고리 스트레인 (r i ng s t ra i n) 이 커서 쉽게
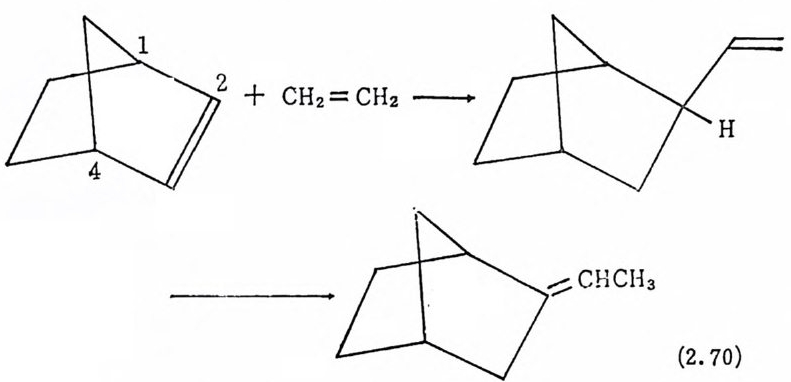 、 (2. 70)
、 (2. 70)
활성 화된다. 따라서 에 틸렌과의 상호二合反應 (cod i mer i za ti on) 은 매 우 낮은 온도에서 선택성을 보여준다. 예를 들면 -97°C 에서 80.6% 의 광학적 수율 (o pti cal yield) 을 준다. 현재까지는 광학적 활성이 있는리간드를 사용하는 연구는 대부분 경험적인 것에 지나지 않는다. 앞으로 더욱 많은 실험적 결과가 쌓 아고, 이들을 토대로 하여 촉매의 구조와 광학적 활성이 있는 생성 물과의 관계가 정립되고, 나아가서는 특정한 광학적 활성이 있는 생 성 물을 얻기 위 한 바 대 칭 성 촉매 (asym metr ic ca t al y s t)합성 을 위 한 연구도 진행되리라고 기대된다. (2) 小重合反應 (o lig ome ri za ti on), 重合反應(p ol y mer i za ti on) 올레핀의 소중합반응및 중합반웅의 촉매계는주로 N,V,VI 族전
이 금속 (T i, V, Cr 둥)의 착물을 포함하는 계 로서 대 표적 인 예 로서 Zi e g ler 형 촉매계가 있다. 여기서는 티탄 (T i (N) )화합물과 할로겐화 알킬알루미늄의 반응으로 만들어지는 T i /Al 촉매계를고찰하고자한 다. 생 성 물의 분자량을 결정 하는 因子는 사슬의 전파단계 (ri, 석 (2. 64)) 와 베 타 - 수소전달반응 (r t, 식 (2. 65) )의 상대 적 인 속도이 다. 죽 rJr t 의 값에 의하여 소중합반응 또는 중합반응이 결정된다. 따라서 촉 매계의 리간드를 변화시키면서 얻어지는 생성물의 분자량을 조사함 으로써 반응에 관한 많은 정보 를 얻을 수 있다. 표 2.3 은 T i /Al 촉매계에 의한 에틸렌중합반응의 결과아다. 즉 티탄과 알루미늄에 결합되어 있는 리간드를변화시키면서 가용성 소 중합체(벤젠 용매에서)와 불용성 중합체(밴첸 용매에서)의 비율을 표 2.3 에 실었다. 여기서 사용된 리간드의 시그마―전자주게 세기 순서 는 C2H5o->C2H5_>CF 이 다. 53) 표 2.3 T i /Al 계에 의한 에틸렌의 소중합반응과 중합반응 결과. 용매, 벤젠 ; T=5°C; Pc211.=l 기 압 52 )• 티탄화합물 알루미늄화합물 소중합체(%) 중합체 (%) Ti C I. C2HsAlCl2 92 8 (C2MsO) Ti C l: ; C2H,AICI2 77 23 (C2Hs0) 3TiC l c2H5AlCl2 56 44 (C2H.O),Ti CzHsAlClz 31 69 Ti C I, (CzHs) zAICl 30 70 (C2H~O) Ti C h (C2Hs) 2AlCl 10 90 표 2.3 에서 시그마-전자주게리간드의 세기가 증가함에 따라 생 성물의 평균분자량이 증가함을 볼 수 있다. 죽 알루미늄화합물의 영소를 에틸기로 치환시키거나 티탄화합물의 염소를 에목시기로 치 환시키거나 같은 효과를 보여준다.
52) G. Henric i·O l ive and S. Oli ve , 0/ igo meriz a ti on of Et hy le ne wi th S oluble Transit ion Meta l Cata l ys t s , Advan. in Poy m er Sc ien ce, 15, 1 (19 74). 53() 1G이1. ).H enric i-O l ive and S. Oli ve , Ang e w. Chem. Inte r nat. Edit . , IO, 105
분자량이 적고 線型 인 에탈렌의 소중합체는 공업적인 면에서 중 요하다. 예 를 들면 생 물 학적 으로 분해 (b i odeg ra c! able) 되 는 세 락제 (de· ter ge n t) , 가소제 (pla sti ci z e r), 합성 고무 및 휘 발유 첨 가제 둥에 널리 쓰이는 소중합체는 분자량이 적고 線 型인 소중합체이다• 따라서 에 틸렌의 중합반응에서 線 型 소중합체를 얻으려는 연구는 홍미를 꿀 었다. 그러나 선형 소중합체의 생성은 많은 문제접을 갖고 있다. 왜냐하면 에틸렌의 소중합반응에서 생성되는 알파一올레핀은 전이 금속의 배위자리를 차지하여 에틸렌의 배위를 감소시킬 가능성이 있기 때문이다. 올레핀은 분자량이 증가함에 따라 금속에 배위되는 능력이 감소하지만 용액에 촌재하게 되는 1- 부맨은 그 농도가 증가 함에 따라 에틸렌과 경쟁적으로 금속에 배위함으로써 에틸렌의 중 합반응을 처해시킨다. 특히 높은 온도에서는 용액 중에 녹아 있는 에 탈렌의 농도가 낮아지기 때문에 l- 부터i의 배위를 무시할 수 없게 된다. 생성된 알파-울레핀이 금속―알킬에 삽입되면 갈래 있는 (branched) 분자가 생성될 것이다. 곧 이어서 베타―수소이동반응이 일어난다 떤 비널이벤과 같은 필요치 않은 분자가 생성될 것이다(식 (2.71) 참 조). 따라서 알파-올레핀의 삽입반응울 방지하기 위해서는 에틸렌 과 알파―올레핀의 배위능력의 차이를 이용할 수 있다. 예를 들면 리간드들을 변화시켜서 금속주위의 전자밀도를 중가시켜주면 오직 한 개의 에틸렌밖에 배위할 수 없게 된다.
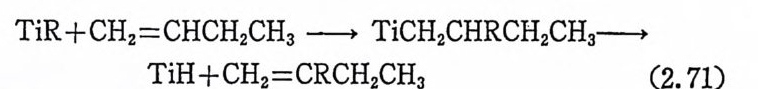 TiR + CH2=CHCH2CH3 一 T i CH2CHRCH2CHa 一
TiR + CH2=CHCH2CH3 一 T i CH2CHRCH2CHa 一
이 렇게 하여 갈래 있는 (branched) 중합체의 생성을 억제하면 표 2.3 에서 보는 바와 같이 생성물의 분자량은 커진다. 그러나 다행스럽 게도 반응온도를 조정함으로써 분자량의 증가를 여제할 수 있다. 죽 전자적 조건을 변화시 키지 않고 온도를 조정 함으로써 분자량이 너무 크지 않고 동시에 갈래없는 중합체를 생성시킬 수 있다. 실제 로 베타-수소이동반응의 활성화에너지는 사슬전파단계의 활성화에 너지보다 적다 .52) 따라서 온도를 내림으로써 생성물의 분자량을 적 게 할 수 있다.
촉매겨 1 의 변화에 의해서 조철되는 울레핀 소중합반응의 예를 하 나 더 든다면 Z i e g ler 형 촉매계에 의한 푸로필렌의 중합반응을 둘 수 있다. 푸로필렌의 소중합체는 양이온성 메카니즘 (ca ti on i c mecha- n i sm) 을 통하여 합성 된다 54)• 반응성 이 큰 카르보 양이 온 (carbon i um ion ) 중간체는 푸로팔렌 단위체와 쉽게 반응하지만, 또한 중합체사 숟(금속에 결합되어 있는)에 결합되어 있는 수소와 반응하는 수소 음이온 이동반응 (h y dr i d e t rans fe r) 을 쉽게 일으킨다. 따라서 갈래 있 는 중합체가 생성된다. 표 2.4 는 푸로필렌의 중합반응에 미치는 리 간드의 영향을 보여준다. 여기서도 리간드를 변화시킵으로써 금속 원자 티탄 주위에 전자밀도를 증가시켜주어 분자량은 적고 線型인 중합체의 생성을 증가시켰다. 올레 핀의 소중합 반응메 카니 즘을 조사하기 위 하여 , (C2Hs0)3TiC l /C2HsAlCl2 촉매계에 의한 에탈렌의 소중합반응에 관한 자세한 반 표 2. 4 분자량이 적 은 푸로필러J.중합체 의 線型度에 미 치 는 리 간드의 영 향 T i화합물 Al 화합물 분자량 線型度(%) TiC l, C2HsAlC! i 516 28 (C2Hs0) 3Ti C l C2HsAICI2 340 49 (C2HsO).Ti C2HsAICl2 432 87 TiC 1 4 (C2Hs) 2AlCl 557 70 (C2HsO) TiC h (C2Hs) 2AlCl llOO 94 옹속도가 측정된 바 있다 52) 이 촉매계에 의한 에틸렌 소중합반응 의 주 생성물은 線型 알파―올레핀이다. 이러한 반응의 경우에는 ' 단 지 다음의 두 반웅울 고려하면 된다. 죽 올레핀 삽입반응, 특히 사 술전과반응 (cha i n pro p a g at i on ) 석 (2. 71) 과 사슬이 동반옹 (cha i n tra ns· fe r) (식 (2. 72) )의 상대 적 인 속도를 고찰함으로써 메 카니 즘 규명 에 유용한 정보를 얻게 된다. 사슬전파속도 rp 는 식 (2. 73) 오로 표현된다. 여 기 서 P* 는 촉매 작 용의 활성을 갖고 있는 촉매종을 의미하며 M 은 올레핀 단위체를
54) E.H. Immergu t, G. Kollman and A. Malate s ta , J. Polym er Scie n ce, 51,. S-57 (19 61 ).
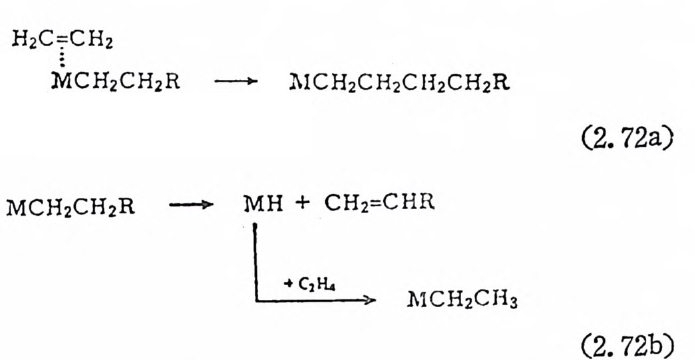 H2C7: CH2
H2C7: CH2
의 미 한다. 석 (2. 73) 은 일반적 으로 가용성 Zie g le r 형 촉매 에 의 한 반 옹에 적용되는 석이다.
![]() r p =k p〔 P 연[ M] (2. 73)
r p =k p〔 P 연[ M] (2. 73)
베타―수소이동반응(식 (2.72) )이 사슬을 배위하고 있는 금속분자 (M-CH 2 CH2R) 의 一分子反 應 ( monomolecular reac ti on) 이 라면 속도 rt 는 식 (2. 74) 로 표현된다.
![]() rt= kI[P *J (2. 74)
rt= kI[P *J (2. 74)
따라서 평 군 重合度 (de g ree of pol ym eriz a ti on ) P,' 은 식 (2. 75) 에 의 해서 주어진다.
![]() Pn=7p/ 7,=kp[ M J/k , (2. 75)
Pn=7p/ 7,=kp[ M J/k , (2. 75)
그러나 실제 실험적으로 발견된 바에 의하면 Pn 은 단위체의 농도 ([M J)에 따라 변하지 않고 반응온도에 만 의 촌한다. 52) 따라서 사슬 전파반웅의 속도결정단계는 울레핀 단위체를 포함하는 반응으로 생 각된다(석 (2. 76) 참조). 다시 말하면 올레 핀 단위 체 는 사술전과반응 분만 아니라 사슬이동반응에도 참여한다.
![]() r1=k,[P*J [M J (2. 76)
r1=k,[P*J [M J (2. 76)
따라서 올레 핀 단위 체 가 소모되는 속도는 식 (2. 77) 로 주어 진다.
![]() -d[M]/dt= rp+ r,=(kp+ k1)[P*J [M ] (2.77)
-d[M]/dt= rp+ r,=(kp+ k1)[P*J [M ] (2.77)
평 군 重 合度 (degr e e of p ol y mer i za ti on) 는 단위 체 의 소모속도와 사슬 이 동단계 (식 (2. 72) )의 속도의 比이 므로 식 (2. 76) 및 식 (2. 77) 로부 터 평군 중합도에 관한 식 (2.78) 을 얻게 된다. 식 (2.78) 은 실험적으 로 얻은 실험식과 일치하는 식이 된다 52)•
![]() 요= (rp+ r,)Jr , = kp/ k, + 1 (2.78)
요= (rp+ r,)Jr , = kp/ k, + 1 (2.78)
이제 사슬이동반응(식 (2.72) )에서 올레핀의 단위체가 어떻게 반 옹에 참여 하는지 살펴 보기 로 한다. 베 타-수소이 동반응(식 (2. 72)) 의 Arrheniu s 활성화에 너 지는 비 슷한 반응들에 관하여 얻어 전 값보 다 훨씬 적다. 표 2.5 에서 보는 바와 같이 AlH 및 HC1 형성과정의 활성화에너지는 T iH형성과정의 활성화에너지보다 훨씬 크다. 이러 한 사실로부터 T iH형성과정의 메카니즘은 HCl 이나 AlH 형성과정 의 메카니즘과 다를 것으로 추측된다. 전이금속에 결합된 알킬기 (사슬을 갖고 있는)는 바닥상태 (gro und s t a t e) 에서도 국성을 가질 수 표 2.5 베타―수소전달반웅들의 Arrhen i us 활성화에너지 반응 EA(kJ /m ol) 참고문헌 Ti H ― CI ― CI 一 _ Ti H+>C =C< ~25 52 I I Al H -cI -CI 一 —--> AIH+> C= C< 84~125 55 I I —CCIl - CHI _ 一 CIH+> C= C< 209~222 56 I I 있 는 것 으로 추측되 며 , 전이 상태 (tra nsit ion s t a t e) 에 서 는 아래 그림 과 같이 에틸렌 단위체를 활성화시킬 수 있는 것으로 제시되었다 .52) 따라서 속도식 (2.76) 이 설명되기도 한다. 55) A. T. Cocks and K. W. Egg e r, J. Gliem . Soc. , Faraday Trans 423 (1972). 561) 9S73. . 'Pa ta i, Ed. , The C}t em i st r y vf the Carhon·Halog e n Bond, Joh n wi! ey ,
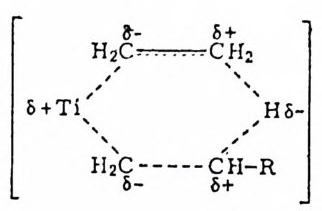 8· 5+
8· 5+
지 금까지 중합반응보다는 주로 소중합반응에 관하여 살펴 보았다. 실제로 에탈렌 또는 푸로필렌 둥과 같은 단순한(치환되지 않은) 올 레핀의 중합반응으로부터 분자량이 큰 중합체를 생성하는 촉매작용 들은 대부분불군일 촉매작용으로 알려졌다. 두개의 가용성 화합물 Ti Q:14 및 Al(C 晶 )3 의 혼합물로 이루어전 Z i e g ler 촉매계도 불균일 계이다. 왜냐하면 두 화합물을 섞으면 곧 T i (N) 는불용성인 Ti (][) 및 Ti( II )로 환원되 기 때 문이 다. Phil lip 촉매 로 불리 우는 크롬산화 물도 대표적인 불군일 촉매로서 올레핀 중합반응에 활성을 보여준 다. 가용성 촉매계의 연구로부터 얻은 일반적인 지식을 불균일 촉매 작용에도 적용시킬 수 있다. 불군일 촉매계에 의한 반응에 관한 자 제한 연구에는 많은 난접이 있어서 실제 찰 연구된 불군일 촉매작 용은 벌로 없다. 몇몇의 경우에 가용성 전이금속착물에 의한 에틸 렌 중합반응이 발표된바있다. 죽디클로로비스(시클로펜타디에널) 티 탄 ((C5H5)2T i Cl2) 및 클로로비 스(시 클로페 타디 에 닐) 에 틸 티 탄 ((C5 Hs)2C 晶 T i Cl) 을 각각 알루미 늄화합물과 혼합하면 각각 에 틸렌 중합 반응에 촉매저 역할을한다 .57) 공업적으로보면 이 촉매겨]는 좋은 촉 매계는 되지 못한다• 왜 냐하면 혼합물에서 T i (N) 화합물은 쉽게 열 분해되어 常磁性이며 가용성인 T i(][)화합물로 전환되면서 촉매적 활성을 잃는다. 그러나 이 촉매계는중합반응의 메카니즘 연구에 매 우 중요한 반응이다. 특히 전이금속 착물에 의한 군일촉매작용의
57) G. Heni: ici -O l ive and S. Oliv e , Ang e w. Chem. Inte r nat. Edit . , 6, 790 (19 67) a11d refe r ences the rein .
일반적인 반응메카니즘 정립에 유용하다. 지금까지는 주로 티탄 (N) 화합물과 알킬알루미늄으로 이루어지는 Zie g le r 형 촉매계 에 의 한 올레 .31J.의 중합반응을 상세 히 고찰하었 다. T i /Al 촉매계만 올레핀 중합반응에 활성울 보여주는 것은 아니다. 단지 지금까지 알려진 바에 의하면 단순(치환되지 않은) 울레핀의 중합반응에 는 Ti/ A l 촉매 계 가 가장 효과적 인 활성 을 보여 준다. 아크탈로니트릴 (CH2=CHCN) 및 메털대트아크릴레이트 (CH2=C(C H3)COOCH3) 둥과 같이 치환된 올레펀들도 전이금속―알킬(또는 수 소)화합물에 의해서 활성화되어 중합된다. 예를 들면 RuCl2(CH2= CHCN)3 은 150°C, 수소기압 =20 기압에서 아크랄로니트릴의 이합 반응을 일으켜 서 1, 4_ 디 시 아노 -l- 부터,l을 생 성 한다. 58) 이 반응은 수 소의 촌재 하에 서 일어 난다는 사실이 홍미 롭다(식 (2. 79) 참조).
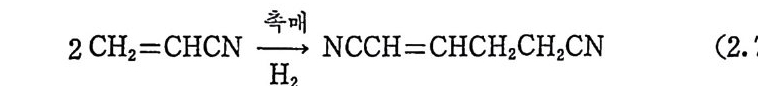 촉매
촉매
아크릴로니트릴, 메트아크릴로니트릴 (CH2=C(CH3)CN) 및 메탈 메트아크릴레이트 둥이 철―알킬착물, 코발트―수소착물 또는 루테 늄―수소착물에 의해서 중합되는 반응도 발표된 바 있다 59)• 이 연 구에서 Yamamo t o 등은 아크릴로니트릴과 메트아크릴로니트릴, 메 트아크릴로니트릴과 메틸메트아크릴레이트, 그리고 아크릴로니트릴 과 메탈메트아크릴레이트의 상호중합반응 (co p ol y mer i za ti on) 연구로 부터 중합체의 생성반응은 자유라디칼 메카니즘으로 진행되는 것도 아니고, 음이온성 메카니즘으로 진행되는 것도 아님을 제시하였다. 죽 촉매인 금속착물로부터 하나의 중성 리간드가 해리되어 올레핀 단위체가 배위할 수 있는 빈 자리가 생김으로써 중합반응이 개시될 수 있다고 저자들은 제시하였다. 생성되는 중합체의 분자량은 106
58) A. Mi so no, Y. Uchid a , M. Hida i and H. Kanai, Chem. Commun. , 35T (19 67). 59) a) A. Yamamoto , A11n. N. Y. Acad. Sci. , 239, 60 (1974). b) A. Yamamoto , T. Shim i zu and S. Ikeda, Makromol. Chem. , 136, 297 0970). c) S. Komi ya, AYa. mYaammoatmo , otAo . aYnadm Sa.m oIkteo d aan, dB Su.l l.I kCehdeam, . BSuollc.. JCahp e .m ,. 4S8o, c.1 01J a0p 9. 7, 5)4.5 ,a )l lTlL.. (19 72).
청도로 상단히 크다. 베타―수소이동반응이 일어나서 반응이 종결 (t erm i na ti on) 되 는 것 이 아니 고, 환원성 제 거 반응에 의 한 종결 이 일 어나며 촉매인 착물은 종결반응과 동시에 분해되며 촉매적 활성을 잃어 버리는 메카니즘이 제시되었다. 5. 酸化反應 (ox i da ti on) 군일촉매작용에 의하여 올레핀을 산화하여 알코올, 알데히드 및 에폭시드를얻는반응은공업적으로매우중요한반응이다. 에틸렌을 산화시 켜 서 아세 트 알데 히 드를 생 산하는 Wacker 공정 (Wacker pro - cess) 은 약 20 여 년전에 개 발되 어 오늘날까지 매 우 유용하게 응용되 고 있다. 팔라듐 금속화합물을 촉매로 사용하여 에틸렌을 산화시키는이 촉 에작용은 많은 사람들에 의해서 연구되어 왔다. 여러 연구자에 의 한 보고는 구체적인 반응메카니즘에서 일치되지 않는 접도 보여주 지만 근본적인 반응메카니즘에는 모두 동의하는 것으로 추측된다. 아래 에 Wacker 공정 을 자세 히 살펴 보기 로 한다. (1) Wacker 공정 에틸렌울 산화시켜 아제트알데히드를 합성하는 Wacker 공정의 개 발은 아세 틸 렌을 초기 물질 (sta r tin g ma t er i al) 로 하는 유기 화합물 생 산체제에 커다란 변화를 가져왔다. 아세틸렌으로부터 얻는 아세트 알데히드는 그 자체가 중요한 유기합성(예를들면 아세트산의 합성) 에 중요한 중간체이었다. 그러나 아세틸렌을 생산하기 위하여서는 많은 에너지가 필요하다. 따라서 처음으로 에틸렌으로부터 바교적 쉽게 아세트알데히드를 합성하는 방법이 개발되었을 때 많은 생산 공정에서 곧 그 방법이 채덱되었다. 금속―카르보닐 화합물을 촉매 로 사용하여 아세트산을 합성하는 방법이 최근에 많이 연구되고 있다. 그러나 Wacker 공정은 현재까지는 가장 많이 응용되는 균일 촉매작용의 하나이다. Wacker 공정은 실제로 오렌 역사를 갖고 있다고 볼 수 있다. 엽
화팔라듐에 의하여 에틸렌이 아세트알데히드로 산화되는 화학량론 적 반응(식 (2. 80)) 은 이 미 1894 년에 알려 졌 다. 60) 그러 나 1956 년에 비로소 처음으로 이 화학량론적 반응(식 (2.80)) 은 이미 알려진 반 웅들(식 (2. 81) 및 식 (2. 82) )과 합쳐 져 하나의 촉매 적 아세 트알데 히 드 합성 공정 이 되 었 다(식 (2. 83) 참조). Wacker 공정은 공업적으로 두 가지 방법으로 전행된다. 첫째 방
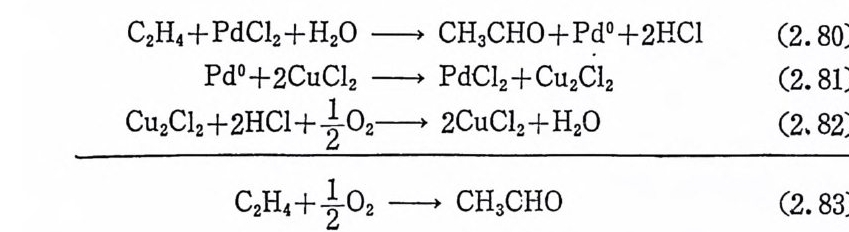 C2H4+PPdd0C+I22C+uHC2I20 ——•.. CPdHC3lC2+HCOu+2CPdl20 +2HCI ((22.. 8810 ))
C2H4+PPdd0C+I22C+uHC2I20 ——•.. CPdHC3lC2+HCOu+2CPdl20 +2HCI ((22.. 8810 ))
법 에 서 는 산소―에 틸렌 혼합물을 PdCI2 와 CuCI2 의 수용액 에 불어 넣고 120°c, 4 기압에서 반응시킨 다음 반응기로부터 생성된 아세 트알데 히 드를 분벌한다. 둘째 방법 에 서 는 PdCI2 와 CuCI2 의 수용액 을 이 용하여 화학량론적 반응(식 (2. 80) )에 따라 아세 트알데 히 드로 산 화시 킨 다음 생 성 된 유기 화합물을 반응기 로부터 제 거 한 후에 Cu2Cl2 를 공기에 의해서 다시 산화시킨다(식 (2.82)). 두 방법 모두 95% 의 수율로 아세트알데 히 드를 생성서 킨다. 소량의 클로로에 한울, 클로 로에탄, 아세트산, 클로로아세트알데히드 및 아세트알데히드의 축 합생성물이 함께 생성된다. 에틸렌보다 분자량이 큰 올레편도 Wacker 공정에 의해서 산화된 다. 말단 울레핀(t erm i nal ole fi n) 은 메틸케론으로 산화된다. 예를 들면 아세돈은 팔라듐화합물에 의한 푸로필렌의 산화에서 생산된다. 주 로 공업에서 이용되고 있는 이 반응은 매우 빠르며 부산물도 없는 ~ 깨끗한 반응이다. 그러나 알킬기의 사슬이 길면 길수복 수율이 낮 아진다. 즉 푸로필렌은 20°c 에 서 5 분 동안에 90% 의 수율로 아세 톤으로 산화되지만 1 떠 l~ 은 70°C 에서 1 시간 동안에 겨우 34% 의 수울로 2- 데 카논으로 변한다. 61) 고리 계 올레 핀 (cy cl i c ole fi n) 도 용야
60) F. C. Phil lips. Am. Chem. J. , 16, 255 (1894). 61) J. Smi dt , Ang e w. Chet> i. , 71, 176 (19 76).
하게 비교적 높은 수율로 고리계 케돈으로 산화된다. 그러나 내부 올레 판 (int e r nal ole fi n) 은 여 러 가지 생 성 물로 산화된다. Wacker 공정 이 라고 일반적 으로 불리 우는 팔라듐촉매 에 의 한 울 레핀의 산화는 반응조건에 따라 상당한 차이룰 보여준다. 아세트산 용액에서 에틸렌울 산화시키면 조건에 따라 비닐아세테이트, 에탈 렌글리콜아세데이트, 또는 2- 클로로에탈아세테이트 등이 각각 주생 성물이 될 수 있다 .62) 한편 메탄올 용액에서는 메틸비닐에테르, 또 는 CH3CH(OCH3)2 를 각각 주생성물로 얻을 수 있다. 수용액에서 는 2 용문로로에 탄올이 주생 성 물이 된다. 63) 우}에서 기술한 것처럼 Wacker 반응의 메카니즘은, 일부 문제점 은 있지만, 비교적 잘 연구되어 왔다. 이제까지 발표된 연구는 공 통적으로 아래의 반응(식 (2.84)~(2.86) )들을 제시하고 있다. 즉 Cl 一 의 농도가 높은 용액에서 반응이 전행되므로 팔라듐은 〔 PdCl 』 2- 로 존재하게 되고 [PdCl 』 2- 중의 Cl-한 개가 에탈렌에 의해서 치환되 는 반옹이 최초의 단계이며 (식 (2.84)), 이어서 계속 일어나는 두 단계의 반응 (식 (2.85) 및 (2.86) 에서 〔 PdCl2(0H)(C2H4) 〕-가 생성 된다. 따라서 이 반응의 속도는 c1- 의 농도가 증가함에 따라 민감 하게 감소한다.
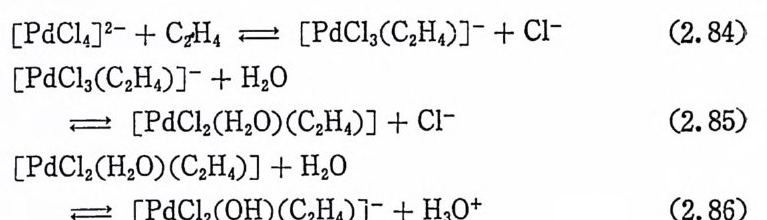 [PdCl4J 2- + CtH 4 •=: [P dClJC C 2H4)]- + c1- c2. 84)
[PdCl4J 2- + CtH 4 •=: [P dClJC C 2H4)]- + c1- c2. 84)
[PdClz( O H) (C2H4) J제 서 [PdCl z( -CH2CH20H)] -로 되 는 과정 에 관하여서는 두 개의 각각 다른 메카니즘이 제시되어 있다(실제로 . Pd-CH2CH20H 화합물의 존재는 실험적으로 확인되지는 못했으나· 항상 중간체로서 논의되고 있다.). 최근까지 Pd-CH2CH20H 의 생
62) R. Jira and W. Freis le ben, Olefi n O xid a ti an anc Relate d Reacti on s wit h Group VIII Noble Meta l Comp ou nds, Orga nomet. Raact. , 3, 1 (19 72). 63) H. Sta n g l and R. Jira , Tetr a hedron Lett . , 3589 (19 70~.
성은 석 (2.87 ) 에서 보여주는 것처럼 팔라듐에 배위된 OH 가 배위 된 에틸렌의 탄소로 이동되는 반응에 의한 것으로 이해되었다(이 반웅은 Pd-OH 결합에 에탈렌이 삽입되는 반응이라고도 볼 수 있
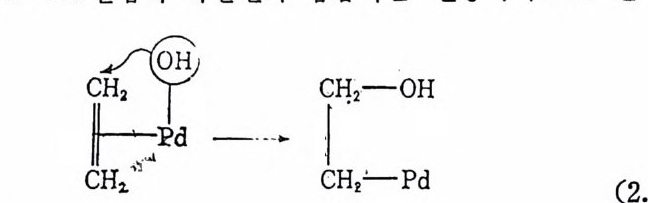 c~<~ d ― ·- - ► 鄧l ― OH
c~<~ d ― ·- - ► 鄧l ― OH
다.). 반응속도론적 실험 데이타를 분석한 결과 식 (2.87) 이 지지되 어 왔다. 그러 나 최근의 CHD=CHD 를 사용한 연구보고는 석 (2. 88) 과 같이 배위되지 않은 찬핵체 (nucleo p h il e) 의 공격에 의해서 Pd-CH2 CH20H 가 생 성 된다고 보고하였 다. 64)
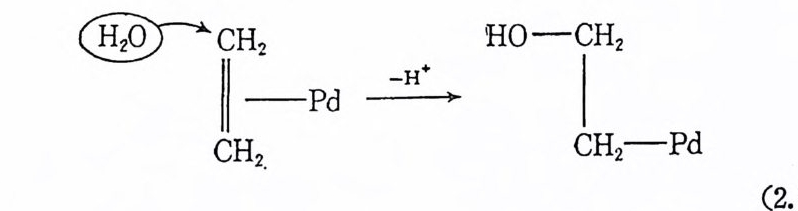 運 cH2 HO 一 CH2
運 cH2 HO 一 CH2
D20 용액에서 에틸렌의 산화반응을 시켜본 결과 생성된 아세트알 데히드는 重水素를포함하지 않았다. 이 결과로부터 Pd 一 CH2CH20H 중간체가 CH3CHO 를 생성하는 과정은 팔라듐의 배위권 내에서 일어 남을 다음과 같이 추측할 수 있다. 죽 Pd-CH2CH20H 는 베 E l-수 소제거반응을 일으켜 비닐알콜히드리도팔라듐착물을 생성하고(식 (2.89)) 이어서 생성된 비널알콜히드리도팔라듐착물은 배위된 비닐
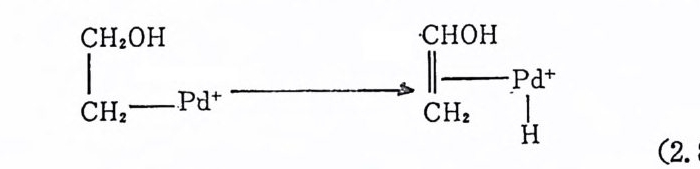 CCIHH 22 _0H_ p tl+ ·CC1HH 1O: H- _pHId + (2. 89)
CCIHH 22 _0H_ p tl+ ·CC1HH 1O: H- _pHId + (2. 89)
64) a) J. E. Backvall, B. Akermark, and S. O. Lju n g gr en, J. Am. Chem. Soc. , 101, 2411 (19 79). b) J. K. Sti lle and R. Div a karuni, J. Orgo met. Chem. , 169, 239 (1979).
기에 다시 분자내 수소첨가반응을 일으켜 알파-히드록시에탈팔라 듐착물을 생 성 한다(식 (2. 90) 참조). 이 렇 게 하여 생 성 된 알파히 드록 시에탈팔라듐 중간체는 다시 베타-수소제거반응을 통하여 아세트 알데 히 드를 생 성 한다(식 (2. 91) 참조). 석 (2. 87) 부터 식 (2. 91) 까지 에
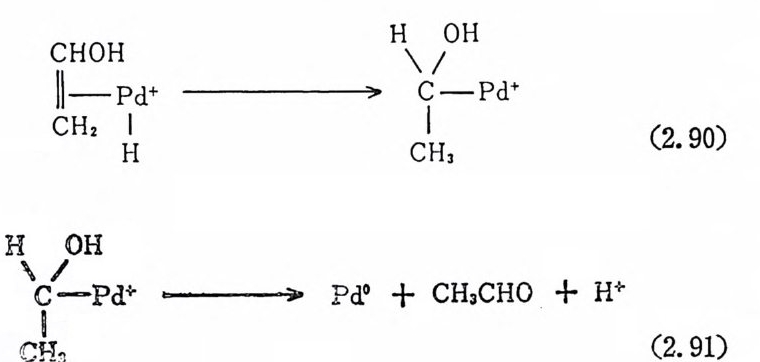 CII—H OHP d+ H\ c/— O H Pd+
CII—H OHP d+ H\ c/— O H Pd+
서는 팔라듐의 산화상태 및 기타 리간드를 표시하지 않았다. 왜냐 하면 대부분 추정에 의한 것이기 때문이다. 식 (2.91) 에 의해서 생 성 되 는 팔라듐화합물은 Pd0 화합물(또는 Pd0 금속자체 )이 거 나 Pd_ H 화합물로 추정된다. 이렇게 하여 생성된 팔라듐화합물은 과량의 염소이온이 존재하는 용액에서 Cu( JI)에 의해서 쉽게 Pd( JI)화합 물로 산화된다. (2) 히드로파산화물에 의한 울레핀의 에쪽시화반응 푸로필렌을 산화하여 산화푸로필렌을 생성하는 새롭고 중요한 군 일촉매작용이 1967 년 Halcon 회사에 의해서 발표되었다 65)( 식 (2.92) 참조). 실제 이 촉매 작용은 이 것 보다 먼저 1965 년에 발표된 다음 과 같은 실험적 견과를 응용한 것이었다. 죽 알킬―히드로과산화물 과 올레핀 사이에 일어나는 산소이동반응 (ox yg en t rans fe r) 은 촉매적 반응이 다라는 사실이 다. 66) 실험적 결과를 살펴본다면 아래와 같다. 소량의 Mo(C0)6 촉매를 6665)) HN.y dI rnodciac rt bo or na nPdr oWc. ., F4. 6,B r-1i4ll1 , (]A. p Ori rl g 1, 9 6C7h).e m. , 30, 2074(1 9 65).
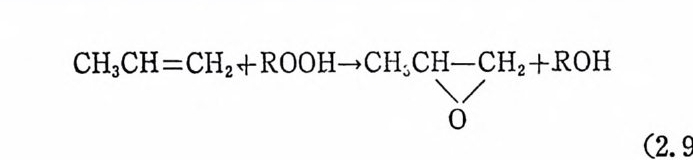 CH3CH=CH2+ROOH->CH. C H>— /CH 2 +ROH
CH3CH=CH2+ROOH->CH. C H>— /CH 2 +ROH
사용하여 히 드로과산화 t-부탈 Ct-b uty l hy dro p erox i de) 용액 을 105°c 에 서 1 시간동안 푸로필렌(고압)과 반응시키면 약 86% 의 수율로 산 화푸로필렌이 생성된다 .67) 다른 히드로과산화알킬을 사용하여도 비 슷한 수율을 얻을 수 있다. 그러나 t-부틸 유도체는 비교적 안정하 기 때문에 많은 실험실에서 사용되고 있다. 대부분의 경우에 과량 의 올레 핀을 사용하여 히 드로과산화물이 완전히 소모되 게 한다. 그 러나 산화바리움이 공촌하면 히드로과산화물은 안정화되어 분해가 일어나지 않으므로 화학량론적 양의 올레핀을 사용할 수 있다 .68) 푸로팔렌분 아니라 다른 여러 종류의 올레핀의 에폭시화반응도 히 드로과산화물과 전이 금속촉매 에 의 하여 일어 난다. 67) 2- 부터l l, 시 콜로 헥센 및 2 - 메틸 -2 홉신덴 동 내부 올레포tl(i n t ernal ole fi n) 은 말단 올레핀 (ter mi na l ole fi n) 보다도 빠르게 반응하며 거 의 정 량적 인 에 폭시 화합 물 생성한다. t -BuOOH 를 사용하는 울레핀의 에폭시 반응은매우 선택적으로 일어난다. 예를 들면 바나듐착물운 촉매로 하여 시클로 옥타디 엔 올 (C y clooc t ad i enol) 을 t-B uOOH 와 반응시 키 면 식 (2. 92h) 과 같이 OH 에 가까운 이중결합에만 에폭시화 반응이 일어난다 .69) 촉
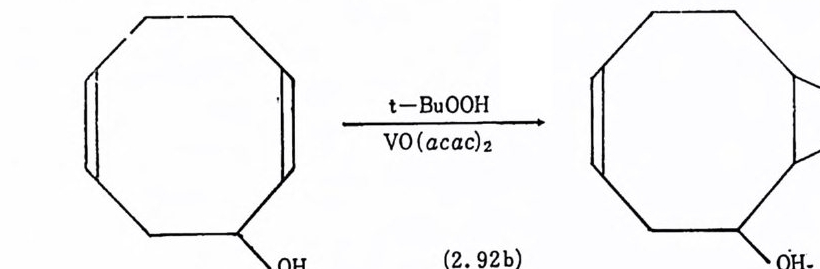 t-B uOOH 。
t-B uOOH 。
67) M. N. Sheng and J. G. Zaja c ek, Hy dr op er oxid e Oxid a ti on s Cata l yz e d by- Meta l s, in F.R. May o , Ed,, Oxid ati on of Orga nic Comp ou nds, vol. 2,. Advances in Chenu'str y Serie s 76, Americ a n Chemi ca l Socie t y 1968, pp, 418. 68) C.Y. Wu and H.E. Swi ft, 1. Cata / ., 43, 380 (1976). 69) T. Itoh , K. Jitsu kawa, K. Kaneda, and S. Teranis h i, J. Am. Chem ► Soc. , 101, 159 (19 70).
매적 에폭시화반응에서 가장 활성이 큰 촉매 1 는 몰리브맨 화합물이 다 .67) 바나듐화합물도 상당히 활성이 크며, 티탄, 지르코늄 및 크 롬화합물도 약간의 활성 을 갖고 있 다. 에 폭시 화반응에 황성 이 크지 않은 전이금속화합물 촉매를 사용할 경우에는 히드로과산화물의 분 해(자유 라디칼에 의한 분해 또는 촉매에 의한 분해 〉 때문에 필요 치 않은 부산물이 생성된다. 예를 들면 히드로과산화 t-부털 또는 히 드로과산화 큐멘 (cumene) 의 반응에 서 아제 본이 생 기 는 것 을 볼 수 있다. 많은 몰리 브 E선 화합물이 에 폭시 화반응에 활성 을 보여 준다. 홍미 로 운 접은 몰리브렌의 산화수가 0 인 Mo(C0)6 와 몰리브덴의 산화수 가 +6 인 Mo03 가 같은 정도의 활성을보여준다는접이다 .6” 이 접 윤 선명하려면 Mo(C0)6 나 Mo03 는 실제 촉매가 아니고 촉매 전구 물질 (ca t al y s t p recursor) 이라고 생각할 수 있다. 실제로 상기 두 몰 리 브 E선 화합물에 의 한 에 폭시 화반응은 반응이 시 작되 기 전에 유발기 (ind ucti on p er i od) 가 있다. 이 유발기 동안에 몰리브덴 촉매는 올레 펀 및 히드로과산화 알킬과 반응할 것으로 추정된다. 울레포l l, 히드 로과산화 알킬 그리고 몰리브덴 (Mo(C0)6 또는 Mo03) 의 반응에서 얻어지는 착물의 생성속도를 실제 측정하여 본 결과 몰리브델, 올 레핀, 그리고 히드로과산화물의 농도에 비례함을 알았다 .70) 6. 올레팬의 상호교환반응 (me t a t hes i s) 올레 펀 상호교환반응 (ole fi n-me t a t hes i s) 는 대 단히 중요한 촉매 반응 이다. 두 개의 탄소―탄소 이중결합이 끊어지고 새로운 두 개의 란 소―탄소 이 중결합이 생 성 되는 올레 핀 상호교환반응은 식 (2. 93) 으. 로 표시된다. 이 반응은 1964 년 처 음으로 Banks 등 7l) 에 의 해서 발표되 었 다. Banks 는 고온 (100~300°C) 에서 몰리브덴과 텅스텐 착물을 촉매로
70) V. N. Sapu nov, I. Yu. Lit vi n s te v , R. B. Svit ych , and N. N. Rzhevskay a , 71K) zR' n .eLt.. KBaanlakls. ,a n1d8 , G4.C08. 0B9a7il7y ), . Ind. Eng . Chem. Prod. Res. Develop ., 3, l,70 (19 64).
 RRHHCC+== CCHHRR'' ~촉 매 RRCCII HH + RR''C CII HH (2. 93)
RRHHCC+== CCHHRR'' ~촉 매 RRCCII HH + RR''C CII HH (2. 93)
사용하여 푸로필렌으로부터 에 탈 렌과 2- 부덴을 합성 하였 다(식 (2. 94)). 이 어 서 Calderon 둥 72) 은 아래 식 (2. 95) 및 (2. 96) 에 서 보여 주 는 바와 같이 두 개 의 시 클로울레 핀 (c y clo-ole fi n) 이 고리 열 림 (rin g -
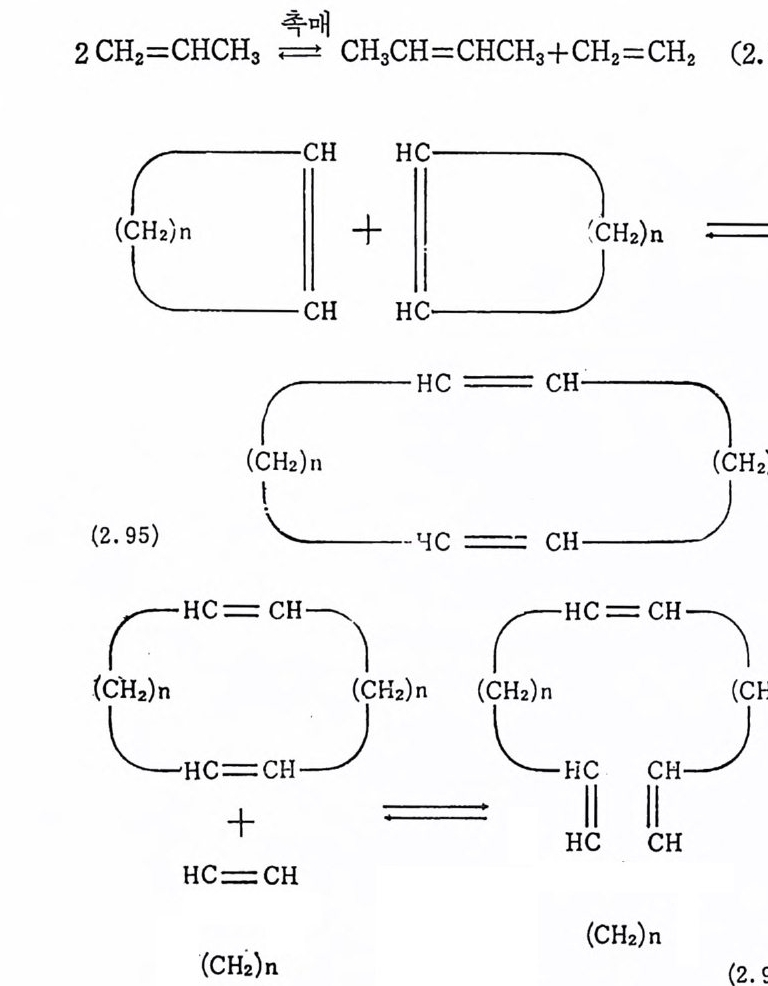 촉매
촉매
72) N. Calderon, E, A. Ofs t e a d, J. P. .Wa rd, W. A. Jud y and K. W ScoH, J. Am. Chem. Soc. , 90, 4133 (19 68).
o p en i ng ) 중합반응을 일으킴 을 발표하면서 이 들 반응듣도 올레 핀 상 호교환반응 경로를 거쳐 일어날 것이라고 제시하였다. (1) 觸媒系 Banks 둥 71) 에 의 해서 최 초로 보고된 촉매 계 는 不均一촉매 계 로서 불용성 산화알루미 늄에 부착된 (sup po rte d ) 산화물리 브덴, 헥 사카르 보닐몰리브덴 또는 헥사카르보닐텅스텐 둥이다. 헥사카르보닐몰리 벤이나핵사카르보닐텅스텐울 산화알루미늄에 부착하여 얻어지는 촉 매계는 최초에는 촉매적 활성이 적다. 그러나 전공에서 가열하면 촉 매적 활성이 증가한다. 이렇게 활성이 증가하면서 배위된 CO 는 금 속으로부터 떨어져 나간다. 실제로 가장 촉매적 활성이 큰 금속화 합물은 CO 를 하나도 배위하고 있지 않다. 이렇게 배위된 CO 를 모 두 잃어버란 몰리브덴 및 텅스텐은 어느 정도 산화되어 각각의 산 화수는 0 보다 크고 +6 보다는 적게 된다. 현재까지 알려진 것 중에서 가장 촉매적 활성이 높은 가용성 均一 촉매계는 할로겐화텅스텐화합물을 포함하는 촉매계이다. 몰리브덴, 레 늄 (Re) 및 탄탈 (Ta) 등도 상당히 높은 촉매 적 활성 도를 갖는 촉매 계 를 이 룬다. 맨族금속의 착물도 올레 펀 상호교환반응에 촉매 적 활 성을 보여준다 .73) 많은 멘族 금속의 착물 촉매에 의한 촉매반응은 알컬알루미늄 또는 기타 유기금속화합을 필요로 하지 않는다. 즉 VIII 族 금속의 착물만 촌재하면 촉매작용은 일어난다. 그러나 그 촉 매적 활성은 비교적 낮은 편이다. 위에서 기술한 바와 같이 대부분의 均一촉매겨]는 Z i e g ler 형 계이 다. 죽 할로겐화전이금속화합물과 할로켄화알킬알루미늄의 상호작 용에 의해서 촉매계가 이루어진다. 초기에 보고된 것 중에서 대부~ 의 촉매 계 는 WC16 및 C2HsAlCl2 등과 같은 강한 Lewi s 의 산을 포 함하고 있으므로 Fri ed el-Craft s 반응과 같은 필요없는 副反應울 동 반한다. 분만 아니라 이상의 촉매계는 용해도가 낮고, 촉매적 활 성이 있는 화학종이 불안정하기 때문에 실험의 재현성 (rep ro duc ibi l ity)
73) G. Dall' Asta , Prep ar ati on and Prop er ti es of Po/ya l kenamers, Rubber Chem. and Technal. , 47, 511 (19 74).
을 얻기가 힘들었다. 이러한 접을 해결하기 위해서 산소를 포함하 논 화합물(알코올, 페놀, 물 또는 히드로과산화물 둥)을 텅스텐/알 루미늄계에 첨가하여 좋은 성과를 얻었다 73). 첨가제는 반드시 할로 젠화알킬알루미늄을 가하기 전에 할로겐화텅스덴화합물에 가해져야 한다. 이 첨가제의 역할은 아직 확실히 밝혀지지는 않았지만, 할로 겐과 같은 리간드와 치환되어 용해도가 높고 안정도가 높은 금속착 물을 형성할 것이라고 추측된다. 상기 첨가제를 사용함으로써 모든 경 우에 서 Fr ied el-Craft s 반 응은 최 소한 어 느정 도 감소시 킬 수 있 었 다. 비 교적 약한 Lewi s 의 산인 Mo( II ) 및 W( II ) 착물 (MCl2(N0)2 12 ; M=Mo,W; L= 트리페널포스펀 또는 피리린)을 촉매로사용하 떤 첨가제를 사용하지 않아도 F ri edel-Cra ft s 반응을 여제할 수 있 으나, 역시 울레핀 상호교환반응의 속도는감소된다 .74) 현재까지 발 표된 것 중에서 WCls/CC 晶 )20/(C 晶 )4Sn 계가 가장 안정하며 또한 Fr ied el-Craft s 반 응도 최 소한으로 줄일 수 있 는 촉매 계 로 알려 졌 다 75)• 모든 경우에서 실제촉매종(실제 촉매적 활성이 있는 화학종은 초 기 물질과 다를 수도 있다)은 최소한 한 개 또는 그 이상의 환원된 금속을 포함하는 것으로 추측된다. 금속의 환원은 알킬알루미늄과 같은 유기금속화합물에 의해서 이루어질 것으로 추측되고 있다. 알킬알루미늄은 Z i e g ler 형 촉매에서와 같이 두가지 역할울하는 것 으로 제시되었다. 즉 알킬알루미늄화합물은 전이금속의 알킬화반응 및 환원을 일으킬 분만 야니라 그 자신이 촉매적 활성이 있는 착물 울 형성하는 것으로 추측된다 .72) (2) 熱力學的안 考察 두개의 이중결합이 끊어지고비슷한두개의 이중결합이 생성되는 올레편 상호교환반응의 반응 '엔 탈피 값은 대단히 적은 값이다. 따 라서 올레핀의 상호교환반응은 엔트로피에 의해서 견정되는 화학평
74) E. A. Zuech, W. B. Hug h es, D. H. Kubic e k and E. T. Kit tlem an, J. Am. Chem. Soc. , 92, 528 (1970). 75) G. Pamp us , G. Lehnert and D. Maerte n s, 164tl i ACS Meeti ng , 1'57 2 .
형아라고 봉수 있다. 입체적 장애효과가 벌로 없고 이중결합의 이 동이 일어나지 않는다면 통계적인 비율로 가능한 모든 생성물이 얻 어 질 것 이 다. 푸로필렌의 상호교환반응(식 (2. 94) )을 예 로 들어 본다 떤 푸로필렌 : 에 틸 렌 : 2- 부텐의 몰 비 율이 2 : 1 : 1 이 되 는 평 형 이 쉽게 얻어진다 .71) 한편 커다란 올레핀의 상호교환반응은 더욱 많은 수의 생성물을 생성시키는데 그 이유는 이중결합의 이동반응 (m ig ra ti on) 에 의한 것으로 해석된다. 그러나 몇몇 均一系에 의한 커다 란 올레핀의 상호교환반응은 이중결합 이동반응에 기인되는 생성물 은 거의 생성시키지 않고 통계적으로 예상되는 비율로 일차생성물 만을 생성시킨다. 입체적인 장애가 상당히 중요하게 작용하면 평형 은 비교적 입체적 장애가 적은 올레핀의 생성방향으로 이동될 것이 다. 고리 열 림 중합반응 (r i n g op en in g p ol y mer i za ti on) 에 서 는 약간 다르게 취급된다• 상기 중합반응에서 결합의 수나 결합의 형태는 크게 변 화되 지 않는다. 그러 나 고리 스트레 인 (rin g s t ra i n) 에 기 인되 는 엔 탈 피만큼 열역학적으로 유리한 방향으로 반응이 진행될 것이다. 죽 고리열림중합반응이 고리스트레인만큼열역학적으로유리할것이다. 고리 의 원자수가 4 또는 5 일 때 고리 스트레 인은 비 교적 크고 (>20 KJ /m ol), 고리 원자수가 증가하면 고리 스트레 인은 적 어 진다 (12~20 KJ /m ol). 예 외 로 시 클로핵 센의 고리 스트레 인은 0 에 가깝다. 고리 열림중합반응에 관하여 엔트로피를 고찰함은 상당히 복잡하다. 예 를 돈다면 식 (2. 95) 및 식 (2. 96) 의 반응은 두 분자가 반응하여 한 분자가 생성되는 반응이므로 엔트로피면으로 보아서 진행될 것 같지 않다. 그러 나 C7 이 상의 커 다란 고리 화합물의 비 들림 (tor sio n ), 또는 기타 진동 (v i bra ti on) 둥의 엔트로피를 고려하면 반응은 진행될 것으 로 예측된다. 따라서 시클로펜텐의 상호교환반응은 엔탈피면으로 보면 상당히 진행될 것으로 예측되지만 엔트로피면으로 보면 약간 반대 방향의 반응이 예측된다. 같은 메카니즘으로 시클로핵센의 중 합반응은 일어나지 않을 것으로 예측된다. 왜냐하면 엔탈피는 0 에 가까운 값을 가지게 될 것이며 엔트로피로도 불리하게 예측되기 때 문이다. 그러나 한판 C7 보다 큰 고리올레핀의 상호교환중합반응은
엔탈피와 엔트로피면에서 모두 반응이 상당히 진행될 것으로 예측 된다. (3) 상호교환반응의 立體特異性 순수한 시스화합물, 또는 순수한 트란스화합물, 또는 시스 및 트 란스-화합물의 혼합물을 초기물질로 하여 올레핀의 상호교환반응 울 시켜 본 결과 이상의 모든 경우에서 열역학적으로 예상되는 올레 판들의 시스―트란스 평형을 얻었다. 예를 들면 고리아닌 올레핀 (acy c lic ole fi n) 의 상호교환반응에서 평형에 있는 혼합물은 0~20°c 에 서 약 80~85% 의 트란스화합물을 포함하고 있 다. 76) 물론 순수한 트란스올레핀은 금속에 배위되는 능력이 낮기 때문에 천천히 반응 할 것이 예상된다. 상호교환반응단계에서 시스와 트란스 이성질체의 평형농도가 얻 어지는 것인지, 또는 반응이 입체득이성을 갖고 있는지, 또는 올레 핀의 평형이 서로 독립적이면서도 동시에 일어나는 이성질화반응의 결과인지는, 현재 확실하지 않다. 고리열립중합반옹에 관하여서는 역시 종 다르게 고찰되어야한다. 몇몇 올레펀 특히 시클로펜텐의 중합반응은 높은 입체특이성을 보 여준다. MoCls/CC 品 )3AI 촉매계에 의해서 일어나는 시클로펜텐의 고리열림중합반응은 99% 이상의 시스이종결합을 포함하는 고리펜 텐중합체 (p ol yp en t eneamer) 를 생 성 한다. 77) 그러 나 한괜 WC16/CHO H(CH2Cl)2/(i-C 4H9)3AI 촉매 계 는 80~85% 트란스이 중결합을 포함하 는 중합체를 생성한다 .77) 촉매성분의 몰 비율을 변화시키거나 반 웅온도를 변화시킴으로써 시스와 트란스의 비율을 조철할 수 있 다 .73),77) 상온에서 만들어지는 WCl5/CC2Hs)4Sn/(C2Hs)20 촉매계는 상온에서 80% 의 트란스이중결합의 고리펜덴중합체를 생성한다 .77) 이 촉매겨 1 는 -30°c 에서는 활성을 잃어버린다. 그러나 이 촉매계 가 ― 30°c 에서 만들어지면 -30°c 에서 촉매적 활성을 보이며 92% 의 시스이중결합중합체를 생성시킨다. 이상의 결과는 다음과 같이 .
76) W. B. Hug h es, Chem. Comnmn. , 431 Q9 69). 77) G. Dall'Asta and G. Mot ro ni, Ang e w. Chem. , 16, 51 (1971 -).
설명되었다 .77) 즉 각각의 경우에 각각 다른 촉매적 활성체, W(N) ((C 品 )20)Cl4 및 W(V)(C 晶 )Cl4 가존재한다. W(V)-C2Hs 착물 은 -30 ° C 이하에써는 안정하고 상온에서는 분해된다. _30 ° c 에서 주로 시스중합체가 생성되는 이유는 입체적인 효과로 추측된다. 죽 W(V)(C 晶 )Cl4 중의 리간드들은 오직 시스중합체를 생성시킬 수 있는 방법으로 촉매와 단위체(시클로펜덴)가 반응하게 한다. 트란 스중합체는 시스중합체를 생성시키는 촉매 (W(C2H5)Cl4) 와는 반응 하지 않는다. 시 스중합체 는 트란스중합체 를 생 성 하게 하는 촉매 계 에 의해서 쉽게 열역학적으로 유리한 트란스이성질체로 변한다. 그 러나 트란스이성질체는 시스이성질체로 변하지 않는다. (4) 반응메카니즘 (reac ti on mechanis m ) 올레핀 상호교환반응의 메카니즘에 관한 첫 의문은 어떤 결합이 끊어지며 어떤 결합이 생성되느냐 하는 것이다. 군일촉매겨]나 불균 일촉매계에서 이 문제의 해답은 이미 아래와 같이 알려져 있다. 운 레핀 상호교환반응의 생성물을 보면 다음의 누 가지 가능성을 생각 하게 된다. (1) 탄소와 탄소 사이의 단일결합이 끊어지고 알킬기의 전달반응이 일어 나는 과정 (식 (2. 97) 의 a) 과 (2) 탄소와 탄소 사이 의 이중결합이 끊어지고, 다시 형성되는과정율포함하는과정(식 (2.97) 의 b) 을 추측할 수 있 다. Calderon 등은 72) 2 - 부덴과 d8-2- 부텐(식
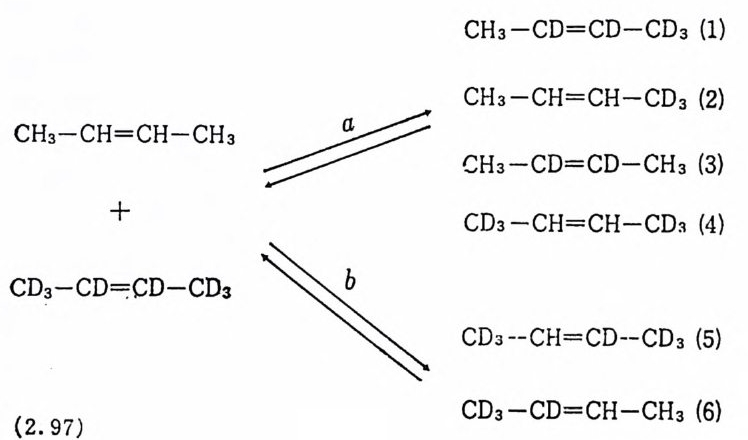 CHa -CD=CD-CDa (1)
CHa -CD=CD-CDa (1)
(2.97) 의 6) 의 상호교환반응에서 생성물로 오직 d~ - 2 - 부텐만을 얻었 다. 이상의 실험적 결과로부터 이 반응은 탄소와탄소사이의 이중결 합이 풍어지는 과정만을 포함하며, 탄소와 탄소 사이의 단일결합은 이 반옹에서 끊어지지 않음을 알 수 있다. 불균일촉매를 사용하여 서도 비슷한 실험적 결과를 얻었다. Mol 둥은 78) 푸로필렌 -2-14C(C H2=14CH-CH3) 의 상호교환반응에서 2 - 부덴과 에틸렌을 얻었는데 l4C 은 오직 부텐에서만 /발 견되었C다H 2( =식= 아(2t. 298+)C 의H 3b -)C. H =14CH-CH3 2 CH=14CH-CH3 \ (2 . 98 ) CH2=CH2+CH3 -C H =14CH 니 CH3 이상의 모든 실험적 결과는 이중결합이 끊어지는 과정만윤 포함 하는 메카니즘과 일치하며, 알킬기의 전달반응메카니즘과는 일치하 지 않는다. 울레핀 상호교환반응의 메카니즘은 탄소와 탄소 사이의 , 이중결합 이 낮은 활성화에너지 경로를 통하여 끊어지고 각종 알킬이벤이 생 성되는 과정을 포함하여야 한다. 이제까지 제시되어 온 메카니즘은 두가지로 구분된다. 첫째는한쌍의 울레.;.J. 사이에 직접적으로알킬 이 맨이 상호교환되 는 경 로 (d i ole fi n mechanis m 또는 pa ir w i se mechani- sm) 이고, 둘째는 두개의 이중결합이 각각 별도로 끊어지고 아어서 각각의 알킬이벤들아 서로 교환되어 전달되는 경로 (non p a i rw i se me· chanis m 또는 meta l -carl:e n e mechanis m ) 이 다. 이 상의 두 메 카니 즘에 관한 실험적 뒷받침둘을 아태에 살펴본다. 1) 디 올레 핀 메 카니 즘 (d i ole fi n mechanis m ) 1967 년 Bradshaw 둥에 79) 의 해 서 처 음으로 더 울레 핀 (dio l efi n) 메 카 니즘이 제시되었다. 이 메카니즘은 식 (2.99) 에서 보여주는 바와 같
78) J. C. Mo!, J. A. Mouli gn , and C. Boelhauwer, Chem. Commun. , 633 (1968). 79) C. P. Bradshaw, E. J. Howman, and L. Turner, J. Cata l . , 7, 269 (1967).
이 시RR 클'--C로CHH부M==탄 CC-HH금— — 속RR ' =착 물 형RR 'C의C|H H M—중 一 간C |C H체H RR ' _형R 성R ' -과-CCI정I ―-- H을H M 포 一함한|CC다 HH•RR( 2 ' .99) 이 어 서 Pet it 둥은 80) 중간체 는 시 클로부탄의 성 질을 갖는 것 이 아 니 고 식 (2.100) 에 서 보여 주는 바와 같이 테 트라카르벤(t e tr acarbene) ―-금속 착물로 추축된다고 하였다. 分子軌道函數물 고려하면 이 메
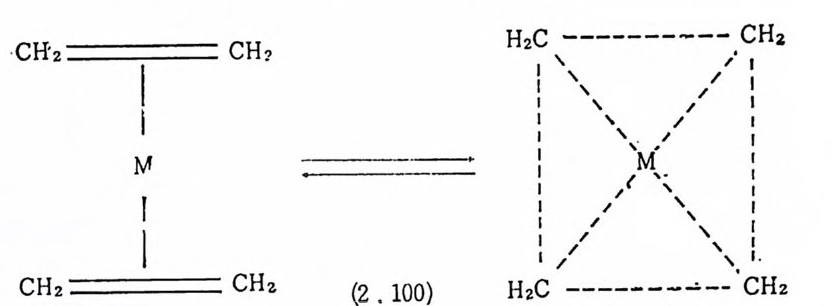 c H2 |IMc H ? H2CI .' -------~--.C/ H, :i
c H2 |IMc H ? H2CI .' -------~--.C/ H, :i
카니즘(식 (2.100) )은 반응이 일어날 수 있는 분자궤도함수적 대칭을 갖고 있다. 그러나 현재까지는아무런뚜렷한실험적 중거를얻지 못 했다. 따라서 다음과 같은 메 카니 즘도 제 시 된 바 있 다(석 (2.101)). Bl)
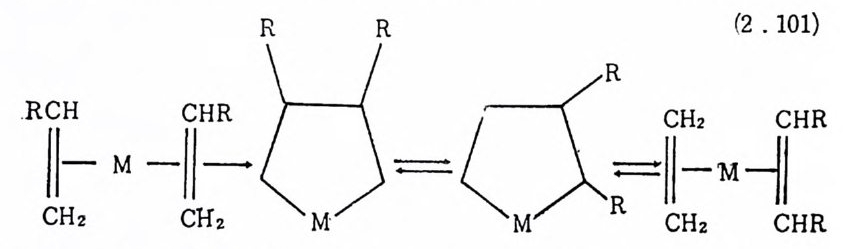 RE M _〔R \R二 〈三」:(2 :. 101)
RE M _〔R \R二 〈三」:(2 :. 101)
· 금속―디 올레 핀 착물이 금속시 클로펜탄 (me t alloc y clo pen t ane) 으로 되 고 後者가 前者로 되는 반응들이 찰 알려져 있기 때문에 식 (2.10 1) 의 첫 단계 는 무리 가 없는 것 같다. 금속고리 (me t alloc y cle) 화합물의 자리바꿈반응의 증거로 육영화텅스덴과 1,4- 디리티오부단의 반응을 들 수 있 다. 중수소로 치 환된 LiC H2CHDCHDCH2Li 와 WC16 는 반
80) F. S. Lewandosl and R. Peti t, Tetr a hedron Lett . , 780 (1'571). 81) C. G. Bief i eld , H. A. Eic k and R. HI. Grubbs, Inorg. Chem. , 12, 2166 (1'573 ).
응하여 같은 몰수의 시스 CHD=CHD 및 CH 2 =CH 2 를 생성한 다(식 (1. 102>). 82 } .L/i + WCl6 一 시 스 CHD=CHD (16%) CH2 =CH2 (l6%) Li CH2 =CHD(68%) (2 . 102 ) 윗 석 (2.102) 에 서 보는 바와 같이 meso-1, 4 - 디 리 티 오부탄을 반 응시키면 오직 시스― 1,2-d2- 에틸렌이 생성되지만, d,l - 1, 4- 디리티 오부탄을 반응시키면 오직 트란스 -1,2 - d 2 - 에틸렌이 생성된다 .83) 만 일 일차적으로 생성된 1,2-d2- 에탈렌아 또다시 금속과 반응하여 이 차적 으로 dr 에 틸 렌을 생 성 한다면 시 스 -l, 2 - d2 _ 에 탈 렌과 트란스 -1, 2 -에틸렌이 사용된 d,l- 이성질체의 비율로 생성될 것이다(그러나 실 제로는 오직 트란스 -1,2-d2- 에틸렌이 생성되었다). 이러한 모든 실 험적 결과는 석 (2.102) 의 반응메카니즘을 지지하여 준다. 그러나 이 상의 디올레핀 메카니즘이 유일하게 모든 실험적 결과를 설명하여 주는 것은 아니다. 2) 금속―카르벤 메 카니 즘 (me t al-carbene mechanis m ) 위에서 기술한 것처럽 울레핀 상호교환반응에 관한 정립된 반응 · 메카니즘은 아직 없다. 그러나 지난 10 여년 동안 쌓여전 많은 실 험적 증거는 금속―카르벤 메카니즘을 지지해 주고 있다. 몰리브덴一또는 텅스덴―카르벤 착물은 할로젠화 알킬알루미늄과 · 반응하여 울레펀 상호교환반응에 촉매적 역할을 하는 촉매계를 형 성함이 발표되었다 .84) 실제 올레핀 상호교환반응은 아니지만, 크롬 ―카르벤 착물과 비널에데르의 반응에서 알파-메목시스티렌이 생
82) a) J. Chatt , R. J. Hain e s, and G. J. Leig h , Chem. Commun. , 1203 (19 72). b) A. R. Fraser, J. Am. Chem. Soc. , 95, 597 (1973). c) L. Porri, Tetr a he- dron Leit . , 11, 879 (1974). 8834))° RW. .H R. . GKrruobllli s a anndd GT. . KDo. y Ble r, unCchke,m J. . CAomm.m uCnh.e m83. 9 S(o1c9. 7 , 19 )4. , 2538 (1972).
성 되 는 반응(식 (2. 103 )85 ) ) 도 금속―카르벤 메 카니 즘에 의 한 울레 핀 의 상호교환반응의 재시에 도움이 되었다. 이 반응에서 카르벤착물 이 비닐에데르의 아중결합을 끊는 것은 틀림없는 사실이다. 텅스텐
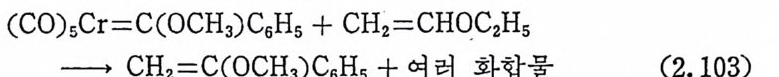 (C0)5Cr=C(OCH3)C 晶 + CH2=CHOC 晶
(C0)5Cr=C(OCH3)C 晶 + CH2=CHOC 晶
-카르벤착물과 알켄의 반응에서는 비슷한 결과를 얻었다(식 (2.104) 참조 86 )) . 이 상의 두 · 반응(식 (2.103) 및 (2.104) ) 을 응용하여 안정 한 금 속―카르벤 착물을 형성할 수 있는 올레펀들을 사용함으로써 금속
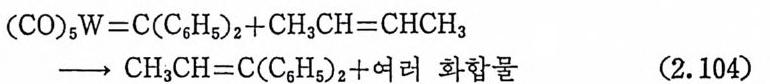 (C0)5W =C(Cs 麟 + CH3CH=CHCH3
(C0)5W =C(Cs 麟 + CH3CH=CHCH3
-카르벤 메카니즘을 제시할 만한 증거를 얻었다 .86) 즉 석 (2.105) 에서 보여주는 바와 같이 알켄의 이중결합이 끊어지는 과정은 4- 원
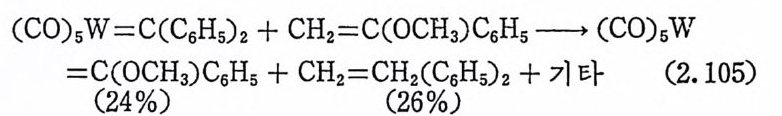 (C0)5W=C(C 晶 )2 + CH2=C(OCH3)C5Hs _ ➔ (C0)5W
(C0)5W=C(C 晶 )2 + CH2=C(OCH3)C5Hs _ ➔ (C0)5W
자고리 화합물울 중간체 로 하는 식 (2. 106) 과 같은 메 카니 즘으로 설 명되었(C다0) .58+6W> =WC iRl k.2 i= n s o(nC 0촉)5매W를I — 사CI R용2 한.= 상( C호0교)5환WII 반 +응 에CII서 R2 실(2.제 1로06 ) 금 R2'C=CH2 R2'C-CH2 R/C CH2
속―카 르벤 중간체 가 분리 확인된 적 도 있 다(식 (2.107)87 )). 울레 핀 상호교환반응이 카르벤메카니즘으로 진행되리라고 믿어지는 또하나 의 실험적 결과를 들어보면 다음과 같다. 즉, 트란스 - 2- 부덴과 드 란스 -4 - 욱텐의 촌재하에서 일어나는 시클로옥텐의 상호교환반응의 초기 단계 에 서 상당량의 CH3CH=CH(CH2)6CH=C3H7(b) 가 생 성 된 다는 사실이다(석 (2.lQ 8 )BB l ). 이상의 실험적 결과는 석 (2.106) 에서
85) E. o. Fis c her and K. H. Dotz , Clzem. Ber. , 105, 3966 (1'5 /2) . 86) C. P. Casey and T. J. Burkhardt, ]. Am. Chem. Soc. , 96, 780!:! (19 74 ). 87) D.J. Cardin , M.J. Doy le and M.F. Lap pe rt, ]. :Jh em. Soc. Chem. Com· -88 m) uT11.. J,. 9K27a t(z 1 '5a1n2d ) . J. McGi nn is , }. Am. Chem. Soc. , 97, 1592 (1'515 ).
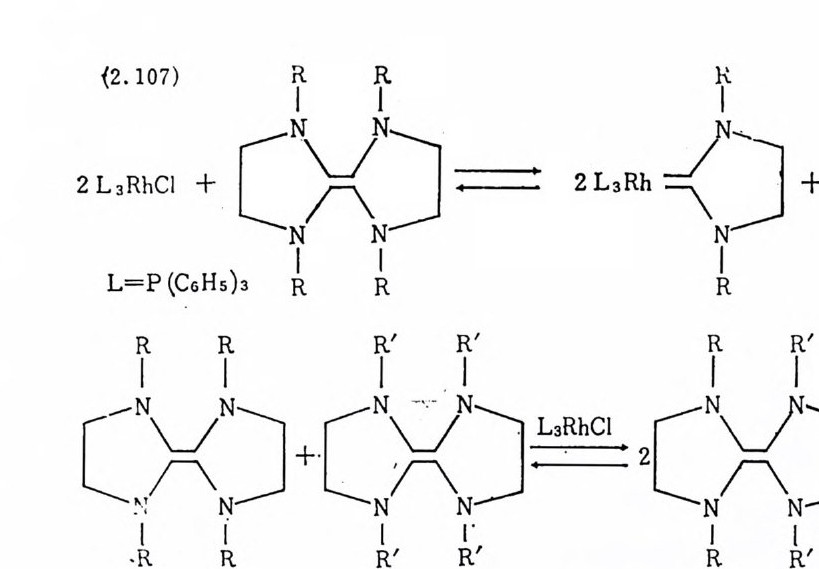 2L{2,. R 1 h0C7I ) + c:NNRI x NNRI: J —ZL,Rh =
2L{2,. R 1 h0C7I ) + c:NNRI x NNRI: J —ZL,Rh =
보여준 바와 같은 카르벤메카니즘으로 가장 찰 설명된다. 또한 고 리울레핀의 고리가 열리면서 일어나는 중합반응도 카르벤메카니즘 · 으0로 찰 설명된+ 다(C식H3 H(2C .=10C9H))C.H593> + GH7CH=CHC3H7 一 c ::::: + c:::3HH37 + 二二 CCHHCC: 89) E. Wasserman, D, A. Ben-Efr ai n and R. Wolovsky, J. Am. Chem. Soc ... 90, 3286 (19 68).
•• ---· 리 • - _-` C M -_- ~ -c M -I- c` c (2.109) c\ -c 금속카르벤은 올레핀의 상호교환반응에서만 논의되어 온것은 아 니 다. 최초의 반응물은 카르벤리 간드물 포함하지 않는 촉매 계 도 반 응과정에 금속-카르벤울 형성한다고 제시되어 왔다. 다음과 같은 예를 들 수 있다. 죽 메틸금속과 D2 가 반응하여 한개 이상의 중수 소를 갖는 메탄이 형성되는 사실을 설명하기 위하여 히드리도G 카르 ~ 벤)금속 착물이 중간체 로서 제 시 된 바 있 다(식 (2.110)). 90) 에 탈금 -
![]() CH3-M ~ CH=M-H (2.1 10)
CH3-M ~ CH=M-H (2.1 10)
속의 반응에서도 비슷한 중간체에 관한 실험적 중거가 보고되었 다 •91) 죽 에탈텅스덴은 베타―수소전달반응을 일으켜 에탈렌과 히 드리도금속 착물을 빠른 속도로 생성하지만 이와 병행해써 비교적 느란 속도로 알파―수소전달반옹을 일으켜 활성이 높은 히드리도 . (카르벤)금속 착물을 생 성 한다고 보고되 었 다(석 (2.111)). m
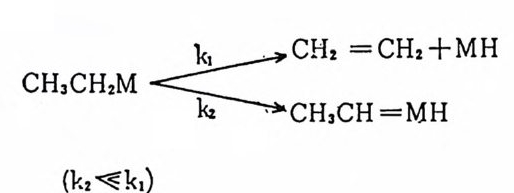 CH,CH2M -C:::::::드二 CH2 =CH2+MH
CH,CH2M -C:::::::드二 CH2 =CH2+MH
90) L. S. Pu ana /\., Yamamoto , ]. Chem. Soc. , Chem. Commu .n. , 9 (1974). 91 ) N. I. Ce ,e,i,e r and M.L.H. Green-, ] . Chem. Soc., Chem. Commun., 761 (Ut74 ).
*참고 문현 1) M. Herberhold, Meta l 11:~ Comp le xes, Elsevie r , Vol. I, Comp le xes wit h Di -a nd Oli go -Olefi nic Lig a nds, 1966 ; Comp le xes wit h Mono-olefi nic Lig a nds, 1974. 2) A. J. Bir c h and I. D. Jen kin s , Transit ion Meta l Comp le xes of Olefi ni c Comp o unds, in H. Alpe r, Ed. , Transit ion Meta l Orga - nometa l lic s in Org a nic Sy n th e sis , Vol. 1, Academi c Press, 1976, pp.2 ~75. 3) W. Keim , The 11:- Allyl Sy s te m in Cata l ys is , in G. N. Schra1,1 - zer, Ed. , Transit ion Meta l s in Homog e neous Cata l ys i s , Marcel Dekker, 1971, p. 59 4) M. Rosenblum, Accounts Chem. Res. , 7, 122 (19 74) . 5) F. J. McQ u il lin, Homog e neous Hy d rog e nati on in Orga nic Che- '6) mYi s. t r Oy ,h taD n . i, RMeid. e lF, uj1i 9m7o6 .t o and A. Yamagi sh i, Bull. Chem. Soc. Jap a n, 50, 1453 (19 77) , 51, 2562 (1978) 52, 3747 (19 79) . 1) G. Lefe b vre and Y. Chauvin , Dim eriz a ti on and Co-dim eriz a ti on of Olefi ni c Comp o unds , in: R. Ug o, Ed. , Asp ec ts of Homog e neous Cata l ys i s , Carlo Manfr ed i, Edit or e, Mi lan o 1970. Vol. I. 8) R. L. Banks, Cata l yt ic Olefi n Di sp r o p or tio n ati on , Top ics in Current Chemi st r y, 25, 39 (19 72) . 9) G. Henric i-O l ive and S. Oli ve Ol igo meriz a ti on of Et h y le ne wi th Soluble Transit ion Meta l Cata l ys t, Adv. in Polym . Sc i. , 15, 1 (19 74). 10) R. Cramer, Transit ion Meta l Cata l ys is Examp lified by Some Rhodiu m -Promote d Reacti on s of Olefi ns , Accounts chem. Res. , 1, 186 (1969) .
제 3 장 一酸化炭素를 包含하는 反應들 전이금속착물 촉매에 의한 군일촉매반응에서 일산화탄소를 포함 하는 반응들은 매우 중요한 반응들이다. 이들 중에서 히드로포르밀 화반응은 1940 년대부터 이미 공업적으로 중요하게 이용되어 왔다. 일산화탄소는 특히 그 자원이 풍부하므로 앞으로도 계속 그 이용도 가 높아질 것으로 예상된다. 현재는 자연가스와 나프타가 일산화탄 소(와 수소)의 주된 資源이지만 앞으로는 석탄이나 重油로부터 얻 어질 것으로 기대된다. 향후 약 20 여 년간은 석탄으로부터 얻어지 는 일산화탄소와 수소가 많은 화학물질의 주원료가 될 것으로 전망 되고있다. 생산가격이나원료확보둥의 문제를고려한다면, 현재 에틸렌으로부터 얻어지는 많은 화학물질은 앞으로는 일산화탄소와 수소의 반응으로부터 얻어질 것으로 추측된다. 1. 一酸化炭素의 配位 일산화탄소는 낮은 산화상태의 금속착물을 안정화시켜주는 데 매 우 효과적인 리간드이다. 실제로 많은 전이금속―카르보닐 착물에 서 전이 금속의 산화상태 는 0 이 다. 3d- 전이 금속(fi rs t -row tran sit ion me t al) 의 착물들 Cr(CO) 。 Fe(C0)5, Ni (C 0)4 등을 예 로서 둘 수 있는데 이러한 착물들은 일반적으로 18- 전자규칙에 찰 적용된다. 금속이 홀수의 전자를 갖게 되 면 Mnz (C 0)10 또는 Co2(CO)e 등 二
核의 안정한 화합물을 형성한다. 4d - 와 5d 켜 1 이금속 (second and thi r d row tra nsit ion me t al) 은 금속―금속결합을 갖는 뭉치화합물 (clus t er) 을 형 성 하는 경 향이 있 다. 대 부분의 전이 금속이 co 리 간드 롤 배위하는 안정화된 뭉치화합물을 형성하지만 특히 Vlll 族 금속은 더 욱 그러 하다. 금속―카르보닐 뭉치 화합물들은 득히 촉매 작용에 많 은 참재적인 가능성을 보여준다. 왜냐하면 이들 뭉치화합물은 군일 촉매작용에 주로 아용되는 단핵-카르보닐화합물의 특성과 불군일촉 매작용에 주로 사용되는 금속표면의 목성을 복합적으로 보여주기 때문이다 .I) CO 를 포함하는 촉매 반응들이 꽁업 적 으로 중요하기 때 문에 금속_ 카르보닐화합물에 관한 연구가 더욱 활발해졌다고도 볼 수 있다. CO 는 유기화합물제조에 널리 쓰여지고 있지만, co 자체의 반응성 온 그리 높지 않다. 실제로 매우 강한 찬전자체 (elec t ro ph il e) 나 매우 강한 천핵체 (nucleo p h il e) 만이 CO 를 공격한다. 그러나 촉매를 사용 함으로써 올레편, 알코올 및 수소와 co 의 반응은 비교적 쉽게 일 어난다. 이러한 반응에 쓰여지는 촉매는 주로 낮은 산화상태의 맨 族금속의 착물들이 다. 목히 코발트와 로듐착물들이 공업 적 으로 중 · 요하게 사용되고있다. 여기서 금속과 CO 간의 결합, 그리고 금속에 배위된 co 의 상 먼질처 및 c반o 응중의성 을산 살소펴와본 다탄.소 금사이속의과 결co합 간을의 이 결해합해을야 할논 의것하이기다 . 전c에o 중의 산소와 탄소사이의 결합은 원자가결합이론 (Valence Bond The- o ry)이나 또는 분자퀘도함수이론 (Molecular Orbit al Theor y)으로 잘 설 명된다. 前者를 利用하여 비교적 간단한 원자궤도함수의 도시로써 살펴보자. 그림 3.1 과 같이 탄소와 산소사이에는 하나의 시그마결 합이 있다. 이 시그마결합은 채워진 산소의 p구i]도 함수와 빈 탄소 의 s p레1 도함수의 중첩으로 이루어전다. 그리고 탄소와산소 사이에 는 두개의 파이결합도 존재한다. 이 두 개의 파이결합은 탄소와 산 소가 갖는 전자가 하나씩 채워진 각각 두 쌍의 p구}도함수들 사이 에 일어나는 중첩에 의해서 이루어진다(그립 3.1 참조). 그림 3.1 에
1) E. L. Muett er tie s , Sc ien ce, 196, 839(1977).
서 산소의 반대 편에 있는 탄소의 S p - 궤 도함수는 두 개 의 전지를 7 가 지고 있으며 이 한 쌍의 전자는 co 가 금속에 배위할 때 co 가 내 어놓는 전자쌍이 된다. 산소는 2s 예]도함수에 한 쌍의 전자를 갖고 있다. 비교적 자세한 분자궤도 함수법으로 co 의 결합을 표현한다 떤 다음과 같다. 그림 3.2 에서 보는 바와 같이 두 개의 시그마결합
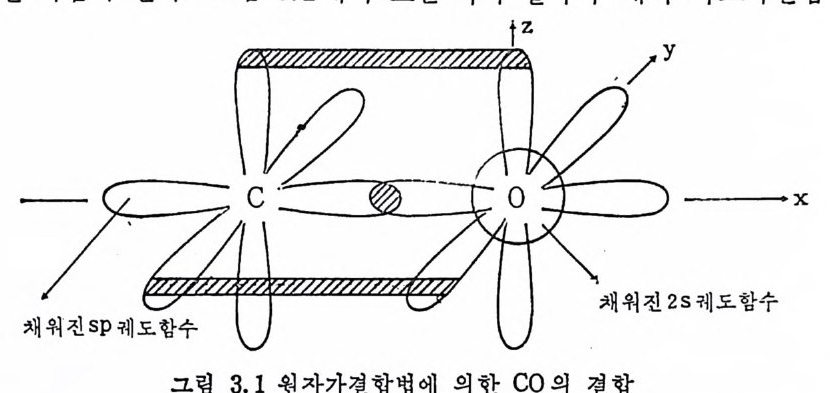 tz
tz
분자궤 도함수(fJ :bond i n g molecular orbit al ) , 어 및 c2 와 두 개 의 파아 결합분자궤 도함수 (1e-bond i n g molecular orbit al ). tr11 그리 고 한 개 의 사 그마반결합분자퀘도함수(fJ ·an ti bond i ng molecular orbit al ), 야는 채워 지고, 파이 반결합분자궤도함수 (1e-an ti bond i ng molecular orbit al) , tr~ 및 시 그마반결 합분자퀘 도함수(fJ ·an ti bond i n g molecular orbit al) , <1, 는
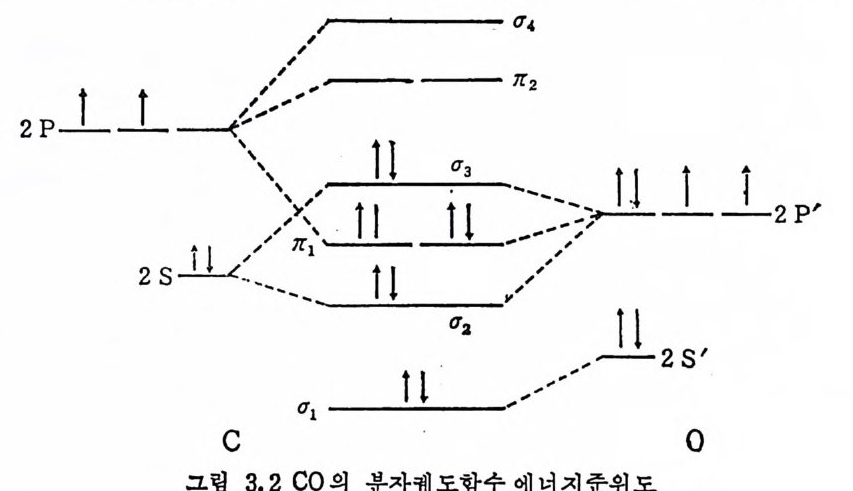 , , - 17,
, , - 17,
비어 있다. 분자궤도함 수의 자세한 계산 결과 산소의 2s 전자들은 주 로 산소에 편재되어 있다. 따라서 그림 3.2 에서 보여 주는 바와 같 이 산소의 2s 궤 도함수와 2p 궤 도함수 사이 에 는 혼성 화 (h y br i d i za ti on) 가 없는 것으로 표현된다. 다음으로 일산화탄소와 금속 간의 결합을 살펴본다. 대부분의 전 이금속은 안정한 금속-카르보닐 착물을 형성하지만, 主族금속 ( ma i n gro up me t al) -카르보닐 화합물은 이제까지 하나도 보고되지 않았다. 그逆 提이供유 ( 는bac k아 d래on와a t i o같n)이 받 설는명 성된 질다.이 크CO기 는 때 과 문이에_ 전금자속받과게 c로o서 사 이전 자에 를는 시그마결합분 아니라 강한 파이결합이 있게 된다. 전이금속과 CO 사이의 파이결합은 채워진 금속의 d- 궤도함수와 빈 co 의 궤도함 수의 겹침에 의해서 일어난다. 그러나 主族금속원소의 d - 궤도함수 는 원자핵 쪽으로 강하게 끌려져 있기 때문에 (즉 원자가껍질, valence shell 이 아니 고 내 부껍 질 , inn er shell 이 다) 주족금속 원 자는 쉽게 d- 전자를 내어 줄 수가 없고, 따라서 CO 와 효과적인 파 이결합을 하지 못한다. 금속과 co 사이의 파이결합에 참여하는 CO 의 궤 도함수는, 分子軌道函數法 (molecular orbit al t heor y)에 의 하면 빈 反結合軌道函數 (an ti bond i n g orb it al) 카 된다(그림 3. 3 참조). 한편 原子價結合法 (valence bond t heor y)에 의 하면 탄소의 2P - 궤 도함수중 의1 \하나그가M1림 금3\.속3 .+과• 분 \자/co궤•. c사도 함아 三 수의 법\o/ 에:파 이 의_결한합_ 금에一 \속广 과참 여cM하o 尸` 는간의 것 :과 으c이 로루결 합설 명된어/)다 \ (그립 1.2 참조). 원자가결합이론에 의한 금속 -CO 간의 결합은 제 1 장 3 철에서 자 제히 고찰되었다. 즉 금속 -CO 간에 오직 시그마배위결합만 촌재할 경우에는 M--c 三。+으로 표현되고, 금속 -CO 간에 과이결합이 매
우 유효하게 존재할 경우에는 M=C=O 으로 표현될 수 있다. 이렇 게 co 가 금속에 배위됨으로써 co 중의 탄소와 산소 간의 걷합력 이 약화되는 것은 분자궈]도함수법에 의해서도 쉽게 설명된다. 즉 그림 3. 3 에 서 보면 금속의 d 예] 도함수 전자를 받아들여 금속 -co 간에 파이결합을 할 수 있는 co 의 분자궤도함수는 반결합궤도함수이므 로 금속 -co 간의 파이 결합이 강해질수록 co 중의 탄소와 산소 사 이의 결합차수는 낮아진다. 이상과 같이 금속과 co 사이의 결합은 co 분자의 반응성을 변화 시킨다. 예를 들면 [Mn(C0)6]+ 와 같은 양이온성 금속一카르보닐 착물의 co 리간드는 아민 (am i nes), 알콕시드 (alkox i des) 및 카르보 음 이 온 (carban i ons) 둥과 같은 의 부로부터 공격 해 오는(같은 금속에 배 위되지 않은) 찬핵체와 비교적 쉽게 반응한다. 그러나 무엇보다도 금속에 배위된 CO 의 반응성은 같은 금속착물내의(죽 같은 금속에 배위된) 다론 리간드와의 반응에서 그 응용성을 보여준다. 예를 들 떤 배위된 알킬기와 금속 간의 결합에 삽입 반응(i nser ti on reac ti on)( 또 는 알킬기의 이동반응 (alk y l m ig ra ti on ) 이라고도 함)은 CO 를 기본 물질로 하는 많은 유기화합물 합성과정의 가장 중요한 단계이다. 2. 히 드로포르밀화반응 (h y dro f orm y la ti on) CO 를 포함하는반응중에서 가장 오래되고가장 대규모로 응용되 는 군일촉매반응은 히드로포르밀화반응이다. 죽 CO 와 올레팬 그리 고 H2 를 반응시켜 알데히드를 만드는 히드로포르밀화반응이다. 가 장 잘 알려진 공업적 응용을 든다면 CO 와 푸로필렌 그리고 H2 를 사용하여 부틸알데히드를 얻는 방법이다(식 (3.1)).
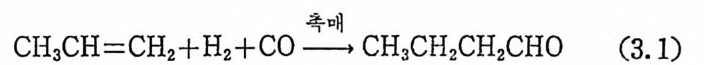 CI-I3 CH=CH2+H2+CO 一촉매 CH3CH2CH2CHO (3.1 )
CI-I3 CH=CH2+H2+CO 一촉매 CH3CH2CH2CHO (3.1 )
(1) 反應조건 및 觸媒 오늘날 공업에서 응용되고 있는 대부분의 히드로포르밀화반응은 100~l80°C, 100~300 기 압, CO 와 H2 의 혼합비 울 1 : 1 의 조건
에서 코발트화합물을 촉매로 사용하고 있 다. 많은 경 우에 반웅물 및 반응생 성 물이 반응의 용매 역 할을 한다. 코발트화합물을 촉매 로 사용하였을 경 우에 실제 촉매 (actu a l ca t al y s t)는 히 드로카르보닐코발 트착물임이 밝혀졌다 .2) 그리고 어떤 종류의 코발트촉매를 사용하 더라도 상기 반웅조건에서는 상기 실제촉매가 형성된다는 사실도 밝혀 졌 다. 죽 코발트 이 온은 수소에 의 해서 Co(O) 으로 환원되 고 다시 CO 와 반응하여 Co2(CO)8 으로 된다(식 (3. 2) 참조). 이 반응 은 발열 반응 (460 k J /Co z( C0)8) 이 며 , 상기 반응조건에 서 는 어 떤 종 류의 코발트(금속 코발트 또는 코발트 영)도 Co2(CO)a 을 형성한 다. Co2(CO)a 논 수소와
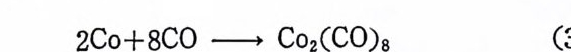 2Co+8CO 一 Co2(C0)8 (3. 2)
2Co+8CO 一 Co2(C0)8 (3. 2)
반응하여 실제 촉매 인 히 드리 도테 트라카르보닐코발트, HCo(C0)4 로 된다(식 (3. 3) 참조).
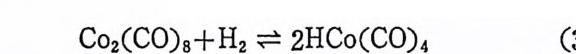 Coz( C O)a+H2 :;= 2HCo(C0)4 (3. 3)
Coz( C O)a+H2 :;= 2HCo(C0)4 (3. 3)
HCo(C0)4 는 상온에서 기체이며, 매우 독성이 강하다. 서서히 석 히면 -26°C 에서 엷은 노란색 고체가 얻어진다. 이 착물은 탄화수 소에 찰 녹으며 물에는 약간 녹는다. 용액 중에서 HCo(C0)4 분자가 안정하게 유지되려면 최소한의 co 압력이 필요하다. 예를 들면 120°c 에서는 10 기압 정도, 그리고 200°c 에서는 100 기압 정도의 co 압력이 필요하다 .3) 그 이하의 co 압력하에서는 금속상태의 코발 트가 침전하며 분해된다 .3) 촉매 중의 co 리 간드를 삼차포스핀(t er ti ar y pho sp h in e ), 삼차아르신 (ter ti ar y arsin e ) 및 삼차포스피 트(t er ti ar y p hos p h it e) 로 치 환시 키 면 , 새로 생성되는 코발트착물도 역시 히드로포르밀화반응에 촉매적 활 성 을 보여 준다. 4) 고온에 서 CO 와 H2 의 압력 하에 서 Co2(CO)8 을
2) W. Rep pe , Ann. Chem, 582, 1, 38, 72, 87, 116, 133 (19 53). 3) J. Falbe, Carbon Monoxid e i1t Orga nic Sy nt h e sis , Sp ri n g e r-Verlag, , New 4) YLo.r Hk,. S1l9a7u0g. h and R. D. Mull ine aux, ]. Orga nometa l . Chem. , 13, 469 (1968).
P (n-C4H9)3 과 반응시키면 Co z( C0)6(P(n-C4H9)3)2 이 얻어진다 .4) Co2(C0)5(P(n-C4H9)3)2 는 히드로포르밀화반응에 촉매져 활성을 보여준다. 이 화합물을 사용한 히드로포르밀화반응에서는 히드리도 코발트착물이 확인되지 않았다. 그러나 위에서 실제 촉매로 소개된 HCo(C0)4 와 비숫한 착물 HCo(CO) i P(n 一 C4H9)3) 이 실제 촉매종 일 것이라고 추측되고 있다. HCo(C0)4 및 HCo(C0)3(P(n-C4H9)3) 에 의 한 히 드로포르밀화반 응을 비교하여 보면 다음과 같다. 포스핀에 의해서 co 가 치환되면 코발트착물은 더 욱 안정 하게 된다(제 1 장 3 참조). 그 이 유는 포스핀 이 co 보다 약한 파이전자받게이기 때문이다. 즉 co 대신에 포스 핀이 배위됨으로써 금속의 전자밀도는 높아지게 되고 금속으로부터 배위된 CO 로 逆提供 (back-dona ti on) 될 전자가 많아지게 되기 때문이 다. 따라서 HCo ( CO) JC P(n-C4H9)3) 에 서 Co->CO 결합은 HCo(CO). 에서의 그것보다 강하다. 실제로 150~200°c 에서 HCo(C0)3(P(n ― C4H9)3) 의 분해를 막기 위해서 필요한 co 의 압력은 10~20 기압 정도면 충분하다. 그러나 HCo(C0)3(P(n 一 C4Hs 〉 3) 이 열적으로. 안정 하기 때문에 그만큼 HCo(C0)4 보다 반응성이 낮다. 왜냐하면 히드 로포르밀화반응의 촉매 순환과정 은 HCo(C0)4 또는 HCo(C0)3(P(n -C 晶 )3) 으로부터 한개의 co 가 해리되는 단계를 거치기 때문이다 (제 2 장 2.(2) 참조). 실례를 돈다면, 145°C 에서 HCo(CO). 를 촉매 로 하여 얻은 히드로포르밀화반응의 속도는 180°C 에서 HCo(C0)3 (P(n-C4H9)3) 을 촉매로 하여 얻은 반응속도보다 다섯배 이상이나 빠르다. 이와같이 CO 를 포스핀으로 치환하면 반응속도는 느려지지 만 아태와 같은 편리한 접도 얻을 수 있다. HCo(CO)(P(n-C4H9)3) 촉매가 열적으로 안정하기 때문에 반응생성물로부터 촉매분리가 비 교적 용이하다. 반응생성물을 단순히 증류해서 간단하게 분리해내 고 촉매는 다시 반응기로 보내질 수 있다. 그러나 HCo(C0)4 를 촉 애로 사용하는 경우에는 화학적 방법을 사용하여 촉매를 분해시킨 다음 반응생성물을 분리할 수밖에 없다 .3) 이제까지 살펴본 코발트-카르보닐 착물 이외에도, 철, 니첼, 크 물 망간, 레늄 등에 의한 히드로포르밀화반응도 발표된 바 있
다 .3),5),6) 현재까지 발표된 히드로포르 밀화반응의 촉매적 역할을 하 는 전이금속착물 중에서 로듐착물이 가장 활성 이 높은 것으로 알려 그겼 것다. 보 로다듐도착 높물다의. ”촉 로매듐 적착 활물성의 도경는 우 에위 도 에 서리 간상드술가한 포코스발핀트으착로물 들치의 환 되면 상기한 코발트착물 촉매반응에서 보여준 것과 같은 결과를 얻 는다 .5) 포스핀 리간드를 이미 배위하고 있는 RhH(CO)(P(Cs H s)a):i 또는 RhCl(CO)(P(CsHs)a)z 를 촉매 로 사용하거 나, 또는 로듐-카르 보닐 착물에 포스판을 가함으로써 촉매 계 를 생 성 시 켜 히 드로포르밀 화반응을 일으킬 수 있 다. 6),8),9) 포스핀을 포함하는 로듐착물 。 촉매 계에 의한 히드로포르밀화반응은 비교적 낮은 온도 (80~150°C) 및 낮은 압력 (5~50 기압)에서 일어난다. 이러한 로듐 착물 촉매계의 득칭은 99% 이상의 올레핀을 알데히드로 바꾼다는 점이다. 즉 올 레핀의 수소화반응은 거의 일으키지 않는 점이다. 또한 올레핀의 이 중결합이 동반응 (double bond m ig ra ti on) 은 거 의 완전하게 여 제된다. 로듐-포스핀 착물 촉매 계 는 말단선형 올레 판 (ter mi na l lin e ar ole fi n) 의 히 드로포르밀화반응에 서 선형 알데 히 드(li near aldeh y de) 를 주로 생 산 하며, 내부올레핀(i nner ole fi n) 의 히드로포르밀화반응에서도 최초의 이중결합위치에 -CHO 기를 갖는 알데히드를 생성한다. 로듐-포 스핀 착물 촉매도 역시, 상기한 코발트-포스핀 착물 촉매와 같이, 열적으로 안정하여 반응 후에 촉매의 회수가 용이하다. 로듐착물 촉매를 사용하는 경우에 이상과 같은 장점이 있기 때문에 비록 로 듐착물이 高價인 화합물이타 하더라도 앞으로 계속해서 그 사용률 이 증가될 것으로 기대된다.
5) F. E. Pauli k, Recent Develop m ents in Hy d rofo rm y la ti on Cata ly s i s , • Cat- al. Rev. , 6, 49(1 9 72). 6) L. Marko, •Hy d rofo rm y la ti on of O!efi ns wi th Carbony l Deriv a ti ve s of Noble Meta ls as Cata l ys ts , • in: R. Ug o, Edit , , Aspe c ts of Homog e neous Cata l ys i s , D. Reid e l Pub). Comp , , 1974, vol. 2. 7) B. Heil and L. Marko, Chem. Ber. , 102, 2238 (19 69). 8) C, K. Brown and G. Wi lkin s on , J. Chem. Soc. , (A), 2753 (19 70). 9)E nag). , JC.hH e.m C. rPardoddo.c kR, esA. .D eHveelrosph ,m , an8,, 2F9.1E, 3. 72P a(1u9l i6 k9 ) .a nd J.F . Roth , Ind.
(2) 反庶메카니즘 히 드리 도코발트착물 HCo(C0)3L(L=CO, PR3) 에 의 한 히 드로포 르밀화반응은 아래 의 식 (3. 4)-(3. 11) 과 같이 전행 되 는 것 으로 알 려졌다. 이 메카니즘은 여러 연구의 결과를 종합한 것이다. 아래에서 각각의 연구결과를 소개하면서 전체반응의 메카니즘을 유도하고자 한다.
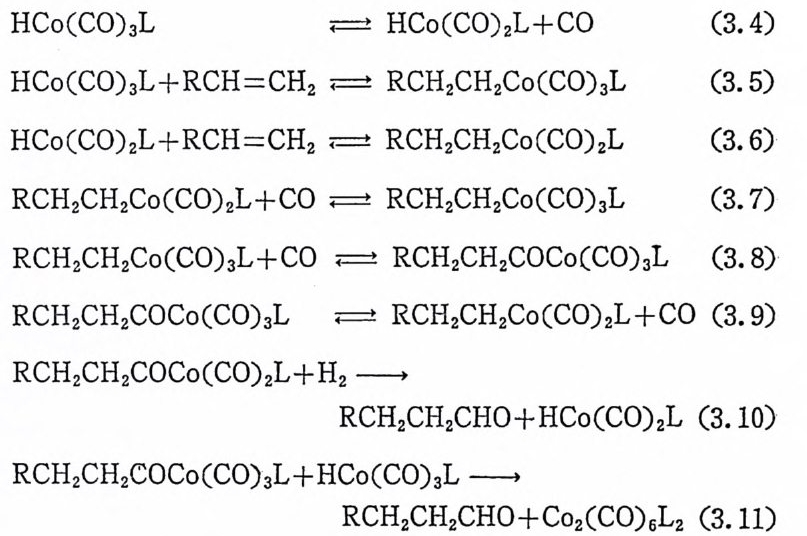 HCo(C0)3L ;==:! HCo(C0)2L+CO (3.4)
HCo(C0)3L ;==:! HCo(C0)2L+CO (3.4)
촉매로 쓰여지는 HCo(C0)3L 는 CO 와 H2 가 촌재하지 않아도 울 레 편만 가해 주면 알데 히 드를 생 성 시 킨다. 10) 죽 HCo(C0)3L 촉매 자 체가 H 와 CO 를 제공하여 알데히드를 생성시킨다(석 (3.12) 참조). 이 경우에는 주로 가지 달란 알데히드 (branched aldeh y de) 가 생성된 다.
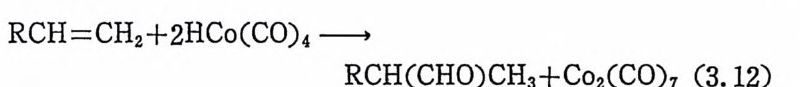 RCH=CH2+2HCo(C0)4 一
RCH=CH2+2HCo(C0)4 一
히드로포르밀화반응이 일어나는 고온이나 고압하에서도 히드리도 카르보닐코발트 착물이 존재한다는 실험적 결과는 고온 및 고압하
10) M. Orchin and W. Rup ilius , On the Mechanis m of the Oxo Reacti on , Cata t . Rev. , 6, 85 (lf/12 ).
에서 사용 할 수 있는 적의선스 펙 트럼 측정장치률 사용함으로써 가 능하였다 .w Co~ C 0)8 또는 Co2 ( C0) 8 +PR?] 를 촉매의 전구물질 ( p recursor) 로 사용하였 을 경 우에 고온, 고압하에 서 반응식 (3.13) 의 평형은 ~ 거의 모두 HCo ( C0)3L 쪽으로 전행된다는 사실도 밝혀졌 다. llb)
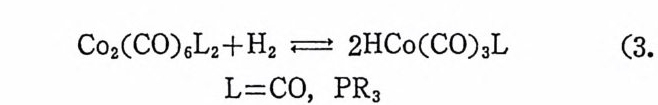 Co2(C0)5L2+H2 .===! 2HCo(C0)3L (3.13)
Co2(C0)5L2+H2 .===! 2HCo(C0)3L (3.13)
18 전자 착물 HCo(C0)3L 에서 co 가 해리되어 반응성이 높은 16 전자착물 HCo(C0)2L 가 생성된다는 사실은 적의선 스펙트럽데이타 로부터 얻지 못했다. 그러나 용액 중에서 측정된 반응속도측정 실험 결 과로부터 HCo(C0)4 에 관하여 해 리 적 메 카니 즘 (d i ssoc i a ti ve mech· an i sm) 이 제시되었다. 죽 식 (3.4) 가 제시되었다 .12) 실제로 18 전자 착물 HCo ( C0)3L 이 올레핀에 대하여 반응성이 있는지 없는지에 관 하여서도 아무런 실험적 증거는 없다. 또한 울레핀의 배위나 삽입 반응이 일어나기 위해서 16 전자 착물이 반드시 형성되어야 하는지 에 관해서도 실험적인 증거는 없다. 어느 경유돈 간에 4 배위 16 전 자 코발트착물의 농도는 매우 낮은 것으로 가정되어 왔다. Co2(CO)8 착물을 촉매로 사용할 경우에 히드로포르밀화반응의 전 체 반응속도 (overall reacti on ra t e) 는 co 의 쉘압력 에 역 비 례 하기 때 문에 반응식 (3.4) 에서 보여주는 바와같은 co ”의 해리단계가 제시되었다. 히 亡-쿠푸 근밀화반응의 속도는 식 (3.14) 와 같은 식으로 얻어졌다 .3) 이 식 (3.14) 는 근사적 인 실험식 이 다. 석 (3.14) 에 의 하면 H2 의 압력 과 co 의 압력 이 같을 경 우에 는 히 드로포르밀화반응의 속도는 전 체압력의 영향을 받지 않는다. 용액 중에 촉매를 안정하게 유지하기 위해서 일정한 co 의 압력이 필요하지만(제 3 장 책 (1)참조) CO 의 압력이 높으면 전체반응속도가늦어지게 된다. 이상의 실험적 결과는
11) a) D.E. Morris and H.B. Tin k er, Chem. Tech. 554(1 '5!4) . b) R. Why m an, J. Orga nometa l . Chem. , 66, C23Cl
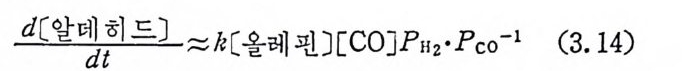 d 〔 알더》히드〕 국 [ 올레고蠶 CO j P tt 2•Pco-1 (3.14)
d 〔 알더》히드〕 국 [ 올레고蠶 CO j P tt 2•Pco-1 (3.14)
직 (3.4) 의 평형을 지지한다. 죽 co 의 압력이 높을 수록 반응성이 높을 것으로 생각되는 4 배위, 16 전자 착물의 농도는 낮아지게 될 것이다. 식 (3.5) 와 석 (3.6) 은 5 배위 18 전자 착물과 4 배위 16 전자 착물 중의 Co — H 결합에 올레핀이 각각 삽입되는 과정들이다. 식 (3.5) 및 (3. 6) 은 단순히 한 단계 의 반응이 아니 고, 두 단계 를 포함하는 과정이다. 죽 일반적으로 알려진 바에 의하면 울레핀은 Co-H 에 삽입되기 전에 먼저 Co 에 배위되어야 한다. 실제로 5 배위 착물에 올레핀의 삽입반응이 일어남울 보여주는 실험적 증거는 얻지 못했 다. 다만 석 (3.6) 에서 생성되는 4 배위 착물은 식 (3.7) 에 의해서 더욱 안정한 5 배위 착물이 될 것으로 생각된다. 식 (3.5) 및 (3.6) 의 반응생성물인 알킬코발트 RCH2CH2Co(C0)3L 및 RCH2CH2Co(C0)2L 도 실험적으로 분리, 확인하지는 못했다. 그 러나 이리듐착물을 이용하는 히드로포르밀화반응에서 알킬-금속 착 물이 명백히 확인되었다 .llb) 따라서 이리듐착물보다는 비교적 불 안정하며 활성이 클 것으로 기대되는 코발트(또는 로듐) 착물의 경 우에 생성되는 알킬-코발트(또는 로듐)착물은 매우 짧은 시간동안 촌재 (short l i ved) 할 것으로 추측된다. 다음 단계는 한 개의 co 리간드가 금속-알킬결합에 삽입되어 아실 코발트 (ac y lcobal t) 착물을 형성하는 단계이다(식 (3.7)). 코발트착물 이 CO 와 반응하여 삽입반응생성물 아실코발트 착물을 생성시키는 예는 13co 를 이용한 실험에 의해서 찰 연구되어졌다. 죽 비교적 안 정 한 코발트착물 CsHsCH2Co(C0)3(P(CsHs)3) 는 용액 중에 서 13co 와 반응하여 아실코발트 착물 C6H5CH2COCo(C0)2(1 3 CO)(P(C6H5)3) 를 생성한다 .13) 히드로포르밀화반응이 일어나는 실험조건에서 실제 로 아신코발트 착물이 적의선 스펙트럼에 의해서 확인되었다 .llb) HCo(C0)4 를 촉매 로 사용할 경 우에 말단 올레 핀의 히 드로포르밀화 13) K. Nag y-M ago s, G. Bor and L. Marko, J. Orga 11omet. Chem. , 14, 20.-i (19 68).
반응은 대단히 빠르게 진행된다. 이 경우에 대부분의 코발트는 야 실코발트 착물로 촌재하며, 아실코발트의 생성단계는 빠르고 그 다 음 단계는 느린 단계로 알려졌다. 내부 울 레핀과 HCo(C0)4 를 사용 하였을 경우와, 말단 올레포J. 또는 내부 올레핀과 HCo(C0)3(PR3) 를 사용하였을 경우에는 아실코발트 착물의 촌재가 관찰되지 않았다. 주로 히드리도코발트 착물만이 촌재하는 것으로 알려졌다. 이러~ 경 우에 는 히 드로포르밀화반응의 전체 반응속도 (overall reacti on rate ) 가 느리다. 적의선 스펙트럼연구에 의하면 올레핀이 삽입되는 단계 (석 (3. 5) 및 (3. 6) )가 속도 결정 단계 (rate dete r mi ni n g s t e p)이 된다. 촉매가 HCo(C0)4 이고 올레핀이 말단 올레핀이면 올레핀 삽입단계 (석 (3.5) 및 (3.6) )가 비교적 용이하게 진행되리라는 것은 촉매와 울 레핀의 입체적 성질로 보아서도 쉽게 이해된다. 알데히드를 생성시키기 위해서는 아실코발트 착물은 수소와 반응 해야 한다. 석 (3.10) 은 수소의 산화성첨가반응 (ox i da ti ve add iti on) 이 다. 5 배 위 착물 아실코발트 (RCH2CH2COCo(C0)3L) 는 두 개 의 빈 배위자리가요구되는 산화성첨가반응을 쉽게 일으키지 못할 것이다. 따라서 석 (3.9) 에 의해서 4 배위 착물이 형성되어야 한다. 반응식 (3. 9) 에 의 하면 co 의 압력 이 높을 수록 히 드로포르밀화반응의 전 . 체반응속도가 느려질 것이다. 이 효과는 위에서 기술한 반응식 (3.4) 에 의한 속도석 (3.14) 의 설명에 추가되어야 할 것이다. 식 (3.10) 은 · 단순한 가수소분해반응 (h y drog enol y s i s) 으로 표현되어 있지만 실제로 . 는 H2 의 산화성 첨 가반응과 환원성 제 거 반응 (reduc ti ve e li m i na ti on) 에 의하여 알데히드가 생성되는 반응의 복합적안 단계다. 여기서 생성 된 HCo(C0)2L 은 식 (3. 4) 의 평 형 에 의 해서 HCo(C0)3L 이 될 것 이다. 마지막으로 식 (3.11) 에 의해서 히드리도코발트착물 (HCo(C0)3L) 과 아실코발트 착물 (RCH2CH2COCo(C0)3L) 이 반응하여 안데히드 를 생성하는 과정을 살펴본다. H2 오} co 가 촌재하지 않는 경우에 착물 HCo(C0)4 는 올레판과 반응하여 알데히드를 생성하는 실험적 결과(식 (3.12) )를 고려한다면, 식 (3.11) 의 제시가 불가피하다. 죽 한 분자의 올레,,tJ.이 히드로포르밀화반응에서 한 분자의 알데히드가 ·
되기 위해서는두개의 H( 그리고 한 분자의 CO) 가 필요하다. 따라서 식 (3.12) 를 선명하기 위해서는 두 분자의 코발트착물 간의 반응이 제시된다. 로듐착물 촉매에 의한 히드로포르밀화반응에 관하여서도 비슷한 반응메카니즘이 제시된 바 있다 .14) 로듐 (0) 뭉치화합물 Rh4(C0)1~ 에 의한 말단올레판의 히드로포르밀화반응의 속도측정실험에서 아 래의 속도석을 얻었다(식 (3.15)).14) 식 (3.15) 에서는, 식 (3.14) 와는 다르게, 히드로포르밀화반응의 전체속도 (overall ra t e) 는 울레핀의 농 도에 영 향을 받지 않는다.
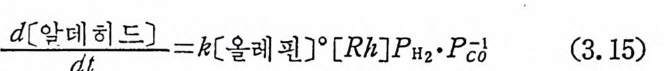 d 잡?t히 드〕 = k 〔올레.3!J_〕 0[Rlz]PH2•P 검 (3.15)
d 잡?t히 드〕 = k 〔올레.3!J_〕 0[Rlz]PH2•P 검 (3.15)
히드로포르밀화반응의 촉매적 역할을 하는 로듐착물로서는 역시 HRh(CO)L3(L=P(CsH5)3) 를 데어 놓을 수는 없다. 이 착물은 CO 가 존재하지 않는 조건에서는 매우 효과적인 올레핀의 수소화반응 의 촉매 직 역 할을 한다. 15) 이 착물에 의 한 히 드로포르밀화반응은 실온에서 그리고 낮은 압력 (PH2=Pco=O.5 기압, 전체기압 =1 기압) 에 서 비 교적 빠른 속도로 진행 된다. 15) 따라서 반웅메 카니 즘을 알기 위한 연구도 실온, 1 기압하에서 비교적 용이하게 이루어졌다. 로 듐(I) 착물 RhH(CO)L3 는 CO 와 반응하여 HRh(C0)2L2 와 [Rh (C0)2L 』 2 를 생성한다. 여기서 생성된 HRh(C0)2L2 는 히드로포르 밀화반응에 활성 이 높은 착물이 며 , [Rh(C0)2L 』 2 는 히 드로포르밀 화반응의 조건 (H 포} co 가 공존하는 조건)에 서 수소와 반응하여 HRh(C0)2L2 를 생 성 하게 된다(식 (3. 16) 참조). HRh(CO)L3 를 사용 하는 히드로포르밀화반응에 관하여서 여러가지
![]() LRh(C0)2L 』 +H2 +== 깍 HRh(C0)2L 』 (3.16)
LRh(C0)2L 』 +H2 +== 깍 HRh(C0)2L 』 (3.16)
반응경로 둥이 제시되었다. 이들을 정리, 종합하면 식 (3.17) 과 같
14) G. Csonto s , B. Heil and L. Marko, Trans. N. Y. Acad. Sci . , 239, 47 (19 74). 15) C. K. Brown and G. Wi lk in s on, J. Chem. Soc. (A). , 2753(1 9 70) and refe r ences the rein .
게 된다. 6), 15) 촉 매 의 농도가 6 X 10-3M 보다 클 때 는 식 (3. 17) 에 서 a 로부터 b,c,d 를 거치는 과정이 주로 일어난다. 4 배위 아실로듐 착물 (RCH 2 CH2C0Rh(CO)L 2 ) 이 생성되어 H 2 와 산화성첨가반응을 일 으켜 야 알데히 드 생 성 이 가능하게 될 것 이 다. 따라서 RCH2CH2C- ORh(CO)L2 의 생성과정은 팔연적이다. 코발트착물에 의한 반응보 -
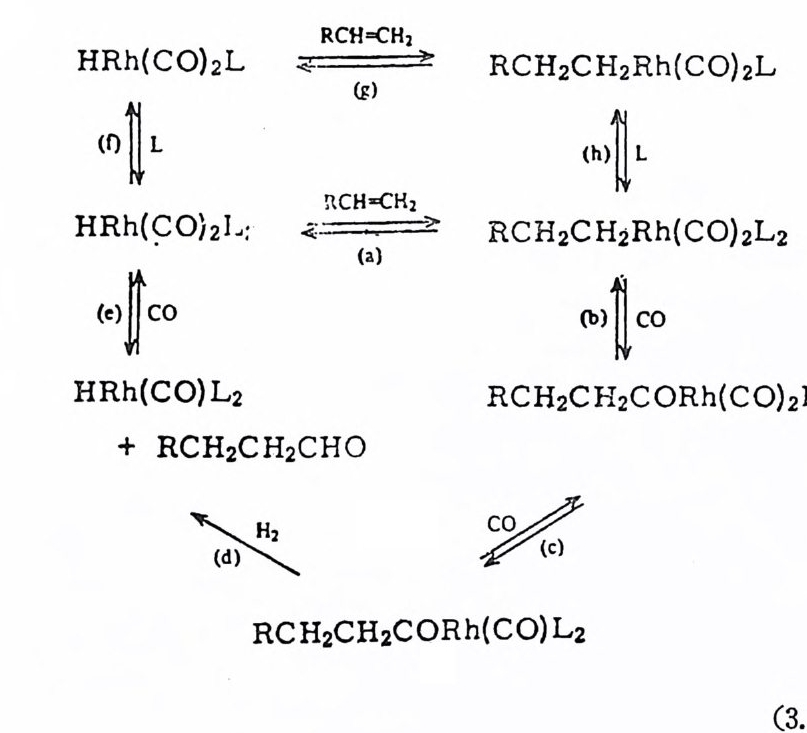 HRh(COhL _, RCH= CH 1 r RCH2CH2Rh(C0)2L
HRh(COhL _, RCH= CH 1 r RCH2CH2Rh(C0)2L
다 로듐착물에 의한 히드로포르밀화반응이 훨씬 용이한 이유는 역 시 로듐착물이 용이하게 산화성첨가반응을 일으킬 수 있다는 접이 . 다 .6) 평형 C 에 의하면 co 의 압력이 증가함에 따라 히드로포르밀 반응은 여제당할 것이다. 로듐착물의 농도가 낮아지면, 또 하나의 포스핀 리간드가 해리하여 더욱 활성이 높은 HRh(C0)2L 이 생성된 다. 따라서 더욱 빠른 히드로포르밀화반응이 진행된다. 이 경우에 반응은 f, g, h, b, c, d 를 거 치 게 된다(석 (3. 17) 참조). 이 상의 내 용(식 (3.17) )은 로듐착물의 농도를 변화시 키 면서 측장
된 히드로포르밀화반응의 속도의 변화와, 과량으로 가해주는 포스판 이 히드로포르밀화반응을 억제시켜 준다는 실험적 견과로부터 얻어 진 것이 다. 식 (3.17) 의 촉매순환과정은 식 (3.4)~(3.11) 에서 보여 준 코발트착물 촉매에 의한 히드로포르밀화반웅의 과정과 실질적으 로 같은 것 이 다. 두 촉매 순환과정 (식 (3. 17) 과 식 (3. 4)~(3. 11)) 모두 가 올레핀이 배위되고 이어서 금속-수소 결합에 삽입되는 단계, 알킬금속을 거쳐 아실금속 착물의 형성 단계, 수소의 산화성첨가반 응, 그리고 환원성 알데히드 제거반웅으로 이루어져 있다. NMR 스펙트럼 연구결과에 의하면 HRh(C0)2L2- i::- 에 틸렌과 25°C 에서 반응하지만 HRh(CO)L2 는 반응하지 않는다. 따라서 히드로 포르밀화반응에 중요한 여할을 하는 착물은 두 개의 co 가 배위되 어 있 는 착물 HRh(C0)2L2 이 다. 16) 따라서 HRh(CO)L2 는 식 (3. 17) 에 포함되 지 않았다. 수소가 존재 하지 않고 HRh(CO)L3, CO 그리 고 말단 울레 핀 (ter m ina l ole fi n) 이 반응하면 아실로듐 착물이 중간체로 촌재하는 것이 보 고된 바 있으며, 에틸렌과 co 의 반응 (Pco=Pc2H4= Q .5 기압)에서 푸로피오닐로듐 착물이 확인되 었다. 17) 그러 나 공업 적 인 히 드로포. 르밀화반응의 조건(高溫, 高壓)하에서는 아실로듐 또는 알킬로~ 착물이 확인된 적이 없다. RhCl(CO)L2(L=P(C6H5)3) 도 히 드로포르밀화반응의 촉매 전구물 질 (p recursor) 로 자주 사용되 는 로듐착물 중의 하나이 다. 비 슷한 반 웅조건하에 서 히 드로포르밀화반응의 속도는 HRh(CO)L3 를 사용하 였을 경우보다 RhCl(CO)L2 를 사용하였을 경우에 훨씬 느리다 .13) 또한 착물 RhCl(CO)L2 를 사용하였을 경우에는 상당한 유발기 (in- ducti on p er i od) 가 있다. 이 기간 동안에 히드리도로듐 착물이 형성 되는 것으로 알려졌다. 트리에틸아민과 같은 유기 영기를 가하면 상기 유발기를 없앨 수 있다. 죽 식 (3.18) 과 같이 쉽게 촉매활성 이 높은 HRh(C0)2L2 가 생성되기 때문일 것이다 .18)
16) D. Evans, G. Yag u ps k y and G. Wi lkin s on, J. Chem. Soc. (A), 2660 (19 68). 17) G. Yag u ps k y , C. K. Brown and G. Wi lki n s on, J. Chem. Soc. , (A), 1392 (19 70).
18) D. Evans, J. A, Osborn and G, Wi lkin s on, J .. Chem. Soc. (A), 3133 (1968).
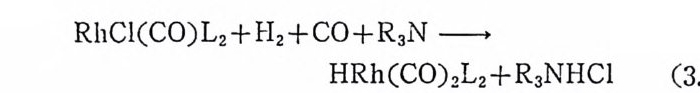 RhCl(CO)L2+H2+CO+R3N 一
RhCl(CO)L2+H2+CO+R3N 一
비교적 최근에 발표된 이리듐착물 Hlr ( C0)3L(L=P (i -C3H7 )3) 에 의한 히드로포르밀화반응의 연구는 촉매순환과정의 각 단계에 관한 많은 정보를 명확히 제공하여 준다.li b) Hir(CO)L3 용액을 50°c 에 서 에틸렌 (Pc2 tt 4=14 기압)과 반응시키면 30 분 이내에 알킬이리듐 착물 C2H5Ir(CO)aL 이 정 량적 으로 생 성 된다. 반응기 내 의 에 틸 렌을 제거하고 C2H5Ir(C0)3L 를 다시 CO(Pco=l4 기압)와 반응시키면 또다시 30 분 이내에 아실이리듐착물 C2HsC Oi r(C0)3L 이 생성된다. 다시 반응기 내의 CO 를제거하고 C 2 H5Ir(C0)3L 를 H2(P tt 2=14 기압) 와 반응시키면 최초의 히드리도이리듐 착물 Hlr(C0)3L 이 다시 생성 되고 푸로피온알데히드가 정량적으로 생성된다. 이상과 같은 각 반 옹은 계속적으로 반복될 수 있다. 이상의 실험적 결과는 코발트착 물에 의한 촉매순환과정(식 (3.4)~(3.11) )과 로듐착물에 의한 촉매 순환과정 (식 (3.17) )의 각 단계 를 그대 로 반영 한다(식 (3. 4)~(3. 11), 식 (3. 17) 및 식 (3. 19) 룸 비 교, 참조). 마지막으로 히드로포르밀화반응에서 생성된 알데히드가 계속 반 응하여 알코올이 되는 과정을 살펴본다. 히드로포르밀화반응에 촉
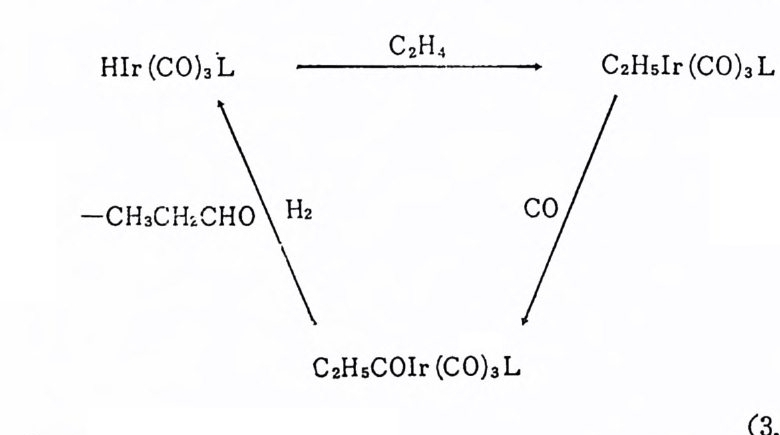 HI r@H이C3.LC c \\ ) C 2H4 c2H5Ir (CO)3 L
HI r@H이C3.LC c \\ ) C 2H4 c2H5Ir (CO)3 L
매적 역할울 하는 금속착물은 생성된 알데히드의 수소화반응에도 축 매적 역할을 할 가능성이 높다. 알데히드의 수소화반응은 히드로포 로밀화 반응보다 높은 온도에서 주로 일어난다. 따라서 히드로포르 밀화반응을 높은 온도에서 진행시키면 단번에 알코올을 얻을 수 있 다. 그러나 실제로는 두 단계 과정을 거쳐 알코올은 생산된다. 즉 히드로포르밀화반응 조전에서 일단 대부분의 올레핀을 알데히드로. 전환시키고 난 다음에 온도를 올려서 생성된 알데히드를 수소화시 켜 알코올을 생 성 한다. 왜 냐하면 처 음부터 높은 온도에 서 반응을 진행시킬 경우에 많은 양의 올레펜이 수소화반응을 일으켜 알칸을 생 성 하기 때 문이 다. 알데 히드의 수소화반응은 식 (3. 20) 과 같이 알 데히드가 금속에 배위되고, 다시 금속-수소결합에 삽입되는 단계를 거쳐 최종적으로 가수소분해반응 (h y dro g enol y s i s) 을 일으키는 것으로 추축되어지고 있다. 생성된 알데히드가 일으킬 수 있는
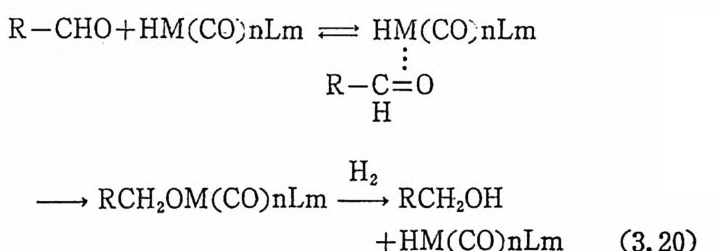 R-CHO+HM(CO) nL m ~ HM(CO; nL m
R-CHO+HM(CO) nL m ~ HM(CO; nL m
또 하나의 반응은 알돌축합반응 (aldol codensa ti on) 이 냐 대 부분의 공 업생산에서는 알둔축합반응이 일어나는 것을 원하지 않는다. 그러 나 알돌축합반응을 일으키기 위해서 M g (OCH3)2 와 같은 촉매를 사 용하는 경 우도 있 다. 예 를 들면 중요한 可塾劑(p las tici zer) 중간체 (i n t ermed i a t e) 인 2- 에 틸핵산울은 푸로필렌의 히드로포르밀화반응, 이 어서 알돌축합반응, 그리고 마지막으로 수소화반응에 의해서 생성 된다. (3) 디엔類 (cl i enes) 의 히드로포르밀화반응 걸러 짝짓지 않는 디 엔 (noncon j cga t ed d i ene) 의 히드로포르밀화반
옹은 모노알데히드와 디알데히드의 혼합체를 생성하는 것으로 알려 쳤다. 또한 이중걷합의 거리가 밀수록 디알데히드가 많이 생성되는 것도 알려졌다. 걸러 짝지은 디엔 (con j u ga t ed d i ene) 의 히드로포르밀화반응도 상당 히 연구되어 왔다. 득히 I, 3- 부타디엔의 히드로포르밀화반응으로 부터 I, 6- 핵 산디 알(1, 6- h exanedia ! ) 또는 I, 6- 핵 산디 올 (hexaned i ol) 을 얻기 위한 연구가 많이 전행되었다. 그러나 대부분의 경우에 포화 된 모노알데히드나 모노알코올을 얻었을 분이다 .19) 죽 두 개의 이중 결합중에서 한개는 수소화반응을 일으키고, 나머지 한개의 이중결 합은 히드로포르밀화반응을 일으킨다. 즉 석 (3.21) 과 같은 파이-알 릴금속 착물을 형성하여 수소화반응을 일으킬 것으로 추측된다. 왜 냐하면 파이-알릴착물은 히드로포르밀화반응을 쉽게 일으키지 않는 것으로 알려졌기 때문이다. 이렇게
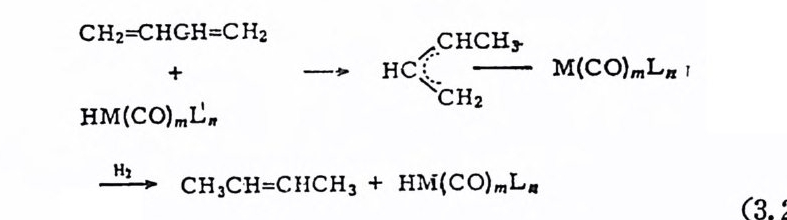 CHHM2(=C COH )m+G Hl .!,=, CH2 츨 HC /`: ·C· HC一H:,- M(CO)mL,. ,
CHHM2(=C COH )m+G Hl .!,=, CH2 츨 HC /`: ·C· HC一H:,- M(CO)mL,. ,
생성된 모노올레핀은 정상적으로 히드로포르밀화반응을 일으킨다. 다음으로 히드로포르밀화반응이 두 번 일어나는 예를 들어 본다。 로듐카르보닐착물+포스핀 촉매계(포스핀/로듐 =40) 에서 부타디엔 의 히드로포르밀화반응은 디알데히드와포화된 모노알데히드의 혼합 물을 생성한다 .19),20) 이 반응에서 반응이 완결되기 전에 반응혼합물 윤 분석해 본 결과불포화된 모노알데히드의 농도가 매우 높은 것이 발견되었다. 따라서 처음에 일어나는 히드로포르밀화반응에서는 주 로 CH2CH=CHCH2CHO 또는 CH=CH-CH2CH2CHO 가 생성되리 라고 추측된다. 왜 냐하면 CHaCH2CH=;CHCHO 는 히 드로포르밀 화 - 19) B. Fell aud W. Boll, Chem. Ztg , , 99, 452, 485(1975). 20) B. Fell and W. Rup ilius , Tetr a hedron Lett , , 27210969).
반응을 일으키지 않는 것으로 알려졌기 때문이다. 따라서 두번째 히 드로포르밀화반응으로부터 는 주로 가지 탈린 디 알데 히 드 (branched d i aldeh y de) 가 생성될 것이다. 이 반응에 사용된 로듐카르보닐+포스 펀 촉매계는 이중결합 이동반응에는 촉매져 역할을 하지 못하는 것 으로 알려졌다. 또한 CH3CH2CH=CHCHO 는 히드로포르밀화반응 울 일으키지 못하는 것으로 보고되었다 .2 1) (4) 치환기가 있는 울레핀의 히드로포르밀화반응 불포화된 알코올, 페놀, 에테르, ‘ 알데히드, 카르복시산, 에스데 르, 무수산, 니트릴, N- 치환된 아미드 그리고 이미드 등도 로듐착 물 촉매계에 의해서 히드로포르밀화반응을 일으킨다 .6) 올레핀기와 치환체의 여중결합 사이에 컨쥬게이션이 있는 화합물(예, a, g-불포 화알데히드, 스티렌)은 히드로포르밀화반응보다는 주로 수소화반응 을 일으킨다. 그러나 로듐착물/포스핀 착물계에 의한 스티렌의 히 드로포르밀화반응은 높은 수율로 페닐푸로판알 이성질체를 생성한 다(식 (3. 22) 참조).
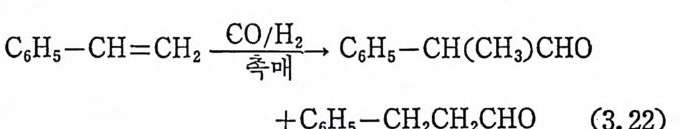 C6Hs— CH =CH2 틀-+ C6H5-CH(CHa)CHO
C6Hs— CH =CH2 틀-+ C6H5-CH(CHa)CHO
a, /3-불포화에스데르는 비교적 좋은 수율로 히드로포르밀화된다. 저온에서 CHO 기가 결합되는 탄소의 위치는 주로 에스데르기의 전 자적 영향을 받는다. a, /3-불포화에스테르에서 이중결합은 단순한· 올레핀보다 훨싼 국성을 떨 것이다@식 (3.23) 참조)• a_ 탄소는 부분 적으로 음전하를 갖게 되므로 이러한 전자적 영향만울 고려하면 석 (3.23) 에서 주로 CI) 이 생성될 것이고 입체적인 영향만을 고려하 면 식 (3.23) 에서 주로 CII) 가 생성될 것이다. 0°c 에서 HCo(C0)4 와 아크릴산 에스데르 (H2C=CHC02R) 의 반응은 80% 이상의 a- 포 르밀에 스데 르 (a- fo rm y les t er) 를 생 성 한다. 22) 따라서 히 드로포르밀화
21) C. Y. Hsu and M. Orchin , J. Am. Chem. Soc, , 97, 3553(1 9 75). 22) R.F. Heck and D.S. Breslow, J. Am. Chem. Soc., 83, 4023(1961 ).
반응의 생성물은 전자적인 영향에 의해서 주로 결정된다고 볼 수 있다. 한편 반응온도를 올려주면 /3-포르밀에스테르의 양이 증가하 여 110°c 에서는
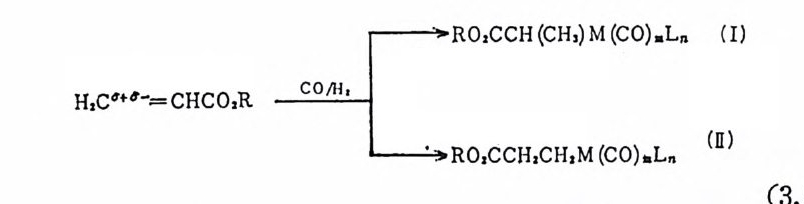 H,C'=CHCO,R ~〔二 RROO,,CcCCHH, (CCHH,,)M M (C (COO) .). L.Lnn (n()I ) (3. 23)
H,C'=CHCO,R ~〔二 RROO,,CcCCHH, (CCHH,,)M M (C (COO) .). L.Lnn (n()I ) (3. 23)
80% 이상이 /3-포르밀에스테르로 생성된다 •3),23) 이상의 실험적 결과 로부터 처온에서는 전자적 영향이 크게 작용하지만 고온에서는 입 체적 영향이 크게 작용하여 /3-생성물을 생성하는 것 같다. 예의적 인 실험결과도 있다. 즉 110°c, 600 기압에서 로듐착물/포스핀 촉 매계에 의한 메틸아크릴산 에스테르의 히드로포르밀화반응은 94% 의 a- 포르밀에스테르를 생성한다(식 (3.24) 참조 ).3) 이것은 고온에서 전자적인 영향이 지배적인 인자가 되어서 입체적으로 불리한 a- 생 성물을 만드는 예이다.
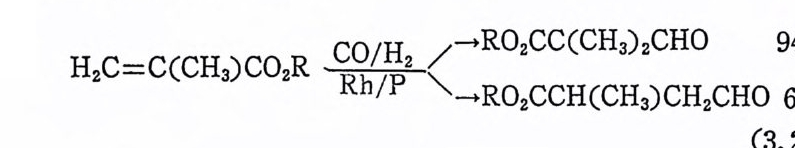 H2C=C(CHa)C02R • CO/Hz /-+R02CC(CHa)2CHO 94%
H2C=C(CHa)C02R • CO/Hz /-+R02CC(CHa)2CHO 94%
a, /3-불포화카르복시산의 히드로포르밀화반응은 락본의 중요한 적 접합성법이 된다. /3-포르밀에스테르가 생성되게 반응조건을 취하 떤, 생성된 /3-포르밀에스테르는 이어서 수소화반응을 일으켜 알코 올이 되고, 이 알코올로부터 락론을 얻을 수 있다(식 (3.25) 참조 ).23)
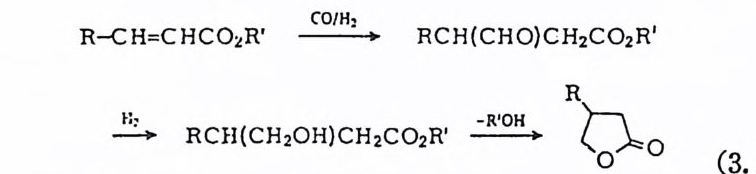 COIH,
COIH,
23) J. Falbe, N. Hup pe s and F. Korte , Chem. Ber. , 97, 863 (19 64).
(5) 非對稱性 히드로포르밀화반응 (as y mme t r i c hy d rofo r my la ti on ) 로듐(또는 코발트)착물 촉매와 광학적 활성윤 갖는 포스핀리간드 를 포함하는 촉매겨 1 에 의한 올레핀의 히드로포르밀화반응의 생성물 은 최 고 27% 의 광학적 순도를 보여 주었 다. 24) 표 3.1 은 HRh(CO) L3(L=P(C 晶 )3) 와 광학적 활성을 갖는 리 간드 (-)-DIOP((-)-2, 2-d i m eth y l- 4, 5-bis ( dip h eny lp h osph in o meth y l) -1, 3 - d i oxolane( 아래 그림))가 이루는 촉매계에 의한 히드로포르밀화반응의 실험적 견 과이다. 비대칭성 히드로포르밀화반응은 낮은 온도, 낮은 압력 하 에서 효과적으로 일어나므로 표 3.1 의 결과는 상온과 낮은 압력에 서 얻은 것이다. 따라서 반응속도는 상당히 느리며, 이상의 결과를 얻기 위해서 오랜 반응시간(예를 물면 며칠)이 걸렀다.
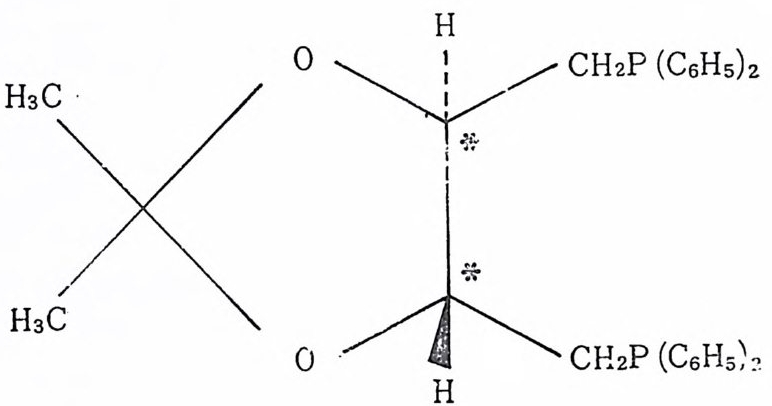 H
H
이상의 족매계가 표 3.1 에서 보여주는 바와 같이 최고로 27% 의 광학적 순도밖에 주지 못하는 이유는 분명치 않다. Rh 에 배위되 어 있는 P(C5Hs)3 가 모두 광학적 확성리간드 DIOP 에 의해서 완 전히 치환되지 않았기 때문이라고도 생각할 수 있지만 역시 뚜렷한 증거는 없다.
24) P. Pin o , G. Consig lio, C. Bott eg h i and C. ·sa lomon, Advan. Chem. Ser. , 132, 295(1'5 74 ).
3 - 매탈 2 렌벤처럼 비대칭탄소를 갖고 있는 올레핀의 히드로포 르밀화반응은 입체적 선덱성을 보여 준다. 죽 타세미 울레핀을 히 드로포르밀화반응시킬 경우에 CR) -광학적 이성질체는 cs) - 광학적 이성질체보다 빠른 속도로 반응하여 (R)-4 - 메탈핵산알을 생성시 킨다. 표 3.-1 HRh(CO) (P(C s Hs)3)3/(-)-DIOP( 몰비융 1:4) 촉매계에 의 한 히드로포르밀화반응의 결과. 20°c, 1 기압 (PH2=Pco=0.5 기압). 분리도i}광학적 거절 황성 합물 광학적순도(%) I-bute n e 2-meth y !b uta n al 18.S(R) 1-octe n e 2-meth y lo cta n al 15. 2(R) cis- bute n e 2-meth y lb uta n al 27.0(S) 3-meth y l- 1-pe nte n e 4-meth y lh exanal 4. 6(R) sty re ne a-ph eny lp r o p a nal 22. 7(R) i-부텐의 히드로포르밀화반응에서 얻은 2 - 메틸부탄알과 시스 -2 - 부텐의 허드로포르밀화반응에서 얻은 2- 메틸부탄알은 각각 다른 비 대칭성 (c l:fi ra lity)를 갖고 있다(표 3.1 참조). 일반적으로 인정을 받는 히드로포르밀화반웅의 메카니즘(식 (3.17) 참조)에 의하면 1- 부텐이나 시스 -2- 부렌은 모두 같은 로듐착물 중간체를 형성할 것이다. 죽 비 대칭 리간드 L* 이 비대칭 중심을 갖는 경우에 중간체는 아래 그림 과 같온 두개의 부분입체이성질체 (d i as t ereo i somer) 로촌재할것이다.
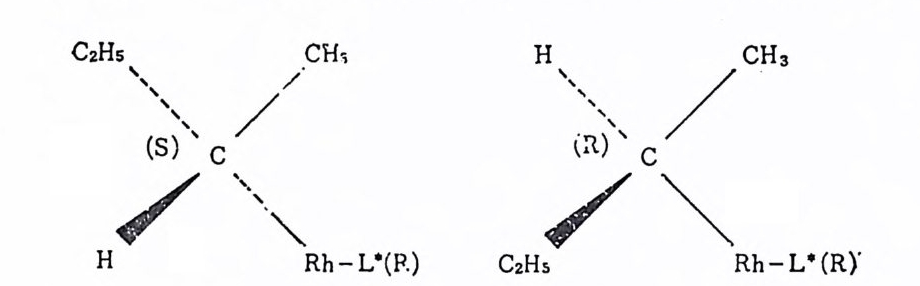 c2 H,s\/鬪 H c //\.Rc H \E ,_R` '` b_' -hC2/HHs '(R\) 、 \C / RC hH-3 L • (R)'
c2 H,s\/鬪 H c //\.Rc H \E ,_R` '` b_' -hC2/HHs '(R\) 、 \C / RC hH-3 L • (R)'
만일 바대칭성 히드로프르밀화반응이 알킬로듐착물 중간체 생성단 계에서 결정되지 않고 그 후에 일어난다면, l- 부덴이나 시스 -2- 부
텐으로부터 얻 어 지 는 알데 히 드의 바 대 칭 성 (Ch i ral ity)과 광학적 순도 (op tica l pur ity)는 같을 것 이 다. 따라서 l - 부덴과 시 스 - 2 - 부덴으로부 터 얻어지는 알데히드가 각각 (R) 와 (S) 의 비대칭성을 갖는다는 사실은 다음과 같은 두 가지 사실을 제시한다. 첫째, 알킬로듐착물 중간체중의 부분입체이성질체 (d i as t ereo i somer) 의 조성은 올레판의 성 질에 따타 결정된다. 둘째, 비대칭성 히드로포르밀화반응은 중간체 인 알킬로듐착물의 생성단계에서 결정된다. 식 (3.26) 은 대칭성인 시스 -2- 부맨을 사용하였을 경우에, 로듐알킬착물 중간체의 생성단 계에서 비대칭성 유발 (as y me t r ic i nduc ti on) 이 어떻게 일어날 수 있는 가를 보여준다. 알킬금속의 부분입체이성질체의 조성을 결정하는 因子는 어떤 것 들인가? 두개의 올레만금속착물의 異形態體 (co nf ormer) 사이의 自 由에너지 差에 의해서 부분 이성질체의 비율이 결정될 수 있을 것
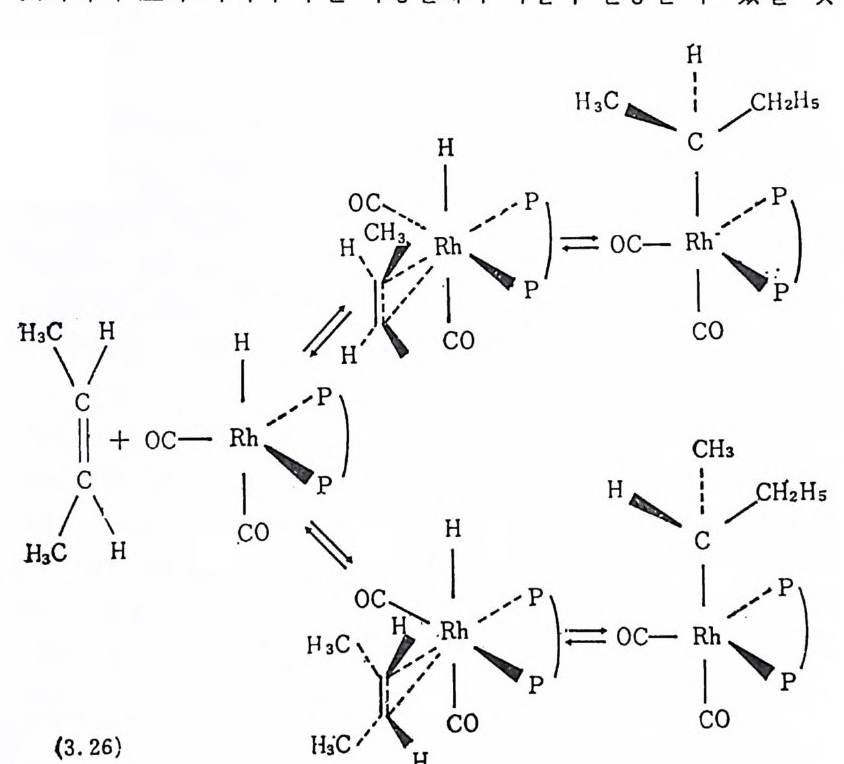 H
H
이다. 죽 熱 力 學 的 因子에 의 해 서 결정될 수 있 다. 한편, 각각의 異形態 f효 (con fo rmer) 를 초기 물 질로 하여 반응시켰을 경우에 입체적 인 이유로 인해서 금속-수소 결합에 울레핀이 삽입되는 반응의 속 도가 달라질 수도 있을 것이다. 죽, 반응속도론적 因子가 있을 수 도있다. 하드로포르밀화반응 자체가 복잡한 여러단계의 순환과정이므로, 비 대 칭 성 유발 (as y mme t r i c i nduc ti on) 을 이 해 한다는 것 이 그리 쉬 운 일이 아니다. 실제로 알킬금속착물의 생성과정이 알데히드의 최종 공간배열 (con fig ura ti on) 을 결정 짓는 과정 인지 아난지 는 명 확하지 않다. 왜 냐 하면, co 의 삽입과정 또는 알데히드가 금속으로부터 떨어쳐 나오 논 과정 둥에서도 생성물의 비대칭이 바뀔 수 있기 때문이다. 3. 카르보닐화반응 (carbon y la ti on) 유기화합물의 카르보닐화반응은 맨族 금속의 카르보닐화합물에 의해서 일어난다. 경우에 따라서 약간씩 다르지만 10~40 기압의 co 압력과 100~300°C 의 온도에서 일어난다. 아세틸렌의 카르보닐 화반응에는 주로 N i (C0)4 · 가 촉매로 쓰여지고, 올레핀의 카르보닐 화반응에 는 Fe, Co, Rh, Pd 및 Ru 금속착물 촉매 들이 흔히 쓰여 지고 있다. 한편 아민 類 의 카르보닐화반응 (N- 포르밀 유도체가 생 성됨)에는 Ru- 카르보닐이 쓰여졌다 .25) 금속-카르보닐화합물만 사용하여 도 카르보널화반응을 일으킬 수 있지만, HCI 또는 HI 와 갈은 산, 또는 I2 와 같은 할로겐을 가하 떤 반응속도는 훨씬 빨라진다. 상기 반응에서 실제 촉매종은 반응 중에 생성되는 히드리도카르보닐 금속착물로 추측된다. 이러한 히 드리 도카르보닐 금속화합물은 금속-카르보닐화합물과 산 (HCI, HI 등)이 반응하여 생성하는 산화성첨가반응 생성물로 추측된다. I2 를 가하는 이유는 J 2 가 수소를 내어줄 수 있는 유기화합물과 반응하여
25) J. J. By e rley , G. L. Remp el and N. 'Fa kebe. Chem. Commun. , 148Z (1971).
HI 를 생성시키고 이렇게 해서 생성된 HI 는 쉽게 금속에 산화성첨 가반응을 일으켜서 히드리도 금속화합물을 생성하기 때문으로 추측 된다. 히드리도카르보널금속 착물이 실제 촉매라면, 카르보닐화반응의 메카니즘은 앞에서 자세히 기술된 히드로포르밀화반응의 메카니즘 (식 (3. 4)~(3. 11) )과 비 슷할 것 이 라고 생 각된다. 단지 카르보닐화 반 응(식 (3. 27)~(3 . 29) )에 서 는 마지 막 단계 에 서 아실금속 (ac y lme t al) 화 합물이 H20 와 같은 수소를 내어줄 수 있는 화합물과 작용하여 생 성 물 (RCH2CH2C02H) 과 실제 촉매 종인 히 드리 도카르보닐금속화 합물 (HM(CO)m) 을 생 성 하는 것 이 다르다(식 (3. 4)~(3.11) 과 식 (3. 27)~(3. 2 9 ) -운 비 교해 볼 것 ).
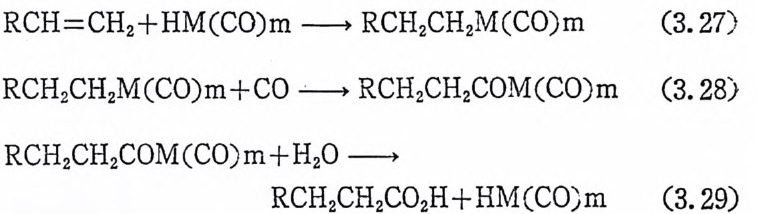 RCH=CH2+HM(CO)m 一 RCH2CH2M(CO)m (3.27)
RCH=CH2+HM(CO)m 一 RCH2CH2M(CO)m (3.27)
올레판, CO 그리고 H20 의 반응은 촉매의 종류 또는 반응조건에 따라 각각 다른 생성물을 줄 수 있다. 예를 들면 300°C 에서 카르 보닐니벨착물을 촉매로 사용하면 에탈렌으로부터 푸로피온산을 높 온 수율로 얻게 된다. 한편, 온도를 240°C 로 내리고 반응혼합물 중 의 산의 농도를 높게 유지하면 산의 무수물 (anhy dr i de) 이 주로 생성 된다. 영기가 존재하는 용액에서 철착물 촉매를 사용하면 푸로필알 코올이 주생성물이 되지만 H20 의 농도를 낮게 유지하며 Co2(CO)s 를 촉매 로 사용하면 푸로피 온산 에 탈 (eth y l p ro pi ona t e) 이 생 성 된다’ 히드로포르밀화반응에서처럼 카르보닐화반응에서도 여러가지 이 성질체들이 얻어지기도 한다. 낮은 온도와 높은 co 의 압력하에서 말단 올레 핀(t erm i nal ole fi n) 의 카르보닐화반응은 반응속도는 느려 지 지만 주로 線型(li near) 생성물을 준다. 포스핀을 포함하는 촉매겨]는 포스핀의 종류에 따라서 상당히 다른 생성물들이 얻어진다. 예를 들어 서 PdCI2(P(C6Hs)3)2 및 PdCli( DI OP)(DIOP=2, 2-dim eth y l- 4,
5-bis ( d ip h eny lp h osph in o meth y l) - l, 3- d io x olane., ( 제 3 장 2 의 (5) 를 참 조바 람 )를 촉매로 하여 알파-메틸스티렌과 co 그리고 C2H50H 의 반 응을 시 킨 견과 각각 다른 생 성 불 을 얻 었 다(식 (3. 20 참조) 〈 PdC12 (DIOP) 촉매를 사용하여 얻어진 에스데르는 비대칭탄소를 갖고 있 다•
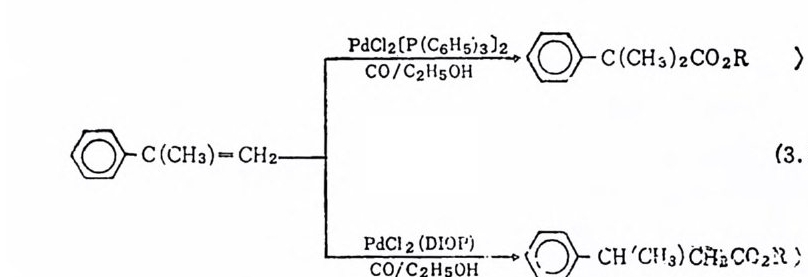 땅麟 2 '1 3 J 2 ; <>-C ( CH.hC02R >9 5%
땅麟 2 '1 3 J 2 ; <>-C ( CH.hC02R >9 5%
야) 메탄을의 카르보닐화반응 메탄올로부터 아세트산의 합성은 공업적으로 상당히 중요한 과정 이다. 히드로포르밀화반응에서와 같이 코발트 및 로듐카르보널착물 이 중요한 촉매 계 를 이 룬다. 반응촉진제 (p romo t er) 로 가해 지 는 할 로겐(주로 요오드화합물)의 역할도 매우 중요하다. 최초로 개발된 과정은 코발트카르보닐촉매와 요오드를 보조촉매 (coca t al y s t)로 사용 하여 210°c 에서, 그리고 700 기압의 co 압력하에서 90% 의 메탄올 을 아세트산으로 바꾸었다 .26) 그러나 최근에 개발된 로듐착물촉매 에 의한 과정은 훨씬 낮은 압력 (1 3~120 기압)의 co 하에서, 그리 고 비교적 낮은 온도(1 75°C) 에서 99% 의 수울로 아세트산을 생산 한다 .27) 이상의 로듐착물에 의한 메탄올의 카르보닐화반응은 비교적 자세 하게 연구되어 왔다. 촉매계는 로듐착물과 요오드화합물의 두 성분 26) H. Hohenschutz , N. V. Kute p o w and W. Him mele, Hy d rocarbon Proc· ess , 45, 1410966). 27) J. F. Roth , J. H. Craddock, A. Hershman and F: E. Pauli k, Chem. Tech. , 600(1 9 71 ).
으로 이루어쳐 있다. 로듐화합물, RhCl3•3H20, Rh2 야, [R h(C0)2 L]-중 어느것을 사용하여도같은 반응속도가 얻어질 분만 아니라 촉진제 로서 HI, CI-1 3 I, l2 의 수용액 중 어 느 것 을 사용하여 도 동일한 반응속도가 얻어진다. 이러한 실험적 결과로부터 어떠한 촉매 전구 물질 (p recursor) (로듐착물)을 사용하여 도, 그리 고 어 떠 한 축전제 (요 오드화합물)를 사용한 경우라도 실제 촉매종은 동일한 화합물로 추 측된다. 이상의 로듐착물 및 요오드화합물중에서 가장 편리한 촉매 계는 쉽게 얻을 수 있는 RhC13•3Hz0 와 HI 를 H20 와 아세트산의 혼합용매에 녹인 용액이다. 메탄올의 카르보닐화반응에서 아세트산이 얻어지는 반응은 아태 와 같이 간단히 표시 될 수 있 다(식 (3. 3,1) 참조). 그러 나 실제 반응은 아래와 같은 여러단계의 평형이 포함되어 있다(식 (3.32) 참조).
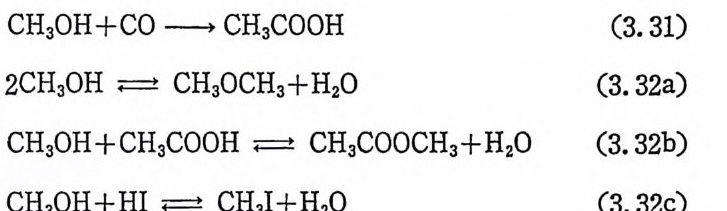 CH30H+co 一 CH3COOH (3. 31 )
CH30H+co 一 CH3COOH (3. 31 )
연구결과에 의하면 반응이 전행되는 동안 CH3I 의 농도는 일정하 케 유지되며, 식 (3.32a) 및 (3.32b) 에 의한 평형은 이동되어 결국 에는 모든 중간체는 아세트산으로 전환된다. 반응속도 측정실험에 의하면 속도식은 아래와 같이 얻어진다(석 (3.33) 참조).
![]() 속도 =k[C0]0 [CH30H].0 [Rh][I-J (3.33)
속도 =k[C0]0 [CH30H].0 [Rh][I-J (3.33)
촉매계 중의 요오드화합물의 여할은 메탄올을 메탄올보다 더욱 천 전자적 인 CH3I 로 바꾸는 것 이 다. 요오드화합물도 그립 (3. 4) 에 서 보는 바와 같이 순환과정을 거찬다. 이 요오드화합물 순환과정은 로듐착물촉매를 포함하는 촉매순환과정 (그립 (3. 5))28) 과 관련지어 설명되어진다. 로듐착물 순환과정은 CH3I 가 [Rh(C0)2I2] 다에 산 28) P. Forste r , Ann. N. Y. Acad. Sc i, 295, 79(1 9 77). Adv. Orga n omet. Chem. , 17, 255(1979).
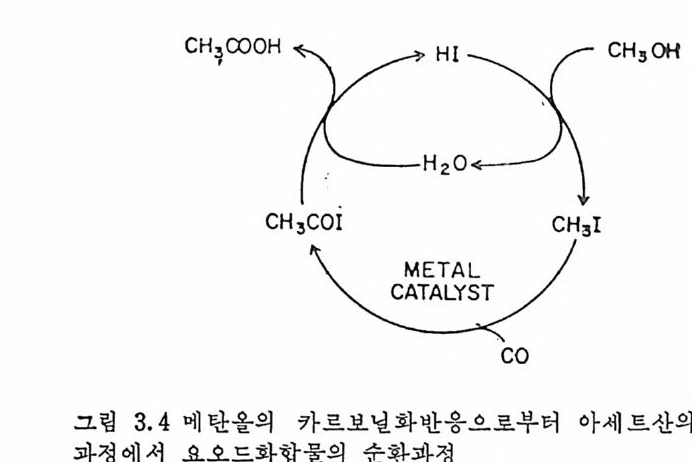 cH 3 ' 8 OH 广二 cH 3 O H
cH 3 ' 8 OH 广二 cH 3 O H
화성첨가반응을 일으킴으로써 시작된다. (RhC13•3H20 는 카르보날 화반응 조건하에서 빠른 속도로 [Rh(C0)2l2] -로 변한다.) Rh( I ) 착물의 산화성첨가반응은 비교적 쉽게 일어나는 것으로 알려져 있 지 만 [Rh(C0)2l2]- 가 CH3I 와 반응하여 [CH3Rh(C0)2l3J -를 생 성 시키는 이 산화성첨가반응은 특히 빠르다 .29) 그 이유로는 음이온성 착물 [Rh(C0)2l2]_ 의 높은 전자밀도 때 문인 것 으로 추측된다. 산화 성첨가반응에 의해서 생성된 알컬로듐착물 ([CH3Rh(C0)2l3]- )은 반 웅속도론적으로 보아서 매우 불안정하여 빠른 속도로 아세틸로듐착 물 ([CH3C0Rh(CO)l3 J-)로 변한다. 실제로 이 아세 틸착물은 분리 , 확인된 바 있다 .28) 알킬로듐착물(〔 CH3Rh(C0)2l3]_) 이 아세 털로듐착물 ([CH3C0Rh (CO)l3]- )로 되는 과정은 찰 알려진 알킬이동 (alk y l m ig ra ti on) (또는 co 의 삽입 (i nser ti on) 반응이 라고도 불리 운다) 과정 이 다. 이 렇 게 해 서 생 성 된 5 배 위 착물, [CHsCORh(CO)l3J -는 또 하나의 CO 를 첨 가 시켜 6 배 위 착물, [CH3CORh(C0)2l3J -를 생 성 한다. 물이 나 알코올 이 존재하지 않는 반응조건에서 [CH~CORh(C0)2l3] -는 쉽게 환원
29) D. Forste r ,]. Am. Chem, Soc. , 97, 951(1 ':!15 ).
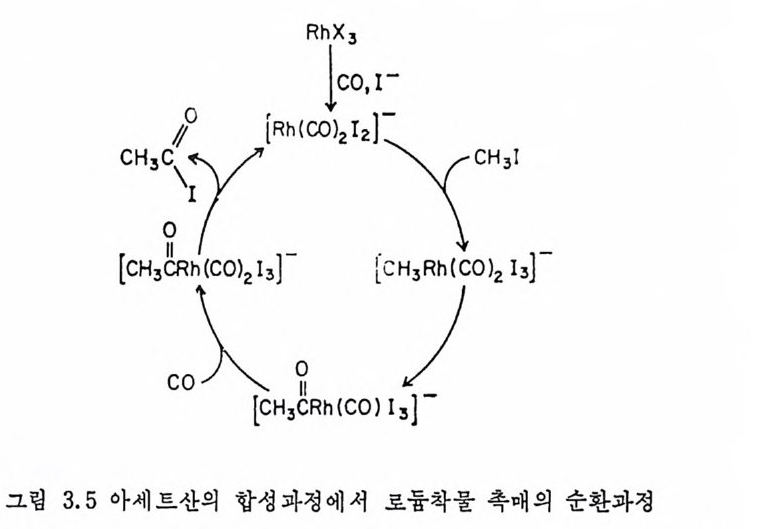 Rh沿CwOhR
Rh沿CwOhR
성 제 거 반응을 일으켜 CH3COI 를 내 어 놓는다. 동시 에 촉매 인 [Rh (C0)2l2]-가 다시 생 성 되 어 또 다시 순환과정 (그립 3. 5) 을 거 처 게 된다. 생성된 CH3COI 는 그림 3.4 에서 보여주는 바와 같이 요오드 화합물 순환과정을 통해서 물과 반응하여 아세트산과 HI 를 생성시 킨다. (2) 올레핀의 카르복시화반응 올레 핀, co 그리 고 수소주게 (hy d rog en donor) 의 반응으로부터 카 르복시 산의 유도체 들이 만들어 지고 있 다. 이 상의 합성 반응둘은 CO2 (CO)s 과 같은 혼히 쓰여지는 금속-카르보닐 촉매에 의해서 진행된 다 .3) 여기서 기술될 말단 올레핀(t erm i nal ole fi n) 으로부터 탄소수가 하나 더 많은 지방족산 (a lip ha ti c acid ) 합성은 위에서 소개된 메탄올 로부터 아세 트산을 생 산하는 과정 (제 3 장 3 의 (1))과 비 슷한 과정 을 거쳐서 일어난다. 위에서 기술된 아세트산의 합성과정이나 에탈 렌으로부터 푸로피온산의 유도체들을 얻는 과정(식 (3.34) )이나 모. 두 아실금속착물 (RCOM) 의 중간체를 거쳐서 전행된다. 푸로피온산은 에탈렌, co 그리고 H20 로부터 직접적으로 만들
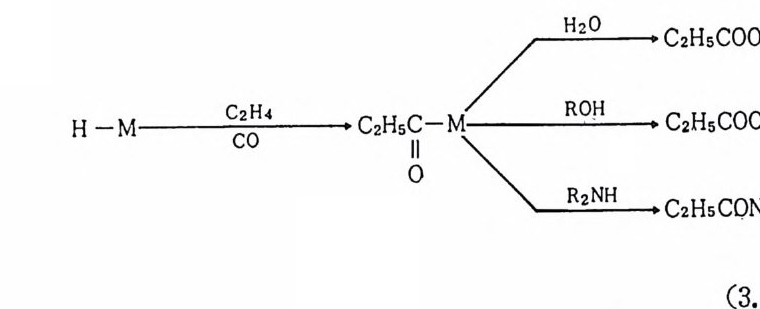 ~c 曲 COO !f
~c 曲 COO !f
수 있다. 그러나 푸로피온산보다 탄소수가 많은 카르복시산은 메탈 이나 에틸에스테르로 만들어진다. 이 반응들은 올레핀의 히드로카 르복시 화반응 (h y drocarbox y la ti on) 이 라고도 불리 운다. 이 러 한 히 드로 카르복시화반응에는 올레핀과 물을 접촉시키기 위해서 용매 또는 相移動劑(p hase tra nsfe r a gen t)가 필요하다. 반응혼합물에 H20 와 co 가 촌재하므로 수성가스이동반응 (wa t er gas shif t reacti on ), CO+ H20 一 C02+H 머 일어날 수 있을 분 아니라 여기서 생성되는 H2 에 의해서 올레판의 수소화반응 (h y dro g ena ti on) 및 히드로포르밀 화반응(제 3 장 2 참조)이 병행해서 일어난다. 올레핀이 비교적 염가 일 경 우에 는 이 러 한 부반응 (s i de reac ti on) 들이 문제 가 되 지 않지 만 · 울레핀이 비교적 고가일 경우에는 올레핀의 수소화반응 및 히드로 . 포르밀화반응이 문제가 되고 있다. 공업 적으로 카르복시화반응에 사용되는 금속촉매는 대 부분 코발트 카르보닐 착물이 다. 그러 나 PdCl2(P(C5Hs)3)2 도 앞으로 사용될 가능 · 성이 있다. 왜냐하면 이 팔라듐착물은 낮은 압력하에서 촉매작용을 하는 것으로 알려졌기 때문이다 .30) 코발트착물 촉매에 의한 올레핀 의 카르복시 화반응의 대 표적 인 예를 돈다면 Co2(CO)s 의 메 탄올용 액 과 1- 펜텐을 100~200 기 압의 co 하에 서 및 시 간 가열 하면 (14 0° ~· 170°C) 80~90% 의 올레핀이 반응한다. 반응생성물의 70% 는 핵산- 30) K. Bit tier, N. Von Kute p o w , D. Neubauer, and H. Reis , Ang e w. Chem~ Int. Ed. , 1, 329(1 9 68).
산 메 틸 (meth y l hexanoa t e) 과 약 30% 의 가지 탈린 에 스태 르들이 생 성된다(소량의 다른 부산물들도 발견되었다 ).3D PdC12(P(C6 H s)3) i - 를 촉매로 사용할 경우에 80~110°c 에서 35 기압의 co 압력하에서 올레 핀의 카르복시 화반응은 일어 난다. 32) 이 상의 실 험 조건에 서 1- 헵 텐으로부터 옥탄산 메 틸 (meth y l oc t anoa t e) 을 얻 을 수 있 는 50 % 이 하 이 다. 왜 냐하면 希앞템 (li near) 생 성 물 형 성 을 위 한 선택 성 (selec ti v ity)이 60% 정도밖에 되지 않기 때문이다. 그러나 SnCl2 를 과량으로 가하 고 반응시키면 이 수운은 76% 로 증가한다 .32) HCl 의 촌재하에서 PdCl2(P(CGHs)3)2 를 사용하여 카르복시화반응을 시켰을 때는 주로 가지 탈린 (branched) 에 스테 르가 생 성 된다. 예 를 들면 푸로필렌, co 그 리고 메탄올의 반응은 HCl 존재하에서 주로 이소부틸산 메틸 (me t hy l i sobu ty ra t e) 을 생 성 시 킨다. 30) 코발트착물에 의 한 카르복시 화반응의 메 카니 즘은 식 (3. 35) 로 표 현된다. 식 (3.35) 의 대부분 과정이 앞에서 소개된 올레판의 히드로 포르밀화반응(식 (3. 4)~(3.11) )과 매 우 흡사하다. Co(2CO)a 은 알코 .
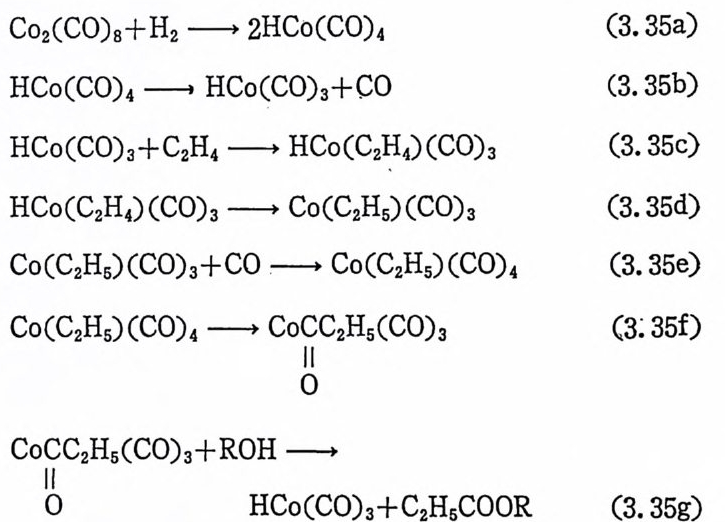 Co i( C0)8 準 一 2HCo(C0)4 (3. 35a)
Co i( C0)8 準 一 2HCo(C0)4 (3. 35a)
31 ) P. Pin o , F . Pia c enti , and M. Bia n chi, Hy dr ocarbo:c yla ti on of Ole/in s , • in I. Wender and P. Pin o , Eds. , Orga nic Sy nt h e sis via Meta l Carbony ls , 32V) oJl.. F 2., KWni ilf et yo- n l ,n .t eJ r .s Oci regn , c eC, hpe.m 2.3 34(11 ,9 7278)8. 5(1 '576 ).
올 ( 또는 H2 를 가해줄 수도 있음)과 반응하여 HCo(C0)4 믈 생성한 댜 HCo ( C0)4 중의 수소는 매우 센 산과 같이 작용한다(특히 국성 용매에서). co 가 과량으로 존재하지 않는 조건하에서 HCo(C0)4 는 매우 불안정하여 쉽게 코발트금속으로 분해된다. 따라서 코발트 카르보닐착물을 촉매로 사용하는 반응에서는 HCo(C0)4 및 촉매순 환과정에서 형성되는 중간체들을 안정화시키기 위해서 높은 압력의 co 가 필요하다. 일반적으로 촉매순환과정은 HCo(C0)4 로부터 co 가 해리되어 HCo(C0)3 가 생성되는 단계로 시작된다고 가정되어 오고 있다. 그 러나 올레핀에 의하여 co 가 치환되는 과정이 S N 2 형의 회합메카니 즘 (asso ci a ti ve mechan i sm) 으로 일어 날 것 이 라는 보고도 있 다. 일단 배위된 에틸렌을 Co_H 결합 사이에 삽입반응을 일으켜 배위적으 된 불포화된 (coordin a ti ve ly unsatu rate d ) 코발트 - 에 틸 착물 (Co(C2H5) (C0)3) 이 형성된다. 이어서 쉽게 co 가 첨가되어 Co(C2H5)(C0)4 가 얻어지고계속해서 Co 一 C2H5 결합사이에 co 의 삽입반응(에틸기 의 이동반응이라고 부르는 것이 더욱 정확한 표현이지만 습관적으 로 co 의 삽입반응이라고 부른다)이 일어나 코발트-아실착물이 생 성된다. 이상의 반응단계들은 전형적인 유기금속화합물의 반응으로 올레핀의 히드로포르밀화반응(제 3 장 2) 에서도 자세히 다루었다. 울 레핀의 히드로포르밀화반응과 올레핀의 카르복시화반응의 차이접은 금속_아실착물에서 아실기가 떨어져 나가는 단계이다. 카르복시화반옹에서는 식 (3.35) 에서 보는 바와 같이 금속-아실착 물은 알코올 또는 물과 반응하여 에스테르 또는 카르복시산울 ' 생산 하고 촉매적 활성이 있는 금속착물 HCo(C0)3 를 되돌려 준다. 이 마지막 단계에 관한 자세한 반응의 매카니즘음 아직 밝혀지지는 않 았다. 그러나 코발트착물과 비슷하면서도 더욱 안정한 망간-아실착 물의 반응에 관한 연구가 상당히 중요한 정보를 제공한다. 즉 석 (3.36) 에서 보여 주는 바와 같이 망간-아실착물은 물이나 알코올과 반응하여 에스테르를 생성하는 것으로 알려졌다 .33) 코발트-아실착 33) R. W. Joh nson and R. G. Pearson, Inorg, Chem. 10, 2091(1971 )
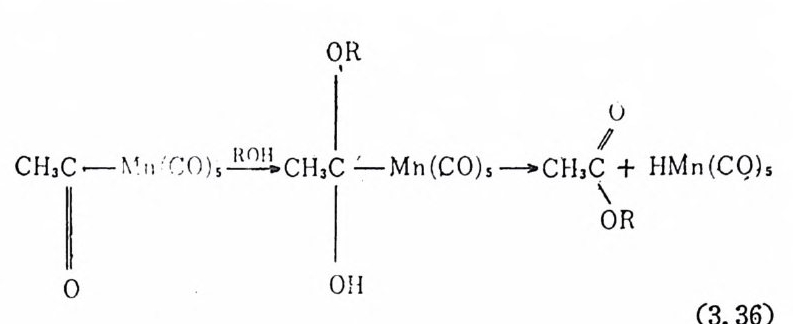 oR ,c
oR ,c
로물 (추Co측C\된C 2다H5.( CO마)지a)막 도 단비계 슷인한 O과H정 로 을부 터거 쳐뭄 에속 스으테로 르 수를소 가형 성전 할달 되것 는으 과정 은 전아 금속-알킬착물이 쉽 게 일으키 는 베 타수소전달반응(제 1 장 4 의 (2) )과 비슷한 반응이다. 팔라듐착물촉매를 사용하는 올레핀의 카르복시화반응에 관하여서 는 찰 정립되지는 않았지만 두 개의 제시된 메카니즘이 있다. 첫째로, HCo(C0)4 를 촉매로 사용하는 경우와 바슷하게 팔라듐 수소화합물이 생성되어 순환과정이 일어나는 메카니즘을들수있다. 즉 PdCl z( P(C6H5)3)2/SnC12 촉매계는 식 (3. 37) 과 같은 반응에서 Pd- H 과 치환반응성이 큰 SnCl3- 를 생성하여 촉매반응을 일으키는 것 으로 추측된다. 32) 비 슷한 예 로서 는 올레 핀의 수소화반응에 촉매 적 활성 을 보여 주는 H2PtC l6/SnCI2 계 를 들 수 있 다. 34) 치 환반응성이 큰 SnC13- 리간드는 다론 리간.E.에게 쉽게 배위자리를 내어줄 분만 아니라 Pd-H 에 올레핀이 삽입되는 방향을 결정하여 주는 것으로 추축된다. 왜 냐하면 SnCI3-에 의 해서 線型에 스데 르와 가지 탈린 에 스테르의 비율이 달라지기 때문이다 .32)
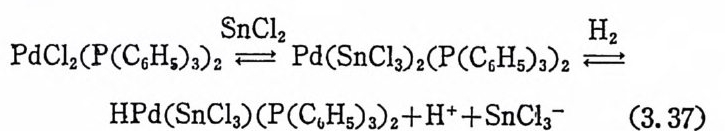 SnCl2 H2
SnCl2 H2
34) G. W. Parshall, J. Am. Chem. Soc. , 94, 얽 16 (lrfl 2).
둘째 로 SnCl2 를 포함하지 않는 팔 라듐촉매 계 에 의 한 촉매 작용의 반응메카니즘을 들 수 있다. SnCl2 가 존재하지 않는 경우에는 가지 탈린 에스데르가 주로 얻어진다 .31) 석 (3.38) 에서 보여 주는 바와같 이 산 (HCI) 이 보조촉매 (coca t al y s t)로 작용한다. PdClz (P( C5Hs)3)2 는 먼처 알코올과 반응하여 치 환반응성 이 높은(l ab i le) 알콕시 착물 PdCI (OR)(P(C6Hs)3)2 를 생성한다. 이어서 co 가 첨가배위되고 배위된 c(Po(C 가6H 5P)d3) 一2 0를 결 형합 성에 한 다삽.입 (되실어제 로카 P르d보— 알CO콕O시 C H착3 단물위 P가d C확I인(-C된O 바O R있) 다 .35)) 푸로필렌이 다시 Pd 一 C 결합에 삽입되어, 트리페닐포스핀과 같CO이O R커 단다위란를 리 형간성드하가게 팔 라된듐다. 주 생위에성 된있 으(므P(로C6,H 5P)3d)-2CCHIP2dC—H C(CH2H C3H) (CH3)COOR 이 베타수소제거반응을 일으키기 전에 산 (HCl) 이 Pd- C
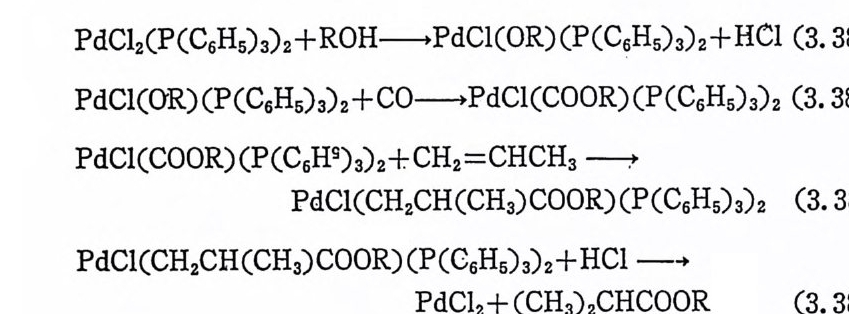 PdCl2(P(C5H 야 )2 + ROH 一 PdCl(OR) (P(C6H5)3) 2+ HCl (3. 38a)
PdCl2(P(C5H 야 )2 + ROH 一 PdCl(OR) (P(C6H5)3) 2+ HCl (3. 38a)
결합을 끊는다. 이 마지막 단계에서 생성물 이소부털산 알킬 (alk y ~ i sobu ty ra t e) 이 얻 어 지 며 촉매 PdCli( P( C5Hs)3)2 가 되 돌려 진다. 만일 베 타수소제 거 반응이 일어 나면 , 메 타크릴산 에 스테 르 (me t hacr y la te: es t er) 가 생 성 되 고 촉매 는 금속 팔라듐 또는 Pd(O) 착물로 된다. 4. 탈카르보닐화反應 (decarbon y la ti on) 탈카르보닐화반응은 그리 많이 응용되는 반응은 아니지만 실험실 에서 복잡한 화합물을 합성하는 데 쓰여지고 있다. 탈카르보닐화반
35) F. Riv e tt i and U. Romano, J. Orga nomet. Chem. 154, 323(1 9 78).
응은 스테로이드 (s t ero i d) 분자로부터 포르밀기를 제거하는 데 옹용되 기도 한다. 알데히드 및 영화아실분만 아니라 無水酸, 케돈 및 케텐 들의 탈카르보닐화반응이 연구, 보고되어 왔다. 알데히드 또는 영 화아실의 탈카르보널화반응은 일반적으로 끓는 접이 높은 용매에서 금속착물과 함께 가열함으로써 일으킬 수 있다. W il k i nson 촉매 RhCI(P(C6H 야 )3 는 가장 활성이 큰 탈카르보닐반응제이다. 이 Rh CI) 착물은 낮은 온도에서도 유기화합물로부터 CO 를 제거하는 반 옹을 일으킨다(식 (3. 39) 참조). 3G) 석 (3. 39) 반응은 촉매 순환과정 이 아 니고 단순한 화학량론적 반응이다. 이렇게 낮은 온도에서는 생성되
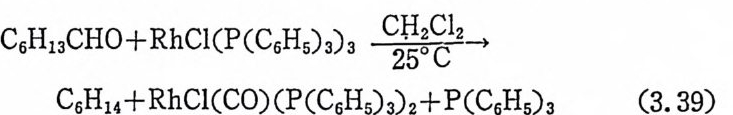 C6H13CHO+RhCl(P(C6H 晶 텔움一
C6H13CHO+RhCl(P(C6H 晶 텔움一
는 로듐-카르보닐착물이 안정하다. 그러나 높은 . 온도에서는 CO 가 유리되며 탈카르보닐화반응이 촉매순환과정이 된다 .36) (식 (3.40) 참조). 탈카르보닐화반응의 촉매로서도 공기 중에서 비교적 안정한
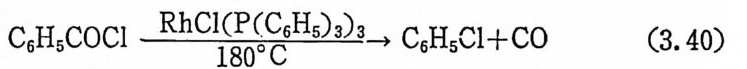 C5HsCOCI ~:얽助 )3 一 C6H&l+co (3.40)
C5HsCOCI ~:얽助 )3 一 C6H&l+co (3.40)
RhCl(CO) (P(C 晶 )3 記] W flki n s on 촉매 만큼 효과적 일 분 아니 라 취 급하기에도 편리하다. 높은 온도를 유지할 필요가 있을 경우에는 P(C5H5)3 대 신 킬레 이 트 리 간드인 (C5Hs)2PCH2CH2P(C5Hs)2 를 포 함하는 Rh(!) 착물을 촉매로 사용할 수도.있다 .3 7) 방향족 알데히드둥의 탈카르보닐화반응은 바교적 좋은 수율로 전 행되지만 지방족 유도체의 탈카르보널화반응은 좀더 복잡하다. 가 끔 영화알킬 이의에도 올레펀 둥이 얻어처기도 하며 알킬기의 이성 질화 반응도 일어난다. 예를 들면 식 (3.41) 에서 보는 바와 같이 영 화팔미 토일 (pa lmi toy l chlor i de) 의 탈카르보널화반응은 올레 편, 영 화 알킬 및 영화아실 등의 이성질체등을 생성한다 .38)
36) K. Ohno and J. Tsuji , J. Am. Chem. Soc. , 90, 99(1968). 37) D. H. Doug ht y and H. Pig n olet, J. Am. Chem. Soc. , 100, 7083(1(5 18 ). 38) T. A. Fog lia, P. A. Barr and M. J. Idacavage , J. Org. Chem. , 41, 3452 (1(516 ).
CHaCCH2)14COCl ~- CH3(CH2) l2CH = CH2 + c16H31Cl + c15H31C0 인 (3.41) C 이성질체들) C 이성질체들)(이성질체言)
일반적으로 제시되어온 탈카르보닐화반응에 관한 메카니즘은 식 (3. 42) 로 표현된다. 식 (3. 42) 는 W ilk in s on 촉매 (RhCl(P(C6H5)3)3) 와 RhCl(CO)(P(CsHs)a)2 중 어느 착물을 촉매로 사용하여도 적용 되는 석이다. 최초의 반응단계는 알데히드나 영화아실 화합물이 산 화성첨가반응에 의하여 로듐(I?}물에 첨가되는과정이다. 영화아 실 화합물의 산화성첨가반응 생성물은 5 배위 아실로듐 cm) 착물로 서 가끔 분리, 확인되기도 하였다 .39) 그러나 알데히드의 첨가생성 물은 비교적 불안정하여서 곧 다음 단계의 반응을 일으킨다. 다음 단계는 산화성첨가생성물, 아실-로듐 cm) 으로부터 co 가 제거되고 알킬-로듐(또는 아린 Car y l) -로듐)이 생성된다. 이 단계는 co 의 삽 입반응의 역반웅이라고 볼 수 있으며, 정확히는 알킬기가 CO 로부 터 로듐으로 이 동되 는 〈알킬이 동 (alk y l m ig ra ti on) 〉반응이 다. 마지 막 단계 는 환원성 제 거 반응으로 RX 와 R.hC l(CO) (P(CsHs)a)2 가 생 성 되 는 과정이다. 처온에서 RhCl(CO)(PCCsHs)3)2 는 안정하여 더 이상 의 반응이 진행되지 않지만, 고온에서 RhCl(CO)(P(C6H6)3)2 는 CO 를 내어 놓고 RhCl(P(C6Hs)s)2 가 되어 탈카르보닐화반응의 촉매순 환과정을 일으킨다.
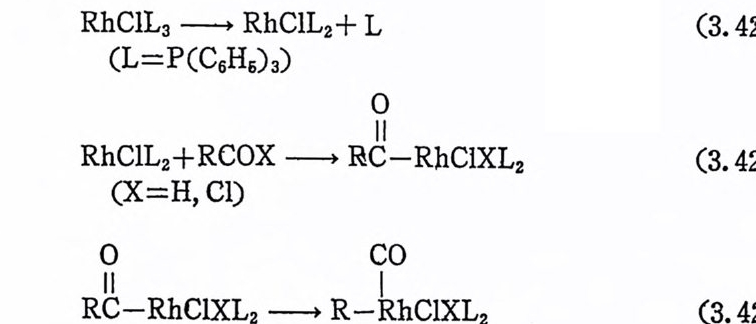 RhClL3 一 RhClL2+ L (3.42a)
RhClL3 一 RhClL2+ L (3.42a)
39) J. K. Sti lle , et al, J. Am. Chem. Soc. , 96, 1508, 1514, 1518(1974) and 99, 5663(1977).
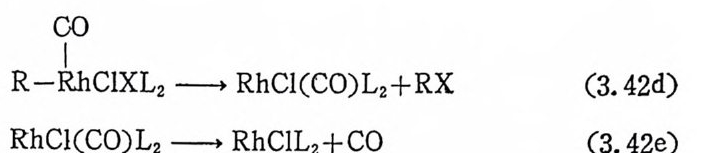 안
안
*참고 문현 1) I. Wender and P. Pin o , Edit . , Orga nic Sy n th e sis via Meta l Car- bony l, Inte r scie n ce Pub!. , New York, 1976, Vol. 2. 2) L. Mark'o, Hy d rofo r my la ti on of Dlefi ns wi th Carbony l Deriv a tl - ves of Noble Meta l s as Cata l ys t s , • in: R. Ug o , Edit . , Asp ec ts of Homog en e011s Cata l ys i s , D. Reid e l Pub!. , Dordrecht, Holland, 1974, vol. 2. 3) F. G. A. Sto n e and R. West, Edit . , Advances in Org a nometa l lic Chemi st r y , vol. 17, Cata l ys i s and Org a nic Sy n th e ses, Academi c Press, 1979. 4) G. W. Parshall, Homog e neous Cata l ys i s , Wi le y -l nte r scie n ce 1980. 5} G. Henric i-O liv e /Ol ive Coordin a ti on and Cata l ys i s (Monog ra p h s in Modern Chemi st r y Serles, Verlag Chemi e- Wein h eim , ) New York, 1977.
제 4 장 二室素 (d i n it ro g en, N2) 의 · 活性化 일반적으로 질소분자는 불활성(i ner t)으로 알려져왔다. 질소분자 {이질소, d i n it rog en 이라고도 불리운다)의 해리에너지는 225Kcal/ mole 로 매우 안정한 분자이다. 히드라진에서 질소-질소의 단일걷 합에너지는 38Kca l/ mole 이며 아조 (azo) 화합물에서 질소一질소의 이 중결합에 너 지 는 98Kcal/ mo le 밖에 되 지 않는다. 죽 이 중결합을 갖는 아조화합물에서부터 삼중결합을 갖는 N2 로 변함에 따라 질소 -질소결합에너지는 커다란 증가를 보여준다. N2 로부터 직접적으 로 질소화합물을 얻기가 그리 쉽지 않다는 사실은 이상과 같이 질 소분자가 득히 안정하기 때문인 것으로 생각된다. 자연계에서 질 소고정 효소에 의한 N2 의 활성화가 상온, 상압하에서 쉽게 이루어 지고 있음은 찰 알려진 사실이냐 그러나 실제 공장에서는 고온과 고압하에서 N2 의 활성화불 일으키고 있다 .• 공업적으로는 300~600°C 및 수백 기 압의 질소 (N2) 와 수소 CH2), 그리 고 촉매 둥이 필요한 공정 (Haber-Bosch p rocess) 에 의 해 서 N2 가 암모니아로고정된다. 그러나땅속에 살고 있는 미생물은공기 중의 N2 를 쉽게 암모니아로 전환시키고, 직접, 간접적으로 식물 내에서 이루어지는 단백질 합성에 질소를 공급하고 활성화시킨다. 이렇게 자연계에서 의해 이루어지는 질소고정은 아마도 공업적으로 생산되 는 비료보다 더욱 중요하게 식물성장에 영향을 미칠 것이디 많은 연구자들이 미생물에 의해서 이질소 (d i n itr o g en) 가 고정되고 환원되
는 메카니즘을 연구하고 있다. 특 히 생화학자들은 생물계로부터 질 소고정효소 (n it ro g enase) 를 분리하여 많은 연구결과를 얻고 있다. 이 계까지 알려진 바에 의하면 질소고정의 기능을 갖고 있는 自然系 (natu ral s y s t em) 는 항상 전이 금속, 득히 철과 몰리 브덴을 포함하고 있다. 따라서 이돌 전이금속이 질소고정과 질소환원에 직접적으로 어떤 역할을 하는 것으로 알려져 있다. 한편화학자들은지난 15 여 년 동안 전이금속착물을 이용하는 질소고정을 연구하여 왔다. 전이 금속 착물에 의한 질소고정에 관한 연구는 다음과 같은 접에서 그 의의를 가지고 있다. 죽 이상의 연구결과로부터 자연계에서 이루어 지는질소고정의 순환과정을이해하는데 도움을얻고자할분만아니 라 비교적 경제적으로 유리한 반응조전 (Haber 공정의 온도와 압력 보다 훨씬 낮은 온도와 압력)에서 질소화합물을 얻을 수 있는 공정 개발에 그 목적이 있다. N2 로부터 질소화합물을 얻는 공업적 촉 매순환과정을 개발하려면 아직 많은 문제들이 해결되어야 한다. 그 러나 몇몇의 연구는 상당한 결과를 가져왔다. 제 4 장에서는 먼처 자연계에서 일어나는 생물학적 二室 素 의 活性 化를 살펴보고 이어서 전이금속착물을 이용하는화학적 二盜素의 活 性{t를 다룰 것이다. I. 생 물학적 (미 생 물에 의 한) 二室素의 活性化 미생물에 의한 생물학적 질소고정은 (1) 질소를 고정하는 미생물 의 종류, (2) 질소고정의 생성물, (3) 질소고정에 필요한 조건 및 (4) 질소고정의 반응메카니즘 둥의 4 부분으로 나뉘어 설명된다. (1) 질소를 고정하는 미생물의 종류 생물학적 질소고정운 자유롭게 사는 박테리 아(fr ee livi n g bacte r ia ) , 共生 박테 리 아 (s y mb i o ti c bacte r ia ) , 光合成울 하는· 靑綠菜類 (Pho t os y n th eti c blue-gr e en alga e) 및 光合成울 하는 미 생 물(p ho t os y n t he ti c mi cr oorga n is m s) 동 4 가지 종류의 미 생 물계 에 의 해 서 이 루어 전 다.
이 상 의 4 부류는 다시 好氣性 (a e r o b i c) 과 無酸素 性 (anaerob i c) 계 로 나누어 질 수 있다. 자유 롭 게 사는 박테 리 아(fr e e livi n g bac t er i a) 로서 질소고정 하는 미 생 물 중 에 서 無酸素性 박테 리 아로는 Clostr i d i u m pa ste uria n um 을 들 수 있다. 이 박 태리아는 흙 , 담수 및 해수에서 발견된다. 자유롭게 사는 박테 리 아 중에 서 好 氣性 박테 라아로는 Azobacte r ag ilis 와 Azobacte r Chroococcum 이 있 다. 이 박테 리 아들도 흙 이 나 물 에 서 발견되 고 있 다. 특히 이 Azobacte r 종류들은 酸度 가 높은 조건에 서 찰 성장한다. 共生 박 테 리 아 또는 혹 (nodule) 박테 리 아라고 불리 우는 Rhiz o biu m 이 콩과식물의 혹에서 발견되었다. Rh i zob i um 의 질소고정 효율 은 식물의 성장여전 및 박테리아의 주위환경 동여러가지 조건에 따 타 변하게 된다. 적철한 조건에서 질소고정은 共生 S9(s y mb i o ti c) 으 로 일어 난다. 죽 식 물은 박테 리 아의 신전대 사 (me t abo li sm) 에 필요한 탄소 를 공급하며, 박테리아는 석물에게 질소를 공급한다. 이와 같 온 공생관계가 없이는 질소고정이 일어나지 못한다. 식물과 박태리 아는 각각 단독적으로 질소를 고정하지 못한다` 콩과석물의 혹이 쪼 개지든지 찌그러지면 질소고정의 효율은 급격히 감소된다. 대부분 의 이러한 共生 系 가 콩과석물의 혹에서 발견되었지만, 콩과석물이 아닌 뿌리혹에서도 발견된 바 있다.1) 光合成울 하는 靑綠 溪 類(p ho t os yn t he ti c blue-gr e en alga e) 중에 서 Anabaena, Tolyp o th rix 등은 질소고정 을 하는 것 으로 밝혀 졌 다. 이 상의 共生 박테리 아와 光合成울 하는 박테 리 아는 모두 好氣性 ` 박테리아이다. 光合成울 하는 미 생 물 중에 서 Rhodospi ri l lum rubrum, 2> Chroma- tium 3> 그리 고 Rhodop s eudomonas pa lustr is3> 둥은 질소고정 을 하는 박테리아로 밝혀졌다. 1) G. Bond, Natu r e, 204, 600(1 9 64). 2) H. Gest and M. D. Kamen, Sci en ce, 109, 558(1 9 49). 3) (1D9. 6I1. ).A mon, M. Losada, M. Nozak i and K. Taga w a, Natu r e, 190, 601
(2) 질소고정의 생성물 식 (4. 1) 은 질소고정 과정 의 가정 적 (假定的)인 중간체 (int e r media t e ) 들을 포함하는 Burr i s4) 의 가정 이 다. 식 (4.1) 에 서 보여 주는 여 러 중 간체 및 암모니아에 관한 확실한 실험적 증거는 없다.
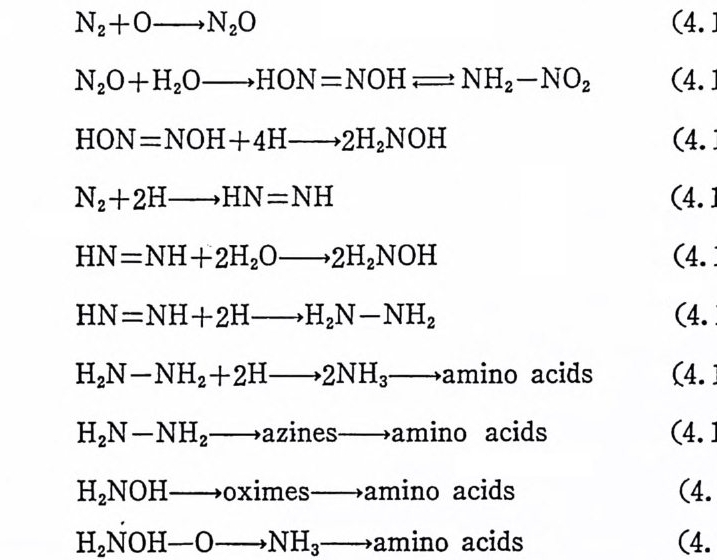 N2+0 一 N20 (4.la)
N2+0 一 N20 (4.la)
암모니아를 거치는 질소고정 경로에서 암모니아와 글루탐산 (glu ta m i c a ci d) 은 중요한 생 성 물이 된다. 이 과정 은 주로 Azoto bac- ter , Rhodosp iri l lum rubrum 및 Clostr i d i u m 둥의 미 생 물에 의 해 서 일어난다고제시되어 오고 있다 .4) 好氣性 Azo t obac t er 에 의해서 암모니 아는 글루트아민(g lu t am i ne) 으로 바뀌고 글루트아민은 가수분 해에 의해서 글루탐산이 생성되는 것으로 추측되고 있다. 또한 Azoto bacte r 의 분비 물에 서 알파-옥소숙신산 (a-oxosuc ci n i c a qi d) 의 옥십 (ox i me) 이 발견되었다는 사실(베타-알라닌(/3 -alan i ne) 및 아스과르트산 (as p ar ti c ac i d) 도 함께 발견되었다 .)5) 로부터 히드록 실아민 (h y drox y lam i ne) 도 질소고정 과정 의 중간체 가 될 것 이 라고 제
4) R.H. Bur.llis , Inorga nic Ni tro g e n Meta b oli sm. W.D. McE!roy and B. Glass, Ed. , p. 316, Joh ns H,o pk in s Press, 1956. 5) A. I. Vir tan en, A. ,Kemp pii, and E. L. Salmenoja , Acta Chem. Scand. 8, 1729(1954).
시되고 있다. 옥십은 최종적으로 효소에 의해서 아미노산으로 환원 된다. (식 (4.Ii) ). 식물 흑의 분비물에서 글루탐산이 발견되었기 때 문에 히 드록실 아민은 주로 암모니 아로 환원되 고, 암모니 아는 알파一 케 토글루타르산 (rx-ke t o g lu t ar i c ac i d) 와 축함반웅을 일으켜 글루탐산 (glu ta m i c a ci d) 이 생성되는 메카니즘이 제시되었다(식 (4.lg) ). 또 하나의 질소고정 경로는 N2 의 산화에 의해서 산화 이질소 (din i t ro g en oxid e 또는 nit ro us oxid e 라고도 불리 운다)가 생 성 되 는 과정 이 다. 생 성 된 산화 이 질소 (N20) 는 수화반응 (h y dr~ ti on) 을 일으켜 하 이포아질산 (H2 沿아, hy po nit ro us ac i d) 이 되고 하이포아질산은 히드 록실 아민으로 환원되 어 (4. le) 욱십 (4. l i)이 나 암모니 아 (4.l j)를 거 쳐 최종적으로 아미노산이 된다. 이상과같은 N2 의 산화생성물 N20 를 거쳐 일어나는 질소고정은 N2 의 환원생성물 HN=NH 를 거쳐 일어나는 과정에 바교하여 매우 적은 양에 불과하다. 실제로 Azo- t obac t er 를 이용한 l6N2 설험에서 질소 (15N) 산화물은 발견되지 않 았다 .G) Mckee 에 의하면 질소고정을 하는 미생물이 질소산화물을 포함하고 있는 것은 질소고정 이외의 다른 신전대사 과정앤서 생성 된 부산물에 의 한 것 으로 추측된다. 7) 환원과정 을 거 쳐 일어 나는 질소고정 은 또한 디 이 미 드 (d ii m i de, HN =NH) 및 히드라전 (h y draz i ne, H2N-NH2) 을 거쳐서도 일어나는 것으 로 추측된다. 중간체인 디이미드는 매우 불안정하여 쉽게 히드라진 으로 환원되는 것이 제시되어 오고 있다. lSN 동위원소를 이용한 실험 에 서 Azoto b acte r 에 의 해 서 히 드라전이 세 종류의 아전 (az i ne) 으로바뀌는것이 발견되었다 .8) 그중하나의 아진은히드라전과알 과-케도글루타르산 (cr-ke t o g lu t ar i c a ci d) 의 축합반응으로부터 얻을 수 있는 2H, · 4H,5H-3- 옥소피리다진 -6- 카르복시산(아태 그림)이다. 분만 아니라 히드라전을 가하지 않아도 Azo t obac t er 는 질소를 고정하여 상기한 아전(아태 그립)을 만들어 내는 것이 밝혀졌다. 실제로 히드 타전의 · 농도가 2X10-5M 이상이면 질소고정이 억제되지만 히드라
6) R. M. Alliso n and R. H. Burris, J. Bio l. Chem. , 224; 351(1957). 7) H. S. Mckee, Ni tro g e n Meta b oli sm in Plaf! IS , Oxfo r d Univ . Press, 1962. 8) M. K. Bach, Bio c lt im. Bio p h y s . Acta , 26, 104(1957)_- • ·.9) A. B. Azim and E. R. Roberts , Bio c lt im. Bio p h ys . Acta , 211, 308(1 9 56).
 H2c /[\N H
H2c /[\N H
진의 농도가 낮으면 질소고정은 촉전됨이 밝혀졌다 .9) (3) 질소고정에 필요한 조건 1) 질소고정 에 필요한 전자 질소고정이 환원적 경로를 거쳐서 일어난다면 환원에 필요한 전 자는 어 디 로부터 공급되 는가 ? Hardy 둥에 의 하면 질소고정 에 팔 요한 전자는 피루부산 이온(py ruva t e) 에 의해서 공급된다 .10) 질소고 정에는 피루부산 이온과 같은 전자주게도 필요하지만 전자를 운반 하는 fe rredox i n( 철을 함유하는 효소)과 같은 전자운반체 (electr o n carr i er) 도 필요하다. 2) 질소고정에 필요한 금속이온 미생물에 의한 질소고정은 미량의 금속이온에 의해서 영향을 받 · 는다. 질소고정에 직접적으로 영향을 주는 금속들은 몰리브밴(血, V), 텅스텐(血, v) 철 (II 』 I) 및 칼슘 CII) 으로 알려져 있다. 코발 트 CII), 망간 CII) 및 구리 CII) 도 또한 어느 정도 질소고정에 관련 이 있는 것으로 알려졌다. Aro t obac t er 세포로부터 많은 몰리브벤 이 포함되어 있는 단백질이 분리된 바 있으나 단백질 중의 몰리브. 벤의 산화상태 (oxid a ti on st a t e) 는 아직 분명 히 밝혀 져 있지 않다. 단 지 , 추출물의 EPR(electr o n pa ramag n eti c resonance) 스펙 트럼 데 이 타로
10) R.W.F. Hardy , E. Knig h t, Jr. , and A.J. D'Eusta c hio , Bio c lte m . Bio p h ys . Res. Comm11n. , 23, 409(1 9 66).
부터 몰리브덴 cm) 및 몰리브덴 (V) 이온이 Azo t obac t er 에 촌재하 리 라고 제 시 된 바 있 다. 11> Azoto bacte r 중의 몰리 브밴은 텅 스텐으 로 치환될 수 있다. 그러나 질소고정에서 텅스텐의 역할은 밝혀 지지 않고 있다. 오늘날까지 알려 진 여 러 好 氣 性 (aerob i c), 無 酸 素 性 (anaerob i c), 光 合成울 하는 (Pho t os y n t he ti c), 그리 고 共生 (s y mb i o tic) 미 생 물에 의 한 질소고정 신전대사에서 철은 필수적인 금속으로 알려지고 있다. 非 헴 類 (non-heme) 의 철 단백 질 (iro n-pr o te i n ) , fer redoxin 은 주로 상기 한 미 생 물들에 의 한 질소고정 메 카니 즘에 서 전자운반체 (electr on carr i er) 의 역 할을 한다. 콩과식 물 혹에 있는 붉은색 소에 헤 모글로빈 이 존재 하며 , 해 모글로반이 콩과석 물의 뿌리 혹박테 리 아 (Rh i zob i a) 의 질소고정과 관계가 있음이 여러 연구보고에서 제시된 바 있다. 칼슘 C II )은 Azoto b acte r 에 의 한 질소고정 에 필수적 인 금속으로. 알려져 있다. 칼슘 (II) 은 질소고정에 동반되는 ATP 합성과정에 영 향을 주는 것으로 추측된다. 질소고정에 칼숭 (II) 이 필요한것은사 실이지만 그 구체적인 역할은 아직 알려져 있지 않다. 코발트 (II), 구리 CII), 칼슘 (II) 및 망간 (II) 동 여러 금속이 질 소고정을 하는 미생물의 신전대사와 관련이 있는 것으로 알려지고 있으나 이들 금속이 어떻게 질소고정의 메카니즘에 참여하는지는 알 려쳐 있지 않다. 3) 이 질소 (d i n it ro g en) 농도의 영 향 질소 (N 기의 농도가 질소고정 의 속도에 미 치 는 영 향은 M ich aeli s- Mento n 의 식 (식 (4. 2) )으로 표현된다. 여 기 서 k 는 질소고정 의 속도 상수이 고, k(max) 는 질소고정 의 最 大속도상수이 며 , PN2 는 질소의 왕력 , 그리 고. KM 은 M ich aeli s 의 상수이 다. 상수 KM 은 1/k 와 1/PN 2 를 도시 하여 철편 (1/k(max)) 과 기 울기 (KM/k(max) )로부터 구한다. KM 은 일 반적 으로 압력 단위 (a t m) 로 표시 되 며 , 이 질소착물 (d i n itr o g en -co mp le x) (질소고정 효소 (n it ro g enase) 가 이 질소착물을 형 성 한다는 가
11) D.J. l; l. Nic h olas, D.J. Fis c her, W.J. Redmond, and W.A. Wrig h t, J. Gen. Mi cr obio l. , 22, 191(1 9 60).
정을 하면)의 해리상수와 같게 된다.
![]() 1/k= l/k(m ax) +Kn/[k(max) 氏] (4.2)
1/k= l/k(m ax) +Kn/[k(max) 氏] (4.2)
여 러 질소고정 미 생 물에 관한 Kn 값은 0. 02~0. 03 기 압 (r it m) 으로 . 알려져 있다. 4) 산소의 영향 산소는 無酸素性 박태 리 아 Clo~rid i u m pa ste uria n iu m 의 수소 화효소 (h y drog enase) 活性度률 완전히 파괴 한다. 好氣性 박테 리 아 Azo t obac t er 도 세포의 성장에 산소가 필요하지만 질소고정에는 팔요하지 않다. 결제 Azoto b acte r 는 clostr idi u m pa ste u ria n iu m - 으로부터 추출된 수소화효소와 전자운반체 인 fer redoxin 그리 고 . APT 의 供給源만 있으면 산소 없이도 질소고정의 기능을 보인 다• 5) 수소 압력의 영향 Azoto bacte r 에 의 한 질소고정 (clostr i d i u m p as t eur i an i um 으로부터 얻 온 수소화효소 및 fer redoxin 이 共存하여 얻 어 지 는)에 서 수소는 전 자주게 (electr o n donor) 의 역 할울 한다. 수소는 또한 clostr i d i u m pa s-· teu ri an iu m 系위 질소고정 (ATP 의 供給源이 共存하여 얻어지는)에 서도 전자주게의 역할을 한다. 수소분자는 질소고정을 여제한다고 발표된 적이 있었다 .12) 그러나 이상의 사실로 보아서 수소는 질소 . 고정에 억제작용을 하지 않을 것으로 추측된다. 好氣性, 無酸素性, 共生性 또는 光合成性 미생물 등 대부분의 질소고정系들은 질소고 정에 필요한님것으로 추측되는 전자를 供給하는 수소화효소 (h y dro g e· nase) 를 포함하고 있다. 질소가 촌재하지’ 않으면 피루브산 이온 (py ruva t e) 과 같은 기 질 (sub st ra t e) 로부터 얻어지는 전자들은 光合成 ~ 性박태리아에 의해서 수소의 光活性에 쓰여전다. 그러나질소가촌. . 재하면 光合成性 박테리아의 기능은 여제되고 수소화효소로부터 얻 어지는 전자는 질소고정에 쓰여진다.
12) A.L. Shug , P.W. Wi lso n, D.E. Green, and H.R. Mahore, /. Am_ Chem. Soc. , 76, 3355(1 9 54).
(4) 질소고정의 메카니즘 1) 共生系 (s y mb i o ti c sys te m s) 共生박테리아系에 의한 질소고정의 메카니즘은 Hoch 둥에 의해서 제 시 되 었 다. (식 (4_. 3), (4. 4) 및 (4. 5))13) 식 (4. 3) 은 수소화효소의 경로이고, 석 (4.4) 및 식 (4.5) 는 질소고정효소에 의한 경로이다. 이상의 효소들의 본질에 관하여서는 극히 일부가 알려져 있다. 이 효소들은 양성자 또는 질소분자를 잡을 수 있는 자리 (s it e) 를 갖고 있는 것으로알려쳐 있다. 이들 효소들은 두개의 전자를 두개의 양 성자에게 전달함으로써 H2 를 발생시키거나 또는 질소를 환원시킬 수 있다. 식 (4.5) 에 의하면 효소는 일산화탄소와 반응하여 카르보 닐-효소 착물을 형성하여 효소의 질소고정기능을 저해시킨다. 산 화이질소 CN20) 도 효소와 착물을 형성하여 효소의 기능울 여제시키 지만 효소 -N20 착물은 식 (4.3) 에 의해서 생성되는 수소원자에 의 해서 이질소 CN2) 착물로 환원되기도 한다(식 (4.5b) 참조).
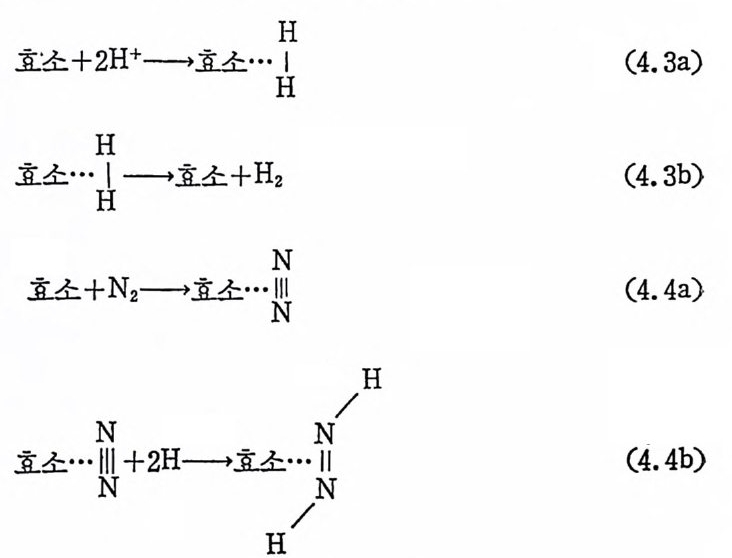 H
H
13) G. E. Hoch and R. H.. Durris , Natu r e, 179, 430(1 9 57) and Bio c h im. Bio p h ys . Acta , 37, 273(1 9 60).
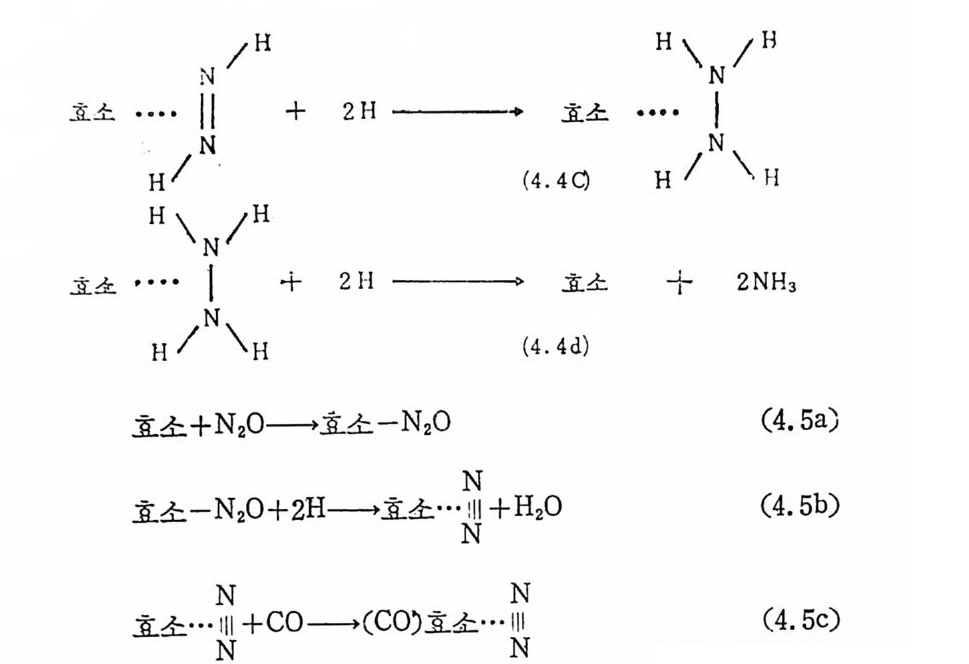 /HIH\H H\.H//H\ H
/HIH\H H\.H//H\ H
2) 자유롭게 사는 박테리 아(fr ee- li v i n g bac t er i a) (無酸素性系 ( anae robic sy st e ms)) 그림 4.1 은 無酸素性系에 의한 질소고정의 일반적인 메카니즘을 보여 준다. w fer redoxin 의 환원에 필요한 전자는 피루브산 이 온 (py ruva t e) 을 공급하며 , 환원제 ATP 와 二價금속 양이 온 Mg ( Il )이 필수적 이 다. 환원된 fer redoxin 으로부터 수소화효소 또는 질소고정 효소로 전자가 전달되는 과정은 아직 자세히 연구되지 못하였다. 질 소가없는 조건에서는 수소화효소에 의해서 수소가 발생된다 CA 강 로). 그러나 질소고정이 계속해서 일어나는 동안이라도 수소화효소 에 의한 수소발생은계속 일어난다. 죽양성자는한원된 효소로부터 얻을 수 있는 전자를 제법 경쟁적으로 취하여 수소를 발생시킨다. Burris 에 의 하면 질소분자가 암모니 아로 환원되는 각 단계 에 서 fer redoxin 과 ATP 가 필요할 분만 아니 라 각 환원단계 에 서 질소
14) R. H. Burris, An11u. Rev. Plant. Phy si o l. 17, 155(1966)
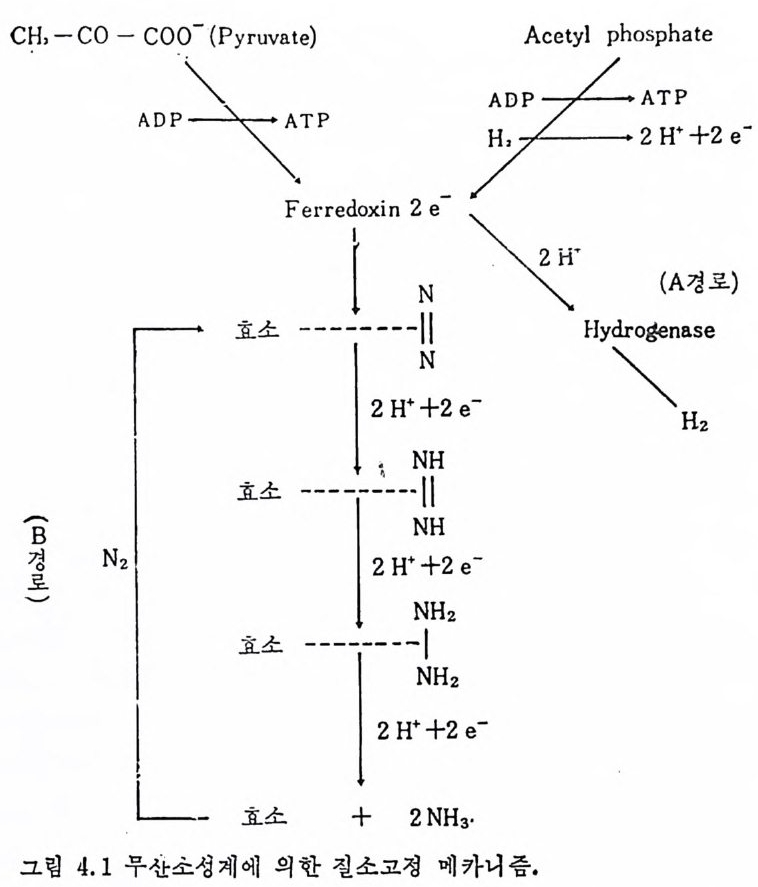 CH, -C O 一 ACODO-P(P ~y ru •vTate P) • _ 3 二Acety l ph oAsTp H h 「 a +te2 e-
CH, -C O 一 ACODO-P(P ~y ru •vTate P) • _ 3 二Acety l ph oAsTp H h 「 a +te2 e-
화합물 중간체들은 항상 효소에 결합되어 있다(그립 4.1 침조). 이상 과 같은 제시는 다음과 같은 실험적 발견에 근거를 두고 있다. 죽 15N2 를 사용하여 실험한 결과 결합되지 않은 15N 를 포함하는 중간 체들이 발견되지 않았으며 ,14) 효소존재하에 동위원소 상호교환반 옹 (14N2+1sN2.:=214Nl5N) 도 일어나지 않는 것으로 밝혀졌다 .15) 질 소고정효소중에 질소를 결합하는 효소자리와 질소고정 반응 활성화 에 관련된 금속이온에 관하여서는 아직 밝혀지지 않은것들이 많다. 질소고정효소의 활성화자리는 이웃하는 두 개의 금속이온일 것으로 15) R. W. F. Hardy and E. Knig h t, Jr. , in Prog re ss in Photb c hemi st ,- y, L. Rein h old, Ed. , p, 387 Wi ley , 1967.
추측되며, 이 두금속은 두개의 몰 리브덴 또는 몰 리브 ti l 과철, 또는 두 개의 철이온으로 추 측 되고 있다. 이 렇 게 두 개의 금속이온이 적 은 분자들을 활성화시키는 예는 이미 알려쳐 있다. 예를 들면 산소 분자는 두 개 의 구리 이 온을 갖고 있 놈 hemocy a nin ( Cu( I )과 Cu( II ) 자리를 갖고 있음) 및 두 개의 철이온을 갖고 있는 hemeryt hr in (두개의 Fe(II) 자리를 갖고 있음)에 의해서 활 성화되며, 이웃하는 두 개 의 Cu( I )자리 를 갖는 합성 된 착물이 수소분자를 활성 화시 킵 온 알려진 사실이다 .16) 3) 자유롭게 사는 박테 리 아(好氣性系 (aerob i c sys t e m s) Hardy 둥은 몰리브덴과 철을 비교적 많이 포함하고 있는 질소고 정 효소인 호기 성 박테 리 아 Azot o bacte r vi ne landii 를 분리 한 바 있 다. 17) Burns 둥은 또한 fer redoxin 과 수소화효소를 공급하는 無 酸 素性 박테 리 아 Clostr i d i u m pa ste u ria n um 이 질소고정 에 필수적 임 울 이미 발표한 바 있다 .18) Hard y등은 이상의 두 박테리 아(호기성 Azot ob acte r vin e landii 및 무산소성 Clostr i d i u m p as t eu ri anum) 에 대한 질소고정을 자세히 연구, 보고하였다 .19),20) 이상의 연구에서 밝혀진 바에 의하면 박테리아 추출물은 질소분 아니라 아지드화 이 온 (N3-), 산화이 질소 CN20), 시 안화산 (HCN), 알킬니 트릴 (RCN), 및 아세틸렌과 그 동족체 (homolo g) 둥을 환원시킨다(식 (4.6) 참조).
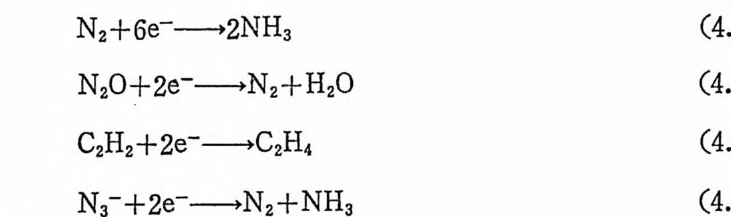 N2+6e 一 --+2NH3 (4.6a)
N2+6e 一 --+2NH3 (4.6a)
16) J. P. Collman, Accounts Chem. Res. , 1, 136(1 9 68). 17) R.C. Burns, R.D. Holste n , and R.W.F. Hardy, Bio c hem. Bi op h ys . Res. 18C) oWm.m Au.n .B , u3ie 9n, , 9R0(.1 C9. 7 0B).u rns, • and J. R. Leconte , Bio c lzem. Bio p h ys . Res. 19C) oRm.mWu.nF. ., H17a,r d2y6, 5(E19.K64n)i.g h t, Jr. , andA.J. D'Eusta c hio , Bi oc hem, Bi op h ys . Res. Commun. 23, 409(1966). 20) R. W. F. Hardy , E. Knig h t, Jr. , and E. K. Jac kson, Sci 1!11 ce 157, 110. (1967).
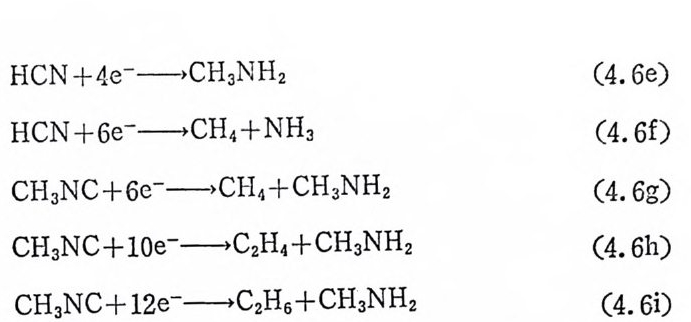 HCN+4e-— )CH 3NH2 (4. 6e)
HCN+4e-— )CH 3NH2 (4. 6e)
아지드화이온은 질소분자와 암모니아로 그리고 산화이질소는 질 소분자로 환원된다. 아세탈렌은 에틸렌으로 환원되며 더이상 에탄 으로 환원되지는 않는다. 메틸니트럴은 에탄과 암모니아로 환원되 는데 그 속도는 시 안화산 (HC N)의 환원속도보다 훨씬 느리 다. 메 틸 아소니트럴은 메탄, 메탈아민, 에틸렌 및 에탄으로 환원된다. 이상 의 환원반응에 필요한 전자수는 2,4,6,8,10 또는 12 개이다. 따라 서 질소고정효소는 환원과정에서 두개씩 단계적으로 전자를 공급하 는 것으로 추측된다 . 호기성 박테리아에 의한 질소고정 메카니즘도 그림 4.1 에서 보 여준 바와 같은 무산소성 박테리아에 의한 질소고정 메카니즘과 비 슷하다. Clostr i d i u m pa ste u ria n um 과 Azoto b acte r vine ladii 로부터 분리된 질소고정효소에 의한 환원은 ATP 가 필요하며, 환원제로서 H2, S20/-또 는 BH4- 둥이 필요하다. 일산화탄소가 존재하면 모든 환원반응이 여제되며 일산화탄소 자체는 환원되지 않는다. Schrauzer 등에 의해서 개발된 질소고정효소의 모델系는 몰리브 뎬산 나트뮴 (sod i um molyb d ate ) , 티 오글리 세 롤(t h i o g l y cero l), 붕소수 소화 나트뮴 (sod i um borohy d rid e ) 및 황산철 CII) 을 포함하는 수용액 아다 .21) 이상의 모델系는 실온, 200 기압의 질소 CN2) 하에서 전체 질 소의 약 15% 를 암모니아로 전환시킨다. 그러나이상의 系에서 몰리 브 E선 화합물율 제거하면 암모니아가 생성되지 않는다. 따라서 아상 의 모델 系에 서 활성 자리 (acti ve s it e) 는 철 CI I )에 의 해 서 환원된 몰리 브밴떠올(t h i o l) 착물일 것으로 추측된다. 21 ) G. N. Schrauzer, G. Schlesin g e r and P. A. Doemeny , J. Am. Chem. Soc. , 93, 1803(1 9 71 ).
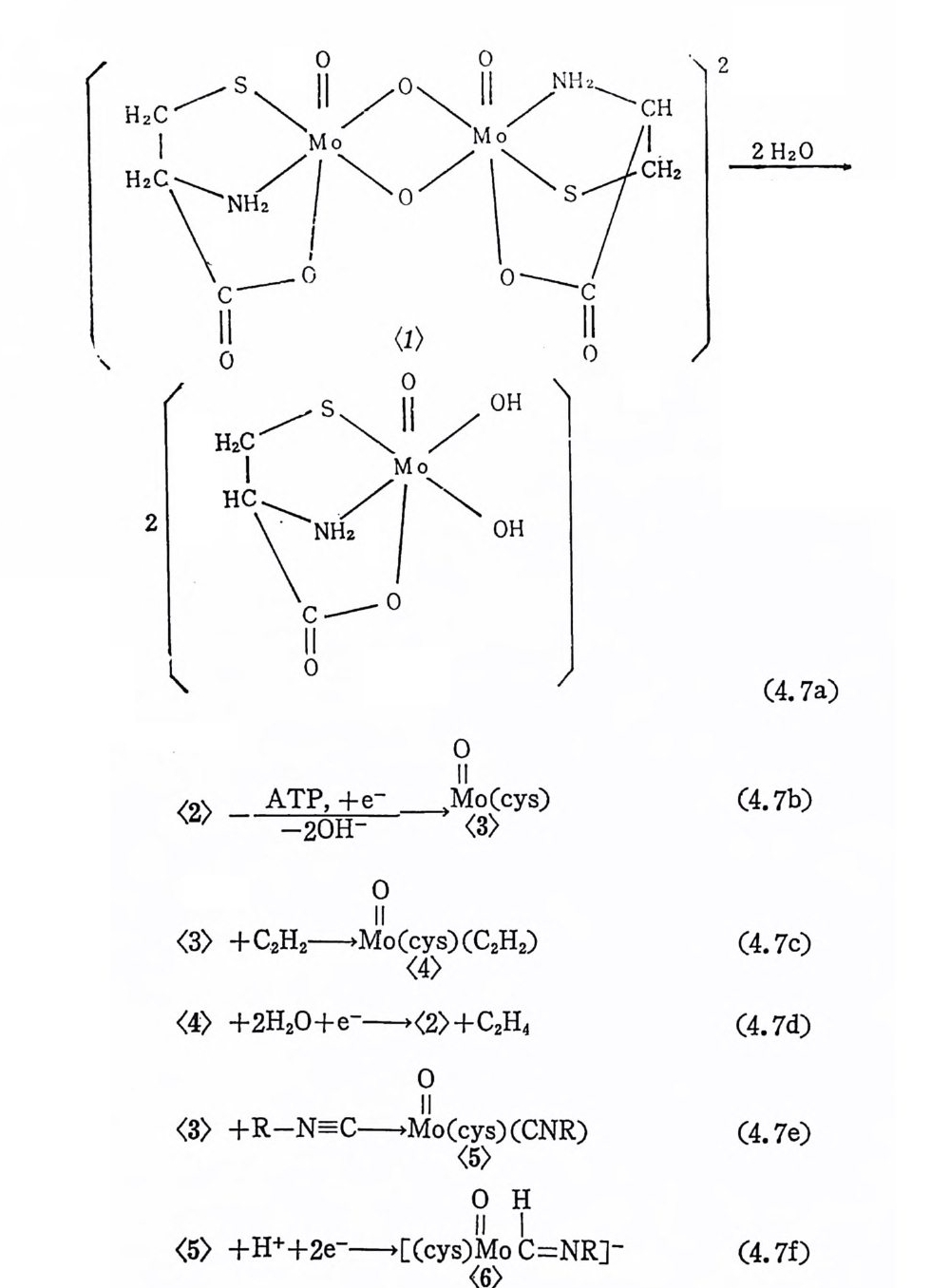 H222 c H<<’I23c>> s/ \\-c110 _+腐_CH C A i H-/T\22P 一0iO0I/,o H ol+|\e/ < > -M - -?o\=\, (- _ ooc/< 4 My。> I Ns \)l? oM(
H222 c H<<’I23c>> s/ \\-c110 _+腐_CH C A i H-/T\22P 一0iO0I/,o H ol+|\e/ < > -M - -?o\=\, (- _ ooc/< 4 My。> I Ns \)l? oM(
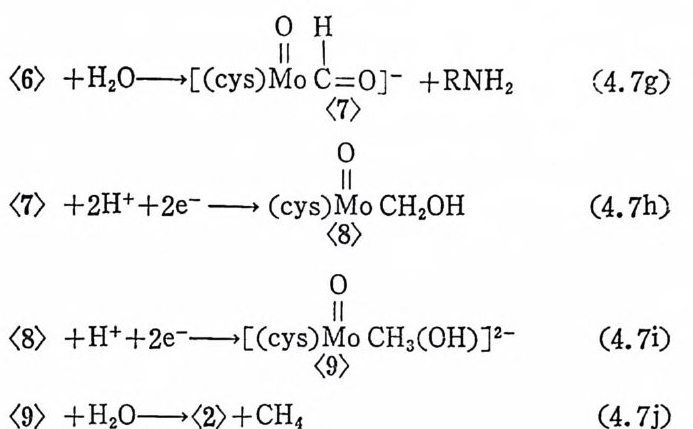 <6> +H20 一 [(c y s)OM11 o CHI =OJ -+ RNH2 (4. 7g )
<6> +H20 一 [(c y s)OM11 o CHI =OJ -+ RNH2 (4. 7g )
Schrauzer 둥은 또한 이 소니 트릴과 아세 틸렌의 환원에 二核 (bin u clear) 몰리 브벤 CV) 착물 Na2Mo204(Csy )2 (식 (4. 7) 에 서 <1 > ) 를 촉매 로 사용하였 다. 22) 착물 〈1 〉은 가수분해반응을 통하여 單核 착물 〈 2 〉로 된 다음 ATP 와 결합하여 반응성이 높은 배위 불포화 화합물인 중간체 몰리브덴 (N) 착물(〈 3 〉)을 생성시킨다(식 (4.7c) 참 조). 착물 〈 2 〉가 〈 3 〉으로 환원되는 반응은 ATP 에 의해서 촉진된 다. 실제 아세틸렌 및 이소니트릴의 환원반응의 활성화에너지는· ATP 가 존재 할 경 우에 ATP 가 존재 하지 않을 경 우보다 4~5Kcal/ mole 이 적다. 착물 〈 3 〉은 아세탈렌 및 이소니트릴과 반응하여 착 물〈 4 〉 및 〈 5 〉를 각각 생 성 하는 것으로 추측되 고 있다. 착물 〈 5 〉는 착물 〈 6 〉~〈 9 〉를 거쳐 몰리브밴 CV) 착물〈 2 〉로 되돌아 가는 것으로 제시되고 있다. 이상에서 기술된 몰리브덴 착물 이의에도 질소고정효소의 모델화 합물에 관한 보고는 더 있다(예를 들어 철착물에 관한 연구 23>). 그. 러 나 상기 한 Schrauzer 의 연구보고를 포함하는 모든 모델착물에 관 한 연구결과는 실제 질소고정효소의 성질이나메카니즘규명등에 커 다란 도움을 주지는 못하였다.
22) G.N. Schrauzer and P.A. Doemeny , J. Am. Chem. Soc., 93, 1608(1 9 71 ) and 94, 36040972). 23) W. E. Newt on , J. L. Carlin , P. W. Schneid e r, and W. A. Bulen, ]. Am. Chem. Soc. , 93, 368(1 9 71).
4) 광합성 을 하는 미 생 물 (ph oto s y n th e ti c sys t e m f .) Gest 등은 光合成울 하는 미 생 물 (Rhodos pi r i llum rubrum) 이 수소 화수소의 기능을 갖고 있음을 발견하였다 .24) 이 미생물은 광합성을 하면서 성장하는 동안 상당한 양의 수소를 발생한다. 그러나 질소 가 수소와 공존하면 수소의 발생은 현저하게 줄고 질소가 고정되며 암모니아가 생성된다. 따라서 이 수소화효소는 질소고정효소의 기 능도 갖고 있는 것으로 추측된다. 상기 미생물 (R. rubrum) 에 의한 질소고정은 빛이 필요할 분 아니타 無酸素 性조전 하에서 일어난다. Arnon 둥게 의해서 제시된 연구내용은 다음과 같다 .25) 죽 피루부 산(py ruva t e), 또는 숙신산 (suc ci na t e) 이 온으로부터 공급되 는 전자 는 cy toc hrome 및 fer redoxin 을 거 쳐 질소고정 효소 또는 수소화효 소둥의 전자받게에게 전달된다. 질소 CN2) 가 존재하지 않고 NH4+ 영 만 촌재한다면 수소화효소에 의해서 H4+ 는 환원되어 H2 가 발생되 고 질소가 존재하는 경우에는 수소발생은 일어나지 않고 질소 CN2) 가 fer redoxin 으로부터 전자를 받아서 NH3 로 환원된다. 2. 轉移金 屬 鑄物에 의 한 二室 素 의 活性化 1965 년에 처 음으로 이 질소 (d i n itr o g en, Nz) 착물이 만들어 지 기 까 지는 이미 상당히 많은 수의 일산화탄소 (carbon monoxid e , CO) 착물 이 알려 져 있 었 다. CO 와 동전자관계 (iso e!ectr o nic ) 인 N2 는 카나다 화학자 Allen 과 Senoff 가 [Ru(NH 야 (N2) J 2+ 를 만들기 까지 는 不 活性기체로 알려져 있었다 .26) 최초의 이질소화합물 [Ru(NH3) s CN2)]” 는 RuC13 • 3H20 와 히드라진 (N2H4) 의 반웅으로부터 얻어 쳤 다. 따라서 히 드라전의 불군등화반응 (d i s p ro p or ti ona ti on) 에 의 해 서 생성되는 이질소와암모니아가 루테늄에 배위되는 것으로추측된다. 즉처음부터 이질소를사용하여 루테늄-이질소착물이 만들어지는 것
24) H. Gest, J. Jud is, and H.D. Peck, Jr. , Inorga nic Ni tro g e n Meta b oli sm p. 298, Joh ns fiop k in s Press, 1956. 25) D. I. Arnon, M. Losada, M. Nozaki, and K. Tag a wa, Natu r e, 190, 266) 01A(.1 D96. 1 A). llen and C. V. Senoff , Chem. Commun. , 621(1965).
이 아니고, 반웅혼합물중의 히드라전으로부터 이질소착물이 만들어 지는 것이다. 그러나 곧 소련 화학자 Shil o v 둥은 이질소 CN2) 를 직접 루테늄 C JI)와 반응시켜 Ru(Il)-N2 착물을 만들었다 .27) 이렇게 합 성 되 는 이 질소착물의 연구로부터 자연계 (n it ro g enase) 에 의 해 아 루어 지는 질소고정에 관한 정보를 얻기 위한 연구가 활발히 진행되어 오고있다. 이어서 여러 전이금속의 이질소착물이 합성되었으며, x- 선 연구 에 의하여 그 구조가 밝혀진 이질소착물도 상당한 수에 이른다(표. 4.l 참조). 이질소는 일반적으로 〈 M-N 三 N 〉과 같은 형으로 배위되 표 4.1 이질소착물의 결합길이 및 N 三 N 신축전동수 화 합 물 M(A— .)N N(:::=AN) (lcNm 三- N1 ) 문참헌고 [Ru(NHJ ) s(N2)]2+ 2.10 1.1 2 2114 28) [O, (NH3) s (N2) J2+ 1. 84 1.1 2 2028 28) CoH(N2) (PRJ )J 1. 81 1.l l 2090 28) Mo (N2) 2( dip h os) 2 2.01 1.1 0 2040 28) [(NHJ ) s RuN2Ru(NH3)s)] ◄ + 1. 93 1. 12 2100) 28) '[[({ 'P1{ 'fJR/65 ——J ) 2CCNs;((i CCN H2 HN3J ))i s s(}}P 22RTZJi rJ) ( 22N N22) ]2 N2 21..0729 11.. 11 26 222888))) 다 리 N2 2.08 1.1 8 끝 N2 2.19 I.11 2040 MoCU(N2)ReCl(PR3)4]2 29) RMoe—- NN 11.. 7959 1. 28 ~1800 [ (C6HsLi) 6NbN2 ( (C2Hs) 20} 2L 1. 35 30) N 三 N• 1. 098 233P 31 ) [Ru (NH3) 6] 2+• 2.14 31 ) a 참고자료, b Raman 데 이 타.
27) A. E. Shil o v, A. K. Shil ov and Yu. G. Borodko, Ki ne ti ka _i Kata l i z. , 7, 287t) i6e8Ds( .1 a n9S d6e6 l)Sl.m ig ann inf i,c aD nic nei ,t rAo 1g1 eg ne- wT. raCnhseitm io. n I nMtee rt an la lC. oEmdp ilte . x , es1:3 S, y6 n 3t9h (e s1i昭s ,) .P rop e r-
며, M-N ― N 은 거의 일직선을 이문다• 이질소가 두 금속의 다리 위치에 있을 때는 M-N-N 一 M 이 거의 일직선을 이룬다. 이질소착물 제법으로 가장 직접적인 방법은 쉽게 치환될 수 있는 리간드를 이질소와 치환시키는 방법이다. 죽 수소 CH2), 물 CH20) 그 리고 에틸렌 (C2H4) 둥은 N2 에 의해서 쉽게 치환되어 이질소착물이 만들어진다(식 (4.8) 참조). 전이금속착물이 강한 환원조전하에서(三
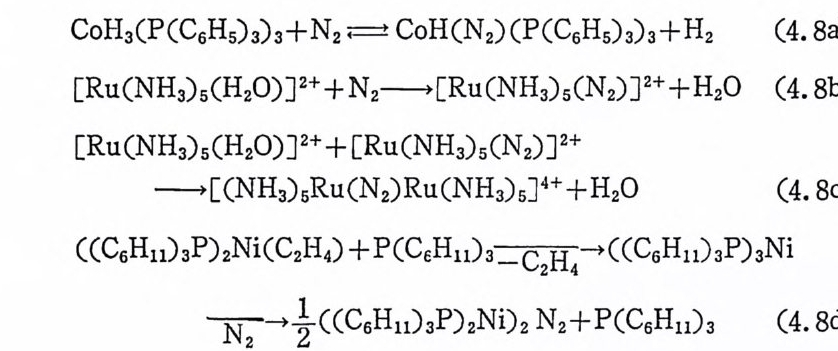 CoH3(P(C6Hs)3)3+N2 .= CoH(N2) (P(C5Hs)3)3+H2 (4. 8a)32>
CoH3(P(C6Hs)3)3+N2 .= CoH(N2) (P(C5Hs)3)3+H2 (4. 8a)32>
次燒 화합물(t er ti ar y p hos p h i ne) 이 존재하는) 이질소와 반응하면 이질 소착물이 합성되기도 한다(식 (4.9) 참조).
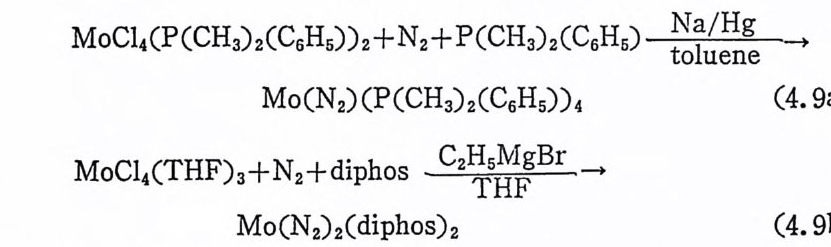 MoC14(P(CH3)2CC 晶 ))2+N2+P(CHa)2CC 晶) tNoal u/Heng e --+
MoC14(P(CH3)2CC 晶 ))2+N2+P(CHa)2CC 晶) tNoal u/Heng e --+
29) P. D . Cradwi ck , J. Chatt , R. H. Crabtr e e and R. L. Ric h ards, Cheni Commun. , 351, (19 75). 30) a) K. Jon as, Ang ew . Chem. Inste m at. Edit . , 12, 997(1 9 73). b) C. Kriig e r and Y. -H. Tsay, Ang e w. Chem. Inte r nat. Edit . , 12, 997(1 9 73} 31) B. R. Davis and J. Ibers, Inorg. Chem. . 9, 2768(1 9 70) 32) A. Yamamoto , S. Kit az ume and S. Ikeda, ]. Am. Chem Soc. , 90, 1089- (1968) 33) D. F. Harris o n, E. Weis s enberge r and H. Taube, Sc ien ce, 159, 320(1 9 68). 34) P. W. Jol ly, K. Jon as, C. Kriig e r and Y. -H. Tsay. ]. Orga nomet. Chem. , 33, 109(1 9 71 ). 35) B. Bell, J. Chatt and G. J. Leig h , Chem. Commun. , 482(1 9 70). 36) J. Chatt , ]. Orga nomet. Chem. 100, 17(1 9 75).
![]() dip h os= (C6H5)2PCH, CH 2P(C5l-1 s )2
dip h os= (C6H5)2PCH, CH 2P(C5l-1 s )2
(1) 二盜素의 配位 1) 二 空素 와 金 扇 간의 結合 일반적으로 이질소착물에서 금속에 배위된 이질소는 파이초十물 처 럼 옆으로 배위하지 않고 한쪽 끝으로 배위되며 (아 래 그럼 참조), M-N-N 은 언제 나 선형 에 가깝다. 28) 따라서 이 질소와 금속간의
![]() M … N三N M … N 三 N·••M
M … N三N M … N 三 N·••M
결합은 일산화탄소와 금속간의 결합으로 비교된다. 일반적인 금속 (M) 과 N2 와의 결합에 관하여서는 제 1 장 3 철에서 자세히 기술되 었다. 여기서는 실제 합성된 금속-이질소착물의 예를 들면서 금속 과 이질소간의 결합을 살펴본다. 실례를 들기 전에 제 1 장에서 기술 된 금속과 N27,} 의 결합을 간단히 살펴보면 다음과같다. 전자가채 위전 N2 분자의 시그마 퀘도함수 하나가 전자가 채워지지 않은 금 속의 시그마 궤도함수 ([Ru(NH3)5(N2)]2+ 와 같은 정팔면체 착물 에 서 는 dZ’ 또는 dX’_ y’)와 작용하여 M-N2 간의 시 그마 결합을 이 루며, 동시에 전자가 채워진 금속의 d 과이궤도함수로부터 빈 N2 분자의 反 結 合軟道函數(군데 1 도함수)로 전자의 逆提供이 일어나며 M-N2 간에 파이 결합이 생긴다(그립 4.2 참조). 이와 같이 금속과 N2 사이의 결합은 二 重 결합의 성격을 가질 수 있다. 표 4.1 에 서 보여 주는 바와 같이 [Ru(NH 야 CN2) J 2+ 및 [(NH3)s. RuN2Ru(NH 야 ]4+ 에 서 Ru-N2 결합거 리 는 Ru-N _ 의 결합이 단일 결합으로 알려진 〔 Ru(NH3)6]” 에서 Ru 一 N 거리보다는상당히 짧~ 것으로 보아 Ru-N2 사이의 결합은 어느정도의 이중결합의 성격을 갖고 있다고 추축된다. 바슷한 예로 CoHCN2)CPR3)3 _ 에서 Co-N 결합거리(1. 81 A.)는 [Co(NH3)s J2+에서 Co-N 결합거리 (2.llA) 보다 상당히 짧은것을들수있다. 금속과질소사이의 이중결합 거리는 약 1.70A 정도로 알려져 있다. ReCl3(NCH3)(PR3)2 에서 Re=N 결합거리는 L69A 으로 밝혀졌으며 m Cl(PR3)4)Re-N2- MoCl4-N2-Re(PR3)4Cl31) 중에 Re-N 결합거 리 도 1. 75A 으로 Re
되 · N2 사이의 걷합은 이중결합에 가까운 것으로 제시된다. 금속과 N2 사이의 파이 결합은 금속의 d 전자가 N2 의 파이 反結 合 !겁 道函數에 채우]침으로써 이루어지기 때문에 N 一 N 결합은 약해 질 것이다. 표 4.1 에서 보떤 배위된 N2 의 N-N 결합거리는 배위 되지 않은(자유로운) N2 의 N-N 거리보다 간 것으로 밝혀졌다. 대 부분의 경우 배위된 N2 의 N-N 거리는 약간 길어졌다. 그러나 Re-N 의 거리가 이중결합 거리에 가까운 것으로 알려진 Cl(PR3)4 Re-N2-M0Cl4-Nz-Re(PR3)4 Cl31) 중에 서 N-N 거 리 (1. 28A) 는 N=N 이중결합거리(아조메탄에서 얻어전 값은 1. 24A31)) 에 가깝다. 표 4.1 의 [(C6H5L i)6 Ni 2N 2((C2H; )20 }2J i 중의 N-N 거 리 에 관하여 서는 아래에서 살펴 볼 것이다(이질소의 끝결합 (end-on land i n g)과 옆 걷 압 (s i de-on 또는 edg e- on to ndin g 참조). 배위된 N2 의 N-N 결합이 배위되지 않은(자유로운) N2 의 N-N 보다 약호匡 l 것 은 전동스펙 트럼 (IR 또는 Raman) 측정 에 서 얻어 지 는 N-N 산축전동수 데이타로부터 쉽게 볼 수 있다. 표 4.1 에서 보는 바와 같이 배위된 N2 의 N-N 신축전동수는 배위되지 않은 N2 의 그것보다 200cm-1 이상 낮은 값을 보여준다. 금속에 배위되지 않은(자유로운) N 군} [(N H3)5RuN2R u(NH3)5]“ 중 N2 의 N 一 N 신축전동은 분자의 대칭성 때문에 Raman 스팩트럼에서만 측정가능 하다. 2) 이 질소 다리 를 갖는 (d i n itr o g en-br i d g ed) 착물에 서 이 질소와 금 속의 결합. 금속으로부터 질소분자의 反結合파이 軌道函數에 제공되는 逆結 合의 효과를 고려한다면, M_N2_M 형의 착물에서 N_N 의 결합 착약물화 는(r ; 상5 一당 C5할(C H것3으) 야로 C N추2측)Z된r 다―. N2 ―표 Z r4(.N12 에) (r;5의— 하C면s(C H二3核)s) 2 지에 르서 코늄다 리 N2 의 N_N 거리와 끝 N2 의 N ― N 거리는 예상되는 바와 같이 상당한 차이 를 보여 준다. 그러 나 한편 [R u(NH3)sCN2)]2 + 와 [(NH3)sRu-N2-Ru(NH3)s]4+ 에 서 N-N 거 리 의 차이 는 매 우 적 다. 이질소 다리를 갖는 二核착물에서 N 一 N 결합의 세기정도는 아래
와 같은 4 - 중십 과 이 분 자궈 ] 도함수 ( fo ur - cen t er ;c- m olecular orb it al) 에 의해서 설명되기도 한다. 4 중심 파이 분자퀘도함수는 금속 M 의 d.,, 금속 M' 의 d.,, 그리고 두 개의 N 으로부터 두 개의 p.'fl]도 함수 둥 고두 4 개의 퀘도함수의 一次결합(li near comb i na ti on) 으로부 터 얻는 4 개의 분자궤도함수를 의미한다. 이렇게 얻은 4 개의 4- 중 심 분자궤도함수는 (그림 4.3) 과 같다. z 축이 결합축이 된다. 4 개 의 분자궤 도함수의 에 너 지 는 마디 면 (nodal p lane) 의 수가 많을수록 높다 (H il ckel M. 0. 의 계 산방법 에 따라서 ). 그림 에 서 보여 주는 4 개 의 분자궤 도함수 이 의 에 도 , 두 금속 (M 과 M') 각각의 d 두 개 , 그리 고 N2 중의 두 개 의 N 이 갖는 Py 두 개 , 모두 4 개 의 원자궤 도함수 가 결합하여 생성하는 4 개의 4 - 중심 분자궤도가 있다. 이들 4 개의 M.O. 는 위에서 기술한(두 개의 금속 d” 와 두 개의 N 의 p.로부 터 얻어지는) 4 개의 M.O. 와 각각 같은 에너지를 갖게 된다. 따라 서 그림 4. 3 의 각 M. O. 는 이 중으로 축되 (doubly deg e nerate d ) 되 어 있다. 그림 4 .3 에서 에너지가 높은 순서는 (I )<(2)<(3)<(4) 가 된다. 두 금속 M 과 M' 의 dxy 궤도함수 두 개는 非 結 合 軌 道函數가 되 며 이 들 비 결합궤 도함수 ( n on•b ond i n g orb it al) 는 그림 4. 3 의 (2) 와
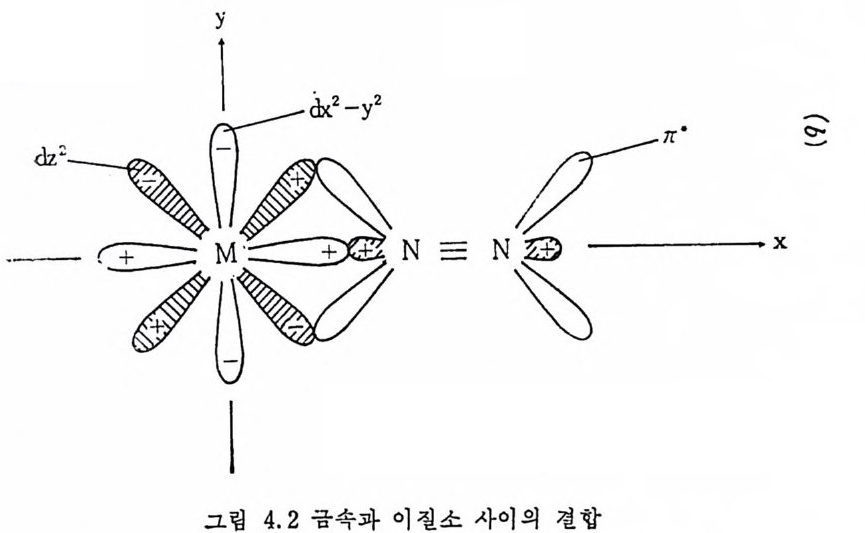 y
y
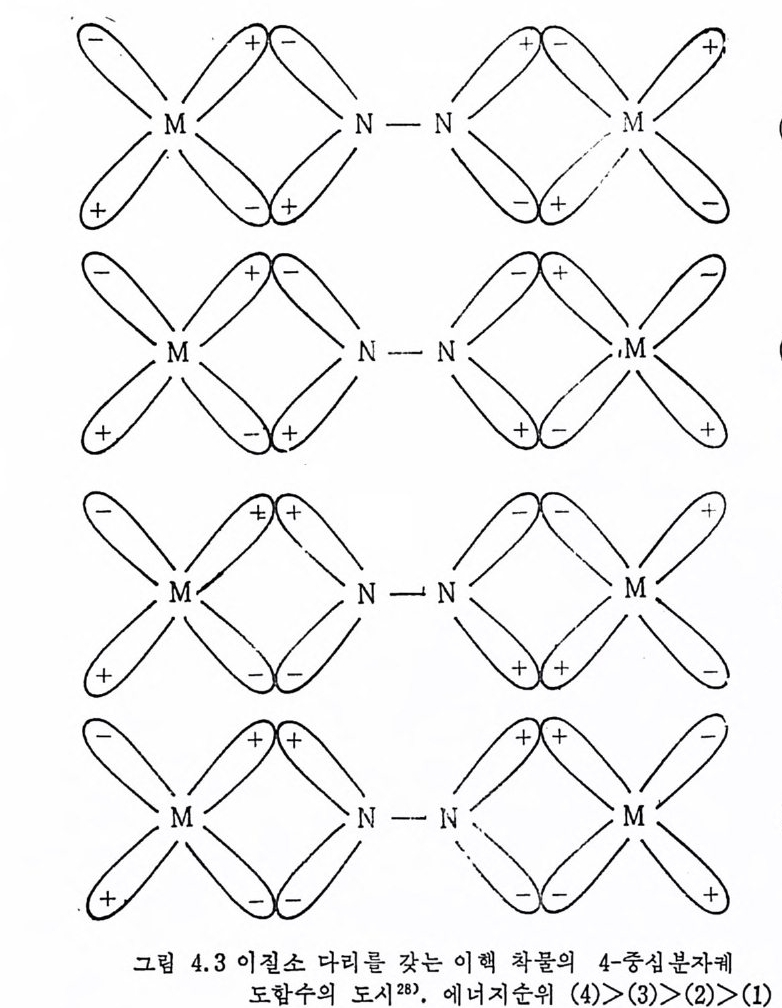 (4>
(4>
(3) 의 중간쯤의 에너지를 가지리라 추측된다. 죽 에너지의 높은 순 위는 (1) <(2)
향을 받을 것이다. 따라서 두 금속 (M 과 M') 의 d _ 전자 배치에 따 라서 N-N( 및 M-N) 의 결합이 달라질 것이다. 그림 4.3 에서 보 는 바와 같이 분자궤도함수 (2) 는 N-N 사이에 反結合성격을 갖고 있으며 M-N2( 또는 M'-N2) 사이에는 結合의 성격을 갖고 있다. 따 라서 (2) 에 전자가 채워지면 N-N 의 결합은 약해지고 M-N( 또는 M'-N) 의 결합은 강해진다. 한편 분자퀘도함수 (3) 은 N-N 사이에 結合성격을 갖고 M-N2( 또는 M'-N2) 사이에는 反結合의 성격을 갖고있다. 따라서 (3) 에 전자가채워지면 N-N 결합은 강해지고 M ― N 결합은 약해질 것이다. 非結合궤도함수인 금속의 dx y궤도함수 에 채워지는 전자는 M-N 및 N_N 결합에 영향을 주지 못한다. 〔 (NH3)5Ru-N2-Ru(NH3) 』 4+ 경 우에 두 개 의 Ru( Il ) 이 온은. d6 전자배치를 갖고 있으므로 12 개의 전자를 제공하게 된다. 따라서 분자궤도함수 (2) 에 4 개, 금속의 dx,(M 및 M' 의 dx y궤도함수) 에 4 개, 그리고 분자궤도함수 (3) 에 4 개의 전자가 채워지게 된다. N-N 사이에 反結合의 성격을 갖는 분자퀘도함수 (2) 의 효과는 N -N 사이에 結合의 성격을 갖는 분자퀘도함수 (3) 에 의한 효과에 의해서 상쇄된다. 따라서 二核착물 [(NH3)5RU 一 N2-Ru(NH3)5]H 에서 N_N 결합은 單核착물 [Ru(NH3)sCN2) 〕 2+ 에서의 N_N 결합과 비슷한 것으로 설명된다. 한편 지르코늄(JI)착물 (1J5 -Cs(CH3)s)2 (N2)Zr-N2-Zr(N2)( ?드 C5(CH3)5)2 에서는 두 개의 Zr( JI)이온은 단지 4 개의 전자밖에 제공하지 못한다. 따라서 분자퀘도함수 (2) 가 겨우 채워질 분이다. 이 경우에 N_N 사이에 反結合의 효과가 유효 하게 되기 때문에 다리 (brid g e ) N2 의 N ― N 결합은 약해지는 것으 로 해석된다. 두개의 다리 이질소를 갖는 三核착물 Cl(PR3)4Re- N2-MoCl4-N2-Re(PR3)4CI 의 경우도 위와 비슷하게 설명된다. 즉 두개의 N2 다리를 중십으로 각각 4- 중십 분자궤도가 만들어지는 것 으로 설명 된다. Re( I )이 온으로부터 6 개 의 전자, 그리 고 Mo(N) 이온이 갖고 있는 두개의 전자 중 한개의 전자, 모두 7 개의 전자는 분자궤도함수 (2) 에 4 개, Re 의 dx y에 2 개, 그리고 Mo 의 dx y에 한개씩 각각 채워질 것이다. Mo의 dx y궤도 함수는 반대편에 있 는 또 하나의 다리 N2 와의 결합에도 쓰여질 것이므로 Mo(N) 이
갖고 있는 두개의 d“ 전자는 짝지어 존재할 것으로 재시되었다. 실 제 상기 Re.( I )-N2-Mo(N)-N2-Re( I ) 착물은 反자성 (dia m ag n e ti sm) 울 보여 준다. 29) 분자궤 도함수 (3) 은 빈 채 로 남아있 게 되 기 때 문에 Re( I )-N2-Mo(N)-N2-Re( I )착물에서 N-N 의 거 리 가 비교적 간 것도 쉽게 설명된다. 물론 여기서 Mo(N)Cl4 기가 대단히 센 전자받게 역할을 하기 때문에 생길 수 있는 분자 내의 국성효과 도 있을 것이다. 3) 이 질소의 끝결합 (end-on bond i n g)과 옆결합 (s i de-on 또는 edg e -on bond i n g)의 비 교. 표 4.1 에 서 보여 준 [(C6H~L i)6 Ni 2N 2[CC2Hs)20}2L 는 이 질소와 금속의 걷합형대에서 이제까지 살펴본 이질소착물과상당히 다르다. 그림 4.4 는 이 착물의 구조를 보여준다. 이 착물은 페닐리튬과 트 란스 -1,5,9- 시클로도데카트리엔니첼 co) 착물의 에테르 용액에 이 질소를 반응시켜 얻어졌다 .30) 착물의 양쪽에 있는두개의 니첼원자 와 이 질소가 이 루는 4 개 의 원자로 된 두 개 의 원자단 (N i 2N2) 은 각각 약간 찌그러진 사면체를 이루고 있다(아태 그림 (a) 참조 바람). 그림 (a) 에 서 보는 바와 같이 이 질소는 금속과 끝결합 (end-on bond i n g)을 이루고 있지는 않다. 이질소와 금속의 결합은 올레핀이나 아세탈렌
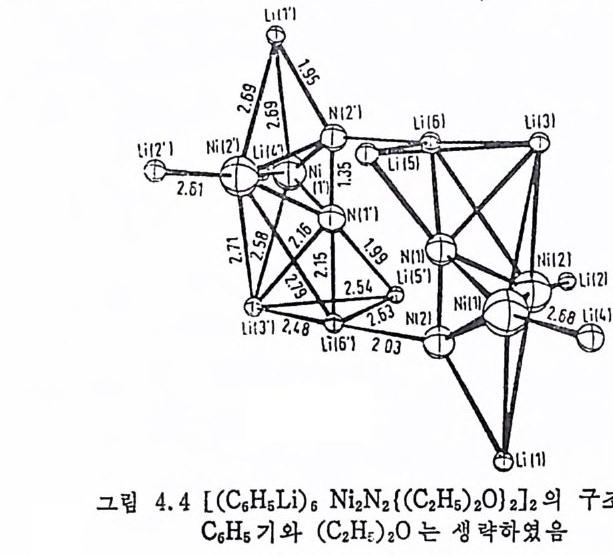 L111 '1
L111 '1
유도 체들 이 금속과 결합 하 는 옆갇합 (s i de-o n bond i n g)에 가까 운 형 태 이다. 위와 똑 같은 예 를 아/세탈렌N\ 유\도 체 i 칙/ ·불 에 서 도 봅 수 있다. \ ,r 1 i -\/ Zi 一 E , N
i즉 핵 사카르보닐더 코발트 디 페 닐 아세 틸 렌 (hexacarbony ld i c o balt dip h e- n y lace t y lene) 에 서 디 페 닐 아세 탈 렌은 두 개 의 코발트와 사면체 형 을 이 루며 결합하고 있다(그림 ( b ) 참조). 이상의 착 물 (N i 2N 2 ) 에서 이질소 는주위의 리 듐 원자들에 의해서 안정하게 결합되는것으로추측되기 도 한다 ( 그 립 4. 4 참조 ). 비 슷한 화합 물 로서 리 둠 이 나트뮴으로 치 환 된 화합 물 도 합 성된 바 있다 3 7 ) 이상의 두 착물이 현재까지는 유일 하게 분리 확인된 이 질소의 옆 결합 (s i de-on bondin g ) 착물 이 다.
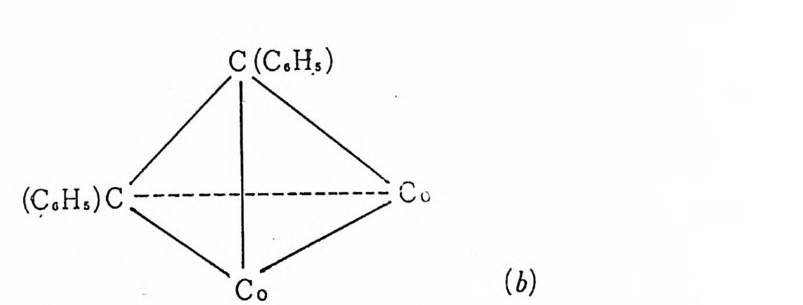 (C• 晶)/ C :\------+C-o- \-/-----:;; C o (b)
(C• 晶)/ C :\------+C-o- \-/-----:;; C o (b)
식 (4.8d) 에서 에틸렌 대신에 이질소가치환될 수 있음을보여 주 었지만 실제로 대누분의 이질소착물에서 이질소는 끝결합을 이루고 있음은 우리들의 관심을끌게 한다(에틸렌은 이미 알고있는바와 같 이 옆결합을 하고 있음에 비교하여). 자연계에서 발견되는 질소고정 효소 (n it ro g enase) 들은 이 질소 분만 아니 라 아세 틸렌도 옆결합을 통하
~) K. Jon as, D. J . Brauer, C. Kriig e r, P. J. Roberts and Y. -H. Tsay, J. Am. Clt em . Soc. , 98, 74(1 9 76).
여 환원시키는 것으로 알려져 있다. 그러나 착물의 안청성과 반응성 은서로 다른 관접에서 고려해야 할 문제이기 때문에 조십스럽게 고 찰되어야 할 것이다. 끝결합과옆결합에 관여하는분자퀘도함수들을 비교하여 보면 쉽게 끝결합이 옆결합보다는 안정할 것이라고 추측된 다(그립 4.5 참조). 그림 4.5 에서 보는 바와같이 끝결합 형태에는금 속과 이질소 사이에 두개의 동등한 파이결합이 형성가능하게 된다. 그러나 옆결합형태에서는오칙 한개의 금속이질소 파이결합이 가능 하다. 따라서 퀘 도함수의 최 대 겹 침 (maxim um overla p)의 원칙 에 의 해서 선형 (line ar) M-N-N 이 더 욱 안정 할 것 으로 예 상된다. 비교적 안정한 끝견합 이질소착물과 비교적 불안정한(반응성은 높
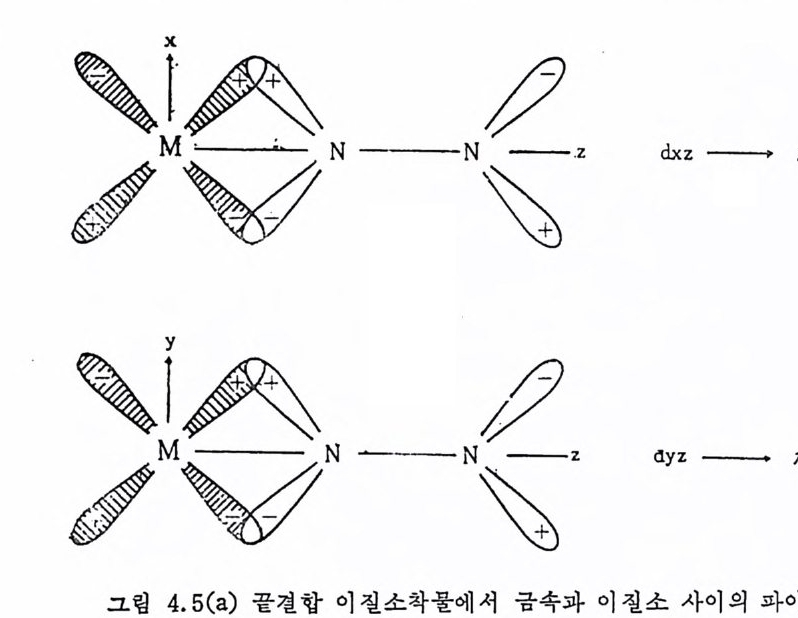 &`M/ • /\‘ \N -N\ / — — .z dxz , '-rx z
&`M/ • /\‘ \N -N\ / — — .z dxz , '-rx z
을 것으로 추측되는) 옆결합이질소착물은 용액 중에서 평형을 이루 고 있을 수도 있다. 이상의 평형이 실제로 제시된실험적 결과가있 다. 38) 죽 14N=l5N 률 사용하여 [Ru(NHs)sCN2)]2+ 를 합성 하면서 Ru-14N=l5N 와 Ru-15N 三 14N 를 포함하는 두 착물을 따로 분리하 였 다. 두 착물에 서 N-N 신축전동수는 lOcm-1 정 도의 차이 를 보여 38) J.N . Armor and H. Taube, J. Am. Clzem. SoC., 92, 2560( 19 70).
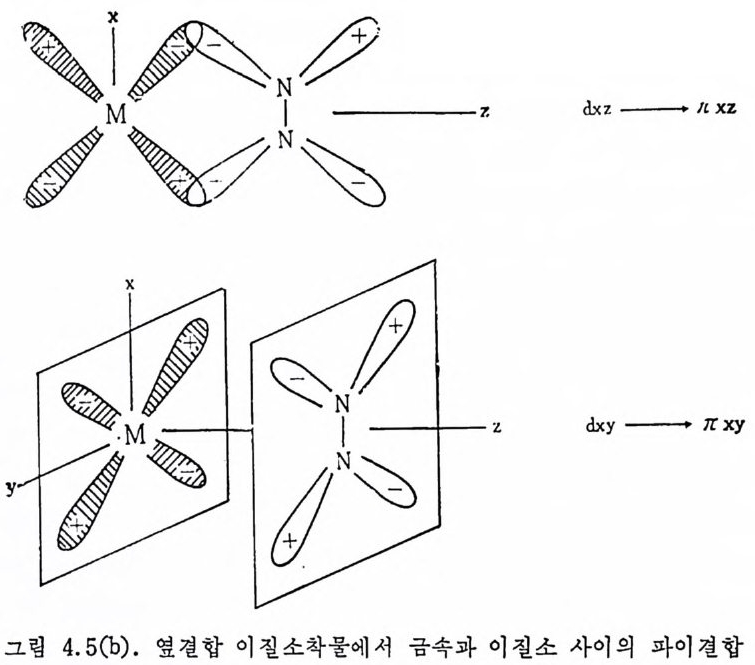 \广\/ 7 dxz , It xz
\广\/ 7 dxz , It xz
준다. 이상의 두 착물 (Ru ― 14N 三 1sN 와 Ru-15N 三 14N) 은 數시간에 걸쳐 평형을 이루는 것으로 밝혀졌다. 이상의 실험결과로부터 옆 결합의 이질소착물이 중간체로 제시되었다(식 (4.10) 참조). 이 이성 질화반응의 열역학적 데이타로부터 옆결합 이질소착물 중간체의 존
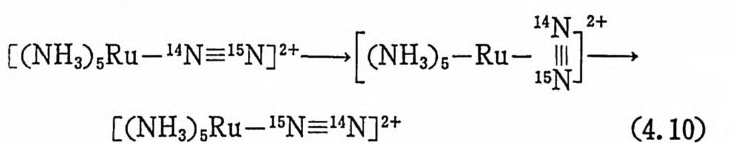 14N..,2+
14N..,2+
속시간은 매우 짧은 것으로 제시되었다. 끝걷합 이질소착물이나 옆결합 이질소착물에서 N-N 결합이 약 해지는 것은 아래와 같은 이론적인 계산에서도 볼 수 있다. 즉 각 각 다론 전이금속 (M) 의 경우에 MN2 부분을 취하여 배위된 이질소 의 시그마결합과 파이결합의 정도 (bond p o p ula ti on) 를계산한결과표. 4.2 에 실은 것과 같은 데이타를 얻었다 .39) 표에서 n.,n 雲 및 n, 값 39) K. B. Yats i m i rs ki, Pure Ap pl. Chem. , 27, 25l(lrr tl).
둘은 각각 시 그 마 결합의 정도 , 파이결합의 정도 및 총( 시그마+과 이)걷합의 정도를 상대적으로 나타낸 값들 이다. 표 4 .2 에 의하면 일반적으로 배위된 N2 의 n .+ 」는 배우]되지 않은 자유로운 N2 의 그 것에 비하여 적다 . 이 러한 계산건과는 실험적으로 얻은 N-N 결합 의 약화(예를 들면 N-N 신 축전동 수의 낮아집 및 N-N 결합거리의 길어집홍 , 4.1 참조 )과일치되는것이다 . 또한옆결합이 질 소의 N-N 결합이 꾼결합 이질소의 그것보다 길 것이라는 것도 표 4 . 2 에서 쉽 게 볼 수 있다 . 즉 옆결합의 경우에 n . + 」값들이 끌결합의 경우에 n0 + 나 보다 일반적으로 적다 . 표 4.2 에 의하면 주기율표에서 왼쪽에 있는 전 이 금속(같은 주기에서 원자번호가 적은 금속)의 이질소착물 에 서 N 一 N 결합이 약해지는 정도는 더욱 크다. 따라서 질소분자를 효과적으로 활성화시키기 위하여 사용되는 금속은 주기율표의 왼쪽 에 있는 것일수목 좋을 것으로 추측된다 . 특히 이질소가 약하게 금 속에 결합되 어 있으면서 끝결합으로부터 옆결합 형태로 전이가 가 능하게 될 경우에 이질소의 활성화가 기대된다 . 표 4.2 MN2 중의 N ― N 결합에 관하여 계산된 시그마 및 과이결 합정 도(t ond pop ul ati on )m. 결 합 형 M n, n, n,,+~ M-N 三 N Cr 0.838 0.577 1. 415 (끝 결 합) Mn 0.8 21 0.6 3 4 1,4 5 5 Fe 0.80 9 o.7 4 7 1. 556 Co 0.80 7 o.7 78 1. 585 Ni 0.8 2 5 0.79 5 1. 620 자유로운 N2 0.7 9 6 0.8 16 1. 621 M- N111 Cr 0.7 31 0.238 0.9 69 N Mn 0.7 33 0.384 1.1 17 ( 옆 견 합) Fe 0.7 38 0.52 4 1. 262 Co o.7 9 7 0.63 5 1. 432 Ni 0.8 5 2 0.7 57 1. 609 자유로운 N2 0.7 96 0. 8 16 . I. 621
(2) 配位된 二登素의 反應 공기 중의 이질소몰 암모니아로 전환시키는 생물학적 질소고정의 첫 단계에 해당하는 전이금속-이질소 착물의 형성은 이미 위에서 살펴본 것처럼 비교적 성공적이라고 할 수 있다. 그러나 두번째 단 계라고 볼 수 있는 이질소의 흰·원에 의해서 암모니아가생성되는단 계에는 비교적 큰 성과가 없다. 죽 이질소로부터 암모니아를 생성 시키는 촉매적 반응으로 효과적인 과정은 벨로 발견되지 않았다. 그러나 배위된 이질소가 비교적 낮은 압력, 낮은 온도에서 암모니 아(또는 그 중간체로 볼 수 있는 히드라전)로전환되는예가발표되 었으며, 기타 배위된 질소분자의 반응이 보고된 바 있다. 이들 반 응둘을 이 절에서 살펴보고자 한다. 1) Zie g le r 형 촉매계에 의한 이질소의 고정 1966 년 소련의 과학자 Volpi n 둥은 전이 금속착물과 강한 환원 제인 유기금속화합물에 의해서 이질소가 두 개의 질소화 (n it r i de) 음 이온으로 환원되는 것을 발견하였다 .40) 이어서 비슷한 반응둘이 여 러 학자들에 의해서 계속 연구되어 왔다 .41) 이상의 반웅들은 실온 (또는 더 낮은 온도)에 서 , 질소기 압이 1~150 기 압하에 서 일어 난다. 이상의 반응들은 유기용매가 반드시 사용되어야 한다. 왜냐하면 알 킬 알루미 늄, Grig n ard 시 약 또는 나프탈렌화나트룹 (sod i um n2p tha l- ide ) 둥의 유기금속 성분이 필요하기 때문이다. 대부분의 경우에 이 질소는 전이금속에 결합된 질소화이온 (-N3- )으로 환원되며, 금속에 결합된 N3 二는 가수분해에 의해서 암모니아로 된다. 대부분의 경우 에 전이금속 한 분자에 암모니아 두 분자(또는 그 이하)가 생성된 다. 강한 환원제인 유기금속화합물에 의해서 전이금속은 용액 내에서 환원되고, 환원된 전이금속은 배위된 이질소에게 전자를 7 제공하여 이질소를 환원시키는 것으로 추측된다. 이상의 추축을 증명하는 하
40) M.E. Volpi n and V.B. Shur, Natu r e 209, 1236(1966). 41) ab)) GR.. MHeunrrriacy i - Oa ln idv e Da. nCd. SS.m Oi tlhi ,v eC , oAorndg. e wC.h eCmh.e mR.e v. I,n t3e . r n4a2t9. (19E6d8)i.t . , a, 650(1 9 69).
나의 실 험 적 예 를 들어 보면 아래 와 같다 4l b ),42) 할로젠화 전이 금속 화합 물 과 나프탈렌화 리 튬 Oit hi u m nap tha lid e , N p ) 으로 이 루어 전 이 질소고정 系 는 적당한 실험조전에서 전이금속한분자당한분자의 아질소를 고정하여 환원시킨다. VC13 와 L i N p로 이루어전 촉매系 에 관한 ESR 측정 연구에 의 하면 전이 금속은 V(O) 또는 V(-II )등 으로 환원된다. 죽 Li N p를 VC13 의 3 배로 가하면(몰비율 Li/V = 3), 반응 용액 중에 비스(나프탈렌)바나듐 (0) 착 물 이 얻어지고, L i /V 의 비율이 더욱 높아지면 V( 一 Il) 화학종이 관찰된다• CrC13/ Li N p系의 경우에는 Li /Cr 의 바울이 높아지면 최초에는 비스(나프 탈렌)크롬 CI )의 ESR 신호가 관찰되 며 , 이 어 서 비 스 ( 나프탈렌)크롬 (-I ) 및 비 스.(나프탈렌)크롬(_ m) 의 ESR 신호도 보여 진다. 43 ) 용 액 중의 Li /M 의 비율이 6 보다 클 경우에야 비로소 Li N p의 ESR 산 호가 관찰된다. 이상으로 보아서 환원된 M(O) 도 계속해서 Li N p로 부터 전자를 받아 M(-x) 로 환원되는 것이 분명하다. VC13 를 사 용할 경우에 한 분자의 바나듐당 한 분자의 이질소가 완전히 환원 되려면 Li/ V 비율이 최소한 6 이 되어야 한다. 따라서 V( 冊)이 6 개의 Li N p로부터 6 개의 전자를 받아 vc-m) 으로 환원된 다음 6 개의 전자를 제공하여 이질소를 환원시키고 (3N2+6e- _- ->2N3-) 다 시 vcm)이 된다고 추측된다. 이상과 같은 系에 의한 반응의 단접이라고 생각되는 것은 질소화 이온으로 환원된 질소가 매우 강하게 전이금속과 결합되어 있는 점 이다. 전이금속에 결합되어 있는 환원된 질소의 제거방법으로. 현재 까지 연구된 것 은 가수분해 반응이 나 또는 가알콜분해 반응 (alcohol y s i s) 이다. van Tamelen 등은 위와 비슷한 질소의 고정, 환원 그리고 알콜분해반응의 순환과정을 개발하였다 .4 4 ) 이들에 의해 개발된 질 소고정 系는 테 트라이 소푸로폭시 티 탄과 나프탈렌화 나트륨을 테 트라
42) G. Henric i O li ve and S. Oli ve , Ang e w. Chem. In!em at. E dit . , 6, 8 73(1 9 67). 43) G. Henric i-O l ive and S. Oli ve , J. Am. Chem. Soc., 92, 4831(1 9 70). 44) a) E. E. van Tamelen, G. Boche and R.H. Greeley, /. Am. Chem. Soc. , 90, 16770968). b) E.E. Van Tamelen, R.B. Fetc h er, S.W. Schneller, G. Boche, R.H. Greeley and B. Akermark, /. Am. Chem. Soc. , 91, 1551(1 9 69).
히드로푸란 (THF) 에 녹인 용엑이다. 이 系에 의하여 환원된 질소화 화합물 (n it r i de) 은 동일 몰의 이소푸로필알콜에 의해서 암모니아로전 환되어 금속으로부터 분리된다. 그 다음, 용액에 나프탈렌화 나 트륨(이미 系는 나프탈렌을 함유하고 있기 때문에 간단히 나트륨금 속울 가해도 된다)을 가하여 촉매系의 활성을재생시킬수 있다. 이 상과 같은 순환과정 을 5 번 반복함으로써 티 탄금속 한 분자당 I. 7 분자의 이질소를 암모니아로 환원시킬 수 있다. Volpi n 둥은 전이금속에 결합되어 있는 질소화 화합물을 뱃치법 (batc h p rocess) 우로 제거하는 데 성공하였다 .45) 따라서 이 방법에 의 하면 질소고정을 뱃치법으로 계속할 수 있다. 이들이 사용한 환원 系는 알루미 늄과 부롬화알루미 늄 (alum i num brom i de) 의 혼합물이 다. 이 혼합물이 TiC 1 4 또는 CrC13 와 같은 전이 금속의 할로겐화 화합물 과 함께 사용되면 전이금속 한 분자당 100 분자 이상의 질소분자가 질소화 화합물로 환원된다. 죽 많은 과량의 알루미 늄과 Lewi s 의 산 (예를 들면 Ti : Al : A1Br3=1 : 600 : 1000) 을 사용하여 130°c 에서 , 100 기압의 질소하에서 30 시간 반응시키면 142 분자의 질소를 환원 시킨다. 여기서 환원된 질소화 이온은 알루미늄에 결합되어 있는것 으로 추측되며, 가수분해반응에 의해서 암모니아로 떨어져 나가는 것으로 추측되고 있다. 이 상과 같이 강한 환원제 인 유기 금속화합물을 포함하는 系를 사 용하는 대 부분의 경 우에 서 이 질소의 환원이 질소화이 온 (N3-) 을 거 쳐 일어난다는 사실온 그렇게 예상 밖의 일은 아니다. 왜냐하면 이 질소의 첫결합을 끊는 데는 527k J /mol 의 에너지가 필요하지만 두 번째 및 세번째 결합을 끊는데는 단지 260kJ/ m ol 및 159k J /mol 밖 에 필요하지 않기 때문이다(표 4.3 참조). Shil ov 둥에 의 해서 개 발된 FeCl3(P(C6H5)3)2/ i -C3H7M g Cl/N2/ 에 테르 系에 의한 질소고정에서는 N-N 결합이 완전히 끊기지 않은 히 드라전 (NH2NH2) 이 소량 얻어 졌 다. 46)
45) M. E. Volpi n, M. A. Ilato v skay a, L. V. Kosya k ova and V. B. Shur, Chem. Commun, 10740968). 46()1 9Y 7u1. ) G. . Borodko, A. E. . Shil ov and L, Yu, Ukhin , Chem, Commun. , 1185
표 4.3 질소―질소 결합에너지 N~ N 946 kJ/ m ol N=N 419 kJ /m ol N-N 159 kJ /m ole 2) Lewi s 의 酸과 反應 안정한 이질소착물중의 이질소는전자적으로 상당한 국성을 가질 것으로 기대된다. 따라서 N-N 신축전동은 강한 적의선홍수 를 보 이는 것이라고 추축된다. 이질소착물의 ESCA 스펙트럼에 의하면 끝결합을 하고 있는 이질소의 전자적 편국현상은명백한것 같다. 트 란스 -RuCl(N2)(AsR3)247> 및 ReCI(N2)(dip h os)248> 중의 질소 ls 스팩 트럼 은 각각 1. 6eV 와 2. 0eV 씩 분리 된 두 개 의 봉우리 (p eak) 들 울 보여준다. 이러한 차이 (1.6 eV 및 2.0eV) 는 ls 전자의 결합에너 지의 차이다. 죽 이 차이는 이질소 중의 두 질소원자가 갖는 전자 수의 차이가 0.3~0.4 개에 해당된다. 죽 끝에 있는 질소원자 ( M N 三 N) 는금속에 결합되어 있는 질소원자 (M-N 三 N) 보다 0.3~0.4 개의 전자만큼 ―의 전하를 갖게 관가는 의미이다 .28) 더우기 이질소 자체가, 어떤 경우에는 Cl 리간드와 비교될 만한, -전하를 갖고 있다. 따라서 單核 이질소착물은 Lew i s 의 영기로 반 응할 것이 기대된다. 특히 N_N 신축전동수가 낮은 착물은 더욱 그러 할 것 이 다. 트란스 -ReCl(N2) (P(CH3)2CCsHs))4 에 서 N_N 십 축전동수는 비 교적 낮은 1925cm-1 이 며 , 이 착물중의 배위 된 이 질 소는 현재까지 알려진 배위된 이질소 중에서 가장 영기성이 센 것 으로 알려 졌 다. 49) 따라서 CrCl3(THFh Ti Cl i T HF)2, MoC14, Al(C2H5) 3, TaCl5 및 NbCl5 등의 Lewi s 산 과 반응하여 다리 이 질 소 二核착물을 생 성 한다(식 (4.11) 참조).
47) P. Fin n and W. L. Jol ly, Inorg, Chem, 11, 1434Clfl1 2 ). 48) G.J. Leig h , J.N . Murrell, W. Bremser and W.G. Procto r , Chem. Comm:m. , 1661(1 9 70). 49J) . J.O rCgha a ntot m, etT, hCe hReema.c, ti 1o0n 0s , o1f 7 CDlifnl1 i 5t r)o. g en in its Mononuclear Comp le xes•,
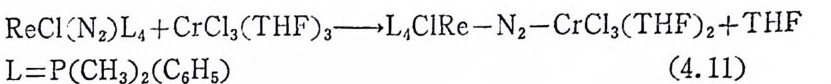 ReCI
ReCI
3) 이 질소착물의 양성 자첨 가반응 ( p ro t ona ti on) 분리 확인된 이질소착물중의 이질소에 양성자첨가반응(p ro t ona ti on) 을 일으키기 위한 많은 시도가 있었다. 그러나 대부분의 경우 에 배위된 이질소는 단순히 치환(또는해리)되든지, 또는금숙에 양 성자첨가반응이 일어날분이다. 그러나 한편 Chatt 둥은 두개의 이 질소를 배위하고 있는 W(O) 착물이 실온에서 H2S04 와 반응하여 암 모니 아를 생성함을 발견하였다(식 (4.12) 참조). 최소한 착물의 90%
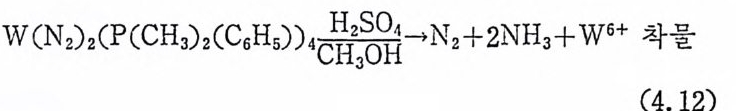 W(N2)2CP(CH3)2CC 晶 ))4 溫醫 -->N2+2NH3+W6+ 착물
W(N2)2CP(CH3)2CC 晶 ))4 溫醫 -->N2+2NH3+W6+ 착물
가 석 (4.12) 에 의해서 반응한다. 배위된 두개의 이질소중에서 한 개는 환원되고, 나머지 한 개는 반응하지 않고 그냥 해리됨이 분명 하다. 텅스밴금속은 이질소의 환원에 필요한 6 개의 전자를 제공하 는 것으로 추측된다. 4 개 의 P(CH3)2CCsHs) 리 간드 대 신에 두 개 의 dip h os((CsH5)2PCH2 CH2PCC 감 I s)2) 를 배위하면서 두개의 이질소를 배위하고 있는 W(O) 착물 및 Mo(O) 착물은 양성 자첨 가반응을 일으켜 H2N2( 암모니 아 생 성반응의 중간체로 생성되는) 리간드를 배위하고 있는 착물을 생성 한다(식 (4.13) 참조). 49) 여 러 종류의 포스핀과 할로겐을 사용하여 M0Cl2(H2N2) (dip h os)2 와 비슷한 많은 착물들이 합성되었다. 하나의 c1- 이 해리된
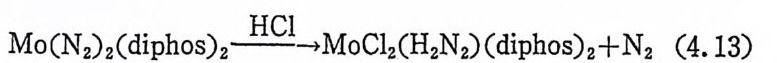 Mo(N2)2(d ip hos)2 ―H―Cl크 M0Cl2CH2N2)(d ip hos)2+N2 (4.13)
Mo(N2)2(d ip hos)2 ―H―Cl크 M0Cl2CH2N2)(d ip hos)2+N2 (4.13)
〔 M0Cl(H2N2)(d ip hos) 』 [B(C 晶 )d 도 합성된 바 있으며, x- 선에 의 한 구조분석 결과에 의 하면 M0Cl2CH2N2) (dip h os)2 에 서 와 [MoCl CH2N2)(d ip hos)2 J+에서의 Mo-CH2N2) 의 결합은 각각 아래 그립 (a) 및 (b)와 같을 것으로 추측되 었다.
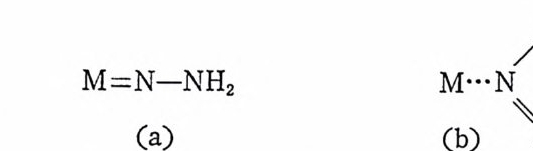 M=N(a—) NH 2 M(b…) N \ NHH
M=N(a—) NH 2 M(b…) N \ NHH
지르코늄(JI)-이질소 착물 {[C5(CH3)sLZr(N2)}2N2 은 양성자첨 가반응을 일으켜 히 드라전 (N2H 4 ) 을생 성 한다. 50) 나트듐 아말감과 〔 Cs(CH3)s Jz ZrCl2 를 질소하에서 반응시키면 얻어지는 상기 Zr(O) 一 이질소 착물은 -80°C 에서 HCl 과 반응하고 난 다음 실온까지 온 도를 높이면 N2,H2 및 N2H4 등의 생성물을 내어놓는다(식 (4.14) 참 조). 식 (4.14) 를 자세히 이해하기는 쉽지 않겠지만 二核 지르코늄 (JI)-이질소 착물이 4 개의 전자를 내어놓고 산화되었으며 배위되 었던 N2 가 4 개의 전자를 받아 N2H4 로 된 것은 확실하다. 상기 Zr( Il )-이 질소착물, 〔 L2Zr(N2) ]z N2(L=C5(CH3)5) 의 분해 반응(식
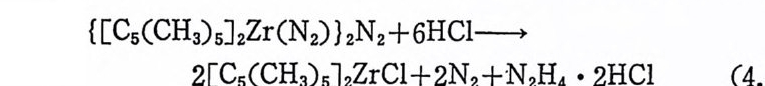 { [Cs(CH3) sJ2 Z r(N2) J2 N2 + 6HCl 一
{ [Cs(CH3) sJ2 Z r(N2) J2 N2 + 6HCl 一
(4.14) )에서 실제로 환원되는 N2 는 어떤 것인가를 조사하기 위하여 아래와 같은 실험도 진행되었다. [L 2Ti (N 2)J2 N 2 중에 치환되기 쉬 운 두개 의 끝(t erm i na l) N z( [L2T i(선 2) Jz N2) 를 15N2 로 치 환시 켜 [L 2Ti (15N2) J N2 를 만든 다음 HCl 과 반응시키고 이어서 열분해시켜 본 걷 과 발생되는 이질소분만 아니라 히드라진도 “N 을 포함하고있음을 ` 알았다. 죽 다리 N2 분 아니 라 끝(t erm i na l) N2 도 환원됨 을 알았다. 이상의 실험적 견과를 명확히 설명하려면 좀더 많은 정보가 얻어져 야 할 것이다. 4) 배위된 이질소의 아실화반응 (ac y la ti on) 및 알킬화반응 (alky la ti on ) 안정한 이질소착물이 영화 유기산 (or g an i c aci d chlor i de) 과 반응하 여 질소를 포함하는 유기 화합물이 생 성 되기 도 한다. Chatt 등에 의 하면 이질소를 두 개 배위하고 있는 텅스텐 (0) 착물(W CN2)z
50) J. M. Manriq u ez and J. E. Bercaw, J. Am. Chem. Soc. , 96, 6229(1 9 74).
(d ip hos)2) 은 석 (4.15 ) 와 같이 영 화아세 탈과 반응한다. 51) 반응 혼합
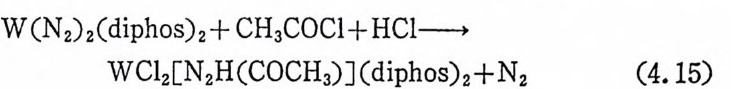 W(N2)2(dip h os)2+ CH3COC1+HCl 一
W(N2)2(dip h os)2+ CH3COC1+HCl 一
물에 존재하는 미량의 水分에 의해서 HCl 이 생성되어 식 (4.15) 에 서 쓰여지는 것으로 알려졌다. 따라서 트리에틸아민을 가하여 HCl 울 제거하면 석 (4.16) 의 반응이 일어난다. W(N2COCH3) 부분의
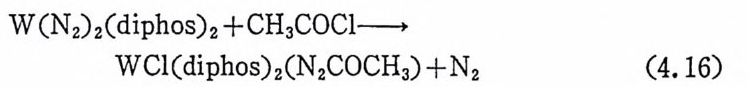 W(N2)2(dip h os)2 +CH3COC1 一
W(N2)2(dip h os)2 +CH3COC1 一
구조는 아래 그림과 같이 아실-아조 (ac y l-azo) 리간드를 배위하는 것 으로 제시되고 있다. 반응속도는 대단히 느리지만 할로겐화 알킬
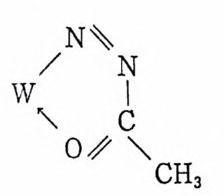 w\/ N\ . NcI
w\/ N\ . NcI
도 배위된 이질소와 반응하는 예가 알려져 있으며 이 반응은 빛쬐 임 (i rrad i a ti on) 에 의 해 서 반응속도가 빨라지 는 것 으로 알려 져 있 다. 할로젠화 알킬은 W(N2)2(dip h os)2 및 Mo(N2) (d ip hos)2 와 반응하여 WBr (N2R) (dip h os) 249) 와 Mol (N2R) (dip h os) 252) 를 생 성 시 킨 다. 두 착물에 서 모두 M 一 N ― N 배 열은 직 선에 가깝고 N 一 N 一 C 각은 120° 및 142° 로 밝혀졌다. 테트라히드로푸란 (THF) 및 부름화메틸 촌재 하에서 상기 W(O) ―이질소 착물에 빛을 쪼이면 (366nm), 배위된 이질소와 THF 가 반응을 일으켜 THF 의 고리가 열리며 (I)-디아조 부탄올 리 간드를 배위하고 있는 금속착물, [MBr(N - N=CH(CH2)3 OH)(d ip hos)2]Br 이 얻어진다 .53) 이상의 반응에 관한 메카니즘도
51 ) J. Chatt , G. A. Heath and G. J. Leig h , C!:em. Commun. , 444, (1972). 52) V. W. Day, T. A. George and S. D. A. Iske, J. Am. Chem. Soc. , 97, 4127 53()1 9P7. 5C).. Bevan, J. Chatt , R. A. Head, P. B. Hi tch cock and G. J. Leig h , Chem. Commun. , 509(1 9 76).
알려져 있지 않다. 1) 전이금속착물에 의한 질소고 정뉘 전망 이제 확실히 질소는 더 이상 不活性 기체가 아니다. 새로운 안정 된 이질소착물이 계속 만들어지고 있다. 그런가 하면 한편 배위된 이질소는 이미 실험실조건 (m i ld cond iti on) 에서 질소화 이온 (n it r i de i on) 으로 환원되고 있다. 이상의 질소환원 방법이 현재 공업적으로 얻어지는 암모니아 생산에, 비용면으로, 비교되지는 못한다. 그러 나 암모니아는 질소화학에서 초기물질에 지나지 않는다. 전이금속 착물에 의한 균일촉매반응 분야에서 최근 10~20 년 사이에 이룩된 질소분자의 활성화는 아민류, 아미드류, 니트닐류 동 질소를 포함 하고 있는 화합물의 생산과정으로 고려할 충분한 가치가 있다. 전이금속착물에 의한 질소고정에는 몇 가지 문제접이 있다. 금속 에 배위되어 있는 이질소몰 환원시키는 과정에서 전이금속의 산화 상태가 어떻게 변하느냐 하는 것이 문제 중의 하나다. 위에서 기술 한 것처럼 하나의 전이금속이 6 개의 전자를 제공할수도 있지만(예 V(-Ill) ―지 (Ill)+6e-) (재 4 장 2 의 (2),1) 참조) 역시 및 개의 전자 룰 동시 에 전달하는 과정 이 문제 다. 따라서 多核착물 (clus t er 또는 pol yn uclear) 촉매 에 의 한 질소의 환원이 기 대 되 기 도 한다. 위 에 시 예 로 돈 바와 같이 LzCN2)Zr-N2-Zr(N2)L2CL=CsCCH3 )5 ) 를 사용 하는 경우 각 지르코늄 원자는 단 두 개의 전자를 제공하여 배위된 이질소를 환원시킨다(식 (4.14) 참조). 제 4 장에서 소개한 질소환원 의 실험적 결과들도 실제로 어떤 多核착물의 중간체를 거쳐 진행될 수도 있다. 이런 문제믈 연구하기 위하여서는 반응속도 측정을 통 한 메카니즘 규명 둥이 도움이 될 것이다. 이질소의 걷합형대도 중요한 관접이 될 수 있다. 현재까지 분 리 , 확인된 대 부분의 착물이 이 질소를 끝으로 배 위하고 있지 만 (end on bond i n g하고 있지만) 위에서 기술한 것처럼 옆결합 (s i de-on bon-
겨< 참고 문헌 1) A. D. Allen and F. Bott om ly, Accounts chem. Res. , 1, 360(1 9 68). 2) R. W. F. Hardy , R. C. Burns and G. W. Parshall, Adv. Chem. Ser. , 100, 219(1 9 71). 3) J. R. Postg a te , Chemi st r y and Bi oc hemi st r y of Ni tro g e n Fi x ati on , Plenum Press (19 71 ) . 4) J. Chatt , J. R. Dil w orth and R. L. Ric h ards, Chem. Rev. , 78, 589 (19 78). 5) F. Bott om ley and R. C. Burns, Edit . , Treati se on Di n it ro g e n Fix a ti on , Wi ley ( 19 79). 6) P. Sobota and B. Jez owska-Trezebia t o w ska, Coord. Chem, Rev. , 26, 71(1 9 78). 7) J. Chatt , The Acti va ti on of Molecular Ni trog e n•, in: D. Dolph in and B. R. Jam es, Edit . , Bio l og ica l Asp ec ts of Inorga nic Chemi st r y , Wi ley ( 19 77) . S) J. E . Bercaw, The Acti va ti on of Molecular Ni tro g e n , in: M. Tsuts u i and R. Ug o , Edit . , Fundamenta l Research in Homog e neous Cata l ys i s , Plenum (19 77) .
제 5 장 기타 중요한 반웅들 1. 일 산화탄소의 산화반응 일산화탄소의 산화반응은 有毒기체의 제거라는 목적하에 그리고 유기화합물 합성에 새로운 방법을 연구 개발하는 목적으로 연구되 어오고 있는 과제이다. 유독한 일산화탄소를 무해한 이산화탄소로 바꾸려는 데 관련되는 제 문제접을 해결하기 위한 연구는 오늘날 활 발하게 진행되고 있다. 일산화탄소의 제거는 여시 촉매를 사용함으 로써 가능할 것이다. 촉매반응은 일반적으로두가지로구분되는 바 均―觸媒反應 (homo g eneous cata l ys i s ) 및 不均一觸媒反應 (he t ero g eneous · ca t al y s i s) 로 불리운다. 군일촉매반응에서는 모든 반응물질이 촉매를 포함하여 동일상(주로 용액상)으로 존재하는데 불군일촉매반응에 서는 반응물질이 두 개 이상의 상(주로 고체[촉매]상 및 기체상 또 는 액체상)으로 촌재한다. 오랫동안 대부분의 화학공업에서는 주로 불군일촉매반응이 응용되어 왔다. 그러나 근래(약 25 년 전부터)에 는 군일촉매반응도 많이 공업적으로 응용될 분 아니라 어떤 경우에 는 군일촉매작용이 더욱 중요하게 응용되고 있다. 상기 두 촉매반 옹은 각각 그 특성을 지니고 있다. 예를 둘떤 군일촉매반응은 선댁 성 (selec ti v ity)이 높고 반면에 불군일촉매 는 다양성 (div e rsit y) 및 활 성 도 (ac ti v ity)가 높다. l) 1) A. L. Robin s on, Sc ien ce, 194, 1150(1976)
용액에서 전행되는 군일 촉 매반응을 연구함으로써 얻을 수 있는 · 것 중에서 특히 중요한것은 반응메카니즘을 조사하는 데 유용한 정 보를 얻을 수 있다는 접이다. 죽 높은 선덱성으로부터 유도되는 유 일한 중간체 (i n t ermed i a t e) 를 분리 하여 분석 할 수 있을 뿐 아니 라, 여 러가지 분광학적 분석기기(예문 들면 시료가 용액으로 있어야만 측 정가능한 핵자기공명)를 이용하여 용액 중에서 조사될 수 있는 장접 을 이용하여 반응메카니즘을 연구할 수 있다는 접이다. 여기에서는 군일촉매반응에 의하여, 특히 전이금속착물을 촉매로 사용하여 일산화탄소를 이산화탄소로 산화시키는 촉매반응을 고찰 하고자 한다. 지금까지 보고된 일산화탄소의 산화반응은 다음의 세 가지 유형으로 분리될 수 있다(식 (5.1), (5.2) 및 (5.3) 참조).
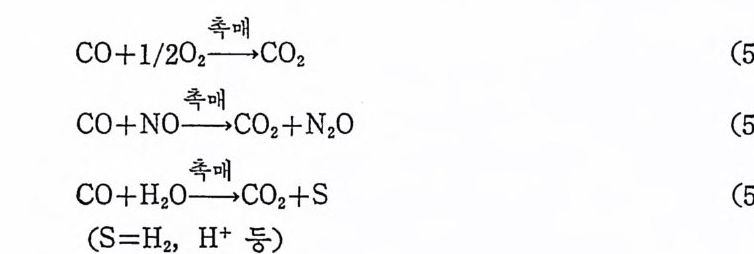 촉매
촉매
(1) 일산화탄소의 활성화 (ac ti va ti on of carbon monoxid e ) 전이금속의 배위화합물에서 일산화탄소는 가장 중요하고 유용한 리간드이다. 일산화탄소는 무기합성화학에서 널리 쓰여질 뿐 아니 라 유기화합물 합성에도 많이 이용되고 있다. 모든 전이금속은 최 소한 한 가지 형태 이상으로 일산화탄소 (CO) 와 배위화합물을 형성 하고 있 다. CO 는 전이 금속과 결합할 때 시 그마주게 (11-donor) 이 며 동시 에 파이 전자받게 (n-acce pt or) 로 알려 쳐 있 다. 이 러 한 결합 메 카 니즘은 많은 안정한 전이금속一일산화탄소 화합물의 촌재를 설명한 다. 일단 전이금속에 배위된 다시 말해서 전이금속에 의해서 활성 화된 CO 는 그 화학적 및 물리적 성질이 배위되지 않은 자유로운 co 의 그것과는 상당히 다르다. 예를 들면 자유로운 co 분자의 C- 0 신축전동수는 2143cm 크 인데 비 하여 전이 금속에 배위된 co 의 신
축전동수는 대 략 2125~1850cm-1( 끝(t erm i na l) CO) 및 1850~1700 cm-1( 다리 (brid g ing ) CO) 정 도이 다. 2) 이 상의 데 이 타는 co 가 전이 금속에 배위됨으로 안해서 C 와 0 사이의 결합력이 약해졌다는 증 거이다. 그리고 자유로운 co( 배위되지 않은 CO) 가 비교적 반응성 이 낮은 반면에 전이금속에 배위된 CO 는 반응성이 높고 다양하다 는 사실도 둘 수 있다 .3),4) 전이금속에 배위된 CO 는 또한 쉽게 치 환 또는 해 리 (d i sso ci a ti on) 되 기 도 한다. 이 렇 게 하여 새 로 치 환되 어 전이금속에 배위되는 다론 리간드룹 활성화시켜 주거나, 또는 CO 의 해리에 의하여 생기는 전이금속 주위에 빈자리 (vacant s it e) 를 형 성하여 분자내 자리 바꿈반응(i n t ramolecular rearrang e ment) , 새로운 리간드의 첨가반응, 그리고 치환반응 등의 새로운 화학적 변화를 일으키게 한나 이상의 전이금속 -co 화합물의 성질을 고려한다면 CO 를 배위할 수 있는 전이금속 화합물은 co 의 산화에 쓰여질 촉 매가 될 수 있는 가능성이 크다고 볼 수 있다. CO 를 배위 할 수 없는 전이금속 화합물은 co 의 산화반응에 측 매로 쓸 수 없다는 것은 결코 아니다. CO 를 배위하지 않은 금속화 합물이타도 co 룹 배위하고 있는 금속화합물보다 여러 가지 면에서 더욱 우수한 co 산화반응의 촉매가 될 수 있다. 한가지 예로서 어 떤 전이금속 화합물은 직접 CO 를 배위하고 있지 않더라도 CO 를· 산화시킬 수 있는 02; NO 및 H20 등을 배위하여 활성화시킬 수 있 기 때문이다. C0,02,NO 도는 H20 등의 배위화합물이 분리, 확인 된 적이 없는 전이금속 화합물일지라도 어떤 특수한 조건하에서는 상기의 리간드를 약하게나마 배위할 수도 있다. 예를 들면 용액 중 에 서 co( 또는 아, NO, H20) 의 농도가 크면(즉 co 의 압력 이 높~ 면) 전이금속― CO 를 형성하지만 CO 를 제거하면 곧 CO 를 잃어버 리는 금속화합물도 많이 보고되고 있다. 이러한 성질을 가지고 있
2) F. A. Cott en and G. Wi lk in s on, Advanced Inorga nic Chemi st r y . 3rd Ed. , p. 687, Joh n Wi le y and Sons, 1972. 3) M. M. T. Khan and A. E. Marte l l, Homog e neous Cata lys i s hy Meta l Com- plc xes, Vol, 1, p, 293, Academi c Press, 1972. 4) G. Henric i-O liv e /Ol ive , Coordin a ti on and Cata l ys is (Monog ra p h in Mod- ern Chemi st r y Ser ies) , p. 234, Verlag Chemi e- Wein h eim , 1977.
는 금속 화합물도 또한 co 의 산화반응에 촉매 작용을 할 가능성 이 있다. (2) 일산화탄소와 산소의 반응, CO+l/202— -CO 2. 촉매 전이금속착물 용액을 촉매로 사용하여 CO 를 산화시키는 데 분자 상태의 산소 (Oz) 를 반응물질로 사용한 예를 자세히 살펴 본다. Roundhil l 둥은 로듐 뭉치 화합물 (clus t er), Rh6(C0)1s 을 촉매 로 하여 CO 와 야 의 반응으로부터 C 아 를 얻 었 다(식 (5. 4) 참조). 촉매
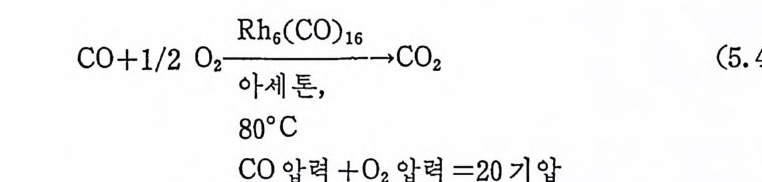 CO+l/2 OzRh-6(-C+0)1C6 Oz (5. 4)5)
CO+l/2 OzRh-6(-C+0)1C6 Oz (5. 4)5)
' (또는 촉매의 전구물질(p recursor)) 로 사용된 Rh6(CO)16 는 상온, 상 압하에서 아세톤에 거의 녹지 않는다. 분만 아니라 용매인 아세돈 이 없거나 핵산 서스펜션에서 상기 촉매반응은 일어나지 않는다. 그러므로 비교적 높은 온도와 높은 압력하에서 반응이 진행된 것은 반응속도의 증가에 의한 효과도 있겠지만 역시 상기 반응은 군일촉 매는 반아응 의의 압목력성 이을 나 나 c타o낸 의 예압 이력 다에. 무상관기하 며반 응자(유식 라(5디. 4 칼) ()f의r ee반 r응ad속ic a 도l) 의 스캐빈저 (scaven g er) 에 의해서 현저히 감소된다 .5) 그러므로 상기 촉매반응(식 (5.4) )은 자유라디칼메카니즘으로 진행되리라고 Roun- dhil l 등은 보고하고 있지만 더이상 구체적인 반응 메카니즘은 제시 되지 않고 있다. Vaska 둥은 동일한 로듐 뭉치화합물인 Rhs (C 0)16 을 사용하여 상온, 1 기압 (CO 의 기압 +02 의 기압)하에서 co 의 산
5) a) G. D. Mercer, J. S. Shu, T. B. Rauchfu s e and D. M. Roundhil l, l. Am. Chem. Soc. , 97, 1967(1975). b) G, D. Mercer, W. B. Beauli eu and D. M. Roundhil l, J. Am. Chem. Soc. , 99, 6551Cl'J l7). 6) Chong Shik Chin , M. S. Sennet and L. Vaska, /. Mol. Cata l ys i s , 4, 添 (1978).
화반응이 일어 남을 보고하였 다(식 (5. 5) 참조). 6) 석 (5. 5) 에 서 보는 바와 같이 식 (5.4) 과 다른 접은 아세돈 대신에 디메틸포동알데히 드 (DMF) 를 용매 로 이 용했다는 점 이 다.
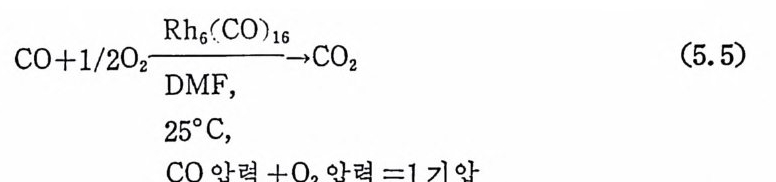 co+112R0h62( C- O-) .16c o2 (5.5)
co+112R0h62( C- O-) .16c o2 (5.5)
DMF 를 용매로 사용할 경우에 촉매반옹(식 (!'i .5) )은 상온, 상압 ·( 1 기압)하에서 전행된다는 사실은 용매의 중요성을 보여준좋은예 이다. 균일촉매반응에서 촉매(또는 촉매의 전구물질)로 쓰이는 전 이금속 화합물의 용해도는여러 가지 면에서 중요하다. 용매를 선택 하는 데는 고려할 점들이 있다. 용매는 혼히 자신이 전이금속에 배 위되어 최초에 용해시켜준 전이금속 화합물과는 다론 화합물을 형 성한다. 그러므로 실제 촉매여할을 하는 화합물도 새로 형성된(용 메가 배위된) 화합물일 수도 있다. DMF 는 용매의 역할(군일계를 만드는 역할) 이의에도 그 분자 자신이 전이금속에 배위하기도 하 며 6) 또한 전이금속一 co 착물을 형성하는 데 co 의 공급물질이 되 기도 한다. 죽 DMF 는 경우에 따라 용매 또는 배위되는 리간드 또는 co 의 공급물질 등제 가지로이용된다. RblC0)16 는 THF( 테 트라히 드로푸란)에 녹아 맑은 갈색 용액 (I Rh6(CO) 리 =3. 0 X 10-4M) 울 이루지만 촉매적 활성이 없다는 사실은 6) 또한 DMF 의 역할이 단순한 용매 에 그치 지 않음을 제시 한다. N2 또는 co 하에 서 Rh6(C 0)16 는 DMF 에 녹아 적 갈색 용액 ([Rhs(C0)15]=3. 0 x 10-3M) 이 되 며 아무런 변화를 보여 주지 않고 CO 와 야 하에 서 는 유발기 간(i ndu cti on p er i od) 이 없 이 즉시 C 아를 생 성 하기 시 작한다. C 야 생 성 시 작 이후 약 1 시간이 지나면 적갈색의 용액은 보라색 용액으로변한후 오랫동안(약 4 일간) 변색이 없으면서 촉매반응(식 (5.5) )의 활성을 보여 준다 .6) Rh6(CO)16 는 홀로 02 와 반응하여 C 아를 생성하지만
7) K. Vrie z e, J. P. Collman, C. T. Sears, Jr. , and Kubota , Inorg. Sy n th e sis , 11, 10.1 (19 68).
DMF 용액에서 그리고 CO 와 0215} 에서 새로운 촉매(보라색 용액) 를 형성하는 것으로 추측된다. 실제 촉 매가 어떤 물질 인지는 현재 연구 조사중이다. 실제 촉매의 역할을 하는 물질이 무엇인지 조사 하기 위하여 촉매활성이 있는 보라색 용액을 갑자기 냉각시켜 짙은 갈색고체를 분리하였다. 이 질은 갈색고체의 적의선 스 펙 트럼은 CO 의 신축전동 흡수떠 (absorpt ion band) 를 보여 주지 않으며 DMF 의 며 (band) 들을보여 주었다. 이 질은 갈색의 고체가 보여 준 DMF 의 흡수떠들은 금속에 배위되지 않은(자유로운) DMF 의 흡수떠들과 같은 진동수를 갖지 않는다. 죽 이 고체 내의 DMF 는 Rh 에 배위 되어 있는 것 같다. 또 하나의 실험에서 Vaska 둥은 Rh6(C0)16 을 DMF 에서 아와 반응시켜 (식 5.6) 을 제시하였다 .6) 산소와 반응시 킨 후 얻은 용액은 상기 촉매반응(식 (5.5) )에 비활성이지만 아를 제거하고 CO 와 반응시켜 얻은 용액은 촉매반응(식 ( 5 .5)) 에 다시 활성을 보여 준다. 이상 사실은 특히 촉매반응에서 중요한 접이다.
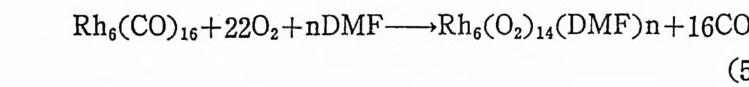 Rhs (C 0) 16 + 2202 + nDMF---+Rhs (02 ) 14(DMF)n + l6C02
Rhs (C 0) 16 + 2202 + nDMF---+Rhs (02 ) 14(DMF)n + l6C02
죽 반응식 (5.6) 이 가역반응일 수도 있지만 산화에 의하여 활성도가 낮아지거나 또는 그 활성이 없어전 촉매를 재생시킬 수 있다는 가 능성 을 보여 준 접 이 다. Vaska 둥은 또한 Rhs(C0)16 와 야 의 반응 에서 Rhs(C0)16 중의 다리 (brid g ing )C O 가 끝(t erm i nal) CO 보다 먼 처 아와 반응하여 C 아를 형성함을 알았다 .8) 현재까지의 연구결 과중 식 (5.5) 의 반응속도는 아의 압력에 일차적으로 비례하고 CO 의 압력에 무관하다는 사실을 얻고 있지만 8) 반웅메카니즘에 관한 더욱 많은 실험이 요구되고 있다. 새로 합성된 Pt (O ) 二核착물인 Pt 2 (µ-PCP)a(PCP=(C6Hs)2PC H2PCCsH 야) 또한 상온, 1 기압 (CO 기압 +02 기압)하에서 co 의 산· 화반응에 촉매 적 역 할울 한다(식 (5. 7) 참조). ” 이 새 로운 화합물 Pt 2 (µ-PCP)a 은 상온, i 기 압하에 서 CO 와 가역 적 으로 반응하며 아 의-
8) Chong Shik Chin and L. Vaska, unp u blish ed results. 9) Chong Shik Chin and L. Vaska, Inorg. Ch im. Acta , 31, L443 (1978).
는 비 가역 적 으로 반응하여 이 산소 (d i ox yg en) 착물을 형 성 한다(식 (5. 8) 및 (5. 9) 참조). 9)
 Pt 2( µ- P CP)3
Pt 2( µ- P CP)3
일단 합성된 P t 2(µ-PCP)a 는 CO 와 반응하여 오직 하나의 화 합물인 두개 의 끝 -CO 를 갖는 (CO)P t (µ-PCP)3P t (CO) 를 생 성 한 다. 그러나그이유는현재 설명되지 않고있지만합성과정에서 CO 와 반응시키면 다리 CO 를 갖는 화합물인 P t (µ-CO)(µ 一 PCP)aP t 를 만들 수 있다(식 (5.10) 참조 ).10) 죽 P t 2(µ ― PCP)a 는 CO 와 반응하 여 두 개의 끝 -CO 를 갖는 화합물 (CO)P t(µ― PCP)3P t (CO) 를 형성 하지만 조전에 따라서 다리― CO 를 갖는화합물을 형성할 가능성도 있다. 실제 Pt 2 (µ-PCP)3 분자의 모형도 다리 -co 화합물의 가능성
10) Chong Shik Chin and L. Vaska, unp ub li sh ed results .
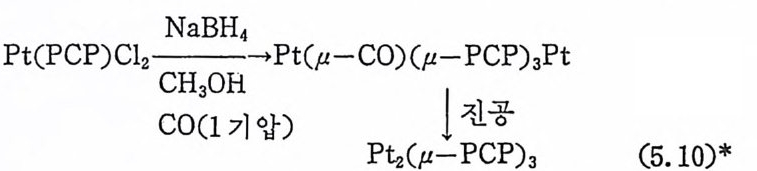 NaBH4
NaBH4
* P t (µ-CO)(µ-PCP)3P t의 수율은 PCP 를 기 준으로 하여 80% 정 도이 며 식 (5. 10) 의 화학량져 조자는 더 이 상 진행 되 지 않았다.
올 보여 주고 있다. 촉매반응 식 (5.7) 은 4~5 일이 경과된 후에는 더 이상 전행되지 않는다. 02 는 반응물이며 동시에 촉매반응의 여제 물질 (inh ib i t or ) 역 할을 한다. 아 는 이 산소 (d i ox yg en) 화합물 (02)P t 2 (µ-PCP)3 울 형 성 하지 만 동시 에 서 서 히 PCP 산화물, (C6Hs)2POC H2PO(C5Hs)2 를 부산물로 만든다. 9) PCP 산화물의 형 성 은 촉매 (또 는 촉매 의 전구물질)인 P t 2(µ-PCP)a 를 파괴 하는 원인이 될 것 이
다. 어는 전형적으로 아가 촉 매반응을 저해하는 경우중의 하나다. 특히 포스판 ( p hosph i ne) 리간드를 갖는 전이금속 화합물을 촉매로 사용하는 산화반응의 문제점으로 연구, 조사되고 있 는 경우의 예이 다. 또다른 경우로는 아와 전이금속이 반응하여 불용성인 금속산 화물을 형성하여 촉매반응의 전행을 저지시키는 경우도 있다. 아에 의한 처해작용은 아의 압력에 비하여 상대적으로 높은 co 의 압력 (Pco>Po2) 을 사용함으로써 그 효과를 감소시 킬 수 있 다. 이 런 조 건 (Pco>Po2) 하에서는 그 부작용으로 co 의 산화속도 자체가 상당 히 느려질 가능성이 있다. 전이금속착물을 이용한 군일촉매반응 중 아에 의한 co 의 산화반 옹은 아칙 초기의 연구단계에 있다고 볼 수 있다. 상기한 바와 같 이 그 반웅메카니즘둥에 관하여서는이렇다 할 제시가 없는 단계이 다. 앞으로 많은 관십 과 노력 이 필요한 분야이 다. (3) 일산화탄소와 산화질소의 반응, co+2NO-C02+N20 산화질소 (NO) 에 의한 일산화질소의 산화는 두 가지 목적을 동시 에 얻을 수 있는 효과를 가지고 있다. co 의 제거분 아니라동시에 NO 의 제거 . 또한 취할 수 있다. NO 는 CO 를 산화시키고 자신은 환원되어 비교적 안정한 N20 를 형성한다. 생성되는 N20 는 대량 으로 존재하지 않는 한 유독한 물질은 아니다. 그러나 NO 가 공기 중의 아와 반응(식 (5.11) )하여 쉽게 만드는 N02 는 치명적인 유해 한 기체이다. 전이금속 배위화합물에서 NO 는 양이온 (NO 망, 음이 온 (NO- ) 또는 거의 중성 (N0°) 으로 배위한다. 이는 적의선 스펙트 럼 데이타 및 X- 선결정구조의 결과로부터 제시되어 온접들이다 .1 1)
![]() NO+l /2 0 2 一 N02 (5.11)
NO+l /2 0 2 一 N02 (5.11)
NO+ 오1- NO-는 각각 CO 및 0 군卜동전자(i soelec t ron i c) 관계 이 다. 따라서 NO 에 의한 co 의 산화반응의 연구는 직접, 간접적으로 02 에 의한 co 의 산화반응에 중요한 정보를 제공할 것이다. 02 에 의
11) K. Nakamoto , Inf ra red Sp ec tr a of Inorga nic and Coordin a ti on Comp ou - nds , 2nd Ed. , p. 200, Wi ley • l nte r scie n ce, 1970.
한 NO 의 산화반응을 동하여서도 또한 02o J] 괴한 co 의 산화반응 에 유용한 지식을 언을 수 있을 것이다. 식 (5.11) 은 촉매의 도움 없이 쉽게 일어나는 반응이다. 그러나 배위된 NO 가 배위된 상태에 서 그대 로 산화되 여 배위된 N02( 니 트로 금속화합물) 화합물이 되 는 과정 12) 및 금속― N02 화합물이 CO 를 산화시 키 는 경 우등도 13) 포함하여 이 곳에 서 고찰하고자 한다. 전이금속착물을 촉매로 이용한 NO 에 의한 co 의 산화반응은 Jo hnson 등에 의 해 서 처 음 그 가능성 이 보고되 었 다. 14' Jo hnson 등 에 의해서 발표된 식 (5.12) 는 두 가지 접에서 중요한 반응이 된다.
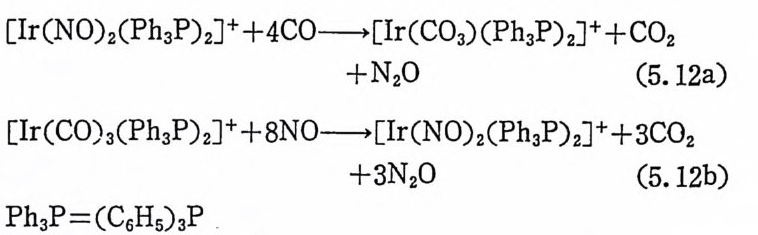 [Ir(N0)2(Ph3P)2]+ +4CO 一〔 Ir(C03) (Ph3P) 나+ + CO2
[Ir(N0)2(Ph3P)2]+ +4CO 一〔 Ir(C03) (Ph3P) 나+ + CO2
첫 째 는 〔 Ir(N0)2(Ph3P)2 J+로부터 [Ir(C0)3(Ph3P)2]+ 를 거 쳐 다시 [Ir(N0)2(Ph3P)2 J+가 될 때까지 4N20 와 4C02 를생성시켰다는 것, 즉 촉매 반응의 순환과정 (cata l yt ic c y cle) 을 지 나면서 생 성 물을 만들 어 냈다는 접이다. 둘째는 배위된 NO 와 co 의 반응, 그리고 배위 된 CO 와 NO 의 반응에서 모두 C 아와 N20 를 공히 만들 수 있다 는 접이다. 이 접은특히 메카니즘 연구조사에 큰 도움이 될 가능성 이 있다. 반응물질 중의 어느 물질 (CO 또는 NO) 이 먼처 전이금속 에 의하여 활성화되더라도 촉매반웅이 일어난다는 사실은 중간체의 분리, 또는 연구조사에 유리할 분 아니라 반응속도 측정방법에 다 양성을 제공하기도 한다. 이어서 lbers 둥은 위와 유사한 Ir 화합물 울 CO 와 반응시켜 CO2 와 N20 를생성시켰다(식 (5.13),(5.14),(5.15} 참조). l” 이 어 서 Ei se nberg 둥은. RhCI3 • 3H20 가 CO 와 반응하여 CO:-
12) J.A... McCleverty , Chemi ca l Revie w , 79, 53(1 9 79). 13) R. D. Felt ha m and J. C. Krie g e , J. Am. Chem. Soc. , 101, 5064(1979)소 14) B. F. G. Joh nson, et al, Chem. Commun. , a) 650(1 9 73), b) 309(1 '574 ). 15) B. L. Haym ore and J. A. Ibers, I. Am. Chem. Soc. , 96, 3325(1'5 74 ).
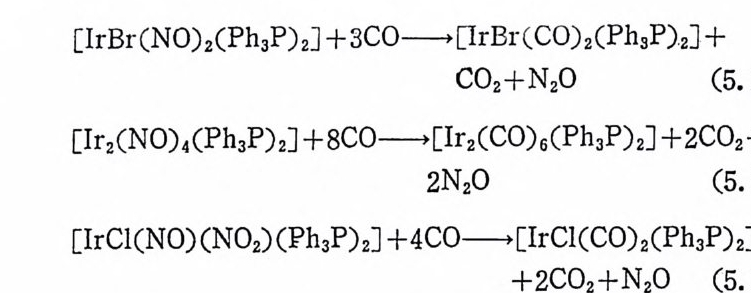 [lrBr (N 0)2(Ph3P) 니 + 3CO 一 [IrB r(C0) 2( PhsP)2J +
[lrBr (N 0)2(Ph3P) 니 + 3CO 一 [IrB r(C0) 2( PhsP)2J +
를 생성한다는 사실(식 (5.16) )을 토대로 하여 아래의 실험을 성 공시켰다 .16) 죽 RhCl3 를 촉매로 이용하여 에틸알콜용액에서 co 가
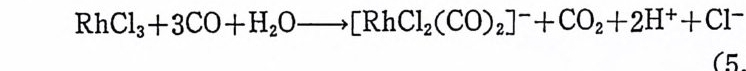 RhC13 +3CO +H20 一 [RhCl z( C0)2 J-+ C02+2H+ + c1-
RhC13 +3CO +H20 一 [RhCl z( C0)2 J-+ C02+2H+ + c1-
NO에 의해 산화되어 C 아 및 N20 를 생성함을 보고하였다. Eis e n· berg 는 또한 이 촉매 반응의 유발기 간(i nduc ti on p er i od) 이 8 시 간(바 교적 긴 시간)이며 이 유발기간 동안에 전한 적색의 용액은 녹색으 로 변하여 촉매 반응의 속도는 대 단히 느림 을 발견 하였 다. 16) RhC13 를 포함하는 용액에 HCl 을 가하거나 또는 용액을 CO 와 미리 충분 히 반응사킨 다음 촉매반응을 시도하면 8 시간이라는 유발기간은 상 당히 짧아진다. 이 같은 사실온 반응식 (5.16) 이 실제 반응의 선수 과정 (p rereq u i s it e) 임을 제시한다. 별도로 합성된 [RhCl z( C0)2]- 울 사용하여 실험함으로써 위의 사실을 증명할 수 있었다(식 (5.17) 참 조). CO 와 NO 하에서 녹색용액과 [R hClz( C 0)2J -사 이에는 평형이 있음을 또한 자외 선스펙 트럼 을 조사함으로써 알았다. 15) 최 근 Vaska
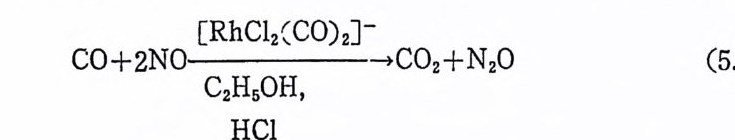 [RhCl2< C 0)2J -
[RhCl2< C 0)2J -
등은 새로 합성 된 P t (O) 화합물이 NO 에 의 한 co 산화반응에 촉매 적 활성 이 있 음을 발견 하였 다(식 (5. 18) 참조). 9) 식 (5. 2) 에 의 한 CO
16) R. Eis e nberg, et al, a) Scie n ce, 184, 568(l r:tl4) , b) J. Am. Chem. Soc. , 98, 4662Clr:t !6 ).
 Pt i(µ- PCP)3
Pt i(µ- PCP)3
의 산화반응에 관한 Joh nson14) 등, 및 Ibers15) 등, Eis nberg1 6 ) 등 및 Vaska 둥에” 의한 연구조사결과를 그 각각에 의하여 제시된 반응 대카니즘에 관하여 아래에 살펴 본다. 최 초로 식 (5. 12) 를 발표한 Joh nson 둥 14a) 은 중간체 로서 5 배 위 착 물인 山 (N0)2(CO)(Ph3P)2 J+을 제시하고 배위된 NO 로부터 산소 (0) 가 배위된 co 에 이동되어 C 아를 형성하고 또하나의 중간체인 소위 금속-니 트렌 (n it rene) 을 형 성 하고 이 어 서 니 트렌은 또 하나의 배위된 NO 와 분자내 반응(i n t ramolecular reac ti on) 을 일으켜 N20 를 형성할 것이라고 제시하였다(식 (5.19) 참조). 그러나 이어서 발표된 보고에 의하면 금속―니트렌 메카니즘의 가능성은 희박해졌다 .15) 즉 Joh nson 둥은 CO2 생 성 에 팔요한 산소 (0) 의 근원을 조사하기 위 한 실험에서 다음의 결과를 얻었다. ® 동일 분자수의 [Rh(1 4 N0)2 (Ph3P)2 J+와 [Rh(1 5 N0)2(Ph3P)2J+ 를 CO 와 반응시 킨 결과 28N20,
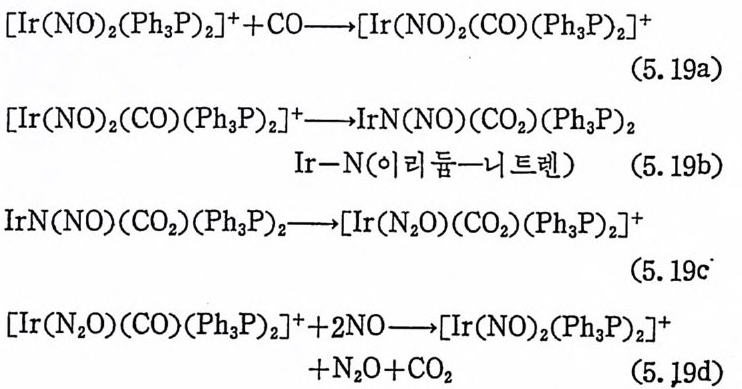 [Ir(N0)2(Ph3P) 2] 나 co 一〔 Ir(N0)2(CO)(Ph3P)2 〕 +
[Ir(N0)2(Ph3P) 2] 나 co 一〔 Ir(N0)2(CO)(Ph3P)2 〕 +
29N20 및 30N20 는 1 : 2 : 1 의 비울로 생성되었다. ® C0-15NO 혼합기 체 하에 서 [Rh(14N0)2(Ph3P)2] +는 위와 동일한 비 율의 N20 기체들을 생성하였다. ® 15NO 와 [Rh(14N0)2(Ph3P)2J+ 사이에
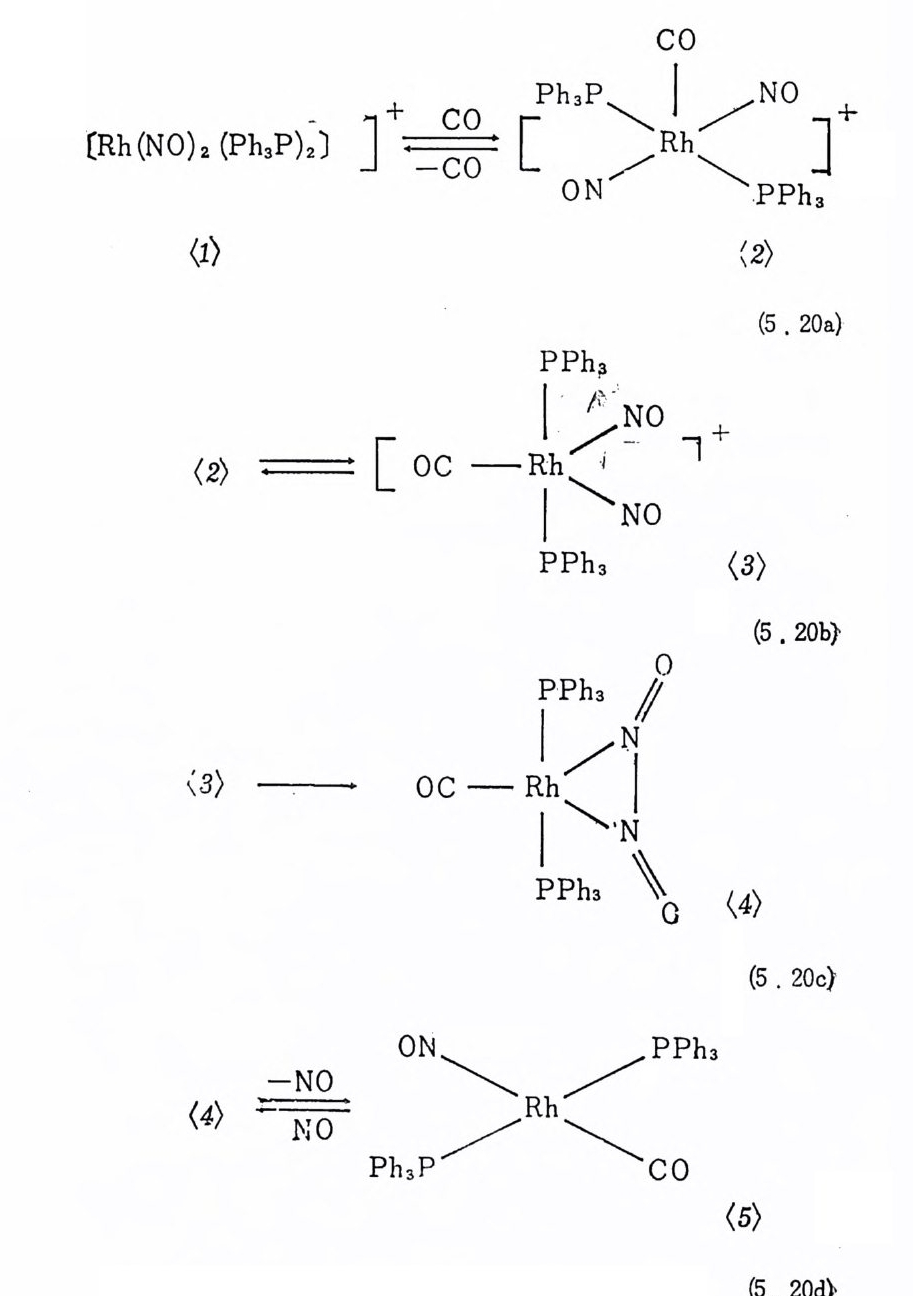 [Rh ( NO) 2 (Ph3P);] 三 [Ph3 P > co< N0 丁
[Rh ( NO) 2 (Ph3P);] 三 [Ph3 P > co< N0 丁
는 NO의 상호교환반응이 일어나지 않았다. @ 이리듐착물로부 터 트리페널포스판 (Ph3P) 리간드는 해리되지 않는다. 이상의 결과 로부터 Jo hnson 등은 금속-니 트렌 메 카니 즘 대 신에 가능한 중간체 로 Rh 一 (N 요) 부분의 형성을 제시하였다(식 (5.20) 참조 )).14b) Pt (Ph3P)n 이 NO 와 반응하여 만들어지는 P t (N2 야 )(Ph3P)z17) 이 CO 와 반응하여 N2O 와 CO2 를 생성하는 예도 후에 발표된 바 있다 .18) 그러나 석 (5.20) 의 반응메카니즘도역시 여러 가지 불충분한접을가 지고 있다. 족 제시된 중간체들 〈 2 〉〈 3 〉및 〈 4 〉을 분리하거나 겁출할 수 없었다는 접 또는 [Rh(CO) a( Ph3P)2 J+가 NO 와 반응하여 [R h(N 못0)하2(는Ph 3접P) 2둥 J이+로다 .되 면Jo서 h nsCoOn2 와동의 N 2동0 위믈원 생소성 실하험는결 과과정는을 14b ) 설R명h하— 지N2 아 중간체를 제시하기에는 불충분한 증거밖에 되지 않음을 Eis e n- berg 둥은 지 적 하였 다. 19) 그후 Joh nson 등은 보충연구에 서 식 (5. 21 ) 과 같은 반응과정율 제시하기도 하였다 .18) Ibers 등은 중간체 로서 N-N 결합이 있는 N2 야 의 배위화합물을 제 시 하였 다. 15) IrBr(N0)2(Ph3P)2 가 IrBr(N2 야 )(Ph3P)2 로 되 고 난 다음 즉 N-N 결합이 형성되고 난 다음 산소 co) 의 전이가 일어날 것이라고 계시하였다. 이상의 lbers 둥의 제의는 N2 아화합물이 중
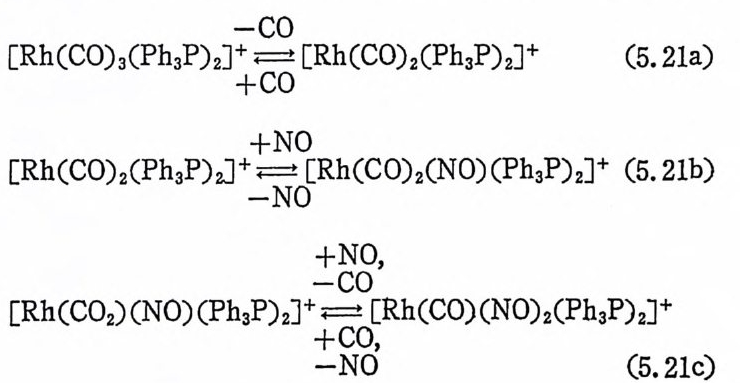 -CO
-CO
17) S. Cenin i , R.Ug o , G. LaMonic a and S.D. Robin s on, Inorg. Chim . Acta , 6, 182 (1'512 ). 18) S. Bhaduri and B. F. G. Joh nson, Transit ion Meta l Chem. , 3, 1210'5 !8) . 19) R. Eis e nberg and C. D. Meye r, Account Chem. Res. , 8, 26(1 9 75).
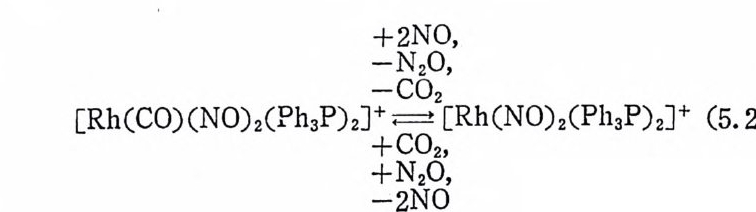 +2NO,
+2NO,
간체로서 제시되었다는 점에서 Jo hnson 둥의 메카니즘과 유사성이 있다. lbers 의 제시는 반응메카니즘을 위한 실험결과에서 얻은 걷 론이 아니고 단순한 제시였다. 다만 Ni (C 0)4 및 [C0Cl. ( en)2(NO)J+ (en= 에 탈랜디 아민)가 NO 와 반응하여 Ni (N O) (N02) 및 [CoCl(e n) z( N02) J+로 되는 과정에서 N i〈 CO)2(N2 아) 및 〔 Co(en)2CN2 아 ]2+ 가 가능한 중간체로 제시되었다는 접을 20) 예로 들고 있다• Eis e nberg 등은 석 (5. 17) 에 관한 반응메 카니 즘 연구에 서 아래 의 내용을 보고하였다 .16 b) 죽 오렌지색〔 RhCl 2 〈 CO) 』-과 NO 一 co 혼합 기체(몰분율 =4 : 3) 는 녹색 중간체 용액을 형성하는데 이 녹색 물 질은 [RhCl2(CO)(N0)2] -일 것이 라고 제시하였다(식 (5.22) 참조). 〔 RhCI2(CO)(N0)2 J-는 분리 , 확인되지 않았지만 Jo hnson14b ' 둥이
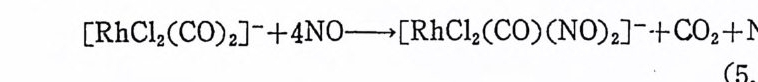 [RhCI2(C0)2J -+ 4NO— +[Rh Clz( C O)(N 0)2J -+ C02 + N20
[RhCI2(C0)2J -+ 4NO— +[Rh Clz( C O)(N 0)2J -+ C02 + N20
제시한 중간체인 [Rh(CO)(NO)lPh3P)2 J+(석 (5.20) 의 g)와 등전자 화합물(i soelec t ron i c) 인 것 이 다. 한편 NO 의 압력 을 상대 적 으로 CO 의 압력보다 높여 주면 질은 적색의 〔 RhCl2(NO) 』-가 생긴다(석 (5. 23) 참조). 다시 [RhC12(NO) 』처] CO 를 반응시 키 면 [R hClz( C 0)2J - 가 재생된다(식 (5.24) 참조). 이렇게 해서 촉매반응의 순환과정이 성 립되며 [RhCl2(CO)(N0)2] 까 중요한 중간체가 된다. 반응속도 측
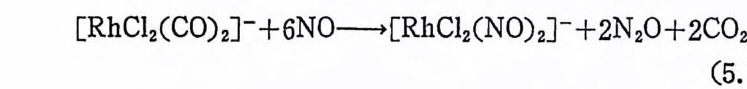 [RhCI2(C0)2 J -+6NO 一 [RhCl2(N0)2 J -+2N20+2C02
[RhCI2(C0)2 J -+6NO 一 [RhCl2(N0)2 J -+2N20+2C02
20) a) R.D. Felth a m, Inorg. Gli em ., 3, 12109.64 ) . b) D. Gwost and K. G. Caulto n , Abstr a ct, 166th ACS Meeti ng , Chic a g o , USA. Aug . , lr:t l3, No. INOR-102.
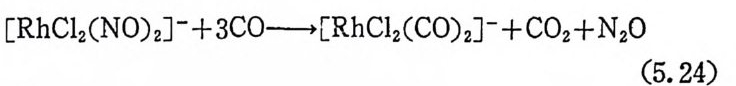 [R hClz( N 0)2J - + 3CO 一 [RhCl z( C0) 2J- + C02 + N20
[R hClz( N 0)2J - + 3CO 一 [RhCl z( C0) 2J- + C02 + N20
정결과에 의하면 〔 RhCl z( CO)(N0)2]- 의 형성과정이 속도결정단계 인 것 같다. 실제 촉매반응식 (5.17) 은산에 의한촉매작용도큰역할 윤 하는 것으로 알려졌다. 그러므로 반응메카니즘에서 H+ 의 참여몰 고려 하여 다음 두 개 의 반응경 로 (석 (5. 25) 및 (5. 26) )가 Eis e nberg 둥에 의해서 제시되었다 .16b) 석 (5.25) 에서 보면 배위된 두개의 NO 가 두개 의 H+ 와 반응하여 하이 포니 트리 트 (h yp o qit r it e) 화합물을 형 성한다. 전이금속一하이포니트리토 (h yp on it r it o) 화합물에 관한 화학 은 많이 알려져 있지 않다. 그러나 촉매에 의한 하이포아질산 (h yp· onit ro us aci d, H2N2 아)의 분해가 N20 와 H20 를 생성시킨다는 사실은 알려 진 사실이 다. 21) 그리 고 몇 몇 P t -N2 야 화합물 (P t (Ph3P)2 (N 2 02), Pt (e n)zCN202), 그리 고 [P t (d i en)zCN2 아)]앙 )17),22) 온 산과 반 응하여 N20 를 생성시킵온 알려진 사실이다. 석 (5.26) 은 또 하나 의 촉매순환과정으로서 역시 N20 및 CO2 의 생성을 보여 준다.
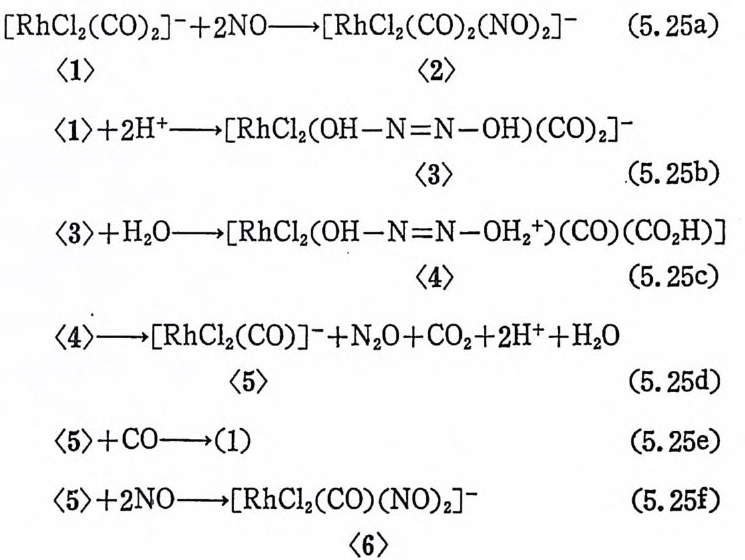 [RhCl2(CO) 』 -+2NO 一〔 RhCl2(C0)2(N0)2 J- (5. 25a)
[RhCl2(CO) 』 -+2NO 一〔 RhCl2(C0)2(N0)2 J- (5. 25a)
21) M, N. Hug h es, Ouate r ly Revie w , Chem. Soc. , 22, 1 (1968). 22) A. I. Ste t s e nko, V. F. Ivanov and A. Barsukov, Koord. Khim . , 1, 791 (19 75).
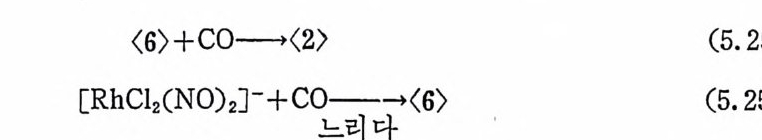 <6> + co— >< 2> (5.25g )
<6> + co— >< 2> (5.25g )
[RhCI2(CO)(N0)2] 제서부터 [RhCl i( NO) 』-의 생성과정은 단순한 평형(식 (5.26a) )으로 표시될 수도 있지만, 석 (5.23) 을 선명하기 위해서는, 죽 생성되는 N20 및 CO2 의 분자수를 설명하기 위해서 는 또 하나의 순환과정 식 (5.26) 아 필요하다. 식 (5.26) 의 순환과정 도 독립적인 NO 에 의한 co 의 산화 반응의 촉매순환과정이 될 ~
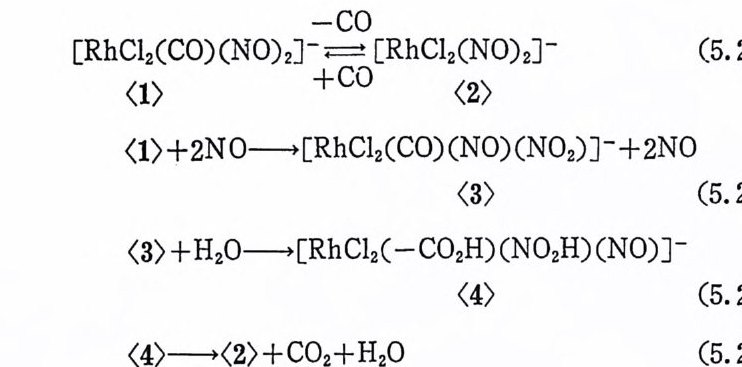 [RhC
[RhC
도 있지만 석 (5.25) 와 동시에 일어나는 과정으로 가정해야만 모든 실험적 결과를 설명할 수 있게 된다. 전이금속착물에 의한 NO의 불균둥화반응 (d i s p ro p or ti ona ti on) 에 의 해서 니 트로―니 트로실 (nit ro -ni- tros y l) 화합물 (M(N02) (NO)) 이 생 성 됨 은 lbers15> 둥과 Hug he s23> 에 의해서 발표된 바 있다. 상기 연구자들은 각각 더니트로실 (d i n i tro syl ) 착물 (M(N0)2) 으로부터 니 트로―니 트로실 착물 (M(N02)CN 0) )이 생성된다고 제시하였다. 산의 존재하에서 금속에 배위된 NO 가 니트로실착물로 되는 예 또한 찾아 볼 수 있다(식 (5.27) 참 조). 24) 최 근 Felth am 둥 13) 과 Ste wart 등 25) 은 배 위 된 N02 가 CO 와 반응하여 니 트로실 착물과 C 아를 생 성 함을 보고하였다(식 (5. 28) 참
23) W. B. Hug h es, Chem. Commun. , 1126(1 9 69). 24) J. B. Godwi n and T. J. Mey e r, Inorg. Chem. , 10, 2150(1 9 71 ). 25) D. T. Doug h ty , G. Gordon and R. P. Ste w art, Jr. , J . Am. Chem. Soc. •· 101, 2645(1 9 79).
조). Felt ha m 둥은 메 카니 즘을 위한 반응속도 측정 결 과로부터 반응
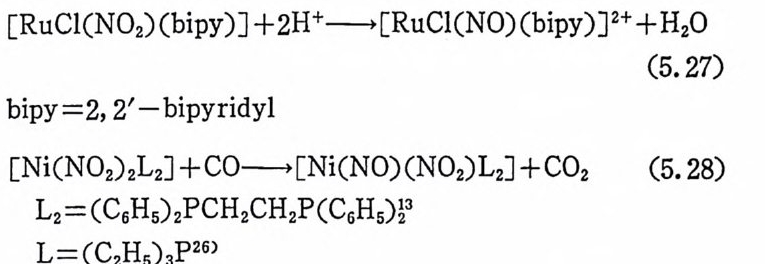 [RuCl(N02)(b ipy)J +2H+ 一 [RuCl(NO)(b ipy)〕 z++H20
[RuCl(N02)(b ipy)J +2H+ 一 [RuCl(NO)(b ipy)〕 z++H20
석 (5. 29) 를 제 시 하였 다. 13) 죽 중간체 인 5 배 위 착물, Ni (N 02)2(CO) L 내에서 CO 는 N02 로부터 O( 산소)를받아서 CO2 가 되는것이다. Eis e nberg 둥이 제시한 반응메카니즘(식 (5.25) 및 (5.26) )에서 CO 는 H20 로부터 0( 산소)를 받아 CO2 가 생성된다고 제시했는데 이 침 이 Felth am 둥의 제 시 (식 (5. 29) )와 다른 접 이 다. Felth am 등의
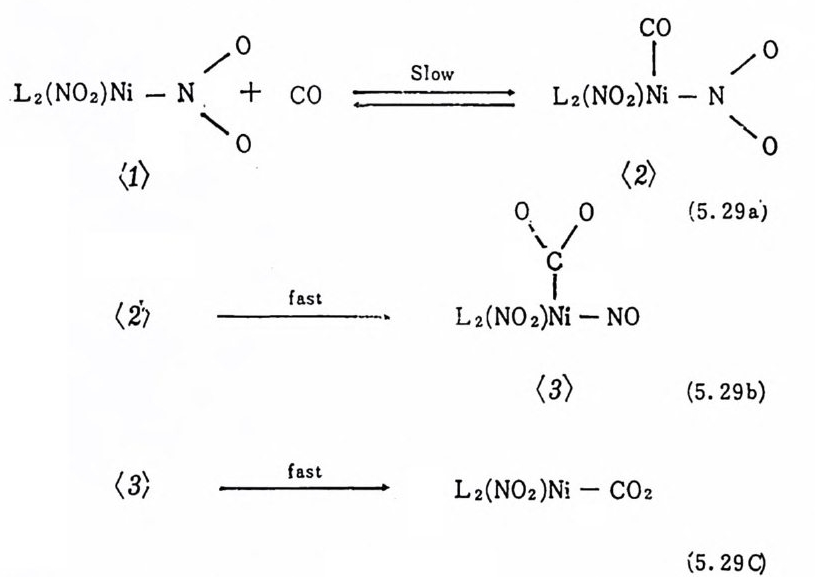 L2(N02)Ni - N ./ 。+ CO Slow L2(N02)cNloi - N /o
L2(N02)Ni - N ./ 。+ CO Slow L2(N02)cNloi - N /o
반응메카니즘을 지지하는 예로서 S t ewar t둥 25) 의 실험을 둘 수 있 다. 죽 S t ewar t둥은 LO 를 사용한 실험에서 N 아가 co 의 산화에 필요한 0( 산소)의 공급처라고결론지었다(식 (5.30) 참조). Felth a m13)
26) C. G. Pie r po nt and R, Eis e nberg, Inorg, Chem. , 10, 1088(1 9 72).
과 S t ewar t 25) 의 연구보고는 중요한 참고적인 사실이지만 Eis e nberg 등이 제 시 한 메 카니 즘(식 (5. 25) 및 (5. 26) 의 옳고 그름에 는 아무 런 영향을 주지 못한다. Fe lt ham 과 S t ewar t는 산이 촌재하지 않
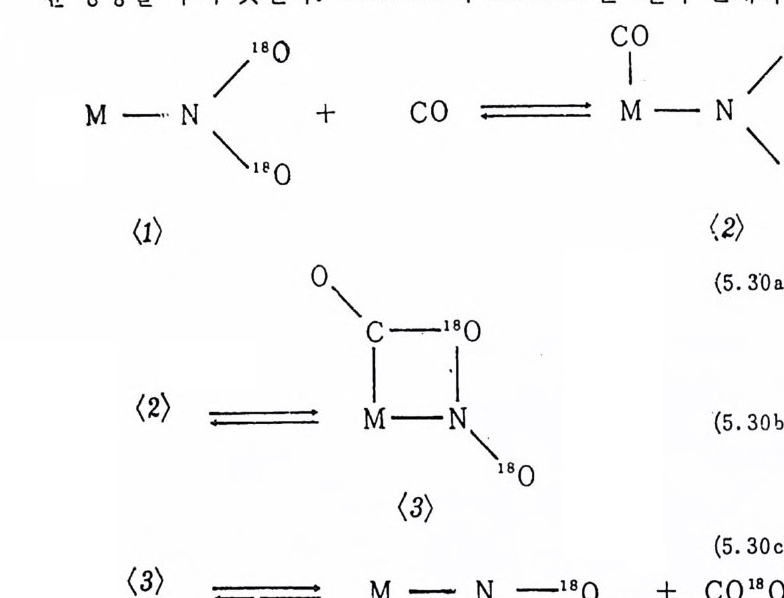 M - .. N / 180 + co cM1o -N / 180
M - .. N / 180 + co cM1o -N / 180
는 비극성 용매에서 실험하였으며 또한 이들이 자용한 금속 배우r 화합물과 E i senber g 16) 가 사용한 촉매 와는 서 로 다른 성 질을 나타내 는 물질이다. 두개의 NO 로부터 N20 의 형성, 즉 N 一 N 결합이 어떠한 경로로 이루어지느냐 하는 문제는 제시된 두 개의 메카니즘(식 (5.25) 및 (5. 26) )에 서 구체 적 으로 논의 되 지 않고 있 다. J ohnson14) 둥과 lbers16>· 둥이 제 시 한 중간체 M(N202) 를 거 치 는 과정 의 에 Eis e nberg1 5 •> 등 은 M(N2 아)와 M(NO+)(NO-) 사이에 평형이 있을 가능성도 있다 고 제시하였다. 찰 알려진 화합물〔 RuCl(NO 업 (NO-)L2]+ 가 열분해 하면 정 량적인 N2 를 생성한다는 사실은 26' M(NO+)(NO-) 중간체 메카니즘을 제시하게 된 이유 중의 하나다. 이 문제논 앞으로의 찰 · 계획된 실험에 의해서 조사 연구 규명될 것이다. Vaska27) 동은 P ti( µ-PCP)3 를 촉매로 사용하는 NO 에 의한 CO 27) Chong Shik Chin and L. Vaska, unp ub li sh ed results .
의 산화반응(식 (5. 18 ) )의 메 카니 즘을 조사하고자 촉매 활성 도가 높 은 반응용액을 급냉시켜서 노란색 고체(최초에 넣어 준 Ptz (µ -PC P)3 는 질은 붉은색 고체)를 분리해 냈다. 이 노란색 고체의 적의선 스펙 트럼 은 2122cm-1(Nujo l ) 및 135 Q cm -1( Nu j ol) 에 서 각각 중간 정 도의 제 기 를 갖는 흡수며 (absorpt ion band) 를 보여 주었 다. 이 상 두 개 의 적 의 선 흡수띠 는 전형 적 인 금속-이 소시 아나토(i soc y ana t o, -NCO) 착물에 서 관찰되 는 떠 들이 다. 28) 즉 2122cm-1 의 떠 는 %(NCO 의 anti sy m metr i c 신축전동)이 며 135Q c m-1 의 띠 는 %(NCO 의 sy - mmetr i c 신축전동)로 볼 수 있 다. 이 상의 사실은 P t一 NCO 형 의 화합물이 반응석 (5.18) 의 중간체 가 됨 을 제 시 해 준다. co 및 H2 에 대한 NO 의 환원반응 중 NCO 기가 생성되는 예는 불군일촉매계에 서 는 몇 몇 발표된 적 이 있 다(식 (5. 31) 참조 ).29> Pt -N CO 형 의 화합 물이 형 성 된다는 사실은 Joh nson 둥이 최 초로 제 시 한 금속-니 트렌 (n it rene)( 식 (5. 19) 참조 ) 메 카니 즘의 가능성 을 보여 준다. NCO 기 의 형성은 금속一니트렌과 CO 와 반응함으로써 가능할 것이다.
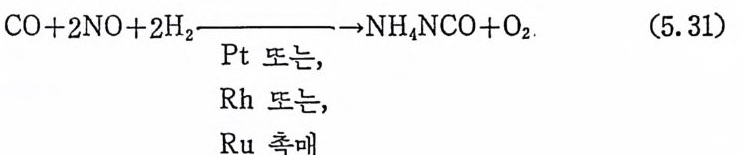 co+2N0+2H2--NH4NC0+02. (5. 31 )
co+2N0+2H2--NH4NC0+02. (5. 31 )
끝으로 전이금속착물 군일촉매에 의한 NO의 동종간주고받기반 웅 (d i s p ro p or ti ona ti on, 불군등화반응이 라고도 한다)(식 (5. 32) 참조)을· 고. 찰하기 로 한다. NO 의 동종간주고받기 반응에 관한 연구조사는 NO 에 의한 CO 의 산화반응을 이해하는 데 도움이 될 것이다.(식 (5.2) 와 (5.32) 비교). 그 이유는 첫째,
 3NO--N20 十 N02 (5.32)
3NO--N20 十 N02 (5.32)
석 (5.2) 와 식 (5.32) 의 유사성이다. 둘째, 배위된 NO 는 혼히 NO+ 에 가까운 성질을 보여 주고 있으며 N 아는 CO 와 둥전자의 관계이
28) Ref. 12, p.1 91. 29) R. J. H. Voorhoeve, L. E. Trim ble and D. J Freed, Sc ien ce, 200, 759(1978).
다. 지금까지 알려진 바에 의하면 배위된 NO 는 여러 경우에 자유 로 운 NO ( 배 위 되 지 않은 NO) 와 반응하여 M-N0 2 와 N2 0 를 생 성 시 켰다 .1 2 ) 예를 들면 Caul t on 등은 LnCo0(NO) 가 NO 와 반웅하여 1 ,nC06(N02) 와 N20 를 생성시킨다고 보고하였다 .30) 이들에 의해서 제 시 된 반응메 카니 즘은 식 (5. 33) 과 같다. 이 어 서 McClever ty 12) 등 은 Caulto n 30) 둥의 메 카니 즘을 재 고찰하여 중간체 3 (식 (5. 33a) 에
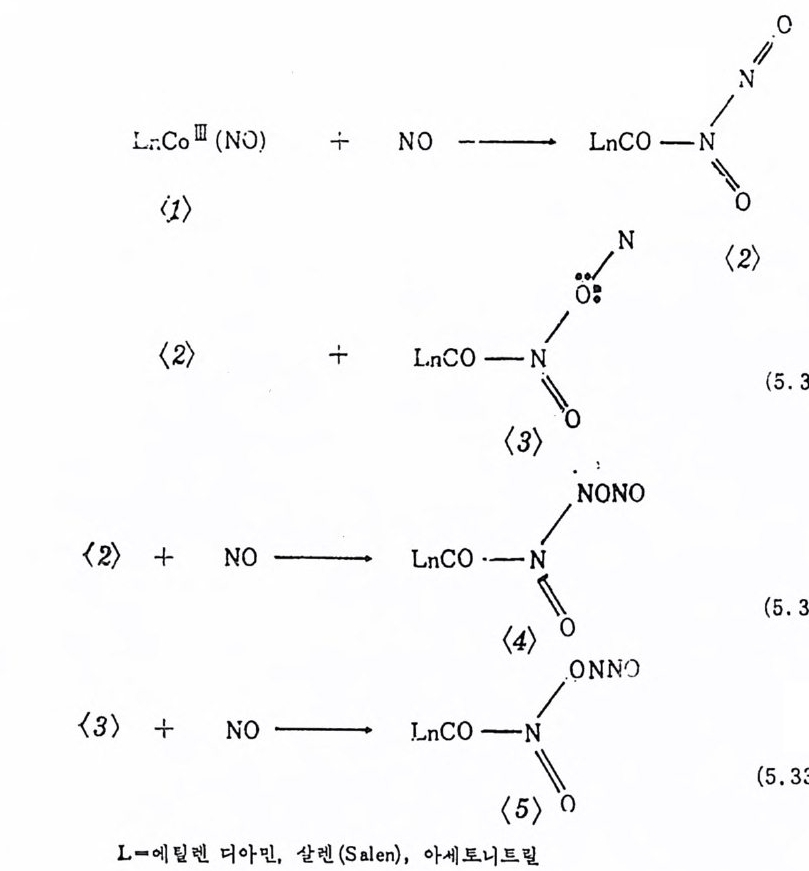 ,0
,0
서)의 가능성을 배제하였고 중간체 〈 2 〉(식 (5.33b) 에서)를 거치는 과정을 자제히 설명하려 하였다(식 (5.34) 참조). 죽 자유로운 NO( 배
30) D. Gwost and K. G. Caulto n , Inorg. Chem, , 13, 414( lff74 ).
위되지 않은 NO) 가 배위된 NO 를 공격함으로써 중간체 〈 2 〉 (식 (5. 33) 과 식 (5. 34) 에 서 )를 형 성 하며 〈 2 〉는 또 하나의 LnC011(NO) 와 반 응하여 〈 7 〉을 생 성 하고 〈 7 〉 은 균형 분열 (homolyt ic cleava g e) 에 의 해 LnCo(N20) 및 LnCo(N02) 를 생 성 시 킨다고 하였 다. 생 성 된 LnCo CN20) 는 곧 NO 와 반응하여 쉽 게 LnCo(NO) 및 N20 를 생 성 시 킬
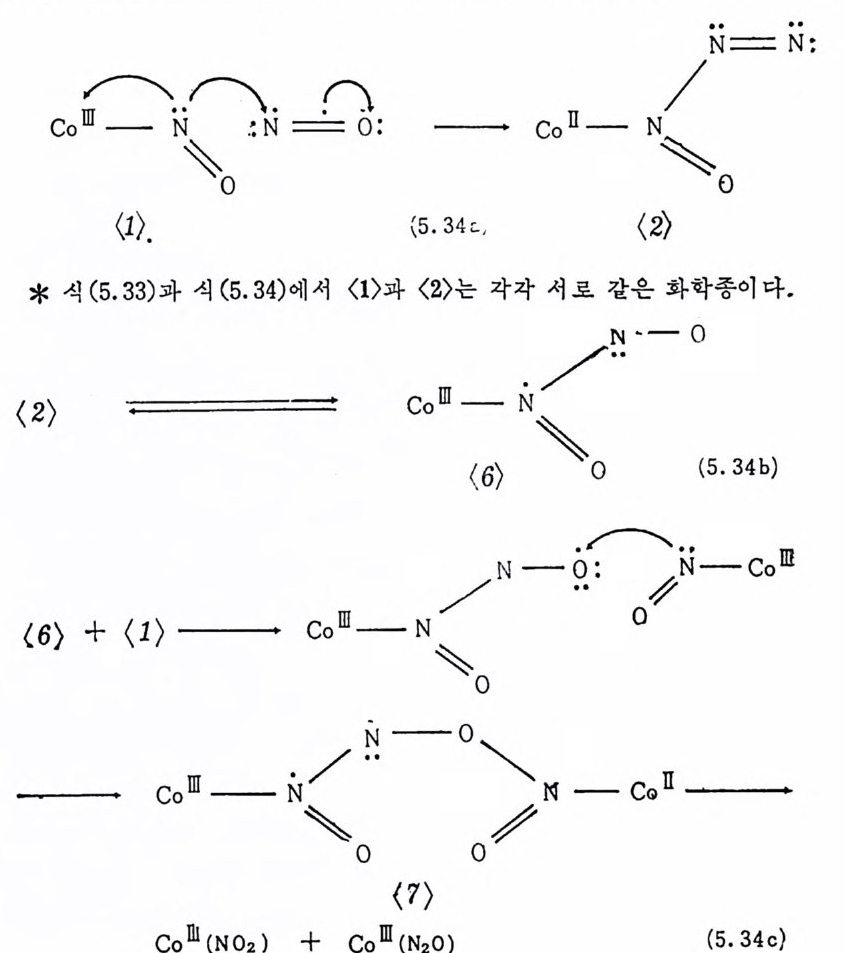 Com~ 一. .Nf\ \。 :. N = =( )O : Co11— N/ ~십。 = = N:
Com~ 一. .Nf\ \。 :. N = =( )O : Co11— N/ ~십。 = = N:
것으로 추측된다. 위와 같이 두 금속원자를 포함하는 중간체 형성 과정을 Gans 에 의해서 제시된 적이 있다 .31) 31 ) P. Gans, ]. Chem. Soc. A. 943(1967).
촉매를 이용하는 NO 에 의한 co 의 산화반응을, 위에서 고찰한 바와 같이, 많은 연구자들이 각각 다론 실험조건하에서 각각 다론 물질을 이 용함으로써 얻은 각각의 반응메 카니 즘은 각각 다를 수도 있는 것으로 기대되기도 한다. (4) 일산화탄소와 물의 반응, CO+H20---촉-:매-- :-->C02+S 촉매를 이용하는 H20 에 의한 co 의 산화는 다음과같은 세 가지 형으로 구분될 수 있다. ® 생성물로서 H+ 이 생성되는 반응(예 : 2Hg 2 ++co+H20— —* Hg /+ +COz+H+). 32> 대 부분이 화학양론적 (sto i c h io m etr i c ) 반응이 며 촉매 순환과정 의 반 웅은 아니다. 그러나 H20 에 의한 co 의 산화촉매반응을 이해하고 응용하는 데 도움을얻고자 연구되어 왔다. @ H20 와 co 가 반응하여 CO2 및 H2 를 생성하는 반응 죽 수 성 가스이 동반응 (wa t er g as shif t reacti on ) (예 : co+H20--co2 +Ha33>). Fe(C0)5 ® 불포화유기 화합물, co 그리 고 H20 의 반응으로부터 포화유 기화합물 및 C 아를 형성하는 반응(예 : R-CH=CHCN+co+H20 ->R-CH2-C H2CN + coi3 4 >) . Rh6(C0)16 첫째, 반응생성물로 H+ 가 생성되는 반응을 살펴보기로 한다. Halpe rn 32) 등은 반응식 (5. 35) 이 산에 서 진행 될 때 속도식 (5. 36) 을 얻었다. 이플 근거로 재시한 반응메카니즘(식 (5.37) 에서 co 가 H g 2+ 와 배위된 H20 사이에 삽입된 다음, 빠른 속도로 C 아를 생 성시키고 생성된 H g는 빠른 속도로 또 하나의 H g 2+ 와 반응하여
32) A.C. Harkness and J. Halpe rn, J. Am .. Chem. Soc., 83, 1258(1 9 61 ). 33) R. B. Kin g , C. C. Frazie r , R. M. Hanes and A. D. Kir ig, Jr. , ]. Am. Chem. Soc. , 100, 2925(1 9 78). 34) T. Kit am ura, N. Sakamoto and T. Job , Chem. Lett . (JA PAN), 379 (lr.rl 3) .
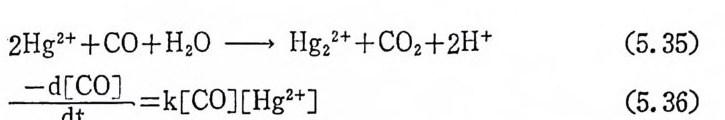 2Hg 2 ++CO+H20 一 Hg /+ +C02+2H+ (5. 35)
2Hg 2 ++CO+H20 一 Hg /+ +C02+2H+ (5. 35)
Hg 22 + 를 형 성 하리 라고 제 시 하였 다. 이 러 한 co 의 삽입 반웅(i nser ti on) 이 속도결정단계가 되는 실례는 H g 2+ 의 메틸알콜 용액에 CO 를 몽
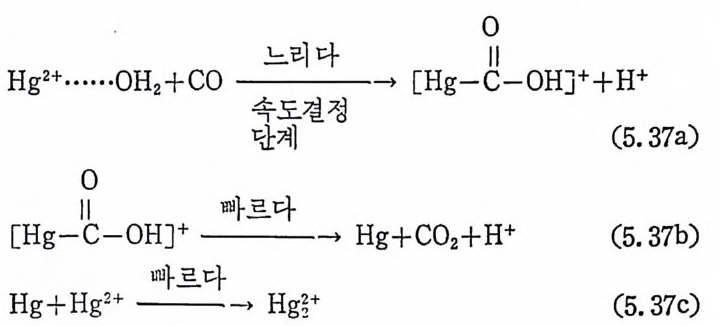 。
。
과시키면 얻어지는 CH3COO … H g ••·COOCH3 에서 볼 수 있다 .35) Pete r s 둥은 아세 데 이 트산 은 (s il ver aceta t e ) 및 과염 소산 은 (s il ver _pe rchlorate ) 용액 이 CO 를 산화시 켜 CO2 를 생 성 시 킵 을 보고하였 다 . •( 식 (5. 38) 참조 ).36) 반응속도 측정으로부터 얻은 속도석은 과염소산
![]() 2Ag + +co+H2 —— 2Ag + C02+2H+ (5. 38)
2Ag + +co+H2 —— 2Ag + C02+2H+ (5. 38)
의 용액 과 아세 테 이 트산의 용액 에 서 각각 다르게 나타났다(식 (5. 39) 및 (5.40) 참조). 이들· 두 속도식을 설명하기 위하여 제시된 각각의 페카니즘은 식 (5.41) 및 식 (5.42) 와 같다. 이들 메카니즘의 중간체
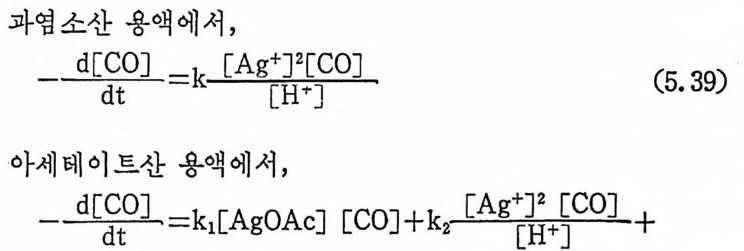 과염소산 용액에서,
과염소산 용액에서,
35) J. Halpe r n and S. F. A. Kett le , Chem. Ind. (London), 6680961 ). 36) R. T. McAndrew and E. Pete r s, Can. Met. Qu art. , 3, 153(1 9 64)
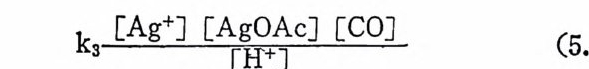 k3 [Ag +] [A [g H0 汀 A c][ C O] (5.40)
k3 [Ag +] [A [g H0 汀 A c][ C O] (5.40)
도 역시 CO 삽입반응의 생성물인 Ag - C-OH 및 Ag - C— OA c 입 0II 0II 으로 Halpe r n 둥이 제 시 한 반응메 카니 즘 (식 (5. 37) )과 비 슷한 것
 Ag + +co+H2 ;::== A g一 C\- OH+H+ (5.41a)
Ag + +co+H2 ;::== A g一 C\- OH+H+ (5.41a)
이다. N i 2+ 착물에 co 의·산화반응도 같은 메카니즘으로 설명된다 (식 ([5N. 4i 3(N) H참3조))n.J 237+ ) +그c밖o+에o 도H -C—u 2+ 수[(용N 액Ha 에)n 서N i도 -C C-OO 는H J +C O2 로 산 & (5.43a)
~) E. Hir s ch and E, Pete r s, Can. Met. Qu art. , 3, 137(1964).
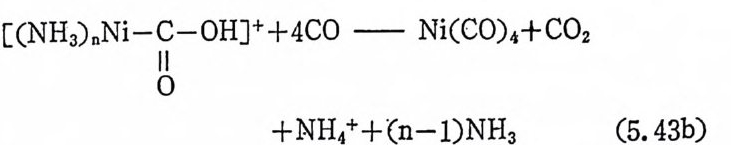 [(NHa)nN i一 C\ -OH J ++4co -Ni (C O),i+ C02
[(NHa)nN i一 C\ -OH J ++4co -Ni (C O),i+ C02
화됨을 볼 수 있다(식 (5.44) 참조 ).38) 제시된 반응메카니즘은 역시 · CO 의2 C삽u2입++반3응C에O+ H의2한0 —중간체2,C uC(CuO-)\C+ +-CO0H2 +를2 H거+치 는 (과5.정 44을) 포
함한다. P t 2+ 를 이용하는 H20 에 의한 co 의 산화반응에서는 영화 알탄 (all y l chlorid e), CO 및 H20 가 배위된 중간체가 제시되었다 \ (식 (5.45) 참조 ).39) 이것은 CO 의 삽입메카니즘(식 (5.37), (5.41),
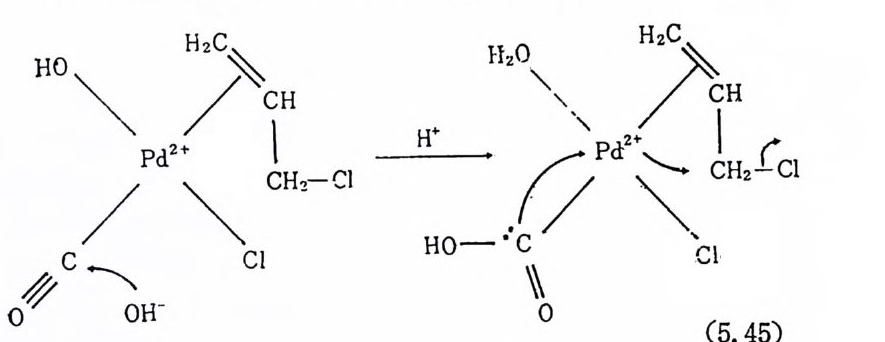 H0\ /H2\CC H HzO .\ \ ,\o/+c_L H_ \H
H0\ /H2\CC H HzO .\ \ ,\o/+c_L H_ \H
·(5. 42) 및 (5. 43) )과는 다른 형 의 반응경 로이 다. 식 (5. 46) 은 Jam es 동에 의 하여 연구된 Rh3+ 에 의 한 co 의 산화반응이 다. 40) 이 들은 반응속도 측정으로부터 제시한 메카니즘에서 co 의 삽입반응에 이
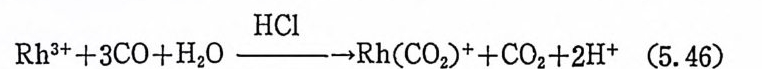 HCl
HCl
어서 일어나는 CO2 의 생성과정에서 얻어지는 Rh+ 이 다시 CO 와 반응하여 Rh(C0)2+ 이 생성된다고 하였다. 이 렇게 해서 생성된 Rh(C0)2+ 는 또 하나의 C 야 생성과정의 촉매역할울 한다고 제시하
38) J. K. Nic h olson, J. Powell and B. L. Shaw, Chem. Commun. , 174(1 9 66). 39) J. J. By er ly and E. Pete r s, Can. J. Chem, , 47, 313(1 9 69). 40) B.R. Jam es and G.L. Remp el , Chem. Commun., 158(1 9 67).
였다(식 (5.47) 참조). ` 마지막 단계인 자체 촉매반응 (au t oca t al ytic reac ti on) 의 자세한 과정에 관한 제시는 없었다. 그러나 마지막 단계 의 중간체로서 서로 다론 산화수를 갖는 Rh3+ 와 Rh+ 가 이루는 二 核착물, 죽 co 또는 Cl 을 다리로 하는 Rh3+-X-Rh+ (X=CO 도 는 Cl) 을 재시하였다.
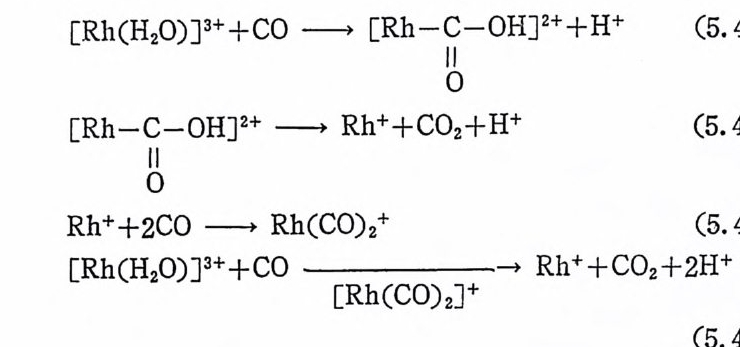 [Rh(H20)]3++co 一 [Rh-C-OH 〕따따 (5.47a)
[Rh(H20)]3++co 一 [Rh-C-OH 〕따따 (5.47a)
이상의 고찰에서 본 바와 같이 H+ 를 생성시키면서 일어나는 C0' 의 산화는 그 데 카니 즘(식 (5. 37), (5. 41) , (5. 42) 및 (5. 43)) 을 보면 co 의 삽입에 의하여 형성된 :fyl -COOH 로부터 CO2 가 생기는 공 통적 인 과정을 포함한다. 둘째로 H20 와 co 가 반응하여 CO2 와 H2 를 생성하는 수성가스 이 동반응 (wa t er- g as sh ift)에 대 한 군일촉매 반응을 고찰하고자 한다. 수성가스이동반동 (CO+H20-C02+H2) 의 응용효과는 여러 가지 떤 에서 찾아볼 수 있다. 유독한 CO 를 제거함과 동시에 에너지로 쑬· 수 있으며 각종 공업(암모니아 합성 둥)에 필요한 H2 를 생성시키 는 것이다. 그리고 CO 와 H2 를 반응시켜 생성되는 액체(예 : CH3. OH) 및 기 체 (예 : CH4) 연료생 산 (F i sher Trops c h Sy n th e sis ) 연구에 서 생성되는 물질의 종류 및 그 비율은 CO 와 H2 의 비율에 큰 영 향을 받는다. 수성 가스이 동반응의 어 해 및 응용은 상기 Fis h er- Trop s ch Sy n th esis 의 반응조건 (예 : H2 와- co 의 비 율) 조정 에 큰 도움이 될 수 있 다. Fis h er-Trop sc h Sy n th e sis 는 특히 최 근에 석 탄 으로부터 깨끗한 에너지를 얻는 연구로 각광을 받아 활발히 연구전 행되고 있다. 군일촉매계에 의한 수성가스 이동반응은 Repp e ¼
이 m 1953 년에 발표한 바 있으나 최근 상기의 중요성을 재인식하 여 다시 이 분야의 연구가 활발히 연구 진행되고 있다. 1977 년에 Ford 등은 전이 금속 뭉치 화합물 (clus t er com p ound) 을 촉매 로 이 용한 연구보고를 하였 다(식 (5. 48) 참조 ). 12) 이 어 서 이 들은 여 러 종류의 전 이금속 뭉치화합물(l r4(C0)12, RhGCC0)16, Ru3(C0)12, Re2(C0)10 및 Fe(C0)5) 을 촉매로 사용하는 수성가스이동 반응을 보고하면서 자제한 반응속도 및 여러 종류의 중간체를 분리 또는 확인하고 반응 메 카니 즘(식 (5. 49) )을 제 시 하였 다. 전이 금속을 M 으로 표시 하는 일 반화시 칸 식 (5. 49) 의 실 례 는 식 (5. 50) 및 (5. 51) 에 서 보여 준다.
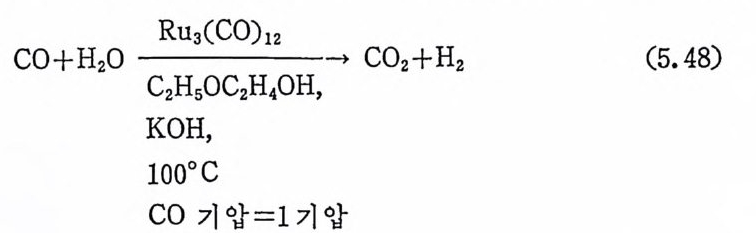 co+H20 -Ru3(C0)-12 C02+H2 (5.48)
co+H20 -Ru3(C0)-12 C02+H2 (5.48)
식 (5. 49) 의 과정 들을 보면 처 음 과정 에 서 H20( 또는 OH- )는 금속에 배위된 CO 와 반응하여 카르복실 금속화합물 〈 2 〉를 형 성 한다. 이 7卜 르복실 금속화합물은 또 하나의 H20 와 반응하여 모노히 드리 도 (monoh y dr i do) ―카르복실-금속화합물〈 3 〉을 형 성 한다. 〈3 〉은 CO2 를 잃 고 디 히 드리 도 (d i h y dr i do) 착물〈 4 〉를 형 성 하며 〈 4 〉는 H2 를 잃 고 배위 불포화 화합물 〈 5 〉가 되어 다시 CO 와 결합하여 최초의 화합 물 〈 1 〉을 형성한다. 이 촉매순환과정에서 「 M 」〈 5 〉은 單核 (mononuc !ear) 또는 多核(p ol y nuclear) 전이 금속 화합물이 될 수 있 다. 석 (5.50) 과 (5.51) 의 반응은 동시에 일어날 수 있는 것으로 제시되었 으며 두개의 식에서 모두 속도결정단계는 마지막 과정인 co 의 도 움으로 H2 가 떨어져 나가논 과정으로 제시되었다. Ford 등은 특 히 더하드리도착물 〈 4 〉의 형성이 필수적이라고 강조했으며 포름산 (for mi c acid ) 또는 포름산이 온(fo rma t e ion ) 등이 가능한 중간체 일 것
41) J. W. Repp e and H. Vett er , Ann. Chem. , 582, 133(1 9 53). 42) a) P. C. Ford, R. G. Rin k er, C. Ung e rmann, R. M. Lain e , V. Landis , and S.A, Moy a , ]. Am. Chem. Soc., 99, 2520'5 77 ).
 M-CO 01\ -r (or -HH 20)2 \\\(OH〉 『
M-CO 01\ -r (or -HH 20)2 \\\(OH〉 『
이라고 제시하 였 다 .4 2 > Ford 둥은 뒷 받침하는 실험으로 Rul C 0)12 가 식 (5. 48) 과 동일한 조건하에 서 포름산 이 온의 분해 반응 (HC02H 一 CO+H2) 의 촉 매적 활 성을 보여중을 발견 했 다 . 42 > Ford 등과 거 의 같은 시기에 Pe ttit등은 또한 전이금속 뭉치화합물 촉매에 의한 수성 가스이 동반응을 발표하면서 실질적 으로 Ford 둥의 메 카니 즘(식 (5.49) 과 동일한 메카니즘을 제시하였다(식 (5.52) 참 조 ).m K i n g등 은 상기 Ford42) 및 Pett it43> 등과 거의 동시에 Fe(C0)5 촉매에 의 한 수성 가스이 동반응을 보고하면서 또 다른 경 로의 반응메 카니 즘
 M+CO _➔ MCO (5. 52a)
M+CO _➔ MCO (5. 52a)
· (식 (5. 53) 참조)을 제 시 하였 다. 33> Kin g 동은 제 시 한 메 카니 즘(식 (5.53) )의 실험적 증거를 다음과 같이 제시하였다. ® 자의선 스 펙트럼의 측정걷과 〔 HFe(CO) 』-는 CO 와 반응하여 Fe(C0)5 를 형 성 한다. ® H-( 예 : NaH) 이 H20 와 격 렬히 반응하여 OH-와 . H2 를 생성함은 찰 알려진 사실이다 .44) ® M_CO 와 OH- 가 반응하 여 M ― COOH 를 형성함은 또한 찰 알려진 사실이다 .45) @ M-
 [HFe(C0)4 『 +co 一 Fe(C0)5+H- (5. 53a)
[HFe(C0)4 『 +co 一 Fe(C0)5+H- (5. 53a)
· COOH 가 C 아를 잃고 M_H 가 형성됨온 또한 찰 알려진 사실이 다. 45), 4 6),4” 이 상 ®로부터 @까지 의 합이 죽 식 (5. 53) 의 메 카니
42) b) C. Ung er mann, V. Landis , S. A. Moy a, H. Cohen, H. Walker, R. G. Pearson, R. G. Rin k er and P. C. Ford, J. Am. Clzem. Soc. , 101, 59220'51 9 ), 43) H. Kang , C. H. Mauldin , T. Cole, W. Slege i r, K. Cann and R. Pett it, J. Am. Clt em . Soc. , 99, 8823(1 9 77) 44) D. T. Hurd, C!t em i st ty of t!te Hy d rid e , Joh n-W iley , 1952. 4465)) WD. .J . HDieab reern sabnodu r'Ig'.. aKndr uJc.k A, . ZF. roNealit c1 h1 r,f oJ t . s c Ah,m .B .C h16em, .7 0S9o(1 c9. ,6 19 )9 , 4726(19Y7) -47 ) H, C. Cl ark, K. R. Dixo n and W. J. Jac obs, Chem. Commun. , 548(1 9 68)
즘이다. Eis e nberg 둥은 [RhCl(CO)J2 가 산성 용액 에 서 수성 가스이 동반옹 의 촉매가 됨을 발견하였다 .48) 자세한 반응메카니즘의 제시는 없었 지만 H2 의 생성은 H+ 와 수소화 금속 (me t al•h y dr i de) 의 반응에서 일 어나며 CO2 의 생성은 금속―카르복실화합물(금속―카르보닐화합물 과 H20 의 반응에서 얻어지는)의 분해에서 일어날 것이라고 제시 하였다. 또 하나의 가능한 H2 의 생성과정으로 Rh3+ -디히드리도 (dih y d rid o ) 착물의 분해 로부터 H2 의 생 성 과 Rh+ 의 생 성 율 제 기 하 기도 하였다. Rh3+ 과 Rh+ 사이의 가역적인 산화-환원반응 (Rh3++ 2e-.=::!Rh+) 이 이상의 촉매반응에 포함될 것은 가능한 사실이다. 이 어 서 Ei se nberg 등은 지금까지 논의 된 수성 가스이 동반응의 촉매 계 오H 즌 상당히 다른 촉매 계 를 보고하였 다(식 (5. 54) 참조). 4” 이 촉 매반응은 P t화합물이 촌재하지 않으면 전행되지 않으며, Sn 화합
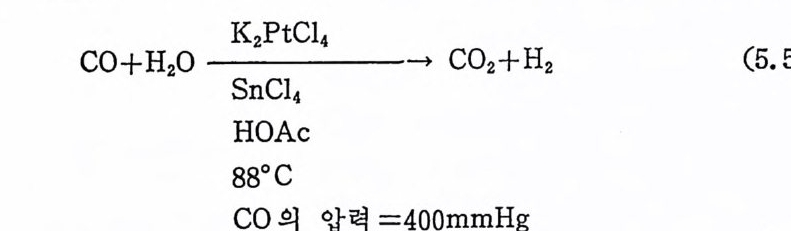 co+H20 K2Pt C l4 --+ C02+H2 (5.54)
co+H20 K2Pt C l4 --+ C02+H2 (5.54)
물이 없으면 매우 느리게 진행되며 이어서 곧 촉매적 활성을 잃는· 다. Ei se nberg 둥은 촉매 활성 이 있 는 용액 을 조사 분석 한 결과 Sn2+ 과 Sn“ 사이 의 가역 적 산화―환원반응 (SnCI52-+2e- .=== SnC13-+ 3c1-) 이 일어남을 알고 상기 식 (5.54) 에 의한 수성가스이동반응은· 두 반응식 (5. 55) 및 (5. 56) 으로 표현될 수 있 다고 제 시 하였 다. 또한 촉매 활성이 있는 용액으로부터 [P t C lz( C O)(SnC13]_ 및 [PtC I(CO),
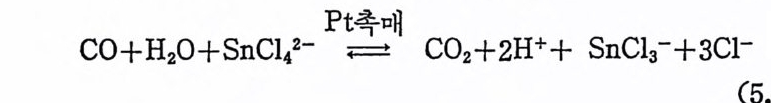 CO+H20+SnCil - P t .=촉==매 C02+2H++ SnCI3-+3c1-
CO+H20+SnCil - P t .=촉==매 C02+2H++ SnCI3-+3c1-
48) C. H. Cheng , D. E. Hendrik s en and R. Eis e nberg, J. Am. Chem. Soc. ,. 99, 2791(1977. 49) C. H. Cheng and R. Eis e nberg, J. Am. Chem. Soc. , 100, 5968(1 9 78).
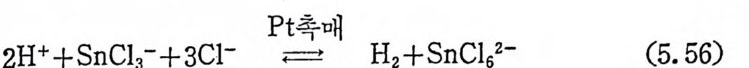 P t촉매
P t촉매
(SnCl3)2] -가 분리되어 확인되었다 .49) 상기한 실험적 근거둘로부 터 식 (5.57) 과 같은 메카니즘이 제시되었다 .• C O2 의 생성과정은· 역 시 M-CO 와 H20 의 반응에서 생간 M-COOH 의 분해과정을 의 미하며 H2 의 생성과정은 H+ 오1- M-H 간의 반응으로 추측된다. 마지 막으로 불포화 유기 화합물과 CO 와 H20 의 반응으로부터 포
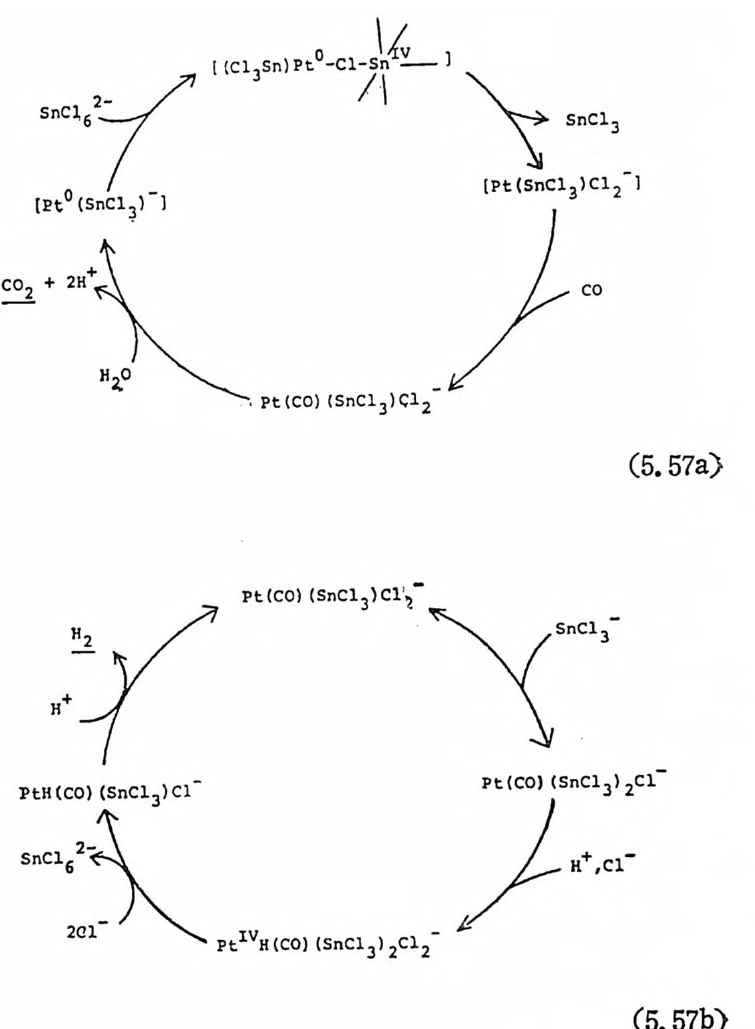 snCl6? [ (C l3sn)P t °-Cl?\소 1 \ snCl3
snCl6? [ (C l3sn)P t °-Cl?\소 1 \ snCl3
화 유기 화합물 및 CO2 를 형 성 하는- 반응을 고찰하고자 한다. 이 반 옹은 co 의 제거 목적보다는 새로운 유기화합물의 합성이라는 과 제로 연구되어근 분야이다. Rep pe 둥에 의해서 처음 발표된 올레 핀, co 및 H20 의 반응으로부터 알데히드를 거쳐 알콜을 합성하 는 과정 이 시 초가 된다. 41' Rep pe 의 반응은 올레 포tl, co 및 H2 의 반응(히 드로포르밀화반응) (제 3 장 2 참조)과 비 교가 되 는 반응이 다 (식 (5. 58) 참조). 죽 히 드로포르밀화반응에 서 사용하는 H2 대 신에 Rep pe 의 반응(석 (5. 58) )에 서 는 H20 를 사용한다는 접 과 Rep pe 의 식에서는 CO2 를 생성시킨다는 접이 다르다. 히드로포르밀화 반응
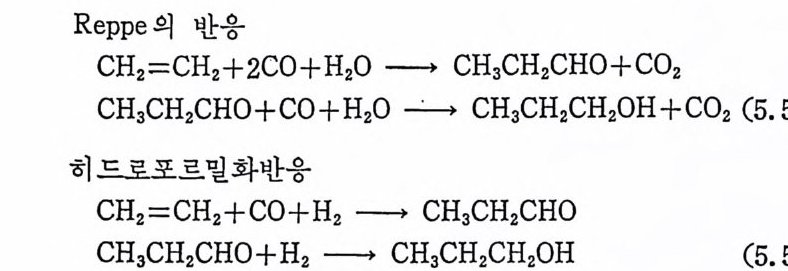 Re pp e 의 반응
Re pp e 의 반응
의 메카니즘은 이 반응(식 (5.58)) 이 처음 발표된 41),50) 오렌 후에 Heck 둥에 의해서 처음 제시되었다(식 (5.60) 참조 ).5 1) 이 반응은 다 음의 4 단계로 이루어진다. (1) 금속-수소 화합—물과 올 레핀 반응 M-H + \/ C = C\ / M ctI 一 CII 一 l— CH ,CH,CHO . c。 - H-!-C 一仁 _L_ 二 M-C 一 c -cI — II I I II I I 。 。 (5. 60)
50) H. At kins and G. Kresk, J . Am. Chem. Soc. 71, 3051(1 9 49). 51) R. F. Heck and D. S. Breslow, J. Am, Chem. Soc, , 83, 4023 0961 ).
에 서 금속_알킬 화합물의 형 성 , (2) co 삽입 반응에 의 한 금속― 아실 (-acy l) 화합물의 형 성 , (3) H2 의 산호格j 첨 가반웅 (o xi da ti ve add iti on) 에 의한 금속―수소―아실 화합물의 형성, (4) 환원성 제거 반응 (reduc ti ve e li m i na ti on) 에 의한 알데히드 및 금속一수소 화합물 의 형성 등이다. 이상과 바슷한 촉매반응의 메카니즘은 여러 연구자 들에 의 해 서 최 근까지 발표되 고 있 다. Repp e 의 반응석 (5. 58) 에 관한 메카니즘의 제시는 최근까지 Ku t e p ow 둥에 의한 것 하나밖에 발표된 것이 없다 .52) 이들에 의해서 제시된 메카니즘(식 (5.61)) 의 첫 단계 (5. 61a) 와 마지 막 단계 (5. 61b) 는 별도의 실험 에 서 확인된 결 과이 다. 제 2 단계 (5. 61c) 와 제 3 단계 는 히 드로포르밀화반응(제 3 장
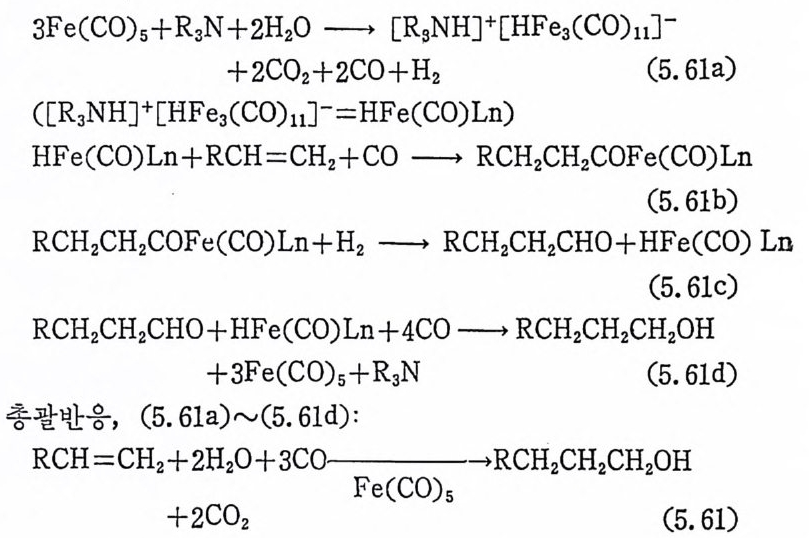 3Fe(C0)5+R3N+2H20 一 [R5NH 四 HFe3(C0)11] 一
3Fe(C0)5+R3N+2H20 一 [R5NH 四 HFe3(C0)11] 一
2 참조)에서 여러 번 제시되어온 과정들이다(식 (5.60) 참조). 이제까지 발표된 유사한 반응들을 아래에 간단히 식으로 소개한 다(식 (5. 62, ), (5. 63), (5. 64) 및 (5. 65) 참조).
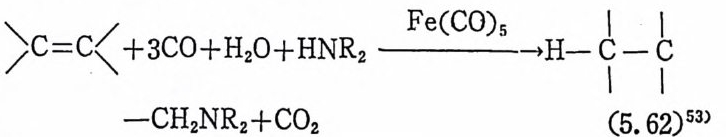 \ / Fe(CO)s I I
\ / Fe(CO)s I I
52) N. V. Kute p o w and H. Kin d ler, Ang e w. Glie m . 72, 802 (19 60). 53) A. F. M. Iqb al, Helv. Chim . Acta , 54, 1440 0971).
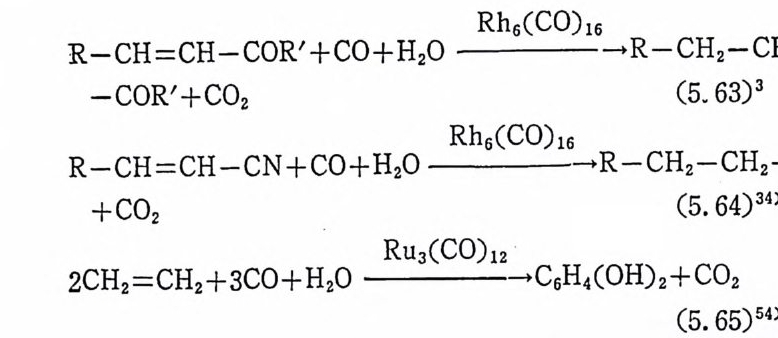 Rh6(C0)16
Rh6(C0)16
이상은 전이금속 배위화합물 촉매에 의한 co 의 산화반응 중 군 일계에서 02, NO 및 H20 에 의한 촉매반응을 고찰한 것이다. 배우] 라는 과정을 동해 전이금속에 의하여 활성화되는 CO, 02, NO 및 H20 의 반응성을 각각의 연구자들에 의하여 제시된 메카니즘을 동 하여 알아보았다. co 의 산화반응은 co 의 제거는 물론 유독기체 인 NO 의 제거, 그리고 H20 로부터 H2 의 생산 및 유기화합물의 합성방법으로 연구되어오고 있음을 살펴보았다. 2. 일산화탄소의 수소화반응 원유로부터 얻어지는 연료의 값이 올라감에 따라 합성연료의 생 산에 관십이 쏠리게 랬다. 분만 아니라 합성연료 생성과정을 이용 하는 유기화합물의 생산도 많은 사람의 연구대상이 되었다. 특히 여 기 서 고찰하고자 하는 일산화탄소의 수소화반응 (h y dro g ena ti on) 은 여러 가지 유용한 생성물을 만드는 연구로 활발히 진행되고 있다. 이 철에서는 지금까지 알려진 반웅 메카니즘을 먼처 살펴보고, 이 어서 현재 이미 공업적으로 사용되고 있는 몇몇 과정을 소개하고자 한다. 여기서는 물론 군일촉매계에 의한 반웅울 주로 다루게 되지만 불 군일촉매 반응으로 비 교가 되 는 반응을 잘 알려 진 Fis c her-Trop sc h 의 반응이다. 또한 아태에 고찰하고자 하는 실험적 결과들도 경우
54) P. Pin o , G. Braca, G. Sbrana and A. Cuccuru, Chem. Ind. , 1732(1968).
에 따라서 군일촉매반응인지 불균일촉매반응안지 구 U검 하기 어려운 경 우도 있 다. 따라서 불군일촉매 반응인 Fis c her-Trop s ch 과정 (식 (5. 66) )을 먼저 살펴 보고, 이 어 서 균일촉매 반응을 고찰하기 로 한다.
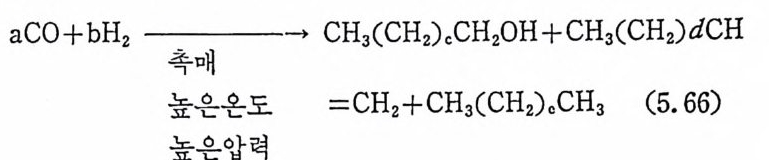 aCO+bH2 --> CHJ CC H2)cCH20H+CHJ CC H2)dCH
aCO+bH2 --> CHJ CC H2)cCH20H+CHJ CC H2)dCH
Fis c her-Trop s ch 과정 은 Fe, Co, Ni 또는 Ru 등의 전이 금속을 산 화알루미 늄 (alum i na) 등 불용성 고분자에 붙여 서 (sup po rte d ) 얻는 불 용성 촉매를 사용하거나 또는 금속산화물 같은 불용성 촉매를 사용 하여 H2 와 co 의 반응으로부터 여러 가지 유기화합물을 얻는 반응 이다. 이 반응의 초기물질인 CO 와 H2 는 석탄과 원유르부터 얻어 지기 때문에 Fis c her-Trop s ch 과정에 의해서 합성연료를 얻는 것은 상당히 비싼 방법이다. 그러나 남아프리카와 같은 많은 값싼 석탄 을 보유하고 있는 나라에서는 이 방법으로 합성연료 (s y n t he ti c fue l) 를 만들고 있기도 하다. 현재 까지 제 시 된 Fis c her-Trop s ch 과정 은 메 카니 즘에 의 하면 첫 단계는 히드리도-포르밀-금속 착물의 형성 단계이다(식 (5.67) 참 조). 이어서 수소의 이동반응, co 의 삽입반응, 그리고울레핀의 제 거반응등이 계속해서 일어나며 분자량이 큰 탄화수소 및 알콜 둥이
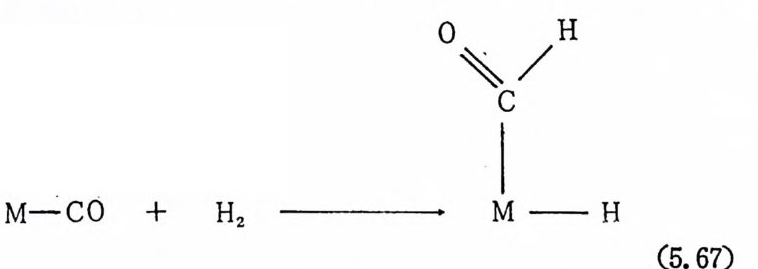 。 \/H
。 \/H
생 성 되는 것 으로 알려 졌 다. 또한 Fis c her-Trop s ch 과정 은 중간체 로 금속―카르벤 (me t al-carbene) 착물형 성 단계 를 포함하는 것 으로 제시되기도 하였다. 아래와 같은 두 실험결과는 금속―카르벤 착물 형성의 메카니즘을 어느 정도 지지해 주기도 한다. (1) 금속-카르
벤 착물은 CO 와 반응하여 #-케 텐 (kete ne) 착물을 형 성 하고 7) 2- 케 텐 착물은 수소와 반응하여 알데히드를 생성한다(식 (5.68) 참조 ).65) (2) 금속―카르벤 착물은 H2 와 반응하여 식 (5. 69) 와 같이 탄화수 소를 생성한다 .66) 이 상은 Fis c her-Trop s ch 반응이 單核 금속착물촉매 에 의 해 서 이 루어질 때 가능한 데카니즘이다. 한편 금속표면이나 多核 금속착물
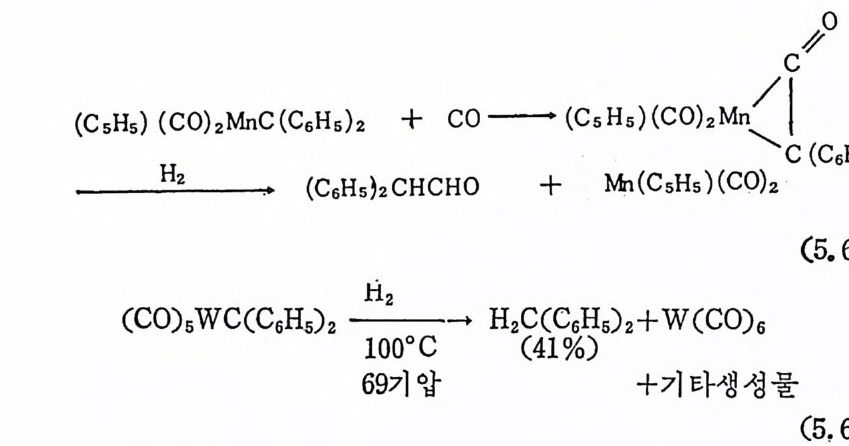 ~o
~o
(불용성 고분자에 붙여 전 전이 금속착물도 多核 금속착물로 취급할 수 있음)에 의한 Fis c her-Trop s ch 반응의 메카니즘은 아래와 같이 제시 되 어 오고 있다. 67) 죽 식 (5. 70) 과 같이 금속一포르밀 착물의 형 성이 첫 단계가 되며, 이어서 배위된 포르밀기는 환원되어 히드록 시카르벤착물을 생성시킨다(식 (5.71) 참조). 죽 여기서도 금속_-카 르벤착물을 경유하는 메카니즘을 논의하고있다. 식 (5.71c) 에서 보 는 바와 같이 co 가 계속해서 삽입되고, 금속—아실기는 환원되어 알킬고리 는 길어 진다. 경 우에 따라서 는 금속―알킬부분은 식 (5. 72) 에서 보여 주는 바와 같이 알칸으로 환원되기도 한다. 또한 경우에
55) W. A. Herrman and J. Plank, Ang e w, Chem. Int. Ed. , 17, 525 (1978). 56) C.P. Casey and S.M. Newman, J. Am. Chem. Soc., 99, 5651 (1977). 57o) trJ a .nP s.i tC ioonll mMaent a al n Cd hLem.Si .s t rH ye , g e Ud nusiv, e Prsriitn y c iSp clie e sn caen dB oAopk sp, li(cla9 t8i o0 n), s p .o f4 3 4O. rga n-
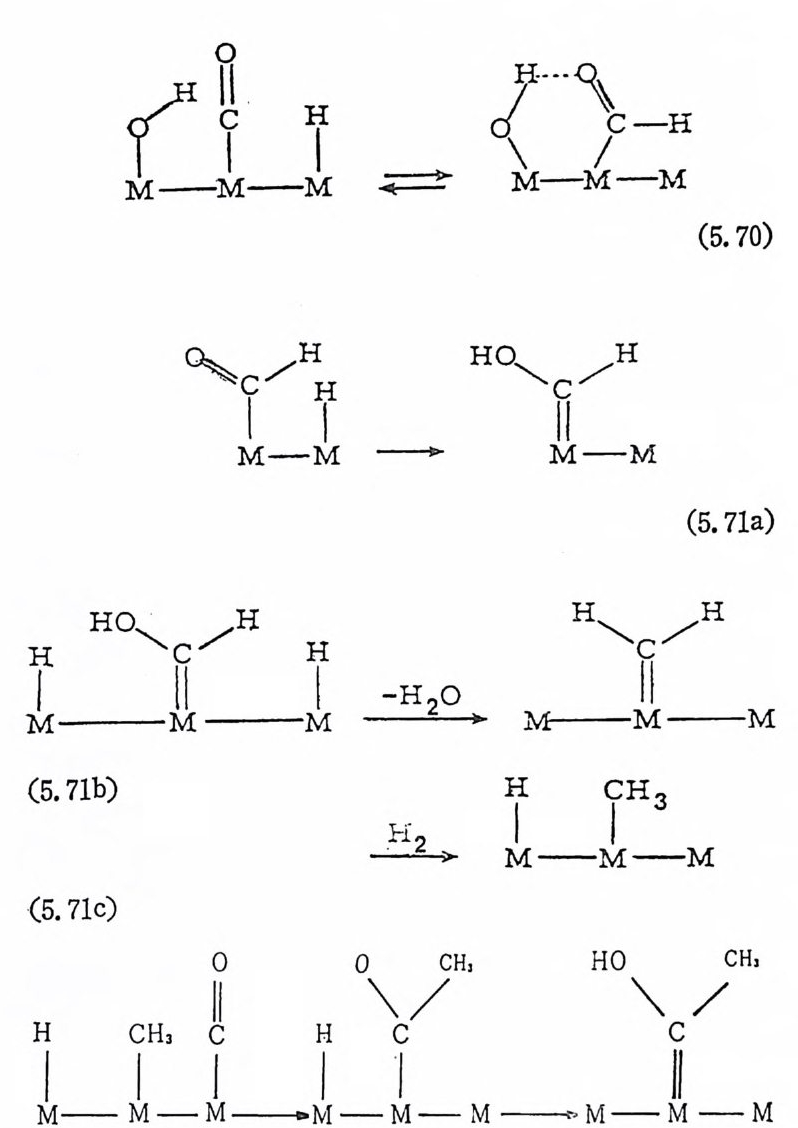 OIIc
OIIc
따라서는 금속-아실 부분은 환원되어 알데히드를 거쳐 알콜을 생성 한다(식 (5.73) 참조). 반응도중에 생성되는 알파―히드록시알킬부분 으로부터 올레핀이 생성되기도 하고 생성된 올레핀은 수소화반응을 일으켜 알칸이 되기도 하는 것으로 제시되고 있다(식 (5.74) 참조 )•57)
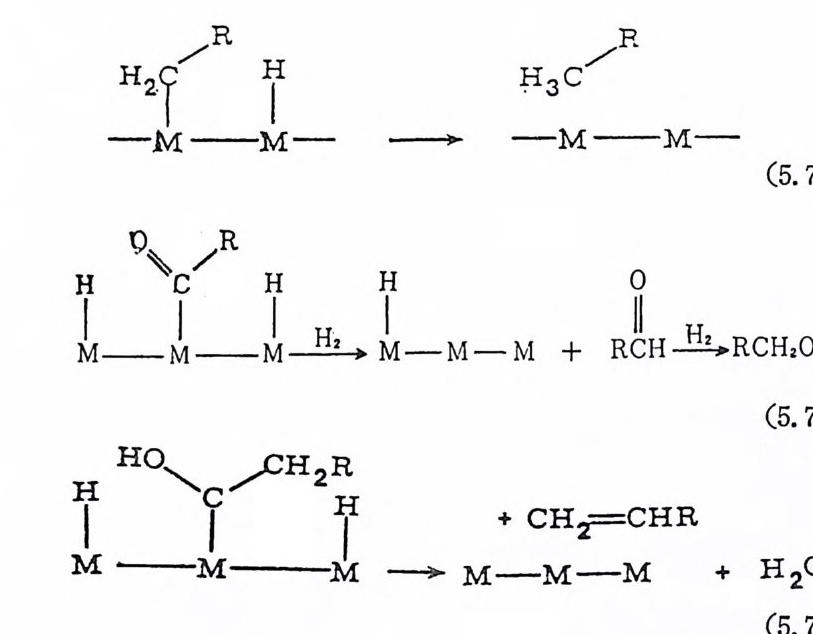 —M —R M — 一 一 M-R M ― (5.72)
—M —R M — 一 一 M-R M ― (5.72)
이 제 까지 살펴 본 Fis c her-Trop sc h 반응의 메 카니 즘은 직 접 실험 적으로 증명된 것보다는 주로 간접적인 이유로 제시된 것들이다. 많은 경우에 비슷한 반응에 관하여 군일계의 연구로부터 얻어전 정 보를 기초로 하였다. 따라서 위에서 제시된 각 반응단계와 비교될 만한 찰 알려진 군일반웅들의 예를 들면서 위의 반응단계를 다시 한번 살펴보기로 한다. Fis c her-Trop sc h 반응의 최 초단계 가 금속—포르밀의 형 성 단계 로 제시되었기 때문에 먼저 금속―포르밀 착물의 예를 찾아 보기로 한 다. 금속—포르밀 착물은 오랫동안 유기금속반웅의 중간체로 제시되 어 왔으나 1973 년에 Collman 둥에 의해서 처음합성되었다(석 (5.75) 참조 ).58) 이어서 여러 방법으로 금속-포르밀 착물의 형성이 보고되 었으나 대부분의 경우에 분리, 확인되지 않고 용액 중에 존재하는 58) J.P . Coil m an and S,R. W int e r , ]. Am, Gli em , Soc. , 95, 4089 (19 73).
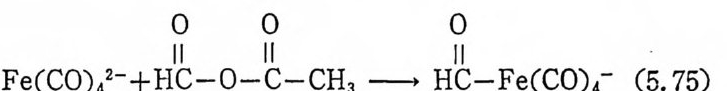 0 0 0
0 0 0
것을 측정한 것이다. 그러나 공기뚱에서도 안정한 레늄-포르밀 착 물 ([Re z( C0)9CHO J-)처 럼 용액 으로부터 결 정 (cr y s t al) 으로 분리 되 어 명백히 확인된 금속―포르밀 착물도 있다 .59) 이 레늄―포르밀 착물 은 찬전자체 (elec t ro ph i le) 와 반응하여 H-를 빼 앗기 고 Re2(C0)10 이 된다(식 (5.76) 참조 ).59) 이렇게 금속-포르밀 착물은 H+ 와 쉽게 반 응할 수 있기 때문에 배위된 포르밀기는 포름알데히드 또는 메탄올 로 환원되 기 도 한다(식 (5. 77) 참조). 죽 철一포르밀 착물은 H+ 와 반
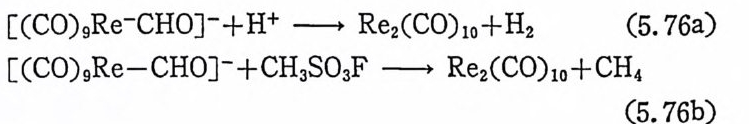 [(C0)9Re-CH 이 -+H+ 一 Re2(C0)1o+H2 (5.76a)
[(C0)9Re-CH 이 -+H+ 一 Re2(C0)1o+H2 (5.76a)
응하여 CH30-를 만들고 CH30-는 H+ J하 반응하여 메 탄올울 생 성 하는 것으로 추측된다(식 (5.78) 참조). 철-포르밀 착물로부터 메탄
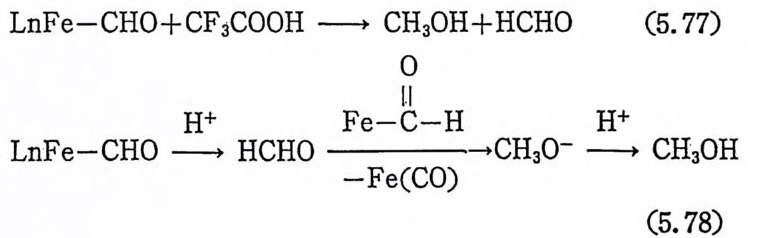 LnFe-CHO+CF3COOH 一 CH30H+HCHO (5.77)
LnFe-CHO+CF3COOH 一 CH30H+HCHO (5.77)
울을 얻는 과정 (직 (5. 77) )에 관한 가능한 또 하나의 메 카니 즘은 철 -히드록시카르벤 착물 (Fe=C 〈십 H) 중간체를 거치는 경로이다. 즉 포르밀기의 산소에 양성자첨가반응이 일어나서 철-히드록시카 르벤 착물이 형성되며 이어서 또 하나의 철-포르밀 착물과 반응하 여 철―히드록시메탈 (Fe~CH20H) 착물을 형성하며 마지막으로 H+ 와 반응하여 메탄올이 얻어진다(식 (5.79) 참조). 식 (5.79) 에서 보 는 바와 같이 금속一포르밀 형 성단계 다음으로는 금속―히드록시 메 틸 착물(또는 알파히드록시알킬-금속착물)의 형성단계가 될 것이
59) C.P. Casey and S.M. Neuman, ]. Am. Chem. Soc, 100, 2544 (19 78).
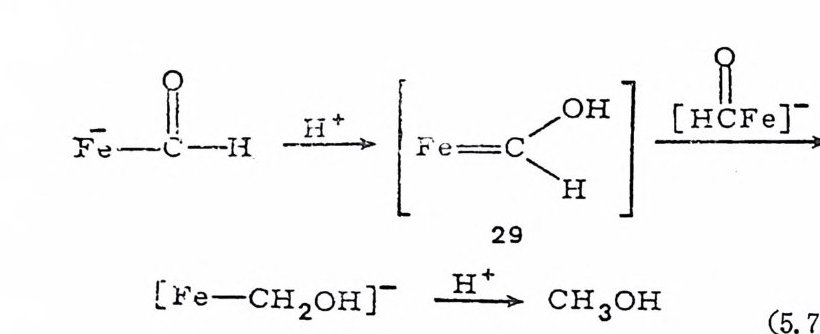 F~— C『· — I1 L-1- + ):,- -F ,e -—— C/\9O H H- [- H oF ec ] -
F~— C『· — I1 L-1- + ):,- -F ,e -—— C/\9O H H- [- H oF ec ] -
다. Casey 둥은 최 초의 히 드록시 메 탈―금속착물 ((CsHs) (NO) (CO) Re-CH20H) 를 합성하였으며 ,60> S t one 둥은 이미 1970 년에 알파히 드록시 알킬-금속착물 ((C5H5) i( C0)2Fe-(C(CF3)20H) 을 보고한 바 있다. 61) 히드록시메틸―금속착물은 금속―카르벤착물에 OH- 를 반응시켜 얻을 수도 있다. 이 반응은 가역반응으로 히드록시메틸 착물 중의 히드록시기는 H+ 에 의해 제거될 수도 있다(식 (5.80) 참조). 카르벤
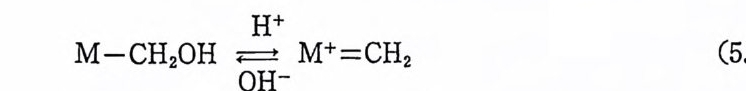 H+
H+
리간드는 히드리도금속 (M-H) 과 반응하여 쉽게 알킬기가 될 것이 다. 이렇게 하여 생성된 금속―알킬 결합에 co 가 삽입되어 탄소고 리는 길게 늘어갈 것이다. 즉 금속―포르밀 중간체를 거치지 않고 얻어지는 금속―카르벤이 금속—알킬로 환원되고, 이어서 co 의 삽 입반응이 일어나 F i scher-Tro p sch 의 반응에서처럼 탄소고리의 길 이가 길어질 수 있다고 추측된다. 실제로 공업적 생산에서도(미국 Unio n Carbid e 회사) 히 드록서 메 틸 착물 중간체 를 거 치 는 과정 을 이용하여 에탈렌글리콜을 생산하고 있다. 이 과정은 아래에 자세히 고찰될 것이다. 이제까지는 Fi sc her-Trop s ch 반응이나 앞으로 논의될 군일촉매계
60) C. P. Casey, M. A. Andrews and D. R. McAl ist e r , J. Am. Chem. Soc. , 611) 0 T1, . 3B37la1c k(1m'5o7r9 e),. M. I. Bruce, P. J. David s on, M. Z. lgb as and F. G. A. Sto n e, J. Chem. Soc. , A, 3153(1 '570 ).
에 의한 co 의 수소화반응의 이해에 도움이 될 만한 반응과정들을 실례를 들면서 살펴보았다. 특히 금속―카르벤 및 금속―포르밀 그 리고 금속―히드록시메탈(또는 금속―알파히드록시알킬)등이 관련 되는 반응들을 살펴보았다. 마지막으로 배위된 co 가 직접적으로 환원되는 과정을 살펴본다. 1968 년에 처 음으로 텅 스텐― 카르보 닐 착물이 NaBH4 에 의 해 서 텅 스텐_알킬로 환원된 것아 발표되었다(식 (5.81) 참조 ).62) 식 (5.81 )
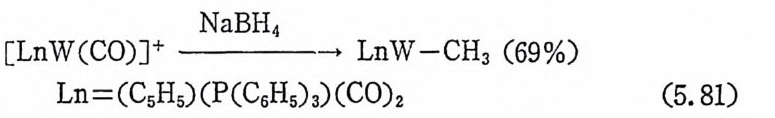 [LnW(CO)J+ -Na-BH4+ LnW 一 CH3 (69%)
[LnW(CO)J+ -Na-BH4+ LnW 一 CH3 (69%)
도 텅스텐―포르밀 중간체를 거쳐 일어날 것으르 제시되었다. 텅스 텐이 가지 고 있는 양전하(p os iti ve charge ) 때 문에 H-의 공격 이 쉬 웠을 것으로 추측된다. 아래의 예들이 위의 추측을 지지해 준다. 족 중성 (+ 또는 -의 전하를 갖지 않는)의 철-아세 틸 착물 (C5H5) (P(C6H5)3)(CO)Fe 一 CO-CH3 는 효과적 인 Lewi s 의 산인 BH3 에 의 해서 철―에 탈 착물 (CsH5)(P(C6H5)3)(CO)Fe-C2H5 로 환원되지 만, NaBH4 에 의해서는 환원되지 않는다 .63) 그러나 한편 양이은성 카르벤착물 [(C sHs)(P(C5Hs)3)(CO)Fe=C(OC2H5)CH3J+ 는 NaBH4 와 반응하여 철―에틸 착물 및 철-알파에목시에틸 착물을 생성한 다(식 (5. 82) 참조). 64) 식 (5. 82) 로부터 철―에 틸 착물은 철-알파에 톡시에틸 착물을 거쳐 생성되는 것으로 추측된다. 이상의 반웅들은 대 부분 부산물 (s i de p roduc t)을 생 성 하는 반웅들이 다(예 : 식 (5. 81) 의
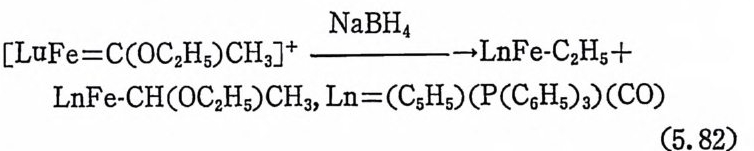 NaBH4
NaBH4
수울은 69% 이 며 , 식 (5. 82) 의 생 성 물은 두 착물이 다).
62) P.M. Treic h el and R.L. Shubkin , Inorg. Chem., 6, 1328 (19 68). 63) J.A . Van Doorn, C. Maste r and H.C. Volge r, J. Orga nomet. Chem., 641) 0A5, . 2D46a(v1 i9s o7 n6 ).a nd D. L. Rege r , J. Am. Chem. Soc. , 94, 9273 (1972).
Bercaw 둥은 최초로 정량적으로 배위된 co 가 수소화되는 반 웅을 발표하였 다(식 (5. 83) 참조). 65) 한편 L2Zr(C 0) 2 와 L2ZrH2 는
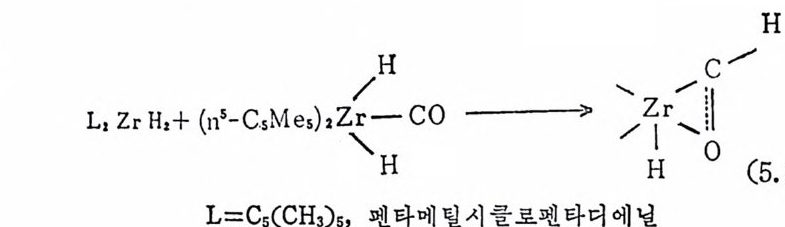 H
H
25°C 에서 H2Cl 기압)하에서 정량적으로 [L2ZrHJ 2( µ-0CH=CHO) 를 생성한다(식 (5.84) 참조 ).6 6 ) 한편 식 (5.84) 에서 얻어지는 二核착 물 [L2ZrH ]z (µ-OCH=CHO) 는 LnZrH2 와 co 의 반웅으로부터 얻
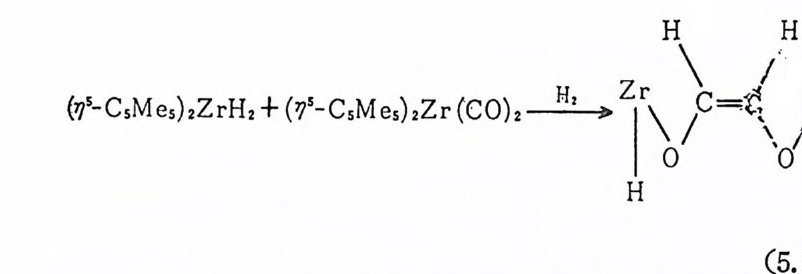 (#-c5M e 5)2ZrH2+(#-C5Me5)2Zr(CO)2 』一 1r\H \ / C= 김/ H 7l.
(#-c5M e 5)2ZrH2+(#-C5Me5)2Zr(CO)2 』一 1r\H \ / C= 김/ H 7l.
을 수 없었다 .66) 따라서 LnZrH2 의 배위된 H 가 LnZr(C0)2 의 배 위된 CO 와 반응하는 것으로 추측된다. 즉 석 (5. 85) 의 반응이 일 어날 것으로 제시되었으며, 식 (5.85) 를 증명하기 위한 신형으로 실
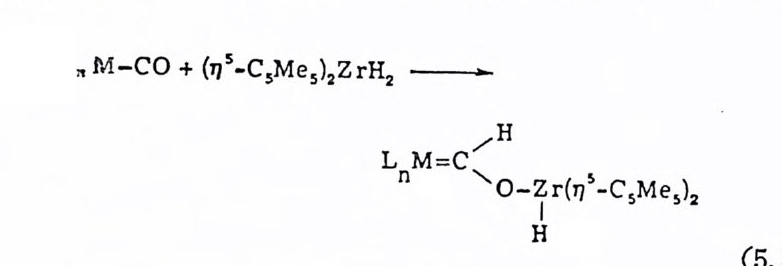 ,, M- CO + (TJ5 -C5Me5)2ZrH2 ———
,, M- CO + (TJ5 -C5Me5)2ZrH2 ———
65) J.M . Marin q u ie z , D.M. McAl ist e r , R.D. Sanner and J.E . Ber.ca w , J. Am. Chem, Soc. , 100, 2716 (19 78). 66) P. T. Wolczanski, R, S. Threlkel and J. E. Bercaw, J. Am. Chem. Soc, , 101, 218 (19 79).
제 L2W(CO) 문 L2ZrH2 9-} 반응시 켜 서 석 (5. 86) 가 정 량적 으로 일어 남을 밝혔다 .66) 즉 배위된 CO 는 배위된 H 에 의해서 환원되었다. 끝으로 L2ZrH2 중의 배 위 된 수소는 수소화 이 온(H-, h y dr i de) 의 성 질이 크며, 배위 중심금속인 지르코늄은 효과적인 Lew i s 의 산으로 알려쳐 있다는 사실이 주목을 끈다. 이상으로 Fis c her-Trop sc h 과
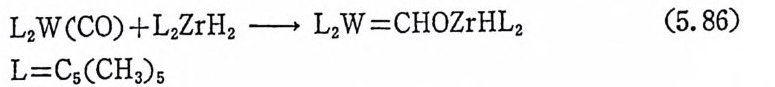 L2W(CO) +L2ZrH2 -一 L2W=CHOZrHL2 (5. 86)
L2W(CO) +L2ZrH2 -一 L2W=CHOZrHL2 (5. 86)
정의 메카니즘을 이해하기 위하여 관련되는 정량적인(촉매순환과정 의 반응이 아닌) 군일반응들을 살펴보았다. 지금부터는 군일촉매계에 의한 co 의 수소화반응의 예를 들면서 살펴 보기로 한다. 1) 알콜합성 C02(CO)s{:-C O 의 수소화반응에 촉매적 역할을 하여 메탄올, 에 탄올, 푸로판올, 및 각각의 포름산 에 스테 르를 생 성 시 킨다. 67 ) 182° C, 300 기 압하에 서 CO 와 H2 의 비 율이 1 : 1 인 혼합기 체 를 사 용하는 경우에 최초의 주생성물은 메탄올이 되지만 소량의 포름산 메틸이 함께 생성된다. 반응을 계속 진행시키면 에탄올, 1- 푸로판 올 및 이들 알콜의 포름산 에스테르가 생성된다(식 (5.87) 참조). 반 웅속도에 관한 데이타를 근거로 하여 이 반응은 군일촉매반응인 것 으로 제 시 되 었 다. 단 10 정 도의 전환수(t urnover number) 가 얻어 졌 다 .67) 이상의 군일촉매반응에 관하여 제시된 메카니즘을 보면 아래
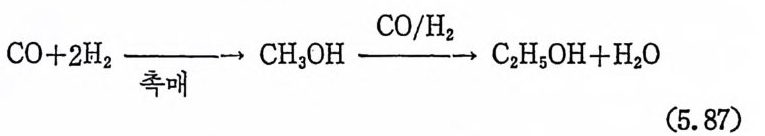 CO/H2
CO/H2
와 같다. Co2(CO)s 가 H2 와 반응하여 HCo(C0)4 를 형 성 함은 찰 알 려진 사실이다(식 (3.3) 참조). 따라서 메탄올의 합성온 HCo(C0)4 와 co 의 반웅에서 얻어지는 자유라디칼에 의해서 진행된다고제시 되었다(식 (5.88) 참조 ).67) 또한 이렇게 포르밀 라디칼이 생기는 식 67 ) J.W . Rath k e and H.M. Feder, J. Am. Chem. Soc., 100, 3623 (19 78).
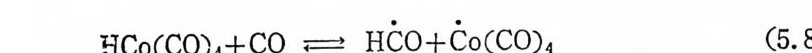 HCo(C0)4+CO ~ HCO+Co(C0)4 (5. 88)
HCo(C0)4+CO ~ HCO+Co(C0)4 (5. 88)
(5.88) 의 단계가 CO 와 H2 로부터 메탄올을 얻는 전체 반응의 속 도결정단계가 될 것이라고 제시되었다. 생성된 포르밀 라디칼이나 포름알데히드는 히드로포르밀화반응에서 알데히드가 알콜로 환원되 는 것처럼 쉽게 알콜로 환원될 것이다(재 3 장 2 참조). 비슷한 二核 ―카르보닐 착물인 Mn z( C0)10 도 240°c, 306 기압 (CO 와 H 거 압 력)에서 소량의 메탄올을 생성시키는 것으로 보고 되었다 .67) Bradly 는 및 및 루테 늄착물 H4RulC0)12, H3Ru4(CO) 귬, 및 Ru6C(C0)1l-동 의 뭉치화합물을 사용하여 CO 와 H2 의 반응으로 부터 메탄올과 포름산 메털을 얻었다 .68) l300 기압과 225~275°C 에 서 일어나는 이 반응의 용액으로부터 분리된 루테늄착물은 모돈 경우에서 Ru(CO)s 분이었다. 따라서 위의 루테륨-카르보닐 뭉치 화합물들은 촉매의 전구물질(p recursor) 에 지나지 않는 것으로 추측 된다. Ru(acac)3(acac= 아세탈아세토나토)을 사용하여도 Ru(CO)s 를 형성하며 메탄을이 생성되기는 마찬가지다. co 의 수소화반응 에 의해서 메탄올이 생성되는 반응은 엔트로피가 감소되는 발열반 웅이다(식 (5.89) 참조). 따라서 메탄올 생성반응은 낮은 온도에서 더 잘 일어날 것이다. 현재 이용되는 불균일촉매계에 의한 메탄올의
![]() co+2H2 —* CH30H 6G=21. 23kJ/ m ole (5. 89)
co+2H2 —* CH30H 6G=21. 23kJ/ m ole (5. 89)
생산과정은 적절한 반응속도를 얻기 위하여 높은 온도에서 진행시 킨다. 이렇게 높은 온도에서는 적철한 평형을 유지시키기 위해서 높은 압력이 필요하게 된다. 이렇게 높은 온도에서는 온도의 조절 이 어려울분아니라가끔촉매자체가활성을잃어버린다. 불군일계 와 비교하여 군일계는 비교적 열(온도)을 조절할 수 있다. 따라서 군일촉매계에 의한 메탄올의 생산온 공업적으로 중요한 의미를 갖 게 된다. 그러나 상기 Ru(C0)5 에 의한 메탄올의 메카니즘에 관한 제시는 없었다. 단 Ru(C0)5 에 의한 메탄올 생성과정의 활성화에 너지는 32Kcal/mole 정도이었다. (위에서 기술한 HCo(C0)4 에 의
68) J. S. Bradly, /. Am. Chem. Soc. , 101, 7421 (19 79).
한 메 탄을의 생 산과정 의 활성 화에 너 지 는 41Kcal/ mo le 이 었 다. 67) 2) 에탈렌글리콜 합성 미 국 Unio n Carbid e 회 사는 합성 가스 (s y n t he ti c gas , H2 : CO = I : I) 로부터 가용성 금속촉매를 사용하여 에틸렌글리콜의 생성을 발표하 였다(식 (5.90) 참조 ). 6” 이 과정은 여러 문제접을 가지고 있다. 독
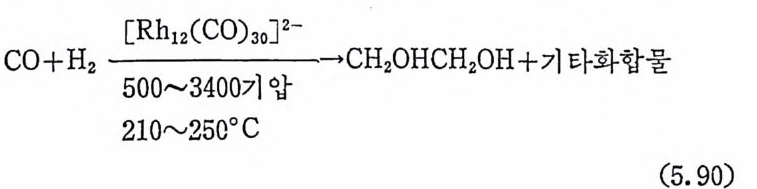 [R h12(CO)30]2_
[R h12(CO)30]2_
히 고압에서 일어날 분 아니라, 생성물이 여러 가지이므로 분리가 문제이다. 그러나 이상의 문제만 해결된다면 경제적으로 상당한 이 접을 가지고 있다. 이 반응에서는 메탄올, 에틸렌굳리콜, 푸로필 렌글리콜 및 글리세몰 동아 함께 생성된다. 그러나 생성물 중의 에틸렌글리콜의 함량을 70% 까지 얻을 수 있다는 접이 이 반응의 장접이 된다. 單核 로듐착물 Rh(C0)2(acac) (acac= 아세틸아제토 나토), 카르보닐 뭉치화합물 Rh4(C0)12 및 Rh6(C0)16 등을 촉매 로 사용하여도 비슷한 결과를 얻게 된다. 180°C 에서 높은 기압하 에서 측정된 용액의 적의선 스펙트럼의 co 신축전동수를 분석한결 과 용액 중에는 〔 Rh12(CO)30]2_ 이 촌재한다고제시되었다 .69) 메카니 즘에 관하여서는 거의 보고되지 않았으며 특허로 되어 있다 .70) 그 러나 히드록시메틸로듐 착물 중간체를 거쳐 에틸렌글리콜이 생성될 것으로 추측되고 있다(식 (5.91) 참조 ).57) 비슷한 예를 망간착물의 반
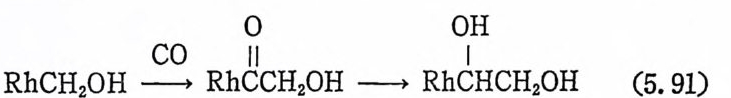 O OH
O OH
응에서 찾아볼 수 있다. 즉 석 (5.92) 에서 보는 바와 같이 알파아실 메틸착물이 co 의 반응에 이어서 수소와 반응하여 에틸렌글리콜의
69) R. L. Pruett , Ann. N. Y. Acad, Sci , , 295, 239 (11:577 ). 70) R. E. Pruett and W. E. Walker, U. S. Pate n t 3957857 Cll:57 6 ).
유도체를 만든다. 71) 아세 트산 코발트 C II )도 co 의 수소화반응을
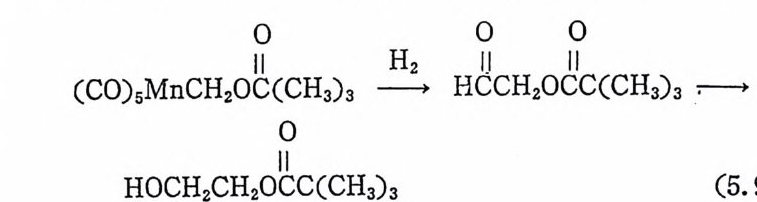 。 0 0
。 0 0
일으켜 에틸렌굳리콜을 생성시킨다 .72) 다만 코발트에 의한 반응은 위에서 기술한 로듐착물에 의한 반응보다 속도도 느리고 선덱성도 낮다. H3)a l아co세n 트회산 사비는닐 c o합 의성 수소화반응으로부터 아세 트산 비 닐 (Vi ny l ace t a t e) 을 생 산하는 과정 을 발표하였 다. 72) 반응과정 을 보면 아래 와 같다(식 (5.93) 참조). 죽 CO 와 H2 로부터 얻어지는 아세트산 메틸
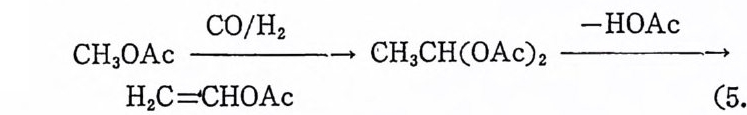 CO/H2 -HOAc
CO/H2 -HOAc
(meth y l ace t a t e) 을 합성 가스 (CO/Hz) 와 반응시 켜 디 아세 트산 에 틸 이 덴 (eth y lide ne d i ace t a t e) 을 생 성 하고, 생 성 된 디 아세 트산 에 틸 이 벤 온 분해되어 아세트산 비닐과 아세트산을 생성한다. 이 반응의 마 지막 단계의 수율은 높다. 그러나 고온에서 금속산화물 촉매가 필 요하다. 아세트산 메틸과 co 의 반응은 로듐(또는 팔라듐) 영과요 오드화 이온(i od i de) 으로 이루어지는 촉매계에 의해서 진행된다. 예 를 들어 RhC13 • 3H20 와 3- 피콜란 (3- pi co li ne) 및 요오드화 메 틸이 이루는 촉매계의 촌재하에서 아세트산 메틸은 1so0c, 140 기압에서 CO 와 H2 의 혼합기 체 (CO:H2=l : 2) 와 반응하여 디 아세 트산 에 틸 이 멘 44%, 무수 아세 트산 (aceti c anhy d rid e ) 6. 5% 및 아세 트알데 히드 0.6% 를 생성한다. 이상의 반응에 관화여 식 (9.54) 와 같은 반 응경로가 제시되었다. 위의 알코올합성에서 고찰되었던 비슷한 과
71) B.D. Dombek, J. Am. Chem. Soc,, 101, 6466(1 9 79). 72) N. Riz k alla and C. N. Wi nn ic k , Ger. Off en leg, 2610035 (1W 6).
청 듈이 재시 되 고 있 다. 아세 트산 메 틸과 요오드화 수소 (h y dro g en i od i de) 의 반응으로 생 성 되 는 요오드화 메 틸은 낮은 산화수를 갖는
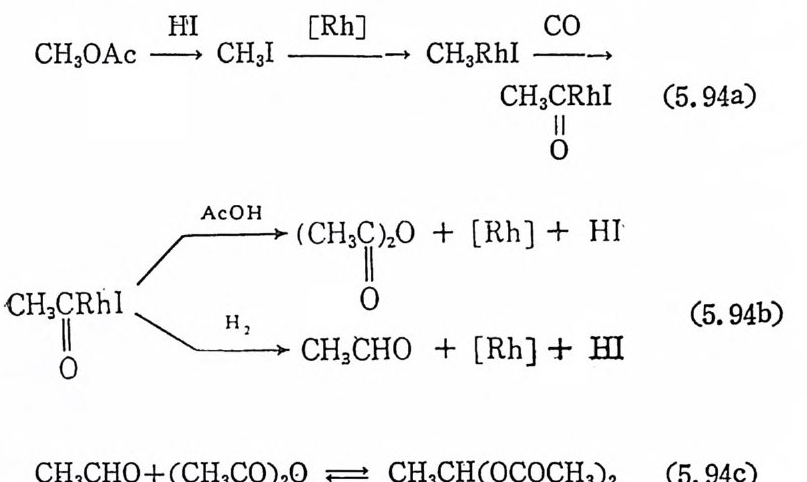 HI 〔 R 町 따
HI 〔 R 町 따
로듐에 산화성 첨가반응을 일으켜 중요한 중간체로 추측되는 Rh- ·CH 3 결합을 만든다. 이 어 서 Rh-CH3 절합에 co 가 삽입 반응을 일 으켜 또 하나의 중요한 중간체인 로듐―아세틸착물을 만든다. 금속 ―아세틸은 아세트산과 반응하여 무수 아세트산을 생성한다. 한편 금속―아세털은 수소와 반응하여 히드로포르밀화반응에서처럼 알데 히드를 생성하기도 한다. 이렇게 하여 생성된 무수 아세트산과 알 데히드의 반응으로부터 디아세트산 에틸이덴이 생성되고 이어서 아 세트산 비널과 아세트산이 생성된다고 추측된다. 이제까지 디아세 트산 아온의 합성에 관한 반응메카니즘이 보고된 적은 없다. 위에 제시된 반응경로(식 (5.94) )는 주로 생성물을 분석하여 얻은 정보를 근거로 제시된 건과이지만 비교적 무난한메카니즘이라고추측된다. 4) 탄화수소의 합성 촉매 전구물질 Ru3(C0)12 을 사용하여 메 탄 또는 기 타 Fis c her- · Tro p sch 반응 생성물을 얻은 보고가 있었으나 Rua(C0)12 의 분해반 옹에 의해서 생기는 루테늄 금속에 의한 것으로 알려졌다 .68),73) Osa 73O) rMg.a nJ.o mDeo ty. le C, hAem.P. ,. 1K74o,u wCe5n5 h(o1v9e 7r,9 ). C.A. Schaap and B. Van Oort, J.
(C0)12 및 lr4(C0)12 의 분해반응에 의한 CO 의 수소화반응은 140,, g 2 기압하에서 메탄을 생성하였으나 이 반응도 불균일촉매반응으로 추측된다. 74) 메 탄화반응 (me t hana ti on) 은 대 부분의 경 우에 전이 금속 (불용성 금속산화물, 할로겐화물 또는 금속) 촉매 를 이 용하는 불균 일 촉매 반응이 다. 75) 따라서 많은 경 우에 co 의 수소화반응에 서 탄 화수소가 얻어지면 전이금속 화합물인 촉매전구물질 (ca t al y s t pr ecur sor) 의 분해에 의해서 생성되는 금속입자에 의한 반응으로 추축되 기도한다. Muett er ti es 는 전이 금속 뭉치 화합물과 Lewi s 의 산 A1Cl3 를 촉 매계로 하여서 CO 와 H2 의 반응으로부터 탄화수소를 얻었다 .76) 즉 비교적 낮은 온도와 낮은 압력 (l80°C, 1 기압)에서 lr4(C0)12 와 용융된 NaCl • 2A1Cl3 를 촉매 겨] 로 하여 Fis c her-Trop s ch 반응의 생
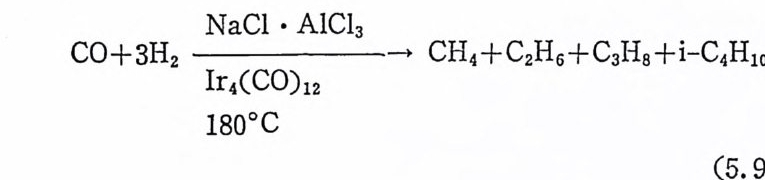 NaCl • AlC13
NaCl • AlC13
성물들을 얻었다(식 (5.95) 참조). 이 반응(식 (5.95) )은 균일촉매반 웅으로 보고되었다. 비교적 낮은 co 의 압력에서 탄소수가 적은 탄 화수소를 생성시킨 반응이다(에탄이 반응초기의 주 생산물이다. 상 기 촉매 반응의 전환수(t urn-over number) 는 상당히 낮다. 그러 나 Ir4(C0)12 는 쉽게 분해되어 금속 이리듐을 생성하지 않는 것으로 알 려졌다. 다른 카르보닐 전이금속 뭉치화합물 Rh4(C0)12, Rh5(C0)16. 및 Ru3(C0)12 둥은 상기 NaCl • AICl3 염 (용융된)에 서 는 쉽 게 분해 되어 금속상태의 루테늄이나 로듐이 생성된다. CO 의 수소화반응 온 H20 를 생성시키므로 AICl3 는 반응이 진행됨에 따라 계속해서 분해된다. AICl3 는 중간체로 생성되는 포름알데히드를 안정화시킨
74) M.G. Thomas, B.F. Beie r and E.L. Muett er tie s; J. Am. Chem_ Soc., 98, 1296 (19 76). 75) M. A. Vannic e , J. Cata / . , 37, 610979). 76) G. C. Demi tra s and E. L. Muett er tie s , J. Am. Chem. Soc. , 99, 2790, (1977).
다는 접을 고려하면 H 2 0 의 생성이 이 촉 매반응(식 (5.95) ) 의 전환 수가 낮음을 설명해 주기도 한다. 3. 물분해에 의한 수소발생 물을 분해하여 수소 (H2) 를 얻는 과정은두가지 면에서 그의의를 찾을 수 있냐 첫째는 물의 자원이 풍부하다는 접이고 둘째로 수소 CH2) 는 깨끗한 에너지라는 접이다. 물을 열분해하기 위하여서는상 당한 양의 에너지가 필요하다(식 (5.96) 참조). 따라서 최근에는 촉
![]() 2H20 一 H2+02 6G0=56.7Kcal/ mo le (5. 96)
2H20 一 H2+02 6G0=56.7Kcal/ mo le (5. 96)
메를 사용하여 물로부터 수소 CH2) 를 얻으려는 연구가 활발히 전행 되고 있다. 물 분해반응의 촉매계는 전이금속 화합물을 포함하고 있으며 불군일계와 군일계로 구별되기도 한다. 현재까지 발표된 대 부분의 촉매계(불군일계 및 군일계 모두 포함해서)는 빛(가시광선 또는 자의선)의 쬐임이 있어야 수소 CH2) 를 발생시칸다. 빛의 쬐임 없이 수소를 발생시키는 촉매계도 물론 보고되었다. 따라서 물 분 해반응은 태양에너지를 전환시키는 방법으로도 연구되어 지고 있다. 빛의 쬐임을 이용하는 촉매계 중에서 트리스 (2,2' -비피리단)루테늄 ( JI )착물을 광증감제 (p ho t osens iti zer) 로 사용하는 촉매 계 가 최 근에 활발히 연구되고 있다. 1) 트리 스 (2, 2' -비 피 리 던)루테 늄( JI )―코발트( JI )마크로시 클 ·(m acrocy cl e) 착물계 최 근에 트리스 (2,2' -바피리단)루테늄(JI) 착물, Ru(bp y)5 +( bP Y =2,2' 네피리단)은 물 분해반응의 촉매로 가장 각광을 받고 있는 착물이다. 아 착물은광(빛)에너지를 받아들뜬상태 (exc it ed s t a t e) 에 있는 發 光性(l um i nescen t) 루테늄착물 *Ru(b py )5+ 를 생성한다. 이 들뜬상대는 환원력이 대단히 강하여 열역학적으로 보면 물을 분해 하여 수소를 발생시킬 수 있을 것으로 기대되고 있다 .77) 현재까지 77) a) N. Suti n and C. Creutz , Adv. Chem. Ser. , 168, 1 (19 78). b) N. Suti n, J. Pholochem. , IO, 190979).
는 군일용엑 중에서 *Ru(b py) 꾼 에 의한 직접적인 물 분해반응은 관찰되 지 않았다. 한편, Ru(b py) 앞 , qL 2 +( L=(Me6[1 4 ]die n eN4) CH20)2) 및 아스코르브산 이 은 (ascor t a t e ion ) 또는 유로퓸 C II )을 포 함하는 수용액에 가시광선 (420 土 20nm) 을 쬐어주면 25°C 에서 H2 가 발생되는 것을 보고하였다 .78) 상기 보고의 내용은 다음과 같이 요 약될 수 있다. 비교적 짧은 수명을 가전 (shor t -l i ved) 환원제인 *R u (b py)꾼논 Er(II) 에 의해서 수명이 길고(l on g-Ii ved) 환원력이 강한 Ru (bpy )3+ 로 환원되고, Ru(b py )3+ 는 C 。 'L2+ 울 환원시켜 C}U 이 되 게 한다. 환원된 C 。 CI )은 빠른 속도로 H30+ 또는 H20 와 반응하 여 반응성이 큰(불안정한) C 。 -H 를 생성하고 이 C 。 -H 는 H+ 과 반응하여 수소 (H2) 를 발생시킨다(식 (5.97) 참조). 빛에 의해서 진행 된 알짜반응 (ne t reac ti on) 은 석 (5. 98) 로 표시 된다. 이 상의 반응메 카 니 즘(식 (5. 97)) 은 그후 보고된 반응속도측정 연구에 의 해서 지지 되기도 하였다 .79)
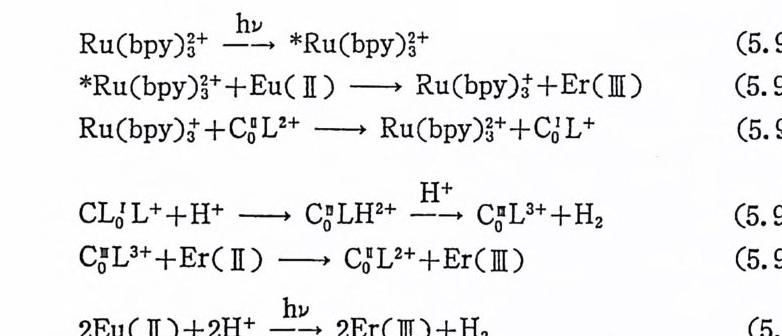 Ru(b py)꾼 —h-lJ+ *Ru(b py)꾼 (5.97a)
Ru(b py)꾼 —h-lJ+ *Ru(b py)꾼 (5.97a)
2) 트리 스 (2, 2' -비 피 리 던)루테 늄 C II )-트리 스 (2, 2' -비 피 리 단) 로듐 노 (IlI)-트 리에탄올아민계 위 의 Ru(b py )5+-C 。( JI ) 촉매 계 를 보고한 Suti n 둥 또 하나의 촉 · 매 계 를 발표하였 다. 80) 즉 Ru(bp y)5 +, Rh(b py)꾼, TEOA( 트리 에
78) G. M. Brown, B. S. Brunschwig , C, Creutz , J. F. Endic o t t and N~ Suti n, . J. Am. Chem. Soc, 101, 1298 (19 79). 79) C. V. .Kr ish nan and N. Suti n, J. Am. Chem. Soc. , 103, 2141 (19 81 ). 80) a) G. M, Brown, S. -F. Chan, C. Creutz , H. A. Schwarz and N. Suti n, JT.. AMma.t s uC bhaerma . anSdoc .N , . 1S0u1,t i n76, 3J8 . (1A9m 79. ). Cbh)e mS.. -SFo. c,C , ha1n0,3 , M3.6 9C h(1o9u8, 1C ).. Creutz , .
탄올아민) 및 K2P t C14( 또는 K2Pt CI G) (Pt 는 없 어 도 H2 는 발생 하 였음 80b) )을 포함하는 수용엑은 25°C 에서 450 士 20nm 의 빛을 쬐어주 면 수소 CH2) 를 발생시키면서 Rh (I)을 생성시킨다. 이 반응에서도 Ru.(b py)참는 광증감제 (ph oto s ensit ize r) 역 할을 한다. Suti n 둥은 연 속적 광분해 (conti nu eous-ph o to l ys i s ) 실 험 을 통하여 광반응 생 성 물의 종류 및 수율(yi eld) 을 조사하고, 섬 광분해 (flas h-p h oto l ys i s ) 실험을 통하여 반응경로 둥에 · 관한 정보를 얻음으로써 아래와 같은 반응 메 카니 즘을 제 시 하였 다. sob> Ru(b py )5 + 는 빛 을 흡수하여 둘뜬상태 의 *Ru(b py) 앙 가 되 며 *Ru(b py)꾼는 Rh(b py)안에 의 해 서 산화 되 어 Ru(b py)앞가 된다. 따라서 Rh(b py)맏 는 Rh(b py)양가 된 다. Ru(b py)앞는 TEOA 에 의해서 Ru(b py)꾼로 환원되기 때문에 Ru(b py )5 막 Rh(bp y)5 + 사이 의 역 반응 (Ru(b py)꾼 + Rh(bp y)5 + 一 Ru(bpy)『 +Rh(b py )33+ )은 일어나지 않는다. Ru(b py)앞을 환원시키면서 생성된 TEOA 자유라디칼은 자리옮김반응 (rearran g em en t)에 의해서 환원력이 있는 자유타디칼이 된다. (더이상의 자세 한 제시는 하지못했음 BOb)) 이 자유라디칼은 Rh(b py)앞을 환원시 켜 Rh( I )을 생 성 한다. 한편 Rh(b py)꾼는 bp y 하나를 해 리 시 키 고 Rh(b py)양가 되 며 , Rh(b py)양는 Rh(b py)꾼와 불균동화반응 (d i s p ro p or ti ona ti on) 을 일으켜 Rh(b py)앞와 Rh( I )을 생 성 한다. Pt 이 공존하는 용액에서는 Rh (I)와 H20 의 반응 (P t는 촉매의 역 할을 하는 반응)에 서 H2 가 발생 한다. Pt 이 촌재하지 않으면 Rh CI I )와 H20 의 반응이 Rh(b py)꾼와 Rh(b py)앞의 붑군동화반응 보다 먼처 일어 나면서 H2 를 발생 시 킨다. 그러 나 Lehn 등은 Rh( II ) 와 H20 의 반응에서는 H2 가 생성되지 않고 Rh (I)와 H20 의 반응 에서 H2 가 발생된다고 제시하였다 .el) 분만 아니라 Suti n 자신도 P t이 촌재하는 경우에 Rh(II) 이 반응하여 H2 를 생성서킬 것이라 고 발표하기도 하였다 .BO•) 그 밖에도 이상의 반응과정에는 몇몇 분 명치 못한 접둘이 있다. 즉 TEOA 의 자리옮김반응, Rh (I)과 H20 의 반응, 그리고 P t촉매의 역할등아직도연구될접이 많다. 그러 81 ) M. Kir c hin , J. -M. Lehn, J. ·P. Sauvage , Helv. Clzi m . Acta , 62, 1345 (19 79).
나 이 상 Suti n 의 실 험 결 과는 80) 비 슷한 촉매 계 를 연구한 Moradp o ur 등에 의해서 제시된 아래의 메카니즘과 거의 일치하는 것이다(식 (5.99) 참조 ).82) 식 (5.99) 는 Su ti n 의 촉매계와 동일한 촉매겨]를 연 구한 Lehn 의 메 카니 즘과도 동일한 것 이 다. 81) ,8 3) 단 식 (5. 99) 의 Q 와 Red 는 Lehn( 또는 Su ti n) 의 촉매 계 에 서 는 각각 Rh(b py)앞와 TEOA 에 해 당된다. Q 는 Ru(b py)꾼 가 Ru(b py)꾼로 산화되 는
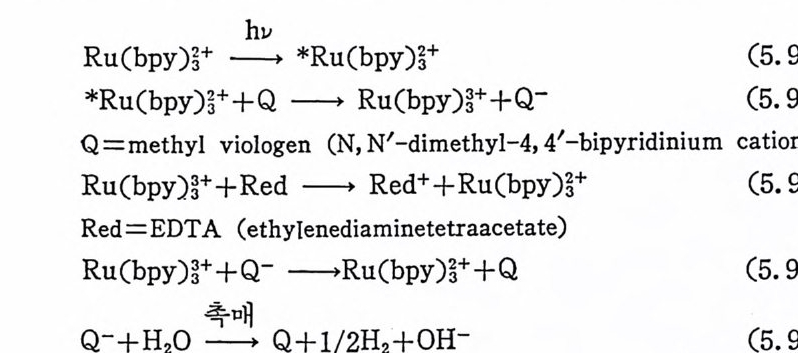 h)J
h)J
과정에서 쉽게 환원될 수 있는 물질이어야 하며 Red 는 산화된 Ru(b py)앙 가 환원된 Q 에 의 해서 다시 환원되는 반응(식 (5. 99d)) 를 막기 위한 것이다. 3) T i O 대자에 지지된 (su pp or t ed) P t과 Ru02-Ru(5 py)꾼과 메틸 비 올로겐 (vio l og e n) 계 Gratz e l 등은 1979 년에 물을 분해 하여 양자수득율(q uan t um yield ) 4 로 수소 (H2) 와 산소 (02) 를 생성시키는 이작용기성 (bif un cti on al) 산 화환원 (redox) 촉매계를 보고하였다(식 (5.100) 참조 ).84) 이 촉매계는
 4hv
4hv
두 개의 계로 나누어져 있다. 하나는 콜로이드성 T i 02 입자에 매우
82) A. Moradp o ur E. Amouy a l, P. Keller and H. Kag a n, Nouv. J. Ch im. , z, 547 (19 78) 83) J. ·M. Lehn and J. -P. Sauvage , Nouv. J. Cli im. , 1, 449(1 9 77). 84) K. Kalya n asundaram and M. Gratz e l, Ang e w. Chem. Int. Ed Eng l . , 18, 701 (19 79).
작은 입자로 된 P t과 Ru 아를 입혀서 만든 이작용기성 산화환원 촉 매(b p계y 이) 『고와, M또V 2+하 ( 나메 는탈 비 광올중로감겐제 = N( p,h No t'o -- s ed nism it e izteh ry ) l- 4역, 4할'-을b i p y하r i는d i n i u Rm u ca ti on) 의 계 이 다. 이 상의 촉매 계 에 의 한 산화환원반응은 Ru(b py)꾼 이 빛을 받아 둘뜬상태의 * Ru ( b py)꾼가 되고(식 (5.97a) 및 식 (5.99a) 참조) *Ru(b py)꾼는 전하를 이 동시 켜 MV2+ 를 환원시 키 면서 시 작 된다. 그후 Gr 쵸t zel 은 메 틸비 올로겐 (MV2+) 이 없어 도 식 (5.100) 의 반응은 진행된다고 발표하였다 .85) 메탈비올로겐이 없으면 산화환원 촉매계에 붙어 있는 광증감제의 일부만이 광활성 (p ho t oac ti v ity)을 보 인다. 이 경우에는 T i 02 의 전도띠 (conducti on band) 가 전자의 이동 울 중계한다 .86> Gra t zel 은 광증강제에 관한 실험에서 Ru(b py)양중 의 비 피 리 단 (b py)에 n- 도데 실 (dodec y l) 기 와 메 틸기 를 아래 그림 (5.1) 과 같이 치환시키면 수소발생의 양자수득울이 훨씬 증가함을 발견 하였다 .8 7 ) 이어서 Gr 쵸t zel 은 여러 실험의 결과로부터 다음과 같은
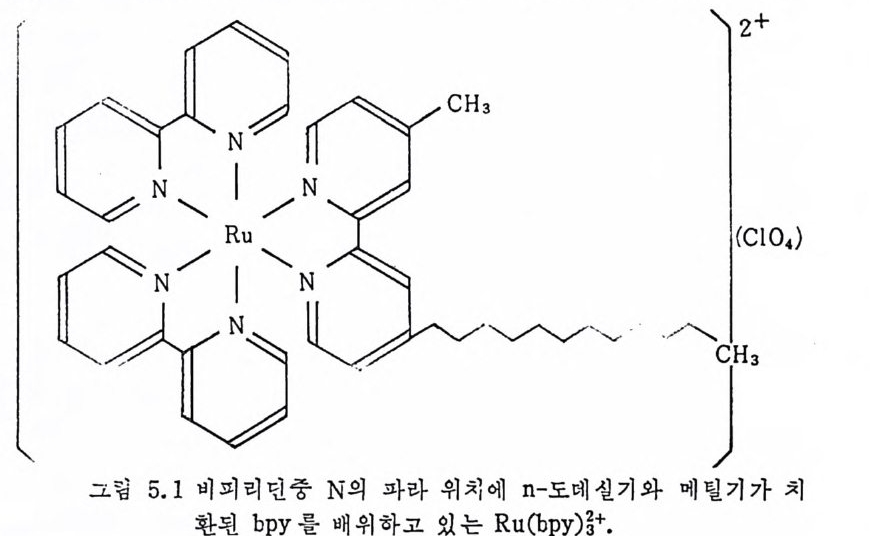 2+
2+
85) E. Borga rello, J. Kiw i , E. Peli zz ett i, M. Vis ca and M. Gratz e l, Natu r e, 289, 158(1 9 80). 86) a) W. D. K. Clark and N. Suti n, J. Am. Chem. Soc. , 99, 4676(1 9 77). b) A. Hamnet, M. P. D, -Edwards, R. D. Wrig h t, K. R. Seddon and J. B. Good- enoug h , J. Phy. Chem. , 83, 3280(1 9 79). 얽) C&E News, 64, Jan . 19 (19 81 ).
반응메카니즘을재시하였다 . 8 8) 즉위에서도여러 번 언급되었지만광 증감제 (Ru(b py)앞)에 의 한 광에 너 지 (가시 광선) 홍 수가 먼저 일어 나고, 이 어 서 전자의 이 동이 일어 난다. MV2+ 가 촌재 하면 MV2+ 에 게로 전자의 이동이 일어난다. MV2+ 가 없는 경우에는 T i 02 의 전 도며 (conducti on band) 로 전하가 이 동되 고, 전자는 다시 Pt 으로 전 달되 어 수소 CH 2 ) 가 발생 된다. 한편 Ru02 는 산화되 었 던 광중감제 (R \l (b py)앞)가 환원되 면서 산소 CO2) 를 발생 시 키 는 과정 에 촉매 적 역할을하는것으로제시되었다(그림 (5.2) 참조 ). 88 ) 산소 CO2) 의 발생 은 식 (5.101) 로 표시된다. 그림 (5.2) 의 단계들은 이미 위에서 설명
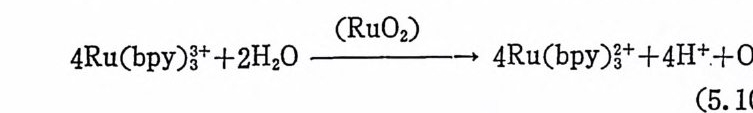 (Ru02)
(Ru02)
한 식 (5. 99a) 및 식 (5. S9b) 단계 등을 포함하기 도 한다. 지 금까 로 살펴본H G20r 죠t zel 의 촉매계도e 아직- -많1은ssI 접 *이 연• ~구02되 어 향야 할 것이 hv /s/H20 · 그림 5.2 T i O 센 지지된 P t와 Ru02-Ru(b py )5+; 세에 의한 물분 해 과정 .88a) s : 광증감제 (Ru(bp y)5 +),CB: 전도며 .
다. 예를 들면 식 (5.101) 에서 Ru02 의 역할, Pt 촉매에 의한 수소 (H2) 의 발생 반응메카니즘 등이 좀더 자세히 밝혀져야 할 문제이 다.
88) a) E. Borga rello, J. Kiw i, E. Peli zz ett i, M. Vis c a and M. Gratz e l, J. Am. Chem. Soc. , 103, 6324(1 9 81 ). b) R. Hump h rey- B aker, J. Lil lie and. M. Gratz e l, J. Am. Chem. Soc, , 104, 422(1 9 82).
4) 로듐-티 탄산 스트론튬 (s t ron ti um tit ana t e) 계 Lehn 둥은 반도체 위에 전이금속을 입혀서 만든 촉매계가 자의선 에 의한 물의 광분해 반응에 효과적인 촉매적 역할을 한다고 발표 하였다 .89) 이 촉매계는 위에서 소개한 것과 같은 광중감제를 포함 하지 않는 순수한 무기화합물로 이루어졌다. 현재까지 가장 좋은 결과를 보여 준 촉매겨]는 티탄산 스트론튬 (s t ron ti um tit ana t e) 에 로듐 울 입혀서 얻은 촉매계이다. 이 고체 촉매를 물에 넣고 자의선을 쬐 어 주면 수소 CH2) 와 산소 CO2) 가 발생 한다. 이 촉매 계 는 위 에 서 본 Su ti n 이나 Gra t zel 의 촉매계보다 여러 면에서 우수한 촉매계로 알 려져 있다 .69b) 이 촉매는 우선 쉽게 만들 수 있다. 예를 들면 영회 로듐의 수용액울 티탄산 스트론튬의 증류수 서스펜션에 가한 다음 자외선을 몇 시간 쬐어주어 얻어지는고체는곧 촉매로 쓰여질 수있 다. 온도와 압력 이 수소 CH2) 와 산소 CO2) 의 발생 에 영 향을 준다. 80°C 에서는 20°c 에서보다 약 4 배에 가까운 기체 발생을 보인다. 낮은 압력에서 기체 발생은 더욱 찰 일어난다. 이 촉매계의 단접은 가시광선에 의하여 반응이 일어나지 않고, 자의선에 의해서만 물의 분해가 일어나기 때문에 태양에너지의 5% 정도밖에 사용할 수 없 다는 접이다. 따라서 가시광선에 의한 촉매반응의 연구가 진행되어 야 할 것이다. 이런문제를 해걷하기 위해서는 촉매작용을 좀더 ~ 본적으로 이해해야 할 것이다. 예를 들어 티탄산 스트론튬에 입혀 전 금속(로듐)의 본질에 대하여 좀더 자세한 연구가 요구된다. 상기한 Lehn 의 촉매계와 비교되는 접으로 홍미로운 접은 다음과 같다. 즉 위 에 서 소개 된 Gratz e l 의 촉매 계 (Ru(b py)꾼, Ru02(Ti0 2 ), Pt (T i0 2 )) 중에 서 광증감제 (Ru(b py)앞)를 제 거 하고도 자의 선을 쬐 어 주면 수소 CH2) 와 산소 CO2) 가 발생된다. (Ru(b py)『)를 넣어 주면 가시광선에 의해서도 물 분해반응은 일어난다.) 상기 용액 (Gr 죠t zel 의 촉매겨 1 에서 Ru(b py)웅내문 제거한)울 어두운 곳에서 저어 주면 발생된 수소 CH2) 와 산소 CO2) 는 재결합한다. 그 다음 다시 빛을 쬐 어 주면 물 분해는 다시 일어난다.
89) a) J. -M. Lehn, J. -P. Sauvage and R. Zie s sel, Nouv. J. Chim . , 4, 623 (19 80). b) C & E News, 64, Jan . 19(1 9 82).
5) 물을 광분해하는 전기화학적 전지 Somorja i 둥은 최초로 광에너지를 에너지원으로 하여 물을 광분 해하는 전기화학적 전지를 발표하였다 .90) 죽 티탄산 스트론듐에 백 금을 입힌 것, 또는 티탄산 스트론튬, 또는 이산화 티탄을 양극 (anode) 으로 하고 인화 갈륨(g a lli um ph osp h id e ) 또는 텔루르화 카드 뮴 (cadm i um t ellur i de) 을 음극 (ca t hode) 으로 하여 물의 광분해로부터 수소 (H2) 를 얻었다. 그러나 이 전지계에도 문제점은 아직 많다. 사 용되는 물질이 고가일 분 아니라 그 물질로부터 얻어지는 반도체 는 화학적 전지에서 불안정하다. 계속적으로 수소 (H2) 를 생성시킬 수 있는 가능성은 있으나 이제 초보적인 연구단계에 지나지 않는다. 6) 물의 열 화학적 분해 (the rmochemi ca l decomp os it ion ) Fong 등은 비 교적 낮은 온도에 서 물을 열분해하여 수소 (H2) 를 발 생시켰다 .91) 죽 P t과 물을 130~210°c 에서 가열하여 소량의 수소 (H2) 를 얻 었 다. 상기 촉매 계 는 산소 (02) 롤 발생 시 키 지 는 않는다. 또한 상기 촉매계에 가시광선을 쬐어 주어도 수소 (H2) 또는 산소 (02) 는 생 성 되 지 않는다. 물을 환원시 켜 수소 (H2) 를 발생 시 키 기 위 해서 P t는 산화될 것이타고 제시되기도 하였다(식 (5.102) 참조). 그러나 더 이상의 자세한 반웅메카니즘은 알려져 있지 않다.
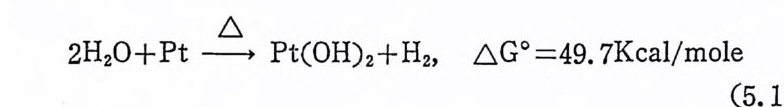 2H20+Pt 一쇼 Pt (O H)2+H2, t:::.G 0=49.7Kcal/ mo le
2H20+Pt 一쇼 Pt (O H)2+H2, t:::.G 0=49.7Kcal/ mo le
지금까지는 불용성 고체 금속 또는 금속화합물을 포함하는 촉매 계(또는 전지)를 이용하는 물 분해반응으로부터 수소 (H2) 가 발생되 는 과정을 살펴보았다. 마지막으로 가용성 금속착물에 의 한 물 분해반응으로부터 수소 (H2) 가 얻어지는 과정을 살펴본다. 7) 로듐 C I )착물과 물의 반응으로부터 수소 CH2) 발생
90) C & E News, 8, Sep t. 20 (19 82). 91 ) L. Galloway , D. R. Frug e, G. M. Haley, A. B. Coddin g ton and F. K. Fong , J. Am. Chem. Soc. , 101, 229(1 9 79).
Ot su ka 둥은 로듐 CI )착물과 물의 반응으로부터 수소 (H2) 가 발 생 함을 발표하였 다. 92) 히 드리 도카르보닐로듐 CI ) 착물 트란스 -RhH(CO)L2(L=P (i so p ro py l)3 ) 는 피리 단 촌재하에서 물과 반응하 여 수소 (H2) 를 발생 하고 트란스 _ [ Rh(CO)( py )L 니OH (py=피 리 던) 가 된다. 92) 이 상의 실 험 적 견 과로부터 반용석 (5. 103), 즉 RhH (CO)Lz 이 물과 산화성 첨 가반응을 일으키 는 반응경 로가 제시 되 었 다. 한편 히 드리 도로듐 CI ) 착물 RhHL a( L=P( i so p ro py 1)3) 은 물과 반응하여 산화성 첨 가 반응을 일으켜 시 스-디 히 드리 도로듐 (Ill) 착
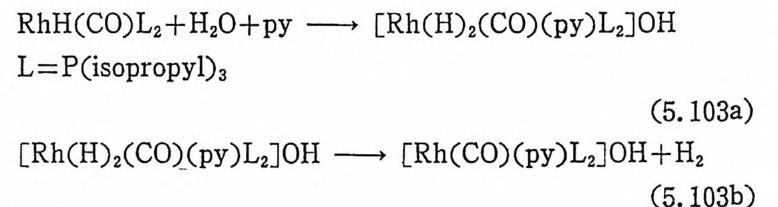 RL h=HP ( (CisOo p) Lro 2p+ yHl) 2 3 0+p y 一 〔 Rh(H)2(CO)( py )L 』 OH
RL h=HP ( (CisOo p) Lro 2p+ yHl) 2 3 0+p y 一 〔 Rh(H)2(CO)( py )L 』 OH
물 〔 Rh(H)2(PY)2L2 J OH 울 생성한다는 사실온 이미 알려져 있다 RL h=HP L(i3s+ o pH r2o 0p +ylp) 3y 一 〔 Rh(H)2(PY)2L 』 OH+L (5.104) (석 (5.104) 참조 ).9” 이 렇게 하여 얻은 착물 [Rh(H2)( py )2L2 J X(X= OH-또 는 B(C 갑 Is)4-) 는 t· C4H9NC 와 반응하면 상온에 서 쉽 게 수소
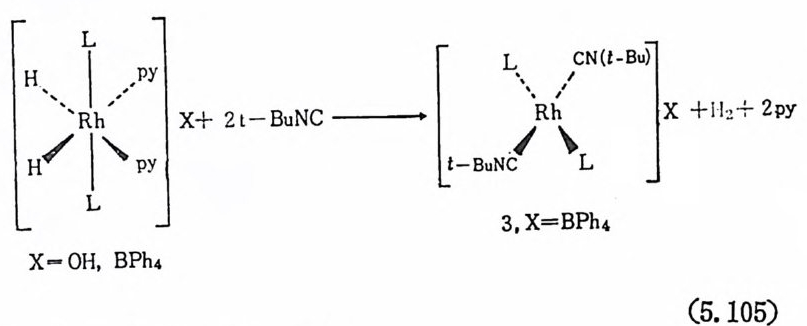 L_ ``_L`_|,|R` ‘,/h,-P x\+B 2L_ BuN C 一 [I-B uNC ;\ ]x +Il2+ 2p y
L_ ``_L`_|,|R` ‘,/h,-P x\+B 2L_ BuN C 一 [I-B uNC ;\ ]x +Il2+ 2p y
92) T. Yoshid a , T. Okano and S. Ots u ka, J. Am. Gli em . Soc. , 102, 5966 (19 80). 931) 1T35. , Y1o9s8h0i. d a , T. Okano, K. Sait o , an d S. Ots u ka, Inorg. Cli im. Acta , 44,
CH2) |� ����� ���(� (5.105) ��)8p. 92 ) 0 Rh(H)2(PY)2L 0[B(6CH 5)~J �� �\� CO @� �Q�X��� }� �� � CH2 |)� ��� X�p� [Rh(CO)(py) L2] 0 B(C vf )4] |� �� 1� \��. t� �X�� �� ��- � �� ܴ�� ij\�д( m ) )�<� [Rh(H)z( py)2L2+�J� o cX� ��Q@� ���� \� �� �� V] �� ܴ�� ij )�<� (Rh(Hzpy)()(C)OL2J+ � 1� ��� D� p� X� �� �� <�\� � �� � �� �(�� (5.106) 8�p�). 92) �� [Rh(H)2(PY)2L2J+\���0� � (H2) ��� @� �� 5���̹ Ȑ��Ȍ����ܴx� <լ�X�(py)t � ��t Ȑ���� ���ܴ�x �co �� X�t�� X�X��t�R h-H ��i�t� }�t��� ��t���\� H2 X� ��� t� ���`� ��<�\� $�����. D�P�� ��� �Q�<�\� �¤� ���ij \�д( m ) )�<� [Rh(H)z(py)2L2J+@� Ȑ��Ȍ� �� �ܴ D� <� �� � (b py ==2, 2'-b ipy r i d i ne) X� �Q�D� �
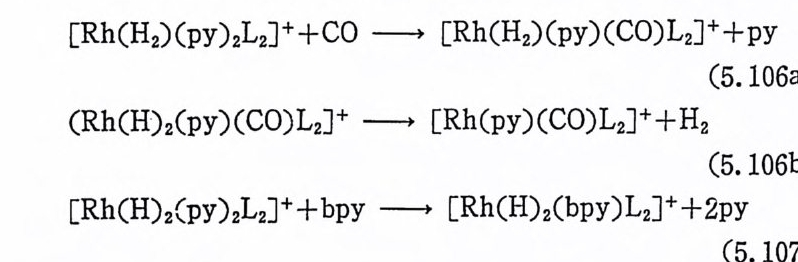 � ��� �. � [hRH() z(py )2L2 J+� � pby@� Q��X���
� ��� �. � [hRH() z(py )2L2 J+� � pby@� Q��X���
X� ���հ����� �L��� �t� $�����. Ȑ�|� ���XՔ� �� [Rh(H2)(pY)2L2J++co N[h(RH2)(py)(CO)L2J++py ( 5.106a) (Rh(H) z(py )(CO) �� N[Rh(py) (CO)L2J+
+H2(5.106h) [Rh(H)z(py)2L2J++bpy * [Rh(H)z(b py))L2)2 |J� + H+��2 pTy�� � ( 5�.�1 0 7�) � ܴ̹(�< �C O� � @ �� t �-�C�4 HD9� N <� �� X�)�@� �� �� � �� ܴ�� ij\�д( ill ) (Rh (H C @� �@�Ȑ�|� L��� �� 0��� ���ܴ�� Rh-H ��i�D� }�T����
룬다(식 (5.103b) 는 식 (5.106b) 와 같은 반응이 다). 즉 수성 가스이 동반응 (wa t er gas shif t) (CO+H2 0 --+ C02+H2) 의 촉매 과정 이 된 다(제 5 장 1 의 (3) 참조). *참고문현 1) C. P. Casey and S. M. Neuman, Adv. Ser. Chem. , 173, Chap ter 12 (19 79). ·2) G. Parshall, Homog e neous Cata l ys i s , Wi ley -l nte r scie n ce, p. 77 (19 80) . 3) E. L. Muett er ti es and J. Ste i n , Chem. Rev. , 79, 479 (19 79). 4) J. Falte , Carbon Monoxid e in Org a m·c Sy n th e sis , Sp ri n g e r-verlag p. 78 ( 1970) . £) E. S. Brown, Asp ec ts of Homog e neous Cata l ys i s 1I , Reid e l, p. 56 (19 74) . 06) I. Wender and P. Pin o , Eds. , Orga nic Sy n th e ses via Meta l Carbony ls , Vol. I (19 68) and Vol. 20977) , Wi ley -I nte r scie n ce. ·7) C. Maste r , Advances in Org a nometa l lic Cl;em i st r y , 17, 61 (19 79).
제 6 장 전이금속 착물에 의한 군일촉매 작용의 경향 George W. Parshall 은 미 국 Du Pont 회 사의 중앙 연구 개 발부 를 이꿀어 나가는 화학자이다. 생산공장의 연구실에서 오랫동안 겅 험 한 Parshall 은 최 근 그의 저 서 『 Homo g enous Cata l ys i s , 1he Ap - plic a ti o n and Chemi st r y of Cata l ys i s by Soluble Tran si t io n Meta l Comp le xes. Wi ley -I nte r sci en ce, 1980 』라는 책 의 끝에 서 〈 군일촉매 작 용의 경향 〉 을 분석하고 예측하였다. 촉매반응을 하나또는둘 더 고 찰하는 것보다는 군일촉매반응에 관한 연구의 방향 또는 전망에 관 하여 살펴보는 것이 군일촉매작용에 관십이 있는 이 책의 독자들에 게 도움이 될 것으로 판단된다. 따라서 G.W. Parshall 의 〈균일촉 매작용의 경향 〉 을 아래에 소개하고자 한다. 1970 년대에는 군일촉매반응의 연구 분야에 몇몇 눈에 뜨이는 뚜 렷한 경향이 있었으며 앞으로도 이 경향은 계속될 것같이 보인다. 그중에서 몇몇은 화학공업에서 필요하기 때문에 생긴 경향이다. 예 를 들면 새로운 형태의 공급물질(fe eds t ock) 을 이용하는군일촉매작용 또는 군일촉매의 장접과 불균일촉매의 장접을 모두 갖고 있으리타 고 생각되는 실질적인 혼성촉매 (h y br i d ca t al y s t)의 개발 등을 들 수 있다. 또 하나의 경향이라고 볼 수 있는 것은 촉매에 관한 과학 자 체가 발전함에 따라 얻어지는 촉매계의 복합성이다. 예를 들면 군 일촉매 반응에서는 선덱성 (selec ti v ity)이 계속 높아지고 있다. 한편 빛 에 의해서 활성화되는 새로운 촉매계가 개발되는가 하면, 하나 이
상의 중심 금속을 갖고 있는 촉매(예 :뭉치화합물)가 계속 개발되 고 있 다. 이 상의 경 향들을 공급물질(fe eds t ock) , 선택성의 향상 (enhanced sele cti v i t y), 혼 성 혹 매 (h y br i d cata l ys t) 그리고 새로운 촉 매화학 (new cata l ys t chemi st r y) 둥 4 부분으로 나누어 살펴 보고자 한다. 1. 새 로운 공급물질 (fee dsto ck) 1973 년과 1979 년 두 번의 오일위기는 지구상의 탄화수소 자원이 한계에 도달하였음을 일깨워 주었다. 이 오일위기가 각 국가에 미치 는 영향이 각각 다를 뿐 아니라 각각 다른 종류의 산업에 미치는 영 향도각각다르게 나타났다. 그러나일반적으로어느 국가나, 어느산 업 에 서 도 철실히 문제 가 된 것 은 석 유(p e tr oleum) 와 자연 가스 (na t ural g as) 에 의촌도를 줄이려고 한 접이다. 화학공업에서 시도한 것 중에 하나는 기본 공급물질로 합성가스 (s y n t hes i s ga s) (CO 와 H2 의 혼합 물)에 관십을 갖게 되었다는 접이다. 합성가스는 탄화수소의 공급 물질(석유 또는 자연가스)로부터 얻을 수 있지만, 석탄이나 기타 유기페기물에서도 얻을 수 있기 때문이다. 따라서 이러한 합성가스 를 기본 공급물질로 하는 화학공업은 탄소의 자원에 상당한 다양성 을 갖게 된다. 합성가스를 기본 공급물질로 하는 화학은 그 응용면 에서도 다양성을 갖게 될 분 아니라 군일촉매작용의 응용에 많은 이 접 을 갖고 있 다. 합성 가스는 알콜이 나 산 (a ci d) 과 같은 생 성 물이 포함하고 있는 산소 (0) 의 좋은 공급물질이 되기도 한다. 일산화탄 소와 수소 (H2) 를 사용하여 탄화수소를 합성하는 F i scher - Tro p sch 과 정(제 5 장 2 참조)은 상당한 비용이 드는 과정이므로 아직도 많이 개 량되어야 할 것이다. 혹자에 의하면 20 세기의 마지막은 군일촉매작용의 역사에서 합 성가스의 시대가 될 것이라고 하였다. 이렇게 예측하는 것이 좀 지 나찬 것이 될지는 몰라도, 20 세기를 아래와 같이 4 개의 공급물질 시대로 구분될 수 있을 것 같다. 1. 1910~1950 아제 틸 렌 (acety le ne) 2. 1950~1980 올레 핀 (olefi n)
3. 1980~2000 합성 가스 (s y n t hes i s ga s) 4. 2000~ bio m ass 군일촉매작용을 최초로 공업에 응용한 것은 아세틸렌의 영소화반 옹 (chlor i na ti on) 이었다. 1940 년대까지는 가용성 전이금속 촉매는 주 로 아세틸렌의 반응에서만 사용되어졌다. 1940 년대와 1950 년대에 이루어진 독일의 연구는 알파-울레판, 선형(li near) 폴리에틸렌 그 리고 아세트알데히드의 생산에 에틸렌을 사용할 수 있는 촉매반응 울 개발하였다. 군일촉매작용에서 합성가스를 공급물질로 이용하는 과정도 1940 년대의 독일 화학자들에 의한 연구결과이다. 이 시기에 처음 개발 된 올레핀의 히드로포르밀화반응이 울레핀의 시대를 열었다고 분 · 수 있다. 합성가스를 기본 공급물질로 하는 아세트산의 생산꽁정은 1960 년대에 공업화되었다. 그러나 경제적으로 이 아세트산의 생 산에 커다란 영향을 끼찬 것은 역시 1973 년의 오일위기였다. 예 를 들면 미 국의 Monsanto 회 사의 아제 트산 생 산공정 은 1970 년에 공 업화된 것으로 생산 시기가 좋아서 상당한 이익을 가져왔다. 위에 기술한 4 번째 시대 (2000 년 이후)인 생물학적 공급물질시대 는 쓰레기, 동물의 분뇨, 나무 조각 그리고 옥수수대 등이 주 공급 물질이 될 것이라고 생각된다. 이러한 물질들을 공급물질로 사용한 다는 것은 석유의 철약이타는 면과 경제적으로 페기물을 처리한다 는면에서 바람직한 일이다. 물을 기본물질로 하는 과정(물의 분해, 수성가스의 이동반응 둥)이 군일촉매작용에 의해서 어떻게 개발될 것인지는 아직 미지수이지만 연구개발할 만한 과제이다. 아세틸렌을 공급물질로 하는 아세트산 및 아세트산 비닐의 생산공정
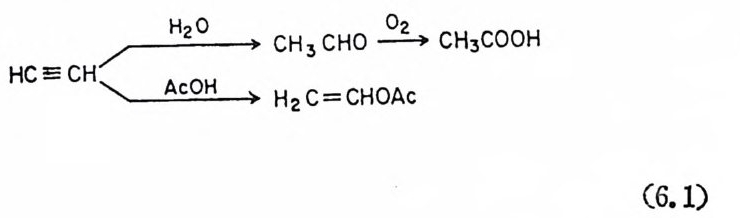 /二드 CH3 CHO ~ CH3COOH
/二드 CH3 CHO ~ CH3COOH
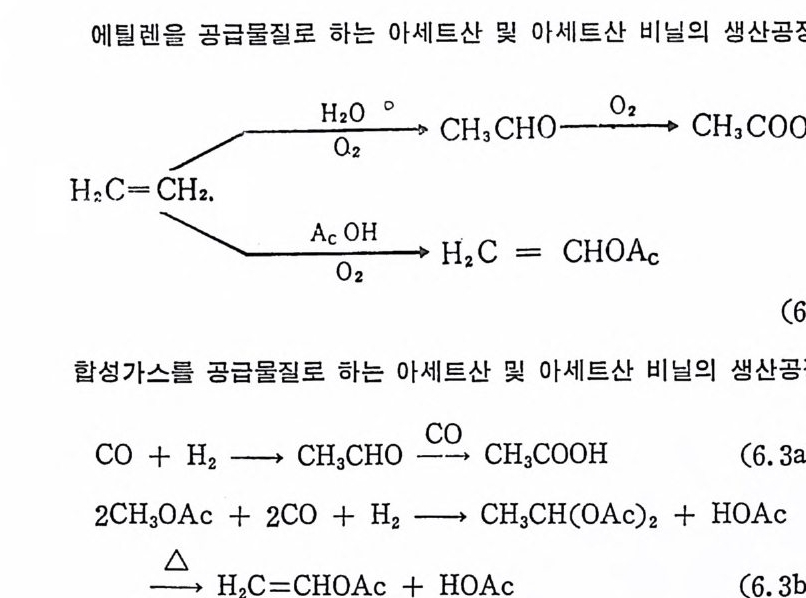 에틸렌을 공급물질로 하는 아세트산 및 아세트산 비닐의 생산공정
에틸렌을 공급물질로 하는 아세트산 및 아세트산 비닐의 생산공정
공업적으로 생산되는 아세트산과 아세트산 비닐 (v i n y l ace t a t e) 의 역사를 보면 위에서 소개한 4 시대 중에서 처음 3 시대(1 910 년부터 2000 년까지)는 비교적 잘 표현된 것으로생각된다(식 (6.1 ),( 6.2), 및 (6.3) 참조). 1930 년부터 1960 년까지 아세트산과 아세트산 비널의 생산은 주로 아세탈렌의 C 三 C 결합에 물 또는 아세트산을 각각 첨 가시키는 반응을 응용한 것이다. 아세트산과 아제트산 비닐의 생산 공정에는 가용성 금속촉매가 사용된다. 또한 아세트알데히드를 아 세트산으로 산화시키는과정에도가용성 금속촉매가 사용된다. 1966 년에 공업화된 Wacker 공정은 아세트알데히드 합성에 에틸렌울 기 본물질로 사용하는 과정이다. Wacker 공정이 경제적인 면에서 성공 울 거두자 이어서 비슷한 화학공정이 개발되었다. 죽 가용성 촉매 또는 불군일촉매에 의한 에 틸렌의 아제독실화반응 (ace t ox y la ti on) 이 개발되었다. 아세트산 비닐의 공업적 생산에 이용되는 촉매는 아래 에 소개 될 소위 혼성 촉매 (hy b rid ca t al y s t)계 (용액 에 서 일 어 나는 형 태 의 화학반응이 고체표면에서 일어나게 하는 촉매)의 예라고 볼 수 있다. 합성가스를 초기물질로 하는 메탄올의 생산은 매우 효율적인 불-
군일촉매공정에 의한다. 이렇게 해서 생성된 메탄올은 다시 CO 와 반응하여 아세트산을 생산하게 된다(식 (6.3a) 참조). 미국의 BASF 와 Monsanto 회사에 서 개 발한 공정 에 는 가용성 금속착물 촉매 를 사 용한다. 그러 나 혼성 촉매 를 사용하여 이 상의 반응(식 (6. 3a) )을 일 으킬 수 있을 가능성이 보여졌으며 혼성촉매는 공업적 공정에 장접 이 있을 것으로 생각하게 되었다. 이러한 경제적인 이접과 합성가 스를 사용할 수 있는 공급물질의 융통성은 군일촉매반응에 밝은 장 래를 예측하기도 한다. 최근의 특허에 의하면 합성가스는 아세트산 비닐의 생산에도 초 기물질로 사용된다 .1) 메탄올과 아세트산으로부터 얻어지는 아세트 산 메탈은· 합성가스와 반응하여(가용성 로듐착물 또는 팔라듐착물 촉매 에 의 해 서 ) 1, 1' -디 아세 목시 에 탄(1, 1-d i ace t oxy e t ane) 으로 된다 (식 (6.3b) 참조). 디아제목시에탄이 열분해되어 아세트산 비닐로되 는 과정은 아세트산 이의에 어떤 부산물도 없는 반응으로 매우 찰 알려진 과정이다(식 (6.3b) 참조). 이 아세트산 비닐의 생성과정은 아직 공업적으로 응용되지 않고 있지만, 합성가스를 기본물질로 하 는 아세트산 생산공정과 같이 경제적으로 상당한 이접을 가지고 있 울 것으로 추측되고 있다. 위의 석 (6.1)~(6.3) 에서 보여 주지는 않았지만 포화 탄화수소 (알칸)와 생물학적 물질들도 또한 관십을 끄는 미래의 공급물질이 다. 현재에도 그렇지만 가까운 장래에도 알칸은 올레판보다는 저령 할 것이며 경제적인 면에서도 합성가스와 경쟁할 수 있을 것이다. 부탄 또는 나프타 (na pt ha) 의 산화반응으로부터 얻는 아세트산의 생 산공정은 그 수율이 낮음에도 불구하고 1950 년초에 소개된 후 관 심의 대상이 되고 있다. 연료로 쓰이는 것 이의에 알칸의 용도는 벌 로 없었다. 가벼운 알칸도 이제는 및몇 중요한 공업생산 공정의 공 급물질로 고려되어야 할 것이다. 자유라디칼에 의한 연쇄산화반응 외에는 알칸의 반응에 응용되는 군일촉매계는 별로 없다. 그러나 알칸의 C 一 H 결합이나 C-C 결합의 활성화에 관한 기초적인 지식 온 이미 많이 연구 보고되고 있다 .2)
1) N. Riz k alla and C. N. W inn ic k , Ger. Of fenl eg . 2, 610, 035 (l':l76 ).
2) a) G. W. Parshall, Cata l ys i s , 1, 335 (1'577 ). b) D. E. Webste r , Adv. Orga nomet. Chem. . 15, 147 (1'577 ). c) A. E. Shil ov and .A. A. Shte i n m an, Coard. Ch11m. Rev. , 24, '57 (19 77).
발효 또는 기타효소과정 은 상당 한 양의 아 세트 산 율 생성한다. 식 품으로 사용되는 식초는 현재 고두 생 물 학적 과정 을 통 하여 생산된 다. 그러나 1950 년까지는 식초는 곡 식으로부터 얻는 알코 올을 군일 촉매 를 사용하여 산화시켜 얻은 소위 합성 아제트산이었다. 현재는 곡식으로부터 얻어지는 알 콜 이나 에탈렌우로부터 얻는 알코 올 이나 모두 비 슷한 가격 이 다. 앞으로 몇 년 후에 는 생 물 학적 물질 (bio m ass) 로부터 얻는 에탄올이 아세트산의 중요한공급물질이 될 가능성이 있 다. 옥수수 대 나 사탕수수 대 로부터 얻 어 지 는 푸르푸르알(fu r fu ra l) 도 상당히 중요한 공급물질이 될 것 같다. 석유가 유기화합물 생산 에 중요한 기본물질로 사용되기 전에는 푸르푸르알이 테트라히드로 푸란 (tet r a hy d rofu r an) 및 1, 6 - 헥 사디 아민 (1, 6-hexad i am i ne) 의 생 산에 기본물질이었다. 1950 년 이전의 공급물질 체제로 돌아간다면 군일 촉매작용의 응용은 한충 활발해질 것이다. 2. 선택 성 의 향상 (enhanced selecti vi t y) 균일촉매작용의 가장 큰 장접은 복잡한 유기화학 반응에서 나타 나 선택성어다. 예를 들면 부타디엔의 이중결합에 두 몰의 HCN 을 입 체 선택 적 (re gi oselec ti ve) 으로 첨 가시 켜 아디 포니 트릴 (adip o nit ril e ) 을 합성하는 과정이다(식 (6.4) 참조). 두 몰의 HCN 이 첨가되는 각 단계에서 CN7] 의 치환이 안쪽으로 일어나느냐 또는 바깥쪽(t er m i nal) 으로 일어 나느냐에 따라 활성 화에 너 지 의 차이 는 적 다. 그러 나 · 균일촉매작용을 일으킬 수 있는 조건(낮은 온도)에서는 높은 선덱 성을 보이면서 아디포니트릴을 생성시킨다.
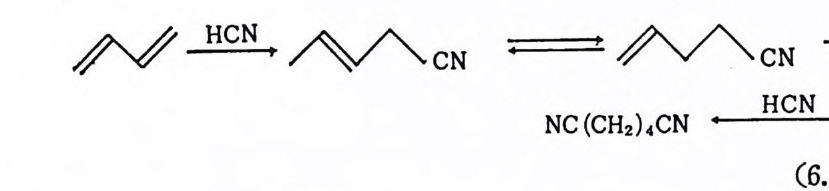 H'~~ CN =NC(~CH2)4cCN N二
H'~~ CN =NC(~CH2)4cCN N二
이러 한 높 은 선택성 은 제 약 공 업 에서 특 히 유 용 하게 응용 원 것 이 다. 왜냐하면 많은 경우예 복잡한 물 질의 어느 한 목 수한 이 성 질 체 에게만 생 물 학적 활 성이 최대로 나타나기 때문이다. 예를 들면 3,4- 디히드록시페닐알라닌의 l - 이성 질 체는 P a rk i nson 씨 병의 치료에 활 성이 있다. 이 광학적 이성질체는 키랄 리간드 를 배위하고 있는 가용성 로듐착 물 촉 매 를 사용하여, 키랄 성을 가 질 수 있는 올레 핀 율 선택 적 으로 수소화시켜 만들어진다 .3) 올레핀의 수소화반응은 비 대칭성 ( a s y mme t r i c) 합성의 방법오로 많이 연구되고 있으나 많 은 다 른 군일 촉 매반응 과정도또한 분자내의 비대 칭 성을 가져온다( 식 (6 . 5) ~(6. 8 ) 참조 ). 4) ~8) 제약공업의 목성은 제품이 고가이며 소량이라는 접이다. 따라서 반응이 빠르게 그리고 쉽게 전행만 된다면 고가인 촉매와 고가인 시약둥이 사용된다 하더라도 개발할 가치가 있다. 그 좋은 예가하 나 있다. 즉 에 덴일 알콜 (e t hen y l alcohol ) 로부터 알파, 베타一불포화 알데히드를 얻는'아래 식 (6.9) 와 같은 선택적인 이성질화반응은 바 나듐산 실 릴 (sil yl vanadate ) 촉매 에 의 해 서 전행 된다. 9) 스테 로이 드의 합성에도 많은 상기와 같은 응용이 있을 것으로 예측된다. 유기~ 학자들이 가용성 금속착물을 시약 또는 촉매로 사용하게 될 때가 되면 그 응용도는 급속도로 늘어날 것이다. 유기금속촉매의 높은 선덱성을 응용하는 이접은 반드시 소량의 고가 제품에만 한정시킬 필요는 없다. 폴리울레핀(p ol y ole fi n) 분야 의 화학은 대 량생 산에 도 입 체 선덱 성 (s t ereoselec ti v ity)의 효과를 이 용-
3) Chem. Week. , 71 (Nov. 20, 1974) ; Ind. Res. , 23 (Oct. 1974). 4) J. Solodar, Chem. Tech. , 421 (19 75). 5) I. Oji ma , K. Yamamoto and M. Kumada, Asp ec ts . Homo. Cata ! . , 3, 186 (19 77). 6) G. Consig li o, P. Pin o , et al. , Ang e w. Chem. Int. Ed. , 12, 669 (1973); H elv. Chim . Acta , 59, 642 (19 76). 7) A. Nakamura, A. Konis h i, Y. Tats u no and S. Ots u ka, ]. Am. Cheni. Soc. , 100, 344 3 , 3449, 6544 0978). 8) K. B. Sharpl e ss, et al. , ]. Am. Chem. Soc. , 99, 1990 0977); S. Yamada, et al. , ]. Am. Chem. Soc. , 99, 1988 (19 77). 9) H. Paulin g , D. A. Andrews and N. C. Hind ley, Helv. Ch im . Acta , 59, 12 33 (19 76).
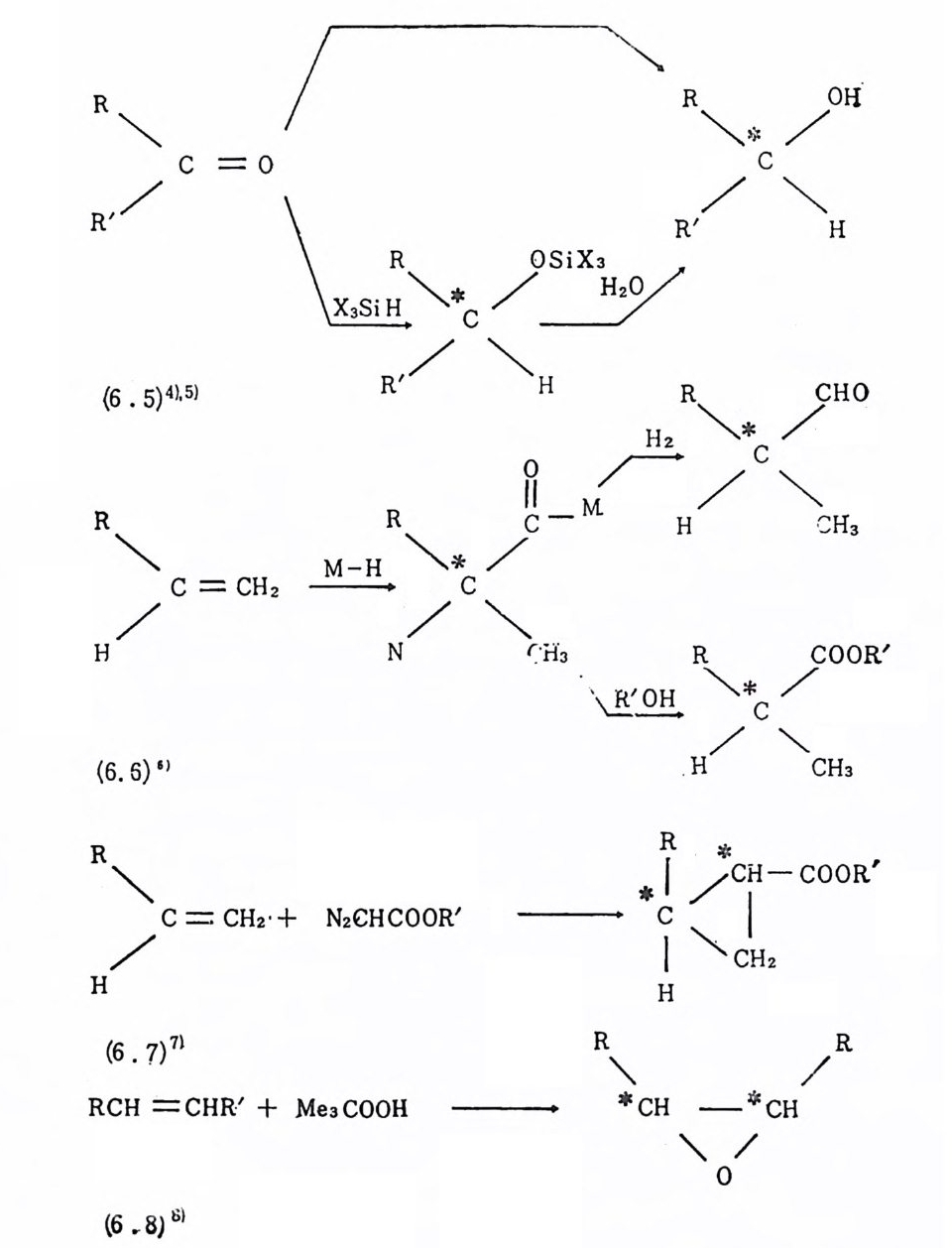 RRI/ 二\ *C 尸 :R'>R / O\H H
RRI/ 二\ *C 尸 :R'>R / O\H H
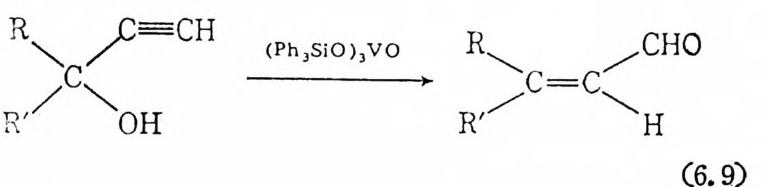 RRI /\ C\/ O 루H CH (Ph,S iO ),VO RR' \, ;c=C/ ~ CHH O
RRI /\ C\/ O 루H CH (Ph,S iO ),VO RR' \, ;c=C/ ~ CHH O
하였다. 죽중합체 내에 있는 수백 개의 비대칭성 중십이 일정한 방 향으로 질서정연하게 배열된 풀리푸로팔렌(i so t ac ti c pol yp ro p yle ne) 제 폼이 만들어지고 있다. 이러한 중합체의 성질은 질서없이 배열된 풀 리 푸로필렌 (ata c ti c p o y l pr. o py lene) 의 성 질과 상당한 차이 를 보여 준다. 비슷한 예로 현재 상품으로 생산되는 시스 -1,4 - 풀리부타디엔은 어 떤 한 득수한 이성질체를 생성하는 데 대단히 높은 선덱성을 보이 고 있는 것이 있다. 입 체선택적 중합반응의 응용 중에서 괄목할 만한 것은 중합반응이 일어나고 있는 동안에 촉매를변화시킴으로써 볼록혼성중합체 (block · co p ol ym er) 를 합성 하는 것 이 다. 시 스 - 1, 4 와 트란스 -1, 4 단위를 포함 하는 볼록 (block) 을 갖고 있는 혼성 중합체 가 이 런 방법 으로 합성 되 었다. 위와 같은 불록중합체를 만들기 위해서 다음과 같은 방법 을 사용한다. 용액 중에 반응성 이 커 다란 유기 금속의 말단기 (end g rou p)가 존재하는 동안에, 죽 아직 중합체가 성장하고 있는 동안 에, 반응조건을 변화시킵으로써 볼록중합체를 합성할 수 있다. 이 러한 방법을 사용하여, 죽 살아 있는 중합체를 조절하는 방법으로, 서로 매우 다른 블록(또는 볼록의 반)들을 갖는 중합체도 생산될 수 있다. 예를 들면 락톤이나 에폭시화 화합물을 성장하고 있는 풀 리부타디엔의 고리에 가하면 최종적으로 얻어지는 중합체는 폴리락 돈이나 폴리에테르의 부분을 갖게 된다. 이렇게 만들어지는 혼성중 합체 는 각 블록이 각각 다른 극성 (p olar ity)을 나타내 기 때 문에 다음 과 같은 유용한 접이 있다. 찰 섞이지 않는 영화풀리비닐과 풀리 스티렌 등을 위에서 설명한 것과 같은 볼록 혼성중합체와 섞어서 갈아 주면 비교적 군일한 조성을 갖는 물질을 얻을 수 있다.
3. 혼성 촉매 (hy b rid cata l ys t ) 많은 경우에 선택성 때문에 흔히 쓰여지는 불균일촉매보다는 가 용성 전이금속 착물 촉매가 사용된다. 그러나 또한 군일촉매는 단 접도 가지고 있다. 공업적 응용에서 가장 큰 단접은 반응이 끝난 후 에 반응혼합물로부터 촉매를 분리하기가 어려운 접이다 .10) 휘발성 이 있는 아세트알데히드 (b. p. 21°C) 와 같은 물질의 분리는 간단히 중류함으로써 가능하다. 그러 나 아디 포니 트탈 (b. p. 295°C) 와 같은 끓는 점이 높은 물 질의 분리는 쉽지 않다. 왜냐하면 쓰여지는 히드 로시안화 반응의 촉매가 고온에서 쉽게 열분해되기 때문이다. 이러한 문제를 해결하는 한 방법으로 가용성 촉매를 불용성 촉 매 받침 (cata l ys t su pp or t)에 십 는 것 이 다. 이 렇 게 만든 혼성 촉매 는 군일 촉매의 이점과 불군일촉매의 이접을 갖게 되므로 현재 이 연구분야 는 많은 연구자들의 관십의 대상이 되고 있다. 이러한 원리가 오래 전부터 응용되어 오고 있는 공정도 있다. 가장 오래된 것 중의 하 나가 S02 를 02 로 산화시키는 촉매적 산화반응에서 S02 와 S02 의 혼합물을 혼성촉매위를 통과시키는 공정이다. 이때 촉매계는 용융 된 알카리 금속의 황산염 에 녹인 바나듐산 영 (eute c ti c sal t)을 실리 카 (산화 알루미늄) 받침에 올란 것이다 .11) 따라서 촉매는 용액 중에 있 지만 반응물이나 생성물과는 다론 상(p hase) 으로 존재한다. 비슷한 경우로 에틸렌, 산소 CO2) 및 아세트산으로부터 아세트산 비닐울 합 성하는 공정을 들 수 있다. 이 경우에 촉매계는 아세트산 칼품과 실리카 받침에 유란 팔라듐-금의 합금이다. 이상의 촉매계에 의한 촉매반응은 촉매의 표면에 있는 아세트산의 얇은 막에서 일어나는 것으로 추측된다. 이와 같이 고체 받침 위에서 군일촉매반응을 일으 키는 방법은 상당한 응용성을 가지고 있다 .12) 이상의 혼성촉매계에
10) ij) G. W. Parshall, J. Am. Chem. Soc. , 94, 8716 (19 72). b) P. R. Rony , Ann. N. Y. Acad. Sc i. , 172, 238 (19 70). U) H.F.A. Top so e and A. Neil so n, Trans. Dan i sl』 Acad. Tech. Sci, , 3, 18 (19 48). 12) a) P. R. Rony and J. F. Roth , ] . Mo/. Cata / ,. 1, 13 (l:i75 ). b) U. S, Pate n t, 3, 855, 307 (19 74).
의한 공정의 문제점은 반응물이나 생성 문 이 반응온도에서 휘발성이 있어야 한다는 접이다. 이상의 방법보다 더욱 일반적인 방법은 고체받침과 전이금속착물 간의 화학결합을 동하여 불균일촉매를 합성하는 방법이다. 현재까 지 가장 연구가 찰 된 것은 실리카 또는 알루마나(산화 알루미늄) 와 같은 금속산화물을 받침 으로 하여 포스핀기 를 갖고 있는 중합체 률 이 용하는 것 이 다. 13) 석 (6. 10 ) 과 (6. 11 ) 은 화학반응을 이 용하여 가용성 금속착물을 불용성 받침 에 붙이 는 과정 을 보여 준다. 석 (6.10) 은 금속산화물 받침 에 크롬착물을 반응시 키 는 미 국 Unio n Carb i de 회사에서 개발한 풀리푸로팔렌 생산의 촉매를 만드는 과정 이다. 크롬오센 (Cr(C5H 야)은 실리카 표면의 히드록시기와 반응한 다. 최초의 반응단계는 크롬에 배위된 시클로 펜타디엔일기에 양성 자첨 가분해 반응(p ro t onol y s i s) 이 일어 나 C5H6 가 떨어 져 나가는 과정 이다 .1 4 ) 이어서 또 하나의 히드록시기가 산화성첨가반응을 일으켜 금속-수소 결합을 형성한다 .15) 일단 Cr-H 의 결합이 생성되면 중 합체의 고리가 성장할 수 있게 된다. 죽 단위체 올랜편이 계속적으 로 삽입되어 중합체의 탄소고리가 길어진다. 실제로 이상의 촉매계 는 상당히 효율적이어서 반응이 끝날 때쯤에는 촉매의 찌꺼기가 중 합체 내에 남아 있어도 문제가 없을 정도이다. 많은 가용성 촉매를 포스핀을 포함하고 있는 폴리스티렌과 반웅 시켜 혼성촉매를 합성하는 방법은(식 (6.11) 참조) 주로 대학의 연구 실에서 연구되고 있다. 몇 개의 포스핀을 포함하고 있는 중합체 분 자들은 폴리스티렌의 치환반응울 동하여 얻어지기도 하고, 또는 p-디 페 닐포스핀오스티 렌 (p- dip h eny lp h osp h in o sty re ne) 과 스티 렌의 혼 성 중합반응 (co p ol y me ri za ti on) 으로부터 얻 어 진다. 이 러 한 포스핀을 포 함하는 중합체는 전자주게 리간드로 촉매금속에 배위된다(식 (6.11) 참조).식 (6.11) 에서 보면 Wi lki n s on 촉매 RhCI (P Ph3)3(Ph=C6Hs) 에
13) a) F. R. Hartl y and P. N. Vezey, Adv. Orga nomet. Gli em . , 15, 189 (19 77). b) Y. Chauvin , D. Commereuc and F. Dawans, Prog . Poly. Sc i. , 5(3~ 4), 95 (19 77). 14) M. H. Chis h olm, F. A. Cott en , M. W. Exti ne and D. C. Rid e out, Inorg. Chem. , 18, 120 (19 79). 15) D. T. Laverty , J. J. Rooney and A. Ste w art, ]. Cata / . , 45, 110 (19 76).
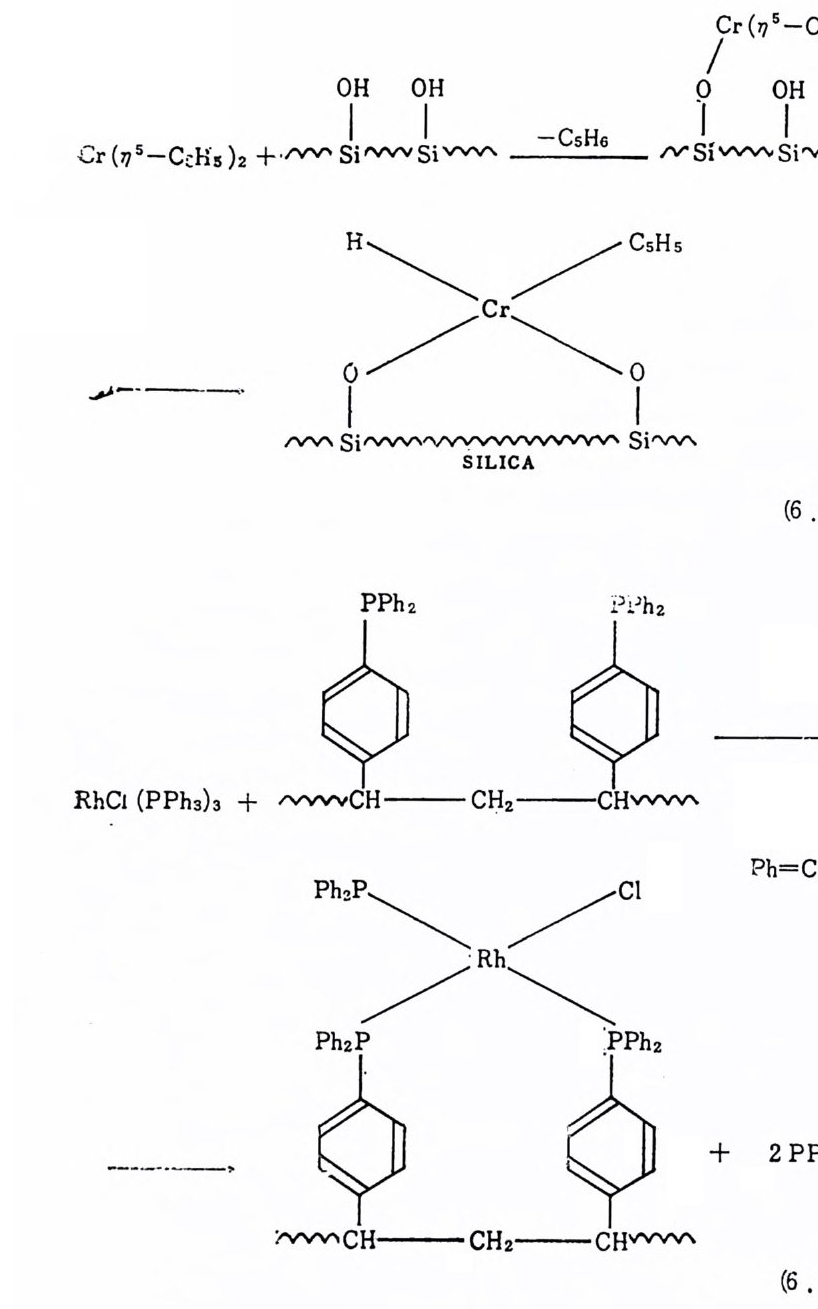 IC r (7/5 -CsH5)
IC r (7/5 -CsH5)
배위되어 있는 세 개의 트리페닐포스판 중에서 두개는 중합체의 포 스핀기에 의해서 치환된다. 치환된 두 개의 트리페널포스핀을 반응 용액으로부터 제거하면 로듐착물은 단단하게 중합체에 결합된 상태 가된다. 이렇게 얻은로듐―풀리스티렌촉매는올레핀의 히드로포르 밀화반응 및 올레팬의 수소화반응에 촉매져 활성을 보여 준다. 이러 한 종류의 촉매는 아직 공업적으로 쓰여지지 않고 있지만 앞으로 공업 에 응용될 가능성 온 크다. 식 (6.10) 과 (6.11) 에서 보여 주는 두 촉매는 혼히 쓰여지는 불군 일촉매의 장점. 및 단접을 모두 가지고 있다. 장접으로는 반응생성 물과 촉매를 쉽게 분리할 수 있다는 접이다. 고체촉매가 들어 있는 관에 반응물을 동과시키는 방법으로 촉매반응을 일으키는 경우에 촉매와 반응물-생성물을 분리시키는 것은 큰 문제는 아니다. 그러 나 포스핀을 포함하는 중합체와 결합시칸 로듐착물 촉매(식 (6.11) 참 조)를 사용하는 경우에 촉매를 오래 사용하면 로듐이 촉매관으로부 터 서서히 녹아 나오는 것이 발견되었다 .16) 불용성 고체촉매(혼성 촉매)를 액체상태의 반응물과 섞어서 얻어지는 혼합물 그대로 반응 시킬 수도 있다. 이턴 경우에는 반응이 끝난 후에 촉매는 여과하여 쉽게 분리된다. 이런 방법은 발열이 십한 반응에 좋다. 왜냐하면 일정한 용기 (예를 들면 촉매가 들어 있는 관 (column) )에 촉매를 넣 어 두면 열율 제거하기가 힘들기 때문이다. 혼히 쓰여지는 불균일촉매를 사용하는 경우에 반응물과 생성물이 고체촉매 입자에 확산되어 들어가는 과정이 속도결정단계가 되기도 한다. 그러나 중합체와 결합한 촉매(예 식 (6.10) 및 (6.11) )가 유 기용매에서 사용되는 경우에 문제는 간단하지 않다. 죽 만일 중합 체내의 교차결합 (cross li nka g e) 정도가 매우 높지만 않다면 유기용매 는 중합체의 격자(l a tti ce) 사이에 확산되어 들어갈 수 있으므로 상당 한 부풀음 (swe lli n g)이 일어난다. 이 부풀음은 반응물과 생성물이 촉 매에 확산되는 것울 증가시키기 위해서는 바람칙한 것이다. 그러 나 이 부풀음은 촉매입자를 파괴할 가능성이 있으므로 조철될 수
16) W.H. Lang , A.T. Jur ewi cz , W.O. Haag, D.D. Whit eh urst and D.L. Rollman, J. Orga nomet. Chem. , 134, 85 (19 77).
있어야 한다. 금속산화물을 받침 (su pp or t) 물질로 하는 경우에 부풀음은 일어나 지 않으며 , 반응물의 확산은 받침 물질의 구멍 구조(p ore s t ruc t ure) 를 통하여 일어난다. 이러한 이유 대문에 전부터 사용되어 온 불군일 촉매에 사용 가능한 실리카와 알루미나 둥의 공업적 응용이 관십의 대상이 되었다. W il k i nson 착물과 같은 촉매도 금속산화물에 결합 시킬 수 있다. 죽 실리카를 먼처 (Et 0) 3SiC H 2CH2PPh2(Et = C2Hs, Ph=C 晶)와 같온 실리 콘 화합과 반응시 킨 후 Wi lkn is o n 착물과 걷 합시 켜 혼성 촉매 가 만들어 진다. 11> (Et 0) 3SiC H 2CH2PPh2 중의 Si 끝 이 실리카에 결합되어 Si— 0-Si 결합을 만들고 포스핀기는 전이금 속에 배위되도록 준비가 된다. 혼성촉매의 공업화는 비록 느리지만 앞으로 실제적으로 많은 공 정에 응용될 것으로 예측된다. 풀리에틸렌 생성촉매반응의 경우에 서 사용하는 방법과 같이, 혼성촉매는 반응초기에 사용될 수 있을 것 같다. 왜냐하면 혼성촉매는 공업적인 면에서 장접이 많은 점도 있지만 경우에 따라서는 특벌한 성질(예를 들면 입체선택성 등 ) 을 보여 주기 때문이다. 혼성촉매를 연구함으로써 얻을 수 있는 또하나 의 수확은 유기금속 화학자들이 불균일촉매에 관하여 더욱 많은 지 식을 얻을 수 있다는 점이다. 4. 새로운 촉매화학 군일촉매작용에서 또 하나의 경향은 새로운 촉매 개념을 적용하 여 촉매져 활성이 더욱 큰 촉매들을 디자인, 개발하는 것이다. 특 히 다음의 두 방법이 독기할 만하다. 첫째는 빛의 쬐임을 이용하여 촉매 를 활성 화시 키 는 광활성 촉매 겨] (ph oto a cti va te d ca t al y s t)이 다. 이 광활성촉매계는 종전의 군일촉매계보다는 낮은 온도에서 반응을 일 으킬 수 있는 장접이 있다. 둘째로는 알칸의 이성질화반응 또는 가
17) a) K. G. Allum, R.D. Hancock, I.V . Howell, T.E. Leste r , S.M. Mc- kenzie , R. C. Pit ke th y l and P. J. Robin s on, J. Orga nomet. Chem. 107, 393 (19 76). b) A. A. Oswald and L. L. Murrell, U. S. Pate n t, 4, 083, 803(1 9 78).
수소분해 반응 (h y dro g enol y s i s) 과 같은 특 히 어 려 운 변환(tr ans fo rma t i o n) 에 필요한 다중 반응자리 (multip le reacti on s it es) 를 갖고 있는 금속뭉 치 화합물 (clus t er) 촉매 계 이 다. 1) 광활성 촉매 (Photo acti va te d cata lys t) 많은 경우에 균일촉매반응의 속도결정 단계는 금속이온으로부터 리간드가 해리되는 단계이다. 리간드 해리단계는 금속 주위에 비어 있는 배위자리를 만들어, 예를 들면 올레판과 같은 반응물과, 반응 할 수 있게 하기 위해서 팔요하다. Cr(C0)6 를 촉매로 사용하는 수 소화반응에서 보는 것처럽 경우에 따라서는 리간드의 해리속도를 적당한 정도로 만들기 위해서는 온도를 100°c 이상으로 울릴 필요 가 있다. co 리간드를 해리하는 데 필요한 에너지는 빛 에너지로부 터 공급받을 수 있다. 따라서 Cr(C0)6 는 300~380nm 의 빛 쬐임 을 받은 다음에 10°c 에서도 디엔 (d i ene) 의 수소화 반응을 일으킨 다 .18) 이렇게 하여 낮은 온도에서도 수소화반응이 일어나게 되면 더엔의 수소화반응의 선태성은 열적으로 활성화된 촉매반응의 선덱 성보다 더 높다. 빛의 쬐임에 의해서 활성화된 Cr(C0)6 의 촉매적 활성온 어둠 속에서도 및 시간 지속된다. 광활성 촉매에 의한 반응 중에서는 선덱적 수소화반응이 가장 활 발히 연구된 분야이다. 이의에도 몇몇 촉매반응이 광활성 촉매에 의해서 가능할 것으로 생각된다. 예를 들면 히드로실릴화반응 (h y dros i l y la ti on) 은 Fe(C0)5 용액 에 빛 을 쬐 어 줍으로써 일으킬 수 있 다 .19) 금속으로부터 CO 의 해리는 비교적 쉽기 때문에 지금까지 연구된 대부분의 광활성 촉매반응은 금속-카르보닐 착물을 이용하 는 반응이다. 그러나 파아―결합을하는리간드들은 일반적으로 CO 와 비슷하게 빛에 의해서 해리가 가능할 것으로 추측된다. 2) 금속 뭉치 화합물 촉매 (meta l cluste r cata l ys t) 예를 들면 알칸의 이성질화반응 또는 N2 의 수소화반응 둥과 같 은 많은 여러 단계 반응들이 불군일촉매에 의해서는 쉽게 일어나지
18) M. S. Wi rg h to n and M. A. Schroeder. J. Am. Chem. Soc. , 95, 5764 (19 73). 19) M. S. Wrig h to n , D. S. Gin l ey, M. A. Schroeder and D. L. Morse, Pure Ap pl. Chem. , 41, 671 (19 75).
만 군일촉매에 의해서는 쉽게 일어나지 않는다. 이상의 반응과 같은 복잡한 변환(t rans fo rma ti on) 을 가져 오는 반응에 는 촉매 자리 (cata l ys t s it e) 가 여러 개 필요하기 때문이타고설명된다. 고체금속표면은 여러 개의 촉매자리를 제공할 수 있지만, 종전의 가용성 촉매는 오직 하 나의 금속이온을 가지고있을 뿐이다. 그러나뭉치화합물 Rhs(C0)1s 는 몇 개 의 반응자리 (reacti on s it e) 를 제 공할 수도 있으며 , 또한 여 러 개 의 전자를 필요로 하는 산화-환원 (multie le ctr o n redox) 에 전자를 공급(또는 소비)할 수도 있을 것이다. 금속一금속 결합을 갖고 있는 다핵착물(p ol y nuclear com p lex) 은 올 레편과 일산화탄소의 반응에 촉매로 활발히 연구되어 왔다 .20) 예를 들면 Rua(C0)12, H4RU4(C0)12 또는 由 aRu i C0)12 『 둥에 의 한 1- 펜 텐의 히 드로포르밀화반응은 n- 핵 산운을 높은 수율로 생 성 시 킨다. 21 ) 이상의 루테늄착물들은 또한 수성가스이동반응 (wa t er gas shif t reac- tion ) (CO + H20 一 CO2 + H2) 에 도 촉매 적 활성 을 보여 준다. 많은 경우에 촉매반응이 일어나는 동안에 뭉치화합물은 그 원래 의 구조를 그대로 유지하고 있는지 알기 어렵다. 몇몇 경우에서는 뭉치화합물이 그들 원래의 구조를 유지하는 것 같다고 보고되고 있 지만 명백한 증거는 없다. 대부분의 경우에 실제로 촉매적 활성을 보이 는 것 은 탄핵 (mononuclear) 착물이 며 그 단핵 착물의 농도는 매 우 낮아서 겁출하기가 힘들 수도 있다. Rua(C0)12 와 Rua(C0)9(PPh3)(Ph=C6H5) 의 광활성화에 의해서 얻어지는 촉매는 최소한 부분적으로 뭉치화합물의 구조를 유지하~근 것 같다 .22) 이상의 루테늄 삼합체(tri mer) 들은 가시광선에 의해서 활성화되어 실온에서 l- 펜렌을 시스 및 트란스 -2-펜 맨으로 전환시 키는 이성질화 반응에 촉매적 역할은 한다. 반응초기에 얻어지는 생성물의 조성 그리고 활성화에너지가 낮다는 접 둥을 고려하면, 이상의 세 루테늄 뭉치화합물의 광활성으로부터 얻어지는 실제 촉·
20) a) E. L. Muett er tie s , Scie n ce, 196, 839 (1977). b) C. U. Pit tm an, and R. C. Ry a n, Chem. Tech. , B, 170 (1'578 ). 21) R.M. Lain e , J. Am. Chem. Soc,, 100, 6451 (19 78). 222)7 3J . (1L'5. 79G ) r. aff , R. D. Sanner and M, S. Wrig h to n , J. Am. Chem. Soc. , IOI~
매는 Ru(CO) i PPh3) 으로부터 얻어지는 실제 촉매와 다른 것 같 다. 광활성 과정은 특히 뭉치화합물을 이용하는 촉매반응에 상당히 효과가 있는 것으로 믿어지고 있다. 뭉치화합물의 리간드 해리반응으로부터 얻어지는 단핵 (mononuc lear) 촉매는 알칸의 분열반응(fr a g mena ti on reac ti on) 에 활성이 없는 것으로 나타난다. 펜탄 메트릭스에서 니첼중기를 응축시켜서 얻은 비교적 작은 니캘 뭉치화합물은 펜탄의 C_H 결합과 C ― C 결합을 끊고, 새로운 C ― C 결합을 형성시킨다 .23) 이 반응은 매우 낮은 온 도 (-130°C) 에서도 일어난다. 비슷한 예로 철울 증발시켜 얻은 Fe2 뭉치화합물은 -250°C 에서 메탄 메트릭스중의 C ― H 결합을 공격한 다 .24) 이 작은 철 뭉치화합물은 금속표면에서 볼 수 있는 것과 같 은 촉매활성을 보여 준다. 금속 뭉치화합물 촉매 자체에 관하여서는 많은 접둘이(정확한 구 조, 분자석 등등) 찰 알려져 있지 않지만, 이들 화합물의 촉매적 활성은 활발히 연구되고 있다. 뭉치화합물을 초기물질로 하여 새로 운 촉매활성도를 갖는 촉매계를 개발하는 분야는 상당한 가능성을 가지고 있다. 뭉치화합물울 고체표면에 붙임으로써 우수한 선덱성 울 갖는 불군일촉매를 얻을 수도 있을 것이다 .25)
23) S. C. Davis and K. J. Klabunde, ]. Am. Chem. Soc. , 100, 5973 (1978). 24) P. H. Barrett , M. Paste r nak and R. G. Pearson, ]. Am. Chem. Soc. , 101. 252)2 2J . M(1.9 7B9)a.s sett and R. Ug o, Aspe c ts Homo. Cata / , , 3 混7 (19 77).
*찾아보기 거 가수소분해 만옹 (h y drog enol y s i s) 3 : 2(2), 6 : 3 가 알코운분해 반응 (alcoho! y s:s) 4 : 2(2) 1) 가지 탈란 알데 히 드 (branched aldehy d e) 3 : 2(3) 강한 장 (s t ron g fiel d) 2 : 2 격 자(格子)(l a tti ce) 6 : 3 결 합차수 (bond order) 1 : 3 고리 스트레 인 (rin g str a in ) 2 : 4(1) 고리 열 림 중합반웅 (r i ng -o p ~n i n g pol ym eriz a ti on ) 2 : 6 공간배 열 (Confi gu rati on ) 3 : 2(5) 공급물질 (fee dsto c k) 6 : 1 공생 박태 리 아 (s y: mb i o ti c bacte r ia ) 4 : 1(1) 광증강제 (ph oto s ensit ize r) 5 : 3 광학적 수울(q uan t um yiel d) 2 : 2(3), 3 : 2(5) 광활성 (ph oto a cti vi t y) 5 : 1 광합성 미 생 물(p ho t os yn t he ti c mi cr oorga n is m ) 4 : 1(1) 광활성 촉매 (ph oto a cti va te d cata l ys t) 6 : 3 교차결 합 (cross link age ) 6 : 3 구멍 구조(p ore str u ctu re) 6 : 3 군일촉매 반응 (homo g eneous cata l ys i s ) 5 : 1 균형 분리 (homo!yt ic spl i tt ing ) 2 : 2(1) 균형 분열 (homol yti c cleavage ) 5 : 1(3) 금속고리 (meta l locy c le) 2 : 6(4) 1) 금속-니 트렌 (me t al-n it rene) 5 : 1(3) 금속-수소아실 (me t al-h y dr i doac y l) 5 : 1(4) 금소-수소화물 (me t al hy d rid e ) 2 : 2(1) 금속수소화물 경 로 (me t al hy d rid e pa th way ) 2 : 2(1) 금속아실착물 (me t al acy l comp le x) 3 : 3(2), 5 : 2 금속알킬착물 (me t al alky l comp le x) 5 : 2
금속-카르벤 메 카니 즘 (me t al-carbene mechanis m ) 2 : 6(4), 5 : 2 끝결 합 (end·on bondin g ) 1 : 3, 4 : 2(1) 끝 CO(te r mi na l CO) 5 : 1(1) L 나프타 (na pt ha) 6 : 1 낮은 스핀착물(l ow spi n comp le x) 2 : 2 E: 다리 CO(brid g ing CO) 5 : 1(1) 다양성 (div e rsit y) 5 : 1 다핵 착물(p ol y nuclear comp le x) 5 : 1(4) 단순 시 그마전자주게 리 간드 (a-donor only liga nd) 1 : 2( 1) 1) 탄핵 착물 (mononuclear comp le x) 5 : 1(4) 동위원소의 영 향(i so t o p e eff ec t) 2 : 2, 2 : 3(2) 동족체 (homolog ) 4 : 1 (4) 동종간 주고받기 반응(불균등화 반옹 )(d i s p rop or ti ona ti on) 4 : 2, 5 : 1(3),. 5 : 3 듈뜬상태 (excit ed sta t e ) 5 : 3 등전자(i soelea t ron i c) 4 : 2, 5 : 1(3) 디 엔 類 (d i enes) 3 : 2(3) 디 올레 핀 메 카니 즘 (d i ole fi n mechanis m ) 2 : 6(4) 디 히 드리 도 착물 (d i h y dr i do comp le x) 5 : 1(4) 드 Repp e 의 반옹 5 : 1(4) 리 간드의 활성 화(lig and acti va ti on ) 1 : 1 리 간드장 안정 화에 너 지 (liga nd sta b il iza ti on energy ) 1 : 2 口 Markownik o f f 법 칙 2 : 4(1) 메 탄화반옹 (me t hana ti on) 5 : 2 모노히 드리 도카르복실 착물 (monoh y drdocarbox y l comp le x) 5 : 1(4) 무산소성 박태 리 아 (anaerob i c bacte r ia ) 4 : 1(1)
뭉치 화합물 (clus t er) 5 : 1(2), 5 : 1(4), 6 : 3 M ich aeli s-M ento n 식 4 : 1(3) 닌 바 닥상태 (gro und sta t e ) 2 : 4(2) Vaska 촉매 1 : 4(3) 반대 이 온 (coun t er ion ) 1 : 1 닌fr Markownik o ff 법 칙 2 : 3(1), 2 : 4 반웅촉진제 (pro mote r ) 3 : 3(1) 발광성 (lum i ne scent) 5 : 3 배 위 결 핍 (coordin a ti on defi cien t) 1 : 1 배 위 권 (coordin a ti on sph ere) 2 : 2 배 위 적 불포화 (coord i na ti vel y unsatu rate d ) 1 : 4(3), 3 : 3(2) 배 우1 중합반응 (coord i na ti on pol ym eriz a ti on ) 1 : 4(2) 배 위 적 포화 (coord i na ti vel y satu r ate d ) 1 : 1 베 타-수소전달(또는 제 거 )반응(fi -h y dro g en tra nsfe r 또는 elim i na ti on ) 1 : 4(1), 1 : 4(2), 2 : 3(3), 2 : 4 베 타-단소제 거 반웅(fi ·carbon eli mi n a ti on ) 2 : 3(4) 베 타-포르밀에 스데 르(fi-fo rm y l este r ) 3 : 2(4) 뱃 치 법 (batc h pr ocess) 4 : 2(2) 보조촉매 (cocata l ys t) 3 : 3(1), 3 : 3(2) 부분입 체 이 성 질체 (dia s te r eois o mer) 3 : 2(5) 분열 반응(fr a g men t a ti on reacti on ) 6 : 4 분자내 첨 가반응(i n t ramolecular addit ion ) 1 : 4(3 ) 분자내 자리 바꿈(i n t ramolecular rearrang e ment) 5 : 1(1) 불군동화반웅(동종간 주고받기 반웅, disp r o p o rtio n ati on ) 4 : 2, 5 : 1(3), 5 : 3 불균일촉매 반웅 (he t ero g eneous cata l ys i s ) 5 : 1 불균형 분리 (hete r olyt ic sp litting ) 2 : 2(2) 볼록 혼성 중합체 (block cop ol ym er) 6 : 2 불활성 기 체 규칙 (ine rt ga s rule) 1 : 1 비 대 칭 성 (chir a li ty) 3 : 2(5)
비 대 칭 유발 (ass y me t r i c ind ucti on ) 3 : 2(5) 비 대 칭 촉매 (assy m etr i c cata l ys t) 2 : 4(1) 버 대 칭 합성 (assy m etr i c syn th e sis ) 2 : 4(1) 빈자리 (vacant sit e) 5 : 1(1) 빛 쬐 임 (irr adia t i on ) 4 : 2(2) 4) 人 사순전달반응 (cha i n tra nsfe r ) 2 : 4(2) 사술전파단계 (chain pro p a g a ti on ) 2 : 4(2) 사중십 과이 분자궤 도함수(fo ur cente r rr-MO) 4 : 2(1) 산소전달반응 (ox yg en tra nsfe r ) • 2 : 5(2) 산화성 첨 가반응 (ox i da ti ve addit ion ) 1 : 4(3), 3 : 2(2), 5 : 1(4} 삼중십 과정 (thr ee cente r pro cess) I : 4(3 ) 삽입 반응(i nser ti on reacti on ) 1 : 4(1), 2 : 4, 5 : 1(4) 상이 동제 (ph ase tra nsfe r ag e nt) 3 : 3(2) 상호교환반응 (me t a t hes i s) 2 : 6 상호보강작용 (s y ner gi c int e r acti on ) 1 : 3 상호이 합반웅 (co p ol y mer i za ti on) 2 : 4(1) 생 물학적 물질 (b i omass) 6 : 1 선수과정 (pr erequ i s i t e) 5 : 1(3) 선택성 (selecti vi t y) 2 : 2(3), 3 : 3(2), 5 : 1, 6 섭 광분해 (flash -ph oto l ys is ) 5 : 3 수성 가스이 동반응 (wa t er ga s shif t reacti on ) 3 : 3(2), 5 : 1(4), 6 : 3- 소중합반응 (o lig er i za ti on) I : 4(2), 2 : 4(2) 수소음이 온전달반응 (h y dr i de tra nsfe r ) 2 : 4(2) 수소주게 (hy d rog e n donor) 3 : 3(2) 수소화반응 (h y dro g ena ti on) 2 : 2, 3 : 3(2), 5 : 2 수소화효소 (h y dro g enase) 4 : 1(3) 스캐 빈저 (scaveng e r) 5 : 1(2) 시 그마전자주게 리 간드 (a-donor liga nd) 1 : 2 시 그마전자주게 겸 파이 전 자주게 리 간드 (a-donor and rr-donor liga nd} 1 : 2(1) 2)
시 그마전자주게 겸 과이 전자받게 리 간드 (a-donor and 1r-accep tor liga nd) 1 : 2(1) 3) 신전 대 사 (me t abol i s m) 4 : 1(1) 실제 촉 대 종 (ac t ual cata l yt ic spe c ie s ) 2 : 2, 2 : 6(1), 3 : 2 14- 전자 착 물(1 4-elec t ron comp le x) 1 : 1 16-18 전자규칙 (16 -1 8 electr o n rule) 1 : 1 18- 전자규칙 (18 -electr o n rule) 1 : 1 。 Arrheniu s 활성 화에 너 지 2 : 4(2) 아세 독 실화반 응 (ace t ox y la ti on) 6 : 1 아실-금속 (ac y l-me t a l) 5 : 1(4) 아실-로듐 (ac y l-rhod i um) 3 : 2(2) 아실-이 리 듐 (ac y l- i r i d i um) 3 : 2(2) 아 실 -코발트 (ac y l - cobal t) 3 : 2(2) 아실화반응 (ac y la ti on) 4 : 2(2) 4) 알자반응 (ne t reacti on ) 5 : 3 알킬-금 속 (alk y l-me t al) 2 : 3(1) 알킬이 동반응 (alk y l mi gr ati on ) 3 : 1, 3 : 3(1) , 3 : 4 알킬화반응 (alk y la ti on) 4 : 2(2) 4) 알파, 베 타-불포화카르복실산 (a, /3- unsatu rate d carbnxy lic aci d) 3 : 2(4) 알과-포르밀에 스데 르 (a- fo rm y l este r ) 양성 자첨 가받옹(p ro t ona ti on) 4 : 2(2) 3) 양성 자첨 가분해 반옹(p ro t onol y s i s) 6 : 3 양이 온성 메 카니 즘 (ca ti on i c mechanis m ) 2 : 4(2) 양자수둑울(q uan t um yiel d) 5 : 3 여 제 물질 (inh ib i t or ) 5 : 1 C2) 에 폭시 화반응 (e p ox i da ti on) 2 : 5(2) 역 결 합 (back bondin g ) 1 : 3 역 제 공 (back donati on ) 1 : 3, 3 : 1 연속적 광분해 (conti nu ous pho to l ys i s ) 5 : 3 열 화학적 분해 (the rmochemi ca l decomp os it ion ) 5 : 3
영 소화반응 (chlor i na ti on) 6 : 1 옆 결 합 (s i de-on bondin g ) 1 : 3, 4 : 2(1) 올레 편 배 우1 경 로 (ole fi n coordin a ti on pat h way ) 2 : 2(1) Wacker 공정 2 : 5(1) 원자가걷 합이 론 (valence bond the ory) 1 : 3, 3 : 1 W ilk in s on 촉매 1 : I, 2 : 2(1), 2 : 6(4) 2), 3 : 4 유발기 (ind ucti on per io d ) 2 : 5(2), 3 : 2(2), 5 : 1(2), 5 : 1(3 ) 이 산소 (d i ox yg en) 5 : 1(2) 이 성 질화반응(i somer i za ti on) 2 : 3(3 ) 이 작용기 성 (bif un cti on al) 5 : 3 이 중결 합 이 동반응 (double bond mi gra ti on ) 2 : 6(2), 3 : 2(1) 이 질 소 (d i n it ro g en) 4 이 질소금속화합물 (d i n it rog en-me t al comp ou nd) 1 : 3 이 질소의 배 위 (din i t ro g e n coordin a ti on ) 4 : 2(1) 이 질소착물 (d i n it ro g en comp le x) 4 : 1(3) 이 합반응 (d i mer i za ti on) 2 : 4(1) 이 형 대 체 (異形 態 體 )(con fo rmer) 3 : 2(5) 일분자반웅 (monomolecular reacti on ) 2 : 4(2) 1, 3- 수소이 동반웅(1, 3-hy d rog e n shif t reacti on ) 2 : 3(2) 1, 3- 영 소이 동반응(1, 3-chlorin e shif t reacti on ) 2 : 3(2) 일차결합(li near combin a ti on ) 4 : 2(1) 입 체 선 택 성 (ste r eoselecti vi t y) 6 : 2 입 체 특이 성 (ste r eospe c ificity) 2 : 2(3) x: 자유라디 칼(fr ee radic a l) 5 : 2(2) 자유롭게 사는 박테 리 아(fr ee livi n g bacte ria ) 4 : 1(1) zeis 의 영 2 : 1 자체 촉매 반옹 (au t oca t al yti c reacti on ) 5 : 1(4) 재 현성 (repr o ducib i l ity) 2 : 6(1) 전구물질 (pr ecursor) 3 : 2(2) 전도며 (conducti on band) 5 : 3
전이 상태 (tr¥ 1 s it ion s.ta te ) 2 : 4(2) 전자운반체 (electr o n carrie r ) 4 : 1(3) 전체 반응속도 (overall reacti on rate ) 3 : 2(2) 전환수(t urnov~r number) 5 : 2 정 류상태 근사법 (ste a dy sta t e app ro xim ati on ) 2 :_2 (1) 중성 질 소배 위 자 리 간드 (neu t ral nit ro g e n lig a nd) 2 : 2(2) 중합반응(p ol y mer i za ti on) 2 : 4(2) Zie g l e r 촉매 2 : 2, 2 : 4(1), 2 : 4(2) 질소고정 효소 (n it ro g enase) 4 질 소화 화합물 (n it r i des) 4 : 2(2) 1) 云: 철-단백 질 (iro n-pr o te i n ) 4 : 1(3) 청 록조류 (blue- g reen alga e) 4 : 1(1) 최 대 겹 침 (maxim um overlap ) 4 : 2( 1) 촉매 받침 (cata l ys t sup po rt) 6 : 3 촉매 순환과정 (cata l yt ic cyc le) 3 : 2(2), 3 : 3(1), 3 : 3(2) 촉매 자리 (cata l ys t sit e) 6 : 4 촉매 전구물질 (cata l ys t pre cursor) 2 : 5(2) 디 카르부닐화반응: (carbon y la ti o l).) 3 : 3 카르보 알콕시 착물 (carboalkox y comp le x) 3 : 3(2) 카르보음이 온 (carban i on) 3 : 1 키 탈 (ch i ral) 2 : 4(1) 드 탄소골격 이 성 질화반응 (carbon skeleta l iso meriz a ti on ) 2 : 3(3) 탈카르보닐화반웅 (decarbon y la ti on) 1 : 4(1), 3 : 4 테 트라카르벤착물(t e t racarbene comp le x) 2 : 6(4) 1) 끄 과이 산 (rr-a ci d) 1 : 2(2)
파이 알릴 착물 (n-all y l comp le x) 2 : 2(3 ), 2 : 3(2), 3 : 2(3 ) 파이 전자받게 (n-accep tor ) 5 : 1(1) 파이 착물 (n-com p lex) 1 : 2(2) 평 군중합도 (avera ge deg re e of po lym eriz a ti on ) 2 : 4(2) 풀리 올레 핀 (po lyo l efi n) 6 : 2 Phil lip 촉매 2 : 4(2) -Io Haber-Bosch 공정 4 하이 포니 트리 트 (h yp on it r it e) 5 : 1(3 ) 합성 가스 (s y n t hes i s ga s) 5 : 2, 6 : 1 합성 연 료 (s y n t he ti c fue l) 5 : 2 해 리 적 메 카니 즘 (d i sso ci a ti ve mechanis m ) 1 : 4(4), 3 : 2(2) hemacy an in 4 : 1(4) hemryt hr in 4 : 1(4) 형 식 산화상태 (for mal oxid a ti on sta t e ) 2 : 2 형 식 전하(fo rmal charge ) 1 : 1 호기 성 박테 리 아 (aerob i c bacte ria ) 4 : 1(1) 혼성 촉매 (hy b rid cata l ys t ) 6 : 3 혼성 화 (h y br i d i za ti on) 3 : 1 화학양론적 (sto i c h io m etr i c ) 4 : 2(2) 4), 5 : 1(4) 환원성 제 거 반응 (reduc ti ve eli mi na ti on ) 1 : 4(3 ), 3 : 2(2), 5 : 1(4) 활성 도 (ac ti v ity) 5 : 1 활성 화 (ac ti va tio n) 1 : 4(3), 5 : 1(1) 활성 화자리 (acti va ti on sit e) 2 : 2(2), 4 : 1(4) 회 합적 메 카니 즘 (asso ci a ti ve mechanis m ) 1 : 4(4), 3 : 3(2) 효소 (enz y me) 4 : 1(4) Fried el-Craft 반웅 2 : 6(1) fer redoxin 4 : 1(3), 4 : 1(4) Fis c her-Trop sc h 합성 과정 5 : 1(4), 5 : 2 흡수며 (absorpt ion band) 5 : 1(2), 5 : 1(3) 히 드로과산화규맨 (h y dro p eroxocumene) 2 : 5(2)
히 드로에 폭시 화합물 (h y droepox i des) 2 : 5(2) 히 드로카르복시 화반웅 (h y drocarbox y la ti on) 3 : 3(2) 히 드로포르밀화반웅 (h y dro fo rm y la ti on) 1 : 1, 3 : 2, 5 : 1(4) 하드록시 카르벤착물 (h y drox y carbene comp le x) 5 : 2 히 드리 도카로벤착물 (h y dr i docarbene comp le x) 2 : 6(4) 2)
陳宗植 연세대학교 화학과 및 同대학원 졸업 Clarkson College of Technolo gy에 서 M. S. , ph . D. 同대학에서 연구원(P os t Docto r ) Univ e rsit y of M i ch ig an 에 서 연구원 (Pos t Docto r ) 현재 서강대학교 화학과 교수 觸媒作用 1983 년 I2 월 5 일 인쇄 1983 년 I2 월 20 일 발행 저 자 陳 宗植 발행인 朴孟浩 발행처 民 音 社 우편번호 110 대 체 구좌 523282 서울 종로구 관철동 44 의 1 724-2000 • 724-4234 • 725-8524 출판등록 1966. 5. 19 제 1-142 호 값 2, 800 원 파본은 교환해 드립 니 다.
대우학술총서 _ 자연과학 1 소립자와게이지상호작용 김진의 2 動力學特論 이병호 3 室素固定 송승달 4 相轉移와臨界現狀 김두철 5 觸媒作用 진종식 6 뫼스바우어分光學 옥항남 7 극미량원소의 영양 승정자 8 水素化湖素와 有機湖素化合物 윤능민 9 抗生物質의 全合成 강석구 10 국소적 형태의 At iya h-Sin g e r 지표이론 지동표 11 Mucop ol ys a ccharid e s 의 生化學 및 生物理學 박l-준우 12 Astr o p hy s ic s 홍승수 13 天우원然식物 化學硏究法