
이도원 서울대학교 식물학과 졸업 동 대학원 환경조경학 석사 미국 버지니아 공과 대학 환경학 박사 조지아 대학 생태학연구소 연구원 한국외국어대학교 환경학과 조교수 역임 현재 서울대학교 환경대학원 환경계획학과 조교수 공저 『 환경 학교 』 『 환경 과학 』 역서 『 생태학 』 논문 ’‘M odell in g pho sp ho ru s _t ra n sp o r t in g ra ss buf fer str i p , 외 다수 조병철 서울대학교 해양학과 졸업 동 대학원 석사 캘리포나아 주립대학 박사 스크립스 해양연구소. 조지아 대학 연구원 한국외국어대학교 조교수 역임 현재 서울대학교 해양학과 조교수 논문 ” Bi og eo chemi ca l sig n if ica nce of bacte r ia l bio m ass in the ocean's eup ho ti c zone 외 다수
토양미생물학과 생화학 
 Soil Mi cr obio l og y and Bio c hemi st r y
Soil Mi cr obio l og y and Bio c hemi st r y
 토양미생물학과 생화학
토양미생물학과 생화학
서문 토양에서 일어나고 있는 생물과 그들에 의해서 매개되는 반g 들을 알아 두어야 하는 필요성이 바로 토양미생물과 토양생화학의 연합 분 야를 형성하는 추전력이 된다. 오래전부터 관심의 대상이었으며, 그 리고 얼추잡아 지금까지 한 세기 동안 조사가 진행되고 있는 토양 과 정들 중에서 탄소의 무기화, 질소고정, 황의 산화, 균근의 형성, 질 산화 작용, 그리고 탈질화 작용들이 있다. 이들과 토양 과정에 대한 지식이 축적되고 있는 것과 같이 농학, 임학, 환경학에서 발생하는 응 용 문제들에 접근하기 위해서 종합적 수준의 연구에 대한 필요성이 강 화되고 있다. 그것이 바로 이 책에서 겨냥하는 목표가 된다. 미생물에 의해서 추전되는 영양소 순환과 기본적인 토양 과정에 대한 일관된 조 망을 제시하고자 이 책의 많은 부분에서 미생물에 의해 매개되는 과정 에 초점을 맞추어 접근했다. 이 책은 환경, 특히 토양에 약간의 지식과 생물학과 화학에 학문적 인 배경을 이미 가지고 있는 고학년을 염두에 두고 집필되었다. 이와 같은 책에서는 필요한 모든 선수과목의 지식울 제시하는 것이 불가능 하다. 토양서식지에 관한 제 2 장과 토양생물에 관한 제 4 장에서는 기 본 방향을 요약했다. 제 1, 3, 5 장 또한 배경울 제시한다. 학생들이 읽는 데 도움이 되도록 각 장의 끝에 참고문헌과 추가적인 읽을거리 룰 그리고 책의 끝에 간단한 용어들을 제시했다.
오늘날 전지구 생태계에 가해지고 있는 압박감 때문에 나타나는 문 제들은 적절한 농경 및 임산자원 관리의 필요성을 강조하고 있다. 미 생물 능력의 유전적 조절로 이루어지고 있는 유전공학의 발전은 숙주 식물과 미생물의 상호작용을 바꾸어 놓을 만큼 거대한 참재력을 발휘 하고 있다. 우리가 이 책을 통해서 가지는 희망은 바로 토양미생물과 토양생화학에 대한 소개와 함께 특히 토양에서 일어나고 있는 기본적 인 미생물 과정에 대한 이해를 돕는 것이다. 그것이 성공한다면 학생 들은 우리들의 학문 영역에서 다가올 발전의 실질적인 응용성들을 마 음속에 그릴 수 있어야 한다. 이와 같이 한 권의 책이 완성되기 위해서는 많은 도움이 있어야만 했 다. Scott Smi th, Wi lliam Horwath , Ken Hort on , David Har-riS 7 } 편집과정에서 베풀어 준 도움에 감사한다. 이 책에서 처음으로 사용된 삽화는 Phy llis Paul 과 Marlene Cameron 의 솜씨에 힘 입 었 다. Lin d a Salemka 에게는 원고 준비와 컴퓨터 입력를 해준 것에 감 사한다. 전에 농업연구소에 근무했고 지금은 공동연구자가 된 Francis Clark 는 그의 동료들이 베풀어 준 여러 가지 유용한 제안에 감사한다. E.A. 폴 F.E . 클라크
차례
서문 5 제 1 장 토양미생물학 및 생화학의 전망 1-1 정의와 범위 13 1-2 선구적인 업적 14 1-3 20 세기 초반의 토양미생물학 16 1-4 최근의 발전과 다양화 18 1-5 토양생물학 문헌 21 1-6 21 세기를 향한 전망 22 참고문헌 25 제 2 장 생물 서식지와 생물반웅 장소로서의 토양 2-1 서론 29 2-2 토양의 구조적인 측면 31 2-3 토양 공기 36 2-4 토양수 41 2-5 산화환원 전위 45 2-6 토양 pH 48 2-7 토양 온도 49 2-8 환경 요인들의 상호작용 54 참고문헌 55 제 3 장 토양생물 연구 방법 3-1 서론 593-2 토양시료 채취 61
3-3 토양의 현미경 관찰 62 3-4 화학적 기법을 이용한 생물량 측정 70 3-5 효소와 그 측정 77 3-6 미생물의 배양계수 79 참고문헌 81 제 4 장 토양 생물군의 구성 4-1 서론 85 4-2 바이러스 86 4-3 세균 87 4-4 진균 99 4-5 조류 107 4-6 지의류 110 4-7 원생동물 111 4-8 토양 후생동물 114 참고문헌 117 제 5 장 토양생물의 발생과 분포 5-1 서론 119 5-2 토양생물군의 지리적 차이 120 5-3 토양 단면 내의 생물 분포 121 5-4 토양 바탕 내의 생물 분포 122 5-5 식물 뿌리와 미생물의 연합 126 5-6 잎 부분과 미생물의 연합 131 5-7 식물 조각과 미생물의 연합 133 5-8 토양생물에 대한 관리 전략의 영향 137 참고문헌 141제 6 장 탄소 순환과 토양 유기물
6-1 서론 143 6-2 범지구적인 탄소 순환 144 6-3 유기 잔여물들의 성분과 대사회전 146 6-4 토양 유기물의 생성 163 6-5 토양 유기물의 구성 167 참고문헌 173 제 7 장 유기 잔여물의 분해와 토양 유기물 대사회전의 역동성 7-1 미생물 전환 과정의 반응속도론 175 7-2 분해의 역동성 183 7-3 식물과 토양 자료의 모형화 185 7-4 모형의 출력 188 7-5 반응속도론과 토양미생물 활동을 포함하는 예제 194 참고문헌 196 제 8 장 유기 질소와 무기 질소의 변환과 질산염으로의 변환 8-1 질소 순환 199 8-2 질소의 무기화 작용 201 8-3 부동화 반응 203 8-4 질산화 작용 210 참고문헌 219 제 9 장 질산염의 환원과 이동 9-1 서론 221 9-2 탈질화 작용 222 9-3 식물 뿌리에 의한 흡수 238 9-4 용탈에 의한 질산염의 제거 2399-5 침식에 의한 질산염의 손실 242
9-6 국지적인 질산염의 축적 243 참고문헌 243 제 10 장 토양으로 질소 회귀―생물 질소고정 10-1 지구상의 질소 분포와 이동 245 10-2 질소고정 생물 248 10-3 방선균근 연합 261 10-4 광합성적 연합 266 10-5 뿌리혹 형성과 콩과 식물에서의 질소고정 269 10-6 질소고정의 생화학 273 10-7 질소고정의 에너지론 280 10-8 접종 282 10-9 생물공학의 도전 285 참고문헌 288 제 11 장 균근 관계 11-1 서론 291 11-2 균근의 형태와 분포 293 11-3 균근의 생리와 기능 309 11-4 균근 식물 협생에서의 탄소 흐름 316 11-5 연구 방법론 319 참고문헌 321 제 12 장 토양에서 인의 변환 12-1 서론 325 12-2 인 순환의 범지구적 양상 326 12-3 무기 인 32912-4 용액 인 330
12- 5 무기 인의 용해 331 12-6 유기 인 331 12-7 식물 뿌리-토양계에서 인의 유동 335 참고문헌 337 제 13 장 토양에서 황의 변환 13-1 서론 339 13-2 자연에서 황의 존재 형태 342 13-3 부식질에서 유기 황의 농도 348 13-4 황의 변환 350 13-5 자연에서 무기 황 화합물의 산화 354 13-6 무기형 황의 환원 359 참고문헌 362 제 14 장 금속의 미생물적 변환 14-1 서론 365 14-2 철의 변환 366 14-3 철관의 형기성 부식 371 14-4 망간의 변환 373 14-5 수은의 변환 374 참고문헌 375 옮긴이 해제 377 용어 정리 387 주요 용어 옮김 395 찾아보기 407제 I 장 토양미생물학 및 생화학의 전망 1-1 정의와 범위 토양미생물학이란 토양 속에 살고 있는 유기체를 연구하는 학문이 다. 주요 세부 내용에는 유기체의 대사활동, 일차 생산과 관련된 에너 지 흐름과 영양 물질 순환에서 미생물의 역항들이 포함된다. 더불어 이 분야는 토양 유기체의 환경 영향과 그들이 야기하는 과정들과도 관 계가 있다. 토양미생물학은 기작을 주로 다루는 관점에서 보면 토양생 화학을 많이 포함한다. 이 공동 분야는 처음엔 토양 속의 현미경적인 생명들을 다루었으나 영역을 확장하여 토양 속에 서식하면서 토양의 역동적인 변화에 참여하는 보다 큰 크기의 생물들도 포함하게 되었다. 현재는 단세포동물과 함께 토양 중형동물 mesofa u na 이라 불리는 작은 무척추동물도 토양 생물군 soil bio t a 에 포함된다. 이들의 크기는 현미 경으로나 볼 수 있을 정도로 아주 미세하거나 육안으로 볼 수 있을 만 큼 크기도 하다. 약간의 원생동물들은 제법 큰데 여러 가지 조류 a lga e 와 전균(이 책에서 용어 〈진균〉과 〈곰팡이〉 〈균류났근 fungi를 옮긴 것으
로 모두 갇은 뜻으로 사용한다 : 옮긴이)은 센티미터 또는 데시미터로 측정할 수 있는 크기의 군체 또는 사상체 구조를 이루기도 한다(이 책 의 원 제목은 토양미생물과 생화학이지만 이 문단에서 보는 바와 같이 책의 많은 부분에서 토양에 거주하는 동물과 식물의 뿌리, 토양에서 영양소 순 환, 그리고 대기화학 및 환경 문제와 연관된 토양미생물의 생태학적 과정을 설명하고 있다 : 옮긴이). 미세한 또는 중간 정도 크기의 동물들은- 유기물 전환에서 보조적인 역할을 하지만 토양의 미생물들 m i cro fl ora 만큼 폭넓은 효소 활동 범 위를 가지고 있지는 않다. 토양미생물의 영역 안에 소형 무척추동물을 포함하게 된 것은 얼마되지 않았다. 균근 m y corrh i zae 도 마찬가지인데 수년 동안 비교적 적은 수의 균학자들만이 균근으로 알려진 진균과 식 물 뿌리의 연합체 asso ci a ti on 에 대한 연구를 했을 뿐이다. 토양미생물 학자들이 영양물질 이동에 더욱 관심을 갖게 됨에 따라서 균근에 대한 연구가 부수적인 연구가 아니라 연구의 중심이 된다는 것을 알게 되었 다. 1-2 선구적인 업적 와인을 생산하는 과일주스의 자연 발효와 우유가 시는 현상은 인류 역사의 시작과 함께 관찰되어 왔지만 과학으로서 토양미생물학은 세균 학 및 원생동물학과 함께 시작되었다고 볼 수 있다. 1676 년 네덜란드 의 렌즈 가공사인 Anto n iu s van Leeuwenhoek 는 자연수와 후춧가 루가 담긴 물에서 미세동물들 a nim alcules 을 보았다고 보고했다. 그의 관찰은 썩어가는 식물체 중의 미생물들에 대해 이루어전 것이기 때문 에 우리는 그를 토양미생물학의 아버지로 볼 수 있다. 그러나 신학문
의 발전에 많은 공헌을 한 Serge i W i no g radsk y (1856-1953) 에게도 이 명예를 안겨 주는 것이 공평할 것이다. 특히 그가 질산균 n it r ifi er 과 함께 질산화작용 n it r ifi ca ti on 에서 질산균이 하는 역할을 발견한 것 은 가치 있는 일이다. 이것은 무기물이 미생물의 성장에너지로 사용된 다는 미생물학적 독립영양 au t o t ro ph y의 개념을 시발시켰다. W i no gr adsk y와 같은 시대에 또 다른 발견, 죽 진균과 식물 뿌리 에 의한 균근의 형성이라는 획기적인 발견의 공로자들이 있었다. 전시 대의 사람들이 진균과 식물 뿌리 연합이 생긴다는 것을 알고 있기는 했더라도 그것의 상호공생 관계에 대한 인식은 P f e ff er(1877) 가 처음 이었다. 1855 년 A. B. Frank 가 균판]라는 용어불 처음으로 제안했 다. 뒤에 그는 의생 균근과 내생 균근(균근 중에서 뿌리 세포 의부에 사 는 것은 의생 균근이고, 뿌리 세포 안에 침두하여 사는 것은 내생 균근이라 하며 이에 대한 자세한 내용은 이 책의 제 11 장에서 설명하고 있다 : 옮긴이) 울 구분했다. 19 세기 후반기는 미생물적인 과정에 관한 다른 중요한 발견들이 있었다. 공생과정을 통한 질소고정 n it ro g en fixa ti on , 탈질화 작용 denit rifica ti on , 황화물 환원 sulfa te reducti on , 그리고 비공생 질 소고정들이 포함된다. 미생물 발효에 대한 Louis Pas t eur 의 연구는 특히 의미심장하다. 그의 연구에 의해 형기성 대사과정에 대한 윤곽을 알 수 있게 되었다. 식물, 동물과 같은 모든 다세포 생물들은 호기성 대사과정에 의존한 다. 어떤 토양 세균둘은 호기성 대사과정만을 할 수 있으며, 일부 또 다른 세균들은 형기성 대사과정만 수행한다. 또 어떤 일부 생물들은 형기성과 호기성 대사과정을 바꿀 수도 있다. Paste u r 이전 시대 몇 사람들이 효모 ye ast 가 발효에 관여한다는 것은 인식하고 있었으나, 미생물들에 의한 알코올과 유기산들의 생산이 공기 없이 살 수 있는 기본 대사와 관련된다는 것은 Pas t eur 가 임중하였다. 18971d
Buchner는 효모 세포들을 분쇄, 세포 없는 액체 상태로 만들어도 알 코올 발효를 일으킬 수 있다는 것을 보였다. 따라서 그는 미생물 효소 학에서 선구적인 일을 이행한 공로자로 인정되어야 한다. Leeuwenhoek 와 W ino g rad sky , Pas t eur 의 발견이 있은 몇 년 사 이에 생물의 자연발생설에 대한 부정, 미생물과 동식물의 질병과의 관 련성, 토양미생물의 기재 분류 descr ipti ve t axonom y의 큰 발전과 갇 은 몇 가지 일반적이고 기본적인 업적들이 있었다. 이명법 분류학의 아버지 L i nnaeus(1709-1778) 는 현미경적 형태를 가전 생명체를 인식 하고서, 이 모든 미생물을 단순히 〈혼돈 Chaos 〉이라고 하는 그룹에 넣 음으로써 ,분류학적인 곤경을 피해가 버렸다. 현재도 마생물 분류는 논 란의 여지가 있지만 적어도 혼란스러운 것에서 실리적인 것으로 발전 되어왔다. 1-3 20 세기 초반의 토양미생물학 금세기가 시작되면서 토양미생물학이라는 젊은 학문은 확고하게 자 리를 굳혔다. 공생에 의한 질소고정, 유기물의 분해, 무기 질소의 변 환 등에 대한 연구가 주로 강조되었다. 콩과 식물에 대한 질소고정균 접종 성공으로 이를 실제 적용하려는 몇 가지 시도를 하게 되었다. 19561 :d Klu yv er 는, 인간사에서 미생물들이 발휘하고 있는 중요한 역 할들에 대한 Pas t eur 의 놀라운 발견이 있은 이래, 과학으로서 미생물 학은 그 뛰어난 실용성 때문에 계속 어려움을 겪어왔다는 것을 관찰했 다. 세기가 바뀔 즈음에, 토양미생물들에 대해 개체군 종류별 크기를 조사 census count 하고 이룰 토양 비옥도의 지수로서 이용하기 위한 많은 노력이 있었다. 이러한 개념은 적어도 한천배지 ag a r pla te s 위에
서 군집을 형성할 수 있는 번식종균p ro pa g ules 의 수는 전체 미생물 개체군의 극히 작은 부분만을 차지한다는 것, 또 토양 비옥도를 결정 하는 요소에는 그의에도 다론 것들이 많으며, L i eb ig의 최소량의 법 칙에 따른다면 그들 결정 요소 중 어떤 것이라도 식물의 생산성을 제 한할 수 있다는 점 등을 고려하지 않고 있다. 토양 속으로 질소고정 효소 n it ro g enas 혀끝 생산하는 미생물을 접종함으로써 비공생 질소고정 울 증가시키려는 시도들도 있었다. 아러한 시도들은 미생물의 경쟁관 계에 대한 지식의 부족으로 실패했다. 그러나 이러한 시도는 적어도 부분적으로 시험관에서가 아닌 실제 자연계에서 미생물들이 무엇을 하 는지 또 하지 않는 일은 무엇인지에 대한 관심으로 바꿔 놓는 역할을 했다. 미생물의 성장과 유기질소의 이동t rans fe r 및 변환t rans fo rma ti on 사 이의 일반적인 관계 정립은 초기의 업적에 속한다• 질소의 순고정 (부 동화)없이 식물 잔여물들을 분해할 수 있는 탄소/질소의 비율은 대략 25 : 1 인 것으로 알려졌다(분해하는 유기물에서 탄소/질소 비율이 25 : 1 이 넘을 때는 분해 미생물이 의부의 질소를 흡수해서 자신의 부족한 질소 양을 보충해야 하는데 이렇게 보충되는 것이 순고정 또는 부동화되는 양이 다. 물론 비율이 25 : 1 보다 작을 때는 분해물질에서 유래되는 질소는 미생 물대사에 사용되고도 남기 때문에 순분비가 있을 것이다 : 옮긴이 ) . 그리고 식물 분해 속도에 영향을 미치는 환경 요인들에 대해서도 정리가 되었 다. 분해 동안 일어나는 질소 배출을 토양 생물의 대사회전 (tur nover, 이 용어는 대사전환으로 제 안하는 분이 있었으나 tra sfo r mati on 3 !}-구 별되 어야 하기 때문에 대사회전이 더 적철하다 : 옮긴이)에 의한 것일 가능성 도 인식되었다. 초기의 업적들을 요약하면서, Harmsen 과 van Schreven(1955) 는 다음과 같이 적었다. 〈토양에서 일어나는 유기질 소의 무기화 작용에 대한 일반적인 과정의 연구는 실용적인 측면에서
는 1935 년에 완성되었다. 오늘날의 논문들이 완전히 해결된 문제들을 다루면서 부가적인 관찰하는 것이 아직도 가치 있다고 여전히 간주하 고 있는 것은 놀라운 일이다. >그 러나 그때 이 저자들은 탄소와 질소, 환경요인들의 영향 사이에 이루어지는 관계들이 각각의 토양에 대해서 결정되어야 한다고 지적했다. 이것은 기초가 되는 원리들이 이해되지 않았음을 가리키는 것이었다. 1-4 최근의 발전과 다양화 시간이 흐르면서 토양미생물학의 범위는 질소와 유기물에 대한 일차 적인 관심에서 토양 효소, 근권 미생물상 rh i zos p here mi cro fl or a, 토양 구조 형성에 미생물들의 참여, 인공 살충제와 다른 난분해성 물질의 분해, 미생물 생태학, 금속의 변환과 환경에 대한 미생물의 영향과 같 온 영역으로 점차적으로 확장되었다. 1950 년에서 1980 년까지 미생물 학자들은 경운과 비료 생산을 위해 값싸고 유용한 에너지가 출현된 것 과 시기를 같이해서 농업 생산성과 산림 관리를 위해 실험적인 접근을 했다. 이 시기에는 또한 방사능 추적자를 이용한 기법들이 개발되기도 했다. 1946 년 Norma~ 이렇게 썼다. 〈안정한 질소 동위원소 “N 와 탄소 동위원소 130 긱 이용은 탄소 순환과 관련하여 다양한 질소의 변환과정을 정량적으로 파악할 수 있게 할 것이며, 토양에 존재히는· 질소 형태들을 찾아내는 데 크게 도움이 될 것이다. > Jan sson (1958) 은 N03- 에 비해서 NH4+ 에 대한 미생물의 선호도 가 높다는 것과 무기화국병유화 mi ne rali za it on -im mobil iza it o ~ 상호 작용들을 기술하는 데 있어 수학식의 이용 편리성에 주목했다. 1960 년대에는 토양 유기물을 부식산 humi c a ci d 과 풀브산 fulv i c a ci~녁i
구분하여 분리하는 고전적인 기법 의에 생물학적으로 더 의미 있게 분 리시킬 수 있는 특성에 대한 초기 문헌연구가 이루어졌다. 부식산이나 풀브산같이 크고 난분해성이어서 대사회전이 느린 것들로 니누는· 개념 보다 작고 영양적으로 활성이 있어서 대사회전이 빠른 것들로 나누어 보는 개념은 토양 유기물의 유동성에 대한 해석을 크게 발전시켰고 토 양유기물의 대사회전에 대해 현실에 가까운 수학 모형을 가능케 했다. 그것은 또한 질소의 참재적 생물 이용성을 알아내려는 토양 실험의 발 전에도 도움이 되었다. 유기 인 및 황의 순환에 대한 인식이 일어나면 서 토양생물학과 효소학이 생태계 연구에 포함되었다. 세균 유전학을 포함한 유전학 연구에 있어 중요한 업적들이 금세기 의 전반기에 나타났다. Gr iffith (1928) 는 Str e p toc occus pn eumnia e 의 살아 있는 무독성 세포들과 함께 열처리로 죽은 독성 세포들을 숙 주동물에게 주입함으로써 무독성의 캡슐이 없는 세포들이 독성의 캡슐 이 있는 세포로 형질전환t rans fo rm 할 수 있다는 것을 보였다. 이는 세균 형질전환의 첫 증거를 제시한 것이다. 1941 년 N. A. Krassil ni- kov 는 비감영성 non i n fe c ti ve 인 Rh i zob i um 이 감염성인 것으로 형질전 환되는 것을 보였는데 하지만 그 종균의 순도에 있어서는 약간의 문제 가 있었다. Aver y (1944) 는 형질전환을 유도하는 물질의 화학적인 성 질을 밝혔는데 이로해서 Cr ic k 과 Wa t so 퍼본 핵산 DNA 의 구조를 알 아냈고 1953 년 노벨상을 받았다. 유전적 조절 기작은 이중나선의 형 태로 두 가닥의 분자들로 배열된 4 가지의 뉴클레오티드 서열에 의해서 결정되는 것으로 밝혀졌다. 풀라스미드 생물학, DNA 서열 결정 (뉴 클레오티드 염기의 독특한 서열 결정), 전사효소.들의 발견 등 1970 년대 의 일은 유전공학 기술의 무대를 마련했다. 이들은 농업과 환경 미생 물학에 이용될 수 있는 커다란 잠재력을 가진다. 이 참재적인 가능성 둘 중 약간은 다음 문단들에서 논의할 것이다.
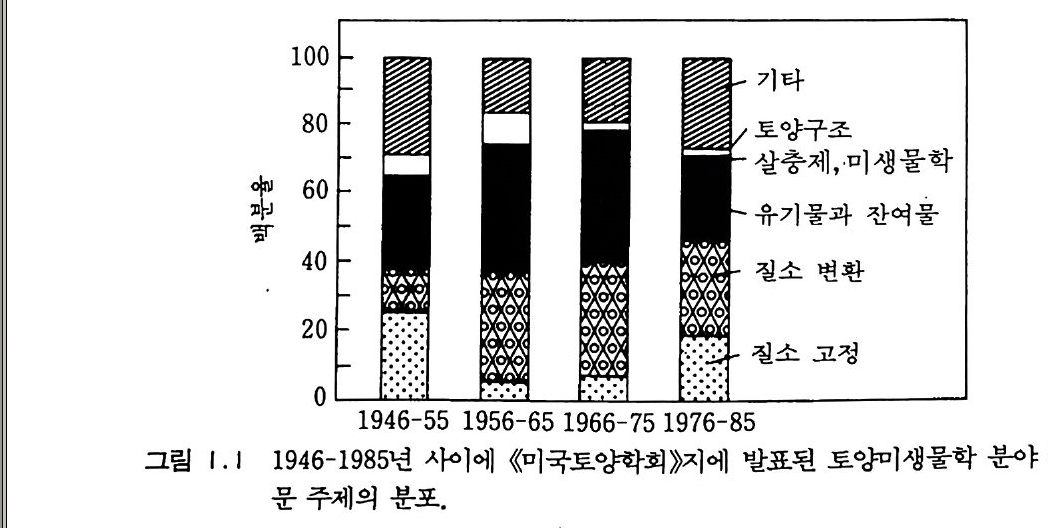
토양미생물학에서 홍미 있게 다루는 분야들의 변천은 지난 1946 년 에서 1985 년 사이 미국토양학회 제 3 분과에서 나온 논문들이 반영하 고 있다(그림 1.1 ). 이 막대그래프는 단지 6 가지 분야만을 보여 주고 있지만, 기타 항목을 포함한다면 대략 12 주제 (예를 들면 동물, 근권, 효소, 개체군 종류별 크기 조사, 항생제, 균근)로 나눌- 수 있는데 이를 따로 분류한다면 각 10 년 마다 발표된 전체 논문 수 중 약 l% 를 차 지한다. 위 기간에서 중간 20 년 동안은 질소고정에 대한 연구들이 적 었던 반면, 같은 기간에 토양 구조와 살충제의 분해에 대한 연구들은 전성기를 이루었고 그 이후 줄어들었다. 토양 구조에 대한 연구는 토 양 구조 형성을 촉진하기 위해 사용하는 첨가제에 많은 관심을 쏟았던 몇 년 동안 많이 일어났다. 살충제 연구에 대한 강조는 환경문제에 관 심을 가지게 되고 미국에서 환경보호국 Envir o nmenta l Prote c ti on Ag e ncy 설립 및 대기정화법 발령, 수질정화법 제정 등이 있었던 기간 에 나타났다. 그림 1. 1 은 U 사의 막대그래프 중 양 H 에서 토양 질소 전 환에 관한 논문들이 가장 큰 소그룹을 이루고 있음울 보여 준다. 이것
 i 18000 t •• 를 冒二구조
i 18000 t •• 를 冒二구조
은 1955 년 이후에는 15N 연구가 인기 있었고 1975 년 후에는 탈질화작 용, 특히 N20 방출에 대한 연구가 인기 있었던 데 뿌리를 두고 있 다. 시기에 따라 연구 분야의 강세가 달라지는 현상은 토양미생물학이 응용과학임을 나타낸다. 1-5 토양생물학 문헌 1900 년 이전 토양미생물학에 대한 연구보고서들은 토양미생물학과 관련있는 제목이 없는 학술 잡지들에 발표되었다. 이 분야를 위해 특 별히 소제목을 붙인 주요 전문 논문집은 1895 년에 처음 생겨났다. 한 독일 논문집이 두번째 소분과에 토양미생물에 관한논문들을 포함시켰 다. 현재는 토양미생물 및 생화학 연구 논문들이 발표되는 학술지를 모두 나열하면 수백 가지에 이론다. 창간시에 토양미생물학을 위해서 분과를 준비한 두 가지 주요 학술지는 《미국토양학회보 Soil Sc ien ce Soc iety of Ameri ca n Proceed i ng s 》 (193 연 제 1 권 발간)와 《국제토양학 회보고서 Transacti on s of the Inte r nati on al Soc iety of Soil Sc ien ce> (1 92 천 첫 보고서 발간)이다. 이들은 각각 미생물학 소분야를 〈토양마 생물학 〉 과 〈 토양생물학 〉 으로 명명했다. 1960 년대 후반 홍미로운 발전은 토양미생물학과 생화학의 공식적인 결합이었다. 1968 년 미국토양학회는 제 3 분과의 명칭울 〈토양미생물 학〉에서 〈토양미생물학과 생화학〉으로 바꾸었다. 거의 동시에 (19 69) 店토 양생물학과 생화학 Soil Bio lo gy and Bio c hemi stry)}ol ~ 제목의 국제 학술지가 출현했다. 196 7\!에 시작하여 〈토양생화학〉이라는 제 목의 연작이 5 권 출간되었다(1 967-1981). 이는 주로 토양미생물학에 란하는 학자들을 위해서 집필되었다(이 연작물은 한 동안 중단되었다
가 90 년대 들어 다시 속간되어 1993 년 현재 8 권까지 발행되었으며, 저자 E.A . Paul 은 연작 중 1975 년에 출간된 3, 4 권과 1981 년에 출간된 5 권의 편 집장이었다 : 옮긴이 ) . 토양미생물학과 다른 토양학 분야들의 연결은 계속되었다. 1985 년 에 《 토양생물학과 비옥도 Bio l ogy and Fertil tiy of So i ls 》 라는 이름의 학술지 제 1 권이 출간되었다. 디른- 여러 분야들과 함께 토양생물학과 관련 있는 심포지움, 워크숍, 학회 동이 지금은 혼하게 열리고 있다. 토양미생물학을 위한 최초의 주요한 교과서는 독일어로 쓰여졌다 . 1910 년 Felix Lohn i햐근 그의 Handbuch der Landwi rtsc haft lich e Bak t e i olog i峰 출판했다. 이 교과서는 19 판까지 인쇄됐으며 ¥R 국어 로 번역되었다. 주목할 만한 또 다론 초기 교과서로는 1923 년 E.J. Russell 이 쓴 『 토양미생물 The Mi cr oorga nis m s of the So il 』과 192 저 Waksman 이 쓴 『토양미생물학 원리 Pr inc iple s of Soil M i crob i olo gy』 가 있다. 또, 『토양과 미생물 The Soil and the M i crobes 』이라는 좀 덜 지루한 책이 Waksman 과 S t arke y에 의해서 1931 년에 출간되었 다. 그 후 영어로 쓰인 많은 책들이 출간되고 있다 (Alexander 1961, 1977 ; Gray and W illiam s 1971 , Hatt or i 1973 ; Walker 1975 ; Hawker and Lin t o n 1979; Subba Rao 1982 ; Ly n ch 1983 ; Ai ke n 의 1985) . 1-6 21 세기를 향한 전망 188 쩌 Be ij e ri nck 에 의해 현재 Rh iz ob i um 으로 알려진 공생적인 질소고정균이 분리된 이래 거의 100 년이 지났다 . W ino g rad sky (1890) 에 의해 질산화 작용과 생물의 독립영양 방식의 원리가 정립되
었는데 이는 아마 토양생화학의 출발점이라 할 수 있을 것이다. 다음 세기로 접어들면서 새로운 많은 요인들이 토양미생물학과 생화학에 영 향을 주고 있다. 다음과 같은 요인들이 거기에 포함된다. 첫째, 자료 처리, 정보교환과 자동화된 기구들의 조정을 위한 컴퓨터의 이용, 둘 째 , 무경 운 zero-ti ll, . 윤작 alte r nate crop ping , 전간수확 whole-tr e e harves ti n g과 갇은 전체 체계 관리 기법의 적용, 셋째 , 유전공학의 영 향, 넷째, 토양미생물학적 과정이 많은 주요 환경 문제들과 영향울 주 고 받는다는 인식, 다섯째, 더욱 효율적인 농업과 삼림관리체계 개발 의 필요성 등이다. 유전공학 기술은 질소고정을 촉진시키며, 난분해성 물질을 분해하 는 미생물 능력을 증대시키고, 농업 해충의 새로운 생물적 방제 bio l og ica l con t rol 를 성취시키기 위해서 이용될 수 있다. 새로이 제조 된 유기체가 토양 속으로 도입됨으로써 환경 파국을 초래할 가능성도 또한 있다. 좋든 나쁘든 토양미생물학과 생화학은 생물공학적 b i o t echnolo gy인 면과 밀접하게 관련되어 있다. 생물공학은 단순히 세 포생물학과 분자생물학 연구로 정의되거나, 더욱 장황하게는 미생물, 배양조직, 세포와 그 일부분이 가진 능력을 기술적으로 응용하기 위해 서 생화학, 미생물학, 공학을 총체적으로 활용하는 것으로 정의된다. L y nch(l983) 는 토양 생물공학을 농작물의 생산성을 최적화하기 위하 여 토양생물과 이들의 대사과정을 연구하고 다루는 분야라고 정의했 다. 그의 정의는 환경의 질을 최적화하기 위한 활동을 토양미생물학의 영역에 포함시키고 있는 것으로 볼 수 있다. 새로운 유기 분자들을 분 해하고, 방출된 석유에서부터, 과잉의 질산염까지, 폐수 성분 오영물 질들을 토양과 표면수로부터 제거하는 데 점점 더 많이 미생물군이 이 용되고있다. 토양미생물학의 제있)기에서 가장 위대한 도전 중의 하나는 새로운
미생물을 공학적인 기술로 만들어 내고 관리하는 것으로 보인다. 공학 적으로 만들어진 생물들이 자연에서 이용되기 위해서는, 자연환경에 성공적으로 접종되고 넓은 범위에 존재하는 천연적인 생물둘과 경쟁에 서 살아남을 수 있어야 한다. 어떤 새로운 생물이 해충으로 될 수 있 다는 매우 현실적인 두려움을 상쇄하기 위해서는 그 생물이 다른 환경 으로 도망할 수 없어야 한다. 또한 천연적인 토양 생물과의 유전적 교 환을 통해 미지의 생물을 만들어 낼 가능성을 가져서도 안 된다. 유전 공학적으로 만들어진 생물들이 새로운 유전물질을 전달할 가능성 때문 에 많은 논의가 일어나고 있으며 , 그 생물들을 자연현장에 적용하는 시험 작업이 지연되고 있다. 새로운 생물이 원하지 않은 파급을 일으 킬지 모른다는 두려움은 집시 나방과 네덜란드 뱀장어가 우연히 아메 리카에 도입되어 문제를 일으켰던 경험에 부분적으로 연유한다. 그러 나 과거에 바람직한 공생관계를 고취시키고 생물적 방제를 조장하기 위해서 많은 양의 자연발생 생물들의 종균을 토양에 뿌리기도 했지만 현재까지 그러한 접종으로 나타난 악영향은 전혀 알려진 바 없다. 유 전공학적으로 제조된 생물들의 운명과 생존에 대한 과거 문헌들의 검 토는 Halvorsen 등(1 985) 에 의해서 수행되었다. 환경 개선을 위하여 유전공학적으로 제조된 생물들을 활용하는 것은 토양생물의 기본 특성에 대한 지식과 관계가 있다. 난분해성 독성 유 기물의 분해 향상과 병원성 오염물질의 신속한 처리는 오수 처리에서 중요한 비용-편익 효과를 가진다. 세계 곳곳에서 농업용 살충제가 지 하수에까지 도달하고 있다. 지하수는 종종 미생물 생장에 필요한 유기 탄소 공급량이 부족하고 생물 활동에 불리한 무생물적 환경조건을 가 지고 있어서 정화하기 쉽지 않다. 살충제의 높은 오염 가능성은 이룰 중요한 연구 분야로 만들고 있다. 살충제의 주요한 부분을· 차지하는 염소 결합 탄화수소들은 일반적으로 퇴적물, 논, 토양 저층과 같은 형
기성 조건 아래서는 잘 분해되지 않는 것으로 밝혀지고 있다. 그러므 로 형기성 조건에서 염소가 결합된 탄화수소들을 분해하는 세균의 개 발은 생물공학적 가능성이 있다. 리그닌을 분해하는 것으로 알려진 흰 곰팡이 whit e- rot fun g i7~ 또한 매우 난분해성이면서 독성을 가전 PCB (po lyc hlorin a te d b ip hen y ls) 들을 대사할 수 있는데 이는 토양미 생물이 가지는 다양성의 보기이다. 이것은 또한 넓은 의미에서 환경문 제에 생명공학을 적용할 수 있는 하나의 실례이기도 하다. 지금보다 나은 생물적 방제 기작들을 이용함으로써 농경지에 살포하 는 살충제 양은 감소될 수 있고 어떤 경우엔 원한다면 완전히 배제될 수도 있다. 이들 생물적 방제 기작은 종합 해충방제 int e g rat e d pes t contr o l, 개량 경운실행 alte r ed tillag e pr acti ce s, 해충에 저항성을 가 지는 식물의 개발과 갇은 다양한 기술을 포함한다. 생물적 방제에 쓰 이는 유전공학적으로 변형된 미생물과 새로운 식물 육종 기술은 토양 미생물학과 생화학에 대한 더욱 깊은 이해에 바탕을 둔 관리 시나리오 의 일부가 되어야 할 것이다. 참고문헌 Aik e n, G. A., McKnig h t. D. L., Wershaw R. L., and MacCart hy., P. ( 19 85) . Humi c Substa n ces in Soil , Sedim ent and Wate r : Geochemi stry, Isola- tion and Charact er i zat i on . Wi le y , New York. Alexander, M . (19 61) . Intr o duc tion to Soil Mi cr obio l ogy . W iley , New York. (19 77) . Intr od ucti on to Soil Mi cr obio l ogy . 2nd ed. Wi ley , New York. Avery , 0. T., MacLeod, C. M. , a nd McCarty . M. (19 44) . Stu d ie s on the chemi cal natu re of the substa n ce ind uc ing tran sfo r mati on of pn eumococcal type s, ]. Exptl. M ed. 79. 137- 15 8. Beije r i nc k, M. W. (1988) . Die Bakte r i en der Pap illon aceen-Knollchen, Bot. Z tg . 46, 724-735.
Buchner, E. ( 18 97) . Alkaholi sc he Gahrung ohne Hefe z ellen, Ber. dts c h. chem. Ges. 30, 112~124. Cric k , F. H. C., and Wats o n. J. D. (19 53) . Molecular str u ctu r e of nucleic acid . a str uc tu r e for deoxy ribo se nucleic acid , Natu r e, Lond. 171, 737- 738. Frank, A. B. (18 85) . Ueber die auf Wurzelsym b io s e beruhende Emahrung ge wis s er Baume durch unte r ir d is c he Pil z e, Ber. deut. bot. Ges. 3, 128-145. Gray, T. R. G., and Wi lliam s, S. T. (19 71) . Soil Mi cr oorga n is ms. Oliv e r & Boy d , Edin b urgh . Gr iffith, F. (1928) . The sig nifica nce of pn eumococcal type s, ]. Hy gien e 27, 113- 15 9. Halvorsen, H. 0., Pramer, D., and Rog ul, M. (19 85) . Eng ine ered Orga nsim s in the Envir on ment: Sc ien ti fic Issues. Am. Soc. Mi cr obio l . , Wa-shig ton . D. C. Harmsen, G. W., and van-S c hreven, D. A. (1955) . Mi ne rali za ti on of orga nic nit rog e n in soil , Adv. Ag ro n. 7, 299. Hatt or i, T. (19 73) . Mi cr ob ial Li fe in the Soil . Dekker, New York. Hawker, L. E., a nd Lin t o n , A. H. (19 79) . Mi cr oorga nis ms, Functi on , Form and Env iro nment. Edward Arnold, :Lo ndon. Jan soon, S. L. (1958) . Tracer stu dies on nitrog e n tra nsfo r mati on s in soil with spe cial att en ti on to mi ne rali za ti on -im mobil iza ti on relati on - ships , Kun gl. l.An tb r ukshogs k olan Ann. 24, 101-361 . Kluyv er , A. J.(1 956). The mi cr obe's contr ibu ti on to bio l ogy . Harvard Un i- versit y lectu re. Carnb~d ge . Krasil' rtlko v, N. A. (19 41) . Varia tion in nodule bac ter i , Mi kr obio l og iya 10, 396-400. Llihnis' F. (19 10) . Handbuch der l.An dwi rtsch tl ic h e Backte r i olo g ier. Bor-ntr ae g e r, Berlin . Ly nc h, T. M, (1983) . Soil Bit ec hnology . Blackwell, Oxfo r d Norman, A. G. (19 46) . Recent advances in soil micr obio l og y, Soil Sc i. Soc. Am. Proc. 11, 4-15. Pfef f er , W . (18 77) . Ueber fleis c h fres sende Pf lan zen, l.An dw. ]ahrb. 6, 969
-998. Russell, E. J. (19 23) . The Mi cr oorga nis m s of the Soil . Long ma ns, Green. London and New York. Subba Rao, N. S., ed. (19 82) . Advances in Ag ricu lt ur al Mi cr obio l og y. Butt er- wort h, London. Walker, N. (19 75) . Soil Mi cr obio l ogy .-A Cr itica l Revie w . Butt er wort h, Lon-
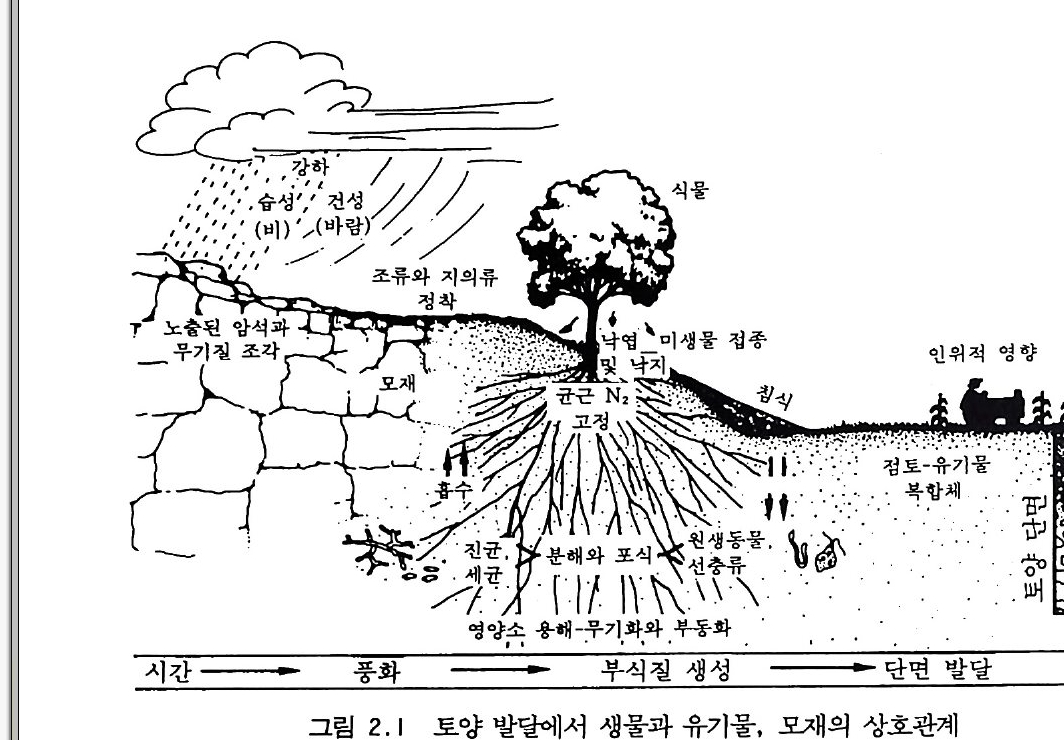
don. Waksman, S. A. (19 27) . Pr inc iple s of Soil Mi cr obio l ogy . W illiam s & W ilk in s , Balt imo re, Mary la nd. Waksman, S. A., and Sta r key, R . L. (19 31) . The Soil and the Mi cro be. W ile y, New York. W ino g rad sky , S.(1 8 90). Recherches sur les orga nis m s de la nit rif ica ti on , Ann. Inst. Paste u r 4, 213- 31 , 257-75, 760-71 . 추가로 읽을 거리 Brill , W. J. (19 85) . Safe ty concerns and ge neti c eng ine erin g in ag ricu ltu r e, Sc ien ce 227, 381-384. Dy k huiz e n, D., and Hart l, D. (1981) . Evoluti on of comp etitive abil ity in Escheri ch ia coli. E voluti on (Lawrence, Kans. ) 35, 581-594. Kolata , G. (1985) . How safe are eng ine ered orga nis m s ? Sc ien ce 229, 34 : -35. Kosug e, T. , a nd Neste r , E. W. (1984) . Plant Mi cr obe lnte r acti on s:Molecular and Geneti c P ers pe cti ves . Vol. I. Macm illa n, New York. Lin c oln, D. R., F is h er, E. S., a nd Lambert . D . (19 85) ReJe a se and conta i n - ment of mi cro orga n ism s for ap plied ge neti c acti vities , Eng . Mi cr ob. Technol. 7, 314. Paul. E. A., and Ladd. J. N., eds. (19 81) . Soil Bi oc hemi stry. Vol. 5. Dekker, New York. Schnit ze r. M., and Khan, S. U. (19 72) . Humi c Substa n ces in the Soil En 파 ronment, Dekker, New York. Tang le y, L. (1985) . Releasin g eng iee red orga n ism s in the env iro runent, Bi o Sc ien ce 35, 470-473.제 2 장 생물 서식지와 생물반응 장소로서의 토양 2-1 서론 토양생물들은 그들이 살고 있는 서식지의 생성 ge nesiso J] 참여한다. 그들은 전체 생물군, 특히 고등식물들과 함께 토양 형성 과정에서 상 호작용하는 다섯 요소 중의 하나이다. 나머지 네 요소는 기후, 지형, 모재 pa rent mate r ia l , 시간이다. 물리적 화학적 분쇄에 의해 커다란 암석은 부피에 비해 표면적이 큰 작은 입자들로 나누어지고 식물 영양 소가 분비됨에 따라 토양 형성 과정이 시발된다(그립 2.1). 토양 형성 초기 과정에서 부족한· 두 가지 주요 영양원소는 탄소와 질소다. 그러 므로 토양 모재의 초기 이주생물은 보통 광합성과 질소고정을 모두 할 수 있는 생물이다. 이에는 남조류로 알려진 시아노박테리아가 우세하 게 나타난다. 고등식물이 들어서게 된 다음에도 토양 과정은 계속된 다. 죽, 토양 과정을 통해서 살아 있는 세포와 죽은 세포, 토양 유기 물 (SOM: soil orga nic matt er ), 토양 특성과 긴밀한 관계가 있는 콜 로이드성 물질들이 상호작용하기에 충분히 작은무기 입자들의 역동적
 조류와 ~지의 ~1 재무저조
조류와 ~지의 ~1 재무저조
인 혼합물이 생산된다. 식생과 시간 요소의 상호작용은 새로 생긴 경관에서 가장 쉽게 연구 된다. 1883 년 크라카토아 Kraka t oa 화산 폭발로 인도네시아 가까이에 는 새로운 모재로 뒤덮인 작은 섬들이 만들어졌다. 이둘 섬에서는 새 로 식생이 형성되고 토양이 생성되는 과정이 여전히 계속되고 있다. 1960 년대에 아이슬랜드 가까이에 형성된 서트지 Surt se y 화산섬과 1980 년대 세인트헬렌스 S t. Helens 산 주변에 화산 분출 다음 형성된 경관은 토양 형성 초기에 대한 더욱 근대적인 보기들을 제공하고 있 다. 석탄이 채굴된 후 버려진 지역과 새로 형성된 연안대의 사주에서 새로 형성된 식생도 또한 식생과 미생물의 활동으로 토양이 발달됨으 로써 안정화되고 있으며 기본적으로는 생명이 없는 지역의 보기이다.
토양의 근대적인 정의는 식물 뿌리에 의해서 이용되는 지구 표면충 과 관계가 있다. 미생물의 성장은 상당히 더 깊은 곳에서도 일어난다. 바위 한가운데 있는 유전 oil well 에서 표면 환경으로 보호되어 수백만 년 동안 살아 있는 생물이 발견된다. 활발한 탈질화 작용은 탄소원이 N03- 과 함께 침투된다면 뿌리 깊이보다 상당히 아래인 지하층에서도 일어난다. 활동중인 화산울 예의로 하면 지구 표면에서 미생물이 존재 하지 않는 자연 지역은 알려져 있지 않다. 미생물은 온도의 일교차가 50°C 에 이르는 고비 사막에도, 영하 50°C 에 달하는 극지의 빙산에도, g o·c 에 이르는 온천에도 존재한다. 살아 있는 세균은 또한 바닷물의 거대한 압력과 고온 아래에 있는 갈라파고스 해구에서도 발견된다고 알려져 있다. 토양미생물학자들이 주로 관계하는 것은 교란되지 않은 상태로 주요 육상 생태계를 구성하고 있거나, 경작 또는 다른 형태로 관리되고 있 어 우리에게 부존자원둘을 제공하고 있는 지표 부분이다. 토양생물들 온 생산적인 토양에서 가장 큰 종 다양성과 가장 큰 개체군 크기롤 보 이고 있다. 미생물 생물량 m ic rob i al b i omass 의 크기는 보통 식물 생 장의 양(일차 생산량) 및 토양 유기물의 수준과 직접적인 상관관계를 가진다. 미생물의 환경에 대한 훌륭한 논의는 Chen 과 Avnim elech (1986) , L ynch 와 Poole (19 79) , • McLaren 과 Skuji ns (1968) , 그리고 Foch t와 Ma rti n(1979) 에 의해서 이루어졌다. 2-2 토양의 구조적 인 측면 토양은 식물 뿌리, 살아 있는 토양 개체군, 여러 가지 분해 단계에 있는 유기물 구성 요소와 함께 다양한 크기와 모양, 그리고 화학적인
 크기 토양 구성요소
크기 토양 구성요소
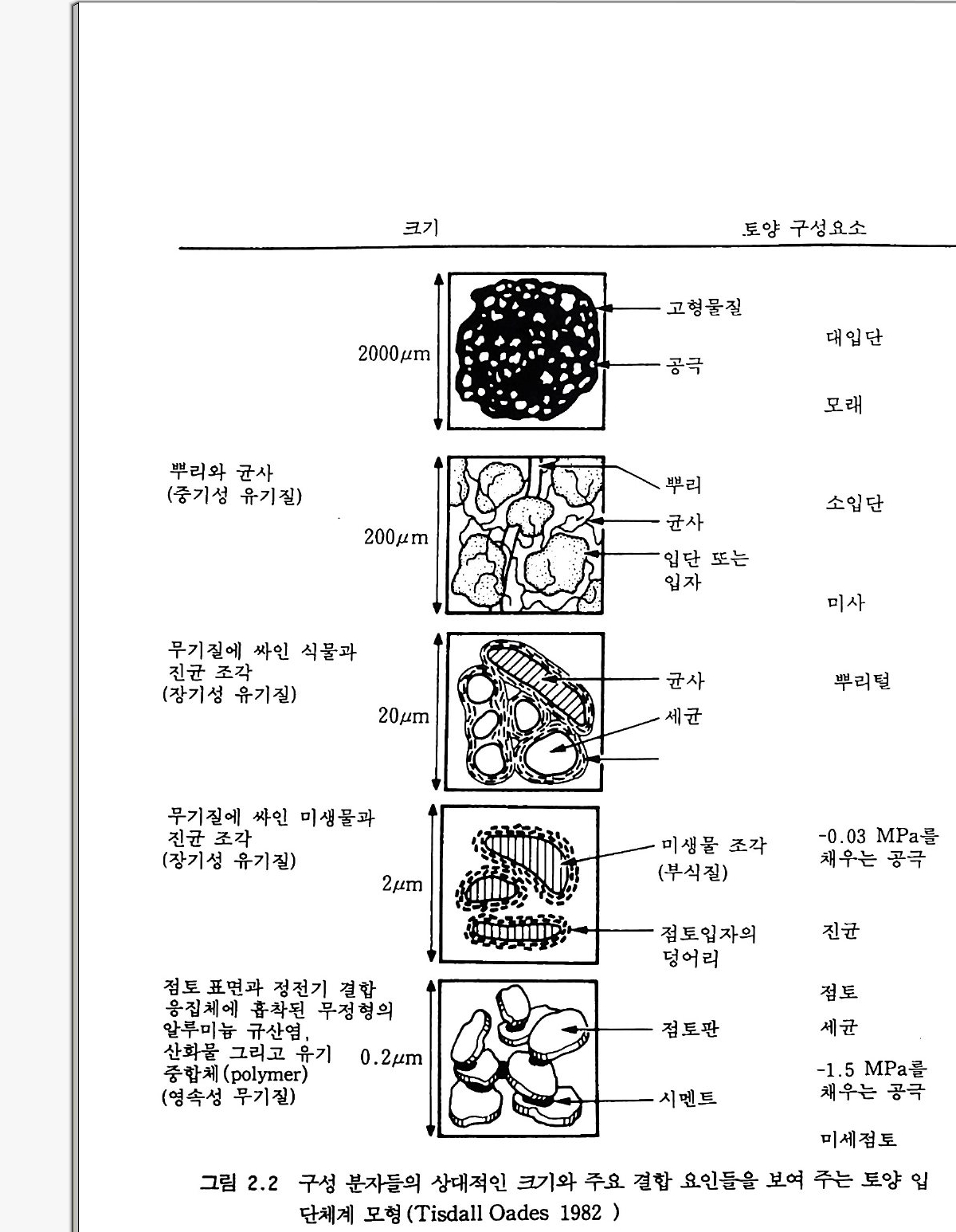
특성을 가전 무기입지들로 이루어진다. 토양 기체, 토양수, 용해된 무기물들이 토양 서식지를 이룬다. 토양 짜임새에 대한 이해는 공간적 인 배열에 대한 지식을 필요로 한다. 이것은 구성 요소들의 크기와 모 양 모두에 관계가 있다. 토양바탕 so il ma t r i x 울 이루는 구성 요소들의 상대적인 크기는 대형입단 macroa ggr e g a t e 과 같이 직경 2mm 이상에 서 세균 및 콜로이드성 입자와 같이 마이크로미터 단위를 가지는 범위 에 분포한다(그림 2.2). 효소 및 다른 분자 수준의 반흥들은 적어도 10 배 이상 작은 크기에서 일어난다• 점토츄卜기물 복합체의 형성과 점토, 미사, 모래 둘이 입단으로 안정 화되는 과정은 대부분 토양의 뚜렷한 구조적 특칭이다. 점토는 입단 형성에서 기본이 된다. 토양학자는 점토 입자를 직경이 2 µm 이하이 고 콜로이드성인 것으로 간주한다. 화학적으로, 콜로이드는 분산과 넓은 표면적을 가지는 특칭이 있다. 점토 입자는 화학자들이 알고 있는 콜로이드성 물질들보다 더 크지만 그 표면적이 넓어서 자연에서 콜로 이드처럼 행동한다. 스멕타이트 smec tit e 같은 점토의 표면적은 대략 점토의 단위 내총i n t erla y er 당 400 ffi 2 g -l 이다. 대부분의 점토는 음전하를 띠고 있다. 미생물들 역시 대부분의 토양 유기물 성분들처럼 중성 p H 에서 음으로 하전된다. 정상적으로는 두 개의 음전하를 띤 단위는 서로를 멀리 할 것이다. 음전하를 띤 단위들 사이의 부착은 다가의 양이온을 통한 이온결합에 의해 가능하다. 결합 손 중의 하나는 미생물이나 유기물에, 다론 하나는 점토에 붙는다. 미 생물의 다당류와 강한 접착성을 가전 가는 섬유질들 또한 토양 입자들 울 서로 묶는다. 많은 열대성 토양들, 특히 화산암에서 유래된 것들은 다양한 전하를 띤 알로패닉(무정형의 알루미늄 규산염)인 점토들이다. 이들 점토는 토양 유기물 성분들을 안정화시키는 데 도움이 되는 철과 알루미늄을 많이 함유하고 있다. 그러한 토양 중 많은 것들은 양호한
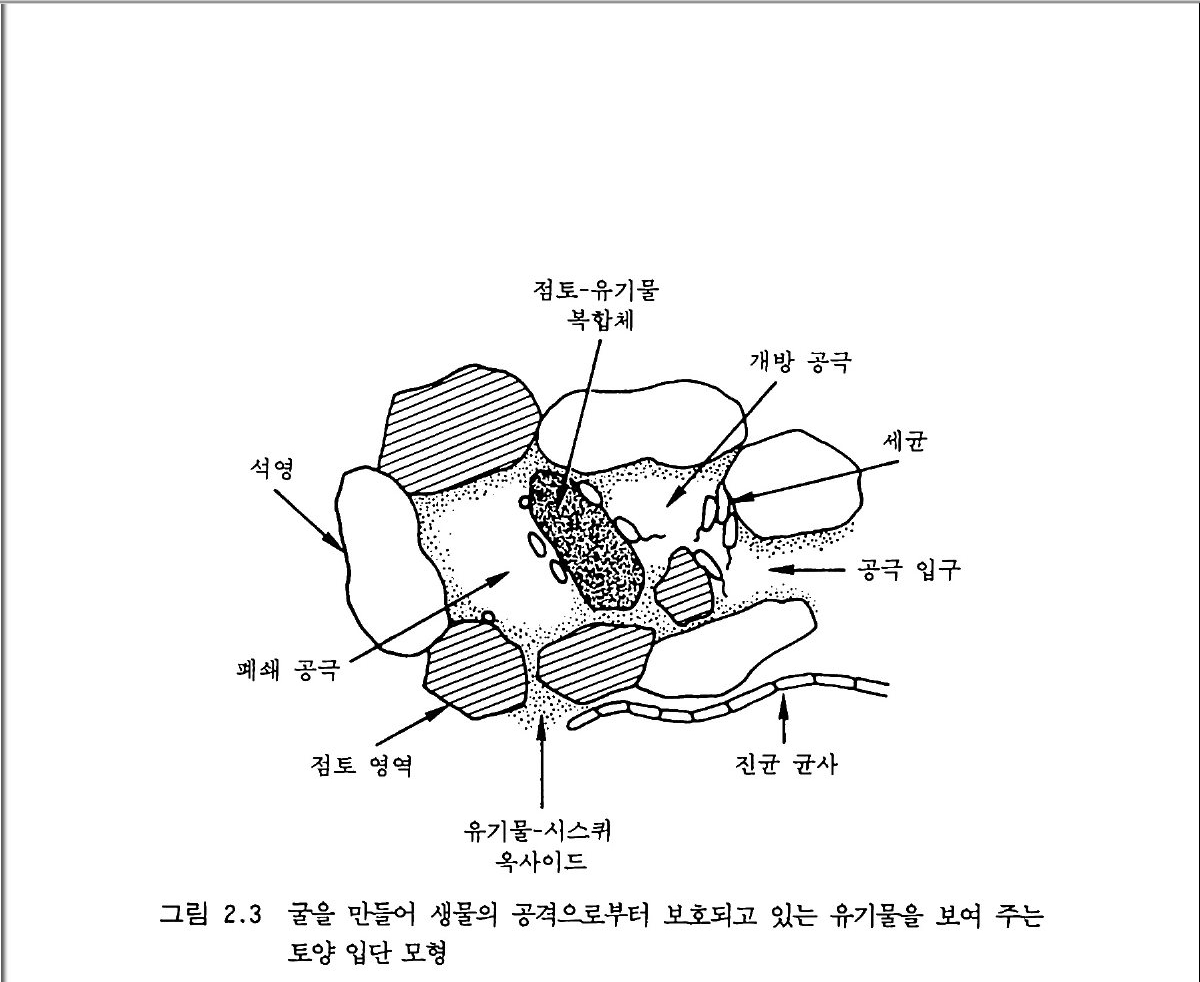
토양 구조를 가지며, 비슷한 기후 조건에서 발달되었으나 알로패닉이 아닌 모재에서 유래된 토양들보다 2 내지 3 배 가량 많은 토양 유기물 함량을보인다. 토양 입단 생성은 미생물의 활동과 토양 유기물 대사회전을 조절하 는 가장 중요한 요소들 중의 하나다. 입단 생성은 접토들을 연결하여 유기물유 L 기물 복합체를 형성하게 히는- 사상체들과 다당류를 마생물 군과 뿌리들이 생산할 때 시작된다. 물리적인 힘 (건조, 수축-팽창, 결 빙-해방 뿌리 성장, 동물 운동, 압축)에 의해 토양 입단이 만들어질 때 토양 구조가 생겨난다. 그림 2.3 은 하나의 입단 안에 있는 미생물들 울 보여 준다. 이 그림은 단순화되어 있고 크기도 다소 차이가 있겠지 만, 토양 공극의 크기가 입자들 간의 거리에 따라 어떻게 달라지는지, 유기물들이 어떻게 보호될 수 있는지를 보여 준다. 입단의 일부를 이 루는 유기물은 미생물과 효소로부터 물리적으로 분리된다면 무기화되 지 않을것이다. 대부분의 미생물들은 입단의 바깥 부분과 입단들 사이에 있는 작은 공국(또는 구멍) 안에 존재한다. 비교적 적은 수가 입단 내부에 거주 한다. 입단 안에 있는 미생물들은 보통 입단이 형성될 때부터 파손될 때까지 그곳에 남아 있게 된다• 전자현미경 사전을 통해 미생물 밀도 롤 계산해 볼 때 미생물이 전체 이용 가능한 공국의 1% 미만을 차지 한다는 것을 알 수 있다• 입단 내부 구멍 입구의 크기에 따라 그 공극 내로 들어올 수 있는 생물 크기, 죽 생물 종류가 결정된다. 어떤 생물 이 들어오느냐는 또한 구멍 안의 수분 함량에 따라서도 달라진다. 직 경이 수 마이크로미터 정도 크기이고 물이 채워져 있는 구명들은 일반 적으로 세균에게 적합하다. 진균은 어느 정도 더 큰 구멍에 들어간다. 구멍의 크기는 동물이 움직일 수 있는 능력을 제한한다. 또 이것은 토 양미생물을 잡아먹는 행위에도 영향을 미친다. 소형 입단 (m ic roa g-
 접토-유기물
접토-유기물
gr e g a t es,50-250µm) 들은 큰 툼새가 있는 대형 입단 (macroa g greg a te , 〉 2mm) 의 하부 단위이다. 대형 입단에 있는 큰 구멍은 미소 동물둘의 피난처를 제공하여, 몸집이 큰 육식동물들로부터 미소동물 울보호한다. 토양 입단과 그 구성 점토는 효소와 기질의 상호작용에 영향을 준 다. 커다란 의부 및 내부 표면적을 가지는 점토 입자는 요소 분해효소 urease 와 단백질 분해효소p ro t ease 같은 효소들을 흡착할 수 있다. 점 토에 홉착된 효소 또는 부식 성분들 humate consti tue nts 3!} 얽혀 있는 효소들은 다론 효소들에 의한 가수분해로부터 보호된다. 흡착은 또한 촉매 부위의 이용도를 감소시킨다. 요소 (NH2CONH2) 와 같은 작은 분자는 요소 분해효소가 있는 지소로 곧장 확산되어 거기서 분해될 수
있다. 단백질과 같은 큰 분자는 단백질 분해효소가 있는 지소로 곧장 확산되지 않으며 결과적으로 요소보다 매우 느린 속도로 분해될 것이 다. 2-3 토양 공기 토양 공기 속에 포함된 주요 기체 형태는 대기에 있는 것들, 즉 N2, 02, CO2 들이다. 때때로 질소 산화물 nit ro g e n oxid e s 같이 생물 활동으로 생겨나는 기체 형태도 존재한다. 이런 기체는 토양 구성 요 소와의 반응성이 매우 높고 생물 활동에 의해 변형되기도 쉽기 때문에 보통 일시적으로 존재한다. 통기가 원활한 토양에서, 02 농도는 iS -20% 이하로 내려가는 경우가 거의 없으며 CO2 는 1-2% 이상으 로 울라가는 경우가 거의 없다. 그러나 접토질 토성과 높은 수분 함량 울 가지면서 미생물 활동이 활발할 때 토양 공기의 CO2 농도는 10% 에 달하기도한다. 토양에서 공기의 확산은 다음과 같이 기체의 운동을 토양의 특성, 토양에서 기체의 농도 및 깊이와 관련시키는 F ic k 의 법칙에 따라 설 명될 수 있다.
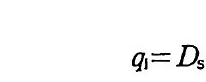 q, =Dsa,I 뚤
q, =Dsa,I 뚤
여기서 q 1 는 기체의 확산 속도(g cm-2 sec-1), D. a.1 는 토양에서 확산 상수 (cm2 sec -1) , c1 는 토양 공기에서 기체의 농도(g cm-3), z 는 깊 이 (cm) 를 나타낸다. 물에서 기체 용해도는 기체의 종류, 온도, 영류의 농도, 대기에서
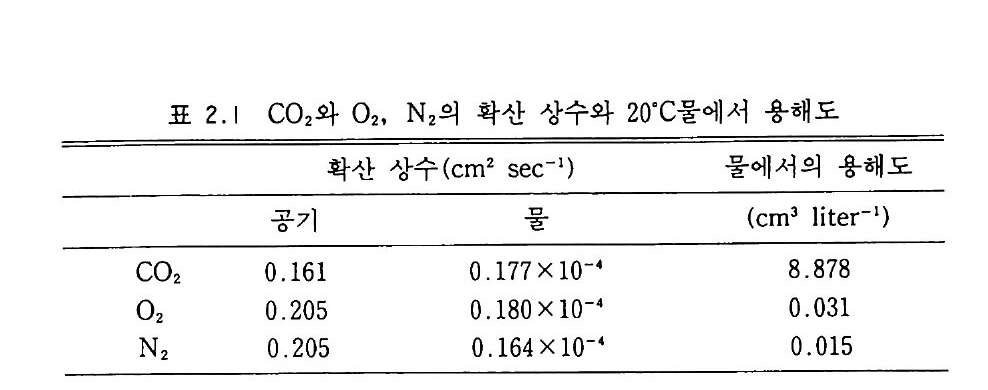 표 2.1 CO2 와 02, N 2 의 확산 상수와 2o·c 물에서 용해도
표 2.1 CO2 와 02, N 2 의 확산 상수와 2o·c 물에서 용해도
그 기체의 분압에 따라 달라진다. 가장 용해되기 쉬운 기체는 물에서 이온화되는 것으로, 예를 들면 CO2, NH3, H2S 들이다. 산소는 매 우 낮은 용해도를 가지며, 질소 기체의 용해도는 더욱 낮다(표 2.1). 대기의 80% 가 N 저지만 물에서 N2 는 매우 낮은 확산속도를 가지기 때문에 질소고정에 있어 제한 요인이 될 수 있다. 통기가 잘 되지 않 는 지소에서 N 려 낮은 확산속도는 또 아세틸렌 (C2H2) 환원 기법을 이용하여 질소고정을 측정할 때 영향을 준다. C2H2 는 물에 용해되기 쉽기 때문에 같은 토심에서 N2 보다 훨씬 이용도가 높다. 따라서 반응 속도의 지표로서 C2H2 환원을 사용할 때 N2 고정을 실제보다 높게 예측하는 오류를 초래할 수 있다. 벼와 습지식물들과 같은 어떤 삭물 들은 공기를 물에 참겨 있는 토양 저층으로 확산시킬 수 있는 특수한 뿌리 통로를 가전다. 벼는 보리보다 토양 저층으로의 공기 확산을 4 배 나 크게 한다. 그리하여 물에 참겨 있는 조건에서 형기성이 될 수밖에 없는 뿌리 주변을 호기성 미세지소로 만든다. 토양에서 통기 정도는 물의 함량에 의해서 추정될 수 있다. 무기입 자들은 보통 2.65g cm-3 의 비중을 가진다. 표면 토양의 용적밀도 bulk dens ity는 일반적으로 0.9-l. 3g cm-3 에 이른다. 그러므로 무기 토양은 보통 50-60% 부피의 공극을 갖는다고 할 수 있다. -0.01 메 가파스칼 (meg a p a scals, MPa) , 죽 포장 용수량 fiel d ca p a cit쩌 1 서 토
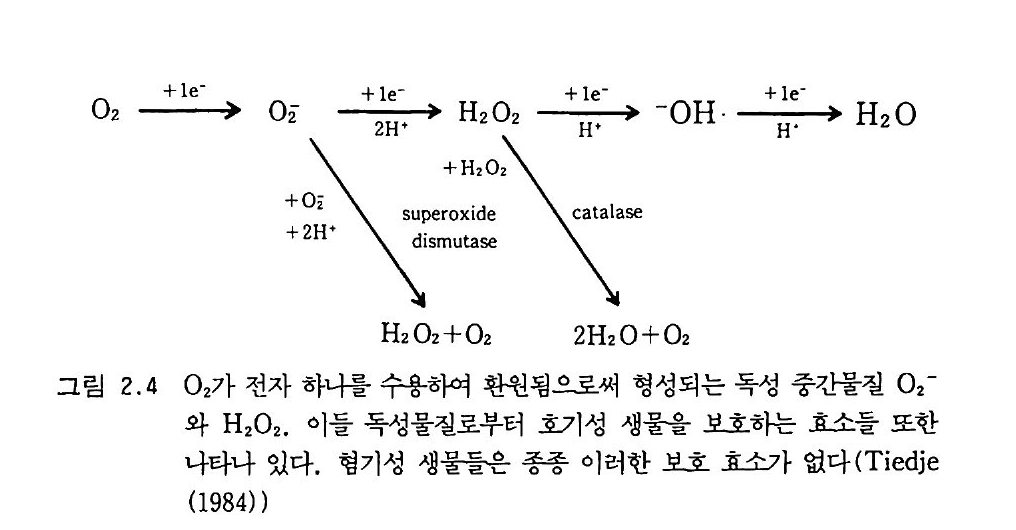
양 수분 함량은 사질 양토 sand y loam 려 경우 15-30%, 점토질 토양 의 경우 40-50% 정도이다. 전체 공극량과 수분 함량의 차이만큼이 공기로 채워진 공간이라 할 수 있다. 최소한 부피 10% 를 공기가 차 지할 때 보통 적당한 통기라고 여겨진다. 45% 의 물을 함유한 점토질 토양은, 용적 밀도가 1. 3 이고 총 공국률 tot a l p oros ity이 50 % 에 불과 하다면 통기에 충분한 공간을 가지지 못할 것이다. 호기성에서 협기성 대사과정으로 전환은 1 % 미만의 02 농도에서 일어나는 것으로 확인되고 있다. 토양 전체의 통기는 흙덩이 하나 하 나와 입단의 통기만큼 중요하지 않다. 반경이 3mm 보다 크고 물이 포화된 흙덩이는 중심부에 02 가 없는 것으로 계산된다 (Harr i s (1981)). 탈질화 작용과 황산염 환원과 같은 형기성 과정들이 많은 토 양에서 일어난디는 사실은 형기성 미세지소들이 매우 혼하게 생긴다는 것을 시사한다. 형기성 미세지소들이 존재한다는 것은 토양의 상층부 에 클로스트리디움 같은 형기성 세균이 흔히 나타난다는 점에서도 유 추될 수 있다. 토양의 상충 수 센티미터에 있는 형기성 세균의 개체군 수는 더 깊은 곳에서보다 10 배 정도나 더 많을 수 있다는 것이 몇몇 연구에서 나타나고 있다. 호기성 세균은 형기성 세균들을 위한 환경을 만들어 주는 역할을 한다. 미세지소 안에서 호기성 세균의 초기 성장 은 거기에 저장된 02 를 소모하며, 따라서 형기성 미생물의 발달을 허 용하게 된다. 형기성 미생물은 02 가 없는 상태에서 에너지를 생성시키고 성장할 수 있는 능력을 가지고 있다. 어떤 생물(절대적 형기성 생물, obli ga te anaerobes) 은 산소가 존재할 때 그 독성으로 죽는다. 이와 갇은 저해 작용은 그립 2.4 에서 보는 바와 같이 독성 중간물질의 생산 때문에 일 어난다. 야에 민감하지 않은 생물들은 독성 중간물질을 제거하는 효 소들 (su pe rox i dase and/or ca t alase) 을 함유한다. 독성 중간물질들은
 02 ~+ le- _ ^_ + le- -- -+• ·le-- -_ -_~ _ + le-
02 ~+ le- _ ^_ + le- -- -+• ·le-- -_ -_~ _ + le-
전자 전달 동안에 생산되기 때문에 저해 작용은 전자공여체 (음식물의 공급)가 있을 때만 나타난다. 절대적 형기성 생물들은 성장을 위한 적 당한 기질이 없으면 호기성 토양 환경에서도 오랜 기간 견뎌낼 수 있 다. 토양에서 이런 경우는 흔히 있다. 어떤 토양생물들은 오랜 지질학적 기간에 토양 공기 내의 높은 CO2 농도에 적응하게 되었다. 어떤 진균종들은 10-20cm 의 토양 깊이를 선호한다. 질산균도 지면의 농도보다 더 높은 CO2 수준을 좋아하는 종이다. 밀폐된 용기에서 공기의 CO2 를 실험적으로 조절하여 질산화 작용을 보았을 때 토양에 존재하는 CO2 수준인 0.07-0.€3% CO2 의 경우에 비해 대기 수준의 CO2 농도인 0.035% 에서 질산화 작용은 거 의 일어나지 않았다. 지표 가까이에 지하수면이 있는 토양에서 CO2 농도를 수직적으로 보면 뿌리가 존재하고 미생물 호홉이 일어나는 지표 부근에서 가장 높 다. 뿌리 호흡은 토양에서 생기는 CO2 의 20-50 %를 공급한다(표 2.2). 그 나머지 50-80% 에 이르는 더 큰 몫이 미생물에 의한 것임을 알 수 있다. 동결되거나 건조되어 있는 토양과 같이 호흡 활동이 없는
 표 2.2 토양 호홉에서 뿌리 호흡의 기여도
표 2.2 토양 호홉에서 뿌리 호흡의 기여도
경우에 토양 기체의 농도는 대기와 평형을 이룬다. 토양에서 과잉의 물은, 산소가 토양 안에서 또는 토양을 통과해서 이동하는 것을 방해하여 미생물이 요구하는 산소량을 충족시키지 못하 게 만들어서 미생물과 그들의 활동을 제한한다. 경작지 토양에서 흔히 나타니는 정도의 토양수 함량일 때는 산소가 주로 확산에 의해 대기로 부터 토양으로 이동한다. 02 를 토양 속으로 이동시키는 데 필요한 기 체의 압력차는 단지 1-3% 정도이다. 따라서 경작지 토양의 02 함량 은 18-20% 수준 아래로 내려가지 않는다. 마찬가지로 토양 속의 호 홉에 의해 CO2 수준이 1 내지 3% 에 다다르기만 하면, 충분히 큰 농 도 구배가 형성되어 이산화탄소는 대기로 (0.035% CO2) 이동한다. 관 개수가 공급되거나 호우에 의해 토양 표면이 물에 완전히 참기는 경우 토양과 대기 사이의 기체의 이동은 거의 멈춘다. 02 는 물에서보다 콩 기에서 거의 10,000 배나 빨리 확산되기 때문에 그것은 놀리운- 일이 아니다. 미생물 활동은 토양 표면이 물에 참김에 따라 바로 감소되지 않고 토양 표면 아래 가둬져 저장되어 있던 산소가 고갈된 후에야 감 소된다. 이 산소 저장소의 크기와 얼마나 오랫동안 식물 뿌리 및 미생 물의 호흡이 적당한 상태로 지속될 수 있느냐는 토양 공극, 토양 공기 에서 02 의 함량, 지하수면까지의 깊이, 그리고 식물 뿌리와 미생물에 의한 야 서용 속도에 대한 지식으로 계산될 수 있다.
2-4 토양수 토양수는 생물이 이용할 수 있는 수분뿐만 아니라 토양의 통기 상 태, 가용성 물질들의 질과 양, 삼두압, 토양 용액의 p H 에 영향을 미 친다. HOH 각도가 105° 인 물 분자의 모양 때문에 산소에는 음의 성 질을, 수소에는 양의 성질을 가진다. 이것은 물리화학적 반응들과 관 련된 물분자의 특성을 많은 부분 설명한다. 이것은 왜 물이 전하를 띤 이온들을 잡아당기는지 설명한다. Na+, K+, Ca2+ 같은 양이온들은 물분자의 음전하를 띤 산소 끝에 끌리기 때문에 수화된다. 물의 극성 은 물에 의해서 왜 수소결합이 형성되는지 설명한다. 각 물분·자의 다 른 물분자와 또는 다른 생물학적 구성 요소들과의 결합이 수용액의 특 성들, 점도, 높은 비열을 설명한다(그림 2.5). 물이 수소결합과 양극 성의 상호작용에 의해서 강하게 표면에 흡착된다는 사실은 토양계에서 와 마찬가지로 미생물 세포 내에서도 특히 중대한 의미를 가진다. 홉 착된 얇은 수막은 0°C 에서 얼지 않은 채로 남아 있고, 가열하여 그것 을 제거하고자 할 때는 105°C 까지 요구된다. 이 결합수는 결합되어 있지 않은 물과 상당히 다른 특성을 가전다. • 토양수의 특성에 대해서 현재 인정되고 있는 용어들은 매트릭 퍼텐 셜과 삼투력 개념에 기초를 두고 있다. 매트릭 퍼텐셜은 위에서 기술 한 바와 같이 고체의 표면에 대해 물이 끌리는 특성에 기인한다. 이것 은 물의 자유에너지를 감소시키기 때문에 매트릭 퍼텐셜은 음의 값을 가진다. 수용액의 특성 때문에 토양에서 용질들은 역시 물의 자유에너 지를 감소시키며 다른 음의 퍼텐셜울 일으키는데 이것이 삼투력이다. 토양수 퍼텐셜 개념은 파스칼 pa scals.£ . 표현된다(보통 메가파스칼로 쓴 다)• 토양수는 보통 세 가지 형태로 존재하는 것으로- 기술된다. 그것은
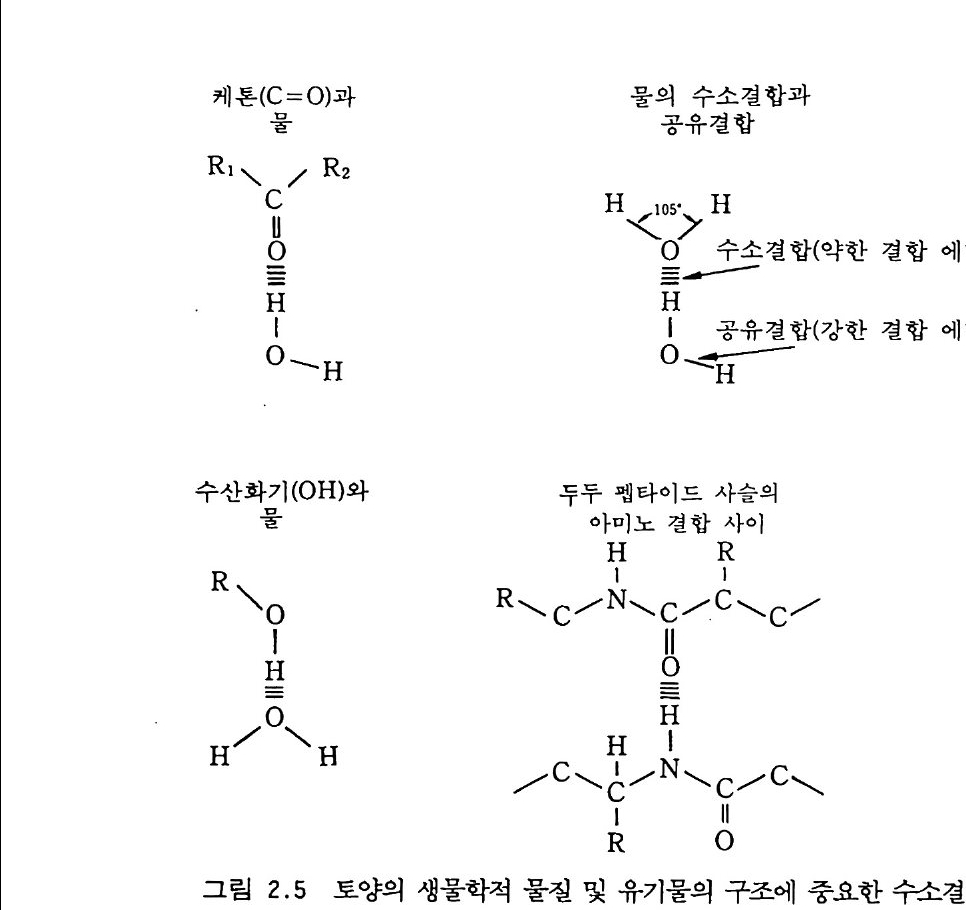 R케 돈\I,. c 물 = [이R과2/ H 물의공 유수결소합결 합과
R케 돈\I,. c 물 = [이R과2/ H 물의공 유수결소합결 합과
중 력 수 grav it at i on al wa t er 와, 모 세 관 수 cap illar y wate r , 홉 습 수 hy d roscop ic wa t er 이다. 첫 두 용어는 주로 용어 그 자체가 의미를 설명한다. 중력수는 중력에 의해서 토양을 통하여 배수된다. 이것은 관개하거나 호우가 지나간 다음 일어날 것이다. 중력수가 빠져 나간 바로 직후의 토양수를 포장 용수량이라고 한다. 이 때에도 미세 또는 모세 공극 (m ic ro-, 또는 cap illay po re) 둘은 여전히 식물과 미생물의 생장에 이용 가능한 물로 채워져 있다. 이 물의 매트릭 퍼텐셜은 -0 . 01 과 0.03MPa 사이에 있을 것이다. 증발 또는 중산에 의해서
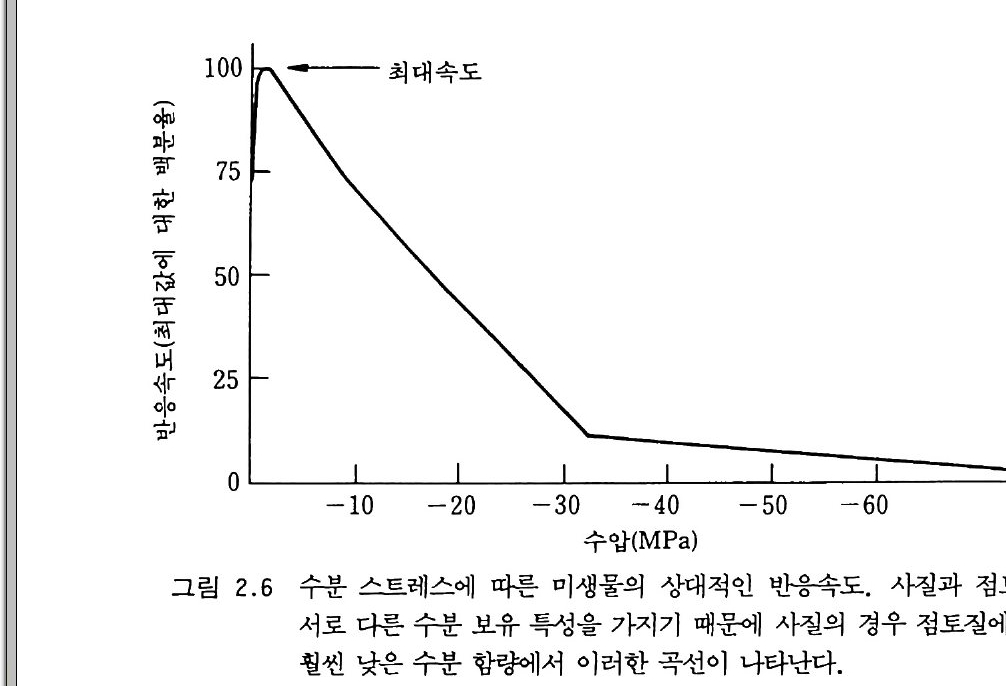
이러한 물이 토양으로부터 손실되어 많이 부족해지면 식물은 밤과 낮 에 모두 팽팽한 상태를 유지할 수 없고 시들게 될 것이다. 이것은 보 통 —1.5 MPa 정도에서 일어나는데 위조점 (姿測點, wi llting p o i n t)이 라고한다. 홉습수논높은상대습도를가지는대기로부터 건조한토양 에 흡수되는 물, 공기 중에서 말린 토양 속에 남아 있는 물, 또는 특 정 상대습도 (RH) 와 온도(보통 98% RH 와 25°C) 에서 평형을 이루고 있을 때 토양에 의해 보유되고 있는 수분 등 여러 가지로 정의된다. 이제 이 세 가지 정의는― __ 용어 p E( 토양수의 장력t ens i o 퍼全 수주 높 이의 센티미터로 표현하고 그것의 로그값을 취한 것)가 구식인 것처럼 ―구식이 되었다. 매트릭 퍼텐셜로 토양수의 이용도를 표현하는 것 이 이룰 반복하여 측정할 수 있고 과학적이기 때문에 훨씬 더 유용한 개념 0] 다. 토양수의 매트릭 퍼텐셜과 삼투력의 합은 생물이 물을 얻기 위해서 거슬러 이겨내야 하는 스트레스이다. 일반적으로 토양에서 미생물 활 동은 -O . OlMPa 에서 최적이고 토양이 물에 참겨 뼈 퍼텐셜에 가까 워지거나 반대로 더욱 건조해져 더 큰 음의 퍼텐셜을 갸지는 값이 됨 에 따라서 미생물 활동은 감소한다(그립 2.6). 그림 2. 6-의 곡선은 분 해 반응에 집합적으로 참여하는 토양미생물의 반응속도를 최대값에 대 한 백분율로 나타낸 것이다. 이것은 다른 생물 그룹이나 그룹 내의 각 종에 대해서도 일률적으로 적용되는 것은 아니다. 전균은 일반적으로 세균보다 높은 수분 퍼텐셜 (더 큰 수분 결핍 스트레스)에서 견뎌낸다. 표 2. 었본 각 미생물들이 견뎌낼 수 있는 수분 퍼텐셜 mois t u r e p o t en ti al 의 상한선을 나타낸다. N£tr o somon a,s 같이 전형적인 질산화 균은 Clos tri d i um 과 Pen£c i!Uu m 같이 전형적인 암모니아화 세균보 다 스트레스에 약하다. 때때로 건조한 토양의 표면충에서 관찰되는 N03- 의 높은 함량은 질산화작용 때문이 아니라 N03- 를 포함한 모세
 : 100
: 100
관수의 상승 때문일 것이다. 토양 표면에서 물이 증발되면서 N03- 가 남게된다. 물은 영양 물질의 확산과 질량 흐름 mass flow , 농도에 영향을 미쳐 미생물과 식물 모두에 영향을 준다. 수분이 많아 수분 자체가 제한 요
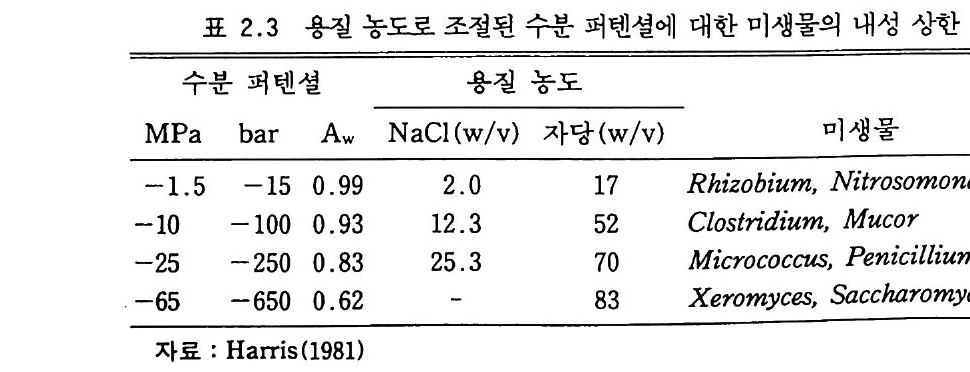 표 2.3 용질 농도로 조절된 수분 퍼텐셜에 대한 미생물의 내성 상한
표 2.3 용질 농도로 조절된 수분 퍼텐셜에 대한 미생물의 내성 상한
인이 아닌 경우에 영양 물질의 확산이 매우 느려 제한 요소가 될 수 있다. 질량 흐름에 의해 N03-같 은 영양 물질은 적절히 식물 뿌리에 공급된다. 그러나 인은 물과 함께 바로 이동되지 않는다. 안이 흡수되 기 위해서는 확산과 뿌리의 확장이 필요하다. 2-5 산화환원 전위 산화환원 반응은 토양의 화학적 • 생물학적 현상을 설명하는 데 중대 한 의미를 가지며, 토양생물을 조절하는 요~ 대한 이러한 개관에 서 다루는 정도보다 훨씬 더 상세히 연구되어야 한다. 다음의 짧은 설 명은 생물학적 부분을 강조한다. 더욱 상세한 정보를 얻기 위해서는 이 장의 마지막에 제안된 부가적인 문헌들이 참조되어야 할 것이다. 산화-환원 반응에 대한 포괄적인 논의는 S t umm 과 Mor g an (1 981) 의 책에 있다. 생물은 환원되어 있는 물질을 산화하는 과정에서 에너지를 얻는다. 죽 생물은 산화반응 동안 생기는 이용가능한 에너지를 포착하기 위해 서 유기물 또는 무기물로부터 전자를 떼어낸다. 이것은 수많은 중간 반응을 포함하는 일련의 반응 단계에서 수행된다. 환원된 화합물로부 터 나온 전자들은 일련의 구성 요소들로 이루어져 있는 호홉 또는 전 자전달계를 따라 움직인다. 기질로부터 최종 전자 수용체인 02 까지 전자를옮겨갈수있는전달계를그림 2.7 에 나타냈다. 0 가 이용될 수 없는 경우에, 생물이 적절한 효소계를 가지면 No3-, Fe3+, Mn2+ , SO/ 가 전쟈뮤용체로서 작용한다. 그림 2.7 은 전자전 달계의 방향성이 좌우대칭이 아니어서 전자와 양자의 이동이 분리되는 것을 보여 준다. 양자들은 막 밖으로 나간다. 전자가 결국엔 02 에 전
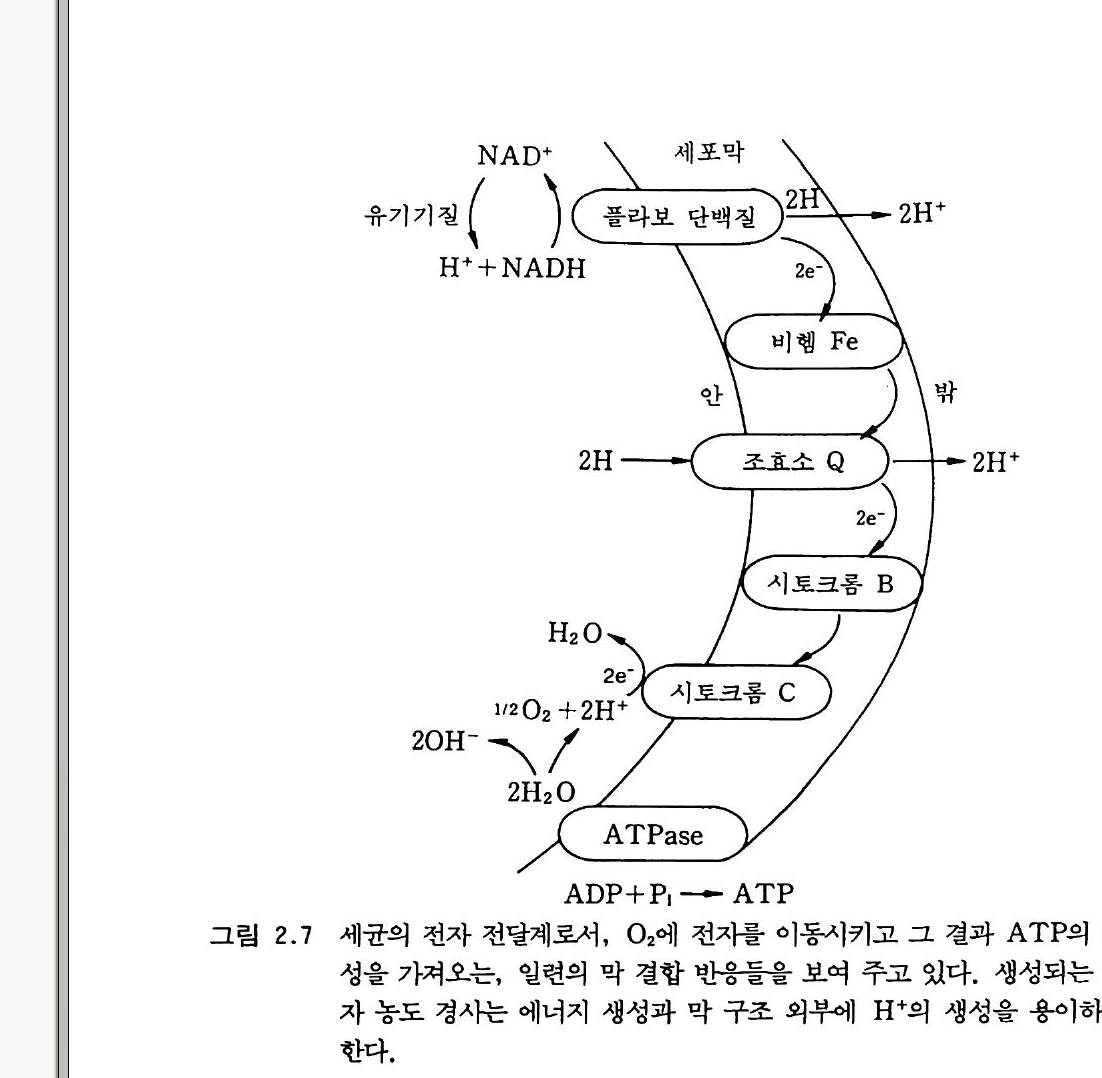 NAD+ \ 세포막
NAD+ \ 세포막
달되어서 막의 내부에서 OH- 를 형성한다. 의부의 H+ 와 내부의 OH - 는 자유로이 막을 통과할 수 없기 때문에 pH 구배와 전기적인 퍼텐셜이 그 막을 사이에 두고 형성된다. 이 양자에 의해서 기인된 힘 은 능동적 수송, 편모충의 편모운동 같은 일을 할 수 있고, ATPase 에 의해 ATP 를 생성함으로써 에너지롤 만드는 데 사용된다. 산과 영기를 각각 양자 공여체, 양자 수용체라고 말하는 것처럼 환
원제와 산화제는 각각 전자 공여체, 전자 수용체라고 정의한다. 음전 하를 띤 전자는 e 또는 e- 로 표시할 수 있는데, 산화 또는 환원 반응 중 하나에 참여한다. 산화제란 다음과 감이 자신은 환원되고(전자를 받고) 산화반응을 일으킬 수 있는 물질이다.
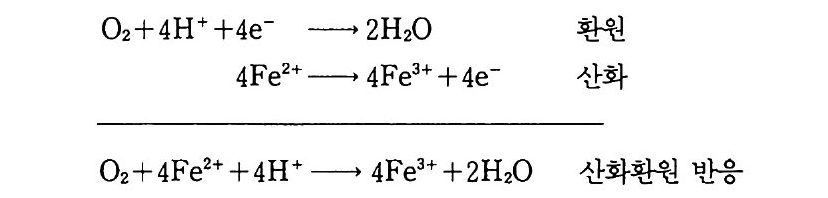 02+4H++4e- 一 2H20 忠
02+4H++4e- 一 2H20 忠
산화-환원 전위의 고전적인 표현은 볼트 vol t를 단위로 하는 용어 & 사용과 관련된다. 지금은 P은 개념이 Eh 를 대신하고 있다. pH =
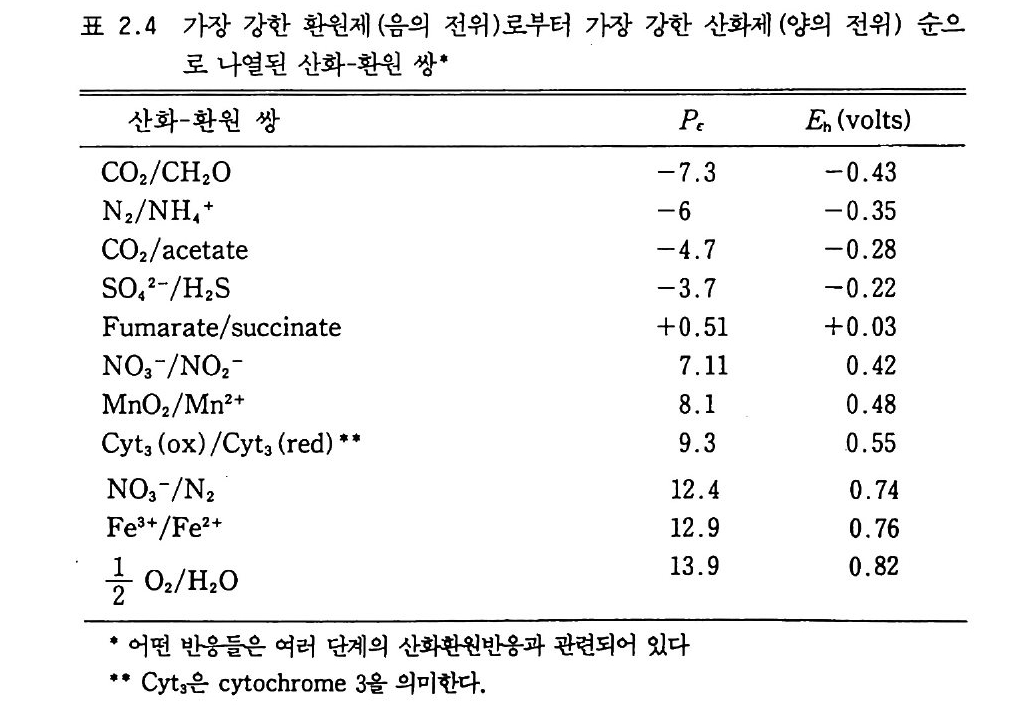 표 2 . 4 가장 강한 환원제 (음의 전위 )로부터 가장 강한 산화제 (양의 전위 ) 순으
표 2 . 4 가장 강한 환원제 (음의 전위 )로부터 가장 강한 산화제 (양의 전위 ) 순으
-log [H 기인 것처럼, 산화환원 전위의 세기는 P£ = -log [e 기라고 할 수 있다. 높은 R 값은 산화시키기 쉬운, 죽 전자를 받아들이기 쉬운 경향을 가리킨다. 산화환원 전위를 표현하는 고전적인 방법인 됴 는 R 은 Pr=Eh.(vol t s)/0.059 라는 관계가 있다. 2s·c, pH 7 에서 광합성부터 분해에 이르는 많은 중요한 생물학적인 반응들의 R 값을 표 2 . 4 에서 보여 준다. 전자 공여체와 최종 수용체 사이의 전위 차이 가 크면 클수록, 생물계에 의해서 에너지가 포착될 가능성이 크다. 2-6 토양 pH 세계의 도처에서 토양은 영양 물질을 포함히는- 있는 비료의 과다 사 용과 산성비로 인해 지나치게 산성화되어 있으며 접점 악화되고 있다. 생물적 질소고정 역시 고정 과정 동안 H+ 를 생산함으로써 토양 산도 를 증가시킨다. 토양 p H 의 측정은 미생물 반응을 뒷받침할 수 있는 토양 능력을 예측하는 데 중요한 기준이 된다. 토양 용액의 pH 측정 은 용이하다. 그러나 음전하를 띤 점토질은 그들을 잡아당기는 양전하 를 띤 이온(양이온)충을 가전다. 점토질이나 음전하를 띠는 유기 입자 를 둘러싸고 있는 이중막 내에는 양이온 농도가 증가되어 있기 때문에 아러한 표면에서 p H 는 토양 용액에서 보다 수 배나 높은 산성일 수 있다. NH4+ 에서 N03- 로 생물학적인 변환(질산화 반응)은 p H에 가장 예 민한 반응 중의 하나이다. 이중막 이론으로 설명되는 pH 차이의 개 념은 질산화 반응에 최적인 p H 나 최소한의 p H 가 왜 실험실 용액과 토양에서 서로 다른지 그 이유를 설명하는 데 사용되고 있다. 질산화 반응이 배양용액에서는 pH 6 이하에서 일어나지 않는 반면, 삼림토양
에서 질산화 과정은 pH 4 이하에서도 일어날 수 있다. 이 수수께끼 는 질소가 풍부한 물질이 분해되는 미세지소가 토양에서 만들어지기 때문인 것으로 설명될 수 있다. 암모니아의 분비는 미세지소 내의 p H 를 토양 용액의 p H 보다 더 높게 만든다. 더 일반적으로 받아들여 지고 있는 또 디론 설명은 산성 토양에서 질산화 작용은 독립영양 질 산균 auto t r o p h ic n it r ifi er~ 다 산도에 내 성 이 큰 종속영 양 질산균에 의해서 일어난다는 것이다. 특수한 지소에서 pH 값에 대한 개념은 미생물의 크기와 미생물 수 준에서 나타니는 효소의 다중성 the multip li c i t y of enzy me g: i!} 관련시 켜야 한다. 하나의 세균 세포는 약 1000 종류의 효소를 가지고 있다. 이 중 많은 것이 pH 의존적이고 세포막과 같은 세포 구성 물질에 붙 어 있다. 효소의 최적 p H 는 흡착 현상에 의해서 영향을 받는다. 토 양 매체에서 토양 부식산에 효소가 흡착 adsor pti on 되면 최적 p H 는 더 높아진다. 경계와 분자의 p H 에 대한 보다 더 잘 이해하게 되고 그 값 울 측정할 수 있기 전까지는 토양미생물학자들은 전통적인 토양 반죽 방법으로 측정되는 p H 에 만족해야만 한다. 이 전통적인 방법은 CaCI2 용액을 토양에 첨가한 후 적당한 전극으로 용액의 p H 를 측정하 는것이다. 2-7 토양 온도 온도는 세포의 생리적인 반응 속도뿐만 아니라 환경의 물리화학적인 특성들 대부분에 영향을 미친다. 이러한 특성의 예로는 토양 부피, 압 력, 산화환원 전위, 확산, 브라운 운동, 점성, 표면장력, 물의 구조 등을 들 수 있다. 다른 생물들과 마찬가지로 미생물 세포의 활동은 열
역학 법칙에 따른다. 그러므로 온도 변화가 미생물 활동에 뚜렷한 영 향을 주는 것은 놀랄 일이 아니다. 화학 반응 속도는 직접적으로 온도와 관련된 함수이며 일반적으로 Arrhen i u 예 의해서 처음으로 기술된 관계를 따른다.
 k=Ae-EtR T
k=Ae-EtR T
여기서 k 는 반응속도 상수, A 는 분자들이 충돌하는 빈도, E 는 반 웅의 활성화 에너지, R 은 기체 상수, 底근 자연로그의 밀, T 는 kelvin s 단위로 표현되는 온도 (K) 이다. 이 식은 아래와 같이 쓸 수 있다.
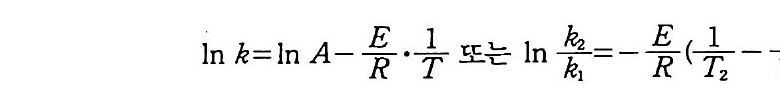 In k= ln A-jE- ·yl 또는 In -%t= -jE- (-1j 广 T1- )
In k= ln A-jE- ·yl 또는 In -%t= -jE- (-1j 广 T1- )
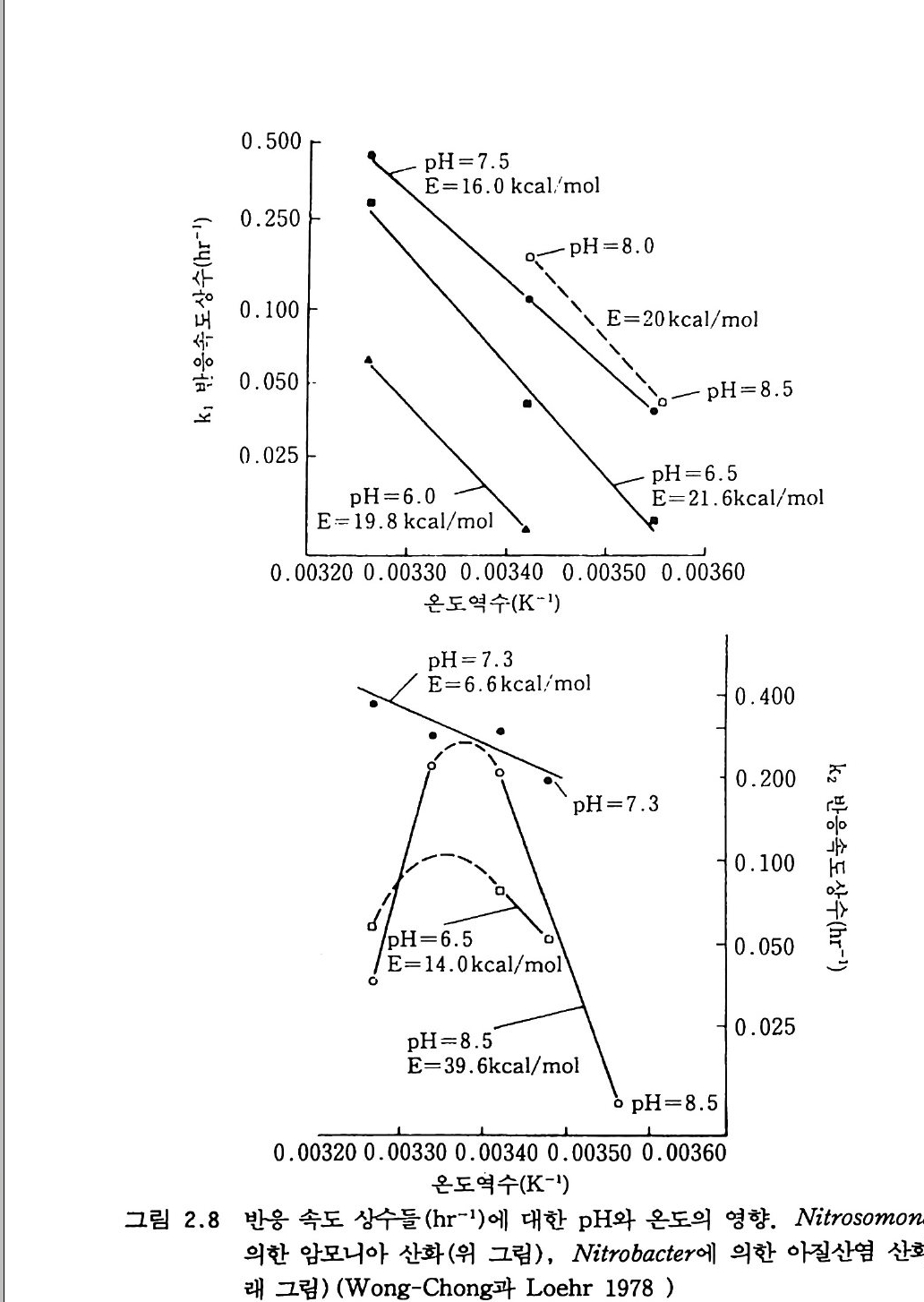
극단적이 아닌 온도 범위 내에서, kelvin s .£ 표시된 온도의 역수에 대해서 반응 속도 상수의 자연로그 값을 그래프로 그리면 기울기가 -E/R, y좌표의 절편이 In A 인 직선이 나온다(이 부분은 원서에서 찰 못된 것을 옮긴이들이 바로 잡았다 : 옮긴이). 기울기에 상수· R 을 곱하면 반웅이 진행됨에 따라서 극복되어야 할 에너지 언덕 (활성화 에너지)이 된다. 그림 2 . 앉곤 Ni t rosomoas 에 의한 NH+ 의 산화와 Ni trob acte r 에 의한 N02_ 산화의 반응속도 상수들에 대한 온도와 p H 의 영향을 보여 준다. 양 끝의 극단적인 온도에서 곡선은 갑작스럽게 떨어전다. 고온에서 갑자기 나타나는 성장 쇠퇴는 온도에 의한 단백질 자연 구조 의 변질과 세포막 투과성의 변화 때문에 일어난다. 성장에 있어 온도 상한은 이러한 파괴적인 힘들이 압도적이 되는 온도이다. 이 온도는 최적 온도에 비해 수 kelvin s 정도밖에 높지 않은 것이 보통이다. p H 와 함께 온도 반웅의 상호작용은 그립 2.8 에서 보여 주는 바와 같 이, 왜 N02- 를 산화하는 Ni t robac t er 가 NH,+ 를 산화하는
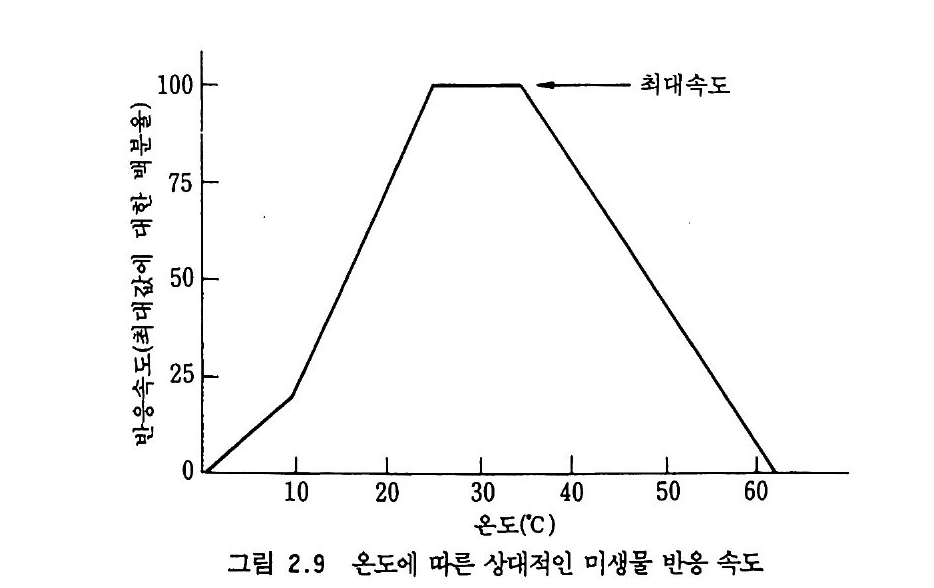
Ni t rosomon (lS보다 환경 조건에 매우 예민한가를 설명한다. N it rosomon (lS는 모든 pH 값에서 온도에 대해 넓으면서 선형적인 반 응울 보여 준다. 반면에 N it robac t er 는 pH 7 . 3 에서만 선형적인 반옹 울보인다. 열에 대한 내성 기작은 효소와 세포 구조물들의 열 변성에 대한 동 역학적 연구에 의해서 밝혀지고 있다. 고온성 the rmop h il ic 세균의 편 모와 리보좀 같은 특수한 단백질은 중온성 meso p h ili c 세균의 그것들보 다 열에 더욱 안정하다. 낮은 온도에서도 활동할 수 있는 미생물의 능력을 조절하는 요소들 또한 세포 구조물과 관련된다. 낮은 온도에서 모든 단백질은 삼차원 구조를 조절하는 화학 결합들이 약화되어 가벼운 구조적인 변화가 일 어난다. 단백질의 모양은 단백질의 유전자 부호를 결정하는 리보좀 같 은 물질에서 가장 중요하기 때문에 보통 세포의 내한성을 증가시키는 변이는 단백질 생산을 위해 유전자 부호를 결정하는 과정에서 일어난 다. 지질의 용융점은 포화지방산 함량과 직접적인 관계가 있다. 죽 세 포막에 있는 지질의 지방산 포화 정도가 주어진 온도에서 유동성을 결 정한다. 세포막의 기능은 유동성에 의존하기 때문에 낮은 온도에서 성 장은 지방산의 불포화도가 증가됨으로써 더욱 용이해진다. 온도에 따른 미생물 활동을 측정한 대부분의 결과는 o·c 에서 성장 이 멈추는 것을 보여 준다. 어떤 저온성 세균은 주변 용액 또는 자체 세포 구성 요소들의 삼두 농도를 충분히 높여서 세포 내부가 얼지 않 도록 함으로써 빙점 이하에서도 생장할 수 있다. 미생물 활동에 대한 일반화된 온도 반응 곡선은 그립 2.9 에서 보여 준다. 10·c 에서 반응 이 갑자기 변화되고 25°C 에서 35°C 사이에서는 반응 속도가 변하지 않는다. 각 종마다 최적 온도가 다르지만 온도 반응 곡선의 일반적인 모양은 많은 생물들에 대해서 아주 비슷하다. 한 생물에 있어 이미 성
 0.5 0 0
0.5 0 0
장이 시작된 다음 계속 성장을 지속할 수 있는 최소 온도는 이제 막 성장을 시작한 경우의 최소 온도보다 약간 더 낮울 것이다. 그래서 성 장 초기의 내성 하한 온도에서 미생물들은 많은 양이 접종 i noculum 된 다면 성장을 하겠지만 적은 양아 접종된다면 성장을 하지 못할 것아 다. 상층부의 온도가 일정하게 유지되는 토양은 거의 없다. 온도 변화는 계절에 따라, 하루의 시간에 따라 일어난다. 물의 비열이 높기 때문에 젖은 토양은 마른 토양보다 하루 동안 온도 변화가 작다. 태양열의 강 도와 반사에 영향을 주는 요소들 중에는 토양의 방위 (남 또는 북의 경 사 방향 등), 경사도, 음영 정도, 지표를 덮은 상태 (식생, 깔짚) 등이 있다. 1 일 동안의 온도 변화는 토양 깊이에 따라 작아진다. 한여름 주 어전 지소의 깊이 5, 10, 30 cm 에서 온도는 각각 15-18°C, 8-10°C 그리고 1-2·0 키 변동을 보였다.
 l 00-75 5025 0
l 00-75 5025 0
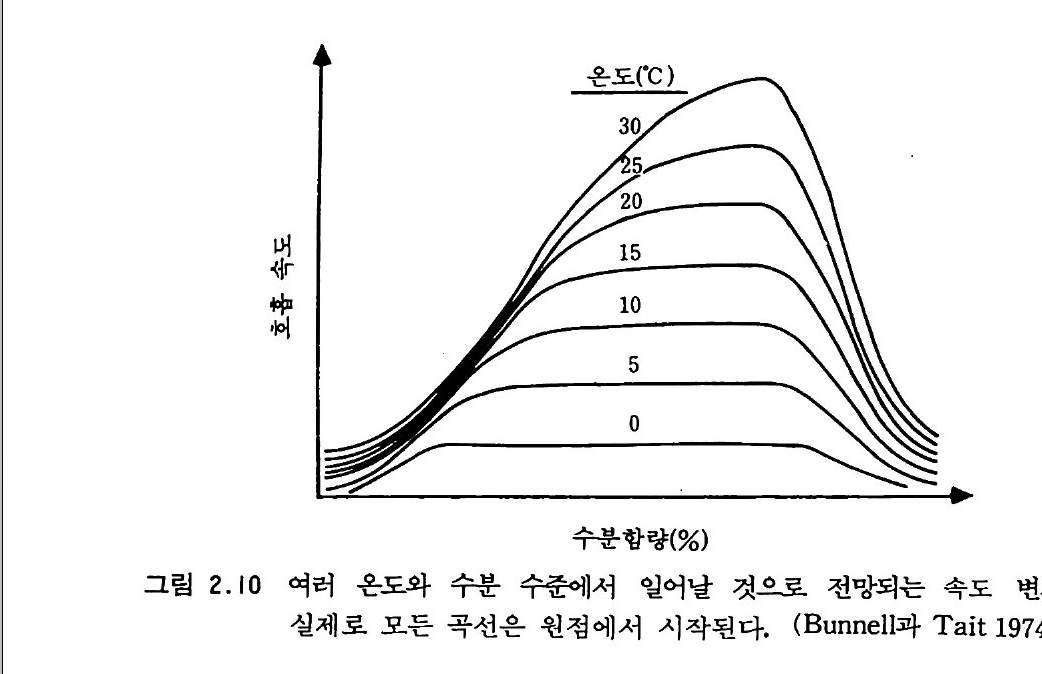
2-8 환경 요인들의 상호작용 온도, 수분, 토양 pH , 통기 정도, 산화-환원 전위, 토양형을 포함 하는 상호작용들에 대한 해석은 쉽지 않다. 자연에서 스트레스 요소들 이 서로 독립적인 경우는 거의 없다. 컴퓨터 모형 기법만이 모든 상호 작용에 대한 설명을 시도할 수 있다. 그림 2.1Q .g. 온도와 수분에 따 른 호흡 속도를 컴퓨터로 계산하여 그림으로 나타낸 것이다. 표 2 . 앉큰 여러 가지 스트레스 요소에 대한 미생물 적응 방식을 요약한 것이다.
 버
버
 표 2.5 스트레스 조건이 미생물에 미치는 영향과 유도된 생화학적인 적응
표 2.5 스트레스 조건이 미생물에 미치는 영향과 유도된 생화학적인 적응
참고문헌 Bunnell., F. L., and Tait, D. E. N. (19 74) . Math e mati ca l sim ulati on models of decomp o sit ion pro cesses, In Soil Orga nis ms and Decomp os i tion in Tundra (A. J. Holdin g et al., eds.) . pp. 297-324. Tundra Ste e rin g Commi ttee , Sto c kholm. Camp b ell, R., and Rovir a , A. D. (19 73) . The stu d y of the rhiz o sph ere by scannin g electr on mi cro scop y, Soil Bio l . Bio c hem. 5, 747-752. Chen, Y., and Av nim elech, Y. (19 86) . The Role of Orga nic Matte r in Modern Ag ricu ltu re . Mart inu s Nij ho ff Pub!., The Hagu e . Focht, D. D., and Mart in, J. P. (1979) . Mi cro bio l og ica l and bio c he mica l aspe cts of semiar i d ag ricu ltu r al soil s, Ecol. Stu d. 34, 119-147. Harr is, R. F. (19 81) . Eff ec t of wate r po te n ti al on mi cro bia l grow th and acti vity, In Wate r Pote n tia l Relati on in Soil mic r ob iolo gy (J. Parr et al., eds.) . Soil Sci. Soc. Arn., Madis o n, Wi sc onsin . Ly nc h. J. M., and Poole, N. J. (19 79) . Mi cr ob ial Ecology : A Concep tual Ap pro ach. Wi ley , New York.
McLaren, A. D., and Skuji ns , J. (19 68) . The ph y si c a l envir o nment of mi cr oorga nis m s in soil , In The Ecology of Soil Bact er i a (T. R. G. Gray and D. Parkin s on, eds.) , pp. 3-24, Univ . of Toronto Press, Toronto . Stu m m, W., and Morga n, J. J. (19 81) . Aq ua ti c Chemi str y: An Intr o ducti on Emp ha siz i n g Chemi ca l Eq u il ib n ·a in Natu r al Wate r s. 2nd ed. Wi le y, New York. Tie d je , J. M., Sexto n e, A. J., Parkin , T. B., Revsbach, N. P., and Shelto n , D. R. (1984) . Anaerobic pro cesses in soil , In Dev. Plant Soil Sc i. 2, 197 -212. Ti sd all, J. M., and Oades, J. M. (1982) . Orga nic matt er and wate r sta b le ag greg a te s in soil , ]. Soil Sc i. 32, 141-163. Wong -C hong , G. M., and Loehr, R. C. (19 78) . Ki ne ti cs of mi cro bia l nit rite nit rog e n oxid a ti on , Wate r Res. 12, 605-609. 추가로 읽을 거리 Brock, T. D., Smi th, D. W., and Madig a n, M. T. (1984) . Bio l ogy of Mi cr o- orga nis ms. 4th ed. Prenti ce -Hall, Eng le wood Cli ffs, New Jer sey. Camp b ell, R. (19 77) . Mi cr obia l Ecology . Blackwell, Oxfo r d. de Jon g , E., and Paul, E. A. (19 79) . Soil aerati on , In Ency c lop e dia of Soil Sc ien ce (R. Fair b rid ge and C. W. Fin k l, Jr., eds.) . pp. 10-19. Dowden, Hutc h in s on & Ross, Str o udsburg, Pennsyl v ania . Emerson, W. W. (1977) . Phy si c a l pro p erties and str uc tu r e, In Soil Fact or s in Crop Producti on in Semi arid Envir o nment (J. S. Russell and E. L. Greacen, eds.) . Univ . of Qu eensland Press, St. Luc ia. Gr iffin, D. M. (19 72) . The influe nce of wate r , In Ecology of Soil Fung i (D. —M(1. 9G 81r i) f.f in.W eadt.e) r , Canhda p mteir c r5 o. biSa yl rastc ru esse s ,U nI niv . APdrveasnsc, eSs y irna c uMsei c, r oNbeiaw l York. Ecology (M. Alexander. ed.) , pp. 91-136, Plenum, New York. Gup ta, S. C., Radke, K., and Larson, W. E. (1981 ) . Pred ict i ng tem p er atu re s of bare and resid u e covered soil s w itho ut a com crop , Soil Sc i. Soc.
Am. ]. 45, 405. Ing ra ham, J. L., Maale, 0., and Neid h art. F. C. (1981) . Growt h of the Bacte r i al Cell. S in a uer Assoc., Sunderland, Massachusett s. Ly n ch, J. M. (1993) . Soil Bio t e c hnology , Mi cr obia l Facto r s in Crop Produc- tivit y . Blackwell, Oxfo r d. Russell, E. W. (19 73) . Soil Condit ion s and Plant Growt h. 10th ed. Long ma ns, Green, London. Soil S c ien ce Socie t y Americ a n Termi no log y Commi ttee (19 84) . Glossary of Soil Sic e nce Terms. rev. ed. Soil S ci. Soc. Am. , M adis o n, W isc onsin . Sto t s k y , G. (19 74) . uActi vi t y, ecolog y, and po p u lati on dyn a mi cs of mi cro - orga nis m s in soil , In Mi cr obia l Ecology (A. Laskin and H. Le- chevalie r . eds.) , pp. 57-135. CRC Press, C leveland, Ohio .
제 3 장 토양생물 연구 방법 3-1 서론 미생물학 연구를 목적으로 채집된 토양 시료는 자연에서 일어나고 있는 수많은 미세 서식처의 혼합물이다 . 특수한 기능들을 밝혀내기 위 해서는 시험관이 필요하지만 농학자와 생태학자의 실질적 의도는 연구 되고 있는 야의에서 분자, 미생물, 전체 식물, 야의 측정을 포함하는 여러 가지 수준의 실험을 수행해야 한다. 그림 3.1 은 토양에 있는 미생물과 식물과 미생물 연합의 종류와 수, 그리고 대사활동들을 추정하기 위한 여러 가지 접근 방법들을 보 여 준다. 이러한 접근 방법들은 토양에 있는 미생물의 형태와 배열의 결정, 하부 집단과 종의 분리와 특칭화, 대사과정의 탐지와 측정들을 포함한다. 이들은 토양에 있는 미생물의 수와 형태, 생물량, 수행하 는 기능들에 대한 일반적인 추정을 집합적으로 제공한다. 토양미생물 을 연구하는 데 필요한 과정들에 대한 상세한 내용은 Gerhardt 등 (1981 ), Pag e (1982), Parkin s on 등 (1972) 의 책을 참조하면 도움이 된다.
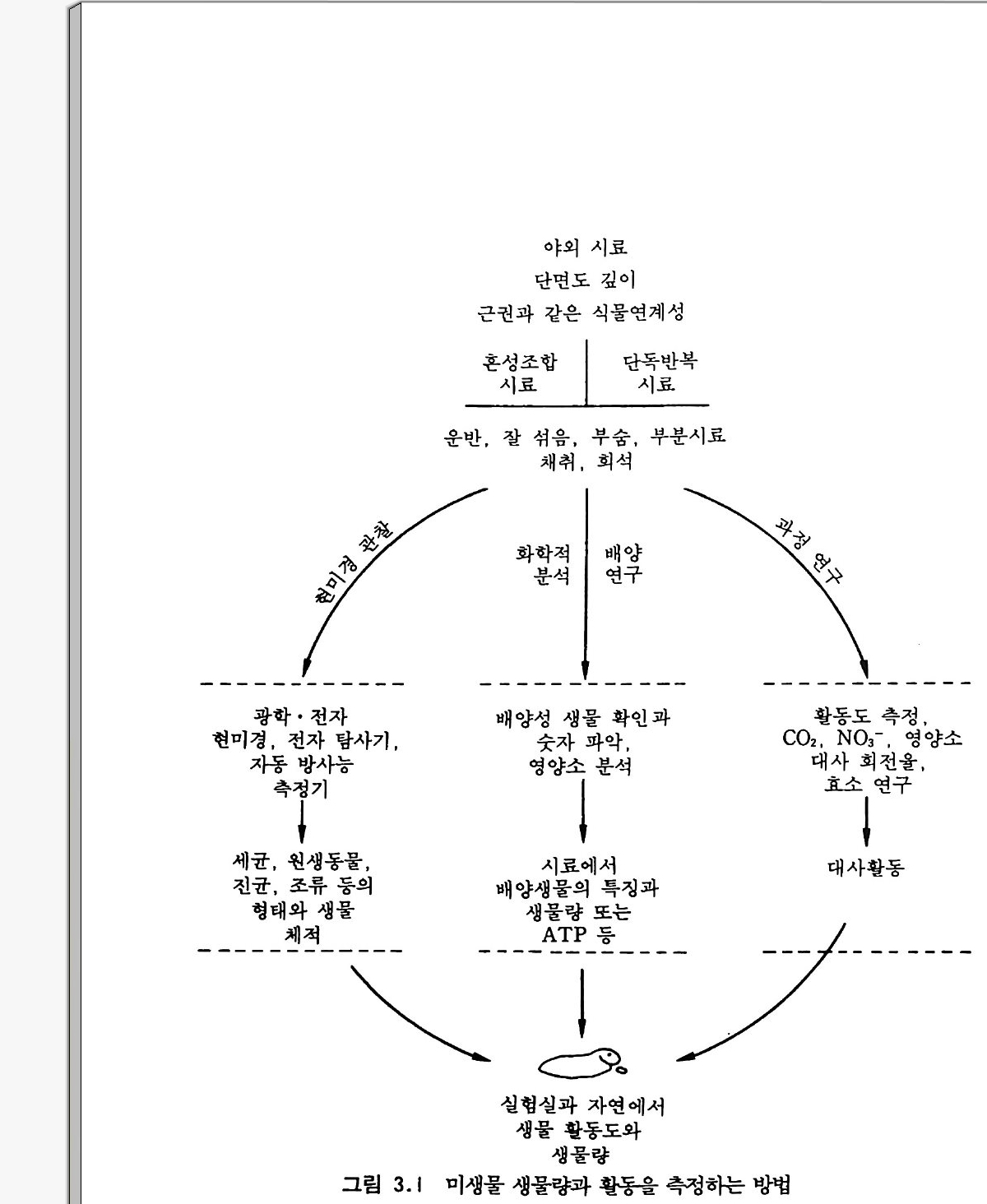 야외 시료
야외 시료
3-2 토양 시료 채취 토양 시료로부터 얻은 분석 자료에 시료 채취 장소에 관한 정보를 보충한다면 시사하는 내용이 더욱 많아지게 된다. 그 중에서 특히 다 음과 같은 물리, 화학, 생물학적 요소들이 매우 가치 있다.
지형 모계 토양형태 수분상태 토양p H
임경 크기와 형태 CO2 와 02 상태 화학적분석 온도의 범위와변화 강우량과분포
식물피복과생산성 식생의 역사 관리 역사 동물존재 유기물 유입량과 석물 뿌리
통계 처리될 수 있는 대표적인 시료를 채취하는· 것이 중요하다. 야 외의 연구 장소에 대한 지식에 따르면 보통 높고 낮은 지접에서는 서 로 다른 토양 특성, 그리고 아마도 매우 다른 영양물 함량을 가지기 때문에 분리해서 채취할 것을 제안한다. 비교적 일률적인 지역에서는 측정 오류를 약 10% 정도로 줄이기 위해서 적어도 네 번의 반복적인 시료 채취를, 그리고 그 각각에 대해서는 적어도 두 번의 독립된 채취 를 하는 것이 필요하다. 토양통계학 또는 그리그 격자법 kr igi n goJJ서는 관찰이 공간적으로 서로 동떨어지지 않은 곳에서 야의 자료를 다루도 록 기안한다. 이것은 야의의 변동들을 더 잘 설명할 수 있고 종종 고 전통계학보다 더욱 더 유용하다 (Marx 와 Thomp s on(1 9 87)). 15N 을 사용하는 것과 같은 영양소 수지 균형에 관한 연구에서는 무작위법에 의한 하부 구성 단위의 시료 채취가 결코 적당한 수지 균형을 보장하 지 않는다. 하부구성 단위의 시료 채취를 하기 전에 전체 포집된 토양 또는 특수한 충돌의 토양을 완전히 섞울 수 있는 원통식 또는 개방식 라이시미터 o p en l y s i me t er 가 필요하다.
화학적 분석에 사용될 토양 시료들은, 가능한 한 즉시 냉동시키거나 말리는 것이 일반적으로 바람직하다. 몇 가지 예의가 있다. 예를 들면 토양 아질산염을 측정할 때 말리는 행위는 아질산염을 훼손하기 때문 에 바람직하지 않다. 질산염의 분석을 위한 토양은 2~] 간 내에 말려 야 한다. 그렇지 않으면 말리기 전 또는 말리는 과정 동안 질산염 수 준이 증가하기 쉽다. 생물학적인 분석을 위해서는 운반과 저장 시간을 최소화해야 한다. 시료가 즉시 분석 진행될 수 없울 때 수분이 있는 토양을 야의 온도나 0°C 에서 저장하는- 것이 한 가지 방법이다. 시료 채취와 함께 부슈갖}으로 일어나는 토양의 교란은 본질적으로- 저장 기 간 토양 생물 개체군에 변화를 초래할 것이다. 그리하여 저장된 시료 에 의한 관찰은 교란되지 않은 야의 토양을 대표하지 않게 될 것이다. 3-3 토양의 현미경 관찰 현미경을 통한 직접적인 조사는 토양에 미생물의 형태나 배열 상태 를 확인할 때 특히 쓸모가 있다. 광학현미경과 함께 토양 미세형태학 에서 사용되는 바와 같이 박막기법 thin- secti on t echn iq u ei든 토양 구 조, 뿌리 침투성, 토양 미세동물들을 관찰할 수 있게 한다. 박막은 통 상 미생물군을 관찰할 수 있을 정도로 충분히 얇지는 않다. 토양 입자 둘의 표면에 빛의 초점을 맞춘다면 술폰산 마그네슘 magn e siu m sulfo nic aci d, 아크리딘 오렌지 acri din e orang e , 플루오레신 이소티오 시아네이트(fl uoresce i n iso th ioc ya n ate , FITC) 같은 형광 염료들은 토 양 입자 위에 있는 미생물 관찰을 가능하게 한다. 박막과 두과 전자현미경 (tran smi ss io n electr o n mi cro scop y, TEM) 은 토양 짜임새-미생물 상호작용에 대한 연구와 뿌리 마디에 있는 미
 그림 3.2 밀뿌리 근권의 얇은 단면. 사진의 아래 부분 뿌리에는 표면에 하나의
그림 3.2 밀뿌리 근권의 얇은 단면. 사진의 아래 부분 뿌리에는 표면에 하나의
생물들을 관찰하는 데 쓸모 있는 것으로 알려져 있다(그립 3.2). 투과 전자현미경에서 사용되는 복합음영기법 comp le x shadow ing tec hniq u e 은 미생물을 토양 입자와 구별하는 것을 어렵게 한다. 怨 R 撲적인 조망 을 할 수 있게 하는 주사 전자현미경 (scannin g electr o n mi cr oscop y, SEM) 은 미생물 서식지와 미생물 자체의 모양과 구조를 보여 주는 데 최상이다. 세균은 종종 끈끈한 점액질 안에 갇혀 있고 보기 어렵지만 진균과 방선균 acti no my c ete s 구조는 쉽게 관찰된다(그립 3 . 3) . 주사
 그림 3.3 썩고 있는 낙엽의 주사현미경 사진. 세균은 정액질에 達갇혀 있 는 경향이
그림 3.3 썩고 있는 낙엽의 주사현미경 사진. 세균은 정액질에 達갇혀 있 는 경향이
현미경은 기본적으로- 전자들이 토양 표면을 가로질러서 빠르게 이동하 는 작은 전자탐침 electr o n p robe 이다. 이들 전자의 배경 분산이 3 차원 적인 효과를 준다. 배경 분산되는 전자들을 특수한 파장에서 측정하거 나 매우 좁게 정의된 파장으로- 초점을 맞출 수 있는 전자탐침을 사용 함으로써 각각의 영양물질을 분석하는 것도 가능하다. 그리하여 약간 의 기계적인 문제점들이 여전히 있기는 하지만 지금은 원래의 자연상 태에서 식물 뿌리와 토양미생물의 분석이 가능하다. 토양에서 미생물들은 공국이나 입단 내부에서 자란다. 따라서 평면 의 슬라이드 표면에 나타니는 관계는 아마도 자연 상태를 완전하게 대 표하지는 않을 것이다. 러시아의 연구자들은- 토양현미경 pe doscop e¾ 사용함으로써 이러한 어려움을 해결했다. 이것은 벽의 내부에 발라서 영양물질을 포함하거나 하지 않은 채 토양 속에 묻울 수 있고 정상상 태 ste a dy s t a t러] 이르도록 충분히 긴 시간 동안 교란되지 않은 채 묻 어 둘 수 있는 얇고 평평한 광학모세관이다. 편편한 광학모세관을 마 련하기 위해서는 많은 노력을 해야 하므로 이 기법은 널리 사용되지는 않는다. 다른 연구자들은 토양 속에 가는 나일론 그물 주머니를 묻어 서 연구한다. 끄집어낸 그물 백 위에 가제 조각을 올리고 염색을 한 다. 묻어 두는 시간을 달리 한 다음 진균에 의해서 채워진 그물눈의 수를 세어서 진균의 발달을 관찰한다. 매설 슬라이드 (bur i ed-sl i de : Ross-Cholodny ) 기법에서는 상당 기 간 유리 슬라이드들을 토양 속에 묻는다. 미생물은 그 슬라이드에 달 러붙게 된다. 그것을 떼어내고 염색하면 토양미생물 개체군의 정성적 인 성질을 관찰할 수 있다. 미생물의 여러 가지 집단과 군집 생성 형 태 사이의 상호관계성은 영양물질을 첨가하지 않은 슬라이드에서 관찰 된다. 셀로판 같은 두명한 포를 씌우면 복합 기질 comp le x substr a te 에서 군집 형성 순서를 관찰하는 것도 가능하다. 미생물들의 배열에
대한 어떤 정보는 유리 슬라이드를 교질의 물질로 씌우고 토양 노출 부위를 끈끈한 표면에 닿게 한 다음 현미경 조사를 실시함으로써 얻을 수있다. 3-3-1 현미경 관찰로 개체수 세기 토양 현탁액의 직접적인 현미경 관찰은 토양미생물을 세기 위한 통 상적인 과정이다. 토양 입단을 분쇄하기 위해서 와링 Warin g 혼합기 에서 Na4P207(sodiu m pyr o p hos pha t e) 나 세제 (Tween 80) 같은 화학 약품들로 분산한다. 적당한 양의 현탁액을 현미경 슬라이드의 l cm2 면적 위에 두거나 치수가 알려진 미생물 계수용 격자 슬라이드 counti ng chambe 데서 한천과 혼합한다. 한천이 굳은 다음 계수실에 서 떼어 내어 고정과 염색을 위해 현미경 슬라이드에 둔다. Jon e& il} Moll iso n 쓸阿드 기법으로 알려진 이 기법은 토양 입자들의 특정한 희석률과 특정한 부피 내의 미생물 수를 제시한다. 이 방법은 특별히 진균에 쓸모가 있다. 세균은 토양 입자와 곧잘 구분되지 않기 때문에 그 수를 세기가 더 어렵다. 물의 연구에서 오랜 역사롤 가전 한 가지 기법은 토양 현탁액을 무색의 또는 검은 탄산염 중합체 여과지로 여과 하는 것이다. 여과되어 있는 미생물과 함께 여과지를 유리 슬라이드 위에 놓고 염색한다. 고형 매체에 강하게 흡착되어 있거나 입단 안에 포획되어 있는 미생물들은 토양 현탁액의 액체상으로 들어가지 못하는 점이 문제다. 많은 염색 기법들이 있다. 전통적인 로즈 벤갈 rose ben g al 과 페놀 아닐린 블루 ph enoli c anil ine blue 염료는 형광성 염료에 밀리고 있다. 가장 오래되고 가장 널리 사용된 아크리딘 오렌지는 세포 내의 DNA 를 염색한다. 살아 있는 세포는 적은 양의 염료를 흡수하여 초록색울
띠게 된다. 기능적인 세포질막을 가지지 않는 죽은 세포는 많은 양의 염료를 흡수하여 붉은 색을 띠게 된다. 그러나 세포의 색깔은 또한 영 료의 농도, 세포벽의 성질, 세포질· 내의 DNA 와 RNA 비율에 따라 달라진냐 따라서 살아 있는 세포와 죽은 세포의 명확한 구분은 어렵 다. 아크리딘 오렌지는 토양 입자에 흡착되어 점토질 토양(또는 식토 clay so il)에서는 양호하게 염색되지 않지만 사질토양(또는 사토 sand y soil ) 에는 쓸모가 있다. 플루오레신 이소티오시아네이트는 단백질의 술피드릴 그룹 sulf yd ryl grou FI 흡착되어 세균에게는 아주 좋으나 모든 진균에는 흡착되지 않는다. 진균에 있어서는 세포의 /3 (1 一 3) -글리칸 연결에 선택적으로 흡착되는 형광성 염료인 수용성 아닐린 블루가 적당하다. 플루오레신 디아세데이트(fl uoresce i n dia c eta t e , FDA) 의 사용은 이론적으로 활성 의 균사를 비활성인 것과 구분하게 한다. 홉수된 후, 처음에 비형광성 인 FDA는 내부의 에스데르 분해효소 es t eras 려 1 의해서 풀루오레신과 아세데이트로 쪼개진다. 유리 플루오레신은 형광을 낼 수 있다. 토양 에 사용될 때 플루오레신은 2-10% 의 균사에 의해서 나타난다. 이것 은 어린 균사와 균사 선단의 좋은 지표가 된다. 3-3-2 생물 체적과 생물량의 계산 미생물의 생물 체적은 미생물의 직경과 길이로 계산한다. 간균은 아 주 작은 원통형의 양 끝에 반구가 붙어 있는 것으로 가정한다. 전조중 량 기준의 미생물 생물량은 표 3.1 에서 보여 주는 공식들로 계산할 수 있다. ― 0.03 에서 —1.3 MPa 의 범위의 토양 수분에서 자라는 대표 적인 토양 진균은 실험실 배양기에서 자랄 때보다 50% 더 무거운 것 으로 밝혀졌다. 이것은 부피 무게 비율의 환산이 종종 인용되는 0.22
 표 3.1 생물량을 계산하는 공식
표 3.1 생물량을 계산하는 공식
의 값 대신 0 . 33 을 사용해야 한디는· 것을 나타낸다. 표 3.1 은 실험실
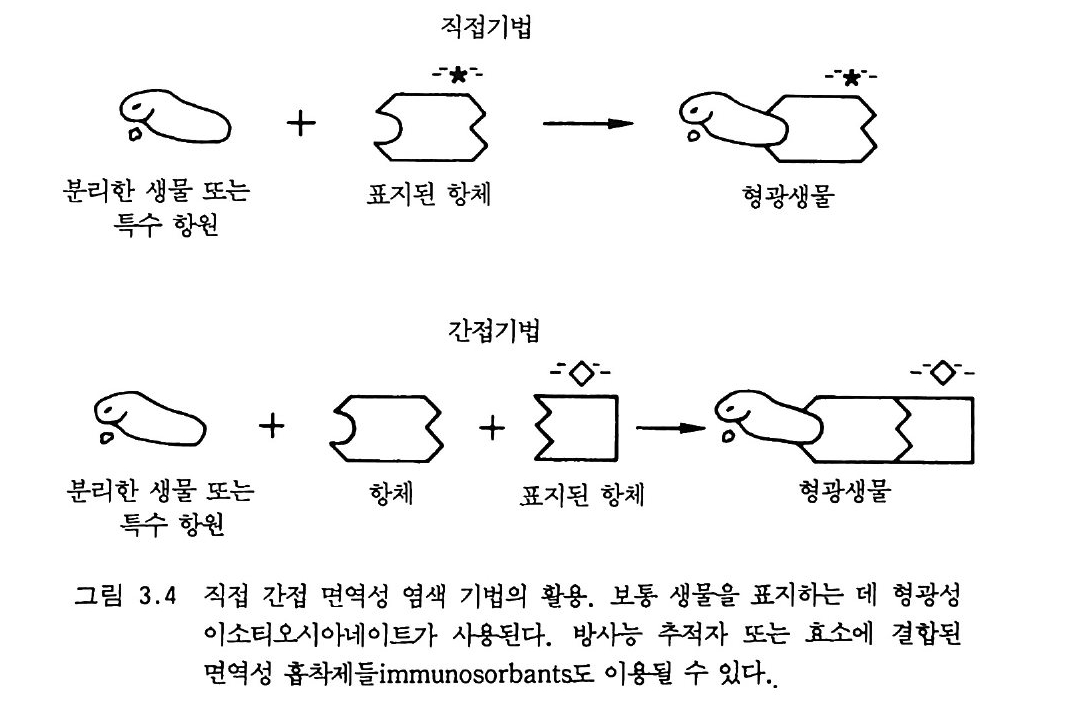
배양 기준으로- 세균의 부피 무게 비율이 0.22 인 것을 보여 준다. 토 양에서 그와 비슷한 조전에서 자란 세균의 경우는 역시 이 값보다 2 배 가량크다. 직접적인 현미경 관찰과 형광성 염색은 토양에서 특수·한 미생물의 수와 생물체적을 결정하는 데 활용될 수 있다. 이것은 면역형광 기법 im munofl uo rescent t echn iq ue~ 로 수행된다(그림 3.4). 특수한 항원 울――-이는 하나의 완전한 세포거나 세포로부터 분리된 물질일 수도 있다-토끼의 정맥을 통하여 몸 안으로 주입한다. 생성된 항혈청을 채취하여 FITC 갇은 형광성 염료로 표지를 붙인다. 현미경 슬라이드 또는 여과지에서 혈청과 미지 생물의 반응은- 특수한 생물에 초록빛 형 광 표지를 달게 된다. 이 기법을 사용하여, 토양과 근계에서
 분리한생물또는 己표지된항직접체기 법 一오형광생물
분리한생물또는 己표지된항직접체기 법 一오형광생물
As pe rgi llu sf lavu s, Rhiz o biu m 종들, 질산균의 구체적인 숫자를 얻 고 있다. 토양에서 특이한 반응을 하지 않은 경우와 특칭 있는 미생물 로 연구해야 할 필요가 있을 때는 이 기법의 적용이 제한된다. FITC 보다 유기 인 분해효소p hos p ha t ase 같은 특수 효소를 항체에 붙이는 것은 이 기법의 적용 범위를 확장하며 사용을 용이하게 한다. 효소에 연결된 면역성 흡착제 ELISA 에 의한 이러한 분석들이 토양에 서 질소고정균의 변종 riz o bia str a in s % 찾아내는 데 쓸모가 있는 것으 로 밝혀지고 있다. 3-4 화학적 기법을 이용한 생물량 측정 클로로포름 (CHC13) 중기에 처리된 토양미생물들의 세포막은 파손· 된다. 이것은 세포 구성물이 토양으로 흘러나오게 한다. 몇몇 탄소, 질소, 황 성분들처럼 세포질 속의 인은 그것을 적절히 추출한 다음 바 로 측정할 수 있다. 그러나 생물체에 포함된 탄소와 질소 양의 측정은 클로로포름 훈증으로 세포막이 녹은 세포를 포함하고 있는 토양에 살 아 있는 미생물 개체군들을 포함하고 있는 토양을 조금 접종한 다음 배양하는 절차를 필요로 한다. 신선하게 죽인 미생물균의 10 일에 걸 친 분해는 CO2 와 NH4+ 를 생산한다. 생산되는 CO2 또는 NH4+ 양과 생물량의 관계는 따로이 “C 가 lSN 으로 표지된 세포들을 토양에 첨가 하고 CHCI3 으로 처리하여 결정한다. 발생하는 탄소 양이 전균과 세 균에 대해서 다르기는 하지만 전균과 세균에 함유된 탄소의 평균 41 %가 C 아로 변한다. 생물량은 다음과 같이 계산된다.
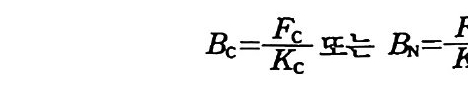 &=운또는凡=沿
&=운또는凡=沿
여기서 Be 는 생물체에 포함된 탄소량 (b i omassC) , 凡은 생물체에 포함된 질소량, Fd .근 클로로포름 처리로 분해되어 발생하는 CO2 증 가량(죽, CHC13 로 처리된 토양으로부터 발생하는 CO2 양에서 처리되지 않은 토양에서 발생하는 CO2 양을 맨 값) , Kd =-생 물체 탄소 중 클로로 포름 처리에 의해 CO2 로 발생되는 생물체 탄소의 비율(많은 토양에 대 해서 0.41) 이다. 클로로포름 증기로 처리하고 배양한 다음 무기화되는 질소의 양은 미생물이 탄소 대 질소 비율에 따라 달라전다. 클로로포름 처리된 다 음 미생물에 의한 질소의 재흡수를 고려하여 KN 의 계산은 다음 공식 으로 되는 것이 밝혀졌다.
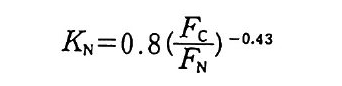 KN = 0 . 8 (FN均 -O. 43
KN = 0 . 8 (FN均 -O. 43
여기서 KN 은 클로로포름으로 처리한 다음 무기화되는 생물체 질소 의 비율, F혼 } FN 은 위에서 정의된 바와 같이 각각 클로로포름 처리 로 발생하는 CO2 와 NH4 증가량이다. 분해된 질소의 재흡수 및 10 일 동안 배양해야 하는 성가심과 관련된 문제는 클로로포름으로 처리한 다음 배양하지 않고 바로 탄소와 질소를 추출하여 측정함으로써 피해 갈 수 있다 (Vance 등 (1987), Amato 9} Ladd(1988) (이것은 IO 일 동안 배양해야 하는 성가심이 있기 때문에 지금은 훈증한 다음 배양하지 않고 바 로 유기 탄소와 암모니아를 추출 측정하여 미생물 탄소와 질소를 추정하는 방법도 발표되었다. 참고문헌 : Sp a rlin g, G.P., and A.W . West( l98 8). A dir e ct extr a cti on meth o d to esti m ate soil mi cro bia l C : cali br ati on in situ usin g mi cr obia l respi ra ti on and 1 ◄ c labelled cells. Soil Bio l. Bi oc hem. 20 : 337-343. Brookes, P.C., A. Landman, G. Pruden, and D. S. Jen kin s on (1985) . Chlorofo r m fw nig a ti on and the release of soil nit ro g e n : a rap id dir e ct extr a cti on meth o d to measure mocrobia l
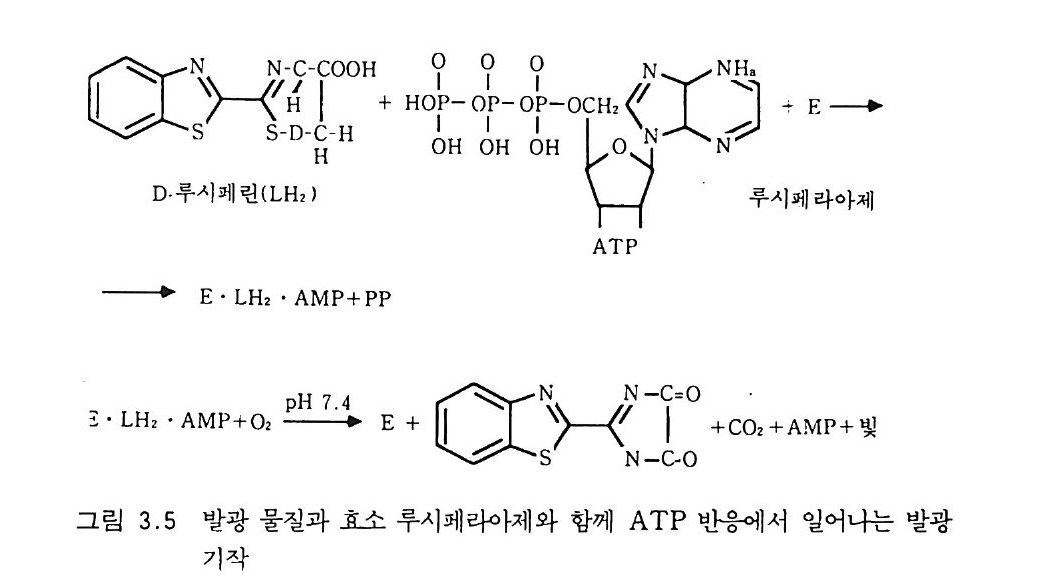
bio m ass nit ro g e n in soil . Soil Bi ol . 17 : 837-842 : 옮긴이) . 클로로포름 기법은 직접적인 현미경 관찰보다 더 간단하다. 이것은 토양 미생물 안으로 투입된 C 라 !SN 갈은 추적지들의 측정을 가능 하게 한다. 토양으로부터 진균를 걸러 내고, 비중 경사 dens ity grad ie n t7 } 있는 용액에서 세균을 분리되게 하는 방법들도 역시 토양 으로부터 미생물의 직접 분리를 가능하게 한다. 3-4-1 ATP의 측정 세포 내의 모든 생합성 및 이화작용 반웅들은 두 개의 고에너지 결 합을 아데노신 일인산 adenosin e monop h osph ate (AMP) 에 더 하여 만 들어지는 아데노신 삼인산 adenosin e tri p h osph ate (ATP) 을 필요로 한 다. 그리하여 ATP 는 인산염 그룹을 다른 대사 중간물질에 주어서 그 들을 활성형으로 바꿀 수 있다. ATP 는 모든 생명체에 공통적으로 존재하며, 환경 요소들과 인산 영 분해효소들에 매우 민감하게 반응한다. 그것은 토양에서 독립적인 상태로 존재하지 않는다. 결과적으로 이 조효소는 토양, 침적토 또는 수계의 생명활동과 양을 결정히는- 데 이상적인 물질이다. ATP 는 많 은 반응들에서 중심적인 반응물이다. 그들 반응의 많은 것들이 이론적 으로 ATP 측정에 이용될 수 있다. 그림 3.5 에서 보여 주는 바와 같 이 루시페린 luc ifer in 반응의 사용은 가장 간단한 것 중의 하나다. 기 질 루시페린은 질소와 황을 포함하며 고리를 이루는 분자로서 마그네 슘의 존재 하에 ATP 및 루시페라아제 lucif erase 와 반응하여 중간물 질인 복합체 효소유느시페린-아데노신 일인산을 만든다. 이 중간물질 은 0 가 있을 때 분해되어 독립적인 AMP 와 무기 인산염을 생산하 고, 빛을 발산한다. 반옹의 첫 153 ::. 동안 매우 예리한 빛의 방출이 있
 ::D 루\시페린며 (LH2〔)H O H + H0O\H- 0O\H- 0\O-HO CRH2 〈〉工 맷N 」루 시드페 E라 一아제
::D 루\시페린며 (LH2〔)H O H + H0O\H- 0O\H- 0\O-HO CRH2 〈〉工 맷N 」루 시드페 E라 一아제
고 그 후 빛의 방출은 1 - 3 분 동안 꽤 일정한 상태로 지속된다. 이 방 출된 빛을 광도계나 섬광계수기 sc i n ti lla ti on coun t er로 측정하여 ATP 함량에 대해서 그래프를 그려 대조 직선 st a ndard curv 여t 얻을 수 있 다. 개똥벌레 꼬리 대신 순수한 루시페라아제와 루시페린을 사용한다 면, 빛의 방출 시간은 연장되고 양은 일정해진다. 미생물 배양에서 얻은 세포들은 분쇄함으로써 ATP 를 추출한다• 순수 배양에서 세포 분쇄는 끓이거나, 산(예를 들면 H2SO 。 HCIO.), 또는 CHCb 처리로 수행한다. 토양과 침적토에서는 끓임으로 적당한 분쇄가 일어나지 않는데 이는 세포가 점토 콜로이드로 보호된다는 것 울 시사한다. 칼슘 함량이 많은 토양에서는 O.SM NaHCO 센서 클 로로포름이 쓸모 있는 것으로 밝혀지고 있다. 그러나 토양의 ATPas 러용이 클로로포름에 의해서 모두 억제되지 않기 때문에 이 방법은 과소평가를 초래한다. 사용 가능한 것으로 밝혀진 추출 시약은 음이온(인산영)과 양이온(파라귓)의 조합을 포함한다. 대부분의 추출
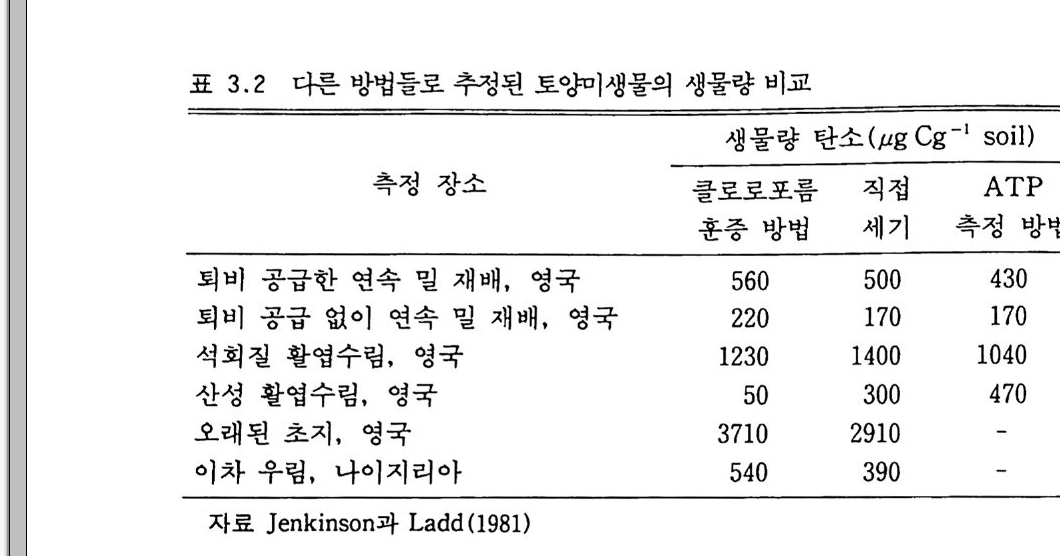 표 3.2 다른 방법들로 추정된 토양미생물의 생물량 바교
표 3.2 다른 방법들로 추정된 토양미생물의 생물량 바교
시약들은 루시페라아제 반응을 어느 정도 억제한다. 그러므로 용액을 ATP 광도계에 두기 전에 가능한 한 많은 배수로 희석한다. 미생물의 생장 동안, 탄소 대 ATP 의 비율은 1000 : 1 에서 40 : 1 까 지 변한다. 휴식 상태에서 ATP 대 세포 영양물질 비율들은 일반적으 로다음과같다.
 ATP : C : N : P : S
ATP : C : N : P : S
많은 토양들에 대해서 클로로포름, ATP, 직접적인 현미경 사용으 로 측정한 생물체의 탄소 함량을 표 3.2 에 보여 준다. ATP 는 생물 량과 생물활동을 동시에 측정하도록 하지만 토양에 포함된 인 함량에 영향을 받는다. 충분한 또는 일정한 인 함량에서 미생물의 활동이 휴 식 상태에 있는 토양들의 생물량을 특정화하는 데 ATP 는 가장 성공 적으로 이용될 수 있다.
3-4-2 호흡 측정 다른 모든 생명과 공통적으로 미생물 세포는 탄수화물과 같은 환원 된 물질을 산화하는데 그 일반적인 화학식은 다음과 같다. CH20+02 一 C02+ H20+ 중간물질+세포물질+에너지 형기성 조건에서 가장 혼한 종속영양적 반응은 발효이다. C6H1206 一 2CH3CH20H+2C02+ 에너지 또는메탄가스의 생산은 H2+C02 一 CH,+H20+ 에너지 이들 대사작용의 기작은 Sta nie r 등(1 986), Lehnin g e r(1 9 82), Dawe 라 Suth e rland(1 9 76), At la s(1984), Brock 등(1 984) 같은 일반 미생물학과 생화학 교과서에 포함되어 있다. 토양 입단이나 침수된 조건에서 생기는 발효산물은 축적되거나 호기 성 지역으로 확산되어 가서 CO2 와 02 로 변환되는 가용성 중간물질들 울 생산한다. 미생물 활동의 호흡에 의한 측정은 CO2 나 02 양을 결 정하는 것이다. 대기의 02 농도가 20% 인 것에 비해서 CO2 농도가 단지 0.035% 이기 때문에 CO2 에 대한 측정이 더 민감하다. CO2 의 측정은 또한 기질 분해와 관련해서 성장에 이용되는 탄소의 직접 대조 를 가능하게 한다. CO2 측정 방법은 통기 노선 aera ti on tra in s ½ 포함 한다. 여기서 공기 흐름이 토양 시료와 접촉하기 전에 NaOH 용액을 통과하여 CO2 가 제거된다. 그 공기 흐름은 토양 시료와 접촉하고 토 양 호흡에서 발생한 CO2 를 포칙하는 데는 또 다시 NaOH 가 이용된 다. 그 반응은 다음과 갇다.
2NaOH+C02 一 Na2C03+H20 적정하기 전에 BaCl2 을 첨가하여 C032- 는 BaC03 로 침전시키고 포집된 co 페 의해서 생산된 산을 충분한 양의 NaOH 로 역적정한 다. 발생한 CO2 를 흡수하는 데 사용된 NaOH 의 각 밀리 당량은 6 m g의 CO2 발생에 해당한다. 실험실에서 밀폐된 항아리에 둔 NaOH 용기는 발생하는 CO2 흡수 에 편리하고 효과적이다. 항아리는 산소 농도가 10% 미만으로 떨어 지지 않을 정도의 간격으로 열어 주어야 한다. Prop a k Q와 같은 칼 럼 물질에서 CO2 를 다른 성분으로부터 분리한 다음 열전도 탐지기가 있는 기체 크로마토그래피로 CO2 농도를 측정할 수도 있다. 기체 크 로마토그래피와 결합된 컴퓨터에 의해서 운용되는 밸브는 지동적으로 작동하여 시간별로 연구를 가능하게 한다. 적의선 가스 분석기들은 C02oJ l 민감해서 정체되거나 유동적인 계 모두에서 이용될 수 있는데 이는 CO2 와 같은 일반 파장에서 흡수하는 물을 제거한 다음 사용한 다. 야의에서 CO2 를 측정하기 위해 토양의 위 또는 주변 지역을 싸는 덮개나 여러 가지 깊이의 토양 속으로 밀어 넣는 관이 흔히 사용된다. 덮개를 사용할 때는 덮개 아래로부터 CO2 가 확산될 가능성과 톰울 통 해서 CO2 흐름이 생길 가능성을 유의해야 한다. 여러 가지 토심에서 관이 이용될 때는 토양 표면으로부터 CO2 분출과 함께 활용될 수 있 다. 미생물 활동의 지수로서 CO2 를 측정할 때는 CO2 탄소가 CaC03 와 평형을 이룰 가능성, CO2 가 물에 융해될 가능성, 식물 뿌리에 의 해 CO2 가 생산되거나 이용될 가능성이 고려되어야 한다. 산소 분석은 보통 CO2 가 NaOH 에 의해서 홉수된 계에서 기압계를 이용하여 수행한다. 폴라그래프 산소분석기와 상자성 산소분석기들도
또한 사용된다. 그러나 CO2 측정 장치만큼 민감하지도 않고 안정된 값을주지 않는다. CO2 측정은 선택된 기질 속으로 “C 를 투입시킴으로써 향상시킬 수 있다 (radio r espi ro metr y , 방사능 호흡 측정 ) . l4 c-를 포도당, 셀룰로오 스, 아미노산 또는 제초제갈이 잘 알려진 분자에 포함시키거나 미생물 세포나 식물 조각 같은 복합적인 물질에 포함시킬 수 있다. 유기 기질 들의 산화는 종속영양적 생장에 주요한 에너지원이며 모든 호기성 분 해는 CO2 를 발생시킨다. 방사능 호흡 측정기는 식물과 동물 조각들이 분해되는 동안 미생물 활동을 추적하는데, 환경에 첨가된 인공적인 화 학물질들의 거동 확인에 이용될 수 있다. 식물 조각의 분해, 미생물 생장, 토양 유기물 생성, 탄소의 지질학적 순환에서 이 기법의 사용은 나중에 논의할것이다. 3-5 효소와 그 측정 생명은 일련의 효소 반응들로 이루어지며 효소는 영양소 순환에서 일어나는 대부분의 반응을 수행한다. 토양 효소에 관해서 수많은 연구 가 수행되는 것은 놀랄 일이 아니다. 표 3.3 은 흔히 측정되는 효소들 을 나열하고 있다. 약간의 효소(예를 들면 요소 분해효소)는 세포 구성 요소로서 세포에 의해서 일상적으로 생성된다. 다른 효소들은· 적응성 또는 유동성이라 단지 반응하는 기질이나 어떤 선구물질이 있을 때만 형성된다. 유도 효소의 한 보기는 셀룰로오스 분해효소 cellulase 이다. 그것은 셀룰로오스:7} 존재할 때 생산된다. 탈수소효소 deh y dro g enases 는 그들이 세포 구성 요소이고 단지 살아 있는 계에서만 발견되기 때 문에 흔히 측정된다. 토양에서 털수소효소의 활성을 측정하기 위하여
표 3.3 토양에서 발견되는 토양 효소들과 그들이 촉매하는 반응 효소 관련 반응 Oxid o reducta s es Cata l ase 2H20 一 2H20+02 Cate c hol oxid a se 0-Di ph enol + 1/2 02 一 0-qu in o n + H20 (tyro sin a se) Dehy d rog e nase XH2+A 一 X+AH2 Dip h nol oxid a se P-D iph enol+ 1 /2 02 一 P-qu in o n+H20 Glucose oxid a se Glucose+02_-+ glu conic acid + H202 Peroxid a se and po lyp h enol A+H20 ----o xid i z e d A+H20 oxid a se Transfr er ase Transami na se R,R,-CH-N+H, + R,R.CO 一 R,R.-CH-N 먀 RIR2co Hy d rolases Acety le ste r ase Aceti c este r +H20 ---a lcohol + aceti c acid a-and fl-A my la se Hy d rolys i s of fJ (1—--+ 4) glu cosid _i c bonds Aspa rag ina se As p ara gi ne+H20 一 aspa rt at e + NH3 Cellulase Hy d rolys i s of p (1一 4) glu can bonds Deami da se Carboxy lic acid ami de + H20 —--+ carboxy lic acid + NH3 a-and /J- Gaia c to s id a se Galacto s id e + H2o ---+ ROH +ga lacto s e a-and p-G lucosid a se Glucosid e + H2o ---+ ROH + Glucose Lip a se Tr igly c eri de +3H2o ---+ gl yc erol + 3 fatty acid s Meta ph osph ata s e Meta p h osp h ate ---o rt ho p h osp h ate Nucleoti da se Deph osph oryl a ti on of nucleoti de s Phosp h ata s e Phosp h ate este r+ H2Q ---+ ROH +ph osph ate Phy tas e Inosit ol hexaph osp h ate + 6H2Q ---+ +6-ph osph ate Prote a se Prote i n s - ----+ pe p ti des + ami n o acid s Pyrop h osp h ata s e Pyrop h osph ate + H2Q ---+ 2-ort ho p h osph ate Urease Urea 一 2NH3+C02
여러 가지 염료, 예를 들면 산화 상태에서는 무색이나 환원 상태에서 는 적색인 tri p h eny lt e t r a zoliu m chlorid e 같은 물질이 토양에 첨가 되고 환원 상태에서 추출된다. 토양 효소는 단백질로서 종종 토양 유기 무기 콜로이드에 갇혀 있 다. 그러므로 토양은 미생물 생물체와 직접적으로 연관되어 있지 않은 세포의 효소들 ex t racellular enz y meSo] 라는 커다란 배경을 가지고 있다. 3-6 미생물 배양계수 토양미생물 배양은 생장을 유도할 수 있는 기질로 종균을 옮겨 심는 과정을 포함한다. 모든 배양 기법들은 선택적이고 특수한 성장형 또는 생화학적 능력을 가전 미생물을 찾아내기 위해서 기안된다. 대부분의 기법들은 토양에서 최초의 미생물들과 관련하여 그들이 필요한 정도로 희석한 토양 현탁액의 사용예 의존한다. 보통 한 번에 열 배의 회석을 하게 되는 일련의 단계적인 희석 과정이, 젖었거나 마른 일정량의 토 양에 수행된다. 토양 입단들은 종종 Na4P201 같은 분산 시약과 함께 와링 혼합기에서 분쇄된다. 적당한 현탁액의 1-ml 양을 고형 또는 액 체상 기질로 반복적으로 옮겨서 거기서 각 개별 종균 pro p a gu le ½ ol 가시적인 성장을 일으켜서 발달되도록 한다. 고형 기질은 평판계수법 pla te coun t예 사용되고 액체상 기질은 소멸희석계수에 사용된다. 평판계수법은 접종물 ino culum 1ml 를 3 또는 앙 R 의 페트리 접시에 두어 녹인 한천 (보통 약 20 ml) 과 so·c 에서 섞는다. 또는 한천을 접시 속으로 부어 넣은 후 접종물을 굳은 한천 표면에 퍼지게 한다. 적당한 배양 후에 각 군집을 세어서 각 군집을 토양 현탁액에서 있던 하나의
종균에서 유래된 것으로 본다. 세균학자들은 보통 종균 대신에 용어 du (colony -form i ng un it)의 사용을 선호한다. 다양한 배양액과 배양조건이 사용될 수 있다. 1 kg 토양을 1 리터 물과 섞고 끓인 후, 원심분리 및 상등액의 여과, 1.5 % 한천으로 추 출액을 굳히는 과정으로 마련한 토양 추출 한천이 가장 많은 군집 수 롤 생산한다. 이 배양액은 토양미생물에 의해서 요구되는 아미노산과 성장 요소들을 여러 범위로 포함하지만 매우 적은 양의 탄소를 공급한 다. 결과적으로 군집 형성은 매우 느리고 그 크기가 매우 작다. 고기 의 추출 성분을 포함하는 영양 한천은 거의 비슷한 수의 군집을 생산 한다. 영양 한천에 에너지 이용도가 높으면 큰 군집둘을 만들어 수를 세기가 쉽다. 여러 생물 집단들의 구분을 위한 배양액 조정은 세균을 제거하지만 진균은 제거하지 않은 스트렙토마이신 같은 항생제를 포함 한다. 악티디온 ac ti d i on 탁즌 세균을 남기고 진균을 제거하고 싶을 때 사용한다. 전균에 대해서 산도가 증가, 그람음성 세균에 대해서 색소 의 사용, 방선균 그룹들, 질소고정균 또는 황산염 산화 세균에 대해서 다양한 선택적인 배양액들이 이용된다• 보통 평판계수법에 의해서 세 균을 세는 것은 직접적인 현미경 관찰에 나타나는 수의 1-5% 이며, 기껏해야 50% 정도에 이른다. 평판계수법이 적당하지 않은 곳에서는 희석계수법 dil ut e coun t을 이 용할 수 있다. 이는 근본적으로 적당한 배양액에서 생장을 제공할 수 있는 가장 높은 토양의 희석률을 결정하는 것이다. 생장이 없을 것으 로 추정되는 희석률에서 10 배의 차이가 있는 3 가지의 연속적인 희석 률을 선택한다. 각각의 희석률로 마련된 반복적인 (보통 10, 최소 5) 접종물을 배양액에 접종했을 때 생기는 가시적인 성장들은 믿을 만한 통계학적인 범위 안에서 미생물의 숫자로 환산할 수 있다. 이 환산울 위한 표들은 통계학 책인 Cochran(1950), Alexander0982), 또는
Gerhardt 등(1 981) 에서 참조하면 된다. 특수한 미생물들의 분리는 보통 배양에 의해서 수행된다. 배양액은 원하는 각각의 개별 종들에 대해서 만들어전다. 분리는 또한 현미경을 이용하여 할 수 있다. 하나의 개별적인 세포, 포자, 또는 균사 조각을 미세 조작장치가 달린 현미경 아래서 뽑아낸다. 특수한 마생물을 포착 하기 위해서 식물이 이용될 수 있다. 민감한 콩과 식물들에 형성된 뿌 리 또는 뿌리혹박태리아의 분리를 위한 하나의 재료를 제공한다. 민감 한 숙주식물을 석재하는 것은 뿌리를 침입하는 병원균들의 혼합물을 분리하게 한다. 항생제에 내성인 변종의 이용은 토양에 접종된 특수한 분리균둘을 재차 분리할 수 있게 한다. 세포에서 특수한 유전 부호를 식별하는 DNA 탐침은 (Pace 등(1 986)) 토양으로부터 배양된 미생물 에 성공적으로 활용되고 있다. 따로 배양을 하지 않은 미생물 DNA 의 칙접적인 검출은 많은 분석적인 문제들과 함께 또한 쓸모 있는 정 보를 제공한다(H olben 동 (1988)). 참고문헌 Alexander, M. (1982) . Most p ro bable number meth o d for mi cro bia l po p u la- tion s, Ag ro n. Monog r. 9, 815-820. Amato , M. , a nd Ladd., J. N. (1988) ...A ssay for mi cro bia l bio m ass based on nin h y d rin - reacti ve nit ro g e n in extr a cts from fum i ga te d soil s, Soil Bio l . B io c hem. 20, 107-114. At la s, R. M. (19 84) . Mi cr obio l ogy , Fundamenta l and Ap pli ca ti on . Macmi llan , New York. Brock, T. C., Smi th, D. W., and Madig a n, M. T. (19 84) . Bio l ogy of Mi cr o- orga nis ms. Prenti ce -Hall, Eng le wood Cli ffs, New Jer sey. Cochran, W. G. (19 50) . Esti m ati on of bacte r ia l densit ies by means of the 'most pro bable number,' Bio m etr ics 6, 105-116.
Dawes. W ., and Suth e rland, I. W. (1976) . Mi cr obia l Phys i o l ogy . Blackwell, Oxfo rd . Foste r , R. C. (19 85) . In situ localiz a ti on of orga nic matt er in soil s , Que st. Ento m ol. 2 1, 609-633. Gerhardt, P., Murray, R. G. E., Costi low . R. N. , N esto r . E. G., W ood, W . A., Kaeg, N. R., and Phil lips, G. B. (19 81) . Manual of Meth o ds for General Bacte r i olo gy . Soc. Amer. Mi cr obio l . Washin g ton , D. C. Holben, W. E., J an sson, J. K., Chelm, B. K., and Ti ed je , J. M. (19 88) . DNA pr obe meth o d for the dete c ti on of spe c ific mi cr oorga nis m s in the soil bacte r ia l communit y, Ap pl. Env. Mi cr obio l . 5 4, 703-711 . Jen kin s on, D. S., and Ladd, J. N. (1981) . Mi cr obia l bio m ass in soil : Measure-ment and tur nover, In Soil Bi oc hemi stry (E. A. Paul and J. N. Ladd, eds.) , vol. 5, pp. 415-471. Dekker, N ew York. Lehnin g e r, A. L. (19 82) . Bi oc hemi stry. Wort h Publi sh ers, New York. Marx, D., and Thomp so n, K. (1987) . Practi ca l aspe cts of agn 'cultu r al kri ging . Bull. 903. Arkansas Ag r. Exp . Sta . Fay e tt ev il le, Arkansas. Pace, N. R., Sta h l, D . A., Lane, D., a nd Olsen, G. J. (19 86) . The analys e s of natu r al mi cr obia l po p u lati on s by rib o somal RNA seq u ences, Adv. in Mi cr ob. Ecol. 9, 1-55. Pag e, A. L., ed. (19 82) . Meth o ds of Soil Analys i s. Part 2. Chemi ca l and Mi cr obio l og ica l Prop er tie s. 2nd ed., A g r onomy , vol. 9. Am. Soc. Ag ron . Madis o n, Wi sc onsin . Parkin s on, D., Gray . T. R. G., and W illiam s. S.T. (1972) . Meth o ds for Stu d yi ng the Ecology of Soil Mi cr oorga nis ms. Blackwell, Oxfo r d. Rovir a , A. D., and Camp b ell, R. (1974) . Scannin g electr o n mi cro scop y of mi cro orga nis m s on the roots of wheat, Mi cr ob. Ecol. l, 15-23. Sta n ie r , R. Y., I ng rah am. J. L., Whealis , M. L., and Pain t e r , P. R. (1986) . The Mi cr obia l World. 5th ed. Prenti ce -Hall, Eng le wood Cli ffs, New Jer -sey. Vance, E. D., Brookes, P. C., and Jen kin s on, D. S. (1987) . An extr a cti on meth o d for measuri ng soil mi cro bia l bio m ass C, Soil Bi ol . Bi oc hem. 19, 703-707.
추가로 읽을 거리 Burge s, A., and Raw, F. (19 67) . Soil Bi ol ogy . Academi c Press, London. Burns, R. G., ed. (1978) . Soil Enzym es. Academi c Press, L ondon. Burns, R. G., and Slate r , H. (19 82) . Expe ri me nta l Mi cr obia l Ecology . Black-well, Oxfo rd . Parkin s on, D. (19 82) . Fil zm ento u s fun g i, Ag r on. Monog r . 9, 949. Schmi dt , E. L., and Paul, E. A. (1982) . Mi cro scop ic meth o ds for soil o rga n- ism s, Ag ro n. Monog r. 9, 808. Wollum, A. G. (19 82) . Cultu r al meth o ds for soil orga nis m s, Ag ro n. Monog r. 9, 782-802.
제 4 장 토양생물군의 구성 4-1 서론 토양생물군의 구성 요소로서 독립 개체로 살아가는 생물은 세균, 전 균, 조류 및 동물 들이다. 바이러스도 있지만 이들은 다른 생물들의 살아 있는 세포 안에서만 자란나. 독립적으로 살아가는 생물군들은 그 각각을 다시 수많은 분류군으로 세분해야 할 정도로 넓은 범위의 형태 적 생리적인 특징들을 가지고 있다. 과학의 각 분야가 그러하듯이 분류학 분야는 계속 변화하고 있으며 결과적으로 분류학적 구분은 시간에 따라 무척 다르게 될지도 모른다. 과거 몇 년 동안 방선균둘은 세균과 진균에 상당할 정도로 논의의 대 상이 되었다. 그 결과 방선균은 세균의 한 아문으로 분류되었고, Berge y 's Manual of Dete r mi na ti ve Bac t e ri olog y에서도 그렇게 취 급되었다. 수년 동안 미생물학자들은 남조류를 조류의 한 아문으로 간 주하였다. 현재 대부분의 토양미생물학자(B er g e y 's Manual 과 함께)들 은 남조류를 시아노박테리아 c y anoba ct e ri쵸i 지명하고 있다.
세균계에는 20~ 정도가 있다. 여기서는 각 속을 독립해서 다루려 는 어떤 논의도 시도하지 않을 것이다. 오히려 토양에 흔히 있는 속들 과 영양소 순환에서 중심적인 역할을 하고 있는 속들을 강조할 것이 다. 진균은 형태적인 특징과 강 class 수준에서 주로 다루고, 토양 동 물들은 매우 개략적으로 취급될 것이다. 그들의 영양 섭취 습성과 토 양생물의 초식자와 포식자로서 역할이 강조된다. 다음에 제시되는 참고사항은 특히 그러한 생물군과 · 익숙하지 않은 독자들을 위해서 토양생물군들에 대한 포괄적인 조망을 제시하고자 기 안되었다. 4-2 바이러스 바이러스는 단백질 껍질과 그 안에 들어 있는 RNA 또는 DNA 분 자들로 이루어져 있다. 바이러스 입자들은 물질대사 측면에서 보면 활 성이 없으며 호흡과 생합성 기능을 수행하지 않는다. 19 세기 후반에 그들은 모든 형태의 밝혀진 세균을 포착할 수 있는 여과지를 통과하는 능력, 살아 있는 생물로서의 성질, 그리고 많은 식물과 동식물에 병을 일으키는 능력에 의해서 처음으로 확인되었다. 1953 년 담배 모자이크 병 바이러스의 결정화는 살아 있는 세포의 특성이 화학 물질과 갇이 결정체로 될 수 있는 인자에서 발견될 수 있다는 것을 보여 주었다. 그들은 단지 숙주세포 안에서만 증식한다. 그들은 살아 있는 숙주세포 들을 유도하여 필요한 바이러스 구성 요소롤 생산하도록 한다. 구성 요소들이 조립된 후 복제된 바이러스들은 다른 새로운 세포를 공격할 수 있는 능력을 가지고 숙주세포를 이탈한다. 숙주의 유전 물질과 상 호 작용할 수 있는 능력을 갖고 있기 때문에 그둘을 제어하기는 어
렵다. 이런 능력이 또한 그들이 다양한 세포들 사이의 전이 인자 tra nsfe r a g en t s 로 작용하게 하고 유전공학에서 유전적 전이 인자 로 활용될 수 있게 하는 이유이다. 바이러스는 인간에서부터 미생물에 이르기까지 모든 범위의 동물과 식물에 감영한다. 세균 세포들에 기생하는 바이러스를 흔히 박테리오 파지 또는 간단히 파지라고 부른다. 토양미생물에 감염하는 바이러스 에 대한 생태학 지식에는 그들이 기생 능력을 보유한 휴면 단위로 토 양에서 존속할 수 있다는 것을 예의로 하고는 거의 알려져 있지 않다. 토양에서 식물과 동물에 병을 일으키는 바이러스의 생존과 지하수로 옮겨 갈 수 있는 바이러스 입자들의 능력은 사람들에게 중요한 관심거 리다. 그들은 역시 잡초나 해충들을 생물학적으로 제어하는 데 활용될 전망이 있는 것 같다. 바람직하지 않는 숙주들에 대해서 바이러스 기 생의 활용이 성공되기만 하면, 질산화 작용과 같은 토양 과정 중 에서 특수한 단계를 맡고 있는 세균 종을 숙주로 하는 파지를 활 용하기 위한 노력이 더욱 활발해질 것으로 기대된다. 4-3 세균 세균은 토양에서 가장 수가 많은 미생물이다. 사실상 세균은 지구 표면의 살아 있는 모든 미생물 중에서 가장 혼하다. 세균은 핵막이 없 어서 원핵세포라 부른다. 전균, 원생동물, 다른 진핵세포 생물들과는 달리, 그들의 핵질은 세포질로부터 분리되어 있지 않다. 세균 세포벽 은 주로펩티도글리칸으로구성되어 있고 이분법에 의해 생식을 한다. 유전 물질의 교환은 접합 con j u g a ti on 과 형질 도입 t ransduc ti on 에 의해 서 수행된다. 집합에는 결합쌍을 이루는 공여 세포와 수용 세포 사이
에 많은 양의 유전 물질 이동을 포함한다. 형질 도입은 세균을 공격한 바이러스(박테리오파지)에 의해서 DNA 의 직접적인 유전적 이동을 포 함한다. 일반적으로 생물뿐만 아니라 세균 사이에 있는 기본적인 생리적 차 이들을 기술하는 데 에너지원과 탄소원이 이용된다. 에너지원으로서 빛을 활용하는 것은 광영양적 p ho t o t ro p h ic이라 하며, 화학적인 데서 에너지를 얻는 것은 화학영양적 chemo t ro ph ic이라 한다. 만약 이산화 탄소가 세포의 탄소원으로서 사용된다면 그 생물은 무기영양적 l it ho t ro ph i c 이라 한다. 만약 탄소가 주로 유기물로부터 얻어전다면 그 생물은 유기 영양적 or g ano t ro ph i c 이라 한다. 본질적으로 무기 영양적 , 그리고 유기영양적이라는 용어는 각각 독립영양적, 그리고 종속영양 적이라는 용어에 해당한다. 알려진 상당한 수의 세균 종들은 화학적 유기영양적 chemoor g ano t ro ph ic이며, 흔히 종속영양 생물이라 일컫는 다. 광 무기영양 생물 p ho t o lit ho t ro p h~ 託든 고등 식물, 대부분의 조 류, 시아노박데리아, 녹색유황 세균gr een sulpu r bacte r ia 들이다. 화 학 무기영양 생물 chemo lit ho t ro p h 혀計논 여러 가지 에너지원을 이용하 는데 예를 들면 NH4+, N02-, Fe2+, S20/-들 이다. 절대적 화학 무기 영 양 생물 obli ga te chemol it ho t ro p hs 은 그들 자신의 세포 구성 물 질을 대사하는 대부분의 다른 생물들에서 보이는 바와 동일한 기본적 인 생리적인 회로(캘빈 회로)를 사용한다. 유기 탄소의 의부 공급원을 사용하는 데 명백히 나타나는 무능력은 세포막을 통해서 유기 분자의 이동을 촉매하는 두과효소p ermeaseS7} 없는 것과 연관이 있을 가능성 이 크다. 유기 분자들은 세포 내에서 생산되어야 한다. 에너지와 세포 탄소원에 기반을 두지 않고 다른 생리적 특칭들의 차 이를 분류에 이용하는 문헌들도 있다. 가장 잘 알려진 것 중에 하나가 W i no gr adsk y에 제 안된 자생성 au t och t honou 러 발효성 zym o g e nous
의 구분아다. 자생성 종들은 쉽게 산화할 수 있는 기질이 없는 토양에 서 천천히 성장하는 생물들로 정의된다. 발효성 종들은 토양에 새로운 기질들이 참가될 때 갑작스레 활동의 증가를 보안다. 이 개념들은 가 치가 있으나 개별 속g enus 이나 종 s p e ci e 혜 7 자생성과 발효성으로 지명 하기는 어렵고 부당하다. 하나의 주어진 종이 어떤 학자들에게는 자생 성에, 다른 학자들에게는 발효성에 속하는 경우가 많이 있다. 먹이 공급과 관련해서 어떤 한 종의 밀도를 조사하는 생태학적 이론 은 r 과 K 선택 개념을 포함한다. 풍부한 에너지원이 공급되고 있는 조건에서 살아가는 것에 적응된 생물종을 K 선택적이라고 한다. 이것 은 떼지어 많이 몰려 있지 않은 그러나 아마도 물리적으로 제한적인 환경에 사는 r 선택종들에 영향을 주는 것들과는 다른 선택압에 노출 되어 있울 것이다. 몰려 있지 않는 환경에서 기질의 갑작스런 공급에 노출된 r 선택종은, K 선택종의 경우 나타나는 것 같은 경쟁보다는 일 정량의 먹이당 높은 성장 증가에 프리미엄을 주게 된다. 보통 뿌리 주 변 생물들과 식물 병원균들은 K 선택적인 반면에, 풍부한 기질에서 자라는 대부분의 토양미생물은 r 선택이다. 염색에 의해서 나타나는 세균 세포들의 형태적인 특성들은 분류학적 으로 쓸모가 있으나, 불행하게도 그 자체만으로는 만족할 만한 생리적 구분에는 적용되지 않는 경우가 자주 있다. 세포 모양이 간상, 구상, 나선형이거나 편모와 내생포자의 유무-가 널리 사용된다. 그람 염료에 대한 반응도 역시 쓸모 있다. 그람 양성은 KI 용액, 알코올, 대조영 색에 처리된 후에도 크리스탈 바이올렛을 잃지 않고 간직하고 있는 세 포들을 지명한다. 그람 음성은 이들에 의해서 크리스탈 바이올렛이 탈 색되는 세포들을 의미한다. 다음 내용들에는 찰 알려진 세균 속들의 약간에 대해서 간단히 기술 한다. 토양 과정에서 우세성과 참여 정도에 관해서 제시하는 참고사항
들이 이미 발표된 문헌들에 바탕을 두고 있는데 이들 문헌이 시험관 내에서 분리하고 배양하기 쉬운 종에 대해서 편파적으로 기술하고 있 울지도 모른다는 접을 독자들은 유의해야 한다. 4-3 기 아스로박터 평판계수법으로 측정할 때 아스로박터 A rt hroba ct er 속의 구성원들 은 토양에서 수적으로 우세한 세균이다. 어떤 추정치는 전체 평판계수 개체군의 40% 정도된다. 그들은 다형태성p leomor ph i sm 과 그람 변성 의 특징을 가진다. 그둘 세포는 성장의 초기 단계에서 가느다란 그람 음성 간상이며 후기에는 매우 짧은 간상 또는 구상의 그람양성으로 된 다. 매우 긴 간상과 가지가 새 기질에 접종된 지 2 시간 내에 관찰된다 (그림 4.1). 많은 아스로박터들은 종종 그냥 지나칠 정도의 미약한 운 동성을 보여 준다. 토양에서 그들의 수가 많은 것에서 예상되는 바와 같이 다양한 기질들이 그들의 산화성 대사과정에 사용된다. 어떤 연구 에서 시험된 180 가지 화합물 중에서 85 가지가 이용되었다. 아스로박 터들은 천천히 자라고(그들은 한천 배지 표면에 작은 군락울 형성한다) 쉽게 분해되는 물질(당류, 아미노산들)이 다른 속들에 의해서 빠르게 흡수되는 시기인 유기 쇄설물의 분해 초기에는 경쟁력이 약하다. 4-3-2 스트랩토미세데스 세 가지의 속 Str e p tom y ce s, Pseudomo 血:s, Bac i llus 의 세균은 토 양에서 흔히 나타나고 있는 점에서는 아스로박터와 경쟁자로서 다툰 다. 셋 중 어느 하나는 여러 시기에 평판계수로 셀 때 전체 세균 수의 5-20 %를 차지한다. 세균계 내에서 S t re pt omy ces 는 방선균목에 속한
 그림 4 . I Ar thr obacte r g lob ifo rm is에서 일어나는 형태 변이
그림 4 . I Ar thr obacte r g lob ifo rm is에서 일어나는 형태 변이
다. 토양에서 혼한 다섯 속의 주요 특칭은 표 4 .1 과 같다. 토양에서 분리한 방선균 균주들 약 90 %가 S t rep t omy ces 속을 차지 할 수 있다. 이들은 한천 배지에 잘 발달되며, 밀집되고 가지가 진 균사체 m y ce li um 와 빽빽하게 찬 군락을 생산한다. 생식은 풍부한 기균사포자 aeria l sp o res 생산과 균사 단편화에 의한다. 스트렙토미세테스는 그람 양성이며 산화성 유기영양 생물이다. 그들은 침수된 토양에는 견디지 못하고 건조에는 진균보다 약하며 일반적으로- 산에 잘 견디지 못한다. 그리하여 감자병을 일으키는 미생물인 St re p tom y c es scab i es 는 모래 같은 완충력이 약한 토양에서는 p H 를 낮추는 유황이나 황산암모늄의
 표 4.1 토양에서 발견되는 몇몇 방선균 속들의 주요 특징
표 4.1 토양에서 발견되는 몇몇 방선균 속들의 주요 특징
처리로 쉽게 방제된다 . 많은 스트렙토미세트들은 세균, 전균, 조류, 바이러스, 원생동물, 종창에 작용하는 다양한 항생제를 생산한다. 토양미생물학자 S.A. Waksman 은 스트렙토마이신의 발견으로 1942 년에 의학 부문의 노벨 상을 받았다. 스트렙토미세테스는 수십 종의 항생제와 게오스민 g eosm i n 을 생산한다. 게오스민은 새로 갈아엎은 토양에서 나는 냄새 의 주범이며, 적어도 토방과 오래된 짚더미에서 나는 진균 냄새의 부 분적인 공범이다. 4-3-3 슈도모나스 슈도모나스 Pseudomonas 속의 미생물들은 그람음성이며 똑바르거나 구부러진 막대 모양으로 몸의 한쪽 끝에 편모가 있다. 그들은 질산염 울 선택적인 전자수용체로서 사용하는 탈질균을 예의로 하고는 호기성 이다. 대부분의 이 종들은 유기영양적이다. 약간은 수소 (H2) 와 일산 화탄소를 에너지원으로 사용하는 임의성 무기영양 생물fa cul t a ti ve lit ho t ro p hs 이다. 슈도모나스는 토양뿐만 아니라 민물과 바닷물에도 있다. 어떤 종들은 식물의 병을 일으키는 반면에 많은 비병원성들은 식물과 아주 가까이 연합되어 있다• 하나의 그룹으로서 슈도모나스는 당류, 아미노산, 알코올, 알도오스 aldose, 탄화수소, 기름, 부식산, 여러 종류의 합성 살충제들을 포함하는 넓은 범위의 유기 기질들을 공 략한다. 여러 종들은 특히 철분이 결핍된 배양액에서 확산하는 성격을 가전 형광 염료를 생산한다. 플루오레신fl uoresce i n 에 결합된 시더로 포어 s i dero ph or 혀~ Fe3+ 에 아주 큰 친화력을 가지고 철의 운반에 EDTA(eth y le nedia m i ne te t r a acetc a ci d) 와 비슷한 작용을 한다. 시더 로포어를 생산하는 슈도모나스는 토양에서 발생하는 식물 병원균들을
생물학적으로 방제하는 데 이용될 수 있다는 증거가 있다. 철의 이용 도가 낮은 알칼리성 토양에서, 슈도모나스는 병원균들로부터 철분량 울탈취해 버릴 수 있다. 슈도모나스와 가까운 관계에 있는 크산토모나스 Xan t homonas 속은, 산소 분자가 유일한 전자수용체며 질산염을 환원할 수 없다는 점을 예 외로 하고는, 슈도모나스와 비슷한 종들로 구성된다. 크산토모나스에 속하는 몇몇 종들은 많은 식물에 대해서 병원성이다. 그들 속 내에는 단지 숙주식물 반웅들의 특이성에 의하여 모식종typ e s p e ci e~ 공로부터 구분되는 아주 많은 명명종 nomens p e ci es 이 있다. 4-3-4 포자를 만드는 간상균 간상균의 구성원들은 그람잉정과 그람염색이 변하는 막대 모양이 다. 대부분의 종들은 운동성이 있다 . 열에 저항성이 강한 내생포자가 만들어지고, 포자 형성은 공기에 노출되어도 억제되지 않는다. 포자 를 만드는 간균은 대부분 왕성한 유기영양 생물이며, 그들의 대사작용 은 엄격한 호흡적 또는 발효적 또는 둘 다이다. 포도당 발효 과정 동 안 다른 종들에 의해서 생성되는 생성물들의 나열에서 나타나는 바와 갇이 이 속에는 아주 큰 종의 다양성이 있다. 발효 과정에는 글리세 롤, 2, 3- 부타네디올 (2, 3-buta n edio l ), 에탄올, H2, 아세돈, 포름 산, 아세트산, 젖산 및 숙신산과 같은 것들이 생산된다. 어떤 종들은 유기 탄소가 없을 때는 H2 를 에너지원으로 사용하는 임의성 무기영양 생물이다. 한 종 (B. p oly myxa)은 N2 를 고정하는 것으로 알려져 있다. 여러 종은 다른 세균에 대해서 파괴적인 분해효소 l ytic enz ym여골과 폴 리펩티드 급의 항생제를 생산한다. B. t hu ringi e nsis에 의해 생산되는 독성 물질은 약간의 곤충 유충들에 병원성이므로 생물적 방제 인자로
널리 사용되고 있다. B. macerans 는 아마섬유를 부드럽게 하는 데 널리 이용되고 있다. B. an t hrac i s는 동물에 아주 강한 유독성을 가 전 병원균이다. 이 속의 세균들은 온도에 대한 내성 범위는 약 —5 -75°C 이며, 산에 대해서는 pH 2 내지 8 에서 견디며, 25% 정도 높은 NaCl 농도에서 견디는, 영에 대한 내성을 가진다. 클로스트리디움 Clostn diu m 또한 포자를 만드는 속이다. 대부분의 이 종들은 엄격한 형기성이나, 몇 종은 미세호기성 m ic roaero p h ic이 다. 한천 표면에 작은 군락들을 형성하지만 공기가 있으면 포자를 생 성하지 않는다. 이 속은 경제적으로 중요하다. 그 종들은 알코올과 상 업용 용매들의 생산울 위해서 상업적으로 사용된다; 여러 종(C. bu tyri cum 과 C. p as t eu ria num) 들이 N2 를 고정하는 것으로 알려져 있 다. 이 속은 토양, 바닷물 및 민물 침적토, 분뇨와 또한 동물의 내장 에 널리 분포한다. 잘 알려진 동물에 대한 병원균은 C. te ta n i와 C. bo t ul i num 으로서 그것의 포자는 토양에서 아주 오랫동안 지속적으로 존재할수있다. 위의 속둘은 토양에서 매우 혼한 발생 때문에 간단하게 기술되었다. 그들은 토양에서 탄소 및 다른 영양소들의 변환에 여러 가지 정도로 참여한다. 토양에는 수백에 이르는 세균 속과 수천 종이 있기 때문에 많은 생 물군-들을 포괄하려는 시도는 현실적이지 못하다. 다음 속들은 토양미생물학 문헌에서 흔히 나오는 것으로서 그들의 이름을 간단히 소개하는 정도로 표시한다. 아조토박터 Azo t obac te r 는 공생적인 관계를 이루지 않고 N2 를 고정 하는 호기성 유기영양 생물이다. 비공생적으로 N2 를 고정하나 널리 알려 지 지 않은 다론 속들은 Azomonas, Beij eri n c ki a, Derx ia, Azo spiri llum 이다. Rh iz ob i um 과 Brady rh iz ob i um 은 공식적으로 N2 를 고정하는 널리 알려진 속이다. 그들 세포는 콩과 식물 뿌리털로
침투하여 뿌리속 형성을 유도하고 세포 내의 공생자로서 자란다. 관련 속으로서 A g robac t e ri um 은 식물에 머 리털 모양의 가는 뿌리 같은 혹 또는 이상비대를 유발하나 N2 를 고정하지는 않는다. Ni tro somonas 와 N it robac t er 는 토양에서 질산화 작용을 일으키는 것으로. 오랫동안 알려진 화학적 무기영양속이다. 전자는 NH4+ 를 N02-로, 후자는 N02- 롤 NO J-로 변환시킨다. Lac t obac i llus 속의 미생물들은 식물의 잎 줄기 부분과 긴밀한 관계 를 가지기 때문에 언급할 가치가 있는 발효성의 유기영양 생물이다. 그들의 젖산 생산은 사일로의 꼴, 버터, 독일김치, 신맛이 나는 빵을 만드는 데 여러 가지로 이용된다. Ente r obacte r 역시 발효성인데 혼 히 동물의 배설물과 오수에서 발견된다. 그러나 어떤 종들은 토양과 식물에 널리 분포한다. 사탕수수를 자른 것과 동상을 입은 목화열매에 풍부하게 자라는 E. cloacae 는 사당수수 분쇄기와 조면기를 디루는- 일 꾼들에게 독성이 있는 먼지를 일으키는 식물성 물질을 생산한다. Cy t op haga 는 활주 세균의 한 구성원이다. 어떤 종들은 한천 배지 갇 은 수분이 있는 표면에서 1 분에 lO µm 정도로 빠르게 미끄러져 갈 수 있다. 이 속은 셀룰로오스를 분해하는 데 매우 활성이 높다. 유황과 금속류를 변환시키는 데 활성적인 여러 세균 속들은 뒤에 있는 장들에 서 이름을 언급할 것이다. 4-3-5 시 아노박테 리 아 원핵생물계는 세균과 시아노박테리아라는 두 개의 문을 포함한다 (Buchan 터 Gib b ons (1974) ) . 앞의 문단들에서 이름이 나온 속들은 세균에 속한다. 시아노박데리아는 영록소와 파이코시아닌p h y cocya ni n 갇은 파이코빌단백질 ph yc o bil ipr ote i n 색소를 포함하여 광합성을 하는
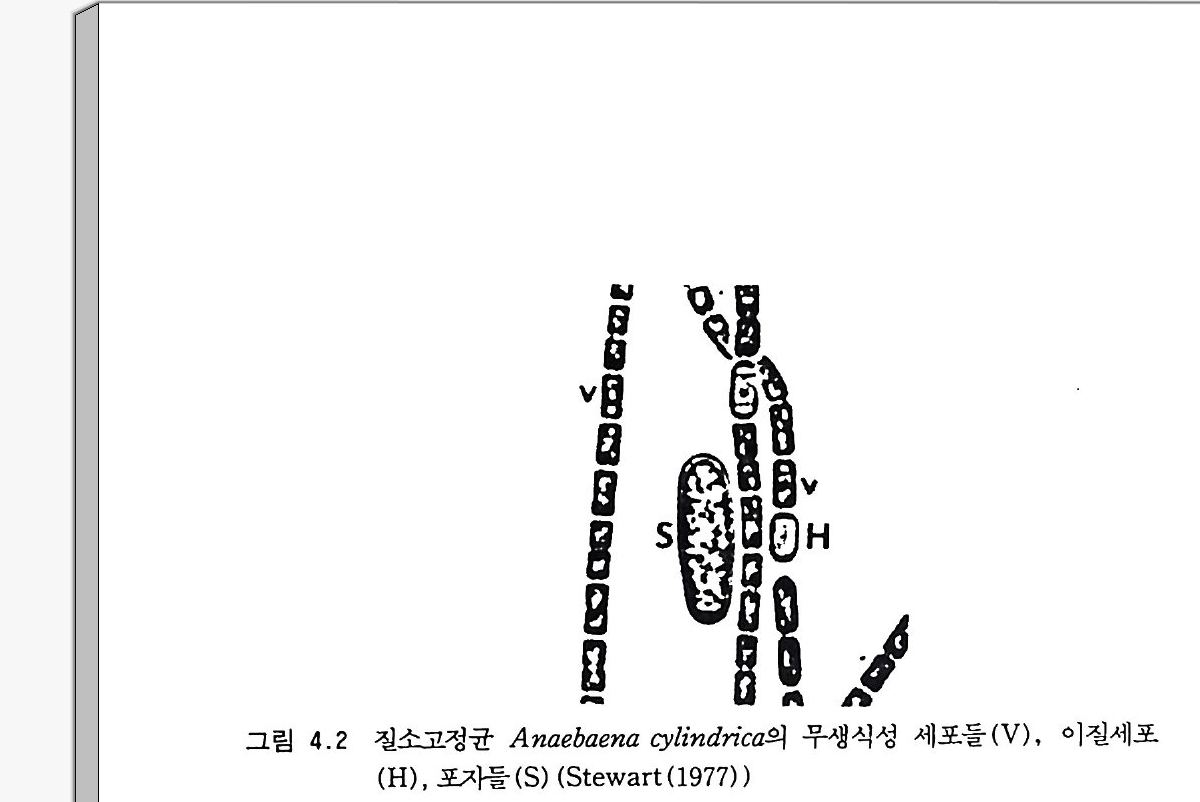
원핵성 생물이다. 조류학자들은 남조류 blue- gr eens7} 고등식물 또는 조류와 유사한 엽록소를 함유하기 때문에 조류로 분류되어야 한다고 주장한다. 광합성 세균둘은 여러 종류의 세균성 엽록소들을 포함하 고, 남조류와 고등식물들처럼 광합성 동안 유리 02 를 방출하지는 않 는다. 시아노박테리아는 단세포, 군재 사상체의 단위로 존재한다(그립 4.2). 굳은 초 shea t hs 에 싸이지 않은 단세포들, 생석세포, 또는 단위와 사상체 형태들은 종종 활주운동성을 나타낸다. 세포질은 바깥 표면이 특징적인 색 소 입자를 포함하는 광합성 라멜라 (티라코이드t h y laco i ds 라 불린다)가 짝을 이룬 구조로 되어 있다. 세포벽은 복잡하거나 다층으로 되어 있으며 그람음성 세균의 세포벽처럼 펩티도글리칸과 분해효소에 의해서 용해되는 점액질 중합체를 함유한다. 의부에는 점액질 초가 흔히 있는데 종종 뚜렷 하게 정의되는 바깥 경계가 없기도 하지만 없기도 하지만 보통은 점액질 다당류와 펙틴산p ec ti c ac i ds 으로 이루어져 있다. 생식은 세포분열에 의 해서 일어나고 수종의 내생포자, 의생포자, 비운동성 포자 a t k i ne t es 와 같은특수화된 세포를포함한다. 단세포성 시아노박테리아는이분법, 다분 법 또는 한쪽 끝에서 연속적으로 의생세포를 방출하여 생산한다 . 사상체 는 무작위적인 단편화와 한쪽 끝에서 연쇄체 horrno g on i a 라 하는 짧은 운동성 세포 고리들의 방출로 생식한다. 어떤 사상체들은 비운동성 포자와 이형포자 he t eroc y s t s 를 생산한다. 비운동성 포자는 발아하여 하나의 연 쇄체를 생산하는 지나치게 커진 휴면기의 무성생식성 세포이다. 이형세포 는 굴절성 입자들과 두꺼운 외벽을 가지는 접에서 인접한 무성 생식성 세 포들과는 구별되는 비생식성 세포이다 . Bold 와 W yn ne (1989) 는 남조류를 세 개의 목으로 분류하고 있다. 곤봉남색말목(내생포자와 의생포자를 생산하는 포자성인 것), 소구체목 (단세포 또는 군집을 이루나 포자를 생산하지 않음), 혼들말목(사상체이고
 a'
a'
포자를 만들지 않음). 다른 학지들은- 사상체의 특징들을 이용하여 마지 막 목을 흔들말목과 참가시남색말목의 두 개로 나눈다. 시아노박테리 아는 도처에 분포되어 있어서 소금물, 민물, 토양, 바위, 모래에서 나타난다. 토양 모재에서 그들은- 독립적인 또는 지의류에서 진균과 공 생관계를 가지는 첫 이주자로서 중요하다. 시아노박데리아는 또한 우 산이끼, 물고사리, 피자식물과 같은 식물체 내에서 발생하기도 한다. 어떤 생태계에서는 시아노박테리아가 질소를 고정하기 때문예 아주 커 다란 의미를 가지기도 한다. 어떤 비이질성 속 (Gloeo t hece) 은 질소를 고정하는 것으로 알려져 있기는 하지만, 이질 세포가 있을 때는 그것 이 특히 활발한 고정 장소이며 고정된 질소가 이질 세포로부터 이웃한 무성생식성 세포들로 이동한다는 좋은 증거가 있다. 시아노박테리아와 다른 생물에 의한 생물적 질소고정에 관한 논의는 제 1 硏 H 卜 참고하기 바람.
4-4 진균 진균은 사상균, 노균병균, 녹병, 깜부기, 효모, 버섯과 말불버섯으 로 지칭되는 여러 진핵성 생물들을 포함한다. 토양 생물 중에서 하나 의 그룹으로서 진균은 평판계수에서 세균의 수보다 작지만, 주로 유기 물 조각들의 분해를 맡고 있는 유기영양 생물이다. 진균은 형태학적인 특징에 의해서 몇 개의 하위 분류군들로 나누어진다. 전형적으로 진균 은 가는 사상체 또는 균사를 형성하며 이들은 격막이 있거나 없으며 흔히 다핵성이다. 집합적으로 균사는 균사체 my ce liu m , 육질체 soma, 또는 영상체 t hallus 를 이룬다. 그러한 형체들은 직경이 수십 센티미터 에 이를 수도 있으며 육안으로 쉽게 확인된다. 진균 세포벽의 구성 물 질은 표 4.2 에 나타나 있다. 토양에 흔히 존재하는 &W 의 진균 강의 특성들은 표 4.3 에 요약된다. 여기에 나오는 참고사항들은 단지 토양 진균을 매우 제한적으로 다루고 있다는 것을 강조해 둔다. 더욱 적당 한 내용을 위해서 독자들은 A i nso wt h 와 Sussman(1 9 65-1973), Alexop o ulos 와 M im s (1979) , Ross (1979) , Gi lm an (1957) 과 Domsch 등 (1981) 의 문헌들을 참조하면 된다. 4-4-1 점균류 세포성 점균강 Acras i om y ce t e s.g. 세포성 점균류 cellular slim e molds 이다. 구조의 단위는 세균을 집어삼켜 포식하는 단핵성 아메바다. 개 별적인 세포들은 세포들이 융합되지 않았으나 하나의 운동성 공통체 단위로서 행동하는 특칭적인 Pseudop lasmod i um 으로 집합되어 있다. Pseudop lasmod i um 은 자실체인 조포낭 s p oroca rp으로 변하는데 , 이는 무성 포자들을 포함하고 있다. 세포성 접균강은 습기 많은 환경에서
 표 4.2 진균 세포벽의 구성 성분들
표 4.2 진균 세포벽의 구성 성분들
썩어 가는 식물성 물질에서 나타난다. 세균을 잡아먹기 때문에, 유기 물 분해의 주요 원인 생물로 간주될 수 없다. 이들에는 8 속이 있으며 D i c ty los t el i um 은 토양에서 분리하기 비교적 쉽고 가장 잘 알려져 있 는속이다. 전점균강 M yx omy c ete s . g. 진정한 점균류이다. 비세포성 포복 변형 acellular creep ing p lasmod i um 을 형성하기 때문에 동물계에 포함시켜 야 한다고 제안되기도 한다. 먹이 섭취, 변형에서 동물 같지만, 생식 구조와 포자 형성에서는 진균 같다. 토양에 널리 분포되어 있는데 특 히 차고 습진 장소에서 썩고 있는 식생들과 관계되어 있다. 어떤 종들 은 식물의 잎 줄기에, 어떤 종들은 동물의 배설물에서 발생한다. 직경 50cm 또는 그 이상에 달하는 변형들이 때때로 초본류에서 눈에 띄지
않게 끈적한 덩어리로 출현하기도 한다. Phy samm 속은 그 수가 100 종 이상에 달하는데 가장 큰 속이고 진균의 형태학적 생리학적 연구 에 실험실에서 널리 사용되고 있다. 4-4-2 편모성 진균 난균강 Oom y ce t es은 물과 토양에서 나타나며 많은 것들이 식물에 대해서 파괴적인 병원성을 가지고 있다. 유주곤자라 불리는 이편모 무성 생식 운동성 포자를 생산한다는 점에서 유일무이하다. Pyt h i um 과 Phy t op h t ora 는 가장 흔히 접 할 수 있는 속둘이 다. Pythi u m deba rya num 은 묘목이 말라 시드는 병의 원인이 된다. Phy top h t o r a i nf e s ta ns 는 감자의 고조병을, Plasmop ar a v iti cola 는 포도의 흰가루 병을 일으킨다. 마지막 종은 보르도액이라는 비산구리 화합물 살균제 에 의해 방제된 첫 생물이다. Sap roleg n i a 속은 흔히 물곰팡이라 불리 는 부류에 속하나 그 종 중 많은 것들이 토양에도 나타난다. 주머니균강 Ch yt r i d i om y ce t e~ 특히 수서 환경에 많이 출현하나 토 양에도 흔히 나타난다. 몸의 한 쪽에 하나의 편모를 가지는 운동성 포 자의 생산은 그들을 다른 진균과 구분되게 한다. 어떤 구성원들은 조 류, 고등식물 또는 곤충의 유충에 기생한다. 이에 속하는 속 중에서 토양에 흔히 보이는 것은 Allomy ces 와 Ph i zop hy d i um 이다. 4-4-3 당진균 접합균강 Z yg om y ce t e~ 다양한 탄수화물 기질에 대한 발효성 때문 에 당진균이라 불린다. 보통 다핵체 coenocy tic hyp h a~] 찰 발달된 균사체, 무성포자낭 포자와 두꺼운 벽을 가전 휴식 접합포자를 생산한
다. 대부분 죽은 시체에 산다. 어떤 것은 식물에 병원성이며 어떤 것 은 다른 진균에 기생하고, 어떤 것은 동물을 포획하는 기작을 가진다 . 털곰팡이목(접합균강에서 가장 큰 목)은 경제적으로 중요하다. 각 종들 이 알코올과 젖산, 구연산, 옥살산 또는 푸마르산 같은 유기산들의 상 업적인 생산에 이용된다. 수 개의 속(예를 들면 Mucor, M y co typ ha) 에 속하는 종들은 형기성 상태에서 자랄 때, 혹은 높은 농도의 포도당( > 5%)이 있으면 호기성 상태에서 자랄 때조차 효모의 형태로 남아 있 다. Rhiz o p us n igri cans 는 혼한 뻥년쳉戶]다. 4-4-4 고동 진균 자낭균강 Ascomy ce te S il} 담자균강 Basid i o m y c ete ~ 때때로 고등 진균 h ig her fu n gi에 속한다. 전자는 유성생식으로 이어지는 자낭포자 (ascospo res, 흔히 4 또는 8) 들이 만들어지는 주머니 또는 자낭 ascus ¾ 형성한다는 점에서 디른 진균들과 구별된다. 자낭울 형성하는 효모, 곰보버섯 (식용 버섯의 일종) , 송로, 반균, 흰가루병곰팡이 , 흔히 검은 색을 띠는 사상균들이 자낭균류에 포함된다. 많은 종들은 토양에서 죽 은 식물에 기생하는데, 균사체는 땅 속에 남아 있으나 일정한 간격으 로 매우 큰 자실체를 위로 내보낸다. 자낭균류는 사람들에게 넓은 범 위의 영향을 미친다 . 많은 것들이 식물에 기생하여 뿌리 부패증, 옥수· 수 알 부패증, 핵과의 갈색 부패증, 흰가루병들을 일으킨다. 자낭균 인 Endoth i a p aras iti ca 는 밤나무에 치명적이고, Cerato c y s ti s u lmi 는 미국느릅나무에 치명적이다. 맥각균 er g o t fun g us (Clavic e p s pu r- p urea) 은 벼과 식물의 생식 구조에 침입하고 사람과 동물들에 알카로 이드성 독성 물질을 생산한다. Chae t om i um 에 속하는 종들은 특히 셀룰로?人쿠 된 직물에 심한 훼손을 준다. 유용한 측면으로, 효모
Saccharom y ces 의 발효성 활동은 오랫동안 맥주, 와인 공업, 제빵에서 활용되어 왔다. 담자균강은 버섯과, 말불버섯, 선반버섯과 걸상버섯, 찻잔버섯, 목 이, 깜부기, 녹병 같은 진균의 넓은 부분을 포함한다. 담자균강은 담 자 bas i d i um 라고 부르는 특수 구조물 위에 담자포자 bas i d i os pores 를 생산한디는 점에서 다른 전균과는 다르다. 식물 기생균으로서, 담자 균강은 경작물과 수목에 천문학적인 손실을 초래한다. 특히 깜부기, 곡류 식물 줄기의 녹병, 삼림과 음수의 병, 목재와 목재 구조물의 부 패로 특히 엄청나게 큰 손상을 입히고 있다. 녹병균목 Ured i nale~ 종들은 특히 식물 녹병을 일으키는 요인으로서 특히 고약하다. 수천 종이 여기에 포함되는데 그들 가운데에는 곡류의 검은 줄기 녹병, 잣 나무 녹병 들을 둘 수 있다. 유익한 측면으로는 식물과 균근울 형성하 는 관계, 식용으로 버섯을 재배하는 것과 같은 상업용의 생산이 있다. Ag a r icu s brunnescens 는 말똥 거름에서 상업용으로 널리 양식되고 있는 종이다. 많은 다른 것들 가운데 Boletu s edul is 는 흔히 채취되는 식용의 야생종이다. 많은 독이 있는 속 (예를 들면 Amanita , Cop rinu s, Clito cy b e, Ps i locy be) 들이 주름버섯목 A g a ic ale 혀 1 있다. 이 목에는 또 한 제 11 장에서 논의되는 많은 균근의 진균이 포함된다. 담자균강은 서 있거나 쓰러진 통나무, 나무 그루터기, 목재 생산물 같은 물질의 왕성한 부패자다. 부분적으로 산화된 검은색의 리그닌을 남기기 때문에 이름이 붙여전 갈색 목재 부후군의 인자들은 셀룰로오 스를 부패시키나 리그린은 부패시키지 못한다. 흰부패증은 셀룰로오 스와 리그닌을 모두 파손시키는 전균에 의해서 생긴다. 나무를 부패시 키는 것들 중에 중요한 속들은 Fomes, Polys po rus, Pori a, Armi lla r- iel la 등이 있다.
4-4-5 불완전 진균 불완전균강 Deu t erom y ce t e g.g. 격막이 있는 균사를 가지나 지금까지 단지 분생자 cond i a 에 의해서 생식하는 것으로 알려진 진균을 - 포함한 다. 유성생식 기간이 없기 때문에 불완전 진균 fun gi i m p er f ec ti이라고 불린다. 유성생식 단계가 처음 명명된 오랜 후에 발견되어 이 종들은 다른 강(보통 자낭균강, 간혹 담자균강)에 포함시킬 필요가 있을지도 모 른다. 어떤 균학자들은 불완전 진균의 많은 것들이 유성생식기가 거의 형성되지 않거나, 자연에서 잘 관찰되지 않거나, 아니면 생활사로부 터 떨어져 나온 자낭균강의 분생자 단계를 나타내는 것으로 믿는다. 준유성생식 생활사가 이들의 일부에서 발견되기 때문에 그러한 진균은 결코 유성생식 단계를 가지지 않을 가능성도 역시 있다. 불완전균강에 포함되는 하나의 하부 그룹이 〈균사형 불완전균류〉로 지명된 것이 있 다. 이 구성원들은 분생지를 생산하지 않는다. 생식은 균사의 분절에 의한다. 토양에서 대부분의 불완전균강은 사물 기생성이나 많은 것들은 다른 진균, 고등식물, 인간과 다른 동물에 기생한다. 하나의 그룹으로서 불완전 진균은 너무 많고 너무 다양해서 몇 개의 문단으로 논의를 끝 낼 수 없다. 다음 장은 특수한 사건들 또는 전환 과정에 참가하는 몇 몇 속을 인용할 것이다. 토양미생물학 문헌에서 흔히 접하게 되는 속 명 들 은 Aspe r ill us, Penic illi u m , Tric h oderma, Fusariu m, Cladosj )o ri um , Ar thr obotr ys, Gl iocl adiu m , Helmi n th o sp o riu m 을 포함한다. Rh iz oc t on ia속은 균사형 불완전균류의 하부 그룹의 실례가 된다. 주요 분류 기준의 요약을 표 4.3 에, 대표적인 구조를 그림 4.3 에서 보여 준다.
 l’ \广泊111 bH훑止 h IU m
l’ \广泊111 bH훑止 h IU m
표 4.3 토양 및 식물과 연관된 진균의 특성 진균군 7J - 특칭 대토표양적내인의속 둘 점균류 세포성 접균강 단핵성의 점액아메바, 헛원형체 Dicty lo seliu m 포자피가 무성의 포자를 생산. 썩고 있는 식물에서 세균을 먹 는다. 진접균강 진점 (변형)균류, 세포성이 아닌 Phys arum 포복성 변형체가 동물 같으나 곰팡이와 같은 생식구조를 생성 한다. 편모균류 난균강 포자체 내에 이편모성 난포자를 Phth i u m , 생산, 배우자 접합 ( ? )으로 생 Plasmop ar a 식 Phyt op ht h o ra Sap ro leg n ia 주머니 주머니균강 수서환경 , 극성 (몸의 한 쪽에 Allomy c es, 균류 치우쳐 있는)단편모가 나중에 Rhiz o p hy d iu m 운동성의 동물성 포자가 된다. 약간은기생성이다. 당균류 접합균강 무격막의 다핵성 균사, 내생성 Mucor, 포자와 두꺼운 벽을 가진 접합 My c oty ph a, 포자, 대부분 사체 기생 , 약간 Rhiz o p us , 은 식물에 병원성이거나 다른 Zyg o rhy n cus 진균에 기생 고등균류 자낭균강 핵분열과 감수분열로 형성되는 Endoth i a , 자낭포자를 가지는 주머니나 자 Cerato c y st u s, 낭이 있다. 죽 유성 단계 , 단세 Clavic e p s , 포성 이스트 또는 분리된 균사 Saccharomy c es 를가짐 담 XH! 담자균강 분리된 균사, 유성생식성 포자 Ag a ri cus , 가 김수분열로 생성되고, 담자 Pori a, 위에 의생적으로 붙어 있다. 많 Boletu s , 은 버섯과 녹균들 등 Fames
진균군 강특칭 대표토적양인내 의속 둘 불완전 불완전균강 격막이 있는 균사가 단지 무성 As pe rgi llu s, 균류 생식성 분생자에 의해 번식한 Tr ich oderma, 다. 유성생식 단계가 있으면 보 Pencil li u m , 통자낭균류 Helmi mt l w s po riu m , Fusari um , A rthr obotr ys (균사형 불완전진균강의 아군, 분생자를 Rhiz o cto n ia 불완전균강 ) 생산하지 않는다. 균사의 분절 로생식한다
4-5 조류 진핵생물인 조류는 연못 더껑이, 물이끼, 해조라는 다른 이름으로 불리는 것들을 포함하고 있다. 조류는 영록소가 있는 가장 단순한 진 핵생물로, 유성생식적 특칭에 의해서 다른 녹색 식물들과 구분할 수 있다. 단세포성 조류는 개체 전체가 배우자로서 기능을 가진다(유성생 식 세포). 다세포성 조류에서는 배우자들이 단세포 또는 다세포에서 생산되는데 모든 배우자 세포 ga meta n g ial cell7} 하나의 배우자를 생 산한다. 무성생식에서 조류는 편모를 가져서 운동성이거나 편모가 없 는 비운동성, 또는 때로 운동성이다가 때로는 비운동성인 포자들을 생 산한다. 조류는 의심할 것도 없이 모든 녹색 식물 중에서 가장 널리 분포되 어 있다. 그들은 수서 환경에서 가장 우세하게 나타나는데 담수, 기 수, 해수에서 나타난다. 영분에 대한 내성은 소금기 0-100% 가까이 에 이르는 범위를 보인다. 수서 조류는 부유성이거나 저생성 (바닥에
고착되어 있는)이다. 육상에 사는 형태들은 토양 위, 안, 바위 위, 진 흙탕, 모래, 눈발, 빌딩 위 등에 나타나며, 식물(줄기, 껍질, 잎)과 동물에 붙어 있기도 한다. 젖은 상태의 조명이 있는 조건에서 저장된 심층의 토양 시료들은 흔히 조류의 물꽃현상을 일으킨다. 지하에 나타 나는 대부분의 조류 단위들은 휴식 상태에 있는 형태들이나 어떤 것은 임의성 유기영양 생물들이다. 초기의 분류는 거의 색소의 특성에 의존했다. 하위 그룹들은 녹조, 갈조, 홍조, 규조류 들이었다. 규조류의 특칭은 유기 껍질과 규산으 로 이루어전 단단한 세포벽에 있다. 규조류의 분류는 세포벽의 구성과 그 위의 무늬 형태에 기초를 두고 있다. 조류에 대한 오늘날의 분류는 색소의 특칭, 세포벽의 성분, 세포조성, 저장산물, 편모의 비교에 기 반하고 있다. Bold 와 W ynne (l 979) 은 조류를 10 개의 주요 아문들로 나누었으며 각 문의 특징에 대한 아주 훌륭한 요약을 제안했다(표 4.4). 일반화된 많은 논의둘이 있는데 조류의 특칭, 생리학과 분류학 에 관하여 Ti ffan y (1 958), Prescott (1 968), Round(1973), Ste w ar- t (l977) 의 저서를 들 수 있다.
표 4.4 몇몇 식물성 조류의 문과중요한특성 문 동명 색소,색 소합체성 체종제들 의 세포벽 서식처 녹조식물문 녹조류 영록소 a, b. a-, 많은 셀룰로오스 FW, /3-, r- 카로틴,수종 (O(1 국)글루코 BW, 의 크산토필둘. 2-5 피라노사이드들) , SW, 티라코이드들/충 하이드로크시프로 T 린 글리코사이드 들 크실란과만난 들 또는벽이 없 음. 약간은 칼슘 집 적 윤조식물문 차축조 엽록소 a, b. ; a-, 셀룰로오스({3-(1-+ FW, /3-, y카로틴, 수 4) 글루코피라노사이 BW 종의 크산토필들. 드들), 약간은 칼슘 다양하게 연결된 티 으로 집적됨 라코 °l 드들 유글레나 연두벌레류 엽록소 a, b. /3-카로 없음 FW, 식물문 틴, 수종의 크산토 BW, 필. 2-6 티라코이 SW, 드/충 T 갈조식물문 갈조류 영록소 a, c. /3- 셀룰로오스, 알긴 FW 카로탄 수종의 크 산, 황화 뮤코폴 리 (매우 산토팔 2-6 티라코 사카라이드(푸코이 드뭄) 이드/충 단) BW, SW 황갈조식물문 황녹조류 엽록소 a,c( 약간 셀룰로오스, 실리 FW, (규조류 은 gt 없음) . a-, 카, 탄산칼슘, 접액 BW, 포함) g_, C 카로틴, 수종 질들, 약간의 키틴 SW, 의 크산토필, 황갈 또는 벽이 없음 T 조강과 규조강, 후 각편모조강에는 후 코산틴이 포함. 양 R 의 티라코이드/충
문동명 색소색, 소합체성체 종제둘 의 세포벽 서식처 황적조식물문 편모조류 영록소 a, C. /J 셀룰로오스 또는 없 FW, -카로틴, 수종의 크 음 : 점액질들 BW, 산토필 ; y粹의 티라 SW 코이드/충 은편모조 암색편모충류 영록소 a, c. a-, /3 없음 FW, 식물문 _, c- 카로틴 , 뚜렷 BW, 한 크산토필(알로크 SW 산신, 크로코산신, 모나도산신), 파이 코벌린들 엄 H 의 타 라코 o] 드/충 홍조식문문 홍조류 영록소 a, (약간의 진 셀룰로오스, 크실 FW 정홍조아강에는 d) . 란, 수종의 황화 다 (약간) R- 과 c- 파이코시 당류 (갈락탄들) 약 BW, 아닌, 알로파이코시 간은 칼슘 집적 SW 아닌. R- 과 B 파이 (대 부 코에리스린. 仕카로 분) 틴 수종의 크산토 팔 하나의 티라코 이드, 연결되어 있 지 않음 자료 Bol~ Whnne (l97 9) BW 기수 brack i sh wate r , FW 담수fr esh wate r , SW 영수 sal t wate r , T 육지 ter restr i a l 4-6 지의류 지의류는 하나의 진균 종과 조류의 연합인데, 둘은 아주 얽혀 자라 서 하나의 영상체 또는 분화되지 않는 몸을 이룬다. 전균 구성원은 보
통 자낭균이며, 가끔 담자균이거나 불완전 조류로 되어 있다. 지의류 를 이루는 자닝균들은 대충 18,00 (H든이 있으며 지의류를 이루지 않는 것은 단지 15,00~ 종 정도가 있는 것으로 추정되고 있다. 식물성 생물 은 진핵성이거나 원핵성이다. 대부분의 지의류들은· 녹조로서 흔히 Treloux i a 속이지만 가끔 시아노박테리아의 Nos t oc 속이기도 하다. 지 의류 공생에는 분류학적인 지위와 이명법의 명명이 주어진다. 하위군 으로 분류는 대부분 전균 공생자에 근거하여 이루어진다. 그리하여 자 낭지의류, 담자지의류, 불완전지의류가 있다. 공생관계에서 식물성 생물은 에너지를 포착한다. 만약 그것이 시아 노박테리아라면 질소도 고정한다. 탄소와 가끔 질소에 대한 반대급부 로 진균성 생물은 무기영양분을 공급하며 공생체의 물과 빛에 대한 요 구들의 조정울 돕는 것으로 믿어진다. 그러한 연합은 분리되면 살아갈 수 없는 혹독한 환경에서 두 공생지들의 생존을 가능하게 한다. 지의류들은 황량한 바위, 토양, 울타리의 말뚝, 지붕 꼭대기, 잎 표면, 나무껍질 같은 기타의 표면에서 관찰된다. 북극 지빙에서 그들 은 적어도 순록의 겨울 먹이의 일부가 된다. 지의류들은 흔히 헐벗은 바위, 토양 모재의 첫 이주자 중에 포함된다. 그리하여 토양 생성의 초기 단계에서 중요한 역할을 말고 있다. 일반적으로 지의류는 매우 생산성이 높은 생태계에서는 탄소와 무기영류들의 순환에 중요하지 않 다. Ahmad ji an 과 Hale(1973) 이 지의류의 형태학, 생리학, 분류학 에 대해서 깊이 있게 논의했다. 4 구 원생동물 원생동물은 단세포성 동물인데 그들의 대부분은· 현미경으로 볼 수
있거나 어떤 것은 제법 큰 것도 있다. 형태와 먹이 섭취 버릇에서 아 주 다양하나 모두 대사활동을 위해 수낭울 필요로 하는 공통점이 있 다. 대략 30,00 眞은 정도의 현존하는 것과 많은 화석종들이 기술되고 있다. 주요 다섯 하위 분류군으로 흔히 나누어전다. 편모류, 섬모류, 나출성 및 개각의 아메바, 포자충류이며, 포자충류는 완전기생성이 다. 토양에서 출현하는 또는 토양생물들과 연관을 가지는 원생동물들 의 요약(표 4.5) 이 Sto ut 등(1 982) 에 의해서 마련되었다. 변형사상균 이 그들의 요약에 포함된 것을 유의해야 한다. 이 사상균은 전균에서 논의되었다. 다른 논란이 될 만한 그룹은 광합성 유글레노이드들이 다. Eug le na g ra ci l is 와 관련 종들은 원생동물학자 (예를 들면 Ni sb et (1984) )와 조류학자(예를 들면 Bold 와 W y nne(l979) )들에 의해서 서로 원생동물과 조류로 분류된다. 여기서는 유글레노이드들을 조류로 취 급한다. 토양에서 독립적으로- 살아 가는 원생동물들은· 용존 유기물과 다른 미생물들을 먹고 산다. 많은 것들은 전체적으로 초식 또는 포식으로 살아 간다. 토양 섬모충들은 주로 세균을 먹이로 한다. 어떤 것은 추 가로 효모와 다른 원생동물을 먹는다. 또한 윤충 같은 작은 후생동물 을 먹기조차 한다. 아메바는 세균, 다른 원생동물, 효모, 전균의 포 자, 조류를 먹는다. 실험실 연구에서 하나의 원생동물이 시간당 수백 에서 수십만의 세균 세포를 소비하는 것으로 관찰되고 있다. 소비되는 수는 원생동물과 세균 크기의 함수이다. 토양 원생동물들은 미생물 군집의 구조와 기능에 영향을 끼친다. 토 양에 새로운 유기 쇄설물을 첨가한 뒤 흔히 관찰되는 세균 수의 증가 는 거의 항상 원생동물 수의 증가가 뒤따르게 한다. 원생동물에 의한 선택적인 섭식은 세균 속의 구성 비율을 변화시킨다. 실험실 소규모 실험에서 유기물 조각들의 분해는 세균만 있을 때보다 원생동물과 세
표 4.5 독립생활형으로 살아가는 주요한 토양 원생동물군' 소형 편모충류 도처에 있음, 예 : O i komonas( 단편모성), Bodo( 이편모성, 하나는 길게 늘어 짐) 나출성 아메바 도처에 있음 소형 단족류 : Vahlkamp fia, Naegl e ri a, Hart m annella ( 기 생 종 포함) 다족류 : Nucleari a 박막충 : Thecamoeba 변 형 균류 : 店 c ty os t el i um 섬모충류 토양 구조, 수분, 통기성을 반영한다 Tr ich osto m es : 거 의 도처 에 있음 : Colp oda( 들쭉날쭉한 세포구가 있는 타원형 또는 평면형 몸 체), L ept o p ha ry nx( 홈에 거친 섬모들이 있는 작고 편편한 몸체) 소형 토양 섬모류 Chil o denella, 배의 표면에 제한되어 섬모가 있으며 둥그스럼함 Cy rtolo p ho sis , 전단부에 들어간 세포구를 가진 계란형 크고 더 복잡한 하모류 : Urolep tus , Keronops is , Gonosto m um 고착성 주모류 : Vor tice lla str iata 육식 성 종 : Spa t h i d i u m , Bresslaua his t o p h ag e : Tetr a hym e na ros t ra ta(임의성 기생) 홉반충류, 유충이 섬모성이며 성충은 고착성 : Podoph r y a 개각류 외 각의 모양이 흔히 토양 수분을 반영 한다. 구형 또는 반구형 외각 : Cy cl op yxis, Phry ga nella 계 란 모양, 정 단 가까이 에 작은 구멍 : Tr ine ma, Cory thi o n , Centr o py xis 높고 둥근 외각, 보통 삼림 낙영 및 낙지와 이끼류에 충현 : Nebela, Difflug i a 편편하고 옆 모양이 위로 볼록한 의각, 보통 열린 구조 예 : 낙엽 및 낙지 (Arceila , Mi cr ochlamy s) ·자료 : Sto u t 등 (1982)
균이 모두 있을 때 더 빠르게 진전된다. 원생동물에 의한 세균의 포식 은 유기물 분해에 생리적으로 더욱 효율적안 활력 있는 세균 개체군들 울 유지하는 것으로 가정된다. 포식자들이 개별적으로는 그렇지 않지 만 전체적으로는 그들의 피식자 생물에 유익한 영향을 주고 있디는- 가 정이 동물 생태학지들에 의해서 오랫동안 옹호되어 오고 있다. 원생동 물들은 영양소 순환을 가속화시키고 토양수에서 그들의 활발한 운동성 은 세균에게 용존 산소와 영양소를 공급하는 데 도움이 될지도 모른 다. 4-8 토양 후생동물 토양미생물학에는 미생물, 원생동물뿐만 아니라 선충, 노래기, 지 네, 윤충, 옹애, 환형동물, 거미, 곤충 같은 토양에 거주하는 많은 작은 다세포 동물(후생동물 me t azoans) 의 연구도 포함한다(그립 4.4). 이와 같이 잡다한 것들 중에서 가장 작은 것 (예를 들면 선충)은 토양입 자들을 교란하지 않고 공극들 사이로 이동할 수 있으며 이들은 종종 토양 원생동물들과 함께 토양 미세동물로 통칭되기도 한다. 적어도 토 양을 파헤치는 영구적인 토양 거주자는 흔히 토양 중형동물이라 불린 다. 선충류, 요충, 모충 들이 토양 후생 동물- 중에서 가장 많은 것들이 다. 그들의 수는 평방미터당 수백만에 이르기도 한다. 대부분 토양 중 형동물들은 너비 0.05mm, 길이 2mm 미만이다. 많은 것들이 식물 과 동물에 기생한다. 토양에서 독립 생활하는 형태의 후생동물은- 미생 물과 디론 동물을 엄청나게 먹어치운다. 지렁이는 종종 토양에서 무척 추 동물 생물량의 주요 부분을 차지하며 전 토양을 통하여 분해되고
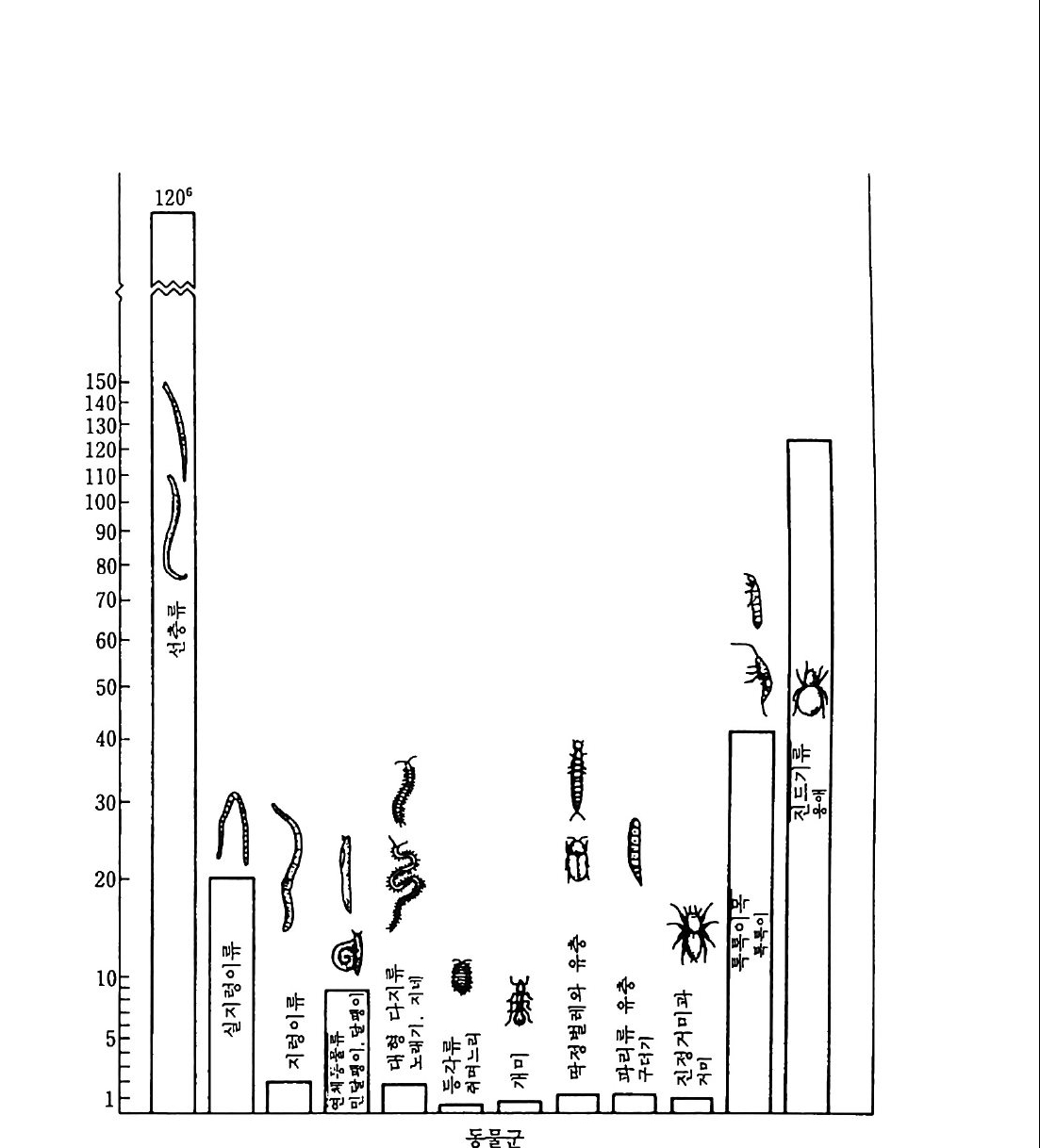 0g
0g
그립 4.4 로그 그래프로 그린 유럽 초지의 토양에서 1 평방미터 당 동물의 수. 거 미와 지네들은 전부 육식성이다. 개미들은 육식성이 우세하게 많고. 딱정벌레, 파리 구더기와 웅애, 선충류는 종에 따라 먹이 습성이 다양 하다, 나머지 그룹들은 주로 썩고 있는 유기물을 먹고 살며, 많은 딱정 벌레는 곰팡이와 다른 미생물들과 밀접하게 연관되어 있다 (Kevna (1965) ) .
있는 낙엽 및 낙지 처리와 유기물 분포에서 매우 활발히 활동한다. 실 지렁이류 (0.2-0.8mm 너비와 5-15mm 길이)는 축축한 산림의 낙엽 및 낙지와 토양에서 가장 혼하다. 응애, 톡토기, 개마, 곤충의 유충들 또한 토양 중형동물의 구성 요소가 된다. 토양에서 중형동물의 중요성은 토양과 유기 쇄설물의 물리적 화학적 특성과 미생물 군집의 구조에 미치는 영향에 있다 . 지렁이, 개미, 흰 개미는 유기물들을 분쇄하고 더 깊은 토층으로 운반한다. 노래기, 응 애, 등각류, 톡토기 또한 낙엽 및 낙지의 분철에 침여한다. 토양을 통 하여 통로를 만들거나 낙엽 및 낙지를 토양과 섞는 중형동물들은· 물의 흡수와 침투 속도에 영향을 준다. 낙엽 및 낙지 특히 나무 그루터기나 통나무 같은 목질 조각둘의 분쇄는 빗물, 이슬, 토양미생물에 노출되 는 물질의 표면적을 크게 증가시킨다. 미세동물과 마찬가지로 중형동 물들은 미생물 군집의 조절에 직접적으로 영향을 줄 수 있다. 선충류 에 의한 세균 홉식 속도는 분당 5000 개의 세포에 이르는 것으로- 추정 하고 있다. 세균과 진균을 포식하는 동물들에 의한 미생물의 전체 소 비량은 미생물의 연간 생체 생산량 중 50% 에 이르는 것으로 추측된 다. 낙엽 및 낙지가 풍부한 토양에서 토양동물을- 없애면 보통 토양호흡 률이 때때로 현저하게 감소하기도 하지만, 토양동물에 의해 칙접 수행 되는 무기화 과정은 미생물 활동에 비할 때 작다. 죽 전체 무기화 과 정의 단지 수 퍼센트 정도인 것으로- 추산한다. 토양과 낙엽 및 낙지의 물리화학적 특성과 토양미생물 구성을 변화시킴으로써 이루어지는 것 과 같은 간접적인 효과에 의한 동물의 분해 촉진 효과와 관련된 기작 들은 아직 제대로 이해되지 않은 상태이다. 닫힌 계에서 얻어진 측정 치들로 실제적인 야의 현상에 직접 적용할 수 없다. 토양과 같은 복잡 한 계에서는 여러 가지 요소들 중에서 어느 하나가 관련되어 있을지도
모른다 . 수 개의 요소들이 동시에 작용하고 있을 때, 어느 하나의 요 소가 닫힌 계의 측 정에서 나타나는 것보다 훨씬 영향이 적을 것으로 기대할수 있다. 참고문헌 Ahmadji an , V., and Hale, M. E., eds (19 73) . The Lich ens. Academi c Press, New York. Ai ns wor th, G. C., and Sussman, A. S., e ds.( 1 9 65-1973). The Fung i : An Advanced Trea t is e 4 vols. Academi c Press, New York. Alexop o ulos, C. J., and Mi m s, C. W. (1979) . Intr o duc tor y My co logy . Wi le y, New York. Brock, T. D., Smi th. D. W. , a nd Madig a n, M. T. (19 84) . Bio l ogy of Mi cr o- orga n is m s. 4th ed. Prenti ce -Hall, Eng le wood Cli ffs, New Jer sey. Buchanan, R. E., a nd Gi bb os, N . E., eds. ( 19 74) . Berge y's M anual of Dete r mi - nati ve Bacte r i olo gy , 8th ed. W illiam s & W ilk in s , Baltim ore, Mary la nd. Domsch, K. H., Gams, W ., a nd Anderson, T. H. (19 81) . Comp en diu m of Soil Fung i. Academi c Press, New York. Gil m an, J. C. (19 57) . A Manual of Soil Fung i, 2 nd ed. Iowa Sta t e Univ . Press, Ames. _ Gooday , D. W. (1979) . In Mi cr obia l Ecology : A Concep tual Ap pr oach (]. M . Ly n ch and N. J. Poole, eds.) , pp. 5-21, Wi ley , New York. Gray , T. R. G., a nd W illiam s. S. T. (1971) . Soil Mi cr oorga nis ms. Oliv e r & Kevan,B oDy. d,K .E, dMin bc uE r. g(1h 9. 65) . The soil fau na —its natu r e and bio l og y. In Ecology of Soil Borne Path o g en s (K. F. Baker and W. C. Sny d er, eds.) , pp. 33-51, Univ . of Cali forn ia Press, Berkeley. Ni sb et, B. (19 84) . Nutr iti.on al Feedin g Str a te g i es in Proto z oa. Croom Helm. London and Canberra. Prescott , G. W. (19 68) . The Alga e : A Revie w . Houg h to n Mi fflin, Bosto n , Massachusett s.
Ross, I. K. (19 79) . Bio l ogy of the Fung i : Their Develop m ent, Regu lati on , and Associa tz o ns. McGraw-Hi ll, New York. Round, F. E. (19 73) . The Bio l ogy of the Alga e. S t. Marti n' s Pr~ss, New York. Ste w art , W. D. P., ed. ( 19 77) . Alga l Phys i o l og y and Bio c hemi stry. Univ . of Califo rn ia Press, Berkeley and Los Ang e les. Sto u t, J. D., Bamf orth, S. S., a nd Lousie r , J. D. (19 82) . Proto z oa, Ag r on. Monogr . 9. Tif fan y , L. H. (19 58) . Alga e : The Grass of Many Wate r s. Thomas, Sp r in g - fiel d, Illin o is . Wi no g rad sky, S. N. (19 49) . Mi cr obio l og u e du sol : pro blemes et meth o des. Massor et cie, Paris. 추가로 읽을 거리 Anderson, R. V., C oleman, D. C., and Cole, C. V. (19 81) . Eff ec ts of sap ro tr o - ph ic graz in g on net mi ne raliz a ti on , Ecol. Bull. 3 3, 101-216. Andrews, J. H. (1984) . Relevance of r-and K-th e ory to the ecolog y of pla nt pa th o g e ns. In Current Pers pe cti ve s in Mi cr obia l Ecology (M. J. Kiu g and C. A. Reddy, eds.) . Am. Soc. Mi cr obio l ., Washin g ton , D. C. Pete r son, H. (19 82) . Qu anti tat i ve ecolog y of mi cr ofu n g i and anim als in soil and litter , Oiko s 39, 288-482.
제 5 장 토양생물의 발생과 분포 5-1 서론 토양에 사는 생물들의 종류와 수 그리고 그들이 차지하는 지소들을 확인하기 위해서는 많은 시간과 노력이 필요하다. 미생물둘은 세계적 으로 분포하게 될 커다란 잠재력을 지질 연대에 걸쳐 획득해 왔다. 현존하는 분포의 지리적 차이와 같은 현상들은 환경에 대한 오랜 시간 의 적응을 반영하는 것이다. 같은 지역뿐만 아니라 다른 지역에서도 바슷한 조건들이 있으면, 비슷한 토양생물군들의 서식이 예상될 수 있 다. 대부분의 토양생물 구성원들은 유기 영양물을 섭취하며, 유기 탄 소의 이용도가 토양에 사는 생물들의 수와 분포 양상을 주로 결정한 다. 주요 탄소 공급원들은 살아 있는 식물 뿌리와 생장 기간을 통하여 토양에 공급되는 유기 잔여물들이다. 뿌리와 미생물의 연합과 관계되 어 있는 매우 중요한 두 과정은 질소고정과 균근의 형성이다. 이 두 주제는 각각 제 10 장과 제 11 장에서 좀 더 폭넓게 논의할 것이다. 이 장에서는 토양생물군의 분포적 구조적 차이들에 관십을 두고 생물들에
의해서 매개되는 영양소 변환 과정은 거의 염두에 두지 않을 것이다. 이 과정들은 바로 다음 장에서 다루게 될 것이다. 5-2 토양생물군의 지리적 차이 인간의 출현 전부터 있었던 바람, 물, 동물에 의한 이동은 미생물의 세계적인 분포를 조장하고 있다. 미생물들은 독립적으로 또는 먼지 입 자나 에어로졸과 연합체로서 간 거리를 공기 매개로 이동되곤 한다. 먼지의 해양성 이동도 기록되고 있으며 미생물들은 고지로부터 굴러 온 눈덩이로부터 눈이 내린 아주 오래된 다음에도 다시 살아날 수 있 다. 해류는 쇄설물들을 대륙 사이로 운반하며, 철새들은 엄청난 거리 를 옮겨다닌다. 그리하여 거의 어떤 미생물 종도 세계 도처에 분포할 기회를 가지게 된다. 대부분의 미생물학자들은- 뒤뜰로 가보기만 하면 거의 모든 미생물 분류군들을 분리해 낼 수 있다. 그럼에도 불구하고 지리적으로 약간의 서로 다른 점들이 있다. 곰핑이들 가운데는 온대 및 한대 기후에서는 A sp ergi llus 보다 Pen i c ill i um 이 더욱 풍부한 반면, 따뜻한 지역에서는 그 반대의 현상 이 나타난다. 러시아의 학자들은 포자형성 간균과 자낭균이 따뜻하고 건조한 토양에서 풍부하며 차고 습기 찬 토양에서는 극단적일 정도로 빈약하다고 보고했다. 미국에서는 북부와 남부의 토양들에서 분리된 포자형성 간균과 질산균이 최적 성장 온도에서 종 사이의 특이한 차이 를 보이는 점이 주목된다. 물과 온도가 아닌 다론 요소들도 역시 영향 력이 있다. 열대에서 Fusa ri um 에 의한 바나나의 시듦이 점토 스펙타 이트롤 함유하는 토양에 한정되어 있다. 남조류는 흔히 중성 내지 알 칼리성의 토양에서 보이나 산성 토양에서는 아주 드물게 나타난다. 현
존하는 차이들이 세계적으로 비슷한 환경에서는 본질적으로 비슷한 토 양생물군이 존재한다는 사실을 흐리게 해서는 안 된다. 5-3 토양 단면 내의 생물 분포 전형적으로 유기물과 마찬가지로 미생물둘은 토양 단면의 깊이에 따 라서 감소한다. 직접적인 평판계수법에 의하여 자연 초원 토양에서 측 정한 세균의 수를 그립 5.1 은 보여 준다. 두 곡선을 비교해 보면 5cm 깊이에서 대충 3% 가, 75cm 깊이에서는 대충 1% 가 있다. 토양 깊이에 따라 한천 배양에서 세었을 때는 곡선의 형태로, 토양에
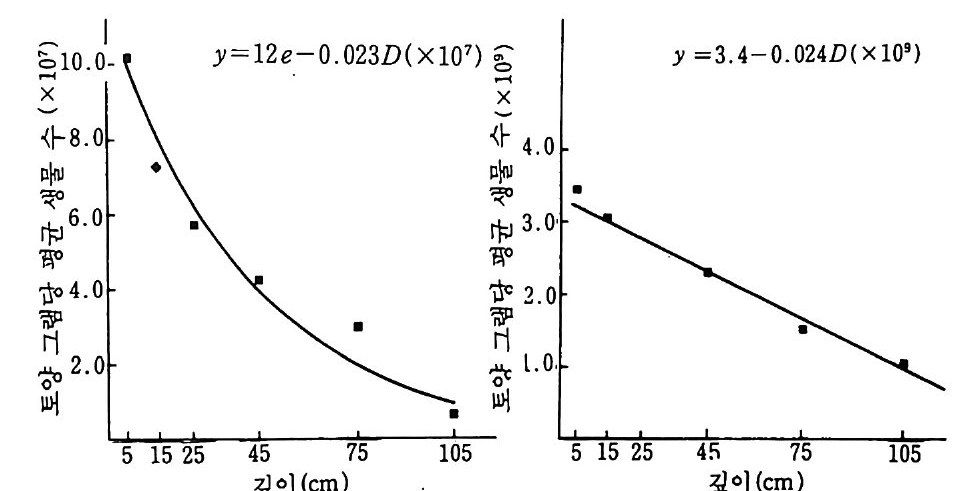 gl 008060y =41 02 e2 0。 。 23 D, 1,x 1。 7 , ,1 (y =3.4-0.0 2 4D(Xl09)
gl 008060y =41 02 e2 0。 。 23 D, 1,x 1。 7 , ,1 (y =3.4-0.0 2 4D(Xl09)
그림 5.1 초원 토양에서 토양 단면의 깊이에 따른 총 세균 수의 변화(왼쪽). 토 양 추출 한천에서 평판계수법으로 측정한 세균 수. y= 12 e-o.0 2 3ox107. D= 깊이. (오른쪽) 현미경으로 직접 센 세균 수. y= 3. 4- 0.024DX109. 두 그래프에서 y좌표 크기가 디름을· 유 의할것
서 칙접 세었을 때는 선형적으로 감소되었다. 이는 토양 추출액 한천 에서는 성장할 수 없는 종, 변종 또는 휴면기에 있는 종균들이 토양 깊은 곳에 많이 살고 있다는 것을 시사한다. 일반적으로 토양에서 개체군 밀도는 깊이에 따라 계속 감소하지 않 으며, 반드시 일정한 수로 또는 아주 조금씩 감소하지도 않는다. 밀도 변동은 더 낮은 지충에서 흔히 나타난다. 충적토에서 개체군은 토성 변화와 함께 변동한다. 미생물들은 굵은 사질총보다 미사층이나 미사 질식토충에 더 많다. 상승된 지하수면 위의 토양 단면에서는 높은 지 대보다는 지하수 인접 지역에서 미생물의 수가 더 많다. 토양 표면 또 는 표면 가까이, 그리고 지하수면 바로 위에 하나씩 뿌리를 발달시켜 서 이중 근계를 가지는 머스키트 같은 식물이 있고, 그 식물의 수 미 터 아래 지하수가 있을 때, 두 근계 사이에 있는 토총보다 깊은 근계 주변 토총에서 미생물 개체군이 더 크다. 토양 단면 깊이에 따른 개체군의 발생을 연구하기 위해 미생물 수를 직접 관찰하여 알 수 있는 개별 세균 종들이 아주· 드물기 때문에 배양 과정이나 면역성 형광 염색에 의존해야 한다. 전체 평판계수법에서 Ba cillus 는 깊은 단면충에서보다 위충에 더 많이 분포되어 있다. 곰팡 이 가운데 Ch ry so sjJ o ri um 은 10 cm 깊이에서보다 30 cm 깊이에서 더 많은 수가 보인다. 대부분의 곰팡이 종들은 위층을 더 좋아한다. 단면 내에서 이주할 수 있는 토양 동물의 구성원들은 수분과 온도 조건이 좋은 곳을 선택적으로 찾는다. 5-4 토양 바탕 내의 생물 분포 토양미생물의 탄소량으로. 살아 있는 생물량과 생물체적을 환산하거
나 또는 경작지 토양에 대해서 용적밀도의 중간값과 공극률을 비교해 보면 미생물은 토양 공국의 0.2-0.4% 이상을 차지하지 않는다. 토양 세균은 구멍에서 붙어 있지 않는 입자상으로 존재하지 않으며 토양으 로부터 쉽게 씻겨지지도 않는다. 그들 세포들은 무기 및 유기 표면에 붙어 있거나 흡착되어 있다. 세균은 세포벽으로부터 뻗어난 가는 섬유 질과 점액질의 세포의 다당류들-(점액질 muc ig els) 에 의해서 모래알둘 에 강한 접착성을 가진다. 모래 알갱이들이 한덩어리가 되기 위해서 미생물과 식물의 점액질, 곰팡이 균사, 작은 뿌리들의 연합이 필요하 다(그림 5.2). 대부분의 세균은 접토 알맹이보다 크며 보통 음전하량이 양전하량보 다 더 크다. 그럼에도 불구하고 음으로 하전된 점토와 밀접하게 연합 하게 된다• 또한 아주 가는 섬유질과 점액질이 연관되어 있다. 접액질 온 토양 주변을 이동하지 않는 고분자들이다. 그러므로 매우 미세한 점토질들이 점액질과 미생물들로 옮겨 가서 입단 형성을 시발시키는 것 같다. 작은 입단은 직경이 250µm 미만이며 큰 입단은 250µm 이상이다. 작은 입단 안에 있는 구멍의 직경은 0.2-2.5µm, 큰 입단 안의 구멍은 25- i OOµm 아다. 바깥과 통하는 구멍이 있는 곳에서 구 멍의 목 크기는 구멍 직경만한 것에서부터 더 작은 것이 있다고 가정 할 수 있다. 구멍의 목 크기는 들어갈 수 있는 미생물들의 크기를 결 정한다. 결과적으로. 작은 입딘에 있는 매우 작은 구멍들로의 침입은 주로 세균에 의해서 이루어진다. 제 2 장에서 논의된 바와 같이 바깥 과 통해 있거나 닫힌 공국 안에는 입단 형성 시기에 갇힌 미생물들이 있을지도 모른다. 건조시켜 저장한 토양에서도 세균은 수십년 동안 살 아남는다고 알려진 것으로 미루어 그렇게 갇힌 종균둘은 오랜 기간 산 채로 남아 있게 될지도 모른다.
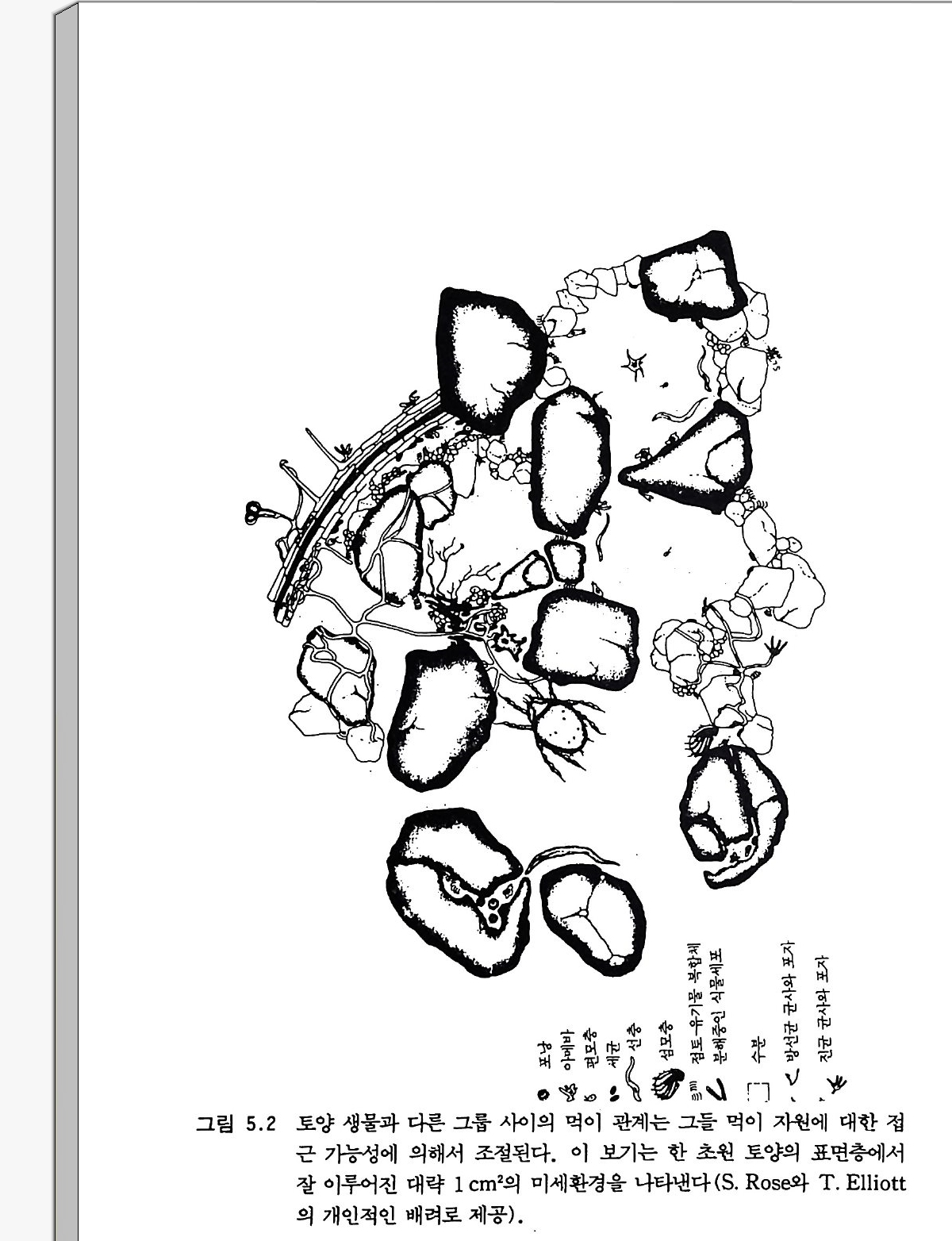 :라pp 버 '才 ;才덟 一古싫
:라pp 버 '才 ;才덟 一古싫
작은 입단에 있는 토양 유기물의 화학적 분석은 포함된 당류들이 주 로 미생물에서 유래된 것임을 보여 준다. 식물에서 유래된 당류는 많 은 양의 크실로오스와 아라비노오스를 포함하고 있는 반면에 미생물에 의해서 합성되는 당류들에는 갈락토오스, 만노오스, 포도당이 우세하 게 많다. 작은 입단에 있는 지극히 얇은 막에 생기는 특이한 발색 또 한 유기물들이 미생물에서 유래되었음을 가리킨다. 점질토와 점액 질 복합체들이 물질 확산의 강한 장벽이 되며 입단 내부가 무산소 상태라는 사실은 그러한 입단이 미생물의 집중적인 거주와 대사활 동 장소가 아님을 시사한다. 큰 입단은 통기와 물의 침수 및 배수, 용해성 물질의 확산, 미생물 의 입주를 허용한다. 그들의 내부 구멍은 미생물과 미세 동물들의 거 주지가 되며, 어떤 구멍의 목은 많은 중형동물들의 유입을 허용할지도 모른다. 매우 큰 입단 (1mm 이상)에는 뿌리나 그들과 밀접한 연합체 의 침투가 나타난다. 큰 입단은 미생물들에 의해 더욱 집중적으로 거 주되며 전체 토양에 비해서 대사작용이 활발한 장소이다. 큰 입단을 화학적으로 분석하면 일반적으로 토양보다 영양소(탄소, 질소, 황, 인) 와 미생물에서 유래된 당류의 함량이 더 높다(이는 입단을 이루는 구성 입자들 사이에 영양소들이 자리를 잡을 수 있어서 미생물, 식물, 동물 들이 합동으로 이루어 가는 육상 생태계의 중요한 영양소 보유 기작으로 작용한 다 : 옮긴이). 표 5.1 은 미세 점토에 대한 분석 자료가 원래의 토양과 다른 정도를 보여 준다. 높은 영양소 함량과 양호한 미세 기후 조건을 가졌기 때문에 큰 입단은 일반적으로 토양에서 보이는 것보다 더 나은 영역을 미생물에게 제공하는 것으로 결론지울 수 있다. 그러나 입단과 연관된 생물 활동의 정도는 뿌리 및 뿌리를 바로 이웃한 토양 영역과 식물 조각이 토양으로 돌아갔을 때 제공하는 영역이라는 두 개의 다른 영역에 연관된 생물 활동보다 작다.
표 5.1 자연 초원 토양의 입자 지름에 따른 유기 무기 영류의 화학적 분 석* 토양 C N mgP / 。g* * P.a••• No( 1~sN) * * *C */N C/P 。 원래 토양 50 4.0 0.58 0.22 11 12.5 87 모래 ••••• (>5 0µm) 27 1.9 0.19 0.0 6 7 14.0 141 굵은 미사 (50-5 µm) 44 3.6 0.4 7 0.1 7 9 11. 2 86 가는 미 사 (5-2 µm) 85 7.9 1.17 0.43 10 10.8 73 굵은 점토질 (2-0.2µm) 82 8.7 1.67 0.56 12 9.5 51 가는 접토질(〈 0 . 2µm) 63 8.0 1.16 0.37 17 7.9 54 ·자료 : Tie s sen 등 (1984) .. p。:유기 인 ... P. : 중탄산영 및 수산화나트륨으로 추출되는 유기 인 ••••a1sN : 공기에 상대적인 “N 의 풍부도 (ppt : pa rt s pe r tho unsand) . •••••모 래 부분은 거칠고 부유성인 유기물(1. 00 g cm-3) 도 포함한다. 5-5 식물 뿌리와 미생물의 연합 근계는 토양 유기물을 가장 많이 부여받은 토양충을 차지한다. 살아 있거나, 노쇠하거나, 죽은 뿌리들이 미생물 생장을 위한 기질 물질들 을 제공한다. 뿌리와 토양의 접촉 부위에서 또는 그 주변에서 일어나 고 있는 현상들의 총합은 식물의 안녕과 토양생물군에 커다란 영향을 미친다. 이 접촉 부위를 논의함에 있어서 우리는 뿌리에 이웃하며 뿌 리의 영향 아래에 있는 토양, 뿌리 표면 그 자체, 뿌리의 내부를 고려 한다. 이들 세 지역은 여러 가지로 명명된다. 1904 년 H iltn er 는 주 로 콩과 식물 주변 세균 생장 지역에 대해서 근권 r hi zos p here 이라는 용어를 사용했다. 그 다음 몇십 년 동안 근권은 일반적으로 식물 뿌리
의 직접적인 영향 아래에 있으며 미생물이 창성하는 토양 지역으로 알 려지게 되었다. 뿌리 표면 자체가 미생물과 식물 사이에 일어나는 상호작용을 위한 결정적인 장소라는 · 인식은 뿌리 표면을 근표면권 rh i z p olaneo ]라고 부 르게 했다. 뿌리의 표피조직 및 피질조직은 공생자와 병원균이 아닌 미생물의 은신처가 되는 것으로 알려지고 있다. 미생물이 서식하는 식 물 조직은 때때로 내부근권 endorh i zos p here 이라 부르기도 하지만 토 양 지역을 표현하는 데는 근권이라는 단어가 널리 사용되고 있기 때문 에 이 용어는 결코 만족할 만한 것이 아니다. 미생물이 서식하는 뿌리 조칙에 대한 명명으로는 조직권 h i s t os p here 또는 피질권 co rt os p hereol 좋을 것이다. 용어에 상관없이 세 지역 (뿌리의 의부와 표면, 내부)에서 미생물 활동을 주로 책임지고 있는 요소는 뿌리에 포함되는 또는 뿌리 로부터 방출되는 유효 탄소이다. 근권에 대한 초기의 연구는 존재하는 미생물들의 수에 주로 관계했 다. 여러 가지 디른 기후 조건과 생물 기후학의 여러 단계에서 다양한 식물 종들과 토양에 대한 한 가지 미생물 종의 R/S 비 (뿌리로부터 독 립된 토양에 대한 근권의 미생물 수의 비)들이 결정되었다. 총 미생물 수 는 근권에서 흔히 10 내지 50 배로 증가하는 것으로 밝혀졌다. 구조적 으로 근권에는 비례적으로 더 많은 그람음성과 탈질균, 더 적은 수의 그람양성과 그람 변화가 있는 미생물들이 사는 것으로 알려져 있다. 이 지역 미생물의 증가는 동물 특히 미생물과 뿌리를 먹는 동물군의 더욱 높은 활동을 수반한다. 5-5-1 뿌리에 의해서 미생물에 공급되는 기질 뿌리의 속, 표면, 가까이에 있는 유기물의 분석에서는 각종 구색의
아미노산, 지방족, 방향족, 아마이드, 당류, 아미노 당류들이 나타난 다. 그러한 용해성 확산성 물질들과 함께 여러 가지 물에 녹지 않는 물질들(예를 들면 셀룰로오스, 리그닌, 단백질)이 뿌리에서 생기고 있으 며 그들은 뿌리로부터 세포가 벗겨져 나갈 때, 그리고 뿌리의 일부가 잘려져 나갈 때 손실된다. 거의 모든 식물의 근권은 거의 모든 당류 들, 유기산 및 아미노산을 여러 가지 수준으로 함유한다. 약간의 좀 더 복잡한 방향족 산들은 특정 근권에서만 생긴다. 마찬가지로 어떤 미생물들을 유인하고 배척하는 물질들의 생산은 어떤 생물 종들에 제 한되어 나타난다. 아스파라거스는 나무 그루터기 뿌리에 주로 나타나 는 선충류들에 독성인 확산성 글리코사이드를 생산하지만 토마토는 생 산하지 않는다. 많은 식물들은 죽은 물질에만 기생하는 생물과 뿌리에 감영하는 병원균들에게 다양한 친생물성 또는 실균성 비확산 화합물들 울 생산 공급하는 것으로 알려져 있다. 그러한 파이토알렉신 중에는 각각 토마토, 양파, 완두콩, 강낭콩 식물들에 의해서 생산되는 토마 틴, 알리신, 피사틴, 파세울린 들이 있다. 뿌리로부터 식물 동화물질들의 분비 경로는 뿌리 생장 동안 세포막 과 뿌리 분비물 및 돌출부를 가로지른 분자들의 누출과 확산, 세포와 조직 조각의 손실을 포함한다. 근관과 근단은 활발한 물질 분비 장소 이다. 그들은 근관과 세포뿐만 아니라 점액질의 물질들을 분비한다. 뿌리의 주근은 주로 용해성 확산성 물질들과 약간의 점액질을 분비한 다. 그러한 손실은 세포 표면과 접합 부분을 포함하는 전 뿌리를 따라 서 일어난다. 뿌리 점액질은 세포 안에서 합성되고 세포막을 통하여 방출되는 다당류들로 구성된다. 점액질은 물을 포함하고 있는데, 전 자현미경 사진에서는 미세한 섬유질의 구조롤 보여 주며 점토와 결합 손을 형성하는 카르복시기를 포함한다. 점액질 1 은 뿌리의 우세한 분 비물이다. 밀 뿌리의 한 연구에서 그것은 호흡에 의하지 않은 뿌리의
표 5.2 식물에 의한 뿌리 분비 물질들의 측정 참고문헌 관찰내용 Shamoot 등 (1968) 7 가지 클로버와 잔디에서 토양으로 뿌리 보유 분의 평균 29% 에 해당하는 비호흡성 탄소 손 실 Barber 와 Gunn 0974) 3 주알 동안 배양에서 키운 보리에서 뿌리 건 량 증가의 5-9% 에 해당하는 아미노산과 당류 의 뿌리를 통한 손실 Barber 와 Marti n ( 19 76) 시 비 되 지 않은 토양에 서 자란 곡류에 서 증가 전량의 18-25% 에 해당하는 동화물질들의 뿌리 를통한손실 Newman(1978) 용존 물질로서 뿌리에서 뿌리 무게의 1-10 % 손실. 때때로 25% 가량이 손실 Helal 과 Sauerbeck(1984) 옥수수에서 제 25 일에 전체 동화물질의 56 % 는 지상부에, 31 %는 뿌리에, 13 %는 뿌리로 부터 손실, 손실되는 13 % 중에서 11 %는 CO2 로, 2 %는 토양에 보태졌다. 미생물과 뿌 리가 함께 CO2 손실에 공헌하는 것으로 가정 했다. 전체 탄소 손실 중 80% 를 맡고 있었다. 떨어져 나온 세포들과 뿌리 의 잘려나간 부분들은 점액질 2 보다 작은 탄소 대 질소 비이며 원래 의 뿌리 조직 그 자체의 구성분들과 아주 비슷하다. 식물 생장 동안 뿌리에서 토양으로 손실되는탄소량은 4C0 선 1 식 물의 잎 부분을 노출시킨 다음, 뿌리, 근권토양, 호홉에 발생하는 co 페 포함된 14(.! 긱 양을 측정함으로써 알 수 있다. 이러한 접근 방 법에 의해서 얻은 선택적인 자료들을 표 5.2 에 요약했다. 거기에서 마지막 자료는 식물동화물질의 11% 가 미생물 호홉으로, 2% 가 토양
유기물로 가는 것을 나타내고 있다. 미생물 생체 탄소에 그러한 토양 탄소의 할당은 27% 의 생장 효율을 가리킨다. 5-5-2 뿌리와 미생물의 공간적인 관계 뿌리 표면으로부터 거리에 따른 토양미생물들의 수는 거리에 반비례 한다. 뿌리 부근에서 대부분 갑작스런 세균 수의 감소가 5µm 이내에 서 일어난다(표 5.3). 균사는 뿌리 표면에서 일어나서 거기로부터 가 닥둘이 수 밀리미터로 무작위로 뻗어나간다. 뿌리 표면의 세균 피복도 는 보통 5-10% 범위인 것으로 보고되고 있다. 균근 형태가 아닌 곰 팡이류들 또한 성건 피도를 보여 준다. 곰팡이와 세균의 피도 사이의 비율은 변화한다. 종종 뿌리 세포벽의 구멍에는 한 종의 세균이, 세포 들의 접합 부분에는 세균 덩어리들이 연관되어 있다. 점액질 충 안에 세균은 보통 한 종류의 세포들로 나타난다. 비병원성균둘의 표충 및 피충 조직에서 서식은 어린 뿌리에서는 드 물지만 뿌리의 나이가 들어감에 따라 널리 퍼지게 된다. 내부 피층으 로의 침입은 의각 조직이 분해되지 않고 일어난다. 세균은 내부 피충 에서 이웃한 표충세포와 사이에 있는 홈을 따라 세로의 분포를 보여 표 5.3 뿌리 표면으로부터 거리에 따른 미생물들의 수 뿌리 표면으로부터 식별 가능한 빈도의 추정치 거리 (mm) 형태들의 수 (106 cells/cm3) 0-1 11 120 1-5 12 96 5-10 5 41 10-15 2 34 15-20 2 13
준다. 뿌리 세포들이 죽음에 따라서 결충 lacunae 또는 공간이 형성되 고 균사체로 채워지게 된다. 5-6 잎 부분과 미생물의 연합 식물들은 정상적으로 풍부한 잎 표면의 생 물군절을 부양한다. 식물 잎과 미생물의 연합에는 영권p h y llos p here 이라는 용어를 사용한다. 서 식의 강도는 기후와 식물 요소에 영향을 받는다. 대부분의 종속영양 생물에 대해서 높은 습도는 유리한 조건이며 태양 광선은 불리한 조건 이다. 두 요소들은 독립영양 생물들에게는 유리한 조건이 된다. 식물 줄기와 껍질에는 조류와 지의류가 종종 서식한다. 활엽식물들은 초본 류보다 그들의 잎 표면에 더 많은 미생물들을 부양한다. 영권에 대해 서 보고된 약간의 생물군들을 표 5 . 4 에서 보여 준다. 그람음성균과 황색세균이 세균의 대부분을 차지하고, 효모는 진균의 대부분을 차지한다; 표 5.5 는 영권 분비물들의 특성과 양에 대한 약간의 관찰들을 요약 하고 있다. 잎의 삼출액과 수관을 통하여 흘러내린 빗물에서 측정될 수 있는 유기 탄소들은 생물군들에게 이용될 가능성이 있는 동화물질 의 대략적인 양을 가리킨다. 식물 호흡과 광합성이 있기 때문에 잎에 표 5.4 잎 표면에서 발견된 미생물 개체군들• 식뭉 미생물(자연 상태의 무게 기준) 클로버 1-30X108g -• (세균) 잔디 0. 1- 10X106g - • (세균) 양파 2 X l06 g-• (효모) 커피나무 10 一 20 x 106 cm-2 잎 표면 (세균) ·자료 : Clark 와 Paul(1970)
표 5.5 잎 분비물과 침출액에서 발견되는 물질의 종류와 양 조사자 식물 종 관찰 내용 Greenh i ll 과 Loliu m per enne 분비 된 방울에 서 글루타민 Chubnall (19 34) Dalbro (19 56) Ma/us sylv estri s 강수는 100 g 탄수화물 m-2 yr- 1 세 척 Tukey 등(1 957) Phaseolus vulga ri s 계속적인 인공 침출로 24 시간 당 7.5mg 탄수화물 획득, 이는 잎 무 게의 4.8% 에 해당함 Carlile 등 (1966) Que rcus pet r a ea 강수는 용존 유기물 130 g m-2 yr- 1 를 세척. 이 탄수화물 중 90 g은 주 로 포도당, 과당 멜레지토오스 Ruin e n(1 9 66) Aloe sp. , 잎에 의해서 분비된 지방산들 중 무 Sansevie r i a sp. 게 기 준으로 60 %는 아세 트산, 5-15.5% 는 팔미트산, 더 적은 양 의 7-29% 는 올레 산, 미 리스트산, 스테아르산, 리놀레산, 리놀렌산 Malcolm 과 Que rcus fal cata , 강수는 2 gm- 2 yr-I 유기물 세척, 1 McCracken 0968) Q. vir g i nia n a, 또는 그 이 상의 유기 산들, 400 mg Pinu s pal ustr is 의 당류, 100 m g의 페놀 중합체들 서 일어나는 미생물 호홉에 의한 CO2 발생량의 측정은 어렵다. 미생 물 생물량에 기초한 계산은 잎 동화물질의 1% 미만이 영권 생물군들 에 의해서 대사된다고 한다• 비병원성 미생물들이 열매, 줄기, 잎의 조칙 안에서 생긴다. 열매
구조로부터 방출되기 전 열매 껍질은 미생물들에 의해서 아주 드물게 차지된다. 씨앗의 분산 동안 공기 감염이나 영권 개체군들의 구성원들 에 기인한 추가적인 미생물들이 씨 껍질의 거주자가 된다. 받아의 시 작과 활발한 종자의 대사작용 성립과 함께 당류와 다른 유기물이 분출 된다. 종자의 분비물은 어린 묘종과 뿌리의 분비물과는 다르다. 많은 양의 바닐산 vanil lic acid 같은 중합체 방향족 산들이 종자의 분비물에 존재한다. 소량의 몇 가지 소당류 (o lig osacchar i des, 이는 3 이상 또는 비교적 적은 수의 단당류들로 이루어진 중합체를.통칭한다. 이와 관련하여 단당류 둘의 결합으로 이루어진 것은 이당류이며, 단당류의 숫자가 많은 것 을 다당류라 한다 : 옮긴이)는 어린 식물과 뿌리 분비물에는 혼하다. 약 간의 종자와 연관된 미생물들은 새로 자라는 어린 묘종에 유익한 오옥 신, 비타민, 지베렐린류의 물질을 생산한다. 어떤 미생물들은 씨앗의 발아를 지연시키는 물질들과 식물의 병원균을 억제하는 물질들을 생산 하는 것으로 알려져 있다. 5-7 식물 조각과 미생물의 연합 자연 생태계와 잘 관리된 삼림 및 초원에서 순 일차 생산량의 주요 부분은 낙엽 및 낙지이다. 초원에서조차 큰 초식 동물들의 소비는 순 일차 생산량의 50% 를 결코 초과하지 않는다. 삼림에서 동물에 의한 녹색 잎줄기 부분의 섭취는 매우 작은 몫이기도 하다. 대부분의 초원 에서 지상부의 낙엽 및 낙지 생산성은 100-300 g m-2 의 일반적인 범 위에 들어간다. 생산성은 채퍼랠과 관목군락 (150-400 g)에서는 비슷한 정도이나 삼림 (200-800 g)에서는 더 높다. 미세한 낙엽 및 낙지의 대 사회전 시간은 2~4 년이다. 따라서 어떤 장소에서 낙엽 및 낙지의 축
적은 연간 공급되는 양의 수 배가 된다. 지상부 낙엽 및 낙지의 초기 침입자들은 주로 영권에 이미 존재하던 생물들이다. 낙엽이 돼 떨어지기 전에 노쇠한 잎은 미생물과 동물에 의해 공격을 당한다. 삼림에서, 서 있는 죽은 나무와 나뭇가지들은 지표의 낙 엽 및 낙지로 되기 전에 중형동물과 리그닌울 분해하는 곰팡이들의 공 격으로 종종 그들 탄소의 반을 손실한다. 잎과 작은 가지나 줄기가 지 상으로 떨어침에 따라서 그 위의 세균 수는 급격 히 증가한다. 축축한 낙엽 및 낙지의 세균 개체군들은 크기에서 약 100 배 정도로 영권의 개체군크기보다크다. 낙엽 및 낙지의 생물군들은 깊이와 썩어가는- 단계에 따라서 변한다. 표 5 . 6 은 초본류의 낙엽에서 곰팡이 속의 관찰 빈도와 밑에 놓여 있 는 부식질에서의 관찰 빈도를 비교한다. 표 5 . 7 에는 썩어가는 침엽수 잎에서 곰팡이의 천이룰보여준다. 토양동물의 활동은초원이나경작지의 낙엽 및 낙지에서보다 삼림에서 더 활발하다. 그러나 삼림에서도 무척 추 동물들은 낙엽 및 낙지에 포함된 탄소의 아주작은 부분만 대사한다(그 표 5.6 벼과 식물의 낙엽과 지상 부식질에서 관찰된 곰 팡이 속둘· 곰팡이 낙엽 부식질 Al ter nari a 71 4 Cladosp o ri um 32 2 My ce lia ste r i lia 70 12 Penic illi u m 。 22 Sp or omi el la 。 20 Tr ich oderma 3 15 Fusari um 10 27 ·숫자는 접종된 집시 중에서 곰팡이를 산출시킨 것의 백분율을나타낸다.
립 5.3). 호흡과 생물량 값들의 비교는 낙엽 및 낙지를 혼합하고 분절 하여 미생물 공격울 위해 더 많은 표면적을 노출시키는 무척추동물의 역할을 고려하지 않고 있다 (1960 년대 이후 낙엽 및 낙지 분해에서 동물 의 역할에 관심을 두고 있다. 실험적으로는 주로 그물눈의 크기가 다른 낙 영주머니나 나프탈렌 같은 살충제를 이용하여 일부 동물이 낙엽에 접근하지 못하도록 한 경우와 그렇지 않은 경우를 - 비교하여 동물들의 역할을 규명하 고 있다:옮긴이). 동물의 생물량은 표면 낙엽 및 낙지들에 집중되어 있고 밀에 놓여 있는 토양의 상충 수 센티미터에서 빠르게 감소한다.
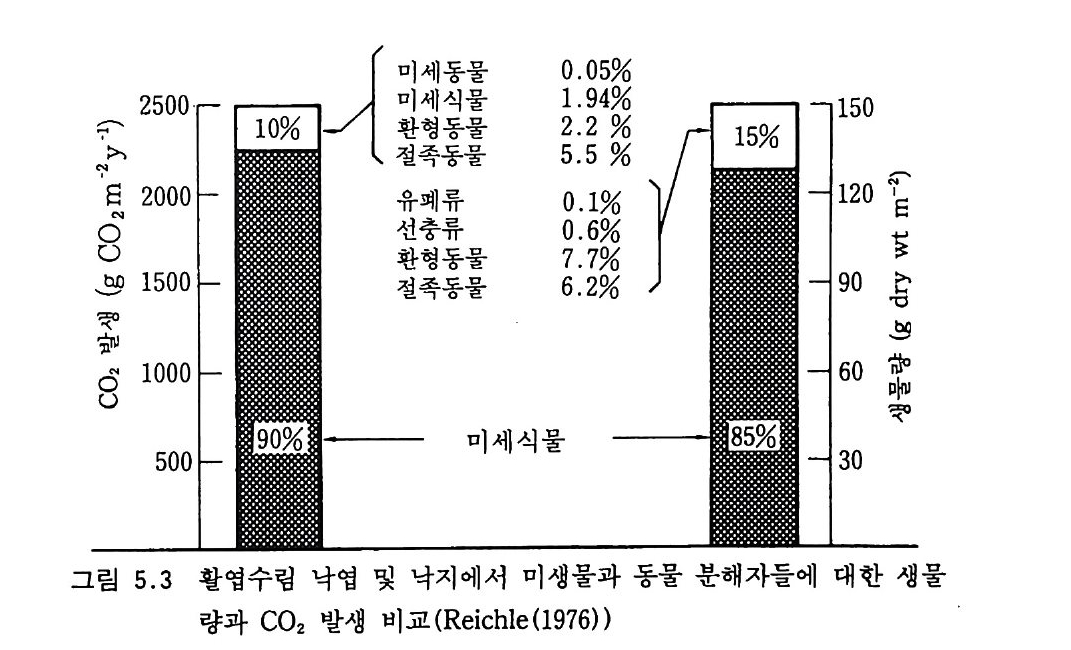 ,gS(I 'K)ztz03 國圖國國 l 。% ~ 환유미선환절미절 세형족폐세형「조층 식동동동류류동동 물물물물물물 0.. 1麟霜깁홀 250076 12 。 t(pN._8E) E
,gS(I 'K)ztz03 國圖國國 l 。% ~ 환유미선환절미절 세형족폐세형「조층 식동동동류류동동 물물물물물물 0.. 1麟霜깁홀 250076 12 。 t(pN._8E) E
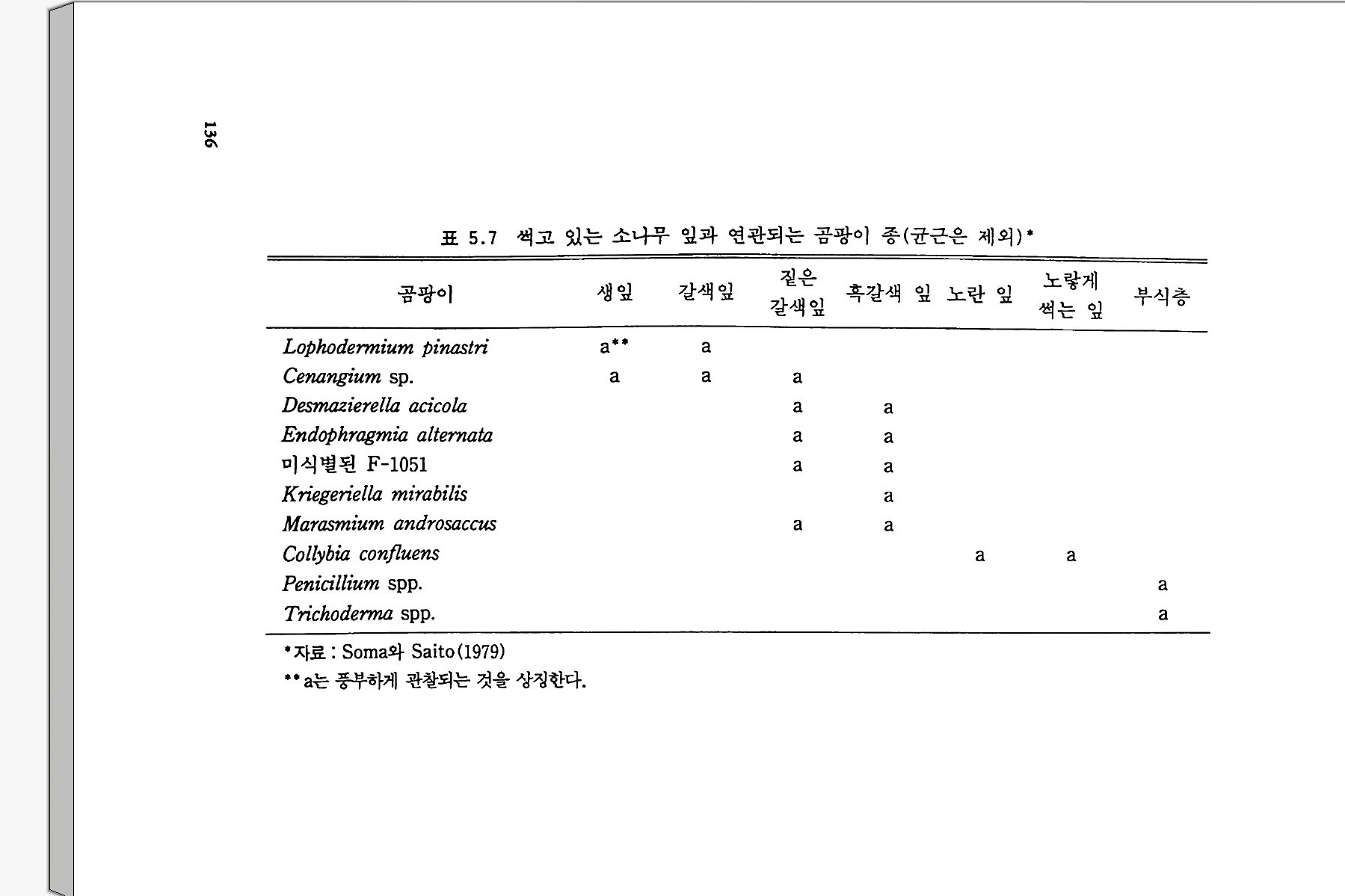 은란
은란
5-8 토양생물에 대한 관리 전략의 영향 토양특성과 식물피도를 변화시키는 한 어떤 관리 전략도 토양생물 군에 영향을 주게 된다. 셀 수 없을 정도로 많은 전략둘이 있는데 그 들 중 어떤 것이든 토양 수분 함량 , 온도, 통기, p H 와 유기 탄소 및 질소에 여러 가지로 영향을 준다. 여기서 검토하기 위해서 선택된 것 들은 토지 경운, 살충제와 다른 화학 물질들의 첨가, 완전 벌목, 통제 발화 con t rolled burnin g 동이 있다. 5-8-1 농경지 경운 흔히 사용되는 3 가지 경운의 절차는 재래식 경운, 감소 경운 , 최소 경운, 또는 피복 경운 (reduced, mi ni m um, or stu b ble-mulch tillag e) , 무경운 no till이다. 재래식 경운은 보습 쟁기를 사용하는데, 보통 원판 형 써레 사용을 덧붙인다. 감소 경운은 지표 유기물과 토양의 가벼운 혼합을 가능하게 하는 기계에 의한 잡초 제거를 포함한다. 무경운은 제초제의 사용으로 잡초를 제거하는 것이다. 이 경우 유일한 토양의 파헤침은 씨 뿌리기와 관련되어 있을 뿐이다. 재래식 경운에는 많은 미생물 수와 높은 토양 호흡률의 증가에서 보 는 바와 갇이 미생물 활동의 자극적인 반응이 있다. 그러한 자극은 토 양 입단들의 파손과 분해 가능한 물질의 증가된 노출 및 통기 결과이 다. 지표 유기 잔여물들의 대사회전과 분쇄는 간 깊이에서 왕성한 미 생물 활동 지대를 육성한다. 대조적으로 감소 경운 및 무경운은 토양 표면 또는 표면 가까이에서 미생물의 활동을 이룬다. 미국 네브라스카 에서의 한 연구는 두 토양 깊이에서 미생물의 숫자를 갈지 않은 토양 과 간 토양에 대해 비교했다. 0~7.5 c m 깊이에서는 전체 호기성 생
표 5.8 무경운 (NT) 과 재래식 경운 (CT) 토양의 두 가지 깊이에서 미생물 개체군 크기의 평균비· 미생물군 NT/CT 비 0-7. 5 c m 7.5 - 1 5cm 호기성 세균 1.41 0.68 임의성 형기성 세균 1.57 1.23 방선균 1.14 0.9 8 NH.+ 산화균 1.25 0.5 5 N02-산 화균 1.58 0.7 5 곰팡이 1.57 1.2 3 ·자료 : Doran(1 9 80) 물(여기서 전체 호기성 생물이란 세균, 자낭균류, 암모니아 산화균, 아질산 염 산화균을 모두 통칭하고 있다 : 옮긴이) 및 임의성 형기성 세균과 곰핑 이의 수가 간 곳에서보다 갈지 않은 곳에서 각각 1.35 , 1. 57 배 높았 다 . 7.5-15 cm 깊이에서는 전체 호기성 생물, 곰팡이, 호기성 세균, 질산균이 갈지 않은 토양에서 모두 유의 수준으로 감소했다(표 5.8). 경운에 따르는 미소동물 개체군들의 변화는 전체 세균 수의 변화를- 반 영한다. 경운과 단종경작 monocul t ur e-g. 일반적으로 중형동물과 대형 동물에게 불리하다 . 5-8-2 살충제와 화학물질 야의에서 살포되는 정도로는 제초제와 잎 부분의 살충제가 토양미생 물에 직접적인 피해를 줄 만큼 충분한 농도가 되지 않는다. 질산균들 이 가장 민감하며 살생제를 잎에 뿌린 다음 때때로 질산화 작용이 억 제되는 것이 관찰된다. 잎이 나기 전과 잎에 사용되는 정상적인 양의 제초제는 뿌리혹박테리아에 뚜렷한 영향을 주지 않지만 숙주식물의 상
해와 성장 저해는 뿌리혹의 수와 질소고정에 영향을 준다. 살포된 살 충제의 종류와 그들의 살포율에 따라서 근권의 비병원성이고 비공생성 의 미생물 개체군들은 증가하거나 감소할지도 모른다. 이 역시, 그 반응둘은 식물의 생리학적인 변화와 특히 뿌리 분비물들의 종류와 양에 의해서 결정된다. 토양 생물군의 더욱 큰 교란은 곰팡이 살균제와 훈증소독제, 다론 근절제 형태의 화학물질들에 기인한다. 어떤 특정 미생물을 근절할 만 한 양으로 토양에 살균제와 훈증소독제를 살포한 다음 일주일 내지 수 주일 동안 흔히 토양 호흡률의 억제가 나타난다. 그러나 한두 달이 지 난 다음에는 살포하지 않은 토양보다 살포한 토양에서 더 큰 누적적인 CO2 발생이 있다. 미생물이 많이 죽으면 죽을수록 토양 호흡에 대한 부분적인 소독 효과는 더욱 현저해진다. 거의모든 비료가 만약 좁은 지역에 시비된다면 부과된 삼두압에 의 하여 미생물 활동의 지영적인 억제를 초래할지도 모른다. 무수 또는 수성 암모니아의 주입은 주입된 부분의 중앙에 살균적인 암모니아 농도를 일으키게 된다. 이에 따라 질산화 작용은 그 주변부에서나 진행될 것이다. 줄을 따라 살포한 요소도 토양미생물에 살균적인 농도의 암모니아를 형성시킬지도 모른다. 5-8-3 완전 벌목과 동제발화 완전 벌목은 목재 수확에 널리 이용되고 있고, 그것은 수확한 다음 여러 해 동안 토양 생물군에 영향을 끼친다. 지역의 질, 기후, 재식생 지 형성에 관련된 종의 차이들이 영향의 지속기간과 정도를 결정한다. 대부분의 연구둘은 첫 수년 동안 미생물과 동물의 생물량에서 현저한 증가가 있으며, 이는 때때로 두번째 해에 절정을 이루고, 때때로 5 내
지 10 년 동안 지속되는 것을 보여 준다. 완전 벌목한 다음 미생물 생 물량이 2, 3 배 증가하는 까닭은 여러 요쇼곡군과 관련되어 있다. 이 경 우 남겨둔 나뭇가지들이 상당히 중요하다. 그러나 가지들을 제거한 경 우와 남겨둔 경우를 비교하니 미생물의 증가가 남겨둔 나~ 부 분적으로만 관계되어 있었다 (Sundman 등 0978)). 더욱 유리한 수분 과 온도에 의한 잔여 낙영 및 낙지들의 증가된 분해 민감도, 죽은 뿌 리의 이용도, 새로이 자라는 초본류와 관목류로부터 쉽게 분해될 수 있는 낙엽 및 낙지들의 공급 등이 모두 미생물 생물량의 증가와 관련 이 있다. 토양 호흡 증가와 유기 질소의 무기화 과정이 미생물의 번성 과 병행하여 일어난다. 간섭받지 않은 삼림으로부터는 냇물로 흘러가 는 지표수를 통하여 질소 손실이 아주 없거나 거의 없다. 완전 벌목한 다음에는 냇물로 많은 양의 질소 유실이 뒤따른다. 벌목 후에 존재하 는 미생물들의 종 구성은 간섭이 있기 전의 것과 관계 있다. 그러나 각 개별 종들의 수적인 우세도는 크게 다르다 (Lund gr en0982)). 통제발화는 삼림에 새 활력을 주고, 이동 농경 shif t ag ricu ltu rei !} 관련하여 지역을 개량하기 위해 사용된다. 방화 기간과 불이 꺼진 직 후에는 완전 벌목과 대조적으로, 미생물과 동물 둘 다 감소된다. 두 그룹은 새로운 식물 성장과 낙엽 및 낙지들의 축적이 생김에 따라 빠 르게 회복한다. 미생물들은 아래에 있는 무기 토양과 젖고 마른- 축적 물질들로부터, 동물들은 불을 피한 낙엽 및 낙지들의 섬으로부터 종균 이나 씨와 같은 번식 수단을 얻게 된다. 참고문헌 Barber, D. A., and Gunn, A. B. (1974) . The eff ec t of mechanic a l for ces on the exudati on of orga nic substr a te s by the roots of cereal pla nts
grow n under ste r ile condit ion s, New Phyt ol . 73, 39. Barber, D . A., and Marti n, J. K. (19 76) . The release of orga nic substa n ces by cereal roots int o soil , New Phyt ol. 76, 69-80. Clark, F. E., and Paul, E. A. (19 70) . The mi cr ofl or a of gra ssland, Adv. Ag ro n. 22, 375-435. Doran, J. W. (19 80) . Soil mi cr obia l and bio c hemi ca l chang e s associa t e d wi th reduced tilla g e , Soil Sc i. S oc. Am. ]. 44, 765-771 . Helal, H . M. , a nd Sauerbeck, D. R. (19 84) . Infl ue nce of pla nt roots on C and P meta b olis m in soil , Bio l og ica l Processes and Fert ilit y (J. Ti ns ley and J. J. Darby sh ir e , eds.) , pp. 175-182. Marti nu s Ni jho ff /D r. W. Jun k. The Hag u e. Lundg ren , B. (1982) . Bacte r ia in a pine for est soil as aff ec te d by clear -cutt ing , Soil Bi ol . Bi oc hem. 14, 537-542. Newman, E. I. (19 78) . Root mi cr oorga nis m s:Their sig n if ica nce in the eco-sys t e m , Bio l . Rev. Cambri dg e Phil o s. Soc. 53, 511-554. Reic h le, D. E. (19 76) . The role of inv erte b rate s in nutr i e n t cyc l in g , Ecol. Bull. 25. 145-154. Shamoot. S., McDonald, I., and Bart ho lomew, W. (19 68) . Rhiz o dep o sit ion of orga nic debris in soil , Soil Sci. Soc. Am. Proc. 32, 817. Soma, K., and Sait o, T. (19 79) . Ecolog ica l stu d ie s of soil orga nis m s wi th refe r ence to decomp o sit ion of pine needles. I, Rev. Ecol. Bi ol . Sol16, 337-354. Sunjm an, V., Huhta , V., and Ni em ela, S. (19 78) . Bi ol og ica l chang e s in a nort he rn spr u ce for est soil aft er clear-cutt ing , Soil Bio l . Bi oc hem. 10, 393-397. Tie s sen, H., Ste w art , J. W . B., and Hunt, H. W. (19 84) . Concep ts of soil orga nic matt er tra nsfo r mati on s in relati on to orga nomi ne ral pa rt icl e siz e frac ti on s, In Bio l og ica l Processes and Soil Fert ility (J. Ti ns ley and J. W. Darby sh ir e , eds.) , pp. 287-295. Martin u s Ni jho ff /D r. W. Jun k, The Hagu e ..
추가로 읽을 거리 Burge s, A., and Raw, F. (19 67) . Soil Bio l og y. Academi c Press, London. Clark, F. E. ( 19 69) . Ecolog ica l associa t i on s among soil mi cr oorga nis m s, Soil Bio l . 9 , 125-161. Gray, T., a nd Parkin s on, D., e ds. ( 19 67) . The Ecology of the Soil Bact er i a. Liv e rpo ol Univ . Press, Liv e rpo ol.
제 6 장 탄소 순환과 토양 유기물 6-1 서론 미생물은 자연에서 쓰레기 처리대행자 역할을 하고 있다. 그들은 유 기물에 있는 탄소를 CO2 로 전환함으로써 광합성으로부터 시작된 생물 학적 탄소 순환을 완성시키게 된다. 〈재로부터 재로, 먼지로부터 먼 지로 〉 라는 인용구는 C ― H 결합에 축적된 에너지로 향한 미생물들의 끊임없는 탐색을 나타낸다. 이것은 토양과 퇴적토에서 유기 화합물과 연관되어 있는 거의 모든 영양소 순환반웅들의 추전력이다. 토양 또는 세포 수준에서 일어나는 탄소의 이동과 변환에 대한 자료는 식물과 미 생물이 이용하는 황, 질소, 인과 같은 다른 영양소들의 행동을 기술하 는 데에도 도움이 된다. 최근에 사람들은 범지구적인 탄소 순환이 생 물 생산성 및 유기물 대사회전과 밀접하게 연관되어 있다는 것을 알고 있다. 화석 연료의 연소, 광역적으로 발생하는 산불, 집중적인 논밭 갈이는 기후 변화에 중대한 영향을 끼칠 정도로 대기 중의 CO2 를 증 가시키고있다• 토양에서 일어나는탄소순환은범지구적인탄소순환
의 맥락에서 소개하는 것이 효과적이다. 이들 둘은- 밀접하게 관련되어 있기 때문이다. 6-2 범지구적인 탄소 순환 범지구적인 탄소 저장소들의 저장량에 대한 추정에 의하면 1860 년 전에 대기는 약 260p pm 농도의 CO2 를 포함했으며, 극히 최근에는 360 pp m 안 것으로 나타났다. 육상 생물군의 탄소는 대기의 500X 109 메가그램 (M g)보다 약간 적으며, 토양에 포함되어 있는 탄소는 대략 1500Xl09M g이다. 대기의 CO2, 육상식물, 토양 구성물들 사이의 계 속적인 생물학적 교환은 범지구적인 탄소 순환의 매우 역동적인 부분 을이룬다. 연간 전체 식물 생산량은 대양에서 40Xl09Mg , 육상에서 70x 109Mg 정도로 추산된다• 1 년 기준 식 물체들의 분해는 식 물 생산과 거의 동등하다. 그러나 일정 기간 나타나는 작은 차이가 중 요한 축적 또는 결손을 초래할 수 있다. 정상 상태 ste a dy s t a t러] 있 던 대기의 이산화탄소 농도는 1800 년대 후반 이래 변하고 있다. 아마 존강 유역에서와 같은 특히 산불과 연계된 산림 벌채와 아메리카, 시 베리아, 호주, 아프리카에 있는 처녀림들의 광역적인 파손은 육상계 로부터 대기로 순 탄소이동을 야기하고 있다. 표 6.1 은 내버려 둔 논 발과 이전에 벌목된 지역의 삼림 재생, 그리고 대양으로. CO2 확산에 의해서 대기에 유입된 양의 일부만 소비되는 것을 보이고 있다. 석탄과 석유 연소는 대기로 매년 7Xl09M g탄소를 유입시켜 범지구적인 대기 CO2 수준에 주요한 영향을 미친다. 이것은 단지 연간 육상에서 일어나는 생물적 순환의 10 분의 1 밖에 되지 않
표 6.I 범세계적인 탄소 저장소들과 주요 저장소 사이의 탄소 순이동량 탄소 저장소 이산화(p탄pm소 ) 농도 009탄M소g 량 C }• 대기 1850 260 560 1890 290 630 1986 360 760 대양 탄산염 20 X 106 용존 유기물 600 입자상과 침적토 유기물 3000 육지 생물군 500 부식질 1500 화석 연료 10000 탄소원과 연간 유동량(1 987) 화석 연료 연소에 의한 방출 73643-9 토지 정지작업 삼림의 수확과 분해 삼립의 재성장 一
대양에 의한 순흡수량(확산) ― 연간 순유동량 • 1 Mg = l06 g= l metr i c ton 지만 계속된다면 문제가 될 수준으로 전체 대기의 CO2 가 증가될 것으 로 예상할 수 있다. 대기의 CO2 가 600 pp m 에 달하게 될 때, 온실효 과에 의한 기온 상승으로 국지는 6-8°C 정도 될 것으로 예측된다. 극지의 온난화는 광대한 빙산의 해빙과 많은 해안 도시의 범람을 초래 할 수 있다. 온난화 경향은 또한 강우 유형과 새로운 지역의 사막화를초래할 수 있다. 유익한 쪽으로는 그것이 더욱 높은 위도 방향으로(더 욱 북쪽과 남쪽으로) 농경지의 확장을 초래할 수 있다. 또한 더욱 높은 CO2 농도는 더 높은 광합성과 수분 이용 효율 및 공생적 질소고정과 균근들에서 일어나는 것과 같은 식물과 미생물 연합의 보다 나은 기능 울유도할수있다. 6-3 유기 잔여물들의 성분과 대사회전 토양으로 들어가는 유기 탄소의 가장 큰 부분은 식물 잔여물 이다. 식물은 셀룰로오스 15-60%, 헤미셀룰로오스 10-30%, 리 그닌 5-30%, 단백질 2-15% 를 포함한다. 당류, 아미노 당 오스, 5-30% 리그닌, 2-15% 단백질을포함한다. 당류, 아미노 당 류, 유기산, 아미노산 같은 가용성 물질들은 전량의 10 %를 이룬다. 그들은 식물 잔여물로부터 곧장 산출되며, 토양미생물에 의해서 재빨 리 이용된다. 식물 잔여물의 분해를 토양 유기물의 그것으로부터 분리 해 내기는 어렵다. 정의에 의하면 미세하고 식별 가능한 잔여물과 미 생물 몸체들은 토양 유기물의 일부이며 거기에 포함된다. 식물 잔여물 분해와 토양 유기물 형성에 대한 검토는 Ste v nson(1982a), Flaig (1975) , Tate (l987) 등에 의해서 이루어졌다. 6-3-1 탄수화물 자연에서 혼한 단량체 monomer 의 당류(그립 6.1) 는 식물, 토양, 미생물에서 여러 구조로결합된다. 식물의 주요저장요소인 녹말은 두 포도당의 중합체 인 아밀로오스와 아밀로펙틴을 포함한다. 아밀로 오스는 a(l-+4) -글루코시딕 결합에 의해서 글루코오스 단위들로 이
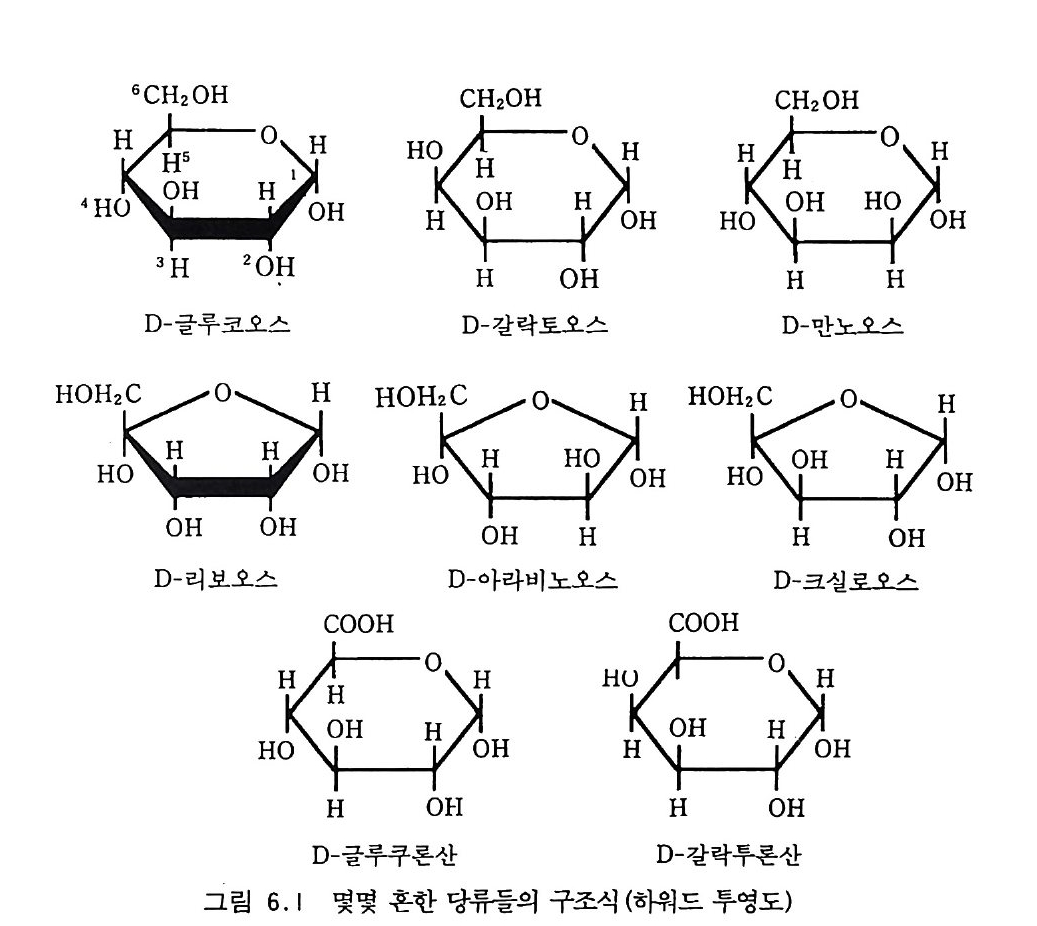 'HQ H H~> \CH 20H
'HQ H H~> \CH 20H
루어전 하나의 가지 없는 고리가 된다(그림 6.2). 아밀로펙틴은 같은 일반적인 구조이지만 a(1-+6) 에 의해 결합된 결고리들이 있다. 많은 세균과 곰핑이들은 통칭 아밀라아제로 알려진 세포의 효소들을 생산함 으로써 녹말을 가수분해한다. a- 아밀라아제는 아밀라아제와 아밀로펙 틴을 여러 개의 포도당 분자 구성 단위들로 분해한다. /3-아밀라아제 는 아밀로오스를 엿당으로 분해한다. 아밀로펙틴은 엿당과 덱스트린 의 혼합물로분해된다. 셀룰로오스는 식물 잔여물들의 가장 혼한 구성물인데 종종 헤미셀룰
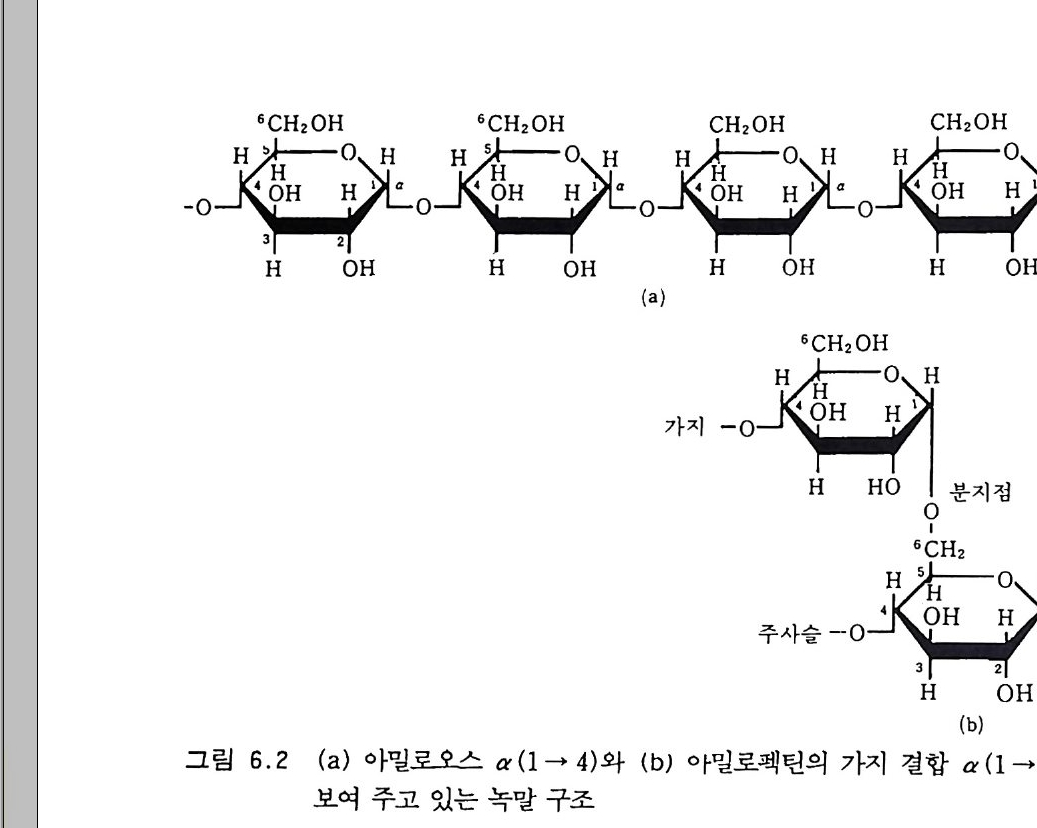 -0 。
-0 。
로오스 및 리그닌과 연관되어 있다. 그것은 분자량 106 인 반결정체 상 태로 생기며 /3( 1-4) 결합을 가전 포도당 단위들로 구성된다. 개개 의 가지가 없는 고리들은 그림 6.3(b) 에서 보여 주는 것처럼 수소결 합에 의해서 연결된다. 분해는 Pseudomonas, Chromobacte r i um , Bacil lu s, Clostr idi u m , Str e p tom y ce s, Cy t op h aga 와 같은 다양한 세균 과 Tr ich oderma, Chaeto m i um , Pen i c i ll i um 과 같은 곰핑이로부터 생성된 셀룰로오스 분해효소에 의해 일어난다• 셀룰로오스 분해효소라 는 용어는 뚜렷한 두 개의 단계로 작용하는 효소 복합체를 나타낸다. 첫째 결정체 구조의 손실이 있고 그 디옴- 중량체의 해체가 일어난다. 그 결과로 생기는 이당류인 셀로비오스는 효소 셀로비아제에 의해 포 도당으로 가수분해된다. 이것은 분해자에 의해 흡수될 수 있거나 가용
성 탄소집소 carbon po ol.£ . 들어갈 수 있다. 예를 들면 Clos tri d i um 과 같은 세균들은 셀룰로오스를 산소 없이 분해할 수 있다. 보통 헤미셀룰로오스라 불리는 이질적인 화합물 집단은 육단당 , 오 탄당 때때로 우론산의 다양한 중합체들이다. 흔히 생기는 이 집단의 단량체는 크실로오스와 만노오스다(그림 6.1). 순수한 상태에서 헤미 셀룰로오스들은 쉽게 분해된다. 자연에서 그들은 종종 분해를 어렵게 만드는 다른 물질들과 복합체를 이루고 있다. 식물 세포벽의 중간 라 베라충에서 이 물질의 중요성 때문에 미생물에 의한 헤미셀룰로오~ 펙틴 (흔히 po lyg a lactr u onic ac i d) 의 공격이 연구되고 있다. 그 과정은 종합적으로 펙티나아제라고 알려진 여러 개의 효소를 포함하는데 그 효소들은 신선한 기질에서는 고농도 수준의 당류에 의해서 억제될지도
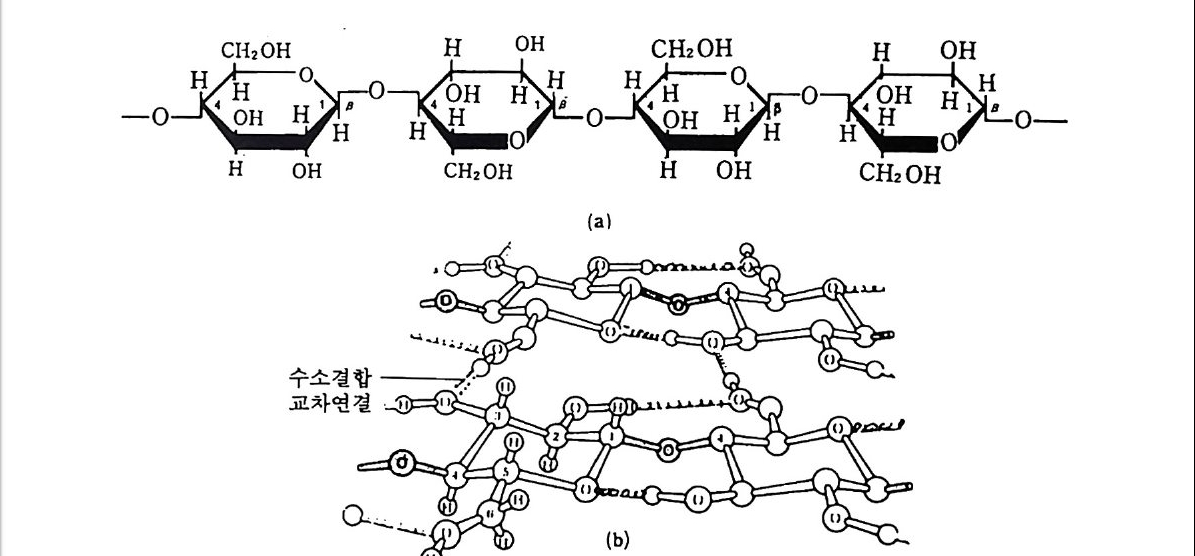 —o OH 。 CH20H OH o—
—o OH 。 CH20H OH o—
그림 6.3 (a) /J( 1 一 4) 결합과 (b) 평행하는 포도당 구성 단위들의 두 고리 사 이의 수소결합 연결을 보여 주는 셀룰로오스 구조. 고리의 구조는 아마 자연에서 발생하는 당류의 형태이다.
모른다. 식물 조직이 분리될 때 곰팡이가 분해 활동을 개시하는 것처럼 보이지만 자낭균들은- 더욱 오랜 기간 공격을 유지할 수 있다. 펙티 나아제들은 아마도 Rh iz ob iu m 과 균근들에 의한 숙주세포의 침두와 관련되어 있다. 토양 탄수화물들은 부식산 핵의 중심 부분은- 아니다. 그들은 둘레의 곁가지로서 붙어 있는데 더욱 자주 독립적인 다당류로 나타난다. 독립 적인 상태에서 그들은 곧장 분해될 수 있으나 결코 토양 탄소의 15% 이상을 차지하지 않는다. 토양 안에서 그들의 내구성에 대한 이유들이 밝혀져야 한다. 점토에 의한 부착과 철, 알루미늄, 구리와 같은 다가 양이온의 금속들과 상호작용은 미생물 공격에 대한 다당류들의 저항력 을 크게 증가시키는 것으로 밝혀지고 있다. 내구성에 대한 가능성 있 는 다른 이유는 다당류들이 토양 입단과 관련되어 있는 주요 요소라는 것이다. 입단 중앙에 있는 다당류들은 경작이나 다른 힘들이 그 표면 울 미생물의 공격에 노출시킬 때까지 더욱 분해되는 것이 방지될 것이 다. 6-3-2 리그닌 리그닌(그림 6.4) 의 구조는 페닐 프로파노이드p hen y l pro p a noid 단 위가 기본이 되는데 이는 방향족 고리와 3 탄소 결고리로 되어 있다. 중합체에 의해서 형성된 리그닌은 방향족 토양 유기물과 같은데 특수 한 효소에 의해서 형성되지 않고 페놀과 유리반응기와 관련된 반응에 서 만들어전다. 그러므로 이 물질은 특수한 구성 분자들의 나열 순서 롤 가지고 있고 셀룰로오스와 헤미셀룰로오스 바탕에 하나의 의피가 되는 물질을 형성한다. 토양 속으로 들어가는 리그닌의 일부는 완전히 분해되지 않고 토양 유기물 생성에서 미생물이 생산한 물질과 반응한 다.
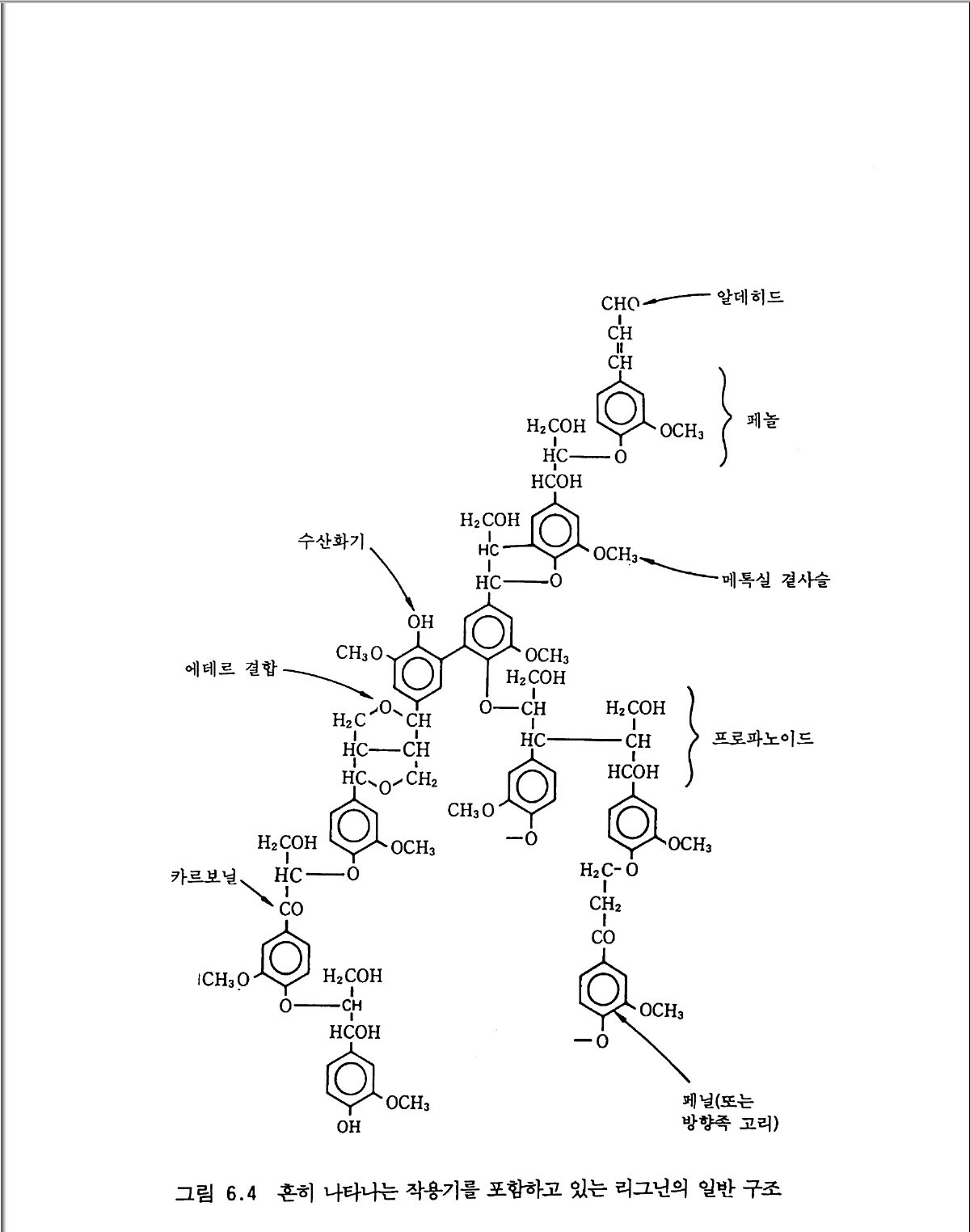 CdiH: ( ).---알 데히드
CdiH: ( ).---알 데히드
리그닌의 분해는 주로 곰팡이에 의한다. 부패한 기질의 색깔은 곰팡 이의 공격 유형을 보여 주는 지표가 된다. 흰가루곰팡이 whit e- rot fu n gi들이 가장 활발한 리그닌 분해 미생물인데 모든 목질성 구성 요 소들을 CO2 와 H20 로 분해해 놓는다. 리그닌 분해에서 흰가루곰팡이 는 종종 여러 가지 이름으로 알려져 있다. Cor iolu s vers i color( 때때 로 Tramete s . Polyp o rus, Poly s ti c t us 속을 포함)는 고리, 메독실 또는 더 긴 결고리 구성 요소들을- 분해한다. Pleurotu s os t rea t us 와 Phanero-chaete ch ry so sj) on·um 도 역시 일차 에너지원과 같이 쉽게 분해될 수 있는 다른 기질과 함께 있는 경우에만 리그닌을 분해하는 것으로 생각 된다. 흰가루곰팡이는 단지 적당한 02 가 있는 경우에 활동적으로 리 그닌을 분해한다. 질소 이용도가 높을 때 리그닌 분해가 억제되는 것 은 홍미롭다• 매우 적은 양의 리그닌 탄소가 리그닌 분해 세균에 의해 서 세포 구성물로 흡수된다. 배양 실험에서 리그닌 “C는 토양 부식질 에 병합되었지만 토양 생물체 안에서는 유의성이 있는 정도로 발견되 지 않았다. 갈색가루곰팡이는 리그닌과 연관되어 있는 다당류들을 분해하여 CH3 하부 그룹과 R-0 -CH 3 결고리를 제거한다. 이것은 페놀울 남 기게 되는데, 이 페놀이 산화하면 갈색으로 변하게 된다. 대표적인 미 생물은 Po ria 와 Gloeop hy llum 이다. 수분이 많은 상황에서 다른 곰팡 이 그룹인 연녹색곰팡이 soft -r ot fun g i7} 중요한데 연목보다 경목의 리 그닌을 더욱 효과적으로 분해하는 것 같다. Chae t om i um 와 Preussia 가 S이tr 들e p의t o m대 y표 e e적s 인와 미N생oc물a이rd다ia. 같 은 자 낭 균 과 Azoto b acte r 와 Pseudomona. s 같은 호기성 그람음성 세균둘은 리그닌 분자의 크기를 줄인다. 그들이 완전한 분해를 일으킬 수 있는지, 그들이 생장을 위해 서 리그닌 탄소 중 어느 일부를 사용할 수 있는지는 명확하게 알려져
있지 않다. 그들이 식물 잔여물에 있는 셀룰로오스와 헤미셀룰로오스 를 감추고 있는 장애물을 제거하기 위해서 리그닌울 공격할 가능성이 있다. 자연에서 방향족 물질들의 대사회전 속도는 토양 유기물 역동성을 결정하는 중요한 요소다. 방향족 물질의 분해에 대한 연구를 하기 위 해 화학적으로 또는 “C 를 붙인 페닐알라닌, 신남산, 포도당을 식 물에 공급함으로써, 리그닌이나 셀룰로오스에 “C 를 포함하는 리그 노셀룰로오스를 만들 수 있다. 배양에서, l4C 를 포함하는 셀룰로 오스 구성요소들로부터 CO2 발생 속도는 짧은 지체기를 가전 후에 매 우 빠르게 증가한다. 리그닌에 대한 분해 속도는 건 잠복기를 보여 주 며 연관된 셀룰로오스 분해속도 4 분의 1 에 해당하는데 이는 구조적 으로 아주 가까이 연관된 물질들조차 다른 속도로 분해하는 것을 나타 낸다. 코니페릴 알코올 conif er yl alcohols, 페룰산 fer ulic a ci d 과 카페산 caff ei c aci ~ 리그닌 구성 단위들과 비슷한 구조를 가진다. 그들의 분해에 대한 연구들은 유기 잔여물의 분해에 대한 쓸모 있는 정보를 만들어 낸다. 많은 방향족 물질들의 “COOH 는 탈카르복시 과정에 의해서 제거되는데 이는 토양 부식질 구성물로는 거의 합체되지 않는 다(그림 6.5). 그립 6.5 는 또한 포도당, 간단한 아미노 화합물들, 방 향족 고리의 14C들 에 대한 상대적인 분해와 안정속도들을 보여 준다. 카페산이 부식산처럼 중합체로 축합되면 모든 고리 탄소가 안정화되 지만 14COOH 는 여전히 선호적으로 떨어져 나가는 탈카르복시기이 다.
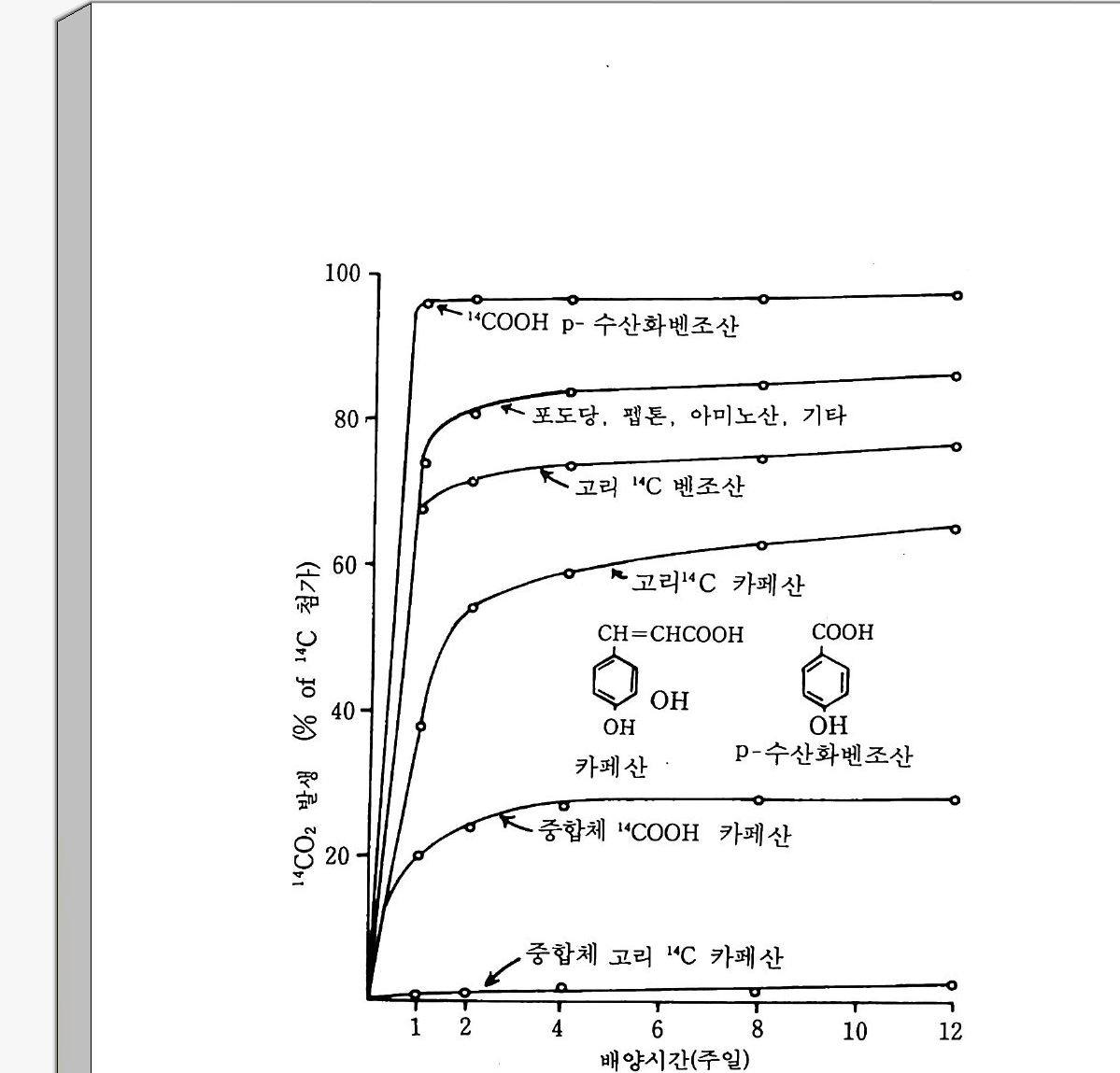 100
100
그림 6.5 그린필드 사질양토에서 uc 특수 표지를 단 벤조산과 카페산, 페놀 중합체와 결합된 카페산, 여러 개의 간단한 유기 화합물들의 분해 (H a i der 와 Marti n ( 1975) ) 6-3-3 질소 화합물 배양된 토양의 유기 질소 함량은 일반적으로 유기 탄소와 비슷한 경 향을 보이는데 탄소/질소의 비는 10 정도이다. 전체 토양 질소 중에 서 적어도 3 분의 1 은 구조식이 밝혀지지 않은 채 남아 있다. 산에 의
한 가수분해 (3 내지 6 N HCI 에서 12 시간 끓임으로써)에 의해 전체 질 소의 반 이상을 아미노산과 아미노당류로 방출한다(표 6.2). 그들의 질소 함량은 높기 1 때문에 아미노산들은 토양 탄소의 약 20% 와 토양 질소의 30-40% 를 포함한다. 그들은 일년 동안 무기화되는 유기 질소의 더 큰 부분을 차지하기도 한다. 아미노산의 총량과 상대적인 양은 경작과 함께 감소히는 경향이 있다. 반면에 아미노당류의상대적 인 질소는 토양 총 질소량이 감소하더라도 일정하게 머물러 있다. 이 것은 아미노산이 토양 질소의 무기화 과정에 공헌되는 만큼 많이 아미 노당류가 공헌하지 않는 것을 나타낸다. 8 장에 기술된 바와 같이 접 토에 고정된 NH4+ 는 산에 의한 가수분해 동안 유출되고 표 6 . 2 에서 보여 주는 암모니아 일부를 이룬다. 황을 포함하지 않고 있는 가장 혼한 아미노산들 중 몇몇의 화학구조 들이 그림 6 . 6 에 나타나 있다. 아미노산의 일반적인 분포는 표 6.3 과 같다. 산의 성질을 띤 아미노산들 (o P-피르트산과 글루탐산)은 열대 성 토양에서 우선적으로 증가하는 것 같지만 일반적으로 전세계의 토 양 범위에 걸쳐 아미노산 구성은 유사한 것이 분명하다. 독립적인 상태에 있는 아미노산들은 빠르게 분해된다. 대부분의 아 표 6.2 토양 질소의 분포* 질소 형 태 (%, 전체 토양 질소량) 기후지대 총(질%)소 산불용성 NH3 0~ 미노산 아미노당 가미수식분별해 질되소는 국지 (6)·· 0.02-0. 16 13.9 土 6 . 6 32.0 土 8.0 33.1 土 9.3 4 . 5 土1.7 16. 5 냉대 (82) 0 . 02-1. 06 13.5 土 6.4 27 . 5 土 12 . 9 35.9 土 11. 5 5.3 土 2.1 17. 8 아열대 (6) 0.0 3 -0.30 15.8 士 4 . 9 18.0 土 4.0 4 1. 7 土 6.8 7 . 4 土 2.1 17.1 열대 (10) 0.02-0.1 6 1 1.1土 3.8 24.0 土 4.5 40 . 7 土 8.0 6 . 7 土1. 2 17. 6 •·• 괄자호료 : 안S의ow d숫e자n 들등은 (1 9조77)사 된 토양의 종류 수를 나타낸다.
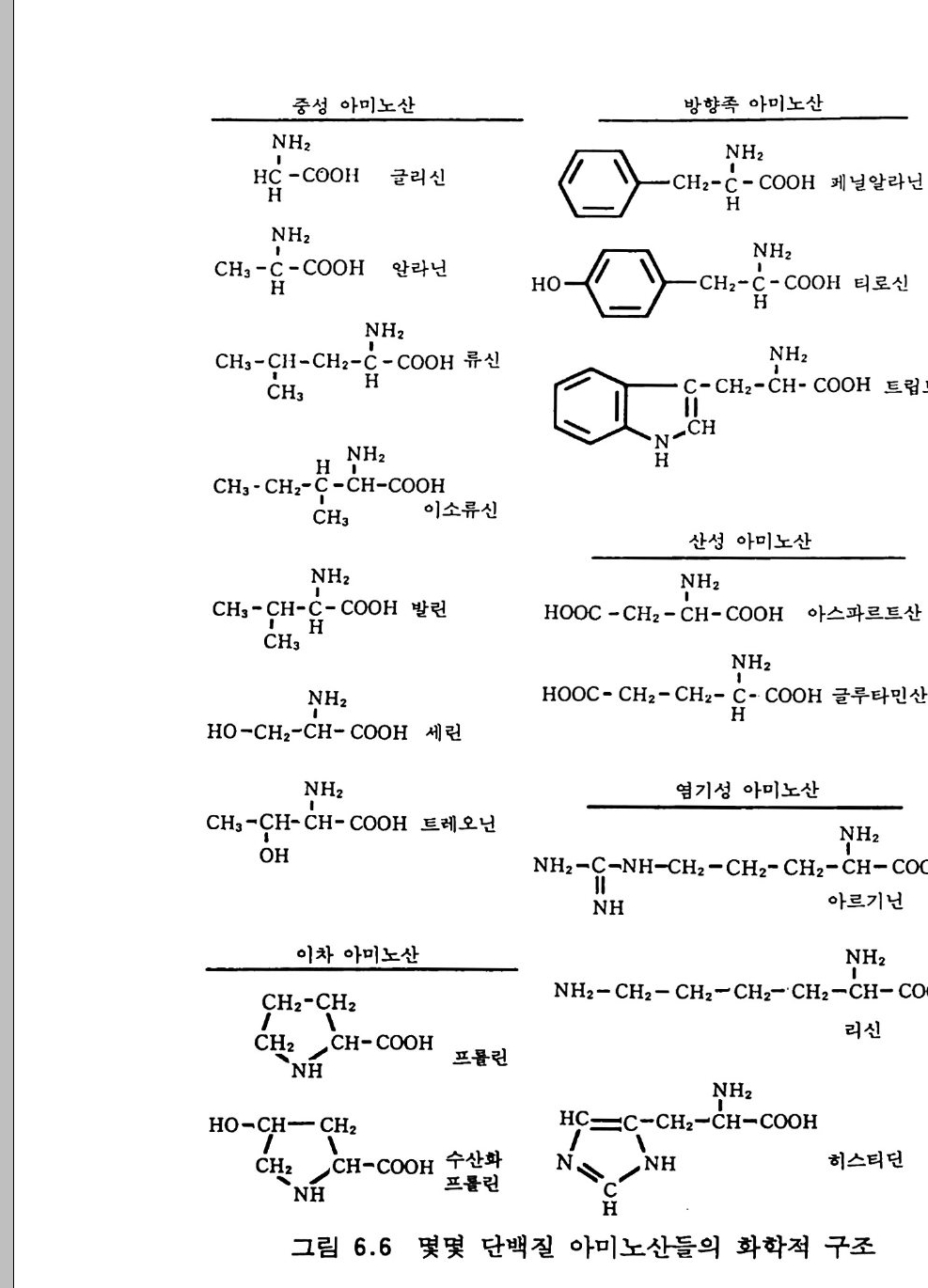 중성 아미노산 방향족 아미노산
중성 아미노산 방향족 아미노산
표 6. 3 주요 토양 기후대에서 아미노산의 분포(%) 아미노산 극지 온대 아열대 열대 사\..0서 16 21 22 26 염기성 26 24 25 20 ?= 「· k0 1 54 50 50 51 황함유 3 3 2 2 기타 1 2 1 2 미노산은 토양에서 비교적 안정된 미생물 생물량의 구성 원소가 되거 나 다른 유기물이나 점토와 상호작용하며 토양 입단 속으로 합류하기 때문이다. 양으로 하전된 아미노 그룹을 하나 이상 가전 염기성 아미 노산들은 산성과 중성의 아미노산들보다 환원성 당류 및 퀴논과 같은 다른 유기 구성물과 빠르게 반응한다• 그들은 또한 음으로 하전된 점 토에 더 잘 부착된다. 분해 속도가 가장 높은 열대성 토양에서 산성 아미노산들이 우세한 것은 이들 아미노산들이 철분 함량이 높은 침철 광 go eth i t e 같은 다가 (mu lti char g ed) 의 점토와 강하게 반응한다 는 발견과 잘 일치한다. 아미노산들은 펩티드 결합(그림 6.7) 으로 서로 합쳐져서 복잡한 단 백질 구조로 형성된다. 단백질은 생물의 가장 풍부한 질소 함유 구성 물이며 많은 토양미생물로부터 공격을 받는다. 단백질 분해효소 pro te o lyt ic enz ym~은 펩티드 결합을 가수분해한다. 트립신 같은 효 소들은 부분적인 가수분해에 의해서 프로테오스p ro t eose 혜 7 생산한다. 프로나아제 p ronase 와 서브틸리신 sub tili s i n 과 같은 미생물 효소들은 말단 아미노산 고리 제거기능을 수행하며 트립신이나 파파인과 같은 동식물 프로테오스들보다 자연에서 더욱 강력한 효력을 가진다• 또 한 실험실 조건에서 토양 유기물의 단백질 구성분을 가수분해하는 데 이용되고있다.
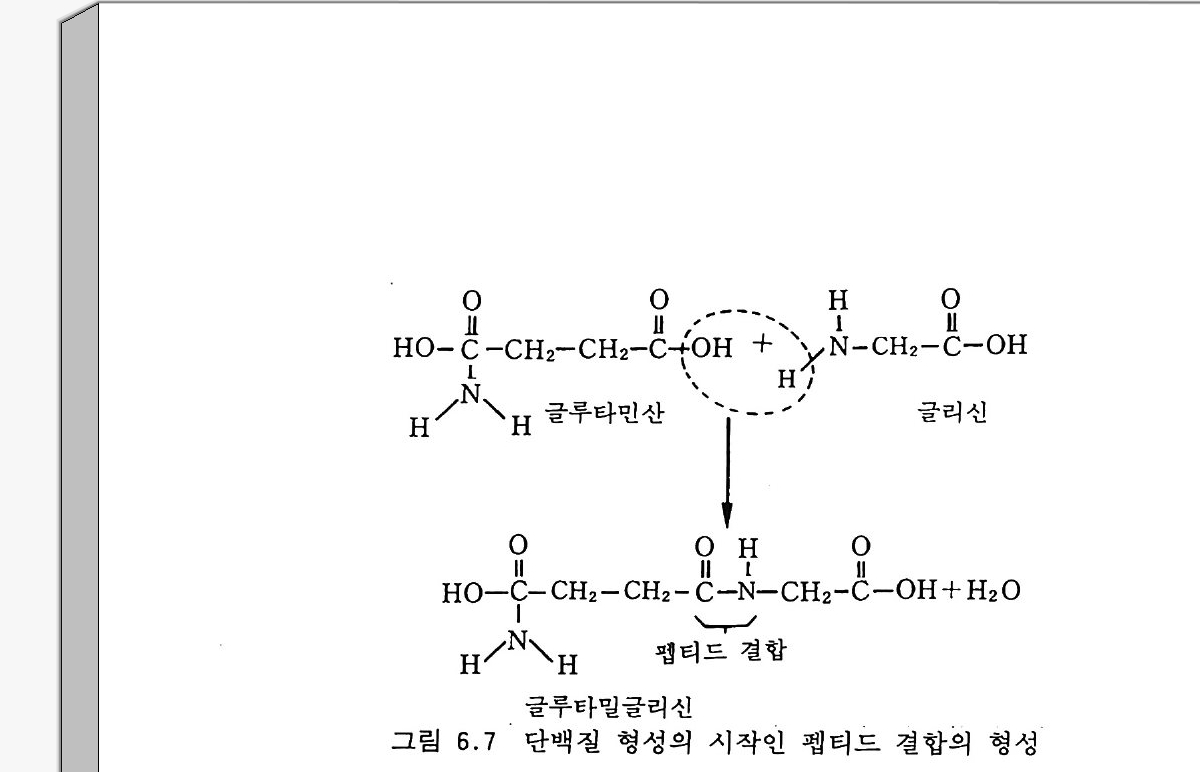 H0 -HO/-ll C C\LHN LH HC타 uHn 민 LF 산 IIOC '+,\`t0 -``HI i `+/H`、 、 '/x ` Hl1,Nc H 2 글 리O신_II c。 H
H0 -HO/-ll C C\LHN LH HC타 uHn 민 LF 산 IIOC '+,\`t0 -``HI i `+/H`、 、 '/x ` Hl1,Nc H 2 글 리O신_II c。 H
케라틴같이 많은 교차결합을 가진 섬유성 단백질들은 St re p tom y c es 와 같은 방선균과 Pen i c i ll i um 과 같은 균류가 결국은 분해할 수 있지 만, 미생물 공격에 대해서 저항성이 있다. 부패에 대한 저항은 케라틴 에 있는 많은 시스틴 분지들 사이에 이황결합 dis u lfid e bond 이 있기 때문이다. 이들 결합이 가압증기 멸균 분쇄, 보올 밀 분쇄 또는 미 생물 작용으로 끊어질 때 케라틴 분자는 여러 단백질 분해효소들 에게 민감하게 반응하여 곧장 분해된다. 식물 잔여물들에 있는 개개의 아미노산들과 단백질이 빠르게 분해된 다고 해도 미생물에 의해 생산된 유기 질소는 토양에서 안정화된다. 이것은 미생물 생체 그 자체의 상대적으로 느린 대사회전과 저항성 있 는 유기물과 연합으로 또는 토양 입단 안에서 유기 질소가 안정되기 때문이다. 유기 구성물로 합체된 질소는 무기화되기 전에 종종 오랜 기간 토양에서 유지된다. 매우 길지 않은 기간에 대사회전되는, 예를 들면 6 개월에서 10 년의 대사회전 기간을 가지는, 토양 영양소들은 토양 유기물 중에서 활성이 있는 부분이다. 더욱 오랜 기간 지속되는
물질들은 저항성 있는 부분으로 있다. 6-3-4 생물의 세포벽 곰팡이와 세균의 세포벽은 토양 유기물 형성의 주요한 선구물질들이 다. 곰팡이 세포벽의 분해는 Str e p tom y ce s, Pseudomonas, Bacil lu s 와 Clostr idi u m 같은 속들에 의해서 일어난다. Mo rti erella 와 같은 곰팡이들은 산성 조건에서 중요하다. 토양에서 아미노당류의 주요한 공헌자들 중의 하나인 키틴은 곰팡이 세포벽의 주요 구성분이다. 키틴 은 곰팡이 세포벽에서 다른 섬유성 탄수화물 구성분들과 연관되어 있 다. 키틴의 아세틸글루코사민 구조(그림 6.8) 는 질소를 포함하며, 그 것의 분해는 질소 결핍으로 제한되는 것 같지 않다. 환경 요인들에 의 해서 조정되는 것에 덧붙여서 분해 속도는 연관되어 있는 물질들의 영 향을 받는다. 많은 조균류의 세포벽들은 셀룰로오스 섬유질을 함유하 고 있다. 반면에 Fusa ri um 와 같은 생물은 당류 /3 (1 --+ 3) -와 /1 (l--+
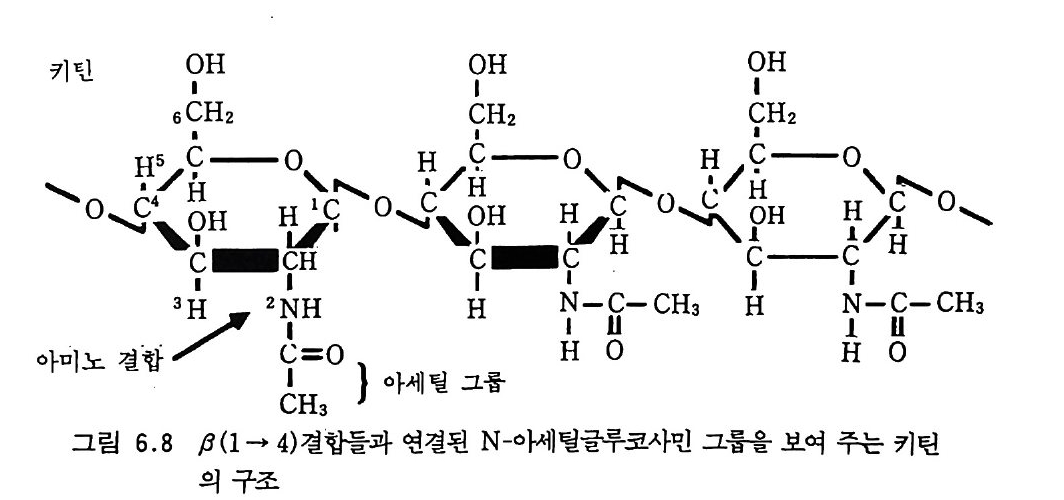 `키 민o HsJ5 /6 vhC0CcIII HH — -2 C2나H?01 H\g ` 。 sH•、 /HHOCcC멘III H H — 2 - C뀌나o' . \ .게I5H. - oC H~ 3 HC IHfHcOgClI HHH2 __ zg H。’- 8 \-~CHo3`
`키 민o HsJ5 /6 vhC0CcIII HH — -2 C2나H?01 H\g ` 。 sH•、 /HHOCcC멘III H H — 2 - C뀌나o' . \ .게I5H. - oC H~ 3 HC IHfHcOgClI HHH2 __ zg H。’- 8 \-~CHo3`
6)- 글루칸의 중합체를 포함한다. 이들 균사가 키틴 분해효소 ch iti nase 와 글루칸 분해효소g lucanas 타] 노출되지 않는다면 그들은 분해되지 않을 것이다. 검은 색소는 더 나아간 보호를 제공하게 되는데, 그리하 여 이들 구성분이 낮은 대사회전 속도에 대한 이유를 보여 준다. 세균의 세포벽은 당류의 두 가지 파생물인 N- 아세틸글루코사민과 N - 아세틸무람산의 고리들로 구성된 딱딱한 충을 가진다. 이들 고리들 은 펩티드 결합을 통하여 연결되어 있는 한정된 수들의 아미노산들에 의하여 서로 결합하게 된다(그림 6.9 ) . 펩티드 교차결합은 아주 종종 L- 알라닌, D- 글루탐산, 메조디아미노 피멜산 mesod i am i no pim eli c acid , D- 알라닌 들로 이루어져 있다. 그람양성균의 두꺼운 세포벽은 디론 세포벽 구성분들과 연결되어 있 는펩티도글리칸을포함하는데 이들 구성분들은 다양한 다당류와 인 에스테르 결합을 통하여 붙어 있는 다중인산염 po lyp h osph ate 분자들 을 포함한다. 대부분 D- 알라닌을 포함한다. 이들 물질은 표면 항원을 구성하는데 의피충을 통한 이온의 통괴에 영향을 미치고 점토에 대한 세균의 부착에 중대하다. 그람음성균은 더욱 복잡한 세포벽을 가진 다. 외막은 리포다당류, 리포단백질, 지질 동으로 이루어져 있다. 하 나의 작은 펩티도글루칸 총의 세포막 바로 바깥에 있다. 세포질 주변 공간은 대부분의 토양 세균 가수분해 활동에 영향을 주는 효소 활동을 위한공간이다. 토양에서 곧장 이용될 수 있는 “C 기질에서 미생물의 성장이 잔여 14C 세포벽 물질들의 조성을 야기하는 것으로 밝혀지고 있다. 이들 물 질들은 분해되기 쉽거나 토양의 활발한 부분 중에서 중요하지만 거의 연구되지 않은 구성요소이다. 이 부분은 더욱 저항성이 있는 토양 부 분보다 질소, 황, 인과 같은 영양소들을 더 많이 공급한다. 오랜 기간 의 실험실 배양 동안 이들 영양소들의 무기화된 형태들 (NH.+,
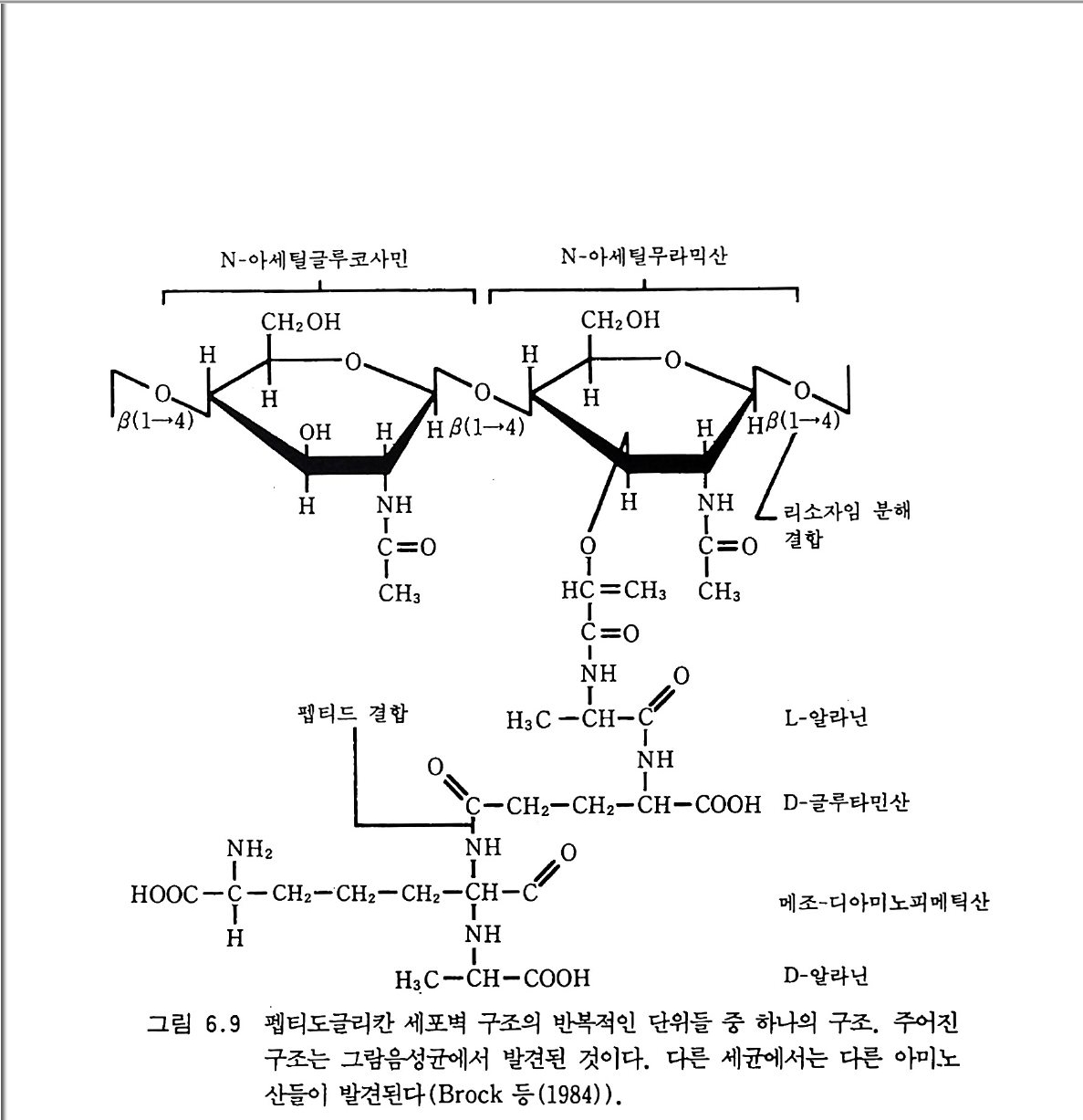 N - 아세딜글루코사민 N- 아세틸무라믹산
N - 아세딜글루코사민 N- 아세틸무라믹산
N03 一, Po.3-, s0.2- )의 축적은 이 부분의 크기를 결정하는 한 수단 이다. 다른 기법은 동위원소 희석실험의 이용이다. 이것은 동위원소 룰 붙인 유기 잔여물을 상당 기간 토양에서 배양해서, 미생물이 생산 한 14() 라 ISN 화합물처럼 쉽게 분해되는, 토양 유기물 양을 측정하는 것 0] 다.
6-3-5 뿌리와 뿌리 분비물 뿌리는 자연 생태계에서 주요한 탄소 저장소를 이루며 대부분의 지 상물질이 제거되는 연속 경작 체계에서 중요한 역할을 한다. 작물 울 이용한 몇몇 연구에서 지상 및 지하부의 물질이 비슷한 분해 속 도를 보이고 있다. 다른 연구들에서는 뿌리가 느리게 분해되기도 했 다. 땅 속으로 옮겨지는 물질의 양은 식물의 생물기후학에 따라 변한 다. 뿌리털과 접액질처럼 떨어져 나간 뿌리 물질들은 주요한 탄소원을 이루는데, 토양에 있는 방사능· 물질로 표지된 전체 양은 수확기에 뿌 리로 떨어져 나가는 양보다 20-50% 가량 높은- 것으로 추적자 실험에 서 나타났다. 이것은 떨어져 나간 뿌리털과 다른 뿌리 파편들 때문인 것으로 본다 (L y nch(1983)). 뿌리 분비물들은 주요한 질적인 영향을 주는데 보통 빨리 분해되기 때문에 오랜 시간의 14C 실험에서는 다만 적은양이 남는다. 다년생 자연 초원의 야의 조건에서는 “CO2 로 표지를 하였을 때, 동화된 탄소의 52% 가 지상에, 36% 가 줄기 기부와 뿌리에 나타났 다. 단지 12 %가 표지되는 기간과 표지가 끝난 직후에 호흡으로 소비 되었다. “C 자료는 역시 반 이상의 잔여 뿌리 탄소가 한 번의 생장 기간에 분해되는 것을 보여 주었다. 나무는 그들 광합성 산물의 큰 몫 울 지하부의 미세한 뿌리로 옮기는 것으로 나타나고 있다• 침엽수 와 관련된 균근은 지상부의 낙엽 및 낙지만큼 많은 양의 탄소롤 토양에 공급하는 것으로 알려져 있다.
6-4 토양 유기물의 생성 토양 유기물은 분해되고 있는 잔여물, 분해를 하고 있는 미생물들에 의해 생산된 부산물, 미생물들 그 자체, 잘 분해되지 않은 부식질들로 이루어져 있다. 식물 잔여물들은 페놀성 물질들의 함량과 셀룰로오스 와 단백질에 대한 리그닌 부분에서 서로 다르다. 탄수화물과 단백질에 대한 미생물들의 공격은 미생물 산물을 생산하고 탄소 : 질소 : 황 : 인 의 비에 따라서 CO2 뿐만 아니라 S042- 와 NH4+ 을 생산한다(그립 6.10). 부식질들의 생산울 설명할 수 있는 물리적인 두 응축 과정들이 있다. 연관된 반응물들이 일련의 관련은 있으나 동일하지 않은 화합 물이기에 중합체 형성과정이라기보다응축과정이라부론다. 부식질의 실제적인 응축과정은 효소가 조절하지 않기에, 결과로 생기는 두 분자
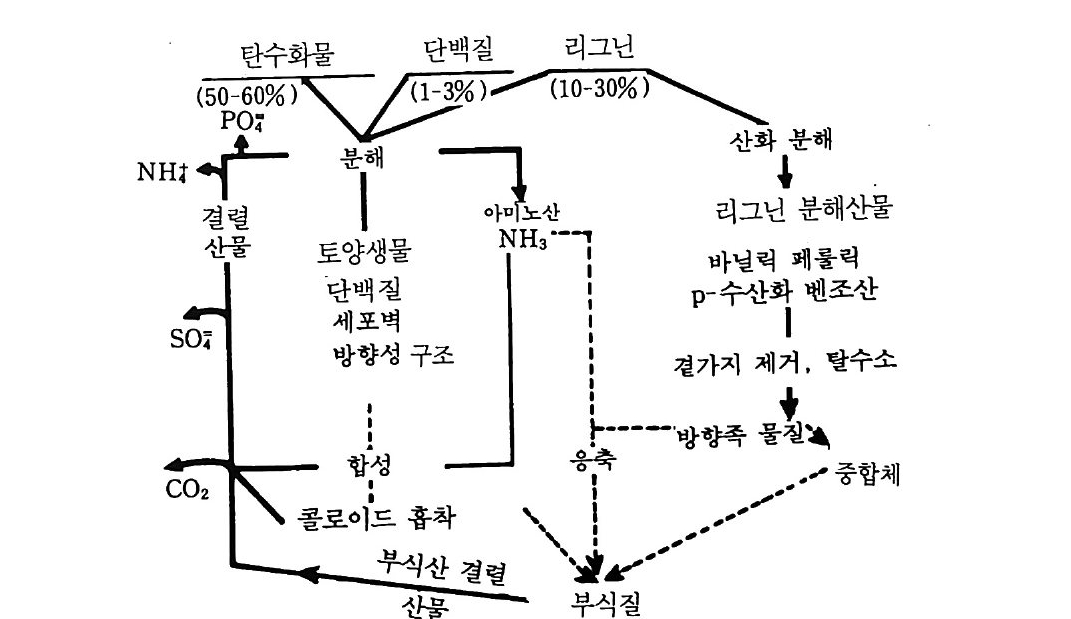 NHl t(5 틀탄 수화물 분「 \단길백질 3 산 _리-,/그 닌 리산그 화j:해해소邊
NHl t(5 틀탄 수화물 분「 \단길백질 3 산 _리-,/그 닌 리산그 화j:해해소邊
그림 6.10 식물 잔여물의 분해와 토양 유기물의 형성
모두 정확히 같은 것으로 기대할 수 없으나 거의 대부분의 지역에 서 부식질의 일반적인 형태는 매우 비슷하다. 그립 6.11 에서 토양 유기물 형성에 대한 두 가지 이론 중 하나를 보여 준다. 이 그림은 하나의 아미노산(여기서는 글리신)이 리그닌의 부분적인 분해 또는 곰팡이 Ep i coccum 에 의해서 생산된 것과 같은 미 생물 색소로부터 유도된 페놀 (ca t echol) 과 반응하는 것을 보여 준다. 이들은 아미노퀴논 중간물질을 형성하는데 이는 응축되어 갈색의 질소 를 가진 부식질을 만들 수 있다. 그립 6.11 과 6.12 에서 보여 주는 퀴논-아미노산 또는 암모니아 (NH3) 반응은 부식질 형성에 갈색화 반 응보다 더욱 중요한 것으로 간주된다(그림 6.13). 갈색화 반응은 당류 (여기서는 포도당)가 글라신과 같은 아미노산과 반응하는 것을 보여 준 다. 결과적으로- 부가되는 화합물들은 재배열하고 분철하여 삼탄소 알 데히드와 케돈, 리단돈, 푸르푸랄 등의 세 개의 중간물질들을 만든다. 이돌 중간물질 모두 아미노 화합물질들과 쉽게 반응하여 어두운 색의 최종 산물을 생성한다. 두 가지 경우에 색깔은 부식질에 포함된 일련
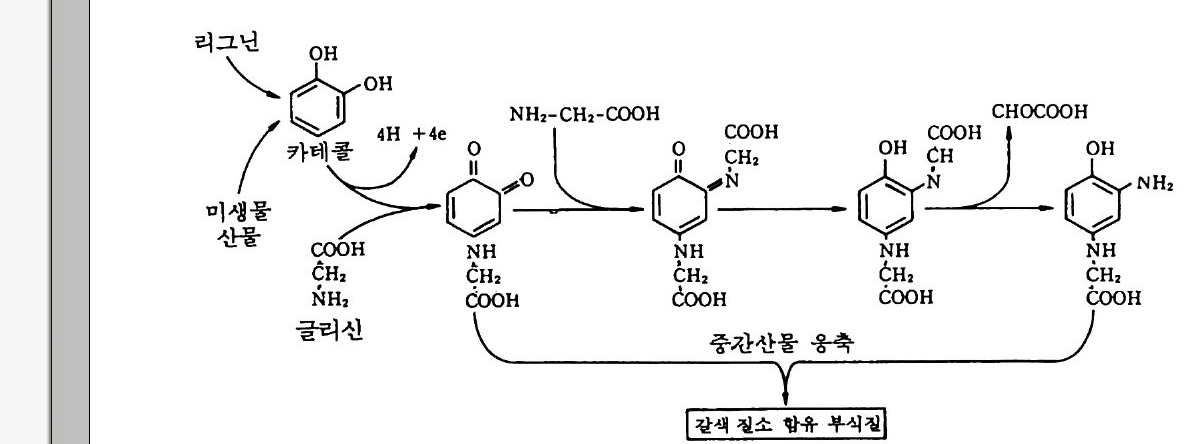 .....땅... : \묘 H
.....땅... : \묘 H
그림 6. II 하나의 페놀(카테콜)과 하나의 아미노 화합물(글리신)의 반응을 보여 주는 부식질 형성에 관한 풀리페놀 기작
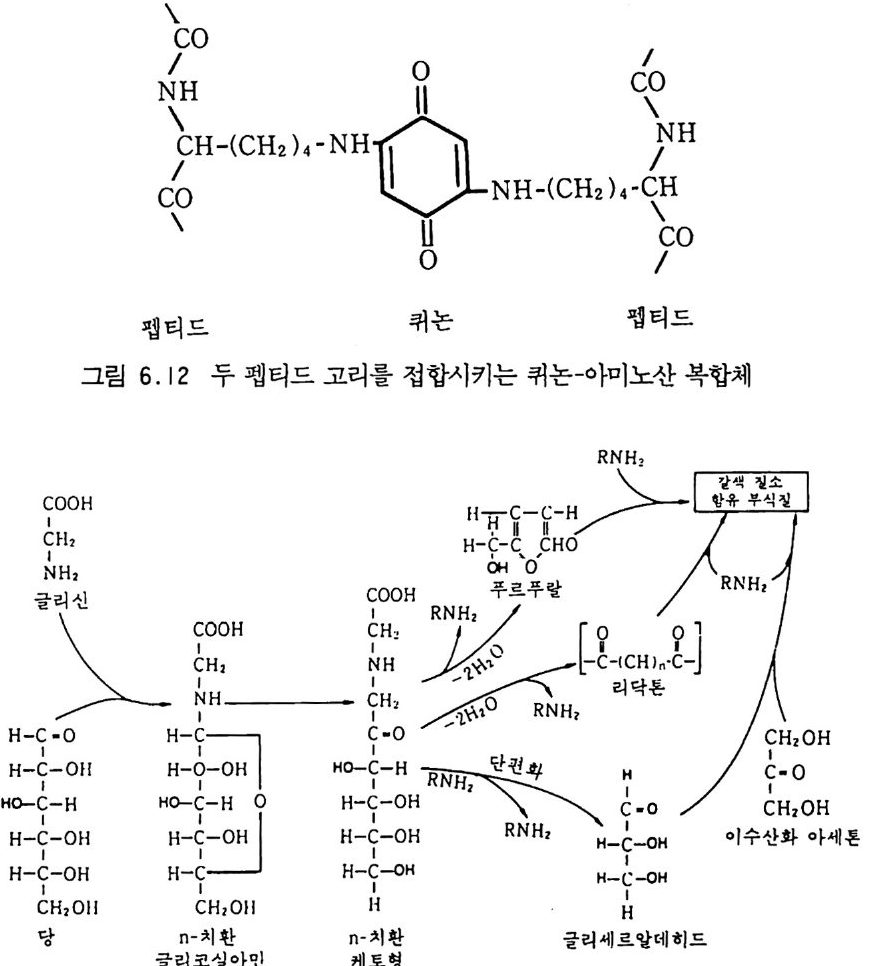 J\;H -(CH, ),-N H0 i -NH-(CH , J• -C/\0
J\;H -(CH, ),-N H0 i -NH-(CH , J• -C/\0
그림 6.13 부식질 형성에 관한 하나의 일반화된 기작으~ 아미노산인 글리신과 당 사이의 갈색화 반응을 보여 준다• 다른 아미노 화합물들과 환원한 당류들이 관련될 수 있다. 의 이중결합에 의해서 나타난다. 더 자세한 내용은 Ste v enson(l982 a), Flai g 등 0975), Aiken 등 (19 函)의 저서에서 설명되고 있다.
6-5 토양 유기물의 구성 토양 유기물의 탄소는 주로 미생물에서 유래된 10 내지 20% 의 탄 수화물, 20% 아미노당류와 아미노산 같은 질소를 함유하는 구성물, 10 내지 20% 의 지방족 지방산들, 알케인 등과 나머지 방향족 탄소들 로 구성되어 있다. 핵자기공명과 열분해 가스 크로마토그래피―질량 분석기를 이용한 연구는 많은 토양의 부식질에서 방향족의 함량이 이전의 화학분해연구에서 측정한값인 50% 보다낮은것을보여 준다. 토양 유기물은 연구하기 전에 전통적으로 점토와 시스퀴옥사이드 sesqu io x id e~ 무기 콜로이드 기질들과 분리해야 하고 액싱에서 분산 시킨다. 고전 분리기법은 NaOH 또는 Na4P207 에 의한 분산을 포함 한다. N 감의 풀림작용, 피로인산염 pyr o p hos p ha t e 의 킬레이트 반응, 높은 알칼리성에 의한 수소결합 파괴 반응에 의해서 분산될 수 없는 것은 휴민이다. 분산되는 물질 중에서 산성 pH 값에서 침전되는 것 은 부식산이다• 산성 pH 값에서 침전되지 않고 용액에 그대로 남아 있는 물질을 풀브산이라 한다 (Schn it zer 와 Khan(1987)). 6-5-1 풀브산 NaOH 에 의해서 추출되고 pH 2 에서 여전히 가용성인 물질은 분 자량이 작은 (10 00-30,000) 풀브산들이다. 풀브산은 많은 곁가지롤 가 지고 매우 산화된 일련의 방향족 고리들로 이루어져 있다. 구성 단위들은 벤젠 카르복시산, 페놀산 들이다. 부식산들을 그림 6.14 에 서 보여 주는 바와 갇이 수소결합이나 반데르발스 힘, 이온결합으로 주로 연결되어 있다. 풀브산들에 대한 X 선 분석, 전자현미경, 점성 측정은 풀브산이 비교적 느슨하고 유동성 있는 구조임을 보여 준다.
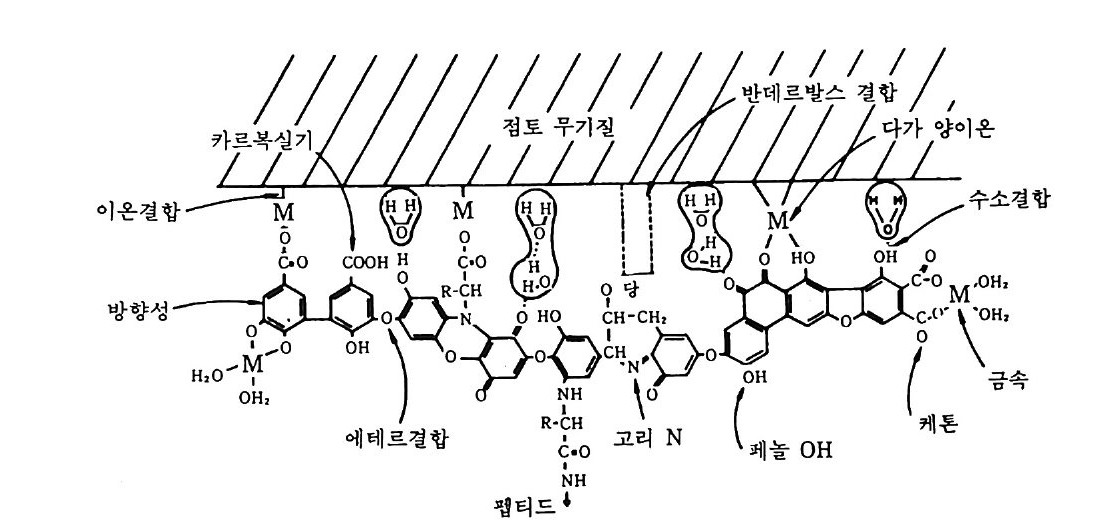 반데I 르발I 스I 결합I /<
반데I 르발I 스I 결합I /<
그림 6.14 토양에서 접토유냐뷰질 복합체의 도식적인 구조 (S t evenso (1 982a)). 이는 여러 가지 크기의 빈 자리가 나 있어서, 그 자리에 맞는 유기 무 기 화합물의 전하가 상호보완적이면 포착하여 고정한다. 스포드솔 B 훈]서처럼 토양 상충의 용탈로 생긴 토양 하층의 풀브 산들은 아주 적은 양의 질소를 포함한다. 그러나 몰리솔 mollis o ls91 풀브산들은 높은 농도의 질소를 함유한다. 이 부분은 또한 분자량이 작은 지방산 및 미생물의 세포질 구성물들뿐만 아니라 아주 많은 양의 다당류 물질들을 포함한다. 그들의 일반적인 원소 및 기능에 대한 분 석 결과는 표 6.3 에 있다. 이들 화합물은 낮은 농도에서는 선형의 유 동적인 콜로이드이며 높은 용액 농도와 낮은 p H 값들에서는 구형의 콜로이드이다. 자연에서 그들의 실제 모양은 서로 연관되어 있는 물질 들과 토양 무기 구성분들에 의해서 결정된다. 6-5-2 부식산과 휴먼 토양으로부터 붉은 알칼리에 의해서 추출되지만 pH 2 에서 침전될 수 있는 유기물들을 부식산이라 부른다• 이들은 방향족 고리, 고리 모
양으로 배열되어 있는 질소와 펩티드 고리에 있는 질소를 포함하는 분 자량이 조금 큰 (10,000-100,000) 물질들이다. 그들의 일반적인 구성 은 표 6.4 에 있다. 셀룰로오스와 단백질의 경우처럼 효소에 의하여 생성되기보디는, 비슷하지만 동일하지 않은 구성 물질의 다중응축 p ol y condensa ti on 에 의해서 생성되기 때문에 어떤 부식산 분자들도 정 확히 같지 않을 것이다. 실제적인 구조들 또한 밝혀지지 않고 있다. 토양유기물 중 많은 부분이 그립 6 . 14 에서 보여 주는 구조처럼 자연에 서 방향족이 아니라는 증거가 “C-NMR 분광기에 의해서 늘어나고 있다 (A i ken 등 (1985)). 이것은 에데르 결합들, 고리 모양의 질소, 수 소결합들에 의해서 함께 붙어 있는 다중방향성과 다중방향성이 아닌 구성 단위들을 보여 준다. 순수한 부식산은 탄수화물 잔여물을 거의 포함하지 않는다. 표 6.4 는 부식산이 57% 탄소롤 포함하고 4% 의 질소가 있을 수 있음울 나타낸다. 작용기는 주로 COOH, 페놀 OH, 알코올 OH 기들과 적은 양의 케톤 산소이다. 부식질들은 Ca2+, Fe3+ (그림 6.14 에서는 M 으로 표시되었다)와 같은 다가의 양이온들에 의해서 배위 (배위자 치환) 또는 pH 8 이하에서 철 표 6.4 부식산과 풀브산의 원소와 작용기 분석 원소 분석(%) 시료 C H N s 。 xI 풀브산 49.5 4.5 0.8 0.8 44.9 2.4 부식산 56.4 5.5 4.1 1.1 32.9 0.9 작용기 의 분석 (meq g-1 ) OCH3 COOH 페놀 OH 총산도 풀브산 0.5 9.1 3.3 12.4 부식산 1.0 4.5 2.1 6.6
과 알루미늄 산화물들에 존재하는 양으로 하전된 부위들에서 음이온 교환을 통하여 수화산화물들과 연관되어 점토에 부착된다. 휴먼은 토양 유기물 중에서 NaOH 에 의해서 분산되지 않는 부분을· 포함한다 . 분리과정에서 대부분의 토양은 비교적 같은 양의 풀브산, 부식산, 휴민으로 나누어진다. NaOH 로 추출되지 않은 물질에서 점토' 를 제거하고 더 분별하면 휴민이 분해되지 않은 셀룰로오스, 리그닌성 물질, 미생물 세포벽과 약간의 목탄 성분과 같은 비용해성 식물 및 미 생물의 구성 물질과 함께 풀브산 및 부식산으로 이루어져 있음을 알 수 있다. 6-5-3 토양 유기물의 양과 분포 토양 유기물은 토양의 구조에 중요 역할을 하며 따라서 수분 침투, 뿌리 발달, 침식 저항에 큰 영향력을 가진다. 그것은 또한 질소, 황, 인과 같은 주요 영양소, 그리고 여러 가지 미량원소들의 저장 창고이 다. 그것은 토양에 색깔을 주고 양이온 흡수 능력을 제공한다. 그러므 로 경작지 및 비경작지 토양의 생산성을 조절하는 가장 큰 하나의 구 성 요쇼:.7} 바로 토양 단면에 존재하는 유기물의 양과 분포 깊이라는 것은 놀라운 일이 아니다. 토양 유기물의 양은 일차 생산성과 분해 속도의 균형에 의하여 변한 다. 미사와 점토의 존재는 일반적으로 특별한 환경 상호작용들을 고려 하면 토양 유기물은 증가하며, 어떤 화산 토양에 있는 것과 같은 무기 영류들의 존재도 더욱 큰 토양 유기물의 보유력을 촉진한다. l m 깊이까지 헥타르당 700 Mg 탄소에 달하는 가장 큰 축적은 생 산성이 높고, 02 의 부족으로 분해가 억제되는 늪과 습원에서 나타난 다(표 6.5 ) . 습기와 건기가 있는 초원은 특히 Ca2+ 에 의해서 안정화
표 6.5 식물 생물량과 토양 유기 탄소의 범세계적인 분포 생태계 (ha면 x적 1 08) (Mg 순C 생ha산-1성 yr- 1) (식M물g C생 h물a-량 1) 토(M양g 유 C기 h탄a-1소) 열대림 25 19 19 100 온대림* 24 12 12 135 관목립과 사바나 23 8 2 50 온대 초지 9 6 0. 7 190 툰드라 8 1 0.3 220 사막 관목지대 18 1 0.01 60 암석지대 및 사막 24 0.03 0.5 1 경작지 14 6 7 1 소택지 및 습원 2 30 700 140 ·활엽수립 및 북부립 (boreal fore st) 된다면 식물 일차 생산성이 6 M g C ha-1 y r-1 로 되는 바와 같이 탄 소 유입량이 북부와 온대 삼림 평균 12 Mg C ha-1 y r-1 의 반밖 에 되지 않지만 오히려 토양의 유기 탄소 수준은 더 높이 유지한다. 연간 평균 순생산성 19 Mg C hr-1 y r-1 를 가지는 열대 삼림은 12 Mg C hr-1 yr -1 의 생산성을 가지는 온대 삼림보다 더 적은 유기 탄소를 유지한다. 탄소/질소 비가 가장 혼하게 15 내지 20 의 범위인 온대 삼 립보다 오히려 경작지 토양의 비율과 비슷한 탄소/질소 비 10 인 열대 삼림 유기물은 토양 전체 단면에 걸쳐서 더욱 깊이 분포된다. 습도와 온도의 상호작용들이 토양 유기물의 축적을 조절하는 것으로 알려져 있다. 습한 상태에서 광합성을 통한 탄소 축적 속도는 분해에 의한 반대 과정보다 더 크다. 세계의 주요 수분과 온도 상호작용 지역 울 대표하는 3600 종류의 배수 양호한 단면 l m 깊이까지 토양에서 채취한 토양의 유기물에 대한 요약 (Z i nke 등(1 984) )에 의하면 모든 온
대지역 중에서 다습한 우림에서 가장 높은 탄소 축적이 나타난다(표 6.6). 홍미롭게도 질소 함량은 탄소 자료와 일치하지 않는다. 건조한 지역에서 질소의 죽적, 즉 낮은 탄소/질소 비가 나타난다. 습한 지역에 서 탄소/질소 비가 커지는 이유는 잘 알려져 있지 않다. 질소 손실이 이들 지역에서 더 높은 것도 가능한 일이다. 디습한 조건에서 질소고 정이 낮을 가능성도 또한 존재한다. 표 6 . 6 여 러 습도와 온도 상호작용 아래 토양의 탄소와 질소의 함량* 온도 습도 상호작용 지대 (Mg m탄 C-소1 )h a-1 (Mg m질 C-소1 )h a 기 탄소/질소 북부 건조 관목대 102 6.3 16 북부습립 150 9.8 15 북부우림 320 15 22 냉온 사막 관목대 99 7.8 13 냉온초지 133 10.3 13 냉온습림 120 6.3 19 냉온우림 200 8.3 25 온난 사막 관목대 60 3.0 20 온난 습립 (mois t for est) 93 6.5 14 온난 습립 (wet for est) 270 18 14 온난우림 270 7.0 38 열대 사막 관목대 10 0.5 20 열대 건립 100 8.9 11 연대 습립 145 6.6 22 열대 우림 180 6.0 30 ·자료 : Zin k e 등 (1984)
참고문헌 Ai ke n, G. R., McKnig h t, D., Wershaw, R., and McCart hy , P. (1985) . Humi c Substa n ces in Soil , Sedim ent and Wate r . W i le y, New York. Brock, T. D., S mi th, D. W., and Madig a n, M. T. (19 84) . Bio l ogy of Mi cr o- orga nis ms. Prenti ce -Hall, Eng le wood Cli ffs, New Jer sey . Flaig , W ., B eute l spa cher, H., and Rie t z , E. (1975) . Chemi ca l comp o sit ion and ph y si c a l pro p e rt ies of humi c substa n ces, In Soil Comp o 꼬 en ts (]. E. Gi es ekin g , ed.) . Vol. l._ pp. 1-211 . Sp ri n g e r Verlag , Berlin and NewYor~. Haid e r, K., and Mart in, J. P . ( 19 75) . Decomp o sit ion of spe cif ica lly carbon -14 labelled benzoic and cinn ami c aci d deriv a ti ve s in soil , Soil Sc i. Soc. Am. Proc. 39, 657-662. Ly nc h. J. M. (19 83) . Soil Bi ot e c hnology , Mi cr obia l Facto r s in Crop Produc- tion . Blackwell. Oxfo r d. Schnit ze r, M., and Khan, S. U., e ds. (19 78) . Soil Orga nic Matt er . Elsevie r , Amste r dam. Sowden, F. J., Chen. Y., a nd Schnit ze r, M. (19 77) . The nit ro g e n dis t r i b u ti on in soil s for med under wi de ly dif fer in g clim ati c condit ion s,'' Geochim . Cosmochim . Acta 41, 1524-1526. Ste v enson, F. J. (1982a) . Humus Chemi stry : Genesis , Comp os it ion , Reac- tion s. Wi ley . New York. Ste v enson, E. J.(1 982 b). In Ni trog e n in Ag ricu lt ur al Soil s (F. J. St e- venson, ed.) . Ag r onomy , vol. 22.Am. So c.Ag ron .,Madis o n,W isc onsin _. Tate , R. L., lII (1987) . Soil Orga nic Matt er . Bi ol og ica l and Ecolog ica l Ef /ecto r s. W iley (lnte r scie n ce) , New York. Zin k e, P. J., Sta n enberge r, A. G., Post, W. M., Emanuel, W . R., and Olson J. S. (1984) . Worldwi de Orga nic Soil Carbon and Ni trog e n Data . Pul., l. 2217. Envir o n. Sc i. Div., Oak Rid g e Natl . Lab., Oak Rid g e . Temes- see.
추가로 읽을 거리 Bolin , B., D eg e ns, E. T., K emp e , S., and Ketn e r, P. eds. ( 19 79) . The Global Carbon Cy c le. Wi ley , New York. Cehn, Y., and Avnim elech, Y. (19 86) . The Role of Orga nic Matt er in Modern Ag ricu lt ur e. Mart inu s Ni jho ff Puhl., The Hagu e . Ghosh, K., a nd Schnit ze r, M. (19 80) . Macromolecular str u ctu r es of hu rnic substa n ces, Soil Sci . 129, 266-276. Hatc h er, P. G., Schnit ze r, M., Dennis , L. W., and Maci el , G. E. ( 19 82) . Aromati ci t y of humi c substa n ces in soil s, Soil Sci. Soc. A m. ]. 45, 1089-1093. Lehnin g e r, A. L. (19 82) . Pr inc i ple s of Bio c hemi stry. Wort h Publi sh ers. New York. Sanchez, P., Gic h uru, M. P., a nd Katz , L. B. (19 82) . Orga nic matt er in majo r soil s of the tro p ica l and tem p e rate reg ion s, Proc. Int. Soc. Soil Sci . Cong ., 12th , 1982, Vol. I, pp. 99-114. Sowden, F. J., Chen, Y., a nd Schnit ze r, M. (19 77) . The nit rog e n dis t r ibu ti on in soil s for med under wi de ly differ in g clim ati c condit ion s, .. Geochim . Cosmochim . Acta 41, 1524-1526. Zie k us,E Jc.o Gl. . (5 1, 9 8221)1 .- 24L3ig . n in meta b olis m and the carbon cyc le, Adv. Mi cr ob.
제 7 장 유기 잔여물의 분해와 토양 유기물 대사회전의 역동성 7-1 미생물 전환 과정의 반응 속도론 식물 잔여물, 미생물 몸체, 토양 유기물의 분해 속도에 대한 지식은 자연에서 탄소, 질소, 황, 인과 같은 유기물의 이용도와 순환을 이해 하는 데 먼저 필요한 것이다. 토양 유기물 분해와 영양소 순환에 관련 된 미생물의 분해 과정에 대한 중요성의 인식은 추적자를 이용한 또는 추적지를 사용하지 않은 자료의 수학적인 분석을 이용하여 아주 잘 이 루어질 수 있다. 효소들이 식물 잔여물의 분해를 중재한다. 복잡한 과 정들이 연관되어 있다 할지라도 전체 분해 속도는 단순한 반응 속도 방정식으로 기술될 수 있다. 분해에 대한 반응속도는 기질 구성요소 (예롤 들면 식물 잔여물)들이 사라지는 양을 계속적으로 추적함으로써 측정할 수 있다. 분해의 반응 속도론적 분석은 측정시간 간격이 짧아 야 한다. 토양에서 기질 분해에 대한 많은 연구들이 측정 간격을 충분 히 짧게 하지 않고 있으며, 그리하여 본래 기질에 대한 분해라기보다 미생물 생산물 또는 유기물 형성에 의한 산물에 대한 분해값을 측정하
고있다• 분해 속도(반응 속도)는 분해되고 있는 하나 또는 그 이상의 기질 농도에 대한 힘수로서 표현될 수 있다. 이것을 반응차수라고 하는데 반웅 속도를 기술할 때 사용되는 지수값이다. 7-1-1 영차 반응 영차 반웅들은 기질의 변환 속도가 기질 농도가 아닌 촉매의 양과 같은 다른 요소에 의해서 결정되기 때문에 기질의 농도 변화에 영향을 받지 않는 경우의 반응둘이다. 만약 기질 A 가 X 로 전환된다면, A 의 변화속도는
 뿜 =-k
뿜 =-k
이다. 적분하면 방정식은 A t =A 。― k t 로 된다. 여기서 A t는 일정 시간이 지난 다음에 남아 있는 기질의 양 (농도)이며, Ao 는 그 계에서 최초의 기질 양(농도), k 는 반응속도 상 수(농도/시간), t는 반응이 시작한 이래 경과된 시간을 나타낸다. 반응 속도론을 기술하는 편리한 용어는 반감기이다. 이는 최초의 기 질 중 50% 가 변환되는 데 걸리는 시간이다. 예를 들면, A t =A 。 /2 가 되는 데 걸리는 시간을 반감기 t1 12 이라고 하면 t Il2=A 。 /2 k 이다. 평균 잔류 시간 mean resid e nce tim e .g. 최초의 양과 같은 양의 물질 이 변화되는 데 걸리는 시간, 이를테면 A t =O( 이 부분은 원서에서 수학 적으로 맞지 않으므로- 바꾸었음 : 옮긴이)될 때의 시간이다.
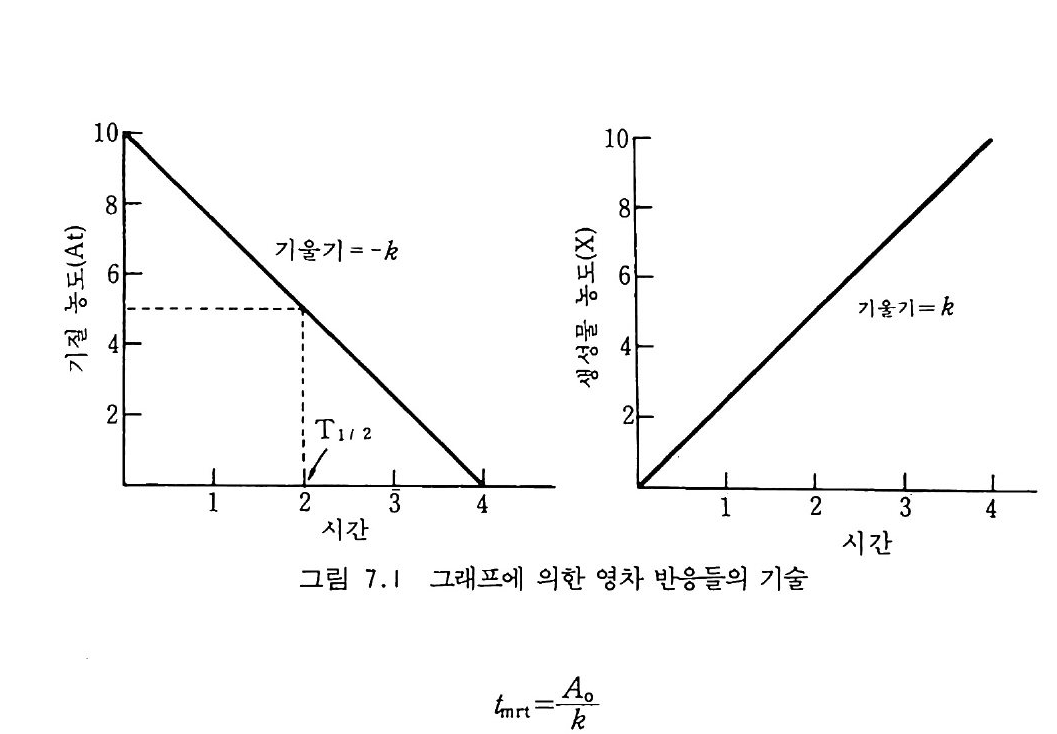 10 1 0864
10 1 0864
기질의 수준이 제한되어 있지 않는 높은 기질 농도에서 효소 반응들 은 보통 영차 반응이다. 예를 들면 높은 NH.+ 농도에서 질산화 반응 과 높은 N03-농 도에서 탈질화 반응둘은 영차 반응이 된다. 그림 7.1 은 영차 반응들의 그래프를 보여 준다. 7-1-2 일차반응 일차 반응에서는 기질의 변환 속도가 기질의 농도에 비례한다. 다음 반응을고려해보자. A— -+X 시간에 따른 반응물질 A 의 변화 속도는
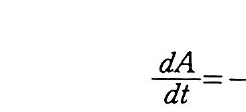 뿔 =_kA
뿔 =_kA
이다. 시간 t와 함께 농도 변화의 감소는 반응속도 상-4- k 와 반응물 A 의 농도를 곱한 것에 종속된다. 적분을 하면 디음 방정식이 얻어전 다.
![]() A t =A 。 e-k t
A t =A 。 e-k t
여기서 A t는 어떤 시간 t에서 남아 있는 기질의 농도다. 반응속도 삼뚜 k 의 단위는 시간의 역수로 죽 단위시간당 어떤 값으로 표현된다 (예를 들면 hr 기, day -1 , yr- 1) . 이 방정식은 실험 결과에 대한 반응 속도를 그래프로 쉽게 결정할 수 있도록 다시 정리할 수 있다. 양변을 A 루 나누고 자연대수를 취함으로써 다음 식이 얻어진다.
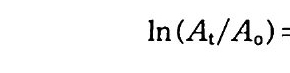 ln(A1/A 。) =_kt
ln(A1/A 。) =_kt
따라서 시간에 대해서 ln(A/A 。)의 값을 그래프로 표시하면 기울 기 ― k 의 직선이 된다. 방정식은 lo g lO 으로 그릴 수도 있는데 이는 기울기를 _k/2.303 으로- 되게 한다. 그림 7.2 는 일차 반응함수의 전형적인 그래프들을 나타낸다. 전체 반응시간을 통하여 기울기가 일 정하므로 속도상수 k( 시간의 역수)는 기질이나 생성물의 농도의는- 독 립적이다(또는 농도에 따라 변하지 않는다). 최초 기질 양의 반 (A 톤 A 。 /2) 이 변환하는 데 걸리는 시간을 계산하기 위해서 우리는 다음과 같이 할수있다.
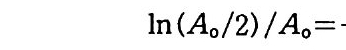 ln (A 。 /2) /A 。= —k t1 ,2
ln (A 。 /2) /A 。= —k t1 ,2
결과적으로 !1,2= 0 . 693/k 이다. 일차 반응에 대한 평균 잔류 시간(대사회전 시간)은 1/k 로 정의된다
(일차 반응에서는 편의상 분해하여 기질 양이 Aoe-1 이 납을 때 , 죽 최초 기 질 양의 36.8% 가 되는 데 걸리는 시간이다. 참고문헌 : Olson, J. S . 1963. Energy sto rag e and the balance of pr oducers and decomp o sers in ecolog ica l sys t e m s, Ecology 44 : 322-331, DeAng e li s, D. S., P. J. Mulholland, J. W. Elwood, A.V . Palumbo, and A. D. Ste i n m an. 1990. Bio g e ochemi cal cyc l in g constr a in t s on str e am ecosys t e m recovery , .. Envir o n. Manag e . 1 4 : 685-697 : 옮긴이 ) 그림 7.2 는 시간 t에 대한 ln( Ai /A 。)의 그래프가 반웅이 일차이면 직선으로 될 것을 나타낸다. 복잡한 기질들의 분해 곡선은 보통 여러 개로 나타난다. 이것은 짚이 속도상수가 다른 여러 구성 요소들로 이 루어져 있음을 나타낸다. 이들은 곡선을 나누는 기법으로 그래프에 의 해서 분석될 수 있다. 이는 전체 분해곡선으로부터 리그닌같이 가장 안정된 구성 요소의 분해에 대한 자료들을 제의히는 느 과정을 포함한다.
 선형축 1log ,o 축 10 86In 축
선형축 1log ,o 축 10 86In 축
이 새로운 자료들의 그래프는 보통 셀룰로오스 같은 하나의 구성 요~ 에 대한 k 를 나타내는 직선을 만들 것이다. 이것은 빨리 분해되는 단 백질에 대한 분해 속도상수를 얻기 위해서 반복할 수 있다. 이 기법은 미생물 성장과 같은 새로운 산물 형성에 대한 값둘이 원래의 분해곡선 에서 제외된 다음에만 적용될 수 있다. 그러한 계산의 보기가 그림 7.6 에 나타난다. 지금은 컴퓨터 분석에 의해 위에서 설명한 그래프 방법보다 여러 구성 부분으로 이루어전 곡선을 더욱 쉽게 풀 수 있다. 7-1-3 쌍곡선 반응 자연에서 발견되는 많은 반응들은 시간에 대한 생성물 (X) 의 그래 프가 어떤 최대값에 접근하는 곡선을 나타내는 속도상수들을 가지고 있다. 이것은 쌍곡선 방정식에 의해서 가장 잘 기술된다. 효소화학에 서 쌍곡선 방정식은 M ic hae li s-Men t en 식으로 알려져 있다. 미생물 생장을 묘사하기 위해서 동일한 일반힘수를 사용할 때는 Monod 식이 라고 부른다. 물리화학에서는 가끔 부착현싱을 기술하기 위해서 어떤 점근선에 접근하는 곡선의 식을 Lan g mu i r 식이라고 한다. 다음 보기 는 쌍곡선 함수를 사용하는 효소 반응속도론에 대한 통상적인 논의에 기초를두고 있다.
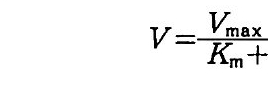 v= Kvmmax+ AA
v= Kvmmax+ AA
여기서 V 는 반응 속도(농도/시간), A 는 기질의 농도(농도), Vmax 는 최대 반응 속도(농도/시간), Km 는 M ic hael i s 상수 또는 반포화 상 수(농도). 이 방정식에 대한그래프모양은그립 7.3 에 있다. 여기서 Vmax는 최대 반응 속도이다. Km 은 V=l/2 Vm 일 때 기질 농도로서 친화력 상수 또는 반포화 상수이다.
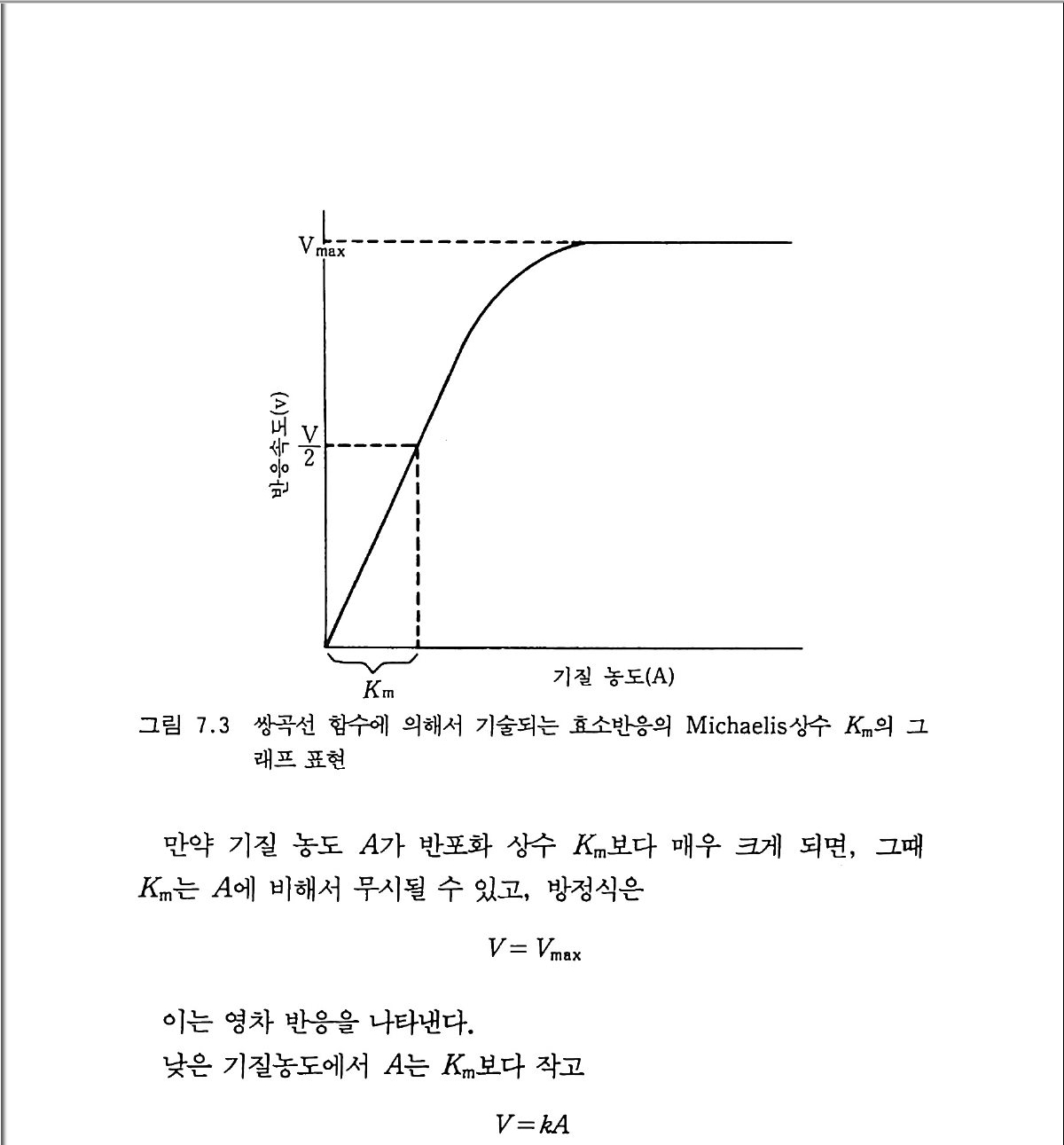 v 뇨-------------
v 뇨-------------
이것은 일차 반응을 나타내며, 여기서 k= Vmax/Km= 상수이다. 일차 반응 곡선은 그래프에서 직선으로 되면 그에 맞는 반응 싱수들 울 가장 쉽게 구할 수 있다. 마찬가지로 쌍곡선 함수를 직선형으로 그 려질 수 있도록 변형하면 분석하기가 매우 용이하다. 쌍곡선 방정식을
가장 잘 알려진 이중역수 그래프 Line weaver-Burk. .£ 변형하여 통 상의 그래프 용지에 그리면 그림 7.4 에 나타난 바와 같은 직선이 된 다. 그러나 컴퓨터의 사용은 직선형의 그래프 방정식으로 변환하지 않 고 쌍곡선 함수의 분석을 더욱 간단하게, 그리고 더욱 의미 있게 한 다. 그리하여 Vmax 또는 Km 에 대하여 가장 의미 있는 값들을 얻기 위해서 많은 그래프 또는 수학적인 분석 방법들을 사용하는 것이 가능 하다. 쌍곡선 방정식 사용의 큰 응용력은 전체 점근선 곡선이 두 개의 값 Vmax 와 Km 에 의하여 기술될 수 있다는 사실에서 유래된다.
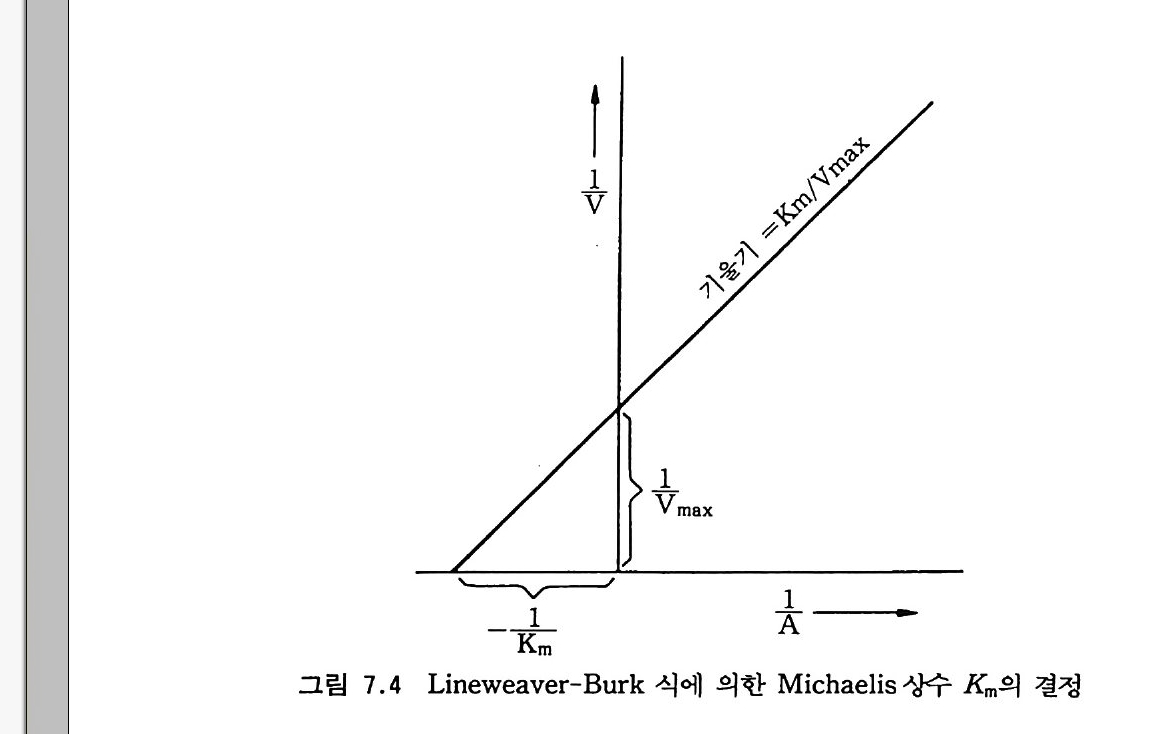 l1V
l1V
7-2 분해의 역동성 식물 잔여물아나 토양 유기물 분해의 역동성을 모형화하는 것은 관 련된 생물학적, 화학적, 물리적 과정에 대한 의미 있는 수학적인 표현 울 필요로 한다. 식물 잔여물의 분해는 일차 반응 속도론에 의해서 꽤 잘 기술되는 것이 실험적으로 밝혀지고 있다. 이것은 식물 잔여물의 분해 속도가 식물 잔여물의 양에 선형적으로 비례하지만 특수한 상수 底 잔여물의 양과 관계가 없다는 것을 의미한다. 전체 반응의 영향 울 기술하는 데 흔히 사용하는 용어인 분해 속도와 분해가 진행되고 있는 식물 잔여물 형태의 특칭인 속도 상수 쩌분 구별하는 것이 중요 하다. 토양 유기물의 분해를 기술하기 위해서 일차 반응 속도론울 사 용하는 것은 토양의 미생물 접종량이 분해 속도를 제한하지 않고 있다 는 것을 의미한다. 종종 높은 토양 미생물의 생물량이 분해에 대한 연 구 기간에 비해서 삐론 생장 속도를 가지기 때문에 이것은 대부분 사 실 0] 다. 이산화탄소 생산량이나 토양에 남은 탄소량을 측정함으로써 분해 속 도를 측정할 때는 실제 분해의 일부분만 설명된다. 미생물들은 새로운 세포 안팎의 물질을 형성하는 생합성을 위해서, 그리고 에너지 공급원 으로서 탄소 화합물들을 사용한다. 후자의 과정에서는 탄소 화합물이 주로 CO2, 미생물 세포, 노폐물로 전환된다. 형기성 상태에서 노폐 물의 수준은 일반적으로 높지 않다. 그러므로 생합성량 또는 미생물 세포 생산량을 CO2 자료로부터 계산할 수 있다. 이것은 미생물 생물 량으로 기질이 전환되는 산출량이나 효율에 대한 지식을 필요로 한다. C= C, (1+ Y (lOO -Y ) ) 여기서 C 는 분해된 기질, c1 는 발생된 CO2 , Y 는 생합성을
표 7. I 실험실 조건에서 토양에 첨가된 유가 화합물 분해에 대한 일차 반 응상수(미생물 생합성에 대한 보정이 있거나 없는 경우) 일차 반응 상수` k(day -1) 보정률(%) 물질 시간(일) 비보정 20 60 짚-귀리 14 0.02 0.03 0.11 헤미셀룰로오스 14 0.03 0.04 0. 11 리그닌 365 0. 00 3 0.006 포도당 I 4. 0 천연 벼과 식물 30 0.006 0.008 0.02 곰팡이 세포질 10 0.04 0.05 0.17 곰팡이 세포벽 10 0.02 0.03 0. 07 위한 탄소의 사용 효율인데 이는 미생물 물질의 생산을 위해서 활용된 전체 탄소의 비율로써 표현된다. 식물 잔여물과 같이 분해되지 않고 토양에 남아 있는 기질 부분의 양을 측정하는 것은 어렵다. 원래 화합물이 화학적으로 결정될 수 있 울 때조차도 분해의 참값을 측정하는 것은 당류의 경우에서처럼 그 특수한 화합물의 미생물적인 생산때문에 방해된다. 분해 속도 상수 K 가 생합성에 대해서 수정될 때 수정되지 않은 것들과는 크게 다르 다(표 7.1). 일반적으로 40% 내지 60% 의 생장 효율은 탄수화물의 분해에 대해서 현실적인 것으로 간주된다. 왁스와 방향족 물질들 갇 은 다른 화합물들은 아주 다른 생장 효율을 나타낸다• 장기간의 자료 들이 이용되는 경우에는, 본래의 기질과 조기의 왕성한 활동으로 생 생산된 미생물 세포들에서 co 가 발생되기 때문에 분해와 미생 물 생장 효율의 참값을 계산하는 것은 가능하지 않다. 연구 자료 들은 공략받는 기질의 일부에 미생물적 생합성을 고려하지 않고 분해 속도를 평가할 때 심각한 찰못을 범하게 된다는 것을 보여 준다.
7-3 식물과 토양 자료의 모형화 야의와 실험실에서 실험들에 의하면 식물체의 분해를 기술하는 분해 속도 상수 妹즌 탄소 첨가가 토양 건중량의 1. 5% 를 초과하지 않는다 면, 거의 항상 첨가된 양에는 무관하다. 더 이상 첨가되면 토양의 특 성을 변화시키고 분해를 느리게 한다. 분해 속도는 식물 탄소, 질소, 리그닌, 탄수화물 구성물에 따라 달 라지는 것으로 밝혀져 있다. 그러한 관계를 표현하는 하나의 방법 중 하나가 Herman 등(1 977) 이 처음으로 사용한 것이다. 거기서 보면 발생 량= (% 탄수화물) 당 잔유물의 C/N X %리그닌 충분한 배양 기간 후에 여러 가지 기후조건에서 다양한 토양에 보유 되는 여러 식물질의 부분은 매우 비슷하고 종종 본래 양의 20% 에 접 근한다. 이것은 초기의 분해 속도가 크게 다르다 하더라도 미생물 생 산과 토양 유기물 안정화에 나타나는 유사성 때문이다. 삼림 낙엽 및 낙지의 연구들 또한 본래 있던 대략 20% 의 탄소가 분해의 초기 기간 이 끝난 다음에 남는 것으로 밝혀지고 있다. 이것은 약간의 잘 분해되 지 않는 리그닌을 포함하나 주로 미생물 생산물들과 토양 부식질 구성 물질들로 이루어져 있다. 장기간의 토양 유기물의 대사회전을 기술하는 유용한 모의 모형이 J enk i nson 과 Ra y ner(1977) 에 의해 제시되었다. 거기서 사용한 자료 는 영국의 로삼스테드에 있는 장기 연구장에서 얻어졌다. 그곳에서는 130 년 동안 밀이 재배되었다• 자료는 첫째, l4C 로 표지를 한 식물질 울 사용한 배양실험(이는 1-10 년이 넘는 자료를 제공한다), 둘째, 토양 유기물의 방사능 단소에 의한 날짜 추정, 이는 오래된 (100 년에서 3000
년의 범위를 가진다) 유기물 부분들의 명확한 연대를 제공한다, 셋째, 열핵분열을 통해서 생성되고 1950- 19 70 년 동안 대기를 통하여 분포 된 방사능 탄소의 영향 (이는 5-20 년 동안 그 토양에 있는 물질들에 대 한 정보를 제공한다), 넷째, 제 3 장에서 기술된 바와 같은 토양미생물 생물량 측정을 위한 클로로포름 (CHC J 3) 훈증 배양방법 (chlorofo r m fum i ga ti on inc ubati on meth o d, CFIM) 으로 얻은 자료, 다섯째 , 식물 유입 수준들에 대한 지식, 여섯째, 실험장에서 장기적으로- 측정된 토 양 유기물의 수준들이었다. 5 가지 토양 탄소 부분이 고려되었다. ® 쉽게 분해할 수 있는 식물질, k=4 ye ar-\ ® 잘 분해되지 않는 식 물질, k=0. 03 ye ar- 1, @ 미생물 생체, k=0.41 ye ar-1, ® 물리 적으로 안정된 유기물, k=0.014 y ear 가 ® 화학적으로 안정된 토 양 유기물, k=0. 00 03 y ea r- 1 로 나누었다. 앞에서 보여 준 바와 같 이 k 값 4 y ea r- 1 는 반감기 0 . 17 년을 나타내는 반면에 안정된 토양 유기물은 반감기가 2000 년이 된다. 이 구성 요소 각각의 분해 속도는 일차 반응에 따르는 것으로 가정되었다. 또한 분해 동안 5 가지 구성 요소 각각은 비슷한 비율로 CO2, 미생물 생체, 물리적으로 안정된 토 양 유기물, 화학적으로 안정된 물질로 변하는 것으로 가정되었다. 모형과 시험장의 장기적인 실험 결과를 비교해 보면 모형이 경작지 토양에 있는 유기물의 대사회전에 대해서 쓸모 있는 표현 수단임을 제 시했다. Jen kin s on-Ray n er 모형으로부터 얻은 출력은 비료가 뿌려 지지 않고 적은 수확량의 밀을 생산하는 시험장에서 매년 미생물 생물 량을 통하여 면적 헥타르당 34 kg ha-1 y ea r- 1 의 질소가 흐르며 , 미 생물 대사회전 시간은 2.5 년인 것을 보여 주었다(표 7.2). Jen kin s on-Ray n er 모형의 사용은 매우 홍미 있는 비교를 가능하게 한다(3f.. 7.2). 밀 재배와 휴경을 교대하고 있는 캐나다의 몰리솔에는
표 7.2 여러 다른 생태계에서 탄소와 질소의 대사회전 •••• 측정 변수 ••• 영국 로삼스데드 캐나다 브라질 토양 무게 (Mg ha-1) 2200 2700 2400 유기 탄소 (M g ha 기 26 65 26 탄소 유입량 (M g- ha-1) 1.2 1.6 13 토양 탄소의 대 사회 전 시 간 (ye ars) 22 40 2.0 미생물 탄소 (k g ha 기 570 1600 460 미생물 질소 (k g ha-1) 95 300 84 미생물 대사회전 시간 (ye ars) 2.5 6.8 0.24 미생물을 통한 질소 이동 34 53 350 (kg ha-1 ye ar -1) 수확에 의한 질소 제거 24 40 220 (kg ha-1 ye ar-1) ·자료 : Paul and Voroney (1984) “서부 캐나다 밀 경작-비경작, 영국 로삼스테드 비료를 뿌리지 않고 연속 밀 경 작, 브라질 사탕수수 토양-식물계 ...M g = meg a g ram =metr i c ton ne 높은 유기 탄소와 질소의 저장력이 있으나 영국의 로삼스테드의 토양 과 비슷한 식물 잔여물이 유입되었다. CFIM으 로 측정한 미생물 질소 는 300 kg N ha-1. 로 나타났다. 6.8 년의 미생물 대사회전 시간은 높 은 토양 유기물 수준을 가진 토양들에서 아주 큰 비활동성 미생물 개 체군들의 안정화 가능성을 보여 준다. 북부 브라질의 사탕수수가 자라고 있는 스포도솔은 계속해서 밀이 경작되고 있는 영국의 로삼스데드 시험장과 비슷한 탄소와 질소 함량 울 가졌다. 그러나 미생물 생체 내의 탄소와 질소는 낮았다. 사탕수수
로부터 높은 탄소의 유입 (13 Mg ha-1) 은 미생물 생물체에 대해서 0.24 년의 계산된 대사회전 시간을 초래했다. 이것은 캐나다의 몰리솔 에 비해서 28 배나 빠르며 생물량이 영양소의 주요한 공급-소멸원으로 보다는 촉매제와 짧은 기간의 저장소로서 더욱 많이 작용하고 있는 상 황을 보여 준다. 브라질에서 미생물 생체에 포함된 질소가 경작물에 의해서 제거되는 질소의 3 분의 1 밖에 되지 않는다 하더라도 이 생물 량을 통한 질소 흐름의 추정치 350k g Nha y r 은 경작지에 의해서 제 거되는 양의 1. 5 배가 된다 . 위의 모형들은 토양 유기물 합성에 식물 생산이 미치는 장기적인 영 향을 기술하기 위해서 개발되었다. 그러나 복잡한 물질들의 분해롤 모 의하기 위해서는 좀 더 역학적인 기작들에 바팅을- 둔 모형이 필요하 다. 7-4 모형의 출력 그립 7.5 와 같은 모형은 경작물의 잔여물과 같은 복잡한 기질의 분 해에 대한 정량적인 측면들에 대한 보다 나은 이해를 가지는 데 도움 이 될 수 있다. 이러한 이해는 또한 원래 기질로부터 이루어지는 미생 물 산물의 생산울 고려할 때 가장 잘 얻어전다. 복합체 기질(짚)이 첫 째, 쉽게 분해될 수 있는 당류들과 아미노산, 둘째, 천천히 분해될 수 있는 셀룰로오스와 헤미셀룰로오스, 셋째, 잘 분해되지 않은 리그닌 의 세부분으로 이루어져 있다고 간주했다. 분해 속도 상수 k 와 미생 물 생장 효율에 대한 지식이 흐름들의 각각을 결정하는 데 필요하며, 표 7 . 3 에서 보여 준다. 이 모형에서 미생물 생체의 분해 속도 상수는
성장에 이바지하는 기질들 이의의 기질들을 요구하는 모든 과정들의 함수이다. 예를 들면 이 과정들은 세포 본래의 모습을 유지하고 영양 소 흡수를 포함한다. 환경 조절 장치로 측정한 것처럼 유지 에너지에 대한 독립된 상수의 개념은 아직 토양 개체군들에 적용될 수 없다. 이 는 토양 개체군들에는 가지각색의 활동 수준들을 가전 여러 하위군들 이 동시에 나타나고 있기 때문이다. 본래 정상상태에 있는 한 토양 개 체군의 유지 에너지 측정은 환경 조절 장치에서 유도된 값보다 매우 낮다. 또한 자연적인 개체군들은 디론 개체군의 사체 유기물을 이용해 자란다. 그러므로 유지율과 사체 이용 성장이라는 개념은 그들을 사망
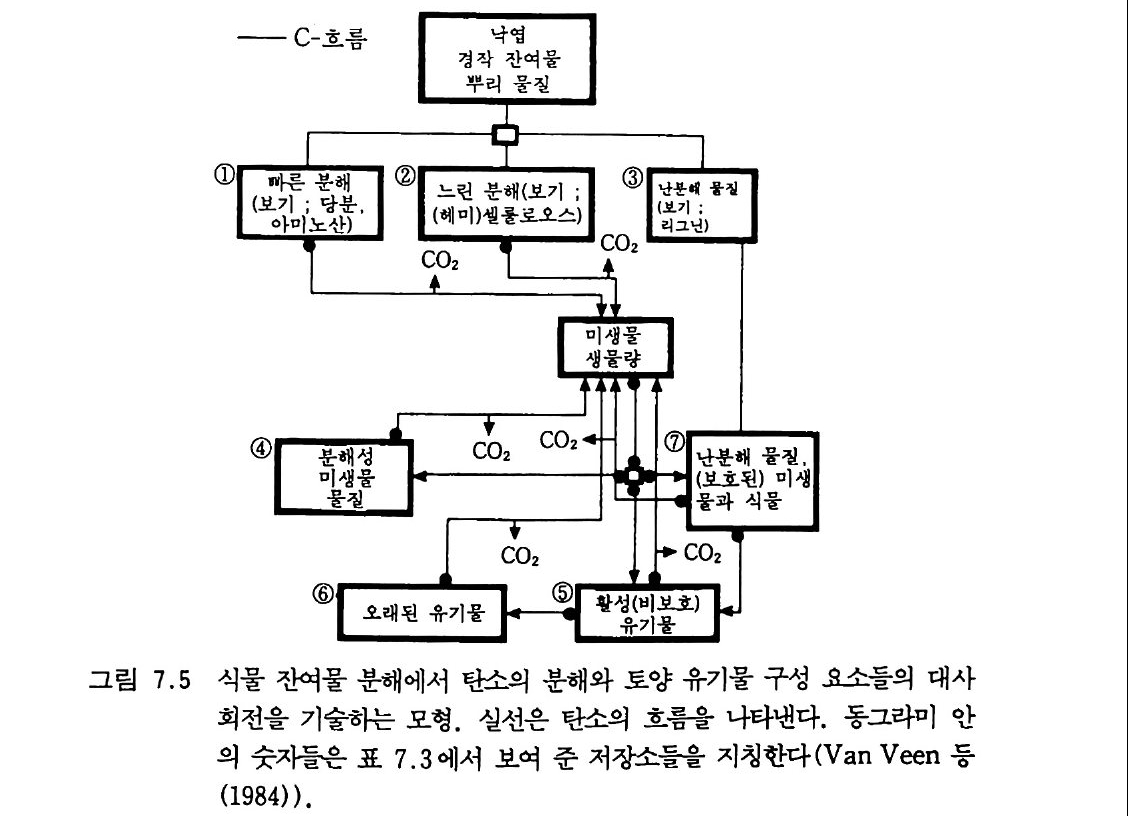 ― c- 흐름 낙영
― c- 흐름 낙영
표 7.3 토양 g당 1000µg 탄소의 분해를 기술하는 탄소 대사회전 모형에 사용된 저장소의 크기와 분해 속도. 미생물 생산 효율 저장소 (잔µg여 g -1 탄 so소il ) 분k해(d속a도 y상기 수 활용(%효) 율 쉽게 분해되는 (1). 150 0. 2 60 느리게 분해되는 (2) 650 0. 08 40 리그닌 (3) 200 0.01 10 분해가능한 미생물 생산물 (4) •• 6 0. 8 40 활성이고 보호된 토양 유기물 (5) 5000 3X 10- ◄ 20 오래된 유기물 (6) 7000 8 X 10-1 20 난분해성 식물 미생물의 생산물 (7) •• 4 0. 3 25 ·괄호 안의 수는 그립 7 . 5 에 있는 갇은 수의 저장소를 가리킨다 . •• 저장소 (4) 와 (7) 의 생물량은 매우 크다. 이들은 초기 속도이다 . 저장소의 크 기는 첨가된 기질로부터 생산된 것을 의미한다 . 률에 묶어서 다룸으로써 가장 쉽게 고려된다. 미생물이 죽으면 미생물 은 쉽게 분해될 수 있는 저장소(세포질)와 더욱 분해가 잘 안 되는 화 합물(세포벽)로서 간주될 수 있다• 일차 반응 속도론에 기초한 모형 출력 (그림 7.6) 은 미생물 생장을 고려하여 수정한 다음 얻게 되는 참값의 분해와 토양에 남아 있는 식 물 탄소만을 사용할 때 측정되는 분해 사이의 큰 차이를 보여 준다. 종종 포도당과 갇은 단순한 기질에 대한 토양 미생물 개체군의 생장을 고려할 때 60% 의 성장률이 나타난다. 표 7.3 에 나타나는 바와 같 이 , 더 복잡한 기질들은 효율이 낮다. 리그닌과 같은 방향족들은 주로 곰팡이와 함께 대사되는 것 같다. 이것은 효소계에 의한 기질의 분해 를 포함하나 에너지 생산울 위해 분해 산물의 홉수는 거의 없다. 곰팡 이는 있다 하더라도 성장을 위해서 거의 에너지를 얻지 않으며 방향족 들의 분해 동안은 거의 탄소를 홉입하지 않는다. 그러므로 방향족의
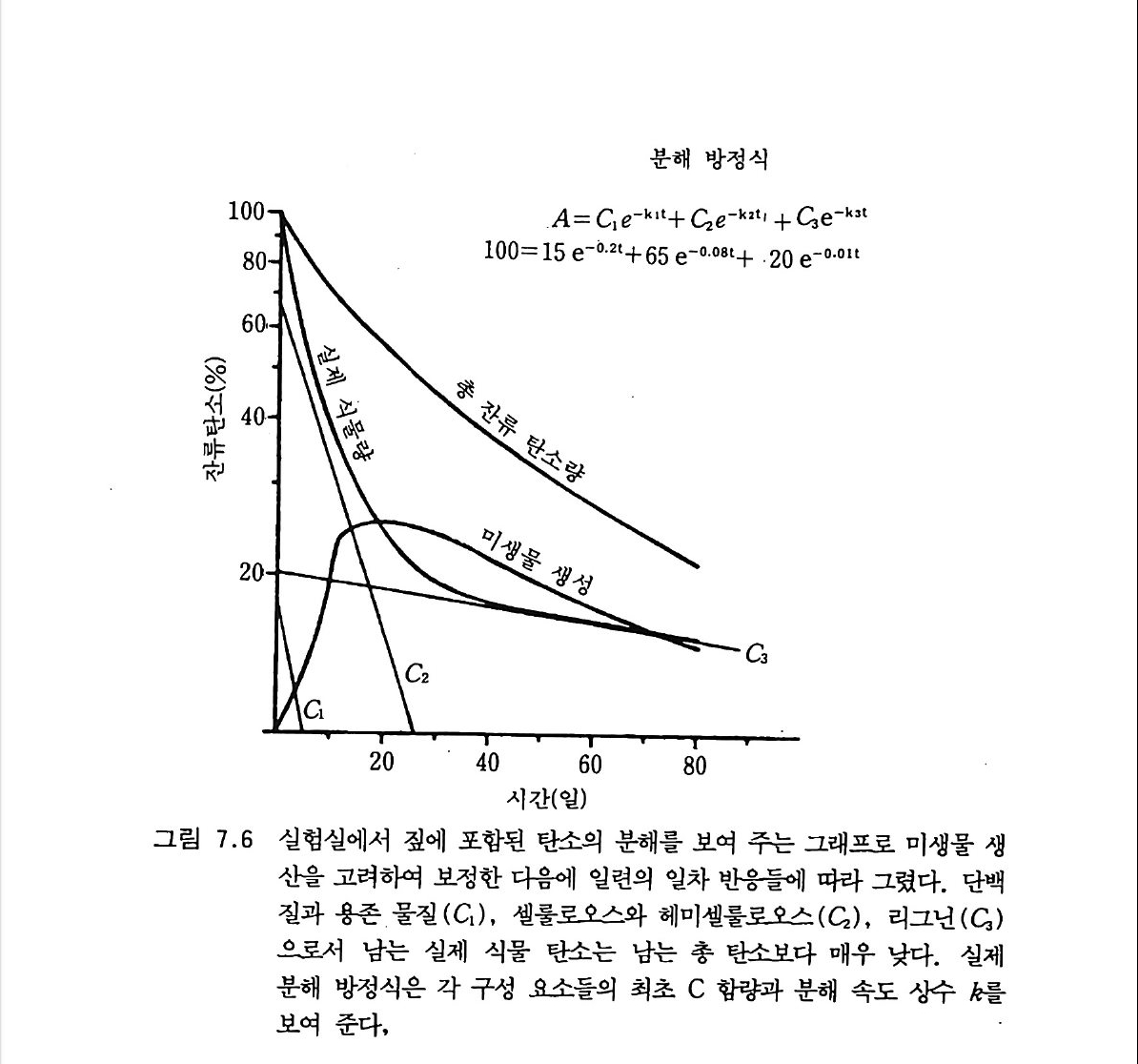 분해 방정식
분해 방정식
분해는 다만 셀룰로오스 같은 다른 이용 가능한 기질이 존재할 때 일 어난다. 그립 7.5 와 표 7 . 3 에서 기술한 모형은 실험실 조건에서 측정된 분 해 속도 상수들에 기초를 두고 그립 7.6 과 같은 출력 곡선을 제공한 다. 야의의 수분과 온도를 고려한 보정은 그립 2.6 과 2.9 에 나타나
표 7.4 토양에 첨가된 식물 잔여물의 분해 속도에 미치는 환경의 영향 잔여물 (dTa11y2 ) (daky -1) 상대속도 밀짚 실험실 9 0.08 1 귀리짚. 나이지리아 17 0.04 0.5 귀리깊 영국 75 0.01 0.125 밀짚 캐나다 사스카툰 160 0.0 0 3 0.05 는 바와 같은 보정인자의 사용을 포함한다. 이 모형이 실험실에서 나 이지리아, 영국, 서부 캐나다에서 진여물의 분해를 적절히 기술하는 것으로 실험적으로 확인되고 있다(표 7.4). 이들 각각에 대한 k 값 0.08, 0.04, 0.01, 0.003 d-1 의 분해 속도들은 수분과 온도의 효과 를 포괄하고 있다. 이것은 추운 겨울과 건조한 여름이 있는 서부 캐나 디에서 평균 분해 속도가 실험실 값의 12 분의 1, 약간의 전조 기간이 있는 열대토양 값 10 분의 1 이 되는 것을 보여 준다. 이들 실험에서 잔여물 분해 속도는 토양의 형태에 따라 민감하게 변 화하지 않았다. 이것은 짚의 형태가 비슷하고 짚의 잔여물들이 미생물 에 대한 그들 자신의 미세 서식처를 형성한 사실에 의해서 설명될 수 있다. 그러나 토양 유기물과 미생물 개체군의 안정화는 토양 형태에 따라 달라전다. 앨로페인 같은 점토의 형태와 토양 미사와 점토의 함 량이 안정화 속도를 조절한다. 수학적인 모형화는 또한 경작지로부터 토양 유기물의 장기적인 변 화, 완전 벌목과 화재 후 임상에 나타나는 영향들을 예측하는 데 가치 를 발휘할 수 있다. 그림 7.7 은 서부 캐나다에서 찰 분해되지 않는 부분에 대한 탄소 연대 추정 자료와 10 년의 야의 실험에서 얻은 식물 잔여물의 분해 속도 측정을 기반한 모형의 출력을 보여 준다. 이 자료 들은 그 다음 장기적인 토양 유기물 분해 모형에서 잔여물 유입수준들
과 관련되었다. 이 모형은 일차 반응의 식물 잔여물 분해 속도, 미생 물 성장과 토양 점토와 미사에 의한 미생물 산물의 안정회를 포함해 넣었다. 이는 여러 가지 경작 방식들과 토양 침식의 장기적인 영향을 예측한다. 이와 같은 자료들은 가장 중요한 세상 자연자원 중 하나인 토양과 관련된 관리전략 결정에 아주 중요할 수 있다. 그들은 또 제 6 장 서론 부분에서 논의한 바와 같이 대기의 CO2 양과 가능·한 기후적 인 변화에 미치는 토양 유기물과 범지구적인 탄소 순환의 상호작용을 추정하는 데 응용될 수 있다.
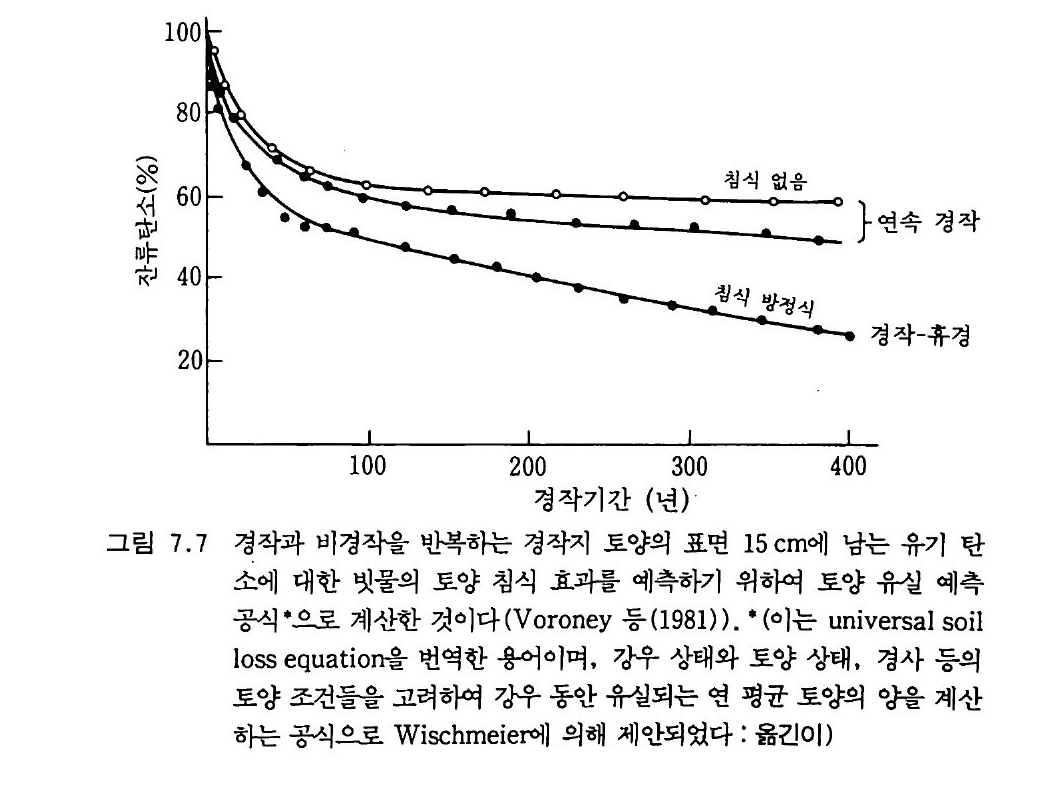 806040
806040
7-5 반응 속도론과 토양미생물 활동을 포함하는 예제 1) 무게를 기준으로 2% 포도당 기질이 분해되기 시작했다. 혼합배 양기에서 2 시간 후 기질의 농도는 1. 6% 였다. 반응이 진행됨에 따라 기질 농도의 변화는 디음과 같았다. 시간 (hr) 남은 기질 농도(%) 。 2.0 2 1.6 4 1.2 6 ? (1) 속도 상수 쩌룹 구하시오. (2) 6 시간 후에 얼마나 많은 기질이 남을까? (3) 최초 기질 수준의 반감기를 구하시오. (4) 평균 잔류 시간을 구하시오. 2) 디움 자료는 변환되는 기질의 양이 기질의 농도에 비례하는 반웅 에서 얻었다. 시간 &에서 최초 기질의 농도는 X=lOOmmol 이고, 반 응 속도 싱수 底근 0 . 3 h r- 1 이다. 10 시간 후 기질 X 의 농도는 얼마일 까? 3) 어떤 반응에서 기질 A 의 최초 농도 Ao 가 50 mmol 이었고 8.5 시간 후에 32 mmol 이 남았다. (1) 이 일차 반응의 속도 상수는 얼마인가 ? (2) 평균 잔류 시간을 구하시오.
4) 최초 농도 60mmol 인 반응이 주어졌고 12 시간 후와 24 시간 후 에 기질의 농도는 각각 40 mmol, 26 . 7 mmol 이 었다. (1) 이 반응의 차수는 일차 또는 영차 반응 중 어느 것일까? (2) k( 반웅 속도 상수)는 무엇인가? (3) 다시 6 시간이 지나면 기질 농도는 어떻게 될까? 5) 미생물에 의해서 매개되는 반웅이 다음의 특징들을 가전다.
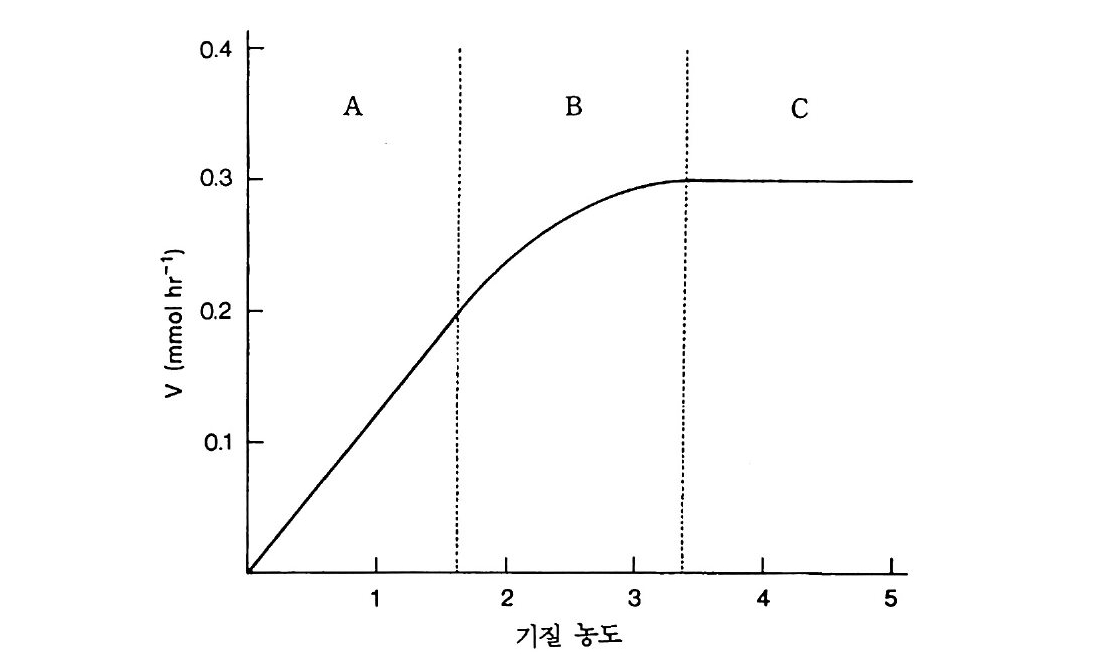 0.4
0.4
(1) 곡선의 어느 부분 (A, B, C, )이 일차 반응을 나타내는가? (2) 곡선의 어느 부분이 영차 반응을 나타내는가? (3) 곡선의 어느 부분이 효소의 기질포화를 나타낼 수 있는가?
참고문헌 Herman, W. A., McGi ll, W. B., and Dormmar, J. F . (1977) . Eff ec ts of ini t ial chemi ca l comp o sit ion on decomp o sit ion of roots of thr ee dif fer ent 항 ass spe cie s , Can. j. Soil Sd. 57, 205-215. Jen kin o sn, D. S., and Ray n er, J. H. (19 77) . The tur nover of soil orga nic matt er in some of the Roth a mste d classic a l exp e rim ents , Soil Sci. 123, 298-305. Paul. E. A., and Van Veen, J. A. (19 78) . The use of tra cers to dete r mi ne the dy n ami c natu r e of orga nic matt er , Trans. Int. Cong r. Soil Sci., 11 th, 1978, Vol. 3, pp. 61-102. Paul, E. A., and Voroney, R. P. (19 84) . Fie l d int e r pr e ta t i on s of mi cr obia l bio m ass and acti vi t y measurements , In Current Pesp e cti ve in Mi - crobia l Ecology . (M. J. Klug and C. A. Reddy , eds.) , pp. 509-514. ASM, Washin g ton D. C. Van Veen, J. A., Ladd, J. N. , a nd Fris s el. M. J. (1984) . Modell ing C & N tur nover thr oug h the mi cro bia l bio m ass in soil , Plant Soil 76, 257 -274. Voroney, R. P., V an Veen, J. A., and Paul, E. A. (19 81) . Org a nic C dy n ami cs in gras sland soil s. 2. Model vali da ti on and sim ulati on of long ter m eff ec ts of culti va ti on and rain f a ll erosio n , Can. ] . Soil Sci. 61, 211-224. 추가로 읽을 거리 Clark, F. E., and Rosswall, T. , e ds. (19 81) . Terrestr ial Ni trog en Cy c les. Ecol. Bull. (Sto c kholm) , Vol. 23. Haid e r, K., and Mart in, J. P. (1975) . Decomp o sit ion of spe c ifica lly carbon -14 labelled benzoic and cinn ami c ac id deriv a te s in soil , Soil Sc i. Soc. Am. Proc. 39, 657-662.
Incorpo rati on of 15N tag g e d mi ne ral nit ro g e n int o sta b le for ms as soil orga nic nit ro g e n, Soil Sci. Soc Am. Proc. 35, 273-275. Marti n, J. P., and Haid e r, K. (19 77) . Decomp os it ion in Soil of Sp ec if ica lly 14 C Labelled PHP and Cornsta l k Ligins , Model Humi c Acid Typ e Polym ers and Conif ery l Alcohols in Soil Orga nic Stu d ie. ~. Vol. 11. IAEA . Vi en na. Pis z kie w i ca , D. (19 77) . Ki ne ti cs of Chemi ca l and Enzym e Cata ly z ed Reac- lio n s. Oxfo r d Univ . Press, London, New York. Sorensen, L. H., and Paul, E. A. (19 71) . Transfo r mati on of carbon int o carbohy d rate s and ami no acid meta b oli tes durin g decomp o sit ion in soil , Soil Bio l . Bio c hem. 3, 173-180. Sowedn, F.]., Chen, Y., and Schnit ze , M. (19 77) . The N dis t r i b u ti on in soil s form ed under wi de ly dif fer in g clim ati c condit ion s, Geochim . Cosmo- chim . Acta 41, 1524-1526. Warembourg, F. R., E, A, (1977) . Seasonal tra nsfe r s of assim i la te d 14C in gras sland : Plant pro ducti on and tur nover, soil and pla nt respi ra - tion , Soil Bi ol . Bio c hem. 9, 295-301. Zie k us, J. G. (1982) . Lig n in meta b oli sm and the carbon cyc l e. Polym e r bio s yn th e sis , bio d eg r adati on and envir o nmenta l recalcit ra nce, Adv. Mi cr ob. Ecol. 5, 211-243.
제 8 장 유기 질소와 무기 질소의 변환과 질산염으로의 변환 8-1 질소 순환 질소는 식물에게 가장 많이 필요한 무기 영양소로 식물체의 구성 성 분 중에서 그 양이 네번째로 많은 원소이다. 식물체에는 탄소, 수소 그리고 산소만이 질소보다 많은 양으로 포함되어 있다. 자연에서 질소 순환은 다른 어떤 원소보다도 더 집중적으로 연구되어 왔다. 질소 원 자는 여러 산화 상태로 존재한다. 질소 원자의 다른 산화 상태로의 변 화는 흔히 토양 생물에 의해 이루어진다. 주요 영양영들 가운데, 질소 는 기체 상태로 존재하는 경향이 가장 크다. 질산염 형태는 물에 잘 녹으며 따라서 용탈되어 물에 의해 운반되기 쉽다. 암모늄 이온 형태 는 휘발될 수도 있지만, 점토와 토양 유기물 (so il orga n ic matt er , SOM) 에 의해 고정되기 쉽다. 산화 상태가 쉽게 변할 수 있다는 것은 생태계로부터 쉽게 유실될 수 있는 무기 형태들의 형성을 초래하게 한 다. 따라서 질소의 결핍은 가끔 식물의 생산성을 제한한다. 또한 기체 상과 용액상의 질소는 환경 오영을 초래하기도 한다.
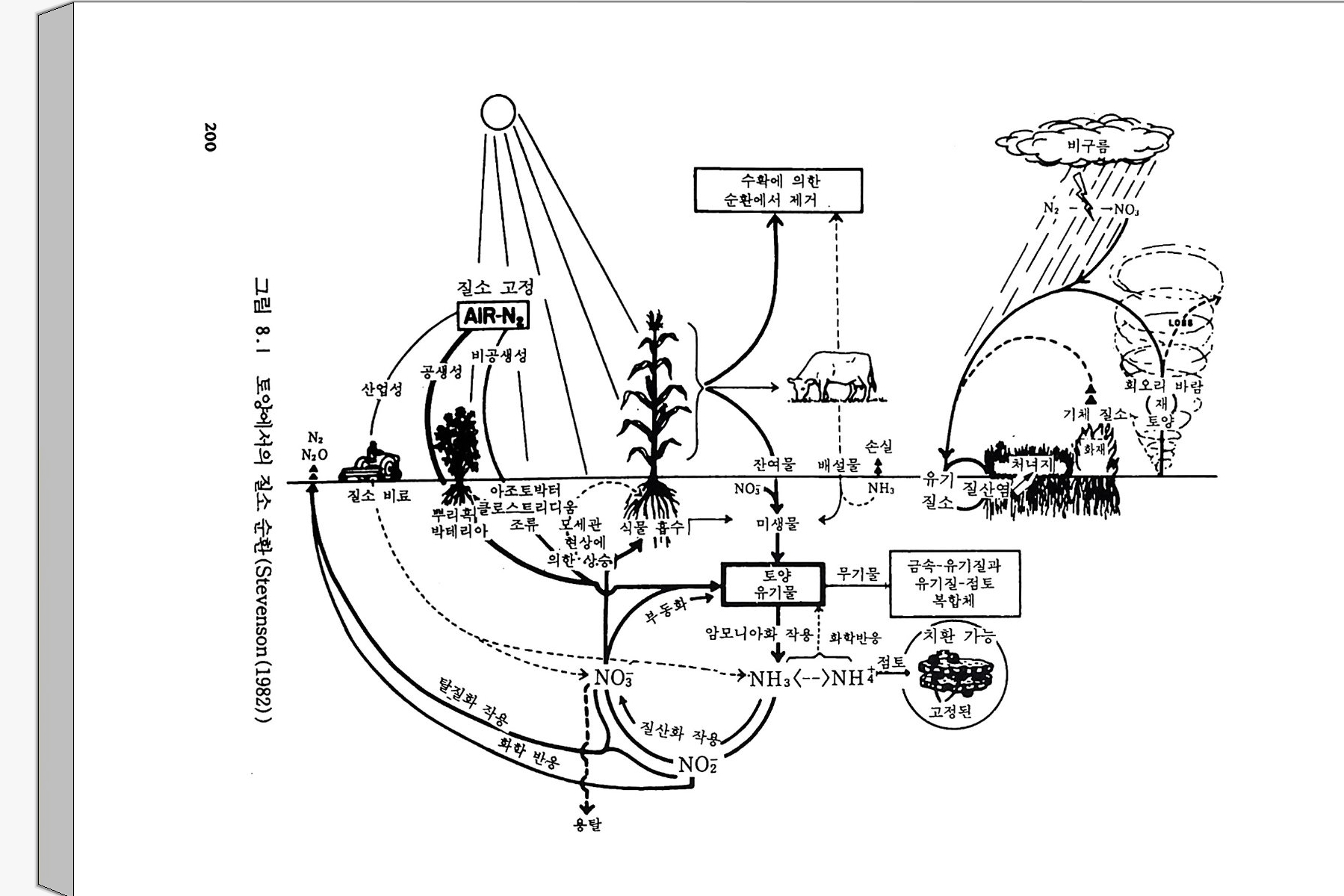 \ - E
\ - E
토양에 있는 질소의 형태들과 미생물이 질소를 한 형태에서 다른 형 태로 바꾸는 역할이 규명된 다음, 질소 순환의 개념이 1913 년 Lohn i s 에 의해 체계화되었다. 그는 N2 를 질소 순환의 중심으로 표현 했고 질소 순환에서 단백질, 아미드 , 암모니아, 아질산염, 질산영의 존재를 파악하였다. 이후 몇십 년이 지나면서 질소 비료의 첨가 효과 (그림 8 . 1) 가 인식된 바와 같이, 용탈, 휘발, 그리고 분해 갇은 과정 의 중요성이 인식되기 시작했다. 1950 년대 이후로 여러 가지 생태계 에 대해서 질소의 흐름과 각 구성 요소들에 포함된 양을 도식으로 표 현하게 되었다. 이 도식들은 매우 복잡한 편이며, 질소 순환의 하위 요소들을 수리적으로 분석하는 것이 흔히 유용하다. 8-2 질소의 무기화 작용 질소의 3 가지 주요 생물학적 형태는 단백질, 미생물의 세포벽 구성 성분(죽 chit in, pe p tido g ly c an) 그리고 핵산 들이다. 단백질은 모든 생물의 기본 성분이다. 단백질 분해효소와 펩티드 분해효~ 의해 분 해과정에서 가수분해되어 펩티드로 된다. 단백질 분해효소는 특정한 아미노산 사이의 펩티드 결합에 대한 공격성 유무에 의해 분류된다. 예를 들면 세린 단백질 분해효소로는 트립신tryp s i n 과 서브틸리신 sub tili s i n 이 있다. 파파인은 식물에서 기원되는 설프히드릴 단백질 분해효소의 한 보기이며, 펩신은 산성 단백질 분해효소이다. 산성 단 백질 분해효소들은 촉매작용에서 금속이온을 포함하며(통상 아연임), 동물과 진균류에서 순수 분리되었다. 그 반웅 기작은 펩티드 결합의 생성과는 반대이다. 천핵 치환반응 동안 질소 그룹이 양성자 (H+) 를 받고, 그 결합의 탄소원자는 OH- 를 받는다.
유기 질소의 무기화 작용은 단백질, 아미노당, 핵산을 분해하여 무 기 상태인 암모니아로 변환하는 것을 말한다. 하나의 아미노산이 에너 지원으로 사용되거나 또는 다른 단백질의 구조물원으로 이용되거나 하 는 것은 일련의 여러 가지 복잡한 되먹임 조절에 달려 있다. 만약에 탄수화물 탄소가 존재하면 아미노산 탄소보다 탄수화물 탄소가 이용될 것이고, 그리하여 아미노산의 골격 탄소가 단백질 합성 이용을 위해 보존될 것이다. 탈아민기 작용 동안에 암모니아의 제거는 글루탐산 탈 수소효소 같은 효소에 의해 가장 많이 일어난다. 이 효소는 환원 당량 의 수용체로서 NAD (nic o ti ne adenin e din u cleoti de ) 조효소를 요구한 다. 암모니아가 토양에 부동화되는지 또는 누적되는지는 미생물의 성장 에 필요한 질소의 요구량에 좌우된다. 미생물의 탄소 대 질소 (C : N) 의 바는 일정치 않다. 전균은 광범위한 C : N 비를 가전다(특히 세포벽 에 셀룰로오스가 있는 조균류가 존재할 경우). 균류의 탄소 함량은 약 45% 로 매우 일정하다. 따라서 3-10% 의 질소 함량을 갖는 진균의 C: N 비는 15: 1 에서 4.5: 1 의 범위에 달한다. 세균은 세포질과 세 포벽의 펩티도글리칸에 질소를 갖고 있다. 세균의 세포 질소 함량은 매우 일정하여, C: N 비가통상 3: 1 에서 5: 1 에 달한다. 단백질이 아닌 질소원으로는 세균과 진균의 세포벽 구성 성분이 포 함된다. 세균의 세포벽 또는 진균의 키틴으로부터 기인된 아미노당은 무기화 과정 동안에 질소의 주요원이다. 키틴의 분해는 키틴 분해효소 에 의하며, 키틴의 구성 성분인 N- 아세틸글루코사민 N-acety l glu cosami ne 단체를 유리해 낸다. 그 글루코사민은 곧이어 인산염 첨 가효소에 의해 분해되며, 이 효소는 6- 인산염 아미노당g lucosam i ne 6-ph osph ate ½ 형성하기 위해 ATP로 부터 인산염기를 이전하는 과정 을 일으킨다. 6- 인산염 아미노당은 탈아미노 작용을 일으켜 NH4+ 를
생성한다. 핵산은 DNA 와 RNA 의 구성 성분으로 에스테르 결합에 의해 인산 염기로 연결된 고리형 질소 화합물이다. 핵산은 토양에서 쉽게 분해되 며, 토양 유기물에서 누적되지 않는, 생물 세포의 몇 가지 구성 성분 의 하나로서 관심을 끈다. 그러나 토양 유기물에는 생물 기원이 알려 져 있지 않은 질소가 전체 질소의 40 %까지 포함된다. 이 토양 유기 물의 질소는 가끔 페놀성 화합물에 부착되며, 생물체에서 발생된 화합 물보다 무기화하기가 한층 더 어렵다. 8-3 부동화 반응 질소의 부동화 과정은 암모니아를 아미노산으로 도입하는 것을 의미 한다. 이는 미생물 성장에 좌우되고, 따라서 이 과정은 탄소 기질 및 무생물적 변수의 이용 가능성에 밀집하게 관련된다. a- 케토글루탐산 에 암모니아를 첨가하여 글루탐산을 형성함은 주요 부동화 반응 중 하 나이다(그림 8.2). 그림에 나타난 반응은 가역적이다. 암모니아를 방 출하거나 또는 흡수하는 동안 글루탐산 탈수소효소에 의해 다른 조효
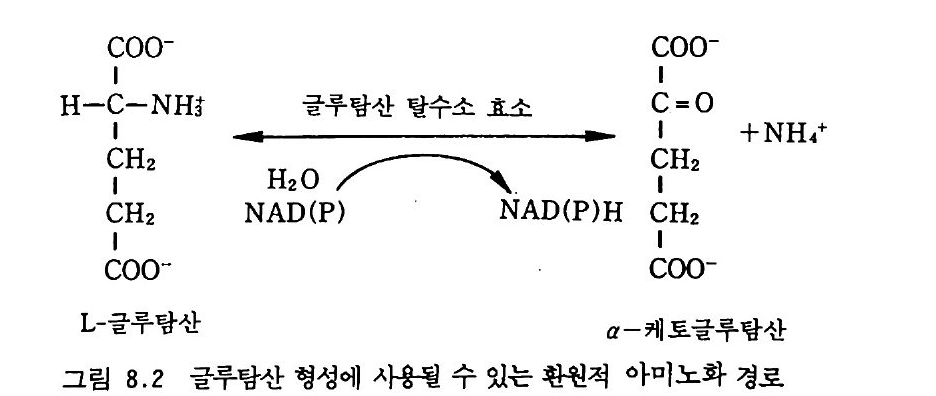 H _c글CCIII_C CHz0H_루Z00 --N담 산田 L N 焉 ~글 루P탐산~ 탈A수D소 (효소P )Ha - 케c뻔C뻔cII o 토o=ooO글 -- 루탐 + N산H .+
H _c글CCIII_C CHz0H_루Z00 --N담 산田 L N 焉 ~글 루P탐산~ 탈A수D소 (효소P )Ha - 케c뻔C뻔cII o 토o=ooO글 -- 루탐 + N산H .+
소 (NAD 또는 NADP) 를 사용함으로써 생물이 무기화_부동화 작용 과 정의 경로를 조절할 수 있다. 앞의 효소는 오직 높은 암모니아 농도에 서만 암모니아를 부동화시킨다. 일반적인 토양에서 나타나는 암모니 아의 농도에서 미생물은 다른 경로를 이용한다. 즉 글루타민 합성효소
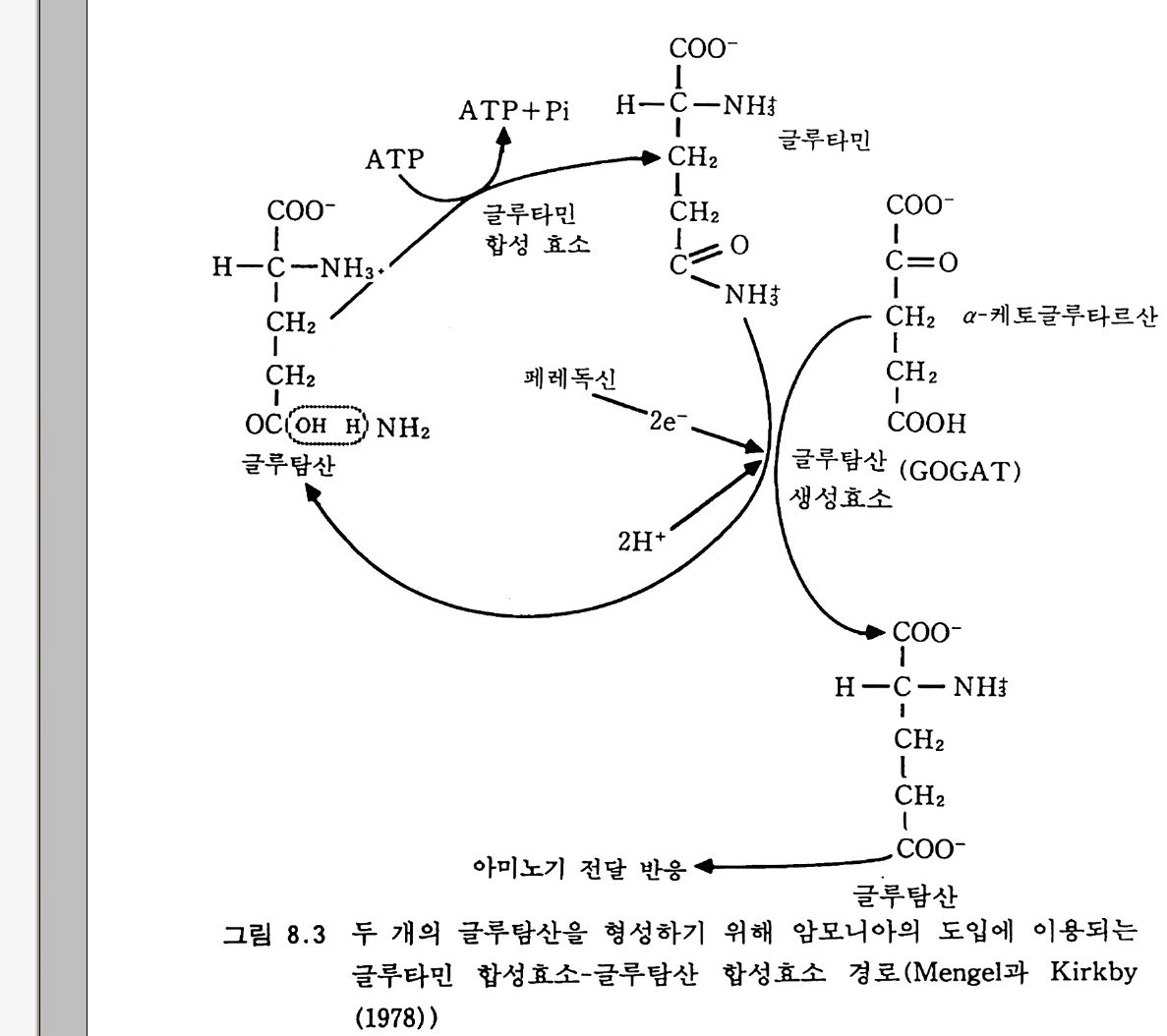 cl0Cl_NClcl0C N
cl0Cl_NClcl0C N
글루탐산 생 성 효소 glu ta m i ne syn th e ta s e-gl u ta m ate syn th a se 경로로 알려져 있는 것으로, 이것은 두 단계로 작용한다. 이러한 순환적 경로 에서는 두 개의 글루탐산이 하나의 글루탐산, 암모니아 그리고 a- 케 토글루타르산으로부터 형성되며, 이러한 대사경로는 아미노산으로 암 모니아가 유입되는 것을 조절하는 데 주요 역할을 한다. 이러한 경로 는 8 개의 다른 억제반응에 의해 누적적인 되먹임 조절을 받게 되며, 이러한 억제반응은 암모니아 유입을 늦추기 위한 부가적 형태로 작용 할수있다. 질소가 세포 내에서 유기 형태로 도입되면, 세포 안의 많은 화합물 울 생성하기 위해 글루탐산에서 케토산으로 암모니아의 전달이 필요하 다. 그림 8.4 는 알라닌이란 아미노산을 만들기 위해 글루탐산에서 피 루브산으로 암모니아기가 이전되는 반응을 보여 준다. 다른 각각의 아 미노산들은 적절한 유기산 전구물질을 요구한다. 우리는 오직 주요 경 로에 대한 예들을 살펴봤다. 특정한 아미노산에 대한 상세한 것은 Lehn i n g er (1 984) 의 저서와 생화학 교재에 나와 있으니 참조하기 바 란다. 토양 생명체는 대개 C: N 비가 5 : 1 에서 8 : 1 의 값을 갖는 것으로 나타났다. 대부분의 미생물 세포는 약 45% 의 탄소를 포함하기 때문
 coo- coo-
coo- coo-
에, 이는 곧 6-9% 의 질소 함량을 의미한다. 위의 C: N 비는 토양의 평균 C: N 비 (10 : 1) 보다 약간 낮아서, 토양 유기물에 비단백질성 성 분이 또한 존재함을 나타낸다· 단순한 기질 죽, 예를 들면, 포도당과 무기 질소를 이용한 미생물의 성장 효율에 대한 지식은 성장에 필요한 질소 요구량을 계산할 수 있 게 한다. 그림 8.5 는 100 g의 포도당이 40% 탄소를 함유하여 40g 의 탄소가 포도당에 포함됨을 보여 준다. 미생물의 생산 계수가 60 % 라면 24 g의 생물량 탄소가 생성되고 총 생물량은 무게 56 g이 된다.
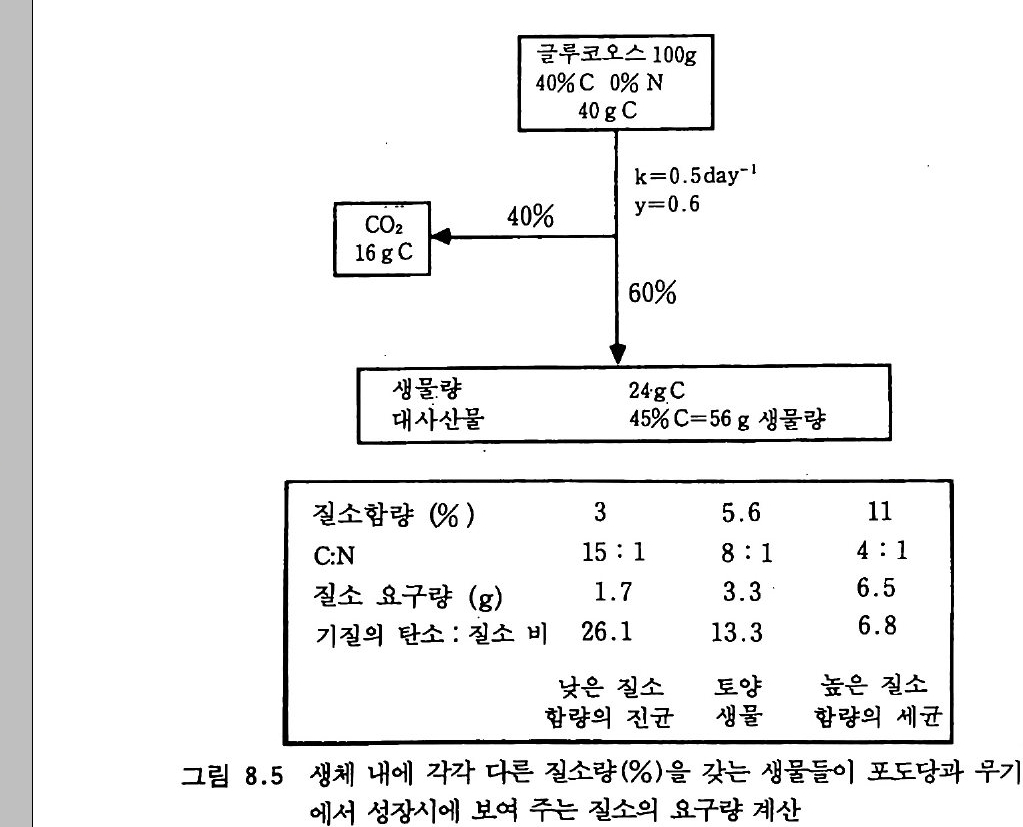 글루코오스 100 g
글루코오스 100 g
진균은 질소 함량이 3% 로서 1. 7 g의 질소를 요구할 것이다. 세균은 질소 함량이 11% 로서 (C: N 비가 4 : 1) 6.4 g의 질소를 체내에 고정 시킨다. 토양에서 흔히 출현하는 혼합 개체군은 중간 정도의 질소량울 요구한다. 여러 가지 분해율을 갖는 복잡한 기질들을 이용한 성장은 제 7 장에 서 본 바와 같이, 그 다양한 조성 화합물들과 토양 유기물의 형성을 추적해야 하기 때문에 컴퓨터 모형이 필요하다• 그림 7.5 에 있는 탄 소에 대해 주어진 모형으로 질소의 흐름을 도입하면 그림 8.6 과 표 8.1 에 있는무기화유냐유화반응모형을이루게 된다. 표 8.1 토양에서 짚의 분해 (lOOOµ g C g -1) 의 탄소-질소 대사회전 모형에 사용된 집소 크기, k 값 및 미생물 생산 효율 집소(p oo l) 잔(µg류 탄g-소1 ) 분(d해ay율 -1 k) 효(%율) (잔µg류 질g-소1 ) C비:N 쉽게 분해될 수 있는 것(1). 150 0.2 60 25 6 서서히 분해될 수 있는 것 (2) 650 0.08 40 12 54 리그닌및 내재된 질소 (3) ** 200 0.01 10·· 3 67 분해(4 ) •가••능 한 미생물의 생산물 6 0.8 40 1 6 완전히 보호된 토양 유기물 (5) 5000 3X 10-• 20 555 9 오래된 유기물 (6) 7000 8X 10-7 20 700 10 분해물의되 기물 질어 (려7)운 미생물과 식 4 0.3 25 0.2 20 NH.++N03--N (8) • 괄호 안의 숫자는 그림 8 . 6 에서 나타난 집소를 가리킨다 . •• 리그닌의 50% 는 분해되기 어렵고, 보호되지 않은 미생물과 식물의 물질 집소로 유입된 다. …생물량의 실질적 집소의 크기는 훨씬 더 크다. 이들 표현된 집소들의 크기는 해당되는 기질로부터 산출됐다• 생물량을 보호하기 위한 토양 보존 능력은 장기간의 현장 모형에 적용될수있다.
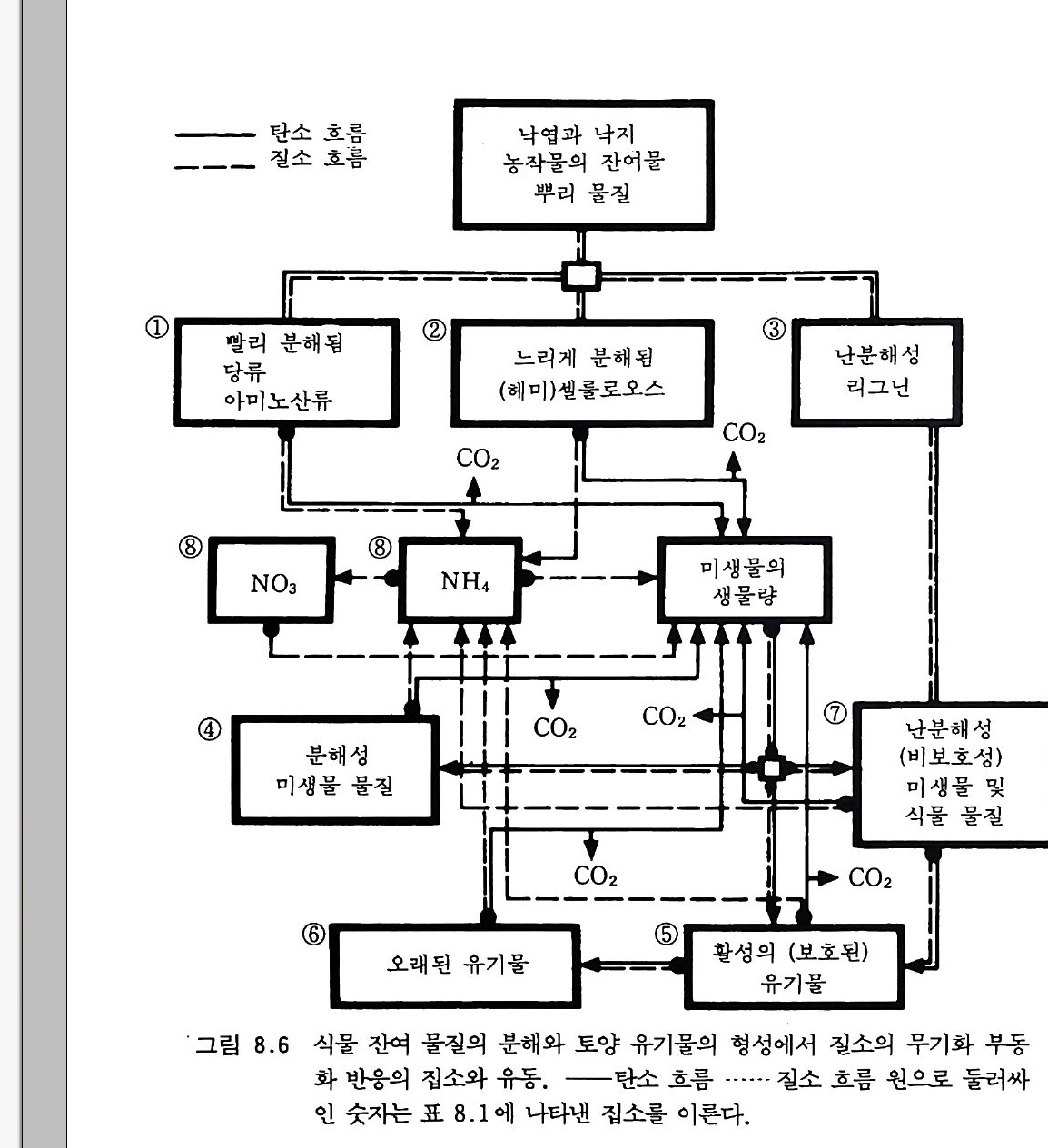 단소흐름 낙영과 낙지
단소흐름 낙영과 낙지
경험적 연구에 의하면 40% 의 탄소와 1. 6% 의 질소 (C:N 비가 25 : 1) 를 갖는 농작물의 잔여물이 분해될 때 통상 순 무기화 작용 또는 순
부동화 작용이 일어나지 않는다는 것이다. 두 과정이 상당한 속도로 일어나더라도, 두 과정의 합은 영이다. 만약에 그 식물의 C: N 비가 25: 1 보다 큰 경우 질소는 무기영 질소원으로부터 흡수가 있거나 또 는 미생물 개체군의 일부가 죽을 때까지 분해가 늦춰질 것이다. 혹은 토양 유기물 (C:N=lO:l) 에 대한 동시적인 분해를 통해 이용할 수 있 는 형태의 질소를 더욱 많이 환경으로 방출시킬 것이다. 이러한 발견 은 1 k g의 질소가 100 k g의 짚에 첨가되어야 한다는 일반적으로 인정 되는 경험적 공식을 설명해 준다. 이 관계식이 성립하는 근거는 짚이 0.6% 의 질소를 갖기 때문이며, 의부 질소의 부동화 작용 없이 짚의 분해에 있어 1. 6% 의 질소가 생물량에 의해 요구되기 때문이다(죽 l k g의 비료 첨가로 충분)• 니무의 잔여물은 리그닌이 많이 포함되어 분 해가 느리고, 미생물의 생물량으로 상당량 전환되지 않는다. 따라서 이 경우 50 : 1 과 같은 높은 C: N 비에서 순 무기화 작용이 나타날 수 있다. 진균은 숲의 잔여물을- 분해하는 주요 분해자로서, 리그린을 분 해하는 능력이 있어서 그 진여물의 질소를 이용할 수 있다. 진균은 균 사를 통해 토양원으로부터 질소를 성장이 빠른 곳으로 운반한다. 따라 서 분해되는 잔여물들은 가끔 현존 질소량의 증가를 보여 준다. 암모니아가 형성된 다음, 가능한 경로가 몇 가지 있다. ® 종종 용액에서 선택적으로 선호되는 질소이며, 식물에 의해서 흡수된 다. 그러나 대부분의 토양에서 암모늄 이온의 양전하는 흡착되며 식물 의 홉수를감소시킨다. ® 마생물 성장에 시용된다. 많은 연구는 암모늄 이온이 이미 환원된 상 태로서 아미노산에 도입될 수 있기 때문에 질산염보다 선호되는 것을 지적한다. 낮은 농도의 암모늄 이온도 종종 질산염 환원에 필요한 효소 를억제한다.
® 암모늄 이온은 이온 교환 복합체에 붙잡혀 있으며, 토양수에서 다른 양이온들에 의해 치환될 수 있다. ® 암모늄 이온은 K 이온과 대략 같은 크기이다. 암모니아는 쉽게 점토 의 총간 부분으로 들어간다. 충간 공간의 붕괴는, 예를 들어 전조에 의 한 붕괴는, 암모니아를 고정시켜서 이온 교환 반응 (KCI 과 같은 용액 으로 추출할 때 일어나는 반응과 같이)에 의해 제거될 수 없다. 토양 의 상부총 lm 에 고정된 암모니아의 양은 표충에서 총 질소량의 5-13 % 가량이며, 토양 하층에서는 총 질소량의 50% 로 증가한다. 토양 의 유기 질소 함량은 경작이나 완전 벌채시에 급격히 떨어지나, 고정 된 암모니아는 통상 더 높은 비율로 유지된다. 그것은 오직 매우 느 리게 이온 교환 반응에 의해 이용될 수 있게 되며, 따라서 미생물과 식물에게도 느리게 이용된다. ® 암모늄 이온은 토양 유기물과 반응하여 퀴논 _NH2 복합체를 형성한 다. 이는 토양 유기물 안정화 관점에서 의미 있는 반응이다. ® 암모니아의 분압은 높다. 만약 부착되어 있지 않은 상태로 존재하면, 죽 노쇠한 또는 부식하는 식물에서, 퇴비에서 혹은 요소 분해효소가 있는 상태에서 요소를 공급한 후에 높은 속도의 암모니아 휘발 현상 이 나타날 수 있다• 야의의 퇴비 표면에선 50% 가량의 질소가 휘발 에 의해 상실될 수 있다. ® 암모늄 이온은 질산화 과정에서 특정한 독립영양 생물들에 의해 에 너지원으로 이용될 수 있다. 8-4 질산화 작용 질산화 작용은 암모늄 이온을 아질산염과 질산염 질소로 변환하는
것이다. 토양에서 일어니는 질산화 작용에 대한 연구는 토양 비옥도의 관점에서 중요하며, 질산염과 탈질화 반응 산물이 환경에 줄 수 있는 잠재적인 악화 요인 때문에 중요하다. 질산염 형성의 현상은 유럽에선 14 세기부터 알려져 있었다• 이때에 초석 (KNO J)이 처음으로 화약가 루와 고기를 절이는 데 사용되었다. 1797 년 나폴레옹 전쟁 때, 프랑 스는 화약 제조에 필요한 수입 초석의 통상금지로 인한 문제를 초석 더미에서부터 질산염을 생산함으로써 해결하였다. 가축 우리에서 가 축의 오줌과 폐수가 토양, 퇴비 그리고 석회와 함께 혼합되어 섞인다. 그 더미는 환풍되며, 초석은 뜨거운 물로 추출된다. 질산염은 토양이 화학적 촉매로서 작용하여 암모니아와 산소를 포함하는 화학반응에 의 해 생성되는 것으로 믿어졌다. 1870 년대에 파스퇴르는 질산염의 생성이 미생물학적이며, 알코올 울 식초로 변환시키는 것과 유사하다고 추측했다. 질산화 작용이 생물 학적이라는 최초의 실험적 증거는 1877 년 Schloes i n g과 M il n t z 에 의해 제공됐다. 그들은 폐수 배출물을 멸균된 모래와 석회석으로 가득 찬 긴 튜브에 담았다. 20 일 후 암모니아가 사라지고 질산염이 존재하 였다. 그 튜브를 가열하거나, 그 튜브에 소독물질의 첨가는 그 변환을 중지시켰다. 또한 정원의 토양을 소량 첨가하여 그 변환 반응이 다시 시작됨을볼수있었다. 1878 년 영국 로삼스테드의 War i n gt o 퍼즌 질산화 작용이 미생물의 두 그룹을 포함하는 두 단계의 과정임을 발견했다. 한 그룹은 암모니 아를 아질산염으로. 산화시키며, 다론 그룹은 아질산염을 질산염으로 산화시킨다. 그러나 그는 그러한 생물을 분리해내지는 못했다. W i no g radsk y는 1890 년에 처음으로 순수배양으로 질산화 세균들을 분리해 냈다.
8-4-1 질산화 세균과 생화학적 반응 W i no g radsk y의 선구적인 연구는 질산화 작용이 어떤 화학적 독립 영양 세균과 전형적으로 연결되어 있음을 확고히 했다. 위의 세균은 엄격한 호기성 세균이며 오직 이산화탄소나 탄산염으로부터 탄소를 취 한다. 그리고 에너지는 암모니아나 또는 아질산염의 산화로부터 얻는 다. 이에 따라서 두 가지의 그룹으로- 구분된다(표 8. 2 ). 대부분의 서 식처에서 두 그룹이 함께 발견되며, 자연에선 아질산염이 거의 누적되 지 않는다. 그림 8.7 에 주요 무기 질소의 변환 경로들에 포함되는 미생물과 조 절들이 나타나 있다. 이 그림은 질산화 작용이 탈질화 작용과 질소 고 표 8.2 화학적 독립영양을 하는 질소 산화 생물의 목록* 속 종 서식지 암모니아를 아질산염으로 산화 Ni tro somonas europ ae a 토양, 물, 오수 Ni tros osp ira bri en sis 토양 Ni tros ococcus nit ro sus 해양 oceanus 해양 mobil is 토양 Ni tro sovib r i o ten uis 토양 아질산영을 질산염으로 산화 Ni trob acte r win o g ra dskyi • • 토양. (agilis ) .. 토양, 물 Ni tros pira gra ci lis 해양 Ni tro coccus mobil is 해양 •Ber g e y의 Manual of Dete r mi na ti ve Bacte r i olg y 제 8 판을 참고 ••Nit rob acte r w i nog rads ky는 적어도 2 개의 혈칭형으로 구성되는데, 그중 하나는 제 8 판 이전에서 N. agi l is로 명시되었다.
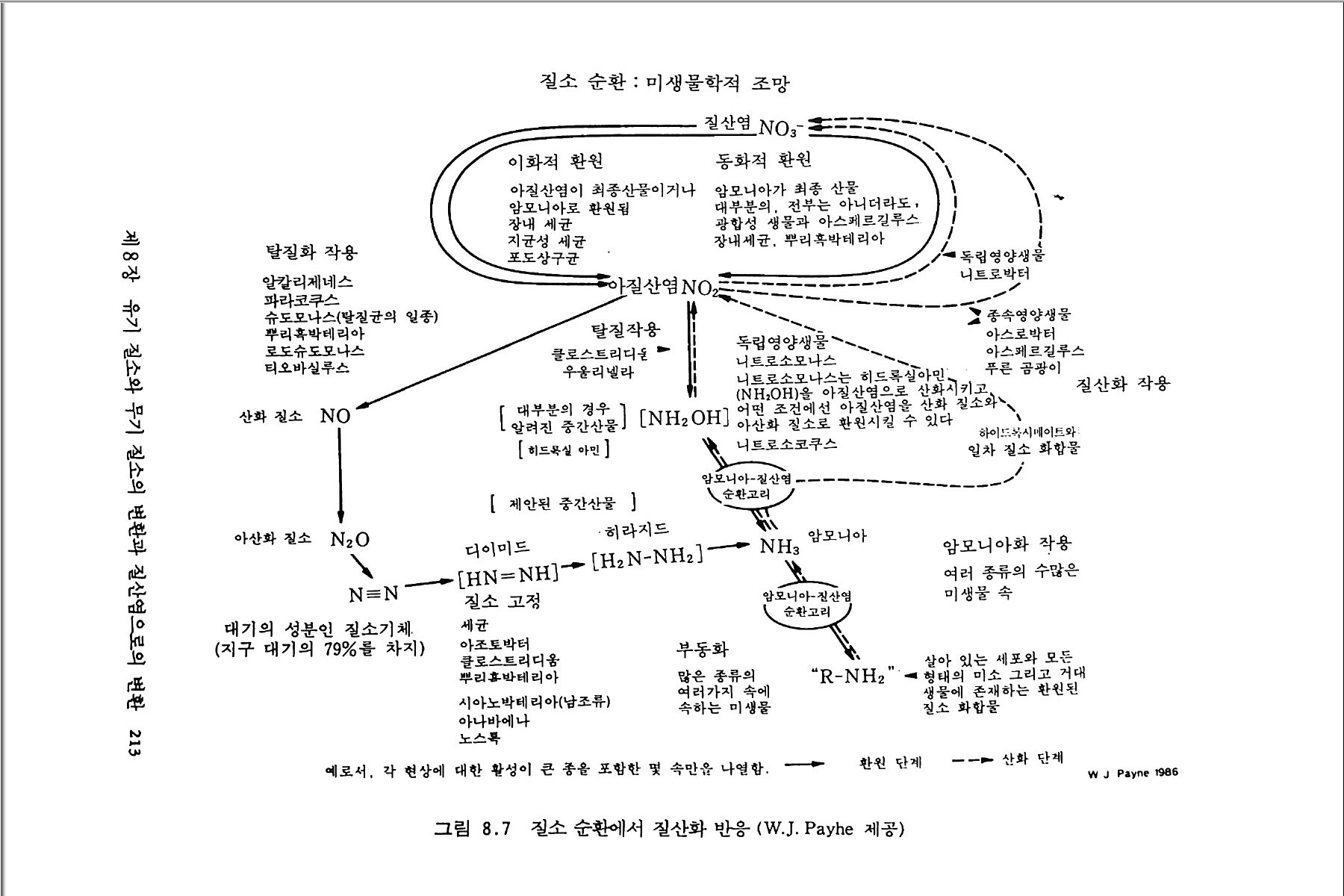 r~ 도 루 -- \ .. ... 麟 - )
r~ 도 루 -- \ .. ... 麟 - )
정뿐만 아니라 동화성 또는 이화성 환원을 포함하는 전체적인 순환의 부분임을 나타내 준다. 이 그림은 또한 종속영양적 질산화 작용의 가 능한 경로도 보여 준다. 이 과정에서 하이드록시메이트 h y drox ym a t es 와 일차 질소 화합물을 거쳐 아질산염과 질산염이 생성되나 자유에너 지는 생기지 않는다. Pa yne 이 요약한 그림은 암모니아를 아질산염으 로 산화시키는 것이 Ni t rosococcus 속과 Ni t rosomonas 속에 의한 것임 울 보여 준다. 이 반응은 히드록실아민 (NH20H) 이란 중간물질을 거 쳐 진행된다 (Pa yn e (1 981)). 히드록실아민으로 암모니아가 산화되는 반응은 홉열반응이다. 다음 단계의 반응 물질은 규명되지 않고 있으나, 니트록실 라디칼 n it rox y l rad i cal 일 것으로 가정되고 있다. 질산염은 이 라디칼과 반응하여 니 트로히드록실아민을 형성하며, 곧 분해되어 두 개의 아질산 분자가 될 것으로- 생각된다. Ni t robac t er 에 의한 아질산염의 질산염으로의 산화 는 또한 산소 분자를 포함한다. 그러나 그 역할은 전자 전달에 국한되 어 있다. 질산염의 산소 원자는 산소 분자로부터가 아니라 물로부터 생성된다. 그 전체적인 반응은 성장에 필요한 에너지롤 생산한다. 그 결대해과서 자 유一 에65너 와지 — 변18화 .는2k c각a각l m o암I-모1니 이다아.와 아질산염의 1 분자의 산화에 8-4-2 질산화 작용에 영향을 주는 요인들 토양 살포 도구가 질산화 작용에 영향을 주는 요인의 연구에 전통적 으로 이용되어 왔다. 그 작동 과정에서 하나의 대사물질이 연속적으로 토양 원주를 통해 스며들게 된다. 반복된 살포는 변환의 반응 속도론 과 환경 변화의 효과를 직접적으로 연구할 수 있게 한다. 다중 채널 펌프에 의해 물과 기질을 공급받을 수 있고, 컴퓨터에 의해 조절되는
시료 채취기와 연결된 토양 원주가 현재 가용하여, 토양의 여러 과정 에 대한 측정이 연속적으로 이루어질 수 있다. 산도 질산염 생산과 산도 사이에 상관성이 유의한 것으로 증명되었다. 최 적 p H 는 6.6 에서 8.0 사이에 나타난다. 전형적으로 경작 토양에서 질산화 작용 속도는 pH 6.0 이하에서 현저하게 감소하게 되며, 4.5 이하에서는 무시할 정도이다. 높은 p H 에서 암모니아는 아질산염이 질산염으로 변환되는 것을 억제한다. 산성 산림 토양은, 불이나 완전 벌채와 같은 교란으로 질소의 부동화 작용보다 더 높은 무기화 작용이 일어날 때, 거의 모두 질산염을 생성한다. 종속영양의 질산화 세균과 또는 미소지역 m ic ros it e 릭 존재는 산림 토양에서의 질산화가 경작 토 양에서만큼 (2 장을 참조) 산성에 예민하지 않다는 사실을 설명할 수 있 다. 통 71 산소는 질산화에 관련된 모든 종의 필수 불가결한 요구물로 통기는 질산화 작용에 필수적이다. 토양으로 산소의 확산, 죽 통기는 토양 수 분, 구조와 같은 요인에 의해 조절된다. 수분 수분은 토양의 통기 체계에 영향을 주므로 토양의 수분 상태는 질산 염 생산에 영향을 준다. 토양이 물에 잠기게 되면 산소의 확산을 제한 하여 질산화 작용이 억압된다. 반대로 극단적으로 물이 부족할 경우 세균의 번식은 지연된다. 최적 수분 수준은 토양에 따라 여러 가지로 나타난다. 그러나 대부분 질산화 작용은 -0.1 에서 -lMPa 의 수분
압력에서 쉽게 진행된다. 암모니아를 생성하는 일반적 무기화 작용 반 응은 수분 스트레스와 저온에 덜 민감하다. 그러므로 암모니아는 물의 부족으로 인해 압박받는 곳이나 저온의 토양에서 누적된다. 온도 질산화 작용은 온도에 의해 뚜렷하게 영향을 받는다. 이 과정은 5° C 이하와 40°C 이상에서 느리다. 최적은 30-35°C 부군이다. 온도, 습도, 통기 그리고 다른 요인들의 상호작용이 계절적인 효과를 가져온 다. 온대지역에서 질산화 작용은 봄과 가을에 가장 크고 여름과 겨울 에 가장느리다. 유기물 오랫동안 유기물이 질산화 세균에 유해하다고 생각되었다. 이는 받 아들여질 수 없는 것으로, 이 과정이 되비와 폐수에서 일어나기 때문 이다. 현재는 유기물 자체가 억제적인 것이 아니고 유기물의 분해가 무기 질소와 산소를 요구하기 때문에 질산화 세균에게 가용한 암모니 아와 산소를 고갈시키기 · 때문으로 생각된다. 8-4-3 종속영양 질산화 작용 몇 가지 종속영양 질산화 세균과 방선균은 암모니아가 포함된 배양 액에서 성장할 때 극소량의 아질산염을 생산할 수 있다. Ar th- robac t e ri.坪 같은 세균과 As pe rgi, llu s fl avus 와 같은 전균은 암모니 아에서 질산염을 생성할 수 있다. 종속영양 생물들은 이러한 산화반응 에서 에너지를 만들진 못하며, 자연에서 이들의 의미성은 알려져 있지 않다. 경작 토양에서 종속영양 세균에 의한 질산염의 생성은 화학적
독립영양 생물에 의해 생성되는 것에 비하면 의미성이 없는 것으로 보 인다. 8-4-4 질산화 작용의 유해한 영향 식물은 쉽게 질산염을 동화하기 때문에, 생물학적 질산화 작용은 토 양 비옥도의 지표로 사용되어 왔다. 그리고 양호한 식물의 성장은 이 과정에 의존하는 것으로 자주 간주되었다. 그러나 질산화 작용은 또한 바람직하지 않은 결과를 일으킬 수도 있다. 암모니아는 양이온으로 토 양에 부착되어 비교적 안정하다. 반면 질산염은 음이온으로 토양수에 서 자유롭게 이동한다. 어떤 조건에서는 특히 사토에선 호우시에 또는 과다한 개간이 시행되면 질산염이 근역 root zon 러 1 서 용탈되어 없어 진다. 또한 탈질화 작용을 통해 손실될 수도 있다. 이 결과 대기가 오 염된다. 토양에서 용출된 과다한 질산염 질소는 종종 호수와 강에 유 입되어, 거기서 식물과 미세조류의 과다한 성장(부영양화)을 가져오 고, 건강 문제, 즉 어린이와 동물의 청색증 me t hemo g lob i nem i a 같은 문제를 야기시키며, 다른 질소 화합물과 반응하여 발암물질인 니트로 사민 nit ro sami ne s¾ 형성시킨다. 8-4-5 질산화 작용의 억제 질산염은 통상 교란되지 않은 초원 또는 성숙한 산림에 누적되지 않 는다. 극상 상태에 있는 생태계는 질산화 세균에 독성인 탄닌과 같은 유기 화합물을 생산하는 것으로 많이 제안되고 있다. 이 과정을 타감 작용 allelo p a t h y이라고 부르며 질소 손실을 자연적으로 조절하는 것을 대표적으로 나타낸다고 볼 수 있다. 그러나 식물 뿌리, 균근 곰팡이,
질소고정 미생물들의 암모니아에 대한 경쟁으로 낮은 농도의 무기 질 소가 유지되어 질산화가 억제된다는 다른 의견이 현재 더 널리 인정되 고있다. 질소의 손실을 줄이기 위한 상당한 연구가 질산화 작용을- 억제하는 화합물을 발견하기 위해 이루어졌다. 몇 가지가 특허를 받았으나, 아 직 일반적인 사용에 채택된 억제제는 없다. 표 8.3 은 현재 이용되고 있으며 특허를 받은 억제제를 보여 준다. 토양의 종류, 온도, 산도 그 리고 습도가 각각의 화학물에 다르게 영향을 준다. 다론 접근 방법은 느리게 방출하는 비료를 개발하는 것이다. 이같은 연구의 목적은 한번 에 손실되는 것을 피하여 비료의 효율을 개선하는 데 있다. 황을 입힌 요소는 그러한 화합물이다. 질산화 작용 동안에 산의 생성이 있기 때 문에 과다한 질산염의 축적을 피하는 것이 중요한 실무적 고려사항이 다. 표 8.3 특허를 받은 몇 가지 질산화 과정의 억제제· 억제도 화합물 상용이름 개발자 (14 일 후 의 %) 2-Chloro-6-(t rich lorometh yl) pyridine N-serve Dow Chemi ca l 82 4-A mino -l, 2, 4, 6-tr iaz ole-HCI ATC Ish iha da Industr ies 78 D2, i4mc-ye Da tnhi adym i lat irm n i aoi zd- i6en -et r ich loro- DCLic-y1 a5 n 8 0 AShmaomewriai d c aD ne nCkyo a n - 5653 Th iou rea TU Ni tto Ryu s o 41 3-Mercap to- l,2,4,-tr iaz ole MT Nip pon 32 2S-uAp lfymartii hmn io aid z- 4ion-leec hloro-6-meth yl- ASTM MMii ttssuuii TTooaattss uu 3311 •Bund y와 Bremner (19 73) .
참고문헌 Alexander, M. (19 77) . Intr o ducti on to Soil Mi cr obio lo gy . W ile y, New York. Bundy, L. G., and Bremner, J. M,. (1 9 73) . Inhib i t ion of nit rif i ca ti on in soil s, Soil Sc i. Soc. Am. Proc. 37, 396-398. Camp b ell, R. (1977) . Mi cro bia l ecolog y, In Basic Mi cr obio l ogy (J. F. W il- kin s on. ed.) Vol. 5. W iley , Toronto . Lehnin g e r, A. L. (19 84) . Bi oc hemi stry. Worth Publis h ers, New York. Lohnis , F. (19 13) . Vorlesung e n ilbe r landwort sch aft lic h e Bacte r i olo gi a. Bor-ntr a eg e r. Berlin . Meng e l, K., and Ki rk by , E. A. (19 78) . Pr inc iple s of Plant Nutr ition . Int. Pota s h Inst., Bern. Mi ller , H. G., Coop er , ]. M., Mi ller, J. D., and Paulin e , D. J. (19 79) . Nutr i e n t cyc les in pine and the ir adap tat i on to po or soil s, Can. ]. For. Res. 9, 19-26. Nommi k. H., and Vahtr a s, K. (1982) . Rete n ti on and fixa ti on of ammoniu m and ammonia in soil s , In Ni tro g e n in Ag r ic u lt ur al Soil s (F. ]. Ste v enson, ed.) . Ag ro nomy , Vol. 22, Am. Soc. Ag ron ., Madis o n. Wi sc onsin . Payn e , W. J. (19 81 ) . Denit rifica ti on . W ile y, New York. Schloesin g ,]. ] . T., and Muntz , A. (18 77) . Sur la Ni trifica ti on pa r les Ferments Orga nis e s, Comp . Rend Acad. Sc i (Pari s) 84, 301-303. Ste v enson, F. J., ed. (1982) . Ni trog e n in Ag ricu lt ur al Soil s. Ag ron omy , Vol. 22. Am. Soc. Ag ron ., M adis o n, W isc onsin . Wari ng ton , R. Ni trif ica ti on , ]. Chem. Soc. 33, 44-51 . W ino g rad sky, S. (18 90) . Recherches sur les orga nis m s de la nit rif ica ti on , Ann. Inst. Paste u r 4, 213-231, 257-275, 760-771 . 추가로 읽을 거리 Belser, L. W. (19 82) . Inh ibi t ion of nitrifica ti on , In Advances in Ag ricu l- tur al Mi cr obio l ogy (N. S. Subba Rao, ed.) . pp. 267-293. Butt er wort h, London.
Focht, D. D., and Verstr a ete . W. (1977) . Bi oc hemi ca l ecolog y of nit rif i ca ti on and denit rif ica ti on , Adv. Mi cr ob. Ecol. l , 135-199. Gosz, J. R . (19 81) . Ni tro g e n cy c lin g in conif ero us ecosys te m s, Ecol. B ull. (Sto c kholm) 33, 405-426. McGi ll, W. B., Hunt, H. W ., W oodmansee, R. G., and Reuss, J. 0. (19 81) . Phoenix , a model of the dy n ami cs of carbon and nit ro g e n in gr ass-land soil s , Ecol. Bull. (St oc kholm) 33, 49-115. Schmi dt , E. L. (19 78) . Ni trif y ing Mi cr oorga nis m s and Their Meth o dol-og y, pp. 288- 29 1 . Am. Soc. Mi cr obia l ., Washin g ton , D. C. Schmi dt , E. L. (19 82) . Ni trif i ca ti on in soil , In Ni tro g e n in Ag ricu lt ur al Soil s (F. J. Ste v enson, ed.) . Ag ron omy . vol. 22, pp. 253-288. Am. Soc. Ag ron ., Madis o n, W isc onsin . Van Ve en J. A., Ladd, J. N., and Fris s el, M. J. (19 84) . Modellin g C & N tu rnover thr oug h the mi cr obia i bio m ass in soil , Plant Soil 76, 257 -274.
제 9 장 질산염의 환원과 이동 9-1 서론 대부분의 토양에서는 토양 유기물이 분해되는 동안 암모니아가 방출 되는데 생물에 의해 죽각 재이용되지 않아 쉽게 질산염으로 변환된다. 비료 질소인 요소나 암모니아도 역시 질산화될 수 있다. 한번 토양에 서 질산염이 형성되면 다음과 같은 운명을 겪는다. ® 미생물에 의해 기체상의 질소 산화물이나 질소 기체로 되는 탈질화 작용이 일어날 수 있다. ® 생물에 의해 흡수되어 아미노산의 합성 (동화성 환원)에 이용 될 수 있다. ® 산소가 없을 때는 미생물에 의해 전자 수용체로 사용 되어 암모니아로 환원될 수 있다(이화성 환원). ® 상충의 토양에서 더 깊은 토양충이나 지하수로 스며들 수 있다. ® 지표 유출수에 의해 다른 곳으로 운반될 수도 있다. ® 휴경지의 경우 질산염이 토양에 그 대로축적될수있다.
9-2 탈질화 작용 질산염이 아질산염으로, 아질산염이 기체상의 N20 와 N2 로 바뀌어 대기로 빠져나가는 미생물적 환원 과정을 탈질화 작용이라 한다. 이 과정은 흔히 효소적 탈질화 작용으로 불리며, 여러 생물의 성장 동안 에 수반되는 질산염의 동화성 환원과 구별되어야 한다. 그리고 산소가 없는 상태에서 어떤 미생물에 의해 일어나는 질산염의 암모니아로의 이화성 환원과도 구분되어야 한다(그립 8.7 참조). 동화성 환원 과정 에서 녹색식물, 세균, 시아노박테리아(또는 남세균이라고도 함) 그리 고 진균류 등은 아미노산과 단백질의 생합성 경로에서 질산염을 암모 니아로 환원한다. 아질산염과 히드록실아민 (NH20H) 은 중간 산물이 다. 이 과정은 산소에 의해 억제되지 않으며 암모니아나 또는 환원형 의 유기 질소 대사산물의 존재에 의해 억제된다. 그 환원효소는 NADPH 와 연관되어 있고, 필요한 조효소 co fac t or 는 몰리브덴이다. 이화성 환원에서 어떤 종류의 미생물종은 산소가 없 는 상태에서 최종 산물로서 기체 질소가 아닌, 암모니아를 만들기 위 해 질산염을 전자 수용체로 사용한다. 이 반응의 예상되는 경로는 다 음과같다.
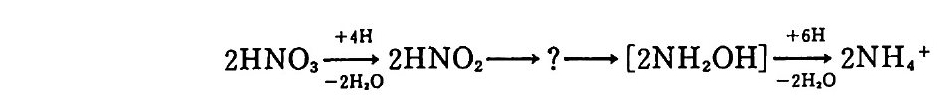 2HN03 一-2+H4H, O 2HN02_宁 一 [2NH20H]- 一- 2+H6H,O 2NH4+
2HN03 一-2+H4H, O 2HN02_宁 一 [2NH20H]- 一- 2+H6H,O 2NH4+
이 경로는 그 계로부터 질소의 손실을 일으키지 않는다. 이는 높은 환원성 조건에서 발생하지만, 자연에서 그 발생의 범위는 잘 알려져 있지 않다. 토양에선 15N03 와 같은 추적자를 이용하지 않는 한, 위의 경로는 똑갇이 암모니아를 만드는 단백질 분해와 구별하기 어렵다. 상 당히 많은 수의 미생물이, 유기물이 존재하고 산소가 없을 때 질산영
울 오직 아질산염으로만 환원시킬 수 있다. 이 과정은 질산염 호흡이 라 하여 직접적인 손실을 야기하지는 않는다. 그러나 아질산염은 매우 반응성이 높아서 간접적으로 손실을 줄 수 있다. 9-2-1 탈질화 작용의 생화학 탈질화 반응 동안 형성이 확인된 산물의 순서는 그림 9 . 1 에 나타난 바와 같이 질산염 , 아질산염 , 아산화질소 (nit ro us oxid e , N20) 그리고 질소 기체이다. 야의 조건에선 모든 기체상의 중간 산물이 각각의 특 이한 환원 효소에 의해서 질소 기체로 바뀌지는 않으며 일부는 대기로 사라진다. 탈질화 작용 동안 전자의 흐름에 대한 상세한 관찰은 탈질 화 작용에 포함된 전자전달계 기작에서 다양한 전자 공여체가 사용될
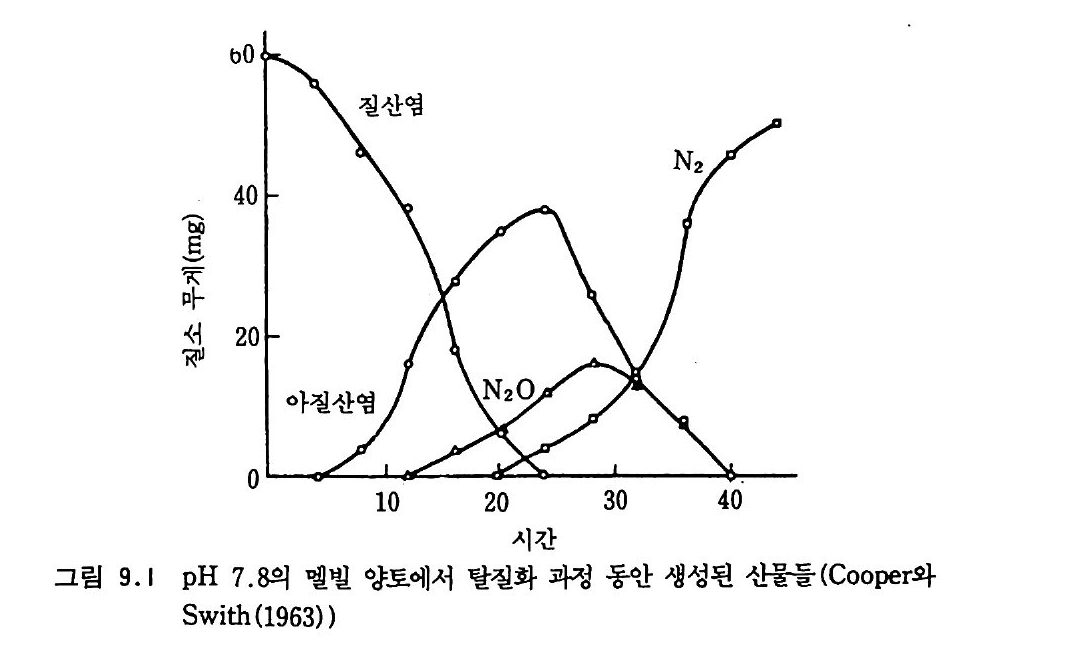 bO
bO
수 있음을 보여 준다(그림 9.2 ) . 전자 전달계의 퀴논 성분은 아마도 산소의 존재에 의해 영향을 받는 것으로 나타났다 . 전자 수용체로서 산소가 이용될 수 없을 때에, 전자 전달은 b- 형의 시토크롬 c yt ochrom 려서 최종 수용체인 산화된 질소의 몇 가지 형태로 분기된 다. 여기에 특정한 환원효소가 각각의 수용체 수준에서 사용된다 . 질 산영 환원효소는 Mo, Fe, 반응하기 쉬운 설파이드기를 포함한다. 위 의 두 금속은 효소 활동에 필수적 구성요소이다. 탈질화 반응의 두번째 단계에 작용하는· 아질산염 (NO 더 환원효소 는 세포 조작에 의해 쉽게 용해된다. 그리고 세포질의 수용성 부분에 서 여러 시기에 나타나기도 하지만, 세포막에 부착되어 있는 것으로 생각된다. 질산염 환원효소처럼 Km 값은 분포 범위가 넓은데, 이는 세포 내에서의 음이온 이동에 대한 의존성 또는 반웅 산물들에 의한 억제 작용에 대한 의존성을 반영하는 것으로 보여진다. 막에 부착된 산화질소 (NO) 환원효소는 분리는 되었지만 아직 순수 정제되지 않았다. 그러므로 그 특성은 잘 알려지지 않고 있다(표 9.1). 그림 9.2 에 나타나 있는 Pa y ne 의 구도는 NO 가 중간 대사산물 임을 보여 준다. 그러나 아질산염이 아산화질소 (N20) 로 환원되는 경 로에 대해 약간의 논란이 있다 . 하나의 가설은 니트로실 n it ro, s.y l 이 유 리니트록실 (HNO) 로 환원됨으로써 산화질소가 형성된다는 것이며, 이 유리 니트로실은 자연발생적으로 이중합체를 이루어 N2 0-를 만든 다. T i ed j e 의 실험실에서의 결과는 N20 가 유리니트록실을 거치는 것 보다 효소에 결합된 니트로실 중간 산물에 대한 아질산염의 친핵반웅 적 공격에 의해 생성됨을 주장한다. 위의 반응에 의해 N ― N 결합이 형성되는 구도는 다음과 같다 (Aerssens 등(1 986)).
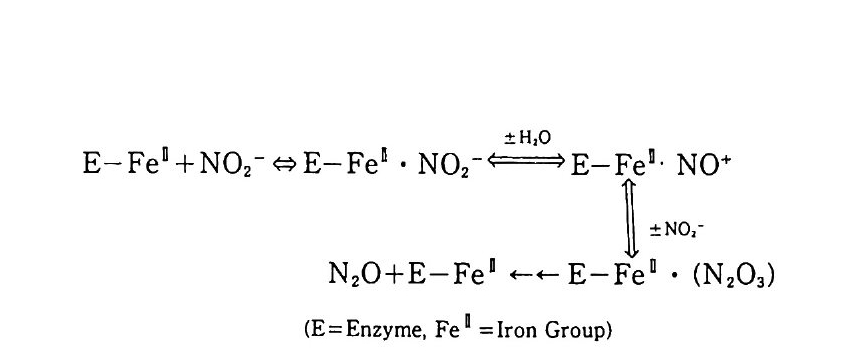 土 H,O lz No,-
土 H,O lz No,-
수 종의 환원효소 중에서도 아산화질소 환원효소는 아세틸렌 (C2H2) 과 설파이드(H S 기에 의해 억제되는 독특한 효소이다. 이러한 특징 온 탈질화 반응에 대한 연구에 편리한 방법을 제공한다. 정상적으로 표 9.I 탈질화 반응에 관여하는 환원효소들의 특성· 트거.0서 N03N - a一R .. N02~N 一i R . . No N-O--R+•• N2N02 -0-R+••N 2 위치 세포내 수용성 부분 + + 막에 부착 + +? + Perip la smi c + 인산화 반응의 발생 + +? ? + 산소 억제 + + + ++ 저해 + +? +? ++ 암모니아에 의한 억제 유도체로서 질소산화물 요구 질산영에 의한 억제 + + 낮은 p H에 의한 억제 + + + ++ 황화물에 의한 억제 ± 土 ? +++ 아세틸렌에 의한 억제 +++ • Knowles(l 98 1) 자료 •• NaR : 질산염 (N03 기 환원효소, NiR : 아질산영환원효소, NOR : 산화질소 환원효 소, N20R : 아산화질소 환원효소
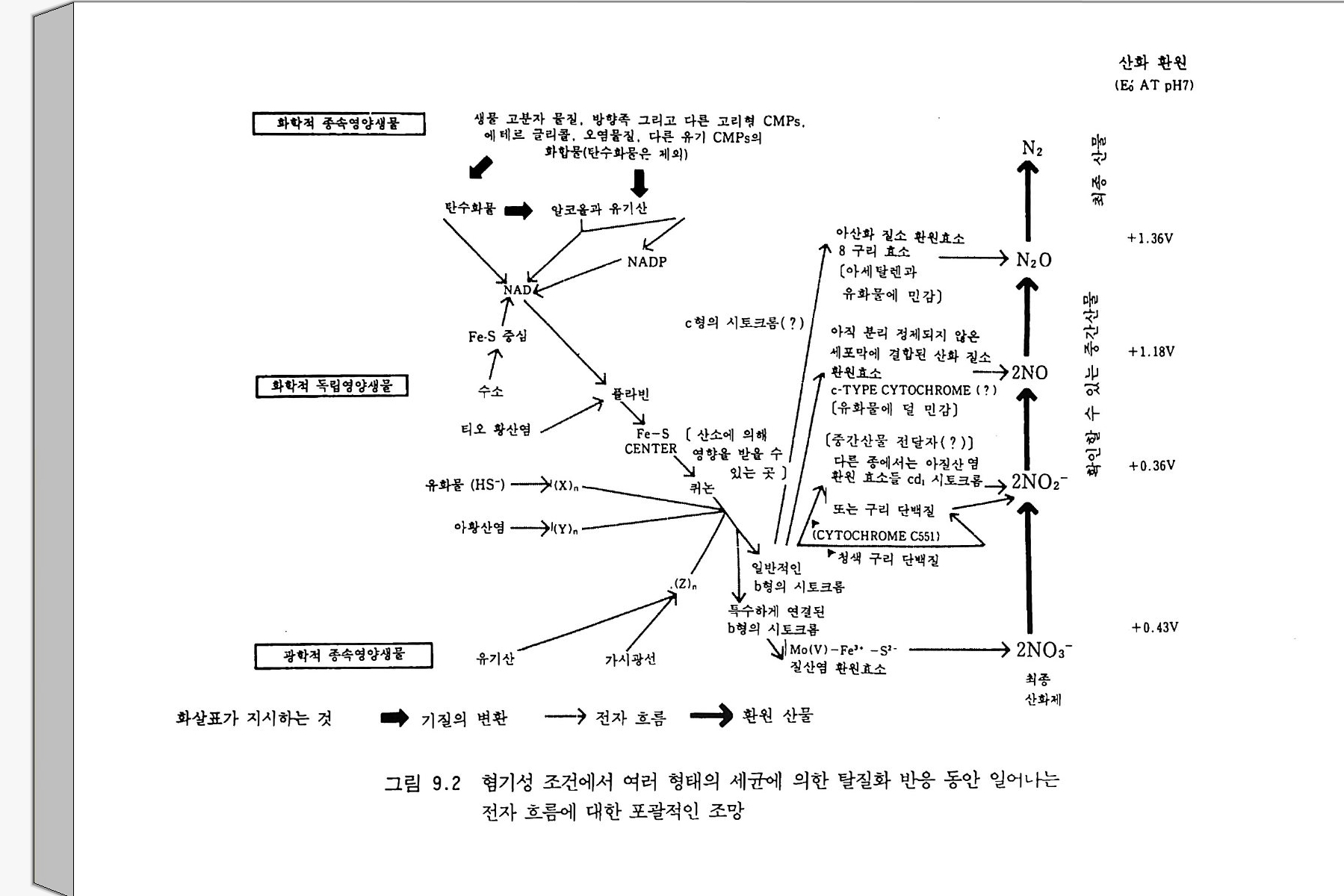 안
안
N20 와 질소 기체는 여러 가지 비율로 생성되며 기질, 환경 조건, 탈 질화 반응에 관여하는 생물, 그리고 탈질화 반응 전행 시간에 따라 달 라진다. 아세틸렌을 이용하여 탈질화 작용을 막으면 N20 가 축적되 고, 이는 기체 크로마토그래피로 측정될 수 있다. 탈질화 반응의 시작 과 N20 가 차단되기 전까지의 전행을 아세틸렌이 억제하지는 않는다 는 사실이 질소 추적자를 이용한 실험에서 입증되었다. 여러 가지 이 유를 근거로 아세틸렌을 이용한 차단기법에 대한 비판이 나타났다. 토 양에서 그 환원효소가 장시간 억제되지 않는 미지의 탈질화 세균이 존 재할 수도 있다. 실험기간 동안의 짧은 시간에 탈질화 반응이 일어나 는 미세지역으로 아세틸렌이 적절히 확산되지 않을 수도 있다. 그러나 15N 추적자를 이용한 야의조사 결과는 일반적으로 아세틸렌을 이용한 차단기법의 신뢰도를 입증하고 있으며, 또 기법이 빠르고 예민한 분석 임을보여 준다. 9-2-2 • 화학적 탈질화 작용 아질산염 환원효소만이 유일하게 아질산염의 변화를 맡고 있는 것은 아니다. 아질산염은 완전한 호기성 조건에서 효소반응이 아닌 경로를 거쳐 기체 질소의 생성을 가져오는 화학반응을 받게 된다. 아질산염의 불안정과 다른 질소 산화물과 기체 질소로의 변화 때문에 아질산염 질 소의 손실은 흔히 화학적 탈질화 작용이라 한다. 때때로 그러한 손실 은 호기성 탈질화 작용이란 용어로 표현됐다. 그러나 이러한 용어는 바람직하지 않다. 그 이유는 그 용어가 의관상 통기가 잘 되는 토양에 서 형기성 미세지역에 나타나는 미생물적 탈질화 작용에 이용되어 왔 기 때문이다. 화학적 탈질화 작용은 또한 부분적으로 잘못된 명칭이 다. 그 이유는 토양에서 아질산염의 생성은 생물적 과정이기 때문이
다. 아질산염의 호기성 변환은 여러 경로에 의해 일어난다. Van Slyk e 반응에선 카르복시기들에 대해 a 위치에 있는 아미노기들이 기체 질소 룰 다음과 같이 생성한다. RNH2+HN02— .. R OH+H20+N2 공기가 있는 토앙에서, pH 5 또는 그 이하에서만 이 반응은 매우 느린속도로일어난다. Van Slyk e 반응과 아주 유사한 반응에서는, 아질산염이 암모니아, 요소, 메틸아민, 푸린, 그리고 피리미딘과 다음과 같이 반응한다. HN02+NH.+ 一 N2+2H20 비슷한 조건에서 이 반응은 Van Slyk e 반응보다 훨씬 느리게 진행 된다. 아질산의 화학적 분해는 다음과 같이 자발적으로 일어날 수 있 다. 3HN02 一 HNOs+ H20+ 2NO NO 는 대기로 방출되거나 또는 산소와 물과 반응하여 질산염을 형 성한다. 2N0+02 一 2N02 一 N20.+H20 ― ► HN02+HN03 몇몇 연구자들은 NH4N02 의 불안정성이 화학적 탈질화 작용에 관 여될 수 있다고 주장했다. 가끔 토양에서 암모니아와 아질산염이 동시 에 존재한다는 점이 관심을 끌었다. 그 경우 NH4N02 의 형성 및 분 해와 관련된 질소 기체의 손실이 있을 수 있다. N02-+ NH.+ 一 NH.N02 一 N2+ H20
Clark (1 962) 와 공동 연구자들은 공기가 잘 통하는 토양에 첨가된 질산염이 몇 주 동안 배양된 후에도 본래의 양으로 존재하였지만, 같 은 실험에서 암모니아 또는 요소질소의 경우 어떤 토양에선 원래의 양 으로 존재하고 다른 토양에선 원래의 양으로 존재하지 않음을 주목했 다. 질산화 작용 동안 많은 양의 아질산염 축적을 보인 토양에서는 본 래 첨가된 질소 양의 반 가까이 되는 결손이 나타났다. 그 조사자들은 종속영양 생물에 의해 생성된 유기 환원성 화합물이 아질산염과 반웅 하여 산성 토양에서뿐만 아니라 중성 및 약알칼리 토양에서도 아질산 염의 화학적 분해를 야기시킨다고 제안했다. 9-2-3 탈질화 작용 생물 상당수의 세균이 산소가 없는 상태에서 질산염을 아질산염으로 환훤 시킬 수 있다. 대개 표 9.2 에 나열된 속들에 포함된 종 중에서 매우 적은 수가 N20 와 N2 로 환원시킬 수 있다. 대부분의 탈질세균은 종속 영양생물이며 Pseudomonas , Bacil lu s, Alcal ig enes 와 같이 흔히 출 현하는 속들의 구성원이다. 대부분은 호기성으로 오직 질소 산화물들 이 존재 할 때만 형기상태에서 성장한다. 그러나 Prop ion ib a cte r i um 의 몇 종은 절대적 발효성이며, Bac i llus 의 몇 종은 조건적 발효성이 다. 탈질화 세균은 질산염, 아질산염, 그리고 아산화질소 환원효소를 가지고 있으나, 어떤 것은 질산염 환원효소가 없고 어떤 것들은 (주로 Pseudomonas) 아산화질소 환원효소가 없다. 탈질화 반응과 질소고정을 할 수 있는 능력이 Azo sj)iri llum 과 뿌리 혹박테리아 Rh i zob i um 의 몇 구성원에 모두 존재한다. 그러나 두 과 정은 동시에 일어나지 않는다. 그리고 질산염의 존재는 질소고정 효소 의 활성을 억제한다. Rhodop seudomonas 속의 어떤 광합성 비황세균
표 9.2 탈질화 작용을 할 수 있는 세균 속 속일부 종들의 홍미로운 특성들 Alcalige n es 흔히 토양으로부터 분리 Ag ro bacte r i um 일부 종은 식물 병원성 Azos pirillu m 질소고정 능력, 벼과 식물과 연합 Bacil lu s 호열성의 탈질화 세균둘이 보고됨 Flavobacte r i um 탈질화 반응을 하는 종이 분리됨 Halobacte r i um 성장시 고농도의 염을 요구 Hy ph omi cr obiu m 하나의 탄소로 된 기질에서 성장 Paracoccus 무기영양과 종속영양으로 성장가능 Prop ion ib a cte r i um 탈질화 반응을 하는 발효균 Pseudomonas 흔히 토양으로부터 분리 Rhiz o biu m 콩과 식물과 공생하며 질소고정을 함 Rhodop s eudomonas 광합성을 함 Thio b a cillu s 일반적으로 화학적 독립영양으로 성장 ·자료 : Fir e sto n e(1 9 82) nonsulfu r bac t e ri a 은 탈질화 작용과 질소고정의 능력을 가지고 있어 홍미롭다. 또한 무기 영 양 탈질화 세 균도 있다. Thio b acil l us den itrifi cans 는 황세균으로서 형기성 조건에서 다음과 같은 반응을 수행한다. 5S+6KN03+2H20 ― ➔ 3N2+K2S0.+4KHSO. 또한 부분적으로 환원된 황화합물을 다음과 같이 산화시킨다. 5K2S203+8KN03+H20 一 ➔ 4N2+9K2S04+H2S04
9-2-4 탈질화 반응의 측정과정 여러 가지 토양, 퇴적물, 그리고 수중 환경에서 일어나는 탈질화 정 도를 측정하는 일은 완벽하게 적합한 측정 방법이 없어서 어려움이 있 다. 사용되는 방법들 몇 가지를 표 9 . 3 에 나열했다. 15N 을 이용한 질 소의 수지 균형 연구는 간접적이기는 하지만-특히 라이시미터 l y s i me t e 라 장기적으로 연구된 유역에서처럼 용탈 손실이 고려될 경 우 가치 있는 추정치를 제공한다. 현징에 있는 상당수의 변수와 불확 실성울고려할 때 !SN은 유용함이 입증되었다. 그러나 질소 기체, N20, NO, NO 가 혼합되어 있을 경우, 분광분석법에서는 특정한 질량 피크에 나타나는 이들 각 성분을 정량하기가 어려워진다. 예를 들 면 떡'1 2 와 NG 는 둘 다 질량 분광법에서 질량 피크가 30 이 된다. 좋은 검출기와 칼럼 내 충전 물질들의 이용은 기체 크로마토그래피 를 가치 있는 도구로 만들었고, 초기 기체싱에서 질소가 없는 경우에 특히 그러하다. 정상적 대기의 질소 농도에서는 현재의 기술로 질소 기체 농도의 작은 변화를 검출할 수 없다. 그러므로 토양의 깊이에 따 른 N20 의 측정은 종종 탈질화 작용의 지표로서 사용된다. N2 : N20 비의 불확실성과 확산 속도의 차이 때문에 실제 발생량을 계산하기 어 렵다. 게다가 N20 환원 속도를 탈질화 작용의 지표로. 사용하는 것은 N20 가 통상 탈질화 과정에서 속도제한 단계가 아니라는 근거에서 문 제가된다. 토양 세균에 의해 N20 가 N2 로 환원되는 것을 아세틸렌이 차단한다 고 밝혀짐에 따라 탈질화 작용의 연구에서 아세틸렌이 널리 사용되었 다. 아세틸렌 농도가 0.02 기압 이하에서 아세틸렌의 차단 효과는 가 역적이라는 것이 증명되었다. 그러나 높은 농도에서는 비가역적이다. 그리고 생산된 N20 의 곧이은 환원도 무시할 정도였다. N20 의 축적
표 9.3 토양에서 탈질화 작용의 측정 방법* 방법 비고 질소 또는 “N 의 수지 균형 바교적 장기적인 연구에 적용해야 함, 정 확도가 떨어지므로 질소나 lSN 를 첨가 질산염이나 아질산염의 소멸 암모니아로 동화 또는 환원될 수 있는 일 부 조건 특히, 탄소가 풍부하고 형기성 일 때 유효함 첨가된 아산화질소의 소멸 환경을 교란시키지 않는 방법임, 아산화 질소의 환원부위가 포화되면 과대평가 될 수 있음. 질산염 또는 아질산영은 전자를 획득하기 위해 경쟁한다 아산화질소와(또는) 질소기체를 아르곤이나 헬륨으로 대치한 질소 기체의 생성 폐쇄계가 필요, 산소 농도를 변화시킴. 15N03- 로부터 “N20 와(또는) lSN2 의 생성 실험실내의 방법 일반적으로 폐쇄계에서 사용. 정확성은 비교적 높으나 지루하고 비용이 많이 듦 현장에서의 방법 단기간 차단된 토양에서 측정된 lSN2 의 유동을 측정. 민감하지 못함• 13N Q 3- 가 “N20 와 (또는) 고감도이나 매우 짧은 반감기 (1 0 분) 를 가 13N2 로 환원 짐. 혼합이 잘 되게 하기 위해 교반된 슬러리에 사용한다. 아세틸렌의 유무에 따른 아산화 아산화질소 환원효소는 아세틸렌에 의해 질소의 생성 서 억제되며 아산화질소는 축적됨. 실험실 내의 방법 0 . 1 기압의 아세틸렌에서 신뢰할 수 있음. 현장에서의 방법 기체가 통과하거나 가스가 새어나가지 않 게 막힌 토양. 때로 완전히 억제되지 못하는 것이 관찰됨. 아세틸렌은 이용 되거나 질산화와 다른 과정을 억제함. ·자료 : Knowles(1 9 82)
은 전자포획검출기가 장치된 기체 크로마토그래피로 쉽게 측정될 수 있다. 기체 시료는 용기나 임관으로 닫혀져 있는 토양 칼럼에서 채취 해야 한다. 이렇게 측정된 값을 공간적 이질성과 연간 변하 효과를 고 려하여 확대 해석하기 위해서는 관련된 토양 변이와 기후 변화에 대한 철저한 지식이 요구된다 . 9-2-5 토양의 탈질화 작용에 영향을 주는 요인들 탈질화 작용이 일어나기 위해서는 산화된 질소가 존재해야 하고 산 소의 공급은 제한되어야만 한다. 또한 탈질화 생물체가 그들 성장에 적합한 환경에 존재해야 한다. 토양에서 탈질화 반응 속도의 중요한 결정 인자들은 ® 질산염의 가용도, ® 대사 가능한 탄소의 공급 , ® 토양의 수분, @토양의 통기, ®토양의 산도, ®온도이다. 따로측 정된 이들 결정 인자들의 정성적인 역할은 아주 잘 정의되어 있으나, 그들의 상호작용으로 인해 야외의 토양으로부터 기체 질소의 실제 유 동을 예견하는 것은 어렵다 . Mosie r 등 (1982) 은 토양으로부터 N20 의 일별 손실을 예측하는 간단한 기작 모형을 제안하였다. 토양의 질산염 함량 탈질화 반응이 효소에 의한 것인 만큼 기질의 농도가 속도의 결정 인자로서 기능을 발휘하는 것은 당연하다. 질산염의 농도가 20µg N mI-1 을 초과하는 경우, 탈질화 반응은 영차 반응식을 따른다 . 죽 존 재하는 질산염의 양에 무관하고, 질산염의 반옹 속도는 질산염 수준보 다는 대사에 필요한 탄소 이용도에 의해 결정될 수 있다. 낮은 질산염 농도에서 환원반응의 반응식은 일차인 것처럼 보인다. 젖은 토양에서 질산염의 농도가 낮울 때 결정 요인은 탈질화 반응 장소로 질산염이
확산되는 속도일 것이다. 질산염 농도는 탈질화 작용의 기체상 생성물 에서의 N2 : N20 비에 영향을 주는 것으로 관측되고 있다. 높은 질산 염 수준에선 질소 기체가 지배적으로 많고, 낮은 질산염 수준에선 종 종 N20 가 지배적이다. 탄소의 이용도 대부분의 탈질화 작용은 종속영양 세균에 의해 이루어지며, 따라서 탄소의 이용도에 따라 그 정도가 크게 달라진다. 토양 유기물 총량과 탈질화 작용의 참재력 사이에는 일반적인 상관관계가 있다. 그러나 쉽 게 분해되는 유기물이 공급되면 상관관계는 더 좋아진다. 이용 가능한 탄소 기질들은 전자를 공급한다. 또한 그들의 분해로 이산화탄소는 생 성되고 산소 수준은 낮아진다. 그리하여 미생물이 성장하는 동안 전자 수용체로서의 질산염 요구가 증가된다. 토양의 탈질화 작용 능력을 예 측하기 위해 즉각 분해될 수 있는 유기물을 측정하는 시도가 있어 왔 다. 토양 내 탈질화 작용의 잠재력 71% 를 수용성 탄소의 양으로 설 명할 수 있었다. 그리고 7 일 동안의 배양에서 무기화되는 탄소의 양은 그 모든 요구를 충분히 충족시켰다. 근권에서 뿌리의 분비물과 뿌리의 박리에 의해 공급되어 쉽게 분해 되는 탄소의 증가량은 비근권의 토양보다 근권의 토양이 탈질화 작용 에 더 적합함을 제시해 준다. 배양 조건들을 일정하게 하고 근권의 토 양과 불과 몇 밀리미터 떨어진 이웃의 토양을 사용한 실내 실험은 근 권 토양에서 더 높은 탈질화 작용이 일어나는 것을 보여 주었다. 야의 실험은 상반적이었다. 휴경지의 토양보다 경작지의 토양에서 감소된 탈질화 작용의 참재력은 식물에 의한 질산염과 물의 섭취에 기인한다. 증발 증산은 식물의 뿌리 부근에서 더 환기가 찰 되는 토양을 제공한 다. 근권이 습한 상태를 유지하는 기간도 또 디른 변수로 작용한다.
단기간의 물 공급 또는 참시 물이 고이는 동안에는 근권의 부가적으로 가용한 탄소가 영향력을 발휘하지만, 침수가 장기간이고 산화 환원 전 위가 낮게 될 때는 근권의 효과가 별로 중요하지 않게 된다. 토양의 수분함량 물의 영향은 미생물 활동 장소로 산소를 확산시키는 역할의 조정과 직결되어 있다. 토양의 수분 함량의 증가가 산소의 확산을 방해하는 수준에 이르면 점전적으로 탈질화 작용 잠재력을 증가시킨다. 산소는 모든 질소 산회뭄 환원효소를 억제하나, 다른 것들보다는 질산염 환원 효소를 약간 덜 억제한다. 토양에서 물과 산소의 상호 관계는 토양의 입단, 공국, 다양한 크기와 형태를 갖는 통로의 존재에 의해 복잡해진 다. 습한 토양은 종종 저온의 토양이며, 생화학적 산소 요구량을 감소 시킨다. 표 9.4 는 주어진 토양의 수분 함량에서 산소량이 증가함에 표 9.4 수분 함량과 02 농도·가 다른 상태에서 3 일 동안 배양**했을 때 일어난 총 탈질화 (0.1 기압 C2H2 가 존재할 때 µmol N20 g-•)와 생성물 중 N20 가 차지하는 평균 몰 분율(괄호 안의 숫자)*** (%수M분WH 함C)량… · 。 기체 상태에4 있는 산소의 8초 기 비율 (%)1 2 33 0.64 (0 .94) 。。 。 60 0.98 (0.72) 0.03 (3.6) 。 。 100 0.98 (0 . 83) 0.68 (0.69) 0.36 (0 .25) 0.34 (0) 200 1.04 (0 . 97) 1.09 (0 . 43) 0.90 (0 .21) 0.58 (0) • Knowles (1981) 자료 •• 배양에 관한 자세한 것은 주석 ·올 보시오 •••N2~ 몰 분율은 아세틸렌이 없을 때 생성된 N20 를 0.1 기압의 아세틸렌 하에서 생 성된 N20 로나눈것 …* MWHC, 최대 용수량
따라 탈질화 작용이 감소하는 것을 보여 준다. 수분 함량이 증가하면 탈질화 작용도 증가한다. 일반적으로 야의에서 비정상적으로. 높은 산 소의 소비율이 없는 한, 탈질화 작용은 용수량의 60 %보다 낮은 수준 (대략 -0.0 1 MPa 수분 스트레스와 동등함)에서 무시할 정도이거나 일어 나지 않는다. 토양의 산도와온도 대부분의 탈질화 세균은 중성 부근의 산도(p H 6-8) 에서 가장 잘 자 란다. 탈질화 작용은 pH 5 이하에서 느려지지만 중요하며, pH 4 이 하에선 무시될 정도이거나 없다. 토양의 산도는 또한 발생되는 기체인 N20:N 려 비에 영향을준다 . 토양의 온도는 직접적으로 탈질화 작용에 영향을 준다. 죽 미생물 활성이 온도의 증가에 따라 아레니우스 식에 의해 지수함수적으로 증 가한다. 그리고 간접적으로 온도는 물에서 산소의 용해도와 확산에 영 향을 준다. 저온 (15-2o·c) 의 토양에서는 온도와 탈질화 작용의 잠재 력 사이에 지수함수적이기보다는 일차 함수적 관계가 존재한다. 탈질화 작용의 최저 온도는 약 5° C 이며, 최고 온도는 약 75° C 이 다. 최고 상한선 근처의 토양 온도에서 호열성 간균은 전부는 아니지 만 대체로 기체 손실에 관여한다. 5o•c 이상에선 아질산염의 화학적 분해는 중요해질 수 있으며, 효소적 분해를 보충할 수 있다. 일부의 토양에서 온도 변화는 발생되는 기체의 N20 : N2 비에 영향을 준다는 것이 밝혀졌다. 9-2-6 토양 질소의 다른 운명들과 비교한 탈질화 작용 손실 질소 수지 균형 연구는 간접적으로 탈질화 작용의 추정치를 얻기 위
표 9.5 토양에서 질소의 경제 제거/손실 범위(%) 작물흡수 0 -6 0 기체 손실 0 -3 0 침식 0 -1 5 부동화 0 -4 0 용탈 0 -1 0 해 자주 이용되었다. 표 9 . 5 에 있는 추정치들은 평균적으로 질소 비 료의 15% 가 대기로 상실됨을 보여 준다. 탈질화 작용의 측정에 아세틸렌을 이용한 방법의 출현으로 다양한 토양과 수확 조건에서 기체 손실에 대한 측정이 시행되었다. 토양으로 부터의 N20 의 유동은 탈질화 작용만으로. 나타나는 것이 아니다. 아 세틸렌으로 처리되지 않은 토양에선 N20 가 질화 작용 동안 생성된 다. 질화될 수 있는 질소(암모니아, 요소)를 가지는 토양에선 질화에 의한 N20 유동량이 총 N20 유동량의 중요한 부분이 될 수 있다. 9-2-7 성층권에 대한 아산화질소의 영향 탈질화 작용은 대기에 아산화질소 (N20) 의 양을 증가시켜 환경에 좋지 않은 영향을 줄 수 있다. 대기의 N2 0!나 불화탄소의 증가는 대 기 상층부에 있는 오존층을 파괴할 수 있다. 그리하여 단파장의 자외 선을 더 많이 통과시켜 피부암의 발생을 중가시킨다. N O!라 N20 는 모두 탈질화작용의 기체만물로서 생성된다 .NO 는 토양에서 반응하거나 또는 대기권 저층에서 존속하지 못한다. 그러나 N20 는 대류권에서 상대적으로 안정하여 성층권으로 확산할 수 있다. 그곳에서 N20 는 광분해되어 NO 를 형성한다. NO 는 곧이어 유입되는 복사열에 방패
역할을 하는 오존의 파괴를 촉진한다. 오존을 파괴하는 여러 가지 다 른 반응뭉게 비하여 N20긱 중요성은 잘 알려져 있지 않다. 대기의 N20 양은 현재 0.3p pm 정도이다. 현재 연간 약 65 메가톤 의 질소 비료가 사용되고 있다. 지구상에서 무기화되는 총 질소는 이 보다 50 배 가량 많은 것으로 추정되었다. 적절한 관리가 없으면 무기 화되는 토양 질소는 첨가된 질소만큼 탈질화될 수 있다. 가능한 대응 조치는 첫째, 질산화 작용 억제제들의 이용 증가, 둘째, 생물적 질소 고정의 이용 증가, 셋째 손실을 감소시키기 위해 비료 사용 시기와 양 의 적정화, 그리고 넷째, 무기화와 부동화 반응의 조절로서 토양 질소 를 유용한 유기 형태로서 가능한 많이 유지시키는 것이다. 토양에서의 탈질화 과정은 토양이 N20 의 소비자로서 또는 생산자로서 작용할 수 있음을 보여준다. 탈질화가 강하게 일어나는 토양으로 대기의 N20 가 확산에 의해 또는 강우에 의해 되돌려지는 정도에 따라 N20 가 질소 기체로 변환된다. 9-3 식물 뿌리에 의한 흡수 생물의 단백질 합성에 필요한 질소 공급원으로서 질산염보다는 암모 니아가 선호된다. 환원형의 질소는 죽각 아미노산으로 들어가나 산화 형의 질소는 먼저 환원되어야 하며, 이 과정에 필요한 에너지는 광합 성 산물로부터 얻어야 한다. 질산염보다 암모니아를 선호한다는 사실 은 미생물 실험으로 쉽게 증명된다. 토양에서 암모니아 이온은 이온교 환 복합체에 붙어 있고, 그리하여 토양수에서의 이동은 크게 제한된 다. 반면에 질산염은 확산 또는 물에 의한 흐름에 의해 뿌리로 이동될 수 있다. 암모니아의 빠론 질산화 작용은, 비록 질소원으로 질산염이
첨가되지 않았지만, 질산염이 식물에 대한 실제적인 이온 공급원인 것 처럼 만든다. 뿌리로의 손쉬운 이동과 아미노산과 아마이드로의 손쉬 운 합성은 식물 흡수에 관여된 유일한 요인들은 아니다. 암모니아의 홉수는 무기질의 양이온, 특히 K+ 이온을 흡수하는 것을 억제한다. 반 면에 질산염은 Cl- 과 S042- 의 흡수를 억제한다. 음이온과 양이온 형 태의 질소 공급원과 관련하여 잔존의 (또는 생리적) 산도 또는 알칼리 도는 직접적으로 또는 변화된 산도의 영향으로 인하여 다른 영양염의 이용도에 영향을 줌으로써 식물의 성장에 영향을 줄 수 있다. 이용할 수 있는 무기 질소의 오직 일부분만을 식물이 섭취한다고 해 도, 생합성에 필요한 요구량보다 홉수량이 많아서 질산염이 식물체 안 에 축적되는 경우가 있다. 높은 질산염의 축적은 토양에는 질산염이 적절히 있으나 식물의 성장 조건이 좋지 않을 때 예상될 수 있다. 질 산염의 환원과 아미노산을 합성하기 위한 유기산의 공급에 필요한 에 너지는 광합성에 의해 공급된다. 질산염 함량이 많은 마초는 소와 양 에게 독성이 있다. 되새김위에서 질산염은 독성이 있는 아질산염으로 환원된다. 아질산염은 되새김위에서 형성되든, 섭취 전에 형성되든 상관 없이 혈관으로 홉수되어 옥시헤모글로빈을 메티모글로빈 me t hemo g lob i~로 산화시켜 산소 운반을 방해한다. 9-4 용탈에 의한 질산염의 제거 용탈은 질산염을 토양의 상층부에서 더 깊은 충과 지하수로의 이동 울 야기시킨다. 이는 이류와 확산에 의해 이루어지는 무생물학적 과정 이다. 이러한 과정에 흔히 사용되는 식은 다음과 같다.
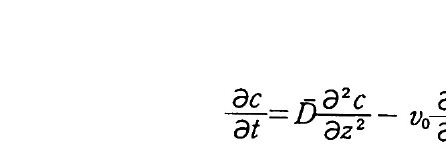 훑=때불一훌
훑=때불一훌
여기서 c 는 질산염의 농도 (m g 1 기. D 는 평균 확산계수 (cm2 day -1) , %는 평균 공극 속도이다 (cm day -1, 이는 물의 흐름 속도를 토 양의 물 부피로 나누어서 얻어진다), 착큰 흐름 방향의 직선거리 (cm) 이 며, t는 시간 (da y s) 이다. 위의 식은 균질한 토양에, 그리고 정상상태의 토양수 조건에 대해 타당하다. 유속은 용탈 부피에 비례하고, 물의 부피에 반비례함을 의 미한다. 복잡한 조직의 토양에서 위의 변수들은 시공간상에서 일정하 지 않다. 물의 이동 속도는 모든 점에서 같지 않다. 죽 토양 공극의 중심 부근이 가장자리보다 더 빠르고, 개방된 통로(균열된 톰, 오래된 뿌리의 통로, 동물이 파헤친 흔적)를 통한 속도는 일련의 상호 연결된 토양 공국을 통한 속도보다 더 빠르다. 확산은 입지들의 표면 근처에 있는 물에서 감소된다. 표면에 흡수된 물은 공국 중심에 있는 물보다 점성이 더 높다. 야의에서 경작충에 존재하는 과량의 질산염은 질산화 작용을· 유도하 는 유기 질소를 방출하는 토양의 능력과 비료 첨가의 시기와 양에 의 해 주로 설명된다. 과거의 토양수 체제와 관리 방식, 그리고 현재의 식물 피도가 물의 홉수율에 영향을 준다. 용탈하기 쉬운 과량의 질산 염은 토양수의 굽이 또는 전단에서 아래로 이동한다. 경작에 의한 초 기 교란에 따라 질산염이 더 깊은 충으로 이동한 사례가 캐나다 토양 울 대상으로 한 연구에서 나타났다(그림 9.3). 심층에서 질산염의 이 러한 농도는 약간 건조한 토양에서만 나타난다. 보다 습한 토양에서 종종 질산염의 대부분은- 비경작 계철 또는 우기에 지하수로 유실된다. 지하수로 용탈되어 우물물로 사용될 경우 유아에게 건강상 위험하 다. 질산염태 질소가 lO pp m 을 초과하면 특히 위험하다. 유아가 그
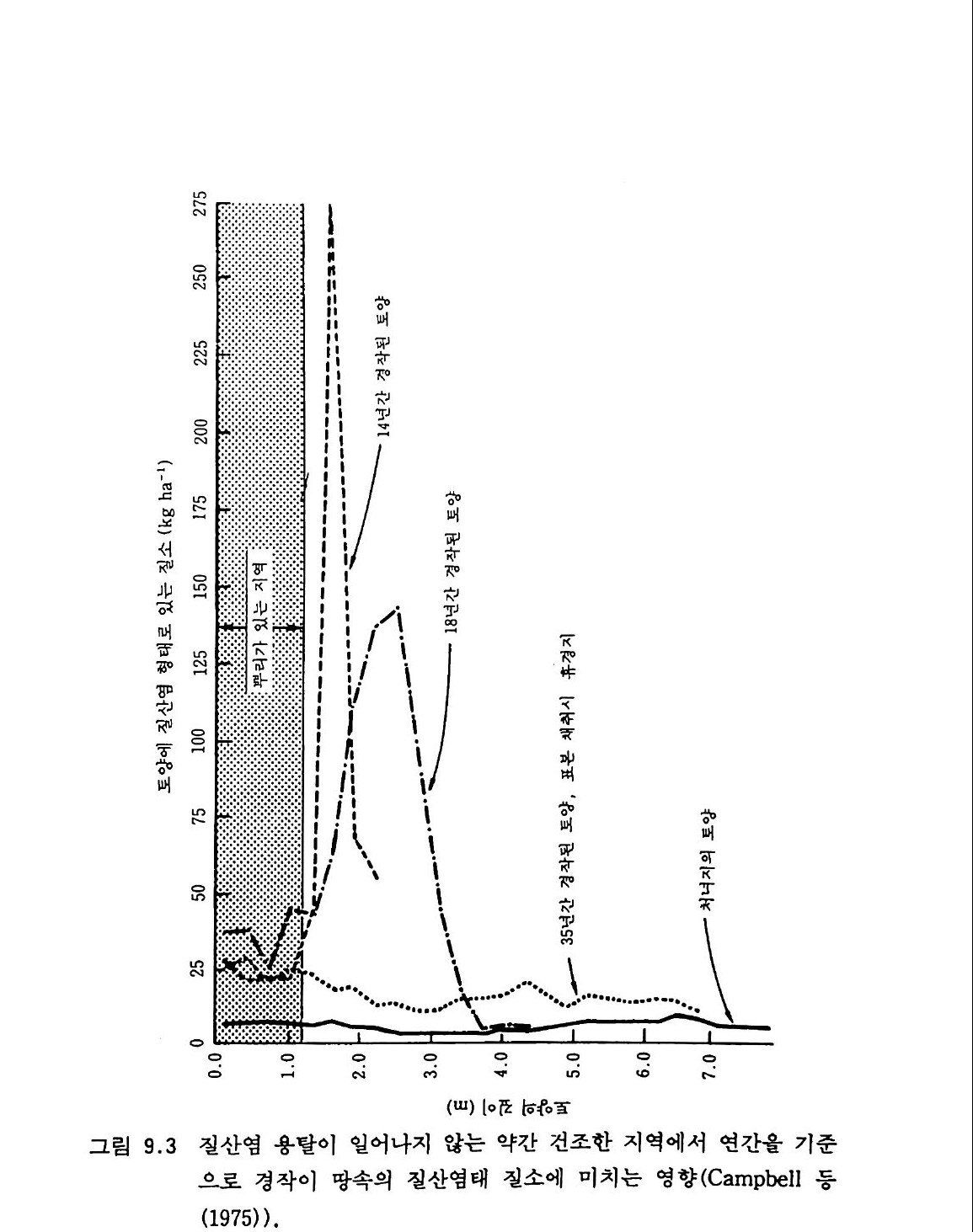 SLZ 仁I
SLZ 仁I
물을 섭취할 경우 질산영은 아질산염으로 환원되며, 아질산염은 혈액 의 헤모글로빈을 메티모글로빈으로 비가역적으로 환원시켜 산소를 결 핍시킴으로써 유아를 사망에 이르게까지 만든다. 이 병은 유아 청색증 me t hemo g lob i nem i죠로 알려져 있다. 어른은 헤모글로빈 양이 많고 체중에 비해 물의 섭취가 적어 거의 이러한 병에 걸리지 않는다. 9-5 침식에 의한 질산염의 손실 질산염은 바람과 물에 의해 다른 장소로 옮겨감으로써 손실될 수 있 다. 물에 의해 침식되는 동안 질산염의 이동은 토양의 이동과 일치하 지 않는다. 즉시 물에 녹을 수 있는 성질 때문에 질산염은 입자들보다 더 쉽게 지표 유출수에 유입된다. 침식은 용탈에 의한 질산염의 제거 를 감소시켜, 용달될 수 있는 질산염을 더 적게 만든다. 토양 단면의 절단과 표토의 제거에 의하여 침식은 무기화와 질산화 작용에 이용될 수 있는 토양 유기물 양을 감소시킨다. 표토와 질산염의 손실을 줄이 거나 막는 좋은 토양 보존 방법은 단순히 침식에 의한 손실을 막을 수 있지만 용탈되기 쉬운 질산염의 양을 증가시킬지도 모른다. 좋은 보존 은 침투수를- 증가시키고 지표 유 출수 를 감소시킨다. 질산염은 바람에 의한 침식에 의해 다른 장소로 운반될 수도 있다; 질산염의 손실은 입자의 제거에 국한되며 이에 비례한다. 그러나 먼지 입자 그 자체는 표토를 대표하지 않을지도 모른다. 가뭄은 보통 바람 에 의한 침식에 앞서 일어난다. 가뭄 동안 표토로 물의 모세관 이동이 일어나면 표토에는 질산염이 풍부하게 될지도 모른다.
9-6 국지적인 질산염의 축적 환원 (동화 또는 이화과정에 의해서)되지 않고, 또 다른 장소로 이동이 되지 않은 질산염은 국지적인 장소에서 다량으로 축적될 수 있다. 장 기 축적은 사막, 큰 동굴, 그리고 먼 바다의 작은 섬들(구아노라는 새 똥이 공급원이다)에서 나타난다. 가장 광범위한 구아노 퇴적은 칠레의 아타카마 사막에 위치한다. 이 퇴적물은 200 메가톤의 질산나트륨을 포함하는 것으로 추정된다. 한때 칠레의 구아노 수출은 소비된 질소비 료의 주요한 부분을 차지했다. 디른 염분과 함께 질산염의 축적은 서 부 미국 폴라야 (n it ers p o t)에서 또한 나타난다. 이러한 축적은 농 경지 토양보다는 암석 모재에서부터 용탈된 질산염에서 비롯된다. 참고문헌 Aerssens, E., T i ed je , J. M., and Averill , B. A. (19 86) . Isoto p e labell ing stu d ie s on the mechanis m of N-N bond for mati on in denit rif i ca ti on , ]. Bio l. Chem. 261, 9652-9658. Camp b ell, C. A., Ni ch olaic h uk, W., and Warder, F. (19 75) . Eff ec t of a wheat summer fal low rota t i on on subsoil NOJ -, Can. ]. Soil Sci . 55, 279 -286. Clark, F. E. (19 62) . Losses of nit ro g e n accomp a ny ing denit rifica ti on , Proc. Int. Soil . Conf Palmersto n Nort h N.Z., pp. 173-176. Coop e r, G. S., and Smi th, R. L. (19 63) . Sequ e nce of pro ducts form ed duri ng denit rifica ti on in some div e rse weste r n soil s, Soil S ci . Soc. Am. Proc. 27, 659-662. Fir e sto n e, M. K. (19 82) . Bi ol og ica l denit rifica ti on , Agro nomy 22, 289-326. Knowles, R. (1981) . Den itrifica ti on , In Soil Bio c hem sistry (E. A. Paul and KnowlJe.s , NR. . L(1a9d 8d2.) e. dsD.)e .n Vi troilf.i c5a. tDi oen k kine rs,o Nil se, w IYn orAk.d vances in Agricu ltu r al
Mi cr obio l ogy (N. S. Subba Rao, ed.) , pp. 244-266,Butt er wort h. L ondon. Mosie r , A. R., Hutc h in s on, G. L., Sabey, ·B. R., and Bay le r, J. ( 19 82) . Ni tro us oxid e emi ss io n s from barley plo t s tre ate d wi th NH,+, N03- o r sew-ag e sludg e, ]. Envir o n. Qual. 1 1, 78-81 . Payn e , J. W. (1981) . Denit rijica ti on . W ile y, New York. 추가로 읽을 거리 Focht, D. (19 78) . Meth o ds for analys i s of denit rif i ca ti on in soil s , In Ni tro - gen i'n the Envir o nment (D. R. Ni el sen and J. G. MacDonald, eds.) , Vol. 2, pp. 433-490. Academi c Press, New York. Jor dan, C. F. (19 85) . Nutr ien t Cy cl es in Trop ica l Forest Ecosy s te m s. W ile y, New York.
제 10 장 토양으로의 질소 회귀 생물 질소고정 10-1 지구상의 질소 분포와 이동 지구상의 질소는 고체상, 용존상 그리고 기체상의 형태로 널리 분포 한다. 질소는 질량면에서 암석과 광물질의 아주 작은 부분을 차지하지 만, 암권 lit hos p her 러] 있는 암석의 질량이 매우 크기 때문에 지구상 에 있는 총 질소의 98% 가 암권에 존재한다. 생물에 의해 이용 가능 한 질소의 가장 큰 저장소는 대기이다. 대기에는 지구 총 질소의 1. 2% 에 해당하는 양이 존재하지만, 기체 질소는 대기의 79% 를 차지 하며, 전체량은 3. 9X 1021g ( 3.9X109 Tg)이다(표 IO.I). 식물들은 나무의 경우 몇 백년의 기간 동안 질소를 축적할 수 있지 만, 일년생 경작물에서는 계절적으로 순환하기도 한다. 식물에 의해 연간 흡수되는 질소량은 탄소 광합성의 양으로 추정할 수 있다. 지구 상에서 연간 광합성에 의한 탄소 고정량은 70,000T g으로 계산된다. 식물 각 부분에 대한 C/N 비는 일정하지 않다. 그러나 나무, 초목 그리고 작물의 상대적 분포를 고려하여 평균 50 : 1 정도로 추정한다.
그러므로 식물에 의해 흡수되는 질소량은 비교적 정확하게 1400 Tg으 로 추정된다. 식물들은 토양에 있는 가용한 무기 질소의 30-60% 만을 사용하는 것으로 알려져 있다. 지구적인 규모의 토양 무기화 능력은 질소 흡수와 흡수 효율에 관한 지식으로부터 계산할 수 있다. 40% 의 흡수 효율에서 약 3500 Tg 또는 토양 질소량 105 , 000 T g의 3 %에 해당하는 양이 무기화된다. 이 값은 이전에 추정된 대부분의 값보다 더 높은데, 이는 통상 고려하지 않았던 다음의 두 가지 요소가 더 포 함되었기 때문이다. 그것은 첫째, 열대지역에서 질소의 빠른 재무기 화 remi ne rali za ti on 와 둘째 , 미 생 물에 의 한 흡수 또는 질소의 부 동화가 통상 실험실에서 토양을 배양하는 동안에 축적되는 무기 질소량(순 무기화 net m i nera li za ti on) 보다 2-3 배 많다는 사실이다. 표 10. | 전지구적 규모의 질소 함량과 토양을 중심으로 한 유동량 질소 함량 (T g) * 연간 유동량 (T g) 대기 질소 3.9Xl09 토양질소 105,000 무기화된 토양 질소 3500 식물흡수 1400 공생적 질소고정 120 공생적 및 독립생활적 고정 50 질소비료 65 이용된 질소 비료 26 대기로부터 유입 25 탈질화 작용, 휘발 135 지표 유출수에 의한 침식 25 용탈 93 •Terragr am (Tg ) 은 1012 g 또는 백 만 론과 갇다.
공생적 질소고정은 연간 유동량이 120 T g으로 토양의 질소 무기화 (3500 T g)에 비해 상대적으로 낮으나, 고정된 질소가 식물로 직접 이 전되기 때문에 식물의 질소 흡수량의 8.5% 를 차지한다. 질소 비료의 사용은 공생적 고정량의 50% 에 해당되지만, 질소의 흡수 효율이 낮 아서 전지구상의 식물이 흡수하는 질소량의 오직 2% 에 불과하다. 표 10.1 에 나타난 질소의 손실은 탈질화 작용, 휘발, 유수 손실, 침식 그리고 용탈을 포함하고 있다. 이들 과정에 대한 값들은 장소마다 크 게 다르나, 표에서 보듯이 장기적으로 보면 질소의 유입량과 거의 균 형을이룬다. 대기는 NO, N02, N20, HN02 그리고 HN03 등의 기체 산화물 을 포함한다. 이들의 농도는 오염된 지역에서 0.5— 2 p pl}S1 범위로 나타난다. 산업으로 인한 오염에서 멀리 있는 곳(청정지역)에서는 0.1 pp묘다 낮은 농도가 관측된다. 암모니아 가스의 농도는 비교적 균일 하게 분포하여, 2-3 pp bE 기 농도로 지구의 대부분에 걸쳐 나타난다.이 들 기체는 잎 표면과 토양으로 흡수될 수 있다. 토양미생물 또한 N20 와 같은 기체를 흡수하여 이용할 수 있는 것으로 알려져 있다. 성숙된 산림과 초지 같은 비교적 폐쇄적인 생태계는 질소의 손실이 낮고, 내 부 재순환 속도가 높다. 따라서 이들 지역은 의부로부터 필요한 것의 대부분을 대기에서 얻는다. 강우에 의한 암모니아와 질산염의 강하율 dep o sit ion ra t送 이들의 대기중의 농도와 강우량에 좌우된다. 질산염 의 습성 강하 we t de p os iti o~ 오염 지역에서 연간 5kg ha-1 가량이 고, 산업 오염원에서 멀리 떨어진 강우량이 적은 지역에서는 0.5 kg ha-1 이하이다. 암모늄태 질소도 유사한 범위를 나타내며, 산업 지역 에서는 토양으로 연간 5-10 kg ha-1 의 강하율을 나타낸다. 툰드라와 같은 원거리 지역에선 0.5kg h a-1 이하이다. 전지구적인 규모에서 보면 이러한 유입량은 연간 25 T g으로 추정된다.
자연 생태계의 교란은 대기와 지하수로 질소의 주요 손실을 초래한 다. 경작지나 교란된 지역은 더 많은 질소 공급을홋규히게 된다. 질 소 비료의 시비는 전지구적 규모에서는 큰 의미가 없으나 집약 농업의 특정 지역에선 매우 중요한 역할을 한다. 10-2 질소고정 생물 콩과 식물의 유익한 효과는 2000 년 전 이전의, 옛 로마의 저서에서 도 나타나고 있다. 같은 기간의 중국 저자들은· 물개구리밥 Azolla 울 벼농사에 이용하는 것이 유익한 효과가 있음을 또한 기록하고 있다. 서기 540 년에 쓰인 『사람을 먹여 살리는 기술』이란 농업 기술 서적은 논에 물개구리밥을 이용하여 재배하는 내용을 기술하고 있다. 윤작에 사용되는 콩과 식물은 농업에 안정성을 부여하여, 서유럽의 산업화를 가능하게 했다. Hump h rey Davey 경은 1813 년에 최초로 질소가 대기로부터 유래된다는 사실을 제안하였다. 그는 〈콩과 식물 이 밀을 위한 토양을 준비하는 데에 매우 적합한 것 같다〉고 기술했 다. J. B. Bouss i ng aul t는 프랑스의 윤작 연구에서 콩과 식물에 의한 질소고정 원리를 수립하는 몇 개의 논문을 1837 년에서 1842 년에 걸 쳐 발표했다. 1856 년 독일에서 Albert Thaer 는 〈최종 작물과 흰 클 로버의 동시 파종이 최근에 매우 일반적이 되어 가고 있다. 오직 냉담 하고 게으론 농업가 또는 관습과 그들의 의견에 집착한 사람들만이 이 롤 무시하고 있다〉라고 기술했다. 공생적 질소고정에서 뿌리흑의 중요성은 1886 년 Helr i e g el 과 W ilfarth에 의해 기술되었다. 1888 년 Be ij er i nck 는 콩과 식물에 의 한 질소고정에 관여하는 생물을 분리하여, Bacil lu s rad i c i cola 라 명
표 10.2 질소고정에 관련된 생물들과 연합· Ag ro bacte n ·um 대표적 원핵생물의 속명 연합 형태 유기영양 생물 호기성 Azoto b acte r , Beij eri nc kia , Derx ia Xanth o bacte r , Rhiz o biu m 조건적 호기성 Baci llu s, Klebsie l la, Azos pirillu m, Thio b acil lu s 형기성 C/o s tr idiu m , Desulf ovi b r i o, Desulj oto m aculum 유전적 조작 Salmonella, Escheri ch ia , Serratia 독립생활형 시아노박테리아 Nosto c , Tr ich odesmi um 광합성 생물 Anabaena, G/oeoth e ce 자주색 비황세균 Rhcdops e udomonas, Rhodos pirillu m 자주색과 녹색 황세균 Chromati um , Chlorobiu m , Thio c aps a 유기영양 생물 근권 Azos pirillu m, · Azoto b act er, Baci llu s 비뿌리혹 및 영권 K/ebsi e/l a, Beij eri nc kia 뿌리혹 생물 콩과식물 Rhzz o b ium 비콩과식물 Rhiz o biu m 비콩과 식물, 방선균 Frankia 비콩과 식물. Gunnera Nosto c 연합적(공생적) 지의류 Nosto c , Sti gno ne ma,
표 10.2 질소고정에 관련된 생물들과 연합* A.gro bacte n ·um 대표적 원핵생물의 속명 연합 형태 광합성 생 물 Caloth r i. x 우산이끼 Nosto c 이 끼 류 Halosip h on 나자식물 (Cy c as) Nosto c 물개 구리 밥 (Azolla) Anabaena Endocyn o ses ( Ooc yst is ) Nosto c ·자료 : Havelka 등 (1982) 명하였다. 이는 후에 Rh iz ob i um 으로 다시 명명되었다. 비공생적 질 소고정 생물인 Clos tri d iu m 은 1890 년 W i no g radsk y에 의해 분리되 었고, 호기성 생물인 Azo t obac te r 는 1901 년 Be ij er i nck 에 의해 분 리되었다. 따라서 19 세기 말에 거의 모든 주요 질소고정 생물의 특징 이 파악되었다. 다양한 군의 원핵생물들이 질소고정을 담당하는 질소고정 효소를 갖 고 있다. 이들 세균은 현재 2 질소 영양생물 d i azo t ro p h s..£. 불리며 유 기 영양세균, 광합성 황세균 그리고 시아노박테리아(남조류 또는 납세 균이라고 함)를 포함한다(표 10.2). 10-2-1 독립생활형 유기영양 생물 호기성으로 독립생활fr ee- li v i n g을 하며 에너지원으로서 유기물을 이용하는 질소고정 세균은 중성 및 알칼리성 토양에서 발견되는 세균 으로 Azo to ba ct er 가 있다. 이와 유사한 세균인 Beij er i nc kia -2} Derx ia는 넓은 pH 범위에서 나타난다. 특히 열대 지역에서는 산성
토양에서 자주 발견된다. 유전적 분석 결과는 Be ij e ri nc kia가 Azo to bac t er 보다 다른 질소고정 세균인 Azo spiri llum 에 더 유연 관 계가 가까운 것으로 나타났다. 이들 세균은 질소를 고정하는 Klebs i ella 와 마찬가지로 토양과 뿌리의 표면뿐만 아니라 잎의 표면이 나 영초 leaf sheath (ph y ll osph ere) 내의 습한 환경에서 성장함이 발견 된다. Azoto b acte r , Beij eri nc kia 그리고 뿌리혹박테리아 Rh i zo bi um 는 질 소고정에 필요한 광범위한 에너지의 생성을 위해 호기적 조건이 필요 하다. 그러나 다른 질소고정 생물처럼, 이들 생물에서 질소고정 효소 의 활성은 산소에 의해 억제된다. 질소고정 효소를 보호하기 위한 특 수 기작은 세포 내에서 막과 질소고정 복합체의 연합을 포함한다. 점 액물질의 생성과 세포덩어리 형성 또한 보호 기작을 제공한다. 이는 산소가 효소로 확산되는 속도를 감소시킨다. 호기성 질소고정 세균의 다른 특칭은 세포 내의 호흡 수준이 높다는 것이다. 이로써 산소 농도 룰 낮게 유지시켜 Azoto b act er 세포 내의 질소고정 효소가 산소로부 터 보호된다. 또한 산소의 존재하에서 질소고정 효소는 보호가 되더라 도 비질소고정 효소로 전환된다는 사실이 제시되었다. 이러한 변화는 가역적이어서, 세포 내의 산소가 존재하지 않을 때 질소고정 효소는 질소고정 상태로 돌아갈 수 있다. 조건적 미호기성 fac ulta t i ve mi cro aerop hilic 생물인 Klebsi ,el la, Azospi ,rillu m 그리고 Bac i llus 는 Azo t oba cte r 의 경우와 같이 산소로 부터 질소고정 효소가 보호되어야 할 필요가 없는 환경에서 산화적 대 사 경로를 거쳐 ATP 의 형태로 에너지를 생산한다. Clos tri d i um 과 같은 형기성 질소고정 세균과 Desu lfo v i b ri o 나 Desulf oto m aculum 같 은 황산염 환원균 또한 전자공여체로서 유기물을 이용한다. 그러나 이 들 생물의 발효 경로는 유기 중간대사 산물을 축적시키고, 오직 소량
의 에너지가 질소고정으로 이용될 수 있게 한다. 그러나 침수 wat er lo ggi n g와 같은 형기적 환경에서 기질의 이용도가 높은 경우에, 이들 생물은 활발한 질소고정을 한다는 것이 밝혀졌다. 협기적 조건은 기질 의 산화로부터 에너지 퍼텐셜을 낮춘다. 그러나 형기적 조건은 또한 호기성 세균과 곰팡이와 같은 다른 미생물에 의한 이들 기질의 경쟁적 이용을감소시킨다. 독립생활형의 2 질소 영양생물과 영권 ph y ll osph ere 생물에 의해 고 정된 질소의 양은 일반적으로 수 kg ha-1 에 불과하다. 자역적으로 양 이 많지는 않지만 조사된 거의 모든 서식지에서 약간의 질소고정이 나 타났다. 독립생활형의 2 질소 영양생물의 영향은 지구 전체로 볼 때 중요하고, 또한 생장 속도가 낮고 질소의 내부 순환이 상대적으로 크 며 의부의 유입에 대한 요구가 적은 지역에서 중요하다. 10-2-2 독립생활형 광합성 생물 시아노박테리아는 1928 년 Drewes 에 의해 (1 977 년 Fogg ol] 의해 인 용) 질소고정을 하는 것으로 밝혀졌고, 많은 수서 환경에서 출현한 다. 또한 많은 토양의 표면이나 지표 바로 아래에서 발견되며, 특히 침식과 산사태에 의해 새로 노출된 토양에서 발견된다. 남조류는 논, 영양 수준이 적당한 작은 호수 등 많은 수서 지역에서 흔히 발견된다. 이러한 ·지역에서 때때로 대번식을 하여 강력한 효력이 있는 동물성 신 경 독성물질을 생산한다. 남조류는 광합성계 ph oto s ys te m Il 롤 가지 며 산소를 배출하는, 고등식물의 특징적인 광합성 기작을 갖고 있는 유일한 원핵생물이지만, 광도와 산소가 낮은 환경에서도 생존할 수 있 다• 독립생활형의 2 질소 영양적 남조류는 3 가지 형태가 있다. 단세포
남조류인 Gloeo t hece( 전에는 Gloeocaps a . £. 알려짐)는 호기적 토양생물 로 높은 광도에 예민하다. 질소고정 효소가 보호되는 기작은, 죽 효소. 롤 광합성에서 생성된 산소로부터 격리시키는 막에 의해서 보호한다는 점에서 Azo t obac t er 에서 기술된 것과 유사하다. 질소고정 능력은 이형세포 (he t erocy s t s, 그림 10.1) 라고 불리는 특수 화된 세포를 갖고 있는 사상형의 남조류에서 특히 우세하다. 두꺼운 벽으로 된 이형세포는 사상체에서 10-15 세포마다 나타나며, 막과 갇 은 물리적 수단에 의해 산소의 확산을 막아서 질소고정 효소의 산소 피해롤 막는다. 이형세포는 산소를 생성하는 광합성계인 광합성계 II 가 없으므로 좀 더 확실히 보호될 수 있게 한다. Nos t oc 은 이러한 예 로서 많은 초원과 사막의 토양 위에 겉껍질 형태로 나타난다. 그 겉껍 질은 대부분 건조한 상태로 존재하나 잠깐의 비나 또는 아침 이슬에 의해 습해지면 성장하고 질소를 고정할 수 있다. 이들은 칼슘 요구도 높아서 석회질 토양을 선호하며, 인산질 비료나 화재에 의해 생성된 인 같은 무기 인의 첨가에 대해서도 반응을 보인다. 제 3 의 형태적 유 형에는 이형세포가 없는 사상형의 Plecto n ema7} 있다(표 10.3).
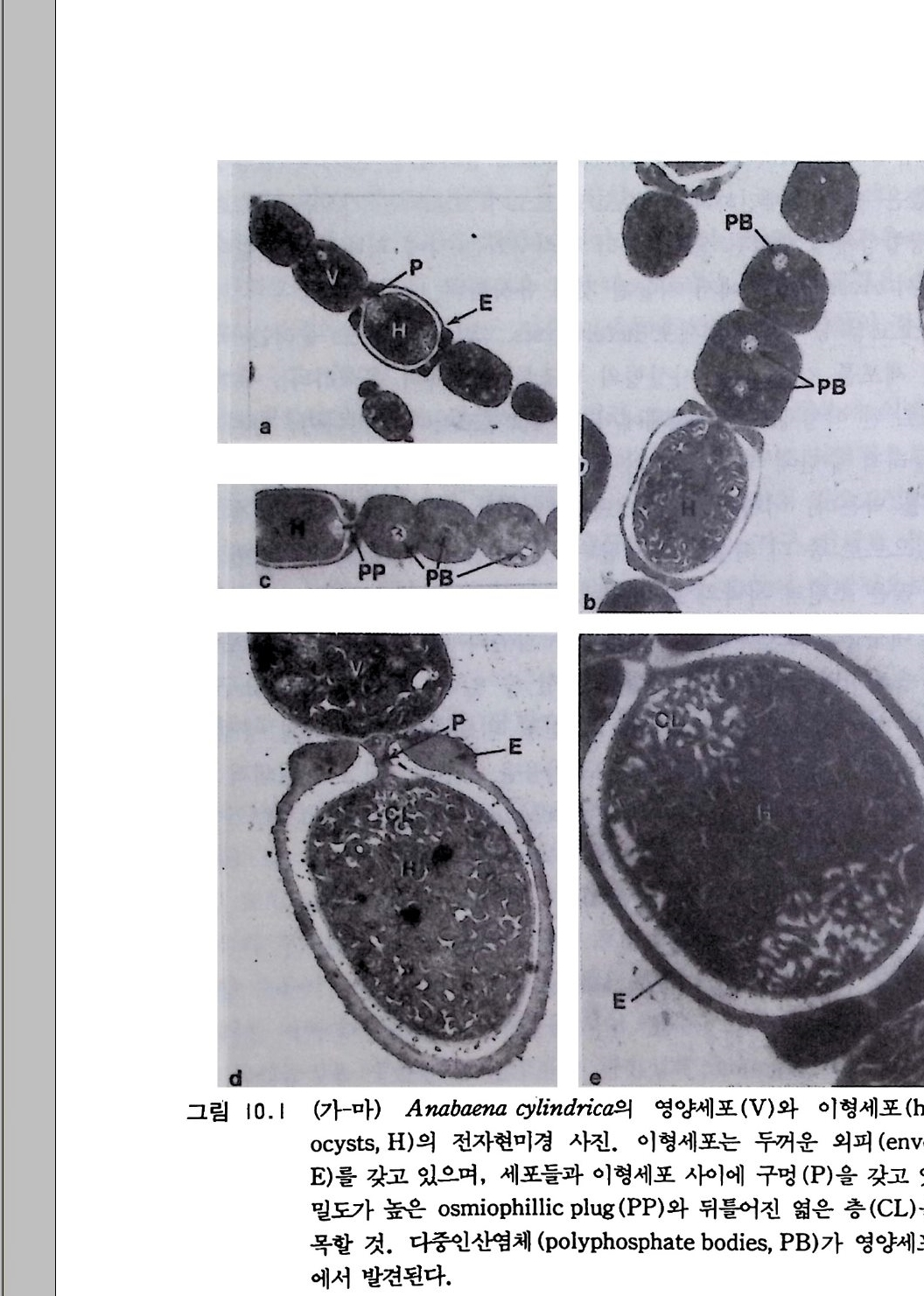 그림 10.1 (가-마) Anabaena 아 l i nd ri• c ~ 영양세포 (V) 와 이형세포 (he t er-
그림 10.1 (가-마) Anabaena 아 l i nd ri• c ~ 영양세포 (V) 와 이형세포 (he t er-
표 10.3 시아노박테리아의 질소고정 질소를 고정하는 목 과 속과종의 수 (괄호안) Chroococcales (약 35 속) Chroococcaceae Gloeoth e ce (1) Osc ill a t or i ales( 약 100 속) Nosto c aceae Anabaena (12) Anabaenops is (1) Ap ha niz o menon (1) Aulori sa (1) Chlorog lo ea (1) Cy li n d rosp e rmum (4) Gloeotr ich ia (1) Nodulari a ( 1) Nosto c (8) Tr ich odesmi um (1) Riv u lari ac eae Caloth r i x (5) Scy ton emata c eae Sc yton ema (2) Tolyp o th r i x (1) Oscil lat o r ia c eae Osci lla to r i a (1) Plecto n ema (I) Schiz o th r i x (1) Sti go nernata l es Sti go ne.m a ta c eae Fis ch erella (2) Hapo l osi ph on (I ) MasHg o cladus (1) Sti go nema (1) Weste l liop s is (1 ) 논은 Anabaena, Gloeot rich ia , 그리고 S cyt one rru.률 포함하는 남 세균에 의한 질소고정이 가장 잘 연구된 곳이다. 이들 생물들은 몇 천
년에 걸쳐 논농사의 장기적 안정에 좋은 영향을 준 것으로 나타났다. 논에서 측정되는 질소고정량은 독립생활형의 유기영양 생물과 독립생 활형의 광합성 생물의 두 그룹에 의한 질소고정을 모두 포함한다. 모 든 질소고정 측정에서처럼, 고정되는 질소 양은 습도, 가용한 영양 염. 그리고 질소고정에 효과적인 기간 등의 환경 조건에 달려있다. 질 소고정량의 추정치는 표 10.4 에서 보듯이 연평균 30k g ha-1 에서 높 게는 70 kg ha..:.1 에 이른다. 남세균 이의의 광합성 질소고정 세균은 해수와 담수의 수생환경에 분포하고 있으며, 물 대신 황화수소와 황이 전자 공여체로 이용된다 (죽 광합성 동안 산소가 배출되지 않는다). 비록 다양한 형태이지만 이들 세균은 슈도모니스목 Pseudomonadales 에 속한다. 이들 세균은 호수 의 침적토와 물의 경계면에서 종종 발견되는데 이곳은 환원된 황 화합 물이 존재하여 산화 환원 전위가 낮게 유지되는 환경이며 빛이 침투될 수 있는 환경이다. 녹색 그리고 자주색 황세균은 전자 공여체로 황화 수소를 이용하며, 빛의 존재하에 이산화탄소를 환원하는 광 무기영양 생물p ho t o lith o t ro p hs 이다. 지주색 비황세균 Rhodo spiri llum 은 광합성 동안 전자 공여체로서 유기 화합물을 이용하며 따라서 광 유기영양생 물p ho t oor g ano t ro p hs 이다. 이들 세균은 유기 화합물을 에너지원으로 이용할 수 있다. 비록 그 광합성은 형기적 상태에서 일어나어: 하지만, 세균은 호기상태에서 종속영양 생물로서 성장할 수 있다. 이들 세균에 의한 질소고정의 기여는 광범위한 대번식이 일어날 때 중요해진다. 10-2-3 초본류와 공생하는 2 질소 영양생물 식물의 표면은 비독립생활형의 2 질소 영양생물의 발달을 위한 탄 소, 습기 그리고 부분적으로 보호된 서식지롤 제공한다. 잎의 표면 혹
은 엽권에는 호기성, 그리고 미호기성 유기 영양 세균과 남조류 등이 있다. 온대에서 가장 흔히 분리되는 형은 Klebsie l la 종이고, Azo to bac te r 와 Be ij e ri nck i a 는 열대식물, 특히 습한 환경에 흔히 존 재한다• 뿌리 부근 또는 근권은 오래전부터 질소 유입이 활발한 곳으로 알려 져 왔다. Dobere i ner 는 c4 식물인 브라질의 풀 Pa spa lum nota t u m 이 Azoto b act er p짝 al i와 함께 성장하면서 상당한 성장과 질소 유입 이 있는 것을 발견하고, 이들의 연합을 강조하였다 (Dobere i ner 와 Day (19 75)). 전에 기술되었던 2 질소 영양생물의 나선균을 재발견하고, 나중에 Azo spiri llum 으로 이름울 바꾸었다. Azosp i,ri llum ! 의 두 종 은 다양한 범위의 식물 숙주에 연합되어 있다. 죽 염습지 salt marsh 의 풀인 스파르티나 spa rtin a , 사팅수수, 수수, 옥수수, 기장 그리고 밀 등에 연합되어 있다. 질소고정 세균은 뿌리 주변의 근권에서 성장하며(그림 10. 2) , 뿌리 의 피충에 침입한다. 질소고정률은 고지의 초본류에서 0-20 kg ha-1 y ear-1 에 달하는데, 아마도 벼에서는 이보다 더 높을 것이다. 이들 2 질소 영양생물은 뿌리의 성장에 영향을 주는 성장호르몬을 또한 생성 한다. 식물 성장에 대한 이들 세균의 기여는 그 연합에 이들 세균이 제공하는 고정된 질소 이의의 다른 기작에 부분적으로 기인하는 듯하 다. 호기성 조건에서 초본류와의 공생에서 나타난 질소고정의 변이의 일부분은 2 질소 영양생물인 Azo spiri llum 과 VA 근균 (ves i cular -arbuscular my c orrhiz a l f un gi)인 Glomus 가 식물 탄소에 대해 경쟁 한다는 관찰에 의해 설명될 수 있을 것이다 . 질고고정은 Glomus 에 의한 감염 정도가 높은 식물에서 낮아지는 것으로 증명되었다. 높은 수준의 토양 인은 균근을 억제하며, 따라서 초본류와 연합된 질소고정 을강화할수있다.
 그림 |0.2 콩(위, Pa triqui n(1982)) 과 기장(아래, F. Dazz d-S기 사진)의 뿌리
그림 |0.2 콩(위, Pa triqui n(1982)) 과 기장(아래, F. Dazz d-S기 사진)의 뿌리
10-2-4 콩과 식물 콩과 식물은 700 속 14 , 000 종의 식물들로 이루어진 식물군이다. 뿌 리흑의 존재와 질소고정은 이들 식물의 상당한 수에서 연구되지 않은 상태이며, 특히 열대림에서 그러하다. 250X l06ha 정도의 토지에서 자라고 있는 농업적으로 중요한 100 여 수종의 콩과 식물이 생물학적 질소고정의 상당한 부분을: 차지한다(표 10.4). 표 10 . 4 에 나타난 140 kg ha-1 yea r- 1 의 추정치는 평균치로서 너무 높은 것으로 비평받아왔 다 . 뉴질랜드의 경우처럼 어떤 지역에서는 800 kg ha-i y ear-1 를 고 정하기도 하지만, 많은 콩과 식물은 건조한 토양에서 성장하며 무시할 만한 고정률을 나타낸다. 게다가 유럽의 콩과 작물의 상당한 부분은 표 10.4 다양한 토지의 이용 형태별 질소고정량* 질소 토지 이용 ha ( X l06) 고정 (kg ha-1 ye ar-1) Tg 콩과식물 250 140 35 벼 135 30 4 기타작물 1,015 5 5 영구 목초지, 초원 3,000 15 45 산림 4,100 10 40 휴경지 4,900 2 10 얼음으로 덮인 토지 」 。。 육상총계 14,900 139 해양 發 1 36 51,000 175 ·자료 ; Burn~ Hardy (l 975)
바료 형태로서 고정된 질소를 받고 있다. 콩이나 땅콩 같은 곡류 콩과 식물은 알팔파 같은 사료용 콩과 식물보다 훨씬 낮은 고정률을 가지는 것으로 알려져 있다. 곡류 콩과 식물은 총 질소 요구의 적어도 50% 가량을 토양 질소에 의존한다. 표 10.5 에 농업적으로 중요한 콩과 식물과 공생하는 2 질소 영양생 물이 열거되어 있다. 느리게 성장하는 Bradyr hiz o biu m lup i n i와 B. j ap on i cum 은 광범위한 숙주에 걸쳐서 접종되는 뿌리혹박테리아의 혼 합군인 광저기군(群)과 같은 분류군에 포함되어 있다. 성장률과 같은 특징뿐만 아니라 디론 특성들은, 즉 단수화물로부터 산의 생성 특성 은, 빠르게 성장하는 뿌리혹박테리아와 느리게 성장하는 뿌리혹박태 리아를 구별한다. 콩과 식물과 연합하는- 공생 세균의 분류는 현재 변 화하고 있다. 혈청학, 핵산, 유사성 그리고 염색체상 유전자의 유전 적 표지와 같은 전단학적 특징들이 표 10.5 에 나타난 균주들의 분류 에 이용된다. 이들 균주둘은 열대의 나무에서 발견된 균주처럼 뿌리혹 박테리아의 많은 종류를 포함하지 않으며, 이들 균주들은 유전적 관접 에서 볼 때 가장 적당한 대표 종도 아니다. 그러나 이러한 분류는 종 균 생산과 같은 목적에 유용하다. 비콩과의 관목인 Para sp on i a 는(종전엔 Trem a.5.료 알려짐) 느릅나무과 Ulmacea 려 속하며 공생 능력이 있는 Brady rh iz ob i um 과 뿌리혹을 만드는 것으로 알려졌다. 이는 이렇게 중요한 2 질소 영양생물이 다른 식물과도 공생을 할 가능성을 제시하는 것이다. 다른 홍미로운 관계들 도 발견되었다. 토양의 질산영태-질소는 뿌리흑의 생성을 억제하며 질소고정 효소의 생성을 억제한다. 질산염 환원효소가 없는 콩과 땅콩 의 품종이 분리되었다. 이들은 질산염이 있어도 질소를 고정할 수 있 다. 그러나 그러한 숙주들은 성장 능력이 일반적으로 저조함이 밝혀졌 다. 다른 콩과 식물인 Sesbania ros t ra ta는 뿌리와 줄기에 모두 뿌리
표 10.5 농업적으로 중요한 콩과 식물에 공생하는 세균의 분류· 주분류 종 숙주식물 빠른성장 Rhiz o biu m melilo ti Medic a g o (알 팔 파) , Melil o t us , Trig o nella trifoli i Trifo li u m (클 로 버 ) leg u mi no sarum Pis u m (완 두 콩) Vicia, Lath y ru s ph aseoli Phaseolus (콩) 느린 성장 Bradyr h iz o biu m lup ini Lup inu s, Lotu s jap o nic u m Gly c i ne( 대두), 일부 광저기 spp . cow pe a ’’ Vig na( 광저기), 그의 pa ras j)o nia e Paras po nia , 광저 기 , 그의 ·자료 : Ber g e y의 Manual of Dete rm i na ti ve Bacte r i olo gy 제 9 판 0983) 혹을 생성하는 능력이 있다. 이는 뿌리혹이 발달하지 않는 습한 조건 에서 식물이 생장하는 경우에도 질소롤 고정할 수 있게 한다. 뿐만 아 니라 줄기 위의 뿌리혹은 뿌리가 토양에서 질산염을 흡수해도 질소를 고정하는 능력이 있는 것을 시사한다. 생물공학적 기술은 광범위한 환경 조건에서 토양에 무기 질소가 있 어도 높은 질소고정 능력을 가전 새로운 식물과 미생물의 연합을 만들 것으로 기대된다. 현재 적절한 질소고정 잠재력이 없는 콩과 식물(예 로서 pea s, dry beans 및 soy b eans) 은 앞으로 개 량되어야 한다. 10-3 방선균근 연합 방선균인 Frank ia는 7 목, 8 과, 17 속에 속하는 170 종의 식물과 연합하여 뿌리혹을 형성한다(표 10.6). 세계적으로 널리 분포하고 있
는 다년생 목본 관목과 교목들은 콩과 식물이 농업에 중요한 만큼 야 지와 산림에서 중요하다. Frank i a 에 대해 가장 잘 알려진 연합은 오 리나무류의 오리나무속 Alnus 형의 뿌리혹이다. 이는 대생 (對生) 분기 (分支)의 산호초형 뿌리혹이 특칭이다(그림 10. 3) . 이들 뿌리혹은 분 홍색이다. 그러나 이 색깔은, 뿌리혹박테리아의 뿌리혹처럼 산소 조 절 단백질인 근립 (根粒) 헤모글로빈 le g hemo g lob i n 에 의해 생성되는 것이 아니고, 안토시아닌 색소 때문이다. Frank i a 에 의해 발달되는 다른 주요 뿌리혹 구조는 소귀나무속구누마황속 My ri ca-Casua ri na 형의 뿌리혹에서 발견되는 것이다. 각 뿌리흑의 정단에서 위로 성장하는 뿌 리가 나와서 뿌리혹 덩어리는 위로 자라는 뿌리로 덮여 있다(그림 10.3). 이러한 상향성 성장 형태는, 종종 이러한 식물둘이 자라는 토 양 습도가 높은 조건에서 나타나는 · 낮은 산소압 조전에서, 대기로부터 질소고정 내생생물 endo p h yte 로 기체의 이동을 촉진시킨다. 방선균 질소고정은 극지에서 열대, 그리고 준사막에서 열대우림에 이르기까지 발견된다. 이러한 사실은 2 kg ha··1 yea r- 1 에서 300 kg ha-1 y ea r- 1 에 걸친 질소고정의 추정에서 반영된다(표 10.6). 목본 수 종인 목마황은 • 열대 기후에 특별한 적응력을 갖고 있으며 , 많은 열 대 지역에서 중요한 연료식물이다• 일반적으로- 늪과 같은 환경에서 발 견되는 소귀나무는 산사태 지역, 침식된 경사지 그리고 북미의 동부 해안의 폐광 쓰레기장에 혼하다. 오리나무는 크기가 관목에서 큰 교목에 이른다. 오리나무는 하천 둑 이나 미국의 태평양 북서부 같은 비가 많은 환경에서 자라는 경향이 있으며, 질소고정량은 연간 300 kg ha-1 에 달하는 것으로 보고되었 다. 일반적으로 오리나무 주변의 토양은 유기물 함량이 높고, 연중 어 떤 시기엔 또한 높은 수준의 질산염을 발달시킨다. 오리나무에서의 질 소고정은 높은 생산력을 가전 콩과 식물 밭의 경우처럼 토양의 산성화
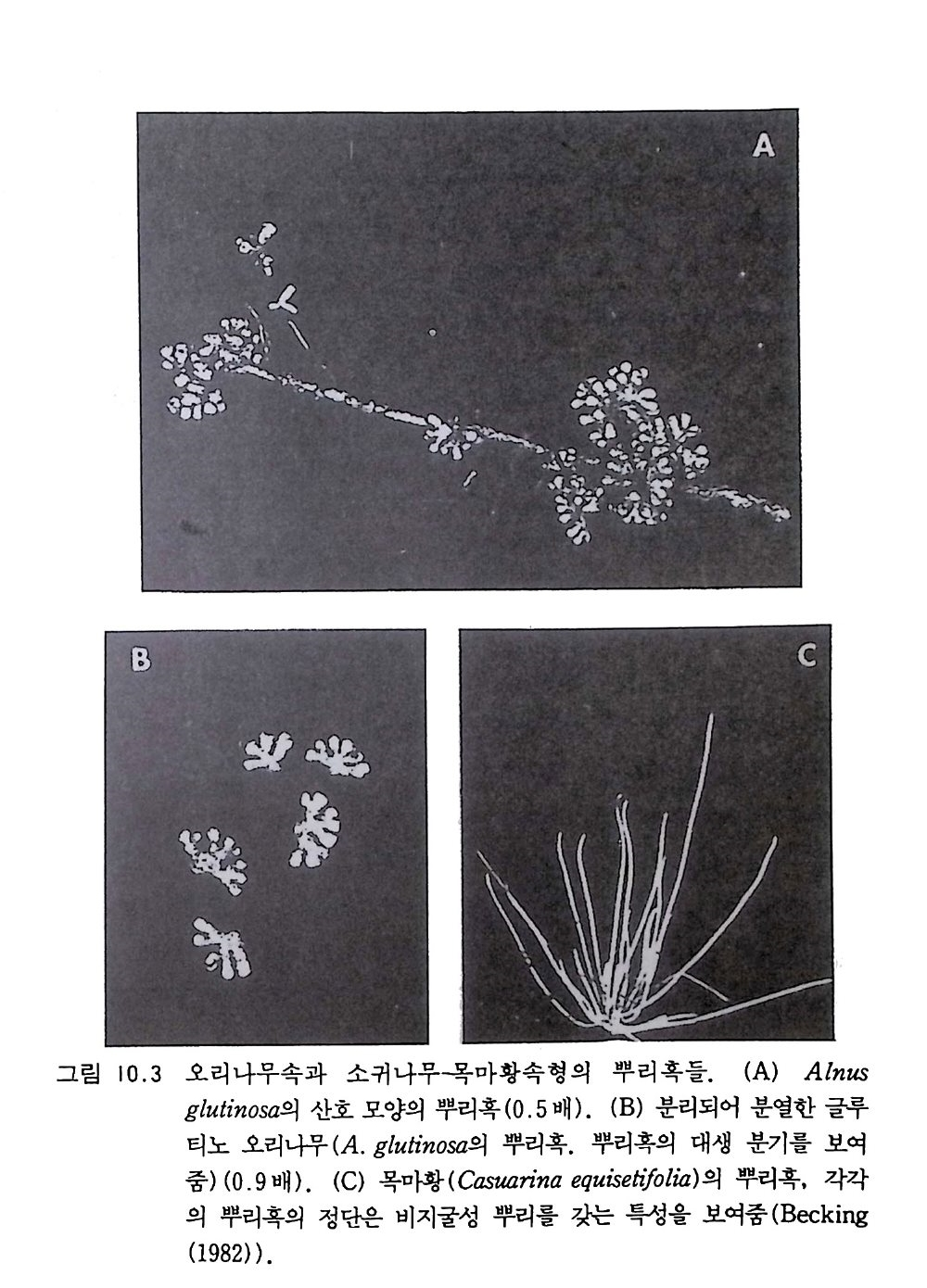 A
A
표 IO.6 Frank ia와 공생하며 2 질소고정울 하는 비콩과 식물인 피자식물의 분류* 목 과 속 형성$멉:譜 수 I겁k g h닳 a - ' y'\e~ aJr>’l) Casuari na les Casuari na ceae Casuari na 24 (45) 230 My ri c a les My rica ceae My rica 26 (35) 3-25 Comp ton ia 1 (1) 26-30 Fag al es Betu l aceae A/nus 33 (35) 26-300 Eleagn a ceae Ele agn us 16 (45) 15 Hip pop h ae 1 (3) 2-1 8 0 ShePherdia 3 (3) 60 Rhamnales Rhamnaceae Ceanoth u s 31 (55) Disca ri a 6 (IO) Colletia 3 (17) Trevoa 1 (6) Cori ar i ai e s Cori ar i ac eae Cori aria 13 (15 ) Rosales Rosaceae Rubus . 1 (250) Dryas 3 (4) 18-60 Pu~hia 2 (2) Cercocarj) us 4 (20) Cucurbit ale s Dati sc aceae Datis ca 2 (2) ·자료 : Beckin g ( 1982) 를 초래한다. 이러한 산도는 질소고정 과정과 그에 따른 더 높은 질소 무기물화의 간접적인 효과이다. 그러므로 오리나무를- 지지하는 토양 은 산성비에 의해 생성된 토양처럼 산성의 영향을 연구하기에 좋은 지 역이다. 질소고정이 있는 경작토가 완충 효과가 크지 않을 경우 석회 석에 의한 pH 조절이 필요하다.
관목인 Sh ep herd i a 와 보리나무속 Ele ag nus 은 북미의 대평원에서 널리 서식한다. 이 식물들은 또한 활발한 식생 (植生) 재생 지역에서 광범위하게 발견된다. 그 같은 지역은 알래스카에서 빙하가 물러감에 따라 생성된 새로운 토양과 그리고 폐광지의 식생 재생 토양에서 발견 된다. 현재 북미의 초원에는 콩과 식물이 광범위하게 분포하고 있지 않다. 현재의 이들 토양에 존재하는 질소가 다량 누적되는 과정에서, 방선균근 관목들이 과거에 주요한 역할을 한 것으로 추측할 수 있다. 장미과의 100 속 중 3 속은 뿌리혹을 형성할 능력이 있다. 이 속들 은 Dr yas , Purshia 그리고 Cercoca ,rp us 이다. D ry as 는 뿌리혹을 형 성하는 알래스카와 유라시아 지역의 키 작은 관목이고, 반면에 Purshia tri den ta 는 미국 서부의 건조지역에서 중요한 목초 식물이 다. Ceano t hus 는 미국 서부의 혼효림 지역과 지중해성 초원에서 채 퍼랠 cha p arra 트 알려진 화형 (火形) 관목 연합의 우세한 질소고정 관 목이다. Ceano t hus 는 고정된 질소의 상당량을 재식재한 나무에 제공 할 수 있지만, 가용한 물에 대해서 재식재한 나무와 경쟁을 할 수도 있다. 남세 균인 Nos to c 은 쌍자영 식물인 Gunnera 와 연합할 때 유기영양 생물로서 작용한다. 이는 Nos t oc 에 의해 침입된 줄기 조직의 형태적 적응의 결과에 기인하며, 뿌리혹 또는 뿌리 선(線)이 생성된다. Gunnera 속은 풀에서부터 1. 5 m 길이의 억센 관목을 포함한다. 이 식물들은 남미, 뉴질랜드, 동남아시아, 아프리카의 습한 환경에서 산 다. 뿌리선 내의 Nos to c 은 독립생활형의 Nos to c 보다 더 많은 이형세 포를 갖는다. 방사성 동위원소로 표지된 이산화탄소가 Nosto c 선으로 전입됨이 없이 질소의 고정이 있다는 사실은 Nos t oc 이 이러한 공생에 서 유기영양 생물임을 짐작하게 하였다. 질소의 고정량은 연간 10-72 kg ha-1 범위이다.
10-4 광합성적 연합 진균류와 조류의 공생이 지의류를 형성한다. 그러한 공생적 연합은 분류학적인 실체로서 인식되었다. 질소를 고정하는 지의류는 광합성 공생자p hy cob i on t.£.서 남세균을 갖고 있다. 납세균은 영양영과 물리 적 보호를 얻고, 반면에 공생하는진균류 m y cob i on t는 광합성 공생자 로부터 탄소와 질소를 얻는다• 이러한 질소고정 지의류는 표 10 . 7 에 나타나 있다. 많은 지의류의 연간 성장은 1 mm 정도이다. Pelt ige ra 같이 성장이 더욱 빠른 것은 연간 2-3 cm 의 증가를 보인다. Pe ltig era 는 극지에 널리 분포하며 다른 질소의 유입이 적은 이 지역 에선 특히 중요하다. 암석의 초기 풍화와 새로 노출된 지표위의 식생 형성에 있어서 산을 생성하는 지의류가 미치는 영향은 또한 주목할 가 치가 있다. 논과 배수 웅덩이같이 조용한 물의 표면에 부유하는 물개구리밥은 전세계에 걸쳐 분포한다. 물개구리밥은 열대에 가장 많으며, 바랑에 의해 교란되지 않으면 두꺼운 담요 두께로 자란다. 4 개의 동정된 식 물 숙주는 이형세포가 있는 납세균 Anabaena 를 포함하며, 이 남세균 표 |0.7 대표적 질소고정 이끼류* 이끼류 시아노박테리아 이끼류 시아노박테리아 Collema Nosto c Ne j)h roma Nosto c Dendri sc ocaulon Sc yton ema Peltig e ra Nosto c Ep he ba Sti go nema Solori na Nosto c Le po g ium Nosto c Ste r eocaulon Nosto c Li ch in a Caloth r i x Sti cta Nosto c Lobari a Nosto c Placy nthi u m Di.ch oth r i x ·자료 ; Mi llba nk (1977)
은 물개구리밥에게 총 질소 요구량의 큰 부분을 공급할· 수 있다. Anabaena 필라멘트는 물개구리밥의 여러 갈래로 이루어진 부유 줄 기의 하부표면 ventr a l surfa c e 내의 공간을 차지한다(그림 10.4). 질 소고정은 물에서 많은 양의 용존· 철과 인을 요구한다. 물개구리밥의 뿌리는 바닥의 퇴적물에 거의 닿지 않는다. 또한 Azolla-Anabaena
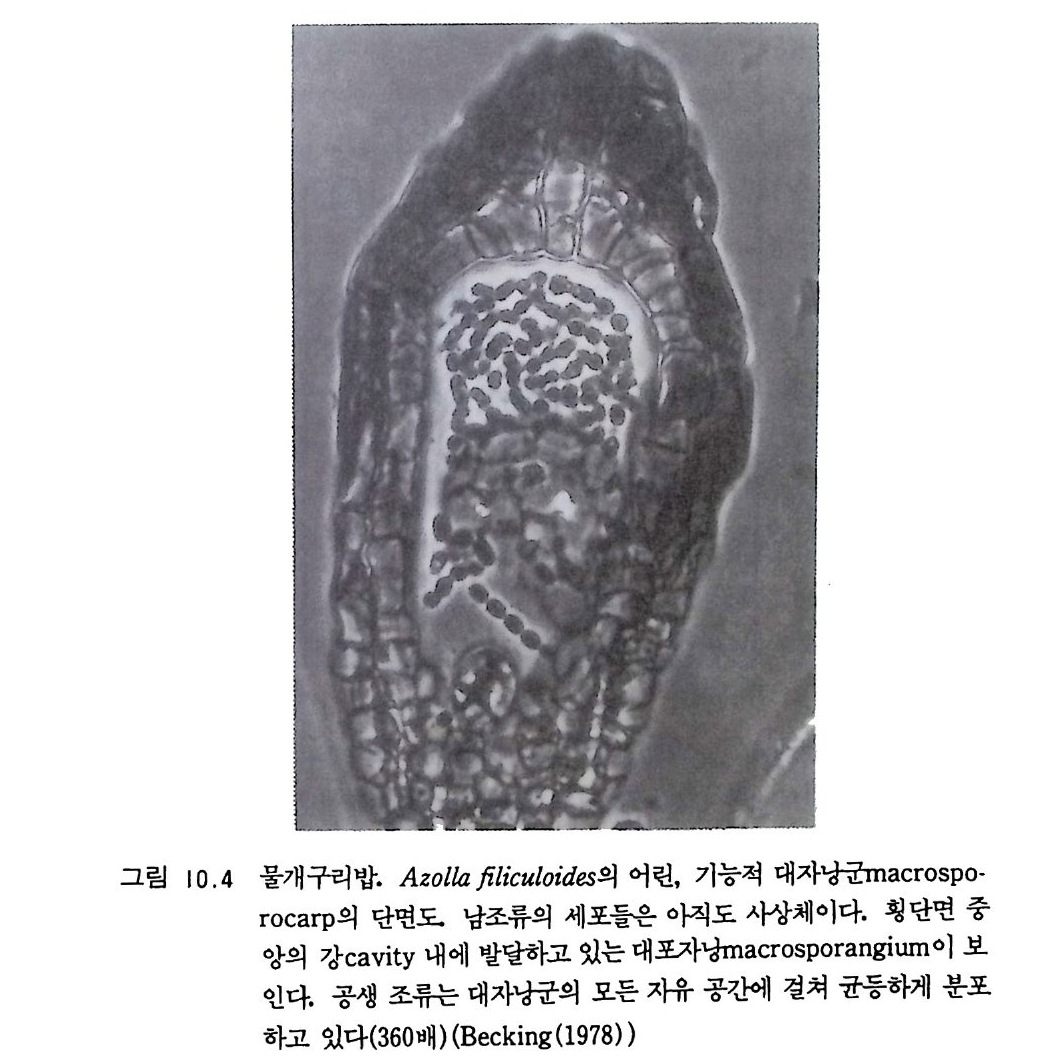 그림 10.4 물개구리밥. Azolla fi l ic ulo i des 의 어린, 기능적 대자낭i!lll acros p o
그림 10.4 물개구리밥. Azolla fi l ic ulo i des 의 어린, 기능적 대자낭i!lll acros p o
복합체 또한 많은 수의 무척추동물에 의해 포식당하며, 최적의 질소고 정은 이들 포식자에 대한 조절이 이루어질 경우 가능해진다. 벼의 일 모직에서 100k g ha-1 의 질소 유입이 있음이 발견되었다. 그리고 330 kg ha-1 의 질소 고정이 222 일의 성장 기간에 걸쳐 발견되었다. Anabaena는 고정된 질소의 50% 를 용존 암모늄으로 배출한다. 물개
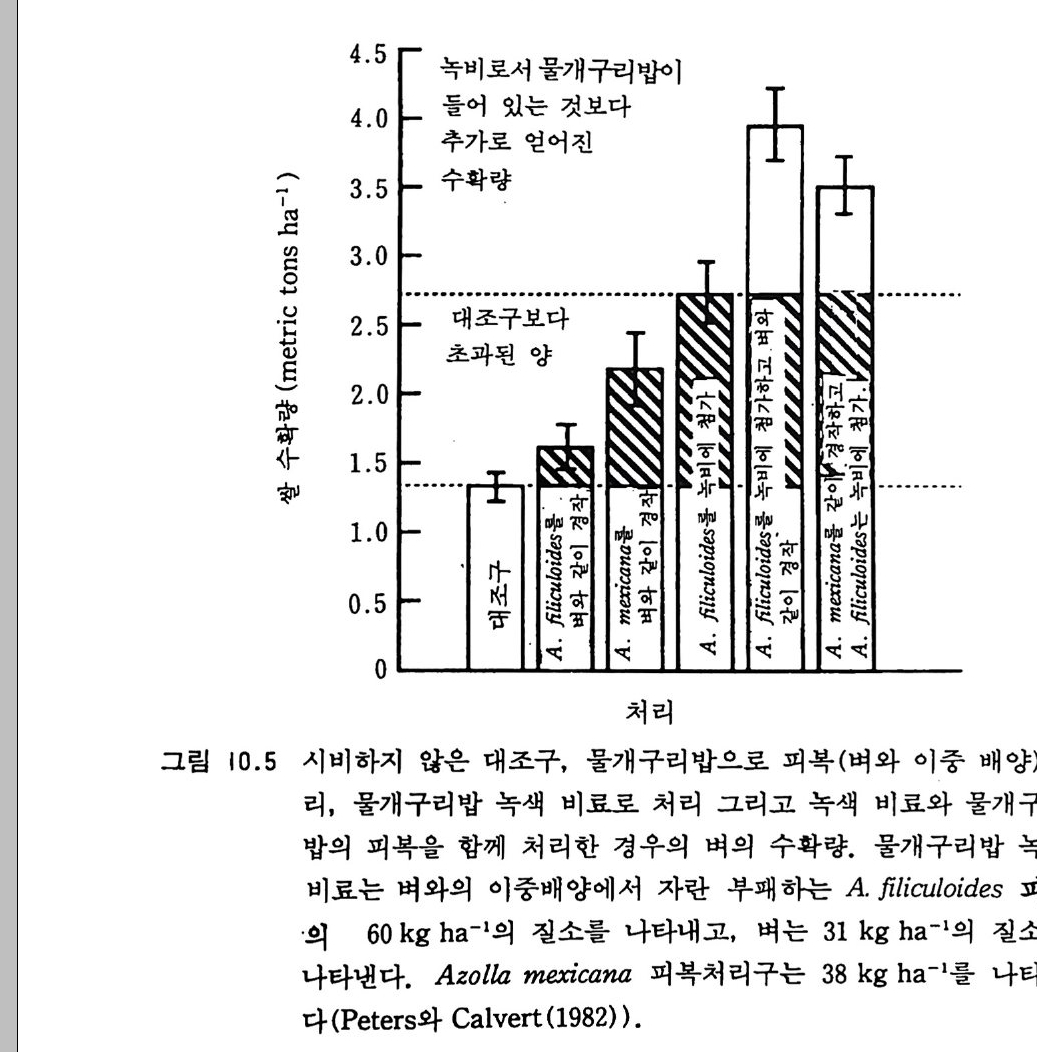 4.54.0녹.3비5.로3서0 물 개 구리밥이
4.54.0녹.3비5.로3서0 물 개 구리밥이
구리밥은 수표면 덮개로서 벼와 함께 성장할 수 있거나 또는 논에 벼 가 없는 동안 녹색 퇴비 직물로서 성장할 수 있다. 북부 베트남 논의 약 40% 가 이들 두 시스템 중 하나를 이용한다(그림 10.5). 물개구리 밥이 없는 벼의 수확(대조구)은 1. 3 돈이었다. 물개구리밥을 녹색 퇴 비로서 이용시 2 배로 증산되었다. 또 다른 1. 3 톤의 증산이 이전에 녹색 시비된 논에 물개구리밥 재접종(죽, 수표면 덮개 처리)하여 벼와 함께 경작될 때 이루어졌다. 물개구리밥 사용의 제한 요소는 접종시에 요구되는 노동력이다. 물개구리밥은 번식되어, 운반되어야 하고, 저 장시에는 영양체 상태로 유지되어야 한다. 접종 방법, 물 속의 철과 인의 공급 유지, 병충해 방지, 포자 형성을 유도하는 기작에 대해 더 많은연구가필요하다. 10-5 뿌리혹 형성과 콩과 식물에서의 질소고정 콩과 식물과 뿌리혹박테리아의 공생관계 설정은 두 공생체의 상호작 용으로 이루어전다. 뿌리혹박테리아는 뿌리 표면으로 유인되어, 왕성 하게 번식하며, 상호보완적 거대분자들의 상호작용을 포함하는 특수 한 기작에 의해 뿌리 세포로 부착된다. 이 거대분자는 콩과 식물의 뿌 리 위에 존재하며 렉틴 lec ti n 이라 부르는 당단백질g l ycop ro t e in.£. 구성 되어 있다. 적합한 뿌리혹 공생 세균은 식물의 렉틴과 선택적으로 상 호작용하는 산성 다당류를 세포 의로 분비한다 (Na t u ri떠 l 1990 년 발표 된 보고에 의하면 황산염기와 지방산이 결합된 형태의 사당류t e t rasac charid e 7} 규명되었음 : 옮긴이). 식물에서 세균으로 그리고 세균에서 식물로의 양 방향으로 정보의 전달이 있다(그립 10.6). 이는 뿌리혹 생성과 연합된 숙주-세균간의 특이성의 일부를· 설명해 준다.
뿌리혹박테리아에 대한 뿌리털의 초기 반응으로 종종 뿌리털 끝이 목자의 지팡이처럼 심하게 구부러진다. 효소 작용에 의해 뿌리털의 세 포벽이 용해되어 감염사가 생성된다. 그리고 식물은 새로운 물질을 합 성하여 침입한 뿌리혹박테리아를 감싸게 된다. 식물의 세포핵이 감염 사의 내부성장을 조절한다. 뿌리털 세포의 기저로의 도달은 감염 후 통상 48 시간이 걸린다. Brady rh iz ob i um 속에 속하는 광저기군의 세균은, 온대지역의 콩과 식물에서 흔히 나타나는 특이성이 없이, 광범위한 콩과 식물(다수가 열대성)과 뿌리혹을 형성한다. 이 세균은 뿌리털이 출현하는 자리에 형성된 툼을 통해 침입한다. 상피세포로 세균의 방출은-감염사로부터이든지 또는 세포간 공 간의 직접적인 침입을 통한 것이든지――-숙주 세포 내에서 세균의 빠 른 번식이 따르게 된다. 세포 내의 세균은 간상(棒狀) 구조를 잃게 되 며 다형태성의 클럽 모양의 세균이 된다(그립 10.7). 세균은 또한 질 소고정에 요구되는 효소 복합체를 발생시킨다. 이러한 형의 세균은 박 테로이드 bac t ero i d 라고 불린다. 활성의 뿌리혹은 숙주 세포의 조직과 세균이 대략 비슷한 양으로 조성되어 있으며, 뿌리 세포당 10,000 개 까지의 박데로이드가 발견될 수 있다. 뿌리혹은 식물의 막 외피 membrane envelo p e 예 의해 구획화되어 있다. 박테로이드는 질소고정에 필요한 높은 수준의 ATP 생성을 위 해 산소를 필요로 하지만, 질소고정 효소는 산소에 지극히 쉽게 손상 받는다. 뿌리혹 조직 내의 산소의 수준은 혈액의 헤모글로빈과 유사한 핑크색의 철-헴 단백질 iro n-heme p ro t e i n 에 의해 조절된다. 이 단백 질은 근립 헤모글로빈이라고 불린다. 비콩과 식물인 Paras po ni ~ 뿌 리혹과 방선균근 관목의 뿌리혹은 근립 헤모글로빈을 갖고 있지 않다. 이 경우에 산소 조절기작은 아직 명확히 밝혀지지 않고 있다.
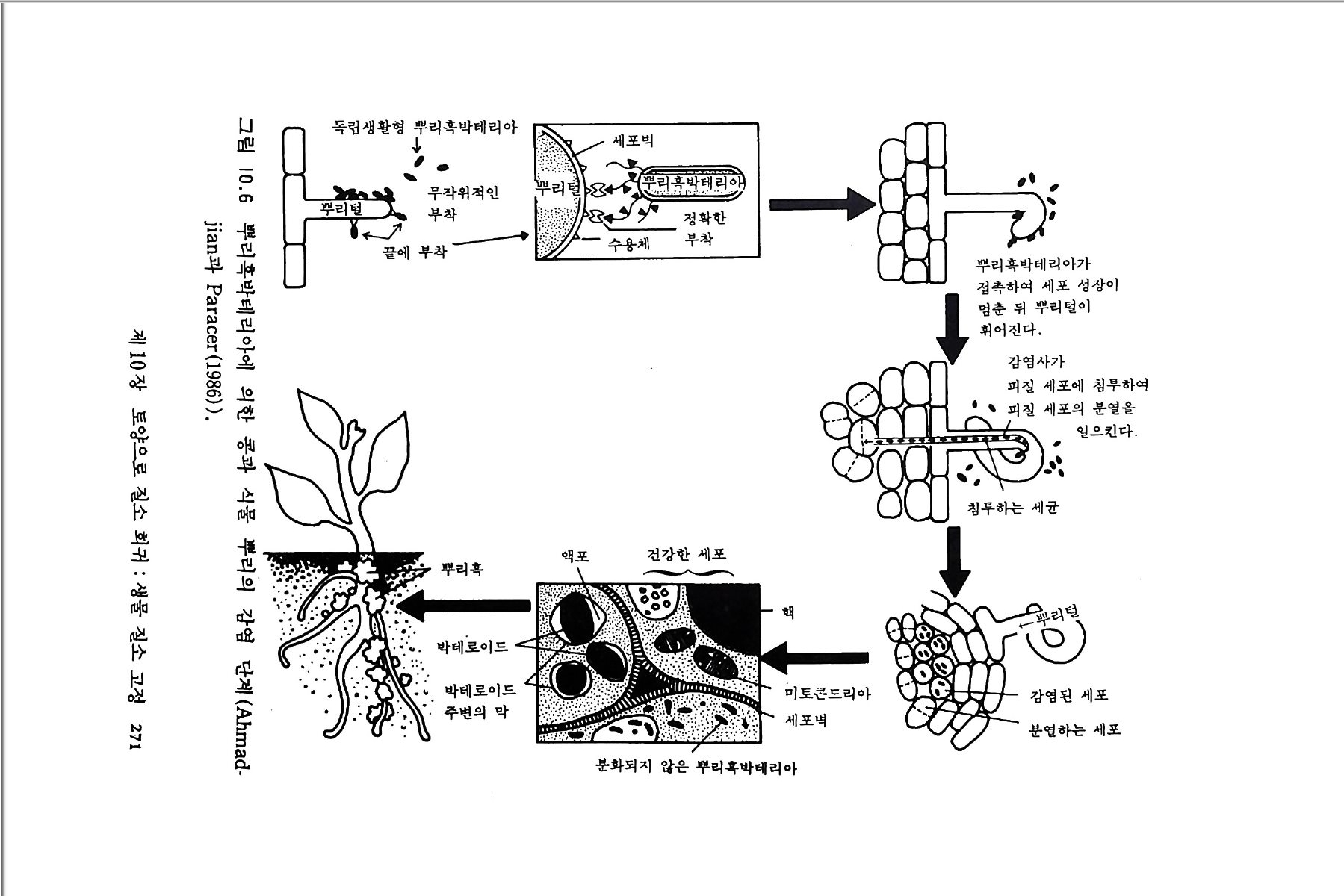
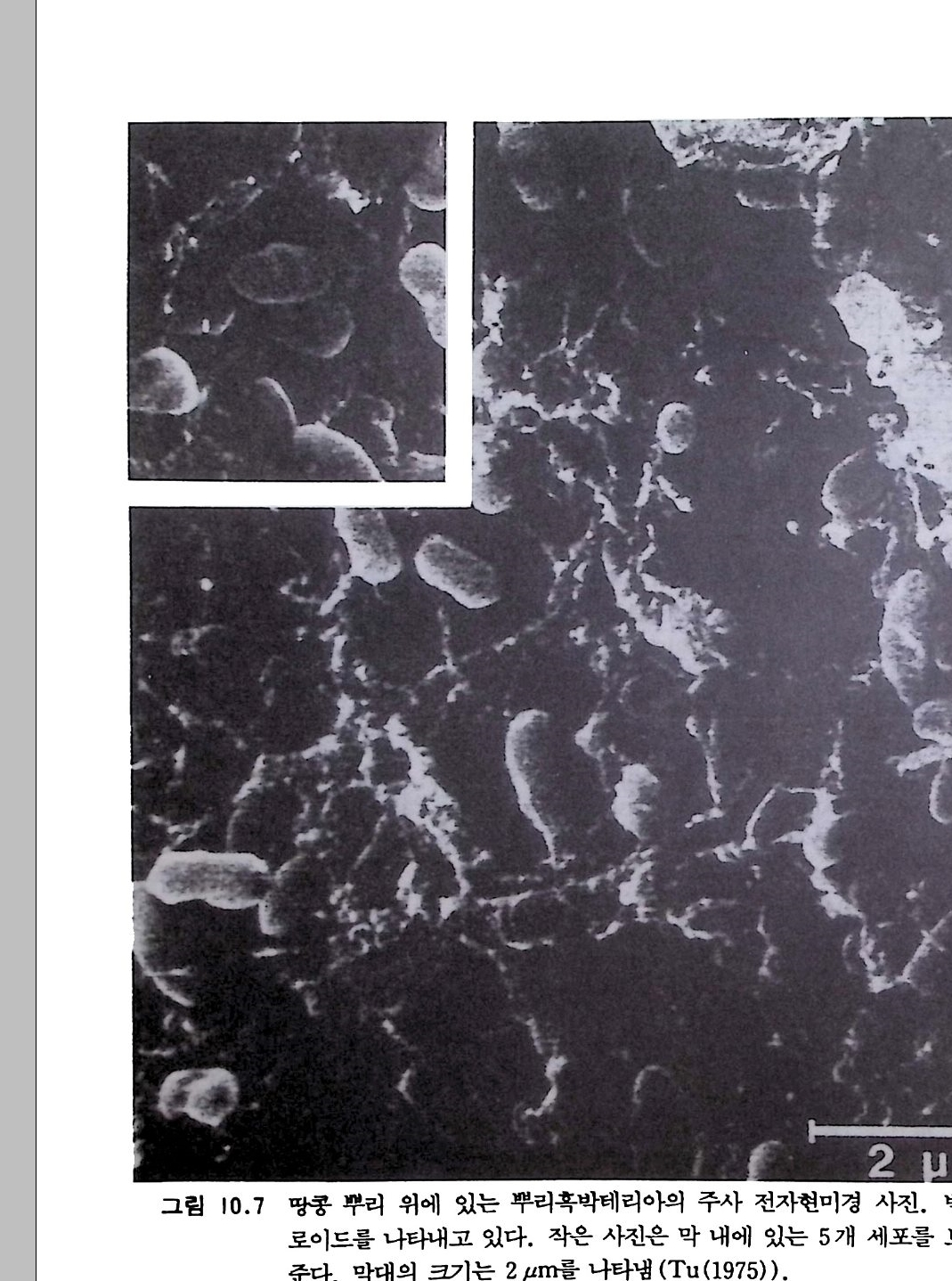 그림 10.7 땅콩 뿌리 위에 있는 뿌리혹박테리아의 주사 전자현미경 사전. 박테
그림 10.7 땅콩 뿌리 위에 있는 뿌리혹박테리아의 주사 전자현미경 사전. 박테
10-6 질소고정의 생화학 질소고정 기작은 질소고정을 하는 대부분의 원핵생물들 내에서 아주 유사하게 나타난다. 질소고정 효소 복합체는 2 개의 철-황 단백질i ron -sulfu r p ro t e i~료 구성되어 있다. 이들 중 하나는 분자량이 60,000 인 철 단백질이다. 이 단백질은 정방형 구조로 4 개의 철과 4 개의 반응 하기 쉬운 황을 포함한다. 분광학적 증거는 철 단백질 내에서 4 개의 철과 4 개의 황 덩어리가 2 가와 3 가의 산화상태 사이에서 작용함을 제시하고 있다. 두번째의 철_황 단백질은 크기가 더 커서 분자당 28_32 개의 철과 28 개의 반응하기 쉬운 황 그리고 2 개의 몰리브덴 원 자를 포함하고 있다. 이 Mo-Fe-S 단백질 분자의 분자량은 200 , 000 에서 300,000 이다. 질소고정 효소가 작용하기 위해선 두 가지의 단 백질이 모두 존재해야만 한다. 이 두 단백질이 질소 기체를 암모니아 로 환원하는 반응을 촉매한다. 또한 이 두 단백질은 아세틸렌을 에틸 렌으로 환원시키며 수소이온을 수소로 환원시키며, 또한 표 10.8 에 표 10.8 질소고정 효소가 관여하는 반응* 이름 분자식 생성물 질소 N=N NH3+H2 아세틸렌 HC=CH H2C=CH2 시아나이드 [C=NJ - CH,+NH3 Allene H2C=C=CH2 H3C-CH=CH2 CAyz aidn eo g e n NN==CN+ --CN= N NCH2+. NH3+N2H. 0R 산화질소 N=N-0 N2+NH3 수소 °l 온 [HJ + H2 ·자료 : Postg a te ( 1982)
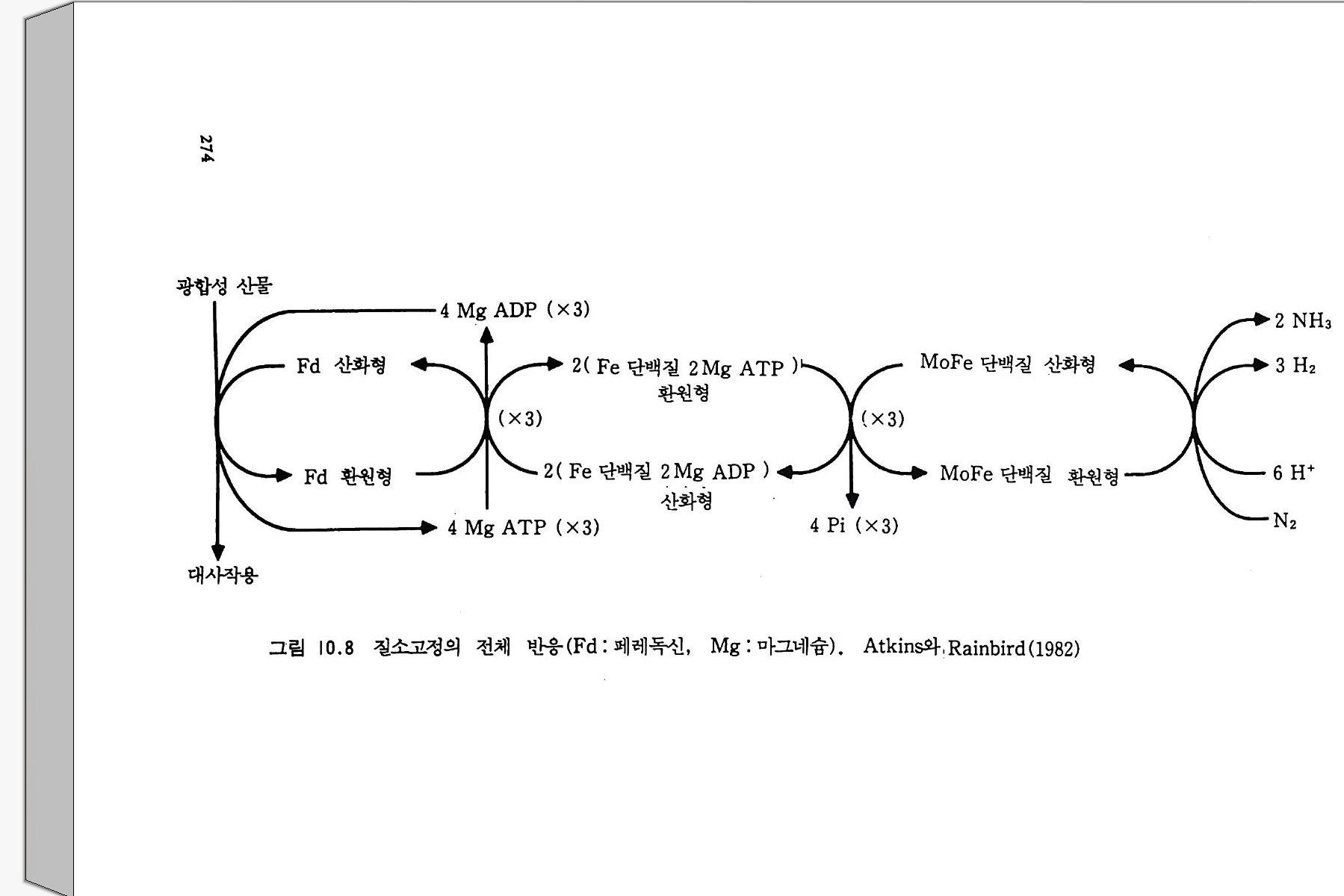 e o ai
e o ai
있는 다른 반응들에도 관여한다. 전자 elec t ro 펴즌 정상적인 대사경로를 통해 페레독신 fe rredox i~효료 흐르고, 그리고 앞서 말한 철 단백질로 흐른다(그림 10. 8) . 철 단백질 이 ATP 와 복합체를 이루면, ADP 의 형성과 무기 인산염 (P, )의 방출 과 함께, 철-황 단백질을 환원시킨다• 질소고정 효소라 불리는 철홍} 단백질이 전자를 기체 질소로 전달시키거나 또는 표 10.8 에 나타낸 환원 가능한 기질들 중의 하나로 전자를 전달시킨다. 질소를 고정하는 동안의 Mo-Fe 효소의 활성은 또한 수소이온을 수소로 동시에 환원시 킨다. 환원된 질소량에 대한 환원된 수소이온의 비율은 변한다. 즉 전 자의 유동량이 낮으면 수소가 우세하게 생성되며, 전자 유동량이 높고 ATP 량이 많은 경우에는 질소 기체가 효율적인 경쟁자이며 암모니아 가 높은 비율로 생성된다. 전달된 전자쌍마다 가수분해된 ATP 양에 있어서의 변이와 환원된 수소이온에 대한 질소 기체의 비율에서의 변이 때문에 전반적인 반응 식의 설정은 어렵다. 최적의 실험실 조건에서 순수 분리된 효소 복합 체를 가지고 실험한 결과, 환원 가능한 기질로 전달된 전자당 2 개의 ATP 가 필요함이 증명됐다. 질소 환원과정은 1982 년 At k in s 2} Ra i nb i rd 에 의해 다음과 갇이 나타났다. M 같• N2+6 e-+12 ATP+8 H+ 一-+ 2 NH4++12 ADP+12 P; 효소 복합체에서 수소이온이 환원됨은 다음과 갇이 수소이온이 질소 와 동등하게 환원된디는 것을 나타낸다. M g' ♦ 2 H++z。 e-+4 ATP 一--+ H2+4 ADP+4 P;
따라서 전체적인 반응은- 다음과 같다. Mg '• N2+16 ATP+8 e-+10 H+— -+ 2 NH4++H2+l6 ADP+P; 수소의 발생은 질소고정 효소 활성의 변함없는 특칭이다. 어떤 생물 에서 수소화효소 h ydro g enas e-9-l 존재는 이 손실된 에너지 (H2) 의 일부 룰 다시 회수시키고, 세포 반응에서 이용되는 ATP 를 생성시키는 결 과를 가져온다. 그림 10.9 는 뿌리혹에서의 전체적인 반응을 보여 준 다. 이 그림은 전자 전달과 산화적 인산화를 통한 광합성 산물의 유입 을 질소고정 효소로 연관시키고 있다. 또한 수소화효소의 작용이 질소 고정 반응을- 변화시키지 않으며, 수소화효소의 작용이 없으면 복합체 로부터 수소 형태로 상실될 에너지의 일부를 재회수함을 보여 준다. 수소 흡수활성 (Hu p+)을 가지는 뿌리혹박테리아에 의해 뿌리혹을 형 성하는 식물과 Hup -( 수소 흡수활성이 없는) 세균으로 형성된 뿌리혹을 가전 식물을 비교 연구한 결과, 특정한 뿌리혹박테리아에서 수소화효 소의 존재가 식물의 질소 함량을 상당히 증가시키는 것으로 나타났다. 고정의 첫번째 산물은 암모니아이다. 암모니아는 독립생활형의 질 소고정자와 공생적 질소고정 생물에 있어서 새로운 질소고정 효소의 생산을 억제하는 효과가 있다. 암모니아에서 형성된 높은 수준의 글루 타민은 암모니아동홉넙스:(글루타민 합성효소)의 아데닐화를 야기시킨 다(그립 10. 10 ). 이는 박테로이드에서 새로운 질소고정 효소의 생산에 대한 유전자 해독 cod i n gol] 영 향을 주게 된다. 질산염은 토양에 존재할 때 뿌리흑의 형성과 질소고정 모두에 억제 효과를 가진다. 그 억제 기작은 명확히 알려져 있지 않다. 질산염의 동화는 많은 양의 유기 기질을 필요로 하고, 또 질산염 환원은 질소고 정계로부터 가용한 탄소 공급을 제거할 수 있다. 다른 이론은 질산염
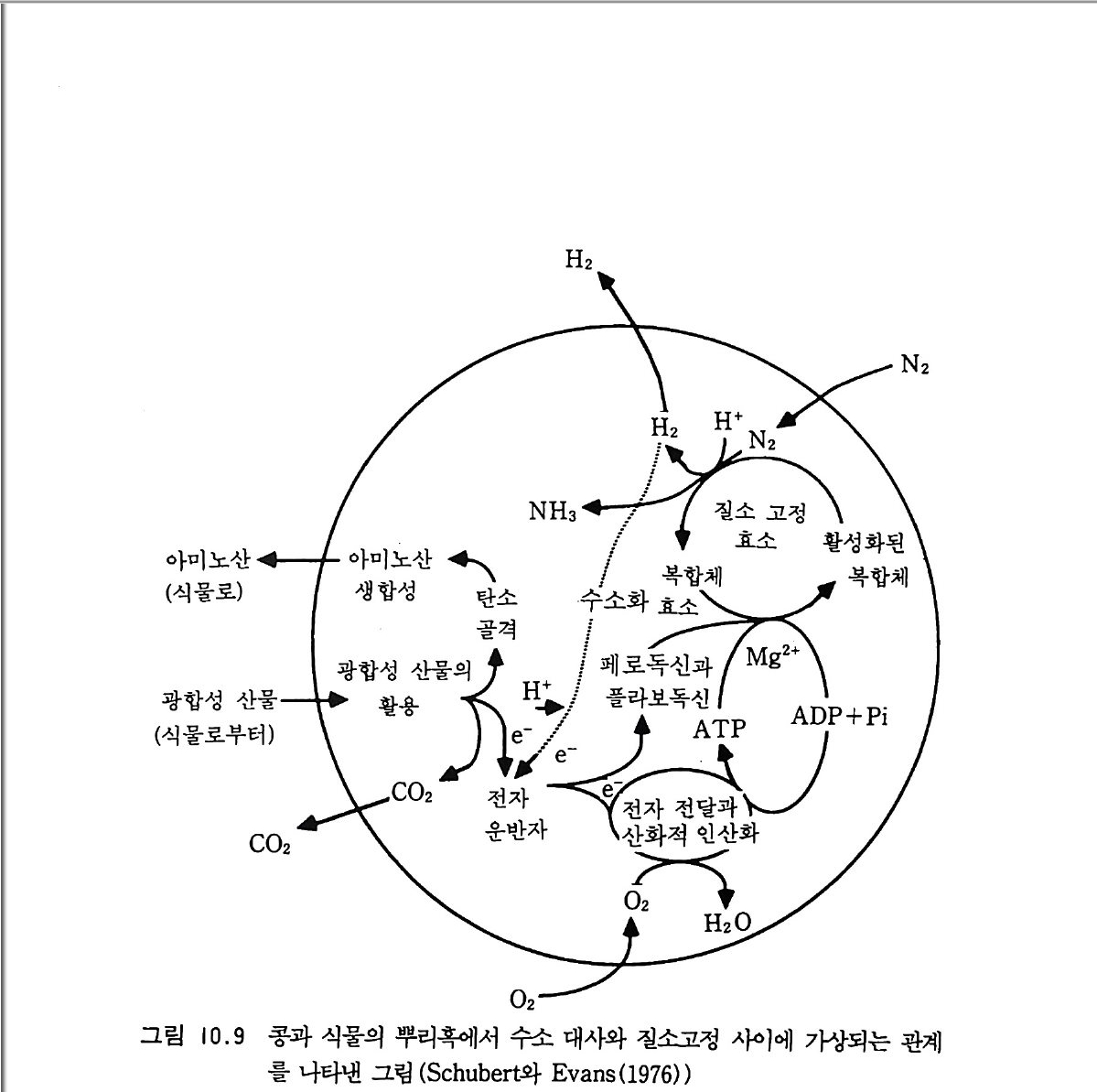 H 2
H 2
의 첫 환원물인 아질산염이 근립 헤모글로빈과 복합체를 형성하여 그 산소조절 능력을 파괴할 수 있다는 것이다. 질산염 환원효소가 없는 콩과 식물이 실험 목적으로 얻어졌다. 이론적으로 이들 식물은 토양 질산염의 존재하에서 질소를 고정할 수 있어야 한다. 콩과 식물의 뿌리혹으로 산소의 확산 속도는 질소고정에 영향을 준 다. 침수는 비록 단기간이어도 뿌리흑의 기능에 치명적이다. 산소의
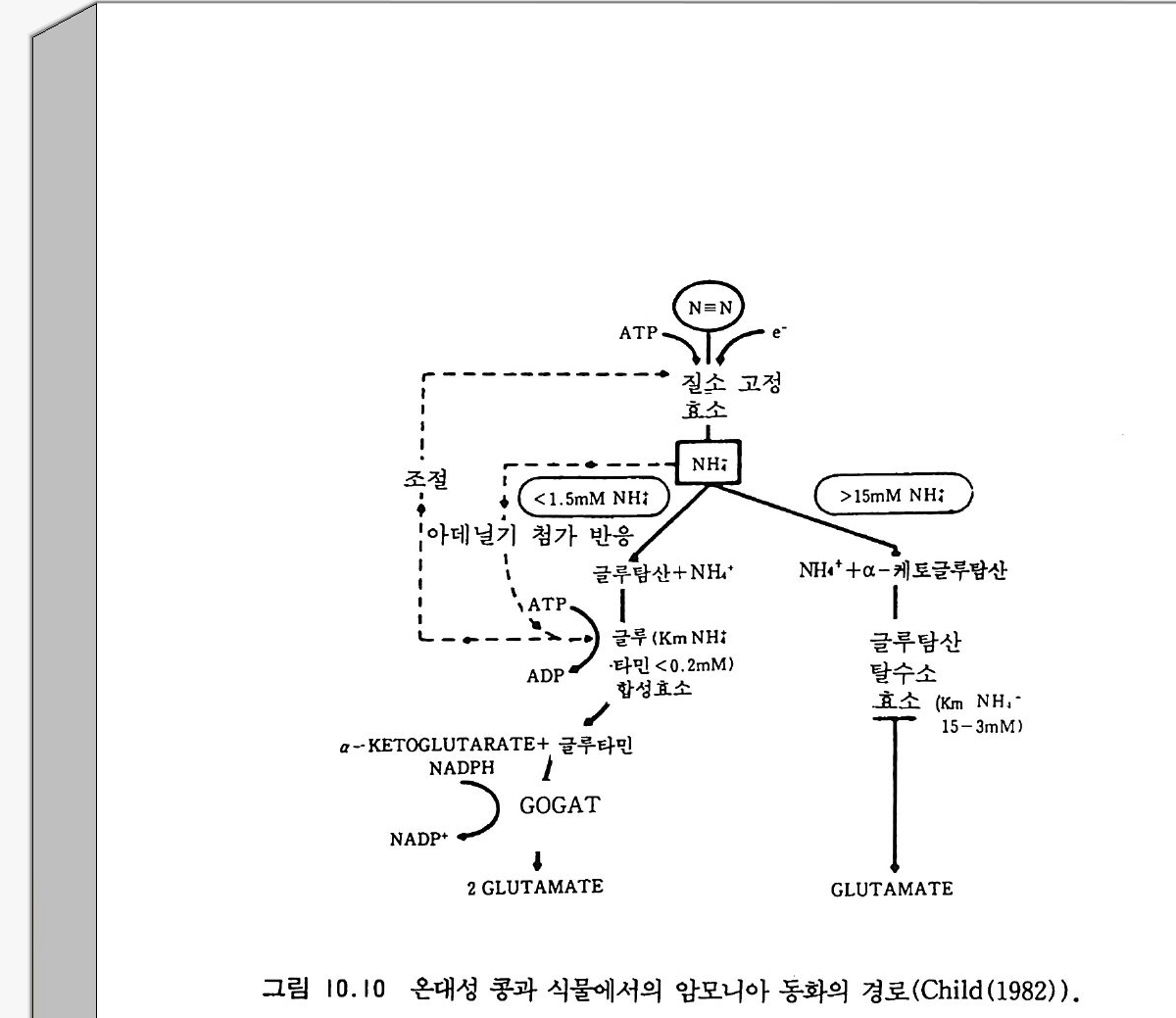 조•:I 절L 아1 데' 닐기♦•1- --첨--가--- 반• -oA - T--P - 》습a r고 K' eJ0
조•:I 절L 아1 데' 닐기♦•1- --첨--가--- 반• -oA - T--P - 》습a r고 K' eJ0
대기 중 농도가 정상적인 농도인 20% 보다 높으면 질소고정이 증가하 지만, 50% 보다 높은 수준에서는 억제되는 결과를 초래한다. 가용한 탄소와 산소의 공급은 둘 다 공생적 질소고정에 중요한 효과를 가전 다. 탄소나 산소의 제한은 질소고정의 효율뿐만 아니라, 수소의 재이 용 효율에도 영향을 준다. 주어전 양의 산소로부터 생성된 ATP 의 양 은 수소가 산화될 때보다 탄수화물이 산화될 때에 더 큰 것으로 보인 다. 암모니아는 남세균과의 공생과 뿌리혹 내의 박테로이드에 의해서도 분비된다. 독립생활형의 유기물 영양체인 2 질소 영양생물은 오직 자
신의 성장을 위해서만 암모니아를 생성하는 것으로 생각되어 왔다. 이 경우에 식물이 고정된 질소를 얻기 위해선 2 질소 영양생물의 사망과 분해가 일어나야만 한다. 그러나 Azo sj>iri llum 과 숙주 식물인 수수를 가지고 실행한 마지 동위원소 실험은 24 시간 동안에 걸쳐 고정된 질소 의 40% 가 식물의 잎에 있는 것을 나타냈다. 따라서 때로 식물과 미 생물의 연합에서 고정된 암모니아의 빠른 방출이 있을 수 있다. 박데로이드에 의해 생성된 암모니아는 공생 식물의 세포에서 유기 형태로 전입된다. 온대 식물의 뿌리혹에는 암모니아 고정의 두 가지 방법 이 존재한다. 글루탐산 탈수소효소 glu ta m ate dehy d rog e nas~ GOGAT 효소계이다. 글루탐산 탈수소효소 경로는 용액내에 1.5 mM 이상의 암모니아를 필요로 한다. 이런 높은 농도의 암모니아는 질소고 정 효소의 합성을 억제한다. 다른 암모니아 전입 경로의 이용 죽, 글 루타민 합성효소 (GS) 와 글루탐산 생성효소 (GOGAT) 의 조합은 암모 니아의 농도를 낮은 수준으로 유지시킨다. 글루타민 합성효소는 또한 질소고정 효소의 합성에 조절작용을 하며, 효소 형성에 필요한 박테로 이드 단백질의 생성에 작용한다(그립 10. 10 ). 일반적으로 글루타민은 목질부를 통해 뿌리를 떠나기 전에 이차적인 반응을 통해 다른 생성물들로 변환된다. 온대 기후에서 성장하는 많은 콩과 식물은 아마이드인 아스파라긴과 글루타민으로 질소를 운반하 고, 일부 열대 콩과 식물은 우레이드 ure i des 인알란토인과 알란토인 산으로. 운반한다. 이들 질소 화합물들은(그립 10.11) 낮은 C: N 비를 갖고 있고, 따라서 적은 양의 탄소를 요구한다. Frank ia -Alnus 와 같은 방선균근의 공생에선 우레이드인 시트룰린을 생성한다. 아스파 라간과 글루타민은 우레이드보다 더 용해되기 쉽다. 따라서 아마도 온 대 콩과식물은 저온도의 조건에 더 찰 적합한 듯하다. 아마이드 또는 유 1 이드의 운반을 결정하는 다른 요인들이 또한 존재할 것이며, 이
 CNl HO2 -NH-CCl H0--NNHH/\ co NCl: OH 2 - C H2-CNl HH2- C OOH
CNl HO2 -NH-CCl H0--NNHH/\ co NCl: OH 2 - C H2-CNl HH2- C OOH
분야에 대한 연구가 더 요망된다. 10-7 질소고정의 에너지론 1982 년 A t k i n 어 Ra i nb i r& 근 이론상으로 질소 기체 1 물의 환원 에 포도당의 0.22 몰에 존재하는 에너지가 요구된다는 것울 보여 주는 연구 자료를 인용했다. 콩과 식물과 독립생활형의 세균에서 질소고정
에 의한 탄소 이용량의 측정 결과, 암모니아 생산량에 대한 수소의 생 성비가 서로 다르게 나타났으며, 수소화효소의 활성 또한 다양한 수준 울 나타냈다. 이용 효율을 측정한 결과 고정된 질소 1 몰당 포도당 0.66- 1. 38 몰이 이용되는 것으로 나타났다(표 10. 9) . 유기물로의 암모 니아 동화 비용은 질소 1 몰당 포도당의 약 0.15 몰로 추정되었다. 고 정된 질소의 운반과 뿌리혹의 성장에 포도당 0.2-0 . 7 몰의 추가 비용 이 든다. 이는 고정된 질소 1 몰당 이용된 포도당이 1. 13-2.37 물에 해당됨을 뜻한다. 그램 기준의 C/N 비율로 변환시키면, 콩과 식물의 공생에서 고정된 질소의 그램당 이용된 광합성 탄소는 2.9-6.1 g으로 추정된다. 질소가 비료로서 공급될 때 화석연료로부터 또는 토양으로 부터 고정된 질소를 얻는 바용과 관련하여 보면 이는 치러야 할 현실 적 비용이다. 그러나 이를 완화시키는 경우가 있다. 질산염을 암모니 아로 환원시킬 경우 상당량의 에너지가 요구된다. 따라서 질산염의 형 태로서 존재하는 질소 비료나 토양의 이용은 에너지 소비면에서 식물 이 대기의 질소를 고정할 때 요구되는 에너지량과 크게 다르지 않다. 영양염 흡수 비용은 야의에서 성장하는 식물의 전체적 능력과 관련 표 10.9 질소고정이 활발한 콩과 식물의 뿌리혹에서 각 과정에 필요한 에 너지 비용의 이론적 추정치· 기능적 분류 고정포된도 질당소몰 1수 몰 당 고정된탄 소질g소수 l g당 질소고정 효소-수소화효소 0.66-1. 38 1.7 -3.5 암모니아 동화 및 0.14-0.16 0.36-0.41 관련된 탄소 대사 고정된 질소의 운반 0.13 0.33 뿌리혹의 성장과 유지 0.2-0.7 0.5-1. 8 1.13 -2.37 2.9-6 . 1 ·자료 : At ki n ~ Rain b ir d (19 82)
되어 있다. 질산염 환원효소에 의한 질산영태 질소의 환원은 뿌리에서 보다 광합성을 하는 잎에서 일어나는 경우, 잎에서 환원물질의 가용도 가 더 크기 때문에 질산염 이용 효율에 영향을 준다. 뿐만 아니라 미 생물과 공생을 하는 식물은 잎의 구조와 이산화탄소의 흡수 효율을 변 화하는 것으로 나타났다. 이는 광합성 효율의 증가를 가져온다. 공생 적 연합의 형성은 한 식물이 공생을 형성하지 않으면 실제 광합성 능 력보다 그 이용도가 낮게 되는 식물의 광합성 능력을 이용하는 것에 달려 있다. 11 장에서 식물이 자신의 공생자가 필요로 하는 것을 광합 성에서 보상하는 가능성에 대해 토의한다. 10-8 접종 새로운 뿌리혹박테리아의 균주를 토양 환경으로 도입하려는 시도나 또는 유전공학적으로 조작된 생물의 도입은 비슷한 문제접을 갖고 있 다. 이는 토양으로 새로운 생물을 접종할 때 나타나는 생물적 그리고 환경적인 문제와 관련이 있다. 뿌리혹박테리아를 접종 균주로 사용하 는 것에 대해 이미 많이 알려져 있다. 따라서 이러한 정보는 유전공학 적으로 조작된 개체의 이용에 대한 모형 체계를 제공할 수 있을 것이 · 다. 광범위한 현장 연구 결과, 효율적인 접종원의 질(質)이 존재하는 것 으로 나타났다. 뿌리혹박태리아의 효율적인 접종원은 단종 균주 또는 다종 균주로 구성될 수 있다. 단종 균주의 접종이 바람직한 경우는 다 음과 같다. 어느 특정 균주가 일반적인 토양 및 기후적 조건에서 특정 한 숙주에 가장 적합하다는 사실이 현장 실험으로 확인될 경우, 그리 고 특정 품종의 식물이 자라고 있는 경우이다. 다종 균주의 접종은 다
양한 변종이나 품종의 식물이 자라는 지역과 토양 및 기후 변화가 넓 은 지역에서 선호된다. 그러나 다종 균주 접종원은 숙주에게 이익을 주지 않고 뿌리혹을 형성하는 뿌리혹박테리아의 균주를 포함해서는 안 된다. 그와 같은 균주는 기생일 수 있고, 또한 유용한 세균의 뿌리혹 생성을방해할수있다. 최대 효력을 위해서 접종원이 알팔파와 같은 작은 종자의 경우에는 적어도 10,000 개체의 활력이 있는 뿌리혹박테리아를 공급해야 하고, 땅콩과 같은 큰 종자는 백만 개체의 뿌리혹박테리아를 공급해야 한다. 여러 유형의 종자에 있어서 필요한 접종원은 종자 1 kg 당 평균 4 g이 다. 보균 배지 carrie r med i um 는 접종 균주를 6 개월의 저장 동안 보 호할 수 있어야 한다. 이는 기체 교환과 습도 유지롤 필요로 한다. 종 자의 적용이 쉬워야 하고, 잘 흡착되어야 하며, 그리고 세균을 건조, 화학 비료 또는 살충제로부터 보호해야 한다. 끝으로 접종 균주는 뿌 리혹박테리아나 종지에 해로운 다른 세균이 없어야 한다. 콩과 식물의 접종원은 두 가지가 있다. 종자에 적용하기 위해 고안 된 것과 토양에 적용하기 위해 고안된 것이 있다. 종자 접종원은 적용 하기 쉽고 일반적으로 효과적이다. 일반적으로 토탄 물질에 보유된, 질이 높은 접종원은 가장 신뢰할 만한 접종원을 공급하는 것으로 생각 된다. 종자에 첨가하는 방법에는 혼합기술이 있다. 이 경우 접종원은 검 gum이나 당을 포함한 물과 혼합되어 흡착이 증진된다. 물 또는 다 른 용액 없이 접종원을 혼합할 경우, 일반적으로 종자와 세균이 균일 하게 섞이지 않는다. 접종 균주와 종자를 작은 덩어리로 만드는 것 pe lleti ng o l 좋은 방법 으로 밝혀졌다. 작은 덩어리를 형성하는 과정은 종지를 토탄으로 만든 접종현탁액 pe at- b ased ino culant slurr y으로 적시고 나서, 미세하게 분쇄된 석회와 같은 화합물로 표면을 코팅하는 과정을 거친다. 열대지
역에서는 석회 대신 분말 인광석이 종종 이용되는데, 이는 석회석이 내산성 세균에 해로울 수 있기 때문이다. 고온의 건조한 토양에 매우 많은 뿌리혹박데리아 접종원이 요구되거나, 또는 비효율적인 자연산 뿌리혹박테리아로 심하게 감염된 토양에 매우 많은 양의 뿌리혹박데리 아 접종원이 필요할 때, 아라비아검 혼합물과 함께 종자 1 k g당 접종 원 4g o] 초기에 사용된다. 그리고'식재하기 바로 직전에 k g당 8 g의 접종원을 추가로 젖은 종자와 섞는다. 폴리비닐 아세데이트, 폴리우레탄, 폴리요소 니스와 같은 수용성 접착제 또는 용매에 녹는 수지가 석회, 인광석 또는 토탄으로 만든 접 종원을 종자에 결합시키기 위해 이용된다. 코팅한 종자의 이점은 더욱 균등한 피종, 손쉬운 심기 그리고 더 나은 발아를 들 수 있다. 식재하 기 몇달 전에 종자가공 회사에 의한 종자의 전 처리 (접종된 종자의 구 입)는 농부들에게 관심을 끌지만, 뿌리혹박테리아의 사망률이 높고 파 종결과도일정치 않다. 종자가 고온 건조한 토양에 파종되거나 독성 살충제로 코팅된 경우, 뿌리혹박데리아는 종자 아래의 습한 토양에 접종될 수 있다. 비효과적 인 자연산 세균의 많은 군집으로 심하게 감염된 토양에 종자를 직접 파종하는 것보다 토양을 배치함으로써 효과적인 뿌리혹박테리아를 더 많이 접종할 수 있다. 그러나 이는 노동력과 비용이 많이 든다. 땅콩 의 경우처럼 토착 세균을 새로운 균주로 바꾸기는 매우 어렵다. 따라 서 처음으로 콩과 식물이 자라는 지역에 가용한· 그리고 가장 효과적인 균주로 접종되도록 하는 것이 매우 중요하다.
10-9 생물공학의 도전 질소고정 생물을 이용한 유전공학 연구가 상당수 전행중이거나 또는 고려중에 있다. 질소고정에 관련된 17 개의 세균 유전자가 알려졌고, 이들 유전자가 한 개체에서 다른 개체로 이전되는 과정에서 하나의 그 룹으로서 이동하는 경향이 있음이 알려졌다. 이는 질소고정 효소의 생 산이 이전되는 그 이상의 내용을 내포하고 있다. 죽 뿌리혹박테리아가 유전공학을 통해 다음과 같은 결과를 가져올 수 있겠는가 ? ® 줄기나 잎에서 대기 질소를 고정할 수 있는가? ® 토양 내의 식물에 이용 가 능한 유효 질소가 있어도 대기 질소를 고정할 수 있는가? ® 토양에 서식하는 다른 개체 또는 다른 뿌리혹박테리아와 성공적인 경쟁자가 될 수 있는가? ® 가뭄, 산도, 알루미늄 또는 다른 독성물들과 같은 환경 스트레스를 극복하는가 ? ® 특히 비콩과 식물과 또는 다른 새로 운 숙주와 성공적인 공생을 형성할 수 있는가? 공생적 질소고정은 숙 주 식물로부터 요구되는 에너지와 비교시 비용이 드는 과정이다. 질소 고정의 효율 증가는 광합성 산물을 더 잘 이용하는 것과 수소의 재포 획에 있어 수소화효소의 효과적인 이용을 수반한다. 잎 또는 줄기의 성공적인 뿌리혹 형성은 광합성 산물의 토양으로의 전이를 불필요하게 하며, 토양에 있는 다량의 길항체 또는 경쟁자로부터 균주를 보호할 것이며 그리고 균근과 뿌리혹박테리아의 활동 영역의 분리로 그들에 의한 공생의 역할에 대한 정의에 더 정확을 기할 수 있을 것이다• 그러나 복잡한 산소 감응 체계를 잎으로 전이할 경우 옥수수 감은 식물에서처럼 많은 문제를 일으킬 것이다. 우리는 또 다른 접근 방식 둘을 고려할 필요가 있다. 옥수수에 질소고정을 도입하는 것보다, 옥 수수의 성장 잠재력과 식량의 특성을 가질 수 있도록 효율적인 질소고 정을 하는 공생적 콩과 식물을 유전적으로 변화시키는 것이 더 쉬울
것 0] 다. 뿌리혹박테리아에 대한 광범위한 분자생물학적인 연구는 그립 10.12 에 있는 분자적 유전자 지도를 만들어냈다. 이는 부착, 뿌리털 뿌리혹 생성, 숙주 특이성 그리고 질소고정 효소 유전자를 포함한다. 그립의 빈 공간은 아직도 규명되야 할 영역임을 나타낸다. 식물의 스 트레스에 대한 반응, 질소고정 기간 동안의 탄소의 할당 그리고 광합 성 경로볼 통해서 공생체계에서 식물이 종종 제한 요인으로 작용하는 것을 발견할 수 있다. 뿌리혹박테리아에 대한 기존의 광범위한 연구
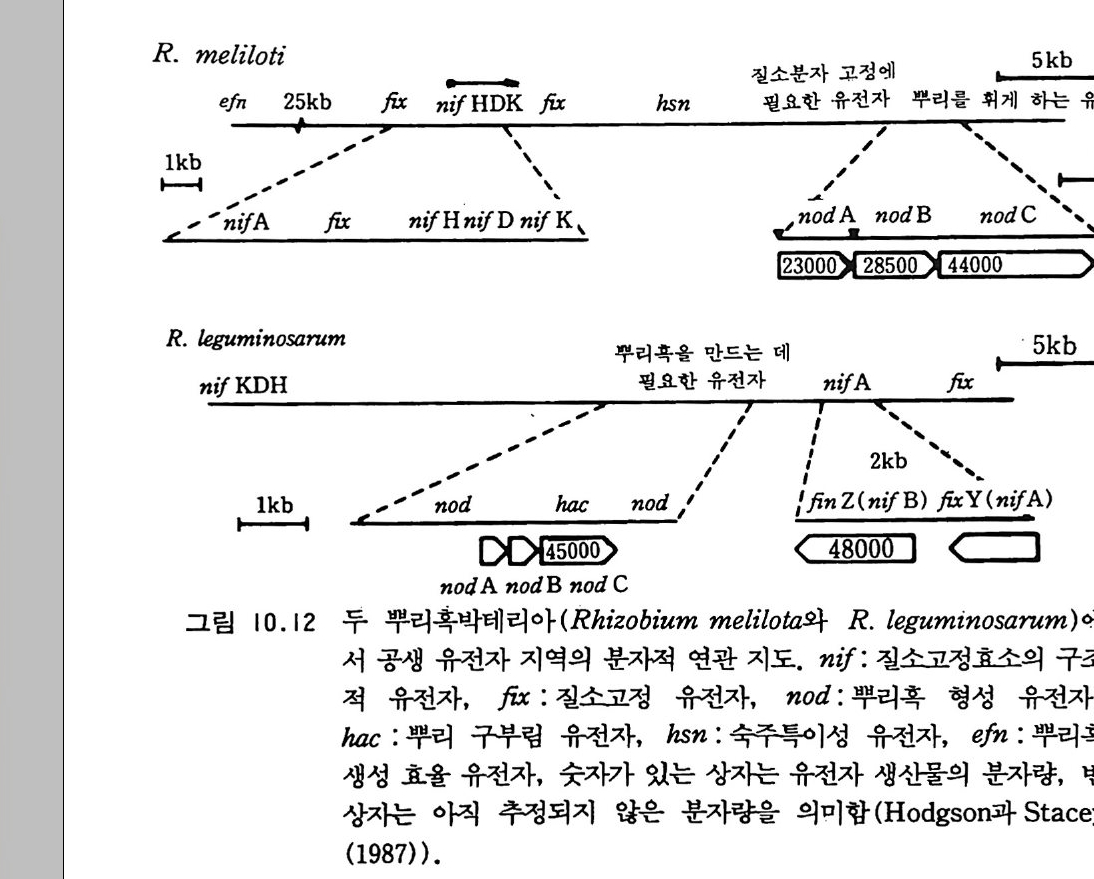 R. meeflni l o ti 2 5kb fix n•i / HD.K” fix hsn 질필소요분한자 유고전정자어 ] 뿌리를 휘1게 하5k는b 유전, 자
R. meeflni l o ti 2 5kb fix n•i / HD.K” fix hsn 질필소요분한자 유고전정자어 ] 뿌리를 휘1게 하5k는b 유전, 자
는, 분자생물학적 기법이 근권에서 일어나는 역동성에 대한 연구의 주 요 발전에 기여할 경우, 다른 토양생물 연구의 모형 체계가 될 수 있 을것이다. 식물과 상호작용하는 많은 뿌리혹박테리아의 능력 (감영력)은 풀라스 미드에 있는 유전자에 의해 결정됨이 입증되었다. 플라스미드는 단지 약 3 개의 유전지를 갖는 아주 작은 것으로부터 토양 세균에서 발견되 듯이 200 개 이상의 유전자를 갖는 매우 큰것이 있다. 공생 미생물들 사이에서 플라스미드의 이전은 숙주 범위의 특이성 host rang e • s p ec ificity의 이전과도 상관관계가 있을 수 있다. 토양미생물학자와 식물 분자생물학자에 주요 관심이 되는 플러스미드는 Ag ro bacte r i um tu mef a c i ens 의 플라스미드이다. 이 세균은 뿌리혹박테리아의 근연종 으로 식물 숙주에 유전 물질을 이전함으로써 식물에 종양을 생기게 한 다. 이러한 풀러스미드의 이전 기작은 식물 세포에 다른 유전 물질을 집어 넣을 수 있게 하는 데 사용되며, 세균의 특성을 식물로 전이시키 는몇 안되는기술중의 하나이다. A g robac t e riu m 으로부터 뿌리혹박테리아로 종양을 형성하는 풀라스 미드의 이전 결과, 뿌리혹박테리아가 종양 형성 생물로 변환됨이 밝혀 졌다. 반대 방향의 이전 죽, 뿌리혹박테리아로부터 A g robac te riu m 으 로의 이전은 뿌리혹은 생성하나 질소고정이 없는 세균을 만들었다. 이 는 콩과식물과 질소고정균 사이에서 공생관계가 설정되기 전에 질소 고정 균주가 염색체의 다른 유전자 또는 다른 풀라스미드의 다른 유전 자를 요구함을 보여 준다. 풀라스미드는 그람음성균 사이에서는 쉽게 이전된다. Klebsi e lla, Rhiz o biu m 그리고 Azoto b acte r 같은 세균은 유전공학에서 가장 찰 연구된 대칭균과 DNA를 교환할 수 있다. 토양으로 다시 도입되는 균주의 규명에 사용될 목적으로 항생제에 저항성 있는 균주가 실험실
에서 이미 상당한 규모로 생산되고 있다. 이러한 균주는 대부분의 토 양 균주의 성칭을 억제하는 항생제가 있는 배지에서도 자랄 수 있는 능력을 이용하여 규명될수 있다. 뿌리혹박테리아로부터 질소고정 유전자가 없는 Azo to bac te r 로의 DNA 의 이전은 질소고정균을 형성시킨다. 이는 질소고정 유전 물질 이 하나의 단위로서 이전됨을 보여 주는 것이다. 참고문헌 Ahmadji an , V., and Paracer, S. ( 19 86) . Sy mb io s es: An Intr o ducti on to Bi ol og- ica l Sys t e m s. Univ e rsit y Press of New Eng la nd, Hannover. At ki n s , C. A. (1982) . Ni tro g e n fix ati on in nodulate d pla nts oth e r tha n leg um es, In Advances in Ag ricu lt ur al Mi cr obio l ogy (N.S. Subba Rao, ed.) , pp. 54- 88 . Butt er wort h, London. At k in s , C. A., and Rain b ir d , R. M. (19 82) . Phy s io l og y and bio chemi st r y in bio l og ica l nit ro g e n fixa ti on in leg ume s, In Advances in Ag ricu lt ur al Mi cr obio l ogy (N. S. Subba Rao, ed.) , pp. 26-52. Butt er wort h, London. Beckin g , J. H. (19 78) . Envir o runenta l role of nit ro g e n fixi n g blue-g ree n alga e and asym bio t i c bacte r ia , Ecol. B ull. 26, 266-281. Beckin g , J. H. (1982) . Ni tro g e n fixa ti on in nodulate d pla nts oth e r tha n legu me s, In Advances in Ag ricu ltu r al Mi cr obio l ogy (N.S. Subba Roa, ed.) , pp. 90-llO. Butt er wort h, London. Burns, R. C., and Hardy , R. W . F. (1975) . Ni trog e n Fw ition in Bacte r i a and Hig h er Plants . Sp ri n ge r-Verlag, Berlin and New York. . Chil d, J. ( 19 81 ) . Bi ol og ica l nit ro g e n fixtion , In Soil Bio c hemi stry (E. A. Paul and J. N. Ladd, eds.) , Vol. 5, pp. 247-322. Dekker, New York. Doberein e r. J., and Day, J. M. (19 75t N i trog e n fixa ti on in the rhiz o sph ere of trop ica l gras s. In Ni trog e n Fw ition by Free-Liv i n g Mi cr o-orga -nis m s (W. D. P. Ste w art , ed.) ,_I nt. Bi ol . P rog ram me 6, pp. 39-56.· Cam :br i dg e Un iv. Press, London and NewYork.
Fog g, G. E. (19 77) . Ni tro g e n fixa ti on , In Alga l Phys i o l ogy and Bio c hemi s- try (W. D. P. Ste w art, ed.) , pp. 560-582. Blackwell, Oxfo r d. Havelka, U. D., Boy le , M. G., and Hardy , R. W . F. 0 982) . Bi ol og ica l nit ro g e n fixa ti on , Ag r onomy 22, 365-413. Hodg so n, A. L., and Sta c ey, G. (19 87) . Pote n it al for Rhiz o biu m im p ro ve-ment, CRC Cr it. Rev. Bio tec hnol. 4, 1-7 3 . Mi llb ank, J. W. (19 77) . Lower pla nt associa t i on s, In A Treatis e on Di ni t ro g e n Fix o.tion (R. W. F. Hardy and W. S. Sil v er, eds.) , Sect. 3, pp. 125-184. W ile y (Int e r scie n ce) , New York. Patr i q u in , D. G. (1982) . New develop m ents in gras s bacte r ia assoc iat i on s, In Advances in Ag n ·cult ur al Mi cr obio l og y (N. S. Subba Rao, ed.) , pp. 139-190. Butt er worth , London. Pete r s, G. A. , a nd Calvert, H. E. (19 82) . The Azolla-Anabaena sym bio s is . In Advances in Ag ricu lt ur al Mi cr obio l ogy (N. S. Subba Rao, ed.) , pp. 191-218. Butt er worth , London. Postg a te , J. R. (19 82) . Fundamenta ls of Ni tro g e n Fix o.tion . Cambrid g e Univ . Press, London and New York. Shubert, K. R., and Evans, H. J. (1976) . Hy d rog e n evoluti on . A majo r fac to r aff ec ti ng the eff icien cy of nit ro g e n fixa ti on in nodulate d sym bio n ts , ·· Proc. Natl. Acad. Sci. U.S .A . 73, 1207-1211 . —Ste w ar t(,1 9W 77. )D . . BP.l u(1e9-7g5r ) e .e Nn ia tlrgg ae en, F Iixn o .Atio nT rbeya tFis er e oen-L D iviinn ig t r oMg ei ncr oFoixr goa.t nioins m(Rs.. Cambrid g e Univ . Press, London and New York. W. F. Hardy and W. S. Sil v er, eds.) , Sect. 3, pp. 63-124. W ile y (Int e r sci en ce) , New York. Tu, J. C . (1975) . Rhiz o bia l root nodules of soy b eans as revealed by scannin g and tra nsmi ss io n electr o n mi cr oscop y, Phyt op a t h o logy 65, 447-454. 추가로 읽을 거리 Bauer, W. D. (19 81) . Inf ec ti on of legu m es by rhiz o bia , Annu. Rev. Plant Phys i o l . 32, 407-409.
Berin g e r, E. R. (19 82) . Mi cr obia l ge neti cs and bio l og ica l nit ro g e n fixa ti on , In Advances in Ag n ·cult ur al Mi cr obio l ogy (N. S. Subba Rao, ed.) , pp. 26-52. Butt er wort h, London. Dommergu e s, Y. R. (19 82) . Scarcely exp lo red means of inc reasin g the soil N po ol thr oug h bio l og ica l N2 fixa ti on , Proc. Int. Cong r . Soil . Sc i., 12t h , 1982, pp. 138- 14 9. Granhall, U. (19 78) . Envir o nmenta l role of nit ro g e n fixi n g blue-gr een alga e and asym bio t i c bacte r ia , Ecol. Bull. ( Sto c kholm) 26. Long, S.R. (19 84) . Geneti cs of rhiz o biu m nodulati on , In Plant Mi cr obe Inte r acti on s (E. Neste r and G. Kosug e , eds.) , pp. 265-306. Macmi ll an, New York. Parker, C. A. (19 77) . Prospe c tive s in bio l og ica l din i t ro g e n fixa ti on , In A tre atis e on Di ni t rog e n Fix ation (R. W . F. Hardy and W . S. Sil v er, eds.) . Sect. 3. pp. 367-471 . Wi ley (Inte r scie n ce) . New York. Pate , J. S. ( 19 77) . Functi on al bio l og y of din i t ro g e n fixa ti on by legu m es, In A Treatis e on Di ni t rog e n Fix ation (R. W. F. Hardy and W . S. Sil ve r, eds.) . Sect. 3. pp. 473~517. Wi lle y (lnte r sci en ce) , New York. Sharunug a n, K. T., Gara, F. 0., Anderson, K., Morandi, C., and Ballanty ne , R.C . (19 78) . Contr o l of bio l og ica l nit ro g e n fixa ti on , In Ni trog e n in the Envir o nment (D. R. Ni el sen and J. G. MacDonald, eds.) , Vol. 2. pp. 393~ 41 6. Academi c Press, New York. Vi nc ent, J. M. (19 77) . Rhiz o biu m ge neral mi cr obio l oy , In A Trea t i se on Dtni t rog e n Fix ation (R. W. F. Hardy and W. S. Sil v er, eds.) . Sect. 3, pp. 277-368. W ile y (Int e r scie n ce) . New York. Food and Ag ricu ltu r al Orga niz a ti on of the Unit ed Nati on s (l98 4) . Legu me Jno culants and Their Use. FAO, Rome.
제 |I 장 균근 관계 11-1 서론 균근 m y corrh i zas은 미생물과 식물 사이의 공생관계를 보여 주는 좋 은 예이다(표 11.1). 질소고정 식물의 경우에 그 관계는 3 중적이다. 콩과 식물의 경우 균근곰팡이, 숙주식물 그리고 뿌리혹박태리아 Rh i zob i um 로 구성되어 있다. 비콩과 식물인 일부 관목에서 그 관계 표 II . I 자연에서 출현하는 주요 미생물들의 공생관계 공생 관계 공생생물 지의류 곰팡이와조류 지의류 곰팡이와 시아노박테리아 산호 강장동물과 조류 콩과식물 콩과 식물, 뿌리훅박테리아 그리고 낭지균근 물개구리밥 Azolla 와 시 아노박테 리 아 방선균근 관목과 피자식물 , Frank ia와 낭지균근 균근 대부분의 식물과 곰팡이
는 녹색식물, 균근곰팡이 그리고 방선균인 Frank i쇼료 구성되어 있 다. 이둘 모든 구성원의 역할에 대한 인식은 중요하다. 어떤 때라도 두 구성원에만 국한된 연구는 야외에서 일어나고 있는 공생 활동에 대 하여 잘못된 결론을 가져 온다. 화석 기록은 균근으로서 인식된 곰팡이-식물뿌리 연합이 육상석물 만큼 오래된 것임을 보여 준다. 가장 최초로 알려진 식물은 3 억 7 천 만년 전의 라이니 수암 Rh y n i e cher t의 화석에 나타난다. 이 식물은 이 장에서 기술될 오늘날의 VA 균근 vesic u lar-arbuscular my c orrhiz a s (주머니와 가지 모양의 구조물로 이루어졌다는 데서 이름이 유래되었 으므로 낭지균근이라고도 옮김 : 옮긴이)과 매우 유사한 곰팡이의 구 조를 보여 주고 있다. 홍미로운 것은 화석에서 나타난 곰팡이와 관련 된 지하의 식물기관은 실제 뿌리가 아니란 것이다. 시간이 지남에 따 라 곰팡이보다 식물에서 더 많은 적응이 일어났다. 이 분야의 역사를 재검토하면서 1985 년에 Tra pp e 와 Berch 는 균 근의 존재에 대한 최초의 실례가 1840 년에 발표됐음울 언급했다. 그 해에 Robert Har tig가 소나무의 균근성의 가는 뿌리를 실제로 입증 했다. 그러나 그는 곰팡이를 독립된 존재자로서 인식하지 못했다. 난 초와 협생하는 균세포가 1847 년에 S. Re i ssek 에 의해 기술되었으며 곰팡이로 인식되었다. 1881 년 F. Kam i ensk i는 일부 나무의 뿌리가 곰팡이 충으로 둘러싸여 있고, 영양영이 식물에 의해 흡수되기 위해선 곰팡이 충을 통과해야만 한다고 지적하였다. 1885 년 A. B. Frank 는 프러시아에서 송로(松露)의 배양 가능성을 연구하도록 요청받았고, 곰 팡이복덕 구조를 알아내어 곰핑이 뿌리를 나타내는 My korrh i zen 이 란 이름을 만들었다. 그는 뿌리에 막을 형성하는 곰팡이를 ecto t r o p i- sch( 의생 영양적이라는 뜻)라 불렀다. 의부에 단단한 막울 형성하지 않 고 뿌리 세포 안으로 균사가 침입해 들어가 있는 협생체를
endotr o p isch (내생 영양적이 라는 뜻) 라 불렀다. 11-2 균근의 형태와 분포 균근 곰팡이는 거의 모든 식물과 연합되어 있다. 사초과 C yp er aceae, 골풀과J uncaceae, 쐐기풀과 Ur ti caceae, 명아주과 Cheno p od i aceae, 석죽과 Caryo p h y ll aceae 그리고 십자화과 Brassic a ceae 의 일부 수종들은 다른 수종들보다 잘 감염되지 않는다. 농경에 많은 피 해를 주는 잡초둘 중 일부가 비균근성인 점은 홍미롭다. 일반적으로 잡초는 영양염이 적절한 지역에서 빨리 성장하기 위해 빠른 성장 특성 과 감영되지 않은 미세한 뿌리털에 의존한다 (Trapp e (1 987)). 일반적으로 미세한 뿌리 (細根) 또는 뿌리털의 출현과 균근의 형성 사이엔 음의 관계가 있다. 초목과 같이 미세한 뿌리와 많은 뿌리털을 갖는 수종들은 영양면에서 균류에 거의 의존하지 않는다. 그러나 오렌 지 나무나 소나무와 같이 뿌리가 굵은 식물이나 또는 콩과 식물과 같 은 주근(主根)의 석물은 영양면에서 균류에 의존한다. 균근을 형성하 는 식물들은 하나의 공통적인 속성이 있다. 이 식물들은 곰팡이의 잠 재적 병원성을 제어할 수 있다는 것이다. Rhiz o cto n ia 균은 옥수수에 유력한 병원균이지만 난초와는 안정된 균근을 형성한다. 난초와 협생 하는 곰팡이들을 제의한 다른 균근들은 일반적으로 자연에서 유기 형 태의 탄소에 대해 다른 분해 생물들보다 경쟁하는 능력이 약한 것으로 알려져 있다. 이들 곰팡이는 탄소 공급을 숙주에 의존한다. 식물 잔여 물 pla nt res i due 과 토양 유기물 (SOM) 에서 자랄 수 있는 담자균류인 그물버섯속 Bole tus의 곰팡이들은 활발한 셀룰로오스 분해효소를 가지 고 있다. 균근을 형성할 수 있는 관련된 몇 종들은 셀룰로오스를 분해
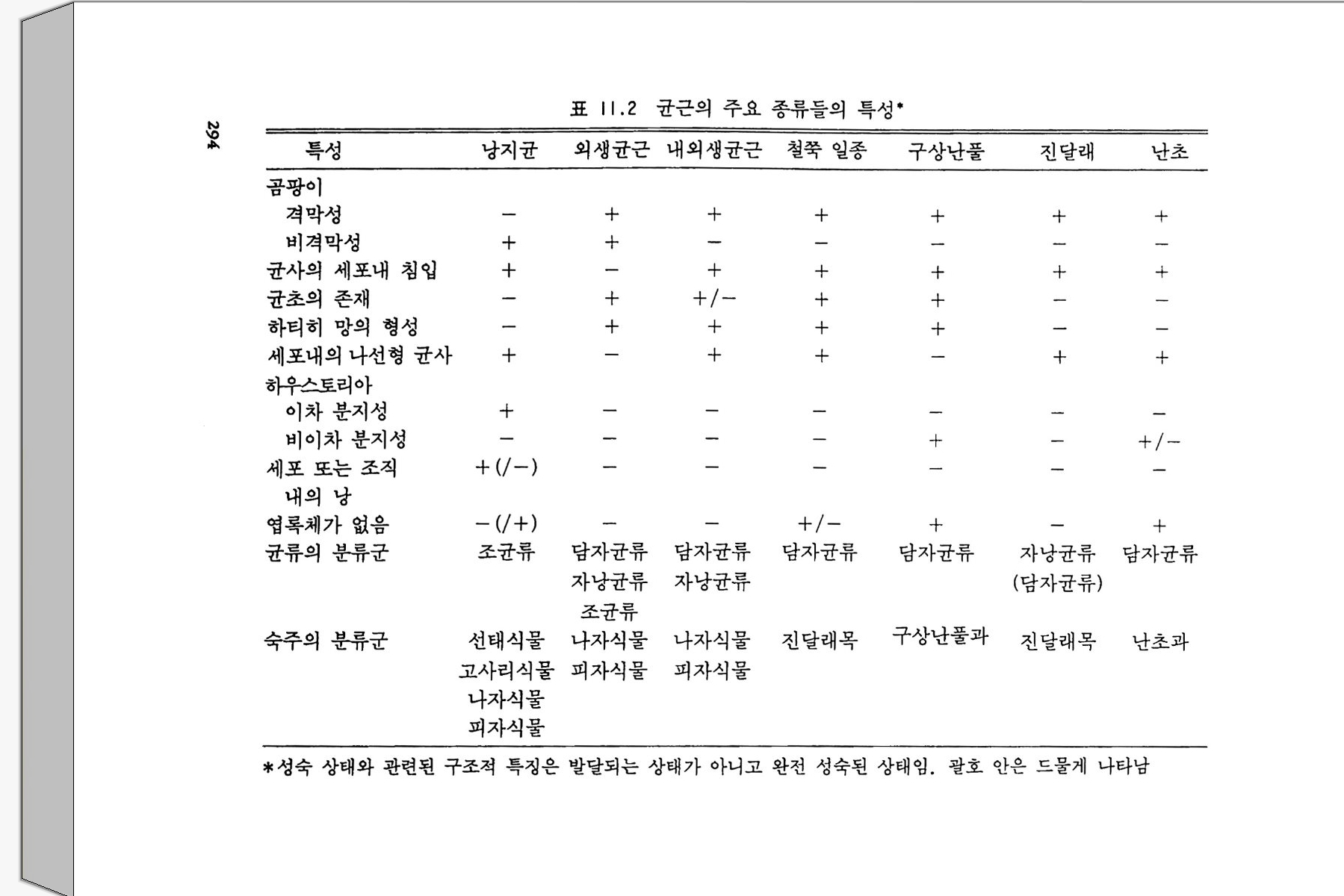 풀 ++++류 과 호
풀 ++++류 과 호
할 수 있는 능력 이 없다. 몇 가지 중요한 의 생 균근 ecto m y co rrhiz a e 은 식물의 리그닌과 리그노 셀룰로오스를 분해하는 능력이 있는 것으 로 입증됐다. 그러나 자연에서의 그들의 역할은 아직 알려지지 않고 있다. Frank 에 의 한 의 생 영 양 ec t o t ro p h i c 과 내 생 영 양 endo t ro p h i c 의 독 창적인 구분 방법은 식물과 식물 공생균에 대한 더 많은 정보가 가용 하면서 확대되었다. 표 1 1. 2 는 1983 년 Harle y와 Sm it h 에 의해 인 식된 7 가지 형을 기술하고 있다. Frank 의 의생 영양의 구분은 오늘 날까지 계속되고 있다. 그러나 그 독창적인 내생 영양의 구분 기술은 더 많은 정보에 기초하여 세분되었다. 난초, 구상난풀, 진달래 들에 속하는 식물은 균근에 대해서 숙주 특이성을 가진다. 내의생 영양 ecte n dotr o p h ic 협생체는 VA 균근과 의생 균근들 사이에 존재하는 연 속성에 대한증거이다. 표 11. 3 공생적 협생의 뿌리에서 균근의 생물량 균 숙주 뿌무리게의 방법 감(%영)률 Glomus fas cic u latu m Centr o sema pub escens 14 키틴 95 Glomus mosseae Centr o sema pub escens 7 키틴 100 Acaulosp o ra laevis Centr o sema pub escens 5 키틴 95 Glomus mosseae V죠 fa ba 6 현미경 60 Glomusmosseae A llium por rum 10 T* 처o 65 Glomus fa,scicu latu m Glyc ine max 16 키틴 70 Glomus fas cic u latu m Sorgh um bic o lor 3 키틴 50 Ecto m y co rrhiz a e Abie s amabil is 23 년 12 균두 백분율에 대한 180 년 3 추정과 시료 채취 Pseudots uga menzie sii 15 현미경과 수확법
11-2-1 VA 균근 VA 균근 (Vesic u lar-arbuscular my c orrhiz a s, VAM) 은 균근 중 가 장 혼한 것으로 접합균 Z yg om y ce t e~로 - 분류된 곰팡이들이 여기에 포함된다. 격막이 없는 균사 ase pt a t e hyp ha 탸근 대부분의 작물, 많은 산림 수종, 가로수, 관목 및 야생 초본종의뿌리세포를 침입한다. 뿌 리나 의부 구조에서 뚜렷한 구조적인 변화가 관찰되지 않는다. 양파와 같은 일부 수종에선 뿌리의 색깔이 약간 노랗게 되기도 하나, 다른 대 부분의 식물에서 VAM 의 존재를 확인하기 위해선 현미경으로 관찰해 야만 한다. VA 란 명칭은 양분 저장 기관을 뜻하는 내부의 낭 ves i cles 에서부터 기인된 것이다. 세포 사이에서 이들 10-100 µm 의 균사의 연장 부분은 통상 지질로 채워져 있다(그림 11 .1 ). 뿌리의 피충 세포 내부에 존재하는 다른 내부 구조는 arbuscules( 영 O.}- 소 교환 장소임)이 다. 이는 식물 병원균의 홉기 (P 及器, haus t or i a) 와 유사한 섬세히 분기 된 균사로 구성되어 있다(그림 11. 2) . arbuscules 는 개개의 식물 세 포 내에서 4-10 일 동안 존재한다. 그 후 식물 세포에 의해 소화되며 , 다른 식물 세포에서 새로운 arbuscleS7} 형성된다. 영양소의 전이 tra nslocati o!h =-섬 세하게 분기된 균사와 매우 함입된 식물 세포막 사 이에서 일어나는 것으로- 생각된다. arbuscle~ 감영된 식물 세포는 감염되지 않는 세포에 비해 식물 세포 물질의 질량이 20 배가 큰 것이 관찰되었다. VAM 균의 의부 구조는 토양을 뚫고 들어가는 균사와 각각의 휴면 포자 resti ng spo res.. £. 되어 있다. 후자는 곧바른 균사 위에 무성생식 에 의해 생성되며 (그림 11. 1 참조) 후막포자 chlam y dos p ores 라고 알려 져 있다. 어떤 VAM균 은 자낭군 s p orocar p 안에 포자의 집단을 갖는 다. 과거에 낭으로 규명된 식물 뿌리의 의부에 있는 구조들은 현재 형
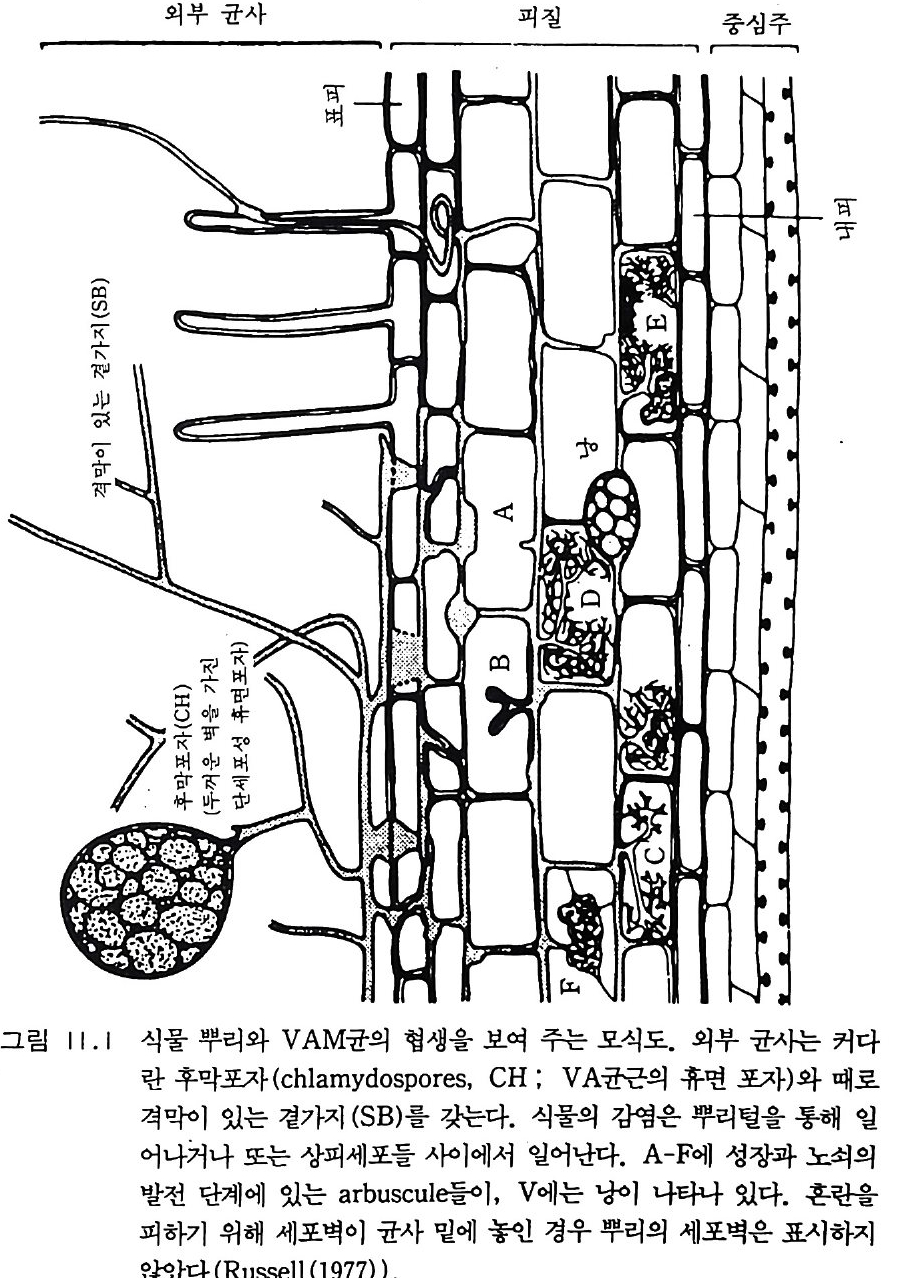 외부균사 피질 중십주
외부균사 피질 중십주
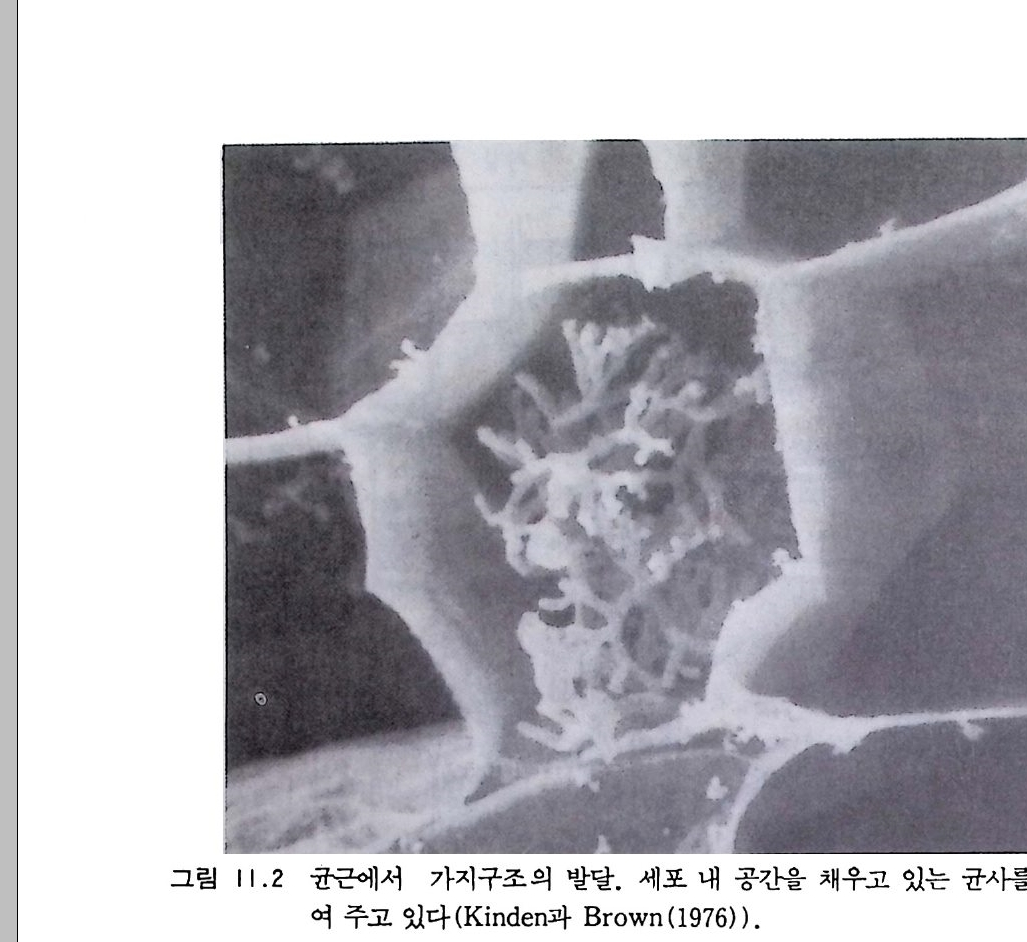 그림 | | .2 균근에서 가지구조의 발달. 세포 내 공간을 채우고 있는 균사를 보
그림 | | .2 균근에서 가지구조의 발달. 세포 내 공간을 채우고 있는 균사를 보
성 단계의 후막포자로 생각된다. 낭이란 용어는 식물 피충 내부의 팽 창된 균사의 끝 부분에 대해서만 사용해야 한다. Endo g onaceae 과의 5 개 주요 속 ge nu~ VAM 을 형성한다. 5 개 속 은 Glomus, Gig asjJo ra, Acaulosj Jo ra, Sclerocys ti s 및 Scute l - lo sjJ ora 이다 .• 이들 균은 휴면포자의 모양에 의해 구분된다(그립 11. 3 과 11. 4) . Glomus 속에는 각각 두꺼운 벽을 갖고 말단의 후막포자를 형성하는 많은 종이 있다. Glomus 는 또한 각각의 후막포자를 내부에 갖고 있는 다중의 포자 형성구조인 자낭군을 생산한다. 성숙하면 포자들은 균사로부터 분리
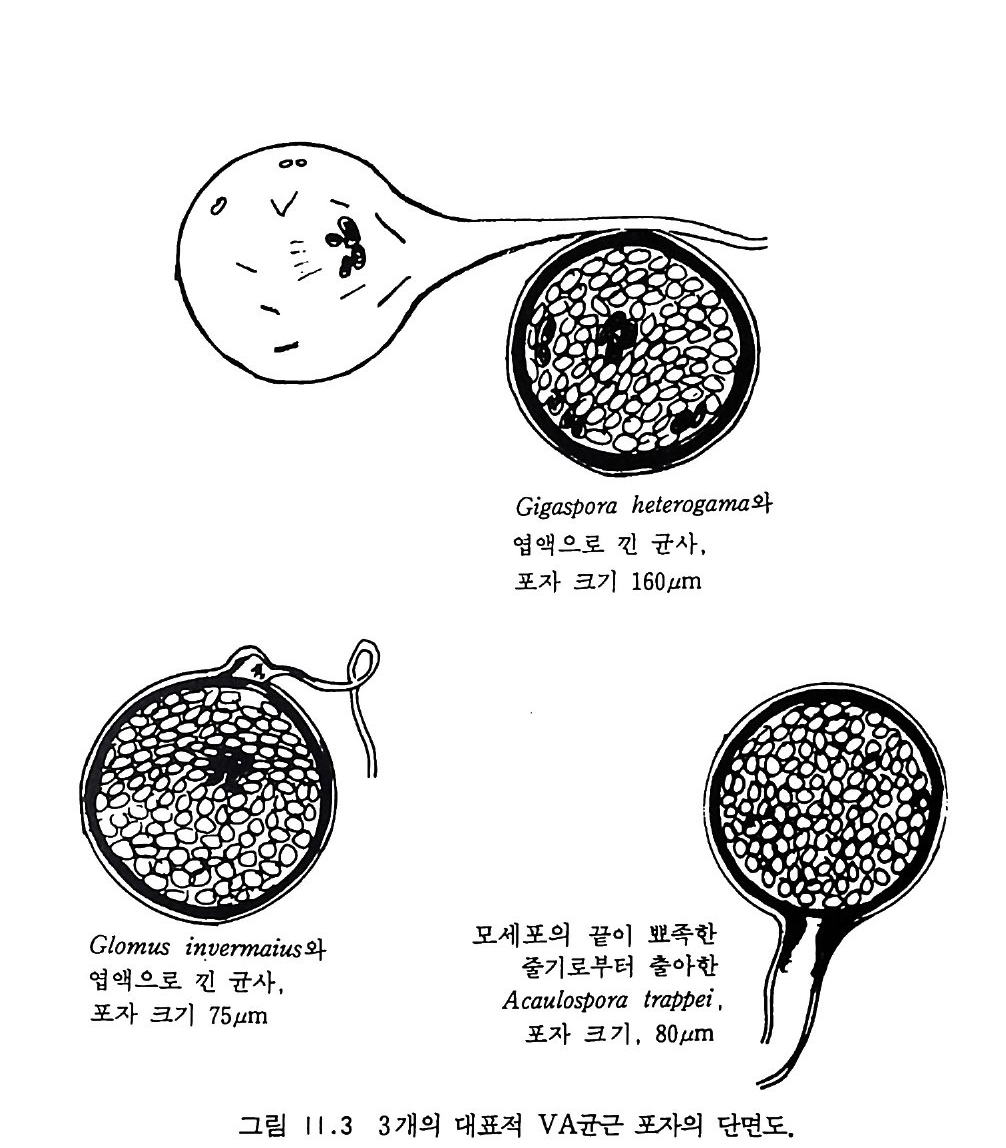 G ig쩍 )ora he t ero ga ma 와
G ig쩍 )ora he t ero ga ma 와
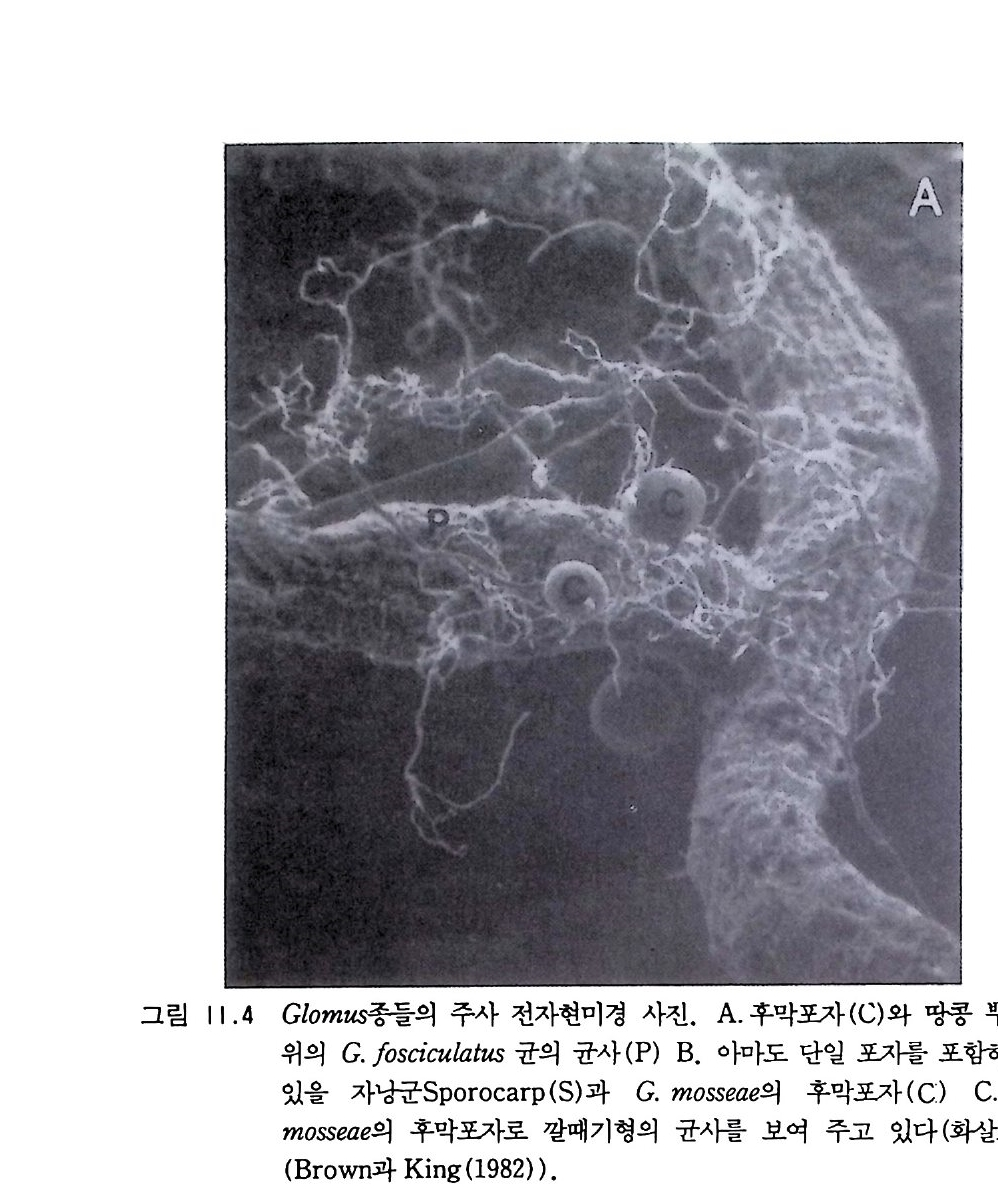 그림 |1.4 Glomus 종들의 주사 전자현미경 사전. A. 후막포자 (C) 와 땅콩 뿌리
그림 |1.4 Glomus 종들의 주사 전자현미경 사전. A. 후막포자 (C) 와 땅콩 뿌리
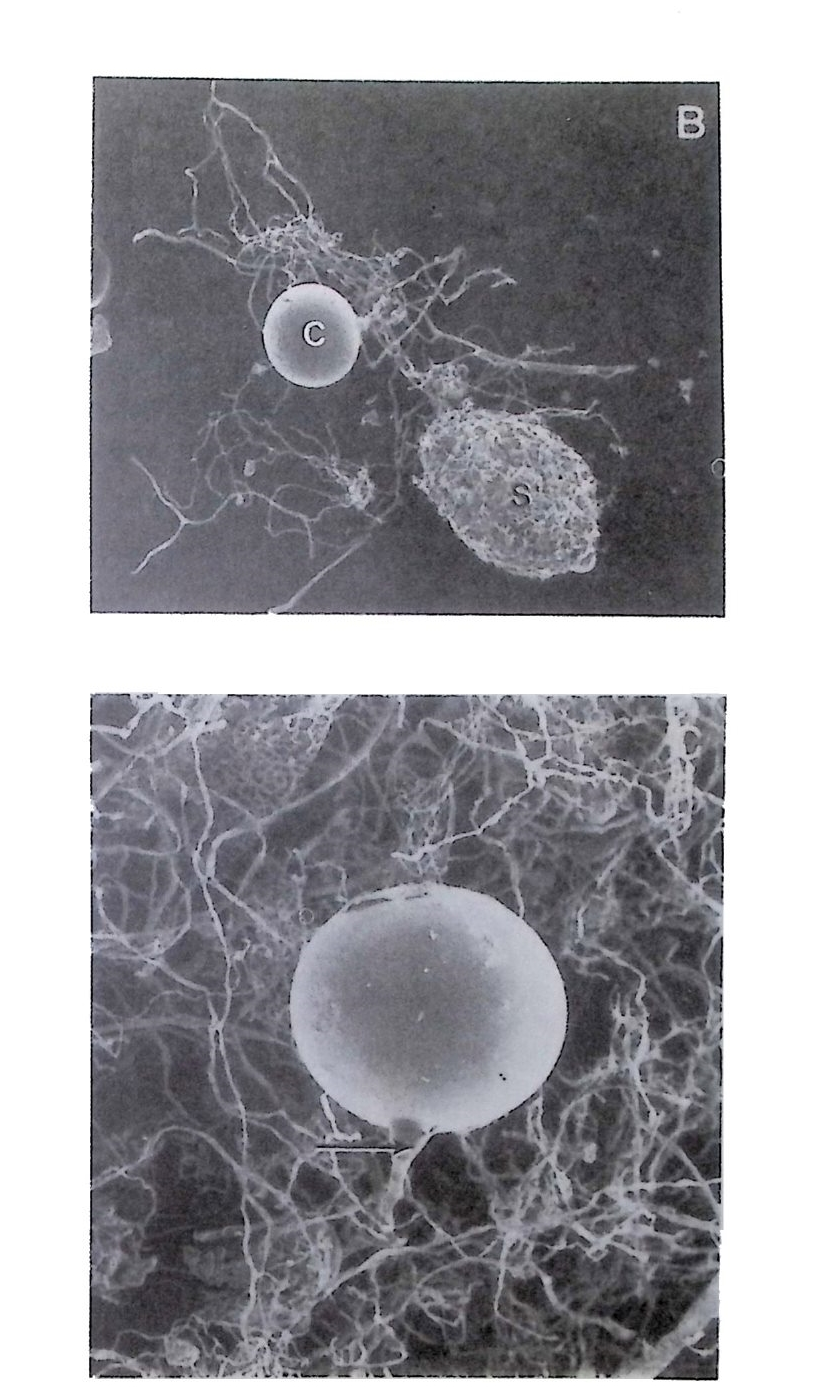
한다. G igasp o 泣속은 낭을 거의 형성하지 않으나, 균사의 둥그런 배병 (旺 柄) 같은 끝에서부터 발아하는 포자를 갖는다. 그 포자들은 접합균의 유성 단계의 접합포자와 유사하다. G igasp ora 는 무성생식이기 때문 에, 그 포자는 지금까지 비접합포자로 불려왔다. 그러나 많은 균학자 는 포자라고 부른다. Acaulo sp o 泣속은 말단의 휴면포자를 생성한다. 이돌은 이전에 발생하였으나 짧은 기간 동안 생존한 모포자로부터 형 성된다. 그 포자들은 토양에서 낱개로 발견되거나 가끔 뿌리 안에서 발견된다. Sclero cys tis 속은 상당수의 후막포자를 포함하고 있는데 , 이 휴면포자들은 자낭군을 형성하고 있는(그림 11 .4 ) 서로 엉킨 균사 의 중심부 근처에 배열되어 있다. 포자의 발아는 Glomus 와 Sclerocy s tis의 경우엔 부착 균사의 재성 장으로부터 , 그리고 G igasp ora 와 Acaulo sp ora 에선 포자의 벽을 통해 일어난다. 발아된 포자의 성장 균사가 뿌리에 접촉하지 않는 경우 그 성장이 제한될 수 있다. 이 경우 포자는 휴면 상태를 계속한다. 대부 분의 균 학자는 포자로부터 균사의 성장 방향이 임의적이라고 믿는다. 일반적으로 식물 뿌리로부터 몇 밀리미터 내에 균사가 있기 전까지는, 성장하는 균사 끝의 방향을 확실케 하는, 식물 뿌리로부터 나와서 발 아하고 있는 포자에게 전달되는, 어떤 메시지가 있는 것 같지는 않다. 균사는 식물 뿌리로부터 몇 밀리미터 내에 있게 되면 뿌리를 감염시키 는 좁은 가지의 (2-7µm) 부채 모양의 복합체를 생성한다. 개개의 VAM 포자들은 지름이 10-400 µm 이나, 대부분 40-200 µm 범위에 있다. 포자의 동정은 포자 크기, 구조 및 벽 모양에 익숙 한 전문가에 의하며 , 현미경 관찰용으로 많은 수의 포자가 필요하다. 벽 구조를 관찰하기 위해서는 포자를 부숴야 한다. 다른 VAM 균은 지름이 5-lO µm 인 균사를 갖고 있는 반면에 지름이 1-3 µm 의 균사를
갖는 섬세한 내생 생물 endo ph yt e 의 경우 지름이 약 lOµm 의 작은 포 자에 의해 특칭된다. 섬세한 내생 생물인 Glomus t enu i s 는 비옥한 토양 조건에서 특히 인의 흡수에 효과적이라고 언급된다. 그러나 Harle y와 Sm ith (1983) 는 이들 내생 생물의 분류가 아직도 의문의 여 지가 있으며, 더 많은 특징이 규명되기까진 단순히 섬세한 내생 생물 로서 간주되어야 할 것인지도 모른다고 주장했다. 11-2-2 외생 균근 의생 균근 (ec t om y corrh i zas, ECM) 은 격막이 있는 균사 세포로 구 성되어 있으며 (표 11. 2) , 온대 교목과 관목들의 뿌리를 감염시킨다. 곰핑이는 뿌리 표면에 단단한 균투 man t le 또는 덮개를 형성하며, 뿌 리 피충 세포들 사이룰 침두하여 하티히 망 Hartig ne t이라고 불리는
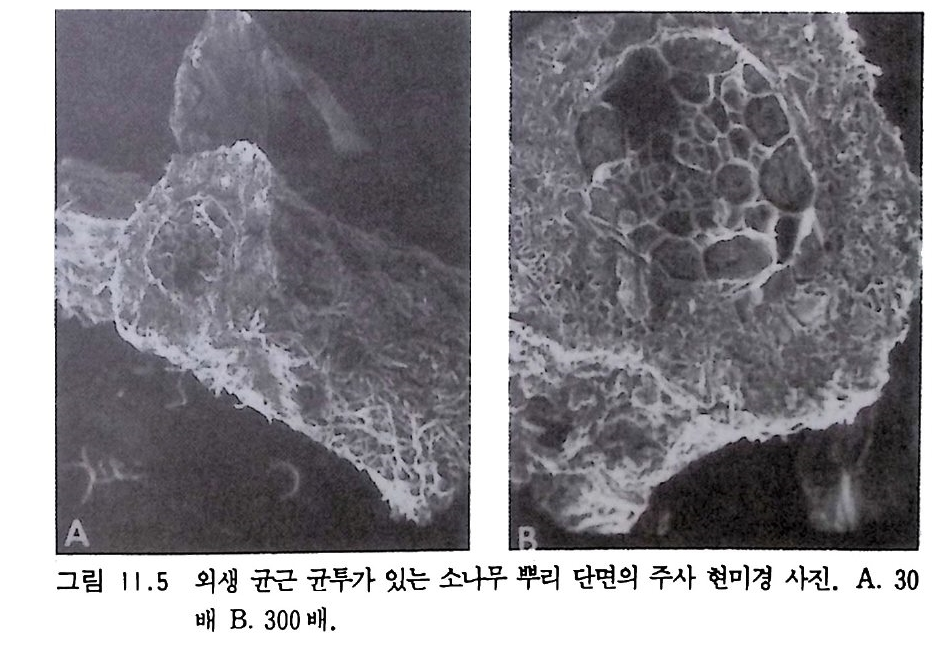 그림 II . 5 의생 균근 균무가 있는 소나무 뿌리 단면의 주사 현미경 사진. A. 30
그림 II . 5 의생 균근 균무가 있는 소나무 뿌리 단면의 주사 현미경 사진. A. 30
복잡한 세포간 시스템을 형성한다(그림 11.5, Harle y와 Smi th (1983) ) .^ 의부에 있는 균두는 두께가 변할 수 있으며 , 세포들 사이의 하티히 망은 다른 균근성 협생 관계에서보다는 일부 균근성 협생에서 더 뚜렷하다. 그림 1 1. 6 에 나타난 전형적인 포크형의 분기는 소나무 의 ECM 에서 전형적이다. La rix(낙엽송)와 Tsug a( 미국 솔송나무)의 잔뿌리들은 뿌리 끝의 광범위한 분기가 많지 않으며, 반면에 더 복잡 하고 두꺼운 균두를 갖고 있다. 가끔 참나무는 ECM 의 감염에 기인 한 뿌리의 분기를 나타내지 않는다.
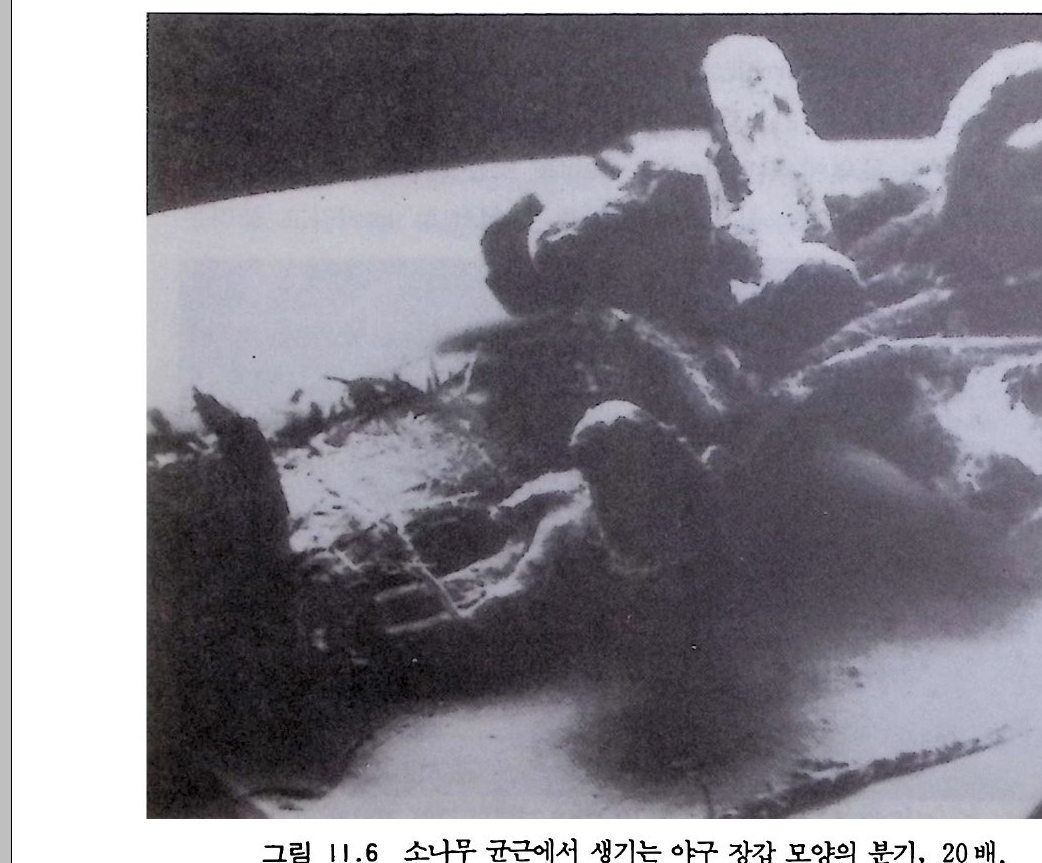 그림 11. 6 소나무 균근에서 생기는 야구 장갑 모양의 분기, 20 배.
그림 11. 6 소나무 균근에서 생기는 야구 장갑 모양의 분기, 20 배.
ECM 균은 오옥신을 생성하며, 오옥신은 균근성 뿌리와 비균근성 뿌리의 일부 의형적 차이에 관련이 있다. 짧은 뿌리는 감염의 결과라 기보다는 감영의 결괴에 선행되는 것으로- 생각된다. 많은 균의 종들이 ECM 을 형성한다. 담자균류, 자닝균류 그리고 조균류가 관여되어 있 다. 주름버섯과 A g ar ic aceae, 그물버섯과 Bole t aceae, 무당버섯과 Rus sulaceae 그리고 끈적버섯과 Cor ti nar i acea 여t 포함하는 많은 버섯류 등은 광범위한 균근을 유도한다. 그리고 이 버섯둘은 또한 알려진 식 용 가능한 자실체를 지상과 지히에 생성한다. 어떤 ECM은 특수화되 어 있고, 단지 하나의 숙주 종과 협생을 한다. 반면에 Cenococcum gra nif orm e (불완전 자낭균의 일종)과 같은 것은 협생할 수 있는 숙주 가여러 가지다. ECM 균의 효과는 잘 기록되어 있다. 나무의 씨를 초원의 토양 또 는 다른 새로운 지역에 심을 때, 그 나무의 균근 동반자의 도입이 없 이 이루어진다는 것은 통상 어렵거나 때로는 불가능하다. 많은 수의 중요한 ECM 균이 숙주 식물로부터 떨어져서 성장할 수 있기 때문 에 , 접종 균주의 생산과 실험화가 가능하다. 모래밭버섯 Pis o lith u s tin c to ri us 과 사마귀버섯 Teleph o ra ter restr ius 같은 균근 동반자로 접 종시엔 소나무의 성장을 크게 강화시키며, 특히 광산처럼 버려진 토양 같이 영양영이 부족하고 독성 금속들이 많은 곳에서 성장을 강화시킨 다. 이들 ECM 균은 영양영의 흡수를 증가시키고, 항생물질을 생성하 는 것 으 로 알 려 져 있 다. 또 한 Pythi u m , Rhiz o cto n ia 그 리 고 Phy to p h th ora 와 같은 뿌리에 감영하는 병원성 생물들에게 장애물을 형성하는 것으로 생각되고 있다. 나무 위의 어떤 균근에서는 의부 균두가 상당히 감소되었거나 또는 심지어 존재하지 않을 수도 있으며, 따라서 내외생 균근을 형성하게 된다. 하티히 망이 잘 발달되어 있으나, 균사가 숙주의 세포 내로 침
두한다. ECM 을 형성하는 같은 균이 다른 숙주 식물에서 또는 다른 조건하에서 내의생 균근을 형성할 수 있으며, 이는 ECM 과 VAM 의 특성을 모두 약간씩 갖고 있다. 일반적으로 북부와 납부의 온대 및 아한대 지역의 삼림에서 ECM 이 많이 존재한다. 또한 열대지역의 고지대에서도 출현한다. 한때는 열대 우림에서만 VAM 이 나타나는 것으로 간주되었었다. 더 많은 연 구 결과 ECM의 출현이 어떤 나무들에서 보고되었으며, 일부 교목성 콩과 식물t ree le gum e 혀 1 서도 보고되었다. 오리나무속 Alnus, 실삼나 무속 Cup ressus, 향나무속 ]un ip erus, 아까시나무속 그리고 목마황속 Casua ri na 의 수총들은 의생 균근과 내의생 균근을 갖고 있는 것으로 보고되어 있다. 11-2-3 진달래과의 균근 Harle y와 Sm ith는 진달래목 Er ic ale 회 식물과 협생하는 균근의 두 가지 형과 구상난풀과 Mono t ro pacea &-1- 협생하는 균근을 따로 분 류하였다(표 11. 2) . 진달래과 식물의 균근은 수 µm 에서 85µm 두께 의 균투로 형성된다. 이는 ECM 의 균투와 갑이 저장기관으로서 기능 울 가질 수 있다. 하티히 망은 발견된다 해도 피질세포의 의부충만을 침두한다. 격막아 있는 균사는 세포 내에서 결국엔 붕괴되는 나선형 균사를 세포 내에 형성한다. 피충 내에서는 측면적 확장이 거의 없기 때문에, 각각의 새로운 세포에 대한 균사의 침입은 토양으로부터 이루 어져야 한다. 진달래 나무의 뿌리 조직계는 긴 뿌리와 짧은 뿌리로 분 화되어 있고, 오직 짧은 뿌리만이 광범위하게 감염된다. 진달래과 식 물형의 예들은 진달래속 rhododendron 과 Arc t os t ap hy los 로서 지중해 성 기후의 미국 캘리포니아에서 광범위하게 발견된다.
진달래과 석물은 산성 또는 이탄토에 특징적이다. 숙주로는 Calluna( 히스속의 식물)와 Vacc i n i um( 산앵두나무속)이 있다. 서유럽 의 히스, 아북극의 둔드라 그리고 남아프리카, 호주, 파키스탄, 오스 트리아의 고지대에 있는 습지의 히스는 전달래과 균근의 주요한 예가 된다. 오직 한 종류의 균이 (어두운 색깔의 느리게 자라는 격막을 가전 자 낭균류임) 히스 식물의 섬세한 뿌리와 협생하고 있음이 발견되어 왔 다. 이 균은 현재 Pez i zell ai료 알려졌으며, 세포 내에서 다중의 나선 형 균사를 형성한다. 뿌리 세포 부피의 42% 까지 균사에 의해 점유될 수 있다. 대부분의 균근곰팡이는 영양염들의 흡수를 도와 주는 것으로 알려져 있다. 전달래과 식물의 균근에 대한 연구는 15NH4+ 의 존재하 에서 토양 유기 질소의 흡수가 증가됨을 보여 주었다. 이는 이들 곰팡 이가 분해 능력이 있음을 증명하는 것으로 보인다. ('SN 은 질소의 안정 한 동위원소로서 질소의 추적자로 사용됨. 13N 은 질소의 방사성 동위원소로 서 그반감기가너무짧아서 일반적으로널리 이용되지 않는다:옮긴이) 구상난풀과의 엽록체가 없는 achlorop h y ll ous 초본 식물은 원래 부 생식물 (腐生植物, sa p ro p h yt e) 로 간주되 었다. 현재는 담자균류인 그물 버섯속 곰팡이가 구상난풀 및 인접하는 나무의 뿌리를 모두 감염시키 는 것으로 간주되고 있다. 구상난풀 Mono t rop a 의 씨는 매우 작으며, 받아를 시작할 경우, 그물버섯균 Bole t us 에 감염이 되어야만 발아 후 에 더 발육하게 된다. 가문비나무와 소나무에 두입된 [uc] 포도당과 [32p ]인 산염은 그물버섯균에 의해 1-2 m 떨어진 구상난풀의 조직으 로 전이되었다. 구상난풀에 대한 이접이 명확하나, 균에 대한 이점은 그리 명백하지 않으며 숙주나무는 기생되고 있는 것으로 간주되어야 할것이다.
11-2-4 난초과의 균근 격막이 있는 균이 12,000-30,000 종의 난초과 식물과 공생한다는 것은 따로 고려할 가치가 있다. 이는 그 협생의 생리적 특성 때문이며 난초가 원예의 문헌에서 차지하는 관심 때문이기도 하다. 어린 난초는 매우 작아서 가장 큰 것이 무게가 약 14µ g이다. 모든 난초는 성체가 엽록체가 있든 chloro p h y llous 또는 없든 achloro phy llous, 광합성을 할 수 없는 어린 식물 단계를 거친다. 난초의 씨는 너무 작아서 충분 한 저장 양분을 함유할 수 없다. 따라서 발아하는 배는 의부에서 탄수 화물의 공급이 없거나 또는 적합한 균근곰팡이에 의해 감염되지 않으 면 더 이상 발생할 수 없다. 한때 이들 균둘은 불완전한, 더미를 형성 하는 Rh iz oc t on ia 라고 인식되었다. 현재 많은 균들이 자실체를 형성 하도록 유도되었다. 낙영버섯속 Marasm i us, 뽕나무버섯속 Arm i l /,aria 그리고 말굽버섯속 Fomes 같은 속이 대표적인 것으로 알려졌다. 비균 근성 단계에서 이들 속들은- 가끔 파괴적인 병원성 생물이다. 난초의 감영은 세포에서 세포로 확산되며, 니선상 균사는 감염된 세 포 안에서 상당량 부피를 차지한다. 세포 내 나선상 균사는 난초의 안 정된 균근 협생에서도 제한된 생명 기간을 갖는다. 균사의 분해는 감 염 시작 후 30-40 시간 내에 빨리 일어날 수 있으며, 그리고 통상 11 일 내에 완결된다. 그러나 같은 세포의 재감염 또는 인접 세포로부터 의 균사의 침입이 일어날 수 있다. 균의 소화가 처음엔 영양영 이전의 근거로 간주되었다. 현재는 영양염의 이전이 연속적인 과정으로 믿어 지고 있으며, 균의 온전한 막을 통해서 그리고 밀접하게 연합되어 있 는 숙주세포를 통해서 일어날 수 있는 것으로 믿어지고 있다. 난초가 숙성하면서 광합성을 할 때, 탄소의 순 이전 ne t tra nsfe r 이 숙주로부 터 곰팡이로 일어날 것이란 직접적인 증거는 거의 없다.
온대 산림에 존재하는 녹색 난초 또는 성체의 난초와 균근 관계에 대한 연구는 거의 없다. 나무 표면에서 자러는· 열대의 부착성 난초는 지지 식물의 조직을 침두하는 균사 연결부를 가지고 있다. 이는 구상 난풀의 경우에서 일찍이 기재된 것처럼, 숙주 식물들의 기생이 일어날 수 있음을 지적해 준다. 그러나 구상난풀의 균은 찰 발달된 균초 fun g a l sheath , 하티히 망, 특수한 홉기를 갖고 있는데, 이러한 구조 물들은 난초 협생에는 없는 것이다. 11-3 균근의 생리와 기능 동일한 일반적인 생리 과정들이 자연에서 출현하는 대부분의 균근 협생에도 적용된다. 균의 주요 공헌은 영양염의 흡수와 전이, 특히 인 의 전이에 있다. 또한 균근 식물은 건조에 대한 저항성이 큰 것으로 알려져 있다. 다른 알려진 효과로는 식물 병원균으로부터의 보호, 선 충류들로부터의 보호 그리고 근계 주변의 중금속으로부터 보호 동이 있다. 균은 그 대가로 식물의 용존 탄소를 요구한다. 성공적인 공생의 바탕은 식물이 영양염류를- 얻는 동안, 식물이 곰팡이에게 탄소를 제공 할 수 있는 능력 (아는 공생이 아닌 경우에는 이용되지 않았을 광합성 능력 을 제공할 수 있는 능력)의 균형에 있다• 기생도 일어날 수 있다. 이 경우 토양의 영양영류의 농도가 낮아서 곰팡이는 추가의 영양영을 추 출해 낼 수 없고, 균에 전달된 탄소에 응답하여 곰팡이가 아무런 혜택 울줄수없을때이다.
11-3-1 영양소 홉수 인, 질소, 아연, 구리 그리고 황 등의 영양영이 균근곰팡이에 의해 흡수되어 숙주로 전이되는 것으로 알려졌다. 광범위한 연구들은 그 홉 수 기작이 균근곰팡이에 의해 이용되는 토양 부피가 많이 증가됨에 기 인하는 것으로 밝혔다(토양의 접촉면의 증가에 기인한다). 또한 곰팡이 는 감영되지 않은 식물의 뿌리보다 더 낮은 농도에서 인을 흡수할 수 있는 것으로 나타났다. 균근곰팡이는 활발한 유기 인 분해요소 ph osph ata s e 활동도를 갖고 있다. 이 효소가 균의 내부에서 인의 이 전에 주로 사용되는 것인지, 또는 하나의 흡수 기작인지는 알려져 있 지 않다• 여러 실험둘은 유기 인의 한 공급원인 ph y tat e 7 } 균근곰팡 이에 의해 분해되며, 그 분해 산물인 인이 흡수되는 것을 입증했다. 다른 실험둘은 균근이 비균근성 뿌리보다 유기 인에 대해 더 큰 친화 력을 갖고 있지 않음을 밝혔다. 토양에서 질산염 이온의 확산도는 10-6cm2 sec-1 이고, 암모늄 이 온의 확산도는 10-1 cm2 sec-1 이며 , 그리고 인산염의 확산도는 10-8 cm2 sec-1 이다. 질산염 이온은 많은 농경지에서 충분히 높은 농도로 존재하며, 높은 확산계수를 갖고 있어서 균근~ 질소의 영양에 거의 영향울 주지 않는다. 영양영 흡수의 가장 큰 효과는 인에서 나타난다. 건조한 토양은 습한 토양보다 10-100 배 낮은 확산율을 갖는다. 그러 한 토양에서 인의 흡수는 균근곰팡이가 없을 경우 종종 제한된다. 일 반적으로 균근의 감염에 대해 양성적인 반응을 하는 식물의 성장은 인 과 같은 영양염의 농도가 용액상 a q ueous p hase 에서 낮은 농도로 존재 하나 흡착된 또는 고형의 저장물을 갖고 있는 토양에서 발견된다. 다 양한 밭 작물들이 균근의 협생으로부터 혜택을 받기 시작하는 경우에, 가장 낮은 인의 토양 용액의 농도는 땅콩의 경우 O.lµg ml-1 부터 카
사바(서인도 제도산의 식물)와 S ty losan t hes 의 경우 1. 6µg m J -1 에 달 한다. 후자의 두 작물은 밭의 조건에서 성장하기 위해서는 균근의 감 염을필요로한다. 오렌지류 식물은 성간 뿌리 구조를 갖고 있고, 통상 균근의 감염에 강하게 반응한다. 그림 11.7 은 균근성의 신 오렌지의 어린 나무가 모 든 인의 처리 수준에서 균근곰핑이에 호의적으로 반응하는 것을 보여 준다. 반면에 트로야 오렌지는 오직 낮은 수준의 인의 농도에서만 호
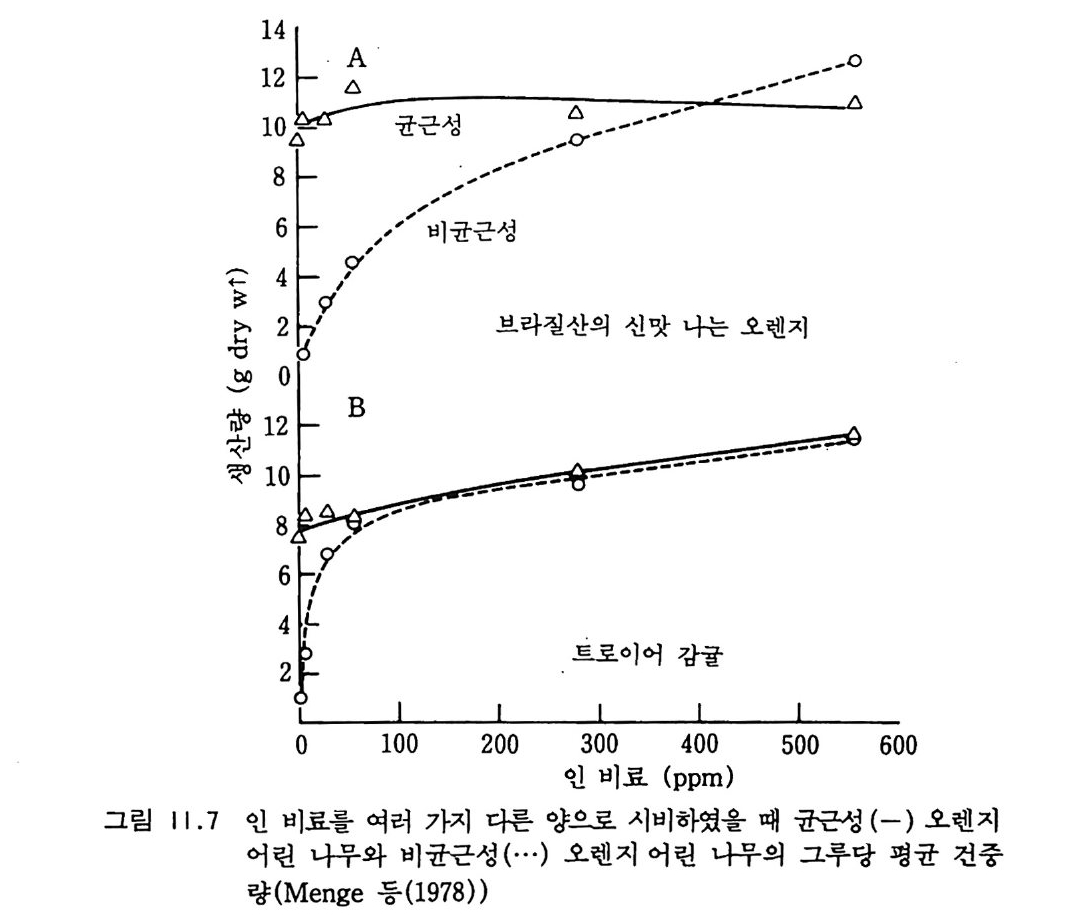 1:806~I- _4一 :2 b0’ ’ ,巳1균 ,, ’ 근2/ B,성u,1 균 zz l 0,근 2 入 ~。/ ? t / / ^b-- tt -- t- 츠--- ---- ,o^
1:806~I- _4一 :2 b0’ ’ ,巳1균 ,, ’ 근2/ B,성u,1 균 zz l 0,근 2 入 ~。/ ? t / / ^b-- tt -- t- 츠--- ---- ,o^
의적인 반응을 보여 준다. 그림 11.8 에 나타난 땅콩에 대한 자료는 많은 식물에 대해 얻어진 자료에 대해 전형적인 것이다. VAM 균으 로 접종하면 인 비료의 첨가로 가능한 잠재 수확량의 30 一 60% 가 얻어 진다. 대부분의 식물은 적절한 농도의 인과 질소가 있을 때 균근의 감 염을 억제하는 능력이 있다. 그러나 실험적으로 인 수준이 높은 토양 에서도 감영할 수 있는 균을 분리해 낼 수 있다는 것을 입증했다. 그 러므로 그 성장 반응곡선(그림 11.8) 을 더 많이 벗어난 높은 인 수준 에서도 균근의 효과를 증가시키는 것이 가능하다. 집약 농업은 값비싼 인 비료의 공급원들을 이용할 여유가 있으나, 세계의 넓은 지역들은 인의 침적물을 갖고 있지 않으며 인울 수입할 여유도 없다. 심지어는 선진국에서도 초지와 산림과 같은 광범위한 경
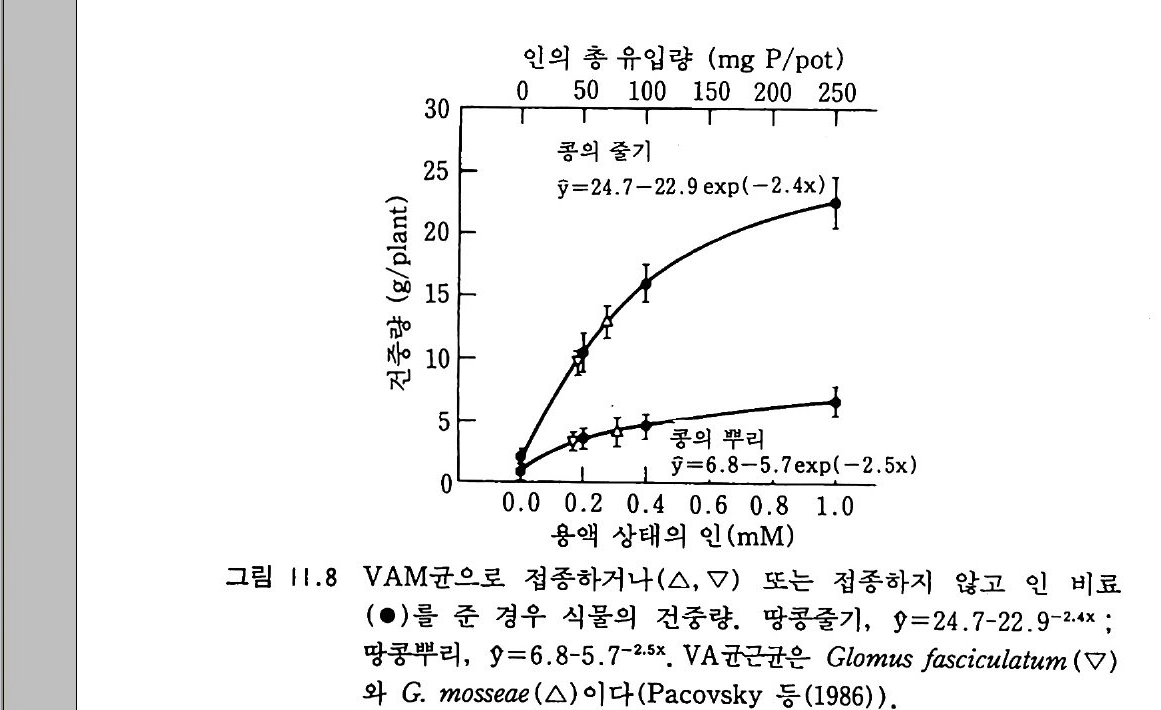 인의 총 유입 량 (mg P/po t)
인의 총 유입 량 (mg P/po t)
영체계에 인의 경제적인 시비를 할 수 없다. 아프리카와 남미의 사바 나 같은 많은 토양은 높은 인 고정 능력을 갖고 있다. 균근곰팡이는 그러한 상황에서 혜택을 주는 듯하다. 인의 흡수 의에도 균근균은 최 근에 무기화된 유기 인이 무기 형태로 고정되기 전에 가로채어 이용할 수있는듯하다. 일반적으로 균근에 감염되기 쉬운 식물은 자연 환경 내의 균주로 이 미 감염되어 있다. ECM 감염에 대한 반응은 자연산 균근이 멸균을 통해 제거된 묘포 nurser i e 허]서 매우 쉽게 얻어진다. 다른 예로 균근 이 존재하지 않으면 성장이 실패되는 새로운 지역으로 ECM 나무의 이식을 들 수 있다. 밭의 조건에서 VAM 을 갖고 행한 실험들은 통상 그렇게 놀랍지 않다. 그러나 밭에서 VAM 을 콩과 식물과 비콩과 식 물에 접종한 많은 실험둘은 낮은 수준 또는 적절한 수준의 유효 인이 있고, 또한 적은 수준의 자연산 균근이 있는 토양에서 약간의 증가가 있음을 나타냈다 (Ha y man (1 987)). 균근 내의 인의 이전에 대한 기작은 세포질 유동에 기인한 것으로 믿어지고 있다. 다중인산염 p ol yp hosp ha te{는 균사에 있는 인의 상당한 부분을 차지하며, 세포질 유동에 의해 이전될 수 있다. 다중인산염은 균근의 균사와 ECM 의 균초(외피)에서 모두 인의 한 저장 형태로 역 할을 할 수 있다. 다중인산염의 불용해성은 내부의 인 농도롤 낮게 유 지하며, 따라서 토양의 용액으로부터 계속적인 인의 흡수를 가능하게 한다. 식물로의 영양영 이전은 VAM 에서는 arbuscul 타t 가로질러서 일 어나며, 난초와 진달래과의 나선형 균사를 통해 그리고 ECM 의 세포 내 하티히 망을 통해 일어난다. 섬세한 균사의 구조와 식물 세포의 특 별히 발달된 원형질막p lasmalemma e.9-J 밀집한 연합이 영양염 이전의 장소를 제공하는 것으로 간주되고 있다. ECM 의 균초와 하티히 망은
9-14 개월의 존속 시간을 갖는다. VAM 의 arbuscule~ 난초와 진 달래과의 가는 나선상 균사는 연속적으로- 형성되고 재형성된다. 두 가 지 형태의 내부 균의 구조에 대한 경우 대사회전 시간은 4-15 일로 관 찰됐다. 질소에 대해서는 인에 대해 알려진 효과만큼 잘 알려져 있지 않다. 그러나 질소에 대한 실험은 인의 경우처럼 그렇게 간단하지는 않다. 암모니아의 흡수가 균근에 의해 더욱 쉬워진디는 - 사실이, 특히 숲의 나무들의 ECM에 대해 정립돼 있다. 균근균이 있음으로 해서, 그렇 지 않으면 이용되지 않았을 유기 질소의 증가된 이용도에 대한 두 가 지 예가 있다. 하나는 전달래과 균근이고, 다른 하니는- VAM 이 다. 15NH4+ 의 존재하에서 동위원소 희석 실험은 균근 식물의 뿌리로 더 높은 비율의 마{가 유입됨을 보여 주었다. 이는 균근 식물이 비균 근 식물보다 비료원이 아닌 질소에 더 큰 접근 및 이용 능력이 있음을 제시해 주었다 . 오칙 몇 종류의 균근곰팡이만이(예, 담자균) 질산염 환원효소가 있 는 듯하다. 이 효소는 질산염 이용의 선행 조건이다. 암모늄은 뿌리 지역을 벗어나서 다른 곳으로 이전되기 전에 유기 화합물로 고정된다. 유기 화합물로 암모늄을 고정시키기 위한 생합성에 필요한 구연산 회 로의 중간 산물들이 뿌리로 운반되어 내려오거나, 또는 뿌리의 포스포 에놀피루브산염 (ph osph oenolpy ruv ate , PEP) 카르복시화 효소계에 의해서 이산화탄소의 고정을 통해 현장에서 생성된다. 균근균에서 유 기 화합물로의 질소의 전입 기작은 '앞서 논의된 질소의 부동화와 질소 고정과 유사하다. 이산화탄소를 생성하는 것으로- 알려진 기관인 뿌리 에서 “CO2 를 고정함은, 비록 전체 탄소 흐름의 수지균형의 면에서 보면 중요하지 않으나, 탄소 추적자 (UC) 를 이동의 지표로서 이용하는 연구와 uc 실험에 기초한 에너지 요구의 계산에 영향을 줄 수 있다.
아연과 구리가 균근에 의해서 흡수될 수 있음이 입증되었다. 이들 이온이 결핍된 조건에서 식물의 수확이 증가하였다. 그러나 구리와 아 연의 부족 현상은 흔히 나타나는 것은 아니다. 그리고 이러한 결핍증 은 비료를 잎에 뿌려 주거나 토양에 공급함으로써 적은 양으로도 쉽게 극복될 수있다. 균근에 의한 중금속으로부터의 보호 현상이 아연, 카드뮴, 망간의 농도가 높은 폐광지에서 자라는 식물에서 발견되었다. 높은 망간량을 가전 토양에서 자라며 VAM 으로 감염된 콩과 식물 Vi c ia fa ba 에서 망 간 독성으로부터의 보호가 또한 입증되었다. 중금속이 진균과 숙주 세 포 사이의 간극 매질 int e r fa cial ma t r ic e 띄 펙틴 화합물(헤미셀룰로오 스) 내의 카르복시기들과 결합하는 것으로- 생각되고 있다. 또한 광산 의 중금속으로 오염되어 버려진 토양에서 자라는 식물들이 이들 금속 에 더 큰 저항이 있도록 선택된 균근을 갖고 있는 것이 입증되었다. 11-3-2 다론 영향들 건조한 환경에서 자라는 식물들은 상당히 많은 경우 균근성이며, 균 근성 식물이 가뭄에 저항성 이라는언급이 많다. 그러한 자료의 해석 은 인과 수분 이용의 상호작용에 의해서 어려워진다. 증가된 인의 수 준은 일반적으로 가뭄에 대한 저항력을 증가시킨다. VAM 균에 대해 이루어전 계산들은 균사를 통해 식물로 이동될 수 있는 물의 양이 식 물의 성장과 생존에 영향을 줄 만큼 충분히 크지 않음을 지시해 준다. 그러나 ECM 균에 대한 결과는 진균의 균사가 식물의 수분 퍼텐셜울 변화시킬 수 있는 능력이 있음을 보여 주었다. 습한 토탄에서 성장하 는 균사를 통해서만 유일하게 물이 공급될 때, 어린 식물은 10 주 동 안 건강한 상태로 유지되었다. 그러나 그 균사를 찰랐을 때 1 주 내에
색깔이 없어지고 죽게 되었다. 균근의 협생은 특히 ECM 에서 변화된 뿌리를 파생시킨다. 균근의 두꺼운 의초는 물리적 보호를 제공한다. Phyt op h th o ra, Py thi u m , Rhiz o cto n ia 같은 병원균으로부터의 보호와 선충류의 공격으로부터의 보호가 입증되었다. 이러한 기작은 기계적인 보호이며, 또한 항생물 질의 생성도 하나의 역할을 할 수 있다. 균근곰팡이는 특히 토성이 거친 사토에 대한 입단 형성 효과를 갖고 있다. 사구의 안정화 그리고 폐광지의 안정화는 광범위한 균근의 생성 을 갖는 식물에 의해 조성된다. ECM 에 의한 호르몬의 생성이 이러한 공생에 전형적인 야구장갑 모양의 뿌리 형성에 관여한다. VAM 공생에 양 二호르몬, 인 영양 그 리고 광합성의 상호작용은 판정하기가 더 어렵다. Allen 등은 1980 년 VAM 공생을 가전 풀의 뿌리와 잎에서 높은 수준의 사이토키닌 c yt ok i n i峰 발견했다. 그들은 식물에서 사이토키닌 증가가 광합성, 증산율, 인의 홉수 그리고 이온의 이동에 영향을 준다고 발표했다. 11. - 4 균근 식물 협생에서의 탄소 흐름 모든 공생 관계에서 숙주로부터 균근균으로 탄소의 흐름은 곰팡이의 성칭에 필요한 탄소를 공급한다. 이에 대한 예의는 난초 균근의 경우 이다. 셀룰로오스와 리그닌을 분해하는 능력을 가진 ECM 균이 그 어떤 종류의 탄소를 이용하는지는 알려지지 않았다. VAM 의 경우, 식물 탄소를 당지방질g l y co lipi追i 전환함은 곰팡이에 의한 기질의 축 적을 이루는 하나의 기작이다. ECM 의 경우 트리할로오스t rehalose 또는 만니톨 m annit ol 처럼 식물 세포에 의해 죽시 대사되지 않는 탄
수화물의 생성은 농도 구배를 제공하여 수더쿠오 :'.':::.sucrose7} 곰팡이 로 이동 가능케 하는 유사한 가능을 가질 수 있다. 뿌리 무게에서 균 근균이 차지하는 부분은 사탕수수속 식물의 섬유성 VAM 근계에서 그리고 180 년 묵은 전나무속 Ab i es 의 ECM 에서 약 3% 이다(표 11. 3) . VAM 콩과 식물, 비콩과 식물 그리고 23 년생 ECM 나무에 서 12-16% 의 값이 발견된다. 표 1 1. 4 는 여러 “C 연구에서 식물에 의해 광합성된 총 탄소의 4-14% 가 공생자에게 배당됨을 보여 준 다. 14c 를 사용하지 않고 연중 다른 시기에 뿌리를 채취한 다음 세척 울 시행한 연구 결과는 삼림군집에서 탄소 대사회전의 50% 까지가 섬 세한 뿌리와 그들 곰팡이의 대사회전에 기인할 수 있음을 나타냈다. 그러나 그와 같은 높은 값은 방사성 표지를 이용한 “C 연구에 의해 확증되지 않았다. 더 좋은 영양에 기인한 성장 증가와 미생물 동반자의 필요성 사이의 균형에 대한 설명은 “C 분배 실험으로 가장 잘 결정될 수 있다. 땅콩 과 Glomus 균근균의 공생에서 지상 및 지하 부분으로의 탄소의 분배 가 그림 11.9 에 나타나 있다. 이들 식물에서 순 광합성물의 약 50% 가 어린 가지에서 발견되고, 6% 가 어린 가지에 의한 밤 동안의 호흡 에 의해 배출되었다. 그리고 42% 는 지하로 이전되었다. 이 42% 는 뿌리혹, 뿌리 그리고 균근균으로 거의 균등하게 (12, 13, 17%) 분배 되었다. 뿌리의 성장은 식물 탄소의 8% 를 차지하고, 뿌리의 호흡은 5% 를 차지했다. 뿌리혹은 고정된 UC 긱 2% 를 부동화시켰으며, 10% 를 호흡으로 소비했다. VAM에서 곰팡이는 뿌리 내의 균사와 토양 내의 뿌리의 균사로 구성되어 있다. 그림 1 1. 9 는 두 구성 요소 의 동등한 중요성을 보여 주고 있다. 죽 식물 C 긱 2.8% 를 나타내 고, “C 호흡의 14% 를 차지한다. 적은 생물량 생산에 비해서 상대적으로 높은 미생물 호흡에 따른 손
표 11.4 공생자에 대한 배당과 광합성에 대한 VAM 균의 효과 공생자에 탄소 흡수*(%) 곰팡이 숙주 대한(% 배) 당 (증가된 광합성) Glomus mosseae Vicia fab a 10 21 Glomus mosseae Vicia fab a 5 8 GGlloommuuss ffaass ceti cc uu llaattuu mm SGolyrgc hin ue m m baixc o lor 144 —2201 Glomus mosseae Alliu m por rum 12 13 ·잎의 건중량 그램당 흡수된 탄소로서의 광합성률 실은 토양의 다른 미생물군들과 균근의 생물들을 구분시킨다 (Harr i s 와 Paul(1987)). 정상적인 토양의 미생물군은 그들의 생물량으로 기질 탄소의 고정에 있어서 높은 효율을 갖고 있다(제 5 장과 제 6 장을 참 조). 그러나 공생하는 미생물들이 탄소를 주로 공생하는 미생물의 성 장을 위해서만 사용할 경우 그들의 공생적 기능을 이행할 수 없는 것 이다. 대기 질소의 고정은 그 비용이 높다는 사실과, 공생하는 균근성 곰핑이에 의한 인의 홉수와 전이에 들어가는 비용은 또한 미생물 공생 자에 의해 받아들여진 탄소의 대부분이 성장보다는 영양염의 흡수에 이용되어야 할 것임을 요구한다. 많은 연구들에 의하면 식물들은 자신의 공생 미생물이 요구하는 양 울 보상하기 위해 식물의 광합성률을 증가시킨다고 한다. 광합성률의 증가는 어린 식물에서 영면적 증가와 잎의 단위무게당 고정된 이산화 탄소량의 증가를 통해서 일어날 수 있다. 여러 다른 식물을 이용한 이 분야에 대한 연구와 균근 공생 미생물의 효율에 대한 연구는 계속되어 하나의 유용한 연구 분야임이 입증되어야 한다. 곰핑이와 뿌리혹박테 리아의 형태에 있어서의 상당한 변이가 있음이 밝혀졌다. 이러한 자연
 순 홉수량 205
순 홉수량 205
적 이질성온 분자 유전학에 의해서 더욱 증가될 수 있으며, 이는 생물 학적인 수단을 통해 영양염 흡수를 증가시킬 가능성을 제시해 준다. 11-5 연구 방법론 VAM 균의 강겸 정도는 일반적으로 감영된 각각의 뿌리 부분의 백 분율을 관찰함으로써 측정된다. 이는 KOH 로 뿌리를 세척하고 푹신
레드fu chs i n red 같은 염색 물질로 염색한 후에 현미경으로 관찰함을 통해 이루어진다. 그러나 그 결과는 곰핑이의 탄소와 관련하여 해석하 기 어렵다. 모래 또는 버미쿨라이트 verm i cu lit터] 식물과 균군균-을 포 함하는 계에서 글루코사민g lucosam i ne 의 함량을 결정하여 곰팡이 조 직의 양을 측정하는 것이 가능하다. 이는 글루코사민이 키틴의 성분으 로 곰팡이의 세포벽에 존재하나, 식물에는 존재하지 않기 때문이다. 그러나 비균근 곰팡이도 또한 글루코사민을 포함하기 때문에, 현장에 서의 비균근 곰팡이의 존재는 이러한 기술의 적용을 불가능하게 한다. 따라서 “CO2 를 이용하여 VAM 의 글루코사민을 단기간의 노출 동안 에 표지를 할 수 있어야 한다. 균사로의 140 긱 이전은 통상 방사성 자동사전법에 의해 측정되어 왔 거나 또는 균사의 일부를 잘라서 방사성 양을 측정하여 이루어졌다. 인의 흡수는 토양으로 32 p의 용액을 첨가하여 이루어진다. 방시능링: 의 측정은 유기 인 또는 불용성 인으로부터 기인한 다른 형태의 인의 흡수에 관련한 용액상 인의 흡수 계산울 가능하게 한다. 뿌리 절단 기 법 sp lit-r oot t echn iq u e{본 균사를 32P 의 용액에 집어넣게 되며, 식물 로 32 p의 전이룰 측정하는 기술이다. VAM 균의 포자는 크기가 10-400 µm 에 달한다. 포자는 비중이 1. 2 인 50% 글리세롤에 뜨게 하여 통기시키는 기술에 의해 토양으로 부터 분리된다. 또는 밀도경사 원심분리 방법에 의해 균사와 유기 잔 여물질로부터 포자를 분리할 수 있다. 일반적으로 VAM 균은 순수 배양이 어렵다. 그러므로 VAM 균의 성장은 살아 있는 숙주식물과 관 련해서만 연구될 수 있다. 이는 이들 균에 대한 생화학적 및 분자생물 학적 연구를 크게 방해하며 균근균의 집종균i noculum 의 · 생산 가능성 울제한한다•
참고문헌 Allen, M. F., Moore, T. S., and Chris t e n sen, M. (19 80) .Phy toh ormone chang e s in Boute l oua gr aci lis inf e c te d by vesic u lar arbuscular my c orr-hiz a e. I. Cy tok in i n inc reases in host pla nt, Can. ]. Bot. 58, 371-374. Brown, M. F., and Ki ng , E. J. (19 82) . Morph olog y and his t o l og y of vesic u lar arbuscular my c orrhiz a e, In Meth o ds and Pr inc ip le s of My c orrhiz a l Research (N.C. Schenk, ed.) , pp. 15-22. Am. Phy top a th o l. Soc., St, Paul. Mi nn esota . Harley, J. L., and Smi th, S. E. (19 83) . My c orrhiz a l Sym bio s is . Academi c Press, L ondon. Harris , D., and Paul, E. A. (19 87) . Carbon req u ir e ments of vesic u lar-arbus-cular my c orrhiz a e, In Ecop h ys i o l ogy of VA My c orrhiz a l Plants (G. R. Safir , ed.) . CRC Press. Boca Rato n , Florid a . Hay m an, D. S. (19 87) . VA my c orrhiz a s in fiel d crop sys te m s. In Eco- phy s i o l ogy of VA My c orrhiz a l Plants (G.R. Safi r, ed.) . pp. 171-192. CRC Press, Boca Rati on , Florid a . Ki nd en, D. A., and Brown, M. F. (1976). Electr o n mi cr oscop y of vesic u lar arbuscular my c orrhiz a e of ye llow po p la r. I V. Host endop h y te int e r ac- tion s durin g arbuscular dete r io r ati on , Can. ]. Mi cr obio l . 22, 64-75. Meng e , J . A., Labanauskas, C . K., Joh nson, E. L. V., a nd Platt , R. G. (19 78) . Part ial substi tut i on of my c orrhi za l fun g i for P fer t iliz a ti on in the gree nhouse cultu re of cit ru s, Soil Sci . Soc. Am. ]. 4 2, 926-930. Moli na , R., and Trapp e , J. M. (19 82) . Ap plied aspe cts of ECM, In Advances in Agricu ltu r al Mi cr obio l og y (N. S. Subba Rao, ed.) , pp. 305 -324. Butt er wort h , London. Pacovsky , R. S., Beth le nfa lv ay, G. J., and Paul, E. A. (19 86) . Comp a riso ns betw een P-fe rtilize d and my c orrhiz a l pla nts , Crop Sc i. 26, 151-156. Sanders, F. E., Mosse, B., and Ti nk er, P. B. (19 76) . Endomy co rrhiz a s. Aca-demi c Press, London. Trapp e , J. M. (19 87) . Phy lo g e neti c a nd ecolog ica l aspe cts of my c otr o p h y in th e ang ios pe rms from an evoluti on ary sta ndp o in t, In Eco- phy s iolo gy of VA My c orrhiz a l Plants (G.R . Safir , ed.) , pp. 5-26. CRC
Press, Boca Rato n , Florid a . Trapp e , J. M., and Berch, S. M.(1985). The pre his t o r y of my c orrhiz a e, In My c orrhiz a e,(R . Moli na , ed.) , pp. 2-11 . For. Res. Lab. Corvall is, Oreg o n. Trapp e , J. M. , and Schenk, N. C.( 19 82). Taxonomy of the fun g i for mi ng endomy c orrhiz a e, In Meth o ds and Prin c ip le s of My c orrhiz a l Research (N. C. Schenk, ed.), pp. 1-9. Am. Phy top a th o l. Soc., St. Paul, Mi nn esota . 추가로 읽을 거리 Barea, J. M., and Azzon-Ag uilar , C. (19 83) . My co rrhiz a s and the ir sig nifica nce in nodulati ng nit ro g e n-fix i n g pla nts , Adv. Ag r on.36, l -54. Brownlee, C., Duddrid g e , J. A., Malib a ri, A., and Read, D. J. (1983) . The str u ctu r e and fun cti on of my c elia l sys te m s of ECM roots wi th spe - cial refe r ence to the ir role in for mi ng int e r pl a nt connec tion and pro vid i n g pa th w ay s for assim i lat e and wate r tra nspo rt , Plant Soil 71, 433-443. Fog el , R., and Hunt, G. (1979) . Fung a l and arboreal bio m ass in a weste r n Orego n Doug la s fir ecosys t e m : Dist r i b u ti on pa tt er ns and tur nover, Can. ]. For. Res. 9, 245-256. France, R. C., a nd Reid , C. P. P. (19 83) . Inte r acti on s of N and C in the ph y si o l og y of ECM, Can. ]. Bot. 61, 964-984. Hall, JF. Re a., tua nre ds Aofb bthoet t ,E Lnd. Kog. a (1n9a 8.c1e) a .e .P 3hrodto egd r .a , pph pi. c 1 S -2li7d. e ICmoelrlemcatiy o nA Ig lrluicsutr l at ut ir nagl Research Centr e and Soil Sc ien ce Dep a rt me nt. Univ e rsit y of Weste r n Austr a li a, Pert h. Moli na , R., ed. (19 85) . My co rrhiz ae . For. Res. Lab., Corvall is, Orego n. Mosse, B., Str i b l ey, D. P., a nd LeTacon, F. (1981) . Ecolog y of my c orrhiz a e and my c orrhia l fun g i, Adv. Mi co rob. Ecol. 5, 147-210. Powell, C. L. (19 82) . My c orrhiz a e. I n Expe ri me nta l Mi cr obia l Ecology (R.J.
Burns and J. H. Slate r , eds.) , pp. 447-471 . Blackwell, Oxfo r d. Reid , C. P. P. (19 84) . My co rrhiz a e : A root/ s oil int e r f ac e in pla nt nutr i - tion , ASA Sp ec . Pub!. 4 7, 29- 50 . Roth w ell, F. M. (19 84) . Ag greg a ti on of surfa c e mi ne soil by int e r acti on betw een VAM fun g i and lig nin deg rad ati on pro ducts of lespe deza, Plant Soil 80, 99- 10 4. Ruehle, J. L., and Marx, D. H. (19 79) . Fib e r, foo d, fue l and fun g a l sym bio n ts , Scie n c e 206, 419. Ti nk er, P. B. H. (19 82) . My c orrhiz a s : The pre sent pos it ion , Proc. Int. Cong . Soil Sci. 1 2th . 1982, pp. 150- 16 6.
제 12 장 토양에서 인의 변환 12-1 서론 인은 탄소나 질소처럼 생물에 의해서 대기로부터 획득되거나 대기로 손실되는 과정이 없으며, 환원된 형태의 탄소와 질소와는 대조적으로 미생물적 산화에 있어서 주요 에너지원의 역할을 하지 않는다. 그럼에 도 불구하고, 토양 생물들은 토양의 인 순환에 본질적으로 연관되어 있다. 토양 생물들은 무기 인의 용해 작용 solub ili za ti on 과 유기 인의 무기화 작용에 관여한다. 또한 토양 유효 인 avail ab le soil ph osph o- ru 려 부동화 작용에서 중요하다. 바록 미생물의 생물량이 고등식물보 다 적지만, 인의 함유량(%)은 아마도 10 배 정도 많을 수 있다. 또한 1 년 내에 다양한 그룹의 토양미생물들은 몇 세대에서 많은 세대에 걸 친 성장을 한다. 그 결과 미생물에 의한 연간 인의 흡수는 고등식물에 의한 인의 흡수를 종종 초과한다. 다행히 인의 미생물적 부동화 작용 은 길게 지속되는 것이 아니고, 수지면에서 볼 때 식물에게 유익할 수 있다. 단기간의 생물 활동에 의한 인의 부동화는 장기간 광물질로 고
정되어 있는 일부 토양의 인을 이용하게 해주기 때문이다. 12-2 인 순환의 범지구적 양상 자연에서 인은 다양한 유기 또는 무기 형태로 존재하나, 물에 녹지 않거나 아주 적게 용해되는 무기 형태로 주로 존재한다. 지각에서 인 의 총량은 l015 톤 정도이다. 인은 주로 인회석 a p a tit죠녁i 존재하며 , 기본 공식은 M 1 。 (P0.)6X 러다. 흔히 M 은 칼슘이며, 음이온 (X) 은 불소fl uor i ne 이다. 음이온은 또한 CI-, OH-, 또는 탄산염 이온이 있 다. 그래서 불화, 염화, 수산 그리고 탄산염 인회석이 존재한다. M 과 X 의 다양한 치환과 결합은 자연에서 약 200 가지 형태의 인이 출 현하게 한다. 탄산염 인회석이 많이 함유된 인광석들이 비료원으로서 가장흔히 채광된다. 표 |2.1 지구의 주요 인 저장소* 저장소 • 총 인 (X 1012 kg ) 육지 토양 96-lbO 광산의 암석 19 생물군 2.6 담수 (용존) 0 . 090 해양 퇴적토 840,000 용존 무기인 80 입자상 쇄설물질 0. 65 생물군 0. 05 0- 0 .12 * 자료 : Bolin 등(1 983)
표 |2.2 캐나다 평원의 3 종류 초원 토양에서 장기적인 경작에 의해 나타 난 인 함량의 변화* 토양종류 원산지 초원 경작토 •• 손실(%) Blain Lake 유기 탄소 (m g g-1 ) 47.9 土 10.2 32.8 士 5.2 32 총 인 (µg g-1 ) 823 士 92 724 土 53 12 유기 인 (µg g-1 ) 645 土 125 528 土 54 18 무기 인(µg g-1 ) 178 士 47 196 士 8 미량 South e rland 유기 탄소 (m g g-1 ) 37.7 士 6.5 23.7 士1. 8 37 총 인(µg g기 756 士 28 661 土 31 12 유기 인(µg g기 492 士 5.2 407 土 30 17 무기 인 (µg g-1 ) 254 土 44 254 土 19 미량 Bradwell 유기 탄소 (m g g기 32.2 土 8 17.4 士1. 6 46 총 인(µg g-1 ) 746 土 101 527 土 15 29 유기 인(µg g-1 ) 446 土 46 315 土 21 29 무기 인(µg g-1 ) 300 土 84 212 士 46 29 ·자료 : Ti es sen 등 (1982) •• 경작은 각각 90, 75 및 60 년임 표 12.1 은 해양 저장소와 육지 저장소에 함유된 인의 양에 대한 추 정값을 나타내고 있다. 가장 큰 저장소는 해양의 퇴적물이다. 해양 퇴 적물은 인의 소멸지 s i nk 이며, 풍화 그리고, 또는 생물상에 의해 작지 만 꾸준히 유출되는 육지 인의 배출구이다. 침식과 인간 활동에 의한 해양으로의 폐기물 유출은 육지에 있는 인의 이동의 주요 공급원이다. 식물성 인은 대체로 잔존물과 유기 쇄설 입자 orga n ic detr itus 9 .] 미생물적 무기화 작용에 의해 재순환된다. 보충되는 인이 없이 경작물 을 장기 재배할 경우 토양에서 인의 고갇울 초래한다. 1982 년
Ti ss en 등에 의해 수집된 자료는 그와 같은 손실을 예시해 준다(표 12.2). 비료 인 또는 동물성 퇴비의 지속적인 첨가는 토양 인의 비옥 화를 가져오며, 또한 토양의 탄소와 질소의 증가를 유발시킨다. 인이 탄소와 질소를 부동화함에 있어서 조절을 하는 중요 원소란 좋 은 증거가 있다. 고전적이며 상당히 논의된 논문에서 Red fi eld 는 인 (P) 이 해양의 탄소 (C)' 질소 (N), 그리고 황 (S) 의 순환을 조절한다 는 가설을 제시했다. 그는 해양의 C: N: P 비가 부유 생물의 C: N: P 비와 평형을 이룬다는 접에 주의했고, 다음의 일반적 관계가 일어 난다고믿었다.
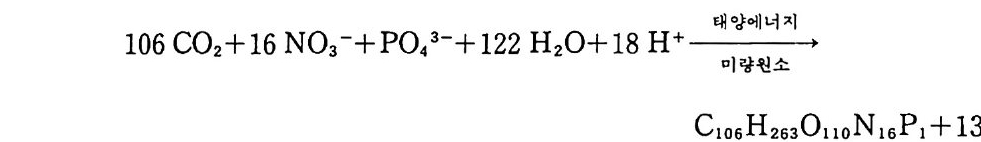 106 CO2 + 16 N03-+PO/-+ 122 H2 0 +18 H+ ~ 태미 양 량 에 원너 소지
106 CO2 + 16 N03-+PO/-+ 122 H2 0 +18 H+ ~ 태미 양 량 에 원너 소지
많은 육상 상황에 대해서 C: N : P 비가 어떠한가를 표 12.3 에 나 타냈다. 수생 조류와 토양 세균은 대략 6 : 1 의 비슷한 C: N 비를 갖 는다. 조류는 세균보다 높은 C: P 비를 가지나, 토양 유기물 (SOM) 에서 발견되는 C: P 비의 범위에 있다. Walker(l965) 의 초기 연구와 공동 연구자들은, 토양 유기물에 함 표 12.3 생물과 토양 유기물에서 C: N : P 비 자연 성분 C N P 해양조류 106 16 1 토양세균 31 5 1 초원의 토양 미개간지 191 6 1 경작지, 시비된 토양 119 9 1 약간 풍화된 토양 80 5 1 상당히 풍화된 토양 200 10
유된 C, N, S, P 의 축적은 토양 모재의 인의 함량에 달려있다는 가 설을 세웠다. 관리되는 초원의 비옥도가 비료 인의 시비로 증가되었 고, 그리고 총 유기물 양이 증가되었던 호주와 뉴질랜드에서의 실제 농사 경험에 의해 이 가설은 입증되었다. 미국 중서부의 일부에서 옥 수수 땅콩 윤작과 같이 과량으로 비료가 이용되는 경작 토양에서의 유 효 인 함량은 현재 대부분의 수확에 필요한 것보다 더 높다. 뉴질랜드 의 초원에서 발견된 것처럼 더 높은 인의 함량이 높은 유기 탄소와 질 소의 축적을 가져온다고는 현재까지 아무도 지적하지 않았다. 뉴질랜 드 초원의 토양은 경작된 토양에 대한 Redfi el d-Walker 가설의 적 용에 좋은 실험 대상이 될 수 있다고 본다. 12-3 무기 인 인의 무기 형태는 철, 알루미늄, 칼슘, 불소 또는 다른 원소들과 결 합하여 나타난다. 토양에서 인의 수백 가지의 조합은 이에 대한 총괄 적인 논의를-개별적으로 그리고 구조적으로보다는 추출 가능성에 의거하여―~필요하게 한다. 앞에서 언급한 것처럼 대부분의 토양 인 산염은 물에 잘 녹지 않거나 또는 매우 적게 용해된다. 인이 용존성 염으로서 토양에 첨가될 때, 인은 고정되거나 부착되어 첨가된 인을 물로 다시 추출하면 거의 추출되지 않는다. 그 대부분의 인은 희석된 산 또는 중탄산영 용액에 의해서도 추출되지. 않는다. 그 보유된 인의 이러한 부분을 흔히 고정된 인이라 부른다. 희석된 산 또는 중탄산영 에 의해 추출될 수 있는 부분을 유효 인이라 부른다. 이 부분이 생물 에 의해 이용될 수 있는 토양 인의 양으로 간주된다. 이렇게 측정된 유효 인은 부분적으로- 무기 인이며, 그리고 부분적으로 유기 인이다.
토양의 총 인 중에서 수지로 추출할 수 있는 부분을 활성 인 labil e p hosp horus 이라 부르고, 이는 주어전 시간 동안에 등이온 교환 iso io n ic exchan g려] 의해 용액으로- 유입될 수 있는 토양 인의 부분으 로정의된다. 12-4 용액 인 토양 용액의 인 농도는 0.1 pp m 에서 l pp m 의 수준이다. 이 범위 롤 초과하는 경우는 아주 드물다. 인의 용해도는 흔히 이온_이온 연합 assoc iat i on , 산도 효과 그리고 접토 광물의 표면에 흡착한 인의 양에 의해 복잡해전다. 용액 인은 활성 인과 빨리 평형을 이루며, 대부분의 토양에 대해 용액 인과 활성 무기 인의 비는 선형적인 관계를 가진다. 식물은 필요한 인을 용액 집소 soluti on po ol 에서 구한다. 인을 세포 질로 이동하는 데 대사에너지가 소비되며, 세포질 내 인의 농도는 토 양 용액 내의 농도보다 50-100 배 높을 수 있다. 밭에서 하루에 뿌리 l g당 1-2 µmol 의 인을 흡수하면, 하루에 8-10 %의 비율로 성장하는 식물은 적합한 인의 농도를 유지할 수 있는 것으로 계산 결과가 나타 났다. 식물 전이 pla nt tra nslocati on 7} 일어날 수 있기 전에 인의 최 소 수준이 뿌리에서 획득되어야 한다. 인의 전이는 초본과 식물의 경 우 약 0.05% 의 최소 수준 아래에선 전혀 일어나지 않으며, 최소 수 준과 약 0.5% 의 상한값 사이에서 뿌리 인의 농도에 비례한다. 뿌리 인 농도의 0.5 % 이상의 증가는 추가적인 전이의 증가를 가져오지 않 는다. 용액 집소로부터 뿌리의 흡수는 거의 이상적인 조건에서 식물 성장 기 동안 하루당 50-250 배까지 이 용액 집소의 재생과정울 필연직으로
수반할지도 모른다. 토양 생물은 유기 인의 무기화 작용과 활성 인에 대한 용해 효과에 의해 용액 집소의 재생에 공헌한다. 12-5 무기 인의 용해 토양 생물과 식물 뿌리는 토양 인의 용해에 있어서 주로 이산화탄소 와 유기 산의 생성을 통해 참여한다. 뿌리 또는 토양 생물에 의해 용 해되는 토양 인에 대한 정밀한 측정은 유기 인의 동시적인 무기화 작 용에 의해 복잡해진다. 무기 산으로 산성화에 의해 초인산염 sup er p hosp ha t es 이 상업적으로 널리 생산되기 전에는, 인광석을 되비 와 혼합함으로써 그리고 밭에 시비하기 전에 배양 기간을 둠으로써 인 산염의 미생물적 용해가 강화되었다. 용해를 일으키는 특정 세균을 분 리해 내는 시도가 있었으며, 그와 같은 생물을 토양 또는 씨의 접종체 로 사용하려는 시도가 있었다. 가장 자주 분리되는 균주는 Pseudomonas 와 Baczllus 이었다. 지난 몇해에 B .. mega te r i um var. p ho sp ha ti cum 이 p hos p hobac t er i~료 알려진 세균 접종체로 널리 사용되었다.비록 소련에서 몇십 년간 과도하게 사용되었지만,효 과가 있었다는 좋은 증거는 전혀 얻을 수 없었다. 총괄적으로 말해서 첨가된 접종체로부터 이득이 없었다 해도 토양 생물이 용해자로서의 중요성이 없다는 것은 아니다. 12-6 유기 인 유기 결합된 인은 통상 대부분의 토양에서 총 인 양의 30-50 %를
구성하나, 그 조성 범위는 낮게는 5% 에서 높게는 95% 까지 분포할 수 있다. 표 12.4 에 미국 서부 8 개 초원의 토양에서 나타난 총 인의 양과 유기 인의 양을 나타내었다. 유기 인은 토양에서 주로 피테이트 ph y tat e s , 핵산과 이들의 파생 물질, 그리고 인지질로서 나타난다. 피 틴 ph ytini폰 대개 이노시톨 육인산염 ino sit ol hexa p hos pha t e 이다(그림 12. 1) . 피틴은 미생물과 식물에 의해 합성되며, 토양에서 가장 안정된 유기 인의 형태이다. 피틴은 49 개의 아이오와 주 토양에서 총 유기 인의 평균 17%(3 - 52% 의 범위)를 차지하는 것으로 밝혀졌다. 토양 총 유기 인의 반 이상이 구조적으로 규명되지 않고 있다. 1-5 개 원자 의 인을 갖고 있는 이노시톨 고리화합물들이 토양에서 출현하고 있다. 이는 이노시톨 육인산염의 분해 산물일 수 있다. 토양 유기물에서 핵산 인의 출현에 관한 증거는 대개 간접적이다. 공급 물질들은 토양 생물과 식물의 잔여물에 의한다. 핵산 분자의 조 성은 토양 추출물의 가수분해에 의해서 규명 가능·하다. 시토신, 아데 닌, 구아닌, 우라실, 하이포잔틴 그리고 잔틴이 그것이다. 마지막 두 표 12.4 북미 초원지역 표충 10cm 에서 총 인과 유기 인 인(µg g-1 토양) 지역 총인 유기 인 Cott on wood, South Dakota 554 310 Br idg er , Monta n a 1234 675 Osag e, Kansas 251 227 Ale, Washin g ton 748 29 Jom ado, New Mexic o 445 37 Panta x , Texas 239 94 Bis o n, Monta n a 835 582 Pawnee, Colorado 345 131
개는 구아닌과 아데닌의 분해 산물이다. 토양의 총 유기 인 중 약 1% 만이 핵산 또는 핵산의 파생물로 규명될 수 있다. 분해되기 쉬운 핵산의 속성은 안정한 유기물로 전입되지 않는 특성과 더불어 토양에 서 핵산이 낮은 수준으로 유지되는 점을 설명해 주는 것으로 보인다. 토양을 알코올 또는 에테르로 추출시에 나타나는 유기 인은 인지질 의 존재를 말해 준다. 콜린은 이미 규명되었으며, 콜린은 레시틴의 가 수분해 산물 중 하나이다. 여러 연구들은 인지질 인이 간혹 34 pp m 의 농도로 관찰되는 경우를 보여주지만, 토양에서 단지 약 l-5 pp m 이 출 현하는 것을 보여 준다. 총 유기 인의 2/3 이상이 규명되지 않은 chernozemi c so il 에 관한 연구는 1-2% 가 인지질 인으로 보고하였 다. 당인산염은 더 적은 양으로 토양에서 출현한다. 당인산염 또한 쉽 게 분해될 수 있으며, 따라서 토양에서 총 유기 인에 대한 평균 잔류 시간인 350-2000 년에 비추어 볼 때, 핵산과 인지질과 함께 토양 총 유기 인의 잔류 시간에 큰 기여를 한다고 볼 수 없다. 토양의 생물량 안에 있는 인은 클로로포름 (CHCb) 으로 세포들을 용 해시킨 다음에 측정할 수 있다. 이렇게 한 후 중탄산염으로 추출을 하 고, 그 인의 값을 클로로포름으로 처리하지 않은 일정량으로부터 추출 된 인의 값과 비교하면 미생물 인의 추정치가 나온다. 산성도가 6.2-8.2 인 토양에서 32 p로 표지를 한 세포를 첨가한 후 클로로포 름으로 처리한 결과 40% 의 미생물 인이 회수되는 것을 보여 주 었다. 미생물 인의 계산은 다음과 같다.
 미생물 인 = 클로로포인름의으 회로수 배율출 된 인 = CHCo1. 4 3 P
미생물 인 = 클로로포인름의으 회로수 배율출 된 인 = CHCo1. 4 3 P
12-7 식물 뿌리-토양계에서 인의 유동 토양 용액에는 매우 낮은 수준의 인이 존재하여 식물의 요구량을 충 족시키기 위해서 자주 회전되어야 한다는 사실은 토양 유기물에 함유 된 인이 무기 인으로 변환됨이 전부는- 아니지만 주로 미생물에 의해서 이루어진디는 것을 암시한다. 식물 뿌리 또한 유기 인 분해효소 p hosp ha t ase 遷 생산하며, 식물들은 유기 인 분해효소를 생산하는 양 이 서로 다르다고 알려졌다. 그러한 차이는 식물 천이에 하나의 경쟁 요인이 될 수 있다. 또한 어떤 식물 종은 유효 인이 낮은 수준으로 있 울 때 체의로 많은 유기 인 분해효소를 생산하는 것으로 알려졌다. 미생물의 유기 인 분해효소는 토양미생물 중 대부분의 유기물 영양 방식의 미생물에 의해서 생산된다. 미생물에 의한 유기 인의 무기화
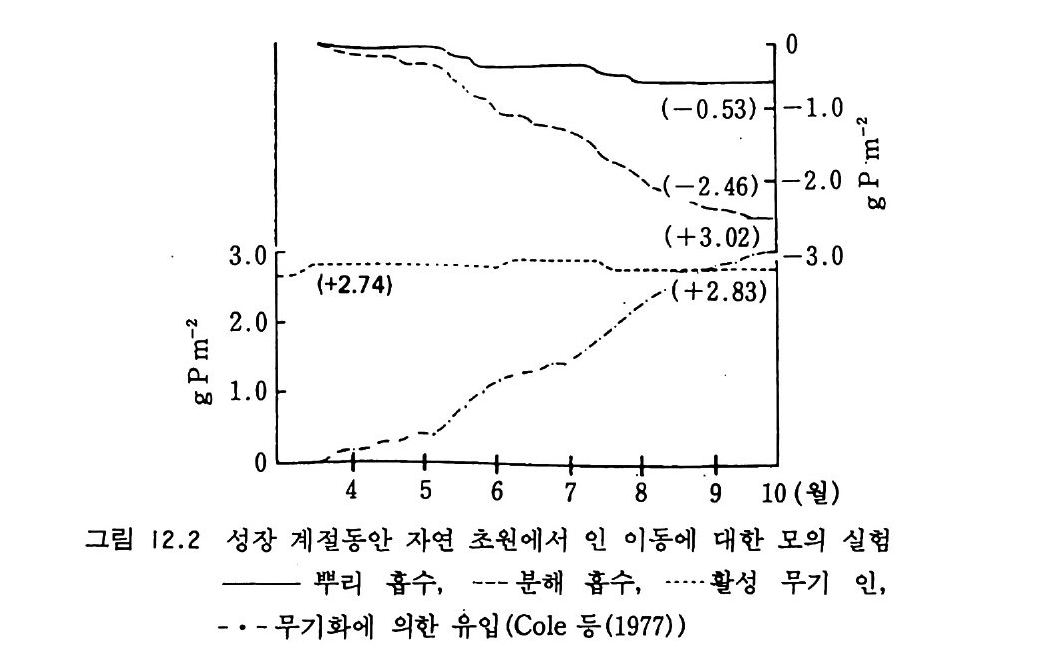 —- ---~-`、 `` '--...__ \\(-2(.-04.65)3 )〕7一-。 2l .. 0O ~:
—- ---~-`、 `` '--...__ \\(-2(.-04.65)3 )〕7一-。 2l .. 0O ~:
작용은 환경 변수에 의해 강하게 영향을 받는다. 적당한 알칼리도는 우기화 작용에 적합하므로 칼슘성 토양은 산성 토양에 비해 더 낮은 유기 인 함량을 가질 것으로 예상된다. 온도 또한 영향력이 있다. 따 라서 일부 목장은 이론 봄에는 뿌려진 인 비료에 반응을 하나, 그 후 에는 그렇지 않다. 그 후에는 토양 온도가 식물의 인 요구량에 적합한 속도로 인의 무기화 작용을 허용하기 때문이다. 한 번의 성장 계절 동안 초원 생태계의 유기 인 유동에 대하여 최선 의 가용한자료들에 의거하여 마련한모의실험이 그립 12.2 에 나타나 있다. 이는 그림 12.3 에 보여 준 여러 가지 토양 인의 상호작용 개념 에 의거한 것이다. 무기화된 인은 식물보다 토양 생물에 의해 더 많이 사용된다. 이는 이해될 수 있는 것으로 미생물군이 1-2% 의 인 함량 울 가지며 식물이 0.05-0.1% 를 가지고 있다. 두 계절 동안 활성 무 기 인의 양이 일정한 것은 식물의 인 요구량을 충족시킴에 있어서 무
기화 과정의 중요성을 강조하는 것이다 .l 인의 이동과 변환은 수확과 생태계 기능에서 가장 중요하다. 미생물의 일종인 균근곰팡이는 일반 토양 개체군보다 인의 이동에서 더 중요한 역할을 한다. 아마도 3 개의 기작이 연관된 듯하다. 먼저 균근의 균사가 호흡에 의해 이산화탄소를 생산함으로써 그리고 유기산 울 분바함으로써 무기물 인산염의 용해에 기여한다. 따라서 근권 효과 를 보충하는 균근권 효과가 있다. 둘째로 균사가 토양의 이용을 확대 하여-식물 뿌리 자체에 의해 토양이 이용되는 그 이상으로一~이 용한다는 것이다. 균사는 뿌리가 뻗어나가는 것보다 더 철저하게 토양 유기물 입자와 대입단 macroa ggr e g a t e s¾ 침투한다. 셋째로 균사는 뿌리가 할 수 있는 것보다 토양 용액 내의 보다 낮은 수준의 농도에서 인을 흡수할 수 있다. 이러한 능력은 특히 아주 적은 보유 자양분을 가지고 있는 씨로부터 발생하는, 따라서 새로이 발생한 뿌리에 의해 토양을 이용하는 능력이 제한되어 있는 어린 식물에 중요하다. 참고문헌 Bolin , B., Rosswell,. T ., Freney, J . R., Ivanov, M. V. , a nd Ric h ey, J. E. (19 83) . C, N, P, and S cyc l es, majo r reservoir s and flux es, In The Majo r Bio g e ochemi ca l Cy cl es and Their Inte r acti on s (B. Boli n and R. B. Cook, eds.) . W ile y and Sons, New York. Cole, C. V. , I nnis , G. S., and Ste w art , J. W. B. (19 77) . Sim ulati on of P cyc l in g in semi ar i d gra sslands, Ecology 58, 1-15. Redfi eld , A. C. (19 58) . Bio l og ica l contr o l of chemi ca l fac to r s in the envir o n-ment, Am. Sci. 46, 205-221 . Ste w art , J. W. B., and McKercher, R. B. (19 82) . Phosph orus cy cl e, In Expe ri me nta l Mi cr obia l Ecology (R. G. Burns and J. H. Slate r , eds.) . pp. 221-238. Blackwell, Oxfo r d.
Tie s sen, H., Ste w art , J. W. B., and Bett an y. J. R. (19 82) . Cultiv a ti on eff ec ts on the amounts and concentr a ti on of carbon, nit ro g e n and ph osph orus in gras sland soil s , Ag ro n. ]. 74, 831-835. Walker, T. W . (19 65) . The sig nifica nce of ph osph orus in pe dog e nesis , In Expe n·menta l Pedeology (E. A. Hallswort h and D. V. Crawf or d, eds.) , pp. 295-315. Butt er wort h, London. 추가로 읽을 거리 Borie , F., and Zunio n o, H. (19 83) . Orga n ic matt er P associa t i on as a sin k in P fixa ti on pro cesses in allop h anic soil s of Chil e , Soil Bi ol . Bi oc hem. 15, 599-603. Coleman, D. C., Reid , C. P. P., and Cole, C. V. (1983) . Bio l og ica l str a te g ies of nutr ien t cyc l in g in soil sys t e m s, Adv. Ecol. Res. 13, 1-55. Gray, L. E., and Gerdemann, J. W. ( 1969) . Up tak e of ph osph orus-32 by vesic u lar-arbuscular my c orrhiz a e, Plant Soil 30, 415-422. Hedley, M. S., and Ste w art , J. W. B. (1982) . Meth o d to measure mi cr obia l ph osph ate in soil s , Soil Bio l . Bi oc hem. 14, 377-385. Larsen, S. ( 1967) . Soil ph osph orus, Adv. Ag ro n. 19, 151-210. Olson, S. R., and Wata n abe, F. S. ( 1963) . Diffus io n of soil P as relate d to soil tex tu r e and pla nt up tak e. Soil Sci. Soc. Am. 29, 154-158. Ste v enson, F. J. (1986) Cy cl es of Soil . W ile y, New York. Ste w art , J.W .B. (19 84) . Inte r relati on of carbon, nit ro g e n, sulf ur and ph os- ph orus cyc l es duri ng decomp o sit ion pr ocesses in soil , In Current Pers pe cti ve s in Mi cr obia l Ecology (M. J. Klug and C. A. Reddy , eds.) . pp. 442-446. Am. Soc. Mi cro bio l . , Washin g ton , D. C. Thomp so n, L. M., Black, C. A., and Zoellner, J. A. (19 54) . Occurrence and mi ne rali za ti on of orga nic P in soil s wi th pa rt icu lar refe r ence to assoc iat i on s wi th N, C and pH , Soil Sc i. 77, 185-196.
제 13 장 토양에서 황의 변환 13-1 서론 토양에서 황을 산화할 수 있는 무기영양Iit ho t ro p h ic 세균의 존재에 대한 인식은 질산화균의 발견과 거의 동시였다. W ino g rad sky (1 877, 1889) 는 어떤 세균들이 황을 황산염으로 산화시킴으로써 성장에 필요 한 에너지를 얻을 수 있다는 것을 인식하였다. 그 후 몇십 년 동안 토 양 내의 황 순환에서 각 생물들의 역할에는 주의를 기울이지 않고, 비 교생리학에 중점적인 강조가 이루어졌다. 질소 순환 연구와 관련되어 황 순환에 대한 많은 연구가 수행되어 왔다. 황은 질소와 함께 단백질 의 필수적인 부분이다. 평균적으로 단백질에는 황 원자 하나에 367H 의 질소 원자가 있다. 두 원소 모두 수용성 음이온으로서 식물에 의해 흡수되며, 토양유기물에는두원소모두무기화될 수 있는가능성 있 는 화합물들이 상당히 저장되어 있다. 또한 두 원소 모두 대기로부터 강하와, 지하수로 용탈되는 과정을 거치며, 가용성 형태는 미생물에 의해서 대기로 손실되는 기체 형태로 환원된다. 놀랄 것도 없이 황에
대한 순환과 운반에 대한 개념들이 많은 면에서 질소에 대한 것과 유 사하다(그림 13.1). 자연에서 황의 미생물적 변환에 대한 대부분의 초기 연구는 해양 퇴 적물의 지화학과 설파이드 광상의 형성에 대한 것이었다. 토양에서 황 의 과다와 결핍에 대한 문제는 늦게 주의를 끌기 시작했다. 단일의 초 인산염 sup er phos p ha t e[Ca(H2P04)2CaS04] 로서 인을, 그리고 황산 염의 형태로서 칼륨과 질소의 첨가를 한 결과 종종 작물이 추가적인 황을 요구함을 인식하게 되었다. 저황 또는 무황의 고분석 비료 h ig h 一 analys i s f er tili zer 의 사용 증가는 황 결핍 경작토가 존재함을 인식하 게 했다. 북미에서 황 결핍 토양은 태평양 북서부의 일부에서 출현하 고 있고, 캐나다의 일부 삼림토양에서도 나타난다. 토양 내의 과다한 농도의 황은 식물에 해롭다. 산성비는 황산염과 질산염을 포함하고 있으며, 호수의 산성화와 숲의 피해에 커다란 잠재 력을 갖고 있다. 대기의 이산화탄소와 평형에 있는 물은 섭씨 25 도에 서 산도 5.7 이지만, 이산화황 황의 1. 5 pp m 만으로도 비의 산도가 4.0 으로 내려가게 한다. 연간 대기로 유입되는, 오염에 기인하는 황 의 양은 65,000,000 톤에 달한다(그림. 13.1). 이 황은 그러나 심하게 산업화된 지역으로부터 불어오는 대기에 농축되어 있다. 그리고 대기 에서 이산화황, 황산염, 에어로졸 및 대기 분전으로서 발견된다. 오 염되지 않은 지역은 연간 헥타르당 약 1 k g을 받게 되며, 노스캐롤라 이나 주와 아이오와 주와 같이 약간 오염된 지역은 10 k g을 받는다. 도시 부근의 오염지역은 100 kg ha-1 y- 1 를 받으며, 이의 15-20% 는 황산으로- 강하될 수 있다. 그 나머지는 이산화황으로 흡수되거나 또는 분전으로서 받아들이게 된다. 도시 부근의 많은 토양은 습성 강하 we t de p os iti o 파다 건성 강하 dry de p os iti ons 넥터 이산화황을 더 많이 홉수한다.
철, 알루미늄 및 망간의 탄산염, 알루미늄 규산염 그리고 산화물들 의 용해는 느리게 일어나며, 주요한 식물 피해가 주지되기까지는 많은 시간이 지나게 된다. 숲에서는 나무껍질 위 지의류의 군락이 천천히 사라지는 현상이 잎에 대한 피해보다 앞서 일어난다. 가용한 양이온이 수확에 의해 고갈된 형기성 사토 sand y so il 에서 과다한 황은 토양 용 액에 설파이드가잔류하도록 할 수 있다. 이는 벼의 아키오츠] akio c hi 병 같은 생리적인 교란을 가속시킨다. 한 가지 개량 방법은 비료에서 칼륨 또는 암모니아 이온의 운반자로서 황산염 대신에 영화이온을 대 치시키는 것이다. 국한된 지역에서 산성비 및 홉수된 이산화황은 토양 의 풍화 과정을 강화시킬 수 있다. 산성비는 건축 자재의 부식을 야기 시킬 수 있다. 가장 잘 알려진 것은 유럽의 성당과 그리스의 대리석에 나타난 것이다. 북미의 호수 산성화와 유럽의 광범위한 숲의 파괴는 산성화와 관련되어 있다. 따라서 자연에서 황의 형태와 반g들은一 집중 적인 연구의 대상이다. 13-2 자연에서 황의 존재 형태 표 13.1 은 일부 대표적인 세계 토양에서의 황의 분포를 보여 준다. 대부분의 경작토는 20-2000µg g -1 의 황을 포함한다. 많은 화산재, 유기 토양 그리고 조간대의 습지 tida l-marsh 토양은 3000µg g- l 또 는 그 이상의 황을 포함한다. 그리고 일부 사막의 토양은 총 황의 함 량이 10,OOOµg g -1 을 초과한다. 토양에서 황은 유기 또는 무기형으 로 나타난다. 아리디솔 ar idi sol 이의의 토양에선 전형적으로 무기 황 부분이 유기 황에 비해 적다.
표 13.1 세계의 여러 토양에서 황의 분포와 양 총 황의 양 (metr i c ton s) 토양의 총 황의 양 유기형 지역 조oT 근 T (µg g-1 ) 무기형, 에스데르 환원가능성 탄소와 결합 황산영 서스캐처원 농업 88-760 0.5 - 13 29-59 41~71 브리티시 초원 286-928 ND 31-61 39-69 컬럼바아 산림 162-2328 ND 20-47 53-80 유기 1122-30,430 ND 28-75 25-72 농업 214-438 2 18-45 55-82 아이오와 농업 57-618 2-8 43-60 7-18 캐롤라이나 조석 습지 3000-35 , 000 하와이 화산재 180-2200 6-50 50-94 50-94 호주동부 농업 38-545 4-13 10-70 24-76 나이지리아 농업 25-177 4-20 80-96 80-96 브라질 농업 43-398 5-23 20~65 24-59 13-2-1 무기 황 무기 황은 자연에서 여러 가지 산화 상태로(황산염의 +6 가에서 황화 수소와 그의 유도체들의 ― 2 가) 존재한다(표 13.2). 황의 함량이 7-53% 에 달하는 황 함유 굉물이 2000 여 가지를 넘으며, 지각에서 13 번째로 가장 풍부한 원소이다. 토양의 형성 동안 풍화는 매우 서서 하 일어나며, 원생 (原生)의 광물성 황은 식물에 유용한 황으로서는 거의 의미가 없다. 약간 건조한 그리고 건조한 지역의 석회질 토양, 화산재 그리고 최근 개간된 조간대의 습지 지역에서 무기 황은 황산염 으로서 주로 존재한다. 무기 황은 석고의 형태로서 (CaSO.), 염기성 황산알루미늄으로서, 그리고 3000 pp m 까지의 높은 농도로 방해석
표 13. 2 무기 황화합물의 산화 상태 형태 화학식 산화 상태 황산염 s0,2- +6 티아황오황산염산 염 sso2302/--< -s -so3-) +—42, +6 티사오티시온산안염산염 Ss ◄ —o 6 C2 - - N- -+22. 5 삼티온산염 -O3ssso3- +6, +2, +6 원소 so 。 이황화물 HS- -2 황화물 s2- 一 2 CaC03 의 오염물로서 존재할 수 있다. 조석' 습지 그리고 영호의 조건하에서 황은 주로 철의 황화~ 그리 고 철의 다중 황화물p ol y sul fi de s.£.서 축적된다. 남동아시아, 열대성 지역의 아프리카, 그리고 열대성 남미 지역의 산성 토양에선, 강우와 수산화 황산알루미늄의 용해 결과로서 높은 황산염 이온의 보유가 나 타난다. 철의 유사 형 태 들은 j aros it라 KFe3(OH)s(SO ◄ 티와 coq u in b it e[F e2 (SO ◄) 3 • 5 H20] 와 같은 화합물을 형성한다. 13-2-2 유기 황 황은 모든 생물계에 필수 영양소이다. 반추동물 이의의 동물들은- 황 이 아미노산의 환원된 형태로 얻어질 때만 황을 체내로 고정할 수 있 다. 식물과 미생물은 다양한 형태의 황을 생산하고 이용할 수 있다. 토양에서 이들 형태의 황은 토양 유기물로 속하게 되며 두 가지의 주 요한 형태로 구분될 수 있다. 탄소에 결합된 황(그립 13.2) 은 시스테 인, 시스틴, 메티오닌과 같은 아미노산과 바이오틴, 티아민, 조효소
A 같은 조효소 co fa c t ors 에서 나타나며, 철-황 단백질(f errodox i ns), 그리고 리포산 lipo ic ac i ds 에서 나타난다. 황을 포함하는 아미노산은 이 황화 결합 dis u lfid e li nka g e 혜「 통해 단백 질의 2, 3, 4 차 구조를 유 지한다. 많은 효소들은 설프히드릴 sul fhy dr y l 기를 파괴하는 시약으로 처리될 때 기능이 억제된다. 설프히드릴기는 또한 효소와 기질의 결합 에 참여한다. 예로서 gly c eraldehy d e-3-ph osph ate dehy d rog e nase
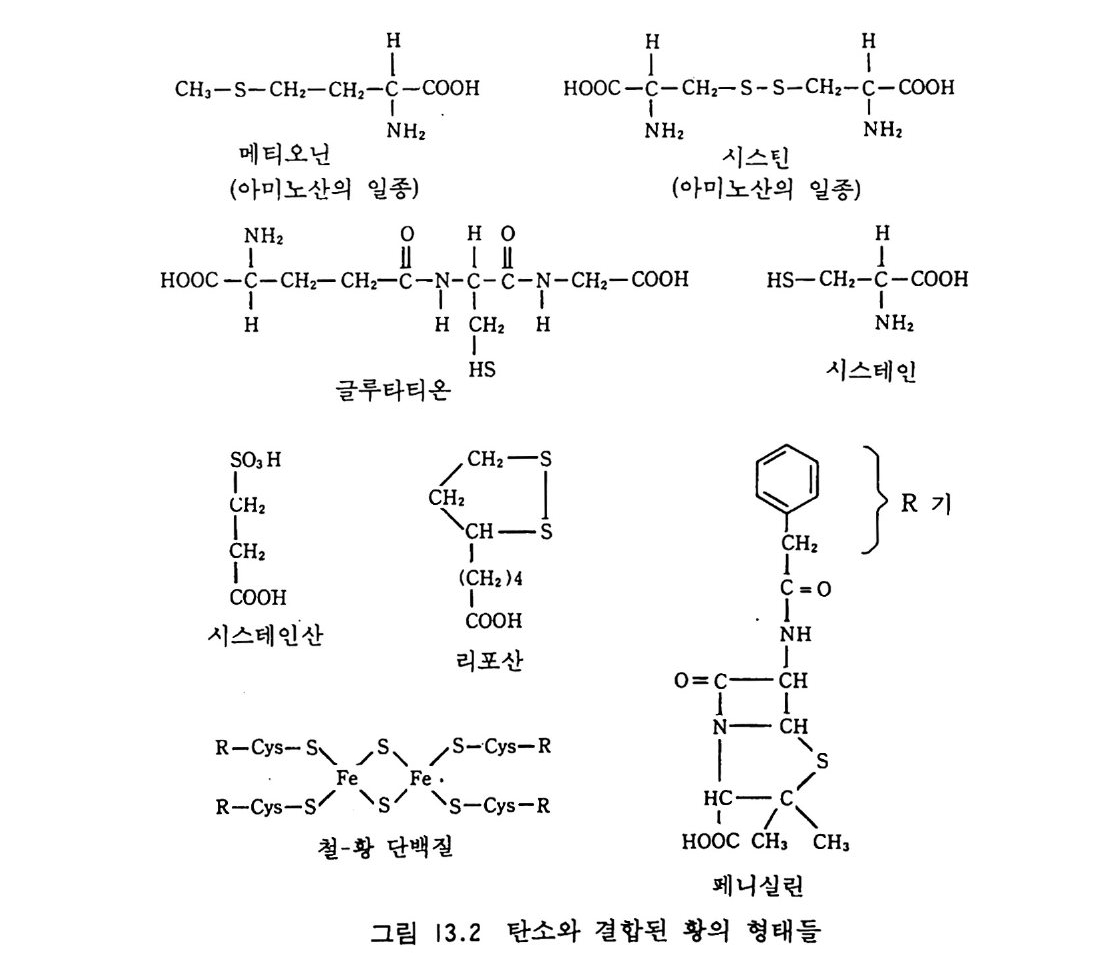 ? HI HI
? HI HI
의 설프히드릴기는 기질을 티오에스데르t h i oes t er 결합을 통해 결합한 다. 토양 유기 황의 두번째 주요 형태로 황은 유기 매질에서 ― 0 一 결 합이나 때로는 — N 一결합을 동해 부착되어 있다(그림 13. 3) . 총괄적 으로 황산염 에스테르라고 구분될 수 있다. 이 형태의 측 정은 요오드 산 (hy d roio d ic acid , HI) 과의 환원을 통해 일어나며 , 종종 HI- 환원 가능한 황으로서 간주된다. 이 형태의 황이 토양에서 생물학적으로 활
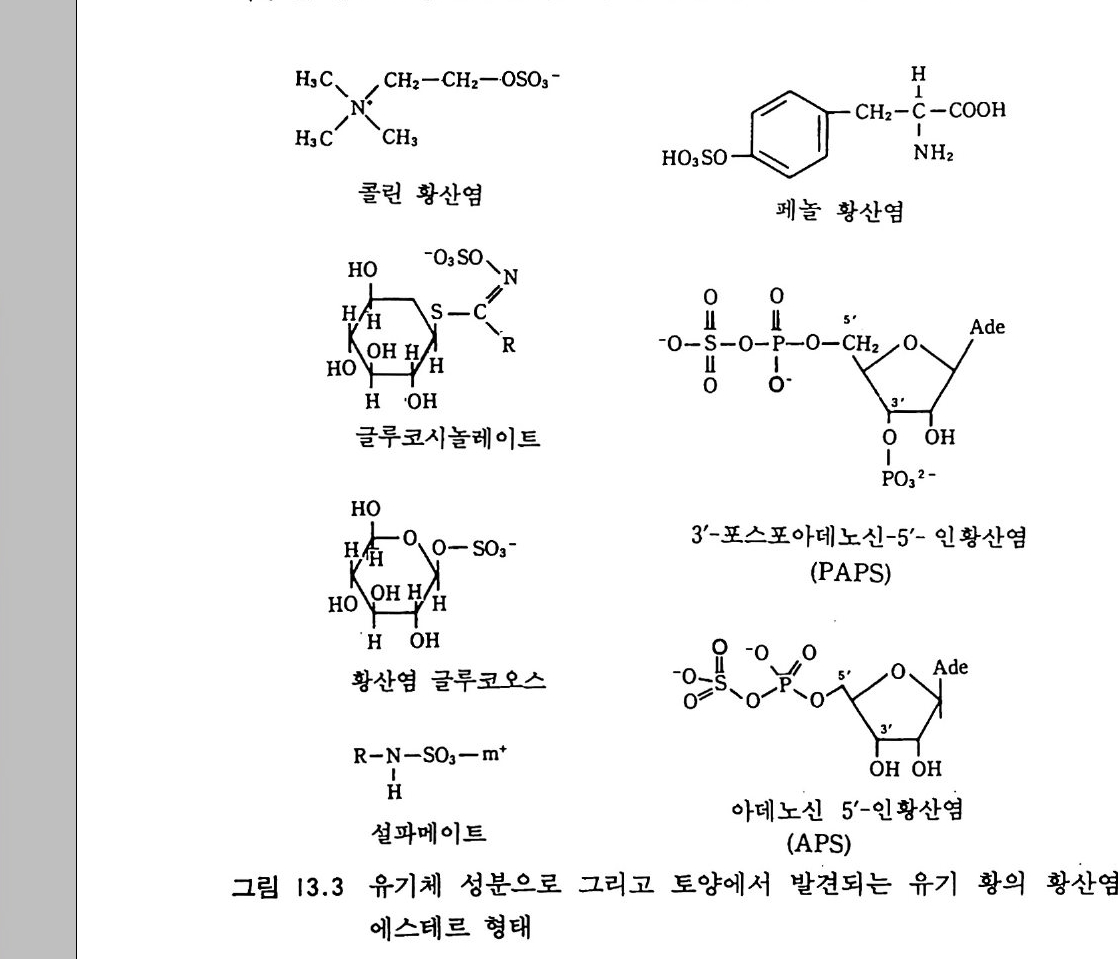 HH,, Cc ·/\, N\/• , · cCHH,2 -CH2 -0 SO,- HO ,S O- e-CH, - ! :~O O H
HH,, Cc ·/\, N\/• , · cCHH,2 -CH2 -0 SO,- HO ,S O- e-CH, - ! :~O O H
성이 더 높은 것으로 또는 활성형으로 간주된다. 종종 과량의 유용한 황이 있는 경우, 이러한 형태의 황이 식물과 미생물에서 저장물이 된 다. 글루코시놀레 이트 g lucos i nola t e~ 곤 십자화과 Brassic a ceae9 -l 식물 (다른 이름은 Cru cif erae) 에서 유기 황산염의 주요한 부분을- 구성한다. 황 화합물의 다른 중요한 그룹은 adenosin e 5-sulfa top h osph ate (APS) , 그 리 고 adenosin e 3-ph osp h ate 5-sulfa top h osph ate (PAPS) 같은 sulfat o p hos p ha t es 이다(그림 13.3). 이들은 많은 무기 황의 전환에 참여한다. 13-2-3 미생물의 황 성분 생물량에 있는 황은 토양 내의 총 유기 황의 2-3% 를 차지한다. 미 생물의 황은 세포를 클로로포름으로 용해시켜, 염화킬슘 (CaCl2) 또는 탄산수소나트륨 (NaHC03) 으로 추출된 황을 측정해서 계산한다. 토양 미생물들의 황 함량 분석은 주요 부분이 아미노산으로 존재함을 보여 준다. A r t hrobac t er 와 Pseudomonas 는 기질에 있는 황 (표 13 . 3) 의 수준이 높거나 또는 낮은 것에 상관 없이 황 함량의 대략 10% 를 산 화된 상태로 갖고 있다. Fusa ri um 균과 Tr i chod~rma 균은 황기질이 낮은 수준에서 자랄 때 유사한 비율을 보이나, 높은 수준에서 자랄 때 는 (16µ g cm 기 황 함량의 약 40% 가 에스테르형으로 있다. 이들 자 료가 특히 홍미로운 것은 이전에는 토양 유기물에 있는 황산염 에스테 르의 공급원을 규명하는 것이 가능하지 않았기 때문이다. 곰팡이는 세 포 내에 황을 콜린황산염 cholin e sulf a te:..으로 저장하는 것으로 보고되어 왔으나, 이를 제의하면 미생물에 의한 에스테르 황화합물의 저장에 대 해서는 거의 알려지지 않았다. 명백히 곰팡이는 합성한 대부분의 에스 테르 황을 보유하는 것 같다. 반면에 세균은 배양 배지로 상당한 부분
표 13.3 다양한 황 농도의 배양 조건에서 성장한 두 가지 곰팡이와 세균의 총 황과 HI- 환원 가능한 황의 양* 총 황의 양(pp m) HI- 환원( %가) 능한 황 생물 S1 •• S2 s3 S1 S2 s3 A rthr obacte r glo bif orm i s 928 1123 1355 10 11 7 Pesudomonas cep a cia 1108 1341 1339 13 10 12 Fusari um solani 1013 2318 2772 12 24 42 Tr ich oderma harzia n um 852 1262 2034 6 17 37 Sagg a r 등(1 981) 자료 ·•s,. s,. s3 는 배양액 1 cm3 당 각각 1, 4, l6µ g의 황이 들어 있음을 나타냄 의 에스데르 황을 배출한다. 다른 형태의 에스데르 황산염으로 황 지 질 sul folipi ds 이 일부 세균에서 보고되었다. 이들 에스테르는 실험실의 배양 상태에서 생산되는 것으로 알려졌으나, 토양에서의 생산에 대한 보고는 아직 없다. 조류의 황산염 에스데르들도 또한 존재한다. 잘 알 려진 조류의 화합물인 한천 a g ar은 선형의 갈락탄g alac t an 황산 에스 테르 o] 다. 황의 다른 형태들, 죽 페닐황산염과 원자 황이 다양한 토양 생물에 서 발견되 었다. 원자 황은 의생 균근 곰팡이 ect om y c orriz a l fu n g텨 자낭군 s p oroca rp s 에서뿐만 아니라, 또한 자가 억제된 다른 휴면 구 조들에서도 확인되었다. 원자 황은 광합성 동안 황화수소를 이용할 수 있는 일부 세균에 의해 축적된다. 13-3 부식질에서 유기 황의 농도 토양 유기물에서 탄소 대 황 (C: S) 의 비는 탄소 대 질소 (C: N) 의
비처럼 일정치 않다. 주요한 차이들은 모재의 종류, 용탈 및 황 두입 량에 기인히는 것으로 밝혀졌다• 평원p ra i r i e~ 몰리솔 moll i so l-€: C: N : S 바가 90 : 8 : 1 이다. 루비솔 luv i sol s:i!} 스포도솔 s p odoso Js.g. 200 : 12 : 1 까지 이른다. 황공급이 적은 지역에서 넓은 범위의 바율이 발견된댜 이는 낮은 황의 순 무기화 잠재성 net sulfu r mi ne rali za ti on p o t en ti al 훑 가져온다. 세계적으로- 일반비는 130 : 10 : 1. 3 이며 , 자 연산 초원 토양과 삼림 토양에서 더 큰 비가 발견된다고 말할 수 있 다. 습성 또는 건성의 오영 물질로서 과량의 황은 토양의 유기 황의 수준을 증가시킬 수 있다. 탄소에 결합된 황은 분석하기 어렵다. 통상 H 匡 환원될 수 있는 황의 값을 총 유기 황으로부터 빼줌으로써 계산 된다. 표 13 .1 은 H 匡- 환원될 수 있는 황이 유기 황의 25-75 %를 차지하는 것을 보여 준다. HI. £. 환원될 수 있는 황의 부분은 일반적 으로 토양 깊이에 따라 증가하는 것을 보여 준다. 점토성 토양 부분에 농축되어 있으며, 토양이 NaOH 또는 Na2P.01 로 추출될 때 풀브산 fu lvic a ci ds 에서 나타난다. HI 에 의해 환원되지 않는 유기 황은 일반적으로. 탄소에 결합된 것 으로 생각할 수 있다. 이중 일부는 라니니켈 (Raney nic k el, 유기 화합 물을 기체 수소로 환원할 때 사용하는 촉매로서 알루미늄과 니켈울 반반씩 융합하여 조제한다 : 옮긴이)에 의해 환원될 수 있다. 이는 탄소에 결합 된 황의 아미노산 부분을 나타내는 것으로 믿어진다.
13-4 황의 변환 13-4-1 유기 황의 무기화 식물이나 미생물로부터 기원하는 C— 0-S, C— N— s, 및 R— C —S 화합물들의 변환은 호기성 및 형기성 경로에 의해 진행될 수 있 다(그림 13.4). 에스데르 황산염들의 가수분해는 유기 황 분해효소 sul fat as 려 의해 0- S 결합의 분해에 의해 일어난다.
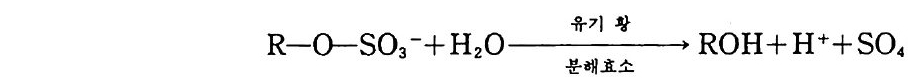 R-0 -S0 3-+H20 분유해기효 황소 ROH+ H++ so/-
R-0 -S0 3-+H20 분유해기효 황소 ROH+ H++ so/-
많은 유기 황 분해효소는 해당되는 분자의 유기물 부분과 황 부분에 대한 높은 특이성에 의해 구분된다. 적어도 3 종류의 유기 황 분해효 소가 (2 개의 aryl s ulfa tas es2 } cho li nesul fat as 여t 포함) 한 종류의 슈 도모나스 세균에 의해 생산되는 것으로 알려져 있다. 황산염이 미생물 성장 요구에 비해 과량으로 있는 경우 에스데르 황 산염의 미생물에 의한 가수분해는, 분해된 황산염이 세포 밖으로 배출 되지 않는 한, 식물 성장에 유용한 황을 공급하지 않는다. 몇몇 연구 들은 몇 가지의 유기 황 분해효소가 세포질 밖에 위치한다는 이론을 뒷받침했으나, 그럼에도 불구하고 유기 황 분해효소 양과 토양 탄소 간의 상관관계는 거의 밝혀지지 않았다. 토양 유기물의 구분 (SOM fr ac ti ona ti on) 에 의거한 연구는 총 황의 양이 , 그리고 특히 에스테르 황산염의 존재가 배양 기간동안 황의 무기화 가능성과 높은 상관관계 를 가지지 않음을 지적했다. 황의 무기화는 질소의 무기회에 비해 탄 소의 분해와 낮은 상관관계를 가졌다• 시스데인 c y s t e i n~ 같은 아미노산의 무기화 작용은 cy st e i n e
 식물의 황
식물의 황
desul fhy dras 짝 seri ne sul fhy dras 려 의해 형기적으로 일어날 수 있 다.
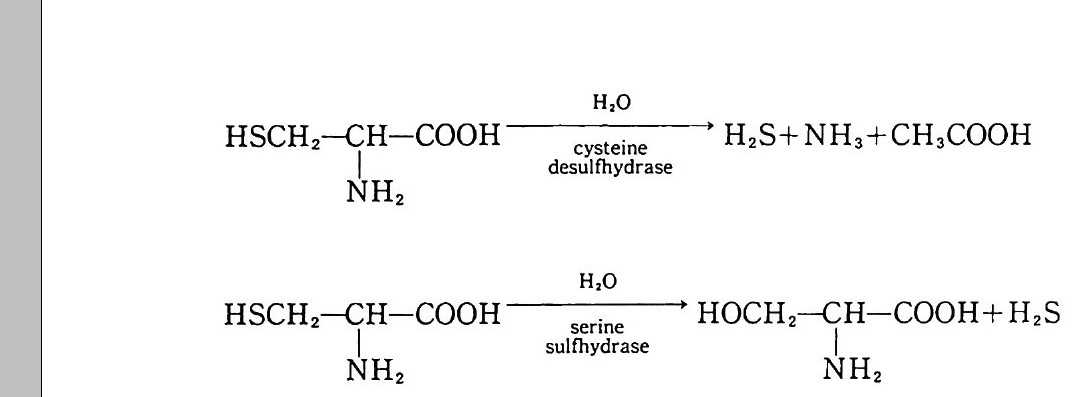 HSCH2- C십 HH 2— CO OH cyH st ,eO i n e H2S+NH3+CH3COOH
HSCH2- C십 HH 2— CO OH cyH st ,eO i n e H2S+NH3+CH3COOH
따라서 무기 황과 무기 질소가 형성될 수 있고, 또는 무기 황만이 생성 될 수 있다. serin e sul fhy dras 허즌 가역 적 이 어서 황의 동회에 또한 참여할 수 있다. 메티오닌은 머캅탄 (merca pt an, CH3SH) 과 암모니아 를 형성하며 분해될 수 있다. 이는 자연에서 악취를 풍기는 휘발성 황 화합물 생성의 보기이다. 식물과 미생물은 일반적으로 황산염을 사용하여 황을 포함하는 아미 노산과 덜 환원된 디론 물질을 형성한다. 이는 황산염의 동화성 환원 을 포함한다. 자연에서 황산염의 동화에 대한 일반 구도는 그림 13.5 에 나타나 있으며,대장균에서 발견되는 것처럼 시스테인 생합성을 보 여 준다. 일단 황산염이 세포막을 통해 흡수되면, 첫번째 반응으로 ATP 와 반응을 하여 AP 혀문 형성한다. 이 반응은 상당한 에너지를 요구하며 낮은 기질 농도에서 기능을 갖는 효소인 APS 키나아제에 의한 두번째 반응에 연결되어야 한다. 세번째 기작에서 무기 피로인산 가수분해효소pyr o p hos p ha t ase7 l- 첫번째 반응에서 배출된 피로인산 pyrop h osph ate ¾ 분해한다. 형성된 PAPS 각각의 분자에 대해 2 개 의 ATP분 자가 전체의 반응에서 사용된다. 2 ATP+S0.2 -—--. ADP+PAPS+PPi PAP 莘 유기 황산염 에스데르를 합성하는 데 이용될 수 있으며,
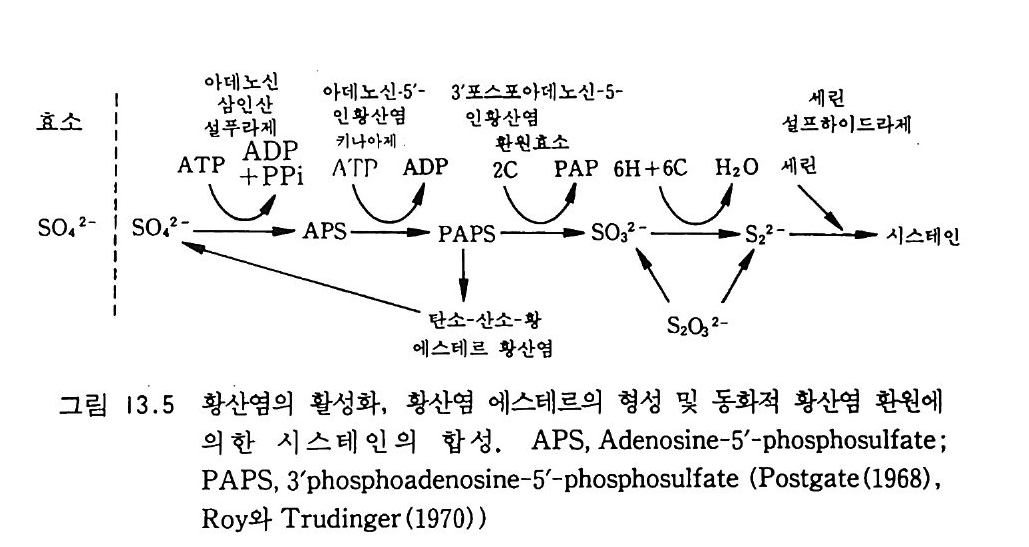 갤삽집 아데노산 5'- 3 ' 포스포아데노신 -5 - 세린
갤삽집 아데노산 5'- 3 ' 포스포아데노신 -5 - 세린
또는 환원되어 세린으로 첨가되며 시스데인을 생성하는 데 이용될 수 있다. 동화적 황산염 환원에 대한 다른 경로는 클로렐라와 시금치의 영 록체에서 처음 발견되었다. 그 경로의 특징은 더 진행될 환원에 대한 기질로서 PAPSll 다는 AP~ 결합된 중간 산물에 의한 황의 이전을 포함한다. 이러한 경로는 또한 대장균에서도 존재하는 것으로 발견되 었다. 식물에서 메티오닌의 합성에 대한 기작들은 대체 경로로서 호모시스 케인으로 이어지는 직접적인 황산 염기 첨가반응 su lf ura ti o fl4 황산 겸기이전반응t ranssul fu ra ti o 머끝 포함한다. 식물에서 황의 고정에 대 한 일반적인 지식은 부족하다. 식물이 황산염을 단백질 합성의 전구물 질인 아미노산으로 전입하는 데 요구되는 양보다 과량으로 홉~ 경 우, 과량의 황산염은(또는 십자화과의 경우 글루코시놀레이트) 조직 에 축적된다. H@-환 원될 수 있는 식물의 황 농도는 토양에서 황 결 핍울 결정하는 훌륭한 방법이다. 몇몇 연구들은 밀의 경우 H~ 환원 되는 황이 총 황 함량의 10% 이상을 차지할 때, 그 식물은 추가의
황에 대해 반응하지 않음을 보였다. 평지의 씨의 경우 임계값 cr iti cal value 이 약 27 %이다. 13-5 자연에서 무기 황 화합물의 산화 환원된 황은 호기성 조건에서 화학적 및 생물적 경로들을 통해서 다 양한 중간 대서산물을 거쳐 산화된다. 산화 상태는 황산염에서의 +6 가로부터 황화수소와 그 유도체들에서의 + 4, + 2, 0, 및 -2 가에 걸 쳐 있다. 그러나 그 중간 물질들은 화학적으로 산화될 수 있기 때문 에, 오칙 황화수소, so, 및 황산염만이 미생물 성장 동안 축적될 수 있다. 산화 경로의 특성은 확실히 기술되지 않고 있으나, so 는 황화 수소의 산화에서 중간 산물이 아니라 저장 산물로서 생성되는 듯하다. 토양에서 황의 산화는 산성화를 일으키며, 토양에 따라 이러한 것이 이롭거나 해롭기도 하다. 토양, 물 및 퇴적토에서 무기 황 화합물의 산화는 다양한 생물군에 의해 이루어전다. 이들은 중성 p H 에서 자라는 것과 산성 p H 에서 자 라는 형태로 구분될 수 있다. 후자는 또한 전자 공여체로서 2 가의 철 울 이용할 수 있으며, 따라서 황과 철의 변환은 밀접하게 짝을 이룬 다. 다음 생물들이 황 산화 생물이다. 13-5-1 황간균 Th io ba cillus 속의 화학적 무기영양 세균은 그람음성 (G- )균이며, 포 자를 만들지 않는 간균이다. 황간균 (Th i obac illi)은 황화수소, 원자 의 황, 티오황산염 및 p ol ythi on it여} 산화시킨다. 다음의 6 가지 종
은 가장 자세히 연구되었다. CD Thio b acil lu s thi o p u r us. p H 가 5 성 범위에서 자라며, 최적은 7 근처°]다. @ Thio b acil l us denit rifican s. T. t h i op urus 와 매 우 유사하다. 전자 수용체로서 산소대신에 질산염으로 대체시킬 수 있다. 2 N03-+S+H20+CaC03 一 CaSO.+N2 생성된 질소는 기체로서 대기로 방출된다. ® Thio b acil l us thi o x id a ns. 통상 전형종typ e s p e ci e~ 로 특정된 다. 성장 pH 범위는 2-5 이다. 운동성이 있고, 엄격한 호기성 생물로 그립 13.6 에 나타난 빈웅들을 수행할 수 있다. @) Thio b acil lu s fe rrooxid a ns. 성장 pH 범위가 1. 5-5 에 걸쳐 있 으며 엄격한 호기성 생물이다. 에너지원으로 2 가의 철을 또한 산화시 키며 상업적 광물의 용탈과 산성 광산수 aci d mi ne wa t er 의 생성에서 주요한 의미를 갖고 있는 생물이다• ' @ Thio b acil lu s in te r mediu s . 성장 pH 범위가 3-7 이며 조건적 무기영양 생물이다. S2032- 를 전자 공여체로 이용할 수 있다. 유기물 이 존재하면 성장이 촉전된다. ® Thio b acil l us thi o c y a noxid a ns. T. t h £op urus 와 매우 유사하다. 황 또는 티오황산염을 이용하여 성장하기 위해선 탄소와 질소가 공급 되어야만 한다. 티오시안산염에서 자랄 때, 죽 하수 배출수에서 발견 되는 것처럼, 다음 반응이 일어난다. C-N-S 가 2 02 + 2 H20 一 SOl-+NH4++C02+220 kcal
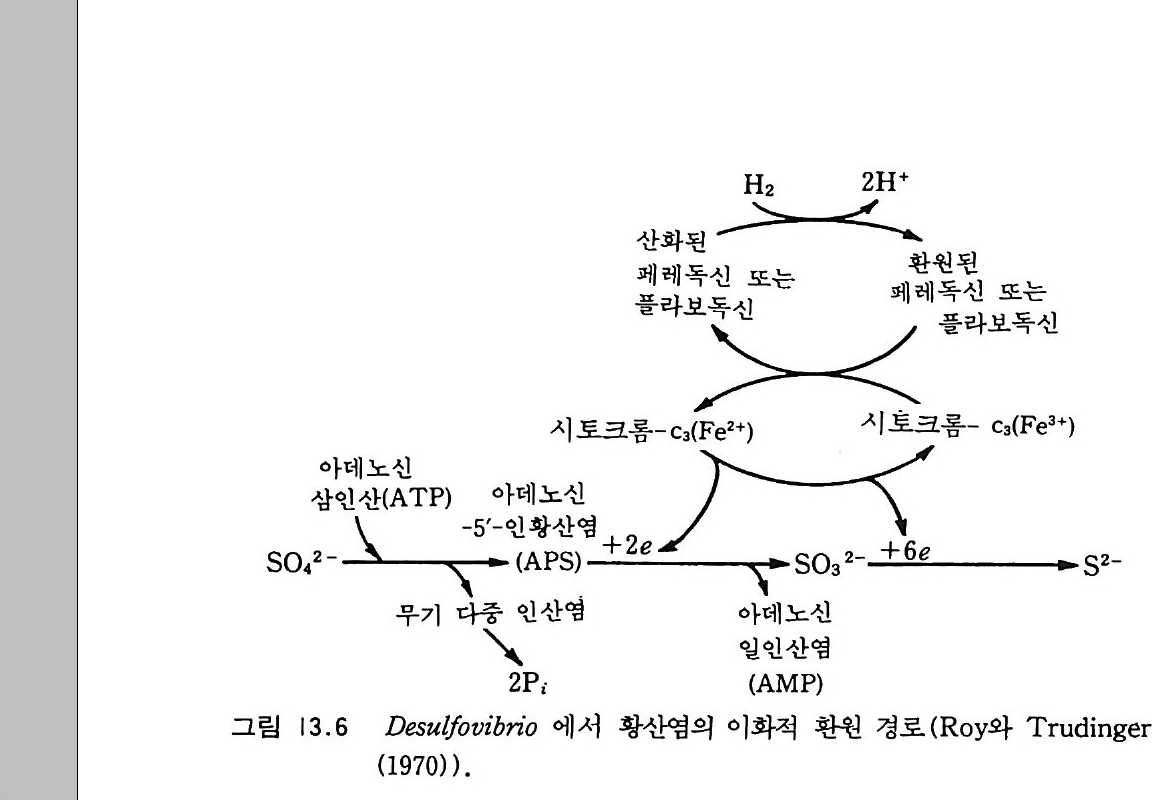 H2.> '- 2H+ 환원된
H2.> '- 2H+ 환원된
13-5-2 Sulf olo bus Su lfo lobus 는 60-80- C , 산도 2-5 의 범위에 걸쳐 자라고 황울 산화 시키며, 고온에서 잘 성장하는 생물을 포함한다. 그러므로 황이 풍부 한 지열천g eo t hermal s p r i n g s 에서 중요하다. 일반적으로 뚜렷한 둥근 돌출부 lobe7} 있는 구형의 생물로 황화수소를 산화할 수 있다. 세포 들은 또한 황의 결정체에 단단하게 부착된다. 13-5-3 Thio m i cr osj )o ra Th i om i cro sp ora는 작은 나선형의 세균을 포함하며 0.22µm 여과 지를 통과할 수 있다. 알려진 두 종 중 하나는 형기적으로 성장할 수
있으며, 질산염을 전자 수용체로서 이용한다. 13-5-4 Thermoth r ix Thermo t hr ix 는 사상의 세균으로 중성에 가까운 온천에서 자라며 산소 또는 질산염을 전자 수용체로서 사용할 수 있다. 이 속은 Su lfo lobus 의 경우와 마찬가지로 화학적 유기 영양을 통해 성장할 수 있다. 13-5-5 Beg gia t oa 와 Thio t h r ix Beg gia to a 와 Thio t h r ix 속 의 구성 원들은 모상체 t r i chome soJ]서 성장 하는 무색의 세포이며 미끄러지는 운동성을 보인다. 그리고 황화수소 의 존재하에서 성장하면 황 입자를 포함한다. 두 생물은 담수와 해양 환경에서 모두 나타난다. 연구 결과들은 비록 황이 대사되지만 이 생 물들은 주로 유기물을 이용하는 생물이라고 지적하고 있다. Beg gi a t oa 가 벼의 근권에서 HS- 를 산화시키는 것이 발견되 었으며 , 따라서 벼룰 이러한 독성 화합물로부터 보호하는 것이 알려졌다. 13-5-6 광 무기 영 양 생물 Pho t ol it ho t ro p hs 녹색 및 자주색 세균은 다양한 모양의 그룹으로 출현하며 구균, 비 브리오균, 간균,· 나선균 및 발아하며 미끄러지는 운동을 하는 생물을 포함한다. 이들에 대해선 10 장에서 이미 논의하였다. 광합성 황 산화 는 Rhodosp o rill ac eae 및 Chroma ti aceae 의 차주색 세균들에 의해 서 형기성 상태에서 수행된다. 그 생물의 색깔은 푸른 자주색에서부터
자주색, 전한 적색 및 오렌지색에서 갈색에 이른다• 이 세균들은- 구 형. 간형 그리고 나선형의 단세포로서 나타난다. 색소로는 세균 엽록 소와 카로티노이드가 있다. 녹색 세균은 다양한 모양의 작은 세균이며 Chlorobaceae 와 Chlorofl ex aceae 에 속한다. 영록소의 존재로 녹색을 띠나, 카로티 노이드가 존재하면 갈색을 떨 수도 있다. 흔히 세포 밖에 원자 황을 침적시킨다. 두 그룹의 광합성 황세균은 흔히 황화수소를 포함하는 진 창과 정체된 물에서 발견되며 빛에 노출되어 있다. 또한 황 온천과 염 호에서 영분 침전물 sal t dep o sit 아래 유색의 충으로 출현한다• 그곳 에서 황화수소는 저충의 형기충에서부터 공급되며, 공급된 황화수소 를 녹색 세균들이 재산화한다. 디옴코} 같이 에너지원으로 빛을 이용하 며 황화수소는 전자원이 된다. 빛에너지 C02+2 H2S-CH20+2 S+H20 빛에너지 3 C02+2 S+ 5 H20-3 CH 20+ 2 H2S04 13-5-7 종속영양 세균 Ar thr obacte r , Bacil lu s, Mi cr ococcus, My c obacte r i um , 그리고 Pseudomonas 같은 세균과, 일부 방선균 그리고 일부 전균들도 또한 무기 황 화합물을 산화시킨다. 명백히 위의 생물들에게 어떠한 에너지 도 가용하게 되지 않으며, 이러한 변환은 주요 대사 경로에 부수적인 듯하다. 이들 생물은 일반적으로 화학적 무기영양 생물 chemo lit h o t ro p h 러 광 무기영양 생물p ho t o lit ho t ro p h 혀 1 비해 토양에 더 많이
있다. 이들은 중성 및 알칼리성 토양에서 황의 산화에 참여하는 주요 생물로서, 토양의 산도를 충분히 낮추어 나중엔 화학적 영양생물인 황 간균과 세균에 의한 산화를 가능케 한다. 통기가 되는 토양에서 유기 황은 상당 부분이 황산염 에스데르의 형 태로 있으며, 오직 적은 농도의 탄소와 결합된 황이 산화에 이용된다. 따라서 오직 적은 수의 황 산화 세균이 정상적으로 존재한다. 토양에 서 황의 결핍울 경감시키는 방법 중의 하니는· 원소 상태의 황을 첨가 하는 것이다. 첨가된 황이 적당한 시간 내에 산화되기 위해선 적절한 황 산화 세균의 개체군이 필수적이다. 야의 연구는 종종 파종 시기에 첨가된 황 산화의 지체기가 충분히 길어서, 그 당시의 경작물에 이득 이 되지 못한다는 것을 보여 주기도 한다. 13-6 무기형 황의 환원 호흡성 황산염 환원으로 알려진 과정은 통상 전자 공여체로 유기산, 알코올 그리고 가끔 수소를 사용하는 유기영양 생물에 의해 형기적으 로 일어난다. 이들 생물들은 물이 차 있는 토양에서, 그리고 퇴적토에 서 황화수소의 형성에 관여한다. 이 경우 전자 수용체로서 황산염과 다른 형태의 무기 황이 사용된다. 이화성 황산염 환원은 현재 8 개 속 의 세균에서 알려져 있다. 가장 잘 알려진 속은 Desu lfo v i b rio 로 토양 과 퇴적토에서 널리 출현하는 편모가 있는 그람음성의 곡선형 간균이 다. Desul joto m aculum 속은 내생 포자를 생성하는 곡선형 G-간 균 또는 직선형 G_ 간균을 포함한다. 다른 속의 구성원둘이 해양 혹은 담수의 형기성 환경으로부터 분리되었다. Desu lfo monas 는 비운동성 이며, 포자를 생성하지 않는, 큰 간균으로 구성되어 있으며
Desu lfo v i b ri o 와 Desu lfo ma ta culum 에 유사한 생 리적 특성을 갖는 다. 장관 int e s ti na l t rac t에서 세균이 주로 분리되 었기 때문에 , 토양에 서 Desu lfo monas 속의 활동은 알려져 있지 않다. 환원 기작들이 완전하게 풀리지 않았지만, 그림 13.7 에 나타난 구 도가 어떤 가능성 있는 단계들을 제시해 준다. 전자들은 환원된 페록 시 단 f errox i dan 과 풀라보독신 flav odoxin s ¾ 통해 시토크롬으로 이 전 된다. 그리고 황산염이 황산염 아데닐기 이전효소와 APS 환원효소에 의해 활성화되어 환원된 설파이드가 최종 산물이 된다. 황산염을 환원 시키는 대부분의 세균은 전자 운반체인 desul fo v i v i d i n 을 포함하며, 이는 알칼리성 조건에서 붉은 형굉에 의해 검출될 수 있다. 수소 기체 를 이용하는 많은 황산염 환원지들의 능력은 전자 전달계를 가짐에 의 하며, 이는 2 장에서 논의된 호흡 구도에서처럼 아마도 막의 퍼텐셜의 생성을가져올수있다. 황산염 환원 세균은 광범위한 산도와 염분 농도에 걸쳐서, 죽 영호, 염전, 심해 퇴적토 그리고 유정에서 발견된다. 이들 생물들은 중금속 과 2% 까지의 용존 설파이드 농도를 견딜 수 있다. 비록 황산영 환 원 세균이 대개 유기물을 이용하는 세균이지만(고정된 탄소의 대부분이 유기물에서 공급된다), 저분자 지방산과 같은 어떤 유기 분자들(부티르 산, 프로피온산 그리고 초산)은 성장을 억제한다. 그러한 경우에 젖산 과 피루브산과 갇은 오직 어떤 종류의 유기 기질들만이 다음에 보여 주는 것처럼 전자 공여체로서 이용된다.
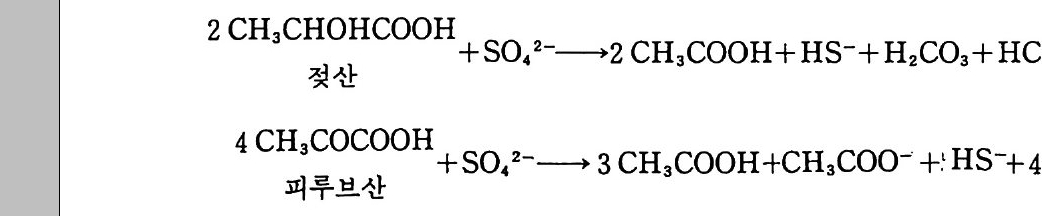 2 CHaCHOHCOOH + SO/- 一 2 CH3COOH+ HS-+ H2COa+ HCOa-
2 CHaCHOHCOOH + SO/- 一 2 CH3COOH+ HS-+ H2COa+ HCOa-
비록 어떤 경우엔 성장을 위해 적은 농도의 복잡한 구조를 가전 유 기물이 요구될지라도, 수소 기체가 전자원으로서 작용할 수 있으며 이 산화탄소가 고정될 수 있다. 이들 유기 화합물들은- 2 가의 철이 고농 도의 HS- 가 있는 경우 Fe~ 료 침전되는 것을 막기 위해 킬레이션 인 자로서 작용할수있다. Desu lfo v i b ri o 가 수소를 이용할 때 , 다음 반웅들이 일어난다. S20a2-+4 H2 一 2 HS-+3 H20 s4o/-+9 H2 一 2 HS-+2 H2S+6 H20 비록 대부분의 황산염 환원이 암모니아를 질소원으로 요구하지만, 어떤 분리된 균주는 기체상의 질소를 암모니아로 환원시킨다. 그러므 로 대기상의 질소와 수소 기체가 있을 경우 탄산염, 황산염을 함유하 는 배지에서 자랄 수 있다. 환경에서 황산염 환원의 결과는 다음과 같다. 첫째, 폐수 시스템에서 황산염의 환원은 설파이드의 생성을 초래한 다. 이는 암석과 콘크리트의 부식에 관련된 것으로 알려져 있으며, 달 걀 썩는 냄새를 풍기며 펌프 및 폐수의 배수계를 부식시키고 막히게 하는 것과도 관련되어 있다. 설파이드 이온의 존재는 폐수 처리에 요 구되는 정상적인 분해 반응둘을 또한 정지시킨다. 오수 정화조에 대한 해답은 그 시스템에 질산염을 첨가하는 것이다. 이는 보다 죽시 가용 한 전자 수용체로서 작용하여 황화수소의 생성을 제거해 준다. 둘째, 퇴적토에서 황산염이 황화수소로 환원되는 석호 la g oon 와 정 체된 호수에서는 광합성 황세균의 작용을 통해 황이 다시 산화될 수 있다. 황간균은 여기에 포함되지 않는데, 그 이유는 형기성 환경 때문 이다. 영호가 마르게 되면서 광합성 황 산화 세균이 활동적이지 않게 되면, 황화수소는 그 환경을 이탈하게 된다.
셋째, 형기성 조건에서 3 가의 철과 황산염은 2 가의 철과 HS- 로 환원된다. 이들 이온들은 Fe S-$기 검은 침전물을 형성하며, 여러 종류 의 설파이드 굉물들 을 형성하는 반응을 일으킨다. 그 환원 과정은 그 시스템의 산도를 중가시킨다. 중국에선 이 원리가 산성 토양의 산도를 증가시키는 데 이용되고 있다. 그 반응은 다음과 같다. Na2SO ◄ +Fe(OH)3+9 H 一 FeS+2 Na0H+5 H20 벼에 있어서 아키오키병의 생성은 줄곧 언급되어 왔다. 이는 질산염 의 첨가에 의해 제거될 수 있으며, 그리고 황을 포함하지 않는 비료 화합물의 이용에 의해 어느 정도 제거될 수 있다. 넷째, 지질학적으로 과거에 형성된 황의 환원은 원유와 석탄에서 환 원된 황의 높은 농도를 가져왔다. 연소과정 동안 제거되지 않는다면, 이 황은 주요한 오영 문제를 일으킬 수 있다. 참고문헌 Brock, T. D., Smi th, D: W ., a nd Madig a n, M. I. (1984) . Bi ol ogy of Mi cr oor- gan is ms. Prenti ce -Hall, E ng le wood Cli ffs, New Jer sey. Postg a te , J. R. (19 68) . Inorga nic S chemi st r y, In The S Cy cl e (G. Ni ck less, ed.) . Am. Elsev ier , New York. Roy , A. B., and Trudin g e r, P. A. (19 70) . The Bi oc hemi stry of Inorga nic Comp ou nds of Sulf ur. Cambrid g e Univ . Press, London and New York. Sag ga r, S., Bett an y , J. R., and Ste w art , J. W. B. (1981) . Measurement of mi cr obia l sulfu r in soil , Soil Bio l . Bio c hem. 13, 493-498. Wi no g rad sky, S. ( 18 87) . Ueber Schwefe lb acte r ie n , Bot. Z t g ·. 45, 489-610. Wi no g rad sky , S. ( 18 89) . Recherches ph y si o l og iqu es sur !es sulph obac ter - ies , Ann. Inst. Paste u r Paris 3, 49-64.
Zehnder, A. J. B., and Zin d er, S. H. (19 80) . The S cyc l e, In Handbook of Envir o nmenta l Chemi stry (D. Hutz i n g e r, ed.) , Vol. l, pp. 103-145. Sp r in g e r-Verlag, Berlin and New York. 추가로 읽을 거리 Adams, F., and Rawajf ih, Z. 0977) . Basalumi ni t e and alunit e : A po ssib l e casue of s0.2 -r ete n ti on by aci d soil , Soil Sci . Soc. Am. ]. 41, 686 -691 . At la s, R. (19 84) . Mi cr obio l ogy : Fundamenta ls and Ap pli ca ti on . Macmi lla n, New York. Bett an y, J. R., and Ste w art , J. W. B. (1982).Sulf ur cyc lin g in soil s , Proc. Int. Sulf ur Inst. 2, 767-785. Chae, Y. M., and Lowe, L.E . (19 80)1 . Dist r i b u ti on of lipid S and tot a l lipids in soil s of Briti sh Columbia , Can ]. Soil Sci. 60, 633-640. Coop e r, P. J. M. (19 72) . Ar y! sulfa tas e acti vi t y in nort he rn Ni ge ri an soil s , Soil Bio l . Bio c hem. 4, 333-337. Ehrlic h , H. L. (19 81) . Geomi cr obio l ogy . pp. 251-280. Dekker, New York. Fit zg e rald, J. W. (19 78) : Natu r ally occurrin g orga no-sulfu r comp o unds in soil s , In Sulf ur in the Envir o nment. Part . ll. Ecolog ica l Imp a cts (J.0 . Nria g u , ed.) , 391-443. Wi ley , New York. Goldhaber, .M . B., and Kap la n, I. R. (1975) . The S cyc l e, In The Sea (E. D. Goldberg, ed.) , Vol. 5. pp. 569-655. Wi ley , New York. Mayn a rd, D. G., Ste w art , J. W. B., and Bett an y , J.R. (19 84) . Sulfu r cy c lin g in gras sland and pa rkland soil s , Bio g e ochemi stry 1, 97-111 . Nep tun e, A. M. L., Tabata b ai, M. A., and Hanway, J. J. ( 19 75) . Sulfu r frac ti on s and carbon-nit ro g e n-ph osph orus-sulfu r relati on sship s in some Brazil ian and Iowa soil s, Soil Sci . Soc. Am. Proc. 39, 51-55. Pepp e r, I. L., and Mi ller, R. H. (19 78) . Comp a riso n of the oxid a ti on of thios ulfa te and elementa l S by tw o hete r otr op h ic bacte r i a and Thio b aci llu s thi o o xi .da ns, Soil Sci . 126, 9-14. Swank, W. T., and Fit zg e rald, J. W. (19 84) . M icr obia l tra nsfo r mati on of so.2 -in for est soil s , Sc ien ce 223, 182-184.
Tabata b ai, M . A., and Bremner, J. M. (19 72) . Forms of sulfu r , and carbon, nit ro g e n and sulfu r relati on ship s in Iowa soil s , Soil Sci. 1 14, 380-386.
제 14 장 금속의 미생물적 변환 14-1 서론 금속의 변환은 두 가지의 주요 범주로 분류할 수 있다. 첫번째 범주 는 무기형 금속의 산화 또는 환원을 들 수 있다. 산화는 미생물 성장 에 대한 에너지원으로 이용될 수 있다. 반면에 보다 쉽게 환원될 수 있는 다른 가질이 없는 환경에서, 다른 에너지원이 이용될 수 있다면 환원은 금속을 전자 수용체로 이용한다. 두번째 범주는 금속을 유기 형태로 전환시키는 결과를, 또는 유기 형태를 무기 형태로 역전환하는 결과를 가져온다. 이러한 반응은 많은 지역의 자연에서 중요하며 첫 째, 토양 형성, 둘째, 낮은 질의 광석으로부터 금속의 재생 이용, 셋 째, 광산 폐수의 산성화, 넷째, 수자원 오염, 다섯째, 지질학적 시간 에 걸친 금속 광맥의 형성을 포함한다. 토양과 지하수가 유기형 및 무 기형의 금속(비소, 수은, 셀렌, 카드뮴 등)으로 오염되어 독성 폐기물 의 폐기 장소의 문제를 야기한다. 오염은 또한 거의 자연적으로 출현 하는 광상(鑛底 dep o sit s) 부근에서 나타나며 , 이는 물의 이동에 의
해 표충수와 지하수의 오염을 가져온다. 소철 (沼鐵) 광싱에서 나타나는 세균은 1838 년에 처음으로 기재되었 다 (Ehrl ic h 에 의해 1981 년 검토됨). 세균은 광상 형성에 기여하는 것으 로 생각되었다. W ir:i o gr adsk y는 그의 초기 연구에서 (1888, 1949) 수 산화철을 침전시키는 Lep t o t h rix라는 세균이 Fe2+ 울 Fe3+ 로 산화시켜 에너지를 얻는 것으로 믿었다. 망간 산화에서 미생물 활동은 철의 경 우와 유사하며 1903 년 M.W. Be ij er i nck 에 의해 처음으로 침전이 기 술되었다. 1950 년대에 탄광 산성수 배출의 기원에 관한 조사는 철을 산화하는 황간균t h i obac illi의 발견을 가져왔다. 이들 미생물들이 철과 구리의 불용성 금속 설파이드를 산화시킬 수 있음이 입증되었다. 이 과정은 금속의 용해와 산성화를 초래한다 (We i nber g (1977)). 14-2 철의 변환 철은 세 가지 산화 상태인 Fe0, Fe2+, Fe3+ 로 존재한다. 산성 상 태에서 금속 철은 (Fe0) 죽각 Fe2+ 로 산화된다. pH 5 이하에서 Fe2+ 상태는 안정하나, p H5 이상에선 화학적으로 Fe3+ 로 산화된다. 다시 Fe3+ 는 쉽게 산성 상태에서 환원되나 알칼리 용액에서 침전된다. Fe2+ 는 pH 5 이상에선 자발적으로 산화되므로- 그 반응이 더 높은 산 도에서 효소에 의해 조절된다는 것을 입증하기 어렵다. 그람음성균의 운동성 간균으로 현재 명명된 Th i obac i llus Je rrox i dans 는 이러한 반 응을 산성 상태에서 수행하며, 에너지와 환원력을 모두 이 반응에서 얻는다. 따라서 이 세균은제 4 장에서 정의한것처럼 화학적 무기영양 생물이라고 말할 수 있다. 이전에 Fe 汀 obac i llus fe rrox i dans 와 F. su lfo x i dans 로 알려전 개체들은 이제 T. fe rrox i dans 로 간주될 수 있
다. Fe2+ 가 미생물적으로 산화되기 전에 유기 화합물에 의해 킬레이트 되어서 철의 용해도를 증가시키게 된다. 산화 동안에 전자들은 ___ 제 2 장에서 기술한 바와 같이 시토크롬 c는 전자 전달계로 들어가는 출 발점으로――전자 전달계를 통해 이동한다. 세포막을 통한 양성자의 통과가 또한 이루어진다고 생각되며, 더 많은 에너지를 공급·하는 것으 로 생각된다. 생물공학을 이용하는채광에서, 설파이드 광석으로부터 금 속을 유리 및 산화시키는 능력이 있는 세균을 찾는 연구를 통해 이 전에 기재되지 않았던 생물체가 발견되었다. 이들 중 어떤 것은 제 13 장에서 기술한 바와 같은 Su lfo lobus 와 유사하다. 다론 것들은 새로 운 명명이 요구될 것이다. Chlam y dobac t er i a 과와 같은 초{껍질)를 형성하는 사상체 세균 주 위에 철의 침전은 우물물괴- 철 파이프에서 일어날 수 있다. 그 중 Lep to t h rix 는 한 보기이다(그림 14.1). 철의 침전을 일으키는 다른 생 물은 Creno th rix 이며 , 거의 구형의 비운동성 세포로 지름이 2µm 이 다. 분열하게 되면 긴 세포들의 사슬을 형성한다. 점액질인 관상의 막 이 약 0.2µm 의 두께로 분바된다. 그 껍질은 굳게·되면 Fe(OH)3 을 함유하게 된다. Creno t h rix는 낮은 농도의 Fe2+ 가 있고 용존 산소가 적은 물에서 자란다. 이 조건에선 Fe(OH)3 가 쌓인다. 또한 파이프 를 막을 수 있는 많은 아교질의 물질을 생산한다. 미생물이 죽게 되면 유기물의 분해로 종종 불쾌한 냄새를 가져오며, Fe(OH)3 막은 붉은 침전을 갖게 된다. 특별히 알려진 처방은 없으나, 철을 침전시키는 세 균은 클로록스 clorox 와 감은 물질로 처리함으로써 제거할 수 있다. 줄기를 형성하는 Gall i onella i.근 콩 모양을 하고 있으며 , 0 . 5X 2 µm 크기의 세포로 200...:300µm 의 편평한 점액질의 리본 형태로 성장하며 Fe(OH)3 껍질로 싸여 있고, 또한 철의 침전에 관여한다. 우물과 관
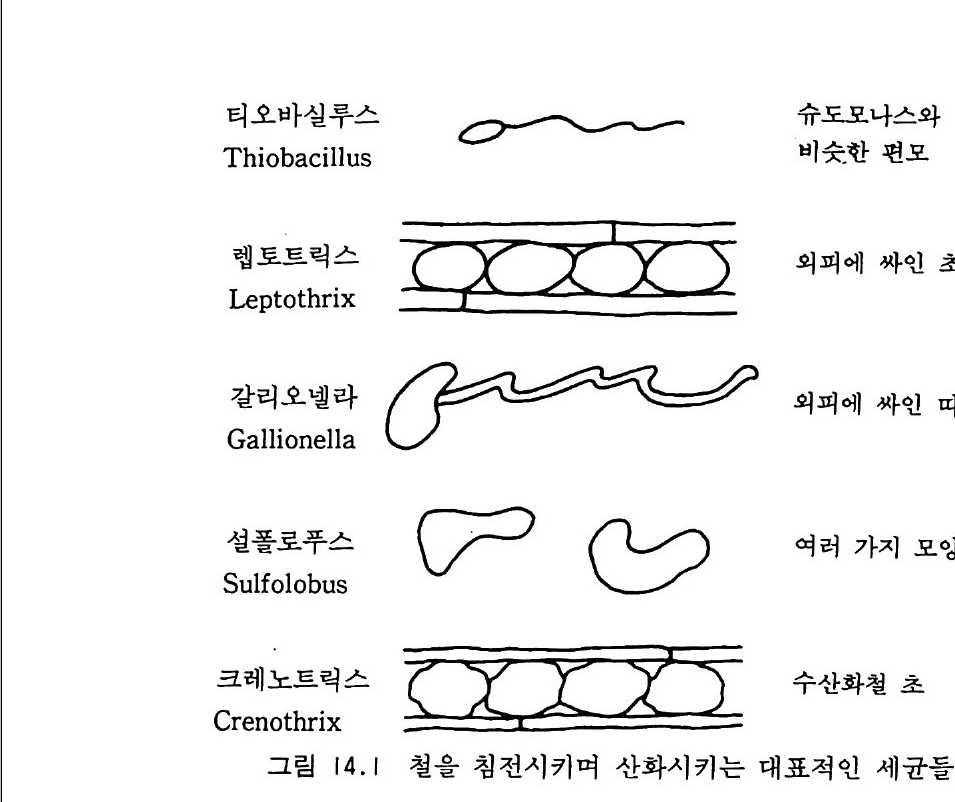 T티h오io 바b a실ci루l lu스s 乙 슈비도슷모한나편스모와
T티h오io 바b a실ci루l lu스s 乙 슈비도슷모한나편스모와
내에서 오영을 일으키는 의에도, 이 생물들은 Fe2+ 로 오염된 개천과 강에서 냄새와 점액질 문제를 일으키기도 한다. 지질학적 시간에 걸친 산화 환원 과정은 퇴적물을 거쳐 퇴적암으로 진행되며, 자연에서 지오사이트g eo t h it e 와 황철광pyrit e 같은 광물의 형성을 초래한다. 황산염과 황산영 환원 세균이 있을 경우, 환원된 철 은 황화수소와 반응하여 수단황철석 h y dro t ro ilit e 이라는 광물을 형성 하며, 이는 지화학적 순환에서 궁극적으로 황철광 (FeS2) 을 형성한 다. 황산염은 바닷물에 과량으로 있으며, 따라서 이 과정은 바닷물에 서 철의 함량을 매우 낮은 농도로 유지한다. 대부분의 토양에 혼한 3 가 철 (Fe 요)은 불용성이다. 따라서 철의 홉 수는 철에 대한 친화도가 높은 유기 화합물과의 반응 또는 양성자의
방출(산성화)을 포함한다. 이들 유기 화합물은 시더포어 sid e rop h ores 또는 페리크롬 fe rr ic hrome~ 로- 알려져 있으며 종종 hy d roxamate s 로 구성되어 있다. h y droxama t es는 분자의 질소 부분과 밀접하게 결합되어 있는 수산기로 구성되어 있다(그림 14.2A). 이 결과, 킬레 이션을 통해 다중결합성인 철에 대한 강한 친화도를 갖게 된다. 알칼 리성 토양에선 토양 내 용액의 철 농도가 식물 성장에 불충분한 것으 로 나타난다. 철은 많은 효소의 구성 성분으로서 모든 생물체에 의해 서 요구되기 때문에, 시더포어를 생산하는 세균에 의해 근권에 있는 가용한 철 농도의 조절은 토양 내에서 일어나는 하나의 중요한 과정이 다. 시더포어를 생산하는 슈도모나스 세균은 근권에서 뿌리 병원성 세
균의 조절 역할을 하는 것으로 가정되어 왔다. 어떤 종의 슈도모나스 에 의해 생산된 시더포어는 가용한 철의 농도를 낮추어 식물의 병원성 균은 억제되나 식물의 흡수는 억제되지 않는 수준으로 만드는 것으로 생각되어 왔다. 철이 효소의 직접적인 작용으로 인해 산화될 수 있거나, 또는 산화 환원 전위나 토양의 산성도를 높이는 미생물에 의해 비효소적으로 산 화될 수 있는 것처럼, 철의 환원도 여러 과정에 의해서 발생될 수 있 다. Fe3+ 은 호흡에서 전자 수용체로 사용될 수 있다. 또한 미생물의 최종 대사산물인 개미산염 for mate 또는 황화수소 등과 반응하여 환원 될 수 있다. A lt erna ria 와 Fu .sa ri .um 같은 진균과 Bacil lu s 같은 세 균은 Fe3+ 를 환원시킬 수 있는 것으로- 알려졌다. 질산영 환원효소는 이들 반응에 연관되어 있을 수 있으며, 질산염의 존재는 통상 철의 환 원을 억제하기에 충분한 산화 환원 전위 (Pc) 를 제공한다. 철의 산화와 환원은 글라이화g le i za ti o~ 료 알려진 토양의 형성과정 에서 주요한 역할을 한다. 물에 잠긴 상태에서는 환원된 철의 존재에 서 기인되는 밝은 회색, 녹색이 생성된다. Fe3+ 은 산소 대신 전자 수 용체로서 작용하여 Fe2+ 로 환원된다. 글라이화된 토양은 통상 Fe203 로 얼룩진 접둘을 갖고 있으며 , 그곳은 뿌리 홈 root channel 혹은 틈 이 국지적인 산화를 야기시킨 곳이다. 이러한 반응은 연못 바닥의 토 양을 밀봉하게 한다. 옛 소련의 연구자들은 대피호의 바닥에 약 15 cm 두께로 짚의 충을 묻고, 토양으로 15 cm 덮게 되면, 유기물의 부 식이 Fe+3 을 Fe+2 로 그리고 S042 - 를 S22- 로 환원시키는 것을 발견했 다. FeS 가 침적되고 토양의 콜로이드들이 용액화된다. 이 결과 모든 톰 밀봉하게 되며, 플라스틱의 얇은 판을 이용하는 것보다 매우 경 제적인 수단이 된다. 토양이 계속하여 물로 참겨 있는 한 영구적인 듯 하며, 인공 호수를 밀봉하는 데 사용될 수 있고, 아마도 폐기물 매립
장에서 사용될 수 있는 것으로 보인다. 철의 이전 t ransloca ti o n{폰 토양의 포드졸화 과정 에 관여되 어 있다. 포드졸화 과정에서 철과 유기물이 풍부한 지하층 subsur fa ce horiz o n 이 형성된다. 이 과정에서 어떤 미생물들은 유기산울 생성하고 철을 용해시키는 킬레이트 물질을 생산한다. 용해성의 철---%기물 복합물은 비가 오는 동안 스며드는 물에 의해 토양 단면을 거쳐 용탈된다. 토양 내의 B 중개서 철의 침적은 스포도솔의 생성을 초래한다. 이 토양은 용탈된 위충과 유기물과 철이 풍부한 아래충 (B) 으로 구성되어 있다. 철이 주로 남게 되고 규산염이 이전되는 토양 형성과정은 열대성 토양 에서 종종 발견되는 라데라이트화 la t er i a ti on 과정을 야기시킨다. 14-3 철관의 혐기성 부식 미생물들은 표 14.1 에 나타난 것처럼 부식 과정에 참여한다. 형기 성 부식에서 금속 표면은 전기 화학적 반응의 양극으로 작용하여 Fe2+ 로 변환된다. 음극 부위에선 당량수의 H+ 가 생성된다. 형기성 황산염 환원세균인 Desu lfo v i b ri o 는 설파이드 (S2-) 이온을 생성한다. 이는 Fe2+ 과 반응하여 Fe 없룹 생성한다. 동시에 물로부터 생긴 수산 기는 H 파 반응한다. 전체 반응은 아래와 같다. 4Fe+ S042-+ 4H20 一 FeS+ 3FeOH2-+ 50H- 위 반응의 요구 조건은 산화 환원 전위가 400 mV (Pe= 6 . 8) 미만 의 형기적 장소를 포함하며, p H 가 5. 誌i다 높고, 황산염과 낮은 유 리 산소 함량의 존재를 포함한다. 이러한 조건에서 3mm 두께의 철 관은 5 구년 안에 부식될 수 있다. 이는 자연에서 가장 경비를 많이 둘
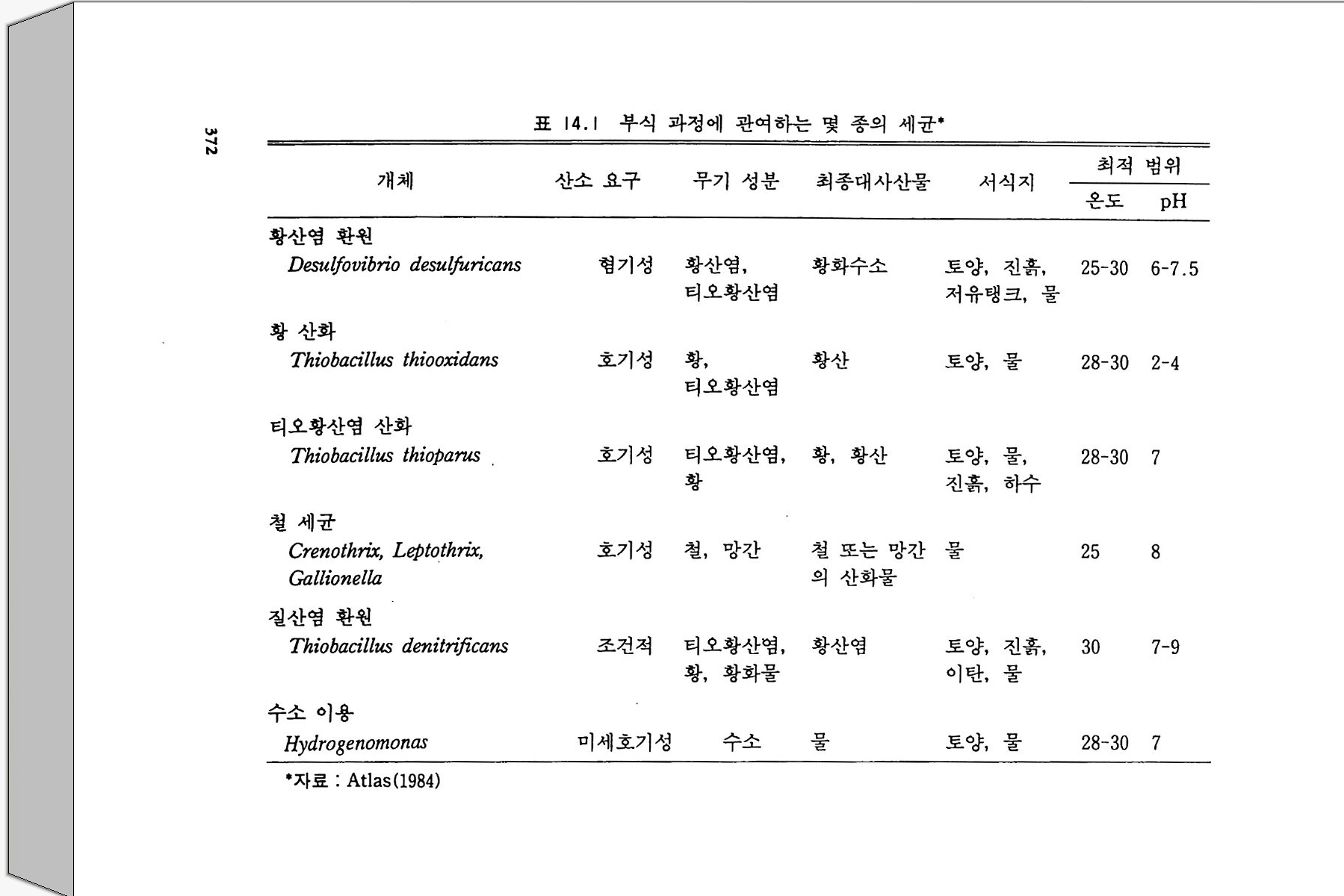 양 유 양 양 흙 양 탄 양
양 유 양 양 흙 양 탄 양
게 하는 미생물적 반응 중의 하나이다. 죽, 땅에 묻힌 철관은 보호받 지 않는 한 계속 교체해야 함을 의미한다. 보호 조치는 관을 따라 아 스팔트와 플라스틱 물질로 조심스럽게 싸거나, 반쪽 전지 전극 형성으 로 부식이 시발되지 않도록 약한 전류의 흐름을一 유지하여 (음국 보호 cath o dic pro te c ti on ) 이루어진다. 표 14.1 에 나타난 바와 갇이 다른 부식 과정은 Gallio n ella-2 } Lep tot h r i x 같은 호기성, 그리고 조건적 세균에 의한 것들을 포함하고 있다. 이돌에 의한 부식은 비록 눈에 크게 띄나 형기성 부식만큼 경제 적으로 중요하지 않다. 간접적인 반웅들은· 황간균에 의한 황 산화에 기인하는 산성 조건을 야기시키는 반응을- 포함한다. 14-4 망간의 변환 세균의 의한 망간 (Mn2+ )산화는 토양과 퇴적물에서 일어난다. 해양 바닥에서 미생물의 활동은 철-망간 단괴의 형성에 관련되어 있다. Mn2+ 의 화학적 산화는 pH 8 이상에서만 일어난다. 그러므로 중성 또는 산성 환경에서 망간의 산화는 미생물에 의해서 일어나야 한다. 많은 토양 세균과 곰팡이는 망간 이온을 산화할 수 있다. 하나의 특수 한 예는 A rt hrobac t er 로 구성 효소 cons tit u ti ve enz ym허 1 의해 이루 어지는 것으로 보인다. 초가 있는 철-산화 세균인 L ept o t h rix도(전에 는 Sp haero ti lus 로 알려짐 ) 또한 Mn2+ 을 Mn” 로 산화시키며 , 초와 사 상체에 Mn02 울 축적시킨다. 망간-산화 세균은 식물에서 망간 결핍 증상과 관련될 수 있다. 귀리 중에서 약한 품종은 회색 반점병을 발생시킨다. 이 경우 망간의 첨가 에 의해 극복될 수 있다. 어떤 토양 조건에서 근권의 세균은 Mn2+ 을
Mn” 로 산화하며, 뿌리의 의부에 Mn02 를 침적시킨다. 이러한 조전 에서 뿌리를 검사하여 보면, Mn02 의 검은 침전이 있음을 보여 준다• 가장 쉬운 구제 방법은 숙주 식물의 유전적 선택으로, 근권 세균의 개 체군을 결과적으로 조절하는 것이다. 한편 과량의 망간에 기인한 망간 독성이 산성 토양에서 일어날 수 있다. 식물로 들어가기 전에 균근성 균의 균사 내에 망간의 침적은 그와 같은 조건에서 망간에 약한 식물 의 성장을 용이하게 한다고 알려져 있다. 14-5 수은의 변환 수은은 금속들이 관련된 보건 문제들에서 가장 흔히 나타나는 금속 이다. 많은 양의 금속성 수은 (H g o) 이 상업용 클로르알칼리 공장 옆의 하천들에 침전되어 있다. 그러한 공장들은 NaOH 와 표백제 (Cl2 와 OCI) 의 생산울 위한 NaCl 의 전기분해에 금속 수은을 사용한디-. 이 결과 강의 퇴적물 오염이 발생한다. 그러나 수은은 금속형으로 남아 있지 않는다. 퇴적물 내의 미생물은 금속 수은을 메틸수은 (CH3H g+) 과 디메틸수은 (CH3H g CH3) 으로 변환시킨다. 메틸화된 수은형은 휘발 성일 뿐만 아니라 금속성 수은보다 훨씬 더 쉽게 흡수되어 동물의 조 직내에 남게 된다. 이는 인간의 수은 중독의 사건을 가져왔다. 불행히 도 지구상의 많은 지역은 높은 수은 농도때문에 지금도 어류의 소비를 규제하여야 하는 곳이 있다. 금속성 수은은 높은 증기압을 갖고 있으며, 약 104 돈의 수은이 대기 권에서 발견된다. 이는 수은을 포함하는 광물에서 나오는 것이며 화석 연료의 연소에 의해서 발생되는 것이다. 석탄은 1200-21, 000 pp bS 거 수은을 함유하며, 원유와 석탄의 연소는 2Xl04-7X104 톤의 수은을
매년 지구로 방출한다. 19 세기 말 이후의 인간 활동은 106 톤의 수은을 방출시켰다. 이는 결국엔 해양으로 유입되는 것이다. 해양에서 발견 되는 108 톤의 수은 중 1% 미만이 인간 활동에 기인하는 것이다. 수 은의 순환을 조절하는 것은 매우 어렵다. 그러나 이에 관련된 미생물 반응의 지식을 더 많이 얻게 됨에 따라, 우리는 토양, 식물성 그리고 동물성 상품에 있는 수은에 대해 더 많이 알게 될 것이며, 수은의 공 해 영향을 감소시키는 책임 있는 방법을 조치할 수 있을 것이다. 참고문헌 At la s, R. M. (19 84) . Mi cr obio l ogy : Fundamenta l s and Ap pli ca ti on s. Mac-mi la n, New York. By e rs, B. R., a nd Arceneaux, S. L. (19 77) . Mi cr obia l tra nsp o rt and uti liza - tion of iro n, In Mi cr oorga nis m s and mi ne rals(R . P. Wein b erg, ed.) , pp. 215-249. Dekker, New York. Ehrlic h , H. L. (19 81) . Geomi cr obio l og y. Dekker, New York. Waksman, S. A. (19 46) . Serge i Ni ko laevit ch Wi no g rad sky : The sto r y of a grea t bac ter io l og ist . Soil Sci. 62, 197-226. Wein b erg, R. P. (1977) . Mi cr oorga nis m s and Mi ne rals. Dekker, N ew York. Wi no g rad sky, S. N. (1949) . Mi cr obio l og ie du sol: Problemes et meth o des. Masson, Paris. 추가로 읽을 거리 Iverson, W. P. (19 74) . Mi cr obia l corrosio n of iro n, In Mi cr obia l Iron Meta b olism : A Comp re hensiv e Treatis (J. B. Neil an d, ed.) . pp. 476 -517. Academi c Press, New York. Konetz k a, W. A. (19 77) . Mi cr obio l og y of meta l tra nsfo rm ati on s, In Mi cr oorga nis ms and Mi ne rals (E. Wein b erg, ed.) . pp. 317-341 . Dekker,
New York. Saji c, J. E. (1969) . Mi cr obia l Bi og e o chemi stry. Academi c Press, New York. Sta r key, R. L., and Halvorson, H. 0. (19 27) . Soil Sc i. 24, 381-402. Summers, N. 0., and Sil v er, S. (19 78) . M icro bia l tra nsfo r mati on s of meta l s, Ann. Rev. Mi cr obia l. 32, 638-672.
옮긴이 해제 M이i c r ob책io은 l o gyE ladnedr AB.i oPc ahuelm 와si ty F *ran ci제s 목 E으. C로l aArkc 이ad e1m98i c9 년 Pr에es s 에So서il 발행한 것을 옮긴 번역서다. 책의 내용은 첫 저자인 Dr. Paul 의 연구 업적을 중심으로 정리되어 있다. 이 책 제 1 장에서 언급한 바와 같이 그는 1967 년에 시작하여 지금까지 총 8 권의 연작물로 출간된 『토양 생화학 Soil B i ochem istry』 중에서 1975 년에 나온 3, 4 권과 1981 년에 나온 5 권의 편집책임자였다. 그가 발표한 논문을- 살펴보면 1980 년까 지 캐나다 삭스캐처원 대학의 토양학과 교수로 재직하며 토양 생화학 과 육상 생태계에서 질소 순환, 미생물을 통한 에너지 흐름에 대한 연 구를 수행한 것으로 이해된다. 1981 년 캘리포니아 대학 버클리 캠퍼 스의 식물 및 토양생물학과 교수로 자리를 옮긴 이후에도 식물-미생물 연합에서 탄소 흐름을 정량한 논문을 〈〈사이언스 Sc i ence)) 에 발표했으 며, 토양에서 유기물의 역동적인 변화와 미생물 생물량과 활동의 중요 성 파악에 관심을 기울였다. 1986 년 이후 미시간 주립대학교의 농학 및 토양학 프로그램 학과장으로 재직하는 중 이 책을 출간했다. 원서의 제목을- 직역하면 〈토양 미생물학과 생화학〉이 된다. 그러나 이 책은 토양 과정과 연관된 전 지구적인 환경 문제를 고려하여 미세
동물, 식물 뿌리, 유기물을 포함하는 지구 생태계의 기능적인 측면을 주로 다루고 있으므로- 토양 생태학으로 하는 것이 더 적절하다고 생각 된다. 1991 년 미국 조지아 대학 생태학연구소의 토양 생태학 연구 그 룹 대부격인 D. A. Crossley, Jr. 등이 편집한 『토양 생태학 현대기법 Mordern Techniq u es in Soil Ecolog y』과 1993 년 워싱턴 주 리칠랜드 소재 배텔 태평양 북서 시험소 Batt el le Pac ific North west Labora- tor i es 환경과학국에 근무하는 토양 생 태 학 전문가 F. B. Mett ing , Jr. 이 편집한 『토양 미생물 생태학 So i l Mi cr obia l Ecolo gy 』 을 이책의 내 용과 비교해 볼 필요가 있다. 만사는 정보, 에너지, 물질을 얻고 잃는 과정의 연속으로- 볼 수 있 다. 이 경우 세상에 나타나는 문제둘은 정보와 에너지, 물질의 흐름에 나타나는 과도한 불균형에서 연유된다. 편의상 세상을 물(수권), 공기 (기권), 땅(지권) 그리고 생물로 이루어진 것으로 볼 때, 이 4 가지 구 성 요소 사이의 상호작용이란 에너지와 물질의 잃고 얻는 과정둘이 자 아내는 하나의 얼개이다. 이들 구성 요쇼: 사이의 잃고 얻는 과정이 마 땅치 않으면 문제가 발생한다. 마땅치 않은 획득과 손실은 구성 요소. 사이에 에너지와 물질의 분포 수준 또는 농도의 변화를 초래한다. 이 변화가 어느 정도까지는 사람을 포함하는 생물에게 새로운 도전이 되 겠지만 과도하면 문제가 된다. 이 책은 특히 땅을 중심으로 하는 생물 과 땅 자체의 잃고 얻는 과정을 설명하고 있다. 이 책에서 일부 에너 지 흐름에 대한 주제가 숨어 있지만 주로 물질 부분이 논의되고 있다. 이처럼 이 책은 이러한 물질 흐름 중에서 토양에서 일어나는 과정들 에 초점을 맞추고 있다. 따라서 전지구적인 차원의 환경 문제를 조망 하기 위하여 토양미생물을 매개로 일어나는 토양과 대기 및 식물들의 관계에 대한 이해가 필수적인 상황에서 이 책은 중요한 의미를 가진 다. 아울러 근간에 실수로 또는 토양을 유해 폐기물 처리장으로 활용
하려는 노력으로- 자연에 방출시킨 유해 물질들의 거동에 대한 연구의 기본적인 방향 제시에도 도움이 될 것이다. 이 책에서 소개하고 있는 미생물 생태학 연구 방법에는 해양미생물과 토양미생물 생태학에서 공 통적으로 사용되고 있는 내용들이 많이 포함되어 있어 두 옮긴이들의 연구 관심을 적당히 포함하고 있기도 했다. 사실상 이 책은 이마 옮긴 이들의 새로운 착상 도출과 실험 결과에 대한 설명 근거 제시에 한 몫 울 했다. 미생물 생태학뿐만 아니라 지구 생태계의 전체적인 과정에 초점을 맞추는 생태학 분야의 독자들에게도 좋은 길잡이가 되리라 믿 는다. 그러나 생물학, 화학, 환경학 그리고 득히 토양 환경에 대해 어느 정도의 기초를 이미 가지고 있는 학부의 고학년이나 대학원생 이상의 수준을 가전 사람들을 대상으로 하여 집필되었다는 사실을 유념해야 할 것 같다. 대체로 지난 2-3 년 동안 토양환경학 교재로서 사용한 경 험에 의하면 환경 관련 과목을- 수강했으나 토양학에 익숙하지 않은 학 부 4 학년 내지 대학원생들은 이 책에서 다루는 내용을 어려워했다는 점을 밝혀둔다. 이제 각 장에서 다루고 있는 내용들을- 간략히 살펴보 기로하자. 이 책은 총 14 장으로 이루어져 있다. 생태학자의 입장에서 보면 제 5 장까지는 서론에 해당한다. 제 6 장 이후는 근간 문제가 되고 있는 지구 온난화와 대기화학 그리고 수질 환경에 영향을 미치는 탄소, 질 소, 황, 인, 금속 순환과 관련된 토양의 생지화학적 과정들을 다루고 있다. 토양에서 일어나고 있는 이들 과정들은 지구생태학g lobal ecolo gy을 이해하는 데 필수적인 내용이다. 각 장은 서문, 본문, 그리 고 참고문헌, 추가적인 읽을거리 제시로 구성되어 있다. 책의 끝부분 에는 간단한 용어집을 수록하여 몇 가지 전문용어들을 독자들이 참조 하도록했다.
제 1 장은 원서의 제목을 잡았던 토양미생물학 및 생화학의 정의와 범위, 주요 업적 및 간단한 역사를 언급하고 있다. 관련 분야 연구의 다양화 과정에 대해 소개하며, 토양생물학의 문헌들에 대한 정보를 간 략히 제공하고 있다. 아울러 21 세기의 토양미생물학 및 생화학의 발 전 전망을 제시하고 있다. 제 2 장은 토양을 생물의 서식지로서 그리고 생물이 상호작용하고 있 는 장소로서 인식하고, 토양 환경의 주요 물리 화학적 요인들에 대해 기술하고 있다. 토양 구조, 토양 공기, 토양 수분, 산화 환원 전위, 산도, 토양 온도와 생물 관계, 기타 환경 인자들의 상호 작용 등 일반 토양학의 기본적인 주제들을 간략히 소개하고 있다. 이 부분은 앞으로 다루게 될 전문적인 내용을 이해하는 데 필수적인 길잡이가 되리라는 배려에서 소개하고 있지만 초보자들에게는 설명이 미흡하다고 판단된 다. 따라서 일반 독자들이 이 책을 과소평가하지 않기 위해서는 일반 토양학에서 다루고 있는 이들 주제에 대한 지식을 보충해야 할 것이 다. 제 3 장은 토양 생물을 연구하는 방법들에 대해 기술하고 있다. 토양 생물의 분포를 이해하는 데 필요한 토양 시료 채취 방법과 채취한 토 양 내의 생물을 직접 현미경으로 관찰하는 방법, 관찰된 미생물들의 생체 부피와 생물량 추정법을 소개하고 있다. 또한 생물량 추정 수단 의 하나인 ATP 함량 측정법과 토양 호흡 측정 기법을 설명했다. 토 。和]서 쟁물의 성장과 활동은 곧 효소의 활성으로 연결되는바 효소 활 성의 측정 방법도 다루고 있으며, 미생물들을 배양하고 계수하는 방법 도설명하고있다. 제 4 장은 토양에 출현하는 바이러스, 세균, 진균, 조류, 지의류, 원생동물, 후생동물과 같은 생물상의 종류들을 분류하여 소개한다. 특히 토양에서 자주 관찰되는 세균인 아스로박터, 스트렙토마이세스,
슈도모나스, 고초균, 시아노박테리아와 진균인 점균류, 편모성 진균 류, 딩곰핑이, 고등 전균, 불완전균 동을 비교적 상세히 기술하고 있 다. 이 장은 생물학에 훈련이 되지 않은 독자들에게는 지나치게 전문 적이고 기재적이라는 느낌이 들겠지만 토양생물학자들 입장에서 보면 턱없이 부족한 내용이다. 따라서 비전문가들은 이런 내용의 필요성 여 부를 판단하기 전에 아예 뛰어넘거나 충분히 보충하는 방법을 택해야 할것이다. 제 5 장은 토양 생물의 출현과 분포, 토양 생물상의 지리적 차이, 토 양에서 생물의 수직 분포, 식물 뿌리에 의해 공급되는 물질과 주변 생 물의 공간적 관계에 대해 기술하고 있다. 아울러 식물의 잎 및 고사한 식물 잔여물과 연관되어 있는 생물과 실질적인 농업 토양 관리에서 나 타나는 토양 생물의 영향들을 논의하고 있다. 여러 가지 독특한 토양 환경에서 나타나는 생물들의 분포에 대한 이해는 이후에 상술될 균근 관계, 근권에서의 과정론을 이해하는 데 필요한 내용이기도 하다. 제 6, 7 장은 전지구적 차원의 온실 효과와 관련이 있는 대기의 이산 화탄소 증가를 염두에 두고, 탄소 순환과 토양의 유기물 분포와 분해 롤 다루고 있다. 그리하여 6 장에서 탄소 순환의 각 과정들과 다양한 종류의 유기물 특칭, 이들의 대사회전에 대해 언급하고 있다. 특히 탄 수화물과 리그닌, 질소화합물, 생물체의 세포벽 성분, 뿌리와 뿌리 분비물들의 대사회전, 토양 유기물의 형성 과정과 형성된 토양 유기물 의 조성, 그 중 풀브산, 부식산과 휴민의 특성, 토양에서 분포 및 정 량 방법에 대해 논의하고 있다. 이런 내용들 또한 생화학적 분야에 익 숙하지 않는 독자들에게는 지루한 감을 줄 수 있지만 환원적인 연구 방법을 사용하는 토양생태학지들에게는 유용한 정보가 될 것이다. 제 7 장에서는 토양 유기물 분해의 역동성과 대사회전의 연구에 도움이 되 는 수학적 모형과 실제 모형 연구 결과들을 기술하고 있다. 먼저 미생
물에 의한 토양 유기물의 대사회전을 이해하는 데 도움이 되는 반응속 도론과, 여러 가지 화학 반응식, 분해의 역동성을 다루고, 식물과 토 양의 자료를 모형화하는 방법을 디루고 있다. 아울러 모형화의 결과와 실제적인 문제를 제시하여 앞에서 터득한 접근 방법의 개념을 경험할 수 있도록 배려하고 있다. 그러나 모형 부분은 저자들이 충분히 소화 하지 못한 탓으로 군데군데 오류를 범하고 있어 옮기는 과정에 바로 잡았다. 제 8, 9, 10 장은 질소 순환을 다루고 있다. 제 8 장은 무기화 및 부 동화 반응들에 대한 내용으로 오랫동안 연구되어 온 질산화 반응에 대 해 상술하고 있으며, 질산화 세균과 그들의 생화학적 반응, 질산화 작 용예 영향을 주는 환경 요인둘(산성도, 통기, 습도 , 온도, 유기물 농도) 에 대해 설명했다. 다음은 종속영양적 질산화 작용과 그 결과 발생하 는 좋지 않은 영향, 그 억제 방안들을 제안했다. 제 9 장은 질산염의 환원과 토양 내의 질산영의 이동에 대해서, 죽 토양 내의 질소의 손실 과정예 대해 다루고 있다. 질산염의 환원과정인 탈질화 작용의 생화학 적 기작과 화학적 탈질화 작용, 여기에 참여하는 생물의 종류 및 특성 과 탈질화 작용을 측정하는 절차와 여기에 영향을 주는 토양의 요인들 (토양의 질산염 농도, 유기 탄소의 이용도, 토양의 수분 함량 , 토양의 산성 도와 온도)에 대해 기술하고 있다. 토양에서 탈질화 작용에 의한 질소 손실과 다른 과정으로- 발생하는 손실을 비교하고, 또한 질소산화물이 성층권에 미치는 주요 영향, 식물 뿌리에 의한 질소 흡수가 생지화학 적 순환에서 하고 있는 역할, 용탈에 의한 질산염의 제거, 침식 작용 에 의한 질산염의 손실, 국지적인 질산염의 축적, 이러한 과정들로 초 래되는 대기의 질소산화물 중가와 부영향화에 의한 수질 오염 문제를 논의하고 있다. 제 10 장은 토양 질소 공급 과정인 생물학적 질소고정 을 설명하고 있다. 범지구적인 질소의 분포와 질소의 이동과 질소고정
세균 및 그 세균들과 공생하는 생물들에 대해 기술하고 있다. 특히 독 립생활형의 유기영양 생물, 독립생활형의 광영양 생물, 초본식물 등 과 연루되어 있는 토양 생물, 콩과 식물들을 디루고 있다. 그리고 콩 과 식물에서 질소고정과 뿌리흑의 생성 및 그와 관련된 생화학적 과정 의 이해를 돕고 있다. 또한 이에 관련된 에너지의 흐름과 이용 및 뿌 리혹박태리아의 접종, 생물공학적 이용의 전망에 대해 기술하고 있 다. 제 11 장은 균근에 관한 내용으로 균근의 분포와 형태에 대해 기술하 고 있다. 특히 낭지 균근과 의생 균근 그리고 진달래과 식물 및 난초 과 식물과 연합되어 있는 균근, 균근의 생리와 기능에 대해 소개하고, 식물 영양소 흡수에서 균근의 역할, 균근의 균과 식물 사이의 탄소의 흐름에 관련된 개념 및 연구 방법에 대해 기술하고 있다. 제 12 장은 토양에서 일어나는 인의 변환에 대해 기술하고 있다. 인 순환의 범지구적 양상, 토양에 분포하는 인의 화학적 형태, 죽 무기 인산염, 용존 유기 인과, 무기 인의 용해, 유기형의 인 화합물, 식물 뿌리와 토양계에서 인의 유동에 대해 소개하고 있다. 제 13 장은 토양에서 일어나는 황의 변환에 관한 내용이다. 자연 상 태에서 출현하는 무기 및 유기 형태의 황, 미생물 세포 내의 황, 부식 질에 있는 유기 황의 농도 및 유기 황의 무기화 과정을 기술하고 있 다. 자연 상태에서 무기 황화합물의 산화와 이에 관여하는 다양한 종 류의 미생물이 맡고 있는 역할과 분류학적 특성, 무기 황이 환원되는 과정에 대해 설명하고 있다. 제 14 장은 금속의 미생물적 변환에 대해 기술하고 있다. 서론에 이 어 철의 변환과 관련이 있는 철강관의 형기성 부식, 망간과 수은의 변 환에 대해 설명하고 있다. 이제 이 책을 우리말로 옮기는 과정에서 옮긴이들이 느꼈던 생각들
울 정리하고자 한다. 자연과학도로서 우리 앞에는 새로운 것을 밝혀 내기 위하여 추전해야 할 일이 너무도 많기에, 이미 밝혀진 사실들을 정리하는 집필 작업, 곧 책을 스스로 저작히는· 일조차 젊어서는 할 일 이 아니다. 대부분의 자연과학도는 이제껏 남들이 알지 못하고 있던 새로움을 처음으로 밝혀 내는 일에서 즐거움을 찾고자 한다. 이런 생 각은 우리들이 학위과정 및 연구원으로 긴 세월 동안 남의 나라 생활 울 마칠 때까지 가졌던 바이다. 그런데 지금 우리는 남의 책을 옮겨서 내어 놓는다. 이 작업의 이면에는 몇 가지 의도가 있었다. 의도의 출발점은 옮긴 이들 자신들의 주어진 환경과 관련이 있었다. 함께 한국외국어대학 재 직시 환경학과의 특성을 만들어 가는 공동작업의 일환으로서 어느 정 도의 공통성을 가지며 토양생태계와 미생물이 각각 옮긴이 두 사람의 주요 관심 분야이기에 원서의 선정에서 의사가 맞았다. 따라서 이 작 업은 적어도 옮긴이들 각자의 분야에, 나아가 상대방이 하는 이웃 분 야에 대한 개인적인 공부가 수행되어야 했다. 무엇보다도 이 책은 기 초 토양학뿐만 아니라 거시적인 환경학, 미생물 생태학, 생태계의 전 체적인 과정에 초점을 맞추는 생태학 분야의 독자들에게는 좋은 길잡 이가 되리라 생각되었다. 드물게 애매한 내용과 잘못된 부분들이 발견되기는 하지만 원저자의 아름답기조차한 단순한 표현들을 옮긴이들이 선점한 점에 대해서는 이 번역서의 독자들에게는 미안한 감이 있다. 시간적인 여유가 있는 분들 은 원서를 꼭 읽어보도록 권유한다. 전공 공부·와 아울러 논문 작성을 위한 영어 표현 공부도 되리라 본다. 그러나 모든 책이 나름대로 한계를 가진다는 점에서 이 책도 예의가 아니다. 먼저 위의 각 문단이 차지하는 지면에서 나타나는 바와 같이 질소와 관련된 논의에 비해서 다른 분야의 안배가 부족흡k 다. 그것은
질소에 대한 연구가 많이 이루어졌고, 또 유익한 연구 결과가 풍부한 탓이기도 하겠지만 상대적으로 다른 분야가 지나치게 간단히 취급되었 다. 아울러 전체적으로 다루고 있는 내용과 다른 연구 분야의 연계성 및 실용적인 측면이 좀더 보강되었으면 한다. 먼저 토양의 미생물학적 생화학적 과정들이 대기 및 수질 환경과의 연관성이 좀더 구체적으로 언급되었더라면 하는 아쉬움이 있다. 이를테면 오늘날 중요한 관심사 인 이산화탄소와 아산화질소의 증가에 따른 기온 상승과 오존층 훼손 이 토양미생물 및 식물에 어떠한 영향을 주고 있는가에 대한 정보가 소개되고 있기는 하지만 부족휴} 편이다. 특히 이런 내용들과 토지 이 용 또는 인간 활동의 상호작용들을 좀더 깊이 있게 논의했더라면 독자 들에게 지구생태학을 인식시키거나 좀더 깊은 연구로 유도할 수 있지 않을까 생각된다. 또한 유독성 무기 또는 유기 오염물에 대한 토양미 생물들의 반응과 토양미생물을 이용한 오염물질 처리 방안 동에 관한 내용이 독립된 장으로 디루어졌더라면 한다. 그러나 책에 대한 아쉬움 은 아마도 읽는 사람의 학문적인 배경과 관심사에 따라 달리 나타나는 것이므로 이러한 아쉬움 때문에 아 책을 과소평가할 수는 없다. 이런 점들을 고려하여 종합적인 평가를 내린다면, 이 저서는 비교적 넓은 범위의 주제를 __- 토양미생물의 분자생물학, 효소의 생화학과 같이 작은 분자 규모에서부터 토양미생물이 지구의 대기에 미치는 영 향과 같은 전지구적 규모에 이르는 주제들―—한정된 분량의 지면에 서 다루고 있음에도 불구하고, 저자들의 의도가 제대로 전달되고 있 다. 특히 미래에 대한 학문의 발전 방향을 감지하고 그 흐름을 톰톰이 제시하고 있어서 저자들의 풍부한 지식과 열의가 돋보인 훌륭한 저서 라하겠다. 이제 번역본이 빛을 보게 하는 데 지원을 베풀어 준 대우재단과 민 음사에 감사한다. 초고를 읽고, 고치고 또 고쳐 주었던 한국외국어대
학교 환경학과 조교였던 조재현 씨와 황학전 씨, 교정된 원고를 컴퓨 터에 입력하여 용어 정리를 해준 한국외국어대학교 환경학과 학생이던 우현진 양, 제 10 장과 제 11 장을 성심껏 개선해 준 서울대학교 산림자 원학과 김종주 씨, 생물의 학명 등 용어에 도움을 주신 임업연구원의 이천용 박사, 서울대학교 미생물학과 정학성교수님, 서울대학교 생물 학과 김명숙씨, 대우재단의 심사과정을 통해서 많은 용어들을 지적해 주신 익명의 심사지에게도 감사한다. 이 심사에서 지적된 사항들은 서 울대학교 환경대학원 환경관리 전공 학생들과 강호정 군의 작업으로 수용되었고, 또다시 옮긴이로 하여금 지겨운 개정작업으로 몰아넣어 거친 표현들을 다듬게 만들었다. 이 모든 사람들이 보태준 시간과 마 음씨를 생각하면 따사로운 세상 기운이 전해 온다. 번역에 완벽을 기하고자 노력하였으나 이 번역서에도 미숙함은 있으 리라 짐작된다. 근본적으로 사람은 실책을 줄이고자 노력할 뿐이지 완 벽할 수 없으므로 독자들의 크고 작은 모든 지적들을 언제든지 고맙게 받아들이고자한다. 1996 년 6 원 10 일 관악에서 이도원,조병철
용어 정리 여러 과학 분야의 개념들이 이 책에서 논의되고 있다. 여기서는 다양한 분아들과 연관된 용어들이 독자에게 장애 요소가 되지 않았 으면 하는 바람에서 제공한다. 사용되고 있는 맥락에서 주어진 용 어의 본질적인 측면을 나타내도록 정리하였다 • 더욱 자세한 정의 둘은 적당한 추가 읽을거리를 이용하기 바란다. Akin e te (비운동성 포자) 한 세포에서 하나가 형성되는 비운동성 포자 로서 모세포벽과 포자벽이 융합되어 있다. Ammonif ica ti on (암모니아화 작용) 질소를 포함하는 유기물로부터 암 모니아 질소가 방출되는 생화학적 과정. An ti b i o ti c( 항생제) (어떤 생물에 의해 생산되어) 다른 생물에 억제적 인 또는치명적인 물질. Assim ilat i on (동화) 무기 또는 유기물들이 세포의 구성 물질로 재구성 (전입). Assim ilat o r y reducti on of n itr a t e( 질산염의 동화적인 환원) 질산염이 아미노산과 단백질들로 사용되기 위해 환원된 질소 형태로 전환되 는것. APS (adenosin e 5-p h osph osulfa te) 황산염의 환원에 관여되는 활성화 된황산영. ATP(adenosin e triph osph ate ) 안산염과 생장 에너지의 주요 전달체이 며 아데닌과 양”의 인산영 그룹으로 구성되어 있다. Auto c hth o nous (자생 성 의 ) 쉽 게 산화될 수 있는 기 질을 포함하지 않은 토양에서 천천히 성장하는, Zy m o g enous 올 보시오. Au t o tr o p h i c( 독립영양적) 성장 에너지는 무기물질원으로부터 그리고 세포 탄소는 co 전]서 얻는 영양 방식. Bac teri o pha g e( 박테리오파지) 세균에 감영하는 바이러스. Bacte r oid (박테로이드) 어떤 세균둘이 특수한 조건에서 취할 수 있는 불규칙한 형태의 세포 모양. 예를 들면 뿌리혹에 있는. Benth ic 수저 (水底)의. Bio l og ica l denit rifica ti on (생물학적 탈질화 작용) den itifica tio ~ 보시
오. B i omass( 생물량) 살아 있는 생물의 총 질량(건조중량)• Chemodenit rifica ti on (화학적 탈질화 작용) 산화된 질소화합물로부터 기체 상태의 질소의 생산을 유도하는 비생물적인 과정으로, 주로 아질산염의 불안정을 통해서 일어남. Chemo tr o p h i c( 화학영양적) 성장 에너지를 화학적인 물질로부터 얻는 영양방식. Chlamy d osp o re (후 막 포 자) 균 사 에 서 발 달 되 나 담 자 basid i a 나 con i d i op hores 에서는 발달되지 않는, 두꺼운 세포벽을 가진 다핵 의 무성생식 포자. 많은 기생성 균류와 균근에 의해서 만들어진 다. Coenoc yt e( 다핵체) 핵분열에 세포질 분열이 뒤따르지 않음으로써 생 기는 다핵성 세포 또는 원형질. Conid i u m (분생자) conid i o p ho re4 불리는 특수한 균사의 정 단에서 생기는 얇은 벽의 이차적인 무성생식 포자. C yt o kinin(사이토키닌) 식물에서 생장조절 호르몬인 치환된 아데 닌 aden i nes. Deam i na ti on( 탈아미노 작용) 아미노기 (-NH2) 를 제거하여 암모니아 를유리시킴. Den itrifi ca ti on( 탈질화 작용) 질산염이나 아질산염이 분자 질소 또는 질소산화물로 환원되는 생물학적 과정. 이 과정은 또한 효소적 또 는 생물학적 탈질화 작용이라 부른다. Dia z otr op h 생장을 위하여 분자질소 N2 를 활용할 수 있는 하나의 생 물또는생물들의 연합. Di ss im ilat o r y reducti on of nit rat e (이화적 질산염 환원 ) 02 가 없는 상 태에서 생물에 의해 이용되는 전자 수용체로서 질산염을 사용, 질 산염을 암모늄영으로- 환원시킨다. DNA(deoxy ribo nucleic acid ) 유전 정보를 보유하는 세포 핵산의 한 형태. 인과 이중 에스데르 결합들p hosp hod i es t er bond 혀 l 의해서 연결된 아데닌, 구아닌, 시토신, 티민과 2- 데옥시리보오스를 포함 하고있다. Ec to m y corr hiz a( 의생 균근) 곰팡이 균사가 식물 뿌리의 외무를 형성
하고 있는 균류복덕의 공생 균사망 m yce li al 의 가닥들이 안으로는 피충세포들 사이로 밖으로-는 주위 토양 속으로 침두해 들어간다. Endom y corrh i za( 내생 균근) 식물 뿌리의 넓은 범위로 세포 사이와 세 포 안으로 진균들이 침두하여 형성된 균류그告리의 공생 . 균사망의 가덕들은 또한 밖으로 주변의 토양 속으로 뻗어 있다. Enzy m ati c denit rifica ti on (효소적 탈질화 작용) Denit rifica ti on ¾ 보시 오. Endop h y te ( 내생 식물) 식물체 안에서 자라고 있는 생물. 아는 기생성 이거나공생관계이다. Eukar y o t e( 진핵생물) 유전 정보가 염색체로 저장되어 있다. 막으로 싸인 핵을 가진 생물로서 예를 들면 곰팡이, 원생동물, 식물들. Fermenta t i on (발효) 유기 기질이나 또는 그 기질로부터 파생된 유기 화합물이 일차 전자 공여체와 말단 전자 수용체로서 쓰이는 산화 환원 반응에 관계되는 에너지 생산 대사작용. Fir s t- o rder reac ti on( 일차 반응) 기질의 전환 속도가 기질의 농도에 비례하는반응. Fulv i cac i d( 풀브산) 토양이나 저니로부터 약한 알칼리로 용출되고 그 용출액을 산성화할 때 침전되지 않은 유기물의 혼합물. Game t e( 배우자) 다른 배우자와 접합 및 접합체의 결합생산j o i n t pro ducti on 후가 될 때까지는 다른 하나의 개체를 만들 수 없는 유성 생식세포 또는 단성생식 원형질체 un i sexual pro to p la smi c body . Gameta n g ium (배우자낭) 하나의 분화된 구조로서 배우자들이 생산되 거나 또는 그 구조 내에 내용물들이 배우자로서 기능을 한다. Gene s pli c i n g(유전자 접합) 한 생물의 DNA 서열로부터 일부 유전자 를 잘라내고 그것을 다른 DNA 속으로 맞추어 잇는 것. Geneti c eng ine erin g (유전공학) 유전자를 한 생뭉에서 다른 생물로 이 식함으로써 한 생물의 유전적인 구조를 조작하는 것. 유전자 접합 ge ne sp licing , 형질도입t ransduc ti on, 전이t rans fo rma ti o 며t 참 고하入 l 오• Gleiz a ti on (글랴기화 작용) 배수가 잘 안 되는 조건에서의 토양 형성 과정으로 철 및 다른 원소들의 환원을 귀착시키고 토양의 회색화와
얼룩을일으킨다. Ha rtig ne t(하티히 망) 외생 균근에서 뿌리 피충세포 사이에 있는 세 포간균사망. He t eroc y s t(이형세포) 시아노박데리아 사상체에서 10-15 세포마다 나 타나는 크고 두꺼운 벽을 가전 세포. 그러한 세포는 이입연쇄체를 분리시키고 종종 질소고정과 관련되어 있다. He te ro tr o p h i c( 종속영양적) 생장에너지와 대부분의 세포 탄소를 다른 유기물로부터 얻는. Wood-Werkman 현상을 보시오. Hormo go ni um( 연쇄체) 시아노박테리아 사상체에서 이형세포에 의해 서 구분되고, 분리되어 하나의 새로운 사상체로 발달할 수 있는 몇 개의 세포로된 한선분• Humi c a ci d( 부식산) 약한 알칼리에 용출되고 그 용출액의 산성화에 의해서 침전되는 토양 부식질의 한 부분·. Hum in(휴민) 약한 알칼리나 피로인산에 의해 분산시킬 수 없는 토양 부식질의 한부분. Humus (부식질) 토양 유기물 중에서 검은 색깔을 띠는 주요 부분으로 유기 조각들의 분해 동안 형성되며, 부식산 및 풀브산과 다른 비교 적 잘 분해되지 않는, 잘 정의되지 않았거나 알려지지 않은 물질들 을함유하고있다. H yp hae( 균사) 사상체의 진균, 조류, 세균에서와 갇이 영양체형을 이 루고 있는 가지가 있거나 없는 사상체들. Hy pe rboli c reac ti on( 쌍곡선 반응) 시간에 대해 형성되는 생산물의 그 래프가 어떤 최대치로 접근하는 곡선이 되어 씽곡선 방정식에 의해 서 가장 잘 기술되는 반응 속도 상수를 가지는 반응. Lang m uir eq u ati on , Mi ch aeli s- Mente n eq u ati on , Monod e q ua ti on 을 보시오. Immob ili za ti on( 부동화) 식물이나 미생물에 의해서 어떤 원소가 무기 질에서 유기질로 바꾸어지는 것. Ka ryo g am y (핵 집합) 하나의 접합체 핵을 이루기 위한 배우자 핵들의 결합. Km M ich aeli s 샹수로 효소 반응 최대속도의 반이 되는 접에서의 기 질의농도. Lang muir e q ua ti on( 랭뮤어 방정식 ) 물리화학에서 흡착현상을 기술할
때 흔히 사용되는 쌍곡선 방정식. hy pe rboli c r eac ti on 을 보시 오 . La t er i za ti on( 라데라이트화) 점토질 부분에서 낮은 규사/시스퀴옥사이 드 비율과 낮은 점토질 활성, 낮은 일차 무기물질 함량과 낮은 가 용성 구성 물질들의 함량 및 높은 단괴의 안정성을 갖는 그리고 보 통 빨간색을 띠는 토양이 되게 하는 습한 열대지방에서 나타나는 토양형성 과정. Legh emog lo bin ( 레그헤모글로빈) 콩과 식물의 뿌리혹에서 산소 농도 를 조절하는 철-헴 단백질i ron-heme pro te i n . L ith o tr o p h i c( 무기영양적) 세포 탄소를 유기물이 아닌 이산화탄소에서 얻는영양방식. Ly so zym e (리소자임 ) 펩티도글리칸을 가수분해하여 세균 세포벽을 분 해하는효소. Meso fa una( 중형동물상) 토양을 통하여 이동할 때 토양 공국울 교란시 킬 만큼 충분히 큰, 토양에 사는, 후생동물들. 선충류, 응애, 톡 토기, 실지렁이, 개미, 곤충의 유충 - 및 기타 많은 것들을 포함한 다. M i crob i o ta(미생물상) 현마경적인 크기를 가지는 토양 생물군. 토양 미생물, 원생동물과 현미경적인 후생동물들을 포함한다. Mi ch aelis - Mente n 방정식 hy pe rbolic reac ti o 때 보시오. M i cro fa una( 미소동물상) 현미경적인 크기의 토양 원생동물과 다른 동 물들로 일반적으로 있는 그대로의 토양 공국을 통해서 이동할 수 있다. M in eral i za ti on( 무기화) 어떤 원소가 유기 형태에서 무기 형태로 전환 되는 것. 총 무기화량gr oss m i nera li za ti o 펴본 분해자인 미생물에 의해서 전환된 전체 양이며 순 무기화량 ne t m i neral i za ti o~ 본 총 무기화량과 생장에 요구된 양 또는 부동화된 양의 차이로 보통 실 험실 배양에서 측정된다. Mo lli sol( 몰리솔), 미국 농무성 토양 분류 체계에서 검은색의 높은 유 기물, 높은 염기포화 base-sa t ura t따를 가진 표면층을 가진 토양 으로 보통 초지와 연루된다. Monod equ ati on (모나드 방정식) 미생물 생장속도를 기술할 때 흔히
사용되는 방정식. M y cel i um( 균사망) 곰팡기 사상체나 균사들에 대한 총칭. 생식기관이 나 단계에 반하여 동화상태에 있는 균사체. M yxarnoeba( 점액아메바) 유주자가 그것의 편모를 떨어뜨리고 아메바 성이 되었을 때 형성되는 껍질이 없는 세포. NADP, NAD(nic o ti ne adenin e d i nucleo ti de) 에 인산영이 결합된 형태. 산화환원 반응에서 조효소가 전자 공여체로서 작용할 때 형 성된다. ng, nanog ram 10-9 그램에 해당하는 무게의 단위 . Nit rat e res pi ra ti on( 질산영 호흡) 질산염의 이화적인 환원울 보시오. N itrifi ca ti on( 질산화 작용) 생물학적으로 암모니아가 아질산염이나 질 산염으로 혹은 아질산영이 질산영으로 산화되는 것. Nit rog e n min e raliza ti on (질소 무기화) 무기화 m i neral i za ti on 와 암모 니아화 ammon ifi ca ti o 머춘 보시오. Nucleic acid ( 핵산) 푸린, 피리미딘 영기와 당류, 인산으로- 이루어진 고분자물질. Or g ano tr o ph i c( 유기영양적) 생장 에너지와 세포 탄소를 유기물로부터 얻는영양방식. PAPS, 3-ph osph oadenosin e 5-ph osp h osulfa te. Pe pti dog l y can( 펩티도글리칸) 세균 세포벽의 단단한 아세틸글루코사 민, 아세틸무람산-아미노산 충. Permease( 두과효소) 막을 통한 기질의 이동 속도를 증가시키는 효소. Pho t o tr o p h i c( 광영양적) 광합성에 의해서 빛으로부터 생장 에너지를 얻는영양방식. Ph y llos p here( 영권), 살아 있는 식물 지상부의 총괄적인 표면. PI, 무기인산영. Plank t on( 플랑크돈) 물에 자유롭게 떠 다니는 부유생물. Plasmo di um( 변형체), 아메바 운동을 보여 주는 껍질이 없고 다핵성인 원형질체. Podzo li za ti on( 포드졸화) 온대 내지 습한 온대의 침영수 또는 침엽수 -낙엽수 혼합립에서 일어나는 토양 형성 과정으로, 심하게 용탈되 고 희백색의 A2 층에 의해서 특징지어진다. PPI, 무기 인산의 중합체.
Prokar y o t e( 원핵생물) 핵에 게놈이 포함되지 않은 세균 같은 생뭉. Respi ra to r y reducti on of nit ra te (호흡적 질산영 환원 ) Diss im i la to ry reducti on of n it ra t峰 보시오. Rh i zo p lane( 근면) 살아 있는 식물 뿌리의 집합적인 표면. Rh i zos p here( 근권) 식물 뿌리를 바로 둘러싸고 있는 지역으로 」 여기의 미생물들은 식물 뿌리의 영향을 받는다. RNA(rib o nucleic acid , 리보 핵산) 리보오스가 3' 5' -인과 이중 에 스테르 결합에 의해서 아데닌, 구아닌, 우라실 또는 시토신 같은 질소 영기에 연결되어 있은 선형의 중합체. Sept ate 격막에 의해서 분리된. S i dero p hore( 시더포어) 일종의 페리크롬fe rr i chrom~ 료 생물에 의 해서 생산되고 철에 대해서 강한 킬레이트성 친화력을 가지며 ; 길 소를 포함하는 hy d roxamate 복합체 . Soil o rga n ic ma tt er( 토양 유기물) 식물과 동물의 진여 물질, 토양 마 생물들, 미생물의 대사물질들, 부식화된 구성물을 포함하는 토양 의 유기성 부분. 보통 직경 2 mm 보다 큰 입자들이 제거된 토양에 서 측정된다• Sp o dosol (스포도솔) 미국 농무성 토양 분류에 포함되는 하나의 목 order 으로, 무기 충적 토양충이 무형의 알루미늄과 유기 탄소를 축적하며 철은 축적하거나 또는 축적하지 않을 수도 있는 토양이 댜 삼림에서 용탈이 많이 되는 조건에서 생긴다. S p orocar p(자낭군) 포자를 생산할 수 있는 다세포체 . 훌씨주머니 송 이라고도함. Subs tr a t e( 기질) 효소(또는 생물)이 작용하는 대상으로서의 화합물. S y mb i os i s( 공생) 서로 다른 두 생물이 밀접한 동아리를 형성하여 서 로 이익을 주고받는 협동관계를 이루며 함께 살아가는 것. Tg (ter rag ra m) 1012 그램에 해당하는 무게 단위 . Thallus( 영상체) 조류, 이끼류, 곰팡이류의 동화체 부분-. Transduc ti on( 형질 도입) 바이러스 매체 (박테리오파지)를 통한 유전 자들의 이동으로 바이러스 DNA 가 숙주생물의 DNA를 붙잡아서 그것을 다른 숙주생물로 이동시킨다. Transfo rm ati on (형질 전환) 한 세균에서 다른 세균으로 DNA 의 직접 적인 이동.
Wood-Werkman ph enomenon (우드-워크만 현상) 종속영양 생물에 의 해 이산화탄소를 흡수하고 그것을 유기물로 전입하는 현상. 추적 자에 의한 연구는 종속영양자가 대부분의 탄소를 다른 유기물로부 터 획득하지만, 약간은 CO2 로부터 얻는 것을 보여 준다. Zero-order reacti on (영차 반웅) 기질의 변환 속도가 기질의 농도 변 화에 독립적인 (무관한) 반응. Zoospo re (유주자) 운동성 포자. Z yg os p ore( 집합포자) 배우자의 집합에 의해서, 또는 접합균강에서는 비슷한 배우자낭g ame t an gi a 의 융합에 의해서 , 형성되는 두꺼운 벽을 가지며 휴면기에 있는 포자. Z y mo g enous( 발효성의) 쉽게 분해될 수 있는 유기질로 살아가는, 새 로 첨가된 유기물에 재빨리 반웅하는.
주요 용어 옮김
제 1 장 orga nis m 유기체 dis c i pli n e 분야 codis c ip li n e s 공동 분야 mesofa u na 중형 (中 型) 동물 soil b io t a 토양생물군 communal 공동체 mi cr ofl or a 미생물상 my co rrhiz a e 균근 associa t i on 연합 anim alcules 미세동물들 auto t r o p h y 독립 영 양 asym b io t i c n it ro g en fixa ti on 비공생 질소고정 descrip tive tax onomy 기 재 적 인 분 류 census count 개체군 조사 ag a r pla te s 한천 배지 pro p a g u les 종균, 번식수단 nit ro g e nase 질소고정 효소 tra nsfe r 이동 tra nsfo r mati on 변환 esta b li sh ment 정 립 a net tie- up (질소의 ) 순고정 im mobil iz a it on 부동화 release 배출 tur nover 대사회전 ge neral course of mi ne raliz a ti on 일 반적인 무기화과정
rhiz o sph ere 근권 humi c acid 부식산 fulv ic acid 풀브산 frac ti on 부분 int e r p r eta t i on 해석 nonin fec ti ve 비전영성 DNA sequ ence 핵산 서열 area 영역 shif t 변화 mi sc ellaneous 기타 부분 Env iro nmenta l Prote c tion Ag e ncy 환경보호국 the enactm ent of clean air 대기 정 화법령 clean wate r leg ist l at i on 수질정화법 제정 jou rnal 전문낡톄 sect ion al pro v isi o n 구분된 항목 Soil Sdence Soc iety of Ameri ca n Proceedin gs 미국토양학회보 Transacti on s of the Inte r nati on al- Soci ,et y of Soil S dence 국제토양학 회보고서 soil bio l og y and bio c hem ist r y 토양 생물학과생화학 Bio l og y and Fert ility of Soil s 토양 생물학과비옥도 con fer ence 학회 모임 zero-til l 무경운 alte r nate crop ping 윤작
whole-tr e e harvesti ng 전간 ( 全g우) 수 확 bio l og ica l contr o l 생물적 방제 bio t e c hnolog y 생물공학 eng ine erin g scie n ce 공학 cost- b enefi t 비용-편익 whit e- rot fun g i 흰곰팡이 int e r gr at e d pe st c otr o l 종합해충방제 alte r ed tilla g e pr acti ce s 개 량 경 운 실행 제 2 장 ge nesis 생성 pa rent mate r ia l 모재 SOM (soil orga nic matt er ) 토양 유 기물 bio m ass 생물량 orga n ic comp o nent 유기물 구성 요 소 matr ix 바탕 relati ve dim ensio n s 상대적인 치수 macroag greg a te 대 형 입 단 order 차수 clay 점토 sand 모래 sil t 미사 disp e r sio n 분산 int e r lay e r 내총 att ac hments 부착 mmiiccrr oofal go gr are a 미te 생s (물50상-2 50 µm) 소형 입
단 macroag gr eg a te ( >2 mm) 대형 입단 urease 요소 분해효소 pr ote a se 단백질 분해효소 humate consti tue nts 부식성 성분들 nit ro g e n oxid e s 질소산화물 aerati on 통기 bulk densit y 용적 밀도(容積密度) sandy loams 사질 양토 tot a l po rosit y 총 공국률 oblig a te anaerobes 필수 형기성 생 물 electr o n donor 전자 공여 체 hy d rate d 수화된 dip o le 양극성 matr i c po te n ti al s 매트릭 퍼텐셜 pa scals 파스칼 grav it at i on al wate r 중력수 cap illar y wate r 모세 관수 hy d roscop ic wate r 홉습수 fiel d cap a c ity 포장 용수량 mi cro -, or cap illay po re 미세 또는 모세공국 tu rgi d 팽창해 있을 wi llting po in t 위조정 (姿馮點) ten sio n 장력 mois t u re po te n ti al 수분 퍼텐셜 mass flow 질량유동 redox po te n ti al 산화환원 전위 asym meti c 좌우대칭 이 아닌 auto tr o p h ic nit rif ier s 독립영양 질산 화균 the multip licity of enzy m es 효소의
다중성 absorpt ion 흡착 electr o de 전국 cell str u ctu r es 세포 구조물들 kin e ti cs 역학적 the rmop h il ic 높은 열을 선호하는 confo rm ati on al chang e s 구 조 적 인 변화 meltin g po in t 용융점 ino culum 접종물 (체 ) 제 3 장 krig ing 그리그 격자법 random subsamp li n g 무작위법에 의 한 하부 구성 단위의 시료 채취 balance 수지 균형 a tot a l enclosed soil 전체 포집된 토 oJ cy lind ers 원통 op e n lys i m ete r 개방식 라이시미터 arrang e ment 배열 상태 thi n - secti on tec hniq u e 박막 기법 mag n esiu m sulfo n ic acid 술巴 마 그네슘 acrid i n e orang e 아크리딘 오렌지 fluo rescein iso th i o c ya nate 풀주오레 신 이소티오시아네이트 TEM tra nsmi ss io n electr on mi c roscop y comp le x shadowi ng tec hniq u e 복합 음영기법
SEM (scannin g electr o n mi cro s-cop y) 주사현미경 acti no my c ete s 방선균 electr o n pro be 전자담사침 burie d -slid e (Ross-Cholodny) 매 설 슬라이드 comp le x substr a te 복합 기질 ped oscop e 토양 현미경 ste a dy sta te 정상상태 counti ng chamber 계수실 pol yc arbonate 디중탄산염 rose beng a l 로츠벤갈 phe nolic anil ine blue 페 놀 아 닐 린 블루 clay soil 식토 sandy soil 사토 FITC (Fluorescein iso th io c y a nate ) 풀루오레신 이소티오시아네이트 sulf yd ryl grou p 설피드릴 그룹 anil in e blue 아닐린 불루 FDA (fluo rescein dia c eta t e ) 플루오 레신 디아세테이트 este r ase 에스테르 분해효소 rod-shap ed 간상체 macroscop e fiel d 현미경 관찰 범위 im munofl uo rescent tec hniq u es 면역 성 형광기법 im munosorbants 면역성 흡착제들 ph osph ata s e 유기 인 분해효소 rhiz o bia str a in s 가근의 변종 bio n ass C 생물체에 포함된 탄소량 densit y grad ien t 비중경사 coenzym e 조효소
aq u ati c sys t e m s 수계 sta n dard curve 표준 곡선 calcareous 칼슘 함량이 많은 aerati on tra in s 통기 노선 flux 유동량 dif fusi o n eq u ati on 확산식 radio r espi ro metr y 방사능을 이용한 호흡측정 방법 urease 요소 분해효소 adap tive 적응성 ind uced 유도성 cellulase 셀룰로오스 분해효소 dehy d rog e nases 탈수소효소 extr a cellular enzy me s 세포의 효소 둘
cult u r al counts 배 양 계수 pla te counts 평 판 계수법 ac tidion e 악티디온 dil ut e count 희석 계수법 mi cro man ipu lato r s 미세 조작 장치 pro bes 탐침 dete c ti on 담지 제 4 장 subd ivi s i o n 아문 cya nobacte r i a 시아노박테리아 nutr ien ts 영 양소 class 강 tran sfe r ag e nts 전이 인자 conju g a ti on 접합 tran sducti on 형질 도입mati ng pa ir s 결합쌍 ph oto t r o p h ic 광영양적 chemotr o p h ic 화학영양적 orga noto p h ic 유기 영 양적 chemorrga notr o p h ic 화학 유기 영 양 적 gree n sulpu r bacte r ia 녹색 유황세균 pe rmeases 두과효소 ge nus 속 spe ci es 종 endop h or 내생 포자 pla te , count 평판계수법 ple omorph is m 다변형 gram varia b il it y 그람 변성 acti no my c ete 방선균 my ce li um 광기실 my c eli al frag me nta t i on 균사 분지 oxid a ti ve orga notr o p h s 산화성 유 기영양생물 scab 감자 병 colony 군락 spo rang ia 포자체들 po lar flag e llati on 끝에 편모가 있는 humi c acid 부식산 type spe ci es 모식종 orga notr o p h 유기영양 생물 lyt ic enzy me 분해효소 Cy a nobacte r ia 시아노박테리아 ph y c ocy a nin 파이코시아닌 ph y c obil ipo rt ei n 파이코빌단백질 blue-gr ee ns 남조류 sheath 초 gran ules 입상
thy la coid e s 티라코이드 lys o zy m es 분해효소 mucop o lys a ccharid e s 접 액 질 다당 류 pe cti c acid s 펙틴산 ap ica l cell 정단 세포 random frag m enta t i on 무작위 적 인 분절 hete r ocy st s 이형세포 veg e ta t i ve 무성생식성 gran ules 입상 pa rent mate r ia l s 모재 mi ld ews 노균병균 rusts 녹병 smuts 깜부기 mushrooms 버섯 pu ff ba lls 말불버섯 slim e molds 점균류 cellular sli me molds 세포성 점균류 Flag e llate Fung i 편모성 진균류 zoospo res 동물성 포자 bif lag e llate asexual moti le 이 편 모 무성생식 운동성 mi ld ew 흰가루병 cop pe r arsenta te comp o und 비산구 리화합물 fun g icide 살균제 po lar unif lag e llate 몸의 한 쪽에 하 나의 편모를가지는 sap r obic 사물기생성 ye ast 효모 High er Fung i 고등 균류 Ascomy ce te s 자낭균강
Basid i o m y c ete s 담자균강 ascospo res 자낭포자 ascus 자낭 basid i u m 담자 basid i o s po res 담자 포자 ste m rust of cereals 곡류식 물 줄기 의녹병 shade tre es 음수(陰樹) wood brown rots 목재 갈색 부패증 whit e r ots 흰부패증 Imp e rf ec t Fung i 불완전 균류 sep tae hy ph ae 격막이 있는 균사 fun g i im p e rf ec ti 불완전곰팡이 my co log ist 균학자 po nd scum 연못 더껑이 wate r moss 물이끼 alga l blooms 조류의 대번성 fac ulta t i ve 임의성의 orga ntr o p h 유기영양 생물 Bail lar i op h ceae 규조류 brackis h wate r 기수 fres h wate r 민물 salt w ate r 해수 assoc iat i on 연합 tha llus 영상 deute r omy ce te 불완전 조류 ph oto b io n t 광합성 공생자 my c obio n t 곰팡기 공생자 wate r envelop m ent 수낭 flag e llate s 편모충 cil iat e s 섬모충 cpor emdmatu i onn.i t ie포s 식군 집
nemato d es 선충 mi llipe des 노래기 centi pe des 지네 roti fer s 윤충 mi tes 왕세 annelid s 환형동물 sp ide rs 거미 ins ects 곤충 meta z oans 후생동물 mi cro fa u na 미세동물 mesofa u na 중형동물 orga nic detr i t us 유기 쇄설물 int a ke 홉식 제 5 장 orga nic resid u e 유기 잔여물 associa t i on 연합 debris 쇄설물 spe cti te 스펙타이트 tex tu r e 토성 sil t 미사 silt y clay 미사질식충 mesqu it e 머스키트 im munofl uo rescent sta i n i n g 면 역 형광염색 rep re senta t i ve bio m ass carbon 대표 적인 생물탄소량 bulk densit y 용적밀도(容積密度) po rosit y value 공극값 xy lo se 크실로오스 arabin o se 아라비노오스
ga lacto se 갈락토오스 mannose 만노 안` root sys t e m 근계 rhiz o sph ere 근권 rhiz o p la ne 근표면권 epi de rmal tiss ue 뿌리의 표피조직 cortic a l tiss ue 피질조직 endorhiz o sph ere 내부근권 his t o s ph ere 조직 권 corto s ph ere 피질권 root pru nin g 뿌리의 일부가 찰려져 나갈때 gly c osid e 글리코사이드 bio s ta ti c 향생물성 ph y toa lexin s 파이토알렉신 tom ati n 토마틴 all ich in 알리신 pisa ti n 피사틴 ph aseolin 파세울린 root cap 근관 root tip 근단 carboxy l grou p 카르복시기 fun g a l my ce lia 곰팡기 균사체 ph y ll osph ere 영권 alga e 조류 lich ens 지의류 bacte r ia l flor a 세균성 식물 vanil lic a c id 바닐산 po lym eric 중합체 oli go saccharid e s 소당류 litter 낙엽과 낙지 tur nover tim e 대사회전 시간 clear-cutt ing 완전 벌목, 개벌
contr o lled burnin g 동제 발화 임 화 (入火) conventi on al tillag e 재래식 경운 reduced, mi ni m um, or stu bble-mulch tilla g e 피복 경운 no till 무경운 fac ulta t i ve anaerobes bacte r ia 조건 적 협기성 박테리아 mi cr ofa u na 미세동물 monocultu re 단종경 작 mesofa u na 중형동물 macrofa u na 대형동물 rhiz o bia 뿌리혹박테리아 fun g ici d e s 살균제 fum i ga nts 훈중소독제 shif t ag ricu ltu r e 이동농경 제 6 장 ste a dy sta t e 정상상태 monomer 단량체 sta r ch 녹말 cellulase 셀룰로오스 분해효소 carbon po ol 탄소 집소 humc i acid core 부식산핵 int e g ral po rt on 중심 부분 ph eny l pro p a noid 페닐프로파노이드 Whit e- rod fun g i 흰 7 뮤곰광기 soft w oods 연욱 침영수재 hardwood 경목, 활엽수재 tu rnover rate 대사회전 속도 cinn ami c; acid 시남산
lag pe rio d 지체기 connif ery l alcohols 콘니페릴알코올 fer ulic aci d 페를산 caff er ic ac id 카페르산 go eth i t e 괴사이트 pro te o lyt ic enzy m e 단백질 분해효소 pro te o se 프로테오스 pro nase 프로나제 subti lisin 서브릴리신 acti no my c es 방선균 dis u lfi de bond 이황결합 pre cursor 선구물질 chit ina se 키틴 분해효소 glu canase 글루칸 분해효소 mesodia m i no pim elic acid 메조디 아 미노피멜릭산 pol yp h osph ate 인산염중합체 pe rip la smi c spa ce 세포막과 세포벽 사이의공간 resid u al carbon-14 잔여 탄소 -14 exte n ded carbon-14 exp erim ent 연 장된 탄소 -14 실험 • condensati on 응축 po lym e riz a ti on 중량체 형성 ca t ec 이 카테콜 sesqu i o x id e s 시스퀴옥사이드 humi c ac id 부식산 spo dsol B horiz o n 스포드솔 B 충 moll iso ns 몰리솔 pol yc o ndensati on 다중응축 fun cti on al grou p 기능단 charcoal 목탄 성분 mi no r elelments 미 량 원소
swamp 습림 marsh 습원 제 7 장 kin e ti cs 반응속도 방정식 sys te m 계 mean resid e nce tim e 평균잔류시간 hy per boli c r eacti on 쌍곡선반응 half- s atu rati on consta n t 반포화상수 ordin a ry grap h pa p e r 통상의 그래 프용지 whole asym ptot i c curve 전체 접근 선곡선 sim ulati on model 의사 모형 CFIM (chlorofo r m fun ig a ti on inc u- bati on meth od) 클 로 로 포 름 (CHC13) 훈중배양법 source-sin k 공급원-소모체 a more mechanis t i c model 좀 더 기 본적인 기작들에 바탕을 둔 모형 correcti on factor s 보정 인자 for est f loo r 임 상 제 8 장 leach ing 용탈 subcomp on ents 하위 요소 peptide s 펩티드 serin e 세린 tryps in 트립신
subti lish in 서브릴리신 sulfh yd ry l pr ote i n a se 설프히드릴 단 백질분해효소 nucleop h il ic dis p la cement reac tion 친핵 치환반웅 fee dback contr o ls 되먹임 조절 chit in 키틴 ph enolic comp o unds 페놀성 화합물 Immobil iza ti on reacti on s 부동화 반 옹 glu ta m ate dehy d rog e nase 글루탐산 탈수스+ keto acid 케토산 pyru vate 피루브산 glu cose 포도당 yiel d coeff icien t 생산계수 surfa c e horiz o ns 표충 subsur fac e horiz o ns 토양 하층 clear-cutt ing 완전 벌채 mois t u re 습기 , 수분 acti no my ce te s 방선균 root zone 근역 my c orrhiz a l fun g i 균근 곰팡이 제 9 장 runoff 유충수 cofa c to r 7-言 수 nit ro us oxid e (N20) 아산화질소 cy toc hrome 시토크롬 Chemodenit rifica ti on 화학적 탈질화 작용
dis m uta t i on 변환 carboxy ls 카르복시기들 nit ro us aci d 아질산 nit rif ica ti on 질산화 작용 oblig a te l y fer menta t i ve 절 대 적 발 효성 fac ulta t i ve ly fer menta t i ve 조 건 적 u갈 효 A3 nonsulfu r bacte r ia 바황세균 lys i m ete r 라기시미터 monit or ed wate r sheds 연구된 유역 pa ckin g mate r ia l 충전 물질 canop y 수관, 임 관 mechanis t i c model 기작 모형 kin e ti cs 동력학반응식 exofo liat e s 박리 nit ro g e n oxid e 질소산화물 nit ro g e n oxid e reducta s e 질소산화 물환원효소 wate r holdin g cap a c ity 수 분 보 유 력,용수량 fate 운명 meth e mog lo bin 메티모글로빈 app a rent mean dif fus io n coeff ice nt 평균확산계수 wate r reg im es 수 체제 wave 굽이 fron t 전단 meth e mog lo bin a emi a 유가청색증 par ent mate r ia l 모재
제 10 장 avail a ble mi ne ral nit ro g e n 가 용 한 무기질소 remi ne rali za ti on 재무기화 int e r nal recyc li ng 내부 재순환 dep o sit ion rate 강하율 Free-liv i n g orga notr op h s 독립 생 활 형 유기영양생물 leaf sheath 영초 Rhiz o biu m 뿌리혹박태리아 slim e 점액물질 fac ulta t i ve mi cr oaerop h il ic 조건 적 미호기성 ph yl l osph ere 영권 crust 겉껍질 Pseudomonas 슈도모나스 ph oto l ith o tr op h s 광 무기영양 생물 Rhodospi rillu m 자주색 비황세균 pho to o rga notr op h s 광 유기 영 양 생 물 salt m arsh 염습지 rhiz o bia 뿌리혹박테리아 endop h y te 내생 식물 ventr al su rfac e 하부 표면 sin g le ric e crop 벼의 일모작 lecti ns 렉틴 gly c o p ro te i n 당단백질 nit rog e nase 질소고정 효소 iro n-heme pro te in 철-행 단백질 ilerog nh - esmuolfgu lro bpirno t e 근i n 립 헤철-모황글 로단빈백 질
fer rye doxin 페레독신 hy d rog e nase 수소화효소 glu ta m ate dehy d rog e nase 글루탐산 탈 pe lleti ng 덩어 리로 만드는 것 host rarig e spe cif icity 숙주 범 위 의 특 o] 성 제 11 장 Rhy n ie chert 라이니 수암 vesic u lar-arbuscular my c orrhiz a s (VAM) 낭지 균근 pl ant resid u e 식물 잔여물 ecto m y c orrhiz a e 의생 균근 ecto t r op h ic 의생 영양적 endotr o p h ic 내생 영양적 ecte n dotr o p h ic 내 의 생 영 양 exp a nsio n s 연장 부분 tra nslocati on 전이 resti ng spo res 휴면포자 vesic l e 낭 ecto m y c orrhi za s (ECM) 의 생 균근 Hart ig net 하티히 망 mantl e 균두(菌~) Arbutu s 진달래과 rhododendron 전달래속 Arcto sta ph y lo s 만자니터 achlorop h y ll ous 영록체가 없는 sapr o p h y te 부생식물(腐生植物) Boletu s 그물버섯균 seedli ng 어린식물
chlorop h y ll ous 영록체가 있는 fun g a l sheath 균초 ph op h ata s e 유기 인 분해요소 aq u eous ph ase 용액상 y iel d po te n ti al 참재 수확량 nurserie s 묘포(苗圓) po lyp h ospa te 다중인산영 sheath 균초 pl asmalemmae 원형질막 tu rnover tim e 대사회 전 시간 inc orpo rate d 고정 된 im mobil iza ti on 부동화 fixa ti on 고정 tra nspo rt 이동 int e r fa c ia l matr i c e s 간극 매질 fuc hsin red 푹신레드 vermi cu li te 버미쿨라이트 gl ucosami ne 글루코사민 spl i t- r oot tec hniq u e 뿌리절단 기법 제 12 장 flux 유동 solubil iza ti on 용해 작용 avail ab le ph osph orus 유효 인 fluo rin e 불소 sin k 소멸지 drain 배출구 litter 낙영과 낙지, 잔존물 orga nic detr i t us 유기 쇄설 입자 reta i n e d ph osph orus 보유된 인 labil e p h osph orus 활성 인
iso io n ic exhang e 등이온 교환 soluti on po ol 용액 집소 pla nt tra nslocati on 식물 전이 ph y tat es 피테이트 ins it ol hexap h osph ate 이노시톨 육 인산영 제 13 장 hig h -analys is fertiliz e r 고분석 비료 wet dep o sit ion 습성 강하 dry dep o sit ion 건성 강하 sandy soil 사토 carrie r 운반자 tida l-marsh 조간대의 습지 arid i s o l 아리디솔 po lys u lfi de s 다중유화물 fer rodoxin s 철-황 단백질 dis u lfi de bond 이황화결합 hy dr oio d ic ac id (HI) 요오드산 labil e for m 활성 형 ecto m y c orriz a l fun g i 의생 균근 곰 팡이 pra ir i e s 평원 moll iso l 몰리솔 !uvis o ls 루비솔 spo dosols 스포도솔 sulfa tas e 유기 황 분해효소
cy st e i n 시스테인 crit ica l value 임계값 chemolith o tr o p h ic 화학적 무기영양 적 type spe cie s 전형종 acid mi ne wate r 산성 광산수 ge oth e rmal spr in g s 지열천 lobe 돌출부 salt d ep o sit 염분 침전물 int e s ti na l tra ct 장관 iso lati on 분리 lag o on 석호 akio c hi dis e ase 아키오키병 제 14 장 dep os it s 광상(鑛床) clorox 클로록스 ge oth ite 지오사이트 pyr it e 황철광 hy d rotr o il it e 수단 황철석 for mate 개미산염 gle iz a ti on 글라이화 subsurf ac e horiz o n 지하층 soil pro fi le 토양 단면 late r iz a ti on 라테라이트화 consti tut i ve enzy me 구성 효소 sheath 초
기 간극 매질 … ………………………… 315 갈락토오스 ………………………… 125 감자병 ……… … ………………… ... 92 강하울 ………………;…………… ··247 개미산염 …………………………… 370 건성 강하…·…………… … ……… .. 341 결합쌍 …………………………… ··· 88 계수실 …………… … … ·… ……… .. 66 고등 균류………………… … …… … 102 고분석 비료……………… … …… … 341 고정…… …… … 15, 17, 94, 98, 111, 314 곤충……………… 87, 94, 101, 114, 116 공국가 ……………………………… 123 광 무기영양 생물 …… … … ……… 256 광상 ………………………………… 365 광영양적 … …… ..... … … … …… … ·88 광 유기영양 생물 ·……………… ··256 괴사이트 ……………………… 157, 368 구성 효소 •• ……………………… .... 373 군락 ……………………………… ···9 0 군집 ……… 17, 63, 79, 92, 95, 114, 116 규조류 ………………………… 108, 109 균근 ……………… 14, 15, 20, 103, 291 균근 곰팡이 ·……………………… .. 217 균사분지 ……………………… 104, 106 균초 ·………………………… ··309, 313 균두 ……………………… … ……… 303 그리그 격자법 …………………… --·61 그물버섯균 •• ……………………… ·293 근계 ………………………… ··· 69, 126
二'- L- 과c …. ... . … … …… …… …… .. … ··128 근권 …… ………… 18, 20, 63, 12 6 , 127 근단 …………………… ……… … ···128 근역 ………… •• … …… …… ……… ·217 근표면권 …… •• …………………… ·127 글라이화 …… … … … …… … …… .. ·370 글루칸 분해효소 •• …… … ………… ·160 글루코사민 ………… …… … ……… 320 글루탐산 탈수소효소 ……·… .. 203, 279 깜부기 … … ………… .. …… …… … ·99 L 낙엽과낙지 …………… 64, 113, 116, 134, 140, 185 남조류 …… 29, 85, 97, 120, 250, 252-2 5 7, 266 낭지 균근 …………………… 292, 296 내부 근권 …………… … … ……… .. 127 내부 재순환………………………… 247 내생식물 …………………… .. …… ·262 내생 영양적 …………………… .. … ·295 내생 포자 ………… .. ………… ·89, 94 내의생 영양……………………… ... 295 내총 ………… … ………………… ... 33 노균병균 …………………………… 99 노래기 ………………………… 114, 116 녹병 ……………………… … ... 9 9, 103 녹색 유황세균 .. …… … …………… ·88 C 다중 유화물…… … ………………… 344
다중 응축………………………… ·· ·1 69 다중 인산염………………… ···160, 313 단백질 분해효소 …………… ···35, 157 단종경작 ………………………… ···138 담자……………………… 103, l'J 4 , 106 담자균강 ·…………………… ··102, 103 담자 포자 … … ••.. … ……………… ··103 당단백질 •••••• ………………… ··· ···269 대사회전 ………… 17, 34, 137, 143, 314 대사회전 속도………… ……… … 17, 34 대사회전 시간……………… 17, 34, 314 대형 입단 ……………………… 33, 337 독립생활형 유기영양 생물 ·……… ··250 독립영양 ……………… ···14, 22, 49, 88 독립영양 질산화균 ………………… 49 동물성 포자………………………… 101 되먹임 조절 •• ………………… ·202, 205 등이온 교환………………………… 330 근 라이시미터 ……………………… ···231 라테러이트화 ……………………… 371 렉틴 ……………………… •• ……… ·269 로즈벤갈 ……………………… .. … ·66 루비솔 ……………………………… 349 □ 만노오스…………………………… 125 말불버섯 ……………………… 99, 102 매설 술라이드 ……………………… 65 매트릭 퍼텐셜 ……………………… 43
머스키트 …………………… ......... 122 메조디아미노 피벨릭산 ·………… ··160 메티모글로빈 … .... ……………… .. 239 면역성 형광기법 •• ……………… ·69, 70 면역성 홉착제 •• …………………… ·69 모세관수 ……………… .... …… ··42, 43 모의 모형 .. ………………………… ·185 모재 ……… 29, 30, 33, 61, 98, 111, 118 목재 갈색 부패증 ……………… ···103 목탄 성분…………………………… 170 몰리솔 ………………………· .. 168, 349 묘 ……… •• ……………………… ·313 무경운 ………………… ···23, 137, 138 무기 질소………………………… ···246 무기화 146, 153, 158, 160, 175, 178, 185 무성생식성 ……………·……… .. 97, 98 물이끼 ……………………………… 107 미사 ……… ······33, 122, 126, 170, 192 미사질식충 ………………………… 122 미생물상 …………………………… 18 미세동물 ……………… 14, 62, 114, 116 l::I 바닐산 ……………………………… 32 바탕 ……………………… 33, 122, 150 박리 ……………………………… ···234 박막 기법 ·………………………… ··62 반응속도 방정식 …………………… 175 반포화상수 ;……………………… ··180 방선균 …6 3, 80, 85, 90,92, 216, 249, 261, 279 배양계수 …………………………… 79
버미쿨라이트 ……… ..... .. …… … ··320 보정 인자 .. ……… ..... ..... . .. …… .. ·192 복합 기질 ……………………… ······65 부동화 ·… ··17, 202, 207, 237, 246, 314 부생식물 ………………… ···· · ·······307 부식산 … •• ……………… ·93, 153, 167 부착 ………… … 34, 150, 157, 160, 170 분산 ...• ……… ………… ··33 , 63, 66, 79 분해효소 …………… …… …·… ··94 , 97 불완전 곰팡이 …………………… ···104 비공생 질소고정 ………………… 15, 17 비중경사 …………………………… 73 비황세균 ………·……… ··229, 249, 256 뿌리절단 기법 ……………………… 320 뿌리혹박테리아… 80, 251, 260, 284, 291 사물기생성 ………………………… 102 사토 … … ……………… •• …… ·67, 342 산성 광산수………… … … …… …… 355 산화성 유기영양 생물 ……………… 92 산화환원 전위 ………………… ···45, 47 살균제 ………………………… 101, 139 생물 공학 …………………… ···2 3, 24 생물량 ……………………… 143 -193 생산계수 ……………………… •• … ·206 서브틸리신 ………………… ···157, 201 석호 ………………………………… 361 선구물질 …………………………… 77 선충 ……………………… 114, 116, 128 섭모충 ………………………… 113, 114 세균성 식물·……………………… ··131 세린 ………………………………… 201 세포성 접균류 ……………………… 99 셀룰로오스 분해효소 ·…………… ··77
人 소택지 …………………………… ···170 소형입단 ••• … ……………………… 33 쇄설물 ………………… ... .. .. …… ··120 수냥 ………………… ••.• :………… ·112 수단 황철석 ………………………… 368 수소화효소 ……… •. ………… ·276, 285 수 체제 …………………………… 240 숙주 범위의 특이성 …………… ···287 슈도모나스 ……………… ••… ·229, 256 스펙타이트 ……………………… ···120 스포드솔 …… ••… …………… ·168, 349 麟습;성: :강::하:…::…:…::…〔…::…::…:…::… : …:.?….' .3:4:1: 시스쿼옥사이드 ………………… ···167 시스데인 …………………………… 350 시아노박테리아 ………… 29, 85, 97, 111, 222, 249, 266 식물 잔여물 … ••• ……………… 17, 293 식물 전이…………………………… 330 식토 ……….……………………… ··67 쌍곡선 반응………………………… 180 。 아라비노오스 ……………………… 125 아리다솔 …………………………… 342 아산화질소 ………… •• …………… ·224 알리신 ……………………………… 128 양극성 ……………………………… 41
에스테르 분해효소 ………………… 67 연목, 침엽수재 …………………… 152 연합·……………… ··126, 131, 133, 146 영분 침전물………………………… 358 염습지 ……………………………… 257 영권 …………………… ···249, 252, 257 영상 ……………………… 99, 110, 131 영초 ………………………………… 251 의생 균근 ………… ···15, 195, 303, 348 의생 영양적 ………………………… 295 요소 분해효소 ………… 35, 36, 77, 210 요오드산 …………………………… 346 용수량 ……………………………… 236 용액 집소·………………………… .. 330 용적 밀도 …………………… ···37, 123 용탈 .. 168, 199, 217, 231, 237, 242, 246 운반자 ……………………………… 342 원형질막 …………………………… 313 유기 쇄설물…………………… 116, 327 유기 영양적 ………·…………… ··88, 93 유기 인 분해효소 ……… .. ,69, 310, 335 유기 잔여물……………… 119, 137, 175 유기 황 분해효소 ………………… 350 유도성 ……………………………… 77 유효 인 …………………………… 325 윤작 ··-……………………………… 23 윤충 …………………………… 112, 114 음수 ………………···……………… ·103 웅애 ………………………………… 114 웅축 ……………………………… ···163 이노시를 육인산염 ………………… 332 이동농경 …………………………… 140 이편모 무성생식 운동성 …… .. ,101, 106
이형세포 ………………… 97, 253, 265 이황화 결합………………………… 345 임계값 ……………………………… 354 임상 ………………………………… 192 임의성 ……………………………… 138 입상 ………………………………… 97 x 자낭 …………………………… 102, 106 자낭균강 ……………………… 102, 104 자낭포자 ……………………… 102, 106 지주색 비황세균 …………… ···249, 256 작용기 ………………………… 151, 169 참재 수확량………………………… 312 장관 ………………………………… 360 재래식 경운………………………… 137 재무기화 …………………………… 246 적응성 ……………………………… 77 전간 수확 …………………………… 23 전이 ………………………………… 296 전자 공여체 ……………………… ···38 전자 탐사침 ……………………… ···65 전형종 ……………………………… 355 절대적 발효성 … •• ………………… ·229 접균류 ……………………………… 99 점액물질 …………………………… 251 점액질 다당류 ……………………… 97 접종물(체) …………………………… 79 집합 ……………………… 87, 101, 106 정단 세포 ………………··………… ··97 정상상태 ……………… ···65, 144, 189 조간대의 습지 ……………………… 342
조건적 미호기성 ……………… ...•• ·251 조건적 발효성 ·……·······………… ·229 조류 13, 29, 85, 93, 96, 101, 107, 109, 114, 131 조직권 ………… ..... …………… ... · 127 구 · 휴수 ……………………………… 70 종균, 번식수단 … … ………… 17, 24, 79, 122, 123, 140 주사현미경 ……'………………… ··62 중력수 ……………………………… 42 중형동물 ……………………… 13, 138 지네 … •• ……………………… ·114, 115 지열천 ·… … ……………………… ··356 지오사이트 ………………………… 368 지의류 ·… ··98, 110, 111, 131, 249, 266 지체기 ……………………………… 153 지하층 ……………………………… 371 질량 유동 …………………………… 44 질산화작용 …·… ··49, 139, 177, 210, 212, 228, 238 질소고정 효소·… ··17, 20, 276, 279, 286 질소산화물 환원효소 ………… 221, 227 云 철-헴 단백질 ……………………… 270 철-황 단백질 …………… 273, 27 '.5, 34'.5 청색증 •• …………………………… •242 초 ……………………………… 97, 309 총 공극뮬 …………………………… 38 충전 물질………………………… ···231 친핵 치환반옹……………………… 201
=' 카테콜 …………………………… ···164 카페르산 ………………………… ···153 케토산 ……… .... .. . …………… … ··205 콘니페릴알코올 ………… … ……… 153 크실로오스 …………… … ………… 125 클로록스 ………………………… ···367 키틴 분해효소 ……………………… 160 드: 탈수소효소 …………………… 77, 202 탐침 …………………·………… ··65, 81 토마틴 ……………………………… 128 토성 …………………………… 36, 122 토양 단면 …………………… 121, 371 토양생물군 ·……………… ··4, 85, 120 토양 유기물 … 19, 31, 33, 126, 130, 293 통기 ……… 36, 37, 54, 75, 113, 137, 125 통제발화, 임화 •• :………………… 139 두과효소 …………………·……… ··88 트립신 ·…………………………… ··201 티라코이드 ………….……… ··97, 109 고 파세울린 …………………………… 128 파스칼 …………………………… 37, 41 파이코빌 단백질 …………………… 97 파이코시아난………………… ··96, 110 파이토알렉신 ……………………… 128
페룰산 ……………………………… 153 펙틴산 …………………………… ···9 7 펩티드 …………… … …………… •• ·2 0 1 편모성 진균류……………………… 101 편모충 ……………………… ···46, 113 평균 잔류시간 ·…………………… ··1 7 6 평균 확산계수 ……………………… 240 평판계수법 ………………… 79, 80, 121 포도당 ……………………… 77, 94, 102 포식 …………………………… 114, 116 포자체들 ……………………… 92, 106 포장 용수량 …………………… 38, 43 푹신레드 …………………………… 320 풀브산 …………………… 167, 168, 349 프로나제 …………………………… 157 프로데오스 •• ……………………… ·157 피복 경운…………………………… 137 피사틴 ……………………………… 128 피질권 ……………………………… 127 피테이트 …………………………… 332 필수 형기성 생물 …………………… 38
-o_ 하위 요소……………………… ······201 항생물성 ………………………… •• ·12 8 형질도입 ……………………… ···87, 88 화학영양적 •• •• • • •• • • •• • •• • • •• • • •• •• • •• • •• • · 88 화학 유기영양적 …………·… ··93, 357 화학적 무기영양 ………………… 354 화학적 탈질화작용 ………………… 227 환형동물 ………………………… ···114 활성 인 ………………………·… ··330 활성형 ……………………………… 347 황철광 ……………………………… 368 효모 ……………………… 15, 102, 112 후생동물 …………………… ···112, 114 훈증소독제 ………………………… 139 휴면포자 …………………………… 296 홉식 ………………………………… 116 흡착 ……………………… 35, 123, 180 흰가루 곰팡이 ……………… ···25, 152 흰가루병 ……………………… 101, 102 흰부패증 …………………………… 103
지은이와 옮긴이 소개 풀 (Eldor A. Paul) 미국 미시건 대학 농과대학장 편저 Soil Bio c hemi stry 3, 4, 5 권 논문 Carbon flow in mi cr obia l a~oc iat i on s 와 다수 클라크 (Fran ci s E. Clark) 미국 농무성과 콜로라도 주립대의 겸임교수 역임 논문 Inte r nal cy cl in g of 15nit ro g e n in shortg ras s pr air i e 의 다수 01 도원 서울대학교 식물학과 졸업 동 대학원 환경조경학 석사 미국 버지니아 공과 대학 환경학 박사 조지아 대학 생태학연구소 연구원 한국의국어대학교 환경학과 조교수 역임 현재 서울대학교 환경대학원 환경계획학과 조교수 공저 『환경학교』『환경과학』 역서 『생태학』 논문 Modell ing ph osph orus tran sp o rt in gras s bu ffer str ips 의다수 조병철 서울대학교 해양학과 졸업 동대학원석사 캘리포니아 주립대학 박사 스크립스 해양연구소, 조지아 대학 연구원 한국의국어대학교 조교수 역임 현재 서울대학교 해양학과 조교수 논문 Bio g e ochemi ca l sig nifica nce of bacte r ia l bio m ass in the ocean's eup h oti c zone 의 다수
토양미생물학과 생화학 대우학술총서 • 번역 84 1 판 1 쇄 찍음 -1996 년 6 월 15 일 1 판 1 쇄 펴냄 -1996 년 6 월 30 일 지은이 -E.A. 폴 F.E. 클라크 옮긴이 ―_이도원 조병철 펴낸이-朴孟浩 펴낸곳-(주)민음사 출판등록 1966. 5. 19. 제 1 6-4 90 호 서울 강남구 신사동 506 515-2000( 대표전화) 515-2007( 팩시밀리) 값 21,000 원 Printed in Seoul, Korea ® (주)민음사, 1996 미생물학 /KDC 475 ISBN 89-374 -40 84-9 94470 89-374 -30 0 0-2 (세트)
대우학술총서 ( 번역 ) 1 유목민족제국사 관텐/송기중 44 표상 포더/이영옥정성호 2 수학의 확실성 클라인/박세희 45 과정과 실재 화이트헤드/오영환 3 중세철학사 와인버그/강영계 46 그리스 국가 에 렌버그/김진경 4 日本語의 起源 밀러/김방한 47 거대한 변환 폴라니/박현수 5 古 代漠 語音 韻 學槪要 48 법인류학 포스피실/이문웅 칼그렌/최영애 49 언어철학 울스튼/곽강제 6 말과 사물 푸코/이광래 50 중세 이슬람 국가와 정부론 7 수리철학과 과학철학 와일/김상문 램톤/김정위 8 기후와 진화 피어슨/김준민 51 전통 쉴즈/김병서신현순 9 이상진리·역사 파트남/김효명 52 몽골문어문법 뽀뻬/유원수 10 사회과학에서의 場 理 論 53 중국신화전설 I 袁Ji !/전인초김선자 레빈 / 박재호 54 중국신화전설 Il 〈근간〉 11 영국의 산업혁명 55 사회생물학 1 윌슨/이병훈 · 박 시 룡 딘/나경수·이정우 56 사회생물학 ll 윌슨/이병훈·박시룡 12 현대과학철학논쟁 57 일반언어학의 제문제 1 쿤 外 / 조승옥김동식 밴베니스트 / 황경자 13 있음에서 됨으로 프리고진/이철수 58 일반언어학의 제문제 ll 14 비교종교학 바하 /김종 서 밴베니스트/황경자 15 동물행동학 하인드 / 장현갑 59 폭력과 성스러 움 16 현대우주론 시아마 / 양종만 지라르/김진식 · 박무호 17 시베리아의 샤머니즘 60 갑골학 60 년 黃作賓/ 이형구 디오세지·호팔 / 최길성 61 현대수학의 여행자 18 조형미술의 형식 피터슨 / 김인수·주형관 힐데브란트/조창섭 62 프랑스 혁명의 지적 기원 19 힐버트 리 드/ 아일해 모르네/주명철 20 원시국가의 진화 하스 / 최몽룡 63 해석학과 과학 21 商文明 張光 直/윤 내현 커널리 · 코이트너/이유선 22 마음의 깃생 태학 베이츤7 저석봉 64 서 힝 ?다경제 핀리/지동식 23 혼돈 속의 질서 65 음악사회학 베버/이건용 프리고진 스텐저스/유기풍 66 앙띠 오이디푸스 24 생명의 기원 밀라오르겔/박인원 들뢰즈 가따리/최명관 25 일 반언어학이론 야콥슨 1 권재일 67 과학커뮤니케이션론 26 국가권력의 이념사 프라이스/남태우 정준민 마이네케/이광주 68 교양교육의 개혁 다니엘 벨/송미섭 27 역사학 논고 브로델/이정옥 69 과학과 가치 래리 라우든/이유선 28 유럽의식의 위기 l 70 초기제국에 있어서의 교역과 시장 아자르/조한경 칼 폴라니/이종욱 29 유럽의식의 위기 Il 71 폭정론과 저항권 헬라 만트/심재우 아자르/조한경 72 생명과학철학 30 일반국가학 켈젠/민준기 데이 비 드 헐/하두봉 • 구혜영 31 일반언어학강의 소쉬르/최승인 73 사랑의 역사 쥴리아 크리스테바/김영 32 일반체계이론 버들란피/현승일 74 大地의 노모스 칼 슈미트/최재훈 33 현대문명의 위기와 기술철학 75 일반 공법학 강의 레옹 뒤기/이광윤 애거시/이군현 76 텍스트학 반 다아크/정시호 34 언어에 대한 지식 촘스키/이선우 77 문명의 발생 찰스 레드만/최몽룡 35 음운학원론 트루베쯔코이/한문희 78 근대국가의 발전 G 폿지/박상섭 36 우주의 발견 하위트/강용희 79 과학적 발견의 패턴 37 수학적 발견의 논리 R 핸슨/송진웅 • 조숙경 라카토스/우정호 80 아랍 문학사 R. A 니콜슨/사희만 38 텍스트 사회학 지마/허창운 81 1 8 세기 중국의 관료제도와 자연재해 39 현대물리학의 철학적 테두리 P. E 빌/정철웅 보움/전일동 82 역사비교언어학개론 40 과학과 가치관의 우선순위 R 안틸라/박기덕 • 남성우 스페리/이남표 83 계몽주의 철학 E. 카시러/박완규 41 신화의 진실 휘브너/이규영 42 대폭발 실크/홍승수 43 大同 書 /,Ji有爲/이성애